ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ
|
|
|
- Φωκάς Καλύβας
- 5 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΟΜΕΑΣ ΒΑΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Διευθυντής: Καθ. Ν. Βαμβακόπουλος «ΜΟΡΙΑΚΗ ΔΙΕΡΕΥΝΗΣΗ ΚΛΗΡΟΝΟΜΙΚΗΣ ΠΑΡΑΜΟΝΗΣ ΕΜΒΡΥΪΚΗΣ ΑΙΜΟΣΦΑΙΡΙΝΗΣ ΣΕ ΕΝΗΛΙΚΕΣ ΚΑΙ ΜΕΛΕΤΗ ΤΩΝ ΣΥΝΔΕΟΜΕΝΩΝ ΠΡΩΤΕΙΝΙΚΩΝ ΠΑΡΑΓΟΝΤΩΝ» ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΤΟΥ ΑΓΓΕΛΟΥ Γ. ΚΑΛΑΜΑΡΑ Βιολόγου ΥΠΟΒΛΗΘΗΚΕ ΣΤΟ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΗΣ ΣΧΟΛΗΣ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΙΑΣ ΛΑΡΙΣΑ
2 2
3 ΕΠΙΒΛΕΠΩΝ ΚΟΛΛΙΑ ΠΑΝΑΓΟΥΛΑ Επίκουρη Καθηγήτρια Μοριακής Γενετικής Ανθρώπου Πανεπιστημίου Αθηνών ΤΡΙΜΕΛΗΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗ ΕΠΙΤΡΟΠΗ ΒΑΜΒΑΚΟΠΟΥΛΟΣ ΝΙΚΟΛΑΟΣ Καθηγητής Βιολογίας Πανεπιστημίου Θεσσαλίας ΚΟΛΛΙΑ ΠΑΝΑΓΟΥΛΑ Επίκουρη Καθηγήτρια Μοριακής Γενετικής Ανθρώπου Πανεπιστημίου Αθηνών ΤΣΕΖΟΥ ΑΣΠΑΣΙΑ Αναπληρώτρια Καθηγήτρια Ιατρικής Γενετικής Πανεπιστημίου Θεσσαλίας ΕΠΤΑΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ ΒΑΜΒΑΚΟΠΟΥΛΟΣ ΝΙΚΟΛΑΟΣ Καθηγητής Βιολογίας Πανεπιστημίου Θεσσαλίας ΚΟΥΚΟΥΛΗΣ ΓΕΩΡΓΙΟΣ Καθηγητής Παθολογικής Ανατομικής Πανεπιστημίου Θεσσαλίας ΣΤΑΘΑΚΗΣ ΝΙΚΟΛΑΟΣ Καθηγητής Παθολογίας Πανεπιστημίου Θεσσαλίας ΚΥΡΙΑΚΟΥ ΔΕΣΠΟΙΝΑ Αναπληρώτρια Καθηγήτρια Ιατρικών Μεταγγίσεων Πανεπιστημίου Θεσσαλίας ΜΑΤΣΟΥΚΑ ΠΑΝΑΓΙΩΤΑ Αναπληρώτρια Καθηγήτρια Αιματολογίας Πανεπιστημίου Θεσσαλίας ΤΣΕΖΟΥ ΑΣΠΑΣΙΑ Αναπληρώτρια Καθηγήτρια Ιατρικής Γενετικής Πανεπιστημίου Θεσσαλίας ΚΟΛΛΙΑ ΠΑΝΑΓΟΥΛΑ Επίκουρη Καθηγήτρια Μοριακής Γενετικής Ανθρώπου Πανεπιστημίου Αθηνών 3
4 4
5 ΠΕΡΙΕΧΟΜΕΝΑ ΣΕΛΙΔΕΣ Περιεχόμενα 5 Πρόλογος ΓΕΝΙΚΟ ΜΕΡΟΣ Το μόριο της αιμοσφαρίνης Δομή της αιμοσφαιρίνης Οι αιμοσφαιρίνες του ανθρώπου Η οργάνωση των γονιδίων σφαιρίνης Ρύθμιση της έκφρασης των σφαιρινικών γονιδίων Ρυθμιστική περιοχή του συμπλέγματος των γονιδίων β -τύπου 23 (LCR) 1.6. Το γ- γονίδιο της σφαιρίνης Εμβρυϊκή αιμοσφαιρίνη στους ενήλικες Προέλευση F κυττάρων ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ Γενικά Μη φυσιολογικές πρωτεΐνες α- Θαλασσαιμία 34 5
6 4. ΣΥΖΗΤΗΣΗ ΣΥΜΠΕΡΑΣΜΑΤΑ Η επιλογή και η κατηγοριοποίηση των δειγμάτων Το μέγεθος και η καταλληλότητα του υπο μελέτη πληθυσμού Η επιλογή των ετεροζυγωτών της β-μα Σύγκριση αποτελεσμάτων των μεταλλαγών σε φορείς β-μα, δβ-μα 172 και HPFH, στο νομό Καρδίτσας σε σχέση με τα γενικά της Θεσσαλίας και της Ελλάδας 4.5 Συσχέτιση επιπέδων HbF με μεταλλαγές στο β-cluster (είτε για β-μα, 174 είτε για δβ-μα) και HPFH 4.6 Συχνότητα της δβ-μα στον Ελληνικό πληθυσμό Ο Ελληνικός τύπος της μη-ελλειπτικής Κληρονομικής Παραμονής 175 Εμβρυϊκής Ατμοσφαιρίνης HPFH. Αποτελέσματα από την ταυτοποίηση μιας νέας μετάλλαξης (g G>T) στην HBG Η διπλή ετεροζυγωτία μη ελλειπτικής (non-deletional)hpfh και δβμεσογειακής αναιμίας 4.9 Ο συνδυασμός της Κληρονομικής Παραμονής Εμβρυϊκής Αιμοσφαιρίνης Κρητικού μη-ελλειπτικού τύπου, με β-μεσογειακή Αναιμία Η 5 ρυθμιστική περιοχή των ανθρώπινων γονιδίων της εμβρυϊκής αιμοσφαιρίνης, ως ένα σημείο γονιδιακής σημειακής αναστροφής. Περίληψη 183 Summary 185 Βιβλιογραφία
7 Στην Κατερίνα Στη Γιούλη Στο Βαγγέλη Στη Μυρτώ 7
8 8
9 Στους γονείς μου 9
10 10
11 ΠΡΟΛΟΓΟΣ Η μεσογειακή αναιμία και τα θαλασσαιμικά σύνδρομα αποτελούν τα γενετικά νοσήματα με τη μεγαλύτερη συχνότητα, τόσο στους πληθυσμούς της Μεσογείου όσο και σε άλλες περιοχές της γης. Η κατανόηση της μοριακής τους βάσης και των εμπλεκόμενων μηχανισμών στη ρύθμιση της έκφρασης των γονιδίων σφαιρ ίνης στα διαφορετικά αναπτυξιακά στάδια του ανθρώπου θα βοηθήσει στην περαιτέρω κατανόηση των μηχανισμών αλληλορύθμισης των συμπλεγμάτων των γονιδίων σφαιρίνης και στην αποτελεσματικότερη πρόληψη, διάγνωση και θεραπεία των ατόμων με θαλασσαιμικά σύνδρομα. Στην παρούσα εργασία μελετήθηκαν οι cisαλληλουχίες του γ-γονιδίου σφαιρίνης για την ταυτοποίηση μεταλλαγών υπεύθυνων για την παρουσία αυξημένης εμβρυϊκής αιμοσφαιρίνης σε ασθενείς με θαλασσαιμικά σύνδρομα [β-θαλασσαιμία, δβ-θαλασσαιμία και κληρονομική παραμονή εμβρυϊκής αιμοσφαιρίνης (HPFH)] με σκοπό την κατανόηση των μηχανισμών αλληλεπίδρασης έκφρασης των γονιδίων σφαιρίνης. Η παρούσα εργασία πραγματοποιήθηκε υπό την εποπτεία της Επίκουρης Καθηγήτριας κας Κόλλια Παναγούλας στο Εργαστήριο Βιολογίας και Μο ριακής Γενετικής και Κυτταρογενετικής του Πανεπιστημίου Θεσσαλίας. Για την πραγματοποίηση της παρούσας μελέτης θα ήθελα να ευχαριστήσω ιδιαίτερα την κα. Κόλλια Παναγούλα, Επίκουρη Καθηγήτρια, για την εμπιστοσύνη, την καθοδήγηση και τη στήριξη που μου έδειξε κατά την εκπόνηση της διατριβής. Επίσης, ευχαριστώ θερμά τον Καθηγητή Βιολογίας του Πανεπιστημίου Θεσσαλίας, κ. Ν. Βαμβακόπουλο, για τη συμμετοχή του στην Τριμελή Συμβουλευτική Επιτροπή της διδακτορικής διατριβής μου και για τις εύστοχες παρατηρήσεις του κατά τη διάρκεια των πειραμάτων. Ιδιαίτερα θα ήθελα να ευχαριστήσω και την Αναπληρώτρια Καθηγήτρια Ιατρικής Γενετικής και μέλος της Τριμελούς Επιτροπής της διατριβής κα. Α. Τσέζου, για την εμπιστοσύνη της. Τέλος, θα ήθελα να ευχαριστήσω τα μέλη της επταμελούς Συμβουλευτικής Επιτροπής: τον Καθηγητή Παθολογίας κ. Ν. Σταθάκη, τον Καθηγητή Παθολογικής Ανατομικής του Πανεπιστημίου Θεσσαλίας κ. Γ. Κουκούλη, την Αναπληρώτρια Καθηγήτρια Αιματολογίας του Πανεπιστημίου Θεσσαλίας κα. Π. Ματσουκά και την Αναπληρώτρια Καθηγήτρια Ιατρικών Μεταγγίσεων του Πανεπιστημίου Θεσσαλίας κα. Δ. Κυριάκου. Για την πολύτιμη συνδρομή τους στην ολοκλήρωση της παρούσας διατριβής ευχαριστώ θερμά τους συνεργάτες και φίλους μου: τους συναδέλφους Βιολόγους του Εργαστηρίου Μοριακής Βιολογίας και Γενετικής του Πανεπιστημιακού Νοσοκομείου Λάρισας κα. Μαρία Σαμαρά, κα. 11
12 Μαρία Σάτρα, κα. Παγώνα Οικονόμου, κα. Σοφία Λυκούση, κα. Ιωάννα Χιώτογλου, κα. Ανδρομάχη Βαγενά και ιδιαιτέρως τον κ. Χρήστο Χασανίδη Μοριακό Βιολόγο για την επιστημονική συνεργασία και ανιδιοτελή βοήθεια τους συναδέλφους κ. Μάνο Παπαδάκη, κα. Φωτεινή Καράμπαμπα και την κα. Κλειώ Σινοπούλου του Κέντρου Μεσογειακής Αναιμίας, Λαϊκό Νοσοκομείο, για την πολύτιμη υποστήριξη και συνδρομή στη διάγνωση δύσκολων περιστατικών τους συναδέλφους Χρήστο Βαγενά και Βέρα Μπαλαμίτσα των Μονάδων Πρόληψης Μεσογειακής Αναιμίας στα Νοσοκομεία Λάρισας και Τρικάλων, αντίστοιχα, για τα στατιστικά στοιχεία τα οποία μου παραχώρησαν την τεχνολόγο του Εργαστηρίου της Μονάδας Πρόληψης Μεσογειακής Αναιμίας του Γενικού Νοσοκομείου Καρδίτσας κα. Πέτρα Κροσιμπλά για τη συνδρομή στη συλλογή του υλικού και της ανάλυσης των αιματολογικών στοιχείων τους τεχνολόγους του Εργαστηρίου Μοριακής Βιολογίας και Γενετικής του Πανεπιστημιακού Νοσοκομείου Λάρισας κα. Ασπασία Παπαγιαννοπούλου, Ασπασία Κυριτσάκα για το άριστο κλίμα συνεργασίας τέλος, οφείλω ένα μεγάλο ευχαριστώ στη σύζυγό μου και τα τρία παιδιά μου, για την κατανόησή τους όλα αυτά τα χρόνια. 12
13 1. ΓΕΝΙΚΟ ΜΕΡΟΣ 1.1. Το μόριο της αιμοσφαιρίνης Η αιμοσφαιρίνη (Hb) (ο όρος δόθηκε από Hoppe-Seyler 1864), είναι η μια από τις σημαντικότερες και διεξοδικά μελετημένες πρωτεΐνες του ανθρώπου. Η βασική λειτουργία της είναι η μεταφορά του Ο 2 από τους πνεύμονες στους ιστούς και αντίστροφα του CO 2 αλλά και η διατήρηση-ρύθμιση σταθερού ph στο αίμα. Αποτελείται από το πρωτεϊνικό μέρος, δύο ζεύγη πολυπεπτιδικών αλυσίδων, των σφαιρινών (ένα ζεύγος τύπου α και ένα ζεύγος τύπου β) και μια σιδηρούχο χρωστική την αίμη, υπεύθυνη για το ερυθρό χρώμα της αιμοσφαιρίνης. Κάθε μόριο σφαιρίνης είναι ενωμένο με ένα μόριο αίμης, που αποτελείται από ένα πρωτοπορφυρινικό δακτύλιο με ένα άτομο Fe ++ στο κέντρο, όπου γίνεται η πρόσδεση του Ο 2. Έτσι το σύμπλεγμα των 4 υπομονάδων συγκροτεί το τεταρτοταγούς δομής αιμοσφαιρινικό μόριο ελλειψοειδούς μορφής με διαστάσεις 64Åx55Åx50Å και Μ.Β Da. Το μόριο της αίμης είναι δισκοειδές με διαστάσεις 14Åx17Å και Μ.Β Da. Οι δύο σφαιρίνες τύπου α (α- like globin chains) αποτελούνται από 141 αμινοξέα εκάστη και οι δύο τύπου β (β-like globin chains) από 146 αντίστοιχα Δομή της αιμοσφαιρίνης Η αιμοσφαιρίνη είναι μία σύνθετη σφαιρική πρωτεΐνη, η οποία περιέχει και μη πρωτεϊνικά στοιχεία. Το πρωτεϊνικό τμήμα αντιστοιχεί σε τέσσερις πολυπεπτιδικές αλυσίδες σφαιρίνης, δύο α-τύπου (α και ζ σφαιρίνες) με 141 αμινοξέα και δύο β-τύπου (β, γ, δ, ε σφαιρίνες) με 146 αμινοξέα. Η κύρια αιμοσφαιρίνη στους ενήλικες είναι η HbA, η οποία αποτελείται από τις α 2 β 2 υπομονάδες. Σε ένα μικρό ποσοστό (~2%) οι ενήλικες διαθέτουν και ένα άλλο είδος αιμοσφαιρίνης την HbA 2, με αντίστοιχα τις υπομονάδες α 2 δ 2. Η κύρια εμβρυϊκή αιμοσφαιρίνη είναι η HbF με σύνθεση α 2 γ 2, ενώ κατά τα πρώτα στάδια της εμβρυϊκής ανάπτυξης εμφανίζονται οι Hb Gower1 (ζ 2 ε 2 ) και Hb Gower2 (α 2 ε 2 ) και Hb Portland (ζ 2 γ 2 ). Η τριτοταγής δομή του μορίου εξασφαλίζει τη δέσμευση άλλων μορίων και την ανταπόκριση σε περιβαλλοντικά μηνύματα. Η κάθε αλυσίδα σφαιρίνης περιλαμβάνει μία χαρακτηριστική προσθετική ομάδα αίμης και μία θέση δέσμευσης του οξυγόνου 13
14 (Ο 2 ) (Eικ. 1Α). Η αίμη, αποτελείται από τέσσερις πυρρολικούς δακτυλίους, οι οποίοι διατάσσονται σταυροειδώς σε ένα επίπεδο, στο κέντρο του οποίου στερεώνεται ένα άτομο δισθενούς σιδήρου (Eικ. 1Β). H προσθετική ομάδα της αίμης διευκολύνει την αντιστρεπτή σύνδεση του οξυγόνου μέσω αλλοστερικών αλληλεπιδράσεων. Σε αυτό, επίσης, συμβάλλει και η θέση του δακτυλίου μέσα σε μία αναδίπλωση προς το εσωτερικό υδρόφοβο τμήμα του μορίου της αιμοσφαιρίνης. Κρυσταλλογραφικές μελέτες με ακτίνες Χ έδειξαν ότι η τεταρτοταγής δομή της αιμοσφαιρίνης αλλάζει σημαντικά με την οξυγόνωση. Το οξυγονωμένο μόριο είναι πιο συμπαγές. Η οξυγόνωση μέσα σε μία υπομονάδα μεταφράζεται σε δομικές αλλαγές στα σημεία επαφής των υπομονάδων. Η πλήρωση και των τεσσάρων θέσεων με μόρια οξυγόνου διαφέρει ενεργειακά. Η συγγένεια δέσμευσης για το δεύτερο και τρίτο οξυγόνο είναι μεταξύ αυτών του πρώτου (λιγότερο ευνοϊκή ενεργειακά) και του τέταρτου. Εικόνα 1Α. Στερεοδιάταξη της αλυσίδας β της αιμοσφαιρίνης. Β. Το μόριο της αίμης (Σιδηροπρωτοπορφυρίνη ΙΧ) 1.3. Οι αιμοσφαιρίνες του ανθρώπου Η διαδικασία της ερυθροποίησης στον άνθρωπο αποτελεί μια πολύ βασική λειτουργία ξεκινώντας από την εμβρυϊκή ζωή και συνεχίζει μέχρι την ενήλικη φάση του ανθρώπου με τη συμμετοχή διαφορετικών οργάνων. Ο λεκιθικός ασκός είναι το πρώτο αιμοποιητικό όργανο έως την 5 η εβδομάδα της κύησης, ο οποίος αντικαθίσταται από το εμβρυϊκό ήπαρ έως την 20 η εβδομάδα. Στη συνέχεια συμμετέχει ο σπλήνας και λίγο πριν τη γέννηση ενεργοποιείται ο μυελός των οστών που παραμένει το αιμοποιητικό όργανο σε όλη την υπόλοιπη ενήλικη ζωή (Εικ. 2). (2-4) Η διαδικασία παραγωγής της ανθρώπινης αιμοσφαιρίνης (Hb) χαρακτηρίζεται από 2 μεγάλες αλλαγές ως προς τη σύνθεση των σφαιρινικών αλυσίδων. Πρώτη, η 14
15 αντικατάσταση των πρωτοεμβρυϊκών από την εμβρυϊκή αιμοσφαιρίνη (HbF), η οποία συμπίπτει με την αλλαγή του οργάνου ερυθροποίησης από τον λεκιθικό ασκό στο ήπαρ. Δεύτερη αλλαγή, από την εμβρυϊκή στην αιμοσφαιρίνη του ενήλικα, η οποία γίνεται λίγο πριν τη γέννηση όπου ο μυελός των οστών έχει ξεκινήσει να συμμετέχει στην ερυθροποίηση, ενώ παράλληλα εξακολουθούν το ήπαρ και ο σπλήνας να αποτελούν αιμοποιητικά όργανα. Οι αντικαταστάσεις των εκφραζομένων γονιδίων στο β σύμπλεγμα, του ε από το γ γονίδιο και ακολούθως του γ από το β γονίδιο, ελέγχονται αποκλειστικά σε επίπεδο μεταγραφής. (5) Η αντικατάσταση του ζ από το α γονίδιο ελέγχεται κατά κύριο λόγο σε επίπεδο μεταγραφής, υπάρχουν όμως και μετα - μεταγραφικές διαδικασίες οι οποίες επηρεάζουν δευτερευόντως. (8) Στους πρώτους μήνες κύησης τα ερυθροκύτταρα περιέχουν κυρίως τις πρωτοεμβρυϊκές αιμοσφαιρίνες (Hb Gower1 και Hb Portland 1), οι οποίες κατά τους 6 τελευταίους μήνες έχουν πλήρως αντικατασταθεί από την εμβρυϊκή αιμοσφαιρίνη (HbF). Τα διαφορετικά μόρια αιμοσφαιρίνης που χαρακτηρίζουν τις μεταβολές αυτές στην ερυθροποίηση κατά την εμβρυϊκή και την ενήλικη ζωή του ανθρώπου φαίνονται στον Πίνακα 1. Όπως φαίνεται από τη σύνθεση όλων των μορίων αιμοσφαιρίνης, με εξαίρεση τις αιμοσφαιρίνες των αρχικών εβδομάδων της εμβρυογένεσης (Hb Gower1: ζ 2 ε 2 και Hb Portland1: ζ 2 γ 2 ), σε όλες τις άλλες περιλαμβάνονται 2α αλυσίδες και 2 μη-α. Το έμβρυο διαθέτει μία χαρακτηριστική μη-α αλυσίδα, τη γ-αλυσίδα, η οποία μετά τη γέννηση αντικαθίσταται από μία άλλη μη-α αλυσίδα, τη β, χαρακτηριστική για τον ενήλικα. Ενώ αρχικά η ζ σφαιρίνη είχε χαρακτηριστεί απλά ως ένα νέο μόριο σφαιρινικής αλυσίδας και ότι προέρχεται από διαφορετικό γονιδιακό σύμπλεγμα, περαιτέρω μελέτες απέδειξαν δομικές ομοιότητές της με την α-σφαιρίνη οι οποίες οδήγησαν τελικά στην κατάταξή της ως μίας α-τύπου σφαιρίνης. (6,7) Έτσι κάθε μόριο αιμοσφαιρίνης του οργανισμού διαθέτει δύο α-τύπου και δύο β τύπου αλυσίδες. Στη γέννηση η HbF αποτελεί το 60-80% της παραγόμενης αιμοσφαιρίνης. Στα βρέφη εβδομάδων συναντάται σε ποσοστό 3% της ολικής αιμοσφαιρίνης και μπορεί να απαιτηθούν και 2 χρόνια για να σταθεροποιηθεί στα φυσιολογικά για τον ενήλικα επίπεδα (0,5-1%). Η HbF συναντάται μέσα σε μικρό αριθμό ερυθροκυττάρων, τα F κύτταρα, τα οποία αποτελούν το 3-7% των ερυθροκυττάρων που παράγονται από το μυελό των οστών. (51) Η δομική διαφορά της εμβρυϊκής αιμοσφαιρίνης (HbF) από την αιμοσφαιρίνη του ενηλίκου (HbA) οδηγεί σε λειτουργικές διαφοροποιήσεις. Μία ουσιαστική ιδιότητα της HbF είναι ότι έχει υψηλότερη συγγένεια με το οξυγόνο κάτω από φυσιολογικές συνθήκες σε σχέση με την HbA. Έτσι μεγιστοποιεί τη μεταφορά του οξυγόνου από τη μητρική κυκλοφορία στο έμβρυο, οξυγονώνοντας την HbF από την άλλη πλευρά του πλακούντα σε βάρος 15
16 της HbA. Η αναλογία σύνθεσης των γ αλυσίδων ( G γ/ Α γ) είναι χαρακτηριστική και αλλάζει κατά τη διάρκεια της οντογένεσης του ανθρώπου, ξεκινώντας 3:1 στο έμβρυο και αλλάζοντας σε 2:3 στον ενήλικα. (14) Στα ερυθροκύτταρα ενηλίκου η κύρια αιμοσφαιρίνη είναι η HbA καθώς και μικρές ποσότητες HbA 2 και HbF. (5) Eικόνα 2. Η σύνθεση των αλυσίδων των αιμοσφαιρινών και τα αντίστοιχα όργανα που συμμετέχουν κατά τη διάρκεια της οντογένεσης του ανθρώπου. Πίνακας 1. Σύνθεση των μορίων των αιμοσφαιρινών του ανθρώπου. Αιμοσφαιρίνες Ανθρώπου Πρωτοεμβρυϊκές Αιμοσφαιρίνες HbGower1:ζ 2 ε 2 HbGower2:α 2 ε 2 Hb Portland Ι: ζ 2 γ 2 Hb Portland ΙΙ: ζ 2 β 2 Εμβρυϊκή Αιμοσφαιρίνη Hb F: α 2 γ 2 Αιμοσφαιρίνη Ενηλίκου HbA: α 2 β 2 Hb A 2 : α 2 δ 2 16
17 1.4. Η οργάνωση των γονιδίων σφαιρίνης. Τα γονίδια των σφαιρινικών αλυσίδων διακρίνονται σε α- και β- τύπου. Τα γονίδια α- τύπου εκτείνονται στο μικρό βραχίονα του χρωμοσώματος 16 (σύμπλεγμα γονιδίων α-τύπου), ενώ τα γονίδια β-τύπου στο μικρό βραχίονα του χρωμοσώματος 11 (σύμπλεγμα γονιδίων β-τύπου). Η διάταξη των γονιδίων από το 5 προς το 3 άκρο, είναι όμοια με τη σειρά με την οποία εκφράζονται τα γονίδια κατά την οντογένεση των αιμοσφαιρινών στον άνθρωπο (Εικ.3). Εικόνα 3. Διάταξη των γονιδίων σφαιρίνης β- και α-τύπου στα χρωμοσώματα 11 και 16, αντίστοιχα Στα γονίδια του συμπλέγματος α-τύπου περιλαμβάνονται κατά σειρά, τα διπλασιασμένα α 1 και α 2, το πρωτοεμβρυϊκό ζ 2. Μεταξύ των α 1 και α 2 εμφανίζεται υψηλή ομολογία και ουσιαστικά κωδικοποιούνται όμοιες πρωτεΐνες. Οι διαφορές τους είναι μόνο σε νουκλεοτίδια των μη κωδικών περιοχών ( IVS-2 και στην 3 μη κωδική περιοχή). Η ομολογία μεταξύ των γονιδίων α και ζ μειώνεται στο 58% των αμινοξέων τους (επί συνόλου 141), καθώς φαίνεται ότι έχουν προκύψει από κοινό πρόγονο, μετά από μία σειρά διπλασιασμών με πολλές αποκλίσεις στην αλληλουχία τους. (1) Στα γονίδια του συμπλέγματος β-τύπου ανήκουν τα ε, Gγ, Αγ, ψβ, δ και β γονίδια. Τα ε και γ γονίδια είναι αποκλειστικά εμβρυϊκά γονίδια, από τα οποία το γ μπορεί να παραμένει σε πολύ μικρή έκφραση για μικρό διάστημα και μετά τη 17
18 γέννηση. Τα δ και β είναι γονίδια του ενήλικα, όπου το δ εκφράζεται φυσιολογικά σε χαμηλά επίπεδα. Στον άνθρωπο το δ γονίδιο της αιμοσφαιρίνης έχει υψηλή ομολογία με το β γονίδιο, αν και παράγεται σε πολύ μικρότερο ποσοστό από το β γονίδιο σφαιρίνης. Η αστάθεια του δ-mrna, η έλλειψη ενός ενισχυτή στο εσωτερικό του γονιδίου, καθώς και η απουσία των συντηρητικών αλληλουχιών του υποκινητή CAAT και CACCC, είναι η πιθανή μοριακή ερμηνεία που μπορεί να δικαιολογήσει τα μικρά ποσοστά έκφρασής του. (3) Η έλλειψη της λειτουργικής δομής CACCC στον υποκινητή του δ γονιδίου και η αδυναμία πρόσδεσης του μεταγραφικού παράγοντα EKLF είναι αρκετή για να οδηγήσει τον υποκινητή του δ γονιδίου σε μειωμένη λειτουργικότητα. (1) Τα G γ και Α γ γονίδια δίνουν δομικά όμοια προϊόντα και είναι αποτέλεσμα γονιδιακού διπλασιασμού και μεταστροφής. (2) Οι αλυσίδες των δύο γ γονιδίων διαφέρουν μόνο στο αμινοξύ της θέσης 136, όπου υπάρχει γλυκίνη (Gly) και αλανίνη (Ala) για τη G γ και Α γ αλυσίδα, αντίστοιχα. Η ομοιότητα στη δομή και η παρουσία ψευδογονιδίων οδηγούν στο συμπέρασμα ότι η ομάδα αυτή των γονιδίων των σφαιρινών προέρχεται από διπλασιασμούς ενός προγονικού γονιδίου. (14) 1.5. Ρύθμιση της έκφρασης των σφαιρινικών γονιδίων. Η ιστοειδική έκφραση των γονιδίων των σφαιρινών καθώς και η ειδικότητα εμφάνισης σε συγκεκριμένο οντογενετικό στάδιο εξασφαλίζεται με τη συμμετοχή κατάλληλων ρυθμιστικών στοιχείων, υποκινητών, ενισχυτών, αποσιωπητών και πρωτεϊνικών παραγόντων. Τα στοιχεία αυτά αλληλεπιδρούν με περιοχές, όπως η ρυθμιστική περιοχή (Locus Control Region, LCR) του συμπλέγματος των γονιδίων β- τύπου και η υπερευαίσθητη περιοχή, HS-40, στο σύμπλεγμα α-τύπου γονιδίων, οι οποίες αν και βρίσκονται σε μεγάλη απόσταση από τα αντίστοιχα γονίδια, έχουν τη δυνατότητα να επηρεάζουν και να επιτυγχάνουν υψηλά επίπεδα γονιδιακής έκφρασης. (17) Οι αλλαγές στη δομή της χρωματίνης, που σταθεροποιούνται από πολυμερή σύμπλοκα μεταγραφικών παραγόντων, επιτρέπουν αυτές τις αλληλεπιδράσεις μεταξύ απομακρυσμένων περιοχών. Τα σύμπλοκα αυτών των δομών αρχικά σχηματίζονται σε συγκεκριμένες θέσεις των γονιδίων, όπως τα TATAbox, CAAT-box και CACCC-box. Ακολούθως σημαντικός αριθμός μεταγραφικών παραγόντων αλληλεπιδρά με το DNA προκειμένου να ολοκληρωθεί η διαδικασία της ιστοειδικής έκφρασης των γονιδίων των σφαιρινών. Το ζ γονίδιο διαθέτει στον υποκινητή του περιοχές, όπως οι TATA- (-28), CAAT- (-66) και CACCC- (-95), ανάλογες με αυτές οι οποίες συναντώνται και σε 18
19 άλλα γονίδια. Σε αυτές τις θέσεις προσδένονται οι μεταγραφικοί παράγοντες CP-2, Sp-1, GATA-1 και άλλοι, μέσω των οποίων ρυθμίζεται η έκφραση του γονιδίου κατά την οντογένεση των αιμοσφαιρινών. (15) Η αναπτυξιακή ρύθμιση του ζ γονιδίου είναι αυτόνομη, καθώς οι διάφορες αλληλουχίες που απαιτούνται για την αποσιώπηση του γονιδίου βρίσκονται εντός ή κοντά στο γονίδιο. Η αποσιώπηση του ζ γονιδίου ελέγχεται από μεταγραφικές και μετα-μεταγραφικές διαδικασίες. (16) Ο υποκινητής του α γονιδίου παρουσιάζει ορισμένες εμφανείς διαφορές σε σχέση με τα άλλα γονίδια. Δεν διαθέτει CACCC περιοχή και έχει μία περιοχή, πλούσια σε CG-επαναλήψεις, η οποία είναι μέρος της νησίδας που δεν γίνεται μεθυλίωση και εκτείνεται μέσα στο γονίδιο, ενώ είναι τμήμα του υποκινητή. Στον υποκινητή προσδένονται μεταγραφικοί παράγοντες οι οποίοι είναι κοινοί και για τα β- τύπου γονίδια, όπως GATA-1, CP-1, καθώς και διαφορετικές πρωτεΐνες, όπως η CP- 2 και η πρωτεΐνη αντίστροφων επαναλήψεων (inverted repeat protein). Ορισμένοι από τους σημαντικότερους μεταγραφικούς παράγοντες για τα γονίδια των σφαιρινών είναι οι ακόλουθοι: (5) 1. GATA-1: Ανήκει στην οικογένεια των μεταγραφικών παραγόντων GATA και στην ομάδα των πρωτεϊνών τύπου δάκτυλο ψευδαργύρου ( zing - finger). Ο κύριος λόγος που οδήγησε τους μελετητές να τον συσχετίσουν με τον πρωτεϊνικό παράγοντα GATA-2, είναι η ύπαρξη υψηλής ομολογίας στις δύο περιοχές σύνδεσης με το DNA που διαθέτουν οι δύο μεταγραφικοί παράγοντες, οι οποίες ονομάζονται «δάκτυλα ψευδαργύρου». Επίσης η περιοχή αυτή εμφανίζει υψηλή ομολογία στα αντίστοιχα μόρια διαφορετικών ειδών οργανισμών. Η περιοχή πρόσδεσης στο DNA είναι η αλληλουχία (T/A)GATA(A/G). Η έκφραση του GATA-1 έχει συνδεθεί ισχυρά με το αιμοποιητικό σύστημα, με άφθονη παρουσία στα προγονικά κύτταρα των ερυθρών (erythroid progenitors), στα μεγακαρυοκύτταρα, τα ηωσινόφιλα και στα μαστικά κύτταρα (mast cell). Στα πολυδύναμα προγονικά κύτταρα εκφράζεται σε μικρότερες ποσότητες. (18) Αρχικά είχε χαρακτηρισθεί ως πυρηνικός παράγοντας, ο οποίος συνδέεται με τον υποκινητή ή τους ενισχυτές των σφαιρινικών γονιδίων όλων των ειδών. Πρόσφατες μελέτες έδειξαν ότι η πλειονότητα των γονιδίων που ειδικά εκφράζονται στα μεγακαρυοκύτταρα, τα ηωσινόφιλα και τα μαστικά κύτταρα, ελέγχονται εν μέρει από τον GATA-1. (19) Έτσι παρόλο που ο GATA-1 έχει χαρακτηρισθεί ως «ερυθροειδικός» μεταγραφικός παράγοντας, λειτουργεί σε πολλαπλούς κυτταρικούς τύπους, οι οποίοι συνδέονται μεταξύ τους μέσω κοινών προγόνων και μπορούν να διαφοροποιηθούν σε δύο ή τρεις διαφορετικούς τύπους κυττάρων. (20) Ενδιαφέρον παρουσιάζει ο τρόπος με τον οποίο ο GATA-1 ασκεί μεταγραφικό έλεγχο. Οι θέσεις πρόσδεσης του GATA-1 βρίσκονται 19
20 συνήθως μέσα σε υποκινητές ή σε ρυθμιστικές περιοχές που βρίσκονται σε απόσταση από το γονίδιο που ελέγχουν, όπως το LCR των γονιδίων β-τύπου και διαμορφώνει κατάλληλα σύμπλοκα σχετιζόμενα με τη χρωματίνη. Μελέτες έδειξαν ότι πρόκειται για έναν αντιστρεπτό μεταγραφικό ενεργοποιητή και η δράση του στα ερυθροειδικά κύτταρα και πολύ πιθανόν και στα μεγακαρυοκύτταρα περιλαμβάνει την ύπαρξη συμπαράγοντα ή ομάδας συμπαραγόντων. (21) Η δομή του, ως πρωτεΐνη τύπου «δάκτυλα ψευδαργύρου», ευνοεί τη συνεργασία του με άλλες πυρηνικές πρωτεΐνες. Είναι γνωστή η συνεργασία του με την οικογένεια πρωτεϊνών τύπου Kruppel, οι οποίες έχουν επίσης τη δομή τύπου «δάκτυλα ψευδαργύρου», όπως τον ερυθροειδικό παράγοντα EKLF, το γενικό μεταγραφικό παράγοντα Sp1, καθώς και το γενικό μεταγραφικό συμπαράγοντα p300/cbp. (22) Επομένως, η αλληλοεπίδραση του GATA-1 με τις άλλες πρωτεϊνες είναι απαραίτητη για να ολοκληρωθεί η διαφοροποίηση των ερυθροκυττάρων και για το λόγο αυτό δε θεωρείται ένας απλός μεταγραφικός παράγοντας αλλά ο αρχιτέκτονας της μεταγραφικής ρύθμισης στην ερυθροποίηση. 2. CREB: Ονομάζεται η ομάδα των πρωτεϊνών οι οποίες αναγνωρίζουν ως θέσεις πρόσδεσης μία αλληλουχία που ανταποκρίνεται στο camp (camp response element-[cre]-binding protein). Σε αυτήν την ομάδα ανήκει και ο συμπαράγοντας CBP/p300. Πρόκειται για μόριο το οποίο συνδέεται με πυρηνικούς υποδοχείς ορμονών (26) και επιδρά στην ακετυλίωση καθώς έχει συνδεθεί με την ενεργότητα της ακετυλοτρανσφεράσης των ιστονών. (29) Η ακετυλίωση είναι απαραίτητη προκειμένου να παραμείνει ανοικτή η χρωματίνη και να διατηρηθεί η μεταγραφική δραστηριότητα. Αρκετές μελέτες υπεδείκνυαν την ομάδα αυτών των πρωτεϊνών ως πιθανούς συμπαράγοντες του GATA-1 (25) και τελικά απέδειξαν ότι πρωτεΐνες CREB συνεργάζονται με τον GATA-1 και είναι απαραίτητες για τη διαφοροποίηση των ερυθροκυττάρων, καθώς ο GATA-1 φαίνεται να «στρατολογεί» τον ευρύτερης έκφρασης συμπαράγοντα CBP προς στοχευμένη κυτταροειδική, γονιδιακή έκφραση και διαφοροποίηση. (27) 3. Oct: Πρόκειται για δύο πρωτεΐνες (οκταμερή), μέλη της οικογένειας POU, Oct-1 και Oct-2, η πρώτη ευρύτατης έκφρασης και η δεύτερη κυρίως εμπλέκεται στην έκφραση των Β-λεμφοκυττάρων (B cells). Είναι ένας μεταγραφικός παράγοντας ο οποίος συμμετέχει στη ρύθμιση μεγάλου αριθμού γονιδίων με ιστοειδική ή ευρύτερη έκφραση, σε ρόλο ενεργοποιητή ή καταστολέα. (32) Πρόσφατες μελέτες απέδειξαν ότι συμμετέχει ουσιαστικά στην ανάπτυξη του εμβρύου και στην ερυθροποίηση. (33) 20
21 4. ΝF-E2: πρωτεΐνη που προσδένεται στην αλληλουχία DNA (T/C)/GCTGA(C/G) TCA(T/C) και απαντάται σε ρυθμιστικές περιοχές των γονιδίων σφαιρινών. Είναι πρωτείνη 45 kd και ανήκει στις πρωτεΐνες τύπου φερμουάρ - λευκίνης. Είναι ένας παράγοντας βασικός για την ανάπτυξη των μεγακαρυοκυττάρων και τη παραγωγή των αιμοπεταλίων, χωρίς να είναι απόλυτα απαραίτητος για την ερυθροποίηση. (23) Ο ρόλος του NF-E2 στην ερυθροποίηση δεν έχει πλήρως διευκρινισθεί. 5. EKLF (erythroid Kruppel-like factor): Είναι μέλος της οικογένειας των SP1 πρωτεϊνών, οι οποίες είναι τύπου δάκτυλα ψευδαργύρου (zing-finger). Συνήθως αποτελούνται από 3 δομές-δάκτυλα, η καθεμία από τις οποίες αναγνωρίζει μία αλληλουχία DNA 3 βάσεων. Συγκεκριμένα ο EKLF αναγνωρίζει την αλληλουχία CCA CAC CCT, η οποία βρίσκεται στην υποκινητή του β γονιδίου. (24) Ο EKLF δρα ως ενεργοποιητής της μεταγραφής του β γονιδίου, είναι απαραίτητος για την έκφρασή του και για την τελική ωρίμανση των ερυθροκυττάρων. (28) Υπάρχουν δεδομένα που δείχνουν ότι παίζει ρόλο στην ενεργοποίηση του LCR, μέσω της αλληλεπίδρασης του με περιοχή πλούσια σε G -υπομονάδες μέσα στην HS3 αλληλουχία. (30) 6. FKLF και FKLF-2 (fetal Kruppel-like factor): Θεωρούνται μέλη της οικογένειας των Sp1 πρωτεϊνών και αλληλεπιδρούν με την CACCC αλληλουχία που βρίσκεται στον υποκινητή του ε και γ γονιδίου σφαιρίνης. (31), που μεταφέρει τη γενετική πληροφορία από τα γονίδια του πυρήνα στα ριβοσώματα Ρυθμιστική περιοχή του συμπλέγματος των γονιδίων β-τύπου (LCR) Η ρύθμιση της ερυθροποίησης στον άνθρωπο ελέγχεται επιπλέον και από την περιοχή LCR (Locus Control Region), η οποία συμμετέχει καθοριστικά στη διαδικασία της μεταστροφής της αιμοσφαιρίνης, η οποία πραγματοποιείται δύο φορές κατά την οντογένεση του ανθρώπου. Η περιοχή αυτή αλληλεπιδρά με καθένα από τα γονίδια των σφαιρινών προκειμένου να εξασφαλιστεί η έκφρασή του στο κατάλληλο οντογενετικό στάδιο. (17) Η περιοχή LCR βρίσκεται περίπου 20 kb 5 του ε γονιδίου και περιλαμβάνει θέσεις υπερευαίσθητες στην DNase I (DNase I hypersensitive sites, HS). Η πρώτη ένδειξη για την ύπαρξη σημαντικών ρυθμιστικών αλληλουχιών μακριά από τα γονίδια σφαιρινών ήταν η περιγραφή μεταλλαγών-ελλείψεων τμημάτων του συμπλέγματος γονιδίων β-τύπου που δεν επηρέαζαν τη δομή του β γονιδίου αλλά προκαλούσαν εικόνα β θαλασσαιμίας (γδβ 0 θαλασσαιμία) στα άτομα που την 21
22 έφεραν. (5) Σε πειράματα με διαγονιδιακά ζώα αποδείχτηκε ότι η περιοχή LCR αποτελείται από πέντε HS περιοχές, HS-1 έως HS-5, και η ενεργότητα τους εντοπίζεται σε έκταση 250 έως 500 bp η κάθε μία. (34) Η HS-2 ευθύνεται για το 40-50% της δράσης της περιοχής LCR, ενώ η HS-1 και η HS-4 για το 5-10%. Μία πέμπτη HS περιοχή έχει βρεθεί στο 3 άκρο του συμπλέγματος β-τύπου και απέχει 21.8 kb από το β γονίδιο, αν και ο ρόλος της παραμένει ακόμα αδιευκρίνιστος. (34) Επιπλέον, έχουν βρεθεί άλλες δύο θέσεις HS (6 και 7) στην περιοχή μεταξύ 3 άκρου του β-γονιδίου και της πέμπτης HS και έτσι το σύμπλεγμα των γονιδίων β-τύπου εκτείνεται σε μία περιοχή 170kb. (35) Η περιοχή LCR διατηρώντας τη χρωματίνη «ανοιχτή» στη συγκεκριμένη περιοχή εξασφαλίζει την πρόσβαση των διαφόρων μεταγραφικών παραγόντων στους υποκινητές των σφαιρινικών γονιδίων. Επίσης θεωρείται ότι μπορεί να λειτουργεί και ως απομονωτής της χρωματίνης για προστασία του συμπλέγματος των γονιδίων β-τύπου. (36) Στη νουκλεοτιδική αλληλουχία του LCR έχουν αναγνωρισθεί θέσεις σύνδεσης του GATA-1 και του NF-E2, καθώς επίσης και οι χαρακτηριστικές περιοχές CACC στις οποίες, όπως έχει αναφερθεί, προσδένεται ποικιλία μεταγραφικών παραγόντων ευρείας δράσης, όπως ο Sp-1. (37,38) Μεγάλο ερευνητικό ενδιαφέρον υπήρξε για τη μελέτη του μηχανισμού μέσω του οποίου επιτυγχάνεται η ρύθμιση της έκφρασης των σφαιρινικών γονιδίων κατά την οντογένεση του ανθρώπου. Σημαντικός αριθμός μελετών κατέληξαν στη διατύπωση ενός διπλού μηχανισμού ελέγχου της μεταστροφής της αιμοσφαιρίνης με τη συμμετοχή του LCR. Αυτό επιτυγχάνεται αφενός καταρχήν με την αποσιώπηση ορισμένων γονιδίων και αφετέρου με το συναγωνισμό μεταξύ γονιδίων στη διεκδίκηση της περιοχής LCR με την οποία θα εξασφαλιστούν υψηλά επίπεδα μεταγραφής. (38) Έτσι τελικά το LCR μπορεί και επιτελεί το ρόλο του, αν και βρίσκεται σε μεγάλη απόσταση. Για τη διαδικασία αυτή έχουν προταθεί τρία διαφορετικά μοντέλα (39) : Δυαδικό μοντέλο ενεργοποίησης (binary activation model), σύμφωνα με το οποίο τα γονίδια συνδέονται με τους μεταγραφικούς παράγοντες στοχαστικά. Όταν η περιοχή ελέγχου είναι ενεργή, καθένα γονίδιο έχει τη δυνατότητα να συνδεθεί με τους μεταγραφικούς παράγοντες χωρίς να λαμβάνει χώρα ανταγωνισμός μεταξύ τους. Το μοντέλο δέχεται ότι τα κοντινά γονίδια έχουν προβάδισμα έναντι των απομακρυσμένων γονιδίων. Η μεταγραφή των κοντινών γονιδίων οδηγεί σε δομικές αλλαγές, μη αναγνωρισμένες, οι οποίες με τη σειρά τους εμποδίζουν τη μεταγραφή των πιο απομακρυσμένων γονιδίων. Αναπτυξιακά καθώς σιωπούν τα πρώτα γονίδια, χάνονται και οι 22
23 προαναφερόμενες επιδράσεις και είναι δυνατή η μεταγραφή των επόμενων γονιδίων. (40) Μοντέλο Ιχνηλασίας (tracking model), προτείνει ότι το LCR λειτουργεί ως σημείο εισόδου για ορισμένα από τα συστατικά της μεταγραφικής μηχανής, τα οποία κινούμενα κατά μήκος του DNA εντοπίζουν το γονίδιο που πρέπει να μεταγραφεί. Έτσι σαφώς τα κοντινότερα σε αυτό γονίδια προηγούνται στη μεταγραφή. (41) Μοντέλο Θηλιάς (looping model), το οποίο προτείνει ότι η έναρξη της μεταγραφής επιτυγχάνεται μετά από αλληλεπίδραση μεταξύ του LCR και των γονιδίων, όπου η ενδιάμεση αλληλουχία του DNA αναδιπλώνεται με τη μορφή θηλιάς. Τελικά η μεταγραφή παραμένει ενεργή για όσο χρονικό διάστημα διατηρείται αυτή η αλληλεπίδραση, ενώ το ποσοστό της μεταγραφής των γονιδίων σφαιρίνης είναι αποτέλεσμα της συχνότητας και της σταθερότητας αυτών των αλληλεπιδράσεων με το LCR. (42) 1.6. Το γ- γονίδιο της σφαιρίνης Στις πρώτες εβδομάδες της κύησης εκφράζονται οι κατάλληλοι μεταγραφικοί παράγοντες οι οποίοι, συνδεόμενοι με τους υποκινητές των γ γονιδίων και την ρυθμιστική περιοχή (LCR), ενεργοποιούν την παραγωγή των εμβρυϊκών γονιδίων των σφαιρινών. Συγκεκριμένα, έχει δειχθεί ότι μεταγραφικοί παράγοντες, όπως οι SSP (Stage Selector Protein), FKLF (Fetal Kruppel-Like Factor), FKLF-2 και NF-E4 (Nuclear Factor Erythroid-4), παίζουν σημαντικό ρόλο στη ρύθμιση της έκφρασης των γ γονιδίων σφαιρίνης (Εικ. 4). ( ,127) Η μελέτη των μεταγραφικών αυτών παραγόντων και η συνεχής αναζήτηση νέων πρωτεϊνικών παραγόντων καθώς και των ενεργοποιούμενων σηματοδοτικών μονοπατιών αποσκοπεί στην κατανόηση του ακριβή μηχανισμού ενεργοποίησης και αποσιώπησης των εμβρυϊκών γονιδίων. (113, 116) Ο υποκινητής αποτελεί περιοχή πρόσδεσης για μεγάλο αριθμό μεταγραφικών παραγόντων. Οι υποκινητές των δύο γ γονιδίων (Gγ και Αγ) είναι ταυτόσημοι και αναγνωρίζονται πολλές από τις χαρακτηριστικές θέσεις πρόσδεσης πρωτεϊνών, όπως μία CAC θέση, δύο CCAAT θέσεις (μέσα σε μια διπλασιασμένη περιοχή 27bp) και μία TATA θέση. (39) Η περιοχή μεταξύ των νουκλεοτιδίων -40 και -60 στο 5 άκρο του γ γονιδίου περιέχει θέση πρόσδεσης για δύο πρωτεΐνες, τις Sp1 και SSP (stage selector protein). Επιπλέον, δύο CpG δινουκλεοτίδια μεταξύ των θέσεων -50 έως -55 του 5 άκρου του γ γονιδίου είναι μεθυλιωμένα σε ερυθροβλάστες 23
24 εμβρυονικού και ενήλικου σταδίου αλλά σπάνια σε εμβρυϊκούς. (55) Η περιοχή μεταξύ των νουκλεοτιδίων -53 και -34 στο 5 άκρο του γ γονιδίου, όπου βρίσκεται η θέση έναρξης της μεταγραφής του γ γονιδίου, λειτουργεί ως περιοχή επιλογής της έκφρασης στο αντίστοιχο οντογενετικό στάδιο (Stage Selector Element, SSE). Πρόκειται για θέση ανάλογη με αυτήν που βρέθηκε στον υποκινητή του β γονιδίου σφαιρίνης του κοτόπουλου, η οποία αλληλεπιδρά με τον β/ε ενισχυτή σε ερυθροκύτταρα ενηλίκου με τη συμμετοχή της πρωτεΐνης SSP. (44) Η ρύθμιση της έκφρασης του γ γονιδίου επηρεάζεται σημαντικά από την περιοχή LCR, η οποία ενισχύει τη μεταγραφή του γ γονιδίου στο κατάλληλο οντογενετικό στάδιο. (46) Υπάρχει μάλιστα γονιδιακή εξειδίκευση στη δράση των HS περιοχών. Συγκεκριμένα η HS3 του LCR ενισχύει επιλεκτικά το γ γονίδιο και η έλλειψή της από τη βασική αλληλουχία οδηγεί σε αποσιώπηση της έκφρασης του γ γονιδίου κατά την εμβρυϊκή ζωή. (45) Ο έλεγχος της έκφρασης του γ γονιδίου ουσιαστικά γίνεται μέσω του μηχανισμού αποσιώπησής του. Οι αλληλουχίες που σχετίζονται με την αποσιώπηση του γ γονιδίου είναι οι περιοχές CACCC και CCAAT που βρίσκονται στον υποκινητή του γ γονιδίου. Η περιοχή του υποκινητή έχει αποδειχθεί απαραίτητη για τον έλεγχο της έκφρασης του γονιδίου στην εμβρυϊκή ζωή και για τη διακοπή της παραγωγής γ- σφαιρίνης στον ενήλικα. Έχει προταθεί ότι η μεθυλίωση μπορεί να ρυθμίζει τη γονιδιακή έκφραση αλληλεπιδρώντας με διάφορους μεταγραφικούς παράγοντες. Συγκεκριμένα η μεθυλίωση του CpG προκαλεί 10 φορές αύξηση στη δράση της πρωτεΐνης Sp1, με παράλληλη μείωση ρυθμού πρόσδεσης του παράγοντα SSP. (55) Οι δύο πρωτεΐνες ανταγωνίζονται για την πρόσδεσή τους καθώς επικαλύπτονται οι θέσεις πρόσδεσης και με τον ανταγωνισμό αυτό επιτυγχάνεται η ενεργοποίηση και η αποσιώπηση του γονιδίου στο κατάλληλο οντογενετικό στάδιο. (46) Εικόνα 4. προσδένονται σε αυτόν. Ο υποκινητής του γ γονιδίου και οι μεταγραφικοί παράγοντες που 24
25 1.7. Εμβρυϊκή αιμοσφαιρίνη στους ενήλικες. Η γ σφαιρίνη εκφράζεται σε μικρό ποσοστό στους ενήλικες σε φυσιολογικές συνθήκες και απαντάται σε εξειδικευμένα κύτταρα, τα F κύτταρα. (47) Η παραγωγή της F μπορεί να αυξηθεί μετά από την πρόκληση οξέος ερυθροποιητικού stress. Ευνοϊκές συνθήκες για την αύξηση της HbF δημιουργούνται σε ασθενείς μετά από χημειοθεραπεία, όπου συμβαίνει συρρίκνωση του μυελού των οστών. Επίσης ενίσχυση της παραγωγής των F κυττάρων παρατηρούμε κατά την αναγέννηση του μυελού των οστών μετά από μεταμόσχευση ή σε οξεία αιμόλυση, σε αντίθεση με τη χρόνια αναιμία όπου δεν παρατηρείται αύξηση του ποσοστού της. Η διαφορά στο ρυθμό παραγωγής των F κυττάρων μεταξύ οξέος και χρόνιου ερυθροποιητικού stress υποδηλώνει ότι η κινητική της αναγέννησης των ερυθροκυττάρων επηρεάζει την παραγωγή ή μη Α ή F κυττάρων. (48) Η αύξηση της παραγωγής των F κυττάρων στο δεύτερο τρίμηνο της εγκυμοσύνης σχετίζεται με την αύξηση του όγκου του αίματος (παραγωγή ερυθροκυττάρων), γεγονός το οποίο μπορεί να σχετιστεί με οξεία ερυθροποίηση. Μία από τις πρώτες παρατηρήσεις στο προφίλ της αιμοσφαιρίνης παιδιών με ομόζυγη β-θαλασσαιμία, ήταν η αυξημένη ποσότητα HbF τόσο στην παιδική όσο και στην ενήλικη φάση της ζωής. Ο έλεγχος του περιφερικού αίματος με ειδικές χρώσεις για την παρουσία HbF έδειξε ότι η αιμοσφαιρίνη αυτή κατανέμεται ετερογενώς στα ερυθροκύτταρα. Οι μέχρι τώρα μελέτες για το μηχανισμό παραμονής των γ αλυσίδων στις β θαλασσαιμίες οδηγούν στη σκέψη ότι η παραγωγή των γ αλυσίδων μπορεί να επηρεάζεται από το φαινόμενο επιλογής κυττάρων καθώς επίσης και από γενετικούς παράγοντες. (5) Οι παράγοντες που σχετίζονται με αυξημένη ποσότητα γ σφαιρίνης στην ενήλικη ζωή παρουσιάζουν μεγάλο ενδιαφέρον και διερευνώνται σε ασθενείς με δρεπανοκυτταρική αναιμία και άλλα μεσογειακά σύνδρομα καθώς η παρουσία αυξημένης HbF είναι καθοριστική για την ποιότητα ζωής του πάσχοντα. 25
26 Προέλευση F κυττάρων Στις αρχές της δεκαετίας του 1970 με τη βοήθεια ανοσοχημικών χρώσεων έγινε δυνατή η ανίχνευση ερυθροκυττάρων με αιμοσφαιρίνη F. Έτσι δείχτηκε ότι η εμβρυϊκή αιμοσφαιρίνη εντοπίζεται σε λίγα ερυθροκύτταρα, τα ονομαζόμενα F κύτταρα. (9) Η διαπίστωση αυτή οδήγησε στη διατύπωση ερωτημάτων όπως: από πού προέρχονται τα F κύτταρα, γιατί η αιμοσφαιρίνη F εμφανίζει κυτταρική απομόνωση. Πολλές ερευνητικές ομάδες μελέτησαν το φαινόμενο καθώς και τη σχέση του με τη μεταστροφή της αιμοσφαιρίνης. Διατυπώθηκε αρχικά η θεωρία ότι στον άνθρωπο η μεταστροφή της αιμοσφαιρίνης λαμβάνει χώρα προκειμένου δύο κυτταρικές σειρές αρχέγονων κυττάρων να πραγματοποιήσουν το διακριτό πρόγραμμα έκφρασης των σφαιρινικών γονιδίων. Πρόκειται για μία σειρά «εμβρυϊκών» αρχέγονων κυττάρων δεσμευμένων να παράγουν εμβρυϊκή σφαιρίνη, η οποία λίγο πριν τη γέννηση αντικαθίσταται από μία δεύτερη σειρά αρχέγονων κυττάρων «ενηλίκου» δεσμευμένων να παράγουν τη σφαιρίνη του ενήλικα. Σύμφωνα με αυτό το μοντέλο τα F κύτταρα που απαντώνται στους ενήλικες είναι τα λίγα εναπομείναντα στο μυελό των οστών από την εμβρυϊκή σειρά. Τη δεκαετία του 1970 με την εφαρμογή των καλλιεργειών ερυθροειδικών κλώνων και την ανάπτυξη απομονωμένων BFUe αποικιών, προερχόμενες από ένα κύτταρο, απορρίφθηκε η προηγούμενη υπόθεση. Στις αποικίες αυτές των BFUe κυττάρων, με τη χρήση αντι-γ και αντι-β αντισωμάτων ήταν δυνατή η αναγνώριση των παραγόμενων αιμοσφαιρινών. Βρέθηκε, επίσης, ότι η πλειονότητα των αποικιών αποτελούνταν από μικτό πληθυσμό F και Α κυττάρων (για παραγωγή HbF και HbA, αντίστοιχα), (11) γεγονός που αποτελεί απόδειξη ότι η εμβρυϊκή και η αιμοσφαιρίνη του ενήλικα παράγονται από κύτταρα προερχόμενα από την ίδια σειρά. Οπότε, σύμφωνα με αυτή την υπόθεση, η μεταστροφή της αιμοσφαιρίνης δεν αντιστοιχεί σε αλλαγή στον πληθυσμό των αρχέγονων κυττάρων, τα οποία διαθέτουν ένα αμετάβλητο πρόγραμμα έκφρασης των σφαιρινικών γονιδίων, αλλά πρόκειται για μία αλλαγή στο ρυθμό μεταγραφής των διαφορετικών γονιδίων σφαιρίνης, η οποία μπορεί να συμβεί σε καθένα κύτταρο προερχόμενο από την ίδια κυτταρική σειρά. (11) Η θεωρία αυτή επιβεβαιώθηκε σε μελέτες που ακολούθησαν, οι οποίες πραγματοποιήθηκαν σε καλλιέργειες κυττάρων ασθενών με αιματολογικά νοσήματα που χαρακτηρίζονται από κλωνικότητα, όπως πολυκυτταραιμία vera και χρόνια μυελογενή λευχαιμία. (21) Επίσης κατά τη δεκαετία του 1980, επιβεβαιώθηκε η προηγούμενη υπόθεση με 26
27 πειράματα σε σωματικά υβριδικά κύτταρα. (12) Άλλες προσπάθειες διατύπωσης θεωριών για την ερμηνεία της μεταστροφής της αιμοσφαιρίνης και του σχηματισμού των F κυττάρων, οδήγησαν στο συμπέρασμα ότι κύτταρα τα οποία εκφράζουν HbF επιλέγονται κατά τη διαφοροποίηση των BFUe κλώνων. Μελέτες που ακολούθησαν έδειξαν ότι η «απόφαση» για την παραγωγή F κυττάρων σχετίζεται με το βαθμό διαφοροποίησης των προγονικών κυττάρων από τα οποία ξεκινά η καλλιέργεια. (13,46) Τέτοιες παρατηρήσεις οδήγησαν στη διατύπωση μιας πιο μηχανιστικής σχέσης μεταξύ της έκφρασης της εμβρυϊκής αιμοσφαιρίνης και της διαδικασίας διαφοροποίησης κατά την ερυθροποίηση του ενήλικα. Η αλλαγή στο μεταγραφικό πρόγραμμα των σφαιρινικών γονιδίων μπορεί να θεωρηθεί ως μία πρόοδος κατά τη διαφοροποίηση, καθώς από ένα πρόγραμμα με κύρια εκφραζόμενο το γ γονίδιο οδηγούμαστε σε αυτό που υποστηρίζει μόνο την έκφραση του β γονιδίου. Στους φυσιολογικούς ενήλικες η πλειονότητα των ερυθροκυττάρων ωριμάζει φυσιολογικά και παράγονται ερυθροβλάστες, οι οποίοι συνθέτουν μόνο αιμοσφαιρίνη του ενήλικα. Μικρός όμως αριθμός προγονικών κυττάρων οδηγούνται πρώϊμα σε τελική ωρίμανση πριν λάβει χώρα η αλλαγή στο πρόγραμμα με αποτέλεσμα να παράγονται F κύτταρα (Εικ. 5α). Αυτή η υπόθεση συμφωνεί και ερμηνεύει πολλές in vivo παρατηρήσεις σε ανθρώπινα και ζωϊκά μοντέλα και ερμηνεύει την αύξηση της HbF κατά την ερυθροποίηση υπό stress (Εικ. 5β). (47,48) Αποτέλεσμα της βεβιασμένης ερυθροποίησης είναι η παραγωγή της HbF, καθώς επιταχύνεται η διαφοροποίηση και προάγεται η παραγωγή κυττάρων τελικού σταδίου ωρίμανσης, χωρίς να έχει ολοκληρωθεί ακόμη το πρόγραμμα παραγωγής αιμοσφαιρίνης. (48) Aυτό υποστηρίζεται από πειράματα σε μπαμπουίνους που χορηγείται ερυθροποιητίνη. (51) Επίσης, η αναστολή της παραγωγής κυττάρων μετά τη δράση των κυτταροτοξικών φαρμάκων ακολουθείται από ένα κύμα αναγέννησης των ερυθροκυττάρων, το οποίο εξαναγκάζει τα προγονικά κύτταρα σε γρήγορη ωρίμανση, με επακόλουθη την αύξηση της παραγωγής HbF (50) (Εικ. 5γ). 27
28 Εικόνα 5. Μοντέλο για τη ρύθμιση της παραγωγής HbF στον ενήλικα. Η τρίτη θεωρία, που προσπάθησε να ερμηνεύσει την προέλευση των F κυττάρων, συνδέει τον έλεγχο της έκφρασης των γονιδίων γ και β με την πρόοδο της ανάπτυξης και διαφοροποίησης του κυττάρου κατά τον κυτταρικό κύκλο. Η έκφραση του β γονιδίου καθορίζεται από τη συσσώρευση μεταγραφικών ενεργοποιητικών παραγόντων σε οριακά επίπεδα προς το τέλος της G1 φάσης. Τα ταχέως διαιρούμενα κύτταρα πιστεύεται ότι συσσωρεύουν ανεπαρκή για την έκφραση του β ποσά μεταγραφικών παραγόντων με αποτέλεσμα να υπερισχύει η σύνθεση γ αλυσίδων. Πιστεύεται ότι υπάρχει ένας ενεργοποιητικός παράγοντας, ο οποίος θα επιτρέψει την έκφραση του β γονιδίου εφόσον η συγκέντρωσή του υπερβεί συγκεκριμένη ποσότητα και δευτερογενώς θα κατασταλεί η έκφραση του γ γονιδίου. (49) 28
29 2. ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ 2.1. Γενικά Οι αιμοσφαιρινοπάθειες οφείλονται σε κληρονομικές διαταραχές που επηρεάζουν τη δομή ή/και το επίπεδο σύνθεσης των σφαιρινικών αλυσίδων. Οι αιμοσφαιρινοπάθειες μπορούν κατά βάση να χωρισθούν σε τέσσερις ομάδες. Η πρώτη αφορά αλλαγές στη δομή των σφαιρινικών αλυσίδων, η δεύτερη τα θαλασσαιμικά σύνδρομα, δηλαδή, την μείωση της σύνθεσης μιας ή περισσότερων αλυσίδων της σφαιρίνης, η τρίτη αλλαγές στην σύνθεση των σφαιρινικών αλυσίδων και τέλος η τέταρτη ομάδα αφορά την αυξημένη σύνθεση της εμβρυϊκής αιμοσφαιρίνης στην ενήλικο ζωή. Οι περισσότερες αλλαγές της δομής των αιμοσφαιρινών είναι σπάνιες και χωρίς κλινική σημασία. Ωστόσο μερικές από αυτές καταλήγουν σε μη φυσιολογική λειτουργία ή αστάθεια των πρωτεϊνικών μορίων, που έχει σαν αποτέλεσμα την μειωμένη μεταφορά οξυγόνου ή αιμολυτική αναιμία. Τέτοιες αλλαγές δημιουργούν τις αιμοσφαιρίνες HbS, HbC, HbE και είναι η αιτία των αιμοσφαιρινοπαθειών της πρώτης ομάδας, που περιγράφονται περαιτέρω. Η δεύτερη ομάδα αφορά τα θαλασσαιμικά σύνδρομα, που χαρακτηρίζονται από μη ισόρροπη σύνθεση των αλυσίδων της σφαιρίνης α και β του ανθρώπου, λόγω μερικής ή πλήρους αναστολής της σύνθεσης της κάθε μίας ή και των δύο εξ αυτών. Μετά από ανάλυση γενεαλογικών δένδρων αποδείχθηκε, ότι οι θαλασσαιμίες κληρονομούνται με αυτοσωμικά υπολειπόμενα γονίδια. Τα θαλασσαιμικά σύνδρομα διακρίνονται σε α- και β-θαλασσαιμίες, στις οποίες υπάρχει μείωση της σύνθεσης των α ή β-αλυσίδων, αντίστοιχα. Οι θαλασσαιμίες εμφανίζουν μεγάλη φαινοτυπική ετερογένεια που μπορεί να είναι αποτέλεσμα του ότι ο φαινότυπος καθορίζεται από ένα πλήθος παραγόντων, την υποκείμενη μετάλλαξη, τη συνύπαρξη ή μη άλλων αιμοσφαιρινοπαθειών και την επίδραση άλλων γενετικών και περιβαλλοντικών παραγόντων. Η δεύτερη και τρίτη ομάδα αιμοσφαιρινοπαθειών περιλαμβάνουν διαταραχές με κλινική εικόνα θαλασσαιμίας. Οι αιμοσφαιρινοπάθειες αυτές προέρχονται από σημειακές μεταλλάξεις στο τρίτο εξόνιο του β- γονιδίου. Ορισμένες από αυτές τις μεταλλάξεις δημιουργούν μεταλλάξεις χωρίς νόημα. Συνέπεια των μεταλλάξεων αυτών είναι η δημιουργία αλυσίδων β- σφαιρίνης με μέγεθος διαφορετικό του φυσιολογικού. Οι αλυσίδας αυτές είναι εξαιρετικά ασταθείς, με αποτέλεσμα ο χρόνος 29
30 ζωής να είναι μικρότερο αυτού που χρειάζεται για τη δημιουργία του τετραμερούς της αιμοσφαιρίνης. Η τέταρτη ομάδα αιμοσφαιρινοπαθειών περιλαμβάνει σύνδρομα, τα οποία οφείλονται στο ότι δεν έγινε η μεταστροφή της εμβρυϊκής αιμοσφαιρίνης σε αυτή των ενηλίκων. Τα σύνδρομα αυτά χαρακτηρίζονται ως «κληρονομική παραμονή της εμβρυϊκής αιμοσφαιρίνης» (HPFH). Άτομα που φέρουν συνδυασμό HPFH συνδρόμου και θαλασσαιμίας εμφανίζουν γονοτυπική αλλά και φαινοτυπική ετερογένεια. Θεωρείται ότι η υψηλή συχνότητα των θαλασσαιμικών και άλλων αιμοσφαιρινοπαθειών οφείλεται στη φυσική επιλογή μέσω του παρασίτου Plasmodium falciparum της ελονοσίας. Την υπόθεση αυτή διατύπωσε πρώτος ο Haldane το 1949 και προκειμένου να επιβεβαιωθεί πραγματοποιήθηκαν πολλές μελέτες. Έτσι μελετήθηκε η κατανομή των θαλασσαιμιών σε περιοχές που υπήρχε ή υπάρχει ελονοσία. Στις περιοχές αυτές βρέθηκε, ότι οι ετεροζυγώτες έχουν επιλεκτικό πλεονέκτημα ως προς τους ομοζυγώτες φυσιολογικούς ή πάσχοντες, έναντι της ελονοσίας. Το επιλεκτικό πλεονέκτημα των ετεροζυγωτών οφείλεται στην καλύτερη προσαρμοστικότητα τους σε περιοχές που υπάρχει ελονοσία. Δηλαδή, η μόλυνση των ετεροζυγωτών από το παράσιτο Plasmodium falciparum σε σχέση με τους φυσιολογικούς ομοζυγώτες εκδηλώνεται ηπιότερα με αποτέλεσμα να πεθαίνει μικρότερος αριθμός ετεροζυγωτών και οι ετερόζυγες μέλλουσες μητέρες να εμφανίζουν μικρότερο ποσοστό αποβολών. Συνέπεια αυτού του πλεονεκτήματος είναι να συντηρούνται μέσω των ετεροζυγωτών και τα δύο αλληλόμορφα (παθολογικό και φυσιολογικό) σε υψηλές συχνότητες στο πληθυσμό αν και οι πάσχοντες πεθαίνουν πρόωρα και δεν αναπαράγονται. Υπάρχει, δηλαδή, στη δεδομένη περίπτωση ισόρροπος πολυμορφισμός. Σε in vitro κυτταροκαλλιέργειες μελετήθηκε η αλληλεπίδραση του παρασίτου με τα θαλασσαιμικά ερυθροκύτταρα, ο μηχανισμός που αυξάνει την ανθεκτικότητά τους στη μόλυνση από το παράσιτο, οι συνέπειες της μόλυνσης στα όργανα του ξενιστή, τα διάφορα στάδια του κύκλου ζωής του παρασίτου, διαφορετικές τροφικές συνήθειες κ.α. Τα αποτελέσματα των μελετών έδειξαν ότι μολυσμένα ερυθρά αιμοσφαίρια έχουν περισσότερες πιθανότητες να υποστούν φαγοκυττάρωση, ενώ η παρουσία HbF και HbC ή μειωμένη παραγωγή σφαιρίνης καθυστερεί την ανάπτυξη του παρασίτου. 30
31 2.2. Μη φυσιολογικές αιμοσφαιρίνες Από το 1949 οπότε ο Pauling και οι συνεργάτες του ανακάλυψαν την HbS, έχουν ανακαλυφθεί πολλές διαφορετικές αιμοσφαιρίνες. Η πλειονότητα αυτών των διαφορετικών αιμοσφαιρινών προέρχεται από αντικατάσταση ενός αμινοξέος, λόγω αντικατάστασης μιας βάσης στην αλληλουχία του DNA τους. Μερικές όμως από αυτές τις αιμοσφαιρίνες προκύπτουν από ελλείψεις τμημάτων DNA, προσθήκες νουκλεοτιδίων ή ανακατατάξεις στο DNA. Η περισσότερο γνωστή μη φυσιολογική αιμοσφαιρίνη είναι η HbS που διαφέρει της HbA σε ένα αμινοξύ, δηλαδή στη θέση 6 μία βαλίνη αντικαθιστά ένα γλουταμινικό οξύ. Ο πολυμερισμός των μορίων της αιμοσφαιρίνης S, που συμβαίνει σε χαμηλές πιέσεις οξυγόνου στα τριχοειδή, δημιουργεί επιμήκεις ίνες, στις οποίες οφείλεται το τυπικό δρεπανοειδές σχήμα των ερυθροκυττάρων. Τα ερυθρά αιμοσφαίρια που έχουν αποκτήσει δρεπανοειδές σχήμα είναι άκαμπτα και η μεταφορά τους δυσχεραίνεται διά μέσω των τριχοειδών, δημιουργώντας συσσωματώματα στην μικροκυκλοφορία και αγγειακές αποφράξεις. Η αυξημένη τους μηχανική ευθραυστότητα οδηγεί στην πρώιμη καταστροφή τους, η οποία καταλήγει σε χρόνια αιμόλυση. Ο ετεροζυγώτης σπάνια εμφανίζει κλινικά συμπτώματα, ενώ ο ομοζυγώτης έχει αιμολυτική αναιμία και άλλα κλινικά συμπτώματα. Η αιμοσφαιρίνη C προέρχεται από την αντικατάσταση του γλουταμινικού οξέος στη θέση 6 από μία λυσίνη. Η μειωμένη διαλυτότης της HbC σε σχέση με αυτή της HbA, είναι η αιτία του σχηματισμού ενδοκυτταρικών ψευδοκρυστάλλων και της απώλειας της πλαστικότητας των ερυθρών αιμοσφαιρίων. Αυτή είναι και η κύρια αιτία που οι ομοζυγώτες για τη HbC πάσχουν από αιμολυτική αναιμία. Η αιμοσφαιρίνη Ε συναντάται κυρίως στους πληθυσμούς της Ν.Α. Ασίας και προέρχεται από την αντικατάσταση του γλουταμινικού οξέος από τη λυσίνη στο κωδικόνιο 26. Η μετάλλαξη που είναι υπεύθυνη για την HbE δεν επηρεάζει μόνο τη δομή αλλά και το ποσοστό σύνθεσης των βε αλυσίδων και για αυτό εμφανίζει φαινότυπο σαν αυτό της ήπιας β θαλασσαιμίας. Αυτό συμβαίνει γιατί η αντικατάσταση ενός νουκλεοτιδίου είναι υπεύθυνη αφενός για την αλλαγή ενός αμινοξέος στην πρωτεΐνη, αφετέρου για την ενεργοποίηση μιας κρυφής θέσης δότη για μάτισμα. Αυτή η νέα θέση ματίσματος επιδρά στον μηχανισμό του ματίσματος με αποτέλεσμα την παραγωγή ενός μη φυσιολογικού RNA μορίου, το οποίο δεν μπορεί να μεταφραστεί σε φυσιολογική σφαιρίνη β. Οι ομοζυγώτες για την HbE παρουσιάζουν ήπια αναιμία. 31
32 2.3. α- Θαλασσαιμία Η α-θαλασσαιμία είναι κληρονομική διαταραχή της σύνθεσης των α-αλυσίδων σφαιρίνης, με αποτέλεσμα την μειωμένη παραγωγή τους στα έμβρυα και στους ενήλικες. Τα φυσιολογικά άτομα φέρουν δύο α- γονίδια στο χρωμόσωμα 16. Πάνω από το 95% των γνωστών α-θαλασσαιμιών οφείλονται σε ελλείψεις του ενός ή και των δύο α- γονιδίων. Οι ελλείψεις της οικογένειας των α γονιδίων, οι οποίες προκαλούν φαινότυπο α-μεσογειακής αναιμίας οφείλονται στην: Έλλειψη ενός α γονιδίου, μερικώς ή πλήρως, (-α, α+-μεσογειακή αναιμία). Οι ελλείψεις αυτές οφείλονται, είτε σε ενδοχρωμοσωμικό ανασυνδυασμό, είτε σε άνισο αμοιβαίο ανασυνδυασμό μεταξύ των διπλασιασμένων α γονιδίων, γεγονός που επιβεβαιώνεται με την ύπαρξη χρωμοσωμάτων με τριπλασιασμό των α γονιδίων. (52) Έλλειψη των δύο α γονιδίων (-/-, α 0 -Μεσογειακή αναιμία), με αποτέλεσμα την αδυναμία παραγωγής α αλυσίδων. Οι ελλείψεις που περιλαμβάνουν και τα δύο α-γονίδια κυμαίνονται σε μέγεθος από 5.2 kb έως και περισσότερο από 30 kb και προκύπτουν από ανασυνδυασμό στην περιοχή που περιλαμβάνει την οικογένεια των α-γονιδίων. (53,54) Επίσης ένα πολύ μικρό ποσοστό α-θαλασσαιμιών, δεν οφείλονται σε ελλείψεις ενός ή περισσότερων γονιδίων α και χαρακτηρίζονται ως «μη ελλειμματικές» α- θαλασσαιμίες. Η πιο συχνή, από αυτές τις α-θαλασσαιμίες, είναι μία μικρή έλλειψη πέντε μόνο νουκλεοτιδίων στο 5 άκρο της IVSI του γονιδίου της σφαιρίνης α2, με αποτέλεσμα την απώλεια της σταθερότητας του συγκεκριμένου RNA. (55,56) 2.4. β- Θαλασσαιμία Γενικά Οι β-θαλασσαιμίες είναι μία ομάδα αιμοσφαιρινοπαθειών, οι οποίες οφείλονται στην πλήρη (β ο ) ή μειωμένη (β + ) σύνθεση β αλυσίδων. Το 1925 οι Cooley και Lee περιέγραψαν τη β-θαλασσαιμία βάσει της κλινικής εικόνας που παρουσίαζαν πέντε παιδιά που έπασχαν από βαριά αναιμία. Τα παιδιά αυτά παρουσίαζαν εκτός από βαριά αναιμία, ωχρότητα, σπληνομεγαλία, ηπατομεγαλία, σκελετικές αλλοιώσεις, καθώς επίσης και διεύρυνση των οστών του 32
33 κρανίου και του προσώπου. Τα ερυθρά τους αιμοσφαίρια παρουσίαζαν αυξημένη ωσμωτική αντίσταση και μία μέτριου μεγέθους λευκοκυττάρωση, ενώ εμφανίζονταν εμπύρηνα ερυθρά στο περιφερικό αίμα. Η βαριά αυτή αναιμία έγινε γνωστή ως αναιμία του Cooley και συμπίπτει απόλυτα με την κλινική εικόνα της ομόζυγης β- θαλασσαιμίας ή β-μεσογειακής αναιμίας (57). Η β-θαλασσαιμία εμφανίζει μεγάλη φαινοτυπική ετερογένεια ωστόσο ιστορικά διακρίνεται στη μείζονα και την ενδιάμεση β-θαλασσαιμία, ανάλογα με την κλινική εικόνα που εμφανίζουν οι ασθενείς Κλινική εικόνα των πασχόντων από ομόζυγη β-θαλασσαιμία Άτομα με ομόζυγη β-θαλασσαιμία δίνουν μία τυπική εικόνα της αναιμίας Cooley. Οι ασθενείς εμφανίζουν εκτός από αναιμία, μη φυσιολογική ερυθροκυτταρική μορφολογία (υποχρωμία, ανισοκυττάρωση, ποικιλοκυττάρωση, στοχοκυττάρωση, πολυχρωματοφιλία και βασεόφιλη στίξη), καθώς και χαμηλότερους σε σχέση με τα φυσιολογικά επίπεδα αιματολογικούς δείκτες (μέσος όγκος ερυθρών MCV, μέσος όρος αιμοσφαιρίνης MCH). Τα ερυθρά τους αιμοσφαίρια περιέχουν έγκλειστα, που οφείλονται στην κατακρήμνιση της περίσσειας αλυσίδων σφαιρίνης α και παρουσιάζουν αυξημένη ωσμωτική αντίσταση. Εξ αιτίας της ατελούς ερυθροποίησης εμφανίζονται εμπύρηνα ερυθρά στο περιφερικό αίμα. Τα επίπεδα των αιμοσφαιρινών Α 2 και F είναι αυξημένα ενώ το επίπεδο της αιμοσφαιρίνης Α είναι ελάχιστο ή μηδενικό. Η ομόζυγη β-θαλασσαιμία προέρχεται είτε από β + ή β ο μεταλλαγές είτε από συνύπαρξη β + και β ο μεταλλαγών. Η ασθένεια εμφανίζεται μετά τους πρώτους μήνες της ζωής των νεογνών (3-24 μήνες), επειδή κατά το διάστημα αυτό οι γ αλυσίδες ελαττώνονται και δεν αντικαθίστανται πλήρως από τις β-αλυσίδες. Τα παιδιά αυτά για να επιβιώσουν έχουν ανάγκη μεταγγίσεων αίματος. Ανάλογα με τα επίπεδα της αιμοσφαιρίνης των ασθενών, οι μεταγγίσεις αρχίζουν στην ηλικία των 3 μηνών ή και αργότερα στην ηλικία 3 έως 5 το πολύ ετών και συνεχίζονται σε τακτά χρονικά διαστήματα ανάλογα με τις ανάγκες τους Κλινική εικόνα των πασχόντων από ενδιάμεση β-θαλασσαιμία Ορισμένοι πάσχοντες από β-θαλασσαιμία εμφανίζουν κλινικά και αιματολογικά ευρήματα που δεν είναι συμβατά με τον φαινότυπο της ομόζυγης β- θαλασσαιμίας. Τα άτομα αυτά χαρακτηρίζονται ως πάσχοντες από ενδιάμεση β- θαλασσαιμία και παρουσιάζουν βαρύτερο φαινότυπο από εκείνο των ετεροζυγωτών της β-θαλασσαιμίας και εμφανίζουν ήπια αναιμία και σπανίως σπληνομεγαλία. Άτομα που πάσχουν από ενδιάμεση β-θαλασσαιμία φέρουν και στα δύο τους αλληλόμορφα 33
34 μεταλλάξεις β-θαλασσαιμίας. Τα άτομα αυτά δίνουν με βάση την κλινική εικόνα τους: Άτομα που εμφανίζουν μέτρια αναιμία και μη ομαλή ερυθροκυτταρική μορφολογία. Το επίπεδο της αιμοσφαιρίνης τους διατηρείται σταθερό περί τα 8 g/dl. Τα άτομα αυτά εμφανίζουν υπερσπληνισμό, όχι καλή ανάπτυξη και σκελετικές αλλοιώσεις. Η ανάγκη για μεταγγίσεις αίματος παρουσιάζεται από ηλικία 6 έως 12 χρόνων. Άτομα που εμφανίζουν πιο ήπια αναιμία και ομαλότερους ερυθροκυτταρικούς δείκτες. Το επίπεδο της αιμοσφαιρίνης τους διατηρείται σταθερό μεταξύ των τιμών από 8-10 g/dl. Τα άτομα αυτά αναπτύσσονται καλά μέχρι την ενηλικίωσή τους και δεν εμφανίζουν έντονες σκελετικές αλλοιώσεις. Συνήθως έχουν ανάγκη μεταγγίσεων αίματος μόνο μετά από κάποια λοίμωξη ή όταν παρουσιάζουν υπερσπληνισμό Στοιχεία της παθοφυσιολογίας της ομόζυγης β-θαλασσαιμίας Η μερική ή ολική μείωση της παραγωγής β αλυσίδων σφαιρίνης έχει ως αποτέλεσμα την ύπαρξη περίσσειας α αλυσίδων και συνεπώς την διαταραχή της αναλογίας α και β αλυσίδων. Εξ άλλου παρατηρείται αύξηση της παραγωγής αλυσίδων γ και κατ επέκταση αύξηση της εμβρυϊκής αιμοσφαιρίνης στα πρόδρομα κύτταρα της ερυθράς σειράς. Η αύξηση αυτή όμως, δεν επαρκεί για να καλύψει όλη την έλλειψη των αλυσίδων β, με αποτέλεσμα η περίσσεια των αλυσίδων α να καθιζάνει και να εμφανίζονται τα έγκλειστα στα πρόδρομα κύτταρα της ερυθράς σειράς. Η ύπαρξη εγκλείστων στους πρώιμους ερυθροβλάστες των πασχόντων από βαριά β-θαλασσαιμία προκαλεί κυτταρική βλάβη, η οποία εκδηλώνεται είτε με την επιμήκυνση της G1 φάσης του κυτταρικού κύκλου, είτε με την πλήρη αδυναμία ολοκλήρωσης του κυτταρικού τους κύκλου, με αποτέλεσμα τον θάνατό τους. Συνέπεια του πρόωρου θανάτου των ερυθροβλαστών εμφανίζεται η ατελής ερυθροποίηση. Ο μικρός χρόνος ζωής των θαλασσαιμικών ερυθρών αιμοσφαιρίων οφείλεται στην παγίδευσή τους στον σπλήνα λόγω των εγλείστων τους. Η β-θαλασσαιμία είναι πρωτίστως δυσερυθροποιητική αναιμία αλλά και συγχρόνως αιμολυτική. Η βαριά αναιμία που προκαλείται από τους παραπάνω μηχανισμούς δημιουργεί υπερπλασία του μυελού των οστών, με αποτέλεσμα την εμφάνιση σκελετικών αλλοιώσεων, που χαρακτηρίζουν τα ομόζυγα άτομα. Τα άτομα αυτά εμφανίζουν επίσης σπληνομεγαλία, ηπατομεγαλία και διαταραχές κατά την ανάπτυξη. 34
35 Στοιχεία της παθοφυσιολογίας της ενδιάμεσης β-θαλασσαιμίας Η παθοφυσιολογία της ενδιάμεσης β-θαλασσαιμίας προκαλείται από τους ίδιους μηχανισμούς με αυτούς της ομόζυγης β-θαλασσαιμίας. Τα φαινόμενα είναι πιο ήπια στην ενδιάμεση β-θαλασσαιμία, επειδή παράγονται διάφορα, κατά περίπτωση, ποσά αλυσίδων β, με αποτέλεσμα την αύξηση της σύνθεσης της αιμοσφαιρίνης Α και την μείωση της περίσσειας των αλυσίδων α. Σε μερικές περιπτώσεις παρατηρείται επαρκής παραγωγή των αλυσίδων γ, με αποτέλεσμα την απάλειψη των εγκλείστων στα πρόδρομα κύτταρα των ερυθρών και στα ερυθρά αιμοσφαίρια. Επί πλέον η αυξημένη παραγωγή των αλυσίδων γ, προκαλεί αύξηση της αιμοσφαιρίνης F. Η HbF έχει μεγαλύτερη ικανότητα δέσμευσης του οξυγόνου, με αποτέλεσμα να δημιουργείται υποξία που προκαλεί αύξηση της ερυθροποιητίνης, η οποία με την σειρά της προκαλεί υπερπλασία του μυελού των οστών. Τα προβλήματα στα άτομα με ενδιάμεση β-θαλασσαιμία εμφανίζονται συνήθως μεταξύ της 3 ης και 5 ης δεκαετίας της ζωής τους. Οι ασθενείς αυτοί φαίνεται ότι επιβιώνουν έχοντας χαμηλό επίπεδο αιμοσφαιρίνης. Όμως, λοιμώξεις ή υπερσπληνισμός είναι δυνατόν να προκαλέσουν απορρύθμιση με αποτέλεσμα την απότομη πτώση σε ακόμα πιο χαμηλά επίπεδα της αιμοσφαιρίνης έτσι ώστε να χρειάζονται μεταγγίσεις αίματος Η ύπαρξη εγκλείστων στα ερυθρά αιμοσφαίρια Τα έγκλειστα είναι χαρακτηριστικό της β-θαλασσαιμίας και η σύστασή τους προσδιορίστηκε αρχικά από τον Φ. Φέσσα (1963) και αργότερα από τον Weatherall D.J. (1973) είναι κυρίως αποτέλεσμα της περίσσειας αλυσίδων σφαιρίνης α, που καθιζάνουν στη μεμβράνη των πρόδρομων κυττάρων της ερυθράς σειράς, προκαλώντας την πρώιμη καταστροφή τους στον μυελό των οστών. Τα έγκλειστα βρίσκονται μέσα στα ερυθρά αιμοσφαίρια των ασθενών που πάσχουν από β- θαλασσαιμία. Διαπιστώθηκε επίσης η ύπαρξη εγκλείστων, που προέρχονται από καθίζηση αλυσίδων β, σε ετεροζυγώτες για Hb Geneva, των οποίων ο λόγος σύνθεσης α/β αλυσίδων ήταν ελάχιστα αυξημένος. Η ανάλυση του β- γονιδίου αυτών των ασθενών έδειξε, ότι ο φαινότυπος αυτός προέρχεται από μεταλλάξεις στο τρίτο εξόνιο του β- γονιδίου. Αποτέλεσμα αυτού είναι η δημιουργία ασταθών β- αλυσίδων σφαιρίνης, οι οποίες καθιζάνουν στα πρόδρομα κύτταρα των ερυθρών και δημιουργούν δυσερυθροποίηση και βαριά αναιμία. 35
36 2.5. Η Μοριακή βάση της β-θαλασσαιμίας Γενικά Στο σύμπλεγμα των γονιδίων β- τύπου, μήκους μεγαλύτερου από 60 kb, έχει κλωνοποιηθεί και έχει προσδιορισθεί μεγάλος αριθμός μεταλλάξεων, που οδηγούν σε δυσλειτουργία του γονιδίου. Η β-θαλασσαιμία προκαλείται κυρίως από σημειακές μεταλλάξεις. Οι μεταλλάξεις αυτές μελετήθηκαν από το 1980 έως το 1987 με ανάλυση των απλοτύπων του β- γονιδίου. Μετά την κλωνοποίηση και τον προσδιορισμό των αλληλουχιών του μεταλλαγμένου β- γονιδίου, προσδιορίσθηκαν διεθνώς περίπου 40 σημειακές μεταλλάξεις. Το 1987 έγινε δυνατή η εκλεκτική ενίσχυση της περιοχής του β- γονιδίου της σφαιρίνης β και ο προσδιορισμός της πρωτοταγούς δομής χρησιμοποιώντας DNA γονιδιώματος από λευκά αιμοσφαίρια. Ο συνολικός αριθμός των σημειακών μεταλλάξεων που βρέθηκε να προκαλούν β-θαλασσαιμία είναι περίπου 120. Η μελέτη του συμπλέγματος των β- τύπου γονιδίων σε β-θαλασσαιμικά άτομα έδωσε πολλές πληροφορίες για τις αλληλουχίες των νουκλεοτιδίων που είναι σημαντικές για την έκφραση των γονιδίων αυτών. Ο μεταλλάξεις που ανιχνεύθηκαν μέχρι σήμερα, ομαδοποιήθηκαν με βάση τη λειτουργία την οποία επηρεάζουν Μεταλλάξεις που επηρεάζουν την μεταγραφή του β- γονιδίου Μεταλλάξεις στην περιοχή του υποκινητή του γονιδίου β Στην περιοχή του υποκινητή του β- γονιδίου ανιχνεύθηκε ένας μεγάλος αριθμός σημειακών μεταλλάξεων σε αλληλουχίες που εδράζονται κατά μήκος της περιοχής του υποκινητή και παίζουν σημαντικό ρόλο στην έκφραση του β-γονιδίου. Πάσχοντες που φέρουν τέτοιες μεταλλάξεις εμφανίζουν ήπιο φαινότυπο β+ θαλασσαιμίας, δεδομένου οτι η έκφραση του β- γονιδίου μειώνεται μόνο κατά 20-30% σε σχέση με την έκφραση του φυσιολογικού γονιδίου. Οι μεταλλάξεις αυτές εμφανίζονται κοντά στο CACCC και στο TATA box, που εκτείνονται από την -93 έως την -85 θέση και από την -31 έως την -25 θέση ως προς τη θέση cap, αντίστοιχα. Ενδεικτικά μερικές από αυτές τις μεταλλάξεις βρίσκονται στις θέσεις -87 (C T), -87 (C G), -90 (C T), -29 (A G) κλπ. Οι μεταλλάξεις αυτές σε ομοζυγωτία δίνουν έναν ήπιο φαινότυπο ενδιάμεσης β-θαλασσαιμίας, ενώ όταν συνυπάρχουν με κάποια μετάλλαξη που συνδέεται με ομόζυγη β-θαλασσαιμία δίνουν επίσης μέτριο έως ήπιο 36
37 φαινότυπο β-θαλασσαιμίας. Μεταλλάξεις από την -108 έως την -101 θέση ως προς τη θέση cap, όπου εδράζεται και το δεύτερο CACC box του β- γονιδίου χαρακτηρίζονται ως «σιωπηλές», γιατί δίνουν πολύ ήπιο φαινότυπο. Το γεγονός αυτό υποδηλώνει ότι η συγκεκριμένη αλληλουχία δεν είναι τόσο σημαντική για την έκφραση του γονιδίου όσο η ίδια μικρή αλληλουχία που βρίσκεται πιο κοντά (-93 έως -85). Η πιο συχνή μετάλλαξη της περιοχής αυτής είναι στη θέση -101 ως προς τη θέση cap. Οι ετεροζυγώτες γι αυτή τη μετάλλαξη εμφανίζουν φυσιολογικούς αιματολογικούς δείκτες, ενώ διπλοί ετεροζυγώτες για τη μετάλλαξη αυτή και για άλλη που συνδέεται με ομόζυγη β- θαλασσαιμία εμφανίζουν φαινότυπο ενδιάμεσης β-θαλασσαιμίας Μεταλλάξεις στην 5 αμετάφραστη περιοχή (5 UTR) του β- γονιδίου Στη 5 αμετάφραστη περιοχή, η οποία εκτείνεται από τη θέση cap έως το κωδικόνιο της έναρξης της μετάφρασης (ATG), υπάρχουν δύο μικρές συντηρημένες αλληλουχίες, από τη +6 θέση έως την +13 και από την +47 θέση έως την +53 ως προς τη θέση cap. Οι μεταλλάξεις που βρίσκονται στην 5 αμετάφραστη περιοχή του γονιδίου πιθανόν μειώνουν τη μεταγραφή ή επιβραδύνουν τη διαδικασία κάλυψης, μειώνοντας τη σταθερότητα του β- mrna. Η μετάλλαξη στη θέση +1 ως προς τη θέση cap σε ομοζυγωτία δίνει ήπιο φαινότυπο β-θαλασσαιμίας, ενώ σε συνύπαρξη με άλλη μετάλλαξη που συνδέεται με ομόζυγη β-θαλασσαιμία δίνει φαινότυπο ομόζυγης β- θαλασσαιμίας. Αντιθέτως, μία μετάλλαξη, έλλειψη θυμίνης στην +10 θέση ως προς τη θέση cap, που ανιχνεύτηκε πρόσφατα, δίνει σε αντίστοιχη διπλή ετεροζυγωτία φαινότυπο ενδιάμεσης β-θαλασσαιμίας, ενώ απλοί ετεροζυγώτες εμφανίζουν φυσιολογικούς αιματολογικούς δείκτες. Άλλες μεταλλάξεις που ανιχνεύτηκαν στην 5 αμετάφραστη περιοχή του γονιδίου β και συνδέονται με ήπια β-θαλασσαιμία αφορούν σημειακές μεταλλάξεις στις θέσεις +20 (C G), +22 (G A) και μία έλλειψη από τη θέση +40 έως την +43 (-AAAC) Μεταλλάξεις που επηρεάζουν τη διαδικασία ωρίμανσης του RNA Κατά την διαδικασία ωρίμανσης του πρόδρομου RNA, απομακρύνονται παρεμβαλόμενες αλληλουχίες (splicing) προκειμένου να δημιουργηθεί το ώριμο β- mrna, το οποίο θα μεταφρασθεί στο κυτταρόπλασμα. Η διαδικασία της σωστής ωρίμανσης του πρόδρομου RNA διαταράσσεται είτε από μεταλλάξεις, κυρίως 37
38 σημειακές σε διατηρημένες κατά την εξέλιξη μικρές αλληλουχίες που εκτείνονται μεταξύ εξονίων και ιντρονίων είτε από μεταλλάξεις μέσα στα εξόνια ή στα ιντρόνια, οι οποίες δημιουργούν νέες θέσεις ματίσματος. Οι μεταλλάξεις αυτές, ανάλογα με τη θέση τους στις συγκεκριμένες περιοχές, συνδέονται με φαινότυπο β ο ή β + θαλασσαιμίας Μεταλλάξεις σε υπάρχουσες θέσεις ματίσματος Όπως σε όλα τα ευκαρυωτικά γονίδια, έτσι και στο β- γονίδιο η διατηρημένη αλληλουχία περιλαμβάνει τα τρία τελευταία νουκλεοτίδια του εξονίου και τα πρώτα έξι νουκλεοτίδια του ιντρονίου, καθώς επίσης και το δινουκλεοτίδιο GT στο 5 άκρο του ιντρονίου και το δινουκλεοτίδιο AG στο 3 άκρο του ιντρονίου. Σημειακές μεταλλάξεις σε αυτά τα δύο δινουκλεοτίδια στα ιντρόνια Ι και ΙΙ του β- γονιδίου συνδέονται με φαινότυπο β ο θαλασσαιμίας. Μετάλλαξη τέτοιου είδους είναι η IVSI-1. H IVSI-1 είναι μια αντικατάσταση βάσης (G A) στο πρώτο νουκλεοτίδιο του ιντρονίου Ι του γονιδίου της σφαιρίνης β που εμποδίζει το μάτισμα του β- RNA, με αποτέλεσμα να μην παράγονται καθόλου β- αλυσίδες. Η μετάλλαξη αυτή, που προκαλεί β ο θαλασσαιμία, απαντάται στην Ελλάδα σε συχνότητα 16,1% και λειτουργεί σε χρωμοσωμικό υπόστρωμα που ανήκει στον απλότυπο V με τον οποίο είναι γενετικά συνδεδεμένη. Η μετάλλαξη IVSII-1 με αντικατάσταση βάσης στο πρώτο νουκλεοτίδιο του ιντρονίου ΙΙ (G A) έχει ως αποτέλεσμα την μη σωστή επεξεργασία του mrna. Η αντικατάσταση αυτή καταστρέφει το GT δινουκλεοτίδιο, που βρίσκεται στο 5 άκρο της δεύτερης παρεμβαλόμενης αλληλουχίας. Η θέση αυτή είναι η θέση ωρίμανσης του β- RNA με αποτέλεσμα να μην παράγονται καθόλου αλυσίδες σφαιρίνης β. Προκαλεί β ο θαλασσαιμία, απαντάται στον ελληνικό πληθυσμό σε συχνότητα 2,3% όπως επίσης και σε άλλους πληθυσμούς της Μεσογείου και συνδέεται με τον απλότυπο ΙΙΙ. Οι πάσχοντες που φέρουν την συγκεκριμένη μετάλλαξη στο ένα αλληλόμορφό τους εμφανίζουν αυξημένα επίπεδα HbF, με αποτέλεσμα την εμφάνιση ενός ήπιου φαινοτύπου ανεξαρτήτως εάν στο άλλο αλληλόμορφο συνυπάρχει μια μετάλλαξη που συνδέεται με ομόζυγη β-θαλασσαιμία. Τέλος, σημειακές μεταλλάξεις μέσα στις μικρές διατηρημένες εξελικτικά αλληλουχίες που αφορούν το μάτισμα έχουν ως αποτέλεσμα το επίπεδο του β- mrna να μειώνεται 25-50% σε σχέση με αυτό των φυσιολογικών β- mrna. Οι μεταλλάξεις προκαλούν β + θαλασσαιμία. 38
39 Μεταλλάξεις που δημιουργούν ή ενεργοποιούν θέσεις ματίσματος Αντικαταστάσεις νουκλεοτιδίου μέσα στα ιντρόνια μπορούν να δημιουργήσουν νέες θέσεις δότη ή δέκτη ματίσματος οι οποίες ανταγωνίζονται ή καθυστερούν την ωρίμανση RNA. Για παράδειγμα, η IVSI-110 μετάλλαξη αφορά την αντικατάσταση μιας βάσης (G A) και έχει ως αποτέλεσμα τη μη σωστή ωρίμανση του RNA. Η μετάλλαξη αυτή είναι συνδεδεμένη κυρίως με τον απλότυπο Ι και είναι η πιο συχνή στην Ελλάδα (41,94) και τις άλλες μεσογειακές χώρες. Είναι μια β + μετάλλαξη, η οποία επηρεάζει την σωστή ωρίμανση του β- RNA κατά 90%, με αποτέλεσμα την εμφάνιση φαινοτύπου ομόζυγης θαλασσαιμίας (58). Στις περισσότερες περιπτώσεις, όταν δε συμβαίνει φυσιολογικό μάτισμα ανιχνεύονται πολύ χαμηλά επίπεδα β- mrna, με αποτέλεσμα να εμφανίζεται ένας βαρύς β + θαλασσαιμικός φαινότυπος. Η αντικατάσταση νουκλεοτιδίου σε ένα από τα εξόνια μπορεί να αλλάξει την αλληλουχία με αποτέλεσμα να εμφανίζεται μια νέα ίδια θέση δότη κατά τη διάρκεια του ματίσματος. Η χρήση αυτής της κρυφής θέσης ως θέσης δότη για το μάτισμα δίνει προϊόντα μη φυσιολογικού ματίσματος του mrna. Στην περίπτωση αυτή το επίπεδο του mrna είναι χαμηλότερο του φυσιολογικού. Τέτοιες μεταλλάξεις προκαλούν αντικατάσταση ενός αμινοξέος όπως στις HbE, Hb Κνωσός, Hb Malay και μας δίνουν έναν ήπιο φαινότυπο β-θαλασσαιμίας. Η IVSI-6 είναι σημειακή μετάλλαξη (Τ C) στο νουκλεοτίδιο 6 της πρώτης παρεμβαλλόμενης αλληλουχίας του β- γονιδίου και ενεργοποιεί μία κρυφή θέση ματίσματος. Η θέση αυτή δεν επηρεάζει σημαντικά την σωστή ωρίμανση του RNA επιτρέποντας έτσι ικανή παραγωγή β- αλυσίδων και κατ επέκταση ικανοποιητική παραγωγή HbA, με αποτέλεσμα ομοζυγώτες για την συγκεκριμένη μετάλλαξη να εμφανίζουν ήπια κλινική εικόνα. Η IVSI-6 μετάλλαξη προσδιορίστηκε αρχικά σε πάσχοντες στη νότια Πορτογαλία και γι αυτό ονομάζεται «Πορτογαλικού τύπου». Είναι κυρίως συνδεδεμένη με τον απλότυπο VI ή τον απλότυπο VII. Η συχνότητα της στην Ελλάδα είναι 11,52%. Τα άτομα που αρχικά μελετήθηκαν ήταν ομοζυγώτες για την IVSI-6 μετάλλαξη και για τον απλότυπο VI και κύριο χαρακτηριστικό τους ήταν το αυξημένο επίπεδο της HbΑ 2 5% έως 8% και το χαμηλό επίπεδο της HbF 3,8% έως 20% της συνολικής Hb. Η αύξηση του επιπέδου της HbF (έως 20%) σε ομοζυγώτες για την IVSI-6 μετάλλαξη είχε συνδεθεί με την συνύπαρξη του απλοτύπου VII. Πρόσφατα όμως βρέθηκε ότι το επίπεδο της HbF σε ομοζυγώτες για την IVSI-6 μετάλλαξη φτάνει έως και το 47%. Τα αυξημένα αυτά επίπεδα της HbF βελτιώνουν ακόμα περισσότερο την καλή αιματολογική εικόνα των ομοζυγωτών. Σε μελέτη που είχε σκοπό τον εντοπισμό διαφορών σε πρωτεϊνικά συμπλέγματα που βρίσκονται σε σημαντικές περιοχές για την έκφραση του 39
40 συμπλέγματος των γονιδίων β- τύπου εξετάσθηκε μία ομάδα ατόμων ομοζυγώτες για την IVSI-6 και τον απλότυπο VI ή τον απλότυπο VII. Το επίπεδο της HbF στα άτομα αυτά κυμαίνονταν από 2-47%, ενώ το επίπεδο της HbΑ 2 ήταν υψηλό (5-8%) και ήταν σε αντίστροφη σχέση με το επίπεδο της HbF. Η μελέτη αυτή όμως δεν αποκάλυψε διαφορές που να δικαιολογούν τα αυξημένα επίπεδα της HbF στα άτομα αυτά Μεταλλάξεις χωρίς νόημα ή αλλαγής πλαισίου ανάγνωσης Οι μεταλλάξεις χωρίς νόημα είναι σημειακές μεταλλάξεις που δημιουργούν κωδικόνια τερματισμού της μετάφρασης. Μεταλλάξεις που οφείλονται σε ελλείψεις μιας ή περισσότερων βάσεων αλλάζουν το πλαίσιο ανάγνωσης και καταλήγουν όπως και οι μεταλλάξεις χωρίς νόημα στην μη παραγωγή β- αλυσίδων. Πάσχοντες που φέρουν στο ένα τους αλληλόμορφο μία τέτοια μετάλλαξη και στο άλλο μία άλλη μετάλλαξη β + θαλασσαιμίας εμφανίζουν φαινότυπο ομόζυγης β-θαλασσαιμίας. Η έλλειψη ενός δινουκλεοτιδίου (-ΑΑ) στο κωδικόνιο για το αμινοξύ 8 (FSC-8) δημιουργεί ένα κωδικόνιο τερματισμού στο νέο 21 κωδικόνιο. Η μετάλλαξη FSC-8 οδηγεί σε πρόωρο τερματισμό της σύνθεσης των β- αλυσίδων. Είναι δηλαδή, μία β ο μετάλλαξη η οποία συνδέεται με τον απλότυπο IV και με αυξημένη παραγωγή HbF. Λόγω της αυξημένης παραγωγής της τελευταίας άτομα που είναι διπλοί ετεροζυγώτες γι αυτή την μετάλλαξη και μία άλλη β ο μετάλλαξη εμφανίζουν φαινότυπο ενδιάμεσης β θαλασσαιμίας. Η β-39 είναι σημειακή (C T) μετάλλαξη χωρίς νόημα, η οποία έχει ως αποτέλεσμα την παραγωγή μη λειτουργικού β- mrna. Το επίπεδο του β- mrna κυμαίνεται από 1% έως 3% σε σχέση με το επίπεδο του φυσιολογικού, δηλαδή είναι περίπου 50 φορές χαμηλότερο της φυσιολογικής τιμής. Συνήθως πάσχοντες οι οποίοι στο ένα αλληλόμορφο φέρουν την συγκεκριμένη μετάλλαξη και στο άλλο μία μετάλλαξη β + εμφανίζουν φαινότυπο ομόζυγης β-θαλασσαιμίας Μεταλλάξεις που επηρεάζουν την αποκοπή και την πολυαδενυλίωση του RNA Η αλληλουχία AAUAAA κοντά στο 3 άκρο των ευκαρυωτικών mrnas φαίνεται να είναι σημαντική γιατί δίνει το σήμα για την αποκοπή του RNA στο 3 άκρο. Μετά την αποκοπή του RNA ακολουθεί η πολυαδενυλίωση που συμβάλλει στην σταθερότητα του mrna. Μεταλλάξεις στην αλληλουχία AAUAAA επιδρούν στη αποκοπή του RNA με αποτέλεσμα να παράγονται πιο επιμήκη και πιθανόν ασταθή 40
41 μόρια mrna. Στις περιπτώσεις αυτές εμφανίζεται ένας β + θαλασσαιμικός φαινότυπος. Οι μεταλλάξεις αυτές βρίσκονται στην 3 μη μεταφραζόμενη περιοχή (3 UTR) του γονιδίου και εντοπίζονται συνήθως στην αλληλουχία που δίνει το σήμα πολυαδενυλίωσης. Ο ρόλος της περιοχής 3 UTR του mrna δεν έχει πλήρως διευκρινιστεί και δεν είναι γνωστό σε ποια διαδικασία ελέγχου της έκφρασης του γονιδίου συμμετέχει. Είναι δυνατό να αλλάζουν την δευτεροταγή δομή του DNA με αποτέλεσμα να σχηματίζεται φουρκέτα η οποία παρεμβάλλεται στη συνέχεια στη διαδικασία πολυαδενυλίωσης ή/και στη μεταφορά του μηνύματος στο κυτταρόπλασμα Μεταλλάξεις που εντοπίζονται σε άλλα χρωμοσώματα Πρόσφατα στο χρωμόσωμα Χ έχουν βρεθεί γενετικοί τόποι που επηρεάζουν την έκφραση των γονιδίων των σφαιρινών. Ένας τέτοιος γενετικός τόπος για παράδειγμα, βρίσκεται στο μικρό σκέλος του χρωμοσώματος Χ (Χp21-11) και αφορά την GATA-1 πρωτεΐνη. Ένας δεύτερος γενετικός τόπος που βρίσκεται επίσης στο μικρό σκέλος του χρωμοσώματος Χ (Xp22,2), ελέγχει τη παραγωγή F-κυττάρων σε φυσιολογικά και δρεπανοκυτταρικά άτομα Ελλείψεις που προκαλούν β-θαλασσαιμία Ελλείψεις σε γονίδια που ανήκουν στο σύμπλεγμα των γονιδίων β- τύπου επηρεάζουν την έκφραση και των άλλων γονιδίων του συμπλέγματος αυτού. Πολλές από αυτές τις ελλείψεις περιλαμβάνουν τα δ- και β- γονίδια, δημιουργώντας τις δβ θαλασσαιμίες και σε αρκετές περιπτώσεις την εμφάνιση συνδρόμου HPFH (κληρονομικής παραμονής HbF). Ελάχιστες και σπάνιες είναι οι ελλείψεις που αφορούν μόνο το β- γονίδιο και προκαλούν β-θαλασσαιμία. Η πιο κοινή από αυτές είναι μια έλλειψη 610 bp που περιλαμβάνει την IVSII, το τρίτο εξόνιο και αλληλουχίες μετά το 3 άκρο του β- γονιδίου. Η έλλειψη αυτή απαντάται στους πληθυσμούς της Ινδίας και αφορά το 1/3 των πασχόντων από β-θαλασσαιμία. 41
42 3. Η δβ-μεσογειακή αναιμία Στη δβ-μα παρατηρούνται ελλείψεις τμημάτων DNA, που αφαιρούν τα δ - και β- γονίδια. Είναι μικρότερες σε μέγεθος (7,2-115 Kb) από τις ελλείψεις HPFH. Στους ετεροζυγώτες δβ-μα έχουμε αυξημένα επίπεδα HbF (2%-25%), επίπεδα HbA 2 φυσιολογικά (2,1%-2,3%) και φαινότυπο φορέων β-μα καθώς και μορφολογία ερυθροκυττάρων. Η HbF έχει ετεροκυτταρική (ανομοιογενή) κατανομή στα ερυθροκύτταρα (Bollekens και Forget, 1991). Έχουμε τις εξής περιπτώσεις δβ-μα (Baysal, 1993). α. GγΑγ(δβ) ο - ΜΑ με έλλειψη στα δ- και β- γονίδια και αναλογία Gγ/Αγ=4/6. β. (δβ) ο -ΜΑ μη ελλειπτικού τύπου, που χαρακτηρίζεται από μεταλλαγές στο β- και Αγ- γονίδιο και τον 3 Αγ-ενισχυτή και έχει φαινότυπο των ελλειπτικών δβ- ΜΑ. γ. Gγ(Αγδβ) ο -ΜΑ. Εδώ οι ελλείψεις παρατηρούνται στα δ τα β- και το Αγ- γονίδιο και παράγονται μόνο Gγ-αλυσίδες. δ. (εγδβ) ο -ΜΑ. Έχουμε έλλειψη σε όλο το σύμπλεγμα των γονιδίων της β- σφαιρίνης καθώς και στην περιοχή Ελέγχου Γενετικού Τόπου LCR (Locus Control Region). (Πίνακες 2, 3, 4). 42
43 Πίνακας 2. Οι γνωστές μορφές Gγ Αγ (δβ) ο μεσογειακής αναιμίας. α/α Τύπος Μήκος Έλλειψης Hb F (%) Gγ (%) Βιβλιογραφία 1 Ινδικός 32,6 kb 16,6 79 Mishima et al, Ιαπωνικός kb Matsunaga et al, Ελληνικός 7.2 kb 1 34 Kulozik et al, Ισπανικός 115 kb Ottolenghi και Giglioni, Νεγρικός 2 12 kb 14,7 50 Waye et al, Ανατολικής 9.5 kb Palena et al, 1994 Ευρώπης 7 Λαοτιανός 12.5 kb 11,5 60 Zhang et al, Ταϋλανδικός 12.5 kb 9,9 - Trent et al, Σικελικός 13.4 kb 4 18, Fritsch et al, 1979 Ottolenghi et al, Μακεδονικός Τουρκικός kb-1.6 kb, 7.6 kb αναστ/φή 6,7 12,8 40 Efremov et al, 1994 Kulozik et al, Βιετνάμ 12,6 kb 20 - Craig et al, Σαρδηνίας Pirastu et al, 1984a Ottolenghi et al, Κινέζικος 5 11,3-22,3 40 Atweh et al, 1986,1987 Balta et al, : Το 3 άκρο της έλλειψης αυτής δεν έχει χαρακτηριστεί. 2: Ο Νεγρικός τύπος δβ- μεσογειακής αναιμίας πρωτοχαρακτηρίστηκε από τους Anagnou et al (1985) σε συνδυασμό με Hb S, η οποία όμως τροποποιούσε τον παραγόμενο φαινότυπο, μάλλον προς HPFH 3: Ο Μακεδονικός και Τουρκικός τύπος της δβ- μεσογειακής αναιμίας χαρακτηρίζεται από την ίδια μοριακή βλάβη (Craig et al, 1995). 4: Η μοριακή βλάβη περιλαμβάνει μεταλλαγές στο Αγ-γονίδιο (Αγ-196 C Τ) και στο β-γονίδιο (β ο -39 C Τ ). 5: Η μοριακή βλάβη περιλαμβάνει μεταλλαγές στον 3 Αγ ενισχυτή (C Τ), 2,4 kb 3 της θέσης πολυαδενυλίωσης του Αγ-γονιδίου και στο β- γονίδιο (β ο -29 Α G). 43
44 Πίνακας 3. Οι γνωστές μορφές Gγ(Αγδβ) ο περιγραφεί μέχρι σήμερα. μεσογειακής αναιμίας που έχουν α/α Τύπος Μήκος έλλειψης Hb F (%) Gγ (%) Βιβλιογραφία 1 Ινδικός 8,5 kb, 13 >90 Jones et al, ,5 kb αναστ/φή 2 Γερμανικός 52 kb Anagnou et al, Μαλαισίας kb Trent et al, Τουρκικός 36,2 kb >95 Fritsch et al, Μαλαισίας kb George et al, Βελγικός 50 kb Losekoot et al, Νεγρικός 35,7 kb 11,2 93,2 Henthorn et al, Κινεζικός 100 kb 11,8 - Mager et al, Yannanese 90 kb Znang et al, : Τα όρια της έλλειψης αυτής δεν είναι γνωστά με ακρίβεια, παρά μόνο κατά προσέγγιση, μετά από χαρτογράφηση με περιοριστικά ένζυμα. Πίνακας 4. Οι γνωστές μορφές (εγδβ) ο μεσογειακής αναιμίας. α/α Τύπος Μήκος έλλειψης Βιβλιογραφία 1 Κροατικός 148 kb Diaz-Chico et al, Καναδικός 185 kb 1 Diaz-Chico et al, Αγγλοσαξ/κός 95,9 kb Orkin et al, 1981b 4 Βρετανικός 100 kb 1 Curtin et al, Ολλανδικός 99,4 kb Van der Ploeg et al, 1980b 6 Σκωτσέζικος 205 kb 1 Trent et al, Μεξικανικός 105 kb 1 Fearon et al, Ισπανικός 30 kb 2 Driscoll et al, Ιρλανδικός 205 kb 1 Fortina et al, : Τα όρια της έλλειψης αυτής δεν είναι γνωστά με ακρίβεια, παρά μόνο κατά προσέγγιση, μετά από χαρτογράφηση με περιοριστικά ένζυμα. 2: Η έλλειψη αυτή αφαιρεί τις τρείς από τις πέντε DNasel υπερευαίσθητες θέσεις της περιοχής LCR, ενώ αφήνει ανέπαφα τα γονίδια του συμπλέγματος της β- σφαιρίνης. 44
45 4. Κληρονομική Παραμονή Εμβρυϊκής Αιμοσφαιρίνης (Hereditary Persistence of Fetal Hemoglobin-HPFH) Με τον όρο Κληρονομική Παραμονή Εμβρυικής Αιμοσφαιρίνης (Hereditary Persistence of Fetal Hemoglobin-HPFH) χαρακτηρίζονται οι περιπτώσεις εκείνες κατά τις οποίες η έκφραση των εμβρυικών Gγ- και Αγ- γονιδίων διατηρείται σε υψηλά επίπεδα και στη ενήλικο ζωή, με αποτέλεσμα το ποσοστό τη ς HbF να υπερβαίνει το 1% και να κυμαίνεται μεταξύ 10%-50%. Η κατανομή της HbF στα ερυθροκύτταρα είναι ομοιογενής (πανκυτταρική κατανομή), η μορφολογία των ερυθροκυττάρων παραμένει αναλλοίωτη, ενώ ο αιματολογικός φαινότυπος είναι κατά τα άλλα φυσιολογικός. (59) Στις περισσότερες περιπτώσεις HPFH το υψηλό ποσοστό της HbF συνοδεύεται από μειωμένο ποσοστό της HbA 2. Οι περιπτώσεις HPFH παρουσιάζουν τεράστιο ερευνητικό ενδιαφέρον, επειδή η εκάστοτε μοριακή βλάβη έχει σαν αποτέλεσμα τη συνεχιζόμενη παραγωγή HbF σε ενήλικες, με συνέπεια να αποτελούν μοντέλο για τη μελέτη του μοριακού μηχανισμού, που εμπλέκεται στη μεταστροφή της έκφρασης των εμβρυικών και ενήλικων γονιδίων της β-σφαιρίνης του ανθρώπου. Το γεγονός αυτό έχει ιδιαίτερη σημασία, μιας και η διαλεύκανση του ρυθμιστικού αυτού μηχανισμού βοηθά στην κατανόηση του τρόπου ρύθμισης της έκφρασης των β-σφαιρινικών γονιδίων, με αποτέλεσμα την αποτελεσματικότερη θεραπευτική αντιμετώπιση των διαφόρων τύπων αιμοσφαιρινοπαθειών. Οι περιπτώσεις HPFH ταξινομούνται, ανάλογα με το είδος της μοριακής βλάβης που τις προκαλεί, σε ελλειπτικού και μη ελλλειπτικού τύπου και περιγράφονται εκτενέστερα στις παρακάτω παραγράφους HPFH ελλειπτικού τύπου (deletional HPFH) Οι περιπτώσεις ελλειπτικού τύπου HPFH χαρακτηρίζονται από εκτεταμένες ελλείψεις τμημάτων DNA (12,9 έως 105 kb), που περιλαμβάνουν κυρίως τα δ- και β-γονίδια, αλλά και ρυθμιστικές περιοχές του συμπλέγματος των β-γονιδίων. Είναι φανερό ότι λόγω της έλλειψης των ενήλικων δ- και β-γονιδίων, ταγονίδια εξακολουθούν να είναι μεταγραφικά ενεργά και στην ενήλικο ζωή με αποτέλεσμα την συνεχιζόμενη παραγωγή HbF σε υψηλά επίπεδα (16%-30%) (59) ενώ για τον ίδιο λόγο τα επίπεδα της HbA 2 είναι ελαττωμένα. Η αύξηση των επιπέδων της HbF στις περιπτώσεις ελλειπτικού τύπου HPFH οφείλεται στο ότι η αφαίρεση συγκεκριμένων τμημάτων DNA από το σύμπλεγμα 45
46 των β-σφαιρινικών γονιδίων φέρνει σε γειτονία με τα εμβρυικά γ-γονίδια αλληλουχίες-ενισχυτές που σε φυσιολογικές συνθήκες βρίσκονται πολύ μακρύτερα. Χαρακτηριστική είναι η περίπτωση της HPFH-1 όπου η περιοχή 3 της έλλειψης βρέθηκε να λειτουργεί σαν ενισχυτής με πειράματα παροδικής έκφρασης (60). Παραπλήσια αποτελέσματα περιγράφονται για την περίπτωση της έλλειψης που ευθύνεται για την HPFH-3. (61) Συγκεκριμένα βρέθηκε ότι μια περιοχή 700 bp, η οποία περιέχει μια αλληλουχία SV40 και μια αλληλουχία CCAAT, προκαλεί αύξηση στην έκφραση του γονιδίου αναφοράς CAT 6-7 φορές, σε κύτταρα Κ562 με πειράματα παροδικής έκφρασης κι αύξηση της μεταγραφής του γ -γονιδίου στο εμβρυικό συκώτι διαγονιδιακών ζώων. Μελέτη της έλλειψης, που ευθύνεται για την HPFH-5 (62) δείχνουν ότι ο φαινότυπος HPFH πιθανά να οφείλεται στη γειτνίαση του ενισχυτή 3 του β-γονιδίου (Behringer et al. 1987, Kollia et al, 1987) με τα γ-γονίδια. Τέλος κλωνοποιήθηκε (63) μια αλληλουχία-ενισχυτής που πιθανά να ευθύνεται για το φαινότυπο της HPFH-6. H αλληλουχία αυτή περιέχει μια σειρά από θέσεις πρόσδεσης των μεταγραφικών παραγόντων GATA-1, GT-I/II, AP-1, YY1, C/EBP, TFIID, GCRE και HNF-1, οι οποίοι όπως δείχνουν πειράματα παροδικής έκφρασης φαίνεται ότι δρούν συνεργιστικά για την πλήρη ενεργότητα της περιοχής αυτής ως ενισχυτή. Μια ενδιαφέρουσα παρατήρηση που αφορά τις ελλείψεις που προκαλούν ελλειπτικού τύπου HPFH είναι ότι ορισμένες από αυτές έχουν παραπλήσια μήκη, ενώ το ίδιο ισχύει και για διάφορες περιπτώσεις ελλείψεων που προκαλούν δβμεσογειακή αναιμία. Το γεγονός αυτό πιθανά να οφείλεται στη γειτνίαση των σημείων αποκοπής πριν τη δημιουργία της έλλειψης, ίσως μέσω της πρόσδεσης τους σε σημεία του πυρηνικού φακέλου κατά την αντιγραφή του DNA (64). Η υπόθεση αυτή ενισχύεται και από δεδομένα των Henthorn et al. (65) σύμφωνα με τα οποία τα σημεία αποκοπής των ελλείψεων που προκαλούν β- ή δβ-μεσογειακή αναιμία και ελλειπτικού τύπου HPFH βρίσκονται, ως επί το πλείστον, μέσα σε μεταγραφόμενες περιοχές του συμπλέγματος των β-σφαιρινικών γονιδίων. Στον πίνακα 5 παρατίθενται οι ελλείψεις που προκαλούν τις γνωστές μορφές ελλειπτικού τύπου HPFH και τα αντίστοιχα χαρακτηριστικά τους. 46
47 Πίνακας 5. Συνοπτική παράθεση των ελλείψεων τμημάτων DNA που ευθύνονται για τις γνωστές μορφές ελλειπτικού τύπου HPFH. α/α Τύπος Μήκος έλλειψης Hb F(%) Gγ (%) Βιβλιογραφία 1 HPFH kb 24,8 50,7 Tuan et al, 1980, HPFH kb 24,4 32,3 Tuan et al, HPFH-3 48,5 kb 22,6 69,3 Henthorn et al, HPFH-4 40 kb Saglio et al, HPFH-5 12,9 kb Carnaschella et al, HPFH-6 70 kb 17,2 20,9 - Winichagoon et al, HPFH-7 30 kb 18, Moturn et al, HPFH μη ελλειπτικού τύπου (non-deletional HPFH) Οι περιπτώσεις μη ελλειπτικού τύπου HPFH χαρακτηρίζονται από σημειακές μεταλλαγές ή μικρές ελλείψεις στην περιοχή του υποκινητή του Gγ ή του Aγ γονιδίου. Οι μεταλλαγές αυτές έχουν σαν αποτέλεσμα να μεταβάλλεται η συγγένεια πρόσδεσης των ερυθροειδικών ή μη ρυθμιστικών πρωτεϊνών (66), η νουκλεοτιδική αλληλουχία η/και η υπερμοριακή δομή ρυθμιστικών περιοχών (67) με αποτέλεσμα τη συνεχιζόμενη έκφραση των γ-γονιδίων στην ενήλικο ζωή. Οι περιπτώσεις μη ελλειπτικού τύπου HPFH χαρακτηρίζονται από μικρότερα, κατά μέσο όρο, ποσοστά HbF σε σχέση με τις ελλειπτικού τύπου HPFH, ενώ η συνεχιζόμενη έκφραση των γ- γονιδίων στις περιπτώσεις αυτές συνδέεται με χαμηλότερα επίπεδα έκφρασης των ενηλίκων δ- και β- γονιδίων. Το γεγονός αυτό οφείλεται στη μερική λειτουργική αναστολή των τελευταίων, λόγω της μεταλλαγής του συνδεδεμένου (in cis) γ-γονιδίου, η οποία φαίνεται να παρεμβάλλεται στη φυσιολογική διαδικασία μεταστροφής της έκφρασης των εμβρυικών, ως προς τα ενήλικα γονίδια (68). Oι μεταλλαγές που προκαλούν μη ελλειπτικού τύπου HPFH εντοπίζονται σε ρυθμιστικές αλληλουχίες του υποκινητή των γ-γονιδίων. Οι μεταλλαγές στις θέσεις -202 και -200 του Gγ-γονιδίου και -202, -198, -196, -195 του Αγ-γονιδίου εντοπίζονται σε μια περιοχή πλούσια σε γουανίνες και κυτοσίνες, στην οποία προσδένεται η πρωτεΐνη Sp1 (69), η οποία αποτελεί μεταγραφικό παράγοντα. Επιπλέον η περιοχή αυτή είναι ευαίσθητη στη DNaseI (70), γεγονός που αποδεικνύει ότι πρέπει να είναι μεταγραφικά ενεργή. Οι Sykes και Kaufman (69 ) έδειξαν ότι η μεταλλαγή Gγ -202 (C G) αυξάνει 5-47
48 10 φορές την πρόσδεση της πρωτεΐνης Sp1, λόγω αύξησης της ομολογίας με την αλληλουχία Sp1, ενώ η αντίστοιχη μεταλλαγή Αγ -202 (C T) μειώνει την ομολογία με την αλληλουχία Sp1, με αποτέλεσμα τα επίπεδα της HbF στην τελευταία περίπτωση να είναι ελαφρώς μικρότερα. Επιπρόσθετα οι Jane et al (71) έδειξαν ότι η πρωτεΐνη SSP (Stage Selector Protein), που προσδένεται φυσιολογικά στη θέση -50, προσδένεται και στη θέση -202 στη περίπτωση της μεταλλαγής Gγ -202 (C G). H τελευταία αναστέλλει τη μεθυλίωση της περιοχής αυτής, με αποτέλεσμα η πρωτεΐνη Sp1 να μη μπορεί να προσδεθεί για να καταστείλει φυσιολογικά την έκφραση του Gγ γονιδίου. Η μεθυλίωση των γ-γονιδίων, έπεται της μεταστροφής της έκφρασης των εμβρυικών στα ενήλικα γονίδια, όπως έχει αποδειχτεί άλλωστε και από πειράματα των Enver et al. (68) Οι Fischer and Nowock (72) έδειξαν ότι η μεταλλαγή Αγ -198 (Τ C) δημιουργεί δυο αλληλοεπικαλυπτόμενες θέσεις πρόσδεσης των πρωτεϊνών Sp1 και της ερυθροειδικής πρωτεΐνης GF-1, με συνέπεια η αλληλεπίδραση των τελευταίων να προκαλεί αύξηση της μεταγραφής του μεταλλαγμένου Αγ-γονιδίου. Αξιοσημείωτη τέλος είναι και η παρατήρηση των Bacolla et al. (67) οι οποίοι διαπίστωσαν ότι η περιοχή -217 έως -209 των γ-γονιδίων αλληλεπιδρά με την περιοχή -203 έως -194 και λαμβάνει κάτω από συγκεκριμένες in vitro συνθήκες μια μορφή ενδομοριακή τριπλής έλικας. Η τελευταία σε συνδυασμό με την πρωτεΐνη BP-8 που σταθεροποιεί την παραπάνω μακρομοριακή δομή, φαίνεται ότι σχετίζεται με την αποσιώπηση της έκφρασης των γ-γονιδίων στην ενήλικη ζωή. Μεταλλαγές, οι οποίες προκαλούν μη ελλειπτικού τύπου HPFH, φαίνεται ότι τροποποιούν αυτή τη μακρομοριακή δομή και αναστέλλουν την αποσιώπηση των γ-γονιδίων. Η μεταλλαγή στη θέση -175, τόσο του Gγ όσο και του Αγ-γονιδίου, τροποποιεί τη θέση πρόσδεσης του παράγοντα OTF-1 (Octamer factor-1) (72) ο οποίος καταστέλλει φυσιολογικά τη μεταγραφή των γ-γονιδίων, ενώ παράλληλα ενισχύει την πρόσδεση του παράγοντα ΝF-Ε1 (73). Tα παραπάνω οδηγούν στην αύξηση των επιπέδων μεταγραφής του μεταλλαγμένου γονιδίου. Οι μεταλλαγές στις θέσεις -114 του Gγ-γονιδίου και αυτές στις θέσεις -117 και -114 του Αγ-γονιδίου τροποποιούν την δεύτερη αλληλουχία CCAAT. Οι Superti- Furga et al. (74) παρατήρησαν ότι η μεταλλαγή Αγ-117 (G A) επιδρά στην πρόσδεση τριών πρωτεϊνικών παραγόντων, των CP-1 (CCAAT- binding Protein-1), CDP (CCAAT Displacement Protein) και της ερυθροειδικής NF-E3 (75) ενώ η μεταλλαγή Gγ -114 (C Τ) αποτρέπει την πρόσδεση της πρωτεΐνης CP1 και ευθύνεται για το φαινότυπο HPFH σε διαγονιδιακά ζώα (76). Το ερώτημα ποια από τις παραπάνω πρωτεΐνες παίζει το σημαντικότερο ρόλο στο φαινότυπο HPFH είναι ακόμα ανοικτό. Πάντως δεδομένα των Rixon kai Gelinas (77) δείχνουν ότι οι 48
49 μεταλλαγές Αγ-117 (G A) και Αγ-196 (C T) είχαν ελάχιστη ως μηδενική έκφραση με πειράματα παροδικής έκφρασης σε μη ερυθροειδικά κύτταρα. Τα παραπάνω προσδίδουν στις ερυθροειδικές πρωτεΐνες έναν πρωτεύοντα ρόλο στην παραγωγή φαινότυπου HPFH. Τέλος, οι μεταλλαγές Gγ -161 (G A), Gγ -158 (C T) και η Αγ-158 (C T) έχουν μικρότερη επίδραση στην έκφραση των αντίστοιχων γονιδίων. Το γεγονός αυτό οφείλεται πιθανά στην απουσία ρυθμιστικών αλληλουχιών από την περιοχή αυτή, ή στο γεγονός ότι βρίσκονται στα όρια ρυθμιστικών περιοχών, όπως η περιοχή -182 έως -175 (octamer motif) και -144 έως -140 (CACCC motif). Αποτελέσματα του Gilman (78) δείχνουν ότι στην περιοχή γ-161/-158 θα πρέπει να προσδένεται μια πρωτεΐνη τετραμερές, μοριακού βάρους 210 kda, η οποία δρα ως ενεργοποιητής της μεταγραφής του γ γονιδίου. Η πρωτεΐνη αυτή αλληλεπιδρά ισχυρότερα με τον μεταλλαγμένο, για τις θέσεις αυτές υποκινητή, γεγονός που πιθανά εξηγεί εν μέρει τα αυξημένα επίπεδα των αντίστοιχων σφαιρινικών αλυσίδων και της HbF. Πάντως η αύξηση των επιπέδων της HbF στις περιπτώσεις της HPFH «Ελβετικού τύπου» σε συνδυασμό με την παρουσία των μεταλλαγών Gγ -161 (G A) ή Gγ -158 (C T) φαίνεται να είναι πιο σύνθετο φαινόμενο, το οποίο πιθανά περιλαμβάνει, εκτός των παραπάνω μεταλλαγών και άλλους γενετικούς τόπους (Craig et al. 1996). Όπως προκύπτει από τα παραπάνω δεν έχουν αναφερθεί μεταλλαγές σε ρυθμιστικές αλληλουχίες, όπως η αλληλουχία ΑΤΑ ή CCAAT στη θέση -84 (proximal CCAAT box), πιθανά λόγω του ότι οι μεταλλαγές αυτές προκαλούν βαριάς μορφής γ-μεσογειακή αναιμία οδηγώντας στο θάνατο των εμβρύων κατά την ενδομήτριο ζωή. Η εκδοχή αυτή φαίνεται να ενισχύεται και από το ότι η αδρανοποίηση του 5 του γ-γονιδίου στους πιθήκους του Νέου Κόσμου οφείλεται, εκτός των άλλων, σε μεταλλαγές της ίδιας αλληλουχίας. 49
50 50
51 ΣΚΟΠΟΣ Η μεταστροφή της αιμοσφαιρίνης στα διάφορα αναπτυξιακά στάδια του ανθρώπου αποτυπώθηκε για πρώτη φορά στη δεκαετία του 1950, ενώ αργότερα ανακαλύφθηκαν πολλές μεταλλαγές οι οποίες οδηγούσαν σε παραμονή της εμβρυϊκής αιμοσφαιρίνης στον ενήλικα. Ο παθοφυσιολογικός ρόλος της εμβρυϊκής αιμοσφαιρίνης στη θαλασσαιμία περιγράφηκε στην αρχή του Ποικίλες γενετικές και βιοχημικές μελέτες έδειξαν ότι η επιβίωση ασθενών με σοβαρές ανωμαλίες στη β αλυσίδα μπορεί να αποδοθεί στην ύπαρξη HbF, η οποία βελτιώνει σημαντικά την κλινική τους εικόνα. Η κληρονομική παραμονή εμβρυϊκής αιμοσφαιρίνης (HPFH) και δβθαλασσαιμία είναι γενετικά νοσήματα, τα οποία χαρακτηρίζονται από σταθερή έκφραση των γ-γονιδίων και υψηλή HbF στην ενήλικη ζωή. Αν και οι περιπτώσεις των HPFH είναι χωρίς συμπτώματα, οι δβ-θαλασσαιμίες έχουν ένα τυπικό θαλασσαιμικό φαινότυπο με ενδιάμεση αναιμία και μειωμένα αιματολογικά στοιχεία. Μεγάλες ελλείψεις που απομακρύνουν το δ- και β-γονίδιο οδηγούν σε δβθαλασσαιμία ή HPFH ελλειπτικού τύπου, ενώ μεταλλαγές στους υποκινητές των γ- γονιδίων οδηγούν σε μη ελλειπτικού τύπου (nd-) HPFH. Και οι δύο περιπτώσεις είναι σπάνιες, αλλά ο συνδυασμός τους βοηθά σημαντικά στη μελέτη και διερεύνηση των μηχανισμών που ρυθμίζουν την έκφραση των γ-γονιδίων και κατ επέκταση στη χρησιμοποίησή τους σε νέες θεραπευτικές προσεγγίσεις των θαλασσαιμικών συνδρόμων. Στη συγκεκριμένη διδακτορική διατριβή μελετήθηκαν οι μεταλλαγές ή/και ελλείψεις που ανιχνεύονται στο β- και γ-γονίδιο, για δβ-θαλασσαιμία και HPFH ελλειπτικού ή μη ελλειπτικού τύπου σε άτομα- ετεροζυγώτες/ ομοζυγώτες ή και διπλούς ετεροζυγώτες για β-θαλασσαιμία, δβ-θαλασσαιμία, δρεπανοκυτταρική αναιμία που έφεραν υψηλή HbF καθώς και άτομα με HPFH. Στη συνέχεια συσχετίστηκαν οι συγκεκριμένες θαλασσαιμικές μεταλλαγές είτε στο β- είτε στο γ-γονίδιο με τα αιματολογικά στοιχεία ώστε να διεξαχθούν συμπεράσματα για την ορθότερη πρόληψη, διάγνωση και θεραπευτική αντιμετώπιση των ασθενών με θαλασσαιμικά σύνδρομα. 51
52 52
53 2. ΕΙΔΙΚΟ ΜΕΡΟΣ - ΥΛΙΚΟ ΚΑΙ ΜΕΘΟΔΟΛΟΓΙΑ 2.1. Επιλογή δειγμάτων Κατά την εκπόνηση της παρούσας διατριβής επιλέχθηκαν οι εξής κατηγορίες περιστατικών: α. Ετεροζυγώτες(φορείς) δβ-μεσογειακής Αναιμίας β. Ετεροζυγώτες (φορείς) HPFH γ. Ετεροζυγώτες (φορείς) β-μεσογειακής Αναιμίας (με αυξημένη HbF). Οι ανωτέρω κατηγορίες αφορούν άτομα ενήλικα, από τα προσερχόμενα για προγεννητικό έλεγχο στη Μονάδα Πρόληψης Μεσογειακής Αναιμίας του Γενικού Νοσοκομείου Καρδίτσας Μελέτη αιμοσφαιρινών- φαινοτυπική εικόνα με βάση τα αιματολογικά δεδομένα Αιμοληψία Γίνεται λήψη 10 ml περιφερικού ολικού αίματος (φλεβικού), με ηπαρινισμένη σύριγγα, σε αντιπηκτικό Κ 3 ΕΚ 3 ΕDTA και απευθείας, από τη σύριγγα, παρασκευή λεπτών επιστρώσεων σε αντικειμενοφόρες πλάκες, για μικροσκοπική παρατήρηση μετά από χρώση May-Grunwald, Giemsa. Τα δείγματα αποθηκεύονται σε θερμοκρασία ψυγείου (4 C) Χρώση May-Grunwald, Giemsa Ρυθμιστικό διάλυμα 1. Na 2 HPO 4 2H 2 O 3,25 gr KH 2 PO 2 6,63 gr Συμπληρώνεται στα 100 cm 3 με απεσταγμένο H 2 O (έλεγχος ph=6,4). 2. Αραίωση του ανωτέρω διαλύματος 1/10 σε απεσταγμένο H 2 O ( H 2 O) (έλεγχος ph=6,4) Χρωστικές (α) May-Grunwald 100 cm 3 και 100 cm 3 διαλύματος 2. (β) Giemsa 2,8 cm 3 μέχρι 100 cm 3 διαλύματος 2. 53
54 Τεχνική - Μονιμοποίηση των παρασκευασμάτων σε 6 με μεθανόλη (CH 3 OH) - Χρώση με May-Grunwald (α) επί 10 - Απόρριψη της χρωστικής - Χρώση με Giemsa (β) επί 40 - Απόρριψη, καλό ξέβγαλμα με νερό βρύσης - Καθάρισμα της κάτω επιφάνειας των αντικειμενοφόρων. - Στέγνωμα σε θερμοκρασία δωματίου Μικροσκοπική παρατήρηση επιχρίσματος περιφερικού αίματος Περιγράφεται η ύπαρξη ή μη: υποχρωμίας, μικροκυττάρωσης, ανισοκυττάρωσης, ποικιλοκυττάρωσης, βασεόφιλης στίξης (καθίζηση ριβοσωμάτων), στοχοκυτάρρωσης, πολυχρωματοφιλίας, μακροκυττάρωσης, στοματοκυττάρωσης, ανισοχρωμίας, σφαιροκυττάρωσης (Εικόνες 6α, β, γ, δ). Εικόνα 6α. Μορφολογία ερυθροκυττάρων υγιούς ατόμου Εικόνα 6β. Μορφολογία ερυθροκυττάρων ατόμου με ετερόζυγη β-μα 54
55 Εικόνα 6γ. Μορφολογία ερυθροκυττάρων ατόμου με ετερόζυγη β-μα και HbF. Διακρίνουμε μικροκυττάρωση, ανισοκυττάρωση και ποικιλοκυττάρωση. Εικόνα 6δ. Μορφολογία ερυθροκυττάρων ατόμου με ετερόζυγη δβ-μα. Διακρίνουμε μικροκυττάρωση και ανισοκυττάρωση Αξιολόγηση αιματολογικών δεδομένων Οι μετρήσεις της γενικής αίματος πραγματοποιήθηκαν σε αυτόματους αιματολογικούς αναλυτές, τύπου Sysmex K-1000 αρχικά και Sysmex K-4500 στη συνέχεια και αξιολογήθηκαν οι παρακάτω παράμετροι: Αιμοσφαιρίνη (Hb): Αντιστοιχεί στην ποσότητα της αιμοσφαιρίνης που εμπεριέχεται στα ερυθροκύτταρα ενός καθορισμένου όγκου ολικού αίματος (Φ.Τ. Άνδρες 15,4±1,0 και Γυναίκες 13,3±0,7). Αιματοκρίτης (Hct): Αντιστοιχεί στο ποσοστό (%) του όγκου που καταλαμβάνουν τα ερυθροκύτταρα σε σχέση με το συνολικό όγκο του αίματος (Φ.Τ. Άνδρες 47,4±3,2 και Γυναίκες 41,2±2,2). 55
56 Αριθμός ερυθροκυττάρων (RBC): Αντιστοιχεί στον αριθμό των ερυθροκυττάρων που περιέχονται σε μια μονάδα ολικού όγκου αίματος (Φ.Τ. Άνδρες 5.170±0.39 και Γυναίκες 4.490±0.32). Επίσης αξιολογούνται οι ερυθροκκυταρικοί δείκτες: MCH: Μέση ποσότητα αιμοσφαιρίνης ανά ερυθρυκύτταρο (Mean Corpuscular Hemoglobin) (Φ.Τ. > 27,5 pg). MCH= αιμοσφαιρίνη σε gr ανά 100 ml αίματος (Hb) αριθμός ερυθροκυττάρων ανά 100 ml αίματος (RBC) MCV: Μέσος όγκος ερυθροκυττάρων (Mean Corpuscular volume) (Φ.Τ. >81,0 fl) MCV = όγκος ερυθροκυττάρων σε 100 ml αίματος (Hct %) αριθμός ερυθροκυττάρων ανά 100 ml αίματος (RBC) MCHC: Μέση πυκνότητα (συγκέντρωση) αιμοσφαιρινών στα ερυθροκύτταρα (Mean corpuscular Hemoglobin concentration) (Φ.Τ. > 32,5) MCHC= αιμοσφαιρίνη σε 100 ml αίματος (Hb) όγκος ερυθροκυττάρων σε 100 ml αίματος (Hct) RDW: Εύρος κατανομής του όγκου των ερυθροκυττάρων. Ο νέος αυτός δείκτης των αιματολογικών αναλυτών εκφράζει την ομοιογένεια ή ετερογένεια του όγκου των ερυθροκυττάρων. Αύξησή του υποδηλώνει διπλό ερυθροκυτταρικό πληθυσμό. Με τη μέθοδο υπολογισμού RDW-CV έχουμε φυσιολογικές τιμές 13±1% και με τη μέθοδο RDW-SD (Φ.Τ. 42±5 fl). 56
57 Ποσοτικός προσδιορισμός αιμοσφαιρινών με τη μέθοδο HPLC Ο ποσοτικός προσδιορισμός των αιμοσφαιρινών HbA, HbA 2, HbF, HbS, HbC, HbO-Arab, HbD-Punjab, HbG-Philadelphia κ.λπ. έγινε αυτόματα με χρωματογραφικό διαχωρισμό σε υγρή χρωματογραφία υψηλής απόδοσης και οπτικών ανιχνευτών (HPLC) (Ηigh Performance Liquid Chromatograpy), (Variant TM - Bio-Rad). Η όλη διαδικασία υποστηρίζεται από κατάλληλο υπολογιστικό και λειτουργικό σύστημα, όπως φαίνεται από τα χρωματογραφήματα στις παρακάτω εικόνες (Εικόνες 7,8,9,10). Εικόνα 7. Χρωματογράφημα υγρής χρωματογραφίας υψηλής απόδοσης σε φυσιολογικό δείγμα ενήλικα. Η φυσιολογική αιμοσφαιρίνη (Hb A) αντιστοιχεί στην υψηλή κορυφή και έχει χρόνο έκλουσης (retention time) περίπου 2,5 λεπτά (2,39 στο συγκεκριμένο δείγμα). Η αιμοσφαιρίνη Α 2 (HbA 2 ) έχει χρόνο έκλουσης λεπτά (3,60). Οι δύο μικρές κορυφές που εμφανίζονται πριν την HbA (Ρ 2, Ρ 3 ) αντιστοιχούν στη γλυκοζυλιωμένη αιμοσφαιρίνη (A 1 C) (Variant TM Bio Rad). 57
58 Εικόνα 8. Χρωματογράφημα ετεροζυγώτη β-μα. με αυξημένη αιμοσφαιρίνη F. Διακρίνεται η HbF (χρόνος έκλουσης 1,14min), η HbA (χρόνος έκλουσης 2,53 min) και η HbA 2 (χρόνος έκλουσης 3,65 min). 58
59 Εικόνα 9. Χρωματογράφημα ετεροζυγώτη δβ-μα. Η αιμοσφαιρίνη Α 2 (HbA 2 ) βρίσκεται σε φυσιολογικό όρια ( % στο συγκεκριμένο μηχάνημα). Διακρίνονται στη σειρά: HbF (χρόνος έκλουσης 1,18 min), HbA (χρόνος έκλουσης 2,52min) και η αιμοσφαιρίνη Α 2 (χρόνος έκλουσης 3,68 min). 59
60 Εικόνα 10. Χρωματογράφημα στην HPFH (Κληρονομική Παραμονή Εμβρυϊκής Αιμοσφαιρίνης F). Διακρίνονται στη σειρά: HbF (χρόνος έκλουσης 1,17min), HbA (χρόνος έκλουσης 2,40min) και η αιμοσφαιρίνη Α 2 (χρόνος έκλουσης 3,60min). 60
61 Ποσοτικός προσδιορισμός της αιμοσφαιρίνης Α 2 (HbA 2 ) Ο ποσοτικός προσδιορισμός της HbA 2 έγινε παράλληλα με τον οπτικό ποιοτικό έλεγχο των αιμοσφαιρινών: HbA, HbS, HbD, Hb Lepore κ.α. σε στήλες χρωματογραφίας διαιθυλαμινοκυτταρίνης (DEAE) με χρήση ρητίνης DE 52 Whatman. Προετοιμασία ρητίνης - Πλύσιμο 2 φορές με απεσταγμένο νερό - Πλύσιμο με διάλυμα Τris 3 φορές. Το ίδιο διάλυμα χρησιμοποιείται για όλη τη διεργασία της χρωματογραφίας. Διάλυμα A: (6,1 gr Τris+100 mgr KCN) σε 1 lt απεσταγμένο Η 2 Ο και ρύθμιση ph=8,3 με οξικό οξύ (CH 3 COOH). Το πλύσιμο της ρητίνης γίνεται με το διάλυμα πριν ρυθμιστεί το ph. Η ρύθμιση γίνεται στο ίδιο το τελευταίο εναιώρημα της ρητίνης. Ετοιμασία στηλών: Με το εναιώρημα της ρητίνης σχηματίζεται στήλη διαμέτρου 1 και ύψους 8 cm περίπου, διαμέσου της οποίας διηθείται συνεχώς το διάλυμα Τεχνική χρωματογραφίας Δημιουργία αιμολύματος (σε θερμοκρασία δωματίου) Σε ποσότητα διαλύματος A ίση με τα 2/10 της αιμοσφαιρίνης κάθε δείγματος, προσθέτουμε 250 ml ολικού όγκου αίματος, φυγοκεντρούμε για 10 min στις στροφές και από το υπερκείμενο αιμόλυμα: α. 500 ml επιστοιβάζεται στη στήλη της ρητίνης αφήνεται να προσροφηθεί και εκλούεται με διάλυμα Α. Η HbA 2 αποχωρίζεται από το κύριο κλάσμα της HbF καθώς και από τα κλάσματα HbS, HbD, Hb Lepore κ.λπ. (εάν υπάρχουν) στα 10 ml και φωτομετρείται στα 418 nm. Η απορρόφηση καθορίζεται ως OD. HbA 2. β. 50 ml διαλύεται σε 10 ml διάλυμα Α και φωτομετρείται στα 418 nm. Η απορρόφηση αντιστοιχεί στην ολική αιμοσφαιρίνη του αιμολύματος. Ο υπολογισμός του ποσοστού της HbA 2 γίνεται με τον τύπο: 61
62 HbA 2 (%) = OD HbA 2 x 10 OD ολικής αιμοσφαιρίνης (Φυσιολογικές τιμές: 1,8-3,0%) Ποιοτικός έλεγχος αιμοσφαιρινών, με ηλεκτροφόρηση αιμοσφαιρίνης σε ταινίες οξικής κυτταρίνης (Cellogel 7,8x15 cm) Αντιδραστήρια 3. Ρυθμιστικό διάλυμα ηλεκτροφόρησης (pη=8,5) TRIS 3,00 gr EDTA-Na 2 0,39 gr Βορικό οξύ (H 3 BO 3 ) 2,50 gr Συμπληρώνεται στα 1000 ml με απεσταγμένο H 2 O 4. Διαλύματα παρασκευής αιμολύματος (α) Νιτρώδες Νάτριο (NaNO 2 ) 2,0 gr Χλωριούχο Νάτριο (NaC1) 8,5 gr Συμπληρώνεται στα 100 ml με απεσταγμένο H 2 O (β) Κυανιούχο Κάλιο (KCN) 1,0 gr Χλωριούχο Νάτριο (NaC1) 8,5 gr Συμπληρώνεται στα 1000 ml με απεσταγμένο H 2 O 5. Χρωστική light-green 500 mg στο ακόλουθο διάλυμα. Μεθανόλη (CH 3 OH) 50 ml, οξεικό οξύ (CH 3 COOH) 10 ml και 40 ml H 2 O. Παρασκευή αιμολυμάτων - Σε ογκομετρικό κωνικό σωληνάριο που περιέχει ποσότητα 10 ml διαλύματος 2α, προσθήκη 200 ml ολικού αίματος. - Φυγοκέντρηση στις 2000 στροφές επί 15 λεπτά. - Απόρριψη υπερκείμενου. - Πλύσιμο των ερυθρών με 10 ml διαλύματος 2β. 62
63 - Φυγοκέντρηση-απόρριψη υπερκείμενου. - Στον τελικό όγκο των ερυθρών προσθέτουμε απεσταγμένο νερό σε όγκο ίσο με το 1/10 της τιμής της αιμοσφαιρίνης του όγκου αίματος (π.χ. Hb 12 gr, όγκος H 2 O 1,2 ml). - Καλός πωματισμός του κωνικού σωληναρίου και ανακίνηση σε ανακινητήρα (shaker) επί 20 λεπτά. - Το αιμόλυμα είναι έτοιμο για ηλεκτροφόρηση Τεχνική ηλεκτροφόρησης Χρησιμοποιούνται σαν ηλεκτροφορητικό μέσο ταινίες οξικής κυτταρίνης (cellogel 7,8x15 cm σε CH 3 OH 30%). - Πριν από την χρήση τους παραμένουν στο διάλυμα ηλεκτροφόρησης επί 15 - Στέγνωμα της ταινίας με διηθητικό χαρτί λίγο πριν από τη χρήση τη ς. - Τοποθέτηση του αιμολύματος από τη θαμπή πλευρά της ταινίας προς την κάθοδο. Η τοποθέτηση γίνεται με λεπτή πιπέττα ή με ειδική συσκευή (applicator). - Τοποθέτηση της ταινίας στη γέφυρα του λουτρού. - Αναμονή επί 5 λεπτά. Η συσκευή της ηλεκτροφόρησης καλύπτεται με το κάλυμμά της. - Ρευματοδότης 1 ma ανά cm πλάτους ταινίας. - Διαχωρισμός αιμοσφαιρινικών κλασμάτων. - Η ηλεκτροφόρηση διαρκεί 1 ώρα και 15 λεπτά. - Ακολουθεί χρώση με χρωστική Light Green για 3 και στη συνέχεια διαδοχικές εκπλύσεις σε διάλυμα οξεικού οξέος 5% σε διαδοχικά δοχεία, μέχρι αποχρωματισμού των ταινιών. Τα αιμοσφαιρινικά κλάσματα χρωματίζονται πράσινα και δεν αποχρωματίζονται Ερμηνεία των αποτελεσμάτων Στην ηλεκτροφόρηση ενός αιμολύματος με τις παραπάνω συνθήκες διακρίνουμε τα ακόλουθα κλάσματα: 63
64 - Αιμοσφαιρίνη Α, που αποτελεί το κύριο κλάσμα και κινείται γρήγορα προς την άνοδο. - Αιμοσφαιρίνη Α 2, που αποτελεί το 1,8-3% και κινείται αργά προς την άνοδο. - Αιμοσφαιρίνη F. Όταν υπάρχει κινείται προς την άνοδο λίγο αργότερα από την αιμοσφαιρίνη Α. Στις αιμοσφαιρινοπάθειες και στις Μεσογειακές αναιμίες: - Οι αιμοσφαιρίνες E, C, O κ.α. κινούνται στο ίδιο ύψος με την HbA 2. - Οι αιμοσφαιρίνες S, Lepore (Πύλος) και O κινούνται σε ίση απόσταση ανάμεσα στις HbA και HbA 2. - Η αιμοσφαιρίνη Η, ελεύθερες β αλυσίδες στη «βαριά» α-μεσογειακή αναιμία, κινείται ταχύτερα από όλες και βρίσκεται αρκετά εμπρός από την αιμοσφαιρίνη Α Ποσοτικός προσδιορισμός HbF με τη μέθοδο Betke Παρασκευή αιμολύματος - Φυγοκέντρηση αίματος σε 2000 στροφές/λεπτό επί 10 λεπτά. Αφαίρεση πλάσματος. - Έκπλυση και φυγοκέντρηση ερυθροκυττάρων σε ισότονο διάλυμα (0,9%) χλωριούχου νατρίου (NaCl) τρεις φορές. - Απομάκρυνση υπερκείμενης στοιβάδας λευκών αιμοσφαιρίων με προσεκτική αναρρόφηση. - Προσθήκη απεσταγμένου νερού σε όγκο ίσο με τον όγκο των ερυθροκυττάρων. - Ανάμειξη και παραμονή σε θερμοκρασία δωματίου επί 30 λεπτά. - Προσθήκη 1 ml τολουόλης. Έντονη ανακίνηση σε vortex και ανάδευση σε shaker επί Φυγοκέντρηση σε 3000 στροφές/λεπτό επί 30 λεπτά. Οι μεμβράνες των ερυθροκυττάρων σχηματίζουν συμπαγή λεπτή στοιβάδα πάνω από το διαυγές αιμόλυμα. - Απόληψη αιμολύματος με πιπέττα Pasteur, που διαπερνούμε «τρυπώντας» τη στοιβάδα των στρωμάτων, και περαιτέρω καθαρισμός του με διήθηση 64
65 μέσα από χάρτινο ηθμό (π.χ. Whatman 3 mm) Μέτρηση εμβρυϊκής αιμοσφαιρίνης HbF (κατά Betke) Στηρίζεται στην ιδιότητα της HbF να αντέχει στην επίδραση αλκαλικών διαλυμάτων καλύτερα από τις άλλες αιμοσφαιρίνες που καταστρέφονται εύκολα. Αντιδραστήρια Α. Σιδηροκυανιούχο κάλιο K 3 Fe (CN) mg Κυανούχο κάλιο (KCN) 200 mg Συμπληρώνονται στα 1000 ml με απεσταγμένο H 2 O Β. Καυστικό νάτριο (ΝaΟΗ) 1,2 N. Παρασκευάζεται με ανάλογη αραίωση προτυπωμένης φύσιγγας διαλύματος NaOH σε απεσταγμένο Η 2 Ο. Γ. Κεκορεσμένο διάλυμα θεϊκού αμμωνίου (ΝΗ 4 ) 2 So 4 σε απεσταγμένο Η 2 Ο. Τεχνική μέτρησης ml αιμολύματος αραιώνονται στα 8,0 ml με διάλυμα Α. - Σε 2,8 ml του αραιωμένου αιμολύματος προστίθενται 0,2 ml διαλύματος Β και αναμειγνύονται αμέσως καλά. Συγχρόνως αρχίζει η χρονομέτρηση. - Μετά 2 λεπτά ακριβώς προστίθενται 2 ml διαλύματος Γ. Καλή ανάμειξη. Παραμονή σε θερμοκρασία δωματίου επί 5 λεπτά. Η μετουσιωμένη αιμοσφαιρίνη κατακρημνίζεται. - Διήθηση με απλό διηθητικό ηθμό. - Φωτομέτρηση του διηθήματος σε μήκος κύματος φωτός 540 nm. - Η ένδειξη ODα αντιστοιχεί στη μη μετουσιωμένη αιμοσφαιρίνη. - Μάρτυρας. 0,28 ml αρχικού αιμολύματος και προσθήκη 4,72 ml Η 2 Ο. - Φωτομέτρηση στα 540. Ένδειξη OD β. Αυτή αντιστοιχεί στο σύνολο της αιμοσφαιρίνης του αιμολύματος. - Υπολογισμός ποσοστού εμβρυϊκής αιμοσφαιρίνης. Η bf(%) = OD α OD x10 β 65
66 Κυτταροχημικός διαχωρισμός HbF Διαλύματα 1. Διάλυμα εκλούσεως FeCl 3 14,8 mmol/l και αιματοξυλίνη 16,5 mmol/l 2. Διάλυμα χρώσεως Ερυθροσίνη 0,1 gr/100 ml Παρασκευάσματα - Λεπτές επιστρώσεις αίματος σε αντικειμενοφόρες πλάκες. - Στέγνωμα στον αέρα επί Μονιμοποίηση με 80% αιθυλική αλκοόλη (CH 3 CH 2 OH) για 5. - Ξέβγαλμα αμέσως με άφθονο νερό βρύσης. - Στέγνωμα. Τεχνική - Βύθιση των μονιμοποιημένων παρασκευασμάτων μέσα στο διάλυμα (1) (20-25 C) για 20 δευτερόλεπτα. - Ξέβγαλμα με νερό της βρύσης. - Χρώση με το διάλυμα (2) για 2 λεπτά. - Ξέβγαλμα καλά με νερό βρύσης και στέγνωμα στον αέρα. - Εξέταση στο μικροσκόπιο. Τα κύτταρα με F είναι χρωματισμένα, ενώ τα χωρίς F έχουν χάσει την αιμοσφαιρίνη τους και φαίνονται σαν σκιές ερυθροκυττάρων Χρώση για αναζήτηση εγκλείστων στα ερυθροκύτταρα 1. Διαπίστωση ενδοκυτταρίων ιζημάτων αιμοσφαιρίνης (χρώση εγκλείστων). Χρησιμεύει για τη διάγνωση της ομόζυγης β-μα, ετερόζυγης β-μα, 66
67 ετερόζυγης δβ-μα, ετερόζυγης γδβμα, όπου οι α αλυσίδες που βρίσκονται σε περίσσεια, καθιζάνουν μόνες τους μέσα στους ερυθροβλάστες. Αντιδραστήριο Α Διάλυμα 1% της χρωστικής ιώδες του μεθυλίου Methyl Violet (Οίκου Merck) σε ισότονο διάλυμα NaCl (1 gr/100 ml), ανάδευση σε υδατόλουτρο 37 C επί 24ωρο μέχρι πλήρους διαλύσεως και επαναλαμβανόμενες διηθήσεις. Τεχνική - Μικρός όγκος αίματος (μερικές σταγόνες) προστίθεται σε ίσο όγκο αντιδραστηρίου Α σε μικρό σωληνάριο. - Παραμονή σε θερμοκρασία δωματίου επί Στη συνέχεια από το εναιώρημα παρασκευάζονται επιστρώσεις σε αντικειμενοφόρες πλάκες, οι οποίες ξηραίνονται στον αέρα. - Η παρατήρηση στο μικροσκόπιο γίνεται κατά προτίμηση με καταδυτικό φακό (μεγάλη μεγέθυνση 1000 χ). - Όταν υπάρχουν έγκλειστα, φαίνονται σαν μικρά ή μεγάλα μωβ άμορφα κοκκία μέσα στο πρωτόπλασμα. 2. Κατακρήμνιση ασταθών αλυσίδων αιμοσφαιρίνης μέσα στα ερυθροκύτταρα. Χρησιμεύει για τη διαπίστωση ασταθών αιμοσφαιρινών και αλυσίδων β, όταν αυτές βρίσκονται σε περίσσεια μέσα στα ερυθροκύτταρα (αιμοσφαιρινοπάθεια Η, ετερόζυγη α-μα). Αντιδραστήριο Β 1280 mg νιτρώδους νατρίου (NaNO 2 ) διαλύονται σε 100 ml απεσταγμένου νερού. Τεχνική 67
68 - 0,5 ml αίματος επωάζεται με 0,1 ml αντιδραστηρίου Β για 30 στους 37 C. - Στη συνέχεια σε μερικές σταγόνες, από το επωασμένο αίμα με το αντιδραστήριο Β, προσθέτουμε ίσο όγκο του αντιδραστηρίου Α. - Παραμονή σε θερμοκρασία δωματίου επί 30 και επίστρωση σύμφωνα με την παραπάνω τεχνική. Τα έγκλειστα που σχηματίζονται μετά την επώαση μοιάζουν με αδρά κοκκία έντονα μωβ χρωματισμένα (Εικ.11). Εικόνα 11. Έγκλειστα ερυθροκκυτάρων στην ετερόζυγη β-μα Ηλεκτροφόρηση αιμοσφαιρίνης σε άγαρ Ρυθμιστικά διαλύματα 2. (α) Κιτρικό Νάτριο (C 6 H 5 Na 3 O 7 H 2 O) 147 gr (β) Κιτρικό Οξύ (H 3 C 6 H 5 O 7 H 2 O) 25 ml 20% Συμπληρώνεται στα 1000 cm 3 με H 2 O 3. Αραίωση 1/10 του διαλύματος 1 (1 ml διαλύματος ml H 2 O AD) Ταινίες ηλεκτροφόρησης, ταινίες κιτρικού άγαρ (citrate agar gel- Corning 12x10 cm). 68
69 Τεχνική - Ετοιμασία λουτρού ηλεκτροφόρησης με το διάλυμα 2 (ph=5,9). - Τοποθέτηση με τριχοειδές σωληνάριο, ελάχιστης ποσότητας αιμολύματος στην ειδική υποδοχή της ταινίας. - Τοποθέτηση της ταινίας στις γέφυρες του λουτρού. - Ρευματοδότηση (200 V) επί ½-1 ώρα. - Χρώση με Light Green, όπως τις ταινίες οξεικής κυτταρίνης (Cellogel). Αναγνώριση κλασμάτων Οι HbA, HbA 2, HbD και άλλες αιμοσφαιρίνες κινούνται ελάχιστα μαζί. Η HbS διαχωρίζεται προς την άνοδο και η HbF προς την κάθοδο (Εικ. 12Α, Β). Αλκαλικό ph 8,6 Όξινο ph 6,2 Εικόνα 12Α. Διαχωρισμός φυσιολογικών και παθολογικών αιμοσφαιρινών σε αλκαλικό και όξινο ph 69
70 Αλκαλική ηλεκτροφόρτηση (ph 8,6) Όξινη ηλεκτροφόρηση (ph 6,2) Εικόνα 12Β. Ηλεκτροφόρηση δειγμάτων αιμοσφαιρίνης σε αλκαλικό και όξινο ph 2.3. Μελέτη σε γονιδιακό επίπεδο (DNA) Απομόνωση γενωμικού DNA από περιφερικό αίμα με εξαλάτωση Η απομόνωση γίνεται από τους πυρήνες των λευκοκυττάρων (WBC) με τη διαδικασία που περιγράφεται από τους Ponoz et al (1982). Αντιδραστήρια Λυτικό διάλυμα Ι 155 mm NH 4 Cl (για ερυθροκύτταρα) 10 mm KHCO 3 1 mm EDTA ph=7,4 Λυτικό διάλυμα II (για ερυθροκύτταρα) 10 mm Tris-HCl ph=7,5 400 mm NaCl 2 mm EDTA 70
71 Πρωτεϊνάση Κ 10 mg/ml SDS 10% NaCl 6M Πρωτόκολλο 1. Τοποθετούμε το ολικό αίμα σε σωληνάριο των 15 ml και αραιώνουμε ως 12 ml περίπου με ddh 2 O αναδεύοντας με πιπέτα pasteur. 2. Φυγοκεντρούμε για 15 min στις 3000 rpm, στους 4 C. 3. Αδειάζουμε το υπερκείμενο. Τα κύτταρα αραιώνονται με ddh 2 O ως 12 ml περίπου. Ανακινούμε έντονα σε vortex. 4. Φυγοκεντρούμε για 15 min στις 3000 rpm, στους 4 C 5. Αδειάζουμε το υπερκείμενο. Προσθέτουμε διάλυμα λύσης λεμφοκυττάρων (διάλυμα λύσης I) μέχρι τα 12 ml. Το διάλυμα λύσης I σπάει τα WBC. 6. Φυγοκεντρούμε για 15 min στις 3000 rpm, στους 4 C. 7. Επαναλαμβάνουμε τα στάδια 5,6 με διάλυμα λύσης II. 8. Αδειάζουμε το υπερκείμενο. Προσθέτουμε διάλυμα λύσης των πυρήνων των λεμφοκυττάρων (διάλυμα λύσης II) μέχρι τα 6 ml. Το διάλυμα λύσης II σπάει τους πυρήνες. Ανακινούμε καλά και επωάζουμε για min. 9. Προσθέτουμε 750 μl SDS 10% και 100 μl πρωτεϊνάση K. Το SDS ανοίγει την πυρηνική μεμβράνη. Η πρωτεϊνάση Κ κάνει πεπτιδική υδρόλυση ή αποδόμηση των πρωτεϊνών. 10. Επωάζουμε στους 37 C Ο/Ν (overnight) σε υδατόλουτρο. 11. (Την επόμενη ημέρα): Προσθέτουμε 2 ml 6 Μ NaCl. Αναδεύουμε ισχυρά για 15 sec. 12. Φυγοκεντρούμε για 15 min σε 3500 rpm, στους 4 C. 13. Στο υπερκείμενο υπάρχει το DNA. Μεταγγίζουμε το υπερκείμενο σε καθαρό κωνικό σωληνάριο των 50 ml. 14. Φυγοκεντρούμε για 15 min σε 3500 rpm, στους 4 C. 15. Ακολουθεί καταβύθιση με 2 όγκους αιθανόλης 100% και 1/10 όγκου του υπερκείμενου CH 3 COONa (οξικό νάτριο) 3Μ ph 5,2. Ανακινούμε. 16. Τοποθετούμε τα δείγματα στους -20 C Ο/Ν (overnight). 17. (Την επόμενη ημέρα): Φυγοκεντρούμε για 50 min σε 3500 rpm, στους 4 C ή για 30 min σε 8000 rpm. Αφαιρούμε το υπερκείμενο. 71
72 18. Ξεπλένουμε το ίζημα με 70% CH 3 CH 2 OH (αιθανόλη) και ξαναφυγοκεντρούμε για 30 min (δις) και για 20 min, σε rpm, στους 4 C. 19. Απομακρύνουμε το υπερκείμενο. 20. Διαλύουμε το τελικό ίζημα σε μl ddh 2 O. 21. Στη συνέχεια γίνεται έλεγχος ποιότητας DNA σε πήκτωμα αγαρόζης: 3-4 μl DNA και 12 μl αραιή χρωστική μπλε της βρωμοφαινόλης. 22. Επίσης φωτομετρούμε για ποσοτικό έλεγχο του DNA: 5 μl DNA και 495 μl ddh 2 O (αραίωση 1:100) στα 260 nm και 280 nm μήκος κύματος. Ο λόγος οπτικών πυκνοτήτων (O.D. 260/O.D. 280) θα πρέπει να κυμαίνεται μεταξύ 1,7 και 1,9. Η συγκέντρωση DNA υπολογίζεται με βάση τον τύπο: αραίωση Χ O.D. 260 Χ 50. (Θεωρούμε ότι η O.D. 1 αντιστοιχεί σε 50 μg DNA/ml σε μήκος κύματος 260 nm.) Ποιοτικός και ποσοτικός προσδιορισμός (έλεγχος συγκέντρωσης) DNA Η ποσότητα και η ποιότητα (καθαρότητα) του DNA εκτιμώνται με φωτομέτρηση γνωστού όγκου διαλύματος DNA, που αραιώνεται σε τελικό όγκο 500 μl με ddh 2 O. Το αραιωμένο διάλυμα DNA τοποθετείται σε κυβέτα χαλαζία. Η φωτομέτρηση γίνεται σε μήκος κύματος 260 nm και 280 nm. Από την οπτική πυκνότητα (O.D.) του δείγματος υπολογίζεται η συγκέντρωση του DNA σ αυτό. Ο λόγος της οπτικής απορρόφησης 260 nm προς 280 nm O.D.260 ( ) καταδεικνύει και την ποιότητα του DNA. O.D.280 O.D.260 Το καθαρό DNA δίνει λόγο =1. 80(αποδεκτά όρια 1,70-1,90) O.D.280 Παράλληλα, ποσότητα δείγματος DNA (3 μl) ηλεκτροφορείται σε πήκτωμα αγαρόζης κατάλληλης σύστασης. Στο πήκτωμα αγαρόζης πε ριέχεται βρωμιούχο αιθίδιο (EtBr) σε συγκέντρωση 0,5 μg/ml, το οποίο συγκρατείται μεταξύ των βάσεων του δίκλωνου DNA και φθορίζει όταν εκτεθεί σε UV ακτινοβολία. Η ένταση του φθορισμού είναι ανάλογη της συγκέντρωσης του κάθε δείγματος. 72
73 Παρασκευή πηκτώματος αγαρόζης Υλικά - Αγαρόζη (SIGMA A 6013) - Ρυθμιστικό διάλυμα ηλεκτροφόρησης 1xΤΒΕ - Διάλυμα βρωμιούχου αιθιδίου (EtBr) σε συγκέντρωση 0,5 μg/ml Πρωτόκολλο - Χρησιμοποίηση ειδικού εκμαγείου. - Προστίθενται 60 ml ρυθμιστικού διαλύματος σε κωνική φιάλη Erlenmeyer. - (Για δημιουργία gel: 1%, 2%, 3% προσθέτουμε αντίστοιχα: 3 gr, 6 gr, 9 gr αγαρόζης σε διάλυμα 1xTBE όγκου 300 ml). - Η φιάλη τοποθετείται σε φούρνο μικροκυμάτων για 2-3 min και αναδεύεται με κυκλικές ανακινήσεις της φιάλης κατά διαστήματα, ώστε να διαλυθούν οι σβώλοι της αγαρόζης. - Προσθέτουμε 15 μl EtBr και αναδεύουμε το διάλυμα για ομοιόμορφη κατανομή του βρωμιούχου αιθιδίου. - Ψύχεται το διάλυμα σε θερμοκρασία 5-10 C ανώτερη από το σημείο πήξεως της αγαρόζης. - Αφήνεται το πήκτωμα αγαρόζης για 1-2 ώρες περίπου σε θερμοκρασία δωματίου για να πήξει και στη συνέχεια αποθηκεύεται στους 4 C Ηλεκτροφόρηση γενωμικού DNA, προϊόντων PCR σε πήκτωμα αγαρόζης Το βρωμιούχο εθίδιο (EtBr) ενσωματώνεται μεταξύ των βάσεων του DNA και φθορίζει σε υπεριώδη ακτινοβολία. Με αυτόν τον τρόπο ανιχνεύονται η επιτυχής απομόνωση γενωμικού υλικού και η επιλεκτική ενίσχυση τμημάτων DNA (προιόντα PCR) (Εικ. 13A, B). 73
74 Εικόνα 13Α. Ηλεκτροφόρηση δειγμάτων γενωμικού DNA N M Εικόνα 13B. Ηλεκτροφόρηση προιόντων PCR δειγμάτων Ν: αρνητικός μάρτυρας Μ: μάρτυρας γνωστού μεγέθους (100 bp ladder, New England Biolabs) Αλυσιδωτή αντίδραση πολυμεράσης (Polymerase chain reaction, PCR) Η αλυσιδωτή αντίδραση πολυμερισμού (Polymerase Chain Reaction, PCR), είναι μια δυναμική μέθοδος στον τομέα της μοριακής βιολογίας και δίνει τη δυνατότητα πολλαπλασιασμού ενός τμήματος DNA μέχρι και πάνω από 100 δισεκατομμύρια αντίγραφα, σε μια in vitro ενζυματική αντίδραση και σε χρονικό διάστημα 3-4 ωρών. Η τεχνική περιγράφηκε από τους Karry and Mullis (1985), Mullis and Faloona (1987) και στηρίζεται στη χρήση μιας θερμοανθεκτικής DNA πολυμεράσης (Taq πολυμεράση, Saiki et al., 1988), που απομονώνεται από τον μ ικροοργανισμό Thermus aquaticus και δεν υφίσταται απώλεια της ενεργότητάς της με 74
75 επαναλαμβανόμενα στάδια θέρμανσης στους C. Η αρχή της αντίδρασης PCR βασίζεται στον ενζυματικό πολλαπλασιασμό μιας συγκεκριμένης αλληλουχίας DNA, έως 3 Kb, που οριοθετείται δεξιά και αριστερά από δύο εκκινητές-ολιγονουκλεοτίδια (primers), μήκους bp. Η αλληλουχία του κάθε εκκινητή είναι συμπληρωματική προς τη μια από τις δύο αλυσίδες του δίκλωνου εκμαγείου και χρησιμεύει ως σημείο έναρξης της σύνθεσης της συμπληρωματικής αλυσίδας του DNA από την πολυμεράση. Απαιτούνται επίσης ελεύθερα δεοξυριβονουκλεοτίδια, ως δομικοί λίθοι του πολλαπλασιασμού του αρχικού μορίου DNA (template DNA) και επίσης κατάλληλο ρυθμιστικό διάλυμα με ιόντα μαγνησίου και καλίου. Η αντίδραση PCR πραγματοποιείται σε ειδικό θερμικό κυκλοποιητή (thermalcycler) σε επαναλαμβανόμενους κύκλους αποδιάταξης του δίκλωνου DNA (denaturation step) σε θερμοκρασία C, υβριδοποίησης των εκκινητών στις συμπληρωματικές τους αλληλουχίες (annealing step) σε θερμοκρασία C και επιμήκυνσης της θυγατρικής αλυσίδας του DNA (elongation step) από την Taq πολυμεράση σε θερμοκρασία έως 72 C (ρυθμός ενσωμάτωσης νουκλεοτιδίων 1000/sec). Η θερμοκρασία τήξης (Tm) του κάθε εκκινητή, δηλαδή η θερμοκρασία στην οποία το 50% ενός πληθυσμού μορίων DNA βρίσκεται σε μονόκλωνη μορφή, ορίζει και τη θερμοκρασία υβριδοποίησής τους στην αλυσίδα του DNA και κυμαίνεται μεταξύ C. Κάθε κύκλος αποτελείται από τρία στάδια (Εικ. 14). 75
76 Εικόνα 14. Τα τρία στάδια του κύκλου της αντίδρασης PCR 76
77 Εκλεκτικός πολλαπλασιασμός αλληλουχιών του β-γονιδίου (PCR) Για να γίνει έλεγχος των μεταλλάξεων του β γονιδίου σφαιρίνης, το γονίδιο έχει χωριστεί σε έξι τμήματα μεγέθους νουκλεοτιδίων που καλύπτουν όλο το γονίδιο καθώς και τις αλληλουχίες των 5 και 3 μη μεταφραζόμενων περιοχών του. Εικόνα 15. Σχηματική απεικόνιση της θέσης των ζευγών εκκινητών στο γονίδιο της β-σφαιρίνης. Μαύρα κουτιά-εξώνια, λευκά κουτιά-εσώνια. Χρησιμοποιώντας κατάλληλα ζεύγη εκκινητών ενισχύεται εκλεκτικά η επιθυμητή αλληλουχία, η οποία βρίσκεται ανάμεσα στις αλληλουχίες των βάσεων του DNA, οι οποίες είναι συμπληρωματικές προς τους ολιγονουκλεοτιδικούς εκκινητές (Εικ. 15). Η νουκλεοτιδική αλληλουχία κάθε εκκινητή, είναι η εξής: Α1 : 5 -TTTAGTAGCAATTTGTACTGA-3 (21 nts) Α2 : 5 -GCCCTGGCTCCTGCCCTCCC-3 (20 nts) Α : 5 -GTACGGCTGTCATCACTTAGACCTCA-3 (26 nts) pco4 : 5 -CAACTTCATCCACGTTCACC-3 (20 nts) apco4 : 5 -GGTGAACGTGGATGAAGTT-3 (19 nts) Β : 5 -TGCAGCTTGTCACAGTGCAGCTCACT-3 (26 nts) C : 5 -GTGTACACATATTGACCAAA-3 (20 nts) D : 5 -AGCACACAGACCAGCACGTT-3 (20 nts) ad : 5 -AACGTGCTGGTCTGTGTGCT-3 (20 nts) X : 5 -AAATGCACTGACCTCCCACA-3 (20 nts) pco3 : 5 -ACACAACTGTGTTCACTAGC-3 (20 nts) 77
78 Οι εκκινητές Α2, Α, και Β έχουν στο 5' άκρο τους ένα GC-clamp μήκους 65 νουκλεοτιδίων. Η αλληλουχία του GC-clamp, είναι: 5 -GCCCGCCCCGCCCCCGTGCCCCCCGCGCCGCCCGCCCCGCCCCC-3 Για την αντίδραση της PCR απαιτούνται: 1. Γενωμικό DNA. 2. Εκκινητές συγκέντρωση 12,5 pmoles/μl και διατηρούνται στους - 20 C. 3. α) ένζυμο Taq πολυμεράση διαλυμένο σε διάλυμα 50% γλυκερόλη, 20mM Tris HCl με pη 8, 0,1 mm EDTA, 1 mm DTT, 200μg/ml ζελατίνη. Τελική συγκέντρωση ενζύμου : 5 u/μl. β) 10Χ buffer ενζύμου: 200 mm Tris με pη 8,4, 500 Mm KCl, 0,1 % ζελατίνη. γ) διάλυμα MgCl 2 : 50 mm. δ) αποδιατακτικό διάλυμα W1%. 4. Μίγμα των 4 δεοξυνουκλεοτιδίων συγκέντρωσης 40 mm (10 mm ως προς το καθένα). 5. ddh 2 O. Πρωτόκολλο αντίδρασης PCR 1. Παρασκευή διαλύματος σε αποστειρωμένο σωληνάριο τύπου eppendorf 0,5 ml με τη διαδοχική προσθήκη : - 10 Χ buffer τελικής συγκέντρωσης 1 X = 5,00 μl - διάλυμα Μg Cl 2 τελικής συγκέντρωσης 2,5 mm = 2,50 μl - διάλυμα W-1 τελικής συγκέντρωσης 0,05% = 2,50 μl - 12,5 pmoles εκκινητή 1 = 1,00 μl - 12,5 pmoles εκκινητή 2 = 1,00 μl - 2 mμ d NTPs = 0,40 μl - 1 u Taq πολυμεράση = 0,16 μl - Συνολικός όγκος =12,56 μl 2. Προσθήκη 0,5-1 μg γενωμικού DNA. 3. Συμπλήρωση του όγκου με ddh 2 O μέχρι τα 50 μl. Τοποθέτηση των δειγμάτων στο ειδικό μηχάνημα για την αντίδραση PCR. 78
79 Το πρόγραμμα που χρησιμοποιείται για PCR των τμημάτων του β -γονιδίου περιέχει συνθήκες οι οποίες τροποποιούνται ανάλογα με τα υπό μελέτη τμήματα και είναι γενικά: STEP-1: 94 C για 4 min. STEP-2: 94 C για 1 min (αποδιάταξη) STEP-3: 60 C για 1,5 min (πρόσδεση εκκινητών) STEP-4: 70 C για 2 min (επιμήκυνση) STEP-5: επανάληψη των 2,3,4, σταδίων για 34 φορές STEP-6: 70 C για 7 min. STEP-7: 4 C για 24 hrs. Λόγω του διαφορετικού Tm των εκκινητών του τμήματος 0, για τον εκλεκτικό πολλαπλασιασμό του τμήματος αυτού η θερμοκρασία πρόσδεσης τοείναι 55 C. Στο τέλος της αντίδρασης το προϊόν της PCR ελέγχεται σε πήκτωμα αγαρόζης 3% Παρασκευή ηλεκτροφόρηση - παρατήρηση αποδιατακτικού πηκτώματος ακρυλαμίδης (Denaturing Gradient Gel Electrophoresis, DGGE) Αποδιατακτικό πήκτωμα πολυακρυλαμίδης Για την παρασκευή πηκτωμάτων διαχωρισμού μικρών τμημάτων DNA, ως πρώτη ύλη χρησιμοποιείται το οργανικό μόριο CΗ 2 =CΗ-CO-ΝΗ 2 (ακρυλαμίδη). Το μονομερές της ακρυλαμίδης παρουσία TEMED (N,N,N,Ν τετραμεθυλαιθυλενοδιαμίνη) και υπερθειϊκού αμμωνίου (APS) σχηματίζει αλυσίδες. Αν στην αντίδραση πολυμερισμού υπάρχει το διμερές CH 2 =CΗ-C-Ν- CH 2 -Ν-C-CΗ=CH 2 (Ν,Ν μεθυλένδιςακρυλαμίδη), οι αλυσίδες συνδέονται διασταυρωτά μεταξύ τους και σχηματίζουν πηκτώματα με μέγεθος πόρων που καθορίζεται από τις συγκεντρώσεις των δύο μορίων. Συνήθως χρησιμοποιείται ακρυλαμίδη σε συγκέντρωση 3,5-20% και δις ακρυλαμίδη σε κατάλληλη αναλογία ώστε να υπάρχει ένα μόριο για κάθε 20 μονομερή. Το υπερθειικό αμμώνιο (APS), βοηθά την έναρξη πολυμερισμού της ακρυλαμίδης, και πρέπει 79
80 να έχει παρασκευασθεί πρόσφατα, ενώ το TEMED, αποτελεί τ ον επιταχυντικό παράγοντα του πολυμερισμού και χρησιμοποιείται ισομοριακά με τον εναρκτή. Όσον αφορά τα αποδιατακτικά πηκτώματα, αυτά πολυμερίζονται παρουσία παραγόντων που καταστέλλουν το ζευγάρωμα των βάσεων, ώστε να είναι δυνατός ο διαχωρισμός μονόκλωνων τμημάτων DNA. Κατάλληλοι τέτοιοι παράγοντες, είναι η ουρία και το φορμαμίδιο. Η ουρία (ΝΗ 2 CONH 2 ) είναι μόριο χωρίς φορτίο, ικανό να διασπά δεσμούς υδρογόνου σε νουκλεϊκά οξέα και πρωτεΐνες, και χρησιμοποιείται ώστε να ενισχύσει την αποδιάταξη. Το φορμαμίδιο έχει την ιδιότητα να διακόπτει τους δεσμούς υδρογόνου. Τα μικρού πάχους πηκτώματα θεωρούνται καλύτερα, γιατί τα μεγάλου πάχους (0,5-2 mm) θερμαίνονται κατά την ηλεκτροφόρηση. Η ακρυλαμίδη είναι νευροτοξική και απορροφάται από το δέρμα έχοντας συσσωρ ευτική δράση, γι αυτό η χρήση της απαιτεί προσοχή. Η πολυμερισμένη ακρυλαμίδη δεν είναι τοξική αλλά μπορεί να περιέχει μικρή ποσότητα μη πολυμερισμένης. Τα αποδιατακτικά πηκτώματα ακρυλαμίδης φτιάχνονται πάντα ανάμεσα σε δύο τζάμια, έτσι ώστε να προστατεύονται από το οξυγόνο, το οποίο εμποδίζει τον πολυμερισμό, καθώς η επαφή με τον αέρα περιορίζεται σε μια λεπτή λωρίδα, στην κορυφή του πηκτώματος. Τα τζάμια που χρησιμοποιούνται πρέπει να είναι πολύ καθαρά, προκειμένου να είναι εύκολη η απομάκρυνση του πηκτώματος από αυτά. Ο πολυμερισμός πραγματοποιείται σε 60 περίπου λεπτά σε θερμοκρασία δωματίου και το πήκτωμα μπορεί να διατηρηθεί σε θερμοκρασία 4 C για 1-2 ημέρες. Στα διαλύματα DNA (προϊόντα PCR) που πρόκειται να ηλεκτροφορηθούν στο πήκτωμα προστίθεται ένα διάλυμα που περιέχει i) χρωστική και ii) ένα υλικό όπως η γλυκόζη, γλυκερόλη, σουκρόζη ή Ficoll για να καθιζάνουν και να μη διαχέονται τα δείγματα από τις θέσεις του πηκτώματος, όπου τοποθετούνται. Η χρωστική έχει κινητικότητα στο πήκτωμα ως μόριο γνωστο ύ μοριακού βάρους, και χρησιμεύει για τον εντοπισμό των θέσεων των άχρωμων μορίων που ηλεκτροφορούνται κάθε στιγμή στο πήκτωμα. Οι πιο κοινές από τις χρωστικές που χρησιμοποιούνται είναι το μπλε της βρωμοφαινόλης και το κυανούν ξυλένιου που αναμειγνύονται με όλους τους κοινούς διαλύτες, εκτός του νερού. Μετά την ηλεκτροφόρηση των δειγμάτων DNA, το πήκτωμα βάφεται με διάλυμα βρωμιούχου αιθιδίου προκειμένου να γίνουν ορατές οι ζώνες του DNA μετά από έκθεση σε υπεριώδη ακτινοβολία. 80
81 Το πήκτωμα που χρησιμοποιήθηκε στο πλαίσιο της συγκεκριμένης πρακτικής εργασίας, είναι αποδιατακτικό, και παρασκευάζεται έτσι ώστε να παρουσιάζει κατά μήκος του γραμμική κλίση συγκέντρωσης αποδιατακτικών παραγόντων, αυξανόμενης από πάνω προς τα κάτω στο πήκτωμα Εξοπλισμός για την παρασκευή, ηλεκτροφόρηση και παρατήρηση του πηκτώματος 2 τζάμια: Ένα διαστάσεων 19,5 cm x 18 cm, πάχους 4 mm και ένα με προεξοχές διαστάσεων 19,5 cm x 18 cm πάχους 4 mm (οι προεξοχές έχουν διαστάσεις 2 cm x 2 cm). Spacers πάχους 0,8 cm. Χτένα πάχους 0,8 cm με δόντια πλάτους 0,5 cm. Συσκευή για την παρασκευή πηκτώματος με κλίση συγκέντρωσης αποδιατακτικού παράγοντα με χωρητικότητα 25 ml. Πρόκειται για δύο γυάλινα ομόκεντρα κυλινδρικά δοχεία που επικοινωνούν μεταξύ τους με λεπτό σωλήνα (διαμέτρου 0,4cm) ενώ ταυτόχρονα διαθέτουν και έναν επιπλέον σωλήνα (διαμέτρου 0,4cm) για την έξοδο του διαλύματος, μετά την ανάδευση που υπόκειται. Μαγνητικός αναδευτήρας Techne MS1. Μαγνήτης μήκους 1 cm. Δεξαμενή ηλεκτροφόρησης: Χρησιμοποιήθηκε δεξαμενή διαστάσεων 20x28x30cm χωρητικότητας 7 lt διαλύματος ηλεκτροφόρησης δυο πηκτωμάτων ταυτόχρονα (Εικ. 16). Εικόνα 16. Ζεύγος τζαμιών που χρησιμοποιούνται για την παρασκευή πηκτώματος Συσκευή ηλεκτροφόρησης από plexiglas διαστάσεων: 22 cm x 20 cm x 8 81
82 cm. Στο πάνω τμήμα της συσκευής βρίσκεται η κάθοδος και στο κάτω η άνοδος (Εικ. 17Α, Β). α Α Β Εικόνα 17Α. Εξοπλισμός για την παρασκευή πηκτώματος. Β. Σχηματική απεικόνιση της δεξαμενής ηλεκτροφόρησης Αντιδραστήρια Ακρυλαμίδη (CH 2 =CH-CO-NH 2 ) (Invitrogen) Ν, Ν μεθυλέν δις ακρυλαμίδη (Invitrogen) Ουρία (NH 2 CONH 2 ) (Applichem) Φορμαμίδιο (HCONH 2 ) (Invitrogen) TEMED (Applichem) Υπερθεϊικό αμμώνιο (APS) (Gimco BRL) Tris HCl (Invitrogen) EDTA Na 2 (αιθυλενοδιαμινοτετραοξικό οξύ) (Applichem) Οξικό ΝΑ (Applichem) Οξικό οξύ (CH 3 COOH) (Aplichem) Mixed Bed Resin AG 501-X8 (BIORAD) Ficoll-400 (Applichem) Bromophenol Blue (BB) (BDH Electran) Xylene cyanol (XC, FF), C 6 H 4 (CH 3 ) 2 (BDH Electran) Διάλυμα Διμεθυλοχλωροσιλάνη (BDH GPR) 82
83 Βρωμιούχο αιθίδιο (Aplichem) Απόλυτη Αιθανόλη (CH 3 CH 2 OH) (Panreac) Διαλύματα 1. Ρυθμιστικό διάλυμα ηλεκτροφόρησης ΤΑΕ (Tris EDTA Οξικό οξύ), ph=8,0 Παρασκευάζεται σε συγκέντρωση 20Χ. Για την παρασκευή 1l t διαλύματος απαιτούνται: - Tris (0,8 M) : g - Na 2 EDTA (0,02 M) : g - Na 2 acetate (0,4 M) : g Γίνεται ρύθμιση του pη με πυκνό οξικό οξύ μέχρι pη=8,0 (36 ml) συμπληρώνεται ο όγκος με Η20 μέχρι 1lt και ακολουθεί διήθηση 2. Διάλυμα ακρυλαμίδης 40% κ.β. (διάλυμα stock). Για παρασκευή 500 ml διαλύματος απαιτούνται: - Ακρυλαμίδη : 200 g - Ν, Ν' μεθυλέν δις ακρυλαμίδη: 5.35 g (ακρυλαμίδη : δις ακρυλαμίδη = 37.5 : 1) Συμπληρώνεται ο όγκος με Η 2 0 μέχρι 500 ml, ακολουθεί διήθηση % αποδιατακτικό διάλυμα (stock διάλυμα) Για παρασκευή 500 ml απαιτούνται: - Ακρυλαμίδη (6%) : 75 ml από το 40% stock - Ουρία (5.6 Μ) : 170 g - Φορμαμίδιο (32%) : 160 ml (απιονισμός με ρητίνη : 2 g ρητίνης/100 ml διαλύματοςανάδευση 30 min-φιλτράρισμα) - ΤΑΕ (IX) : 25 ml από το stock 20Χ Συμπληρώνεται ο όγκος με Η 2 Ο μέχρι 500ml, ακολουθεί διήθηση. 4. 0% αποδιατακτικό διάλυμα (stock διάλυμα) Για παρασκευή 500 ml απαιτούνται: 83
84 - Ακρυλαμίδη (6%): 75 ml από το 40% stock - ΤΑΕ (IX): 25 ml από το stock 20X - Συμπληρώνεται ο όγκος με Η 2 0 μέχρι 500 ml, ακολουθεί διήθηση 5. Διάλυμα υπερθεϊκού αμμωνίου (APS) 10% Για 10 ml διαλύματος απαιτείται διάλυση 1 g APS σε 10 ml Η TEMED 7. Διάλυμα βρωμιούχου αιθιδίου 0,5 μg/ml 8. Διάλυμα χρωστικής (loading buffer) % μπλε της βρωμοφαινόλης % κυανούν του ξυλένιου - 15% Ficoll σε ddη Παρασκευή πηκτώματος - Πολυμερισμός Όπως έχει ήδη αναφερθεί χρησιμοποιούνται αποδιατακτικά πηκτώματα ακρυλαμίδης που περιέχουν διαβάθμιση συγκέντρωσης ουρίας και φορμαμίδιου, αυξανόμενης από την κορυφή προς τη βάση. Στα συγκεκριμένα πηκτώματα μπορεί να ηλεκτροφορηθεί μεγάλος αριθμός δειγμάτων. Για την παρασκευή του πηκτώματος ακολουθούνται τα εξής βήματα: Προσεκτική πλύση με σαπούνι, νερό και αλκοόλη των δύο τζαμιών που χρησιμοποιούνται και προσεκτικό στέγνωμα τους ώστε να είναι εύκολη η αποκόλληση του πηκτώματος και η παρατήρηση του. Ένωση των δύο τζαμιών μεταξύ τους με τοποθέτηση των spacers μεταξύ τους και στεγανοποίηση τους με κάλυψη τους μ ε ταινία στις τρεις πλευρές τους. Τοποθέτηση του ζεύγους των τζαμιών σε κατακόρυφη θέση. Προετοιμασία 5 ml διαλύματος 80% αποδιατακτικού και προσθήκη 80 μl APS 10% και 12 μl TEMED. Το διάλυμα αναδεύεται και χύνεται με πιπέτα Pasteur ανάμεσα στα δυο τζάμια. Σχηματίζεται έτσι μια ζώνη πηκτώματος ύψους 2 cm περίπου στο τέλος των δυο τζαμιών που χρησιμεύει ως επιπλέον προστασία για αποφυγή τυχόν διαρροών του διαλύματος ακρυλαμίδης. Χρόνος πολυμερισμού της ζώνης πηκτώματος περίπου 30 λεπτά. Προσεκτική τοποθέτηση της χτένας ανάμεσα στα δυο τζάμια, σε βάθος περίπου 1,5 cm, κατά τέτοιο τρόπο ώστε να μπορεί να διαφύγει ο αέρας. 84
85 Τοποθέτηση του σωλήνα εξόδου της συσκευής παρασκευής του πηκτώματος ανάμεσα στα δυο τζάμια (η συσκευή πρέπει να είναι απόλυτα καθαρή και στεγνή). Παρεμπόδιση της ροής στο σωλήνα εξόδου και στο συνδετικό σωλήνα μεταξύ των δύο τμημάτων της συσκευής με την παρεμβολή κατάλληλων σφιγκτήρων. Κατασκευή των δύο διαλυμάτων αποδιατακτικών παραγόντων που αντιστοιχούν στις ακραίες τιμές της επιθυμητής κλί σης συγκέντρωσης αποδιατακτικού. Κάθε διάλυμα αποδιατακτικού παρασκευάζεται μετά από ανάμειξη των δύο stock διαλυμάτων αποδιατακτικού (80% και 0%) σε κατάλληλες αναλογίες. Προετοιμασία 16 ml από το κάθε διάλυμα και προσθήκη στο καθένα 120 μl APS 10% (αντιστοιχεί περίπου σε 1/100 του όγκου του διαλύματος) και 14 μl TEMED (αντιστοιχεί περίπου σε 1/2000 του όγκου του διαλύματος). Μετά την παρασκευή των διαλυμάτων των αποδιατακτικών παραγόντων ακολουθεί γρήγορη ανάδευση τους και μεταφορά τους στη συσκευή παραγωγής πηκτώματος με κλίση αποδιατακτικού παράγοντα. Το διάλυμα με τη μεγαλύτερη συγκέντρωση αποδιατακτικής ουσίας τοποθετείται στον εσωτερικό κύλινδρο, ενώ στο εξωτερικό δοχείο τοποθετείται το διάλυμα μικρότερης συγκέντρωσης. Απελευθέρωση της ροής στο σωλήνα της εξόδου, μέχρι να γεμίσει με διάλυμα, και στη συνέχεια κλείνεται ξανά. Κατόπιν, ελευθερώνεται η ροή των δύο κυλινδρικών δοχείων, ενώ ταυτόχρονα αρχίζει η ανάδευση του διαλύματος στον εσωτερικό κύλινδρο, με τη βοήθεια μικρού μαγνήτη. Μόλις παρατηρηθεί ανάμειξη μεταξύ των δύο διαλυμάτων διαφορετικής συγκέντρωσης, ελευθερώνεται η ροή στο σωλήνα εξόδου και διοχετεύεται ανάμεσα στα δύο τζάμια. Προκύπτει τελικά το διάλυμα ακρυλαμίδης με διαβάθμιση συγκέντρωσης αποδιατακτικών παραγόντων. Η διαδικασία διαρκεί περίπου 5-10 λεπτά. Το πήκτωμα αφήνεται να πολυμεριστεί περίπου 1 ώρα και μπορεί να ηλεκτροφορηθεί 1 ώρα μετά την παρασκευή του ή να φυλαχθεί στους 4 C για 1 ή 2 μέρες. 85
86 Ηλεκτροφόρηση πηκτώματος Μετά την ολοκλήρωση του πολυμερισμού, ακολουθεί προσεκτι κή αφαίρεση της χτένας και αποκάλυψη των θέσεων φόρτωσης των δειγμάτων. Το πήκτωμα πολυακρυλαμίδης τοποθετείται στη δεξαμενή η οποία περιέχει ρυθμιστικό διάλυμα ηλεκτροφόρησης ΤΑΕ IX. Οι θέσεις φόρτωσης των δειγμάτων καθαρίζονται των δειγμάτων με ρυθμιστικό διάλυμα (με τη βοήθεια σύριγγας), ώστε να απομακρυνθεί η ουρία και η μη πολυμερισμένη ακρυλαμίδη. Τα δείγματα που πρόκειται να ηλεκτροφορηθούν, είναι προϊόντα PCR που παρασκευάζονται, όπως αναφέρθηκε παραπάνω. Σε κάθε δείγμα, προστίθενται 2-5 μl πυκνής χρωστικής (1μl χρωστικής/10 μl διαλύματος DNA). Σε κάθε ηλεκτροφόρηση χρησιμοποιούνται μl προϊόντος PCR. Η τοποθέτηση κάθε δείγματος στην αντίστοιχη θέση στην κορυφή του πηκτώματος, γίνεται με ειδικά tips (duck-bill tips). Η ηλεκτροφόρηση διαρκεί 16 ώρες, και πραγματοποιείται σε τάση 50 Volts (αντιστοιχεί σε ένταση ρεύματος περίπου 30 ma). Εναλλακτικά, μπορεί να χρησιμοποιηθεί η ηλεκτροφόρηση σε 160 Volts (διάρκεια 5 ώρες) Ανάλυση της πρωτοταγούς αλληλουχίας βάσεων (SEQUENCING) Αναλύσαμε την αλληλουχία των περιοχών που ενισχύθηκαν επιλεκτικά με αλυσιδωτή αντίδραση πολυμεράσης (PCR). Το πρωτόκολλο που ακολουθήθηκε είναι το εξής: Το προϊόν PCR καθαρίστηκε με το Qiaquick PCR purification kit σύμφωνα με τις οδηγίες του κατασκευαστή και ηλεκτροφορήθηκε παρουσία μάρτυρα γνωστού μεγέθους και μοριακού βάρους (100bp, New England Biolabs) σε πήκτωμα αγαρόζης 3%. Με βάση το μοριακό βάρος (ng) κάθε ζώνης του μάρτυρα εκτιμήθηκε η συγκέντρωση των καθαρισμένων προϊόντων PCR. Στη συνέχεια, ποσότητα του καθαρισμένου προϊόντος PCR ενισχύθηκε επιλεκτικά με κατάλληλα σημασμένους εκκινητές για να αναλυθεί στη συνέχεια. 86
87 ΑΝΤΙΔΡΑΣΤΗΡΙΑ Καθαρισμένο Seguencing mix Εκκινητές H 2 O PCR (ABI BigDye Terminators) 2F/2R ΟΓΚΟΣ/ ΔΕΙΓΜΑ x * 4 μl 1 μl y * x * η ποσότητα (ng) που πρέπει να βάλω από το συγκεκριμένο προϊόν PCR στην αντίδραση ανάλογα με πυκνότητα του δείγματος για να διαβάσει τη συγκεκριμένη αλληλουχία, σύμφωνα με τον κανόνα ng=0,1 x bp που προτείνεται. y * η ποσότητα νερού έτσι ώστε να έχουμε να τελικό όγκο αντίδρασης 10μl Οι συνθήκες της PCR είναι: 95 ο C 20 δευτερόλεπτα, στάδιο αποδιάταξης 50 ο C 15 δευτερόλεπτα, στάδιο υβριδοποίησης x 25 κύκλοι 60 ο C 60 δευτερόλεπτα, στάδιο επιμήκυνσης Ακολουθεί Kαθαρισμός των αντιδράσεων με Sephadex ως εξής: Παρασκευή διαλύματος Sephadex : Διαλύω 0,5gr σε 8ml dd H 2 Ο Aναδεύω 30 λεπτά σε πάγο. Καθαρισμός με Sephadex: Μεταφέρω μl υγρού Sephadex σε στήλη. Φυγοκεντρώ για 3 λεπτά στις 3470rpm στους 8 ο C. Πετάω το νερό που έχει περάσει από τη στήλη και η στήλη είναι έτοιμη. Φορτώνω προσεκτικά 10μl του PCR στη στήλη και αφήνω για 15 λεπτά στον πάγο και σε σκοτάδι. Φυγοκεντρώ για 3 λεπτά στις 3470rpm στους 8 ο C. Μετά τον καθαρισμό φορτώνω το προϊόν που εκλούεται από τη στήλη σε πλάκα 96 θέσεων και το τοποθετώ σε αναλυτή Megabase 1000 Amersham. 87
88 2.4. Μελέτη σε μοριακό επίπεδο της δβ-μεσογειακής Αναιμίας (δβ-μα) της μεθόδου Η φαινοτυπική εικόνα των δειγμάτων της δβ-μα μελετήθηκε σε μοριακό επίπεδο με την τεχνική PCR (GAP-PCR Craig et al 1994). Βασίζεται στον εκλεκτικό πολλαπλασιασμό τμημάτων DNA διαφορετικών σε μέγεθος (φυσιολογικό ή μη χρωμόσωμα). Η επεξεργασία γίνεται με τρεις εκκινητές, ανά ζεύγη (π.χ. Α, Β και Α, C). Για το φυσιολογικό χρωμόσωμα από τη χρήση των εκκινητών Α και Β προκύπτει προϊόν PCR, ενώ από τη χρήση των εκκινητών Α και C δεν προκύπτει προϊόν PCR, λόγω της μεταξύ τους απόστασης. Για το χρωμόσωμα με έλλειψη για τη δβ-μα, με τους εκκινητές Α και C παίρνουμε προϊόν PCR, ενώ με τους εκκινητές Α και Β όχι, επειδή λόγω της έλλειψης δε λειτουργεί η συμπληρωματική αλληλουχία του εκκινητή Β Πρωτόκολλο εκτέλεσης της αλυσιδωτής αντίδρασης πολυμεράσης για δβ-μεσογειακή Αναιμία (δβ-μα) δβ-μα Σικελικού τύπου 1. Σε αποστειρωμένο σωληνάριο eppendorf τοποθετούμε 6 μl διαλύματος DNA (1,5-3 μgr γενωμικού DNA) 2. Παρασκευάζουμε στη συνέχεια διάλυμα (mix) προσθέτοντας διαδοχικά: - 10 Χ buffer τελικής συγκέντρωσης 1 X = 5,0 μl - διάλυμα Μg Cl 2 τελικής συγκέντρωσης 2,5 mm = 2,5 μl - διάλυμα W-1 τελικής συγκέντρωσης 0,05% = 2,5 μl - 12,5 pmoles εκκινητή δβ-sic = 3,0 μl - 2 mμ d NTP s = 0,5 μl - 1 u Taq πολυμεράση = 0,5 μl Συνολικός όγκος διαλύματος (mix) =14,0 μl Τα υλικά κρατούνται σε πάγο, σε όλη τη διάρκεια της διαδικασίας. 88
89 3. Το παραπάνω διάλυμα προστίθεται στο eppendorf μαζί με τα 6 μl διαλύματος DNA και ο όγκος συμπληρώνεται με dd H 2 O ώστε να έχουμε τελικό όγκο 50 μl (προσθέτουμε δηλαδή 30 μl dd H 2 O). 4. Σε αρνητικό μάρτυρα, που δεν περιέχει DNA, συμπληρώνουμε αντίστοιχα με 36 μl dd H 2 O σε eppendorf με 14 μl διαλύματος (mix) δβ-μα Τουρκικού τύπου Α ή Β (οι αναλογίες είναι ίδιες) 1. Σε αποστειρωμένο σωληνάριο eppendorf τοποθετούμε 4 μl διαλύματος DNA (1-2 μgr γενωμικού DNA) 2. Παρασκευάζουμε στη συνέχεια διάλυμα (mix) για δβ-μα Turk ή δβ-ma Turk Β προσθέτοντας διαδοχικά: - 10 Χ buffer τελικής συγκέντρωσης 1 X = 5,0 μl - διάλυμα Μg Cl 2 τελικής συγκέντρωσης 2,5 mm = 2,5 μl - διάλυμα W-1 τελικής συγκέντρωσης 0,05% = 2,5 μl - 12,5 pmoles εκκινητών δβ-turk A ή δβ-turk B = 1,0 μl - 2 mμ d NTP s = 0,5 μl - 1 u Taq πολυμεράση = 0,5 μl Συνολικός όγκος διαλύματος (mix) =12,0 μl Τα υλικά κρατούνται σε πάγο, σε όλη τη διάρκεια της διαδικασίας. 3. Το παραπάνω διάλυμα προστίθεται στο eppendorf μαζί με τα 4 μl διαλύματος DNA και ο όγκος συμπληρώνεται με dd H 2 O ώστε να έχουμε τελικό όγκο 50 μl (προσθέτουμε δηλαδή 34 μl dd H 2 O). 4. Σε αρνητικό μάρτυρα συμπληρώνουμε αντίστοιχα με 38 μl dd H 2 O σε eppendorf με 14 μl διαλύματος (mix). Τα παραπάνω δείγματα τοποθετούνται σε θερμοκυκλοποιητές, για πραγματοποίηση της αντίδρασης πολυμερισμού in vitro. Χρησιμοποιήθηκ ε το μηχάνημα: MJ Research PTC-200, Peltier Thermal cycler. 89
90 Τα προγράμματα που χρησιμοποιούνται είναι τα εξής: δβ-μα Σικελικού τύπου STEP-1: STEP-2: STEP-3: STEP-4: STEP-5: STEP-6: 94 C για 5 min. 94 C για 1 min (αποδιάταξη). 60 C για 1 min (πρόσδεση εκκινητή). 72 C για 1,5 min (επιμήκυνση). Επαναλαμβάνουμε τα βήματα 2,3,4 για 30 φορές 72 C για 10 min. STEP-7: 4 C για 24 h. δβ-μα Τουρκικού τύπου Α STEP-1: STEP-2: STEP-3: STEP-4: STEP-5: STEP-6: 94 C για 5 min. 94 C για 1 min (αποδιάταξη). 65 C για 1 min (πρόσδεση εκκινητή). 72 C για 1 min (επιμήκυνση). Επαναλαμβάνουμε τα βήματα 2,3,4 για 30 φορές 72 C για 10 min. STEP-7: 4 C για 24 h. δβ-μα Τουρκικού τύπου Β STEP-1: STEP-2: STEP-3: STEP-4: STEP-5: STEP-6: 94 C για 5 min. 94 C για 1 min (αποδιάταξη). 57 C για 1 min (πρόσδεση εκκινητή). 72 C για 1 min (επιμήκυνση). Επαναλαμβάνουμε τα βήματα 2,3,4 για 30 φορές 72 C για 10 min. STEP-7: 4 C για 24 h. 90
91 Στο τέλος της εκλεκτικής ενίσχυσης, τα προϊόντα ελέγχονται σε πήκτωμα αγαρόζης 3%, που περιέχει βρωμιούχο αιθίδιο σε συγκέντρωση 0,5 μ g/ml. Η αξιολόγηση του μεγέθους των ζωνών, της ηλεκτροφόρησης των προϊόντων PCR, γίνεται με σύγκριση με το DNA μάρτυρα που ηλεκτροφορείται παράλληλα. Η νουκλεοτιδική αλληλουχία των παραπάνω εκκινητών είναι: δβ-σικελικού Τύπου: 5 -ΤΤgggTTTCTgATAggCACTg-3 5 -gtgtcacccattaatgccttgtac-3 5 -TAgATCCCTTTgCCATTATg-3 δβ-τουρκικού Τύπου: 5 -gacacacatgacagaacagccaat-3 5 -gaagagcaggtaaaagaacc-3 5 -TTCCACTATCTTACTTACACAT-3 5 -CAAAgCAgCAATACTAAACAggAg-3 5 -TgCTgAggATTgTTTAggTC-3 5 -gaatagcagtggtgagagag Μελέτη σε μοριακό επίπεδο της HPFH - Εκλεκτικός πολλαπλασιασμός των αλληλουχιών των Αγ- και Gγ- γονιδίων Οι υποκινητές των δύο γονιδίων της σφαιρίνης μελετήθηκαν προκειμένου να ανιχνευτούν αλλαγές στην αλληλουχία τους, όπως μεταλλαγές που προκαλούν HPFH φαινότυπο ή πολυμορφισμούς που δίνουν διαφορετικούς απλότυπους. Τα δύο γονίδια παρουσιάζουν εκτεταμένη ομολογία στην αλληλουχία τους. Η μοριακή μελέτη των γονιδίων αυτών πραγματοποιήθηκε σε όλα τα δείγματα, δηλαδή: Στην δβ-μα, τη β-μα με αυξημένα επίπεδα HbF καθώς και στην HPFH. 91
92 Ο προσδιορισμός της μοριακής βλάβης διερευνήθηκε ενισχύοντας με PCR την περιοχή του υποκινητή των Αγ- και Gγ- γονιδίων. Αρχικά με τους πρώτους εκκινητές πολλαπλασιάσαμε ένα μεγά λο τμήμα τους και στη συνέχεια 1 μl από το προϊόν αυτό της PCR πολλαπλασιάστηκε για τη δεύτερη αντίδραση PCR με δύο άλλους εκκινητές αντίστοιχα. α. Το Αγ- γονίδιο στην 5 περιοχή, αρχικά ενισχύεται με τους εκκινητές: γ 4 - GCγ 4 681bp και στη συνέχεια με τους εκκινητές: γ 4 -γ 6 -GCγ 4 (327 bp). β. Το Gγ- γονίδιο, στην 5 περιοχή, ενισχύεται με τους εκκινητές: γ 1 -GCγ 4 (678 bp) και στη συνέχεια με τους εκκινητές: γ 1 -γ 6 -GCγ 4 (327 bp). γ. Η περιοχή του 3 άκρου του Αγ- γονιδίου ενισχύεται με τους εκκινητές: γ 7 /αγ 7 και στη συνέχεια το PCR προϊόν επωάζεται με το ένζυμο DdeΙ. Στη συνέχεια έγινε ανάλυση της νουκλεοτιδικής αλληλουχίας του προϊόντος PCR (Sequencing). Η νουκλεοτιδική αλληλουχία των παραπάνω εκκινητών είναι: Gamma 4: 5 - ACTgTggTCTTTATgAAAATTgT-3 Gamma 1: 5 - ACTgTTgCTTTATAggAT-3 GC gamma 4: 5 - gcgggcggggcgggggcacggggggcgcgggcggggcctcagac gttccagaagcga-3 Gamma 6: 5 - gactgaatcggaacaaggcaa Το πρωτόκολλο των αντιδράσεων PCR για τον εκλεκτικό πολλαπλασιασμό των Αγ- και Gγ- γονιδίων είναι: Α. Για το Αγ- γονίδιο στην 5 περιοχή (681 bp) 1. Σε αποστειρωμένο σωληνάριο eppendorf τοποθετούμε 5 μl διαλύματος DNA 2. Παρασκευάζουμε στη συνέχεια διάλυμα (mix) προσθέτοντας διαδοχικά: - 10 Χ buffer = 10,0 μl - Μg Cl 2 = 4,0 μl - W-1 % = 5,0 μl 92
93 - γ 4 = 2,0 μl - GCγ 4 = 2,0 μl - dntp S = 2,0 μl - Taq πολυμεράση = 0,5 μl Συνολικός όγκος διαλύματος (mix) = 25,5 μl Σε όλη τη διάρκεια της διαδικασίας, τα υλικά κρατούνται σε πάγο. 3. Το παραπάνω διάλυμα προστίθεται στο eppendorf μαζί με τα 5 μl διαλύματος DNA και ο όγκος συμπληρώνεται με dd H 2 O ώστε να έχουμε τελικό όγκο 100 μl (προσθέτουμε δηλαδή 69,5 μl dd H 2 O). 4. Σε αρνητικό (Negative) μάρτυρα, χωρίς DNA, συμπληρώνουμε αντίστοιχα με 74,5 μl dd H 2 O σε eppendorf με 25,5 μl διαλύματος (mix). 5. Ακολουθεί ανάδευση σε vortex και φυγοκέντρηση για 1 min. Τα δείγματα τοποθετούνται σε θερμοκυκλοποιητή για την αντίδραση PCR και το πρόγραμμα που ακολουθούμε για την αντίδραση είναι: STEP-1: STEP-2: STEP-3: STEP-4: STEP-5: STEP-6: 94 C για 5 min. 94 C για 1 min (αποδιάταξη). 45 C για 0,5 min (πρόσδεση εκκινητή). 60 C για 2 min (επιμήκυνση). Επαναλαμβάνουμε τα βήματα 2,3,4 για 35 φορές 72 C για 10 min. STEP-7: στους 4 C για h. Το προϊόν ελέγχεται σε πήκτωμα αγαρόζης 2% παρουσία μάρτυρα γνωστού μεγέθους (Εικ. 18, 19). 93
94 Μ Ν Εικόνα 18. Επιλεκτική ενίσχυση τμήματος της 5 περιοχής του Αγ γονιδίου με χρήση εκκινητών γ4-gcγ4 (681 bp) (Ν: αρνητικός μάρτυρας, Μ: μάρτυρας γνωστού μεγέθους 100 bp, New England Biolabs) Ν Μ Εικόνα 19. Επιλεκτική ενίσχυση τμήματος της 5 περιοχής του Αγ γονιδίου με χρήση εκκινητών γ4-gcγ4 (681 bp) (Ν: αρνητικός μάρτυρας, Μ: μάρτυρας γνωστού μεγέθους 100 bp, New England Biolabs) 94
95 Α 1. Για εσωτερικά τμήματα του Αγ- γονιδίου στην 5 περιοχή (327 bp) 1. Σε αποστειρωμένο σωληνάριο eppendorf τοποθετούμε 2 μl διαλύματος DNA από το προηγούμενο προϊόν PCR product. 2. Παρασκευάζουμε στη συνέχεια διάλυμα (mix) προσθέτοντας διαδοχικά: - 10 Χ buffer = 10,0 μl - Μg Cl 2 = 5,0 μl - W-1 % = 5,0 μl - γ 6 = 4,0 μl - GCγ 4 = 4,0 μl - dntp S = 2,0 μl - Taq πολυμεράση = 0,5 μl Συνολικός όγκος διαλύματος (mix) = 30,5 μl Σε όλη τη διάρκεια της διαδικασίας, τα υλικά κρατούνται σε πάγο. 3. Το παραπάνω διάλυμα προστίθεται στο eppendorf μαζί με τα 2 μl διαλύματος DNA και ο όγκος συμπληρώνεται με dd H 2 O ώστε να έχουμε τελικό όγκο 100 μl (προσθέτουμε δηλαδή 67,5 μl dd H 2 O). 4. Σε αρνητικό μάρτυρα συμπληρώνουμε αντίστοιχα με 69,5 μl dd H 2 O σε eppendorf με 30,5 μl διαλύματος (mix). 5. Ακολουθεί ανάδευση σε vortex και φυγοκέντρηση για 1 min. Τα δείγματα τοποθετούνται σε θερμοκυκλοποιητή για την αντίδραση PCR, και το πρόγραμμα που ακολουθούμε για την αντίδραση είναι: STEP-1: STEP-2: STEP-3: STEP-4: STEP-5: STEP-6: 94 C για 5 min. 94 C για 1 min (αποδιάταξη). 60 C για 0,5 min (πρόσδεση εκκινητή). 72 C για 2 min (επιμήκυνση). Επαναλαμβάνουμε τα βήματα 2,3,4 για 26 φορές 72 C για 10 min. STEP-7: στους 4 C για 24 h. 95
96 Το προϊόν ελέγχεται σε πήκτωμα αγαρόζης 2% και μάρτυρα γνωστού μεγέθους (100bp, New England Biolabs) (Εικ. 20) N M Εικόνα 20. Επιλεκτική ενίσχυση εσωτερικού τμήματος της 5 περιοχής του Gγ γονιδίου με χρήση εκκινητών γ4-γ6-gcγ4 (327 bp) (Ν: αρνητικός μάρτυρας, Μ: μάρτυρας γνωστού μεγέθους 100 bp, New England Biolabs) Β. Για το Gγ- γονίδιο στην 5 περιοχή (678 bp) 1. Σε αποστειρωμένο σωληνάριο eppendorf τοποθετούμε 5 μl διαλύματος DNA 2. Παρασκευάζουμε στη συνέχεια διάλυμα (mix) προσθέτοντας διαδοχικά: - 10 Χ buffer = 10,0 μl - Μg Cl 2 = 4,0 μl - W-1 % = 5,0 μl - γ 1 = 6,0 μl - GCγ 4 = 2,0 μl - dntp S = 2,0 μl - Taq πολυμεράση = 0,5 μl Συνολικός όγκος διαλύματος (mix) = 29,5 μl Σε όλη τη διάρκεια της διαδικασίας, τα υλικά κρατούνται σε πάγο. 3. Το παραπάνω διάλυμα προστίθεται στο eppendorf μαζί με τα 5 μl 96
97 διαλύματος DNA και ο όγκος συμπληρώνεται με dd H 2 O ώστε να έχουμε τελικό όγκο 100 μl (προσθέτουμε δηλαδή 65,5 μl dd H 2 O). 4. Σε αρνητικό μάρτυρα, συμπληρώνουμε αντίστοιχα με 70,5 μl dd H 2 O σε eppendorf με 29,5 μl διαλύματος (mix). 5. Ακολουθεί ανάδευση σε vortex και φυγοκέντρηση για 1 min. Τα δείγματα τοποθετούνται σε θερμοκυκλοποιητή για την αντίδραση PCR, και το πρόγραμμα που ακολουθούμε για την αντίδραση είναι: STEP-1: STEP-2: STEP-3: STEP-4: STEP-5: STEP-6: 94 C για 5 min. 94 C για 1 min (αποδιάταξη). 45 C για 0,5 min (πρόσδεση εκκινητή). 60 C για 2 min (επιμήκυνση). Επαναλαμβάνουμε τα βήματα 2,3,4 για 35 φορές 72 C για 10 min. STEP-7: στους 4 C για 24 h. Το προϊόν ελέγχεται σε πήκτωμα αγαρόζης 2% παρουσία μάρτυρα γνωστού μεγέθους (Εικ. 21) Μ Ν Εικόνα 21. Επιλεκτική ενίσχυση τμήματος της 5 περιοχής του Gγ γονιδίου με χρήση εκκινητών γ1-gcγ4 (678 bp) (Ν: αρνητικός μάρτυρας, Μ: μάρτυρας γνωστού μεγέθους 100 bp, New England Biolabs). 97
98 Β 1. Για τα εσωτερικά τμήματα του Gγ- γονιδίου στην 5 περιοχή (327 bp) Ακολουθούμε πανομοιότυπη πορεία όπως και στα εσωτερικά τμήματα του Αγ- γονιδίου στην 5 περιοχή (Εικ. 22) Ν Μ Εικόνα 22. Επιλεκτική ενίσχυση εσωτερικού τμήματος της 5 περιοχής του Gγ γονιδίου με χρήση εκκινητών γ1-γ6-gcγ4 (327 bp) (Ν: αρνητικός μάρτυρας, Μ: μάρτυρας γνωστού μεγέθους 100 bp, New England Biolabs). Γ. Για το Αγ- γονίδιο στην 3 περιοχή (681 bp) 1. Σε αποστειρωμένο σωληνάριο eppendorf τοποθετούμε 5 μl διαλύματος DNA 2. Παρασκευάζουμε στη συνέχεια διάλυμα (mix) προσθέτοντας διαδοχικά: - 10 Χ buffer = 5,0 μl - Μg Cl 2 = 2,5 μl - W-1 % = 2,5 μl - γ 7 = 2,0 μl - αγ 7 = 2,0 μl - dntp S = 1,5 μl - Taq πολυμεράση = 0,5 μl Συνολικός όγκος διαλύματος (mix) =16,0 μl Σε όλη τη διάρκεια της διαδικασίας, τα υλικά κρατούνται σε πάγο. 98
99 3. Το παραπάνω διάλυμα προστίθεται στο eppendorf μαζί με τα 5 μl διαλύματος DNA και ο όγκος συμπληρώνεται με dd H 2 O ώστε να έχουμε τελικό όγκο 50 μl (προσθέτουμε δηλαδή 29 μl dd H 2 O). 4. Σε αρνητικό (Negative) μάρτυρα, χωρίς DNA, συμπληρώνουμε αντίστοιχα με 34 μl dd H 2 O σε eppendorf με 16 μl διαλύματος (mix). 5. Ακολουθεί ανάδευση σε vortex και φυγοκέντρηση για 1 min. Τα δείγματα τοποθετούνται σε θερμοκυκλοποιητή για την αντίδραση PCR, και το πρόγραμμα που ακολουθούμε για την αντίδραση είναι: STEP-1: STEP-2: STEP-3: STEP-4: STEP-5: STEP-6: 94 C για 5 min. 94 C για 1 min (αποδιάταξη). 57 C για 1 min (πρόσδεση εκκινητή). 72 C για 1 min (επιμήκυνση). Επαναλαμβάνουμε τα βήματα 2, 3, 4 για 35 φορές 72 C για 10 min STEP-7: 4 C για 24 h. Το προϊόν ελέγχεται σε πήκτωμα αγαρόζης 2% και μάρτυρα γνωστού μεγέθους (Εικ. 23). Ακολουθεί πέψη του ανωτέρω προϊόντος PCR product με ένζυμο DdeΙ με την ακόλουθη διαδικασία (Εικ. 24, 25): 1. Σε αποστειρωμένο σωληνάριο eppendorf τοποθετούμε 30 μl διαλύματος DNA από το προηγούμενο προϊόν PCR product. 2. Παρασκευάζουμε στη συνέχεια διάλυμα (mix) προσθέτοντας διαδοχικά: - 10 Χ buffer = 6,0 μl - DdeI = 3,0 μl - ddh 2 O =21,0 μl Συνολικός όγκος διαλύματος (mix) =30,0 μl Σε όλη τη διάρκεια της διαδικασίας, τα υλικά κρατούνται σε πάγο. 3. Το παραπάνω διάλυμα προστίθεται στο eppendorf μαζί με τα 30 μl διαλύματος DNA και έτσι έχουμε τελικό όγκο 60 μl. 4. Σε αρνητικό μάρτυρα, χωρίς DNA, τοποθετούμε 30 μl dd H 2 O και 30 μl διαλύματος (mix). 99
100 5. Ακολουθεί ανάδευση σε vortex και φυγοκέντρηση για 1 min. 6. Τοποθετούμε τα δείγματα σε υδατόλουτρο στους 37 C για 24 h (overnight) Ν Μ Εικόνα 23. Επιλεκτική ενίσχυση τμήματος της 3 περιοχής του Αγ γονιδίου με χρήση εκκινητών γ7-αγ7 (681 bp) (Ν: αρνητικός μάρτυρας, Μ: μάρτυρας γνωστού μεγέθους φχ/haeiii, New England Biolabs). Μ Μ2 Εικόνα 24. Προιόν PCR της 3 περιοχής του Αγ γονιδίου που έχει υποστεί πέψη με DdeΙ ένζυμο (Δείγματα 1-10, Μ1: φχ/haeiii, Μ2: 100 bp, New England Biolabs) Εκτίμηση: 1, 2, 4, 9, 10, 11 (41883 C/A) 5, 7, 8 (41883 C/C) 3, 6 (41883 A/A). 100
101 Μ Μ2 Εικόνα 25. Προιόν PCR της 3 περιοχής του Αγ γονιδίου που έχει υποστεί πέψη με DdeΙ ένζυμο (Δείγματα 1-15, Μ1: φχ/haeiii, Μ2: 100 bp, New England Biolabs) Εκτίμηση: 1,2,4,5,6,7, 11, 14, 15 (41883C/A) 8 (41883A/A) - 3,9,10,12,13 (41883C/C) 101
102 102
103 3. ΑΠΟΤΕΛΕΣΜΑΤΑ 3.1. Αποτελέσματα σε φαινοτυπικό επίπεδο Αξιολόγηση των φαινοτυπικών (αιματολογικών-βιοχημικών κ.λπ.) δεδομένων (στα δείγματα της συγκεκριμένης εργασίας). Η μελέτη περιλαμβάνει 160 δείγματα ενηλίκων επιλεγμένα από το γενικό πληθυσμό των προσερχομένων στη Μ.Π.Μ.Α. (Μονάδα Πρόληψης Μεσογειακής Αναιμίας) του Γενικού Νοσοκομείου Καρδίτσας. Αυτά ταξινομήθηκαν στις κάτωθι κατηγορίες: 1. Ετεροζυγώτες (φορείς) δβ-μεσογειακής Αναιμίας 2. Ετεροζυγώτες (φορείς) HPFH. 3. Ετεροζυγώτες (φορείς) β-μεσογειακής Αναιμίας με αυξημένη HbF. Η κατηγοριοποίηση αυτή έγινε (όπως προαναφέρθηκε) με βάση: α. Τα αιματολογικά τους δεδομένα, (Hb, Hct, RBC, MCH, MCV, MCHC, RDW) β. Τη μορφολογία των ερυθροκυττάρων, αναζήτηση εγκλείστων κ.λπ. γ. Τον ποιοτικό έλεγχο των αιμοσφαιρινών (ηλεκτροφόρηση σε ταινίες οξεικής κυτταρίνης και κιτρικό άγαρ). δ. Τον ποσοτικό προσδιορισμό της αιμοσφαιρίνης Α 2 (%) με χρωματογραφία στηλών (στήλες DEAE) και της HbF (%), μέθοδος ΒΕΤΚΕ. ε. Τον ποσοτικό προσδιορισμό των αιμοσφαιρινών Α 2, F, S, A, D, (%) με χρωματογραφία στηλών υψηλής πιέσεως (HPLC). Στον Πίνακα 6, παρατίθενται τα αποτελέσματα των δειγμάτων 160 ατόμων, που μελετήθηκαν στην παρούσα διατριβή. 103
104 Πίνακας 6. Δείγματα ετεροζυγωτών, δβ-μα, β-μα με HbF και HPFH α/α ΦΥΛΟ ΔΙΑΓΝΩΣΗ Hb Hct RBC MCH MCV MCHC HbA 2 (%) σε στήλη DEAE HbF(%) μέθοδος ΒΕΤΚΕ HPLC Hb Hb Α 2 F (%) (%) HbA (%) DNA - PCR δβ-μα β-μα Aγ-γ 4 δβ- Turk δβ- Sic Αγγ 6-γ 4 Gγ-γ 1 Gγγ 6- γ 1 Αγ-ενισχ. (Αγ3 ) 1 Αρρεν HPFH Θήλυ HPFH C/C 3 Αρρεν HPFH C/A Αρρεν HPFH C/A 5 Αρρεν HPFH+β-ΜΑ β C/C 6 Θήλυ HPFH+δ-ΜΑ C/A Θήλυ HPFH C/A 8 Θήλυ HPFH C/A Αρρεν HPFH C/A 10 Αρρεν HPFH+β-ΜΑ β Nl Nl C/A 11 Θήλυ HPFH C/A Θήλυ HPFH Nl Nl Nl Nl C/C 13 Θήλυ HPFH Nl Nl C/A 14 Αρρεν HPFH+HbS / Nl C/A 15 Αρρεν β-μα F Nl Nl A/A 16 Θήλυ β-μα F IVS1-1 Nl Nl C/C 17 Θήλυ β-μα F FSC C/A Αρρεν β-μα F FSC-6 Nl Nl C/A Θήλυ β-μα F IVS1- Nl Nl C/A Θήλυ β-μα F IVS1-110 Nl Nl C/A 21 Άρρεν β-μα F β39 del4 del4 Nl Nl C/A 22 Θήλυ β-μα F IVS1-1 Nl Nl C/C 104
105 2 23 Θήλυ HPFH Nl Nl -158/ / Α/Α 24 Θήλυ δβ-μα Nl Nl Nl Nl C/Α 25 Θήλυ β-μα F β39 del4 del4 Nl Nl C/Α 26 Θήλυ β-μα F β39 Nl Nl Nl Nl C/C 27 Άρρεν δβ-μα del4 del4 Nl Nl C/Α 28 Άρρεν β-μα F IVS1-1 Nl Nl Nl Nl C/C 29 Άρρεν δβ-μα / / C/C - 30 Θήλυ δβ-μα del4 del4 Nl Nl C/Α 105
106 HPLC DNA-PCR α/α ΦΥΛΟ ΔΙΑΓΝΩΣΗ Hb Hct RBC MCH MCV MCHC HbA 2 Hβ Hb Hb HbF(%) Αγ- Gγγ 1 γ 6 -γ 1 (Αγ3 ) Gγ- Αγ-ενισχ (%) σε Α μέθοδος 2 F A δβ-μα β-μα Αγ-γ 4 γ στήλη (%) (%) (%) 6 -γ 4 BETKE DEAE δβ- δβ- Turk Sic 31 Θήλυ HPFH+β-ΜΑ IVS1-1 Nl Nl Nl Nl 41883C/C 32 Θήλυ δβ-μα Nl Nl Nl 41883C/C 33 Άρρεν δβ-μα Nl Nl C/A Άρρεν δβ-μα Nl Nl Nl Nl 41883C/C 35 Θήλυ β-μα F IVS Nl Nl 41883C/C +Cd2 36 Θήλυ δβ-μα del4 del4 Nl Nl 41883C/A 37 Θήλυ HPFH Nl Nl 41883C/C 38 Άρρεν δβ-μα del4 Nl Nl 41883C/A 39 Άρρεν δβ-μα Nl Nl Nl Nl 41883C/C 40 Άρρεν δβ-μα C/A Άρρεν δβ-μα del4 del4 Nl Nl 41883C/A 42 Θήλυ δβ-μα Nl Nl Nl Nl 41883C/A 43 Άρρεν δβ-μα del4 del4 - Nl 41883A/A Άρρεν δβ-μα del4 del A/A Άρρεν δβ-μα Nl Nl Nl Nl 41883C/A 46 Θήλυ δβ-μα Nl Nl 41883C/A 47 Άρρεν β-μα F I ΙVS2-745 Nl Nl C/A 158 +(πολ.+20) 48 Άρρεν δβ-μα del4 del4 Nl Nl 41883A/A 49 Θήλυ β-μα F IVS1-1 Nl Nl Nl Nl 41883C/C 50 Θήλυ β-μα IVS1-110 Nl Nl C/A Θήλυ δβ-μα del4 del4 Nl Nl 41883C/A 52 Άρρεν δβ-μα Nl Nl Nl Nl 41883A/A 53 Άρρεν δβ-μα Nl Nl Nl Nl 41883C/A 54 Άρρεν δβ-μα del4 del4 Nl Nl 41883C/A 55 Θήλυ δβ-μα del4 del A/A 106
107 56 Θήλυ β-μα F IVS1-1 Nl Nl C/A 57 Θήλυ β-μα F IVS1-110 Nl Nl C/A Θήλυ δβ-μα Nl Nl Nl Nl 41883C/C 59 Άρρεν β-μα F IVS1-1 Nl Nl C/A Θήλυ δβ-μα del4 del4 Nl Nl 41883C/A 107
108 α/α ΦΥΛΟ ΔΙΑΓΝΩΣΗ Hb Het RBC MCH MCV MCHC HbA 2 (%) σε στήλη DEAE HbF( %) μέθοδ ος BETK E HPLC Hβ Hb Α 2 F (%) (%) HbA (%) DNA-PCR δβ-μα β-μα Αγ-γ 4 Αγγ 6-γ 4 δβ- Turk δβ- Sic 61 Άρρεν δβ-μα Nl Nl Nl Nl 41883C/A 62 Θήλυ β-μα F β39+c d C/A 63 Θήλυ δβ-μα Nl Nl 41883C/A 64 Θήλυ HPFH A/A 65 Θήλυ β-μα F IVS1- Nl Nl 41883C/C Άρρεν β-μα F IVS1-110 Nl Nl 41883C/C 67 Άρρεν β-μα F IVS1-1 + Cd C/A 68 Θήλυ δβ-μα Nl Nl Nl Nl 41883C/C 69 Θήλυ β-μα F IVS1-110 Nl Nl 41883C/A 70 Άρρεν δβ-μα+δ-μα del4 del A/A 71 Άρρεν β-μα F β Άρρεν β-μα F IVS1-1 Nl Nl Nl Nl 41883C/C 73 Άρρεν HPFH Nl Nl 41883C/C 74 Άρρεν δβ-μα del4 del4 Nl Nl 41883C/A 75 Άρρεν δβ-μα del4 del4 Nl Nl 41883C/A 76 Θήλυ δβ-μα del4 del A/A 77 Θήλυ δβ-μα Nl Nl C/A 78 Άρρεν δβ-μα Nl Nl 41883C/A 79 Θήλυ δβ-μα+ δβμα Nl Nl Nl Nl 41883C/C 80 Άρρεν δβ-μα del4 del4 Nl Nl 41883C/A 81 Άρρεν δβ-μα Nl Nl C/A 82 Θήλυ δβ-μα del4 del A/A 83 Άρρεν β-μα F IVS2-1 [G>A] C/A 84 Θήλυ β-μα F IVS1-1 Nl Nl Nl Nl 41883C/C 85 Θήλυ β-μα F β39 Nl Nl C/A 86 Θήλυ δβ-μα Nl Nl 41883C/A 87 Θήλυ β-μα F Β39 del4 del4 Nl Nl 41883C/A 88 Θήλυ δβ-μα del4 del4 Nl Nl 41883C/A 89 Άρρεν δβ-μα del4 del4 Nl Nl 41883C/A Gγ-γ 1 Gγγ 6-γ 1 Αγ-ενισχ (Αγ3 ) 108
109 90 Θήλυ β-μα F IVS1-110 Nl Nl C/A 109
110 α/α ΦΥΛΟ ΔΙΑΓΝΩΣ Η Hb Het RBC MCH MCV MCHC HbA 2 (%) σε στήλη DEAE HbF(%) μέθοδος BETKE HPLC Hβ Hb Α 2 F (%) (%) Hb A (%) DNA-PCR δβ-μα β-μα Αγ-γ 4 Αγγ 6 -γ 4 Gγ-γ 1 Gγγ 6 -γ 1 Αγ-ενισχ (Αγ3 ) δβ- Turk δβ- Sic 91 Άρρεν HPFH Nl Nl 41883C/C 92 Άρρεν HPFH Nl Nl 41883C/C 93 Άρρεν δβ-μα del4 del A/A 94 Θήλυ δβ-μα Nl Nl Nl Nl 41883C/C 95 Άρρεν δβ-μα Nl Nl 41883C/A 96 Θήλυ β-μα F β A/A 97 Άρρεν β-μα F IVS1-1 Nl Nl C/A 98 Θήλυ β-μα F +a1cd14 [G>A] IVS1-1 Nl Nl C/A 99 Θήλυ HPFH δβ-μα 100 Άρρεν δβ-μα C/A 101 Θήλυ δβ-μα Nl Nl Nl Nl 41883C/C 102 Άρρεν β-μα F IVS2-1 Nl Nl C/A [G>A] 103 Θήλυ β-μα F β39 del4 del A/A 104 Άρρεν β-μα F β39+c Nl Nl C/A d2 105 Θήλυ β-μα F IVS1-1 Nl Nl Nl Nl 41883C/C 106 Άρρεν δβ-μα Nl Nl 41883C/A 107 Θήλυ β-μα F β39 Nl Nl C/C 108 Θήλυ δβ-μα IVS1-1 del4 del4 Nl Nl 41883C/A 109 Θήλυ HPFH+ δβ-μα del4/ -117 del4/- 117 Nl Nl 41883C/A 110 Θήλυ δβ-μα A/A 111 Άρρεν HPFH Nl Nl 41883C/C 112 Θήλυ HPFH+a1 Cd del4 del4 Nl Nl 41883C/A 113 Θήλυ β-μα F IVS1-1 del4 del4 Nl Nl 41883C/A 114 Θήλυ β-μα F IVS C/A 115 Θήλυ β-μα F IVS1-1 Nl Nl Nl Nl 41883C/C 116 Θήλυ δβ-μα del4 del4 Nl Nl 41883C/A 117 Θήλυ β-μα F IVS1-1 [G>A] Nl Nl C/A 118 Θήλυ δβ-μα Nl Nl Nl Nl 41883C/A 119 Θήλυ δβ-μα Nl Nl 41883C/A 120 Άρρεν HPFH Nl Nl -158/ / A/A 110
111 α/α ΦΥΛΟ ΔΙΑΓΝΩΣΗ Hb Het RBC MCH MCV MCHC HbA 2 (%) σε στήλη DEAE HbF(%) μέθοδο ς BETKE HβΑ 2 (%) HPLC HbF (%) HbA (%) DNA-PCR δβ-μα β-μα Αγ-γ 4 Αγγ 6-γ Άρρεν HPFH Nl -117 Nl Nl 41883C/C 122 Άρρεν β-μα F IVS Nl Nl C/A 123 Θήλυ β-μα F Nl Nl Nl Nl 41883C/C 124 Θήλυ HPFH Nl Nl 41883C/C 125 Θήλυ HPFH Nl Nl -158/ / 41883C/A Άρρεν β-μα F β3 9 Nl Nl 41883C/A 127 Άρρεν HPFH Nl Nl 41883C/A 128 Άρρεν β-μα F IVS C/C 129 Άρρεν HPFH C/A 130 Άρρεν HPFH Nl Nl -158/ -158/ 41883A/A Θήλυ HPFH Nl Nl -158/ / A/A 132 Θήλυ (β+δβ)μα β C/A 133 Θήλυ HPFH Nl Nl 41883C/C 134 Άρρεν HPFH C/A 135 Θήλυ HPFH+β-ΜΑ IVS C/C 136 Θήλυ HPFH Nl Nl Nl Nl 41883C/C 137 Θήλυ δβ-μα Nl Nl 41883C/A 138 Θήλυ δβ-μα Nl Nl Nl Nl 41883C/C 139 Άρρεν δβ-μα Nl Nl Nl Nl 41883A/A 140 Άρρεν β-μα F C/C 141 Άρρεν β-μα F IVS1-1 Nl Nl Nl Nl 41883C/C 142 Θήλυ δβ-μα del4 del4 Nl Nl 41883C/A 143 Θήλυ HPFH C/A 144 Θήλυ δβ-μα Nl Nl Nl Nl 41883A/A 145 Θήλυ β-μα F IVS1-1 Nl Nl Άρρεν β-μα F+ α IVS Nl Nl Nl 41883C/C ΜΑ(-3,7) 147 Άρρεν δβ-μα Nl Nl Nl Nl 41883C/C 148 Άρρεν β-μα F V FSC-6 Nl Nl Άρρεν δβ-μα Θήλυ δβ-μα A/A δβ- Turk δβ- Sic Gγ-γ 1 Gγγ 6- γ 1 Αγ-ενισχ (Αγ3 ) 111
112 α/α ΦΥΛΟ ΔΙΑΓΝΩΣΗ Hb Het RBC MCH MCV MCHC HbA 2 HbF(%) HPLC DNA-PCR (%) σε στήλη μέθοδος BETKE HβΑ 2 (%) HbF (%) HbA (%) δβ-μα β-μα Αγ-γ 4 Αγγ 6-γ 4 Gγ-γ 1 Gγ-γ 6-γ 1 Αγ-ενισχ (Αγ3 ) DEAE δβ- Turk δβ- Sic 151 Θήλυ HPFH Nl Nl Θήλυ β-μα F FSC-6 Nl Nl C/A 153 Άρρεν δβ-μα Nl Nl Nl Nl 41883A/A 154 Θήλυ δβ-μα Nl Nl Nl Nl Άρρεν β-μα F β A/A 156 Θήλυ δβ-μα A/A 157 Θήλυ β-μα F IVS Θήλυ β-μα F β C/A 159 Άρρεν δβ-μα Θήλυ δβ-μα
113 Από τα 160 δείγματα καταχωρήθηκαν: α. 63 ετεροζυγώτες δβ-μεσογειακής Αναιμίας β. 51 ετεροζυγώτες β- Μεσογειακής Αναιμίας με αυξημένη HbF. γ. 30 ετεροζυγώτες HPFH (Κληρονομικής Παραμονής Εμβρυϊκής Αιμοσφαιρίνης F). δ. 1 διπλός ετεροζυγώτης HPFH και Δρεπανοκυτταρικής Αναιμίας (HbS). ε. 1 ομοζυγώτης δβ-μα στ. 2 διπλοί ετεροζυγώτες HPFH και δβ-μα ζ. 4 διπλοί ετεροζυγώτες HPFH και β-μα η. 1 διπλός ετεροζυγώτης β-μα και δβ-μα θ. 1 διπλός ετεροζυγώτης HPFH και δ-μα ι. 1 διπλός ετεροζυγώτης δβ-μα + δ-μα κ. 2 διπλοί ετεροζυγώτες β-μα +α-μα λ. 1 διπλός ετεροζυγώτης HPFH +α-μα μ. 2 ετεροζυγώτες β-μα 113
114 Αξιολόγηση των φαινοτυπικών (αιμοτολογικών βιοχημικών κ.λπ.) δεδομένων (στο γενικό πληθυσμό). Στους πίνακες 7 και 8 και στα αντίστοιχα Διαγράμματα 1 και 2 αποτυπώνονται τα αποτελέσματα των εξετάσεων, που πραγματοποιήθηκαν στη Μονάδα Πρόληψης Μεσογειακής Αναιμίας (Μ.Π.Μ.Α.) του Γενικού Νοσοκομείου Καρδίτσας, κατά τα έτη 1991 έως 2006, στο γενικό πληθυσμό. Ο έλεγχος αφορά πρωτίστως ζευγάρια (εγκύους και μη) αλλά και νεαρά άτομα (συνήθως ενήλικα), που πρόκειται να τεκνοποιήσουν. Επίσης στη στατιστική επεξεργασία των αποτελεσμάτων συμπεριλαμβάνονται και άτομα, τα οποία νοσηλεύονταν στις κλινικές του νοσοκομείου, αλλά και άτομα από τη Μονάδα Μεταγγίσεων όλα σχεδόν μεγαλύτερα των ετών. Δεν υπάρχουν δηλαδή γεννήσεις ομοζυγωτών ή διπλών ετεροζυγωτών τα τελευταία χρόνια στο Νομό. Πίνακας 7. Αποτελέσματα εξετάσεων στη Μ.Π.Μ.Α. (Μονάδα Πρόληψης Μεσογειακής Αναιμίας) του Γενικού Νοσοκομείου Καρδίτσας από 1991 έως 2006 ΕΞΕΤΑΣΘΕΝΤΑ ΑΤΟΜΑ (Υγιείς, φορείς κ.λπ.) ΑΡΙΘΜΗΤΙΚΑ ΠΟΣΟΤΙΚΑ (%) Υγιείς ,49 Ετερόζυγοι β-μα ,21 Ετερόζυγοι α-μα 937 4,37 Ετερόζυγοι HbS 620 2,89 Ετερόζυγοι δβ-μα 187 0,87 HPFH 56 0,26 Αιμοσφαιρινοπάθεια Η 52 0,24 Ετερόζυγοι Hb Lepore (Πύλος) 45 0,21 Διπλοί ετεροζυγώτες (HbS+α-ΜΑ) 39 0,18 Διπλοί ετεροζυγώτες (β-μα+α-μα) 20 0,09 Ετερόζυγοι HbD 16 0,07 Λοιποί συνδυασμοί 159 0,74 Σιδηροπενία ,34 Αδιευκρίνιστα ,99 ΣΥΝΟΛΟ ,00 114
115 ,49 Υγιείς Ετερόζυγοι β-μα Ετερόζυγοι α-μα Διάγραμμα 1. Διαγραμματική απεικόνιση αποτελεσμάτων του Πίνακα 1 14,21 4,37 2,89 Ετερόζυγοι HbS Ετερόζυγοι δβ-μα 0,87 0,26 HPFH Αιμοσφαιρινοπάθεια Η Ετερόζυγοι Hb Lepore (πύλος) 0,24 0,21 Διπλοί ετεροζυγώτες (HbS+α-ΜΑ) Διπλοί ετεροζυγώτες (β-μα+α-μα) 0,18 0,09 0,07 0,74 Ετερόζυγοι HbD Λοιποί συνδυασμοί *** 5,34 Σιδηροπενία Αδιευκρίνιστα 5,99 Διάγραμμα 1. Διαγραμματική απεικόνιση των αποτελεσμάτων του Πίνακα
116 * Αναφορικά με τα σιδηροπενικά άτομα, στην επεξεργασία των δεδομένων καταγράφονται από την αρχική εξέταση (όχι μετά από σιδηροθεραπεία) και αφορούν στην πλειονότητά τους εγκύους, αλλά και μικρά παιδιά. ** Στους αδιευκρίνιστους περιλαμβάνονται: α) Άτομα με οριακούς αιματολογικούς δείκτες (MCH, MCV, MCHC) και συνήθως χαμηλές αιματολογικές παραμέτρους (Hb, HCl, RBC) β) Άτομα φυσιολογικών παραμέτρων (Hb, Hct) αλλά με σχετικά υψηλά RBC σε σχέση με την αιμοσφαιρίνη και τον αιματοκρίτη. γ) Άτομα με οριακή αιμοσφαιρίνη Α 2 (HbA 2 ) στα ανώτερα φυσιολογικά όρια (περί του 2,3 έως 3,5%), τα οποία ελέγχονται με ανάλυση DNA, σε μοριακό επίπεδο, για ήπιες μεταλλάξεις με συνηθισμένη την -101 μετάλλαξη στα β- γονίδια. δ) Άτομα με οριακή αιμοσφαιρίνη Α 2 (HbA 2 ) στα κατώτερα φυσιολογικά όρια (>2%), τα οποία ελέγχονται με ανάλυση DNA, σε μοριακό επίπεδο, για ήπιες μεταλλάξεις (με συνηθισμένη την Hb Κνωσσός). ε) Άτομα με φυσιολογικές, όλες τις παραμέτρους εξαγωγής συμπερασμάτων, αλλά με όχι φυσιολογική μορφολογία ερυθροκυττάρων. Όλα τα ανωτέρω άτομα παραπέμπονται στο Κέντρο Μεσογειακής Αναιμίας για περαιτέρω έλεγχο, βιοσύνθεση αιμοσφαιρινών και ανάλυση DNA. *** Στους αναφερόμενους ως λοιπούς συνδυασμούς του Πίνακα 7, περιλαμβάνονται: Άτομα από τη Μονάδα Νοσηλείας Μεσογειακής Αναιμίας ήτοι: ομόζυγα Cooley (β-μα και λιγότερα β-μα+δβ-μα), με μικροδεπανοκυτταρική αναιμία (HbS+β-ΜΑ και πιο λίγα HbS+δβ-MA), ομόζυγα HbS. Στα ανωτέρω άτομα πραγματοποήθηκε, παράλληλα με την παρούσα διατριβή και γονοτυπική ανάλυση DNA. Περιλαμβάνονται επίσης και πιο «σπάνιοι» συνδυασμοί όπως: Διπλοί ετεροζυγώτες β-μα+hpfh, ετεροζυγώτες Hb AGR (Αγρινίου), διπλοί ετεροζυγώτες β-μα+hbd, διπλοί ετεροζυγώτες β-μα+hblepore, διπλοί ετεροζυγώτες δβ- ΜΑ+HPFH, ομοζυγώτες τύπου AGR, διπλοί ετεροζυγώτες α-μα+δβ-μα. 116
117 Πίνακας 8. Προγεννητικός έλεγχος ζευγαριών, με άμεση ανάλυση DNA από τα κύτταρα του εμβρύου (με αμνιοπαρακέντηση ή τροφοβλάστη) κατά την περίοδο από 1991 έως 2006 στη Μονάδα Πρόληψης Μεσογειακής Αναιμίας του Γενικού Νοσοκομείου Καρδίτσας ΣΥΝΔΥΑΣΜΟΙ ΖΕΥΓΑΡΙΩΝ ΑΡΙΘΜΟΣ ΖΕΥΓΑΡΙΩΝ Ετερόζυγος β-μα / Ετερόζυγος β-μα (β/β) 63 Ετερόζυγος β-μα / Ετερόζυγος HbS (β/s) 35 Ετερόζυγος β-μα / Ετερόζυγος δβ-μα (β/δβ) 8 Ετερόζυγος HbS / Ετερόζυγος HbS (S/S) 4 Ετερόζυγος δβ-μα / Ετερόζυγος HbS (δβ/s) 3 Ετερόζυγος β-μα / Διπλός ετεροζυγώτης (HbS+α-ΜΑ) (β/s+a) 3 Ετερόζυγος β-μα / Διπλός ετεροζυγώτης (HbS+β-ΜΑ) (β/s+β) 1 Ετερόζυγος Hb Lepore (Πύλος) / Ετερόζυγος HbS (Lepore/S) 1 Ετερόζυγος HbS / Διπλός ετεροζυγώτης (HbS + β-μα) (S/S+β) 1 ΣΥΝΟΛΟ
118 Διάγραμμα 2. Διαγραμματική απεικόνιση αποτελεσμάτων Πίνακα Ετερόζυγος β-μα / Ετερόζυγος β- ΜΑ (β/β) Ετερόζυγος β-μα / Ετερόζυγος HbS (β/s) Ετερόζυγος β-μα / Ετερόζυγος δβ- ΜΑ (β/δβ) Ετερόζυγος HbS / Ετερόζυγος HbS (S/S) Ετερόζυγος δβ-μα / Ετερόζυγος HbS (δβ/s) Ετερόζυγος β-μα / Διπλός ετεροζυγώτης (HbS-ΜΑ) (β/s+a) (β/s+a) Ετερόζυγος β-μα / Διπλός ετεροζυγώτης (HbS+β-ΜΑ) (β/(s+β) (β/s+β) Ετερόζυγος Hb Lepore (πύλος) / Ετερόζυγοι HbS (Lepore/S) Ετερόζυγος HbS / Διπλός ετεροζυγώτης (HbS + β-μα) (S/(S+β) (S/S+β Διάγραμμα 2. Διαγραμματική απεικόνιση των αποτελεσμάτων του Πίνακα
119 Στους Πίνακες 9 (Α-Ξ) αποτυπώνεται η γενική εικόνα υγιών ατόμων και διαφόρων τύπων ετεροζυγωτών. 9Α. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ υγιούς ενηλίκου ανδρός υγιούς ενηλίκου γυναικός (μη εγκύου) υγιούς ενηλ. γυν. (3 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 15,2 13,4 12,2 Αιματοκρίτης (Hct) % 45,3 40,2 36,8 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 29,6 30,0 29,6 MCV fl 88,1 90,1 89,3 MCHC % 33,6 33,3 33,2 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 Α Α 2 Α Α 2 Α 2,65% 2.47% 2.75% <2% <2% <2% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (-) (-) (-) HPLC Hb A 2 2,8% 2,6% 3,0% Hb F 0,3% 0,2% 0,6% Hb S 0,0% 0,0% 0,0% Hb A 88,6% 89,2% 86,9% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση ± ± Ανισοκυττάρωση ± ± Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση (-) (-) (-) (-) (-) (-) 119
120 Στοματοκυττάρωση Σφαιροκυττάρωση 9Β. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζύγου β-μα ενηλίκου ανδρός ετεροζύγου β-μα ενηλίκου γυναικός (μη εγκύου) ετεροζύγου β-μα ενηλ. γυν. (3 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 13,1 11,0 9,5 Αιματοκρίτης (Hct) % 42,7 36,5 30,4 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 20,0 19,0 20,6 MCV fl 65,3 62,9 65,8 MCHC % 30,7 30,1 31,3 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 Α Α 2 Α Α 2 Α 4,85% 4,98% 4,30% <2% <2% <2% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 5,2% 5,6% 4,5% Hb F 0,4% 0,7% 1,6% Hb S 0,0% 0,0% 0,0% Hb A 85,2% 85,2% 84,9% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση +/ Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση (+) (-) (+) (-) (+) (-) 120
121 Στοματοκυττάρωση Σφαιροκυττάρωση 9Γ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζύγου β-μα με αυξημένη HbF ενηλ. ανδρός ετεροζύγου β-μα με αυξημένη HbF ενηλ. γυν. (μη εγκύου) ετεροζύγου β-μα με αυξημένη HbF ενηλ. γυν. (3 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 13, ,6 Αιματοκρίτης (Hct) % 41, Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 21,5 19,4 20,9 MCV fl 67,3 62,6 67,1 MCHC % 32, ,1 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 -F-A Α 2 -F-A Α 2 -F-A 5,39% 4,80% 4,68% 5,45% 4,33% 5,8% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 5,4% 5,3% 5,4% Hb F 5,2% 4,2% 6,8% Hb S 0,0% 0,0% 0,0% Hb A 79,4% 82,9% 80,1% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση Ανισοκυττάρωση Ποικιλοκυττάρωση (+) (-) (+) (-) (+) (-) 121
122 Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση 9Δ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζύγου α-μα ενηλίκου ανδρός ετεροζύγου α-μα ενηλ. γυν. (μη εγκύου) ετεροζύγου α-μα ενηλ. γυν. (2 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 12,1 11,7 10,1 Αιματοκρίτης (Hct) % 40,5 38,3 35,9 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 20,8 22,2 19,3 MCV fl 69,6 72,5 68,8 MCHC % 29,9 30,5 28,1 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 A Α 2 A Α 2 A 2,45% 2,36% 1,85% <2% <2% <2% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 2,6% 2,4% 1,9% Hb F 0,0% 0,2% 0,3% Hb S 0,0% 0,0% 0,0% Hb A 86,7% 88,1% 88,2% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση +/++ +/++ +/++ (-) (+) (-) (+) (-) (+) 122
123 Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση 9Ε. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζύγου δρεπανοκυ ττα-ρικής αναιμίας (HbS) ενηλίκου ανδρός ετεροζύγου δρεπανοκυ ττα-ρικής (HbS) ενηλ. γυν. (μη εγκύου) ετεροζύγου δρεπανοκυττ α-ρικής αναιμίας (HbS) ενηλ. γυν. (2 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 15,7 13,7 12,5 Αιματοκρίτης (Hct) % 46,5 41,7 37,2 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 28,3 28,4 27,8 MCV fl 83,8 86,5 82,7 MCHC % 33,8 32,9 33,6 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 -S 40%- A Α 2 -S 40%- A Α 2 -S 40%-A 2,85% 2,78% 2,85% <2% <2% <2% Δοκιμασία Δρεπανώσεως (+) (+) (+) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 και τμήμα της HbS 4,3% 4,2% 4,5% Hb F 0,5% 0,5% 0,6% Hb S 36,3% 38,3% 40,0% Hb A 50,7% 51,5% 50,6% (-) (-) (-) (-) (-) (-) 123
124 ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση Ανισοκυττάρωση ± + + Ποικιλοκυττάρωση ± ± Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση 9ΣΤ. ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζύγου δβ-ma ενηλίκου ανδρός ΓΕΝΙΚΗ ΕΙΚΟΝΑ ετεροζύγου δβ-ma ενηλ. γυν. (μη εγκύου) ετεροζύγου δβ-ma ενηλ. γυν. (2 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 12,1 11,3 10,0 Αιματοκρίτης (Hct) % 39,1 35,9 33,2 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 20,6 22,0 21,3 MCV fl 66,7 69,8 70,8 MCHC % 30,9 31,5 30,1 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 -F-A Α 2 -F-A Α 2 -F-A 2,22% 1,92% 2,41% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 2,9% 2,6% 2,9% Hb F 9,0% 10,4% 6,9% Hb S 0,0% 0,0% 0,0% Hb A 78,7% 78,0% 84,0% (+) (-) (+) (-) (+) (-) 124
125 ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση 9Ζ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ενηλίκου ανδρός με HPFH ενηλίκου γυναικός με HPFH. (μη εγκύου) ενηλίκου γυναικός με HPFH (2 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 16,1 12,4 12,3 Αιματοκρίτης (Hct) % 47,6 37,1 37,0 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 30,2 28,9 30,3 MCV fl 89,3 86,5 91,1 MCHC % 33,8 33,4 33,2 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 -F-A Α 2 -F-A Α 2 -F-A 1,98% 1,47% 1,72% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (-) (-) (-) HPLC (-) (-) (-) (-) (-) (-) 125
126 Hb A 2 1,9% 2,3% 1,8% Hb F 14,0% 13,3% 16,7% Hb S 0,0% 0,0% 0,0% Hb A 74,8% 75,5% 74,3% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία ± Μικροκυττάρωση Ανισοκυττάρωση ± ± ± Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση 9Η. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ενηλίκου ανδρός με Αιμοσφαιρινοπάθεια Η ενηλίκου γυναικός (μη εγκύου) με Αιμοσφαιρινοπάθεια Η ενηλίκου γυναικός (1 ος μήνας κυήσεως) με Αιμοσφαιρινοπάθεια Η Αιμοσφαιρίνη (Ηb) gr/dl 11,1 9,2 8,2 Αιματοκρίτης (Hct) % 38,1 34,2 29,3 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 17,6 17,9 17,0 MCV fl 60,5 66,7 60,8 MCHC % 29,1 26,9 28,0 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 -Α- Η 10% Α 2 -Α-Η 8% Α 2 -Α-Η 10% 1,44% 1,87% 1,56% <2% <2% <2% (-) (+++++) έγκλειστα στο 90% των (-) (+++++) έγκλειστα στο 90% των (-) (+++++) έγκλειστα στο 90% των κυττάρων 126
127 κυττάρων κυττάρων Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 1,5% 2,7% 1,7% Hb F 0,0% 1,3% 0,4% Hb S 0,0% 0,0% 0,0% Hb A 91,2% 89,8% 92,2% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση + +/++ ++ Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση Θ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζύγου Hb-Lepore ενηλίκου ανδρός ετεροζύγου Hb-Lepore ενηλίκου γυναικός (μη εγκύου) ετεροζύγου Hb-Lepore ενηλίκου γυναικός (2 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl ,2 9.0 Αιματοκρίτης (Hct) % , Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg ,9 19,4 MCV fl ,5 63,7 MCHC % ,0 30,4 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- Α 2 -Lepore 10%-A Α 2 -Lepore 10%-A Α 2 -Lepore 10%-A 2,98% 2,88 2,26% <2% <2% <2% (+) (+) (+) 127
128 αλυσίδες) (-) (-) (-) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 + HbLepore 12,3% 13,4% 11,0% Hb F 1,4% 2,1% 1,4% Hb S 0,0% 0,0% 0,0% Hb A 76,7% 74,1% 77,3% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση /++ Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση 9Ι. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ διπλού ετεροζυγώτ η (HbS+α- ΜΑ) ενηλίκου ανδρός διπλού ετεροζυγώτ η (HbS+α- ΜΑ) ενηλ. γυν. (μη εγκύου) διπλού ετεροζυγώτη (HbS+α-ΜΑ) ενηλ. γυν. (2 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 14,0 13,0 11,2 Αιματοκρίτης (Hct) % 43,9 43,1 36,9 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 22,9 21,2 20,7 MCV fl 71,7 70,3 68,2 MCHC % 31,9 30,2 30,4 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Α 2 -S 25%- A Α 2 -S 25%- A Α 2 -S 25%-A 2,85% 2,05% 2,25% Μέτρηση αιμοσφαιρίνης F(HbF) <2% <2% <2% 128
129 - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Δοκιμασία Δρεπανώσεως (+) (+) (+) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 (+ τμήμα της Hbs) 3,8% 4,3% 4,7% Hb F 0,7% 0,5% 0,8% Hb S 24,8% 25,9% 25,3% Hb A 64,4% 63,4% 63,3% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση (-) (+) (-) (+) (-) (+) 9Κ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ διπλού ετεροζυγώτ η (β-μα+α- ΜΑ) ενηλίκου ανδρός διπλού ετεροζυγώτ η (β-μα+α- ΜΑ) ενηλ. γυν. (μη εγκύου) διπλού ετεροζυγώτη (β-μα+α-μα) ενηλ. γυν. (3 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 11,9 11,2 9,7 Αιματοκρίτης (Hct) % 40,6 36,3 33,4 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 24,9 22,0 16,4 MCV fl 84,9 71,3 56,7 MCHC % 29,3 30,9 29,0 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Α 2 -A Α 2 -A Α 2 -A 129
130 Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) 5,11% 4,75% 5,00% <2% <2% <2% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 Hb F Hb S Hb A ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση (+) (+) (+) (+) (+) (+) 9Λ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζυγώτ η HbD Punjab ενηλίκου ανδρός ετεροζυγώτ η HbD Punjab ενηλ. γυν. (μη εγκύου) ετεροζυγώτη HbD Punjab ενηλ. γυν. (2 ος μήνας κυήσεως) Αιμοσφαιρίνη (Ηb) gr/dl 15,8 12,6 12,9 Αιματοκρίτης (Hct) % 44,6 38,9 37,8 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 30,3 26,3 29,7 MCV fl 85,6 81,0 86,9 MCHC % 35,4 32,4 34,1 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε Α 2 -D 40%- Α 2 -D 40%- Α 2 -D 40%-A 130
131 μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) A A 1,95% 1,80% 1,56 <2% <2% <2% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 1,7% 1,9% 1,1% Hb F 0,6% 0,4% 0,5% Hb S 38,4% 36,8% 39,5% Hb A 50,4% 52,1% 52,9% ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση Ανισοκυττάρωση Ποικιλοκυττάρωση + - Βεσεόφιλη στίξη - Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση (-) (-) (-) (-) (-) (-) 9Μ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ διπλού ετεροζυγ ώτη (β- MA+HbD ενηλίκου ανδρός διπλού ετεροζυγ ώτη (β- MA+HPF H) ενηλίκου ανδρός διπλού ετεροζυγώ τη (β- MA+Hb Lepore) ενηλίκου ανδρός ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ διπλού ετεροζυγ ώτη (α- MA+δβ- ΜΑ) ενηλίκου ανδρός Αιμοσφαιρίνη (Ηb) gr/dl ,6 7,6 13,4 Αιματοκρίτης (Hct) % 31,2 34,7 24,9 43,4 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 21,2 19,5 20,7 23,6 MCV fl 68,9 58, ,4 MCHC % 30,8 33,4 30,5 30,9 Λευκά (/cm 3 )
132 ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 - D 85%- F 20%-Α ίχνη Α 2 - F 30%-Α Α 2 -Lepore- F-Α ίχνη Α 2 --F10%- A 3,12% 4,32% 3,50% 2,90% 19,57 % 29,72% 37,48% 10,56% Δοκιμασία Δρεπανώσεως (-) (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) (+) HPLC Hb A 2 Hb F Hb S Hb A ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση +/ Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση + + Στοματοκυττάρωση + + Σφαιροκυττάρωση (+) (-) (+) (-) (+) (-) (-) (+) 9Ν. ΓΕΝΙΚΗ ΕΙΚΟΝΑ διπλού ετεροζυγώτ η (δβ- MA+HPFH) ενηλίκου γυναικός ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ Αιμοσφαιρίνη (Ηb) gr/dl 12,3 Αιματοκρίτης (Hct) % 36,6 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 24,4 MCV fl 72,5 132
133 MCHC % 33,6 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 -F 40%-Α 1,43% 37,03 % (+) Δοκιμασία Δρεπανώσεως (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (-) Hb A 2 Hb F Hb S Hb A Υποχρωμία ++ Μικροκυττάρωση ++ Ανισοκυττάρωση ++ Ποικιλοκυττάρωση ++ Βεσεόφιλη στίξη + Πολυχρωματοφιλία + Στοχοκυττάρωση + Μακροκυτάρρωση Στοματοκυττάρωση Σφαιροκυττάρωση 9Ξ. ΓΕΝΙΚΗ ΕΙΚΟΝΑ ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΕΛΕΓΧΟΣ ετεροζυγώτ η (Hb Agrinio/NI) ενηλίκου ανδρός ετεροζυγώτ η (Hb Agrinio/NI) ενηλ. γυναικός ομοζυγώτη (Hb Agrinio/Hb Agrinio ενηλ. γυναικός Αιμοσφαιρίνη (Ηb) gr/dl 13,9 13,0 6,6 Αιματοκρίτης (Hct) % 42,3 40,8 23,0 Ερυθρά αιμοσφαίρια (RBC) (x10 3 /cm 3 ) MCH pg 27,2 24,8 18,9 133
134 MCV fl 82,5 77,1 65,7 MCHC % 32,3 31,9 28,7 Λευκά (/cm 3 ) ΒΙΟΧΗΜΙΚΗ ΜΕΛΕΤΗ ΑΙΜΟΣΦΑΙΡΙΝΗΣ Ηλεκτροφόρηση αιμοσφαιρίνης σε μεμβράνη οξεικής κυταρρίνης- Αιμοσφαιρινικά κλάσματα Μέτρηση αιμοσφαιρίνης Α 2 (ΗbΑ 2 ) - Διαχωρισμός σε στήλη DEAE: Μέτρηση αιμοσφαιρίνης F(HbF) - Μέθοδος BETKE: ΕΓΚΛΕΙΣΤΑ ΕΡΥΘΡ/ΡΩΝ - Πριν από επώαση (αδέσμευτες α- αλυσίδες) - Μετά από την επώαση (αδέσμευτες β- αλυσίδες) Α 2 -A Α 2 -A Α 2 -A 2,6% 2,75 2,7% <2% <2% 1,9% Δοκιμασία Δρεπανώσεως (-) (-) (-) Ωσμωτική αντίσταση ερυθροκυττάρων (+) (+) (+) HPLC Hb A 2 Hb F Hb S Hb A ΜΟΡΦΟΛΟΓΙΑ ΕΡΥΘΡΟΚΥΤΤΑΡΩΝ Υποχρωμία Μικροκυττάρωση Ανισοκυττάρωση Ποικιλοκυττάρωση Βεσεόφιλη στίξη + Πολυχρωματοφιλία Στοχοκυττάρωση Μακροκυτάρρωση + Στοματοκυττάρωση + Σφαιροκυττάρωση + (-) (+) (-) (+) (+) (+) 134
135 3.2 Αποτελέσματα σε μοριακό επίπεδο Ο προσδιορισμός της μοριακής βλάβης έγινε με ενίσχυση του PCR (polymerase chain Reaction): α. Της περιοχής του β-γονιδίου. β. Της περιοχής των δ- και β-γονιδίων για την ανίχνευση της έλλειψης για δβ-θαλασσαιμία. γ. Περιοχής του υποκινητή των Gγ και Αγ-γονιδίων. Για το Αγ-γονίδιο, αρχικά ενισχύεται με τους εκκινητές: γ 4- GCγ 4 [681 bese paire (bp)] και στη συνέχεια με τους εκκινητές: γ 4 -γ 6- GC γ 4 (327 bp). Για το Gγ-γονίδιο, στην 5 περιοχή, με τους εκκινητές: γ 1 GCγ 4 (678 bp) και στη συνέχεια με τους εκκινητές: γ 1 γ 6 -GCγ 4 (327 bp) και δ. Περιοχής του 3 άκρου του Αγ-γονιδίου. Η 3 περιοχή του Αγ-γονιδίου ενισχύεται με τους εκκινητές: γ 7 / α-γ 7 και στη συνέχεια το PCR προϊόν επωάζεται με το ένζυμο Ddel. Η μελέτη του πρoιόντος του PCR έγινε με DGGE ηλεκτροφόρηση σε πηκτώματα ακρυλαμίδης με κλίση αποδιατακτικών παραγόντων (Denaturing Gradient Gel Electrophoresis). Επίσης έγινε μελέτη της νουκλεοτιδικής αλληλουχίας του προϊόντος της PCR με DNA Sequencing Εκλεκτικός πολλαπλασιασμός του β-γονιδίου Το γονίδιο της β-σφαιρίνης προκειμένου να μελετηθεί χωρίζεται σε έξι τμήματα τα οποία καλύπτουν όλο το γονίδιο όπως και τις 3 και 5 μη μεταφραζόμενες περιοχές τα οποία πολλαπλασιάστηκαν εκθετικά με τη χρήση αντίστοιχων ζευγών εκκινητών μέσω της αλυσιδωτής αντίδρασης πολυμεράσης (Εικ. 26). 135
136 Εικόνα 26. Το γονίδιο της β-σφαιρίνης. Παρατηρούνται τα ζεύγη των ειδικών εκκινητών και ο «χωρισμός» του γονιδίου σε έξι τμήματα. Μετά την εκλεκτική ενίσχυση κάθε τμήματος τα αποτελέσματα της αντίδρασης ελέγχονται με ηλεκτροφόρηση του προϊόντος PCR σε πήκτωμα αγαρόζης. Ως μάρτυρας μεγέθους χρησιμοποιείται DNA φάγου φχ174 που έχει υποστεί πέψη με την περιοριστική ενδονουκλεάση HaeIII έτσι ώστε να προκύψουν τμήματα DNA με μεγέθη (σε Kb): 1.35, 1.07, 0.87, 0.60, 0.31, 0.27, 0.23, 0.19, 0.11, Στις εικόνες 27, 28, 29, 30 που ακολουθούν φαίνονται τα προϊόντα αντίδρασης πολυμερισμού όπως προκύπτουν χρησιμοποιώντας τα αντίστοιχα ζεύγη εκκινητών Ν Μ Εικόνα 27. PCR για FR 0 στα δείγματα: 1, 2, 3, 4, Ν, Μ: φχ/haeiii, New England Biolabs. 136
137 Ν Μ Εικόνα 28. PCR για FR 1 στα δείγματα 1-7, N, M: φχ/haeiii, New England Biolabs Ν Μ Εικόνα 29. PCR για FR 2 στα δείγματα 1-11, N, M:100bp, New England Biolabs Ν Μ Εικόνα 30. PCR για FR 5 στα δείγματα 1-10, Ν, Μ: φχ/haeiii, New England Biolabs. * Στις θέσεις FR 0 / FR 1 / FR 2 / FR 5, ανιχνεύονται οι κάτωθι βασικές μεταλλάξεις αντίστοιχα: -101,-87 / FSC6 ή Codon6, FSC5, FSC8, IVS2-745, πολυμορφισμός +20, 137
138 HbS, Cd 2 / IVS1-1, IVS1-5, IVS1-6, IVS1-110, β39. Στο σημείο αυτό πρέπει να τονισθεί ότι κατά την εκπόνηση της συγκεκριμένης διατριβής χρησιμοποιήθηκαν κυρίως τέσσερα ζεύγη εκκινητών πράγμα που σημαίνει πως οι απολύτως αναγκαίες αντιδράσεις πολυμερισμού για την διάγνωση των δειγμάτων των ασθενών ήσαν αυτές των τμημάτων (fragments, FR), FR0, FR1, FR2, FR5. Ήδη από προηγούμενες μελέτες μας ήταν γνωστό το γεγονός πως οι περισσότερες μεταλλάξεις βρίσκονται στα συγκεκριμένα τμήματα του γονιδίου. Στις εικόνες 31, 32, 33, 34, 35 που ακολουθούν, αποτυπώνονται τα αποτελέσματα των μεταλλάξεων με ηλεκτροφόρηση σε πηκτώματα ακρυλαμίδης με κλίση αποδιατακ τικών παραγόντων (Denaturing Gradient Gel Electrophoresis, DGGE). 138
139 Εικόνα 31. DGGE στα τμήματα FR 0, FR 1. Διακρίνονται οι μεταλλάξεις: -101, HbS 139
140 Εικόνα 32. DGGE στα τμήματα FR 0, FR 1 και FR 2. Διακρίνονται οι μεταλλάξεις: πολυμορφισμός +20, Cd 2, IVS1-110, β39, IVS
141 Εικόνα 33. DGGE στα τμήματα FR 0, FR 2, FR 1 και FR 5. Διακρίνονται οι μεταλλάξεις: - 101, IVS1-110, cd2. 141
142 Εικόνα 34. DGGE στα τμήματα FR 5 (ηλεκτροφόρηση διάρκειας 19 ωρών) 142
143 Εικόνα 35. DGGE στα τμήματα FR 5 (ηλεκτροφόρηση διάρκειας 5 ωρών) 143
144 3.2. Αποτελέσματα ανάλυσης σε μοριακό επίπεδο των μεταλλαγών του β - γονιδίου Η ανάλυση με DGGE για το β-γονίδιο ανέδειξε τις παρακάτω μεταλλάξεις (Πίνακας 10, Διάγραμμα 3) Πίνακας 10. Οι μεταλλλάξεις των β-γονιδίων σε ετεροζυγώτες β-μα με αυξημένη HbF. α/α Μετάλλαξη Αριθμός δειγμάτων Ποσοστό % 1 Β ,64 2 Β39 + Cd2* 2 3,77 26,41 3 IVS1-1[G>A]** 19 35,84 4 IVS1-1[G>A] + α1cd14[g>a] 1 1,88 5 IVS1-1[G>A]+Cd2 2 3,77 41,50 6 IVS1-110[G>A] 8 15,09 7 IVS2-745[C>G]+ (πολυμορφισμός+20) 2 3,77 8 IVS2-1[G>A] 2 3,77 9 IVS2-1-[G>A]+(-3,7) για α-μα 1 1,88 5,66 10 Codon 6[-A] ή FSC-6*** 4 7,54 Σύνολο ,00 * Cd= Codon (κωδικόνιο) **IVS= intervening sequences ή intron (παρεμβαλλόμενη αλληλουχία ή εσώνιο) ***FSC=frameshift codon (κωδικόνιο πλαισίου ανάγνωσης), επίσης το αρνητικό πρόσημο αναφέρεται σε μεταλλάξεις στην περιοχή του προαγωγού (promotοr), π.χ , -87. IVS ,77% IVS ,09% β39 26,41% IVS2-1 5,66% Codon6[-A] 7,54% IVS1-1 41,50% 144
145 Κυκλικό διάγραμμα 3. Απεικόνιση των μεταλλάξεων των β-γονιδίων του ανωτέρου πίνακα, στους ετεροζυγώτες β-μα με αυξημένη HbF. Στη συνέχεια αποτυπώνονται στους Πίνακες 11 έως 17 τα ποσοστά (%) των αιμοσφαιρινών Α 2, F και Α καθώς και οι αντίστοιχες μεταλλάξεις στα γ-γονίδια (Αγ5, Gγ5 και Αγ3 ) στους φορείς β-μα με αυξημένη HbF. Πίνακας 11. Ποσοστά των αιμοσφαιρινών Α2, F και Α σε ετεροζυγώτες β-μα με αυξημένη ( ) HbF, καθώς και οι αντίστοιχες μεταλλάξεις στα γ-γονίδια. α/α Αρ. δειγμ. HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια (%) (%) (%) Αγ5 Gγ5 Αγ ,53 3,5 Nl Α/Α ,43 6,0 Nl -158 CIA ,1 6,9 79,7 Nl -158 CIA ,22 12,52 Nl -158 CIA 5 47* 3,6 4,1 82,1 Nl -158 CIA ,7 1,2 85,5 Nl -158 CIA ,4 6,7 80,1 Nl -158 CIA ,0 6,3 81,2 Nl -158 CIA ,7 4,3 84,1 Nl -158 CIA ,2 10,4 76,6 Nl -158 CIA ,7 5,9 81,3 Nl -158 CIA ,2 5,6 82,3 Nl -158 CIA 13 98** 3,0 5,9 82,3 Nl -158 CIA ,6 5,3 79,9 Nl -158 CIA ,0 6,0 80,5 Nl -158 CIA ,6 6,2 81,8 Nl -158 CIA ,1 3,2 83,9 Nl -158 CIA ,5 4,6 82,4 Nl ,4 5,0 80,5 Nl ,9 11,1 76,2 Nl -158 CIA ,4 5,2 79,4-158 CIA ,6 5,9 82,5-158 A/A ,4 9,0 80, CIA ,9 3, CIA ,1 8,0 del4 Nl CIA ,6 4,4 81,8 del4 Nl CIA ,4 6,8 80,1 del4 Nl CIA ,7 4,9 83,2 del4 Nl CIA ,7 4,2 83,4 del4 Nl CIA ,7 4,1 81,8 del4 AIA ,9 5,2 82,2-117 Nl CIC ,5 4,1 84,4 Nl -109 CIC ,3 4,2 82,2 Nl Nl CIC ,2 1,3 82,6 Nl Nl CIC ,6 5,9 82,5 Nl Nl CIC ,6 5,4 83,1 Nl Nl CIC ,6 10,4 78,0 Nl N CIC ,8 2,2 85,0 Nl Nl CIC 145
146 ,6 3,4 82,8 Nl Nl CIC ,2 5,6 82,8 Nl Nl Α/Α ,3 4,6 81,8 Nl Nl C/C *** 7,2 4,1 81,5-369 Nl C/C ,94 8,93 Nl C/C ,5 18,2 71,6 Nl C/C ,9 5,0 81,9 Nl C/C ,6 4,5 81,8 Nl C/C ,3 5,3 83,5 Nl CIA ,5 5,2 80,7 CIA ,5 6,9 79,1 Nl CIA ,8 6,6 80,8 CIA ,5 4,2 81,0 C/C ,6 3,1 83,9 C/C ,4 3,0 81,9 A/A ,4 5,3 81, ,8 4,6 82,1 C/A ,1 6,4 79,6 Μ.Ο. 4,53 5,72 81,43 * IVS2-745+(πολυμορφισμός+20) ** IVS1-1+α 1 Cd14[G>A] για α-μα *** IVS2-1+(-3,7) για α-μα Αναφορικά με τα επίπεδα της HbF, του ανωτέρου πίνακα, παρατηρούμε τα εξής: Στις μεταλλάξεις Nl /-158 στα Αγ5 / Gγ5 γονίδια, που συνοδεύονται από τις μεταλλάξεις C/A, ως επί το πλείστον, στα Αγ3 γονίδια, τα επίπεδα της HbF είναι κατά Μ.Ο. 5,99% (με γενικό Μ.Ο. 5,72%). Επίσης στις μεταλλάξεις del4 / Nl στα Αγ5 / Gγ5 γονίδια, που επίσης συνοδεύονται από τις αντίστοιχες C/A, ως προς τα Αγ3 γονίδια, τα επίπεδα της HbF είναι κατά Μ.Ο. 5,4%. Οι μεταλλάξεις Nl / Nl, αντίθετα, συνοδεύονται από τις μεταλλάξεις C/C στα Αγ3 γονίδια και έχουν κατά Μ.Ο. 5,99% HbF. Στους συγκεκριμένους ετεροζυγώτες β-μα με αυξημένη HbF, τα ποσοστά που αντιπροσωπεύουν οι μεταλλάξεις Αγ5 /Gγ5 είναι: Nl/ %, del4 / Nl 13,63% και Nl / Nl 36,36%. Παρατηρήθηκαν επίσης οι μεταλλάξεις α / -158 με αντίστοιχη C/A και HbF 3,9% β. Ο ομοζυγώτης -158 / -158 με C/A και HbF 9% γ. Η -117 / Nl με C/C και HbF 5,2% και δ. Η νέα μετάλλαξη Nl / -109 στα Αγ5 / Gγ5 γονίδια και αντίστοιχα C/C στα Αγ3 γονίδια με HbF 4,1%. 146
147 Πίνακας 12. Η μετάλλαξη β39 HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,1 8,0 del4 Nl C/A ,6 4,4 81,8 del4 Nl C/A ,4 6,8 80,1 del4 Nl C/A ,7 4,1 81,8 del4 A/A ,2 10,4 76,6 Nl -158 C/A ,0 6,0 80,5 Nl -158 C/A ,6 5,9 82,5-158 A/A ,5 4,1 84,4 Nl -109 C/C ,3 4,2 82,2 Nl Nl C/C ,5 6,9 79,1 Nl C/A ,5 5,2 80,7 C/A ,8 4,6 82,1 C/A ,4 3,0 81,9 A/A ,1 6,4 79,6 M.O. 5,05 5,71 81,02 *β39+cd2 Στη μετάλλαξη β39, ως προς τα Αγ5 /Gγ5 γονίδια παρατηρούνται οι μεταλλάξεις: del4/nl, Nl/-158, Nl/-109 και Nl/Nl. Πίνακας 13. Η μετάλλαξη IVS1-1 [G>A] HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,4 9,0 80, C/A ,6 6,2 81,8 Nl -158 C/A 3 98* 3,0 5,9 82,3 Nl -158 C/A ,2 5,6 82,3 Nl -158 C/A ,4 6,7 80,1 Nl -158 C/A ,7 4,3 84,1 Nl -158 C/A ,5 4,6 82,4 Nl ,7 4,9 83,2 del4 Nl C/A ,7 4,2 83,4 del4 Nl C/A 10 35** 2,9 5,2 82,2-117 Nl C/C ,2 1,3 82,6 Nl Nl C/C ,6 5,9 82,5 Nl Nl C/C ,6 5,4 83,1 Nl Nl C/C ,6 10,4 78,0 Nl Nl C/C ,8 2,2 85,0 Nl Nl C/C ,6 3,4 82,8 Nl Nl C/C ,3 4,6 81,8 Nl Nl C/C ,5 18,2 71,6 Nl C/C ,94 8,93 Nl C/C 20 67** 2,8 6,6 80,8 C/A ,5 4,2 81,0 C/C ,4 5,3 81,4 Μ.Ο. 3,99 6,04 81,58 *IVS1-1+α 1 Cd14[G>A] Πίνακας 5. Η μετάλλαξη IVS1-110 [G>A] ** IVS1-1+Cd2 Πίνακας 14. Η μετάλλαξη IVS1-110 [G>A] Στη μετάλλαξη IVS1-1[G>A] επικρατούν αντίστοιχα οι μεταλλάξεις: Nl/-158, del4/nl και Nl/Nl, καθώς και η μετάλλαξη -117/Nl. 147
148 Πίνακας 14. Η μετάλλαξη IVS1-110 [G>A] HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,1 6,9 79,7 Nl -158 C/A ,22 12,52 Nl -158 C/A ,7 1,2 85,5 Nl -158 C/A ,0 6,3 81,2 Nl -158 C/A ,7 5,9 81,3 Nl -158 C/A ,9 5,0 81,9 Nl C/C ,6 4,5 81,8 Nl C/C ,3 5,3 83,5 Nl C/A Μ.Ο 4,69 5,95 82,12 Πίνακας 15. Η μετάλλαξη IVS2-745 [C>G] HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,1 3,2 83,9 Nl -158 C/A 2 47* 3,6 4,1 82,1 Nl -158 C/A Μ.Ο 4,35 3,65 83,00 *IVS2-745+(πολυμορφισμός+20) Πίνακας 16. Η μετάλλαξη IVS2-1 [G>A] HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,6 5,3 79,9 Nl -158 C/A ,4 5,2 79,4-158 C/A 3 146* 7,2 4,1 81,5-369 Nl C/C Μ.Ο 6,06 4,86 80,26 *IVS2-1+(-3,7) για α-μ.α Πίνακας 17. Η μετάλλαξη Codon6 [-A] ή FSC-6 HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,9 3, C/A ,43 6,0 Nl -158 C/A ,9 11,1 76,2 Nl -158 C/A ,4 5,0 80,5 Nl -158 M.O 5,15 6,5 78,35 148
149 Αποτελέσματα των μεταλλάξεων σε μοριακό επίπεδο της δβ-μα Με την ηλεκτροφόρηση των προϊόντων της PCR σε πήκτωμα αγαρόζης 2%, για τα φυσιολογικά άτομα προκύπτει ένα τμήμα DNA. Για τα ετερόζυγα άτομα δβ-μα προκύπτουν δύο τμήματα DNA, που αντιστοιχούν στο φυσιολογικό χρωμόσωμα και σε αυτό με την έλλειψη. Επίσης ένα τμήμα DNA μεγαλύτερου όμως μεγέθους προκύπτει και για ένα άτομο ομόζυγο για δβ-μα Σικελικού τύπου. Με την ανωτέρω διαδικασία πραγματοποιήθηκε η ανίχνευση ετερ οζυγωτών δβ-μα Σικελικού τύπου (Εικ. 36) η οποία οφείλεται σε έλλειψη DNA μήκους 13,4 Kb. Μ Ν Εικόνα 36. Ανίχνευση ελλείψεων, υπεύθυνων για δβ -ΜΑ Σικελικού τύπου. Ν: αρνητικός μάρτυρας, Μ: φχ 174/Hae IIΙ, New England Biolabs. 1: Nl/Nl, 2, 3: ετεροζυγώτες δβ-μα Σικελικού τύπου. Ο τύπος αυτός, ενώ απαντά σε μεγάλη συχνότητα στο σύνολο του ελληνικού πληθυσμού, σε σχέση με τους ετεροζυγώντες δβ -ΜΑ Τουρκικού τύπου, παρατηρείται εντελώς το αντίθετο στους φορείς δβ -ΜΑ, που εξετάζονται στην παρούσα διατριβή. Τα επίπεδα της HbF είναι εξαιρετικά ετερογενή και κυμαίνονται για μεν τους φορείς δβ-μα Τουρκικού τύπου από 3,9% έως 28,5%, με Μ.Ο. 13,42%, για δε τους φορείς δβ-μα Σικελικού τύπου από 3,9% έως 18,8% με Μ.Ο. 10,06%. Όσον αφορά τις αιματολογικές παραμέτρους, τους αιματολογικούς δείκτες, τις βιοχημικές τιμές κ.λπ. και εν γένει τους φαινοτύπους και των δύο τύπων ετεροζυγωτών δβ-μα που παρατηρήθηκαν. αυτοί είναι αντίστοιχοι με τυπικούς 149
150 φορείς β-μα με εξαίρετη την HbA 2 που κυμαίνεται σε φυσιολογικά επίπεδα δηλαδή: 2,0-3,2% με μέτρηση σε HPLC (Variant Tm του οίκου Bio-Rad) ή 1,8-3% σε κλασσικές στήλες χρωματογραφίας DEAE. Ενίοτε δε προς τα χαμηλότερα φυσιολογικά επίπεδα. Η δβ-μα Τουρκικού τύπου οφείλεται σε δύο ελλείψεις τμήματος DNA μήκους 11,5 kb και 1,6 Kb καθώς και σε μια αναστροφή τμήματος DNA μήκους 7,6 Kb (Εικ. 37) Ν Μ Εικόνα 37. Ανίχνευση ελλείψεων, υπεύθυνων για δβ -ΜΑ Τουρκικού τύπου, Ν: αρνητικός μάρτυρας, Μ: 100 bp, New England Biolabs. 1, 5, 6, 8: Nl/Nl, 2, 3, 4, 7, 9: ετεροζυγώτες δβ-μα Τουρκικού τύπου. Αναφορικά με τα επίπεδα HbF σε ετεροζυγώτες δβ-μα (Σικελικού και Τουρκικού τύπου), (Μέτρηση σε στήλη HPLC σε Variant Tm του οίκου Bio-Rad), παρατηρείται μεγάλη διαφοροποίηση στις αντίστοιχες τιμές (Γραφική παράσταση 1). Αντίθετα στα επίπεδα της HbA 2 δεν υπάρχει σημαντική διαφοροποίηση των ποσοστών, στους δύο τύπους ετεροζυγωτών δβ-μα. Σε ότι αφορά τα επίπεδα της HbA η ελάττωσή της είναι αντίστοιχη της αύξησης της HbF: Μ.Ο. HbF στους φορείς δβ-μα (Turk) 13,42% M.O. HbF στους φορείς δβ-μα (Sic) 10,06% 150
151 Γραφική παράσταση 1. Διαγραμματική απεικόνιση των επιπέδων της αιμοσφαιρίνης HbF στους ετεροζυγώτες δβ-μα. Τουρκικού τύπου Σικελικού τύπου
152 Μελέτη (γονοτυπική και φαινοτυπική) της δβ-μεσογειακής Αναιμίας Η κατανομή των περιπτώσεων της δβ-μα βάσει των φαινοτυπικώναιματολογικών δεδομένων είναι: 0,34% στο σύνολο του ελληνικού πληθυσμού και 0,87% στο σύνολο του πληθυσμού στο Ν. Καρδίτσας ** Αναφορικά με τη μελέτη του προϊόντος του PCR, σε μοριακό επίπεδο, για τους ετεροζυγώτες δβ-μα, βρέθηκαν οι κάτωθι μεταλλάξεις (Πίνακας 18). Πίνακας 18: Κατανομή ετεροζυγωτών δβ-μα στο νομό Καρδίτσας σε σχέση με το σύνολο του ελληνικού πληθυσμού Τύπος δβ-μα δβ-sic (Σικελικός) δβ-turk (Τουρκικός) Άτομα Ποσοστό % στο Ν. Καρδίτσας Ποσοστό % πανελλαδικά 13 23,2 94, ,8 5,1 ΣΥΝΟΛΟ ,0 100,0 ** Στοιχεία της Μ.Π.Μ.Α. Στοιχεία του Κ.Μ.Α. 152
153 Στον Πίνακα 18 παραθέτουμε τις τιμές των αιματολογικών παραμέτρων και δεικτών στους ετεροζυγώτες δβ-μα. Πίνακας 19. Αιματολογικές παράμετροι και δείκτες σε ετρεοζυγώτες δβ-σικελικού τύπου (δβ-sik) και δβ- Τουρκικού τύπου (δβ-turk) Αιματολογικές Παράμετροι δβ-sic από έως (Μέσος όρος) δβ-turk από έως (Μέσος όρος) Άρρενες Θήλεις Άρρενες Θήλεις Hb 11,6-16,3(13,2) 9,8-12,9(11,4) 9,3-14,8(12,7) 9,5-13,6(11,5) Hct 38,7-53,0(43,5) 32,6-42,5(37,2) 30,5-47,8(41,2) 32,5-43,5(37,0) RBC (6.293) 5.730(5.261) 6.830(5.839) 5.740(5.054) MCH 19,4-24,1(20,9) 18,5-24,6(21,7) 19,6-25,9(21,8) 19,3-25,3(22,8) MCV 65,3-78,4(69,1) 61,4-76,6(70,7) 64,1-79,5(70,6) 64,9-79,6(73,4) MCHC 28,7-31,2(30,3) 30,0-32,1(30,7) 29,5-32,5(30,8) 29,6-32,8(31,2) Ακολούθως αποτυπώνονται στους Πίνακες 20, 21 και 22 τα ποσοστά (%) των αιμοσφαιρινών Α 2,F και Α, καθώς και αντίστοιχες μεταλλαγές στα γ -γονίδια (Αγ5, Gγ5 και Αγ3 ) στους φορείς δβ-μα. Πίνακας 20. Τα ποσοστά των αιμοσφαιρινών Α2, F και Α σε ετεροζυγώτες δβ-μα (δβ-turk) Τουρκικού τύπου, καθώς και οι αντίστοιχες μεταλλάξεις στα γ-γονίδια. HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,8 10,0 77,5 del4 Nl 41883C/A ,5 17,6 71,2 del4 Nl C/A ,4 13,4 72,4 del4 Nl C/A ,5 3,9 84,3 del4 Nl C/A ,4 7,9 79,9 del4 Nl C/A ,5 15,1 73,0 del4 Nl C/A ,2 9,7 71,5 del4 Nl C/A ,2 20,4 73,4 del4 Nl C/A ,7 11,2 77,1 del4 Nl C/A ,6 16,7 71,3 del4 Nl C/A ,47 10,64 del4 Nl C/A ,9 10,0 79,8 del4 Nl C/A ,9 6,6 81,8 del4 Nl C/A ,9 5,1 84,6 del4 Nl C/A ,2 17,6 72,0 del4 Nl C/A 153
154 ,7 7,6 80,6 del4 Nl A/A ,4 11,2 76,2 del4-158 A/A ,2 22,1 72,0 del4-158 A/A ,7 21,9 71,2 del4-158 A/A ,06 21,15 del4-158 A/A ,9 9,0 78,7 del4-158 A/A ,5 19,9 73,5 del4-309 A/A ,3 16,4 74,2-158 A/A ,4 28,5 65,3-158 A/A ,7 12,9 76,5 Nl Nl C/A ,5 22,5 70,6 Nl Nl C/A ,6 25,2 67,2 Nl Nl C/A ,8 10,1 77,8 Nl Nl C/A ,4 11,8 77,7 Nl Nl C/A ,0 14,8 69,0 Nl Nl C/C ,9 6,8 83,1 Nl Nl A/A ,9 22,8 71,3 Nl Nl A/A ,2 11,0 77,4 Nl Nl A/A ,8 11,2 77,0 Nl Nl A/A ,5 12,2 75,9 Nl C/A ,6 8,1 77,6 Nl C/A ,8 10,2 77,1 Nl C/A ,5 15,6 73,7 Nl C/A ,7 8,9 78,3 Nl C/A ,3 7,6 80,6 Nl C/A ,6 8,7 80,4 Nl C/A ,9 9,74 78,8 C/A Μ.Ο 2,57 13,42 75,78 Πίνακας 21. Τα ποσοστά των αιμοσφαιρινών Α2, F και Α σε ετεροζυγώτες δβ -ΜΑ (δβ-sic) Σικελικού τύπου, καθώς και οι αντίστοιχες μεταλλάξεις στα γ-γονίδια. HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,2 8,4 78, / C/C ,5 13,2 75,6-369 Nl C/C ,9 13,3 74,8 Nl -158 C/A ,21 5,64 Nl -158 C/A ,6 8,4 79,7 Nl -158 C/A ,7 9,1 79,1-158 C/A ,8 12,2 76,7 Nl Nl C/C ,8 6,8 81,7 Nl Nl C/C ,7 5,4 83,2 Nl Nl C/C ,7 9,6 78,8 Nl Nl C/C ,7 13,4 75,9 Nl Nl C/C ,6 25,1 68,0 Nl Nl C/C ,1 4,2 84,1 Nl Nl C/C ,9 5,9 83,1 Nl Nl C/A ,8 15,1 73,9 Nl C/A ,4 18,8 75,3 A/A ,1 3,9 84,2 154
155 ,9 6,5 82, ,7 6,3 83,7 Μ.Ο 2,75 10,06 78,75 α/α Πίνακας 22. Τα ποσοστά των αιμοσφαιρινών Α2, F και Α σε διπλούς ετεροζυγώτες δβ-μα και άλλων αιμοσφαιρινοπαθειών. 1 δβ-μα(turk)+ δ-μα 2 Ομόζυγο δβ-μα (δβ-sic+δβ-sic) 3 δβ. ΜΑ(Turk)+ β-μα (β39) HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ3 70 1,1 6,0 83,1 del A/A 79 0,0 86,3 9,1 Nl Nl C/C 132 3,7 90,8 2,2 C/A 3.3 Αποτελέσματα των μεταλλάξεων σε μοριακό επίπεδο της HPFH. Στον Πίνακα 23, απεικονίζονται τα αποτελέσματα των μεταλλάξεων στην HPFH. Πίνακας 23. Ποσοστά των αιμοσφαιρινών Α2, F και A στην HPFH και οι αντίστοιχες μεταλλάξεις στα γ-γονίδια (Αγ5, Gγ5, Αγ3 ). HbA2 HbF HbA Μεταλλάξεις στα γ-γονίδια α/α Αρ. δειγμ. (%) (%) (%) Αγ5 Gγ5 Αγ ,5 11, C/A 2 4 1,8 8, C/A 3 8 2,2 15, C/A 4 9 1,42 15, C/A 155
156 5 11 1,89 10, C/A ,8 16,7 74, C/A ,1 14,3 74,1-117 Nl C/C ,0 15,8 71,6-117 Nl C/C ,1 19,3 75,9-117 Nl C/C ,2 14,1 74,7-117 Nl C/C ,9 14,0 74,0-117 Nl C/C ,8 13,4 75,6-117 Nl C/C ,3 13,3 75,6-117 Nl C/C ,5 4,48 Nl -158 C/A ,3 3,7 86,5 Nl ,7 5,3 84,6 Nl -158/-158 A/A ,9 7,4 79,2 Nl -158/-158 A/A ,0 5,1 85,4 Nl -158/-158 A/A ,3 2,7 84,9 Nl -158/-158 A/A ,8 5,6 84,0 Νl -158/-158 C/A * 2,96 9,92 del4 Nl C/A ,43 14,56 Nl Nl C/C ,9 5,9 82,4 Nl Nl C/C ,0 19,1 71,5 Nl C/C ,7 4,6 87,0 Nl C/A ,4 4,0 86,2 A/A ,2 16,9 72,3 C/C ,5 6,4 77,8 C/A ,2 15,2 74,3 C/A ,41 10,56 C/A ,94 15,00 Μ.Ο. 2,19 10,89 78,66 *HPFH + α 1 Cd14 [G>A] Στη συνέχεια καταγράφονται (Πίνακας 24) τα αποτελέσματα των μεταλλάξεων σε μοριακό επίπεδο των διπλών ετεροζυγωτών HPFH και άλλων αιμοσφαιρινοπαθειών. Πίνακας 24. Ποσοστά των αιμοσφαιρινών Α 2, F και A στους διπλούς ετεροζυγώτες HPFH και άλλων αιμοσφαιρινοπαθειών. Αρ. δειγμ. HbA2 (%) HbF (%) HbA (%) Μεταλλάξεις στα γ- γονίδια α/ Αγ5 Gγ5 Αγ3 α 1 HPFH+β39(β-ΜΑ) 10 2,01 21,0-117 Nl C/A 2 HPFH+β39(β-ΜΑ) 5 2,64 23,16 C/C 3 HPFH+IVS1-1(β- 31 2,7 9,2 80,0 Nl Nl C/C ΜΑ) 4 HPFH+IVS1-1(β ,2 36,2 56,4 C/C ΜΑ) 5 HPFH+δβ Turk 99 1,2 46,4 51,8 156
157 6 HPFH+δβ Turk 109 0,7 67,2 34,8 del4/-117 Nl C/A 7 HPFH+HbS 14 2,5 12,5 52, / -369 C/A 8 HPFH+α 1 Cd14[G>A] 112 2,96 9,92 del4 Nl C/A 9 HPFH+δ-ΜΑ 6 0,53 17, C/A Ακολούθως καταγράφονται (Πίνακας 25) τα αποτελέσματα των μεταλλάξεων των γ-γονιδίων: Αγ5 και Gγ5 ως προς τις μεταλλάξεις Αγ3 σε δείγματα με υψηλή HbF, ήτοι: φ. δβ-μ.α, φ. β-μ.α. με HbF και HPFH. 157
158 Πίνακας 25. Οι μεταλλάξεις Αγ5 / Gγ5, ως προς τις Αγ3, αναλογίες και ποσοστά (%) 158
159 Ακολούθως δίνονται (Πίνακας 26 έως 41) οι μεταλλάξεις στα γονίδια Αγ5 / Gγ5, σε σχέση με τα ενισχυμένα Αγ3, τους αντίστοιχους φαινοτύπους καθώς και τα ποσοστά (%) της HbF. Πίνακας 26. Η μετάλλαξη -117/Nl (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF (%) 1 10* HPFH + β39 21,0 C/A IVS1-1 + Cd2 5,2 C/C HPFH 14,3 C/C HPFH 15,8 C/C HPFH 19,3 C/C HPFH 14,1 C/C HPFH 14,0 C/C HPFH 13,4 C/C C/C HPFH 13,3 * HPFΗ + β39 Παρατηρείται μια σταθερή αναλογία της HbF στη συγκεκριμένη μετάλλαξη, με γενικό Μ.Ο. 14,4% και επιμέρους στην HPFΗ 14,8%. Η συγκεκριμένη μετάλλαξη συνοδεύεται από την μετάλλαξη C/C στα Αγ3 γονίδια. 159
160 Πίνακας 27. Η μετάλλαξη Nl/-158 (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF (%) C/A IVS1-1 4, C/A IVS1-1 5,6 3 98* C/A IVS1-1 5, C/A IVS1-1 6, C/A IVS1-1 6, IVS1-1 4, C/A IVS , C/A IVS , C/A IVS , C/A IVS , C/A IVS , C/A FSC6ήCodon6[-A] 6, C/A FSC6ήCodon6[-A] 11, FSC6ήCodon6[-A] 5, C/A δβ-sic 13, C/A δβ-sic 5, C/A δβ-sic 8, C/A β-39 10, ** C/A β-39 +Cd2 6, C/A IVS , *** C/A IVS , C/A IVS2-1 5, C/A HPFH 4, HPFH 3, A/A 3,5 Μ.Ο. 6,2 *IVS1-1+α 1 Cd14[G>A] **β39+cd2 ***IVS (πολυμορφισμός +20) Η μετάλλαξη Nl /-158 στα Αγ5 /Gγ5 γονίδια αντίστοιχα, συνοδεύεται από τη μετάλλαξη C/A στα Αγ3 γονίδια. Ο Μ.Ο. της HbF είναι συνολικά 6,2% και επιμέρους: IVS1-1 5,5% IVS ,5% FSC6ήCodon6[-A] 7,3% δβ-sic 9,1% 160
161 Πίνακας 28. Η μετάλλαξη -369/Nl (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF. (%) C/C δβ-sic 13, * C/C IVS2-1 4,1 *IVS2-1 + (-3,7) για α-μα Πίνακας 29. Η μετάλλαξη Nl/-109 (Αγ5 /Gγ5 ) α/α Αριθμός Αγ3 Γονότυπος HbF δείγματος (%) 1 107* 41883C/C β39 4,1 Nέα μετάλλαξη (-109) Πίνακας 30. Η μετάλλαξη Nl / (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF (%) Α/Α HPFH 5, Α/Α HPFH 2, Α/Α HPFH 7, Α/Α HPFH 5, C/A HPFH 5,6 Μ.Ο. 5,2 Η μετάλλαξη Nl / -158 στα Αγ5 /Gγ5 γονίδια συνοδεύονται από τη μετάλλαξη 41883Α/Α -158 στα Αγ3 γονίδια. Πίνακας 31. Η μετάλλαξη del4-117 / Nl (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF (%) C/A HPFH+δβ- Turk 67,2 161
162 Πίνακας 32. Η μετάλλαξη -117/-158 (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF (%) C/A HPFH 11, C/A HPFH 8,35 3 6* C/A HPFH 17, C/A HPFH 14, C/A HPFH 15, C/A HPFH 10, C/A HPFH 16,70 Μ.Ο. 13,3 *HPFH+δ-Μ.Α. Η μετάλλαξη -117/-158 στα Αγ5 /Gγ5 γονίδια συνοδεύεται από τη μετάλλαξη C/A στα Αγ3 γονίδια. Πίνακας 33. Η μετάλλαξη Nl/Nl (Αγ5 / Gγ5) α/α Αριθμός Αγ3 Γονότυπος HbF(%) δείγματος C/C HPFH+IVS1-1 9, C/C IVS1-1 1, C/C IVS1-1 5, C/C IVS1-1 5, C/C IVS1-1 10, C/C IVS1-1 2, C/C IVS1-1 3, C/C δβ-sic 12, C/C δβ-sic 6, C/C δβ-sic 5, C/C δβ-sic 9, C/C δβ-sic 13, C/C δβ-sic+δβ-sic 86, C/A δβ-sic 5, C/A δβ-turk 12, C/A δβ-turk 22, C/A δβ-turk 25, C/A δβ-turk 10, C/A δβ-turk 11, A/A δβ-turk 6, A/A δβ-turk 22, A/A δβ-turk 11, Α/Α δβ-turk 11, C/C δβ-turk 14, C/C HPFH 14, C/C HPFH 5, C/C β39 4, C/C 5, C/C δβ-sic 25,1 162
163 C/C IVS1-1 4, C/C δβ-sic 4, δβ-sic 2,9 Μ.Ο. Ο τύπος Nl/Nl στα Αγ5 /Gγ5 γονίδια, συνοδεύεται κατά κύριο λόγω από τη μετάλλαξη 41883C/C (67,7%) στα Αγ3 γονίδια και δευτερευόντως από τις μεταλλάξεις 41883C/A (19,3%) και 41883Α/Α (12,9%). Ο Μ.Ο. της αιμοσφαιρίνης της HbF είναι συνολικά 9,9% και επιμέρους: IVS1-1 4,7% δβ-sic 10,6% δβ-turk 14,9% Πίνακας 34. Η μετάλλαξη -158/-158 (Αγ5 /Gγ5 ) α/α Αριθμός Αγ3 Γονότυπος HbF(%) δείγματος C/A IVS1-1 9,0 Πίνακας 35. Η μετάλλαξη -117 / -309 (Αγ5 /Gγ5 ) -369 α/α Αριθμός Αγ3 Γονότυπος HbF δείγματος (%) C/A HPFH+HbS 12,5 Πίνακας 36. Η μετάλλαξη -369/-158 (Αγ5 /Gγ5 ) α/α Αριθμός Αγ3 Γονότυπος HbF(%) δείγματος C/A FSC6ή Codon 6[-Α] 3,9 163
164 Πίνακας 37. Η μετάλλαξη del4/nl (Αγ5 /Gγ5 ) α/α Αριθμός Αγ3 Γονότυπος HbF(%) δείγματος C/A δβ-turk 10, C/A δβ-turk 17, C/A δβ-turk 13, C/A δβ-turk 3, C/A δβ-turk 7, C/A δβ-turk 15, C/A δβ-turk 9, C/A δβ-turk 20, C/A δβ-turk 11, C/A δβ-turk 16, C/A δβ-turk 10, C/A δβ-turk 10, C/A δβ-turk 6, C/A δβ-turk 5, C/A δβ-turk 17, A/A δβ-turk 7, C/A β39 8, C/A β39 4, C/A β39 6, C/A IVS1-1 4, C/A IVS1-1 4, * C/A HPFH+α 1 Cd14[G>A] 9,92 M.O. 10,0 * HPFH + α 1 Cd14[G>A] Η μετάλλαξη del4/nl στα (Αγ5 /Gγ5 ) γονίδια αντίστοιχα στη δβ-turk συνοδεύεται από μετάλλαξη C/A στα Αγ3 γονίδια όπως και στη β39 και στην IVS1-1. Τα ποσοστά της HbF είναι στο γενικό Μ.Ο 10,0% και επιμέρους: δβ-turk 11,4% β39 6,4% IVS1-1 4,5% Πίνακας 38. Η μετάλλαξη -369 / -158 (Αγ5 /Gγ5 ) -158 α/α Αριθμός Αγ3 Γονότυπος HbF δείγματος (%) C/C δβ-sic 8,4 164
165 Πίνακας 39. Η μετάλλαξη del4/-158 (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF (%) Α/Α δβ-turk 11, Α/Α δβ-turk 22,1 3 70* Α/Α δβ-turk 6, Α/Α δβ-turk 21, Α/Α δβ-turk 21, Α/Α δβ-turk 9,0 Μ.Ο. 15,2 *δβ-μα+δ-μα Η μετάλλαξη del4/-158 στα Αγ5 /Gγ5 γονίδια αντίστοιχα παρατηρείται στη δβ- Turk και συνοδεύεται από τη μετάλλαξη Α/Α στα Αγ3 γονίδια με Μ.Ο. HbF 15,2%. Πίνακας 40. Η μετάλλαξη del4/-309 (Αγ5 /Gγ5 ) α/α Αριθμός δείγματος Αγ3 Γονότυπος HbF (%) Α/ Α δβ-turk 19,9 Πίνακας 41. φ.β. Μ.Α. με HbF, φ.δβ - Μ.Α. και HPFH Αγ3 φ.β-μ.α. με HbF φ.δβ-μ.α. HPFH ΓΟΝΟΤΥΠΟΣ ΑΝΑΛΟΓΙΑ ΠΟΣΟΣΤΟ% ΑΝΑΛΟΓΙΑ ΠΟΣΟΣΤΟ% ΑΝΑΛΟΓΙΑ ΠΟΣΟΣΤΟ% C/C 13/38 34,20% 14/65 22,40 16/44 36,39 A/A 4/38 10,50% 15/65 15,30 6/44 13,60 C/A 21/38 55,20% 36/65 55,30 22/44 56,00 Στις εικόνες απεικονίζεται ενδεικτικά η ανάλυση των αλληλουχιών του DNA, που πραγματοποιήθηκε με την τεχνική DNA sequencing για τις μεταλλάξεις που αφορούν τα Αγ5 και Gγ5 γονίδια. 165
166 Εικόνα 38. Ετεροζυγώτης για τη μετάλλαξη del4 στα Αγ5 γονίδια. Ανάλυση του προϊόντος PCR με DNA Sequencing. Εικόνα 39. Ετεροζυγώτης για τη μετάλλαξη -158 στα Gγ5 γονίδια. Ανάλυση του προϊόντος PCR με DNA Sequencing. 166
167 Εικόνα 40. Ετεροζυγώτης για τη μετάλλαξη -117 στα Aγ 5 γονίδια. Ανάλυση του προϊόντος PCR με DNA Sequencing. Εικόνα 41. Ετεροζυγώτης για τη μετάλλαξη -369 στα Aγ5 γονίδια (θέση 222). 167
168 Εικόνα 42. Ετεροζυγώτης για τη μετάλλαξη -309 στα Gγ 5 γονίδια (θέση 273). Ανάλυση του προϊόντος PCR με DNA Sequencing. Εικόνα 43. Ομοζυγώτης για τη μετάλλαξη -158/-158 στα Gγ5 γονίδια (θέση 76 G Τ). 168
Διαταραχές των αιμοσφαιρινών Συνηθέστερη μονογονιδιακή διαταραχή στους ανθρώπους Το 5% του πληθυσμού είναι φορείς γονιδίων για κλινικώς σημαντικές
 1 Διαταραχές των αιμοσφαιρινών Συνηθέστερη μονογονιδιακή διαταραχή στους ανθρώπους Το 5% του πληθυσμού είναι φορείς γονιδίων για κλινικώς σημαντικές διαταραχές της αιμοσφαιρίνης 2 Αποτελείται από δύο α
1 Διαταραχές των αιμοσφαιρινών Συνηθέστερη μονογονιδιακή διαταραχή στους ανθρώπους Το 5% του πληθυσμού είναι φορείς γονιδίων για κλινικώς σημαντικές διαταραχές της αιμοσφαιρίνης 2 Αποτελείται από δύο α
ΑΙΜΟΣΦΑΙΡΙΝΗ: ΟΜΗ ΕΚΦΡΑΣΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΘΑΛΑΣΑΙΜΙΕΣ. Α. ΠΑΠΑΧΑΤΖΟΠΟΥΛΟΥ 15 Μαρτίου 2017
 ΑΙΜΟΣΦΑΙΡΙΝΗ: ΟΜΗ ΕΚΦΡΑΣΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΣΦΑΙΡΙΝΙΚΩΝ ΓΟΝΙ ΙΩΝ ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΘΑΛΑΣΑΙΜΙΕΣ Α. ΠΑΠΑΧΑΤΖΟΠΟΥΛΟΥ 15 Μαρτίου 2017 ομή της αιμοσφαιρίνης Α του ανθρώπου γονιδιακοί τόποι ευθύνονται για
ΑΙΜΟΣΦΑΙΡΙΝΗ: ΟΜΗ ΕΚΦΡΑΣΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΣΦΑΙΡΙΝΙΚΩΝ ΓΟΝΙ ΙΩΝ ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΘΑΛΑΣΑΙΜΙΕΣ Α. ΠΑΠΑΧΑΤΖΟΠΟΥΛΟΥ 15 Μαρτίου 2017 ομή της αιμοσφαιρίνης Α του ανθρώπου γονιδιακοί τόποι ευθύνονται για
ΑΙΜΟΣΦΑΙΡΙΝΗ: ΟΜΗ ΕΚΦΡΑΣΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΘΑΛΑΣΑΙΜΙΕΣ. Α. ΠΑΠΑΧΑΤΖΟΠΟΥΛΟΥ 23 Φεβρουαρίου 2016
 ΑΙΜΟΣΦΑΙΡΙΝΗ: ΟΜΗ ΕΚΦΡΑΣΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΣΦΑΙΡΙΝΙΚΩΝ ΓΟΝΙ ΙΩΝ ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΘΑΛΑΣΑΙΜΙΕΣ Α. ΠΑΠΑΧΑΤΖΟΠΟΥΛΟΥ 23 Φεβρουαρίου 2016 ομή της αιμοσφαιρίνης Α του ανθρώπου γονιδιακοί τόποι ευθύνονται
ΑΙΜΟΣΦΑΙΡΙΝΗ: ΟΜΗ ΕΚΦΡΑΣΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΣΦΑΙΡΙΝΙΚΩΝ ΓΟΝΙ ΙΩΝ ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΘΑΛΑΣΑΙΜΙΕΣ Α. ΠΑΠΑΧΑΤΖΟΠΟΥΛΟΥ 23 Φεβρουαρίου 2016 ομή της αιμοσφαιρίνης Α του ανθρώπου γονιδιακοί τόποι ευθύνονται
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ)
 ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» Η κυκλοφορία του αίματος και
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» Η κυκλοφορία του αίματος και
αμινοξύ. Η αλλαγή αυτή έχει ελάχιστη επίδραση στη στερεοδιάταξη και τη λειτουργικότητα της πρωτεϊνης. Επιβλαβής
 Κεφάλαιο 6: ΜΕΤΑΛΛΑΞΕΙΣ -ΘΕΩΡΙΑ- Μεταλλάξεις είναι οι αλλαγές που συμβαίνουν στο γενετικό υλικό ενός οργανισμού, τόσο σε γονιδιακό επίπεδο (γονιδιακές μεταλλάξεις) όσο και σε χρωμοσωμικό επίπεδο (χρωμοσωμικές
Κεφάλαιο 6: ΜΕΤΑΛΛΑΞΕΙΣ -ΘΕΩΡΙΑ- Μεταλλάξεις είναι οι αλλαγές που συμβαίνουν στο γενετικό υλικό ενός οργανισμού, τόσο σε γονιδιακό επίπεδο (γονιδιακές μεταλλάξεις) όσο και σε χρωμοσωμικό επίπεδο (χρωμοσωμικές
Αιμοσφαιρίνες. Αιμοσφαιρίνη Συμβολισμός Σύσταση A HbA α 2 β 2 F HbF α 2 γ 2 A 2 HbA 2 α 2 δ 2 s. Σύγκριση γονιδιακών και χρωμοσωμικών μεταλλάξεων
 A. ΔΙΑΓΡΑΜΜΑ Αιμοσφαιρίνες Αιμοσφαιρίνη Συμβολισμός Σύσταση A HbA α 2 β 2 F HbF α 2 γ 2 A 2 HbA 2 α 2 δ 2 S HbS s α 2 β 2 Σύγκριση γονιδιακών και χρωμοσωμικών μεταλλάξεων ΓΟΝΙΔΙΑΚΕΣ Αλλαγή σε αζωτούχες
A. ΔΙΑΓΡΑΜΜΑ Αιμοσφαιρίνες Αιμοσφαιρίνη Συμβολισμός Σύσταση A HbA α 2 β 2 F HbF α 2 γ 2 A 2 HbA 2 α 2 δ 2 S HbS s α 2 β 2 Σύγκριση γονιδιακών και χρωμοσωμικών μεταλλάξεων ΓΟΝΙΔΙΑΚΕΣ Αλλαγή σε αζωτούχες
Εισαγωγή. Οι β-θαλασσαιμίες αποτελούν μία ετερογενή ομάδα κληρονομικών νοσημάτων που χαρακτηρίζονται από μειωμένη σύνθεση των β-αλυσίδων της αιμοσφαιρ
 03 εδbοτχ 155 Εισαγωγή. Οι β-θαλασσαιμίες αποτελούν μία ετερογενή ομάδα κληρονομικών νοσημάτων που χαρακτηρίζονται από μειωμένη σύνθεση των β-αλυσίδων της αιμοσφαιρίνης. Στην ομόζυγη κατάσταση προκαλούν
03 εδbοτχ 155 Εισαγωγή. Οι β-θαλασσαιμίες αποτελούν μία ετερογενή ομάδα κληρονομικών νοσημάτων που χαρακτηρίζονται από μειωμένη σύνθεση των β-αλυσίδων της αιμοσφαιρίνης. Στην ομόζυγη κατάσταση προκαλούν
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
ΒΙΟΛΟΓΙΑ. 1 ο ΔΙΑΓΩΝΙΣΜΑ ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ 1 o
 ΘΕΜΑ 1 o Γ ΛΥΚΕΙΟΥ-ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ 1 ο ΔΙΑΓΩΝΙΣΜΑ Α. Γιατί τα βακτήρια μπορούν να χρησιμοποιηθούν σαν «εργοστάσια παραγωγής ανθρώπινων πρωτεϊνών»; Β. Σε ένα βακτήριο εισάγεται με τη μέθοδο του ανασυνδυασμένου
ΘΕΜΑ 1 o Γ ΛΥΚΕΙΟΥ-ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ 1 ο ΔΙΑΓΩΝΙΣΜΑ Α. Γιατί τα βακτήρια μπορούν να χρησιμοποιηθούν σαν «εργοστάσια παραγωγής ανθρώπινων πρωτεϊνών»; Β. Σε ένα βακτήριο εισάγεται με τη μέθοδο του ανασυνδυασμένου
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΠΑΝΕΛΛΗΝΙΩΝ 2017 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII Δ Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Στους προκαρυωτικούς
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΠΑΝΕΛΛΗΝΙΩΝ 2017 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII Δ Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Στους προκαρυωτικούς
ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ
 27 Μαΐου 2016 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων (Νέο & Παλιό Σύστημα) ΘΕΜΑ Γ Γ.1 Ο χαρακτήρας της ομάδας αίματος στον άνθρωπο
27 Μαΐου 2016 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων (Νέο & Παλιό Σύστημα) ΘΕΜΑ Γ Γ.1 Ο χαρακτήρας της ομάδας αίματος στον άνθρωπο
ΠΑΝΕΛΛAΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛAΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 16-06-2017 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α. φωσφορική ομάδα (Ι) E. υδροξύλιο (II) Β. mrna
ΠΑΝΕΛΛAΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 16-06-2017 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α. φωσφορική ομάδα (Ι) E. υδροξύλιο (II) Β. mrna
ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 16-2-2014 ΘΕΜΑ 1 ο Α. Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση. (Μονάδες 25)
 ΤΣΙΜΙΣΚΗ &ΚΑΡΟΛΟΥ ΝΤΗΛ ΓΩΝΙΑ THΛ: 270727 222594 ΑΡΤΑΚΗΣ 12 - Κ. ΤΟΥΜΠΑ THΛ: 919113 949422 ΕΠΩΝΥΜΟ:... ΟΝΟΜΑ:... ΤΜΗΜΑ:... ΗΜΕΡΟΜΗΝΙΑ:... ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 16-2-2014 ΘΕΜΑ 1 ο Α. Να βάλετε σε
ΤΣΙΜΙΣΚΗ &ΚΑΡΟΛΟΥ ΝΤΗΛ ΓΩΝΙΑ THΛ: 270727 222594 ΑΡΤΑΚΗΣ 12 - Κ. ΤΟΥΜΠΑ THΛ: 919113 949422 ΕΠΩΝΥΜΟ:... ΟΝΟΜΑ:... ΤΜΗΜΑ:... ΗΜΕΡΟΜΗΝΙΑ:... ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 16-2-2014 ΘΕΜΑ 1 ο Α. Να βάλετε σε
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο 1. β 2. γ 3. α 4. γ 5. δ ΘΕΜΑ 2ο 1. Σχολικό
1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο 1. β 2. γ 3. α 4. γ 5. δ ΘΕΜΑ 2ο 1. Σχολικό
ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ ΠΡΟΛΟΓΟΣ ΠΡΟΕΛΕΥΣΗ-ΠΑΡΟΥΣΙΑ ΣΗΜΕΡΑ
 ΠΡΟΛΟΓΟΣ ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ Η μεσογειακή αναιμία ή θαλασσαιμία είναι κληρονομική αυτοσωμική υπολειπόμενη νόσος η οποία εντοπίζεται κυρίως στην περιοχή της Μεσογείου Θάλασσας. Στη Μεσογειακή αναιμία η γονιδιακή
ΠΡΟΛΟΓΟΣ ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ Η μεσογειακή αναιμία ή θαλασσαιμία είναι κληρονομική αυτοσωμική υπολειπόμενη νόσος η οποία εντοπίζεται κυρίως στην περιοχή της Μεσογείου Θάλασσας. Στη Μεσογειακή αναιμία η γονιδιακή
Κεφάλαιο 6: Μεταλλάξεις
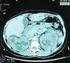 Κεφάλαιο 6: Μεταλλάξεις ΕΛΕΓΧΟΣ ΓΝΩΣΕΩΝ 1. Τι ονομάζονται μεταλλάξεις και ποια τα κυριότερα είδη τους; 2. Ποιες οι διαφορές μεταξύ γονιδιακών και χρωμοσωμικών μεταλλάξεων; 3. Οι μεταλλάξεις στα σωματικά
Κεφάλαιο 6: Μεταλλάξεις ΕΛΕΓΧΟΣ ΓΝΩΣΕΩΝ 1. Τι ονομάζονται μεταλλάξεις και ποια τα κυριότερα είδη τους; 2. Ποιες οι διαφορές μεταξύ γονιδιακών και χρωμοσωμικών μεταλλάξεων; 3. Οι μεταλλάξεις στα σωματικά
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ ΕΞΕΤΑΣΗΣ: ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: 16 / 06 / 2017 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ Θέμα Α Α1: δ Α2:
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ ΕΞΕΤΑΣΗΣ: ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: 16 / 06 / 2017 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑΤΩΝ Θέμα Α Α1: δ Α2:
ΘΕΜΑ Α. 1. δ 2. δ 3. β 4. γ 5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI Δ VII Ε II ΣΤ III Ζ V Η -
 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ 2017 ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΙΜΕΛΕΙΑ: Π. ΚΡΥΣΤΑΛΛΙΔΗΣ 1. δ 2. δ 3. β 4. γ 5. α ΘΕΜΑ Α Β1. Α I Β IV Γ VI Δ VII Ε II ΣΤ III Ζ V Η - ΘΕΜΑ Β Β2. Η εικόνα αντιστοιχεί
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ 2017 ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΙΜΕΛΕΙΑ: Π. ΚΡΥΣΤΑΛΛΙΔΗΣ 1. δ 2. δ 3. β 4. γ 5. α ΘΕΜΑ Α Β1. Α I Β IV Γ VI Δ VII Ε II ΣΤ III Ζ V Η - ΘΕΜΑ Β Β2. Η εικόνα αντιστοιχεί
ΦΡΟΝΤΙΣΤΗΡΙΟ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΗΡΑΚΛΕΙΤΟΣ ΚΩΛΕΤΤΗ
 ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΟΥΝΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ε Ν Δ Ε Ι Κ Τ Ι Κ Ε Σ Α Π Α Ν Τ Η Σ Ε Ι Σ Θ Ε Μ Α Τ Ω Ν ΘΕΜΑ Α Α1-δ Α2-δ Α3-β
ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΟΥΝΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ε Ν Δ Ε Ι Κ Τ Ι Κ Ε Σ Α Π Α Ν Τ Η Σ Ε Ι Σ Θ Ε Μ Α Τ Ω Ν ΘΕΜΑ Α Α1-δ Α2-δ Α3-β
ΜΕΛΕΤΗ ΜΗΧΑΝΙΣΜΩΝ ΔΡΑΣΗΣ ΤΗΣ ΥΔΡΟΞΥΟΥΡΙΑΣ ΣΕ ΣΥΝΔΥΑΣΜΟ ΜΕ ΑΛΛΕΣ ΚΥΤΤΑΡΟΚΙΝΕΣ ΣΕ ΚΑΛΛΙΕΡΓΕΙΕΣ ΑΡΧΕΓΟΝΩΝ ΑΙΜΟΠΟΙΗΤΙΚΩΝ ΚΥΤΤΑΡΩΝ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΗΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ ΜΕΛΕΤΗ ΜΗΧΑΝΙΣΜΩΝ ΔΡΑΣΗΣ ΤΗΣ ΥΔΡΟΞΥΟΥΡΙΑΣ ΣΕ ΣΥΝΔΥΑΣΜΟ ΜΕ ΑΛΛΕΣ ΚΥΤΤΑΡΟΚΙΝΕΣ ΣΕ ΚΑΛΛΙΕΡΓΕΙΕΣ ΑΡΧΕΓΟΝΩΝ ΑΙΜΟΠΟΙΗΤΙΚΩΝ ΚΥΤΤΑΡΩΝ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΗΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ ΜΕΛΕΤΗ ΜΗΧΑΝΙΣΜΩΝ ΔΡΑΣΗΣ ΤΗΣ ΥΔΡΟΞΥΟΥΡΙΑΣ ΣΕ ΣΥΝΔΥΑΣΜΟ ΜΕ ΑΛΛΕΣ ΚΥΤΤΑΡΟΚΙΝΕΣ ΣΕ ΚΑΛΛΙΕΡΓΕΙΕΣ ΑΡΧΕΓΟΝΩΝ ΑΙΜΟΠΟΙΗΤΙΚΩΝ ΚΥΤΤΑΡΩΝ
ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ <=> R
 ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ R ΔΕΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ ΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ (Σταθερότητα, χαμηλή συγγένεια για Ο2Εύκαμπτη, υψηλή συγγένεια για Ο2) Λόγο των
ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ R ΔΕΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ ΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ (Σταθερότητα, χαμηλή συγγένεια για Ο2Εύκαμπτη, υψηλή συγγένεια για Ο2) Λόγο των
«β-μεσογειακή αναιμία: το πιο συχνό μονογονιδιακό νόσημα στη χώρα μας»
 Εργαστήριο Κυτταρογενετικής ΕΚΕΦΕ «Δημόκριτος» «β-μεσογειακή αναιμία: το πιο συχνό μονογονιδιακό νόσημα στη χώρα μας» Ζαχάκη Σοφία - Ουρανία Βιολόγος, MSc, PhD β μεσογειακή αναιμία Η θαλασσαιμία ή νόσος
Εργαστήριο Κυτταρογενετικής ΕΚΕΦΕ «Δημόκριτος» «β-μεσογειακή αναιμία: το πιο συχνό μονογονιδιακό νόσημα στη χώρα μας» Ζαχάκη Σοφία - Ουρανία Βιολόγος, MSc, PhD β μεσογειακή αναιμία Η θαλασσαιμία ή νόσος
ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (ΘΑΛΑΣΣΑΙΜΙΑ)
 ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (ΘΑΛΑΣΣΑΙΜΙΑ) Αλεξάνδρα Κουράκλη-Συμεωνίδου Απαρτιωμένη διδασκαλία Φεβρουάριος-Μάρτιος 2015 ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (Θαλασσαιμία) Πρόκειται για μία ετερογενή ομάδα κληρονομικών αναιμιών (αυτοσωματικών-υπολοιπόμενων)
ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (ΘΑΛΑΣΣΑΙΜΙΑ) Αλεξάνδρα Κουράκλη-Συμεωνίδου Απαρτιωμένη διδασκαλία Φεβρουάριος-Μάρτιος 2015 ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (Θαλασσαιμία) Πρόκειται για μία ετερογενή ομάδα κληρονομικών αναιμιών (αυτοσωματικών-υπολοιπόμενων)
ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (ΘΑΛΑΣΣΑΙΜΙΑ)
 ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (ΘΑΛΑΣΣΑΙΜΙΑ) Αλεξάνδρα Κουράκλη-Συμεωνίδου Διευθύντρια ΕΣΥ Υπεύθυνη Μον. Μεσογ. Αναιμίας ΠΓΝ Πατρών Απαρτιωμένη διδασκαλία Αιματολογίας Μάρτιος 2017 Εκπαιδευτικοί στόχοι Κλινική ταξινόμηση
ΜΕΣΟΓΕΙΑΚΗ ΑΝΑΙΜΙΑ (ΘΑΛΑΣΣΑΙΜΙΑ) Αλεξάνδρα Κουράκλη-Συμεωνίδου Διευθύντρια ΕΣΥ Υπεύθυνη Μον. Μεσογ. Αναιμίας ΠΓΝ Πατρών Απαρτιωμένη διδασκαλία Αιματολογίας Μάρτιος 2017 Εκπαιδευτικοί στόχοι Κλινική ταξινόμηση
ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2018
 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ
ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ
ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦ. 6 ο ΜΕΤΑΛΛΑΞΕΙΣ
 ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦ. 6 ο ΜΕΤΑΛΛΑΞΕΙΣ Μεταλλάξεις είναι οι αλλαγές στην αλληλουχία των νουκλεοτιδίων που συμβαίνουν στο γενετικό υλικό ενός οργανισμού τόσο σε γονιδιακό επίπεδο (γονιδιακές μεταλλάξεις)
ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦ. 6 ο ΜΕΤΑΛΛΑΞΕΙΣ Μεταλλάξεις είναι οι αλλαγές στην αλληλουχία των νουκλεοτιδίων που συμβαίνουν στο γενετικό υλικό ενός οργανισμού τόσο σε γονιδιακό επίπεδο (γονιδιακές μεταλλάξεις)
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. δ Α2. γ Α3. δ Α4. β Α5. α 2 β 5 γ 6 δ 1 ε 3 ΑΠΑΝΤΗΣΕΙΣ
1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 18 ΙΟΥΝΙΟΥ 2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. δ Α2. γ Α3. δ Α4. β Α5. α 2 β 5 γ 6 δ 1 ε 3 ΑΠΑΝΤΗΣΕΙΣ
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων. Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014. Απαντήσεις Θεμάτων
 Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
ΠΑΝΕΛΛΗΝΙΕ 2017 ΑΠΑΝΣΗΕΙ ΣΟ ΜΑΘΗΜΑ ΣΗ ΒΙΟΛΟΓΙΑ ΠΡΟΑΝΑΣΟΛΙΜΟΤ
 ΠΑΝΕΛΛΗΝΙΕ 2017 ΑΠΑΝΣΗΕΙ ΣΟ ΜΑΘΗΜΑ ΣΗ ΒΙΟΛΟΓΙΑ ΠΡΟΑΝΑΣΟΛΙΜΟΤ 16/06/2017 ΕΠΙΜΕΛΕΙΑ: ΑΝΔΡΙΑΝΗ ΠΑΡΑΧΗ ΘΕΜΑ Α A1. Δ Α2. Δ Α3. Β Α4. Γ Α5.Α ΘΕΜΑ Β Β1) I A II E III Σ IV Β V Ζ VI Γ VII Δ Β2) ε προκαρυωτικό γιατί
ΠΑΝΕΛΛΗΝΙΕ 2017 ΑΠΑΝΣΗΕΙ ΣΟ ΜΑΘΗΜΑ ΣΗ ΒΙΟΛΟΓΙΑ ΠΡΟΑΝΑΣΟΛΙΜΟΤ 16/06/2017 ΕΠΙΜΕΛΕΙΑ: ΑΝΔΡΙΑΝΗ ΠΑΡΑΧΗ ΘΕΜΑ Α A1. Δ Α2. Δ Α3. Β Α4. Γ Α5.Α ΘΕΜΑ Β Β1) I A II E III Σ IV Β V Ζ VI Γ VII Δ Β2) ε προκαρυωτικό γιατί
Αιμοσφαιρίνη και αιμοσφαιρινοπάθειες
 Αιμοσφαιρίνη και αιμοσφαιρινοπάθειες Αιμοσφαιρίνη Η ανθρώπινη αιμοσφαιρίνη μπορεί να μελετηθεί ευκολότερα από οποιαδήποτε άλλη πρωτεΐνη του ανθρώπου. Παράδειγμα για: ομή και λειτουργία πρωτεϊνών, ομή και
Αιμοσφαιρίνη και αιμοσφαιρινοπάθειες Αιμοσφαιρίνη Η ανθρώπινη αιμοσφαιρίνη μπορεί να μελετηθεί ευκολότερα από οποιαδήποτε άλλη πρωτεΐνη του ανθρώπου. Παράδειγμα για: ομή και λειτουργία πρωτεϊνών, ομή και
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / Γ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 29/12/2016
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / Γ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 29/12/2016 ΘΕΜΑ 1 ο 1. α 2. β 3. γ 4. γ 5. δ ΘΕΜΑ 2ο Β1. Σημειώστε κάθε πρόταση με Σωστό ή Λάθος παραθέτοντας μια σύντομη δικαιολόγηση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / Γ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 29/12/2016 ΘΕΜΑ 1 ο 1. α 2. β 3. γ 4. γ 5. δ ΘΕΜΑ 2ο Β1. Σημειώστε κάθε πρόταση με Σωστό ή Λάθος παραθέτοντας μια σύντομη δικαιολόγηση
Βιολογία Κατεύθυνσης Γ Λυκείου ΚΥΡΙΑΚΗ 9 ΜΑΡΤΙΟΥ 2014 ΑΠΑΝΤΗΣΕΙΣ
 Βιολογία Κατεύθυνσης Γ Λυκείου ΚΥΡΙΑΚΗ 9 ΜΑΡΤΙΟΥ 2014 ΑΠΑΝΤΗΣΕΙΣ Επιμέλεια: Δημήτρης Κοτρόπουλος ΘΕΜΑ Α Α1. γ Α2. γ Α3. γ Α4. δ Α5. δ ΘΕΜΑ B B1. Στήλη Ι Στήλη ΙΙ 1. στ 2. ζ 3. ε 4. α 5. δ 6. β 7. γ Β2.
Βιολογία Κατεύθυνσης Γ Λυκείου ΚΥΡΙΑΚΗ 9 ΜΑΡΤΙΟΥ 2014 ΑΠΑΝΤΗΣΕΙΣ Επιμέλεια: Δημήτρης Κοτρόπουλος ΘΕΜΑ Α Α1. γ Α2. γ Α3. γ Α4. δ Α5. δ ΘΕΜΑ B B1. Στήλη Ι Στήλη ΙΙ 1. στ 2. ζ 3. ε 4. α 5. δ 6. β 7. γ Β2.
Αθήνα, 16/06/2017 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΒΙΟΕΠΙΣΤΗΜΟΝΩΝ
 Αθήνα, 16/06/2017 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΒΙΟΕΠΙΣΤΗΜΟΝΩΝ Σας αποστέλλουμε τις προτεινόμενες απαντήσεις και το Δελτίο Τύπου που αφορούν τα θέματα της Βιολογίας Προσανατολισμού των Ημερησίων Γενικών Λυκείων. Η
Αθήνα, 16/06/2017 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΒΙΟΕΠΙΣΤΗΜΟΝΩΝ Σας αποστέλλουμε τις προτεινόμενες απαντήσεις και το Δελτίο Τύπου που αφορούν τα θέματα της Βιολογίας Προσανατολισμού των Ημερησίων Γενικών Λυκείων. Η
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 26/01/2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 26/01/2014 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Αλλαγές στην ποσότητα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 26/01/2014 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Αλλαγές στην ποσότητα
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων. Εξεταζόμενο Μάθημα: Βιολογία Θετικής Προσανατολισμού Θετικών Σπουδών, Ημ/νία: 16 Ιουνίου 2017
 Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Προσανατολισμού Θετικών Σπουδών, Ημ/νία: 16 Ιουνίου 2017 Απαντήσεις Θεμάτων ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Προσανατολισμού Θετικών Σπουδών, Ημ/νία: 16 Ιουνίου 2017 Απαντήσεις Θεμάτων ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής
 Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
ΚΕΦ. 6 ο ΕΡΩΤΗΣΕΙΣ ΚΡΙΣΕΩΣ
 ΚΕΦ. 6 ο ΕΡΩΤΗΣΕΙΣ ΚΡΙΣΕΩΣ 1. Μπορούν τα γονίδια που ελέγχουν τη σύνθεση της α-αλυσίδας της αιμοσφαιρίνης να χαρακτηριστούν ως πολλαπλά αλληλόμορφα; Τα γονίδια που ελέγχουν την α-αλυσίδα της αιμοσφαιρίνης
ΚΕΦ. 6 ο ΕΡΩΤΗΣΕΙΣ ΚΡΙΣΕΩΣ 1. Μπορούν τα γονίδια που ελέγχουν τη σύνθεση της α-αλυσίδας της αιμοσφαιρίνης να χαρακτηριστούν ως πολλαπλά αλληλόμορφα; Τα γονίδια που ελέγχουν την α-αλυσίδα της αιμοσφαιρίνης
Βιολογία ΘΕΜΑ Α ΘΕΜΑ B
 Βιολογία προσανατολισμού Α. 1. β 2. γ 3. δ 4. γ 5. δ ΘΕΜΑ Α B1. 4,1,2,6,8,3,5,7 ΘΕΜΑ B B2. Σχολικό βιβλίο σελ. 103 Η γενετική καθοδήγηση είναι.υγιών απογόνων. Σχολικό βιβλίο σελ. 103 Παρ ότι γενετική καθοδήγηση
Βιολογία προσανατολισμού Α. 1. β 2. γ 3. δ 4. γ 5. δ ΘΕΜΑ Α B1. 4,1,2,6,8,3,5,7 ΘΕΜΑ B B2. Σχολικό βιβλίο σελ. 103 Η γενετική καθοδήγηση είναι.υγιών απογόνων. Σχολικό βιβλίο σελ. 103 Παρ ότι γενετική καθοδήγηση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / Γ ΙΑΤΡ ΓΘΕΤ 2 ΗΜΕΡΟΜΗΝΙΑ: 20/03/2016 ΘΕΜΑ Α
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / Γ ΙΑΤΡ ΓΘΕΤ 2 ΗΜΕΡΟΜΗΝΙΑ: 20/03/2016 ΘΕΜΑ Α 1. α 2. δ 3. γ 4. δ 5. γ. ΘΕΜΑ Β 1. Τα αντισώματα αποτελούν το πιο αποτελεσματικό φυσικό φάρμακο για την αντιμετώπιση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / Γ ΙΑΤΡ ΓΘΕΤ 2 ΗΜΕΡΟΜΗΝΙΑ: 20/03/2016 ΘΕΜΑ Α 1. α 2. δ 3. γ 4. δ 5. γ. ΘΕΜΑ Β 1. Τα αντισώματα αποτελούν το πιο αποτελεσματικό φυσικό φάρμακο για την αντιμετώπιση
ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ
 ΑΣΘΕΝΕΙΕΣ ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑΣ ΣΥΝΕΠΕΙΕΣ ΕΙΔΟΣ ΜΕΤΑΛΛΑΞΗΣ Οικογενή υπερχοληστερολαιμία Αυτοσωμική επικρατής κληρονομικότητα Σχετίζεται με αυξημένο
ΑΣΘΕΝΕΙΕΣ ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑΣ ΣΥΝΕΠΕΙΕΣ ΕΙΔΟΣ ΜΕΤΑΛΛΑΞΗΣ Οικογενή υπερχοληστερολαιμία Αυτοσωμική επικρατής κληρονομικότητα Σχετίζεται με αυξημένο
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου
 Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Δομή που αποτελείται από DNA και πρωτεΐνες είναι: α. το ριβόσωμα β. το ινίδιο χρωματίνης γ. το πολύσωμα δ. το πριμόσωμα Α2. Αν σε πυρήνα γαμετικού κυττάρου
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Δομή που αποτελείται από DNA και πρωτεΐνες είναι: α. το ριβόσωμα β. το ινίδιο χρωματίνης γ. το πολύσωμα δ. το πριμόσωμα Α2. Αν σε πυρήνα γαμετικού κυττάρου
ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΔΙΑΓΝΩΣΗ
 ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΔΙΑΓΝΩΣΗ ΔΩΡΙΖΑ ΖΑΜΠΕΤΑ Επιμελήτρια Β Αιματολογικού Εργαστηρίου Γ.Ν.Α. «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ» Οι αιμοσφαιρινοπάθειες αποτελούν τις πιο κοινές μονογονιδιακές ασθένειες παγκοσμίως.
ΑΙΜΟΣΦΑΙΡΙΝΟΠΑΘΕΙΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΔΙΑΓΝΩΣΗ ΔΩΡΙΖΑ ΖΑΜΠΕΤΑ Επιμελήτρια Β Αιματολογικού Εργαστηρίου Γ.Ν.Α. «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ» Οι αιμοσφαιρινοπάθειες αποτελούν τις πιο κοινές μονογονιδιακές ασθένειες παγκοσμίως.
Θετικών Σπουδών. Ενδεικτικές απαντήσεις θεμάτων
 Πανελλαδικές Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο μάθημα: Βιολογία Προσανατολισμού Θετικών Σπουδών Παρασκευή, 16 Ιουνίου 2017 Ενδεικτικές απαντήσεις θεμάτων Θέμα Α Α1. α) 3 CAT 5 β) 3 TAC 5
Πανελλαδικές Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο μάθημα: Βιολογία Προσανατολισμού Θετικών Σπουδών Παρασκευή, 16 Ιουνίου 2017 Ενδεικτικές απαντήσεις θεμάτων Θέμα Α Α1. α) 3 CAT 5 β) 3 TAC 5
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ // Γ γ ΙΑΤΡ λυκείου Γ ΘΕΤ2 ΗΜΕΡΟΜΗΝΙΑ: 29/12/
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ // Γ γ ΙΑΤΡ λυκείου Γ ΘΕΤ2 ΗΜΕΡΟΜΗΝΙΑ: 29/12/2015 29 12 2016 ΘΕΜΑ 1 ο Επιλέξτε τη σωστή απάντηση που συμπληρώνει τις παρακάτω προτάσεις: 1. Η περιοριστική
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ // Γ γ ΙΑΤΡ λυκείου Γ ΘΕΤ2 ΗΜΕΡΟΜΗΝΙΑ: 29/12/2015 29 12 2016 ΘΕΜΑ 1 ο Επιλέξτε τη σωστή απάντηση που συμπληρώνει τις παρακάτω προτάσεις: 1. Η περιοριστική
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ Α Α1. β Α2. γ Α3. δ Α4. γ Α5. β
 ΘΕΜΑ Α Α1. β Α2. γ Α3. δ Α4. γ Α5. β 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ:
ΘΕΜΑ Α Α1. β Α2. γ Α3. δ Α4. γ Α5. β 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ:
ΑΠΑΝΤΗΣΕΙΣ ΣΤΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ 2107 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ ΛΥΚΕΙΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ Β Β1. Ι: κωδική αλυσίδα (Δ) ΙΙ: μεταγραφόμενη αλυσίδα (Γ) ΙΙΙ: αμινομάδα (ΣΤ) ΙV: mrna (Β) V: RNA πολυμεράση (Ζ) VI: φωσφορική
ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ Β Β1. Ι: κωδική αλυσίδα (Δ) ΙΙ: μεταγραφόμενη αλυσίδα (Γ) ΙΙΙ: αμινομάδα (ΣΤ) ΙV: mrna (Β) V: RNA πολυμεράση (Ζ) VI: φωσφορική
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1 δ Α2 γ Α3 β Α4 γ Α5 β ΘΕΜΑ Β Β1 Κατά σειρά τα βήματα που οδηγούν στην κατασκευή του καρυότυπου είναι τα ακόλουθα: 4 2 1 6 3 5 Β2 α DNA πολυμεράσες
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1 δ Α2 γ Α3 β Α4 γ Α5 β ΘΕΜΑ Β Β1 Κατά σειρά τα βήματα που οδηγούν στην κατασκευή του καρυότυπου είναι τα ακόλουθα: 4 2 1 6 3 5 Β2 α DNA πολυμεράσες
ΕΚΤΟ ΚΕΦΑΛΑΙΟ ΜΕΤΑΛΛΑΞΕΙΣ
 ΕΚΤΟ ΚΕΦΑΛΑΙΟ ΜΕΤΑΛΛΑΞΕΙΣ ΜΕΤΑΛΛΑΞΕΙΣ Γίνονται μόνο στο γενετικό υλικό των κυττάρων, δηλαδή στο DNA και έχουν μόνιμο χαρακτήρα. Δεν θεωρούνται μεταλλάξεις, μεταβολές των προϊόντων της έκφρασης του γενετικού
ΕΚΤΟ ΚΕΦΑΛΑΙΟ ΜΕΤΑΛΛΑΞΕΙΣ ΜΕΤΑΛΛΑΞΕΙΣ Γίνονται μόνο στο γενετικό υλικό των κυττάρων, δηλαδή στο DNA και έχουν μόνιμο χαρακτήρα. Δεν θεωρούνται μεταλλάξεις, μεταβολές των προϊόντων της έκφρασης του γενετικού
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑ 1 Ο Α. Να επιλέξετε την ορθή πρόταση: ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1. Το κωδικόνιο του mrna που κωδικοποιεί το αµινοξύ µεθειονίνη είναι α. 5 GUA
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑ 1 Ο Α. Να επιλέξετε την ορθή πρόταση: ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1. Το κωδικόνιο του mrna που κωδικοποιεί το αµινοξύ µεθειονίνη είναι α. 5 GUA
ΑΠΑΝΤΗΣΕΙΣ. Β2. Η εικόνα αντιστοιχεί σε προκαρυωτικό κύτταρο. Στους προκαρυωτικούς οργανισμούς το mrna αρχίζει να μεταφράζεται σε πρωτεΐνη πριν ακόμη
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΚΑΙ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 207 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α. δ Α2. δ Α3. β Α4. γ Α5.
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΚΑΙ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 207 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α. δ Α2. δ Α3. β Α4. γ Α5.
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ
 ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις:
 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Τα γονίδια Ι Α και i που καθορίζουν τις ομάδες αίματος: Α. είναι ατελώς επικρατή Β. είναι συνεπικρατή
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Τα γονίδια Ι Α και i που καθορίζουν τις ομάδες αίματος: Α. είναι ατελώς επικρατή Β. είναι συνεπικρατή
ΜΕΤΑΛΛΑΞΕΙΣ ΚΑΙ ΚΑΡΚΙΝΟΣ ΕΡΓΑΣΙΑ ΣΤΟ ΜΑΘΗΜΑ ΤΗΣ ΒΙΟΛΟΓΙΑΣ ΟΝΟΜΑ:ΕΥΑΓΓΕΛΙΑ ΕΠΙΘΕΤΟ:ΠΡΙΦΤΗ ΤΑΞΗ:Γ ΤΜΗΜΑ:4
 ΜΕΤΑΛΛΑΞΕΙΣ ΚΑΙ ΚΑΡΚΙΝΟΣ ΕΡΓΑΣΙΑ ΣΤΟ ΜΑΘΗΜΑ ΤΗΣ ΒΙΟΛΟΓΙΑΣ ΟΝΟΜΑ:ΕΥΑΓΓΕΛΙΑ ΕΠΙΘΕΤΟ:ΠΡΙΦΤΗ ΤΑΞΗ:Γ ΤΜΗΜΑ:4 Τι εννοούμε με τον όρο μεταλλάξεις; Το γενετικό υλικό μπορεί να υποστεί αλλαγές με πολλούς διαφορετικούς
ΜΕΤΑΛΛΑΞΕΙΣ ΚΑΙ ΚΑΡΚΙΝΟΣ ΕΡΓΑΣΙΑ ΣΤΟ ΜΑΘΗΜΑ ΤΗΣ ΒΙΟΛΟΓΙΑΣ ΟΝΟΜΑ:ΕΥΑΓΓΕΛΙΑ ΕΠΙΘΕΤΟ:ΠΡΙΦΤΗ ΤΑΞΗ:Γ ΤΜΗΜΑ:4 Τι εννοούμε με τον όρο μεταλλάξεις; Το γενετικό υλικό μπορεί να υποστεί αλλαγές με πολλούς διαφορετικούς
ΜΕΝΔΕΛΙΚΗ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑ. Ο Mendel καλλιέργησε φυτά σε διάστημα 8 ετών για να φτάσει στη διατύπωση των νόμων της κληρονομικότητας
 ΜΕΝΔΕΛΙΚΗ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑ Ο Mendel καλλιέργησε 28.000 φυτά σε διάστημα 8 ετών για να φτάσει στη διατύπωση των νόμων της κληρονομικότητας Λόγοι επιτυχίας των πειραμάτων του Mendel 1. Μελέτησε μία ή δύο
ΜΕΝΔΕΛΙΚΗ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑ Ο Mendel καλλιέργησε 28.000 φυτά σε διάστημα 8 ετών για να φτάσει στη διατύπωση των νόμων της κληρονομικότητας Λόγοι επιτυχίας των πειραμάτων του Mendel 1. Μελέτησε μία ή δύο
Προτεινόμενες λύσεις ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 16/6/17
 Πανελλήνιες 2017 Προτεινόμενες λύσεις ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 16/6/17 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ ΘΕΜΑ Β Β1. Ι-Α ΙΙ-Ε ΙΙΙ-ΣΤ ΙV-Β V-Ζ VI-Γ VII-Δ Β2. Η εικόνα 1 αντιστοιχεί σε Προκαρυωτικό κύτταρο.
Πανελλήνιες 2017 Προτεινόμενες λύσεις ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 16/6/17 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ ΘΕΜΑ Β Β1. Ι-Α ΙΙ-Ε ΙΙΙ-ΣΤ ΙV-Β V-Ζ VI-Γ VII-Δ Β2. Η εικόνα 1 αντιστοιχεί σε Προκαρυωτικό κύτταρο.
ΒΙΟΛΟΓΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Να σημειώσετε το γράμμα που συμπληρώνει κατάλληλα τη φράση:
 Κανάρη 36, Δάφνη Τηλ. 210 9713934 & 210 9769376 ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ ΒΙΟΛΟΓΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑ Α Να σημειώσετε το γράμμα που συμπληρώνει κατάλληλα τη φράση: Α1. Ποιο από τα παρακάτω αντικωδικόνια
Κανάρη 36, Δάφνη Τηλ. 210 9713934 & 210 9769376 ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ ΒΙΟΛΟΓΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑ Α Να σημειώσετε το γράμμα που συμπληρώνει κατάλληλα τη φράση: Α1. Ποιο από τα παρακάτω αντικωδικόνια
Α1) Μία περιοριστική ενδονουκλεάση μπορεί να κόψει: Α2) Η 5 αμετάφραστη περιοχή της μη κωδικής αλυσίδας ενός συνεχούς γονιδίου:
 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ ΗΜΕΡΟΜΗΝΙΑ : ΟΝΟΜΑΤΕΠΩΝΥΝΟ : ΘΕΜΑ 1 ο Να γράψετε στο τετράδιό σας τον αριθμό κάθε μίας από τις παρακάτω ημιτελείς προτάσεις Α1 έως Α5 και δίπλα το γράμμα,
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ ΗΜΕΡΟΜΗΝΙΑ : ΟΝΟΜΑΤΕΠΩΝΥΝΟ : ΘΕΜΑ 1 ο Να γράψετε στο τετράδιό σας τον αριθμό κάθε μίας από τις παρακάτω ημιτελείς προτάσεις Α1 έως Α5 και δίπλα το γράμμα,
Ενδεικτικές απαντήσεις βιολογίας κατεύθυνσης 2014
 Θέμα Α Α1. δ Α2. γ Α3. β Α4. γ Α5. β Θέμα Β ΑΓ.ΚΩΝΣΤΑΝΤΙΝΟΥ 11 -- ΠΕΙΡΑΙΑΣ -- 18532 -- ΤΗΛ. 210-4224752, 4223687 Ενδεικτικές απαντήσεις βιολογίας κατεύθυνσης 2014 Β1. 4 2 1 6 3 5 Β2. α. DNA πολυμεράση
Θέμα Α Α1. δ Α2. γ Α3. β Α4. γ Α5. β Θέμα Β ΑΓ.ΚΩΝΣΤΑΝΤΙΝΟΥ 11 -- ΠΕΙΡΑΙΑΣ -- 18532 -- ΤΗΛ. 210-4224752, 4223687 Ενδεικτικές απαντήσεις βιολογίας κατεύθυνσης 2014 Β1. 4 2 1 6 3 5 Β2. α. DNA πολυμεράση
γ ρ α π τ ή ε ξ έ τ α σ η σ τ ο μ ά θ η μ α ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 γ ρ α π τ ή ε ξ έ τ α σ η σ τ ο μ ά θ η μ α ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ' ΛΥΚΕΙΟΥ Τάξη: Γ Λυκείου Τμήμα: Βαθμός: Ονοματεπώνυμο: Καθηγητές: Θ Ε Μ Α A 1. Να επιλέξετε τη σωστή απάντηση: Α1. Το γονίδιο
γ ρ α π τ ή ε ξ έ τ α σ η σ τ ο μ ά θ η μ α ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ' ΛΥΚΕΙΟΥ Τάξη: Γ Λυκείου Τμήμα: Βαθμός: Ονοματεπώνυμο: Καθηγητές: Θ Ε Μ Α A 1. Να επιλέξετε τη σωστή απάντηση: Α1. Το γονίδιο
«Μεταλλάξεις και ο ρόλος τους στην γενετική ποικιλότητα» Εργασία στο μάθημα της Βιολογίας ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ
 «Μεταλλάξεις και ο ρόλος τους στην γενετική ποικιλότητα» Εργασία στο μάθημα της Βιολογίας ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ Μια εργασία των: Μακρυδάκη Ελευθερία Μπούρλα Ελένη Τμήμα: Γ 3 Ημερομηνία: 27/1/2015 Γενικά με
«Μεταλλάξεις και ο ρόλος τους στην γενετική ποικιλότητα» Εργασία στο μάθημα της Βιολογίας ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ Μια εργασία των: Μακρυδάκη Ελευθερία Μπούρλα Ελένη Τμήμα: Γ 3 Ημερομηνία: 27/1/2015 Γενικά με
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ)
 ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» ΜΕΝΔΕΛΙΚΑ ΚΛΗΡΟΝΟΜΟΥΜΕΝΑ ΝΟΣΗΜΑΤΑ
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» ΜΕΝΔΕΛΙΚΑ ΚΛΗΡΟΝΟΜΟΥΜΕΝΑ ΝΟΣΗΜΑΤΑ
Βιολογία Προσανατολισμού Γ Λυκείου. Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις:
 Βιολογία Προσανατολισμού Γ Λυκείου 04 01-2018 Νότα Λαζαράκη Αλέξανδρος Παπαγιαννακόπουλος ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Ένζυμο που διασπά
Βιολογία Προσανατολισμού Γ Λυκείου 04 01-2018 Νότα Λαζαράκη Αλέξανδρος Παπαγιαννακόπουλος ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Ένζυμο που διασπά
ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Ως φορείς κλωνοποίησης χρησιμοποιούνται:
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Γ ΛΥΚΕΙΟΥ ΧΕΙΜΕΡΙΝΑ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 04/03/12 ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Ως φορείς κλωνοποίησης
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ / Γ ΛΥΚΕΙΟΥ ΧΕΙΜΕΡΙΝΑ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 04/03/12 ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Ως φορείς κλωνοποίησης
ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 5 ο -6 ο Κεφ. ΑΠΑΝΤΗΣΕΙΣ
 ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 5 ο -6 ο Κεφ. ΑΠΑΝΤΗΣΕΙΣ Θέμα Α : Α1.β, Α2.γ, Α3.β, Α4.γ, Α5β. Θέμα Β: Β1. Αυτόματες : Οι μεταλλάξεις που εμφανίζονται αιφνίδια μέσα στον πληθυσμό ονομάζονται αυτόματες
ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 5 ο -6 ο Κεφ. ΑΠΑΝΤΗΣΕΙΣ Θέμα Α : Α1.β, Α2.γ, Α3.β, Α4.γ, Α5β. Θέμα Β: Β1. Αυτόματες : Οι μεταλλάξεις που εμφανίζονται αιφνίδια μέσα στον πληθυσμό ονομάζονται αυτόματες
Νικολακοπούλου Κωνσταντίνα Κάτσα Ελένη-Μαρία Δάσκου Μαρία. β-θαλασσαιμία
 Νικολακοπούλου Κωνσταντίνα Κάτσα Ελένη-Μαρία Δάσκου Μαρία β-θαλασσαιμία Θάλασσα + αίμα = θαλασσαιμία Εισαγωγή Η πιο κοινή γενετική νόσος που κληρονομείται Mενδελικά ~ 1 : 100.000 παγκοσμίως ~ 1 : 10.000
Νικολακοπούλου Κωνσταντίνα Κάτσα Ελένη-Μαρία Δάσκου Μαρία β-θαλασσαιμία Θάλασσα + αίμα = θαλασσαιμία Εισαγωγή Η πιο κοινή γενετική νόσος που κληρονομείται Mενδελικά ~ 1 : 100.000 παγκοσμίως ~ 1 : 10.000
Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΒΙΟΛΟΓΙΑ ΑΠΑΝΤΗΣΕΙΣ ÏÅÖÅ
 1 Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΒΙΟΛΟΓΙΑ ΘΕΜΑ 1 ο 1 γ 2 δ 3 β 4 α 5 γ ΘΕΜΑ 2 ο ΑΠΑΝΤΗΣΕΙΣ Μονάδες 25 (5Χ5) Α. ιαγονιδιακά ζώα ονοµάζονται εκείνα στα οποία το γενετικό τους υλικό έχει τροποποιηθεί µε την
1 Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΒΙΟΛΟΓΙΑ ΘΕΜΑ 1 ο 1 γ 2 δ 3 β 4 α 5 γ ΘΕΜΑ 2 ο ΑΠΑΝΤΗΣΕΙΣ Μονάδες 25 (5Χ5) Α. ιαγονιδιακά ζώα ονοµάζονται εκείνα στα οποία το γενετικό τους υλικό έχει τροποποιηθεί µε την
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων. Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014. Απαντήσεις Θεμάτων
 Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
1) Τα γονίδια της β-θαλασσαιμίας κληρονομούνται ως:
 ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ-ΚΕΦ. 5-6 Θέμα 1 ο Στις παρακάτω ημιτελείς προτάσεις, να επιλέξετε το γράμμα που συμπληρώνει σωστά την πρόταση: 1) Τα γονίδια της β-θαλασσαιμίας κληρονομούνται
ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ-ΚΕΦ. 5-6 Θέμα 1 ο Στις παρακάτω ημιτελείς προτάσεις, να επιλέξετε το γράμμα που συμπληρώνει σωστά την πρόταση: 1) Τα γονίδια της β-θαλασσαιμίας κληρονομούνται
Εξέλιξη και ανθρώπινος πολιτισμός: Η ρύθμιση του γονιδίου της λακτάσης
 Εξέλιξη και ανθρώπινος πολιτισμός: Η ρύθμιση του γονιδίου της λακτάσης Η διατήρηση του ενζύμου της λακτάσης στους ενήλικες είναι ένα παράδειγμα πρόσφατης εξέλιξης στον άνθρωπο. Μας δείχνει επίσης πώς μεταλλαγές
Εξέλιξη και ανθρώπινος πολιτισμός: Η ρύθμιση του γονιδίου της λακτάσης Η διατήρηση του ενζύμου της λακτάσης στους ενήλικες είναι ένα παράδειγμα πρόσφατης εξέλιξης στον άνθρωπο. Μας δείχνει επίσης πώς μεταλλαγές
Φάσμα& Group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι.
 σύγχρονο Φάσμα& Group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο 1. 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990 50.20.990 2. 25ης Μαρτίου 74 Π. ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 3. Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ
σύγχρονο Φάσμα& Group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο 1. 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990 50.20.990 2. 25ης Μαρτίου 74 Π. ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 3. Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ
 ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
Χρωμοσώματα και ανθρώπινο γονιδίωμα Πεφάνη Δάφνη
 Χρωμοσώματα και ανθρώπινο γονιδίωμα Πεφάνη Δάφνη 12.02.2019 Νουκλεoτίδια-Δομικοί λίθοι του DNA H διπλή έλικα του DNAχωροπληρωτικό μοντέλο To ευκαρυωτικό DNA οργανώνεται σε χρωμοσώματα Τα χρωμοσώματα περιέχουν
Χρωμοσώματα και ανθρώπινο γονιδίωμα Πεφάνη Δάφνη 12.02.2019 Νουκλεoτίδια-Δομικοί λίθοι του DNA H διπλή έλικα του DNAχωροπληρωτικό μοντέλο To ευκαρυωτικό DNA οργανώνεται σε χρωμοσώματα Τα χρωμοσώματα περιέχουν
ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις:
 ΜΑΘΗΜΑ / ΤΑΞΗ: ΒΙΟΛΟΓΙΑ ΟΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/01/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΝΟΤΑ ΛΑΖΑΡΑΚΗ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Από
ΜΑΘΗΜΑ / ΤΑΞΗ: ΒΙΟΛΟΓΙΑ ΟΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/01/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΝΟΤΑ ΛΑΖΑΡΑΚΗ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Από
www.epignosi.edu.gr ΘΕΜΑ Α
 ΘΕΜΑ Α Να γράψετε στην κόλλα σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία συμπληρώνει σωστά την ημιτελή πρόταση.
ΘΕΜΑ Α Να γράψετε στην κόλλα σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία συμπληρώνει σωστά την ημιτελή πρόταση.
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΟΜΑΔΑΣ ΥΓΕΙΑΣ & ΖΩΗΣ
 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΟΜΑΔΑΣ ΥΓΕΙΑΣ & ΖΩΗΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α. I, Β. IV, Γ. VI, Δ. VII, Ε. ΙΙ, ΣΤ. III, Ζ. V Β2. Αντιστοιχεί σε προκαρυωτικό οργανισμό. Στους προκαρυωτικούς
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΟΜΑΔΑΣ ΥΓΕΙΑΣ & ΖΩΗΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α. I, Β. IV, Γ. VI, Δ. VII, Ε. ΙΙ, ΣΤ. III, Ζ. V Β2. Αντιστοιχεί σε προκαρυωτικό οργανισμό. Στους προκαρυωτικούς
ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
 ΘΕΜΑ Α ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 27 5 2016 Α1. β Α2. β Α3. δ Α4. γ Α5. γ ΘΕΜΑ Β Β1. 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Β2. Σχολ. βιβλίο σελ. 20 με την παλιά έκδοση ή σελ. 24 με τη νέα έκδοση : «Τα
ΘΕΜΑ Α ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ 27 5 2016 Α1. β Α2. β Α3. δ Α4. γ Α5. γ ΘΕΜΑ Β Β1. 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Β2. Σχολ. βιβλίο σελ. 20 με την παλιά έκδοση ή σελ. 24 με τη νέα έκδοση : «Τα
ΘΕΜΑ Α ΘΕΜΑ Β ΑΠΑΝΤΗΣΕΙΣ. Α1. β. Α2. γ. Α3. δ. Α4. γ. Α5. β Β1. 5, 4, 2, 1, 3. Β2. Τα δομικά μέρη του οπερονίου της λακτόζης είναι κατά σειρά τα εξής:
 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. β Α2. γ Α3. δ Α4. γ Α5. β ΘΕΜΑ
ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. β Α2. γ Α3. δ Α4. γ Α5. β ΘΕΜΑ
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ
 ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
ΠΑΝΕΛΛΗΝΙΕΣ Απαντήσεις Βιολογίας κατεύθυνσης (ΗΜΕΡΗΣΙΟ)
 ΠΑΝΕΛΛΗΝΙΕΣ 2016 Απαντήσεις Βιολογίας κατεύθυνσης (ΗΜΕΡΗΣΙΟ) Μιχάλης Χαλικιόπουλος ΘΕΜΑ Α Α1 β Α2 β Α3 δ Α4 γ Α5 γ ΘΕΜΑ Β Β1 Β2 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Τα μεταφασικά χρωμοσώματα ενός κυττάρου διαφέρουν
ΠΑΝΕΛΛΗΝΙΕΣ 2016 Απαντήσεις Βιολογίας κατεύθυνσης (ΗΜΕΡΗΣΙΟ) Μιχάλης Χαλικιόπουλος ΘΕΜΑ Α Α1 β Α2 β Α3 δ Α4 γ Α5 γ ΘΕΜΑ Β Β1 Β2 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Τα μεταφασικά χρωμοσώματα ενός κυττάρου διαφέρουν
Πανελλαδικές εξετάσεις 2017
 Πανελλαδικές εξετάσεις 2017 Ενδεικτικές απαντήσεις στο μάθημα «ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ» Θέμα Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α Θέμα Β Β1 I: Α, ΙΙ: E, III: ΣΤ, ΙV: B, V:Z, VI: Γ, VII: Δ Η έννοια πυρηνική
Πανελλαδικές εξετάσεις 2017 Ενδεικτικές απαντήσεις στο μάθημα «ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ» Θέμα Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α Θέμα Β Β1 I: Α, ΙΙ: E, III: ΣΤ, ΙV: B, V:Z, VI: Γ, VII: Δ Η έννοια πυρηνική
ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
 ΠΑΝΕΛΛΑΔΙΙΚΕΣ ΕΞΕΤΑΣΕΙΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΙΟΥ ΓΕΝΙΙΚΟΥ ΛΥΚΕΙΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΙΟΥΝΙΙΟΥ 2017 ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΜΑ Α Α1. δ, Α2. δ, Α3. β, Α4. γ, Α5. α. ΘΕΜΑ Β Β1. I Α II Ε III ΣΤ IV
ΠΑΝΕΛΛΑΔΙΙΚΕΣ ΕΞΕΤΑΣΕΙΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΙΟΥ ΓΕΝΙΙΚΟΥ ΛΥΚΕΙΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΙΟΥΝΙΙΟΥ 2017 ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΜΑ Α Α1. δ, Α2. δ, Α3. β, Α4. γ, Α5. α. ΘΕΜΑ Β Β1. I Α II Ε III ΣΤ IV
ΘΕΜΑ Α Α1. δ Α2. β Α3. α Α4. β Α5. γ
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΠΑΡΑΣΚΕΥΗ 21 ΜΑΪΟΥ 2010 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. δ Α2. β Α3. α Α4.
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΠΑΡΑΣΚΕΥΗ 21 ΜΑΪΟΥ 2010 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. δ Α2. β Α3. α Α4.
«Μεταλλάξεις και ο ρόλος τους στην γενετική ποικιλότητα»
 «Μεταλλάξεις και ο ρόλος τους στην γενετική ποικιλότητα» «Τι είναι Μετάλλαξη» Γενικά με τον όρο μετάλλαξη ονομάζουμε τις αλλαγές στο γενετικό υλικό, το DNA δηλαδή ενός ζωντανού οργανισμού και πρόκειται
«Μεταλλάξεις και ο ρόλος τους στην γενετική ποικιλότητα» «Τι είναι Μετάλλαξη» Γενικά με τον όρο μετάλλαξη ονομάζουμε τις αλλαγές στο γενετικό υλικό, το DNA δηλαδή ενός ζωντανού οργανισμού και πρόκειται
β) Σχολικό βιβλίο σελ. 96: «Αν κατά τη διάρκεια της µείωσης...τρισωµία», σελ. 97: «Η έλλειψη είναι η απώλεια γενετικού
 ΠΡΟΣΟΜΟΙΩΣΗ ΑΠΟΛΥΤΗΡΙΩΝ ΕΞΕΤΑΣΕΩΝ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 4 ΜΑΪΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. α, Α2. β, Α3. δ, Α4. β, Α5. β ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Β Β1.
ΠΡΟΣΟΜΟΙΩΣΗ ΑΠΟΛΥΤΗΡΙΩΝ ΕΞΕΤΑΣΕΩΝ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 4 ΜΑΪΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1. α, Α2. β, Α3. δ, Α4. β, Α5. β ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Β Β1.
Η Επιτροπή Παιδείας της ΠΕΒ. Αθήνα, 4/6/2014 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΒΙΟΕΠΙΣΤΗΜΟΝΩΝ
 Αθήνα, 4/6/2014 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΒΙΟΕΠΙΣΤΗΜΟΝΩΝ Σας αποστέλλουμε τις προτεινόμενες απαντήσεις που αφορούν τα θέματα της Βιολογίας Θετικής Κατεύθυνσης των Ημερησίων Γενικών Λυκείων και ΕΠΑΛ (Ομάδα Β ).
Αθήνα, 4/6/2014 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΒΙΟΕΠΙΣΤΗΜΟΝΩΝ Σας αποστέλλουμε τις προτεινόμενες απαντήσεις που αφορούν τα θέματα της Βιολογίας Θετικής Κατεύθυνσης των Ημερησίων Γενικών Λυκείων και ΕΠΑΛ (Ομάδα Β ).
ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΛΥΣΕΙΣ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΛΥΣΕΙΣ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α. 1. β 2. β 3. γ 4. β Β. Ζύμωση: Διαδικασία ανάπτυξης μικροοργανισμών σε υγρό θρεπτικό υλικό κάτω από οποιεσδήποτε συνθήκες Υβριδοποίηση:
ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΛΥΣΕΙΣ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α. 1. β 2. β 3. γ 4. β Β. Ζύμωση: Διαδικασία ανάπτυξης μικροοργανισμών σε υγρό θρεπτικό υλικό κάτω από οποιεσδήποτε συνθήκες Υβριδοποίηση:
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ 1ο 1. γ 2. γ 3. β 4. α 5. δ
 ΘΕΜΑ 1ο 1. γ 2. γ 3. β 4. α 5. δ 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 9 ΣΕΠΤΕΜΒΡΙΟΥ 2009 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΒΙΟΛΟΓΙΑ
ΘΕΜΑ 1ο 1. γ 2. γ 3. β 4. α 5. δ 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 9 ΣΕΠΤΕΜΒΡΙΟΥ 2009 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΒΙΟΛΟΓΙΑ
ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ
 ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΙΑΓΩΝΙΣΜΑ Θέµα 1 ο 1. Τα άτοµα που είναι ετερόζυγα για τη β-θαλασσαιµία: α. Εµφανίζουν ήπια αναιµία β. Έχουν ευαισθησία στην ελονοσία γ. Συνθέτουν µεγάλη ποσότητα HbF δ.
ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΙΑΓΩΝΙΣΜΑ Θέµα 1 ο 1. Τα άτοµα που είναι ετερόζυγα για τη β-θαλασσαιµία: α. Εµφανίζουν ήπια αναιµία β. Έχουν ευαισθησία στην ελονοσία γ. Συνθέτουν µεγάλη ποσότητα HbF δ.
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ
 ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 Ο Α. 1.α, 2.β, 3.δ, 4.γ, 5.α ΜΟΝΑ ΕΣ 10 (2 ΓΙΑ ΚΑΘΕ ΣΩΣΤΗ ΕΠΙΛΟΓΗ) Β. i) λήξης ii) αµινικό iii) τροποποιήσεις,
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 Ο Α. 1.α, 2.β, 3.δ, 4.γ, 5.α ΜΟΝΑ ΕΣ 10 (2 ΓΙΑ ΚΑΘΕ ΣΩΣΤΗ ΕΠΙΛΟΓΗ) Β. i) λήξης ii) αµινικό iii) τροποποιήσεις,
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ 2017 ΑΠΑΝΤΗΣΕΙΣ ËÁÌÉÁ
 ΘΕΜΑ Α Α1: δ Α2: δ Α3: β Α4: γ Α5: α ΘΕΜΑ Β ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ 2017 ΑΠΑΝΤΗΣΕΙΣ Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII - Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Αυτό
ΘΕΜΑ Α Α1: δ Α2: δ Α3: β Α4: γ Α5: α ΘΕΜΑ Β ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ 2017 ΑΠΑΝΤΗΣΕΙΣ Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII - Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Αυτό
ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ
 16 Ιουνίου 2017 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων ΘΕΜΑ Α Α.1 δ Α.2 δ Α.3 β Α.4 γ Α.5 α ΘΕΜΑ B B.1 I. A II. E III. ΣΤ IV.
16 Ιουνίου 2017 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων ΘΕΜΑ Α Α.1 δ Α.2 δ Α.3 β Α.4 γ Α.5 α ΘΕΜΑ B B.1 I. A II. E III. ΣΤ IV.
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΓΕΝΙΚΟ ΛΥΚΕΙΟ
 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΓΕΝΙΚΟ ΛΥΚΕΙΟ 19-6-2019 ΘΕΜΑ Α Α1. - α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ Β Β1. α1 αντιθρυψίνη-εμφύσημα Πρωτεΐνη επιθηλικών κυττάρων κυστική ίνωση Απαμινάση της αδενοσίνης Ανοσολογική
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΓΕΝΙΚΟ ΛΥΚΕΙΟ 19-6-2019 ΘΕΜΑ Α Α1. - α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ Β Β1. α1 αντιθρυψίνη-εμφύσημα Πρωτεΐνη επιθηλικών κυττάρων κυστική ίνωση Απαμινάση της αδενοσίνης Ανοσολογική
ΠΑΝΕΛΛΗΝΙΕΣ Απαντήσεις Βιολογίας κατεύθυνσης (ΕΠΑΝΑΛΛΗΠΤΙΚΕΣ ΗΜΕΡΗΣΙΟ)
 ΠΑΝΕΛΛΗΝΙΕΣ 2016 Απαντήσεις Βιολογίας κατεύθυνσης (ΕΠΑΝΑΛΛΗΠΤΙΚΕΣ ΗΜΕΡΗΣΙΟ) Μιχάλης Χαλικιόπουλος ΘΕΜΑ Α Α1 β Α2 γ Α3 γ Α4 α Α5 δ ΘΕΜΑ Β Β1. Το βακτήριο Agrobacterium tumefaciens, το οποίο ζει στο έδαφος,
ΠΑΝΕΛΛΗΝΙΕΣ 2016 Απαντήσεις Βιολογίας κατεύθυνσης (ΕΠΑΝΑΛΛΗΠΤΙΚΕΣ ΗΜΕΡΗΣΙΟ) Μιχάλης Χαλικιόπουλος ΘΕΜΑ Α Α1 β Α2 γ Α3 γ Α4 α Α5 δ ΘΕΜΑ Β Β1. Το βακτήριο Agrobacterium tumefaciens, το οποίο ζει στο έδαφος,
Φάσμα group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι.
 σύγχρονο Φάσμα group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. µαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990
σύγχρονο Φάσμα group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. µαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΟΥΝΙΟΥ 2017
 Σ ε λ ί δ α 1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΟΥΝΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΕΠΙΜΕΛΕΙΑ: ΛΑΜΠΡΙΝΗ ΓΑΒΡΙΗΛ ΘΕΜΑ Α Α1.
Σ ε λ ί δ α 1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΟΥΝΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΕΠΙΜΕΛΕΙΑ: ΛΑΜΠΡΙΝΗ ΓΑΒΡΙΗΛ ΘΕΜΑ Α Α1.
ΚΕΦΑΛΑΙΟ 6 ο...2 I. Μεταλλάξεις...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7
 ΚΕΦΑΛΑΙΟ 6 ο ΚΕΦΑΛΑΙΟ 6 ο...2 I. Μεταλλάξεις...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 1 ΚΕΦΑΛΑΙΟ 6 ο I. Μεταλλάξεις Εκπαιδευτικοί στόχοι: Μετά την ολοκλήρωση της µελέτης αυτού του κεφαλαίου ο µαθητής θα πρέπει
ΚΕΦΑΛΑΙΟ 6 ο ΚΕΦΑΛΑΙΟ 6 ο...2 I. Μεταλλάξεις...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 1 ΚΕΦΑΛΑΙΟ 6 ο I. Μεταλλάξεις Εκπαιδευτικοί στόχοι: Μετά την ολοκλήρωση της µελέτης αυτού του κεφαλαίου ο µαθητής θα πρέπει
Α2. Το αντικωδικόνιο είναι τριπλέτα νουκλεοτιδίων του α. mrna β. snrna γ. trna δ. rrna Μονάδες 5
 ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις Α1 έως Α5 και δίπλα στο γράμμα που αντιστοιχεί στη λέξη ή στη φράση, η οποία συμπληρώνει
ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις Α1 έως Α5 και δίπλα στο γράμμα που αντιστοιχεί στη λέξη ή στη φράση, η οποία συμπληρώνει
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΟ
 ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΟ 1-2-4-5-6 ΘΕΜΑ 1 Ο Α. Να γράψετε τον αριθμό της καθεμιάς από τις παρακάτω προτάσεις 1-5 και δίπλα του τη λέξη Σωστό αν η πρόταση είναι σωστή,
ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΟ 1-2-4-5-6 ΘΕΜΑ 1 Ο Α. Να γράψετε τον αριθμό της καθεμιάς από τις παρακάτω προτάσεις 1-5 και δίπλα του τη λέξη Σωστό αν η πρόταση είναι σωστή,
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1 α Α2 β Α3 γ Α4 γ Α5 β ΘΕΜΑ Β Β1. 1 ζ 2 στ 3
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1 α Α2 β Α3 γ Α4 γ Α5 β ΘΕΜΑ Β Β1. 1 ζ 2 στ 3
