Μελέτη της πολυμορφικότητας πρωτεϊνών φαρμακευτικού ενδιαφέροντος: Η περίπτωση της ανθρώπινης ινσουλίνης
|
|
|
- Ήλιόδωρος Μελετόπουλος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΔΙΠΛΩΜΑ ΕΙΔΙΚΕΥΣΗΣ Μελέτη της πολυμορφικότητας πρωτεϊνών φαρμακευτικού ενδιαφέροντος: Η περίπτωση της ανθρώπινης ινσουλίνης ΚΑΡΑΒΑΣΙΛΗ ΦΩΤΕΙΝΗ Επιβλέποντες: ΓΕΩΡΓΙΟΣ Α. ΣΠΥΡΟΥΛΙΑΣ ΜΑΡΓΙΩΛΑΚΗ ΕΙΡΗΝΗ ΠΑΤΡΑ 2012
2 Ευχαριστίες Το ερευνητικό μέρος της μεταπτυχιακής εργασίας εκπονήθηκε στο Πανεπιστήμιο Πατρών, στο Εργαστήριο Δομικής Βιολογίας, του τομέα Γενετικής, Βιολογίας Κυττάρου & Ανάπτυξης, του Τμήματος Βιολογίας σε συνεργασία με το Τμήμα Φαρμακευτικής, υπό τον Αν. καθηγητή Σπυρούλια Γεώργιο κατά το χρονικό διάστημα Η ανάθεση και επίβλεψη της εργασίας έγιναν από τη Λέκτορα του τμήματος Βιολογίας, Ειρήνη Μαργιωλάκη. Όπως κάθε πειραματική ερευνητική εργασία, έτσι και αυτή είναι αποτέλεσμα της αρμονικής αλληλεπίδρασης με μια πληθώρα καθηγητών, ερευνητών και συνεργατών. Αρχικά θα ήθελα να ευχαριστήσω θερμά τους επιβλέποντες κ.κ. Μαργιωλάκη Ειρήνη και Σπυρούλια Γεώργιο που μου έδωσαν την ευκαιρία να ασχοληθώ με ένα τόσο ενδιαφέρον και σύγχρονο ερευνητικό θέμα, καθώς και την συνεχή και άρτια καθοδήγηση που μου προσέφεραν κατά τη διάρκεια των δύο αυτών ετών. Τους οφείλω ένα μεγάλο ευχαριστώ καθώς ήταν και οι δύο πάντα παρόντες και πρόθυμοι να επιλύσουν οποιοδήποτε πρόβλημα μου παρουσιάστηκε. Ευχαριστώ τους Gerd Schluckebier, Mathias Norrman και Lene Drube, από τη φαρμακευτική εταιρεία Novo Nordisk, για την προσφορά ινσουλίνης, τη φιλοξενία στις εγκαταστάσεις της εταιρείας με σκοπό την εκμάθηση τεχνικών κρυστάλλωσης, καθώς και για τις εποικοδομητικές συζητήσεις σε θέματα που αφορούσαν την ινσουλίνη. Ευχαριστώ την ερευνητική ομάδα του Ευρωπαϊκού σύγχροτρου, European Synchrotron Radiation Facility, (E.S.R.F.) της Γαλλίας και συγκεκριμένα τους Andrew N. Fitch και Jonathan P. Wright, για την υλικοτεχνική υποστήριξη που μας παρείχαν στα πειράματα περίθλασης, για τις συμβουλές και την καθοδήγηση τους επί της πειραματικής διαδικασίας και επί των αποτελεσμάτων, καθώς και για την άριστη συνεργασία αυτών των δύο ετών. Ευχαριστώ επίσης, το τρίτο μέλος της Συμβουλευτικής Επιτροπής, τον Επ. καθηγητή Πουλά Κωνσταντίνο, για τις ενδιαφέρουσες επιστημονικές συζητήσεις κατά τη διάρκεια των μαθημάτων, αλλά και πέραν αυτών. Επίσης, καθότι προέρχομαι από τον κλάδο της φυσικής, δεν θα μπορούσα να έχω καλύψει σε τόσο σύντομο χρονικό διάστημα σημαντικές ελλείψεις σε θέματα Βιολογίας, χωρίς τη βοήθεια της Γιαννοπούλου Αναστασίας-Ευδοκίας και Κοτσιλίτη Έλενας, οι οποίες με μεγάλη προθυμία και υπομονή με βοηθούσαν να κατανοήσω τον τρόπο λειτουργίας διαφόρων βιολογικών μηχανισμών. Ευχαριστώ επίσης τη μεταπτυχιακή φοιτήτρια Ειρήνη Νικολούλη, για την πολύ καλή συνεργασία και τη βοήθεια στην επεξεργασία των δεδομένων. Τέλος, ευχαριστώ την Επιτροπή Ερευνών του Πανεπιστημίου Πατρών, για την οικονομική υποστήριξη, μέσω του προγράμματος ΚΑΡΑΘΕΟΔΩΡΗ D.211 (Επιστημονική Υπεύθυνη: Μαργιωλάκη Ειρήνη, Τίτλος: Δομικός χαρακτηρισμός 1
3 πρωτεϊνών φαρμακευτικού ενδιαφέροντος και προερχόμενων από ιούς με στόχο την δημιουργία νέων φαρμάκων). Μέρος των αποτελεσμάτων αυτής της εργασίας παρουσιάζεται στην παρακάτω δημοσίευση, η οποία παρατίθεται στο τέλος της εργασίας (παράρτημα Β): Karavassili F., Giannopoulou E.A., Kotsiliti E., Knight L., Norrman M., Schluckebier G., Drube L., Fitch Α., Wright J.P. & Μargiolaki I., Structural studies of Human Insulin co-crystallized with Phenol or Resorcinol via Powder Diffraction, Acta Cryst. D,
4 ΠΕΡΙΛΗΨΗ Στην παρούσα μεταπτυχιακή εργασία πραγματοποιήθηκε μελέτη του πολυμορφισμού της ινσουλίνης μέσω της κρυσταλλογραφίας ακτίνων-χ. Για το σκοπό αυτό πραγματοποιήθηκαν πολυάριθμα πειράματα κρυστάλλωσης της ινσουλίνης υπό διαφορετικές συνθήκες (ph, οργανικοί προσδέτες). Οι κρύσταλλοι που προέκυψαν χρησιμοποιήθηκαν σε πειράματα περίθλασης ακτίνων-χ τα οποία πραγματοποιήθηκαν στο Ευρωπαϊκό σύγχροτρον, ESRF, της Γαλλίας και στο Ελβετικό σύγχροτρον, SLS. Η τεχνική που ακολουθήθηκε για τα πειράματα περίθλασης ήταν αυτή του powder diffraction, η οποία τα τελευταία χρόνια έχει αναδειχθεί σε ένα σημαντικό εργαλείο χαρακτηρισμού των πρωτεϊνικών πολυκρυσταλλικών ιζημάτων. Από τη μελέτη αυτή, προέκυψαν διάφορα πολύμορφα της ινσουλίνης που χαρακτηρίζονται από διαφορετικές συμμετρίες, ενώ πραγματοποιήθηκε ο προσδιορισμός κάθε κρυσταλλικής φάσης στο επίπεδο της μοναδιαίας κυψελίδας. Ενδιαφέρον αποτελεί ο εντοπισμός δύο νέων κρυσταλλικών φάσεων της ινσουλίνης, μονοκλινούς συμμετρίας, οι οποίες ενδέχεται να είναι υψηλής φαρμακευτικής σημασίας. ABSTRACT In this thesis the polymorphism of insulin via X-ray powder crystallography has been carried out. For this purpose numerous experiments of insulin crystallization have been performed under different conditions (ph, organic ligands). The resulting crystals were employed in X-ray diffraction experiments, which took place at the European synchrotron, ESRF, in France and at the Swiss synchrotron, SLS. The technique employed for the X- Ray diffraction experiments, was the powder diffraction method, which has been proven to be an important tool for the determination of polycrystalline protein precipitants during the last decade. From this study, a number of insulin polymorphs were identified in different crystal systems and furthermore, each crystalline phase was determined at the level of unit cell symmetry and dimensions. An interesting point occurs from the characterization of two novel insulin phases, belonging to monoclinic symmetry, which are potentially associated with high pharmaceutical importance. 3
5 Περιεχόμενα Εισαγωγή... 6 Θεωρητικό Μέρος Ινσουλίνη και Διαβήτης Βιοσύνθεση της ινσουλίνης Έκκριση της Ινσουλίνης Μορφές της Ινσουλίνης Τύποι Σακχαρώδη διαβήτη Θεραπεία Κρυσταλλογραφία Ακτίνων-Χ Ακτίνες-Χ Περίθλαση ακτίνων-χ Η συμβολή του Laue Νόμος του Bragg Κρυσταλλογραφία Πλέγματα Bravais Space groups Κρυσταλλογραφικά επίπεδα και δείκτες Miller Αποστάσεις κρυσταλλογραφικών επιπέδων Ευθύ και αντίστροφο πλέγμα Σφαίρα του Ewald Περίθλαση από μονοκρύσταλλο Περίθλαση από πολυκρυσταλλικό δείγμα (powder diffraction) Παράγοντας Δομής Η ηλεκτρονιακή πυκνότητα ως σειρά Fourier Το πρόβλημα φάσης Η μέθοδος Rietveld Συστηματικές κατασβέσεις Κρυστάλλωση Πρωτεϊνών Παράγοντες που επηρεάζουν την κρυστάλλωση Τεχνικές κρυστάλλωσης
6 Όργανα και μέθοδοι Παραγωγή Ακτίνων-Χ Εργαστηριακά περιθλασίμετρα Ακτινοβολία Σύγχροτρον Ευρωπαϊκό Σύγχροτρον ESRF (European Synchrotron Radiation Facility) Ελβετικό Σύγχροτρον SLS (Swiss Light Source): MS- X04SA: Materials Science Beamline Πειραματικό Μέρος Κρυστάλλωση Κρυστάλλωση με Phenol Κρυστάλλωση με Resorcinol Κρυστάλλωση με 4- Chlororesorcinol Κρυστάλλωση με 4- Bromoresorcinol Κρυστάλλωση με Ακετυλοσαλικυλικό οξύ Προετοιμασία δειγμάτων πριν τη συλλογή δεδομένων περίθλασης ακτίνων-χ Αποτελέσματα Συζήτηση Βιβλιογραφία
7 Εισαγωγή Η πρόοδος της δομικής βιολογίας κατά τα τελευταία χρόνια μας προσέφερε μια εις βάθος εξερεύνηση των μηχανισμών της ζωής. Η ανεύρεση της τρισδιάστατης δομής των πρωτεϊνών και άλλων βιολογικών μακρομορίων, έχει συνεισφέρει ανεκτίμητα στην κατανόηση της λειτουργίας διαφόρων βιολογικών συστημάτων και φαινομένων. Το σημερινό ερευνητικό οπλοστάσιο της δομικής βιολογίας απαρτίζεται από διάφορες μεθόδους και τεχνικές κάθε μια από τις οποίες βρίσκει μεμονωμένα ή συνδυαστικά, εφαρμογή στα διάφορα βιολογικά συστήματα. Η πιο συχνά χρησιμοποιούμενη μέθοδος για τον προσδιορισμό, σε ατομική κλίμακα, των δομικών στοιχείων των πρωτεϊνών, είναι η κρυσταλλογραφία ακτίνων- Χ από μονοκρυσταλλικό δείγμα. Από το 1912 που πραγματοποιήθηκαν τα πρώτα πειράματα περίθλασης με ακτίνες-χ σε μονοκρυστάλλους έως και σήμερα, η κρυσταλλογραφία ακτίνων-χ θεωρείται υψηλής σημασίας στις φυσικές επιστήμες. Μέσω αυτής της τεχνικής έγινε αρχικά η σύνδεση μεταξύ της δομής του κρυστάλλου και των φυσικοχημικών ιδιοτήτων του κρυσταλλικού υλικού. Για την εφαρμογή αυτής της μεθόδου, αρχικά αναζητούνται οι κατάλληλες συνθήκες κρυστάλλωσης του βιολογικού μακρομορίου και στη συνέχεια αναπτύσσεται ο κρύσταλλος ο οποίος ακτινοβολείται, υπό διαφορετικές γωνίες, από δέσμη ακτίνων-χ για τη συλλογή δεδομένων περίθλασης. Αυτά τα δεδομένα αναλύονται κατάλληλα και εξάγεται η δομή του βιολογικού μακρομορίου. Ωστόσο, στη συγκεκριμένη μέθοδο, μια από τις κύριες δυσκολίες που συχνά προκύπτει είναι η αδυναμία απόκτησης ενός μονοκρυστάλλου κατάλληλου μεγέθους και ποιότητας. Στις περιπτώσεις που κρίνεται αδύνατη η ανάπτυξη ενός τέτοιου μονοκρύσταλλου, οι δομικοί βιολόγοι τείνουν να ανατρέχουν σε άλλες μεθόδους προσδιορισμού της δομής. Μεταξύ άλλων, σε αυτές συγκαταλέγονται η ηλεκτρονική μικροσκόπια και ο πυρηνικός μαγνητικός συντονισμός (Nuclear Magnetic Resonance, NMR), κατά τον οποίο δεν απαιτείται η μετάβαση στη στερεά φάση. Ένα σημείο όμως το οποίο για πολλά χρόνια δεν έτυχε της προσοχής που του αναλογούσε, κατά την προσπάθεια ανάπτυξης ενός μονοκρυστάλλου, ήταν ότι πολυάριθμα υποπροϊόντα απορρίπτονταν, μεταξύ αυτών και τα κρυσταλλικά ιζήματα που περιέχουν τεράστιο όγκο πληροφοριών. Τα κρυσταλλικά ιζήματα αποτελούνται από μεγάλο αριθμό πολύ μικρών κρυστάλλων της τάξης μεγέθους έως και λίγων νανομέτρων. Αυτοί οι μικροκρυστάλλοι είναι της ίδιας ακριβώς φύσης με ένα μονοκρύσταλλο, με τη μοναδική διαφορά να εντοπίζεται στο μέγεθος τους. Συνεπώς αποτελούν και αυτοί δείγμα από το οποίο μπορούμε να εξάγουμε δομικές πληροφορίες. Όμως σε κάθε πείραμα περίθλασης ο μονοκρύσταλλος καλείται να έχει αρκετά μεγάλο μέγεθος, καθώς όσο μεγαλύτερος είναι ο κρύσταλλος, τόσο πιο ισχυρό είναι το σήμα περίθλασης που ανιχνεύεται. Αν απομονώσουμε έναν μικροκρύσταλλο από το ίζημα, το σήμα περίθλασης θα είναι ασθενές και δεν θα 6
8 καταφέρουμε να το καταγράψουμε. Χρησιμοποιώντας όμως μικρή ποσότητα ιζήματος, που περιέχει χιλιάδες μικροκρυστάλλους, καταγράφουμε ισχυρό σήμα περίθλασης το οποίο στη συνέχεια μπορούμε να επεξεργαστούμε. Ένα τέτοιο πείραμα, στο οποίο καταγράφεται ταυτόχρονα σήμα περίθλασης από πολλούς κρυστάλλους, είναι γνωστό ως πείραμα περίθλασης από πολυκρυσταλλικό δείγμα ή πείραμα περίθλασης σκόνης (powder diffraction). Η μέθοδος της περίθλασης από πολυκρυσταλλικά δείγματα αναπτύχθηκε το 1916 από τους Debye και Scherrer. Για περισσότερο από μισό αιώνα, αυτή η μέθοδος είχε χρησιμοποιηθεί μόνο για ποιοτική ανάλυση φάσης, ημι-ποσοτική ανάλυση φάσης καθώς και για τη μέτρηση του στρες των υλικών. Ιστορικά, η καθυστέρηση ανάπτυξης της μεθόδου, ως μέσο προσδιορισμού της δομής, οφείλεται στην ουσιαστική δυσκολία ανάλυσης των διαγραμμάτων περίθλασης. Σε αντίθεση με ένα πείραμα μονοκρυστάλλου, στα πολυκρυσταλλικά δείγματα δεν είναι δυνατόν να εξαναγκάσουμε όλους τους μικροκρυστάλλους σε κοινό προσανατολισμό, και έτσι οι κρύσταλλοι βρίσκονται τυχαία προσανατολισμένοι προς όλες τις κατευθύνσεις μέσα στο διάλυμα. Καθώς λοιπόν ακτινοβολία ακτίνων-χ προσπίπτει πάνω στο δείγμα, συλλέγεται το διάγραμμα περίθλασης πολλών κρυστάλλων, στο οποίο διακρίνονται ομόκεντροι κύκλοι, καθένας από τους οποίους προέρχεται από τη συμβολή όλων των εντάσεων των ανακλάσεων που απέχουν ίδια χαρακτηριστική απόσταση d. Το γεγονός αυτό, οδηγεί σε τυχαία ή συστηματική επικάλυψη των ανακλάσεων καθιστώντας την ανάλυση των διαγραμμάτων περίθλασης και την ανακατασκευή της τρισδιάστατης δομής αρκετά περίπλοκες. Παρ όλα αυτά η εξέλιξη των ηλεκτρονικών υπολογιστών και των υπολογιστικών προγραμμάτων, σε συνδυασμό με τη βελτίωση των οργάνων και των πηγών ακτίνων-χ που εξάγουν καλύτερης ποιότητας διαγράμματα περίθλασης, διευκόλυναν σε μεγάλο βαθμό την επεξεργασία των δεδομένων περίθλασης από πολυκρυσταλλικά δείγματα. Μεγάλη συμβολή προς την κατεύθυνση αυτή έχει επιφέρει και η χρήση ακτινοβολίας σύγχροτρον. Αυτή η σχετικά νέα πηγή ακτινοβολίας προσφέρει σημαντικά ποιοτικότερα δεδομένα περίθλασης, καθώς υπερέχει σε πολλά σημεία σε σχέση με τις εργαστηριακές πηγές παραγωγής ακτίνων-χ. Βασικά πλεονεκτήματα της ακτινοβολίας σύγχροτρον είναι η δυνατότητα επιλογής του επιθυμητού μήκους κύματος για τη διεξαγωγή κάθε πειράματος, ενώ τα δεδομένα περίθλασης που προκύπτουν χρησιμοποιώντας τέτοιες πηγές χαρακτηρίζονται από αυξημένη ευκρίνεια. Αυτά τα πλεονεκτήματα είναι κρίσιμης σημασίας, ιδίως όταν τα υπό μελέτη υλικά εμφανίζουν κάποια χαρακτηριστικά που δυσχεραίνουν την επεξεργασία των δεδομένων (όπως κρύσταλλοι με μεγάλες σταθερές πλέγματος ή συστήματα που εμφανίζουν ασθενείς εντάσεις) και τα πειράματα περίθλασης χρειάζεται να προσαρμοστούν στις απαιτήσεις του εκάστοτε συστήματος, 7
9 προκειμένου να εξαχθούν ποιοτικά δεδομένα περίθλασης, μέγιστης δυνατής ευκρίνειας. Μάλιστα κατά τις τελευταίες δεκαετίες καταγράφεται μια σταδιακή αύξηση της ευκρίνειας των δεδομένων που λαμβάνουμε με ακτινοβολία σύγχροτρον, πλησιάζοντας όλο και περισσότερο το μέγεθος της ακτίνας του ατόμου (1Å). Η αύξηση αυτή, μας επιτρέπει να διακρίνουμε περισσότερη δομική λεπτομέρεια και να εξάγουμε πιο αξιόπιστες δομικές πληροφορίες. Παράλληλα, η μεγαλύτερη ευκρίνεια στα δεδομένα επιτρέπει την επίλυση όλο και πιο περίπλοκων κρυσταλλικών δομών. Αυτός είναι ο βασικός λόγος για τον οποίο η κρυσταλλογραφία συνεχίζει μέχρι και σήμερα να θεωρείται ισχυρό εργαλείο προσδιορισμού της δομής βιολογικών μακρομορίων. Μάλιστα διατηρεί το βάθρο της, έχοντας υψηλότερο ποσοστό ανάμεσα στις υπόλοιπες μεθόδους δομικού προσδιορισμού, σημειώνοντας επιπλέον, κατά τις τελευταίες δεκαετίες, εκθετική αύξηση των κατατιθέμενων δομών που επιλύονται μέσω της κρυσταλλογραφίας. Στη συγκεκριμένη εργασία, η πειραματική μέθοδος που χρησιμοποιήθηκε είναι η περίθλαση από πολυκρυσταλλικά δείγματα με χρήση ακτινοβολίας σύγχροτρον, με σκοπό τον προσδιορισμό της κρυσταλλικής δομής διαφόρων πολυμόρφων της ινσουλίνης. Ως πολύμορφα μιας ουσίας ορίζουμε τις διαφορετικές κρυσταλλικές μορφές στις οποίες απαντάται η ουσία αυτή, όταν υπόκειται σε κάποια αλλαγή. Η αλλαγή αυτή αναφέρεται σε μεταβολές του περιβάλλοντος της ουσίας ή των συνθηκών κρυστάλλωσής της. Οι διαφορετικές κρυσταλλικές μορφές που δημιουργούνται, διαφοροποιούνται ως προς τη διάταξη των δομικών τους μονάδων (άτομα, μόρια, σύμπλοκα) στο χώρο. Αυτή η διαφοροποίηση, παρόλο που φαίνεται μικρή, επηρεάζει τελικά πολλές από τις ιδιότητες τους γι αυτό και ο πολυμορφισμός αποτελεί αντικείμενο μελέτης πολλών επιστημονικών κλάδων. Ιδιαίτερο ενδιαφέρον παρουσιάζει το φαινόμενο του πολυμορφισμού στις ουσίες φαρμακευτικού ενδιαφέροντος, καθώς ενδέχεται διαφορετικά πολύμορφα της ίδιας ουσίας να εμφανίζουν διαφορετικές ιδιότητες άρρηκτα συνδεδεμένες με τη φαρμακευτική τους δράση, γεγονός με μεγάλη σημασία σε θέματα υγείας. Η πρωτεΐνη που μελετάται στη παρούσα εργασία, η ινσουλίνη, είναι γνωστή για τη φαρμακευτική της δράση εδώ και πολλές δεκαετίες. Τα πολύμορφα της ινσουλίνης που μελετήθηκαν, προέκυψαν μεταβάλλοντας μερικούς από τους παράγοντες που επηρεάζουν την κρυστάλλωση της, όπως είναι η αλλαγή του ph και η συγκρυστάλλωση της πρωτεΐνης με διάφορους προσδέτες. Οι μελέτες που έγιναν αποσκοπούν στη χαρτογράφηση των κρυσταλλικών πολυμόρφων και των συνθηκών που το κάθε ένα εμφανίζεται, καθώς και στο σαφή προσδιορισμό των παραμέτρων που τα χαρακτηρίζουν. 8
10 Θεωρητικό Μέρος 1. Ινσουλίνη και Διαβήτης Ο σακχαρώδης διαβήτης αποτελεί μια νόσο που δημιουργεί ιδιαίτερα προβλήματα στην καθημερινή ζωή των ασθενών και απαιτεί καθημερινά τη ρύθμιση των επιπέδων γλυκόζης του αίματος με κατάλληλη δίαιτα, αντιδιαβητικά δισκία ή μέσω της εξωγενούς χορήγησης ινσουλίνης. Η γλυκόζη είναι απαραίτητο συστατικό του κυτταρικού μεταβολισμού και αποτελεί τη βασική πηγή ενέργειας του οργανισμού. Κάθε τροφή που καταναλώνουμε μετατρέπεται σε γλυκόζη, η οποία προκειμένου να αξιοποιηθεί από τον οργανισμό μας, πρέπει να εισέλθει στο εσωτερικό των κυττάρων. Ο οργανισμός προσπαθεί να κρατήσει σταθερή την ποσότητα γλυκόζης που παρέχεται στα κύτταρα. Στις περιπτώσεις όπου η τιμή της γλυκόζης αυξάνεται, αποθηκεύεται στο ήπαρ και στους μύες υπό τη μορφή γλυκαγόνου. Αντίθετα, στις περιπτώσεις όπου η τιμή της γλυκόζης μειώνεται, ο οργανισμός ανατρέχει στην αποθηκευμένη γλυκαγόνη, ενεργοποιείται η γλυκόζη και διεγείρει το άτομο να καταναλώσει τροφή. Προκειμένου να παραμένει σταθερή η ποσότητα γλυκόζης στο αίμα, ο ανθρώπινος οργανισμός έχει δύο ορμόνες αντίθετης δράσης: τη γλυκαγόνη και την ινσουλίνη. Η γλυκαγόνη, που παράγεται από τα α κύτταρα του παγκρέατος, είναι ικανή να αυξήσει τα επίπεδα της γλυκόζης στο αίμα, ενώ ινσουλίνη που παράγεται από τα β κύτταρα του παγκρέατος, μειώνει τα επίπεδα της γλυκόζης. Η απόλυτη ή σχετική ανεπάρκεια έκκρισης της ινσουλίνης ή της δράσης της, οδηγούν στην ανάπτυξη του σακχαρώδη διαβήτη. Συγκεκριμένα, στην περίπτωση που το πάγκρεας δεν παράγει αρκετή ινσουλίνη ή παράγει ινσουλίνη η οποία δε δρα σωστά, η γλυκόζη δεν εισέρχεται στα κύτταρα με αποτέλεσμα την αύξηση των επιπέδων σακχάρου στο αίμα (υπεργλυκαιμία) και την εμφάνιση του σακχαρώδη διαβήτη. Αποτελέσματα της ανεπάρκειας της ινσουλίνης είναι οι διαταραχές στο μεταβολισμό των υδατανθράκων, των λιπών και των ηλεκτρολυτών. 1.1 Βιοσύνθεση της ινσουλίνης Το μόριο της ινσουλίνης αποτελείται από δύο πεπτιδικές αλυσίδες, Α και Β. Η πρόδρομη μορφή της προϊνσουλίνης (preproinsulin), συντίθεται στα ριβοσώματα των παγκρεατικών κύτταρων και έχει μοριακό βάρος ΜΒ: Da. Αυτή η μορφή της ινσουλίνης περιλαμβάνει, εκτός από τις δύο αλυσίδες Α και Β, ένα επιπλέον πεπτίδιο που τις συνδέει, το πεπτίδιο C, καθώς και μια οδηγό αλληλουχία. Στη συνέχεια η πρώιμη προϊνσουλίνη εισέρχεται στο ενδοπλασματικό δίκτυο των β-κυττάρων, των νησιδίων του Langerhans. Εκεί υφίσταται άμεση πρωτεολυτική διάσπαση από τα ένζυμα, με αποτέλεσμα την παραγωγή της προϊνσουλίνης 9
11 (proinsulin), μοριακού βάρους ΜΒ: 9.000Da. Η προϊνσουλίνη αποτελείται από τις δύο πεπτιδικές αλυσίδες, Α και Β, οι οποίες συνδέονται μεταξύ τους μέσω δισουλφιδικών δεσμών και ενώνονται μέσω του C πεπτιδίου. Μετά το σχηματισμό της, η προϊνσουλίνη μεταφέρεται στο σύστημα Golgi, όπου και αποθηκεύεται, παρουσία ψευδαργύρου (Zn), σε εξαμερή προϊνσουλίνης (G. Dodson, 1998). Όταν ο οργανισμός έχει ανάγκη από ινσουλίνη, η προϊνσουλίνη θα υποστεί πρωτεολυτική διάσπαση σε δύο σημεία ώστε να αποκοπεί το βιολογικά ανενεργό πεπτίδιο C και να σχηματισθεί δραστική ινσουλίνη, μοριακού βάρους ΜΒ: Da. Σχήμα 1.1: Η σύνθεση της ινσουλίνης. Αρχικά συντίθεται η πρώιμη μορφή της προϊνσουλίνης (preproinsulin) η οποία μετατρέπεται σε προϊνσουλίνη (proinsulin) με την αποκόλληση της αλληλουχίας οδηγού (signal sequence). Μέσα στο σύστημα Golgi αποκολλάται από την προϊνσουλίνη και το πεπτίδιο C δημιουργώντας τη δραστική ινσουλίνη, (Πηγή: Η τελική μορφή της ινσουλίνης αποτελείται από 21 αμινοξέα στην Α αλυσίδα και 30 αμινοξέα στη Β αλυσίδα, ενώ οι δύο αλυσίδες συνδέονται μεταξύ τους με δυο δισουλφιδικούς δεσμούς (CysΑ7-CysΒ7 & CysΑ20-CysΒ19). Επιπλέον ένας εσωτερικός δισουλφιδικός δεσμός αναπτύσσεται μεταξύ δύο αμινοξέων κυστεΐνης (CysΑ6-CysΑ11) της Α αλυσίδας (Σχήμα 1.2). Αυτές οι δύο αλυσίδες αποτελούν το μονομερές της ινσουλίνης. 10
12 Σχήμα 1.2: Οι δύο αλυσίδες που αποτελούν την ινσουλίνη. Η Α αλυσίδα, με μπλε χρώμα, αποτελείται από 21 αμινοξέα, ενώ η Β, με κόκκινο χρώμα, αποτελείται από 30 αμινοξέα (Πηγή: Støy J.et al. PNAS 2007, Vol. 104, 15042). 1.2 Έκκριση της Ινσουλίνης Η έκκριση της ινσουλίνης διεγείρεται από την αύξηση της στάθμης της γλυκόζης του αίματος, όπως χαρακτηριστικά συμβαίνει μετά το γεύμα. Η γλυκόζη εισέρχεται στα β-κύτταρα μέσω του μεταφορέα της γλυκόζης (glucose transporter, GLUT 2) και διεγείρει την έκκριση ινσουλίνης. Άλλοι παράγοντες διέγερσης για την έκκριση της ινσουλίνης, αλλά όχι τόσο ισχυροί, μπορεί να είναι ορμόνες του γαστρεντερικού συστήματος, οι οποίες συμμετέχουν στη διαδικασία της πέψης, αλλά και ορισμένα αμινοξέα της τροφής. Όσο αυξάνει η συγκέντρωση γλυκόζης στο αίμα, τόσο αυξάνει ο ρυθμός έκκρισης ινσουλίνης. Η υπογλυκαιμία, αντίθετα, αναστέλλει την έκκριση ινσουλίνης. Αφού πραγματοποιηθεί η έκκριση ινσουλίνης από το πάγκρεας, η ινσουλίνη στη συνέχεια προσδένεται από τους υποδοχείς της. Υποδοχείς της ινσουλίνης υπάρχουν κυρίως στο ήπαρ και το λιπώδη ιστό. Μετά την πρόσδεση ινσουλίνης και ανάλογα τη φύση των κυττάρων, εισέρχεται ποσότητα γλυκόζης στα κύτταρα και ενεργοποιούνται μηχανισμοί σύνθεσης γλυκογόνου και γλυκόλυσης. Αυτό οδηγεί σε μείωση της συγκέντρωσης της ινσουλίνης στο αίμα και όταν η συγκέντρωση προσεγγίζει τα φυσιολογικά επίπεδα, σταματά η έκκριση ινσουλίνης. 1.3 Μορφές της Ινσουλίνης Η ινσουλίνη σε υδατικά διαλύματα υφίστανται ως μονομερές, αλλά παρουσία αλάτων και δισθενών ιόντων (όπως ο ψευδάργυρος ή το ασβέστιο) σχηματίζει σταθερά διμερή και εξαμερή ινσουλίνης. Η ινσουλίνη αποθηκεύεται στον οργανισμό ως εξαμερές, ωστόσο, η βιολογικά δραστική μορφή της είναι η μονομερής (G.D. Smith, 1984). Καθώς οι κρύσταλλοι ινσουλίνης απελευθερώνονται στην κυκλοφορία του αίματος, 11
13 συναντούν μια μεταβολή στο ph από ~ 5.5 σε ~ 7.4. Αυτή η μεταβολή σε συνδυασμό με τη μείωση της συγκέντρωσης των ιόντων ψευδάργυρου και ασβεστίου οδηγούν στην απότομη αποσύνθεση των κρυστάλλων και τη δημιουργία μονομερών ινσουλίνης (G. Dodson, 1998). Στη μονομερή μορφή της ινσουλίνης, η Β αλυσίδα εμφανίζει κεντρικά διαμόρφωση α-έλικας ενώ περιβάλλεται από δύο περιοχές επιμηκυμένης διαμόρφωσης (extended conformation) στα δύο άκρα, που αποτελούνται από τα αμινοξέα Β 1 -Β 8 και Β 20 -Β 30. Σχήμα 1.3: Το μονομερές της ανθρώπινης ινσουλίνης. Διακρίνονται η Α αλυσίδα, με πράσινο και η Β αλυσίδα, με μπλε χρώμα. (Πηγή: Μοντέλο Protein Data Bank, PDBe: 3Ι3Ζ) Το εξαμερές της ινσουλίνης μπορεί να θεωρηθεί ως ένα τριμερές από διμερή, ενώ σταθεροποιείται ιδιαίτερα παρουσία ιόντων ψευδαργύρου (Zn) τα οποία τοποθετούνται στο κέντρο του. Σε κάθε εξαμερές αντιστοιχούν συνήθως 2 ιόντα ψευδαργύρου, κάθε ένα εκ των οποίων συνδέεται είτε με τρεις ιστιδίνες (HisB 10 ) και ένα ανιόν (tetrahedral coordination), είτε με τρεις ιστιδίνες (HisB 10 ) και τρία μόρια νερού (octahedral coordination) (Norrman M., 2007). Σχήμα 1.4: Αριστερά: Δομή του εξαμερούς της ινσουλίνης. Με μπλε χρώμα απεικονίζεται η αλυσίδα Α ενώ με μωβ η αλυσίδα Β. Τα ιόντα Zn 2+ απεικονίζονται με κόκκινο χρώμα. Στην εικόνα φαίνεται μόνο το ένα εκ των δύο ιόντων Zn 2+ που υπάρχουν σε κάθε εξαμερές. Δεξιά: Περιοχή του χάρτη ηλεκτρονιακής πυκνότητας που απεικονίζει τη θέση και τη σύνδεση των ιόντων ψευδαργύρου (κόκκινο) με τρεις ιστιδίνες HisB10 (πράσινο). Ο χάρτης (total omit map) προέκυψε με βάση το δομικό μοντέλο 2A3G της Protein Data Bank (Smith et al., 2005) και δημιουργήθηκε με το πρόγραμμα SFCHECK (Margiolaki et al.,acta Cryst. D., submitted). 12
14 Έχουν παρατηρηθεί τρεις διαφορετικές διαμορφώσεις του εξαμερούς, που ονομάζονται Τ 6, R 6 και T 3 R 3 f (N. C. Kaarsholm, 1989). Οι ονομασίες αυτές αναφέρονται στην αναδίπλωση του αμινοτελικού άκρου της Β-αλυσίδας και για κάθε μια από τις τρείς μορφές η αναδίπλωση έχει ως εξής: Στην Τ 6 μορφή τα αμινοξέα Β 1 -Β 8 αποκτούν εκτεταμένη διαμόρφωση. Στην R 6 μορφή τα αμινοξέα Β 1 -Β 8 αποκτούν ελικοειδή διαμόρφωση. Στην T 3 R 3 f μορφή, στα 3 μονομερή τα αμινοξέα Β 1 -Β 3 αποκτούν εκτεταμένη διαμόρφωση, ενώ τα αμινοξέα Β 4 -Β 8 αποκτούν ελικοειδή διαμόρφωση και τα υπόλοιπα 3 μονομερή αποκτούν εκτεταμένη διαμόρφωση. Και στις τρεις αυτές μορφές τα αμινοξέα της Β-αλυσίδας από το Β 9 έως το Β 19 εμφανίζουν ελικοειδή διαμόρφωση. Σχήμα 1.5: Επάνω: Οι τρείς διαμορφώσεις της ινσουλίνης στην εξαμερική μορφή, (a) Τ 6, (b) R 6 και (c) T 3 R 3 f. Με κόκκινο φαίνεται η διαμόρφωση του αμινοτελικόυ άκρου, σε ένα από τα μονομερή του εξαμερούς, που διαφοροποιεί τις τρεις μορφές. Κάτω: Απεικονίζεται με λεπτομέρια η διάταξη του αμινοτελικού άκρου της Β αλυσίδας για κάθε μια από τις τρεις μορφές αντίστοιχα, (Πηγές: Επάνω: Norrman M., 2006), J.Appl.Cryst.39, & Κάτω: Sonika Bhatnagar, Deepa Srivastava, M.S.K. Jayadev, A.K. Dubey, Progress in Biophysics and Molecular Biology 91 (2006), ). Η μορφή Τ 6 προκύπτει με τη συμμετοχή δύο ατόμων ψευδαργύρου (ανά εξαμερές) σε συνδυασμό με χαμηλές συγκεντρώσεις ανιόντων (συνήθως Cl -, SCN - ). 13
15 Η μορφή R 6 παρατηρείται με συμμετοχή δύο ατόμων ψευδαργύρου, παρουσία ανιόντων (συνήθως Cl -, SCN - -, Ν 3,ΝΟ - 2 ) και φαινολικών παραγώγων. Η φαινόλη και γενικότερα τα φαινολικά παράγωγα χρησιμοποιήθηκαν αρχικά ως συντηρητικά μέσα των φαρμακευτικών σκευασμάτων (Brage, 1987). f Η μορφή T 3 R 3 παρατηρείται με συμμετοχή τεσσάρων ατόμων ψευδαργύρου σε συνδυασμό με υψηλές συγκεντρώσεις ανιόντων (συνήθως Cl -, SCN - ) χωρίς την προσθήκη φαινολικών παραγώγων. Οι τρεις διαφορετικές αλλοστερικές μορφές επηρεάζουν τη σταθερότητα του εξαμερούς. Στην Τ 6 μορφή, η εκτεταμένη διαμόρφωση του αμινοτελικού T 6 R 6 T 3 R 3 f Σχήμα 1.6: Οι τρείς διαμορφώσεις του αμινοτελικού άκρου της Β αλυσίδας της ινσουλίνης, Τ 6, R 6, T 3 R 3 f σε υπέρθεση (Πηγή: Norrman M., 2007). άκρου αφήνει εκτεθειμένα τα ιόντα ψευδαργύρου στο διάλυμα που περιβάλλει την ινσουλίνη. Έτσι υπάρχει πιθανότητα ο ψευδάργυρος να αποκολληθεί και το εξαμερές να καταρρεύσει. Η συνεχής ελικοειδή διαμόρφωση της Β-αλυσίδας (από το Β 1 έως το Β 19 ) κρατάει κοντά τα αμινοτελικά άκρα, με αποτέλεσμα να θωρακίζει τον ψευδάργυρο και η δομή αυτή να είναι η πιο σταθερή. Αυτός είναι και ο λόγος για τον οποίο η T 3 R 3 f μορφή είναι η επόμενη πιο σταθερή δομή, ενώ η δομή Τ 6 είναι η πιο ασταθής (Norrman M., 2007). Φυσικοχημικά χαρακτηριστικά του εξαμερούς της ινσουλίνης υποδεικνύουν ότι: (α) Τα ιόντα ψευδαργύρου, Zn 2+ ή και ασβεστίου, Ca 2+ που απαιτούνται για τη δημιουργία του εξαμερούς της προϊνσουλίνης, συνθέτουν μια δομή η οποία προφυλάσσει τμήματα της πολυπεπτιδικής αλυσίδας, καθώς αυτά παραμένουν προστατευμένα μέσα στις υπομονάδες του εξαμερούς και αφήνουν το πεπτίδιο C εκτεθειμένο. Έτσι η ινσουλίνη προστατεύεται από την πρωτεολυτική διάσπαση που προκαλούν ένζυμα όπως η θρυψίνη (G. Dodson, 1998). (β) Κατά τη μετατροπή του εξαμερούς προϊνσουλίνης σε εξαμερές ινσουλίνης, παρατηρείται μια μεταβολή στη διαλυτότητα η οποία ευνοεί την κρυστάλλωσή της ινσουλίνης. Η κρυστάλλωση κατά συνέπεια παρέχει επιπλέον προστασία στις νεοσυντιθέμενες αλυσίδες ινσουλίνης. (γ) Μελέτες in vitro αποδεικνύουν ότι το εξαμερές της ινσουλίνης είναι πολύ πιο σταθερό ως προς τη χημική και φυσική αποικοδόμηση, σε σχέση με το μονομερές. Συμπερασματικά, ο σχηματισμός του εξαμερούς και η κρυστάλλωσή του σταθεροποιούν και προστατεύουν την ινσουλίνη από την αποικοδόμησή της όσο αυτή παραμένει αποθηκευμένη στον οργανισμό (Emdin 1980, Dunn 2005). Ο σχηματισμός εξαμερών παρουσία ψευδαργύρου, αλλά και συμπλόκων τους με απλές πρωτεΐνες (όπως η πρωταμίνη), αξιοποιούνται φαρμακευτικά. 14
16 1.4 Τύποι Σακχαρώδη διαβήτη Οι κυριότεροι τύποι Σακχαρώδη Διαβήτη είναι ο Σακχαρώδης Διαβήτης Τύπου Ι, ο Σακχαρώδης Διαβήτης Τύπου ΙΙ και ο Σακχαρώδης Διαβήτης Κύησης. Στη συνέχεια παρουσιάζονται τα βασικά χαρακτηριστικά τους. Σακχαρώδης Διαβήτης Τύπου Ι. Αυτός ο τύπος διαβήτη ονομάζεται και ινσουλινοεξαρτώμενος ή νεανικός διαβήτης. Οφείλεται σε βλάβη των β-κυττάρων του παγκρέατος, επομένως ο οργανισμός παράγει ελάχιστη ή και καθόλου ινσουλίνη. Αυτός είναι και ο λόγος για τον οποίο, τα συμπτώματα μπορεί να εμφανιστούν πολύ νωρίς, δηλαδή κατά την παιδική ηλικία, διότι χάνεται ο έλεγχος της γλυκόζης στο αίμα. Ο διαβήτης είναι αποτέλεσμα επίθεσης του ανοσοποιητικού συστήματος στον ίδιο τον οργανισμό και επομένως αποτελεί "αυτοάνοσο" νόσημα. Ο διαβήτης τύπου Ι ελέγχεται αποτελεσματικά με χορήγηση ινσουλίνης. Με τον έλεγχο της γλυκόζης του αίματος, με τη χορήγηση ινσουλίνης και τον έλεγχο της διατροφής ελαχιστοποιούνται οι πιθανότητες μελλοντικών βλαβών στα αιμοφόρα αγγεία, στα νεύρα και στα διάφορα όργανα, επιτρέποντας έτσι στους πάσχοντες να έχουν μια φυσιολογική ζωή (Chausmer, 1998). Σακχαρώδης Διαβήτης Τύπου ΙΙ. Εμφανίζεται ως σύνδρομο αντοχής προς την ινσουλίνη. Δηλαδή φαίνεται πως τα κύτταρα δεν αποκρίνονται προς την ινσουλίνη κατά τον αναμενόμενο τρόπο. Παρά τις μεγάλες ερευνητικές προσπάθειες, η πηγή του προβλήματος δεν είναι βέβαιη. Σε κάποιους ασθενείς το πρόβλημα εντοπίζεται στους κυτταρικούς υποδοχείς της ινσουλίνης, σε ορισμένες περιπτώσεις εμφανίζεται κάποιο πρόβλημα στη διάδοση (χημικού) σήματος της ινσουλίνης, ενώ σε άλλες ο οργανισμός δεν παράγει ινσουλίνη. Επειδή δεν υπάρχει (τουλάχιστον αρχικά) κάποιο πρόβλημα στην έκκριση ινσουλίνης, η χορήγησή της δεν αποτελεί αποτελεσματική θεραπεία όπως στην περίπτωση του διαβήτη τύπου Ι. Η ασθένεια συνήθως ελέγχεται με κατάλληλη δίαιτα, σωματική άσκηση και υπογλυκαιμικά σκευάσματα (Chausmer, 1998). Οι πάσχοντες από διαβήτη τύπου ΙΙ αποτελούν το 90-95% του πληθυσμού των διαβητικών. Κατά κανόνα εμφανίζεται σε μεγάλη ηλικία και εκτιμάται ότι από διαβήτη τύπου ΙΙ πάσχει περίπου το 20% των ατόμων με ηλικία 65 χρονών ή μεγαλύτερη (στη Βόρεια Αμερική). Σακχαρώδης Διαβήτης Κύησης. Αυτός ο τύπος διαβήτη εμφανίζεται για πρώτη φορά κατά τη διάρκεια της κύησης και υποχωρεί μετά τον τοκετό. Το κοινό χαρακτηριστικό του σε σχέση με τον Σακχαρώδη Διαβήτη Τύπου ΙΙ είναι ο συνδυασμός της μειωμένης έκκρισης ινσουλίνης, με τη χαμηλή ευαισθησία των κυττάρων στην ινσουλίνη (Chausmer, 1998). Ποσοστό περίπου 30-40% των γυναικών που θα αναπτύξουν Σακχαρώδη Διαβήτη Κύησης στο μέλλον θα εμφανίσουν Σακχαρώδη Διαβήτη Τύπου ΙΙ. 15
17 1.5 Θεραπεία Όπως προαναφέρθηκε, για να διατηρηθούν τα επίπεδα γλυκόζης του αίματος σε φυσιολογικά επίπεδα, στα άτομα με Διαβήτη Τύπου Ι απαιτείται η χορήγηση ινσουλίνης είτε με ενέσιμη μορφή είτε μέσω αντλιών ινσουλίνης. Τα διαβητικά άτομα πρέπει κατά τη διάρκεια της ημέρας να μετρούν τη γλυκόζη και να λαμβάνουν 3-4 φορές τη μέρα την κατάλληλη ποσότητα ινσουλίνης, ανάλογα και με την άσκηση, τη διατροφή, τις παρελθοντικές τιμές γλυκόζης αλλά και την τάση ανόδου ή καθόδου της γλυκόζης. Γίνεται δηλαδή μια προσπάθεια αντικατάστασης του εσωτερικού μηχανισμού μεταβολισμού γλυκόζης. Αυτό είναι αρκετά δύσκολο για αυτό και έχουν δημιουργηθεί διάφοροι τύποι ινσουλίνης, όπως μακράς, ταχείας και ενδιάμεσης δράσης ενώ εξακολουθούν να γίνονται μελέτες σχετικά με τη δράση των φαρμάκων που χορηγούνται. Μελέτες γίνονται επίσης και για τη χρήση φαρμάκων κρυσταλλικής ινσουλίνης. Τα κρυσταλλικά φάρμακα γενικά φέρουν πολλά πλεονεκτήματα έναντι των συμβατικών φαρμάκων καθώς οι κρύσταλλοι: Παρέχουν υψηλό βαθμό συγκέντρωσης σκευάσματος σε σύγκριση με υγρές συνθέσεις. Παρουσιάζουν μεγαλύτερη σταθερότητα και αντοχή στις χημικές τροποποιήσεις και είναι λιγότερο ευαίσθητες στην μετουσίωση και την αποδιάταξη της τρισδιάστατης δομής τους (Basu S. K., 2004). Προστατεύουν την πρωτεΐνη από τα πρωτεολυτικά ενζυμα, (Halban P. A., 1987). Προσφέρουν ελεγχόμενη απελευθέρωση in vivo. Οι διαφορετικοί τύποι κρυστάλλων έχουν διαφορετική διαλυτότητα, γεγονός που ίσως επηρεάζει τη διάρκεια δράσης του σκευάσματος στο σώμα, δίνοντας μας τη δυνατότητα επιλογής ανάμεσα στην άμεση και την παρατεταμένη αποδέσμευση του φαρμάκου. Ιστορικά οι πρώτοι κρύσταλλοι ινσουλίνης παρήχθησαν το 1926 και όπως προέκυψε υιοθετούσαν τη ρομβοεδρική συμμετρία (Rhombohedral, R3) με διαμόρφωση Τ 6 (Abel, 1926). Αργότερα, ο David Aylmer Scott, το 1934 παρατήρησε ότι η προσθήκη ψευδαργύρου (Zn) και άλλων δισθενών μέταλλων (όπως Cd, Co, Ni) ήταν απαραίτητα για τη δημιουργία κρυστάλλων (Scott, 1934). Ως προς το χρόνο δράσης των ενέσεων ινσουλίνης, η πρώτη βελτίωση παρατηρήθηκε όταν ο Hagedorn το 1936 ανέμειξε ινσουλίνη, ψευδάργυρο (Ζn) και πρωταμίνη, NPH, (H.C. Hagedorn, 1936) που παρήγαγε σκευάσματα παρατεταμένης δράσης. Δέκα χρόνια αργότερα ο πρώτος σταθερός κρύσταλλος παρατεταμένης δράσης, που περιείχε ινσουλίνη, ψευδάργυρο (Zn) και πρωταμίνη σε ουδέτερο ph, παρουσιάστηκε από τους Krayenbuhl και Rosenburg. Μερικά χρόνια αργότερα ξεκίνησε η παραγωγή της σειράς Lente (Moller, 1965) και ρυθμίζοντας το ph, τον ψευδάργυρο και τις 16
18 συγκεντρώσεις ινσουλίνης (χωρίς πρωταμίνη) πραγματοποιήθηκε η δημιουργία τριών παρασκευασμάτων διαφορετικής δράσης: Άμορφης ινσουλίνης (Semilente) Συνδυασμός άμορφης και κρυσταλλικής μορφής (Lente) Ινσουλίνης σε κρυσταλλική μορφή (Ultralente) Η κρυσταλλική μορφή (Ultralente) παρείχε παρατεταμένης διάρκειας δράση, ενώ το άμορφο (Semilente) και ο συνδυασμός άμορφης και κρυσταλλικής μορφής (Lente) παρείχαν μικρότερης διάρκειας δράση. Τα τελευταία χρόνια πραγματοποιείται έρευνα με σκοπό την εύρεση νέων διαμορφώσεων της ινσουλίνης οι οποίες θα μπορούσαν να μιμηθούν όσο το δυνατόν καλύτερα τη φυσιολογική απόκριση της ενδογενούς ινσουλίνης, προκειμένου να μειωθεί ο αριθμός των χορηγήσεων που δίνονται στους ασθενείς. Σήμερα πλέον, η ευρύτατα χρησιμοποιούμενη ανθρώπινη ινσουλίνη δε λαμβάνεται από τα β κύτταρα του ανθρώπινου παγκρέατος, αλλά παράγεται εργαστηριακά από γενετικώς τροποποιημένα βακτήρια Escherichia coli ή κύτταρα ζύμης τα οποία περιέχουν στο γονιδίωμά τους ανθρώπινα γονίδια. Παράγονται και απομονώνονται οι δύο αλυσίδες Α και Β από δύο διαφορετικά στελέχη και στη συνέχεια συνδέονται στο εργαστήριο με δισουλφιδικούς δεσμούς. Κατά την αναζήτηση νέων διαμορφώσεων η ινσουλίνη έχει κρυσταλλωθεί σε διάφορες συμμετρίες (Crystal Systems & Space groups). Όλες αυτές οι κρυσταλλώσεις έχουν οδήγησει στο συμπέρασμα ότι οι βασικοί παράγοντες που επηρεάζουν τη συμμετρία των κρυστάλλων της ινσουλίνης είναι: η προσθήκη ψευδαργύρου η παρουσία φαινολικών παραγώγων η παρουσία ανιόντων που δεσμεύουν τον ψευδάργυρο το ph Στον παρακάτω πίνακα (Πίνακας 1.1) φαίνονται οι συνηθέστερες κρυσταλλικές μορφές στις οποίες κρυσταλλώνεται η ανθρώπινη ινσουλίνη (Norrman M., 2007). 17
19 Πίνακας 1.1: Οι συνηθέστερες μορφές στις οποίες κρυσταλλώνεται η ανθρώπινη ινσουλίνη. Στον πίνακα αναγράφονται εκτός από τις συμμετρίες (Crystal system, Space group) και η διαμόρφωση της Β αλυσίδας (B-chain configuration), (Πηγή: Norrman M., 2007). 18
20 2. Κρυσταλλογραφία Ακτίνων-Χ 2.1 Ακτίνες-Χ Ένα σημαντικό μέρος των πληροφοριών που καταλήγουν σε εμάς από τον κόσμο γύρω μας, έχει τη μορφή ηλεκτρομαγνητικής ακτινοβολίας. Η ηλεκτρομαγνητική ακτινοβολία είναι η ενέργεια που μεταφέρεται στο χώρο μέσω ηλεκτρομαγνητικών κυμάτων, τα οποία παράγονται από την ταυτόχρονη διάδοση του ηλεκτρικού και μαγνητικού πεδίου στο χώρο και το χρόνο. Τα διάφορα είδη των κυμάτων αυτών διαφέρουν ως προς τη μέθοδο δημιουργίας τους και κατηγοριοποιούνται ανάλογα με την κλίμακα μήκους κύματος (λ). Λόγω της τελευταίας παραμέτρου, λ, τα διαφορετικά είδη ηλεκτρομαγνητικής ακτινοβολίας παρουσιάζουν μεγάλες διαφορές στις εφαρμογές τους. Το σύνολο των ηλεκτρομαγνητικών αυτών κυμάτων αποτελεί το ηλεκτρομαγνητικό φάσμα. Σχήμα 2.1: Το ηλεκτρομαγνητικό φάσμα (Πηγή: Οι ακτίνες-χ ανακαλύφθηκαν από τον Wilhelm Röntgen το 1895, και τα πρώτα πειράματα έδειξαν ότι πρόκειται για ηλεκτρομαγνητική ακτινοβολία µε μήκος κύματος το οποίο εντοπίζεται στην περιοχή του φάσματος από 10 έως 0.01 nm (1nm=10-9 m). Τα όρια αυτά συνορεύουν με δύο περιοχές των ηλεκτρομαγνητικών κυμάτων: την περιοχή των υπεριωδών ακτίνων και την περιοχή των ακτίνων γ (Σχήμα 2.1). Οι ακτίνες-χ παράγονται κυρίως κατά την πρόσκρουση ταχύτατα κινούμενων ηλεκτρονίων σε κάποιο μεταλλικό σώμα. Κατά την απότομη μεταβολή της κινητικής ενέργειας των ηλεκτρονίων, ποσοστό περίπου 99% μετατρέπεται σε θερμότητα, ενώ μόλις το 1% αυτής εκπέμπεται ως ακτινοβολία Χ. Ακτίνες των οποίων το μήκος κύματος είναι μεγαλύτερο από 2Å, χαρακτηρίζονται ως «μαλακές», ενώ όσες έχουν μήκος κύματος μικρότερο του 1Å ως «σκληρές». Οι πρώτες απορροφούνται ευκολότερα και για το λόγο αυτό είναι περισσότερο επικίνδυνες για τους ζώντες οργανισμούς. Στην ιατρική χρησιμοποιούνται ακτίνες-χ με μήκος κύματος μικρότερο του 0.1 Å. 19
21 Οι ακτίνες-χ παρουσιάζουν υψηλή διαπεραστική ικανότητα, γεγονός που οφείλεται στο πολύ μικρό μήκος κύματος. Επίσης ιονίζουν τα σώματα που διαπερνούν κι έτσι προκαλούν βιολογικές επιδράσεις στους ζωντανούς ιστούς. 2.2 Περίθλαση ακτίνων-χ Όπως και στους άλλους τύπους ηλεκτρομαγνητικής ακτινοβολίας, έτσι και στις ακτίνες-χ, η αλληλεπίδραση μεταξύ των ηλεκτρονίων της ακτινοβολίας και των ηλεκτρονίων της ύλης, προκαλεί σκέδαση. Το φαινόμενο της περίθλασης είναι η απόκλιση μιας φωτεινής δέσμης από την ευθύγραμμη διάδοση όταν αυτή συναντάει ένα άνοιγμα ή εμπόδιο. Η αλλαγή της πορείας της δέσμης συνοδεύεται από χωρική ανακατανομή της έντασης της δέσμης με την εμφάνιση μεγίστων και ελαχίστων έντασης σε διάφορες διευθύνσεις του χώρου ως προς την αρχική διεύθυνση της δέσμης και τη θέση του εμποδίου. Αυτές οι εναλλασσόμενες φωτεινές και σκοτεινές περιοχές είναι γνωστές με τον όρο κροσσοί περίθλασης. Πρόκειται για ένα φαινόμενο που οφείλεται στην κυματική φύση του φωτός και ερμηνεύεται με βάση την κυματική θεωρία, δηλαδή την περιγραφή του φωτός ως διαδιδόμενης κυματικής διαταραχής μέσω της ηλεκτρομαγνητικής θεωρίας. Όταν φωτεινή δέσμη προσπίπτει πάνω σε μία λεπτή σχισμή τότε (σύμφωνα με την αρχή του Huygens) κάθε μέρος της σχισμής γίνεται με την σειρά του πηγή εκπομπής φωτεινών ακτίνων (Σχήμα 2.2). Έτσι στην περίπτωση που υπάρχουν δύο σχισμές, οι φωτεινές ακτίνες των δευτερευόντων πηγών συμβάλλουν είτε καταστρεπτικά, είτε ενισχυτικά, ακολουθώντας τους κανόνες της ενισχυτικής και καταστρεπτικής συμβολής. Αν αυξήσουμε το πλήθος των σχισμών και προς τις δύο κατευθύνσεις, σχηματίζεται μια διάταξη που ονομάζεται φράγμα περίθλασης. Σχήμα 2.2: Αριστερά: Η αρχή του Huygens. Καθώς φωτεινή δέσμη προσπίπτει πάνω σε λεπτή σχισμή, η σχισμή γίνεται πηγή εκπομπής φωτεινών ακτίνων (Πηγή: Δεξιά: (α) Ενισχυτική συμβολή κυμάτων που βρίσκονται μεταξύ τους σε φάση και (β) καταστρεπτική συμβολή κυμάτων που εμφανίζουν το ένα μέγιστο και το άλλο ελάχιστο στις ίδιες θέσεις. 20
22 Κατά τον ίδιο τρόπο, όταν οι ακτίνες-χ σκεδάζονται εντός ενός κρυστάλλου, δηλαδή σε ένα αυστηρά περιοδικό περιβάλλον, παρατηρείται συμβολή (ενισχυτική ή καταστρεπτική) των σκεδαζόμενων ακτίνων, επειδή οι αποστάσεις μεταξύ των κέντρων σκέδασης του κρυστάλλου είναι του ίδιου μεγέθους με το μήκος κύματος της ακτινοβολίας Η συμβολή του Laue Κατά την περίοδο που ανακαλύφθηκαν οι ακτίνες-χ, άρχισε παράλληλα να μορφοποιείται η ιδέα στην επιστημονική κοινότητα ότι τα άτοµα σε ένα κρυσταλλικό στερεό είναι διευθετημένα στις θέσεις ενός πλέγματος, σε µια κατά διαστήµατα επαναλαμβανόμενη διάταξη. Μάλιστα, η εκτιμώμενη απόσταση μεταξύ των ατόμων θεωρήθηκε ότι ήταν στην περιοχή των Å (1Å=10-10 m). Συνδυάζοντας τις δύο αυτές ιδέες ο Max von Laue το 1912 πρότεινε ότι θα ήταν δυνατό ένας κρύσταλλος να αποτελέσει ένα είδος τρισδιάστατου φράγματος περίθλασης ακτίνων-χ. Επομένως, µια δέσµη ακτίνων-χ θα μπορούσε να υποστεί σκέδαση από τα μεμονωμένα άτοµα ενός κρυστάλλου, ενώ τα σκεδασθέντα κύματα θα μπορούσαν να συμβάλλουν, όπως ακριβώς τα φωτεινά κύματα από ένα φράγμα περίθλασης. Τα πρώτα πειράματα περίθλασης ακτίνων-χ πραγματοποιήθηκαν από τον Friederich Knipping και από τον Max von Laue το Τα πειράματα αυτά έδειξαν ότι οι ακτίνες-χ έχουν κυματικές ιδιότητες και ότι τα άτομα στα κρυσταλλικά στερεά βρίσκονται σε περιοδική διάταξη. Όταν δέσμη ακτίνων-χ προσκρούει στην επιφάνεια ενός κρυστάλλου υπό τυχαία γωνία θ, ένα ποσοστό της δέσμης σκεδάζεται από το επιφανειακό στρώμα των ατόμων. Το ποσοστό της δέσμης που δε σκεδάζεται εισέρχεται στο δεύτερο στρώμα ατόμων, όπου και πάλι ένα τμήμα θα σκεδασθεί, ενώ το υπόλοιπο θα εισέλθει στο τρίτο στρώμα και ούτω καθεξής. Το αθροιστικό αποτέλεσμα της σκέδασης αυτής από τα αυστηρώς διαταγμένα κέντρα του κρυστάλλου είναι η περίθλαση της δέσμης. Μερικά χρόνια αργότερα εδραιώθηκε η σκέψη ότι η περίθλαση ακτίνων-χ, είναι μια μέθοδος μέσω της οποίας μπορεί να πραγματοποιείται ο προσδιορισμός της κρυσταλλικής δομής διαφόρων υλικών Νόμος του Bragg Το 1912 ο Βρετανός φυσικός William Henry Bragg ( ) μαζί με τον γιό του Lawrence Bragg ( ), επίσης φυσικό, κατάφεραν να μελετήσουν την κρυσταλλική δομή των ενώσεων με τη βοήθεια των ακτίνων-χ και να ανακαλύψουν το νόμο που φέρει το όνομά τους. Υπολόγισαν τις αποστάσεις μεταξύ των διατομικών επιπέδων του κρυστάλλου και ανέλυσαν τη γεωμετρική διευθέτηση των 21
23 ατόμων στους απλούς κρυστάλλους. Το σημαντικότερο επίτευγμά τους ήταν ότι κατάφεραν να περιγράψουν το φαινόμενο της περίθλασης, συνδέοντας με έναν πολύ απλό νόμο τα πιο σημαντικά μεγέθη του φαινομένου. Ο νόμος αυτός συνδέει το μήκος κύματος λ των ακτίνων-χ, με τη γωνία πρόσπτωσης θ πάνω στα διαδοχικά επίπεδα ενός κρυστάλλου καθώς και με την μεταξύ τους απόσταση d. Στο Σχήμα 2.3 φαίνονται οι συνθήκες που κρίνονται αναγκαίες για την παραγωγή ισχυρά περιθλώμενης δέσμης από έναν κρύσταλλο. Σχήμα 2.3 Σχηματικά ο νόμος του Bragg και οι αναγκαίες συνθήκες για την παραγωγή μιας ισχυρά περιθλώμενης δέσμης. Εάν η διαφορά δρόμων μεταξύ των δύο ακτινών R1και R2 είναι ίση με ένα ακέραιο πολλαπλάσιο του μήκους κύματος λ, τότε οι εξερχόμενες ακτίνες συμβάλλουν εποικοδομητικά με αποτέλεσμα την εμφάνιση μεγίστου σκέδασης. Θεωρούμε, ένα υλικό που αποτελείται από άπειρα, παράλληλα, ισαπέχοντα κρυσταλλογραφικά επίπεδα που απέχουν μεταξύ τους απόσταση d. Οι τελείες αναπαριστούν τα σημεία του πλέγματος δύο κρυσταλλογραφικών παραλλήλων επιπέδων. Δύο ακτίνες μονοχρωματικής δέσμης, R 1 και R 2, μήκους κύματος λ, προσπίπτουν στη συγκεκριμένη διάταξη, υπό γωνία θ. Εποικοδομητική συμβολή των εξερχόμενων, από τα επίπεδα, ακτίνων εμφανίζεται όταν η διαφορά δρόμων των ακτινοβολιών, είναι μηδενική ή ίση με ακέραιο πολλαπλάσιο του μήκους κύματος. Δηλαδή : (2.1) όπου d είναι η απόσταση των επιπέδων, θ η γωνία πρόσπτωσης, λ το μήκος κύματος των ακτίνων-χ και 22
24 n είναι ένας ακέραιος που αντιπροσωπεύει την τάξη της αντίστοιχης περίθλασης. Ο νόμος του Bragg αποτελεί αναγκαία συνθήκη ώστε η σκεδαζόμενη δέσμη να λάβει μέγιστη ένταση, ως αποτέλεσμα εποικοδομητικής συμβολής. Αν η διαφορά δρόμων είναι ίση με n λ, τότε τα κύματα R1 και R2 είναι σε φάση, δηλαδή (2.2) όπου φ η γωνία φάσης. Το πλάτος του κύματος που προκύπτει από την ενισχυτική συμβολή των κυμάτων R1 και R2 μπορεί να εκφραστεί ως: (2.3) όπου τα μεγέθη Fhkl και φ είναι το πλάτος και η φάση της σκεδαζόμενης δέσμης, αντίστοιχα. Για κάποιες γωνίες πρόσπτωσης θ των εισερχόμενων ακτίνων, στις οποίες τυχαίνει τα κύματα των ακτινοβολιών να μη βρίσκονται σε φάση, επέρχεται καταστρεπτική συμβολή των κυμάτων, με αποτέλεσμα να παρατηρείται μηδενική ένταση της ακτινοβολίας, ενώ για άλλες γωνίες πρόσπτωσης η σκεδαζόμενη ακτινοβολία λαμβάνει ενδιάμεσες τιμές μεταξύ της μέγιστης και της ελάχιστης τιμής της έντασης. Γενικά, το φαινόμενο της περίθλασης παρατηρείται όταν το εμπόδιο ή η σχισμή που συναντά η δέσμη, έχουν διαστάσεις ίδιας τάξης μεγέθους προς το μήκος κύματος της ίδιας της δέσμης. Έτσι για να παρατηρήσουμε περίθλαση του φωτός πρέπει να έχουμε πολύ μικρές οπές ή πολύ μικρά εμπόδια. 2.3 Κρυσταλλογραφία Απαραίτητη προϋπόθεση για τον προσδιορισμό της δομής ενός υλικού, μέσω της περίθλασης ακτίνων-χ, αποτελεί η ύπαρξη κρυστάλλων που προέρχονται από το συγκεκριμένο υλικό. Ένας κρύσταλλος ή ακριβέστερα ένας μονοκρύσταλλος, ορίζεται μακροσκοπικά ως ένα στερεό αντικείμενο, με ομοιόμορφη χημική σύσταση, που όπως απαντάται στη φύση ή σχηματίζεται στο εργαστήριο, διαμορφώνεται από επίπεδες έδρες, οι σχέσεις των οποίων δείχνουν μια τυπική συμμετρία. Αν ένα στερεό δεν παρουσιάζει μια ορισμένη κρυσταλλική δομή, τότε είναι άμορφο. Ο κρύσταλλος αποτελείται από δομικές μονάδες (άτομα, ιόντα ή μόρια) που συγκρατούνται με χημικούς δεσμούς, σε διάταξη η οποία επαναλαμβάνεται περιοδικά στις τρεις διαστάσεις. Η δομική μονάδα ενός κρυστάλλου καλείται μοναδιαία ή θεμελιώδης κυψελίδα (unit cell). 23
25 Για τον μαθηματικό ορισμό της μοναδιαίας κυψελίδας, απαιτούνται έξι (6) παράμετροι: οι τρεις άξονες-ακµές της κυψελίδας (a, b, c) και οι τρεις γωνίες (α, β, γ) μεταξύ των ακμών. Κατά σύμβαση, έχει οριστεί ως α η γωνία μεταξύ των πλευρών b και c, ως β η γωνία μεταξύ των πλευρών a και c και ως γ η γωνία μεταξύ των πλευρών a και b (Σχήμα 2.4). Σχήμα 2.4 Απεικόνιση των πλευρών (a, b, c) και των γωνιών (α, β, γ) σε μια κυψελίδα. Η εσωτερική τάξη και συμμετρία που υπάρχει σε ατομικό επίπεδο, αντανακλάται και μακροσκοπικά στη μορφολογία των κρυστάλλων οι οποίοι σχηματίζουν κανονικά γεωμετρικά σχήματα. Υπάρχουν επτά (7) βασικοί τύποι μοναδιαίων κυψελίδων οι οποίοι κατατάσσονται σε ένα από τα επτά κρυσταλλικά συστήματα (Crystal systems): Κυβικό, Τετραγωνικό, Ορθορομβικό, Εξαγωνικό, Τριγωνικό (Ρομβοεδρικό), Μονοκλινές και Τρικλινές. Τα χαρακτηριστικά συμμετρίας των κρυσταλλικών συστημάτων δίνονται στον Πίνακα 2.1 και οι άξονες στις τρεις διαστάσεις φαίνονται στον Πίνακα 2.2. Κρυσταλλικό σύστημα Πλευρές Γωνίες Κυβικό a= b= c α=β=γ=90 Τετραγωνικό a= b c α=β=γ=90 Ορθορομβικό a b c α=β=γ=90 Εξαγωνικό a= b c α=β=90, γ=120 Τριγωνικό / Ρομβοεδρικό a= b= c α=β=γ < Μονοκλινές a b c α=γ=90, β 90 Τρικλινές a b c α β γ 90 Πίνακας 2.1: Τα επτά κρυσταλλικά συστήματα και τα χαρακτηριστικά τους. Το ρομβοεδρικό κρυσταλλικό σύστημα θεωρείται υποπερίπτωση του τριγωνικού, καθώς παρουσιάζει πλευρές μεταξύ τους ίσες (a= b= c) και γωνίες α= β= 90, γ=
26 Πίνακας 2.2: Τα κρυσταλλικά συστήματα. Στην κατάταξη του πίνακα, οι κρύσταλλοι με εξαγωνική, τριγωνική και ρομβοεδρική συμμετρία μελετώνται στα πλαίσια του ίδιου κρυσταλλικού συστήματος, δηλαδή με τους ίδιους κρυσταλλογραφικούς άξονες. Γι αυτό και τα κρυσταλλικά συστήματα παρουσιάζονται ως έξι στο σύνολο (Πηγή: Η εμβάθυνση στην κρυσταλλική δομή απαιτεί τη γνώση του τρόπου με τον οποίο οι δομικές μονάδες διατάσσονται στο χώρο. Για το λόγο αυτό, εισάγεται στην κρυσταλλογραφία, η έννοια του χωροπλέγματος και ορίζεται ότι η δομή των κρυστάλλων μπορεί να περιγραφεί ως συνάρτηση ενός τρισδιάστατου δικτύου σημείων, του γεωμετρικού χωροπλέγματος (ή απλά πλέγματος), σε κάθε σημείο του οποίου αντιστοιχεί μια δομική μονάδα. Γεωμετρικά, το πλέγμα είναι μια κανονική, επαναλαμβανόμενη επ άπειρον, διάταξη σημείων. Το περιβάλλον κάθε διακεκριμένου σημείου είναι το ίδιο με αυτό κάθε άλλου σημείου του πλέγματος. Η αρχή της κυψελίδας μπορεί να επιλεγεί αυθαίρετα οπουδήποτε στον χώρο του πλέγματος, συνεπώς μπορεί να συμπίπτει ή όχι με πλεγματικό σημείο. Όταν περιέχει μόνο ένα πλεγματικό σημείο, η μοναδιαία κυψελίδα είναι θεμελιώδης (ή απλή ή πρωτογενής: primitive unit cell), όπως και τα διανύσματα μεταφοράς που την καθορίζουν. Η θεμελιώδης κυψελίδα είναι ο μικρότερος όγκος, που παράγει με επανάληψη την κρυσταλλική δομή ή αλλιώς, που αποδίδει την πλήρη συμμετρία της κρυσταλλικής δομής. Οτιδήποτε ισχύει για τη θεμελιώδη κυψελίδα (συμμετρίες, διάταξη ατόμων κλπ.) ισχύει επακριβώς για οποιαδήποτε άλλη ίδια κυψελίδα του υπό μελέτη κρυστάλλου Πλέγματα Bravais Στο πλαίσιο τώρα ενός κρυσταλλικού συστήματος, υπάρχει η δυνατότητα επιλογής νέων, μη θεμελιωδών τύπων πλεγμάτων που διατηρούν τη συμμετρία σημείου του συγκεκριμένου συστήματος. Τα πλέγματα αυτά προκύπτουν με μια διαδικασία που ονομάζεται κέντρωση (centering) και η οποία εισάγει πλεγματικά σημεία στις θέσεις υψηλής συμμετρίας ενός θεμελιώδους πλέγματος. Καθένα από 25
27 τα μη θεμελιώδη πλέγματα ενός κρυσταλλικού συστήματος περιγράφεται με μια «συμβατική», ή τυπική κεντρωμένη μοναδιαία κυψελίδα διαφορετική της θεμελιώδους. Ορίζονται τέσσερις τύποι κεντρωμένων πλεγμάτων, ανάλογα με τη θέση των πλεγματικών σημείων: Απλό πλέγμα (Primitive, P): Η κυψελίδα περιέχει πλεγματικά σημεία στις κορυφές των εδρών της. Χωροκεντρωμένο πλέγμα (Body centered, I): Η αντίστοιχη κυψελίδα περιέχει πλεγματικά σημεία στις κορυφές και ένα σημείο στο κέντρο της κυψελίδας. Εδροκεντρωμένο πλέγμα ή ολοεδρικώς κεντρωμένο (Face centered, F): Η αντίστοιχη κυψελίδα περιέχει πλεγματικά σημεία στις κορυφές και ένα σημείο στο κέντρο κάθε έδρας. Βάση-κεντρωμένο πλέγμα (Base centered, A, B ή C): Η αντίστοιχη κυψελίδα περιέχει πλεγματικά σημεία στις κορυφές και στα κέντρα δυο απέναντι εδρών. Σχήμα 2.5: Διακρίνονται από αριστερά προς τα δεξιά (α) το απλό κυβικό (simple cubic-sc), (β) το χωροκεντρωμένο κυβικό (body-centered cubic- bcc), (γ) το εδροκεντρωμένο κυβικό (face centered cubic- fcc) και (δ) το κυβικό βάση-κεντρωμένο C πλέγμα (Πηγή: Σύμφωνα με τα παραπάνω κάποιος θα περίμενε ότι τα επτά βασικά κρυσταλλικά συστήματα σε συνδυασμό με τους έξι τύπους κυψελίδων που δυνητικά θα μπορούσαν να εμφανιστούν στο καθένα, θα δημιουργούσαν 6x7=42 τύπους πλεγμάτων. Αυτό όμως δεν συμβαίνει καθώς λόγοι συμμετρίας απαγορεύουν τη δημιουργία ορισμένων πλεγμάτων. Για παράδειγμα μια Α, Β ή C βαση-κεντρωμένη κυβική δομή δεν είναι δυνατόν να υπάρξει σε κάθε σύστημα γιατί αμέσως καταστρέφεται η κυβική συμμετρία. Η διαδοχική περιστροφή της μοναδιαίας κυψελίδας κατά 90 ο προς οποιαδήποτε κατεύθυνση, δεν δίνει ίδια κυψελίδα, πράγμα που ισχύει στην κυβική συμμετρία. Αντίθετα εδροκεντρωμένη ή χωροκεντρωμένη κυβική κυψελίδα είναι δυνατόν να υπάρξει χωρίς να επηρεάζονται τα στοιχεία της κυβικής συμμετρίας. Τελικά, διαπιστώνεται πως ο αριθμός των δυνατών διαφορετικών (θεμελιωδών και μη) τύπων πλεγμάτων, είναι δεκατέσσερα (14). Καθένα από αυτά περιγράφεται με μία είτε θεμελιώδη, είτε κεντρωμένη, μοναδιαία κυψελίδα. Τα 14 αυτά κρυσταλλικά πλέγματα, ονομάζονται πλέγματα Bravais (Bravais lattices) και παρακάτω φαίνεται η ομαδοποίησή τους στα επτά κρυσταλλικά συστήματα. 26
28 Σχήμα 2.6: Τα δεκατέσσερα πλέγματα Bravais (Πηγή: Space groups Για να καθορίσουμε πλήρως τη συμμετρία μιας κρυσταλλικής δομής, πρέπει να λάβουμε υπόψη επιπλέον δυο διαδικασίες. Η πρώτη είναι η διαδικασία μετατοπίσεως του πλέγματος η οποία αφήνει αμετάβλητη την εικόνα του πλέγματος, είναι δηλαδή μια διαδικασία συμμετρίας μετατοπίσεως του πλέγματος στο χώρο. Και η δεύτερη είναι μια διαδικασία συμμετρίας κατά την οποία δε μετατοπίζεται το κρυσταλλικό πλέγμα, δηλαδή τουλάχιστον ένα πλεγματικό σημείο παραμένει ακίνητο. Όταν η εφαρμογή των διαδικασιών συμμετρίας δε μετατοπίζει το κρυσταλλικό πλέγμα πρόκειται για συμμετρία σημείου, ενώ αντίθετα όταν μετατοπίζει όλα τα σημεία του, πρόκειται για συμμετρία χώρου. 27
29 Συμμετρία σημείου Οι διαδικασίες συμμετρίας σημείου είναι οι εξής: Συμμετρία περιστροφής (Rotation). Συμμετρία περιστροφής επιτρέπεται όταν κατά την περιστροφή του πλέγματος υπό ορισμένη γωνία, γύρω από άξονα ο οποίος διέρχεται από πλεγματικό σημείο, εμφανίζεται δομή ταυτόσημη με την αρχική. Η συμμετρία αυτή χαρακτηρίζεται από τον αριθμό των βημάτων που απαιτούνται για την επαναφορά του πλέγματος στην αρχική του δομή, χωρίς το πλέγμα να αλλάζει όψη σε κάθε βήμα. Ένα τετραγωνικό πλέγμα, για παράδειγμα, επανέρχεται στην αρχική του δομή μετά από τέσσερις περιστροφές κατά 2π/4 η κάθε μια. Εάν η γωνία περιστροφής είναι 2π/n (n=ακέραιος) ο άξονας θα ονομάζεται n-οστής τάξης. Έτσι μπορεί να έχουμε άξονες περιστροφής 2 ης, 3 ης, 4 ης και 6 ης τάξης οι οποίοι επαναφέρουν τον κρύσταλλο στην αρχική του δομή 1 με περιστροφή κατά 2π/2, 2π/3, 2π/4 και 2π/6 ακτίνια αντίστοιχα. Στροφή κατά 2π/5 ή 2π/7 ακτίνια δεν φέρνει το πλέγμα σε ταυτόσημη με την αρχική δομή. Συμμετρία καθρέπτη (mirror). Η κατοπτρική συμμετρία ορίζεται όταν το πλέγμα περιέχει ένα επίπεδο που τέμνει το σχήμα του και το χωρίζει σε δύο ακριβώς ίδια μέρη. Αυτό το επίπεδο ονομάζεται κατοπτρικό επίπεδο και η διεργασία συμμετρίας που προκαλεί εκφράζεται μαθηματικώς με έναν μετασχηματισμό ορθογωνίων συντεταγμένων. Για παράδειγμα, η συμμετρία ανακλάσεως που γίνεται ως προς το επίπεδο xy (τρισορθογώνιου συστήματος) παριστάνεται με τον μετασχηματισμό x =x, y =y, z = -z. Το κατοπτρικό επίπεδο συμβολίζεται στο διεθνές σύστημα συμβολισμού με το γράμμα m (από τη λέξη mirror). Γενικά κατοπτρική συμμετρία συναντάται παντού στην φύση. Το ανθρώπινο σώμα είναι ένα παράδειγμα που παρουσιάζει πλευρική κατοπτρική συμμετρία. Συμμετρία Αναστροφής ως προς σημείο (Inversion centre). Η συμμετρία αυτή προϋποθέτει την ύπαρξη ενός ακλόνητου σημείου, του κέντρου συμμετρίας ως προς το οποίο πραγματοποιείται προβολή του πλέγματος (κεντροσυμμετρία). Ένας κρύσταλλος διαθέτει κέντρο συμμετρίας, αν οποιαδήποτε ευθεία που ξεκινά από μια κρυσταλλική έδρα και διέρχεται από το σημείο αυτό, καταλήγει σε ισοδύναμο σημείο κρυσταλλικής έδρας, σε ίση απόσταση από το σημείο αναστροφής. Η συμμετρία αυτή εκφράζεται μαθηματικώς με το μετασχηματισμό των συντεταγμένων x = -x, y = -y, z = -z και συμβολίζεται με το. 1 Όχι στην αρχική του θέση. 28
30 Σχήμα 2.7: Οι συμμετρίες σημείου. Συμμετρία περιστροφής, κατοπτρική συμμετρία και συμμετρία αναστροφής ως προς σημείο. Στο σχήμα δεξιά ο άξονας κατοπτρικής συμμετρίας είναι ο άξονας Οy ενώ το κέντρο συμμετρίας είναι το σημείο O (Πηγή: Από το συνδυασμό των παραπάνω στοιχείων μεταξύ τους καθώς και με τη συμμετρία μεταφοράς προκύπτουν δύο νέοι τύποι συμμετρίας (Meier, 1984). Η συμμετρία που προκύπτει από την περιστροφή και την αναστροφή ως προς το κέντρο συμμετρίας ονομάζεται συμμετρία στροφοαναστοφής (Rotoinversion axis). Συμβολίζεται με μια παύλα πάνω από τον αριθμό που δείχνει την τάξη του άξονα περιστροφής δηλαδή,,, ή. Πολλοί κρύσταλλοι διαθέτουν άξονες περιστροφής (2, 3, 4, 6) κάθετους σε κατοπτρικά επίπεδα (m). Αυτή η συμμετρία περιστροφής και καθρέπτη ονομάζεται στροφοκατοπτρική και συμβολίζεται ως n/m (δηλαδή 2/m, 3/m, 4/m και 6/m αντίστοιχα). 2 2 Ο άξονας στροφοαναστροφής ισοδυναμεί με το κέντρο συμμετρίας, ο άξονας ισοδυναμεί με τη συμμετρία καθρέπτη (mirror) και ο άξονας είναι ισοδύναμος με το συνδιασμό 3/m. Γι αυτό οι άξονες αυτοί συνήθως αναφέρονται με τα ισοδύναμα στοιχεία συμμετρίας. 29
31 Σχήμα 2.8: Στην εικόνα επάνω αναπαριστάται γραφικά η συμμετρία στροφοαναστοφής και στην εικόνα κάτω απεικονίζεται η στροφοκατοπτρική συμμετρία. Οι κύκλοι κάτω από κάθε σχήμα είναι οι προβολές που προκύπτουν ως προς τον άξονα περιστροφής. Σε αυτές τις προβολές οι μαύρες κουκίδες αντιστοιχούν στα σημεία πάνω από το σημείο αναστροφής, ενώ οι λευκές κουκίδες αντιστοιχούν στα σημεία κάτω από το σημείο αναστροφής (Πηγή: Τα παραπάνω στοιχεία συμμετρίας μπορούν να συνδυαστούν με διάφορους τρόπους. Με άλλα λόγια κάθε κρύσταλλος μπορεί να περιγραφεί με ένα συγκεκριμένο συνδυασμό στοιχείων συμμετρίας σημείου. Από αυτές τις συμμετρίες και τους συνδυασμούς τους στις τρείς διαστάσεις, προκύπτουν οι 32 ομάδες συμμετρίας σημείου (Point Groups). Ομάδα συμμετρίας σημείου (Point group) ονομάζεται το σύνολο των διαδικασιών συμμετρίας, εκτός των μετατοπίσεων, οι οποίες όταν εφαρμοστούν σε ένα πλέγμα το αφήνουν αμετάβλητο. Στις τρεις διαστάσεις υπάρχουν 32 συμμετρίες σημείου Συμμετρία χώρου Η βάση ενός κρυστάλλου μπορεί να είναι ένα πολύπλοκο μόριο το οποίο να έχει συμμετρία διαφορετική του πλέγματος στο οποίο ανήκει. Έτσι όταν 30
32 εφαρμοστούν οι διαδικασίες συμμετρίας πρέπει τόσο το πλέγμα όσο και η βάση να επανέλθουν στον εαυτό τους. Στις περιπτώσεις αυτές εκτός των συμμετριών σημείου, απαιτείται συχνά και μετατόπιση στο χώρο. Η συμμετρία μετατοπίσεως γίνεται κυρίως με τη χρήση του πλεγματικού διανύσματος R. Υπάρχουν όμως και περιπτώσεις όπου η διαδικασία μετατοπίσεως είναι διαφορετική. Συγκεκριμένα μπορούμε να χρησιμοποιήσουμε δυο νέες διαδικασίες μετατοπίσεως σε συνδυασμό με τη συμμετρία σημείου. Άξονες βίδας (Screw axes). Η κρυσταλλική δομή που έχει άξονα βίδας, συμπίπτει με τον εαυτό της εφαρμόζοντας συνδυαστικά μια διαδικασία μετατόπισης (με διάνυσμα μετατόπισης το οποίο δεν είναι θεμελιώδες) και μια περιστροφή γύρω από τον άξονα στον οποίο έγινε η μετατόπιση. Περιγράφεται από το σύμβολο n z το οποίο υποδηλώνει περιστροφή κατά 360/n και μεταφορά κατά z/n κατά τον άξονα στον οποίο εμφανίζεται η συμμετρία αυτή (π.χ. 2 1, 3 1 ). Επίπεδα ολίσθησης (Glide planes). Με τη χρήση αυτής της συμμετρίας η κρυσταλλική δομή συμπίπτει με τον εαυτό της ύστερα από μετατόπιση με διάνυσμα (επίσης διάφορο των θεμελιωδών διανυσμάτων του πλέγματος) και συμμετρία καθρέπτη από επίπεδο το οποίο περιλαμβάνει το χρησιμοποιούμενο διάνυσμα μετατόπισης. Η συμμετρία αυτή συμβολίζεται, με βάση τον άξονα συμμετρίας καθρέπτη, με τα γράμματα a, b, c, d, n, e. Τέλος, η συμμετρία που προκύπτει από το συνδυασμό συμμετρίας του screw axis και της συμμετρίας καθρέπτη, συμβολίζεται ως n z /m. Συνδυάζοντας όλα τα στοιχεία συμμετρίας του τρισδιάστατου χώρου με τα 14 πλέγματα Bravais, προκύπτουν συνολικά 230 ομάδες συμμετρίας χώρου που ονομάζονται Space groups. Κάθε Space group, συμβολίζεται χρησιμοποιώντας ένα συνδυασμό (δύο έως τεσσάρων) χαρακτήρων, οι οποίοι περιγράφουν πλήρως τη συμμετρία του. Υπάρχουν πολλές σχολές συμβολισμού των Space groups. Στη συγκεκριμένη εργασία όλα τα Space groups περιγράφονται με τη χρήση των συμβόλων Hermann-Maguin, συμβολισμός που έχει οριστεί ως διεθνής. Σύμφωνα με αυτόν, ο πρώτος χαρακτήρας κάθε Space group, είναι ένα γράμμα που υποδεικνύει τον τύπο του πλέγματος Bravais (απλό, χωροκεντρωμένο, εδροκεντρωμένο, βάση-κεντρωμένο) και οι υπόλοιποι χαρακτήρες αναφέρονται στα στοιχεία συμμετρίας που αναπαράγουν ισοδύναμες θέσεις (equivalent positions). O συμβολισμός των Space groups επεξηγείται αναλυτικά στους διεθνείς πίνακες κρυσταλλογραφίας ( To Space Group περιγράφει τα στοιχεία συμμετρίας χώρου, που αν επαναληφθούν στο χώρο δίνουν μια ορισμένη κρυσταλλική δομή. Στις τρεις διαστάσεις υπάρχουν 230 Space Groups. Γενικά λοιπόν η διαδικασία συμμετρίας σε ένα πλέγμα, είναι η μεταβολή της θέσης του στο χώρο κατά τέτοιο τρόπο ώστε το πλέγμα στο τέλος της διαδικασίας να 31
33 επανέρχεται στην αρχική του δομή. Ένα πλέγμα που περιγράφεται από πολλά στοιχεία συμμετρίας χαρακτηρίζεται από υψηλή συμμετρία (high symmetry). Ενώ αν περιγράφεται από σχετικά λίγα στοιχεία συμμετρίας, χαρακτηρίζεται από χαμηλή συμμετρία (low symmetry). Ο κύβος (κυβικό σύστημα) χαρακτηρίζεται από την υψηλότερη δυνατή συμμετρία καθώς διαθέτει τα περισσότερα στοιχεία συμμετρίας. Αυτά είναι 9 κατοπτρικά επίπεδα (τρία επίπεδα που διέρχονται από τις διχοτόμους των πλευρών και έξι επίπεδα που διέρχονται διαγώνια από τις ακμές), 3 άξονες 4 ης τάξης, 4 άξονες 3 ης τάξης και 6 άξονες 2 ης τάξης. Σχήμα 2.9: Στοιχεία συμμετρίας του κύβου. Φαίνονται οι 3 άξονες 4 ης τάξης (πράσινο), οι 4 άξονες 3 ης τάξης (κίτρινο) και οι 6 άξονες 2 ης τάξης (μπλε) (Πηγή: Στη φύση υπάρχουν μόρια τα οποία δεν ταυτίζονται με τα κατοπτρικά τους είδωλα, δηλαδή εμφανίζουν δυο εναντιομερείς μορφές. Αυτά τα μόρια ονομάζονται χειρόμορφα (chiral) και οι δυο μορφές αντικειμένου- ειδώλου καθρέπτη ονομάζονται ισομερές L και ισομερές D. Τα έμβια όντα αντιλαμβάνονται και ξεχωρίζουν τα δεξιόστροφα από τα αριστερόστροφα μόρια. Μάλιστα η κατανάλωση των κατοπτρικών τους μορφών μπορεί να είναι ανωφελής έως και επιβλαβής για τον ανθρώπινο οργανισμό. Για παράδειγμα στις πρωτεΐνες απαντώνται μόνο τα L αμινοξέα που είναι αριστερόστροφα. Σχήμα 2.10: Δύο χειρόμορφες ενώσεις.(α) Η δεξιοστροφη ένωση, D-Dopa η οποία δεν έχει καμια βιολογική δράση και (β) η αριστερόστροφη, L-Dopa η οποία εμφανίζει θεραπευτική δράση κατά της νόσου του Parkinson (Πηγή:Ε.Μαλαμίδου-Ξενικάκη,Διαλέξεις Στερεοχημείας, 2012). Σε όλα τα χειρόμορφα μόρια δεν υπάρχει άξονας συμμετρίας που να είναι ταυτόχρονα και άξονας περιστροφής. Έτσι λοιπόν κάποιοι από τους κανόνες συμμετρίας δεν μπορούν να εφαρμοστούν σε αυτές τις περιπτώσεις. Τελικά οι 32
34 περιορισμοί που επιβάλλονται καθιστούν επιτρεπτά μόνο 65 Space group για τα πρωτεϊνικά μόρια (Παράρτημα Α) Κρυσταλλογραφικά επίπεδα και δείκτες Miller Συχνά γίνεται αναφορά σε συγκεκριμένες κατευθύνσεις μέσα στον κρύσταλλο οι οποίες ενδέχεται να παρουσιάζουν κάποια ιδιαίτερα χαρακτηριστικά. Για να γίνει όμως μια τέτοια αναφορά θα πρέπει να ορισθούν και να ονομαστούν με σαφήνεια οι κατευθύνσεις, οι διευθύνσεις και τα επίπεδα μέσα στον κρύσταλλο. Αυτό επιτυγχάνεται με τους κρυσταλλογραφικούς δείκτες. Κάθε κρυσταλλογραφικό επίπεδο μπορεί να χαρακτηριστεί από τρεις αριθμητικές παραμέτρους (hkl), οι οποίες ονομάζονται δείκτες Miller. Έστω μια κυψελίδα ορισμένη σε σχετική θέση επάνω σε σύστημα συντεταγμένων xyz, με αρχή συντεταγμένων το σημείο Ο. Το κρυσταλλογραφικό επίπεδο ABC (Σχήμα 2.11) ορίζεται ως εξής: (2.4) όπου x, y, z οι συντεταγμένες του επιπέδου ABC ως προς την αρχή των αξόνων, δηλαδή οι συντεταγμένες των σημείων τομής με τους άξονες a, b, c του κρυστάλλου. Σχήμα 2.11: Το κρυσταλλογραφικό επίπεδο ABC εντός μιας κυψελίδας του πλέγματος. Από τον ορισμό αυτό προκύπτει ότι οι δείκτες των επιπέδων των παραλλήλων προς τους άξονες b και c, c και a, a και b είναι αντίστοιχα οι (h00), (0k0), (00l), ενώ των παραλλήλων προς τους άξονες a, b, c είναι (0kl), (h0l), (hk0). Τα τρία επίπεδα (100), (010), (001) χαρακτηρίζονται ως θεμελιώδη επίπεδα και ταυτίζονται με τις βασικές έδρες της κυψελίδας. Οι κρυσταλλογραφικές διευθύνσεις χαρακτηρίζονται με βάση τους δείκτες Miller των επιπέδων στα οποία είναι κάθετες και ορίζονται με τη χρήση αυτών των δεικτών Miller μέσα σε ορθογώνιες παρενθέσεις. Για παράδειγμα η κρυσταλλογραφική διεύθυνση [201] είναι η διεύθυνση της καθέτου στο κρυσταλλογραφικό επίπεδο (201). 33
35 Σε κάθε πλέγμα εντοπίζονται διάφορες ομάδες παραλλήλων ευθειών που ισαπέχουν μεταξύ τους και εμφανίζουν παρόμοια χαρακτηριστικά. Κάθε τέτοια ομάδα μπορεί να ορισθεί ως οικογένεια επιπέδων και χαρακτηρίζεται από τους δείκτες Miller μέσα σε άγκιστρα, { }, ή < >. Ο συμβολισμός <111> αναφέρεται στο σύνολο των επιπέδων με διευθύνσεις [111], [-111], [1-11] και [11-1]. Μπορεί εύκολα να γίνει αντιληπτό ότι ο τύπος <100> αναφέρεται σε όλες τις πλευρές του κύβου, ο τύπος <110> αναφέρεται στις διαγωνίους των πλευρών και ο τύπος <111> στις διαγωνίους του κύβου. Στο Σχήμα 2.12 παρουσιάζονται μερικές από τις κυριότερες κρυσταλλογραφικές διευθύνσεις ενός κρυστάλλου. Σχήμα 2.12: Τα κρυσταλλογραφικά επίπεδα (100), (110) και (111) Αποστάσεις κρυσταλλογραφικών επιπέδων Από τα προηγούμενα προκύπτει ότι κάθε οικογένεια κρυσταλλογραφικών επιπέδων με δείκτες Miller (hkl) περιλαμβάνει επίπεδα του πλέγματος που είναι παράλληλα μεταξύ τους και σε σταθερή απόσταση, d hkl μεταξύ δύο διαδοχικών επιπέδων. H απόσταση αυτή είναι μια πολύ σημαντική παράμετρος, εξαρτάται από το κρυσταλλικό σύστημα και τις διαστάσεις της μοναδιαίας κυψελίδας για αυτό και αποτελεί χαρακτηριστικό μέγεθος. Σχήμα 2.13: Το κρυσταλλογραφικό επίπεδο ABC και το κάθετο διάνυσμα d. 34
36 Επειδή το επίπεδο ABC είναι ορισμένο στο σύστημα αξόνων Ο, xyz του κρυστάλλου, θα είναι επίσης ορισμένο και το κάθετο στο επίπεδο διάνυσμα OD = d hkl. Το μέτρο d hkl του διανύσματος αυτού εκφράζει την ισαπόσταση (d-space) μεταξύ δύο ομοίων διαδοχικών παραλλήλων επιπέδων (Σχήμα 2.13). Η απόσταση d hkl μεταξύ δύο διαδοχικών επιπέδων της κρυσταλλογραφικής οικογένειας (hkl) υπολογίζεται για τα διάφορα κρυσταλλικά συστήματα από τις σχέσεις του Πίνακα2.3. Τύπος κρυσταλλικού συστήματος Αποστάσεις επιπέδων Κυβικό Τετραγωνικό Ορθορομβικό Εξαγωνικό Ρομβοεδρικό Μονοκλινές Τρικλινές Πίνακας 2.3: Οι σχέσεις που συνδέουν τις πλεγματικές σταθερές με τις αποστάσεις d hkl, στα διάφορα κρυσταλλογραφικά συστήματα. Από τον πίνακα αυτό προκύπτουν οι χαρακτηριστικές αποστάσεις των κρυσταλλικών επιπέδων κάθε συστήματος Ευθύ και αντίστροφο πλέγμα Όλα τα σημεία του πλέγματος συνδέονται μεταξύ τους με διανύσματα. Κάθε διάνυσμα r που συνδέει δύο σημεία του πλέγματος, είναι ένας γραμμικός συνδυασμός 35
37 των διανυσμάτων βάσης του ορθού πλέγματος a, b, c. Τα διανύσματα r που ορίζονται από τη σχέση: R = n 1 a+ n 2 b+ n 3 c, (2.5) όπου a, b, c τρία μη συνεπίπεδα διανύσματα (ή αλλιώς a 1, a 2, a 3 ) και n 1, n 2, n 3 ακέραιοι αριθμοί, αποτελούν τα διανύσματα πλέγματος που αναπαράγουν το κρυσταλλικό πλέγμα. Κάθε σημείο που προκύπτει από το διάνυσμα R, προσδιορίζει και ένα σημείο της περιοδικής διάταξης του υλικού, δηλαδή τις θέσεις των ατόμων στη μοναδιαία κυψελίδα. Το σύνολο των σημείων αυτών ονομάζεται κρυσταλλικό πλέγμα ή ευθύ πλέγμα. Σημαντική ιδιότητα του κρυσταλλικού πλέγματος αποτελεί ότι το περιβάλλον κάθε σημείου που το αποτελεί, είναι ακριβώς το ίδιο. Σε κάθε πείραμα περίθλασης οι θέσεις των μεγίστων συμβολής των σκεδαζόμενων ακτίνων-χ, δεν εμφανίζουν τυχαία κατανομή, αλλά αντιθέτως οι συντεταγμένες τους περιγράφονται απόλυτα και σχηματίζουν μια νέα περιοδική διάταξη που ονομάζεται αντίστροφο πλέγμα. Η διάταξη αυτή περιγράφεται απόλυτα από τα διανύσματα που προέρχονται από την εξής σχέση: G = ha*+kb*+ lc*, (2.6) όπου h,k,l (ακέραιοι αριθμοί) οι δείκτες Miller του πλεγματικού επιπέδου και a*, b*, c* τα θεμελιώδη διανύσματα του αντίστροφου πλέγματος (ή αλλιώς a 1 *, a 2 *, a 3 *). Δηλαδή το G είναι το διάνυσμα θέσης, που προσδιορίζει την απόσταση ενός σημείου από την αρχή (Ο) και αποτελεί το αντίστοιχο μέγεθος του διανύσματος R που συναντήσαμε στο ευθύ πλέγμα, για το αντίστροφο πλέγμα. Με βάση τα τρία διανύσματα μετατόπισης a, b, c, του ορθού πλέγματος μπορούμε να ορίσουμε την συμπληρωματική τριάδα διανυσμάτων a*, b* και c* χρησιμοποιώντας τις σχέσεις: a b c 2 a b c b c a 2 a b c c a b 2 a b c (2.7) που αποτελούν τα θεμελιώδη διανύσματα του αντιστρόφου πλέγματος. Σημείωση: i i * = 1 και i j = 0, (όπου i,j= a, b, c). Το διάνυσμα θέσης του αντιστρόφου πλέγματος (G) συχνά συμβολίζεται ως r * κατ αναλογία με τα θεμελιώδη διανύσματα και συνδέεται αντιστρόφως ανάλογα με την απόσταση μεταξύ των επιπέδων: (2.8) Μια χρήσιμη περιγραφή του φαινομένου της περίθλασης των ακτίνων-χ από κρυστάλλους, εισήγαγε ο Max von Laue, χρησιμοποιώντας τα διανύσματα του ορθού 36
38 και αντιστρόφου πλέγματος. Ο Laue για να ερμηνεύσει το φαινόμενο, βασίστηκε στη θεωρία της ενισχυτικής συμβολής σφαιρικών κυμάτων. Τα δευτερογενή κύματα τα οποία διεγείρονται από προσπίπτον επίπεδο κύμα έχουν αρχή ένα μεγάλο αριθμό κέντρων σκέδασης τοποθετημένων στα σημεία ενός πλέγματος Bravais. Τα κέντρα σκέδασης μπορεί να είναι άτομα, ή πιο πολύπλοκες βάσεις, χωρίς να αλλάζει το τελικό αποτέλεσμα της περίθλασης. Παρακάτω αναλύονται οι προϋποθέσεις ώστε ένα κύμα να σκεδαστεί από έναν κρύσταλλο. Σχήμα 2.14 Γεωμετρία της σκέδασης επίπεδου κύματος από πλέγμα. Τα κέντρα σκέδασης που βρίσκονται εντός του κρυστάλλου είναι άτομα ή πιο πολύπλοκες βάσεις. Θεωρούμε ότι από όλα τα σημεία του πλέγματος ξεκινούν σφαιρικά κύματα που διεγείρονται από το προσπίπτον επίπεδο κύμα. Αν όλες οι ισοφασικές επιφάνειες των σφαιρικών κυμάτων δημιουργούν προς κάποια κατεύθυνση επίπεδο κύμα τότε έχουμε ενισχυτική συμβολή προς την κατεύθυνση αυτή, Η συνθήκη για να συμβεί αυτό, η συνθήκη Laue είναι k-k'=g όπου G ένα οποιοδήποτε διάνυσμα του αντιστρόφου πλέγματος (Πηγή: Π. Τζανετάκης, Σημειώσεις εισαγωγής στη φυσική των ημιαγωγών, 1998). Στο Σχήμα 2.14 αποτυπώνονται τα βασικά στοιχεία της γεωμετρίας του προβλήματος. Ένα επίπεδο κύμα, με κυματάνυσμα k, της μορφής: F(r,t)= F 0 e j(kr + ωt) (2.9) προσπίπτει υπό τυχαία γωνία σε έναν κρύσταλλο που αποτελείται από πανομοιότυπα κέντρα σκέδασης διατεταγμένα σε πλέγμα. Κάθε κέντρο σκέδασης μπορεί να σκεδάζει ή όχι, προς μια κατεύθυνση στον χώρο. Επειδή το ζητούμενο είναι μια γενική, αναγκαία, αλλά όχι ικανή, συνθήκη σκέδασης, σε αυτό το στάδιο της ανάλυσης εξετάζουμε μόνο τη φάση των σκεδαζόμενων κυμάτων και όχι το πλάτος τους ή τη γωνιακή εξάρτηση. Θεωρούμε λοιπόν ότι κάθε κέντρο σκέδασης εκπέμπει ένα σφαιρικό κύμα, υπό τη διέγερση του πρωτογενούς προσπίπτοντος 37
39 επίπεδου κύματος. Για να υπάρξει ενισχυτική συμβολή των σφαιρικών κυμάτων σε κάποια διεύθυνση πρέπει οι σφαιρικές ισοφασικές επιφάνειες από όλα τα κέντρα σκέδασης να εφάπτονται σε ένα επίπεδο με σταθερό προσανατολισμό στο χώρο. Τότε παρατηρείται σκεδαζόμενη ένταση, σε διεύθυνση κάθετη στο επίπεδο αυτό. Έστω k' το σκεδαζόμενο κύμα. Επιλέγουμε δύο τυχαία σημεία σκέδασης, τα Α και Β, με το Β να βρίσκεται στη θέση r σε σχέση με το Α, την χρονική στιγμή t=0. Θα πρέπει να υπάρχει διαφορά φάσης στην κατεύθυνση k', ακέραιο πολλαπλάσιο του 2π ώστε να παρατηρείται ενισχυτική συμβολή και σκεδαζόμενο κύμα k'. Η διαφορά φάσης του προσπίπτοντος κύματος στο σημείο Β, σε σχέση με το Α, είναι k r. Η διαφορά φάσης του σκεδαζόμενου σφαιρικού κύματος στο Α μέχρι το επίπεδο που είναι κάθετο στην διεύθυνση k' και περνά από το Β, είναι η προβολή του r στην διεύθυνση k'. Άρα η συνολική διαφορά φάσης είναι: k r - k r = (k-k ) r = Δφ (2.10) Η διαφορά αυτή θα πρέπει να είναι ακέραιο πολλαπλάσιο του 2π για όλα τα διανύσματα r του πλέγματος. (k-k ) R = 2πm (2.11) Αντικαθιστώντας στη σχέση αυτή τη σχέση R = n 1 a + n 2 b + n 3 c, παίρνουμε τις εξισώσεις : (k-k ) a = 2πh (k-k ) b = 2πk (2.12) (k-k ) c = 2πl Οι εξισώσεις αυτές ονομάζονται συνθήκες του Laue. Η γενική λύση των εξισώσεων Laue (2.10) είναι ένας γραμμικός συνδιασμός των διανυσμάτων του αντιστρόφου πλέγματος και μπορεί να γραφεί στη μορφή : G = (k-k ) = ha* + kb* + lc* (2.13) όπου h,k,l (ακέραιοι αριθμοί) οι δείκτες Miller. Αντικατάσταση της σχέσης αυτής στην πρώτη συνθήκη Laue δίνει : G a = ha* a + kb* b + lc * c = 2πh (2.14) Πράγματι ακέραιο πολλαπλάσιο του 2π. Όμοια ικανοποιούνται και οι υπόλοιπες εξισώσεις. Το διάνυσμα G χαρακτηρίζει όπως αναφέρθηκε και νωρίτερα τις θέσεις εποικοδομητικής συμβολής (σημεία του αντιστρόφου πλέγματος). Η συνθήκη εποικοδομητικής συμβολής γράφεται με τη μορφή : k - k = G (συνθήκη εποικοδομητικής συμβολής Laue) (2.15) 38
40 όπου k, k κυματανύσματα της προσπίπτουσας και της ανακλώμενης ακτινοβολίας αντίστοιχα και G οποιοδήποτε διάνυσμα του αντιστρόφου πλέγματος. Επίσης ισχύει ότι : G R = (h a* + k b*+ l c*) (n 1 a + n 2 b + n 3 c )= hn 1 a a* + kn 2 b b* + ln 3 c c* = (h n 1 + k n 2 + l n 3 ) 2π = (ακέραιος) 2π (2.16) ή e ig R = 1. (2.17) Η συνθήκη αυτή δίνει ένα κατώτατο όριο κυματανύσματος που μπορεί να σκεδαστεί από πλέγμα. Εφόσον το μέτρο του ανακλώμενου κυματανύσματος θα είναι το πολύ ίσο, στην ελαστική σκέδαση, με το μέτρο του προσπίπτοντος, δεν είναι δυνατό να ικανοποιηθεί η συνθήκη του Laue για k < G min /2, όπου G min το μικρότερο δυνατό άνυσμα του αντιστρόφου πλέγματος Σφαίρα του Ewald Η επινόηση και η χρήση του αντιστρόφου πλέγματος εκτός από το γεγονός ότι απλουστεύει την επίλυση πολύπλοκων προβλημάτων της δομής της ύλης, ταυτόχρονα ερμηνεύει ευκολότερα και τα φαινόμενα της περίθλασης. Το αντίστροφο πλέγμα αποσαφηνίζει τη σημασία της εξίσωσης Bragg με έναν πολύ παραστατικό τρόπο. Θεωρούμε έναν κρύσταλλο, Κ, στη διεύθυνση της προσπίπτουσας δέσμης ακτίνων-χ, συγκεκριμένου μήκους κύματος λ, και μια τομή του αντιστρόφου πλέγματος. Θεωρούμε επίσης κύκλο κέντρου Κ και διαμέτρου ΒΟ=2/λ. Από το σχήμα 2.15 αποδεικνύεται ότι κάθε σημείο Ρ του αντιστρόφου πλέγματος το οποίο βρίσκεται επάνω στον κύκλο αυτό, πληροί την εξίσωση Bragg. Σχήμα 2.15 Σχηματική απεικόνιση της σφαίρας του Ewald σε σχέση με την αρχή του αντιστρόφου πλέγματος. 39
41 Πράγματι αν ΡΒΟ = θ hkl τότε ΡΚΟ = 2θ hkl, ενώ από το ορθογώνιο τρίγωνο ΡΒΟ έχουμε: Επειδή όμως το σημείο Ρ είναι σημείο του αντιστρόφου πλέγματος ισχύει: οπότε η σχέση(2.18) με αντικατάσταση της (2.19) γίνεται: (2.18) (2.19) (2.20) Η σχέση (2.20) είναι ταυτόσημη με τη σχέση (2.1), δηλαδή είναι η εξίσωση Bragg. Ο κύκλος κέντρου Κ και ακτίνας 1/λ ονομάζεται σφαίρα ανάκλασης ή σφαίρα του Ewald. Όπως φαίνεται στο Σχήμα 2.18, το σημείο Ο αναπαριστά την αρχή του αντιστρόφου πλέγματος, η ευθεία ΚΡ την ανακλώμενη δέσμη η ΟΡ το διάνυσμα θέσης r* hkl του σημείο Ρ του αντιστρόφου πλέγματος και τέλος στο σχήμα διακρίνεται το ανακλών επίπεδο hkl. Το σημαντικότερο χαρακτηριστικό της σφαίρας Ewald είναι ότι κάθε σημείο της επιφάνειάς της επαληθεύει την εξίσωση Bragg. Δηλαδή, καθώς περιστρέφουμε τον κρύσταλλο, αν ένα σημείο του αντιστρόφου πλέγματος έρθει σε επαφή με την επιφάνεια της σφαίρας ακτίνας 1/λ, τότε ικανοποιείται η εξίσωση Bragg και προκύπτει υποχρεωτικά ανάκλαση. Ένα σημαντικό σημείο στο σχεδιασμό ενός πειράματος περίθλασης αποτελεί η επιλογή του κατάλληλου μήκους κύματος λ, με σκοπό τη συλλογή του μέγιστου δυνατού αριθμού ανακλάσεων. Ο αριθμός των ανακλάσεων που μπορεί να αναπαραχθεί περιστρέφοντας τον κρύσταλλο, σε όλους τους πιθανούς προσανατολισμούς σε σχέση με τη δέσμη ακτίνων-χ, είναι ίσος με τον αριθμό των σημείων του αντιστρόφου πλέγματος που έρχονται σε επαφή με τη σφαίρα ανάκλασης. Αν θεωρήσουμε ότι η δέσμη με τον κρύσταλλο στρέφονται στο χώρο, έτσι ώστε η διεύθυνση ΒΚ να διέρχεται σταθερά από το σημείο Ο, τότε όλες οι αντίστοιχες σφαίρες ανάκλασης διέρχονται από το σημείο Ο και περιβάλλονται από την οριακή σφαίρα (Ο,2/λ), (Σχήμα 2.16). Η σφαίρα αυτή περικλείει τα σημεία του αντιστρόφου πλέγματος που έχουν τη δυνατότητα να μας δώσουν ανακλάσεις στο συγκεκριμένο μήκος κύματος. 40
42 Σχήμα 2.16: Σχηματική απεικόνιση οριακής σφαίρας του Ewald, ακτίνας 2/λ, η οποία περιλαμβάνει όλες τις σφαίρες ανάκλασης ακτίνας 1/λ. Όπως γίνεται αντιληπτό μικρότερα μήκη κύματος δημιουργούν μεγαλύτερες σφαίρες ανάκλασης περικλείοντας μεγαλύτερο αριθμό ανακλάσεων στη μετρήσιμη περιοχή. Επίσης μεγαλύτερες μοναδιαίες κυψελίδες στο ευθύ πλέγμα, αντιστοιχούν σε μικρότερες μοναδιαίες κυψελίδες στο αντίστροφο πλέγμα, γεμίζοντας την οριακή σφαίρα με σημεία πολύ πυκνά τοποθετημένα μεταξύ τους, τα οποία κατά συνέπεια αυξάνουν τον αριθμό των μετρήσιμων ανακλάσεων. Η κατασκευή του Ewald καθιστά σαφή σημαντικά χαρακτηριστικά της περίθλασης ακτίνων-χ σε κρυστάλλους: Ορίζει το μέγιστο μήκος κύματος της περίθλασης σε κάθε κρύσταλλο. Όταν χρησιμοποιηθεί μήκος κύματος μεγαλύτερο από αυτό, τότε η σφαίρα Ewald είναι τόσο μικρή που πλέον είναι αδύνατο να ακουμπούν στην επιφάνεια της ταυτόχρονα δύο σημεία του αντιστρόφου πλέγματος. Μονοχρωματική ακτινοβολία που προσπίπτει από τυχαία αλλά σταθερή διεύθυνση σε κρύσταλλο είναι δυνατόν να μη σκεδάζεται καθόλου ακόμα και αν το μήκος κύματός της είναι κατάλληλο. Ακτίνες-Χ ευρέως φάσματος, όταν προσπίπτουν με σταθερή διεύθυνση σε κρύσταλλο δίνουν μονοχρωματικά σκεδαζόμενη δέσμη σε συγκεκριμένες διευθύνσεις σε σχέση με τον κρύσταλλο Περίθλαση από μονοκρύσταλλο Από την αλληλεπίδραση των ακτίνων-χ με το κρυσταλλικό δείγμα προκύπτει το διάγραμμα περίθλασης το οποίο αποτελεί ένα είδος δακτυλικού αποτυπώματος του δείγματος. Σε κάθε πείραμα περίθλασης, η διάταξη που εφαρμόζεται αποτελείται από το προς μελέτη δείγμα τοποθετημένο μπροστά από τη δέσμη ακτίνων-χ. Σε πείραμα μονοκρυστάλλου, ο κρύσταλλος είτε συγκρατείται από έναν 41
43 δειγματοφορέα τύπου θηλειάς (loop), είτε τοποθετείται μέσα σε κυλινδρικό τριχοειδή σωλήνα (capillarie) σταθερά μπροστά από τη δέσμη. Υπάρχουν δύο βασικές πειραματικές μέθοδοι λήψης δεδομένων περίθλασης από μονοκρυσταλλικά δείγματα. Κατά τη μέθοδο Laue ο κρύσταλλος τοποθετείται μπροστά από μια δέσμη ακτίνων-χ μεταβλητού μήκους κύματος λ (πολυχρωματική ακτινοβολία), ενώ ο κρύσταλλος παραμένει και πραγματοποιείται η λήψη των δεδομένων. Κατά τη μέθοδο των Debye-Scherrer μονοχρωματική, παράλληλη δέσμη προσπίπτει επάνω στον κρύσταλλο, ο οποίος περιστρέφεται γύρω από έναν άξονα στροφής. Καθώς η δέσμη προσπίπτει στο δείγμα υπό ορισμένη γωνία θ, ο νόμος του Bragg ικανοποιείται για κάποια κρυσταλλογραφικά επίπεδα και λαμβάνουμε σήμα περίθλασης. Στη συνέχεια ο κρύσταλλος περιστρέφεται ως προς άξονα στροφής και λαμβάνεται το επόμενο διάγραμμα περίθλασης. Έτσι συλλέγουμε μια σειρά δεδομένων περίθλασης για κάθε δείγμα. Ένα διάγραμμα περίθλασης μονοκρυστάλλου αποτελείται από κουκίδες, με χαρακτηριστική διάταξη στις δύο διαστάσεις. Οι κουκίδες αυτές εμφανίζονται στις γωνίες 2θ για τις οποίες υπήρξε ενισχυτική συμβολή και φαίνονται έντονες ή πιο εξασθενημένες ανάλογα με την ένταση της ακτινοβολίας που συμβάλλει για την κάθε μια. Σχήμα 2.17: Τυπικά διαγράμματα περίθλασης από μονοκρυσταλλικά δείγματα. Αριστερά: Διάγραμμα από δείγμα Βηρυλλίου όπως προέκυψε μέσω της μεθόδου του Laue, (Πηγή: Δεξιά: Διάγραμμα από δείγμα Ινσουλίνης, απουσία ψευδαργύρου, που προέκυψε χρησιμοποιώντας τη μέθοδο των Debye-Scherrer (Πηγή: Ο προσδιορισμός της κρυσταλλικής δομής βασίζεται στο γεγονός ότι οι γωνίες στις οποίες παρατηρούνται ανακλάσεις, εξαρτώνται άμεσα από το κρυσταλλικό σύστημα στο οποίο ανήκει το δείγμα και τις πλεγματικές σταθερές που το χαρακτηρίζουν (Πίνακας 2.3), ενώ οι εντάσεις των κορυφών από τις θέσεις και το είδος των ατόμων που το αποτελούν. 42
44 2.3.8 Περίθλαση από πολυκρυσταλλικό δείγμα (powder diffraction) Η περίθλαση ακτίνων-χ βρίσκει εφαρμογή σε μονοκρυσταλλικά αλλά και σε πολυκρυσταλλικά δείγματα, καθώς οι αρχές που διέπουν το φαινόμενο της περίθλασης όπως περιγράφηκαν σε προηγούμενες ενότητες, ισχύουν εξίσου για τους δυο τύπους δειγμάτων. Καθώς σε πολλές περιπτώσεις η ανάπτυξη μονοκρυστάλλων κατάλληλου μεγέθους (μεγαλύτερων των 5μm) για πειράματα περίθλασης αποβαίνει μια απαιτητική και χρονοβόρα διαδικασία, ένας εναλλακτικός τρόπος διεξαγωγής πειραμάτων για τη συλλογή δεδομένων προκύπτει από την αξιοποίηση των πολυκρυσταλλικών δειγμάτων. Ένα πολυκρυσταλλικό δείγμα αποτελείται από πολύ μεγάλο αριθμό κρυστάλλων, τυχαία προσανατολισμένων, με διαστάσεις της τάξεως των 100 nm- 5 μm. Αυτοί οι μικροκρυστάλλοι είναι ίδιας φύσης με ένα μονοκρύσταλλο, με τη μοναδική διαφορά να εντοπίζεται στην κλίμακα μεγέθους. Συνεπώς σε μεγάλες ποσότητες, τα πολυκρυσταλλικά ιζήματα είναι ικανά να περιθλούν ισχυρά τις ακτίνες-χ, όπως συμβαίνει με τους μονοκρυστάλλους. Κατά αναλογία με τα πειράματα από δείγματα μονοκρυστάλλου, για τα πολυκρυσταλλικά δείγματα, η μέθοδος των Debye-Scherrer αποτελεί επίσης διαδεδομένη μέθοδο λήψης δεδομένων περίθλασης. Στη μέθοδο αυτή, μονοχρωματική παράλληλη δέσμη προσπίπτει επάνω στο δείγμα το οποίο βρίσκεται μέσα σε κυλινδρικό τριχοειδή σωλήνα από γυαλί. Το γεγονός ότι το δείγμα είναι πολυκρυσταλλικό επιτρέπει στην ακτινοβολία την ταυτόχρονη πρόσκρουση στα διάφορα κρυσταλλογραφικά επίπεδα hkl του δείγματος, με αποτέλεσμα να παρατηρείται πλήθος ανακλάσεων. Οι ανακλάσεις αυτές, καθώς προέρχονται από διαφορετικά σημεία του δείγματος, σχηματίζουν κώνους. Κάθε κώνος έχει προκύψει από την περίθλαση από ένα σύνολο επίπεδων και συνεπώς αντιστοιχεί σε μια συγκεκριμένη τιμή d hkl. Σχήμα 2.18: Η διάταξη ενός πειράματος περίθλασης από πολυκρυσταλλικό δείγμα. Η δέσμη εισέρχεται από τα αριστερά και καθώς προσπίπτει στο δείγμα περιθλαται από κάθε επίπεδο, υπό χαρακτηριστική γωνία, δημιουργώντας κώνους περίθλασης. Από την τομή των κώνων αυτών με την επιφάνεια του ανιχνευτή λαμβάνουμε κυκλους (Πηγή: 43
45 Οι κώνοι αυτοί καθώς προσπίπτουν στη δισδιάστατη επιφάνεια του ανιχνευτή, χάνουν τη μία τους διάσταση και αποτυπώνονται με τη μορφή ομόκεντρων κύκλων (Debye - Scherrer circles) που έχουν ως κέντρο την αρχική διεύθυνση της ακτινοβολίας. Οι ομόκεντροι κύκλοι αποτελούν το διάγραμμα περίθλασης από ένα πείραμα πολυκρυσταλλικού δείγματος, το οποίο είναι ανάλογο με το σύνολο των ανακλάσεων που θα παρατηρούσαμε από την περιστροφή του δείγματος σε ένα πείραμα μονοκρυστάλλου. Στο Σχήμα 2.19 απεικονίζεται το αποτύπωμα των κύκλων που λαμβάνουμε στον ανιχνευτή. Κάθε ανάκλαση (κύκλος) που παρατηρείται αντιστοιχεί σε μια ορισμένη τιμή d hkl. Ξεκινώντας από το κέντρο και συνεχίζοντας προς τους εξωτερικούς κύκλους, η γωνία 2θ αυξάνεται και συναντάμε διαδοχικά τις ανακλάσεις επιπέδων μικρότερης απόστασης d hkl. Συνηθίζεται, για πρακτικούς λόγους, τα διαγράμματα περίθλασης πολυκρυσταλλικών δειγμάτων να παρουσιάζονται ως διαγράμματα δύο αξόνων, έτσι ώστε κάθε κύκλος στο διάγραμμα αριστερά να αντιστοιχεί σε μια κορυφή στο διάγραμμα δεξιά. Σε αυτά τα διαγράμματα ο κατακόρυφος άξονας αναπαριστά την τιμή των εντάσεων I, ενώ ο οριζόντιος άξονας τη γωνία 2θ. Έτσι ποσοτικοποιούνται αυτά τα δυο μεγέθη και καθίσταται πιο εύκολη η επεξεργασία των δεδομένων. Σχήμα 2.19: Στο σχήμα απεικονίζονται (α) Οι ομόκεντροι κύκλοι που σχηματίζουν τα δεδομένα περίθλασης πολυκρυσταλλικού δείγματος και (β) Τα δεδομένα περίθλασης πολυκρυσταλλικού υλικού όπως προκύπτουν από τη μετατροπή τους σε ισοδύναμο διάγραμμα, με κατακόρυφο άξονα την ένταση Ι της ακτινοβολίας και οριζόντιο άξονα τη γωνία 2θ. Τα πειραματικά δεδομένα αναπαριστώνται με κουκίδες, η γραμμή γκρι χρώματος που τις συνδέει είναι η θεωρητική προσομοίωση, ενώ με μαύρη γραμμή αναπαριστάται η διαφορά μεταξύ θεωρητικής και πειραματικής καμπύλης. Εικόνες λυσοζύμης από κρυστάλλους τετραγωνικής συμμετρίας (Πηγή: I. Margiolaki et al, Z.Kristallogr. Suppl. 26, 2007). Παρατηρούμε ότι για κάποιες γωνίες πρόσπτωσης της ακτινοβολίας, η ένταση λαμβάνει μηδενική τιμή. Αυτό συμβαίνει, είτε επειδή οι ακτίνες σκεδάζονται τυχαία και δεν ικανοποιείται ο νόμος του Bragg, είτε επειδή η δέσμη συμβάλει καταστρεπτικά και έτσι το αποτέλεσμα είναι αναιρετικό. Στις περιπτώσεις όπου 44
46 εμφανίζονται υψηλές τιμές της έντασης, η δέσμη έχει προσπέσει σε κάποια οικογένεια κρυσταλλογραφικών επιπέδων υπό τέτοια γωνία ώστε να ισχύει ο νόμος του Bragg και εμφανίζεται ενισχυτική συμβολή. Επίσης, ένας ακόμη ισοδύναμος τρόπος απεικόνισης των δεδομένων περίθλασης προκύπτει χρησιμοποιώντας στους δυο άξονες, κατακόρυφο και οριζόντιο, τα μεγέθη I και Q αντίστοιχα. Ως Q ορίζεται το μέγεθος που δίνεται από τον τύπο: (2.21) Με αυτό τον τρόπο γίνονται συγκρίσιμα τα διαγράμματα που προέρχονται από πειράματα διαφορετικού μήκους κύματος λ. Για να συλλέξουμε ποιοτικά δεδομένα περίθλασης, απαιτείται το δείγμα μας να εμπεριέχει μεγάλο αριθμό κρυστάλλων. Όσο μεγαλύτερος είναι ο αριθμός των κρυστάλλων, τόσο αυξάνεται η πιθανότητα πολλά επίπεδα να ικανοποιούν ταυτόχρονα τη συνθήκη Bragg. Στη συγκεκριμένη τεχνική είναι πολύ σημαντικό να εκτεθούν στην ακτινοβολία, κάθε φορά, όλοι οι δυνατοί προσανατολισμοί. Και επειδή ο τυχαίος προσανατολισμός των κρυστάλλων υποκαθιστά την περιστροφή του δείγματος, είναι πολύ σημαντικό να αυξήσουμε όσο δυνατόν γίνεται αυτή την τυχαιότητα. Για το σκοπό αυτό και εφόσον το πολυκρυσταλλικό δείγμα τοποθετηθεί εντός του τριχοειδή σωλήνα, εκτίθεται σε πολύ υψηλούς ρυθμούς περιστροφής (spinning) πριν το πείραμα περίθλασης. Σχήμα 2.20: Παραδείγματα διαγραμμάτων περίθλασης ομόκεντρων κύκλων που προέρχονται από πολυκρυσταλλικά δείγματα τυχαίου προσανατολισμού (αριστερά) και προτιμητέου προσανατολισμού (δεξιά). Οι τελείες απεικονίζουν το αντίστοιχο σήμα περίθλασης από πείραμα μονοκρυστάλλου. Στο διάγραμμα αριστερά παρατηρούνται ομοιόμορφοι σχηματισμοί ισοδύναμης έντασης και πάχους κατά μήκος κάθε κύκλου, που υποδηλώνει τη γωνία 2θ. Αντιθέτως στο διάγραμμα δεξιά διακρίνονται σημεία στα οποία έχουν συνεισφέρει άλλοτε περισσότερα και άλλοτε λιγότερα κρυσταλλογραφικά επίπεδα, αποδίδοντας ανομοιόμορφες εντάσεις κατά μήκος κάθε κύκλου. Τα βέλη επισημαίνουν τα ίδια σημεία στα δύο διαγράμματα (Πηγή: www. crystal.mat.ethz.ch). 45
47 Με αυτόν τον τρόπο εξασφαλίζεται η μέγιστη δυνατή τυχαιότητα προσανατολισμού των κρυστάλλων του δείγματος και τα διάφορα κρυσταλλογραφικά επίπεδα συνεισφέρουν στατιστικά ισοδύναμα προς όλες τις κατευθύνσεις. Σαν αποτέλεσμα, τα διαγράμματα περίθλασης δεν παρουσιάζουν διαφοροποιήσεις στις εντάσεις κατά μήκος κάθε κύκλου και αποτελούνται από ομοιόμορφους ομόκεντρους κύκλους. Ακόμη ένα πλεονέκτημα της μεθόδου που πρέπει να αναφερθεί, αφορά τα πολυκρυσταλλικά δείγματα που αποτελούνται από μια ή και περισσότερες κρυσταλλικές φάσεις. Η συγκεκριμένη μέθοδος επιτρέπει τον ποσοτικό προσδιορισμό των φάσεων που συνυπάρχουν στο υπό μελέτη δείγμα. Κάθε κρυσταλλική φάση του δείγματος παράγει το δικό της διάγραμμα περίθλασης ανεξάρτητα από τα υπόλοιπα συστατικά που υπάρχουν στο μείγμα. Υπολογίζοντας τις σχετικές εντάσεις των κορυφών διαφορετικών φάσεων μπορούμε να προσδιορίσουμε το ποσοστό στο οποίο εμφανίζεται κάθε φάση μέσα στο άγνωστο δείγμα (Hull, 1919) Παράγοντας Δομής Η συνθήκη περίθλασης κατά Bragg προσδιορίζει με καθαρό και σαφή τρόπο τις γωνίες και επομένως τις κρυσταλλογραφικές διευθύνσεις στις οποίες εμφανίζεται εποικοδομητική συμβολή των σκεδαζόμενων ακτίνων. Ο προσδιορισμός των γωνιών αυτών αποτελεί μόνο ένα μέρος της πληροφορίας που χρειάζεται κανείς για τον πλήρη καθορισμό της κρυσταλλικής δομής. Το υπόλοιπο μέρος της πληροφορίας αντλείται από την ένταση της σκεδαζόμενης ακτινοβολίας, δηλαδή το πλάτος του σκεδαζόμενου κύματος. Σχήμα 2.21: (α) Αρχικό πλέγμα και διάφορα παράλληλα πλεγματικά επίπεδα εντός αυτού: Κάθε διεύθυνση του πλέγματος, αντιστοιχεί σε διαφορετική απόσταση d hkl, (β) Δεύτερο πλέγμα με αποστάσεις παράλληλων επιπέδων ίσες με αυτές του σχήματος (α) αλλά με διαφορετική βάση και μοναδιαία κυψελίδα. 46
48 Στο Σχήμα 2.21(α) και (β) απεικονίζονται δύο διαφορετικού τύπου πλέγματα. Εάν η πληροφορία που χρειαζόμασταν συνδεόταν με την εύρεση των διευθύνσεων εποικοδομητικής συμβολής, τότε οι δύο αυτές δομές, αν και διαφορετικές μεταξύ τους, θα έδιναν την ίδια πληροφορία. Αντίθετα, η ένταση της σκεδαζόμενης ακτινοβολίας διαφέρει σημαντικά ανάμεσα στις δύο δομές. Δηλαδή, ενώ η γωνία στην οποία παρατηρείται σκέδαση εξαρτάται από τον τύπο του πλέγματος, η ένταση που καταγράφεται εξαρτάται από τη φύση του κέντρου σκέδασης. Το συνολικό πλάτος του σκεδαζόμενου κύματος, που καταγράφει ο ανιχνευτής και αντιστοιχεί σε μια συγκεκριμένη ανάκλαση που προέρχεται από κάποιο κρυσταλλογραφικό επίπεδο hkl, μπορεί να περιγραφεί ως το άθροισμα της συμβολής όλων κυμάτων από τα κέντρα σκέδασης της μοναδιαίας κυψελίδας. Αυτό το άθροισμα που περιγράφει μια σκεδαζόμενη δέσμη ονομάζεται παράγοντας δομής, F hkl. Η εξίσωση του παράγοντα δομής μπορεί να περιγραφεί με πολλούς διαφορετικούς τρόπους. Ένας εύχρηστος τρόπος είναι υπό τη μορφή αθροίσματος στο οποίο κάθε όρος περιγράφει την περίθλαση από κάθε άτομο της κυψελίδας και τελικά η σειρά αποτελείται από τόσους όρους, όσα είναι και τα άτομα της κυψελίδας. Η εξίσωση του παράγοντα δομής μπορεί επίσης να γραφεί ως σειρά Fourier, στην οποία κάθε όρος προέρχεται από τη συνεισφορά του κάθε ατόμου στην ανάκλαση hkl. Έστω ότι ένα άτομο βρίσκεται στη θέση j σε μία μοναδιαία κυψελίδα και περιγράφεται από το διάνυσμα θέσης r j, τότε ο παράγοντας δομής, F hkl, που οφείλεται σε αυτό το άτομο, μπορεί να γραφεί ως: (2.22) Ο όρος f j ονομάζεται ατομικός παράγοντας δομής. Ο παράγοντας αυτός διαφέρει για κάθε στοιχείο καθώς εξαρτάται από τον ατομικό αριθμό (Ζ). Θεωρείται όμως γνωστό μέγεθος και βρίσκεται καταχωρημένο σε κρυσταλλογραφικούς πίνακες για όλα τα στοιχεία. Το εκθετικό στη σχέση (2.22) αναπαριστά μια τρισδιάστατη περιοδική συνάρτηση, όπου τα x j, y j, z j αναπαριστούν τις κλασματικές συντεταγμένες 3 του ατόμου j στη θεμελιώδη κυψελίδα (πραγματικός χώρος) και τα h,k,l (ακέραιοι αριθμοί) είναι οι δείκτες Miller. Η φάση του κύματος συμπεριλαμβάνεται στον εκθετικό όρο του παράγοντα δομής και εξαρτάται μόνο από τις ατομικές συντεταγμένες ( x j, y j, z j ) του ατόμου. Πιο συγκεκριμένα η φάση του περιθλώμενου κύματος ενός ατόμου είναι ίση με. Σε συμφωνία με τον νόμο του Bragg, όλα τα άτομα που βρίσκονται σε μια σειρά από παράλληλα επίπεδα περιθλούν σε φάση μεταξύ τους. Χρησιμοποιώντας τον ορισμό της φάσης στην σχέση (2.19) ο παράγοντας δομής κάθε ατόμου j γράφεται ως: 3 Οι κλασματικές συντεταγμένες προκύπτουν διαιρώντας τις Καρτεσιανές συντεταγμένες με τα μήκη των πλευρών της θεμελιώδους κυψελίδας (δηλαδή, x j =x/a 1, y j =y/a 2, z j = z/a 3 ). 47
49 (2.23) Στην περίπτωση μιας θεμελιώδους κυψελίδας, η οποία περιλαμβάνει n άτομα, ο παράγοντας δομής F hkl προκύπτει ως το άθροισμα όλων τον παραγόντων δομής, f hkl κάθε μεμονωμένου ατόμου: (2.24) Ο όρος, της εξίσωσης είναι ο παράγοντας Debye-Waller ο οποίος περιγράφει το φαινόμενο της θερμικής δόνησης που προκαλεί μεγαλύτερη διάχυση στο ηλεκτρονικό νέφος, μειώνοντας έτσι την αποδοτικότητα σκέδασης σε μεγαλύτερες γωνίες. Η απλούστερη περίπτωση της θερμικής κίνησης που προέρχεται από ισοδύναμο μαγνητικό πεδίο σε όλες τις διευθύνσεις δίνεται από την έκφραση Β = 8π 2 <u 2 >, όπου <u 2 > είναι ο μέσος όρος της μετατόπισης ενός ατόμου από τη θέση ηρεμίας του. Ένας ακόμη τρόπος περιγραφής του παράγοντα δομής F hkl προκύπτει χρησιμοποιώντας το άθροισμα της συνεισφοράς της ηλεκτρονιακής πυκνότητας από κάθε στοιχείο όγκου της θεμελιώδους κυψελίδας. Η ηλεκτρονιακή πυκνότητα ενός σημείου του κρυστάλλου είναι δηλαδή η τοπική συγκέντρωση ηλεκτρονίων και συμβολίζεται ως ρ(r). Ο παράγοντας δομής και η ηλεκτρονιακή πυκνότητα σχετίζονται καθώς τα ηλεκτρόνια αποτελούν κέντρα σκέδασης της ακτινοβολίας. Για ένα στοιχείο όγκου που βρίσκεται στο σημείο (x,y,z), η ηλεκτρονιακή πυκνότητα είναι κατά προσέγγιση ο μέσος όρος ρ(x,y,z) όλων των σημείων του στοιχείου αυτού. Λαμβάνοντας υπ' όψιν απειροστά μικρά στοιχεία όγκου, μπορούμε να γράψουμε την εξίσωση του παράγοντα δομής με τον εξής τρόπο: (2.25) Η τελευταία εξίσωση αποδεικνύει ότι ο παράγοντας δομής F hkl είναι ένας μετασχηματισμός Fourier της ηλεκτρονιακής πυκνότητας ρ(x,y,z) μιας σειράς κρυσταλλογραφικών επιπέδων (hkl). Ο μετασχηματισμός Fourier περιγράφει επακριβώς τη μαθηματική σχέση που υπάρχει μεταξύ ενός αντικειμένου και της εικόνας περίθλασης που αυτό εμφανίζει. Η χρήση του επιτρέπει τη μετατροπή σειρών Fourier που περιγράφουν τις ανακλάσεις σε σειρές Fourier που περιγράφουν την ηλεκτρονιακή πυκνότητα. Η ηλεκτρονιακή πυκνότητα περιγράφεται με σειρά Fourier στην οποία κάθε όρος είναι παράγοντας δομής. Στην κρυσταλλογραφία, οι μετασχηματισμοί Fourier χρησιμοποιούνται για να μετατρέψουν τους παράγοντες δομής στην επιθυμητή εξίσωση ηλεκτρονιακής πυκνότητας ρ(x,y,z). 48
50 Για την περίθλαση ακτίνων-χ, η σχέση αναλογίας μεταξύ του πλάτους της σκεδαζόμενης ακτινοβολίας και του παράγοντα δομής είναι: (2.26) Τα δύο μεγέθη στον παραπάνω τύπο δε συνδέονται με σύμβολο ισότητας, καθώς συντελούν διάφοροι παράγοντες στη διαμόρφωση της τελικής τιμής του πλάτους έντασης. Μερικοί από τους παράγοντες αυτούς είναι οι συντελεστές απορρόφησης, θερμοκρασίας, πόλωσης, αλλά και άλλοι συντελεστές που εξαρτώνται από τις πειραματικές συνθήκες κάθε φορά, όπως το μέγεθος του κρυστάλλου, η ένταση της δέσμης κ.α Η ηλεκτρονιακή πυκνότητα ως σειρά Fourier εξής: Η ηλεκτρονιακή πυκνότητα μπορεί να υπολογιστεί από την εξίσωση (2.24) ως (2.27), όπου V είναι ο όγκος της μοναδιαίας κυψελίδας και ισούται με V = a (b c) = b (c a) = c (a b). Η εξίσωση (2.27) αποδεικνύει ότι ο προσδιορισμός της ηλεκτρονιακής πυκνότητας, απαιτεί την κατασκευή της σειράς Fourier των παραγόντων δομής. Καθώς η εξίσωση F hkl είναι μια περιοδική συνάρτηση εμπεριέχει μεγέθη όπως είναι το πλάτος, η συχνότητα και η φάση. Επίσης, εφόσον η δέσμη ακτίνων-χ που εξέρχεται είναι ένα σκεδαζόμενο κύμα, θα έχει συχνότητα ίση με τη συχνότητα της εισερχόμενης δέσμης, της πηγής δηλαδή. Το πλάτος, F hkl θα είναι ανάλογο του τετραγώνου της έντασης της ανάκλασης, I hkl, με συνέπεια τα πλάτη να προκύπτουν άμεσα από τις μετρούμενες εντάσεις των ανακλάσεων. Παρ όλα αυτά η φάση του κύματος F hkl δεν προκύπτει άμεσα από μια και μοναδική μέτρηση της έντασης της ανάκλασης. Προκειμένου να υπολογίσουμε την ηλεκτρονιακή πυκνότητα ρ(x,y,z) από τους παράγοντες δομής, πρέπει να γνωρίζουμε εκτός από την ένταση της κάθε ανάκλασης και τη φάση της κάθε σκεδαζόμενης δέσμης. Μια βολική αναπαράσταση του παράγοντα δομής είναι υπό τη μορφή μιγαδικού αριθμού (F hkl = Α + iβ). Σύμφωνα με την εξίσωση (2.27) και το γεγονός ότι οι μιγαδικοί αριθμοί μπορούν να παρασταθούν από σημεία στις δύο διαστάσεις, μπορούμε να αποσυνδέσουμε το F hkl σε δυο μέρη. Το πρώτο είναι το πλάτος F hkl, που αποτελεί και το πραγματικό μέρος (Α) του μιγαδικού και το δεύτερο είναι η φάση φ hkl, που αντιστοιχεί στη γωνία που σχηματίζει το διάνυσμα με τη γραμμή τον άξονα των πραγματικών αριθμών. Δηλαδή τελικά ο παράγοντας δομής γράφεται 49
51 . Αυτό μας επιτρέπει να εκφράσουμε το ρ(x,y,z) σα συνάρτηση του μετρούμενου πλάτους F hkl και της άγνωστης φάσης φ hkl με την εξής μορφή: (2.28) Η εξίσωση (2.28) αναπαριστά την πυκνότητα ρ(x,y,z) με σειρά Fourier, στην οποία η φάση κάθε παράγοντα δομής είναι καθορισμένη. Κάθε όρος αυτής της σειράς είναι ένα κύμα τριών διαστάσεων με πλάτος F hkl, φάση φ hkl και συχνότητες h κατά μήκος του άξονα x, k κατά μήκος του y και l κατά μήκος του άξονα z. Ο προσδιορισμός της φάσης φ hkl της κάθε ανάκλασης, γνωστό ως πρόβλημα φάσης, είναι ένα από τα απαιτητικότερα προβλήματα στην κρυσταλλογραφία Το πρόβλημα φάσης Από τη σχέση του παράγοντα δομής, που αναφέρθηκε στην προηγούμενη ενότητα γίνεται αντιληπτό ότι για να προσδιορίσουμε τους παράγοντες δομής των ανακλάσεων πρέπει να γνωρίζουμε τα μέτρα τους και τις αντίστοιχες φάσεις τους. Αν συνέβαινε αυτό θα μπορούσε να υπολογιστεί κατ ευθείαν η κατανομή της ηλεκτρονιακής πυκνότητας στην κυψελίδα και κατά συνέπεια θα εντοπίζονταν οι θέσεις των ατόμων. Έτσι η επίλυση της δομής των κρυστάλλων θα ήταν μια υπολογιστική διαδικασία. Όμως από τη μέτρηση των ολοκληρωμένων εντάσεων των ανακλάσεων προκύπτουν μόνο τα μέτρα των παραγόντων δομής ( ) ενώ παραμένουν άγνωστες οι φάσεις τους ( ). Η αδυναμία της άμεσης μέτρησης των φάσεων αποτελεί το ονομαζόμενο πρόβλημα φάσεων. Για την επίλυση του προβλήματος αυτού έχουν επινοηθεί διάφορες μέθοδοι που χωρίζονται στις άμεσες και στις έμμεσες. Οι έμμεσες μέθοδοι οδηγούν στην επίλυση της δομής έχοντας ως αφετηρία κάποιες γνωστές φάσεις. Οι άμεσες μέθοδοι ξεκινούν με όλες τις φάσεις άγνωστες (G.M. Sheldrick, 2006). Οποιαδήποτε μέθοδος και αν επιλεχθεί, ακολουθείται μια λογική επίλυσης που διακρίνεται σε τρία βασικά στάδια. Στο πρώτο στάδιο δημιουργείται ένα κατάλληλο υποθετικό δομικό πρότυπο (structural model), το οποίο ανταποκρίνεται στις πειραματικές τιμές των παραγόντων δομής (F observed ), ενώ οι φάσεις είναι παραπλήσιες με τις πραγματικές. Στο δεύτερο στάδιο, με βάση το πρότυπο φάσεων, πραγματοποιούνται διαδοχικοί υπολογισμοί (κύκλοι) των παραγόντων δομής (F calculated ) και της ηλεκτρονιακής πυκνότητας (ρ(r)), ώσπου να προσδιοριστεί η θέση όλων των ατόμων του μορίου ή της χημικής μονάδας. 50
52 Τέλος, στο τρίτο στάδιο, με διαδοχικούς κύκλους υπολογισμού των ελαχίστων τετραγώνων γίνεται βελτιστοποίηση (refinement) των συντεταγμένων της θέσης των ατόμων, καθώς και του θερμικού τους παράγοντα, ώστε να επιτευχθεί όσο το δυνατόν μεγαλύτερη συμφωνία μεταξύ των πειραματικών τιμών (F observed ) και των τιμών που υπολογίσθηκαν (F calculated ) και να προκύψει η σωστή δομή. Οι άμεσες μέθοδοι βασίζονται στη θεωρία πιθανοτήτων. Και οι υπολογισμοί πραγματοποιούνται με την ανάλυση των παραγόντων δομής των πειραματικών δεδομένων (F observed ). Από τις έμμεσες μεθόδους, αυτές που χρησιμοποιούνται πιο συχνά για την επίλυση του προβλήματος φάσης είναι η μέθοδος του βαρέως ατόμου, η μέθοδος Patterson, η ισόμορφη αντικατάσταση και η μοριακή αντικατάσταση, η ανώμαλη σκέδαση ακτίνων-χ (Single or Multi-wavelength Anomalous Diffraction, SAD or MAD phasing) καθώς και συνδυαστικές μέθοδοι αυτών. Για τη μέθοδο του βαρέως ατόμου, κατά τη διαδικασία της κρυστάλλωσης προστίθεται ένα βαρύ στοιχείο, μεγάλου ατομικού αριθμού, συνήθως μέταλλο, το οποίο ενσωματώνεται στη δομή του υπό μελέτη υλικού (συγκρυστάλλωση). Στο διάγραμμα περίθλασης που προκύπτει, η συνεισφορά των βαρέων ατόμων είναι πολύ έντονη. Έτσι λοιπόν, οι κορυφές που ανήκουν σε αυτά τα στοιχεία εντοπίζονται εύκολα και κατά συνέπεια μπορούν να προσδιοριστούν και οι θέσεις των ατόμων αυτών μέσα στο πλέγμα. Στη συνέχεια εντοπίζονται οι φάσεις όλων των ανακλάσεων που οφείλονται στη συνεισφορά των βαρέων ατόμων και καθίσταται δυνατή η δημιουργία ενός αρχικού χάρτη ηλεκτρονιακής πυκνότητας από τον οποίο αποκαλύπτονται οι θέσεις ελαφρύτερων ατόμων. Η διαδικασία επαναλαμβάνεται ώσπου να αποκαλυφθούν όλα τα άτομα στο χάρτη ηλεκτρονιακής πυκνότητας. Η μέθοδος επίλυσης που πρότεινε ο Patterson, μεσω του υπολογισμού της ομώνυμης συνάρτησης (Patterson, 1934) για κάθε σημείο της κυψελίδας, οδηγεί στην κατασκευή ενός τρισδιάστατου χάρτη. Ο χάρτης αυτός περιλαμβάνει κορυφές, οι οποίες αντιστοιχούν στις άκρες των διανυσμάτων που ενώνουν, ανά δύο, τα άτομα της δομής. Η τιμή της συνάρτησης Patterson στην άκρη του διανύσματος που συνδέει δύο άτομα με ατομικούς αριθμούς Ζ 1 και Ζ 2, Σχήμα 2.22: Η μέθοδος Patterson. (a) Ένας δισδιάστατος κρύσταλλος τριών ατόμων και (b) η κατασκευή του αντίστοιχου χάρτη Patterson (Πηγή: 51
53 είναι ανάλογη του γινομένου Ζ 1 Ζ 2. Επομένως εάν η δομή έχει μερικά ελαφριά άτομα, μικρού ατομικού αριθμού και μερικά βαριά άτομα, οι υψηλότερες κορυφές στο χάρτη προέρχονται από τα διανύσματα μεταξύ βαριών ατόμων. Έτσι προσδιορίζονται αρχικά οι θέσεις των βαριών ατόμων και σταδιακά και των υπολοίπων ατόμων. Η μέθοδος της ισόμορφης αντικατάστασης (Single Isomorphous Replacement SIR ή Multiple Isomorphous Replacement ΜIR) προϋποθέτει την ύπαρξη τουλάχιστον δύο κρυστάλλων οι οποίοι διαφέρουν κατά ένα άτομο (ή κατά μικρό αριθμό ατόμων) και εμφανίζουν στο μεγαλύτερο ποσοστό τους κοινή δομή. Ένας τρόπος για τη δημιουργία παράγωγου κρυστάλλου (derivative), είναι βυθίζοντας τον αρχικό κρυσταλλο (native) σε διάλυμα που περιέχει βαρέα άτομα. Η αντικατάσταση ενός ατόμου από άλλο άτομο, διαφορετικού ατομικού αριθμού, στην περίπτωση που επιφέρει παρατηρήσιμες μεταβολές στα διαγράμματα περίθλασης, μας επιτρέπει να εντοπίσουμε τη θέση του βαρέως ατόμου. Βρίσκοντας τη θέση του μπορεί να υπολογιστεί η συνεισφορά του σε κάθε όρο του παράγοντα δομής καθώς και η φάση τόσο του αρχικού όσο και του παράγωγου κρυστάλλου. Επομένως, για τη συγκεκριμένη μέθοδο αρκεί να να μπορούμε να αντικαταστήσουμε ένα ελαφρύ άτομο του κρυστάλλου από ένα βαρύ. Η μέθοδος της μοριακής αντικατάστασης (Molecular Replacement - MR) αναφέρεται όταν υπάρχει ένα ομόλογο της υπό μελέτη δομής, το οποίο λειτουργεί ως αναφορά για τις αρχικές φάσεις των παραγόντων δομής. Με διάφορες μεθόδους που εφαρμόζονται, προσδιορίζεται τελικά ο σωστός προσανατολισμός και η θέση στη μοναδιαία κυψελίδα της άγνωστης δομής. Τη μέθοδο αυτή ανέπτυξαν για πρώτη φορά οι Μ. Rossman και D.Blow. (M.G.Rossman, 1962). Η μέθοδος της ανώμαλης σκέδασης βασίζεται στο φαινόμενο της ανώμαλης διασποράς που παρατηρείται όταν επιλέγεται προσπίπτον μήκος κύματος ίσο με την τιμή απορρόφησης ενός χημικού στοιχείου του δείγματος. Το φαινόμενο της διασποράς προκαλεί εμφανείς μετατοπίσεις στο διάγραμμα περίθλασης αποκαλύπτοντας στοιχεία για τη φάση του κύματος. Όταν το μήκος κύματος είναι συγκεκριμένο για ένα πείραμα ανώμαλης σκέδασης, τότε η μέθοδος ονομάζεται Single wavelength Anomalous Diffraction - SAD. Ο παράγοντας δομής στην κλασσική περίθλαση είναι ανεξάρτητος του μήκους κύματος. Κατά την ανώμαλη σκέδαση όμως εμφανίζει μεγάλη εξάρτηση από το μήκος κύματος. Για να ληφθεί η μέγιστη τιμή του παράγοντα δομής μπορεί να πραγματοποιηθεί πείραμα περίθλασης με κάποιο εύρος τιμών μήκους κύματος. Πειράματα τέτοιου τύπου ονομάζονται Multi-wavelength Anomalous Diffraction - MAD Η μέθοδος Rietveld Κατά την ανάλυση των διαγραμμάτων περίθλασης ο συνηθέστερος τρόπος επεξεργασίας των δεδομένων συνήθιζε να γίνεται με τη μέτρηση της έντασης κάθε 52
54 ανάκλασης Bragg ξεχωριστά. Η μέθοδος αυτή έχει εύκολη εφαρμογή σε κρυσταλλικές δομές που παρουσιάζουν λίγες και εύκολα διαχωρίσιμες κορυφές ανακλάσεων, αλλά η εφαρμογή της δυσκολεύει όσο οι δομές γίνονται πιο περίπλοκες και η συμμετρία μειώνεται. Καθώς τα διαγράμματα περίθλασης από πολυκρυσταλλικά υλικά προέρχονται από κρυστάλλους τυχαία προσανατολισμένους, οι κορυφές που εμφανίζονται είναι πολύ συχνά αποτέλεσμα της αλληλοεπικάλυψης κορυφών που αντιστοιχούν σε διαφορετικές ανακλάσεις. Αποτέλεσμα αυτού του φαινομένου είναι η απώλεια πληροφορίας η οποία οδήγησε στην ανάγκη δημιουργίας μιας νέας τεχνικής επεξεργασίας των δεδομένων αυτών. Η μέθοδος Rietveld είναι μια Σχήμα 2.23: Συνεισφορά τριών ανακλάσεων σε μια κορυφή (Πηγή: Lecture Notes, Andrew Wills, τεχνική προσδιορισμού των παραμέτρων του πλέγματος και των παραμέτρων δομής απευθείας από την ολική περίθλαση ακτινοβολίας από πολυκρυσταλλικά δείγματα, χωρίς να απαιτείται διαχωρισμός των ανακλάσεων που συνεισφέρουν σε κάθε κορυφή. Πρώτος ο H.M.Rietveld εργάστηκε συστηματικά και αναλυτικά χρησιμοποιώντας υπολογιστικά προγράμματα ώστε να αξιοποιήσει όλες τις πληροφορίες από τα δομικά πρότυπα που προέρχονται από πολυκρυσταλλικά δείγματα. Στη συνέχεια δημοσίευσε αυτές τις εργασίες του καθώς και τα υπολογιστικά προγράμματα που χρησιμοποίησε, συνεισφέροντας έτσι σε μεγάλο βαθμό, στον τρόπο εξαγωγής της δομικής πληροφορίας από πολυκρυσταλλικά δείγματα που ακολουθούσε έως τότε η επιστημονική κοινότητα. Η συγκεκριμένη μέθοδος δε μπορεί να χρησιμοποιηθεί για τον προσδιορισμό άγνωστων δομών. Για αυτό χρησιμοποιεί γνωστά δομικά πρότυπα για τις διάφορες κρυσταλλικές φάσεις που περιέχονται στο υπό μελέτη υλικό. Συνεπώς ένα κρίσιμο σημείο που καθορίζει την έκβαση της ανάλυσης, είναι η επιλογή του καταλληλότερου μοντέλου που θα ορισθεί ως αρχικό και θα πρέπει να αποτελεί πολύ καλή προσέγγιση του πειραματικού. Χρησιμοποιώντας την ανάλυση Rietveld μπορούμε να προσδιορίσουμε τις παραμέτρους δομής, τις παραμέτρους του πλέγματος, το υπόβαθρο (background), το εύρος των ανακλάσεων, τη συνάρτηση μορφής του προφίλ καθώς και την προτιμώμενη διεύθυνση προσανατολισμού. Το αποτέλεσμα που προκύπτει είναι η συνισταμένη της συμβολής όλων των επιμέρους αποτελεσμάτων που προκύπτουν από τα προτεινόμενα μοντέλα κρυσταλλικής δομής και βασίζεται στο φαινόμενο της περίθλασης και σε παράγοντες όπως ο παράγοντας δομής ή σε διάφορους 53
55 παραμέτρους δομής που ποικίλουν ανάλογα με το μοντέλο που επιλέγουμε να εφαρμόσουμε. Με τη χρήση του ηλεκτρονικού υπολογιστή πραγματοποιούνται υπολογισμοί που βελτιώνουν διαρκώς τις τιμές των εντάσεων των αλληλεπικαλυπτόμενων ανακλάσεων καθώς με την επαναλαμβανόμενη εφαρμογή των ελαχίστων τετραγώνων βελτιώνονται συνεχώς οι παράμετροι των επί μέρους δομικών μοντέλων και γίνεται σαφέστερος ο διαχωρισμός της έντασης, που αντιστοιχεί στο καθένα από αυτά. Το υπόβαθρο που εμφανίζει ένα διάγραμμα περίθλασης μπορεί να οφείλεται σε πολλούς παράγοντες. Για παράδειγμα μπορεί να προέρχεται από κάποια άμορφη φάση που εμπεριέχεται στο δείγμα. Επιπλέον μπορεί να οφείλεται στη διάχυση της ακτινοβολίας που προκαλούν ο αέρας ή και η διαλυτή ουσία που περιβάλλει τους κρυστάλλους, καθώς επίσης και το γυαλί, μέσα στο οποίο βρίσκεται το δείγμα (glass capillarie) Συστηματικές κατασβέσεις Αφού πραγματοποιηθεί η συλλογή των δεδομένων, από ένα πείραμα μονοκρυστάλλου λαμβάνουμε, όπως αναφέρθηκε και νωρίτερα, διαγράμματα περίθλασης που αποτελούνται από ανακλάσεις (spots) διαφορετικών εντάσεων. Υπάρχουν όμως και κάποια σημεία στα διαγράμματα, στα οποία ενώ θα περιμέναμε να εμφανίζονται οι ανακλάσεις σε συμμετρικές θέσεις, τελικά κάποιες ανακλάσεις φαίνεται να απουσιάζουν συστηματικά. Το ίδιο φαινόμενο παρατηρείται και στις κορυφές των εντάσεων από πειράματα πολυκρυσταλλικών υλικών. Στις περιπτώσεις που λαμβάνουμε μηδενική, ή σχεδόν μηδενική, ένταση ανάκλασης από τα κρυσταλλογραφικά επίπεδα και οφείλεται στην ύπαρξη κεντρωμένου πλέγματος ή στα στοιχεία συμμετρίας του πλέγματος, λέμε ότι εμφανίζονται συστηματικές κατασβέσεις. Από τις συστηματικές κατασβέσεις που παρατηρούνται, κάποιες παρουσιάζουν τιμή έντασης σχεδόν μηδενική επειδή πολύ μικρός αριθμός ηλεκτρονίων του κρυστάλλου συμβάλλει στην περίθλαση από το αντίστοιχο επίπεδο, ενώ άλλες ανακλάσεις παρουσιάζουν τιμή έντασης μηδενική λόγω της καταστρεπτικής συμβολής των συμβαλλόμενων κυμάτων ακτίνων-χ. Παρόλο που θα περίμενε κανείς αυτές οι απουσίες να καθιστούν τον προσδιορισμό της συμμετρίας ακόμα πιο δύσκολο, στην πραγματικότητα διευκολύνουν την αναγνώρισή των στοιχείων συμμετρίας. Αυτό συμβαίνει επειδή είναι γνώστες οι αναμενόμενες απουσίες για κάθε Space Group και συνεπώς ελέγχοντας τις ανακλάσεις που απουσιάζουν, μπορούμε να πιστοποιήσουμε τη συμμετρία που υπάρχει. Οι προϋποθέσεις που πρέπει να πληρούνται ώστε να παρατηρούμε ανακλάσεις σε ένα διάγραμμα περίθλασης, ονομάζονται reflection conditions. Στους πίνακες που ακλουθούν παρατίθενται συνοπτικά οι προϋποθέσεις αυτές για 54
56 κάθε στοιχείο συμμετρίας. Οι συμβολισμοί και οι συνθήκες αναλύονται εκτενώς στα άρθρα της Διεθνούς Κρυσταλλογραφικής Ένωσης - IUCr (A. Looijenga-Vos, 2006). Πίνακας 2.1: Reflection conditions που σχετίζονται με την κέντρωση του πλέγματος. Ονομάζονται και γενικές κατασβέσεις (Πηγή: MIT OpenCourseWare, ocw.mit.edu). Πίνακας 2.2: Reflection conditions που σχετίζονται με τα sxcrew axis (αριστερά) και τα glide planes (δεξιά) (Πηγή: MIT OpenCourseWare, ocw.mit.edu). 55
57 3. Κρυστάλλωση Πρωτεϊνών Με τον όρο κρυστάλλωση περιγράφουμε μια σειρά βιοχημικών/ φυσικοχημικών διεργασιών, τελικό αποτέλεσμα των οποίων είναι ο σχηματισμός μιας νέας στερεάς φάσης μέσα σε ένα ομογενές διάλυμα, δηλαδή ο σχηματισμός των κρυστάλλων. Το σύνολο των διεργασιών της κρυστάλλωσης πραγματοποιείται μέσα σε ένα φυσικοχημικό σύστημα που εξαρτάται από πολλές παραμέτρους. Η μελέτη αυτών των περίπλοκων συστημάτων απασχολεί έναν ολόκληρο επιστημονικό κλάδο που εξετάζει τον τρόπο και το βαθμό δράσης κάθε παράγοντα στη διαδικασία της κρυστάλλωσης. Επειδή κάθε βιολογικό σύστημα είναι μοναδικό, οι συνθήκες κρυστάλλωσης θα είναι διαφορετικές για κάθε σύστημα. Παρ όλα αυτά, η διαδικασία που ακολουθείται για την εύρεση των κατάλληλων συνθηκών κρυστάλλωσης, μπορεί να γενικευθεί σε όλα τα συστήματα. Οι σχέσεις ισορροπίας και οι μεταβάσεις φάσεων που παρατηρούνται κατά τη διαδικασία αυτή αναπαριστώνται με τα διαγράμματα φάσης. Γνωρίζοντας το διάγραμμα φάσεων μιας πρωτεΐνης, γνωρίζουμε τον τρόπο με τον οποίο μπορούμε να μεταβούμε στη ζώνη που επιθυμούμε. Προκειμένου να κρυσταλλώσουμε μια πρωτεΐνη πρέπει να εξασφαλίσουμε σε πρώτο στάδιο την υψηλή καθαρότητα της πρωτεΐνης αυτής. Μάλιστα, αρχικά η κρυστάλλωση των πρωτεϊνών χρησιμοποιήθηκε για τον έλεγχο της καθαρότητάς τους, καθώς η ανάπτυξη κρυστάλλων αποτελούσε ένδειξη της καθαρότητας των πρωτεϊνών. Με την πορεία των χρόνων όμως αποδείχθηκε ότι οι πρωτεϊνικοί κρύσταλλοι μπορεί να περιέχουν προσμίξεις σε ποσοστό έως και 10% και έτσι η κρυστάλλωση αντικαταστάθηκε από άλλες, πιο ακριβείς μεθόδους. Επιπλέον, αναγκαία αλλά όχι ικανή συνθήκη για την ανάπτυξη κρυστάλλων είναι η δημιουργία ενός υπέρκορου διαλύματος πρωτεΐνης. Το διάλυμα που περιέχει τη μέγιστη δυνατή ποσότητα διαλυτής ουσίας, υπό συγκεκριμένες συνθήκες πίεσης και θερμοκρασίας, ονομάζεται κορεσμένο διάλυμα. Το κορεσμένο διάλυμα είναι ενδεικτικό του ορίου διαλυτότητας ενός συστήματος. Ένα διάλυμα το οποίο περιέχει επιπλέον ποσότητα διαλυτής ουσίας, σε σχέση με το κορεσμένο στις ίδιες συνθήκες, ονομάζεται υπέρκορο, ενώ το διάλυμα που περιέχει μικρότερη ποσότητα, ονομάζεται ακόρεστο ή υπόκορο. Εμφάνιση κρυστάλλων παρατηρείται μόνο σε υπέρκορα διαλύματα. Για να αποκτήσουμε ένα υπέρκορο διάλυμα από ένα ακόρεστο, μπορούμε για παράδειγμα είτε να αυξήσουμε τη συγκέντρωση της διαλυτής ουσίας στο διάλυμα, είτε να απομακρύνουμε σταδιακά το διαλύτη μέσω του φαινομένου της εξάτμισης. 56
58 Στα διαγράμματα φάσης η καμπύλη διαλυτότητας (solubility curve) διαχωρίζει την ακόρεστη περιοχή από την υπέρκορη περιοχή. Κάτω από την καμπύλη, η μόνη φάση που μπορεί να υπάρξει είναι η υγρή, κατά συνέπεια εκεί δεν αναπτύσσονται κρύσταλλοι. Σχήμα 3.1: Διάγραμμα Φάσεων που περιγράφει τα στάδια κρυστάλλωσης των πρωτεϊνών. Στον κατακόρυφο άξονα αναπαριστάται η συγκέντρωση της πρωτεΐνης ενώ στον οριζόντιο οι παράμετροι που συμβάλλουν στην καθίζηση της πρωτεΐνης όπως είναι η θερμοκρασία, το ph και η προσθήκη αλάτων, οργανικών διαλυτών και πολυμερών. Το διάγραμμα αποτελείται από τέσσερις περιοχές, την ακόρεστη (undersaturation), τη μετασταθή ζώνη (metastable), τη ζώνη πυρήνωσης (nucleation or labile) και τη ζώνη καθίζησης (precipitation). Η καμπύλη διαλυτότητας (solubility curve) διαχωρίζει τη ακόρεστη περιοχή από τη μετασταθή ζώνη στην οποία το διάλυμα είναι υπέρκορο και επιτρέπει την κρυσταλλική ανάπτυξη. Στη ζώνη πυρήνωσης δημιουργούνται συσσωματώματα τα οποία αποτελούν πυρήνες των κρυστάλλων που θα σχηματιστούν στη συνέχεια στην μετασταθή περιοχή. Στο διάγραμμα επίσης απεικονίζεται η διαδρομή που ακολουθείται σε κάθε μια από τις τέσσερις βασικές τεχνικές κρυστάλλωσης (i) μέθοδος batch, (ii) μέθοδος διάχυσης ατμών - vapor diffusion, (iii) διαπίδυση και (iv) ελεύθερη διάχυση μεταξύ επιφανειών (free interference diffusion FID) (Πηγή: Naomi E. Chayen & Emmanuel Saridakis, 2008, Nature Methods Vol.5, ). Πάνω από την καμπύλη διαλυτότητας και υπό κατάλληλες συνθήκες πιθανόν να αναπτυχθούν κρύσταλλοι. Η ενέργεια του συστήματος σε σταθερές συνθήκες πίεσης και θερμοκρασίας, παραμένει επίσης σταθερή, χωρίς αυτό να σημαίνει ότι το ενεργειακό επίπεδο είναι ακριβώς το ίδιο σε όλα τα σημεία του διαλύματος. Υπάρχουν διακυμάνσεις της ενέργειας γύρω από μια κεντρική τιμή και σε περιοχές του διαλύματος όπου βαθμός υπερκορεσμού είναι κατάλληλος και η ενέργεια αυξάνεται, ευνοείται η ανάπτυξη κρυστάλλων (Mullin, 1972). Μόρια της διαλυμένης ουσίας σε αυτά τα σημεία του διαλύματος διατάσσονται αυθόρμητα με τρόπο χαρακτηριστικό της νέας φάσης. Οι σχηματισμοί που δημιουργούνται 57
59 ονομάζονται συσσωματώματα και η δημιουργία τους μειώνει τελικά την ελεύθερη ενέργεια του συστήματος (Ενέργεια Gibbs). Τα συσσωματώματα αποτελούν πυρήνες των κρυστάλλων που επιδιώκουμε να αποκτήσουμε για αυτό και στο διάγραμμα φάσης αναφέρεται ως ζώνη πυρήνωσης (nucleation zone ή labile zone). Σχήμα 3.2: Στάδια ανάπτυξης κρυστάλλων. Αρχικά στο διάλυμα δημιουργούνται συσσωματώματα. Αφού πραγματοποιηθεί η μετάβαση από τη διαλυτή φάση στη ζώνη πυρήνωσης, τα συσσωματώματα συνεχίζουν να αναπτύσσονται ώσπου να υπερβούν το ενεργειακό φράγμα (Ε) που θα τους επιτρέψει να διαμορφωθούν σε κρυστάλλους. Η ανάπτυξη των κρυστάλλων οδηγεί το σύστημα σε χαμηλότερη ενέργεια Gibbs και ευνοείται ενεργειακά. Τα μόρια θα τοποθετηθούν μέσα στο κρυσταλλικό πλέγμα στις θέσεις όπου οι ελκτικές δυνάμεις είναι μεγαλύτερες (Nagalingam S., 1982). Η ανάπτυξη των κρυστάλλων ευνοείται καθώς με τον τρόπο αυτό, το σύστημα μεταβαίνει σε κατάσταση χαμηλότερης ελεύθερης ενέργειας, ενώ ο σχηματισμός πολλών νέων χημικών δεσμών δημιουργεί μια υψηλής οργάνωσης εσωτερική δομή. Το στάδιο αυτό πραγματοποιείται με τη μετάβαση σε χαμηλότερη ζώνη στο διάγραμμα φάσης, εντός των ορίων του υπέρκορου διαλύματος, η οποία ονομάζεται μετασταθής ζώνη (metastable zone). Σε αυτή τη ζώνη οι πυρήνες μετασχηματίζονται στους ζητούμενους καλοσχηματισμένους κρυστάλλους. Ωστόσο, η συγκεκριμένη περιοχή δεν ευνοεί την εξ ολοκλήρου απ την αρχή ανάπτυξη κρυστάλλων. Μόνο στις περιπτώσεις που ένας ήδη σχηματισμένος πυρήνας βρεθεί στη μετασταθή περιοχή, μπορεί να συνεχίσει να αναπτύσσεται. Γι αυτό, όπως φαίνεται και στο διάγραμμα φάσης, η διαδικασία περιλαμβάνει αρχικά τη μετάβαση από την ακόρεστη (ή κορεσμένη) περιοχή στην υπέρκορη και στη συνέχεια πάλι πίσω στην κατάσταση ισορροπίας όπου και θα εμφανιστούν οι κρύσταλλοι. Καθώς οι κρύσταλλοι μεγαλώνουν, η συγκέντρωση της διαλυμένης 58
60 πρωτεΐνης μειώνεται, με αποτέλεσμα η μετασταθής ζώνη να μετατοπίζεται. Για αυτό κατά τη διαδικασία της κρυστάλλωσης οφείλουμε να επικεντρωνόμαστε στη συνεχή παρακολούθηση της μετασταθούς ζώνης. Η τελευταία περιοχή που εμφανίζεται δεξιά στα διαγράμματα φάσης είναι η ζώνη καθίζησης (precipitation zone). Τα μόρια του διαλύματος που αποδεσμεύονται με άτακτο τρόπο από το διάλυμα, βυθίζονται και σχηματίζουν ένα άμορφο ίζημα. Για τα πειράματα μονοκρυστάλλων, στόχος δεν είναι η δημιουργία πολλών πυρήνων, αλλά η δημιουργία μερικών έστω πυρήνων που θα αποδώσουν κρυστάλλους μεγάλου μεγέθους και καλής ποιότητας. Έτσι αρκεί να προσεγγίσουμε το κάτω όριο της ζώνης πυρήνωσης στο οποίο, όπως περιγράφηκε παραπάνω, ξεκινά η δημιουργία των κρυστάλλων, ώστε οι κρύσταλλοι να μεταβούν άμεσα στη μετασταθή περιοχή και να συνεχιστεί η ανάπτυξή τους. Για τη δημιουργία πολυκρυσταλλικών δειγμάτων (powder) όμως, τα οποία αποτελούνται από άπειρους κρυστάλλους μικρότερου μεγέθους, η περιοχή που προσπαθούμε να προσεγγίσουμε είναι το άνω όριο μεταξύ της ζώνης πυρήνωσης και της ζώνης καθίζησης. Στο άνω όριο της ζώνης πυρήνωσης δημιουργούνται ποσοτικά περισσότεροι πυρήνες κρυστάλλων, οι οποίοι θα αποδώσουν κρυσταλλικό ίζημα με μεγάλο αριθμό κρυστάλλων, όπως απαιτούν τα πολυκρυσταλλικά δείγματα. 3.1 Παράγοντες που επηρεάζουν την κρυστάλλωση Η κρυστάλλωση είναι μια πολυπαραμετρική διαδικασία και κάθε παράγοντας που την επηρεάζει δεν δρα ανεξάρτητα από τους υπόλοιπους. Γενικά, η θεωρία της κρυστάλλωσης θα λέγαμε ότι συνοψίζεται στη μελέτη των μεταβολών της διαλυτότητας του πρωτεϊνικού διαλύματος. Μια βασική παρατήρηση είναι ότι ο ρυθμός ελάττωσης της διαλυτότητας της πρωτεΐνης πρέπει να είναι ελεγχόμενος. Απότομη ελάττωση της διαλυτότητας οδηγεί σε άμορφα ιζήματα καθώς για να αναπτυχθεί ένας κρύσταλλος τα μεμονωμένα μόρια πρέπει να έχουν την ευκαιρία να αποτεθούν κανονικά στην επιφάνεια της ανάπτυξης του κρυστάλλου. Για αυτό η προσέγγιση του σημείου υπερκορεσμού γίνεται με πολύ αργό ρυθμό. Οι παράγοντες που επηρεάζουν τη διαλυτότητα όπως η συγκέντρωση, η ιοντική ισχύς, η θερμοκρασία, το ph του πρωτεϊνικού διαλύματος αλλάζουν βαθμιαία. Παρακάτω περιγράφεται η γενική συμπεριφορά που εμφανίζουν οι βασικότεροι παράγοντες στη διαδικασία της κρυστάλλωσης πρωτεϊνών. Η πρωτεΐνη παραμένει υπό μορφή διαλύματος μέχρι μια συγκεκριμένη τιμή συγκέντρωσης. Όταν ξεπεραστεί αυτή η οριακή τιμή, όπου λέμε ότι έχουμε υπερκορεσμό, το διάλυμα παύει να είναι ομογενές και μια νέα φάση αρχίζει να εμφανίζεται, (Asherie, 2004). Αυτό συμβαίνει επειδή το υπέρκορο διάλυμα, 59
61 παρουσιάζει μικρή διαλυτότητα πρωτεΐνης που επιτρέπει στα μόρια της πρωτεΐνης να πλησιάσουν πολύ κοντά και να δημιουργήσουν συσσωματώματα. Κατά αυτό τον τρόπο η μικρή διαλυτότητα διευκολύνει τη διαδικασία κρυστάλλωσης. Αντίθετα, η υψηλή διαλυτότητα απομακρύνει τα μόρια της πρωτεΐνης μεταξύ τους δυσκολεύοντας τη διαδικασία κρυστάλλωσης. Η συγκέντρωση της πρωτεΐνης σε ένα διάλυμα ορίζει, με άμεσο τρόπο, τη διαλυτότητα της πρωτεΐνης. Αύξηση της συγκέντρωσης της πρωτεΐνης που περιέχεται μέσα σε ένα διάλυμα οδηγεί στη μείωση της διαλυτότητάς της. Συνεπώς στο διάγραμμα φάσεων οδηγούμαστε στην περιοχή επάνω από την καμπύλη διαλυτότητας, όπου οι συνθήκες είναι ευνοϊκές για τη δημιουργία κρυστάλλων. Αλλαγή της θερμοκρασίας στην οποία βρίσκεται το διάλυμα της πρωτεΐνης, μεταβάλλει τη διαλυτότητά της. Αύξηση της θερμοκρασίας αυξάνει τη διαλυτότητα των πρωτεϊνών, γεγονός που δεν ευνοεί τις συνθήκες κρυστάλλωσης. Σε πολλές περιπτώσεις μάλιστα έχει παρατηρηθεί ότι η μεταβολή σε υψηλότερη θερμοκρασία κατέστρεψε τους ήδη υπάρχοντες κρυστάλλους. Άλλωστε οι υψηλές θερμοκρασίες μπορεί να αποβούν καταστροφικές ακόμα και για τη φύση των πρωτεϊνών καθώς προκαλούν τη μετουσίωσή τους. Οι πιο συνηθισμένες τιμές θερμοκρασίας για τα πειράματα κρυσταλλώσεων είναι είτε στους 4 C, είτε σε θερμοκρασία δωματίου ( 25 C). Άλλος ένας παράγοντας που επηρεάζει την κρυστάλλωση είναι η τιμή του ph. Για πολλά χρόνια, το ιδανικό ph για την κρυστάλλωση μιας πρωτεΐνης θωρούνταν ότι ήταν στο ισοηλεκτρικό σημείο της πρωτεΐνης (pi), όπου το ολικό φορτίο είναι μηδενικό. Η πρωτεΐνη στο ισοηλεκτρικό της σημείο φέρει ίσο αριθμό θετικών και αρνητικών φορτίων και επομένως είναι ηλεκτροστατικά ουδέτερη. Αυτή θεωρούνταν η καλύτερη συνθήκη για την ανάπτυξη αμοιβαίων ηλεκτροστατικών αλληλεπιδράσεων. Επιπλέον, τα περισσότερα μακρομόρια εμφανίζουν την ελάχιστη διαλυτότητα στο ισοηλεκτρικό σημείο ενώ αρκετά δημιουργούν κρυσταλλικό ίζημα σε αυτό. Όμως στατιστικές μελέτες που πραγματοποιήθηκαν σε βάσεις δεδομένων που περιέχουν πληροφορίες σχετικά με τις συνθήκες κρυστάλλωσης των πρωτεϊνών απέκλισαν τη συσχέτιση μεταξύ του ισοηλεκτρικού σημείου και της εμφάνισης κρυστάλλων (G.L. Gilliland, 1994). Μάλιστα στο ισοηλεκτρικό σημείο τείνει να σχηματίζεται άμορφο ίζημα. Τελικά οι περισσότερες πρωτεΐνες, όπως προέκυψε, κρυσταλλώνονται επιτυχώς κοντά στη φυσιολογική τους τιμή ph, συνεπώς αυτή φαίνεται να είναι η καλύτερη επιλογή. Το γεγονός αυτό φέρει το επιπλέον πλεονέκτημα ότι ελαχιστοποιείται ο κίνδυνος μετουσιώσεως της πρωτεΐνης. Μείωση της διαλυτότητας μπορεί επίσης να επιτευχθεί με την προσθήκη διαφόρων παραγόντων στο διάλυμα της πρωτεΐνης. Αυτοί οι παράγοντες είναι γνωστοί ως precipitants και σε αυτούς συμπεριλαμβάνονται τα άλατα, τα υδρόφιλα πολυμερή και οι οργανικοί διαλύτες. 60
62 Η ιοντική ισχύς του πρωτεϊνικού διαλύματος σχετίζεται με την παρουσία κάποιου άλατος. Μέσα σε ένα διάλυμα μπορεί να προστεθεί ένα ή και περισσότερα είδη αλάτων σε μικρές ή μεγάλες συγκεντρώσεις. Τα άλατα μόλις προστεθούν στο διάλυμα διίστανται. Στη συνέχεια, ανάλογα με το σύστημα, υπάρχουν δύο μηχανισμοί δράσης. Κατά τον πρώτο μηχανισμό τα ιόντα του άλατος ανταγωνίζονται τα μόρια της πρωτεΐνης ως προς τα μόρια νερού, με αποτέλεσμα να απομακρύνονται μόρια νερού από την επιφάνεια της πρωτεΐνης και να μειώνουν τη διαλυτότητα. Αυτό το φαινόμενο είναι γνωστό ως salting out, κατά το οποίο η κρυστάλλωση επωφελείται με την προσθήκη άλατος. Κατά τον δεύτερο μηχανισμό τα ιόντα του άλατος δεσμεύονται στην επιφάνεια της πρωτεΐνης και αυξάνουν την υδροφιλικότητά της. Έτσι το πρωτεϊνικό διάλυμα οδεύει προς την ακόρεστη περιοχή και η παρουσία άλατος δεν ευνοεί την κρυστάλλωση. Το φαινόμενο αυτό ονομάζεται salting in και απαιτείται ελάττωση της συγκέντρωσης του άλατος (Ι.Χαμόδρακας 1993, McPherson 2004). Τα πολυμερή αποτελούν έναν επιπλέον παράγοντα που ελαττώνει τη διαλυτότητα των πρωτεϊνών. Το δημοφιλέστερο πολυμερές στα πειράματα κρυστάλλωσης είναι το PEG (polyethylene glycol) καθώς αυξάνει σε πολύ μεγάλο βαθμό το ιξώδες του νερού του διαλύματος, ευνοώντας την κρυστάλλωση σε θερμοκρασίες δωματίου (S. Patel 1996, A. Polson 1964). Είναι πολύ σημαντικό το γεγονός ότι τα πολυμερή ευνοούν την κρυστάλλωση σε συνθήκες δωματίου. Υπερτερούν, ως προς αυτό, σε σχέση με άλλους παράγοντες καθίζησης, καθώς δεν δημιουργούν κίνδυνο μετουσίωσης της πρωτεΐνης. Επιπλέον η προσθήκη πολυμερούς φαίνεται να παράγει καθαρότερα προϊόντα με την προσθήκη αλάτων, ενώ οι κρύσταλλοι αναπτύσσονται σε μικρότερο χρόνο (Ingham 1990, Polson A., 1964). Από μελέτες διαπιστώθηκε ότι η προσθήκη μικρών συγκεντρώσεων πολυμερών μεγάλου μοριακού βάρους προκαλεί τον ίδιο βαθμό καθίζησης με την προσθήκη μεγάλων συγκεντρώσεων πολυμερών μικρού μοριακού βάρους. Όταν οργανικοί διαλύτες προστίθενται στο πρωτεϊνικό διάλυμα τροποποιούν τη διηλεκτρική σταθερά και έτσι καθορίζουν τις αλληλεπιδράσεις που διεξάγονται. Καθώς η συγκέντρωση του οργανικού διαλύτη αυξάνεται μέσα στο πρωτεϊνικό διάλυμα, περισσότερα μόρια διαλύτη δεσμεύονται στις πολικές ομάδες επιφανειακά της πρωτεΐνης, μειώνοντας την πολικότητα της. Κατά συνέπεια οι ελκτικές δυνάμεις μεταξύ των πρωτεϊνικών μορίων πληθαίνουν και ο διαλύτης καθίσταται λιγότερο αποτελεσματικός. Παρατηρείται δηλαδή μείωση της διαλυτότητας της πρωτεΐνης που ευνοεί την εμφάνιση στερεάς κατάστασης. Στα πειράματα κρυστάλλωσης πρωτεϊνών χρησιμοποιούνται συχνότερα διαλύματα αιθανόλης, μεθανόλης, βουτανόλης και ακετόνης, τα οποία όλα εμφανίζουν υδρόφοβες και πολικές περιοχές (S. Englard 1990, Ι. Χαμόδρακας 1993). 61
63 Ο χρόνος είναι η πιο απλή παράμετρος που επηρεάζει την κρυστάλλωση και ευτυχώς η πάροδος του χρόνου επηρεάζει θετικά την κρυσταλλική ανάπτυξη. Κάποιες πρωτεΐνες κρυσταλλώνονται σχεδόν άμεσα αφού προστεθούν στο διάλυμα, ενώ άλλες απαιτούν μεγάλα χρονικά διαστήματα από εβδομάδες έως και μήνες. Για την κρυστάλλωση μιας πρωτεΐνης ακολουθείται μια σειρά πειραμάτων ώστε να βρεθεί το σύνολο των παραμέτρων που είναι κατάλληλες για το συγκεκριμένο σύστημα και οδηγούν σε έναν πρωταρχικό σχηματισμό κρυστάλλων, (Joseph R. Luft, 2001). Προκειμένου να ελεγχθούν πολλές συνθήκες ταυτόχρονα, στα πειράματα κρυστάλλωσης χρησιμοποιούνται crystallization plates. Κάθε ένα από αυτά αποτελείται από μικρά πηγαδάκια στα οποία τοποθετούνται το πρωτεϊνικό διάλυμα και το διάλυμα με τους παράγοντες καθίζησης, σε διαφορετική αναλογία κάθε φορά. Υπάρχουν plates που διαθέτουν 9, 24, 96 ακόμα και 1536 πηγαδάκια ώστε να παρακολουθούνται παράλληλα διαφορετικές συνθήκες. Σχήμα 3.3: Αριστερά: Crystallization plates 96 πηγαδίων, δυο τύπων (Πηγή: Δεξιά: Σχηματική απεικόνιση της διάταξης ενός ρομπότ κρυστάλλωσης (Πηγή: Τέτοια πειράματα συχνά πραγματοποιούνται από ρομπότ κρυστάλλωσης, δηλαδή αυτόματα συστήματα, που απαιτούν πολύ μικρές ποσότητες πρωτεΐνης (1-2μl σε κάθε συνθήκη) για τον εντοπισμό των ευνοϊκότερων συνθηκών κρυστάλλωσης. Στη συνέχεια γίνεται επιλογή των καλύτερων συνθηκών και τα πειράματα επαναλαμβάνονται σε μεγαλύτερη κλίμακα ώστε να γίνει βελτιστοποίηση των συνθηκών και να προκύψουν ποσοτικά και ποιοτικά καλύτεροι κρύσταλλοι, κατάλληλοι για τη διεξαγωγή πειραμάτων ακτίνων-χ. 62
64 3.2 Τεχνικές κρυστάλλωσης Οι τέσσερις βασικές μέθοδοι κρυστάλλωσης που χρησιμοποιούνται σήμερα για την απόκτηση κρυστάλλων είναι μέσω της διάχυσης ατμών (vapor diffusion) και μέσω ελεύθερης διάχυσης μεταξύ επιφανειών (free interference diffusion FID), κρυστάλλωση με διάλυση και κρυστάλλωση με τη μέθοδο batch (Chayen, 2004). Οι μέθοδοι αυτοί διαφέρουν μεταξύ τους ως προς την διαλυτότητα του πρωτεϊνικού διαλύματος και τον τρόπο με τον οποίο εκτίθεται το διάλυμα αυτό στους παράγοντες καθίζησης. Κρυστάλλωση μέσω διάχυσης ατμών. Σε αυτή τη μέθοδο, χρησιμοποιούμε ακόρεστο διάλυμα πρωτεΐνης στο οποίο προσθέτουμε κάποιους ρυθμιστικούς παράγοντες (ph buffer) και τους παράγοντες καθίζησης. Από το διάλυμα αυτό απομονώνουμε μια σταγόνα και την τοποθετούμε σε δοχείο το οποίο περιέχει διάλυμα (reservoir solution) με παρόμοιους παράγοντες, ρυθμιστικούς και καθίζησης, σε υψηλότερες συγκεντρώσεις. Σχήμα 3.4: Η μέθοδος της διάχυσης ατμών. (α) Η τεχνική της κρεμάμενης σταγόνας (hanging drop) και (β) η τεχνική της καθήμενης σταγόνας (sitting drop). Προκειμένου να επέλθει ισορροπία στο σύστημα, μεταξύ της σταγόνας και του διαλύματος πραγματοποιείται ανταλλαγή ατμών και μέσω αυτής της ήπιας διαδικασίας το πρωτεϊνικό διάλυμα από ακόρεστο γίνεται σταδιακά υπέρκορο. Εντός του υπέρκορου πρωτεϊνικού διαλύματος δημιουργούνται πυρήνες κρυστάλλωσης που σηματοδοτούν την πιθανή ανάπτυξη κρυστάλλων. Υπάρχουν δύο τρόποι εφαρμογής της συγκεκριμένης μεθόδου. Στην πρώτη η σταγόνα του πρωτεϊνικού διαλύματος τοποθετείται εσωτερικά του δοχείου, σε μια υπερυψωμένη βάση πάνω από την επιφάνεια του διαλύματος (reservoir 63
65 solution). Η διάταξη αυτή (Σχήμα 3.4α) ονομάζεται sitting drop (μέθοδος καθήμενης σταγόνας). Στη δεύτερη διάταξη, η σταγόνα του πρωτεϊνικού διαλύματος τοποθετείται σε μια μεμβράνη στην εσωτερική οροφή του δοχείου, όπου και συγκρατείται λόγω της επιφανειακής τάσης που δημιουργείται, ώστε να βρίσκεται πάνω από το διάλυμα (reservoir solution). Η διάταξη αυτή (Σχήμα 3.4β) ονομάζεται hanging drop (μέθοδος κρεμάμενης σταγόνας). Κρυστάλλωση μέσω ελεύθερης διάχυσης μεταξύ επιφανειών (free interference diffusion FID). Σε αυτή τη μέθοδο φέρνουμε προσεκτικά σε επαφή το κορεσμένο πρωτεϊνικό διάλυμα και το διάλυμα που περιέχει παράγοντες καθίζησης. Τα δυο διαλύματα αλληλεπιδρούν σταδιακά και στη διεπιφάνεια μεταξύ τους δημιουργούνται τοπικά περιοχές με υπέρκορο διάλυμα στις οποίες εμφανίζονται πυρήνες κρυστάλλωσης. Καθώς η διάχυση συνεχίζεται οι μικροί πυρήνες αναπτύσσονται και μετατρέπονται σε κρυστάλλους. Σχήμα 3.5: Η μέθοδος ελεύθερης διάχυσης μεταξύ επιφανειών (FID) (Πηγή: Mirjam Leunissen, 2001). Όταν τα δυο διαλύματα έχουν διαφορετική διαλυτότητα το διάλυμα αποτελείται από διαχωρίσιμες ζώνες, καθώς τα πιο κορεσμένα διαλύματα καταλαμβάνουν τα κατώτερα στρώματα. Ένα πρόβλημα που πιθανόν να προκύψει σε αυτές τις περιπτώσεις είναι ότι οι πρωτεϊνικοί κρύσταλλοι που αναπτύσσονται στη συνέχεια βυθίζονται σε ζώνες που περιέχουν παράγοντες καθίζησης σε πολύ υψηλή συγκέντρωση. Σε αυτές τις ζώνες η ανάπτυξη συνεχίζεται και εάν ο ρυθμός ανάπτυξης των κρυστάλλων είναι πολύ υψηλός, οι κρύσταλλοι που προκύπτουν δεν είναι καλής ποιότητας (Leunissen, 2001). Κρυστάλλωση μέσω διαπίδυσης (dialysis). Σε αυτή τη μέθοδο μια ημιπερατή μεμβράνη τοποθετείται ανάμεσα στο πρωτεϊνικό διάλυμα και το διάλυμα που περιέχει τους παράγοντες καθίζησης (Σχήμα 3.6). Η συγκέντρωση της 64
66 πρωτεΐνης παραμένει σταθερή καθώς ο όγκος στον οποίο βρίσκεται το διάλυμα δεν μεταβάλλεται. Ωστόσο το πρωτεϊνικό διάλυμα μπορεί να κινηθεί αργά προς το σημείο καθίζησης μέσω της διαπίδυσης που πραγματοποιείται με το διάλυμα που περιέχει σε υψηλή συγκέντρωση τους παράγοντες καθίζησης. Καθώς η διαφορά μεταξύ των συγκεντρώσεων των διαλυμάτων εντός και εκτός της μεμβράνης μειώνεται με την πάροδο του χρόνου, μειώνεται και ο ρυθμός με τον οποίο όλο το σύστημα έρχεται σε ισορροπία. Έτσι αφού εμφανιστούν οι πυρήνες, αναπτύσσονται σε κρυστάλλους με όλο και πιο αργό ρυθμό, γεγονός που επιτρέπει την ενδεχόμενη ανάπτυξη κρυστάλλων καλής ποιότητας. Σχήμα 3.6: Η μέθοδος της διαπίδυσης (dialysis). Το πρωτεϊνικό διάλυμα βρίσκεται, μερικώς απομονωμένο με μια ημιπερατή μεμβράνη, στο εσωτερικό του διαλύματος που περιέχει τους παράγοντες καθίζησης (Πηγή: Mirjam Leunissen, 2001). Η μέθοδος εφαρμόζεται τόσο σε μεγάλη κλίμακα, χρησιμοποιώντας μεγάλους όγκους διαλυμάτων, όσο και σε μικρή κλίμακα, για παράδειγμα μέσα σε γυάλινους τριχοειδείς σωλήνες (capillaries) και ονομάζεται microdialysis. Στα πλεονεκτήματα της μεθόδου συγκαταλέγεται επίσης η διατήρηση της πρωτεϊνικής συγκέντρωσης, έτσι ώστε μια μόνο παράμετρος να μεταβάλλεται κάθε φορά. Έτσι διαχωρίζεται η δράση του κάθε παράγοντα και γίνεται κατανοητός ο τρόπος με τον οποίο καθένας επηρεάζει τη διαδικασία της κρυστάλλωσης. Κρυστάλλωση με τη μέθοδο batch. Σε αντίθεση με τις υπόλοιπες μεθόδους στις οποίες το πρωτεϊνικό διάλυμα αρχικά δεν είναι υπέρκορο αλλά μεταβαίνει σταδιακά σε υπερκορεσμό, ώστε να έρθει σε ισορροπία με το περιβάλλον του, στη μέθοδο batch ο υπερκορεσμός επέρχεται άμεσα κατά την ανάμιξη των διαλυμάτων, (Chayen, 2004). Στη συγκεκριμένη μέθοδο όλα τα συστατικά και των δύο διαλυμάτων αναμιγνύονται στις τελικές τους συγκεντρώσεις, μέσα σε κλειστό δοχείο. Στη συνέχεια το διάλυμα αφήνεται υπό σταθερές συνθήκες. Κάθε ένας από τους παράγοντες καθίζησης του τελικού διαλύματος συμβάλει σε διαφορετικό βαθμό στην διαδικασία της κρυστάλλωσης και η ταυτόχρονη δράση του συνόλου των παραγόντων οδηγεί στην ταχύτατη δημιουργία κρυσταλλικού ιζήματος. Το 65
67 διάλυμα, στο διάγραμμα φάσης, μεταβαίνει άμεσα στην μετασταθή περιοχή όπου εμφανίζονται κρύσταλλοι. Το γεγονός ότι η αλληλεπίδραση μεταξύ των παραγόντων του διαλύματος είναι άμεση σημαίνει ότι κατά τη διάρκεια της κρυστάλλωσης οι συνθήκες δε θα μεταβληθούν έντονα. Το γεγονός αυτό, αφενός είναι θετικό γιατί μας επιτρέπει να γνωρίζουμε επακριβώς τις συνθήκες στις οποίες κρυσταλλώθηκε το σύστημα, αφετέρου όμως για την εφαρμογή της μεθόδου απαιτείται να γνωρίζουμε με αρκετή ακρίβεια τις συνθήκες που είναι κατάλληλες για την ανάπτυξη κρυστάλλων στο συγκεκριμένο σύστημα. Σχήμα 3.7: Η μέθοδος batch. Το πρωτεϊνικό διάλυμα αναμιγνύεται με το διάλυμα που περιέχει τους παράγοντες καθίζησης και αφήνεται να κρυσταλλωθεί (Πηγή: Mirjam Leunissen, 2001). Πλεονέκτημα της μεθόδου αποτελεί ότι καθώς τα δείγματα δεν εκτίθενται καθόλου στον αέρα κατά τη διάρκεια της κρυστάλλωσης, προστατεύονται από τους ρύπους που μπορεί να περιέχει ο αέρας. Αυτή η απλή και ταχεία μέθοδος ανάπτυξης κρυστάλλων είναι κατάλληλη για πειράματα περίθλασης από πολυκρυσταλλικά δείγματα, όπου απαιτούνται μεγάλες ποσότητες μικροκρυσταλλικών ιζημάτων. Η πορεία που ακολουθείται στη διαδικασία της κρυστάλλωσης για κάθε μια από τις τέσσερις αυτές μεθόδους φαίνεται στο διάγραμμα του σχήματος
68 Όργανα και μέθοδοι 4. Παραγωγή Ακτίνων-Χ Οι τυπικές αποστάσεις μεταξύ γειτονικών ατόμων σε ένα στερεό είναι της τάξης του 1Å (1Å=10-10 m). Για την ανίχνευση της μικροσκοπικής δομής των στερεών, θα πρέπει το μήκος κύματος της ακτινοβολίας να είναι της ίδιας τάξης μεγέθους. Τέτοια μήκη κύματος αντιστοιχούν σε ενέργειες της τάξης των: (3.1) Αυτές οι ενέργειες είναι χαρακτηριστικές των ακτίνων-χ. Όταν τα ηλεκτρόνια επιταχύνονται από υψηλό δυναμικό V και προσκρούουν σε στόχο ο οποίος αποτελείται από μεταλλικό υλικό μεγάλου ατομικού αριθμού, εκπέμπονται ακτίνες- Χ, τόσο σε συνεχές φάσμα (λόγω της συνεχούς επιβράδυνσης) όσο και στο διακριτό φάσμα (που οφείλεται στην αποδιέγερση των ατόμων του στόχου). Σχήμα 4.1: Σχηματική απεικόνιση παραγωγής των ακτίνων-χ (Πηγή: Στο Σχήμα 4.1 φαίνεται η τομή μιας τυπικής λυχνίας ακτινοβολίας-χ. Η πηγή των ηλεκτρονίων είναι ένα νήμα πυρακτώσεως Βολφραμίου, W (κάθοδος). Λόγω του θερμοηλεκτρικού φαινομένου ηλεκτρόνια αποσπώνται από την κάθοδο και επιταχυνόμενα προσκρούουν πάνω σε μια μεταλλική επιφάνεια χαλκού (Cu) ή Μολυβδενίου (Mo), (άνοδος), παράγοντας ακτινοβολία-χ. Το Σχήμα 3.2 απεικονίζει ένα φάσμα ακτίνων-χ, όπου διακρίνονται το συνεχές και το διακριτό τμήμα του φάσματος. Το συνεχές φάσμα προκύπτει από την επιβράδυνση των ηλεκτρονίων και ονομάζεται ακτινοβολία πέδησης (Bremsstrahlung). Οι χαρακτηριστικές κορυφές του φάσματος προκύπτουν από την αποδιέγερση των ατόμων του στόχου και το μήκος κύματος στο οποίο ανιχνεύεται 67
69 κάθε κορυφή εξαρτάται από τον ατομικό αριθμό Z του στόχου και την μετάβαση που συμβαίνει (ηλεκτρονιακός φλοιός). Σχήμα 4.2: Φάσμα εκπομπής ακτίνων-χ, που προκύπτει από τη σύγκρουση επιταχυνόμενων ηλεκτρονίων με στόχο Μολυβδενίου (Μο). Στο δεύτερο σχήμα φαίνονται σε μεγέθυνση οι χαρακτηριστικές γραμμές εκπομπής (Πηγή: Το ελάχιστο μήκος κύματος του συνεχούς φάσματος προσδιορίζεται από την αρχή διατήρησης της ενέργειας, ως (3.2) Καθώς τα ηλεκτρόνια αλληλεπιδρούν πολύ ισχυρά με την ύλη, όταν η ενέργειά τους είναι χαμηλή, δεν εισχωρούν βαθιά στο δείγμα με αποτέλεσμα οι πληροφορίες που παίρνουμε να αφορούν κυρίως την επιφάνεια. 4.1 Εργαστηριακά περιθλασίμετρα Οι εργαστηριακές διατάξεις παραγωγής ακτινών-χ για τη διεξαγωγή πειραμάτων περίθλασης ονομάζονται περιθλασίμετρα. Τα βασικά μέρη από τα οποία αποτελείται ένα περιθλασίμετρο είναι μια πηγή παραγωγής ακτίνων-χ, ένα γωνιόμετρο και ένας ανιχνευτής ακτινοβολίας (μετρητής Geiger). Η ακτινοβολία που παράγει η πηγή ακτίνων-χ του περιθλασίμετρου, όπως αναλύθηκε στην προηγούμενη ενότητα δεν είναι αυστηρά καθορισμένη, αλλά έχει μήκος κύματος το οποίο κυμαίνεται σε μια μικρή περιοχή τιμών (Σχήμα 4.2). Ένα πείραμα περίθλασης όμως προαπαιτεί τη χρήση ενός συγκεκριμένου μήκους κύματος και για αυτό παρεμβάλλονται μεταξύ της δέσμης και του δείγματος, φίλτρα και μονοχρωμάτορες. Τα φίλτρα που παρεμβάλλονται αποκόπτουν συγκεκριμένα μήκη κύματος. Είναι λεπτού πάχους μέταλλα, τα οποία έχουν ατομικό αριθμό πολύ σχετικό με 68
70 αυτόν του υλικού του στόχου. Συνήθως πρόκειται για το ακριβώς προηγούμενο στοιχείο, στον περιοδικό πίνακα, από αυτό της ανόδου. Στη συνέχεια, καθώς η προσπίπτουσα ακτινοβολία εισέρχεται στο μονοχρωμάτορα (κρύσταλλικός γραφίτης), αναλύεται και διαδοχικά επιλέγεται μια καθορισμένη στενή φασματική περιοχή Δλ με κεντρικό μήκος κύματος λ. Αυτή η συνιστώσα της ακτινοβολίας προσπίπτει τελικά στην περιοχή του μετρούμενου δείγματος. Τελικά τα εργαστηριακά περιθλασίμετρα, κατασκευάζονται έτσι ώστε να λαμβάνουν μόνο μια τιμή μήκους κύματος, η οποία εξαρτάται από το υλικό του στόχου. Για την περίπτωση του χαλκού (Cu) που είναι το πιο σύνηθες υλικό στόχου, το μήκος κύματος είναι ίσο με λ= Å. Το σταθερό μήκος κύματος, σε πολλές περιπτώσεις δειγμάτων αποβαίνει περιοριστικός ή και απαγορευτικός παράγοντας για τη λήψη δεδομένων. Στο Σχήμα 4.3 φαίνεται η γεωμετρία της διάταξης. Η θέση της πηγής, παραμένει σταθερή ενώ μεταβάλλονται η κλίση του δείγματος και του ανιχνευτή. Η επιφάνεια του δειγματοφορέα βρίσκεται στο κέντρο ενός κύκλου, του γωνιομετρικού κύκλου, που διέρχεται από το σημείο εκπομπής των ακτίνων-χ και από το σημείο που ανιχνεύονται οι περιθλώμενες ακτίνες-χ. Σχήμα 4.3: Σχηματική αναπαράσταση της διάταξης περιθλασίμετρου το οποίο βασίζεται στη γεωμετρία Bragg-Brettano. Η διακριτική ικανότητα (resolution) του διαγράμματος περίθλασης καθορίζεται από τον χρήστη με κατάλληλη επιλογή του ανοίγματος των διαφραγμάτων σχισμής εντός του κύκλου του γωνιομέτρου, (Πηγή: Αν η γωνία που σχηματίζεται μεταξύ του επιπέδου του δείγματος και της πηγής των ακτίνων-χ είναι θ (γωνία πρόσπτωσης) δηλαδή είναι η γωνία Bragg, η γωνία μεταξύ της αρχικής διεύθυνσης της ακτινοβολίας και του ανιχνευτή θα είναι 2θ. Για αυτό το λόγο η γεωμετρία της συγκεκριμένης διάταξης είναι γνωστή ως θ-2θ (Γεωμετρία Bragg-Brentano). Κατά την περιστροφή του δείγματος η ακτινοβολία συναντά διαδοχικά κρυσταλλογραφικά επίπεδα, από όλους τους κρυστάλλους, κάποια εκ των οποίων ικανοποιούν τη συνθήκη Bragg σε συγκεκριμένες γωνίες 2θ και σκεδάζουν ισχυρά 69
71 την ακτινοβολία. Παράλληλα με το δείγμα, περιστρέφεται και ο ανιχνευτής που καταγράφει την ένταση της σκεδαζόμενης δέσμης συναρτήσει της γωνίας 2θ. Το εύρος των γωνιών 2θ που χρησιμοποιείται σε κάθε πείραμα καθορίζεται από την κρυσταλλική δομή των υλικών και τη χρονική διάρκεια του πειράματος. Υλικά χαμηλότερης κρυσταλλικής συμμετρίας απαιτούν τη λήψη μεγαλύτερου όγκου δεδομένων για τη διεξαγωγή της δομής, άρα αυξημένο εύρος γωνιών. Ένας διαχωρισμός των περιθλασίμετρων πραγματοποιείται με βάση τον αριθμό των δυνατών περιστροφών, με τη βοήθεια των οποίων είναι δυνατή η λήψη και η μέτρηση των ανακλάσεων. Έτσι λοιπόν υπάρχουν περιθλασίμετρα δύο κύκλων και τεσσάρων κύκλων. Σχήμα 4.4: Διάταξη του περιθλασίμετρου (α) δύο κύκλων, (β) τεσσάρων κύκλων (Πηγή: Materials science, Paul Midgley, 12 lectures, University of Cambridge). 4.2 Ακτινοβολία Σύγχροτρον Η ακτινοβολία σύγχροτρον είναι ηλεκτρομαγνητική ακτινοβολία η οποία εκπέμπεται από ηλεκτρόνια τα οποία βρίσκονται μέσα σε ειδικές διατάξεις, τους επιταχυντές σωματιδίων, και κινούνται με σχετικιστικές ταχύτητες, δηλαδή ταχύτητες συγκρίσιμες με αυτή του φωτός. Η υψηλή ταχύτητα που αναπτύσσουν τα ηλεκτρόνια εντός του επιταχυντή, αντιστοιχεί σε εκπεμπόμενη ακτινοβολία πολύ υψηλής ενέργειας. Αυτού του τύπου η ακτινοβολία υπερτερεί σε πολλά σημεία σε σύγκριση με την ακτινοβολία που παρέχεται από τα απλά περιθλασίμετρα και έχει συμβάλλει Σχήμα 4.5: Σχηματική απεικόνιση του επιταχυντή σωματιδίων Tantalus στο Πανεπιστήμιο Wisconsin - Madison (Πηγή: 70
72 σημαντικά στη βελτίωση της έρευνας διαφορών επιστημονικών κλάδων. Η πρώτη παρατήρηση εκπομπής ακτινοβολίας σύγχροτρον έγινε το 1946, στα εργαστήρια της General Electric από έναν επιταχυντή σωματιδίων, ενέργειας 70MeV. Είκοσι χρόνια αργότερα τέθηκε σε λειτουργία η δεύτερη διάταξη ενέργειας 240MeV, στο Πανεπιστήμιο του Wisconsin - Madison της Αμερικής, όπου και πραγματοποιήθηκαν τα πρώτα πειράματα περίθλασης πολύ μικρότερης ενεργειακής κλίμακας σε σύγκριση με τα σημερινά δεδομένα. Στο Σχήμα 4.5 διακρίνεται η ακτίνα του επιταχυντή που αντιστοιχεί σε μερικά μόλις μέτρα (m). Σήμερα πλέον οι διατάξεις σύγχροτρον, είναι εγκαταστάσεις πολύ μεγάλου μεγέθους, με δακτυλίους ακτίνας μερικών εκατοντάδων μέτρων. Οι διατάξεις δεύτερης γενιάς που διαθέτουν σήμερα οι περισσότερες εγκαταστάσεις αποτελούνται από μια πηγή ηλεκτρονίων και δύο δακτυλίους (Σχήμα 4.6). Τα ηλεκτρόνια που παράγονται από την πηγή, επιταχύνονται αρχικά από έναν γραμμικό επιταχυντή (linac) ο οποίος συνδέεται με έναν σχετικά μικρό δακτύλιο (booster ring), μέσα στον οποίο τα ηλεκτρόνια επιταχύνονται ακόμη περισσότερο για να εισέλθουν τελικά στο μεγάλο δακτύλιο στον οποίο αποθηκεύονται κινούμενα για αρκετές ώρες σε κυκλικές τροχιές (storage ring). Στη συνέχεια τα ηλεκτρόνια, υπό την επίδραση του μαγνητικού πεδίου, αποκλίνουν από την κυκλική τους τροχιά και Σχήμα 4.6: Απεικόνιση της διάταξης σύγχροτρον. Τα μέρη της διάταξης είναι η πηγή παραγωγής ακτινοβολίας, ο δακτύλιος επιτάχυνσης (booster synchrotron) και ο δακτύλιος αποθήκευσης (storage ring). Περιμετρικά του δακτυλίου αποθήκευσης εξέρχονται, εφαπτομενικά, δέσμες ακτινοβολίας προς αξιοποίηση (Πηγή: εξαναγκάζονται σε μείωση της ταχύτητάς τους με αποτέλεσμα να εκπέμπουν εφαπτομενικά δέσμες ακτίνων-χ. Τα βασικά χαρακτηριστικά αυτού του τύπου ακτινοβολίας είναι ότι πρόκειται για παράλληλη δέσμη φωτός, γραμμικά πολωμένης στο οριζόντιο επίπεδο και κυκλικά πολωμένης πάνω και κάτω από αυτό (χαρακτηριστικό που βρίσκει 71
73 εφαρμογή στα μαγνητικά υλικά), ενώ είναι υψηλής έντασης με μήκη κύματος που καλύπτουν ευρεία περιοχή ενεργειών (που απορρέουν από την επιβράδυνση των ηλεκτρόνιων). Κυρίως η μεγάλη ισχύς της ακτινοβολίας, που αντιστοιχεί σε μικρά μήκη κύματος, αλλά και η δυνατότητα επιλογής του επιθυμητού μήκους κύματος μέσα από ένα συνεχές φάσμα τιμών, καθιστούν αυτού του τύπου την ακτινοβολία απαραίτητο εργαλείο για τη διεξαγωγή πειραμάτων υψηλών απαιτήσεων. Επίσης ένα ακόμη μέγεθος που χαρακτηρίζει την ακτινοβολία είναι η λαμπρότητα (brilliance) η οποία αποτελεί μέτρο της ποιότητάς της. Η λαμπρότητα είναι συνάρτηση της ενέργειας των φωτονίων. Μελέτες και μετατροπές στις διατάξεις σύγχροτρον αποσκοπούν στη διαρκή βελτίωση των χαρακτηριστικών της ακτινοβολίας που παράγεται. Σε αυτές τις μετατροπές συγκαταλέγεται και η προσθήκη μαγνητικών διατάξεων στο δακτύλιο αποθήκευσης η οποία αύξησε σημαντικά τη λαμπρότητα της δέσμης. Τα αποτελέσματα από αυτή την εισαγωγή ήταν τόσο σημαντικά ώστε δημιουργήθηκαν οι πηγές σύγχροτρον τρίτης γενιάς βασισμένες σε αυτή. Η μέγιστη λαμπρότητα από πηγή σύγχροτρον τρίτης γενιάς είναι περίπου φορές μεγαλύτερη από αυτή μιας συμβατικής λυχνίας παραγωγής ακτίνων-χ. Αυτή η εξέλιξη επέτρεψε το σχεδιασμό νέων, πρωτοποριακών πειραμάτων Ευρωπαϊκό Σύγχροτρον ESRF (European Synchrotron Radiation Facility) Παγκοσμίως, η πρώτη πηγή ακτίνων-χ τρίτης γενιάς εμφανίστηκε το 1994 στο Ευρωπαϊκό σύγχροτρον, ESRF, της Γαλλίας. Για την παραγωγή υπεριώδους ακτινοβολίας και ακτίνων-χ μαλακού φάσματος, επαρκούν ενέργειες μικρότερες των 2GeV. Αντιθέτως, για την παραγωγή σκληρών ακτίνων-χ, μήκους κύματος της τάξης των angström (Å) που είναι απαραίτητες για ορισμένους τομείς της φυσικής, της χημείας και της βιολογίας, απαιτούνται υψηλότερες τιμές ενέργειας. Συνολικά σήμερα υπάρχουν τρεις εγκαταστάσεις παραγωγής σκληρών ακτίνων-χ σε λειτουργία: το ESRF στη Grenoble της Γαλλίας (6 GeV), το APS στο Argonne της Αμερικής (7 GeV), και το Spring8 στο Nishi Harima της Ιαπωνίας (8 GeV), (Helliwell, 2006). Η λειτουργία της διάταξης του ESRF έχει ως εξής: Ο γραμμικός επιταχυντής (linac), προσφέρει αρχικά ενέργεια στα ηλεκτρόνια ίση με 200 MeV. Τα ηλεκτρόνια στη συνέχεια εισέρχονται στο δακτύλιο επιτάχυνσης (booster ring) περιφέρειας 300m, από τον οποίο εξέρχεται δέσμη έντασης 200 ma και ενέργειας 6GeV. Η περιφέρεια ολόκληρης της διάταξης, δηλαδή του δακτυλίου αποθήκευσης, αγγίζει τα 844m. Εντός αυτού του δακτυλίου τα ηλεκτρόνια κατευθύνονται από συστοιχίες μαγνητών ώστε να ακλουθούν καμπύλη τροχιά ενώ περιστρέφονται με ρυθμό 35 72
74 10 4 στροφών ανά δευτερόλεπτο. Ολόκληρη η διάταξη βρίσκεται υπό συνθήκες υψηλού κενού, πιέσεως 5 x 10-8 mbar. Όπως σε κάθε διάταξη σύγχροτρον έτσι και στο ESRF, οι δέσμες ακτινοβολίας προς χρήση (beamlines) εξέρχονται εφαπτομενικά του δακτυλίου αποθήκευσης. Γύρω από κάθε εφαπτομενική δέσμη έχουν χτιστεί εργαστήρια διαφόρων εφαρμογών που εκμεταλλεύονται πειραματικά την ακτινοβολία σύγχροτρον. Το Σχήμα 4.7 απεικονίζει τη διάταξη των εγκαταστάσεων του ESRF και τις δέσμες ακτινοβολίας (beamlines). Σε κάθε εργαστήριο αναφέρεται ο τύπος της πηγής ακτινοβολίας: Insertion Devices (ID) ή Bending Magnets (BM). Σχήμα 4.7: Η διάταξη των εργαστηρίων του ESRF, γύρω από τον δακτύλιο αποθήκευσης (Πηγή: Η παραγωγή ακτίνων-χ γίνεται με τη χρήση μαγνητών δύο τύπου. Είτε με μαγνήτες τύπου bending magnets, όπου τα αντίστοιχα εργαστήρια λαμβάνουν ονομασία ΒΜ, είτε με τύπου wigglers και undulators (Attwood 1999, Fitch 2004) που χρησιμοποιούν τα εργαστήρια με επιπλέον διατάξεις παρεμβολής και ονομάζονται ID (Insertion Devices). 73
75 Σχήμα 4.8: Οι δύο τύποι μαγνητών. Αριστερά ο μαγνήτης τύπου bending magnet και δεξιά ο μαγνήτης τύπου undulator. Οι μαγνήτες τύπου undulator, αποτελούνται απο σειρές μαγνητών εναλλασσόμενου μαγνητικού πεδίου εξαναγκάζοντας τα ηλεκτρόνια να διαγράφουν κυματική τροχιά. Οι ακτίνες της δέσμης που εκπέμπονται λόγω αυτής της κίνησης αλληλεπιδρούν μεταξύ τους και συμβάλλουν για να δημιουργήσουν μια πολύ πιο έντονη δέσμη ακτινοβολίας από ότι αυτή των bending magnets. (Πηγή: Καθώς τα ηλεκτρόνια, με τη χρήση μαγνητών, αποκλίνουν από την κυκλική πορεία που είχαν εντός του δακτυλίου αποθήκευσης και επιβραδύνονται, εκπέμπουν εφαπτομενικά δέσμη ακτίνων-χ αυστηρά εστιασμένη στη θέση του δείγματος. Αυτές θεωρούνται και οι παραδοσιακές πηγές ακτινοβολίας σύγχροτρον (ΒΜ), παράγουν όμως ακτινοβολία σχετικά μικρής έντασης. Η μικρότερη πυκνότητα ροής δέσμης που τις χαρακτηρίζει συνεπάγεται περισσότερο χρόνο ακτινοβόλησης του δείγματος για τη λήψη ποιοτικών δεδομένων, γεγονός που τις καθιστά ακατάλληλες για τη μελέτη ευαίσθητων υλικών, όπως είναι τα βιολογικά μακρομόρια. Παρ όλα αυτά οι πηγές αυτές συνεχίζουν να χρησιμοποιούνται καθώς παρουσιάζουν ευρύ φάσμα ενεργειών και είναι εύκολα προσβάσιμες για τους ερευνητές από ότι είναι άλλες πηγές. Από την άλλη, οι διατάξεις παρεμβολής (ID) αποτελούνται από μικρούς μαγνήτες, διαδοχικά τοποθετημένους έτσι ώστε να παρουσιάζουν εναλλασσόμενη πολικότητα. Η κύρια διαφορά μεταξύ των δύο τύπων μαγνητών που ενσωματώνουν αυτές οι διατάξεις εντοπίζεται στο γεγονός ότι οι μεν wigglers εξαναγκάζουν τη δέσμη ηλεκτρονίων σε έντονη ταλάντωση παρέχοντας δέσμη ευρέως φάσματος, ενώ οι undulators παράγουν δέσμη συγκεκριμένων κορυφών στο ενεργειακό φάσμα. Για τη διεξαγωγή των πειραμάτων περίθλασης που παρουσιάζονται στη συγκεκριμένη εργασία χρησιμοποιήθηκε δέσμη από τις πηγές ID11 και ID31 του ESRF, δηλαδή από διατάξεις παρεμβολής. 74
76 Σχήμα 4.9: Απεικόνιση των χαρακτηριστικών της ακτινοβολίας που παράγουν οι διάφοροι τύποι μαγνητών, (a) bending magnet, (b) wiggler και (c) undulator. Οι τύποι ακτινοβολίας που απεικονίζονται διαφέρουν ως προς το εύρος αλλά και την ενέργεια της δέσμης (Πηγή: Soft X-Rays and extreme ultraviolet radiation, D. Attwood, Cambridge University Press, 1999) The Materials Science Beamline ID11 Η πηγή ακτινοβολίας ID11, υψηλής ενέργειας, χρησιμοποιείται για τη διεξαγωγή πειραμάτων περίθλασης υψηλής ευκρίνειας ή για μελέτες απεικόνισης διαφόρων συστημάτων που παρουσιάζουν ενδιαφέρον όσον αφορά τις φυσικές, μηχανικές ή χημικές τους ιδιότητες. Η ακτινοβολία που εξέρχεται από τη συγκεκριμένη διάταξη έχει μεταβαλλόμενο μέγεθος δέσμης με ελάχιστες διαστάσεις 0.2 x 0.05 µm 2 και μέγιστες 1200 x 1000 µm 2, ενώ παρέχει εύρος ενεργειών kev (R. Baruzzo). Όσο σημαντικά είναι τα χαρακτηριστικά της ακτινοβολίας που επιλέγεται, τόσο σημαντική είναι επίσης η χρήση του κατάλληλου ανιχνευτή. Η συγκεκριμένη διάταξη διαθέτει ανιχνευτές που ονομάζονται area detectors. Τέτοιου τύπου ανιχνευτές επιτρέπουν την καταγραφή ολόκληρων των δακτυλίων που παρατηρούνται από το πολυκρυσταλλικό δείγμα, με μια μόνο ακτινοβόληση. Αυτή η ικανότητά τους συντελεί στη δραστική μείωση του χρόνου διεξαγωγής του πειράματος, με αποτέλεσμα το δείγμα να μην προλαβαίνει να καταστραφεί πριν το τέλος της μέτρησης. Επίσης, οι area detectors συλλέγουν πολύ καλής ποιότητας δεδομένα, σε μεγάλες γωνίες περίθλασης 2θ. Αυτό είναι και το σημαντικότερο πλεονέκτημα της χρήσης τους, καθώς η περιοχή των μεγάλων γωνιών παρουσιάζει σημαντικά μειωμένες εντάσεις της περιθλώμενης δέσμης και απαιτεί περισσότερο 75
77 χρόνο για τη συλλογή στατιστικά βελτιωμένων δεδομένων (I. Margiolaki). Παρ όλα αυτά, το μέγεθος του area detector είναι καθορισμένο, για αυτό και τα δεδομένα παρουσιάζουν περιορισμένη ευκρίνεια. Για το ID11 η ευκρίνεια των δεδομένων λαμβάνει οριακή τιμή στα 4.15 Å. Η μέγιστη γωνία στην οποία μπορούμε να διακρίνουμε κορυφές σε ένα διάγραμμα περίθλασης αντιστοιχεί, μέσω του νόμου του Bragg, στην ελάχιστη απόσταση d (d- spacing) που ονομάζεται ευκρίνεια των δεδομένων (Resolution). Μεγαλύτερη ευκρίνεια των δεδομένων ή αλλιώς μικρότερο d- spacing επιτρέπει, κατά την επεξεργασία των δεδομένων, τον προσδιορισμό της δομής με μεγαλύτερη σαφήνεια. The High Resolution Powder Diffraction Beamline ID31 Η πηγή ακτινοβολίας ID31, σχεδιάστηκε για τη λήψη δεδομένων περίθλασης υψηλής γωνιακής ευκρίνειας με πολύ μικρή διάρκεια μέτρησης. Η ακτινοβολία της συγκεκριμένης διάταξης έχει διαστάσεις δέσμης που κυμαίνονται από 50 x 50 µm 2 έως 2.5 x 1.5 mm 2, ενώ παρέχει εύρος ενεργειών 6-62keV. Η ακτινοβολία που παρέχει θεωρείται η καταλληλότερη στον τομέα της κρυσταλλογραφίας πρωτεϊνών, ιδίως όταν χρησιμοποιείται μήκος κύματος λ, μεγαλύτερο του 1 Å. Αρχικά ακτινοβολία παράγεται από τρεις μαγνήτες, τύπου undulators και η εξαιρετικά ευθυγραμμισμένη δέσμη που προκύπτει, προσπίπτει στη συνέχεια σε ένα μονοχρωμάτορα που αποτελείται από διπλό κρύσταλλο πυριτίου (Si), προσανατολισμού 111. Καθώς η δέσμη εξέρχεται από το μονοχρωμάτορα, προσπίπτει, αυστηρά εστιασμένη, στο πολυκρυσταλλικό δείγμα το οποίο είναι τοποθετημένο σε γυάλινο τριχοειδή σωλήνα (glass capillarie). Ένα από τα πιο σπουδαία χαρακτηριστικά αυτού του σταθμού λήψης δεδομένων είναι το σύστημα καταγραφής σήματος το οποίο βρίσκεται στο βραχίονα του περιθλασίμετρου και συλλέγει εντάσεις περίθλασης, συναρτήσει της γωνίας 2θ. Στην περίπτωση αυτή, σε αντίθεση με τον area detector που καταγράφει ολόκληρους τους δακτυλίους της περίθλασης, πραγματοποιείται καταγραφή ενός μόνο τμήματος αυτών των δακτυλίων, που όμως επαρκεί για την επεξεργασία των δεδομένων. Ο βραχίονας του περιθλασίμετρου είναι εξοπλισμένος με 9 αναλυτές δέσμης, που είναι επίσης από πυρίτιο (Si), προσανατολισμού 111 και με κανάλια ανιχνευτών που σαρώνουν την περιοχή των αποτελεσμάτων. Αυτοί οι ανιχνευτές απέχουν μεταξύ τους απόσταση περίπου 2 και καταγράφουν ταυτόχρονα εννέα διαγράμματα περίθλασης, υψηλής ευκρίνειας (Fitch, 2004). 76
78 Σχήμα 4.10: Σχεδιάγραμμα της πειραματικής διάταξης του συστήματος ID31 (Πηγή: Λόγω της ενιαίας κίνησης των εννέα ανιχνευτών σα να ήταν μια μονάδα, τα διαγράμματα περίθλασης συλλέγονται διαδοχικά με βήμα μετατόπισης 2 μεταξύ τους. Ο συνδυασμός των εννέα αναλυτών, που εξαλείφουν τυχόν παραμορφώσεις που εμφανίζουν τα δεδομένα περίθλασης 4, η υψηλή ευθυγράμμιση της δέσμης, καθώς και η εξαιρετική μηχανική ακεραιότητα του συγκεκριμένου συστήματος, έχουν επιφέρει σημαντική βελτίωση στις θέσεις εντοπισμού των κορυφών καθώς και στο εύρος και το σχήμα των κορυφών του διαγράμματος. 5 Αυτά τα χαρακτηριστικά είναι ιδιαιτέρως σημαντικά σε όλες τις κρυσταλλογραφικές μελέτες της δομής πολυκρυσταλλικών δειγμάτων. Σε όλα τα πειράματα μέτρησης πολυκρυσταλλικών δειγμάτων που περιγράφονται παρακάτω, χρησιμοποιήθηκαν τριχοειδείς σωλήνες από γυαλί, διαμέτρου mm. Η διάταξη του περιθλασίμετρου επιτρέπει την περιστροφή των δειγμάτων πριν τη διεξαγωγή του πειράματος, γεγονός που όπως αναφέρθηκε σε προηγούμενη ενότητα, είναι απαραίτητο για την τυχαιοποίηση του προσανατολισμού των κρυστάλλων του δείγματος. Η απόσταση μεταξύ του δείγματος και του ανιχνευτή (sample to detector distance) στα πειράματα μας ήταν 794,7 mm. Τέλος, το ευρύ φάσμα ενεργειών που προσφέρει αυτή η διάταξη, αλλά και η σωστή επιλογή του μεγέθους των τριχοειδών σωλήνων ελαχιστοποιούν την απορρόφηση ακτινοβολίας από το δείγμα, ακόμη και για υλικά που περιέχουν στοιχεία υψηλής ενεργειακής απορρόφησης. 4 Παραμορφώσεις των δεδομένων περίθλασης μπορεί να οφείλονται, για παράδειγμα, στη κακή ευθυγράμμιση του δείγματος ως προς τον άξονα του περιθλασίμετρου. 5 Το σφάλμα του οργάνου για το εύρος των κορυφών θεωρείται στον άξονα 2θ, ενώ για τις θέσεις των κορυφών ορίζεται σε μερικά δέκατα της κλίμακας των millidegree. 77
79 Το εύρος κάθε κορυφής ορίζεται ως το πλάτος που παρουσιάζει η κορυφή στον οριζόντιο άξονα 2θ (σε μοίρες), όταν η ένταση λαμβάνει τιμή ίση με το ήμισυ της μέγιστης έντασης, Ι max /2. Το εύρος αυτό ονομάζεται FWHM (Full Width at Half Maximum). Σχήμα Ελβετικό Σύγχροτρον SLS (Swiss Light Source): MS- X04SA: Materials Science Beamline Επιπλέον πειραματικές μετρήσεις για τη συγκεκριμένη εργασία, πραγματοποιήθηκαν στις εγκαταστάσεις σύγχροτρον της Ελβετίας (SLS), του ερευνητικού ινστιτούτου Paul Scherrer που βρίσκονται στην περιοχή Villigen. Πρόκειται για μια εγκατάσταση σύγχροτρον επίσης τρίτης γενιάς, με δέσμη που χαρακτηρίζεται από υψηλή λαμπρότητα. Η περιφέρεια του δακτυλίου αποθήκευσης είναι 288m ενώ η δέσμη που παρέχει είναι εντάσεως 400 ma και ενέργειας ίσης με 2.4 GeV (Bergamaschi A., et al., 2010). Ο τομέας της επιστήμης των υλικών του SLS (Materials Science Beamline: MS-X04SA) εξειδικεύεται στη διεξαγωγή πειραμάτων περίθλασης πολυκρυσταλλικών δειγμάτων από πρωτεϊνικά μόρια. Για το σκοπό αυτό, διαθέτει ένα εργαστήριο κατάλληλης δέσμης και συστήματος ανίχνευσης, ώστε να επιτυγχάνεται ο μικρότερος δυνατός χρόνος συλλογής δεδομένων, όπως απαιτούν τα βιολογικά μακρομόρια που καταστρέφονται άμεσα κατά την έκθεσή τους στην ακτινοβολία. Η δέσμη που παρέχει το συγκεκριμένο εργαστήριο εξέρχεται από μια διάταξη μαγνητών τύπου wiggler και παράγει συνεχές φάσμα ενεργειών, εύρους 5-40 kev (B. Schmitt, 2003). Προκειμένου ο ανιχνευτής του περιθλασίμετρου να καλύψει τις υψηλές απαιτήσεις πειραμάτων με ευαίσθητα δείγματα, σχεδιάστηκε από το συγκεκριμένο ινστιτούτο, μια νέου τύπου διάταξη ανιχνευτή, που ονομάστηκε MYTHEN (microstrip system for time resolved experiments). Στα προτερήματα του MYTHEN συγκαταλέγονται η υψηλή ικανότητα ανίχνευσης και ο μεγάλος ρυθμός καταγραφής σήματος (rapid acquisition times), της τάξης των 250μs (B. Schmitt, 2003). Η διάταξή του αποτελείται από δύο βραχίονες καταγραφής των εντάσεων που καλύπτουν γωνιακή περιοχή 60 μοιρών μετρημένων σε γωνία 2θ. Αυτό σημαίνει ότι ο ανιχνευτής έχει τη δυνατότητα να καταγράφει ταυτόχρονα σήμα περίθλασης από μια γωνιακή περιοχή συνολικά 120 μοιρών (σε γωνία θ). Για αυτό και η μέτρηση έχει ελάχιστη διάρκεια (Α. Bergamaschi, 2009). 78
80 Σχήμα 4.12: Αριστερά: Ανέγερση του Ελβετικού Σύγχροτρον, SLS (Πηγή: ιστοσελίδα του Ecole Polytechnique Federale De Lausanne, Δεξιά: Φωτογραφία από το εργαστήριο επιστήμης των υλικών στο Ελβετικό σύγχροτρον (SLS). (a) O αναλυτής MYTHEN. (b) Μονοκρυσταλλικός αναλυτής, (c) Η θέση τοποθέτησης του δείγματος. Η δέσμη της ακτινοβολίας έρχεται από τα δεξιά όπου διακρίνεται ο ευθύγραμμος αγωγός (Πηγή: A. Bergamaschi et al., 2009). Τα κανάλια πυριτίου που διαθέτει ο ανιχνευτής απέχουν μεταξύ τους και σε αυτή την περίπτωση, απόσταση περίπου 2 στην κλίμακα γωνιών 2θ. Το σύστημα εσωτερικά περιέχει αέριο ήλιο (He), αντί αέρα, το οποίο συνεισφέρει στη μείωση του θορύβου των δεδομένων που συλλέγονται. 6 6 Το ελάχιστο σφάλμα στο εύρος των κορυφών που οφείλεται στο όργανο, υπολογίζεται σε στον άξονα 2θ. Το σφάλμα αυτό εξαρτάται από την απόσταση δείγματος-ανιχνευτή (760 mm)και επιπλέον αυξάνεται όσο μεγαλύτερη είναι η διάμετρος του τριχοειδούς σωλήνα (capillarie) που επιλέγεται. Σε πειράματα που χρησιμοποιούνται τριχοειδείς σωλήνες διαμέτρου 0.1mm το σφάλμα υπολογίζεται σε
81 5.Πειραματικό Μέρος 5.1 Κρυστάλλωση Οι κρυσταλλώσεις ανθρώπινης ινσουλίνης (η οποία χορηγήθηκε από τη Novo Nordisk A/S) πραγματοποιήθηκαν στο τμήμα Βιολογίας του Πανεπιστημίου Πατρών. Πραγματοποιηθήκαν σειρές κρυσταλλώσεων με προσθήκη ψευδαργύρου (Zn) και με διάφορες οργανικές ουσίες που αποτελούν προσδέτες (ligands) της ινσουλίνης. Σε αυτούς τους προσδέτες συγκαταλέγονται η φαινόλη, μερικά φαινολικά παράγωγα καθώς και το ακετυλοσαλικυλικό οξύ (ασπιρίνη). Συγκεκριμένα χρησιμοποιήθηκαν οι εξής προσδέτες: 1. Phenol 2. Resorcinol 3. 4-Chlororesorcinol 4. 4-Bromoresorcinol 5. Ακετυλοσαλικυλικό οξύ Οι κρυσταλλώσεις έγιναν χρησιμοποιώντας την μέθοδο batch και όλα τα διαλύματα διατηρήθηκαν, σε θερμοκρασία δωματίου. Για κάθε προσδέτη πραγματοποιήθηκαν κρυσταλλώσεις σε ένα εύρος τιμών ph προκειμένου να ελεγχθεί ο τρόπος με τον οποίο επηρεάζει αυτή η παράμετρος την κρυστάλλωση. Για το σκοπό αυτό παρασκευάσθηκαν ρυθμιστικά διαλύματα με διαφορετικές τιμές ph, σταθερού βήματος τα οποία χρησιμοποιήθηκαν σε όλες τις σειρές κρυσταλλώσεων. Τα ρυθμιστικά διαλύματα (buffers) έχουν την ιδιότητα να διατηρούν σταθερό το ph του διαλύματος στο οποίο βρίσκονται, κάτι το οποίο είναι επιθυμητό ώστε να έχουμε σταθερές συνθήκες κρυστάλλωσης. Οι τιμές του ph στις οποίες έγινε έλεγχος των συνθηκών κρυστάλλωσης κυμαίνονταν από 4.00 έως Για το σκοπό αυτό, παρασκευάσθηκαν αρχικά δυο ρυθμιστικά διαλύματα σε αυτές τις δυο ακραίες τιμές ph, τα οποία στη συνέχεια αναμιχθήκαν σε διαφορετικές αναλογίες ώστε να προκύψουν ρυθμιστικά διαλύματα με βήμα ph 0.2. Τα διαλύματα που επιλέχθηκαν ήταν το τρις-ένυδατωμένο δισόξινο φωσφορικό κάλιο (KH 2 PO 4 *3H 2 O) και το δις-ενυδατωμένο όξινο φωσφορικό νάτριο (Na 2 HPO 4 *2H 2 O). Για την παρασκευή τους χρησιμοποιήθηκαν οι ποσότητες που αναγράφονται στον παρακάτω πίνακα, καθώς επίσης αναγράφονται και οι τιμές ph των διαλυμάτων που προέκυψαν όπως μετρήθηκαν πειραματικά: 80
82 Διάλυμα KH 2 PO 4 *3H 2 O Na 2 HPO 4 *2H 2 O Μοριακό βάρος MW (gr/mol) 136, ,99 Μάζα m (gr) 54, ,196 Όγκος V (ml) Συγκέντρωση C (M) 2 2 Διαλύτης dd H 2 O dd H 2 O ph 4,28 8,82 Για τα παραπάνω διαλύματα χρησιμοποιήθηκαν φίλτρα (Filtropur syringe filter, Sarsted) με μέγεθος πόρων 0,20μm. Στη συνέχεια παρασκευάσθηκε το διάλυμα που περιείχε τα ιόντα ψευδαργύρου, Zinc acetate (ZnAc 2 ). Το διάλυμα αυτό απαιτείται ώστε η ινσουλίνη να κρυσταλλωθεί παρουσία ιόντων ψευδαργύρου καθώς αυτά ευθύνονται για τη δημιουργία και τη σταθερότητα των εξαμερών ινσουλίνης. Διάλυμα ZnAc 2 Μοριακό βάρος MW (gr/mol) 219,49 Μάζα m (gr) 0,02195 Όγκος V (ml) 10 Συγκέντρωση C (M) 0,01 Διαλύτης dd H 2 O Επίσης παρασκευάσθηκε διάλυμα το οποίο περιείχε δισθενή ανιόντα, SCN -. Διάλυμα NaSCN Μοριακό βάρος MW (gr/mol) 81,072 Μάζα m (gr) 1,62144 Όγκος V (ml) 2 Συγκέντρωση C (M) 1 Διαλύτης dd H 2 O Για την συγκρυστάλλωση της ινσουλίνης με προσδέτες προετοιμάστηκαν επιπλέον διαλύματα, τα οποία περιείχαν τους προσδέτες αυτούς. Διάλυμα Phenol Resorcinol 4-Chlororesorcinol 4- Bromoresorcinol Ακετυλοσαλικυλικό οξύ Μοριακό βάρος MW (gr/mol) 94,11 110,11 144,56 189,01 180,16 Μάζα m (gr) 1,8822 2,2022 2,8912 3,7802 3,6032 Όγκος V (ml) Συγκέντρωση C (M) Διαλύτης Ethanol dd H 2 O DMSO dd H 2 O DMSO 81
83 Για τα διαλύματα που δε διαλύονταν εύκολα σε νερό χρησιμοποιήθηκε είτε αιθανόλη, είτε ο οργανικός διαλύτης Dimethyl sulfoxide (DMSO). Τα διαλύματα αφού παρασκευάσθηκαν, διατηρήθηκαν σε θερμοκρασία 277Κ (4 ο C). Ομοίως και αυτά τα διαλύματα πέρασαν από φίλτρα μεγέθους πόρων 0.22μm. Αφού προετοιμάσθηκαν όλα τα παραπάνω διαλύματα ακολούθησε η διαδικασία ανάμιξής τους, σε συγκεκριμένες ποσότητες, για την κρυστάλλωση μέσω της μεθόδου batch. Τα ph των διαλυμάτων κρυστάλλωσης μετρήθηκαν πριν από την κρυστάλλωση καθώς και μετά την διεξαγωγή των πειραμάτων περίθλασης και παρατηρήθηκε, στα περισσότερα δείγματα, μια μικρή μετατόπιση προς μεγαλύτερες τιμές ph. Οι τιμές ph που αναφέρονται στην παρούσα εργασία, αποτελούν τη μέση τιμή των δύο παραπάνω μετρήσεων Κρυστάλλωση με Phenol Οι κρυσταλλώσεις πραγματοποιήθηκαν σύμφωνα με τα πρωτόκολλα της φαρμακευτικής εταιρίας Novo Nordisk. Αρχικά παρασκευάσθηκε το διάλυμα ινσουλίνης (insulin solution) για το οποίο αναμίχθηκαν mg ινσουλίνης, σε λυοφιλοποιημένη μορφή, με 21 ml ddh 2 O. Η συγκέντρωση ινσουλίνης στο διάλυμα αυτό προκύπτει ότι είναι 17,6 mg ml -1, όπως επιβεβαιώθηκε και πειραματικά, μέσω φωτομέτρησης. Για την προετοιμασία του πρωτεϊνικού διαλύματος (protein mixture), απομονώθηκαν 17 ml από το διάλυμα της ινσουλίνης, τα οποία τοποθετήθηκαν σε ένα δοχείο falcon και στη συνέχεια προστέθηκαν σε αυτό 1,97 ml διαλύματος Zinc acetate (ZnAc 2 ), συγκέντρωσης 0.01 M καθώς και 0,510 ml Phenol, συγκέντρωσης 2M διαλυμένης σε αιθανόλη, καθαρότητας 100%. Στη συνέχεια το διάλυμα αυτό αφέθηκε σε ηρεμία και μετά από την πάροδο 5 λεπτών προστέθηκαν 0,255 ml διαλύματος NaSCN, συγκέντρωσης 1M. Οι ποσότητες αυτές αναγράφονται συνοπτικά στον παρακάτω πίνακα. Διαλύματα Ποσότητες Insulin Solution 17 ml 0.01 Μ ZnAc 2 1,97 ml 2Μ Phenol 0,510 ml 1Μ NaSCN 0,255 ml Σχήμα 5.1: Η οργανική ένωση Phenol (Πηγή: Το τελικό διάλυμα που προέκυψε ήταν συνολικού όγκου 19,735 ml και η τελική συγκέντρωση της φαινόλης στο διάλυμα ήταν 41 mm. Για την κρυστάλλωση σε εύρος τιμών ph, απομονώθηκε από το συγκεκριμένο διάλυμα 1ml για κάθε συνθήκη στο οποίο προστέθηκαν 250μl ph buffer. Τα δείγματα που πρόεκυψαν διατηρήθηκαν σε θερμοκρασία δωματίου 82
84 (298Κ). Μετά την πάροδο μιας ημέρας τα δείγματα εμφάνισαν κρυστάλλους ινσουλίνης, οι οποίοι αφέθηκαν να αναπτυχθούν μέχρι τα πειράματα περίθλασης. Σχήμα 5.2: Μορφολογία των κρυστάλλων ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με τον οργανικό προσδέτη phenol, όπως μεταβάλλονται με την αύξηση του ph Κρυστάλλωση με Resorcinol Ομοίως και σε αυτόν τον προσδέτη, ακολουθήθηκε το ίδιο πρωτόκολλο όπως περιγράφηκε με τη φαινόλη. Οι ακριβείς ποσότητες που χρησιμοποιήθηκαν αναγράφονται στον παρακάτω πίνακα. Διαλύματα Ποσότητες Insulin Solution 17 ml 0.01 Μ ZnAc 2 1,97 ml 2Μ Resorcinol 0,258 ml 1Μ NaSCN 0,255 ml Σχήμα 5.3: Η οργανική ένωση Resorcinol (Πηγή: Για την κρυστάλλωση σε εύρος τιμών ph, απομονώθηκε από το διάλυμα που προέκυψε 1ml, για κάθε συνθήκη, στο οποίο προστέθηκαν 250μl ph buffer. Τα δείγματα που πρόεκυψαν διατηρήθηκαν σε θερμοκρασία δωματίου (298Κ). Και με τον συγκεκριμένο προσδέτη μετά την πάροδο μιας ημέρας η πλειοψηφία των δειγμάτων εμφάνισε κρυστάλλους ινσουλίνης, οι οποίοι αφέθηκαν να αναπτυχθούν μέχρι τα πειράματα περίθλασης. Σχήμα 5.4: Μορφολογία των κρυστάλλων ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με τον οργανικό προσδέτη resorcinol, όπως μεταβάλλονται με την αύξηση του ph. 83
85 5.1.3 Κρυστάλλωση με 4- Chlororesorcinol Με το ίδιο πρωτόκολλο οι ποσότητες που χρησιμοποιήθηκαν ήταν: Διαλύματα Ποσότητες Insulin Solution 6,9 ml 0.01 Μ ZnAc 2 0,798 ml 2Μ 4-Chlororesorcinol 0,206 ml 1Μ NaSCN 0,103 ml Σχήμα 5.5: Η οργανική ένωση 4-Chlororesorcinol (Πηγή: Για την κρυστάλλωση σε εύρος τιμών ph, απομονώθηκε από το διάλυμα που προέκυψε 1ml, για κάθε συνθήκη, στο οποίο προστέθηκαν 250μl ph buffer. Τα δείγματα που πρόεκυψαν διατηρήθηκαν σε θερμοκρασία δωματίου (298Κ). Και με τον συγκεκριμένο προσδέτη μετά την πάροδο μιας ημέρας η πλειοψηφία των δειγμάτων εμφάνισε κρυστάλλους ινσουλίνης, οι οποίοι αφέθηκαν να αναπτυχθούν μέχρι τα πειράματα περίθλασης. Σχήμα 5.6: Μορφολογία των κρυστάλλων ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με τον οργανικό προσδέτη 4 Chlororesorcinol, όπως μεταβάλλονται με την αύξηση του ph Κρυστάλλωση με 4- Bromoresorcinol Για την κρυστάλλωση, με τον προσδέτη 4- Bromoresorcinol, χρησιμοποιήθηκαν οι ίδιες ακριβώς ποσότητες όπως και προηγουμένως. Τα δείγματα που πρόεκυψαν διατηρήθηκαν σε θερμοκρασία δωματίου (298Κ). Και με τον συγκεκριμένο προσδέτη μετά την πάροδο μιας ημέρας η πλειοψηφία των δειγμάτων εμφάνισε κρυστάλλους ινσουλίνης, οι οποίοι αφέθηκαν να αναπτυχθούν μέχρι τα πειράματα περίθλασης. Σχήμα 5.7: Η οργανική ένωση 4- Bromororesorcinol (Πηγή: 84
86 Σχήμα 5.8: Μορφολογία των κρυστάλλων ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με τον 4- Bromoresorcinol, όπως μεταβάλλονται με την αύξηση του ph Κρυστάλλωση με Ακετυλοσαλικυλικό οξύ Για την κρυστάλλωση, με το ακετυλοσαλικυλικό οξύ, χρησιμοποιήθηκαν οι ίδιες ακριβώς ποσότητες όπως και προηγουμένως. Συνολικά πρόεκυψαν 7 δείγματα τα οποία διατηρήθηκαν σε θερμοκρασία δωματίου (298Κ). Και με τον συγκεκριμένο προσδέτη μετά την πάροδο μιας ημέρας η πλειοψηφία των δειγμάτων εμφάνισε κρυστάλλους ινσουλίνης, οι οποίοι αφέθηκαν να αναπτυχθούν μέχρι τα πειράματα περίθλασης. Σχήμα 5.9: Η οργανική ένωση του ακετυλοσαλικυλικού οξέως (Πηγή: Σχήμα 5.10: Μορφολογία των κρυστάλλων ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με το ακετυλοσαλικυλικό οξύ, όπως μεταβάλλονται με την αύξηση του ph. 85
87 5.2 Προετοιμασία δειγμάτων πριν τη συλλογή δεδομένων περίθλασης ακτίνων-χ Για τη συλλογή δεδομένων περίθλασης, κάθε πολυκρυσταλλικό δείγμα τοποθετήθηκε μέσα σε borosilicate glass capillary. Στη συνέχεια κάθε δείγμα φυγοκεντρήθηκε προκειμένου να επιτευχθεί το μέγιστο δυνατό πακετάρισμα του υλικού στο κάτω άκρο. Η περίσσεια μητρικού υγρού απομακρύνθηκε και τα τριχοειδή σφραγίστηκαν με σιλικόνη (silicone grease) για να αποτραπεί η αφυδάτωση του δείγματος. Οι κρύσταλλοι των μακρομορίων περιέχουν διαλύτη σε μεγάλο ποσοστό (25%- 90%), ο οποίος καταλαμβάνει χώρο γύρω από τα πρωτεϊνικά μόρια. Το μητρικό υγρό δηλαδή, αποτελεί όπως και τα ίδια τα μακρομόρια, μέρος του κρυστάλλου. Ενδεχόμενη αφυδάτωση του δείγματος οδηγεί στην κατάρρευση της κρυσταλλικής δομής. Συνεπώς οι κρύσταλλοι πρέπει να διατηρούνται σε επαφή με το μητρικό υγρό καθ όλη τη διάρκεια συλλογής δεδομένων. Σχήμα 5.11: Διαδικασία προετοιμασίας των δειγμάτων πριν την ακτινοβόληση. Η διαδικασία περιλαμβάνει φυγοκέντρηση του δείγματος, τοποθέτηση σε capillarie, δεύτερη φυγοκέντρηση και απομάκρυνση του μητρικού υγρού. Στη συνεχεια το capillarie κόβεται ώστε να τοποθετηθεί στην υποδοχή του περιθλασίμετρου και τέλος σφραγίζεται (Πηγή: Yves Watier, "Etudes de diffraction de poudres de proteines", 2011). Κάθε δείγμα στη συνέχεια τοποθετήθηκε στο ειδικό γωνιόμετρο στον κεντρικό άξονα του περιθλασίμετρου έτσι ώστε να βρίσκεται σταθερά στο κέντρο της δέσμης ακτίνων-χ κατά τη διάρκεια διεξαγωγής του πειράματος (Σχήμα 5.12). Επόμενο στάδιο, λίγο πριν την ακτινοβόληση του δείγματος, ήταν η περιστροφή του capillariy, με ρυθμό περιστροφής περίπου 1000 rpm, ώστε να εξασφαλισθεί η τυχαιότητα του προσανατολισμού των κρυστάλλων που περιείχε. 86
88 Σχήμα 5.12: (a) Πολυκρυσταλλικό δείγμα τοποθετημένο μέσα γυάλινο capillarie.(b) Η θέση του δείγματος στην πειραματική διάταξη του ID31 (Πηγή: Ines Collings, Report, 2009). Πραγματοποιήθηκε συλλογή δεδομένων από πολλές περιοχές κάθε δείγματος, καθώς το capillary μετακινούνταν περιοδικά, ώστε να εκτίθεται στην ακτινοβολία, κάθε φορά, μια νέα περιοχή. Η σάρωση του δείγματος και η λήψη πολλαπλών διαγραμμάτων περίθλασης, μας εξασφαλίζει στατιστικά βελτιωμένα δεδομένα. Τα δεδομένα συλλέχθησαν σε θερμοκρασία δωματίου. Μετρήσεις πραγματοποιήθηκαν τόσο στο ESRF στα beamlines ID31 και ID11, όσο και στο SLS στη δέσμη επιστήμης υλικών, MS- X04SA. Το μήκος κύματος σε κάθε ένα από τα beamlines ρυθμίστηκε συγκεκριμένα για κάθε πείραμα ως λ 1 = (16) Å, λ 2 = (3) Å & λ 3 = (3) Å για το ID31, λ 3 = (3) Å & λ 4 =0.5339(5) Å για το ID11 και λ 5 =1.3781(2) Å για το MS- X04SA. Τα δεδομένα που συλλέχθησαν από το ID11 επιβεβαίωσαν την επαναληψιμότητα των μετρήσεων που πραγματοποιήθηκαν στο ID31 καθώς και την ομοιογένεια κάθε δείγματος, ενώ τα δεδομένα από το SLS χαρακτηρίζονταν από μικρότερη γωνιακή ευκρίνεια αλλά υψηλότερη στατιστική των δεδομένων ειδικά σε υψηλές γωνίες 2θ. 87
89 Σχήμα 5.13: Σύγκριση διαγραμμάτων περίθλασης τα οποία συλλέχθηκαν στο ESRF από το ID31, (γαλάζιο) και το ID11, (μωβ), από δείγματα ίδιας συμμετρίας. Όπως προκύπτει, τα δεδομένα από το ID31 χαρακτηρίζονται από πολύ σαφείς κορυφές μικρού εύρους, που επιτρέπουν τον ακριβή προσδιορισμό των γωνιών 2θ, ενώ τα δεδομένα από το ID11 έχουν κορυφές μεγαλύτερου εύρους. Τα διαγράμματα που απεικονίζονται προέρχονται από δείγματα ανθρώπινης ινσουλίνης, κρυσταλλωμένων παρουσία Resorcinol, σε παραπλήσια ph~6.7 (space group: C222 1 ). 88
90 Σχήμα 5.14: (a) Σύγκριση διαγραμμάτων περίθλασης τα οποία συλλέχθηκαν από το ID31, ESRF (μπλε) και το MS-X04SA, SLS (πράσινο) από δείγματα ίδιας συμμετρίας. Όπως προκύπτει, τα δεδομένα από το ESRF αποτελούνται από οξείες κορυφές (διάγραμμα b), που επιτρέπουν το σαφή προσδιορισμό των γωνιών 2θ, ενώ τα δεδομένα από το SLS χαρακτηρίζονται από υψηλή στατιστική και λιγότερο θόρυβο (διαγράμμα c), με αποτέλεσμα να διακρίνουμε κορυφές σε πολύ μεγάλες γωνίες 2θ. Τα διαγράμματα που απεικονίζονται προέρχονται από δείγμα ανθρώπινης ινσουλίνης, κρυσταλλωμένης παρουσία 4-Chlororesorcinol, σε ph 5.08 (space group: P2 1 ). 89
91 6. Αποτελέσματα Αφού ολοκληρώθηκε η συλλογή των πειραματικών δεδομένων τα διαγράμματα περίθλασης επεξεργάστηκαν με τη χρήση υπολογιστικών προγραμμάτων. Η ταυτοποίηση κάθε πολυμόρφου (indexing) πραγματοποιήθηκε με το πρόγραμμα DASH (David W.I.F., 1998) στο οποίο χρησιμοποιούνται οι 20 τουλάχιστον πρώτες κορυφές των δεδομένων πολυκρυσταλλικών δειγμάτων. Από τα δεδομένα που εξήχθησαν μπορέσαμε να προσδιορίσουμε τη συμμετρία των κρυστάλλων καθώς και τις πλεγματικές σταθερές που τα χαρακτηρίζουν. Προκειμένου να εξαχθούν αξιόπιστες τιμές πλεγματικών σταθερών και να χαρακτηρισθούν οι συντελεστές που περιγράφουν το σχήμα των κορυφών (peak shape) και το θόρυβο των μετρήσεων (background), τα δεδομένα επεξεργάστηκαν μέσω της μεθόδου Pawley (Pawley, 1981), χρησιμοποιώντας το πρόγραμμα βελτιστοποίησης PRODD (Wright, 2004). Το πρόγραμμα αυτό μέσω της εφαρμογής διαδοχικών υπολογισμών ελαχίστων τετραγώνων, μεταβάλλει τις πλεγματικές σταθερές ώσπου να επιτευχθεί η μέγιστη δυνατή συμφωνία μεταξύ πειραματικών μετρήσεων και των θεωρητικών υπολογισμών που πραγματοποιούνται. Η συμφωνία αυτή εκφράζεται μέσω των μεγεθών x 2 και R wp που αντιστοιχούν σε ένα σύνολο μαθηματικών εξισώσεων. Στη συνέχεια παρατίθενται τα αποτελέσματα όπως προέκυψαν από την επεξεργασία των δεδομένων. Καθώς όμως πραγματοποιήθηκαν αρκετές σειρές πειραμάτων για δείγματα που προέκυψαν με τις ίδιες συνθήκες, προκειμένου να επιβεβαιώσουμε την αξιοπιστία και την επαναληψιμότητα των αποτελεσμάτων, αναφέρονται αντιπροσωπευτικά για κάθε συνθήκη τα αποτελέσματα σε ένα εκ των πειραμάτων. Κρυστάλλωση με Phenol και Resorcinol Από την ανάλυση των δεδομένων περίθλασης που προέκυψαν από δείγματα ανθρώπινης ινσουλίνης συγκρυσταλλωμένης με Phenol και Resorcinol παρατηρήθηκαν παραπλήσιες συμμετρίες για αυτό και τα αποτελέσματα παρατίθενται μαζί. Η κρυστάλλωση της ινσουλίνης με Phenol ανέδειξε τέσσερις διαφορετικούς τύπους συμμετρίας με την αύξηση της τιμής του ph. Τα Space groups που ταυτοποιήθηκαν ήταν τα εξής: P2 1(α), C222 1, C2 και P2 1(β), εκ των οποίων το πρώτο χαρακτηρίζεται από σταθερές πλέγματος που δεν έχουν δημοσιευθεί έως σήμερα. Τα δύο πολύμορφα P2 1(α) και P2 1(β) παρότι ανήκουν στην ίδια συμμετρία ομάδας χώρου, χαρακτηρίζονται από διαφορετικές πλεγματικές σταθερές, για αυτό και 90
92 εισάγαμε τους δείκτες (α) και (β) ώστε να διακρίνεται το πολύμορφο στο οποίο αναφερόμαστε κάθε φορά. Ομοίως από τα αποτελέσματα της κρυστάλλωσης με Resorcinol ταυτοποιήθηκαν οι εξής συμμετρίες: P2 1(α), C222 1 και P2 1(β) από τις οποίες προκύπτει ότι παραλείπεται η C2 συμμετρία. Στον επόμενο πίνακα αναγράφονται αναλυτικά οι πλεγματικές σταθερές, η συμμετρία και ο όγκος της θεμελιώδους κυψελίδας σε κάθε τιμή ph των δεδομένων κρυσταλλωσης με Phenol. Επιπλέον αναφέρεται η ευκρίνεια των δεδομένων για κάθε μια από τις συμμετρίες. Οι τιμές στις παρενθέσεις υποδεικνύουν το σφάλμα. Space Group ph a (Å) b (Å) c (Å) β ( ) Όγκος κυψελίδας (Å 3 ) Resolution Range P2 1(α) 5,47 114,518(5) 338,05(1) 49,366(2) 101,452(3) (131) P2 1(α) 5,70 114,682(6) 337,63(2) 49,270(4) 101,555(6) (200) 112,2-7,5 C ,93 60,2151(4) 221,884(1) 228,743(2) (34) C ,14 60,287(1) 221,797(6) 228,812(5) (117) C ,40 60,3633(7) 221,763(3) 228,766(3) (69) 115-7,5 C ,54 60,3917(6) 221,759(3) 228,643(2) (59) C2 6,70 103,000(1) 61,3255(6) 63,582(1) 117,195(2) (9) C2 6,75 103,0115(5) 61,3213(2) 63,5783(4) 117,2244(5) (3) 45,9-5,3 P2 1(β) 7,01 61,4134(5) 61,8494(4) 47,8957(4) 110,7157(7) (2) P2 1(β) 7,26 61,1889(4) 61,8369(3) 47,9198(3) 110,6595(6) (2) P2 1(β) 7,46 61,0920(4) 61,8279(4) 47,9302(4) 110,6253(7) (2) 45-4,4 P2 1(β) 8,11 61,0095(4) 61,8700(3) 47,9820(3) 110,5368(5) (2) P2 1(β) 8,25 61,0130 (5) 61,8896(3) 47,99454(4) 110,4703(7) (2) Πίνακας 6.1 Βελτιστοποιημένες (refined) πλεγματικές σταθερές από κρυστάλλους ινσουλίνης συγκρυσταλλωμένης με phenol στα διάφορα ph, όπως εξήχθησαν από την επεξεργασία των διαγραμμάτων περίθλασης μέσω της μεθόδου Pawley. Τα αποτελέσματα προέκυψαν από το πείραμα που πραγματοποιήθηκε στο ID31 με μήκος κύματος λ= (16) Å. Ο πίνακας περιλαμβάνει και ένα δείγμα σε συμπληρωματικό ph (με γκρι χρώμα) από επόμενο πείραμα που πραγματοποιήθηκε με μήκος κύματος λ= (3) Å. Κατά την αύξηση του ph παρατηρήθηκαν μεταβολές των παραμέτρων που περιγράφονται καλυτέρα μέσω της μεταβολής του όγκου της κυψελίδας. Πιο συγκεκριμένα, στο Space group P2 1(α) παρατηρήθηκε μεταβολή του όγκου κατά ΔV/V i = -0.21%, ενώ στο Space group C222 1 κατά ΔV/V i = 0.19%. Επίσης η μεταβολή 91
93 του όγκου κατά τη μετάβαση από την P2 1(α) φάση στην C222 1, υπολογίστηκε ως ΔV (P21(α) C2221) /V C2221 = 63.5%. Το πολύμορφο C222 1 εμφανίζει πλεγματικές σταθερές παρόμοιες με αυτές των δομών που έχουν κατατεθεί στην PDB με κωδικούς 2ΟΜΟ και 2ΟΜ1 (Norrman, Μ. & Schluckebier,G., 2007). Καθώς η φάση C2 έχει πολύ μικρότερο όγκο θεμελιώδους κυψελίδας σε σχέση με τους κρυστάλλους C222 1, κατά τη μετάβαση παρατηρήθηκε μεταβολή του όγκου της κυψελίδας ίση με ΔV (C2221 C2) /V C2 = %. Εντός του πολυμόρφου C2 η αύξηση του ph προκάλεσε σχεδόν μηδενική μεταβολή του όγκου, ΔV/V i = 0.03%. Το πολύμορφο C2 εμφανίζει πλεγματικές σταθερές παρόμοιες με αυτές των δομών που έχουν κατατεθεί στην PDB με κωδικούς 2ΟLY και 2ΟLZ (Norrman Μ. & Schluckebier G., 2007). Η τρίτη μετάβαση από το C2 στο P2 1(β) πολύμορφο συνοδεύεται από μείωση του όγκου κατά ΔV (C2 P21(β)) /V P21(β) = %. Σε αυτή την κρυσταλλική φάση σημειώθηκε ο μικρότερος όγκος της μοναδιαίας κυψελίδας σε σχέση με όλα τα προηγούμενα πολύμορφα ινσουλίνης κρυσταλλωμένης παρουσία φαινόλης. Εντός του πολυμόρφου P2 1(β) η μεταβολή του όγκου ήταν ΔV/V i = -0.22%. Το πολύμορφο P2 1(β) εμφανίζει πλεγματικές σταθερές παρόμοιες με αυτές των δομών που έχουν κατατεθεί στην PDB με κωδικούς 1EVR και 1EV6 (Smith G.D. et al., 2000). Σχήμα 6.1: Διαγράμματα που δείχνουν τη μεταβολή των κανονικοποιημένων πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με φαινόλη σε αυξανόμενο ph, για τα space group (a) P2 1(α), (b) C222 1, (c) C2 και (d) P2 1(β). Τα μαύρα σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα κόκκινα στον b-άξονα και τα πράσινα στον c-άξονα. Οι τιμές a 0, b 0 και c 0 αντιστοιχούν στις πλεγματικές σταθερές του πρώτου δείγματος στο οποίο εντοπίστηκε το κάθε space group. 92
94 Η ανάλυση των δεδομένων περίθλασης από τα δείγματα ανθρώπινης ινσουλίνης συγκρυσταλλωμένης με τον προσδέτη Resorcinol ανέδειξε τρεις διαφορετικούς τύπους συμμετρίας με την αύξηση της τιμής του ph. Αναλυτικά οι πλεγματικές σταθερές για κάθε δείγμα με την αλλαγή του ph είναι οι εξής: Space Group ph a (Å) b (Å) c (Å) β ( ) Όγκος κυψελίδας (Å 3 ) Resolution Range P2 1(α) 5,29 114,028(8) 335,43(3) 49,211(6) 101,531(8) (293) P2 1(α) 5,46 114,051(5) 334,99(1) 49,398(3) 101,488(4) (154) 112,2-7,5 C ,93 60,4325(2) 220,8862(5) 228,2074(6) (13) C ,13 60,4835(4) 220,916(2) 228,303(2) (39) C ,40 60,5579(7) 220,907(3) 228,320(3) (63) C ,54 60,5864(3) 220,824(1) 228,207(1) (25) C ,75 60,6251(2) 220,7959(6) 228,1699(7) (15) 115-7,5 C ,01 60,6819(3) 220,873(1) 228,191(1) (23) C ,26 60,7273(6) 220,792(2) 228,232(2) (51) C ,45 60,841(1) 220,881(4) 228,559(3) (85) P2 1(β) 7,53 60,9724(4) 61,8540(3) 47,7823(3) 110,1894(5) (2) P2 1(β) 7,74 60,9619(5) 61,8718(4) 47,8235(5) 110,2911(8) (3) 45-4,4 P2 1(β) 8,22 61,0008(4) 62,0041(3) 47,8823(3) 110,0465(5) (2) Πίνακας 6.2: Οι πλεγματικές σταθερές της ινσουλίνης συγκρυσταλλωμένης με resorcinol στα διάφορα ph, όπως εξήχθησαν από την επεξεργασία των διαγραμμάτων περίθλασης. Τα αποτελέσματα προέκυψαν από το πείραμα που πραγματοποιήθηκε στο ID31 με μήκος κύματος λ= (16). Ομοίως και με τον συγκεκριμένο προσδέτη, κατά την αύξηση του ph παρατηρήθηκαν μεταβολές του όγκου της κυψελίδας. Στο Space group P2 1(α) παρατηρήθηκε μεταβολή του όγκου κατά ΔV/V i = -0.29%, δηλαδή μεταβολή ίδιας τάξης μεγέθους με αυτή που είχε παρατηρηθεί και με τη φαινόλη στα αντίστοιχα ph, ενώ στο Space group C222 1 κατά ΔV/V i = 0.68%. H μεταβολή του όγκου κατά τη μετάβαση από την P2 1(α) φάση στην C222 1, στα δεδομένα με resorcinol, υπολογίστηκε ως ΔV (P21(α) C2221) /V C2221= 63.5%. Μεταβαίνοντας από το C222 1 πολύμορφο στο P2 1(β), παρατηρήθηκε πολύ μεγάλη μεταβολή του όγκου της κυψελίδας σε ποσοστό ΔV (C2221 P21(β)) /V P21(β) = %, καθώς και σε αυτήν την περίπτωση το πολύμορφο της P2 1(β) συμμετρίας εμφανίζει το μικρότερο όγκο της μοναδιαίας κυψελίδας σε σχέση με τα προηγούμενα πολύμορφα ινσουλίνης. Εντός του πολυμόρφου P2 1(β) η μεταβολή του όγκου ήταν ίση με ΔV/V i = -0.13%. 93
95 Οι μεταβολές αυτές γίνονται πιο εύκολα αντιληπτές από τα παρακάτω διαγράμματα μεταβολής των πλεγματικών σταθερών συναρτήσει του ph. Σχήμα 6.2: Διαγράμματα απεικόνισης της μεταβολής των κανονικοποιημένων πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με resorcinol σε βαθμιαία αύξηση του ph, για τα space group (a)p2 1(α), (b) C222 1, (c) C2 και (d) P2 1(β). Τα μαύρα σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα κόκκινα στον b-άξονα και τα πράσινα στον c-άξονα. Οι τιμές a 0, b 0 και c 0 αντιστοιχούν στις πλεγματικές σταθερές του πρώτου δείγματος στο οποίο εντοπίστηκε το κάθε space group. Στις εικόνες που ακολουθούν απεικονίζονται τα διαγράμματα περίθλασης. Καθώς οι συμμετρίες που προέκυψαν από τα δύο ligands παρουσιάζουν παραπλήσιες πλεγματικές σταθερές, τα διαγράμματα περίθλασης που συλλέχθηκαν έχουν την ίδια μορφή. 94
96 Intensity (arbitrary units) Intensity (arbitrary units) 8.0x x x x x x x x x x (degrees) Σχήμα 6.3: Pawley fit της νέας P2 1(α) φάσης από δείγμα της ανθρώπινης ινσουλίνης με τον προσδέτη resorcinol σε ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ= (6) Å. Οι μαύρες, κόκκινες και μπλε γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group (degrees) Σχήμα 6.4: Pawley fit της C222 1 φάσης από δείγμα της ανθρώπινης ινσουλίνης με τον προσδέτη resorcinol σε ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ= (16) Å. Οι μαύρες, κόκκινες και μπλε γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. 95
97 Intensity (arbitrary units) Intensity (arbitrary units) (degrees) Σχήμα 6.5: Pawley fit της C2 φάσης από δείγμα της ανθρώπινης ινσουλίνης με τον προσδέτη phenol σε ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ= (16) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. Iobs-Back Icalc-Back (Iobs-Icalc) (degrees) Σχήμα 6.6: Pawley fit της P2 1(β) φάσης από δείγμα της ανθρώπινης ινσουλίνης με τον προσδέτη resorcinol σε ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ= (16) Å. Οι μαύρες, κόκκινες και μπλε γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. 96
98 Το νέο πολύμορφο P2 1(α) Κατά την κρυστάλλωση ανθρώπινης ινσουλίνης παρουσία phenol σε εύρος τιμών ph ή παρουσία resorcinol σε εύρος ph παρατηρήθηκε η εμφάνιση της νέας κρυσταλλικής φάσης μονοκλινούς συμμετρίας η οποία ονομάστηκε P2 1(α). Οι πλεγματικές σταθερές που προσδιορίστηκαν στη συγκεκριμένη συμμετρία δεν έχουν κατατεθεί έως σήμερα, ως πολύμορφο της ινσουλίνης, στη βάση δεδομένων των πρωτεϊνών (PDB). Όπως φαίνεται και από τους παραπάνω πίνακες, οι σταθερές a και b λαμβάνουν πολύ μεγάλες τιμές σε αυτή τη συμμετρία δυσχεραίνοντας τη διαδικασία της ταυτοποίησης (dominant zone problem) καθώς υπάρχει αλληλοεπικάλυψη των κορυφών, ιδιαίτερα στις μικρές γωνίες 2θ. Τελικά, με τη χρήση των κανόνων των συστηματικών κατασβέσεων προέκυψε ότι το διάγραμμα περίθλασης ανήκει πράγματι στην P2 1 συμμετρία, καθώς η παρουσία των ανακλάσεων (020), (040), (060) και (080) και η απουσία των (030), (050) και (070) στα δεδομένα (Σχήμα 6.5), επιβεβαιώνουν την ύπαρξη ενός screw axis. Σχήμα 6.7: Αριστερά: Pawley fit στην περιοχή των μικρών γωνιών 2θ του πολυμόρφου P2 1(α) της ανθρώπινης ινσουλίνης από δείγμα κρυσταλλωμένο με resorcinol στο ph Λόγω του πολύ μεγάλου b-άξονα πολλές ανακλάσεις δε διακρίνονται εύκολα, λόγω της αλληλοεπικάλυψης των κορυφών. Δεξιά: Pawley fit των κορυφών που ανήκουν σε μικρές γωνίες, στις οποίες μόνο οι κύριες ανακλάσεις (hk0) που προέρχονται από τους άξονες a και b χρησιμοποιήθηκαν, ενώ διακρίνονται και οι επιπλέον κορυφές που οφείλονται στον μικρότερο c-άξονα. Οι κάθετες μαύρες γραμμές αντιστοιχούν στις θεωρητικές hk0 ανακλάσεις Bragg. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα. 97
99 Κρυστάλλωση με 4- Chlororesorcinol Η ανάλυση των δεδομένων περίθλασης από τα δείγματα ανθρώπινης ινσουλίνης συγκρυσταλλωμένης με τον προσδέτη 4- Chlororesorcinol ανέδειξε τρεις διαφορετικούς τύπους συμμετρίας με την αύξηση της τιμής του ph. Τα Space groups που ταυτοποιήθηκαν ήταν: P2 1(γ), C2 και P2 1(β). Και σε αυτά τα δεδομένα παρατηρήθηκε η εμφάνιση της νέας κρυσταλλικής φάσης, επίσης μονοκλινούς συμμετρίας, η οποία ονομάστηκε P2 1(γ) ώστε να τη διακρίνουμε από τις προηγούμενες φάσεις επίσης μονοκλινούς συμμετρίας. Οι πλεγματικές σταθερές που ταυτοποιήθηκαν στη συγκεκριμένη συμμετρία δεν έχουν κατατεθεί έως σήμερα, ως πολύμορφο της ινσουλίνης, στη βάση δεδομένων των πρωτεϊνών (PDB). Αναλυτικά οι πλεγματικές σταθερές για κάθε τιμή ph είναι οι εξής: Space Group ph a (Å) b (Å) c (Å) β ( ) Όγκος κυψελίδας (Å 3 ) P2 1(γ) 4,54 87,519(3) 69,885(2) 47,911(2) 106,823(4) (19) Resolution Range P2 1(γ) 4,73 87,396(3) 69,842(2) 47,893(2) 106,700(3) (16) P2 1(γ) 4,9 87,581(4) 69,849(3) 47,957(3) 106,851(5) (25) P2 1(γ) 5,08 87,615(3) 69,875(2) 47,968(3) 106,895(3) (20) 46,4-7,3 P2 1(γ) 5,25 87,607(4) 69,868(2) 48,016(3) 106,997(4) (21) P2 1(γ) 5,43 87,237(6) 69,708(3) 47,534(5) 107,478(6) (35) C2 5,81 100,70(1) 61,569(5) 62,167(8) 115,47(1) (64) C2 6,16 103,106(9) 61,505(3) 63,342(8) 117,13(1) (60) C2 6,33 102,967(9) 61,376(3) 63,312(8) 117,18(1) (59) 46,4-7,8 C2 6,51 103,062(5) 61,363(2) 63,297(5) 117,139(6) (34) P2 1(β) 6,69 57,572(8) 65,21(2) 47,38(2) 114,86(3) (73) P2 1(β) 6,83 61,919(1) 62,380(3) 47,794(3) 112,966(4) (12) P2 1(β) 6,92 61,930(3) 62,372(6) 47,923(6) 113,041(1) (27) 46,4-6,8 P2 1(β) 7,05 62,005(3) 62,382(5) 47,956(5) 113,125(6) (23) P2 1(β) 7,7 62,335(2) 63,193(3) 48,101(3) 114,748(4) (12) Πίνακας 6.3: Βελτιστοποιημένες πλεγματικές σταθερές από κρυστάλλους ανθρώπινης ινσουλίνης με 4- Chlororesorcinol όπως εξήχθησαν από την επεξεργασία μέσω της μεθόδου Pawley. Τα αποτελέσματα προέκυψαν από δεδομένα που συλλέχθηκαν από το MS- X04SA, του SLS, με μήκος κύματος λ= (2) Å. 98
100 Στο Space group P2 1(γ) παρατηρήθηκε μεταβολή του όγκου, με την αύξηση του ph κατά ΔV/V i = -1.70%, ενώ στο Space group C2 κατά ΔV/V i = 2.37%. H μεταβολή του όγκου κατά τη μετάβαση από την P2 1(α) φάση στην C222 1, στα δεδομένα με τον προσδέτη 4- Chlororesorcinol, υπολογίστηκε ως ΔV (P21(α) C2221) /V C2221 = 26.21%. Μεταβαίνοντας από το C2 πολύμορφο στο P2 1(β), παρατηρήθηκε έντονη μεταβολή του όγκου της κυψελίδας σε ποσοστό ΔV (C2 P21(β)) /V P21(β) = %, ενώ και σε αυτήν την περίπτωση το πολύμορφο της P2 1(β) συμμετρίας εμφανίζει το μικρότερο όγκο της μοναδιαίας κυψελίδας σε σχέση με τα προηγούμενα πολύμορφα. Εντός του πολυμόρφου P2 1(β) η μεταβολή του όγκου ήταν ίση με ΔV/V i = 6.61%. Σχήμα 6.8: Τα διαγράμματα απεικονίζουν τη μεταβολή των κανονικοποιημένων πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με 4-Chororesorcinol με σταδιακή αύξηση του ph, για τα space group (a) P2 1(γ), (b) C2 και (c) P2 1(β). Τα μαύρα σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα κόκκινα στον b-άξονα και τα πράσινα στον c-άξονα. Οι τιμές a 0, b 0 και c 0 αντιστοιχούν στις πλεγματικές σταθερές του πρώτου δείγματος στο οποίο εντοπίστηκε το κάθε space group. 99
101 Intensity (arbitrary units) Intensity (arbitrary units) Iobs-back icalc-back I Iobs-back icalc-back Iobs2-Icalc (degrees) Σχήμα 6.9: Pawley fit της P2 1(γ) φάσης από δείγμα ανθρώπινης ινσουλίνης με 4- Chlororesorcinol στο ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ=1.3781(2) Å. Οι μαύρες, κόκκινες και μπλε γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group (degrees) Σχήμα 6.10: Pawley fit της C2 φάσης από δείγμα ανθρώπινης ινσουλίνης με 4- Chlororesorcinol στο ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ=1.3781(2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. 100
102 Intensity (arbitrary units) F G H (degrees) Σχήμα 6.11: Pawley fit της P2 1(β) φάσης από δείγμα ανθρώπινης ινσουλίνης με 4- Chlororesorcinol στο ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ=1.3781(2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. Όπως φαίνεται από τα διαγράμματα περίθλασης τα δεδομένα εμφανίζουν υψηλό background. Αυτό οφείλεται στον άμορφο διαλύτη που περιέχεται στο εσωτερικό των κρυστάλλων. 101
103 Κρυστάλλωση με 4- Bromoresorcinol Η ανάλυση των δεδομένων περίθλασης από τα δείγματα ανθρώπινης ινσουλίνης συγκρυσταλλωμένης με τον προσδέτη 4- Bromoresorcinol ανέδειξε δύο τύπους συμμετρίας με την αύξηση της τιμής του ph. Τα Space groups που ταυτοποιήθηκαν ήταν: P2 1(γ) και P2 1(β) σε παραπλήσια ph με αυτά που εμφανίστηκαν για τον προσδέτη 4- Chlororesorcinol. Αναλυτικά οι πλεγματικές σταθερές για κάθε τιμή ph είναι οι εξής: Space Group ph a (Å) b (Å) c (Å) β ( ) Όγκος κυψελίδας (Å 3 ) Resolution Range P2 1(γ) 4,55 87,371(3) 70,029(2) 47,977(2) 106,459(3) (15) P2 1(γ) 4,89 87,428(3) 70,088(2) 47,100(2) 106,599(3) (17) P2 1(γ) 5,05 87,002(7) 69,658(5) 47,733(5) 106,836(7) (42) 46,3-7,7 P2 1(γ) 5,44 87,265(6) 70,124(4) 48,037(4) 106,643(6) (34) P2 1(β) 6,47 62,348(5) 61,983(3) 47,658(5) 113,419(7) (22) P2 1(β) 6,67 62,51(2) 62,34(1) 47,69(2) 113,61(3) (99) P2 1(β) 6,84 62,495(8) 62,167(6) 47,878(8) 113,62(1) (40) 44,9-6,93 P2 1(β) 7,01 62,814(4) 62,117(2) 48,131(3) 113,254(6) (18) P2 1(β) 7,17 62,701(5) 62,332(3) 47,888(5) 113,892(8) (22) Πίνακας 6.4: Οι πλεγματικές σταθερές της ινσουλίνης συγκρυσταλλωμένης με 4- Bromoresorcinol στα διάφορα ph, όπως εξήχθησαν από την επεξεργασία των διαγραμμάτων περίθλασης. Τα αποτελέσματα προέκυψαν από το πείραμα που πραγματοποιήθηκε στο MS- X04SA, του SLS, με μήκος κύματος λ= (2) Å. Δυστυχώς τα κρυσταλλογραφικά δεδομένα στις κεντρικές τιμές ph ( ) αλλά και στις ακραίες τιμές ph ( ) δεν μπόρεσαν να ταυτοποιηθούν καθώς τα διαγράμματα περίθλασης ήταν αρκετά ελλιπή σε αυτές τις περιοχές. Η ανάλυση τους πιθανόν να οδηγούσε σε ίδια αποτελέσματα συμμετρίας με αυτά που παρατηρήθηκαν για το 4-Chlororesorcinol, καθώς οι μέχρι τώρα αναλύσεις μεταξύ των δυο προσδετών εμφανίζουν μεγάλη συμφωνία. Οι μεταβολές των παραμέτρων στο πρώτο Space group P2 1(γ), με την αύξηση του ph κατά μια μονάδα περίπου, ήταν αμελητέες, καθώς η ποσοστιαία μεταβολή του όγκου της κυψελίδας, υπολογίστηκε ίση με ΔV/V i = 0.04%. H μεταβολή του όγκου κατά τη μετάβαση από την P2 1(γ) φάση στην P2 1(β), υπολογίστηκε ως ΔV (P21(γ) 102
104 Intensity (arbitrary units) P21(β))/V P21(β) = % καθώς το πολύμορφο P2 1(β) εμφανίζει μικρότερες πλεγματικές σταθερές. Εντός του πολυμόρφου P2 1(β) αύξηση της τιμής του ph, μικρότερης της μονάδας, προκάλεσε ποσοστιαία μεταβολή του όγκου ίση με ΔV/V i = 1.25%. Σχήμα 6.12: Μεταβολή των κανονικοποιημένων πλεγματικών σταθερών της ανθρώπινης ινσουλίνης, κρυσταλλωμένης με 4-Bromoresorcinol με βαθμιαία αύξηση του ph, για τα space group (a) P2 1(γ) και (b) P2 1(β). Τα μαύρα σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα κόκκινα στον b-άξονα και τα πράσινα στον c-άξονα. Οι τιμές a 0, b 0 και c 0 αντιστοιχούν στις πλεγματικές σταθερές του πρώτου δείγματος στο οποίο εντοπίστηκε το κάθε space group Iobs-back icalc-back Iobs2-Icalc2 Iobs-back icalc-back iobs - i calc zoom (degrees) Σχήμα 6.13: Pawley fit της P2 1(γ) φάσης από δείγμα ανθρώπινης ινσουλίνης με 4- Bromoresorcinol στο ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ=1.3781(2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. 103
105 Intensity (arbitrary units) F G I (degrees) Σχήμα 6.14: Pawley fit της P2 1(β) φάσης από δείγμα ανθρώπινης ινσουλίνης με 4- Bromoresorcinol στο ph Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ=1.3781(2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. 104
106 Κρυστάλλωση με Ακετυλοσαλικυλικό οξύ Τα δείγματα της ανθρώπινης ινσουλίνης συγκρυσταλλωμένης με ακετυλοσαλικυλικό οξύ στις ακραίες τιμές ph δεν εμφάνισαν κρυστάλλους. Η έλλειψη της κρυσταλλικότητας επιβεβαιώθηκε από τα διαγράμματα περίθλασης. Από την ανάλυση των δεδομένων περίθλασης στα ενδιάμεσα ph ταυτοποιήθηκε η R3 συμμετρία. Η σύγκριση μεταξύ των πλεγματικών σταθερών που πρόεκυψαν και των ήδη γνωστών σταθερών για κάθε μια από τις διαμορφώσεις του εξαμερούς (Πίνακας1.1) μας οδήγησε στο συμπέρασμα ότι με αύξηση της τιμής του ph το σύστημα μεταβαίνει από την Τ 6 διαμόρφωση στη T 3 R 3 f διαμόρφωση. Αναλυτικά οι πλεγματικές σταθερές για κάθε τιμή ph είναι οι εξής: Space Group ph Διαμόρφωση a (Å) b (Å) c (Å) γ ( ) Όγκος κυψελίδας (Å 3 ) R3 5,485 Τ 6 82,906(2) 82,906(2) 33,9983(6) (9) R3 5,92 80,963(2) 80,963(2) 34,0267(5) (7) R3 6,975 T 3 R 3 f 80,7013(5) 80,7013(5) 37,5486(2) (2) Resolution Range 42-3,4 R3 7,315 T 3 R 3 f 80,7274(5) 80,7274(5) 37,5423(1) (2) R3 7,42 T 3 R 3 f 80,7191(5) 80,7191(5) 37,5868(2) (2) Πίνακας 6.5: Βελτιστοποιημένες πλεγματικές σταθερές από κρυστάλλους ανθρώπινης ινσουλίνης με ακετυλοσαλικυλικό οξύ, όπως εξήχθησαν από την επεξεργασία μέσω της μεθόδου Pawley. Τα αποτελέσματα προέκυψαν από δεδομένα που συλλέχθηκαν από το ID31 με μήκος κύματος λ= (3) Å. Για την Τ 6 διαμόρφωση το πολύμορφο εμφανίζει παραπλήσιες πλεγματικές σταθερές με το δομικό μοντέλο που είναι καταχωρημένο στην PDB με κωδικό 1MSO (Smith, G.D. et al., 2003), ενώ το πολύμορφο με διαμόρφωση T 3 R 3 f παραπλήσιες με του μοντέλου 1TRZ (Smith G.D., Ciszak E., 1994). Οι μεταβολές των παραμέτρων, κατά τη μετάβαση από την πιθανή Τ 6 διαμόρφωση στην T 3 R 3 f, μετέβαλλαν τον συνολικό όγκο της μοναδιαίας κυψελίδας, σε ποσοστό ΔV/V i = 4.65%. Στο διάγραμμα που ακολουθεί (Σχήμα 6.12) φαίνεται η μεταβολή των πλεγματικών σταθερών συναρτήσει του ph, από το οποίο προκύπτει ότι η αλλαγή στη διαμόρφωση φαίνεται να οφείλεται στην μεταβολή της πλευράς c καθώς οι πλευρές a και b παραμένουν σχεδόν σταθερές. 105
107 Intensity (arbitrary units) Σχήμα 6.15: Μεταβολή των κανονικοποιημένων πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με ακετυλοσαλικυλικό οξύ με βαθμιαία αύξηση του ph, στην R 3 συμμετρία. Τα μαύρα σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα πράσινα στον b-άξονα και τα μοβ στον c-άξονα. Οι τιμές a 0, b 0 και c 0 αντιστοιχούν στις πλεγματικές σταθερές του πρώτου δείγματος στο οποίο εντοπίστηκε το space group io ic io iobs-ba icalc-ba iobs2-ic (degrees) Σχήμα 6.16: Pawley fit της R 3 φάσης από δείγμα ανθρώπινης ινσουλίνης με ακετυλοσαλικυλικό οξύ στο ph (Πιθανή διαμόρφωση εξαμερούς: Τ 6 ). Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ= (3) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. 106
108 Intensity (arbitrary units) i i i (degrees) Σχήμα 6.17: Pawley fit της R 3 φάσης από δείγμα ανθρώπινης ινσουλίνης με ακετυλοσαλικυλικό οξύ στο ph (Πιθανή διαμόρφωση εξαμερούς: Τ 3 R 3 f ). Το διάγραμμα προέκυψε από πειράματα περίθλασης που πραγματοποιήθηκαν με μήκος κύματος λ= (3) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, τη θεωρητική καμπύλη και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες γραμμές αντιστοιχούν στις ανακλάσεις Bragg που αντιστοιχούν στο συγκεκριμένο space group. 107
109 7. Συζήτηση Στην παρούσα εργασία πραγματοποιήθηκε συστηματική μελέτη της πολυμορφικότητας της ινσουλίνης κατά τη μεταβολή των συνθηκών κρυστάλλωσής της. Για το σκοπό αυτό πραγματοποιήθηκαν πειράματα κρυστάλλωσης με τους προσδέτες Phenol, Resorcinol, 4- Chlororesorcinol, 4- Bromoresorcinol καθώς και με το Ακετυλοσαλικυλικό οξύ σε κλίμακα τιμών ph από 4 έως 8.5. Από τα πειράματα αυτά προέκυψαν κρυσταλλικά ιζήματα, τα οποία χρησιμοποιήθηκαν σε πειράματα περίθλασης πολυκρυσταλλικών υλικών με ακτίνες-χ (X-ray powder diffraction), σε εγκαταστάσεις σύγχροτρον. Από την επεξεργασία των δεδομένων περίθλασης επιτεύχθηκε ο προσδιορισμός κάθε κρυσταλλικής φάσης στο επίπεδο της μοναδιαίας κυψελίδας. Συνολικά εντοπίσθηκαν 6 διαφορετικά πολύμορφα, τα οποία κατατάσσονται σε 4 ομάδες συμμετρίας (Space groups: P2 1, C222 1, C2, R3). Τα αποτελέσματα που εξήχθησαν επιβεβαιώνουν την υψηλή πολυμορφικότητα της ινσουλίνης και συνοψίζονται στο παρακάτω διάγραμμα φάσης. Διάγραμμα φάσης της ανθρώπινης ινσουλίνης παρουσία προσδετών, σε συνάρτηση με το ph. Κάθε χρώμα αντιστοιχεί σε ένα διαφορετικό πολύμορφο. Με κόκκινο και γκρι χρώμα απεικονίζονται τα δύο νέα πολύμορφα μονοκλινούς συμμετρίας, P2 1(α) & P2 1(γ), τα οποία εντοπίστηκαν στην παρούσα εργασία. Ενδιαφέρον αποτελεί ο εντοπισμός δύο νέων κρυσταλλικών φάσεων της ινσουλίνης, μονοκλινούς συμμετρίας (P2 1(α) & P2 1(γ) ) οι οποίες εντοπίστηκαν στις χαμηλές τιμές ph της κλίμακας (παρουσία των προσδετών Phenol, Resorcinol & 4- Chlororesorcinol, 4- Bromoresorcinol αντίστοιχα για κάθε φάση). Τα νέα αυτά πολύμορφα ενδέχεται να είναι υψηλής φαρμακευτικής σημασίας καθώς παράλληλα με τη συμμετρία κάθε πολυμόρφου μεταβάλλονται και οι ιδιότητες που αυτό 108
110 παρουσιάζει, αλλά και αντιστρόφως μεταβολή των ιδιοτήτων οδηγεί σε μεταβολή της συμμετρίας. Οι ιδιότητες που μεταβάλλονται είναι φυσικοχημικές και σχετίζονται με την πυκνότητα, τη διαλυτότητα και τη σταθερότητα των κρυστάλλων, δηλαδή ιδιότητες στενά συνδεδεμένες με τη φαρμακευτική δράση κάθε σκευάσματος. Τα πολυκρυσταλλικά διαλύματα ινσουλίνης ήδη σήμερα χρησιμοποιούνται ευρέως σε φαρμακευτικά σκευάσματα λόγω της σταθερότητάς τους και του παρατεταμένου προφίλ δράσης τους (J. Brange, 1992). Κατά συνέπεια ο εντοπισμός νέων πολύμορφων ινσουλίνης θα μπορούσε ενδεχομένως να οδηγήσει στη δημιουργία νέων φαρμακευτικών σκευασμάτων τα οποία να φέρουν διαφορετική δράση ανάλογα με τις ανάγκες των ασθενών ή να σχετίζονται με εναλλακτικούς τρόπους χορήγησης, όπως είναι για παράδειγμα τα σκευάσματα εισπνεόμενης χορήγησης. Επιπλέον, στα αποτελέσματα που προέκυψαν από τα δείγματα με ακετυλοσαλικυλικό οξύ, παρατηρήθηκε μια πολύ ενδιαφέρουσα μεταβολή των πλεγματικών σταθερών των πολυμόρφων που, σύμφωνα με τη βιβλιογραφία, μας οδηγεί στο συμπέρασμα ότι η ινσουλίνη, με αύξηση του ph, μεταβαίνει από την T 6 διαμόρφωση στην T 3 R 3 f διαμόρφωση. Στην παρούσα φάση, συνεχίζουμε την ανάλυση των πειραματικών δεδομένων που παρουσιάζονται σε αυτή την εργασία προκειμένου να επιτευχθεί η πλήρης επίλυση της δομής των πολυμόρφων της ινσουλίνης που παρατηρήθηκαν, καθώς και την εύρεση των θέσεων πρόσδεσης των φαινολικών παραγώγων στο πρωτεϊνικό εξαμερές. Τα αποτελέσματα αυτής της περαιτέρω εργασίας πρόκειται να παρουσιασθούν σε δημοσιεύσεις που βρίσκονται σε στάδιο προετοιμασίας προς υποβολή. 109
111 Βιβλιογραφία Abel J. J., "Crystalline insulin", Proc. Natl. Acad. Sci., Vol. 12, Ashcroft N., "Protein crystallizatin and phase diagrams", Methods, Vol.34, 2004, Attwood D., "Soft X - Rays and extreme ultraviolet radiation", Cambridge University Press, Baruzzo R., Stevanato A., Lamanna G.V., Vaughan G., Wright J.P., Bytchkov A., Curfs C., Gundlach C., Rossat M., Buslaps T., "Laue Laue monochromator for ID11 beamline at ESRF". Basu Sujit K., Govardhan C. P., Jung Chu W., Margolin Alexet L., "Protein crystals for the delivery of biopharmaceuticals", Expert Opinion on Biological Therapy, Vol. 4, No. 3, 2004, Bergamaschi Α., Cervellino A., Dinapoli R., Gozzo F., Henrich B., Johnson I., Mozzanica P. A., Schmitt B., Shi X., "Photon counting microstrip detector for powder diffraction experiments", Nuclear Instruments and Methods in Physics Research A, 2009, Bergamaschi A., Cervellino A., Dinapoli R., Gozzo F., Henrich B., Johnson I., "The MYTHEN detector for X-ray powder diffraction experiments at the Swiss Light Source", Journal of Synchrotron Radiation, Vol. 17, 2010, Bogue R, "The fast-moving world of MEMS technology", Assembly Automation, 2009, Brange J., Havelund S., Hougaard P., "Chemical Stability of Insulin. 1. Hydrolytic Degradation During Storage of Pharmaceutical Preparations", Pharm Res, Vol. 9, 1992, Brange J., Havelund S., Hougaard P., "Chemical stability of insulin. 2. Formation of higher molecular weight transformation products during storage of pharmaceutical preparations", Pharm Res, Vol. 9, 1992, Brage J., "Galenics of insulin", Berlin Heidelberg: Springer- Verlag, Chausmer Arthur B., "Zinc, Insulin and Diabetes", Journal of the American College of Nutrition, Vol. 17, No. 2, 1998, Chayen N.E., "Turning protein crystallisation from an art into a science" (review), Biophysical methods, David W. I. F., Shankland K., Shankland N., Chem. Commun., Vol.8, 1998, Derewenda U., Derewenda Z., Dodson E.J., Dodson G.G., Reynolds C.D., Smith G.D., Sparks C., Swenson D., Nature Lond. 338, 1989, Dodson G., Steiner D., "The role of assembly in insulin's biosynthesis", Current Opinion in Structural Biology, Vol. 8, Issue 2, 1998, Dunn M.F., "Zinc ligand interactions modulate assembly and stability of the insulin hexamer", BioMetals, Vol. 18, 2005,
112 Emdin S.O., Dodson G.G., Cutfield J.M.and Cutfield S.M., "Role of Zinc in Insulin Biosynthesis", Diabetologia 19, 1980, Englard S., Seifter S., "Precipitation Techniques", Methods In Enzymology, Vol. 182, 1990, Fitch A. N., "Journal Res. Natl. Inst. of Standards and Technology", 2004, Vol. 109, Gozzo Fabia, Cervellino Antonio, Leoni Matteo, Scardi Paolo, Bergamaschi Anna, Schmitt Bernd, "Instrumental profile of MYTHEN detector in Debye-Scherrer geometry", Z. Kristallogr., Vol. 225, 2010, Gilliland G.L., Tung M., Blakeslee D.M. and Ladner J.E., NIST/CARB BMC:Biological macromolecule crystallization, database version 3.0: New features, data and the NASA archive for protein crystal, Acta Cryst.D 50, 1994, 408. Hagedorn H.C., Jensen B. N., Krarup N.B., Wodstrup I., "Protamine insulinate", JAMA, Vol. 106, 1936, Halban P. A., R. Mutkoski, G. Dodson & L. Orci, "Resistance of the insulin crystal to lysosomal proteases: implications for pancreatic B-cell crinophagy", Diabetologia, Vol. 30, 1987, Helliwell J., "Synchrotron-radiation instrumentation, methods and scientific utilization", International Tables for Crystallography, Vol. F, Chapter 8.1, 2006, Hill R., J. Appl. Cryst., Vol. 25, 1992, 589. Hull A., "A new method of Chemical Analysis". J. Am. Chem. Soc., Vol. 41(8), 1919, Ingham K.C., "Precipitation of Proteins with Polyethylene Glycol", Methods in Enzymology, Vol. 182, 1990, Joseph R. Luft, J. W., "Macromolecular crystallization in a high throughput laboratory-the search phase", Journal of Crystal Growth, Vol. 232, 2001, Kittel C., "Intoduction to Solid State Physics", John Wiley & Sons Inc., Leunissen Mirjam, "Protein Crystallization", Department of solid state chemistry, Looijenga-Vos A., M. J., "Space-group determination and diffraction symbols", International Tables for Crystallography, Vol. A, Chapter 3.1, 2006, Margiolaki I., Wright J.P., Fitch A.N., Fox G.C., Labrador A., Von Dreele R.B., Miura K., Gozzo F., Schiltz M., Besnard C., Camus F., Pattison P., Beckers D. and Degen T., "Powder diffraction studies on proteins: An overview of data collection approaches", Z. Kristallogr. Suppl, Vol. 26, 2007, Margiolaki I., Thesis, McPherson A., "Introduction to protein crystallization", Methods 34, 2004, Meier W. M., "Space Group Patterns", University College Cardiff Press, Moller K. H., "The Lente insulins", Diabetes, Vol. 5, 1965, Mullin J. W., "Crystallization", Butterworth-Heinemann,
113 Nagalingam S., Vasudevan S., Ramasamy P., Laddha G.S., "Studies On Two- Dimensional Nucleation", Journal of Crystal Growth, Vol. 57, 1982, Norrman M., Stahl K., Schluckebier G., "Characterization of insulin microcrystals using powder diffraction and multivariate data analysis", J.Appl.Cryst, Vol. 39, 2006, Niels C. Kaarsholm, H.-C. K., "Comparison of Solution Structural Flexibility and Zinc Binding Domains for Insulin, Proinsulin, and Miniproinsulin", Biochemistry, Vol. 28,1989, Norrman M., "Crystallographic characterization of insulin microcrystals", Doctoral Dissertation, Lund University, Patel Sam, Cudney Bob, McPherson Alex, "Polymeric Precipitants for the Crystallization Of Macromolecules", Biochemical and Biophysical Research Communications, 1996, Patterson A. L., "A Fourier Series Method for the Determination", Phys. Rev., Vol. 46, Issue 5, Pawley G., "Journal of Applied Crystallography", Vol. 14, 1981, Polson A., Potgieter G.M., Largier J.F., Mears G.E.F.,.Joubert F.J, "The fractionation of Protein Mixtures By linear Polymers of High Molecular Weight", Biohimica et Biophysica Acta, 1964, Rietveld H., Acta Cryst., Vol. 22, 1967, 151. Rietveld H., J. Appl. Cryst. Vol.2, 1969, 65. Robert L. A., Principles of Solid State Physics. Academic Press, Inc., Rossman M.G., Blow D.M., "The detection of sub-units within the crystallographic asymmetric unit", Acta Cryst., Vol. 15, 1962, Schmitt B., Ch. Bronnimann et al., "Mythen Detector System", NuclearInstr. and Methods in Physics Research, Vol. 501, 2003, Sheldrick G.M., Hauptman H.A., Weeks C.M., Miller R., Uson I., "Direct methods- Ab initio phasing", International Tables for Crystallography, Vol. F, Chapter 16.1, 2006, Scott D. A., "Crystalline Insulin", Biochem, Vol. 28(4), 1934, Smith G.D., Swenson D.C., Dodson E.J., Dodson G.G. and Reynolds C.D., "Structural stability in the 4-zinc human insulin hexamer", Proc. Nati. Acad. Sci. USA, Vol. 81, 1984, Watier Y., "Etudes de diffraction de poudres de proteines", Wright J.P., Z.Krist., 2004, Zimmermann H., Burzlaff H., "Space group symbols", International tables for Crystallography, Vol A, Chapter 12.2, 2006, Ι.Χαμόδρακας Σ., Θεματα Μοριακής Βιοφυσικής, Συμμετρία, Ιστοσελίδα ESRF, Ιστοσελίδα Protein Crystallization, Ιστοσελίδα SLS, Καμαράτος Μ., Εισαγωγή στη Φυσική Στερεάς Κατάστασης,
114 Στεργίου Α. Χ., Μέθοδοι Κρυσταλλοδομής. Τμήμα Φυσικής, Α.Π.Θ., Τζανετάκης Π., Σημειώσεις εισαγωγής στη φυσική των ημιαγωγών,
115 Παράρτημα Α: Επιτρεπτά Space Groups για τα πρωτεϊνικά μόρια Chiral Space Groups (List of Hermann Mauguin Space Group Symbols) TRICLINIC P 1 MONOCLINIC P 2 P 2 1 C 2 ORTHORHOMBIC P P P P C C F I I TETRAGONAL P 4 P 4 1 P 4 2 P 4 3 I 4 I 4 1 P P P P P P P P I I TRIGONAL P 3 P 3 1 P 3 2 R 3 P P P P P P R 3 2 HEXAGONAL P 6 P 6 1 P 6 5 P 6 2 P 6 4 P 6 3 P P P P P P CUBIC P 2 3 F 2 3 I 2 3 P I P P F F I P P I
116 Παράρτημα B: Επιστημονική δημοσίευση Structural studies of Human Insulin co-crystallized with Phenol or Resorcinol via Powder Diffraction Fotini Karavassili, a Anastasia E. Giannopoulou, a Eleni Kotsiliti, a Lisa Knight, b Mathias Norrman, c Gerd Schluckebier, c Lene Drube, c Andrew N. Fitch, b Jonathan P. Wright, b & Irene Margiolaki, a a Department of Biology, Section of Genetics, Cell Biology and Development, University of Patras, GR-26500, Patras, Greece. b European Synchrotron Radiation Facility, BP-220, F-38043, Grenoble Cedex 9, France. c Diabetes Protein Engineering, Novo Nordisk A/S, Novo Nordisk Park, DK imargiola@upatras.gr Måløv, Denmark. Abstract The effects of the ligands phenol and resorcinol on the crystallization of human insulin have been investigated as a function of ph. Powder diffraction data were used to characterize several distinct polymorphic forms. A previously unknown polymorph with monoclinic symmetry (P2 1 ) was identified for both kinds of ligands with similar characteristics (lattice parameters for insulin - resorcinol complex: a= (8) Å, b= (3) Å, c= (6) Å and β= (8) ). Keywords: Powder Diffraction; Human Insulin; Synchrotron Radiation; ph variation 1. Introduction Insulin is a small protein built up by two chains which are linked to each other by two disulfide bridges. It is first synthesized as pre-insulin in β-cells, located in the pancreas (Itoh & Okamoto, 1980; Leibowitz et al., 2002). This hormone, due to its biological function (Banting & Best, 1922) is used in the medical treatment of diabetes. The primary administration route is by subcutaneous injections of microcrystals or mixtures of microcrystals and amorphous protein. After the injection, the insulin crystals dissolve slowly, thus leading to a gradual release of insulin into the blood stream (Norrman & Schluckebier, 2007). A crystallographic structure for insulin was first determined in 1969 (Adams et al., 1969). Since then, a number of polymorphs have been identified, crystallizing in various space groups with the most common belonging to the monoclinic, rhombohedral, cubic and tetragonal crystal systems. The determination of the type, size and morphology of the crystals is crucial, as these characteristics affect the speed with which insulin is 115
117 released into the blood stream (Norrman & Schluckebier, 2007). Nowadays, the use of insulin microcrystals in new administration approaches, such as pulmonary delivery, is of great interest to improve treatments for diabetes (Basu et al., 2004). Powder diffraction has been previously exploited as a technique for fingerprinting different human insulin crystalline forms and allowed for the rapid phase identification and quantification of mixtures (Norrman et al., 2006). Highresolution powder instrumentation is designed to obtain the sharpest possible diffraction peaks in reciprocal space and also to determine accurate peak positions (Margiolaki et al., 2007). These features are complementary to area-detector singlecrystal experiments, where the aim is normally to measure diffraction peaks at the highest possible scattering angles, to improve the direct-space resolution in an electron-density map. The first protein structure refinements and solution via the molecular replacement method using powder data were reported by Von Dreele (1999, 2000). The use of high-resolution synchrotron data together with new analysis procedures, has made powder crystallography a powerful complementary method for structural characterization of proteins (Margiolaki, Wright, Fitch et al., 2007; Margiolaki & Wright, 2008). Microcrystalline powders can be obtained for many proteins by batch precipitation (Von Dreele, 2003), which is of great advantage, as growing a suitable single crystal is often a more demanding procedure. Thus powder methods are ideal for the systematic study of crystallization conditions as it is possible to characterize microcrystalline precipitates. However, in the powder technique there is a severe loss of information due to the collapse of the 3-d diffraction pattern onto a single dimension with the accompanying overlap of Bragg peaks which becomes progressively worse at higher scattering angles and complicates structural analysis in comparison to single crystal methods. In this paper, we employ synchrotron X-ray powder diffraction to investigate the effect of ph on the crystallization of human insulin with two different ligands, phenol and resorcinol. Phenol and phenol-like compounds were originally added to insulin preparations as anti-bacterial agents. It turns out that phenol binds to the insulin hexamer and has a dramatic effect on the insulin conformation, driving it to the R-state (Derewenda et al., 1989). The presence of zinc is crucial to the formation and stability of the insulin hexamer, whereas zinc-free solutions of insulin consist of monomers and dimers. A series of phase transitions was observed with ph variation, resulting in four distinct polymorphs in the case of co-crystallization with phenol and three polymorphs with resorcinol. In addition to the already known C222 1, C2 (Norrman & Schluckebier, 2007) and P2 1 (Smith et al., 2000) conformations, a new monoclinic phase of insulin has been found (space group: P2 1 ). Accurate lattice parameters were extracted for all crystalline phases as a function of ph. Human insulin has a remarkably rich phase diagram and polycrystalline precipitates could be obtained 116
118 and studied under a continuous range of crystallization conditions using powder diffraction. 2. Experimental 2.1 Crystallization Human insulin was provided by Novo Nordisk (batch: RO10219A). The crystallization method used was the salting-out procedure in batch. The stock protein solution was prepared by adding mg of as-received freeze-dried insulin to 21 ml of d.d.h 2 O, resulting in a concentration of 17.6 mg ml -1. For the preparation of the protein mixture, 17 ml of the protein solution were extracted and placed in one falcon tube, along with 1.97 ml of 0.01 M zinc acetate (ZnAc 2 ) solution and either ml of 2M phenol diluted in 100% ethanol, or ml of 2M aqueous resorcinol solution. Finally, after 5 minutes of incubation, ml of 1M sodium thiocyanate (NaSCN), was added to the protein mixture. Furthermore, we prepared two buffer samples of 2M Na 2 HPO 4 and KH 2 PO 4 that were mixed in order to set a ph gradient starting from ph 4.0 to 8.9, with a step of roughly 0.3 units. The NaSCN solution was filtered through 0.22 μm filters, whereas the buffer solutions were filtered with 0.20 μm Filtropur filters, before being used. In each sample that was produced, 1.2 ml of the protein mixture and 300 μl of the ph buffer mixture were placed in an eppendorf tube, yielding a final protein concentration of 12.1 mg ml -1. Final resorcinol concentration was 20mM while phenol concentration was 41 mm. The samples were left to crystallize in an incubator at 298K. Over the next few days polycrystalline precipitates were visible at the bottom of the eppendorf tube of each tray, with clear solution above (Figures 1 & 2). The ph of the crystallization solutions was measured before crystallization, as well as after the diffraction experiments and a very small shift toward higher ph values was observed for the majority of the samples. The reported ph levels correspond to the average values of the above measurements X-ray data collection and processing Powder X-ray diffraction data were collected at room temperature with a wavelength of (16) Å using the high-resolution powder diffraction beamline ID31 at ESRF, Grenoble (Fitch, 2004). All samples were loaded into mm diameter borosilicate glass capillaries and centrifuged in order to enhance crystal packing. Excess mother liquor was removed and the capillaries were sealed with silicone vacuum grease to prevent dehydration. The capillaries were mounted on the diffractometer and spun at 1000 rpm to ensure adequate powder averaging. An automatic sample-changing robot was used for loading and unloading all the samples by mounting the capillaries in self-centering magnetic bases. Several scans 117
119 were collected per sample position, with the capillaries being periodically translated axially to expose a fresh region of sample that was unaffected by the synchrotron beam. Radiation damage effects are accompanied by marked changes in lattice parameters, along with gradual increases in peak broadening and can be monitored by comparing the profile measured in each of the nine detector channels during a single scan, as well as by comparing subsequent scans. The first scans, for which the sample had just been translated to expose fresh material, were combined, leading to improved counting statistics without compromising the data quality for structure analysis, while the subsequent scans showed detectable degradation and were employed only to follow the evolution of cell dimensions with increasing exposure time. Additional measurements were performed at the materials science beamline ID11 of the ESRF using an area detector. The samples were mounted using both borosilicate glass capillaries (as above) and Kapton capillaries as described by Von Dreele (2006). Data were collected at room temperature. Two subsequent experiments were performed at wavelengths of (5) Å and (3) Å respectively. The beam was focused using refractive lenses (Vaughan et al, 2011) on the surface of a Frelon4M 2k 2k CCD camera with μm 2 pixel size (Labiche et al., 2007). The sample-detector distance was mm, calibrated using silver behenate (Huang et al., 1993). A series of images was collected with 1 minute exposures at room temperature (RT). The two-dimensional images were transformed into one-dimensional powder diffraction patterns via Fit2D (Hammersley, 1997). Similar patterns were then merged to enhance counting statistics. The area detector data (ID11) verified the reproducibility of our high resolution measurements (ID31) and sample homogeneity. In an area detector image from a crystalline powder sample there is a series of concentric rings as shown in Fig. 3. Each ring represents the set of reflections corresponding to a particular d-spacing in the sample. Smooth rings show that the sample is an ideal powder containing millions of crystallites. Any preferred orientation of the microcrystals would produce intensity variations around the rings with larger crystallites giving dominant diffraction spots. The patterns were typically indexed with the DASH software package (David et al., 1998) using the fitted positions of at least the first 20 reflections, of the powder diffraction profiles collected from the ID31 samples. From the extracted data, we were able to determine the symmetry and unit cell dimensions. For example, a monoclinic C2 unit cell was found for the sample co-crystallized with phenol in ph 6.75, with unit cell parameters a= (5) Å, b= (2) Å, c= (4) Å and β= (5). This phase is in agreement with the monoclinic insulin phase crystallized under similar conditions with the addition of resorcinol and urea in ph 7 (Norrman, & Schluckebier, 2007). In order to obtain reliable values of the lattice parameters and characterize the peak shape and background coefficients 118
120 without a structural model, Pawley (1981) fits were performed using the PRODD profile refinement program (Wright, 2004). 3. Results The unit cell parameters of the crystalline phases obtained with phenol and resorcinol with the evolution of ph are presented in Tables (1) and (2) Novel monoclinic (P2 1 ) phase alpha When human insulin was crystallized with phenol in the ph range of , a novel phase of monoclinic symmetry (space group: P2 1, from now on referred to as P2 1(α) ) was observed. Owing to the very large a and b-axes in comparison to the c axis, indexing suffered from the dominant zone problem (Fig. 4). The indexing of such a unit cell is particularly challenging, since most of the low angle reflections belong to the dominant zone in reciprocal space and many reflections may not be observed due to peak overlap. However, the combined use of ID31 and ID11 data led to the identification of the monoclinic cell P2 1(α) with lattice parameters a= (6) Å, b=337.63(2) Å, c=49.270(4) Å and β= (6). The presence of the (020), (040), (060) and (080) reflections and absences of the (030), (050) and (070) reflections in the ID11 data confirm the existence of a screw axis (Fig.5), where spots from individual crystallites are observed, overcoming the powder overlap problem for these reflections. The Pawley fit to the data was satisfactory with agreement factors (sample crystallized at ph 5.7: R wp = and χ 2 = 2.83). The data acquired from the P2 1(α) crystals extended to a resolution of approximately ~7.5 Å (Fig. 6). The evolution of the normalized unit cell parameters is shown in Fig. 7(a) and of the unit cell volume in Fig. 8(a). This is the first report of this specific crystallographic phase of human insulin. Crystallization of human insulin with resorcinol at ph 5.29 and 5.46 had the essentially same effect as the crystallization screens with phenol and yielded a phase with monoclinic symmetry (space group: P2 1, lattice parameters: a= (8) Å, b= (3) Å, c= (6) Å and β= (8) ). Pawley fits to both datasets were performed in order to extract accurate lattice dimensions, resulting in acceptable agreement factors (sample crystallized at ph 5.29: R wp = 5.7 and x 2 = 1.58). Data obtained from these samples extended to a resolution of ~ 7.5 Å (Fig. 6). The increase of ph from 5.29 to 5.46 resulted in slight increase of the unit cell volume by ΔV/V i = 0.29%. Furthermore, the lattice dimensions of the samples with phenol indicate a larger unit cell than the ones with resorcinol. Structure solution is necessary in order to identify the exact positions of the ligand-binding sites and the effect on the volume of the monoclinic unit cell. The evolution of the normalized lattice dimensions with ph is shown in Fig. 9(a) and that of the unit cell volume in Fig. 8(b). 119
121 3.2. Orthorhombic (C222 1 ) phase Human insulin crystallized in the presence of phenol in the slightly higher ph range of and resorcinol in the slightly higher ph range of , produced crystals with orthorhombic symmetry (space group: C222 1, see tables 1 & 2 for unit cell parameters), containing three protein hexamers per asymmetric unit (asu) (Norrman, Schluckebier, 2007). The data obtained from these samples extended to a resolution of ~ 7.5 Å (Fig.10(a)). In both cases, the increase in ph resulted in minor alterations of the unit cell dimensions and no indication of a first order phase transition. In the case of phenol, this specific variation of ph led to a slight increase in the unit cell volume by ΔV/V i = 0.19% and in the case of resorcinol, there was an increase by ΔV/V i = 0.83%. The lattice parameters of this phase are in good agreement with structural models reported previously with PDB codes 2OM0, 2OM1 (Norrman, Schluckebier, 2007). At ph 5.7 and in the presence of resorcinol, the P2 1(α) and C222 1 phases co-exist. Consequently, the transition from the first crystal type to the second, causes a volume modification of about ΔV (P21(α) C2221)/V P21(α) = 64.70%. The evolution of the normalized lattice parameters for human insulin with phenol and resorcinol is illustrated in Fig. 7(b) and Fig. 9(b) respectively Monoclinic (C2) phase Two samples of insulin crystallized in the presence of phenol at ph 6.70 and 6.75 were found to belong to the monoclinic space group C2 (see Table 1), containing one protein hexamer per asu. The data for this phase extended to a resolution of ~ 5.3 Å (Fig.10(b)) and the results showed that the C2 phase has a smaller unit cell volume compared to the C222 1 crystals, as a result of the large change of the unit cell dimensions. This change resulted in a significant reduction in the unit cell volume by ΔV (C2221 C2) /V i = % approximately, as the space group changed from C222 1 to C2. The evolution of the normalized lattice parameters is shown in Fig. 7(c). The unit cell parameters of this model were very similar to those of models 2OLY and 2OLZ, available on the PDB (Norrman, Schluckebier, 2007). The evolution of the unit cell volume is shown in Fig. 8(a) Monoclinic (P2 1 ) phase beta Samples of human insulin co-crystallized in higher ph values with phenol (ph ) and resorcinol (ph ), caused the formation of crystals with monoclinic symmetry (P2 1, from now on referred to as P2 1(β), see Tables 1 & 2) with one protein hexamer in the asu. The data resolution of these samples extended to approximately ~4.4 Å (Fig.10(c)). This phase has the smallest unit cell volume of all the insulin/phenol polymorphs reported in this study, with the volume decreasing by ΔV (C2 P21(β))/V C2 = % during the phase transition between C2 and P2 1(β). According to Matthews Coefficient calculation the C2 phase contains four hexamers per unit cell and 52% solvent content (Matthews Coefficient= 2.56 Å 3 /Da), whereas 120
122 the P2 1(β) phase contains two hexamers per unit cell and 49.4% solvent content (Matthews Coefficient= 2.43 Å 3 /Da). Furthermore, there is a very small decrease in the unit cell volume within this ph range (by ΔV/V i = -0.22%), which is reflected on the slightly anisotropic lattice parameter evolution observed with the increase of ph (see table 3). This result might be indicative of solvent rearrangements, slight changes of the protein conformation or changes in packing contacts. In the case of co-crystallization with resorcinol, there is also a very small increase in the unit cell volume within the space group, by ΔV/V i = %, which is reflected on the slightly anisotropic lattice parameter evolution observed with the increase of ph (table 3). The unit cell parameters of this phase closely matched the ones of PDB models 1EVR and 1EV6 (Smith, et al., 2000). The evolution of the normalized lattice parameters with ph is shown in Fig. 7(d) and 9(c), for phenol and resorcinol respectively. 4. Discussion Polymorphism of molecular crystals is an important and well researched field (Bernstein, 2002). For macromolecular crystals, insulin serves as a model system due to its biomedical and pharmacological importance and long history of research on crystallization (Abel, 1926, Krayenbühl, 1948, Schlichtkrull 1958, Brange 1992). For wild-type human insulin a large number of different crystal polymorphs have been identified over the last 80 years, often associated with different self-association and allosteric states of the insulin molecule. Microcrystalline insulin suspensions are even after more than 50 years of their existence the most widely used pharmaceutical insulin preparations owing to their stability and their protracted action profile (Brange et al, 1992). These pharmaceutical preparations contain insulin, zinc and a phenolic ligand. Knowledge of the crystallization properties of such mixtures will on the one hand aid in optimization of production processes, but might also lead to the development of novel insulin preparations for alternative delivery, such as sustained release formulations or pulmonary delivery (Basu et al. 2004), as the choice of the right polymorph influences properties such as stability, solubility and bioavailability of insulin crystals. Here we have undertaken a systematic study of the effect of ph on the crystallization behavior of insulin in complex with zinc, the stabilizing zinc ligand thiocyanate and a phenolic ligand, with the surprising and unexpected discovery of an until now not described crystal form of insulin. In the present study, our primary focus is to examine the effects of ph, in addition to co-crystallization with the small organic ligands phenol and resorcinol on the obtained crystal motifs of human insulin. We have made accurate measurements of the evolution of the unit cell parameters with ph, which are illustrated by the smooth anisotropic shifts in the peak positions. Furthermore, the reproducibility of 121
123 these results and the precision of the powder diffraction data have been verified by carrying out multiple crystallization and diffraction experiments at room temperature. The obtained results using different instrumental configurations for improving data accuracy are discussed elsewhere (Margiolaki et al., 2007; Margiolaki & Wright, 2008; Margiolaki, In Press). High resolution powder diffraction measurements have revealed seven distinct phases in total, which correspond to four packing agreements (P2 1(α), C222 1, C2 and P2 1(β) ). The results show that human insulin crystallized in the presence of phenol and resorcinol can be greatly affected by ph. Distinct polymorphs characterized by altered crystallographic symmetries and/or cell dimensions were obtained depending on different ph values (Tables 1 & 2). Insulin crystallized with either of the ligands in the approximate ph of 5.5 forms crystals that assume the novel P2 1(α) symmetry, as shown by the presented data. With the exception of C2 phase which was only observed in co-crystallization with phenol, the rest of the phases obtained coincide in the two crystallization experiments. Although phenol and resorcinol can substitute for each other as allosteric ligands to the insulin hexamer without detectable changes in insulin structure (Smith et al. 2000), the choice of ligand apparently influences crystallization behavior. This is noteworthy, as the phenolic binding site is buried, and does not contribute to crystal contacts. The complete unit cell parameters of the crystalline phases obtained with phenol and resorcinol with the evolution of ph are presented in Tables 4 and 5 (Supplementary Information). Our results demonstrate that systematic screening of crystallization conditions in combination with synchrotron X-ray Powder Diffraction yields an exact and unambiguous picture of insulin s crystallization behavior even around its pi (ca. 5.9), where its solubility is lowest and growth of macroscopic crystals suitable for single crystal X-ray structure determination is less likely to succeed. We believe that this kind of systematic approach further extends the applicability of powder diffraction methods for systematic macromolecular crystal screening in wide range of crystallization conditions. The low instrumental contribution to the diffraction lines and the high precision of the determination of unit cell parameters allowed small variations of the unit cell parameters to be quantified precisely. The use of a systematic variation of sample preparation conditions is likely to be particularly useful for the detection of protein ligand complex formation by variations of ligand concentration (Von Dreele, 2001, 2005). Acknowledgments We would like to thank the ESRF for provision of beam time at the ID31 and ID11 beam lines and Novo Nordisk S/A for the provision of Human Insulin and their valuable advice on crystallization procedures. Irene Margiolaki is grateful to the Unesco L Oreal foundations for the award of the international fellowship for women in life sciences (2010). This research has been co-financed by the European Union (European Regional Development Fund ERDF) and Greek 122
124 national funds through the Operational Program "Regional Operational Programme" of the National Strategic Reference Framework (NSRF) - Research Funding Program: Support for research, technology and innovation actions in Region of Western Greece. Finally, EU FP7 REGPOT CT SEE-DRUG project has supported this work. 123
125 References Abel, J.J. (1926). Proc. Natl. Acad. Sci. U.S.A. 12(2), Adams, M. J., Blundell, T. L., Dodson, E. J., Dodson, G. G., Vijayan, M., Baker, E. N., Harding, M. M., Hodgkin, D. C., Rimmer, B. & Sheat, S. (1969). Nature 224, Banting, F. G. & Best, C. H. (1922). J. Lab. Clin. Med. 7, Basso, S., Fitch, A. N., Fox, G. C., Margiolaki, I. & Wright, J. P. (2005). Acta Cryst. D61, Basu, S.K., Govardhan, C.P., Jung, C.W. & Margolin, A.L. (2004). Expert Opin Biol. Ther. 4, Brange, J., Langkjaer, L., Havelund, S., & Vølund, A. (1992) Pharm Res 9: Bernstein, J. (2002) Polymorphism in Molecular Crystals. Oxford University Press, USA. Boultif, A., Louër, D. (1991). J. Appl. Cryst., 24, Ciszak, E. & Smith, G.D. (1994). Biochemistry 33: Collings, I., Watier, Y., Giffard, M., Dagogo, S., Kahn, R., Bonneté, F., Wright, J. P., Fitch, A. N., Margiolaki I. (2010). Acta Cryst. D66, David, W. I. F., Shankland & K., Shankland, N. (1998). Chem. Commun. 8, David, W. I. F., Shankland, K., van de Streek, J., Pidcock, E., Sam Motherwell, W. D., Cole, J. C. (2006). J. Appl. Cryst., 39, Derewenda, U., Derewenda, Z., Dodson, E.J., Dodson, G.G., Reynolds, C.D., Smith, G.D., Sparks, C. and Swenson, D. (1989). Nature Lond. 338, Dinnebier, R. E., Sieger, P., Nar, H., Shankland, K., David, W. I. F. (2000). J. Pharm. Sci., 89, Durairaj, R. B., Resorcinol: Chemistry, Technology and Applications (2005), 9, Fitch, A. N. (2004). J. Res. Natl Inst. Stand. Technol. 109, Hammersley, A. P. ESRF Internal Report ESRF 97HA02T Huang, T. C., Toraya, H., Blanton, T. N., Wu, Y. (1993). Journal of Applied Crystallography, 26, Itoh, N. & Okamoto, H. (1980). Nature 283, Kaarsholm, N.C., Ko, H.C., and Dunn, M.F. (1989). Biochemistry 28: Kantardjieff, KA., Rupp, B. (2003) Protein Science, 12: Krayenbüh C, Rosenberg,T (1946), Rep Steno Mem Hosp Nord Insulinlab, Labiche, J. C., Mathon, O., Pascarelli, S., Newton, M. A., Ferre, G. G., Curfs, C., Vaughan, G., Larson A. C. & Von Dreele R. B. (2004). Los Alamos National Laboratory Report LAUR Leibowitz, G., Uckaya, G., Oprescu, A. I., Cerasi, E., Gross, D. J. & Kaiser, N. (2002). Endocrinology 143, Matthews, BW. (1968). J Mol Biol., 33: Margiolaki, I., Wright, J. P., Fitch, A. N., Fox, G. C. & Von Dreele, R. B. (2005). Acta Cryst. D61,
126 Margiolaki, I., Wright, J. P., Fitch, A. N., Fox, G. C., Labrador, A., Von Dreele, R. B., Miura, K., Gozzo, F., Schiltz, M., Besnard, C., Camus, F., Pattison, P., Beckers, D., Degen, T. (2007). Z. Kristallogr. Suppl. 26, Margiolaki, I. & Wright, J. P. (2008). Acta Cryst. A, 64(1), Margiolaki, I. Macromolecular Powder Diffraction. International tables of Crystallography, Volume H: Powder Diffraction (In Press). Norrman, M., Ståhl, K., Schluckebier, G. and Al-Karadaghi, S. (2006). J. Appl. Cryst, 39, Norrman M. & Schluckebier G. (2007). Struct. Biol. 19, 83 Norrman, M. (2007) Insulin Polymorphism: Crystallographic characterization of Insulin Microcrystals. Lund University, PhD thesis. Nowell, H., Attfield, J. P., Cole, J. C., Cox, P. J., Shankland, K., Maginn, S. J., Sam Motherwell, W. D. (2002). New J. Chem., 26, Pawley, G.S. (1981). J. Appl. Cryst. 14, Pettersen, EF., Goddard, TD., Huang, CC., Couch, GS., Greenblatt, DM., Meng, EC., Ferrin, TE. (2004) J. Comput. Chem. Oct;25(13): Schlichtkrull, J. (1958). Insulin Crystals. Munksgaard, Copenhagen. Smith, G. D., Ciszak, E, Magrum, L. A., Pangborn, W. A. & Blessing, R. H. (2000). Acta Cryst. D56, Smith, G., D., Pangborn, W. A., Blessing, R. H. (2005). Acta Cryst. D61, Vaughan, G. B. M., Wright, J. P., Bytchkov, A., Rossat, M., Gleyzolle, H., Snigireva, I. & Snigirev, A. (2011). Journal of Synchrotron Radiation, 18, Von Dreele, R.B. (1999). J. Appl. Cryst. 32, Von Dreele, R.B. (2000). Acta Cryst. D56, Von Dreele, R.B. (2003). Methods in Enzymology, Vol. 368, Macromolecular Crystallography, Prt C, edited by R. M. Sweet & C. W. Carter Jr, pp San Diego: Academic Press. Von Dreele, R. B. (2005). Acta Cryst. D61, Von Dreele R. B. (2006). J. Appl. Cryst. 39, Wright, J.P. (2004) Z.Krist. 219, Wright, J. P., Besnard, C., Margiolaki I., Basso, S., Camus, F., Fitch, A. N., Fox, G. C., Pattison, P. & Schiltz, M. (2008). J. Appl. Cryst. 41,
127 Figures Figure 1: Microcrystalline samples of human insulin co-crystallized with phenol in the four different space groups (a) P2 1(α), (b) C222 1, (c) C2, and (d) P2 1(β), each corresponding to ph 5.47, 6.14, 6.75 and 7.46 respectively. Figure 2: Microcrystalline samples of human insulin co-crystallized with resorcinol in the three different space groups (a) P2 1(α), (b) C222 1, and (c, d) P2 1(β), each corresponding to ph 5.46, 6.40, 7.46 and 8.22 respectively. 126
128 Figure 3: Area detector images and integrated profiles obtained using software Fit2D of human insulin co-crystallized with phenol at ph 5.75 and 6.78 corresponding to phases (a, b) P2 1(α) and (c, d) C The data were collected at RT (ID11, λ= (5) Å). Figure 4: Left panel: Pawley fit of the low-angle region of P2 1(α) polymorph of human insulin co-crystallized with resorcinol at ph Due to the very large b-axis and the dominant zone effect, many reflections may not be observed, as a result of peak overlaps. Right panel: Pawley fit of the low-angle peaks, in which only the dominant zone reflections (hk0) have been considered and the additional peaks due to the short c axis are evident. The vertical bars correspond to the theoretical hk0 Bragg reflections and the black, red, and lower blue lines represent the experimental data, calculated pattern, and difference between experimental and calculated profiles respectively. 127
Καταστάσεις της ύλης. Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο.
 Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
Νέα Οπτικά Μικροσκόπια
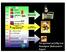 Νέα Οπτικά Μικροσκόπια Αντίθεση εικόνας (contrast) Αντίθεση πλάτους Αντίθεση φάσης Αντίθεση εικόνας =100 x (Ι υποβ -Ι δειγμα )/ Ι υποβ Μικροσκοπία φθορισμού (Χρησιμοποιεί φθορίζουσες χρωστικές για το
Νέα Οπτικά Μικροσκόπια Αντίθεση εικόνας (contrast) Αντίθεση πλάτους Αντίθεση φάσης Αντίθεση εικόνας =100 x (Ι υποβ -Ι δειγμα )/ Ι υποβ Μικροσκοπία φθορισμού (Χρησιμοποιεί φθορίζουσες χρωστικές για το
Επιστήμη των Υλικών. Πανεπιστήμιο Ιωαννίνων. Τμήμα Φυσικής
 Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Κρυσταλλικά Συστήματα Κυβικό Εξαγωνικό Τετραγωνικό Ρομβοεδρικό ή Τριγωνικό Ορθορομβικό Μονοκλινές Τρικλινές Κρυσταλλική δομή των
Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Κρυσταλλικά Συστήματα Κυβικό Εξαγωνικό Τετραγωνικό Ρομβοεδρικό ή Τριγωνικό Ορθορομβικό Μονοκλινές Τρικλινές Κρυσταλλική δομή των
ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ. Ενότητα 2: ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 2: ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 2: ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ
 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ 1. ΓΕΝΙΚΑ Από τις καταστάσεις της ύλης τα αέρια και τα υγρά δεν παρουσιάζουν κάποια τυπική διάταξη ατόμων, ενώ από τα στερεά ορισμένα παρουσιάζουν συγκεκριμένη διάταξη ατόμων
ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ 1. ΓΕΝΙΚΑ Από τις καταστάσεις της ύλης τα αέρια και τα υγρά δεν παρουσιάζουν κάποια τυπική διάταξη ατόμων, ενώ από τα στερεά ορισμένα παρουσιάζουν συγκεκριμένη διάταξη ατόμων
Γενική Φυσική V (Σύγχρονη Φυσική) Φυσική Ακτίνων-Χ και Αλληλεπίδραση Ακτίνων-Χ και Ηλεκτρονίων με την Ύλη
 Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Τμήμα Φυσικής Εργαστήριο Εφαρμοσμένης Φυσικής Γενική Φυσική V (Σύγχρονη Φυσική) Φυσική Ακτίνων-Χ και Αλληλεπίδραση Ακτίνων-Χ και Ηλεκτρονίων με την Ύλη Περιεχόμενα
Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Τμήμα Φυσικής Εργαστήριο Εφαρμοσμένης Φυσικής Γενική Φυσική V (Σύγχρονη Φυσική) Φυσική Ακτίνων-Χ και Αλληλεπίδραση Ακτίνων-Χ και Ηλεκτρονίων με την Ύλη Περιεχόμενα
Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης
 Βιοφυσική & Νανοτεχνολογία Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης Ημερομηνία εκτέλεσης άσκησης... Ονοματεπώνυμα... Περίληψη Σκοπός της άσκησης είναι η εξοικείωση με την χρήση
Βιοφυσική & Νανοτεχνολογία Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης Ημερομηνία εκτέλεσης άσκησης... Ονοματεπώνυμα... Περίληψη Σκοπός της άσκησης είναι η εξοικείωση με την χρήση
Μέθοδοι έρευνας ορυκτών και πετρωμάτων
 Μέθοδοι έρευνας ορυκτών και πετρωμάτων Μάθημα 9 ο Φασματοσκοπία Raman Διδάσκων Δρ. Αδαμαντία Χατζηαποστόλου Τμήμα Γεωλογίας Πανεπιστημίου Πατρών Ακαδημαϊκό Έτος 2017-2018 Ύλη 9 ου μαθήματος Αρχές λειτουργίας
Μέθοδοι έρευνας ορυκτών και πετρωμάτων Μάθημα 9 ο Φασματοσκοπία Raman Διδάσκων Δρ. Αδαμαντία Χατζηαποστόλου Τμήμα Γεωλογίας Πανεπιστημίου Πατρών Ακαδημαϊκό Έτος 2017-2018 Ύλη 9 ου μαθήματος Αρχές λειτουργίας
2.1 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ
 2.1 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ ΕΙΣΑΓΩΓΗ Ένας κρύσταλλος ή ακριβέστερα ένας µονοκρύσταλλος, µπορεί να οριστεί µακροσκοπικά ως ένα στερεό αντικείµενο µε οµοιόµορφη χηµική σύσταση που, όπως απαντάται στη φύση
2.1 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ ΕΙΣΑΓΩΓΗ Ένας κρύσταλλος ή ακριβέστερα ένας µονοκρύσταλλος, µπορεί να οριστεί µακροσκοπικά ως ένα στερεό αντικείµενο µε οµοιόµορφη χηµική σύσταση που, όπως απαντάται στη φύση
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ. Ενότητα 2: Κρυσταλλική Δομή των Μετάλλων. Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών
 Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 2: Κρυσταλλική Δομή των Μετάλλων Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Φυσική ΜΕΤΑΛΛΟΥΡΓΙΑ Ενότητα 2: Κρυσταλλική Δομή των Μετάλλων Γρηγόρης Ν. Χαϊδεμενόπουλος Πολυτεχνική Σχολή Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Ερωτησεις στη Βιοφυσική & Νανοτεχνολογία. Χειμερινό Εξάμηνο 2012
 Ερωτησεις στη Βιοφυσική & Νανοτεχνολογία. Χειμερινό Εξάμηνο 2012 1) Ποιο φυσικό φαινόμενο βοηθάει στην αυτοσυναρμολόγηση μοριακών συστημάτων? α) Η τοποθέτηση μοριων με χρήση μικροσκοπίου σάρωσης δείγματος
Ερωτησεις στη Βιοφυσική & Νανοτεχνολογία. Χειμερινό Εξάμηνο 2012 1) Ποιο φυσικό φαινόμενο βοηθάει στην αυτοσυναρμολόγηση μοριακών συστημάτων? α) Η τοποθέτηση μοριων με χρήση μικροσκοπίου σάρωσης δείγματος
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ
 ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 3. ΟΙ 32 ΚΡΥΣΤΑΛΛΙΚΕΣ ΤΑΞΕΙΣ Ταξινόμηση των κρυστάλλων σαν στερεά σχήματα και οι συμμετρίες Ηλίας Χατζηθεοδωρίδης,
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 3. ΟΙ 32 ΚΡΥΣΤΑΛΛΙΚΕΣ ΤΑΞΕΙΣ Ταξινόμηση των κρυστάλλων σαν στερεά σχήματα και οι συμμετρίες Ηλίας Χατζηθεοδωρίδης,
ΑΣΚΗΣΗ 1. Περίληψη. Θεωρητική εισαγωγή. Πειραματικό μέρος
 ΑΣΚΗΣΗ 1 Περίληψη Σκοπός της πρώτης άσκησης ήταν η εξοικείωση μας με τα όργανα παραγωγής και ανίχνευσης των ακτίνων Χ και την εφαρμογή των κανόνων της κρυσταλλοδομής σε μετρήσεις μεγεθών στο οεργαστήριο.
ΑΣΚΗΣΗ 1 Περίληψη Σκοπός της πρώτης άσκησης ήταν η εξοικείωση μας με τα όργανα παραγωγής και ανίχνευσης των ακτίνων Χ και την εφαρμογή των κανόνων της κρυσταλλοδομής σε μετρήσεις μεγεθών στο οεργαστήριο.
ΚΕΦΑΛΑΙΟ 11: Περίθλαση Ακτίνων-Χ και Νετρονίων από Κρυσταλλικά Υλικά
 ΚΕΦΑΛΑΙΟ 11: Περίθλαση Ακτίνων-Χ και Νετρονίων από Κρυσταλλικά Υλικά Εν γένει τρεις µεταβλητές διακυβερνούν τις διαφορετικές τεχνικές περίθλασης ακτίνων-χ: (α) ακτινοβολία µονοχρωµατική ή µεταβλητού λ
ΚΕΦΑΛΑΙΟ 11: Περίθλαση Ακτίνων-Χ και Νετρονίων από Κρυσταλλικά Υλικά Εν γένει τρεις µεταβλητές διακυβερνούν τις διαφορετικές τεχνικές περίθλασης ακτίνων-χ: (α) ακτινοβολία µονοχρωµατική ή µεταβλητού λ
Κυματική Φύση του φωτός και εφαρμογές. Περίθλαση Νέα οπτικά μικροσκόπια Κρυσταλλογραφία ακτίνων Χ
 Κυματική Φύση του φωτός και εφαρμογές Περίθλαση Νέα οπτικά μικροσκόπια Κρυσταλλογραφία ακτίνων Χ Επαλληλία κυμάτων Διαφορά φάσης Δφ=0 Ενίσχυση Δφ=180 Απόσβεση Κάθε σημείο του μετώπου ενός κύματος λειτουργεί
Κυματική Φύση του φωτός και εφαρμογές Περίθλαση Νέα οπτικά μικροσκόπια Κρυσταλλογραφία ακτίνων Χ Επαλληλία κυμάτων Διαφορά φάσης Δφ=0 Ενίσχυση Δφ=180 Απόσβεση Κάθε σημείο του μετώπου ενός κύματος λειτουργεί
Παραγωγή ακτίνων Χ. V e = h ν = h c/λ λ min = h c/v e λ min (Å) 12400/V
 Παραγωγή ακτίνων Χ Οι ακτίνες Χ είναι ηλεκτροµαγνητική ακτινοβολία µε µήκη κύµατος της τάξης των Å (=10-10 m). Στο ηλεκτροµαγνητικό φάσµα η ακτινοβολία Χ εκτείνεται µεταξύ της περιοχής των ακτίνων γ και
Παραγωγή ακτίνων Χ Οι ακτίνες Χ είναι ηλεκτροµαγνητική ακτινοβολία µε µήκη κύµατος της τάξης των Å (=10-10 m). Στο ηλεκτροµαγνητικό φάσµα η ακτινοβολία Χ εκτείνεται µεταξύ της περιοχής των ακτίνων γ και
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΑΣΚΗΣΕΙΣ ΚΥΜΑΤΙΚΗΣ ΟΠΤΙΚΗΣ
 ΑΣΚΗΣΕΙΣ ΚΥΜΑΤΙΚΗΣ ΟΠΤΙΚΗΣ ΑΣΚΗΣΗ 1: Ένα οπτικό φράγμα με δυο σχισμές που απέχουν μεταξύ τους απόσταση d=0.20 mm είναι τοποθετημένο σε απόσταση =1,20 m από μια οθόνη. Το οπτικό φράγμα με τις δυο σχισμές
ΑΣΚΗΣΕΙΣ ΚΥΜΑΤΙΚΗΣ ΟΠΤΙΚΗΣ ΑΣΚΗΣΗ 1: Ένα οπτικό φράγμα με δυο σχισμές που απέχουν μεταξύ τους απόσταση d=0.20 mm είναι τοποθετημένο σε απόσταση =1,20 m από μια οθόνη. Το οπτικό φράγμα με τις δυο σχισμές
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ
 ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
Πειραματικός υπολογισμός του μήκους κύματος μονοχρωματικής ακτινοβολίας
 Πειραματικός υπολογισμός του μήκους κύματος μονοχρωματικής ακτινοβολίας Τάξη : Γ Λυκείου Βασικές έννοιες και σχέσεις Μήκος κύματος - Μονοχρωματική ακτινοβολία - Συμβολή ηλεκτρομαγνητικών κυμάτων - Κροσσοί
Πειραματικός υπολογισμός του μήκους κύματος μονοχρωματικής ακτινοβολίας Τάξη : Γ Λυκείου Βασικές έννοιες και σχέσεις Μήκος κύματος - Μονοχρωματική ακτινοβολία - Συμβολή ηλεκτρομαγνητικών κυμάτων - Κροσσοί
ΠΕΡΙΘΛΑΣΗ ΗΛΕΚΤΡΟΝΙΩΝ
 ΠΕΡΙΘΛΑΣΗ ΗΛΕΚΤΡΟΝΙΩΝ Αποδείξαμε πειραματικά, με τη βοήθεια του φαινομένου της περίθλασης, ότι τα ηλεκτρόνια έχουν εκτός από τη σωματιδιακή και κυματική φύση. Υπολογίσαμε τις σταθερές πλέγματος του γραφίτη
ΠΕΡΙΘΛΑΣΗ ΗΛΕΚΤΡΟΝΙΩΝ Αποδείξαμε πειραματικά, με τη βοήθεια του φαινομένου της περίθλασης, ότι τα ηλεκτρόνια έχουν εκτός από τη σωματιδιακή και κυματική φύση. Υπολογίσαμε τις σταθερές πλέγματος του γραφίτη
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 3 η σειρά διαφανειών Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα διατάσσονται στο χώρο ώστε να σχηματίσουν στερεά? Τύποι Στερεών
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 3 η σειρά διαφανειών Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα διατάσσονται στο χώρο ώστε να σχηματίσουν στερεά? Τύποι Στερεών
Κυματική οπτική. Συμβολή Περίθλαση Πόλωση
 Κυματική οπτική Η κυματική οπτική ασχολείται με τη μελέτη φαινομένων τα οποία δεν μπορούμε να εξηγήσουμε επαρκώς με τις αρχές της γεωμετρικής οπτικής. Στα φαινόμενα αυτά περιλαμβάνονται τα εξής: Συμβολή
Κυματική οπτική Η κυματική οπτική ασχολείται με τη μελέτη φαινομένων τα οποία δεν μπορούμε να εξηγήσουμε επαρκώς με τις αρχές της γεωμετρικής οπτικής. Στα φαινόμενα αυτά περιλαμβάνονται τα εξής: Συμβολή
Ο Πυρήνας του Ατόμου
 1 Σκοποί: Ο Πυρήνας του Ατόμου 15/06/12 I. Να δώσει μία εισαγωγική περιγραφή του πυρήνα του ατόμου, και της ενέργειας που μπορεί να έχει ένα σωματίδιο για να παραμείνει δέσμιο μέσα στον πυρήνα. II. III.
1 Σκοποί: Ο Πυρήνας του Ατόμου 15/06/12 I. Να δώσει μία εισαγωγική περιγραφή του πυρήνα του ατόμου, και της ενέργειας που μπορεί να έχει ένα σωματίδιο για να παραμείνει δέσμιο μέσα στον πυρήνα. II. III.
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ. Οι ρυθμιστές του οργανισμού
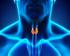 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
ΝΑΝΟΥΛΙΚΑ ΚΑΙ ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΣΤΕΛΛΑ ΚΕΝΝΟΥ ΚΑΘΗΓΗΤΡΙΑ
 ΣΤΕΛΛΑ ΚΕΝΝΟΥ ΚΑΘΗΓΗΤΡΙΑ 1 ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ Πλέγμα στο χώρο Πλέγμα Bravais Διάταξη σημείων στο χώρο έτσι ώστε κάθε σημείο να έχει ταύτοσημο περιβάλλον Αυτό προσδιορίζει δύο ιδιότητες των πλεγμάτων Στον
ΣΤΕΛΛΑ ΚΕΝΝΟΥ ΚΑΘΗΓΗΤΡΙΑ 1 ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ Πλέγμα στο χώρο Πλέγμα Bravais Διάταξη σημείων στο χώρο έτσι ώστε κάθε σημείο να έχει ταύτοσημο περιβάλλον Αυτό προσδιορίζει δύο ιδιότητες των πλεγμάτων Στον
ΑΣΚΗΣΕΙΣ ΚΥΜΑΤΙΚΗΣ ΟΠΤΙΚΗΣ
 ΑΣΚΗΣΕΙΣ ΚΥΜΑΤΙΚΗΣ ΟΠΤΙΚΗΣ ΑΣΚΗΣΗ 1: Ένα οπτικό φράγμα με δυο σχισμές που απέχουν μεταξύ τους απόσταση =0.0 mm είναι τοποθετημένο σε απόσταση =1,0 m από μια οθόνη. Το οπτικό φράγμα με τις δυο σχισμές φωτίζεται
ΑΣΚΗΣΕΙΣ ΚΥΜΑΤΙΚΗΣ ΟΠΤΙΚΗΣ ΑΣΚΗΣΗ 1: Ένα οπτικό φράγμα με δυο σχισμές που απέχουν μεταξύ τους απόσταση =0.0 mm είναι τοποθετημένο σε απόσταση =1,0 m από μια οθόνη. Το οπτικό φράγμα με τις δυο σχισμές φωτίζεται
Θεωρία Μοριακών Τροχιακών (ΜΟ)
 Θεωρία Μοριακών Τροχιακών (ΜΟ) Ετεροπυρηνικά διατομικά μόρια ή ιόντα (πολικοί δεσμοί) Το πιο ηλεκτραρνητικό στοιχείο (με ατομικά τροχιακά χαμηλότερης ενεργειακής στάθμης) συνεισφέρει περισσότερο στο δεσμικό
Θεωρία Μοριακών Τροχιακών (ΜΟ) Ετεροπυρηνικά διατομικά μόρια ή ιόντα (πολικοί δεσμοί) Το πιο ηλεκτραρνητικό στοιχείο (με ατομικά τροχιακά χαμηλότερης ενεργειακής στάθμης) συνεισφέρει περισσότερο στο δεσμικό
Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Σχολή Θετικών Επιστημών - Τμήμα Φυσικής Εργαστήριο Ακτίνων-Χ, Οπτικού Χαρακτηρισμού και Θερμικής Ανάλυσης
 Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Σχολή Θετικών Επιστημών - Τμήμα Φυσικής Εργαστήριο Ακτίνων-Χ, Οπτικού Χαρακτηρισμού και Θερμικής Ανάλυσης ΑΣΚΗΣΗ Σκοπός της άσκησης είναι ο υπολογισμός των μηκών
Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Σχολή Θετικών Επιστημών - Τμήμα Φυσικής Εργαστήριο Ακτίνων-Χ, Οπτικού Χαρακτηρισμού και Θερμικής Ανάλυσης ΑΣΚΗΣΗ Σκοπός της άσκησης είναι ο υπολογισμός των μηκών
Πως διαδίδονται τα Η/Μ κύματα σε διαφανή διηλεκτρικά?
 Πως διαδίδονται τα Η/Μ κύματα σε διαφανή διηλεκτρικά? (Μη-μαγνητικά, μη-αγώγιμα, διαφανή στερεά ή υγρά με πυκνή, σχετικά κανονική διάταξη δομικών λίθων). Γραμμικά πολωμένο κύμα προσπίπτει σε ηλεκτρόνιο
Πως διαδίδονται τα Η/Μ κύματα σε διαφανή διηλεκτρικά? (Μη-μαγνητικά, μη-αγώγιμα, διαφανή στερεά ή υγρά με πυκνή, σχετικά κανονική διάταξη δομικών λίθων). Γραμμικά πολωμένο κύμα προσπίπτει σε ηλεκτρόνιο
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
Γραπτή εξέταση προόδου «Επιστήμη και Τεχνολογία Υλικών Ι»-Νοέμβριος 2016
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Θέμα 1: Ερωτήσεις (10 Μονάδες) (Σύντομη αιτιολόγηση.
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) Θέμα 1: Ερωτήσεις (10 Μονάδες) (Σύντομη αιτιολόγηση.
Περίθλαση από ακµή και από εµπόδιο.
 ρ. Χ. Βοζίκης Εργαστήριο Φυσικής ΙΙ 63 6. Άσκηση 6 Περίθλαση από ακµή και από εµπόδιο. 6.1 Σκοπός της εργαστηριακής άσκησης Σκοπός της άσκησης αυτής, καθώς και των δύο εποµένων, είναι η γνωριµία των σπουδαστών
ρ. Χ. Βοζίκης Εργαστήριο Φυσικής ΙΙ 63 6. Άσκηση 6 Περίθλαση από ακµή και από εµπόδιο. 6.1 Σκοπός της εργαστηριακής άσκησης Σκοπός της άσκησης αυτής, καθώς και των δύο εποµένων, είναι η γνωριµία των σπουδαστών
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Φασματοφωτομετρία
 1 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Φασματοφωτομετρία Ιωάννης Πούλιος Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124
1 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Φασματοφωτομετρία Ιωάννης Πούλιος Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124
EΡΩΤΗΣΕΙΣ ΑΣΚΗΣΕΙΣ ΠΡΟΒΛΗΜΑΤΑ ΣΤΑ ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΚΑ ΚΥΜΑΤΑ ΑΝΑΚΛΑΣΗ ΔΙΑΘΛΑΣΗ ΟΛΙΚΗ ΑΝΑΚΛΑΣΗ
 ΤΟ ΥΛΙΚΟ ΕΧΕΙ ΑΝΤΛΗΘΕΙ ΑΠΟ ΤΑ ΨΗΦΙΑΚΑ ΕΚΠΑΙΔΕΥΤΙΚΑ ΒΟΗΘΗΜΑΤΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ http://wwwstudy4examsgr/ ΕΧΕΙ ΤΑΞΙΝΟΜΗΘΕΙ ΑΝΑ ΕΝΟΤΗΤΑ ΚΑΙ ΑΝΑ ΤΥΠΟ ΓΙΑ ΔΙΕΥΚΟΛΥΝΣΗ ΤΗΣ ΜΕΛΕΤΗΣ ΣΑΣ ΚΑΛΗ ΕΠΙΤΥΧΙΑ ΣΤΗ
ΤΟ ΥΛΙΚΟ ΕΧΕΙ ΑΝΤΛΗΘΕΙ ΑΠΟ ΤΑ ΨΗΦΙΑΚΑ ΕΚΠΑΙΔΕΥΤΙΚΑ ΒΟΗΘΗΜΑΤΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ http://wwwstudy4examsgr/ ΕΧΕΙ ΤΑΞΙΝΟΜΗΘΕΙ ΑΝΑ ΕΝΟΤΗΤΑ ΚΑΙ ΑΝΑ ΤΥΠΟ ΓΙΑ ΔΙΕΥΚΟΛΥΝΣΗ ΤΗΣ ΜΕΛΕΤΗΣ ΣΑΣ ΚΑΛΗ ΕΠΙΤΥΧΙΑ ΣΤΗ
οµή των στερεών ιάλεξη 4 η
 οµή των στερεών ιάλεξη 4 η Ύλη τέταρτου µαθήµατος Οι καταστάσεις της ύλης, Γιατί τις µελετάµε; Περιοδική τοποθέτηση των ατόµων, Κρυσταλλική και άµορφη δοµή, Κρυσταλλικό πλέγµα κρυσταλλική κυψελίδα, Πλέγµατα
οµή των στερεών ιάλεξη 4 η Ύλη τέταρτου µαθήµατος Οι καταστάσεις της ύλης, Γιατί τις µελετάµε; Περιοδική τοποθέτηση των ατόµων, Κρυσταλλική και άµορφη δοµή, Κρυσταλλικό πλέγµα κρυσταλλική κυψελίδα, Πλέγµατα
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ
 ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
ΦΑΣΜΑΤΑ ΕΚΠΟΜΠΗΣ ΑΠΟΡΡΟΦΗΣΗΣ
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
ΔΙΑΤΑΡΑΧΕΣ (DISLOCATIONS )
 ΔΙΑΤΑΡΑΧΕΣ (DISLOCATIONS ) 1. ΕΙΣΑΓΩΓΉ Η αντοχή και η σκληρότητα είναι μέτρα της αντίστασης ενός υλικού σε πλαστική παραμόρφωση Σε μικροσκοπική κλίμακα, πλαστική παραμόρφωση : - συνολική κίνηση μεγάλου
ΔΙΑΤΑΡΑΧΕΣ (DISLOCATIONS ) 1. ΕΙΣΑΓΩΓΉ Η αντοχή και η σκληρότητα είναι μέτρα της αντίστασης ενός υλικού σε πλαστική παραμόρφωση Σε μικροσκοπική κλίμακα, πλαστική παραμόρφωση : - συνολική κίνηση μεγάλου
ΠΕΙΡΑΜΑ 4: ΟΠΤΙΚΗ ΦΑΣΜΑΤΟΣΚΟΠΙΑ AΠΟΡΡΟΦΗΣΗΣ
 ΠΕΙΡΑΜΑ 4: ΟΠΤΙΚΗ ΦΑΣΜΑΤΟΣΚΟΠΙΑ AΠΟΡΡΟΦΗΣΗΣ [1] ΘΕΩΡΙΑ Σύμφωνα με τη κβαντομηχανική, τα άτομα απορροφούν ηλεκτρομαγνητική ενέργεια με διακριτό τρόπο, με «κβάντο» ενέργειας την ενέργεια hv ενός φωτονίου,
ΠΕΙΡΑΜΑ 4: ΟΠΤΙΚΗ ΦΑΣΜΑΤΟΣΚΟΠΙΑ AΠΟΡΡΟΦΗΣΗΣ [1] ΘΕΩΡΙΑ Σύμφωνα με τη κβαντομηχανική, τα άτομα απορροφούν ηλεκτρομαγνητική ενέργεια με διακριτό τρόπο, με «κβάντο» ενέργειας την ενέργεια hv ενός φωτονίου,
Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Νοέμβριος 2017
 Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Νοέμβριος 017 Ερώτηση 1 (5 μονάδες ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ
Γραπτή εξέταση προόδου στο μάθημα «Επιστήμη & Τεχνολογία Υλικών Ι»-Νοέμβριος 017 Ερώτηση 1 (5 μονάδες ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Συστήματα συντεταγμένων
 Κεφάλαιο. Για να δημιουργήσουμε τρισδιάστατα αντικείμενα, που μπορούν να παρασταθούν στην οθόνη του υπολογιστή ως ένα σύνολο από γραμμές, επίπεδες πολυγωνικές επιφάνειες ή ακόμη και από ένα συνδυασμό από
Κεφάλαιο. Για να δημιουργήσουμε τρισδιάστατα αντικείμενα, που μπορούν να παρασταθούν στην οθόνη του υπολογιστή ως ένα σύνολο από γραμμές, επίπεδες πολυγωνικές επιφάνειες ή ακόμη και από ένα συνδυασμό από
ΠΡΟΤΥΠΟ ΠΕΙΡΑΜΑΤΙΚΟ ΛΥΚΕΙΟ ΕΥΑΓΓΕΛΙΚΗΣ ΣΧΟΛΗΣ ΣΜΥΡΝΗΣ
 ΠΡΟΤΥΠΟ ΠΕΙΡΑΜΑΤΙΚΟ ΛΥΚΕΙΟ ΕΥΑΓΓΕΛΙΚΗΣ ΣΧΟΛΗΣ ΣΜΥΡΝΗΣ ΕΠΙΛΟΓΗ ΘΕΜΑΤΩΝ ΑΠΟ ΤΗΝ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ «Β ΘΕΜΑΤΑ ΦΩΣ» ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Β ΛΥΚΕΙΟΥ Χ. Δ. ΦΑΝΙΔΗΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 04-05 ΠΟΡΕΙΑ ΑΚΤΙΝΑΣ. Β. Στο διπλανό
ΠΡΟΤΥΠΟ ΠΕΙΡΑΜΑΤΙΚΟ ΛΥΚΕΙΟ ΕΥΑΓΓΕΛΙΚΗΣ ΣΧΟΛΗΣ ΣΜΥΡΝΗΣ ΕΠΙΛΟΓΗ ΘΕΜΑΤΩΝ ΑΠΟ ΤΗΝ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ «Β ΘΕΜΑΤΑ ΦΩΣ» ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Β ΛΥΚΕΙΟΥ Χ. Δ. ΦΑΝΙΔΗΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 04-05 ΠΟΡΕΙΑ ΑΚΤΙΝΑΣ. Β. Στο διπλανό
 Τι γνώριζαν για τους κρυστάλλους: ΚΡΥΣΤΑΛΛΙΚΑ ΣΤΕΡΕΑ - ΚΡΥΣΤΑΛΛΟΙ Πρώτοι παρατηρητές: Κανονικότητα της εξωτερικής μορφής των κρυστάλλων οι κρύσταλλοι σχηματίζονται από την κανονική επανάληψη ταυτόσημων
Τι γνώριζαν για τους κρυστάλλους: ΚΡΥΣΤΑΛΛΙΚΑ ΣΤΕΡΕΑ - ΚΡΥΣΤΑΛΛΟΙ Πρώτοι παρατηρητές: Κανονικότητα της εξωτερικής μορφής των κρυστάλλων οι κρύσταλλοι σχηματίζονται από την κανονική επανάληψη ταυτόσημων
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΚΕΦΑΛΑΙΟ 2ο: ΜΗΧΑΝΙΚΑ- ΗΛΕΚΤΡΟΜΑΓΝΗΤΙΚΑ ΚΥΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ.
 ΤΟ ΥΛΙΚΟ ΕΧΕΙ ΑΝΤΛΗΘΕΙ ΑΠΟ ΤΑ ΨΗΦΙΑΚΑ ΕΚΠΑΙΔΕΥΤΙΚΑ ΒΟΗΘΗΜΑΤΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ http://www.study4exams.gr/ ΕΧΕΙ ΤΑΞΙΝΟΜΗΘΕΙ ΑΝΑ ΕΝΟΤΗΤΑ ΚΑΙ ΑΝΑ ΤΥΠΟ ΓΙΑ ΔΙΕΥΚΟΛΥΝΣΗ ΤΗΣ ΜΕΛΕΤΗΣ ΣΑΣ ΚΑΛΗ ΕΠΙΤΥΧΙΑ ΣΤΗ
ΤΟ ΥΛΙΚΟ ΕΧΕΙ ΑΝΤΛΗΘΕΙ ΑΠΟ ΤΑ ΨΗΦΙΑΚΑ ΕΚΠΑΙΔΕΥΤΙΚΑ ΒΟΗΘΗΜΑΤΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ http://www.study4exams.gr/ ΕΧΕΙ ΤΑΞΙΝΟΜΗΘΕΙ ΑΝΑ ΕΝΟΤΗΤΑ ΚΑΙ ΑΝΑ ΤΥΠΟ ΓΙΑ ΔΙΕΥΚΟΛΥΝΣΗ ΤΗΣ ΜΕΛΕΤΗΣ ΣΑΣ ΚΑΛΗ ΕΠΙΤΥΧΙΑ ΣΤΗ
κρυστάλλου απείρου μεγέθους.
 Κρυστάλλωση Πολυμερών Θερμοδυναμική της κρυστάλλωσης πολυμερών Θερμοκρασία ρασία τήξης πολυμερών Μεταβολή ειδικού όγκου ως προς τη θερμοκρασία σε γραμμικό πολυαιθυλένιο:., ακλασματοποίητο πολυμερές, ο,
Κρυστάλλωση Πολυμερών Θερμοδυναμική της κρυστάλλωσης πολυμερών Θερμοκρασία ρασία τήξης πολυμερών Μεταβολή ειδικού όγκου ως προς τη θερμοκρασία σε γραμμικό πολυαιθυλένιο:., ακλασματοποίητο πολυμερές, ο,
ΑΝΟΡΓΑΝΑ ΥΛΙΚΑ. Μάθημα 3ο. Συμμετρία
 ΑΝΟΡΓΑΝΑ ΥΛΙΚΑ Μάθημα 3ο Συμμετρία 1 Συμμετρία Μια κατάσταση στην οποία μέρη τα οποία ευρίσκονται σε αντίθετες μεταξύ τους θέσεις ενός επιπέδου, γραμμής ή σημείου φανερώνει διευθετήσεις οι οποίες αλληλοσυνδέονται
ΑΝΟΡΓΑΝΑ ΥΛΙΚΑ Μάθημα 3ο Συμμετρία 1 Συμμετρία Μια κατάσταση στην οποία μέρη τα οποία ευρίσκονται σε αντίθετες μεταξύ τους θέσεις ενός επιπέδου, γραμμής ή σημείου φανερώνει διευθετήσεις οι οποίες αλληλοσυνδέονται
Δομικός χαρακτηρισμός πρωτεϊνών φαρμακευτικού ενδιαφέροντος
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Δομικός χαρακτηρισμός πρωτεϊνών φαρμακευτικού ενδιαφέροντος Μεταπτυχιακή εργασία Γιαννοπούλου Ευδοκία- Αναστασία, Α.Μ. 473 Οκτώβριος 2012 1 Ευχαριστίες: Η παρούσα μεταπτυχιακή εργασία
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Δομικός χαρακτηρισμός πρωτεϊνών φαρμακευτικού ενδιαφέροντος Μεταπτυχιακή εργασία Γιαννοπούλου Ευδοκία- Αναστασία, Α.Μ. 473 Οκτώβριος 2012 1 Ευχαριστίες: Η παρούσα μεταπτυχιακή εργασία
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ
 ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 4 η σειρά διαφανειών Δημήτριος Λαμπάκης Ορισμός και ιδιότητες των μετάλλων Τα χημικά στοιχεία διακρίνονται σε μέταλλα (περίπου 70 τον αριθμό)
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 4 η σειρά διαφανειών Δημήτριος Λαμπάκης Ορισμός και ιδιότητες των μετάλλων Τα χημικά στοιχεία διακρίνονται σε μέταλλα (περίπου 70 τον αριθμό)
Εργαστηριακή άσκηση 01. Τα επτά συστήματα κρυστάλλωσης και κρυσταλλικές μορφές
 Εργαστηριακή άσκηση 01 Τα επτά συστήματα κρυστάλλωσης και κρυσταλλικές μορφές Ηλίας Χατζηθεοδωρίδης Οκτώβριος / Νοέμβριος 2004 Τι περιλαμβάνει η άσκηση Θα μάθετε τα 7 κρυσταλλογραφικά συστήματα και πως
Εργαστηριακή άσκηση 01 Τα επτά συστήματα κρυστάλλωσης και κρυσταλλικές μορφές Ηλίας Χατζηθεοδωρίδης Οκτώβριος / Νοέμβριος 2004 Τι περιλαμβάνει η άσκηση Θα μάθετε τα 7 κρυσταλλογραφικά συστήματα και πως
Βιοφυσική. ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο ) 3 η Διάλεξη
 Βιοφυσική ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο 2009-10) 3 η Διάλεξη Από την προηγούμενη διάλεξη: Οι πρωτεΐνες εκτελούν τις περισσότερες βιολογικές λειτουργίες π.χ Ενζυμική κατάλυση (επιτάχυνση
Βιοφυσική ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο 2009-10) 3 η Διάλεξη Από την προηγούμενη διάλεξη: Οι πρωτεΐνες εκτελούν τις περισσότερες βιολογικές λειτουργίες π.χ Ενζυμική κατάλυση (επιτάχυνση
Δx
 Ποια είναι η ελάχιστη αβεβαιότητα της ταχύτητας ενός φορτηγού μάζας 2 τόνων που περιμένει σε ένα κόκκινο φανάρι (η η μέγιστη δυνατή ταχύτητά του) όταν η θέση του μετράται με αβεβαιότητα 1 x 10-10 m. Δx
Ποια είναι η ελάχιστη αβεβαιότητα της ταχύτητας ενός φορτηγού μάζας 2 τόνων που περιμένει σε ένα κόκκινο φανάρι (η η μέγιστη δυνατή ταχύτητά του) όταν η θέση του μετράται με αβεβαιότητα 1 x 10-10 m. Δx
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ»
 «ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
Περίθλαση από µία σχισµή.
 ρ. Χ. Βοζίκης Εργαστήριο Φυσικής ΙΙ 71 7. Άσκηση 7 Περίθλαση από µία σχισµή. 7.1 Σκοπός της εργαστηριακής άσκησης Σκοπός της άσκησης είναι η γνωριµία των σπουδαστών µε την συµπεριφορά των µικροκυµάτων
ρ. Χ. Βοζίκης Εργαστήριο Φυσικής ΙΙ 71 7. Άσκηση 7 Περίθλαση από µία σχισµή. 7.1 Σκοπός της εργαστηριακής άσκησης Σκοπός της άσκησης είναι η γνωριµία των σπουδαστών µε την συµπεριφορά των µικροκυµάτων
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΕΦΑΡΜΟΣΜΕΝΩΝ ΜΑΘΗΜΑΤΙΚΩΝ ΚΑΙ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΤΕΥΘΥΝΣΗ ΜΑΘΗΜΑΤΙΚΟΥ ΕΦΑΡΜΟΓΩΝ ΡΟΕΣ ΣΤΑΤΙΣΤΙΚΗΣ ΑΝΑΛΥΣΗΣ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ του Γεωργίου Π. Νίνη «Η Θεωρία Ομάδων και
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΕΦΑΡΜΟΣΜΕΝΩΝ ΜΑΘΗΜΑΤΙΚΩΝ ΚΑΙ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΤΕΥΘΥΝΣΗ ΜΑΘΗΜΑΤΙΚΟΥ ΕΦΑΡΜΟΓΩΝ ΡΟΕΣ ΣΤΑΤΙΣΤΙΚΗΣ ΑΝΑΛΥΣΗΣ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ του Γεωργίου Π. Νίνη «Η Θεωρία Ομάδων και
ΟΡΓΑΝΟΛΟΓΙΑ ΦΑΣΜΑΤΟΜΕΤΡΙΚΩΝ ΟΡΓΑΝΩΝ ΜΕΤΡΗΣΗΣ: ΑΠΟΡΡΟΦΗΣΗΣ ΦΘΟΡΙΣΜΟΥ, ΦΩΣΦΩΡΙΣΜΟΥ, ΣΚΕΔΑΣΗΣ ΕΚΠΟΜΠΗΣ, ΧΗΜΕΙΟΦΩΤΑΥΓΕΙΑΣ
 ΟΡΓΑΝΟΛΟΓΙΑ ΦΑΣΜΑΤΟΜΕΤΡΙΚΩΝ ΟΡΓΑΝΩΝ ΜΕΤΡΗΣΗΣ: ΑΠΟΡΡΟΦΗΣΗΣ ΦΘΟΡΙΣΜΟΥ, ΦΩΣΦΩΡΙΣΜΟΥ, ΣΚΕΔΑΣΗΣ ΕΚΠΟΜΠΗΣ, ΧΗΜΕΙΟΦΩΤΑΥΓΕΙΑΣ ΠΗΓΕΣ ΑΚΤΙΝΟΒΟΛΙΑΣ ΣΥΝΕΧΕΙΣ ΠΗΓΕΣ ΠΗΓΕΣ ΓΡΑΜΜΩΝ ΚΟΙΛΗΣ ΚΑΘΟΔΟΥ & ΛΥΧΝΙΕΣ ΕΚΚΕΝΩΣΕΩΝ
ΟΡΓΑΝΟΛΟΓΙΑ ΦΑΣΜΑΤΟΜΕΤΡΙΚΩΝ ΟΡΓΑΝΩΝ ΜΕΤΡΗΣΗΣ: ΑΠΟΡΡΟΦΗΣΗΣ ΦΘΟΡΙΣΜΟΥ, ΦΩΣΦΩΡΙΣΜΟΥ, ΣΚΕΔΑΣΗΣ ΕΚΠΟΜΠΗΣ, ΧΗΜΕΙΟΦΩΤΑΥΓΕΙΑΣ ΠΗΓΕΣ ΑΚΤΙΝΟΒΟΛΙΑΣ ΣΥΝΕΧΕΙΣ ΠΗΓΕΣ ΠΗΓΕΣ ΓΡΑΜΜΩΝ ΚΟΙΛΗΣ ΚΑΘΟΔΟΥ & ΛΥΧΝΙΕΣ ΕΚΚΕΝΩΣΕΩΝ
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ AΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ)
 ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ AΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» 22/12/2015 Δ.Δ. Λεωνίδας 1
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ AΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» 22/12/2015 Δ.Δ. Λεωνίδας 1
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ
 ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων
 5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o προβλέπετε με βάση τη συμμετρία αν ένα μόριο έχει μόνιμη
5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o προβλέπετε με βάση τη συμμετρία αν ένα μόριο έχει μόνιμη
ΠΟΥ ΔΙΑΔΙΔΕΤΑΙ ΤΟ ΦΩΣ
 1 ΦΩΣ Στο μικρόκοσμο θεωρούμε ότι το φως έχει δυο μορφές. Άλλοτε το αντιμετωπίζουμε με τη μορφή σωματιδίων που ονομάζουμε φωτόνια. Τα φωτόνια δεν έχουν μάζα αλλά μόνον ενέργεια. Άλλοτε πάλι αντιμετωπίζουμε
1 ΦΩΣ Στο μικρόκοσμο θεωρούμε ότι το φως έχει δυο μορφές. Άλλοτε το αντιμετωπίζουμε με τη μορφή σωματιδίων που ονομάζουμε φωτόνια. Τα φωτόνια δεν έχουν μάζα αλλά μόνον ενέργεια. Άλλοτε πάλι αντιμετωπίζουμε
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ Ένα σημαντικό αποτέλεσμα της κβαντομηχανικής θεωρίας είναι ότι τα μόρια, όχι μόνο βρίσκονται σε διακριτές ενεργειακές
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ Ένα σημαντικό αποτέλεσμα της κβαντομηχανικής θεωρίας είναι ότι τα μόρια, όχι μόνο βρίσκονται σε διακριτές ενεργειακές
Βασικές διαδικασίες παραγωγής πολωμένου φωτός
 Πόλωση του φωτός Βασικές διαδικασίες παραγωγής πολωμένου φωτός πόλωση λόγω επιλεκτικής απορρόφησης - διχρωισμός πόλωση λόγω ανάκλασης από μια διηλεκτρική επιφάνεια πόλωση λόγω ύπαρξης δύο δεικτών διάθλασης
Πόλωση του φωτός Βασικές διαδικασίες παραγωγής πολωμένου φωτός πόλωση λόγω επιλεκτικής απορρόφησης - διχρωισμός πόλωση λόγω ανάκλασης από μια διηλεκτρική επιφάνεια πόλωση λόγω ύπαρξης δύο δεικτών διάθλασης
Γραπτή εξέταση προόδου «Επιστήμη και Τεχνολογία Υλικών Ι»-Νοέμβριος 2015
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) ΘΕΜΑ 1 ο (15 Μονάδες) Πόσα γραμμάρια καθαρού κρυσταλλικού
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ (Καθ. Β.Ζασπάλης) ΘΕΜΑ 1 ο (15 Μονάδες) Πόσα γραμμάρια καθαρού κρυσταλλικού
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β
 ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ
 ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
γ) Να σχεδιάσετε τις γραφικές παραστάσεις απομάκρυνσης - χρόνου, για τα σημεία Α, Β και Γ, τα οποία απέχουν από το ελεύθερο άκρο αντίστοιχα,,
 1. Κατά μήκος μιας ελαστικής χορδής μεγάλου μήκους που το ένα άκρο της είναι ακλόνητα στερεωμένο, διαδίδονται δύο κύματα, των οποίων οι εξισώσεις είναι αντίστοιχα: και, όπου και είναι μετρημένα σε και
1. Κατά μήκος μιας ελαστικής χορδής μεγάλου μήκους που το ένα άκρο της είναι ακλόνητα στερεωμένο, διαδίδονται δύο κύματα, των οποίων οι εξισώσεις είναι αντίστοιχα: και, όπου και είναι μετρημένα σε και
Κρυσταλλογραφία: επιστήμη που ασχολείται με τη περιγραφή της γεωμετρίας των κρυστάλλων και της διάταξης στο εσωτερικό τους.
 I. Κρυσταλλική Δομή Κρυσταλλογραφία Κρυσταλλογραφία: επιστήμη που ασχολείται με τη περιγραφή της γεωμετρίας των κρυστάλλων και της διάταξης στο εσωτερικό τους. Η συμμετρία του κρυστάλλου επηρεάζει τις
I. Κρυσταλλική Δομή Κρυσταλλογραφία Κρυσταλλογραφία: επιστήμη που ασχολείται με τη περιγραφή της γεωμετρίας των κρυστάλλων και της διάταξης στο εσωτερικό τους. Η συμμετρία του κρυστάλλου επηρεάζει τις
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΑ 7,8,9
 ΠΕΙΡΑΜΑΤΙΚΟ ΛΥΚΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΜΑΚΕΔΟΝΙΑΣ ΖΑΡΦΤΖΙΑΝ Μ. ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΑ 7,8,9 ΕΡΩΤΗΣΕΙΣ - ΑΣΚΗΣΕΙΣ 1. Διαφορές κλειστής και συνεχούς καλλιέργειας (θρεπτικά, απομάκρυνση, φάσεις μικροοργανισμών)
ΠΕΙΡΑΜΑΤΙΚΟ ΛΥΚΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΜΑΚΕΔΟΝΙΑΣ ΖΑΡΦΤΖΙΑΝ Μ. ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΑ 7,8,9 ΕΡΩΤΗΣΕΙΣ - ΑΣΚΗΣΕΙΣ 1. Διαφορές κλειστής και συνεχούς καλλιέργειας (θρεπτικά, απομάκρυνση, φάσεις μικροοργανισμών)
Φύση του φωτός. Θεωρούμε ότι το φως έχει διττή φύση: διαταραχή που διαδίδεται στο χώρο. μήκος κύματος φωτός. συχνότητα φωτός
 Γεωμετρική Οπτική Φύση του φωτός Θεωρούμε ότι το φως έχει διττή φύση: ΚΥΜΑΤΙΚΗ Βασική ιδέα Το φως είναι μια Η/Μ διαταραχή που διαδίδεται στο χώρο Βασική Εξίσωση Φαινόμενα που εξηγεί καλύτερα (κύμα) μήκος
Γεωμετρική Οπτική Φύση του φωτός Θεωρούμε ότι το φως έχει διττή φύση: ΚΥΜΑΤΙΚΗ Βασική ιδέα Το φως είναι μια Η/Μ διαταραχή που διαδίδεται στο χώρο Βασική Εξίσωση Φαινόμενα που εξηγεί καλύτερα (κύμα) μήκος
ΕΝΔΕΙΚΤΙΚΕΣ ΑΣΚΗΣΕΙΣ ΦΥΣΙΚΗΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Β ΛΥΚΕΙΟΥ
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΣΚΗΣΕΙΣ ΦΥΣΙΚΗΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Β ΛΥΚΕΙΟΥ 1. Δυο ακίνητα σημειακά φορτία Q 1=10μC και Q 2=40μC απέχουν μεταξύ τους απόσταση r=3m.να βρείτε: A) το μέτρο της δύναμης που ασκεί το ένα φορτίο
ΕΝΔΕΙΚΤΙΚΕΣ ΑΣΚΗΣΕΙΣ ΦΥΣΙΚΗΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Β ΛΥΚΕΙΟΥ 1. Δυο ακίνητα σημειακά φορτία Q 1=10μC και Q 2=40μC απέχουν μεταξύ τους απόσταση r=3m.να βρείτε: A) το μέτρο της δύναμης που ασκεί το ένα φορτίο
ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ
 ΦΥΣΙΚΗ Γ.Π. Γ Λυκείου / Το Φως 1. Η υπεριώδης ακτινοβολία : a) δεν προκαλεί αμαύρωση της φωτογραφικής πλάκας. b) είναι ορατή. c) χρησιμοποιείται για την αποστείρωση ιατρικών εργαλείων. d) έχει μήκος κύματος
ΦΥΣΙΚΗ Γ.Π. Γ Λυκείου / Το Φως 1. Η υπεριώδης ακτινοβολία : a) δεν προκαλεί αμαύρωση της φωτογραφικής πλάκας. b) είναι ορατή. c) χρησιμοποιείται για την αποστείρωση ιατρικών εργαλείων. d) έχει μήκος κύματος
Μονάδες Το γραμμικό φάσμα του ατόμου του υδρογόνου ερμηνεύεται με
 Προτεινόµενα Θέµατα Γ Λυκείου Οκτώβριος 20 Φυσική ΘΕΜΑ A γενιικής παιιδείίας Στις ερωτήσεις -5 να γράψετε τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.. Η υπεριώδης ακτινοβολία
Προτεινόµενα Θέµατα Γ Λυκείου Οκτώβριος 20 Φυσική ΘΕΜΑ A γενιικής παιιδείίας Στις ερωτήσεις -5 να γράψετε τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.. Η υπεριώδης ακτινοβολία
Ακτίνες Χ (Roentgen) Κ.-Α. Θ. Θωμά
 Ακτίνες Χ (Roentgen) Είναι ηλεκτρομαγνητικά κύματα με μήκος κύματος μεταξύ 10 nm και 0.01 nm, δηλαδή περίπου 10 4 φορές μικρότερο από το μήκος κύματος της ορατής ακτινοβολίας. ( Φάσμα ηλεκτρομαγνητικής
Ακτίνες Χ (Roentgen) Είναι ηλεκτρομαγνητικά κύματα με μήκος κύματος μεταξύ 10 nm και 0.01 nm, δηλαδή περίπου 10 4 φορές μικρότερο από το μήκος κύματος της ορατής ακτινοβολίας. ( Φάσμα ηλεκτρομαγνητικής
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
Εφαρμοσμένη Οπτική. Περίθλαση Fraunhofer Περίθλαση Fresnel
 Εφαρμοσμένη Οπτική Περίθλαση Fraunhofer Περίθλαση Fresnel Περίθλαση - Ορισμός Περίθλαση είναι κάθε απόκλιση από την ευθύγραμμη διάδοση του φωτός, η οποία προκαλείται από παρεμβολή κάποιου εμποδίου. Στη
Εφαρμοσμένη Οπτική Περίθλαση Fraunhofer Περίθλαση Fresnel Περίθλαση - Ορισμός Περίθλαση είναι κάθε απόκλιση από την ευθύγραμμη διάδοση του φωτός, η οποία προκαλείται από παρεμβολή κάποιου εμποδίου. Στη
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ
 ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
ΗΛΕΚΤΡΟΝΙΚΗ ΜΙΚΡΟΣΚΟΠΙΑ ΔΡ. ΒΑΣΙΛΕΙΟΣ ΜΠΙΝΑΣ Τμήμα Φυσικής, Πανεπιστήμιο Κρήτης Email: binasbill@iesl.forth.gr Thl. 1269 Crete Center for Quantum Complexity and Nanotechnology Department of Physics, University
Περίθλαση και εικόνα περίθλασης
 Περίθλαση και εικόνα περίθλασης Η περίθλαση αναφέρεται στη γενική συμπεριφορά των κυμάτων, τα οποία διαδίδονται προς όλες τις κατευθύνσεις καθώς περνούν μέσα από μια σχισμή. Ο όρος εικόνα περίθλασης είναι
Περίθλαση και εικόνα περίθλασης Η περίθλαση αναφέρεται στη γενική συμπεριφορά των κυμάτων, τα οποία διαδίδονται προς όλες τις κατευθύνσεις καθώς περνούν μέσα από μια σχισμή. Ο όρος εικόνα περίθλασης είναι
4.1 Εύρεση του Συνόλου των ιεργασιών Συμμετρίας ενός Μορίου
 4. Ομάδες Σημείου ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o ορίζετε την έννοια της ομάδας σημείου ενός μορίου o διακρίνετε τις βασικές κατηγορίες ομάδων σημείου
4. Ομάδες Σημείου ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o ορίζετε την έννοια της ομάδας σημείου ενός μορίου o διακρίνετε τις βασικές κατηγορίες ομάδων σημείου
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
Μέθοδοι έρευνας ορυκτών και πετρωμάτων
 Μέθοδοι έρευνας ορυκτών και πετρωμάτων Μάθημα 8 ο Φασματοσκοπία απορρόφησης υπερύθρων (IR) και Φασματοσκοπία απορρόφησης υπερύθρων με μετασχηματισμό Fourier (FTIR) Διδάσκων Δρ. Αδαμαντία Χατζηαποστόλου
Μέθοδοι έρευνας ορυκτών και πετρωμάτων Μάθημα 8 ο Φασματοσκοπία απορρόφησης υπερύθρων (IR) και Φασματοσκοπία απορρόφησης υπερύθρων με μετασχηματισμό Fourier (FTIR) Διδάσκων Δρ. Αδαμαντία Χατζηαποστόλου
Κρυσταλλογραφία Ακτίνων Χ
 Κρυσταλλογραφία Ακτίνων Χ Τι είναι η κρυσταλλογραφία ακτίνων Χ; Η µελέτη του κρυσταλλικού πλέγµατος, µέσω της χρήσης ακτίνων Χ. Αποκαλύπτει τη διάταξη των δομικών μερών τα οποία συγκροτούν τον κρύσταλλο
Κρυσταλλογραφία Ακτίνων Χ Τι είναι η κρυσταλλογραφία ακτίνων Χ; Η µελέτη του κρυσταλλικού πλέγµατος, µέσω της χρήσης ακτίνων Χ. Αποκαλύπτει τη διάταξη των δομικών μερών τα οποία συγκροτούν τον κρύσταλλο
ΚΕΦΑΛΑΙΟ 11 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
 ΚΕΦΑΛΑΙΟ 11 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ 1o ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11207, 96ο ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11303 Ι. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν
ΚΕΦΑΛΑΙΟ 11 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ 1o ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11207, 96ο ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11303 Ι. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν
Οργανική Χημεία. Κεφάλαια 12 &13: Φασματοσκοπία μαζών και υπερύθρου
 Οργανική Χημεία Κεφάλαια 12 &13: Φασματοσκοπία μαζών και υπερύθρου 1. Γενικά Δυνατότητα προσδιορισμού δομών με σαφήνεια χρησιμοποιώντας τεχνικές φασματοσκοπίας Φασματοσκοπία μαζών Μέγεθος, μοριακός τύπος
Οργανική Χημεία Κεφάλαια 12 &13: Φασματοσκοπία μαζών και υπερύθρου 1. Γενικά Δυνατότητα προσδιορισμού δομών με σαφήνεια χρησιμοποιώντας τεχνικές φασματοσκοπίας Φασματοσκοπία μαζών Μέγεθος, μοριακός τύπος
3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική αναπνοή.
 5ο ΓΕΛ ΧΑΛΑΝΔΡΙΟΥ Μ. ΚΡΥΣΤΑΛΛΙΑ 2/4/2014 Β 2 ΚΕΦΑΛΑΙΟ 3 ΒΙΟΛΟΓΙΑΣ 3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική
5ο ΓΕΛ ΧΑΛΑΝΔΡΙΟΥ Μ. ΚΡΥΣΤΑΛΛΙΑ 2/4/2014 Β 2 ΚΕΦΑΛΑΙΟ 3 ΒΙΟΛΟΓΙΑΣ 3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ
 ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 5 Δομή ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Κρυσταλλικά υλικά Άμορφα υλικά Κρύσταλλος είναι ένα υλικό που παρουσιάζει τρισδιάστατη περιοδική τάξη ατόμων,
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 5 Δομή ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Κρυσταλλικά υλικά Άμορφα υλικά Κρύσταλλος είναι ένα υλικό που παρουσιάζει τρισδιάστατη περιοδική τάξη ατόμων,
ΚΕΦΑΛΑΙΟ 7 Τι είναι οι καλλιέργειες μικροοργανισμών; Τι είναι το θρεπτικό υλικό; Ποια είναι τα είδη του θρεπτικού υλικού και τι είναι το καθένα;
 ΚΕΦΑΛΑΙΟ 7 Τι είναι οι καλλιέργειες μικροοργανισμών; Καλλιέργεια είναι η διαδικασία ανάπτυξης μικροοργανισμών με διάφορους τεχνητούς τρόπους στο εργαστήριο ή σε βιομηχανικό επίπεδο. Με τη δημιουργία καλλιεργειών
ΚΕΦΑΛΑΙΟ 7 Τι είναι οι καλλιέργειες μικροοργανισμών; Καλλιέργεια είναι η διαδικασία ανάπτυξης μικροοργανισμών με διάφορους τεχνητούς τρόπους στο εργαστήριο ή σε βιομηχανικό επίπεδο. Με τη δημιουργία καλλιεργειών
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Εργαστήριο Τεχνολογίας Υλικών
 Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 02 Μεταλλογραφική Παρατήρηση Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών Πάτρα 2011
Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 02 Μεταλλογραφική Παρατήρηση Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών Πάτρα 2011
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΑΣΚΗΣΗ. Θανάσης Ζ. Τζιαμούρτας, Ph.D.
 ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΑΣΚΗΣΗ Θανάσης Ζ. Τζιαμούρτας, Ph.D. Τι είναι σακχαρώδης διαβήτης; Παθοφυσιολογική κατάσταση η οποία χαρακτηρίζεται από αυξημένη συγκέντρωση σακχάρου στο αίμα Καμπύλη σακχάρου (75
ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΑΣΚΗΣΗ Θανάσης Ζ. Τζιαμούρτας, Ph.D. Τι είναι σακχαρώδης διαβήτης; Παθοφυσιολογική κατάσταση η οποία χαρακτηρίζεται από αυξημένη συγκέντρωση σακχάρου στο αίμα Καμπύλη σακχάρου (75
Κεφάλαιο 35 ΠερίθλασηκαιΠόλωση. Copyright 2009 Pearson Education, Inc.
 Κεφάλαιο 35 ΠερίθλασηκαιΠόλωση ΠεριεχόµεναΚεφαλαίου 35 Περίθλαση απλής σχισµής ή δίσκου Intensity in Single-Slit Diffraction Pattern Περίθλαση διπλής σχισµής ιακριτική ικανότητα; Κυκλικές ίριδες ιακριτική
Κεφάλαιο 35 ΠερίθλασηκαιΠόλωση ΠεριεχόµεναΚεφαλαίου 35 Περίθλαση απλής σχισµής ή δίσκου Intensity in Single-Slit Diffraction Pattern Περίθλαση διπλής σχισµής ιακριτική ικανότητα; Κυκλικές ίριδες ιακριτική
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5
 ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
Βιολογία Β Λυκείου θέματα
 Ι. Οι υδατάνθρακες διακρίνονται σε μονοσακχαρίτες, δισακχαρίτες και πολυσακχαρίτες. α) Να αναφέρετε από δύο παραδείγματα μονοσακχαριτών, δισακχαριτών και πολυσακχαριτών. (6μ) β) Σε ένα κύτταρο συναντώνται
Ι. Οι υδατάνθρακες διακρίνονται σε μονοσακχαρίτες, δισακχαρίτες και πολυσακχαρίτες. α) Να αναφέρετε από δύο παραδείγματα μονοσακχαριτών, δισακχαριτών και πολυσακχαριτών. (6μ) β) Σε ένα κύτταρο συναντώνται
ΘΕΩΡΗΤΙΚΗ ΑΣΚΗΣΗ. Διάθλαση μέσω πρίσματος - Φασματοσκοπικά χαρακτηριστικά πρίσματος.
 Ο1 ΘΕΩΡΗΤΙΚΗ ΑΣΚΗΣΗ. Διάθλαση μέσω πρίσματος - Φασματοσκοπικά χαρακτηριστικά πρίσματος. 1. Σκοπός Όταν δέσμη λευκού φωτός προσπέσει σε ένα πρίσμα τότε κάθε μήκος κύματος διαθλάται σύμφωνα με τον αντίστοιχο
Ο1 ΘΕΩΡΗΤΙΚΗ ΑΣΚΗΣΗ. Διάθλαση μέσω πρίσματος - Φασματοσκοπικά χαρακτηριστικά πρίσματος. 1. Σκοπός Όταν δέσμη λευκού φωτός προσπέσει σε ένα πρίσμα τότε κάθε μήκος κύματος διαθλάται σύμφωνα με τον αντίστοιχο
ΜΕΤΑΦΟΡΑ ΑΕΡΙΩΝ ΠΡΟΣ ΚΑΙ ΑΠΟ ΤΟΥΣ ΣΤΟΥΣ ΙΣΤΟΥΣ
 ΜΕΤΑΦΟΡΑ ΑΕΡΙΩΝ ΠΡΟΣ ΚΑΙ ΑΠΟ ΤΟΥΣ ΣΤΟΥΣ ΙΣΤΟΥΣ Μεταφορά οξυγόνου (Ο 2 ) από τον αέρα μέσω κυψελίδων στο αίμα και ιστούς Μεταφορά διοξειδίου άνθρακα (CO 2 ) από ιστούς σε κυψελίδες Οι κλίσεις των μερικών
ΜΕΤΑΦΟΡΑ ΑΕΡΙΩΝ ΠΡΟΣ ΚΑΙ ΑΠΟ ΤΟΥΣ ΣΤΟΥΣ ΙΣΤΟΥΣ Μεταφορά οξυγόνου (Ο 2 ) από τον αέρα μέσω κυψελίδων στο αίμα και ιστούς Μεταφορά διοξειδίου άνθρακα (CO 2 ) από ιστούς σε κυψελίδες Οι κλίσεις των μερικών
