Δομικός χαρακτηρισμός πρωτεϊνών φαρμακευτικού ενδιαφέροντος
|
|
|
- Ἀριστοφάνης Λαιμός
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Δομικός χαρακτηρισμός πρωτεϊνών φαρμακευτικού ενδιαφέροντος Μεταπτυχιακή εργασία Γιαννοπούλου Ευδοκία- Αναστασία, Α.Μ. 473 Οκτώβριος
2 Ευχαριστίες: Η παρούσα μεταπτυχιακή εργασία εκπονήθηκε στο Πανεπιστήμιο Πατρών, στο Εργαστήριο Δομικής Βιολογίας του τομέα Γενετικής, Βιολογίας Κυττάρου & Ανάπτυξης του Τμήματος Βιολογίας. Η ανάθεση και η επίβλεψη της εργασίας έγιναν από την λέκτορα του τμήματος Βιολογίας, Ειρήνη Μαργιωλάκη. Θα ήθελα να ευχαριστήσω την κ. Μαργιωλάκη που μου έδωσε την ευκαιρία να συμπεριληφθώ στην ομάδα της, ανοίγοντας νέους ορίζοντες και επιτρέποντάς μου να ασχοληθώ με ένα τόσο ερευνητικά ενδιαφέρον θέμα. Ευχαριστώ επίσης τις Καραβασίλη Φωτεινή και Κοτσιλίτη Έλενα για την φιλία και τη βοήθειά τους. Ακόμα, ευχαριστώ τους κ. Αναστάσιο Μίντζα και κ. Γεώργιο Σπυρούλια που δέχτηκαν να συμμετέχουν ως μέλη της Τριμελούς Συμβουλετικής Επιτροπής. Τέλος, θα ήθελα να ευχαριστήσω τους Gerd Schluckebier, Matthias Norrman και Lene Drube της Novo Nordisk, οι οποίοι μας προσέφεραν την πρώτη ύλη για τη διεξαγωγή των πειραμάτων μας και μας έλυναν οποιαδήποτε απορία σχετικά με την ινσουλίνη και την κρυστάλλωσή της, καθώς και τους Jonathan Wright και Andrew Fitch (ESRF) για τις σημαντικές συμβουλές και τη βοήθειά τους κατά την διάρκεια της διεξαγωγής των πειραμάτων στο Ευρωπαϊκό σύγχροτρον (ESRF). Η συγκεκριμένη εργασία πραγματοποιήθηκε στα πλαίσια του προγράμματος τριετούς χρηματοδότησης του Ιδρύματος Καραθεοδωρή και της Επιτροπής Ερευνών του Πανεπιστημίου Πατρών (Επιστημονική Υπεύθυνη: κ. Ειρήνη Μαργιωλάκη, Τίτλος: Δομικός χαρακτηρισμός πρωτεϊνών φαρμακευτικού ενδιαφέροντος και προερχόμενων από ιούς με στόχο την δημιουργία νέων φαρμάκων. Κωδικός Έργου: D.211). Καθώς και της υποτροφίας της κ. Ειρήνης Μαργιωλάκη: Unesco L Oreal στα πλαίσια των διεθνών βραβείων «UNESCO- L'OREAL Cosponsored fellowships for Young Women in Life Sciences 2010» 1 Μέρος της εργασίας αυτής παρουσιάζεται στις παρακάτω δημοσιεύσεις: Karavassili, F., Giannopoulou, E.A., Kotsiliti, E., Knight, L., Norrman, M., Schluckebier, G., Drube, L., Fitch, A.N., Wright, J.P., & Margiolaki, I. Acta Cryst. D (Απόδειξη διαθέσιμη) Margiolaki, Ι., Fitch, Α.,Ν., Giannopoulou, Α.Ε., Knight, L., Norrman, M., Schluckebier, G., Von Dreele,R.B., & Wright, J.P. Acta Cryst. D (Submitted). 1 _unesco/back/18256/ 2
3 Περίληψη- Abstract Η μεταπτυχιακή εργασία αφορά στον δομικό χαρακτηρισμό πρωτεϊνών φαρμακευτικού ενδιαφέροντος. Στα πλαίσια της εργασίας πραγματοποιείται κρυστάλλωση και μετρήσεις περίθλασης ακτινών-χ. Κρυσταλλογραφικές μέθοδοι εφαρμόζονται για την ανάλυση και την ερμηνεία των πειραματικών δεδομένων. Επιπλέον, σε συνεργασία με την φαρμακευτική εταιρείαnovo Nordisk A/S μελετάμε την ενδεχόμενη δημιουργία φαρμάκων υπό την μορφή μικροκρυσταλλικών ιζημάτων η οποία έχει εφαρμοστεί ήδη στην περίπτωση της ανθρώπινης ινσουλίνης. Τα πλεονεκτήματα των μικροκρυσταλλικών φαρμάκων έναντι των φαρμάκων υπό την μορφή διαλύματος περιλαμβάνουν την μεγαλύτερη σταθερότητα, υψηλότερη συγκέντρωση φαρμακευτικής ουσίας και τον ακριβή δομικό χαρακτηρισμό του μορίου. Η τεχνική περίθλασης ακτινοβολίας από πολυκρυσταλλικά υλικά (powder diffraction) αποτελεί ένα σημαντικό εργαλείο για τον χαρακτηρισμό των διάφορων πολυμόρφων πρωτεϊνικών μικροκρυσταλλικών ιζημάτων. Για αυτό τον σκοπό, πραγματοποιούμε πειράματα κρυστάλλωσης των υπό μελέτη βιομορίων κάτω από διαφορετικές συνθήκες (ph, προσδέτες) και στη συνέχεια, συλλέγουμε δεδομένα περίθλασης ακτινών-χ από επιλεγμένα δείγματα, χρησιμοποιώντας όργανα υψηλής ευκρίνειας που βρίσκονται σε ερευνητικά ινστιτούτα μεγάλης κλίμακας (Ευρωπαϊκό σύγχροτρον, ESRF, Grenoble, France & Ελβετικό σύγχροτρον, SLS, Villigen, Switzerland). 3
4 Περιεχόμενα 1. Εισαγωγή Θεωρία Διαβήτης Ινσουλίνη Βιοσύνθεση της Ινσουλίνης Μηχανισμός δράσης της ινσουλίνης Θεραπευτική χρήση Θεωρία της Κρυστάλλωσης Πρωτεϊνών Φάσεις Κρυστάλλωσης Παράγοντες που επηρεάζουν την κρυστάλλωση Κρυσταλλικός πολυμορφισμός Μέθοδοι κρυστάλλωσης Πολυκρυσταλλικά φάρμακα Αρχές της Κρυσταλλογραφίας Έννοιες Συμμετρίας Ατομικά επίπεδα και Παράμετροι Miller Περίθλαση Ακτίνων-Χ Νόμος του Bragg Αντίστροφο Πλέγμα (Reciprocal Lattice) Η Σφαίρα του Ewald Ατομικός Παράγοντας σκέδασης και Παράγοντας Δομής Ηλεκτρονιακή Πυκνότητα και το πρόβλημα φάσης Περίθλαση Ακτίνων-Χ από πολυσκρυσταλλικά υλικά (X-ray Powder Diffraction) General και Systematic Absences Όργανα και Μέθοδοι Σύγχροτρον- Ακτινοβολία Σύγχροτρον Το Ευρωπαϊκό (ESRF) και το Ελβετικό Σύγχροτρον (SLS) Πειραματικοί σταθμοί- Beamlines Μέθοδοι και πειραματική διαδικασία Συγκρυστάλλωση ινσουλίνης με οργανικούς προσδέτες Συλλογή δεδομένων Περίθλασης Ακτίνων-Χ Επεξεργασία δεδομένων- Προγράμματα Αποτελέσματα
5 4.1. Ανθρώπινη ινσουλίνη κρυσταλλωμένη με φαινόλη Ανθρώπινη ινσουλίνη κρυσταλλωμένη με m-cresol Ανθρώπινη ινσουλίνη κρυσταλλωμένη με 4-nitrophenol Ανθρώπινη ινσουλίνη κρυσταλλωμένη με 4-ethyl-resorcinol Η περίπτωση της T 6 Bovine ινσουλίνης Συζήτηση Bιβλιογραφία
6 1. Εισαγωγή Γενικά Η Δομική Βιολογία έχει εξελιχθεί σε μια επιστήμη που κατέχει βασικό ρόλο στην κατανόηση των διάφορων μηχανισμών της ζωής. Η γνώση της δομής σε ατομικό επίπεδο είναι πολύ σημαντική για την πρόβλεψη της συμπεριφοράς και της λειτουργίας ενός μορίου. Τα τελευταία εκατό περίπου χρόνια, η κρυσταλλογραφία έχει συνεισφέρει σε μεγάλο βαθμό στην επέκταση της γνώσης και της κατανόησης της ατομικής δομής της ύλης. Στην αρχή αυτού του αιώνα, με τη βοήθεια της κρυσταλλογραφίας αποκαλύφθηκαν οι πρώτες ατομικές διατάξεις σε δομές αλάτων, ορυκτών και μικρού μοριακού βάρους οργανικών και μέταλλο-οργανικών ουσιών. Στη συνέχεια, μία προς μία, οι δομές των βιολογικών μορίων άρχισαν να αποκαλύπτονται σε ατομικό επίπεδο και με πολύ μεγάλη ακρίβεια, αρχίζοντας το 1950, όταν η περίθλαση ινιδίων βοήθησε στην επίλυση της δομής του DNA και έπειτα, των δομών πολυσακχαριτών, ινωδών πρωτεϊνών και νηματοειδών ιών. Σαν επακόλουθο, επικράτησε η μέθοδος περίθλασης από μονοκρύσταλλο και οι δομές που επιλύθηκαν τη δεκαετία του 1960 συμπεριλάμβαναν την μυοσφαιρίνη, την αιμοσφαιρίνη και τη λυσοζύμη, οι οποίες θεωρήθηκαν «ηρωϊκά» επιτεύγματα από την επιστημονική κοινότητα. Σήμερα περίπου 5 με 10 πρωτεϊνικές δομές επιλύονται καθημερινά, το 85% των οποίων μέσω κρυσταλλογραφικών μεθόδων και το 15% από τη μέθοδο NMR (Πυρηνικός Μαγνητικός Συντονισμός). To 1912, o Max Von Laue ανακάλυψε ότι οι κρυσταλλικές ουσίες μπορούν να λειτουργήσουν σαν τρισδιάστατα φράγματα περίθλασης, για ακτίνες-χ με μήκη κύματος συγκρίσιμα με τις αποστάσεις ανάμεσα στα επίπεδα ενός κρυσταλλικού πλέγματος. Πλέον, η περίθλαση ακτίνων-χ είναι μια κοινή τεχνική που χρησιμοποιείται για την μελέτη των κρυσταλλικών δομών και των ατομικών αποστάσεων. Παρ όλα αυτά, ένα από τα κύρια προβλήματα της μεθόδου αυτής είναι η απόκτηση κρυστάλλου κατάλληλου μεγέθους και ποιότητας. Τέτοιοι κρύσταλλοι είναι συχνά πολύ δύσκολο, εως αδύνατο να αποκτηθούν και τότε οι δομικοί βιολόγοι επικεντρώνονται σε άλλες τεχνικές επίλυσης της δομής του προς-ανάλυση-μορίου. 6
7 Μεταξύ άλλων, μπορούμε να αναφέρουμε τον Πυρηνικό Μαγνητικό Συντονισμό (Nuclear Magnetic Resonance, NMR) που μπορεί να χρησιμοποιηθεί για τον καθορισμό της δομής πρωτεϊνών ή πεπτιδίων σε μορφή διαλύματος. Η τεχνική αυτή προσφέρει καθαρό προβάδισμα σε σχέση την κρυστάλλωση, η οποία δεν είναι απαραίτητη για την εφαρμογή του NMR. Έχοντας το μόριο που μας ενδιαφέρει σε διαλυτή μορφή γίνεται δυνατή η διερεύνηση των δυναμικών του ιδιοτήτων, προσφέροντας, πιθανώς, γνώση για τη βιολογική του δραστηριότητα. Ωστόσο, η τεχνική NMR περιορίζεται σε μόρια πρωτεϊνών, το μέγεθος των οποίων συνήθως δε ξεπερνά τα 100 kda, περιορίζοντας έτσι το εύρος των μορίων που μπορούν να μελετηθούν. Μια άλλη τεχνική είναι η Σκέδαση Ακτίνων-Χ Μικρών Γωνιών (Small Angle X-ray Scattering, SAXS), η οποία δεν έχει κάποιο περιορισμό όσον αφορά το μέγεθος της πρωτεΐνης. Παρ όλα αυτά, η μέθοδος SAXS μπορεί να δώσει πληροφορίες μόνο για τον αριθμό και το σχήμα των διατεταγμένων επικρατειών της πρωτεΐνης, χωρίς επιπλέον πληροφορίες για τις λεπτομερείς θέσεις των ατόμων. Επιπλέον, η Ηλεκτρονική Μικροσκοπία (Electron Microscopy, EM) είναι μια τεχνική ιδιαίτερα χρήσιμη για την διερεύνηση της δομής μεγάλων πρωτεϊνικών συμπλεγμάτων ή συγκροτημάτων όπως είναι για παράδειγμα οι ιοί. Αντίθετα από την κρυσταλλογραφία ακτίνων-χ και το NMR, η ευκρίνεια που αποκτάται από δεδομένα EM είναι πολύ πιο μικρή και τυπικά δεν μπορεί να προσδώσει καμία πληροφορία σε ατομικό επίπεδο. Εντούτοις, ακόμα και δεδομένα μικρής ευκρίνειας μπορούν να προσφέρουν γνώση για την οργάνωση των πρωτεϊνικών συμπλεγμάτων και κατ επέκταση, κατανόηση της βιολογικής τους λειτουργίας. Τέλος, μπορεί να χρησιμοποιηθεί μια καθαρά υπολογιστική προσέγγιση, κατά την οποία η δομή της πρωτεΐνης «προβλέπεται» είτε από την αλληλουχία των αμινοξέων, είτε «μοντελοποιείται» με βάση την ομοιότητα της αμινοξικής αλληλουχίας με την αλληλουχία μιας άλλης πρωτεΐνης με γνωστή τρισδιάστατη δομή. Η τεχνική της περίθλασης ακτίνων-χ είναι, παρά τους περιορισμούς της, η πιο συχνά χρησιμοποιούμενη και πλέον ακριβέστερη μέθοδος για την επίλυση δομών πρωτεϊνών. Όπως αναφέρθηκε, κύριο προαπιτούμενο για την εφαρμογή αυτής της μεθόδου είναι η ύπαρξη ενός μονοκρυστάλλου της πρωτεΐνης που μας 7
8 ενδιαφέρει. Ωστόσο, η απόκτηση ενός τέτοιου μονοκρυστάλλου είναι συνήθως μια χρονοβόρα και επίπονη διαδικασία καθώς δημιουργούνται παράλληλα διάφορα παραπροϊόντα, όπως κρυσταλλικά ιζήματα, τα οποία περιέχουν μεγάλο ποσοστό πληροφοριών για τη δομή. Αυτά τα κρυσταλλικά ιζήματα αποτελούνται από μεγάλο αριθμό τυχαία προσανατολισμένων μικροκρυστάλλων, οι οποίοι έχουν ακριβώς την ίδια φύση με έναν μονοκρύσταλλο, εκτός βέβαια από το μικρότερο μέγεθος. Ένας μονοκρύσταλλος χρειάζεται να είναι αρκετά μεγάλος ώστε να δώσει σήμα περίθλασης. Ένας μικροκρύσταλλος προερχόμενος από κρυσταλλικό ίζημα λόγω του μικρού του μεγέθους, δεν δίνει ισχυρό σήμα περίθλασης, συγκριτικά με ένα πείραμα από μονοκρύσταλλο. Το ίζημα στο σύνολό του, εντούτοις, το οποίο περιέχει χιλιάδες μικροκρυστάλλους, θα μπορούσε να δώσει αρκετά ισχυρό σήμα περίθλασης, δυνατό να καταγραφεί. Σε αυτή τη περίπτωση, επειδή καταγράφεται η περίθλαση από χιλιάδες κρυστάλλους ταυτόχρονα, το πείραμα μπορεί να χαρακτηριστεί ως «Περίθλαση Ακτίνων-Χ από Πολυκρυσταλλικά Υλικά» (X-ray Powder Diffraction). Αντίθετα με ένα πείραμα περίθλασης από μονοκρύσταλλο, σε αυτή την περίπτωση είναι αδύνατο να επιτευχθεί ο ίδιος προσανατολισμός για όλους τους μικροκρυστάλλους, καθώς τις περισσότερες φορές είναι τυχαία προσανατολισμένοι. Για αυτό το λόγο, το διάγραμμα περίθλασης που προκύπτει αποτελείται από ομόκεντρους δακτυλίους, οι οποίοι είναι αποτέλεσμα της συμβολής όλων των εντάσεων από τις ανακλάσεις με το ίδιο d-spacing. Η μέθοδος περίθλασης Ακτίνων-Χ από Πολυκρυσταλλικά Υλικά αναπτύχθηκε στις αρχές του 20 ου αιώνα από τους Debye και Scherrer και αρχικά χρησιμοποιούταν για ποιοτικές αναλύσεις φάσης, ημι-ποσοτικές αναλύσεις φάσεις, καθώς και μετρήσεις του στρες των υλικών. Η καθυστέρηση της χρήσης αυτής της τεχνικής για τον προσδιορισμό της δομής, οφείλεται στην εγγενή δυσκολία της περίθλασης από τέτοιου είδους πολυκρυσταλλικά υλικά. Η δυσκολία αυτή είναι αποτέλεσμα της τυχαίας ή συστηματικής αλληλεπικάλυψης δεδομένων από ανακλάσεις, καθώς ο τρισδιάστατος «αντίστροφος χώρος» (reciprocal space) προβάλλεται σε μία διάσταση (άξονας 2θ). Η βελτίωση των οργάνων και των πηγών ακτίνων-χ, σε συνδυασμό με την εξέλιξη νέων υπολογιστικών συστημάτων επέτρεψε την χρήση της περίθλασης ακτίνων-χ 8
9 από πολυκρυσταλλικά υλικά ως μέσο για την ανάλυση δομών πολλών χημικών μορίων. Υπάρχουν πολλές πιθανές εφαρμογές για τη μελέτη πρωτεϊνών μέσω της τεχνικής Powder Diffraction. Η τεχνική αυτή μπορεί να χρησιμοποιηθεί σαν εργαλείο αξιολόγησης της κρυσταλλικής ποιότητας των δειγμάτων που παράγονται, καθώς και σε περιπτώσεις ελέγχου των συνθήκων κρυστάλλωσης (screening), προκειμένου να γίνει επιλογή της πιο αποδοτικής συνθήκης. Επιπλέον, η πιο ενδιαφέρουσα χρήση της μεθόδου Powder Diffraction, αν και μακρόχρονη, είναι η επίλυση νέων δομών. Ένας από τους περιοριστικούς παράγοντες της τεχνικής σχετικά με την εφαρμογή της σε βιολογικά μόρια όπως οι πρωτεΐνες είναι η ποσότητα του πρωτεϊνικού δείγματος που είναι απαραίτητο για ένα πείραμα περίθλασης από πολυκρυσταλλικά υλικά. Η έκφραση και ο καθαρισμός (expression and purification) της επιθυμητής πρωτεΐνης, απαραίτητες διαδικασίες για τη σωστή κρυστάλλωσή της, είναι ιδιαίτερα χρονοβόρες, και ειδικά για τα πειράματα powder diffraction που χρειάζονται σχετικά μεγάλες ποσότητες πρωτεΐνης. Η τεχνική powder diffraction έχει αξιοποιηθεί σαν μέθοδος ταυτοποίησης διάφορων κρυσταλλικών ουσιών, καθώς επιτρέπει την γρήγορη αναγνώριση και ποσοτικοποίηση μιγμάτων. Όργανα υψηλής ευκρίνειας χρησιμοποιούνται για την απόκτηση όσο το δυνατόν «στενότερων» κορυφών στον αντίστροφο χώρο και για τον προσδιορισμό των ακριβών θέσεων των κορυφών. Η χρήση δεδομένων Σύγχροτρον υψηλής ευκρίνειας σε συνδυασμό με νέες διαδικασίες ανάλυσης, προκάλεσε την εξέλιξη της μεθόδου Powder Diffraction σε μια ισχυρή, συμπληρωματική τεχνική για το δομικό χαρακτηρισμό των πρωτεϊνων (Margiolaki, Wright, Fitch et al., 2007; Margiolaki & Wright, 2008). Μικροκρυσταλλικά δείγματα μπορούν να αποκτηθούν εύκολα για μεγάλο εύρος πρωτεϊνών μέσω καθίζησης με τη μέθοδο batch, γεγονός ιδιαίτερα σημαντικό καθώς προσφέρει πλεονέκτημα έναντι της απόκτησης μονοκρυστάλλων, η οποία είναι μια δύσκολη και χρονοβόρα διαδικασία. Για αυτό το λόγο, οι μέθοδοι που αξιοποιούν τη δημιουργία πολυκρυσταλλικών ιζημάτων είναι ιδανικές για τη μελέτη συνθηκών κρυστάλλωσης μεγάλου ευρους παραμέτρων, αφού 9
10 επιτρέπουν την ταυτοποίηση μικροκρυσταλλικών και άμορφων ιζημάτων. Τα πολυκρυσταλλικά δείγματα αποτελούνται από μεγάλο αριθμό τυχαία προσανατολισμένων μικροκρυστάλλων. Αυτοί οι μικροκρύσταλλοι περιθλούν τις ακτίνες-x σε διαφορετικές κατευθύνσεις, προκαλώντας την αλληλεπικάλυψη των τρισδιάστατων δεδομένων πάνω σε έναν ανιχνευτή. Η απώλεια πληροφοριών λόγω αυτής της αλληλεπικάλυψης επιδεινώνεται σταδιακά σε υψηλότερες γωνίες, το οποίο τείνει να κάνει πολύπλοκη την δομική ανάλυση σε σχέση με μεθόδους μονοκρυστάλλων. Η πρώτη επίλυση πρωτεϊνικής δομής από πολυκρυσταλλικά δεδομένα αναφέρεται το 1999 από τον Von Dreele, ο οποίος χρησιμοποίησε δεδομένα υψηλής ευκρίνειας από κρυστάλλους της T3R3 μορφής της ανθρώπινης ινσουλίνης με ψευδάργυρο. Σε αυτή τη διπλωματική εργασία, χρησιμοποιείται η μέθοδος περίθλασης ακτίνων-χ από πολυκρυσταλλικά υλικά για το δομικό χαρακτηρισμό της ιδιαίτερα πολυμορφικής πρωτεΐνης ινσουλίνης. Η ινσουλίνη μπορεί να κρυσταλλωθεί σε διαφορετικές συνθήκες ph και με μεγάλο εύρος οργανικών προσδετών (ligands), δημιουργώντας κρυστάλλους οι οποίοι αντιστοιχούν σε διαφορετικές κρυσταλλογραφικές συμμετρίες. 10
11 2. Θεωρία 2.1. Διαβήτης Ο Diabetes mellitus ή απλούστερα, διαβήτης, είναι μια ομάδα μεταβολικών ασθενειών που προκαλούνται από χαμηλά επίπεδα ή χαμηλή ευαισθησία στην πρωτεϊνική ορμόνη ινσουλίνη. Η ινσουλίνη είναι μια ορμόνη που παράγεται από τα β-κύτταρα των νησίδων του Langerhans του παγκρέατος και κατέχει ιδιαίτερα σημαντικό ρόλο στην ρύθμιση του μεταβολισμού των υδατανθράκων και των λιπών του σώματος. Κύρια αποτέλεσματα της δράσης της είναι η πρόσλήψη της γλυκόζης που βρίσκεται στην κυκλοφορία του αίματος από τα κύτταρα του ήπατος, των μυών και του λιπώδη ιστού. Στη συνέχεια, η γλυκόζη αποθηκεύεται στους συγκεκριμένους ιστούς με τη μορφή του γλυκογόνου. Υπάρχουν δύο κύριοι τύποι διαβήτη. Ο διαβήτης τύπου 1 είναι αποτέλεσμα της αδυναμίας του σώματος να παράγει ινσουλίνη και για την αντιμετώπισή του είναι απαραίτητη η πρόσληψη ινσουλίνης. Για αυτό το λόγο, αναφέρεται συχνά και ως ινσουλινο-εξαρτώμενος διαβήτης (Insulin-dependent diabetes mellitus, IDDM). O διαβήτης τύπου 1 χαρακτηρίζεται από την απώλεια των β-κυττάρων του παγκρέατος, τα οποία, όπως αναφέρθηκε, είναι υπεύθυνα για την παραγωγή ινσουλίνης, οδηγώντας σε έλλειψη αυτής της ορμόνης. Αυτός ο τύπος διαβήτη μπορεί να χαρακτηριστεί ως ανοσο-διαμεσολαβούμενος ή ιδιοπαθής. Η πλειοψηφία των ασθενών με διαβήτη τύπου 1 πάσχουν από την ανοσο-διαμεσολαβούμενη μορφή, στην οποία τα β-κύτταρα αναγνωρίζονται ως «ξένα» από τον οργανισμό και εξαλείφονται από τα Τ κύτταρα ως αυτοάνοση απόκριση. Ο τύπος 1 εμφανίζεται συνήθως σε νεαρής ηλικίας άτομα, τα οποία για την αντιμετώπιση των συμπτωμάτων της νόσου χρειάζονται δια βίου παροχή εξωγενούς ινσουλίνης. Από την άλλη, ο διαβήτης τύπου 2 είναι αποτέλεσμα της αντίστασης του οργανισμού στην ινσουλίνη, μια κατάσταση στην οποία τα κύτταρα δεν μπορούν να χρησιμοποιήσουν την ινσουλίνη σωστά, ενώ μπορεί να οδηγήσει αρκετές φορές και σε πλήρη ανεπάρκεια ινσουλίνης. Αυτή η μορφή του διαβήτη αναφέρεται πολλές φορές και ως μη-ινσουλινο-εξαρτώμενος διαβήτης (Non 11
12 insulin dependent diabetes mellitus, NIDDM) ή αλλιώς, «διαβήτης των ενηλίκων». Πιο συγκεκριμένα χαρακτηρίζεται από υψηλό βαθμό αντίστασης στην ινσουλίνη, η οποία μπορεί να συνδυαζεται σε ορισμένες περιπτώσεις και με πολύ μειωμένα επίπεδα έκκρισής της. Η ελαττωματική απόκριση των ιστών του σώματος στην ινσουλίνη φαίνεται να έχει σχέση με τον υποδοχέα της ορμόνης, αν και δεν είναι γνωστή ακόμα η ακριβής αιτία. Για την αντιμετώπιση αυτού του τύπου διαβήτη δεν είναι πάντοτε απαραίτητη η πρόσληψη εξωγενούς ινσουλίνης, καθώς η σωστή διατροφή και η άσκηση μπορούν να μειώσουν την εμφάνιση των συμπτωμάτων της νόσου. Παρ όλα αυτά, συμπληρωματική θεραπεία με αντιδιαβητικά φάρμακα (Oral Antidiabetic Agents, OADs) είναι πολλές φορές απαραίτητη. Τα φάρμακα αυτά δρουν διεγείρωντας την έκκριση της ινσουλίνης, παρεμποδίζοντας την πρόσληψη της γλυκόζης δια μέσου του πεπτικού συστήματος ή και μειώνοντας την σύνθεση της γλυκόζης και της απελευθέρωσής της από το ήπαρ. Ένας τρίτος τύπος διαβήτη, ο διαβήτης της κύησης, εμφανίζεται μόνο σε έγκυες γυναίκες οι οποίες δεν έχουν διαγνωστεί με την ασθένεια προηγουμένως, προκαλώντας αυξημένα επίπεδα γλυκόζης στο αίμα. Από τους δύο προαναφερθέντες τύπους διαβήτη, ο τύπος 2 είναι ο πιο ευρέως εξαπλωμένος. Σύμφωνα με τον Παγκόσμιο Οργανισμό Υγείας (World Health Organisation, WHO) ο διαβήτης είναι μια από τις παγκόσμιες απειλές για την δημόσια υγεία Ινσουλίνη Μια από τις πρωταρχικές λειτουργίες της ινσουλίνης είναι η διέγερση της πρόσληψη της γλυκόζης από τη συστηματική κυκλοφορία του αίματος, καθώς και η καταστολή της ηπατικής γλυκονεογένεσης δίνοντας της έτσι έναν πρωταρχικό ρόλο στην ομοιόσταση της γλυκόζης και στην παρεμπόδιση της εμφάνισης της μεταβολικής ασθένειας του διαβήτη. Η ινσουλίνη ήταν η πρώτη πεπτιδική ορμόνη που ανακαλύφθηκε. Πριν την κρυσταλλώσει ο Abel, το 1926, και οι Jensen και Evans κατάφεραν να 12
13 υδρολύσουν την φαινυλαλανίνη του Ν-τελικού άκρου της, αποδεικνύοντας ότι η ινσουλίνη είναι όντως πρωτεΐνη, όλες οι ορμόνες θεωρούνταν μικρά μόρια. Η ινσουλίνη είναι μια αναβολική πεπτιδική ορμόνη που αποτελείται από 51 αμινοξέα και εκκρίνεται από τα β- κύτταρα των νησίδων του Langerhans. Αποτελείται από δύο πολυπεπτιδικές αλυσίδες, τις ονομαζόμενες Α και Β, οι οποίες αποτελούνται από 21 και 30 αμινοξέα αντίστοιχα, ενώ έχει μοριακή μάζα ~5808 Da. Οι δύο αλυσίδες συνδέονται μεταξύ τους με δύο δισουλφιδικές γέφυρες ανάμεσα στα αμινοξέα CysΑ7-CysΒ7 και CysΑ20- CysΒ19, ενώ μια τρίτη δισουλφιδική γέφυρα ενώνει τα αμινοξέα CysΑ6- CysΑ11. Η μεγαλύτερη Β αλυσίδα έχει επιμηκυσμένη διαμόρφωση (extended conformation) και στα δύο άκρα στις περιοχές Β1-Β8 και Β20-Β30, ενώ το κεντρικό τμήμα έχει διαμόρφωση α- έλικας. Η ινσουλίνη σε διάλυμα υπάρχει σε μορφή μονομερούς, αλλά παρουσία αλάτων και δισθενών ιόντων (όπως ο ψευδάργυρος) συγκεντώνεται σε διμερή και εξαμερή. Το εξαμερές μπορεί να θεωρηθεί ένα τριμερές διμερών όπου δύο άτομα ψευδαργύρου βρίσκονται τοποθετημένα στο κέντρο του, δημιουργώντας δεσμούς είτε με τρεις ιστιδίνες (HisB10) και ένα ανιόν (τετραεδρική συμμετρία) είτε τρεις ιστιδίνες (HisB10) και τρία μόρια νερού (οκταεδρική συμμετρία). Εικόνα 1: Δημιουργία του εξαμερούς της ινσουλίνης. Μια Β αλυσίδα (μπλε) συνδέεται με μια Α αλυσίδα (ροζ) και σχηματίζουν ένα μονομερές. Έξι τέτοια μονομερή παρουσία 2 ατόμων ψευδαργύρου (κόκκινη σφαίρα) δημιουργούν ένα εξαμερές. (Πηγή: Margiolaki et al., submitted). 13
14 Η δομή της ινσουλίνης περιγράφηκε πρώτη φορά το 1969 από τον Adams και τους συνεργάτες του, όταν κατάφεραν να παράξουν κρυστάλλους Εικόνα 2: Οι τρεις διαφορετικές διαμορφώσεις του εξαμερούς της ινσουλίνης (α) R6, (b) T3R3 f, (c) T6. (πηγή: Norrman et al., 2006) ρομβοεδρικής συμμετρίας. Έχει βρεθεί ότι ανάλογα με τις συνθήκες κρυστάλλωσης, τα εξαμερή της ινσουλίνης μπορούν να καταλάβουν τρεις διαφορετικές διαμορφώσεις (Kaarsholm et al., 1989). Η αλλοστερικές ιδιότητες του εξαμερούς της ινσουλίνης έχουν διερευνηθεί σε βάθος. Έχουν βρεθεί δύο αλλοστερικές θέσεις πρόσδεσης: μια θέση πρόσδεσης ανιόντων και μια θέση πρόσδεσης φαινολικών παραγόγων. Σε χαμηλές συγκεντρώσεις ανιόντων (κυρίως Cl - και SCN - ) και χωρίς προσθήκη φαινολικών παραγόγων αποκτάται η διαμόρφωση T6 (Baker et al., 1988, Smith et al., 2003), στην οποία ο Zn είναι οκταεδρικά συντονισμένος και το Ν-τελικό άκρο της B αλυσίδας (αμινοξέα Β1-Β8) είναι επιμηκυσμένο σε όλα τα μονομερή του εξαμερούς. Η διαμόρφωση R6 (Derewenda et al., 1989, Smith and Dodson, 1992) όπου τα αμινοξέα Β1-Β8 του Ν-τελικού άκρου κάθε Β αλυσίδας του εξαμερούς έχουν μορφή α-έλικας, αποκτάται με προσθήκη φαινολικών παραγόγων και ανιόντων. Τέλος, μια ενδιάμεση διαμόρφωση T3R3 f (Ciszac et al., 1994; Whittingham et al., 1995) η οποία αποκτάται με ενδιάμεσες συγκεντρώσεις φαινολικών παραγόγων και ανιόντων, χαρακτηρίζεται από επιμηκυσμένη διαμόρφωση των τριών μονομερών (αμινοξέα Β1-Β8) ενώ τα άλλα τρία μονομερή παρουσιάζουν ελικοειδή διαμόρφωση στα αμινοξέα Β4-Β8 και επιμηκυσμένη στα Β1-Β3 (βλ. Εικόνα 2). Στον παρακάτω πίνακα συνοψίζονται όλες οι γνωστές δομές της ινσουλίνης καθώς και η διαμόρφωσή τους σε σχέση με την Β-αλυσίδα. 14
15 Κρυσταλλικό Space group Διαμόρφωση Κωδικός PDB Σύστημα Β-αλυσίδας Μονοκλινές P2 1 R 6 1EV6 Μονοκλινές C2 R 6 2OLZ, 2OLY Κυβικό I2 13 T 6 1APH Ρομβοεδρικό R3 R 6 1EV3 Ρομβοεδρικό R3 T 6 1MSO Ρομβοεδρικό R3 T 3R f 3 1TRZ Τετραγωνικό P R 6 7INS Ορθορομβικό C222 1 R 6 2OM0, 2OM1 Πίνακας 1: Τα σημαντικότερα space group στα οποία κρυσταλλώνεται η ινσουλίνη Βιοσύνθεση της Ινσουλίνης Η ινσουλίνη συντίθεται αρχικά ως προ-προϊνσουλίνη (pre-proinsulin, ~12 kda) που μεταγράφεται από το γονίδιο INS στα β-κύτταρα των νησίδων του Langerhans του παγκρέατος. Η σύνθεσή της Εικόνα 3: Ο γενετικός τόπος του γονιδίου INS του ανθρώπου βρίσκεται στο 11 ο χρωμόσωμα, στη θέση 11p15.5. (πηγή: ρυθμίζεται στο επίπεδο μεταγραφής του mrna καθώς και στο επίπεδο μετάφρασης της προ-προϊνσουλίνης, από την αύξηση των επιπέδων γλυκόζης. Ο μηχανισμός της βιοσύνθεσης και της επεξεργασίας του πρόδρομου μορίου της ινσουλίνης στην ενεργή της μορφή γίνεται μέσω μεταμεταφραστικών τροποποιήσεων. Αρχικά, όταν η προ-προϊνσουλίνη μεταγραφεί σαν ενιαία πολυπεπτιδική αλυσίδα συνίσταται εκτός από τα τμήματα που θα αποτελέσουν τις αλυσίδες Α και Β, από μια επιπλέον σηματοδοτική αλληλουχία 24 υδρόφοβων αμινοξέων στο Ν-τελικό της άκρο, καθώς και ένα συνδετικό C-πεπτίδιο 31 αμινοξέων ανάμεσα στα τμήματα Α και Β. Μέσα στον αυλό του ενδοπλασματικού δικτύου, η προ-προϊνσουλίνη τροποποιείται μετά-μεταγραφικά με αφαίρεση της σηματοδοτικής αλληλουχίας μέσω του ενζύμου πεπτιδάση σήματος (signal peptidase) και στη συνέχεια υπόκειται ταχεία αναδίπλωση και σχηματισμό δισουλφιδικών δεσμών, προκειμένου να λάβει την ενγενή τριτοταγή δομή της 15
16 προϊνσουλίνης (proinsulin). Η προκύπτουσα προϊνσουλίνη αποτελείται από 86 αμινοξέα, οπού τα τμήματα Α και Β συνδέονται μέσω του πεπτιδίου-c. Το πρόδρομο αυτό μόριο μεταφέρεται στο σύμπλεγμα Golgi όπου η παρουσία δισθενών ιόντων ψευδαργύρου Zn 2+ δημιουργεί εξαμερή προϊνσουλίνης. Η δημιουργία εξαμερών στο εσωτερικό των αποθηκευτικών κυστιδίων προστατεύει τα μόρια από ενζυματική αποικοδόμηση. Η συγκέντρωση των αποθηκευτικών κυστιδίων σε ψευδάργυρο είναι από τις πιο υψηλές στο ανθρώπινο σώμα, υποδεικνύοντας την σημαντικότητά του όσον αφορά την αποθήκευση και την έκκριση της ινσουλίνης. Με τον σχηματισμό των αποθηκευτικών κυστιδίων, η προϊνσουλίνη μετατρέπεται σε ινσουλίνη μέσω πρωτεολυτικής αποκοπής του πεπτιδίου-c από δύο ειδικές ενδοπεπτιδάσες (prohormone convertases, PC1 και PC2). Η απομάκρυνση του πεπτιδίου-c προκαλεί πτώση της διαλυτότητας του εξαμερούς, έχοντας ως αποτέλεσμα την κρυστάλλωση του εξαμερούς, συμβάλλοντας επίσης στην προστασία του μορίου από πρωτεόλυση. Όταν γίνει απαραίτητο, η ινσουλίνη απελευθερώνεται μέσω εξωκυττάρωσης κατά την οποία τα αποθηκευτικά κυστίδια συντήκονται με την κυτταροπλασματική μεμβράνη των β-κυττάρων. Καθώς η ινσουλίνη απελευθερώνεται στην αιματική κυκλοφορία, το ph του περιβάλλοντός τους μεταβάλλεται από ~5.5 σε ~7.4. Παράλληλα, η συγκέντρωση των ιόντων ψευδαργύρου μειώνεται δραματικά, προκαλώντας την αποσυσχέτιση τους από τα εξαμερή και στη συνέχεια, την αποσταθεροποίηση των εξαμερών. Οι δύο παραπάνω παράγοντες προκαλούν την διάσπαση των εξαμερών σε μονομερή και διμερή. Σηματοδοτική αλληλουχία: χαρακτηριστική αλληλουχία στο N-τελικό άκρο των εκκρινόμενων προωτεϊνών, υπεύθυνη για τη μεταφορά τους στον αυλό του αδρού ενδοπλασματικού δικτύου (ER) μέσω αλληλεπιδράσεων της σηματοδοτικης αλληλουχίας με το στοιχείο απόκρισης του υποδοχέα SRP (Signal Recognition Particle) στην μεμβράνη του ER. 16
17 Εικόνα 4: Βιοσύνθεση της ινσουλίνης. ( Μηχανισμός δράσης της ινσουλίνης Είναι γνωστό ότι ειδικοί μεμβρανικοί μεταφορείς διευκολύνουν την μετακίνηση της γλυκόζης μέσα στα κύτταρα ως απόκριση διέγερσης από την ινσουλίνη, προκειμένου να μειώσουν τα επίπεδα της γλυκόζης στο αίμα. Η γλυκόζη που έχει μεταφερθεί χρησιμοποιείται στη συνέχεια σαν μεταβολικό «καύσιμο» ή αποθηκεύεται με τη μορφή μιας περίπλοκης μακρομοριακής δομής, του γλυκογόνου. Ο υποδοχέας της ινσουλίνης, όπως ισχύει γενικότερα για τις πρωτεϊνικές ορμόνες, βρίσκεται ενσωματωμένος στην κυτταροπλασματική μεμβράνη των κυττάρων. Αποτελείται από δύο υπομονάδας α και δύο β, οι οποίες συνδέονται μεταξύ τους μέσω δισουλφιδικών δεσμών. Οι αλυσίδες α, στις οποίες βρίσκεται η επικράτεια πρόσδεσης της ινσουλίνης, εντοπίζεται εξωκυτταρικά, ενώ οι δύο 17
18 αλυσίδες β διαπερνούν την μεμβράνη. Ο υποδοχέας της ινσουλίνης (Insulin Receptor, IR) είναι μια κινάση τυροσίνης. Με άλλα λόγια, λειτουργεί σαν ένζυμο που μεταφέρει φωσφρορικές ομάδες από το ATP στην τυροσύνη ενδοκυτταρικών πρωτεϊνών-στόχων. Πρόσδεση της ινσουλίνης στις α επικράτειες προκαλεί την αυτο-φωσφορυλίωση των β επικρατειών, με αποτέλεσμα την ενεργοποίηση της καταλυτικής ενεργότητας του υποδοχέα. Ο ενεργός υποδοχέας στη συνέχεια φωσφορυλιώνει έναν αριθμό ενδοκυτταρικών πρωτεϊνών, μεταβάλοντας την δράση τους και προκαλόντας βιολογική απόκριση. Εικόνα 5: Δομή του υποδοχέα της ινσουλίνης IR (Πηγή: ) Διάφορες ενδοκυτταρικές πρωτεΐνες έχουν ταυτοποιηθεί ως υποστρώματα φωσφορυλίωσης του υποδοχέα της ινσουλίνης, γνωστότερο από τα οποία είναι το IRS-1 (Insulin receptor substrate-1). Όταν ενεργοποιηθεί ο IRS-1 με τη φωσφορυλίωση, λειτουργεί σαν «βάση σύνδεσης» για την πρόσληψη και ενεργοποίηση άλλων ενζύμων που είναι απαραίτητα για να παράγουν την απόκριση στο σήμα της ινσουλίνης. Μεταβολισμός των υδατανθράκων Η γλυκόζη απελεθερώνεται από την υδρόλυση υδατανθράκων που προέρχονται κυρίως από την τροφή και απορροφάται στην κυκλοφορία του αίματος από το λεπτό έντερο. Υψηλά επίπεδα γλυκόζης στο αίμα διεγείρουν την απελευθέρωση της ινσουλίνης, η οποία επιδρά στα κύτταρα του σώματος για να προκαλέσει την πρόσληψη, χρήση και την αποθήκευση της γλυκόζης. Οι επιδράσεις της ινσουλίνης στο μεταβολισμό της γλυκόζης ποικίλουν ανάλογα με τον ιστό-στόχο. Οι δύο κυριότερες είναι: Η ινσουλίνη διευκολύνει την είσοδο της γλυκόζης στα κύτταρα του μυϊκού, λιπώδους καθώς και άλλων ιστών. Ο μόνος μηχανισμός με τον οποίο τα κύτταρα μπορούν να προσλάβουν γλυκόζη είναι μέσω 18
19 διευκολυνόμενης διάχυσης διαμέσου μιας οικογένειας μεταφορέων εξόζης. Σε πολλούς ιστούς, όπως για παράδειγμα στον μυϊκό ιστό, ο κύριος μεταφορέας που χρησιμοποιείται για την πρόσληψη της γλυκόζης είναι ο GLUT4, ο οποίος διατίθεται στην κυτταροπλασματική μεμβράνη μετά από την επίδραση της ινσουλίνης. Όταν η συγκέντρωση της ινσουλίνης είναι χαμηλή, οι GLUT4 μεταφορείς γλυκόζης εντοπίζονται σε κυτταροπλασματικά κυστίδια οπού δεν μπορούν να επιτελέσουν την κύρια λειτουργία τους και είναι ανενεργά. Πρόσδεση της ινσουλίνης στον υποδοχέα της σε αυτά τα κύτταρα, οδηγεί σε γρήγορη σύντηξη αυτών των κυστιδίων με την κυτταροπλασματική μεμβράνη, δίνοντας στο κύτταρο την ικανότητα πρόσληψης γλυκόζης. Όταν τα επίπεδα της ινσουλίνης μειωθούν και πάλι και οι υποδοχείς της ινσουλίνης δεν είναι πλέον κατειλημμένοι, οι μεταφορείς της γλυκόζης «ανακυκλώνονται» πίσω στο κυτταρόπλασμα. Η ινσουλίνη διεγείρει την αποθήκευση γλυκοζης υπό μορφή γλυκογόνου στο ήπαρ. Ένα μεγάλο τμήμα της γλυκόζης που απορροφάται από το λεπτό έντερο προσλαμβάνεται κατευθείαν από ηπατοκύτταρα, τα οποία το μετατρέπουν στο αποθηκευτικό πολυμερές, το γλυκογόνο. Η ινσουλίνη επιδρά με διάφορους τρόπους στο ήπαρ, διεγείροντας την σύνθεση του γλυκογόνου. Πρώτον, ενεργοποιεί το ένζυμο εξωκινάση, το οποίο φωσφορυλιώνει τη γλυκόζη, παγιδεύοντάς τη μέσα στο κύτταρο. Συμπτωματικά, η ινσουλίνη δρα παρεμποδίζοντας την λειτουργία του ενζύμου φωσφατάση της γλυκόζης (glucose-6-phosphatase), η οποία δρα με τον αντίθετο τρόπο από την εξωκινάση. Ακόμα, η ινσουλίνη ενεργοποιεί μια σειρά από ένζυμα τα οποία εμπλέκονται άμεσα με την Εικόνα 6: Η γλυκόζη αποθηκεύεται με τη μορφή γλυκογόνου (Πηγή: σύνθεση του γλυκογόνου, όπως η φωσφοφρουκτοκινάση και η συνθετάση του γλυκογόνου. Το καθαρό αποτέλεσμα είναι σαφές: όταν η προσφορά σε γλυκόζη είναι άφθονη, η ινσουλίνη «καθοδηγεί» το ήπαρ να την αποθηκεύσει, ωστέ να είναι δυνατή η χρήση της αργότερα. 19
20 Θεραπευτική χρήση Το σημαντικότερο χαρακτηριστικό του διαβήτη τύπου 1 είναι η έλλειψη ινσουλίνης και για αυτό το λόγο η κύρια θεραπευτική προσέγγιση είναι η αντικατάσταση της ινσουλίνης. Δυστυχώς, οι απαιτήσεις του οργανισμού σε ινσουλίνη μεταβάλλονται συνεχώς κατά της διάρκεια της μέρας, με μεγάλες συγκεντρώσεις να χρειάζονται μετά τα γεύματα και ένα βασικό επίπεδο για την υπόλοιπη ημέρα. Μόνο η μονομερής ινσουλίνη βρίσκεται σε ενεργή μορφή στο επίπεδο του υποδοχέα, αλλά έχει την φυσική προδιάθεση να δημιουργεί διμερή και εξαμερή που αποσυσχετίζονται με την διάλυση. Χάρη στην πληροφορία των τρισδιάστατων δομών που έχουν αποκτηθεί από δεκάδες δομές της ινσουλίνης, είτε ως άγριου τύπου, είτε ως μεταλλαγμένη και σε συμπλέγματα με ψευδάργυρο ή άλλα μικρά μόρια όπως η φαινόλη, έχει γίνει δυνατή η ρύθμιση της κινητικής της αποσυσχέτισης της ινσουλίνης. Η προκύπτουσα διαθεσιμότητα μιας ποικιλίας σκευασμάτων ινσουλίνης με γρήγορο ή μακροπρόθεσμο προφίλ δράσης, έχει βελτιώσει την ποιότητα της ζωής για εκατομμύρια ανθρώπους. Ο διαβήτης τύπου 1 τυπικά αντιμετωπίζεται με έναν συνδυασμό απλής και NPH ινσουλίνης, ή μέσω συνθετικών αναλόγων ινσουλίνης. Όταν η ινσουλίνη χρησιμοποιείται για την αγωγή του διαβήτη τύπου 2, συνήθως προστίθενται αρχικά σκευάσματα με μακροπρόθεσμο προφίλ δράσης, ενώ συνεχίζεται παράλληλα η δια του στόματος χορήγηση φαρμάκων. Η απλή ινσουλίνη (Humulin R, Novolin R) είναι η βασικότερη μορφή ινσουλίνης για την αντιμετώπιση των συμπτωμάτων του διαβήτη, η οποία είναι πανομοιότυπη με το μόριο που παράγεται από τον οργανισμό. Έχει βραχυπρόθεσμο προφίλ δράσης. Η ινσουλίνη NPH (Neutral Protamine Hagedorn είναι ένα σκεύασμα με ενδιάμεσο προφίλ δράσης. Αποτελεί εναιώρημα κρυσταλλικής ινσουλίνης με Zn, προσθέτοντας σε αυτήν ουδέτερη πρωταμίνη. 20
21 2.3. Θεωρία της Κρυστάλλωσης Πρωτεϊνών Ο πρωταρχικός σκοπός της κρυστάλλωσης είναι ο προσδιορισμός της τρισδιάστατης δομής μιας πρωτεΐνης μέσω πειραμάτων περίθλασης ακτίνων-χ. Η κρυστάλλωση των πρωτεϊνών είναι μια διαδικασία με μεγάλη πρακτική σημασία, τόσο ως μέθοδος καθαρισμού αλλά και ως εργαλείο για την απόκτηση υψηλής ποιότητας κρυστάλλων, κατάλληλων για δομικό χαρακτηρισμό των υπό μελέτη μορίων. Η μεγαλύτερη διαφορά ανάμεσα στους κρυστάλλους βιολογικών μακρομορίων και των περισσοτέρων ανόργανων υλικών, είναι ότι στα πρώτα την επαναλαμβανόμενη δομική μονάδα αποτελούν μόρια ή ομάδες μορίων, ενώ στα δεύτερα, επαναλαμβανόμενες μονάδες είναι άτομα ή ομάδες ατόμων. Αυτό υποδηλώνει ότι οι δυνάμεις που αναπτύσσονται ανάμεσα σε μια επαναλαμβανόμενη ομάδα με την επόμενη είναι αρκετά πιο ασθενείς, με πιο συνήθεις τις αλληλεπιδράσεις van der Waals, τους δεσμούς υδρογόνου και τις υδρόφοβες αλληλεπιδράσεις. Αντίθετα, οι δεσμοί που αναπτύσσονται μεταξύ των ατόμων στην δεύτερη περίπτωση κρυστάλλου αντιστοιχούν σε πολύ πιο ισχυρούς ομοιοπολικούς και ιοντικούς δεσμούς. Επομένως, γίνεται προφανές ότι οι κρύσταλλοι των βιολογικών μακρομορίων είναι πιο «μαλακοί» και εύθραυστοι, σε σχέση με τους κρυστάλλους των ανόργανων υλικών. Μια άλλη διαφορά είναι το μέγεθος των κρυστάλλων. Τα βιολογικά και οργανικά μόρια συνήθως δημιουργούν πολύ μικρούς κρυστάλλους (περίπου μm 3 ), ενώ τα ανόργανα υλικά σχηματίζουν μεγαλύτερου μεγέθους κρυστάλλους (περίπου 1 mm 3-1 cm 3 ). Ακόμα, οι βιολογικοί κρύσταλλοι συνήθως σχηματίζονται μέσα σε διάλυμα και αποτελούνται κατά μεγάλο βαθμό από διαλύτη (large solvent content). Αυτό ισχύει κυρίως για τους κρυστάλλους μακρομορίων όπως οι πρωτεΐνες και τα νουκλεϊκά οξέα όπου ο διαλύτης μπορεί να καταλάβει από 30% εως και το 80% του κρυστάλλου. 21
22 Φάσεις Κρυστάλλωσης Η διαδικασία της κρυστάλλωσης των μορίων από αρχική μορφή διαλύματος, όπως είναι σύνηθες για τις πρωτεΐνες, αντιπροσωπεύει ένα αντιστρεπτό φαινόμενο ισορροπίας, καθοδηγούμενο από την ελαχιστοποίηση της ελεύθερης ενέργειας του συστήματος. Τα μόρια χάνουν την ελευθερία περιστροφής και μετακίνησης δημιουργώντας πολλούς νέους και σταθερούς μηομοιοπολικούς χημικούς δεσμούς, και μειώνουν την ενέργεια του συστήματος. Γενικότερα, για να κρυσταλλωθεί μια ουσία μέσα σε ένα διάλυμα, είναι αναγκαίο να ελαττωθεί η διαλυτότητά της με ελεγχόμενο τρόπο, δηλαδή πρέπει πρώτα να έρθουν τα μόρια σε μια υπέρκορη κατάσταση (supersaturated state). Ο υπερκορεσμός είναι η κινητήρια δύναμη για την κρυστάλλωση, και για αυτό το λόγο θεωρείται η πιο κρίσιμη παράμετρος, επηρεάζοντας το ρυθμό πυρήνωσης και ανάπτυξης των κρυστάλλων. υπέρκορο διάλυμα, το οποίο αποτελεί μια θερμοδυναμικά ασταθή κατάσταση, αποσταθεροποιούνται οι αλληλεπιδράσεις μεταξύ της πρωτεΐνης και του διαλύτη και γι αυτό γίνεται δυνατός ο σχηματισμός κρυστάλλων. Όταν το διάλυμα επανέλθει σε ισορροπία, τα μόρια της πρωτεΐνης καθιζάνουν, είτε με μορφή κρυστάλλων, είτε ως άμορφα ιζήματα. Ο υπερκορεσμός αυτός μπορεί να επιτευχθεί μέσω σταδιακής αφυδάτωσης του διαλύτη και μέσω αλλαγής της διαλυτότητας του βιολογικού μορίου. Ένα διάλυμα, στο οποίο τα μόρια διαχέονται αντιστοιχεί στο σύστημα σε κατάσταση ισορροπίας, δηλαδή η ελεύθερη ενέργεια του βρίσκεται στο ελάχιστο. Αν περισσότερα μόρια προστεθούν στο διάλυμα, το σύστημα υπόκειται εσωτερικές μεταβολές μέχρι να φτάσει στο σημείο στο οποίο ο διαλύτης δεν είναι αρκετός. Σε αυτήν την υπερκορεσμένη κατάσταση (supersaturated state), το σύστημα δε βρίσκεται πλέον σε ισορροπία. Για αυτό το λόγο, θα οδηγηθεί θερμοδυναμικά σε μια νέα ισορροπία στην οποία θα αντιστοιχεί κάποιο άλλο ελάχιστο ελεύθερης ενέργειας. Στο Εικόνα 7: (a) Άμορφο πρωτεϊνικό ίζημα, (b) Κρυσταλλικό πρωτεϊνικό ίζημα. (Πηγή: ems.com ) 22
23 Κρύσταλλος είναι μια φάση της στερεάς κατάστασης στην οποία τα μόρια είναι περιοδικά διευθετημένα στις τρεις διαστάσεις. Αντίθετα, σε ένα άμορφο ίζημα τα μόρια δεν κατέχουν οποιαδήποτε μορφή διευθέτησης στο χώρο και ενδεχομένως να σχηματίζουν συσσωματώματα. Κάτω από τυπικές συνθήκες δημιουργίας κρυστάλλων, οι αλληλεπιδράσεις πρωτεΐνης- πρωτεΐνης χαρακτηρίζονται από ισχυρές απωστικές δυνάμεις και μικρής εμβέλειας ελκτικές αλληλεπιδράσεις. Οι κρύσταλλοι παρουσιάζουν ένα μεγάλο βαθμό τάξης στο τρισδιάστατο εσωτερικό τους και μια σαφή, αν και όχι απαραίτητα στοιχειομετρική χημική σύσταση. Η αποδιοργάνωση αυτής της τάξης μπορεί να προκαλέσει την απώλεια της κρυσταλλικής ιδιότητας τους υλικού. Το μέγεθος και η πολυπλοκότητα των πρωτεϊνών γενικά δυσκολεύει την κρυστάλλωσή τους σε σχέση με μικρότερα μόρια και ανόργανες ουσίες. Η φύση της διαδικασίας της κρυστάλλωσης διέπεται από θερμοδυναμικούς και κινητικούς παράγοντες, οι οποίοι μπορούν να την καταστήσουν εξαιρετικά μεταβλητή και κατά συνέπεια δύσκολη να ελεγχθεί. Μια μεγάλη ποικιλία παραγόντων επηρεάζουν σε μεγάλο βαθμό την ικανότητα κρυστάλλωσης της πρωτεΐνης (οι παράγοντες που επηρεάζουν την κρυστάλλωση θα αναφερθούν αναλυτικότερα στο κεφάλαιο 2.3.2). Σε πολλές περιπτώσεις η επιτυχημένη κρυστάλλωση μιας πρωτεΐνης είναι αποτέλεσμα εμπειρικών πειραματισμών και δε βασίζεται στη γνώση και την κατανόηση των μηχανισμών που διέπουν την δημιουργία κρυστάλλων. Η διαδικασία της κρυστάλλωσης αποτελείται από δύο κύρια φαινόμενα: την πυρήνωση (nucleation) και την ανάπτυξη των κρυστάλλων (crystal growth). Η πυρήνωση είναι το βήμα στο οποίο τα μόρια της διαλυμένης ουσίας, τα οποία βρίσκονται στο διάλυμα, αρχίζουν να συγκεντρώνονται σε συστάδες κλίμακας νανομέτρου (προκαλώντας αύξηση της συγκέντρωσης σε μια ή πολλαπλές μικρές περιοχές του διαλύματος), οι οποίες στη συνέχεια σταθεροποιούνται κάτω από συγκεκριμένες συνθήκες. Αυτές οι σταθερές συστάδες ονομάζονται πυρήνες (nuclei). Ωστόσο, όταν οι συστάδες χάσουν τη σταθερότητά τους, επαναδιαλυτοποιούνται. Για αυτό το λόγο, πρέπει να ξεπεράσουν ένα κρίσιμο μέγεθος προκειμένου να γίνουν σταθεροί πυρήνες. Το 23
24 κρίσιμο αυτό μέγεθος καθορίζεται από τις συνθήκες που επικρατούν στο περιβάλλον του διαλύματος. Στο στάδιο της πυρήνωσης τα άτομα διατάσσονται με καθορισμένο και περιοδικό τρόπο, ο οποίος χαρακτηρίζει την κρυσταλλική δομή στο εσωτερικό και κατ επέκταση στο εξωτερικό του κρυστάλλου. Εικόνα 8: Η πυρήνωση διακρίνεται σε διάφορους τύπους ανάλογα με τον τρόπο που επάγεται. Η πυρήνωση μπορεί να είναι ομοιογενής ή πιο συχνά ετερογενής όταν περιλαμβάνει και ξένα σωματίδια. Μια ομογενής πυρήνωση έχει ως αποτέλεσμα την τοπική μεταβολή των συγκεντρώσεων του διαλύματος. Η ανάπτυξη του κρυστάλλου είναι η επακόλουθη ανάπτυξη των πυρήνων που επιτυγχάνουν το κατάλληλο μέγεθος και σταθερότητα. Η πυρήνωση και η ανάπτυξη συνεχίζουν να συμβαίνουν ταυτόχρονα σε συνθήκες υπερκορεσμού. Ανάλογα με τις συνθήκες, είναι δυνατό να επικρατεί είτε η πυρήνωση είτε η ανάπτυξη και ως αποτέλεσμα λαμβάνονται κρύσταλλοι με διαφορετικα μεγέθη και σχήματα. Μια κλασσική εξήγηση της δημιουργίας κρυσταλλικών πυρήνων δίνεται από το δισδιάστατο διάγραμμα διαλυτότητας που απεικονίζεται στην εικόνα 9. Η καμπύλη διαλυτότητας χωρίζει τη συγκέντρωση σε δύο τμήματα- την υπόκορη (undersaturated) και την υπέρκορη (supersaturated) ζώνη. Κάθε σημείο στην καμπύλη αντιστοιχεί σε μια συγκέντρωση στην οποία το διάλυμα βρίσκεται σε ισορροπία με ένα παράγοντα καθίζησης (π.χ. ένα αλάτι). περιοχή που βρίσκεται κάτω από την καμπύλη διαλυτότητας, το διάλυμα είναι 24 Στη
25 υπόκορο και δεν είναι δυνατή η κρυστάλλωση. Πάνω από την καμπύλη διαλυτότητας βρίσκεται η υπέρκορη ζώνη, οπού για δεδομένη συγκέντρωση ενός παράγοντα καθίζησης, η συγκέντρωση της πρωτεΐνης είναι υψηλότερη από αυτήν στη κατάσταση ισορροπίας. Ανάλογα με την κινητική πορεία που ακολουθείται για την επίτευξη ισορροπίας ή αλλιώς υπερκορεσμό, αυτή η περιοχή μπορεί να διαιρεθεί στις τρεις παρακάτω ζώνες: Εικόνα 9: Σχηματική αναπαράσταση διαγράμματος φάσης κρυστάλλωσης, που δείχνει την μεταβολή στην συγκέντρωση πρωτεϊνικών μορίων ως προς έναν παράγοντα καθίζησης. Η ζώνη καθίζησης (precipitation zone) αντιστοιχεί στην περιοχή οπου τα πρωτεϊνικά μόρια που βρίσκονται σε περίσσεια διαχωρίζονται από το υπόλοιπο διάλυμα, δημιουργωντας άμορφα ιζήματα. Η ζώνη πυρήνωσης (nucleation zone) περιγράφει την περιοχή όπου τα πρωτεϊνικά μόρια συσσωματώνονται. Κοντά στη ζώνη καθίζησης, η κρυστάλλωση μπορεί να συμβεί με τη δημιουργία πολλών μικροκρυστάλλων (shower of microcrystals), δύσκολο να διακριθούν από το άμορφο ίζημα (δημιουργία πολυκρυσταλλικού δείγματος). Η μετασταθής ζώνη, στην οποία ένα υπέρκορο διάλυμα δε μπορεί να δημιουργήσει πυρήνες για ένα μεγάλο χρονικό διάστημα, εκτός εαν τεθεί 25
26 υπό συνθήκες μηχανικού στρες ή εάν προστεθεί ένας ήδη υπάρχον κρύσταλλος σε αυτό (seed crystal). Παύση της κρυσταλλικής ανάπτυξης (cessation of growth) μπορεί να συμβεί για διάφορους λόγους. Ο πιο προφανής είναι η μείωση της συγκέντρωσης της διαλυτής ουσίας που δημιουργεί τον κρύσταλλο Παράγοντες που επηρεάζουν την κρυστάλλωση Η κρυστάλλωση των πρωτεϊνών αφορά τη συστηματική αναζήτηση των οριακών τιμών των παραμέτρων που επιδρούν στο σχηματισμό των κρυστάλλων. Σκοπός είναι να βρεθούν μία ή περισσότερες ομάδες παραμέτρων οι οποίες είναι κατάλληλες και οδηγούν στο σχηματισμό πυρήνων και κατ επέκταση κρυστάλλων. Πολλοί παράγοντες κατέχουν σημαντικό ρόλο στο εαν ένα πρωτεϊνικό δείγμα θα κρυσταλλωθεί ή όχι. Μερικοί από αυτούς τους παράγοντες, όπως αναφέρθηκαν και παραπάνω, περιλαμβάνουν την καθαρότητα, την διαλυτότητα και την συγκέντρωση της πρωτεΐνης, το ph, τη θερμοκρασία, το χρόνο, την ιοντική ισχύ, τους διάφορους προσδέτες, τους μη πολικούς διαλύτες, καθώς και άλλους παράγοντες καθίζησης. Όλοι αυτοί οι παράγοντες επηρεάζουν τις μικροσκοπικές αλληλεπιδράσεις ανάμεσα στις πρωτεΐνες, ενώ η ρύθμισή τους εξυπηρετεί δύο σκοπούς: Διασφαλίζουν, όσο γίνεται, ότι τα μόρια καταλαμβάνουν μια συγκεκριμένη διαμόρφωση, και Αυξάνουν την ισχύ της αλληλεπίδρασης, μειώνοντας την διαλυτότητα και προκαλώντας την κρυστάλλωση. Όσο περισσότερο ομοιογενής είναι η πρωτεΐνη μέσα στο διάλυμα, τόσο μεγαλύτερη η πιθανότητα να δημιουργήσει κρύσταλλο. Σύμφωνα με τα τυπικά πρότυπα η καθαρότητα της πρωτεΐνης πρέπει να είναι τουλάχιστον στο επίπεδο του 97%. Ακόμα, οι συνθήκες ph είναι ιδιαίτερα σημαντικές, καθώς διαφορετικές τιμές ph μπορεί να οδηγήσουν σε διαφορετικούς προσανατολισμούς πακεταρίσματος των μορίων. Ρυθμιστικά διαλύματα όπως το Tris-HCl, είναι επίσης συχνά απαραίτητα για την διατήρηση μιας συγκεκριμένης τιμής ph. 26
27 Καθαρότητα της πρωτεΐνης Η καθαρότητα της πρωτεΐνης είναι μια σημαντική παράμετρος που σχετίζεται με την παρουσία ή όχι άλλων παραγόντων στο πρωτεϊνικό διάλυμα, όπως σωματίδια σκόνης, αποδιατεταγμένη πρωτεΐνη ή άλλα ξένα σωματίδια, που θα επηρεάσουν την κρυστάλλωση. Στην περίπτωση που γίνει δυνατή η κρυστάλλωση ενός τέτοιου δείγματος, τα δεδομένα περίθλασης που θα αποκτηθούν από αυτό πιθανότατα θα είναι κακής ποιότητας. Διαλυτότητα της πρωτεΐνης Όσο μεγαλύτερη η διαλυτότητα μιας πρωτεΐνης, τόσο μεγαλύτερο το καθαρό της φορτίο, με τη μικρότερη διαλυτότητα να εμφανίζεται στο ισοηλεκτρικό σημείο. Το ισοηλεκτρικό σημείο (pi) μιας πρωτεΐνης είναι το ph εκείνο όπου το ολικό φορτίο της είναι ίσο με το μηδέν, σαν άθροισμα των αρνητικών και θετικών φορτίων κάθε αμινοξέος. Έτσι, είναι δυνατόν να γίνει πακετάρισμα στη στερεή κρυσταλλική κατάσταση λόγω των ηλεκτροστατικών αλληλεπιδράσεων, χωρίς τη συσσώρευση ενός καθαρού φορτίου υψηλής ενέργειας. Συγκέντρωση της πρωτεΐνης Γενικότερα, υψηλότερες συγκεντρώσεις πρωτεΐνης έχουν ως αποτέλεσμα τον υπερκορεσμό του διαλύματος και την επακόλουθη αποσταθεροποίηση της ισορροπίας του συστήματος που θα οδηγήσει στην καθίζηση και στο σχηματισμό κρυσταλλικού ιζήματος. ph Το ph του διαλύματος επηρεάζει το φορτίο των πλευρικών ομάδων των επαμφοτερίζοντων αμινοξέων της πρωτεΐνης με αποτέλεσμα να επηρεάζονται οι αλληλεπιδράσεις ανάμεσα στα μόρια πρωτεΐνης-πρωτεΐνης και πρωτεΐνηςδιαλύτη. Μερικά από τα αμινοξέα της επιφάνειας της πρωτεΐνης όταν αυτή βρίσκεται σε άμορφη κατάσταση, ερχόμενα σε επαφή με το διαλύτη, χρειάζεται να αλληλεπιδράσουν με αυτόν ώστε να γίνει η έναρξη της κρυσταλλικής πυρήνωσης. Ως επακόλουθο, πολύ μικρές διακυμάνσεις του ph μπορεί να έχουν μεγάλες επιπτώσεις στην πυρήνωση και στην απόκτηση κρυστάλλων. 27
28 Θερμοκρασία Η επίδραση της θερμοκρασίας στη διαλυτότητα χαρακτηρίζεται ως ένας από τους σημαντικότερους παράγοντες που επηρεάζουν την κρυστάλλωση ενός μορίου. Αύξηση της θερμοκρασίας οδηγεί σε αύξηση της διαλυτότητας του πρωτεϊνικού μορίου, κάτι που καθιστά την επίτευξη της κρυστάλλωσης προβληματική. Επομένως είναι απαραίτητο το δείγμα να μην εκτίθεται σε θερμοκρασιακές διακυμάνσεις. Οι πιο συνήθεις θερμοκρασίες για πρωτεϊνική κρυστάλλωση είναι μεταξύ 4 και 20 ο C. Η θερμοκρασία μπορεί να επιδράσει με τέτοιο τρόπο, ώστε κρύσταλλοι οι οποίοι αναπτύσσονται σε δύο διαφορετικές θερμοκρασίες να έχουν και διαφορές στη μορφολογία τους. Χρόνος Ο χρόνος είναι ένας άλλος παράγοντας που επηρεάζει την κρυστάλλωση. Μερικοί κρύσταλλοι χρειάζονται μόνο λίγες ώρες για να αναπτυχθούν ενώ άλλοι εβδομάδες ή ακόμα και μήνες. Όταν ο κρύσταλλος φθάσει ένα συγκεκριμένο μέγεθος τότε αυθόρμητα θα σταματήσει να αναπτύσσεται. Ιοντική ισχύς Η προσθήκη αλάτων στο διάλυμα κρυστάλλωσης προκαλεί μεταβολές στην ιοντική ισχύ του. Τα άλατα αλληλεπιδρούν με τα μόρια νερού του διαλύματος καθώς με την εισαγωγή τους σε αυτό διίστανται. Έτσι δρουν ανταγωνιστικά με την πρωτεΐνη ως προς αυτό και μειώνουν τη διαλυτότητά της, οδηγώντας την έτσι στην πυρήνωση και κατ επέκταση στη δημιουργία κρυστάλλων. Υπάρχουν ωστόσο, δύο μέθοδοι που χρησιμοποιούνται και επηρεάζουν την κρυστάλλωση: η μέθοδος «salting out», στην οποία ένα πολύ διαλυτό άλας προστίθεται στο διάλυμα της πρωτεΐνης. Επειδή η διαλυτότητά του είναι κατά πολύ μεγαλύτερη από της πρωτεΐνης, η προσθήκη του ελαττώνει την ικανότητα του διαλύτη να την διαλύει και έτσι η πρωτεΐνη καθιζάνει. η μέθοδος «salting in». Μερικές πρωτεΐνες γίνονται πιο διαλυτές παρουσία αλάτων, επειδή τα ιόντα των αλάτων δεσμεύονται στην επιφάνειά τους και αυξάνουν την υδροφιλικότητά τους. Σε αυτή τη 28
29 περίπτωση, η πρωτεΐνη μπορεί να κρυσταλλωθεί μειώνοντας την συγκέντρωση του άλατος. Προσδέτες (ligands) Η προσθήκη οργανικών μορίων ή ιόντων μετάλλων που αλληλεπιδρούν με τα μόρια της πρωτεΐνης, μπορεί να επηρεάσει την διαδικασία κρυστάλλωσης, καθώς αυτά τα μόρια, προσδενόμενα στην πρωτεΐνη, μπορούν να μεταβάλλουν την αναδίπλωσή της και κατ επέκταση την επιφάνεια αλληλεπίδρασης με τα υπόλοιπα γειτονικά μόρια. Μη πολικοί διαλύτες Μη πολικοί διαλύτες όπως για παράδειγμα η αιθανόλη, μπορούν να αναμιχθούν με το υδατικό διάλυμα και να ελαττώσουν τη διαλυτότητα της πρωτεΐνης. Θεωρητικά, τα μόρια των διαλυτών αυτών προσδένονται στις πολικές ομάδες της επιφάνειας της πρωτεΐνης, καθιστόντας την λιγότερο πολική, ή εναλλακτικά, μειώνουν τον αποτελεσματικό αριθμό πολικών ομάδων του διαλύτη. Άλλοι παράγοντες καθίζησης Χρήση πολυμερών όπως για παράδειγμα η πολυαιθυλενική γλυκόλη (Polyethylene Glycol, PEG), μειώνεται η διαλυτότητα των πρωτεϊνικών μορίων καθώς τα πολυμερή εμποδίζουν την επαφή του διαλύτη και της πρωτεΐνης Κρυσταλλικός πολυμορφισμός Ως πολυμορφισμός ορίζεται η ικανότητα μιας ουσίας να υφίσταται σε μία ή παραπάνω κρυσταλλικές φάσεις, διακρινόμενες από διαφορετικό κρυσταλλικό πακετάρισμα ή και διαμόρφωση των μορίων. Ο πολυμορφισμός είναι ένα σύνηθες φαινόμενο, και μάλιστα όπως αναφέρει ο McCrone «Κάθε ουσία έχει διαφορετικές πολυμορφικές μορφές, και γενικότερα, ο αριθμός των μορφών που είναι γνωστές για μια δεδομένη ουσία είναι ανάλογη με τον χρόνο και τα χρήματα που έχουν ξοδευτεί για την έρευνα πάνω σε αυτή την ουσία». Μικρές μεταβολές στις παραμέτρους που διέπουν την διαδικασία της κρυστάλλωσης μπορεί να αλλάξουν την κατανομή του μεγέθους ή τη μορφολογία των 29
30 κρυστάλλων ή ακόμα και τον κρυσταλλικό τύπο και να επηρεάσουν την πρωτεϊνική δομή. Οι διαμοριακές επαφές ανάμεσα στα πρωτεϊνικά μόρια στη κρυσταλλική φάση καθορίζουν τη μηχανική σταθερότητα του κρυστάλλου. Αν οι συνθήκες κρυστάλλωσης μεταβληθούν, τότε ο αριθμός και ο χαρακτήρας αυτών των επαφών μπορεί να αλλάξει με αποτέλεσμα την εμφάνιση πολυμόρφων. Τα πολύμορφα διακρίνονται από διαφορετικές πλεγματικές σταθερές (βλ. Ενότητα 2.4.1) και κατ επέκταση διαφορετικές μοριακές διαμορφώσεις μέσα στον κρύσταλλο. Ένα παράδειγμα πολυμοφισμού σε πρωτεϊνικό μόριο είναι αυτό της λυσοζύμης (Hen Egg-White Lysozyme, HEWL), η οποία μπορεί να σχηματίσει τετραγωνικούς, τρικλινείς, μονοκλινείς και ορθορομβικούς κρυστάλλους, ανάλογα με το ph, τη θερμοκρασία και την φύση των αλάτων. Στη φαρμακευτική βιομηχανία, ο πολυμορφισμός είναι ένας σημαντικός παράγοντας για πολλούς λόγους, καθώς μια νέα κρυσταλλική δομή μπορεί να σημαίνει την δυνατότητα παραγωγής ενός νέου φαρμακευτικού σκευάσματος με νέες φυσικές και χημικές ιδιότητες Μέθοδοι κρυστάλλωσης Υπάρχουν διάφορες μέθοδοι για την κρυστάλλωση πρωτεϊνών. Οι πιο συχνά χρησιμοποιούμενες για την ανάπτυξη μονοκρυστάλλων αξιοποιούν την διάχυση αερίων (vapour diffusion) ανάμεσα σε δύο υγρά (μέθοδοι hanging drop και sitting drop) καθώς και τη μέθοδο της μικροδιάλυσης (microdialysis), ενώ για την απόκτηση πολυκρυσταλλικών δειγμάτων χρησιμοποιείται η μέθοδος κρυστάλλωσης μεγάλης κλίμακας (batch crystallization). Διάχυση αερίων (Vapour diffusion) Σε αυτή τη κατηγορία ανήκουν δύο από τις πλέον χρησιμοποιούμενες μεθόδους που χρησιμοποιούνται για την κρυστάλλωση πρωτεϊνών, γνωστές με τα ονόματα μέθοδος κρεμάμενης σταγόνας (hanging drop) και μέθοδος καθιζάμενης σταγόνας (sitting drop). Και οι δύο περιλαμβάνουν μια σταγόνα που περιέχει καθαρή πρωτεΐνη, ένα ρυθμιστικό διάλυμα (Buffer) και έναν 30
31 παράγοντα καθίζησης, τα οποία έρχονται σε κατάσταση ισορροπίας με ένα παρόμοιο ρυθμιστικό διάλυμα μεγαλύτερης συγκέντρωσης (reservoir solution). Αρχικά, η σταγόνα του πρωτεϊνικού διαλύματος περιέχει ανεπαρκή-για-τηνκρυστάλλωση συγκέντρωση του παράγοντα καθίζησης, αλλά καθώς το νερό εξατμίζεται από τη σταγόνα και μεταφέρεται στο reservoir solution, η συγκέντρωση του παράγοντα καθίζησης αυξάνεται σε επίπεδο τέτοιο που να ευνοεί τη κρυστάλλωση μέσα στη σταγόνα. Αφού το σύστημα βρίσκεται σε ισορροπία, αυτές οι ευνοϊκές συνθήκες διατηρούνται μέχρι να ολοκληρωθεί η κρυστάλλωση. Η μέθοδος hanging drop διαφέρει από την sitting drop, ως προς τη θέση της σταγόνας μέσα στο σύστημα (εικόνα 10). Είναι σημαντικό να σημειωθεί ότι και για τις δύο μεθόδους το σύστημα πρέπει να είναι κλειστό, ωστέ να μην έρχεται σε επαφή με το εξωτερικό περιβάλλον. Πρακτικά, το κάτω μέρος ενός πηγαδιού γεμίζεται με μητρικό υγρό (mother liquor) το οποίο περιέχει όλα τα συστατικά που χρειάζονται σε μια συγκεκριμένη συγκέντρωση. Στην περίπτωση της μεθόδου hanging drop, η σταγόνα με την πρωτεΐνη κρέμεται πάνω από το πηγάδι και λογω της υψηλοτερης συγκέντρωσης του διαλύματος του μητρικού υγρού γίνεται ανταλλαγή αερίων μέχρι το σύστημα να φτάσει σε ισορροπία. Το ίδιο συμβαίνει και στη μέθοδο sitting drop μόνο ) που η σταγόνα σε αυτή τη περίπτωση βρίσκεται τοποθετημένη σε μια υπερυψωμένη θέση στη μέση του πηγαδιού που περιέχει το μητρικό υγρό. Εικόνα 10: (Α) Μέθοδος hanging drop. (B) Μέθοδος sitting drop. (Πηγή: ) Οι παραπάνω μέθοδοι είναι ιδιαίτερα χρήσιμες όταν απαιτούνται μικρές ποσότητες κρυσταλλικού υλικού, όπως για παράδειγμα στη περίπτωση πειράματος από μονοκρύσταλλο. 31
32 Μικροδιάλυση (Microdialysis) Η κρυστάλλωση μέσω διάλυσης είναι μια παραλλαγή στην τυπική μέθοδο διάχυσης αερίων που χρησιμοποιείται για την ανάπτυξη κρυστάλλων. Στη μέθοδο της μικροδιάλυσης, το δείγμα διαχωρίζεται από τον παράγοντα καθίζησης μέσω μιας ημι-διαπερατής μεμβράνης, η οποία επιτρέπει σε μικρά μόρια, όπως ιόντα, πρόσθετα, ρυθμιστικό διάλυμα και άλατα, αλλά παρεμποδίζει τα βιολογικά Εικόνα 11: Η μέθοδος της μικροδιάλυσης (Πηγή: ). μακρομόρια από το να διαπερνούν την μεμβράνη. Η κινητική της ισορροπίας εξαρτάται από το κατώτατο όριο μοριακού βάρους που επιτρέπει η μεμβράνη, από τον παράγοντα καθίζησης, την αναλογία των όγκων, τη συγκέντρωση των συστατικών μέσα και έξω από την κυψελίδα στην οποία συμβαίνει η μικροδιάλυση καθώς και στη γεωμετρία της. Κρυστάλλωση μεγάλης κλίμακας (Batch crystallization) Η κρυστάλλωση με τη μέθοδο batch είναι πολύ πιο απλή και ιδανικότερη όταν απαιτούνται μεγάλοι όγκοι πρωτεϊνικών κρυστάλλων. Σε ένα τέτοιο πείραμα όλα τα συστατικά αναμιγνύονται στις τελικές τους συγκεντρώσεις από Εικόνα 12: Κρυστάλλωση κατά batch. (Πηγή: X- Ray Crystallography of Biomacromolecules, 2007) την αρχή μέσα σε ένα δοχείο eppendorf. Συνήθως, οι συγκεντρώσεις που χρειάζονται για ένα πείραμα batch είναι υψηλότερες για τους παράγοντες καθίζησης, αλλά και σε πρωτεΐνη ορισμένες φορές. Λόγω των υψηλότερων συγκεντρώσεων, η καθίζηση είναι συνήθως γρηγορότερη και πολλές φορές μπορεί να γίνει σε μια μέρα. Δυστυχώς, αυτή η μέθοδος δε μπορεί να χρησιμοποιηθεί σε όλες τις πρωτεΐνες, καθώς δεν αντιδρούν όλες το ίδιο καλά κάτω από αυτές τις συνθήκες γρήγορης κρυστάλλωσης. 32
33 Πολυκρυσταλλικά φάρμακα Σήμερα η ινσουλίνη είναι η πιο ευρέως χορηγούμενη πρωτεΐνη σε κρυσταλλική μορφή, αλλά ένας ικανοποιητικός αριθμός άλλων πρωτεϊνών και πεπτιδίων με μορφή κρυστάλλων χρησιμοποιείται επίσης για φαρμακευτική χρήση. Υπάρχουν ποικίλα πλεονεκτήματα στη χρήση κρυσταλλικών φαρμάκων. Η κρυσταλλική κατάσταση μιας πρωτεΐνης είναι η πιο συγκεντρωμένη της μορφή, κάτι που καθιστά τους κρυστάλλους ευνοϊκούς σε περιπτώσεις που χρειάζονται υψηλές δόσεις του σκευάσματος καθώς και για τη μείωση της συχνότητας των δόσεων. Ένα από τα μεγαλύτερα προβλήματα χορήγησης πολυπεπτιδίων σαν θεραπευτικά σκευάσματα είναι η χημική και βιολογική αστάθεια. Σε κρυσταλλική μορφή, τα πρωτεϊνικά μόρια προστατεύονται καλύτερα ενάντια σε χημικές μετατροπές και είναι λιγότερο ευαίσθητα στην αποδιάταξη και την απώλεια της ενγενούς τους τρισδιάστατης δομής. Επιπλέον, η κρυσταλλική κατάσταση προστατεύει πιο αποδοτικά την πρωτεΐνη από διάφορα πρωτεολυτικά ένζυμα σε σχέση με την άμορφη κατάσταση. Όσον αφορά την μακροπρόθεσμη αποθήκευση, οι κρύσταλλοι μπορούν να αποξηραθούν υπό κενό ή να λυοφιλοποιηθούν, κάτι που μειώνει ακόμα περισσότερο την πιθανότητα χημικών μετατροπών. Επίσης, διαφορετικοί κρυσταλλικοί τύποι μπορεί να χαρακτηρίζονται, για παράδειγμα, από διαφορετική διαλυτότητα, η οποία μπορεί να επηρεάσει την διάρκεια δράσης του κρυσταλλικού σκευάσματος στον οργανισμό και με αυτόν τον τρόπο μπορεί να επιτευχθεί καλύτερος έλεγχος της απελευθέρωσης της ουσίας in vivo. 33
34 2.4. Αρχές της Κρυσταλλογραφίας Έννοιες Συμμετρίας Το ευθύ πλέγμα είναι μια τρισδιάστατη περιοδική επανάληψη επιπέδων διάφορων προσανατολισμών, τα οποία τέμνονται μεταξύ τους ανα ομάδες και σχηματίζουν τα επίπεδα του κρυστάλλου. Η μικρότερη μονάδα η οποία επαναλαμβανόμενη στις τρεις διαστάσεις μπορεί να σχηματίσει τον κρύσταλλο, ονομάζεται θεμελιώδης κυψελίδα (unit cell). Οι διαστάσεις της κυψελίδας μπορούν να οριστούν με έξι παραμέτρους: τα μήκη των τριών πλευρών a, b και c και των τριών γωνιών α, β και γ. Εικόνα 13: Αριστερά: Παράλληλα επίπεδα τα οποία τέμνονται στα κομβικά σημεία (lattice points) δημιουργώντας ένα τρισδιάστατο πλέγμα. Δεξιά: Η μικρότερη μονάδα ενός κρυστάλλου ονομάζεται θεμελιώδης ή μοναδιαία κυψελίδα (unit cell) και χαρακτηρίζεται από τις διαστάσεις a,b και c και τις γωνίες α, β και γ. (Πηγή: Υπάρχουν επτά συστήματα (Κρυσταλλικά Συστήματα) για την περιγραφή των κρυστάλλων και είναι η βάση για την ταξινόμησή τους. Ανάλογα με τις σχέσεις ανάμεσα στις σταθερές της κυψελίδας, ο κρύσταλλος κατατάσσεται ανάλογα σε ένα από τα παρακάτω συστήματα: Κυβικό, Τετραγωνικό, Ορθορομβικό, Εξαγωνικό, Ρομβοεδρικό (και Τριγωνικό), Μονοκλινές και Τρικλινές. Στον πίνακα 2 συνοψίζονται τα χαρακτηριστικά κάθε συστήματος. Επιπλέον, υπάρχουν 14 διαφορετικοί τύποι πλεγμάτων Bravais (Bravais Lattices), τα οποία προκύπτουν από τον συνδυασμό των επτά 34
35 κρυσταλλικών συστημάτων με την κέντρωση των σημείων του πλέγματος (lattice centering). Πίνακας 2: Τα 7 κρυσταλλικά συστήματα και οι σχέσεις ανάμεσα στις πλεγματικές σταθερές που τα χαρακτηρίζουν. Κάθε πλέγμα Bravais αποκρίνεται σε ένα συγκεκριμένο τύπο πλέγματος. Οι τύποι κέντρωσης του πλέγματος είναι οι παρακάτω: Κρυσταλλικό σύστημα Κυβικό (Cubic) Τετραγωνικό (Tetragonal) Ορθορομβικό (Orthorhombic) Εξαγωνικό (Hexagonal) / Τριγωνικό (Trigonal) Χαρακτηριστικά a= b= c και α=β=γ=90 a= b c και α=β=γ=90 a b c και α=β=γ=90 a = b and α = β = 90 and γ= 120 Ρομβοεδρικό (Rhombohedral) a= b= c και α=β=γ 90 Μονοκλινές (Monoclinic) a b c και α=γ=90, β 90 Τρικλινές (Triclinic) a b c και α β γ 90 Απλό (Primitive centering, P): όπου υπάρχουν σημεία του πλέγματος μόνο στις ακμές της κυψελίδας. Χωροκεντρωμενο (Body-centered, I): όπου υπάρχει ένα επιπλέον σημείο του πλέγματος στο κέντρο της κυψελίδας. Εδροκεντρωμένο (Face-centered, F): οπού υπάρχει από ένα επιπλέον σημείο του πλέγματος σε κάθε έδρα της κυψελίδας. Βαση-κεντρωμένο (Base-centered, A, B ή C): όπου υπάρχει ένα επιπλέον σημείο του πλέγματος στο κέντρο ενός από τα ζεύγη εδρών της κυψελίδας. Εικόνα 14: Το σύνολο των συστημάτων 35 Bravais για όλα τα κρυσταλλικά συστήματα. (Πηγή:
36 Δεν είναι δυνατοί όλοι οι συνδυασμοί των κρυσταλλικών συστημάτων και των θέσεων των μορίων που απαιτούνται για να περιγραφούν τα πιθανά πλέγματα. Στην πραγματικότητα υπάρχουν 7 6=42 συνδυασμοί, αλλά μπορεί εύκολα να αποδειχθεί ότι πολλοί από αυτούς τους συνδυασμούς είναι ισοδύναμοι μεταξύ τους. Τα 14 πλέγματα Bravais συνοψίζονται στην εικόνα 14. Η συμμετρία της θεμελιώδους κυψελίδας περιγράφεται από την έννοια του space group (συμμετρία ομάδας χώρου). Τα space groups δημιουργούνται από συνδυασμούς των 32 κρυσταλλογραφικών point group με τα 14 πλέγματα Bravais, το καθένα από τα οποία ανήκει σε κάποιο από τα 7 κρυσταλλικά συστήματα. Σαν αποτέλεσμα, προκύπτουν 230 διαφορετικά space groups (πηγή: International tables for X- ray crystallography) τα οποία περιγράφουν όλες τις πιθανές κρυσταλλικές συμμετρίες. Παρ ολα αυτά, η χειρόμορφη φύση των πρωτεϊνών (αποτελούνται μόνο από L- αμινοξέα και είναι αδύνατη η εφαρμογή ορισμένων στοιχείων συμμετρίας) περιορίζει τον αριθμό των πιθανών space group που μπορούν να καταληφθούν από αυτές στα 65. Τα απλούστερα στοιχεία συμμετρίας (symmetry operations) που απαιτούνται για να περιγράψουν τη συμμετρία των μοναδιαίων κυψελίδων είναι: (α) η μετακίνηση (translation), (β) η περιστροφή γύρω από έναν άξονα (στοιχείο: άξονας περιστροφής, rotational axis) και (γ) η ανάκλαση (στοιχείο: επίπεδο-καθρέφτης, mirror-plane). Συνδυασμοί αυτών των στοιχείων παράγουν πολυπλοκότερα στοιχεία συμμετρίας, συμπεριλαμβανομένων των κέντρων συμμετρίας (symmetry centers), οι άξονες βίδας (screw axis) και επίπεδα ολίσθησης (glide planes). Μετακίνηση σημαίνει απλά κίνηση κατά συγκεκριμένη απόσταση. Σε γενικές γραμμές, οι άξονες περιστροφής αντιπροσωπεύονται στο σύμβολο του space group από έναν αριθμό n. Συνδυασμός της μετακίνησης και της περιστροφής έχει σαν αποτέλεσμα το στοιχείο screw axis που αναφέρθηκε παραπάνω. Το point group περιγράφει τη συμμετρία αντικειμένων με πεπερασμένες διαστάσεις (π.χ. ένα σημείο) και εφαρμόζεται σαν έννοια εξίσου για κρυσταλλική μορφολογία ή μοριακές δομές. Συνολικά υπάρχουν 32 point groups. 36
37 Το κάθε space group αντιπροσωπεύεται με ένα σύνολο συμβόλων στο οποίο αναγνωρίζεται ο τύπος του πλέγματος (πλέγματα Bravais) καθώς και τα στοιχεία συμμετρίας που είναι επιτρεπτά. Για παράδειγμα, για το space group P nm μπορούμε να πούμε ότι ανήκει σε απλό πλέγμα (primitive), ενώ το σύμβολο nm αντιπροσωπεύει έναν διπλής τάξης (n-fold) screw axis με μια μετακίνηση ανά τη μονάδα κατά m/n. Επιπλέον, είναι σημαντικό να αναφερθεί ότι στις περισσότερες περιπτώσεις, η θεμελιώδης κυψελίδα περιέχει πολλαπλά πανομοιώτυπα μόρια ή συμπλέγματα ολιγομερών διευθετημένα έτσι ώστε να μπορούν να αναπαράγουν μια περιοδική σειρά, εάν εφαρμοστούν σε αυτά συγκεκριμένα στοιχεία συμμετρίας. Στη θεμελιώδη κυψελίδα, η μεγαλύτερη συνάθροιση μορίων που δεν κατέχει καθόλου στοιχεία συμμετρίας, αλλά μπορεί να βρεθεί δίπλα σε άλλες όμοιες συναθροίσεις μορίων μέσω εφαρμογής στοιχείων συμμετρίας ονομάζεται ασύμμετρη μονάδα (asymmetric unit, ASU) Ατομικά επίπεδα και Παράμετροι Miller Τα πιο εμφανή επίπεδα σε ένα κρυσταλλικό πλέγμα ορίζονται από τις έδρες των μοναδιαίων κυψελίδων. Αυτά και άλλα ισαπέχοντα επίπεδα τα οποία περνούν από σημεία του πλέγματος μπορούν να θεωρηθούν ως πηγές της περίθλασης και χαρακτηρίζονται από τρεις παραμέτρους που ονομάζονται σταθερές πλέγματος. Συγκεκριμένα, μια οικογένεια ισοδύναμων επιπέδων του πλέγματος μπορεί να παρασταθεί από τρεις αριθμητικές παραμέτρους h, k, l οι οποίες είναι ευρύτερα γνωστές ως παράμετροι Miller. H σταθερά h δίνει τον αριθμό των επιπέδων στον άξονα x ή, Εικόνα 15: Απεικόνιση των επιπέδων (001) και (100) σε μια θεμελιώδη κυψελίδα (πηγή: Baker & Cohen, 2004). 37
38 αντίστοιχα, τον αριθμό των τμημάτων στα οποία τέμνεται η a πλευρά της θεμελιώδους κυψελίδας από μια οικογένεια επιπέδων. Με την ίδια λογική, οι σταθερές k και l δίνουν τον αριθμό των επιπέδων στους άξονες y και z. Κατά κανόνα, οι σταθερές Miller ορίζουν την κατεύθυνση και τον προσανατολισμό των επιπέδων μέσα σε ένα κρυσταλλικό πλέγμα. Μπορεί να αναφέρονται σε μια συγκεκριμένη έδρα του κρυστάλλου, μια κατεύθυνση, ένα σύνολο εδρών ή ένα σύνολο κατευθύνσεων. Σταθερές που περιγράφουν ένα μόνο κρυσταλλογραφικό επίπεδο σημειώνονται με παρενθέσεις, αυτές που αναφέρονται σε ένα σύνολο συμμετρικά ισοδύναμων επιπέδων σημειώνονται με αγκύλες, ενώ αυτές που υποδηλώνουν κατεύθυνση σημειώνονται με τετράγωνες αγκύλες. Κάθε προσανατολισμένο επίπεδο μέσα στο πλέγμα υποδεικνύουν μια σειρά ατόμων. Ένα επίπεδο είναι δυνατό να έχει υψηλότερη ατομική πυκνότητα από ένα άλλο Περίθλαση Ακτίνων-Χ Το 1912 οι Friedrich, von Laue και Knipping κατάφεραν να πάρουν το πρώτο διάγραμμα περίθλασης (diffraction pattern) από έναν μονοκρύσταλλο θειϊκού χαλκού και θειώδους ψευδαργύρου (copper sulfate και zinc sulfite), αξιοποιώντας τις ιδιότητες των ακτίνων-χ. Βασιζόμενος σε αυτά τα πειράματα, ο von Laue ανέπτυξε τη θεωρία της Περίθλασης Ακτίνων-Χ. Την ίδια περίοδο οι W.L. Bragg και W.H. Bragg εκτέλεσαν τα δικά τους πειράματα περίθλασης και στη συνέχεια χρησιμοποίησαν έναν εναλλακτικό αλλά ισοδύναμο τρόπο από αυτόν του von Laue για να εξηγήσουν τα ανεστραμμένα αποτελέσματα που λαμβάνονταν κατά την περίθλαση. Μέχρι σήμερα οι λεγόμενες προϋποθέσεις Laue και η εξίσωση Bragg αποτελούν τη βάση της περίθλασης ακτίνων-χ από κρυσταλλικά υλικά. Όπως και το ορατό φως, μια δέσμη ακτίνων-χ είναι ένα ηλεκτρομαγνητικό κύμα το οποίο χαρακτηρίζεται από την ύπαρξη ενός ηλεκτρικού πεδίου και ενός κάθετου σε αυτό, μαγνητικού πεδίου. Παρ όλα αυτά, το κύμα αυτό συγκρινόμενο με ένα κύμα ορατού φωτός, έχει πολύ πιο μικρό μήκος κύματος. Έτσι, ενώ το φάσμα του ορατού φωτός μπορεί να έχει μήκη κύματος από Å, ενώ οι ακτίνες-χ έχουν τυπικά μήκη κύματος από 38
39 Å. Λόγω του γεγονότος ότι αυτά τα μήκη κύματος είναι συγκρίσιμα με τις διατομικές αποστάσεις σε ένα κρυσταλλικό υλικό, είναι δυνατό να παρατηρηθούν οι χαρακτηριστικές αλληλεπιδράσεις ανάμεσα στα φωτόνια που αποτελούν τις ακτίνες-χ και των ηλεκτρονίων που βρίσκονται σε σειρά σε μια κρυσταλλική δομή. Αυτές οι αλληλεπιδράσεις καθιστούν τις ακτίνες-χ την πιο σημαντική πηγή περίθλασης για την ανάλυση της δομής. Η πρόσπτωση των ηλεκτρομαγνητικών κυμάτων ακτίνων-χ πάνω σε ένα αντικείμενο έχει ως αποτέλεσμα την σκέδασή τους από τα ηλεκτρόνια του αντικειμένου. Το πεδίο των ακτίνων-χ εξαναγκάζει τα ηλεκτρόνια του υλικού να ταλαντωθούν και αυτά με τη σειρά τους αρχίζουν να εκπέμπουν δευτερογενή κύματα της ίδιας συχνότητας και μήκους κύματος ίδιο με αυτό των αρχικών. Αυτά τα κύματα υπερτίθενται και στην περίπτωση της ενισχυτικής συμβολής προκύπτουν φαινόμενα περίθλασης που είναι κατά κανόνα πιο ισχυρά όταν οι αποστάσεις ανάμεσα στα άτομα του κρυσταλλικού υλικού είναι συγκρίσιμες με το μήκος κύματος της προσπίπτουσας ακτινοβολίας Νόμος του Bragg Ο κύριος νόμος που διέπει το φαινόμενο της περίθλασης είναι ο νόμος που διατυπώθηκε από τον Sir William Henry Bragg και τον γιό του Sir William Lawrence Bragg. Σύμφωνα με αυτό τον νόμο, οι γωνίες με τις οποίες εξέρχονται οι περιθλούμενες ακτίνες από έναν κρύσταλλο μπορούν να υπολογιστούν εάν η περίθλαση θεωρηθεί ως ανάκλαση από μια ομάδα ισοδύναμων, παράλληλων επιπέδων αποτελούμενα από τα άτομα ενός κρυστάλλου. Η «Περίθλαση Bragg» προτάθηκε όταν ανακαλύφθηκε ότι τα στερεά κρυσταλλικής φύσης παράγουν μη-αναμενόμενα πρότυπα ανακλώμενων ακτίνων-χ. Οι ακτίνες-χ ανακαλύφθηκαν το 1895 από τον W.C. Röntgen. Βρίσκονται μεταξύ του υπεριώδους φωτός και των ακτίνων γ, στην κλίμακα μήκους κύματος. Η ενέργειά τους κυμαίνεται από τα 100 ev εώς τα 100 kev. Ακτίνες-Χ με ενέργεια μέχρι 10 kev ανήκουν στην κατηγορία των «μαλακών» ακτίνων-χ, ενώ αυτές που έχουν ενέργεια από 10 kev ή περισσότερο, θεωρούνται «σκληρές», λόγω των διεισδυτικών τους ικανοτήτων. 39
40 Η περίθλαση των ακτίνων-χ από ένα επίπεδο, είναι δυνατό να περιγραφεί από το Νόμο του Bragg ο οποίος διατυπώνεται από την παρακάτων εξίσωση: n λ = 2 d sin(ϑ) (1) όπου n είναι ένας ακέραιος αριθμός, λ το μήκος κύματος της ακτινοβολίας, d η απόσταση ανάμεσα στα παράλληλα επίπεδα του πλέγματος και 2ϑ η γωνία της περίθλασης. Έστω δύο παράλληλα κρυσταλλικά επίπεδα με απόσταση d μεταξύ τους. Παράλληλες ακτίνες-χ μήκους κύματος λ προσπίπτουν με γωνία πρόσπτωσης Εικόνα 16: Η περίθλαση Bragg σε δύο διαδοχικά κρυσταλλικά επίπεδα. ϑ στις θέσεις Α και Β οι οποίες απέχουν επίσης απόσταση d και ανακλώνται με την ίδια γωνία ϑ, σύμφωνα με τον νόμο της ανάκλασης. Προκειμένου να παρατηρηθεί έντονα το φαινόμενο της περίθλασης πρέπει τα δύο ανακλώμενα κύματα να συμβάλλουν ενισχυτικά (constructive interference), δηλαδή να παρουσιάζουν την ίδια χρονική στιγμή μέγιστα και ελάχιστα. Αυτό γίνεται όταν η απόσταση που έχει διανύσει το ένα κύμα σε σχέση με το άλλο διαφέρει κατά ένα ακέραιο πολλαπλάσιο του μήκους κύματος, δηλαδή κατά n λ, όπου n ένας ακέραιος αριθμός. Στην εικόνα 16, ισχύει CB= BD= x, Πρέπει n λ= 2 x (2), προκειμένου να ισχύει η προϋπόθεση της ενισχυτικής συμβολής. Ωστόσο, στο τρίγωνο ABD (το οποίο είναι ορθογώνιο) ισχύει: sin(ϑ)= Άρα x= d sin(ϑ) 40 =
41 Σύμφωνα με τα παραπάνω, η εξίσωση (2) γίνεται n λ= 2 x n λ=2 d sin(ϑ), που αποτελεί τον κύριο όρο για το φαινόμενο της περίθλασης και της λήψης σήματος Αντίστροφο Πλέγμα (Reciprocal Lattice) Από τη σχέση (1) που διατυπώνει τον νόμο του Bragg, γίνεται προφανής η αντίστροφη σχέση ανάμεσα στην γωνία περίθλασης ϑ και την απόσταση μεταξύ των κρυσταλλογραφικών επιπέδων. Αυτή η σχέση, μαζί με τις σχετικές γεωμετρικές συνθήκες οδηγούν στην κατασκευή του λεγόμενου αντίστροφου πλέγματος. Το ευθύ πλέγμα χαρακτηρίζεται όπως είναι γνωστό από τα τρία διανύσματα, σε αυτούς όρους και. Το αντίστροφο πλέγμα ορίζεται από τους αντίστροφους *, * και * και σχετίζεται με το ευθύ πλέγμα μέσω των παρακάτω εξισώσεων: *=, *=, *= Η θέση κάθε σημείου στο αντίστροφο πλέγμα περιγράφεται από συντεταγμένες h, k και ℓ στις κατευθύνσεις που ορίζονται από τα διανύσματα του αντιστρόφου πλέγματος *, * και *. Η απόσταση κάθε σημείου του αντίστροφου πλέγματος από την αρχή των αξόνων υπολογίζεται ανάλογα με το κρυσταλλικό σύστημα από τους τύπους που συνοψίζονται στον πίνακα 3. 41
42 Τύπος κρυσταλλικού συστήματος Αποστάσεις επιπέδων Κυβικό Τετραγωνικό Ορθορομβικό Εξαγωνικό Ρομβοεδρικό Μονοκλινές Τρικλινές γ α Πίνακας 3: Στον πίνακα δίνονται οι τύποι για τον υπολογισμό της απόστασης κάθε σημείου του αντίστροφου πλέγματος από την αρχή των αξόνων Η Σφαίρα του Ewald Η Σφαίρα του Ewald (ή αλλιώς σφαίρα ανάκλασης) είναι μια γεωμετρική κατασκευή που χρησιμοποιείται στην κρυσταλλογραφία για να περιγράψει τη σχέση ανάμεσα στο μήκος κύματος της προσπίπτουσας και της εκπεμπόμενης ακτινοβολίας, στη γωνία περίθλασης για μια συγκεκριμένη ανάκλαση, καθώς και το αντίστροφο πλέγμα του κρυστάλλου. Μπορεί να χρησιμοποιηθεί για την εύρεση της μέγιστης ευκρίνειας που μπορεί να ληφθεί από ακτινοβολία συγκεκριμένου μήκους κύματος και από τις διαστάσεις της θεμελιώδους κυψελίδας. Η κατασκευή αυτή είναι ένα σημαντικό εργαλείο για την εξέταση του αν εκπληρώνονται οι προϋποθέσεις της περίθλασης για ένα σημείο του αντίστροφου χώρου, δηλαδή εάν τα επίπεδα Bragg έχουν το σωστό προσανατολισμό προκειμένου να γίνει περίθλαση. 42
43 Εικόνα 17: Σχηματικό διάγραμμα της γεωμετρίας της σφαίρας του Ewald. Έστω μια σφαίρα με ακτίνα 1/λ και κέντρο τον κρύσταλλο στο σημείο Ο. Η αρχή του αντιστρόφου πλέγματος τοποθετείται στο σημείο Α, όπου η προσπίπτουσα δέσμη επιπέδων είναι σε θέση να προκαλέσει περίθλαση, τότε το ακτίνων-χ συναντάει τη σφαίρα και εξέρχεται από αυτήν. Όπως μπορούμε να δούμε και από την εικόνα 17 αν ένα σύνολο διάνυσμα έχει την άκρη του στο σημείο Β της σφαίρας. Η συνθήκη για να παριστάνει μια ακτίνα της σφαίρας ΟΒ την διεύθυνση των περιθλώμενων ακτίνων-χ ικανοποιείται εφ όσον το σημείο Β είναι σημείο του αντιστρόφου πλέγματος (hkl). Το διάνυσμα ΑΒ σε αυτή τη περίπτωση ονομάζεται διάνυσμα σκέδασης και συμβολίζεται με. Επομένως, για να παρατηρηθεί μια ανάκλαση hkl πειραματικά, ο κρύσταλλος θα πρέπει να περιστραφεί κατά τέτοιο τρόπο ώστε το αντίστοιχο σημείο hkl να συμπέσει με ένα σημείο της σφαίρας του Ewald. Με τη χρήση των αρχών της γεωμετρίας είναι δυνατόν να αποδειχθεί ότι το διάνυσμα ισούται με το αντίστροφο της απόστασης dhkl. Το τρίγωνο ΟΑΒ είναι ισοσκελές με ΟΑ=ΟΒ=. Η OC είναι κάθετος και διχοτόμος οπότε στο ορθογώνιο τρίγωνο ΟΑC ισχεύει: sinϑ= AC= OA sinϑ (3) Ακόμα, από τον νόμο του Bragg ισχύει sinϑ= l, οπότε η σχέση (3) γίνεται ΑC= = l l και = 43
44 Αν το διάνυσμα < γίνεται αδύνατο να παρατηρηθεί η αντίστοιχη ανάκλαση. Αυτή η προϋπόθεση ορίζει την σφαίρα περιορισμού (limiting sphere), η οποία έχει κέντρο Α και ακτίνα. Μόνο σημεία του πλέγματος που εμπεριέχονται στη σφαίρα περιορισμού μπορούν να δώσουν σήμα περίθλασης (για αυτό το λόγο πολύ σημαντική είναι η επιλογή του μήκους κύματος που θα χρησιμοποιηθεί στο πείραμα). Σημαντικό είναι να σημειωθεί ότι στην σφαίρα του Ewald έχουμε δύο αρχές. Η αρχή του ευθέος πλέγματος βρίσκεται στο κέντρο της σφαίρας στο σημείο που έχουμε τοποθετήσει τον κρύσταλλο. Η αρχή του αντιστρόφου πλέγματος, όπως είπαμε, βρίσκεται στο σημείο της σφαίρας απ όπου θα εξέρχονταν οι ακτίνες-χ εάν δεν είχε μεσολαβήσει η περίθλαση από τον κρύσταλλο. Με την περιστροφή του κρυστάλλου συμβαίνει παράλληλα ταυτόχρονη περιστροφή των επιπέδων Bragg και περιστροφή του αντίστροφου πλέγματος κατά την ίδια φορά. Δεδομένου ότι η περίθλαση από ένα κρύσταλλο περιορίζεται στα σημεία σχετικά με το αντίστροφο πλέγμα (που αντιστοιχεί στα επίπεδα που μπορούν να καθοριστούν με ακεραίους αριθμούς), μπορούμε να θεωρήσουμε ότι περιστρέφουμε το αντίστροφο πλέγμα όταν περιστρέφουμε τον κρύσταλλο. Η παρακάτω εικόνα δείχνει σχηματικά αυτό, απεικονίζοντας τα επίπεδα των σημείων του αντιστρόφου πλέγματος. Τα επίπεδα των σημείων στο αντίστροφο πλέγμα τέμνουν την σφαίρα του Ewald δίνοντας έναν κύκλο σημείων όταν γίνεται περίθλαση. Όταν τα επίπεδα αυτά ευθυγραμμιστούν κάθετα ως προς τη δέσμη ακτίνων-χ, οι κύκλοι αυτοί στη σφαίρα του Ewald θα προβάλλονται σε κύκλους σημείων γύρω από την θέση άμεση πορείας των ακτίνων-χ (σημείο Α). 44
45 Εικόνα 18: Αριστερά: Ο κρύσταλλος είναι προσανατολισμένος με τέτοιο τρόπο ώστε τα επίπεδα στο αντίστροφο πλέγμα να είναι κάθετα στην δέσμη ακτίνων-χ. Τα επίπεδα, οι διατομές των κύκλων καθώς και οι περιθλασμένες απο το δείγμα ακτίνες απεικονίζονται με διαφορετικό χρώμα για κάθε επίπεδο. Δεξιά: Με περιστροφή του αντιστρόφου πλέγματος ένα ακόμα επίπεδο (κόκκινο) εμφανίζεται στη σφαίρα του Ewald. (Πηγή: Εαν θεωρήσουμε ότι το κέντρο του ανιχνευτή βρίσκεται ευθυγραμμισμένο με τον αρχικό άξονα διάδοσης της ακτινοβολίας, η εικόνα που θα πάρουμε από την περίθλαση θα μοιάζει με «κηλίδες» γύρω από ένα κέντρο Ο, η θέση των οποίων θα συμπίπτει με το σημείο τομής της περιθλούσας ακτινοβολίας με τη σφαίρα του Ewald και απόσταση από το κέντρο Ο ίση με το μέτρο του διανύσματος σκέδασης, δηλαδή l Εικόνα 19: Αριστερά: η σφαίρα του Ewald. Δεξιά: Προφίλ περίθλασης ακτίνων-χ από μονοκρύσταλλο (πηγή: 45
46 Ατομικός Παράγοντας σκέδασης και Παράγοντας Δομής Κάθε κύμα περιθλούσας ακτινοβολίας που προσπίπτει σε έναν ανιχνευτή παράγει ένα σήμα, το οποίο μπορεί να περιγραφεί ως το άθροισμα της συνεισφοράς όλων των ηλεκτρονίων ενός κρυσταλλογραφικού επιπέδου hkℓ τα οποία συνέβαλλαν στη σκέδαση της ακτινοβολίας. Ένας μετασχηματισμός Fourier αντιπροσωπεύει μια συνάρτηση σε όρους ημιτονοειδών κυμάτων. Γενικά, κάθε συνάστηση μπορεί να περιγραφεί μέσω του μετασχηματισμού Fourier, ο οποίος, απλούστερα, είναι το άθροισμα ενός αριθμού ημιτονοειδών κυμάτων κατάλληλων συχνοτήτων, πλατών και φάσεων. Αυτό το άθροισμα ονομάζεται παράγοντας δομής, Fhkℓ (structure factor). H εξίσωση του παράγοντα δομής μπορεί να γραφτεί ως μετασχηματισμός Fourier, όπου ο κάθε παράγοντας αντιστοιχεί στη συνεισφορά ενός ατόμου στην ανάκλαση hkℓ. Ο ατομικός παράγοντας σκέδασης fhkℓ (form factor ή scattering factor) συμβολίζει την συνεισφορά ενός μόνο ατόμου στην ανάκλαση. Ο παράγοντας σκέδασης θεωρεί το κάθε άτομο σαν μια σφαίρα ηλεκτρονιακής πυκνότητας και αλλάζει ανάλογα με τον ατομικό αριθμό του κάθε ατόμου. Ο παράγοντας δομής (structure factor), ο οποίος αποτελεί το άθροισμα των ατομικών παραγόντων σκέδασης των ατόμων ενός συγκεκριμένου επιπέδου, μπορεί να υπολογιστεί από τον παρακάτω τύπο: F = = Όπου φ είναι η φάση της κύμανσης. Πρέπει να σημειωθεί ότι η ένταση της περίθλασης είναι ανάλογη με το τετράγωνο του παράγοντα δομής, οπότε ισχύει: Ι ( Ιδιαίτερα σημαντικός είναι ο )2 παράγοντας Debye-Waller, ο οποίος συνυπολογίζει τη θερμική κίνηση των ηλεκτρονίων. Η επίδρασή της στο ηλεκτρονιακό νέφος έχει ως αποτέλεσμα τη διασπορά των ηλεκτρονίων και κατ επέκταση τη μείωση της σκεδαστικής απόδοσης στις μεγάλες γωνίες σκέδασης. Εαν ληφθεί υπ όψην ο παράγοντας αυτός, ο τύπος που δίνει τον παράγοντα δομής μετατρέπεται στην παρακάτω σχέση: Fhk = 46
47 Όπου,ο παράγοντας Debye-Waller. Επιπροσθέτως, ο παράγοντας δομής μπορεί να γραφτεί ως το ολοκλήρωμα της ηλεκτρονιακής πυκνότητας στον όγκο της θεμελιώδους κυψελίδας. Η ηλεκτρονιακή πυκνότητα ενός στοιχείου όγκου στη θέση (x, y, z) υπολογίζεται ως o μέσος όρος της ηλεκτρονιακής πυκνότητας ρ(x, y, z) σε κάθε σημείο. Έτσι, έχουμε: F = Η τελευταία αυτή σχέση δείχνει ότι ο παράγοντας δομής είναι ο μετασχηματισμός Fourier της ηλεκτρονιακής πυκνότητας ρ(x, y, z) σε ένα σύνολο επιπέδων hkl Ηλεκτρονιακή Πυκνότητα και το πρόβλημα φάσης Ηλεκτρονιακή πυκνότητα είναι το μέτρο της πιθανότητας ύπαρξης ενός ηλεκτρονίου σε μια συγκεκριμένη θέση σε ένα άτομο. Δίνεται από τον τύπο: ρ(x,y,z)= l l l όπου V ο όγκος της θεμελιώδους κυψελίδας. Η εξίσωση αυτή δείχνει ότι προκειμένου να υπολογιστεί Φάση είναι ένας όρος που χρησιμοποιείται για να περιγράψει τη θέση ενός κύματος σε σχέση με ένα άλλο κύμα. Δυο ίδια κύματα βρίσκονται «σε φάση» όταν τα μέγιστα και τα ελάχιστά τους συμπίπτουν και «εκτός φάσης» όταν το μέγιστο του ενός κύματος συμπίπτει με το ελάχιστο του άλλου. η ηλεκτρονιακή πυκνότητα πρέπει πρώτα να κατασκευαστεί μια σειρά μετασχηματισμών Fourier των παραγόντων δομής. Καθώς ο Fhkl είναι μια περιοδική συνάρτηση, έχει πλάτος, συχνότητα και φάση. Επειδή προέρχεται από την περίθλαση ακτινών-χ, η συχνότητα παραμένει ίδια με αυτή της πηγής της ακτινοβολίας. Το πλάτος είναι ανάλογο με την τετραγωνική ρίζα της έντασης, Ιhkl και έτσι μπορούν να ληφθούν άμεσα από τις μετρήσεις. Παρ όλα αυτά, η φάση φhkl δεν μπορεί να υπολογιστεί άμεσα από μια μέτρηση. 47
48 Προκειμένου να μπορέσει να υπολογιστεί η ηλεκτρονιακή πυκνότητα από τους παράγοντες δομής πρέπει πρώτα να γίνει γνωστή η φάση κάθε περιθλασμένης ακτίνας. Το παραπάνω είναι γνωστό ως το κρυσταλλογραφικό πρόβλημα φάσης και η λύση του αποτελεί μεγάλη πρόκληση για την επίλυση μιας δομής. Από τη μέτρηση των εντάσεων των ανακλάσεων προκύπτουν μόνο τα μέτρα των παραγόντων δομής, ενώ παραμένουν άγνωστες οι φάσεις τους. Η λύση του προβλήματος φάσης ισοδυναμεί με την επίλυση της δομής του κρυστάλλου μέσω της εύρεσης των θέσεων των ατόμων μέσα στη θεμελιώδη κυψελίδα. Ένας αριθμός μεθόδων έχει αναπτυχθεί για την επίλυση του προβλήματος φάσης, οι οποίες χωρίζονται σε άμεσες και έμμεσες. Οι έμμεσες οδηγούν στην επίλυση της δομής βασιζόμενες σε κάποιες γνωστές φάσεις, ενώ οι άμεσες ξεκινούν με όλες τις φάσεις άγνωστες. Μια ισχυρή μέθοδος επίλυσης είναι η Multi-wavelength Anomalous Diffraction (MAD). Σε αυτή τη τεχνική, τα ηλεκτρόνια εσωτερικών στοιβάδων των ατόμων απορροφούν ακτίνες-χ συγκεκριμένου μήκους κύματος και επανεκπέμπουν τις ακτίνες-χ μετα από μια μικρή χρονική καθυστέρηση, επάγοντας μια αλλαγή στις φάσεις όλων των ανακλάσεων, φαινόμενο γνωστό ως ανώμαλη διασπορά (anomalous dispersion). Ανάλυση των μεταβολών που προκύπτουν στις φάσεις των ανακλάσεων έχει ως αποτέλεσμα την επίλυσή τους. Άλλες πειραματικές μέθοδοι επίλυσης του προβλήματος φάσης περιλαμβάνουν την Πολλαπλή Ισόμορφη Αντικατάσταση (Multiple Isomorphus Replacement, MIR), όπου βαρεά άτομα εισέρχονται στη δομή (συνήθως μέσω σύνθεσης πρωτεϊνων με ανάλογα ή μέσω soaking) και την Ανώμαλη Διασπορά ενός Μήκους Κύματος (Single Wavelenght Anomalous Dispersion, SAD). Οι τιμές των φάσεων μπορούν επίσης να υπολογιστούν χρησιμοποιώντας την μέθοδο της Mοριακής Aντικατάστασης (molecular replacement), όπου οι φάσεις ενός παρόμοιου μορίου (π.χ. πρωτεϊνες με μεγάλη ομοιότητα στις αμινοξικές τους αλληλουχίες) συνδυάζονται με τις πειραματικά καθοριζόμενες τιμές. 48
49 Μέσω της άμεσης μεθόδου, οι κρυσταλλογραφικές φάσεις προσδιορίζονται χρησιμοποιώντας μια τριπλή σχέση (μια τριάδα ανακλάσεων στις οποίες η ένταση και η φάση της μιας μπορούν να εξηγηθούν σε σχέση με τις άλλες δύο), ενώ η έμμεση μέθοδος, χρησιμοποιεί την συνάρτηση Patterson, μέσω της οποίας κατ αρχήν υπολογίζονται οι θέσεις των βαρεών ατόμων που έχουν εισαχθεί στη δομή Περίθλαση Ακτίνων-Χ από πολυσκρυσταλλικά υλικά (X-ray Powder Diffraction) H περίθλαση ακτίνων-χ πολυκρυσταλλικών υλικών είναι μια από τις πιο ευρέως χρησιμοποιούμενες μεθόδους για τον χαρακτηρισμό της δομής μηβιολογικών, αλλά και βιολογικών υλικών. Παλαιότερα η τεχνική αυτή χρησιμοποιούταν σαν εργαλείο για ποσοτική και ποιοτική ανάλυση, όπως για την εξακρίβωση της κρυσταλλικής φάσης (phase identification), της κρυσταλλικότητας, καθώς και για τη μελέτη της σύστασης των υλικών. Ένα πολυκρυσταλλικό δείγμα αποτελείται από ένα πολύ μεγάλο αριθμό τυχαία προσανατολισμένων μικροκρυστάλλων, διαστάσεων 1-10 μm. Οι ίδιοι κανόνες που διέπουν την περίθλαση από ένα μονοκρύσταλλο, όπως περιγράφτηκαν παραπάνω, ισχύουν και για την περίθλαση από πολυκρυσταλλικά υλικά. Ωστόσο, λόγω του τυχαίου προσανατολισμού των κρυστάλλων, υπάρχουν πολλά επίπεδα hkl που μπορούν να ικανοποιήσουν τον νόμο του Bragg ταυτόχρονα. Σε ένα πολυκρυσταλλικό δείγμα, το διάνυσμα σκέδασης Εικόνα 20: Σχηματική αναπαράσταση των διαφορετικών προσανατολισμών των μικροκρυστάλλων στο δείγμα (Dinnebier & Friese). μπορεί να βρεθεί σε όλους τους πιθανούς προσανατολισμούς σε σχέση με τη δέσμη ακτίνων-χ, σχηματίζοντας τους λεγόμενους κώνους Debye- Scherrer. 49
50 Με την πρόσπτωση μια ισχυρά εστιασμένης, παράλληλης δέσμης ακτίνων-χ συγκεκριμένου μήκους κύματος πάνω σε ένα πολυκρυσταλλικό δείγμα και την σκέδασή της από αυτό, παράγεται ένας αριθμός ομο-αξονικών κώνων περίθλασης. Η κατεύθυνση της αρχικής δέσμης εξυπηρετεί σαν τον άξονα των κώνων Debye- Scherrer, οι οποίοι μπορούν να προκύπτουν προς όλες τις κατευθύνσεις. Εικόνα 21: Κώνοι Debye-Scherrer στον ευθύ χώρο (Dinnebier & Friese). Η τομή αυτών των κώνων με τη σφαίρα του Ewald έχει ως αποτέλεσμα την δημιουργία ομόκεντρων δακτυλίων κάθετων στην φορά διάδοσης της δέσμης ακτίνων-χ. Αυτό που πρέπει να μετρηθεί σε ένα πείραμα περίθλασης από πολυκρυσταλλικά υλικά είναι η προκύπτουσα ένταση και η θέση 2ϑ. Στα πειράματα αυτά, το μεγαλύτερο πρόβλημα είναι η «κατάρρρευση» των τρισδιάστατου πλέγματος στο δισδιάστατο χώρο. Αυτό προκαλεί μερική ή ολική αλληλεπικάλυψη των κορυφών με παρόμοιο d-spacing και κατ επέκταση απώλεια δομικής πληροφορίας. Εικόνα 22: Αριστερά: H σφαίρα του Ewald για πολυκρυσταλλικά υλικά. Διακρίνονται οι κώνοι Debye-Scherrer. Δεξιά: Εικόνα από area detector από περίθλαση πολυκρυσταλλικού δείγματος. Εμφανείς είναι οι δακτύλιοι περίθλασης (πηγή: Von Dreele, 50
51 Κάθε δακτύλιος αντιπροσωπεύει ένα σύνολο ανακλάσεων που αντιστοιχούν σε μια συγκεκριμένη απόσταση d μέσα στο δείγμα. Η ομαλή κατανομή της έντασης γύρω από τον κάθε δακτύλιο σημαίνει ότι το δείγμα έχει την ιδανική πολυκρυσταλλική μορφή, αποτελούμενο από εκατομμύρια κρυστάλλους σε τυχαίο προσανατολισμό. Εαν, αντίθετα υπήρχε το φαινόμενο του προτιμώμενου προσανατολισμού (preferred orientation) τότε στο παραπάνω προφίλ θα υπήρχαν διαφορές στις εντάσεις σε κάθε δακτύλιο. Ολοκλήρωση της έντασης της περίθλασης γύρω από τον κάθε δακτύλιο έχει ως αποτέλεσμα την απεικόνιση ενός προφίλ powder diffraction ως συνάρτηση της έντασης I με τη γωνία περίθλασης 2ϑ. Εικόνα 23: Δεδομένα Περίθλασης ακτίνων-χ από πολυκρυσταλλικά υλικά, στο οποίο τα δεδομένα απεικονίζονται σαν συνάρτηση της έντασης της περιθλούσας ακτινοβολίας (άξονας y) ως προς την γωνία περίθλασης 2ϑ. Από μια τέτοια απεικόνιση των δεδομένων, όπως αυτή της εικόνας 23 μπορούμε να επεξεργαστούμε πιο εύκολα τα δεδομένα. Η θέση των κορυφών στον άξονα x (γωνία 2ϑ) μπορεί να μας δώσει πληροφορία για τη συμμετρία της θεμελιώδους κυψελίδας και τις ακριβείς τιμές των πλεγματικών σταθερών a, b, c και α, β, γ. Από την άλλη, από τις τιμές της έντασης στον άξονα y είναι δυνατόν να υπολογιστεί ο παράγοντας δομής Fhkl και στη συνέχεια να κατασκευαστούν χάρτες ηλεκτρονιακής πυκνότητας που θα δείχνουν τις θέσεις των ατόμων μέσα στη δομή. 51
52 General και Systematic Absences Όταν συλλεχθεί ένα προφίλ περίθλασης, είναι φυσιολογικό οι έντασεις των ανακλάσεων να διαφέρουν μεταξύ τους, ενώ πολλές φορές κάποιες ανακλάσεις απουσιάζουν εντελώς. Κάποιες από αυτές τις ανακλάσεις έχουν εντάσεις κοντά στο μηδέν, καθώς πολύ λίγα ηλεκτρόνια του συγκεκριμένου επιπέδου της κρυσταλλικής δομής συνεισφέρουν στην περίθλαση, ενώ άλλες ανακλάσεις έχουν εντάσεις ακριβώς ίσες με το μηδέν λόγω της καταστροφικής συμβολής των εξερχόντων από τον κρύσταλλο ακτίνων-χ. Αυτού του είδους οι απουσίες των ανακλάσεων επηρεάζονται από τις θέσεις των ατόμων που σχετίζονται με συμμετρία (symmetry-related atoms) μέσα στην κρυσταλλική δομή. Κανονικά, κάθε ανάκλαση σχετίζεται με ένα συγκεκριμένο επίπεδο Miller (h,k,l) και έχει μια συγκεκριμένη τιμή παρατηρούμενης έντασης. Όταν = 0, τότε η ανάκλαση είναι απούσα από τα δεδομένα. Εικόνα 24: Ένα πρότυπο περίθλασης σε ανιχνευτή τύπου area detector. Διακρίνονται η διαφορά στην ένταση των ανακλάσεων, καθώς και η απουσία ορισμένων. (Πηγή: SYSTEMATIC ABSENCES IN CRYSTAL DATA). Ένα σημαντικό μέρος για την επίλυση της κρυσταλλικής δομής βασίζεται στον καθορισμό του τύπου του πλέγματος και του space group. Αυτή η πληροφορία εμπεριέχεται στο πρότυπο της περίθλασης κάθε κρυσταλλικού τύπου πλέγματος, συνεισφερόμενη από 52 την ύπαρξη και την απουσία συγκεκριμένων ανακλάσεων. Όπως γίνεται γνωστό από τους τύπους τους, οι παράγοντες δομής περιέχουν πληροφορία σχετική με τα επίπεδα Miller και τις συντεταγμένες κάθε ατομικού τύπου μέσα στη θεμελιώδη κυψελίδα. Εξετάζοντας τις ανακλάσεις των προτύπων περίθλασης, είναι δυνατόν να καθοριστεί η θέση όλων των ατόμων και μορίων μέσα σε μια κυψελίδα.
53 Οι απούσες ανακλάσεις στα πρότυπα περίθλασης μπορούν να διακριθούν σε δύο τύπους: στις γενικές απουσίες (general absences), οι οποίες σχετίζονται με τον τύπο του πλέγματος, και τις συστηματικές απουσίες (systematic absences), οι οποίες σχετίζονται με τα στοιχεία συμμετρίας μετακίνησης (translational symmetry elements) όπως για παράδειγμα τον screw axis, και κατά συνέπεια με το space group. Οι κανόνες που επικρατούν για κάθε μία από τις δύο περιπτώσεις συνοψίζονται στους παρακάτω πίνακες: Τύπος Κανόνες για General Absences πλέγματος P Kανένας A k+l= 2n+1 B h+l= 2n+1 C h+k=2n+1 F Οι ανακλάσεις πρέπει να έχουν όλες τις σταθερές περιττές ή άρτιες για να παρατηρηθούν I h+k+l=2n+1 Στοιχείο Κανόνες για Systematic Absences συμμετρίας Screw axis 2 1, 4 2 (h,0,0) h=2n+1 πλευράς a 4 1, 4 3 (h,0,0) h=4n+1 Screw axis 2 1, 4 2 (0,k,0) k=2n+1 πλευράς b 4 1, 4 3 (0,k,0) k=4n+1 Screw axis 2 1, 4 2, 6 3 (0,0,l) l=2n+1 πλευράς c 3 1, 3 2, 6 2, 6 4 (0,0,l) l=3n+1 4 1, 4 3 (0,0,l) l=4n+1 6 1,6 5 (0,0,l) l=6n+1 Πίνακας 4: Οι κανόνες που διέπουν τις γενικές και συστηματικές απουσίες. 53
54 3. Όργανα και Μέθοδοι 3.1. Σύγχροτρον- Ακτινοβολία Σύγχροτρον Η μέθοδος της κρυσταλλογραφίας ακτίνων-χ, καθώς και πλήθως άλλων μεθόδων, απαιτούν την ύπαρξη ικανών πηγών Ακτίνων-Χ κατάλληλης ενέργειας που μπορούν να χρησιμοποιηθούν σε εύρος πειραματικών διαδικασιών. Το Σύγχροτρον είναι ένας μεγάλης κλίμακας κυκλικός επιταχυντής ηλεκτρονίων που παράγει ακτινοβολία υψηλής έντασης, η οποία ονομάζεται Ακτινοβολία Σύγχροτρον. Τα χαρακτηριστικά της ακτινοβολίας Συγχροτρον είναι τέτοια που την κάνουν ιδανική για πειράματα κρυσταλλογραφίας καθώς τα δεδομένα που λαμβάνονται από τέτοια πειράματα είναι υψηλής ποιότητας. Ανάμεσα σε αυτά τα χαρακτηριστικά είναι: το μεγάλο εύρος μηκών κύματος, που καλύπτει από μικροκύματα μέχρι «σκληρές» ακτίνες-χ, με αποτέλεσμα να είναι δυνατή η επιλογή του μήκους κύματος από τους χειριστές του οργάνου ανάλογα με το πείραμα που διεξάγουν. Υψηλή ροή φωτονίων, η οποία επιτρέπει την διεξαγωγή των πειραμάτων σε μικρούς χρόνους ή αλλιώς την χρήση κρυστάλλων με μικρή απόδοση περίθλασης. Υψηλή ένταση, καθώς η δέσμη των φωτονίων είναι σε μεγάλο βαθμό ευθυγραμμισμένη. Μεγάλη σταθερότητα σε βαθμό submicron. Υψηλή πολωσιμότητα Μεγάλη γωνιακή και ενεργειακή ευκρίνεια. Συγκρίνοντας τις ακτίνες-χ που παράγονται από ακτινοβολία Σύγχροτρον, σε σχέση με αυτές μιας τυπικής εργαστηριακής πηγής, μπορούμε να πούμε ότι η πρώτη είναι εκατομμύρια φορές πιο φωτεινή. 54
55 Πως όμως παράγεται η Ακτινοβολία Σύγχροτρον; Η ακτινοβολία Σύγχροτρον αποτελεί το «φως» που εκπέμπεται από τα ηλεκτρόνια που κινούνται με μεγάλη ταχύτητα και αναγκάζονται να αλλάξουν κατεύθυνση διάδοσης μέσω ενός μαγνητικού πεδίου. Το μήκος κύματος της ακτινοβολίας εξαρτάται από τα χαρακτηριστικά των ηλεκτρονίων τα οποία κυκλοφορούν στον κεντρικό δακτύλιο που ονομάζεται δακτύλιος αποθήκευσης (storage ring). Εικόνα 25: Άποψη του ESRF. Απεικονίζονται ο γραμμικός επιταχυντής (LINAC), ο δακτύλιος booster καθώς και ο δακτύλιος αποθύκευσης (πηγή: Τα ηλεκτρόνια παράγονται στο κέντρο μέσω μιας συσκευής που ονομάζεται electron gun και επιταχύνονται σε βαθμό % της ταχύτητας του φωτός από έναν γραμμικό επιταχυντή (Linac). Τα ηλεκτρόνια στη συνέχεια μεταφέρονται σε ένα κυκλικό επιταχυντή, τον δακτύλιο booster (Booster ring), οπού αυξάνεται η ενέργειά τους λόγω της γρήγορης κυκλικής επιτάχυνσης. Στη συνέχεια, μεταφέρονται στον εξωτερικό δακτύλιο αποθήκευσης (storage ring). Εκεί, τα ηλεκτρόνια επιταχύνονται περαιτέρω ενώ παράλληλα περνούν και απο ειδικές διατάξεις μαγνητών που διαχωρίζονται από ευθεία τμήματα. Καθώς τα ηλεκτρόνια εκτρέπονται μέσω του μαγνητικού πεδίου που δημιουργείται από τους μαγνήτες, εκπέμπουν ηλεκτρομαγνητική ακτινοβολία, έτσι ώστε να παράγεται μια δέσμη ακτινοβολίας Σύγχροτρον σε κάθε διάταξη μαγνητών. Υπάρχουν δύο τύποι διατάξεων μαγνητών που χρησιμοποιούνται για την παραγωγή φωτονίων μέσα στον δακτύλιο αποθήκευσης: οι μαγνήτες κάμψης (bending magnets) και οι συσκευές παρεμβολής (insertion devices) οι οποίες διακρίνονται περαιτέρω σε wigglers και undulators. 55
56 Oι μαγνήτες κάμψης αποτελούν την πλέον «παραδοσιακή» πηγή ακτινοβολίας Σύγχροτρον, οι οποίοι εκτρέπουν τα ηλεκτρόνια από την κυκλική τους πορεία. Αποτέλεσμα αυτής της εκτροπής είναι η εκπομπή ακτινοβολίας εφαπτομενικά στην αρχική κυκλική τροχιά. Εικόνα 26: Σχηματική αναπαράσταση μαγνήτη κάμψης. (πηγή: Hammond, P. Οι συσκευές παρεμβολής, όπως αναφέρθηκε διακρίνονται σε wigglers και undulators. Και οι δύο τύποι συσκευών παρεμβολής αποτελούνται από μια διαδοχική διάταξη μικρών μαγνητών με εναλλασσόμενη πολικότητα. Τα εναλλασσόμενα μαγνητικά πεδία αναγκάζουν τα ηλεκτρόνια να ταλαντωθούν γύρω από μια ευθύγραμμη τροχιά. Στους wigglers η ένταση αυξάνεται αναλογικά με τον αριθμό των μαγνητών και το ενεργειακό φάσμα είναι συνεχές. Στα άκρα του wiggler, όπου η ταλάντωση των ηλεκτρονίων είναι μεγαλύτερη, εκπέμπεται δέσμη φωτονίων υψηλής ενέργειας. Οι wigglers εκπέμπουν ένα ευρύ φάσμα ακτινοβολίας από το υπέρυθρο φως ως ακτίνες-χ. Παρόμοιοι με τους wigglers, οι undulators διαφέρουν στο ό,τι προκαλούν μικρότερη εκτροπή της δέσμης ηλεκτρονίων και το φως που παράγεται είναι ημι-συνεκτικό. Οι undulators αποτελούνται από περισσότερους μαγνήτες και οι διαφορετικοί «κώνοι φωτός» που παράγονται από την κάμψη της δέσμης ηλεκτρονίων από τους μαγνήτες αλληλεπικαλύπτονται και παρεμβάλλονται μεταξύ τους. Το φάσμα φωτονίων που παράγεται από τους undulators αποτελείται από ισχυρές κορυφές δύο τάξεις μεγέθους υψηλότερες σε λαμπρότητα από αυτές ενός wiggler. Εικόνα 27: Σχηματική αναπαράσταση διάταξης μαγνητών τύπου wiggler. (πηγή: Hammond, P. Εικόνα 28: Σχηματική αναπαράσταση διάταξης μαγνητών τύπου undulator. (πηγή: Hammond, P. 56
57 Ενώ οι μαγνήτες κάμψης μπορούν να εκπέμψουν χρησιμοποιήσημη ακτινοβολία, η πιο ηψηλής έντασης ακτινοβολία λαμβάνεται μέσω των συσκευών παρεμβολής στα ευθεία τμήματα του δακτυλίου. Σε σύγκριση με μια εργαστηριακή πηγή ακτίνων Χ, μια δέσμη ακτίνων Χ παραγόμενη από ένα σταθμό Σύγχροτρον έχει σημαντικώς μικρότερη απόκλιση και υψηλότερη ένταση. Όσον αφορά τα πολυκρυσταλλικά δείγματα, το σημαντικότερο πλεονέκτημα της χρήσης ακτινοβολίας Σύγχροτρον είναι η υψηλή γωνιακή ευκρίνια των δεδομένων που λαμβάνονται. Όπως αναφέρθηκε παραπάνω τα φωτόνια εκτρέπονται από την τροχιά τους εφαπτομενικα στον δακτύλιο αποθήκευσης στις θέσεις που υπάρχουν οι διατάξεις μαγνητών. Στις θέσεις αυτές έχουν χτιστεί πειραματικοί σταθμοί (beamlines) οι οποίοι εξυπηρετούν διαφορετικές λειτουργίες. Τα οπτικά χαρακτηριστικά κάθε beamline είναι προσαρμοσμένα στον τύπο των πειραμάτων που διεκπεραιώνονται στο συγκεκριμένο σταθμό. Εικόνα 29: Αριστερά: Απεικονίζεται το εσωτερικό του δακτυλίου αποθήκευσης και οι διατάξεις μαγνητών που υπάρχουν μέσα σε αυτό. Δεξιά: Κάθε πειραματικός σταθμός (beamline) χτίζεται εφαπτομενικά του δακτυλίου αποθήκευσης στις θέσεις που παράγεται η ακτινοβολία. (Πηγή: ). 57
58 Το Ευρωπαϊκό (ESRF) και το Ελβετικό Σύγχροτρον (SLS) Για τα πειράματά μας χρησιμοποιήθηκαν οι πειραματικοί σταθμοί για περίθλαση ακτίνων-χ από πολυκρυσταλλικά υλικά (Powder Diffraction beamlines) του Ευρωπαϊκού και του Ελβετικού Σύγχροτρον. Το Ευρωπαϊκό Σύγχροτρον (European Synchrotron Radiation Facility, ESRF) είναι μια Ευρωπαϊκή πηγή ακτινοβολίας. Εντοπίζεται στην Grenoble της Γαλλίας, ενώ υποστηρίζεται οικονομικά και μοιράζεται από 19 χώρες. Ο εξωτερικός δακτύλιος αποθήκευσης (storage ring, ενέργεια 6 GeV) έχει περιφέρεια 844 m γύρω από την οποία έχουν χτιστεί 40 πειραματικοί σταθμοί που εξυπηρετούν μεγάλο εύρος πειραματικών δυνατοτήτων. Εικόνα 30: Αριστερά: Επισκόπηση των πειραματικών σταθμών που υπάρχουν σήμερα στο ESRF. Δεξιά: Εικόνα του ESRF στην οποία διακρίνεται ο δακτύλιος αποθήκευσης. (πηγή: Το Ελβετικό Σύγχροτρον (Swiss Light Source, SLS) βρίσκεται στο Paul Scherrer Institute στο Villigen της Ελβετίας. Είναι ένα Σύγχροτρον τρίτης γενιάς, με την περίμετρο του δακτύλιου αποθήκευσης να είναι 288 m. Με ενέργεια 2.4 GeV, προσφέρει δέσμες φωτονίων υψηλής λαμπρότητας για την έρευνα στους τομείς της Επιστήμης Υλικών, Βιολογίας και Χημείας. 58
59 Εικόνα 31: Αριστερά: Επισκόπηση των πειραματικών σταθμών που υπάρχουν σήμερα στο SLS. Δεξιά: Εικόνα του SLS στην οποία διακρίνεται ο δακτύλιος αποθήκευσης. (πηγή: Πειραματικοί σταθμοί- Beamlines Κάθε πειραματικός σταθμός έχει τις δικές του προδιαγραφές. Για τα πειράματα που θα παρουσιαστούν σε αυτήν την εργασία χρησιμοποιήθηκαν τα beamlines ID31 (ESRF), ID11 (ESRF) και το MS - X04SA (SLS) και για αυτό το λόγο θα παρουσιαστούν ορισμένα από τα σημαντικότερα χαρακτηριστικά τους. ID31 Beamline (ESRF) Το ID31 (Fitch, 2004) είναι το beamline Περίθλασης από Πολυκρυσταλλικά Υλικά Υψηλής Ευκρίνειας, το οποίο προσφέρει δεδομένα υψηλής ευκρίνειας (High Resolution Powder Diffraction beamline) του ESRF. Όπως γίνεται προφανές και από το όνομά του, το μεγαλύτερο πλεονέκτημα του ID31 είναι η δυνατότητα καταγραφής δεδομένων περίθλασης ακτίνων-χ από πολυκρυσταλλικά υλικά με πολύ μεγάλη γωνιακή ευκρίνεια. Αποτέλεσμα αυτής της ιδιότητας του οργάνου είναι η ικανότητα διάκρισης ανάμεσα σε πολύ κοντινές αλλά όχι πλήρως επικαλυπτώμενες ανακλάσεις. Αυτό επιτρέπει υψηλή ευκρίνεια στον αντίστροφο χώρο (high reciprocal space resolution), η οποία είναι ιδιαίτερα σημαντική για τα πειράματα περίθλασης 59 την
60 πολυκρυσταλλικών υλικών σε σχέση με τους μονοκρυστάλλους. Για την ίδια μέγιστη ευκρίνεια d-διαστήματος (d-spacing) που επιτυγχάνεται από ένα δείγμα, η υψηλότερη γωνιακή ευκρίνεια θα αυξήσει τον αριθμό των διακριτών ανακλάσεων, επιτρέποντας έναν πιο ακριβή προσδιορισμό της δομής. Η περιθλάση από πολυκρυσταλλικά υλικά απαιτεί μια μεγάλη δέσμη σε θέση να φωτίσει έναν μεγάλο όγκο δείγματος. Αυτός είναι ο λόγος που η οπτική του ID31 παραμένει απλή, χωρίς οπτική εστίασης. Οι ακτίνες Χ παράγονται από τρεις 11-mm-gap undulators, 1 U35 και 2 U32, οι οποίοι καλύπτουν ολόκληρο το φάσμα της ενέργειας από 5 kev έως 60 kev. Η λευκή δέσμη εξέρχεται από την πηγή και προσπίπτει σε ένα κρυοστατικά ψυχόμενο μονοχρωμάτορα αποτελείται από δύο κρυστάλλους πυριτίου Si(111). Για την απόκτηση δεδομένων περίθλασης Ακτίνων-Χ από πολυκρυσταλλικά υλικά υψηλής ευκρίνειας, το συγκεκριμένο beamline χρησιμοποιεί έναν ανιχνευτή-αναλυτή εννέα κανάλιών (nine channel multi-analyser detector). Κάθε ανιχνευτής προηγείται από έναν αναλυτή κρύσταλλο Si(111) οι οποίοι διαχωρίζονται ανα 2 μεταξύ τους, ενώ η μέτρηση της περιθλώμενης δέσμης γίνεται παράλληλα ως ολοκληρωμένη μονάδα. Οι προκύπτουσες κορυφές περίθλασης που καταγράφονται είναι ιδιαίτερα στενές (μεγάλη γωνιακή ευκρίνεια), η συμβολή του οργάνου στο FWHM (Full Width at Half Maximum) περίπου στις 0,003, ενώ οι θέσεις είναι ακριβείς και αναπαράξιμες σε λίγα δέκατα του millidegree. Οι ανακλάσεις καταγράφονται ανεξάρτητα στον ανιχνευτή και πρέπει στη συνέχεια να αθροίζονται. Αυτό επιτρέπει μια ακριβέστερη άθροιση των δεδομένων, η οποία απαιτείται για την ανάλυση δεδομένων από δείγματα πρωτεϊνών. Εφόσον οι εννέα ανιχνευτές συλλέγουν παράλληλα πάνω από 18 σε γωνία 2ϑ, γίνεται δυνατή η συλλογή των δεδομένων περίθλασης σε πιο μικρούς χρόνους, το οποίο είναι καλύτερο για τα δείγματα που μπορούν εύκολα να καταστραφούν από την ακτινοβολία, όπως οι πρωτεϊνες (radiation damage). Ένας μονοχρωμάτορας είναι μια οπτική συσκευή που εκπέμπει ένα μηχανικά επιλεγόμενο εύρος μηκών κύματος ακτινοβολίας, επιλέγοντάς το από ένα μεγαλύτερο εύρος μηκών κύματος. 60
61 Εικόνα 32: Σχηματική αναπαράσταση της πειραματικής διάταξης του ID31. (Πηγή: Το κύριο πλεονέκτημα του ID31 είναι οι άριστης ποιότητας συλλεγόμενες πληροφορίες, ικανές να χρησιμοποιηθούν για βελτιστοποίηση της δομής του προς ανάλυση μορίου (structure refinement). Το μειονέκτημα είναι η ποσότητα του δείγματος που απαιτείται για την κατάγραφή του σήματος, καθώς και ο ελάχιστος χρόνος που απαιτείται για να συλεγεί ένα μοτίβο. ID11 Beamline (ESRF) To ID11 είναι το beamline της Επιστήμης των Υλικών του ESRF. Είναι εξοπλισμένο με ένα δεύτερο πειραματικό χώρο (experimental hutch) εκτός του κύριου δακτυλίου αποθήκευσης που έχει κύριο σκοπό να εξασφαλίσει μέγιστη εστίαση. Δύο undulators (U23 και U22) υπό συνθήκες κενού χρησιμοποιούνται για την παραγωγή των ακτίνων-χ. Ένας οριζόντιος μονοχρωμάτορας Laue-Laue αποτελούμενος από δύο κυρτούς κρυστάλλους πυριτίου Si(111) επιτρέπει ενέργεια εύρους kev. Ο πρώτος πειραματικός κλωβός έχει ιδιαίτερα υψηλή ροή φωτονίων, ακόμα και σε μεγάλες ενέργειες, καθιστώντας το κατάλληλο για περίθλαση χρονικής ανάλυσης (time-resolved diffraction). Για τα πειράματα Περίθλασης Ακτίνων-Χ από Πολυκρυσταλλικά Υλικά, το ID11 χρησιμοποιείται όταν απαιτείται δέσμη μεγάλης ακρίβειας για ιδιαιτέρως ευαίσθητα ή μικρής ποσότητας δείγματα. 61
62 Εικόνα 33: Σχηματική αναπαράσταση της πειραματικής διάταξης του ID11 (πηγή: Bacon, D.H. et al., 2011). Τα κύρια μειονεκτήματα του ID11 περιλαμβάνουν την δυσκολία εκτέλεσης του πειράματος, καθώς είναι απαραίτητη η ρύθμιση των παραμέτρων του οργάνου πριν από κάθε πείραμα. Για παράδειγμα, το περιθλασίμετρο, ο ανιχνευτής και το δείγμα πρέπει να ευθυγραμμιστούν χειροκίνητα πριν από το κάθε πείραμα, ενώ πρέπει να γίνουν ρυθμίσεις για κάθε κίνηση του ανιχνευτή. Από την άλλη, τα πλεονεκτήματα του ID11 είναι το μεγάλο εύρος των πιθανών πειραματικών δυνατοτήτων, τα οποία μπορεί να είναι συμβατά με τους απαιτούμενους όρους για κάποια δύσκολα πειράματα (όπως για παράδειγμα το ασθενές σήμα περίθλασης, το μέγεθος του δείγματος, η καταστροφή του δείγματος λόγω της υψηλής έντασης της ακτινοβολίας κ.α.). Επιπλέον, σε περιπτώσεις ύπαρξης μεγάλης ποσότητας δείγματος, η χρήση ενός περιθλασίμετρου μεγάλης ευκρίνειας θα επιτρέψει την συλλογή δεδομένων με καλύτερη γωνιακή ευκρίνεια. MS - X04SA: Materials Science Beamline (SLS) Το beamline MS-X04SA της Επιστήμης των υλικών βρίσκεται στο Ελβετικό Σύγχροτρον. Περίθλαση από πολυκρυσταλλικά υλικά γίνεται στον πειραματικό χώρο 1 (Experimental Hutch 1). Η πηγή της ακτινοβολίας είναι μια διάταξη μαγνητών wiggler που παράγει ένα συνεχές φάσμα φωτονίων ενεργειακού εύρους 5-40 kev. Το περιθλασίμετρο MS Powder έχει τρεις ανεξάρτητες, ομοαξονικές, γωνιακές κινήσεις, μία για το δείγμα προς μέτρηση (ή το περιβάλλον του δείγματος) καθώς και δύο επιλέον συστήματα ανιχνευτή: 62
63 Ένα μοναδικό ανιχνευτή τύπου solid-state silicon microstrip, που ονομάζεται ΜΥΤΗΕΝ (Microstrip system for Time-rEsolved experimeνts). O ανιχνευτής MYTHEN είναι ένας γενικής χρήσης ανιχνευτής με μέγιστη ευκρίνεια 3.7 mdeg στα 2θ, με πολύ υψηλή απόδοση και μεγάλο ρυθμό καταγραφής σήματος (rapid acquisition times), καθώς με την κίνησή του καλύπτει ταυτόχρονα 120 2θ. Ο ανινευτής αυτός χρησιμοποιείται κυρίως σε περιπτώσεις που η ισχύς σκέδασης από το δείγμα είναι πολύ χαμηλή ή όταν ο χρόνος απόκτησης σήματος πρέπει να είναι πολύ μικρός. Ένα σύστημα πολλαπλών κρυστάλλων ανάλυσης και ανιχνευτών (multi analyser crystal detector system), ο οποίος χρησιμοποιείται μόνο σε συγκεκριμένες περιπτώσεις καθώς έχει το μειονέκτημα πολύ μικρού ρυθμού καταγραφής σήματος. Ο MYTHEN single-photon-counting silicon microstrip ανιχνευτής κατασκευάστηκε στο Ελβετικό Σύγχροτρον για πειράματα περίθλασης πολυκρυσταλλικών υλικών χρονικής ανάλυσης (time-resolved powder diffraction experiments). Επιτρέπει την απόκτηση προτύπων περίθλασης σε γωνίες πάνω από 120 σε 2ϑ σε χρόνο μερικών δευτερολέπτων. Η ποιότητα των δεδομένων είναι συγκρίσιμη με αυτή που μπορεί να αποκτηθεί από όργανα υψηλής ευκρίνειας όσον αφορά το FWHM και το σχήμα των κορυφών, με το επιπλέον πλεονέκτημα της γρήγορης απόκτησής τους. Εικόνα 34: Σχηματική αναπαράσταση της πειραματικής διάταξης του MS - 63 X04SA. (Πηγή: Schmitt, B. et al., 2002).
64 3.2. Μέθοδοι και πειραματική διαδικασία Ο σκοπός αυτής της διπλωματικής εργασίας είναι πρωταρχικά η κρυστάλλωση ανθρώπινης ινσουλίνης με τους οργανικούς προσδέτες φαινόλη, m-cresol, 4-nitrophenol και 4-Ethyl-Resorcinol σε κλίση ph, με στόχο την ταυτοποίηση νέων πολυμορφικών δομών και η ολοκλήρωση του διαγράμματος φάσης της ινσουλίνης. Η φαινόλη και τα φαινολικά παράγωγα επιλέχθηκαν, καθώς από παλαιότερα αυτές οι ουσίες προστίθενταν στα σκευάσματα ινσουλίνης ως αντιβακτηριακοί παράγοντες, ενώ έχει αποδειχθεί από τον Derewenda και τους συνεργάτες του ότι η φαινόλη προσδένεται στο εξαμερές της ινσουλίνης και επηρεάζει δραματικά τη διαμόρφωσή της, οδηγώντας την στη διαμόρφωση R Συγκρυστάλλωση ινσουλίνης με οργανικούς προσδέτες Κρυστάλλωση με φαινόλη Στο πρώτο βήμα της πειραματικής διαδικασίας έγινε κρυστάλλωση ανθρώπινης ινσουλίνης (αριθμός παρτίδας: RO10219A, Novo Nordisk) με τον οργανικό προσδέτη φαινόλη (εικόνα 35), μέσω της μεθόδου κρυστάλλωσης batch. Το πρωτεϊνικό διάλυμα ετοιμάστηκε με την διάλυση mg λυοφιλοποιημένης ινσουλίνης σε μορφή σκόνης σε 21 ml διπλά απεσταγμένου H2O (double distilled, d.d. H2O), με τελική συγκέντρωση διαλύματος 17.6 mg ml -1. Στη συνέχεια, 17 ml πρωτεϊνικού διαλύματος τοποθετήθηκαν σε ένα δοχείο falcon, μαζί με 1.97 ml διαλύματος zinc acetate (ZnAc2) 0.01 M. Η παρουσία του ψευδαργύρου είναι κρίσιμη για το σχηματισμό και τη σταθερότητα του εξαμερούς της ινσουλίνης, ενώ αντίθετα σε απουσία του, το πρωτεϊνικό διάλυμα θα αποτελούταν μόνο από μονομερή και διμερή. Στο ίδιο δοχείο τοποθετήθηκαν επίσης 0.51 ml διαλύματος φαινόλης συγκέντρωσης 2Μ σε 100% αιθανόλη. Τελικά, μετά από επώαση 5 λεπτών, στο μίγμα προστέθηκαν ml sodium thiocyanate (NaSCN) 1M, το οποίο δρα σαν άλας, προκαλώντας την μείωση της διαλυτότητας του συμπλόκου ινσουλίνης-ψευδαργύρουφαινόλης. Εικόνα 35: Τρισδιάστατη δομή του μικρού οργανικού μορίου της φαινόλης (Πηγή: 64
65 Επιπλέον, προετοιμάστηκαν δύο ρυθμιστικά διαλύματα Na2HPO4 και KH2PO4, σε συγκέντρωση 2Μ, τα οποία αναμίχθηκαν σε διαφορετικές αναλογίες προκειμένου να θέσουν μια κλίση διαλυμάτων ph αρχίζοντας από 4.0 το πιο όξινο και 8.9 το πιο βασικό, με βήμα περίπου 0.3 μονάδες ph. Πριν τη χρήση, τα διαλύματα των αλάτων πέρασαν από φιλτρα 0.22 μm και των buffer από φίλτρα Filtropur 0.20 μm. Τέλος, για κάθε δείγμα που παρασκευάστηκε, τοποθετήθηκαν 1.2 ml πρωτεϊνικού μίγματος και 300 μl από το ρυθμιστικό διάλυμα ph σε σωληνάκια eppendorf, με αποτέλεσμα τελική συγκέντρωση πρωτεΐνης 12.1 mg ml -1. Κρυστάλλωση Ανθρώπινης Ινσουλίνης με Φαινόλη Διαλύμα Ινσουλίνης σε d.d. H2O (c 17.6 mg 17 ml ml -1 ) ZnAc 2 (0.01 M) 1.97 ml Διαλύμα φαινόλης (2Μ) 0.51 ml ~Επώαση για 5 λεπτά~ NaSCN (1M) ml ~1.2 ml πρωτεϊνικού διαλύματος και 300 μl buffer ρύθμισης ph (Na 2HPO 4/KH 2PO 4) ~ Πίνακας 5: Κρυστάλλωση ανθρώπινης ινσουλίνης με τον προσδέτη φαινόλη. Η τελική συγκέντρωση της φαινόλης στο διάλυμα ήταν 41 mm. Τα διαλύματα αφέθηκαν για κρυστάλλωση σε έναν επωαστικό θάλαμο σε θερμοκρασία 298Κ. Στις επόμενες ημέρες, πολυκρυσταλλικά ιζήματα άρχισαν να γίνονται ορατά μέσα στα δοχεία eppendorf. Εικόνα 36: Μικροκρυσταλλικά δείγματα ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση 65 με τον οργανικό προσδέτη φαινόλη στα ph (a) 5.47, (b) 6.14, (c) 6.75 και (d) 7.46.
66 Τα ph των διαλυμάτων κρυστάλλωσης μετρήθηκαν πριν από την κρυστάλλωση καθώς και μετά την διεξαγωγή των πειραμάτων περίθλασης και παρατηρήθηκε μια μικρή μετατόπιση προς μεγαλύτερες τιμές ph για τα περισσότερα δείγματα. Οι τιμές ph που αναφέρονται σε αυτή τη διπλωματική εργασία, αποτελούν τις μέσες τιμές από τις δύο προαναφερθείσες μετρήσεις. Η κρυστάλλωση της ινσουλίνης με τον οργανικό προσδέτη φαινόλη έγινε δύο φορές στις τιμές ph που παρατίθενται στον παρακάτω πίνακα. Σημειώνεται ότι τα ph αυτά αντιστοιχούν σε μέσες τιμές. Αριθμός δείγματος ph (Κρυστάλλωση Ι) ph (Κρυστάλλωση ΙΙ) Πίνακας 6: Οι μέσες τιμές των ph που λήφθηκαν μετά από την κρυστάλλωση ανθρώπινης ινσουλίνης με φαινόλη. 66
67 Κρυστάλλωση με m-cresol Για την κρυστάλλωση ανθρώπινης ινσουλίνης με το μικρό οργανικό προσδέτη m-cresol ακολουθήθηκε ακριβώς η ίδια διαδικασία με παραπάνω, με τη διαφορά ότι η m-cresol όντας σε Εικόνα 37: Τρισδιάστατη δομή του μικρού οργανικού μορίου της m- cresol. (Πηγή: υγρή μορφή διαλύθηκε σε διάλυμα 100% αιθανόλης σε συγκέντρωση 25% v/v. Οι μέσες τιμές των ph που χρησιμοποιήθηκαν για τις δύο κρυσταλλώσεις με αυτόν τον προσδέτη συνοψίζονται στον παρακάτω πίνακα: Αριθμός δείγματος ph (Κρυστάλλωση Ι) ph (Κρυστάλλωση ΙΙ) Πίνακας 7: Οι μέσες τιμές των ph που λήφθηκαν μετά από την κρυστάλλωση ανθρώπινης ινσουλίνης με m-cresol. 67
68 Μετά από μια ημέρα περίπου κρυστάλλωσης σε επωαστικό θάλαμο στους 298Κ, άρχισε να εμφανίζεται πολυκρυσταλλικό ίζημα στα περισσόττερα από τα δείγματα. Παρατήρηση στο μικροσκόπιο έδειξε ότι η μορφολογία των κρυστάλλων αλλάζει με μεταβολή του ph, είτε σε σχήμα είτε σε μέγεθος, κάτι που απ ό,τι θα γίνει φανερό στα αποτελέσματα, ανταποκρίνεται σε αλλαγή της συμμετρίας της θεμελιώδους κυψελίδας. Εικόνα 38: Μικροκρυσταλλικά δείγματα ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με τον οργανικό προσδέτη m-cresol στα ph (a) 6.37, (b) 6.70, και (c) Κρυστάλλωση με 4-Nitrophenol Εικόνα 39: Τρισδιάστατη δομή του μικρού οργανικού μορίου της 4-nitrophenol (Πηγή: Διαλύθηκε ποσότητα του μικρού οργανικού μορίου 4-nitrophenol (εικόνα 39) σε DMSO (Dimethyl sulfoxide) σε συγκέντρωση 2Μ και στη συνέχεια ακολουθήθηκε η ίδια διαδικασία κρυστάλλωσης όπως έχει αναφερθεί στις δύο προηγούμενες ενότητες. 68
69 Η κρυστάλλωση έγινε στις παρακάτω μέσες τιμές ph, σε δύο πειράματα κρυσταλλώσεων: Αριθμός δείγματος ph (Κρυστάλλωση Ι) ph (Κρυστάλλωση ΙΙ) Πίνακας 8: Οι μέσες τιμές των ph που λήφθηκαν μετά από την κρυστάλλωση ανθρώπινης ινσουλίνης με 4- nitrophenol. Μετά από 24 περίπου ώρες παρατηρήθηκε πολυκρυσταλλικό ίζημα στο κάτω μέρος των δοχείων eppendorf το οποίο παρατηρήθηκε στο οπτικό μικροσκόπιο (εικόνα 40). Εικόνα 40: Πολυκρυσταλλικά δείγματα ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με τον οργανικό προσδέτη 4-nitrophenol στα ph 5.75 (αριστερά) και 6.17 (δεξιά). 69
70 Κρυστάλλωση με 4-Ethyl-Resorcinol Για την συγκρυστάλλωση της ινσουλίνης με τον μικρό οργανικό προσδέτη 4-ethyl-resorcinol, διαλύθηκε ποσότητα αυτού (εικόνα 41) σε DMSO (Dimethyl sulfoxide) σε συγκέντρωση 2Μ και στη συνέχεια ακολουθήθηκε η ίδια διαδικασία κρυστάλλωσης όπως έχει αναφερθεί παραπάνω. Oι μέσες τιμές των ph που χρησιμοποιήθηκαν για τις δύο κρυσταλλώσεις με αυτόν τον προσδέτη συνοψίζονται στον παρακάτω πίνακα: Εικόνα 41: Τρισδιάστατη δομή του μικρού οργανικού μορίου της 4-Ethyl-Resorcinol (Πηγή: Αριθμός δείγματος ph (Κρυστάλλωση Ι) ph (Κρυστάλλωση ΙΙ) Πίνακας 9: Οι μέσες τιμές των ph που λήφθηκαν μετά από την κρυστάλλωση ανθρώπινης ινσουλίνης με 4- ethyl-resorcinol 70
71 Τα διαλύματα αφέθηκαν για κρυστάλλωση σε έναν επωαστικό θάλαμο σε θερμοκρασία 298Κ. Στις επόμενες ημέρες, πολυκρυσταλλικά ιζήματα άρχισαν να γίνονται ορατά μέσα στα δοχεία eppendorf. Εικόνα 42: Πολυκρυσταλλικά δείγματα ανθρώπινης ινσουλίνης μετά από συγκρυστάλλωση με τον οργανικό προσδέτη 4-ethyl-resorcinol στα ph (a) 4.55, (b) 5.45, (c) 5.88 και (d)
72 Συλλογή δεδομένων Περίθλασης Ακτίνων-Χ Συλλογή δεδομένων στο ID31 Τα πειράματα περίθλασης από τα πολυκρυσταλλικά δείγματα ινσουλίνης έγιναν σε θερμοκρασία δωματίου με μήκος κύματος λ= (16) Å. Όλα τα δείγματα φορτώθηκαν σε σε βοριοπυριτικά τριχοειδή σωληνάρια (borosilicate capillaries) διαμέτρου mm και στη συνέχεια φυγοκεντρήθηκαν σε υψηλή ταχύτητα για 15 λεπτά προκειμένου να αυξήσουν το πακετάρισμα των μικροκρυστάλλων στον πυθμένα των τριχοειδών. Η περίσσεια του μητρικού υγρού της κρυστάλλωσης αφαιρέθηκε και τα τριχοειδή σφραγίστηκαν με silicone vacuum grease, για την απόφευξη της αφυδάτωσης του δείγματος κατά την διάρκεια της μέτρησης. Στη συνέχεια, τα τριχοειδή τοποθετήθηκαν στο περιθλασίμετρο, ενώ είναι απαραίτητη η γρήγορη περιστροφή τους στα 1000 rpm για την αποφυγή του φαινομένου του προτιμητέου προσανατολισμού (preferred orientation). Για την αλλαγή των δειγμάτων χρησιμοποιήθηκε αυτοματοποιημένο σύστημα με ρομπότ. Για κάθε θέση κατά μήκος του τριχοειδούς σωληναρίου λήφθηκε ένας αριθμός scans, ενώ τα τριχοειδή μετακινούνταν περιοδικά για να εκθέσουν μια νέα (fresh) περιοχή του δείγματος στην ακτινοβολία. Μετά από την καταγραφή αρκετών scans, παρατηρήθηκαν σημαντικές αλλαγές στο πρότυπο περίθλασης, συμπεριλαμβάνοντας την μεταβολή των πλεγματικών σταθερών, μια σταδιακή αύξηση στο εύρος των κορυφών της περίθλασης, καθώς και μείωση της έντασης τους. Αυτές οι Εικόνα 43: Δεδομένα περίθλασης από πολυκρυσταλλικό πρωτεϊνικό δείγμα σε area detector. Είναι εμφανές το φαινόμενο του προτιμώμενου προσανατολισμού. Η ένταση δεν είναι κατανεμημένη με τον ίδιο τρόπο στην περιφέρεια κάθε δακτυλιδιού περίθλασης, κάτι που προκαλεί προβλήματα στην αξιοπιστεία των δεδομένων που λήφθηκαν. μεταβολές υποδεικνύουν καταστροφή του πρωτεϊνικού δείγματος με την αύξηση του χρόνου έκθεσης του στη δέσμη ακτίνων-χ. Η καταστροφή των δειγμάτων από την ακτινοβολία (radiation damage) πρέπει να λαμβάνεται υπ όψη κατά τη διεξαγωγή του πειράματος καθώς επηρεάζει την στατιστική 72
73 αξιοπιστεία των δεδομένων και την ποιότητα των δεδομένων. Τα αποτελέσματα της καταστροφής του δείγματος από την ακτινοβολία μπορούν να παρατηρηθούν συγκρίνοντας τα προφίλ των δεδομένων από καθένα από τα 9 κανάλια του ανιχνευτή, καθώς και με σύγκριση του κάθε scan με τα επόμενα. Τα πρώτα scans, για τα οποία δεν είχε επέλθει ακόμα καταστροφή του δείγματος, συνδυάζονται και χρησιμοποιούνται για περαιτέρω ανάλυση. Εικόνα 44: Αριστερά: Πολυκρυσταλλικά δείγματα τοποθετημένα σε capillaries και στα ειδικά-για-το-id31 holders. Δεξιά: Δείγμα τοποθετημένο στο περιθλασίμετρο. Η επαφή γίνεται μέσω μαγνήτη που βρίσκεται στο πίσω μέρος του holder. Συλλογή δεδομένων στο ID11 Περισσότερες μετρήσεις πραγματοποιήθηκαν στο beamline ID11, το οποίο, όπως αναφέρθηκε, χρησιμοποιεί ανιχνευτή τύπου area detector. Τα δείγματα τοποθετήθηκαν σε τριχοειδή σωληνάρια τύπου borosilicate, όπως και στην προηγούμενη περίπτωση, αλλά και σε τριχοειδή σωληνάρια τύπου kapton. Τα δεδομένα συλλέχθησαν σε θερμοκρασία δωματίου. Έγιναν δύο πειράματα στο ID11 σε μήκη κύματος λ1=0.5339(5) Å και λ2=0.3444(3) Å. Η δέσμη εστιάστηκε χρησιμοποιώντας διαθλαστικούς φακούς (Vaughan et al., 2011) στην επιφάνεια μιας CCD κάμερας Frelon4M 2k x 2k, με μέγεθος pixel 50 x 50 μm 2 (Labiche et al., 2007). Η απόσταση ανάμεσα στο δείγμα και στον ανιχνευτή ήταν mm. Μια σειρά δεδομένων μετά από έκθεση στη δέσμη για 1 min, συλλέχθησαν σε θερμοκρασία δωματίου. Οι δισδιάστατες εικόνες μετατράπηκαν σε μονοδιάστατα προφίλ περίθλασης πολυκρυσταλλικών δεδομένων χρησιμοποιώντας το πρόγραμμα Fit2D (Hammersley, 1997). Πολλά τέτοια προφίλ συνδυάστηκαν για την βελτιστοποίηση της στατιστικής των δεδομένων. 73
74 Η χρήση του area detector του ID11, επέτρεψε μεγαλύτερη απόδοση στη στατιστική καταμέτρησης φωτονίων (photon counting statistics), λόγω της πολύ μεγάλης επιφάνειας ανίχνευσης της CCD κάμερας που σημαίνει ότι ένας μεγαλύτερος αριθμός κώνων Debye-Scherrer μπορούν να ανιχνευτούν παράλληλα. Παρ όλα αυτά, η αύξηση της απόδοσης αυτής έρχεται με το κόστος της ελάττωσης της αναλογίας του σήματος/θόρυβος, λόγω αύξησης του background. Σαν αποτέλεσμα, μπορεί να παρατηρηθεί μείωση της γωνιακής ευκρίνειας και αύξηση του εύρους των κορυφών της περίθλασης. Εικόνα 45: Σύγκριση δύο διαγραμμάτων περίθλασης από το ίδιο δείγμα ανθρώπινης ινσουλίνης συγκρυσταλλωμένης με φαινόλη σε ph 5.7. Με μωβ απεικονίζονται τα δεδομένα από το ID11, ενώ με ροζ, τα δεδομένα από το ID31. Στα ID11 δεδομένα παρατηρείται αύξηση του εύρους των κορυφών περίθλασης και ελάττωση της γωνιακής ευκρίνειας σε σύγκριση με τα ID31 δεδομένα. Η ανάλυση των δεδομένων από το ID11 επαλήθευσε την αναπαραξιμότητα των αποτελεσμάτων που λάβαμε στο ID31 καθώς και την ομοιογένεια των δειγμάτων. Συλλογή δεδομένων στο MS - X04SA Τα πολυκρυσταλλικά δείγματα τοποθετήθηκαν σε τριχοειδή σωληνάρια από borosilicate, όπως στις προηγούμενες μετρήσεις, με τη διαφορά ότι η διάμετρος τους ήταν 0.5 mm. Σε περιπτώσεις οργάνων που δεν έχουν κρυστάλλους ανάλυσης όπως το συγκεκριμένο, η μικρότερη διάμετρος των τριχοειδών έχει ως αποτέλεσμα την μικρότερη παρεμβολή του μητρικού υγρού της κρυστάλλωσης στην περίθλαση και ως συνέπεια, τη μείωση του 74
75 πειραματικού θορύβου. Ιδιαίτερα σημαντική για τη σωστή διεξαγωγή των μετρήσεων σε αυτό το όργανο, είναι η ευθυγράμμιση του δείγματος με τη δέσμη της ακτινοβολία και η μείωση της ταλάντωσης του capillary γύρω από τον άξονά του. Εικόνα 46: Σύγκριση δύο διαγραμμάτων περίθλασης, προερχόμενα από το ID31 (γαλάζιο) και το MSX04SA (πορτοκαλί). Τα πολυκρυσταλλικά δείγματα ανθρώπινης ινσουλίνης είναι συγκρυσταλλωμένα με mcresol σε ph 6.31 και 6.37 αντίστοιχα και ανήκουν στο ίδιο space group (P21). Στο ένθετο, απεικονίζεται μια περιοχή που αντιστοιχεί σε μεγαλύτερες γωνίες Επεξεργασία δεδομένων- Προγράμματα Indexing- Πρόγραμμα DASH Το πρώτο βήμα για την επεξεργασία των δεδομένων περίθλασης είναι η εύρεση της συμμετρίας και των πλεγματικών σταθερών (πλευρών a, b, c και γωνιών α, β, γ) της θεμελιώδους κυψελίδας του κρυστάλλου μέσω μιας διαδικασίας που ονομάζεται indexing. Τυπικά, για να γίνει το indexing χρησιμοποιείται το πρόγραμμα DASH (David et al., 1998), το οποίο εκμεταλλεύεται τις παρατηρούμενες θέσεις τουλάχιστον 20 κορυφών περίθλασης (στον άξονα 2ϑ) και μέσω των παρακάτω εξισώσεων, είναι ικανό να δώσει την απαιτούμενη πληροφορία. 2d sinθ=nλ + 75
76 Με το DASH και μέσω της μεθόδου Pawley είναι δυνατό να προσωμειωθεί το προφίλ των δεδομένων περίθλασης από πολυκρυσταλλικά υλικά, χωρίς να προαπαιτείται η ύπαρξη ενός αρχικού δομικού μοντέλου. Αυτό γίνεται μέσω χρήσης (α) της διαφοράς μεταξύ πειραματικών δεδομένων και θεωρητικών τιμών, (β) ενός συνόλου παραμέτρων που περιγράφουν το σχήμα κάθε κορυφής, (γ) τη μετατόπιση του άξονα 2ϑ σε σχέση με ένα σημείο μηδέν, (δ) τις πλεγματικές σταθερές, καθώς και (ε) την ένταση κάθε ανάκλασης. Η επιτυχία της θεωρητικής προσομοίωσης με τα πειραματικά δεδομένα εκφράζεται μέσω ειδικών στατιστικών δεικτών, όπως του Rwp και του χ 2, οι οποίοι προκύπτουν από τη μέθοδο ελαχίστων τετραγώνων. Μέθοδος Pawley- Πρόγραμμα PRODD Για την απόκτηση των αξιόπιστων τιμών των πλεγματικών σταθερών και για τον χαρακτηρισμό του σχήματος των κορυφών περίθλασης, χρησιμοποιήθηκε η μέθοδος Pawley, μέσω του προγράμματος βελτιστοποίησης προφίλ περίθλασης, PRODD (Wright, 2004). Η μέθοδος Pawley, σαν μέθοδος βελτιστοποίησης ολόκληρων προφίλ περίθλασης (full profile refinement), χρησιμοποιείται ευρέως για την εξαγωγή των εντάσεων από δεδομένα περίθλασης πολυκρυσταλλικών υλικών. Εκτός από το προφίλ περίθλασης και τις πλεγματικές σταθερές, οι εντάσεις βελτιστοποιούνται μεμονομένα μέσω μιας διαδικασίας ελαχίστων τετραγώνων. Με το PRODD είναι δυνατή η εξαγωγή εντάσεων από πολλά προφίλ δεδομένων περίθλασης ταυτόχρονα. Τα προφίλ αυτά μπορούν να έχουν ελαφρώς διαφορετικές πλεγματικές σταθερές, όπως στην περίπτωση διαφορετικού βαθμού καταστροφής του δείγματος από την ακτινοβολία. Το PRODD είναι ένα διαδραστικό εργαλείο γραμμής εντολών που χρησιμοποιεί τη γλώσσα προγραμματισμού PYTHON, καθώς και μια σειρά αρχείων που πρέπει να προετοιμαστούν πριν τη χρήση του. Τα πιο σημαντικά είναι τα παρακάτω: Ένα αρχείο τύπου.dat, που περιέχει τα δεδομένα της περίθλασης σε τρεις στήλες (γωνία 2θ, ένταση και σφάλμα της έντασης) Ένα αρχείο τύπου.ccl που περιέχει τις οδηγίες για την εκτέλεση του προγράμματος. 76
77 4. Αποτελέσματα 4.1. Ανθρώπινη ινσουλίνη κρυσταλλωμένη με φαινόλη Ανάλυση των δεδομένων περίθλασης που αποκτήθηκαν από τα πολυκρυσταλλικά δείγματα ανθρώπινης ινσουλίνης με τον προσδέτη φαινόλη με αυξανόμενο ph, έδειξαν την εμφάνιση τεσσάρων διαφορετικών τύπων κρυσταλλικών συμμετριών P21(α), C2221, C2 και P21(β), η πρώτη από τις οποίες δεν είχε αναφερθεί στο παρελθόν. Με P21(α) αναγράφεται η νέα μονοκλινής φάση, ενώ με P21(β) η μονοκλινής φάση που είχε αναφερθεί σε προηγούμενες μελέτες. Στον πίνακα 10 αναγράφονται με λεπτομέρεια οι βελτιστοποιημένες πλεγματικές σταθερές κάθε τύπου πολυμόρφου που εμφανίστηκε στην κρυστάλλωση με τη φαινόλη. ph Space Group a (Å) b (Å) c (Å) β ( ) Volume (Å 3 ) Resolution Range 5.7 P21(α) (6) (2) (4) (6) 1,869,070(200) C (1) (6) (5) 90 3,059,560(117) C (5) (2) (4) (5) 357,121(9) P21(β) (4) (4) (4) (7) 169,437(2) Πίνακας 10: Βελτιστοποιημένες πλεγματικές σταθερές από κρυστάλλους ανθρώπινης ινσουλίνης με φαινόλη στα space group, P21(α), C2221, C2 και P21(β), όπως εξάχθηκαν από προσομοιώσεις Pawley στα πειραματικά δεδομένα. Το νέο πολύμορφο P21(α) Όταν ανθρώπινη ινσουλίνη κρυσταλλώνεται με τον οργανικό προσδέτη φαινόλη στο εύρος ph από , παρατηρήθηκε η εμφάνιση μιας νέας φάσης μονοκλινούς συμμετρίας (P21(α)). Λόγω των μεγάλων διαστάσεων των αξόνων a και b, το indexing υπέφερε από το πρόβλημα υπερισχύουσας ζώνης (dominant zone problem). 77
78 Εικόνα 47: Αριστερά: Pawley fit την περιοχής μκρών γωνιών του πολυμόρφου P21(α) της ανθρώπινης ινσουλίνης. Λόγω του πολύ μεγάλου b-άξονα και της επίδρασης της dominant zone, πολλές ανακλάσεις δεν είναι δυνατόν να παρατηρηθούν, ως αποτέλεσμα αλληλεπικαλύψεων των κορυφών. Δεξιά: Pawley fit των κορυφών που ανήκουν σε μικρές γωνίες, στις οποίες μόνο οι ανακλάσεις της dominant zone (hk0)έχουν ληφθεί υπόψη, ενώ εμφανείς είναι και οι επιπλέον κορυφές που προκύπτουν λόγω του μικρού c-άξονα. Οι κάθετες μπάρες αντιστοιχούν στις θεωρητικές hk0 ανακλάσεις Bragg, και οι μαύρη, κόκκινη και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα. To indexing μιας τέτοιας θεμελιώδους κυψελίδας αποτελεί μια ιδιαίτερη πρόκληση, καθώς οι περισσότερες ανακλάσεις των μικρών γωνιών 2ϑ ανήκουν στη dominant zone στο αντίστροφο πλέγμα και πολλές από αυτές δεν είναι παρατηρήσιμες λόγω αλληλεπικάλυψης. Παρ όλα αυτά, συνδυαστική χρήση των δεδομένων που προήλθαν από τα ID31 και ID11 οδήγησε στην ταυτοποίηση της μονοκλινούς κυψελίδας P21(α) με πλεγματικές σταθερές a= (6) Å, b=337.63(2) Å, c=49.270(4) Å και β= (6). Η παρουσία των ανακλάσεων (020), (040), (060) και (080) και οι απουσίες των (030), (050) και (070) στα δεδομένα του ID11 επιβεβαιώνουν την ύπαρξη ενός screw axis (εικόνα 48), όπου παρατηρούνται ανακλάσεις από μεμονομένους μικροκρυστάλλους. 78
79 Εικόνα 48: Άνω μέρος: εικόνα 2D, στην οποία διακρίνονται οι ανακλάσεις από μονοκρυστάλλους στο πολυκρυσταλλικό P21(α) δείγμα. Κάτω μέρος: Η περιοχή αντιστοιχεί σε μεγέθυνση της σημειωμένης περιοχής της εικόνας του άνω μέρους. Οι ανακλάσεις με (0k0), k=2n τριών διαφορετικών κρυστάλλων είναι κυκλωμένες με μπλέ. Η απουσία των ανακλάσεων (030), (050) και (070) υποδηλώνει ότι το space group είναι το P21(α). Τα δεδομένα λήφθηκαν στο ID11 με μήκος κύματος λ= (3) Å. Το Pawley fit στα δεδομένα για αυτή την περίπτωση ήταν ικανοποιητικό με παράγοντες Rwp= και χ2=2.83 για το δείγμα που κρυσταλλώθηκε με φαινόλη σε ph 5.7. Τα δεδομένα που λήφθηκαν από τους P21(α) κρυστάλλους εκτείνονταν σε ευκρίνεια d-spacing ίση με ~7.5 Å. 4 5x10 4 4x10 4 Intensity (arbitrary units) 4x10 4 3x10 4 3x10 4 2x10 4 1x10 4 2x x x (degrees) Εικόνα 49: Pawley fit της νέας P21(α) φάσης από το δείγμα της ανθρώπινης ινσουλίνης με φαινόλη σε ph 5.7. Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (16) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. 79
80 Intensity (arbitrary units) Το πολύμορφο C2221 Ανθρώπινη ινσουλίνη κρυσταλλωμένη παρουσία φαινόλης σε ελαφρώς υψηλότερες τιμές ph ( ) σχημάτισε κρυστάλλους ορθορομβικής συμμετρίας και συγκεκριμένα του space group C2221 (οι πλήρεις πλεγματικές σταθερές αναγράφονται στον πίνακα 10), το οποίο περιέχει τρία πρωτεϊνικά εξαμερή ανά ασύμμετρη μονάδα (asymmetric unit, ASU). Τα δεδομένα από αυτούς τους κρυστάλλους εκτείνονταν σε ευκρίνεια d-spacing ~7.5 Å (εικόνα 50). Παρατηρήθηκε ότι αύξηση του ph προκαλεί μικρές μεταβολές στις διαστάσεις της θεμελιώδους κυψελίδας, χωρίς όμως να προκαλεί αλλαγή στην κρυσταλλική φάση. Πιο συγκεκριμένα, η αύξηση του ph προκάλεσε μια μικρή αύξηση του όγκου κατά, ΔV/Vi=0.19%. Οι πλεγματικές σταθερές αυτής της φάσης βρίσκονται σε συμφωνία με τα δομικά μοντέλα που είχαν αναφερθεί νωρίτερα, με κωδικούς 2OM0 και 2ΟΜ1 (Norrman & Schluckebier, 2007), στην Protein Data Bank (PDB) Εικόνα 50: Pawley fit της C2221 φάσης από το δείγμα της ανθρώπινης ινσουλίνης με φαινόλη σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (16) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group (degrees) Το πολύμορφο C2 Δύο δείγματα ινσουλίνης κρυσταλλωμένης με φαινόλη στα ph 6.7 και 6.75 έδωσαν κρυστάλλους που ανήκουν στο μονοκλινές space group, C2 (βλ. Πίνακα 10), το οποίο περιέχει ένα πρωτεϊνικό εξαμερές ανά ασύμμετρη μονάδα. Τα δεδομένα για αυτή τη φάση είχαν ευκρίνεια ~5.3 Å και τα αποτελέσματα έδειξαν ότι η φάση C2 έχει πολύ μικρότερο όγκο θεμελιώδους κυψελίδας σε 80
81 Intensity (arbitrary units) σχέση με τους κρυστάλλους C2221, ως αποτέλεσμα της μεγάλης αλλαγής των πλεγματικών σταθερών που παρατηρείται (ο όγκος της κυψελίδας μεταβάλεται κατά περίπου ΔV(C2221 C2)/VC2221 = % ) (degrees) Εικόνα 51: Pawley fit της C2 φάσης από το δείγμα της ανθρώπινης ινσουλίνης με φαινόλη σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (16) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. Η μεταβολή των κανονικοποιημένων πλεγματικών σταθερών με την αύξηση του ph απεικονίζεται στο διάγραμμα της εικόνας 52. Οι σταθερές της θεμελιώδους κυψελίδας αυτού του μοντέλου είναι όμοιες με αυτές των μοντέλων 2OLY και 2OLZ (Norrman & Schluckebier, 2007), που βρίσκονται καταθετημένα στην PDB. Εικόνα 52: Η εξέλιξη των πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με φαινόλη σε αυξανόμενο ph, για τα space group (a)p21(α), (b) C2221, (c) C2 και (d) P21(β). Τα μαύρα σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα κόκκινα στον b-άξονα και τα πράσινα στον c-άξονα. Οι τιμές a0, b0 και c0 συμβολίζουν τις βελτιστοποιημένες τιμές των πλεγματικών σταθερών στο ph που συναντήθηκαν πρώτη φορά. Οι γραμμές που συνδέουν τα σύμβολα βοηθούν στη καθοδήγηση του ματιού. 81
82 Intensity (arbitrary units) Το πολύμορφο P21(β) Δείγματα ανθρώπινης ινσουλίνης κρυσταλλωμένα με φαινόλη σε υψηλότερα ph ( ), σχημάτισαν κρύσταλλoυς μονοκλινούς συμμετρίας, και ειδικότερα του space group P21(β) (βλ. Πίνακα 10), το οποίο περιέχει ένα πρωτεϊνικό εξαμερές ανά ασύμμετρη μονάδα. Τα δεδομένα που λήφθηκαν από το ID31 εκτείνονταν σε ευκρίνεια d-spacing ~4.4 Å. 2.0x x x x x x x x Aυτή η κρυσταλλική φάση διαθέτει τον μικρότερο όγκο θεμελιώδους κυψελίδας από όλα τα προηγούμενα πολύμορφα ινσουλίνης/φαινόλης, με τον όγκο να μειώνεται κατά ΔV(C2 P21(β))/VC2 = % κρυσταλλικής φάσης από C2 σε P21(β). Σύμφωνα με το συντελεστή Matthews η C2 φάση περιέχει τέσσερα εξαμερή ινσουλίνης μέσα στη θεμελιώδη κυψελίδα και 52% περιεκτικότητα σε διαλύτη (Matthews coefficient= 2.56 Å 3 /Da), ενώ η P21(β) φάση περιέχει δύο εξαμερή ανά κυψελίδα και 49.4% περιεκτικότητα σε διαλύτη (Matthews coefficient= 2.43 Å 3 /Da) (degrees) Εικόνα 53: Pawley fit της P21(β) φάσης από το δείγμα της ανθρώπινης ινσουλίνης με φαινόλη σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (16) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. στη μεταβολή της Ο συντελεστής Matthews (Matthews coefficient, V Μ) ορίζεται ως ο κρυσταλλικός όγκος ανά μονάδα πρωτεϊνικού μοριακού βάρους. Έχει αποδειχθεί ότι έχει ευθέως ανάλογη σχέση με τον όγκο του διαλύτη στον κρύσταλλο. 82
83 Επιπλέον, παρατηρείται μια μικρή μείωση στον όγκο της κυψελίδας μέσα στο συγκεκριμένο εύρος ph (κατά ΔV/Vi=-0.22%), η οποία αντικατοπτρίζει μια ελαφρώς ανισοτροπική μεταβολή των πλεγματικών σταθερών καθώς αυξάνεται το ph. Το παραπάνω αποτέλεσμα μπορεί να υποδεικνύει ανακατατάξεις του διαλύτη, μικρές αλλαγές στη διαμόρφωση της πρωτεϊνης ή αλλαγές στις επαφές πακεταρίσματος. Οι πλεγματικές σταθερές αυτού του πολυμόρφου μοιάζουν σημαντικά με αυτές των μοντέλων 1EVR και 1EV6 (Smith et al., 2000). Εικόνα 54: Προσομοιώσεις των περιεχομένων της θεμελιώδους κυψελίδας για τα space group C2221, C2 και P21(β), οι οποίες αντιστοιχούν στα μοντέλα 2OM0, 2OLZ και 1EV6 (PDB). Αριστερά: Space group C2221. Περιέχει 3 εξαμερή ινσουλίνης/ ASU και συνολικά 24 εξαμερή στη θεμελιώδη κυψελίδα. Κέντρο: Space group C2. Περιέχει 1 εξαμερές ινσουλίνης/ ASU και συνολικά 4 εξαμερή στη θεμελιώδη κυψελίδα. Δεξιά: Space group P21(β). Περιέχει 1 εξαμερές ινσουλίνης/ ASU και συνολικά 2 εξαμερή στη θεμελιώδη κυψελίδα. Οι λευκές γραμμές ανταποκρίνονται στους άξονες της θεμελιώδους κυψελίδας. Οι προσομοιώσεις έγιναν μέσω του λογισμικού Chimera (Pettersen, EF. et al, 2004) Ανθρώπινη ινσουλίνη κρυσταλλωμένη με m-cresol Κρυστάλλωση της ινσουλίνης με τον οργανικό προσδέτη m-cresol σε αυξανόμενη κλίση ph, είχε ως αποτέλεσμα την εμφάνιση τριών διαφορετικών πολυμόρφων P21(γ), P21(β) και το τριγωνικό R3. Η P21(γ) κρυσταλλική φάση είναι ένα νέο πολύμορφο μονοκλινούς συμμετρίας, με τις πλεγματικές του σταθερές να διαφέρουν από τις ήδη υπάρχουσες. Στον πίνακα 11 αναγράφονται με λεπτομέρεια οι βελτιστοποιημένες πλεγματικές σταθερές κάθε τύπου πολυμόρφου που εμφανίστηκε στην κρυστάλλωση με τη m-cresol. 83
84 ph Space a (Å) b (Å) c (Å) β ( ) Volume (Å3) Group Resolution Range 4.68 P21(γ) (3) (2) (2) (3) 280,564(18) P21(β) (3) (2) (3) (5) 171,850(15) R (5) (5) (2) (21) Πίνακας 11: Βελτιστοποιημένες πλεγματικές σταθερές από κρυστάλλους ανθρώπινης ινσουλίνης με φαινόλη στα space group, P21(γ), P21(β) και R3 όπως εξάχθηκαν από προσομοιώσεις Pawley στα πειραματικά δεδομένα. Όλα τα δείγματα μετρήθηκαν με λ= (2) Å. Το νέο πολύμορφο P21(γ) Ανθρώπινη ινσουλίνη κρυσταλλωμένη με m-cresol στο εύρος ph σχηματίζει κρυστάλλους μονκλινούς συμμετρίας (space group: P21(γ), οι πλεγματικές σταθερές του οποίου αναγράφονται στον πίνακα 11). Το Pawley fit για τα δεδομένα αυτής της κρυσταλλικής φάσης ήταν ιδιαίτερα καλό με Rwp=0.261 και χ2= Το προφίλ εκτείνεται σε ευκρίνεια d-spacing ~4.1 Å (εικόνα 55). 1.5x x x10 3 Intensity (arbitrary units) 4 1.5x x x Εικόνα 55: Pawley fit της P21(γ) φάσης από το δείγμα ανθρώπινης ινσουλίνης με φαινόλη σε ph της (degrees) Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. 84
85 Intensity (arbitrary units) Με αύξηση του ph παρατηρείται μια μικρή αύξηση του όγκου κατά ΔV/Vi=2.19%, ενώ οι μεταβολή των πλεγματικών σταθερών αναπαρίσταται στο διάγραμμα της εικόνας 57. Το πολύμορφο P21(β) Όπως και με την κρυστάλλωση της ινσουλίνης με φαινόλη, έτσι και σε αυτή την περίπτωση προσδέτη, εμφανίζεται ένα δείγμα σε ph 6.7, το οποίο έχει υιοθετήσει την μονοκλινή P21(β) συμμετρία (πίνακας 11). Τα δεδομένα είχαν ευκρίνεια ~3.9 Å και το Pawley fit χαρακτηριζόταν από Rwp=0.256 και χ 2 = x10 4 2x10 4 1x x Εικόνα 56: Pawley fit της P21(β) φάσης από το δείγμα της ανθρώπινης ινσουλίνης με φαινόλη σε ph 6.7. Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group (degrees) Το πολύμορφο R3 Τρία δείγματα ινσουλίνης με m-cresol σε ph από κρυσταλλώνονται σε τριγωνική συμμετρία του space group R3 (πίνακας 11). Η διαμόρφωση του μορίου, όπως υποδυκνύεται από τις σταθερές της θεμελιώδους κυψελίδας είναι η R6, κατά την οποία τα αμινοξέα Β1-Β8 του αμινοτελικού άκρου της Β αλυσίδας της ινσουλίνης σχηματίζουν έλικα. Αυτό έρχεται σε συμφωνία με προηγούμενες μελέτες που υποστηρίζουν ότι υψηλές συγκεντρώσεις φαινολικών παραγόγων (όπως είναι και η m-cresol) αναγκάζουν το μόριο να λάβει τη συγκεκριμένη διαμόρφωση. Τα δεδομένα αυτά εκτείνονται σε ευκρίνεια d-spacing ~3.2 Å, ενώ τα Pawley fits ήταν ικανοποιητικά με Rwp=0.323 και χ 2 =1.58 (εικόνα 57). 85
86 2.50x Intensity (arbitrary units) 1.00x x x x x Εικόνα 57: Pawley fit της R3 φάσης από το δείγμα της ανθρώπινης ινσουλίνης με φαινόλη σε ph 7.7. Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group (degrees) Η μεταβολή των πλεγματικών σταθερών για τα πολύμορφα P21(γ) και R3 απεικονίζονται στην εικόνα 58. Normalized lattice parameters c/c b/b a/a ph ph Εικόνα 58: Η εξέλιξη των πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με Mcresol σε αυξανόμενο ph, για τα space group P21(γ) (αριστερά) και R3 (δεξιά). Τα πορτοκαλί σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα σκούρα μπλέ στον b-άξονα και τα γαλάζια στον c-άξονα. Οι τιμές a0, b0 και c0 συμβολίζουν τις βελτιστοποιημένες τιμές των πλεγματικών σταθερών στο ph που συναντήθηκαν πρώτη φορά. Οι γραμμές που συνδέουν τα σύμβολα βοηθούν στη καθοδήγηση του ματιού Ανθρώπινη ινσουλίνη κρυσταλλωμένη με 4-nitrophenol Κρυστάλλωση της ινσουλίνης με τον οργανικό προσδέτη 4-nitrophenol σε αυξανόμενη κλίση ph, είχε ως αποτέλεσμα την εμφάνιση δύο διαφορετικών πολυμόρφων: του P21(γ) και του τριγωνικού R3. Στον πίνακα 12 αναγράφονται με λεπτομέρεια οι βελτιστοποιημένες πλεγματικές σταθερές κάθε τύπου 86
87 πολυμόρφου που εμφανίστηκε στην κρυστάλλωση με τη 4-nitrophenol. Τα δείγματα που ανήκουν στη κρυσταλλική φάση R3 μετρήθηκαν αρχικά στο ESRF με μήκος κύματος λ= (3) Å, ενώ τα δείγματα που ανήκουν στην κρυσταλλική φάση P21(γ) μετρήθηκαν συμπληρωματικά στο SLS με μήκος κύματος λ= (2) Å. ph Space Group a (Å) b (Å) c (Å) β ( ) Volume (Å 3 ) Resolution Range 6.19 P21(γ) (3) (2) (2) (3) 286,246(16) R (1) (1) (5) ,151(3) Πίνακας 12: Βελτιστοποιημένες πλεγματικές σταθερές από κρυστάλλους ανθρώπινης ινσουλίνης με 4- nitrophenol στα space group, P21(γ) και R3 όπως εξάχθηκαν από προσομοιώσεις Pawley στα πειραματικά δεδομένα. Το νέο πολύμορφο P21(γ) Ανθρώπινη ινσουλίνη κρυσταλλωμένη με 4-nitrophenol στο εύρος ph σχηματίζει κρυστάλλους μονoκλινούς συμμετρίας (space group: P21(γ), οι πλεγματικές σταθερές του οποίου αναγράφονται στον πίνακα 12). Το Pawley fit για τα δεδομένα αυτής της κρυσταλλικής φάσης ήταν ιδιαίτερα καλό με Rwp=0.263 και χ 2 =1.48. Το προφίλ εκτείνεται σε ευκρίνεια d-spacing ~3.12 Å, ενώ η μεταβολή των κανονικοποιημένων πλεγματικών σταθερών με την αύξηση του ph απεικονίζεται διαγραμματικά στην εικόνα
88 x10 Normalized lattice parameters Intensity (arbitrary units) 2.0x x x x a/a c/c b/b x ph 2 (degrees) Εικόνα 59: Αριστερά: Pawley fit της P21(γ) φάσης από το δείγμα της ανθρώπινης ινσουλίνης με 4-nitrophenol σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. Δεξιά: Η εξέλιξη των πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με 4-nitrophenol σε αυξανόμενο ph, για το space group P21(γ). Τα πορτοκαλί σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, τα σκούρα μπλέ στον b-άξονα και τα γαλάζια στον c-άξονα. Οι τιμές a0, b0 και c0 συμβολίζουν τις βελτιστοποιημένες τιμές των πλεγματικών σταθερών στο ph που συναντήθηκαν πρώτη φορά. Οι γραμμές που συνδέουν τα σύμβολα βοηθούν στη καθοδήγηση του ματιού. Το πολύμορφο R3 Τα δείγματα ινσουλίνης που κρυσταλλώθηκαν με 4-nitrophenol σε κλίση ph από σχηματίζουν κρυστάλλους τριγωνικής συμμετρίας του space group R3 (πίνακας 12). Η διαμόρφωση του μορίου, όπως υποδυκνύεται από τις σταθερές της θεμελιώδους κυψελίδας είναι η Τ3R3f, η οποία χαρακτηρίζεται από επιμηκυσμένη διαμόρφωση των τριών μονομερών του εξαμερούς της ινσουλίνης (αμινοξέα Β1-Β8), ενώ τα άλλα τρία μονομερή του παρουσιάζουν ελικοειδή διαμόρφωση στα αμινοξέα Β4-Β8 και επιμηκυσμένη στα Β1-Β3. Τα δεδομένα αυτής της κρυσταλλικής φάσης εκτείνονται σε ευκρίνεια d-spacing ~3.66 Å, ενώ τα Pawley fits ήταν ικανοποιητικά με χ2=1.05 (εικόνα 60). 88
89 Normalized lattice parameters Intensity (arbitrary units) 1.5x x x x a/a c/c ph 2 (degrees) Εικόνα 60: Αριστερά: Pawley fit της R3 φάσης από το δείγμα της ανθρώπινης ινσουλίνης με 4-nitrophenol σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (3) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. Δεξιά: Η εξέλιξη των πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με 4-nitrophenol σε αυξανόμενο ph, για το space group R3. Τα πορτοκαλί σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας και τα γαλάζια στον c-άξονα. Οι τιμές a0 και c0 συμβολίζουν τις βελτιστοποιημένες τιμές των πλεγματικών σταθερών στο ph που συναντήθηκαν πρώτη φορά. Οι γραμμές που συνδέουν τα σύμβολα βοηθούν στη καθοδήγηση του ματιού Ανθρώπινη ινσουλίνη κρυσταλλωμένη με 4-ethyl- resorcinol Κρυστάλλωση της ινσουλίνης με τον οργανικό προσδέτη 4-ethylresorcinol σε αυξανόμενη κλίση ph, είχε ως αποτέλεσμα την εμφάνιση τριών διαφορετικών πολυμόρφων μονοκλινούς συμμετρίας: P21(γ), C2 και P21(β). Όλα τα δείγματα μετρήθηκαν στο SLS με μήκος κύματος λ= (2) Å. Στον πίνακα 13 αναγράφονται με λεπτομέρεια οι βελτιστοποιημένες πλεγματικές σταθερές κάθε τύπου πολυμόρφου που εμφανίστηκε στην κρυστάλλωση με την 4-ethyl-resorcinol. ph Space a (Å) b (Å) c (Å) β ( ) Volume (Å3) Group Resolution Range 5.45 P21(γ) (2) (1) (1) (2) 281,859(10) C (2) (7) 63.47(2) (3) 358,201(151) P21(β) (3) (2) (3) (4) 173,254(14) Πίνακας 13: Βελτιστοποιημένες πλεγματικές σταθερές από κρυστάλλους ανθρώπινης ινσουλίνης με 4ethyl-resorcinol στα space group P21(γ), C2 και P21(β) όπως εξάχθηκαν από προσομοιώσεις Pawley στα πειραματικά δεδομένα. 89
90 Intensity (arbitrary units) Normalized lattice parameters Το νέο πολύμορφο P21(γ) Ανθρώπινη ινσουλίνη κρυσταλλωμένη με 4-ethyl-resorcinol στο εύρος ph σχηματίζει κρυστάλλους μονoκλινούς συμμετρίας που ανήκουν στο space group P21(γ) (πλεγματικές σταθερές στον πίνακα 13). Το Pawley fit για τα δεδομένα αυτά ήταν καλό με Rwp=0.377 και χ 2 =0.64. Το προφίλ εκτείνεται σε ευκρίνεια d-spacing ~3.12 Å, ενώ η μεταβολή των κανονικοποιημένων πλεγματικών σταθερών με την αύξηση του ph απεικονίζεται διαγραμματικά στην εικόνα x x b/b x x x x a/a x (degrees) Εικόνα 61: Αριστερά: Pawley fit της P21(γ) φάσης από το δείγμα της ανθρώπινης ινσουλίνης με 4-ethyl-resorcinol σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. Δεξιά: Η εξέλιξη των πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με 4-ethyl-resorcinol σε αυξανόμενο ph, για το space group P21(γ). Τα πορτοκαλί σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, σκούρα μπλέ στον b-άξονα και τα γαλάζια στον c-άξονα. Οι τιμές a0, b0 και c0 συμβολίζουν τις βελτιστοποιημένες τιμές των πλεγματικών σταθερών στο ph που συναντήθηκαν πρώτη φορά. Οι γραμμές που συνδέουν τα σύμβολα βοηθούν στη καθοδήγηση του ματιού. ph c/c 0 90
91 Intensity (arbitrary units) Normalized lattice parameters Tο πολύμορφο C2 Δύο δείγματα ανθρώπινης ινσουλίνης κρυσταλλωμένα με 4-ethylresorcinol στα ph σχημάτισαν κρυστάλλους που ανήκουν στο space group C2 (πλεγματικές σταθερές στον πίνακα 13). Αυτή η συμμετρία έχει εμφανιστεί και στην περίπτωση κρυστάλλωσης με φαινόλη. Το Pawley fit για τα δεδομένα αυτά ήταν καλό με Rwp= και χ 2 = Το προφίλ εκτείνεται σε ευκρίνεια d-spacing ~3.95 Å, ενώ η μεταβολή των κανονικοποιημένων πλεγματικών σταθερών με την αύξηση του ph απεικονίζεται διαγραμματικά στην εικόνα x x x b/b 0 1.0x x x a/a x10 3 c/c 0-1.0x (degrees) ph Εικόνα 62: Αριστερά: Pawley fit της C2 φάσης από το δείγμα της ανθρώπινης ινσουλίνης με 4-ethyl-resorcinol σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. Δεξιά: Η εξέλιξη των πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με 4-ethyl-resorcinol σε αυξανόμενο ph, για το space group C2. Τα πορτοκαλί σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, σκούρα μπλέ στον b-άξονα και τα γαλάζια στον c-άξονα. Οι τιμές a0, b0 και c0 συμβολίζουν τις βελτιστοποιημένες τιμές των πλεγματικών σταθερών στο ph που συναντήθηκαν πρώτη φορά. Οι γραμμές που συνδέουν τα σύμβολα βοηθούν στη καθοδήγηση του ματιού. Το πολύμορφο P21(β) Τα δείγματα που κρυσταλλώθηκαν σε κλίση ph από με τον οργανικό προσδέτη 4-ethyl-resorcinol, έδωσαν κρυστάλλους μονοκλινούς συμμετρίας, του ήδη γνωστού space group P21(β) (πλεγματικές σταθερές στον πίνακα 13). Το fit των δεδομένων χαρακτηρίζεται από Rwp=0.286 και χ 2 = 0.41, ενώ το δεδομένα είχαν ευκρίνεια ~4.1 Å. Παρατηρείται μια ανισοτροπική μεταβολή των πλεγματικων σταθερών κατά την οποία το μήκος του a-άξονα 91
92 Intensity (arbitrary units) Normalized latttice parameters σταδιακά μειώνεται, ενώ των αξόνων b και c αυξάνεται, όπως φαίνεται και στο διάγραμμα της εικόνας x10 4 b/b x x x x c/c x a/a (degrees) ph Εικόνα 63: Αριστερά: Pawley fit της P21(β) φάσης από το δείγμα της ανθρώπινης ινσουλίνης με 4-ethyl-resorcinol σε ph Όλα τα δείγματα μετρήθηκαν χρησιμοποιώντας ένα μήκος κύματος λ= (2) Å. Οι μαύρες, κόκκινες και μπλέ γραμμές αντιπροσωπεύουν τα πειραματικά δεδομένα, το θεωρητικό πρότυπο και τη διαφορά τους αντίστοιχα, ενώ οι κάθετες μαύρες μπάρες αντιστοιχούν στις ανακλάσεις Bragg που είναι συμβατές με το συγκεκριμένο space group. Δεξιά: Η εξέλιξη των πλεγματικών σταθερών της ανθρώπινης ινσουλίνης κρυσταλλωμένης με 4-ethyl-resorcinol σε αυξανόμενο ph, για το space group P21(β). Τα πορτοκαλί σύμβολα αντιστοιχούν στον a- άξονα της κυψελίδας, σκούρα μπλέ στον b-άξονα και τα γαλάζια στον c-άξονα. Οι τιμές a0, b0 και c0 συμβολίζουν τις βελτιστοποιημένες τιμές των πλεγματικών σταθερών στο ph που συναντήθηκαν πρώτη φορά. Οι γραμμές που συνδέουν τα σύμβολα βοηθούν στη καθοδήγηση του ματιού Η περίπτωση της T6 Bovine ινσουλίνης Συνεχίζοντας πειράματα που διεξήχθησαν στο ESRF τα προηγούμενα χρόνια, αναλύθηκαν δεδομένα μιας σειράς πολυκρυσταλλικών δειγμάτων ινσουλίνης βοειδών της διαμόρφωσης Τ6 (space group: R3). Τα 14 αυτά δείγματα είχαν κρυσταλλωθεί σε κλίση ph από με μεταβολή ανά 0.2 μονάδες. Η μέθοδος περίθλασης ακτίνων-χ από πολυκρυσταλλικά δείγματα χρησιμοποιήθηκε για την διερεύνηση των ανισοτροπικών επιδράσεων της αύξησης του ph και του χρόνου ακτινοβόλησης του δείγματος κατά τη συλλογή δεδομένων, στις πλεγματικές σταθερές της T6 bovine ινσουλίνης. Η ανισοτροποική αυτή μεταβολή, προκαλεί μια αλλαγή στο πρότυπο των αλληλεπικαλύψεων των κορυφών, επιτρέποντας στις συμβαλλόμενες ανακλάσεις των αλληλεπικαλυπτόμενων κορυφών να διαχωριστούν σταδιακά. Ένα κοινό φαινόμενο για την περίπτωση του χρόνου ακτινοβόλησης του 92
93 δείγματος, είναι η μη-αναστρεφόμμενη διαστολή του πλέγματος, αν και ο μηχανισμός με τον οποίο γίνεται αυτό δεν είναι πλήρως κατανοητός. Ανισοτροπικές επιδράσεις του χρόνου ακτινοβόλησης Σε πολλές περιπτώσεις, οι ανισοτροπικές αυτές μεταβολές του πλέγματος μπορούν να εκμεταλλευτούν αλληλεπικαλυπτόμενων για την κορυφών ενός βελτίωση της ευκρίνειας πολυκρυσταλλικού των προτύπου δεδομένων. Στην περίπτωση της καταστροφής πολυκρυσταλλικών δειγμάτων λόγω της ακτινοβολίας (radiation damage effects), κοινά χαρακτηριστικά είναι οι σημαντικές μεταβολές στις πλεγματικές σταθερές, συνοδευόμενες από μια σταδιακή αύξηση του εύρους των κορυφών περίθλασης καθώς και σημαντική απώλεια της έντασής τους. Για την bovine insulin, συλλέχθησαν πολλαπλά πρότυπα δεδομένων από πολυκρυσταλλικά δείγματα του ίδιου όγκου, έτσι ώστε κάθε προφίλ να αντιστοιχεί σε διαφορετικό χρόνο έκθεσης στην ακτινοβολία. Ανάλυση Pawley επιβεβαίωσε ότι δεν επάγεται κάποια αλλαγή στην κρυσταλλική Volume (Å) φάση μετά από έκθεση 5 λεπτών και ότι όλα τα προφίλ δεδομένων ανήκουν στην T6 διαμόρφωση Στα διαγράμματα της εικόνας Normalized Lattice Dimensions Exposure time (sec) c / c φαίνεται η ανισοτροπική μεταβολή των τριγωνικών πλεγματικών σταθερών αυξανόμενου του χρόνου ακτινοβόλησης (Δa/ai=-0.152%, Δc/ci=0.340%, ΔV/Vi= %) a / a Exposure time (sec) Εικόνα 64: Μεταβολή του όγκου της θεμελιώδους κυψελίδας (άνω) και των κανονικοποιημένων πλεγματικών σταθερών (κάτω), που εξήχθησαν από δεδομένα του ID31 για την T6 bovine insulin κρυσταλλωμένη σε ph 7.6 με αύξηση του χρόνου εκθεσης στην ακτινοβολία. Οι διακεκομμένες γραμμές καθοδηγούν το μάτι. 93 Οι πλήρεις πλεγματικές σταθερές συνοψίζονται στον πίνακα 14.
94 Intensity (arbitrary units) Intensity (arbitrary units) Intensity (arbitrary units) Intensity (arbitrary units) Intensity (arbitrary units) Exposure time (sec) a (Å) c (Å) Volume (Å 3 ) (1) (3) (2) (1) (4) (3) (1) (4) (3) (1) (6) (4) (2) (6) (5) Πίνακας 14: Βελτιστοποιημένες πλεγματικές σταθερές για το δείγμα της bovine insulin κρυσταλλωμένο σε ph 7.6 με αυξανόμενο χρόνο ακτινοβόλησης. Η εικόνα 65 απεικονίζει τμήματα της περιοχής χαμηλών γωνιών περίθλασης του δείγματος bovine insulin με ph 7.6, οπού είναι εμφανείς οι μεταβολές στη θέση των κορυφών καθώς και στην έντασή τους theta (degrees) theta (degrees) theta (degrees) theta (degrees) theta (degrees) Εικόνα 65: Δεδομένα από περίθλαση του πολυκρυσταλλικού δείγματος με ph 7.6, που δείχνουν σταδιακή καταστροφή του δείγματος από την ακτινοβολία. Το σχήμα δείχνει μεγεθύνσεις επιλεγμένων περιοχών 2ϑ για χρόνους ακτινοβόλησης 1 min (μαύρη γραμμή), 2 min (κόκκινη), 3 min (μπλέ) και 4 min (μωβ) αντίστοιχα. Οι πλεγματικές σταθερές που εξήχθησαν από τα δεδομένα μετά από 1 min ακτινοβόληση είναι a = (4) Å, c = (9) Å. Τα δεδομένα συλλέχθησαν σε θερμοκρασία 295Κ (ID31, λ= (9) Å. 94
95 Intensity (arbitrary units) Intensity (arbitrary units) Intensity (arbitrary units) Intensity (arbitrary units) Ανισοτροπικές επιδράσεις της αύξησης του ph Καλής ποιότητας πολυκρυσταλλικά δείγματα bovine insulin παρήχθησαν στο εύρος τιμών ph από , ενώ το δείγμα σε ph 7.8 ήταν άμορφο. Άμεση σύγκριση των 14 συλλεγμένων προφίλ υποδεικνύει μια καθαρά ανισοτροπική μετατόπιση των θέσεων των κορυφών με το ph theta (degrees) theta (degrees) theta (degrees) Εικόνα 66: Μεγεθύνσεις επιλεγμένων περιοχών 2ϑ για τα προφίλ που συλλέκτηκαν σε ph 5.4 (μαύρη γραμμή- a= (3) Å, c = (9) Å, V = (2) Å 3 ), ph 6.6 (κόκκινη γραμμή- a = (6) Å, c = (5) Å, V = (3) Å 3, ph 7.0 (μπλέ γραμμή- a = (6) Å, c = (5) Å, V = (3) Å 3 ) και ph 7.6 (ροζ γραμμή- a= (6) Å, c = (5) Å, V = (3) Å 3 ). Τα δεδομένα συλλέχθησαν σε θερμοκρασία 295Κ (ID31, λ= (9). Αυτό το σχήμα απεικονίζει την ανισοτροπική μεταβολή των πλεγματικών σταθερών με αύξηση του ph, η οποία οδηγεί στον διαχωρισμό των μερικώς επικαλυπτόμενων ανακλάσεων Bragg. H ανισοτροπική μεταβολή των πλεγματικών σταθερών υποστηρίζεται και ποσοτικοποιείται από την ανάλυση Pawley, η οποία δίνει τις ακριβείς τιμές των διαστάσεων της κυψελίδας (πίνακας 15). 95
96 ph a (Å) c (Å) Volume (Å3) (9) (3) (2) (3) (2) (1) (4) (6) (1) (5) (2) (1) (6) (2) (1) (8) (1) (3) (5) (2) (1) (1) (4) (3) (5) (2) (1) (6) (2) (1) (5) (2) (1) (5) (2) (1) (4) (2) (1) (6) (3) (1) Πίνακας 15: Βελτιστοποιημένες πλεγματικές σταθερές για τα T6 δείγματα bovine insulin κρυσταλλωμενα σε διαφορετικές τιμές ph από το 5.0 εώς το 7.6. Η εικόνα 67 δείχνει ότι ο κρυσταλλογραφικός άξονας a μειώνεται κατά Δa/ ai= 0.401% και ο άξονας c κατά Δc/ci= 0.518% αυξανόμενου του ph. Ομοίως, παρατηρείται ελάττωση του όγκου της τριγωνικής κυψελίδας κατά ΔV/Vi=0.286%. c / c0 Normalized Lattice Dimensions Εικόνα 67: Μεταβολή των κανονικοποιημένων πλεγματικών σταθερών από τα δεδομένα του ID31 της Τ6 bovine insulin με αύξηση του ph a / a ph
97 Γενικότερα, μπορούμε να πούμε ότι και στις δύο περιπτώσεις παραγόντων που επηρεάζουν την εξέλιξη των πλεγματικών σταθερών, παρατηρήθηκε μια σημαντική ελάττωση του άξονα a και μια αύξηση του άξονα c, αν και στην περίπτωση μεταβολής του ph το φαινόμενο είναι πιο εμφανές. Οι σχετικά μικρές μεταβολές στον όγκο της θεμελιώδους κυψελίδας και στις δύο πριπτώσεις, υποδεικνύει ότι οι περισσότερες μεταβολές γίνονται στην αναλογία των σταθερών του πλέγματος. 5. Συζήτηση Ο πολυμορφισμός των μοριακών κρυστάλλων είναι ένα σημαντικό και ευρέως μελετημένο ερευνητικό πεδίο (Bernstein, 2002). Για τους μακρομοριακούς κρυστάλλους, η ινσουλίνη αποτελεί ένα καλό μοντέλο λόγω της βιοϊατρικής και φαρμακολογικής της σημασίας, καθώς και λογω της μακράς ιστορίας της όσον αφορά την κρυστάλλωση (Abel, 1926, Krayenbuhl, 1948, Schlichtkrull 1958, Brange 1992). Για την ινσουλίνη άγριου-τύπου, έχει ταυτοποιηθεί τα τελευταία 80 χρόνια ένας μεγάλος αριθμός διαφορετικών κρυσταλλικών πολυμόρφων, τα οποία συχνά συσχετίζονται με διαφορετικές καταστάσεις αυτο-σύνδεσης (self-association) και αλλοστερικές καταστάσεις του μορίου της ινσουλίνης. Τα μικροκρυσταλλικά διαλύματα ινσουλίνης χρησιμοποιούνται ευρέως σε φαρμακευτικά σκευάσματα λόγω της σταθερότητάς τους και του παρατεταμένου προφίλ δράσης τους (Brange et al, 1992). Αυτά τα φαρμακευτικά σκευάσματα περιέχουν ινσουλίνη, ψευδάργυρο και κάποιο φαινολικό προσδέτη. Γνώση των ιδιοτήτων κρυστάλλωσης τέτοιων μιγμάτων μπορεί να βοηθήσει στην βελτιστοποίηση της διαδικασίας παραγωγής, αλλά μπορεί επίσης να οδηγήσει στην ανάπτυξη νέων σκευασμάτων ινσουλίνης που χρησιμοποιούν εναλλακτικούς τρόπους χορήγησης, όπως σκευάσματα παρατεταμένης απελευθέρωσης ή σκευάσματα εισπνεόμενης χορήγησης (Basu et al. 2004), καθώς η επιλογή του σωστού πολύμορφου επηρεάζει ιδιότητες όπως η σταθερότητα, η διαλυτότητα και η βιοδαθεσιμότητα των κρυστάλλων της ινσουλίνης. 97
98 Σε αυτή τη διπλωματική εργασία πραγματοποιήθηκε η συστηματική μελέτη της επίδρασης του ph στην συμπεριφορά της κρυστάλλωσης της ινσουλίνης σε σύμπλοκο με ψευδάργυρο και παρουσία ενός φαινολικού παραγώγου όπως για παράδειγμα η ίδια η φαινόλη, η m-cresol, η 4-nitrophenol και η 4-ethyl-resorcinol. Εκτός από τις ήδη γνωστές κρυσταλλικές μορφές, βρέθηκαν δύο ακόμα πολύμορφα μονοκλινούς συμμετρίας, τα οποία δεν είχαν αναφερθεί σε προηγούμενες μελέτες. Έγιναν ακριβείς μετρήσεις της μεταβολής των πλεγματικών σταθερών με το ph, οι οποίες περιγράφονται από τις ομαλές ανισοτροπικές αλλαγές στις θέσεις των κορυφών περίθλασης. Επιπλέον, η αναπαραξιμότητα αυτών των αποτελεσμάτων και η ακρίβεια των δεδομένων από τα πολυκρυσταλλικά δείγματα, επαληθεύονται μέσω διεξαγωγής πολλαπλών πειραμάτων κρυστάλλωσης και περίθλασης σε θερμοκρασία δωματίου. Δεδομένα υψηλής ευκρίνειας από πολυκρυσταλλικά δείγματα συνοψίζονται στο διάγραμμα φάσης της εικόνας 68. Τα αποτελέσματα δείχνουν ότι η κρυστάλλωση της ανθρώπινης ινσουλίνης παρουσία φαινολικών παραγώγων μπορεί να επηρεαστεί σε μεγάλο βαθμό από τη μεταβολή του ph. Τα διάφορα πολύμορφα χαρακτηρίζονται από μεταβλημένες κρυσταλλογραφικές συμμετρίες ή διαστάσεις της θεμελιώδους κυψελίδας, οι οποίες λαμβανονται ανάλογα με την τιμή του ph σε κάθε περίπτωση. Επίσης σημαντική είναι η επιλογή του οργανικού προσδέτη, η οποία επηρεάζει περαιτέρω την κρυστάλλωση του μορίου. Εικόνα 68: Διάγραμμα φάσεων της ανθρώπινης ινσουλινης. Φαίνονται όλοι οι τύποι των πολυμόρφων που προκύπτουν σε κάθε περίπτωση προσδέτη σε συνάρτηση με το ph. 98
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
πρωτεΐνες πολυμερείς ουσίες δομούν λειτουργούν λευκώματα 1.Απλές πρωτεΐνες 2.Σύνθετες πρωτεΐνες πρωτεΐδια μη πρωτεϊνικό μεταλλοπρωτεΐνες
 ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
Η κυτταρική µετατόπιση των πρωτεϊνών
 9-1 Κεφάλαιο 9 Η κυτταρική µετατόπιση των πρωτεϊνών Εισαγωγή Στο κύτταρο η έκφραση των πρωτεϊνών γίνεται από µόνο ένα τύπο ριβοσώµατος (εκτός των µιτοχονδριακών και των χλωροπλαστικών που µοιάζουν µε αυτά
9-1 Κεφάλαιο 9 Η κυτταρική µετατόπιση των πρωτεϊνών Εισαγωγή Στο κύτταρο η έκφραση των πρωτεϊνών γίνεται από µόνο ένα τύπο ριβοσώµατος (εκτός των µιτοχονδριακών και των χλωροπλαστικών που µοιάζουν µε αυτά
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
τα βιβλία των επιτυχιών
 Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ AΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ)
 ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ AΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» 22/12/2015 Δ.Δ. Λεωνίδας 1
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ AΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» 22/12/2015 Δ.Δ. Λεωνίδας 1
Τα χημικά στοιχεία που είναι επικρατέστερα στους οργανισμούς είναι: i..
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
Βιολογία Γενικής Παιδείας Β Λυκείου
 Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ <=> R
 ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ R ΔΕΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ ΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ (Σταθερότητα, χαμηλή συγγένεια για Ο2Εύκαμπτη, υψηλή συγγένεια για Ο2) Λόγο των
ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ R ΔΕΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ ΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ (Σταθερότητα, χαμηλή συγγένεια για Ο2Εύκαμπτη, υψηλή συγγένεια για Ο2) Λόγο των
ΠΡΩΤΕΪΝΕΣ. Φατούρος Ιωάννης Αναπληρωτής Καθηγητής
 ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
Β. ΚΑΜΙΝΕΛΛΗΣ ΒΙΟΛΟΓΙΑ. Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα).
 ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Νέα Οπτικά Μικροσκόπια
 Νέα Οπτικά Μικροσκόπια Αντίθεση εικόνας (contrast) Αντίθεση πλάτους Αντίθεση φάσης Αντίθεση εικόνας =100 x (Ι υποβ -Ι δειγμα )/ Ι υποβ Μικροσκοπία φθορισμού (Χρησιμοποιεί φθορίζουσες χρωστικές για το
Νέα Οπτικά Μικροσκόπια Αντίθεση εικόνας (contrast) Αντίθεση πλάτους Αντίθεση φάσης Αντίθεση εικόνας =100 x (Ι υποβ -Ι δειγμα )/ Ι υποβ Μικροσκοπία φθορισμού (Χρησιμοποιεί φθορίζουσες χρωστικές για το
Θέματα πριν τις εξετάσεις. Καλό διάβασμα Καλή επιτυχία
 Θέματα πριν τις εξετάσεις Καλό διάβασμα Καλή επιτυχία 2013-2014 Θέματα πολλαπλής επιλογής Μετουσίωση είναι το φαινόμενο α. κατά το οποίο συνδέονται δύο αμινοξέα για τον σχηματισμό μιας πρωτεΐνης β. κατά
Θέματα πριν τις εξετάσεις Καλό διάβασμα Καλή επιτυχία 2013-2014 Θέματα πολλαπλής επιλογής Μετουσίωση είναι το φαινόμενο α. κατά το οποίο συνδέονται δύο αμινοξέα για τον σχηματισμό μιας πρωτεΐνης β. κατά
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ
 BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 1. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 2. BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ Ι. ΑΤΟΜΑ ΚΑΙ ΜΟΡΙΑ ΙΙ. ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΙΙΙ. ΜΑΚΡΟΜΟΡΙΑ ΣΤΑ ΚΥΤΤΑΡΑ
BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 1. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 2. BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ Ι. ΑΤΟΜΑ ΚΑΙ ΜΟΡΙΑ ΙΙ. ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΙΙΙ. ΜΑΚΡΟΜΟΡΙΑ ΣΤΑ ΚΥΤΤΑΡΑ
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
Ερωτησεις στη Βιοφυσική & Νανοτεχνολογία. Χειμερινό Εξάμηνο 2012
 Ερωτησεις στη Βιοφυσική & Νανοτεχνολογία. Χειμερινό Εξάμηνο 2012 1) Ποιο φυσικό φαινόμενο βοηθάει στην αυτοσυναρμολόγηση μοριακών συστημάτων? α) Η τοποθέτηση μοριων με χρήση μικροσκοπίου σάρωσης δείγματος
Ερωτησεις στη Βιοφυσική & Νανοτεχνολογία. Χειμερινό Εξάμηνο 2012 1) Ποιο φυσικό φαινόμενο βοηθάει στην αυτοσυναρμολόγηση μοριακών συστημάτων? α) Η τοποθέτηση μοριων με χρήση μικροσκοπίου σάρωσης δείγματος
ΒΙΟΧΗΜΕΙΑ Ι. ΚΕΦΑΛΑΙΟ 2 ο Βιοχημική εξέλιξη
 ΒΙΟΧΗΜΕΙΑ Ι ΚΕΦΑΛΑΙΟ 2 ο Βιοχημική εξέλιξη ΣΥΝΔΕΣΗ ΜΕ ΤΑ ΠΡΟΗΓΟΥΜΕΝΑ Τι είναι ΒΙΟΧΗΜΕΙΑ DNA ΠΡΩΤΕΙΝΕΣ ΑΛΛΑ ΣΥΝΔΕΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΧΗΜΕΙΑΣ (Δεσμοί, ενέργεια, δομή) ΕΞΕΛΙΞΗ ΤΗΣ ΖΩΗΣ Υπάρχει μια συνεχή εξελικτική
ΒΙΟΧΗΜΕΙΑ Ι ΚΕΦΑΛΑΙΟ 2 ο Βιοχημική εξέλιξη ΣΥΝΔΕΣΗ ΜΕ ΤΑ ΠΡΟΗΓΟΥΜΕΝΑ Τι είναι ΒΙΟΧΗΜΕΙΑ DNA ΠΡΩΤΕΙΝΕΣ ΑΛΛΑ ΣΥΝΔΕΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΧΗΜΕΙΑΣ (Δεσμοί, ενέργεια, δομή) ΕΞΕΛΙΞΗ ΤΗΣ ΖΩΗΣ Υπάρχει μια συνεχή εξελικτική
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΒΙΟΧΗΜΕΙΑ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ. Στοιχείο O C H N Ca P K S Na Mg περιεκτικότητα % ,5 1 0,35 0,25 0,15 0,05
 ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του
 ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του ΤΑ ΜΟΝΟΜΕΡΗ ΣΥΝΔΕΟΝΤΑΙ ΜΕ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ. 1. ΠΡΩΤΕΪΝΕΣ
ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του ΤΑ ΜΟΝΟΜΕΡΗ ΣΥΝΔΕΟΝΤΑΙ ΜΕ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ. 1. ΠΡΩΤΕΪΝΕΣ
Καταστάσεις της ύλης. Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο.
 Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Μεταβολισμός του γλυκογόνου. Μεταβολισμός των υδατανθράκων κατά την άσκηση. Από που προέρχεται το μυϊκό και ηπατικό γλυκογόνο;
 Μεταβολισμός των υδατανθράκων κατά την άσκηση Μεταβολισμός του γλυκογόνου Το γλυκογόνο είναι ο αφθονότερος υδατάνθρακας των ζώων Το γλυκογόνο αποθηκεύεται κυρίως στο ήπαρ (3-7% κατά βάρος) και στους μύες
Μεταβολισμός των υδατανθράκων κατά την άσκηση Μεταβολισμός του γλυκογόνου Το γλυκογόνο είναι ο αφθονότερος υδατάνθρακας των ζώων Το γλυκογόνο αποθηκεύεται κυρίως στο ήπαρ (3-7% κατά βάρος) και στους μύες
3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική αναπνοή.
 5ο ΓΕΛ ΧΑΛΑΝΔΡΙΟΥ Μ. ΚΡΥΣΤΑΛΛΙΑ 2/4/2014 Β 2 ΚΕΦΑΛΑΙΟ 3 ΒΙΟΛΟΓΙΑΣ 3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική
5ο ΓΕΛ ΧΑΛΑΝΔΡΙΟΥ Μ. ΚΡΥΣΤΑΛΛΙΑ 2/4/2014 Β 2 ΚΕΦΑΛΑΙΟ 3 ΒΙΟΛΟΓΙΑΣ 3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01%
 ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου. Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση:
 KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης
 Βιοφυσική & Νανοτεχνολογία Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης Ημερομηνία εκτέλεσης άσκησης... Ονοματεπώνυμα... Περίληψη Σκοπός της άσκησης είναι η εξοικείωση με την χρήση
Βιοφυσική & Νανοτεχνολογία Εργαστηριακή Άσκηση Β3: Πειράματα περίθλασης από κρύσταλλο λυσοζύμης Ημερομηνία εκτέλεσης άσκησης... Ονοματεπώνυμα... Περίληψη Σκοπός της άσκησης είναι η εξοικείωση με την χρήση
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ»
 «ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑ 1 Ο Α. Να επιλέξετε την ορθή πρόταση: ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1. Το κωδικόνιο του mrna που κωδικοποιεί το αµινοξύ µεθειονίνη είναι α. 5 GUA
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑ 1 Ο Α. Να επιλέξετε την ορθή πρόταση: ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1. Το κωδικόνιο του mrna που κωδικοποιεί το αµινοξύ µεθειονίνη είναι α. 5 GUA
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ
 ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
ΒΙΟΛΟΓΙΑ. Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ.
 ΒΙΟΛΟΓΙΑ Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ. Ηλιούπολης Κεφάλαιο 1ο ΒΙΟΛΟΓΙΚΑ ΜΑΚΡΟΜΟΡΙΑ Η ΙΕΡΑΡΧΙΑ ΤΩΝ ΒΙΟΜΟΡΙΩΝ ΠΡΟΔΡΟΜΕΣ
ΒΙΟΛΟΓΙΑ Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ. Ηλιούπολης Κεφάλαιο 1ο ΒΙΟΛΟΓΙΚΑ ΜΑΚΡΟΜΟΡΙΑ Η ΙΕΡΑΡΧΙΑ ΤΩΝ ΒΙΟΜΟΡΙΩΝ ΠΡΟΔΡΟΜΕΣ
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ. 3.1 Ενέργεια και οργανισμοί
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ ΚΕΦΑΛΑΙΟ 3 3.1 Ενέργεια και οργανισμοί Την ενέργεια και τα υλικά που οι οργανισμοί εξασφαλίζουν από το περιβάλλον τους συνήθως δεν μπορούν να τα αξιοποίησουν άμεσα. Η αξιοποίησή τους
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ ΚΕΦΑΛΑΙΟ 3 3.1 Ενέργεια και οργανισμοί Την ενέργεια και τα υλικά που οι οργανισμοί εξασφαλίζουν από το περιβάλλον τους συνήθως δεν μπορούν να τα αξιοποίησουν άμεσα. Η αξιοποίησή τους
Εργασία για το μάθημα της Βιολογίας. Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου
 Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
Θέµατα ιάλεξης ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ ΠΡΩΤΕΪΝΕΣ. ιαχωρισµός Αµινοξέων
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
Κεφάλαιο 10 ΤΟ ΟΠΕΡΟΝΙΟ (σελ )
 Κεφάλαιο 10 ΤΟ ΟΠΕΡΟΝΙΟ (σελ. 387-417) Ένα ρυθμιστικό γονίδιο κωδικοποιεί μια πρωτεΐνη που δρα σε μια θέση-στόχο πάνω στο DNA και ρυθμίζει την έκφραση ενός άλλου γονιδίου. Στον αρνητικό έλεγχο, μία trans-δραστική
Κεφάλαιο 10 ΤΟ ΟΠΕΡΟΝΙΟ (σελ. 387-417) Ένα ρυθμιστικό γονίδιο κωδικοποιεί μια πρωτεΐνη που δρα σε μια θέση-στόχο πάνω στο DNA και ρυθμίζει την έκφραση ενός άλλου γονιδίου. Στον αρνητικό έλεγχο, μία trans-δραστική
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ)
 ΣΧΟΛΗ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΜΠ ΤΕΧΝΙΚΑ ΥΛΙΚΑ 1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ) Ε. Βιντζηλαίου (Συντονιστής), Ε. Βουγιούκας, Ε. Μπαδογιάννης Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΣΧΟΛΗ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΜΠ ΤΕΧΝΙΚΑ ΥΛΙΚΑ 1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ) Ε. Βιντζηλαίου (Συντονιστής), Ε. Βουγιούκας, Ε. Μπαδογιάννης Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
3.2 ΕΝΖΥΜΑ ΒΙΟΛΟΓΙΚΟΙ ΚΑΤΑΛΥΤΕΣ
 ΠΕΡΙΛΗΨΗ ΣΤΟ 3 Ο ΚΕΦΑΛΑΙΟ: ΜΕΤΑΒΟΛΙΣΜΟΣ ΚΥΡΙΑΚΟΣ Γ. Β1 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί
ΠΕΡΙΛΗΨΗ ΣΤΟ 3 Ο ΚΕΦΑΛΑΙΟ: ΜΕΤΑΒΟΛΙΣΜΟΣ ΚΥΡΙΑΚΟΣ Γ. Β1 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί
Κλαίρη Μ. Εργασία στη Βιολογία Α'2 Λυκείου
 Κλαίρη Μ. Εργασία στη Βιολογία Α'2 Λυκείου Διαβήτης. Ακούμε καθημερίνα γύρω μας πως εκατομμύρια άνθρωποι στον κόσμο πάσχουν από διαβήτη ή παχυσαρκία. Όμως, τι πραγματικά είναι αυτό; Τι ειναι ο σακχαρώδης
Κλαίρη Μ. Εργασία στη Βιολογία Α'2 Λυκείου Διαβήτης. Ακούμε καθημερίνα γύρω μας πως εκατομμύρια άνθρωποι στον κόσμο πάσχουν από διαβήτη ή παχυσαρκία. Όμως, τι πραγματικά είναι αυτό; Τι ειναι ο σακχαρώδης
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 15: Διαλύματα
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΘΕΜΑ 1 ο. 1.2 Όξινο είναι το υδατικό διάλυμα του α. ΝaCl. β. ΝΗ 4 Cl. γ. CH 3 COONa. δ. KOH. Μονάδες 5 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΤΕΛΟΣ 1ΗΣ ΑΠΟ 7 ΣΕΛΙ ΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 30 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 30 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί οργανισμοί μετατρέπουν την ηλιακή ενέργεια με τη διαδικασία
3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί οργανισμοί μετατρέπουν την ηλιακή ενέργεια με τη διαδικασία
BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι. ΒΙΟΧΗΜΕΙΑ (Lubert Stryer)
 BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 17.1 Η πυροσταφυλική αφυδρογονάση συνδέει τη γλυκόλυση με τον κύκλο του κιτρικού οξέος 17.2 O κύκλος του κιτρικού οξέος οξειδώνει μονάδες δύο ατόμων
BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 17.1 Η πυροσταφυλική αφυδρογονάση συνδέει τη γλυκόλυση με τον κύκλο του κιτρικού οξέος 17.2 O κύκλος του κιτρικού οξέος οξειδώνει μονάδες δύο ατόμων
Εφαρμοσμένη Διατροφική Ιατρική
 Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης
 ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ. Οι ρυθμιστές του οργανισμού
 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
Βιοφυσική. ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο ) 3 η Διάλεξη
 Βιοφυσική ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο 2009-10) 3 η Διάλεξη Από την προηγούμενη διάλεξη: Οι πρωτεΐνες εκτελούν τις περισσότερες βιολογικές λειτουργίες π.χ Ενζυμική κατάλυση (επιτάχυνση
Βιοφυσική ΦΥΣ 415 Διδάσκων Σ. Σκούρτης (χειμερινό εξάμηνο 2009-10) 3 η Διάλεξη Από την προηγούμενη διάλεξη: Οι πρωτεΐνες εκτελούν τις περισσότερες βιολογικές λειτουργίες π.χ Ενζυμική κατάλυση (επιτάχυνση
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ. Καρβουντζή Ηλιάνα Βιολόγος
 Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ. Χημεία της ζωής 1
 ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής
 1 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής Μικροσκοπικοί οργανισμοί που ρυθμίζουν τη λειτουργία του ανθρώπινου σώματος σε
1 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής Μικροσκοπικοί οργανισμοί που ρυθμίζουν τη λειτουργία του ανθρώπινου σώματος σε
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια
 πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
Από πού προέρχεται η θερμότητα που μεταφέρεται από τον αντιστάτη στο περιβάλλον;
 3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
Ασκήσεις 5& 6. Διαμόρφωση Βιομορίων μέσω Φασματοσκοπίας NMR. Σύγκριση & Ανάλυση Δομών Βιομορίων
 Ασκήσεις 5& 6 Διαμόρφωση Βιομορίων μέσω Φασματοσκοπίας NMR Σύγκριση & Ανάλυση Δομών Βιομορίων Διαμόρφωση Βιομορίων μέσω Φασματοσκοπίας NMR Κρυσταλλογραφία Ακτίνων-Χ & Φασματοσκοπία ΝΜR Πλεονεκτήματα -
Ασκήσεις 5& 6 Διαμόρφωση Βιομορίων μέσω Φασματοσκοπίας NMR Σύγκριση & Ανάλυση Δομών Βιομορίων Διαμόρφωση Βιομορίων μέσω Φασματοσκοπίας NMR Κρυσταλλογραφία Ακτίνων-Χ & Φασματοσκοπία ΝΜR Πλεονεκτήματα -
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
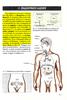 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ
 ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΜΟΝΤΕΛΑ ΜΕΜΒΡΑΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ 1. Μονοστιβάδες 2. Διπλοστιβάδες 3. Λιποσώματα 1.1 ΜΟΝΟΣΤΙΒΑΔΕΣ Σχηματίζονται από μη-πολικά μόρια στη μεσόφαση αέρα/νερού Συσκευή
ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΜΟΝΤΕΛΑ ΜΕΜΒΡΑΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ 1. Μονοστιβάδες 2. Διπλοστιβάδες 3. Λιποσώματα 1.1 ΜΟΝΟΣΤΙΒΑΔΕΣ Σχηματίζονται από μη-πολικά μόρια στη μεσόφαση αέρα/νερού Συσκευή
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ
 2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράμμα που αντιστοιχεί στη σωστή απάντηση:
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
 Τι γνώριζαν για τους κρυστάλλους: ΚΡΥΣΤΑΛΛΙΚΑ ΣΤΕΡΕΑ - ΚΡΥΣΤΑΛΛΟΙ Πρώτοι παρατηρητές: Κανονικότητα της εξωτερικής μορφής των κρυστάλλων οι κρύσταλλοι σχηματίζονται από την κανονική επανάληψη ταυτόσημων
Τι γνώριζαν για τους κρυστάλλους: ΚΡΥΣΤΑΛΛΙΚΑ ΣΤΕΡΕΑ - ΚΡΥΣΤΑΛΛΟΙ Πρώτοι παρατηρητές: Κανονικότητα της εξωτερικής μορφής των κρυστάλλων οι κρύσταλλοι σχηματίζονται από την κανονική επανάληψη ταυτόσημων
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
Μελέτη της πολυμορφικότητας πρωτεϊνών φαρμακευτικού ενδιαφέροντος: Η περίπτωση της ανθρώπινης ινσουλίνης
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΔΙΠΛΩΜΑ ΕΙΔΙΚΕΥΣΗΣ Μελέτη της πολυμορφικότητας πρωτεϊνών φαρμακευτικού ενδιαφέροντος: Η περίπτωση της ανθρώπινης ινσουλίνης ΚΑΡΑΒΑΣΙΛΗ ΦΩΤΕΙΝΗ Επιβλέποντες:
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΔΙΠΛΩΜΑ ΕΙΔΙΚΕΥΣΗΣ Μελέτη της πολυμορφικότητας πρωτεϊνών φαρμακευτικού ενδιαφέροντος: Η περίπτωση της ανθρώπινης ινσουλίνης ΚΑΡΑΒΑΣΙΛΗ ΦΩΤΕΙΝΗ Επιβλέποντες:
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ
 ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ ΕΝΟΤΗΤΑ: ΕΝΖΥΜΑ ΚΑΘΗΓΗΤΗΣ: ΠΑΤΗΡ ΑΝΑΣΤΑΣΙΟΣ ΙΣΑΑΚ 1. Να εξηγήσετε γιατί πολλές βιταμίνες, παρά τη μικρή συγκέντρωσή τους στον οργανισμό, είναι πολύ σημαντικές για
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ ΕΝΟΤΗΤΑ: ΕΝΖΥΜΑ ΚΑΘΗΓΗΤΗΣ: ΠΑΤΗΡ ΑΝΑΣΤΑΣΙΟΣ ΙΣΑΑΚ 1. Να εξηγήσετε γιατί πολλές βιταμίνες, παρά τη μικρή συγκέντρωσή τους στον οργανισμό, είναι πολύ σημαντικές για
ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ
 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 2 ο 1. Με ποιο μηχανισμό αντιγράφεται το DNA σύμφωνα με τους Watson και Crick; 2. Ένα κύτταρο που περιέχει ένα μόνο χρωμόσωμα τοποθετείται σε θρεπτικό υλικό που περιέχει ραδιενεργό
ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 2 ο 1. Με ποιο μηχανισμό αντιγράφεται το DNA σύμφωνα με τους Watson και Crick; 2. Ένα κύτταρο που περιέχει ένα μόνο χρωμόσωμα τοποθετείται σε θρεπτικό υλικό που περιέχει ραδιενεργό
ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΟΛΥΣΗΣ, ΓΛΥΚΟΝΕΟΓΕΝΕΣΗ & ΟΜΟΙΟΣΤΑΣΙΑ ΤΗΣ ΓΛΥΚΟΖΗΣ
 ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΟΛΥΣΗΣ, ΓΛΥΚΟΝΕΟΓΕΝΕΣΗ & ΟΜΟΙΟΣΤΑΣΙΑ ΤΗΣ ΓΛΥΚΟΖΗΣ Σύνοψη: Ρύθμιση Γλυκόλυσης Στάδια γλυκόλυσης 1 ο Στάδιο: Δέσμευση & ενεργοποίηση γλυκόζης Εξοκινάση 6-Φωσφορική Γλυκόζη (-ΑΤΡ), Iσομεράση
ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΟΛΥΣΗΣ, ΓΛΥΚΟΝΕΟΓΕΝΕΣΗ & ΟΜΟΙΟΣΤΑΣΙΑ ΤΗΣ ΓΛΥΚΟΖΗΣ Σύνοψη: Ρύθμιση Γλυκόλυσης Στάδια γλυκόλυσης 1 ο Στάδιο: Δέσμευση & ενεργοποίηση γλυκόζης Εξοκινάση 6-Φωσφορική Γλυκόζη (-ΑΤΡ), Iσομεράση
ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ
 ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ Προσοµοίωση Είναι γνωστό ότι η εξάσκηση των φοιτητών σε επίπεδο εργαστηριακών ασκήσεων, µε χρήση των κατάλληλων πειραµατοζώων, οργάνων και αναλωσίµων
ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ Προσοµοίωση Είναι γνωστό ότι η εξάσκηση των φοιτητών σε επίπεδο εργαστηριακών ασκήσεων, µε χρήση των κατάλληλων πειραµατοζώων, οργάνων και αναλωσίµων
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (2) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (2) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΤΗΤΑΣ (1) Επίδραση κοινού ιόντος Εάν σε κορεσµένο διάλυµα δυσδιάλυτου ηλεκτρολύτη (π.χ. AgCl) προστεθεί
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (2) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΤΗΤΑΣ (1) Επίδραση κοινού ιόντος Εάν σε κορεσµένο διάλυµα δυσδιάλυτου ηλεκτρολύτη (π.χ. AgCl) προστεθεί
Φυσική Στερεών στις Πρωτεΐνες
 Φυσική Στερεών στις Πρωτεΐνες Νίκος Απ. Παπανδρέου Τ.Ε.Ι. Πειραιά Φεβρουάριος 2010 Ένα ελικοϊδές μονοπάτι Χημική δομή μίας πρωτεΐνης Μήκος αλυσίδας ~30 έως ~1000 αµινοξέα Συνολικός αριθµός ατόµων έως ~
Φυσική Στερεών στις Πρωτεΐνες Νίκος Απ. Παπανδρέου Τ.Ε.Ι. Πειραιά Φεβρουάριος 2010 Ένα ελικοϊδές μονοπάτι Χημική δομή μίας πρωτεΐνης Μήκος αλυσίδας ~30 έως ~1000 αµινοξέα Συνολικός αριθµός ατόµων έως ~
ΚΕΦΑΛΑΙΟ 15. Κυτταρική ρύθμιση. Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1
 ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης
 Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
ΜΕΤΑΒΟΛΙΣΜΟΣ ΝΗΣΤΙΚΟΥ ΚΑΙ ΤΡΑΦΕΝΤΟΣ ΟΡΓΑΝΙΣΜΟΥ Tον ανθρώπινο µεταβολισµό το χαρακτηρίζουν δύο στάδια. Tοπρώτοείναιηκατάστασητουοργανισµούµετά
 ΜΕΤΑΒΟΛΙΣΜΟΣ ΝΗΣΤΙΚΟΥ ΚΑΙ ΤΡΑΦΕΝΤΟΣ ΟΡΓΑΝΙΣΜΟΥ Tον ανθρώπινο µεταβολισµό το χαρακτηρίζουν δύο στάδια. Tοπρώτοείναιηκατάστασητουοργανισµούµετά απόκάποιογεύµα, οπότετοαίµαείναιπλούσιοσε θρεπτικές ύλες από
ΜΕΤΑΒΟΛΙΣΜΟΣ ΝΗΣΤΙΚΟΥ ΚΑΙ ΤΡΑΦΕΝΤΟΣ ΟΡΓΑΝΙΣΜΟΥ Tον ανθρώπινο µεταβολισµό το χαρακτηρίζουν δύο στάδια. Tοπρώτοείναιηκατάστασητουοργανισµούµετά απόκάποιογεύµα, οπότετοαίµαείναιπλούσιοσε θρεπτικές ύλες από
ΑΣΚΗΣΗ 1. Περίληψη. Θεωρητική εισαγωγή. Πειραματικό μέρος
 ΑΣΚΗΣΗ 1 Περίληψη Σκοπός της πρώτης άσκησης ήταν η εξοικείωση μας με τα όργανα παραγωγής και ανίχνευσης των ακτίνων Χ και την εφαρμογή των κανόνων της κρυσταλλοδομής σε μετρήσεις μεγεθών στο οεργαστήριο.
ΑΣΚΗΣΗ 1 Περίληψη Σκοπός της πρώτης άσκησης ήταν η εξοικείωση μας με τα όργανα παραγωγής και ανίχνευσης των ακτίνων Χ και την εφαρμογή των κανόνων της κρυσταλλοδομής σε μετρήσεις μεγεθών στο οεργαστήριο.
Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR
 Φασματοσκοπία Ερμηνεία & εφαρμογές : Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR Ποια φαινόμενα παράγουν τα
Φασματοσκοπία Ερμηνεία & εφαρμογές : Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR Ποια φαινόμενα παράγουν τα
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής
 Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Παράγοντες που εξηγούν τη διαλυτότητα. Είδη διαλυμάτων
 Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
ΚΕΦΑΛΑΙΟ 11: Περίθλαση Ακτίνων-Χ και Νετρονίων από Κρυσταλλικά Υλικά
 ΚΕΦΑΛΑΙΟ 11: Περίθλαση Ακτίνων-Χ και Νετρονίων από Κρυσταλλικά Υλικά Εν γένει τρεις µεταβλητές διακυβερνούν τις διαφορετικές τεχνικές περίθλασης ακτίνων-χ: (α) ακτινοβολία µονοχρωµατική ή µεταβλητού λ
ΚΕΦΑΛΑΙΟ 11: Περίθλαση Ακτίνων-Χ και Νετρονίων από Κρυσταλλικά Υλικά Εν γένει τρεις µεταβλητές διακυβερνούν τις διαφορετικές τεχνικές περίθλασης ακτίνων-χ: (α) ακτινοβολία µονοχρωµατική ή µεταβλητού λ
Φυσιολογία ΙΙ Ενότητα 2:
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 2: Ορμόνες Ανωγειανάκις Γεώργιος Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 2: Ορμόνες Ανωγειανάκις Γεώργιος Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών
 Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Το φωσφορικό ανιόν δεν ανάγεται µέσα στο φυτό. Παραµένει στην υψηλότερη οξειδωτική µορφή του
 Το φωσφορικό ανιόν δεν ανάγεται µέσα στο φυτό Παραµένει στην υψηλότερη οξειδωτική µορφή του 1)ελεύθερο Pi (inorganic phosphate) 2)προσαρτηµένο ως φωσφορική οµάδα πάνω σε κάποιο µόριο το συµβολίζουµε ως
Το φωσφορικό ανιόν δεν ανάγεται µέσα στο φυτό Παραµένει στην υψηλότερη οξειδωτική µορφή του 1)ελεύθερο Pi (inorganic phosphate) 2)προσαρτηµένο ως φωσφορική οµάδα πάνω σε κάποιο µόριο το συµβολίζουµε ως
Διαγώνισμα Βιολογίας Προσανατολισμού Γ Λυκείου
 Διαγώνισμα Βιολογίας Προσανατολισμού Γ Λυκείου ΘΕΜΑ Α Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση ή στη φράση που συμπληρώνει σωστά την πρόταση. Α1. Ουδέτερη μετάλλαξη μπορεί να είναι:
Διαγώνισμα Βιολογίας Προσανατολισμού Γ Λυκείου ΘΕΜΑ Α Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση ή στη φράση που συμπληρώνει σωστά την πρόταση. Α1. Ουδέτερη μετάλλαξη μπορεί να είναι:
Μέθοδοι έρευνας ορυκτών και πετρωμάτων
 Μέθοδοι έρευνας ορυκτών και πετρωμάτων Μάθημα 9 ο Φασματοσκοπία Raman Διδάσκων Δρ. Αδαμαντία Χατζηαποστόλου Τμήμα Γεωλογίας Πανεπιστημίου Πατρών Ακαδημαϊκό Έτος 2017-2018 Ύλη 9 ου μαθήματος Αρχές λειτουργίας
Μέθοδοι έρευνας ορυκτών και πετρωμάτων Μάθημα 9 ο Φασματοσκοπία Raman Διδάσκων Δρ. Αδαμαντία Χατζηαποστόλου Τμήμα Γεωλογίας Πανεπιστημίου Πατρών Ακαδημαϊκό Έτος 2017-2018 Ύλη 9 ου μαθήματος Αρχές λειτουργίας
Aναδίπλωση και επεξεργασία των πρωτεϊνών
 Aναδίπλωση και επεξεργασία των πρωτεϊνών Aναδίπλωση και επεξεργασία των πρωτεϊνών Πρωτεϊνοσύνθεση: τελευταίο στάδιο της ροής της γενετικής πληροφορίας * Αλληλουχία νουκλεοτιδίων DNA Μεταγραφή - Μετάφραση
Aναδίπλωση και επεξεργασία των πρωτεϊνών Aναδίπλωση και επεξεργασία των πρωτεϊνών Πρωτεϊνοσύνθεση: τελευταίο στάδιο της ροής της γενετικής πληροφορίας * Αλληλουχία νουκλεοτιδίων DNA Μεταγραφή - Μετάφραση
ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΑΣΚΗΣΗ. Θανάσης Ζ. Τζιαμούρτας, Ph.D.
 ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΑΣΚΗΣΗ Θανάσης Ζ. Τζιαμούρτας, Ph.D. Τι είναι σακχαρώδης διαβήτης; Παθοφυσιολογική κατάσταση η οποία χαρακτηρίζεται από αυξημένη συγκέντρωση σακχάρου στο αίμα Καμπύλη σακχάρου (75
ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΑΣΚΗΣΗ Θανάσης Ζ. Τζιαμούρτας, Ph.D. Τι είναι σακχαρώδης διαβήτης; Παθοφυσιολογική κατάσταση η οποία χαρακτηρίζεται από αυξημένη συγκέντρωση σακχάρου στο αίμα Καμπύλη σακχάρου (75
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5
 ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
