II. gimnazija Maribor PROJEKTNA NALOGA. Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika
|
|
|
- Φίλητος Ζωγράφου
- 7 χρόνια πριν
- Προβολές:
Transcript
1 II. gimnazija Maribor PROJEKTNA NALOGA Mentor vsebine: Irena Ilc, prof. Avtor: Andreja Urlaub Mentor oblike: Mirko Pešec, prof. Predmet: kemija - informatika Selnica ob Dravi, januar 2005
2 KAZALO VSEBINE Projektna naloga: O RAZTOPINAH RAZTOPINE... 5 AGREGATNO STANJE RAZTOPIN... 6 VRSTE TOPIL... 6 VRSTE RAZTOPIN GLEDE NA VELIKOST DELCEV TOPLJENCA:... 7 VZROKI RAZTAPLJANJA... 7 KVANTITATIVNA OPREDELITEV RAZTOPIN LASTNOSTI RAZTOPIN FIZIKALNE KOLIGATIVNE LASTNOSTI RAZTOPIN OSMOZA STVARNO KAZALO LITERATURA Andreja Urlaub 1.c, II.gimnazija Maribor 2
3 SLIKOVNO KAZALO Slika 1: raztopina... 4 Slika 2: raztapljanje ionskega kristala... 8 Slika 3: raztapljanje molekulskega kristala... 9 Slika 4: ionizacija ali disocijacija molekul Slika 5: osmoza Andreja Urlaub 1.c, II.gimnazija Maribor 3
4 R UVOD aztopine v našem življenju redno srečujemo, čeprav se mnogokrat njihove prisotnosti sploh ne zavedamo. (npr. sok, ki ga pijemo je pogosto raztopina vode in neke snovi, čaj, ki si ga sladkamo ) Ko si pripravljamo čaj, seveda ne izmerimo natančno, koliko sladkorja bomo dali vanj. V kemiji pa je mnogokrat pomembna še posebej natančnost merjenja, s katero pripravimo neko raztopino. Slika 1: raztopina Andreja Urlaub 1.c, II.gimnazija Maribor 4
5 RAZTOPINE Kemijsko definiramo pravo raztopino kot homogeno zmes več snovi (topila in topljenca) s spremenljivim razmerjem komponent. Snov, ki se raztaplja v neki drugi snovi imenujemo topljenec (, snov, ki to snov topi pa topilo (A). Ponavadi je topila več kot topljenca. Količina topljenca, ki se raztaplja v določeni količini topila je omejena z njegovo topnostjo. TOPNOST je lastnost snovi pri določeni temperaturi, da se majhni delci snovi (najpogosteje gradniki snovi) porazdelijo med gradnike druge snovi. Topnost je odvisna od vrste topljenca, topila in temperature, pri plinih pa tudi od tlaka. Topnost s temperaturo ponavadi narašča pri plinih pa pada, vendar obstajajo tudi izjeme, pri katerih se topnost pri povečani temperaturi zmanjša (npr. CaS, Ca(OH) 2 ). a) nasičena raztopina vsebuje pri določeni temperaturi največjo možno količino topljenca v določeni količini topila. b) razredčena raztopina je tista raztopina, ki vsebuje veliko količino topila in malo količino topljenca c) koncentrirana raztopina je tista raztopina, ki vsebuje veliko količino topljenca in malo količino topila Andreja Urlaub 1.c, II.gimnazija Maribor 5
6 AGREGATNO STANJE RAZTOPIN Topilo in topljenec sta lahko v vseh agregatnih stanjih izjema je le plinasto, saj plinast topljenec in topilo, ki se mešata prištevamo k plinskim mešanicam. Najpogostejše so raztopine trdnih snovi v tekočih topilih. Primere raztopin, ki jih dobimo, ko mešamo različna topila in topljence nam prikazuje spodnja tabela. Tabela št.1: agregatno stanje raztopin TOPILO (agregatno TOPLJENEC PRIMER stanje) (agregatno stanje) RAZTOPINE trdno trdno zlitina trdno tekoče zlitina z živim srebrom trdno plinasto vodik v paladiju tekoče trdno raztopina kuhinjske soli tekoče tekoče raztopina alkohola tekoče plinasto radenska plinasto trdno dim plinasto tekoče megla plinasto plinasto ni raztopina VRSTE TOPIL Poznamo polarna in nepolarna topila. Najbolj znano in razširjeno polarno topilo je voda, poleg nje pa še etanol. Pri nepolarnih je najbolj znan ogljikov tetraklorid, zaradi velike nevarnosti pri delu z njim pa velikokrat uporabljamo bencin. Polarne snovi se tako raje topijo v polarnih topilih, medtem ko se nepolarne raje v nepolarnih. Andreja Urlaub 1.c, II.gimnazija Maribor 6
7 VRSTE RAZTOPIN GLEDE NA VELIKOST DELCEV TOPLJENCA: prave raztopine koloidne raztopine grobo disperzne sisteme (suspenzije) Tabela 2: raztopine ločene glede na velikost delcev vrsta raztopine prava raztopina koloidna raztopina suspenzija velikost delcev manjši od 10-9 m večji od 10-9 m in večji od 10-7 m manjši od 10-7 m vrsta delcev molekule, ioni amorfni delci, velike molekule veliki amorfni ali kristalčni delci VZROKI RAZTAPLJANJA Med molekulami topila in gradniki na površini topljenca se lahko vzpostavijo molekulske vezi. Pri tem se sprošča energija, ki se porabi za prekinitev vezi, s katerimi so gradniki na površini kristala vezani v kristalno strukturo. Tako se od kristalne strukture loči plast gradnikov in proces se nadaljuje. Andreja Urlaub 1.c, II.gimnazija Maribor 7
8 a) RAZTAPLJANJE IONSKEGA KRISTALA Primer: raztapljanje NaCl v vodi Ko vržemo v vodo kristalček NaCl se polarne molekule usmerijo proti ionom, ki so na površini topljenca, z negativnim koncem proti pozitivnim ionom in z pozitivnim koncem proti negativnim ionom. Polarne molekule vode oslabijo vezi med ioni v kristalu NaCl. Ta pojav imenujemo hidratacija. Molekule vode odtrgajo ione iz kristalov. Te ione imenujemo hidratizirani ioni ioni obdani s šopom molekul vode. Tako nastane raztopina. Hidratacija je eksotermen proces. Energija, ki nastane se porabi za prekinitev vezi med ioni v kristalu. V primeru, da topilo ni voda, ne uporabljamo pojma hidratacija ampak solvatacija. NaCl (s) + H 2 O (aq) Na + (aq) + Cl - (aq) Slika 2: raztapljanje ionskega kristala Andreja Urlaub 1.c, II.gimnazija Maribor 8
9 b) RAZTAPLJANJE MOLEKULSKEGA KRISTALA Primer: raztapljanje molekule sladkorja (C 12 H 22 O 11 ) v vodi Vzrok za raztapljanje pa je prav tako hidratacija. C 12 H 22 O 11 (s) + H 2 O (aq) C 12 H 22 O 11 (aq) Slika 3: raztapljanje molekulskega kristala Andreja Urlaub 1.c, II.gimnazija Maribor 9
10 c) IONIZACIJA ELEKTROLITSKA DISOCIACIJA Hidratacija pa je v nekaterih primerih tako močna, da se molekule topljenca raztrgajo. Pri tem nastanejo iz molekul ioni. Ta pojav imenujemo elektrolitska disociacija. Primer: raztapljanje HCl v vodi Polarne molekule HCl se hidratizirajo in nato disocirajo v ione: HCl (aq) + H 2 O H 3 O + (aq) + Cl - (aq). Nastala raztopina je elektrolit (klorovodikova kislina). Vsebuje hidratizirane ione H 3 O + in Cl - ter v manjši meri nedisocirane molekule HCl. Če je energija pri hidrataciji večja od mrežne enrgije, se med raztapljanjem energija sprošča (eksotermna reakcija), če pa je mrežna energija večja od hidratacijske pa se energija porablja (endotermna reakcija). Slika 4: ionizacija ali disocijacija molekul Andreja Urlaub 1.c, II.gimnazija Maribor 10
11 KVANTITATIVNA OPREDELITEV RAZTOPIN V kemiji moramo raztopine kvantitativno opredeliti (torej poznati moramo količino topila in topljenca). Za opredelitev teh dveh količin uporabljamo veliko fizikalnih veličin. Sestavo raztopin lahko tako opišemo z: 1. deleži: -masni -množinski -prostorninski 2. koncentracijami: -masna -množinska - volumska 3. razmerji: -masno -množinsko -prostorninsko 4. molalnostjo 1. DELEŽI Deleži so veličine, ki nakazujejo kolikšen del vzorca pripada posamezni komponenti. Nimajo enote, izrazimo jih v odstodkih. a) masni delež (ali masni odstotek) definicijska enačba: w( = A) + Andreja Urlaub 1.c, II.gimnazija Maribor 11
12 b) množinski delež definicijska enačba: x ( = n( n( A) + n( c) prostorninski delež definicijska enačba: φ ( = V ( * V ( A) + V ( *V (A) +V( pred mešanjem Primer naloge: Imamo 72 g vode in 45, 98g NaCl. Izračunaj množinski in masni delež NaCl v tej raztopini! m (A) = 72g m ( = 45,98g w ( =? x ( =? w( = A) + m (R) = m (A) + m ( m (R) = 72g + 45,98 R)=117,98g Andreja Urlaub 1.c, II.gimnazija Maribor 12
13 45,98g w( = 117,98g w( = 0,3897 w( = 38,97% n ( = M ( x ( = x ( = n( n( A) + n( 2mol 6mol 54,98gmol n ( = 22,99g n ( = 2 mol x ( = 0,3333 x ( = 3,33% n (A) = A) M ( A) n (A) = 72gmol 18g n (A) = 4 mol n (R) = n (A) + n ( n (R) = 4 mol + 2 mol n (R) = 6 mol Andreja Urlaub 1.c, II.gimnazija Maribor 13
14 2. KONCENTRACIJE Koncentracije so veličine, ki nakazujejo količino ene komponente v razmerju z volumnom zmesi. Koncentracije imajo merske enote. a) masna koncentracija definicijska enačba: γ ( = V ( R) b) množinska koncentracija definicijska enačba: c ( = n( V ( R) c) volumska koncentracija definicijska enačba: δ ( = V ( V ( R) Primer naloge: Fiziološka raztopina, ki se uporablja v medicini po opravljenih operacijah, vsebuje NaCl s koncentracijo 0,154 mol/l. Koliko gramov se nahaja v 500mL take raztopine? Andreja Urlaub 1.c, II.gimnazija Maribor 14
15 c (NaCl) = 0,154 mol/l V (R) = 500mL = 0,5L m (NaCl) =? c ( = n( V ( R) n (NaCl) = c (NaCl) V (R) M ( = c (NaCl) V (R) m (NaCl) = c (NaCl) V (R) M ( m (NaCl) = 0,154 mol/l 0,5 L 58,44 g/mol m (NaCl) = 4,499g = 4,5 g Andreja Urlaub 1.c, II.gimnazija Maribor 15
16 3. RAZMERJA Razmerje neke raztopine nam pove koliko je topljenca glede na topilo, ali pa obratno. Nimajo enote. a. masno razmerje A) b. množinsko razmerje n( n( A) c. prostorninsko razmerje V ( V ( A) Primer naloge: Kolikšno je masno in množinsko razmerje topljenca in topila v raztopini ki vsebuje 3 mole vode in 27g MgS? a) masno razmerje n (H 2 O) = 3 mol m (H 2 O) = 54g m (MgS) = 27g n (MgS) = 1,1 mol A) 27g = 54g = 2 1 Andreja Urlaub 1.c, II.gimnazija Maribor 16
17 b) množinsko razmerje n (H 2 O) = 3 mol m (H 2 O) = 54g m (MgS) = 27g n(mgs) = 1,1 mol n( n( A) = 1,1 mol 3mol = 1 2,7 LASTNOSTI RAZTOPIN Raztopine olajšajo potek kemijskih resakcij Primer: NaOH + HCl NaCl + H 2 O Prudukt sicer ni takoj viden, vendar bi se ob uparjanju raztopine izločili kristalčki NaCl. Pri tej kemijski reakciji smo uporabili raztopino NaOH in raztopino HCl v vodi. Ta reakcija pa nebi potekla enako hitro, če bi imeli na voljo trden NaCl in plinast HCl. FIZIKALNE KOLIGATIVNE LASTNOSTI RAZTOPIN Fizikalne lastnosti raztopin so odvisne od koncentracije raztopin (torej od števila raztopljenih molekul ionov ). Raztopina ima višje vrelišče in nižje tališče, nižji parni tlak*. Molekule lahko prehajajo iz tekoče v plinsko fazo, pri čemer nastaja para. Število molekul v pari narašča, dokler ni doseženo dinamično ravnovesje med obema fazama, ko molekule iz tekoče prehajajo v plinsko fazo in nazaj tako, da je hitrost izhlapevanja enaka hitrosti kondenzacije. Tlak pare, ki je v ravnotežju s tekočino v zaprti posodi, imenujemo parni tlak. Normalno vrelišče je definirano kot temperatura, pri kateri doseže parni tlak tekočine vrednost normalnega tlaka.pri drugačnih pogojih (npr. visoko v gorah ali globoko v rudnikih) je parni Andreja Urlaub 1.c, II.gimnazija Maribor 17
18 tlak enak zunanjemu tlaku pri drugačni temperaturi, zato je vrelišče iste snovi različno. Raztopina ima nižji parni tlak od samega topila. Vzrok je v tem, da molekule topila sodelujejo pri raztapljanju topljenca torej težnja po prehodu v plinsko fazo se zmanjša. To je tudi vzrok, da se vrelišče raztopin zviša in da se tališče zniža. Z merjenjem zvišanja vrelišča in znižanja tališča lahko določimo molsko maso topljenca.pri tem računanju sta nam v pomoč dve konstanti. 1. Za zvišanje vrelišča uporabljamo ebulioskopijsko konstanto: ΔT = K c b( 1 2. Za znižanje tališča pa uporabljamo krioskopsko konstanto: ΔT = K k b( Obe konstanti sta odvisni od topila. Vrednosti teh konstant pa lahko najdemo v različnih priročnikih, nekaj primerov je navedenih tudi v spodnji tabeli. topilo zvišanje vrelišča (ºC) znižanje tališča (ºC) voda 0,51-1,86 benzen 2,63-5,12 ocetna kislina 3,14-3,90 1 b( = n( = A) M( A) Andreja Urlaub 1.c, II.gimnazija Maribor 18
19 Topnost različnih snovi v odvisnosti od temperature. Andreja Urlaub 1.c, II.gimnazija Maribor 19
20 OSMOZA Osmoza pomeni prehajanje topila skozi polprepustno membrano iz raztopine z manjšo koncentracijo v raztopino z večjo koncentracijo. Polprepustna membrana prepušča le molekule topila. Osmoza je posledica težnje raztopine pa razredčenju. Polprepustne membrane so lahko iz naravnega ali umetnega materiala. V kemiji zelo poznana in pogosto uporabljena je tanka plast spojine Cu 2 [Fe(CN) 6 ] na prozornem keramičnem lončku. Pojav osmoze je pomemben tudi v bioloških sistemih. Celične membrane v organizmih prepuščajo nekatere topljence in vodo. Koncentracija soli v krvni plazmi je enaka kot v 0,9% raztopini NaCl v vodi. Če damo krvne celice v čisto vodo, gredo molekule vode skozi membrano in razredčijo celično tekočino. Celice zato nabreknejo in počijo. Zardi tega je potrebno paziti, da imajo tekočine, ki jih dodajamo krvi enako koncentracijo kot sama kri. Tukaj lahko tudi iščemo vzrok zakaj se ljudje prej utopijo v sladki kot v slani vodi. Slika 5: osmoza Andreja Urlaub 1.c, II.gimnazija Maribor 20
21 STVARNO KAZALO Deleži...11 Ebulioskopijska konstanta...18 Grobo disperzni sistem...7 Koloidne raztopine...7 Koncentracije...14 Koncentrirana raztopina...5 Krioskopska konstanta...18 Nasičena raztopina...5 Osmoza...20 Prave raztopine...7 Razmerja...16 Razredčena raztopina...5 Topilo...6 Topljenec...6 Topnost... 5 Andreja Urlaub 1.c, II.gimnazija Maribor 21
22 LITERATURA BRENČIČ, J., LAZARINI, F Splošna in anorganska kemija za gimnazije, strokovne in tehniške šole. Ljubljana: DZS Kemija. Ljubljana: Cankarjeva založba HOLMAN, J Svet snovi. Maribor: Založba Obzorja Andreja Urlaub 1.c, II.gimnazija Maribor 22
Diferencialna enačba, v kateri nastopata neznana funkcija in njen odvod v prvi potenci
 Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Linearna diferencialna enačba reda Diferencialna enačba v kateri nastopata neznana funkcija in njen odvod v prvi potenci d f + p= se imenuje linearna diferencialna enačba V primeru ko je f 0 se zgornja
Simbolni zapis in množina snovi
 Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Simbolni zapis in množina snovi RELATIVNA MOLEKULSKA MASA ON MOLSKA MASA Relativna molekulska masa Ker so atomi premajhni, da bi jih merili z običajnimi tehtnicami, so ugotovili, kako jih izračunati. Izražamo
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 5. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 5. december 2013 Primer Odvajajmo funkcijo f(x) = x x. Diferencial funkcije Spomnimo se, da je funkcija f odvedljiva v točki
Funkcijske vrste. Matematika 2. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 2. april Gregor Dolinar Matematika 2
 Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Matematika 2 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 2. april 2014 Funkcijske vrste Spomnimo se, kaj je to številska vrsta. Dano imamo neko zaporedje realnih števil a 1, a 2, a
Tretja vaja iz matematike 1
 Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Tretja vaja iz matematike Andrej Perne Ljubljana, 00/07 kompleksna števila Polarni zapis kompleksnega števila z = x + iy): z = rcos ϕ + i sin ϕ) = re iϕ Opomba: Velja Eulerjeva formula: e iϕ = cos ϕ +
Slika, vir: http://www.manataka.org
 KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
KEMIJA Slika, vir: http://www.manataka.org RAZTOPINE SPLOŠNE INFORMACIJE O GRADIVU Učno gradivo je nastalo v okviru projekta Munus 2. Njegovo izdajo je omogočilo sofinanciranje Evropskega socialnega sklada
Tabele termodinamskih lastnosti vode in vodne pare
 Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
Univerza v Ljubljani Fakulteta za strojništvo Laboratorij za termoenergetiko Tabele termodinamskih lastnosti vode in vodne pare po modelu IAPWS IF-97 izračunano z XSteam Excel v2.6 Magnus Holmgren, xsteam.sourceforge.net
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 21. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 21. november 2013 Hiperbolične funkcije Hiperbolični sinus sinhx = ex e x 2 20 10 3 2 1 1 2 3 10 20 hiperbolični kosinus coshx
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 22. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 22. oktober 2013 Kdaj je zaporedje {a n } konvergentno, smo definirali s pomočjo limite zaporedja. Večkrat pa je dobro vedeti,
Ravnotežja v raztopini
 Ravnotežja v raztopini TOPILO: komponenta, ki jo je več v raztopini.v analizni kemiji uporabljamo organska in anorganska topila. Topila z veliko dielektrično konstanto (ε > 10) so polarna in ionizirajo
Ravnotežja v raztopini TOPILO: komponenta, ki jo je več v raztopini.v analizni kemiji uporabljamo organska in anorganska topila. Topila z veliko dielektrično konstanto (ε > 10) so polarna in ionizirajo
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 14. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 14. november 2013 Kvadratni koren polinoma Funkcijo oblike f(x) = p(x), kjer je p polinom, imenujemo kvadratni koren polinoma
PONOVITEV SNOVI ZA 4. TEST
 PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
PONOVITEV SNOVI ZA 4. TEST 1. * 2. *Galvanski člen z napetostjo 1,5 V požene naboj 40 As. Koliko električnega dela opravi? 3. ** Na uporniku je padec napetosti 25 V. Upornik prejme 750 J dela v 5 minutah.
1. Trikotniki hitrosti
 . Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
. Trikotniki hitrosti. Z radialno črpalko želimo črpati vodo pri pogojih okolice z nazivnim pretokom 0 m 3 /h. Notranji premer rotorja je 4 cm, zunanji premer 8 cm, širina rotorja pa je,5 cm. Frekvenca
u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê
 kemija 1_2.qxd 26.6.2009 7:56 Page 123 y u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê ê } ê ê ê ê ê ê ê ê w ê êr ê ê r ê ê ê 7. 1 Vodne raztopine so v nas in okoli nas Z raztopinami se sre~ujemo vsak dan. Pri
kemija 1_2.qxd 26.6.2009 7:56 Page 123 y u ê ê ê ê ê : ê ê ê } ê ê ê ê ê ê ê ê ê } ê ê ê ê ê ê ê ê w ê êr ê ê r ê ê ê 7. 1 Vodne raztopine so v nas in okoli nas Z raztopinami se sre~ujemo vsak dan. Pri
1. Splošna varnostna priporočila za ravnanje z biološkim materialom. 2. Opredelitev nekaterih kemijskih pojmov
 Splošni del 1. Splošna varnostna priporočila za ravnanje z biološkim materialom Pri ravnanju z biološkim materialom veljajo splošna varnostna priporočila: biološki material je potencialno kužen in nevaren;
Splošni del 1. Splošna varnostna priporočila za ravnanje z biološkim materialom Pri ravnanju z biološkim materialom veljajo splošna varnostna priporočila: biološki material je potencialno kužen in nevaren;
Kontrolne karte uporabljamo za sprotno spremljanje kakovosti izdelka, ki ga izdelujemo v proizvodnem procesu.
 Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Kontrolne karte KONTROLNE KARTE Kontrolne karte uporablamo za sprotno spremlane kakovosti izdelka, ki ga izdeluemo v proizvodnem procesu. Izvaamo stalno vzorčene izdelkov, npr. vsako uro, vsake 4 ure.
Stehiometrija za študente veterine
 Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Univerza v Ljubljani Veterinarska fakulteta Stehiometrija za študente veterine Učbenik s praktičnimi primeri Petra Zrimšek Ljubljana, 01 Petra Zrimšek Stehiometrija za študente veterine Izdajatelj: Univerza
Numerično reševanje. diferencialnih enačb II
 Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
Numerčno reševanje dferencaln enačb I Dferencalne enačbe al ssteme dferencaln enačb rešujemo numerčno z več razlogov:. Ne znamo j rešt analtčno.. Posamezn del dferencalne enačbe podan tabelarčno. 3. Podatke
Kotne in krožne funkcije
 Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
Kotne in krožne funkcije Kotne funkcije v pravokotnem trikotniku Avtor: Rok Kralj, 4.a Gimnazija Vič, 009/10 β a c γ b α sin = a c cos= b c tan = a b cot = b a Sinus kota je razmerje kotu nasprotne katete
Booleova algebra. Izjave in Booleove spremenljivke
 Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
Izjave in Booleove spremenljivke vsako izjavo obravnavamo kot spremenljivko če je izjava resnična (pravilna), ima ta spremenljivka vrednost 1, če je neresnična (nepravilna), pa vrednost 0 pravimo, da gre
VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO
 OSNOVNA ŠOLA PRIMOŽA TRUBARJA LAŠKO VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO (RAZISKOVALNO DELO) Avtorici: Lea Lešek Povšič in
OSNOVNA ŠOLA PRIMOŽA TRUBARJA LAŠKO VPLIV REAKCIJSKIH SPREMENLJIVK NA POTEK IN HITROST MODELNE REAKCIJE NATRIJEVEGA TIOSULFATA S KLOROVODIKOVO KISLINO (RAZISKOVALNO DELO) Avtorici: Lea Lešek Povšič in
KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK
 1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
1 / 24 KODE ZA ODKRIVANJE IN ODPRAVLJANJE NAPAK Štefko Miklavič Univerza na Primorskem MARS, Avgust 2008 Phoenix 2 / 24 Phoenix 3 / 24 Phoenix 4 / 24 Črtna koda 5 / 24 Črtna koda - kontrolni bit 6 / 24
Osnovne stehiometrijske veličine
 Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
Osnovne stehiometrijske veličine Stehiometrija (grško: stoiheion snov, metron merilo) obravnava količinske odnose pri kemijskih reakcijah. Fizikalne veličine, s katerimi kemik najpogosteje izraža količino
2.1. MOLEKULARNA ABSORPCIJSKA SPEKTROMETRIJA
 2.1. MOLEKULARNA ABSORPCJSKA SPEKTROMETRJA Molekularna absorpcijska spektrometrija (kolorimetrija, fotometrija, spektrofotometrija) temelji na merjenju absorpcije svetlobe, ki prehaja skozi preiskovano
2.1. MOLEKULARNA ABSORPCJSKA SPEKTROMETRJA Molekularna absorpcijska spektrometrija (kolorimetrija, fotometrija, spektrofotometrija) temelji na merjenju absorpcije svetlobe, ki prehaja skozi preiskovano
Sladke pijače = sladkorne bombe?
 Sladke pijače = sladkorne bombe? Slika 1:Sladke pijače Slika 2: Žlička sladkorja nad kozarcem vode Modul za poučevanje kemije v 8./9. razredu osnovne šole, raztopine molekulskih spojin. Povzetek Modul
Sladke pijače = sladkorne bombe? Slika 1:Sladke pijače Slika 2: Žlička sladkorja nad kozarcem vode Modul za poučevanje kemije v 8./9. razredu osnovne šole, raztopine molekulskih spojin. Povzetek Modul
matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):
![matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij): matrike A = [a ij ] m,n αa 11 αa 12 αa 1n αa 21 αa 22 αa 2n αa m1 αa m2 αa mn se števanje po komponentah (matriki morata biti enakih dimenzij):](/thumbs/87/96579490.jpg) 4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
4 vaja iz Matematike 2 (VSŠ) avtorica: Melita Hajdinjak datum: Ljubljana, 2009 matrike Matrika dimenzije m n je pravokotna tabela m n števil, ki ima m vrstic in n stolpcev: a 11 a 12 a 1n a 21 a 22 a 2n
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * NAVODILA ZA OCENJEVANJE. Sreda, 3. junij 2015 SPLOŠNA MATURA
 Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
Državni izpitni center *M15143113* SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sreda, 3. junij 2015 SPLOŠNA MATURA RIC 2015 M151-431-1-3 2 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor Naloga Odgovor
IZPIT IZ ANALIZE II Maribor,
 Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Maribor, 05. 02. 200. (a) Naj bo f : [0, 2] R odvedljiva funkcija z lastnostjo f() = f(2). Dokaži, da obstaja tak c (0, ), da je f (c) = 2f (2c). (b) Naj bo f(x) = 3x 3 4x 2 + 2x +. Poišči tak c (0, ),
Odvod. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 10. december Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 10. december 2013 Izrek (Rolleov izrek) Naj bo f : [a,b] R odvedljiva funkcija in naj bo f(a) = f(b). Potem obstaja vsaj ena
SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK
 SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
SKUPNE PORAZDELITVE SKUPNE PORAZDELITVE VEČ SLUČAJNIH SPREMENLJIVK Kovaec vržemo trikrat. Z ozačimo število grbov ri rvem metu ( ali ), z Y a skuo število grbov (,, ali 3). Kako sta sremelivki i Y odvisi
MATEMATIČNI IZRAZI V MAFIRA WIKIJU
 I FAKULTETA ZA MATEMATIKO IN FIZIKO Jadranska cesta 19 1000 Ljubljan Ljubljana, 25. marec 2011 MATEMATIČNI IZRAZI V MAFIRA WIKIJU KOMUNICIRANJE V MATEMATIKI Darja Celcer II KAZALO: 1 VSTAVLJANJE MATEMATIČNIH
I FAKULTETA ZA MATEMATIKO IN FIZIKO Jadranska cesta 19 1000 Ljubljan Ljubljana, 25. marec 2011 MATEMATIČNI IZRAZI V MAFIRA WIKIJU KOMUNICIRANJE V MATEMATIKI Darja Celcer II KAZALO: 1 VSTAVLJANJE MATEMATIČNIH
SEMINAR IZ KOLEGIJA ANALITIČKA KEMIJA I. Studij Primijenjena kemija
 SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
SEMINAR IZ OLEGIJA ANALITIČA EMIJA I Studij Primijenjena kemija 1. 0,1 mola NaOH je dodano 1 litri čiste vode. Izračunajte ph tako nastale otopine. NaOH 0,1 M NaOH Na OH Jak elektrolit!!! Disoira potpuno!!!
KEMIJA PRVEGA LETNIKA
 KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
KEMIJA naravoslovna znanost oz. veda, ki proučuje zakonitosti v naravi družboslovje proučuje zakonitosti v medčloveških odnosih matematika je veda, ki služi kot pripomoček k drugim naravoslovnim in družboslovnim
SEKUNDARNE VEZE međumolekulske veze
 PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
PRIMARNE VEZE hemijske veze među atomima SEKUNDARNE VEZE međumolekulske veze - Slabije od primarnih - Elektrostatičkog karaktera - Imaju veliki uticaj na svojstva supstanci: - agregatno stanje - temperatura
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih
 Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
Homogena snov je snov, ki ima vsepovsod enake lastnosti in sestavo Heterogena snov je snov, katere sestava in lastnosti so na različnih mestih različne Postopki ločevanja zmesi:iz zmesi je mogoče ločiti
[ ]... je oznaka za koncentracijo
![[ ]... je oznaka za koncentracijo [ ]... je oznaka za koncentracijo](/thumbs/62/48148191.jpg) 9. Vaja: Elektrolitska disociacija a) Osnove: Elektroliti so snovi, ki prevajajo električni tok; to so raztopine kislin, baz in soli. Elektrolitska disociacija je razpad elektrolita na ione. Stopnja elektrolitske
9. Vaja: Elektrolitska disociacija a) Osnove: Elektroliti so snovi, ki prevajajo električni tok; to so raztopine kislin, baz in soli. Elektrolitska disociacija je razpad elektrolita na ione. Stopnja elektrolitske
Raztopine. Raztopine. Elektroliti. Elektrolit je substanca, ki pri raztapljanju (v vodi) daje ione. A a B b aa b+ + bb a-
 Raztopine Mnoge analizne metode temeljijo na opazovanju ravnotežnih sistemov, ki se vzpostavijo v raztopinah. Najpogosteje uporabljeno topilo je voda! RAZTOPINE: topljenec topilo (voda) (Enote za koncentracije!)
Raztopine Mnoge analizne metode temeljijo na opazovanju ravnotežnih sistemov, ki se vzpostavijo v raztopinah. Najpogosteje uporabljeno topilo je voda! RAZTOPINE: topljenec topilo (voda) (Enote za koncentracije!)
Zaporedja. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 15. oktober Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 15. oktober 2013 Oglejmo si, kako množimo dve kompleksni števili, dani v polarni obliki. Naj bo z 1 = r 1 (cosϕ 1 +isinϕ 1 )
Osnove elektrotehnike uvod
 Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
Osnove elektrotehnike uvod Uvod V nadaljevanju navedena vprašanja so prevod testnih vprašanj, ki sem jih našel na omenjeni spletni strani. Vprašanja zajemajo temeljna znanja opredeljenega strokovnega področja.
1. Definicijsko območje, zaloga vrednosti. 2. Naraščanje in padanje, ekstremi. 3. Ukrivljenost. 4. Trend na robu definicijskega območja
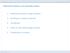 ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
ZNAČILNOSTI FUNKCIJ ZNAČILNOSTI FUNKCIJE, KI SO RAZVIDNE IZ GRAFA. Deinicijsko območje, zaloga vrednosti. Naraščanje in padanje, ekstremi 3. Ukrivljenost 4. Trend na robu deinicijskega območja 5. Periodičnost
Kotni funkciji sinus in kosinus
 Kotni funkciji sinus in kosinus Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z oznako cos x, DEFINICIJA V PRAVOKOTNEM TRIKOTNIKU: Kotna funkcija sinus je definirana kot razmerje
Kotni funkciji sinus in kosinus Oznake: sinus kota x označujemo z oznako sin x, kosinus kota x označujemo z oznako cos x, DEFINICIJA V PRAVOKOTNEM TRIKOTNIKU: Kotna funkcija sinus je definirana kot razmerje
KEMIJA ZA GIMNAZIJE 1
 Nataša Bukovec KEMIJA ZA GIMNAZIJE 1 Zbirka nalog za 1. letnik gimnazij VSEBINA Predgovor 1. VARN DEL V KEMIJSKEM LABRATRIJU 5 Laboratorijski inventar 5 Znaki za nevarnost opozorilne besede stavki o nevarnosti
Nataša Bukovec KEMIJA ZA GIMNAZIJE 1 Zbirka nalog za 1. letnik gimnazij VSEBINA Predgovor 1. VARN DEL V KEMIJSKEM LABRATRIJU 5 Laboratorijski inventar 5 Znaki za nevarnost opozorilne besede stavki o nevarnosti
2 VAJA: POVRŠINSKO AKTIVNE SNOVI IN KRITIČNA MICELSKA KONCENTRACIJA
 MEDFAZNA NAPETOST IN MOČENJE 2 VAJA: POVRŠINSKO AKTIVNE SNOVI IN KRITIČNA MICELSKA KONCENTRACIJA 2.1 Površinska in medfazna napetost Vsako molekulo v tekočini privlačijo sosednje molekule in rezultante
MEDFAZNA NAPETOST IN MOČENJE 2 VAJA: POVRŠINSKO AKTIVNE SNOVI IN KRITIČNA MICELSKA KONCENTRACIJA 2.1 Površinska in medfazna napetost Vsako molekulo v tekočini privlačijo sosednje molekule in rezultante
Molekule. Za vodik dobimo gostoto 0,09 g/dm 3, za kisik 1,43 g/dm 3 in za ogljikov oksid 2,00 g/dm 3. Merilni balon
 23 Molekule Tehtanje plinov Reakcijska razmerja Molekule v plinih Molekule v gosti snovi Valenca atomov Velikost molekul Kilomol in kilomolska masa Splošna plinska konstanta Raztopine Osmozni tlak Reakcijske
23 Molekule Tehtanje plinov Reakcijska razmerja Molekule v plinih Molekule v gosti snovi Valenca atomov Velikost molekul Kilomol in kilomolska masa Splošna plinska konstanta Raztopine Osmozni tlak Reakcijske
KOLI»INSKI ODNOSI. Kemik mora vedeti, koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane.
 KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
KOLI»INSKI ODNOSI Kemik mora vedeti koliko snovi pri kemijski reakciji zreagira in koliko snovi nastane 4 Mase atomov in molekul 42 tevilo delcev masa in mnoæina snovi 43 RaËunajmo maso mnoæino in πtevilo
Energije in okolje 1. vaja. Entalpija pri kemijskih reakcijah
 Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
Entalpija pri kemijskih reakcijah Pri obravnavi energijskih pretvorb pri kemijskih reakcijah uvedemo pojem entalpije, ki popisuje spreminjanje energije sistema pri konstantnem tlaku. Sistemu lahko povečamo
13. Vaja: Reakcije oksidacije in redukcije
 1. Vaja: Reakcije oksidacije in redukcije a) Osnove: Oksidacija je reakcija pri kateri posamezen element (reducent) oddaja elektrone in se pri tem oksidira (oksidacijsko število se zviša). Redukcija pa
1. Vaja: Reakcije oksidacije in redukcije a) Osnove: Oksidacija je reakcija pri kateri posamezen element (reducent) oddaja elektrone in se pri tem oksidira (oksidacijsko število se zviša). Redukcija pa
8. Diskretni LTI sistemi
 8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
8. Diskreti LI sistemi. Naloga Določite odziv diskretega LI sistema s podaim odzivom a eoti impulz, a podai vhodi sigal. h[] x[] - - 5 6 7 - - 5 6 7 LI sistem se a vsak eoti impulz δ[] a vhodu odzove z
Funkcije. Matematika 1. Gregor Dolinar. Fakulteta za elektrotehniko Univerza v Ljubljani. 12. november Gregor Dolinar Matematika 1
 Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 12. november 2013 Graf funkcije f : D R, D R, je množica Γ(f) = {(x,f(x)) : x D} R R, torej podmnožica ravnine R 2. Grafi funkcij,
Matematika 1 Gregor Dolinar Fakulteta za elektrotehniko Univerza v Ljubljani 12. november 2013 Graf funkcije f : D R, D R, je množica Γ(f) = {(x,f(x)) : x D} R R, torej podmnožica ravnine R 2. Grafi funkcij,
MODERIRANA RAZLIČICA
 Dr`avni izpitni center *N07143132* REDNI ROK KEMIJA PREIZKUS ZNANJA Maj 2007 NAVODILA ZA VREDNOTENJE NACIONALNO PREVERJANJE ZNANJA b kncu 3. bdbja MODERIRANA RAZLIČICA RIC 2007 2 N071-431-3-2 NAVODILA
Dr`avni izpitni center *N07143132* REDNI ROK KEMIJA PREIZKUS ZNANJA Maj 2007 NAVODILA ZA VREDNOTENJE NACIONALNO PREVERJANJE ZNANJA b kncu 3. bdbja MODERIRANA RAZLIČICA RIC 2007 2 N071-431-3-2 NAVODILA
BRONASTE PREGLOVE PLAKETE
 ŠOLSKO TEKMOVNJE IZ ZNNJ KEMIJE Z RONSTE PREGLOVE PLKETE Tekmovalna pola za. letnik. marec 08 Pred vami je deset tekmovalnih nalog, ki so različnega tipa. Pri reševanju lahko uporabljajte le priložen periodni
ŠOLSKO TEKMOVNJE IZ ZNNJ KEMIJE Z RONSTE PREGLOVE PLKETE Tekmovalna pola za. letnik. marec 08 Pred vami je deset tekmovalnih nalog, ki so različnega tipa. Pri reševanju lahko uporabljajte le priložen periodni
Delovna točka in napajalna vezja bipolarnih tranzistorjev
 KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
KOM L: - Komnikacijska elektronika Delovna točka in napajalna vezja bipolarnih tranzistorjev. Določite izraz za kolektorski tok in napetost napajalnega vezja z enim virom in napetostnim delilnikom na vhod.
vaja Izolacija kromosomske DNA iz vranice in hiperkromni efekt. DNA RNA Protein. ime deoksirbonukleinska kislina ribonukleinska kislina
 transkripcija translacija Protein 12. vaja Izolacija kromosomske iz vranice in hiperkromni efekt sladkorji deoksiriboza riboza glavna funkcija dolgoročno shranjevanje genetskih informacij prenos informacij
transkripcija translacija Protein 12. vaja Izolacija kromosomske iz vranice in hiperkromni efekt sladkorji deoksiriboza riboza glavna funkcija dolgoročno shranjevanje genetskih informacij prenos informacij
NEPARAMETRIČNI TESTI. pregledovanje tabel hi-kvadrat test. as. dr. Nino RODE
 NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
NEPARAMETRIČNI TESTI pregledovanje tabel hi-kvadrat test as. dr. Nino RODE Parametrični in neparametrični testi S pomočjo z-testa in t-testa preizkušamo domneve o parametrih na vzorcih izračunamo statistike,
Katedra za farmacevtsko kemijo. Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks. 25/11/2010 Vaje iz Farmacevtske kemije 3 1
 Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
Katedra za farmacevtsko kemijo Sinteza mimetika encima SOD 2. stopnja: Mn 3+ ali Cu 2+ salen kompleks 25/11/2010 Vaje iz Farmacevtske kemije 3 1 Sinteza kompleksa [Mn 3+ (salen)oac] Zakaj uporabljamo brezvodni
KISLINE IN BAZE ARRHENIUSOVA DEFINICIJA KISLIN IN BAZ
 6. KISLINE IN BAZE KISLINE IN BAZE ARRHENIUSOVA DEFINICIJA KISLIN IN BAZ kisline so snovi, ki v vodni raztopini disocirajo vodikove ione (H + ), baze pa snovi, ki v vodni raztopini disocirajo hidroksidne
6. KISLINE IN BAZE KISLINE IN BAZE ARRHENIUSOVA DEFINICIJA KISLIN IN BAZ kisline so snovi, ki v vodni raztopini disocirajo vodikove ione (H + ), baze pa snovi, ki v vodni raztopini disocirajo hidroksidne
Sestava topil Topila s šibkimi vodikovimi vezmi:
 TOPILA Večina premazov vsebuje hlapne komponente, ki izhlapijo tekom aplikacije (nanosa) in nastanka filma. Hlapne komponente premaza s skupnim imenom imenujemo topila, kljub temu, da se smola v določenih
TOPILA Večina premazov vsebuje hlapne komponente, ki izhlapijo tekom aplikacije (nanosa) in nastanka filma. Hlapne komponente premaza s skupnim imenom imenujemo topila, kljub temu, da se smola v določenih
REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI. Marjeta Prašnikar
 REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI Andrej Nika Cebin Godec Manica Ivan Perdan Leban - Ocepek Marjeta Prašnikar 2 Rešitve VARNO EKSPERIMENTALNO DELO Kemija je eksperimentalna veda (str. 8)
REŠITVE LABORATORIJSKE VAJE ZA KEMIJO V GIMNAZIJI Andrej Nika Cebin Godec Manica Ivan Perdan Leban - Ocepek Marjeta Prašnikar 2 Rešitve VARNO EKSPERIMENTALNO DELO Kemija je eksperimentalna veda (str. 8)
Aleš Mrhar. kinetični ni vidiki. Izraženo s hitrostjo in maso, dx/dt očistkom
 Izločanje zdravilnih učinkovin u iz telesa: kinetični ni vidiki Biofarmacija s farmakokinetiko Univerzitetni program Farmacija Aleš Mrhar Izločanje učinkovinu Izraženo s hitrostjo in maso, dx/ k e U očistkom
Izločanje zdravilnih učinkovin u iz telesa: kinetični ni vidiki Biofarmacija s farmakokinetiko Univerzitetni program Farmacija Aleš Mrhar Izločanje učinkovinu Izraženo s hitrostjo in maso, dx/ k e U očistkom
Fazni diagram binarne tekočine
 Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
Fazni diagram binarne tekočine Žiga Kos 5. junij 203 Binarno tekočino predstavljajo delci A in B. Ti se med seboj lahko mešajo v različnih razmerjih. V nalogi želimo izračunati fazni diagram take tekočine,
Enačba, v kateri poleg neznane funkcije neodvisnih spremenljivk ter konstant nastopajo tudi njeni odvodi, se imenuje diferencialna enačba.
 1. Osnovni pojmi Enačba, v kateri poleg neznane funkcije neodvisnih spremenljivk ter konstant nastopajo tudi njeni odvodi, se imenuje diferencialna enačba. Primer 1.1: Diferencialne enačbe so izrazi: y
1. Osnovni pojmi Enačba, v kateri poleg neznane funkcije neodvisnih spremenljivk ter konstant nastopajo tudi njeni odvodi, se imenuje diferencialna enačba. Primer 1.1: Diferencialne enačbe so izrazi: y
UPOR NA PADANJE SONDE V ZRAKU
 UPOR NA PADANJE SONDE V ZRAKU 1. Hitrost in opravljena pot sonde pri padanju v zraku Za padanje v zraku je odgovorna sila teže. Poleg sile teže na padajoče telo deluje tudi sila vzgona, ki je enaka teži
UPOR NA PADANJE SONDE V ZRAKU 1. Hitrost in opravljena pot sonde pri padanju v zraku Za padanje v zraku je odgovorna sila teže. Poleg sile teže na padajoče telo deluje tudi sila vzgona, ki je enaka teži
0,00275 cm3 = = 0,35 cm = 3,5 mm.
 1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
1. Za koliko se bo dvignil alkohol v cevki termometra s premerom 1 mm, če se segreje za 5 stopinj? Prostorninski temperaturni razteznostni koeficient alkohola je 11 10 4 K 1. Volumen alkohola v termometru
KISLINE, BAZE IN SOLI
 KISLINE, BAZE IN SOLI Kako prepoznamo kisline in baze, zakaj so te snovi tako pomembne snovi in kakπne so njihove reakcije? 1.1 Kje vse najdemo kisline in baze? 1.2 Kako razlikujemo kisle in baziëne vodne
KISLINE, BAZE IN SOLI Kako prepoznamo kisline in baze, zakaj so te snovi tako pomembne snovi in kakπne so njihove reakcije? 1.1 Kje vse najdemo kisline in baze? 1.2 Kako razlikujemo kisle in baziëne vodne
Gimnazija Krˇsko. vektorji - naloge
 Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Vektorji Naloge 1. V koordinatnem sistemu so podane točke A(3, 4), B(0, 2), C( 3, 2). a) Izračunaj dolžino krajevnega vektorja točke A. (2) b) Izračunaj kot med vektorjema r A in r C. (4) c) Izrazi vektor
Termodinamika vlažnega zraka. stanja in spremembe
 Termodinamika vlažnega zraka stanja in spremembe Termodinamika vlažnega zraka Najpogostejši medij v sušilnih procesih konvektivnega sušenja je VLAŽEN ZRAK Obravnavamo ga kot dvokomponentno zmes Suhi zrak
Termodinamika vlažnega zraka stanja in spremembe Termodinamika vlažnega zraka Najpogostejši medij v sušilnih procesih konvektivnega sušenja je VLAŽEN ZRAK Obravnavamo ga kot dvokomponentno zmes Suhi zrak
Mojca Slemnik POSKUSI V FIZIKALNI KEMIJI. zbrano gradivo, zbirka vaj
 Mojca Slemnik POSKUSI V FIZIKALNI KEMIJI zbrano gradivo, zbirka vaj Maribor, februar 2014 Mojca Slemnik, Poskusi v fizikalni kemiji Avtor: Vrsta publikacije: Založnik: Naklada: Dostopno: Doc. dr. Mojca
Mojca Slemnik POSKUSI V FIZIKALNI KEMIJI zbrano gradivo, zbirka vaj Maribor, februar 2014 Mojca Slemnik, Poskusi v fizikalni kemiji Avtor: Vrsta publikacije: Založnik: Naklada: Dostopno: Doc. dr. Mojca
Matematika 2. Diferencialne enačbe drugega reda
 Matematika 2 Diferencialne enačbe drugega reda (1) Reši homogene diferencialne enačbe drugega reda s konstantnimi koeficienti: (a) y 6y + 8y = 0, (b) y 2y + y = 0, (c) y + y = 0, (d) y + 2y + 2y = 0. Rešitev:
Matematika 2 Diferencialne enačbe drugega reda (1) Reši homogene diferencialne enačbe drugega reda s konstantnimi koeficienti: (a) y 6y + 8y = 0, (b) y 2y + y = 0, (c) y + y = 0, (d) y + 2y + 2y = 0. Rešitev:
H = E + PV ( 1 ) de = TdS - PdV ( 3 ) G = H - TS ( 4 ) G = E + PV - TS ( diferenciranje ) ( 5 ) dg = VdP - SdT ( 8 )
 H E + PV ( 1 ) de dq - PdV ( ds dq / T ) ( ) de TdS - PdV ( 3 ) G H - TS ( 4 ) G E + PV - TS ( difereciraje ) ( 5 ) dg de + PdV + VdP TdS SdT ( 6 ) upoštevamo eačbo ( 3 ): dg TdS-PdV+ PdV+ VdP-TdS-SdT
H E + PV ( 1 ) de dq - PdV ( ds dq / T ) ( ) de TdS - PdV ( 3 ) G H - TS ( 4 ) G E + PV - TS ( difereciraje ) ( 5 ) dg de + PdV + VdP TdS SdT ( 6 ) upoštevamo eačbo ( 3 ): dg TdS-PdV+ PdV+ VdP-TdS-SdT
DISKRETNA FOURIERJEVA TRANSFORMACIJA
 29.03.2004 Definicija DFT Outline DFT je linearna transformacija nekega vektorskega prostora dimenzije n nad obsegom K, ki ga označujemo z V K, pri čemer ima slednji lastnost, da vsebuje nek poseben element,
29.03.2004 Definicija DFT Outline DFT je linearna transformacija nekega vektorskega prostora dimenzije n nad obsegom K, ki ga označujemo z V K, pri čemer ima slednji lastnost, da vsebuje nek poseben element,
Srednja šola za gostinstvo in turizem v Ljubljani NARAVOSLOVJE I
 Srednja šola za gostinstvo in turizem v Ljubljani NARAVOSLOVJE I Interno nelektorirano gradivo Izobraževanje odraslih Gastronomske in hotelske storitve (1. letnik) Pripravil: Jernej Grdun, prof Ljubljana,
Srednja šola za gostinstvo in turizem v Ljubljani NARAVOSLOVJE I Interno nelektorirano gradivo Izobraževanje odraslih Gastronomske in hotelske storitve (1. letnik) Pripravil: Jernej Grdun, prof Ljubljana,
p 1 ENTROPIJSKI ZAKON
 ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
ENROPIJSKI ZAKON REERZIBILNA srememba: moža je obrjea srememba reko eakih vmesih staj kot rvota srememba. Po obeh sremembah e sme biti obeih trajih srememb v bližji i dalji okolici. IREERZIBILNA srememba:
Talna kemija. Kaj je potrebno poznati:
 Talna kemija Kaj je potrebno poznati: splošno kemijo mol, molaren, normalnost, ekvivalent ionska jakost, aktivnost ravnotežne konstante funkcionalne skupine hidratacija, hidroliza redoks reakcije Redoks
Talna kemija Kaj je potrebno poznati: splošno kemijo mol, molaren, normalnost, ekvivalent ionska jakost, aktivnost ravnotežne konstante funkcionalne skupine hidratacija, hidroliza redoks reakcije Redoks
vaja Kvan*ta*vno določanje proteinov. 6. vaja Kvan*ta*vno določanje proteinov. 6. vaja Kvan*ta*vno določanje proteinov
 28. 3. 11 UV- spektrofotometrija Biuretska metoda Absorbanca pri λ=28 nm (A28) UV- spektrofotometrija Biuretska metoda vstopni žarek intenziteta I Lowrijeva metoda Bradfordova metoda Bradfordova metoda
28. 3. 11 UV- spektrofotometrija Biuretska metoda Absorbanca pri λ=28 nm (A28) UV- spektrofotometrija Biuretska metoda vstopni žarek intenziteta I Lowrijeva metoda Bradfordova metoda Bradfordova metoda
ODGOVORI NA VPRAŠANJA V UČBENIKU. Margareta Vrtačnik Katarina S. Wissiak Grm Saša A. Glažar Andrej Godec
 ODGOVORI NA VPRAŠANJA V UČBENIKU Margareta Vrtačnik Katarina S. Wissiak Grm Saša A. Glažar Andrej Godec 1. KAJ JE KEMIJA KEMIJA JE EKSPERIMENTALNA VEDA (str. 14) 1. Kemija je nauk o snovi in njenih spremembah.
ODGOVORI NA VPRAŠANJA V UČBENIKU Margareta Vrtačnik Katarina S. Wissiak Grm Saša A. Glažar Andrej Godec 1. KAJ JE KEMIJA KEMIJA JE EKSPERIMENTALNA VEDA (str. 14) 1. Kemija je nauk o snovi in njenih spremembah.
Podobnost matrik. Matematika II (FKKT Kemijsko inženirstvo) Diagonalizacija matrik
 Podobnost matrik Matematika II (FKKT Kemijsko inženirstvo) Matjaž Željko FKKT Kemijsko inženirstvo 14 teden (Zadnja sprememba: 23 maj 213) Matrika A R n n je podobna matriki B R n n, če obstaja obrnljiva
Podobnost matrik Matematika II (FKKT Kemijsko inženirstvo) Matjaž Željko FKKT Kemijsko inženirstvo 14 teden (Zadnja sprememba: 23 maj 213) Matrika A R n n je podobna matriki B R n n, če obstaja obrnljiva
Kvantni delec na potencialnem skoku
 Kvantni delec na potencialnem skoku Delec, ki se giblje premo enakomerno, pride na mejo, kjer potencial naraste s potenciala 0 na potencial. Takšno potencialno funkcijo zapišemo kot 0, 0 0,0. Slika 1:
Kvantni delec na potencialnem skoku Delec, ki se giblje premo enakomerno, pride na mejo, kjer potencial naraste s potenciala 0 na potencial. Takšno potencialno funkcijo zapišemo kot 0, 0 0,0. Slika 1:
ZAKLJUČNI PROCESI V BIOTEHNOLOGIJI. Membranski separacijski procesi: diafiltracija, elektrodializa, reverzna osmoza, pervaporacija
 ZAKLJUČNI PROCESI V BIOTEHNOLOGIJI Membranski separacijski procesi: diafiltracija, elektrodializa, reverzna osmoza, pervaporacija Membranski separacijski procesi v biotehnologiji proces mikrofiltracija
ZAKLJUČNI PROCESI V BIOTEHNOLOGIJI Membranski separacijski procesi: diafiltracija, elektrodializa, reverzna osmoza, pervaporacija Membranski separacijski procesi v biotehnologiji proces mikrofiltracija
IZZIVI DRUŽINSKE MEDICINE. U no gradivo zbornik seminarjev
 IZZIVI DRUŽINSKE MEDICINE Uno gradivo zbornik seminarjev študentov Medicinske fakultete Univerze v Mariboru 4. letnik 2008/2009 Uredniki: Alenka Bizjak, Viktorija Janar, Maša Krajnc, Jasmina Rehar, Mateja
IZZIVI DRUŽINSKE MEDICINE Uno gradivo zbornik seminarjev študentov Medicinske fakultete Univerze v Mariboru 4. letnik 2008/2009 Uredniki: Alenka Bizjak, Viktorija Janar, Maša Krajnc, Jasmina Rehar, Mateja
IZVODI ZADACI (I deo)
 IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
IZVODI ZADACI (I deo) Najpre da se podsetimo tablice i osnovnih pravila:. C`=0. `=. ( )`= 4. ( n )`=n n-. (a )`=a lna 6. (e )`=e 7. (log a )`= 8. (ln)`= ` ln a (>0) 9. = ( 0) 0. `= (>0) (ovde je >0 i a
Tekočinska kromatografija
 Tekočinska kromatografija Kromatografske tehnike uporabljamo za ločevanje posameznih komponent v vzorcu. Ločitev temelji na različnem porazdeljevanju komponent med stacionarno fazo, ki se nahaja v kromatografski
Tekočinska kromatografija Kromatografske tehnike uporabljamo za ločevanje posameznih komponent v vzorcu. Ločitev temelji na različnem porazdeljevanju komponent med stacionarno fazo, ki se nahaja v kromatografski
RANKINOV KROŽNI PROCES Seminar za predmet JTE
 RANKINOV KROŽNI PROCES Seminar za predmet JTE Rok Krpan 16.12.2010 Mentor: izr. prof. Iztok Tiselj Carnotov krožni proces Iz štirih sprememb: dveh izotermnih in dveh izentropnih (reverzibilnih adiabatnih)
RANKINOV KROŽNI PROCES Seminar za predmet JTE Rok Krpan 16.12.2010 Mentor: izr. prof. Iztok Tiselj Carnotov krožni proces Iz štirih sprememb: dveh izotermnih in dveh izentropnih (reverzibilnih adiabatnih)
*M * Osnovna in višja raven MATEMATIKA NAVODILA ZA OCENJEVANJE. Sobota, 4. junij 2011 SPOMLADANSKI IZPITNI ROK. Državni izpitni center
 Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Državni izpitni center *M40* Osnovna in višja raven MATEMATIKA SPOMLADANSKI IZPITNI ROK NAVODILA ZA OCENJEVANJE Sobota, 4. junij 0 SPLOŠNA MATURA RIC 0 M-40-- IZPITNA POLA OSNOVNA IN VIŠJA RAVEN 0. Skupaj:
Izločanje zdravilnih učinkovin iz telesa:
 Izločanje zdravilnih učinkovin iz telesa: kinetični vidiki Biofarmacija s farmakokinetiko Aleš Mrhar Izločanje učinkovin Izraženo s hitrostjo in maso, dx/dt = k e U očistkom in volumnom, Cl = k e V Hitrost
Izločanje zdravilnih učinkovin iz telesa: kinetični vidiki Biofarmacija s farmakokinetiko Aleš Mrhar Izločanje učinkovin Izraženo s hitrostjo in maso, dx/dt = k e U očistkom in volumnom, Cl = k e V Hitrost
fosfat fosfat H deoksiriboza H O KEMIJA Z BIOKEMIJO učbenik za študente visokošolskega strokovnega študija kmetijstva
 Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
Cl Cl Na + Cl Na + Na + Cl Na + O H H Cl Cl O H H Na + O H H fosfat H deoksiriboza N C N fosfat H H N C C C N N C H H O H C C C N N C N deoksiriboza CH 3 C O C N O C C N fosfat H deoksiriboza H H N C H
VAJE IZ KEMIJE. Zbirka računskih nalog. za študente Fizikalne merilne tehnike
 VAJE IZ KEMIJE Zbirka računskih nalog za študente Fizikalne erilne tehnike Šolsko leto 008/009 MERSKE ENOTE Osnovne fizikalne veličine SI (International Syste of Units, ednarodni siste erskih enot) Ie
VAJE IZ KEMIJE Zbirka računskih nalog za študente Fizikalne erilne tehnike Šolsko leto 008/009 MERSKE ENOTE Osnovne fizikalne veličine SI (International Syste of Units, ednarodni siste erskih enot) Ie
Državni izpitni center SPOMLADANSKI IZPITNI ROK *M * FIZIKA NAVODILA ZA OCENJEVANJE. Petek, 10. junij 2016 SPLOŠNA MATURA
 Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
Državni izpitni center *M16141113* SPOMLADANSKI IZPITNI ROK FIZIKA NAVODILA ZA OCENJEVANJE Petek, 1. junij 16 SPLOŠNA MATURA RIC 16 M161-411-3 M161-411-3 3 IZPITNA POLA 1 Naloga Odgovor Naloga Odgovor
Poglavje 7. Poglavje 7. Poglavje 7. Regulacijski sistemi. Regulacijski sistemi. Slika 7. 1: Normirana blokovna shema regulacije EM
 Slika 7. 1: Normirana blokovna shema regulacije EM Fakulteta za elektrotehniko 1 Slika 7. 2: Principielna shema regulacije AM v KSP Fakulteta za elektrotehniko 2 Slika 7. 3: Merjenje komponent fluksa s
Slika 7. 1: Normirana blokovna shema regulacije EM Fakulteta za elektrotehniko 1 Slika 7. 2: Principielna shema regulacije AM v KSP Fakulteta za elektrotehniko 2 Slika 7. 3: Merjenje komponent fluksa s
13. poglavje: Energija
 13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
13. poglavje: Energija 1. (Naloga 3) Koliko kilovatna je peč za hišno centralno kurjavo, ki daje 126 MJ toplote na uro? Podatki: Q = 126 MJ, t = 3600 s; P =? Če peč z močjo P enakomerno oddaja toploto,
IZVODI ZADACI ( IV deo) Rešenje: Najpre ćemo logaritmovati ovu jednakost sa ln ( to beše prirodni logaritam za osnovu e) a zatim ćemo
 IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
IZVODI ZADACI ( IV deo) LOGARITAMSKI IZVOD Logariamskim izvodom funkcije f(), gde je >0 i, nazivamo izvod logarima e funkcije, o jes: (ln ) f ( ) f ( ) Primer. Nadji izvod funkcije Najpre ćemo logarimovai
MERITVE LABORATORIJSKE VAJE. Študij. leto: 2011/2012 UNIVERZA V MARIBORU. Skupina: 9
 .cwww.grgor nik ol i c NVERZA V MARBOR FAKTETA ZA EEKTROTEHNKO, RAČNANŠTVO N NFORMATKO 2000 Maribor, Smtanova ul. 17 Študij. lto: 2011/2012 Skupina: 9 MERTVE ABORATORJSKE VAJE Vaja št.: 4.1 Določanj induktivnosti
.cwww.grgor nik ol i c NVERZA V MARBOR FAKTETA ZA EEKTROTEHNKO, RAČNANŠTVO N NFORMATKO 2000 Maribor, Smtanova ul. 17 Študij. lto: 2011/2012 Skupina: 9 MERTVE ABORATORJSKE VAJE Vaja št.: 4.1 Določanj induktivnosti
Bojan Božič, Jure Derganc, Gregor Gomišček, Vera Kralj-Iglič, Janja Majhenc, Mojca Mally, Praktikum iz biofizike Študijsko leto 2017/2018
 Bojan Božič, Jure Derganc, Gregor Gomišček, Vera Kralj-Iglič, Janja Majhenc, Mojca Mally, Primož Peterlin, Saša Svetina in Boštjan Žekš Praktikum iz biofizike Študijsko leto 2017/2018 Ljubljana, oktober
Bojan Božič, Jure Derganc, Gregor Gomišček, Vera Kralj-Iglič, Janja Majhenc, Mojca Mally, Primož Peterlin, Saša Svetina in Boštjan Žekš Praktikum iz biofizike Študijsko leto 2017/2018 Ljubljana, oktober
Za šolsko leto 2008/2009 bosta še naprej na razpolago zbirki»fluor ni flour«in»anenin«.
 Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim načrtom. Urejena je v osem poglavij (Varno eksperimentalno
Zbirka nalog Kemijo razumem, kemijo znam 1 je namenjena dijakom 1. letnika gimnazije in drugih srednjih šol ter je v celoti usklajena z novim učnim načrtom. Urejena je v osem poglavij (Varno eksperimentalno
Ponovi in utrdi svoje znanje Rešitve
 1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
1. poglavje: Kakšne so lastnosti vode? 10. Ni dosežena, saj podgana zaužije 188,8 mg/kg. 11. LD 50 = 0,480 mg/kg 2. poglavje: Kaj je največje čudo na Zemlji? 5. Edini stabilni izotop natrija ima masno
ANORGANSKI PRAKTIKUM
 ANORGANSKI PRAKTIKUM Odgovori na izpitna vprašanja Kemijska tehnologija 2014/2015 Koordinacijske spojine. Preparati. Priprava bakrovega (I) klorida. Priprava kalijevega heksaizotiocianatokromata(iii).
ANORGANSKI PRAKTIKUM Odgovori na izpitna vprašanja Kemijska tehnologija 2014/2015 Koordinacijske spojine. Preparati. Priprava bakrovega (I) klorida. Priprava kalijevega heksaizotiocianatokromata(iii).
CM707. GR Οδηγός χρήσης... 2-7. SLO Uporabniški priročnik... 8-13. CR Korisnički priručnik... 14-19. TR Kullanım Kılavuzu... 20-25
 1 2 3 4 5 6 7 OFFMANAUTO CM707 GR Οδηγός χρήσης... 2-7 SLO Uporabniški priročnik... 8-13 CR Korisnički priručnik... 14-19 TR Kullanım Kılavuzu... 20-25 ENG User Guide... 26-31 GR CM707 ΟΔΗΓΟΣ ΧΡΗΣΗΣ Περιγραφή
1 2 3 4 5 6 7 OFFMANAUTO CM707 GR Οδηγός χρήσης... 2-7 SLO Uporabniški priročnik... 8-13 CR Korisnički priručnik... 14-19 TR Kullanım Kılavuzu... 20-25 ENG User Guide... 26-31 GR CM707 ΟΔΗΓΟΣ ΧΡΗΣΗΣ Περιγραφή
S t r a n a 1. 1.Povezati jonsku jačinu rastvora: a) MgCl 2 b) Al 2 (SO 4 ) 3 sa njihovim molalitetima, m. za so tipa: M p X q. pa je jonska jačina:
 S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
S t r a n a 1 1.Povezati jonsku jačinu rastvora: a MgCl b Al (SO 4 3 sa njihovim molalitetima, m za so tipa: M p X q pa je jonska jačina:. Izračunati mase; akno 3 bba(no 3 koje bi trebalo dodati, 0,110
a) Kateri tip hibridnih orbital na klorovem atomu uporabimo? a) Kateri tip hibridnih orbital na fosforjevem atomu uporabimo?
 76. Narišite strukturo karbonatnega iona. Upoštevajte dejstvo, da so vse vezi enako dolge. Kateri tip hibridizacije na ogljikovem atomu moramo uporabiti? Ogljik je element 4. skupine. a) sp 2 b) sp 3 c)
76. Narišite strukturo karbonatnega iona. Upoštevajte dejstvo, da so vse vezi enako dolge. Kateri tip hibridizacije na ogljikovem atomu moramo uporabiti? Ogljik je element 4. skupine. a) sp 2 b) sp 3 c)
V kristalu so atomi, ioni ali molekule geometrijsko urejeni po povsem določeni zakonitosti.
 3. KRISTALI IN KRISTALITI Večina trdnih snovi je v kristalnem stanju. V splošnem lahko rečemo, da so kristali periodična prostorska razporeditev atomov, molekul in ionov. V poljubni smeri kristala so enaki
3. KRISTALI IN KRISTALITI Večina trdnih snovi je v kristalnem stanju. V splošnem lahko rečemo, da so kristali periodična prostorska razporeditev atomov, molekul in ionov. V poljubni smeri kristala so enaki
Eliminacijski zadatak iz Matematike 1 za kemičare
 Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
Za mnoge reakcije vrijedi Arrheniusova jednadžba, koja opisuje vezu koeficijenta brzine reakcije i temperature: K = Ae Ea/(RT ). - T termodinamička temperatura (u K), - R = 8, 3145 J K 1 mol 1 opća plinska
