ΠΑΡΑΡΤΗΜΑ III ΤΡΟΠΟΠΟΙΗΜΕΝΗ ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ΤΟΥ ΚΡΑΤΟΥΣ ΜΕΛΟΥΣ ΑΝΑΦΟΡΑΣ
|
|
|
- Σταματία Γαλάνη
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΡΑΡΤΗΜΑ III ΤΡΟΠΟΠΟΙΗΜΕΝΗ ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ΤΟΥ ΚΡΑΤΟΥΣ ΜΕΛΟΥΣ ΑΝΑΦΟΡΑΣ Σηµείωση: Το παρόν SPC (Περίληψη Χαρακτηριστικών Προϊόντος ) αποτελούσε παράρτηµα της Απόφασης της Επιτροπής σχετικά µε το παραπεµπτικό σύµφωνα µε το Αρθρο 7(5) που αφορά το Genotropin και σχετικές ονοµασίες. Τα κείµενα ήταν τότε έγκυρα. Μετά την Απόφαση της Επιτροπής, οι Αρµόδιες Αρχές του Κράτους Μέλους θα ενηµερώσουν τις πληροφορίες του προϊόντος όπως απαιτείται. Ως εκ τούτου, το παρόν SPC πιθανά να µην αντανακλά τα τρέχοντα κείµενα. CPMP/3477/03 1/10 EMEA 2003
2 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ <Επινοηθείσα ονοµασία> 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Somatropin (INN), ανασυνδυασµένη προερχόµενη από DNA ανθρώπινη αυξητική ορµόνη που παράγεται σε E.coli. Για έκδοχα, βλ ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ Στείρα λυόφιλη σκόνη και διαλύτης για παρασκευή ενέσιµου διαλύµατος. <Στο φυσίγγιο δύο διαµερισµάτων υπάρχει λευκή κόνις στο πρόσθιο διαµέρισµα και διαυγές διάλυµα στο οπίσθιο διαµέρισµα.> 4. ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ 4.1 Θεραπευτικές ενδείξεις Παιδιά ιαταραχές ανάπτυξης που οφείλονται σε ανεπαρκή έκκριση αυξητικής ορµόνης και διαταραχές ανάπτυξης που σχετίζονται µε σύνδροµο Turner ή χρόνια νεφρική ανεπάρκεια. ιαταραχές ανάπτυξης (πραγµατικό ύψος SDS < -2,5 και ύψος SDS < -1 προσαρµοσµένο στους γονείς) σε κοντού αναστήµατος παιδιά που γεννήθηκαν µικρά σε σχέση µε την ηλικία κύησής τους (SGA), µε βάρος και/ή µήκος κατά τη γέννηση κάτω από 2 SD, που δεν κατόρθωσαν να εµφανίσουν φυσιολογική ανάπτυξη (HV SDS < 0 κατά τη διάρκεια του περασµένου έτους) µέχρι την ηλικία των 4 ετών ή αργότερα. Σύνδροµο Prader-Willi, για βελτίωση της ανάπτυξης και της σύστασης του σώµατος. Η διάγνωση του συνδρόµου Prader-Willi θα πρέπει να επιβεβαιωθεί µε κατάλληλες γενετικές δοκιµασίες. Ενήλικες Θεραπεία υποκατάστασης σε ενήλικες µε αυξηµένη ανεπάρκεια αυξητικής ορµόνης. Ασθενείς µε σοβαρή ανεπάρκεια αυξητικής ορµόνης ως ενήλικες ορίζονται σαν ασθενείς µε γνωστή παθολογική κατάσταση της υποθαλαµο-υποφυσιακής περιοχής και τουλάχιστον µια γνωστή ανεπάρκεια ορµόνης της υπόφυσης εκτός από προλακτίνη. Στους ασθενείς αυτούς θα πρέπει να διενεργείται µια δυναµική δοκιµασία για διάγνωση ή αποκλεισµό ανεπάρκειας αυξητικής ορµόνης. Σε ασθενείς µε προϋπάρχουσα ανεπάρκεια αυξητικής ορµόνης στην παιδική ηλικία (χωρίς ενδείξεις νόσου υποθαλάµου-υπόφυσης ή κρανιακή ακτινοβολία), συνιστάται η διενέργεια δύο δοκιµασιών, εκτός στην περίπτωση ασθενών µε χαµηλές συγκεντρώσεις IGF-I (<2 SDS) στους οποίους θα πρέπει να διενεργείται µια δοκιµασία. Το σηµείο περάτωσης της δυναµικής δοκιµασίας θα πρέπει να είναι επακριβές. 4.2 οσολογία και τρόπος χορήγησης Το δοσολογικό σχήµα και ο τρόπος χορήγησης εξατοµικεύονται. Η ένεση πρέπει να χορηγείται υποδορίως και το σηµείο της ένεσης πρέπει να εναλλάσσεται, για αποφυγή ατροφίας του λιπώδους ιστού. CPMP/3477/03 2/10 EMEA 2003
3 Ανεπαρκής έκκριση της αυξητικής ορµόνης σε παιδιά: Γενικά συνιστάται δόση 0,025-0,035 mg/kg βάρους σώµατος την ηµέρα ή 0,7-1,0 mg/m 2 επιφανείας σώµατος την ηµέρα. Έχουν χορηγηθεί όµως και µεγαλύτερες δόσεις. Σύνδροµο Prader-Willi, για βελτίωση της ανάπτυξης και της σύστασης του σώµατος σε παιδιά: Γενικά, συνιστάται δόση 0,035 mg/kg βάρους σώµατος την ηµέρα ή 1,0 mg/m 2 επιφανείας σώµατος την ηµέρα. εν πρέπει να χορηγείται δόση υψηλότερη από 2,7 mg ηµερησίως. Η θεραπεία δεν πρέπει να εφαρµόζεται σε παιδιά µε ρυθµό ανάπτυξης µικρότερο από 1 εκ. ετησίως και που πλησιάζει το κλείσιµο των επιφύσεών τους. Σύνδροµο Turner: Συνιστάται δόση 0,045-0,050 mg/kg βάρους σώµατος την ηµέρα ή 1,4 mg/m 2 επιφανείας σώµατος την ηµέρα. Χρόνια νεφρική ανεπάρκεια: Συνιστάται δόση 1,4 mg/m 2 επιφανείας σώµατος την ηµέρα (περίπου 0,045-0,050 mg/kg βάρους σώµατος την ηµέρα). Υψηλότερες δόσεις µπορεί να χρειαστούν εάν η ταχύτητα ανάπτυξης είναι πάρα πολύ χαµηλή. ιόρθωση της δόσης µπορεί να χρειασθεί µετά από έξι µήνες θεραπείας. ιαταραχές ανάπτυξης σε κοντού αναστήµατος παιδιά που γεννήθηκαν µικρά σε σχέση µε την ηλικία κύησής τους (SGA): Συνήθως συνιστάται δόση 0,035 mg/kg βάρους σώµατος ηµερησίως (1 mg/m 2 επιφάνειας σώµατος ηµερησίως) µέχρις ότου επιτευχθεί το τελικό ύψος (βλ. λήµµα 5.1). Η θεραπεία θα πρέπει να διακόπτεται µετά τον πρώτο χρόνο θεραπείας αν η αλλαγή στην ταχύτητα της ανάπτυξης SDS είναι κάτω από + 1. Η θεραπεία θα πρέπει να διακόπτεται όταν η ταχύτητα της ανάπτυξης είναι κάτω των 2 cm ετησίως και, αν απαιτείται επιβεβαίωση, η οστική ηλικία είναι >14 ετών (κορίτσια) ή >16 ετών (αγόρια), που αντιστοιχεί µε το κλείσιµο των επιφυσιακών χόνδρων. Ενδειξη Συστάσεις δοσολογίας σε Παιδιά Ασθενείς Ανεπαρκή έκκριση αυξητικής ορµόνης σε παιδιά Σύνδροµο Prader-Willi σε παιδιά mg/kg βάρους σώµατος Ηµερήσια δόση 0,025-0,035 0,7-1,0 0,035 1,0 Σύνδροµο Turner 0,045 0,050 1,4 Χρόνια νεφρική 0,045 0,050 1,4 ανεπάρκεια Παιδιά που γεννήθηκαν µικρά σε σχέση µε την ηλικία κύησής τους (SGA) 0,035 1,0 mg/m 2 επιφάνειας σώµατος Ηµερήσια δόση Ανεπάρκεια αυξητικής ορµόνης σε ενήλικες: Η θεραπεία θα πρέπει να αρχίζει µε χαµηλή δόση, 0,15-0,3 mg ηµερησίως. Η δόση θα πρέπει να αυξάνεται βαθµιαία σύµφωνα µε τις εξατοµικευµένες απαιτήσεις του κάθε ασθενούς όπως καθορίζονται από τη συγκέντρωση της IGF-I. Στόχος της θεραπείας θα πρέπει να είναι οι συγκεντρώσεις του οµοιάζοντος µε την ινσουλίνη αυξητικού παράγοντα (IGF-I) να βρίσκονται εντός 2 τυπικών αποκλίσεων από τη µέση τιµή που έχει διορθωθεί ως προς την ηλικία. Οι ασθενείς µε φυσιολογικές συγκεντρώσεις IGF-I κατά την έναρξη της θεραπείας θα πρέπει λαµβάνουν αυξητική ορµόνη µέχρι το επίπεδο της IGF-I να βρίσκεται στο ανώτατο φυσιολογικό όριο, που δεν υπερβαίνει τις 2 τυπικές αποκλίσεις. Η κλινική ανταπόκριση και οι ανεπιθύµητες ενέργειες µπορούν επίσης να χρησιµοποιηθούν για τον καθορισµό της τιτλοποίησης της δόσης. Η ηµερήσια δόση συντήρησης σπάνια υπερβαίνει το 1,0 mg ηµερησίως. Οι γυναίκες µπορεί να χρειαστούν υψηλότερες δόσεις από τους άντρες, και οι άντρες εµφανίζουν αυξανόµενη ευαισθησία στην IGF-I µε την πάροδο του χρόνου. Αυτό σηµαίνει ότι υπάρχει ο κίνδυνος οι γυναίκες, ειδικά εκείνες που υποβάλλονται σε θεραπεία ορµονικής υποκατάστασης (οιστρογόνων) από το CPMP/3477/03 3/10 EMEA 2003
4 στόµα, να λαµβάνουν χαµηλότερη δόση ενώ οι άνδρες λαµβάνουν υψηλότερη δόση. Εποµένως, η ακρίβεια της δόσης της αυξητικής ορµόνης θα πρέπει να ελέγχεται ανά εξάµηνο. Καθώς η φυσιολογική παραγωγή αυξητικής ορµόνης µειώνεται µε την ηλικία, οι δοσολογικές ανάγκες µπορεί να µειωθούν. Θα πρέπει να χρησιµοποιείται η ελάχιστη αποτελεσµατική δόση. 4.3 Αντενδείξεις Το <Επινοηθείσα ονοµασία> δεν πρέπει να χορηγηθεί σε ασθενείς οι οποίοι εµφανίζουν ενδείξεις υπάρξεως όγκου σε εξέλιξη. Πριν από κάθε θεραπεία µε αυξητική ορµόνη πρέπει να έχει ολοκληρωθεί η αντινεοπλασµατική θεραπεία. Το <Επινοηθείσα ονοµασία>δεν πρέπει να χορηγηθεί για προώθηση της ανάπτυξης σε ασθενείς µε κλειστές επιφύσεις. Οι ασθενείς µε οξεία κρίσιµη ασθένεια που πάσχουν από επιπλοκές µετά από εγχείρηση ανοικτής καρδιάς, εγχείρηση στην κοιλιακή χώρα, πολλαπλά τραύµατα από ατύχηµα ή οξεία αναπνευστική ανεπάρκεια δεν θα πρέπει να υποβάλλονται σε θεραπεία µε <Επινοηθείσα ονοµασία>. ( Οσον αφορά ασθενείς που υποβάλλονται σε θεραπεία υποκατάστασης, βλ. 4.4 Ειδικές προειδοποιήσεις και προφυλάξεις κατά τη χρήση ). 4.4 Ειδικές προειδοποιήσεις και ιδιαίτερες προφυλάξεις κατά τη χρήση Η διάγνωση και η θεραπεία µε <Επινοηθείσα ονοµασία> θα πρέπει να αρχίζει και να παρακολουθείται από γιατρούς µε επαρκή προσόντα και πείρα στη διάγνωση και αντιµετώπιση ασθενών µε τη θεραπευτική ένδειξη για χρήση του προϊόντος. εν εφαρµόζεται στο Miniquick Η µυοσίτις αποτελεί πολύ σπάνια ανεπιθύµητη ενέργεια που µπορεί να σχετίζεται µε το συντηρητικό µετα-κρεσόλη. Στην περίπτωση µυαλγίας ή δυσανάλογου πόνου στο σηµείο της ένεσης, η µυοσίτιδα πρέπει να ληφθεί υπόψη και, αν επιβεβαιωθεί, πρέπει να χρησιµοποιείται <Επινοηθείσα ονοµασία> χωρίς µετα-κρεσόλη. Η σωµατοτροπίνη µπορεί να προκαλέσει αντίσταση στην ινσουλίνη και σε µερικούς µπορεί να προκαλέσει υπεργλυκαιµία. Εποµένως οι ασθενείς θα πρέπει να παρακολουθούνται για ενδείξεις δυσανεξίας στη γλυκόζη. Σε σπάνιες περιπτώσεις τα διαγνωστικά κριτήρια για σακχαρώδη διαβήτη τύπου ΙΙ µπορεί να πληρούνται σαν αποτέλεσµα της θεραπείας µε σωµατοτροπίνη, ωστόσο παράγοντες κινδύνου όπως παχυσαρκία (συµπεριλαµβανοµένων παχύσαρκων ασθενών µε σύνδροµο Prader-Willi) οικογενειακό ιστορικό, θεραπεία µε στεροειδή ή προϋπάρχουσα δυσανεξία στη γλυκόζη, έχουν παρατηρηθεί στις περισσότερες περιπτώσεις όπου αυτό συµβαίνει. Σε ασθενείς µε ήδη έκδηλο σακχαρώδη διαβήτη, η αντιδιαβητική αγωγή µπορεί να χρειάζεται αναπροσαρµογή όταν αρχίζει η θεραπεία µε σωµατοτροπίνη. Κατά τη διάρκεια της θεραπείας µε σωµατοτροπίνη έχει παρατηρηθεί αυξηµένη µετατροπή Τ4 σε Τ3, που µπορεί να προκαλέσει µείωση στη συγκέντρωση της Τ4 στον ορό και αύξηση στη συγκέντρωση της Τ3. Σε γενικές γραµµές, τα περιφερικά επίπεδα θυρεοειδούς ορµόνης παραµένουν εντός των ορίων αναφοράς υγιών ατόµων. Οι επιδράσεις της σωµατοτροπίνης στα επίπεδα των ορµονών του θυρεοειδή µπορεί να είναι κλινικής σηµασίας σε ασθενείς µε κεντρικό υποκλινικό υποθυρεοειδισµό στους οποίους µπορεί θεωρητικά να αναπτυχθεί υποθυρεοειδισµός. Αντίθετα, σε ασθενείς που υποβάλλονται σε θεραπεία υποκατάστασης µε θυροξίνη, µπορεί να εµφανισθεί ήπιος υπερθυρεοειδισµός. Συνιστάται εποµένως ο έλεγχος της λειτουργίας του θυρεοειδούς πριν την έναρξη της θεραπείας µε σωµατοτροπίνη και µετά από τις ρυθµίσεις της δοσολογίας. Σε περίπτωση εµφάνισης δευτεροπαθούς ανεπάρκειας αυξητικής ορµόνης λόγω θεραπευτικής αγωγής κακοήθους νεοπλασίας, συνιστάται να αναζητώνται σηµεία υποτροπής της νεοπλασίας. CPMP/3477/03 4/10 EMEA 2003
5 Σε ασθενείς µε ενδοκρινείς δυσλειτουργίες, συµπεριλαµβα-νοµένης και της ανεπάρκειας Α.Ο. µπορεί να παρουσιασθεί συχνότερα επιφυσιολίσθηση σε σύγκριση µε το γενικό πληθυσµό. Κάθε παιδί που παρουσιάζει χωλότητα κατά τη διάρκεια της θεραπείας µε somatropin, πρέπει να εξετάζεται κλινικά. Στην περίπτωση σοβαρού ή επαναλαµβανόµενου πονοκεφάλου, προβληµάτων όρασης, ναυτίας και/ή έµετου, συνιστάται βυθοσκόπηση για τον αποκλεισµό οιδήµατος της οπτικής θηλής. Στην περίπτωση που επιβεβαιωθεί η ύπαρξη οιδήµατος της οπτικής θηλής, θα πρέπει να θεωρηθεί σκόπιµο, η διάγνωση καλοήθους ενδοκρανιακής υπέρτασης ώστε στην περίπτωση αυτή, εάν κριθεί αναγκαίο, να διακοπεί η θεραπεία αυξητικής ορµόνης. Μέχρι σήµερα δεν υπάρχουν αρκετές ενδείξεις ώστε να δοθούν συγκεκριµένες συµβουλές για τη συνέχιση της θεραπείας µε αυξητική ορµόνη σε ασθενείς µε ενδοκρανιακή υπέρταση σε αποδροµή. Ωστόσο, η κλινική εµπειρία δείχνει ότι η επανέναρξη της θεραπείας είναι συχνά εφικτή χωρίς την επανεµφάνιση της ενδοκρανιακής υπέρτασης. Αν ξαναεφαρµοσθεί η θεραπεία µε αυξητική ορµόνη, απαιτείται στενή παρακολούθηση των συµπτωµάτων της ενδοκρανιακής υπέρτασης. H εµπειρία σε ασθενείς ηλικίας µεγαλύτερης των 60 ετών είναι περιορισµένη. Σε ασθενείς µε σύνδροµο Prader-Willi, η θεραπεία θα πρέπει πάντα να εφαρµόζεται σε συνδυασµό µε δίαιτα περιορισµένων θερµίδων. Συχνά παρατηρείται σκολίωση σε ασθενείς µε σύνδροµο Prader-Willi. Η σκολίωση µπορεί να επιδεινωθεί σε κάθε παιδί κατά τη διάρκεια της ταχείας ανάπτυξης. Τα κλινικά ευρήµατα της σκολίωσης θα πρέπει να παρακολουθούνται κατά τη διάρκεια της θεραπείας. Ωστόσο, δεν έχει δειχθεί ότι η θεραπεία µε αυξητική ορµόνη αυξάνει τη συχνότητα εµφάνισης ή τη σοβαρότητα της σκολίωσης. Η εµπειρία µε παρατεταµένη θεραπεία σε ενήλικες και σε ασθενείς µε σύνδροµο Prader-Willi είναι περιορισµένη. Σε κοντού αναστήµατος παιδιά που γεννήθηκαν µικρά σε σχέση µε την ηλικία κύησής τους SGA, θα πρέπει πριν από την έναρξη της θεραπείας, να αποκλείονται άλλες ιατρικές αιτίες ή θεραπείες που θα µπορούσαν να ερµηνεύσουν τις διαταραχές στην ανάπτυξη. Σε παιδιά SGA συνιστάται η µέτρηση της ινσουλίνης και της γλυκόζης στο αίµα, σε κατάσταση νηστείας, πριν από την έναρξη της θεραπείας και στη συνέχεια σε ετήσια βάση. Σε ασθενείς µε αυξηµένο κίνδυνο για σακχαρώδη διαβήτη (π.χ. οικογενειακό ιστορικό διαβήτη, παχυσαρκία, σοβαρή αντοχή στην ινσουλίνη, µελανίζουσα ακάνθωση) θα πρέπει να εκτελείται δοκιµασία αντοχής γλυκόζης από το στόµα (OGTT). Αν υπάρχει φανερός διαβήτης, δεν θα πρέπει να χορηγηθεί αναπτυξιακή ορµόνη. Σε παιδιά SGA συνιστάται η µέτρηση του επιπέδου IGF-I πριν από την έναρξη της θεραπείας και στη συνέχεια δυο φορές ετησίως. Στην περίπτωση που, µε επαναλαµβανόµενες µετρήσεις, τα επίπεδα IGF-I υπερβαίνουν το +2 SD σε σύγκριση µε πρότυπα αναφοράς για ηλικία και εφηβική κατάσταση, θα πρέπει να θεωρηθεί η χρήση της αναλογίας IGF-I/IGFΒΡ-3 σαν οδηγός για τη ρύθµιση της δόσης. Η εµπειρία στην έναρξη της θεραπείας σε ασθενείς SGA κοντά στην έναρξη της εφηβείας είναι περιορισµένη. εν συνιστάται εποµένως η έναρξη της θεραπείας κοντά στην έναρξη της εφηβείας. Η εµπειρία σε ασθενείς µε σύνδροµο Silver-Russell είναι περιορισµένη. Ένα µέρος από το κέρδος του ύψους που επιτυγχάνεται µε τη θεραπεία παιδιών κοντού αναστήµατος που γεννήθηκαν SGA µε αυξητική ορµόνη µπορεί να απολεσθεί αν η θεραπεία διακοπεί πριν επιτευχθεί το τελικό ύψος. Στη χρόνια νεφρική ανεπάρκεια, η νεφρική λειτουργία πρέπει να είναι κάτω του 50% της κανονικής, πριν την έναρξη της θεραπείας. Για την επιβεβαίωση της διαταραχής της σωµατικής ανάπτυξης, η ανάπτυξη θα πρέπει να παρακολουθείται για ένα χρόνο πριν την έναρξη της θεραπείας. Συντηρητική CPMP/3477/03 5/10 EMEA 2003
6 θεραπεία για τη νεφρική ανεπάρκεια θα πρέπει να έχει καθιερωθεί και διατηρηθεί κατά τη διάρκεια της θεραπείας. Η θεραπεία πρέπει να διακόπτεται µε τη µεταµόσχευση νεφρού. Μέχρι σήµερα, δεν υπάρχουν στοιχεία για το τελικό ύψος σε ασθενείς µε χρόνια νεφρική ανεπάρκεια θεραπεία που υποβάλλονται σε θεραπεία µε <Επινοηθείσα ονοµασία>. Τα αποτελέσµατα του <Επινοηθείσα ονοµασία> στην ανάνηψη µελετήθηκαν σε δύο ελεγχόµενες µε placebo µελέτες που περιελάµβαναν 522 ενήλικες ασθενείς σε κρίσιµη κατάσταση µε επιπλοκές µετά από εγχείρηση ανοικτής καρδιάς, εγχείρηση στην κοιλιακή χώρα, πολλαπλά τραύµατα από ατύχηµα ή οξεία αναπνευστική ανεπάρκεια. Η θνησιµότητα ήταν υψηλότερη σε ασθενείς που έλαβαν 5,3 ή 8 mg <Επινοηθείσα ονοµασία> ηµερησίως σε σύγκριση µε ασθενείς που έλαβαν placebo, 42% έναντι 19%. Με βάση τις πληροφορίες αυτές, οι εν λόγω ασθενείς δεν θα πρέπει να υποβάλλονται σε θεραπεία µε <Επινοηθείσα ονοµασία>. εδοµένου ότι δεν υπάρχουν πληροφορίες αναφορικά µε την ασφάλεια της θεραπείας υποκατάστασης µε αυξητική ορµόνη σε ασθενείς σε οξεία κρίσιµη κατάσταση, τα οφέλη της συνεχιζόµενης θεραπείας στην περίπτωση αυτή θα πρέπει να αντισταθµίζονται µε τους ενδεχόµενους κινδύνους. Σε όλους τους ασθενείς που αναπτύσσουν άλλες ή ανάλογες, οξείες κρίσιµες καταστάσεις, τα πιθανά οφέλη της θεραπείας µε <Επινοηθείσα ονοµασία>, θα πρέπει να µελετώνται σε σχέση µε τους ενδεχόµενους κινδύνους. 4.5 Αλληλεπιδράσεις µε άλλα φαρµακευτικά προϊόντα και άλλες µορφές αλληλεπίδρασης Τα στοιχεία από µία µελέτη αλληλεπίδρασης που διεξήχθη σε ενήλικες µε ανεπάρκεια ΑΟ δείχνουν ότι η χορήγηση σωµατοτροπίνης µπορεί να αυξήσει την κάθαρση ενώσεων γνωστών ότι µεταβολίζονται από το κυτόχρωµα Ρ450 3Α4 (π.χ. στεροειδή, κορτικοστεροειδή, αντισπασµωδικά και κυκλοσπορίνη). Η κλινική σηµασία αυτού δεν είναι γνωστή. Βλ. επίσης λήµµα 4.4 για οδηγίες αναφορικά µε τον σακχαρώδη διαβήτη και τις διαταραχές του θυρεοειδούς και λήµµα 4.2 για οδηγίες σε σχέση µε τη θεραπεία υποκατάστασης οιστρογόνων από το στόµα. 4.6 Κύηση και γαλουχία εν υπάρχει κλινική εµπειρία της χρήσης σε έγκυες γυναίκες. Οι µελέτες αναπαραγωγής σε πειραµατόζωα είναι ελλειπείς. Η θεραπεία µε <Επινοηθείσα ονοµασία> πρέπει να διακοπεί σε περίπτωση σύλληψης. Κατά τη διάρκεια της φυσιολογικής εγκυµοσύνης τα επίπεδα της αυξητικής ορµόνης µειώνονται σαφώς µετά από την 20ή εβδοµάδα της κύησης, και αντικαθίστανται σχεδόν πλήρως από αυξητική ορµόνη του πλακούντα µέχρι την 30ή εβδοµάδα. Εν όψει του γεγονότος αυτού, δεν θεωρείται πιθανό ότι η συνεχιζόµενη θεραπεία υποκατάστασης µε σωµατοτροπίνη είναι απαραίτητη σε γυναίκες µε ανεπάρκεια αυξητικής ορµόνης στο τρίτο τρίµηνο της εγκυµοσύνης. εν είναι γνωστό αν η σωµατοτροπίνη αποβάλλεται στο µητρικό γάλα, ωστόσο η απορρόφηση ανέπαφης πρωτεΐνης από τον γαστρεντερικό σωλήνα του βρέφους δεν θεωρείται πιθανή. 4.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισµού µηχανών εν έχουν παρατηρηθεί επιδράσεις την ικανότητα οδήγησης και χειρισµού µηχανηµάτων. 4.8 Ανεπιθύµητες ενέργειες Οι ασθενείς µε ανεπάρκεια αυξητικής ορµόνης χαρακτηρίζονται από ανεπάρκεια εξωκυτταρικού όγκου. Με την έναρξη της θεραπείας µε σωµατοτροπίνη η έλλειψη αυτή αποκαθίσταται ταχέως. Σε ενήλικες ασθενείς µε ανεπιθύµητες ενέργειες που σχετίζονται µε κατακράτηση υγρών, όπως περιφερικό οίδηµα, εµφανίζεται δυσκαµψία των άκρων, αρθραλγία, µυαλγία και παραισθήσεις. Σε γενικές γραµµές οι ανεπιθύµητες ενέργειες αυτές είναι ήπιες µέχρι µέτριες, εµφανίζονται κατά τη διάρκεια των πρώτων µηνών της θεραπείας και εξαφανίζονται µόνες τους ή µε ελάττωση της δόσης. CPMP/3477/03 6/10 EMEA 2003
7 Η συχνότητα εµφάνισης των ανεπιθύµητων ενεργειών αυτών σχετίζεται µε τη χορηγηθείσα δόση, την ηλικία των ασθενών, και πιθανώς εµφανίζει αντίστροφη σχέση µε την ηλικία των ασθενών κατά την έναρξη της ανεπάρκειας της αυξητικής ορµόνης. Σε παιδιά οι ανεπιθύµητες ενέργειες αυτές δεν είναι συχνές. Παροδική τοπική δερµατική αντίδραση στο σηµείο της ένεσης σε παιδιά είναι συνηθισµένη. Εχουν αναφερθεί σπάνιες περιπτώσεις σακχαρώδους διαβήτη τύπου ΙΙ. Εχουν αναφερθεί σπάνιες περιπτώσεις καλοήθους ενδοκρανιακής υπέρτασης. Το σύνδροµο καρπιαίου σωλήνα δεν παρατηρείται συχνά σε ενήλικες. Στο 1% των ασθενών που έλαβαν <Επινοηθείσα ονοµασία> αναπτύχθηκαν αντισώµατα. Η ικανότητα δέσµευσης των αντισωµάτων αυτών ήταν χαµηλή και γενικά χωρίς κλινική σηµασία. Νεοπλάσµατα, καλοήθη και κακοήθη Πολύ σπάνια (<1/10 000): Λευχαιµία. ιαταραχές του ανοσοποιητικού συστήµατος Συχνά (>1/100, <1/10): Σχηµατισµός αντισωµάτων. ιαταραχές του ενδοκρινικού συστήµατος Σπάνια (>1/10 000, <1/1000): Σακχαρώδης διαβήτης τύπου ΙΙ. ιαταραχές του νευρικού συστήµατος Συχνά (>1/100, <1/10): Σε ενήλικες παραισθήσεις. Οχι συχνά (>1/1000, <1/100): Σε ενήλικες σύνδροµο καρπιαίου σωλήνα, Σε παιδιά παραισθήσεις. Σπάνια (>1/10 000, <1/1000): Καλοήθης ενδοκρανιακή υπέρταση. ιαταραχές του δέρµατος και των µαλακών µορίων Συχνά (>1/100, <1/10): Σε παιδιά παροδικές τοπικές δερµατικές αντιδράσεις. ιαταραχές του µυοσκελετικού συστήµατος, του συνδετικού ιστού και των οστών Συχνά (>1/100, <1/10): Σε ενήλικες ακαµψία των άκρων, αρθραλγία, µυαλγία. Οχι συχνά (>1/1000, <1/100): Σε παιδιά ακαµψία των άκρων, αρθραλγία, µυαλγία. Γενικές διαταραχές και διαταραχές στο σηµείο της ένεσης Συχνά (>1/100, <1/10): Σε ενήλικες περιφερικό οίδηµα. Οχι συχνά (>1/1000, <1/100): Σε παιδιά περιφερικό οίδηµα. Εχει αναφερθεί ότι η σωµατοτροπίνη µειώνει τα επίπεδα της κορτιζόλης στον ορό, πιθανώς επηρεάζοντας τις πρωτεϊνες φορείς. εν έχουν αναφερθεί αλλαγές στα επίπεδα της µη δεσµευµένης κορτιζόλης στον ορό. Η κλινική σηµασία των ευρηµάτων αυτών φαίνεται περιορισµένη. Ωστόσο, η θεραπεία αντικατάστασης µε κορτικοστεροειδή θα πρέπει να βελτιστοποιείται πριν από την έναρξη της θεραπείας µε <Επινοηθείσα ονοµασία>. Πολύ σπάνιες περιπτώσεις λευχαιµίας έχουν αναφερθεί σε παιδιά µε ανεπάρκεια αυξητικής ορµόνης τα οποία υποβλήθηκαν σε θεραπεία µε σωµατοτροπίνη, ωστόσο η συχνότητα εµφάνισης φαίνεται όµοια µε εκείνη σε παιδιά χωρίς ανεπάρκεια αυξητικής ορµόνης. CPMP/3477/03 7/10 EMEA 2003
8 4.9 Υπερδοσολογία εν έχει αναφερθεί περίπτωση υπερδοσολογίας ή τοξικότητας. Η οξεία υπερδοσολογία µπορεί αρχικά να προκαλέσει υπογλυκαιµία και στη συνέχεια υπεργλυκαιµία. Η µακροχρόνια υπερδοσολογία µπορεί να επιφέρει ενδείξεις και συµπτώµατα όµοια µε εκείνα που προκαλούνται από υπερβολική ποσότητα ανθρώπινης αυξητικής ορµόνης. 5. ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ Ι ΙΟΤΗΤΕΣ 5.1 Φαρµακοδυναµικές ιδιότητες Κωδικός ATC: H01A C01 Η σωµατοτροπίνη είναι ισχυρή µεταβολική ορµόνη σηµαντική για τον µεταβολισµό των λιπιδίων, των υδατανθράκων και των πρωτεϊνών. Σε παιδιά µε ανεπαρκή ενδογενή αυξητική ορµόνη η σωµατοτροπίνη ενισχύει τη γραµµική ανάπτυξη και αυξάνει την ταχύτητα ανάπτυξης. Σε ενήλικες καθώς και σε παιδιά η σωµατοτροπίνη διατηρεί τη φυσιολογική σύσταση του σώµατος αυξάνοντας την κατακράτηση αζώτου και τη διέγερση της ανάπτυξης των σκελετικών µυών, και κινητοποιώντας το σωµατικό λίπος. Ο σπλαχνικός λιπώδης ιστός είναι ιδιαίτερα ευαίσθητος στη σωµατοτροπίνη. Επιπλέον µε την αυξηµένη λιπόλυση, η σωµατοτροπίνη µειώνει την πρόσληψη τριγλυκεριδίων στις αποθήκες του σωµατικού λίπους. Οι συγκεντρώσεις του IGF-I και του IGFBP3 αυξάνονται από τη σωµατοτροπίνη. Επιπλέον, έχουν καταδειχθεί οι εξής δράσεις: - Μεταβολισµός λιπιδίων: Η σωµατοτροπίνη διεγείρει τους ηπατικούς υποδοχείς της ηπατικής LDL χοληστερόλης και επηρεάζει την εικόνα των λιπιδίων και των λιποπρωτεϊνών στον ορό. Σε γενικές γραµµές, η χορήγηση σωµατοτροπίνης σε ασθενείς µε ανεπάρκεια Α.Ο. προκαλεί µείωση της LDL και των απολιποπρωτεϊνών Β του ορού. Μπορεί επίσης να παρατηρηθεί µείωση στην ολική χοληστερόλη του ορού. - Μεταβολισµός υδατανθράκων: Η σωµατοτροπίνη αυξάνει την ινσουλίνη, ωστόσο η γλυκόζη στο αίµα µετά από νηστεία, συχνά παραµένει αµετάβλητη. Τα παιδιά µε υπολειτουργία της υπόφυσης µπορεί να εµφανίσουν υπογλυκαιµία νηστείας. Η κατάσταση αυτή ανατρέπεται από τη σωµατοτροπίνη. - Μεταβολισµός νερού και µετάλλων: Η ανεπάρκεια της αυξητικής ορµόνης σχετίζεται µε µειωµένο όγκο πλάσµατος και εξωκυτταρικό όγκο. Και οι δύο όγκοι αυτοί αυξάνονται ταχέως µετά τη θεραπεία µε σωµατοτροπίνη. Η σωµατοτροπίνη προκαλεί την κατακράτηση νατρίου, καλίου και φωσφόρου. - Μεταβολισµός οστών: Η σωµατοτροπίνη διεγείρει τον ρυθµό δηµιουργίας και αποκατάστασης του σκελετικού οστού. Η µακροχρόνια χορήγηση σωµατοτροπίνης σε ασθενείς µε ανεπάρκεια αυξητικής ορµόνης µε οστεοπενία προκαλεί αύξηση στην περιεκτικότητα οστεϊκών µετάλλων και στην πυκνότητα σε σηµεία που φέρουν βάρος. - Σωµατική ικανότητα: Η µυϊκή δύναµη και η ικανότητα για σωµατική άσκηση βελτιώνονται µετά από µακροχρόνια θεραπεία µε σωµατοτροπίνη. Επίσης η σωµατοτροπίνη αυξάνει την καρδιακή παροχή, ωστόσο ο µηχανισµός δεν έχει ακόµη διευκρινισθεί. Η µείωση στην περιφερική αγγειακή αντίσταση θα µπορούσε να συµβάλλει στη δράση αυτή. Σε κλινικές µελέτες σε παιδιά κοντού αναστήµατος που γεννήθηκαν SGA χρησιµοποιήθηκαν δόσεις 0,033 και 0,067 mg/kg βάρους σώµατος ηµερησίως µέχρι την επίτευξη του τελικού ύψους. Σε 56 ασθενείς που υποβλήθηκαν σε συνεχή θεραπεία και που επέτυχαν (σχεδόν) τελικό ύψος, η µέση αλλαγή από ύψος κατά την έναρξη της θεραπείας ήταν + 1,90 SDS (0,033 mg/kg βάρους σώµατος ηµερησίως) και + 2,19 SDS (0,067 mg/kg βάρους σώµατος ηµερησίως). Βιβλιογραφικά στοιχεία από παιδιά που δεν υποβλήθηκαν σε θεραπεία, χωρίς πρώιµη αυτόµατη εµφάνιση φυσιολογικής CPMP/3477/03 8/10 EMEA 2003
9 ανάπτυξης υποδηλώνουν αργοπορηµένη ανάπτυξη + 0,5 SDS. Τα στοιχεία για µακροπρόθεσµη ασφάλεια είναι ακόµη περιορισµένα. 5.2 Φαρµακοκινητικές ιδιότητες Απορρόφηση Περίπου το 80% του <Επινοηθείσα ονοµασία> που χορηγείται υποδορίως απορροφάται τόσο σε υγιή άτοµα όσο και σε ασθενείς µε ανεπάρκεια αυξητικής ορµόνης. Μία υποδόρια δόση 0,035 mg/kg <Επινοηθείσα ονοµασία> προκαλεί τιµές C max και t max στο πλάσµα που κυµαίνονται από ng/ml και 3-6 ώρες αντίστοιχα. Αποβολή Ο µέσος τελικός χρόνος ηµιζωής του <Επινοηθείσα ονοµασία> µετά από ενδοφλέβια χορήγηση σε ενήλικες µε ανεπάρκεια αυξητικής ορµόνης είναι περίπου 0,4 ώρες. Ωστόσο, µετά από υποδόρια χορήγηση, επιτυγχάνεται χρόνος ηµιζωής 2-3 ωρών. Η διαφορά που παρατηρείται οφείλεται πιθανώς σε βραδεία απορρόφηση από το σηµείο της ένεσης µετά από υποδόρια χορήγηση. Υπο-πληθυσµοί Η απόλυτη βιοδιαθεσιµότητα του <Επινοηθείσα ονοµασία> φαίνεται όµοια σε άνδρες και σε γυναίκες µετά από υποδόρια χορήγηση. Πληροφορίες αναφορικά µε την φαρµακοκινητική του <Επινοηθείσα ονοµασία> σε ηλικιωµένα άτοµα και σε παιδιά, σε διαφορετικές φυλές καθώς και σε ασθενείς µε νεφρική, ηπατική ή καρδιακή ανεπάρκεια είτε δεν υπάρχουν ή είναι ελλειπείς. 5.3 Προκλινικά δεδοµένα για την ασφάλεια Σε µελέτες που αφορούν γενική τοξικότητα, τοπική ανοχή και τοξικότητα αναπαραγωγής δεν παρατηρήθηκαν επιδράσεις κλινικής σηµασίας. Οι µελέτες γενοτοξικότητας που διεξάχθηκαν in vitro και in vivo σε µεταλλάξεις γονιδίων καθώς και σε πρόκληση χρωµοσωµιακών παρεκκλίσεων ήταν αρνητικές. Παρατηρήθηκε αυξηµένη ευθραυστότητα χρωµατοσωµάτων σε µία in vitro µελέτη σε λεµφοκύτταρα που ελήφθησαν από ασθενείς µετά από µακροχρόνια θεραπεία µε σωµατοτροπίνη και µετά την προσθήκη του ραδιοµιµητικού φαρµάκου bleomycin. Η κλινική σηµασία του ευρήµατος αυτού δεν είναι σαφής. Σε µία άλλη µελέτη, δεν βρέθηκε καµία αύξηση στις χρωµοσωµιακές ανωµαλίες στα λεµφοκύτταρα ασθενών που είχαν υποβληθεί σε µακροχρόνια θεραπεία µε σωµατοτροπίνη. 6. ΦΑΡΜΑΚΕΥΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ 6.1 Κατάλογος εκδόχων 6.2 Ασυµβατότητες 6.3 ιάρκεια Ζωής CPMP/3477/03 9/10 EMEA 2003
10 6.4 Ιδιαίτερες προφυλάξεις κατά τη φύλαξη του προϊόντος 6.5 Φύση και συστατικά του περιέκτη 6.6 Οδηγίες χρήσης και χειρισµού και απόρριψη 7. ΚΑΤΟΧΟΣ ΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 8. ΑΡΙΘΜΟΣ (ΟΙ) Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 9. ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ ΕΓΚΡΙΣΗΣ / ΑΝΑΝΕΩΣΗΣ ΤΗΣ Α ΕΙΑΣ 10. ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ CPMP/3477/03 10/10 EMEA 2003
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ GENOTROPIN 5,0 mg, 5,3 mg ή 12 mg, κόνις και διαλύτης για ενέσιμο διάλυμα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1. GENOTROPIN
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ GENOTROPIN 5,0 mg, 5,3 mg ή 12 mg, κόνις και διαλύτης για ενέσιμο διάλυμα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1. GENOTROPIN
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. ZOMACTON 10 mg/ml, κόνις και διαλύτης για παρασκευή ενέσιµου διαλύµατος σε προγεµισµένη σύριγγα.
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ZOMACTON 10 mg/ml, κόνις και διαλύτης για παρασκευή ενέσιµου διαλύµατος σε προγεµισµένη σύριγγα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Somatropin*....10 mg (10 mg/ml
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ZOMACTON 10 mg/ml, κόνις και διαλύτης για παρασκευή ενέσιµου διαλύµατος σε προγεµισµένη σύριγγα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Somatropin*....10 mg (10 mg/ml
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Omnitrope 1,3 mg/ml κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Μετά την ανασύσταση,
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Omnitrope 1,3 mg/ml κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Μετά την ανασύσταση,
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. ZOMACTON 4 mg, κόνις και διαλύτης για ενέσιµο διάλυµα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ZOMACTON 4 mg, κόνις και διαλύτης για ενέσιµο διάλυµα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Somatropin* 4 mg (1,3 ή 3,3 mg/ml µετά από ανασύσταση) * Παράγεται σε κύτταρα
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ZOMACTON 4 mg, κόνις και διαλύτης για ενέσιµο διάλυµα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Somatropin* 4 mg (1,3 ή 3,3 mg/ml µετά από ανασύσταση) * Παράγεται σε κύτταρα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
Γράφει: Ελένη Αναστασίου, Υπεύθυνη Διαβητολογικού Κέντρου Κύησης του Α' Ενδοκρινολογικού Τμήματος» του Νοσοκομείου «Αλεξάνδρα»
 Γράφει: Ελένη Αναστασίου, Υπεύθυνη Διαβητολογικού Κέντρου Κύησης του Α' Ενδοκρινολογικού Τμήματος» του Νοσοκομείου «Αλεξάνδρα» Παρακάτω θα αναφερθούμε χωριστά στις επιπτώσεις και την αντιμετώπιση (α) του
Γράφει: Ελένη Αναστασίου, Υπεύθυνη Διαβητολογικού Κέντρου Κύησης του Α' Ενδοκρινολογικού Τμήματος» του Νοσοκομείου «Αλεξάνδρα» Παρακάτω θα αναφερθούμε χωριστά στις επιπτώσεις και την αντιμετώπιση (α) του
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SmPC) NEPHROTECT. 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Nephrotect, διάλυµα για έγχυση
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SmPC) NEPHROTECT 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Nephrotect, διάλυµα για έγχυση 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1000 ml περιέχουν: L-isoleucine
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SmPC) NEPHROTECT 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Nephrotect, διάλυµα για έγχυση 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1000 ml περιέχουν: L-isoleucine
Ανακούφιση των συμπτωμάτων ήπιας έως μέτριας οστεοαρθρίτιδας των γονάτων.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ:
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ NutropinAq 10 mg/2ml (30 IU), ενέσιµο διάλυµα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα φυσίγγιο περιέχει 10 mg (30 IU) σωµατροπίνης*.
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ NutropinAq 10 mg/2ml (30 IU), ενέσιµο διάλυµα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα φυσίγγιο περιέχει 10 mg (30 IU) σωµατροπίνης*.
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Saizen 8 mg click.easy
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Saizen 8 mg click.easy 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Saizen 8 mg click.easy, κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Saizen 8 mg click.easy 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Saizen 8 mg click.easy, κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
ΔΥΣΛΙΠΙΔΑΙΜΙΑ. Νικολούδη Μαρία. Ειδικ. Παθολόγος, Γ.Ν.Θ.Π. «Η Παμμακάριστος»
 ΔΥΣΛΙΠΙΔΑΙΜΙΑ Νικολούδη Μαρία Ειδικ. Παθολόγος, Γ.Ν.Θ.Π. «Η Παμμακάριστος» Ο όρος δυσλιπιδαιμία εκφράζει τις ποσοτικές και ποιοτικές διαταραχές των λιπιδίων του αίματος. Τα λιπίδια όπως η χοληστερόλη και
ΔΥΣΛΙΠΙΔΑΙΜΙΑ Νικολούδη Μαρία Ειδικ. Παθολόγος, Γ.Ν.Θ.Π. «Η Παμμακάριστος» Ο όρος δυσλιπιδαιμία εκφράζει τις ποσοτικές και ποιοτικές διαταραχές των λιπιδίων του αίματος. Τα λιπίδια όπως η χοληστερόλη και
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, Wednesday, 19 December :05 -
 SUPERAMIN ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία Προϊόντος: SUPERAMIN α) Πόσιμο διάλυμα σε συσκευασία μιας δόσης 1 g/10ml FL & g/10ml FL β) Ενέσιμο διάλυμα 1 g/5ml AMP & 2g/5ml AMP 1.2 Σύνθεση: Δραστική
SUPERAMIN ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία Προϊόντος: SUPERAMIN α) Πόσιμο διάλυμα σε συσκευασία μιας δόσης 1 g/10ml FL & g/10ml FL β) Ενέσιμο διάλυμα 1 g/5ml AMP & 2g/5ml AMP 1.2 Σύνθεση: Δραστική
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Αυτές οι μεταβολές στη ΠΧΠ και το φύλλο οδηγιών χρήσης θα είναι εν ισχύ κατά την έκδοση της Κοινοτικής
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Αυτές οι μεταβολές στη ΠΧΠ και το φύλλο οδηγιών χρήσης θα είναι εν ισχύ κατά την έκδοση της Κοινοτικής
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE. Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ:
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: MEGACE 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: MEGACE 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
Μήπως έχω µεγαλακρία; Πώς θα το καταλάβω;
 Μήπως έχω µεγαλακρία; Πώς θα το καταλάβω; MegalakriaBroshure.indd 1 17/11/2010 1:27:39 μμ Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών
Μήπως έχω µεγαλακρία; Πώς θα το καταλάβω; MegalakriaBroshure.indd 1 17/11/2010 1:27:39 μμ Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Water for Injection/Baxter (Viaflo) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε σάκος περιέχει 100% w/v Water for Injections.
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Water for Injection/Baxter (Viaflo) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε σάκος περιέχει 100% w/v Water for Injections.
Αύξηση & Ανάπτυξη. Υπερπλασία: αύξηση του αριθµού των κυττάρων & Υπερτροφία : αύξηση του µεγέθους των κυττάρων
 Αύξηση & Ανάπτυξη Αύξηση Κυτταρική διαίρεση και καθαρή πρωτεϊνική σύνθεση & Ανάπτυξη Αύξηση διαστάσεων (ανάστηµα) Αύξηση οστών (σπονδυλική στήλη και κάτω άκρα) Αύξηση σκελετικού µυ Αύξηση σπλάχνων Υπερπλασία:
Αύξηση & Ανάπτυξη Αύξηση Κυτταρική διαίρεση και καθαρή πρωτεϊνική σύνθεση & Ανάπτυξη Αύξηση διαστάσεων (ανάστηµα) Αύξηση οστών (σπονδυλική στήλη και κάτω άκρα) Αύξηση σκελετικού µυ Αύξηση σπλάχνων Υπερπλασία:
SALONPAS HOT â (Capsicum extract)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â (Capsicum extract) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε έµπλαστρο SALONPAS HOT â, µεγέθους
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â (Capsicum extract) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε έµπλαστρο SALONPAS HOT â, µεγέθους
ΤΡΕΧΟΥΣΕΣ Ο ΗΓΙΕΣ ΓΙΑ ΤΗ ΧΡΗΣΗ ΑΝΤΙ-ΙΙΚΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΑΣΘΕΝΩΝ ΜΕ ΓΡΙΠΗ ΑΠΟ ΤΟ ΝΕΟ ΙΟ Α/Η1Ν1 ΚΑΙ ΤΩΝ ΣΤΕΝΩΝ ΕΠΑΦΩΝ ΤΟΥΣ
 ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ ΤΡΕΧΟΥΣΕΣ Ο ΗΓΙΕΣ ΓΙΑ ΤΗ ΧΡΗΣΗ ΑΝΤΙ-ΙΙΚΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΑΣΘΕΝΩΝ ΜΕ ΓΡΙΠΗ ΑΠΟ ΤΟ ΝΕΟ ΙΟ Α/Η1Ν1 ΚΑΙ ΤΩΝ ΣΤΕΝΩΝ ΕΠΑΦΩΝ ΤΟΥΣ Ιούλιος 2009 Το παρόν έγγραφο
ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ ΤΡΕΧΟΥΣΕΣ Ο ΗΓΙΕΣ ΓΙΑ ΤΗ ΧΡΗΣΗ ΑΝΤΙ-ΙΙΚΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΑΣΘΕΝΩΝ ΜΕ ΓΡΙΠΗ ΑΠΟ ΤΟ ΝΕΟ ΙΟ Α/Η1Ν1 ΚΑΙ ΤΩΝ ΣΤΕΝΩΝ ΕΠΑΦΩΝ ΤΟΥΣ Ιούλιος 2009 Το παρόν έγγραφο
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ INFLABION. ( ιακετυλρεΐνη)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ INFLABION ( ιακετυλρεΐνη) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ INFLABION 50 mg σκληρά καψάκια 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε καψάκιο περιέχει 50 mg διακετυλρεΐνη.
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ INFLABION ( ιακετυλρεΐνη) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ INFLABION 50 mg σκληρά καψάκια 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε καψάκιο περιέχει 50 mg διακετυλρεΐνη.
Κανένα για αυτήν την παρουσίαση. Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini,
 Κανένα για αυτήν την παρουσίαση Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini, 2 Κυκλοσπορίνη-θεραπευτικές ενδείξεις 3 Θεραπεία σοβαρών μορφών
Κανένα για αυτήν την παρουσίαση Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini, 2 Κυκλοσπορίνη-θεραπευτικές ενδείξεις 3 Θεραπεία σοβαρών μορφών
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
Αρχικά θα πρέπει να προσδιορίσουμε τι είναι η παχυσαρκία.
 Αρχικά θα πρέπει να προσδιορίσουμε τι είναι η παχυσαρκία. Παχυσαρκία είναι η παθολογική αύξηση του βάρους του σώματος, που οφείλεται σε υπερβολική συσσώρευση λίπους στον οργανισμό. Παρατηρείται γενικά
Αρχικά θα πρέπει να προσδιορίσουμε τι είναι η παχυσαρκία. Παχυσαρκία είναι η παθολογική αύξηση του βάρους του σώματος, που οφείλεται σε υπερβολική συσσώρευση λίπους στον οργανισμό. Παρατηρείται γενικά
Κωνσταντίνος Τζιόμαλος Επίκουρος Καθηγητής Παθολογίας Α Προπαιδευτική Παθολογική Κλινική ΑΠΘ, Νοσοκομείο ΑΧΕΠΑ
 Στατίνες και σακχαρώδης διαβήτης Κωνσταντίνος Τζιόμαλος Επίκουρος Καθηγητής Παθολογίας Α Προπαιδευτική Παθολογική Κλινική ΑΠΘ, Νοσοκομείο ΑΧΕΠΑ Σακχαρώδης διαβήτης και καρδιαγγειακός κίνδυνος Μετα-ανάλυση
Στατίνες και σακχαρώδης διαβήτης Κωνσταντίνος Τζιόμαλος Επίκουρος Καθηγητής Παθολογίας Α Προπαιδευτική Παθολογική Κλινική ΑΠΘ, Νοσοκομείο ΑΧΕΠΑ Σακχαρώδης διαβήτης και καρδιαγγειακός κίνδυνος Μετα-ανάλυση
Παράρτημα II. Επιστημονικά πορίσματα και λόγοι απόρριψης που παρουσιάστηκαν από τον EMA
 Παράρτημα II Επιστημονικά πορίσματα και λόγοι απόρριψης που παρουσιάστηκαν από τον EMA 29 Επιστημονικά πορίσματα Γενική περίληψη της επιστημονικής αξιολόγησης των Norditropin SimpleXx, Norditropin NordiFlex,
Παράρτημα II Επιστημονικά πορίσματα και λόγοι απόρριψης που παρουσιάστηκαν από τον EMA 29 Επιστημονικά πορίσματα Γενική περίληψη της επιστημονικής αξιολόγησης των Norditropin SimpleXx, Norditropin NordiFlex,
O S T E O V I L E (Alfacalcidol)
 O S T E O V I L E (Alfacalcidol) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OSTEOVILE 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ OSTEOVILE 0,25 mcg/cap: Περιέχει 0,25 mcg/cap alfacalcidol
O S T E O V I L E (Alfacalcidol) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OSTEOVILE 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ OSTEOVILE 0,25 mcg/cap: Περιέχει 0,25 mcg/cap alfacalcidol
ΟΡΟΛΟΣΤΗΣΑΣΚΗΣΗΣΣΤΟ ΜΕΤΑΒΟΛΙΚΟΣΥΝ ΡΟΜΟ, ΣΤΑ ΛΙΠΙ ΙΑ ΚΑΙ ΣΤΙΣ ΛΙΠΟΠΡΩΤΕΪΝΕΣ
 ΟΡΟΛΟΣΤΗΣΑΣΚΗΣΗΣΣΤΟ ΜΕΤΑΒΟΛΙΚΟΣΥΝ ΡΟΜΟ, ΣΤΑ ΛΙΠΙ ΙΑ ΚΑΙ ΣΤΙΣ ΛΙΠΟΠΡΩΤΕΪΝΕΣ ΒασίληςΜούγιος, PhD ΤΕΦΑΑ ΑΠΘ http://mougios.webpages.auth.gr Μεταβολικό σύνδροµο Παθολογική κατάσταση που χαρακτηρίζεται από:
ΟΡΟΛΟΣΤΗΣΑΣΚΗΣΗΣΣΤΟ ΜΕΤΑΒΟΛΙΚΟΣΥΝ ΡΟΜΟ, ΣΤΑ ΛΙΠΙ ΙΑ ΚΑΙ ΣΤΙΣ ΛΙΠΟΠΡΩΤΕΪΝΕΣ ΒασίληςΜούγιος, PhD ΤΕΦΑΑ ΑΠΘ http://mougios.webpages.auth.gr Μεταβολικό σύνδροµο Παθολογική κατάσταση που χαρακτηρίζεται από:
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης
 Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. 194.1μg 99μg
 1 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VITALIPID ( ADULT ) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1ml VITALIPID ADULT περιέχει: Δραστικά συστατικά Retinopalmitate
1 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VITALIPID ( ADULT ) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1ml VITALIPID ADULT περιέχει: Δραστικά συστατικά Retinopalmitate
gr
 Η επίδραση της περίσσειας θυρεοειδικών ορµονών στα οστά ήταν γνωστή πριν από την εµφάνιση των αντιθυρεοειδικών φαρµάκων. Μία από τις πρώτες αναφορές καταγράφηκε το 1891από τον von Recklinghausen και αναφέρει
Η επίδραση της περίσσειας θυρεοειδικών ορµονών στα οστά ήταν γνωστή πριν από την εµφάνιση των αντιθυρεοειδικών φαρµάκων. Μία από τις πρώτες αναφορές καταγράφηκε το 1891από τον von Recklinghausen και αναφέρει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΡΩΤΟΚΟΛΛΑ ΘΕΡΑΠΕΥΤΙΚΗΣ ΑΣΚΗΣΗΣ ΣΤΙΣ ΔΥΣΛΙΠΙΔΑΙΜΙΕΣ
 ΠΡΩΤΟΚΟΛΛΑ ΘΕΡΑΠΕΥΤΙΚΗΣ ΑΣΚΗΣΗΣ ΣΤΙΣ ΔΥΣΛΙΠΙΔΑΙΜΙΕΣ Η δυσλιπιδαιμία χαρακτηρίζει τις μη φυσιολογικές συγκεντρώσεις λιπιδίων και λιποπρωτεϊνών στο αίμα. Ορίζεται περαιτέρω ως η ύπαρξη αυξημένων συγκεντρώσεων
ΠΡΩΤΟΚΟΛΛΑ ΘΕΡΑΠΕΥΤΙΚΗΣ ΑΣΚΗΣΗΣ ΣΤΙΣ ΔΥΣΛΙΠΙΔΑΙΜΙΕΣ Η δυσλιπιδαιμία χαρακτηρίζει τις μη φυσιολογικές συγκεντρώσεις λιπιδίων και λιποπρωτεϊνών στο αίμα. Ορίζεται περαιτέρω ως η ύπαρξη αυξημένων συγκεντρώσεων
Φυσιολογική Αύξηση Παιδιού & Εφήβου & Διαταραχές
 Φυσιολογική Αύξηση Παιδιού & Εφήβου & Διαταραχές Φλώρα Μπακοπούλου Επίκουρη Καθηγήτρια Παιδιατρικής - Εφηβικής Ιατρικής Ειδικό Κέντρο Εφηβικής Ιατρικής (Ε.Κ.Ε.Ι.) Α Παιδιατρική Κλινική ΕΚΠΑ Νοσοκομείο
Φυσιολογική Αύξηση Παιδιού & Εφήβου & Διαταραχές Φλώρα Μπακοπούλου Επίκουρη Καθηγήτρια Παιδιατρικής - Εφηβικής Ιατρικής Ειδικό Κέντρο Εφηβικής Ιατρικής (Ε.Κ.Ε.Ι.) Α Παιδιατρική Κλινική ΕΚΠΑ Νοσοκομείο
Dr ΣΑΡΡΗΣ Ι. - αµ. επ. καθηγ. ΑΒΡΑΜΙ ΗΣ Α. ενδοκρινολόγοι. gr
 Dr ΣΑΡΡΗΣ Ι. - αµ. επ. καθηγ. ΑΒΡΑΜΙ ΗΣ Α. ενδοκρινολόγοι ΕΙΣΑΓΩΓΗ Κατά τη διάρκεια υποσιτισµού ή βαριάς µη θυρεοειδικής νόσου, παρατηρούνται µεταβολές των επιπέδων των θυρεοειδικών ορµονών στο αίµα, που
Dr ΣΑΡΡΗΣ Ι. - αµ. επ. καθηγ. ΑΒΡΑΜΙ ΗΣ Α. ενδοκρινολόγοι ΕΙΣΑΓΩΓΗ Κατά τη διάρκεια υποσιτισµού ή βαριάς µη θυρεοειδικής νόσου, παρατηρούνται µεταβολές των επιπέδων των θυρεοειδικών ορµονών στο αίµα, που
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΑΡΕΝΤΕΡΙΚΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ
 ΠΑΡΕΝΤΕΡΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ https://users.auth.gr/epontiki Ελένη Ποντίκη Θεσσαλονίκη 2018 Παρεντερικά διαλύματα Αποστειρωμένα διαλύματα που προορίζονται: για την στοιχείων αναπλήρωση
ΠΑΡΕΝΤΕΡΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ https://users.auth.gr/epontiki Ελένη Ποντίκη Θεσσαλονίκη 2018 Παρεντερικά διαλύματα Αποστειρωμένα διαλύματα που προορίζονται: για την στοιχείων αναπλήρωση
AMINOPLASMAL HEPA-10%
 AMINOPLASMAL HEPA-10% ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1.ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Αminoplasmal Hepa 10% 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 1000ml διαλύματος περιέχουν: L-Isoleucin
AMINOPLASMAL HEPA-10% ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1.ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Αminoplasmal Hepa 10% 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 1000ml διαλύματος περιέχουν: L-Isoleucin
Ηλίας Ν. Μυγδάλης. Β Παθολογική Κλινική και Διαβητολογικό Κέντρο, Γενικό Νοσοκομείο ΝΙΜΤΣ, Αθήνα
 ΕΤΟΣ ΙΔΡΥΣΕΩΣ 1942 «Έναρξη ινσουλίνης στα άτομα με σακχαρώδη διαβήτη τύπου 2: πότε και πως ;» Ηλίας Ν. Μυγδάλης Β Παθολογική Κλινική και Διαβητολογικό Κέντρο, Γενικό Νοσοκομείο ΝΙΜΤΣ, Αθήνα Ειδικό φροντιστήριο
ΕΤΟΣ ΙΔΡΥΣΕΩΣ 1942 «Έναρξη ινσουλίνης στα άτομα με σακχαρώδη διαβήτη τύπου 2: πότε και πως ;» Ηλίας Ν. Μυγδάλης Β Παθολογική Κλινική και Διαβητολογικό Κέντρο, Γενικό Νοσοκομείο ΝΙΜΤΣ, Αθήνα Ειδικό φροντιστήριο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8%
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8% 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Νάτριο Ανθρακικό Όξινο/DEMO (Sodium Bicarbonate/DEMO) 2. ΠΟΙΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8% 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Νάτριο Ανθρακικό Όξινο/DEMO (Sodium Bicarbonate/DEMO) 2. ΠΟΙΟΤΙΚΗ
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
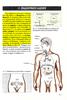 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
Σακχαρώδης Διαβήτης. Ένας σύγχρονος ύπουλος εχθρός
 Σακχαρώδης Διαβήτης Ένας σύγχρονος ύπουλος εχθρός Φιρούζα Κουρτίδου Ειδικός Παθολόγος με μετεκπαίδευση στο Σακχαρώδη Διαβήτη Φιρούζα Κουρτίδου Ειδικός Παθολόγος Μετεκπαιδευθείσα στο Σακχαρώδη Διαβήτη Περιεχόμενα
Σακχαρώδης Διαβήτης Ένας σύγχρονος ύπουλος εχθρός Φιρούζα Κουρτίδου Ειδικός Παθολόγος με μετεκπαίδευση στο Σακχαρώδη Διαβήτη Φιρούζα Κουρτίδου Ειδικός Παθολόγος Μετεκπαιδευθείσα στο Σακχαρώδη Διαβήτη Περιεχόμενα
ΠΑΡΑΡΤΗΜΑ ΙII ΙΟΡΘΩΣΕΙΣ ΣΤΗΝ ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΩΝ ΦΥΛΛΩΝ Ο ΗΓΙΩΝ ΧΡΗΣHΣ
 ΠΑΡΑΡΤΗΜΑ ΙII ΙΟΡΘΩΣΕΙΣ ΣΤΗΝ ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΩΝ ΦΥΛΛΩΝ Ο ΗΓΙΩΝ ΧΡΗΣHΣ 26 ΠΑΡΑΓΡΑΦΟΥΣ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΤΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ ΠΟΥ ΠΕΡΙΕΧΟΥΝ
ΠΑΡΑΡΤΗΜΑ ΙII ΙΟΡΘΩΣΕΙΣ ΣΤΗΝ ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΩΝ ΦΥΛΛΩΝ Ο ΗΓΙΩΝ ΧΡΗΣHΣ 26 ΠΑΡΑΓΡΑΦΟΥΣ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΤΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ ΠΟΥ ΠΕΡΙΕΧΟΥΝ
Εφαρμοσμένη Αθλητική Εργοφυσιολογία
 Εφαρμοσμένη Αθλητική Εργοφυσιολογία Άσκηση και προπόνηση για παιδιά και εφήβους Βασίλης Πασχάλης Επίκουρος καθηγητής ΤΕΦΑΑ - ΕΚΠΑ Ανάπτυξη, εξέλιξη και ωρίμανση Ανάπτυξη: αύξηση του σώματος ή μελών του
Εφαρμοσμένη Αθλητική Εργοφυσιολογία Άσκηση και προπόνηση για παιδιά και εφήβους Βασίλης Πασχάλης Επίκουρος καθηγητής ΤΕΦΑΑ - ΕΚΠΑ Ανάπτυξη, εξέλιξη και ωρίμανση Ανάπτυξη: αύξηση του σώματος ή μελών του
Εφαρμογές αρχών φαρμακολογίας
 Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
Παράρτημα ΙΙΙ. Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης
 Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης Σημείωση : Οι τροποποιήσεις στην Περίληψη των Χαρακτηριστικών του Προϊόντος
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης Σημείωση : Οι τροποποιήσεις στην Περίληψη των Χαρακτηριστικών του Προϊόντος
Diabetes_ protect our future.mp4
 Diabetes_ protect our future.mp4 14/11 Γενέθλια του νομπελίστα γιατρού Φρέντερικ Μπάντινγκ 1991 από τη Διεθνή Ομοσπονδία για το Διαβήτη 2007:επίσημη Ημέρα από τα Ηνωμένα Έθνη Θέμα 2009 2013: Εκπαίδευση
Diabetes_ protect our future.mp4 14/11 Γενέθλια του νομπελίστα γιατρού Φρέντερικ Μπάντινγκ 1991 από τη Διεθνή Ομοσπονδία για το Διαβήτη 2007:επίσημη Ημέρα από τα Ηνωμένα Έθνη Θέμα 2009 2013: Εκπαίδευση
Από τον Κώστα κουραβανα
 Από τον Κώστα κουραβανα Περιεχόμενα Γενικός ορισμός παχυσαρκίας Ορμονικοί-Γονιδιακοί-παράγοντες Επιπτώσεις στην υγεία Θεραπεία-Δίαιτα Γενικός ορισμός παχυσαρκίας Παχυσαρκία είναι κλινική κατάσταση στην
Από τον Κώστα κουραβανα Περιεχόμενα Γενικός ορισμός παχυσαρκίας Ορμονικοί-Γονιδιακοί-παράγοντες Επιπτώσεις στην υγεία Θεραπεία-Δίαιτα Γενικός ορισμός παχυσαρκίας Παχυσαρκία είναι κλινική κατάσταση στην
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 Πολυσακχαριδικό πολυδύναμο εμβόλιο ττνευμονιόκοκκου 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 PNEUMO 23* Ενέσιμο διάλυμα 25 mcg χ 23 / 0,5 ml P.F.Syringe (1 Dose) 1.2 Σύνθεση Δραστική ουσία: Purified
Πολυσακχαριδικό πολυδύναμο εμβόλιο ττνευμονιόκοκκου 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 PNEUMO 23* Ενέσιμο διάλυμα 25 mcg χ 23 / 0,5 ml P.F.Syringe (1 Dose) 1.2 Σύνθεση Δραστική ουσία: Purified
2.2 Ποσοτική σύνθεση 100ml διαλύματος περιέχουν 25g πρωτεΐνης πλάσματος με τουλάχιστον το 95% ανθρώπινη λευκωματίνη.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Plasbumin 25 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 2.1 Ποιοτική σύνθεση Ανθρώπινη λευκωματίνη από ανθρώπινο πλάσμα 2.2 Ποσοτική
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Plasbumin 25 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 2.1 Ποιοτική σύνθεση Ανθρώπινη λευκωματίνη από ανθρώπινο πλάσμα 2.2 Ποσοτική
6ο Διαβητολογικό. Συνέδριο. 20 έως 22 Νοεμβρίου 2009. Σακχαρώδης Διαβήτης Γνώση βασισμένη στην ένδειξη. Κάνουμε το σωστό; Πάτρα.
 Ιατρική Σχολή Πανεπιστημίου Πατρών Πανεπιστημιακή Παθολογική Κλινική Διαβητολογικό Κέντρο 6ο Διαβητολογικό Συνέδριο Σακχαρώδης Διαβήτης Γνώση βασισμένη στην ένδειξη Κάνουμε το σωστό; Ενα διαχρονικό δίλημμα
Ιατρική Σχολή Πανεπιστημίου Πατρών Πανεπιστημιακή Παθολογική Κλινική Διαβητολογικό Κέντρο 6ο Διαβητολογικό Συνέδριο Σακχαρώδης Διαβήτης Γνώση βασισμένη στην ένδειξη Κάνουμε το σωστό; Ενα διαχρονικό δίλημμα
Κάθε επικαλυμένο με λεπτό υμένιο δισκίο περιέχει 5 mg levocetirizine dihydrochloride.
 Xozal 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Xozal 5 mg επικαλυμένα με λεπτό υμένιο δισκία 1.2 Σύνθεση Δραστική ουσία: Ievocetiiizine dihydrochloride Έκδοχα: microcrystalline cellulose,
Xozal 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Xozal 5 mg επικαλυμένα με λεπτό υμένιο δισκία 1.2 Σύνθεση Δραστική ουσία: Ievocetiiizine dihydrochloride Έκδοχα: microcrystalline cellulose,
ΠΕΡΙΛΗΨΗ TΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ. Ενα g ρινικής αλοιφής περιέχει 21,5mg Mupirocin calcium που αντιστοιχεί σε 20mg (2% w/w) Mupirocin.
 ΠΕΡΙΛΗΨΗ TΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BACTROBAN Ρινική αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ενα g ρινικής αλοιφής περιέχει 21,5mg Mupirocin calcium που αντιστοιχεί
ΠΕΡΙΛΗΨΗ TΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BACTROBAN Ρινική αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ενα g ρινικής αλοιφής περιέχει 21,5mg Mupirocin calcium που αντιστοιχεί
2.4.4 Κύηση Επειδή η ενδορινική καλσιτονίνη ενδείκνυται σε µετεµµηνοπαυσιακές γυναίκες, δεν έχουν διεξαχθεί µελέτες σε έγκυες γυναίκες ή θηλάζουσες
 Calcitonin/Target Salmon calcitonin ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Oνοµασία προϊόντος Calcitonin/ Target 1.2 Σύνθεση ραστική ουσία: Καλσιτονίνη σολοµού. Έκδοχα: Sodium
Calcitonin/Target Salmon calcitonin ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Oνοµασία προϊόντος Calcitonin/ Target 1.2 Σύνθεση ραστική ουσία: Καλσιτονίνη σολοµού. Έκδοχα: Sodium
AΣΘΜΑ ΚΑΙ ΕΓΚΥΜΟΣΥΝΗ ΑΛΛΗΛΕΠΙΔΡΑΣΕΙΣ ΑΣΘΜΑΤΟΣ & ΚΥΗΣΗΣ
 AΣΘΜΑ ΚΑΙ ΕΓΚΥΜΟΣΥΝΗ Το άσθμα είναι ένα από τις πιο συχνές νόσους που περιπλέκει την εγκυμοσύνη. Πρόσφατες μελέτες δείχνουν πως περίπου 8-10% των εγκύων έχουν άσθμα και μπορεί να επηρεάσει την εγκυμοσύνη
AΣΘΜΑ ΚΑΙ ΕΓΚΥΜΟΣΥΝΗ Το άσθμα είναι ένα από τις πιο συχνές νόσους που περιπλέκει την εγκυμοσύνη. Πρόσφατες μελέτες δείχνουν πως περίπου 8-10% των εγκύων έχουν άσθμα και μπορεί να επηρεάσει την εγκυμοσύνη
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Cetrotide 0,25 mg κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φιαλίδιο περιέχει 0,25
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Cetrotide 0,25 mg κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φιαλίδιο περιέχει 0,25
ΤΟΥ ΣΑΚΧΑΡΩ Η ΙΑΒΗΤΗ. ρ. Μυλωνάκη Θεοχαρούλα. Υπεύθυνη ιαβητολογικού Ιατρείου
 ΕΓΚΑΙΡΗ ΙΑΓΝΩΣΗ & ΑΝΤΙΜΕΤΩΠΙΣΗ ΤΟΥ ΣΑΚΧΑΡΩ Η ΙΑΒΗΤΗ ρ. Μυλωνάκη Θεοχαρούλα ιευθύντρια Β Παθολογικής Κλινικής Γ.Ν. Χανίων Υπεύθυνη ιαβητολογικού Ιατρείου Πινακοθήκη ήµου Χανίων, 17/02/2012 Συχνότητα του
ΕΓΚΑΙΡΗ ΙΑΓΝΩΣΗ & ΑΝΤΙΜΕΤΩΠΙΣΗ ΤΟΥ ΣΑΚΧΑΡΩ Η ΙΑΒΗΤΗ ρ. Μυλωνάκη Θεοχαρούλα ιευθύντρια Β Παθολογικής Κλινικής Γ.Ν. Χανίων Υπεύθυνη ιαβητολογικού Ιατρείου Πινακοθήκη ήµου Χανίων, 17/02/2012 Συχνότητα του
ΜΑΘΗΜΑΤΑ ΦΥΣΙΟΛΟΓΙΑΣ
 ΜΑΘΗΜΑΤΑ ΦΥΣΙΟΛΟΓΙΑΣ ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ KAI ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ Νικόλαος Χ. Σύρμος ANAΠΑΡΑΓΩΓΗ Ο άνθρωπος αναπαράγεται με αμφιγονική αναπαραγωγή. Δύο γαμετικά κύτταρα,το ωάριο (θηλυκό)
ΜΑΘΗΜΑΤΑ ΦΥΣΙΟΛΟΓΙΑΣ ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ KAI ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ Νικόλαος Χ. Σύρμος ANAΠΑΡΑΓΩΓΗ Ο άνθρωπος αναπαράγεται με αμφιγονική αναπαραγωγή. Δύο γαμετικά κύτταρα,το ωάριο (θηλυκό)
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BTVPUR AlSap 4, ενέσιµο εναιώρηµα για πρόβατα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δόση του
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BTVPUR AlSap 4, ενέσιµο εναιώρηµα για πρόβατα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δόση του
Οστεοπόρωση. Διάγνωση, πρόληψη και θεραπεία. Δρ. Χρήστος Κ. Γιαννακόπουλος Ορθοπαιδικός Χειρουργός
 Οστεοπόρωση Διάγνωση, πρόληψη και θεραπεία Δρ. Χρήστος Κ. Γιαννακόπουλος Ορθοπαιδικός Χειρουργός Η οστεοπόρωση είναι πιο συχνή από τις παθήσεις της καρδιάς και των πνευμόνων Οστεοπόρωση: Η σιωπηλή επιδημία
Οστεοπόρωση Διάγνωση, πρόληψη και θεραπεία Δρ. Χρήστος Κ. Γιαννακόπουλος Ορθοπαιδικός Χειρουργός Η οστεοπόρωση είναι πιο συχνή από τις παθήσεις της καρδιάς και των πνευμόνων Οστεοπόρωση: Η σιωπηλή επιδημία
Φαρμακοκινητική. Χρυσάνθη Σαρδέλη
 Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
ΕΦΑΡΜΟΓΗ HACCP ΣΤΗΝ ΚΟΥΖΙΝΑ ΝΟΣΟΚΟΜΕΙΟΥ ΕΙΔΙΚΕΣ ΔΙΑΙΤΕΣ. Ελπίδα Παπαδοπούλου Διαιτολόγος, Ε. Α. Ν. Πειραιά «ΜΕΤΑΞΑ»
 ΕΦΑΡΜΟΓΗ HACCP ΣΤΗΝ ΚΟΥΖΙΝΑ ΝΟΣΟΚΟΜΕΙΟΥ ΕΙΔΙΚΕΣ ΔΙΑΙΤΕΣ Ελπίδα Παπαδοπούλου Διαιτολόγος, Ε. Α. Ν. Πειραιά «ΜΕΤΑΞΑ» ΣΧΕΣΗ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΥΓΕΙΑΣ Πρόληψη εμφάνισης νοσημάτων Θεραπεία ασθενών στο χώρο του νοσοκομείου
ΕΦΑΡΜΟΓΗ HACCP ΣΤΗΝ ΚΟΥΖΙΝΑ ΝΟΣΟΚΟΜΕΙΟΥ ΕΙΔΙΚΕΣ ΔΙΑΙΤΕΣ Ελπίδα Παπαδοπούλου Διαιτολόγος, Ε. Α. Ν. Πειραιά «ΜΕΤΑΞΑ» ΣΧΕΣΗ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΥΓΕΙΑΣ Πρόληψη εμφάνισης νοσημάτων Θεραπεία ασθενών στο χώρο του νοσοκομείου
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΙΠΠΟΚΡΑΤΕΙΕΣ ΗΜΕΡΕΣ ΚΑΡΔΙΟΛΟΓΙΑΣ 2019 ΠΡΟΛΗΨΗ ΚΑΡΔΙΑΓΓΕΙΑΚΩΝ ΠΑΘΗΣΕΩΝ ΣΤΑ ΠΑΙΔΙΑ. ΡΟΥΜΤΣΙΟΥ ΜΑΡΙΑ Νοσηλεύτρια CPN, MSc Α Παιδιατρικής κλινικής ΑΠΘ
 ΙΠΠΟΚΡΑΤΕΙΕΣ ΗΜΕΡΕΣ ΚΑΡΔΙΟΛΟΓΙΑΣ 2019 ΠΡΟΛΗΨΗ ΚΑΡΔΙΑΓΓΕΙΑΚΩΝ ΠΑΘΗΣΕΩΝ ΣΤΑ ΠΑΙΔΙΑ ΡΟΥΜΤΣΙΟΥ ΜΑΡΙΑ Νοσηλεύτρια CPN, MSc Α Παιδιατρικής κλινικής ΑΠΘ «Η μεγαλύτερη δύναμη της δημόσιας υγείας είναι η πρόληψη»
ΙΠΠΟΚΡΑΤΕΙΕΣ ΗΜΕΡΕΣ ΚΑΡΔΙΟΛΟΓΙΑΣ 2019 ΠΡΟΛΗΨΗ ΚΑΡΔΙΑΓΓΕΙΑΚΩΝ ΠΑΘΗΣΕΩΝ ΣΤΑ ΠΑΙΔΙΑ ΡΟΥΜΤΣΙΟΥ ΜΑΡΙΑ Νοσηλεύτρια CPN, MSc Α Παιδιατρικής κλινικής ΑΠΘ «Η μεγαλύτερη δύναμη της δημόσιας υγείας είναι η πρόληψη»
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ EVATON-B. Ενέσιμο διάλυμα.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ EVATON-B Ενέσιμο διάλυμα 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ EVATON-B, ενέσιμο διάλυμα (10+4+4+40+6)mg/2ml AMP 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ανά 2ml: Thiamine
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ EVATON-B Ενέσιμο διάλυμα 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ EVATON-B, ενέσιμο διάλυμα (10+4+4+40+6)mg/2ml AMP 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ανά 2ml: Thiamine
ΤΑ 10 ΜΥΣΤΙΚΑ ΤΗΣ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡ ΙΑΣ. Κέντρο Πρόληψης Γυναικείων Καρδιολογικών Νοσηµάτων Β Καρδιολογική Κλινική. Ενηµερωτικό Έντυπο
 ΤΑ 10 ΜΥΣΤΙΚΑ ΤΗΣ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡ ΙΑΣ Β Καρδιολογική Κλινική Ενηµερωτικό Έντυπο ΤΑ 10 ΜΥΣΤΙΚΑ ΤΗΣ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡ ΙΑΣ Οι γυναίκες σήµερα πληρώνουν (όπως και οι άνδρες) το τίµηµα της σύγχρονης ζωής. Η παράταση
ΤΑ 10 ΜΥΣΤΙΚΑ ΤΗΣ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡ ΙΑΣ Β Καρδιολογική Κλινική Ενηµερωτικό Έντυπο ΤΑ 10 ΜΥΣΤΙΚΑ ΤΗΣ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡ ΙΑΣ Οι γυναίκες σήµερα πληρώνουν (όπως και οι άνδρες) το τίµηµα της σύγχρονης ζωής. Η παράταση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ERRKES. Οφθαλμικές σταγόνες, διάλυμα
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
Επιπλέον η έλλειψη ασβεστίου μπορεί να οδηγήσει στις παρακάτω παθολογικές καταστάσεις:
 Γράφει: Φανή Πρεβέντη, MSc Κλινική Διαιτολόγος - Διατροφολόγος Το σώμα μας περιέχει μεγάλες ποσότητες ασβεστίου. Συγκεκριμένα, το ασβέστο είναι υπεύθυνο για το 1,5-2% του σωματικού μας βάρους. Είναι το
Γράφει: Φανή Πρεβέντη, MSc Κλινική Διαιτολόγος - Διατροφολόγος Το σώμα μας περιέχει μεγάλες ποσότητες ασβεστίου. Συγκεκριμένα, το ασβέστο είναι υπεύθυνο για το 1,5-2% του σωματικού μας βάρους. Είναι το
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann, Μασώμενα δισκία, (100 + 0,350) mg/δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ (σε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann, Μασώμενα δισκία, (100 + 0,350) mg/δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ (σε
Γράφει: Ευθυμία Πετράτου, Ειδική Παθολόγος, Υπεύθυνη Ιατρείου Διαταραχής Λιπιδίων, Ιατρικού Π. Φαλήρου
 Γράφει: Ευθυμία Πετράτου, Ειδική Παθολόγος, Υπεύθυνη Ιατρείου Διαταραχής Λιπιδίων, Ιατρικού Π. Φαλήρου Οι δυσλιπιδαιμίες είναι παθολογικές καταστάσεις με διαταραχές των λιπιδίων του αίματος ποσοτικές αλλά
Γράφει: Ευθυμία Πετράτου, Ειδική Παθολόγος, Υπεύθυνη Ιατρείου Διαταραχής Λιπιδίων, Ιατρικού Π. Φαλήρου Οι δυσλιπιδαιμίες είναι παθολογικές καταστάσεις με διαταραχές των λιπιδίων του αίματος ποσοτικές αλλά
ΟΡΜΟΝΙΚΕΣ ΜΕΤΑΒΟΛΕΣ ΚΑΤΑ ΤΗΝ ΑΘΛΗΣΗ
 ΟΡΜΟΝΙΚΕΣ ΜΕΤΑΒΟΛΕΣ ΚΑΤΑ ΤΗΝ ΑΘΛΗΣΗ Βασίλης Μούγιος, PhD ΤΕΦΑΑ ΑΠΘ http://users.auth.gr/mougios Παράγοντες που επηρεάζουν τις ορµονικές αποκρίσεις στην άσκηση Τύπος άσκησης Οξεία Χρόνια Προσαρµογές Αντοχής/δυναµική/αερόβια
ΟΡΜΟΝΙΚΕΣ ΜΕΤΑΒΟΛΕΣ ΚΑΤΑ ΤΗΝ ΑΘΛΗΣΗ Βασίλης Μούγιος, PhD ΤΕΦΑΑ ΑΠΘ http://users.auth.gr/mougios Παράγοντες που επηρεάζουν τις ορµονικές αποκρίσεις στην άσκηση Τύπος άσκησης Οξεία Χρόνια Προσαρµογές Αντοχής/δυναµική/αερόβια
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ. T r a v o g e n (Isoconazole)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ T r a v o g e n (Isoconazole) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Travogen 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 g κολπικής κρέµας Travogen περιέχει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ T r a v o g e n (Isoconazole) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Travogen 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 g κολπικής κρέµας Travogen περιέχει
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
Παράρτημα I Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων άδειας(-ών) κυκλοφορίας
 Παράρτημα I Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων άδειας(-ών) κυκλοφορίας Επιστημονικά πορίσματα Λαμβάνοντας υπόψη την έκθεση αξιολόγησης της PRAC σχετικά με την (τις) Έκθεση(-εις)
Παράρτημα I Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων άδειας(-ών) κυκλοφορίας Επιστημονικά πορίσματα Λαμβάνοντας υπόψη την έκθεση αξιολόγησης της PRAC σχετικά με την (τις) Έκθεση(-εις)
Σακχαρώδης διαβήτης και οστεοπόρωση - Ο Δρόμος για την Θεραπεία Τρίτη, 23 Νοέμβριος :22
 Δημήτρης Ι. Χατζηδάκης, Αναπληρωτής Καθηγητής Παθολογίας - Ενδοκρινολογίας, Υπεύθυνος Ενδοκρινολογικής Mονάδας Β' Προπαιδευτικής Παθολογικής Κλινικής Πανεπιστημίου Αθηνών, Πανεπιστημιακό Γενικό Νοσοκομείο
Δημήτρης Ι. Χατζηδάκης, Αναπληρωτής Καθηγητής Παθολογίας - Ενδοκρινολογίας, Υπεύθυνος Ενδοκρινολογικής Mονάδας Β' Προπαιδευτικής Παθολογικής Κλινικής Πανεπιστημίου Αθηνών, Πανεπιστημιακό Γενικό Νοσοκομείο
ΠΑΡΑΡΤΗΜΑ ΟΡΟΙ Ή ΠΕΡΙΟΡΙΣΜΟΙ ΟΣΟΝ ΑΦΟΡΑ ΤΗΝ ΑΣΦΑΛΗ ΚΑΙ ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΧΡΗΣΗ ΤΟΥ ΦΑΡΜΑΚΟΥ ΠΟΥ ΠΡΕΠΕΙ ΝΑ ΕΦΑΡΜΟΣΤΟΥΝ ΑΠΟ ΤΑ ΚΡΑΤΗ ΜΕΛΗ
 ΠΑΡΑΡΤΗΜΑ ΟΡΟΙ Ή ΠΕΡΙΟΡΙΣΜΟΙ ΟΣΟΝ ΑΦΟΡΑ ΤΗΝ ΑΣΦΑΛΗ ΚΑΙ ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΧΡΗΣΗ ΤΟΥ ΦΑΡΜΑΚΟΥ ΠΟΥ ΠΡΕΠΕΙ ΝΑ ΕΦΑΡΜΟΣΤΟΥΝ ΑΠΟ ΤΑ ΚΡΑΤΗ ΜΕΛΗ ΟΡΟΙ Ή ΠΕΡΙΟΡΙΣΜΟΙ ΟΣΟΝ ΑΦΟΡΑ ΤΗΝ ΑΣΦΑΛΗ ΚΑΙ ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΧΡΗΣΗ ΤΟΥ
ΠΑΡΑΡΤΗΜΑ ΟΡΟΙ Ή ΠΕΡΙΟΡΙΣΜΟΙ ΟΣΟΝ ΑΦΟΡΑ ΤΗΝ ΑΣΦΑΛΗ ΚΑΙ ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΧΡΗΣΗ ΤΟΥ ΦΑΡΜΑΚΟΥ ΠΟΥ ΠΡΕΠΕΙ ΝΑ ΕΦΑΡΜΟΣΤΟΥΝ ΑΠΟ ΤΑ ΚΡΑΤΗ ΜΕΛΗ ΟΡΟΙ Ή ΠΕΡΙΟΡΙΣΜΟΙ ΟΣΟΝ ΑΦΟΡΑ ΤΗΝ ΑΣΦΑΛΗ ΚΑΙ ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΧΡΗΣΗ ΤΟΥ
Ο σακχαρώδης διαβήτης ( ΣΔ ) είναι το κλινικό σύνδρομο που οφείλεται. είτε σε έλλειψη ινσουλίνης λόγω μείωσης η παύσης παραγωγής (σακχαρώδης
 ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΚΑΤΟΙΚΙΔΙΑ ΖΩΑ Ο σακχαρώδης διαβήτης ( ΣΔ ) είναι το κλινικό σύνδρομο που οφείλεται είτε σε έλλειψη ινσουλίνης λόγω μείωσης η παύσης παραγωγής (σακχαρώδης διαβήτης τύπου 1 ) είτε
ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ ΚΑΙ ΚΑΤΟΙΚΙΔΙΑ ΖΩΑ Ο σακχαρώδης διαβήτης ( ΣΔ ) είναι το κλινικό σύνδρομο που οφείλεται είτε σε έλλειψη ινσουλίνης λόγω μείωσης η παύσης παραγωγής (σακχαρώδης διαβήτης τύπου 1 ) είτε
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
ΚΕΝΤΡΟ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡΔΙΑΣ
 ΚΕΝΤΡΟ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡΔΙΑΣ Τα καρδιαγγειακά νοσήματα παραδοσιακά θεωρούνται νοσήματα των ανδρών. Ωστόσο, τα στοιχεία δείχνουν ότι οι καρδιαγγειακές παθήσεις αποτελούν την κύρια αιτία θανάτου στις γυναίκες
ΚΕΝΤΡΟ ΓΥΝΑΙΚΕΙΑΣ ΚΑΡΔΙΑΣ Τα καρδιαγγειακά νοσήματα παραδοσιακά θεωρούνται νοσήματα των ανδρών. Ωστόσο, τα στοιχεία δείχνουν ότι οι καρδιαγγειακές παθήσεις αποτελούν την κύρια αιτία θανάτου στις γυναίκες
Η απώλεια του καλίου μειώνει την διεγερσιμότητα των μυϊκών κυττάρων (μυϊκή κόπωση
 Ηλεκτρολύτες Η απώλεια του καλίου μειώνει την διεγερσιμότητα των μυϊκών κυττάρων (μυϊκή κόπωση Αυξάνεται με την οξεία, έντονη σωματική άσκηση (προσωρινή αύξηση), από υπερβολική χρήση νατρίου, ανεπαρκή
Ηλεκτρολύτες Η απώλεια του καλίου μειώνει την διεγερσιμότητα των μυϊκών κυττάρων (μυϊκή κόπωση Αυξάνεται με την οξεία, έντονη σωματική άσκηση (προσωρινή αύξηση), από υπερβολική χρήση νατρίου, ανεπαρκή
Παχυσαρκία και Σακχαρώδης Διαβήτης
 Παχυσαρκία και Σακχαρώδης Διαβήτης Τι είναι ο Σακχαρώδης Διαβήτης τύπου 2 (ΣΔ2) Ο Σακχαρώδης Διαβήτης γενικά είναι μια πάθηση κατά την οποία ο οργανισμός και συγκεκριμένα το πάγκρεας δεν παράγει ή δεν
Παχυσαρκία και Σακχαρώδης Διαβήτης Τι είναι ο Σακχαρώδης Διαβήτης τύπου 2 (ΣΔ2) Ο Σακχαρώδης Διαβήτης γενικά είναι μια πάθηση κατά την οποία ο οργανισμός και συγκεκριμένα το πάγκρεας δεν παράγει ή δεν
ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΙΑΓΝΩΣΗ & ΘΕΡΑΠΕΙΑ ΤΩΝ ΜΕΤΑΒΟΛΙΚΩΝ ΙΑΤΑΡΑΧΩΝ
 ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΙΑΓΝΩΣΗ & ΘΕΡΑΠΕΙΑ ΤΩΝ ΜΕΤΑΒΟΛΙΚΩΝ ΙΑΤΑΡΑΧΩΝ Το Ερρίκος Ντυνάν Hospital Center ακολουθώντας σύγχρονες διεθνείς πρακτικές στην παροχή υπηρεσιών υγείας προχώρησε στη δηµιουργία του Κέντρου
ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΙΑΓΝΩΣΗ & ΘΕΡΑΠΕΙΑ ΤΩΝ ΜΕΤΑΒΟΛΙΚΩΝ ΙΑΤΑΡΑΧΩΝ Το Ερρίκος Ντυνάν Hospital Center ακολουθώντας σύγχρονες διεθνείς πρακτικές στην παροχή υπηρεσιών υγείας προχώρησε στη δηµιουργία του Κέντρου
Υγεία και Άσκηση Ειδικών Πληθυσμών ΜΚ0958
 ΣΧΟΛΙΑΣΜΟΣ ΠΡΟΟΔΟΥ ΛΑΝΘΑΣΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΥΠΟΓΛΥΚΑΙΜΙΑ ΕΙΝΑΙ Η ΜΕΓΑΛΗ ΠΡΟΣΛΗΨΗ ΣΑΚΧΑΡΩΝ-ΠΡΟΤΕΙΝΕΤΑΙ ΑΣΚΗΣΗ ΣΕ ΑΛΜΥΡΟ ΝΕΡΟ ΥΠΟΓΛΥΚΑΙΜΙΑ ΑΠΟΤΕΛΕΣΜΑ ΑΡΤΗΡΙΑΚΗ ΥΠΕΡΤΑΣΗΣ ΑΣΚΗΣΗ ΣΤΟΝ ΣΔ -ΜΕΙΩΣΗ ΥΠΕΡΒΟΛΙΚΗΣ
ΣΧΟΛΙΑΣΜΟΣ ΠΡΟΟΔΟΥ ΛΑΝΘΑΣΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΥΠΟΓΛΥΚΑΙΜΙΑ ΕΙΝΑΙ Η ΜΕΓΑΛΗ ΠΡΟΣΛΗΨΗ ΣΑΚΧΑΡΩΝ-ΠΡΟΤΕΙΝΕΤΑΙ ΑΣΚΗΣΗ ΣΕ ΑΛΜΥΡΟ ΝΕΡΟ ΥΠΟΓΛΥΚΑΙΜΙΑ ΑΠΟΤΕΛΕΣΜΑ ΑΡΤΗΡΙΑΚΗ ΥΠΕΡΤΑΣΗΣ ΑΣΚΗΣΗ ΣΤΟΝ ΣΔ -ΜΕΙΩΣΗ ΥΠΕΡΒΟΛΙΚΗΣ
ΑΥΞΗΤΙΚΗ ΟΡΜΟΝΗ, ΙΝΣΟΥΛΙΝΟΜΙΜΗΤΙΚΟΣ ΑΥΞΗΤΙΚΟΣ ΠΑΡΑΓΟΝΤΑΣ-Ι ΚΑΙ ΑΣΚΗΣΗ
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΑΥΞΗΤΙΚΗ ΟΡΜΟΝΗ, ΙΝΣΟΥΛΙΝΟΜΙΜΗΤΙΚΟΣ ΑΥΞΗΤΙΚΟΣ ΠΑΡΑΓΟΝΤΑΣ-Ι ΚΑΙ ΑΣΚΗΣΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Η αυξητική
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΑΥΞΗΤΙΚΗ ΟΡΜΟΝΗ, ΙΝΣΟΥΛΙΝΟΜΙΜΗΤΙΚΟΣ ΑΥΞΗΤΙΚΟΣ ΠΑΡΑΓΟΝΤΑΣ-Ι ΚΑΙ ΑΣΚΗΣΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Η αυξητική
ΔΙΑΒΗΤΗΣ ΚΑΙ ΚΥΗΣΗ ΚΡΙΘΑΡΙΩΤΗ ΙΩΑΝΝΑ ΙΜΠΡΙΣΙΜΗ ΑΝΝΑ ΤΕ ΝΟΣΗΛΕΥΤΡΙΑ ΤΕ ΝΟΣΗΛΕΥΤΡΙΑ Δ ΠΑΘΟΛΟΓΙΚΗ Δ ΠΑΘΟΛΟΓΙΚΗ Γ.Ν.Θ. ΙΠΠΟΚΡΑΤΕΙΟ Γ.Ν.
 ΔΙΑΒΗΤΗΣ ΚΑΙ ΚΥΗΣΗ ΚΡΙΘΑΡΙΩΤΗ ΙΩΑΝΝΑ ΤΕ ΝΟΣΗΛΕΥΤΡΙΑ Δ ΠΑΘΟΛΟΓΙΚΗ Γ.Ν.Θ. ΙΠΠΟΚΡΑΤΕΙΟ ΙΜΠΡΙΣΙΜΗ ΑΝΝΑ ΤΕ ΝΟΣΗΛΕΥΤΡΙΑ Δ ΠΑΘΟΛΟΓΙΚΗ Γ.Ν.Θ ΙΠΠΟΚΡΑΤΕΙΟ ΕΓΚΥΜΟΣΥΝΗ ΕΝΑ ΜΑΓΙΚΟ ΤΑΞΙΔΙ Ένα μακρύ «υπεραντλαντικό αεροπορικό
ΔΙΑΒΗΤΗΣ ΚΑΙ ΚΥΗΣΗ ΚΡΙΘΑΡΙΩΤΗ ΙΩΑΝΝΑ ΤΕ ΝΟΣΗΛΕΥΤΡΙΑ Δ ΠΑΘΟΛΟΓΙΚΗ Γ.Ν.Θ. ΙΠΠΟΚΡΑΤΕΙΟ ΙΜΠΡΙΣΙΜΗ ΑΝΝΑ ΤΕ ΝΟΣΗΛΕΥΤΡΙΑ Δ ΠΑΘΟΛΟΓΙΚΗ Γ.Ν.Θ ΙΠΠΟΚΡΑΤΕΙΟ ΕΓΚΥΜΟΣΥΝΗ ΕΝΑ ΜΑΓΙΚΟ ΤΑΞΙΔΙ Ένα μακρύ «υπεραντλαντικό αεροπορικό
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά : α) Κάθε φιαλίδιο πόσιμου διαλύματος
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά : α) Κάθε φιαλίδιο πόσιμου διαλύματος
B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 29 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Parsabiv 2,5 mg ενέσιμο διάλυμα Parsabiv 5 mg ενέσιμο διάλυμα Parsabiv 10 mg ενέσιμο διάλυμα etelcalcetide Το φάρμακο αυτό τελεί
B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 29 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Parsabiv 2,5 mg ενέσιμο διάλυμα Parsabiv 5 mg ενέσιμο διάλυμα Parsabiv 10 mg ενέσιμο διάλυμα etelcalcetide Το φάρμακο αυτό τελεί
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Genotropin MiniQuick 1,0 mg, 1,4 mg και 2,0 mg κόνις και διαλύτης για ενέσιμο διάλυμα σωματοτροπίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Genotropin MiniQuick 1,0 mg, 1,4 mg και 2,0 mg κόνις και διαλύτης για ενέσιμο διάλυμα σωματοτροπίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΠΑΡΑΡΤΗΜΑ Ι ΟΝΟΜΑΣΙΑ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ, ΠΕΡΙΕΚΤΙΚΟΤΗΤΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ, ΖΩΙΚΑ ΕΙ Η, Ο ΟΙ ΧΟΡΗΓΗΣΗΣ ΚΑΙ ΚΑΤΟΧΟΣ ΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 1/8
 ΠΑΡΑΡΤΗΜΑ Ι ΟΝΟΜΑΣΙΑ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ, ΠΕΡΙΕΚΤΙΚΟΤΗΤΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ, ΖΩΙΚΑ ΕΙ Η, Ο ΟΙ ΧΟΡΗΓΗΣΗΣ ΚΑΙ ΚΑΤΟΧΟΣ ΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 1/8 Κράτος µέλος Αιτών ή κάτοχος της άδειας κυκλοφορίας
ΠΑΡΑΡΤΗΜΑ Ι ΟΝΟΜΑΣΙΑ, ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ, ΠΕΡΙΕΚΤΙΚΟΤΗΤΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ, ΖΩΙΚΑ ΕΙ Η, Ο ΟΙ ΧΟΡΗΓΗΣΗΣ ΚΑΙ ΚΑΤΟΧΟΣ ΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 1/8 Κράτος µέλος Αιτών ή κάτοχος της άδειας κυκλοφορίας
ΦΥΣΙΟΛΟΓΙΚΗ ΛΕΙΤΟΥΡΓΙΑ ΤΗΣ ΥΠΟΦΥΣΗΣ
 ΕΙΣΑΓΩΓΗ Η υπόφυση είναι ένας μεγάλης σημασίας ενδοκρινής αδένας, που ρυθμίζεται από τον υποθάλαμο και βρίσκεται στη βάση του εγκεφάλου, πίσω από τη μύτη και στο ύψος των ματιών, σε μία περιοχή που λέγεται
ΕΙΣΑΓΩΓΗ Η υπόφυση είναι ένας μεγάλης σημασίας ενδοκρινής αδένας, που ρυθμίζεται από τον υποθάλαμο και βρίσκεται στη βάση του εγκεφάλου, πίσω από τη μύτη και στο ύψος των ματιών, σε μία περιοχή που λέγεται
(προγεμισμένος περιέκτηςτων 10 ml σε σχήμα κουταλιού) περιέχει Carbocysteine Lysine M onohydrate που αντιστοιχεί σε
 Ονομασία, μορφή: σε συσκευασία μιας δόσης. Σύνθεση: Δραστικά συστατικά: Carbocysteine Lysine Monohydrate. Εκδοχα: Sorbitol sol 70%, xylitol, ammonium glycyrrhizinate, carboxymethylcellulose sodium, glycerol,
Ονομασία, μορφή: σε συσκευασία μιας δόσης. Σύνθεση: Δραστικά συστατικά: Carbocysteine Lysine Monohydrate. Εκδοχα: Sorbitol sol 70%, xylitol, ammonium glycyrrhizinate, carboxymethylcellulose sodium, glycerol,
ΣΤΕΦΟΣ Θ.
 Επηρεάζει την αύξηση του βάρους κατά τη διάρκεια της κύησης Επηρεάζει τη μακροχρόνια διατήρηση των προσληφθέντων κιλών κατά τη διάρκεια της κύησης (5-9μήνες) Επηρεάζει την εμφάνιση παχυσαρκίας σε γυναίκες
Επηρεάζει την αύξηση του βάρους κατά τη διάρκεια της κύησης Επηρεάζει τη μακροχρόνια διατήρηση των προσληφθέντων κιλών κατά τη διάρκεια της κύησης (5-9μήνες) Επηρεάζει την εμφάνιση παχυσαρκίας σε γυναίκες
