Στερεοχημεία. Αντικείμενα της Οργανικής Χημείας. Μεταξύ των άλλων είναι και η. Μελέτη της δομής των οργανικών ενώσεων
|
|
|
- Φαραώ Κλαύδιος Αγγελόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Οργανική Χημεία Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, Αθήνα Τηλ.: , Fax:
2 Στερεοχημεία 2
3 Στερεοχημεία 1. Εισαγωγή στη Στερεοχημεία 2. Εναντιομέρεια 3. Οπτική Ενεργότητα 4. Σχετική και Απόλυτη Απεικόνιση 5. Διαστερεομέρεια 6. Διαμόρφωση Ελεύθερη Περιστροφή 7. Γεωμετρική Ισομέρεια 3
4 Στερεοχημεία Αντικείμενα της Οργανικής Χημείας Μεταξύ των άλλων είναι και η Μελέτη της δομής των οργανικών ενώσεων 1. Στερεοχημεία των οργανικών ενώσεων 2. Φασματοσκοπία Φασματοσκοπικές Μέθοδοι Ανάλυσης 4
5 Εισαγωγή στη Στερεοχημεία Πώς γράφουμε τις οργανικές ενώσεις; Μοριακός Τύπος: C 5 12 Δομή Kekulé και Δομή Lewis Συμπυκνωμένη δομή και Μερικώς συμπυκνωμένη δομή Σκελετική δομή Δομή Kekulé Συμπυκνωμένες δομές Σκελετική δομή 5
6 Εισαγωγή στη Στερεοχημεία Πώς γράφουμε τις οργανικές ενώσεις; Μοριακός Τύπος: C 5 12 Δομή Kekulé και Δομή Lewis Συμπυκνωμένη δομή και Μερικώς συμπυκνωμένη δομή Σκελετική δομή 6
7 Εισαγωγή στη Στερεοχημεία Η Οργανική Χημεία είναι η επιστήμη των τριών διαστάσεων και η μοριακή διάταξη μιας ένωσης στο χώρο έχει συνήθως καίρια σημασία για τον καθορισμό της χημικής συμπεριφοράς 7
8 Εισαγωγή στη Στερεοχημεία Τι είναι η Στερεοχημεία; Είναι ο κλάδος της χημείας που ασχολείται με τη μελέτη της τρισδιάστατης δομής των ενώσεων δηλ. με τη δομή των ενώσεων στο χώρο. Τι είναι Στερεοχημικοί τύποι; Οι τύποι που παριστάνουν τη διευθέτηση στο χώρο των ατόμων ενός μορίου. 8
9 Εισαγωγή στη Στερεοχημεία Στερεοχημικός τύπος Ο στερεοχημικός τύπος είναι μια τρισδιάστατη αναπαράσταση του μορίου η οποία δείχνει την ακριβή θέση του κάθε ατόμου μέσα στο μόριο. Τα άτομα αναπαρίστανται από σφαίρες και αν μεταξύ δύο ατόμων υπάρχει ομοιοπολικός δεσμός οι δύο σφαίρες μπορεί να επικαλύπτονται. Γωνία δεσμού 109,5 ο Μήκος δεσμού 1,10Å 9
10 Εισαγωγή στη Στερεοχημεία Μοριακός Τύπος: C 4 Συντακτικός Τύπος: Δείχνει τη διευθέτηση των ατόμων σ ένα μόριο στο επίπεδο Στερεοχημικός Τύπος: Δείχνει τη διευθέτηση των ατόμων ενός μορίου στο χώρο 10
11 Εισαγωγή στη Στερεοχημεία Ισομερή: Ενώσεις με τον ίδιο μοριακό τύπο αλλά διαφορετικές δομές. 2 C 3 π.χ. C 4 C C 3 10 Διαφορετικοί ανθρακικοί σκελετοί π.χ. C 2 6 Ο 3 C C 2 Βουτάνιο C 3 C C 3 Ισοβουτάνιο C 3 C 2 O C 3 OC 3 Διαφορετικές Αιθυλική αλκοόλη Διμέθυλο αιθέρας χαρακτηριστικές ομάδες π.χ. C 3 9 N Διαφορετικές θέσεις χαρακτηριστικών ομάδων Προπυλαμίνη N 2 C 3 C 2 C 2 N 2 C 3 CC 3 Ισοπροπυλαμίνη Συντακτικά ισομερή: Διαφορετική σύνδεση μεταξύ των ατόμων 11
12 Εισαγωγή στη Στερεοχημεία Ισομερή: Ενώσεις με τον ίδιο μοριακό τύπο αλλά διαφορετικές δομές. π.χ. C 2 6 Ο Οι δύο ενώσεις έχουν τον ίδιο μοριακό τύπο αλλά διαφέρουν με τον τρόπο που τα άτομα είναι ενωμένα μεταξύ τους. Ο διμεθυλο αιθέρας είναι άχρωμο αέριο, η αιθανόλη είναι υγρό. Διαφορετικές χαρακτηριστικές ομάδες Συντακτικά ισομερή: Διαφορετική σύνδεση μεταξύ των ατόμων 12
13 Εισαγωγή στη Στερεοχημεία Ισομερή: Ενώσεις με τον ίδιο μοριακό τύπο αλλά διαφορετικές δομές. π.χ. C Ο O O 5-isopropyl-2-methylphenol Chemical Formula: C O Molecular Weight: 150 Ρίγανη Καρβακρόλη 2-isopropyl-5-methylphenol Chemical Formula: C O Molecular Weight: 150 Θυμάρι Θυμόλη Διαφορετικές θέσεις χαρακτηριστικών ομάδων Συντακτικά ισομερή: Διαφορετική σύνδεση μεταξύ των ατόμων 13
14 Εισαγωγή στη Στερεοχημεία Ισομερή: Ενώσεις με τον ίδιο μοριακό τύπο αλλά διαφορετικές δομές. π.χ. C 3 6 Ο 3 C 3 C(O)COO O 3 C C COO Γαλακτικό οξύ OOC Στερεοϊσομερή: μόρια που έχουν τα άτομα ενωμένα με την ίδια σειρά, διαφέρουν στον τρόπο με τον οποίο τα άτομα αυτά διευθετούνται στο χώρο. C C 3 O 14
15 Εισαγωγή στη Στερεοχημεία Γιατί μας ενδιαφέρει η μελέτη ύπαρξης των στερεοϊσομερών μορφών; COO O 3 C C O 3 C C COO Γιατί τα διαφορετικά στερεοϊσομερή έχουν διαφορετικές βιολογικές ιδιότητες. 15
16 Εισαγωγή στη Στερεοχημεία Γιατί μας ενδιαφέρει η μελέτη ύπαρξης των στερεοϊσομερών μορφών; O COO OOC O O D-Dopa (καμιά βιολογική δράση) N 2 2 N O L-Dopa (φαρμακευτική δράση κατά της νόσου του Parkinson) S(+) ιβουπροφαίνη δραστικό αναλγητικό R(-) ιβουπροφαίνη αδρανές 16
17 Εισαγωγή στη Στερεοχημεία Γιατί μας ενδιαφέρει η μελέτη ύπαρξης των στερεοϊσομερών μορφών; O COO OOC O O O D-Dopa (καμιά βιολογική δράση) N 2 2 N O L-Dopa (φαρμακευτική δράση κατά της νόσου του Parkinson) O C 3 C 3 (+)-Καρβόνη (στους σπόρους του αγριοκύμινου) (-)-Καρβόνη (στο εκχύλισμα του δυόσμου) 17
18 Εισαγωγή στη Στερεοχημεία Γιατί μας ενδιαφέρει η μελέτη ύπαρξης των στερεοϊσομερών μορφών; Στα φαρμακευτικά προϊόντα, μικρές διαφορές στην τρισδιάστατη χωροδιάταξη μπορεί να ευθύνονται για τη δράση τους. Ισομερή που έχουν τον ίδιο τρόπο σύνδεσης των ατόμων τους αλλά διαφορετική τρισδιάστατη χωροδιάταξή τους καλούνται ΣΤΕΡΕΟισομερή 18
19 Εισαγωγή στη Στερεοχημεία 19
20 Εισαγωγή στη Στερεοχημεία Τι πρέπει να γνωρίζουμε για να μελετήσουμε τη στερεοχημική διάταξη μιας ένωσης; Τη στερεοχημική δομή των ατόμων της, δηλαδή τη κατεύθυνση των μονάδων σθένους στο χώρο Στερεοχημική δομή του άνθρακα 20
21 Εισαγωγή στη Στερεοχημεία Στερεοχημική δομή του άνθρακα Kekulé και Couper ανεξάρτητα ο ένας από τον άλλο διατύπωσαν την άποψη ότι πάντα ο άνθρακας έχει τέσσερις «μονάδες συγγένειας». Δηλαδή ο άνθρακας είναι τετρασθενής Friedrich August Kekulé 21 21
22 Εισαγωγή στη Στερεοχημεία Στερεοχημική δομή του άνθρακα van't off και Le Bel διατύπωσαν την απόψη ότι οι τέσσερις δεσμοί του άνθρακα έχουν συγκεκριμένη κατεύθυνση Τα άτομα με τα οποία είναι συνδεδεμένος ο άνθρακας τοποθετούνται στις γωνίες ενός κανονικού τετραέδρου, με τον άνθρακα στο κέντρο Η διακεκομμένη γραμμή κατευθύνεται πίσω από το επίπεδο της σελίδας Οι κανονικές γραμμές βρίσκονται πάνω στο επίπεδο της σελίδας Η γραμμή με παχύ άκρο (σφήνα) κατευθύνεται έξω από το επίπεδο της σελίδας J.. van t off 22 22
23 Εισαγωγή στη Στερεοχημεία Στερεοχημική δομή του άνθρακα Τετραεδρικό Άτομο Άνθρακα Δεσμός προς τα πίσω της σελίδας Δεσμοί στο επίπεδο της σελίδας κανονικό τετράεδρο Δεσμός έξω από το επίπεδο της σελίδας Τετραεδρική διάταξη του άνθρακα 23 23
24 Εισαγωγή στη Στερεοχημεία Στερεοχημική δομή του άνθρακα Τετραεδρικό Άτομο Άνθρακα - Στερεοσκοπική άποψη Γωνία δεσμού 109,5 ο Μήκος δεσμού 1,10Å 24 24
25 Στερεοϊσομέρεια Χειρομορφία Κάθε αντικείμενο μπορεί να αντικατοπτριστεί σε έναν καθρέφτη αποκαλύπτοντας το είδωλο του. Το αντικείμενο και το είδωλο του ταυτίζονται αν τοποθετηθούν με υπέρθεση Το αντικείμενο και το είδωλο του δεν ταυτίζονται αν τοποθετηθούν με υπέρθεση Είστε ένα χειρόμορφο αντικείμενο. Κοιταχτείτε στον καθρέφτη και υψώστε το δεξί σας χέρι. Το είδωλό σας υψώνει το αριστερό του χέρι. 25
26 Στερεοϊσομέρεια Χειρομορφία Μερικά αντικείμενα δεν είναι τα ίδια με τα κατοπτρικά είδωλα τους (δεν έχουν κανένα επίπεδο συμμετρίας) Ένα δεξί γάντι είναι διαφορετικό από ένα αριστερό γάντι, και επομένως ένα γάντι αριστερού χεριού δεν μπορεί να χωρέσει στο δεξί χέρι, γιατί ένα δεξί χέρι είναι διαφορετικό από ένα αριστερό χέρι Η ιδιότητα αυτή καλείται συνήθως «χειρικότητα ή χειρομορφία» Αριστερό χέρι Δεξί χέρι 26
27 Εναντιομέρεια Χειρομορφία Πολλά οργανικά μόρια (συμπεριλαμβανομένων των περισσότερων βιοχημικών ενώσεων) παρουσιάζουν το φαινόμενο της χειρικότητας ή χειρομορφίας που συνδέεται άμεσα με την τετραεδρική στερεοχημεία του άνθρακα Αριστερό χέρι Δεξί χέρι 27
28 Εναντιομέρεια Χειρομορφία: Μόρια τύπου CXYZ C Μόριο Κάτοπτρο Κατοπτρικό είδωλο 28
29 Εναντιομέρεια Χειρομορφία: Μόρια τύπου CXYZ C Μόριο Κατοπτρικό είδωλο Κάτοπτρο Ένα μόριο καλείται εναντιομερές όταν δεν είναι πανομοιότυπο με το κατοπτρικό του είδωλο (δηλαδή δεν ταυτίζονται μεταξύ τους). Αν το μόριο και το κατοπτρικό του είδωλο είναι πανομοιότυπα ή δεν είναι πανομοιότυπα εξαρτάται από τους υποκαταστάτες. 29
30 Εναντιομέρεια Χειρομορφία: Μόρια τύπου CXYZ C Μόριο Κάτοπτρο Κατοπτρικό είδωλο Όταν οι υποκαταστάτες είναι διαφορετικοί, το μόριο και το κατοπτρικό του είδωλο ΔΕΝ ΕΙΝΑΙ πανομοιότυπο (δηλαδή δεν ταυτίζονται). Τότε το μόριο λέγεται ότι είναι εναντιομερές. 30
31 Εναντιομέρεια Χειρομορφία: Μόρια τύπου CXYZ C Μόριο Κάτοπτρο Μόρια που δεν ταυτίζονται με τα κατοπτρικά τους είδωλα και επομένως απαντούν με δύο εναντιομερείς μορφές καλούνται χειρικά ή χειρόμορφα. Εναντιομέρεια ή χειρομορφία (chirality) Κατοπτρικό είδωλο 31
32 Εναντιομέρεια Χειρομορφία: Μόρια τύπου CXYZ Κάτοπτρο C C Αριστερό χέρι Δεξί χέρι Μόρια που δεν ταυτίζονται με τα κατοπτρικά τους είδωλα και επομένως απαντούν με δύο εναντιομερείς μορφές καλούνται χειρικά ή χειρόμορφα. 32
33 Εναντιομέρεια Χειρομορφία: Μόρια τύπου CXYZ Γαλακτικό οξύ X C Y Z Δεν συμπίπτουν Δεν συμπίπτουν Δεν συμπίπτουν Δεν συμπίπτουν 33
34 Εναντιομέρεια Μόρια τύπου CΗ 4 CΗ 3 Χ, CΗ 2 ΧΥ Τα μόρια CΗ 4, CΗ 3 Χ, CΗ 2 ΧΥ είναι πανομοιότυπα, ταυτίζονται με το είδωλο τους, άρα δεν εμφανίζουν χειρικότητα. 34
35 Εναντιομέρεια Το αίτιο της χειρικότητας στα μόρια Ένα μόριο δεν μπορεί να είναι χειρόμορφο, εάν περιέχει κάποιο επίπεδο συμμετρίας. Επίπεδο συμμετρίας, διαχωρίζει ένα αντικείμενο ή μόριο σε δύο κομμάτια με τέτοιο τρόπο, ώστε το ένα κομμάτι να αποτελεί ακριβές είδωλο το άλλου. Έχει επίπεδο συμμετρίας Δεν έχει επίπεδο συμμετρίας 35
36 Εναντιομέρεια Το αίτιο της χειρικότητας στα μόρια Ένα μόριο, το οποίο διαθέτει επίπεδο συμμετρίας, είναι πανομοιότυπο με το είδωλο του και χαρακτηρίζεται ως μη χειρόμορφο. Μόριο 36
37 Εναντιομέρεια Το αίτιο της χειρικότητας στα μόρια Ένα μόριο, το οποίο διαθέτει επίπεδο συμμετρίας, είναι πανομοιότυπο με το είδωλο του και χαρακτηρίζεται ως μη χειρόμορφο. Επίπεδο συμμετρίας ΟΧΙ Επίπεδο συμμετρίας Προπανοϊκό οξύ (μη χειρομόρφο) Γαλακτικό οξύ (χειρομόρφο) 37
38 Εναντιομέρεια Το αίτιο της χειρικότητας στα μόρια Η χειρομορφία στα οργανικά μόρια οφείλεται στην παρουσία ενός ατόμου άνθρακα συνδεδεμένου με 4 διαφορετικές ομάδες. * Ασύμμετρο άτομο άνθρακα *C, ασύμμετρο κέντρο, ή στερεογονικό κέντρο ή χειρόμορφο κέντρο 38
39 Εναντιομέρεια Παραδείγματα Cl F Cl C Cl C I Έχει επίπεδο συμμετρίας (ορίζεται από Cl - Cl - C) Μη χειρόμορφο Έχει ασύμμετρο κέντρο Δεν έχει επίπεδο συμμετρίας Χειρόμορφο 39
40 Εναντιομέρεια Παραδείγμα 5-Βρωμοδεκάνιο (χειρομόρφο) Υποκαταστάτες στον άνθρακα 5 40
41 Εναντιομέρεια Παραδείγματα Επίπεδο συμμετρίας * Μεθυλοκυκλοεξάνιο (μη χειρομόρφο) Δύο ίδιοι υποκαταστάτες Δεν υπάρχει στερεογονικό κέντρο 2-Μεθυλοκυκλοεξανόνη (χειρομόρφο) Τέσσερεις διαφορετικοί υποκαταστάτες Ο 2-άνθρακας είναι στερεογονικό κέντρο 41
42 Εναντιομέρεια Παραδείγματα Καρβόνη (αιθέριο έλαιο του δυόσμου) Νουτκατόνη (αιθέριο έλαιο του γκρέιπφρουτ) 42
43 Εναντιομέρεια Πρόβλημα Κωνειίνη (από το δηλητήριο κώνειο) Μενθόλη (συστατικό αιθέριων ελαίων) Δεξτρομεθορφάνιο (αντιβηχικό) 43
44 Εναντιομέρεια Πρόβλημα Απάντηση Κωνειίνη (από το δηλητήριο κώνειο) Μενθόλη (συστατικό αιθέριων ελαίων) Δεξτρομεθορφάνιο (αντιβηχικό) 44
45 Εναντιομέρεια Πότε ένα μόριο παρουσιάζεται με δύο μορφές; Όταν δεν είναι συμμετρικό: Δεν έχει επίπεδο συμμετρίας Δεν έχει κέντρο συμμετρίας Ασύμμετρα: δεν έχουν κανένα στοιχείο συμμετρίας 45
46 Στερεοϊσομέρεια Στερεοϊσομερή: τα μόρια που έχουν τα άτομα ενωμένα με την ίδια σειρά, διαφέρουν στον τρόπο με τον οποίο τα άτομα αυτά διευθετούνται στο χώρο Εναντιομερή, Χειρόμορφα ή Αντίποδες: τα μόρια που έχουν σχέση ειδώλου προς αντικείμενο. 1. Δεν μπορούν να ταυτιστούν με το είδωλο τους 2. Δεν έχουν επίπεδο ή κέντρο συμμετρίας Ρακεμικό μίγμα: έχει τον ίδιο αριθμό μορίων από κάθε εναντιομερές Ρακεμοποίηση: η μετατροπή ενός αντίποδα στο ρακεμικό μίγμα. 46
47 Οπτική Ενεργότητα Biot (1830) Ενώσεις όπως τα σάκχαρα στρέφουν το επίπεδο του πολωμένου φωτός Pasteur (1849) Ανακάλυψε τα εναντιομερή του μετά νατρίου και αμμωνίου άλατα του τρυγικού οξέος Kekule (1858) Αρχή της τετρασθενίας του άνθρακα και ισοτιμίας των μονάδων σθένους του van t off και Le Bel (1875) Τετραεδρική γεωμετρία του άνθρακα 47
48 Οπτική Ενεργότητα Το φως που διέρχεται από έναν πολωτή είναι μοναδικό και ονομάζεται πολωμένο στο επίπεδο φως. Όταν μια δέσμη πολωμένου στο επίπεδο φωτός διέλθει από ένα διάλυμα μη χειρόμορφων ενώσεων παραμένει σε αυτό το επίπεδο. Διάλυμα χειρόμορφων ενώσεων στρέφουν το επίπεδο της πόλωσης και οι ενώσεις αυτές ονομάζονται οπτικά ενεργές. Το φαινόμενο αυτό μελετήθηκε για πρώτη φορά από τον Biot στις αρχές του 19ου αιώνα. Παρατηρητής Φωτεινή πηγή Μη Πολωτής πολωμένο φως Κυψελίδα δείγματος Αναλυτής 48
49 Οπτική Ενεργότητα 49
50 Οπτική Ενεργότητα Η στροφή που προκαλεί το διαλύματα οπτικά ενεργών ουσιών μετριέται με το πολωσίμετρο. Το μέγεθος της στροφής συμβολίζεται με α και εκφράζεται σε μοίρες Οπτικά ενεργά μόρια που είναι: D-Dextrorotary, "δεξιόστροφο" (+) L-Levorotary, "αριστερόστροφο" (-) Παρατηρητής Φωτεινή πηγή Μη Πολωτής πολωμένο φως Κυψελίδα δείγματος Αναλυτής 50
51 Οπτική Ενεργότητα Ειδική στροφή [α] D Παρατηρητής Φωτεινή πηγή Μη Πολωτής πολωμένο φως Κυψελίδα δείγματος [α] D = α / (l x C) α = Μετρούμενη γωνία στροφής, σε μοίρες Αναλυτής [α] D = Ειδική γωνία στροφής, χαρακτηριστική για δεδομένη ένωση l = Μήκος οπτικού διαστήματος, σε dm C = Συγκέντρωση (g/ml) Ειδική στροφή [α] D : Είναι αυτή που παρατηρείται σε διάλυμα 1 g/ml σε κυψελίδα διαδρομής 10 cm χρησιμοποιώντας το φως που εκπέμπουν λάμπες Νατρίου (589 nm) 51
52 Οπτική Ενεργότητα Τα "χειρομορφικά" μόρια είναι "οπτικά ενεργά", παρουσιάζουν δηλαδή μια οπτική στροφική ικανότητα. Το φαινόμενο παρατηρείται με τα πολωσίμετρα Τα "εναντιομερή" λέγονται και "οπτικοί αντίποδες" Ρακεμικό μίγμα: μίγμα των δύο αντιπόδων σε ίσες ποσότητες Το Ρακεμικό τους μίγμα είναι οπτικά ανενεργό 52
53 Οπτική Ενεργότητα Που οφείλεται η οπτική ενεργότητα; Στην ασύμμετρη κατασκευή των κρυστάλλων Δύο κρυσταλλικές δομές με σχέση ειδώλου προς αντικείμενο μεταξύ τους Οπτική Στροφική Ικανότητα ή Οπτική Ενεργότητα Παρουσιάζουν οργανικές και οι ανόργανες ενώσεις Οι οργανικές ενώσεις διατηρούν την ιδιότητα και 1. στην υγρή και 2. στην αέρια κατάσταση Οπτικά Ισομερή Ίδιες φυσικές και χημικές ιδιότητες Διαφέρουν στο ότι στρέφουν δεξιά ή αριστερά το επίπεδο του πολωμένου φωτός, κατά την ίδια απόλυτη τιμή 53
54 Στερεοχημική απεικόνιση (configuration) Με τον όρο στερεοχημική απεικόνιση ή απλά απεικόνιση εννοούμε τη διάταξη στο χώρο των ατόμων ή ομάδων ατόμων ενός στερεοϊσομερούς. Υπάρχουν δύο τρόποι απεικόνισης: η σχετική απεικόνιση και η απόλυτη απεικόνιση. 54
55 Προβολές κατά Fischer Προβολή των στερεοχημικών απεικονίσεων σε μια επίπεδη επιφάνεια κατά Fisher A Δ C Γ B Δ A C B Δ A B Γ Γ 55
56 Προβολές κατά Fischer Προβολή των στερεοχημικών απεικονίσεων σε μια επίπεδη επιφάνεια κατά Fisher O COO C C 3 Οι δεσμοί που εξέρχονται από το επίπεδο Οι δεσμοί στο επίπεδο της σελίδας COO C 3 O 56
57 Προβολές κατά Fischer Επιτρεπτές κινήσεις στις προβολές κατά Fisher 1. Μια προβολή κατά Fisher μπορεί να περιστραφεί στο χαρτί κατά 180 ο Περιστροφή 180 ο 2. Μια προβολή κατά Fisher μπορεί να διατηρήσει αμετακίνητη τη μια ομάδα και οι υπόλοιπες να περιστρέφονται δεξιόστροφα ή αριστερόστροφα. Αμετακίνητη ομάδα COO Ίδιο με 3 C O 57
58 Σχετική απεικόνηση Βασίζεται στη συσχέτιση της της δομής μιας ένωσης με τη δομή της Γλυκεριναλδεΰδης: OC 2 *C(O)CO Διαθέτει ένα στερεογονικό κέντρο και επομένως δύο εναντιομερή Η συσχέτιση αυτή καθιερώθηκε από τον Fischer Ο πλέον οξειδωμένος υποκαταστάτης επάνω CO O C C 2 O D- γλυκεριναλδεΰδη L- γλυκεριναλδεΰδη Κάτοπτρο Dextrus = δεξιός Laevus = αριστερός 58
59 Σχετική απεικόνιση π.χ. γαλακτικό οξύ D-γαλακτικό οξύ L-γαλακτικό οξύ CO O C C 2 O Κάτοπτρο D- γλυκεριναλδεΰδη L- γλυκεριναλδεΰδη Οι οπτικά ενεργές ενώσεις ταξινομούνται στην D- και L- σειρά με βάση τη δομή της D- και L- γλυκεριναλδεΰδης. 59
60 Σχετική απεικόνιση π.χ. αμινοξέα L-αμινοξύ COO L- σερίνη 2 N C 2 O L- γλυκεριναλδεΰδη L- γλουταμινικό οξύ Οι οπτικά ενεργές ενώσεις ταξινομούνται στην D- και L- σειρά με βάση τη δομή της D- και L- γλυκεριναλδεΰδης. 60
61 Απόλυτη απεικόνιση Ο συσχετισμός των οπτικών αντιπόδων με τις D- και L- γλυκεριναλδεΰδη δεν είναι πάντα εφικτός. Για το λόγο αυτό προτάθηκε από τους Cahn, Ingold και Prelog η Απόλυτη Απεικόνιση R ή S των ασυμμέτρων ενώσεων σύμφωνα με τους κανόνες προτεραιότητας των υποκαταστατών. R - S - Σειρά προτεραιότητας: 1. Προηγούνται οι υποκαταστάτες με το μεγαλύτερο ατομικό αριθμό 2. Μεταξύ των ανθρακούχων ομάδων, προηγούνται οι πιο πολύπλοκες και εκείνες με το μεγαλύτερο βαθμό οξείδωσης. 3. στους άνθρακες με διαφορετικό υβριδισμό έχουμε τη σειρά: sp > sp2 > sp3, -Ι > -Βr > -Cl > -F > -SO 3 > -SC 3 > -S > -O > -NR 2 - > -N 2 > -COOC 3 > -COO > -CON 2 > -C=O > -C(C 3 ) 3 - > - C 2 C 3 > -C 3 > - 61
62 Απόλυτη απεικόνιση Κανόνες προτεραιότητας Οι κανόνες αυτοί είναι: 1. Μεγαλύτερη προτεραιότητα έχουν οι υποκαταστάτες των οποίων τα άτομα που είναι ενωμένα με το στερεογονικό κέντρο έχουν τον μεγαλύτερο ατομικό αριθμό. Για παράδειγμα το Ο (Ζ=8) έχει προτεραιότητα έναντι του Ν (Ζ=7). 2. Εάν δύο υποκαταστάτες έχουν όμοια άτομα συνδεόμενα με το στερεογονικό κέντρο, ελέγχουμε τα δεύτερα άτομα. Αν και αυτά είναι όμοια τα τρίτα κ.ο.κ. Για παράδειγμα το C 2 C 3 (αιθύλιο) το C 3 (μεθύλιο). Τα πρώτα άτομα είναι όμοια (άνθρακες). Τα δεύτερα για μεν το μεθύλιο είναι τρία υδρογόνα για δε το αιθύλιο δύο υδρογόνα και ένας άνθρακας. Ο άνθρακας έχει ατομικό αριθμό 6 και το υδρογόνο 1. Επομένως υψηλότερη προτεραιότητα έχει το αιθύλιο. 3. Έστω ο υποκαταστάτης Α=Β. Το άτομο Α θεωρείται ότι συνδέεται με δύο άτομα Β. Ας θεωρήσουμε τους υποκαταστάτες C=O (φόρμυλο) και C 2 O (υδροξυμέθυλο). Τα πρώτα άτομα είναι ίδια (άνθρακες). Τα δεύτερα είναι για μεν την φόρμυλο ομάδα δύο άτομα οξυγόνου και ένα υδρογόνου για δε την υδροξυμέθυλο ομάδα ένα άτομο οξυγόνου και δύο άτομα υδρογόνου. Ο ατομικός αριθμός του οξυγόνου είναι 8 ενώ του ατόμου υδρογόνου 1. Άρα η φόρμυλο έχει υψηλότερη προτεραιότητα. 62
63 Απόλυτη απεικόνιση Α) Το σύστημα Cahn, Ingold και Prelog 1. Χρησιμοποιώντας τους ατομικούς αριθμούς, καθορίστε την προτεραιότητα των 4 ομάδων που συνδέονται με το χειρομορφικό κέντρο 2. Περιστρέψτε το μόριο στο χώρο έτσι ώστε η ομάδα χαμηλότερης προτεραιότητας να είναι στραμμένη προς την αντίθετη κατεύθυνση από εσάς 3. Εξετάστε εάν η σειρά προτεραιότητας των ομάδων ακολουθεί τη φορά των δεικτών του ρολογιού (δεξιόστροφη) ή την αντίθετη (αριστερόστροφη) φορά 4. Δεξιόστροφη = R και Αριστερόστροφη = S 63
64 Απόλυτη απεικόνιση Το σύστημα Cahn, Ingold και Prelog 1. Χρησιμοποιώντας τους ατομικούς αριθμούς, καθορίστε την προτεραιότητα των 4 ομάδων που συνδέονται με το χειρομορφικό κέντρο ΠΡΟΣΟΧΗ: Η προτεραιότητα βασίζεται στο πρώτο σημείο διαφοροποίησης, ΟΧΙ στο άθροισμα των ατομικών αριθμών 64
65 Απόλυτη απεικόνιση Γλυκεριναλδεΰδη β 120 o α αμετακίνητη β δ αμετακίνητη α γ γ D - R - β β 120 o γ δ δ L - S - α δ α γ 65
66 Απόλυτη απεικόνιση Προβολή Newman Παρατηρητής Απεικόνιση R Δεξιά στροφή του τιμονιού 66
67 Απόλυτη απεικόνιση 2-χλωρο-2-υδροξυ-ακεταμίδιο γ αμετακίνητη γ 120 o β α δ β R γ δ α Προβολή Newman β α 67
68 Απόλυτη απεικόνιση Γαλακτικό οξύ Προβολές Newman α β Απεικόνιση R γ α β γ Απεικόνιση S 68
69 Απόλυτη απεικόνιση Χαρακτηρίστε ως R ή S τη δομή 1 2 S αμετακίνητη C 6 8 O C C 6 O 8 O Απόδοση προτεραιότητας με βάση τον ατομικό αριθμό Cahn-Ingold-Prelog 69
70 Απόλυτη απεικόνιση Χαρακτηρίστε ως R ή S τη δομή α Cl α Cl Απάντηση S β Cl 2 C C(C 3 ) 2 γ C 3 δ Cl 2 C β C(C 3 ) 2 γ Το C 3 που είναι τελευταίο στην προτεραιότητα, προβάλλεται πίσω από το επίπεδο του χαρτιού και δεν εξετάζεται στον καθορισμό της σειράς 70
71 Απόλυτη απεικόνιση Β) Τρόπος εύρεσης απόλυτης απεικόνισης με τη χρήση του χεριού 1ο βήμα: Καθορίζουμε την προτεραιότητα των υποκαταστατών με βάση τους κανόνες προτεραιότητας. 2ο βήμα: Συμβολίζουμε με αριθμούς (1,2,3,4) ή με γράμματα (α,β,γ,δ) τους υποκαταστάτες κατά σειρά ελαττούμενης προτεραιότητας. 3ο βήμα: Τοποθετούμε τον αντίχειρα του δεξιού μας χεριού στην κατεύθυνση του τέταρτου υποκαταστάτη, ο οποίος έχει και τη χαμηλότερη προτεραιότητα. 4ο βήμα: Κλείνουμε τα υπόλοιπα τέσσερα δάκτυλα του δεξιού μας χεριού. Αν η φορά κλεισίματος των δακτύλων ταυτίζεται με την ακολουθία των υποκαταστατών τότε η απεικόνιση χαρακτηρίζεται ως R (Rectus = δεξιός) αν όχι ως S (Sinister = αριστερός). 71
72 Απόλυτη απεικόνιση Προσδιορισμός της απεικόνισης R S R-Γαλακτικό οξύ 3 S-Γαλακτικό οξύ 72
73 Απόλυτη απεικόνιση Χαρακτηρίστε ως R ή S τη δομή 2-χλωροβουτάνιο R 73
74 Απόλυτη απεικόνιση Προσδιορισμός απεικονίσεων R ή S στις προβολές κατά Fisher Προβολή των στερεοχημικών απεικονίσεων σε μια επίπεδη επιφάνεια κατά Fisher O COO C C 3 Οι δεσμοί που εξέρχονται από το επίπεδο Οι δεσμοί στο επίπεδο της σελίδας COO C 3 O 74
75 Απόλυτη απεικόνιση Γ) Προσδιορισμός απεικονίσεων R ή S στις προβολές κατά Fisher 1. Προσδιορίζουμε τις προτεραιότητες των τεσσάρων υποκαταστατών. 2. Εκτελούμε κάποια από τις δύο επιτρεπτές κινήσεις ώστε η ομάδα χαμηλής προτεραιότητας να τοποθετηθεί στην κορυφή της προβολής κατά Fisher. i. Μια προβολή κατά Fisher μπορεί να περιστραφεί στο χαρτί κατά 180 ο ii. Μια προβολή κατά Fisher μπορεί να διατηρήσει αμετακίνητη τη μια ομάδα και οι υπόλοιπες να περιστρέφονται δεξιόστροφα ή αριστερόστροφα. 3. Προσδιορίζουμε την κατεύθυνση της περιστροφής μεταβαίνοντας από τον υποκαταστάτη με υψηλότερη προτεραιότητα στον υποκαταστάτη με χαμηλότερη προτεραιότητα. 4. Καθορίζουμε την απεικόνιση: Αν η ακολουθία 1 2 3, των τριών άλλων υποκαταστατών, ακολουθεί τη φορά κίνησης των δεικτών του ρολογιού τότε η απεικόνιση χαρακτηρίζεται ως R αν όχι ως S 75
76 Απόλυτη απεικόνιση Προσδιορισμός απεικονίσεων R ή S στις προβολές κατά Fisher R Αμετακίνητη ομάδα 3 3 R 76
77 Απόλυτη απεικόνιση Προσδιορισμός απεικονίσεων R ή S στις προβολές κατά Fisher 4 2 COO 4 1 O R CO C N 4 C 3 3 Παραμένει ακίνητο 2 OOC N 2 1 C 3 3 S 77
78 Απόλυτη απεικόνιση Προσδιορισμός απεικονίσεων R ή S στις προβολές κατά Fisher 1,2- διμεθυλοκυκλοπεντανόλη 2 O 1 4 Προβολή Fischer 3 Αμετακίνητη ομάδα S 78
79 Διαστερεομέρεια Η διαστερεομέρεια αποτελεί γενικότερη περίπτωση στερεοχημικής ισομέρειας, που εμφανίζουν ενώσεις με δύο ή περισσότερα ασύμμετρα άτομα C. 1. Οι διαστερεομερείς ενώσεις δεν έχουν σχέση ειδώλου με αντικείμενο. 2. Παρουσιάζουν οπτική ενεργότητα, αλλά η γωνία στροφής παρουσιάζει διαφορές. 79
80 Διαστερεομέρεια 80
81 Διαστερεομέρεια Σχετική Απεικόνιση 2,3,4-τριυδροξυβουτανάλη: OC-CO-CO-C * * 2 O D θρεο (1) L θρεο (2) D ερυθρο (3) L ερυθρο (4) (1)-(2) και (3)-(4): εναντιοστερομερή-οπτικοί αντίποδες (1)-(3), (1)-(4), (2)-(3) και (2)-(4): διαστερεομερή Διαστερεομερή: στερεοϊσομέρη τα οποία έχουν δύο ή περισσότερα ασύμμετρα άτομα άνθρακα τα οποία δεν είναι εναντιομερή (δεν έχουν σχέση ειδώλου με αντικείμενο). ν = *C, 2 ν : διαστερεομερή και 2 ν-1 : ζεύγη εναντιομερών ή οπτικών αντιπόδων 81
82 Διαστερεομέρεια Σχετική Απεικόνιση * * τρυγικό οξύ: ΟΟC-CO-CO-CΟΟ D θρεο L θρεο D ερυθρο (5) (6) (7) (5)-(6): εναντιομερή-οπτικοί αντίποδες και L ερυθρο (8) (7)-(8): είναι όμοια μεσομορφές, i- (inactivus=ανενεργός) Επομένως όταν υπάρχει επίπεδο συμμετρίας τα διαστερεομερή είναι 2 ν
83 Διαστερεομέρεια Απόλυτη Απεικόνιση R, S 1 C 3 Br 2 4 C 3 3 Br 1 2 * S 2 * 4 R 3 * Cl * Cl C C 3 83
84 Διαστερεομέρεια Απόλυτη Απεικόνιση R, S 1 C 3 Br 2 * 2S 2R 3S 3R 3 * Cl C
85 Διαστερεομέρεια Απόλυτη Απεικόνιση R, S C 3 Br Br C 3 C 3 Br Br C 3 Cl Cl Cl Cl Cl C 3 C 3 C 3 C 3 2S,3R 2R,3S 2S,3S 2R,3R εναντιομερή εναντιομερή διαστερομερή 85
86 Διαστερεομέρεια Απόλυτη Απεικόνιση R, S Κάτοπτρο 2-αμινο-3-υδροξυβουτανοϊκό οξύ Κάτοπτρο εναντιομερή διαστερομερή εναντιομερή 86
87 Διαστερεομέρεια Απόλυτη Απεικόνιση R, S Br C 3 C 3 Br C 3 Br Br C 3 * * Br Br Br Br C 3 C C C (2R,3R) (2S,3S) (2R,3S) (2S,3R) εναντιομερή Μεσο-ενώσεις 87
88 Διαστερεομέρεια Απόλυτη Απεικόνιση R, S Κάτοπτρο τρυγικό οξύ: Κάτοπτρο εναντιομερή Μεσο-ενώσεις Επίπεδο συμμετρίας 88
89 Στερεοϊσομέρεια Φυσικές Ιδιότητες Στερεοϊσομερών Τα εναντιομερή διαφέρουν ως προς πρόσημο της στροφής του πολωμένου στο επίπεδο φωτός, αλλά οι άλλες φυσικές τους ιδιότητες είναι ίδιες. Τα διαστερομερή έχουν διαφορετικές φυσικές ιδιότητες Τα ρακεμικά μίγματα αποτελούν μίγματα των (+) και (-) εναντιομερών, σε αναλογία 50:50. Τα ρακεμικά μίγματα πρέπει να εμφανίζουν μηδενική οπτική στροφή. Τα ρακεμικά μίγματα και τα μεμονωμένα διαστερομερή διαφέρουν ως προς τις φυσικές τους ιδιότητες. 89
90 Ισομέρεια Ισομερή Συντακτικά Ισομερή Στερεοϊσομερή Εναντιομερή (κατοπτρικά είδωλα) Διαστερεομερή (μη καπτροπτικά είδωλα) Διαστερεομερή απεικόνισης, D-L, R-S Διαστερεομερή Cis-Trans, Z-E (Γεωμετρικά ισομερή) 90
91 Στερεοχημεία Σχετική Βιβλιογραφία Οργανική Χημεία για τις Επιστήμες της Ζωής David Klein Κεφάλαια: 1, 2, 4, 5, «Οργανική Χημεία», Wade JR. 6η έκδοση, Κεφάλαια: 3, ( ), 5 «Οργανική Χημεία», John McMurry, 6η έκδοση, Κεφάλαια 3, 4, 6, 9, 26.2,
Περίληψη Κεφαλαίων 6 & 7
 Περίληψη Κεφαλαίων 6 & 7 Αλκένια: υδρογονάνθρακες µε 1 ή περισσότερους διπλούς δεσµούς Παρεµπόδιση περιστροφής γύρω από δ.δ. cis-trans ισοµέρεια (Ε ή Ζ) Αλκένια δίνουν αντιδράσεις ηλεκτρονιόφιλης προσθήκης
Περίληψη Κεφαλαίων 6 & 7 Αλκένια: υδρογονάνθρακες µε 1 ή περισσότερους διπλούς δεσµούς Παρεµπόδιση περιστροφής γύρω από δ.δ. cis-trans ισοµέρεια (Ε ή Ζ) Αλκένια δίνουν αντιδράσεις ηλεκτρονιόφιλης προσθήκης
5 o Μάθημα (α) Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους
 Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 5 o Μάθημα (α) Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Οργανική Χημεία Θεωρία Μαθήματα Ακαδημαϊκού Έτους 2017-2018 5 o Μάθημα (α) Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό Προσωπικό,
Κυκλικοί υδρογονάνθρακες
 Κυκλικοί υδρογονάνθρακες C 2 Y C 2 Y C 2 C 2 C n 2n+2 C n 2n : Κορεσμένοι = Ισομερή των αλκενίων C n 2n C n 2n-2 : Μονοακόρεστοι = ισομερή των αλκινίων 1 1. Καύση Αντιδράσεις Αλκανίων C 3 -C 2 -C 3 + 5
Κυκλικοί υδρογονάνθρακες C 2 Y C 2 Y C 2 C 2 C n 2n+2 C n 2n : Κορεσμένοι = Ισομερή των αλκενίων C n 2n C n 2n-2 : Μονοακόρεστοι = ισομερή των αλκινίων 1 1. Καύση Αντιδράσεις Αλκανίων C 3 -C 2 -C 3 + 5
ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ
 ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ 1 Ισομέρεια, ή ισομερισμός (ως αποτέλεσμα επιδράσεων), λέγεται το φαινόμενο κατά το οποίο δύο ή περισσότερες χημικές ενώσεις αν και αποτελούνται από τα ίδια χημικά στοιχεία, του αυτού
ΕΝΟΤΗΤΑ 1: ΙΣΟΜΕΡΕΙΑ 1 Ισομέρεια, ή ισομερισμός (ως αποτέλεσμα επιδράσεων), λέγεται το φαινόμενο κατά το οποίο δύο ή περισσότερες χημικές ενώσεις αν και αποτελούνται από τα ίδια χημικά στοιχεία, του αυτού
ΣΤΕΡΕΟΧΗΜΕΙΑ: Κλάδος της Χημείας που μελετά τη
 ΣΤΕΡΕΟΧΗΜΕΙΑ: Κλάδος της Χημείας που μελετά τη διάταξη στο χώρο (τρισδιάστατη δομή) των δομικών στοιχείων των ενώσεων Στερεοϊσομερή: Ισομερείς ενώσεις που διαφέρουν στηστερεοχημικήτουςδομή Παραδείγματα
ΣΤΕΡΕΟΧΗΜΕΙΑ: Κλάδος της Χημείας που μελετά τη διάταξη στο χώρο (τρισδιάστατη δομή) των δομικών στοιχείων των ενώσεων Στερεοϊσομερή: Ισομερείς ενώσεις που διαφέρουν στηστερεοχημικήτουςδομή Παραδείγματα
Διαμόρφωση-διαμορφωμερή
 Οργανική Χημεία Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax:
Οργανική Χημεία Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax:
ΣΤΕΡΕΟΧΗΜΕΙΑ. Καθηγητής Μόσχος Πολυσίου, / Εργαστήριο Γενικής Χημείας Γ.Π.Α.
 ΣΤΕΡΕΟΧΗΜΕΙΑ Καθηγητής Μόσχος Πολυσίου, / Εργαστήριο Γενικής Χημείας Γ.Π.Α. ΙΣΟΜΕΡΕΙΑ Ισομερείς είναι οι ενώσεις με ίδιο μοριακό αλλά διαφορετικό συντακτικό τύπο (συντακτικά ισομερείς) ή με ίδιο μοριακό,
ΣΤΕΡΕΟΧΗΜΕΙΑ Καθηγητής Μόσχος Πολυσίου, / Εργαστήριο Γενικής Χημείας Γ.Π.Α. ΙΣΟΜΕΡΕΙΑ Ισομερείς είναι οι ενώσεις με ίδιο μοριακό αλλά διαφορετικό συντακτικό τύπο (συντακτικά ισομερείς) ή με ίδιο μοριακό,
7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο
 7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο Πολλές αντιδράσεις µετατρέπουν µη χειρόµορφα αντιδρώντα σε χειρόµορφα προϊόντα. Εν τούτοις, είναι σηµαντικό να αναγνωρίσουµε, οτι εάν όλα τα συστατικά
7.9 Αντιδράσεις που δηµιουργούν ένα στερεογονικό κέντρο Πολλές αντιδράσεις µετατρέπουν µη χειρόµορφα αντιδρώντα σε χειρόµορφα προϊόντα. Εν τούτοις, είναι σηµαντικό να αναγνωρίσουµε, οτι εάν όλα τα συστατικά
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο. Θεωρία δεσμού σθένους (Valence bond theory)
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Για την περιγραφή του ομοιοπολικού δεσμού έχουν διατυπωθεί πολλές
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Για την περιγραφή του ομοιοπολικού δεσμού έχουν διατυπωθεί πολλές
Δομή και ισομέρεια ενώσεων σύνταξης
 ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε μια από τις σημαντικότερες ιδιότητες των συμπλόκων που σχετίζονται με την ηλεκτρονική δομή και τη φύση του δεσμού στα σύμπλοκα, την ισομέρεια και
ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε μια από τις σημαντικότερες ιδιότητες των συμπλόκων που σχετίζονται με την ηλεκτρονική δομή και τη φύση του δεσμού στα σύμπλοκα, την ισομέρεια και
5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων
 5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o προβλέπετε με βάση τη συμμετρία αν ένα μόριο έχει μόνιμη
5. Συμμετρία, Πολικότητα και Οπτική Ενεργότητα των μορίων ιδακτικοί στόχοι Μετά την ολοκλήρωση της μελέτης του κεφαλαίου αυτού θα μπορείτε να... o προβλέπετε με βάση τη συμμετρία αν ένα μόριο έχει μόνιμη
Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 9ος
 Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 9ος 22-0231_l_c_chemistry_bm 251-300 28b.indd 1 1/17/17 1:26:15 PM ΣΤΟΙΧΕΙΑ ΑΡΧΙΚΗΣ ΕΚ ΟΣΗΣ Το παρόν βιβλίο περιέχει τα παρακάτω κεφάλαια:
Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 9ος 22-0231_l_c_chemistry_bm 251-300 28b.indd 1 1/17/17 1:26:15 PM ΣΤΟΙΧΕΙΑ ΑΡΧΙΚΗΣ ΕΚ ΟΣΗΣ Το παρόν βιβλίο περιέχει τα παρακάτω κεφάλαια:
Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 5ος
 Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 5ος 22-0231_l_c_chemistry_bm 251-334 18b.indd 1 5/9/17 3:02 PM ΣΤΟΙΧΕΙΑ ΑΡΧΙΚΗΣ ΕΚ ΟΣΗΣ Το παρόν βιβλίο περιέχει τα παρακάτω κεφάλαια: α) Από
Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 5ος 22-0231_l_c_chemistry_bm 251-334 18b.indd 1 5/9/17 3:02 PM ΣΤΟΙΧΕΙΑ ΑΡΧΙΚΗΣ ΕΚ ΟΣΗΣ Το παρόν βιβλίο περιέχει τα παρακάτω κεφάλαια: α) Από
7.6 Το συµβολικό σύστηµα R-S των Cahn, Ingold, Prelog
 7.6 Το συµβολικό σύστηµα R-S των ahn, Ingold, Prelog ρ Χάρης Ε. Σεµιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Για να καθοριστεί η απόλυτη στερεοαπεικόνιση ενός συστήµατος απαιτούνται δυο προϋποθέσεις: 1. Χρειάζονται
7.6 Το συµβολικό σύστηµα R-S των ahn, Ingold, Prelog ρ Χάρης Ε. Σεµιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Για να καθοριστεί η απόλυτη στερεοαπεικόνιση ενός συστήµατος απαιτούνται δυο προϋποθέσεις: 1. Χρειάζονται
Οργανική Χημεία. 24-4. Που οφείλεται η ικανότητα του άνθρακα να σχηματίζει τόσες πολλές ενώσεις; Ο άνθρακας έχει ιδιαίτερα χαρακτηριστικά :
 Οργανική Χημεία ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 24-1. Με τι ασχολείται η Οργανική Χημεία; Πεδίο ενασχόλησης του κλάδου της Χημείας που ονομάζεται Οργανική Χημεία είναι οι ενώσεις του άνθρακα (C). 24-2. Ποιες
Οργανική Χημεία ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 24-1. Με τι ασχολείται η Οργανική Χημεία; Πεδίο ενασχόλησης του κλάδου της Χημείας που ονομάζεται Οργανική Χημεία είναι οι ενώσεις του άνθρακα (C). 24-2. Ποιες
Κεφάλαιο 7 Στερεοχηµεία
 Κεφάλαιο 7 Στερεοχηµεία 7.1 Μοριακή χειροµορφία: Εναντιοµερή Χειροµορφία Ένα µόριο είναι χειρόµορφο εάν οι δυο µορφές του που έχουν σχέση ειδώλου-αντικειµένου δεν συµπίπτουν η µια πάνω στην άλλη. Ένα µόριο
Κεφάλαιο 7 Στερεοχηµεία 7.1 Μοριακή χειροµορφία: Εναντιοµερή Χειροµορφία Ένα µόριο είναι χειρόµορφο εάν οι δυο µορφές του που έχουν σχέση ειδώλου-αντικειµένου δεν συµπίπτουν η µια πάνω στην άλλη. Ένα µόριο
ΚΕΦΑΛΑΙΟ ΠΕΝΤΕ. [Στερεοϊσομερή]
![ΚΕΦΑΛΑΙΟ ΠΕΝΤΕ. [Στερεοϊσομερή] ΚΕΦΑΛΑΙΟ ΠΕΝΤΕ. [Στερεοϊσομερή]](/thumbs/52/30410343.jpg) ΚΕΦΑΛΑΙΟ ΠΕΝΤΕ [Στερεοϊσομερή] Στερεοϊσομερή Τα φυσιολογικά αποτελέσματα των δύο εναντιομερών του βρογχοδιασταλτικού φαρμάκου αλβουτερόλη διαφέρουν δραματικά. Το R-εναντιομερές του αυξάνει τη διάμετρο
ΚΕΦΑΛΑΙΟ ΠΕΝΤΕ [Στερεοϊσομερή] Στερεοϊσομερή Τα φυσιολογικά αποτελέσματα των δύο εναντιομερών του βρογχοδιασταλτικού φαρμάκου αλβουτερόλη διαφέρουν δραματικά. Το R-εναντιομερές του αυξάνει τη διάμετρο
ΣΥΣΚΕΥΗ ΦΑΙΝΟΜΕΝΩΝ ΠΟΛΩΣΗΣ POA01 ΦΥΛΛΑΔΙΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ
 ΣΥΣΚΕΥΗ ΦΑΙΝΟΜΕΝΩΝ ΠΟΛΩΣΗΣ POA01 ΦΥΛΛΑΔΙΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ 1 ΣΚΟΠΟΣ Η παρατήρηση του φαινομένου της πόλωσης και η μέτρηση της γωνίας στροφής του πολωμένου φωτός διαλυμάτων οπτικά ενεργών ουσιών π.χ. σάκχαρα.
ΣΥΣΚΕΥΗ ΦΑΙΝΟΜΕΝΩΝ ΠΟΛΩΣΗΣ POA01 ΦΥΛΛΑΔΙΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ 1 ΣΚΟΠΟΣ Η παρατήρηση του φαινομένου της πόλωσης και η μέτρηση της γωνίας στροφής του πολωμένου φωτός διαλυμάτων οπτικά ενεργών ουσιών π.χ. σάκχαρα.
9 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΤΩΝ ΥΔΑΤΑΝΘΡΑΚΩΝ
 9 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΤΩΝ ΥΔΑΤΑΝΘΡΑΚΩΝ Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των υδατανθράκων (μονοσακχαριτών και πολυσακχαριτών). Τρόποι δόμησης των πολυσακχαριτών από μονοσακχαρίτες,
9 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΤΩΝ ΥΔΑΤΑΝΘΡΑΚΩΝ Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των υδατανθράκων (μονοσακχαριτών και πολυσακχαριτών). Τρόποι δόμησης των πολυσακχαριτών από μονοσακχαρίτες,
C n (H 2 O) ν 22/11/2016 2
 22/11/2016 1 1 C n (H 2 O) ν 22/11/2016 2 Εκτιμάται πως ετησίως παράγονται 100 δισεκατομμύρια τόνοι υδατανθράκων με τη διαδικασία της φωτοσύνθεσης 22/11/2016 3 δεν μπορούν να υδρολυθούν σε άλλα μικρότερα
22/11/2016 1 1 C n (H 2 O) ν 22/11/2016 2 Εκτιμάται πως ετησίως παράγονται 100 δισεκατομμύρια τόνοι υδατανθράκων με τη διαδικασία της φωτοσύνθεσης 22/11/2016 3 δεν μπορούν να υδρολυθούν σε άλλα μικρότερα
Me O N H C 2. S D 2 χειρική δοµή. R εναντιοµερές
 ΠΡΟΒΛΗΜΑ 1.1 Απάντηση/ ανάλυση Για την επεξεργασία του συγκεκριµένου προβλήµατος είναι κατάλληλες οι απεικονίσεις κατά Newmman κάθετα στο διφαινυλικό δεσµό. Εάν επιπλέον δεχθούµε ότι το αµιδικό σύστηµα
ΠΡΟΒΛΗΜΑ 1.1 Απάντηση/ ανάλυση Για την επεξεργασία του συγκεκριµένου προβλήµατος είναι κατάλληλες οι απεικονίσεις κατά Newmman κάθετα στο διφαινυλικό δεσµό. Εάν επιπλέον δεχθούµε ότι το αµιδικό σύστηµα
Οργανική Χημεία. Βιολογικές Επιστήμες Βιολογία Γεωπονία Ιατρική κ.α. Βιοχημεία. Οργανική Χημεία. Φυσικές Επιστήμες Φυσική Μαθηματικά
 Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax: 210 529 4265 Βιοχημεία
Πέτρος Ταραντίλης Αναπληρωτής Καθηγητής Εργαστήριο Χημείας, Τμήμα Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax: 210 529 4265 Βιοχημεία
Περίληψη Κεφαλαίου 2
 Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
ΙΣΟΜΕΡΕΙΑ. Χημεία Α Λυκείου Χημεία ΓΠ Β Λυκείου (Επανάληψη) Ιωάννης Σ. Κάτσενος (Φυσικός MSc)
 ΙΣΟΜΕΡΕΙΑ Χημεία Α Λυκείου Χημεία ΓΠ Β Λυκείου (Επανάληψη) Ιωάννης Σ. Κάτσενος (Φυσικός MSc) Εισαγωγή Είναι το φαινόμενο κατά το οποίο 2 ή περισσότερες ενώσεις έχουν τον ίδιο μοριακό τύπο αλλά διαφορετικές
ΙΣΟΜΕΡΕΙΑ Χημεία Α Λυκείου Χημεία ΓΠ Β Λυκείου (Επανάληψη) Ιωάννης Σ. Κάτσενος (Φυσικός MSc) Εισαγωγή Είναι το φαινόμενο κατά το οποίο 2 ή περισσότερες ενώσεις έχουν τον ίδιο μοριακό τύπο αλλά διαφορετικές
Οργανική Χημεία. Κεφάλαιο 26: Βιομόρια: υδατάνθρακες
 Οργανική Χημεία Κεφάλαιο 26: Βιομόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισμό Άμυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαμβάκι είναι καθαροί υδατάνθρακες
Οργανική Χημεία Κεφάλαιο 26: Βιομόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισμό Άμυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαμβάκι είναι καθαροί υδατάνθρακες
Συντακτικός τύπος. Ο Στερεοχημικός τύπος μας δίνει την διάταξη των ατόμων στο χώρο. Ο Συντακτικός τύπος μας δίνει την διάταξη των ατόμων στο επίπεδο.
 Ι σ ο μ έ ρεια 27 Ισομέρεια ονομάζουμε το φαινόμενο κατά το οποίο, δύο ή περισσότερες οργανικές ενώσεις έχουν τον ίδιο Μοριακό Τύπο, αλλά διαφέρουν στον Συντακτικό ή στον Στερεοχημικό Τύπο. π.χ. στο μοριακό
Ι σ ο μ έ ρεια 27 Ισομέρεια ονομάζουμε το φαινόμενο κατά το οποίο, δύο ή περισσότερες οργανικές ενώσεις έχουν τον ίδιο Μοριακό Τύπο, αλλά διαφέρουν στον Συντακτικό ή στον Στερεοχημικό Τύπο. π.χ. στο μοριακό
ΣΤΟΙΧΕΙΑ ΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑΣ ΜΕ ΧΡΗΣΗ ΠΟΛΥΜΕΣΩΝ
 2 Ο ΣΥΝΕΔΡΙΟ ΣΤΗ ΣΥΡΟ ΤΠΕ ΣΤΗΝ ΕΚΠΑΙΔΕΥΣΗ 405 ΣΤΟΙΧΕΙΑ ΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑΣ ΜΕ ΧΡΗΣΗ ΠΟΛΥΜΕΣΩΝ Κορακάκης Γώργιος Τεχνολόγος γραφικών τεχνών-χημικός- Msc ΔιΧηΝΕΤ gk1966@yahoo.com Μουτεβέλη- Μηνακάκη Παναγιώτα
2 Ο ΣΥΝΕΔΡΙΟ ΣΤΗ ΣΥΡΟ ΤΠΕ ΣΤΗΝ ΕΚΠΑΙΔΕΥΣΗ 405 ΣΤΟΙΧΕΙΑ ΣΤΕΡΕΟΪΣΟΜΕΡΕΙΑΣ ΜΕ ΧΡΗΣΗ ΠΟΛΥΜΕΣΩΝ Κορακάκης Γώργιος Τεχνολόγος γραφικών τεχνών-χημικός- Msc ΔιΧηΝΕΤ gk1966@yahoo.com Μουτεβέλη- Μηνακάκη Παναγιώτα
Οργανική Χηµεία. Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες
 Οργανική Χηµεία Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισµό Άµυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαµβάκι είναι καθαροί υδατάνθρακες
Οργανική Χηµεία Κεφάλαιο 26: Βιοµόρια: υδατάνθρακες 1. Γενικά Ενώσεις που απαντούν σε κάθε ζωντανό οργανισµό Άµυλο και ζάχαρη στις τροφές και κυτταρίνη στο ξύλο, χαρτί και βαµβάκι είναι καθαροί υδατάνθρακες
Πως διαδίδονται τα Η/Μ κύματα σε διαφανή διηλεκτρικά?
 Πως διαδίδονται τα Η/Μ κύματα σε διαφανή διηλεκτρικά? (Μη-μαγνητικά, μη-αγώγιμα, διαφανή στερεά ή υγρά με πυκνή, σχετικά κανονική διάταξη δομικών λίθων). Γραμμικά πολωμένο κύμα προσπίπτει σε ηλεκτρόνιο
Πως διαδίδονται τα Η/Μ κύματα σε διαφανή διηλεκτρικά? (Μη-μαγνητικά, μη-αγώγιμα, διαφανή στερεά ή υγρά με πυκνή, σχετικά κανονική διάταξη δομικών λίθων). Γραμμικά πολωμένο κύμα προσπίπτει σε ηλεκτρόνιο
επßπεδο ανüκλασηò κüθετο στη σελßδα η σελßδα Απεικονίσεις της αχειρικής ένωσης 1,1- διχλωροαιθάνιο.
 rflsym1 1 Κατοπτρική συµµετρία και χειρικότητα. Κατοπτρική συµµετρία έχει µια δοµή όταν µια δεύτερη δοµή που δηµιουργείται (κατοπτρική δοµή, είδωλο) µε αντιστοίχηση όλων των σηµείων της πρώτης σε ισαπέχουσες
rflsym1 1 Κατοπτρική συµµετρία και χειρικότητα. Κατοπτρική συµµετρία έχει µια δοµή όταν µια δεύτερη δοµή που δηµιουργείται (κατοπτρική δοµή, είδωλο) µε αντιστοίχηση όλων των σηµείων της πρώτης σε ισαπέχουσες
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ποιο άτομο έχει το ακόλουθο διάγραμμα ηλεκτρονικής δομής; 3d 4s 4p Ar 2. Σε καθεμιά από τις ακόλουθες σφαίρες αντιστοιχείστε τα άτομα των στοιχείων K, Rb, Ca και Br.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ποιο άτομο έχει το ακόλουθο διάγραμμα ηλεκτρονικής δομής; 3d 4s 4p Ar 2. Σε καθεμιά από τις ακόλουθες σφαίρες αντιστοιχείστε τα άτομα των στοιχείων K, Rb, Ca και Br.
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Μοριακά Πρότυπα (Μοντέλα)
 Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
Περίληψη Κεφαλαίου 3
 Περίληψη Κεφαλαίου 3 Λειτουργική οµάδα: άτοµο ή σύνολο ατόµων ενός µορίου που προσδίδει χαρακτηριστική χηµική συµπεριφορά στο µόριο Αλκάνια: κατηγορία υδρογονανθράκων µε γενικό µοριακό τύπο C v H 2v+2
Περίληψη Κεφαλαίου 3 Λειτουργική οµάδα: άτοµο ή σύνολο ατόµων ενός µορίου που προσδίδει χαρακτηριστική χηµική συµπεριφορά στο µόριο Αλκάνια: κατηγορία υδρογονανθράκων µε γενικό µοριακό τύπο C v H 2v+2
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Οπτική Πολωσιμετρία
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Οπτική Πολωσιμετρία Ιωάννης Πούλιος Αθανάσιος Κούρας Λίντα Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124 ΘΕΣΣΑΛΟΝΙΚΗ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Οπτική Πολωσιμετρία Ιωάννης Πούλιος Αθανάσιος Κούρας Λίντα Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124 ΘΕΣΣΑΛΟΝΙΚΗ
Οργανική Χημεία. Κεφάλαιο 1: Δομή και δεσμοί
 Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Συστήματα συντεταγμένων
 Κεφάλαιο. Για να δημιουργήσουμε τρισδιάστατα αντικείμενα, που μπορούν να παρασταθούν στην οθόνη του υπολογιστή ως ένα σύνολο από γραμμές, επίπεδες πολυγωνικές επιφάνειες ή ακόμη και από ένα συνδυασμό από
Κεφάλαιο. Για να δημιουργήσουμε τρισδιάστατα αντικείμενα, που μπορούν να παρασταθούν στην οθόνη του υπολογιστή ως ένα σύνολο από γραμμές, επίπεδες πολυγωνικές επιφάνειες ή ακόμη και από ένα συνδυασμό από
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών
 Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Ενίσχυση και ανίχνευση χειρομορφίας μέσω
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Ενίσχυση και ανίχνευση χειρομορφίας μέσω
Bιομόρια : Υδατάνθρακες (1)
 Bιομόρια : Υδατάνθρακες () C δομή, ταξινόμηση C απεικονίσεις, διαμορφώσεις C αντιδράσεις Bιομόρια : Υδατάνθρακες (2) C ταξινόμηση - δομή C η γλυκόζη ήταν ο πρώτος απλός υδατάνθρακας που απομονώθηκε σε
Bιομόρια : Υδατάνθρακες () C δομή, ταξινόμηση C απεικονίσεις, διαμορφώσεις C αντιδράσεις Bιομόρια : Υδατάνθρακες (2) C ταξινόμηση - δομή C η γλυκόζη ήταν ο πρώτος απλός υδατάνθρακας που απομονώθηκε σε
Περίληψη 1 ου Κεφαλαίου
 Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Βασικές διαδικασίες παραγωγής πολωμένου φωτός
 Πόλωση του φωτός Βασικές διαδικασίες παραγωγής πολωμένου φωτός πόλωση λόγω επιλεκτικής απορρόφησης - διχρωισμός πόλωση λόγω ανάκλασης από μια διηλεκτρική επιφάνεια πόλωση λόγω ύπαρξης δύο δεικτών διάθλασης
Πόλωση του φωτός Βασικές διαδικασίες παραγωγής πολωμένου φωτός πόλωση λόγω επιλεκτικής απορρόφησης - διχρωισμός πόλωση λόγω ανάκλασης από μια διηλεκτρική επιφάνεια πόλωση λόγω ύπαρξης δύο δεικτών διάθλασης
Tα λογικά βήματα της λύσης μπορεί να είναι αναλυτικά τα ακόλουθα:
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση-Στερεοχημεία και Μηχανισμοί. Μάθημα 629,Επιλεγόμενο Διδάσκων: Κ. Χ. Φρούσιος Εξεταστική Περίοδος Ιουνίου 2013 Διάρκεια εξέτασης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση-Στερεοχημεία και Μηχανισμοί. Μάθημα 629,Επιλεγόμενο Διδάσκων: Κ. Χ. Φρούσιος Εξεταστική Περίοδος Ιουνίου 2013 Διάρκεια εξέτασης
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές)
 Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 4 Κανόνες ονοματολογίας ανθρακικών ομάδων. Ισομέρεια McMurry σελ. 47-54, 73-121 145-156, 47-54 Διδάσκων: Στ. Μπογιατζής
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 4 Κανόνες ονοματολογίας ανθρακικών ομάδων. Ισομέρεια McMurry σελ. 47-54, 73-121 145-156, 47-54 Διδάσκων: Στ. Μπογιατζής
Α Ε Τ. ΤΕΙ Αθήνας. Στ. Μπογιατζής, επίκουρος καθηγητής ΤΕΙ Αθήνας. ΤΕΙ Αθήνας / ΣΑΕΤ / Στ. Μπογιατζής
 Στ. Μπογιατζής, επίκουρος καθηγητής Ομοιοπολικές χημικές ενώσεις Ενώσεις του άνθρακα Χαρακτηριστικές ομάδες Τετραεδρική μοριακή δομή Επίπεδη τριγωνική μοριακή δομή Ευθύγραμμη μοριακή δομή Τα οργανικά μόρια
Στ. Μπογιατζής, επίκουρος καθηγητής Ομοιοπολικές χημικές ενώσεις Ενώσεις του άνθρακα Χαρακτηριστικές ομάδες Τετραεδρική μοριακή δομή Επίπεδη τριγωνική μοριακή δομή Ευθύγραμμη μοριακή δομή Τα οργανικά μόρια
ΚΕΦΑΛΑΙΟ 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ
 ΚΕΦΑΛΑΙΟ 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανικές ενώσεις Οργανική Χημεία είναι ο κλάδος της Χημείας που ασχολείται με τις ενώσεις του άνθρακα (C). Οργανικές ενώσεις ονομάζονται οι χημικές ενώσεις που
ΚΕΦΑΛΑΙΟ 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανικές ενώσεις Οργανική Χημεία είναι ο κλάδος της Χημείας που ασχολείται με τις ενώσεις του άνθρακα (C). Οργανικές ενώσεις ονομάζονται οι χημικές ενώσεις που
Προβλήματα Οργανικής Χημείας
 Γράψτε ένα αποδεκτό όνομα κατά IUPA για τα παρακάτω μόρια (να γίνει όπου προκύπτει χαρακτηρισμός E ή Z και cis ή trans). 1. 2. 3. 4 5. 6. 7. 8. 9. 10. 11. 12. Πέτρος Α. Ταραντίλης 1 Ποια από τα παρακάτω
Γράψτε ένα αποδεκτό όνομα κατά IUPA για τα παρακάτω μόρια (να γίνει όπου προκύπτει χαρακτηρισμός E ή Z και cis ή trans). 1. 2. 3. 4 5. 6. 7. 8. 9. 10. 11. 12. Πέτρος Α. Ταραντίλης 1 Ποια από τα παρακάτω
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. Βιολογικές Επιστήμες Βιολογία Γεωπονία Ιατρική κ.α. Βιοχημεία. Οργανική Χημεία. Φυσικές Επιστήμες Φυσική Μαθηματικά
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ Βιοχημεία Βιολογικές Επιστήμες Βιολογία Γεωπονία Ιατρική κ.α Οργανική Χημεία Φυσικές Επιστήμες Φυσική Μαθηματικά ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ.η... Organic Οργανική hemistry Χημεία has έχει literally
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ Βιοχημεία Βιολογικές Επιστήμες Βιολογία Γεωπονία Ιατρική κ.α Οργανική Χημεία Φυσικές Επιστήμες Φυσική Μαθηματικά ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ.η... Organic Οργανική hemistry Χημεία has έχει literally
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ ΚΥΡΙΟΤΕΡΕΣ ΧΑΡΑΚΤΗΡΙΣΤΙΚΕΣ ΟΜΑΔΕΣ
 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ -Χαρακτηριστική ομάδα: ονομάζεται ένα άτομο ή μια ομάδα ατόμων στην οποία οφείλονται οι περισσότερες ιδιότητες της ένωσης στην οποία ανήκει. ΚΥΡΙΟΤΕΡΕΣ ΧΑΡΑΚΤΗΡΙΣΤΙΚΕΣ
1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ -Χαρακτηριστική ομάδα: ονομάζεται ένα άτομο ή μια ομάδα ατόμων στην οποία οφείλονται οι περισσότερες ιδιότητες της ένωσης στην οποία ανήκει. ΚΥΡΙΟΤΕΡΕΣ ΧΑΡΑΚΤΗΡΙΣΤΙΚΕΣ
ΠΙΝΑΚΑΣ ΟΝΟΜΑΤΟΛΟΓΙΑΣ Δεύτερο συνθετικό (κορεσμένη ή ακόρεστη;) (απλοί, διπλοί, τριπλοί δεσμοί;)
 Θ. Καπίας 1 ο ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ ΚΟΡΔΕΛΙΟΥ, Β ΛΥΚΕΙΟΥ, ΧΗΜΕΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1 - ΦΥΛΛΑΔΙΟ ΒΑΣΙΚΟΙ ΚΑΝΟΝΕΣ ΟΝΟΜΑΤΟΛΟΓΙΑΣ Πρώτο συνθετικό (αριθμός ατόμων C κύριας ανθρακικής αλυσίδας) 1 C μεθ- 2 C
Θ. Καπίας 1 ο ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ ΚΟΡΔΕΛΙΟΥ, Β ΛΥΚΕΙΟΥ, ΧΗΜΕΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1 - ΦΥΛΛΑΔΙΟ ΒΑΣΙΚΟΙ ΚΑΝΟΝΕΣ ΟΝΟΜΑΤΟΛΟΓΙΑΣ Πρώτο συνθετικό (αριθμός ατόμων C κύριας ανθρακικής αλυσίδας) 1 C μεθ- 2 C
Υποδειγματικά Λυμένα Προβλήματα Κεφαλαίου 4
 ΔΟΜΗ, ΔΡΑΣΤΙΚΟΤΗΤΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ STRUTURE, REATIVITY AND MEANISM IN ORGANI EMISTRY Διονύσης Α. Παπαϊωάννου Καθηγητής Οργανικής Χημείας Dionysios A. Papaioannou Professor of Organic
ΔΟΜΗ, ΔΡΑΣΤΙΚΟΤΗΤΑ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΣΤΗΝ ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ STRUTURE, REATIVITY AND MEANISM IN ORGANI EMISTRY Διονύσης Α. Παπαϊωάννου Καθηγητής Οργανικής Χημείας Dionysios A. Papaioannou Professor of Organic
ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ
 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανικές ενώσεις ονομάζονται οι χημικές ενώσεις που περιέχουν άνθρακα, εκτός από τις ενώσεις μονοξείδιο του άνθρακα (C), διοξείδιο του άνθρακα (C 2 ), ανθρακικό οξύ (H
1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανικές ενώσεις ονομάζονται οι χημικές ενώσεις που περιέχουν άνθρακα, εκτός από τις ενώσεις μονοξείδιο του άνθρακα (C), διοξείδιο του άνθρακα (C 2 ), ανθρακικό οξύ (H
Οργανική Χημεία. Πέτρος Ταραντίλης Επίκουρος Καθηγητής Εργαστήριο Χημείας, Γενικό Τμήμα, Τηλ.: , Fax:
 Πέτρος Ταραντίλης Επίκουρος Καθηγητής Εργαστήριο Χημείας, Γενικό Τμήμα, Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax: 210 529 4265 Θεωρία -Ύλη μαθήματος Ανθρακας-ταξινόμηση
Πέτρος Ταραντίλης Επίκουρος Καθηγητής Εργαστήριο Χημείας, Γενικό Τμήμα, Ιερά Οδός 75, 118 55 Αθήνα, e-mail: ptara@aua.gr, Τηλ.: 210 529 4262, Fax: 210 529 4265 Θεωρία -Ύλη μαθήματος Ανθρακας-ταξινόμηση
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Β ΤΑΞΗ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 21/04/ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6)
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Β ΤΑΞΗ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 21/04/2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Β ΤΑΞΗ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 21/04/2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις
 Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής
 ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ
 ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή
 7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
7.13 Χημικές αντιδράσεις που παράγουν διαστερεομερή Στερεοχημεία της προσθήκης στα αλκένια C C + E Y E C C Y Για να μάθετε να κατανοείτε τη στερεοχημεία του προϊόντος, χρειάζεται να γνωρίζετε δυο πράγματα:
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Για να παρασκευάσετε ένα διάλυμα ορισμένου p στο Εργαστήριο χρησιμοποιήσατε το ρυθμιστικό ζεύγος C 3 COOΗ / C 3 COONa 3 2 O. Έστω τώρα ότι θέλετε να παρασκευάσετε,
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Για να παρασκευάσετε ένα διάλυμα ορισμένου p στο Εργαστήριο χρησιμοποιήσατε το ρυθμιστικό ζεύγος C 3 COOΗ / C 3 COONa 3 2 O. Έστω τώρα ότι θέλετε να παρασκευάσετε,
Μάθημα 20 ο. Το σχήμα των μορίων
 Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Εισαγωγικά. Σύνταξη, ταξινόμηση και τάξεις οργανικών ενώσεων. Τρόποι γραφής οργανικών ενώσεων. Λειτουργικές ομάδες.
 ΤΜΗΜΑ ΓΕΩΠΟΝΙΑΣ - Μάθημα «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ» Ακαδημαϊκό έτος 2012-2013 ΠΡΟΓΡΑΜΜΑ ΘΕΩΡΗΤΙΚΩΝ, ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΑΙ ΦΡΟΝΤΙΣΤΗΡΙΑΚΩΝ ΜΑΘΗΜΑΤΩΝ ΤΡΙΤΗ 9.00-12.00 (Ι3 - Θεωρία) ΠΕΜΠΤΗ 10.00 12.00 (I3-Θεωρία) ή (Εργαστήρια)
ΤΜΗΜΑ ΓΕΩΠΟΝΙΑΣ - Μάθημα «ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ» Ακαδημαϊκό έτος 2012-2013 ΠΡΟΓΡΑΜΜΑ ΘΕΩΡΗΤΙΚΩΝ, ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΑΙ ΦΡΟΝΤΙΣΤΗΡΙΑΚΩΝ ΜΑΘΗΜΑΤΩΝ ΤΡΙΤΗ 9.00-12.00 (Ι3 - Θεωρία) ΠΕΜΠΤΗ 10.00 12.00 (I3-Θεωρία) ή (Εργαστήρια)
διπλός δεσμός τριπλός δεσμός
 Ακόρεστοι Υδρογονάνθρακες Αλκένια Αλκίνια Αρωματικές ενώσεις Αλκένια διπλός δεσμός Αλκίνια τριπλός δεσμός Αρωματικοί υδρογονάνθρακες Βενζόλιο Αλκένια-ΑλκίνιαΑλκίνια Μη πολικές ενώσεις Αδιάλυτες στο νερό
Ακόρεστοι Υδρογονάνθρακες Αλκένια Αλκίνια Αρωματικές ενώσεις Αλκένια διπλός δεσμός Αλκίνια τριπλός δεσμός Αρωματικοί υδρογονάνθρακες Βενζόλιο Αλκένια-ΑλκίνιαΑλκίνια Μη πολικές ενώσεις Αδιάλυτες στο νερό
ΑΝΑΠΤΥΞΗ ΔΙΑΔΙΚΤΥΑΚΟΥ ΕΚΠΑΙΔΕΥΤΙΚΟΥ ΥΛΙΚΟΥ ΓΙΑ ΤΗΝ ΟΠΤΙΚΗ ΙΣΟΜΕΡΕΙΑ ΜΕ ΧΡΗΣΗ ΤΡΙΣΔΙΑΣΤΑΤΩΝ ΜΟΡΙΑΚΩΝ ΜΟΝΤΕΛΩΝ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΔΙΑΠΑΝΕΠΙΣΤΗΜΙΑΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ιδακτική της Χημείας και Νέες Εκπαιδευτικές Τεχνολογίες (Δι.Χη.ΝΕΤ) ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΔΙΑΠΑΝΕΠΙΣΤΗΜΙΑΚΟ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ιδακτική της Χημείας και Νέες Εκπαιδευτικές Τεχνολογίες (Δι.Χη.ΝΕΤ) ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ
Φυσικό αέριο. Ορισμός: Το φυσικό αέριο είναι μίγμα αέριων υδρογονανθράκων με κύριο συστατικό το μεθάνιο, CH 4 (μέχρι και 90%).
 Φυσικό αέριο Ορισμός: Το φυσικό αέριο είναι μίγμα αέριων υδρογονανθράκων με κύριο συστατικό το μεθάνιο, CH 4 (μέχρι και 90%). Το φυσικό αέριο χρησιμοποιείται ως καύσιμο και παρουσιάζει δύο βασικά πλεονεκτήματα
Φυσικό αέριο Ορισμός: Το φυσικό αέριο είναι μίγμα αέριων υδρογονανθράκων με κύριο συστατικό το μεθάνιο, CH 4 (μέχρι και 90%). Το φυσικό αέριο χρησιμοποιείται ως καύσιμο και παρουσιάζει δύο βασικά πλεονεκτήματα
Αλκυλαλογονίδια. Επίκουρος καθηγητής Χρήστος Παππάς
 Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
Αλκυλαλογονίδια Επίκουρος καθηγητής Χρήστος Παππάς 1 Αλκυλαλογονίδια Αλκυλαλογονίδια ονομάζονται οι οργανικές ενώσεις οι οποίες, ως λειτουργική ομάδα, διαθέτουν την ομάδα C-X: -X= -F, -Cl, -Br, -I. Η ισχύς
Μάθημα 21 ο. Το σχήμα των μορίων. Θεωρία VSEPR. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια)
 relst1 1 ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια) Οι θέσεις των διάφορων υποκαταστατών ενός κυκλικού µορίου µε αναφορά στο επίπεδο του δακτυλίου,
relst1 1 ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΗΣ ΣΧΕΤΙΚΗΣ ΣΤΕΡΕΟΧΗΜΕΙΑΣ ΥΠΟΚΑΤΕΣΤΗΜΕΝΩΝ ΚΥΚΛΙΚΩΝ ΕΝΩΣΕΩΝ (cis trans ισοµέρεια) Οι θέσεις των διάφορων υποκαταστατών ενός κυκλικού µορίου µε αναφορά στο επίπεδο του δακτυλίου,
Γραμμικώς πολωμένα κύματα σε κάθετο επίπεδο
 ΚΥΚΛΙΚΟΣ ΔΙΧΡΩΙΣΜΟΣ Γραμμικώς πολωμένα κύματα σε κάθετο επίπεδο όταν το διάνυσμα του ηλεκτρικού πεδίου ταλαντεύεται κατά μήκος μιας ίσιας γραμμής τότε τα κύματα λέγονται επίπεδα ή γραμμικώς πολωμένα Γραμμικώς
ΚΥΚΛΙΚΟΣ ΔΙΧΡΩΙΣΜΟΣ Γραμμικώς πολωμένα κύματα σε κάθετο επίπεδο όταν το διάνυσμα του ηλεκτρικού πεδίου ταλαντεύεται κατά μήκος μιας ίσιας γραμμής τότε τα κύματα λέγονται επίπεδα ή γραμμικώς πολωμένα Γραμμικώς
Μοριακή Γεωμετρία Πολικότητα των Μορίων. Εισαγωγική Χημεία
 Μοριακή Γεωμετρία Πολικότητα των Μορίων Εισαγωγική Χημεία 2013-14 1 Τα σχήματα των μορίων Οι δομές Lewis δίνουν πληροφορίες για την σύνδεση μεταξύ των ατόμων : Μας πληροφορούν για το ποια άτομα συνδέονται
Μοριακή Γεωμετρία Πολικότητα των Μορίων Εισαγωγική Χημεία 2013-14 1 Τα σχήματα των μορίων Οι δομές Lewis δίνουν πληροφορίες για την σύνδεση μεταξύ των ατόμων : Μας πληροφορούν για το ποια άτομα συνδέονται
Σχεδιάστε τύπους ανακλίντρων για τις ενώσεις Α και Β και εξηγήστε σχετικά. Yπόδειξη : Η αντίδραση Μichael θεωρείται γενικά αντιστρεπτή αντίδραση.
 1 1 H 3 C H 3 C αναγωγή H 3 C H 3 C H H ± A B Η διφαινυλική κετόνη Α εµφανίζει ατροποϊσοµέρεια και σε συνήθη θερµοκρασία µπορεί να αναλυθεί σε δυο σταθερές έναντιοµερικές µορφές. 1. Χαρακτηρίστε τις πλευρές
1 1 H 3 C H 3 C αναγωγή H 3 C H 3 C H H ± A B Η διφαινυλική κετόνη Α εµφανίζει ατροποϊσοµέρεια και σε συνήθη θερµοκρασία µπορεί να αναλυθεί σε δυο σταθερές έναντιοµερικές µορφές. 1. Χαρακτηρίστε τις πλευρές
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ Η ΧΗΜΕΙΑ ΤΩΝ ΠΡΟΪΝΤΩΝ ΚΑΘΗΜΕΡΙΝΗΣ ΧΡΗΣΗΣ
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ Η ΧΗΜΕΙΑ ΤΩΝ ΠΡΟΪΝΤΩΝ ΚΑΘΗΜΕΡΙΝΗΣ ΧΡΗΣΗΣ Ισομέρεια, Β! Τάξη,1 ο ΕΠΑΛ 1 Ο Μαγευτικός αόρατος μικρόκοσμος της Οργανικής Χημείας Ασπιρίνη 2 Ο Άνθρακας, ο μοναδικός! Ο Άνθρακας είναι μοναδικός
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ Η ΧΗΜΕΙΑ ΤΩΝ ΠΡΟΪΝΤΩΝ ΚΑΘΗΜΕΡΙΝΗΣ ΧΡΗΣΗΣ Ισομέρεια, Β! Τάξη,1 ο ΕΠΑΛ 1 Ο Μαγευτικός αόρατος μικρόκοσμος της Οργανικής Χημείας Ασπιρίνη 2 Ο Άνθρακας, ο μοναδικός! Ο Άνθρακας είναι μοναδικός
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού
 7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Προβλέψτε τον υβριδισμό καθενός ατόμου που συνδέεται με περισσότερα από ένα άλλα άτομα στο ακόλουθο μόριο. Πόσες μοίρες είναι περίπου η γωνία Ο C 1 C 2 ; 2. Σε ποιο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Προβλέψτε τον υβριδισμό καθενός ατόμου που συνδέεται με περισσότερα από ένα άλλα άτομα στο ακόλουθο μόριο. Πόσες μοίρες είναι περίπου η γωνία Ο C 1 C 2 ; 2. Σε ποιο
Χημικοί Τύποι Ενώσεων
 Χημικοί Τύποι Ενώσεων Οι χημικές ενώσεις γράφονται με τους παρακάτω τύπους: Εμπειρικός τύπος: είναι ο τύπος που δείχνει από ποια στοιχεία αποτελείται η ένωση καθώς και την αναλογία τους σε αυτήν. Π.χ.
Χημικοί Τύποι Ενώσεων Οι χημικές ενώσεις γράφονται με τους παρακάτω τύπους: Εμπειρικός τύπος: είναι ο τύπος που δείχνει από ποια στοιχεία αποτελείται η ένωση καθώς και την αναλογία τους σε αυτήν. Π.χ.
5.1 Ονοματολογία Αλκενίων. ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας
 5.1 Ονοματολογία Αλκενίων ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Αλκένια Τα αλκένια είναι υδρογονάνθρακες που περιέχουν ένα διπλό δεσμό άνθρακα-άνθρακα λέγονται επίσης "ολεφίνες" χαρακτηρίζονται
5.1 Ονοματολογία Αλκενίων ρ. Χάρης Ε. Σεμιδαλάς Επίκουρος Καθηγητής ΑΤΕΙ Αθήνας Αλκένια Τα αλκένια είναι υδρογονάνθρακες που περιέχουν ένα διπλό δεσμό άνθρακα-άνθρακα λέγονται επίσης "ολεφίνες" χαρακτηρίζονται
H 2 N CH 2 CH 3 O S. Σχήµα 1. Τα τέσσερα στερεοϊσοµερή µιας ένωσης µε 2 χειρικά κέντρα.
 corlst1 1 Στερεοχηµικοί συσχετισµοί. Απόλυτη και σχετική στερεοχηµεία. Σύγκριση δυο χειρικών κέντρων στο ίδιο µόριο. Έστω για παράδειγµα η διαπίστωση της στερεοχηµείας ενός απλού µορίου µε δυο χειρικά
corlst1 1 Στερεοχηµικοί συσχετισµοί. Απόλυτη και σχετική στερεοχηµεία. Σύγκριση δυο χειρικών κέντρων στο ίδιο µόριο. Έστω για παράδειγµα η διαπίστωση της στερεοχηµείας ενός απλού µορίου µε δυο χειρικά
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2013
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 14 Απριλίου 01 ιάρκεια Εξέτασης: ώρες ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθµό
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 14 Απριλίου 01 ιάρκεια Εξέτασης: ώρες ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθµό
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Οργανική Χημεία 24 4
 Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού
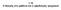 1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
Επαγωγικό φαινόμενο (Inductive Effect)- Συζυγιακό φαινόμενο (Conjugative Effect) ή Συντονισμός (Resonance) Αρωματικότητα (aromaticity)
 Επαγωγικό φαινόμενο (Inductive Effect)- Συζυγιακό φαινόμενο (Conjugative Effect) ή Συντονισμός (Resonance) Αρωματικότητα (aromaticity) Επίκουρος Καθηγητής Χρήστος Παππάς Επαγωγικό φαινόμενο (I) Τι είναι;
Επαγωγικό φαινόμενο (Inductive Effect)- Συζυγιακό φαινόμενο (Conjugative Effect) ή Συντονισμός (Resonance) Αρωματικότητα (aromaticity) Επίκουρος Καθηγητής Χρήστος Παππάς Επαγωγικό φαινόμενο (I) Τι είναι;
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Το κατιόν Α 2+ ενός ατόμου Α στη θεμελιώδη κατάσταση έχει δύο ηλεκτρόνια με n = 1, οκτώ ηλεκτρόνια με n = 2, δεκαοκτώ ηλεκτρόνια με n = 3 και οκτώ ηλεκτρόνια με n
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Το κατιόν Α 2+ ενός ατόμου Α στη θεμελιώδη κατάσταση έχει δύο ηλεκτρόνια με n = 1, οκτώ ηλεκτρόνια με n = 2, δεκαοκτώ ηλεκτρόνια με n = 3 και οκτώ ηλεκτρόνια με n
Φασματοσκοπία Υπερύθρου (IR, FTIR)
 Φασματοσκοπία Υπερύθρου (IR, FTIR) Εργαστήριο Ανάλυσης ΤΕΙ Αθήνας 2016-2017 Διδάσκοντες Βασιλεία Σινάνογλου Παναγιώτης Ζουμπουλάκης Σωτήρης Μπρατάκος Γενικά Στην φασματοσκοπία υπερύθρου μελετάμε την απορρόφηση
Φασματοσκοπία Υπερύθρου (IR, FTIR) Εργαστήριο Ανάλυσης ΤΕΙ Αθήνας 2016-2017 Διδάσκοντες Βασιλεία Σινάνογλου Παναγιώτης Ζουμπουλάκης Σωτήρης Μπρατάκος Γενικά Στην φασματοσκοπία υπερύθρου μελετάμε την απορρόφηση
Δείτε πώς δυο άνθρακες δίνουν με υδρογόνο τρείς διαφορετικές χημικές ενώσεις:
 Τι μελετά η Οργανική χημεία; Ποιες οι εξαιρέσεις; Τι υποστηρίζει η βιταλιστική θεωρία; Η 1 η σύνθεση οργανικής ουσίας στο εργαστήριο! Η βιταλιστική θεωρία καταρρίπτεται Πόσες οι οργανικές ενώσεις ; Περισσότερες
Τι μελετά η Οργανική χημεία; Ποιες οι εξαιρέσεις; Τι υποστηρίζει η βιταλιστική θεωρία; Η 1 η σύνθεση οργανικής ουσίας στο εργαστήριο! Η βιταλιστική θεωρία καταρρίπτεται Πόσες οι οργανικές ενώσεις ; Περισσότερες
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΔΙΕΥΘΥΝΣΗ ΑΝΩΤΕΡΗΣ ΚΑΙ ΑΝΩΤΑΤΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΥΠΗΡΕΣΙΑ ΕΞΕΤΑΣΕΩΝ ΠΑΓΚΥΠΡΙΕΣ ΕΞΕΤΑΣΕΙΣ 2015
 ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΔΙΕΥΘΥΝΣΗ ΑΝΩΤΕΡΗΣ ΚΑΙ ΑΝΩΤΑΤΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΥΠΗΡΕΣΙΑ ΕΞΕΤΑΣΕΩΝ ΠΑΓΚΥΠΡΙΕΣ ΕΞΕΤΑΣΕΙΣ 2015 Μάθημα: Χημεία Ημερομηνία και ώρα εξέτασης: Πέμπτη, 28 Μαΐου, 2015 8:00 11:00
ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΔΙΕΥΘΥΝΣΗ ΑΝΩΤΕΡΗΣ ΚΑΙ ΑΝΩΤΑΤΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΥΠΗΡΕΣΙΑ ΕΞΕΤΑΣΕΩΝ ΠΑΓΚΥΠΡΙΕΣ ΕΞΕΤΑΣΕΙΣ 2015 Μάθημα: Χημεία Ημερομηνία και ώρα εξέτασης: Πέμπτη, 28 Μαΐου, 2015 8:00 11:00
Μοριακά Πρότυπα και Ομοιοπολικός Δεσμός
 Μοριακά Πρότυπα και Ομοιοπολικός Δεσμός ΣΚΟΠΟΣ Σκοπός αυτής της άσκησης είναι να κατανοήσουμε πληρέστερα τις θεωρίες που αναφέρονται στη δημιουργία του ομοιοπολικού δεσμού και στη γεωμετρία των μορίων,
Μοριακά Πρότυπα και Ομοιοπολικός Δεσμός ΣΚΟΠΟΣ Σκοπός αυτής της άσκησης είναι να κατανοήσουμε πληρέστερα τις θεωρίες που αναφέρονται στη δημιουργία του ομοιοπολικού δεσμού και στη γεωμετρία των μορίων,
O H ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση. Στερεοχημεία-Μηχανισμοί (Μάθημα 629, Επιλεγόμενο) Διδάσκων :Κ.Χ.Φρούσιος Τμηματικές Εξετάσεις 08 ΣΕΠ 2010 Διάρκεια εξέτασης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανική Σύνθεση. Στερεοχημεία-Μηχανισμοί (Μάθημα 629, Επιλεγόμενο) Διδάσκων :Κ.Χ.Φρούσιος Τμηματικές Εξετάσεις 08 ΣΕΠ 2010 Διάρκεια εξέτασης
Χημεία. ΘΕΜΑ Α A1. α - 5 μονάδες
 Β ΓΕΛ 21 / 04 / 2019 Χημεία ΘΕΜΑ Α A1. α - 5 μονάδες A2. β - 5 μονάδες A3. α - 5 μονάδες A4. δ - 5 μονάδες A5. α - 5 μονάδες ΘΕΜΑ Β Β1. Σε ένα χημικό εργαστήριο διαθέτουμε ισοπροπυλική αλκοόλη (δευτεροταγής
Β ΓΕΛ 21 / 04 / 2019 Χημεία ΘΕΜΑ Α A1. α - 5 μονάδες A2. β - 5 μονάδες A3. α - 5 μονάδες A4. δ - 5 μονάδες A5. α - 5 μονάδες ΘΕΜΑ Β Β1. Σε ένα χημικό εργαστήριο διαθέτουμε ισοπροπυλική αλκοόλη (δευτεροταγής
Οργανική Χημεία. Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες
 Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
Οργανική Χημεία Χημεία καρβονυλικών ενώσεων & Κεφάλαιο 19: Αλδεϋδες και κετόνες 1. Καρβονυλικές ενώσεις Καρβονυλική ομάδα C=O σημαντικότερη λειτουργική ομάδα οργανικής χημείας Καρβονυλικές ομάδες βρίσκονται
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ο άργυρος εμφανίζεται στη φύση υπό τη μορφή δύο ισοτόπων τα οποία έχουν ατομικές μάζες 106,905 amu και 108,905 amu. (α) Γράψτε το σύμβολο για καθένα ισότοπο του αργύρου
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ο άργυρος εμφανίζεται στη φύση υπό τη μορφή δύο ισοτόπων τα οποία έχουν ατομικές μάζες 106,905 amu και 108,905 amu. (α) Γράψτε το σύμβολο για καθένα ισότοπο του αργύρου
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 7: Μοριακή γεωμετρία. Τόλης Ευάγγελος
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 7: Μοριακή γεωμετρία Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 7: Μοριακή γεωμετρία Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΕΣΜΟΥ
 ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
Θεωρία δεσµού σθένους - Υβριδισµός. Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης. Αντιδράσεις υποκατάστασης Πολυµερισµός
 11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
Μεθοδολογία Προβλημάτων
 Μεθοδολογία Προβλημάτων 39 Α. Προβλήματα εύρεσης του Μοριακού Τύπου χημικής ένωσης Ο Μοριακός τύπος μιας ένωσης μας δίνει το είδος των ατόμων που περιέχονται στο μόριο της ένωσης, αλλά και τον ακριβή τους
Μεθοδολογία Προβλημάτων 39 Α. Προβλήματα εύρεσης του Μοριακού Τύπου χημικής ένωσης Ο Μοριακός τύπος μιας ένωσης μας δίνει το είδος των ατόμων που περιέχονται στο μόριο της ένωσης, αλλά και τον ακριβή τους
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη. Ιοντικός χαρακτήρας δεσμών. Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
 Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2016 Β ΦΑΣΗ ΧΗΜΕΙΑ. Ηµεροµηνία: Τετάρτη 4 Μαΐου 2016 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 4 Μαΐου 2016 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από
ΤΑΞΗ: Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 4 Μαΐου 2016 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από
