ΜεΛετη τησ εκβασησ ΑΣΘεΝΩΝ Με ΝεΑΝΙΚη ΙΔΙOΠΑΘη ΑΡΘΡΙτΙΔΑ. ΓεΝετΙΚεΣ ΣΥΣΧετΙΣεΙΣ
|
|
|
- Οινώνη Αθανασιάδης
- 7 χρόνια πριν
- Προβολές:
Transcript
1 APIΣTOTEΛEIO ΠANEΠIΣTHMIO ΘEΣΣAΛONIKHΣ IATPIKO ΤΜΗΜΑ ΣΧOΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ TOMEAΣ ΠΑΘOΛOΓΙΑΣ Α ΠΑΘOΛOΓΙΚΗ ΚΛΙΝΙΚΗ ΔIEYΘYNTΗΣ: KAΘHΓHTΗΣ ΜΙΧΑΗΛ ΔΑΝΙΗΛΙΔΗΣ ΠANEΠ. ETOΣ Αριθμ ΜεΛετη τησ εκβασησ ΑΣΘεΝΩΝ Με ΝεΑΝΙΚη ΙΔΙOΠΑΘη ΑΡΘΡΙτΙΔΑ. ΓεΝετΙΚεΣ ΣΥΣΧετΙΣεΙΣ ΔεΣΠOΙΝΑ ΔηΜOΠOΥΛOΥ ΙΑΤΡOΣ ΠΑΘOΛOΓOΣ ΔIΔAKTOPIKH ΔIATPIBH YΠOBΛHΘHKE ΣTO IATPIKO ΤΜΗΜΑ ΤΗΣ ΣΧOΛΗΣ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ TOY APIΣTOTEΛEIOY ΠANEΠIΣTHMIOY ΘEΣΣAΛONIKHΣ ΘEΣΣAΛONIKH 2014
2 TPIMEΛHΣ ΣΥΜΒOΥΛεΥτΙΚη EΠITPOΠH ΔΑΝΙηΛΙΔηΣ ΜΙΧΑηΛ, ΚΑΘΗΓΗΤΗΣ TΡΑΧΑΝΑ ΜΑΡΙΑ, ΕΠΙΚ. ΚΑΘΗΓΗΤΡΙΑ ΣΙΔηΡOΠOΥΛOΣ ΠΡOΔΡOΜOΣ, ΕΠΙΚ. ΚΑΘΗΓΗΤΗΣ EΠTAMEΛHΣ εξεταστικη EΠITPOΠH ΔΑΝΙηΛΙΔηΣ ΜΙΧΑηΛ, ΚΑΘΗΓΗΤΗΣ TΡΑΧΑΝΑ ΜΑΡΙΑ, ΕΠΙΚ. ΚΑΘΗΓΗΤΡΙΑ ΣΙΔηΡOΠOΥΛOΣ ΠΡOΔΡOΜOΣ, ΕΠΙΚ. ΚΑΘΗΓΗΤΗΣ ΣεττΑΣ ΛOΥΚΑΣ, OΜOΤΙΜOΣ ΚΑΘΗΓΗΤΗΣ ΚΥΡΙΑΖηΣ ΓεΩΡΓΙOΣ, ΚΑΘΗΓΗΤΗΣ ΜΠεΝOΣ ΑΛεΞΙOΣ, ΚΑΘΗΓΗΤΗΣ ΧΑΪΔΙτΣ ΜΠετΙΝΑ, ΕΠΙΚ. ΚΑΘΗΓΗΤΡΙΑ «Ἡ ἔγκρισις τῆς Διδακτoρικῆς Διατριβῆς ὑπό τῆς Ἰατρικῆς Σχoλῆς τoῦ Ἀριστoτελείoυ Πανεπιστημίoυ Θεσσαλoνίκης δέν ὑπoδηλoῖ ἀπoδoχήν τῶν γνωμῶν τoῦ συγγραφέως». (Nόμoς 5343/32, ἄρθρ καί ν. 1268/82, ἄρθρ. 50 8)
3 APIΣTOTEΛEIO ΠANEΠIΣTHMIO ΘEΣΣAΛONIKHΣ ΤΜΗΜΑ ΙATPIKHΣ ΣXOΛHΣ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠPOEΔPOΣ TOΥ ΤΜΗΜΑΤOΣ KAΘΗΓΗΤΗΣ ΑΛΕΞΑΝΔΡOΣ ΓΑΡΥΦΑΛΛOΣ
4
5 Στην αγαπημένη μου οικογένεια
6
7 Π Ε Ρ Ι Ε Χ O Μ Ε Ν Α ΠΡOΛOΓOΣ ΓΕΝΙΚO MEΡOΣ 1. ΝεαΝικh ιδιoπαθhσ αρθρiτιδα - ιστoρικh αναδρoμh OΡιΣμOΣ-ταξιΝOμηΣη τησ ΝεαΝικhΣ ιδιoπαθoyσ αρθρiτιδασ κατa ilar επιδημιoλoγiα επίπτωση και επιπολασμός επιδημιολογικά χαρακτηριστικά της νόσου ΠαθOΓεΝεια τησ ΝεαΝικηΣ ιδιoπαθoυσ αρθριτιδασ Παθοφυσιολογικοί μηχανισμοί αιτιοπαθογενετικοί μηχανισμοί Περιβαλλοντικοί παράγοντες Γενετικοί παράγοντες η μοριακή γενετική και η γενετική ανάλυση στα πολυπαραγοντικά νοσήματα Oι μονονουκλεοτιδικοί πολυμορφισμοί στο ανθρώπινο γονιδίωμα μελέτες γενετικής συσχέτισης μελέτες συσχέτισης που καλύπτουν το πλήρες γονιδίωμα (GWAS) και πολυπαραγοντικά νοσήματα O ρόλος των hla και non-hla γονιδίων στη Νεανική ιδιοπαθή αρθρίτιδα hla συσχετίσεις non-hla συσχετίσεις TRAF1/C
8 STAT PTPN PTPN CD κλινικa χαρακτηριστικa των διαφoρων ΥΠOOμAδωΝ ΝεαΝικhΣ ιδιoπαθoyσ αρθρiτιδασ Συστηματική αρθρίτιδα Oλιγοαρθρίτιδα: εμμένουσα και επεκταθείσα Πολυαρθρίτιδα Πολυαρθρίτιδα RF-αρνητική Πολυαρθρίτιδα RF-θετική Ψωριασική αρθρίτιδα αρθρίτιδα που σχετίζεται με ενθεσίτιδα αδιαφοροποίητη αρθρίτιδα ιριδoκυκλiτιδα επιπτωσεισ τησ ΝεαΝικηΣ ιδιoπαθoyσ αρθρiτιδασ τοπικές διαταραχές ανάπτυξης Γενικευμένη διαταραχή της ανάπτυξης Oστεοπενία αμυλοείδωση Ποιότητα ζωής των ασθενών με Νεανική ιδιοπαθή αρθρίτιδα μακρoχρoνια EκβαΣη τησ ΝεαΝικhΣ ιδιoπαθoyσ αρθρiτιδασ κλινική ύφεση στη Νεανική ιδιοπαθή αρθρίτιδα αρθρική και εξωαρθρική καταστροφή Ποσοτική εκτίμηση αρθρικής και εξωαρθρικής καταστροφής (Juvenile Arthritis Damage index, JADi) ακτινολογικές βλάβες των αρθρώσεων διαταραχές ανάπτυξης χειρουργική αποκατάσταση Oφθαλμική βλάβη Λειτουργική ικανότητα Σωματική ικανότητα (Physical ability). ερωτηματολόγιο εκτίμησης της υγείας (health Assessment Questionnaire- Disability index, haq-di) κοινωνικοοικονομική κατάσταση Ψυχοκοινωνική κατάσταση... 81
9 9. ΠΡOΓΝωΣτικOι ΠαΡαΓOΝτεΣ κινδυνoυ θεραπευτικη ΠΡOΣεΓΓιΣη τησ ΝεαΝικηΣ ιδιoπαθoυσ αρθριτιδασ μη στεροειδή αντιφλεγμονώδη φάρμακα (μσαφ) κορτικοστεροειδή μεθοτρεξάτη Άλλα μη βιολογικά ανοσοτροποποιητικά της νόσου φάρμακα (Disease Modifying Anti-Rheumatic Drugs, DMARDS) βιολογικές ανοσοτροποποιητικές θεραπείες ανταγωνιστές του παράγοντα νέκρωσης των όγκων TNFα (inh-tnfα βιολογικοί παράγοντες) Abatacept (Orencia ) Anti-interleukin (il)-1 παράγοντες Anti-interleukin (il)-6 παράγοντας (Tocilizumab, Ro-Actempra ) Rituximab (Mabthera ) αυτόλογη μεταμόσχευση άωρων αιμοποιητικών κυττάρων (Autologous Stem Cell Transplantation, ASCT) θεραπεία συστηματικής αρθρίτιδας θεραπεία του συνδρόμου ενεργοποίησης των μακροφάγων θεραπεία ολιγοαρθρικής έναρξης Νεανικής ιδιοπαθούς αρθρίτιδας θεραπεία πολυαρθρίτιδας με αρνητικό ρευματοειδή παράγοντα (RF) θεραπεία πολυαρθρίτιδας με θετικό ρευματοειδή παράγοντα (RF) θεραπεία ψωριασικής αρθρίτιδας θεραπεία της αρθρίτιδας που σχετίζεται με ενθεσίτιδα θεραπεία ιριδοκυκλίτιδας EΙΔΙΚO ΜΕΡOΣ 1. ΣκOΠOΣ τησ μελετησ και ερευνητικα ερωτηματα κλινικη μελετη ασθενείς-κριτήρια εισαγωγής στο κλινικό μέρος της μελέτης Υλικό και μέθοδοι καταγραφή δεδομένων από τους φακέλους των ασθενών - Oρισμός μεταβλητών
10 κλινικοεργαστηριακή εκτίμηση - Oρισμός μεταβλητών εκτίμηση της κατάστασης ενεργότητας νόσου εκτίμηση της σωματικής λειτουργικής ικανότητας κλινική εκτίμηση της αρθρικής και εξωαρθρικής καταστροφής ακτινολογικός έλεγχος εκτίμηση ψυχολογικής επιβάρυνσης καταγραφή της κοινωνικοοικονομικής κατάστασης των ασθενών Υπολογισμός δείκτη μάζας σώματος εργαστηριακός έλεγχος Oφθαλμολογική εκτίμηση τυποποιημένη συνέντευξη Στατιστική ανάλυση κλινικής μελέτης ΓεΝετικη μελετη ασθενείς και ομάδα ελέγχου - κριτήρια εισαγωγής στο γενετικό μέρος της μελέτης Υλικό και μέθοδοι εκχύλιση ολικού γενωμικού DNA ανάλυση των γενετικών πολυμορφισμών των γονιδίων TRAF1/C5, STAT4 και PTPN ανάλυση των γενετικών πολυμορφισμών των γονιδίων CD247 και PTPN Στατιστική ανάλυση γενετικής μελέτης απoτελεσματα δεδομένα από την παρακολούθηση των ασθενών κατά τη συνολική πορεία της νόσου δημογραφικά και κλινικά χαρακτηριστικά των ασθενών εργαστηριακά χαρακτηριστικά των ασθενών κατά τη διάγνωση της νόσου Συνολική διάρκεια ενεργότητας κατά τη διάρκεια της νόσου κλινική ύφεση κατά τη συνολική διάρκεια της νόσου χειρουργικές επεμβάσεις Oφθαλμική βλάβη δεδομένα κατά την τελευταία επίσκεψη παρακολούθησης εργαστηριακά χαρακτηριστικά
11 Kατάσταση ενεργότητας της νόσου (disease activity status) ενεργότητα νόσου κλινική ύφεση αρθρική και εξωαρθρική καταστροφή ακτινολογικές βλάβες τελικό ύψος και δείκτης μάζας σώματος (Body Mass index, BMi) Oφθαλμική βλάβη Σωματική λειτουργική ικανότητα (physical ability) Ψυχολογική επιβάρυνση κοινωνικοοικονομική κατάσταση Oικογενειακή κατάσταση μορφωτικό επίπεδο επαγγελματική κατάσταση διαμονή δεδομένα από την παρακολούθηση των ασθενών τα πρώτα 2 έτη από την έναρξη της νόσου δεδομένα από την παρακολούθηση των ασθενών τα πρώτα 5 έτη από την έναρξη της νόσου φαρμακευτική αντιμετώπιση κατά τη διάρκεια της νόσου φαρμακευτική αγωγή των ασθενών κατά την τελευταία επίσκεψη Συσχετίσεις και προγνωστικοί παράγοντες Συσχετίσεις του ποσοστού διάρκειας ενεργότητας κατά τη συνολική πορεία της νόσου και ειδικοί προγνωστικοί παράγοντες Συσχετίσεις του ποσοστού διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή κατά τη συνολική πορεία της νόσου και ειδικοί προγνωστικοί παράγοντες Συσχετίσεις του τελικού βαθμού αρθρικής καταστροφής (JADi-A) και ειδικοί προγνωστικοί παράγοντες Συσχετίσεις του τελικού βαθμού εξωαρθρικής καταστροφής (JADi-E) Συσχετίσεις του τελικού βαθμού ακτινολογικής βλάβης (Συνολικό τροποποιημένο Sharp van der heijde σκορ, TmSvdhS) και ειδικοί προγνωστικοί παράγοντες Συσχετίσεις του βαθμού σωματικής λειτουργικής ικανότητας (haq-di) και ειδικοί προγνωστικοί παράγοντες
12 Συσχετίσεις του βαθμού ψυχολογικής επιβάρυνσης (GhQ-28) και ειδικοί προγνωστικοί παράγοντες Προγνωστικοί παράγοντες ανάπτυξης οφθαλμικής προσβολής χαρακτηριστικά, πορεία και μακροχρόνια έκβαση των ασθενών που πέτυχαν ή όχι κλινική ύφεση μέσα στα πρώτα 2 έτη από την έναρξη της νόσου μακροχρόνια έκβαση των ασθενών βάσει της διάρκειας ενεργότητας τα πρώτα 5 έτη από την έναρξη της νόσου μακροχρόνια έκβαση των ασθενών σε σχέση με τη συνολική διάρκεια ενεργότητας της νόσου χαρακτηριστικά, πορεία και έκβαση των ασθενών με θετικά και αρνητικα αντιπυρηνικά αντισώματα (Antinuclear Antibodies, ανα) κατά τη διάγνωση της νόσου χαρακτηριστικά, πορεία και έκβαση της νόσου στους ασθενείς με θετικά και αρνητικά αντισώματα έναντι κυκλικών κιτρουλλινιωμένων πεπτιδίων (anti-cyclic Citrullinated Peptide antibodies, anti-ccp antibobies) χαρακτηριστικά, πορεία και έκβαση της νόσου στους ασθενείς που ανέπτυξαν ιερολαγονίτιδα μακροχρόνια έκβαση της Νεανικής ιδιοπαθούς αρθρίτιδας στους ασθενείς με διάγνωση νόσου πριν και μετά το διαφορά στη μακροχρόνια έκβαση της Νεανικής ιδιοπαθούς αρθρίτιδας μεταξύ των ασθενών που έλαβαν βιολογική θεραπεία και είχαν διάγνωση της νόσου μετά το έτος 2000 και αυτών που έλαβαν βιολογική θεραπεία και είχαν διάγνωση της νόσου πριν το έτος Γενετικές συσχετίσεις hla συσχετίσεις non-hla συσχετίσεις O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου TRAF1/C5 στη ΝiA O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου PTPN22 στη Νια O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου STAT4 στην Νια O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου CD247 στην ΝiA
13 O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου PTPN2 στην Νια ΣΥΖητηΣη ΠεΡιOΡιΣμOι εγκυρoτητασ τησ μελετησ ΣΥμΠεΡαΣματα τελικα ΣΥμΠεΡαΣματα ΠεΡιΛηΨη SUMMARY βιβλιoγραφια ΣΥΝτμηΣειΣ - ακρωνυμια
14
15 Π Ρ OΛOΓOΣ η Νεανική ιδιοπαθής αρθρίτιδα (NiA) είναι η πιο συχνή παιδική ρευματοπάθεια, της οποίας η επίπτωση ανά έτος υπολογίζεται σε περιπτώσεις ανά 100,000 παιδιά. O όρος NiA περιλαμβάνει σαν ομπρέλα μια ετερογενή ομάδα διαταραχών οι οποίες χαρακτηρίζονται από παρατεταμένη υμενίτιδα, εξελικτική καταστροφή των αρθρώσεων και ελαττωμένη ποιότητα ζωής. ωστόσο, δεν είναι μόνο νόσημα της παιδικής ηλικίας, αφού το ένα τρίτο περίπου των ασθενών θα συνεχίσει να έχει ενεργό νόσο και μετά την ενηλικίωσή του. η μετάβαση των εφήβων από το Παιδορευματολογικό τμήμα σε Ρευματολογικό τμήμα παρακολούθησης ενηλίκων δεν είναι όρος συνώνυμος με τη μετακίνησή τους σε αυτό κάποια δεδομένη στιγμή, αντίθετα πρόκειται για μία ενεργό, μακρόχρονη διαδικασία. η εξομάλυνση αυτής της μετάβασης προϋποθέτει τη στενή συνεργασία παιδορευματολόγων και ρευματολόγων ενηλίκων προκειμένου να αναπτυχθεί ένα πολυδιάστατο πρόγραμμα που αφενός θα λειτουργεί σε επίπεδο συμβουλευτικής και αφετέρου θα στοχεύει στην κάλυψη των ιατρικών-νοσηλευτικών, ψυχοκοινωνικών και κοινωνικοοικονομικών αναγκών των ασθενών. αυτός είναι ο λόγος που τα τελευταία χρόνια πολλά επιστημονικά συνέδρια έχουν ενσωματώσει στα προγράμματά τους ειδικές για το πρόβλημα αυτό θεματικές ενότητες. η οργάνωση ενός τέτοιου προγράμματος απαιτεί την κατανόηση της πορείας, της μακροχρόνιας έκβασης των ασθενών με NiA, καθώς και των παραγόντων κινδύνου που προδιαθέτουν για επιθετικότερη νόσο. δεδομένα σχετικά με την έκβαση των ασθενών με NiA λείπουν για τον ελληνικό πληθυσμό. αποτελεί ευτύχημα για τον βορειοελλαδικό χώρο η ύπαρξη του Παιδορευματολογικού κέντρου στην α Παιδιατρική κλινική του α.π.θ, η οργάνωση του οποίου πραγματοποιήθηκε από την ομότιμη, σήμερα, καθηγήτρια κ. φλωρεντία κανακούδη-τσακαλίδου και τους συνεργάτες της. Ένας σημαντικός αριθμός των νεαρών ρευματοπαθών του κέντρου, μετά την ενηλικίωσή τους, αποτέλεσε τη δεξαμενή ασθενών της παρούσης μελέτης. η τελευταία κατέστη εφικτή, χάρη στη στενή συνεργασία του Παιδορευματολογικού κέντρου με το τμήμα Νο- 15
16 16 σημάτων Συνδετικού ιστού της δ Παθολογικής κλινικής του α.π.θ. η παρούσα διδακτορική διατριβή προέκυψε από την ανάγκη να απαντηθούν ορισμένα αναπάντητα, μέχρι σήμερα, για τον ελληνικό πληθυσμό κρίσιμα ερευνητικά ερωτήματα: Η Νεανική Ιδιοπαθής Αρθρίτιδα είναι μία ήπια ή μία βαριά νόσος στην Ελλάδα; Η πρόγνωση της Νεανικής Ιδιοπαθής Αρθρίτιδας έχει βελτιωθεί τα τελευταία χρόνια στην Ελλάδα; Είναι προβλέψιμη η πορεία και μακροχρόνια έκβαση της Νεανικής Ιδιοπαθούς Αρθρίτιδας και ποιοι είναι οι παράγοντες εκείνοι που προδιαθέτουν για επιθετικότερη νόσο; h NiA, ως σύνθετη νόσος, θεωρείται ότι προκύπτει ως αποτέλεσμα απορρύθμισης του ανοσολογικού συστήματος λόγω αλληλεπιδράσεων μεταξύ γενετικών και περιβαλλοντολογικών παραγόντων. το τέταρτο ερευνητικό ερώτημα που τέθηκε είναι: Υπάρχει γενετική συσχέτιση πέντε συγκεκριμένων SNPs, οποίοι βρέθηκε ότι συσχετίζονται με NIA σε διάφορους άλλους εθνικούς πληθυσμούς, με τη επιδεκτικότητα της NIA στην Ελλάδα; Στην παρούσα μελέτη διερευνάται για πρώτη φορά εάν πέντε γονίδια, τα οποία σε προηγούμενες μελέτες βρέθηκε ότι συσχετίζονται με αυξημένο κίνδυνο ανάπτυξης NiA, συσχετίζονται, επίσης, με επιδεκτικότητα για NiA στον ελληνικό πληθυσμό. η γενετική μελέτη ολοκληρώθηκε χάρη στη συνεργασία με το εργαστήριο μοριακής ιατρικής και Γενετικής του ανθρώπου του ιατρικού τμήματος του Πανεπιστημίου κρήτης. από τη θέση αυτή, θα ήθελα να εκφράσω τις βαθύτατες ευχαριστίες μου στην υπεύθυνη του Παιδορευματολογικού κέντρου και μέλος της τριμελούς μου επιτροπής, επίκουρη καθηγήτρια κ. μαρία τραχανά, για την αμέριστη συμπαράσταση και ουσιαστική καθοδήγηση από τα πρώτα βήματα μέχρι το τέλος της παρούσης διδακτορικής διατριβής. θεωρώ υποχρέωσή μου να ευχαριστήσω τον κ. μιχαήλ δανιηλίδη, επιβλέποντα καθηγητή για την επιμέλεια και τις χρήσιμες υποδείξεις του, που συνέβαλλαν στην ολοκλήρωση της μελέτης. επίσης, θα ήθελα να ευχαριστήσω τον κ. Πρόδρομο Σιδηρόπουλο, επίκουρο καθηγητή Πανεπιστημίου κρήτης, για την ουσιαστική καθοδήγησή του στη διάρκεια εκπόνησης της διδακτορικής διατριβής. θερμές ευχαριστίες οφείλω στην ομότιμη καθηγήτρια κ. φλωρεντία κανακούδη-τσακαλίδου για το σύνολο του σπουδαίου έργου που έχει επιτελέσει και που είχε ως αποτέλεσμα τη δημιουργία του Παιδορευματολογικού κέντρου
17 της α Παιδιατρικής κλινικής, στο οποίο παρακολουθήθηκαν ως παιδιά, οι ενήλικες ασθενείς που συμμετείχαν στην ερευνητική αυτή εργασία. Oλόψυχα ευχαριστώ την Παιδίατρο κ. τζένη Πρατσίδου-Γκέρτση, επιστημονική Συνεργάτη του Παιδορευματολογικού κέντρου για την επιστημονική βοήθεια και τις χρήσιμες συμβουλές της. Στον κ. Γεώργιο Γουλιέλμο, αναπληρωτή καθηγητή Πανεπιστημίου κρήτης θα ήθελα να εκφράσω τις βαθύτατες ευχαριστίες μου για την εξαιρετικά πολύτιμη βοήθειά του, χάρη στην οποία πραγματοποιήθηκε και ολοκληρώθηκε το σύνολο του γενετικού μέρους αυτής της διδακτορικής διατριβής. η συμβολή της ιατρού ακτινολόγου κ. ανθής μοριχοβίτου στην ανάγνωση και εκτίμηση των ακτινογραφιών της παρούσης μελέτης υπήρξε εξαιρετικά σημαντική. ιδιαίτερα ευχαριστώ τον αναπληρωτή καθηγητή κ. Γεώργιο Γαρύφαλλο για τη συμβολή του στη διερεύνηση και ερμηνεία των αποτελεσμάτων στον τομέα της ψυχολογικής επιβάρυνσης των ασθενών με NiA. θα ήθελα, επίσης, να ευχαριστήσω τον καθηγητή αλέξιο μπένο, μέλους της επταμελούς εξεταστικής επιτροπής, για τις πολύτιμες υποδείξεις του από τα αρχικά στάδια σχεδιασμού της διατριβής. τον ομότιμο καθηγητή κ. Λουκά Σέττα, τον καθηγητή κ. Γεώργιο κυριαζή και την επίκουρη καθηγήτρια κ. μπετίνα χάιδιτς, λοιπά μέλη της επταμελούς εξεταστικής επιτροπής, τους ευχαριστώ για το χρόνο που διέθεσαν και τις εύστοχες παρατηρήσεις τους κατά την εξεταστική διαδικασία. ευχαριστώ, επίσης, το τμήμα αιμοδοσίας του ιπποκρατείου Νοσοκομείου και τη διευθύντριά του κ. Γεωργία Παπαϊωάννου για τη βοήθεια που πρόσφεραν προκειμένου να γίνει η συλλογή των δειγμάτων αίματος των ατόμων που αποτέλεσαν το δείγμα υγιών μαρτύρων του γενετικού μέρους της μελέτης. θα ήταν παράλειψη να μην ευχαριστήσω τη φίλη Ρευματολόγο κ. αθηνά θεοδωρίδου, επιστημονική Συνεργάτη της δ Παθολογικής κλινικής για τις πολύτιμες παρατηρήσεις της στα αρχικά στάδια της μελέτης. την κ. ελένη βερυκούκη την ευχαριστώ για την ουσιαστική βοήθειά της στην στατιστική επεξεργασία των αποτελεσμάτων. τέλος, θα ήθελα να εκφράσω τις ευχαριστίες μου στον καθηγητή αλέξανδρο Γαρύφαλλο, διευθυντή της δ Παθολογικής κλινικής, υπεύθυνο του τμήματος Νοσημάτων Συνδετικού ιστού και αρχικό επιβλέποντα της διδακτορικής διατριβής, για τη σύλληψη της ιδέας της επιστημονικής αυτής μελέτης και την όλη συμπαράστασή του. η βοήθειά του υπήρξε πολύτιμη. μάθημα ζωής πήρα από τους ασθενείς με NiA που συμμετείχαν στη μελέτη. τους ευχαριστώ όλους από καρδιάς. 17
18
19 ΓENiKO μερoσ
20
21 1. Ν Ε Α Ν Ι Κ Η Ι Δ Ι O Π Α Θ Η Σ Α Ρ Θ Ρ Ι Τ Ι Δ Α - Ι Σ Τ O Ρ Ι Κ Η Α Ν Α Δ Ρ O Μ Η η μελέτη των παιδικών αρθροπαθειών έχει μια σχετικά βραχεία ιστορία, αν και αναφορές σχετικά με την παρουσία διογκωμένων αρθρώσεων που εμφα νίζουν μειωμένη λειτουργικότητα μπορεί να βρεθούν τόσο σε πορτραίτα όσο και σε κείμενα που χρονολογούνται πριν από 500 χρόνια και πλέον. Πριν τα τέλη του 19ου αιώνα, έχουν δημοσιευτεί τριάντα οχτώ περιπτώσεις αρθρίτιδας σε παιδιά, οι οποίες ανασκοπήθηκαν από τον Diamant-Berger το 1891 σε μια προσπάθειά του να ορίσει διαφορετικές υποομάδες της νόσου. το 1897 ο George Frederic Still ανακοίνωσε 22 περιστατικά παιδιών με χρόνια αρθρίτιδα όπου σχολιάζει τονίζοντας ότι η αρθρίτιδα της παιδικής ηλικίας είναι περισ σότερες της μίας νόσοι και διαφέρει από την αρθρίτιδα που συναντάται στους ενήλικες. Έκτοτε, μετά από τις πρώτες αυτές αναφορές, έχουν χρησιμο ποιηθεί διάφορα ονόματα που περιγράφουν την αρθρίτιδα στην παιδική ηλικία και έχουν αναπτυχθεί διάφορα συστήματα ταξινόμησης της νόσου (πίνακας 1). δύο βασικά συστήματα ταξινόμησης είχαν τύχει ευρείας αποδοχής στη βόρεια αμερική, η ταξινόμηση του αμερικανικού κολλεγίου Ρευματολογίας (American College of Rheumatology, ACR) που έδωσε τον όρο Νεανική Ρευματοειδής αρθρίτιδα (ΝΡα) 1, και η ευρωπαϊκή Oμάδα εναντίον των Ρευματικών Νοσημάτων (European League Against Rheumatism,EULAR) 2, η οποία εισήγαγε τον όρο Νεανική χρόνια αρθρίτιδα (Νχα). τόσο η μία ταξινόμηση, όσο και η άλλη βασίστηκαν στον τρόπο έναρξης της νόσου και περιέλαβε τρεις διακριτές υποομάδες: τη συστηματική αρθρίτιδα, την ολιγοαρθρίτιδα και την πολυαρθρίτιδα. ωστόσο, καμία από τις δύο ταξινομήσεις δεν περιέλαβε όλες τις μορφές νεανικής αρθρίτιδας (πίνακας 2), καθιστώντας με αυτό τον τρόπο δύσκολη τη σύγκριση των επιδημιολογικών, κλινικών, ορολογικών και γενετικών δεδομένων που προέκυπταν από τις διάφορες μελέτες. 21
22 22 Πίνακας 1. Oρόσημα στην ταξινόμηση της νεανικής αρθρίτιδας 1864 Πρώτη λεπτομερής περιγραφή της νεανικής αρθρίτιδας από τον Cornil 1891 Πρώτη ταξινόμηση της παιδικής αρθρίτιδας σε 3 μορφές από τον Diamant- Berger 1897 Περιγραφή της παιδικής αρθρίτιδας ως περισσότερες της μίας νόσου από τον Still 1959 Περιγραφή διαφορετικών σχημάτων έναρξης της νόσου από την Ansell και βywaters 1968 κριτήρια διάγνωσης της νόσου Still (Taplow κριτήρια) 1972 κριτήρια της αμερικανικής Ρευματολογικής εταιρίας (ARA) για την ταξινόμηση της Nεανικής Ρευματοειδούς αρθρίτιδας (ΝΡA) 1977 αναθεώρηση των κριτηρίων της ARA για την ΝΡα 1978 EULAR κριτήρια για τη Νεανική χρόνια αρθρίτιδα (Νχα) 1995 ilar κριτήρια για τη Νεανική ιδιοπαθή αρθρίτιδα (ΝiA), Santiago, Vancouver κριτήρια για τη νεανική ψωριασική αρθρίτιδα 1998 Πρώτη αναθεώρηση των ilar κριτηρίων, Durban, δεύτερη αναθεώρηση των ilar κριτηρίων, Edmonton, 2001 Από Minden K. Classification and epidemiology of juvenile idiopathic arthritis. In Rheumatology. Hochberg CM, Silman AJ, Smolen JS, Wewinblatt MH, eds.mosby Elsevier 5 th ed. 2011:p988
23 2. O Ρ Ι Σ Μ O Σ - Τ Α Ξ Ι Ν O Μ Η Σ Η Τ Η Σ Ν Ε Α Ν Ι Κ Η Σ Ι Δ Ι O Π Α Θ O Υ Σ Α Ρ Θ Ρ Ι Τ Ι Δ Α Σ Κ Α Τ Α I L A R Σε μια προσπάθεια υπερκέρασης των περιορισμών που είχαν προκύψει από τις προϋπάρχουσες κατατάξεις και αντικατάστασής τους από ένα μοναδικό διεθνώς αποδεκτό σύστημα ταξινόμησης, το 1994 η διεθνής ομάδα ilar (international League of Associations For Rheumatology) πρότεινε μια νέα ταξινόμηση, χρησιμοποιώντας τον όρο Νεανική ιδιοπαθής αρθρίτιδα (Νια), προκειμένου να περιγραφούν όλες οι χρόνιες αρθρίτιδες αγνώστου αιτιολογίας που ξεκινούν στην παιδική ηλικία 3. Έκτοτε, τα ilar κριτήρια έχουν αναθεωρηθεί 2 φορές 4,5. Έτσι, ως Νια ορίστηκε κάθε αρθρίτιδα αγνώστου αιτιολογίας, η οποία ξεκινά πριν την ηλικία των 16 χρόνων και επιμένει για τουλάχιστον 6 εβδομάδες. Σύμφωνα με την ταξινόμηση κατά ilar, η Νια μπορεί να διαγνωσθεί μετά την πάροδο τουλάχιστον 6 εβδομάδων από την έναρξη των συμπτωμάτων, ενώ η ένταξη του ασθενούς σε μια συγκεκριμένη υποομάδα της, απαιτεί διάστημα μεγαλύτερο από αυτό των 6 μηνών. τα ilar κριτήρια δε δημιουργήθηκαν αποσκοπώντας στη λήψη κλινικών αποφάσεων και για το λόγο αυτό η χρήση τους δεν ενδείκνυται για την κλινική διάγνωση της νόσου. Oι υποομάδες της Νια (πίνακας 3) διακρίνονται βάσει των κλινικών χαρακτηριστικών που υπάρχουν μετά τους 6 πρώτους μήνες από την έναρξη της νόσου, του αριθμού των προσβεβλημένων αρθρώσεων, της ανάπτυξης εξωαρθρικών εκδηλώσεων, αλλά και της παρουσίας του ρευματοειδούς παράγοντα (Rheu - ma toid Factor, RF). η ταξινόμηση κατά ilar, σύμφωνα με τη δεύτερη αναθεώρηση παρουσιάζεται στον πίνακα 3, ενώ στον πίνακα 4 αναλύονται οι ορισμοί των κλινικών σημείων και συμπτωμάτων. Ένας μεγάλος αριθμός επιπλέον μεταβλητών, τόσο κλινικών όσο και ορολογικών (πχ ηλικία έναρξης της νόσου, θετικά αντιπυρηνικά αντισώματα [αntinuclear αntibodies, ANA], χρόνια ή οξεία ιριδοκυκλίτιδα), χρησιμο- 23
24 24 ποιείται προκειμένου να συλλεχθούν πληροφορίες που περιγράφουν καλύτερα την κάθε υποομάδα, ωστόσο αυτές δεν αποτελούν στοιχεία στην ταξινόμηση της Νια. Σε πολλές εργασίες γίνεται λόγος ότι με την ταξινόμηση κατά ilar ορίζονται ανοσογενετικά διακριτές υποομάδες ασθενών, οι οποίες διαφέρουν ως προς τα κλινικά τους χαρακτηριστικά, την απάντησή τους στη θεραπεία, την πορεία, αλλά και τη μακροχρόνια έκβασή τους 6,7. Πίνακας 2. Ταξινομήσεις της αρθρίτιδας στα παιδιά Σύστημα ταξινόμησης ACR EULAR ILAR Όρος Νεανική Ρευματοειδής Νεανική χρόνια Νεανική ιδιοπαθής αρθρίτιδα (ΝΡα) αρθρίτιδα (Νχα) αρθρίτιδα (Νια) Ηλικία έναρξης της αρθρίτιδας <16 ετών <16 ετών <16 ετών Διάρκεια της αρθρίτιδας >6 εβδομάδες >3 μήνες >6 εβδομάδες Υποομάδες έναρξης Εξαιρέσεις Νεανική αγκυλοποιητική Oροθετική αντιδραστική σπονδυλίτιδα, νεανική πολυαρθρίτιδα αρθρίτιδα ψωριασική αρθρίτιδα, αρθρίτιδα της φλεγμονώδους νόσου του εντέρου. ACR= American College of Rheumatology, EULAR= European League Against Rheumatism, ILAR= International League of Associations For Rheumatology, ΝΡΑ= Νεανική Ρευματοειδής Αρθρίτιδα, ΝΧΑ= Νεανική Χρόνια Αρθρίτιδα, ΝΙΑ=Νεανική Ιδιοπαθής Αρθρίτιδα Από Minden K. Classification and epidemiology of juvenile idiopathic arthritis. In Rheumatology. Hochberg CM, Silman AJ, Smolen JS, Wewinblatt MH, eds.mosby Elsevier 5 th ed.2011:p988
25 25 Πίνακας 3. Σύγχρονη ταξινόμηση της Νεανικής ιδιοπαθούς αρθρίτιδας (NIA), σύμφωνα με τα κριτήρια ILAR: Δεύτερη αναθεώρηση, EDMONDON, 2001 Κατηγορία Oρισμός Εξαιρέσεις 1. Συστηματική αρθρίτιδα αρθρίτιδα σε μία ή περισσότερες αρθρώσεις με ή με προηγηθέντα πυρετό τις τελευταίες α,β,γ,δ 2 εβδομάδες, ο οποίος πιστοποιείται ότι είναι καθημερινός για 3 ημέρες και συνοδεύεται από ένα ή περισσότερα από τα ακόλουθα: 1. ακαθόριστο ερυθηματώδες εξάνθημα 2. Γενικευμένη διόγκωση λεμφαδένων 3. ηπατομεγαλία και/ή σπληνομεγαλία 4. Oρογονίτιδα 2. Oλιγοαρθρίτιδα αρθρίτιδα που προσβάλλει μία έως τέσσερις αρθρώσεις κατά τη διάρκεια των πρώτων α,β,γ,δ,ε 6 μηνών της νόσου. εμμένουσα αρθρίτιδα που δεν προσβάλλει περισσότερες από τέσσερις αρθρώσεις στην πορεία της νόσου. επεκταθείσα αρθρίτιδα που προσβάλλει συνολικά περισσότερες από τέσσερις αρθρώσεις, μετά τους πρώτους 6 μήνες της νόσου. 3. Πολυαρθρίτιδα αρθρίτιδα που προσβάλλει 5 ή περισσότερες αρθρώσεις κατά τη διάρκεια των πρώτων α,β,γ,δ,ε (RF-αρνητική) 6 μηνών της νόσου. O έλεγχος του RF είναι αρνητικός. 4. Πολυαρθρίτιδα αρθρίτιδα που προσβάλλει 5 ή περισσότερες αρθρώσεις κατά τη διάρκεια των πρώτων α,β,γ,ε (RF-θετική) 6 μηνών της νόσου. δύο ή περισσότερες θετικές τιμές του RF, με διάστημα μεσολάβησης τουλάχιστον 3 μηνών κατά τη διάρκεια των πρώτων 6 μηνών της νόσου. 5. Ψωριασική αρθρίτιδα αρθρίτιδα και ψωρίαση ή αρθρίτιδα και τουλάχιστον 2 από τα παρακάτω: β,γ,δ,ε 1. δακτυλίτιδα 2. εντυπώματα ονύχων ή ονυχόλυση 3. Ψωρίαση σε συγγενή πρώτου βαθμού
26 26 Πίνακας 3. (συνέχεια). Κατηγορία Oρισμός Εξαιρέσεις 6. Aρθρίτιδα σχετιζόμενη 1. ιστορικό ή παρουσία πόνου στην ιερολαγόνια άρθρωση και/ή φλεγμονώδη οσφυοϊερό πόνο. με ενθεσίτιδα 2. Παρουσία hla-b27 αντιγόνου. 3. Έναρξη της αρθρίτιδας σε αγόρι μεγαλύτερο των έξι ετών. 4. Oξεία (συμπτωματική) πρόσθια ιριδοκυκλίτιδα. 5. ιστορικό αγκυλοποιητικής σπονδυλίτιδας, αρθρίτιδας που σχετίζεται με ενθεσίτιδα, ιερολαγονίτιδα με φλεγμονώδη νόσο του εντέρου, σύνδρομο Reiter ή οξεία πρόσθια ιριδοκυκλίτιδα σε πρώτου βαθμού συγγενή. 7. αταξινόμητη αρθρίτιδα αρθρίτιδα που δεν πληροί τα κριτήρια καμίας κατηγορίας ή πληροί κριτήρια 2 ή περισσότερων από τις παραπάνω κατηγορίες. εξαιρέσεις: α. Ψωρίαση ή ιστορικό ψωρίασης στον ασθενή ή σε συγγενή πρώτου βαθμού. β. Αρθρίτιδα σε αγόρι HLA-B27 θετικό η οποία ξεκινά μετά τα 6 α γενέθλια. γ. Αγκυλοποιητική σπονδυλίτιδα, αρθρίτιδα που σχετίζεται με ενθεσίτιδα, ιερολαγονίτιδα με φλεγμονώδη νόσο του εντέρου, σύνδρομο Reiter ή οξεία πρόσθια ιριδοκυκλίτιδα ή ιστορικό μιας από αυτές τις διαταραχές σε πρώτου βαθμού συγγενή. δ. Παρουσία IgM ρευματοειδούς παράγοντα σε τουλάχιστον δύο μετρήσεις με μεσολάβηση διαστήματος τουλάχιστον 3 μηνών. ε. Παρουσία συστηματικής NIA στον ασθενή.
27 Πίνακας 4.Oρισμός των όρων στην ταξινόμηση της Νεανικής Ιδιοπαθούς Αρθρίτιδας (NIA), σύμφωνα με τα κριτήρια ILAR. Αρθρίτιδα: διόγκωση μιας άρθρωσης ή περιορισμός του εύρους της κίνησης της άρθρωσης με πόνο στην άρθρωση, η οποία εμμένει για τουλάχιστον 6 εβδομάδες, παρατηρείται από ιατρό και δεν οφείλεται σε πρωτοπαθείς μηχανικές διαταραχές ή σε άλλες αδιευκρίνιστες αιτίες. Δακτυλίτιδα: διόγκωση σε ένα ή περισσότερα δάκτυλα, συνήθως με ασύμμετρη κατανομή, η οποία επεκτείνεται πέρα από τα όρια της άρθρωσης. Ενθεσίτιδα: πόνος στην κατάφυση ενός τένοντα, συνδέσμου, αρθρικής κάψας ή περιτονίας, στο οστό. Φλεγμονώδης οσφυοϊερός πόνος: οσφυοϊερός πόνος στην κατάκλιση με πρωινή δυσκαμψία, η οποία βελτιώνεται με την κίνηση. Εντυπώματα ονύχων: τουλάχιστον 2 εντυπώματα σε ένα ή περισσότερα νύχια σε οποιαδήποτε στιγμή. Αριθμός προσβεβλημένων αρθρώσεων: αρθρώσεις οι οποίες μπορούν εξατομικευμένα να εκτιμηθούν κλινικά, μετρώνται ως ξεχωριστές αρθρώσεις. Θετικός έλεγχος για ρευματοειδή παράγοντα (RF): τουλάχιστον 2 θετικά αποτελέσματα, με μεσολάβηση διαστήματος τουλάχιστον 3 μηνών, κατά τη διάρκεια των πρώτων 6 μηνών της νόσου. Ψωρίαση: διαγνωσμένη από ιατρό (όχι απαραίτητα δερματολόγο) Καθημερινός πυρετός: O πυρετός ο οποίος ανέρχεται σε >39 ο C μία φορά την ημέρα και επιστρέφει σε > 37 ο C ανάμεσα στις αιχμές του πυρετού. Oρογονίτιδα: περικαρδίτιδα και/ή πλευρίτιδα και/ή περιτονίτιδα. Ιερολαγονίτιδα: παρουσία πόνου κατά την απευθείας πίεση πάνω στις ιερολαγόνιες αρθρώσεις. Σπονδυλοαρθροπάθεια: φλεγμονή των ενθέσεων και αρθρώσεων της οσφυοϊερής μοίρας της σπονδυλικής στήλης. Ιριδοκυκλίτιδα: χρόνια πρόσθια ιριδιοκυκλίτιδα, διαγνωσμένη από οφθαλμίατρο. Δεδομένα από Petty RE. Southwood TR, Manners P. et al. Classification of juvenile idiopathic arthritis; second revision, Edmonton, J Rheumatol 2004;31: Από Gare A. and Fasth A. Presentations, clinical features, and special problems in children. In Rheumatology. Hochberg CM, Silman AJ, Smolen JS, Wewinblatt MH, eds.mosby Elsevier 5 th ed.2011:p
28 3. Ε Π Ι Δ Η Μ Ι OΛOΓ Ι Α η επιδημιολογία της χρόνιας αρθρίτιδας στα παιδιά αποτέλεσε αντικείμενο ικανού αριθμού μελετών. ωστόσο, τα διαθέσιμα δεδομένα που αφορούν στη νοσηρότητα της χρόνιας αρθρίτιδας στα παιδιά, στα χαρακτηριστικά, στους παράγοντες κινδύνου και στη φυσική πορεία της νόσου είναι δύσκολο να τεθούν υπό συγκριτικό έλεγχο, δεδομένου της ετερογένειας της νόσου, διαφορών στα κριτήρια ταξινόμησης καθώς και διαφορών στην προέλευση των πληθυσμών. Σε αυτό το σημείο, θα χρησιμοποιηθούν οι όροι Νεανική χρόνια αρθρίτιδα (Νχα), Νεανική Ρευματοειδής αρθρίτιδα (ΝΡα) και Νεανική ιδιοπαθής αρθρίτιδα (Νια) προκειμένου να σημαίνεται, με ποια κριτήρια έχουν οριστεί, οι υπό μελέτη ομάδες. 3.1 Επίπτωση και Επιπολασμός η Νια αποτελεί την πιο συχνή χρόνια φλεγμονώδη ρευματοπάθεια στα παιδιά. Έχει παγκόσμια κατανομή, ωστόσο, τα αποτελέσματα διαφόρων μελετών που αφορούν στην επίπτωση και στον επιπολασμό της νόσου παρουσιάζουν σημαντικές διακυμάνσεις ανάμεσα στις διάφορες γεωγραφικές περιοχές. Oι δημοσιευμένοι δείκτες επίπτωσης της νόσου κυμαίνονται μεταξύ 0.8 και 23 ανά 100,000 και οι δείκτες επιπολασμού από 7 έως 400 ανά 100,000 παιδιά ηλικίας μικρότερης των 16 ετών (πίνακας 5). η ελαφρώς μικρότερη επίπτωση στις μελέτες που χρησιμοποιούν τα ACR κριτήρια, πιθανώς οφείλεται στην εξαίρεση των παιδιών με οροαρνητικές σπονδυλοαρθροπάθειες, τα οποία έχουν συμπεριληφθεί στις υπόλοιπες κατατάξεις. τονίζεται, ωστόσο, ότι υπάρχουν και πραγματικές διαφορές στην κατανομή της νόσου στα διάφορα μέρη του κόσμου. Έτσι, η ευρώπη φαίνεται ότι στο σύνολό της πλήττεται συχνότερα συγκριτικά με την αφρική, ασία και ανατολική ινδία. Πράγματι, ο δείκτης επιπολασμού της τάξης του 0.83/ παιδιά που παρατηρήθηκε στην ιαπωνία είναι από τους χαμηλότερους που έχουν καταγραφεί παγκοσμίως
29 μία αυξανόμενη επίπτωση της νόσου παρατηρήθηκε σε ορισμένες περιοχές της εσθονίας και της φινλανδίας, κάτι που ίσως ήταν αναμενόμενο, δεδομένου της μεγαλύτερης επαγρύπνησης και κατά συνέπεια της πιο έγκαιρης διάγνωσης στις χώρες αυτές 12,17. Παρόλα αυτά, αρκετές άλλες μελέτες δεν μπόρεσαν να επιβεβαιώσουν αυτήν την υπόθεση 8. Oι ασθενείς με Νια παρουσιάζουν, επιπρόσθετα, υψηλούς δείκτες θνησιμότητας και θνητότητας από τη νόσο. δύο πληθυσμιακές μελέτες ανακοίνωσαν τέσσερις φορές αύξηση στην συνολική θνητότητα των ασθενών με Νια σε σύγκριση με το γενικό πληθυσμό. Oι Thomas και συν. υπολόγισαν ότι οι δείκτες τυποποιημένης αναλογίας θνησιμότητας (Standardized Mortality Ratio, SMR) στις γυναίκες και στους άνδρες με NiA ήταν 5 και 3 αντιστοίχως, διπλάσιοι από εκείνους που εκτιμώνται για τους άνδρες και τις γυναίκες με ρευματοειδή αρθρίτιδα Επιδημιολογικά χαρακτηριστικά της νόσου η εικόνα της Νια διαφέρει από περιοχή σε περιοχή, οδηγώντας στη σκέψη ότι υπάρχουν πραγματικές διαφορές στην έκφραση της νόσου, απότοκες ανοσογενετικών ή περιβαλλοντολογικών παραγόντων ή συνδυασμού και των δύο. Στους λευκούς πληθυσμούς της βόρειας αμερικής και της ευρώπης, η ολιγοαρθρικού τύπου έναρξης υποομάδα συνιστά τουλάχιστον τις μισές περιπτώσεις. η εμφάνιση πολυαρθρικής πορείας περιγράφεται στο 20%-50% των ασθενών με ολιγοαρθρική έναρξη (ολιγοαρθρίτιδα επεκταθείσα) 27,28. Περίπου 20% έχουν πολυαρθρικού τύπου και λιγότερο από 10% συστηματικού τύπου έναρξης Νια (πίνακας 6). Στην ασία, η ολιγοαρθρίτιδα αναφέρεται ότι είναι σχετικά σπάνια. Σε μια ανάλυση 570 ασθενών με ΝΡα στην ιαπωνία, βρέθηκε από τους Fujikawa και Okuni ότι 54% των ασθενών είχαν συστηματική αρθρίτιδα, 25% είχαν πολυαρθρική νόσο και μόνο 21% είχαν ολιγοαρθρίτιδα 32. Oι Saurenmann και συν. σε μια πολυεθνική μελέτη που περιέλαβε περισσότερα από 800 παιδιά, επιβεβαιώνουν σημαντικές διαφορές στην κατανομή των υποομάδων της νόσου μεταξύ των διαφόρων εθνοτήτων 29. Συνολικά, περισσότερα κορίτσια παρά αγόρια προσβάλλονται από τη νόσο. η κατανομή του φύλου ποικίλλει ανάλογα με την υποομάδα έναρξης, με υπεροχή των γυναικών έναντι των ανδρών στην ολιγοαρθρικής και πολυαρθρικής έναρξης νόσο (κορίτσια:αγόρια περίπου 3:1), υπεροχή των ανδρών στην αρθρίτιδα που σχετίζεται με ενθεσίτιδα (αγόρια:κορίτσια 2-3:1) και παρόμοια ποσοστά προσβολής των δύο φύλων στη συστηματική αρθρίτιδα. 29
30 30 Πίνακας 5. Πληθυσμιακές, κατά βάση, μελέτες επιπολασμού και/ή επίπτωσης της παιδικής χρόνιας αρθρίτιδας σε πληθυσμούς, κυρίως, της λευκής φυλής. Πηγή δεδομένων Μελέτη Σύστημα Επίπτωση Επιπολασμός ταξινόμησης (ανά (ανά πληθυσμού κατά έτος) πληθυσμού) ερευνητική πληθυσμιακή Manners et al, αυστραλία, EULAR μελέτη και εκτίμηση εξειδικευμένων ιατρών επαγγελματίες υγείας ή δεδομένα Peterson et al, U.S, ACR βασισμένα σε καταγραφή (Register-based) Von Koskulle et al, Γερμανία, EULAR 7 15 huemer et al, αυστρία, ACR 4 - Kaipiainen-Seppanen et al, φιλανδία, ACR 20 - Savolainen et al, φιλανδία, ilar 23 - Berntson et al, Νορβηγία, φιλανδία, ilar 15 - Σουηδία, δανία, ισλανδία, hanova et al, τσεχία, ilar Danner et al, Γαλλία, ilar 3 20 Pruunsild et al, εστονία, ,18 ilar Riise et al, Νορβηγία, ilar 14 - κλινικές μελέτες Oen et al, καναδάς, ACR 5 97 Symmons et al, U.K, ,21 EULAR 10 - Malleson et al, καναδάς, ,22 ACR 3 - Kiessling et al, Γερμανία, ,23 EULAR 4 20 Moe et al, Νορβηγία, ,24 EULAR Aπό Minden K. Classification and epidemiology of juvenile idiopathic arthritis. In Rheumatology. Hochberg CM, Silman AJ, Smolen JS, Wewinblatt MH, eds.mosby Elsevier 5 th ed.2011:p989.
31 η ηλικία έναρξης της Νια διαφέρει μεταξύ των διαφόρων υποομάδων. η ολιγοαρθρίτιδα είναι τυπικά νόσος των μικρών παιδιών, αν και η έναρξη της νόσου πριν την ηλικία των 6 μηνών είναι εξαιρετικά σπάνια. η ηλικία έναρξης της ολιγοαρθρίτιδας παρουσιάζει αιχμή στα 2 με 3 χρόνια, ενώ η αρθρίτιδα που σχετίζεται με ενθεσίτιδα και η πολυαρθρίτιδα με θετικό ρευματοειδή παράγοντα σε ηλικία μεγαλύτερη των 8 ετών. Στη νεανική ψωριασική αρθρίτιδα, η ηλικία έναρξης είναι διφασική με μια αιχμή γύρω στα 2 χρόνια και μια δεύτερη στην όψιμη παιδική ηλικία 33. Γενικά, υπάρχουν μεταξύ των ηλικιών δύο μεγάλες αιχμές στην έναρξη της νόσου μία μεταξύ των 2 και 3 ετών και μία μεταξύ των 11 και 12 ετών. τα αντιπυρηνικά αντισώματα (Antinuclear Antibodies, ANA) είναι τα πιο συχνά αυτοαντισώματα που ανιχνεύονται στη Νια (περίπου στο 50% των περιπτώσεων). Παρατηρούνται συχνότερα στους ασθενείς με ολιγοαρθρικής έναρξης νόσο. O igm ρευματοειδής παράγοντας (Rheumatoid Factor, RF) σπάνια ανευρίσκεται θετικός (<5%), και εξ ορισμού μόνο στους ασθενείς με πολυαρθρίτιδα RF-θετική ή αταξινόμητη μορφή. Oι εξωαρθρικές εκδηλώσεις διαφέρουν, επίσης, μεταξύ των διαφόρων υποομάδων της νόσου. Όπως δηλώνεται και από την ονομασία της, τα συστηματικά χαρακτηριστικά αποτελούν μέρος της κλινικής εικόνας της συστηματικής μορφής, ενώ η ενθεσίτιδα είναι διακριτό στοιχείο της αρθρίτιδας που σχετίζεται με ενθεσίτιδα (Enthesitis-Related Arthritis, ERA). δακτυλίτιδα παρατηρείται συχνότερα στη νεανική ψωριασική αρθρίτιδα 33. ιριδοκυκλίτιδα συναντάται κυρίως στους ασθενείς με επεκταθείσα ολιγοαρθρίτιδα (25%- 30%) και ακολουθούν αυτοί με εμμένουσα ολιγοαρθρίτιδα (16%-18%), οροαρνητική πολυαρθρίτιδα (4%-14%) ή ψωριασική αρθρίτιδα (10%-12%) 34,35. αρκετές μελέτες έχουν δείξει ότι ο θετικός τίτλος αντιπυρηνικών αντισωμάτων (ANA), η ηλικία έναρξης της νόσου μικρότερη των 6 ετών και η υποομάδα της νόσου αποτελούν ανεξάρτητους παράγοντες κινδύνου για την εμφάνιση ιριδοκυκλίτιδας. Σε περίπου 90% των ασθενών με οφθαλμική προσβολή, αυτή αναπτύσσεται στα πρώτα 4 έτη από την έναρξη της αρθρίτιδας. εμφανίζεται, κυρίως, υπό την μορφή της πρόσθιας ιριδοκυκλίτιδας, η οποία συνήθως είναι ασυμπτωματική στους περισσότερους ασθενείς. 31
32 32 Πίνακας 6. Μέσες σχετικές συχνότητες των υποομάδων της NIA σε δείγματα κυρίως ασθενών λευκής φυλής * και χαρακτηριστικά των υποομάδων βασισμένα σε μεγάλα, περισσότερα των 500 περιστατικών, δείγματα ασθενών** Υποομάδα Νια Συχνότητα (%) ηλικία έναρξης νόσου, κορίτσια ANA θετικά hla-b27 θετικό έτη (διάμεσος τιμή) (%) (%) (%) Συστηματική αρθρίτιδα Oλιγοαρθρίτιδα Πολυαρθρίτιδα RF αρνητική Πολυαρθρίτιδα RF θετική Ψωριασική αρθρίτιδα αρθρίτιδα που σχετίζεται με ενθεσίτιδα Σύνολο Από Minden K. Classification and epidemiology of juvenile idiopathic arthritis. In Rheumatology. Hochberg CM, Silman AJ, Smolen JS, Wewinblatt MH, eds.mosby Elsevier 5 th ed.2011:p990. * Βλ. αναφορές (14, 17, 29 και 30) **Βλ. αναφορές (7, 29, 30 και 31) ΑΝΑ= αντιπυρηνικά αντισώματα
33 4. Π Α Θ O Γ Ε Ν Ε Ι Α Τ Η Σ Ν Ε Α Ν Ι Κ Η Σ Ι Δ Ι O Π Α Θ O Υ Σ Α Ρ Θ Ρ Ι Τ Ι Δ Α Σ 4.1 Παθοφυσιολογικοί μηχανισμοί η εξελικτική φλεγμονώδη διαδικασία στη Νια περιλαμβάνει υπερπλασία του αρθρικού υμένα, διόγκωση των μαλακών μορίων, συλλογή υγρού στην άρθρωση, καταστροφή του χόνδρου η οποία τελικά οδηγεί σε διάβρωση του οστού. Λεμφοκύτταρα, πλασματοκύτταρα, μακροφάγα και δενδριτικά κύτταρα ανευρίσκονται όλα αυξημένα στη φλεγμαίνουσα άρθρωση. Oι ανοσοπαθογενετικοί μηχανισμοί στη Νια έχουν αποτελέσει αντικείμενο εκτεταμένης έρευνας, παρόλα αυτά, όμως, δεν είναι καλώς κατανοητοί μέχρι και σήμερα. από τη μια πλευρά, η ανεύρεση τ κυττάρων και η χρόνια υμενίτιδα υποδηλώνουν κυτταρική διαμεσολάβηση, ενώ από την άλλη η ανίχνευση ανοσοσυμπλεγμάτων και συμπληρώματος πιθανολογεί β-κυτταρική διαμεσολάβηση στη φλεγμονώδη απάντηση. O αρθρικός υμένας διηθείται από φλεγμονώδη κύτταρα στα οποία περιλαμβάνονται, ουδετερόφιλα, πλασματοκύτταρα, δενδριτικά κύτταρα καθώς και σε μεγάλη αναλογία ενεργοποιημένα τ-λεμφοκύτταρα. O κυτταρικός πληθυσμός που επικρατεί στον αρθρικό υμένα των παιδιών με Νια είναι τα CD4+ T λεμφοκύτταρα που παρουσιάζουν φαινοτυπικά και λειτουργικά χαρακτηριστικά κυττάρων,τα οποία έχουν προηγουμένως ενεργοποιηθεί in vivo. αυτά τα χαρακτηριστικά περιλαμβάνουν την έκφραση υποδοχέων il-2 (CD25), CD69 (early activation antigen), CD45RO (memory phenotype), VLA-1 (Very Late Activation Antigen type 1) και hla-ii αντιγόνα. Υποστηρίζεται ότι η ενεργοποίηση αυτή θα μπορούσε να προκληθεί από αυτοαντιγόνο, το οποίο εδράζεται στις φλεγμαίνουσες αρθρώσεις. το 2003, αναγνωρίστηκε ένας υποπληθυσμός των τ κυττάρων, που ονομάστηκαν ρυθμιστικά τ κύτταρα (Tregs). βρέθηκε ότι εκφράζουν το μετα- 33
34 34 γραφικό παράγοντα Foxp3 και θεωρούνται ότι έχουν κομβικό ρόλο στη ρύθμιση της φλεγμονώδους διαδικασίας 36. τα Tregs είναι σημαντικά για τη διατήρηση της ομοιόστασης του ανοσιακού συστήματος. διαταραχές της λειτουργίας των Tregs ή ελάττωση του αριθμού τους έχει παρατηρηθεί σε αρκετά αυτοάνοσα νοσήματα, συμπεριλαμβανομένου της ρευματοειδούς αρθρίτιδας και της νεανικής ιδιοπαθούς αρθρίτιδας καταστάσεις οι οποίες ευνοούν την ανάπτυξη των Tregs και προάγουν την ανοσολογική ανοχή, δύνανται να υπονομευθούν από φλεγμονώδη σήματα, τα οποία παράλληλα προωθούν τη γένεση ενός άλλου πληθυσμού τ κυττάρων, που ανακαλύφθηκε πιο πρόσφατα, των Th τα Th17 κύτταρα, τα οποία είναι CD4+ κύτταρα που εκκρίνουν την il-17 φλεγμονώδη κυτταροκίνη, βρέθηκε ότι έχουν κεντρικό ρόλο στην αρθρίτιδα που αναπτύσσεται σε πειραματικά πρότυπα ποντικών και πρόσφατα αποδείχθηκε ότι είναι οι βασικοί συντελεστές σε πολλές αυτοάνοσες νόσους, συμπεριλαμβανομένης της οροαρνητικής ρευματοειδούς αρθρίτιδας των ενηλίκων και της νεανικής ιδιοπαθούς αρθρίτιδας 40,41,42,43. Έχει βρεθεί μια αντίστροφη συσχέτιση ανάμεσα στα Th17 κύτταρα και στα Foxp3+ Tregs, γεγονός που πιθανώς σημαίνει ότι η ισορροπία μεταξύ των Th17 κυττάρων και των Tregs μπορεί να επηρεάζει την πορεία και έκβαση της νόσου 43. Σε πειραματικά ζωικά πρότυπα, η ενίσχυση της διαφοροποίησης των Th17 κυττάρων λαμβάνει χώρα εις βάρος των Tregs, με αποτέλεσμα ο συνδυασμός αυτών των μεταβολών να προάγει την ανάπτυξη αυτοανοσίας. Πρόσφατα, έχουν έλθει στο φως διάφοροι μηχανισμοί που ελέγχουν την αμοιβαία σχέση μεταξύ των Tregs και των Th17 κυττάρων, στους οποίους συμπεριλαμβάνεται η δράση φλεγμονωδών κυτταροκινών, όπως είναι η il-1β 40. βιολογικές θεραπείες που θα στοχεύουν στην αποκατάσταση της ισορροπίας Tregs/Th17 υπέρ των Tregs, μπορεί να ανοίξουν το δρόμο για την επαναρρύθμιση της ανοσιακής ανοχής. O αυξημένος αριθμός μακροφάγων και δενδριτικών κυττάρων καθώς και η υπερπλασία των υμενοκυττάρων που ομοιάζουν με τους ινοβλάστες (κύτταρα τύπου α) και των υμενοκυττάρων που ομοιάζουν με τα μακροφάγα (κύτταρα τύπου β) είναι, επιπρόσθετα, τυπικά ευρήματα του αρθρικού υμένα των παιδιών με Νια. η ανίχνευση κυτταροκινών που εκκρίνονται από αυτά τα κύτταρα, παρέχει επιπλέον ένδειξη για το σημαντικό ρόλο αυτών των κυττάρων στη συνεχιζόμενη υμενίτιδα. η παρουσία μακροφάγων που παράγουν il-1 στο φλεγμαίνοντα αρθρικό υμένα, έχει παρατηρηθεί πρώτη φορά από το Marini και τους συνεργάτες του το 1986 και έκτοτε επιβεβαιώθηκε από πλήθος μελετών 44. η ανάλυση της έκφρασης του παράγοντα νέκρωσης των όγκων-α (Tu-
35 mor Necrosis Factor-α, TNFα) και της κατανομής των υποδοχέων του στον αρθρικό υμένα ασθενών με νεανική ρευματοειδή αρθρίτιδα παρείχε ισχυρές ενδείξεις για το ρόλο, τόσο του TNF-α όσο και του TNF-β στη διατήρηση της υμενίτιδας. το επίπεδο της έκφρασης του TNF-α συσχετίζεται στενά με το βαθμό της φλεγμονώδους διήθησης της αρθρικής μεμβράνης. η il-6, μια ακόμη κυτταροκίνη που προέρχεται από τα μακροφάγα, έχει βρεθεί στο αρθρικό υγρό των ασθενών με Νια. Πιο σημαντικό, όμως, είναι ότι στους ασθενείς με συστηματικής έναρξης νόσο, οι συγκεντρώσεις της il-6 είναι αυξημένες όχι μόνο στον αρθρικό υμένα αλλά και στον ορό και επιπλέον οι συγκεντρώσεις της il-6 στον ορό συσχετίζονται με την έκταση της αρθρικής συμμετοχής και της περιφερικής θρομβοκυττάρωσης. O σημαντικός ρόλος της il-6 στην παθογένεια της συστηματικής υποομάδας της Νια υποστηρίζεται από πλήθος γενετικών μελετών. Παρά το γεγονός ότι τα τ-λεμφοκύτταρα και τα μακροφάγα είναι πολυπληθέστερα στο φλεγμονώδη αρθρικό υμένα, παρατηρείται, ωστόσο, και δραστηριότητα β-λεμφοκυττάρων, τόσο στο περιφερικό αίμα, όσο και στην άρθρωση. το αποτέλεσμα της αυξημένης δραστηριότητας των β-λεμφοκυττάρων είναι η υπερσφαιριναιμία, τα κυκλοφορούντα ανοσοσυμπλέγματα, τα αντιπυρηνικά αντισώματα (ανα) και οι ρευματοειδείς παράγοντες, συνήθη ευρήματα σε αρκετούς ασθενείς με Νια. Ένας μεγάλος αριθμός μελετών, έδειξε ότι τα αντισώματα έναντι κιτρουλινιωμένων πρωτεϊνών (anti-cyclic citrullinated peptide antibodies, anti-ccp) είναι σημαντικά αυξημένα, μόνο στην οροθετική πολυαρθρική μορφή της Νια. τα anti-ccp αντισώματα έχει βρεθεί ότι βοηθούν στον καθορισμό της πρόγνωσης των ενήλικων ασθενών με ρευματοειδή αρθρίτιδα. μελέτες σε ασθενείς με NiA δείχνουν ότι η παρουσία των anti-ccp είναι σημαντικά αυξημένη στους ασθενείς με πολυαρθρίτιδα RF-θετική. Oι Ferrucci και συν. βρήκαν ότι anti-ccp αντισώματα δημιουργούνται κυρίως στις hla-dr4 θετικές περιπτώσεις και συσχετίζονται με πολυαρθρική έναρξη και διαβρωτική νόσο 45. τέλος, είναι ενδιαφέρον να αναφερθεί ότι η συστηματική μορφή της Νια τείνει να θεωρηθεί πλέον ως ένα αυτοφλεγμονώδες νόσημα, παρά ως μια κλασσική αυτοάνοση νόσος 46,47. Πράγματι, πολλά κλινικά χαρακτηριστικά της μορφή αυτής είναι παρόμοια με αυτά που συναντώνται στα αυτοφλεγμονώδη νοσήματα. O πυρετός, η πολυοργανική συμμετοχή και η πολυκυκλική πορεία σε κάποιους ασθενείς είναι μερικά από αυτά. επιπλέον, δεν ανιχνεύονται συνήθως, αυτοαντιδρώντα τ λεμφοκύτταρα, στους ασθενείς με συστηματικής έναρξης νόσο. Σπανίως τα αντιπυρηνικά αντισώματα είναι θετικά, 35
36 36 ενώ ο ρευματοειδής παράγοντας συνήθως είναι απών. Γίνεται ολοένα πιο ξεκάθαρο ότι η φυσική ανοσία (κυτταροκίνες όπως il-1, il-6, il-18, ουδετερόφιλα και μονοκύτταρα/μακροφάγα), παρά η επίκτητη παίζει το σημαντικότερο ρόλο στην παθογένεια της συστηματικής μορφής, σε αντίθεση με ότι συμβαίνει στις υπόλοιπες μορφές. αυτό υποστηρίζεται και σε γενετικό επίπεδο, αφού ένα διακριτό χαρακτηριστικό της υποομάδας αυτής αποτελεί η έλλειψη ισχυρών συσχετίσεων με τα μόρια του μείζονος συμπλέγματος ιστοσυμβατότητας τάξης ιι (MhC ii) Αιτιοπαθογενετικοί μηχανισμοί η αιτιοπαθογένεια της NiA δεν είναι καλά κατανοητή, θεωρείται, όμως, ως σύνθετη νόσος (complex disease), η οποία επηρεάζεται από συνδυασμό περιβαλλοντολογικών και γενετικών παραγόντων Περιβαλλοντικοί παράγοντες το επικρατέστερο αιτιολογικό μοντέλο της Νια, είναι η είσοδος ενός λοιμογόνου παράγοντα σε ένα γενετικά προδιατεθειμένο ξενιστή. O περισσότερο καλά μελετημένος μηχανισμός, μέσω του οποίου η λοίμωξη επιδρά στην αύξηση του κινδύνου ανάπτυξης της νόσου, είναι αυτός της μοριακής μίμησης. Άλλοι μηχανισμοί που πιθανώς εμπλέκονται είναι η πολυκλωνική διέγερση των λεμφοκυττάρων και η αυξημένη ανοσογενετικότητα των οργάνων, που ακολουθείται μετά από μία μικροβιακή φλεγμονή 48,49. Πιθανοί λοιμογόνοι παράγοντες, που έχουν συσχετισθεί και φαίνεται να εμπλέκονται στην παθογένεια της Νια είναι πάρα πολλοί, μερικοί από τους οποίους είναι οι ιοί της ερυθράς, της γρίπης α η2ν2, ο ParvoB-19, ο Coxsackie β4, ο Epstein Barr, το μυκόπλασμα της πνευμονίας, ο στρεπτόκοκκος, το χλαμύδιο του τραχώματος, η Υersinia enterocolitica και η Escherischia Coli Πρόσφατα, δημοσιεύτηκε ότι οποιαδήποτε λοίμωξη κατά το πρώτο έτος της ζωής για την οποία απαιτήθηκε νοσηλεία, συσχετίζεται με αυξημένο κίνδυνο ανάπτυξης NiA στο μέλλον 48,55. η παραπάνω μελέτη ήταν προοπτική Σουηδική μελέτη, που συμπεριέλαβε 3334 ασθενείς με NiA και υγιείς μάρτυρες 55. αξίζει να αναφερθεί ότι ακόμη ένα στοιχείο που υποστηρίζει την επίδραση των λοιμογόνων παραγόντων στην εμφάνιση NiA είναι το γεγονός ότι ο εμβολιασμός έναντι ιών, έχει ενοχοποιηθεί σε κάποιες περιπτώσεις για την αύξηση του κινδύνου εμφάνισης της νόσου 56. από την άλλη πλευρά, ενδιαφέρον παρουσιάζει τα τελευταία χρόνια η αναφερόμενη ως «υπόθεση της υγιεινής», κατά την οποία η μειωμένη έκθεση σε μικροβιακούς παράγοντες τα πρώτα χρόνια της ζωής, μπορεί να σχετίζεται με αυξημένο κίνδυνο ανάπτυξης αλλεργικών
37 και αυτοανόσων νοσημάτων κατά τη διάρκεια της παιδικής ηλικίας. Παραμένει, ωστόσο, να διευκρινιστεί ο μηχανισμός, μέσω του οποίου η λοίμωξη παρέχει προστασία έναντι αλλεργικών και αυτοάνοσων αντιδράσεων, η κεντρική όμως ιδέα είναι ότι η έκθεση σε μικροβιακούς παράγοντες χρησιμεύει στην καλύτερη «προετοιμασία» του ανοσοσολογικού συστήματος. Συγκεκριμένα, έχει προταθεί ότι τα ρυθμιστικά κύτταρα τα οποία διεγέρθηκαν από την είσοδο του λοιμογόνου παράγοντα, χρησιμεύουν, επίσης, και για την προς τα κάτω ρύθμιση της ανοσιακής απάντησης σε αυτοαντιγόνα. επίσης, η διέγερση της φυσικής ανοσίας από τους μικροβιακούς παράγοντες, μέσω των Toll-Like υποδοχέων (Toll-Like Receptors, TLRs), μπορεί να συμβάλλει στην προστασία έναντι αυτοανόσων απαντήσεων 48,49. Έτσι, σε απουσία επαρκούς προετοιμασίας, το ανοσιακό σύστημα συγκεκριμένων ατόμων (για παράδειγμα αυτών που είναι γενετικά προδιατεθειμένο) μπορεί ευκολότερα να κατευθυνθεί προς μία αλλεργική ή αυτοάνοση φλεγμονώδη απάντηση. Πέρα από τις λοιμώξεις, η βιταμίνη D και η έκθεση στον ήλιο, βρέθηκε ότι παίζουν σημαντικό ρόλο στην ελάττωση του κινδύνου ανάπτυξης αυτοανοσίας, μέσω αύξησης της ανοσολογικής ανοχής 48,57. Υπάρχει εκτεταμένη έρευνα προς αυτήν την κατεύθυνση και τα πρώτα αποτελέσματα από παρεμβατικές μελέτες χορήγησης βιταμίνης D στη ρευματοειδή αρθρίτιδα ενηλίκων, είναι θετικά 58, Γενετικοί παράγοντες Η μοριακή γενετική και η γενετική ανάλυση στα πολυπαραγοντικά νοσήματα τα δεδομένα από τη γενετική του ανθρώπου συσσωρεύονται με συνεχώς αυξανόμενο ρυθμό και οι αλληλουχίες ολόκληρου του γονιδιώματος για πολλαπλούς εθνικούς πληθυσμούς είναι τώρα δημόσια διαθέσιμες 60,61,62. η αυξανόμενη ανακάλυψη της ανθρώπινης γενετικής ποικιλότητας διευκολύνει την κατανόηση της διαφοροποίησης της προδιάθεσης σε συχνές νόσους μεταξύ ατόμων και πληθυσμών, ενώ η εξέλιξη της γενετικής θα βοηθήσει πιθανόν και στη βελτίωση της αποτελεσματικότητας και ασφάλειας των θεραπευτικών φαρμάκων. η γνώση αυτή σχετίζεται με το θεμελιώδες ερώτημα της προέλευσης, των ομοιοτήτων και των διαφορών μεταξύ των ανθρώπων. η δεκαετία που διανύουμε έχει γνωρίσει επαναστατικές προόδους στη γενετική ανθρώπου. από αυτές, η πιο σχετική με τις μελέτες γενετικής συσχέτισης ήταν η ολοκλήρωση της πλήρους αλληλούχισης του ανθρώπινου γονιδιώματος, η αναγνώριση μεγάλων αριθμών γενετικών δεικτών, κυρίως SNPs, η ανάπτυξη τεχνολογιών για μαζική γονοτύπηση των SNPs και η κα- 37
38 38 τανόηση της σχέσης μεταξύ γειτονικών SNPs και της ανισορροπίας σύνδεσης (LD, Linkage Disequilibrium). μαζί με νέες αναλυτικές τεχνικές, τα εργαλεία αυτά παρέχουν ολοκληρωμένες, μεγάλης κλίμακας, μελέτες συσχέτισης των SNPs για τον προσδιορισμό γονιδίων και περιοχών, που συμβάλλουν είτε στην προδιάθεση για νόσο είτε σε άλλα χαρακτηριστικά. Oι παραλλαγές του ανθρώπινου γονιδιώματος συμβάλλουν στη φυσικά παρατηρούμενη ποικιλομορφία μεταξύ ατόμων. Σύμφωνα με μία πρόσφατη εκτίμηση, πάνω από το 99.9% της αλληλουχίας του ανθρώπινου γονιδιώματος είναι παρόμοια ή πανομοιότυπη, ενώ μόνο το 0.1% μπορεί να διαφοροποιείται οδηγώντας στα ατομικά χαρακτηριστικά 63. Πολυμορφισμός στην αλληλουχία DNA συνήθως ορίζεται ως παραλλαγή παρούσα σε συχνότητα μεγαλύτερη από το 1% του πληθυσμού. αν και ο όρος χρησιμοποιείται εναλλακτικά με τον όρο «μετάλλαξη», συμβατικά ως μετάλλαξη χαρακτηρίζεται στην ανθρώπινη γενετική έρευνα κάθε γενωμική παραλλαγή με συχνότητα μικρότερη του 1% στον πληθυσμό 64. η διάκριση αυτή βασίζεται στη συχνότητα εμφάνισης της παραλλαγής στον πληθυσμό και όχι στον τύπο της ή στη λειτουργική σημασία της. μελέτες πλήρους αλληλούχισης του ανθρώπινου γονιδιώματος έδειξαν ότι οι πιο συχνοί πολυμορφισμοί είναι οι μονονουκλεοτιδικοί πολυμορφισμοί (SNPs) που αριθμούν περίπου 3-4 εκατομμύρια και στους οποίους ένα από τα τέσσερα πιθανά νουκλεοτίδια στην αλληλουχία DNA αντικαθίσταται από άλλο, γεγονός που συμβαίνει κατά μέσο όρο κάθε νουκλεοτίδια κατά μήκος του γονιδιώματος. Άλλοι, μη μονονουκλεοτιδικοί, πολυμορφισμοί στην αλληλουχία αφορούν απαλοιφές (deletions) και εισαγωγές (insertions) ενός ή περισσοτέρων νουκλεοτιδίων, αναδιατάξεις (rearrangements) και επαναλήψεις (repeating) αλληλουχιών. η πλειονότητα των πολυμορφισμών στην αλληλουχία DNA δεν έχουν λειτουργική σημασία αν και μερικοί τροποποιούν τη δομή του παραγόμενου πεπτιδίου, όπως για παράδειγμα οι αμινοξικές αλλαγές και οι αλλαγές μετατόπισης του αναγνωστικού πλαισίου ή αλλαγές που προκαλούν πρόωρο τερματισμό της μετάφρασης 65. από τις μέχρι τώρα αναγνωρισμένες μορφές γενετικών παραλλαγών, τα δύο σημαντικότερα συστατικά της ανθρώπινης γενετικής ποικιλομορφίας, είναι οι μονονουκλεοτιδικοί πολυμορφισμοί (SNPs) και οι παραλλαγές του αριθμού των αντιγράφων (copy-number variants). εκατομμύρια SNPs έχουν ανακαλυφθεί στους ανθρώπους και σε επίπεδο μεμονωμένου νουκλεοτιδίου, δύο άνθρωποι διαφέρουν περίπου σε 1 ανά 1000 bp 66.
39 Oι μονονουκλεοτιδικοί πολυμορφισμοί στο ανθρώπινο γονιδίωμα Μελέτες γενετικής συσχέτισης Tο αποτέλεσμα της ισχυροποίησης των τεχνολογικών εφαρμογών για την ανίχνευση παραλλαγών στο γονιδίωμα, οδήγησε στη διαπίστωση ότι οι περισσότερες από τις παραλλαγές που ανιχνεύθηκαν την τελευταία 20ετία είναι μικρές και ποιοτικές, κυρίως μονονουκλεοτιδικές αλλαγές. Σύμφωνα με δημοσιευμένα αποτελέσματα, το 50% των SNPs βρίσκεται σε μη κωδικοποιούσες περιοχές, ενώ από το υπόλοιπο ποσοστό που εντοπίζεται σε κωδικοποιούσες περιοχές, το 25% οδηγεί σε «μη-συνώνυμες αλλαγές» (και άρα αλλαγές αμινοξέων) και το υπόλοιπο 25% σε «σιωπηρές αλλαγές» 67, για τις οποίες θα ήταν πιο δόκιμος ο όρος «συνώνυμες αλλαγές». τα μη-συνώνυμα SNPs μπορούν να παράγουν νόσο και για αυτό το λόγο υπόκεινται σε φυσική επιλογή. τα συνώνυμα SNPs, αν και αρχικά θεωρήθηκαν ως αδιάφορα για τη γενετική διαδικασία, πρόσφατα δεδομένα καταρρίπτουν αυτήν την υπόθεση, ενώ ισχυροποιούν την άποψη ότι τα «συνώνυμα» SNPs επηρεάζουν το μάτισμα, τη σταθερότητα και τη δομή του mrna αλλά και πολύ πρόσφατα βρέθηκε να επηρεάζουν και την αναδίπλωση της παραγόμενης πρωτεΐνης (για ανασκόπηση του ρόλου των συνώνυμων SNPs βλ. βιβλιογραφία 68). Oι κύριες πιθανές προσεγγίσεις στη χαρτογράφηση γονιδίων που είναι υπεύθυνα για την εμφάνιση νόσων ή ποσοτικών χαρακτηριστικών ομαδοποιούνται πρακτικά σε δύο κύριες κατηγορίες: α) τις μελέτες του «υποψήφιου γονιδίου» (candidate-gene approaches), που χρησιμοποιoύν προσεγγίσεις είτε συσχέτισης είτε επαναλληλούχισης ολόκληρου του γονιδίου και β) τις μελέτες σε ολόκληρο το γονιδίωμα (genome-wide studies), που περιλαμβάνουν τόσο τη χαρτογράφηση σύνδεσης (linkage mapping) όσο και τις μελέτες συσχέτισης σε ολόκληρο το γονιδίωμα (genome-wide association studies) 69. Oι μελέτες γενετικής συσχέτισης βασίζονται σε μεγάλους αριθμούς εμπλεκομένων ατόμων και ήρθαν να δώσουν διέξοδο στο πρόβλημα που παρατηρήθηκε με τα πολυπαραγοντικά νοσήματα. Στις μελέτες αυτές οι ασθενείς συγκρίνονται με καλά αντιστοιχισμένους (από άποψη φύλου και ηλικίας) υγιείς μάρτυρες από τον ίδιο πληθυσμό, δίνοντας μεγαλύτερες πιθανότητες ανίχνευσης μικρών γενετικών επιδράσεων. Σε μια απλή εκδοχή τους, οι μελέτες γενετικής συσχέτισης συγκρίνουν τις συχνότητες αλληλομόρφων ή γονοτύπων, για μία συγκεκριμένη παραλλαγή, μεταξύ ασθενών και υγιών. Oι μελέτες συσχέτισης του «υποψήφιου γονιδίου», αναγνώρισαν πολλά από τα γονίδια που συμβάλλουν στην προδιάθεση για σύνθετες νόσους 70. αυτές οι μελέτες διευκολύνθηκαν σημαντικά από τη χρήση έμμεσων μεθόδων, όπως 39
40 40 η «ανισορροπία Σύνδεσης» (Linkage Disequilibrium), αλλά εξακολουθούν να βασίζονται στη σωστή πρόβλεψη του γονιδίου ή των γονιδίων, συνήθως στη βάση της βιολογικής υπόθεσης, η οποία όσο ευρεία και αν είναι, θα αναγνωρίσει ένα μόνο μέρος των γενετικών παραγόντων κινδύνου, ακόμα και αν η παθοφυσιολογία της νόσου είναι καλά κατανοητή Μελέτες συσχέτισης που καλύπτουν το πλήρες γονιδίωμα (GWAS) και πολυπαραγοντικά νοσήματα η προσέγγιση της γενετικής συσχέτισης που καλύπτει πλήρως το γονιδίωμα (GWAS) αποσκοπεί στην αποκάλυψη γενετικών παραλλαγών, που αφορούν νοσήματα ή/και χαρακτηριστικά αυτών και ειδικές κλινικές εκδηλώσεις τους. εκατοντάδες χιλιάδες SNPs ελέγχονται για συσχετίσεις με νόσο σε εκατοντάδες ή χιλιάδες άτομα. Oι μελέτες αυτές έχουν προκαλέσει πραγματική επανάσταση στην έρευνα για τις γενετικές επιδράσεις σε σύνθετα χαρακτηριστικά 71,72. Oι πολυπαραγοντικές νόσοι, σε αντίθεση με τις μονογονιδιακές, προκαλούνται από την αθροιστική δράση πολλαπλών περιβαλλοντικών και γενετικών παραγόντων, με κάθε έναν από αυτούς να συμμετέχει με χαμηλή επίδραση στο συνολικό φαινότυπο και ελάχιστους μόνο να απαιτούνται απόλυτα για την εμφάνιση της νόσου. το μεγάλο πλεονέκτημα αυτής της προσέγγισης αναφέρεται στο γεγονός ότι δεν υπάρχει κάποια «αρχική υπόθεση» σχετικά με τη γενωμική εντόπιση των διαφόρων γενετικών παραλλαγών και, επομένως, αυτή η προσέγγιση μπορεί να εκμεταλλευθεί τα πλεονεκτήματα των μελετών συσχέτισης, χωρίς όμως να προϋποθέτει προϋπάρχουσα γνώση για τα πιθανά γονίδια. Έτσι, αντιπροσωπεύει μία απόλυτα αμερόληπτη, αρκετά ολοκληρωμένη επιλογή, που μπορεί να επιχειρηθεί ακόμα και απουσία πειστικής μαρτυρίας αναφορικά με τη λειτουργία ή την τοποθεσία των αιτιολογικών (για τη νόσο) γονιδίων. Oι GWAS υπόσχονται να αποκαλύψουν γονίδια που δεν είχαν προηγου - μένως εμπλακεί στην παθογένεση της νόσου και να βοηθήσουν στον υπολογι - σμό της γενετικής δράσης αυτών (με προσθετικό ή μη τρόπο), καθώς και στην αποκάλυψη πλειοτροπικών φαινομένων δράσης με αντικειμενικό τρόπο. μέχρι τον Oκτώβριο του 2010, είχαν δημοσιευτεί 702 GWAS σε ανθρώπους, η πλειοψηφία των οποίων είχε σχέση με νοσήματα του ανθρώπου ( Oι μελέτες αυτές προϋποθέτουν γνώση των συχνών παραλλαγών στο γονιδίωμα αλλά και την ικανότητα για γονοτύπηση ενός πολύ μεγάλου αριθμού παραλλαγών σε μεγάλα δείγματα συμμετεχόντων. η βάση δεδομένων dbsnp περιλαμβάνει τώρα πάνω από έντεκα εκατομμύρια SNPs με συχνότητα ελάσσονος αλληλομόρφου μεγαλύτερη από
41 1% που υπολογίζεται ότι υπάρχουν στο ανθρώπινο γονιδίωμα 73. Oι μέθοδοι γονοτύπησης έχουν εξελιχθεί τεχνικά και δίνουν τη δυνατότητα γρήγορων αποτελεσμάτων, σε μικρό χρόνο και με μικρό κόστος σε ένα μεγάλο αριθμό συμμετεχόντων. τέλος, η ευρεία γνώση των προτύπων ανισορροπίας Σύνδεσης που προέκυψε με την εξέλιξη του σχεδίου hapmap, επέτρεψε την ευκολότερη επιλογή δεικτών, ικανών να παρέχουν τη μεγαλύτερη δυνατή πληροφορία 74. με βάση προηγούμενες μελέτες αλλά και δεδομένα του σχεδίου hapmap, μερικές εκατοντάδες χιλιάδες καλά επιλεγμένα SNPs θα μπορούσαν να ήταν αρκετά ώστε να παρέχουν πληροφορίες για τις περισσότερες συχνές πολυμορφικές θέσεις στο γονιδίωμα. το διεθνές πρόγραμμα hapmap είχε ως στόχο τη χαρτογράφηση των εκατομμυρίων SNPs που είχαν ανακαλυφθεί κατά την αλληλούχιση του ανθρώπινου γονιδιώματος, ή και μεταγενέστερα 75,76. επιπρόσθετα, η βάση δεδομένων του hapmap αποτελεί και μία εξαιρετικά χρήσιμη πηγή για την ανάπτυξη των «μικροσυστοιχιών γονοτύπησης». τα δεδομένα χρησιμοποιούνται για να βελτιστοποιήσουν την κάλυψη του γονιδιώματος αξιοποιώντας τη δυνατότητα χρήσης αντιπροσωπευτικών SNPs (tag SNPs). Όπως όλες οι μεγάλες τομές στο χώρο της επιστήμης και οι επαναστατικές ερευνητικές αποκαλύψεις, έτσι και οι GWAS ήγειραν πλήθος συζητήσεων και επιφυλάξεων για το κατά πόσο δύνανται να εμφανίσουν «τεχνικά» προβλήματα ή να οδηγήσουν και σε κάποιες παρερμηνείες. είναι μεγάλο πλεονέκτημα αυτής της προσέγγισης ότι δεν απαιτείται κάποια αρχική υπόθεση, ότι χρησιμοποιούνται ψηφιακά δεδομένα (που μπορούν να εμπλουτιστούν χωρίς να καταστραφούν), ότι ενισχύεται ο σχηματισμός μεγάλων συνεργαζόμενων ομάδων, ότι παρέχει δεδομένα για την καταγωγή κάθε ατόμου βοηθώντας στη σωστή αντιστοίχιση υγιών και ασθενών, ενώ παρέχεται επίσης η δυνατότητα συλλογής δεδομένων τόσο για την αλληλουχία γονιδίων όσο και για την εμφάνιση γενετικής ποικιλομορφίας. Παράλληλα όμως, μπορεί να υπάρξουν και παρερμηνείες διότι αποκαλύπτονται συχνά δεδομένα μόνο για γενετικούς πολυμορφισμούς με μεγάλο βαθμό δράσης, ενώ αποκλείονται ταυτόχρονα αλληλόμορφα με μικρότερη επίπτωση τα οποία, ναι μεν δεν έχουν μεγάλη προγνωστική δράση, αλλά είναι σημαντικά για την ολοκληρωμένη διατύπωση νέων παθογενετικών μηχανισμών που οδηγούν στο υπό μελέτη νόσημα. ακόμα, απαιτείται πολύ μεγάλος αριθμός δειγμάτων (τα οποία δεν είναι πάντα εύκολο να συλλεχθούν), που να ανιχνεύουν μόνο εκείνα τα αλληλόμορφα που συναντούνται αρκετά συχνά στους πληθυσμούς (>5%), ενώ για να είναι πειστικά τα όποια ευρήματα απαιτείται επανάληψη σε εξίσου μεγάλους πληθυσμούς διαφορετικής εθνικής ή φυλετικής προέλευσης. Παρά 41
42 42 τους περιορισμούς τους, οι GWAS εμφάνισαν ορισμένα εντυπωσιακά ευρήματα. το πρώτο από αυτά αφορά την ανεύρεση συσχετίσεων SNPs εντοπιζόμενων σε γονίδια που αρχικά δεν θεωρούνταν ως έχοντα κάποιο ρόλο στην παθογένεια της μελετώμενης νόσου. το δεύτερο εντυπωσιακό εύρημα που προέκυψε από τις GWAS είναι η ανεύρεση γενετικών τόπων που είναι κοινοί σε κλινικές καταστάσεις, που προηγουμένως θεωρούνταν ως μη σχετιζόμενες μεταξύ τους. μάλιστα, οι μαρτυρίες για κοινή γενετική προδιάθεση μεταξύ διαφορετικών νόσων, αυξάνονται συνεχώς. είναι φυσικά προφανές ότι απαιτείται ακόμα αρκετή δουλειά για να καθοριστεί η λειτουργική βάση των παρατηρούμενων συσχετίσεων, να αποκαλυφθεί δηλαδή η λειτουργική σημασία των αποκαλυφθέντων γενετικών παραγόντων κινδύνου και να γίνει τελικά εφικτή κάποια νέα θεραπευτική παρέμβαση. O απώτερος στόχος της γενετικής έρευνας εντοπίζεται στη μετάφραση των όποιων ευρημάτων σε προόδους στην κλινική πράξη. Oι πρόσφατες επιτυχίες στην αναγνώριση γενετικών παραλλαγών προδιάθεσης (ή παραγόντων κινδύνου) που σχετίζονται με σημαντικούς βιοϊατρικούς φαινοτύπους, έχουν αυξήσει την πεποίθηση ότι η πληροφορία αυτή μπορεί να μεταφραστεί σε κλινικά χρήσιμη βελτίωση στην αντιμετώπιση των νόσων. Γενικά υπάρχουν δύο κύριες οδοί μέσω των οποίων τα ευρήματα μπορούν να μεταφραστούν στην κλινική πράξη. η πρώτη αφορά στην αναγνώριση των μοριακών μονοπατιών, παρέχοντας νέες ευκαιρίες για κλινική πρόοδο είτε για όλους τους ασθενείς είτε για άτομα που κατατάσσονται σε ομάδα υψηλού κινδύνου για να νοσήσουν από τη συγκεκριμένη νόσο. η δεύτερη «μεταφραστική οδός» αφορά σε μεμονωμένα άτομα και τη χρήση της εξατομικευμένης ιατρικής (personalized medicine) με βάση τα ατομικά γενετικά προφίλ και, κατ επέκταση, τα πρότυπα προδιάθεσης στο να εμφανίσουν είτε μεγαλύτερη αποτελεσματικότητα σε μια συγκεκριμένη θεραπεία είτε στο να εμφανίσουν (ή να μην εμφανίσουν) παρενέργειες στη θεραπεία αυτή O ρόλος των HLA και non-hla γονιδίων στη ΝΙΑ ενδείξεις ότι γενετικοί παράγοντες συμμετέχουν στην παθογένεια της Νια, προκύπτουν από μελέτες που έχουν διεξαχθεί σε διδύμους, σε οικογένειες ή από συγκριτικές μελέτες συσχετισμού ασθενών-μαρτύρων. η Νια κατατάσσεται στις σύνθετες γενετικές νόσους (complex diseases). αυτές δεν ακολουθούν κάποιον από τους τύπους της μενδέλειας κληρονομικότητας, αλλά πιστεύεται ότι προκύπτουν από την αλληλεπίδραση γενετικών και περιβαλλοντικών παραγόντων. η πιο καλά μελετημένη γενετική συσχέτιση στη Νια, είναι η παρουσία πολυμορφισμών σε γονίδια που κωδικοποιούν
43 τα αντιγόνα του μείζονος συμπλέγματος ιστοσυμβατότητας hla (ηuman Leukocyte Antigens). από το συνολικό αυξημένο κίνδυνο, που έχουν τα αδέλφια πασχόντων με Νια να εμφανίσουν τη νόσο, μόνο περίπου το 8-13% μπορεί να αποδοθεί σε πολυμορφισμούς, που αφορούν στα hla μόρια Συνεπώς, η αιτιοπαθογένεια της Νια θα πρέπει να αναζητηθεί, όχι μόνο στις hla συσχετίσεις, αλλά και σε non-hla συσχετίσεις HLA συσχετίσεις τα γονίδια που κωδικοποιούν τα hla μόρια εντοπίζονται σε μια περιοχή του γονιδιώματος που ονομάζεται μείζων σύμπλεγμα ιστοσυμβατότητας και βρίσκεται στο χρωμόσωμα 6p21.3. τα hla μόρια διαιρούνται στα hla τάξης ι (hla A, B και C) και στα hla τάξης ιι (hla DR, DQ και DP). Συνοπτικά, τα hla τάξης ι μόρια εκφράζονται στην επιφάνεια όλων των εμπύρηνων κυττάρων και παρουσιάζουν ενδογενή αντιγόνα στα CD8+ κυτταροτοξικά τ λεμφοκύτταρα, ενώ τα hla τάξης ιι μόρια εκφράζονται μόνο στην επιφάνεια των κυττάρων που συμμετέχουν στην ανοσιακή απάντηση (π.χ. μακροφάγα, δενδριτικά κύτταρα, β λεμφοκύτταρα και ενδοθηλιακά κύτταρα) και παρουσιάζουν εξωγενή αντιγόνα στα CD4+ βοηθητικά τ λεμφοκύτταρα. το γεγονός ότι τα hla μόρια παίζουν σημαντικό ρόλο στο ανοσιακό σύστημα, έχει οδηγήσει στη θεώρηση των hla γονιδίων ως σημαντικών παραγόντων σε πολλές νόσους, ειδικά σε αυτές που πιστεύεται ότι έχουν ανοσιακή βάση, όπως είναι η Νια. η πλειοψηφία των hla μελετών στη νεανική αρθρίτιδα, έχει διεξαχθεί σε παιδιά που έχουν ταξινομηθεί σύμφωνα είτε με τα EULAR είτε με τα ACR κριτήρια. Oι μελέτες αυτές έχουν ανασκοπηθεί από τους Donn και Ollier 81. Oι Murray K και συν., σε μια μελέτη που περιελάμβανε 600 παιδιά με Νια και 254 μάρτυρες επιβεβαίωσαν αρκετές από τις ήδη γνωστές hla συσχετίσεις 82. επίσης, έχει δημοσιευθεί μελέτη των hla συσχετίσεων σε ένα μεγάλο δείγμα ασθενών με NiA από το ηνωμένο βασίλειο, οι οποίοι έχουν ταξινομηθεί, σύμφωνα με τα ilar κριτήρια 7. μέχρι σήμερα έχει αναφερθεί, ένας μεγάλος αριθμός συσχετίσεων ανάμεσα στα hla αλλήλια και στις υποομάδες της NiA. (πίνακας 7). 43
44 44 Πίνακας 7. Συσχετίσεις αλληλίων HLA τάξης Ι και τάξης ΙΙ με τις υποομάδες της NIA. HLA συσχέτιση Τάξης Ι hla B27 Υποομάδα ασθενούς αρθρίτιδα σχετιζόμενη με ενθεσίτιδα Όψιμης έναρξης ολιγοαρθρίτιδα σε αγόρια Oλιγοαρθρικής έναρξης νόσος σε μικρή ηλικία hla A2 Τάξης ΙΙ hla-drb1*08, hla-drb1*11 Πρώιμης έναρξης ολιγοαρθρίτιδα (υπότυπος του hla-dr5) hla-drb1*04, hla-drb1*07 Πρώιμης έναρξης ολιγοαρθρίτιδα hla DPB1*0201 Πρώιμης έναρξης ολιγοαρθρίτιδα εμμένουσα και επεκταθείσα ολιγοαρθρίτιδα hla-dr8/hla-drb1*08 Πολυαρθρική RF αρνητική hla-dp3/ DPB1*0301 Πολυαρθρική RF αρνητική hla-dq4 (DQA1*0401/ DQB1*0402) Πολυαρθρική RF αρνητική hla-dr4 Πολυαρθρική RF θετική hla-drb1*01, hla-dqa1*0101 Ψωριασική hla-drb1*01, hla-dqα1*0101/ DQB1*05 αρθρίτιδα σχετιζόμενη με ενθεσίτιδα hla-drb1*04, hla-drb1*08, hla-dr5, DRB1*11 Συστηματικής έναρξης αρθρίτιδα Όλες οι HLA συσχετίσεις του πίνακα προσδίδουν αυξημένο κίνδυνο επιδεκτικότητας, με εξαίρεση του που προσδίδει χαμηλό κίνδυνο. Από Minden K. Classification and epidemiology of juvenile idiopathic arthritis. In Rheumatology. Hochberg CM, Silman AJ, Smolen JS, Wewinblatt MH, eds.mosby Elsevier 5 th ed.2011:p991. Oι περισσότεροι hla συσχετισμοί δεν μπορούν να εξηγηθούν σε βάση μιας Aνισορροπίας Σύνδεσης, (Linkage Disequilibrium LD), γεγονός που μπορεί να υποστηρίζει την υπόθεση ότι αρκετοί hla τόποι συμβάλλουν ανεξάρτητα στην επιδεκτικότητα της Νια και των υποομάδων της. Όπως αναφέρθηκε προηγουμένως, από το συνολικό αυξημένο κίνδυνο που έχουν τα αδέλφια πασχόντων με Νια να εμφανίσουν τη νόσο, μόνο περίπου το 8-13% μπορεί να αποδοθεί σε πολυμορφισμούς, που αφορούν στα hla μόρια επομένως, και άλλα μη hla γονίδια θα πρέπει να σχετίζονται με τη νόσο.
45 non-hla συσχετίσεις Πολλοί διαφορετικοί non-hla γενετικοί τόποι έχουν διερευνηθεί σε παιδιά με αρθρίτιδα. κάθε συσχετισμός που έχει αναφερθεί, μπορεί να βοηθήσει στην αποκωδικοποίηση της αιτιοπαθογένειας της Νια, μόνο και εφόσον τα γενετικά ευρήματα είναι επαληθεύσιμα. Πρόσφατες γενετικές μελέτες που αφορούν σε αυτοάνοσα νοσήματα έχουν αποκαλύψει την ύπαρξη γενετικών τόπων που αποτελούν παράγοντες κινδύνου για διαφορετικά νοσήματα, εμφανίζεται δηλαδή μια πλειοτροπική δράση 83 γεγονός που έχει επιτρέψει την ανάπτυξη (σε κάποιες περιπτώσεις) κοινών θεραπευτικών προσεγγίσεων και πρωτοκόλλων (εικόνα 1). η Ρευματοειδής αρθρίτιδα (Ρα) αποτελεί ένα αυτοάνοσο νόσημα που εμφανίζει τις περισσότερες ομοιότητες με τη Νια σε επίπεδο παθοφυσιολογικών μηχανισμών, κλινικών χαρακτηριστικών καθώς και παθολογοανατομικών ευρημάτων 86,86. τα τελευταία χρόνια, έχουν αποκαλυφθεί πολλά γονίδια που σχετίζονται με αυξημένη προδιάθεση για Ρα, τα οποία έχουν επιβεβαιωθεί σε ανεξάρτητους πληθυσμούς. 45 HLA-DR4 Other autolmmune disease Shared epitope alleles PADI4 TNFAIP3 STAT4 TRAFI-C5 PTPN22 CTLA4* 4q27* IL2RA* CD40 CCL2I* CD244 IL2RB TNFRSFI4 PRKCQ PIP4K2V CDK6* Εικόνα 1: Γονίδια που συσχετίζονται με αυξημένη προδιάθεση εμφάνισης Ρευματοειδούς Αρθρίτιδας. Τα γονίδια που εμφανίζονται σε πλαίσιο εμπλέκονται στην ανάπτυξη τουλάχιστον ενός ακόμα αυτοάνοσου νοσήματος 84. με βάση αυτά τα ευρήματα, θεωρήθηκε ότι πολλοί από τους γενετικούς τόπους που σχετίζονται με την ανάπτυξη της Ρα θα μπορούσαν να εμπλέκονται και στην εμφάνιση της Νια, αποτελώντας έτσι πολύ σημαντικά υποψήφια γονίδια προς έλεγχο για το νόσημα αυτό. με βάση αυτό το σκεπτικό, επιβεβαιώθηκε όντως ότι αρκετά γονίδια που συσχετίζονται με τη Ρα αποτελούν και παράγοντες αυξημένης προδιάθεσης για NiA, όπως είναι το STAT4 85, η περιοχή TRAF1/C5 του χρωμοσώματος 9 85,87, ο πολυμορφισμός C1858T του γονιδίου PTPN22 88,89, μια περιοχή του χρωμοσώματος 10p15 κοντά στο
46 46 γονίδιο PRKCQ 85 καθώς και τα γονίδια CD247 86, 6q23/TNFAIP3 85, PTPN2, COG6 και ANGPT1 90, IL2RA 86, CCR5 91, AFF3 και IL2/IL21 92, CD80- KTELC1 και JMJD1C 78,79 (εικόνα 2). τέλος, μεταξύ των γενετικών πολυμορφισμών για τους οποίους έχει βρεθεί μέχρι τώρα συσχέτιση με τη Νια, υπάρχουν και κάποιοι για τους οποίους η συσχέτιση είναι τόσο υψηλή που φτάνει τα επίπεδα που προκύπτουν από μία μελέτη γενετικής συσχέτισης που καλύπτει το πλήρες γονιδίωμα (GWAS), δηλαδή 0.5 x Oι πολυμορφισμοί αυτοί αφορούν στα γονίδια IL2RA και PTPN2 86. Σε τελευταία μελέτη των hinks και συν. επιτεύχθηκε υψηλή γενετική συσχέτιση (σε επίπεδο GWAS >0.5x10-8 ) 16 non-hla περιοχών (PTPN22, STAT4, PTPN2, ANKRD55, il2-il21, TYK2, il2ra, Sh2B3-ATXN2, ERAP2-LNPEP, UBE2L3, C5orf6- irf1, RUNX1, il2rb, ATP8B2-iL6R, FAS, ZFP36L1) με τις υποομάδες ολιγοαρθρίτιδα και πολυαρθρίτιδα RF αρνητική 80. Εικόνα 2: Γονίδια εμπλεκόμενα στην έναρξη της ανοσιακής απόκρισης μέσω αντιγονοπαρουσιαστικών κυττάρων. Παρουσιάζεται συνοπτικά μία από τις τρέχουσες υποθέσεις της παθογένειας της Ρευματοειδούς Αρθρίτιδας μέσω της ενεργοποίησης των Τ- κυττάρων από αντιγόνα που παρουσιάζονται μέσω των μορίων MHC τάξης ΙΙ στα αντιγονοπαρουσιαστικά κύτταρα (APCs) 84
47 από όλο τον όγκο των δημοσιευμένων συσχετίσεων, παρακάτω παρουσιάζονται αναλυτικά τα 5 non-hla γονίδια (TRAF1/C5, STAT4, PTPN22, CD247 και PTPN2) που επιλέχτηκαν να μελετηθούν στην παρούσα μελέτη TRAF1/C5 η περιοχή του TRAF1/C5 περιλαμβάνει τα γονίδια TRAF1 (που κωδικοποιεί τον Παράγοντα 1 που σχετίζεται με τον υποδοχέα του παράγοντα νέκρωσης των όγκων -TNF-Receptor Associated Factor 1) και C5 (που κωδικοποιεί το 5 ο συστατικό του συμπληρώματος). και τα δύο είναι γονίδια που εμπλέκονται στην ανοσία και εμπλέκονται ισχυρά στην έναρξη και/ή επιδείνωση της φλεγμονώδους διαδικασίας. το γονίδιο TRAF1 κωδικοποιεί μία ενδοκυττάρια πρωτεΐνη που διαμεσολαβεί στη μεταβίβαση του σήματος από τους υποδοχείς 1 και 2 του παράγοντα νέκρωσης των όγκων (TNF) και τον CD40. από λειτουργική άποψη, ο TRAF1 φαίνεται να είναι αρνητικός ρυθμιστής της σηματοδότησης του υποδοχέα του TNF 93. O TNF είναι από τις σημαντικότερες κυτταροκίνες στην παθογένεια της NiA και ανταγωνιστές του TNF αποτελούν σήμερα αποτελεσματικά θεραπευτικά εργαλεία. από την άλλη πλευρά, το ενεργοποιημένο συστατικό C5 του συμπληρώματος δρα ως ισχυρός χημειοτακτικός παράγοντας των ουδετεροφίλων και επομένως η διαταραγμένη λειτουργία του, πιθανώς συμβάλλει στη διατήρηση της φλεγμονής. Πρόσφατα, περιγράφηκε ότι ο πολυμορφισμός ενός νουκλεοτιδίου (rs ) στην περιοχή TRAF1/C5, (που βρίσκεται στο χρωμόσωμα 9q33-34), συσχετίζεται με επιδεκτικότητα για την οροαρνητική πολυαρθρική μορφή της Νια και η συσχέτισή του γενικότερα με τη NiA επιβεβαιώθηκε σε περισσότερα του ενός δείγματος ασθενών 78, STAT4 το STAT4, μέλος της οικογένειας πρωτεϊνών-μεσολαβητών του σήματος και ενεργοποιητών της μεταγραφής (STATs) εκφράζεται σε ενεργοποιημένα μονοκύτταρα του περιφερικού αίματος, δενδριτικά κύτταρα (DC) και μακροφάγα σε σημεία φλεγμονής και συμμετέχει στα σηματοδοτικά μονοπάτια σημαντικών κυτταροκινών, όπως της il-12 και του τύπου i ιντερφερονών καθώς και της il το STAT4 διαμεσολαβεί τη σηματοδότηση της ιl-12 που είναι βασική για την ανάπτυξη της άμυνας σε ενδοκυττάρια λοίμωξη. O μηχανισμός της διαμεσολαβούμενης από την STAT4 σηματοδότηση της il- 12 είναι εξαρτώμενος από την επαγωγή της Th1 απόκρισης και την παραγωγή της ιντερφερόνης-γ 96 (εικόνα 3). 47
48 48 Εικόνα 3: Πρότυπο που προτάθηκε από τους Kariuki et al 97, το οποίο δείχνει το σηματοδοτικό μονοπάτι της IFN-α στο Συστηματικό Ερυθηματώδη Λύκο και περιλαμβάνει τα μόρια IRF5 και STAT PTPN22 το γονίδιο PTPN22 βρίσκεται στο βραχύ βραχίονα του χρωμοσώματος 1 κοντά στο τελομερές (1p ) (εικόνα 4). αποτελείται από bp και συγκροτείται από 24 εξώνια, και κωδικοποιεί μια πρωτεΐνη 807 αμινοξέων. Εικόνα 4: Στο χρωμόσωμα 1 εδράζεται το γονίδιο PTPN22 ( gene /PTPN22)
49 η πρωτεΐνη PTPN22 εμπλέκεται στη μεταγωγή σημάτων που βοηθούν στη ρύθμιση της δραστηριότητας των τ λεμφοκυττάρων. O γενετικός πολυμορφισμός του PTPN22, που σχετίζεται με προδιάθεση στην αυτοανοσία (C/T) στη θέση 1858, υποκαθιστά μια αργινίνη (Arg, R) σε τρυπτοφάνη (Trp,W) στην κωδικοποιούσα πρωτεΐνη Lyp. η Lyp είναι μια ενδοκυττάρια PTP και προσδένεται στην Csk κινάση, η οποία είναι ένα σημαντικό γονίδιο καταστολής της κινάσης που μεσολαβεί στην ενεργοποίηση των τ κυττάρων. η ικανότητα των Csk και Lyp να αναστέλλουν τη σηματοδότηση των υποδοχέων των τ κυττάρων απαιτεί την φυσική τους σύνδεση. O πολυμορφισμός C1858T εμποδίζει την αλληλεπίδραση μεταξύ Lyp και Csk, αναστέλλοντας το σχηματισμό του συμπλόκου και έτσι επιτυγχάνεται ενεργοποίηση των τ κυττάρων (εικόνα 5). O πολυμορφισμός (SNP) (C1858T) στην περιοχή του γονιδίου PTPN22 έχει συσχετισθεί με τη NiA, καθώς και με άλλες νόσους αυτοανόσου χαρακτήρα όπως PA, ΣεΛ και Σδ τύπου ι και άλλες 88,89, Εικόνα 5: H Lyp που κωδικοποιείται από το γονίδιο PTPN22 αναστέλλει τη μεταγωγή σήματος, αποφωσφορυλιώνοντας τρείς κινάσες σημαντικές για τη μετάδοση του σήματος στον TCR (T-cell receptor), οδηγώντας σε περιορισμένη ενεργοποίηση των Τ κυττάρων. Η αντικατάσταση αργινίνης από τρυπτοφάνη εμποδίζει την πρόσδεση της Lyp στην CsK και τελικά αυξάνει την ενεργοποίηση των Τ κυττάρων. Η Lyp πιθανώς δρα και στον αντιγονικό υποδοχέα των Β- κυττάρων (BCR, B-cell antigen receptor), είτε σε άλλους υποδοχείς που ρυθμίζουν την ανάπτυξη 98.
50 PTPN2 το PTPN2 γονίδιο (Protein Tyrosine Phosphatase Nonreceptor type 2, που είναι επίσης γνωστό και ως TC-PTP ή PTP-S2, κωδικοποιεί μια άλλη πρωτεΐνη της οικογένειας των PTPs, στην οποία ανήκει και το PTPN22. Oι PTP πρωτεΐνες ρυθμίζουν διαδικασίες μεταγωγής σήματος, κατά τις οποίες η πρωτεΐνη μεταβιβάζει το σήμα από το εξωτερικό περιβάλλον του κυττάρου στον πυρήνα του. αυτό το σήμα δίνει οδηγίες στο κύτταρο να πολλαπλασιαστεί ή να ωριμάσει και να αναλάβει εξειδικευμένες λειτουργίες. η πρωτεΐνη PTPN2 πιθανώς παίζει κάποιο σημαντικό ρόλο στην ενεργοποίηση των τ κυττάρων. η μεταλλαγή του PTPN2 συσχετίζεται με μειωμένη έκφραση της πρωτεΐνης σε CD4+ T κύτταρα καθώς και σε μετασχηματισμένες σειρές β κυττάρων 104. ακόμα, βρέθηκε πρόσφατα ότι η πρωτεΐνη αυτή ελέγχει γονίδια που σχετίζονται με το μηχανισμό της αυτοφαγίας, ενώ παίζει και κάποιο προστατευτικό ρόλο στην εντερική χλωρίδα και τη διατήρηση της κυτταρικής ομοιόστασης 105 (εικόνα 6). Listeria apical LC3B-II Autophagosomes ATG16L1 PTPN2 mtor induces inhibits EGFr basolateral TNF+IFNγ, MDP Εικόνα 6: O TNF-α και η IFN-γ, καθώς και ο MDP επάγουν την πρωτεΐνη PTPN2 στα εντερικά επιθηλιακά κύτταρα (IEC). Η PTPN2 αναστέλλει τον EGFR που επάγεται από κυτταροκίνες και, πιθανώς έμμεσα, την mtor ενεργότητα, επάγοντας έτσι την αυτοφαγία 106.
51 CD247 το γονίδιο CD247 που βρέθηκε να συσχετίζεται με Ρα αλλά και με NiA 86, έχει συσχετιστεί και με αυξημένη προδιάθεση εμφάνισης Συστηματικού ερυθηματώδους Λύκου (ΣεΛ) 107, σκληροδέρματος 108 και κοιλιοκάκης 109. το γονίδιο αυτό κωδικοποιεί μια πρωτεΐνη που είναι σημαντική για την ενεργοποίηση και σηματοδότηση των τ κυττάρων και αντιπροσωπεύει την υπομονάδα «ζήτα» (CD3ζ) του υποδοχέα των τ κυττάρων (TCR), αποτελώντας έτσι ένα συστατικό του συμπλόκου (TCR)/CD η πρωτεΐνη αυτή παίζει ένα σημαντικό ρόλο στο σχηματισμό και τη μεταφορά του συμπλόκου TCR/CD3 στην κυτταρική επιφάνεια. μελέτες που έγιναν σχετικά με το ρόλο της πρωτεΐνης CD247 στον ΣεΛ έδειξαν ότι η έκφραση της πρωτεΐνης μειώ - νεται σημαντικά ή γίνεται μηδενική (εικόνα 7). 51 Normal T-cell TCR-CD3 complex SLE T-cell Normal expression of CD247 Defective expression of CD247 Normal signaling Aberrant signaling Normal T-cell function T-cell dysfunction Hypo-responsiveness Decrease of IL-2 production Failure of immune tolerance Εικόνα 7: Σε φυσιολογικά Τ κύτταρα η μεταγωγή σήματος μέσω του συμπλόκου (TCR)/CD3 γίνεται κανονικά και οδηγεί σε φυσιολογική λειτουργία των κυττάρων αυτών. Μειωμένη έκφραση παρατηρείται σε Τ κύτταρα ασθενών με ΣΕΛ με επακόλουθη μείωση της παραγωγής της IL-2, η οποία οδηγεί σε απώλεια της ανοσιακής ανοχής 107. με την ανάπτυξη των νέων στατιστικών μεθόδων (που μπορούν να υπολογίσουν την κληρονομικότητα σε επίπεδο πληθυσμού με την αξιολόγηση ταυτόχρονα όλων των SNPs που προέκυψαν από γενετικές συσχετίσεις που καλύπτουν το πλήρες γονιδίωμα (GWAS)), υπολογίστηκε ότι περίπου το ένα τρίτο του κινδύνου ανάπτυξης NiA μπορεί να αποδοθεί σε γονίδια που εντοπίζονται στην περιοχή που είναι κοινή για τα αυτοάνοσα νοσήματα. τονίζεται, επομένως, η ανάγκη για μελέτη επιπλέον γενετικών παραγόντων, όπως είναι οι αλληλεπιδράσεις μεταξύ γονιδίων
52 5. Κ Λ Ι Ν Ι Κ Α Χ Α Ρ Α Κ Τ Η Ρ Ι Σ Τ Ι Κ Α Τ Ω Ν Δ Ι Α Φ O Ρ Ω Ν Υ Π O O Μ Α Δ Ω Ν Ν Ε Α Ν Ι Κ Η Σ Ι Δ Ι O Π Α Θ O Υ Σ Α Ρ Θ Ρ Ι Τ Ι Δ Α Σ 5.1 Συστηματική αρθρίτιδα η υποομάδα αυτή της Νια περιλαμβάνεται τόσο στην ταξινόμηση κατά ilar, όσο και στην ταξινόμηση βάσει των ACR και EULAR κριτηρίων. η συστηματικού τύπου έναρξης αρθρίτιδα παρουσιάζει τη χειρότερη πρόγνωση καθώς συνδυάζεται με υψηλή θνησιμότητα, αλλά και θνητότητα 111,112,113. αποτελεί το 5%, περίπου, του πληθυσμού της Ναι. Προσβάλλει κορίτσια και αγόρια με την ίδια συχνότητα και η έναρξή της μπορεί να συμβεί σε όλη τη διάρκεια της παιδικής ηλικίας. Oι εξωαρθρικές εκδηλώσεις μπορεί να προηγούνται της αρθρίτιδας για εβδομάδες ή μήνες ή ακόμη και για περισσότερα από 10 χρόνια. O πυρετός πρέπει να διαρκεί για τουλάχιστον 2 εβδομάδες και τις τελευταίες 3 ημέρες να αυξάνει σε επίπεδα μεγαλύτερα των 39 ο C ημερησίως, επιστρέφοντας σε θερμοκρασία μικρότερη των 37 ο C ανάμεσα στα πυρετικά κύματα, έτσι ώστε η διάγνωση της συστηματικής Νια να θεωρείται πιθανή (πίνακας 3). O πυρετός συνήθως παρατηρείται 1 ή 2 φορές την ημέρα και συχνά εμφανίζεται αργά το απόγευμα ή το βράδυ, επιστρέφοντας σε φυσιολογικά ή κατώτερα του φυσιολογικού επίπεδα τις πρωινές ώρες. Στα 90% των περιπτώσεων της συστηματικού τύπου έναρξης Νια, υπάρχει έκθυση ενός χαρακτηριστικού σομόν χρώματος κηλιδώδους ή κηλιδοβλατιδώδους εξανθήματος, το οποίο εμφανίζεται, συχνότερα, στον κορμό ή στα κάτω άκρα και συνοδεύει συνήθως τα κύματα του πυρετού. το εξάνθημα μπορεί να αναπαραχθεί με σκαριφισμό του δέρματος (φαινόμενο Köbner) ή με ζεστό λουτρό. Περιστασιακά, μπορεί να συνοδεύεται από κνησμό. Περίπου το 50-75% των ασθενών αναπτύσσουν γενικευμένη λεμφαδενοπάθεια και ηπατοσπληνομεγαλία. Oι λεμφαδένες είναι, συνήθως, ευκίνητοι, μικροί 52
53 και ανώδυνοι, ενώ η ιστολογική τους εξέταση αποκαλύπτει οζώδη υπερπλασία και σπανίως νεκρωτική λεμφαδενίτιδα. το παιδί με συστηματική Νια μπορεί να παραπονεθεί για κοιλιακό άλγος, εξαιτίας της ηπατομεγαλίας. Συχνά, ανευρίσκονται υψηλές τιμές τρανσαμινασών, ενώ ηπατική ανεπάρκεια συμβαίνει εξαιρετικά σπάνια. Πολυορογονίτιδα παρατηρείται συχνά και περίπου το 30% των ασθενών αναπτύσσει περικαρδίτιδα, η οποία τις περισσότερες φορές είναι υποκλινική. καρδιακός επιπωματισμός και μυοκαρδίτιδα μπορεί να συμβούν, αλλά οι εκδηλώσεις αυτές είναι σπάνιες. η προσβολή των πνευμόνων είναι, εξίσου, σπάνια και εκδηλώνεται ως πνευμονίτιδα, πλευριτική συλλογή ή πνευμονική ίνωση. Συμμετοχή του κνσ με εκδηλώσεις κώματος ή μηνιγγίτιδας έχει περιγραφεί, αλλά είναι ασυνήθης 111,112,113. Ποσοστό περίπου 50% των παιδιών με συστηματική Νια αναπτύσσει πολυαρθρίτιδα, σε χρονικό διάστημα 3-12 μήνες από την εμφάνιση του πυρετού. Oι καρποί, τα γόνατα και οι ποδοκνημικές αρθρώσεις είναι αυτές που προσβάλλονται συχνότερα, ενώ ακολουθούν η αυχενική μοίρα της σπονδυλικής στήλης, τα ισχία, οι κροταφογναθικές αρθρώσεις και οι αρθρώσεις των άκρων χειρών 113,114. τα παθολογικά εργαστηριακά ευρήματα των ασθενών με συστηματική Νια περιλαμβάνουν λευκοκυττάρωση, θρομβοκυττάρωση, αναιμία, αύξηση των ηπατικών ενζύμων και υψηλούς δείκτες οξείας φάσης, όπως ταχύτητα καθίζησης ερυθρών (τκε), C-αντιδρώσα πρωτεΐνη (CRP) και φερριτίνη. αντιπυρηνικά αντισώματα (ανα) ανευρίσκονται στο 5-10% των παιδιών, ενώ θετικός RF είναι σπάνια παρών (<2%) 111,112,113. Σε απουσία της αρθρίτιδας, ο κλινικός ιατρός πρέπει να διαφοροδιαγνώσει τη νόσο από λοιμώξεις, κακοήθειες, ρευματικό πυρετό, καθώς και από άλλες ρευματικές νόσους, όπως αγγειίτιδα και Συστηματικό ερυθηματώδη Λύκο. η πορεία καθώς και η βαρύτητα της νόσου παρουσιάζουν ετερογένεια μεταξύ των ασθενών με συστηματική αρθρίτιδα Περίπου στο 40%, η νόσος είναι μονοφασική, ενώ περισσότεροι από τους μισούς ασθενείς παρουσιάζουν χρόνια, εμμένουσα πορεία. μια μικρή ομάδα ασθενών εμφανίζει υποτροπιάζουσα, πολυκυκλική πορεία. Γενικότερα, τα συστηματικά συμπτώματα τείνουν να υποχωρούν μέσα στα επόμενα έτη, ωστόσο μπορεί να υποτροπιάσουν παράλληλα με τις εξάρσεις της νόσου. Στους περισσοτέρους ασθενείς η προοδευτική, καταστροφική αρθρίτιδα παραμένει η σημαντικότερη επιπλοκή, οδηγώντας σε σοβαρή αναπηρία και αύξηση της θνησιμότητας. Στους πρώιμους προγνωστικούς δείκτες καταστροφικής αρθρίτιδας περιλαμβάνονται η πολυαρθρική νόσος, η προσβολή του ισχίου, η θρομβοκυττάρωση 53
54 54 και η παρουσία συστηματικών εκδηλώσεων 6 μήνες μετά τη διάγνωση της νόσου μια σοβαρή, αλλά ευτυχώς ασυνήθης, επιπλοκή που μπορεί να συμβεί στους ασθενείς με συστηματική Νια, είναι το σύνδρομο ενεργοποίησης των μακροφάγων (μacrophage Activation Syndrome, MAS) ή αντιδραστική αιμοφαγοκυτταρική λεμφοϊστιοκυττάρωση. το σύνδρομο ενεργοποίησης των μακροφάγων μπορεί, επίσης, να παρατηρηθεί σε λοιμώξεις, όπως είναι η λοιμώδης μονοπυρήνωση καθώς και σε κακοήθειες. η αιτιολογία του συνδρόμου είναι άγνωστη, χαρακτηρίζεται δε από ανεξέλεγκτη ενεργοποίηση των τ λεμφοκυττάρων και των μακροφάγων, η οποία οδηγεί σε υπερέκκριση φλεγμονωδών κυτταροκινών και ανεπάρκεια πολλαπλών οργάνων 116. τα κυριότερα κλινικά χαρακτηριστικά του συνδρόμου είναι: μη υφέσιμος πυρετός, εξάνθημα, ηπατοσπληνομεγαλία, λεμφαδενοπάθεια, νευρολογικές διαταραχές και διαταραχές της λειτουργίας των πνευμόνων, καρδιάς και ήπατος. τα εργαστηριακά ευρήματα συνήθως προηγούνται και περιλαμβάνουν αναιμία, ουδετεροπενία, θρομβοκυτταροπενία, ιδιαίτερα αυξημένα επίπεδα φερριτίνης, ταχεία άνοδο των τρανσαμινασών, διάχυτη ενδαγγειακή πήξη, αυξημένη γαλακτική δεϋδρογενάση, υπερτριγλυκεριδαιμία, χαμηλή λευκωματίνη και χαμηλή τκε απότοκο της υποϊνωδογοναιμίας. η διάγνωση του MAS είναι δύσκολη και συστήνεται ότι αυτή μπορεί να εδραιωθεί όταν πληρούνται 5 από τα παρακάτω 8 διαγνωστικά κριτήρια: δύο κλινικά, πυρετός και σπληνομεγαλία και τρία από τα πέντε εργαστηριακά, κυτταροπενία, υπερτριγλυκεριδαιμία και/ή υποϊνωδογοναιμία, αυξημένη φερριτίνη (>500 mg/l), παρουσία αιμοφαγοκυττάρωσης στην οστεομυελική βιοψία, απούσα ή χαμηλή δραστηριότητα των Νκ κυττάρων και αυξημένα επίπεδα scd25 (sil2r) στον ορό καθώς η θνητότητα του συνδρόμου είναι πολύ υψηλή, κυμαινόμενη από 8%-22%, απαιτείται ταχεία αντιμετώπιση του ασθενούς με ενδοφλέβιες ώσεις υψηλών δόσεων μεθυλπρεδνιζολόνης (30mg/Kg/day, για 3-5 ημέρες). Σε ασθενείς ανθεκτικούς στα στεροειδή ή στις σοβαρότερες μορφές του συνδρόμου απαιτείται η προσθήκη κυκλοσπορίνης α (3-7 mg/κg/day). τα στεροειδή και η κυκλοσπορίνη είναι τα πλέον χρησιμοποιούμενα φάρμακα, καθώς έχει αποδειχθεί η αποτελεσματικότητά τους. ωστόσο, έχουν χρησιμοποιηθεί και άλλες θεραπείες, όπως υψηλές δόσεις γ-σφαιρίνης, ετοποσίδη, αντιθυμοκυτταρική σφαιρίνη, εtanercept και τέλος πλασμαφαίρεση Oλιγοαρθρίτιδα: εμμένουσα και επεκταθείσα αποτελεί την πιο συχνή υποομάδα, αντιπροσωπεύοντας το 40% όλων των περιπτώσεων Νια. Oρίζεται ως αρθρίτιδα, η οποία προσβάλλει 1-4 αρ-
55 θρώσεις κατά τη διάρκεια των πρώτων 6 μηνών της νόσου. αναγνωρίζονται 2 υποκατηγορίες: η εμμένουσα ολιγοαρθρίτιδα, η οποία δεν προσβάλλει περισσότερες από 4 αρθρώσεις σε όλη τη διάρκεια της νόσου και η επεκταθείσα ολιγοαρθρίτιδα, η οποία προσβάλλει περισσότερες από 4 αρθρώσεις, μετά από τους πρώτους 6 μήνες της νόσου. Υπάρχουν και σε αυτή την υποομάδα κριτήρια αποκλεισμού (πίνακας 3). η πλειονότητα των παιδιών με ολιγοαρθρίτιδα εμφανίζουν τη νόσο πριν την ηλικία των 5 χρόνων, με μια αιχμή ανάμεσα στο 1 ο και 3 ο έτος. η μορφή αυτή της Νια εμφανίζεται συχνότερα στα κορίτσια και συγκεκριμένα σε αναλογία 2:1 για την εμμένουσα και 5:1 για την επεκταθείσα ολιγοαρθρίτιδα. τα εργαστηριακά ευρήματα, εκτός της σχετικά αυξημένης συχνότητας θετικών ανα, είναι στις περισσότερες των περιπτώσεων φυσιολογικά. Συνήθως, δεν παρατηρείται αύξηση της τκε και της CRP, ούτε και λευκοκυττάρωση. η άρθρωση του γόνατος, είναι αυτή που προσβάλλεται συχνότερα, περίπου στο 47% των περιπτώσεων, ακολουθεί η ποδοκνημική άρθρωση και στη συνέχεια οι μικρές αρθρώσεις των άκρων χειρών ή ο αγκώνας. τέλος, συμμετοχή της κροταφογναθικής άρθρωσης καθώς και της αυχενικής μοίρας της σπονδυλικής στήλης είναι συνήθεις, ενώ οι άλλες αρθρώσεις προσβάλλονται λιγότερο συχνά. αρθρίτιδα που περιορίζεται στο ισχίο, είναι εξαιρετικά σπάνια σε αυτήν την υποομάδα της Νια και εφόσον υπάρχει, η διάγνωση θα πρέπει να αναθεωρηθεί. τα ANA είναι θετικά στο 40-85% του συνόλου των παιδιών με ολιγοαρθρική μορφή και συνδυάζονται με χρόνια πρόσθια ιριδοκυκλίτιδα. O κίνδυνος εμφάνισης χρόνιας πρόσθιας ιριδοκυκλίτιδας είναι μεγάλος σε παιδιά, ηλικίας μικρότερης των 5 ετών, με θετικά ανα και ολιγοαρθρίτιδα, ανεξαρτήτως φύλου. η ιριδοκυκλίτιδα είναι ασυμπτωματική και για το λόγο αυτό, η οφθαλμολογική εξέταση των παιδιών σε τακτική βάση είναι επιβεβλημένη Πολυαρθρίτιδα η πολυαρθρικού τύπου έναρξης αρθρίτιδα απαντά στο 25% των παιδιών με Νια και για τη διάγνωσή της απαιτείται η προσβολή 5 ή περισσότερων αρθρώσεων μέσα στους πρώτους 6 μήνες της νόσου. η μορφή αυτή της Νια διαιρείται σε 2 υποομάδες ανάλογα με την παρουσία ή όχι θετικού igμ Ρευματοειδούς Παράγοντα (RF) στην πολυαρθρίτιδα με αρνητικό RF (οροαρνητική) και στην πολυαρθρίτιδα με θετικό RF (οροθετική) (πίνακας 3). 55
56 Πολυαρθρίτιδα RF-αρνητική η οροαρνητική πολυαρθρική μορφή της Νια μπορεί να συνοδεύεται από χαμηλό πυρετό και ήπια ηπατοσπληνομεγαλία και η έναρξή της είναι δυνατόν να συμβεί οποτεδήποτε κατά τη διάρκεια της παιδικής ηλικίας. η προσβολή των αρθρώσεων είναι συνήθως συμμετρική. τα γόνατα, οι καρποί και οι ποδοκνημικές αρθρώσεις προσβάλλονται συχνότερα. Στην προσβολή των άκρων χειρών συμμετέχουν οι μετακαρπιοφαλαγγικές και οι εγγύς φαλαγγοφαλαγγικές αρθρώσεις, ενώ η αυχενική μοίρα της σπονδυλικής στήλης προσβάλλεται επίσης με σχετικά υψηλή συχνότητα. χρόνια πρόσθια ιριδοκυκλίτιδα αναπτύσσεται στο 5% των παιδιών, ενώ το ποσοστό των θετικών ανα ανέρχεται στο 40-50% Πολυαρθρίτιδα RF-θετική η οροθετική πολυαρθρική μορφή της Νια παρουσιάζει πολλές ομοιότητες με την οροθετική ρευματοειδή αρθρίτιδα των ενηλίκων. Oι περισσότεροι ασθενείς είναι κορίτσια. εμφανίζεται, συνήθως, κατά το τέλος της παιδικής ηλικίας, μεταξύ 12 και 16 ετών. τυπική είναι η συμμετρική προσβολή των μετακαρπιοφαλαγγικών, εγγύς φαλαγγοφαλαγγικών και των ματαταρσιοφαλαγγικών αρθρώσεων. Oι μεγάλες αρθρώσεις, μπορεί, επίσης, να συμμετέχουν, ενώ οι συστηματικές εκδηλώσεις είναι σπάνιες. Oι ασθενείς με θετικό igm RF και θετικά αντι-ccp αντισώματα, έχουν την τάση να εμφανίζουν εμμένουσα ενεργότητα νόσου, ρευματοειδή οζίδια, όμοια με αυτά που ανευρίσκονται στη ρευματοειδή αρθρίτιδα των ενηλίκων και πρώιμες διαβρώσεις στον ακτινολογικό έλεγχο. Oι επιπλοκές που αναπτύσσονται σε αυτήν την υποομάδα περιλαμβάνουν την καθυστέρηση στην ανάπτυξη και ωρίμανση των δευτερογενών χαρακτηριστικών του φύλου, την οστεοπενία, το σύνδρομο καρπιαίου σωλήνα και το ατλαντοαξονικό υπεξάρθρημα με νευρολογική σημειολογία. Στους ασθενείς αυτής της υποομάδας εμφανίζονται συχνότερα πνευμονική ίνωση και σύνδρομο Felty Ψωριασική αρθρίτιδα Σύμφωνα με τα ilar κριτήρια, ορίζεται ως αρθρίτιδα που συνυπάρχει με ψωρίαση ή αρθρίτιδα σε συνδυασμό με τουλάχιστον 2 από τα παρακάτω: δακτυλίτιδα, ανωμαλίες ονύχων ή παρουσία ψωρίασης σε συγγενή πρώτου βαθμού (πίνακας 3). η δακτυλίτιδα, οι ανωμαλίες των ονύχων, η προσβολή των άπω φαλαγγοφαλαγγικών αρθρώσεων και η ασύμμετρη οροαρνητική
57 περιφερική αρθρίτιδα είναι τυπικά ευρήματα, όπως και στην ψωριασική αρθρίτιδα των ενηλίκων. Σημαντικός αριθμός παιδιών εμφανίζουν σπονδυλαρθρίτιδα και ιερολαγονίτιδα. Σε μία επιδημιολογική μελέτη από τη Σκανδιναβία, θετικά ANA βρέθηκαν στο 1/3 των παιδιών που πληρούσαν τα ilar κριτήρια για ψωριασική αρθρίτιδα 14. μεταξύ των παιδιών με ψωριασική αρθρίτιδα, η ηλικία έναρξης της νόσου εμφανίζει διφασική πορεία, με πρώτη αιχμή γύρω από την ηλικία των 2 ετών και δεύτερη αιχμή αργότερα, στην όψιμη παιδική ηλικία. Oι ασθενείς ηλικίας μικρότερης των 5 ετών είναι πιθανότερο να είναι κορίτσια, με δακτυλίτιδα, προσβολή των μικρών αρθρώσεων των άκρων χειρών και θετικά αντιπυρηνικά αντισώματα. η ανάπτυξη πολυαρθρικής νόσου είναι πιο συχνή στους νεότερους ασθενείς, αν και στην πλειονότητα των περιπτώσεων η νεανική ψωριασική αρθρίτιδα παραμένει ολιγοαρθρικής έναρξης και πορείας. αντιθέτως, οι μεγαλύτεροι ασθενείς είναι συνήθως αγόρια και έχουν την τάση να αναπτύσσουν συχνότερα αξονική προσβολή, ενθεσίτιδες και εμμένουσα ολιγοαρθρίτιδα. Ίσως προκαλεί έκπληξη η παρόμοια συχνότητα ιριδοκυκλίτιδας μεταξύ των δύο ηλικιακών ομάδων 123, Αρθρίτιδα που σχετίζεται με ενθεσίτιδα Oρίζεται ως αρθρίτιδα μαζί με ενθεσίτιδα ή αρθρίτιδα ή ενθεσίτιδα σε συνδυασμό με 2 τουλάχιστον από τα παρακάτω: 1) ιστορικό ή παρουσία άλγους στην ιερολαγόνια άρθρωση και/ή φλεγμονώδης οσφυοϊερός πόνος, 2) παρουσία αντιγόνου hlaβ27, 3) έναρξη της αρθρίτιδας σε αγόρι μετά την ηλικία των 6 ετών, 4) οξεία (συμπτωματική) πρόσθια ιριδοκυκλίτιδα, 5) αγκυλοποιητική σπονδυλίτιδα, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα, ιερολαγονίτιδα στα πλαίσια φλεγμονώδους νόσου του εντέρου, σύνδρομο Reiter ή οξεία πρόσθια ιριδοκυκλίτιδα σε συγγενή πρώτου βαθμού (πίνακας 3). αυτή η υποομάδα της Νια προσβάλλει συχνότερα τα αγόρια σε σχέση με τα κορίτσια και πιο συχνά εμφανίζεται μετά την ηλικία των 9 χρόνων. τείνει να προσβάλλει τα κάτω άκρα, ιδιαίτερα την άρθρωση του γόνατος και την ποδοκνημική, αλλά σε αντίθεση με τη μορφή της ολιγοαρθρίτιδας που ξεκινά σε μικρή ηλικία, η αρθρίτιδα που σχετίζεται με ενθεσίτιδα μπορεί να προσβάλλει συχνά και την άρθρωση του ισχίου. η ενθεσίτιδα είναι δύσκολο να διαφοροποιηθεί από την αρθρίτιδα, ειδικά σε ένα παιδί με άλγος στη ράχη. Πολλά από αυτά τα παιδιά, αναπτύσσουν ιερολαγονίτιδα αρκετά χρόνια αργότερα 112,113. Στην υποομάδα αυτή της Νια περιλαμβάνονται όλες οι κλασικές σπον- 57
58 58 δυλοαρθροπάθειες που συναντώνται στους ενήλικες, όπως είναι η νεανική αγκυλοποιητική σπονδυλίτιδα, το σύνδρομο της Oροαρνητικής ενθεσοπάθειας και αρθροπάθειας (syndrome of Seronegative Enthesopathy and Arthropathy, SEA syndrome) και η αρθρίτιδα που συσχετίζεται με φλεγμονώδη νόσο του εντέρου. η αρθρίτιδα σχετιζόμενη με ενθεσίτιδα είναι δύσκολο να διαγνωσθεί κατά τη διάρκεια της παιδικής ηλικίας, αφού η πλήρης εικόνα της νόσου δύναται να μην έχει αναπτυχθεί μέχρι το παιδί να ενηλικιωθεί και να παραπεμφθεί προς παρακολούθηση σε ρευματολόγο ενηλίκων. η συσχέτιση με το hla-b27 είναι ισχυρή και τα παιδιά με θετική hla- B27 αρθρίτιδα και θετικό οικογενειακό ιστορικό σπονδυλαρθροπάθειας είναι πολύ πιθανό να αναπτύξουν με τη σειρά τους σπονδυλαρθροπάθεια τα επόμενα χρόνια. Στο 15-25% των παιδιών αυτής της υποομάδας εμφανίζεται ιρίτιδα, συνήθως οξεία και συμπτωματική επίσης, συχνή είναι η σοβαρή βλάβη της κατ ισχίον άρθρωσης, για την οποία απαιτείται πρώιμα, ολική αρθροπλαστική και αντικατάσταση της άρθρωσης. Στην υποομάδα αυτή, όταν εμφανίζεται πυρετός, ο οποίος επιμένει και συσχετίζεται με την αρθρίτιδα, πρέπει πάντοτε να εγείρει την υπόνοια φλεγμονώδους νόσου του εντέρου, αφού βέβαια αποκλειστεί πρώτα η πιθανότητα σηπτικής αρθρίτιδας. 5.6 Αδιαφοροποίητη αρθρίτιδα η εισαγωγή της κατηγορίας αυτής είναι το αποτέλεσμα της αδυναμίας των ilar κριτηρίων να ορίσουν ομοιογενείς υποομάδες. Oι ασθενείς που εντάσσονται σε αυτήν την κατηγορία, είναι αυτοί που εξαιρούνται από τις υπόλοιπες υποομάδες, είτε γιατί πληρούν κριτήρια από δύο ή περισσότερες μορφές είτε γιατί ένα κριτήριο αποκλεισμού δεν τους επιτρέπει να ενταχθούν σε κάποια υποομάδα (πίνακας 3). Στον πίνακα 8 περιγράφονται τα κυριότερα χαρακτηριστικά των υποομάδων της NiA 115.
59 59 Πίνακας 8. χαρακτηριστικά των υποομάδων της Νια Υποομάδα Ηλικία Αρθρώσεις Συστηματικές Κυριότερες έναρξης που προσβάλλονται εκδηλώσεις επιπλοκές Oλιγοαρθρίτιδα Πρώιμη μεγάλες αρθρώσεις, μη συμμετρική Oχι χρόνια ιριδοκυκλίτιδα εμμένουσα παιδική ηλικία (γόνατο, αγκώνας, καρπός κφγ, τοπικές διαταραχές ανάπτυξης ΣΣ, αστράγαλος) Oλιγοαρθρίτιδα Πρώιμη παιδική Ίδια με τα παραπάνω, αλλά >4 Oχι τοπικές επεκταθείσα ηλικία προσβεβλημένες αρθρώσεις μετά τους διαταραχές ανάπτυξης πρώτους 6 μήνες Πολυαρθρίτιδα, Σε όλη τη διάρκεια Oποιεσδήποτε, συνήθως καταβολή, δεκατική RF (-) αρνητική της παιδικής ηλικίας συμμετρική προσβολή πυρετική κίνηση Πολυαρθρίτιδα, εφηβεία Oποιεσδήποτε, τυπικά συμμετρική, καταβολή, δεκατική RF (+) θετική προσβολή μικρών αρθρώσεων πυρετική κίνηση Συστηματική Σε όλη τη διάρκεια Oποιεσδήποτε ή Υψηλός πυρετός, εξάνθημα, Oξεία: σύνδρομο της παιδικής ηλικίας καμία πολυορογονίτιδα, ενεργοποίησης των εκσεσημασμένη μακροφάγων. φλεγμονώδης χρόνιες: αμυλοείδωση, απάντηση γενικευμένη διαταραχή της ανάπτυξης Ψωριασική καθυστερημένη ΣΣ, κάτω άκρα, Ψωρίαση αρθρίτιδα παιδική ηλικία άπω φαλαγγοφαλαγγικές αρθρίτιδα καθυστερημένη ΣΣ, ιερολαγόνιες, φλεγμονώδης Oξεία συμπτωματική σχετιζόμενη με παιδική ηλικία κάτω άκρα νόσος του εντέρου ιριδοκυκλίτιδα. ενθεσίτιδα φλεγμονώδης νόσος του εντέρου Από Gare A. and Fasth A. Presentations, clinical features, and special problems in children. In Rheumatology. Hochberg CM, Silman AJ, Smolen JS, Wewinblatt MH, eds.mosby Elsevier 5 th ed.2011:p995.
60 6. Ι Ρ Ι Δ O Κ Υ Κ Λ Ι Τ Ι Δ Α Σύμφωνα με μελέτες βασισμένες σε πληθυσμό ασθενών με Νια, ιριδοκυκλίτιδα προκαλείται στο 3-16% αυτών, με υπεροχή των παιδιών με ολιγοαρθρική μορφή της νόσου 14,113,125,126. Στην πλειονότητα των περιπτώσεων, η ιριδοκυκλίτιδα είναι «σιωπηλή» ή ασυμπτωματική. Προσβάλλονται περισσότερα τα κορίτσια, σε σχέση με τα αγόρια και οι ασθενείς στο 50-80%, έχουν θετικά ανα. είναι ενδιαφέρον ότι σε ορισμένες γεωγραφικές περιοχές, για παράδειγμα στην Costa-Rica, στην ινδία και στη Νότια αφρική, αναφέρονται πολύ λίγες περιπτώσεις ασθενών με ολιγοαρθρίτιδα και θετικά ανα που συνδυάζεται με ιριδοκυκλίτιδα, τονίζοντας, έτσι, τη διαφορά στις εκδηλώσεις της νόσου, ως αποτέλεσμα ανοσογενετικών, περιβαλλοντικών παραγόντων ή συνδυασμού και των δύο. Oι συμπτωματικές, οξείες περιπτώσεις ιριδοκυκλίτιδας συμβαίνουν συχνότερα στα αγόρια και συνδυάζονται, συνήθως, με θετικό hla-b27 και αρθρίτιδα που σχετίζεται με ενθεσίτιδα ,126. O μέσος όρος έναρξης της Νια που σχετίζεται με ιριδοκυκλίτιδα είναι τα 5 χρόνια (εύρος 1-16 χρόνια). τουλάχιστον οι μισοί από τους ασθενείς, εμφανίζουν ιριδοκυκλίτιδα κοντά στην έναρξη της αρθρίτιδας, αν και καθυστερημένες περιπτώσεις προσβολών μπορεί να συμβούν. Στα περισσότερα παιδιά η οφθαλμική νόσος συμβαίνει στα επόμενα 7 χρόνια από την έναρξη της αρθρίτιδας. η ιριδοκυκλίτιδα είναι αμφοτερόπλευρη στο 50-60% των περιπτώσεων 113,126. η εξέταση με σχισμοειδή λυχνία είναι απαραίτητη για την έγκαιρη διάγνωση της οφθαλμικής προσβολής. η πορεία της οφθαλμικής νόσου δεν ακολουθεί την πορεία της αρθρίτιδας και μπορεί να παραμένει και αφού η αρθρίτιδα έχει υφεθεί 113,126,127. Σημαντικές επιπλοκές που προκύπτουν από τη χρόνια ενεργό φλεγμονή και από την παρατεταμένη τοπική χρήση κορτικοειδών είναι οι συνέχειες, ο καταρράκτης και το γλαύκωμα. 60
61 Συμπερασματικά, τονίζεται η σημασία της έγκαιρης διάγνωσης της ιριδοκυκλίτιδας και της επιθετικής θεραπείας που πρέπει να εφαρμόζεται, όταν διαπιστώνεται ενεργός φλεγμονή. ωστόσο, υπάρχουν λίγοι ασθενείς, οι οποίοι δεν απαντούν στην εφαρμοζόμενη εντατική θεραπεία, με αποτέλεσμα να εμφανίζουν σοβαρή απώλεια όρασης. η αμερική Παιδιατρική ακαδημία έχει συστήσει ένα πρόγραμμα για τακτική οφθαλμολογική εξέταση, όπως φαίνεται στον Πίνακα 9. από τη στιγμή που διαγνωσθεί ιριδοκυκλίτιδα, ο παιδοφθαλμίατρος θα καθορίσει τη συχνότητα που θα εκτιμά τον ασθενή, ανάλογα με την απάντηση στη θεραπεία και τις επιπλοκές που πιθανώς θα προκύψουν. εξαιτίας, του σημαντικού αριθμού ασθενών που αναπτύσσουν ιριδοκυκλίτιδα πολύ κοντά μετά τη διάγνωση της αρθρίτιδας, η αρχική οφθαλμολογική εκτίμηση πρέπει να γίνεται μέσα στον πρώτο μήνα από τη διάγνωση της αρθρίτιδας Πίνακας 9. Συχνότητα οφθαλμολογικής εξέτασης σε ασθενείς με Νεανική Ρευματοειδή Αρθρίτιδα (ΝΡΑ). Υποομάδα ΑΝΑ Ηλικία έναρξης Διάρκεια Kατηγορία Συχνότητα της νόσου, έτη νόσου, έτη κινδύνου οφθαλμολογικής εξέτασης, μήνες Oλιγοαρθρίτιδα ή πολυαρθρίτιδα Υψηλή > 4 μέτρια > 7 χαμηλή 12 + > 6 4 μέτρια 6 + > 6 > 4 χαμηλή μέτρια 6-6 >4 χαμηλή 12 - >6 Να χαμηλή 12 Συστηματική νόσος Να Να Να χαμηλή 12 ΑΝΑ= Antinuclear antibodies, αντιπυρηνικά αντισώματα, ΝΑ=Not Applicable Από Cassidy J, Kivlin J, Lindsley C, et al. Ophthalmologic examinations in children with juvenile rheumatoid arthritis. Pediatrics 2006;117:
62 7. Ε Π Ι Π Τ Ω Σ Ε Ι Σ Τ Η Σ Ν Ε Α Ν Ι Κ Η Σ Ι Δ Ι O Π Α Θ O Υ Σ Α Ρ Θ Ρ Ι Τ Ι Δ Α Σ ειδικά προβλήματα απότοκα, κυρίως, της συνεχιζόμενης φλεγμονώδους διαδικασίας και συγκεκριμένα διαταραχές στην ανάπτυξη, οστεοπενία και αμυλοείδωση, είναι δυνατό να παρουσιαστούν στα παιδιά και στους εφήβους που έχουν νοσήσει. αν και οι επιπτώσεις αυτές μπορεί σε μεγάλη έκταση να μετριασθούν με την επιθετική θεραπεία η οποία είναι διαθέσιμη σήμερα, ωστόσο, δεν επιτυγχάνεται πάντα ικανοποιητική απάντηση, με αποτέλεσμα να επηρεάζεται η ποιότητα ζωής και η μακροχρόνια πορεία των ασθενών αυτών. 7.1 Τοπικές διαταραχές ανάπτυξης αποτέλεσμα της φλεγμονής μιας άρθρωσης είναι η παραγωγή κυτταρο - κινών, οι οποίες μέσω ενεργοποίησης των οστεοβλαστών σε τοπικό επίπεδο, προκαλούν κατά μήκος αύξηση των οστών και εφόσον παραμένουν, οδηγούν στην ωρίμανση και στην πρόωρη σύγκλιση των επιφύσεων. ακόμα, ο μυϊκός σπασμός, η καταστροφική υμενίτιδα, που διαβρώνει τις αρθρικές επιφάνειες, καθώς και τα υπεξαρθρήματα επηρεάζουν την τοπική ανάπτυξη 113. η πιο συχνά προσβεβλημένη άρθρωση είναι αυτή του γόνατος, οδηγώντας σε ανισοσκελία, με το μακρύτερο μέλος στην πλευρά της βλάβης, ιδιαίτερα αν η νόσος ξεκινά πριν από την ηλικία των 3 ετών 113. ανισοσκελία μεγαλύτερη των 0.5 εκ. θεωρείται κλινικά σημαντική και επιβάλλεται η χορήγηση υποδηματικού πάτου στο υγιές σκέλος που θα εξισορροπήσει τη διαφορά, προκειμένου να αποφευχθεί λειτουργική σκολίωση. εφόσον η νόσος ελεγχθεί, τα μήκη των δύο σκελών θα εξισωθούν, καθώς το παιδί αναπτύσσεται. Σε αντίθετη περίπτωση, αποτέλεσμα της συνεχιζόμενης ενεργότητας της νόσου στην άρθρωση, είναι η πρόωρη σύγκλιση των επιφύσεων και η μόνιμη πια εγκατάσταση βραχύτερου σκέλους στην πλευρά του προσβεβλημένου γόνατος 111,
63 δεύτερη σε σειρά συχνότητας άρθρωση που εμφανίζει αναπτυξιακές διαταραχές είναι αυτή του καρπού. Σε αντίθεση με το γόνατο, η υπολειμματική ανάπτυξη του καρπού, ενώ είναι εμφανής ακτινολογικά, δε διαπιστώνεται εύκολα στην κλινική πρακτική. Υπεξάρθρημα και σοβαρή παραμόρφωση προκύπτει από διαταραχή στην ανάπτυξη της ωλένης, ενώ διάφορου βαθμού βραχυδακτυλία είναι το αποτέλεσμα της πρόωρης σύγκλισης των επιφύσεων στα δάκτυλα τόσο των χεριών όσο και των ποδιών. Στην πολυαρθρική νόσο (ιδιαίτερα με θετικό ρευματοειδή παράγοντα), ακτινολογικές βλάβες μπορεί να ανιχνευθούν κατά την έναρξη της νόσου, γεγονός που θέτει επιτακτική την ανάγκη για έγκαιρη διάγνωση και έναρξη θεραπείας. το ισχίο παρουσιάζει διαταραχές της ανάπτυξης στο 35% των παιδιών με Νια 113. η εκτίμηση των κροταφογναθικών αρθρώσεων συχνά παραλείπεται, καθώς τα παιδιά παρουσιάζουν δυσκολία στην περιγραφή υποκειμενικών συμπτωμάτων από την συγκεκριμένη περιοχή. Για το λόγο αυτό, είναι σημαντικό να αναγνωρίζονται έγκαιρα κλινικά σημεία απότοκα δυσλειτουργίας της γνάθου, όπως είναι το ελαττωμένο εύρος ανοίγματος του στόματος, ο κριγμός και η περιορισμένη δυνατότητα οριζόντιων κινήσεων της γνάθου. Σε μια μελέτη βασισμένη σε πληθυσμό παιδιών με Νχα, περισσότεροι από το 50% των ασθενών ηλικίας μεγαλύτερης των 7 ετών ανέφεραν συμπτώματα από τις κροταφογναθικές αρθρώσεις. κατά την οδοντιατρική εκτίμηση, 30% του συνόλου των παιδιών είχαν κλινικά σημεία προσβολής των κροταφογναθικών αρθρώσεων και 40% είχαν ακτινολογικές αλλοιώσεις στην αξονική τομογραφία. Στην ίδια μελέτη, στο 20% των παιδιών παρατηρήθηκε πρόσθια ασυμμετρία του προσώπου ή μικρογναθία ή και τα δύο. ετερόπλευρη προσβολή της μιας κροταφογναθικής άρθρωσης οδηγεί σε απόκλιση προς την πλευρά της βλάβης κατά τη διάνοιξη του στόματος. η υποπλασία της γνάθου προκύπτει λόγω της φλεγμονής και καταστροφής της κροταφογναθικής άρθρωσης 113. Προσβολή των κροταφογναθικών αρθρώσεων μπορεί να συμβεί σε όλες τις υποομάδες της Νια: στη συστηματική παρατηρείται σε ποσοστό 67%, στην εμμένουσα ολιγοαρθρίτιδα 39%, στην επεκταθείσα ολιγοαρθρίτιδα 75%, στην πολυαρθρίτιδα με αρνητικό RF 59%, στην πολυαρθρίτιδα με θετικό RF 33%, στην ψωριασική αρθρίτιδα 33% και στην αρθρίτιδα σχετιζόμενη με ενθεσίτιδα 13%. Συστήνεται, επομένως, τακτική παρακολούθηση όλων των παιδιών με Νια από παιδοδοντίατρο ή ορθοδοντικό που θα δίνει τη δυνατότητα για πρώιμη διάγνωση και παρέμβαση 111,113,
64 Γενικευμένη διαταραχή της ανάπτυξης Παρατηρείται σε παιδιά με εμμένουσα ενεργότητα νόσου και σχετίζεται με την ένταση και τη διάρκεια της ενεργότητας. κατά τη διάρκεια περιόδων ύφεσης της νόσου, το ύψος μπορεί να φτάσει σε φυσιολογικά επίπεδα, αρκεί να μην έχει συμβεί σύγκλιση των επιφύσεων. η αιτιολογία της καθυστέρησης της ανάπτυξης σε ύψος και βάρος είναι ασαφής, αλλά, σίγουρο είναι ότι συνδέεται με το επίπεδο της γενικευμένης φλεγμονώδους αντίδρασης. Σε παλαιότερες μελέτες, η πλειονότητα των παιδιών παρουσίαζε καθυστέρηση στην ανάπτυξη, ενώ στις πιο πρόσφατες φαίνεται να επηρεάζεται μόνο το 5-10% των παιδιών, πιθανώς ως αποτέλεσμα του καλύτερου ελέγχου της νόσου. η επιπλοκή αυτή αφορά, κυρίως, παιδιά με συστηματική μορφή ή παιδιά που παρουσιάζουν πολυαρθρική πορεία με μακρά διαστήματα ενεργού νόσου 113. η θεραπεία με κορτικοστεροειδή, επίσης, εμποδίζει την ανάπτυξη του ύψους και είναι πιθανό να συμβεί όταν χορηγούνται δόσεις μεγαλύτερες από 5 mg/m 2 την ημέρα για 6 μήνες ή για περισσότερο. τα επίπεδα της αυξητικής ορμόνης (Growth hormone, Gh) και των ινσουλινόμορφων αυξητικών παραγόντων ι και ιι [insulin Growth Factor i, (igf-i) και insulin Growth Factor ii, (igf-ii)] είναι συνήθως φυσιολογικά, αλλά περιστασιακά μπορεί να βρεθούν ελαττωμένα. τα επίπεδα του igf-i, έχει βρεθεί ότι συσχετίζονται απευθείας με τα επίπεδα της ιl-6 στη συστηματική μορφή της νόσου 113. η απάντηση στην αυξητική ορμόνη είναι μεγαλύτερη όταν αυτή χορηγείται σε περιόδους που η νόσος βρίσκεται σε ύφεση ή όταν δε χρησιμοποιούνται παράλληλα κορτικοστεροειδή 113,129. Oι ενήλικοι ασθενείς με Νια βρέθηκαν να έχουν φυσιολογικό ύψος, βάρος και δείκτη μάζας σώματος (Body Mass, index, BMi), με εξαίρεση τις γυναίκες με συστηματική μορφή νόσου και αυτών που χρησιμοποιούσαν για μεγάλα διαστήματα κορτικοειδή Oστεοπενία η οστεοπενία ή η χαμηλή για την ηλικία οστική μάζα, αναγνωρίζεται σήμερα ως μια από τις σημαντικότερες επιπλοκές της Νια. η μέγιστη οστική μάζα καθορίζεται γενετικά σε συνδυασμό με τη διατροφή, την άσκηση και τις ορμόνες, ειδικά τα οιστρογόνα. τα μακρά διαστήματα ενεργότητας νόσου, η πτωχή δίαιτα σε ασβέστιο και βιταμίνη D, η θεραπεία με κορτικοστεροειδή, η απουσία φυσικής άσκησης και η καθυστερημένη εμμηναρχή, επηρεάζουν συνολικά τη μέγιστη οστική μάζα στα παιδιά με Νια. Περισσότερο επηρεάζεται η οργανική, σε σχέση με την ανόργανη οστική πυκνότητα 113.
65 χαμηλή οστική μάζα έδειξε το 41% των εφήβων με πρώιμης έναρξης Νια ύστερα από διάστημα μεγαλύτερο των 11 ετών και συσχετίσθηκε με τη διάρκεια και τη βαρύτητα της νόσου, τους δείκτες οστικής απορρόφησης, το ύψος και το βάρος 131. Προσφάτως, η θεραπεία με διφωσφονικά, έχει οδηγήσει σε μια αύξηση της οστικής πυκνότητας, όπως αυτή εκτιμάται κατά την οστική μέτρηση με (Dual-Energy X-ray Absorptiometry DEXA), αλλά οι μακροχρόνιες επιδράσεις στο αναπτυσσόμενο οστό, είναι άγνωστες. 7.4 Αμυλοείδωση ασθενείς με εμμένουσα ενεργότητα νόσου που παρουσιάζουν υψηλή τκε, χαμηλή αιμοσφαιρίνη και χαμηλή λευκωματίνη στον ορό, πρέπει να υποβάλλονται σε σπινθηρογράφημα με σεσημασμένο αμυλοειδές P του ορού, η οποία αποτελεί την πιο ευαίσθητη μέθοδο ανίχνευσης των εναποθέσεων του αμυλοειδούς. η επίπτωση της αμυλοείδωσης στη Νια, σύμφωνα με πρόσφατες μελέτες, φαίνεται ότι είναι πτωτική, εξαιτίας ίσως, της επιθετικότερης αντιφλεγμονώδους θεραπείας που χρησιμοποιείται σήμερα 113. Σε παλαιότερες μελέτες, η θνητότητα λόγω αμυλοείδωσης κυμαινόταν από 4% έως 7%, ενώ σε νεότερες είναι συνήθως κοντά στο 0%, με εξαίρεση τη συστηματική μορφή της νόσου 132,133. Σε μια μεγάλη σειρά ασθενών με συστηματική αρθρίτιδα, μεταξύ των 122 ασθενών καταγράφηκαν 2 θάνατοι λόγω αμυλοείδωσης Ποιότητα ζωής των ασθενών με Νεανική Ιδιοπαθή Αρθρίτιδα (NIA) η ποιότητα ζωής του παιδιού με Νια επηρεάζεται σημαντικά από τον πόνο, την κόπωση και τις διαταραχές του ύπνου. O πόνος είναι συχνό σύμπτωμα όλων των ασθενών με αρθρίτιδα. το μυοσκελετικό άλγος, η κεφαλαλγία και το άτυπο κοιλιακό άλγος είναι αυτά που αναφέρονται συχνότερα. τα κορίτσια γενικότερα εκφράζουν δυνατότερο πόνο συγκριτικά με τα αγόρια, τα οποία μπορεί να τον υποεκτιμούν προκειμένου να φανούν θαρραλέα. ωστόσο, πίσω από αυτήν την παραδοχή ίσως υπάρχουν και πραγματικές βιολογικές διαφορές ανάμεσα στα δύο φύλα, καθώς έχει βρεθεί χαμηλότερος ουδός πόνου στα κορίτσια. Όπως και να έχει όμως, δεδομένο είναι ότι ο πόνος προκαλεί καθημερινή αβεβαιότητα, αφού ο ασθενής δεν μπορεί να προβλέψει αν πρόκειται για μια «καλή μέρα» με λίγο πόνο, ή για μια «κακή μέρα» με αφόρητο πόνο. επιπλέον, δημιουργείται 65
66 66 μια αυξημένη εξάρτηση από τους γονείς, σε εποχές που η προοδευτικά κερδισμένη μεγαλύτερη ανεξαρτησία θεωρείται πλέον φυσιολογική 113. το συχνό, καθημερινό άλγος σε συνδυασμό με ψυχολογικές διαταραχές, κυρίως φοβίες και άγχος, ενοχοποιούνται για τις παρατηρούμενες διαταραχές ύπνου στα παιδιά με NiA. O ύπνος είναι πρωταρχικής σημασίας για τη σωματική και την πνευματική ανάπτυξη και οι διαταραχές ύπνου, που ξεκινούν στην παιδική ηλικία, μπορεί να συνεχίζονται και στην ενήλικο ζωή. η διακοπή του ύπνου οδηγεί σε κόπωση και ευερεθιστότητα κατά τη διάρκεια της ημέρας, γεγονός που έχει αντίκτυπο στην κοινωνική ζωή και στη σχολική επίδοση των παιδιών με Νια 113.
67 8. Μ Α Κ Ρ O Χ Ρ O Ν Ι Α Ε Κ Β Α Σ Η Τ Η Σ Ν Ε Α Ν Ι Κ Η Σ Ι Δ Ι O Π Α Θ O Υ Σ Α Ρ Θ Ρ Ι Τ Ι Δ Α Σ η μακροχρόνια έκβαση των χρόνιων νοσημάτων, όπως είναι η Νια αποτελεί σύνθετο φαινόμενο με πολλές διαστάσεις και επιβάλλεται η θεώρησή του από ποικίλες πλευρές. Σύμφωνα με τον Παγκόσμιο Oργανισμό Υγείας (World health Organization, WhO), η υγεία ορίζεται ως «η φυσική, πνευματική και κοινωνική ευεξία». Έτσι, η μελέτη της μακροχρόνιας έκβασης της NiA είναι σκόπιμο να κατευθυνθεί προς δύο ευρύτερα πεδία το πρώτο αφορά στη μελέτη της πορείας και των ανατομικών προβλημάτων που προκύπτουν από την εξέλιξη της νόσου (κλινική ύφεση, αρθρική καταστροφή και οφθαλμική βλάβη) και το δεύτερο οφείλει να εστιάζει σε ειδικούς τομείς που χαρακτηρίζουν τη λειτουργικότητα του ατόμου (σωματική, ψυχοκοινωνική και κοινωνικοοικονομική). ανεξάρτητα ποια διάσταση της έκβασης ερευνάται, οι συγκρίσεις μεταξύ των μελετών είναι δυσχερείς, εξαιτίας διαφόρων παραγόντων. Σε αυτούς περιλαμβάνονται τα διαφορετικά εργαλεία που χρησιμοποιούνται στην εκτίμηση της νόσου, η διαφορετική ταξινόμηση των ασθενών, το αν η ανάλυση περιλαμβάνει όλες τις υποομάδες ή είναι δομημένη βάσει υποτύπου, η διαφορετική προέλευση των ασθενών και τέλος η διαφορετική διάρκεια παρακολούθησης. 8.1 Κλινική ύφεση στη Νεανική Ιδιοπαθή Αρθρίτιδα μια συχνά λανθασμένη άποψη είναι ότι η παιδική αρθρίτιδα θα εξαφανιστεί μετά την ενηλικίωση. κατά την ανασκόπηση, όμως, δεδομένων των τελευταίων 4 δεκαετιών δεν υπάρχουν ενδείξεις ότι πρόκειται συνολικά για μια ήπια νόσο 134,135,136. Στις μελέτες παρακολούθησης ασθενών με Νια που δημοσιεύτηκαν μετά το 1994, το ποσοστό των ασθενών με ανενεργό νόσο ή νόσο σε ύφεση ποικίλλει από 35% έως 60%, φανερώνοντας με τον τρόπο αυτόν ότι περίπου οι μισοί ασθενείς έχουν ενεργό νόσο που συνεχίζεται κατά τη μετάβασή τους στην ενήλικη ζωή (πίνακας 10). 67
68 68 Πίνακας 10. Πρόσφατες μελέτες έκβασης της νεανικής αρθρίτιδας (NIA, ΝΧΑ, ΝΡΑ) με τα αντίστοιχα ποσοστά Ερευνητές (χώρα, έτος) N Μέση Κριτήρια Κριτήρια % των ασθενών διάρκεια κατάταξης ύφεσης σε ύφεση στην νόσου τελευταία τους επίσκεψη Fantini και συν. (ιταλία, 2003) EULAR EULAR 32.8 Minden και συν. (Γερμανία, 2002) ilar ACR 40 Solari και συν. (ιταλία, 2008) ilar Wallace 1.8 Oen και συν. (καναδάς, 2002) ACR EULAR 39 Nordal και συν. (Σκανδιναβία, 2011) ilar Wallace 51.3 Flato και συν. (Νορβηγία, 2003) ACR ACR 50 Bertilsson και συν. (Σουηδία, 2013) EULAR EULAR 40 Susic και συν. (Σερβία, 2011) ilar Wallace 54 Flato και συν. (Νορβηγία, 2009) 144 * ilar Wallace 55 Flato και συν. (Νορβηγία, 2006) 145 ** ilar Wallace 44 NXA= Νεανική Χρόνια Αρθρίτιδα, ΝΡΑ= Νεανική Ρευματοειδής Αρθρίτιδα, ILAR= International League of Associations for Rheumatology, ACR= American College of Rheumatology, EU- LAR=European League Against Rheumatism *μελέτη που συμπεριέλαβε μόνο ασθενείς με ψωριασική αρθρίτιδα ** μελέτη που συμπεριέλαβε μόνο ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα ύφεσης της νόσου στην τελευταία επίσκεψη παρακολούθησης η απουσία, μέχρι προσφάτως, κριτηρίων ύφεσης, που να χρησιμοποιούνται παγκοσμίως από τον ιατρικό κόσμο, κάνει τη σύγκριση των διαφόρων μελετών ιδιαίτερα δύσκολη. Oι περισσότερες μελέτες που αφορούν στην εξέταση ύφεσης χρησιμοποιούν είτε τα ACR είτε τα EULAR κριτήρια ύφεσης. βάσει των ACR κριτηρίων, η παρουσία ύφεσης στηρίζεται σε υποκειμενικές αναφορές, ενώ δε λαμβάνεται υπ όψη η λήψη ή μη φαρμακευτικής αγωγής.
69 Στα κριτήρια αυτά περιλαμβάνονται όλα τα παρακάτω: πρωινή δυσκαμψία μικρότερη των 15 min, απουσία κόπωσης, απουσία αρθρικού πόνου, απουσία ευαίσθητων αρθρώσεων, απουσία διόγκωσης της άρθρωσης ή των ελύτρων των τενόντων και τ.κ.ε μικρότερη από 20 mm/ώρα 146. κατά τα EULAR κριτήρια, η ύφεση ορίζεται ως απουσία ενεργού αρθρίτιδας και/ή εξωαρθρικών εκδηλώσεων χωρίς φαρμακευτική αγωγή για 2 έτη 146. το έτος 2005, οι οργανισμοί PRiNTO (Pediatric Rheumatology international Trials Organization) και PRCSG (Pediatric Rheumatology Collaborative Study Group), συνεργάστηκαν με την CAPRA (Chilhood Arthritis and Rheumatology Research Alliance), προκειμένου να αναπτυχθούν ισχυρά και ενιαία κριτήρια που να ορίζουν τη μη ενεργό νόσο και την κλινική ύφεση για κάθε υποομάδα της Νια 147,148. το πρόγραμμα που οδήγησε στην ανάπτυξη των παραπάνω κριτηρίων ύφεσης, ξεκίνησε το 2002 από την Wallace και συν τα πρώιμα κριτήρια για τη μη ενεργό νόσο και κλινική ύφεση στη Νια παρουσιάζονται στον πίνακα 11. Πίνακας 11. Πρώιμα κριτήρια για μη ενεργό νόσο και κλινική ύφεση σε επιλεγμένες υποομάδες της NIA (ολιγοαρθρίτιδα εμμένουσα και επεκταθείσα, πολυαρθρίτιδα RF(-), πολυαρθρίτιδα RF(+) και συστηματική αρθρίτιδα) Μη ενεργός νόσος απουσία αρθρώσεων με ενεργό αρθρίτιδα απουσία πυρετού, εξανθήματος, ορογονίτιδας, σπληνομεγαλίας ή γενικευμένης λεμφαδενοπάθειας που οφείλεται στη Νια. απουσία ενεργού ιριδοκυκλίτιδας φυσιολογική τιμή τκε ή CRP (αν εξετάζονται και τα δύο, και τα δύο πρέπει να είναι φυσιολογικά) απουσία ενεργότητας νόσου, σύμφωνα με τη γενική εκτίμηση του ιατρού. Κλινική ύφεση δύο τύποι κλινικής ύφεσης προτείνονται. κλινική ύφεση με φαρμακευτική θεραπεία. Όλα τα κριτήρια για μη ενεργό νόσο θα πρέπει να πληρούνται για τουλάχιστον για 6 συνεχόμενους μήνες εφόσον ο ασθενής λαμβάνει φαρμακευτική αγωγή, έτσι ώστε να θεωρείται ότι ο ασθενής είναι σε κατάσταση κλινικής ύφεσης με φαρμακευτική θεραπεία. κλινική ύφεση χωρίς φαρμακευτική θεραπεία. Όλα τα κριτήρια για μη ενεργό νόσο θα πρέπει να πληρούνται για τουλάχιστον για 12 συνεχόμενους μήνες, εφόσον ο ασθενής δε λαμβάνει φαρμακευτική αγωγή (είτε για αρθρίτιδα είτε για ιριδοκυκλίτιδα), ώστε να θεωρείται ότι ο ασθενής είναι σε κατάσταση κλινικής ύφεσης χωρίς φαρμακευτική θεραπεία. RF = Rheumatoid Factor, NIA = Νεανική Ιδιοπαθής Αρθρίτιδα, ΤΚΕ = Ταχύτητα Καθίζησης Ερυθρών, CRP = C-Reactive Protein 69
70 70 η πρώτη μελέτη που χρησιμοποίησε τα παραπάνω κριτήρια κλινικής ύφεσης, ήταν αυτή των Wallace και συν O σχεδιασμός της συγκεκριμένης μελέτης διέφερε, καθώς στόχευε στη διερεύνηση του συνολικού διαστήματος που περνούσαν οι ασθενείς με ενεργό ή μη ενεργό νόσο κατά τη διάρκεια της περιόδου παρακολούθησης. Σε προηγούμενες αναλύσεις διερευνάται το ποσοστό ύφεσης σε κάποια συγκεκριμένη χρονική στιγμή, που συνήθως επιλέγεται να είναι η τελευταία επίσκεψη του διαστήματος παρακολούθησης ή η πρώτη επίσκεψη μετά την ενηλικίωση. Oι παραπάνω ερευνητές βρήκαν ότι σε 434 ασθενείς με Νια, μόνο το 25% από τα 878 επεισόδια μη ενεργού νόσου κατέληξαν σε κλινική ύφεση χωρίς φαρμακευτική αγωγή κατά τη διάρκεια περιόδου παρακολούθησης τεσσάρων τουλάχιστον ετών. Σε αντιστοιχία με τις προηγούμενες μελέτες, τα παιδιά με εμμένουσα ολιγοαρθρίτιδα διέτρεχαν σχετικά μεγαλύτερο διάστημα σε κατάσταση κλινικής ύφεσης, ενώ το διάστημα αυτό βρέθηκε να είναι μικρότερο στα παιδιά με οροθετική πολυαρθρίτιδα. Σε μια άλλη μελέτη, οι Lurati και συν. χρησιμοποίησαν τα νέα κριτήρια ύφεσης σε 761 ασθενείς με Νια που παρακολουθούνταν από το 1970 και εξήγαγαν τα παρακάτω συμπεράσματα: συνολικά 247 (32,46%) ασθενείς, κατά τη διάρκεια της περιόδου παρακολούθησης, πέτυχαν κλινική ύφεση χωρίς θεραπεία. από αυτούς 42,9% αφορούσε στην εμμένουσα ολιγοαρθρίτιδα, 13,1% στην επεκταθείσα ολιγοαρθρίτιδα, 22,4% στην οροαρνητική πολυαρθρίτιδα, 0% στην οροθετική πολυαρθρίτιδα, 33,7 στη συστηματική αρθρίτιδα και 33,4% στο συνδυασμό αρθρίτιδας σχετιζόμενης με ενθεσίτιδα και ψωριασικής αρθρίτιδας. Στην παραπάνω μελέτη σημειώνεται ότι η εξελικτική πορεία της Νια δεν είναι ικανοποιητική, αφού μόνο το 1/3 των ασθενών πέτυχε ύφεση χωρίς φαρμακευτική αγωγή κατά τη διάρκεια 4 δεκαετιών 150. μέχρι σήμερα, τα κριτήρια για μη ενεργό νόσο και κλινική ύφεση της Wallace και συν. χρησιμοποιούνται ευρέως και αναφέρονται σε περισσότερες από 80 δημοσιεύσεις 133,140,143,151. ωστόσο, δεν έχουν σταθμιστεί ακόμη για τους ασθενείς με ψωριασική αρθρίτιδα, με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και για αυτούς με μεμονωμένη ιριδοκυκλίτιδα. Πολύ πρόσφατα, στα παραπάνω κριτήρια πραγματοποιήθηκαν από τους ίδιους ερευνητές τρεις νέες τροποποιήσεις. η πρώτη αφορούσε στον ορισμό της ιριδοκυκλίτιδας, η δεύτερη στον ορισμό της μη φυσιολογικής τκε και η τρίτη ήταν η προσθήκη της πρωινής δυσκαμψίας (πίνακας 12) 152. Στη δημοσίευση που περιλάμβανε τις παραπάνω τροποποιήσεις, γίνεται λόγος, επίσης, ότι είναι προτιμότερο να χρησιμοποιείται ο όρος «κλινικά μη ενεργός νόσος» καθώς τα συγκεκριμένα κριτήρια δεν έχει αποδειχθεί ότι ορίζουν και τη βιολογικά ανενεργό νόσο 152. η διαθεσιμότητα των παραπάνω σταθμισμένων,
71 σε επιλεγμένες κατηγορίες της Νια και διεθνώς συμφωνημένων, κριτηρίων ύφεσης της Νια δίνει τη δυνατότητα στους ρευματολόγους να χρησιμοποιούν το ίδιο λεξιλόγιο, προκειμένου να περιγράψουν την ίδια κλινική κατάσταση. θα ήταν παράλειψη να μην γίνει αναφορά στα εργαλεία που μετρούν τη δραστηριότητα της νόσου με τη μορφή συνεχούς μεταβλητής και χρησιμοποιούνται στην κλινική πράξη για την εκτίμηση των ενήλικων ασθενών με Νια. Oι συνεχείς μεταβλητές δίνουν τη δυνατότητα σε κάποιον να έχει στα χέρια του μια «απόλυτη» τιμή της δραστηριότητας της νόσου σε μία δεδομένη χρονική στιγμή ή με τον καθορισμό συγκεκριμένου εύρους ορίων- να μπορεί να ορίσει την παρούσα κατάσταση της ενεργότητας της νόσου, όπως για παράδειγμα ύφεση. μεταξύ των σύνθετων αυτών εργαλείων, τα πλέον ευρέως χρησιμοποιούμενα είναι το DAS (Disease Activity Score) 153, το DAS28 (Disease Activity Score 28) 154, το SDAi (Simplified Disease Activity index) 155 και το CDAi (Clinical Disease Activity index) 156. Για τον υπολογισμό των DAS και DAS28 χρειάζεται αριθμομηχανή, ενώ η χρήση της δεν είναι απαραίτητη για τα υπόλοιπα δύο. Σε μελέτες μακροχρόνιας έκβασης της νόσου που δημοσιεύτηκαν τα τελευταία 10 χρόνια, η εκατοστιαία αναλογία των ασθενών που βρέθηκαν σε κλινική ύφεση κατά την τελευταία εξέτασή τους, ποικίλλει από 0% έως 50% για τη συστηματική αρθρίτιδα, 50%-80% για την εμμένουσα ολιγοαρθρίτιδα, 12-35% για την επεκταθείσα ολιγοαρθρίτιδα, 23%-46% για την πολυαρθρίτιδα με αρνητικό RF, 0%-15% για την πολυαρθρίτιδα με θετικό RF, 30-40% για τη ψωριασική αρθρίτιδα και 0%-30% για την αρθρίτιδα που σχετίζεται με ενθεσίτιδα 134,138,139,141,144,145,157. τα παραπάνω ευρήματα δηλώνουν ότι κλινική ύφεση πετυχαίνουν συχνότερα οι ασθενείς με εμμένουσα ολιγοαρθρίτιδα και σπανιότερα οι ασθενείς με οροθετική πολυαρθρίτιδα. τα ποσοστά ύφεσης στη συστηματική αρθρίτιδα ποικίλλουν ευρέως αντανακλώντας πιθανώς την αδιαμφισβήτητη ετερογένεια της υποομάδας αυτής 146,157,158. χρησιμοποιώντας καμπύλες επιβίωσης, η πιθανότητα ύφεσης 10 έτη μετά την έναρξη της νόσου εκτιμάται περίπου στο 30%-35% συνολικά, αλλά κυμαίνεται ευρέως μεταξύ των διαφόρων υποομάδων. Συγκεκριμένα, η πιθανότητα ύφεσης είναι μεγαλύτερη στην ολιγοαρθρίτιδα, σε ποσοστό περίπου 50% και μικρότερη στην πολυαρθρίτιδα με θετικό RF σε ποσοστό που αγγίζει μόλις το 5%. η πιθανότητα επίτευξης ύφεσης μειώνεται προοδευτικά μετά τα 10 έτη και μετά από αυτό το διάστημα, πιθανότατα να μη συμβεί ποτέ 159. Στις παραπάνω μελέτες, υποστηρίζεται, τελικά, ότι η Νια δεν είναι μια νόσος ήπια, ότι συχνά επιμένει και συνεχίζεται και μετά την ενηλικίωση. 71
72 72 Πίνακας 12. Kριτήρια για μη ενεργό κλινικά νόσο σε επιλεγμένες υποομάδες της NIA (ολιγοαρθρίτιδα εμμένουσα και επεκταθείσα, πολυαρθρίτιδα RF (-), πολυαρθρίτιδα RF (+) και συστηματική αρθρίτιδα Μη ενεργός νόσος απουσία αρθρώσεων με ενεργό αρθρίτιδα απουσία πυρετού, εξανθήματος, ορογονίτιδας, σπληνομεγαλίας ή γενικευμένης λεμφαδενοπάθειας που οφείλεται στη Νια. απουσία ενεργού ιριδοκυκλίτιδας, όπως ορίστηκε από την ομάδα εργασίας SUN*. φυσιολογική τιμή τκε. ή CRP (αν εξετάζονται και τα δύο, και τα δύο πρέπει να είναι φυσιολογικά). απουσία ενεργότητας νόσου, σύμφωνα με τη γενική εκτίμηση του ιατρού. διάρκεια πρωινής δυσκαμψίας 15 λεπτά. RF= Rheumatoid Factor, NIA= Νεανική Ιδιοπαθής Αρθρίτιδα, ΤΚΕ= Ταχύτητα Καθίζησης Ερυθρών, CRP=C-Reactive Protein *Η ομάδα εργασίας για την τυποποίηση της ονοματολογίας της ιριδοκυκλίτιδας (Standardization of Uveitis Nomenclature, SUN) ορίζει την μη ενεργό πρόσθια ιριδοκυκλίτιδα ως «βαθμό 0 κύττα - ρα», που σημαίνει < 1 κύτταρο ανά οπτικό πεδίο του 1mm, με χρήση 1 mm-σχισμοειδούς λυχνίας. 8.2 Αρθρική και εξωαρθρική καταστροφή Σημαντικός παράγοντας που αξιολογείται στις μελέτες μακροχρόνιας έκβασης των ασθενών με Νια είναι η παρουσία ή όχι μόνιμης δομικής βλάβης, όπως αυτή εκτιμάται με το JADi-A και το JADi-E, τον ακτινολογικό έλεγχο και την ανάγκη διενέργειας χειρουργικών επεμβάσεων στις αρθρώσεις που έχουν καταστραφεί. ιδιαίτερη αναφορά γίνεται συχνά στην παρουσία μικρογναθίας ή ασυμμετρίας της γνάθου καθώς και σε γενικευμένες διαταραχές στην ανάπτυξη, όπως είναι το τελικό ύψος Ποσοτική εκτίμηση αρθρικής και εξωαρθρικής καταστροφής (Juvenile Arthritis Damage Index, JADI) O δείκτης JADi, αναπτύχθηκε το 2005 από τους Viola και συν. με σκοπό τη διάθεση ενός κλινικού εργαλείου, το οποίο θα μετρά την αρθρική και εξωαρθρική καταστροφή στους ασθενείς με Νια 160. O δείκτης JADi προκύπτει από τη φυσική εξέταση και από μια σύντομη ανασκόπηση του κλινικού ιστορικού του ασθενούς και αποτελείται από 2 μέρη: την εκτίμηση της αρθρικής καταστροφής (JADi-α) και την εκτίμηση της εξωαρθρικής καταστροφής (JADi-E). με τον JADi-A καταγράφονται οι μόνιμες βλάβες σε 36 αρθρώσεις ή ομάδες αρθρώσεων με μέγιστο συνολικό σκορ το 72. Oι αρθρώσεις πρέπει να είναι στην ίδια κατάσταση τουλάχιστον τους τελευταίους 6 μήνες,
73 ανεξαρτήτως φαρμακευτικής αγωγής ή φυσικοθεραπείας. Λόγω του ότι ο δείκτης δεν αξιολογεί την ενεργότητα της νόσου, αλλά το αποτέλεσμα προηγουμένων επεισοδίων φλεγμονής των αρθρώσεων, τείνει να αυξάνεται με την πάροδο του χρόνου ή έστω να παραμένει σταθερός. με το δείκτη JADi-E αξιολογούνται οι εξωαρθρικές βλάβες, οι οποίες ορίζονται ως εμμένουσες αλλαγές στην ανατομία, παθολογοανατομία, φυσιολογία ή λειτουργία των οργάνων στόχων. Oι αλλοιώσεις οφείλουν να έχουν συμβεί μετά την έναρξη της νόσου, να είναι απότοκες προηγούμενης ενεργότητας της νόσου ή της θεραπείας της και να είναι παρούσες για τουλάχιστον 6 μήνες. εκτιμώνται 13 παράμετροι που κατανέμονται σε 5 όργανα/συστήματα. το μέγιστο συνολικό σκορ για τις εξωαρθρικές εκδηλώσεις είναι το 17. Στη μελέτη των Solari και συν. χρησιμοποιώντας το δείκτη JADi αναδείχθηκε καταστροφή σε 1 άρθρωση ή ομάδα αρθρώσεων σε 34.2% των ασθενών, ενώ σε 26.1% των ασθενών παρουσιάστηκαν εξωαρθρικές αλλοιώσεις, μετά από μέση διάρκεια νόσου 6.7 έτη 133. Σε μια προοπτική μελέτη των Susic και συν. μετά από μέση διάρκεια νόσου 5.2 έτη, βρέθηκε ότι, τόσο τα σκορ JADi-A και JADi-E, όσο και οι ακτινολογικές αλλοιώσεις χειροτέρευαν με το πέρασμα του χρόνου, σε αντίθεση με τη λειτουργική ικανότητα των ίδιων ασθενών 143. Oι Nordal και συν. βρήκαν ότι το υψηλότερο JADi σκορ παρατηρήθηκε στους ασθενείς με πολυαρθρική RF-αρνητική και σε αυτούς με συστηματική μορφή της νόσου 140. Σε όλες τις μελέτες, ο δείκτης JADi-A εμφανίζει καλή συσχέτιση με τους ακτινολογικούς δείκτες βλάβης των αρθρώσεων Ακτινολογικές βλάβες των αρθρώσεων Στις βλάβες των αρθρώσεων, που μπορεί να διαπιστωθούν με τον ακτινολογικό έλεγχο, περιλαμβάνονται οι διαβρώσεις, η στένωση του μεσάρθριου διαστήματος, η περιαρθρική οστεοπενία και η παρουσία υπεξαρθρήματος ή αγκύλωσης. μέχρι πρόσφατα δεν υπήρχε κάποια σταθμισμένη και εδραιωμένη ακτινολογική μέθοδος, που να μπορεί να ποσοτικοποιήσει τις παρατηρούμενες αλλοιώσεις στο παιδιατρικό πληθυσμό. ωστόσο, κάποιοι ερευνητές επιχείρησαν μια τέτοιου είδους προσέγγιση. Συγκεκριμένα, οι Oen και συν. βρήκαν σημαντικές ακτινολογικές αλλοιώσεις σε όλες τις μορφές της ΝΡα. αναλυτικότερα, διαβρώσεις διαπιστώθηκαν στο 63%, 39%, 75% και 25%, ενώ στένωση του μεσάρθριου διαστήματος στο 38%, 43%,79% και 14% των ασθενών με συστηματική, πολυαρθρική με αρνητικό RF, πολυαρθρική με θετικό RF και ολιγοαρθρική μορφή της νόσου αντιστοίχως, με μέσο όρο 8 έτη 73
74 74 από την έναρξη της νόσου 161. h μελέτη των Boyer και συν. ανέδειξε παρόμοια αποτελέσματα 162. Στη μελέτη τους, οι Flato και συν. διαπίστωσαν ένα συνολικό ποσοστό διαβρώσεων της τάξης του 24%, το οποίο είναι σαφώς μικρότερο από αυτό που βρέθηκε στις άλλες μελέτες, παρά το γεγονός ότι η διάρκεια της νόσου υπήρξε μεγαλύτερη 141. αυτό είναι ίσως αποτέλεσμα του μικρότερου μεγέθους του δείγματος και του λιγότερο ακριβούς ορισμού της βλάβης στην τελευταία μελέτη. Υπάρχει σχετικά μικρός αριθμός μελετών που έχουν συσχετίσει την ακτινολογική βλάβη των αρθρώσεων με συγκεκριμένα χαρακτηριστικά της νόσου. Oι Al Matar και συν. βρήκαν ότι η συμμετρική νόσος και η προσβολή των καρπών και/ή των ποδοκνημικών αρθρώσεων ήταν προγνωστικός παράγοντας διαβρωτικής νόσου στην ολιγοαρθρικής-έναρξης μορφής της νόσου 163. Στη μελέτη των Oen και συν. η ανάπτυξη διαβρώσεων και στένωσης του μεσάρθριου διαστήματος συσχετίστηκε με μεγαλύτερη διάρκεια ενεργού νόσου καθώς και με την υποομάδα με συστηματική και πολυαρθρική (ανεξαρτήτως RF) έναρξη. επιπλέον, η στένωση του μεσάρθριου διαστήματος συσχετίστηκε θετικά με το βαθμό της λειτουργικής ανικανότητας 161,164. η ανάπτυξη διαβρώσεων βρέθηκε να συσχετίζεται με πρώιμη έναρξη, μεγάλο αριθμό συνολικά προσβεβλημένων αρθρώσεων, θετικό RF, μακρά διάρκεια υψηλής τκε και παρουσία συμμετρικής αρθρίτιδας στη μελέτη των Flato και συν. Στην ίδια μελέτη ο κίνδυνος ανάπτυξης διαβρώσεων ήταν αυξημένος στους ασθενείς με απουσία του DPB1*02 και παρουσία του συνδυασμού DRB1*08 και hla B Σε μια άλλη ιταλική μελέτη, το Pozanski score συσχετίστηκε ισχυρά με τον αριθμό των αρθρώσεων με περιορισμένο εύρος κίνησης σε ασθενείς με διάρκεια νόσου 10 έτη 165. Σε όλες τις παραπάνω μελέτες προκύπτει ότι η παρουσία ακτινολογικών βλαβών συσχετίζεται ισχυρά με τη σωματική λειτουργικότητα των ασθενών, όπως αυτή μετράται με το ChAQ ( ή το haq) ή με την κλίμακα Steinbrocker. το Sharp score υπήρξε το πρώτο εργαλείο που περιλάμβανε ξεχωριστό αθροιστικό αποτέλεσμα για τις διαβρώσεις και για τη στένωση του μεσάρθριου διαστήματος, ως αντανάκλαση της καταστροφής του οστού και του χόνδρου αντιστοίχως, κάτι που μπορεί να παράγει ανεξάρτητες πληροφορίες 166. η τροποποίησή του από τη van der heijde (το modified Sharp/van der heijde score) χρησιμοποιείται ευρέως στους ενήλικες ασθενείς με Ρευματοειδή αρθρίτιδα 167. Προσφάτως, το Sharp/van der heijde score έχει σταθμιστεί και στον παιδιατρικό πληθυσμό και μπορεί πλέον να χρησιμοποιηθεί, με ορισμένες τροποποιήσεις, για την εκτίμηση της ακτινολογικής εξέλιξης, στα παιδιά με Νια που έχουν αναπτύξει πολυαρθρική πορεία 168,169. εκτός από τις 2 δη-
75 μοσιεύσεις των ερευνητών που συμμετείχαν στη στάθμιση του Sharp/van der heijde score στα παιδιά, μοναδική, επί του παρόντος, εργασία στην οποία έχει χρησιμοποιηθεί το παραπάνω σκορ σε ασθενείς με Νια, είναι αυτή των Omar και συν., οι οποίοι βρήκαν ότι η μέση συνολική τιμή του τροποποιημένου Sharp/van der heijde score είναι σημαντικά υψηλότερη στους ασθενείς με πολυαρθική νόσο και θετικά anti-ccp αντισώματα Διαταραχές ανάπτυξης Σαφώς αναγνωρισμένες τοπικές διαταραχές της ανάπτυξης αποτελούν η ανισοσκελία, η μικρογναθία ή ασυμμετρία της γνάθου και η βράχυνση δακτύλων χεριών και ποδιών. Σε μελέτη των Minden και συν. ανισοσκελία (κατά μέσο όρο 1 cm) παρατηρήθηκε σε 52 ασθενείς (24%), από τους οποίους το 1/3 περίπου χρησιμοποιούσαν ειδικούς πάτους υποδημάτων 138. Oι Packham και συν. βρήκαν στη δική τους μελέτη ποσοστό ασθενών 11.3% με διαφορά μέλους και έδειξαν ότι στους ενήλικες με Νια, ο κύριος αιτιολογικός παράγοντας αυτής της διαταραχής ήταν η προηγούμενη χειρουργική επέμβαση 171. η μικρογναθία ήταν η δεύτερη συχνότερη διαταραχή της ανάπτυξης στη μελέτη των Minden και συν., παρατηρούμενη σε ποσοστό 9.5% όλων των ασθενών 138. μικρογναθία (άνοιγμα στόματος μικρότερο από 3 cm) σε ιδιαίτερα υψηλό ποσοστό, που ανήλθε στο 40,2%, παρατηρήθηκε στη μελέτη των Packham και συν. με τους ασθενείς της συστηματικής μορφής να προσβάλλονται συχνότερα (53.8%) 171. η καθυστέρηση ανάπτυξης σε ύψος προκαλείται δευτεροπαθώς, εξαιτίας των παρατεταμένων διαστημάτων ενεργότητας της νόσου σε συνδυασμό με τις μακρές περιόδους χρήσης κορτικοειδών. Για το λόγο αυτό, είναι πιθανότερο να εντοπιστεί στους ασθενείς με συστηματική και πολυαρθρική μορφή. η ανάπτυξη σε ύψος βρέθηκε να υπολείπεται στους ασθενείς της μελέτης των Packham και συν., όταν συγκρίθηκε με αυτήν που παρατηρείται στον υγιή πληθυσμό. επιπλέον, υπήρξε σημαντική αρνητική συσχέτιση μεταξύ του τελικού ύψους και της διάρκειας θεραπείας με στεροειδή από του στόματος. επιπρόσθετες μελέτες, αναφέρουν χαμηλό ανάστημα σε 1%-17% των ενηλίκων ασθενών με Νια (το τελικό ύψος εκφράζεται ως standard deviation score, SDS ή ως % ποσοστό υπολογισμένο βάσει των δεδομένων που υπάρχουν για το ύψος στο γενικό πληθυσμό) 135,138,171. Σε γερμανική μελέτη, παρά το γεγονός ότι το τελικό ύψος, γυναικών και ανδρών ηλικίας 18 ετών με Νια, δε διέφερε από αυτό της ομάδας αναφοράς, ωστόσο η κατανομή του ύψους στους ασθενείς με Νια ήταν σαφώς διαφορετική
76 Χειρουργική αποκατάσταση η Νια προκαλεί αρθρική καταστροφή σε βαθμό που σε αρκετές περιπτώσεις απαιτείται χειρουργική παρέμβαση, συχνά σε νεαρή ηλικία. Oι κυριότερες χειρουργικές επεμβάσεις που σχετίζονται με τη νεανική αρθρίτιδα περιλαμβάνουν τις παρακάτω: ολική αρθροπλαστική ισχίου, εκτομή κεφαλής μηριαίου, ολική αρθροπλαστική γόνατος, διορθωτική επέμβαση της γνάθου, αρθρόδεση κερκιδοκαρπικής άρθρωσης και αρθρόδεση των αρθρώσεων των άκρων ποδών. η ανάγκη αρθροπλαστικής καταγράφηκε στο 7% των ασθενών στη μελέτη των Oen και συν., αφορούσε δε κυρίως στην άρθρωση του ισχίου και του γόνατος. Στην ίδια μελέτη, σε αρθροπλαστική οδηγούνταν συχνότερα οι ασθενείς με πολυαρθική RF (+) (23%) και ακολούθως οι ασθενείς με συστηματικής έναρξης (17%) νόσο 139. ιδιαίτερα υψηλή βρέθηκε η συχνότητα αντικατάστασης μιας άρθρωσης με προσθετική, στη μελέτη των Packman και συν. αφού από τη συνολική ομάδα των παιδιών με Νια που συμπεριλήφθηκαν στη μελέτη, το 51.2% είχαν υποβληθεί σε τουλάχιστον μια αντικατάσταση άρθρωσης ύστερα, όμως, από σαφώς μακρότερη διάρκεια νόσου συγκριτικά με την προηγούμενη μελέτη. η άρθρωση του ισχίου, ήταν η θέση, η οποία απαιτούσε πιο συχνά ορθοπεδική παρέμβαση και ακολουθούσε η άρθρωση του γόνατος. O κίνδυνος αντικατάστασης μιας άρθρωσης βρέθηκε ιδιαίτερα αυξημένος στη συστηματική μορφή της νόσου, συγκριτικά με τις υπόλοιπες υποομάδες (p<0.001). Άλλοι παράγοντες που συσχετίστηκαν στατιστικώς σημαντικά με τον παραπάνω κίνδυνο ήταν η διάρκεια και η εμμένουσα ενεργότητα νόσου (p<0.001). Oι ασθενείς με ολιγοαρθρίτιδα και ψωριασική αρθρίτιδα οδηγούνταν σε αντικατάσταση μιας άρθρωσης λιγότερο συχνά 171. ωστόσο, στη μελέτη των Zak και Pedersen, στην οποία οι ασθενείς είχαν παρόμοια διάρκεια νόσου με αυτήν των Packham και συν., το ποσοστό αυτών που υποβλήθηκαν σε χειρουργική επέμβαση στις κατεστραμμένες αρθρώσεις, βρέθηκε εμφανώς μικρότερο, αγγίζοντας μόνο το 22% 172. τέλος, σε μια αναδρομική συγκριτική μελέτη, φάνηκε ότι η επιβίωση της προσθετικής άρθρωσης του ισχίου ήταν σημαντικά πτωχότερη (p=0.001) στους ασθενείς με μακροχρόνια χρήση κορτικοειδών και σημαντικά καλύτερη (p=0.02) στους ασθενείς που ελάμβαναν μεθοτρεξάτη Oφθαλμική βλάβη η αναζήτηση οφθαλμικής βλάβης είναι επιβεβλημένη στα πλαίσια μελέτης της μακροχρόνιας έκβασης των ασθενών με Νια. η πορεία είναι χειρότερη στους ασθενείς, στους οποίους η ιριδοκυκλίτιδα συμβαίνει πριν ή
77 κατά την έναρξη της αρθρίτιδας, σε αυτούς που είχαν σοβαρή νόσο κατά τη διάγνωση και σε αυτούς που έχουν συνεχιζόμενη ενεργό φλεγμονή. Περίπου 13% των ασθενών αναπτύσσουν ιριδοκυκλίτιδα και το 1/3 από αυτούς αναμένεται να έχει σοβαρή απώλεια όρασης από τις επιπλοκές της. επιπλοκές της συνεχιζόμενης φλεγμονώδους διαδικασίας καθώς και της τοπικής χρήσης κορτικοειδών είναι οι συνέχειες, ο καταρράκτης και το γλαύκωμα. η έγκαιρη εξέταση και η επιθετική θεραπεία φαίνεται να έχουν βελτιώσει σημαντικά την πρόγνωση της ιριδοκυκλίτιδας. Παλαιότερες μελέτες από οφθαλμολογικές κλινικές, όπου βέβαια παρακολουθούνταν οι πιο σοβαρές περιπτώσεις, ανέφεραν ποσοστό 30-40% τύφλωσης, σε έδαφος ιριδοκυκλίτιδας που σχετίζονταν με τη νεανική ρευματοειδή αρθρίτιδα. ευτυχώς, σήμερα τύφλωση παρατηρείται σπανίως (< 1%) 174. Σε μια μεγάλη αναδρομική μελέτη των Saurenmann και συν. βρέθηκε ότι από τους 1081 ασθενείς με Νια, οι 142 (13.1%) είχαν αναπτύξει ιριδοκυκλίτιδα στην πορεία της νόσου. ως παράγοντες κινδύνου, αναγνωρίσθηκαν η νεαρή ηλικία κατά τη διάγνωση, το θήλυ φύλο, τα θετικά ανα και η υποομάδα έναρξης της νόσου. επιπλοκές της ιριδοκυκλίτιδας εμφανίστηκαν σε 53 ασθενείς (37.3%), και μόνο σε 13% των προσβεβλημένων ασθενών εντοπίστηκε μέγιστη διορθωμένη οπτική οξύτητα μικρότερη των 20/40. Oι ασθενείς με ολιγοαρθρική μορφή εμφάνισαν το υψηλότερο ποσοστό ιριδοκυκλίτιδας (20.9%), ακολουθούμενοι από τους ασθενείς με πολυαρθρίτιδα RF-αρνητική (14%). το χαμηλότερο ποσοστό παρατηρήθηκε στη συστηματική (<1%) και πολυαρθρική με θετικό RF. O καταρράκτης υπήρξε η συχνότερη επιπλοκή της ιριδοκυκλίτιδας (23.2%) και ακολουθούσαν οι συνέχειες (21.8%) και το γλαύκωμα (15.5%) 35. Στη μελέτη των Packham και συν. το 22% των παιδιών εμφάνισαν ιριδοκυκλίτιδα, κάποια στιγμή κατά την πορεία της νόσου τους. η προσβολή ιριδοκυκλίτιδας ήταν συχνότερη στην εμμένουσα ολιγοαρθρική (p<0.05) και στην επεκταθείσα ολιγοαρθρική μορφή (p<0.001) και λιγότερο συχνή στη συστηματική και την οροθετική πολυαρθρική (p<0.005) μορφή της νόσου. το γλαύκωμα ήταν σχετικά ασύνηθες προσβάλλοντας μόνο το 4.1% των ασθενών. βρέθηκε μόνο στους ασθενείς με προηγούμενη προσβολή ιριδοκυκλίτιδας και ήταν συχνότερο σε αυτούς με επεκταθείσα ολιγοαρθρίτιδα και ιριδοκυκλίτιδα και μάλιστα σε ποσοστό 31.8% των ασθενών αυτής της υποομάδας. το γλαύκωμα δε συσχετίστηκε με την ιριδοκυκλίτιδα, η οποία εμφανίζεται στα πλαίσια αρθρίτιδας σχετιζόμενης με ενθεσίτιδα ή ψωριασικής αρθρίτιδας, παρά το γεγονός ότι σε αυτήν την υποομάδα η ιριδοκυκλίτιδα βρέθηκε να προσβάλλει 26.6% των ασθενών. Tο ποσοστό του καταρράκτη ήταν 77
78 % και το αντίστοιχο ποσοστό των παιδιών που χρειάστηκαν χειρουργική οφθαλμολογική επέμβαση ήταν 10.6%. και οι δύο καταστάσεις εμφανίσθηκαν πιο συχνά στην ομάδα των ασθενών με επεκταθείσα ολιγοαρθρίτιδα. Στη συστηματική μορφή, όλες οι περιπτώσεις καταρράκτη παρατηρήθηκαν σε ασθενείς, με προηγούμενη χρήση στεροειδών. η υποομάδα της αρθρίτιδας που σχετίζεται με ενθεσίτιδα, παρουσίασε στατιστικώς σημαντικά χαμηλότερη επίπτωση καταρράκτη, συγκρινόμενη με τις υπόλοιπες ομάδες. η ιριδοκυκλίτιδα συσχετίσθηκε με την παρουσία θετικών ανα στους ασθενείς με επεκταθείσα ολιγοαρθρίτιδα (90.5%, p<0.001) και οροαρνητική πολυαρθρίτιδα (30%, p<0.05) 171. Σε άλλη μελέτη, το ποσοστό ιριδοκυκλίτιδας βρέθηκε παρόμοιο μεταξύ των ασθενών με εμμένουσα και επεκταθείσα ολιγοαρθρίτιδα, με συνολικό κίνδυνο 30% στα 4 πρώτα χρόνια της νόσου Λειτουργική ικανότητα Σωματική ικανότητα (Physical Αbility). Ερωτηματολόγιο εκτίμησης της υγείας (Health Assessment Questionnaire- Disability Index, HAQ-DI) η σωματική ικανότητα των ασθενών με Νια, δηλαδή η δυνατότητα ή όχι, για απλές καθημερινές δραστηριότητες, φαίνεται ότι έχει βελτιωθεί σημαντικά τις τελευταίες δεκαετίες. Σε μελέτες που δημοσιεύτηκαν πριν το 1980, το ποσοστό των ασθενών που ταξινομήθηκαν στην τάξη Steinbrocker ιιι ή iv ήταν 30%-55%, ενώ το αντίστοιχο ποσοστό σε μελέτες μετά το 1990, ήταν 5%-15% 134. Σε πρόσφατη ιταλική μελέτη, το ποσοστό αυτό, βρέθηκε ακόμη μικρότερο, της τάξης του 3.6% 133. Στις νεότερες μελέτες μακροχρόνιας έκβασης χρησιμοποιείται, ευρέως, εκτός από τη λειτουργική τάξη κατά Steinbrocker, ένας πιο ευαίσθητος δείκτης, που μετρά τη σωματική λειτουργική ικανότητα των ενηλίκων με Νια, ο δείκτης haq-di. (health Assessment Questionnaire-Disability index ή ερωτηματολόγιο εκτίμησης της υγείας-δείκτης Σωματικής ανικανότητας) 174. το haq-di είναι ένα ερωτηματολόγιο, με το οποίο ο ίδιος ο ασθενής βαθμολογεί τη δυνατότητά του για αυτοεξυπηρέτηση και εκτέλεση των συνηθισμένων δραστηριοτήτων της καθημερινής του ζωής. Λαμβάνει τιμές από 0 έως 3, όπου μία τιμή >1,5 υποδεικνύει σοβαρή έκπτωση της λειτουργικότητάς του. Περίπου το 40% του συνόλου των ασθενών με Νια, παρουσιάζουν, σύμφωνα με το δείκτη haq-di, κάποιου βαθμού μείωση της λειτουργικής τους ικανότητας. επιπλέον, 10% περίπου χρειάζεται βοήθεια στη διεκπεραίωση των καθημερινών αναγκών του (πίνακας 13) 133, ,172.
79 Στην πολυαρθρική υποομάδα έναρξης της νόσου, περισσότεροι από τους μισούς ασθενείς εμφανίζουν μειωμένη λειτουργική ικανότητα και είναι η υποομάδα που παρουσιάζει τις υψηλότερες τιμές στο δείκτη haq-di. Παρόμοια υψηλά ποσοστά λειτουργικής ανικανότητας εμφανίζουν οι ασθενείς με συστηματικής έναρξης νόσο με μετάπτωση σε πολυαρθρίτιδα. αντιθέτως, περίπου το 80% των ασθενών με εμμένουσα ολιγοαρθρίτιδα δεν εμφανίζει δυσκολία στις καθημερινές του δραστηριότητες. ωστόσο, δε συμβαίνει το ίδιο και με την επεκταθείσα ολιγοαρθρίτιδα, στην οποία το ποσοστό αναπηρίας είναι παρόμοιο με αυτό των ασθενών με πολυαρθρικής έναρξης νόσο 133,135, ,146,171,172. Σε μια από τις μεγαλύτερες μελέτες, των Packham και συν. σημειώνεται σοβαρός περιορισμός της λειτουργικότητας (haq-di score >1,5), στο 42,9% όλων των ασθενών με Νια που εξετάσθηκαν. επίσης, στην ίδια μελέτη σημειώνεται ότι η τιμή του haq score ήταν στατιστικώς σημαντικά χειρότερη, όσο μεγαλύτερη ήταν η διάρκεια της νόσου (p<0.001) 171. Στη μελέτη των Flato και συν. που εστιάστηκε σε ασθενείς με ψωριασική αρθρίτιδα, βρέθηκε τιμή haq-di > 0.12 σε 45% αυτών, ενώ σε μια άλλη μελέτη του ίδιου συγγραφέα που αφορούσε ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα τιμή haq-di>0 παρουσίασαν 28 από τους 55 ασθενείς (51%) 144,145. ειδικά, όσον αφορά στους ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και αξονική προσβολή έχει χρησιμοποιηθεί, επιπλέον, ο δείκτης haq- S(hAQ modified for Spondyloarthropathy) 145,175. O δείκτης haq-s προκύπτει με την προσθήκη στο δείκτη haq-di, 5 επιπλέον ερωτήσεων που κατανέμονται σε 2 νέες ενότητες, αυτών της ικανότητας για κάμψη και οδήγηση. 79
80 80 Πίνακας 13. Αναλογία (%) ασθενών με ελαττωμένη λειτουργική ικανότητα (HAQ- DI>0) σε μελέτες μακροχρόνιας έκβασης της Νεανικής Ιδιοπαθούς Αρθρίτιδας (ΝIA) μελέτη αριθμός ασθενών που μέση διάρκεια αναλογία (%) ασθενών (χώρα, έτος) αξιολογήθηκαν νόσου (έτη) με haq-di > 0 Oen et al. (καναδάς, 2002) * 55 Minden et al. (Γερμανία, 2002) * 39 Flato et al. (Νορβηγία, 2003) Zak-Pedersen (δανία, 2000) Nordal et al. (δανία, Σουηδία, Νορβηγία, φιλανδία, 2011) Bertillson et al. (Σουηδία, 2013) Solari et al. (ιταλία, 2008) * διάμεσος τιμή Κοινωνικοοικονομική κατάσταση Σε πολλές μελέτες, έχει βρεθεί ότι οι ενήλικες με νεανική αρθρίτιδα αποκτούν συγκρίσιμο ή και υψηλότερο, σε σχέση πάντα με τα υγιή άτομα της ίδιας ηλικίας, μορφωτικό επίπεδο, όπως αυτό εκτιμάται από το ποσοστό αποφοίτησης, τους τελικούς βαθμούς αποφοίτησης καθώς από τα συνολικά έτη σπουδών 138,141, Στον τομέα της εργασιακής απασχόλησης, τα αποτελέσματα βρέθηκαν να ποικίλουν 141,176, Σε κάποιες μελέτες δεν αναδείχθηκε διαφορά ανάμεσα στους ενήλικες με Νια και στην ομάδα σύγκρισης και οι περισσότεροι βρέθηκαν να είναι ενεργοί επαγγελματίες 138,177,178. Σε αυτές τις μελέτες το εύρος των ηλικιών των ενηλίκων με Νια που συμμετείχαν ήταν στενό. Για παράδειγμα οι Arkela-Kautiaineh και συν. συμπεριέλαβαν στη μελέτη άτομα ηλικίας ετών 178 και οι Minden και συν. άτομα ηλικίας ετών 138. Σε αντίθεση με τις παραπάνω μελέτες, κάποιες άλλες που συμπεριλάβαν ενήλικες με Νια ηλικίας μέχρι και πάνω από 68 ετών, βρήκαν
81 περισσότερες δυσκολίες στην εργασιακή απασχόληση των ατόμων που μελέτησαν 141,176,179. μια πιθανή ερμηνεία των παραπάνω αποκλίσεων θα μπορούσε να δοθεί μέσω της βελτίωσης της φαρμακευτικής αγωγής της νεανικής αρθρίτιδας, όπως επίσης και μέσω της αποδοχής των ενηλίκων με σωματικά προβλήματα στην εργασία, που είναι φανερό ότι συγκρινόμενη με αυτήν πριν από χρόνια έχει βελτιωθεί στις μέρες μας Ψυχοκοινωνική κατάσταση Oι έφηβοι με Νια, πριν την ενηλικίωση τους καλούνται να επιτύχουν ανεξαρτησία από τους γονείς τους, να εδραιώσουν σχέσεις έξω από την οικογένεια και ευρύτερα να αποκτήσουν τη δική τους ταυτότητα. η εικόνα του σώματός τους είναι σημαντική για όλους τους έφηβους και η χρόνια νόσος μπορεί να επιδράσει, δυσμενώς, επάνω σε αυτήν την εικόνα, μέσω διαφόρων μηχανισμών 180. το χαμηλό ανάστημα, οι τοπικές διαταραχές στην ανάπτυξη όπως π.χ. ένα βραχύτερο μέλος, η μικρογναθία, η κεντρική παχυσαρκία, η ακμή και οι ραγάδες του δέρματος, αποτέλεσμα της χρήσης στεροειδών, επηρεάζουν δυσμενώς την αυτοεκτίμησή τους. Πέρα από αυτά, η περιορισμένη κινητικότητα των ασθενών αυτών, τους κρατά μακριά από κοινωνικές δραστηριότητες οδηγώντας τους, με την πάροδο του χρόνου, σε άγχος, απομόνωση και κατάθλιψη 176. η σχέση με το αντίθετο φύλο χρειάζεται περισσότερο χρόνο για να εδραιωθεί και συχνά τα άτομα αυτά πραγματοποιούν μακροχρόνιες σχέσεις με ανθρώπους που έχουν ανάλογα προβλήματα 176,180. Στη μελέτη των Packham και hall, το ποσοστό των ασθενών που ήταν άγαμοι έφτανε το 48.6%, το οποίο είναι 12.9% υψηλότερο σε σύγκριση με αυτό του γενικού πληθυσμού. Υψηλός αριθμός των ασθενών πραγματοποιούσε σταθερή σχέση μεταξύ των ηλικιών 35 και 45 έτη 180. διάφορα εργαλεία που μετρούν την ποιότητα ζωής έχουν χρησιμοποιηθεί στους ασθενείς με Νια, με πιο δημοφιλή την κλίμακα Short Form-36 (SF-36) 181. Σε μελέτη τους, οι Ostlie και συν. ενώ βρήκαν σημαντική ελάττωση της σωματικής υγείας των ενηλίκων με Νια που συμπεριέλαβαν στο δείγμα τους, ωστόσο δε διαπίστωσαν διαφορά στη ψυχοκοινωνική τους κατάσταση σε σύγκριση με το γενικό νορβηγικό πληθυσμό. Oι παραπάνω συγγραφείς εξήγαγαν τα συμπεράσματά τους, χρησιμοποιώντας τα ερωτηματολόγια SF-36 και τη νορβηγική έκδοση του ερωτηματολογίου γενικής υγείας GhQ-30 (General health Questionnaire-30) 182. το GhQ-30 μετρά την ψυχολογική επιβάρυνση σε τομείς όπως το άγχος, η κατάθλιψη και η κοινωνική δυσλειτουργία. 81
82 9. Π Ρ O Γ Ν Ω Σ Τ Ι Κ O Ι Π Α Ρ Α Γ O Ν Τ Ε Σ Κ Ι Ν Δ Υ Ν OΥ η υποομάδα της Νια θεωρείται ο βασικός οδηγός που καθορίζει την έκβαση της νόσου. ειδικότερα, παιδιά με ολιγοαρθρικής έναρξης νόσο έχουν καλύτερη πρόγνωση συγκρινόμενα με αυτά με πολυαρθρίτιδα ή συστηματική αρθρίτιδα 183. ανάμεσα στους παράγοντες κινδύνου για εμμένουσα ενεργότητα νόσου είναι η ανάπτυξη πολυαρθρίτιδας κατά την έναρξη, αλλά και κατά την πορεία της νόσου, ειδικά στο γυναικείο φύλο, οι αυξημένοι δείκτες φλεγμονής κατά την έναρξη και ο θετικός ρευματοειδής παράγοντας 183. Oι προγνωστικοί παράγοντες για μειωμένη λειτουργική ικανότητα και αρθρική καταστροφή είναι παρόμοιοι (συνεχής ενεργότητα νόσου, πολυαρθρίτιδα, γυναικείο φύλο, θετικός ρευματοειδής παράγοντας) 183,184. ωστόσο, φάνηκε ότι η επίτευξη μη ενεργού νόσου τουλάχιστον μία φορά τα πρώτα 5 έτη συνδέεται, μακροχρονίως, με μικρότερη αρθρική καταστροφή και τάση για λιγότερο επηρεασμένη σωματική λειτουργική ικανότητα 185. Παράγοντες κινδύνου πτωχής έκβασης και μεγαλύτερης λειτουργικής ανικανότητας στη συστηματική μορφή είναι η έναρξη της νόσου πριν την ηλικία των 5 ετών, η περικαρδίτιδα, η θρομβοκυττάρωση, η εμμένουσα ενεργότητα τα πρώτα 5 έτη και οι εξελισσόμενες ακτινολογικές αλλοιώσεις 183,
83 1 0. Θ Ε Ρ Α Π Ε Υ Τ Ι Κ Η Π Ρ O Σ Ε Γ Γ Ι Σ Η Τ Η Σ Ν Ε Α Ν Ι Κ Η Σ Ι Δ Ι O Π Α Θ O Υ Σ Α Ρ Θ Ρ Ι Τ Ι Δ Α Σ η αντιμετώπιση της NiA έχει διαφοροποιηθεί σε μεγάλη έκταση τα τελευταία 20 χρόνια. μέχρι τα τέλη της δεκαετίας του 1980, η ασπιρίνη και τα άλλα μη στεροειδή αντιφλεγμονώδη φάρμακα (μσαφ) αποτελούσαν τη βάση της θεραπείας των παιδιών με NiA, με επιπρόσθετη χορήγηση κορτικοστεροειδών, υδροξυχλωροκίνης, αλάτων χρυσού, και D-πενικιλλαμίνης. η πρώτη μεγάλη αλλαγή έλαβε χώρα στα τέλη της δεκαετίας του 1980 με την αύξηση της χρήσης των κορτικοειδών μέσω ενδαρθρικών εγχύσεων στα παιδιά με ολιγοαρθρίτιδα και την εισαγωγή της μεθοτρεξάτης στη θεραπεία των παιδιών με πολυαρθρίτιδα. η δεύτερη μεγάλη αλλαγή πραγματοποιήθηκε στα τέλη της δεκαετίας του 1990 με την ανακάλυψη των βιολογικών ανοσοτροποποιητικών παραγόντων, πρώτα αυτών έναντι του παράγοντα νέκρωσης όγκου (Tumor Necrosis Factor-α-inhibitor) και αργότερα των βιολογικών τροποποιητών που στοχεύουν άλλες κυτταροκίνες που εμπλέκονται στη φλεγμονώδη διαδικασία. η φιλοσοφία της θεραπευτικής προσέγγισης της NiA έχει, επίσης, αναθεωρηθεί τα τελευταία χρόνια. Στο παρελθόν, η αντιμετώπιση βασιζόταν στο πρότυπο της πυραμίδας, αρχικά δηλαδή χρησιμοποιούνταν διάφοροι τύποι μη στεροειδών αντιφλεγμονωδών φαρμάκων και κορτικοστεροειδών και σταδιακά προστίθενται άλλες κατηγορίες φαρμάκων. μελέτες, όμως, στα τέλη της δεκαετίας του 1980 άρχισαν να δείχνουν ότι η προηγούμενη προσέγγιση δεν ήταν σωστή, αφού οι ακτινολογικές αλλοιώσεις, που παλαιότερα θεωρούνταν ότι εμφανίζονται αργά στην πορεία της νόσου, προκαλούνται στους περισσότερους ασθενείς με συστηματική και πολυαρθρική μορφή, μέσα στα πρώτα 2 έτη από την έναρξη της νόσου 186. η υπόθεση ότι η NiA θα εξαφανιστεί με την είσοδο στην ενήλικο ζωή, θεωρείται, σήμερα, επίσης, ότι δεν ευσταθεί. μελέτες έχουν δείξει ότι πο- 83
84 84 σοστό 50%-70% των ασθενών με πολυαρθρίτιδα ή συστηματική αρθρίτιδα και 40%-50% των ασθενών με ολιγοαρθρίτιδα θα συνεχίσουν να έχουν ενεργό νόσο και μετά την ενηλικίωσή τους. επιπλέον, ένα σημαντικό ποσοστό ασθενών που κυμαίνεται μεταξύ 25% και 50% θα χρειαστεί κάποια μεγάλη χειρουργική επέμβαση στην πορεία της νόσου, κυρίως ολική αρθροπλαστική 186. επομένως, το φορτίο της νόσου για τον ασθενή, την οικογένειά του και την ευρύτερη κοινωνία είναι μεγάλο και προκύπτει επιτακτική ανάγκη για έγκαιρη αναγνώριση της νόσου και επιθετική θεραπεία πρώιμα, πριν την εγκατάσταση μόνιμων μη αναστρέψιμων βλαβών. O σχεδιασμός της θεραπείας στη NiA εξαρτάται σε μεγάλο βαθμό από τον υπότυπο της νόσου και στοχεύει πρωτίστως, στην επίτευξη κλινικής ύφεσης ή χαμηλής δραστηριότητας νόσου. η διατήρηση μακροχρόνιας ύφεσης εξασφαλίζει μακροπρόθεσμα ικανοποιητική ανάπτυξη και καλή λειτουργική ικανότητα. η επίτευξη αυτών των στόχων προϋποθέτει τη συνεργασία ομάδας που περιλαμβάνει παιδορευματολόγους, ρευματολόγους ενηλίκων, ορθοπεδικούς, οφθαλμιάτρους, οδοντιάτρους, νοσηλευτές, φυσιοθεραπευτές, κοινωνικούς λειτουργούς, ψυχολόγους καθώς και τη συμμετοχή γονέων και δασκάλων Μη στεροειδή αντιφλεγμονώδη φάρμακα (ΜΣΑΦ) η ακριβής αποτελεσματικότητα των μσαφ δεν είναι γνωστή, αφού δεν υπάρχουν μελέτες ελεγχόμενες με εικονικό φάρμακο. Συνολικά, περίπου 25%-33% των ασθενών, κυρίως αυτών με ολιγοαρθρίτιδα, παρουσιάζουν σημαντική απάντηση στα μσαφ. απαραίτητη είναι η χορήγηση ενός μσαφ για τέσσερις εβδομάδες προκειμένου να αξιολογηθεί η αποτελεσματικότητά του. τα μσαφ φαίνεται ότι δεν αλλάζουν την πορεία της νόσου, ούτε εμποδίζουν την καταστροφή των αρθρώσεων, για το λόγο αυτό χρησιμοποιούνται κυρίως στην αντιμετώπιση του πόνου, της δυσκαμψίας και του πυρετού που παρατηρείται στη συστηματική αρθρίτιδα. δεν υπάρχει κάποιο συγκεκριμένο μσαφ που να υπερέχει σε σύγκριση με τα υπόλοιπα στην αντιμετώπιση της αρθρίτιδας, ωστόσο θεωρείται ότι η ινδομεθακίνη ίσως είναι περισσότερο ευεργετική στην αντιμετώπιση του εμπυρέτου και της περικαρδίτιδας στα πλαίσια της συστηματικής αρθρίτιδας, καθώς και στην αρθρίτιδα που σχετίζεται με ενθεσίτιδα 186. τα μσαφ που έχουν εγκριθεί από το FDA (Food and Drug Administration) για τη χρήση τους στη NiA είναι η τολμετίνη, η ναπροξένη, η ιμπουπροφένη, η μελοξικάμη και η σελεκοξίμπη.
85 Oι σοβαρές ανεπιθύμητες ενέργειες από το γαστρεντερικό σύστημα είναι σπάνιες, αν και περίπου 28% των παιδιών εμφανίζουν γαστρεντερικά συμπτώματα. Άλλες ανεπιθύμητες ενέργειες που μπορεί να αναπτυχθούν είναι η ψευδοπορφυρία, η κεφαλαλγία και ο αποπροσανατολισμός, κυρίως με την ινδομεθακίνη. ανεπιθύμητες ενέργειες από τους νεφρούς, ειδικά νέκρωση των θηλών και διαταραχές της λειτουργίας των σωληναρίων είναι ασυνήθης στα παιδιά και παρατηρούνται συχνότερα με την ταυτόχρονη χρήση περισσότερων του ενός μσαφ Κορτικοστεροειδή τα παιδιά με ολιγοαρθρίτιδα αντιμετωπίζονται αρχικά συνήθως με μσαφ ως μονοθεραπεία ή μόνο με ενδαρθρική χορήγηση κορτικοειδών ή με συνδυασμό και των δύο. Περίπου 70% των ασθενών με ολιγοαρθρίτιδα δεν παρουσιάζουν υποτροπή της νόσου στην άρθρωση που έγινε η έγχυση για το επόμενο έτος και στο 40%-60% αυτών το ευεργετικό αποτέλεσμα μπορεί να διαρκέσει για διάστημα περισσότερο των 2 ετών 186,187. μελέτες έδειξαν ότι σημαντικά λιγότεροι ασθενείς αναπτύσσουν ανισοσκελία όταν εφαρμόζεται πρώιμα στην κλινική πρακτική ενδαρθρική χορήγηση κορτικοστεροειδών 186,187. Oι ανεπιθύμητες ενέργειες που προκύπτουν λόγω των ενδαρθρικών εγχύσεων είναι ελάχιστες και συγκεκριμένα περιλαμβάνουν την περιαρθρική υποδόρια ατροφία και/ή την ανάπτυξη ασυμπτωματικών ενδαρθρικών επασβεστώσεων. η ιατρική κοινότητα έχει προσπαθήσει να περιορίσει στο ελάχιστο τη χρήση κορτικοειδών συστηματικά, εξαιτίας των σημαντικών ανεπιθύμητων ενεργειών που αφορούν, κυρίως, στα οστά αλλά και στην ανάπτυξη. δεν έχει αποδειχθεί ότι τα κορτικοειδή τροποποιούν την πορεία της νόσου. Oι κυριότερες ενδείξεις της χρήσης τους στη NiA είναι η αντιμετώπιση του εμπυρέτου, της ορογονίτιδας και του συνδρόμου ενεργοποίησης των μακροφάγων στους ασθενείς με συστηματική αρθρίτιδα. επίσης, συχνά χρησιμοποιούνται ως γέφυρα θεραπείας μέχρι την έναρξη της δράσης κάποιου ανοσοτροποποιητικού φαρμάκου Μεθοτρεξάτη η χρήση της μεθοτρεξάτης είναι ο ακρογωνιαίος λίθος στην αντιμετώπιση των περισσοτέρων ασθενών με πολυαρθρίτιδα. η πρώιμη απάντηση στη χορήγηση μεθοτρεξάτης μπορεί να είναι προγνωστική της μακροχρόνιας έκβασης της νόσου. χορηγείται είτε από του στόματος είτε παρεντερικώς 85
86 86 (υποδόρια ή ενδομυϊκά) σε δόση mg/m 2 /εβδομάδα (σε δόση >12.5 mg/m 2 προτιμάται η παρεντερική χορήγηση) με μέγιστη συνιστώμενη δόση τα 30 mg/m 2. δεν έχει αποσαφηνισθεί πότε ακριβώς πρέπει να αποφασίζεται η διακοπή της χορήγησής της στους ασθενείς που έχουν απαντήσει. Σε περισσότερους από 60% των ασθενών η διακοπή της μεθοτρεξάτης ακολουθείται από έξαρση της νόσου συνήθως 18 μήνες αργότερα. Περίπου 90% των ασθενών θα απαντήσουν και πάλι μετά την επαναχορήγησή της 186,189. η θεραπεία με μεθοτρεξάτη συνοδεύεται πάντα με φυλλικό ή με φολινικό οξύ μία φορά εβδομαδιαίως συνήθως την ημέρα μετά τη χορήγησή της. Ναυτία και άλλα γαστρεντερικά συμπτώματα είναι δυστυχώς, συχνά στα παιδιά και πολλές φορές οδηγούν σε αποτυχία της θεραπείας λόγω αδυναμίας συμμόρφωσής τους. Συχνά παρατηρείται ήπια άνοδος των ηπατικών ενζύμων, ωστόσο, δεν έχουν παρατηρηθεί σοβαρές, μη αναστρέψιμες περιπτώσεις ηπατικής βλάβης στα παιδιά με NiA. Oι εμβολιασμοί με μη-ζώντες μικροοργανισμούς είναι σε γενικές γραμμές ασφαλείς και ανεπιφύλακτα συστήνεται ο εμβολιασμός έναντι της εποχιακής γρίπης Άλλα μη βιολογικά ανοσοτροποποιητικά της νόσου φάρμακα (Disease Modifying Anti-Rheumatic Drugs, DMARDS) Oι περισσότερες ελεγχόμενες μελέτες στα παιδιά έχουν δείξει ότι η υδροξυχλωροκίνη, τα άλατα χρυσού και η D-πενικιλλαμίνη δεν είναι, σε σημαντικό επίπεδο, αποτελεσματικά στην αντιμετώπιση της NiA, αν και σε μία μελέτη βρέθηκε ότι η D-πενικιλλαμίνη υπερίσχυε έναντι του εικονικού φαρμάκου στην αντιμετώπιση τόσο της ολιγοαρθρίτιδας όσο και της πολυαρθρίτιδας 186,190. Oι περισσότερες μελέτες με τη σουλφασαλαζίνη δεν ήταν ελεγχόμενες. Σε μία ελεγχόμενη μελέτη φάνηκε ότι η σουλφασαλαζίνη ήταν αποτελεσματική στην αντιμετώπιση της ολιγοαρθρίτιδας και πολυαρθρίτιδας και ότι η πρώιμη εισαγωγή της στη θεραπεία μπορεί να οδηγήσει σε καλύτερη μακροχρόνια έκβαση 186. Σε πολλές ανοιχτές μελέτες η σουλφασαλαζίνη εμφανίζει μεγαλύτερη αποτελεσματικότητα στα μεγαλύτερα αγόρια με ολιγοαρθρίτιδα, τα οποία πιθανώς αντιπροσωπεύουν παιδιά με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα. ανεπιθύμητες ενέργειες παρατηρούνται συχνά, με κυριότερες το εξάνθημα, τα γαστρεντερικά συμπτώματα και τη λευκοπενία, με αποτέλεσμα τη διακοπή του φαρμάκου στο ένα τρίτο των ασθενών περίπου. η δόση της σουλφασαλαζίνης αυξάνεται σταδιακά, προκειμένου να γίνει περισσότερο
87 ανεκτή. Oι ανεπιθύμητες ενέργειες μπορεί να είναι σοβαρές ιδιαίτερα στα παιδιά με συστηματική αρθρίτιδα, στα οποία υπάρχει κίνδυνος ανάπτυξης του συνδρόμου ενεργοποίησης των μακροφάγων. η λεφλουνομίδη έχει αποδειχθεί αποτελεσματική στη θεραπεία της NiA. Σε ελεγχόμενη μελέτη που σύγκρινε τη λεφλουνομίδη με τη μεθοτρεξάτη στα παιδιά με πολυαρθρίτιδα, σημαντικά μεγαλύτερη απάντηση παρατηρήθηκε στην ομάδα της μεθοτρεξάτης, αν και υψηλά ποσοστά ανταπόκρισης καταγράφηκαν και στην ομάδα της λεφλουνομίδης. τα περισσότερα από τα παιδιά που δεν απάντησαν στη λεφλουνομίδη ήταν < 40 Kg και έπαιρναν 10mg μέρα παρά μέρα. Oι ανεπιθύμητες ενέργειες της λεφλουνομίδης ήταν γαστρεντερικές διαταραχές και ήπια άνοδος των ηπατικών ενζύμων και δε διέφεραν σημαντικά μεταξύ των δύο ομάδων 186,189. δεν υπάρχουν ελεγχόμενες μελέτες για την κυκλοσπορίνη στη NiA. μπορεί να αποδειχθεί ευεργετική στον έλεγχο του πυρετού και να συμβάλει στη μείωση της δόσης των κορτικοειδών, ωστόσο δεν είναι αποτελεσματική στην αρθρίτιδα των ασθενών με συστηματική μορφή. ιδιαίτερα σημαντική είναι η δράση της όταν αναπτύσσεται σύνδρομο ενεργοποίησης των μακροφάγων. Oι ανεπιθύμητες ενέργειες της κυκλοσπορίνης είναι πολλές, προερχόμενες κυρίως από τους νεφρούς 186. Σε ελεγχόμενη μελέτη της αζαθειοπρίνης στη NiA δε βρέθηκε ότι υπερέχει σημαντικά έναντι του εικονικού φαρμάκου στην αντιμετώπιση της αρθρίτιδας 190. ελεγχόμενες μελέτες για τη χορήγηση συνδυασμού μη βιολογικών DMARDs με ή χωρίς μεθοτρεξάτη δεν υπάρχουν μέχρι σήμερα Βιολογικές ανοσοτροποποιητικές θεραπείες Ανταγωνιστές του παράγοντα νέκρωσης των όγκων TNFα (inh-tnfα βιολογικοί παράγοντες) Σήμερα στη NiA χρησιμοποιούνται τρείς βιολογικοί παράγοντες που στοχεύουν στον TNFα: το Etanercept (Enbrel ), ένας γενετικά ανασυνδυασμένος διαλυτός p75-υποδοχέας του TNFα που έχει συντηχθεί με το τμήμα Fc της ανθρώπινης ανοσοσφαιρίνης igg1, το Adalimumab (Humira ), εξανθρωποποιημένο αντίσωμα έναντι του TNFα και το Infliximab (Remicade ), ένα χιμαιρικό μονοκλωνικό αντίσωμα έναντι του TNFα, αποτελούμενο 25% από igg1 ποντικού και 75% από igg1 ανθρώπου. Σε αντίθεση με το etanercept, το adalimumab και το infliximab δεσμεύουν τόσο το διαλυτό, όσο και τον μεμβρανικό TNFα. 87
88 88 το Etanercept ήταν ο πρώτος ανταγωνιστής του TNFα που πήρε ένδειξη για χορήγησή του στη NiA το 1999 (το 2000 στην ελλάδα), ενώ πρόσφατα εγκρίθηκε από το FDA στη θεραπεία της μέτριας-σοβαρής πολυαρθρικής έναρξης NiA σε παιδιά ηλικίας μεγαλύτερα ή ίσα των 2 ετών. μέχρι σήμερα έχει δημοσιευθεί μία τυχαιοποιημένη ελεγχόμενη μελέτη του etanercept στην αντιμετώπιση της NiA 186. Oι Lovell και συν. έδειξαν ότι οι ασθενείς που τυχαιοποιήθηκαν να συνεχίσουν να παίρνουν etanercept, είχαν σημαντικά μακρύτερο διάμεσο χρονικό διάστημα μέχρι την επόμενη έξαρση της νόσου, συγκριτικά με τους ασθενείς που τυχαιοποιήθηκαν να παίρνουν εικονικό φάρμακο, μετά από αρχική τρίμηνη θεραπεία με etanercept (116 ημέρες έναντι 28 ημέρες) 191. μετά από αυτήν τη βασική αρχική τυχαιοποιημένη ελεγχόμενη μελέτη, οι περισσότερες βιβλιογραφικές αναφορές σχετικά με την αποτελεσματικότητα του Etanercept στη NiA προέρχονται από μη ελεγχόμενες ανοιχτές μελέτες και σειρές ασθενών με πολυαρθρικής και συστηματικής έναρξης NiA, ανθεκτικής στη θεραπεία με μη-βιολογικά DMARDS. Παρά το γεγονός ότι στις μελέτες αυτές έχουν ενταχθεί ασθενείς με επιθετική νόσο, ωστόσο έχουν σημειωθεί σημαντικά αποτελέσματα. Πρόσφατα δεδομένα της Γερμανικής καταγραφής (registry) παρείχαν πληροφορίες σχετικά με τη θεραπεία με Etanercept, χορηγούμενο είτε ως μονοθεραπεία, είτε ως συνδυασμένη θεραπεία με μεθοτρεξάτη, 431 παιδιών που ανήκαν σε διάφορες υποομάδες της NiA. μετά από 12 μήνες παρακολούθησης, 62% των παιδιών που έπαιρναν συνδυασμένη θεραπεία πέτυχαν απάντηση ACRpedi 70, ενώ μόνο 45% των παιδιών που έπαιρναν μονοθεραπεία με Etanercept πέτυχαν την ίδια απάντηση (p<0.01) 192. το Adalimumab είναι ο δεύτερος ανταγωνιστής του TNFα που πήρε ένδειξη στην αντιμετώπιση της μέτριας-σοβαρής πολυαρθρικής NiA σε παιδιά μεγαλύτερα ή ίσα των 4 ετών. Σε τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη του Adalimumab, βρέθηκε ότι οι ασθενείς που είχαν αρχικά απαντήσει στη χορήγηση του Adalimumab και μετά συνέχισαν με το εικονικό φάρμακο, παρουσίασαν σε υψηλότερο ποσοστό υποτροπή της νόσου, συγκριτικά με τους υπόλοιπους που είχαν απαντήσει αρχικά και συνέχισαν τη θεραπεία με Adalimumab. (71% έναντι 43% διαφορά μεταξύ των ομάδων που δεν έπαιρναν ταυτόχρονα μεθοτρεξάτη p=0.03 και 65% έναντι 37% μεταξύ των ομάδων που έπαιρναν συνδυασμένη θεραπεία με μεθοτρεξάτη p=0.02) 193. το έτος 2007 δημοσιεύτηκαν τα αποτελέσματα μιας διεθνούς, πολυκεντρικής, τυχαιοποιημένης, ελεγχόμενης μελέτης του infliximab χορηγούμενο
89 σε συνδυασμό με τη μεθοτρεξάτη στη θεραπεία της πολυαρθρικής NiA. Στις 14 εβδομάδες, υψηλότερο ποσοστό ασθενών που τυχαιοποιήθηκαν στο infliximab πέτυχαν απάντηση ACR Pedi 30 σε σύγκριση με τους ασθενείς που έπαιρναν το εικονικό φάρμακο. ωστόσο, η διαφορά αυτή δεν ήταν στατιστικώς, σημαντική. Στη μετέπειτα ανοιχτή φάση της μελέτης, 70% και 52% των παιδιών πέτυχαν απάντηση ACR Pedi 50 και ACRpedi 70 αντίστοιχα μέχρι το τέλος του έτους 194. Oι ανεπιθύμητες ενέργειες των inh-τnfα παραγόντων, αν και δυνητικά σοβαρές, είναι σε γενικές γραμμές ήπιες, κυρίως αντιδράσεις στην περιοχή της έγχυσης, λοιμώξεις ανώτερου αναπνευστικού και κεφαλαλγίες. το FDA έχει προειδοποιήσει το 2008 για τον αυξημένο κίνδυνο ανάπτυξης κακοήθειας, κυρίως μελανώματος, λεμφώματος και λευχαιμίας στα παιδιά και στους εφήβους που λαμβάνουν θεραπεία με ανταγωνιστές του TNFα. είναι, όμως, ασαφές, εάν πρόκειται για πραγματική αύξηση του ποσοστού συγκριτικά με αυτό που αναμένεται στον παιδιατρικό πληθυσμό. ωστόσο, έχει αναφερθεί αυξημένη συχνότητα φαινομένων αυτοανοσίας, όπως σακχαρώδης διαβήτης μετά από 2 μήνες θεραπείας με Etanercept, Λύκος επαγόμενος από φάρμακα, δερματική αγγειίτιδα και απομυελίνωση κεντρικού νευρικού συστήματος. αρκετές περιπτώσεις υποτροπής ιριδοκυκλίτιδας ή νέας εμφάνισης ιριδοκυκλίτιδας έχουν αναφερθεί μετά από χορήγηση θεραπείας με Etanercept. Συνολικά, το ποσοστό σοβαρών ανεπιθύμητων ενεργειών από τη χρήση inh- TNFα θεραπείας υπολογίζεται σε συμβάντα ανά ασθενο-έτος θεραπείας. Έλεγχος φυματίωσης, πριν την έναρξη θεραπείας με inh-tnfα, σύμφωνα με τις κατευθυντήριες οδηγίες που ισχύουν για τους ενήλικες και αποφυγή εμβολίων με ζώντες εξασθενημένους ιούς, περιλαμβάνονται στις σύγχρονες συστάσεις για τους ασθενείς που λαμβάνουν inh-tnfα θεραπεία 186,191, Abatacept (Orencia ) το Abatacept είναι ανασυνδυασμένος εκλεκτικός αναστολέας του σήματος συνδιέγερσης που απαιτείται για την ενεργοποίηση των T λεμφοκυττάρων (CTLA-4ig). η προς τα κάτω ρύθμιση της ενεργοποίησης των T κυττάρων οδηγεί σε μείωση της διέγερσης των β κυττάρων και των μακροφάγων και κατά συνέπεια στην τροποποίηση πολλών από τα μονοπάτια των φλεγμονωδών κυτταροκινών που εμπλέκονται στην παθογένεια της NiA. βρέθηκε αποτελεσματικό στη θεραπεία της πολυαρθρικής έναρξης νεανικής Νια σε μια τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη που περιέλαβε 190 ασθενείς 196. Στις συνήθεις ανεπιθύμητες ενέργειες του 89
90 90 φαρμάκου περιλαμβάνονται οι αντιδράσεις κατά τη διάρκεια της έγχυσης, η κεφαλαλγία, η διάρροια και οι λοιμώξεις του ανώτερου αναπνευστικού συστήματος, ενώ σοβαρές λοιμώξεις έχουν αναφερθεί μόνο σποραδικά. το Abatacept εγκρίθηκε από το FDA για χρήση του στην πολυαρθρικής έναρξης NiA σε παιδιά μεγαλύτερα των 4 ετών. χορηγείται με ενδοφλέβιες εβδομαδιαίες εγχύσεις σε δόση 10 mg/kg Anti-Interleukin (IL)-1 παράγοντες Στην ελλάδα κυκλοφορούν δύο αντι-il-1 παράγοντες με διαφορετικούς μηχανισμούς δράσης. το αnakinra (Kineret ), που είναι ανταγωνιστής του υποδοχέα της il-1 και το Canakinumab (ilaris ), που είναι πλήρως εξανθρωποποιημένο μονοκλωνικό αντίσωμα έναντι της il-1. Περισσότερες μελέτες και μεγαλύτερη κλινική εμπειρία υπάρχει με το αnakinra. Έτσι, αρκετές μελέτες έχουν δείξει όφελος της χορήγησης του αnakinra στη θεραπεία της συστηματικής έναρξης NiA, συμπεριλαμβανομένων και των ασθενών που δεν απάντησαν στη θεραπεία με inh-tnfα παράγοντες. Συγκεκριμένα, στη μελέτη του αnakinra στην πολυαρθρίτιδα, οι ασθενείς με συστηματικής έναρξης NiA, έδειξαν ευνοϊκότερη απάντηση συγκριτικά με τους ασθενείς με πολυαρθρικής και ολιγοαρθρικής έναρξης NiA 197. ωστόσο, φαίνεται ότι δεν απαντούν όλοι οι ασθενείς με συστηματική έναρξη στη θεραπεία με αnakinra. Έχει δημοσιευθεί, σε ευρωπαϊκές μελέτες, ότι υπάρχουν δύο υποομάδες ασθενών όσον αφορά στην απάντησή τους στο αnakinra, με το 50% αυτών να δείχνουν θεαματική αποτελεσματικότητα παρόμοια με αυτήν που συναντάται στα αυτοφλεγμονώδη σύνδρομα που σχετίζονται με την κρυοπυρίνη και τους υπόλοιπους να έχουν μικρή ή καθόλου απάντηση 198,199. Oι κυριότερες ανεπιθύμητες ενέργειες περιλαμβάνουν τοπικές αντιδράσεις στο σημείο της ένεσης, ουδετεροπενία, θρομβοπενία και ηωσινοφιλία 186. το Canakinumab πρόσφατα πήρε ένδειξη για τη χορήγησή του στη συστηματικής έναρξη NiA. Γενετικές μελέτες γονιδιακής έκφρασης βρίσκονται σε εξέλιξη, προκειμένου να γίνει εφικτή η πρόβλεψη των ασθενών που θα απαντήσουν στην αντι-il1 θεραπεία Anti-Interleukin (IL)-6 παράγοντας (Tocilizumab, Ro-Actempra ) η il-6 είναι μία σημαντική κυτταροκίνη που εμπλέκεται στην παθογένεια της συστηματικής έναρξης NiA και ιδιαίτερα των συστηματικών εκδηλώσεων, της θρομβοκυττάρωσης, της οστεοπόρωσης και της καθυστέρησης στην ανάπτυξη. τα υψηλά επίπεδα της il-6 στο πλάσμα βρέθηκε ότι συσχετίζονται με υψηλή ενεργότητα νόσου στους ασθενείς με NiA και κυρίως στους
91 ασθενείς με συστηματικής έναρξης υποομάδα της νόσου 189. το Tocilizumab είναι το πρώτο ανασυνδυασμένο μονοκλωνικό αντίσωμα που συνδέεται με τον υποδοχέα της il-6 και εμποδίζει τη σηματοδότηση μέσω της φλεγμονώδους αυτής κυτταροκίνης. χορηγείται ενδοφλεβίως σε δόση 4 ή 8 mg/kg κάθε 4 εβδομάδες. Σε ελεγχόμενη, δύο φάσεων μελέτη, 91% των ασθενών που έπαιρναν Tocilizumab έδειξαν απάντηση ACRPedi 30 και 68% ACRPedi 70. Oι εξάρσεις της νόσου ήταν σημαντικά περισσότερες στην ομάδα των ασθενών που έπαιρνε το εικονικό φάρμακο 200. Oι σοβαρές ανεπιθύμητες ενέργειες περιλάμβαναν κυρίως αναφυλακτικές αντιδράσεις και μη ευκαιριακές λοιμώξεις. μπορεί, επίσης, να παρατηρηθεί συχνά υπερλιπιδιαιμία Rituximab (Mabthera ) το Rituximab είναι μονοκλωνικό αντίσωμα έναντι του CD20 της επιφάνειας των B λεμφοκυττάρων. Υπάρχουν στη βιβλιογραφία μόνο σποραδικές αναφορές περιστατικών από τη χορήγησή του Rituximab στη NiA Αυτόλογη μεταμόσχευση άωρων αιμοποιητικών κυττάρων (Autologous Stem Cell Transplantation, ASCT) Υπάρχουν ακόμη αρκετά ασαφή ζητήματα που αφορούν στην επιλογή των ασθενών, στην προετοιμασία του μοσχεύματος και στη φροντίδα που απαιτείται στην περίοδο μετά την μεταμόσχευση. Για τους λόγους αυτούς, η ASCT πρέπει να θεωρείται ως μία πειραματική μέθοδος που φυλάσσεται για επιλεγμένους ασθενείς με σοβαρή, μη υφέσιμη νόσο Θεραπεία συστηματικής αρθρίτιδας Για την αντιμετώπιση της υποομάδας αυτής της NiA υπάρχουν λιγότερα δεδομένα βασισμένα σε αποδείξεις. Σύμφωνα με την επικαιροποίηση το 2013 των αρχικών συστάσεων (2011) του αμερικανικού κολλεγίου Ρευματολογίας, η αντιμετώπιση της συστηματικής αρθρίτιδας εξαρτάται από το αν επικρατούν τα συστηματικά χαρακτηριστικά ή οι εκδηλώσεις από τις αρθρώσεις 201,202. τα μσαφ και τα συστηματικώς χορηγούμενα κορτικοστεροειδή συχνά είναι απαραίτητα για την ανακούφιση των συστηματικών εκδηλώσεων της νόσου (πυρετός, ορογονίτιδα). η ενδαρθρική έγχυση κορτικοστεροειδών, η μεθοτρεξάτη και οι inhτνf-α εμφανίζονται λιγότερο αποτελεσματικοί, συγκριτικά με τις υπόλοιπες υποομάδες της NiA, τόσο στην αντιμετώπιση της αρθρίτιδας, όσο και των συστηματικών συμπτωμάτων της νόσου. η ενδοφλέβια χορήγηση γ-σφαιρίνης (ivig), ενώ δεν είναι αποτελεσματική στην αντιμετώπιση της 91
92 92 αρθρίτιδας, ωστόσο φαίνεται ότι δρα ευνοϊκά στην αντιμετώπιση των συστηματικών εκδηλώσεων, στη μείωση της δόσης των συστηματικά χορηγούμενων κορτικοστεροειδών και στο σύνδρομο ενεργοποίησης των μακροφάγων, που συχνά επιπλέκει την συστηματικής έναρξης αρθρίτιδα. Oι αντι-il1 και αντιil6 παράγοντες εμφανίζονται περισσότερο αποτελεσματικοί συγκριτικά με τη θεραπεία με inhtnfα. Πολλοί παιδορευματολόγοι επιλέγουν να χορηγήσουν anti-il1 παράγοντα πρώιμα στην πορεία της νόσου, ακόμα νωρίτερα και από τη χρήση άλλων συμβατικών ανοσοτροποποιητικών φαρμάκων ή παραγόντων έναντι του τnfα. Για τους ασθενείς με σοβαρή νόσο, που δεν ανταποκρίνεται σε καμία θεραπεία, η αυτόλογη μεταμόσχευση άωρων αιμοποιητικών κυττάρων μπορεί να χρησιμοποιηθεί ως τελευταία προσπάθεια, αν και υπάρχει υψηλό ποσοστό θνητότητας που σχετίζεται με τη συγκεκριμένη θεραπεία 186. Σχηματικά, ο αλγόριθμος αντιμετώπισης της συστηματικής αρθρίτιδας, σύμφωνα με τις συστάσεις 2013, απεικονίζεται στην εικόνα Θεραπεία του συνδρόμου ενεργοποίησης των μακροφάγων η αντιμετώπιση του συνδρόμου ενεργοποίησης των μακροφάγων περιλαμβάνει ώσεις υψηλών δόσεων κορτικοστεροειδών και ivig. αν δεν υπάρξει άμεσο αποτέλεσμα τότε προστίθεται κυκλοσπορίνη. η χορήγηση ετοποσίδης πρέπει να θεωρείται σοβαρά ως επιλογή για τους ασθενείς με ταχεία εξέλιξη της νόσου. Πρόσφατα, η αντι-il1 θεραπεία έχει αποδειχθεί αποτελεσματική σε κάποιους ασθενείς 116,117, Θεραπεία ολιγοαρθρικής έναρξης NIA Περίπου το ένα τρίτο ή το ένα τέταρτο των ασθενών με ήπια νόσο θα απαντήσει στη χορήγηση μσαφ. Στους ασθενείς που δεν απαντούν στα μσαφ μετά από θεραπεία 4-6 εβδομάδων, οι ενδαρθρικές εγχύσεις κορτικοστεροειδών είναι συνήθως αποτελεσματικές στην πλειονότητα των ασθενών. Στους ασθενείς που δε θα απαντήσουν ούτε στις ενδαρθρικές εγχύσεις ή στους ασθενείς με ολιγοαρθρίτιδα επεκταθείσα ή όταν υπάρχει συμμετοχή των μικρών αρθρώσεων, η νόσος πλέον αντιμετωπίζεται όπως αντιμετωπίζεται η πολυαρθρίτιδα 201 (εικόνα 9α) Θεραπεία πολυαρθρίτιδας με αρνητικό ρευματοειδή παράγοντα (RF) τα μσαφ δεν είναι αποτελεσματικά ως τροποποιητικά της νόσου φάρ-
93 μακα και δεν πρέπει να χορηγούνται ως μονοθεραπεία. η χρήση τους περιορίζεται στον έλεγχο των συμπτωμάτων της νόσου. μεθοτρεξάτη πρέπει να χορηγηθεί νωρίς στην πορεία της νόσου, αρχικά σε δόση 10mg/m 2 /εβδομάδα και στην περίπτωση που δεν ελεγχθεί η φλεγμονή, η δόση της να αυξηθεί σε 15 mg/m 2 /εβδομάδα, με αλλαγή της οδού χορήγησης από δια του στόματος σε παρεντερική. Άλλες επιλογές ανοσοτροποποιητικών φαρμάκων αποτελούν η σουλφασαλαζίνη, ειδικά στα μεγαλύτερα αγόρια, και η λεφλουνομίδη. αν αποτύχει η θεραπεία με αυτούς τους παράγοντες, τότε μπορεί να χρησιμοποιηθεί αντι-tnfα θεραπεία ή Abatacept. ωστόσο, δεν υπάρχουν ακόμη σαφή δεδομένα αν η συνδυασμένη θεραπεία με μεθοτρεξάτη και inhtnfα ή Abatacept είναι αποτελεσματικότερη συγκριτικά με τη χορήγηση μονοθεραπείας μόνο με βιολογικό παράγοντα. εξαίρεση αποτελεί το infliximab για το οποίο θεωρείται απαραίτητη η συγχορήγησή του με μεθοτρεξάτη (η άλλο μη βιολογικό ανοσοτροποποιητικό φάρμακο), λόγω μικρότερου κινδύνου ανάπτυξης αντισωμάτων έναντι του infliximab που μειώνουν τη δραστικότητά του. Oι ενδαρθρικές εγχύσεις κορτικοστεροειδών μπορεί να χρησιμοποιηθούν ως συμπληρωματική θεραπεία σε μία ή σε λίγες πολύ επώδυνες ή διογκωμένες αρθρώσεις. η περιστασιακή χορήγηση κορτικοστεροειδών είναι πολλές φορές απαραίτητη ως θεραπεία «γέφυρας» αναμένοντας την έναρξη της δράσης του ανοσοτροποποιητικού φαρμάκου ή κατά τη διάρκεια σοβαρών εξάρσεων μέχρι να επέλθει έλεγχος της νόσου 201 (εικόνα 9β). Πρόσφατα, το Tocilizumab (Roactempra ) πήρε ένδειξη για χορήγησή του στην πολυαρθρική υποομάδα έναρξης της NiA σε παιδιά 2 ετών Θεραπεία πολυαρθρίτιδας με θετικό ρευματοειδή παράγοντα (RF) Oι ασθενείς που ανήκουν στην υποομάδα αυτή της NiA έχουν συνήθως κακή πρόγνωση όσον αφορά στην έκβαση της νόσου και πρέπει από την αρχή να αντιμετωπίζονται επιθετικά και συγκεκριμένα με πρώιμη έναρξη μεθοτρεξάτης και προσθήκη inhtnfα ή Abatacept ή Tocilizumab στους ασθενείς που έχουν ανεπαρκή απάντηση στη μεθοτρεξάτη. το Tocilizumab (RoActempra ), όπως αναφέρθηκε προηγουμένως, πήρε πρόσφατα ένδειξη για χορήγησή του στην πολυαρθρική υποομάδα έναρξης της NiA σε παιδιά 2 ετών 201 (εικόνα 9β). αν και στα παιδιά δεν υπάρχει ακόμη μεγάλη εμπειρία, άλλες θεραπευτικές επιλογές (πχ Rituximab) ή συνδυασμοί θεραπείας, αποτελεσματικοί στη Ρευματοειδή αρθρίτιδα των ενηλίκων, μπορεί να αποδειχθούν χρήσιμοι στον έλεγχο της νόσου στη δυσίατη αυτή υποομάδα της NiA. 93
94 Θεραπεία ψωριασικής αρθρίτιδας δεν υπάρχουν ακόμη μελέτες σχετικά με τη θεραπεία της υποομάδας αυτής στα παιδιά. η έναρξη και η πορεία της ψωριασικής αρθρίτιδας μπορεί να ομοιάζει είτε με αυτήν της ολιγοαρθρικής έναρξης είτε της πολυαρθρικής έναρξης NiA, είτε της αρθρίτιδας που σχετίζεται με ενθεσίτιδα και μέχρι να υπάρξουν νέα δεδομένα, η ψωριασική αρθρίτιδα στα παιδιά αντιμετωπίζεται ανάλογα με αυτά που ισχύουν για τις παραπάνω υποομάδες Θεραπεία της αρθρίτιδας που σχετίζεται με ενθεσίτιδα iσχυρά δεδομένα δεν υπάρχουν για την αντιμετώπιση της υποομάδας αυτής. ωστόσο, έχει φανεί ότι η σουλφασαλαζίνη δρα ευνοϊκά σε αυτούς τους ασθενείς, ειδικά στα μεγαλύτερα αγόρια με περιφερική αρθρίτιδα. δεν υπάρχουν μελέτες για τη μεθοτρεξάτη στη μορφή αυτή της νόσου. Σε ανοιχτές σειρές ασθενών έχει βρεθεί ότι η αντι-tnf θεραπεία είναι ιδιαίτερα αποτελεσματική Θεραπεία ιριδοκυκλίτιδας η τοπική έγχυση σταγόνων κορτικοστεροειδών και μυδριατικών φαρμάκων, που εμποδίζουν την ανάπτυξη συμφύσεων, αποτελεί τη θεραπεία εκλογής. δυστυχώς, παρά τις γνωστές επιπλοκές της ιριδοκυκλίτιδας και της θεραπείας της με τοπικά κορτικοστεροειδή (καταρράκτης, γλαύκωμα), μέχρι προσφάτως η πλειονότητα των ασθενών δεν αντιμετωπιζόταν με κάποιο ανοσοτροποποιητικό φάρμακο, που θα βοηθούσε στη μείωση της δόσης των κορτικοειδών. η χρησιμότητα των μη βιολογικών ανοσοτροποποιητικών φαρμάκων, και ιδιαίτερα της μεθοτρεξάτης, έχει αναφερθεί σε αρκετές μη ελεγχόμενες μελέτες. Για τους ασθενείς που δεν απαντούν στη μεθοτρεξάτη, η προσθήκη του ιnfliximab ή του αdalimumab, αλλά όχι του εtanercept, εμφανίζεται να είναι αποτελεσματική. η κυκλοσπορίνη δε φαίνεται να δρα σημαντικά. τέλος, υπάρχουν λίγα δεδομένα όσον αφορά στην αποτελεσματικότητα του μυκοφενολικού οξέως και της αζαθειοπρίνης στην ιριδοκυκλίτιδα που σχετίζεται με τη NiA 186.
95 95 Εικόνα 8. Μονοπάτια αντιμετώπισης των ασθενών με συστηματική αρθρίτιδα οι οποίοι έχουν συστηματικά συμπτώματα και διαφόρου βαθμού υμενίτιδα update of the 2011 American College of Rheumatology recommendations for the treatment of juvenile idiopathic arthritis: recommendations of the medical therapy of children with systemic juvenile idiopathic arthritis and tuberculosis screening among children receiving biologic medications. Arthritis Care Res 2013;65(10):
96 96 History of Arthritis of 4 or Fewer Joints History of Arthritis of 5 or more Joints Escalation of Therapy Disease activity: High Poor Prognostic Features: Present Following Initial Joint Injection(s): Disease activity: Moderate Poor Prognostic Features: Present -OR- Disease activity: High Poor Prognostic Features: Irrespective Disease activity: Low, Moderate or High Poor Prognostic Features: Irrespective Glucocorticoid Joint Injection(s) Methotrexate* Disease activity: Low Poor Prognostic Features: Absent No Joint Contracture Following 2 months NSAID: Disease activity: Low, Moderate or High Poor Prognostic Features: Irrespective Adjunct NSAID as needed Following Initial Joint Injection(s): Disease activity: Low Poor Prognostic Features: Present -OR- Disease activity: Moderate Poor Prognostic Features: Irrespective Adjunct NSAID or Joint Injection as needed NSAID monotherapy Escalation of Therapy Following 1 month NSAID: Disease activity: High Disease activity: Low Poor Prognostic Features: Poor Prognostic Features: Irrespective -OR- Present -OR- Disease activity: Moderate Following 1 to 2 months NSAID: Poor Prognostic Features: Disease activity: Moderate Present Poor Prognostic Features: Irrespective Adjunct NSAID Methotrexate* or Joint Injection as needed Following 3 months MTX: Following 6 months MTX: Disease activity: Moderate, Disease activity: Low High Poor Prognostic Features: Poor Prognostic Features: Irrespective Irrespective Adjunct NSAID TNFα inhibitor or Joint Injection as needed Following 3 months MTX: Disease activity: Moderate or High Poor Prognostic Features: Present Following 6 months MTX: Disease activity: High Poor Prognostic Features: Irrespective Following 4 months TNFα inhibitor: Disease activity: Moderate, High Poor Prognostic Features: Irrespective TNFα inhibitor Adjunct NSAID or Joint Injection as needed 2nd TNFα inhibitor or Abatacept Εικόνα 9. Συστάσεις αντιμετώπισης των ασθενών με ιστορικό προσβολής 4 ή λιγότερων αρθρώσεων (Α). Συστάσεις αντιμετώπισης των ασθενών με ιστορικό προσβολής 5 ή περισσοτέρων αρθρώσεων (Β). Beukelman T, Patkar N, Saag K, et al American College of Rheumatology recommendations for the treatment of juvenile idiopathic arthritis: initiation and safety monitoring of theurapeutic agents for the treatment of arthritis and systemic features. Arthritis Care Res (Hoboken) 2011;63(4):
97 ειδικo μερoσ
98
99 1. Σ Κ OΠOΣ Τ Η Σ Μ Ε Λ Ε Τ Η Σ Κ Α Ι Ε Ρ Ε Υ Ν Η Τ Ι Κ Α Ε Ρ Ω Τ Η Μ Α Τ Α η Νεανική ιδιοπαθής αρθρίτιδα (NiA) είναι το πιο συχνό ρευματικό νόσημα που συναντάται στα παιδιά και θεωρείται το αποτέλεσμα απορρύθμισης του ανοσιακού συστήματος, εξαιτίας αλληλεπιδράσεων μεταξύ γενετικών και περιβαλλοντολογικών παραγόντων. δεδομένα σχετικά με την έκβαση των ασθενών με NiA λείπουν για τον ελληνικό πληθυσμό. O πρώτος από τους στόχους της παρούσης μελέτης είναι η ανάλυση της συνολικής πορείας και της μακροχρόνιας έκβασης των ασθενών με NiA καθώς και η ανάδειξη παραγόντων κινδύνου κατά την έναρξη που προδιαθέτουν για επιθετικότερη νόσο στον ελληνικό πληθυσμό ασθενών. η γνώση της πορείας και της μακροχρόνιας έκβασης των ασθενών με NiA είναι αναγκαία τόσο σε επίπεδο συμβουλευτικής, όσο και για τη δυνατότητα να παρουσιάζονται οι κατάλληλες θεραπευτικές επιλογές στους ασθενείς και στις οικογένειές τους. η χρήση των σύγχρονων κριτηρίων ταξινόμησης και των νεότερων εργαλείων εκτίμησης της νόσου θα επιτρέψουν τη σύγκριση με πρόσφατες μελέτες σε άλλους εθνικούς ή φυλετικούς πληθυσμούς. O δεύτερος στόχος μας είναι η διερεύνηση της σχέσης πέντε γονιδίων με αυξημένη επιδεκτικότητα της NiA στον ελληνικό πληθυσμό. τα γονίδια που εξετάσαμε έχει βρεθεί σε προηγούμενες μελέτες ότι συσχετίζονται με αυξημένο κίνδυνο ανάπτυξης NiA σε άλλους εθνικούς ή φυλετικούς πληθυσμούς. με την παρούσα μελέτη προσεγγίζεται η απάντηση σε καθένα από τα παρακάτω ερευνητικά ερωτήματα: 1. Η Νεανική Ιδιοπαθής Αρθρίτιδα είναι μία ήπια νόσος στην Ελλάδα, όπως προκύπτει από την εμπειρία του παιδορευματολογικού και ρευματολογικού κέντρου αναφοράς στη Θεσσαλονίκη; 2. Η πρόγνωση της Νεανικής Ιδιοπαθής Αρθρίτιδας (στην Ελλάδα) έχει βελτιωθεί τα τελευταία χρόνια; 99
100 Είναι προβλέψιμη η πορεία και μακροχρόνια έκβαση της Νεανικής Ιδιοπαθούς Αρθρίτιδας και ποιοι είναι οι παράγοντες εκείνοι που προδιαθέτουν για επιθετικότερη νόσο; 4. Υπάρχει γενετική συσχέτιση πέντε συγκεκριμένων SNPs, οποίοι βρέθηκε ότι συσχετίζονται με NIA σε άλλους εθνικούς πληθυσμούς, με την επιδεκτικότητα της NIA στην Ελλάδα;
101 2. Κ Λ Ι Ν Ι Κ Η Μ Ε Λ Ε Τ Η 2.1 Ασθενείς - Κριτήρια εισαγωγής στο κλινικό μέρος της μελέτης μεταξύ ιανουαρίου 2008 και δεκεμβρίου 2011 μελετήθηκαν συνολικά 102 ασθενείς οι οποίοι πληρούσαν συγκεκριμένα κριτήρια εισαγωγής: Κριτήρια εισαγωγής στη κλινικό μέρος της μελέτης: 1) τρέχουσα ηλικία στην τελευταία επίσκεψη παρακολούθησης 18 ετών, 2) διάρκεια νόσου 5 έτη, 3) σαφής διάγνωση NiA, σύμφωνα με τα αναθεωρημένα, κατά το 2001, ilar κριτήρια, 4) παρακολούθηση, αποκλειστικά, στα εξωτερικά ιατρεία του ρευματολογικού τμήματος της δ Παθολογικής κλινικής, με επιτρεπόμενο διάστημα παρακολούθησης εκτός κέντρου (σε άλλο νοσοκομείο ή σε ιδιώτη ιατρό) μικρότερο από 6 μήνες, 5) διάγνωση, παρακολούθηση μέχρι την ενηλικίωση χωρίς κενά >6 μήνες και παραπομπή των ασθενών από το ρευματολογικό τμήμα της α Παιδιατρικής κλινικής, 6) έγγραφη συγκατάθεση συμμετοχής τους στη μελέτη. Oι ασθενείς που διαγνώσθηκαν, πριν τη δημοσίευση των ilar κριτηρίων, επαναταξινομήθηκαν, εφαρμόζοντας τα παραπάνω κριτήρια. Oι ασθενείς αυτοί αποτέλεσαν το δείγμα του κέντρου αναφοράς. επιπλέον, προκειμένου να γίνει αντικειμενικότερη προσέγγιση της μακροχρόνιας έκβασης των ασθενών με NiA στον ελληνικό χώρο, επιχειρήθηκε τηλεφωνική επικοινωνία με άλλους 285 ασθενείς με σαφή διάγνωση NiA, οι οποίοι είχαν διαγνωσθεί στο ρευματολογικό τμήμα της α Παιδιατρικής κλινικής, είχαν διάρκεια νόσου 5 έτη, τρέχουσα ηλικία 18 έτη και δεν παρακολουθήθηκαν στο ρευματολογικό τμήμα της δ Παθολογικής κλινικής ως ενήλικες. μετά την επιλογή των παραπάνω ασθενών από το αρχείο που διατηρεί η α Παιδιατρική κλινική, καταγράφηκαν αναδρομικά από τους φακέλους παρακολούθησης, το φύλο, η ημερομηνία γέννησης, η ημερομηνία έναρξης της νόσου και η υποομάδα της ΝiA, σύμφωνα με τα αναθεωρημένα, κατά το 2001, ilar κριτήρια. Oι ασθενείς που διαγνώσθηκαν, πριν τη δη- 101
102 102 μοσίευση των ilar κριτηρίων, επαναταξινομήθηκαν και πάλι βάσει των παραπάνω κριτηρίων. από τους 285 ασθενείς (153 γυναίκες και 132 άντρες) οι οποίοι αναζητήθηκαν τηλεφωνικά, οι 77 (42 γυναίκες και 35 άντρες) δεν απάντησαν, είχαν αλλάξει τηλεφωνικό αριθμό ή δε θέλησαν να συμμετάσχουν στη μελέτη. τρεις ασθενείς είχαν αποβιώσει, οι δύο λόγω νόσου (ένα κορίτσι με οροαρνητική πολυαρθρικής έναρξης NiA και ένα αγόρι με συστηματική αρθρίτιδα) και μία ασθενής εξαιτίας ατυχήματος. επομένως, στη μελέτη τελικά συμπεριλήφθηκαν 205 ασθενείς (109 γυναίκες και 96 άντρες) που αποτέλεσαν το δείγμα βασισμένο σε πληθυσμό ασθενών με NiA. τελικά προέκυψε συνολικό δείγμα 307 ασθενών. 2.2 Υλικό και Μέθοδοι Καταγραφή δεδομένων από τους φακέλους των ασθενών - Oρισμός μεταβλητών Για τους ασθενείς που πληρούσαν τα κριτήρια εισαγωγής στο κλινικό μέρος της μελέτης συλλέχθησαν αναδρομικά στοιχεία από τους φακέλους πα ρα - κολούθησής τους και οι ίδιοι εκτιμήθηκαν κλινικά και κατόπιν εργαστη ρια κού και ακτινολογικού ελέγχου στην τελευταία επίσκεψη παρακολούθησής τους. αναλυτικά, τα στοιχεία που καταγράφηκαν από τους φακέλους για κάθε ασθενή είναι τα παρακάτω: 1. το φύλο. 2. η ημερομηνία γέννησης. 3. η ημερομηνία διάγνωση της νόσου. 4. η ηλικία του ασθενούς, κατά την έναρξη της νόσου. η ηλικία του κατά την έναρξη της νόσου ορίστηκε ως η ημερομηνία κατά την οποία η αρθρίτιδα ή τα συστηματικά συμπτώματα τεκμηριώθηκαν από ιατρό. 5. η παρουσία θετικού τίτλου RF, ANA κατά την έναρξη της νόσου. 6. τα hla γονίδια A,B,DRB1. 7. η διάρκεια νόσου. 8. η υποομάδα της νόσου κατά ilar. Όλοι οι ασθενείς που διαγνώσθηκαν ότι πάσχουν από νεανική αρθρίτιδα πριν τη δημοσίευση των ilar κριτηρίων, ταξινομήθηκαν εκ νέου, χρησιμοποιώντας τα παραπάνω κριτήρια. 9. Oι αρθρώσεις που έχουν προσβληθεί. 10. η πορεία της νόσου (πολυαρθρική ή ολιγοαρθρική). 11. η προσβολή ή όχι των ιερολαγόνιων αρθρώσεων και της σπονδυλικής στήλης. 12. το ιστορικό ιριδοκυκλίτιδας.
103 το χρονικό διάστημα που μεσολάβησε ανάμεσα στην εμφάνιση αρθρίτιδας και ιριδοκυκλίτιδας. 14. η παρουσία ιστορικού ψωρίασης και το χρονικό διάστημα που μεσολάβησε ανάμεσα στην εμφάνιση ψωρίασης και αρθρίτιδας. 15. το οικογενειακό ιστορικό αρθρίτιδας (ρευματοειδούς, ψωριασικής, αγκυλοποιητικής σπονδυλοαρθρίτιδας καθώς και νεανικής ιδιοπαθούς αρθρίτιδας) σε συγγενείς πρώτου και δεύτερου βαθμού. 16. η συνύπαρξη αυτοανόσων νοσημάτων στον ίδιο ασθενή. 17. η συνύπαρξη άλλων, μη αυτοανόσων νοσημάτων, στον ίδιο ασθενή. 18. O αριθμός των χειρουργείων στις αρθρώσεις που υποβλήθηκε ο κάθε ασθενής, ποιες αρθρώσεις χρειάστηκαν χειρουργική παρέμβαση και το χρονικό διάστημα ανάμεσα στην έναρξη της νόσου και στην πραγματοποίηση του πρώτου χειρουργείου. 19. το ιστορικό χειρουργικής επέμβασης στους οφθαλμούς και το χρονικό διάστημα ανάμεσα στην έναρξη της νόσου και στην διενέργεια του πρώτου χειρουργείου. 20. Σε κάθε κλινική επίσκεψη καταγράφηκε η χορηγούμενη φαρμακευτική αγωγή και καθορίστηκε για κάθε ασθενή η φάση ενεργότητας της νόσου (ενεργός νόσος έναντι μη ενεργός νόσος). Για τον ορισμό της μη ενεργού νόσου και της κλινικής ύφεσης χρησιμοποιήθηκαν τα κριτήρια της Wallace και συν, σύμφωνα με τα οποία οι ασθενείς χαρακτηρίστηκαν ότι έχουν μη ενεργό νόσο, εφόσον πληρούνται όλα τα παρακάτω: απουσία ενεργού αρθρίτιδας, απουσία πυρετού, εξανθήματος, ορογονίτιδας, σπληνομεγαλίας ή γενικευμένης λεμφαδενοπάθειας που μπορεί να αποδοθεί στην Νια, απουσία ενεργού ιριδοκυκλίτιδας, φυσιολογική τκε ή CRP (ή εφόσον είναι αυξημένες δεν πρέπει να σχετίζονται με τη Νια), απουσία ενεργού νόσου στην εκάστοτε χρησιμοποιούμενη κλίμακα κατά τη συνολική εκτίμηση του ιατρού και πρωινή δυσκαμψία 15 λεπτά 147,152. Λόγω του γεγονότος ότι τα κριτήρια της Wallace έχουν σταθμιστεί μόνο για τους ασθενείς με περιφερική αρθρίτιδα, προκειμένου να θεωρηθεί μη ενεργός η νόσος στους ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα ή ψωριασική αρθρίτιδα και προσβολή του αξονικού σκελετού ήταν επιπλέον απαραίτητη η καταγραφή της αναφοράς απουσίας συμπτωμάτων οσφυοϊερού πόνου από τον ασθενή και η κλινική εκτίμηση του ιατρού που να δηλώνει απουσία ενθεσίτιδας και ενεργότητας από τις ιερολαγόνιες αρθρώσεις. αν η φάση της νόσου δε μπορούσε να τεκμηριωθεί, λόγω ανεπαρκών ή ασαφών δεδομένων, τότε χαρακτηριζόταν ως «μη ταξινομήσιμη». 17. Για κάθε ασθενή υπολογίστηκε ο αριθμός των επεισοδίων και η
104 104 διάρκεια του κάθε επεισοδίου μη ενεργού νόσου, τόσο κατά τη διάρκεια των πρώτων 5 ετών, όσο και κατά τη συνολική διάρκεια της νόσου. Για τους ασθενείς που η νόσος τους παρουσίαζε διαλείπουσα πορεία, με εξάρσεις και υφέσεις, η συνολική ενεργότητα νόσου αποτέλεσε το άθροισμα των επεισοδίων ενεργού νόσου. Oι ασθενείς μπορούσαν να έχουν πολλά επεισόδια ενεργής και μη ενεργής νόσου. η έναρξη ενός επεισοδίου μη ενεργής νόσου, ορίστηκε ως η μέρα της κλινικής επίσκεψης, όπου ο ασθενής τεκμηριώθηκε ότι έχει μη ενεργό νόσο και η κλινική του κατάσταση στην αμέσως προηγούμενη επίσκεψή είχε χαρακτηριστεί ως ενεργός. η λήξη ενός επεισοδίου μη ενεργού νόσου ορίστηκε ως η πρώτη ημερομηνία της κλινικής επίσκεψης που διαπιστώθηκε εκ νέου ενεργός νόσος. κάθε επεισόδιο μη ενεργού νόσου, επίσης, εκτιμήθηκε αν πληροί τα κριτήρια κλινικής ύφεσης με φαρμακευτική αγωγή (6 μήνες μη ενεργού νόσου, ενώ λαμβάνει οποιοδήποτε φάρμακο για την αρθρίτιδα ή την ιριδοκυκλίτιδα) ή χωρίς φαρμακευτική αγωγή (12 μήνες μη ενεργού νόσου, ενώ δε λαμβάνει κάποιο φάρμακο για την αρθρίτιδα ή την ιριδοκυκλίτιδα). Όλοι οι ασθενείς θεωρήθηκαν ότι έχουν ενεργό νόσο στην πρώτη τους επίσκεψη και σε κάθε επακόλουθη επίσκεψη, όπου η νόσος χαρακτηρίστηκε ως ενεργός και στην αμέσως προηγούμενη επίσκεψη, η νόσος είχε θεωρηθεί ως μη ενεργός. το τέλος ενός επεισοδίου ενεργού νόσου, ορίστηκε ως η ημερομηνία της πρώτης κλινικής επίσκεψης, στην οποία ο ασθενής πληρούσε τα κριτήρια για μη ενεργό νόσο. 18. η επίτευξη ή όχι κλινικής ύφεσης τα πρώτα 2 έτη από την έναρξη της νόσου είτε με φαρμακευτική αγωγή, είτε χωρίς φαρμακευτική αγωγή. 19. η φαρμακευτική αγωγή που έχει λάβει, συνολικά, σε όλη τη διάρκεια της νόσου. 20. το χρονικό διάστημα (σε μήνες) που έλαβε το καθέ φάρμακο. 21. αν ο ασθενής έχει λάβει μόνο μονοθεραπεία ή αν έχει λάβει και συνδυασμένη θεραπεία κατά τη διάρκεια της νόσου. 22. Ποια φάρμακα έχουν δοθεί ως μονοθεραπεία και ποιοι συνδυασμοί συνιστούσαν τη συνδυασμένη θεραπεία. 23. το χρονικό διάστημα (σε μήνες) που ο ασθενής έχει λάβει μονοθεραπεία ή συνδυασμένη θεραπεία τόσο συνολικά, όσο και για κάθε φάρμακο ή συγκεκριμένο συνδυασμό φαρμάκων. 24. το χρονικό διάστημα που μεσολάβησε ανάμεσα στην έναρξη της νόσου και στη χορήγηση βιολογικού παράγοντα η ένταξη των ασθενών στη μελέτη έλαβε χώρα μεταξύ ιανουαρίου 2008 και δεκεμβρίου Στην τελευταία επίσκεψη παρακολούθησης των ασθε-
105 105 νών στο εξωτερικό ιατρείο, που αποτέλεσε και την επίσκεψη αξιολόγησής τους στα πλαίσια της μελέτης, πραγματοποιήθηκε κλινική εξέταση και καθορισμός της κατάστασης ενεργότητας νόσου, της σωματικής λειτουργικής ικανότητάς τους και κλινική εκτίμηση της αρθρικής και εξωαρθρικής καταστροφής. μετρήθηκε, κατόπιν, το τελικό ύψος και ο δείκτης μάζας σώματος και ακολούθησε αξιολόγηση της γενικής υγείας των ασθενών και καταγραφή της κοινωνικοοικονομικής τους κατάστασης. επιπλέον, οι ασθενείς υποβλήθηκαν σε ακτινολογικό, εργαστηριακό και οφθαλμολογικό έλεγχο. τέλος, ακολούθησε σε όλους τυποποιημένη συνέντευξη. αναλυτικά, τα εργαλεία που χρησιμοποιήθηκαν και οι μέθοδοι που ακολουθήθηκαν, κατά την επίσκεψη στα πλαίσια της μελέτης είναι οι παρακάτω: Κλινικοεργαστηριακή εκτίμηση - Oρισμός μεταβλητών Εκτίμηση της κατάστασης ενεργότητας νόσου καταγράφηκε ο αριθμός των διογκωμένων αρθρώσεων, ο αριθμός των αρθρώσεων με ευαισθησία και πραγματοποιήθηκε πλήρης κλινική εξέταση για πιθανή παρουσία πυρετού, εξανθήματος, σπληνομεγαλίας και γενικευμένης λεμφαδενοπάθειας. χρησιμοποιήθηκε η οπτική αναλογική κλίμακα μήκους 10cm (Visual Analogue Scale, VAS, όπου 0=απουσία ενεργότητας και 10=μέγιστη ενεργότητα νόσου), για τη σφαιρική εκτίμηση της ενεργότητας νόσου από τον ίδιο τον ασθενή και από τον ιατρό. η κλίμακα VAS αναφέρεται, τυπικά, στην τελευταία εβδομάδα. Για τους ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και ψωριασική αρθρίτιδα με προσβολή του αξονικού σκελετού υπολογίστηκε ο δείκτης ASDAS (Ankylosing Spondylitis Disease Activity Score) 203. κανένας από τους ασθενείς με αδιαφοροποίητη αρθρίτιδα δεν είχε αξονική προσβολή. Για τον υπολογισμό του δείκτη ASDAS είναι αναγκαία η εισαγωγή στην ειδική εφαρμογή των παρακάτω μεταβλητών: εκτίμηση από τον ασθενή του οσφυϊκού του πόνου, του πόνου/διόγκωσης των περιφερικών αρθρώσεων, της διάρκειας πρωινής δυσκαμψίας και της σφαιρικής εκτίμησης της ενεργότητας νόσου του (όλα τα προηγούμενα σε αριθμητική κλίμακα 0-10), και η τιμή της CRP σε mg/dl (ή της τιμής της τκε, σε περίπτωση που δεν είναι διαθέσιμη η CRP). O υπολογισμός του δείκτη ASDAS απαιτεί αριθμομηχανή και δίνεται από τον τύπο: ASDAS-CRP=0.12 Oσφυϊκός πόνος διάρκεια πρωινής δυσκαμψίας Σφαιρική εκτίμηση της ενεργότητας νόσου περιφερικός πόνος/διόγκωση Ln(CRP +1)
106 106 Σύμφωνα με το δείκτη ASDAS, τιμή < 1.3 υποδεικνύει μη ενεργό νόσο, >1.3 και <2.1 μέτρια ενεργότητα, >2.1 και <3.5 υψηλή ενεργότητα και >3.5 πολύ υψηλή ενεργότητα νόσου. Για τον ορισμό της κλινικής ύφεσης, εφαρμόστηκαν τα κριτήρια της Wallace, σύμφωνα με τα οποία, απαιτείται η παρουσία μη ενεργού νόσου για 6 συνεχόμενους μήνες, όταν ο ασθενής λαμβάνει φαρμακευτική αγωγή (κλινική ύφεση με φαρμακευτική αγωγή) ή για 12 συνεχόμενους μήνες, ενώ ο ασθενής δε λαμβάνει φαρμακευτική αγωγή, τόσο για την αρθρίτιδα, όσο και για την ιριδοκυκλίτιδα. η μη ενεργός νόσος, όπως αναφέρθηκε και νωρίτερα, ορίζεται ως απουσία ενεργού αρθρίτιδας, πυρετού, εξανθήματος, ορογονίτιδας, σπληνομεγαλίας, γενικευμένης λεμφαδενοπάθειας, ενεργού ιριδοκυκλίτιδας σε συνδυασμό με φυσιολογικά επίπεδα τκε ή CRP, διάρκεια πρωινής δυσκαμψίας <15 λεπτά και απουσία ενεργότητας κατά την εκτίμηση του ιατρού (βαθμολόγηση με το καλύτερο δυνατό σκορ, ανάλογα με την κλίμακα που χρησιμοποιείται). Για τους ασθενείς με αξονική προσβολή, o ορισμός της μη ενεργού νόσου απαιτούσε επιπλέον και τιμή του δείκτη ASDAS <1.3. Oι ασθενείς κρίθηκε ότι έχουν μη ενεργό νόσο, ανεξάρτητα από την παρουσία ή όχι ψωρίασης. Σε όλους τους ασθενείς εφαρμόστηκε ο δείκτης DAS και ξεχωριστά σε αυτούς που βρέθηκαν ότι έχουν ενεργό νόσο, έτσι ώστε να υπάρχει αριθμητική τιμή για το βαθμό ενεργότητάς τους. O δείκτης DAS28 υπολογίζεται, εισάγοντας στην ειδική εφαρμογή τον αριθμό των διογκωμένων αρθρώσεων (αδα), τον αριθμό των ευαίσθητων αρθρώσεων (αεα), την τιμή της σφαιρικής εκτίμησης της υγείας του ασθενούς από τον ιατρό (Γη), (σε αριθμητική κλίμακα VAS 0-100), και την τιμή της τκε την 1η ώρα. Για τον υπολογισμό του DAS28, εκτιμήθηκαν οι 28 συγκεκριμένες αρθρώσεις και όχι το σύνολο των αρθρώσεων που εξετάσθηκαν. Για τον υπολογισμό του δείκτη DAS28 απαιτείται, επίσης, αριθμομηχανή και η τιμή του δίνεται από τον τύπο: DAS28 (με 4 μεταβλητές) = 0.56X (AEA) X (Aδα) χ lognat (τκε) χ (Γη) Σύμφωνα με το δείκτη DAS28, τιμή <2.6 υποδηλώνει ύφεση, χαμηλή ενεργότητα νόσου, μέτρια ενεργότητα και τιμή >5.1 υψηλή ενεργότητα νόσου. Oι 205 ασθενείς με τους οποίους προηγήθηκε μόνο τηλεφωνική συνέντευξη θεωρήθηκε ότι βρίσκονται σε κατάσταση μακροχρόνιας ύφεσης της νόσου, εφόσον απαντούσαν αρνητικά και στις τρεις παρακάτω ερωτήσεις: 1) αν παίρνουν κάποια φαρμακευτική αγωγή που σχετίζεται με αρθρίτιδα, ιριδοκυκλίτιδα ή ψωρίαση τα τελευταία 2 έτη, 2) αν έχουν εμφανίσει πόνο
107 107 ή διόγκωση σε μία ή περισσότερες αρθρώσεις συνοδευόμενο ή όχι από πυρετό ή εξάνθημα τα τελευταία 2 έτη και 3) αν έχουν επισκεφθεί ρευματολόγο, οποίος διαπίστωσε ενεργότητα της νόσου ή χρειάστηκε να νοσηλευθούν εξαιτίας εκδηλώσεων που αποδόθηκαν στη NiA, τα τελευταία 2 έτη Εκτίμηση της σωματικής λειτουργικής ικανότητας Για την εκτίμηση της σωματικής λειτουργικής ικανότητας των ασθενών, χρησιμοποιήθηκε η ελληνική έκδοση του ερωτηματολογίου haq-di (health Assessment Questionnaire- Disability index). με το haq-di, εκτιμάται η ικανότητα των ασθενών να πραγματοποιούν τις δραστηριότητες της καθημερινής τους ζωής και απευθύνεται στην προηγούμενη εβδομάδα. αποτελείται από 20 ερωτήσεις που αφορούν κινήσεις στις οποίες εμπλέκονται τα άνω και/ή τα κάτω άκρα, οι οποίες είναι οργανωμένες στις παρακάτω 8 ενότητες: ντύσιμο και καθαριότητα, έγερση, φαγητό, περπάτημα, υγιεινή, άπλωμα χεριού, σφίξιμο χεριού και συνήθεις δραστηριότητες. κάθε ερώτηση βαθμολογείται με τιμή από 0 έως 3 (όπου 0=χωρίς καμία δυσκολία, 1=με κάποια δυσκολία, 2=με πολύ δυσκολία και 3=ανικανότητα να πραγματοποιήσει τη συγκεκριμένη δραστηριότητα). η ερώτηση με την υψηλότερη τιμή καθορίζει και την τιμή για τη συγκεκριμένη λειτουργική ενότητα. εάν είναι απαραίτητη η χρήση βοηθημάτων ή συγκεκριμένου εξοπλισμού ή απαιτείται βοήθεια από άλλο άτομο, προκειμένου να φέρει ο ασθενής σε πέρας κάποια από τις δραστηριότητες, τότε ο δείκτης haq-di λαμβάνει τιμή τουλάχιστον 2 για τη συγκεκριμένη κατηγορία. η τιμή του haq-di, προκύπτει ως ο μέσος όρος των τιμών στις 8 επιμέρους κατηγορίες και κυμαίνεται από 0 έως 3, όπου οι υψηλό - τερες τιμές υποδηλώνουν μεγαλύτερη έκπτωση της λειτουργικής ικανότητας. Για το σκοπό της μελέτης, οι τιμές του haq-di, διαιρέθηκαν σε 4 κατηγορίες: 0=φυσιολογική σωματική λειτουργική ικανότητα, =ήπιος περιορισμός της σωματικής λειτουργικής ικανότητας, =μέτριος περιορισμός της σωματικής λειτουργικής ικανότητα και =σοβαρός περιορισμός της σωματικής λειτουργικής ικανότητας. τα όρια αυτά έχουν χρησιμοποιηθεί σε προηγούμενες μεγάλες μελέτες 133,204. κάθε ασθενής ταξινομήθηκε σε μία από τις προαναφερόμενες κατηγορίες σωματικής λειτουργικής ικανότητας. Για τους ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και ψωριασική αρθρίτιδα με προσβολή του αξονικού σκελετού, η σωματική λειτουργική ικανότητα εκτιμήθηκε, επιπρόσθετα, με το δείκτη BASFi (Bath Ankylosing Spondylitis Functional index) 205. Σε ενήλικες ασθενείς με Νια, τα δεδομένα από τη χρήση του παραπάνω δείκτη είναι ελάχιστα 206,207, ωστόσο, στις φλεγ-
108 108 μονώδεις σπονδυλοαρθρίτιδες των ενηλίκων, ο δείκτης BASFi, χρησιμοποιείται ευρέως και έχει καθιερωθεί στη μέτρηση της σωματικής λειτουργικής ικανότητας των ασθενών 205. Πρόκειται για ερωτηματολόγιο που περιλαμβάνει συνολικά 10 ερωτήσεις, από τις οποίες οι 8 εστιάζουν στην αναζήτηση παρουσίας περιορισμού στις δραστηριότητες που εξαρτώνται από την κινητικότητα της σπονδυλικής στήλης και των κάτω άκρων και οι 2 σε άλλες καθημερινές δραστηριότητες. κάθε ερώτηση βαθμολογείται σε αριθμητική κλίμακα από 0-10, όπου 0= πραγματοποιώ χωρίς καμία δυσκολία και 10=ανίκανος/η να πραγματοποιήσω. O μέσος όρος της τιμής των 10 ερωτήσεων δίνει το BASFi σκορ. η εκτίμηση της λειτουργικής ικανότητας των 205 ασθενών με τους οποίους υπήρξε μόνο τηλεφωνική επικοινωνία επιτεύχθηκε μέσω του ερωτηματολογίου haq-di, το οποίο εφαρμόστηκε στους παραπάνω ασθενείς μέσω της τηλεφωνικής συνέντευξης. Στη συνέχεια οι ασθενείς, βάσει των απαντήσεών τους στο ερωτηματολόγιο, ταξινομήθηκαν σε δύο μεγάλες, αδρές κατηγορίες: α) σε αυτούς που δεν ανέφεραν κανένα περιορισμό (haq-di=0) και β) σε αυτούς που είχαν κάποιο βαθμό περιορισμού (haq-di>0) Κλινική εκτίμηση της αρθρικής και εξωαρθρικής καταστροφής O βαθμός της αρθρικής και εξωαρθρικής καταστροφής εκτιμήθηκε με το εργαλείο Juvenile Arthritis Damage index (JADi) 160. Όπως αναφέρθηκε και νωρίτερα, το JADi συνίσταται από 2 μέρη: το JADi-A, με το οποίο καταγράφεται η αρθρική καταστροφή και το JADi-ε με το οποίο σημειώνεται η εξωαρθρική καταστροφή. αναλυτικότερα, με το δείκτη JADi-A, καταγράφονται οι μόνιμες αλλοιώσεις σε 36 αρθρώσεις ή ομάδες αρθρώσεων οι οποίες βαθμολογούνται με 1 βαθμό, σε περίπτωση μερικής καταστροφής ή με 2 βαθμούς όταν παρατηρείται σοβαρή βλάβη, αγκύλωση ή έχει προηγηθεί αρθροπλαστική. Oι αρθρώσεις ή οι ομάδες αρθρώσεων που αξιολογούνται είναι οι παρακάτω: Κροταφογναθικές: εκτιμώνται μαζί, ως μία ομάδα. ελέγχεται η παρουσία μικρογναθίας ή ασυμμετρίας του προσώπου, που είναι αρκετά σοβαρή έτσι ώστε να προκαλείται αισθητικό πρόβλημα και/ή διαταραχές της ευθυγράμμισης των οδόντων (βαθμός 1) ή σοβαρός περιορισμός στη διάνοιξη του στόματος (που δεν επιτρέπει την εισαγωγή 3 δακτύλων) με συνοδό ακτινογραφικές αλλαγές στις αρθρώσεις (βαθμός 2). Αυχενική μοίρα της σπονδυλικής στήλης: έκταση <50% του φυσιολογικού εύρους ή υπεξάρθρημα διαπιστωμένο ακτινολογικά (βαθμός 1), αγκύλωση ή ιστορικό πίεσης του μυελού ή χειρουργική επέμβαση (βαθμός 2).
109 109 Ώμοι: έξω στροφή <50% του φυσιολογικού εύρους και/ή απαγωγή <180 (βαθμός 1), αγκύλωση ή πρόθεση (βαθμός 2) Αγκώνες: σύγκαμψη <30 (βαθμός 1), σύγκαμψη >30, αγκύλωση ή πρόθεση (βαθμός 2). Καρποί: έκταση ή κάμψη < 50% του φυσιολογικού εύρους ή υπεξάρθρημα ή παλαμιαία, ωλένια ή κερκιδική απόκλιση (βαθμός 1), αγκύλωση ή πρόθεση (βαθμός 2). Μετακαρποφαλαγγικές: σύγκαμψη, ωλένια ή κερκιδική απόκλιση (βαθμός 1), υπεξάρθρημα, αγκύλωση ή πρόθεση (βαθμός 2) Εγγύς μεσοφαλαγγικές: σύγκαμψη (βαθμός 1), δυσμορφία δίκην λαιμού κύκνου ή Boutonniere ή αγκύλωση (βαθμός 2). Ισχία: έσω στροφή <10 (βαθμός 1), αγκύλωση ή πρόθεση (βαθμός 2) Γόνατα: βλαισσότητα >15 απότοκη της αρθρίτιδας, ή σύγκαμψη <25 (βαθμός 1), σύγκαμψη >25 ή πρόθεση (βαθμός 2). Ποδοκνημικές: εκτιμώνται μαζί ως μία ομάδα. μόνιμη βλαισσότητα <20 (βαθμός 1), μόνιμη βλαισσότητα > 20, αγκύλωση, αρθρόδεση ή πρόθεση (βαθμοί 2). Μεταταρσιοφαλλαγγικές: εκτιμώνται μαζί ως μία ομάδα. εμφανής δυσμορφία, λόγω της αρθρίτιδας (βαθμός 1), αρθροπλαστική (βαθμός 2). μια βλάβη βαθμολογείται μόνο όταν είναι παρούσα, δικαιολογείται από προηγούμενη προσβολή της άρθρωσης, δεν οφείλεται στην ύπαρξη ενεργού αρθρίτιδας τη στιγμή της εξέτασης και είναι παρούσα τους τελευταίους, τουλάχιστον, 6 μήνες. το μοναδικό εργαλείο που απαιτείται είναι ένα γωνιόμετρο, ωστόσο, οι περισσότερες αρθρώσεις μπορεί να εκτιμηθούν και χωρίς αυτό. O δείκτης JADi-A, λαμβάνει μέγιστη τιμή το 72. με το δείκτη JADi-E, αξιολογούνται 13 σημεία, που είναι κατανεμημένα σε 5 όργανα/συστήματα. κάθε σημείο βαθμολογείται με 0 ή 1, ανάλογα με το εάν η βλάβη είναι απούσα ή παρούσα, αντιστοίχως. εξαιτίας, του μεγάλου αντίκτυπου που έχει η οφθαλμική βλάβη στην υγεία του ασθενούς, αποφασίστηκε να δοθούν, για κάθε μάτι, 2 βαθμοί, στη περίπτωση που έχει προηγηθεί χειρουργική επέμβαση και 3 βαθμοί, όταν έχει πλέον, εγκατασταθεί μόνιμη τύφλωση. Όπως τονίστηκε και για το δείκτη JADi-A, οι βλάβες πρέπει να είναι μη αναστρέψιμες και παρούσες για τους τελευταίους, τουλάχιστον, 6 μήνες. η μέγιστη συνολική τιμή που λαμβάνει ο δείκτης JADi-E είναι το 17. αναλυτικότερα, τα 13 σημεία που αξιολογούνται είναι τα παρακάτω: Oφθαλμοί: καταρράκτης και/ή άλλη επιπλοκή της ιριδοκυκλίτιδας (1 βαθμός), 2 βαθμοί σε περίπτωση χειρουργείου στον οφθαλμό ή 3 βαθμοί στην περίπτωση μόνιμης τύφλωσης.
110 110 Μυοσκελετικό σύστημα (με εξαίρεση τις αρθρώσεις): βαθμολογείται η σοβαρή μυϊκή ατροφία, το οστεοπορωτικό κάταγμα ή η καθίζηση της σπονδυλικής στήλης, η άσηπτη νέκρωση οστού, η σημαντική διαταραχή της καμπύλης της σπονδυλικής στήλης, που προκύπτει λόγω ανισοσκελίας ή βλάβης του ισχίου και ξεχωριστά η σημαντικού βαθμού ανισοσκελία ή άλλη τοπική διαταραχή της ανάπτυξης ενός οστού. Δέρμα: βαθμολογείται η παρουσία ραγάδων και η υποδόρια ατροφία του δέρματος λόγω ενδαρθρικών ενέσεων κορτιζόνης. Ενδοκρινείς αδένες: βαθμολογείται η ανεπαρκής ανάπτυξη, η καθυστέρηση της εφηβείας και η εμφάνιση σακχαρώδους διαβήτη. Δευτεροπαθής αμυλοείδωση: βαθμολογείται η ανάπτυξη συμπτωματικής αμυλοείδωσης, η οποία πρέπει να επιβεβαιώνεται σε βιοψία ιστού με ερυθρό του κογκό Ακτινολογικός έλεγχος Όλοι οι ασθενείς υποβλήθηκαν σε ακτινολογικό έλεγχο των άκρων χειρών, των καρπών και των άκρων ποδών και οι αλλοιώσεις βαθμολογήθηκαν με την εφαρμογή της μεθόδου Sharp/van der heijde από ειδικό ακτινολόγο. Σύμφωνα με το συνολικό τροποποιημένο Sharp/van der heijde σκορ (TmSvdhS), οι αρθρώσεις εκτιμώνται χωριστά για την πιθανή παρουσία διαβρώσεων και χωριστά για την πιθανή ανάπτυξη στένωσης του μεσάρθριου διαστήματος. Oι αρθρώσεις που εκτιμώνται για την παρουσία διαβρώσεων είναι οι παρακάτω: οι 10 μετακαρπιοφαλαγγικές αρθρώσεις, οι 8 εγγύς μεσοφαλαγγικές αρθρώσεις (ii-v), οι 2 μεσοφαλαγγικές αρθρώσεις στους αντίχειρες(i), η εγγύς επιφάνεια του πρώτου μετακάρπιου οστού, δεξιά και αριστερά, η άπω επιφάνεια των οστών της κερκίδας και της ωλένης, δεξιά και αριστερά, το τραπέζιο και το τραπεζοειδές(ως ενιαία μονάδα, το πολύγωνο), δεξιά και αριστερά, το σκαφοειδές οστό, δεξιά και αριστερά, το μηνοειδές οστό, δεξιά και αριστερά, οι 10 μεταταρσιοφαλαγγικές αρθρώσεις και οι 2 μεσοφαλαγγικές αρθρώσεις των πρώτων δακτύλων των ποδιών. Oι διαβρώσεις βαθμολογούνται με 0 βαθμούς όταν απουσιάζουν, με 1 βαθμό, όταν υπάρχει σαφής διακοπή της φλοιικής επιφάνειας, με 2-5 βαθμούς όταν υπάρχουν μεγαλύτερα ή περισσότερα ελλείμματα στην φλοιική επιφάνεια (ή 2-10 όταν πρόκειται για τις αρθρώσεις των ποδιών). βαθμολογούνται συνολικά 44 αρθρώσεις και το μέγιστο σκορ διαβρώσεων ανά ασθενή είναι το 280 (160 για τα χέρια και 120 για τα πόδια). Oι αρθρώσεις που εκτιμώνται για την ανίχνευση στένωσης του μεσάρθριου διαστήματος είναι οι παρακάτω: οι 10 μετακαρπιοφαλαγγικές, οι 8 εγγύς φαλαγγοφαλαγγικές (ii-v), η τρίτη, τέ-
111 111 ταρτη και πέμπτη καρπομετακαρπική άρθρωση δεξιά και αριστερά, οι αρθρώσεις πολύγωνο-σκαφοειδές, δεξιά και αριστερά, οι αρθρώσεις κεφαλωτό-μηνοειδές-σκαφοειδές, δεξιά και αριστερά, η κερκιδοκαρπική άρθρωση, δεξιά και αριστερά, οι 10 μεταταρσιοφαλαγγικές αρθρώσεις και οι 2 μεσοφαλαγγικές αρθρώσεις των πρώτων δακτύλων των ποδιών. Oι αρθρώσεις βαθμολογούνται με 0 βαθμούς, όταν δεν υπάρχει καθόλου στένωση του μεσάρθριου διαστήματος, με 1 βαθμό όταν η στένωση είναι τοπική ή αμφίβολη, με 2 βαθμούς όταν υπάρχει γενικευμένη στένωση < 50% του φυσιολογικού διαστήματος, με 3 βαθμούς όταν υπάρχει γενικευμένη στένωση, αλλά > 50% του φυσιολογικού διαστήματος και με 4 βαθμούς όταν έχει αναπτυχθεί αγκύλωση. βαθμολογούνται συνολικά 42 αρθρώσεις και το μέγιστο σκορ που λαμβάνει η στένωση του μεσάρθριου διαστήματος ανά ασθενή είναι το 168 (120 για τα χέρια και 48 για τα πόδια). το μέγιστο συνολικό τροποποιημένο Sharp/van der heijde σκορ ανά ασθενή είναι το Στους ασθενείς με ψωριασική αρθρίτιδα για τον υπολογισμό του TmSvdhS, υπολογίζονται επιπλέον οι 8 άπω φαλαγγοφαλαγγικές αρθρώσεις των άκρων χειρών (ιι-v) για το σκορ των διαβρώσεων και της στένωσης του μεσάρθριου διαστήματος και οι 2 μεσοφαλαγγικές αρθρώσεις των πρώτων δακτύλων (i) των άκρων χειρών μόνο για το σκορ της στένωσης του μεσάρθριου διαστήματος. Έτσι, το μέγιστο σκορ για τις διαβρώσεις είναι 320 και για τη στένωση του μεσάρθριου διαστήματος 208, δίνοντας μέγιστο συνολικό σκορ 528. Όταν υπάρχει σε μία άρθρωση οστεόλυση ή διαμόρφωση τύπου «μολύβι σε μολυβοθήκη» τότε η άρθρωση παίρνει το μέγιστο σκορ, όσον αφορά τόσο στις διαβρώσεις όσο και στη στένωση του μεσάρθριου διαστήματος Εκτίμηση ψυχολογικής επιβάρυνσης O βαθμός ψυχικής καταπόνησης των ασθενών εκτιμήθηκε με τη συμπλήρωση της σταθμισμένης ελληνικής έκδοσης του ερωτηματολογίου γενικής υγείας, GhQ-28 (General health Questionnaire-28) 209. η συμπλήρωση του ερωτηματολογίου, όπως ορίζεται, απαιτήθηκε να γίνει από τους ίδιους τους ασθενείς, χωρίς τη μεσολάβηση γονέων, ιατρού ή νοσηλευτή. το GhQ-28, περιλαμβάνει 28 ερωτήσεις που κατανέμονται σε 4 πεδία: σωματικά συμπτώματα ψυχικής καταπόνησης (somatization), άγχος-αϋπνία (anxiety), κοινωνική δυσλειτουργία (social dysfunction) και κατάθλιψη (depression). Σύμφωνα με το ερωτηματολόγιο, προκειμένου να ανιχνευθούν περιπτώσεις ασθενών με κάποιο ψυχολογικό πρόβλημα (cases), οι απαντήσεις βαθμολογούνται ως , με πιθανό σκορ Όσο υψηλότερο είναι το σκορ, τόσο μεγαλύτερη είναι η ψυχολογική καταπόνηση. ως σημείο διαχω-
112 112 ρισμού (cut-off-point) της ύπαρξης ή όχι ψυχολογικού προβλήματος χρησιμοποιείται στην ελληνική έκδοση το 4/5. Για τη διερεύνηση της ύπαρξης διαφοράς μεταξύ συγκεκριμένων ομάδων σε μία ή σε περισσότερες από τις 4 κατηγορίες ψυχικής διαταραχής που εξετάζονται, οι απαντήσεις βαθμολογήθηκαν σε κλίμακα Likert ( ), με πιθανό σκορ της κάθε κατηγορίας το 0-21 και συνολικό το η σταθμισμένη ελληνική έκδοση του GhQ-28, έχει χρησιμοποιηθεί σε πλήθος μελετών Καταγραφή της κοινωνικοοικονομικής κατάστασης των ασθενών Oι ασθενείς συμπλήρωσαν ένα δεύτερο ερωτηματολόγιο που περιελάμβανε ερωτήσεις σχετικά με την κοινωνικοοικονομική τους κατάσταση. αναλυτικότερα, καταγράφηκε το μορφωτικό τους επίπεδο (υποχρεωτική, δευτεροβάθμια, τεχνική και τριτοβάθμια εκπαίδευση), η οικογενειακή τους κατάσταση (αν μένουν μόνοι, με το σύντροφό τους ή με τους γονείς τους, αν είναι άγαμοι, έγγαμοι και ο αριθμός των τέκνων), η επαγγελματική τους κατάσταση (σπουδαστές, άνεργοι, εργαζόμενοι) και ο τόπος διαμονής τους κατά το μεγαλύτερο διάστημα της ζωής τους (αγροτική, ημιαστική ή αστική περιοχή). αστική θεωρήθηκε η περιοχή που έχει περισσότερους από κατοίκους, ημιαστική η περιοχή με πληθυσμό μεταξύ 3000 και κατοίκων και αγροτική η περιοχή με λιγότερους από 3000 κατοίκους. Για τους ασθενείς που ήταν ακόμη μαθητές της Γ Λυκείου, στην ερώτηση που αφορούσε στο μορφωτικό επίπεδο υπήρχε, επιπλέον, η επιλογή «μαθητές». Oι ίδιοι ασθενείς, καθώς και αυτοί που ακόμη φοιτούσαν σε κάποια σχολή (τεχνική ή ανώτατη) στην ερώτηση που αφορούσε στην κατηγορία «επαγγελματική κατάσταση» υπήρχε, επιπλέον, η επιλογή «σπουδαστής» Υπολογισμός δείκτη μάζας σώματος Σε όλους τους ασθενείς μετρήθηκε το βάρος και το ύψος και κατόπιν υπολογίστηκε, στον καθένα, ο δείκτης μάζας σώματος (BMi, Body Mass index), διαιρώντας το βάρος(kg) με το τετράγωνο του ύψους (meters). BMi= βάρος/ Υψος 2 Σύμφωνα με τον Παγκόσμιο Oργανισμό Υγείας, τα όρια που στοιχειοθετούν τις κατηγορίες του βμι είναι τα παρακάτω: βμι< 18.5 =ελλιπές βάρος, 18.5 βμι 24.9 = φυσιολογικό βάρος, 25 βμι 29.9 = προ-παχυσαρκία, βμι > 30 = παχυσαρκία. το ύψος των ασθενών συγκρίθηκε με το μέσο ύψος (50 η θέση) των ενηλί - κων γυναικών ή ανδρών ηλικίας 18 ετών του γενικού ελληνικού πληθυσμού, χρησιμοποιώντας τις καμπύλες ύψους που χρησιμοποιούνται ευρέως στην κλινική πράξη.
113 Εργαστηριακός έλεγχος Έγινε αιμοληψία 10 ml αίματος, το οποίο εξετάστηκε για τη μέτρηση όλων των παρακάτω εργαστηριακών παραμέτρων: της τκε (παθολογική θεωρήθηκε τιμή >20mm/hour), της C-αντιδρώσας πρωτεϊνης (C-Reactive Protein, CRP) (θετική θεωρήθηκε σε τίτλους > 3mg/l), του τίτλου των ANA (ελέγχθηκαν με έμμεσο ανοσοφθορισμό, χρησιμοποιώντας hep-2 κύτταρα και τίτλος 160 θεωρήθηκε θετικός), του ρευματοειδούς παράγοντα (ο οποίος ελέγχθηκε με νεφελομετρία και θεωρήθηκε θετικός σε τίτλους >15 u/ml), του τίτλου των anti-ccp αντισωμάτων (τίτλος >5 u/ml θεωρήθηκε θετικός) και τέλος του τίτλου των αντιθυρεοειδικών αντισωμάτων (ατα) (θετικός τίτλος >60 iu/ml). Oι παραπάνω φυσιολογικές τιμές καθορίζονται από το αιμα - τολογικό και ανοσολογικό εργαστήριο του ιπποκράτειου Nοσοκομείου θεσσαλονίκης Oφθαλμολογική εκτίμηση 113 Στους ασθενείς δόθηκε μια τυποποιημένη μονόφυλλη έντυπη φόρμα, που περιλαμβάνει πεδία που παρακαλείται να συμπληρώσει ο θεράπων οφθαλμίατρος, κατόπιν οφθαλμολογικής εξέτασης του ασθενούς. η οφθαλμολογική εκτίμηση δεν έγινε σε όλους από τον ίδιο οφθαλμίατρο, ο οποίος μπορούσε να είναι είτε νοσοκομειακός, είτε ιδιώτης ιατρός. τα πεδία που ζητήθηκε να απαντηθούν ήταν τα παρακάτω: η παρουσία ή όχι ενεργού ιριδοκυκλίτιδας (μη ενεργός ιριδοκυκλίτιδα <1 κύτταρο κ.ο.π, στην εξέταση με 1mm-σχισμοειδή λυχνία), η διορθωμένη οπτική οξύτητα σε κάθε οφθαλμό, η παρουσία ή όχι επιπλοκών της νόσου ή της θεραπείας της (καταρράκτης, συνέχειες, γλαύκωμα). η μακροχρόνια έκβαση της οφθαλμικής νόσου, ορίστηκε βάσει της διορθωμένης οπτικής οξύτητας, όπως αυτή μετρήθηκε από το θεράποντα οφθαλμίατρο, στην τελευταία επίσκεψη παρακολούθησης (ή μετά από μεσολάβηση χρονικού διαστήματος έως 15 ημερών) που πραγματοποιήθηκε στα πλαίσια της μελέτης. Oρίστηκαν 3 κατηγορίες οπτικής οξύτητας, σύμφωνα με τα συνήθη όρια που χρησιμοποιούνται για την απόκτηση άδειας οδήγησης και σύμφωνα με αυτά με τα οποία ορίζεται, επισήμως, η τύφλωση. Oι παραπάνω κατηγορίες είναι οι εξής: 1. καλή οπτική οξύτητα: μέγιστη διορθωμένη οπτική οξύτητα 20/40 ή υψηλότερη. 2. ελαττωμένη οπτική οξύτητα: μέγιστη διορθωμένη οπτική οξύτητα μεταξύ 20/50 και 20/ τύφλωση: μέγιστη διορθωμένη οπτική οξύτητα 20/200 ή χαμηλότερη.
114 Τυποποιημένη συνέντευξη τέλος, διεξήχθη σε όλους τους συμμετέχοντες συνέντευξη με την οποία επιβεβαιώθηκαν ή ενημερώθηκαν στοιχεία που είχαν ληφθεί από τους φακέλους. Συγκεκριμένα, τα δεδομένα που επαληθεύτηκαν ήταν τα παρακάτω: η ημερομηνία γέννησης και η τρέχουσα ηλικία, η τρέχουσα φαρμακευτική αγωγή, τα φάρμακα που έχει λάβει ο ασθενής κατά τη διάρκεια της νόσου, το χρονικό διάστημα που μεσολάβησε από την τελευταία έξαρση, τα συνυπάρχοντα νοσήματα, το οικογενειακό ιστορικό αρθρίτιδας, το χρονικό διάστημα που μεσολάβησε ανάμεσα στην εμφάνιση αρθρίτιδας και ιριδοκυκλίτιδας, η παρουσία ιστορικού ψωρίασης και το χρονικό διάστημα που μεσολάβησε ανάμεσα στην εμφάνιση ψωρίασης και αρθρίτιδας, ο αριθμός των χειρουργείων στις αρθρώσεις που υποβλήθηκε ο κάθε ασθενής, ποιες αρθρώσεις χρειάστηκαν χειρουργική παρέμβαση και το χρονικό διάστημα ανάμεσα στην έναρξη της νόσου και στην πραγματοποίηση του πρώτου χειρουργείου, το ιστορικό χειρουργικής επέμβασης στους οφθαλμούς και το χρονικό διάστημα ανάμεσα στην έναρξη της νόσου και στη διενέργεια του πρώτου χειρουργείου. επίσης, επιβεβαιώθηκαν τα στοιχεία που αφορούσαν στην κοινωνικοοικονομική κατάσταση των ασθενών. 2.3 Στατιστική ανάλυση κλινικής μελέτης η στατιστική ανάλυση έγινε με το στατιστικό πρόγραμμα SPSS 20.0 (Statistical Package forthe Social Sciences, SPSS inc., Chicago, il). αρχικά η κανονικότητα της κατανομής των μεταβλητών εξετάστηκε με το κριτήριο Kolmogorov-Smirnov. Για τη σύγκριση ποσοστών και τον έλεγχο συνάφειας μεταξύ κατηγορικών μεταβλητών χρησιμοποιήθηκε ο έλεγχος ανεξαρτησίας χ 2. Oι συσχετίσεις μεταξύ των ποσοτικών μεταβλητών που ακολουθούσαν κανονική κατανομή ελέγχθηκαν μέσω του συντελεστή γραμμικής συσχέ - τισης r του Pearson, όπως για παράδειγμα στην περίπτωση της διερεύνησης της σχέσης μεταξύ βμι και ηλ. Έναρξης Νόσου. Για τη σύγκριση ανεξάρτητων μετρήσεων χρησιμοποιήθηκε ο στατιστικός έλεγχος independent samples t-test, όπως για παράδειγμα στη σύγκριση του βμι μεταξύ ανδρών και γυναικών. αντίστοιχα, για τη σύγκριση ανεξάρτητων μετρήσεων σε περισσότερες των δύο ομάδων χρησιμοποιήθηκε one-way ANOVA, σε συνδυασμό με τον post-hoc έλεγχο κατά Tukey (Tukey s hsd test).για την πολυμεταβλητή ανάλυση χρησιμοποιήθηκαν μοντέλα γραμμικής παλινδρόμησης για την εξέταση της επίδρασης διαφόρων παραγόντων ενδιαφέροντος στις εξαρτημένες μεταβλητές. Για δίτιμες εξαρτημένες μεταβλητές χρησιμοποιήθηκαν αντίστοιχα μοντέλα λογιστικής παλινδρόμησης.
115 3. Γ Ε Ν Ε Τ Ι Κ Η Μ Ε Λ Ε Τ Η το γενετικό μέρος της μελέτης σχεδιάστηκε ως μελέτη συσχέτισης ασθενών μαρτύρων. 3.1 Ασθενείς και ομάδα ελέγχου - Κριτήρια εισαγωγής στο γενετικό μέρος της μελέτης Στη γενετική μελέτη συμπεριλήφθησαν 137 ασθενείς με NiA, που παρακολουθούνται σε δύο ρευματολογικά τμήματα (α Παιδιατρικής κλινικής και δ Παθολογικής κλινικής) του ιπποκρατείου Νοσοκομείου θεσσαλονίκης, οι οποίοι πληρούσαν συγκεκριμένα κριτήρια εισαγωγής. Κριτήρια εισαγωγής στο γενετικό μέρος της μελέτης: 1) σαφής διάγνωση NiA, σύμφωνα με τα αναθεωρημένα, κατά το 2001, ilar κριτήρια, 2) έγγραφη συγκατάθεση συμμετοχής τους στη μελέτη. Όλοι οι ασθενείς που διαγνώσθηκαν πριν τη δημοσίευση των αναθεωρημένων κατά το 2001 ilar κριτηρίων επαναταξινομήθηκαν, βάσει των κριτηρίων αυτών. Για τους ασθενείς που ήταν μικρότεροι των 18 ετών, έγγραφη συγκατάθεση συμμετοχής τους στη μελέτη αποκτήθηκε από τους γονείς τους. ενενήντα πέντε ασθενείς συμμετείχαν ταυτόχρονα και στο κλινικό και στο γενετικό τμήμα της μελέτης. διακόσιοι είκοσι ένας υγιείς ενήλικες επιλέγχθηκαν τυχαία από το τμήμα αιμοδοσίας του ιπποκράτειου Νοσοκομείου θεσσαλονίκης και χρησιμοποιήθηκαν ως ομάδα ελέγχου στη γονοτύπηση. η μελέτη εγκρίθηκε από την επιτροπή βιοηθικής του ιατρικού τμήματος του α.π.θ και από την επιστημονική επιτροπή του ιπποκρατείου Νοσοκομείου θεσσαλονίκης, διενεργήθηκε δε σύμφωνα με τη διακήρυξη του ελσίνκι. 3.2 Υλικό και μέθοδοι Εκχύλιση ολικού γενωμικού DNA Γενωμικό DNA, από ασθενείς και μάρτυρες, εκχυλίστηκε από τα λευ- 115
116 116 κοκύτταρα περιφερικού αίματος συλλεχθέντος σε αντιπηκτικό EDTA χρησιμοποιώντας το εμπορικά διαθέσιμο kit PureGeneTM Genomic Whole Blood DNA Purification kit (Gentra Systems) σύμφωνα με τις οδηγίες του κατασκευαστή. το εκχυλισμένο DNA επαναιωρήθηκε σε διάλυμα Tris-EDTA σε συγκέντρωση 100 ng/ml και αποθηκεύθηκε στους -20 ο C μέχρι τη χρησιμοποίηση του Ανάλυση των γενετικών πολυμορφισμών των γονιδίων TRAF1/C5, STAT4 και PTPN22 η γονοτύπηση για τους πολυμορφισμούς των γονιδίων TRAF1/C5, PTPN22 και STAT4 πραγματοποιήθηκε με συνδυασμό της αλυσιδωτής αντίδρασης της πολυμεράσης (PCR) και ανάλυσης μεγέθους περιοριστικών τμημάτων (Fragments Length Polymorphisms, RFLPs). O ευθύς εκκινητής 5 - GCA GCA GCA GAA CTA CGT GA-3 και ο ανάστροφος εκκινητής 5 - GCT TGC TGT TGA AAT CCT GAA GG-3 χρησιμοποιήθηκαν για να πολλαπλασιαστεί μία περιοχή 226 ζευγών βάσεων (bp) του γονιδίου TRAF1/C5, μέσα στην οποία εντοπίζεται ο πολυμορφισμός rs Oμοίως, ο ευθύς εκκινητής 5 -AAA GAA GTG GGA TAA AAA GAA GTT TG-3 και ο ανάστροφος εκκινητής 5 -CCA CTG AAA TAA GAT AAC CAC TGT-3 χρησιμοποιήθηκαν για να πολλαπλασιαστεί μία περιοχή 147 ζευγών βάσεων (bp) του γονιδίου STAT4, μέσα στην οποία εντοπίζεται ο μονονουκλεοτιδικός πολυμορφισμός rs τέλος, ο ευθύς εκκινητής 5 - TCA CCA GCT TCC TCA ACC ACA -3 και ο ανάστροφος εκκινητής 5 - GAT AAT GTT GCT TCA ACG GAA TTT -3 χρησιμοποιήθηκαν για να πολλαπλασιαστεί μία περιοχή 215 ζευγών βάσεων (bp) του γονιδίου PTPN22, μέσα στην οποία εντοπίζεται ο μονονουκλεοτιδικός πολυμορφισμός rs η PCR πραγματοποιήθηκε σε τελικό όγκο 25μl χρησιμοποιώντας 100ng γενωμικού DNA, 1x ρυθμιστικού διαλύματος της πολυμεράσης, 1.5mM MgCl 2, 250μM από κάθε dntp, 0.25μμ από κάθε εκκινητή και 1.0 U Taq πολυμεράσης (GoTaq Flexi DNA Polymerase, Promega). Tα τέσσερα τριφωσφορικά δεοξυριβονουκλεοτίδια (datp, dttp, dgtp και dctp), τα οποία αναφέρονται ως dntps (deoxyribonucleotide Triphosphate), χρησιμοποιήθηκαν από ένα παρασκευασθέν μείγμα που τα περιείχε ταυτόχρονα σε ισομοριακές ποσότητες. Όλα τα αντιδραστήρια της αλυσιδωτής αντίδρασης της πολυμεράσης φυλάσσονταν στους -20 C και ο χειρισμός τους κατά την προετοιμασία των αντιδράσεων γινόταν στον πάγο. ως μάρτυρας συμπεριλήφθη και μια αντίδραση (για κάθε γενετικό πολυμορφισμό) χωρίς γονιδιωματικό DNA,
117 117 προκειμένου να αποκλειστεί η πιθανότητα μολύνσεων. τα τμήματα των γονιδίων που έφεραν τους υπό μελέτη γενετικούς πολυμορφισμούς υπέστησαν γονιδιακή επέκταση (μέσω της αντίδρασης της PCR) με διαφορετικές συνθήκες, οι οποίες ήταν οι βέλτιστες για κάθε γονίδιο. Έτσι, στην περίπτωση του γενετικού πολυμορφισμού TRAF1/C5, μετά από την αρχική αποδιάταξη του DNA στους 94 ο C για 5 λεπτά, που είχε σαν στόχο την πλήρη αποδιάταξη αυτού αλλά και την καταστροφή των δευτεροταγών δομών του DNA, η PCR πραγματοποιήθηκε για 35 κύκλους που ο κάθε ένας περιελάμβανε αποδιάταξη του προϊόντος (94 ο C, 15 δευτερόλεπτα), υβριδοποίηση των εκκινητών στην αλληλουχία στόχο (60 ο C, 15 δευτερόλεπτα) και επέκταση της νεοσυντιθέμενης αλύσου (72 ο C, 30 δευτερόλεπτα). Στο τέλος των 35 κύκλων πραγματοποιήθηκε ένα τελικό στάδιο επιμήκυνσης στους 72 ο C για 7 λεπτά και τα προϊόντα της PCR φυλάχθηκαν στους 4 ο C. αντίστοιχα, στην περίπτωση του γενετικού πολυμορφισμού STAT4, μετά από την αρχική αποδιάταξη του DNA στους 95 ο C για 15 λεπτά, η PCR πραγματοποιήθηκε για 35 κύκλους που ο κάθε ένας περιελάμβανε αποδιάταξη του προϊόντος (95 ο C, 20 δευτερόλεπτα), υβριδοποίηση των εκκινητών στην αλληλουχία στόχο (56 ο C, 30 δευτερόλεπτα) και επέκταση της νεοσυντιθέμενης αλύσου (72 ο C, 60 δευτερόλεπτα). Στο τέλος των 35 κύκλων πραγματοποιήθηκε ένα τελικό στάδιο επιμήκυνσης στους 72 ο C για 3 λεπτά και τα προϊόντα της PCR φυλάχθηκαν στους 4 ο C. Στην περίπτωση του γενετικού πολυμορφισμού PTPN22, μετά από την αρχική αποδιάταξη του DNA στους 94 ο C για 5 λεπτά, η PCR πραγματοποιήθηκε για 35 κύκλους που ο κάθε ένας περιελάμβανε αποδιάταξη του προϊόντος (94 ο C, 20 δευτερόλεπτα), υβριδοποίηση των εκκινητών στην αλληλουχία στόχο (58 ο C, 30 δευτερόλεπτα) και επέκταση της νεοσυντιθέμενης αλύσου (72 ο C, 30 δευτερόλεπτα). Στο τέλος των 35 κύκλων πραγματοποιήθηκε ένα τελικό στάδιο επιμήκυνσης στους 72 ο C για 3 λεπτά και τα προϊόντα της PCR φυλάχθηκαν στους 4 ο C. η γονοτύπηση για το μονονουκλεοτιδικό πολυμορφισμό rs του TRAF1/C5 έγινε με ανάλυση του μεγέθους περιοριστικών θραυσμάτων χρησιμοποιώντας την Sdui περιοριστική ενδονουκλεάση (Fermentas), η οποίο πέπτει ειδικά το DNA που πολλαπλασιάζεται από το αλληλόμορφο G (αλλά όχι και το A) σε δύο θραύσματα των 169 και 57 ζευγών βάσεων (bp). ανάλογα, το STAT4 rs προϊόν της PCR (147 ζεύγη βάσεων) επωάστηκε με το περιοριστικό ένζυμο Hpai (New England Biolabs), το οποίο πέπτει μόνο το DNA που προκύπτει από το μεταλλαγμένο αλληλόμορφο (T) σε θραύσματα 122 και 25 ζευγών βάσεων. το προϊόν που προέκυψε από τον πολλαπλα-
118 118 σιασμό του κατάλληλου τμήματος του γονιδίου PTPN22 επωάστηκε με την περιοριστική ενδονουκλεάση XcmI, η οποία αναγνωρίζει και πέπτει μόνο το αλληλόμορφο Τ σε δύο τμήματα μεγέθους 170 και 45 bp, αφήνοντας άκοπο το τμήμα που φέρει το αλληλόμορφο C, οποίο έχει μέγεθος 215 bp. κάθε αντίδραση πέψης πραγματοποιήθηκε με 2.5 Units (U) της κατάλληλης περιοριστικής ενδονουκλεάσης και διήρκεσε 3 ώρες στους 37 ο C, σε μία αντίδραση συνολικού όγκου 20μl αποτελούμενη από 8μl προϊόντος της PCR και 1x ρυθμιστικό διάλυμα του ενζύμου. τα προϊόντα της πέψης ηλεκτροφορήθηκαν σε 2.5% πήκτωμα αγαρόζης και παρατηρήθηκαν μετά από χρώση με βρωμιούχο αιθίδιο. η γονοτύπηση έγινε «τυφλά» και επαναλήφθηκε για όλα τα αμφίβολα αποτελέσματα. Ένα ποσοστό 10% αναλύθηκε ξανά για να ελεγχθεί η ακρίβεια των αποτελεσμάτων. η επαναληψιμότητα της μεθόδου ήταν 100% Ανάλυση των γενετικών πολυμορφισμών των γονιδίων CD247 και PTPN2 Oι γενετικοί πολυμορφισμοί CD247 rs και PTPN2 rs μελετήθηκαν χρησιμοποιώντας γενωμικό DNA με τη μέθοδο Taqman, σε Real-Time PCR machine (ABi 7000), χρησιμοποιώντας κατάλληλα κits που είναι εμπορικά διαθέσιμα από την Applied Biosystems. Για τους προαναφερθέντες γενετικούς πολυμορφισμούς χρησιμοποιήθηκαν τα κits C_54383_10 και C_ _20, αντίστοιχα. 3.3 Στατιστική ανάλυση γενετικής μελέτης η στατιστική ανάλυση διενεργήθηκε με το στατιστικό πρόγραμμα GraphPad Prism (GraphPad Software, San Diego, CA). μόνο μη συγγενικά άτομα συμμετείχαν στις συγκρίσεις γενετικής συσχέτισης. Oι πολυμορφισμοί προς μελέτη και για τα δύο γονίδια ελέγχθηκαν για αποκλίσεις από την ισορροπία hardy-weinberg με σύγκριση των αναμενόμενων και των παρατηρηθεισών συχνοτήτων των γονοτύπων στην ομάδα ελέγχου με τη δοκιμασία x τετράγωνο (x 2 ). η δοκιμασία x 2 με ένα βαθμό ελευθερίας χρησιμοποιήθηκε για να ελέγξει διαφορές στην κατανομή γονοτύπων και αλληλομόρφων, μεταξύ ασθενών και ομάδων ελέγχου. τα Odds ratios (OR) μαζί με τα 95% διαστήματα εμπιστοσύνης τους υπολογίστηκαν ως δείκτης του σχετικού κινδύ - νου. τα αποτελέσματα παρουσιάζονται ως μέση τιμή ± σταθερό λάθος για τις ποσοτικές μεταβλητές εκτός και αν αναφέρεται διαφορετικά. τιμή p μικρότερη από ορίστηκε ως στατιστικά σημαντική.
119 4. Α Π O Τ Ε Λ Ε Σ Μ Α Τ Α 4.1 Δεδομένα από την παρακολούθηση των ασθενών κατά τη συνολική πορεία της νόσου Δημογραφικά και κλινικά χαρακτηριστικά των ασθενών Συμπεριλήφθησαν στη μελέτη συνολικά 102 ασθενείς, 72 γυναίκες (70.6%) και 30 άνδρες (29.4%). η αναλογία γυναικών:ανδρών ήταν 2.4:1. η μέση ηλικία που είχαν οι ασθενείς κατά την έναρξη της νόσου βρέθηκε 7.7 έτη (εύρος τιμών έτη) και η μέση διάρκεια νόσου 17.2 έτη (εύρος τιμών έτη). η μέση ηλικία των ασθενών τη στιγμή της αξιολόγησης, δηλαδή η τρέχουσα ηλικία τους, ήταν 25.0 έτη (εύρος τιμών έτη) (Πίνακας 14.) η κατανομή των ασθενών στις διάφορες υποομάδες έναρξης της NiA, σύμφωνα με τα ilar κριτήρια, ήταν η παρακάτω: 13 ασθενείς (12.7%) είχαν συστηματική αρθρίτιδα, 8 (7.8%) ολιγοαρθρίτιδα εμμένουσα, 22 (21.6%) ολιγοαρθρίτιδα επεκταθείσα, 19 (18.6%) πολυαρθρίτιδα με RF αρνητικό, 11 (10.8%) πολυαρθρίτιδα με RF θετικό, 9 (8.8%) ψωριασική αρθρίτιδα, 18 (17.6%) αρθρίτιδα που σχετίζεται με ενθεσίτιδα και 2 (1.9%) είχαν αδιαφοροποίητη αρθρίτιδα (Σχήμα 1A). Oι ασθενείς αυτοί είναι κατά τεκμήριο ασθενείς με σοβαρότερη νόσο που συνεχίζουν την παρακολούθησή τους σε τριτοβάθμιο κέντρο. Όταν το δείγμα επεκτάθηκε στους 307 ασθενείς, η κατανομή των διαφόρων υποομάδων έναρξης της NiA άλλαξε, για το λόγο ότι συμπεριλήφθηκαν και ασθενείς με ηπιότερη νόσο, κυρίως με εμμένουσα ολιγοαρθρίτιδα. η συχνότητα της συστηματικής αρθρίτιδας παρέμεινε υψηλή. Συγκεκριμένα, η κατανομή των 307 ασθενών στις διάφορες υποομάδες έναρξης της NiA ήταν η παρακάτω: 42 ασθενείς (13.7%) είχαν συστηματική αρθρίτιδα, 111 (36.1%) εμμένουσα ολιγοαρθρίτιδα, 37 (12.1%) επεκταθείσα ολιγοαρθρίτιδα, 27 (8.8%) πολυαρθρίτιδα με RF αρνητικό, 14 (4.6%) πολυαρθρίτιδα με RF θετικό, 20 (6.5%) ψωριασική αρθρίτιδα, 50 (16.3%) αρθρίτιδα που σχετίζεται με ενθεσίτιδα και 6 (2%) είχαν αδιαφοροποίητη αρθρίτιδα (Σχήμα 1β). 119
120 120 18% 2% 13% 9% 11% 8% 21% Συστηµατική αρθρίτιδα Oλιγοαρθρίτιδα εµµένουσα Oλιγοαρθρίτιδα επεκταθείσα Πολυαρθρίτιδα RF αρνητική Πολυαρθρίτιδα RF θετική Ψωριασική αρθρίτιδα Αρθρίτιδα σχετιζόµενη µε ενθεσίτιδα Αδιαφοροποίητη αρθρίτιδα 18% Σχήμα 1Α. Ταξινόμηση των 102 ασθενών της μελέτης στις διάφορες υποομάδες έναρξης της ΝΙΑ. 16% 6% 5% 9% 2% 14% 36% Συστηµατική αρθρίτιδα Oλιγοαρθρίτιδα εµµένουσα Oλιγοαρθρίτιδα επεκταθείσα Πολυαρθρίτιδα RF αρνητική Πολυαρθρίτιδα RF θετική Ψωριασική αρθρίτιδα Αρθρίτιδα σχετιζόµενη µε ενθεσίτιδα Αδιαφοροποίητη αρθρίτιδα 12% Σχήμα 1B. Ταξινόμηση των 307 ασθενών της μελέτης στις διάφορες υποομάδες έναρξης της ΝΙΑ.
121 121 Oγδόντα τέσσερις ασθενείς (82.4%) εκδήλωσαν πολυαρθρική πορεία νόσου έναντι 18 ασθενών (17.6%), στους οποίους η νόσος παρέμεινε ολιγοαρθρική σε όλη τη διάρκεια παρακολούθησης. Αξονική προσβολή εμφάνισαν 12 ασθενείς (11.8%). αξίζει να σημειωθεί ότι 45 ασθενείς (44.1%) παρουσίασαν κάποια στιγμή κατά τη διάρκεια της νόσου τους, προσβολή της άρθρωσης του ισχίου (Πίνακας 14.) Ψωρίαση εμφανίστηκε σε 9 ασθενείς. από αυτούς οι 8 διαγνώσθηκαν ότι έχουν ψωριασική αρθρίτιδα και ο ένας αδιαφοροποίητη αρθρίτιδα. Στον ασθενή με διάγνωση ψωριασικής αρθρίτιδας χωρίς ψωρίαση, ο πατέρας έπασχε από ψωρίαση δέρματος. το μέσο χρονικό διάστημα που μεσολάβησε ανάμεσα στην εμφάνιση αρθρίτιδας και ψωρίασης ήταν 87.3 μήνες (εύρος τιμών μήνες). Σε έναν μόνο ασθενή η εμφάνιση ψωρίασης προηγήθηκε της εκδήλωσης αρθρίτιδας κατά 12 μήνες. Oικογενειακό ιστορικό αρθρίτιδας (ρευματοειδής αρθρίτιδας ή φλεγμονώδης σπονδυλοαρθρίτιδα ή νεανική ιδιοπαθής αρθρίτιδα), περιγράφηκε σε 20/101 ασθενείς (19.6%) και αφορούσε σε συγγενή πρώτου ή δευτέρου βαθμού συγγένειας (Πίνακας 14). Συνοσηρότητα. Σε 38 ασθενείς (37.3%) εντοπίσθηκε τουλάχιστον ένα συνυπάρχον νόσημα, που δε σχετίζεται με τη διάγνωση της NiA. Oι συνοδές νοσηρές καταστάσεις που καταγράφηκαν ταξινομήθηκαν στις παρακάτω 6 κατηγορίες: αυτοάνοσα νοσήματα, ιδιοπαθή φλεγμονώδη νοσήματα του εντέρου, ψυχιατρικές διαταραχές, κακοήθη νεοπλάσματα, νοσήματα με αλλεργικό υπόστρωμα και κληρονομικά νοσήματα του αίματος (Πίνακας 14, Σχήμα 2). αναλυτικότερα, 15 ασθενείς (14.7%) παρουσίαζαν μία επιπλέον αυτοάνοση νόσο. Συγκεκριμένα, τα αυτοάνοσα νοσήματα που περιγράφηκαν ήταν: θυρεοειδίτιδα hashimoto (8 ασθενείς), λεύκη (1 ασθενής), σακχαρώδης διαβήτης (1 ασθενής), κοιλιοκάκη (1 ασθενής), αυτοάνοση αιμολυτική αναιμία (1 ασθενής), μορφέα/τοπικό σκληρόδερμα (2 ασθενείς), σύνδρομο Raynaud (2 ασθενείς), πολλαπλή σκλήρυνση (1 ασθενής), γυροειδής αλωπεκία (1 ασθενής), πρωτοπαθής χολική κίρρωση (1 ασθενής), σύνδρομο Sjogren (1 ασθενής). τρεις από τους παραπάνω ασθενείς είχαν δύο επιπλέον αυτοάνοσα νοσήματα. O πρώτος έπασχε από θυρεοειδίτιδα hashimoto και σύνδρομο Raynaud, o δεύτερος από θυρεοειδίτιδα hashimoto και γυροειδή αλωπεκία και ο τρίτος από πολλαπλή σκλήρυνση και κοιλιοκάκη. Ένας μόνο ασθενής εμφάνιζε τρία συνοδά αυτοάνοσα νοσήματα και συγκεκριμένα θυρεοειδίτιδα hashimoto, λεύκη και σακχαρώδη διαβήτη. δύο ασθενείς (1.9%) έπασχαν από ιδιοπαθές φλεγμονώδες νόσημα του εντέρου (ΙΦΝΕ) και, συγκεκριμένα, από νόσο Crohn.
122 122 Ψυχιατρικές διαταραχές καταγράφηκαν σε 6 ασθενείς (5.9%). απαραίτητη προϋπόθεση προκειμένου να οριστεί ψυχική επιβάρυνση σε κάποιον ασθενή ήταν η σχετική γνωμάτευση από ειδικό ψυχίατρο (πρόσφατη ή παλαιά) ή η λήψη από τον ασθενή ειδικής φαρμακευτικής αγωγής, όχι μόνο κατά τη διάρκεια της παρούσας μελέτης, αλλά και κατά το παρελθόν. αναλυτικά, 5 ασθενείς είχαν διάγνωση κατάθλιψης, 1 ασθενής διαταραχές συμπεριφοράς και 1 ασθενής νευρογενή ανορεξία. Κακοήθη νεοπλάσματα παρατηρήθηκαν σε 2 ασθενείς (1.9%). O ένας εμφάνισε θηλώδες νεόπλασμα θυρεοειδούς αδένα, 12 έτη μετά την έναρξη της NiA και ο δεύτερος δυσπλασία τραχήλου της μήτρας σταδίου ιιι-ιv, 24 έτη μετά την έναρξη της αρθρίτιδας. O πρώτος ασθενής είχε υπότυπο νόσου ολιγοαρθρίτιδα εμμένουσα και ο δεύτερος ψωριασική αρθρίτιδα. Νοσήματα με αλλεργικό υπόστρωμα καταγράφηκαν σε 2 ασθενείς (1.9%), οι οποίοι έπασχαν και οι δύο από έκζεμα και αλλεργική ρινίτιδα. Κληρονομικά νοσήματα του αίματος περιγράφηκαν σε 11 ασθενείς (10.8%). Oι 8 ασθενείς είχαν ετερόζυγη β-μεσογειακή αναιμία, ένας είχε ομόζυγη β-μεσογειακή αναιμία και 2 ασθενείς έπασχαν από υπογαμμασφαιριναιμία. τέλος, ένας ασθενής παρουσίασε θρομβωτική θρομβοπενική πορφύρα (ΘΘΠ) για την οποία χρειάστηκαν συνεδρίες πλασμαφαίρεσης. O ασθενής αυτός έπασχε, επιπλέον, από θυρεοειδίτιδα hashimoto και ετερόζυγη β-μεσογειακή αναιμία.
123 123 Πίνακας 14. Κλινικά χαρακτηριστικά των 102 ασθενών της μελέτης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Γυναίκες- Άνδρες a Ηλικία έναρξης νόσου, b έτη 7 (1-15.5) 6 (1.5-10) 7.8 (1-13) 3.8 ( ) 6.5 ( ) 10 (4-14) 6.5 (2-11) 11.3 (6-15.5) 13.8 ( ) Διάρκεια νόσου, b έτη 17 (5-31.5) 21 (8-31) 24.8 ( ) 16.8 (5-31.5) 17.5 (6-24) 17 (6-29) 16.5 (9-27.5) 13 (5-25) 11.3 (8.5-14) Ηλικία ασθενών στην τελευταία επίσκεψη, b έτη 24 (18-41) 27 (18-39) 32 (18-41) 20.5 (18-35) 22 (18-30) 28(18-37) 23 (19-31) 24.5 (18-36) 25 (22-28) Πολυαρθρική πορεία a (%) 84 (82.4) 10 (76.9) - 22 (100) 19 (100) 11 (100) 5 (55.6) 15 (83.3) 2 (100) Αξονική προσβολή a (%) 12 (11.8) (11.1) 11 (61.1) - Προσβολή ισχίου a (%) 45 (44.1) 8 (61.5) 0 (0) 5 (22.7) 11 (57.9) 7 (63.6) 6 (66.7) 8 (44.4) 0 (0) Oικογενειακό ιστορικό αρθρίτιδας a (%) 20 (19.6) - 2 (25) 3 (13.6) 4 (21) 1 (9.1) 5 (55.6) 6 (33.3) - Συνυπάρχοντα αυτοάνοσα νόσήματα a (%) 15(14.7) (9.1) 7 (36.8) 3 (27.3) 3 (33.3) - a αριθμός ασθενών b διάμεσος τιμή (κατώτερο-ανώτερο όριο)
124 124 Σχήμα 2. Συνοσηρότητα των ασθενών της μελέτης. NIA = Νεανική Ιδιοπαθής Αρθρίτιδα, ΙΦΝΕ = Ιδιοπαθή Φλεγμονώδη Νοσήματα Εντέρου, ΘΘΠ =Θρομβωτική Θρομβοπενική Πορφύρα Εργαστηριακά χαρακτηριστικά των ασθενών κατά τη διάγνωση της νόσου από τους φακέλους παρακολούθησης των ασθενών του παιδορευματολογικού τμήματος καταγράφηκε η παρουσία θετικού ή αρνητικού ρευματοειδούς παράγοντα (Rheumatoid Factor, RF) και και η παρουσία θετικών ή αρνητικών αντιπυρηνικών αντισωμάτων (antinuclear antibodies, ανα) κατά τη διάγνωση της νόσου. θετικό ρευματοειδή παράγοντα παρουσίαζαν οι 12 από τους 102 ασθενείς (11.8%) και θετικά ανα οι 33 από τους 99 ασθενείς της μελέτης (33.3%) για τους οποίους υπήρχε η αντίστοιχη μέτρηση (Πίνακας 15).
125 125 Πίνακας 15. Εργαστηριακά χαρακτηριστικά των ασθενών κατά τη διάγνωση της νόσου Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Ασθενείς με θετικό ρευματοειδή παράγοντα (RF) a (%) 12/102 (11.8) 0/13 (0) 0/8 (0) 0/22 (0) 0/19 (0) 11/11 (100) 0/9 (0) 0/18 (0) 1/2 (50) Ασθενείς με θετικό τίτλο αντιπυρηνικών αντισωμάτων (ΑΝΑ) a (%) 33/99 (33.3) 0/13 (0) 4/8 (50) 12/21 (57.1) 4/18 (22.2) 5/11 (45.5) 5/9 (55.6) 3/17 (17.6) 0/2 (0) a αριθμός θετικών/ συνολικό αριθμό ασθενών που ελέγχθησαν
126 Συνολική διάρκεια ενεργότητας κατά τη διάρκεια της νόσου βάσει των στοιχείων που προέκυψαν από τους φακέλους παρακολούθησης των ασθενών, υπολογίστηκε για κάθε ασθενή η συνολική διάρκεια ενεργότητας, ως το άθροισμα των επιμέρους επεισοδίων ενεργού νόσου σε ολόκληρη την πορεία της νόσου του. διαθέσιμα στοιχεία υπήρχαν για τους 98 από τους 102 ασθενείς. με τον τρόπο αυτό βρέθηκε ότι η διάμεση τιμή της διάρκειας ενεργότητας νόσου για το συνολικο δείγμα ήταν 94.5 μήνες (εύρος τιμών μήνες) (Πίνακας 16). κατόπιν, υπολογίστηκε για κάθε ασθενή η αναλογία της διάρκειας ενεργού νόσου προς τη συνολική διάρκεια νόσου και βρέθηκε ότι ο μέσος όρος του ποσοστού αυτού για το συνολικό δείγμα ασθενών ήταν 52.7%. αυτό σημαίνει ότι οι ασθενείς διατρέχουν περισσότερη από τη μισή και συγκεκριμένα, ποσοστό 52.7% της διάρκειας νόσου τους με ενεργότητα. το υπόλοιπο χρονικό διάστημα (47.3%) καλύπτεται από τις περιόδους μη ενεργότητας της νόσου, που μπορεί να είχαν οδηγήσει σε κλινική ύφεση ή όχι (Πίνακας 17) Κλινική ύφεση κατά τη συνολική διάρκεια της νόσου η διάμεση τιμή του συνολικού διαστήματος μη ενεργού νόσου σε ολόκληρο το διάστημα παρακολούθησης ήταν 81±72.6 μήνες και αφορούσε τους 98 ασθενείς για τους οποίους υπήρχαν διαθέσιμες πληροφορίες από τους φακέλους. Όπως αναφέρεται στην προηγούμενη ενότητα, αυτό αντιστοιχεί σε ποσοστό 47.3% του συνολικής διάρκειας νόσου. Κλινική ύφεση, όπως ορίζεται αυτή με τα κριτήρια της Wallace, πέτυχαν κατά τη διάρκεια της νόσου, έστω και μία φορά, συνολικά 92 από τους 98 ασθενείς (93.8%) (Πίνακας 18). αναλύοντας τώρα τα αποτελέσματα, κλινική ύφεση με φαρμακευτική αγωγή πέτυχαν 87 από τους 98 ασθενείς που μελετήθηκαν (88.8%). Oι 21 ασθενείς από τους 87 πέτυχαν μία φορά, οι 22 πέτυχαν δύο φορές, οι 18 τρεις φορές, οι 10 τέσσερις φορές, οι 7 πέντε φορές, οι 5 έξι φορές, οι 3 επτά φορές και ένας πέτυχε οκτώ φορές κλινική ύφεση με φαρμακευτική αγωγή. O μέσος όρος του αριθμού των επεισοδίων κλινικής ύφεσης με φαρμακευτική αγωγή βρέθηκε 2.9±1.7 (εύρος τιμών 1-8) και η μέση τιμή της διάρκειας κάθε επεισοδίου 23.2±14 μήνες (εύρος τιμών 7-85 μήνες). η μέση τιμή του συνολικού διαστήματος ύφεσης με φαρμακευτική αγωγή υπολογίστηκε σε 61.7±37.4 μήνες (εύρος τιμών μήνες).
127 127 Πίνακας 16. Διάρκεια ενεργότητας και μη ενεργότητας νόσου κατά το συνολικό διάστημα παρακολούθησης στο συνολικό δείγμα ασθενών και στους ασθενείς ανά υποομάδα της ΝΙΑ Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Ασθενείς με θετικό που αξιολογήθηκαν Διάρκεια ενεργότητας 94.5± ± ± ± ±62 158±93 60± ± ±60.1 νόσου, μήνες a (12-348) (18-298) (15-214) (12-289) (14-203) (61-348) (29-235) (15-202) (42-127) Διάρκεια μη ενεργότητας 81± ± ± ± ± ± ± ± ±13.4 νόσου, μήνες a (0-292) (0-264) (55-292) (18-272) (0-217) (0-108) (47-270) (0-259) (41-60) a διάμεσος τιμή ± τυπική απόκλιση (κατώτερο- ανώτερο όριο)
128 128 Πίνακας 17. Ποσοστό (%) συνολικής διάρκειας παρακολούθησης που περνούσαν οι ασθενείς με ενεργό ή μη ενεργό νόσο στο συνολικό δείγμα και στους ασθενείς ανά υποομάδα της ΝΙΑ Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Ποσοστό (%) διάρκειας 2.7± ± ± ± ± ± ± ± ±24.3 ενεργότητας/ διάρκεια ( ) ( ) ( ) ( ) ( ) ( ) ( ) ( ) ( ) νόσου a Ποσοστό (%) διάρκειας 47.3± ± ± ± ± ± ± ± ±24.3 μη ενεργότητας/διάρκεια (0-96.4) (0-92.7) ( ) ( ) (0-96.4) (0-49.2) ( ) (0-91.8) ( ) νόσου a a μέση τιμή ± τυπική απόκλιση (κατώτερο- ανώτερο όριο) Πίνακας 18. Αριθμός ασθενών που πέτυχαν κλινική ύφεση με και χωρίς φαρμακευτική αγωγή συνολικά ανά υποομάδα της ΝΙΑ Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Κλινική ύφεση με ΦΑ a 87/98 (88.8) 8/11 (72.7) 6/8 (75) 20/22 (90.9) 18/19 (94.7) 9/11 (81.8) 9/9 (100) 15/16 (93.8) 2/2 (100) Κλινική ύφεση χωρίς ΦΑ a 37/98 (37.8) 4/11 (36.4) 7/8 (87.5) 8/22 (36.4) 6/19 (31.6) 0/11 (0) 3/9 (33.3) 7/16 (43.8) 2/2 (100) Αποτυχία επίτευξης ύφεσης a 6/98(6.1) 2/11 (18.2) - - 1/19 (5.3) 2/11 (18.2) - 1/16 (6.3) - a αριθμός ασθενών/ αριθμό ασθενών για τους οποίους υπήρχαν πληροφορίες (%)
129 129 Κλινική ύφεση χωρίς φαρμακευτική αγωγή επιτεύχθηκε σε 37 από τους 98 ασθενείς (37.8%) της μελέτης (Πίνακας 18). Oι 29 από τους 37 ασθενείς πέτυχαν 1 φορά, οι 7 πέτυχαν δύο φορές και ένας πέτυχε τρεις φορές κατάσταση κλινικής ύφεσης χωρίς θεραπεία. O μέσος όρος του αριθμού των επεισοδίων κλινικής ύφεσης χωρίς φαρμακευτική αγωγή για τους 37 ασθενείς ήταν 1.2±0.5 (κατώτερο-ανώτερο όριο 1-3 επεισόδια) και η μέση διάρκεια κάθε επεισοδίου υπολογίστηκε σε 98.2±89.5 μήνες (κατώτερο-ανώτερο όριο μήνες). τέλος, ο μέσος όρος του συνολικού διαστήματος κλινικής ύφεσης εκτός θεραπείας στους 37 ασθενείς βρέθηκε 107.7±87.6 μήνες (κατώτερο-ανώτερο όριο μήνες). η κλινική ύφεση εκτός θεραπείας στους 27 από τους 37 ασθενείς (73%) κράτησε τουλάχιστον ακόμη ένα έτος ( 2 έτη συνολικά) και στους 19 από τους 37 ασθενείς (51.4%), στους μισούς δηλαδή περίπου, κράτησε για χρονικό διάστημα 5 έτη. Oι 19 από τους 37 ασθενείς (51.4%) υποτροπίασαν, με νέα περίοδο ενεργότητας μετά την επίτευξη επεισοδίου κλινικής ύφεσης εκτός θεραπείας. Oι 8 από αυτούς τους 37 ασθενείς (21.6%) που πέτυχαν κλινική ύφεση εκτός θεραπείας, πέτυχαν και δεύτερο επεισόδιο μετά την υποτροπή τους. το δεύτερο επεισόδιο κλινικής ύφεσης εκτός θεραπείας στους ασθενείς που υποτροπίασαν, εφόσον επιτεύχθηκε, κράτησε κατά μέσο όρο μικρότερο χρονικό διάστημα συγκριτικά με το πρώτο (22.5±10.3 μήνες στο δεύτερο επεισόδιο, κατώτερο-ανώτερο όριο μήνες, έναντι 50.3±50.5 μήνες στο πρώτο επεισόδιο, κατώτερο-ανώτερο όριο μήνες). Στους 11 ασθενείς που πέτυχαν μία φορά κλινική ύφεση εκτός θεραπείας, υποτροπίασαν και δεν κατόρθωσαν να επιτύχουν και δεύτερη φορά αυτήν την κατάσταση, ο μέσος όρος του μοναδικού αυτού επεισοδίου ήταν 33.5±28.3 μήνες (διάμεσος τιμή 22 μήνες, κατώτερο-ανώτερο όριο μήνες). Oι 18 από τους 37 ασθενείς (48.6%), περίπου το ένα πέμπτο του συνολικού δείγματος (18.4%) που πέτυχε κλινική ύφεση εκτός θεραπείας και δεν υποτροπίασε είχε μέσο όρο κλινικής ύφεσης εκτός θεραπείας 157.6±88.2 μήνες (διάμεσος 180 μήνες, κατώτερο-ανώτερο όριο μήνες). Σε 15 από αυτούς (15.3%) επιτεύχθηκε κλινική ύφεση χωρίς φαρμακευτική αγωγή η οποία διατηρήθηκε, χωρίς υποτροπή, για εξαιρετικά μεγάλο χρονικό διάστημα 179.4±77.7 μήνες (κατώτερο-ανώτερο όριο ). η διάμεσος τιμή του ποσοστού της διάρκειας νόσου που περνούσαν οι 98 ασθενείς σε κατάσταση κλινικής ύφεσης χωρίς φάρμακα βρέθηκε 0%, και ο μέσος όρος 17.8%±28.7% (ελάχιστο 0% και μέγιστο 93.8%) (πίνακας 19).
130 130 Πίνακας 19. Ποσοστό (%) της διάρκειας παρακολούθησης που περνούσαν οι ασθενείς σε κατάσταση κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στο συνολικό δείγμα και στους ασθενείς ανά υποομάδα της ΝΙΑ Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Ποσοστό ( %) διάρκειας 17.8±28.7 (0) 23.0±34.4 (0) 51.6± ±30.3 (0) 8.2±17.5 (0) (0) 11.6±17.6(0) 22.5±30.8 (0) 29.6±31.7 κλινικής ύφεσης χωρίς (0-93.8) (0-83.3) (70.8) (0-93.8) (0-61.9) 0 (0-39.6) (0-83.8) (29.6) (7.1-52) ΦΑ/διάρκεια νόσου a (0-87.5) ΦΑ= Φαρμακευτική Αγωγή a μεσος όρος ± τυπική απόκλιση (διάμεσος τιμή) (κατώτερο όριο - ανώτερο όριο)
131 4.1.5 Χειρουργικές επεμβάσεις 131 Oρθοπεδική παρέμβαση με αντικατάσταση της άρθρωσης και ολική αρθροπλαστική απαιτήθηκε, τουλάχιστον μία φορά, σε 6 από τους 102 ασθενείς του δείγματός μας (5.9%). δύο ασθενείς οδηγήθηκαν σε διορθωτικές επεμβάσεις αποκατάστασης των μικρών αρθρώσεων των άκρων χειρών, ένας ασθενής σε αρθρόδεση της κερκιδοκαρπικής άρθρωσης και 4 ασθενείς σε αντίστοιχες παρεμβάσεις στις αρθρώσεις των άκρων ποδών. επιπλέον, ένας ασθενής υποβλήθηκε σε διορθωτική επέμβαση της γνάθου, κατόπιν χειρουργικής παρέμβασης στις δύο κροταφογναθικές αρθρώσεις. Έτσι, συνολικά 11 ασθενείς (10.8%) οδηγήθηκαν στο χειρουργείο, εξαιτίας των φθορών που προκάλεσε η βασική τους νόσος (Πίνακας 20, Σχήμα 3). η συχνότερη άρθρωση, η οποία είχε αντικατασταθεί από προσθετική ήταν η άρθρωση του ισχίου. Συνολικά, 5 ασθενείς (4.9%) υποβλήθηκαν σε ολική αρθροπλαστική του ισχίου. Στους 4 αφορούσε και στα δύο ισχία και στον πέμπτο αφορούσε στο ένα ισχίο. Ένας από τους παραπάνω 4 ασθενείς, υποβλήθηκε σε επανάληψη της αρθροπλαστικής και στα δύο ισχία, λόγω φθοράς της προσθετικής άρθρωσης. το μέσο χρονικό διάστημα που μεσολάβησε από την έναρξη της νόσου μέχρι το πρώτο χειρουργείο στην άρθρωση του ισχίου βρέθηκε 16.4 έτη (εύρος έτη). Σε ολική αρθροπλαστική γόνατος υποβλήθηκαν 3 ασθενείς (2.9%), οι δύο αμφοτερόπλευρα και ο ένας ετερόπλευρα. Στον έναν από τους 2 που χειρουργήθηκαν και στα δύο γόνατα, ακολούθησε επανάληψη της αρθροπλαστικής που αφορούσε πάλι και στις 2 κατά γόνυ αρθρώσεις. το μέσο χρονικό διάστημα που μεσολάβησε από την έναρξη της νόσου μέχρι το πρώτο χειρουργείο στην άρθρωση του γόνατος βρέθηκε 12.6 έτη (εύρος έτη). αντικατάσταση της άρθρωσης του ώμου με προσθετική καταγράφηκε σε έναν ασθενή (0.9%) μετά από πάροδο 17.1 ετών από την έναρξη της νόσου. διορθωτική επέμβαση στην άρθρωση του καρπού παρατηρήθηκε, επίσης, σε έναν ασθενή (0.9%) μετά από χρονικό διάστημα 16.9 ετών από την έναρξη της νόσου του. O μέσος όρος χειρουργικών επεμβάσεων στις αρθρώσεις ανά ασθενή βρέθηκε 2.55±2.33 (εύρος 1-9).
132 132 Πίνακας 20. Συχνότητα ασθενών που υποβλήθηκαν στον κάθε τύπο χειρουργικής επέμβασης των αρθρώσεων Τύπος και θέση χειρουργικής επέμβασης Αριθμός ασθενών(%) Oλική αρθροπλαστική ισχίου 5 (4.9) Oλική αρθροπλαστική γόνατος 3 (2.9) Oλική αρθροπλαστική ώμου 1 (0.9) ρθρόδεση κερκιδοκαρπικής άρθρωσης 1 (0.9) Διορθωτική επέμβαση άκρας χείρας 2 (1.9) Διορθωτική επέμβαση άκρου ποδός 4 (3.9) Γναθοχειρουργική επέμβαση 1 (0.9) Oποιαδήποτε χειρουργική επέμβαση 11(10.8) Σχήμα 3. Συχνότητα ασθενών που υποβλήθηκαν σε χειρουργική επέμβαση των αρθρώσεων.
133 4.1.6 Oφθαλμική βλάβη 133 από τους 102 ασθενείς της μελέτης, οι 11 (10.8%) ανέπτυξαν ιριδοκυκλίτιδα, κάποια περίοδο, κατά τη διάρκεια της νόσου. από αυτούς οι 10 ήταν γυναίκες (90.9%) και ο ένας ήταν άνδρας (9.1%), με αναλογία γυναικών : ανδρών 10:1. Στους 10 από τους 11 ασθενείς (90.9%) που ανέπτυξαν ιριδοκυκλίτιδα, η οφθαλμική προσβολή προέκυψε στα επόμενα 3.25 έτη από την έναρξη της αρθρίτιδας (μέσος όρος 1.13± έτη), ενώ σε 1 μόνο ασθενή η εμφάνισή της συνέβη 13 έτη μετά. Σε κανέναν ασθενή η ιριδοκυκλίτιδα δεν προηγήθηκε της εμφάνισης αρθρίτιδας και σε 1 ασθενή, ιριδοκυκλίτιδα και αρθρίτιδα διαγνώσθηκαν ταυτοχρόνως. Συμπεριλαμβανομένου και του ασθενή που εμφάνισε οφθαλμική προσβολή 13 έτη μετά τη διάγνωση της αρθρίτιδας, ο μέσος όρος εμφάνισης της ιριδοκυκλίτιδας στο συνολικό δείγμα ασθενών υπολογίστηκε σε 2.21± έτη (εύρος τιμών 0-13 έτη) μετά την έναρξη της αρθρίτιδας. Oι ασθενείς με ολιγοαρθρικής έναρξης νόσο παρουσίαζαν υψηλότερο ποσοστό εμφάνισης ιριδοκυκλίτιδας και συγκεκριμένα περίπου ένας στους τρεις (30%). αναλυτικά, οφθαλμική προσβολή συνέβη σε 2/8 ασθενείς (25%) που είχαν ολιγοαρθρίτιδα εμμένουσα, σε 7/22 ασθενείς (31.8%) με ολιγοαρθρίτιδα επεκταθείσα, σε 1/19 ασθενείς (5.2%) με πολυαρθρίτιδα RF αρνητική και σε 1/18 ασθενείς (5.6%) που έπασχαν από αρθρίτιδα που σχετίζεται με ενθεσίτιδα. αντιθέτως, κανείς από τους ασθενείς με διάγνωση συστηματικής έναρξης αρθρίτιδας, πολυαρθρίτιδας RF θετική, ψωριασικής αρθρίτιδας και αταξινόμητης αρθρίτιδας δεν εκδήλωσαν ιριδοκυκλίτιδα στη διάρκεια της νόσου (Πίνακας 21, Σχήμα 4). Σε όλους τους ασθενείς με ιριδοκυκλίτιδα η νόσος είχε ξεκινήσει πριν την ηλικία των 6.5 ετών, με μέση ηλικία έναρξης τα 3.09 έτη, έναντι της μέσης ηλικίας έναρξης των 8.35 ετών που καταγράφηκε στους ασθενείς χωρίς οφθαλμική προσβολή. θετικά αντιπυρηνικά αντισώματα (ανα) παρατηρήθηκαν σε υψηλότερο ποσοστό στους ασθενείς με προσβολή ιριδοκυκλίτιδας (9/11 ασθενείς, 81.8%), σε σύγκριση με τους υπόλοιπους χωρίς οφθαλμική προσβολή (24/88 ασθενείς, 27.3%). Σε τρείς ασθενείς, χωρίς ιστορικό οφθαλμικής προσβολής, δεν υπήρχε καταγεγραμένος στον αντίστοιχο φάκελο παρακολούθησης ο τίτλος των ανα.
134 134 Πίνακας 21. Συχνότητα εμφάνισης ιριδοκυκλίτιδας στη συνολική πορεία της νόσου στο συνολικό δείγμα ασθενών και στους ασθενείς ανά υποομάδα της ΝΙΑ Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Ιστορικό ιριδοκυκλίτιδας a 11 (10.8) - 2 (25) 7 (31.8) 1(5.3) - - 1(5.6) - a αριθμός ασθενών (%) Σχήμα 4. Συχνότητα εμφάνισης ιριδοκυκλίτιδας στη συνολική πορεία της νόσου στο συνολικό δείγμα ασθενών και στους ασθενείς ανά υποομάδα της ΝΙΑ
135 Στο δείγμα των ασθενών μας, η ιριδοκυκλίτιδα προσέβαλλε συχνότερα και τα δύο μάτια και συγκεκριμένα ποσοστό 81.8% των ασθενών (9/11 ασθενείς)εμφάνισαν αμφοτερόπλευρη προσβολή έναντι 18.2% (2/11 ασθενείς) που παρουσίασαν μόνο ετερόπλευρη προσβολή (Πίνακας 22, Σχήμα 5). Πίνακας 22. Εντόπιση προσβολής ιριδοκυκλίτιδας (ΙΚ) κατά τη συνολική πορεία της νόσου. Αριθμός ασθενών Αναλογία (%) * Αμφοτερόπλευρη προσβολή ΙΚ Ετερόπλευρη προσβολή ΙΚ *επί του συνόλου των ασθενών που εμφάνισαν ΙΚ. ΙΚ= ιριδοκυκλίτιδα 135 Σχήμα 5. Εντόπιση προσβολής ιριδοκυκλίτιδας (ΙΚ) στη συνολική πορεία της νόσου Στους 5 από τους 11 ασθενείς με ιστορικό ιριδοκυκλίτιδας (45.4%), εκδηλώθηκε τουλάχιστον μία οφθαλμική επιπλοκή. Συνέχειες εμφάνισαν 4/11 ασθενείς (36.3%), καταρράκτη 4/11 ασθενείς (36.3%) και γλαύκωμα εκδήλωσαν, επίσης, 4/11 ασθενείς (36.3%). Σε 3/11 ασθενείς (27.3%) παρουσιάστηκαν και οι τρεις εξεταζόμενες επιπλοκές της ιριδοκυκλίτιδας (Πίνακας 23, Σχήμα 6).
136 136 Πίνακας 23. Συχνότητα επιπλοκών ιριδοκυκλίτιδας στους ασθενείς κατά τη συνολική πορεία της νόσου Αριθμός ασθενών Αναλογία (%) * Συνέχειες Καταρράκτης Γλαύκωμα *επί του συνόλου των ασθενών που εμφάνισαν επιπλοκή ιριδοκυκλίτιδας Σχήμα 6. Συχνότητα επιπλοκών ιριδοκυκλίτιδας στους ασθενείς κατά τη συνολική πορεία της νόσου Σε χειρουργική επέμβαση στα μάτια υποβλήθηκαν 3/11 ασθενείς (27.3%) με ιστορικό ιριδοκυκλίτιδας. Στους 2 ασθενείς απαιτήθηκε χειρουργική παρέμβαση και στους δύο οφθαλμούς και μάλιστα περισσότερες της μία φοράς. Στον ένα από τους παραπάνω δύο ασθενείς, η πρώτη χειρουργική επέμβαση πραγματοποιήθηκε 10 έτη και στον άλλο 3.75 έτη μετά την πρώτη προσβολή ιριδοκυκλίτιδας. Στον τρίτο ασθενή το χειρουργείο αφορούσε στο ένα μόνο μάτι και πραγματοποιήθηκε μία φορά, 5.8 έτη μετά την εμφάνιση της ιριδοκυκλίτιδας.
137 Δεδομένα κατά την τελευταία επίσκεψη παρακολούθησης τα κλινικά και εργαστηριακά χαρακτηριστικά των 102 ασθενών κατά την τελευταία επίσκεψη τους στο κέντρο αναφοράς όπου συνεχίζουν την παρακολούθησή τους περιγράφονται στον πίνακα 24. Oι 205 ασθενείς (109 γυναίκες-96 άνδρες) που συμμετείχαν μόνο με τηλεφωνική συνέντευξη και αποτέλεσαν το δείγμα βασισμένο σε πληθυσμό ασθενών με NiA είχαν μέση ηλικία (±SD) κατά τη στιγμή της συνέντευξης 25.9±6.2 έτη και μέση διάρκεια νόσου (±SD) 17.5±6.4 έτη. τα δύο δείγματα ασθενών (δείγμα κέντρου αναφοράς δείγμα βασισμένο σε πληθυσμό ασθενών με NiA) δε διέφεραν σημαντικά ως προς τη μέση ηλικία και τη μέση διάρκεια νόσου των ασθενών (p=0.229, p=0.721 αντίστοιχα). η κατανομή των 205 ασθενών του δείγματος βασισμένου σε πληθυσμό ασθενών με NiA στις διάφορες υποομάδες έναρξης της νόσου ήταν: συστηματική αρθρίτιδα 29 ασθενείς, ολιγοαρθρίτιδα εμμένουσα 105 ασθενείς, ολιγοαρθρίτιδα επεκταθείσα 15 ασθενείς, πολυαρθρίτιδα RF-αρνητική 8 ασθενείς, πολυαρθρίτιδα RF-θετική 3 ασθενείς, ψωριασική αρθρίτιδα 11 ασθενείς, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα 32 ασθενείς και αταξινόμητη αρθρίτιδα 4 ασθενείς. το δείγμα βασισμένο σε πληθυσμό ασθενών με NiA αξιολογήθηκε μόνο ως προς την τρέχουσα παρουσία ή όχι μακροχρόνιας κλινικής ύφεσης εκτός θεραπείας και ως προς τον άξονα της μακροχρόνιας έκβασης που αφορά στη σωματική λειτουργική ικανότητα Εργαστηριακά χαρακτηριστικά Στον εργαστηριακό έλεγχο που πραγματοποιήθηκε στην τελευταία επίσκεψη παρακολούθησης στα πλαίσια της μελέτης, ανιχνεύθηκε θετικός ρευματοειδής παράγοντας σε 12/102 ασθενείς (11.8%), θετικά αντισώματα έναντι κυκλικών κιτρουλλινοποιημένων πεπτιδίων (anti-cyclic Citrullinated Peptide, anti-ccp) σε 11/81 ασθενείς (13.6%), θετικά αντιπυρηνικά αντισώματα (ανα) σε 33/99 ασθενείς (33.3%) και θετικά αντιθυρεοειδικά αντισώματα (AntiThyroid Antibodies, ατα) σε 5/67 ασθενείς (7.5%). τα παραπάνω εργαστηριακά ευρήματα στο συνολικό δείγμα και στους ασθενείς ανά υποομάδα της νόσου περιγράφονται στον πίνακα 24. τονίζεται ότι οι ασθενείς που είχαν θετικό ρευματοειδή παράγοντα καθώς και οι ασθενείς που είχαν θετικό τίτλο ανα κατά τη διάγνωση της νόσου, βρέθηκαν θετικοί κατά τον έλεγχο στην τελευταία επίσκεψη παρακολούθησης. Oι τρεις ασθενείς για τους οποίους δεν υπήρχε, κατά τη διάγνωση, μέτρηση των ανα καταγεγραμένη στο φάκελο παρακολούθησης, βρέθηκαν ότι είχαν αρνητικό τίτλο ανα.
138 138 Πίνακας 24. Κλινικά και εργαστηριακά χαρακτηριστικά των 102 ασθενών στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Θετικός RF β (%) 12/102 (11.8) 0/13 (0) 0/8 (0) 0/22 (0) 0/19 (0) 11/11 (100) 0/9 (0) 0/18 (0) 1/2 (50) Θετικός τίτλος anti-ccp β (%) 11/81 (13.6) 1/12 (8.3) 1/8 (12.5) 2/17 (11.8) 2/14 (14.3) 4/7 (57.1) 0/6 (0) 0/15 (0) 1/2 (50) Θετικός τίτλος ΑΝΑ β (%) 33/102 (32.4) 0/13 (0) 4/8 (50) 12/22 (54.5) 4/19 (21.1) 5/11 (45.5) 5/9 (55.6) 3/18 (16.7) 0/2 (0) Θετικός τίτλος ΑΤΑ β (%) 5/67 (7.5) 0/8 (0) 0/7 (0) 0/15 (0) 4/13 (30.8) 1/6 (16.7) 0/9 (0) 0/11 (0) 0/2 (0) Ταχύτητα καθίζησης ερυθρών, mm/h a * (n=102) 19.9± ± ± ± ± ± ± ± ±4.2 C-Reactive Protein, mg/l a ** (n=102) 7.5± ± ±0 4.0± ± ± ± ± ±0 Αριθμός διογκωμένων αρθρώσεων a (n=102) 1.3± ±4 0.1± ± ± ± ± ± ±0 Αριθμός ευαίσθητων αρθρώσεων a (n=102) 1.9± ± ± ± ± ± ± ± ±0 Διάρκεια πρωϊνής δυσκαμψίας, λεπτά a (n=102) 23.9± ± ± ± ± ± ± ± ±0 Σφαιρική εκτίμηση της ενεργότητας νόσου από τον ιατρό (VAS 0-10cm) a (n=102) 2.1± ± ± ± ± ± ± ± ±0.4
139 139 Πίνακας 24. (συνέχεια). Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Σφαιρική εκτίμηση της ενεργότητας νόσου από τον ασθενή (VAS 0-10cm) a (n=102) 1.9± ± ± ± ± ± ± ± ±0.4 Ενεργός ιριδοκυκλίτιδα, αρ. (%) (n=102) 1 (1) (4.5) DAS28 a (n=102) 2.6± ± ± ± ± ± ± ± ±1.0 ASDAS a (n=12) 2.1± ±1.5 (11) 2.0 (1) - a μέσος όρος±τυπική απόκλιση β αριθμός θετικών/ συνολικό αριθμό ασθενών που ελέγχθησαν *Φυσιολογική τιμή <20 mm/h **Φυσιολογική τιμή <3 mg/l ( όλες οι τιμές < 3 mg/l μετατράπηκαν σε 1mg/l)
140 Kατάσταση ενεργότητας της νόσου (disease activity status) Ενεργότητα νόσου Στην τελευταία επίσκεψη παρακολούθησης που πραγματοποιήθηκε στα πλαίσια της μελέτης, διαπιστώθηκε ενεργότητα νόσου σε 53 ασθενείς (52%), σύμφωνα με τα κριτήρια της Wallace (Πίνακας 25, Σχήμα 7). Σαράντα δύο ασθενείς (41.1%) παρουσίασαν τουλάχιστον μία διογκωμένη άρθρωση και αριθμός των διογκωμένων αρθρώσεων κυμάνθηκε από μία έως 14 (μέσος όρος 1.3± 2.7 και διάμεση τιμή 2). Σε 52 ασθενείς (50.9%) διαπιστώθηκε παρουσία τουλάχιστον μια άρθρωσης με ευαισθησία και ο αριθμός των ευαίσθητων αρθρώσεων κυμάνθηκε από μία έως 24 (μέσος όρος 1.9± 3.7 και διάμεση τιμή 2). Πυρετός που σχετιζόταν με τη Νια διαπιστώθηκε σε 2 ασθενείς, ενώ κανείς δεν εμφάνιζε κάποιο από τα υπόλοιπα συστηματικά χαρακτηριστικά της νόσου και συγκεκριμένα εξάνθημα, ορογονίτιδα, σπληνομεγαλία ή γενικευμένη λεμφαδενοπάθεια. Ένας μόνο ασθενής (1%) είχε ενεργό ιριδοκυκλίτιδα. η σφαιρική εκτίμηση της ενεργότητας νόσου από τον ιατρό (EGA), χρησιμοποιώντας την οπτική αναλογική κλίμακα VAS, κυμάνθηκε από 0 έως 10 (μέσος όρος 2.1± 2.3). h σφαιρική εκτίμηση της ενεργότητας νόσου από τον ίδιο τον ασθενή (PGA) κυμάνθηκε και αυτή από 0 έως 10, αλλά με λίγο μικρότερη μέση τιμή (μέσος όρος 1.9 ± 2.2) η τ.κ.ε βρέθηκε αυξημένη σε 36 ασθενείς και η μέση τιμή της σε αυτούς τους ασθενείς ήταν 40.1 mm/hour (εύρος τιμών mm/hour). Παθολογική τιμή CRP παρατηρήθηκε σε 35 ασθενείς, στους οποίους η μέση τιμή της ανήλθε σε 21.8 mg/l (εύρος τιμών mg/l). Στους 53 ασθενείς που παρουσίαζαν ενεργό νόσο, εφαρμόστηκε, ξεχωριστά, ο δείκτης DAS28, προκειμένου να έχουμε ποσοτική εκτίμηση της ενεργότητας. Σύμφωνα με το δείκτη DAS28, οι 9 ασθενείς βρισκόταν σε κατάσταση κλινικής ύφεσης (DAS28<2.6), οι 10 είχαν χαμηλή δραστηριότητα νόσου (DAS28: ), οι 27 ασθενείς μέτρια (DAS28: ) και 7 ασθενείς εμφάνιζαν υψηλή δραστηριότητα νόσου (DAS28>5.1). O μέσος όρος του DAS28 στους 53 ασθενείς βρέθηκε 3.7±1.2. Όλοι οι ασθενείς με μη ενεργό νόσο, σύμφωνα με τα κριτήρια της Wallace, είχαν DAS28< 2.6. η μέση τιμή του δείκτη DAS28 στους 102 ασθενείς ήταν 2.6±1.5 (εύρος τιμών ) Όπως περιγράφηκε σε προηγούμενη ενότητα, στους ασθενείς με αξονική προσβολή, απαιτήθηκε επιπρόσθετα, τιμή του δείκτη ASDAS <1.3, προκειμένου να θεωρηθεί η νόσος τους ανενεργός. Στους 12 ασθενείς με προσβολή του αξονικού σκελετού, ο μέσος όρος του δείκτη ASDAS ήταν
141 2.20±0.43 (διάμεσος τιμή 1.80, εύρος τιμών 0.8-6). Συγκεκριμένα, οι 4 ασθενείς εμφάνιζαν κλινικά ανενεργό νόσο (ASDAS<1.3), 3 ασθενείς παρουσίαζαν μέτρια (ASDAS <2.1), 4 ασθενείς υψηλή (ASDAS< 3.5) και 1 ασθενής πολύ υψηλή ενεργότητα νόσου (ASDAS >3.5) Κλινική ύφεση 141 από τους 49 ασθενείς (48%) στους οποίους η νόσος ήταν μη ενεργός, σύμφωνα με τα κριτήρια της Wallace, οι 43 (42.2%) βρισκόταν σε κατάσταση κλινικής ύφεσης. από αυτούς οι 19 (18.6%) παρουσίαζαν κλινική ύφεση με φαρμακευτική αγωγή, (αφού η νόσος τους ήταν ανενεργός για περισσότερους από 6 μήνες, ενώ συνέχιζαν να λαμβάνουν θεραπεία), ενώ οι 24 (23.5%) διένυαν διάστημα κλινικής ύφεσης χωρίς φαρμακευτική αγωγή (είχαν ανενεργό νόσο για περισσότερους από 12 μήνες, ενώ βρισκόταν εκτός θεραπείας). Σε 6 ασθενείς (5.9%) βρέθηκε ότι η νόσος ήταν μη ενεργός, δεν πληρούσαν, όμως, τα κριτήρια που θα τους τοποθετούσαν σε κατάσταση κλινικής ύφεσης (Πίνακας 26, Σχήμα 8). από τους 205 που συμμετείχαν με τηλεφωνική συνέντευξη, οι 122 ασθενείς (59.5%), 72 γυναίκες και 50 άντρες, θεωρήθηκε, σύμφωνα με τις απαντήσεις τους, ότι βρίσκονται σε κατάσταση μακροχρόνιας κλινικής ύφεσης. Υπενθυμίζεται ότι η κλινική ύφεση, κατόπιν τηλεφωνικής και μόνο συνέντευξης, ορίστηκε ως η κατάσταση στην οποία ισχύουν και τα τρία από τα παρακάτω: α) μη λήψη φαρμακευτικής αγωγής που σχετίζεται με αρθρίτιδα, ιριδοκυκλίτιδα ή ψωρίαση τα τελευταία 2 έτη, β) απουσία εμφάνισης πόνου ή διόγκωσης σε μία ή περισσότερες αρθρώσεις συνοδευόμενο ή όχι από πυρετό ή εξάνθημα τα τελευταία 2 έτη και γ) απουσία ενεργότητας νόσου σύμφωνα με την εκτίμη - ση ρευματολόγου (εάν και εφόσον είχε προηγηθεί επίσκεψη) ή ανάγκης νοσηλείας εξαιτίας εκδηλώσεων που αποδόθηκαν στη NiA τα τελευταία 2 έτη. από τους 122 ασθενείς που βρέθηκε ότι διανύουν διάστημα κλινικής ύφεσης, οι 88 ασθενείς είχαν εμμένουσα ολιγοαρθρίτιδα, με προσβολή 4 αρθρώσεις σε όλη τη διάρκεια της νόσου (72.1% επί του συνόλου των ασθενών σε κλινική ύφεση που απάντησαν και 85.4% των ασθενών με ολιγοαρθρίτιδα εμμένουσα που απάντησαν). από τους υπόλοιπους, 12 ασθενείς είχαν διάγνωση συστηματικής αρθρίτιδας (9.8% επί του συνόλου των ασθενών σε κλινική ύφεση που απάντησαν και 41.4% των ασθενών με συστηματικής έναρξης αρθρίτιδα που απάντησαν), 4 ολιγοαρθρίτιδας επεκταθείσας (3.3% επί του συνόλου των ασθενών σε κλινική ύφεση που απάντησαν και 26.7% των ασθενών με ολιγοαρθρίτιδα επεκταθείσα που απάντησαν), 4 πολυαρθρίτιδας με αρνητικό RF (3.3% επί του συνόλου των ασθενών σε κλινική ύφεση που
142 142 απάντησαν και 50% των ασθενών με πολυαρθρίτιδα RF αρνητική που απάντησαν), 5 ψωριασικής αρθρίτιδας (4% επί του συνόλου των ασθενών σε κλινική ύφεση που απάντησαν και 45.5% των ασθενών με ψωριασική αρθρίτιδα που απάντησαν), 8 αρθρίτιδας που σχετίζεται με ενθεσίτιδα (6.6% επί του συνόλου των ασθενών σε κλινική ύφεση που απάντησαν και 25% των ασθενών με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα που απάντησαν) και ένας είχε αταξινόμητη μορφή (0.8% επί του συνόλου των ασθενών σε κλινική ύφεση που απάντησαν και 25% των ασθενών με αταξινόμητη αρθρίτιδα που απάντησαν). κανείς ασθενής που έπασχε από πολυαρθρικής έναρξης NiA με θετικό RF δε βρέθηκε σε κατάσταση μακροχρόνιας ύφεσης. Oγδόντα τρεις ασθενείς (40.5%) από αυτούς που απάντησαν δε βρέθηκαν σε κατάσταση κλινικής ύφεσης. Έτσι, συνολικά από τους 307 ασθενείς (205 που αποτέλεσαν το δείγμα βασισμένο σε πληθυσμό και 102 προερχόμενους από το κέντρο αναφοράς) το ποσοστό αυτών που βρέθηκαν σε κλινική ύφεση εκτός θεραπείας ήταν 47.6% (146/307 ασθενείς). αναλυτικά, το ποσοστό των 42 ασθενών με συστηματική αρθρίτιδα (29 που απάντησαν τηλεφωνικά και 13 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) που βρέθηκε σε κλινική ύφεση γενικά και σε κλινική ύφεση εκτός θεραπείας βρέθηκε 40.5% (17/42 ασθενείς) και 35.7% (15/42 ασθενείς) αντίστοιχα. τα ανάλογα ποσοστά για τους 111 ασθενείς με ολιγοαρθρίτιδα εμμένουσα (103 που απάντησαν τηλεφωνικά και 8 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) βρέθηκαν 84.6% (94/111 ασθενείς) και 82.9% (92/111 ασθενείς) αντίστοιχα, για τους 37 ασθενείς με ολιγοαρθρίτιδα επεκταθείσα (15 που απάντησαν τηλεφωνικά και 22 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) 35.1% (13/37 ασθενείς) και 24.3% (9/37 ασθενείς) αντίστοιχα, για τους 27 ασθενείς με πολυαρθρίτιδα RF αρνητική (8 που απάντησαν τηλεφωνικά και 19 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) 40.7% (11/27 ασθενείς) και 25.9% (7/27 ασθενείς) αντίστοιχα, για τους 20 ασθενείς με ψωριασική αρθρίτιδα (11 που απάντησαν τηλεφωνικά και 9 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) 45% (9/20 ασθενείς) και 30% (6/20 ασθενείς) αντίστοιχα, για τους 50 ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα (32 που απάντησαν τηλεφωνικά και 18 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) 36% (18/50 ασθενείς) και 28% (14/50) αντίστοιχα και τέλος για τους 6 ασθενείς με αταξινόμητη αρθρίτιδα (4 που απάντησαν τηλεφωνικά και 2 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) 50% (3/6 ασθενείς). από τους 14 ασθενείς με πολυαρθρίτιδα RF(+) θετική (3 που απάντησαν τηλεφωνικά και 11 που εκτιμήθηκαν με κλινικοεργαστηριακό έλεγχο) κανείς δε βρέθηκε σε κατάσταση κλινικής ύφεσης (Πίνακας 27, Σχήμα 9).
143 143 Πίνακας 25. Συχνότητα ασθενών με και χωρίς ενεργότητα νόσου στο συνολικό δείγμα και στους ασθενείς ανά υποομάδα της ΝΙΑ στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Ενεργός νόσος a 53 (52) 7 (53.8) 2 (25) 11 (50) 10 (52.6) 10 (90.9) 5 (55.6) 8 (44.4) 0(0) Μη ενεργός νόσος a 49 (48) 6 (46.2) 6 (75) 11 (50) 9 (47.4) 1 (9.1) 4 (44.4) 10 (55.6) 2 (100) a αριθμός ασθενών (%) Σχήμα 7. Αναλογία(%) ασθενών με ενεργό και μη ενεργό νόσο στο συνολικό δείγμα ασθενών και ανά υπομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης.
144 144 Πίνακας 26. Αναλογία (%) ασθενών με κλινική ύφεση (με ή χωρίς φαρμακευτική αγωγή) και χωρίς κλινική ύφεση (μη ενεργός νόσο < 6 μήνες) στο σύνολο των ασθενών με μη ενεργό νόσο, στο δείγμα ασθενών του κέντρου αναφοράς και ανά υποομάδα της ΝΙΑ στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Κλινική ύφεση 43 (42.2) 5 (38.5) 6 (75) 9 (40.9) 7 (36.8) 0 (0) 4 (44.4) 10 (55.6) 2 (100) Κλινική ύφεση με ΦΑ a 19 (18.6) 2 (15.4) 2 (25) 4 (18.2) 4 (21) 0 (0) 3 (33.3) 4 (22.2) 0 (0) Κλινική ύφεση χωρίς ΦΑ a 24 (23.5) 3 (23.1) 4 (50) 5 (22.7) 3 (15.8) 0 (0) 1 (11.1) 6 (33.3) 2 (100) Μη ενεργός νόσος <6 μήνες a 6 (5.9) 1 (7.7) 0 (0) 2 (9.1) 2 (10.5) 1 (9.1) 0 (0) 0 (0) 0 (0) a αριθμός ασθενών (% των ασθενών) Σχήμα 8. Αναλογία (%)των ασθενών με κλινική ύφεση (με ή χωρίς φαρμακευτική αγωγή) και χωρίς κλινική ύφεση (ανενεργός νόσο < 6 μήνες) στο σύνολο των ασθενών με μη ενεργό νόσο, στο δείγμα ασθενών του κέντρου αναφοράς και ανά υπομάδατης NIA στην τελευταία επίσκεψη παρακολούθησης.
145 145 Πίνακας 27. Συχνότητα ασθενών με κλινική ύφεση χωρίς φαρμακευτική αγωγή στο δείγμα του κέντρου αναφοράς στην τελευταία επίσκεψη, στο δείγμα βασισμένο σε πληθυσμό ασθενών με NIA και στο συνολικό δείγμα Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Αρ. ασθενών (N) a/b/c 102/205/307 13/ 29/ 42 8/ 103/ / 15/ 37 19/ 8/ 27 11/ 3/ 14 9/ 11/ 20 18/ 32/ 50 2/ 4/ 6 Κλινική ύφεση χωρίς 24 (23.5) a 3 (23.1) a 4 (50.0) a 5 (22.7) a 3 (15.8) a 0 a 1 (11.1) a 6 (33.3) a 2 (100.0) a φαρμακευτική αγωγή, 122 (59.5) b 12 (41.4) b 88 (85.4) b 4 (26.7 ) b 4 (50.0 ) b 0 b 5 (45.5) b 8 (25.0) b 1 (25.0) b αρ.(%) 146 (47.6) c 15 (35.7) c 92 (82.9) c 9 (24.3 ) c 7 (25.9) c 0 c 6 (30.0) c 14 (28.0) c 3 (50.0) c a δείγμα του κέντρου αναφοράς, b δείγμα βασισμένο στο πληθυσμό, c συνολικό δείγμα (δείγμα κέντρου αναφοράς συν δείγμα βασισμένο στο πληθυσμό). Σχήμα 9. Συχνότητα ασθενών με κλινική ύφεση χωρίς φαρμακευτική αγωγή στο δείγμα του κέντρου αναφοράς στην τελευταία επίσκεψη, στο δείγμα βασισμένο σε πληθυσμό ασθενών με NIA και στο συνολικό δείγμα.
146 Αρθρική και εξωαρθρική καταστροφή χρησιμοποιώντας το δείκτη JADi-α, με τον οποίο αξιολογείται σε κλινικό επίπεδο, η καταστροφή σε 36 αρθρώσεις ή ομάδες αρθρώσεων, βρέθηκε ότι 89 ασθενείς (87.2%) εμφάνιζαν περιορισμό εύρους κίνησης ή παραμόρφωση, απότοκου αρθρικής καταστροφής λόγω νόσου, σε μία τουλάχιστον άρθρωση ή ομάδα αρθρώσεων (Πίνακας 28). η διάμεση τιμή του δείκτη JA- Di-A, στο συνολικό δείγμα των ασθενών βρέθηκε 6±18.25 ( μέσος όρος 14.7, εύρος τιμών 0-67) (Πίνακας 29). Συχνότερα προσβεβλημένες αρθρώσεις εμφανίστηκαν αυτές του καρπού και οι εγγύς μεσοφαλαγγικές, ακολουθούμενες από τις κροταφογναθικές και τις αρθρώσεις των άκρων ποδών. εξωαρθρικές βλάβες διαπιστώθηκαν σε περισσότερους από τους μισούς ασθενείς και συγκεκριμένα 59 ασθενείς (57.8%), εμφάνισαν τουλάχιστον μία αλλοίωση σε κάποιο από τα 13 σημεία που αξιολογούνται με το δείκτη JADi-E. Συχνότερα παρατηρήθηκε οφθαλμική βλάβη και ανισοσκελία. η διάμεση τιμή του JADi-E βρέθηκε 1±1.23 ( μέσος όρος 1εύρος τιμών 0-5). αναλυτικά, 43 ασθενείς δεν είχαν καμία εξωαρθρική βλάβη (JADi-E=0), 30 ασθενείς είχαν JADi-E=1, 19 ασθενείς είχαν JADi-E=2, 5 ασθενείς είχαν JADi-E=3, 1 ασθενής είχε JADi-E=4 και 4 ασθενείς είχαν JADi-E=5 (Πίνακας 30, Σχήμα 10). από τις τοπικές διαταραχές της ανάπτυξης αξιολογήθηκαν ξεχωριστά μόνο η παρουσία ανισοσκελίας και η ασυμμετρία της γνάθου ή η μικρογναθία. ανισοσκελία 1cm μεταξύ των δύο κάτω άκρων διαπιστώθηκε σε 30 ασθενείς (29.4%) (Πίνακας 31, Σχήμα 11). ασυμμετρία της γνάθου ή μικρογναθία παρατηρήθηκε σε 37 ασθενείς (36.3%) (Πίνακας 31, Σχήμα 11).
147 147 Πίνακας 28. Αρθρική καταστροφή, σύμφωνα με το δείκτη JADI-Α, στους 102 ασθενείς της μελέτης και στους ασθενείς ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) JADI-A=0 a 13 (12.8) 3 (23) 4 (50) 1 (4.5) 0 (0) 1 (9) 2 (22.2) 2 (11.1) 0 (0) JADI-A >0 a 89 (87.2) 10 (77) 4 (50) 21 (95.5) 19 (100) 10 (91) 7 (77.8) 16 (88.9) 2 (100) a αριθμός ασθενών (%) Πίνακας 29. Αρθρική καταστροφή, σύμφωνα με το δείκτη JADI-Α, στους 102 ασθενείς της μελέτης και στους ασθενείς ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) JADI-A=0 a 6± ± ±0.53 6±9.7 15± ± ±20 4±7.2 4±1.4 (0-67) 0-63) (0-1) (0-41) (2-67) (0-59) (0-48) (0-26) (3-5) a διάμεσος τιμή ± τυπική απόκλιση (κατώτερο - ανώτερο όριο)
148 148 Πίνακας 30. Εξωαρθρική καταστροφή, σύμφωνα με το δείκτη JADI-Ε,στους 102 ασθενείς της μελέτης στην τελευταία επίσκεψη Δείκτης JADI-E Συνολικό δείγμα (n=102) a JADI-Ε=0 43 (42.2) JADI-Ε =1 30 (29.4) JADI-E=2 19 (18.7) JADI-E=3 5 (4.9) JADI-E=4 1 (0.9) JADI-E=5 4 (3.9) a αριθμός ασθενών (%) Σχήμα 10. Εξωαρθρική καταστροφή, σύμφωνα με το δείκτη JADI-Ε, στους 102 ασθενείς της μελέτης στην τελευταία επίσκεψη παρακολούθησης.
149 149 Πίνακας 31. Τοπικές διαταραχές ανάπτυξης των 102 ασθενών της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Ανισοσκελία 1 cm a 30 (29.4) 3 (23.1) 2 (25) 11 (50) 5 (26.3) 2 (18.2) 3 (33.3) 4 (22.2) 0 (0) Ασυμμετρία γνάθου ή Μικρογναθία a 37 (36.3) 3 (23.1) 0(0) 9 (40.9) 13 (68.4) 5 (45.5) 3 (33.3) 3 (16.7) 1 (50) a αριθμός ασθενών (%) Σχήμα 11. Τοπικές διαταραχές ανάπτυξης των 102 ασθενών της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης.
150 Ακτινολογικές βλάβες Όλοι οι ασθενείς με περιφερική προσβολή των αρθρώσεων (n=102), υποβλήθηκαν σε ακτινολογικό έλεγχο (με απλές ακτινογραφίες) των άκρων χειρών, των καρπών και των άκρων ποδών και κατόπιν οι βλάβες που αναδείχθηκαν βαθμολογήθηκαν, εφαρμόζοντας τη μέθοδο modified Sharp/van der heijde. από τους 102 ασθενείς, οι 86 (84.3%) παρουσίασαν συνολικό modified Sharp/van der heijde score (TmSvdhS) μεγαλύτερη του μηδενός (Πίνακας 32). η διάμεση τιμή του TmSvdhs στο συνολικό δείγμα ασθενών βρέθηκε 112.5±140 (μέσος όρος 153.7, εύρος τιμών 0-448). αναλυτικά, η διάμεσος τιμή της βαθμολογίας των διαβρώσεων (modified /van der heijde score Erosion (msvdhs-e) ήταν 56.5±89.5 (μέσος όρος 91.3, εύρος τιμών 0-280) και η διάμεσος τιμή της βαθμολογίας που αφορούσε στη στένωση του μεσάρθριου διαστήματος (modified Sharp/van der heijde score -Joint Space Narrowing, msvdhs-jsn) βρέθηκε 59±52.22 (μέσος όρος 62.3, εύρος τιμών 0-168). η διάμεσος τιμή της βαθμολογίας του msvdhs που αντιστοιχεί στα άνω άκρα ήταν 74.5±91.9 (μέσος όρος 98.9, εύρος τιμών 0-280) και αντιστοίχως η διάμεση τιμή που αφορά στα κάτω άκρα βρέθηκε 40± (μέσος όρος 54.7, εύρος τιμών 0-168) (Πίνακας 33, Σχήματα 12-14). ιστορικό ακτινολογικά επιβεβαιωμένης ιερολαγονίτιδας διαπιστώθηκε σε 12 ασθενείς (11.7%). Oι 11 ανήκαν στην κατηγορία της αρθρίτιδας που σχετίζεται με ενθεσίτιδα και ο ένας έπασχε από ψωριασική αρθρίτιδα. Σε κανένα ασθενή από αυτούς που εξετάσθηκαν δεν αποκαλύφθηκε ιερολαγονίτιδα για πρώτη φορά, αντιθέτως σε όλους τους παραπάνω ασθενείς, η ιερολαγονίτιδα ήταν, ήδη, γνωστή.
151 151 Πίνακας 32. Παρουσία ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποπιημένο Sharp/ Van der Heijde score (TmSvdHS) στους 102 ασθενείς της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης. Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) TmSvdHS = 0 a 16 (15.6) 3 (23.1) 6 (75) 1 (4.5) 0 (0) 0 (0) 3 (33.3) 3 (16.7) 0 (0) TmSvdHS > 0 a 86 (84.3) 10 (76.9) 2 (25) 21 (95.5) 9 (100) 11 (100) 6 (66.7) 15 (83.3) 2 (100) a αριθμός ασθενών (%) TmSvdHS= Total modified Sharp/van der Heijde score Πίνακας 33. Βαθμός ακτινολογικής βλάβης, σύμφωνα με το τροποποιημένο Sharp/ Van der Heijde score (msvdhs) στους 102 ασθενείς της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) TmSvdHS a 112.5± ± ± ± ± ± ± ± ±3.5 (0-448) (0-448) (0-18) (0-364) (18-448) (50-448) (0-386) (0-271) (96-101) msvdhs- E a 56.5± ± ±3.8 76± ± ± ± ± ±14.2 (0-280) (0-280) (0-10) (0-228) (4-280) (30-280) (0-240) (0-158) (50-70) msvdhs-jsn a 59± ±64.9 0± ± ± ± ± ± ±10.6 (0-168) (0-168) (0-12) (0-136) (12-168) (20-168) (0-146) (0-106) (31-46) msvdhs- Άνω Άκρα a 74.5± ± ± ±67 154± ±78 72± ± ±19 (0-280) (0-280) (0-18) (0-250) (0-280) (50-280) (0-250) (0-148) (31-58) msvdhs- Κάτω Άκρα a 40± ±66 0±0 36± ± ± ± ± ±22.6 (0-168) (0-168) (0-168) (0-168) (0-168) (0-136) (0-132) (38-70) a διάμεσος τιμή ± τυπική απόκλιση (κατώτερο- ανώτερο όριο) TmSvdHS = Total modified Sharp/ van der Heijde score, msvdhs-e = modified Sharp/van der Heijde Score -Erosions, msvdhs-jsn = modified Sharp/ Van der Heijde Score-Joint Space Narrowing.
152 152 Σχήμα 12. Βαθμός ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποποιημένο Sharp/van der Heijde score (ΤmSvdHs) στους 102 ασθενείς της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Σχήμα 13. Βαθμός ακτινολογικής βλάβης, σύμφωνα με το τροποποιημένο Sharp/van der Heijde score που αφορά στις διαβρώσεις (msvdh-es) και στη στένωση του μεσάρθριου διαστήματος (msvdh-jsns) στους 102 ασθενείς της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης
153 153 Σχήμα 14. Βαθμός ακτινολογικής βλάβης, σύμφωνα με το τροποποιημένο Sharp/van der Heijde score που αφορά στα άνω άκρα (msvdh-άνω Άκρα) και στα κάτω άκρα (msvdh-κάτω Άκρα) στους 102 ασθενείς της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Τελικό ύψος και δείκτης μάζας σώματος (Body Mass Index, BMI) το μέσο ύψος των αρρένων στη μελέτη μας βρέθηκε εκατοστά και των θηλέων εκατοστά. Σύμφωνα με τις καμπύλες ύψους που υπάρχουν για τον ελληνικό πληθυσμό, το μέσο ύψος (50 η θέση) των ελλήνων είναι 177 κατοστά, ενώ το αντίστοιχο των ελληνίδων είναι 163 εκατοστά. το τελικό ύψος των ανδρών με NiA δε βρέθηκε να διαφέρει σημαντικά από αυτό των ανδρών του γενικού πληθυσμού (p=0.891). αντιθέτως, το τελικό ύψος των γυναικών με NiA του δείγματος διέφερε στατιστικώς σημαντικά από το αντίστοιχο των γυναικών του γενικού πληθυσμού (p=0.010). Σύμφωνα με το δείκτη BMi, από τους 102 ασθενείς της μελέτης, οι 5 (4.9%) ήταν λιποβαρείς, οι 85 (83.3%) είχαν φυσιολογικό βάρος για το ύψος τους, οι 11 (10.8%) εμφανίστηκαν υπέρβαροι και ένας (0.9%) μόνο ήταν παχύσαρκος (Πίνακας 34). η διάμεση τιμή του δείκτη BMi στους άνδρες βρέθηκε 22.6±2 και στις γυναίκες 21±3, διαφορά η οποία δεν ήταν στατιστικώς σημαντική (p=0.068). επίσης, καμία από τις υποομάδες της νόσου δεν παρουσίασε θετική ή αρνητική συσχέτιση με την τιμή του βμι, σε στατιστικώς σημαντικό επίπεδο (p=0.546). Έτσι, η διάμεση τιμή του βμι στους άνδρες και στις γυναίκες με συστηματική αρθρίτιδα βρέθηκε 21.4 (εύρος τιμών 19.1-
154 ) και 19.8 ( ), με ολιγοαρθρίτιδα εμμένουσα 25.2 ( ) και 22.3 (εύρος τιμών ), με ολιγοαρθρίτιδα επεκταθείσα 21.1 (εύρος τιμών ), με πολυαρθρίτιδα RF αρνητική 20.9 (εύρος τιμών ) και 21.5 (εύρος τιμών ), με πολυαρθρίτιδα RF θετική 21.2 (εύρος τιμών ) και 20.8 (εύρος τιμών ), με ψωριασική αρθρίτιδα 23.2 (εύρος τιμών ) και 22.1 (εύρος τιμών ), με αρθρίτιδα που σχετίζεται με ενθεσίτιδα 22.6 (εύρος τιμών ) και 20.9 (εύρος τιμών ) και με αδιαφοροποίητη αρθρίτιδα 23.7 και 23 αντίστοιχα (πίνακας 35). Πίνακας 34. Κατάταξη των 102 ασθενών της μελέτης βάσει του δείκτη BMI (Body Mass Index). Αριθμός ασθενών Αναλογία (%) Λιποβαρείς (BMI<18.5) Φυσιολογικού βάρους (BMI= ) Υπέρβαροι (BMI= ) Παχύσαρκοι (BMI>30.0)
155 155 Πίνακας 35. Δείκτης μάζας σώματος (BMI) σε γυναίκες και άνδρες του συνολικού δείγματος ασθενών και ανά υποoμάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) BMI γυναικών a 21 ±3 19.8± ± ± ± ±2 22.1± ± ( ) ( ) ( ) ( ) ( ) ( ) ( ) ( ) BMI ανδρών a 22.6±2 21.4± ±3-20.9± ± ± ± ( ) ( ) ( ) ( ) ( ) ( ) ( ) a διάμεσος τιμή ± τυπική απόκλιση (κατώτερο - ανώτερο όριο) ΒΜΙ= Body Mass Index
156 Oφθαλμική βλάβη ιστορικό ιριδοκυκλίτιδας είχε καταγραφεί σε 11 από τους 102 ασθενείς της μελέτης (10.8%). ενεργός ετερόπλευρη ιριδοκυκλίτιδα διαγνώστηκε σε έναν μόνο ασθενή από αυτούς, στην τελευταία επίσκεψη παρακολούθησης (9.1%). O ασθενής αυτός ανήκε στην υποομάδα της ολιγοαρθρίτιδας επεκταθείσας. κανένας από τους υπόλοιπους ασθενείς χωρίς ιστορικό οφθαλμικής νόσου δε βρέθηκε να έχει στοιχεία φλεγμονής, κατά την εξέτασή του από τον οφθαλμίατρο. η τελική έκβαση της οφθαλμικής νόσου, βάσει της μέγιστης διορθωμένης οπτικής οξύτητας, σύμφωνα με το θεράποντα οφθαλμίατρο, στους 11 ασθενείς με ιστορικό ιριδοκυκλίτιδας κυμάνθηκε, σύμφωνα με τις οδηγίες, ως εξής (Πίνακας 36, Σχήμα 15): 2/11 ασθενείς (18.2%) εμφάνισαν μόνιμη τύφλωση στο ένα μάτι. 1/11 ασθενής (9.1%) παρουσίασε ελαττωμένη όραση στο ένα μάτι και στο άλλο μάτι τύφλωση. 9/11 ασθενείς (81.8%) είχαν καλή όραση και στα 2 μάτια. Πίνακας 36. Τελική έκβαση οφθαλμικής νόσου, βάσει της μέγιστης διορθωμένης οπτικής οξύτητας στους ασθενείς με ιριδοκυκλίτιδα Αριθμός ασθενών Αναλογία (%) * Μόνιμη ετερόπλευρη τύφλωση Ελαττωμένη ετερόπλευρη όραση 1 9 Καλή αμφοτερόπλευρη όραση *επί του συνόλου των ασθενών που είχαν ιστορικό ιριδοκυκλίτιδας. Σχήμα 15. Τελική έκβαση οφθαλμικής νόσου, βάσει της μέγιστης διορθωμένης οπτικής οξύτητας στους ασθενείς με ιριδοκυκλίτιδα.
157 4.2.7 Σωματική λειτουργική ικανότητα (physical ability) 157 από το συνολικό δείγμα ασθενών που συμπεριλήφθηκαν στη μελέτη, οι 54 ασθενείς (52.9%), παρουσίαζαν φυσιολογική λειτουργική ικανότητα στην εκτέλεση των καθημερινών τους δραστηριοτήτων, σύμφωνα με το δείκτη haq-di (haq-di=0). η διάμεση τιμή του δείκτη haq-di στους 102 ασθενείς της μελέτης βρέθηκε 0±0.6 (μέσος όρος 0.35, εύρος τιμών ), ενώ στους 48 ασθενείς (47.1%) που εμφάνιζαν κάποιου βαθμού περιορισμό (haq-di>0) ήταν 0.6±0.6 ( μέσος όρος 1.7, εύρος τιμών ) (Πίνακας 37). αναλυτικά, 18 ασθενείς (17.6%) εμφάνιζαν ήπιο (haq-di= ), 25 ασθενείς (24.5%) μέτριο (haq-di= ) και 5 ασθενείς (4.9%) σοβαρό (haq-di=1.51-3) περιορισμό της λειτουργικής τους ικανότητας (Πίνακας 38, Σχήμα 16). Στους 12 ασθενείς με αξονική προσβολή εφαρμόστηκε, επιπλέον, ο δείκτης BASFi του οποίου η διάμεσος τιμή βρέθηκε 1.5±2.23 (μέσος όρος 2.13, εύρος τιμών 1-8.7). το ερωτηματολόγιο haq-di συμπληρώθηκε τηλεφωνικά και από τους 205 ασθενείς που αποτέλεσαν το δείγμα βασισμένο σε πληθυσμό ασθενών με NiA. μειωμένη σωματική λειτουργική ικανότητα (haq-di>0) αναφέρθηκε σε 45 (22%) και καθόλου περιορισμός σε 160 (78%) από τους 205 ασθενείς. Συνολικά, 93 ασθενείς (48 προερχόμενοι από το κέντρο αναφοράς και 45 που απάντησαν τηλεφωνικά) από τους 307 (30.3%) παρουσίαζαν κάποιου βαθμού περιορισμό στην εκτέλεση των καθημερινών τους δραστηριοτήτων (Σχήμα 17). και οι 122 ασθενείς που θεωρήθηκε ότι διανύουν διάστημα κλινικής ύφεσης ανέφεραν ότι δεν έχουν κανένα περιορισμό στην εκτέλεση των καθημερινών τους δραστηριοτήτων.
158 158 Πίνακας 37. Σωματική ικανότητα των 102 ασθενών της μελέτης συνολικά και ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης, σύμφωνα με το ερωτηματολόγιο εκτίμησης υγείας (HAQ-DI) Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) HAQ-DI =0 a 54 (52.9) 5 (38.5) 6 (0.75) 12 (54.5) 8 (42.1) (36.4) 6 (66.7) 11 (61.1) 2 (100) HAQ-DI >0 a 48 (47.1) 8 (61.5) 2 (0.25) 10 (45.5) 11 (57.9) 7 (63.6) 3 (33.3) 7 (38.9) 0 (0) HAQ-DI b 0± ±0.81 0±0.06 0± ± ±0.44 0±0.66 0± (0-2.75) (0-2.75) (0-0.13) (0-1.63) (0-2.5) (0-1.25) (0-2) (0-2.5) (0) a αριθμός ασθενών (%) b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο - ανώτερο όριο) HAQ-DI= Health Assessment Questionnaire- Disability Index
159 Πίνακας 38. Κατάσταση σωματικής ικανότητας των 102 ασθενών της μελέτης στην τελευταία επίσκεψη παρακολούθησης, σύμφωνα με το ερωτηματολόγιο εκτίμησης υγείας HAQ-DI Κατάσταση σωματικής λειτουργικής ικανότητας Αριθμός ασθενών Αναλογία (%) Φυσιολογική (haq-di = 0) Ήπια περιορισμένη (haq-di = ) Μέτρια περιορισμένη (haq-di = ) Σοβαρά περιορισμένη (haq-di = ) 159 Σχήμα 16. Κατάσταση σωματικής λειτουργικής ικανότητας των ασθενών του συνολικού δείγματος στην τελευταία επίσκεψη παρακολούθησης, σύμφωνα με το ερωτηματολόγιο εκτίμησης υγείας HAQ-DI.
160 160 Σχήμα 17. Κατάσταση σωματικής λειτουργικής ικανότητας των ασθενών του δείγματος του κέντρου αναφοράς, του δείγματος βασισμένου σε πληθυσμό ασθενών με NIA και του συνολικού δείγματος στην τελευταία επίσκεψη παρακολούθησης, σύμφωνα με το ερωτηματολόγιο εκτίμησης υγείας HAQ-DI Ψυχολογική επιβάρυνση O βαθμός της ψυχολογικής καταπόνησης αξιολογήθηκε στους 96 από τους 102 ασθενείς που δέχτηκαν να συμπληρώσουν το Eρωτηματολόγιο Γενικής Υγείας GhQ-28. από αυτούς, οι 18 ασθενείς (18.75%) βρέθηκε να έχουν κάποια ψυχολογική διαταραχή (cases), καθώς το συνολικό GhQ-28 σκορ ήταν 5 (Πίνακας 39). η διάμεση τιμή ± τυπική απόκλιση του GhQ- 28 στους παραπάνω 18 ασθενείς βρέθηκε 9.5±3.1 (μέσος όρος 9.4, εύρος τιμών 5-17), ενώ η αντίστοιχη τιμή σε όλους τους ασθενείς ήταν 1± 3.8 (μέσος όρος 2.6, εύρος τιμών 0-17) (Πίνακας 40). Στοχεύοντας στην αναζήτηση του ειδικού πεδίου στο οποίο εστιάζεται η ψυχολογική διαταραχή, το ερωτηματολόγιο, εν συνεχεία, βαθμολογήθηκε χρησιμοποιώντας κλίμακα Likert ( ). η διάμεση τιμή ± τυπική απόκλιση του τομέα σωματικά ενοχλήματα, άγχος-αϋπνία, κοινωνική δυσλειτουργία, κατάθλιψη βρέθηκε αντίστοιχα 5±3.8, 6±3.6, 5±3.5, 0±1.7 (Πίνακας40).
161 161 Πίνακας 39. Παρουσία ψυχολογικής επιβάρυνσης, σύμφωνα με το General Health Questionnaire -28 (GHQ-28) στο σύνολο των ασθενών και στους ασθενείς ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Συνολικό GHQ-28 < 5 a 78/96 (81.25) 10/13 8/8 (100) 15/19 (78.9) 15/19 (78.9) 8/11 (72.7) 7/8 (87.5) 13/16 (81.3) 2/2 (100) Συνολικό GHQ-28 5 a 18/96 (18.75) 3/13 0/8 (0) 4/19 (21.1) 4/19 (21.1) 3/11 (27.3) 1/8 (12.5) 3/16 (18.7) 0/2 (0) a αριθμός ασθενών/ αριθμό ασθενών που συμπλήρωσαν το ερωτηματολόγιο (%) GHQ-28= General Health Questionnaire-28
162 162 Πίνακας 40. Ψυχολογική επιβάρυνση, σύμφωνα με το ερωτηματολόγιο γενικής υγείας (GHQ-28) στο σύνολο των ασθενών και στους ασθενείς ανά υποομάδα της NIA στην τελευταία επίσκεψη παρακολούθησης Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Αριθμός ασθενών που συμπλήρωσαν το ερωτηματολόγιο Συνολικό GHQ-28 a 1± 3.8 2±5 0±0.9 0±3.5 0±3.2 1± ±4.4 1±3.6 0±0 (0-17) (0-17) (0-2) (0-11) (0-10) (0-13) (0-13) (0-12) (0) Σωματικά ενοχλήματα 5± 3.8 4±4.8 3±2.4 4±3.9 6±3.2 6±4.8 7± ±3.4 2±1.4 (GHQ28-A) a (0-17) (0-17) (0-8) (1-15) (0-9) (0-16) (2-12) (0-11) (1-3) Άγχος-Αϋπνία 6±3.6 7±4.7 3±2.8 6±2.9 7±3.7 6±4 6±2.3 6± ±3.5 (GHQ28-Β) a (0-16) (1-16) (1-9) (0-10) (0-12) (0-13) (2-9) (0-15) (1-6) Κοινωνική δυσλειτουργία 5±3.5 7±3.2 2±2 5±2.8 5±2.8 7±3.6 5± ± ±5 (GHQ28-C) a (0-18) (2-13) (0-5) (0-10) (0-9) (0-11) (1-17) (0-18) (0-7) Μείζονα κατάθλιψη 0±1.7 0± ±1.4 0±1.7 1±0.7 0±1.4 0±1.5 0 (GHQ28-D) a (0-11) (0-11) (0-6) (0-7) (0-2) (0-4) (0-6) a διάμεσος τιμή ± τυπική απόκλιση (κατώτερο- ανώτερο όριο) GHQ-28= General Health Questionnaire-28
163 Κοινωνικοοικονομική κατάσταση Oικογενειακή κατάσταση από τους 102 ασθενείς που συμμετείχαν στη μελέτη, οι 18 (17.6%), ήταν έγγαμοι και οι 84 (82.4%) άγαμοι. από αυτούς που δεν είχαν παντρευτεί οι 62 ( 60.7%) συνέχιζαν να μένουν με τους γονείς τους, οι 17 (16.6%) έμεναν μόνοι τους και οι 5 (4.9%) με το σύντροφο ή τη σύντροφό τους (Πίνακας 41, Σχήμα 18). Oι 11 από τους 102 ασθενείς (10.78%) είχαν αποκτήσει τουλάχιστον 1 παιδί. Συγκεκριμένα, 7 ασθενείς είχαν 1 παιδί, 3 ασθενείς είχαν από 2 παιδιά και 1 ασθενής είχε αποκτήσει 4 παιδιά. Όλοι οι ασθενείς που έγιναν γονείς ήταν έγγαμοι. δε διαπιστώθηκε διαφορά τόσο ανάμεσα στα δύο φύλα, όσο και μεταξύ των υποομάδων της νόσου, σε επίπεδο οικογενειακής κατάστασης p=1 και p=0.244 αντίστοιχα. Πίνακας 41. Oικογενειακή κατάσταση των 102 ασθενών της μελέτης στην τελευταία επίσκεψη παρακολούθησης. Αριθμός ασθενών Αναλογία (%) Έγγαμοι Συμβιώνουν με γονείς Συμβιώνουν με σύντροφο Ζούνε μόνοι Σχήμα 18. Oικογενειακή κατάσταση των 102 ασθενών της μελέτης στην τελευταία επίσκεψη παρακολούθησης.
164 Μορφωτικό επίπεδο Oι 12 από τους 102 ασθενείς της μελέτης (11.8%) ήταν ακόμη μαθητές της Γ Λυκείου. από τους υπόλοιπους, 6 ασθενείς (5.9%) είχαν ολοκληρώσει την υποχρεωτική τους εκπαίδευση, χωρίς να συνεχίσουν τις σπουδές τους, οι 15 (14.7%) πήραν απολυτήριο Λυκείου σταματώντας στη δευτεροβάθμια εκπαίδευση, οι 20 (19.6%) έλαβαν τεχνική εκπαίδευση και οι 49 (48%) ήταν φοιτητές ή είχαν ολοκληρώσει τη φοίτησή τους σε ανώτατες σχολές (τει ή αει) (Πίνακας 42, Σχήμα 19). το μορφωτικό επίπεδο των ασθενών, όπως παρατηρήθηκε και στην περίπτωση της οικογενεικής κατάστασης, δε διέφερε σημαντικά ανάμεσα στα δύο φύλα (p=0.218), ούτε μεταξύ των υποομάδων της νόσου p= Πίνακας 42. Μορφωτικό επίπεδο των 102 ασθενών της μελέτης στην τελευταία επίσκεψη παρακολούθησης Αριθμός ασθενών Αναλογία (%) Μαθητές Υποχρεωτική εκπαίδευση Δευτεροβάθμια εκπαίδευση Τεχνική εκπαίδευση Τριτοβάθμια εκπαίδευση Σχήμα 19. Μορφωτικό επίπεδο των 102 ασθενών της μελέτης στην τελευταία επίσκε - ψη παρακολούθησης
165 Επαγγελματική κατάσταση Σαράντα πέντε ασθενείς (44.1%) καταγράφηκαν ως σπουδαστές (μαθητές ή φοιτητές), 39 ασθενείς (38.2%) εργαζόταν με πλήρη ή μερική απασχόληση και οι 18 (17.6%) ήταν άνεργοι (Πίνακας 43, Σχήμα 20). Περισσότεροι άνδρες συγκριτικά με τις γυναίκες βρέθηκε ότι ήταν εργαζόμενοι p=0.02. Πίνακας 43. Επαγγελματική κατάσταση των 102 ασθενών της μελέτης στην τελευταία επίσκεψη παρακολούθησης. Αριθμός ασθενών Αναλογία (%) Σπουδαστές Εργαζόμενοι Άνεργοι Σχήμα 20. Επαγγελματική κατάσταση των 102 ασθενών της μελέτης στην τελευταία επίσκεψη παρακολούθησης.
166 Διαμονή Σε αστική περιοχή κατοικούσε και είχε περάσει το μεγαλύτερο μέρος της ζωής του ποσοστό 82.4% των ασθενών (84/102 ασθενείς), ενώ σε ημιαστική και σε αγροτική περιοχή συνέχιζε να διαμένει το 5.9% (6/102 ασθενείς) και 11.8% των ασθενών (12/102 ασθενείς) αντίστοιχα (Πίνακας 44, Σχήμα 21). Πίνακας 44. Περιοχή διαμονής των 102 ασθενών της μελέτης κατά το μεγαλύτερο μέρος της ζωής τους. Αριθμός ασθενών Αναλογία (%) Αστική περιοχή Ημιαστική περιοχή Αγροτική περιοχή Σχήμα 21. Περιοχή διαμονής των 102 ασθενών της μελέτης κατά το μεγαλύτερο μέρος της ζωής τους.
167 Δεδομένα από την παρακολούθηση των ασθενών τα πρώτα 2 έτη από την έναρξη της νόσου από τους 102 ασθενείς της μελέτης, οι 62 (60.8%) δεν κατόρθωσαν να επίτύχουν, σύμφωνα με την αναδρομική εφαρμογή των κριτηρίων της Wallace, κλινική ύφεση τα πρώτα 2 έτη από τη διάγνωση της νόσου. Oι υπόλοιποι 40 (39.2%) πέτυχαν στο ίδιο χρονικό διάστημα κλινική ύφεση με ή χωρίς φαρμακευτική αγωγή. Συγκεκριμένα, σε μόνο τρεις από αυτούς (2.9%) επιτεύχθηκε κλινική ύφεση εκτός θεραπείας. Συχνότερα, κλινική ύφεση τα πρώτα 2 έτη της νόσου επιτεύχθηκε από τους ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα (66.7%) και ολιγοαρθρίτιδα εμμένουσα (62.5%), ενώ σπανιότερα η κατάσταση αυτή επιτυγχάνοταν από τους ασθενείς με οροθετική πολυαρθρίτιδα (18.2%) (Πίνακας 45). h διαφορά, όμως, μεταξύ των υποομάδων της νόσου δεν ήταν στατιστικώς σημαντική (Chi-Square Tests, p=0.086).
168 168 Πίνακας 45. Συχνότητα ασθενών που πέτυχαν ή όχι κλινική ύφεση τα πρώτα 2 έτη από τη διάγνωση στο συνολικό δείγμα και στους ασθενείς ανά υποομάδα της NIA Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Επίτευξη κλινικής 40 (39.2) 4 (30.8) 5 (62.5) 9 (40.9) 5 (26.3) 2 (18.2) 2 (22.2) 12 (66.7) 1 (50) ύφεσης τα πρώτα 2 έτη από τη διάγνωση a Αποτυχία επίτευξης 62 (60.8) 9 (69.2) 3 (37.5) 13 (59.1) 14 (73.7) 9 (81.8) 7 (77.8) 6 (33.3) 1 (50) κλινικής ύφεσης τα πρώτα 2 έτη από τη διάγνωση a a αριθμός ασθενών (%)
169 Δεδομένα από την παρακολούθηση των ασθενών τα πρώτα 5 έτη από την έναρξη της νόσου διαθέσιμα στοιχεία υπήρχαν για τους 100 από τους 102 ασθενείς. Όπως έγινε και για τη συνολική διάρκεια νόσου, έτσι και για τη διάρκεια των πρώτων 5 ετών από τη διάγνωση, υπολογίστηκε για κάθε ασθενή η συνολική διάρκεια ενεργότητας, ως το άθροισμα των επιμέρους επεισοδίων ενεργού νόσου. με τον τρόπο αυτό βρέθηκε ότι η διάμεση τιμή της διάρκειας ενεργότητας νόσου τα πρώτα 5 έτη για το συνολικο δείγμα ήταν 36.5 μήνες (εύρος τιμών 6-60 μήνες). επομένως, προκύπτει ότι οι ασθενείς διατρέχουν κατά μέσο όρο μεγαλύτερη από τη μισή και συγκεκριμένα ποσοστό 59.1% της διάρκειας των πρώτων 5 ετών με ενεργότητα. το υπόλοιπο χρονικό διάστημα καλύπτεται και εδώ από τις περιόδους μη ενεργότητας της νόσου, που μπορεί να είχαν οδηγήσει σε κλινική ύφεση ή όχι. η διάμεση τιμή του συνολικού διαστήματος μη ενεργού νόσου κατά τη διάρκεια των πρώτων 5 ετών από τη διάγνωση ήταν 23.5 μήνες (εύρος τιμών 0-54) και αφορούσε πάλι τους 100 ασθενείς για τους οποίους υπήρχαν επαρκή στοιχεία. αντιστοιχούσε σε μέσο όρο διάρκειας 40.9% του συνολικού διαστήματος των 5 πρώτων ετών. η διάρκεια ενεργού και μη ενεργού νόσου καθώς και η αναλογία (%) ενεργού και μη ενεργού νόσου τα πρώτα 5 έτη παρακολούθησης στο συνολικό δείγμα ασθενών και στους ασθενείς ανά υποομάδα της νόσου περιγράφονται στους πίνακες 46 και 47 αντίστοιχα.
170 170 Πίνακας 46. Διάρκεια ενεργότητας και μη ενεργότητας νόσου τα πρώτα 5 έτη παρακολούθησης στο συνολικό δείγμα ασθενών και στους ασθενείς ανά υποoμάδα της NIA Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Αριθμός ασθενών που αξιολογήθηκαν Διάρκεια ενεργότητας 36.5± ± ± ± ± ± ± ± ±2.8 νόσου τα πρώτα 5 έτη, (6-60) (9-60) (6-53) (9-56) (10-58) (14-60) (8-45) (13-60) (31-35) μήνες a Διάρκεια μη ενεργότητας 23.5±15 17± ± ± ±15.6 8± ± ± ±2.8 νόσου τα πρώτα 5 έτη, (0-54) (0-51) (7-54) (4-51) (2-50) (0-46) (15-52) (0-47) (25-29) μήνες a a μέση τιμή ± τυπική απόκλιση (κατώτερο- ανώτερο όριο)
171 171 Πίνακας 47. Αναλογία (%) διάρκειας ενεργού και μη ενεργού νόσου στο συνολικό δείγμα ασθενών και στους ασθενείς ανά υπoομάδα της NIA στα 5 πρώτα έτη της νόσου Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Αναλογία (%) ενεργότητας 59.1± ± ± ± ± ± ± ± ±4.7 νόσου στα πρώτα 5 έτη a (6-100) (15-100) ( ) ( ) (6-96.7) ( ) ( ) ( ) ( ) Αναλογία (%) συνολικής 40.9± ± ± ± ± ± ± ±.9 45±4.7 μη ενεργότητας νόσου (0-94) (0-85) ( ) (6.7-85) (3.3-94) (0-76.7) ( ) (0-78.3) ( ) στα πρώτα 5 έτη a a μέση τιμή ± τυπική απόκλιση (κατώτερο- ανώτερο όριο)
172 172 Κλινική ύφεση, σύμφωνα πάντοτε με τα κριτήρια της Wallace, πέτυχαν, συνολικά 78 από τους 100 ασθενείς (78%) σε διάστημα έως 5 ετών από τη διάγνωση της νόσου. αναλυτικά τώρα, κλινική ύφεση με φαρμακευτική αγωγή στα πρώτα 5 έτη επιτεύχθηκε, έστω και μία φορά, σε 74 από τους 100 ασθενείς (74%). Κλινική ύφεση χωρίς φαρμακευτική αγωγή στα πρώτα 5 έτη πέτυχαν οι 12 από τους 100 ασθενείς (12%) που μελετήθηκαν. και στους 12 ασθενείς, η κατάσταση αυτή επιτεύχθηκε μία μόνο φορά. η διάμεση τιμή της συνολικής διάρκειας κλινικής ύφεσης εκτός θεραπείας στα πρώτα 5 έτη της νόσου σε αυτούς τους ασθενείς βρέθηκε 23 μήνες (εύρος τιμών μήνες). O αριθμός των ασθενών που πετυχαν κλινική ύφεση με και χωρίς φαρμακευτική αγωγή στο συνολικό δείγμα και στους ασθενείς ανά υποομάδα της νόσου περιγράφεται στον πίνακα 48.
173 173 Πίνακας 48. Αριθμός ασθενών που πέτυχαν κλινική ύφεση με και χωρίς φαρμακευτική αγωγή στο συνολικό δείγμα και στους ασθενείς ανά υποομάδα της NIA στα 5 πρώτα έτη της νόσου Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) Κλινική ύφεση με ΦΑ στα 74/100 (74) 6/13 (46.2) 6/8 (75) 17/22 (77.3) 16/19 (84.2) 6/11 (54.5) 8/9 (88.9) 13/16 (72.2) 2/2 (100) πρώτα 5 έτη της νόσου a Κλινική ύφεση χωρίς ΦΑ 12/100 (12) 2/13 (15.4) 3/8 (37.5) 2/22 (9.1) 2/19 (10.5) 0/11 (0) 1/9 (11.1) 1/16 (5.6) 1/2 (50) στα πρώτα 5 έτη της νόσου a Αποτυχία επίτευξης 22/100 (22) 6/13 (46.2) 1/8 (12.5) 3/22 (13.6) 3/19 (15.8) 5/11 (45.5) 1/9 (11.1) 3/16 (18.8) - ύφεσης στα πρώτα 5 έτη της νόσου a a αριθμός ασθενών/ αριθμό ασθενών για τους οποίους υπήρχαν πληροφορίες (%)
174 Φαρμακευτική αντιμετώπιση κατά τη διάρκεια της νόσου κατά τη συνολική διάρκεια της νόσου, όλοι οι ασθενείς (100%) έλαβαν, για άλλοτε άλλο χρονικό διάστημα, θεραπεία με μη-στεροειδή αντιφλεγμονώδη φάρμακα (μσαφ). η διάμεση τιμή του χρόνου χορήγησης μσαφ ήταν 72.5±61.6 μήνες (εύρος μήνες). κορτικοστεροειδή, χορηγήθηκαν συστηματικά (από του στόματος) σε 70 ασθενείς (68.6%), ενώ μέσω ενδοαρθρικής έγχυσης σε 55 (53.9%). η διάμεση τιμή της διάρκειας χορήγησης κορτικοστεροειδών συστηματικά βρέθηκε 62±65 μήνες (εύρος μήνες). μη-βιολογικά ανοσοτροποιητικά της νόσου φάρμακα (non-biologic DMARDS) έλαβαν συνολικά 87 από τους 102 ασθενείς (85.3%). μεθοτρεξάτη, είτε από του στόματος, είτε παρεντερικώς, χορηγήθηκε σε 71 ασθενείς (69.6%). Ένα ή περισσότερα από τα υπόλοιπα μη-βιολογικά ανοσοτροποιητικά της νόσου φάρμακα (κυκλοσπορίνη, σουλφασαλαζίνη, υδροξυχλωροκίνη, λεφλουνομίδη, D-πενικιλλαμίνη, άλατα χρυσού, αζαθιοπρίνη) έλαβε ίδιο, περίπου, ποσοστό ασθενών με αυτούς που έλαβαν μεθοτρεξάτη και συγκεκριμένα 72 από τους 102 ασθενείς (70.6%). αναλυτικά, κυκλοσπορίνη πήραν 43 ασθενείς (42.1%), σουλφασαλαζίνη 29 ασθενείς (28.4%), υδροξυχλωροκίνη 24 ασθενείς (23.5%), λεφλουνομίδη 13 ασθενείς (12.7%), D-πενικιλλαμίνη 10 ασθενείς (9.8%), άλατα χρυσού 8 ασθενείς (7.8%) και αζαθιοπρίνη 4 ασθενείς (3.9%).
175 Πίνακας 49. Χορηγηθέντα φάρμακα στους 102 ασθενείς της μελέτης κατά τη συνολική διάρκεια παρακολούθησης. Είδος φαρμάκου Αριθμός ασθενών Αναλογία (%) μσαφ κορτικοστεροειδή (από του στόματος) κορτικοστεροειδή (ενδοαρθρικά) μη βιολογικά DMARDS μεθοτρεξάτη κυκλοσπορίνη Σουλφασαλαζίνη Υδροξυχλωροκίνη Λεφλουνομίδη D-πενικιλλαμίνη Άλατα χρυσού αζαθιοπρίνη βιολογικοί παράγοντες inh-tnf παράγοντες Etanercept Adalimumab infliximab Golimumab 1 1 μη-anti TNF βιολογικοί παραγ. 6) 5.9 Anakinra Rituximab Tocilizumab
176 176 Σχήμα 22. Χορηγηθέντα φάρμακα στους 102 ασθενείς της μελέτης κατά τη συνολική διάρκεια παρακολούθησης. η διάμεση τιμή της χρονικής διάρκειας χορήγησης μεθοτρεξάτης βρέθηκε 84±57.5 μήνες (εύρος μήνες). Όσον αφορά στα υπόλοιπα DMARDS, η διάμεση τιμή του χρονικού διαστήματος χορήγησης κυκλοσπορίνης ήταν 38±39.5 μήνες (εύρος μήνες), σουλφασαλαζίνης 24±34.6 μήνες (εύρος μήνες), υδροξυχλωροκίνης 27±54.2 μήνες (εύρος μήνες), λεφλουνομίδης 16±22.4 μήνες (εύρος 3-60 μήνες), D-πενικιλλαμίνης 20±39.6 μήνες (εύρος μήνες), αλάτων χρυσού 33±38.9 μήνες (εύρος μήνες) και αζαθιοπρίνης 32±12.2 μήνες (εύρος μήνες). από τους 87 ασθενείς που πήραν μη-βιολογικά ανοσοτροποιητικά της νόσου φάρμακα, οι 26 ασθενείς έλαβαν μόνον ένα, οι 33 έλαβαν δύο, οι 17 έλαβαν τρία, οι 6 έλαβαν τέσσερα, οι 3 έλαβαν πέντε και 2 ασθενείς έλαβαν έξι διαφορετικά DMARDS (Σχήμα 23). O μέσος όρος του αριθμού των διαφορετικών DMARDS που πήραν οι 87 ασθενείς βρέθηκε 2.23 (εύρος 1-6). βιολογικοί παράγοντες, χορηγήθηκαν σε 52 από τους 102 ασθενείς (51%), κατά τη συνολική πορεία της νόσου. από τους 52 ασθενείς, θεραπεία με inh-tnf παράγοντες (etanercept, adalimumab, infliximab, golimumab) έλαβαν όλοι ( 100% από αυτούς που πήραν βιολογικούς παράγοντες και 51% από το συνολικό δείγμα ασθενών). αναλυτικά, etanercept πήραν 31 ασθενείς (59.6% από αυτούς έλαβαν inh-tnf παράγοντες και 30.4% από το συνολικό δείγμα ασθενών), adalimumab πήραν 27 ασθενείς (51.9% από αυτούς έλαβαν
177 177 inh-tnf παράγοντες και 26.5% από το συνολικό δείγμα ασθενών), infliximab πήραν 21 ασθενείς (40.4% από αυτούς έλαβαν inh-tnf παράγοντες και 20.6% από το συνολικό δείγμα ασθενών) και golimumab πήρε μόνο 1 ασθενής (1.9% από αυτούς έλαβαν inh-tnf παράγοντες και 1% από το συνολικό δείγμα ασθενών). η μέση χρονική διάρκεια χορήγησης etanercept βρέθηκε 40.5±22.6 μήνες (εύρος μήνες), adalimumab 31±19.5 μήνες (εύρος 7-72 μήνες), infliximab 24±24 μήνες (εύρος 3-96 μήνες). Golimumab πήρε, όπως αναφέρθηκε, ένας μόνο ασθενής για διάστημα 6 μηνών. Mη inh-tnf βιολογικοί παράγοντες (anakinra, rituximab, tocilizumab) χορηγήθηκαν σε 6 συνολικά ασθενείς στην πορεία της νόσου (11.5% από αυτούς που πήραν βιολογικούς παράγοντες και 5.9% από το συνολικό δείγμα ασθενών). Συχνότερα συνταγογραφούμενος μη inh-tnf βιολογικός παράγοντας αναδείχθηκε το rituximab. αναλυτικά, 4 ασθενείς πήραν rituximab (7.6% από αυτούς που πήραν βιολογικούς παράγοντες και 3.9% από το συνολικό δείγμα ασθενών) 2 ασθενείς πήραν anakinra (3.8% από αυτούς που πήραν βιολογικούς παράγοντες και 1.9 % από το συνολικό δείγμα ασθενών) και 2 ασθενείς πήραν tocilizumab (3.8% από αυτούς που πήραν βιολογικούς παράγοντες και 1.9% από το συνολικό δείγμα ασθενών). η διάμεση τιμή της χρονικής διάρκειας χορήγησης rituximab ήταν 13±9.3 μήνες (εύρος 6-26 μήνες), anakinra 9±1.4 μήνες (εύρος 8-10 μήνες) και tocilizumab 7±1.41 μήνες (εύρος 6-8 μήνες). από τους 52 ασθενείς που πήραν βιολογικούς παράγοντες, οι 28 ασθενείς έλαβαν μόνον ένα, οι 19 έλαβαν δύο, ένας έλαβε τρεις, 3 έλαβαν τέσσερις και ένας έλαβε πέντε διαφορετικούς βιολογικούς παράγοντες (Σχήμα 24). O μέσος όρος του αριθμού των διαφορετικών βιολογικών παραγόντων που χρησιμοποιήθηκε ανά ασθενή βρέθηκε 1.65 (εύρος 1-5). η συχνότητα των ασθενών στο συνολικό δείγμα που έλαβε το κάθε φάρμακο στην πορεία της νόσου περιγράφεται στον πίνακα 49 και απεικονίζεται στο σχήμα 22. η διάρκεια χορήγησης κάθε φαρμάκου περιγράφεται στον πίνακα 50 για το συνολικό δείγμα και στους πίνακες για τους ασθενείς κάθε υποομάδας. Πρόσβαση σε βιολογική θεραπεία μέσα στα πρώτα 2 έτη από την έναρξη της νόσου είχαν οι 28 από τους 102 ασθενείς ( 27.5%). από αυτούς οι 13 χρειάστηκε, τελικά, να λάβουν βιολογικό παράγοντα, κατά τη συνολική διάρκεια της νόσου τους. Ένας μόνο ξεκίνησε βιολογική θεραπεία πριν το πέρασμα 2 ετών και συγκεκριμένα 6 μήνες από την έναρξη της νόσου. Στους υπόλοιπους 74 ασθενείς (72.5%) που δεν είχαν αντίστοιχη πρόσβαση, συνέβαλλαν διάφοροι παράγοντες, μεταξύ των οποίων σημαντικότεροι ήταν η καθυστέ-
178 178 ρηση στη διάγνωση της νόσου πριν την εκτίμηση του παιδιού από το Παιδορευματολογικό κέντρο και κυρίως η απουσία επίσημης ένδειξης χορήγησης βιολογικής θεραπείας πριν το από τους 74 ασθενείς, οι 38 πήραν τελικά βιολογική θεραπεία, αργότερα στην πορεία της νόσου. η διάμεση τιμή του χρονικού διαστήματος που μεσολάβησε από την έναρξη της νόσου μέχρι τη χορήγηση του πρώτου βιολογικού παράγοντα στους 52 ασθενείς βρέθηκε 138±78.4 μήνες (εύρος μήνες). τέλος, 13 ασθενείς από τους 102 (12.7%), έλαβαν θεραπεία μόνο με μσαφ± κορτικοστεροειδή σε όλη τη διάρκεια της νόσου. Πίνακας 50. Διάρκεια χορήγησης του κάθε φαρμάκου στο σύνολο των ασθενών κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης μήνες* μσαφ ±61.6 (5-290) κορτικοστεροειδή (από του στόματος) 70 62±65.8 (4-269) μη βιολογικά DMARDS 87 72±58.4 (12-281) μεθοτρεξάτη 71 84±56.3 (4-219) κυκλοσπορίνη 43 38±39.5 (4-150) Σουλφασαλαζίνη 29 24±34.6 (3-180) Υδροξυχλωροκίνη 24 27±54.2 (7-216) Λεφλουνομίδη 13 16±22.4 (3-60) D-πενικιλλαμίνη 10 20±39.6 (6-130) Άλατα χρυσού 8 33±38.9 (12-108) αζαθιοπρίνη 4 32±12.2 (22-47) βιολογικοί παράγοντες 52 50±30.9 (4-117) inh-tnf παράγοντες ±29.6 (4-117) Etanercept ±22.6 (4-108) Adalimumab 27 31±19.5 (7-72) infliximab 21 24±24 (3-96) Golimumab 1 6 μη-inh TNF βιολογικοί παραγ. 6 18±8.7 (6-26) Anakinra 2 9 ±1.4 (8-10) Rituximab 4 13± 9.3 (6-26) Tocilizumab 2 7±1.4 (6-8) * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
179 Πίνακας 51. Διάρκεια χορήγησης του κάθε φαρμάκου στους 13 ασθενείς με συστηματική αρθρίτιδα κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης μήνες* μσαφ 13 (100) 74±76.3 (9-264) κορτικοστεροειδή (από του στόματος) 13 (100) 72±74.2 (4-229) κορτικοστεροειδή (ενδοαρθρικά) 5 (38.5) μη βιολογικά DMARDS 11(84.6) 75±57 (12-199) μεθοτρεξάτη 9 (69) 79±65.3 (12-188) κυκλοσπορίνη 7 (53.8) 16±34.5 (6-105) Σουλφασαλαζίνη 1 (7.6) 36 Υδροξυχλωροκίνη 3 (23) 54±67.4 (7-140) Λεφλουνομίδη 5 (38.5) 16±20.6 (8-55) D-πενικιλλαμίνη 1(7.6) 13 Άλατα χρυσού 2 (15.4) 29.5±17.7 (17-42) αζαθιοπρίνη - - βιολογικοί παράγοντες 5 (38.5) 79±35.3 (12-101) inh-tnf παράγοντες 5 (38.5) 79±31.5 (12-87) Etanercept 4 (30.7) 46.5±12.3 (32-62) Adalimumab 3 (23) 39±4.6 (39-47) infliximab 2 (15.4) 7.5±6.3 (3-12) Golimumab - - μη-inh TNF βιολογικοί παραγ. 2 (15.4) 14±11.3 (6-22) Anakinra 1(7.6) 8 Rituximab 1(7.6) 6 Tocilizumab 2 (15.4) 7±1.4 (6-8) * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 179
180 180 Πίνακας 52. Διάρκεια χορήγησης του κάθε φαρμάκου στους 8 ασθενείς με ολιγοαρθρίτιδα εμμένουσα κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης, μήνες* μσαφ 8 (100) 55±31.1 (12-109) κορτικοστεροειδή (από του στόματος) 2 (25) 91±26.8 (72-110) κορτικοστεροειδή (ενδοαρθρικά) 5 (62.5) μη βιολογικά DMARDS 3 (37.5) 65±40.2 (13-92) μεθοτρεξάτη 2 (25) 27.5±17.7 (15-40) κυκλοσπορίνη 1 (12.5) 38 Σουλφασαλαζίνη 2 (25) 45±46.6 (12-78) Υδροξυχλωροκίνη 3 (37.5) 13±27.1 (13-60) Λεφλουνομίδη - - D-πενικιλλαμίνη - - Άλατα χρυσού - - αζαθειοπρίνη 1 (12.5) 24 βιολογικοί παράγοντες 2 (25) 76.5±30.4 (55-99) inh-tnf παράγοντες 2 (25) 77±31.1 (55-99) Etanercept - - Adalimumab 2 (25) 50±31.1 (28-72) infliximab 2 (25) 26.5±0.7 (26-27) Golimumab - - μη-inh TNF βιολογικοί παραγ. - - Anakinra - - Rituximab - - Tocilizumab - - * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
181 Πίνακας 53. Διάρκεια χορήγησης του κάθε φαρμάκου στους 22 ασθενείς με ολιγοαρθρίτιδα επεκταθείσα κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης, μήνες* μσαφ 22 (100) 70±49.8 (13-200) κορτικοστεροειδή (από του στόματος) 18 (81.8) 54.5±38.2 (6-138) κορτικοστεροειδή (ενδοαρθρικά) 17 (77.3) μη βιολογικά DMARDS 20 (90.9) 72.5±34.2 (12-138) μεθοτρεξάτη 18 (81.8) 68.5±32.4 (23-141) κυκλοσπορίνη 11 (50) 48±54.5 (7-150) Σουλφασαλαζίνη 5 (22.7) 9±4.4 (3-14) Υδροξυχλωροκίνη 2 (9) 66±62.2 (22-110) Λεφλουνομίδη 2 (9) 58±2.8 (56-60) D-πενικιλλαμίνη 1(4.5) 6 Άλατα χρυσού - - αζαθειοπρίνη - - βιολογικοί παράγοντες 12 (54.5) 31±32.8 (4-97) inh-tnf παράγοντες 12 (54.5) 31±33.8 (4-97) Etanercept 7(31.8) 24±19.8 (4-54) Adalimumab 8 (36.4) 23±14.3 (12-50) infliximab 2 (9) 51.5±62.9 (7-96) Golimumab - - μη-inh TNF βιολογικοί παραγ. - - Anakinra - - Rituximab - - Tocilizumab - - * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 181
182 182 Πίνακας 54. Διάρκεια χορήγησης του κάθε φαρμάκου στους 19 ασθενείς με πολυαρθρίτιδα RF αρνητική κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης, μήνες* μσαφ 19 (100) 95±65.8 (5-248) κορτικοστεροειδή (από του στόματος) 16 (84.2) 86.5±71.8 (5-226) κορτικοστεροειδή (ενδοαρθρικά) 7 (36.8) μη βιολογικά DMARDS 18 (94.7) 75±61.7 (22-208) μεθοτρεξάτη 17 (89.4) 96±60.1 (16-208) κυκλοσπορίνη 10 (52.6) 39.5±25.3 (12-90) Σουλφασαλαζίνη 5 (26.3) 26±10 (12-36) Υδροξυχλωροκίνη 2 (10.5) 21.5±3.5 (19-24) Λεφλουνομίδη 1 (5.2) 3 D-πενικιλλαμίνη 4(21) 32.5±51.3 (20-130) Άλατα χρυσού 3 (15.8) 24±52.3 (12-108) αζαθειοπρίνη 2 31±12.7 (22-40) βιολογικοί παράγοντες 11(57.9) 66±31.7 (7-117) inh-tnf παράγοντες 11(57.9) 64±32.6 (7-117) Etanercept 6 (31.6) 50±27.9 (31-108) Adalimumab 7 (36.8) 15±27.9 (7-67) infliximab 4 (21) 25±13 (9-41) Golimumab - - μη-inh TNF βιολογικοί παραγ. 2 (10.5) 17±12.7 (8-26) Anakinra - - Rituximab 2 (10.5) 17± 12.7(8-26) Tocilizumab - - * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
183 Πίνακας 55. Διάρκεια χορήγησης του κάθε φαρμάκου στους 11 ασθενείς με πολυαρθρίτιδα RF θετική κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης, μήνες* μσαφ 11 (100) 132±89.6 (16-290) κορτικοστεροειδή (από του στόματος) 10 (90.9) 91±97.6 (18-269) κορτικοστεροειδή (ενδοαρθρικά) 5 (45.5) μη βιολογικά DMARDS 11 (100) 89±61.2 (30-254) μεθοτρεξάτη 11(100) 105±63 (4-219) κυκλοσπορίνη 5 (45.5) 26±49.9 (5-125) Σουλφασαλαζίνη 3 (27.2) 22±8.1 (9-24) Υδροξυχλωροκίνη 6 (54.5) 32.5±44.8 (8-108) Λεφλουνομίδη 3 (27.2) 9±7.3 (6-20) D-πενικιλλαμίνη 2 (18.2) 43.5±40.3 (15-72) Άλατα χρυσού - - αζαθειοπρίνη 1 (9) 47 βιολογικοί παράγοντες 9 (81.8) 54±27.8 (12-107) inh-tnf παράγοντες 9 (81.8) 54±24.4 (12-89) Etanercept 6 (54.5) 48.5±20.2 (12-68) Adalimumab 3 (27.2) 31±17 (28-59) infliximab 5 (45.5) 24±18.6 (6-54) Golimumab - - μη-inh TNF βιολογικοί παραγ. 1(9) 18 Anakinra - - Rituximab 1 (9) 18 Tocilizumab - - * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 183
184 184 Πίνακας 56. Διάρκεια χορήγησης του κάθε φαρμάκου στους 9 ασθενείς με ψωριασική αρθρίτιδα κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης, μήνες* μσαφ 9 (100) 86.5±57.7 (6-166) κορτικοστεροειδή (από του στόματος) 4 (44.4) 86.5 ±39.4 (48-141) κορτικοστεροειδή (ενδοαρθρικά) 4 (44.4) μη βιολογικά DMARDS 7 (77.8) 72±97.2 (17-281) μεθοτρεξάτη 5 (55.6) 180±80.4 (17-192) κυκλοσπορίνη 4 (44.4) 57±30.1 (4-72) Σουλφασαλαζίνη 1 (11.1) 33 Υδροξυχλωροκίνη 3 (33.3) 12±42.7 (8-84) Λεφλουνομίδη - - D-πενικιλλαμίνη - - Άλατα χρυσού 1 (11.1) 81 αζαθειοπρίνη - - βιολογικοί παράγοντες 6 (66.7) 44±10.1 (36-60) inh-tnf παράγοντες 6 (66.7) 44±10.1 (36-60) Etanercept 4 (44.4) 32.5±15.9 (24-60) Adalimumab 2 (22.2) 28±22.6 (12-44) infliximab 1 (11.1) 21 Golimumab - - μη-inh TNF βιολογικοί παραγ. 1 (11.1) 9 Anakinra 1 (11.1) 9 Rituximab - - Tocilizumab - - * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
185 Πίνακας 57. Διάρκεια χορήγησης του κάθε φαρμάκου στους 18 ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης, μήνες* μσαφ 18 (100) 59±32.8 (25-144) κορτικοστεροειδή (από του στόματος) 5 (27.8) 34±18.2 (12-51) κορτικοστεροειδή (ενδοαρθρικά) 12 (66.7) μη βιολογικά DMARDS 14 (94.4) 58±62.7 (24-216) μεθοτρεξάτη 7(38.9) 50±39.3 (24-135) κυκλοσπορίνη 2 (11.1) 79.5±23.3 (63-96) Σουλφασαλαζίνη 9 (50) 36±51 (12-180) Υδροξυχλωροκίνη 2 (11.1) 118.5±137.9 (21-216) Λεφλουνομίδη - - D-πενικιλλαμίνη 1 (5.6) 19 Άλατα χρυσού - - αζαθειοπρίνη - - βιολογικοί παράγοντες 6 (33.3) 44±25.1(4-70) inh-tnf παράγοντες 6 (33.3) 44±25.1 (4-70) Etanercept 3 (16.7) 24±20 (4-44) Adalimumab 1 (5.6) 44 infliximab 4 (22.3) 37.5±45.9 (5-70) Golimumab 1 (5.6) 6 μη-inh TNF βιολογικοί παραγ. - - Anakinra - - Rituximab - - Tocilizumab - - * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 185
186 186 Πίνακας 58. Διάρκεια χορήγησης του κάθε φαρμάκου στους 2 ασθενείς με αδιαφοροποίητη αρθρίτιδα κατά τη διάρκεια της νόσου Είδος φαρμάκου Αριθμός ασθενών (%) Διάρκεια χορήγησης, μήνες* μσαφ 2 (100) 34.5±14.8 (24-25) κορτικοστεροειδή (από του στόματος) 2 (100) 30.5±7.8 (25-36) κορτικοστεροειδή (ενδοαρθρικά) - μη βιολογικά DMARDS 2 (100) 44±28.3 (24-64) μεθοτρεξάτη - - κυκλοσπορίνη 1(50) 40 Σουλφασαλαζίνη 1(50) 13 Υδροξυχλωροκίνη 1(50) 64 Λεφλουνομίδη - - D-πενικιλλαμίνη - - Άλατα χρυσού - - αζαθειοπρίνη - - βιολογικοί παράγοντες 1(50) 15 inh-tnf παράγοντες 1(50) 15 Etanercept - - Adalimumab - - infliximab 1(50) 15 Golimumab - - μη-inh TNF βιολογικοί παραγ. - - Anakinra - - Rituximab - - Tocilizumab - - * διάμεση τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
187 187 Σχήμα 23. Αριθμός διαφορετικών μη- βιολογικών DMARD που χορηγήθηκαν στους ασθενείς κατά τη συνολική διάρκεια της νόσου. Σχήμα 24. Αριθμός διαφορετικών βιολογικών παραγόντων που χορηγήθηκαν στους ασθενείς κατά τη συνολική διάρκεια της νόσου.
188 188 μονοθεραπεία με ένα DMARD± μσαφ± κορτικοστεροειδή χορηγήθηκε σε 86 από τους 100 ασθενείς (86%) για τους οποίους υπήρχαν επαρκή στοιχεία από τους φακέλους. Για τους υπόλοιπους 2 ασθενείς οι πληροφορίες ήταν αμφίβολες και για το λόγο αυτό, κρίθηκε σκόπιμο να εξαιρεθούν από τους υπολογισμούς που αφορούν στην παρούσα ενότητα. από τους 86 παραπάνω ασθενείς, οι 62 (62%) έλαβαν μονοθεραπεία με μεθοτρεξάτη± μσαφ±κορτικοστεροειδή. Oι υπόλοιποι 24 ασθενείς (24%) έλαβαν μονοθεραπεία με κάποιο από τα άλλα πλην της μεθοτρεξάτης DMARD. η διάμεση τιμή της χρονικής διάρκειας μονοθεραπείας με μεθοτρεξάτη ± μσαφ± κορτικοστεροειδή ήταν 36±46 μήνες (εύρος τιμών 5-219). μονοθεραπεία με inh-tnf παράγοντα ± μσαφ± κορτικοστεροειδή έλαβαν 16 ασθενείς (16%) κατά τη διάρκεια της νόσου. η διάμεση τιμή του χρονικού διαστήματος μονοθεραπείας με inh-tnf παράγοντα ± μσαφ± κορτικοστεροειδή ήταν 32±23.3 (εύρος τιμών 4-88). μονοθεραπεία με άλλον, πλην των inh-tnf, βιολογικό παράγοντα έλαβαν 2 ασθενείς (2%) για χρονικό διάστημα με διάμεση τιμή 12±8.5 μήνες (εύρος τιμών 6-18 μήνες). Συνδυασμένη θεραπεία χορηγήθηκε στους 57 από τους 100 ασθενείς (57%) στη συνολική διάρκεια της νόσου. Συνδυασμό θεραπείας με δύο ή τρία διαφορετικά μη-βιολογικά DMARDs ± μσαφ± κορτικοστεροειδή έλαβαν 42 ασθενείς (42%). η διάμεση χρονική διάρκεια χορήγησης συνδυασμένης θεραπείας με 2 ή 3 μη-βιολογικά DMARDs βρέθηκε 33±25 μήνες (εύρος τιμών μήνες). Συνδυασμό θεραπείας με μη-βιολογικό DMARD και inh-tnf παράγοντα ± μσαφ± κορτικοστεροειδή έλαβαν 46 ασθενείς (46%). η διάμεση χρονική διάρκεια χορήγησης της παραπάνω συνδυασμένης θεραπείας ήταν 40±29.7 μήνες (εύρος τιμών μήνες). Συνδυασμό θεραπείας με μη-βιολογικό DMARD και άλλον μη inh- TNF βιολογικό παράγοντα ± μσαφ± κορτικοστεροειδή έλαβαν 3 ασθενείς (3%) για χρονικό διάστημα με διάμεσο τιμή 22±9.5 μήνες (εύρος τιμών 8-26 μήνες). Συνδυασμένη θεραπεία που περιελάμβανε τη μεθοτρεξάτη (συν δεύτερο ή τρίτο μη-βιολογικό DMARD ή συν inh-tnf παράγοντα ή συν άλλο, πλην των inh-tnf, βιολογικό παράγοντα ± μσαφ± κορτικοστεροειδή) έλαβαν 48 ασθενείς (48%) για χρονικό διάστημα με διάμεσο τιμή 52.5±41.5 μήνες (εύρος τιμών μήνες). τα σχήματα θεραπείας που χορηγήθηκαν στους ασθενείς της μελέτης κατά τη συνολική διάρκεια παρακολούθησης περιγράφονται στους πίνακες
189 Πίνακας 59. Σχήματα θεραπείας που χορηγήθηκαν στους ασθενείς της μελέτης κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) b Διάρκεια θεραπείας, μήνες c μονοθεραπεία με μη-βιολογικό DMARD 86 53±56.2 (5-281) μονοθεραπεία με μεθοτρεξάτη 62 36±46 (5-219) μονοθεραπεία με inh-tnf παράγοντα 16 32±23.3 (4-88) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 2 12±8.5 (6-18) Συνδυασμένη θεραπεία 57 63±40.2 (4-177) Συνδυασμένη θεραπεία με DMARDS 42 33±25 (12-106) Συνδυασμένη θεραπεία με DMARD(s)+ inh-tnf παράγοντα 45 40±29.7 (4-117) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 3 22±9.5 (8-26) Συνδυασμένη θεραπεία με μεθοτρεξάτη ±41.5 (4-177) 189 a ± ΜΣΑΦ±κορτικοστεροειδή b ο αριθμός και το % ποσοστό ταυτίζονται καθώς ο συνολικός αριθμός ασθενών που αξιολογήθηκαν ήταν 100. c διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
190 190 Πίνακας 60. Σχήματα θεραπείας που χορηγήθηκαν στους 13 ασθενείς της μελέτης με συστηματική αρθρίτιδα κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 11 (84.6) 44±48.2 (5-179) μονοθεραπεία με μεθοτρεξάτη 9 (69.2) 21±20.3(5-57) μονοθεραπεία με inh-tnf παράγοντα 0 - μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 1(7.7) 6 Συνδυασμένη θεραπεία 8(61.5) 100±46.7 (12-127) Συνδυασμένη θεραπεία με DMARDS 7(53.8) 23±31.1 (18-105) Συνδυασμένη θεραπεία με DMARD(s) + + inh-tnf παράγοντα 5(38.5) 79±31.5 (12-87) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 1 (7.7) 22 Συνδυασμένη θεραπεία με μεθοτρεξάτη 7(53.8) 102±49.7 (12-127) a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
191 Πίνακας 61. Σχήματα θεραπείας που χορηγήθηκαν στους 8 ασθενείς της μελέτης με ολιγοαρθρίτιδα εμμένουσα κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 3 (37.5) 53±33.2 (13-79) μονοθεραπεία με μεθοτρεξάτη 2 (25) 14.5±0.7(14-15) μονοθεραπεία με inh-tnf παράγοντα 2(25) 27±1.4(26-28) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 0 Συνδυασμένη θεραπεία 2(25) 62.5±31.8 (40-85) Συνδυασμένη θεραπεία με DMARDS 2(25) 12.5±0.7 (12-13) Συνδυασμένη θεραπεία με DMARD(s)+ + inh-tnf παράγοντα 2(25) 50±32.5 (27-73) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία με μεθοτρεξάτη 7(53.8) 102±49.7 (12-127) a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 191
192 192 Πίνακας 62. Σχήματα θεραπείας που χορηγήθηκαν στους 22 ασθενείς της μελέτης με ολιγοαρθρίτιδα επεκταθείσα κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπεία a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 20 (90.9) 45.5±28.7 (12-110) μονοθεραπεία με μεθοτρεξάτη 15 (68.2) 43±24.4(10-96) μονοθεραπεία με inh-tnf παράγοντα 3 (13.6) 12±46.3 (4-88) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία 16 (72.7) 52±42.1 (4-130) Συνδυασμένη θεραπεία με DMARDS 12(54.5) 35±28 (13-106) Συνδυασμένη θεραπεία με DMARD(s)+ + inh-tnf παράγοντα 12 (54.5) 22±30.1 (4-97) Συνδυασμένη θεραπεία με DMARD(s)+ + βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία με μεθοτρεξάτη 14 (63.6) 27.5±39.7 (4-130) a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
193 Πίνακας 63. Σχήματα θεραπείας που χορηγήθηκαν στους 19 ασθενείς της μελέτης με πολυαρθρίτιδα με αρνητικό RF κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 18 (94.7) 53±63.3 (7-206) μονοθεραπεία με μεθοτρεξάτη 16(84.2) 33.5±48.5 (7-170) μονοθεραπεία με inh-tnf παράγοντα 3(15.8) 13±20.9 (4-44) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία 13 (68.4) 79±47.2 (27-177) Συνδυασμένη θεραπεία με DMARDS 9(47.4) 45±20.1 (16-71) Συνδυασμένη θεραπεία με DMARD(s)+ + inh-tnf παράγοντα 11(57.9) 45±34.1 (7-117) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 2 (10.5) 17±12.7 (8-26) Συνδυασμένη θεραπεία με μεθοτρεξάτη 12(63.2) 70.5±50.6 (7-177) a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 193
194 194 Πίνακας 64. Σχήματα θεραπείας που χορηγήθηκαν στους 11 ασθενείς της μελέτης με πολυαρθρίτιδα με θετικό RF κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 18 (94.7) 53±63.3 (7-206) μονοθεραπεία με μεθοτρεξάτη 16(84.2) 33.5±48.5 (7-170) μονοθεραπεία με inh-tnf παράγοντα 3(15.8) 13±20.9 (4-44) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία 13 (68.4) 79±47.2 (27-177) Συνδυασμένη θεραπεία με DMARDS 9(47.4) 45±20.1 (16-71) Συνδυασμένη θεραπεία με DMARD(s)+ + inh-tnf παράγοντα 11(57.9) 45±34.1 (7-117) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 2 (10.5) 17±12.7 (8-26) Συνδυασμένη θεραπεία με μεθοτρεξάτη 12(63.2) 70.5±50.6 (7-177) a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
195 Πίνακας 65. Σχήματα θεραπείας που χορηγήθηκαν στους 8 ασθενείς της μελέτης με ψωριασική αρθρίτιδα κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 11(100) 62±68 (30-254) μονοθεραπεία με μεθοτρεξάτη 9 (81.8) 35±69.8(12-219) μονοθεραπεία με inh-tnf παράγοντα 2 (18.2) 51.5±6.4(47-56) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 1(9) 18 Συνδυασμένη θεραπεία 9 (81.8) 66±27.7 (40-137) Συνδυασμένη θεραπεία με DMARDS 6(54.5) 37±12.1 (23-50) Συνδυασμένη θεραπεία με DMARD(s)+ + inh-tnf παράγοντα 9 (81.8) 43±21.6 (12-87) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία με μεθοτρεξάτη 9 (81.8) 54±30 (40-137) a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 195
196 196 Πίνακας 66. Σχήματα θεραπείας που χορηγήθηκαν στους 17 ασθενείς της μελέτης με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 14(82.4) 47.5±47.8 (24-199) μονοθεραπεία με μεθοτρεξάτη 6 (35.3) 42±27.9(20-89) μονοθεραπεία με inh-tnf παράγοντα 4(23.5) 34±22.3 (22-70) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία 4(23.5) 53±30.8 (27-96) Συνδυασμένη θεραπεία με DMARDS 3(17.6) 63±28.6 (39-96) Συνδυασμένη θεραπεία με DMARD(s)+ + inh-tnf παράγοντα 2 (11.8) 15.5±16.3 (4-27) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία με μεθοτρεξάτη 3(17.6) 39±20.5 (27-67) a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο)
197 Πίνακας 67. Σχήματα θεραπείας που χορηγήθηκαν στους 2 ασθενείς της μελέτης με αταξινόμητη αρθρίτιδα κατά τη συνολική διάρκεια παρακολούθησης Σχήματα θεραπείας a Αριθμός ασθενών (%) Διάρκεια θεραπείας, μήνες b μονοθεραπεία με μη-βιολογικό DMARD 2(100) 37.5±19 (24-51) μονοθεραπεία με μεθοτρεξάτη 0 - μονοθεραπεία με inh-tnf παράγοντα 0 - μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία 2(100) 14±1.4 (13-15) Συνδυασμένη θεραπεία με DMARDS 1(50) 13 Συνδυασμένη θεραπεία με DMARD(s) + + inh-tnf παράγοντα 1(50) 15 Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα 0 - Συνδυασμένη θεραπεία με μεθοτρεξάτη 0 - a ± ΜΣΑΦ±κορτικοστεροειδή b διάμεσος τιμή ± τυπική απόκλιση (κατώτερο-ανώτερο όριο) 197
198 Φαρμακευτική αγωγή των ασθενών κατά την τελευταία επίσκεψη Στην τελευταία επίσκεψη παρακολούθησης, που πραγματοποιήθηκε στα πλαίσια της μελέτης, 35 από τους 102 ασθενείς (34.3%) δεν ελάμβανε καμία θεραπεία. από τους υπόλοιπους, οι 19 ελάμβαναν μσαφ (18.6% του συνόλου των ασθενών και 28.4% των ασθενών που έπαιρναν κάποια αγωγή), οι 18 κορτικοστεροειδή (17.6% του συνόλου των ασθενών και 26.9% των ασθενών που έπαιρναν κάποια αγωγή), οι 28 μεθοτρεξάτη (27.5% του συνόλου των ασθενών και 41.8% των ασθενών που έπαιρναν κάποια αγωγή), οι 18 έπαιρναν κάποιο/α από τα άλλα μη-βιολογικά DMARDs (17.6% του συνόλου των ασθενών και 26.9% των ασθενών που έπαιρναν κάποια αγωγή) και οι 42 ελάμβαναν θεραπεία με βιολογικό παράγοντα (41.2% του συνόλου των ασθενών και 62.6% των ασθενών που έπαιρναν κάποια αγωγή). αναλυτικότερα, από τους 18 ασθενείς που έπαιρναν κάποιο/α από τα άλλα μη-βιολογικά DMARDs, οι 5 ελάμβαναν κυκλοσπορίνη, οι 3 σουλφασαλαζίνη, οι 6 υδροξυχλωροκίνη, οι 5 λεφλουνομίδη και ένας έπαιρνε αζαθιοπρίνη. inh-tnf παράγοντας χορηγούνταν σε 38 ασθενείς. από αυτούς, 19 έπαιρναν etanercept, 15 adalimumab, 3 infliximab και ένας golimumab. Άλλο, μη inh-tnf, βιολογικό παράγοντα έπαιρναν 4 ασθενείς. Σε δύο χορηγούνταν rituximab και σε άλλους 2 ασθενείς χορηγούνταν tocilizumab (Πίνακας 68, Σχήμα 25).
199 Πίνακας 68. Συχνότητα ασθενών με Νεανική Ιδιοπαθή Αρθρίτιδα που λάμβανε το κάθε φάρμακο στην τελευταία επίσκεψη παρακολούθησης και κατά τη συνολική διάρκεια παρακολούθησης Αριθμός ασθενών (%) Αριθμός ασθενών (%) που λαμβάνει το κάθε έλαβε το κάθε φάρμακο φάρμακο στην τελευταία κατά τη συνολική Φαρμακευτική αγωγή επίσκεψη παρακολούθησης διάρκεια της νόσου καμία φαρμακευτική αγωγή 35 (34.3) - μσαφ 19 (18.6) 102 (100) Συστηματικά κορτικοστεροειδή 18 (17.6) 70 (68.6) μη βιολογικά DMARDS 43 (42.2) 87 (85.3) μεθοτρεξάτη 28 (27.5) 71 (69.6) κυκλοσπορίνη 5 (4.9) 43 (42.2) Σουλφασαλαζίνη 3 (2.9) 29 (28.4) Υδροξυχλωροκίνη 6 (5.9) 24 (23.5) Λεφλουνομίδη 5 (4.9) 13 (12.7) D-πενικιλλαμίνη - 10 (9.8) Άλατα χρυσού - 8 (7.8) αζαθειοπρίνη 1 (0.9) 4 (3.9) βιολογικοί παράγοντες 42 (41.2) 52 (51) inh-tnf παράγοντες 38 (37.3) 52 (51) Etanercept 19 (18.6) 31 (30.4) Adalimumab 15 (14.7) 27 (26.5) infliximab 3 (2.9) 21 (20.6) Golimumab 1 (0.9) 1 (0.9) μη-inh TNF βιολογικοί παραγ. 4 (3.9) 6 (5.9) Anakinra - 2 (1.9) Rituximab 2 (1.9) 4 (3.9) Tocilizumab 2 (1.9) 2 (1.9) 199
200 200 Σχήμα 25. Συχνότητα ασθενών με Νεανική Ιδιοπαθή Αρθρίτιδα που λάμβανε το κάθε φάρμακο στην τελευταία επίσκεψη παρακολούθησης και κατά τη συνολική διάρκεια παρακολούθησης. μονοθεραπεία έπαιρναν οι 35 ασθενείς (34.3% του συνόλου των ασθενών κα 52.2% των ασθενών που έπαιρναν κάποια αγωγή). Oι 17 έπαιρναν μονοθεραπεία με μη-βιολογικό DMARD±μΣαφ± κορτικοστεροειδή και οι 18 έπαιρναν μονοθεραπεία με βιολογικό παράγοντα±μσαφ± κορτικοστεροειδή. μεθοτρεξάτη ±μσαφ± κορτικοστεροειδή χορηγούνταν σε 9 από τους 17 ασθενείς και στους υπόλοιπους 8 χορηγούνταν άλλο, πλην της μεθοτρεξάτης, μη βιολογικό DMARD (λεφλουνομίδη σε 3 ασθενείς, υδροξυχλωροκίνη σε 3 ασθενείς και σουλφασαλαζίνη σε 2 ασθενείς). από τους 18 ασθενείς που έπαιρναν μονοθεραπεία με βιολογικό παράγοντα, οι 16 έπαιρναν inh-tnf και οι 2 rituximab ή tocilizumab. Συνδυασμένη θεραπεία καταγράφηκε σε 26 ασθενείς (25.5% του συνόλου των ασθενών κα 38.9% των ασθενών που έπαιρναν κάποια αγωγή). φαρμακευτική αγωγή που περιελάμβανε συνδυασμό δύο μη βιολογικών DMARD ±μσαφ± κορτικοστεροειδή βρέθηκε να παίρνουν 2 ασθενείς (ο ένας μεθοτρεξάτη και κυκλοσπορίνη και ο άλλος κυκλοσπορίνη και υδροξυχλωροκίνη). Συνδυασμό θεραπείας με βιολογικό παράγοντα συν ένα ή δύο μη βιολογικά DMARDs ±μσαφ± κορτικοστεροειδή έπαιρναν 24 ασθενείς. Στους 22 ο βιολογικός παράγοντας ήταν inh-tnf και στους 2 rituximab ή tocilizumab. από τους 22 που έπαιρναν συνδυασμένη θεραπεία με inh-tnf και μη βιο-
201 201 λογικό DMARD, στους 16 ασθενείς, ο συνδυασμός αυτός ήταν inh-tnf και μεθοτρεξάτη. τριπλή θεραπεία με δύο DMARD και anti TNF καταγράφηκε σε 3 ασθενείς. τέλος, σε 6 ασθενείς (5.9% του συνόλου των ασθενών και 9% των ασθενών που έπαιρναν κάποια αγωγή) καταγράφηκε η λήψη θεραπείας που περιελάμβανε μόνο μσαφ± κορτικοστεροειδή (Πίνακας 69). Πίνακας 69. Σχήματα θεραπείας που χορηγούνται στους 102 ασθενείς της μελέτης στην τελευταία επίσκεψη παρακολούθησης Σχήματα θεραπείας στην τελευταία επίσκεψη παρακολούθησης Αριθμός ασθενών (%) μσαφ ±κορτικοστεροειδή 6 (5.9) μονοθεραπεία με μη-βιολογικό DMARD a 17 (16.7) μονοθεραπεία με μεθοτρεξάτη a 9 (8.8) μονοθεραπεία με inh-tnf παράγοντα a 16 (15.7) μονοθεραπεία με βιολογικό μη inh-tnf παράγοντα a 2 (1.9) Συνδυασμένη θεραπεία a 26 (25.5) Συνδυασμένη θεραπεία με DMARDS a 2 (1.9) Συνδυασμένη θεραπεία με DMARD(s)+ inh-tnf παράγοντα a 22 (21.6) Συνδυασμένη θεραπεία με DMARD(s)+ βιολογικό μη inh-tnf παράγοντα a 2 (1.9) Συνδυασμένη θεραπεία με μεθοτρεξάτη a 18 (17.6) a ±ΜΣΑΦ ± κορτικοστεροειδή 4.7 Συσχετίσεις και προγνωστικοί παράγοντες Στην ενότητα αυτή περιγράφονται οι βασικές συσχετίσεις των πεδίων έκβασης της NiA που μετρήθηκαν στην τελευταία επίσκεψη παρακολούθησης με τα αρχικά κλινικά και εργαστηριακά χαρακτηριστικά των ασθενών και διερευνώνται οι προγνωστικοί παράγοντες που προδιαθέτουν για επιθετικότερη νόσο. επίσης, αναφέρονται οι οριζόντιοι συσχετισμοί μεταξύ των πεδίων έκβασης της νόσου. Oι επτά άξονες που στηρίχτηκε η μελέτη της μακροχρόνιας έκβασης, οι τελικές δηλαδή, μεταβλητές έκβασης της νόσου που χρησιμοποιήθηκαν είναι το ποσοστό διάρκειας ενεργότητας κατά τη συνολική διάρκεια της νόσου, το μέγεθος της αρθρικής και εξωαρθρικής καταστροφής,
202 202 οι ακτινολογικές βλάβες, το επίπεδο σωματικής λειτουργικής ικανότητας, το ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας κατά τη διάρκεια της νόσου και τέλος ο βαθμός ψυχολογικής επιβάρυνσης στην τελευταία επίσκεψη παρακολούθησης. τέλος, περιγράφονται οι παράγοντες κινδύνου που βρέθηκαν ότι συνδέονται με ανάπτυξη οφθαλμικής προσβολής Συσχετίσεις του ποσοστού διάρκειας ενεργότητας κατά τη συνολική πορεία της νόσου και ειδικοί προγνωστικοί παράγοντες Όπως έχει αναφερθεί νωρίτερα, από τη μελέτη μας προέκυψε ότι οι ασθενείς διέτρεξαν κατά μέσο όρο περισσότερη από τη μισή και συγκεκριμένα, ποσοστό 52.7% της διάρκειας νόσου τους με ενεργότητα. καθώς η διάρκεια νόσου ποικίλλει σημαντικά μεταξύ των 102 ασθενών της μελέτης, κυμαινόμενη, όπως έχει περιγραφεί σε προηγούμενη ενότητα, από 5 έως 31.5 έτη, η χρησιμοποίηση της συνολικής διάρκειας που πέρασαν οι ασθενείς με ενεργότητα κατά τη διάρκεια της νόσου τους (ως αποτέλεσμα του αθροίσματος των χρονικών διαστημάτων, σε μήνες, ενεργότητας της νόσου) ως ένα από τα σκέλη που εξετάζονται κατά τη μελέτη της μακροχρόνιας έκβασης θα ήταν μια λανθασμένη προσέγγιση, οδηγώντας σε αμφίβολα συμπεράσματα. Για τον ορθότερο, λοιπόν, σχεδιασμό της μελέτης της τελικής έκβασης της νόσου, χρησιμοποιήθηκε ως εξαρτημένη μεταβλητή το ποσοστό που οι ασθενείς περνούσαν με ενεργότητα κατά τη συνολική διάρκεια της νόσου τους. δε διαπιστώθηκε σημαντική διαφορά μεταξύ των δύο φύλων όσον αφορά στο ποσοστό της διάρκειας ενεργότητας (p=0.313) (Πίνακας 70, Σχήμα 26α.). αντιθέτως, αναδείχθηκε διαφορά μεταξύ των διαφόρων υποομάδων έναρξης της νόσου (p=0.006). αναλύοντας τα αποτελέσματα, μεγαλύτερη αναλογία διάρκειας ενεργότητας στη διάρκεια της νόσου καταγράφηκε στην υπομάδα της πολυαρθρίτιδας με θετικό ρευματοειδή παράγοντα, η οποία διέφερε σημαντικά από την αντίστοιχη αναλογία που καταγράφηκε στους ασθενείς με ολιγοαρθρίτιδα εμμένουσα (p=0.005), ολιγοαρθρίτιδα επεκταθείσα (p=0.035) και αρθρίτιδα σχετιζόμενη με ενθεσίτιδα (p=0.019). Σε αντίθεση με τους ασθενείς με θετικό ρευματοειδή παράγοντα, οι ασθενείς με θετικά anti-ccp αντισώματα δε διέφεραν σημαντικά στo ποσοστό της διάρκειας νόσου τους που περνούσαν με ενεργότητα (p=0.191)(πίνακας 70, Σχήμα 26β) η ηλικία έναρξης της νόσου, επίσης, δε συνέβαλε σημαντικά στην τελική αναλογία διάρκειας ενεργότητας προς διάρκεια νόσου που καταγράφηκε (p=0.439).
203 203 μικρότερο ποσοστό διάρκειας με ενεργότητα κατά τη διάρκεια της νόσου διαπιστώθηκε στους ασθενείς που είχαν πετύχει κλινική ύφεση μέσα στα πρώτα 2 έτη (p<0.001) από την έναρξη της νόσου και είχαν λιγότερους μήνες ενεργότητας τα πρώτα 5 έτη (p<0.001). Oι ασθενείς με μικρότερο ποσοστό διάρκειας ενεργότητας είχαν πετύχει, επίσης, συχνότερα τουλάχιστον μία φορά κλινική ύφεση χωρίς φαρμακευτική αγωγή τα πρώτα 5 έτη της νόσου (p<0.001) (Πίνακας 70). το ποσοστό διάρκειας νόσου με ενεργότητα βρέθηκε μικρότερο στους ασθενείς που ζούσαν σε αστική περιοχή έναντι αυτών που είχαν μεγαλώσει σε αγροτική ή ημιαστική περιοχή (p=0.002) (Πίνακας 70, Σχήμα 26Γ) Oι ασθενείς που διένυσαν μεγαλύτερο ποσοστό της διάρκειας νόσου τους με ενεργότητα, βρέθηκαν στην τελευταία επίσκεψη παρακολούθησης να έχουν σοβαρότερο βαθμό αρθρικής και εξωαρθρικής καταστροφής (p<0.001), σύμφωνα με το JADi-α και JADi-E, περισσότερες και μεγαλύτερες ακτινολογικές βλάβες στο TmSvdhS (<0.001) και μεγαλύτερο περιορισμό της σωματικής τους λειτουργικής ικανότητας (p<0.001), σύμφωνα με την τιμή του haq-di (Πίνακας 89, Σχήματα 41 και 42). επιπλέον, οι ίδιοι ασθενείς είχαν συχνότερα ασυμμετρία γνάθου ή μικρογναθία (p<0.001), δε διέφεραν ως προς το τελικό ανάστημα, αλλά είχαν σημαντικά μικρότερο δείκτη μάζας σώματος (p=0.048). Oριακή, αλλά ωστόσο μη σημαντική, βρέθηκε η συσχέτιση του ποσοστού της διάρκειας νόσου που περνούσαν οι ασθενείς με ενεργότητα με το βαθμό ψυχολογικής επιβάρυνσης, όπως αυτή μετρήθηκε με το ερωτηματολόγιο GhQ28 στην τελευταία επίσκεψη παρακολούθησης (p=0.056) (Πίνακας 89). η διάρκεια χορήγησης κορτικοστεροειδών, η διάρκεια μονοθεραπείας με DMARDS και ο αριθμός των διαφορετικών μη βιολογικών DMARDS που είχαν συνταγογραφηθεί ήταν μεγαλύτερος, όσο μεγαλύτερο ήταν και το ποσοστό της διάρκειας ενεργότητας κατά τη διάρκεια της νόσου (p<0.001, p=0.035, p<0.001 αντίστοιχα). επιπλέον, οι ασθενείς με μεγαλύτερο ποσοστό διάρκειας ενεργότητας είχαν λάβει συχνότερα θεραπεία με inhtnfα (p=0.001) (Πίνακας 71).
204 204 Πίνακας 70. Συσχετίσεις του ποσοστού της διάρκειας ενεργότητας στην πορεία της νόσου κατά τη μονοπαραγοντική ανάλυση Ποσοστό διάρκειας ενεργότητας κατά τη διάρκεια της νόσου Μεταβλητή Μέσος t test, N όρος±sd df r p φύλο Άρρεν ± θήλυ ± ηλικία έναρξης της νόσου τίτλος RF αρνητικός ±27.0 θετικός ±17.5 τίτλος Anti-CCP αρνητικός ± θετικός ± τίτλος ανα αρνητικός ± θετικός ± ιριδοκυκλίτιδα όχι ± ναι ± < διαμονή αγροτική/ ± /ημιαστική 96 διάρκεια ενεργότητας <0.001 τα πρώτα 5 έτη 1 επεισόδιο κλινικής ύφεσης χωρίς φαρμα- όχι ± κευτική αγωγή τα ναι ± <0.001 πρώτα 5 έτη επίτευξη όχι ± κλινικής ύφεσης - <0.001 τα πρώτα 2 έτη ναι ±
205 205 Σχήμα 26. Συσχετίσεις του ποσοστού της διάρκειας ενεργότητας στην πορεία της νόσου με Α.το φύλο Β. την παρουσία ρευματοειδούς παράγοντα (RF) και Γ. τη διαμονή.
206 206 Πίνακας 71. Συσχετίσεις του ποσοστού της διάρκειας ενεργότητας στην πορεία της νόσου με μεταβλητές που αφορούν στη θεραπεία, κατά τη μονοπαραγοντική ανάλυση Ποσοστό διάρκειας ενεργότητας κατά τη διάρκεια της νόσου Μέσος t test, Μεταβλητή N όρος±sd df r p διάρκεια θεραπείας με κορτικοστεροειδή <0.001 διάρκεια μονοθεραπείας με μεθοτρεξάτη διάρκεια μονοθεραπείας με DMARDS διάρκεια συνδυασμένης θεραπείας διάρκεια συνδυασμένης θεραπείας με inh-tnfα διάρκεια συνδυασμένης θεραπείας με μη-βιολογικά DMARDS αριθμός διαφορετικών μη βιολογικών DMARDS που έχουν χορηγηθεί <0.001 αριθμός διαφορετικών inh-tnfα που έχουν χορηγηθεί ιστορικό θεραπείας ναι ± με inh-tnfα όχι ±30.2 Παράγοντες κινδύνου για περισσότερο επίμονη ενεργότητα, με μεγαλύτερο ποσοστό ενεργότητας κατά τη διάρκεια της νόσου, βρέθηκαν, στην πολυπαραγοντική ανάλυση, η πολυαρθρίτιδα (RF αρνητική και RF θετική) κατά την έναρξη β= %Ci (0.086, 0.312) p=0.001 και η μεγαλύτερη διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου β= %Ci (0.004, 0.011) p<0.001 (Πίνακας 72). από το μοντέλο εξαιρέθηκαν οι ασθενείς με ψωριασική, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και αταξινόμητη αρθρίτιδα, λόγω της ετερογένειας της κάθε παραπάνω υποομάδας σε σύγκριση με τις υπόλοιπες.
207 207 Πίνακας 72. Προγνωστικοί παράγοντες επίμονης ενεργότητας νόσου Πολυπαραγοντικό μοντέλο γραμμικής παλινδρόμησης για τη σχέση μεταξύ μεταβλητών κατά την έναρξη και ποσοστού διάρκειας νόσου με ενεργότητα Εξαρτημένη μεταβλητή έκβασης Ποσοστό διάρκειας με ενεργότητα κατά τη διάρκεια της νόσου Ν 71 Ανεξάρτητες μεταβλητές που εισήχθησαν στο μοντέλο Β (95% CI) p intercept (0.055, 0.326) Συστηματικού τύπου έναρξης νόσος (-0.087, 0.224) Πολυαρθρικού τύπου έναρξης (RF- και RF+) νόσος (0.086, 0.312) Oλιγοαρθρικού τύπου έναρξης νόσος Oμάδα αναφοράς RF θετικός (-0.056, 0.275) RF αρνητικός Oμάδα αναφοράς διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου (0.004, 0.011) <0.001 αποτυχία κλινικής ύφεσης τα πρώτα 2 έτη από τη διάγνωση (-0.019, 0.242) επιτυχία κλινικής ύφεσης τα πρώτα 2 έτη από τη διάγνωση Oμάδα αναφοράς
208 Συσχετίσεις του ποσοστού διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή κατά τη συνολική πορεία της νόσου και ειδικοί προγνωστικοί παράγοντες το ποσοστό της διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή κατά τη διάρκεια της νόσου ήταν μεγαλύτερο στους άρρενες (p=0.040) και στους ασθενείς με ολιγοαρθρίτιδα εμμένουσα συγκριτικά με τους ασθενείς με πολυαρθρίτιδα RF θετική (p=0.002) και πολυαρθρίτιδα RFαρνητική (p=0.003). Oι ασθενείς με μικρότερο ποσοστό διάρκειας κλινικής ύφεσης χωρίς φάρμακα είχαν επιδείξει μακρύτερα διαστήματα ενεργότητας νόσου τα πρώτα 5 έτη (p=0.002) και είχαν συχνότερα προσβολή του ισχίου (p=0.001) (Πίνακας 73, Σχήμα 27). το μακρύτερο διάστημα κλινικής ύφεσης εκτός θεραπείας στη διάρκεια της νόσου συσχετίστηκε σημαντικά με μικρότερο JADi-A (p=0.008), JADi- E(p<0.001), TmSvdhS (p=0.002) και haq-di (p=0.018) στην τελευταία επίσκεψη παρακολούθησης (Πίνακας 89, Σχήματα 46-48). επιπλέον, οι ίδιοι ασθενείς εμφάνιζαν σπανιότερα τοπικές διαταραχές ανάπτυξης της γνάθου (p=0.001). Oριακά μη σημαντική ήταν η συσχέτιση της διάρκειας κλινικής ύφεσης εκτός θεραπείας με το τελικό GhQ28 σκορ (p=0.056) (Πίνακας 73).
209 Πίνακας 73. Συσχετίσεις του ποσοστού της διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στην πορεία της νόσου κατά τη μονοπαραγοντική ανάλυση Ποσοστό διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή κατά τη διάρκεια της νόσου Μεταβλητή Μέσος t test, N όρος±sd df r p φύλο Άρρεν ± θήλυ ± ηλικία έναρξης της νόσου τίτλος RF αρνητικός ± <0.001 θετικός ± τίτλος Anti-CCP αρνητικός ± θετικός ± τίτλος ανα αρνητικός ± θετικός ± ιριδοκυκλίτιδα όχι ± ναι ± Προσβολή του όχι ± ισχίου ναι ± διάρκεια ενεργότητας τα πρώτα 5 έτη (μήνες) 209 Στην πολυπαραγοντική ανάλυση, σημαντικότεροι παράγοντες κινδύνου για μικρότερο ποσοστό διάρκειας νόσου σε κλινική ύφεση εκτός θεραπείας βρέθηκε η πολυαρθρικού τύπου έναρξης νόσος β= %Ci ( , ) p=0.004 και η μεγαλύτερη διάρκειας ενεργότητας τα πρώτα 5 έτη β= %Ci (-1.048, ) p=0.001 (Πίνακας 74). από το μοντέλο εξαιρέθηκαν και πάλι οι ασθενείς με ψωριασική, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και αταξινόμητη αρθρίτιδα, λόγω της ετερογένειας της κάθε παραπάνω υποομάδας σε σύγκριση με τις υπόλοιπες.
210 210 Πίνακας 74. Προγνωστικοί παράγοντες μικρότερης διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στην πορεία της νόσου Πολυπαραγοντικό μοντέλο γραμμικής παλινδρόμησης για τη σχέση μεταξύ μεταβλητών κατά την έναρξη και ποσοστού διάρκειας νόσου σε κλινική ύφεση χωρίς φαρμακευτική αγωγή. Εξαρτημένη μεταβλητή έκβασης Ποσοστό διάρκειας νόσου σε κλινική ύφεση χωρίς φαρμακευτική αγωγή Ν 71 Ανεξάρτητες μεταβλητές που εισήχθησαν στο μοντέλο Β (95% CI) p intercept (0.055, 0.326) θήλυ φύλο ( , ) Άρρεν φύλο Oμάδα αναφοράς Συστηματικού τύπου έναρξης νόσος ( , ) Πολυαρθρικού τύπου έναρξης (RF- και RF+) νόσος ( , ) Oλιγοαρθρικού τύπου έναρξης νόσος Oμάδα αναφοράς RF θετικός ( , ) RF αρνητικός Oμάδα αναφοράς διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου (-1.048, ) 0.001
211 211 Σχήμα 27. Συσχέτιση του ποσοστού διάρκειας κλινικής ύφεσης εκτός θεραπείας με Α. το φύλο Β. το ιστορικό προσβολής του ισχίου και Γ. την παρουσία ρευματοειδούς παράγοντα.
212 212 Oι ασθενείς που πέτυχαν κλινική ύφεση χωρίς φαρμακευτική αγωγή, έστω μία φορά κατά την συνολική πορεία της νόσου τους, δε διέφεραν από αυτούς που δεν πέτυχαν την παραπάνω κατάσταση, όσον αφορά στο φύλο (Pearson Chi-Square Value=2.628, df=1, p=0.105), στην ηλικία έναρξης της νόσου (t test =-0.140, df=96, p=0.890), στην παρουσία θετικού τίτλου anti- CCP αντισωμάτων (Pearson Chi-Square Value=0.002, df=1, p=0.962), θετικού τίτλου ανα (Pearson Chi-Square Value=0.184, df=1, p=0.668), ιστορικού εμφάνισης ιερολαγονίτιδας (Pearson Chi-Square Value=0.186, df=1, p=0.666) και ιριδοκυκλίτιδας (Pearson Chi-Square Value=0.052, df=1, p=0.819). αντίθετα, οι ασθενείς που δεν πέτυχαν ποτέ κλινική ύφεση χωρίς φάρμακα ανήκαν συχνότερα στην υποομάδα της οροθετικής πολυαρθρίτιδας (Pearson Chi-Square Value=19.048, df=7, p=0.008). Συγκεκριμένα, κανείς από τους 11 ασθενείς με πολυαρθρίτιδα RF θετική δεν πέτυχε κλινική ύφεση χωρίς φαρμακευτική αγωγή στην πορεία της νόσου. επίσης, οι ασθενείς που δεν πέτυχαν κλινική ύφεση χωρίς φάρμακα είχαν συχνότερα τοπικές διαταραχές ανάπτυξης της γνάθου (Pearson Chi-Square Value=6.933, df=1, p=0.008), ιστορικό προσβολής της άρθρωσης του ισχίου (Pearson Chi-Square Value=6.557, df=1, p=0.010) και υψηλότερο βαθμό αρθρικής (p=0.009), εξωαρθρικής καταστροφής (p=0.019) και ακτινολογικής βλάβης (p=0.003). τέλος, οι ίδιοι ασθενείς παρουσίαζαν μακρύτερη διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου (t test =3.103, df=96, p=0.003) Συσχετίσεις του τελικού βαθμού αρθρικής καταστροφής (JADI-A) και ειδικοί προγνωστικοί παράγοντες το μέγεθος της αρθρικής καταστροφής, σύμφωνα με το δείκτη JADi- A, βρέθηκε υψηλότερο στις γυναίκες σε σύγκριση με τους άνδρες, σε στατιστικώς σημαμαντικό επίπεδο (p=0.023) (Πίνακας 75, Σχήμα 28). Υψηλότερη τιμή του JADi-A παρατηρήθηκε στους ασθενείς με πολυαρθρίτιδα RF θετική, η οποία όμως διέφερε στατιστικώς σημαντικά μόνο από την αντίστοιχη τιμή των ασθενών με ολιγοαρθρίτιδα εμμένουσα (p=0.012) και αυτών με αρθρίτιδα που σχετίζεται με ενθεσίτιδα (p=0.022). Oι ασθενείς με υψηλότερο δείκτη JADi-A βρέθηκε ότι είχαν μακρύτερη διάρκεια νόσου (p=0.021), ενώ εφαρμόζοντας T-test εμφάνιζαν, όπως ήταν αναμενόμενο, συχνότερα πολυαρθρική πορεία (p<0.001) καθώς και συχνότερη προσβολή της άρθρωσης του ισχίου (p<0.001). Oι ασθενείς με οφθαλμική προσβολή εμφάνιζαν χαμηλότερη τιμή του δείκτη JADi-A σε σύγκριση με αυτούς χωρίς οφθαλμική προσβολή, σε επίπεδο στατιστικής σημαντικό-
213 213 τητας (p=0.041). Oι ασθενείς που διέμεναν το μεγαλύτερο χρονικό διάστημα της ζωής τους είτε σε αστική, είτε σε ημιαστική, είτε σε αγροτική περιοχή δε διέφεραν σημαντικά μεταξύ τους, ως προς το τελικό επίπεδο αρθρικής καταστροφής. Όσο μεγαλύτερη ήταν η διάρκεια ενεργότητας της νόσου τα πρώτα 5 έτη από τη διάγνωση, τόσο μεγαλύτερη ήταν και η αρθρική καταστροφή που καταγράφηκε με το JADi-A στην τελευταία επίσκεψη παρακολούθησης (p<0.001). Σημαντική, επίσης, είναι η παρατήρηση ότι οι ασθενείς που πέτυχαν έστω μία φορά κλινική ύφεση χωρίς φαρμακευτική αγωγή τα πρώτα 5 έτη της νόσου, είχαν μικρότερο βαθμό αρθρικής καταστροφής, σύμφωνα με το δείκτη JADi-A (p=0.006). αντιθέτως, οι ασθενείς που πέτυχαν έστω μία φορά κλινική ύφεση τα πρώτα 5 έτη της νόσου,ανεξάρτητα αν έπαιρναν ή όχι φαρμακευτική αγωγή, είχαν μεν χαμηλότερο JADi-A συγκριτικά με τους υπόλοιπους, αλλά σε μη σημαντικό επίπεδο (p=0.126). Περισσότερο αναμενόμενο είναι το χειρότερο αποτέλεσμα σε επίπεδο αρθρικής καταστροφής στους ασθενείς που είχαν συνολικά μακρύτερη διάρκεια ενεργότητας της νόσου (p<0.001). το υψηλότερο ποσοστό ενεργότητας παρουσιάζει, επίσης, ισχυρή θετική συσχέτιση και στατιστικώς σημαντική με την τιμή του JADi-A (r= 0.537, p<0.001). Όπως σημειώθηκε και προηγουμένως, οι ασθενείς που πέτυχαν έστω μία φορά κατάσταση κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στη συνολική διάρκεια της νόσου, εμφάνιζαν καλύτερο JADi-A, σε σύγκριση με αυτούς στους οποίους δεν επιτεύχθηκε ποτέ παρόμοια κατάσταση (p=0.009). επιπλέον, όσο μεγαλύτερος ήταν ο αριθμός των επεισοδίων κλινικής ύφεσης χωρίς φαρμακευτική αγωγή που επιτεύχθηκε, τόσο χαμηλότερη ήταν και η προκύπτουσα τιμή του JADi-A (p=0.014). Παράλληλα, η επίτευξη κλινικής ύφεσης έστω μία φορά κατά τη διάρκεια της νόσου, ασχέτως της λήψης ή όχι φαρμακευτικής αγωγής, συσχετίστηκε με καλύτερη τιμή του δείκτη JADi-A, αλλά σε μη σημαντικό επίπεδο (p=0.181) (Πίνακας 75).. η ποσοτική κλινική εκτίμηση των αρθρικών βλαβών, όπως αυτή αντικατροπτίζεται στο δείκτη JADi-A, παρουσίαζε πολύ ισχυρή θετική συσχέτιση (r=0.894) και στατιστικώς σημαντική (p<0.001) με την έκταση των ακτινολογικών αλλοιώσεων στις άκρες χείρες, στον καρπό και στους άκρους πόδες, σύμφωνα με το TmSvdhS. επιπλέον, πολύ ισχυρή θετική συσχέτιση και στατιστικώς σημαντική (p<0.001) παρατηρήθηκε ανάμεσα στο δείκτη JADi-A και στα επιμέρους σκορ του τροποποιημένου Sharp/Van der heijde που αφορούν στα άνω άκρα, στα κάτω άκρα, στις διαβρώσεις και στη στένωση του μεσάρθριου διαστήματος. Όσο μεγαλύτερος ήταν ο βαθμός της αρθρικής
214 214 βλάβης, τόσο μεγαλύτερος ήταν και ο περιορισμός της σωματικής λειτουργικής ικανότητας, όπως υποδηλώνεται από την ανεύρεση ισχυρής θετικής συσχέτισης (r=0.536) και στατιστικώς σημαντικής (p<0.001) του δείκτη JA- Di-A με την τιμή του δείκτη haq-di (Πίνακας 89, Σχήματα 43,45,47). Oι ασθενείς με τοπικές διαταραχές ανάπτυξης της γνάθου (μικρογναθία ή ασυμμετρία γνάθου) στην τελευταία επίσκεψη εμφάνιζαν υψηλότερη τιμή του δείκτη JADi-A, σε στατιστικά σημαντικό επίπεδο (p<0.001). επιπλέον, οι ασθενείς με υψηλότερο JADi-A είχαν χαμηλότερο ανάστημα (p=0.027). O αριθμός των χειρουργικών επεμβάσεων στις αρθρώσεις κατά τη διάρκεια της νόσου, επίσης, παρουσίαζε μέτρια θετική συσχέτιση (r=0.490) και στατιστικώς σημαντική (p<0.001) με την τιμή του JADi-A (Πίνακας 75). τέλος, η τιμή του JADi-A δε βρέθηκε να διαφέρει στατιστικώς σημαντικά ανάμεσα στους ασθενείς που ήταν άγαμοι ή έγγαμοι καθώς και ανάμεσα σε αυτούς με χαμηλότερο ή υψηλότερο μορφωτικό επίπεδο. αντιθέτως, σημαντικά υψηλότερη βρέθηκε η τιμή του μεταξύ των ασθενών που ήταν άνεργοι (p=0.010), δεδομένο που χρήζει περαιτέρω διερεύνησης σε επίπεδο πλέον επάρκειας κοινωνικών δομών. η διάρκεια θεραπείας με κορτικοστεροειδή, η διάρκεια μονοθεραπείας με μεθοτρεξάτη, η διάρκεια μονοθεραπείας με DMARD συσχετίστηκαν θετικά με την τιμή του JADi-A, σε στατιστικώς σημαντικό επίπεδο p<0.001, p=0.002, p<0.001 αντιστοίχως. επιπλέον, οι ασθενείς στους οποίους χορηγήθηκε κατά τη διάρκεια της νόσου μεγαλύτερος αριθμός διαφορετικών μη βιολογικών DMARDS παρουσίαζαν υψηλότερο JADi-A σε στατιστικώς σημαντικό επίπεδο p<0.001 (Πίνακας 76, Σχήμα 29).
215 Πίνακας 75. Συσχετίσεις του τελικού βαθμού αρθρικής καταστροφής (JADI-A) στην μονοπαραγοντική ανάλυση JADI-A Μεταβλητή Μέσος t test, N όρος±sd df r p φύλο Άρρεν ± θήλυ ± διάρκεια νόσου ηλικία έναρξης της νόσου RF θετικός ± αρνητικός ± ιριδοκυκλίτιδα ναι ± όχι ± Συνολική διάρκεια ενεργότητας ενεργότητας της νόσου διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου < <0.001 επίτευξη κλινικής ναι ± ύφεσης στα πρώτα 2 έτη όχι ± από την έναρξη της νόσου 1 επεισόδιο κλινικής ύφεσης χωρίς φαρμακευτική όχι ± αγωγή τα πρώτα 5 έτη ναι ± της νόσου < Σχήμα 28. Συσχέτιση του τελικού βαθμού αρθρικής καταστροφής (JADI-A) με το φύλο.
216 216 Πίνακας 76. Συσχετίσεις του τελικού βαθμού αρθρικής καταστροφής ( JADI-A) με τη διάρκεια καθενός από τα σχήματα θεραπείας κατά την πορεία της νόσου, στην μονοπαραγοντική ανάλυση JADI-A Μεταβλητή r p διάρκεια θεραπείας με κορτικοστεροειδή <0.001 διάρκεια μονοθεραπείας με μεθοτρεξάτη διάρκεια μονοθεραπείας με DMARDS <0.001 διάρκεια συνδυασμένης θεραπείας διάρκεια συνδυασμένης θεραπείας με inh-tnf a διάρκεια συνδυασμένης θεραπείας με μη-βιολογικά DMARDS αριθμός διαφορετικών μη βιολογικών DMARDS που έχουν χορηγηθεί <0.001 αριθμός διαφορετικών inh-tnfa που έχουν χορηγηθεί ιστορικό θεραπείας ναι ± με ihn-tnfα όχι ±
217 217 Σχήμα 29. Συσχέτιση του τελικού βαθμού αρθρικής καταστροφής (JADI-A) με Α. τη διάρκεια θεραπείας με κορτικοστεροειδή και Β. με τη διάρκεια μονοθεραπείας με μη βιολογικά DMARDs
218 218 Στην πολυπαραγοντική ανάλυση, στο μοντέλο γραμμικής παλινδρόμησης διαπιστώθηκε ότι παράγοντες κινδύνου για υψηλότερο βαθμό αρθρικής καταστροφής, βάσει του εργαλείου JADi-A ήταν το θήλυ φύλο β= %Ci (1.224,18.107) p=0.025, η υποομάδα της συστηματικού τύπου έναρξης B= %Ci (8.044, ) p<0.001, η υποομάδα της πολυαρθρικής έναρξης β= % Ci (2.703, ) p=0.007, η μεγαλύτερη συνολική διάρκεια ενεργότητας β= %Ci (0.025, 0.114) p=0.002 και τέλος η μακρύτερη διάρκεια χορήγησης μονοθεραπείας με DMARDS B= %Ci (0.034, 0.094) p<0.001( Πίνακας 77). από το μοντέλο εξαιρέθηκαν και πάλι οι ασθενείς με ψωριασική, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και αταξινόμητη αρθρίτιδα, λόγω της ετερογένειας της κάθε παραπάνω υποομάδας σε σύγκριση με τις υπόλοιπες.
219 219 Πίνακας 77. Προγνωστικοί παράγοντες κίνδύνου μεγαλύτερου βαθμού αρθρικής καταστροφής (JADI-A) Πολυπαραγοντικό μοντέλο γραμμικής παλινδρόμησης για τη σχέση μεταξύ μεταβλητών κατά την έναρξη της νόσου και βαθμού αρθρικής καταστροφής Εξαρτημένη μεταβλητή έκβασης JADI-A Ν 71 Μεταβλητές που εισήχθησαν στο μοντέλο Β (95% CI) p intercept ( , ) θήλυ φύλο (1.224,18.107) Άρρεν φύλο Oμάδα αναφοράς Συστηματικού τύπου έναρξης νόσος (8.044, ) <0.001 Πολυαρθρικού τύπου έναρξης (RF- και RF+) νόσος (2.703, ) Oλιγοαρθρικού τύπου έναρξης νόσος Oμάδα αναφοράς ηλικία έναρξης της νόσου (-0.589, 1.288) RF θετικός ( , 9.821) RF αρνητικός Oμάδα αναφοράς διάρκεια ενεργότητας νόσου (0.025, 0.114) διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου (-0.066, 0.390) αποτυχία κλινικής ύφεσης τα πρώτα 2 έτη από τη διάγνωση ( , 3.986) επιτυχία κλινικής ύφεσης τα πρώτα 2 έτη από τη διάγνωση Oμάδα αναφοράς διάρκεια μονοθεραπείας με μη βιολογικά DMARDS (0.034, 0.094) <0.001
220 Συσχετίσεις του τελικού βαθμού εξωαρθρικής καταστροφής (JADI-E) O βαθμός εξωαρθρικής καταστροφής, όπως αυτός μετρήθηκε με το εργαλείο JADi-E, βρέθηκε υψηλότερος στις γυναίκες συγκριτικά με τους άνδρες σε στατιστικώς σημαντικό επίπεδο p=0.012, ενώ η τιμή του δε συσχετίστηκε σημαντικά με κάποια από τις υποομάδες της νόσου (p=0.688). αντιθέτως, οι ασθενείς με υψηλότερη τιμή JADi-E είχαν μικρότερη ηλικία έναρξης της νόσου (p<0.001) και μακρύτερη διάρκεια νόσου (p=0.009). Σημαντικό, όμως, είναι το γεγονός ότι όσο μεγαλύτερη ήταν η διάρκεια ενεργότητας (r=0.519, p<0.001) και όσο μεγαλύτερο ήταν το ποσοστό ενεργού νόσου κατά τη διάρκεια της νόσου ενός ασθενή, τόσο μεγαλύτερο ήταν και το μέγεθος της εξωαρθρικής καταστροφής που παρατηρήθηκε (r=0.360, p<0.001). το ίδιο διαπιστώθηκε και για τους ασθενείς που δε πέτυχαν ποτέ κλινική ύφεση χωρίς φαρμακευτική αγωγή κατά τη διάρκεια της νόσου τους (p=0.019). επιπλέον, εξίσου σημαντική είναι η διαπίστωση ότι όσο μεγαλύτερη ήταν η διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου, τόσο βαρύτερη ήταν και η εξωαρθρική βλάβη στην τελευταία επίσκεψη παρακολούθησης (p=0.003). κατά αντιστοιχία με προηγούμενη παρατήρηση, οι ασθενείς που δεν πέτυχαν κλινική ύφεση χωρίς φαρμακευτική αγωγή τα πρώτα 5 έτη της νόσου, είχαν και μεγαλύτερο βαθμό εξωαρθρικής καταστροφής (p=0.031) (Πίνακας 78, Σχήματα 30 και 31). η τιμή του JADi-E συσχετίστηκε θετικά με την τιμή του JADi-A (p<0.001) και του συνολικού τροποποιημένου TmSvdhS (p<0.001), γεγονός που υποδηλώνει ότι ο βαθμός της εξωαρθρικής βλάβης ήταν μεγαλύτερος στους ασθενείς με εκτενέστερη αρθρική καταστροφή, τόσο σε κλινικό όσο και σε απεικονιστικό επίπεδο. Σημαντικότερος βρέθηκε, επίσης, ο περιορισμός της σωματικής λειτουργικής ικανότητας των ασθενών αυτών, καθώς η τιμή του δείκτη haq-di ήταν υψηλότερη στους ασθενείς με μεγαλύτερη εξωαρθρική βλάβη, σε στατιστικώς σημαντικό επίπεδο (p<0.001) (Πίνακας 89). επιπλέον, όσο υψηλότερη ήταν η τιμή του JADi-E τόσο χαμηλότερο ήταν το τελικό ύψος (p=0.034) και τόσο μικρότερος ήταν ο δείκτης μάζας σώματος (p=0.022). τέλος, το μακρύτερο διάστημα θεραπείας με κορτικοειδή καθώς και μονοθεραπείας με μη βιολογικό DMARD συχετίστηκε θετικά με χειρότερη τιμή του JADi-E, σε επίπεδο στατιστικής σημαντικότητας p=0.001 και p=0.039 αντίστοιχα. Υψηλότερο JADi-E εμφάνιζαν και οι ασθενείς που είχαν αλλάξει περισσότερα διαφορετικά μη βιολογικά DMARDS (p=0.004) και περισσότερους inhtnfα (p=0.005) (Πίνακας 79).
221 Πίνακας 78. Συσχετίσεις του βαθμού εξωαρθρικής καταστροφής ( JADI-Ε) κατά την τελευταία επίσκεψη στην μονοπαραγοντική ανάλυση JADI-E Μεταβλητή Μέσος t test, N όρος±sd df r p φύλο Άρρεν ± θήλυ ± διάρκεια νόσου <0.001 ηλικία έναρξης της νόσου <0.001 RF θετικός ± αρνητικός ± Συνολική διάρκεια ενεργότητας νόσου <0.001 διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου επεισόδιο κλινικής ύφεσης χωρίς φαρμακευτική όχι ± αγωγή τα πρώτα 5 έτη ναι ± της νόσου
222 222 Σχήμα 30. Συσχέτιση του βαθμού εξωαρθρικής καταστροφής με Α. το φύλο και B.
223 Πίνακας 79. Συσχετίσεις του τελικού βαθμού εξωαρθρικής καταστροφής ( JADI-Ε) με τη διάρκεια καθενός από τα σχήματα θεραπείας στην μονοπαραγοντική ανάλυση JADI-E Μεταβλητή Μέσος t test, N όρος±sd df r p διάρκεια θεραπείας με κορτικοστεροειδή διάρκεια μονοθεραπείας με DMARDS διάρκεια μονοθεραπείας με μεθοτρεξάτη διάρκεια συνδυασμένης θεραπείας διάρκεια συνδυασμένης θεραπείας με inh-tnfα διάρκεια συνδυασμένης θεραπείας με μη-βιολο γικά DMARDS αριθμός διαφορετικών μη βιολογικών DMARDS που έχουν χορηγηθεί αριθμός διαφορετικών inh-tnfα που έχουν χορηγηθεί ιστορικό θεραπείας με ναι ± inh-tnfα όχι ±
224 224 Σχήμα 31. Συσχέτιση του τελικού βαθμού εξωαρθρικής καταστροφής (JADI-E)με τη διάρκεια θεραπείας με κορτικοστεροειδή Συσχετίσεις του τελικού βαθμού ακτινολογικής βλάβης (Συνολικό τροποποιημένο Sharp van der Heijde σκορ, TmSvdHS) και ειδικοί προγνωστικοί παράγοντες O βαθμός των ακτινολογικών αλλοιώσεων, όπως ορίστηκε με το TmSvdhS, βρέθηκε ότι διέφερε μεταξύ των δύο φύλων, με τις γυναίκες να εμφανίζουν σοβαρότερες ακτινολογικές βλάβες συγκριτικά με τους άνδρες σε στατιστικώς σημαντικό επίπεδο (p=0.001). μεγαλύτερο TmSvdhS διαπιστώθηκε στους ασθενείς με πολυαρθρίτιδα RF θετική, το οποίο όμως, διέφερε σημαντικά μόνο από το αντίστοιχο σκορ των ασθενών με ολιγοαρθρίτιδα εμμένουσα και αρθρίτιδα που σχετίζεται με ενθεσίτιδα (p<0.001). δεύτερη στη σειρά ομάδα ασθενών που παρουσίαζε υψηλότερο TmSvdhS ήταν αυτοί που ανήκαν στην υποομάδα της πολυαρθρίτιδας με αρνητικό RF. και σε αυτήν, όμως, την περίπτωση η τιμή του διέφερε στατιστικώς σημαντικά μόνο από το αντίστοιχο των ασθενών με ολιγοαρθρίτιδα εμμένουσα (p=0.003) και αρθρίτιδα που σχετίζεται με ενθεσίτιδα (p=0.015). τέλος, τρίτο μεγαλύτερο σκορ παρατηρήθηκε στους ασθενείς με συστηματική μορφή, το οποίο διέφερε σημαντικά μόνο από αυτό των ασθενών με ολιγοαρθρίτιδα εμμένουσα (p=0.028). το συνολικό Svdh σκορ, ενώ βρέθηκε υψηλότερο στους ασθενείς με θετικό RF (p=0.003), ωστόσο η τιμή του δε διέφερε σημαντικά μεταξύ των ασθενών που είχαν θετικά ή αρνητικά anti-ccp αντισώματα (p=0.632). κάποιες διαφορές εντοπίστηκαν μεταξύ των επιμέρους σκορ του τρο-
225 225 ποποιημένου TmSvdhS και των υποομάδων της νόσου. Συγκεκριμένα, το TmSvdhS που αφορά στα άνω άκρα βρέθηκε, επίσης, υψηλότερο στους ασθενείς με πολυαρθρίτιδα RF θετική, το οποίο, όμως επιπλέον, διέφερε σημαντικά, εκτός από το αντίστοιχο των ασθενών με ολιγοαρθρίτιδα εμμένουσα και αρθρίτιδα που σχετίζεται με ενθεσίτιδα, και από αυτό των ασθενών με ολιγοαρθρίτιδα επεκταθείσα (p=0.027). απεναντίας, το TmSvdhS που αφορά στα κάτω άκρα βρέθηκε ότι διαφέρει σημαντικά μόνο μεταξύ ολιγοαρθρίτιδας εμμένουσας και πολυαρθρίτιδας RF θετικής (p=0.014) και RF αρνητικής (p=0.026). Στο επιμέρους msvdhs που αφορά στη στένωση του μεσάρθριου διαστήματος msvdhs-jsn διαπιστώθηκε, πέρα των συσχετίσεων που περιγράφηκαν για το συνολικο TmSvdhS, επιπλέον, σημαντική διαφορά μεταξύ ολιγοαρθρίτιδας επεκταθείσας και ολιγοαρθρίτιδας εμμένουσας (p=0.034). τέλος, για το msvdhs που αφορά στις διαβρώσεις (msvdhs-e) διαπιστώθηκαν μεταξύ των υποομάδων οι ίδιοι συσχετισμοί σε σημαντικό επίπεδο με αυτούς του TmSvdhS. Oι ασθενείς με υψηλότερο TmSvdhS, δηλαδή αυτοί με τις περισσότερες και μεγαλύτερες ακτινολογικές βλάβες, είχαν μακρύτερη διάρκεια νόσου (p=0.019). αξίζει, ωστόσο, να σημειωθεί ότι μόνο το επιμέρους msvdhs που αφορούσε στο καρπό και στις άκρες χείρες (msvdhs-handswrists) δεν παρουσίαζε σημαντική συσχέτιση με τη διάρκεια της νόσου. επίσης, σημαντικό είναι να αναφερθεί ότι το συνολικό Svdh score και τα επιμέρους Svdh score που αφορούσαν στο καρπό και στις άκρες χείρες (msvdh-handswrists) και στη στένωση του μεσάρθριου διαστήματος (msvdh-jsn) παρουσίαζαν χαμηλή μεν, αρνητική συσχέτιση, αλλά στατιστικώς σημαντική με την ηλικία έναρξης της νόσου. αυτό σημαίνει ότι οι ασθενείς με μικρότερη ηλικία κατά την έναρξη της νόσου εμφάνιζαν περισσότερες βλάβες στον καρπό και στις άκρες χείρες (r=-0.212, p=0.033) καθώς και σημαντικότερη στένωση του μεσάρθριου διαστήματος (r=-0.202, p=0.041). Tο TmSvdhS βρέθηκε υψηλότερο, όπως ήταν αναμενόμενο, στους ασθενείς με πολυαρθρική πορεία (p<0.001). επιπλέον, το TmSvdhS ήταν σημαντικά μεγαλύτερο στους ασθενείς με προσβολή της άρθρωσης του ισχίου (p<0.001). Σε αντίθεση με το JADi-A, δεν παρατηρήθηκε σημαντική διαφορά τόσο στο συνολικό, όσο και στα επιμέρους ακτινολογικά σκορ του msvdhs, μεταξύ των ασθενών με και χωρίς οφθαλμική προσβολή. επίσης, δεν παρατηρήθηκε διαφορά τόσο στο TmSvdhS, όσο και στα επιμέρους ακτινολογικά σκορ του msvdhs, μεταξύ των ασθενών με ιερολαγονίτιδα και χωρίς ιερολαγονίτιδα. Όπως περιγράφηκε και στην ενότητα της αρθρικής καταστροφής που μετρήθηκε με το JADi-A, έτσι και εδώ, ο βαθμός των ακτινολογικών βλαβών στην
226 226 τελευταία επίσκεψη παρακολούθησης, σύμφωνα με το TmSvdh score, βρέθηκε μεγαλύτερος στους ασθενείς που είχαν μεγαλύτερη διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου (p<0.001) και δεν πέτυχαν ούτε μία φορά κλινική ύφεση χωρίς φαρμακευτική αγωγή κατά το ίδιο χρονικό διάστημα (p=0.001). η επίμονη ενεργότητα νόσου οδήγησε σε σοβαρότερες ακτινολογικές αλλοιώσεις, αφού διαπιστώθηκε ότι τόσο το συνολικό όσο και τα επιμέρους msvdhs παρουσίασαν ισχυρή θετική συσχέτιση και στατιστικώς σημαντική (p<0.001) με τη συνολική διάρκεια ενεργότητας. Oι ασθενείς με υψηλότερο ποσοστό διάρκειας ενεργότητας στη διάρκεια της νόσου είχαν και υψηλότερο TmSvdhS (Πίνακας 89, Σχήμα 41). επιπλέον, οι ασθενείς που πέτυχαν έστω μία φορά κλινική ύφεση χωρίς φαρμακευτική αγωγή, εμφάνιζαν λιγότερες ακτινολογικές βλάβες συγκριτικά με αυτούς που δεν πέτυχαν την παραπάνω κατάσταση ποτέ στη διάρκεια της νόσου (p=0.003). επιπρόσθετα, όσο μεγαλύτερος ήταν ο αριθμός των επεισοδίων κλινικής ύφεσης χωρίς φαρμακευτική αγωγή που επιτέυχθηκε, τόσο καλύτερο ήταν και TmSvdhS (p=0.009). Oι ασθενείς στους οποίους επιτεύχθηκε κατάσταση κλινικής ύφεσης με φαρμακευτική αγωγή, είτε τα πρώτα 5 έτη είτε στο συνολικό διάστημα παρακολούθησης εμφάνιζαν μεν μικρότερο βαθμό ακτινολογικών βλαβών στο TmSvdhS, αλλά σε μη σημαντικό επίπεδο (p=0.539 και p=0.948 αντιστοίχως). Oι ασθενείς με ασυμμετρία της γνάθου ή μικρογναθία είχαν υψηλότερη τιμή TmSvdhS συγκριτικά με τους υπόλοιπους (p<0.001) και είχαν υποβληθεί κατά τη διάρκεια της νόσου σε περισσότερες χειρουργικές επεμβάσεις στις αρθρώσεις (p<0.001). Σημαντική είναι η διαπίστωση ότι το TmSvdhS συσχετίστηκε αρνητικά με το τελικό ύψος (r=-0.256, p=0.009) (Πίνακας 80, Σχήματα 32 και 33). O βαθμός των ακτινολογικών βλαβών συσχετίστηκε θετικά με τον περιορισμό της λειτουργικής ικανότητας των ασθενών, που μετρήθηκε με το δείκτη haq-di και μάλιστα σε ιδιαίτερα σημαντικό επίπεδο (p<0.001) (Πίνακας 89, Σχήμα 44). Oι ασθενείς, δηλαδή, με τις σοβαρότερες ακτινολογικές βλάβες είχαν και μικρότερη λειτουργική ικανότητα στην εκτέλεση των καθημερινών τους δραστηριοτήτων. Σημαντικό είναι ότι μεγαλύτερος βαθμός συσχέτισης με τον περιορισμό της λειτουργικής ικανότητας παρατηρήθηκε στο επιμέρους msvdhs-jsn που αφορούσε στη στένωση του μεσάρθριου διαστήματος (r=0.448, p<0.001). δεν παρατηρήθηκε στατιστικώς σημαντική διαφορά ανάμεσα στους ασθενείς που πέρασαν το μεγαλύτερο μέρος της ζωής τους σε αστική, ημιαστική ή αγροτική περιοχή, όσον αφορά στο TmSvdhS. επίσης, δε διαπιστώθηκε σημαντική διαφορά στο μορφωτικό επίπεδο των ασθενών με χαμηλότερο TmSvdhS.
227 227 Πίνακας 80. Συσχετίσεις του τελικού βαθμού ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποποιημένο Sharp-van der Heijde σκορ (TmSvdHS) στην μονοπαραγοντική ανάλυση Μεταβλητή Μέσος t test, N όρος±sd df r p φύλο Άρρεν ± θήλυ ± διάρκεια νόσου ηλικία έναρξης της νόσου RF θετικός ± αρνητικός ± ιριδοκυκλίτιδα ναι ± όχι ± Συνολική διάρκεια ενεργότητας νόσου <0.001 διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου < επεισόδιο κλινικής ύφεσης χωρίς φαρμα- όχι ± κευτική αγωγή τα πρώ- ναι ± τα 5 έτη της νόσου
228 228 Σχήμα 32. Συσχέτιση του τελικού βαθμού ακτινολογικής βλάβης σύμφωμα με το συνολικό τροποποιημένο Sharp-van der Heijde σκορ (TmSvdHS) με Α. το φύλο και Β. την παρουσία ρευματοειδούς παράγοντα (RF).
229 229 Σχήμα 33. Συσχέτιση του τελικού βαθμού ακτινολογικής βλάβης σύμφωμα με το συνολικό τροποποιημένο Sharp-van der Heijde σκορ (TmSvdHS) με Α. το ιστορικό προσβολής του ισχίου και Β. την ανάπτυξη μικρογναθίας/ασυμμετρίας της γνάθου.
230 230 Σε αντιστοιχία με το JADi-A, η διάρκεια θεραπείας με κορτικοστεροειδή, η διάρκεια μονοθεραπείας με μεθοτρεξάτη, η διάρκεια μονοθεραπείας με DMARD, συσχετίστηκαν θετικά με την τιμή του TmSvdhS, σε στατιστικώς σημαντικό επίπεδο p<0.001, p=0.038, p<0.001, αντιστοίχως. Σε όλα τα παραπάνω σχήματα, η διάρκεια θεραπείας συσχετίστηκε σημαντικά, εκτός από το συνολικό και με τα επιμέρους ακτινολογικά σκορ που αφορούν στα άνω, στα κάτω άκρα, στις διαβρώσεις και στη στένωση του μεσάρθριου διαστήματος. εξαίρεση αποτέλεσε η διάρκεια μονοθεραπείας με μεθοτρεξάτη, η οποία παρουσίασε σημαντική θετική συσχέτιση μόνο με το επιμέρους ακτινολογικό σκορ που αφορούσε στη στένωση του μεσάρθριου διαστήματος (msvdhs-jsn) (p=0.022) και με τις ακτινολογικές βλάβες που αφορούσαν στον καρπό και στις άκρες χείρες (msvdhs-hw) (p=0.047). επιπλέον, οι ασθενείς στους οποίους χορηγήθηκε κατά τη διάρκεια της νόσου μεγαλύτερος αριθμός διαφορετικών μη βιολογικών DMARDS και είχαν ιστορικό θεραπείας με inhtnfα εμφάνιζαν υψηλότερο TmSvdhS σε στατιστικώς σημαντικό επίπεδο p<0.001 και p=0.015 αντιστοίχως (Πίνακας 81, Σχήμα 34). τέλος, σημειώνεται ότι το TmSvdhS παρουσιάζει πολύ ισχυρή θετική συσχέτιση με τα επιμέρους ακτινολoγικά σκορ που αφορούν στα άνω άκρα (r=0.967), στα κάτω άκρα (r=0.908), στις διαβρώσεις (r=0.993) και στη στένωση του μεσάρθριου διαστήματος (r=0.998).
231 Πίνακας 81. Συσχετίσεις του τελικού βαθμού ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποποιημένο Sharp-van der Heijde σκορ (TmSvdHS) με τη διάρκεια καθενός από τα σχήματα θεραπείας στην μονοπαραγοντική ανάλυση Συνολικό τροποποιημένο Sharp-van der Heijde score (TmSvdHS) Μεταβλητή Μέσος t test, N όρος±sd df r p διάρκεια θεραπείας με κορτικοστεροειδή <0.001 διάρκεια μονοθεραπείας με DMARDS <0.001 διάρκεια μονοθεραπείας με μεθοτρεξάτη διάρκεια συνδυασμένης θεραπείας διάρκεια συνδυασμένης θεραπείας με inh-tnfa διάρκεια συνδυασμένης θεραπείας με μη-βιολογικά DMARDS αριθμός διαφορετικών μη βιολογικών DMARDS <0.001 που έχουν χορηγηθεί αριθμός διαφορετικών inh-tnfa που έχουν χορηγηθεί ιστορικό θεραπείας με ναι ± inh-tnfα όχι ±
232 232 Σχήμα 34. Συσχέτιση του τελικού βαθμού ακτινολογικής βλάβης, σύμφωμα με το συνολικό τροποποιημένο Sharp van der Heijde σκορ (TmSvdHS) με Α. τη διάρκεια θεραπείας με κορτικοστεροειδή και Β. με τη διάρκεια μονοθεραπείας με μη βιολογικά DMARDs. Στην πολυπαραγοντική ανάλυση, στο μοντέλο γραμμικής παλινδρόμησης διαπιστώθηκε ότι παράγοντες κινδύνου για υψηλότερο τελικό TmSvdhS ήταν το θήλυ φύλο β= %Ci (51.935, ) p<0.001, η υποομάδα της συστηματικού τύπου έναρξης B= %Ci (38.802, ) p=0.003 και η υποομάδα πολυαρθρικού τύπου έναρξης νόσου B= %Ci (39.061, ) p=0.001, η μεγαλύτερη συνολική διάρκεια ενεργότητας β= %Ci (0.105, 0.838) p=0.012, η μεγαλύτερη διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου β= %Ci (0.206, 4.022) p=0.030, και τέλος η μακρύτερη διάρκεια χορήγησης μονοθεραπείας με DMARDS B= %Ci (0.515, 1.514) p< από το μοντέλο εξαιρέθηκαν και πάλι οι ασθε-
233 νείς με ψωριασική, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και αταξινόμητη αρθρίτιδα, λόγω της ετερογένειας της κάθε παραπάνω υποομάδας σε σύγκριση με τις υπόλοιπες (Πίνακας 82.) Πίνακας 82. Προγνωστικοί παράγοντες κινδύνου μεγαλύτερου βαθμού ακτινολογικής βλάβης (TmSvdHS) Πολυπαραγοντικό μοντέλο γραμμικής παλινδρόμησης για τη σχέση μεταξύ μεταβλητών κατά την έναρξη της νόσου και τελικής ακτινολογικής βλάβης Εξαρτημένη μεταβλητή έκβασης Ν 71 Συνολικό τροποποιημένο Sharp van der Heijde score (TmSvdHS) Μεταβλητές που εισήχθησαν στο μοντέλο Β (95% CI) p intercept ( , ) θήλυ φύλο (51.935, ) <0.001 Άρρεν φύλο Oμάδα αναφοράς Συστηματικού τύπου έναρξης νόσος (38.802, ) Πολυαρθρικού τύπου έναρξης (RF- και RF+) νόσος (39.061, ) Oλιγοαρθρικού τύπου έναρξης νόσος Oμάδα αναφοράς ηλικία έναρξης της νόσου (-4.514, 9.472) RF θετικός ( , ) RF αρνητικός Oμάδα αναφοράς διάρκεια ενεργότητας νόσου (0.105, 0.838) διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου (0.206, 4.022) αποτυχία κλινικής ύφεσης τα πρώτα 2 έτη από τη διάγνωση ( , 0.311) επιτυχία κλινικής ύφεσης τα πρώτα 2 έτη από τη διάγνωση Oμάδα αναφοράς διάρκεια μονοθεραπείας με μη βιολογικά DMARDS (0.515, 1.514) <0.001
234 Συσχετίσεις του βαθμού σωματικής λειτουργικής ικανότητας (HAQ- DI) και ειδικοί προγνωστικοί παράγοντες Oι γυναίκες που συμμετείχαν στη μελέτη δε διέφεραν σημαντικά από τους άνδρες σε επίπεδο ικανότητας στην εκτέλεση των καθημερινών τους δραστηριοτήτων, όπως αυτό μετρήθηκε με το δείκτη haq-di (p=0.773). επίσης, δεν παρατηρήθηκαν στατιστικώς σημαντικές διαφορές, ως προς τη σωματική ικανότητα (physical ability) των ασθενών μεταξύ των διαφόρων υπομάδων της νόσου. η τιμή του haq-di δε συσχετίστηκε σε σημαντικό επίπεδο με τη διάρκεια νόσου, ούτε με την ηλικία έναρξης της νόσου (p=0.761 και p=0.669 αντιστοίχως). ωστόσο, οι ασθενείς που εμφάνιζαν μεγαλύτερο περιορισμό της σωματικής τους ικανότητας ήταν αυτοί με πολυαρθική πορεία (p<0.001), με προσβολή της άρθρωσης του ισχίου (p=0.003). Όπως διαπιστώθηκε με το JADi-A και το TmSvdhS, οι ασθενείς που είχαν μεγαλύτερη διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου κατέληξαν να έχουν σοβαρότερο περιορισμό της φυσικοσωματικής λειτουργικής τους ικανότητας στην τελευταία επίσκεψη παρακολούθησης (p<0.001). επίσης, οι ασθενείς που πέτυχαν έστω μια φορά κλινική ύφεση χωρίς φαρμακευτική αγωγή το ίδιο χρονικό διάστημα εμφάνιζαν καλύτερο τελικό haq-di σκορ (p=0.007). Σε αντίθεση με το JADi-A και το TmSvdhS, η επίτευξη γενικά κλινικής ύφεσης, ασχέτως της λήψης ή όχι φαρμακευτικής αγωγής, τα πρώτα 5 έτη της νόσου συσχετίστηκε σημαντικά με καλύτερη έκβαση της φυσικοσωματικής λειτουργικής ικανότητας (p=0.036). η συνολική διάρκεια ενεργότητας κατά τη διάρκεια της νόσου συσχετίστηκε στατιστικώς σημαντικά με χειρότερο haq-di σκορ (r=0.343, p=0.001). το ίδιο παρατηρήθηκε και στους ασθενείς με μεγαλύτερο το ποσοστό διάρκειας ενεργού νόσου στην πορεία της νόσου (r=0.410 p<0.001) (πίνακας 89, Σχήμα 42). ωστόσο, ενώ διαπιστώθηκε μικρότερη τιμή του haq- Di σε αυτούς που πέτυχαν συγκριτικά με αυτούς που δεν πέτυχαν κλινική ύφεση χωρίς φαρμακευτική αγωγή κατά τη διάρκεια της νόσου, η διαφορά δεν έφτανε σε επίπεδο στατιστικής σημαντικότητας (p=0.124). το ίδιο παρατηρήθηκε και μεταξύ των ασθενών που πέτυχαν και δεν πέτυχαν κλινική ύφεση κατά τη διάρκεια της νόσου, ασχέτως της λήψης φαρμακευτικής αγωγής (p=0.069) (Πίνακας 83). Όπως αναφέρθηκε και στα προηγούμενα κεφάλαια, ο βαθμός της έκπτωσης της φυσικοσωματικής λειτουργικής ικανότητας συσχετίστηκε θετικά και στατιστικώς σημαντικά τόσο με το βαθμό της αρθρικής καταστροφής που μετρήθηκε με το JADi-A (p<0.001), όσο και με το βαθμό των ακτινολογικών βλαβών που δόθηκαν με το TmSvdhS (p<0.001) (Πίνακας 89, Σχήματα 44και
235 235 45). Oι ασθενείς με τοπικές διαταραχές ανάπτυξης της γνάθου εμφάνιζαν υψηλότερη τιμή haq-di σε στατιστικώς σημαντικό επίπεδο (p=0.029) και είχαν υποβληθεί κατά τη διάρκεια της νόσου σε μεγαλύτερο αριθμό χειρουργικών επεμβάσεων (p<0.001). ενδιαφέρον είναι ότι ο μεγαλύτερος περιορισμός της φυσικοσωματικής λειτουργικής ικανότητας συσχετίστηκε θετικά με μεγαλύτερο βαθμό ψυχολογικής επιβάρυνσης, σύμφωνα με το ερωτηματολόγιο GhQ28 (p<0.001), κάτι που δεν παρατηρήθηκε με το JADi-A και το TmSvdhS (Πίνακας 83, Σχήμα 35Γ). Σημαντική πληροφορία που αφορά στο haq-di, είναι ότι η τιμή του συσχετίστηκε σημαντικά με την παρουσία ενεργότητας νόσου στην τελευταία επίσκεψη παρακολούθησης (p<0.001). Προχωρώντας την ανάλυση βρέθηκε ότι ο περιορισμός της σωματικής λειτουργικής ικανότητας συσχετίστηκε ισχυρά και στατιστικώς σημαντικά με το DAS28 (p<0.001), με την τιμή της CRP (p<0.001), της τκε (p<0.001), καθώς και με την τιμή του δείκτη ASDAS (p=0.003) (Πίνακας 83, Σχήμα 35ακαι 35β). μεγαλύτερο haq-di σκορ, δηλαδή μεγαλύτερος περιορισμός της φυσικοσωματικής λειτουργικής ικανότητας συσχετίστηκε θετικά με μακρύτερη διάρκεια θεραπείας με κορτικοστεροειδή (p=0.002) (Πίνακας 84, Σχήμα 37). επιπλέον, οι ασθενείς στους οποίους χορηγήθηκε κατά τη διάρκεια της νόσου μεγαλύτερος αριθμός διαφορετικών μη βιολογικών DMARDS καθώς και διαφορετικών anti-tnf παραγόντων παρουσίαζαν υψηλότερο haq-di σε στατιστικώς σημαντικό επίπεδο p=0.011και p=0.009 αντιστοίχως (Πίνακας 84). τέλος, ενδιαφέρουσα είναι η διαπίστωση ότι οι ασθενείς που έζησαν το μεγαλύτερο μέρος της ζωής τους σε αστική περιοχή, εμφάνιζαν μικρότερο περιορισμό στη φυσικοσωματική τους λειτουργική ικανότητα σε σύγκριση με αυτούς που πέρασαν το αντίστοιχο χρονικό διάστημα σε αγροτική περιοχή (p=0.037). η διαπίστωση αυτή δεν αφορούσε και αντίστοιχες διαφορές, όπως αναφέρθηκε νωρίτερα, στο δείκτη JADi-A και στο TmSvdhS. διαφορές, επίσης, δεν παρατηρήθηκαν στην οικογενειακή κατάσταση (έγγαμοι-άγαμοι), ούτε στο μορφωτικό επίπεδο των ασθενών με χαμηλότερη τιμή haq-di. ωστόσο, οι ασθενείς με μεγαλύτερο περιορισμό της φυσικής τους λειτουργικής ικανότητας ήταν συχνότερα άνεργοι (p=0.005). Στους ασθενείς με ιστορικό ακτινολογικά διεγνωσμένης ιερολαγονίτιδας, το επίπεδο σωματικής ικανότητας, σύμφωνα με το δείκτη BASFi συσχετίστηκε πολύ ισχυρά με την τιμή του haq-di (r=0.897, p<0.0001) (Σχήμα 36) και του GhQ28 σκορ (r=0.759, p=0.007), καθώς και με το συνολικό χρονικό διάστημα ύφεσης της νόσου, με το οποίο παρουσίασε ισχυρή αρνητική συσχέτιση (r=-0.626, p=0.039).
236 236 Πίνακας 83. Συσχετίσεις του βαθμού σωματικής λειτουργικής ικανότητας (HAQ-DI) στην μονοπαραγοντική ανάλυση HAQ-DI score Μεταβλητή Μέσος t test, N όρος±sd df r p φύλο Άρρεν ±0.56 θήλυ ± διάρκεια νόσου ηλικία έναρξης της νόσου RF θετικός ± αρνητικός ± ιριδοκυκλίτιδα ναι ± όχι ± ενεργότητα νόσου ναι ± στην τελευταία επίσκε- - <0.001 όχι ± ψη παρακολούθησης DAS <0.001 ASDAS Συνολική διάρκεια ενεργότητας νόσου διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου < επεισόδιο κλινικής ύφεσης χωρίς φαρμακευ- όχι ± τική αγωγή τα πρώτα 5 ναι ± έτη της νόσου
237 237 Σχήμα 35. Συσχέτιση του βαθμού σωματικής λειτουργικής ικανότητας (HAQ-DI) κατά την τελευταία επίσκεψη με Α. την σύγχρονη παρουσία ενεργότητας νόσου Β. το βαθμό ενεργότητας νόσου (DAS28) και Γ. το βαθμό ψυχολογικής επιβάρυνσης (GHQ- 28) κατά την ίδια περίοδο.
238 238 Σχήμα 36. Συσχέτιση του βαθμού σωματικής λειτουργικής ικανότητας (HAQ-DI) στους ασθενείς με αξονική προσβλολή με το δείκτη BASFI (Bath Ankylosing Spondylitis Functional Index) κατά την τελευταία επίσκεψη. Πίνακας 84. Συσχετίσεις της σωματικής λειτουργικής ικανότητας (HAQ-DI) με τη διάρκεια καθενός από τα σχήματα θεραπείας στην πορεία της νόσου, στην μονοπαραγοντική ανάλυση HAQ-DI score Μεταβλητή Μέσος t test, N όρος±sd df r p διάρκεια θεραπείας με κορτικοστεροειδή διάρκεια μονοθεραπείας με DMARDS διάρκεια μονοθεραπείας με μεθοτρεξάτη διάρκεια συνδυασμένης θεραπείας διάρκεια συνδυασμένης θεραπείας με inh-tnfa διάρκεια συνδυασμένης θεραπείας με μη-βιολογικά DMARDS
239 Πίνακας 84. (συνέχεια). αριθμός διαφορετικών μη βιολογικών DMARDS που έχουν χορηγηθεί αριθμός διαφορετικών inh-tnfa που έχουν χορηγηθεί ιστορικό θεραπείας με όχι ± inh-tnfα ναι ± Σχήμα 37. Συσχέτιση της σωματικής λειτουργικής ικανότητας (HAQ-DI) κατά την τελευταία επίσκεψη με τη διάρκεια θεραπείας με κορτικοστεροειδή στην πορεία της νόσου. Στο μοντέλο λογιστικής παλινδρόμησης της πολυπαραγοντικής ανάλυσης βρέθηκε ότι παράγοντας κινδύνου για μεγαλύτερη έκπτωση της λειτουργικής ικανότητας (haq-di>0) στην τελευταία επίσκεψη παρακολούθησης ήταν μόνο η παρούσα ενεργότητα νόσου OR= %Ci (0.358, 2.563) p=0.009 (Πίνακας 85). από το μοντέλο εξαιρέθηκαν και πάλι οι ασθενείς με ψωριασική, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και αταξινόμητη αρθρίτιδα, λόγω της ετερογένειας της κάθε παραπάνω υποομάδας σε σύγκριση με τις υπόλοιπες.
240 240 Πίνακας 85. Προγνωστικοί παράγοντες κινδύνου μείωσης της σωματικής λειτουργικής ικανότητας, σύμφωνα με το HAQ-DI Πολυπαραγοντικό μοντέλο γραμμικής παλινδρόμησης για τη σχέση μεταξύ μεταβλητών κατά την έναρξη της νόσου και τελικής ακτινολογικής βλάβης Εξαρτημένη μεταβλητή έκβασης Ν 71 HAQ-DI>0 Μεταβλητές που εισήχθησαν στο μοντέλο OR (95% CI) p intercept (0.031, 0.709) Συστηματικού τύπου έναρξης νόσος (0.372, ) Πολυαρθρικού τύπου έναρξης (RF- και RF+) νόσος (0.289, 3.658) Oλιγοαρθρικού τύπου έναρξης νόσος Oμάδα αναφοράς διάρκεια ενεργότητας νόσου (0.995, 1.013) διάρκεια ενεργότητας τα πρώτα 5 έτη της νόσου (0.960, 1.037) Παρούσα ενεργότητα νόσου (1.430, ) απούσα ενεργότητα νόσου Oμάδα αναφοράς msvdhs-jsn (0.998, 1.025) διαμονή σε αγροτική ή ημιαστική περιοχή (0.139, 2.774) διαμονή σε αστική περιοχή Oμάδα αναφοράς Συσχετίσεις του βαθμού ψυχολογικής επιβάρυνσης (GHQ-28) και ειδικοί προγνωστικοί παράγοντες δε διαπιστώθηκε στατιστικώς σημαντική διαφορά στην τιμή του GhQ28 μεταξύ των δύο φύλων (p=0.161), καθώς και μεταξύ των υποομάδων της νόσου (p=0.660). αντιθέτως, ο βαθμός ψυχολογικής επιβάρυνσης βρέθηκε υψηλότερος στους ασθενείς με ενεργότητα νόσου στην τελευταία επίσκεψη παρακολούθησης (p=0.002) και μάλιστα όσο σοβαρότερη ήταν η ενεργότητα νόσου, σύμφωνα με το δείκτη DAS28, τόσο υψηλότερη ήταν και η τιμή του GhQ28 (p<0.001, r=0.446) (Πίνακας 86, Σχήμα 38α). Yψηλή θετική συσχέτιση και στατιστικώς σημαντική διαπιστώθηκε, επίσης, μεταξύ του GhQ28 και του
241 241 δείκτη ASDAS (p<0.001, r=0.751) στους ασθενείς με προσβολή του αξονικού σκελετού. η σφαιρική εκτίμηση της ενεργότητας νόσου τόσο από τον ιατρό (EGA) όσο και από τον ίδιο τον ασθενή (PGA) παρουσίασαν σημαντική θετική συσχέτιση με την τιμή του GhQ28, σε επίπεδο στατιστικής σημαντικότητας (p<0.001) (Πίνακας 86, Σχήμα 38β). Σημαντική είναι η διαπίστωση ότι οι ασθενείς που διένυαν χρονικό διάστημα κλινικής ύφεσης χωρίς φαρμακευτική αγωγή βρέθηκε να έχουν σημαντικά μικρότερο βαθμό ψυχολογικής επιβάρυνσης, σύμφωνα με το ερωτηματολόγιο GhQ28 (p<0.001) (Πίνακας 86, Σχήμα 38Γ). επίσης, ενδιαφέρουσα είναι η παρατήρηση ότι όσο μακρύτερο ήταν το συνολικό διάστημα ύφεσης της νόσου, τόσο χαμηλότερο ήταν και το GhQ28 σκορ στην τελευταία επίσκεψη παρακολούθησης (p=0.029). το μακρύτερο διάστημα κλινικής ύφεσης εκτός θεραπείας παρουσίασε οριακά μη σημαντική συσχέτιση με το τελικό GhQ28 σκορ (p=0.056). η παρουσία μόνιμων δομικών βλαβών στις αρθρώσεις, όπως αυτές καταγράφηκαν τόσο με το JADi-A, όσο και με το TmSvdhS, δε βρέθηκε να επηρεάζουν σε σημαντικό επίπεδο το ψυχολογικό προφιλ των ασθενών (p=0.784 και p=0.683 αντιστοίχως) (Πίνακας 89). το ίδιο παρατηρήθηκε και στους ασθενείς με ή χωρίς οφθαλμική προσβολή (p=0.872). επίσης, το ιστορικό χειρουργικής επέμβασης στις αρθρώσεις, ή στα μάτια δε συσχετίστηκε με υψηλότερη τιμή του GhQ28 (p=0.972 και p=0.552 αντιστοίχως). αντίθετα, ο περιορισμός της λειτουργικής ικανότητας των ασθενών, σύμφωνα με το haq-di, συσχετίστηκε σημαντικά με μεγαλύτερο βαθμό ψυχολογικής καταπόνησης (r=0.401, p<0.0001) (Πίνακας 89, Σχήμα 35). αντίστοιχα, πολύ ισχυρή θετική συσχέτιση παρατηρήθηκε και με τους ασθενείς με υψηλότερο δείκτη BASFi (r=0.759, p=0.007). αντιθέτως, δε διαπιστώθηκε σημαντική συσχέτιση της τιμής του GhQ28 με την τρέχουσα λήψη κορτικοειδών (p=0.125) ή τη διάρκεια λήψης κορτικοειδών (p=0.270), ενώ σημαντικά υψηλότερο βρέθηκε το GhQ28 σκορ στους ασθενείς που είχαν αλλάξει πολλούς βιολογικούς παράγοντες (p=0.038) (Πίνακας 86).
242 242 Πίνακας 86. Συσχετίσεις του βαθμού ψυχολογικής επιβάρυνσης, σύμφωνα με το ερωτηματολόγιο γενικής υγείας (GHQ-28) κατά την τελευταία επίσκεψη στη μονοπαραγοντική ανάλυση General Health Questionnaire-28 (GHQ-28) Μεταβλητή Μέσος t test, Person Sig. (2- N όρος±sd df correlation tailed) φύλο Άρρεν ± θήλυ ± ενεργότητα νόσου στην όχι ± τελευταία επίσκεψη παρακολούθησης ναι ± κλινική ύφεση χωρίς φαρμακευτική αγωγή όχι ± στην τελευταία επίσκεψη ναι ± παρακολούθησης - <0.001 DAS <0.001 ASDAS EGA (VAS 0-10) <0.001 PGA (VAS 0-10) <0.001 Συνολική διάρκεια ύφεσης τρέχουσα θεραπεία με όχι ± με κορτικοστεροειδή ναι ± διάρκεια θεραπείας με κορτικοστεροειδή
243 243 Σχήμα 38. Συσχέτιση του βαθμού ψυχολογικής επιβάρυνσης (GHQ-28) κατά την τελευταία επίσκεψη με Α. το βαθμό ενεργότητας νόσου (DAS28) Β τη σφαιρική εκτίμηση της ενεργότητας της νόσου του από τον ασθενή (PGA) και Γ. την παρουσία κλινικής ύφεσης χωρίς φαρμακευτική αγωγή την ίδια περίοδο.
244 244 Στην πολυπαραγοντική ανάλυση βρέθηκε ότι η μόνη μεταβλητή που επηρεάζει σημαντικά το GhQ-28, είναι η σφαιρική εκτίμηση της ενεργότητας της νόσου του από τον ίδιο τον ασθενή (PGA) στην οπτική αναλογική κλίμακα VAS (0-10cm) β= %Ci (0.017, 0.097) p=0.005 (Πίνακας 87). Πίνακας 87. Παράγοντες που επιδρούν σημαντικά στο βαθμό ψυχολογικής επιβάρυνσης των ασθενών με NIA, σύμφωνα με το Ερωτηματολόγιο Γενικής Υγείας (GHQ- 28) Πολυπαραγοντικό μοντέλο γραμμικής παλινδρόμησης για τη σχέση μεταξύ μεταβλητών και ψυχολογικής καταπόνησης, σύμφωνα με το Ερωτηματολόγιο Γενικής Υγείας (GHQ-28) Εξαρτημένη μεταβλητή έκβασης Ν 92 GHQ-28 σκορ Μεταβλητές που εισήχθησαν στο μοντέλο B (95% CI) p intercept (-0.702, 2.870) haq-di> (-0.836, 2.243) haq-di=0 Oμάδα αναφοράς Συνολική διάρκεια ύφεσης της νόσου (-0.011, 0.009) Σύγχρονη ενεργότητα της νόσου (-1.757, 1.699) PGA (VAS 0-10cm) (0.017, 0.097) Σε μια προσπάθεια εντοπισμού του ή των ειδικού/ών πεδίου/ων του GhQ28, στο οποίο εστιάζεται η διαφορά μεταξύ συγκεκριμένων ομάδων διαπιστώθηκαν τα παρακάτω: οι ασθενείς με ενεργό νόσο στην τελευταία επίσκεψη παρακολούθησης εμφάνιζαν μεγαλύτερη κοινωνική δυσλειτουργία (p=0.008) και υψηλότερο βαθμό κατάθλιψης (p=0.032), συγκριτικά με αυτούς στους οποίους η νόσος βρέθηκε μη ενεργός (Πίνακας 88, Σχήμα 39). Στα ίδια πεδία βρέθηκε να διαφέρουν και οι ασθενείς που βρισκόταν ή όχι σε κατάσταση κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στην τελευταία επίσκεψη παρακολούθησης. Συγκεκριμένα, η παρουσία κλινικής ύφεσης χωρίς φαρμακευτική αγωγή, βρέθηκε ότι συσχετίζεται με μικρότερο βαθμό κοινωνικής δυσλειτουργίας (p=0.034) και κατάθλιψης (p=0.001). Oι ασθενείς χωρίς ή με ήπιο περιορισμό της σωματικής τους λειτουργικής ικανότητας (haq-di ) διέφεραν από αυτούς με μέτριο ή σοβαρό περιορισμό (haq-di 0.5-3) ως προς το πεδίο της σωματοποίησης (p=0.004)
245 245 και της κοινωνικής δυσλειτουργίας (p<0.001) (Πίνακας 88, Σχήμα 40). δεν διαπιστώθηκε σημαντική διαφορά τόσο μεταξύ των δύο φύλων, όσο και μεταξύ των διαφόρων υποομάδων της νόσου, σε κάποιο από τα επιμέρους πεδία του GhQ28. αντίθετα, βρέθηκε ότι οι ασθενείς που ήταν άνεργοι είχαν υψηλότερο βαθμό κατάθλιψης, συγκριτικά με αυτούς που ήταν εργαζόμενοι (p=0.018). Στα υπόλοιπα τρία πεδία δεν εντοπίστηκαν στατιστικώς σημαντικές διαφορές μεταξύ ανέργων και εργαζομένων. μεγαλύτερος βαθμός κατάθλιψης καταγράφηκε στους ασθενείς που είχαν ολοκληρώσει μόνο την υποχρεωτική τους εκπαίδευση και ακολουθούσαν οι μαθητές της Γ Λυκείου. η παρουσία κατάθλιψης διέφερε σημαντικά μεταξύ της καθεμίας των παραπάνω δύο ομάδων και αυτών που είχαν λάβει τριτοβάθμια εκπαίδευση (p=0.018 και p=0.024 αντιστοίχως). Στα υπόλοιπα πεδία, επίσης, δεν διαπιστώθηκαν διαφορές μεταξύ των ομάδων διαφόρου μορφωτικού επιπέδου. τέλος, αναφέρεται ότι οι ομάδες που ορίστηκαν βάσει της οικογενειακής κατάστασης των ασθενών δε διέφεραν σημαντικά μεταξύ τους τόσο στο συνολικό GhQ28, όσο και σε κάποιον από τους επιμέρους τομείς του.
246 246 Πίνακας 88. Διαφορές στα τέσσερα πεδία του GHQ28 μεταξύ των ασθενών με και χωρίς ενεργότητα νόσου και μεταξύ των ασθενών με κανένα/ ήπιο περιορισμό και μέτριο /σοβαρό περιορισμό της σωματικής ικανότητας (HAQ-DI), στην μονοπαραγοντική ανάλυση Ενεργότητα νόσου στην τελευταία Μεταβλητή επίσκεψη παρακολούθησης HAQ-DI β Ναι Όχι p p N n=50 n=46 n=67 n=29 Σωματικά συμπτώματα (GhQ28-A) α ± ± ± ± Άγχος - αϋπνία δυσλειτουργία (GhQ28-C) a ± ± ± ± κοινωνική δυσλειτουργία (GhQ28-C) a ± ± ± ±4.2 <0.001 κατάθλιψη (GhQ28-D) a ± ± ± ± a μέσος όρος ± SD, β HAQ-DI = 0-0,49 ορίζεται ως κανένας/ήπιος περιορισμός της σωματικής ικανότητας, HAQ-DI = ορίζεται ως μέτριος/σοβαρός περιορισμός της σωματικής ικανότητας
247 247 Σχήμα 39. Συσχέτιση των συμπτωμάτων Α. κοινωνικής δυσλειτουργίας και Β. κατάθλιψης με την παρουσία ενεργότητας νόσου κατά την τελευταία επίσκεψη.
248 248 Σχήμα 40. Συσχέτιση των συμπτωμάτων Α. σωματοποίησης Β. κοινωνικής δυσλειτουργίας με τη σωματική λειτουργική ικανότητα (HAQ-DI) κατά την τελευταία επίσκεψη.
249 249 Πίνακας 89. Συσχετίσεις μεταξύ των επτά πεδίων μακροχρόνιας έκβασης των ασθενών με NIA που μελετήθηκαν % διάρκεια κλινικής ύφεσης εκτός θεραπείας/διάρκεια JADI-A JADI-E TmSvHs HAQ-DI GHQ28 νόσου % διάρκειας Pearson Correlation ενεργότητας/ Sig.(2-tailed) < / διάρκεια νόσου N JADI-A Pearson Correlation Sig.(2-tailed) N JADI-E Pearson Correlation Sig.(2-tailed) N TmSvdHS Pearson Correlation Sig.(2-tailed) N HAQ-DI Pearson Correlation Sig.(2-tailed) N GHQ28 Pearson Correlation Sig.(2-tailed) N
250 250 Σχήμα 41. Συσχέτιση του ποσοστού διάρκειας ενεργότητας στην πορεία της νόσου με το βαθμό ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποποιημένο Sharpvan der Heijde σκορ.. Σχήμα 42. Συσχέτιση του ποσοστού διάρκειας ενεργότητας στην πορεία της νόσου με το βαθμό σωματικής λειτουργικής ικανότητας ( HAQ-DI).
251 251 Σχήμα 43. Συσχέτιση του βαθμού αρθρικής καταστροφής, όπως εκτιμάται κλινικά (JADI-A) με το βαθμό ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποποιημένο Sharp-van der Heijde σκορ.. Σχήμα 44. Συσχέτιση του βαθμού σωματικής λειτουργικής ικανότητας (HAQ-DI) με το βαθμό ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποποιημένο Sharp-van der Heijde σκορ.
252 252 Σχήμα 45. Συσχέτιση του βαθμού σωματικής λειτουργικής ικανότητας (HAQ-DI) με το βαθμό αρθρικής καταστροφής, όπως εκτιμάται κλινικά (JADI-A).. Σχήμα 46. Συσχέτιση του ποσοστού διάρκειας κλινικής ύφεσης εκτός θεραπείας στην πορεία της νόσου με το βαθμό ακτινολογικής βλάβης, σύμφωνα με το συνολικό τροποποιημένο Sharp-van der Heijde σκορ.
253 253 Σχήμα 47. Συσχέτιση του ποσοστού διάρκειας κλινικής ύφεσης εκτός θεραπείας στην πορεία της νόσου με το βαθμό αρθρικής καταστροφής, όπως εκτιμάται κλινικά (JADI-A).. Σχήμα 48. Συσχέτιση του ποσοστού διάρκειας κλινικής ύφεσης εκτός θεραπείας στην πορεία της νόσου με το βαθμό σωματικής λειτουργικής ικανότητας (HAQ-DI).
254 Προγνωστικοί παράγοντες ανάπτυξης οφθαλμικής προσβολής Παρά το υψηλότερο ποσοστό οφθαλμικής προσβολής στις γυναίκες (13.9%), η διαφορά του από το αντίστοιχο στους άνδρες (3.3%) δε βρέθηκε στατιστικώς σημαντική (p=0.224). Oι ασθενείς με ολιγοαρθρικής έναρξης νόσο παρουσίαζαν υψηλότερο ποσοστό εμφάνισης ιριδοκυκλίτιδας και συγκεκριμένα περίπου ένας στους τρεις (30%). η διαφορά αυτή στην εμφάνιση ιριδοκυκλίτιδας μεταξύ ολιγοαρθρικής έναρξης νόσου και των υπόλοιπων υποομάδων βρέθηκε στατιστικώς σημαντική (p=0.01). Στους ασθενείς με οφθαλμική προσβολή, η έναρξη της νόσου και συγκεκριμένα της αρθρίτιδας, συνέβαινε σε σημαντικά μικρότερη ηλικία συγκριτικά με αυτούς οι οποίοι δεν εμφάνισαν ποτέ οφθαλμική προσβολή (p<0.001). η παρουσία ιστορικού ιριδοκυκλίτιδας διέφερε στατιστικώς σημαντικά μεταξύ της υποομάδας των ασθενών με ηλικία έναρξης της νόσου μικρότερης ή ίσης των 6.5 ετών και της υποομάδας με ηλικία έναρξης μετά την ηλικία των 6.5 ετών, σε επίπεδο σημαντικότητας p=0.001.συγκεκριμένα, σε όλους τους ασθενείς με ιριδοκυκλίτιδα η νόσος είχε ξεκινήσει πριν την ηλικία των 6.5 ετών, με μέση ηλικία έναρξης τα 3.09 έτη, έναντι της μέσης ηλικίας έναρξης των 8.35 ετών που καταγράφηκε στους ασθενείς χωρίς οφθαλμική προσβολή. θετικά αντιπυρηνικά αντισώματα (ανα) παρατηρήθηκαν σε υψηλότερο ποσοστό στους ασθενείς με προσβολή ιριδοκυκλίτιδας (9/11 ασθενείς, 81.8%), σε σύγκριση με τους υπόλοιπους χωρίς οφθαλμική προσβολή (24/88 ασθενείς, 27.3%), διαφορά που έφτανε σε επίπεδο στατιστικής σημαντικότητας p= Σε τρείς ασθενείς, χωρίς ιστορικό οφθαλμικής προσβολής, δεν υπήρχε καταγεγραμένος στον αντίστοιχο φάκελο παρακολούθησης ο τίτλος των ανα. Στην πολυπαραγοντική ανάλυση, στο μοντέλο λογιστικής παλινδρόμησης παράγοντες κινδύνου εμφάνισης ιριδοκυκλίτιδας βρέθηκαν η μικρή ηλικία έναρξης της νόσου OR= %Ci (0.381, 0.829) p=0.004 και η παρουσία θετικών ANA κατά τη διάγνωση OR= %Ci (1.821, ) p= αντίθετα, η νόσος ολιγοαρθρικού τύπου έναρξης (ολιγοαρθρίτιδα εμμένουσα και επεκταθείσα) δε συσχετίστηκε με αυξημένο κίνδυνο ανάπτυξης ιριδοκυκλίτιδας, σε σύγκριση με τις υπόλοιπες υποομάδες (συστηματική αρθρίτιδα, πολυαρθρίτιδα αρνητική, πολυαρθρίτιδα θετική, ψωριασική αρθρίτιδα, αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και αταξινόμητη αρθρίτιδα) (p=0.139) (Πίνακας 90).
255 Πίνακας 90. Παράγοντες κινδύνου ανάπτυξης ιριδοκυκλίτιδας στην πορεία της νόσου Πολυπαραγοντικό μοντέλο λογιστικής παλινδρόμησης για τη σχέση μεταξύ μεταβλητών κατά την έναρξη και εμφάνισης ιριδοκυκλίτιδας στην πορεία της νόσου Εξαρτημένη μεταβλητή Ν 99 Ιριδοκυκλίτιδα Μεταβλητές που εισήχθησαν στο μοντέλο OR (95% CI) p Υποομάδες πλην ολιγοαρθρικού τύπου έναρξης (0.037, 1.585) Oλιγοαρθρικού τύπου έναρξης νόσος Oμάδα αναφοράς ηλικία έναρξης της νόσου (0.381, 0.829) θετικός τίτλος ανα (1.821, ) αρνητικός τίτλος ανα Oμάδα αναφοράς 255 Παρακάτω συνοψίζονται τα αποτελέσματα στη μακροχρόνια έκβαση (ποσοστό διάρκειας ενεργότητας κατά τη διάρκεια της νόσου, ποσοστό διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή κατά τη διάρκεια της νόσου αρθρική, εξωαρθρική καταστροφή, ακτινολογικές βλάβες, σωματική λειτουργική ικανότητα, ψυχολογική επιβάρυνση) ανάλογα της επίτευξης ή όχι κλινικής ύφεσης στα πρώτα 2 έτη από τη διάγνωση, της διάρκειας ενεργότητας τα πρώτα 5 έτη και της συνολικής διάρκειας ενεργότητας της νόσου. 4.8 Χαρακτηριστικά, πορεία και μακροχρόνια έκβαση των ασθενών που πέτυχαν ή όχι κλινική ύφεση μέσα στα πρώτα 2 έτη από την έναρξη της νόσου Συνολικά, 40 από τους 102 ασθενείς (39.2%) της μελέτης εμφάνισαν τουλάχιστον ένα επεισόδιο κλινικής ύφεσης (με και/ή χωρίς φαρμακευτική αγωγή) μέσα στα πρώτα 2 έτη από τη διάγνωση της νόσου. μόνο 3 ασθενείς από αυτούς πέτυχαν κλινική ύφεση χωρίς φαρμακευτική αγωγή το παραπάνω χρονικό διάστημα. Oι ασθενείς που πέτυχαν κλινική ύφεση τα 2 πρώτα έτη ήταν συχνότερα αγόρια (p=0.011) και είχαν μεγαλύτερη ηλικία κατά την έναρξη της νόσου (p=0.011). Oι δύο ομάδες των ασθενών που πέτυχαν και δεν πέτυχαν αντίστοιχα κλινική ύφεση δε διέφεραν στατιστικώς σημαντικά στην υποομάδα έναρξης της νόσου (p=0.086), στην παρουσία θετικού ρευματοειδή παράγοντα (p=0.165) ή θετικών anti-ccp αντισωμάτων (p=0.164).
256 256 η μακροχρόνια έκβαση της NiA στους ασθενείς που πέτυχαν κλινική ύφεση τα πρώτα 2 έτη από τη διάγνωση ήταν ηπιότερη συγκριτικά με αυτήν των ασθενών που δεν πέτυχαν την παραπάνω κατάσταση. Συγκεκριμένα, στην τελευταία επίσκεψη παρακολούθησης εμφάνιζαν μικρότερο βαθμό αρθρικής (p<0.001) και εξωαρθρικής καταστροφής (p=0.033), καθώς και λιγότερες ακτινολογικές βλάβες (p=0.002) (Πίνακας 91, Σχήματα 50-52). Παρά το γεγονός ότι οι δύο ομάδες ασθενών δε διέφεραν σημαντικά στη διάρκεια νόσου (p=0.122), ωστόσο οι ασθενείς που πέτυχαν κλινική ύφεση τα πρώτα 2 έτη διένυσαν τα επόμενα χρόνια μικρότερo χρονικό διάστημα με ενεργότητα νόσου (p<0.001). αυτό φαίνεται και από τη σημαντική διαφορά που προέκυψε μεταξύ των δύο ομάδων όσον αφορά στο ποσοστό διάρκειας ενεργότητας προς συνολική διάρκεια νόσου (p<0.001) (Πίνακας 91, Σχήμα 49) καθώς και στο ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας στην πορεία της νόσου (p<0.001)(πίνακας 91). επιπλέον, οι ασθενείς που πέτυχαν κλινική ύφεση τα πρώτα 2 έτη από τη διάγνωση εμφανίζονται να πετυχαίνουν συχνότερα κλινική ύφεση χωρίς φαρμακευτική αγωγή, τόσο μέσα στα πρώτα 5 έτη (p=0.002), όσο και συνολικά στη διάρκεια της νόσου (p<0.001). τέλος, σημαντική είναι η διαπίστωση ότι στους ασθενείς που πέτυχαν κλινική ύφεση τα πρώτα 2 έτη της νόσου χρειάστηκε μετέπειτα μικρότερο χρονικό διάστημα χορήγησης κορτικοστεροειδών για τον έλεγχο της νόσου (p=0.002). Oι ίδιοι ασθενείς έλαβαν, επίσης, μικρότερο χρονικό διάστημα θεραπεία με συνδυασμό μη βιολογικών DMARDS (Πίνακας 91).
257 257 Πίνακας 91. Χαρακτηριστικά, πορεία και μακροχρόνια έκβαση των ασθενών που πέτυχαν ή όχι κλινική ύφεση κατά το χρονικό διάστημα των πρώτων 2 ετών από τη διάγνωση της νόσου. Ασθενείς που πέτυχαν Ασθενείς που δεν πέτυχαν κλινική ύφεση τα 2 κλινική ύφεση τα 2 πρώτα έτη της νόσου πρώτα έτη της νόσου N=40 N=62 θήλυ φύλο, αρ. (%) 22 (55) 50 (80.6) ηλικία έναρξης της νόσου,έτη a 9.1± ± διάρκεια νόσου, έτη a 16± ± διάρκεια ενεργότητας νόσου, έτη a 6± ±6.3 <0.001 Ποσοστό διάρκειας ενεργού νόσου/ διάρκεια νόσου, (%) a 36.8± ±24.3 <0.001 Ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας/ διάρκεια νόσου, (%) a 63.2± ±24.3 <0.001 διάρκεια ενεργότητας τα πρώτα 5 έτη, μήνες a 25.2± ±13.2 <0.001 επίτευξη κλινικής ύφεσης χωρίς φα τα πρώτα 5 έτη της νόσου, αρ. (%) 10/38 (26.3) 2/62 (3.2) επίτευξη κλινικής ύφεσης με φα κατά τη διάρκεια της νόσου,αρ. (%) 34/38 (89.5) 53/60 (88.3) 1 επίτευξη κλινικής ύφεσης χωρίς φα κατά τη διάρκεια της νόσου, αρ. (%) 24/38 (63.2) 13/60 (21.7) <0.001 RF θετικός, αρ. (%) 2 (5) 10 (16.1) τίτλος anti-ccp θετικός, αρ.(%) 2/34 (5.9) 9/47 (19.1) ανα θετικά, αρ. (%) 11/38 (28.9) 22/61 (36.1) Προσβολή του ισχίου, αρ.(%) 12 (30) 33 (53.2) haq-di a 0.28± ± p
258 258 Πίνακας 91. (συνέχεια). Ασθενείς που πέτυχαν Ασθενείς που δεν πέτυχαν κλινική ύφεση τα 2 κλινική ύφεση τα 2 p πρώτα έτη της νόσου πρώτα έτη της νόσου N=40 N=62 BASFi a 1.7± ± JADi-A a 7.6± ±20.9 <0.001 JADi-E a 0.73± ± TmSvdhS a 104.2± ± msvdhs-erosions a 59.0± ± msvdhs-jsn a 45.2± ± ασυμμετρία γνάθου/μικρογναθία, αρ. (%) 10 (25) 27 (43.5) Xειρουργική επέμβαση στις αρθρώσεις, αρ. (%) 3 (7.5) 8 (12.9) διάρκεια θεραπείας με κορτικοστεροειδή, μήνες a 49.9±44.8 (21) 94.8±69.2 (48) διάρκεια μονοθεραπείας με DMARDS a 51.1±38.8 (29) 72.9±62.3 (57) διάρκεια συνδυασμένης θεραπείας με DMARDS a 27.9±11.1 (10) 43.0±27.1 (32) διάρκεια συνδυασμένης θεραπείας με inh-tnfα a 43.4± ± αριθμός διαφορετικών μη-βιολογικών DMARDS που έχουν χρησιμοποιηθεί a 1.9± ± αριθμός διαφορετικών inh-tnf που έχουν χρησιμοποιηθεί a 1.8± ± a μέση τιμή±τυπική απόκλιση
259 259 Σχήμα 49. Σύγκριση του ποσοστού της διάρκειας ενεργότητας στη διάρκεια της νόσου μεταξύ των ασθενών που πέτυχαν ή όχι κλινική ύφεση στα πρώτα 2 έτη από την έναρξη της νόσου.. Σχήμα 50. Σύγκριση του τελικού βαθμού ακτινολογικής βλάβης (συνολικό τροποποιημένο Sharp-van der Heijde σκορ) μεταξύ των ασθενών που πέτυχαν ή όχι κλινική ύφεση στα πρώτα 2 έτη από την έναρξη της νόσου.
260 260 Σχήμα 51. Σύγκριση του τελικού βαθμού αρθρικής καταστροφής (JADI-A) μεταξύ των ασθενών που πέτυχαν ή όχι κλινική ύφεση στα πρώτα 2 έτη από την έναρξη της νόσου.. Σχήμα 52. Σύγκριση του του ποσοστού της διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στη διάρκεια της νόσου μεταξύ των ασθενών που πέτυχαν ή όχι κλινική ύφεση στα πρώτα 2 έτη από την έναρξη της νόσου.
261 Μακροχρόνια έκβαση των ασθενών βάσει της διάρκειας ενεργότητας νόσου τα πρώτα 5 έτη από την έναρξη της νόσου Oι ασθενείς που δεν πέτυχαν κλινική ύφεση τα πρώτα 2 έτη της νόσου, παρουσίασαν συνολικά περισσότερους μήνες ενεργότητας τα πρώτα 5 έτη (p<0.001). η μεγαλύτερη διάρκεια ενεργότητας νόσου σε αυτό το χρονικό διάστημα συσχετίστηκε σε σημαντικό επίπεδο με χειρότερη μακροχρόνια έκβαση. Συγκεκριμένα, οι ασθενείς που διένυσαν μακρύτερες περιόδους με ενεργότητα νόσου τα πρώτα 5 έτη, βρέθηκε ότι παρουσιάζουν μεγαλύτερο βαθμό αρθρικής και εξωαρθρικής καταστροφής, σύμφωνα με την τιμή του JADi-A (p<0.001) και του JADi-E (p=0.003) αντίστοιχα. το ίδιο παρατηρήθηκε και σε επίπεδο ακτινολογικών βλαβών, όπως αυτές μετρήθηκαν με τη μέθοδο Sharp-van der heijde, στην τελευταία επίσκεψη παρακολούθησης (p<0.001) και αφορούσε τόσο το μέγεθος και την έκταση των διαβρώσεων (msvdhs- E), (p<0.001), όσο και το βαθμό στένωσης του μεσάρθριου διαστήματος (msvdhs-jsn) των εξεταζόμενων αρθρώσεων (p<0.001). το ποσοστό της διάρκειας νόσου τους που διένυαν οι ασθενείς με ενεργότητα καθώς και το συνολικό διάστημα ενεργότητας νόσου ήταν σημαντικά μεγαλύτερο στους ασθενείς με μακρύτερo διάστημα ενεργότητας τα πρώτα 5 έτη (p<0.001). επιπλέον, οι ασθενείς που είχαν μακρύτερο διάστημα ενεργότητας νόσου τα πρώτα 5 έτη ήταν λιγότερο πιθανό να επιτύχουν κλινική ύφεση εκτός θεραπείας κάποια στιγμή στην πορεία (p=0.003) και περνούσαν μικρότερο χρονικό διάστημα της νόσου τους σε κλινική ύφεση χωρίς φαρμακευτική αγωγή (p=0.002). τέλος, οι ασθενείς με μακρύτερα διαστήματα ενεργότητας νόσου τα πρώτα 5 έτη, εμφάνισαν μεγαλύτερο περιορισμό της φυσικοσωματικής λειτουργικής τους ικανότητας μετά από μέσο όρο 17.2 έτη από τη διάγνωση, όπως αυτό αντικατοπτρίζεται στη μεγαλύτερη τιμή του haq-di (p<0.001) στην τελευταία επίσκεψη παρακολούθησης. Στον πίνακα συνοψίζονται οι σημαντικοί συσχετισμοί στη μονοπαραγοντική ανάλυση της διάρκειας ενεργότητας τα πρώτα 5 έτη από τη διάγνωση. Στην πολυπαραγοντική ανάλυση η μεγαλύτερη διάρκεια ενεργότητας νόσου τα πρώτα 5 έτη βρέθηκε ότι αποτελεί προγνωστικό παράγοντα για επίμονη ενεργότητα (p<0.001) και μικρότερη διάρκεια κλινικής ύφεσης εκτός θεραπείας στην πορεία της νόσου (p=0.001) καθώς και για μεγαλύτερο βαθμό ακτινολογικής βλάβης (p=0.030).
262 262 Πίνακας 92. Σύνοψη των συσχετίσεων της διάρκειας ενεργότητας τα πρώτα 5 έτη από τη διάγνωση με τις μεταβλητές βάσει των οποίων ορίστηκε η μακροχρόνια έκβαση Μεταβλητή Pearson s Correlation (r) p Ποσοστό διάρκειας ενεργότητας κατά τη <0.001 διάρκεια της νόσου JADi-A <0.001 JADi-E TmSvdhS <0.001 msvdhs-e <0.001 msvdhs-jsn <0.001 haq-di <0.001 Ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας στη διάρκεια της νόσου Σχήμα 53. Συσχέτιση του ποσοστού διάρκειας ενεργότητας στην πορεία της νόσου με τη διάρκεια ενεργότητας (σε μήνες) τα πρώτα 5 έτη από την έναρξη της νόσου.
263 263 Σχήμα 54. Συσχέτιση του ποσοστού διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στην πορεία της νόσου με τη διάρκεια ενεργότητας (σε μήνες) τα πρώτα 5 έτη από την έναρξη της νόσου. Σχήμα 55. Συσχέτιση του τελικού βαθμού ακτινολογικής βλάβης (συνολικό τροποποιημένο Sharp van der Heijde score) με τη διάρκεια ενεργότητας (σε μήνες) τα πρώτα 5 έτη από την έναρξη της νόσου.
264 264 η επίτευξη κατάστασης κλινικής ύφεσης χωρίς φαρμακευτική αγωγή τα πρώτα 5 έτη της νόσου συσχετίστηκε στη μονοπαραγοντική ανάλυση με μικρότερο ποσοστό διάρκειας ενεργότητας (p<0.001) και υψηλότερο ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας στην πορεία της νόσου (p<0.001), με χαμηλότερο JADi-A (p=0.006), χαμηλότερο JADi-E (p=0.031), χαμηλότερο TmSvdhS (p=0.001), χαμηλότερο haq-di (p=0.007) και χαμηλότερο δείκτη BASFi (p<0.001) στην τελευταία επίσκεψη (Πίνακας 93, Σχήμα 56). Πίνακας 93. Σύγκριση των ασθενών που πέτυχαν ή όχι κλινική ύφεση χωρίς φαρμακευτική αγωγή στα πρώτα 5 έτη από την έναρξη της νόσου ως προς τις μεταβλητές μακροχρόνιας έκβασης Ασθενείς που πέτυχαν Ασθενείς που δεν πέκλινική ύφεση χωρίς τυχαν κλινική ύφεση φαρμακευτική αγωγή χωρίς φαρμακευτική στα πρώτα 5 έτη αγωγή στα πρώτα 5 από την έναρξη της έτη από την έναρξη νόσου της νόσου Μεταβλητή έκβασης Ν=12 Ν=86 p Ποσοστό διάρκειας ενεργότητας κατά τη διάρκεια της 19.8± ±26.1 <0.001 νόσου Ποσοστό διάρκειας κλινικής ύφεσης χωρίς φαρμακευτική 71.1± ±20.6 <0.001 αγωγή κατά τη διάρκεια της νόσου TmSvdhS 51.3± ± JADi-A 4.7± ± JADi-E 0.33± ± haq-di 0.09± ± BASFi - 2.1±2.2 <0.001
265 265 Σχήμα 56. Σύγκριση A. του τελικού βαθμού ακτινολογικής βλάβης (συνολικό τροποποιημένο Sharp van der Heijde score) Β.του τελικού βαθμού αρθρικής καταστροφής (JADI-A) και Γ. του τελικού βαθμού εξωαρθρικής καταστροφής (JADI-E) μεταξύ των ασθενών που πέτυχαν ή όχι κλινική ύφεση χωρίς φαρμακευτική αγωγή τα πρώτα 5 έτη από την έναρξη της νόσου.
266 Μακροχρόνια έκβαση των ασθενών σε σχέση με τη συνολική διάρκεια ενεργότητας της νόσου η διάρκεια ενεργότητας της νόσου διαπιστώθηκε ότι αποτελεί παράγοντα που επηρεάζει σημαντικά τη μακροχρόνια έκβαση των ασθενών. Έτσι συνοψίζοντας τα αποτελέσματα από τις προηγούμενες ενότητες, στη μονοπαραγοντική ανάλυση βρέθηκε υψηλή θετική συσχέτιση της διάρκειας ενεργότητας με την τιμή του JADi-A (p<0.001), του JADi-E (p<0.001), του TmSvdhS (p<0.001) και του haq-di (p<0.001) (Πίνακας 94, Σχήμα 57). αυτό σημαίνει ότι όσο μακρύτερη ήταν η συνολική διάρκεια ενεργότητας της νόσου, τόσο μεγαλύτερος ήταν ο βαθμός αρθρικής και εξωαρθρικής καταστροφής, ακτινολογικής βλάβης και έκπτωσης της λειτουργικής ικανότητας που παρατηρήθηκε μετά από μέσο όρο 17.2 έτη διάρκειας νόσου. η επίπτωση της ασυμμετρίας της γνάθου ή μικρογναθίας ήταν μεγαλύτερη στους ασθενείς με μακρύτερη διάρκεια ενεργότητας νόσου (p<0.001). επίσης, οριακά σημαντική αρνητική συσχέτιση παρουσίαζε η συνολική διάρκεια ενεργότητας με το δείκτη μάζας σώματος (βμι) (r=-0.200, p=0.048). Στην πολυπαραγοντική ανάλυση, η συνολική διάρκεια ενεργότητας βρέθηκε σημαντικός προγνωστικός παράγοντας για μεγαλύτερο βαθμό αρθρικής καταστροφής (p=0.002) και ακτινολογικής βλάβης (p=0.012). η επίτευξη τουλάχιστον ενός επεισοδίου κλινικής ύφεσης χωρίς φαρμακευτική αγωγή στην πορεία της νόσου επηρέασε ευνοϊκά τη μακροχρόνια έκβαση που αφορούσε στο τελικό JADi-A (p=0.009), JADi-E (p=0.019), TmvdhS (p=0.003) και GhQ28 score (p<0.001). το GhQ28 score συσχετίστηκε, επιπλέον, με το συνολικό χρονικό διάστημα ύφεσης της νόσου (r= , p=0.029). Παρόμοια συσχέτιση, αλλά ισχυρότερη παρατηρήθηκε και μεταξύ του συνόλου ύφεσης και του δείκτη BASFi (r=-0.626, p=0.039). τέλος, επαναλαμβάνεται ότι οι ασθενείς που δεν πέτυχαν κλινική ύφεση τα πρώτα 2 έτη της νόσου και είχαν μακρύτερα διαστήματα ενεργότητας τα πρώτα 5 έτη, εμφάνισαν στην πορεία μακρύτερη διάρκεια ενεργότητας νόσου.
267 Πίνακας 94. Σύνοψη των συσχετίσεων της συνολικής διάρκειας ενεργότητας στην πορεία της νόσου με τις μεταβλητές βάσει των οποίων ορίστηκε η μακροχρόνια έκβαση Ανεξάρτητη μεταβλητή Ν 98 Συνολική διάρκεια ενεργότητας νόσου Εξαρτημένες μεταβλητές έκβασης Pearson Correlation (r) p JADi-A <0.001 JADi-E <0.001 TmSvdhS <0.001 msvdhs-e <0.001 msvdhs-jsn <0.001 haq-di JADI-A=Juvenile Arthritis Disease Index-Articular, JADI-E=Juvenile Arthritis Disease Index-Extra-articular, TmSvdHS=Συνολικό τροποποιημένο Sharp van der Heijde σκορ, msvdhs-e=τροποποιημένο Sharp van der Heijde- Διαβρώσεις, msvdhs-jsn=τροποποιημένο Sharp van der Heijde-Στένωση μεσάρθριου διαστήματος, HAQ-DI=Health Assessment Questionnaire-Disability Index 267 Σχήμα 57. Συσχέτιση Α. του τελικού βαθμού ακτινολογικής βλάβης (TmSvdHS), Β. του τελικού βαθμού αρθρικής καταστροφής, όπως εκτιμάται κλινικά (JADI-A), Γ. του τελικού βαθμού εξωαρθρικής καταστροφής (JADI-E) και Δ. του βαθμού σωματικής λειτουργικής ικανότητας (HAQ-DI) στην τελευταία επίσκεψη, με τη διάρκεια ενεργότητας (σε μήνες) κατά τη συνολική πορεία της νόσου.
268 268 Στις ενότητες που ακολουθούν περιγράφονται τα χαρακτηριστικά, η πορεία και η έκβαση των ασθενών χωρισμένων σε ομάδες βάσει συγκεκριμένων εργαστηριακών δεικτών (παρουσία-απουσία αντιπυρηνικών αντισωμάτων [ανα], παρουσία-απουσία αντισωμάτων έναντι κυκλικών κιτρουλλινιωμένων πεπτιδίων [anti-ccp]), ακτινολογικών ευρημάτων (ανάπτυξη ή όχι ιερολαγονίτιδας) και επιδημιολογικών χαρακτηριστικών (διάγνωση της νόσου πριν και μετά το έτος 2000, θεραπεία με βιολογικούς παράγοντες στους ασθενείς με διάγνωση πριν και μετά το έτος 2000) Χαρακτηριστικά, πορεία και έκβαση των ασθενών με θετικά αντιπυρηνικά αντισώματα (Antinuclear Antibodies, ΑΝΑ) κατά τη διάγνωση της νόσου το τελευταίο χρονικό διάστημα, υπάρχουν αναφορές στη βιβλιογραφία, ότι οι ασθενείς που έχουν θετικά αντιπυρηνικά αντισώματα, αποτελούν ομοιογενή υποομάδα, με ιδιαίτερα χαρακτηριστικά, οι οποίοι, όμως, μέχρι σήμερα κατατάσσονται σε διαφορετικές υποομάδες της NiA. Στο δείγμα της δικής μας μελέτης, 33 ασθενείς είχαν θετικό τίτλο αντιπυρηνικών αντισωμάτων κατά τη διάγνωση της νόσου και 66 ασθενείς ήταν αρνητικοί. αξίζει να σημειωθεί ότι οι ασθενείς που βρέθηκαν θετικοί στην τελευταία επίσκεψη παρακολούθησης, είχαν θετικό τίτλο αντιπυρηνικών αντισωμάτων και κατά την έναρξη της νόσου. Συγκρίνοντας τις δύο ομάδες ασθενών, αυτών με θετικά ανα και αυτών με αρνητικά ανα, βρέθηκε ότι διαφέρουν στατιστικώς σημαντικά στην ηλικία έναρξης της νόσου (p=0.038), στη συχνότητα της υποομάδας ολιγοαρθρικής έναρξης (p=0.004) της νόσου και στην ανάπτυξη ιριδοκυκλίτιδας (p=0.001). Συγκεκριμένα, στους ασθενείς με θετικά ανα η νόσος εκδηλώθηκε σε νεότερη ηλικία, προσέβαλλε κατά την έναρξη λιγότερες από 5 αρθρώσεις και στην πορεία αναπτύχθηκε συχνότερα ιριδοκυκλίτιδα (Σχήμα 58). τα χαρακτηριστικά των δύο ομάδων περιγράφονται στον πίνακα 95.
269 269 Πίνακας 95. Χαρακτηριστικά και έκβαση της νόσου των ασθενών με θετικά ή αρνητικά αντιπυρηνικά αντισώματα (ΑΝΑ) ΑΝΑ- θετικοί ασθενείς ΑΝΑ-αρνητικοί ασθενείς N=33 N=66 p θήλυ φύλο, αρ. (%) 26 (78.8) 45 (68.2) ηλικία έναρξης της νόσου, έτη a 6.4± ± διάρκεια νόσου, έτη a 18.6±6.8 17± Oλιγοαρθρικής έναρξης νόσος, αρ. (%) 16 (48.5) 13 (19.7) ιριδοκυκλίτιδα, αρ. (%) 9 (27.3) 2 (3) Aναλογία διάρκειας ενεργότητας νόσου/ διάρκεια νόσου, (%) a 54.0± ± επίτευξη κλινικής ύφεσης τα 2 πρώτα έτη από τη διάγνωση της νόσου, αρ (%) 11 (33.3) 27 (40.9) επίτευξη 1 επεισόδιο κλινικής ύφεσης εκτός θεραπείας, αρ.(%) 11/32 (34.4) 26/63 (41.3) Ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας/ διάρκεια νόσου, (%) a 12.9± ± διάρκεια ενεργότητας τα πρώτα 5 έτη, μήνες a 33.6± ± RF θετικός, αρ. (%) 5 (15.2) 7 (10.6) Anti-CCP θετικά, αρ. (%) 4/22 (18.2) 7/56 (12.5) ατα θετικά, αρ. (%) 2/21 (9.5) 3/45 (6.7) 1 Oικογενειακό ιστορικό αρθρίτιδας θετικό, αρ. (%) 7 (21.2) 11/65 (16.9) Πολυαρθρική πορεία, αρ. (%) 27 (81.8) 54 (81.8) 1 ιστορικό ιερολαγονίτιδας, αρ. (%) 2 (6) 9 (13.6) Προσβολή του ισχίου, αρ. (%) 10 (30.3) 33 (50) 0.099
270 270 Πίνακας 95. (συνέχεια). ΑΝΑ- θετικοί ασθενείς ΑΝΑ-αρνητικοί ασθενείς N=33 N=66 p Παρουσία συνοδού αυτοάνοσου νοσήματος, αρ. (%) 7 (21.2) 8 (12.1) ενεργότητα νόσου στην τελευταία επίσκεψη παρακολούθησης, αρ. (%) 19 (57.6) 31 (47) DAS28 a 2.9± ± CRP, mg/l a 7.4± ± τκε, mm/h a 22.1± ± διάρκεια πρωινής δυσκαμψίας, λεπτά a 27.3± ± EGA (VAS 0-10) a 23.1± ± PGA (VAS 0-10) a 20.1± ± haq-di a 0.24± ± JADi-A a 13.9± ± JADi-E a 1.3±1.5 1± TmSvdhS a 154.4± ± ασυμμετρία γνάθου/μικρογναθία, αρ. (%) 16 (48.5) 20 (30.3) GhQ28 case scorea 2.59± ± ιστορικό αγωγής με inh-tnf παράγοντα, αρ. (%) 18 (54.5) 31 (47.7) τρέχουσα αγωγή με βιολογικό παράγοντα, αρ. (%) 13 (39.4) 26 (39.4) 1 τρέχουσα αγωγή με inh-tnf παράγοντα, αρ. (%) 13 (39.4) 23 (34.8) διάρκεια θεραπείας με κορτικοειδή, έτη a 7.7± ± τρέχουσα αγωγή με κορτικοστεροειδή, αρ. (%) 7 (21.2) 9 (13.6) a μέση τιμή±τυπική απόκλιση
271 271 Σχήμα 58. Σύγκριση των ασθενών με θετικό τίτλο ΑΝΑ έναντι αυτών με αρνητικό τίτλο ΑΝΑ ως προς Α. την ηλικία έναρξης της νόσου Β. την παρουσία ιστορικού ιριδοκυκλίτιδας και Γ. την ολιγοαρθρικής έναρξης νόσο.
272 Χαρακτηριστικά, πορεία και έκβαση της νόσου στους ασθενείς με θετικά και αρνητικά αντισώματα έναντι κυκλικών κιτρουλλινιωμένων πεπτιδίων (anti-cyclic Citrullinated Peptides antibodies, anti-ccp antibodies) O έλεγχος των anti-ccp αντισωμάτων πραγματοποιήθηκε σε 81 ασθενείς από τους οποίους στους 11 ανιχνεύθηκε θετικός τίτλος. Παρά το μικρό αριθμό του δείγματος, οι ασθενείς που βρέθηκαν θετικοί, είχαν συχνότερα θετικό και τον ρευματοειδή παράγοντα, σε επίπεδο στατιστικής σημαντικότητας p< Όπως αναμενόταν, θετικός τίτλος anti-ccp αντισωμάτων ανιχνεύτηκε σε σημαντικά μεγαλύτερο ποσοστό στους ασθενείς που ανήκαν στην υποομάδα της πολυαρθρίτιδας με θετικό ρευματοειδή παράγοντα (57.1%), ποσοστό που διέφερε στατιστικώς σημαντικά από αυτό που βρέθηκε στο σύνολο των λοιπών υποομάδων (9.5%) (p=0.006). ωστόσο, δε διαπιστώθηκαν άλλες διαφορές μεταξύ των δύο ομάδων, αυτών δηλαδή με θετικά και αυτών με αρνητικά anti-ccp αντισώματα, παρά μόνο μεγαλύτερη συχνότητα χρήσης συστηματικών κορτικοστεροειδών (p=0.035) και διαφορετικών μη βιολογικών DMARDS (p=0.011), καθώς επίσης και μακρύτερη διάρκεια συνδυασμένης θεραπείας με inh-tnf παράγοντα στην ομάδα των ασθενών με θετικά anti-ccp αντισώματα (p=0.020). τα χαρακτηριστικά, η πορεία και η έκβαση της νόσου, όπως καταγράφηκε με τα διάφορα εργαλεία εκτίμησης, στους ασθενείς με θετικά και αρνητικά anti-ccp αντισώματα περιγράφονται στον πίνακα 96. το ύψος των anti-ccp αντισωμάτων στον ορό των ασθενών δε συσχετίστηκε σημαντικά με κάποια από τις παραμέτρους έκβασης της νόσου (συνολικό τροποποιημένο Svdh σκορ p=0.767, επιμέρους Svdh που μετρά τις διαβρώσεις p=0.630, επιμέρους Svdh που μετρά τη στένωση του μεσάρθριου διαστήματος p=0.996, JADi-A p=0.508, JADi-E p=0.412, haq-di p=0.323, ποσοστό ενεργότητας στη διάρκεια της νόσου p=0.954), ούτε με την παρουσία ενεργότητας p=0.220 και το δείκτη DAS28 p=0.278 στην τελευταία επίσκεψη. αντίθετα, εντύπωση προκαλεί η ανεύρεση πολύ ισχυρής θετικής συσχέτισης ανάμεσα στο επίπεδο των anti-ccp αντισωμάτων και στο βαθμό ψυχολογικής επιβάρυνσης, σύμφωνα με το ερωτηματολόγιο GhQ28 (r=0.859, p=0.001), το οποίο, όπως έχει αναφερθεί, συμπληρώθηκε στην τελευταία επίσκεψη παρακολούθησης, όταν έγινε και η μέτρηση των anti-ccp αντισωμάτων στον ορό.
273 273 Πίνακας 96. Χαρακτηριστικά, πορεία και έκβαση της νόσου στους ασθενείς με θετικό και αρνητικό τίτλο αντισωμάτων έναντι κυκλικών κιτρουλλινοποιημένων πεπτιδίων (anti-cyclic Citrullinated Peptides antibodies, anti-ccp) Ασθενείς με θετικά Aσθενείς με αρνητικά anti-ccp anti-ccp N=11 N=70 θήλυ φύλο, αρ. (%) 7 (63.6) 44 (62.8) 1 ηλικία έναρξης της νόσου, έτη a 8.1± ± διάρκεια νόσου, έτη a 18± ± Πολυαρθρικής έναρξης νόσος 6 (54.5) 15 (21.4) ιριδοκυκλίτιδα, αρ. (%) 1 (9) 6 (8.6) 1 Ποσοστό διάρκειας ενεργότητας /διάρκεια νόσου, (%) a 62.6± ± επίτευξη κλινικής ύφεσης τα 2 πρώτα έτη από τη διάγνωση της νόσου, αρ (%) 2 (18.2) 32 (45.7) επίτευξη 1 επεισόδιο κλινικής ύφεσης εκτός θεραπείας, αρ. (%) 4 (36.4) 28/66 (42.4) Ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας/ διάρκεια νόσου, (%) a 17.1± ± διάρκεια ενεργότητας τα πρώτα 5 έτη, μήνες a 40.8± ± RF θετικός, αρ. (%) 5 (45.5) 3 (4.3) <0.001 ανα θετικά, αρ. (%) 4 (36.4) 18 (25.7) ατα θετικά, αρ. (%) 1 (10) 4/55 (7.3) 1 Oικογενειακό ιστορικό αρθρίτιδας θετικό, αρ. (%) 1(9) 14/69 (20.3) Πολυαρθρική πορεία, αρ. (%) 9 (81.8) 56 (80) 1 p
274 274 Πίνακας 96. (συνέχεια) Ασθενείς με θετικά Aσθενείς με αρνητικά anti-ccp anti-ccp N=11 N=70 BMi a 22.3± ± Ύψος, εκατοστά a 169.4± ± Προσβολή του ισχίου, αρ. (%) 4 (36.4) 30 (42.8) Παρουσία συνοδού αυτοάνοσου νοσήματος, αρ. (%) 1 (9) 11 (15.7) ενεργότητα νόσου στην τελευταία επίσκεψη παρακολούθησης, αρ. (%) 6 (54.5) 35 (50) 1 DAS28 a 2.9± ± CRP, mg/l a 5.6± ± τκε, mm/h a 19.6± ± διάρκεια πρωινής δυσκαμψίας, λεπτά a 20.5± ± EGA (VAS 0-10) a 2± ± PGA (VAS 0-10) a 1.8± ± haq-di a 0.2 ± ± JADi-A a 12.7± ± JADi-E a 0.9±1.5 1± TmSvdhS a 172.2± ± msvdhs-erosions a 104.5± ± msvdhs-jsn a 67.7± ± ασυμμετρία γνάθου/μικρογναθία, αρ. (%) 3 (27.3) 24 (34.3) p
275 275 Πίνακας 96. (συνέχεια) Ασθενείς με θετικά Aσθενείς με αρνητικά anti-ccp anti-ccp N=11 N=70 GhQ28 a 3.3± ± καπνιστές/πρώην καπνιστές, αρ. (%) 4 (36.4) 31 (44.3) θεραπεία με inh-tnf παράγοντα κατά τη διάρκεια της νόσου, αρ. (%) 6 (54.5) 31 (44.3) αριθμός διαφορετικών inhtnfα που χορηγήθηκαν a 1.8± ± τρέχουσα αγωγή με βιολογικό παράγοντα, αρ. (%) 5 (45.5) 23 (32.8) διάρκεια συνδυασμένης θεραπείας με inh-tnf παράγοντα, μήνες a 74± ± ιστορικό αγωγής με κορτικοειδή, αρ. (%) 11 (100) 44 (62.9) διάρκεια θεραπείας με κορτικοειδή, έτη a 6.5± ± τρέχουσα αγωγή με κορτικοστεροειδή, αρ. (%) 1 (9) 14 (20) αριθμός διαφορετικών μη-βιολογικών DMARDS που έχουν χρησιμοποιηθεί a 3.3± ± a μέση τιμή±τυπική απόκλιση p
276 Χαρακτηριστικά, πορεία και έκβαση της νόσου στους ασθενείς που ανέπτυξαν ιερολαγονίτιδα Oι ασθενείς που εμφάνισαν προσβολή ιερολαγονίτιδας κατά τη διάρκεια της νόσου, όπως αναφέρθηκε σε προηγούμενη ενότητα, ήταν συνολικά 12, 8 άνδρες (66.7%) και 4 γυναίκες (33.3%), διαφορά που βρέθηκε στατιστικώς σημαντική (p=0.007). Oι 11 από τους 12 ασθενείς με ιερολαγονίτιδα κατατάσσονταν στην υποομάδα της αρθρίτιδας που σχετίζεται με ενθεσίτιδα και ο ένας έπασχε από ψωριασική αρθρίτιδα. η παρουσία ιερολαγονίτιδας συσχετίστηκε ισχυρά με την υποομάδα της αρθρίτιδας που σχετίζεται με ενθεσίτιδα σε επίπεδο σημαντικότητας p< ωστόσο, 7 από τους 18 ασθενείς με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα (38.9%) δεν είχαν αναπτύξει ιερολαγονίτιδα στον ακτινολογικό έλεγχο. Συνοπτικά, οι ασθενείς που ανέπτυξαν ιερολαγονίτιδα ήταν, κυρίως, άνδρες (p=0.007), ταξινομούνταν στην υποομάδα της αρθρίτιδας σχετιζόμενης με ενθεσίτιδα (p<0.001), ήταν μεγαλύτεροι σε ηλικία κατά την έναρξη της νόσου (p=0.001) και παρουσίαζαν συχνότερα οικογενειακό ιστορικό αρθρίτιδας (p=0.023). δε διέφεραν σημαντικά σε κάποια από τις παραμέτρους έκβασης της νόσου, παρά μόνο στο τελικό ανάστημα που βρέθηκε υψηλότερο στους ασθενείς με ιερολαγονίτιδα (p=0.014), αποτέλεσμα ίσως της μεγαλύτερης συχνότητας ιερολαγονίτιδας στους άνδρες. τα κύρια χαρακτηριστικά, η πορεία και η έκβαση της νόσου, όπως εκτιμήθηκε με τα διάφορα εργαλεία, στους ασθενείς με και χωρίς ιερολαγονίτιδα περιγράφονται στον πίνακα 97.
277 277 Πίνακας 97. Χαρακτηριστικά, πορεία και έκβαση της νόσου στους ασθενείς με και χωρίς ιερολαγονίτιδα Ασθενείς με Aσθενείς χωρίς ιερολαγονίτιδα ιερολαγονίτιδα p N=12 N=90 Άρρεν φύλο, αρ.(%) 8 (66.7) 4 (33.3) ηλικία έναρξης της νόσου, έτη a 11.3± ± διάρκεια νόσου, έτη a 11.7±5.8 18± αρθρίτιδα που σχετίζεται με ενθεσίτιδα αρ. (%) 11 (91.7) 7 (7.8) <0.001 ιριδοκυκλίτιδα, αρ. (%) 0 (0) 11 (12.2) Ποσοστό διάρκειας ενεργότητας /διάρκεια νόσου, (%) a 57.2± ± επίτευξη 1 επεισόδιο κλινικής ύφεσης εκτός θεραπείας, αρ. (%) 3 (27.3) 34/87 (39.1) Ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας/διάρκεια νόσου, (%) a 8.9± ± διάρκεια ενεργότητας τα πρώτα 5 έτη, μήνες a 31.2± ± RF θετικός, αρ. (%) 0 (0) 12 (13.3) Anti-CCP θετικά, αρ.(%) 0/9 (0) 11/72 (15.3) ανα θετικά, αρ. (%) 2/11 (18.2) 31/88 (35.2) Oικογενειακό ιστορικό αρθρίτιδας θετικό, αρ. (%) 6/12(50) 15/90 (16.7) Πολυαρθρική πορεία, αρ. (%) 11 (91.7) 73 (81.1) Ύψος, εκατοστά a 174.8± ± Προσβολή του ισχίου, αρ.(%) 8(66.7) 37(41.1) Παρουσία συνυπάρχοντος αυτοάνοσου νοσήματος, αρ. (%) 0(0) 15 (16.7) ενεργότητα νόσου στην τελευταία επίσκεψη παρακολούθησης, αρ. (%) 8 (66.7) 45 (50) 0.437
278 278 Πίνακας 97. (συνέχεια) Ασθενείς με Aσθενείς χωρίς ιερολαγονίτιδα ιερολαγονίτιδα p N=12 N=90 DAS28 a 2.5± ± CRP, mg/l a 14.2± ± τκε, mm/h 23.2± ± διάρκεια πρωινής δυσκαμψίας, λεπτά a 37.5± ± EGA (VAS 0-10) a 2.6± ± PGA (VAS 0-10) a 2.5± ± haq-di a 0.51± ± JADi-A a 11.3± ± JADi-E a 0.92± ± TmSvdhS a 111.6± ± ασυμμετρία γνάθου/μικρογναθία, αρ. (%) 2/12(16.7) 35/90(38.9) GhQ28 score a 3.9± ± ιστορικό αγωγής με inh-tnf παράγοντα, αρ. (%) 7 (58.3) 44 (48.9) διάρκεια θεραπείας με inh-tnf, μήνες a 21.3± ± τρέχουσα αγωγή με inh-tnf παράγοντα, αρ. (%) 7 (58.3) 31 (34.4) ιστορικό αγωγής με κορτικοειδή, αρ.(%) 6 (50) 65 (72.2) διάρκεια θεραπείας με κορτικοειδή, έτη a 3.9± ± τρέχουσα αγωγή με κορτικοστεροειδή, αρ. (%) 0(0) 18 (20) αριθμός διαφορετικών μη βιολογικών DMARDS που έχουν χορηγηθεί a 1.7± ± a μέση τιμή±τυπική απόκλιση
279 4.14 Μακροχρόνια έκβαση της Νεανικής Ιδιοπαθούς Αρθρίτιδας στους ασθενείς με διάγνωση νόσου πριν και μετά το Oι ασθενείς με νεανική ιδιοπαθή αρθρίτιδα που διαγνώσθηκαν μετά το έτος 2000 βρέθηκαν ότι ήταν συνολικά είκοσι οχτώ. Oι παραπάνω ασθενείς δε διέφεραν σημαντικά στα δημογραφικά χαρακτηριστικά και στους παράγοντες κινδύνου με τους υπόλοιπους 74 ασθενείς που διαγνώσθηκαν πριν το έτος Oι 6 ασθενείς που διαγνώσθηκαν κατά τα έτη 1999 και 2000 υπολογίστηκαν στην ομάδα των ασθενών που διαγνώσθηκαν μετά το 2000 για το λόγο ότι οι στρατηγικές θεραπείας που ακολουθήθηκαν σε αυτούς ήταν περισσότερο συμβατές με αυτές που ακολουθούνται μετά το Συγκεκριμένα, οι δύο ομάδες δε διέφεραν ως προς το φύλο (p=1), την υποομάδα έναρξης της νόσου (p=0.211), την παρουσία θετικού ρευματοειδή παράγοντα (RF) (p=1) και θετικού τίτλου anti-ccp αντισωμάτων (p=0.584). αντίθετα, διέφεραν στη διάρκεια νόσου (p<0.001). η ομάδα των ασθενών, στους οποίους η διάγνωση της νόσου έπεται το έτος 2000, βρέθηκε ότι είχε ευνοϊκότερη έκβαση σε βάθος χρόνου, που αφορούσε στην αρθρική και εξωαρθρική καταστροφή, στις ακτινολογικές βλάβες και στον αριθμό των χειρουργικών επεμβάσεων που πραγματοποιήθηκαν (Πίνακας 98, Σχήματα 59,61). η σωματική λειτουργική ικανότητα των ασθενών δε φάνηκε να διαφέρει μεταξύ των δύο ομάδων (p=0.553) (Σχήμα 60). Σημαντική, επίσης, για την ίδια ομάδα ασθενών είναι η εμφάνιση μικρότερου διαστήματος ενεργότητας νόσου τα πρώτα 5 έτη από τη διάγνωση (p=0.02) (Πίνακας 98, Σχήμα 62). αξίζει, επίσης, να σημειωθεί ότι οι ασθενείς που διαγνώσθηκαν πριν το 2000, χρειάστηκε να λάβουν συστηματικά κορτικοστεροειδή για μακρύτερα χρονικά διαστήματα (p<0.001), καθώς και να αλλάξουν περισσότερα διαφορετικά μη βιολογικά DMARDS (p<0.001) (Πίνακας 98, Σχήμα 63). αναλυτικά, τα χαρακτηριστικά, η πορεία και η μακροχρόνια έκβαση των δύο ομάδων, με διάγνωση πριν και μετά το έτος 2000 περιγράφονται στον πίνακα 98.
280 280 Πίνακας 98. Χαρακτηριστικά, πορεία και μακροχρόνια έκβαση της νόσου στους ασθενείς με διάγνωση Νεανικής Ιδιοπαθούς Αρθρίτιδας πριν και μετά το έτος 2000 Ασθενείς με διάγνωση Ασθενείς με διάγνωση της ΝΙΑ μετά το έτος 2000 της ΝΙΑ πριν το έτος 2000 p N=28 N=74 ηλικία έναρξης της νόσου, έτη a 10.9± ±3.9 <0.001 διάρκεια νόσου, έτη a 8.9± ±4.8 <0.001 ιριδοκυκλίτιδα, αρ. (%) 0(0) 11 (14.9) διάρκεια ενεργότητας νόσου, έτη a 4.4± ±6.6 <0.001 επίτευξη κλινικής ύφεσης τα 2 πρώτα έτη από τη διάγνωση της νόσου, αρ (%) 14(50) 26 (35.1) Ποσοστό διάρκειας ενεργότητας /διάρκεια νόσου, (%) a 49± ± διάρκεια ενεργότητας τα πρώτα 5 έτη, μήνες a 29.7± ± επίτευξη κλινικής ύφεσης με φα κατά τη διάρκεια της νόσου, αρ. (%) 25 (92.6) 62 (87.3) επίτευξη κλινικής ύφεσης χωρίς φα κατά τη διάρκεια της νόσου, αρ. (%) 9 (33.3) 28 (39.4) Ποσοστό διάρκειας κλινικής ύφεσης χωρίς θεραπεία/διάρκεια νόσου, (%) a 13.3± ± RF θετικός, αρ. (%) 3 (10.7) 9 (12.1) 1 ανα θετικά, αρ.(%) 7/26 (26.9) 26/73 (35.6) τίτλος anti-ccp θετικός, αρ. (%) 1 (6.3) 10 (15.4) Oικογενειακό ιστορικό αρθρίτιδας θετικό, αρ. (%) 9/27 (33.3) 12 (16.2) Πολυαρθρική πορεία, αρ.(%) 25 (89.3) 59 (79.7) τελικό ύψος, εκατοστά a 164.4± ± Προσβολή του ισχίου, αρ. (%) 14 (50) 31 (41.9) Παρουσία συνοδού αυτοάνοσου νοσήματος, αρ. (%) 5 (17.9) 10 (13.5) ενεργότητα νόσου στην τελευταία επίσκεψη παρακολούθησης, αρ. (%) 15 (53.6) 38 (51.3) 1 DAS28 a 2.5± ±
281 281 Πίνακας 98. (συνέχεια) Ασθενείς με διάγνωση Ασθενείς με διάγνωση της ΝΙΑ μετά το έτος 2000 της ΝΙΑ πριν το έτος 2000 Ρ N=28 N=74 CRP, mg/l a 7.8± ± τκε, mm/h a 20.8± ± διάρκεια πρωινής δυσκαμψίας, λεπτά a 24.5± ± EGA (VAS 0-10) a 1.6± ± PGA (VAS 0-10) a 15.3± ± haq-di a 0.3 ± ± JADi-A a 6.9± ±19.9 <0.001 JADi-E a 0.6± ± TmSvdhS 83.6± ±149 <0.001 msvdhs-erosions a 45.6± ±96 <0.001 msvdhs-jsn a 37.7± ±55 <0.001 ασυμμετρία γνάθου/μικρογναθία, αρ.(%) 9 (32.1) 28 (37.8) GhQ28 a 3.5± ± αριθμός χειρουργικών επεμβάσεων στις αρθρώσεις a ± θεραπεία με inh-tnf παράγοντα κατά τη διάρκεια της νόσου, αρ. (%) 13 (46.4) 39 (52.7) τρέχουσα αγωγή με βιολογικό παράγοντα, αρ. (%) 11 (39.3) 31 (41.9) ιστορικό αγωγής με κορτικοστεροειδή, αρ. (%) 18 (64.3) 53 (71.6) τρέχουσα αγωγή με κορτικοστεροειδή, αρ. (%) 3 (10.7) 15 (20.3) διάρκεια θεραπείας με κορτικοστεροειδή, μήνες a 31.2± ±69 <0.001 αριθμός διαφορετικών μη-βιολογικών DMARD που έχουν χρησιμοποιηθεί a 1.6± ±1.2 <0.001 αριθμός διαφορετικών inh-tnf που έχουν χρησιμοποιηθεί a 1.2± ± a μέση τιμή±τυπική απόκλιση
282 282 Σχήμα 59. Σύγκριση των ασθενών με διάγνωση νόσου πριν και μετά το έτος 2000 ως προς τον τελικό βαθμό ακτινολογικής βλάβης (Συνολικό τροποποιημένο Sharp van der Heijde σκορ) στην τελευταία επίσκεψη. Σχήμα 60. Σύγκριση των ασθενών με διάγνωση νόσου πριν και μετά το έτος 2000 ως προς το βαθμό σωματικής λειτουργικής ικανότητας (HAQ-DI) στην τελευταία επίσκεψη.
283 283 Σχήμα 61. Σύγκριση των ασθενών με διάγνωση νόσου πριν και μετά το έτος 2000 ως προς τον τελικό βαθμό Α. αρθρικής καταστροφής(jadi-a) και Β. εξωαρθρικής καταστροφής (JADI-E) στην τελευταία επίσκεψη.
284 284 Σχήμα 62. Διάρκεια (σε μήνες) ενεργότητας τα πρώτα 5 έτη από την έναρξη της νόσου στους ασθενείς με διάγνωση νόσου πριν και μετά το έτος Σχήμα 63. Διάρκεια (σε μήνες) συνολικής θεραπείας με κορτικοστεροειδή στους ασθενείς με διάγνωση νόσου πριν και μετά το έτος 2000.
285 Διαφορά στη μακροχρόνια έκβαση της Νεανικής Ιδιοπαθούς Αρθρίτιδας μεταξύ των ασθενών που έλαβαν βιολογική θεραπεία και είχαν διάγνωση της νόσου μετά το έτος 2000 και αυτών που έλα βαν βιολογική θεραπεία και είχαν διάγνωση της νόσου πριν το έτος 2000 βιολογική θεραπεία, όπως έχει περιγραφεί σε προηγούμενη ενότητα, χορηγήθηκε συνολικά σε 52 από τους 102 ασθενείς της μελέτης. από αυτούς οι 13 διαγνώσθηκαν μετά το έτος 2000 και είχαν τη δυνατότητα έγκαιρης έναρξης βιολογικής θεραπείας και οι 39 διαγνώσθηκαν πριν το έτος 2000 και δεν είχαν τη δυνατότητα αντίστοιχης πρόσβασης. O όρος «έγκαιρη» δεν ταυτίζεται με τον όρο «πρώιμη» πρόσβαση σε βιολογική θεραπεία, δηλαδή, σε χρονικό διάστημα μικρότερο ή ίσο των 2 ετών από την έναρξη της νόσου. Όπως τονίστηκε και προηγουμένως, από τους 13 ασθενείς ένας μόνο έλαβε βιολογικό παράγοντα μέσα στα πρώτα 2 έτη της νόσου, έλαβε δηλαδή πρώιμα θεραπεία με βιολογικό παράγοντα. Oι 3 ασθενείς που διαγνώσθηκαν κατά τα έτη 1999 και 2000 υπολογίστηκαν στην ομάδα των ασθενών που διαγνώσθηκαν μετά το 2000 για το λόγο ότι οι στρατηγικές θεραπείας που ακολουθήθηκαν σε αυτούς ήταν περισσότερο συμβατές με αυτές που ακολουθούνται μετά το Oι παραπάνω ασθενείς δε διέφεραν σημαντικά στα δημογραφικά χαρακτηριστικά και στους παράγοντες κινδύνου με τους υπόλοιπους 39 ασθενείς που δεν έτυχαν αντίστοιχης πρόσβασης. Συγκεκριμένα, οι δύο ομάδες δεν διέφεραν ως προς το φύλο (p=0.579), την υποομάδα έναρξης της νόσου (p=0.206), την παρουσία θετικού ρευματοειδή παράγοντα (RF) (p=832) και θετικού τίτλου anti-ccp αντισωμάτων (p=1). αντίθετα, διέφεραν στη ηλικία έναρξης της νόσου (p<0.001) και όπως ήταν αναμενόμενο στη διάρκεια νόσου (p<0.001). η ομάδα των ασθενών, που είχε πρόσβαση σε βιολογική θεραπεία έγκαιρα μετά την έναρξη της νόσου, βρέθηκε ότι είχε ευνοϊκότερη έκβαση σε βάθος χρόνου, που αφορούσε στην αρθρική και εξωαρθρική καταστροφή, στις ακτινολογικές βλάβες, στον αριθμό των χειρουργικών επεμβάσεων που πραγματοποιήθηκαν και στη φυσική λειτουργική ικανότητα που παρουσίαζαν στην τελευταία επίσκεψη παρακολούθησης (πίνακας 99, Σχήματα 64-66). ωστόσο, η μέση τιμή του ποσοστού της συνολικής διάρκειας με ενεργότητα προς τη συνολική διάρκεια νόσου διέφερε μεν, αλλά όχι σημαντικά μεταξύ των δύο ομάδων (p=0.065) και συγκεκριμένα, οι ασθενείς που είχαν έγκαιρη πρόσβαση περνούσαν μακρύτερα διαστήματα χωρίς ενεργότητα στην πορεία της νόσου τους. Σημαντική είναι η διαπίστωση ότι στην ομάδα των ασθενών αυτών χρειάστηκε χορήγηση κορτικοειδών για βραχύτερο χρονικό διάστημα (p<0.001). αναλυτικά, τα χαρακτηριστικά, η πορεία και η μακροχρόνια έκβαση των δύο ομάδων που έλαβαν βιολογική θεραπεία, με και χωρίς έγκαιρη πρόσβαση σε αυτή, περιγράφονται στον πίνακα 99.
286 286 Πίνακας 99. Χαρακτηριστικά, πορεία και μακροχρόνια έκβαση της νόσου στους ασθενείς που έλαβαν βιολογική θεραπεία, χωρισμένοι σε δύο ομάδες ανάλογα με το αν η διάγνωσή τους προηγείται ή έπεται του έτους Ασθενείς με διάγνωση νόσου Ασθενείς με διάγνωση μετά το 2000 που έχουν πριν το 2000 που έχουν p λάβει βιολογική θεραπεία λάβει βιολογική θεραπεία N=13 N=39 θήλυ φύλο, αρ. 11 (84.6) 28 (71.8) ηλικία έναρξης της νόσου, έτη a 12.1± ±3.9 <0.001 διάρκεια νόσου, έτη a 8.4± ±5.1 <0.001 ιριδοκυκλίτιδα, αρ. (%) 0(0) 7 (17.9) Ποσοστό διάρκειας ενεργότητας /διάρκεια νόσου, (%) a 52.4± ± διάρκεια ενεργότητας τα πρώτα 5 έτη, μήνες a 34.3± ± επίτευξη κλινικής ύφεσης χωρίς φα τα πρώτα 5 έτη, αρ. (%) 2 (16.7) 0(0) 0.08 επίτευξη κλινικής ύφεσης με φα κατά τη διάρκεια της νόσου, αρ. (%) 12 (100) 36 (94.7) 1.00 επίτευξη κλινικής ύφεσης χωρίς φα κατά τη διάρκεια της νόσου, αρ. (%) 2 (16.7) 5(13.5) 1.00 Ποσοστό διάρκειας κλινικής ύφεσης εκτός θεραπείας/διάρκεια νόσου, (%) a 2.5± ± RF θετικός, αρ. (%) 3/13 (23) 6/39 (15.4) ανα θετικά, αρ. (%) 3 (25) 16 (42.1) τίτλος anti-ccp θετικός, αρ. (%) 1/7 (14.3) 5/31 (16.1) ιστορικό ιερολαγονίτιδας, αρ. (%) 3 (23.1) 4 (10.3) Oικογενειακό ιστορικό αρθρίτιδας θετικό, αρ. (%) 5 (38.5) 8(20.5) Πολυαρθρική πορεία, αρ. (%) 12 (92.3) 35 (89.7) τελικό ύψος, εκατοστά a 163.7± ±
287 287 Πίνακας 99. (συνέχεια) Ασθενείς με διάγνωση νόσου Ασθενείς με διάγνωση μετά το 2000 που έχουν πριν το 2000 που έχουν p λάβει βιολογική θεραπεία λάβει βιολογική θεραπεία N=13 N=39 Body Mass index (BMi) a 21.9±2 22.3± Προσβολή του ισχίου, αρ. (%) 7 (53.8) 21 (53.8) Παρουσία συνοδού αυτοάνοσου νοσήματος, αρ. (%) 1 (7.7) 6 (15.3) ενεργότητα νόσου στην τελευταία επίσκεψη παρακολούθησης, αρ. (%) 8 (61.5) 26 (66.7) κλινική ύφεση χωρίς φα στην τελευταία επίσκεψη παρακολούθησης, αρ. (%) 1(7.7) DAS28 a 2.6± ± CRP, mg/l a 4.8± ± τκε, mm/h a 20.2± ± διάρκεια πρωινής δυσκαμψίας, λεπτά a 23.5± ± EGA (VAS 0-10) a 1.6±1.7 3± PGA (VAS 0-10) a 1.4± ± haq-di a 0.1 ± ± JADi-A a 5.8±7 21.5±20.6 <0.001 JADi-E a 0.6± ± TmSvdhS a 101.4± ± msvdhs-erosions a 55± ±96.7 <0.001 msvdhs-jsn a 45.8± ± ασυμμετρία γνάθου/μικρογναθία, αρ. (%) 4 (30.8) 18 (46.2) 0.517
288 288 Πίνακας 99. (συνέχεια) Ασθενείς με διάγνωση νόσου Ασθενείς με διάγνωση μετά το 2000 που έχουν πριν το 2000 που έχουν p λάβει βιολογική θεραπεία λάβει βιολογική θεραπεία N=13 N=39 GhQ28 a 4±5 3.1± αριθμός χειρουργικών επεμβάσεων στις αρθρώσεις a ± τρέχουσα αγωγή με βιολογικό παράγοντα, αρ. (%) 10 (76.9) 31 (79.5) 1.00 ιστορικό αγωγής με κορτικοστεροειδή, αρ. (%) 10 (76.9) 36 (92.3) τρέχουσα αγωγή με κορτικοστεροειδή, αρ. (%) 2 (15.4) 13 (33.3) διάρκεια θεραπείας με κορτικοστεροειδή, μήνες a 37.1± ±62.5 <0.001 αριθμός διαφορετικών μη-βιολογικών DMARDS που έχουν χρησιμοποιηθεί a 1.7± ± αριθμός διαφορετικών inh-tnf που έχουν χρησιμοποιηθεί a 1.2± ± a μέση τιμή±τυπική απόκλιση
289 289 Σχήμα 64. Σύγκριση των ασθενών που έλαβαν βιολογική θεραπεία και είχαν διάγνωση νόσου πριν ή μετά το έτος 2000 ως προς τον τελικό βαθμό ακτινολογικής βλάβης (συνολικό τροποποιημένο Sharp van der Heijde σκορ) στην τελευταία επίσκεψη. Σχήμα 65. Σύγκριση των ασθενών που έλαβαν βιολογική θεραπεία με διάγνωση νόσου πριν ή μετά το έτος 2000 ως προς το βαθμό σωματικής λειτουργικής ικανότητας (HAQ-DI) στην τελευταία επίσκεψη.
290 290 Σχήμα 66. Σύγκριση των ασθενών που έλαβαν βιολογική θεραπεία με διάγνωση νόσου πριν ή μετά το έτος 2000 ως προς τον τελικό βαθμό Α. αρθρικής καταστροφής(jadi- A) και Β. εξωαρθρικής καταστροφής (JADI-E) στην τελευταία επίσκεψη.
291 4.16 Γενετικές συσχετίσεις HLA συσχετίσεις 291 τα hla γονίδια εντοπίζονται σε μια περιοχή του γονιδιώματος που ονομάζεται μείζων σύμπλεγμα ιστοσυμβατότητας και βρίσκεται στο χρωμόσωμα 6p21.3. τα hla μόρια διαιρούνται στα hla τάξης ι (hla A,B και C) και στα hla τάξης ιι (hla DR, DQ και DP). τα hla αλλήλια των οποίων η συχνότητα καταγράφηκε από τους φακέλους παρακολούθησης των ασθενών ήταν τα παρακάτω: HLA-A2, HLA-A23/24 (A9), HLA-B27, HLA-B35, HLA-DRB1*01, HLA-DRB1*04, HLA-DRB1*11/12 (DR5), HLA-DRB1*13/14 (DR6) και HLA-DRB1*08. η επιλογή των παραπάνω αλληλίων έγινε εξαιτίας της ήδη υπάρχουσας στη διεθνή βιβλιογραφία συσχέτισής τους με συγκεκριμένες υποομάδες της νόσου. τα hla μόρια τάξης ii, DQ και DP, δε μελετήθηκαν, λόγω του μικρού αριθμού ασθενών στους οποίους είχαν ελεγχθεί. Στον πίνακα 100 περιγράφονται οι συχνότητες των αλληλίων HLA-A2, HLA- A23/24 (A9), HLA-B27, HLA-B35, HLA-DRB1*01, HLA-DRB1*04, HLA-DRB1*11/12 (DR5), HLA-DRB1*13/14 (DR6), HLA-DRB1*08 στους ασθενείς της μελέτης συνολικά και ανά υποομάδα έναρξης της NiA. O έλεγχος για το αν οι συχνότητες των προαναφερθέντων αλληλίων διαφέρουν από τις αντίστοιχες που συναντώνται στο γενικό πληθυσμό έγινε χρησιμοποιώντας τη βάση δεδομένων που υπάρχει για τις συχνότητες των hla γονιδίων τάξης i και ii σε 500 υγιείς ενήλικες προερχόμενους από τη β. ελλάδα ( (εικόνα 10). η στατιστική ανάλυση έγινε με έλεγχο χ2 καλής προσαρμογής και χρησιμοποιήθηκε το Stata 11.0 Oι συχνότητες των αλληλίων HLA-Α2, HLA-A23/24 (Α9), HLA-B35, HLA- DRB1*01, HLA-DRB1*04, HLA-DRB1*13/14 (DR6) και HLA DRB1*08 βρέθηκε ότι δε διαφέρουν σημαντικά μεταξύ των ασθενών με NiA και αυτών του γενικού πληθυσμού της β.ελλάδας. αντιθέτως, τα αλλήλια HLA-B27 και HLA DRB1*11/12 (DR5) βρέθηκε ότι εκφράζονται σε σημαντικά μεγαλύτερη συχνότητα στους ασθενείς με NiA (p<0.001 και p= αντίστοιχα). κατόπιν, ακολούθησε σύγκριση της συχνότητας κάποιων αλληλίων, που έχουν βιβλιογραφικά γνωστή συσχέτιση με συγκεκριμένες υποομάδες της NiA, με τη συχνότητα που εμφανίζονται στις ίδιες υποομάδες έναρξης της νόσου στους ασθενείς της μελέτης. Παρά το μικρό μέγεθος του δείγματος, βρέθηκε ότι οι ασθενείς που ανήκουν στην υποομάδα της αρθρίτιδας που σχετίζεται με ενθεσίτιδα παρουσιάζουν, μεγαλύτερη συχνότητα φορείας του αλληλίου HLA-B27, σε σύγκριση με το γενικό πληθυσμό (p< ). h συχνότητα εμφάνισης του αλ-
292 292 ληλίου HLA-DRB1*04 βρέθηκε σημαντικά υψηλότερη στους ασθενείς με πολυαρθρίτιδα με θετικό RF (p=0.0436). η συχνότητα του αλληλίου HLA-A2 βρέθηκε σημαντικά υψηλότερη στους ασθενείς με ολιγοαρθρικής έναρξης NiA (p=0.0392), ενώ δε διαπιστώθηκε αντίστοιχη διαφορά στη συχνότητα του HLA-DRB1*08 μεταξύ των ίδιων ασθενών και του γενικού πληθυσμού (p=0.1641). Στη βιβλιογραφία το αλλήλιο HLA-DRB1*08 έχει συσχετιστεί με την ολιγοαρθρίτιδα που έχει έναρξη σε νεαρή ηλικία καθώς και με την πολυαρθρίτιδα με αρνητικό RF. Για το λόγο αυτό, ελέγχθηκε χωριστά το αλλήλιο HLA-DRB1*08 στην επεκταθείσα ολιγοαρθρίτιδα, που χαρακτηρίζεται από ολιγοαρθρική έναρξη και πολυαρθρική πορεία. διαπιστώθηκε μία τάση αυξημένης εμφάνισής του στην υποομάδα αυτή σε σύγκριση με το γενικό πληθυσμό (p=0.0532). το αλλήλιο HLA DRB1*11/12 (DR5), παρά τη συχνότερη εμφάνιση του στο συνολικό δείγμα ασθενών με NiA, δε συσχετίστηκε σημαντικά με κάποια από τις υποομάδες της νόσου.
293 293 Πίνακας 100. Συχνότητα των HLA αλληλίων τάξης Ι και τάξης ΙΙ στο συνολικό δείγμα ασθενών και στους ασθενείς ανά υποομάδα της ΝIA. Συνολικό Συστηματική Oλιγο- Oλιγο- Πολυ- Πολυ- Ψωριασική Αρθρίτιδα Αδιαφοροδείγμα Αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα αρθρίτιδα σχετιζόμενη ποίητη (Ν=102) (Ν=13) Εμμένουσα Επεκταθείσα RF αρνητική RF θετική Αρθρίτιδα με ενθεσίτιδα αρθρίτιδα (Ν=8) (Ν=22) (Ν=19) (Ν=11) (Ν=9) (Ν=18) (Ν=2) HLA A2 a (%) 43/140 (30.7) 4/16 (25) 5/13 (38.5) 14/36 (38.9) 5/26 (19.2) 4/13 (30.8) 4/11 (36.4) 7/25 (28) δε HLA A 23/24 (A9) a (%) 24/140(17.1) 4/16 (25) 1/13 (7.7) 4/36 (11.1) 10/26 (38.5) 1/13 (7.7) 1/11 (9.1) 3/25 (12) δε HLA B27 a (%) 15/142(10.6) 0/15 (0) 0/12 (0) 0/34 (0) 0/27 (0) 3/15 (20) 0/10 (0) 12/29 (41.4) δε HLA B35 a (%) 32/142 (22.5) 5/15 (33.3) 3/12 (25) 10/34 (29.4) 6/27 (22.2) 2/15 (20) 3/10 (30) 3/29 (10.3) δε HLA DRB1* 01 a (%) 12/130 (9.2) 1/11 (9.1) 0/13 (0) 4/33 (12.1) 2/27 (7.4) 1/15 (6.7) 1/11 (9.1) 3/20 (15) δε HLA DRB1* 04 a (%) 15/130 (11.5) 1/11 (9.1) 1/13 (7.7) 3/33 (9.1) 2/27 (7.4) 4/15 (26.7) 3/11 (27.3) 1/20 (5) δε HLA DRB1* 11/12 (DR5) a (%) 50/130 (38.5) 6/11 (54.5) 4/13 (30.8) 13/33 (39.4) 12/27 (44.4) 4/15 (26.7) 4/11 (36.4) 7/20 (35) δε HLA DRB1* 13/14 (DR6) a (%) 16/130 (12.3) 1/11 (9.1) 2/13 (15.4) 5/33 (15.2) 3/27 (11.1) 1/15 (6.7) 1/11 (9.1) 3/20 (15) δε HLA DRB1 * 08 a (%) 4/130 (3.1) 0/11 (0) 0/13 (0) 2/33 (6.1) 0/27 (0) 0/15 (0) 0/11 (0) 2/20 (10) δε a αριθμός θετικών/ συνολικό αριθμό αλληλίων που ελέχθησαν, ΔΕ= Δεν Ελέχθησαν HLA =Human Leukocyte Antigen
294 294 Εικόνα 10. Συχνότητα των HLA αλληλίων τάξης Ι και τάξης ΙΙ σε 500 υγιείς ενήλικες προερχόμενους από τη Β. Ελλάδα ( Από την εικόνα έχουν αφαιρεθεί τα αλλήλια που δε συμπεριλήφθηκαν στη μελέτη. Πίνακας 101. Συσχέτιση της συχνότητας των HLA αλληλίων τάξης Ι και τάξης ΙΙ μεταξύ του συνολικού δείγματος ασθενών με NIA και του υγιούς γενικού πληθυσμού της Βόρειας Ελλάδας Υγιής γενικός Συνολικό δείγμα πληθυσμός ασθενών με ΝΙΑ Β. Ελλάδος HLA alleles Ν = 102 Ν = 500 p HLA-A2 (n=140) HLA-A23/24 (Α9) (n=140) HLA-B27 (n=142) < HLA-B35 (n=142) HLA-DRB1*01 (n=130) HLA-DRB1*04 (n=130) HLA-DRB1*11/12 (DR5)(n=130) HLA-DRB1*08 (n=130) HLA-DRB1*13/14(DR6) (n=130)
295 Πίνακας 102. Σύγκριση της συχνότητας εμφάνισης των αλληλίων HLA-DRB1*04, HLA-DRB1*11/12, HLA-DRB1*08 μεταξύ των ασθενών του δείγματος με συστηματικής έναρξης NIA και του υγιούς γενικού πληθυσμού Β.Ελλάδας Συστηματικής Υγιής γενικός έναρξης πληθυσμός αρθρίτιδα Β. Ελλάδος HLA alleles Ν = 13 Ν = 500 p HLA-DRB1*04 (n=11) HLA-DRB1*11/12 (n=11) HLA-DRB1*08 (n=11) Πίνακας 103. Σύγκριση της συχνότητας εμφάνισης των αλληλίων HLA-DRB1*11/12, HLA-DRB1*08 μεταξύ των ασθενών του δείγματος με πολυαρθρίτιδα RF αρνητική και του υγιούς γενικού πληθυσμού Β.Ελλάδας Υγιής γενικός Πολυαρθρίτιδα πληθυσμός RF αρνητική Β. Ελλάδος HLA alleles Ν = 19 Ν = 500 p HLA-DRB1*11/12 (n=27) HLA-DRB1*08 (n=27) Πίνακας 104. Σύγκριση της συχνότητας εμφάνισης του αλληλίου HLA-DRB1*04 μεταξύ των ασθενών του δείγματος με πολυαρθρίτιδα RF θετική και του υγιούς γενικού πληθυσμού Β.Ελλάδας Υγιής γενικός Πολυαρθρίτιδα πληθυσμός RF θετική Β. Ελλάδος HLA allele Ν = 11 Ν = 500 p HLA-DRB1*04 (n=15)
296 296 Πίνακας 105. Σύγκριση της συχνότητας εμφάνισης του αλληλίου HLA-DRB1*11/12 (DR5) μεταξύ των ασθενών του δείγματος με ψωριασικη αρθρίτιδα και του υγιούς γενικού πληθυσμού Β. Ελλάδας Υγιής γενικός Ψωριασική πληθυσμός αρθρίτιδα Β. Ελλάδος HLA allele n = 9 n = 500 p HLA-DRB1*11/12 (DR5) (n=11) Πίνακας 106. Σύγκριση της συχνότητας εμφάνισης των αλληλίων HLA-Β27 και HLA- DRB1*01 μεταξύ των ασθενών του δείγματος με αρθρίτιδα σχετιζόμενη με ενθεσίτιδα και του υγιούς γενικού πληθυσμού Β.Ελλάδας Αρθρίτιδα Υγιής γενικός σχετιζόμενη με πληθυσμός ενθεσίτιδα Β. Ελλάδος HLA alleles Ν = 18 n = 500 p HLA-B27 (n=29) HLA-DRB1*01 (n=20) Πίνακας 107. Σύγκριση της συχνότητας εμφάνισης των αλληλίων HLA-Α2 και HLA- DRB1*08 μεταξύ των ασθενών του δείγματος με ολιγοαρθρικής έναρξης NIA και του υγιούς γενικού πληθυσμού Β.Ελλάδας Υγιής γενικός Oλιγοαρθρικής πληθυσμός έναρξης Β. Ελλάδος HLA allele Ν = 30 n = 500 p HLA A2 (n=46) HLA DRB1*08 (n=46)
297 Πίνακας 108. Σύγκριση της συχνότητας εμφάνισης του αλληλίου HLA-DRB1*08 μεταξύ των ασθενών του δείγματος με ολιγοαρθρίτιδα επεκταθείσα και του υγιούς γενικού πληθυσμού Β.Ελλάδας Υγιής γενικός Oλιγοαρθρίτιδα πληθυσμός επεκταθείσα Β. Ελλάδος HLA allele Ν = 22 Ν = 500 p HLA DRB1*08 (n=33) non-hla συσχετίσεις O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου TRAF1/C5 στη ΝIA το ηλεκτροφορητικό πρότυπο των δειγμάτων για τον πολυμορφισμό rs του γονιδίου TRAF1/C5 παρουσιάζεται στην εικόνα 11. Εικόνα 11. Ηλεκτροφορητική ανάλυση δειγμάτων για τον πολυμορφισμό TRAF1/C5 A/G rs Oι γονότυποι των δειγμάτων που παρουσιάζονται είναι οι εξής: 1o G/G, 2o A/G. 3o A/A, 4o -5o A/G, 6o A/A, 7o A/G, 80 A/A, MWM (molecular weight marker). Oι συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs στην ομάδα μελέτης ασθενών και μαρτύρων παρουσιάζονται στον πίνακα 109. η ανάλυση έδειξε στατιστικά σημαντική διαφορά τόσο στην κατανομή των γονοτύπων όσο και στην κατανομή των αλληλομόρφων μεταξύ ασθενών και μαρτύρων. Συγκεκριμένα, ο γονότυπος α/α βρέθηκε σε μεγαλύ-
298 298 τερη συχνότητα σε ασθενείς με NiA από ό,τι στους υγιείς μάρτυρες (p = 0.036, odds ratio [OR] 2.3, 95% confidence interval [Ci] ). ακόμα, το έλασσον αλληλόμορφο A αντιπροσωπευόταν σε υψηλότερη συχνότητα στους ασθενείς σε σύγκριση με τα υγιή άτομα (p = 0.045, OR = 1.37, 95%Ci ). Πίνακας 109. Συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs του γονιδίου TRAF1/C5 στην ομάδα μελέτης ασθενών και μαρτύρων ΓOΝOΤΥΠOΙ NIA OΜΑΔΑ ΕΛΕΓΧOΥ rs N=128 Ν=221 p OR (95%CI) A/A 21 (16.41%) 21 (9.50%) A/G 74 (57.81%) 124 (56.11%) p=0.16 a 1.67 ( ) G/G 33 (25.78%) 76 (34.39%) p=0.036 a 2.3 ( ) ΑΛΛΗΛΙΑ Ν=256 Ν=442 A 116 (45.31%) 166 (37.56%) G 140 (54.69%) 276 (62.44%) p=0.045 b 1.37 ( ) CI: confidence interval (διάστημα εμπιστοσύνης), OR: odds ratio. a p τιμές με ένα βαθμό ελευθερίας (df=1) και OR (95% CI) υπολογίστηκαν με γονότυπο αναφοράς τον A/A. b p τιμή υπολογίστηκε με το έλασσον αλληλόμορφο (Α) ως αλληλόμορφο αναφοράς O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου PTPN22 στη ΝΙΑ το ηλεκτροφορητικό πρότυπο των δειγμάτων για τον πολυμορφισμό rs του γονιδίου PTPN22 παρουσιάζεται στην εικόνα 12. Εικόνα 12. Ηλεκτροφορητική ανάλυση δειγμάτων για τον πολυμορφισμό rs του γονιδίου PTPN22. Oι γονότυποι των δειγμάτων που παρουσιάζονται είναι οι εξής: 1o-5ο C/C, 6o-7o C/T, 8o C/C, MWM, 9o-10o C/C.
299 299 Oι συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs του γονιδίου PTPN22 στην ομάδα μελέτης ασθενών και μαρτύρων παρουσιάζονται στον Πίνακα 110. Όπως φαίνεται από την ανάλυση που πραγματοποιήθηκε, η ετεροζυγωτία C/T εμφανίζεται σε μεγαλύτερη συχνότητα στους ασθενείς από ό,τι στους υγιείς (11.72% έναντι 5.43%, p = 0.039, OR = 0.43, 95% Ci ). αυτό έχει ως αποτέλεσμα το έλασσον αλληλόμορφο (τ) να εμφανίζει σημαντικά αυξημένη συχνότητα στους ασθενείς σε σχέση με τους υγιείς μάρτυρες (p = 0.043, OR =0.44, 95%Ci ). Πίνακας 110. Συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs του γονιδίου PTPN22 στην ομάδα μελέτης ασθενών και μαρτύρων ΓOΝOΤΥΠOΙ NIA OΜΑΔΑ ΕΛΕΓΧOΥ rs N=128 Ν=221 p OR (95%CI) C/C 113 (88.28%) 209 (94.57%) p=0.039 a 0.43 ( ) C/T 15(11.72%) 12 (5.43%) T/T 0 (0%) 0 (0%) ΑΛΛΗΛΙΑ Ν=256 Ν=442 C 241 (94.14%) 430 (97.28%) p=0.043 b 0.44 ( ) T 15 (5.86%) 12 (2.72%) CI: confidence interval (διάστημα εμπιστοσύνης), OR: odds ratio. a p τιμές με ένα βαθμό ελευθερίας (df=1) και OR (95% CI) υπολογίστηκαν με γονότυπο αναφοράς τον C/T. b p τιμή υπολογίστηκε με το έλασσον αλληλόμορφο (T) ως αλληλόμορφο αναφοράς O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου STAT4 στην ΝΙΑ το ηλεκτροφορητικό πρότυπο των δειγμάτων για τον πολυμορφισμό rs του γονιδίου STAT4 παρουσιάζεται στην εικόνα 13.
300 300 Εικόνα 13. Ηλεκτροφορητική ανάλυση δειγμάτων για τον πολυμορφισμό rs του γονιδίου STAT4. Oι γονότυποι των δειγμάτων που παρουσιάζονται είναι οι εξής: Διπλή ζώνη: G/Τ (147 bp bp + 25 bp), υψηλότερη ζώνη: G/G (147 bp), κατώτερη ζώνη (και μια μικρή δυσδιάκριτη): T/T (122 bp +25 bp). Σημειώνεται ότι η αναλυτική ικανότητα του πηκτώματος αγαρόζης δεν είναι η κατάλληλη για την εμφάνιση της μικρής ζώνης των 25 bp, η οποία εμφανίζεται ξεκάθαρα σε πήκτωμα πολυακρυλαμίδης. Oι συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs του γονιδίου STAT4 στην ομάδα μελέτης ασθενών και μαρτύρων παρουσιάζονται στον Πίνακα 111. Όπως φαίνεται από την ανάλυση που πραγματοποιήθηκε, τόσο οι γονοτυπικές συχνότητες όσο και αυτές των αλληλομόρφων δεν εμφανίζουν καμιά στατιστικά σημαντική διαφορά μεταξύ των ασθενών με Νια και των υγιών μαρτύρων. Πίνακας 111. Συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs του γονιδίου STAT4 στην ομάδα μελέτης ασθενών και μαρτύρων ΓOΝOΤΥΠOΙ NIA OΜΑΔΑ ΕΛΕΓΧOΥ rs N=128 Ν=221 p OR (95%CI) G/G 68 (53.13%) 137 (61.99%) p=0.44 a 0.49 ( ) G/T 56 (43.75%) 80 (36.20%) p=0.72 a 0.70 ( ) T/T 4 (3.12%) 4 (1.81%) ΑΛΛΗΛΙΑ Ν=256 Ν=442 G 192 (75 %) 354 (80.09 %) p=0.13b 0.74 ( ) T 64 (25 %) 88 (19.91 %) CI: confidence interval (διάστημα εμπιστοσύνης), OR: odds ratio. a p τιμές με ένα βαθμό ελευθερίας (df=1) και OR (95% CI) υπολογίστηκαν με γονότυπο αναφοράς τον T/T. b p τιμή υπολογίστηκε με το έλασσον αλληλόμορφο (T) ως αλληλόμορφο αναφοράς.
301 O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου CD247 στην ΝIA η γονοτύπηση των δειγμάτων για το πολυμορφισμό rs του γονιδίου CD247 απαιτούσε πολύ υψηλή ποιότητα καθαρού DNA, για το λόγο αυτό μπορέσαμε να συμπεριλάβουμε μόνο 95 ασθενείς και 115 μάρτυρες από τα δείγματά μας. το πρότυπο γονοτύπησης των δειγμάτων για τον πολυμορφισμό rs του γονιδίου CD247 παρουσιάζεται στην εικόνα 14. Εικόνα 14. Ανάλυση δειγμάτων για τον πολυμορφισμό rs του γονιδίου CD247. O γονότυπος Α/Α εμφανίζεται με κόκκινο χρώμα, ενώ ό γονότυπος Α/G με πράσινο. Oι συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs στην ομάδα μελέτης ασθενών και μαρτύρων παρουσιάζονται στον Πίνακα 112. Όπως φαίνεται από την ανάλυση που πραγματοποιήθηκε, η συχνότητα του ετεροζυγώτη G/A διαφέρει σημαντικά από τη συχνότητα του ομοζυγώτη α/α μεταξύ των ασθενών με Νια και των υγιών (p = 0.039,
302 302 OR = 1.89, 95% Ci ), ενώ το αλληλόμορφο α δεν βρέθηκε ότι αποτελεί παράγοντα αυξημένης προδιάθεσης για την εμφάνιση της νόσου (p = 0.14, OR =1.37, 95% Ci ( ). Πίνακας 112. Συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs του γονιδίου CD247 στην ομάδα μελέτης ασθενών και μαρτύρων ΓOΝOΤΥΠOΙ NIA OΜΑΔΑ ΕΛΕΓΧOΥ rs N=95 Ν=115 p OR (95%CI) A/A 39 (41.05%) 31 (26.96%) p=0.039a 1.89 ( ) A/G 56 (58.95%) 84 (73.04%) G/G 0 (0%) 0 (0%) ΑΛΛΗΛΙΑ Ν=190 Ν=230 A 134 (70.53%) 146 (63.48%) p=0.14b 1.37 ( ) G 56 (29.47%) 84 (36.52%) CI: confidence interval (διάστημα εμπιστοσύνης), OR: odds ratio. a p τιμές με ένα βαθμό ελευθερίας (df=1) και OR (95% CI) υπολογίστηκαν με γονότυπο αναφοράς τον A/G. b p τιμή υπολογίστηκε με το έλασσον αλληλόμορφο (G) ως αλληλόμορφο αναφοράς O ρόλος του γενετικού πολυμορφισμού rs του γονιδίου PTPN2 στην ΝΙΑ Όπως και για το προηγούμενο γονίδιο, έτσι και για το πολυμορφισμό rs του γονιδίου PTPN2, η γονοτύπηση των δειγμάτων απαιτούσε πολύ υψηλή ποιότητα καθαρού DNA, για το λόγο αυτό μπορέσαμε να συμπεριλάβουμε μόνο 95 ασθενείς και 115 μάρτυρες από τα δείγματά μας. το πρότυπο γονοτύπησης των δειγμάτων για τον πολυμορφισμό rs του γονιδίου PTPN2 παρουσιάζεται στην εικόνα 15.
303 303 Εικόνα 15. Ανάλυση δειγμάτων για τον πολυμορφισμό rs του γονιδίου PTPN2. O γονότυπος Α/Α εμφανίζεται με κόκκινο χρώμα, ο γονότυπος A/G με πράσινο και ο γονότυπος G/G με μπλε χρώμα. Oι συχνότητες γονοτύπων και αλληλομόρφων για τον πολυμορφισμό rs γονιδίου PTPN2 στην ομάδα μελέτης ασθενών και μαρτύρων παρουσιάζονται στον Πίνακα 113. Όπως φαίνεται από την ανάλυση που πραγματοποιήθηκε, τόσο οι γονοτυπικές συχνότητες όσο και αυτές των αλληλομόρφων δεν εμφανίζουν καμιά στατιστικά σημαντική διαφορά μεταξύ των ασθενών με Νια και των υγιών μαρτύρων.
Ηλίας Κουρής - Ρευματολόγος. www.rheuma,gr
 Πολλες από τις ρευματικες παθησεις των ενηλικων προσβαλουν και τα παιδια,αν και σε μικροτερη συχνοτητα. Επιπλεον καποιες παθησεις όπως είναι ο συστηματικης έναρξης ή ο ολιγοαρθρικος τυπος εναρξης της Νεανικης
Πολλες από τις ρευματικες παθησεις των ενηλικων προσβαλουν και τα παιδια,αν και σε μικροτερη συχνοτητα. Επιπλεον καποιες παθησεις όπως είναι ο συστηματικης έναρξης ή ο ολιγοαρθρικος τυπος εναρξης της Νεανικης
Ρευματολογία. Ψωριασική Αρθρίτιδα. Στέφανος Πατεράκης Φυσικοθεραπευτής, καθηγητής φυσ/πείας
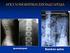 Ρευματολογία Ψωριασική Αρθρίτιδα Στέφανος Πατεράκης Φυσικοθεραπευτής, καθηγητής φυσ/πείας Τι είναι η ψωριασική αρθρίτιδα; Η ψωριασική αρθρίτιδα είναι μια χρόνια φλεγμονώδης πάθηση που προσβάλλει τις αρθρώσεις
Ρευματολογία Ψωριασική Αρθρίτιδα Στέφανος Πατεράκης Φυσικοθεραπευτής, καθηγητής φυσ/πείας Τι είναι η ψωριασική αρθρίτιδα; Η ψωριασική αρθρίτιδα είναι μια χρόνια φλεγμονώδης πάθηση που προσβάλλει τις αρθρώσεις
Νεανική σπονδυλοαρθρίτιδα/αρθρίτιδα που σχετίζεται με ενθεσίτιδα (jspa/era)
 www.printo.it/pediatric-rheumatology/gr/intro Νεανική σπονδυλοαρθρίτιδα/αρθρίτιδα που σχετίζεται με ενθεσίτιδα (jspa/era) Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Η ΝΕΑΝΙΚΗ ΣΠΟΝΔΥΛΟΑΡΘΡΙΤΙΔΑ/ΑΡΘΡΙΤΙΔΑ ΠΟΥ ΣΧΕΤΙΖΕΤΑΙ
www.printo.it/pediatric-rheumatology/gr/intro Νεανική σπονδυλοαρθρίτιδα/αρθρίτιδα που σχετίζεται με ενθεσίτιδα (jspa/era) Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Η ΝΕΑΝΙΚΗ ΣΠΟΝΔΥΛΟΑΡΘΡΙΤΙΔΑ/ΑΡΘΡΙΤΙΔΑ ΠΟΥ ΣΧΕΤΙΖΕΤΑΙ
Νεανική ιδιοπαθής αρθρίτις (ΝΙΑ)
 www.printo.it/pediatric-rheumatology/gr/intro Νεανική ιδιοπαθής αρθρίτις (ΝΙΑ) Έκδοση από 2016 2. ΔΙΑΦΟΡΕΤΙΚΕΣ ΜΟΡΦΕΣ ΝΙΑ 2.1 Υπάρχουν διαφορετικές μορφές της νόσου; Υπάρχουν αρκετές μορφές ΝΙΑ. Κυρίως
www.printo.it/pediatric-rheumatology/gr/intro Νεανική ιδιοπαθής αρθρίτις (ΝΙΑ) Έκδοση από 2016 2. ΔΙΑΦΟΡΕΤΙΚΕΣ ΜΟΡΦΕΣ ΝΙΑ 2.1 Υπάρχουν διαφορετικές μορφές της νόσου; Υπάρχουν αρκετές μορφές ΝΙΑ. Κυρίως
Νεανική ιδιοπαθής αρθρίτιδα: Απλή και χρηστική αρχική προσέγγιση για τον ρευματολόγο των ενηλίκων. Μαρία Τραχανά
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ Νεανική ιδιοπαθής αρθρίτιδα: Απλή και χρηστική αρχική προσέγγιση για τον ρευματολόγο των ενηλίκων Μαρία Τραχανά Α Παιδιατρική Κλινική ΑΠΘ Παιδιατρικό Ανοσολογικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ Νεανική ιδιοπαθής αρθρίτιδα: Απλή και χρηστική αρχική προσέγγιση για τον ρευματολόγο των ενηλίκων Μαρία Τραχανά Α Παιδιατρική Κλινική ΑΠΘ Παιδιατρικό Ανοσολογικό
Ο ρόλος των αντισωμάτων κατά του κυκλικού κιτρουλλιωμένου πεπτιδίου στη διάγνωση και θεραπεία της νεανικής ιδιοπαθούς αρθρίτιδας
 ΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥ ΩΝ "ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΛΟΓΙΑ - ΘΕΡΑΠΕΥΤΙΚΗ" Ο ρόλος των αντισωμάτων κατά του κυκλικού κιτρουλλιωμένου πεπτιδίου στη διάγνωση και θεραπεία της νεανικής
ΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥ ΩΝ "ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΛΟΓΙΑ - ΘΕΡΑΠΕΥΤΙΚΗ" Ο ρόλος των αντισωμάτων κατά του κυκλικού κιτρουλλιωμένου πεπτιδίου στη διάγνωση και θεραπεία της νεανικής
Το γόνατο ως στόχος ρευματικών νοσημάτων
 Το γόνατο ως στόχος ρευματικών νοσημάτων Χ. Μ. ΜουτσόπουΛος Αντεπιστέλλον μέλος της Ακαδημίας Αθηνών, Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών α ρευματικά νοσήματα είναι ασθένειες που προσβάλλουν
Το γόνατο ως στόχος ρευματικών νοσημάτων Χ. Μ. ΜουτσόπουΛος Αντεπιστέλλον μέλος της Ακαδημίας Αθηνών, Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών α ρευματικά νοσήματα είναι ασθένειες που προσβάλλουν
Ταξινόμηση νεανικής αρθρίτιδας
 Δελτ Α Παιδιατρ Κλιν Πανεπ Αθηνών 54, 2007 153 ΑΝΑΣΚΟΠΗΣΗ Ταξινόμηση νεανικής αρθρίτιδας Φ. Ψύχου ΠΕΡΙΛΗΨΗ Στις νεανικές αρθροπάθειες περιλαμβάνονται διάφορα νοσήματα με αρθρίτιδα νεανικής έναρξης, η ταξινόμηση
Δελτ Α Παιδιατρ Κλιν Πανεπ Αθηνών 54, 2007 153 ΑΝΑΣΚΟΠΗΣΗ Ταξινόμηση νεανικής αρθρίτιδας Φ. Ψύχου ΠΕΡΙΛΗΨΗ Στις νεανικές αρθροπάθειες περιλαμβάνονται διάφορα νοσήματα με αρθρίτιδα νεανικής έναρξης, η ταξινόμηση
Δημήτρης Καρόκης Ρευματολόγος ΕΠΕΜΥ, Λευκάδα 22/6/2012
 Δημήτρης Καρόκης Ρευματολόγος ΕΠΕΜΥ, Λευκάδα 22/6/2012 *Παλιότερα θεωρούνταν ήπια νόσος *Νεώτερα δεδομένα: ~ 20% των ασθενών αναπτύσσουν διαβρωτική και δυνητικά «αναπηρική» νόσο *Αναζήτηση δεικτών για
Δημήτρης Καρόκης Ρευματολόγος ΕΠΕΜΥ, Λευκάδα 22/6/2012 *Παλιότερα θεωρούνταν ήπια νόσος *Νεώτερα δεδομένα: ~ 20% των ασθενών αναπτύσσουν διαβρωτική και δυνητικά «αναπηρική» νόσο *Αναζήτηση δεικτών για
Διαχείριση του ενήλικα με Νεανική Ιδιοπαθή Αρθρίτιδα
 Διαχείριση του ενήλικα με Νεανική Ιδιοπαθή Αρθρίτιδα Δέσποινα Δημοπούλου Πανεπιστημιακή υπότροφος Δ Παθολογική Κλινική Α.Π.Θ 1 η επίσκεψη μετάβασης των ασθενών με ΝΙΑ στο ιατρείο ενηλίκων Αναλυτική παρουσίαση
Διαχείριση του ενήλικα με Νεανική Ιδιοπαθή Αρθρίτιδα Δέσποινα Δημοπούλου Πανεπιστημιακή υπότροφος Δ Παθολογική Κλινική Α.Π.Θ 1 η επίσκεψη μετάβασης των ασθενών με ΝΙΑ στο ιατρείο ενηλίκων Αναλυτική παρουσίαση
Ρευματοειδής αρθρίτιδα. Μαρία Γ. Τεκτονίδου Επίκουρος Καθηγήτρια Ρευματολογίας Α Παθολογική Κλινική, Ιατρική Σχολή Αθηνών
 Ρευματοειδής αρθρίτιδα Μαρία Γ. Τεκτονίδου Επίκουρος Καθηγήτρια Ρευματολογίας Α Παθολογική Κλινική, Ιατρική Σχολή Αθηνών Ρόλος Ανοσοποιητικού Συστήματος Προστασία του οργανισμού έναντι εξωτερικών εισβολέων
Ρευματοειδής αρθρίτιδα Μαρία Γ. Τεκτονίδου Επίκουρος Καθηγήτρια Ρευματολογίας Α Παθολογική Κλινική, Ιατρική Σχολή Αθηνών Ρόλος Ανοσοποιητικού Συστήματος Προστασία του οργανισμού έναντι εξωτερικών εισβολέων
Παμπελοννησιακό Ιατρικό Συνέδριο Πάτρα, 23 Οκτ. 2010
 Σπονδυλαρθροπάθειες Η σημασία της πρώιμης διάγνωσης Δαούσης Δημήτριος Λέκτορας Παθολογίας/Ρευματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών Παμπελοννησιακό Ιατρικό Συνέδριο Πάτρα, 23 Οκτ. 2010 Σπονδυλαρθροπάθειες
Σπονδυλαρθροπάθειες Η σημασία της πρώιμης διάγνωσης Δαούσης Δημήτριος Λέκτορας Παθολογίας/Ρευματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών Παμπελοννησιακό Ιατρικό Συνέδριο Πάτρα, 23 Οκτ. 2010 Σπονδυλαρθροπάθειες
ΣΥΣΧΕΤΙΣΗ HLA ΑΛΛΗΛΙΩΝ ΚΑΙ ΚΑΠΝΙΣΜΑΤΟΣ ΣΤΗΝ ΕΚΔΗΛΩΣΗ ANTI-CCP(+) ΡΕΥΜΑΤΟΕΙΔΟΥΣ ΑΡΘΡΙΤΙΔΑΣ (ΡΑ) ΣΕ ΕΛΛΗΝΕΣ ΑΣΘΕΝΕΙΣ
 ΣΥΣΧΕΤΙΣΗ HLA ΑΛΛΗΛΙΩΝ ΚΑΙ ΚΑΠΝΙΣΜΑΤΟΣ ΣΤΗΝ ΕΚΔΗΛΩΣΗ ANTI-CCP(+) ΡΕΥΜΑΤΟΕΙΔΟΥΣ ΑΡΘΡΙΤΙΔΑΣ (ΡΑ) ΣΕ ΕΛΛΗΝΕΣ ΑΣΘΕΝΕΙΣ Β. Κίτσιου 1, Αικ. Ταράση 1, Ε. Μολέ 2, Κ. Σουφλερός 1, Θ. Αθανασιάδης 1, Δ. Κουνιάκη
ΣΥΣΧΕΤΙΣΗ HLA ΑΛΛΗΛΙΩΝ ΚΑΙ ΚΑΠΝΙΣΜΑΤΟΣ ΣΤΗΝ ΕΚΔΗΛΩΣΗ ANTI-CCP(+) ΡΕΥΜΑΤΟΕΙΔΟΥΣ ΑΡΘΡΙΤΙΔΑΣ (ΡΑ) ΣΕ ΕΛΛΗΝΕΣ ΑΣΘΕΝΕΙΣ Β. Κίτσιου 1, Αικ. Ταράση 1, Ε. Μολέ 2, Κ. Σουφλερός 1, Θ. Αθανασιάδης 1, Δ. Κουνιάκη
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων
 Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Ρευματοειδής αρθρίτιδα
 Ρευματοειδής αρθρίτιδα Μ.Ν. Μανουσάκης En. Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών ρευματοειδής αρθρίτιδα είναι μία χρόνια φλεγμονή των αρθρώσεων (Πιν. 1). Με τον όρο χρόνια φλεγμονή των αρθρώσεων,
Ρευματοειδής αρθρίτιδα Μ.Ν. Μανουσάκης En. Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών ρευματοειδής αρθρίτιδα είναι μία χρόνια φλεγμονή των αρθρώσεων (Πιν. 1). Με τον όρο χρόνια φλεγμονή των αρθρώσεων,
Νεανική σπονδυλοαρθρίτιδα/αρθρίτιδα που σχετίζεται με ενθεσίτιδα (jspa/era)
 www.printo.it/pediatric-rheumatology/gr/intro Νεανική σπονδυλοαρθρίτιδα/αρθρίτιδα που σχετίζεται με ενθεσίτιδα (jspa/era) Έκδοση από 2016 2. ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ 2.1 Πως γίνεται η διάγνωση; Οι γιατροί
www.printo.it/pediatric-rheumatology/gr/intro Νεανική σπονδυλοαρθρίτιδα/αρθρίτιδα που σχετίζεται με ενθεσίτιδα (jspa/era) Έκδοση από 2016 2. ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ 2.1 Πως γίνεται η διάγνωση; Οι γιατροί
ΙΕΡΟΛΑΓOΝΙΕΣ ΑΡΘΡΩΣΕΙΣ-ΣΠΟΝΔΥΛΙΚΗ ΣΤΗΛΗ ΠΟΤΕ Ο ΚΛΙΝΙΚΟΣ ΠΑΡΑΠΕΜΠΕΙ ΓΙΑ MRI ΝΙΚΟΛΑΟΣ ΚΟΥΓΚΑΣ ΕΠΙΚ. ΕΠΙΜΕΛΗΤΗΣ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΓΝΗ
 ΙΕΡΟΛΑΓOΝΙΕΣ ΑΡΘΡΩΣΕΙΣ-ΣΠΟΝΔΥΛΙΚΗ ΣΤΗΛΗ ΠΟΤΕ Ο ΚΛΙΝΙΚΟΣ ΠΑΡΑΠΕΜΠΕΙ ΓΙΑ MRI ΝΙΚΟΛΑΟΣ ΚΟΥΓΚΑΣ ΕΠΙΚ. ΕΠΙΜΕΛΗΤΗΣ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΓΝΗ Καμία σύγκρουση συμφερόντων Περίγραμμα Εισαγωγικά στοιχεία Η ανάγκη
ΙΕΡΟΛΑΓOΝΙΕΣ ΑΡΘΡΩΣΕΙΣ-ΣΠΟΝΔΥΛΙΚΗ ΣΤΗΛΗ ΠΟΤΕ Ο ΚΛΙΝΙΚΟΣ ΠΑΡΑΠΕΜΠΕΙ ΓΙΑ MRI ΝΙΚΟΛΑΟΣ ΚΟΥΓΚΑΣ ΕΠΙΚ. ΕΠΙΜΕΛΗΤΗΣ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΓΝΗ Καμία σύγκρουση συμφερόντων Περίγραμμα Εισαγωγικά στοιχεία Η ανάγκη
Γνωριμία με τα αυτοάνοσα ρευματικά νοσήματα
 Γνωριμία με τα αυτοάνοσα ρευματικά νοσήματα Αντώνης Φανουριάκης Μονάδα Ρευματολογίας και Κλινικής Ανοσολογίας Δ Πανεπιστημιακή Παθολογική Κλινική Πανεπιστημιακό Γενικό Νοσοκομείο «Αττικόν» Αθήνα, 01/02/2016
Γνωριμία με τα αυτοάνοσα ρευματικά νοσήματα Αντώνης Φανουριάκης Μονάδα Ρευματολογίας και Κλινικής Ανοσολογίας Δ Πανεπιστημιακή Παθολογική Κλινική Πανεπιστημιακό Γενικό Νοσοκομείο «Αττικόν» Αθήνα, 01/02/2016
ΟΡΟΑΡΝΗΤΙΚΕΣ ΣΠΟΝΔΥΛΑΡΘΡΟΠΑΘΕΙΕΣ
 ΟΡΟΑΡΝΗΤΙΚΕΣ ΣΠΟΝΔΥΛΑΡΘΡΟΠΑΘΕΙΕΣ Η έννοια της οροαρνητικής ΣπΑ Προακτινολογική ΣπΑ ΣΠΥΡΟΣ ΑΣΛΑΝΙΔΗΣ ΣπΑ Ομάδα φλεγμονωδών αρθροπαθειών Με κοινά κλινικά χαρακτηριστικά και γενετικούς προδιαθεσικούς παράγοντες
ΟΡΟΑΡΝΗΤΙΚΕΣ ΣΠΟΝΔΥΛΑΡΘΡΟΠΑΘΕΙΕΣ Η έννοια της οροαρνητικής ΣπΑ Προακτινολογική ΣπΑ ΣΠΥΡΟΣ ΑΣΛΑΝΙΔΗΣ ΣπΑ Ομάδα φλεγμονωδών αρθροπαθειών Με κοινά κλινικά χαρακτηριστικά και γενετικούς προδιαθεσικούς παράγοντες
ΑΣΘΕΝΗΣ ΜΕ ΠΙΘΑΝΟ ΣΥΝΔΡΟΜΟ SAPHO ΝΙΚΟΛΑΟΣ ΚΟΥΓΚΑΣ ΕΠΙΚ. ΕΠΙΜΕΛΗΤΗΣ ΡΕΥΜΑΤΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΠΑΓΝΗ
 ΑΣΘΕΝΗΣ ΜΕ ΠΙΘΑΝΟ ΣΥΝΔΡΟΜΟ SAPHO ΝΙΚΟΛΑΟΣ ΚΟΥΓΚΑΣ ΕΠΙΚ. ΕΠΙΜΕΛΗΤΗΣ ΡΕΥΜΑΤΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΠΑΓΝΗ Καμία σύγκρουση συμφερόντων Περίγραμμα Εισαγωγή-επιδημιολογία Παθογένεια Κλινική εικόνα Διάγνωση Θεραπεία
ΑΣΘΕΝΗΣ ΜΕ ΠΙΘΑΝΟ ΣΥΝΔΡΟΜΟ SAPHO ΝΙΚΟΛΑΟΣ ΚΟΥΓΚΑΣ ΕΠΙΚ. ΕΠΙΜΕΛΗΤΗΣ ΡΕΥΜΑΤΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΠΑΓΝΗ Καμία σύγκρουση συμφερόντων Περίγραμμα Εισαγωγή-επιδημιολογία Παθογένεια Κλινική εικόνα Διάγνωση Θεραπεία
Κατευθυντήριες οδηγίες. για τη θεραπεία της. Νεανικής Ιδιοπαθούς Αρθρίτιδας
 ΕΛΛΗΝΙΚΗ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΕΤΑΙΡΕΙΑ & ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΝΩΣΗ ΡΕΥΜΑΤΟΛΟΓΩΝ ΕΛΛΑΔΟΣ (Ε.Ρ.Ε.-ΕΠ.Ε.Ρ.Ε.) Έτος Ιδρύσεως 1960 Κατευθυντήριες οδηγίες για τη θεραπεία της Νεανικής Ιδιοπαθούς Αρθρίτιδας Μάρτιος 2015 Συγγραφείς:
ΕΛΛΗΝΙΚΗ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΕΤΑΙΡΕΙΑ & ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΝΩΣΗ ΡΕΥΜΑΤΟΛΟΓΩΝ ΕΛΛΑΔΟΣ (Ε.Ρ.Ε.-ΕΠ.Ε.Ρ.Ε.) Έτος Ιδρύσεως 1960 Κατευθυντήριες οδηγίες για τη θεραπεία της Νεανικής Ιδιοπαθούς Αρθρίτιδας Μάρτιος 2015 Συγγραφείς:
13 Επιστημονική Συνάντηση Ρευματολόγων Βορειοδυτικής 21 & 22 Ιανουαρίου 2011, Μέτσοβο. Ο ρόλος της µαγνητικής τοµογραφίας στις σπονδυλοαρθροπάθειες
 13 Επιστημονική Συνάντηση Ρευματολόγων Βορειοδυτικής Ελλάδος 21 & 22 Ιανουαρίου 2011, Μέτσοβο Ο ρόλος της µαγνητικής τοµογραφίας στις σπονδυλοαρθροπάθειες Σε ασθενείς µε οροαρνητική σπονδυλαρθροπάθεια
13 Επιστημονική Συνάντηση Ρευματολόγων Βορειοδυτικής Ελλάδος 21 & 22 Ιανουαρίου 2011, Μέτσοβο Ο ρόλος της µαγνητικής τοµογραφίας στις σπονδυλοαρθροπάθειες Σε ασθενείς µε οροαρνητική σπονδυλαρθροπάθεια
Ερωτήµατα προς απάντηση
 Κεφ. 9. Ανοσιακή ανοχή και αυτοανοσία: Η διάκριση εαυτού-ξένου και οι διαταραχές της Ερωτήµατα προς απάντηση Πως διατηρεί το ανοσοποιητικό σύστηµα τηµη απαντητικότητα σε εαυτά αντιγόνα (=ανοχή); Ποιοι
Κεφ. 9. Ανοσιακή ανοχή και αυτοανοσία: Η διάκριση εαυτού-ξένου και οι διαταραχές της Ερωτήµατα προς απάντηση Πως διατηρεί το ανοσοποιητικό σύστηµα τηµη απαντητικότητα σε εαυτά αντιγόνα (=ανοχή); Ποιοι
ΣΥΣΧΕΤΙΣΗ ΓΕΝΕΤΙΚΩΝ ΠΟΛΥΜΟΡΦΙΣΜΩΝ ΣΤΟ ΓΟΝΙ Ι0 MYD88 ΜΕ ΤΗΝ ΑΝΑΠΤΥΞΗ ΦΥΜΑΤΙΩΣΗΣ
 ΣΥΣΧΕΤΙΣΗ ΓΕΝΕΤΙΚΩΝ ΠΟΛΥΜΟΡΦΙΣΜΩΝ ΣΤΟ ΓΟΝΙ Ι MYD88 ΜΕ ΤΗΝ ΑΝΑΠΤΥΞΗ ΦΥΜΑΤΙΩΣΗΣ Φωτεινή Μάλλη 1, Ειρήνη Γερογιάννη 1 Καλλιόπη Αγγέλου 1, Βίκυ Μολλάκη 2, Φωτεινή Μπαρδάκα 1, Κωνσταντίνος Ι. Γουργουλιάνης
ΣΥΣΧΕΤΙΣΗ ΓΕΝΕΤΙΚΩΝ ΠΟΛΥΜΟΡΦΙΣΜΩΝ ΣΤΟ ΓΟΝΙ Ι MYD88 ΜΕ ΤΗΝ ΑΝΑΠΤΥΞΗ ΦΥΜΑΤΙΩΣΗΣ Φωτεινή Μάλλη 1, Ειρήνη Γερογιάννη 1 Καλλιόπη Αγγέλου 1, Βίκυ Μολλάκη 2, Φωτεινή Μπαρδάκα 1, Κωνσταντίνος Ι. Γουργουλιάνης
ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ ΤΜΗΜΑ ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΟΙΚΟΝΟΜΙΚΑ και ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΟΙΚΟΝΟΜΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΕΝΟΣ ΒΙΟΛΟΓΙΚΟΥ ΑΝΟΣΟΤΡΟΠΟΠΟΙΗΤΙΚΟΥ ΑΝΤΙΡΡΕΥΜΑΤΙΚΟΥ ΦΑΡΜΑΚΟΥ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ ΤΜΗΜΑ ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΟΙΚΟΝΟΜΙΚΑ και ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΟΙΚΟΝΟΜΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΕΝΟΣ ΒΙΟΛΟΓΙΚΟΥ ΑΝΟΣΟΤΡΟΠΟΠΟΙΗΤΙΚΟΥ ΑΝΤΙΡΡΕΥΜΑΤΙΚΟΥ ΦΑΡΜΑΚΟΥ
Αρχική εμπειρία από την χορήγηση anakinra σε δέκα ενήλικες ασθενείς με ανθεκτική ιδιοπαθή υποτροπιάζουσα περικαρδίτιδα
 Αρχική εμπειρία από την χορήγηση anakinra σε δέκα ενήλικες ασθενείς με ανθεκτική ιδιοπαθή υποτροπιάζουσα περικαρδίτιδα Γ. Λάζαρος, Π. Βασιλείου, Κ. Αντωνάτου, Χ. Κουτσιανάς, Γ. Γεωργιόπουλος, Δ. Βασιλόπουλος,
Αρχική εμπειρία από την χορήγηση anakinra σε δέκα ενήλικες ασθενείς με ανθεκτική ιδιοπαθή υποτροπιάζουσα περικαρδίτιδα Γ. Λάζαρος, Π. Βασιλείου, Κ. Αντωνάτου, Χ. Κουτσιανάς, Γ. Γεωργιόπουλος, Δ. Βασιλόπουλος,
Γράφει: Μιλτιάδης Μαρκάτος, Πνευμονολόγος
 Γράφει: Μιλτιάδης Μαρκάτος, Πνευμονολόγος Πάνω από ένα αιώνα πριν, ο J. Hutchinson, ένας χειρουργός-δερματολόγος, αναγνώρισε την πρώτη περίπτωση σαρκοείδωσης, στο Λονδίνο. Στα χρόνια πριν και μετά την
Γράφει: Μιλτιάδης Μαρκάτος, Πνευμονολόγος Πάνω από ένα αιώνα πριν, ο J. Hutchinson, ένας χειρουργός-δερματολόγος, αναγνώρισε την πρώτη περίπτωση σαρκοείδωσης, στο Λονδίνο. Στα χρόνια πριν και μετά την
ΚΥΡΙΕΣ ΚΑΤΗΓΟΡΙΕΣ ΟΣΦΥΑΛΓΙΑΣ. Μηχανικού τύπου Φλεγμονώδους τύπου
 ΚΥΡΙΕΣ ΚΑΤΗΓΟΡΙΕΣ ΟΣΦΥΑΛΓΙΑΣ Μηχανικού τύπου Φλεγμονώδους τύπου Σπονδυλαρθρίτιδες Σπονδυλαθρίτιδες (SpA) οικογένεια διαταραχών που μοιράζονται κοινά κλινικά, ακτινολογικά και γεννετικά στοιχεία Ρευματολογικές
ΚΥΡΙΕΣ ΚΑΤΗΓΟΡΙΕΣ ΟΣΦΥΑΛΓΙΑΣ Μηχανικού τύπου Φλεγμονώδους τύπου Σπονδυλαρθρίτιδες Σπονδυλαθρίτιδες (SpA) οικογένεια διαταραχών που μοιράζονται κοινά κλινικά, ακτινολογικά και γεννετικά στοιχεία Ρευματολογικές
Αυτοάνοσα νοσήματα. Χ.Μ. Μουτσόπουλος
 Αυτοάνοσα νοσήματα Χ.Μ. Μουτσόπουλος Καθηγητής Παθολογίας στην Ιατρική Σχολή Πανεπιστημίου Αθηνών Η έγκαιρη αντιμετώπιση αποτελεί «κλειδί» για τον έλεγχο των αυτοάνοσων ασθενειών- της μεγάλης αυτής κατηγορίας
Αυτοάνοσα νοσήματα Χ.Μ. Μουτσόπουλος Καθηγητής Παθολογίας στην Ιατρική Σχολή Πανεπιστημίου Αθηνών Η έγκαιρη αντιμετώπιση αποτελεί «κλειδί» για τον έλεγχο των αυτοάνοσων ασθενειών- της μεγάλης αυτής κατηγορίας
Οικογενησ Μεσογειακοσ Πυρετοσ
 www.printo.it/pediatric-rheumatology/gr/intro Οικογενησ Μεσογειακοσ Πυρετοσ Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Ο ΟΙΚΟΓΕΝΗΣ ΜΕΣΟΓΕΙΑΚΟΣ ΠΥΡΕΤΟΣ 1.1 Τι είναι; Ο Οικογενής Μεσογειακός Πυρετός (ΟΜΠ) είναι ένα γενετικά
www.printo.it/pediatric-rheumatology/gr/intro Οικογενησ Μεσογειακοσ Πυρετοσ Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Ο ΟΙΚΟΓΕΝΗΣ ΜΕΣΟΓΕΙΑΚΟΣ ΠΥΡΕΤΟΣ 1.1 Τι είναι; Ο Οικογενής Μεσογειακός Πυρετός (ΟΜΠ) είναι ένα γενετικά
ΕΛΛΗΝΙΚΗ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΕΤΑΙΡΕΙΑ & ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΝΩΣΗ ΡΕΥΜΑΤΟΛΟΓΩΝ ΕΛΛΑΔΟΣ ΗΜΕΡΑ ΑΡΘΡΙΤΙΔΑΣ
 ΕΛΛΗΝΙΚΗ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΕΤΑΙΡΕΙΑ & ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΝΩΣΗ ΡΕΥΜΑΤΟΛΟΓΩΝ ΕΛΛΑΔΟΣ ΗΜΕΡΑ ΑΡΘΡΙΤΙΔΑΣ 12 ΟΚΤΩΒΡΙΟΥ 2013 TI ENNOOYME ΛΕΓΟΝΤΑΣ «ΑΡΘΡΙΤΙΔΑ» Ο όρος «ΑΡΘΡΙΤΙΔΑ» περιλαμβάνει μια ομάδα μυοσκελετικών παθήσεων
ΕΛΛΗΝΙΚΗ ΡΕΥΜΑΤΟΛΟΓΙΚΗ ΕΤΑΙΡΕΙΑ & ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΝΩΣΗ ΡΕΥΜΑΤΟΛΟΓΩΝ ΕΛΛΑΔΟΣ ΗΜΕΡΑ ΑΡΘΡΙΤΙΔΑΣ 12 ΟΚΤΩΒΡΙΟΥ 2013 TI ENNOOYME ΛΕΓΟΝΤΑΣ «ΑΡΘΡΙΤΙΔΑ» Ο όρος «ΑΡΘΡΙΤΙΔΑ» περιλαμβάνει μια ομάδα μυοσκελετικών παθήσεων
ΕΡΕ ΘΕΡΑΠΕΥΤΙΚΑ ΠΡΩΤΟΚΟΛΛΑ Αξονική Σπονδυλαρθρίτιδα
 ΕΡΕ ΘΕΡΑΠΕΥΤΙΚΑ ΠΡΩΤΟΚΟΛΛΑ Αξονική Σπονδυλαρθρίτιδα Δήμος Κ. Πατρίκος Εκ Μέρους της Διαρκούς «Επιτροπής Παρακολούθησης και Επικαιροποίησης των Διαγνωστικών και Θεραπευτικών Ρευματολογικών Πρωτοκόλλων»
ΕΡΕ ΘΕΡΑΠΕΥΤΙΚΑ ΠΡΩΤΟΚΟΛΛΑ Αξονική Σπονδυλαρθρίτιδα Δήμος Κ. Πατρίκος Εκ Μέρους της Διαρκούς «Επιτροπής Παρακολούθησης και Επικαιροποίησης των Διαγνωστικών και Θεραπευτικών Ρευματολογικών Πρωτοκόλλων»
2 Ο Περιστατικό: Ασθενής με ταχέως εξελισσόμενη νόσος
 2 Ο Περιστατικό: Ασθενής με ταχέως εξελισσόμενη νόσος Ασθενής με ταχέως εξελισσόμενη νόσος Γυναίκα, 32 ετών, πωλήτρια Από διμήνου: Συμμετρική πολυαρθρίτιδα TJC= 10, SJC= 8 ΤΚΕ: 54mm/1h CRP: 7,9 mg% (ΦΤ:
2 Ο Περιστατικό: Ασθενής με ταχέως εξελισσόμενη νόσος Ασθενής με ταχέως εξελισσόμενη νόσος Γυναίκα, 32 ετών, πωλήτρια Από διμήνου: Συμμετρική πολυαρθρίτιδα TJC= 10, SJC= 8 ΤΚΕ: 54mm/1h CRP: 7,9 mg% (ΦΤ:
ΚΛΙΝΙΚΗ ΕΚΤΙΜΗΣΗ ΑΣΘΕΝΟΥΣ ΜΕ ΟΡΟΑΡΝΗΤΙΚΗ ΣΠΟΝΔΥΛΟΑΡΘΡΙΤΙΔΑ
 ΚΛΙΝΙΚΗ ΕΚΤΙΜΗΣΗ ΑΣΘΕΝΟΥΣ ΜΕ ΟΡΟΑΡΝΗΤΙΚΗ ΣΠΟΝΔΥΛΟΑΡΘΡΙΤΙΔΑ Αθηνά Πυρπασοπούλου Παθολόγος, Επιμελήτρια Β ΕΣΥ Β Προπ. Παθολογική Κλινική, ΓΝΘ «Ιπποκράτειο» Οροαρνητικές σπονδυλοαρθροπάθειες Ομάδα παθήσεων
ΚΛΙΝΙΚΗ ΕΚΤΙΜΗΣΗ ΑΣΘΕΝΟΥΣ ΜΕ ΟΡΟΑΡΝΗΤΙΚΗ ΣΠΟΝΔΥΛΟΑΡΘΡΙΤΙΔΑ Αθηνά Πυρπασοπούλου Παθολόγος, Επιμελήτρια Β ΕΣΥ Β Προπ. Παθολογική Κλινική, ΓΝΘ «Ιπποκράτειο» Οροαρνητικές σπονδυλοαρθροπάθειες Ομάδα παθήσεων
Εισαγωγή στη νοσολογία του μυοσκελετικού συστήματος
 Εισαγωγή στη νοσολογία του μυοσκελετικού συστήματος Δημήτριος Βασιλόπουλος B Παθολογική Κλινική και Ομώνυμο Εργαστήριο Ιατρική Σχολή Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών Ιπποκράτειο ΓΝΑ Μυοσκελετικά
Εισαγωγή στη νοσολογία του μυοσκελετικού συστήματος Δημήτριος Βασιλόπουλος B Παθολογική Κλινική και Ομώνυμο Εργαστήριο Ιατρική Σχολή Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών Ιπποκράτειο ΓΝΑ Μυοσκελετικά
CROWNED DENS SYNDROME Γ. ΚΑΤΣΙΚΑΣ ΡΕΥΜΑΤΟΛΟΓΟΣ ΓΝΑ «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ»
 CROWNED DENS SYNDROME Γ. ΚΑΤΣΙΚΑΣ ΡΕΥΜΑΤΟΛΟΓΟΣ ΓΝΑ «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ» CROWNED DENS SYNDROME Ονομασία από Bouvet et al το 1985 1 Εναπόθεση κρυστάλλων CPP (ή ΗΑ) στην ΑΜΣΣ Η εναπόθεση πέριξ του οδόντα είναι
CROWNED DENS SYNDROME Γ. ΚΑΤΣΙΚΑΣ ΡΕΥΜΑΤΟΛΟΓΟΣ ΓΝΑ «Ο ΕΥΑΓΓΕΛΙΣΜΟΣ» CROWNED DENS SYNDROME Ονομασία από Bouvet et al το 1985 1 Εναπόθεση κρυστάλλων CPP (ή ΗΑ) στην ΑΜΣΣ Η εναπόθεση πέριξ του οδόντα είναι
«Επιδημιολογία του Ερυθηματώδους Λύκου- Η εμπειρία της Ομάδας Μελέτης Λύκου της Θεσσαλονίκης» Στεφανίδου Στυλιανή
 «Επιδημιολογία του Ερυθηματώδους Λύκου- Η εμπειρία της Ομάδας Μελέτης Λύκου της Θεσσαλονίκης» Στεφανίδου Στυλιανή Ορισμός Ο συστηματικός ερυθηματώδης λύκος (ΣΕΛ) είναι ένα τυπικό μη οργανοειδικό αυτοάνοσο
«Επιδημιολογία του Ερυθηματώδους Λύκου- Η εμπειρία της Ομάδας Μελέτης Λύκου της Θεσσαλονίκης» Στεφανίδου Στυλιανή Ορισμός Ο συστηματικός ερυθηματώδης λύκος (ΣΕΛ) είναι ένα τυπικό μη οργανοειδικό αυτοάνοσο
1.1. ΙΑΦΟΡΙΚΗ ΙΑΓΝΩΣΗ Ψωριασική αρθρίτιδα, διαβρωτική οστεοαρθρίτιδα, ρευματοειδής αρθρίτιδα, ουρική αρθρίτιδα.
 1.1 ΠΕΡΙΠΤΩΣΗ ΚΛΙΝΙΚΟ ΙΣΤΟΡΙΚΟ Άνδρας 37 ετών με οιδηματώδη δάκτυλα χεριών. ΕΙΚΟΝΑ 1.1 ΕΥΡΗΜΑΤΑ Οπισθιοπρόσθια (ΟΠ) ακτινογραφία άκρων χεριών. Στο αριστερό άκρο χέρι, η διόγκωση των μαλακών μορίων σαν
1.1 ΠΕΡΙΠΤΩΣΗ ΚΛΙΝΙΚΟ ΙΣΤΟΡΙΚΟ Άνδρας 37 ετών με οιδηματώδη δάκτυλα χεριών. ΕΙΚΟΝΑ 1.1 ΕΥΡΗΜΑΤΑ Οπισθιοπρόσθια (ΟΠ) ακτινογραφία άκρων χεριών. Στο αριστερό άκρο χέρι, η διόγκωση των μαλακών μορίων σαν
Παιδιά και νέοι με χρόνια προβλήματα υγείας και ειδικές ανάγκες. Σύγχρονες ιατρικές θεωρήσεις και ελληνική πραγματικότητα.
 Παιδιά και νέοι με χρόνια προβλήματα υγείας και ειδικές ανάγκες. Σύγχρονες ιατρικές θεωρήσεις και ελληνική πραγματικότητα. Μαρία Φωτουλάκη Επίκουρη καθηγήτρια Παιδιατρικής-Παιδιατρικής Γαστρεντερολογίας
Παιδιά και νέοι με χρόνια προβλήματα υγείας και ειδικές ανάγκες. Σύγχρονες ιατρικές θεωρήσεις και ελληνική πραγματικότητα. Μαρία Φωτουλάκη Επίκουρη καθηγήτρια Παιδιατρικής-Παιδιατρικής Γαστρεντερολογίας
Μήπως έχω Σκληρόδερµα;
 Μήπως έχω Σκληρόδερµα; Για να πληροφορηθώ µýëïò ôçò Σπάνιος ναι... Μόνος όχι Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών σπανίων παθήσεων
Μήπως έχω Σκληρόδερµα; Για να πληροφορηθώ µýëïò ôçò Σπάνιος ναι... Μόνος όχι Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών σπανίων παθήσεων
Επιδημιολογία Λοιμώξεων Βασικά στοιχεία. Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας Ιατρική Σχολή ΕΚΠΑ
 Επιδημιολογία Λοιμώξεων Βασικά στοιχεία Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας Ιατρική Σχολή ΕΚΠΑ Επιδημία είναι κάθε κατάσταση στην οποία παρατηρείται αυξημένη συχνότητα (επίπτωση) ενός νοσήματος
Επιδημιολογία Λοιμώξεων Βασικά στοιχεία Ιωσήφ Παπαπαρασκευάς Εργαστήριο Μικροβιολογίας Ιατρική Σχολή ΕΚΠΑ Επιδημία είναι κάθε κατάσταση στην οποία παρατηρείται αυξημένη συχνότητα (επίπτωση) ενός νοσήματος
www.pediatric-rheumathology.printo.it ΝΕΑΝΙΚΗ Ι ΙΟΠΑΘΗΣ ΑΡΘΡΙΤΙ Α
 www.pediatric-rheumathology.printo.it ΝΕΑΝΙΚΗ Ι ΙΟΠΑΘΗΣ ΑΡΘΡΙΤΙ Α Τι είναι; Η Νεανική Ιδιοπαθής Αρθρίτιδα (ΝΙΑ) είναι µία χρόνια νόσος που χαρακτηρίζεται από επίµονη φλεγµονή των αρθρώσεων. Οι τυπικές
www.pediatric-rheumathology.printo.it ΝΕΑΝΙΚΗ Ι ΙΟΠΑΘΗΣ ΑΡΘΡΙΤΙ Α Τι είναι; Η Νεανική Ιδιοπαθής Αρθρίτιδα (ΝΙΑ) είναι µία χρόνια νόσος που χαρακτηρίζεται από επίµονη φλεγµονή των αρθρώσεων. Οι τυπικές
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ. Εργαστήριο Γενετικής, ΓΠΑ
 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
ΘΕΡΑΠΕΥΤΙΚΟ ΠΡΩΤΟΚΟΛΛΟ ΑΞΟΝΙΚΗΣ ΣΠΟΝΔΥΛΑΡΘΡΙΤΙΔΑΣ
 ΘΕΡΑΠΕΥΤΙΚΟ ΠΡΩΤΟΚΟΛΛΟ ΑΞΟΝΙΚΗΣ ΣΠΟΝΔΥΛΑΡΘΡΙΤΙΔΑΣ Η Αξονική Σπονδυλαρθρίτιδα (ΑξΣπΑ) διακρίνεται σε αγκυλοποιητική σπονδυλαρθρίτιδα (ΑΣ) ή αξονική σπονδυλαρθρίτιδα με ακτινολογικά ευρήματα (ιερολαγονίτιδα
ΘΕΡΑΠΕΥΤΙΚΟ ΠΡΩΤΟΚΟΛΛΟ ΑΞΟΝΙΚΗΣ ΣΠΟΝΔΥΛΑΡΘΡΙΤΙΔΑΣ Η Αξονική Σπονδυλαρθρίτιδα (ΑξΣπΑ) διακρίνεται σε αγκυλοποιητική σπονδυλαρθρίτιδα (ΑΣ) ή αξονική σπονδυλαρθρίτιδα με ακτινολογικά ευρήματα (ιερολαγονίτιδα
Μαριάνθη Γεωργίτση Επίκουρη Καθηγήτρια Ιατρικής Βιολογίας-Γενετικής
 Μαριάνθη Γεωργίτση Επίκουρη Καθηγήτρια Ιατρικής Βιολογίας-Γενετικής Τομέας Βιολογικών Επιστημών και Προληπτικής Ιατρικής Σχολή Επιστημών Υγείας Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης E-mail: margeorgitsi@auth.gr
Μαριάνθη Γεωργίτση Επίκουρη Καθηγήτρια Ιατρικής Βιολογίας-Γενετικής Τομέας Βιολογικών Επιστημών και Προληπτικής Ιατρικής Σχολή Επιστημών Υγείας Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης E-mail: margeorgitsi@auth.gr
Υποστηρίζοντας τα παιδιά με γενετικά νοσήματα - Ο Δρόμος για την Θεραπεία Πέμπτη, 16 Ιούνιος :58
 Από: K-Life (Καθημερινή) Τα γενετικά νοσήματα είναι ιδιαίτερα σπάνιες ασθένειες που οφείλονται σε μεταλλάξεις γονιδίων. Τα παιδιά που πάσχουν από αυτά χρειάζονται φροντίδα, ψυχολογική στήριξη αλλά και
Από: K-Life (Καθημερινή) Τα γενετικά νοσήματα είναι ιδιαίτερα σπάνιες ασθένειες που οφείλονται σε μεταλλάξεις γονιδίων. Τα παιδιά που πάσχουν από αυτά χρειάζονται φροντίδα, ψυχολογική στήριξη αλλά και
Πρότυπα περίθαλψης (ΠΠ) για ανθρώπους με ρευματοειδή αρθρίτιδα
 Πρότυπα περίθαλψης (ΠΠ) για ανθρώπους με ρευματοειδή αρθρίτιδα Μετάφρασ η σε: Ολοκληρώθ ηκε από: Email: ΠΠ 1 Οι άνθρωποι με συμπτώματα ρευματοειδούς αρθρίτιδας (ΡΑ) θα πρέπει να έχουν έγκαιρη πρόσβαση
Πρότυπα περίθαλψης (ΠΠ) για ανθρώπους με ρευματοειδή αρθρίτιδα Μετάφρασ η σε: Ολοκληρώθ ηκε από: Email: ΠΠ 1 Οι άνθρωποι με συμπτώματα ρευματοειδούς αρθρίτιδας (ΡΑ) θα πρέπει να έχουν έγκαιρη πρόσβαση
ΘΕΡΑΠΕΥΤΙΚΗ ΠΡΟΣΕΓΓΙΣΗ ΑΣΘΕΝΗ ΜΕ ΟΡΟΑΡΝΗΤΙΚΗ ΣΠΟΝΔΥΛΑΡΘΡΟΠΑΘΕΙΑ. Χατζημιχαηλίδου Σοφία
 ΘΕΡΑΠΕΥΤΙΚΗ ΠΡΟΣΕΓΓΙΣΗ ΑΣΘΕΝΗ ΜΕ ΟΡΟΑΡΝΗΤΙΚΗ ΣΠΟΝΔΥΛΑΡΘΡΟΠΑΘΕΙΑ Χατζημιχαηλίδου Σοφία ΟΡΟΑΡΝΗΤΙΚΕΣ ΣΠΟΝΔΥΛΑΡΘΡΙΤΙΔΕΣ Οσφυαλγία (φλεγμονώδους τύπου) Ιερολαγονίτιδα Ασύμμετρη περιφερική αρθρίτιδα Ενθεσίτιδα
ΘΕΡΑΠΕΥΤΙΚΗ ΠΡΟΣΕΓΓΙΣΗ ΑΣΘΕΝΗ ΜΕ ΟΡΟΑΡΝΗΤΙΚΗ ΣΠΟΝΔΥΛΑΡΘΡΟΠΑΘΕΙΑ Χατζημιχαηλίδου Σοφία ΟΡΟΑΡΝΗΤΙΚΕΣ ΣΠΟΝΔΥΛΑΡΘΡΙΤΙΔΕΣ Οσφυαλγία (φλεγμονώδους τύπου) Ιερολαγονίτιδα Ασύμμετρη περιφερική αρθρίτιδα Ενθεσίτιδα
Σχετιζομενος Με Το NLRP-12 Υποτροπιαζων Πυρετος
 www.printo.it/pediatric-rheumatology/cy/intro Σχετιζομενος Με Το NLRP-12 Υποτροπιαζων Πυρετος Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Ο ΣΧΕΤΙΖΟΜΕΝΟΣ ΜΕ ΤΟ NLRP12 ΥΠΟΤΡΟΠΙΑΖΩΝ ΠΥΡΕΤΟΣ 1.1 Τι είναι; Ο σχετιζόμενος με
www.printo.it/pediatric-rheumatology/cy/intro Σχετιζομενος Με Το NLRP-12 Υποτροπιαζων Πυρετος Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Ο ΣΧΕΤΙΖΟΜΕΝΟΣ ΜΕ ΤΟ NLRP12 ΥΠΟΤΡΟΠΙΑΖΩΝ ΠΥΡΕΤΟΣ 1.1 Τι είναι; Ο σχετιζόμενος με
Παρουσίαση κλινικού περιστατικού. Αλεξάνδρα Φιλιπποπούλου Ειδικευόμενη ιατρός Ρευματολογίας Πανεπιστημιακού Γενικού Νοσοκομείου Πατρών
 Παρουσίαση κλινικού περιστατικού Αλεξάνδρα Φιλιπποπούλου Ειδικευόμενη ιατρός Ρευματολογίας Πανεπιστημιακού Γενικού Νοσοκομείου Πατρών Απρίλιος 2009 Ρευματολογική εκτίμηση νοσηλευόμενου ασθενούς εις ΟΦΘΑΛΜΟΛΟΓΙΚΗ
Παρουσίαση κλινικού περιστατικού Αλεξάνδρα Φιλιπποπούλου Ειδικευόμενη ιατρός Ρευματολογίας Πανεπιστημιακού Γενικού Νοσοκομείου Πατρών Απρίλιος 2009 Ρευματολογική εκτίμηση νοσηλευόμενου ασθενούς εις ΟΦΘΑΛΜΟΛΟΓΙΚΗ
Simponi (γολιμουμάμπη)
 EMA/792301/2018 EMEA/H/C/000992 Περίληψη EPAR για το κοινό Ανασκόπηση του Simponi και αιτιολογικό έγκρισης στην ΕΕ Τι είναι το Simponi και σε ποιες περιπτώσεις χρησιμοποιείται; Το Simponi είναι αντιφλεγμονώδες
EMA/792301/2018 EMEA/H/C/000992 Περίληψη EPAR για το κοινό Ανασκόπηση του Simponi και αιτιολογικό έγκρισης στην ΕΕ Τι είναι το Simponi και σε ποιες περιπτώσεις χρησιμοποιείται; Το Simponi είναι αντιφλεγμονώδες
Οικογενησ Μεσογειακοσ Πυρετοσ
 www.printo.it/pediatric-rheumatology/gr/intro Οικογενησ Μεσογειακοσ Πυρετοσ Έκδοση από 2016 2. ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ 2.1 Πως μπαίνει η διάγνωση; Γενικά ακολουθείται η παρακάτω προσέγγιση: Κλινική υποψία:
www.printo.it/pediatric-rheumatology/gr/intro Οικογενησ Μεσογειακοσ Πυρετοσ Έκδοση από 2016 2. ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ 2.1 Πως μπαίνει η διάγνωση; Γενικά ακολουθείται η παρακάτω προσέγγιση: Κλινική υποψία:
«β-μεσογειακή αναιμία: το πιο συχνό μονογονιδιακό νόσημα στη χώρα μας»
 Εργαστήριο Κυτταρογενετικής ΕΚΕΦΕ «Δημόκριτος» «β-μεσογειακή αναιμία: το πιο συχνό μονογονιδιακό νόσημα στη χώρα μας» Ζαχάκη Σοφία - Ουρανία Βιολόγος, MSc, PhD β μεσογειακή αναιμία Η θαλασσαιμία ή νόσος
Εργαστήριο Κυτταρογενετικής ΕΚΕΦΕ «Δημόκριτος» «β-μεσογειακή αναιμία: το πιο συχνό μονογονιδιακό νόσημα στη χώρα μας» Ζαχάκη Σοφία - Ουρανία Βιολόγος, MSc, PhD β μεσογειακή αναιμία Η θαλασσαιμία ή νόσος
4 Ο Περιστατικό: Ασθενής με προβλήματα λειτουργικότητας
 4 Ο Περιστατικό: Ασθενής με προβλήματα λειτουργικότητας Ασθενής με προβλήματα λειτουργικότητας Άνδρας, 60 ετών, συνταξιούχος εργάτης Από μηνός: Συμμετρική πολυαρθρίτιδα TJC= 22, SJC= 19 ΤΚΕ: 110 mm/1h
4 Ο Περιστατικό: Ασθενής με προβλήματα λειτουργικότητας Ασθενής με προβλήματα λειτουργικότητας Άνδρας, 60 ετών, συνταξιούχος εργάτης Από μηνός: Συμμετρική πολυαρθρίτιδα TJC= 22, SJC= 19 ΤΚΕ: 110 mm/1h
Πρώιµη έναρξη βιολογικής θεραπείας στις σπονδυλαρθρίτιδες. Γιάννης Ελ. Πάκας Ρευµατολόγος
 Πρώιµη έναρξη βιολογικής θεραπείας στις σπονδυλαρθρίτιδες Γιάννης Ελ. Πάκας Ρευµατολόγος Σπονδυλαρθρίτιδες(ΣπΑ) Κύριες εκδηλώσεις 1. Aξονική προσβολή/φλεγµονή ΣΣ 2. Περιφερική αρθρίτιδα 3. Περιφερική ενθεσίτιδα
Πρώιµη έναρξη βιολογικής θεραπείας στις σπονδυλαρθρίτιδες Γιάννης Ελ. Πάκας Ρευµατολόγος Σπονδυλαρθρίτιδες(ΣπΑ) Κύριες εκδηλώσεις 1. Aξονική προσβολή/φλεγµονή ΣΣ 2. Περιφερική αρθρίτιδα 3. Περιφερική ενθεσίτιδα
ΑΝΤΙ-DFS70 ΑΝΤΙΣΩΜΑΤΑ: ΝΕΟΣ ΒΙΟΔΕΙΚΤΗΣ ΣΤΗ ΔΙΑΓΝΩΣΤΙΚΗ ΠΡΟΣΕΓΓΙΣΗ ΤΩΝ ΣΥΣΤΗΜΑΤΙΚΩΝ ΑΥΤΟΑΝΟΣΩΝ ΡΕΥΜΑΤΙΚΩΝ ΝΟΣΗΜΑΤΩΝ
 ΑΝΤΙ-DFS70 ΑΝΤΙΣΩΜΑΤΑ: ΝΕΟΣ ΒΙΟΔΕΙΚΤΗΣ ΣΤΗ ΔΙΑΓΝΩΣΤΙΚΗ ΠΡΟΣΕΓΓΙΣΗ ΤΩΝ ΣΥΣΤΗΜΑΤΙΚΩΝ ΑΥΤΟΑΝΟΣΩΝ ΡΕΥΜΑΤΙΚΩΝ ΝΟΣΗΜΑΤΩΝ Α. Γιαννακού 2, Κ. Σουφλερός 1, Μ. Μπανταδάκη 2, Ε. Συνοδινού 1, Α.Μ. Μαρκαντωνάτου 2,
ΑΝΤΙ-DFS70 ΑΝΤΙΣΩΜΑΤΑ: ΝΕΟΣ ΒΙΟΔΕΙΚΤΗΣ ΣΤΗ ΔΙΑΓΝΩΣΤΙΚΗ ΠΡΟΣΕΓΓΙΣΗ ΤΩΝ ΣΥΣΤΗΜΑΤΙΚΩΝ ΑΥΤΟΑΝΟΣΩΝ ΡΕΥΜΑΤΙΚΩΝ ΝΟΣΗΜΑΤΩΝ Α. Γιαννακού 2, Κ. Σουφλερός 1, Μ. Μπανταδάκη 2, Ε. Συνοδινού 1, Α.Μ. Μαρκαντωνάτου 2,
Ορισμός επιδημιολογίας
 Ορισμός επιδημιολογίας Επιδημιολογία είναι η μελέτη της κατανομής των παραγόντων που επηρεάζουν τη συχνότητα των νοσημάτων στον άνθρωπο (MacMahon, 1970) Επιδημιολογία είναι η μελέτη της κατανομής των παραγόντων
Ορισμός επιδημιολογίας Επιδημιολογία είναι η μελέτη της κατανομής των παραγόντων που επηρεάζουν τη συχνότητα των νοσημάτων στον άνθρωπο (MacMahon, 1970) Επιδημιολογία είναι η μελέτη της κατανομής των παραγόντων
Dr. X. Baraliakos Rheumazentrum Ruhrgebiet Herne Ruhr-University Bochum Germany. 23-26 Ιουνίου 2011
 Ο ρευµατολόγος και η χρήση του µαγνητικού συντονισµού στην πρώιµη διάγνωση των σπονδυλαρθιτίδων και στην παρακολούθηση της αποτελεσµατικότητας της θεραπείας 23-26 Ιουνίου 2011 Dr. X. Baraliakos Rheumazentrum
Ο ρευµατολόγος και η χρήση του µαγνητικού συντονισµού στην πρώιµη διάγνωση των σπονδυλαρθιτίδων και στην παρακολούθηση της αποτελεσµατικότητας της θεραπείας 23-26 Ιουνίου 2011 Dr. X. Baraliakos Rheumazentrum
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
Γενικά χαρακτηριστικά στις αρθρίτιδες
 Γενικά χαρακτηριστικά στις αρθρίτιδες Φλεγμονώδεις αρθρίτιδες: Πόνος σε ηρεμία, βελτίωση με δραστηριότητα Εκφυλιστικές αρθροπάθειες: Πόνος με την καταπόνηση, βελτίωση με την ανάπαυση Εισβολή Απότομη: στην
Γενικά χαρακτηριστικά στις αρθρίτιδες Φλεγμονώδεις αρθρίτιδες: Πόνος σε ηρεμία, βελτίωση με δραστηριότητα Εκφυλιστικές αρθροπάθειες: Πόνος με την καταπόνηση, βελτίωση με την ανάπαυση Εισβολή Απότομη: στην
ΑΛΛΕΡΓΙΑ: Ο ΑΟΡΑΤΟΣ ΕΧΘΡΟΣ ΠΩΣ ΓΙΝΕΤΑΙ ΚΑΠΟΙΟΣ ΑΛΛΕΡΓΙΚΟΣ;
 ΑΛΛΕΡΓΙΑ: Ο ΑΟΡΑΤΟΣ ΕΧΘΡΟΣ ΠΩΣ ΓΙΝΕΤΑΙ ΚΑΠΟΙΟΣ ΑΛΛΕΡΓΙΚΟΣ; Αλλεργία, όπως ορίζει και η λέξη, σημαίνει άλλο έργο. Είναι η μη αναμενόμενη αντίδραση του ανοσιακού συστήματος του οργανισμού εναντίον ακίνδυνων
ΑΛΛΕΡΓΙΑ: Ο ΑΟΡΑΤΟΣ ΕΧΘΡΟΣ ΠΩΣ ΓΙΝΕΤΑΙ ΚΑΠΟΙΟΣ ΑΛΛΕΡΓΙΚΟΣ; Αλλεργία, όπως ορίζει και η λέξη, σημαίνει άλλο έργο. Είναι η μη αναμενόμενη αντίδραση του ανοσιακού συστήματος του οργανισμού εναντίον ακίνδυνων
Σύνοψη της προσέγγισης ασθενούς με πανκυτταροπενία. Ιατρικό Τμήμα Πανεπιστημίου Πατρών Απαρτιωμένη διδασκαλία στην Αιματολογία Αργύρης Συμεωνίδης
 Σύνοψη της προσέγγισης ασθενούς με πανκυτταροπενία Ιατρικό Τμήμα Πανεπιστημίου Πατρών Απαρτιωμένη διδασκαλία στην Αιματολογία Αργύρης Συμεωνίδης Αρχική κλινική προσέγγιση Συμπτωματικός ή μη συμπτωματικός
Σύνοψη της προσέγγισης ασθενούς με πανκυτταροπενία Ιατρικό Τμήμα Πανεπιστημίου Πατρών Απαρτιωμένη διδασκαλία στην Αιματολογία Αργύρης Συμεωνίδης Αρχική κλινική προσέγγιση Συμπτωματικός ή μη συμπτωματικός
 www.printo.it/pediatric-rheumatology/cy/intro Το σύνδρομο Blau Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ ΤΟ ΣΥΝΔΡΟΜΟ BLAU / ΝΕΑΝΙΚΗ ΣΑΡΚΟΕΙΔΩΣΗ 1.1 Τι είναι; Το σύνδρομο Blau είναι ένα γενετικό νόσημα που χαρακτηρίζεται
www.printo.it/pediatric-rheumatology/cy/intro Το σύνδρομο Blau Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ ΤΟ ΣΥΝΔΡΟΜΟ BLAU / ΝΕΑΝΙΚΗ ΣΑΡΚΟΕΙΔΩΣΗ 1.1 Τι είναι; Το σύνδρομο Blau είναι ένα γενετικό νόσημα που χαρακτηρίζεται
Ανι χνευση μεταλλα ξεων στον καρκι νο και εξατομικευμε νη θεραπει α
 Ανι χνευση μεταλλα ξεων στον καρκι νο και εξατομικευμε νη θεραπει α Περικλής Μακρυθανα σης, MD, PhD, FMH, PD Κλινικός γενετιστής Κύριος Ερευνητής Ίδρυμα Ιατροβιολογικών Ερευνών της Ακαδημι ας Αθηνών 4o
Ανι χνευση μεταλλα ξεων στον καρκι νο και εξατομικευμε νη θεραπει α Περικλής Μακρυθανα σης, MD, PhD, FMH, PD Κλινικός γενετιστής Κύριος Ερευνητής Ίδρυμα Ιατροβιολογικών Ερευνών της Ακαδημι ας Αθηνών 4o
ITP Ιδιοπαθής/ αυτοάνοση θρομβοπενική πορφύρα
 ITP Ιδιοπαθής/ αυτοάνοση θρομβοπενική πορφύρα Αθανασία Μουζάκη, Καθηγήτρια Εργαστηριακής Αιματολογίας-Αιμοδοσίας, Αιματολογικό Τμήμα, Παθολογική Κλινική, Τμήμα Ιατρικής, Παν/ο Πατρών Τα είδη της ITP είναι:
ITP Ιδιοπαθής/ αυτοάνοση θρομβοπενική πορφύρα Αθανασία Μουζάκη, Καθηγήτρια Εργαστηριακής Αιματολογίας-Αιμοδοσίας, Αιματολογικό Τμήμα, Παθολογική Κλινική, Τμήμα Ιατρικής, Παν/ο Πατρών Τα είδη της ITP είναι:
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας
 Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
-Αναστολή της οργανικής σύνδεσης του ιωδίου που προσλαμβάνεται από το θυρεοειδή αδένα -Ανοσοκατασταλτική δράση με αποτέλεσμα τη μείωση της παραγωγής
 Άννα Ναξάκη Επιμελήτρια Α Γ Παθολογική Κλινική ΠΑΡΑΓΩΓΑ ΘΕΙΟΥΡΙΑΣ(ΠΡΟΠΥΛΟ ΚΑΙ ΜΕΘΥΛΟΘΕΙΟΥΡΑΚΙΛΗ) ΠΑΡΑΓΩΓΑ ΙΜΙΔΑΖΟΛΗΣ(ΚΑΡΒΙΜΑΖΟΛΗ ΚΑΙ ΘΕΙΑΜΑΖΟΛΗ) -Αναστολή της οργανικής σύνδεσης του ιωδίου που προσλαμβάνεται
Άννα Ναξάκη Επιμελήτρια Α Γ Παθολογική Κλινική ΠΑΡΑΓΩΓΑ ΘΕΙΟΥΡΙΑΣ(ΠΡΟΠΥΛΟ ΚΑΙ ΜΕΘΥΛΟΘΕΙΟΥΡΑΚΙΛΗ) ΠΑΡΑΓΩΓΑ ΙΜΙΔΑΖΟΛΗΣ(ΚΑΡΒΙΜΑΖΟΛΗ ΚΑΙ ΘΕΙΑΜΑΖΟΛΗ) -Αναστολή της οργανικής σύνδεσης του ιωδίου που προσλαμβάνεται
ενήλικες με ενεργή και εξελισσόμενη ψωριασική αρθρίτιδα (νόσος που προκαλεί ερυθρές, φολιδωτές κηλίδες στο δέρμα και φλεγμονή των αρθρώσεων)
 EMA/178267/2015 EMEA/H/C/000481 Περίληψη EPAR για το κοινό αδαλιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
EMA/178267/2015 EMEA/H/C/000481 Περίληψη EPAR για το κοινό αδαλιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα
 Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
Το Humira είναι φάρμακο που δρα στο ανοσοποιητικό σύστημα και χρησιμοποιείται για τη θεραπεία των ακόλουθων παθήσεων:
 EMA/518634/2017 EMEA/H/C/000481 Περίληψη EPAR για το κοινό αδαλιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
EMA/518634/2017 EMEA/H/C/000481 Περίληψη EPAR για το κοινό αδαλιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
Η ζωη µου. µε την ψωριαση. Eνημερωτικό φυλλάδιο για τη νόσο της ψωρίασης
 Πανελλήνιος Σύλλογος Ασθενών με Ψωρίαση και Ψωριασική Αρθρίτιδα Αριστοτέλους 21, Θεσσαλονίκη, τηλ 21315 553 780, email:epidermia.greece@gmail.com www.epidermia.gr Επιστημονική Επιμέλεια Ελληνική Δερματολογική
Πανελλήνιος Σύλλογος Ασθενών με Ψωρίαση και Ψωριασική Αρθρίτιδα Αριστοτέλους 21, Θεσσαλονίκη, τηλ 21315 553 780, email:epidermia.greece@gmail.com www.epidermia.gr Επιστημονική Επιμέλεια Ελληνική Δερματολογική
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών
 Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Διερεύνηση των μηχανισμών δυσλειτουργίας
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Διερεύνηση των μηχανισμών δυσλειτουργίας
Ασθενής με προβλήματα στη συμμόρφωση. Μαρία Ευσταθίου
 Ασθενής με προβλήματα στη συμμόρφωση Μαρία Ευσταθίου Ασθενής με ιδιαιτερότητες στον τρόπο ζωής Άνδρας, 30 ετών, μουσικός Από διμήνου: Συμμετρική πολυαρθρίτιδα TJC= 8, SJC= 7 ΤΚΕ: 51mm/1h CRP: 8,1 mg% (ΦΤ:
Ασθενής με προβλήματα στη συμμόρφωση Μαρία Ευσταθίου Ασθενής με ιδιαιτερότητες στον τρόπο ζωής Άνδρας, 30 ετών, μουσικός Από διμήνου: Συμμετρική πολυαρθρίτιδα TJC= 8, SJC= 7 ΤΚΕ: 51mm/1h CRP: 8,1 mg% (ΦΤ:
Πολυξένη Πρατσίδου-Γκέρτση Παιδιατρικό Ανοσολογικό & Ρευματολογικό Κέντρο Αναφοράς Α Παιδιατρική Κλινική ΑΠΘ Ιπποκράτειο Νοσοκομείο, Θεσσαλονίκη
 Νεανική Ιδιοπαθής Αρθρίτιδα: Σπανιότερες μορφές και πιο άτυπες εκδηλώσεις Πολυξένη Πρατσίδου-Γκέρτση Παιδιατρικό Ανοσολογικό & Ρευματολογικό Κέντρο Αναφοράς Α Παιδιατρική Κλινική ΑΠΘ Ιπποκράτειο Νοσοκομείο,
Νεανική Ιδιοπαθής Αρθρίτιδα: Σπανιότερες μορφές και πιο άτυπες εκδηλώσεις Πολυξένη Πρατσίδου-Γκέρτση Παιδιατρικό Ανοσολογικό & Ρευματολογικό Κέντρο Αναφοράς Α Παιδιατρική Κλινική ΑΠΘ Ιπποκράτειο Νοσοκομείο,
Το Simponi είναι αντιφλεγμονώδες φάρμακο. Χορηγείται για τη θεραπεία των ακόλουθων νόσων:
 EMA/412395/2016 EMEA/H/C/000992 Περίληψη EPAR για το κοινό γολιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
EMA/412395/2016 EMEA/H/C/000992 Περίληψη EPAR για το κοινό γολιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
είναι τα αυτοάνοσα νοσήματα
 είναι τα αυτοάνοσα νοσήματα Χ.Μ. Μουτσόπουλος Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών ο ανοσολογικό (αμυντικό) σύστημα έχει σκοπό την προστασία του οργανισμού από ξένους εισβολείς, όπως είναι τα
είναι τα αυτοάνοσα νοσήματα Χ.Μ. Μουτσόπουλος Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών ο ανοσολογικό (αμυντικό) σύστημα έχει σκοπό την προστασία του οργανισμού από ξένους εισβολείς, όπως είναι τα
Το Simponi είναι αντιφλεγμονώδες φάρμακο. Χορηγείται σε ενήλικες για τη θεραπεία των ακόλουθων νόσων:
 EMA/411054/2015 EMEA/H/C/000992 Περίληψη EPAR για το κοινό γολιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
EMA/411054/2015 EMEA/H/C/000992 Περίληψη EPAR για το κοινό γολιμουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
4Πανελλήνιο. A Ανακοίνωση. Ρευµατικών & Αυτοάνοσων Παθήσεων. Κεντρικής Ελλάδος Σεπτεμβρίου. Σε συνεργασία.
 o 4Πανελλήνιο Συνέδριο Ρευµατικών & Αυτοάνοσων Παθήσεων Κεντρικής Ελλάδος 26-28 2014 Σεπτεμβρίου Larissa Imperial Hotel Λάρισα Σε συνεργασία με τη Ρευματολογική Κλινική Πανεπιστημίου Θεσσαλίας Υπό την
o 4Πανελλήνιο Συνέδριο Ρευµατικών & Αυτοάνοσων Παθήσεων Κεντρικής Ελλάδος 26-28 2014 Σεπτεμβρίου Larissa Imperial Hotel Λάρισα Σε συνεργασία με τη Ρευματολογική Κλινική Πανεπιστημίου Θεσσαλίας Υπό την
Η θέση των αντι-tnf παραγόντων στην αντιμετώπιση της Ψωριασικής Αρθρίτιδας. Κυριακή Μποκή Λευκάδα
 Η θέση των αντι-tnf παραγόντων στην αντιμετώπιση της Ψωριασικής Αρθρίτιδας Κυριακή Μποκή Λευκάδα 23-6-2012 Κύριες κλινικές εκδηλώσεις της Ψωριασικής Αρθρίτιδας, σύμφωνα με την ομάδα GRAPPA 94% % 53% 46%
Η θέση των αντι-tnf παραγόντων στην αντιμετώπιση της Ψωριασικής Αρθρίτιδας Κυριακή Μποκή Λευκάδα 23-6-2012 Κύριες κλινικές εκδηλώσεις της Ψωριασικής Αρθρίτιδας, σύμφωνα με την ομάδα GRAPPA 94% % 53% 46%
 www.printo.it/pediatric-rheumatology/gr/intro Majeed Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ ΤΟ MAJEED 1.1 Τι είναι; Το σύνδρομο Majeed είναι ένα σπάνιο γενετικό νόσημα. Τα προσβεβλημένα παιδιά πάσχουν από χρόνια
www.printo.it/pediatric-rheumatology/gr/intro Majeed Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ ΤΟ MAJEED 1.1 Τι είναι; Το σύνδρομο Majeed είναι ένα σπάνιο γενετικό νόσημα. Τα προσβεβλημένα παιδιά πάσχουν από χρόνια
Οστεοαρθρίτιδα την 3 η χιλιετία. Διευθυντής Ε.Σ.Υ. Ρευματολογική Κλινική - Γ.Ν.Α. «Γιώργος Γεννηματάς»
 Η Οστεοαρθρίτιδα την 3 η χιλιετία Δρ Αθανάσιος Γεωργούντζος Διευθυντής Ε.Σ.Υ. Ρευματολογική Κλινική - Γ.Ν.Α. «Γιώργος Γεννηματάς» Σύγκρουση συμφερόντων Conflict of interest Κανένα για αυτήν την παρουσίαση
Η Οστεοαρθρίτιδα την 3 η χιλιετία Δρ Αθανάσιος Γεωργούντζος Διευθυντής Ε.Σ.Υ. Ρευματολογική Κλινική - Γ.Ν.Α. «Γιώργος Γεννηματάς» Σύγκρουση συμφερόντων Conflict of interest Κανένα για αυτήν την παρουσίαση
ΠΡΩΤΟΚΟΛΛΟ ΕΡΕΥΝΑΣ ΜΥΟΚΑΡ ΙΑΚΗ ΑΝΑΓΕΝΝΗΣΗ ΜΕΤΑ ΤΟ ΕΜΦΡΑΓΜΑ ΕΡΕΥΝΗΤΙΚΗ ΟΜΑ Α
 ΠΡΩΤΟΚΟΛΛΟ ΕΡΕΥΝΑΣ ΜΥΟΚΑΡ ΙΑΚΗ ΑΝΑΓΕΝΝΗΣΗ ΜΕΤΑ ΤΟ ΕΜΦΡΑΓΜΑ ΕΡΕΥΝΗΤΙΚΗ ΟΜΑ Α ΘΕΟΦΙΛΟΣ ΚΩΛΕΤΤΗΣ ΑΠΟΣΤΟΛΟΣ ΠΑΠΑΛΟΗΣ ΓΙΑΝΝΗΣ ΜΠΑΛΤΟΓΙΑΝΝΗΣ ΗΜΗΤΡΙΟΣ ΟΙΚΟΝΟΜΙ ΗΣ ΜΑΡΙΑ ΑΓΓΕΛΑΚΗ ΑΝΤΩΝΙΟΣ ΒΛΑΧΟΣ ΑΓΑΘΟΚΛΕΙΑ ΜΗΤΣΗ
ΠΡΩΤΟΚΟΛΛΟ ΕΡΕΥΝΑΣ ΜΥΟΚΑΡ ΙΑΚΗ ΑΝΑΓΕΝΝΗΣΗ ΜΕΤΑ ΤΟ ΕΜΦΡΑΓΜΑ ΕΡΕΥΝΗΤΙΚΗ ΟΜΑ Α ΘΕΟΦΙΛΟΣ ΚΩΛΕΤΤΗΣ ΑΠΟΣΤΟΛΟΣ ΠΑΠΑΛΟΗΣ ΓΙΑΝΝΗΣ ΜΠΑΛΤΟΓΙΑΝΝΗΣ ΗΜΗΤΡΙΟΣ ΟΙΚΟΝΟΜΙ ΗΣ ΜΑΡΙΑ ΑΓΓΕΛΑΚΗ ΑΝΤΩΝΙΟΣ ΒΛΑΧΟΣ ΑΓΑΘΟΚΛΕΙΑ ΜΗΤΣΗ
Με ποια συμπτώματα μπορεί να εκδηλώνεται η κοιλιοκάκη;
 ΚΟΙΛΙΟΚΑΚΗ Σαββίδου Αβρόρα Η κοιλιοκάκη είναι η δυσανεξία (κάτι που ο οργανισμός δεν ανέχεται) στη γλουτένη, πρωτεΐνη που υπάρχει στο σιτάρι, το κριθάρι, τη βρώμη και τη σίκαλη. Η αντίδραση του οργανισμού
ΚΟΙΛΙΟΚΑΚΗ Σαββίδου Αβρόρα Η κοιλιοκάκη είναι η δυσανεξία (κάτι που ο οργανισμός δεν ανέχεται) στη γλουτένη, πρωτεΐνη που υπάρχει στο σιτάρι, το κριθάρι, τη βρώμη και τη σίκαλη. Η αντίδραση του οργανισμού
Σύγχρονη θεραπευτική στρατηγική ασθενών με ρευματοειδή αρθρίτιδα
 Στρογγυλό Τραπέζι Ρευματολογία Σύγχρονη θεραπευτική στρατηγική ασθενών με ρευματοειδή αρθρίτιδα Δημήτριος Βασιλόπουλος Ιατρική Σχολή ΕΚΠΑ Β Παθολογική Κλινική και Ομώνυμο Εργαστήριο Ιπποκράτειο Γενικό
Στρογγυλό Τραπέζι Ρευματολογία Σύγχρονη θεραπευτική στρατηγική ασθενών με ρευματοειδή αρθρίτιδα Δημήτριος Βασιλόπουλος Ιατρική Σχολή ΕΚΠΑ Β Παθολογική Κλινική και Ομώνυμο Εργαστήριο Ιπποκράτειο Γενικό
Επιστημονικό Πρόγραμμα
 Επιστημονικό Πρόγραμμα Πέμπτη 23 Μαΐου 2013 17.00-20.30 Ώρες λειτουργίας Γραμματείας - Εγγραφές 19.30-19.45 Τελετή Έναρξης Καλοσώρισμα προέδρου Προεδρείο: Λάζαρος Σακκάς, Χαράλαμπος Μπερμπερίδης 19.45-20.30
Επιστημονικό Πρόγραμμα Πέμπτη 23 Μαΐου 2013 17.00-20.30 Ώρες λειτουργίας Γραμματείας - Εγγραφές 19.30-19.45 Τελετή Έναρξης Καλοσώρισμα προέδρου Προεδρείο: Λάζαρος Σακκάς, Χαράλαμπος Μπερμπερίδης 19.45-20.30
Δείκτες ποιότητας της υγειονοµικής περίθαλψης (HCQI) όσον αφορά την οστεοαρθρίτιδα (OA)
 Δείκτες ποιότητας της υγειονοµικής περίθαλψης (HCQI) όσον αφορά την οστεοαρθρίτιδα (OA) HCQI OA 1: Όταν διαγιγνώσκεται συµπτωµατική οστεοαρθρίτιδα σε έναν ασθενή, θα πρέπει να αξιολογείται ο πόνος, η λειτουργική
Δείκτες ποιότητας της υγειονοµικής περίθαλψης (HCQI) όσον αφορά την οστεοαρθρίτιδα (OA) HCQI OA 1: Όταν διαγιγνώσκεται συµπτωµατική οστεοαρθρίτιδα σε έναν ασθενή, θα πρέπει να αξιολογείται ο πόνος, η λειτουργική
Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I. Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ.
 Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 14/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Γενικά στοιχεία
Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 14/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Γενικά στοιχεία
Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών
 Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών Οι ρευματικές παθήσεις είναι συχνές στην αναπαραγωγική ηλικία των γυναικών. Στην πρόσφατη πανελλήνια επιδημιολογική έρευνα για τις ρευματικές παθήσεις στο γενικό
Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών Οι ρευματικές παθήσεις είναι συχνές στην αναπαραγωγική ηλικία των γυναικών. Στην πρόσφατη πανελλήνια επιδημιολογική έρευνα για τις ρευματικές παθήσεις στο γενικό
Επιλεγόµενο µάθηµα:λευχαιµίες. Γεωργόπουλος Χρήστος Καρκατσούλης Μάριος Μπρίκος Νικήτας
 Επιλεγόµενο µάθηµα:λευχαιµίες Γεωργόπουλος Χρήστος Καρκατσούλης Μάριος Μπρίκος Νικήτας Ανοσολογία και καρκίνος Γενετικές και κυτταρικές αλλαγές που συµβαίνουν στον καρκίνο προσφέρουν στο ανοσιακό σύστηµα
Επιλεγόµενο µάθηµα:λευχαιµίες Γεωργόπουλος Χρήστος Καρκατσούλης Μάριος Μπρίκος Νικήτας Ανοσολογία και καρκίνος Γενετικές και κυτταρικές αλλαγές που συµβαίνουν στον καρκίνο προσφέρουν στο ανοσιακό σύστηµα
Εισαγωγή στη νοσολογία του µυοσκελετικού συστήµατος
 Εισαγωγή στη νοσολογία του µυοσκελετικού συστήµατος ηµήτριος Βασιλόπουλος B Παθολογική Κλινική και Οµώνυµο Εργαστήριο Ιατρική Σχολή Εθνικού και Καποδιστριακού Πανεπιστηµίου Αθηνών Ιπποκράτειο ΓΝΑ Μυοσκελετικά
Εισαγωγή στη νοσολογία του µυοσκελετικού συστήµατος ηµήτριος Βασιλόπουλος B Παθολογική Κλινική και Οµώνυµο Εργαστήριο Ιατρική Σχολή Εθνικού και Καποδιστριακού Πανεπιστηµίου Αθηνών Ιπποκράτειο ΓΝΑ Μυοσκελετικά
ΑΝΟΣΟΒΙΟΛΟΓΙΑ. Εξεταστική Ιανουαρίου 2010
 Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
ΠΡΟΚΑΤΑΡΚΤΙΚΟ ΕΠΙΣΤΗΜΟΝΙΚΟ και ΩΡΟΛΟΓΙΟ ΠΡΟΓΡΑΜΜΑ
 ΕΠΙΣΤΗΜΟΝΙΚΗ ΕΤΑΙΡΕΙΑ ΓΙΑ ΤΗ ΜΥΟΣΚΕΛΕΤΙΚΗ ΥΓΕΙΑ - (ΕΠΕΜΥ) 6 ο Επιστημονικό Συμπόσιο Μυοσκελετικών Παθήσεων - ΕΠΕΜΥ 2014 «Εξελίξεις στις φλεγμονώδεις ρευματικές παθήσεις και στα νοσήματα του οστικού μεταβολισμού»
ΕΠΙΣΤΗΜΟΝΙΚΗ ΕΤΑΙΡΕΙΑ ΓΙΑ ΤΗ ΜΥΟΣΚΕΛΕΤΙΚΗ ΥΓΕΙΑ - (ΕΠΕΜΥ) 6 ο Επιστημονικό Συμπόσιο Μυοσκελετικών Παθήσεων - ΕΠΕΜΥ 2014 «Εξελίξεις στις φλεγμονώδεις ρευματικές παθήσεις και στα νοσήματα του οστικού μεταβολισμού»
ΚΛΙΝΙΚΗ ΕΡΕΥΝΑ ΣΤΗΝ ΠΑΙΔΟΨΥΧΙΑΤΡΙΚΗ
 ΠΑΝΕΠΙΣΤΗΜΙΑΚΗ ΠΑΙΔΟΨΥΧΙΑΤΡΙΚΗ ΚΛΙΝΙΚΗ ΝΟΣΟΚΟΜΕΙΟ ΠΑΙΔΩΝ «Η ΑΓΙΑ ΣΟΦΙΑ» ΚΛΙΝΙΚΗ ΕΡΕΥΝΑ ΣΤΗΝ ΠΑΙΔΟΨΥΧΙΑΤΡΙΚΗ Γιώργος Γιαννακόπουλος, Ειδ. Παιδοψυχίατρος Στρογγυλό Τραπέζι: «Οι διάφορες διαστάσεις της Διασυνδετικής-
ΠΑΝΕΠΙΣΤΗΜΙΑΚΗ ΠΑΙΔΟΨΥΧΙΑΤΡΙΚΗ ΚΛΙΝΙΚΗ ΝΟΣΟΚΟΜΕΙΟ ΠΑΙΔΩΝ «Η ΑΓΙΑ ΣΟΦΙΑ» ΚΛΙΝΙΚΗ ΕΡΕΥΝΑ ΣΤΗΝ ΠΑΙΔΟΨΥΧΙΑΤΡΙΚΗ Γιώργος Γιαννακόπουλος, Ειδ. Παιδοψυχίατρος Στρογγυλό Τραπέζι: «Οι διάφορες διαστάσεις της Διασυνδετικής-
ΠΡΩΤΟΚΟΛΛΑ ΘΕΡΑΠΕΥΤΙΚΗΣ ΑΣΚΗΣΗΣ ΣΤΙΣ ΟΣΤΕΟΑΡΘΡΙΤΙΔΕΣ
 ΠΡΩΤΟΚΟΛΛΑ ΘΕΡΑΠΕΥΤΙΚΗΣ ΑΣΚΗΣΗΣ ΣΤΙΣ ΟΣΤΕΟΑΡΘΡΙΤΙΔΕΣ Οι αρθρίτιδες και γενικά τα ρευματικά νοσήματα είναι από τις κυριότερες αιτίες μυοσκελετικού άλγους και αναπηρίας παγκοσμίως. Ενας στους 7 ασθενείς
ΠΡΩΤΟΚΟΛΛΑ ΘΕΡΑΠΕΥΤΙΚΗΣ ΑΣΚΗΣΗΣ ΣΤΙΣ ΟΣΤΕΟΑΡΘΡΙΤΙΔΕΣ Οι αρθρίτιδες και γενικά τα ρευματικά νοσήματα είναι από τις κυριότερες αιτίες μυοσκελετικού άλγους και αναπηρίας παγκοσμίως. Ενας στους 7 ασθενείς
Ρευματικός Πυρετός και Μεταστρεπτοκοκκική Αντιδραστική Αρθρίτιδα
 www.printo.it/pediatric-rheumatology/gr/intro Ρευματικός Πυρετός και Μεταστρεπτοκοκκική Αντιδραστική Αρθρίτιδα Έκδοση από 2016 2. Διάγνωση και θεραπεία 2.1 Πώς μπαίνει η διάγνωση; Τα κλινικά ευρήματα και
www.printo.it/pediatric-rheumatology/gr/intro Ρευματικός Πυρετός και Μεταστρεπτοκοκκική Αντιδραστική Αρθρίτιδα Έκδοση από 2016 2. Διάγνωση και θεραπεία 2.1 Πώς μπαίνει η διάγνωση; Τα κλινικά ευρήματα και
ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ. Εισαγωγή στην αιματολογία
 ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ Εισαγωγή στην αιματολογία Αιματολογία Κλινική και εργαστηριακή Διαγνωστική και θεραπευτική Αυτόνομη και συνεργατική Αίμα-Λειτουργίες Μεταφορά οξυγόνου Απομάκρυνση
ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ Εισαγωγή στην αιματολογία Αιματολογία Κλινική και εργαστηριακή Διαγνωστική και θεραπευτική Αυτόνομη και συνεργατική Αίμα-Λειτουργίες Μεταφορά οξυγόνου Απομάκρυνση
Αντιγριπικός εμβολιασμός για τους επαγγελματίες υγείας
 Αντιγριπικός εμβολιασμός για τους επαγγελματίες υγείας 1. Γιατί είναι απαραίτητος ο εμβολιασμός; o Η γρίπη είναι σοβαρή νόσος και ευθύνεται για ένα σημαντικό ποσοστό νοσηρότητας και θνητότητας ετησίως.
Αντιγριπικός εμβολιασμός για τους επαγγελματίες υγείας 1. Γιατί είναι απαραίτητος ο εμβολιασμός; o Η γρίπη είναι σοβαρή νόσος και ευθύνεται για ένα σημαντικό ποσοστό νοσηρότητας και θνητότητας ετησίως.
Εβδομαδιαία Έκθεση Επιδημιολογικής Επιτήρησης της Γρίπης 2 Φεβρουαρίου 2012
 ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ Εβδομαδιαία Έκθεση Επιδημιολογικής Επιτήρησης της Γρίπης 2 Φεβρουαρίου 2012 Κατά την τρέχουσα περίοδο, γίνεται εβδομαδιαία ανακεφαλαίωση των επιδημιολογικών
ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ Εβδομαδιαία Έκθεση Επιδημιολογικής Επιτήρησης της Γρίπης 2 Φεβρουαρίου 2012 Κατά την τρέχουσα περίοδο, γίνεται εβδομαδιαία ανακεφαλαίωση των επιδημιολογικών
Ρευματοειδής αρθρίτιδα. Δημήτριος Βασιλόπουλος B Παθολογική Κλινική Ιατρική Σχολή Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών Ιπποκράτειο ΓΝΑ
 Ρευματοειδής αρθρίτιδα Δημήτριος Βασιλόπουλος B Παθολογική Κλινική Ιατρική Σχολή Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών Ιπποκράτειο ΓΝΑ Μυοσκελετικά νοσήματα Φλεγμονώδεις παθήσεις: - μυοσκελετικού
Ρευματοειδής αρθρίτιδα Δημήτριος Βασιλόπουλος B Παθολογική Κλινική Ιατρική Σχολή Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών Ιπποκράτειο ΓΝΑ Μυοσκελετικά νοσήματα Φλεγμονώδεις παθήσεις: - μυοσκελετικού
ΠΕΡΙΛΗΨΗ ΑΠΟ ΤΟ FALK SYMPOSIUM 196 6 & 7 MARCH, 2015 FRANKFURT, GERMANY
 ΠΕΡΙΛΗΨΗ ΑΠΟ ΤΟ FALK SYMPOSIUM 196 6 & 7 MARCH, 2015 FRANKFURT, GERMANY Βασικά σημεία ενδιαφέροντος στο τελευταίο Falk Symposium No196 στη Φρανκφούρτη της Γερμανίας αποτέλεσαν οι εξελίξεις στο πεδίο της
ΠΕΡΙΛΗΨΗ ΑΠΟ ΤΟ FALK SYMPOSIUM 196 6 & 7 MARCH, 2015 FRANKFURT, GERMANY Βασικά σημεία ενδιαφέροντος στο τελευταίο Falk Symposium No196 στη Φρανκφούρτη της Γερμανίας αποτέλεσαν οι εξελίξεις στο πεδίο της
