Διερεύνηση της γενετικής προδιάθεσης της Πλάγιας Αμυοτροφικής Σκλήρυνσης στον Ελληνικό πληθυσμό
|
|
|
- Ἀδελφός Γεννάδιος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Μεταπτυχιακό Δίπλωμα Ειδίκευσης: Διερεύνηση της γενετικής προδιάθεσης της Πλάγιας Αμυοτροφικής Σκλήρυνσης στον Ελληνικό πληθυσμό ΜΕΡΚΟΥΡΗ - ΠΑΠΑΔΗΜΑ ΕΛΕΝΗ ΠΑΤΡΑ, ΣΕΠΤΕΜΒΡΙΟΣ
2 Τριμελής Εξεταστική Επιτροπή Γεώργιος Π. Πατρινός (Επιβλέπων) Αναπληρωτής Καθηγητής Φαρμακευτικής Βιοτεχνολογίας και Φαρμακογενωμικής, Τμήμα Φαρμακευτικής Πανεπιστημίου Πατρών Κωνσταντίνος Πουλάς Αναπληρωτής Καθηγητής Βιοχημείας, Τμήμα Φαρμακευτικής Πανεπιστημίου Πατρών Σταύρος Τοπούζης Επίκουρος Καθηγητής Τοξικολογίας και Φαρμακολογίας, Τμήμα Φαρμακευτικής Πανεπιστημίου Πατρών 2
3 Στον Παππού μου, Γεώργιο Σ. Παπαδήμα 3
4 Πρόλογος και Ευχαριστίες Η παρούσα εργασία εκπονήθηκε στα πλαίσια του Μεταπτυχιακού Διπλώματος Ειδίκευσης για την ολοκλήρωση του κύκλου σπουδών, στα πλαίσια του Προγράμματος Μεταπτυχιακών Σπουδών στις Φαρμακευτικές Επιστήμες και την Τεχνολογία του τμήματος Φαρμακευτικής, του Πανεπιστημίου Πατρών. Το εργαστηριακό κομμάτι, στο μεγαλύτερο μέρος του, πραγματοποιήθηκε στο Εργαστήριο Μοριακής Βιολογίας και Ανοσολογίας κατά τα ακαδημαϊκά έτη , υπό την επίβλεψη του Αναπληρωτή Καθηγητή Δρ. Πατρινού Π. Γεώργιου. Μέρος του Μεταπτυχιακού Διπλώματος Ειδίκευσης εκπονήθηκε στο Πανεπιστήμιο του Κάλιαρι της Ιταλίας, Universita di Cagliari, Dipartamento di Scienze Mediche M.ARESU, υπό την επίβλεψη και καθοδήγηση του Dr. Sandro Orrù, και του συνεργάτη του Nicola Orrù στα πλαίσια του τρίμηνου Προγράμματος Κινητικότητας Δια Βίου Μάθηση / Erasmus Placements , τους οποίους και ευχαριστώ πολύ. Μιλώντας από καρδιάς, αισθάνομαι την ανάγκη να ευχαριστήσω θερμά τον αναπληρωτή καθηγητή Γεώργιο Π. Πατρινό για την ευκαιρία που μου έδωσε να εργαστώ δίπλα του και την εμπιστοσύνη που μου έδειξε, καθώς και τη στήριξη και καθοδήγηση που μου προσέφερε σε όλα τα στάδια της Προπτυχιακής και μετέπειτα Μεταπτυχιακής διπλωματικής μου εργασίας. Επίσης θα ήθελα να ευχαριστήσω από καρδιάς τον αναπληρωτή καθηγητή Κωνσταντίνο Πουλά για την πολύπλευρη βοήθεια που προσέφερε στην προσπάθεια μου ως καθηγητής και ως άνθρωπος και τον επίκουρο καθηγητή Σταύρο Τοπούζη για τις χρήσιμες συμβουλές και τις γνώσεις που μου προσέφερε. Ιδιαίτερες ευχαριστίες οφείλω στη Δρ. Μαριάννα Γεωργίτση, στη Δρ. Θεοδώρα Κατσίλα και στην υποψήφια Διδάκτωρ Ζωή Ζαγορίτη που η συμβολή τους ήταν καθοριστική στην εξέλιξη της μεταπτυχιακής μου εργασίας. Επίσης, επιθυμώ να ευχαριστήσω ειδικά, για τις συμβουλές τους, τη βοήθεια τους στην πορεία μου στο Εργαστήριο Μοριακής Βιολογίας και Ανοσολογίας και την άριστη συνεργασία τους, τον Δρ. Γεώργιο Λαγουμιτζή, τον Δρ. Μανούσο Καμπούρη, την υποψήφια Διδάκτωρ Ευαγγελία-Ειρήνη Τσερμπίνη αλλά και τις υποψήφιες μεταπτυχιακές φοιτήτριες Ελένη Νταλαμπύρα και Νάντια Φλωρά, για τις γνώσεις που απέκτησα κατά την συνεργασία μας και την υποστήριξη. Επίσης, ευχαριστώ πολύ όλα τα άτομα του Εργαστηρίου Μοριακής Βιολογίας και Ανοσολογίας, τα οποία συντέλεσαν με τον τρόπο τους στην επιτυχή ολοκλήρωση του μεταπτυχιακού μου. Τέλος, θα ήθελα να εκφράσω την ευγνωμοσύνη μου στην οικογένεια μου και τους φίλους μου γιατί στάθηκαν δίπλα μου σε αυτή μου την προσπάθεια, προσφέροντας μου συμπαράσταση και κατανόηση σε κάθε δύσκολη μου στιγμή. Ελένη Μερκούρη Παπαδήμα Αύγουστος
5 ΠΕΡΙΕΧΟΜΕΝΑ ΣΥΝΤΜΗΣΕΙΣ - ΞΕΝΟΓΛΩΣΣΟΙ ΟΡΟΙ 7 Α. ΠΕΡΙΛΗΨΗ ABSTRACT..140 Β. ΕΙΣΑΓΩΓΗ..8 Β.1 Πλάγια Αμυοτροφική Σκλήρυνση (ALS)..9 Β.1.1 Γενικά στοιχεία για την Πλάγια Αμυοτροφική Σκλήρυνση... 9 Β.1.2 Οικογενής και Σποραδική μορφή της Πλάγιας Αμυοτροφικής Σκλήρυνσης Β.1.3 Επιδημιολογικά στοιχεία για τη νόσο 9 Β.1.4 Μηχανισμοί παθογένειας Β.1.5 Ευαισθησία των νευρικών κυττάρων Β.1.6 Κλινικά και Ιστοπαθολογικά Ευρήματα...20 Β.1.7 Κριτήρια Διάγνωσης και Διαφορική Διάγνωση Β Κριτήρια διάγνωσης El Escorial Β Διαγνωστικές κατηγορίες Β Διαφορική διάγνωση Β Παράγοντες πρόγνωσης Β.1.8 Θεραπεία και θεραπευτικές προσεγγίσεις. 26 Β.1.9 Γενετικοί παράγοντες που σχετίζονται με την Πλάγια Αμυοτροφική Σκλήρυνση Β Ετερογένεια της νόσου. 30 Β Γενετική στη διάγνωση της ALS.. 30 Β Διερεύνηση της Γενετικής προδιάθεσης...30 Β H γενετική βάση της Οικογενούς Πλαγίας Αμυοτροφικής Σκλήρυνσης..34 Β Από τη γενετική αιτία στην εκδήλωση του φαινοτύπου.36 Β Τα κυριότερα γονίδια..37 Β Γενετική της Σποραδικής Πλάγιας Αμυοτροφικής Σκλήρυνσης Β Τροποποιητικά της νόσου γονίδια.44 Γ. ΣΚΟΠΟΣ ΤΗΣ ΕΡΓΑΣΙΑΣ. 45 Δ. ΥΛΙΚΑ ΚΑΙ ΜΕΘΟΔΟΙ...47 Δ.1 Επεξεργασία δεδομένων Αλληλούχησης Ολόκληρου του Γονιδιώματος..48 Δ.1.1 Επιλογή πολυμορφισμών - στόχων 1η προσέγγιση.48 Δ.1.2 Επιλογή πολυμορφισμών - στόχων 2 η προσέγγιση Δ.1.3 Επιλογή πολυμορφισμών - στόχων, 3 η προσέγγιση
6 Δ.1.4 Εντοπισμός της μετάλλαξης στο SPG Δ.2 Πληθυσμιακό δείγμα. 60 Δ.3 Απομόνωση γενωμικού DNA Δ.3.1 Απομόνωση γενωμικού DNA από αίμα Δ.3.2 Απομόνωση γενωμικού DNA από σίελο..61 Δ.4 Προσδιορισμός της συγκέντρωσης του DNA σε υδατικό διάλυμα..63 Δ.5 Σχεδιασμός εκκινητών (primers).. 65 Δ.6 Αλυσιδωτή Αντίδραση Πολυμεράσης (PCR Polymerase chain reaction) Δ.6.1 Αρχή της μεθόδου.. 67 Δ.6.2 Υλικά PCR Δ.6.3 Βελτιστοποίηση παραμέτρων PCR..70 Δ.6.4 Πρωτόκολλα PCR αντιδράσεων...70 Δ.7 Ηλεκτροφόρηση σε πήκτωμα αγαρόζης. 73 Δ.7.1 Αρχή ηλεκτροφόρησης..73 Δ.7.2 Υλικά πηκτώματος αγαρόζης. 76 Δ.7.3 Η διαδικασία παρασκευής πηκτώματος αγαρόζης 1%...78 Δ.8 PCR-ARMS (Amplification Refractory Mutation System).80 Δ.8.1 Η μέθοδος PCR-ARMS...78 Δ.8.2 Το πρωτόκολλο για τον πολυμορφισμό rs του TBC1D Δ.9 PCR-RFLP (PCR-Restriction Fragment Length Polymorphism)...82 Δ.9.1 Αρχή μεθόδου PCR-RFLP 82 Δ.9.2 Διαδικασία πέψης..82 Δ.9.3 Αναλυτικά για κάθε πολυμορφισμό. 83 Δ.10 Καθαρισμός των προϊόντων της PCR.. 88 Δ.10.1 Καθαρισμός προϊόντων με στήλες απευθείας μετά την PCR αντίδραση...88 Δ.10.2 Καθαρισμός προϊόντων της PCR με απομόνωση από το πήκτωμα αγαρόζης και με τη χρήση στηλών...89 Δ.10.3 Καθαρισμός PCR προϊόντων με το ένζυμο ExoSAP IT Δ.10.4 Σύγκριση μεθόδων καθαρισμού..90 Δ.11 Αλληλούχηση (Sequencing)..91 Δ.11.1 Εφαρμογή αλληλούχησης κατά Sanger Διαδικασία Δ.11.2 Εφαρμογή αλληλούχησης κατά Sanger Διαδικασία Δ.12 Ανάλυση Ετεροδιμερών (HDA Heteroduplex Analysis) 97 Δ.13 Ηλεκτροφόρηση DNA σε πήκτωμα πολυακρυλαμιδίου (PAGE Polyacrylamide Gel Electrophoresis) 100 6
7 Δ.13.1 Γενικά για τη μέθοδο ηλεκτροφόρησης DNA σε πήκτωμα πολυακρυλαμιδίου Δ.13.2 Η χρήση της PAGE σε συνδυασμό με HDA. 101 Δ.13.3 Στήσιμο της κάθετης συσκευής ηλεκτροφόρησης Δ.13.4 Υλικά και Προετοιμασια πηκτώματος πολυακρυλαμιδίου 8% Δ Ηλεκτροφόρηση πηκτώματος πολυακρυλαμιδίου Δ.13.6 Χρώση πηκτώματος πολυακρυλαμιδίου.104 Δ.14 Mεθοδοι στατιστικής επεξεργασίας των αποτελεσμάτων γονοτυπικής ανάλυσης Δ.14.1 Η ισορροπία Hardy-Weinberg Δ.14.2 Το κριτήριο χ Δ.14.3 Αμφίπλευρος ακριβής έλεγχος του Fisher..107 Ε. ΑΠΟΤΕΛΕΣΜΑΤΑ 109 Ε.1 Αποτελέσματα γονοτύπησης ασθενών και υγιών για τους πολυμορφισμούς που επιλέγχθηκαν από την 1η προσέγγιση του WGS Ε.1.1 Γονίδιο Α2LD1, πολυμορφισμός rs Ε.1.2 Γονίδιο TBC1D1, πολυμορφισμός rs Ε.1.3 Αποτελέσματα πέψης με περιοριστικά ένζυμα Ε Γονίδιο A2LD1, πολυμορφισμός rs (C>T) 115 Ε Γονίδιο ΚΑΖΝ, πολυμορφισμός rs (c>t) Ε Γονίδιο FAM181B, πολυμορφισμός rs (C>T) Ε Γονίδιο FΤΟ, πολυμορφισμοί rs (C>T) και rs (G>C).119 Ε.2 Αποτελέσματα γονοτύπησης ασθενών και υγιών για τους πολυμορφισμούς που επιλέγχθηκαν από την 2 η προσέγγιση του WGS Ε.2.1 Γονίδιο FGF13, 5 UTR. 124 Ε.2.2 Γονίδιο SLC36A1, Chr5: Ε.3 Αποτελέσματα επαλήθευσης μετάλλαξης στο εξώνιο 1 του γονιδίου SPG7 σε οικογένεια ασθενών με διάγνωση πιθανής ALS και στους υγιείς συγγενείς 1ου βαθμού 127 ΣΤ. ΣΥΜΠΕΡΑΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΤΣΗ.131 ΣΤ.1 Συζήτηση και συμπεράσματα επί των αποτελεσμάτων.132 ΣΤ.2 Μελλοντικές προοπτικές και συμπληρωματικά δεδομένα Z. ΒΙΒΛΙΟΓΡΑΦΙΑ ΠΑΡΑΡΤΗΜΑ.152 7
8 ΣΥΝΤΜΗΣΕΙΣ - ΞΕΝΟΓΛΩΣΣΟΙ ΟΡΟΙ Amyotrophic Lateral Sclerosis (ALS): Πλάγια Αμυοτροφική Σκλήρυνση DeoxyriboNucleic Acid (DNA): Δεοξυριβονουκλεϊκό οξύ ή γενετικό υλικό RiboNucleic Acid (RNA): Ριβονουκλεϊκό οξύ Excitatory Amino Acid Transporters (ΕΑΑΤ): Μεταφορείς Διεγερτικών Αμινοξέων Single Nucleotide Polymorphism (SNP): Μονονουκλεοτιδικοί πολυμορφισμοί Endoplasmic Reticulum Stress (ER Stress): Καταπόνηση ενδοπλασματικού δικτύου Upper Motor Neuron (UMN) ή Ανώτερος Κινητικός Νευρώνας (ΑΚΝ) Lower Motor Neuron (LMN) ή Κατώτερος Κινητικός Νευρώνας (ΚΚΝ) Linkage Disequilibrium (LD): Ανισορροπία σύνδεσης Amplification refractory mutation system (ARMS): Σύστημα Ανίχνευσης Μεταλλάξεων Ανθεκτικών στην Ενίσχυση Restriction fragment length polymorphism (RFLP): Πολυμορφισμός μήκους περιοριστικού θραύσματος Genome wide association study (GWAS): Μελέτη γενετικής συσχέτισης σε γονιδιωματική κλίμακα Untranslated region (UTR): Μη μεταφραζόμενη περιοχή Motor Neuron Disease (MND): Νόσος Του Κινητικού Νευρώνα Reactive Oxygen Species (ROS): Ενεργές Ρίζες Οξυγόνου ΜΣΑΦ : Μη στεροειδή αντιφλεγμονώδη φάρμακα Whole exome sequencing (WES): Αλληλούχηση όλων των εξωνικών περιοχών του γονιδιώματος Whole Genome Sequencing (WGS): Αλληλούχηση ολόκληρου του γονιδιώματος Messenger RNA (mrna): Αγγελιαφόρο RNA DNA Nanoballs (DNBs): Νανοσφαιρίδια Δεοξυνουκλεϊκών οξέων Small interfering RNA (sirna): Μικρά Παρεμβαλλόμενα RNA Copy Number Variants (CNV): Παραλλαγές Αριθμού Αντιγράφων Των Γονιδίων Spinal Muscular Atrophy (SMA): Νωτιαία Μυϊκή Ατροφία Frontotemporal Dementia (FTD): Μετωποκροταφική Άνοια Hereditary Spastic Paraplegia (HSP): Οικογενής Σπαστική Παραπληγία Frontotemporal Dementia and Parkinsonism (FTDP): Μετωποκροταφική Άνοια και Παρκινσονισμός Optical Density (O.D.): Οπτική Απορρόφηση 8
9 Α. ΠΕΡΙΛΗΨΗ - ABSTRACT 9
10 Η Πλάγια Αμυοτροφική Σκλήρυνση είναι μια ετερογενής νόσος, που οφείλεται στην εκφύλιση των ανώτερων και κατώτερων κινητικών νευρώνων. Αρχικά η νόσος εκδηλώνεται είτε με μυϊκή αδυναμία και σπαστικότητα των άνω ή κάτω άκρων, είτε με δυσχέρεια στην ομιλία. Η εξέλιξη της νόσου είναι μοιραία και ο αναμενόμενος χρόνος επιβίωσης είναι 3 5 χρόνια. Με την εμφάνιση της νόσου έχουν συσχετιστεί πολλοί γενετικοί και περιβαλλοντικοί παράγοντες. Ταυτοχρόνως, έχουν προταθεί και πολλοί μηχανισμοί παθογένειας. Παρόλα αυτά, η ALS παραμένει ανίατη και οι υπάρχουσες θεραπείες αποσκοπούν στην βελτίωση της κλινικής εικόνας ή / και στην παράταση της επιβίωσης. Ιδιαίτερα στον ελληνικό πληθυσμό, η γενετική αιτία της νόσου δεν έχει διερευνηθεί επαρκώς. Μεταλλάξεις στα γονίδια SOD1, TARDBP και FUS στις οποίες οφείλεται το 30% των οικογενών περιπτώσεων ALS σύμφωνα με τη βιβλιογραφία, δεν απαντώνται στους ασθενείς με ελληνική καταγωγή. Για αυτό το λόγο, με τη βοήθεια της αλληλούχησης ολόκληρου του γονιδιώματος και χρησιμοποιώντας διάφορες προσεγγίσεις πάνω στα δεδομένα που εξήχθησαν, εστιάσαμε την έρευνά μας σε συγκεκριμένες παραλλαγές. Στόχος μας ήταν ο έλεγχος για πιθανές συσχετίσεις μεταξύ των παραλλαγών αυτών και της εμφάνισης της νόσου. Η επιλογή των παραλλαγών στηρίχθηκε στους κοινούς μεταξύ των ασθενών πολυμορφισμούς που δεν υπήρχαν στο δείγμα αναφοράς. Από αυτή την προσέγγιση, επιλέχθηκαν οι κοινοί πολυμορφισμοί rs (TBC1D1), rs (FTO), rs (FTO), rs και rs (A2LD1), rs (FAM181B) και rs (KAZN). Η δεύτερη προσέγγιση, περιλάμβανε τις νέες παραλλαγές που εντοπίστηκαν στο γονιδίωμα τουλάχιστον ενός εκ των ασθενών. Μεταξύ αυτών, επιλέχθηκαν 2 παραλλαγές, στην 5 αμετάφραστη περιοχή των γονιδίων FGF13 και SLC36A1. Σε δεύτερο χρόνο, αντιπαρατέθηκαν οι παραλλαγές των γονιδιωμάτων, με τη βάση δεδομένων Human Gene Mutation Database (HGMD) και συγκεκριμένα, με τις μεταλλάξεις που έχουν συσχετιστεί με την ALS. Ωστόσο, δεν κρίθηκε σκόπιμη η περαιτέρω διερεύνηση των αποτελεσμάτων αυτών. Το δείγμα των ασθενών επεκτάθηκε για τις επιλεγμένες παραλλαγές και τα αποτελέσματα της γονοτύπησης των ασθενών συγκρίθηκαν με τα αποτελέσματα της γονοτύπησης που πραγματοποιήθηκε σε δείγμα αναφοράς. Οι παραλλαγές που έδωσαν στατιστικά σημαντικό αποτέλεσμα, αναλύθηκαν και σε πληθυσμό Σαρδηνίων ασθενών ALS έναντι υγιών ατόμων. Εξετάσθηκε επίσης και η περίπτωση μιας οικογένειας στην οποία υπήρχαν τέσσερα άτομα τα οποία εμφάνιζαν ιδιαίτερο φαινότυπο και είχαν διαγνωστεί με πιθανή ALS. Συλλέχθηκε το πλήρες ιατρικό ιστορικό των ατόμων της οικογένειας που νοσούσαν, ενώ με τη χρήση της μεθόδου νέας γενιάς αλληλούχησης εντοπίστηκε πιθανή μετάλλαξη. Μεταξύ των συνολικά οχτώ παραλλαγών που μελετήθηκαν (από την πρώτη και δεύτερη προσέγγιση), από την ανάλυση των δύο προέκυψε στατιστικά σημαντική διαφορά μεταξύ υγιών και ασθενών σε επίπεδο γονοτύπων, αλλά όχι σε επίπεδο αλληλομόρφων. Οι συσχετίσεις με την ALS αφορούν τους πολυμορφισμούς, rs (TBC1D1), rs και rs (FTO), στον ελληνικό πληθυσμό. Επιπλέον, οι rs και rs συνδέθηκαν με απλότυπο. Οι διαφορές αυτές δεν υπήρχαν στο δείγμα των Σαρδηνίων. Αναφορικά με την οικογένεια, επιβεβαιώθηκε η ύπαρξη μετάλλαξης μεγέθους 25 βάσεων στο γονίδιο SPG7 σε ομόζυγη κατάσταση, στα μέλη της οικογένειας που φέρουν τον φαινότυπο της ALS / HSP (Οικογενούς Σπαστικής Παραπληγίας) και σε ετερόζυγη κατάσταση στα υγιή άτομα της οικογένειας που ελέγχθηκαν. 10
11 Amyotrophic Lateral Sclerosis is a heterogeneous disorder, caused by upper and lower motor neuron degeneration. At the first stages of the disease, muscle weakness as well as spasticity of upper or lower limbs or alternatively, impaired speech become obvious. The patients deteriorate rapidly and finally die 3 5 years after the initiation of the symptoms. Many genetic and environmental factors have been correlated with ALS. At the same time, a wide range of pathogenesis mechanisms have been proposed. Nevertheless, ALS remains a fatal disease and the existing therapies, aim to symptom relief and/ or a slight prolongation of life time expectancy. In particular, the genetic causes of ALS in Greek population, have not been thoroughly investigated. Mutations in SOD1, TARDBP and FUS exons to which 30% of FALS cases are attributed according to the bibliography, are under-represented in patients with a Hellenic ancestry. Herein, we obtained whole genome sequencing data from 10 Greek ALS patients. To interpret our data we used several approaches, which then helped us focus on certain variations. The aim of the project was to investigate those variations and their possible association with the disease. The variations of interest were chosen according to the following criteria; polymorphisms (i) being common to all patients, (ii) not present in healthy individuals and (iii) located near genes. From this approach, we chose the common polymorphisms rs (TBC1D1), rs (FTO), rs (FTO), rs and rs (A2LD1), rs (FAM181B) and rs (KAZN). The second approach, includes the annotation of all the novel variants found in at least one patient. Among these variants, two were chosen, both located in the 5 untranslated regions of the genes FGF13 and SLC36A1. Subsequently, the patients genomes variants were juxtaposed with the Human Gene Mutation Database (HGMD) and only those associated with ALS were selected. In this case, however, no further investigation has been performed. Our patients population was expanded for the overall chosen variations and their genotypes were compared to the genotypes of healthy individuals. Whenever the outcome had a statistical significance, a replication study was attempted in Sardinian ALS patients compared to healthy individuals. In parallel, we came across a case of a family with interesting phenotype features; four individuals in this family were diagnosed with possible ALS / HSP (Hereditary spastic paraparesis) and their full medical history was acquired. Through a next generation sequencing method a new possible mutation was identified. Overall, eight variations were studied (from the first and second approach). The polymorphisms rs (TBC1D1), rs and rs (FTO) showed a statistically significant association with ALS at a genotype level in the Greek population. At the same time, rs and rs were correlated with the existence of a haplotype. On the contrary, rs and rs showed no statistical significant differences, when Sardinian ALS patients were compared to healthy Sardinian individuals. As far as the family mentioned above is concerned, the existence of a homozygous 25bp deletion in the SPG7 gene was confirmed. All the members of the family, who manifested symptoms, bear the deletion. 11
12 Β. ΕΙΣΑΓΩΓΗ 12
13 Β.1 Πλάγια Αμυοτροφική Σκλήρυνση (ALS) Β.1.1 Γενικά στοιχεία για την Πλάγια Αμυοτροφική Σκλήρυνση Η πλάγια αμυοτροφική σκλήρυνση (ΑLS - Amyotrophic Lateral Sclerosis) είναι μια ταχέως εξελισσόμενη και με όψιμη έναρξη νευροεκφυλιστική διαταραχή, η οποία επί του παρόντος δε θεραπεύεται και οδηγεί σε θάνατο. Εμφανίζεται με κόπωση, κράμπες και μυϊκή αδυναμία στα άνω ή/και κάτω άκρα ή εκδηλώνεται με δυσφαγία ή δυσκολία στην ομιλία και οδηγεί σε παράλυση και πρόωρο θάνατο κατά μέσο όρο μέσα σε 3-5 χρόνια από την έναρξη των συμπτωμάτων. H νόσος ALS είναι δισυπόστατη. Η μια της «όψη» αφορά στην κοινή ALS, ενώ η δεύτερη σε ένα σύνολο συνδρόμων, που αναφέρονται ως «νόσος του κινητικού νευρώνα» (MND - motor neuron disease). Στην κοινή ALS συνυπάρχει η εκφύλιση των ανώτερων και κατώτερων κινητικών νευρώνων και αποτελεί την πιο συνηθισμένη μορφή της νόσου. Περιγράφηκε από τον J.M Charcot το 1874 και ονομάζεται και νόσος του Lou Gehrig από τον διάσημο παίχτη του μπέιζμπολ που πέθανε από αυτήν το Στην νόσο του κινητικού νευρώνα συμπεριλαμβάνεται η κοινή ALS και άλλα σύνδρομα, που έχουν ως κοινό στοιχείο το ότι σχετίζονται με τον εκφυλισμό των ανώτερων και κατώτερων κινητικών νευρώνων και φέρουν κοινή μοριακή και κυτταρική παθολογία και χαρακτηριστικά, έγκλειστα στον πυρήνα των νευρώνων. Αναλύοντας την ετυμολογία της ονομασίας «πλάγια αμυοτροφική σκλήρυνση», η αμυοτροφία αφορά την ατροφία των μυϊκών ινών χάρη στη σταδιακή απονεύρωσή τους, λόγω εκφυλισμού των νευρώνων. Η πλάγια σκλήρυνση αναφέρεται στη σκλήρυνση των προσθίων και πλάγιων πυραμιδικών οδών, καθώς οι νευρώνες σε αυτές τις περιοχές εκφυλίζονται και αντικαθίστανται από γλοίωση (Wijesekera and Leigh 2009). Β.1.2 Οικογενής και Σποραδική μορφή της Πλάγιας Αμυοτροφικής Σκλήρυνσης Η ALS, αρχικά, περιγράφηκε ως σποραδική ασθένεια, έως το 1880, οπότε παρατηρήθηκε η πρώτη οικογένεια στο Vermont, από τον sir William Osler (Siddique and Siddique 2008). Η ηλικία έναρξης και εξέλιξης της νόσου ποικίλει, ενώ μπορεί να έχει ελλειπή διεισδυτικότητα από γενιά σε γενιά. Η αυτοσωμική υπολειπόμενη οικογενής (FALS - familial ALS) είναι σπανιότερη και εμφανίζεται, κυρίως, σε νεαρές ηλικίες ή σε άτομα με διπλή μετάλλαξη στο γονίδιο SOD1. Κλινικο - παθολογικά η σποραδική (SALS sporadic ALS) και η οικογενής ALS είναι ίδιες (Hand and Rouleau 2002). Όσον αφορά τη SALS, εικάζεται ότι η αιτιολογία της είναι πιο πολύπλοκη και συνδυάζει πολλά πιθανά γονίδια με περιβαλλοντικούς παράγοντες (Siddique and Siddique 2008). Β.1.3 Επιδημιολογικά στοιχεία για τη νόσο Η ALS είναι μια πολυπαραγοντική ασθένεια, η επίπτωση της οποίας στην Ευρώπη είναι κατά μέσο όρο 2,08 ανά άτομα και ο μέσος επιπολασμός ανέρχεται σε 5,4 ανά
14 άτομα. Η εκτίμηση αυτή είναι μικρότερη για την Αμερική και την Ασία, με εξαίρεση την Ιαπωνία, που εμφανίζει την μεγαλύτερη επίπτωση και επιπολασμό για τη νόσο (Chiò, Logroscino, et al. 2013). Για τον δυτικό Ειρηνικό, τα νούμερα είναι φορές μεγαλύτερα (Wijesekera and Leigh 2009). Στην Ελλάδα, το 2003, η επίπτωση εκτιμάται ίση προς 1,1 ανά άτομα (Chiò, Logroscino, et al. 2013). Παράγοντες κινδύνου θεωρούνται κατά κύριο λόγο η ηλικία και το φύλο. Όσον αφορά την ηλικία εμφάνισης της νόσου είναι κατά μέσο όρο τα 62 έτη και η μέση ηλικία διάγνωσης της νόσου τα 65 έτη. Προς χάριν διευκρίνησης, αξίζει να αναφερθεί ότι η επίπτωση στο 77 % των μελετών κυμαίνεται μεταξύ των ηλικιών 60 έως 75 ετών. Στους άνδρες υπάρχει μεγαλύτερη συχνότητα εμφάνισης της τάξης του 1,5:1 (Majoor-Krakauer 2005, Chiò, Logroscino, et al. 2013, Wijesekera and Leigh 2009). Τα 2/3 των ασθενών παρουσιάζουν, αρχικά, διαταραχές του μυϊκού τόνου στα άκρα, λόγω προσβολής του νωτιαίου μυελού. Μόνο το 5 % εμφανίζει ALS πριν τα 30 (Wijesekera and Leigh 2009). Έτεροι πιθανοί παράγοντες κινδύνου είναι το κάπνισμα, οι τραυματισμοί, οι ιοί, πρωτεΐνες prions, τα βαρέα μέταλλα, η εξαντλητική άσκηση, η ραδιενέργεια και το ηλεκτροσόκ, ενώ υπάρχει και πιθανότητα συσχέτισης με τις βιομηχανίες χρωμάτων, πετρελαίου, γαλακτοκομικών και υλικών συγκόλλησης (Majoor- Krakauer 2005, Kunst 2004). Οι περιβαλλοντικοί παράγοντες δε φαίνεται να είναι η αιτία της εκδήλωσης, αλλά αντίθετα να συνδυάζονται με τη γενετική προδιάθεση. Αυτή εικάζεται ότι είναι και η αιτία των γεωγραφικών διαφορών στη συχνότητα εμφάνισης της νόσου. Ενδεικτικά, οι πληθυσμοί του Guam και των Σκανδιναβικών χωρών έχουν βρεθεί να έχουν μια σπάνια Β2 ομάδα αίματος που προδιαθέτει σε μια σπάνια υπολειπόμενη μορφή ALS1. Συγκεκριμένα, υπάρχουν (i) ενδείξεις αλληλεπίδρασης μεταξύ γονιδίων ή και γονιδιακών προϊόντων, (ii) επιβλαβή γονιδία με ελλειπή προστασία των νευρικών κυττάρων έναντι αυτών και (iii) ενδείξεις ότι μη φυσιολογικές πρωτεΐνες μπορεί να ρυθμίζουν μη φυσιολογικά την έκφραση στους νευρώνες. Στη φυλή Chamorro, στα νησιά Guam στον δυτικό Ειρηνικό, η συσχέτιση περιβαλλοντικών παραγόντων και γενετικής προδιάθεσης έχει μελετηθεί αρκετά λόγω του αυξημένου επιπολασμού της νόσου στην περιοχή. Παρατηρήθηκε λοιπόν, ένας συγκεκριμένος πολυμορφισμός στο γονίδιο ΜΑΡΤ, που κωδικοποιεί tau πρωτεΐνες (πρωτεΐνες συσχετιζόμενες με τους μικροσωληνίσκους, οι οποίες αφθονούν στο κεντρικό νευρικό σύστημα) και ένας άλλος στο CYP2D6, που συμμετέχει στο μεταβολισμό εξωγενών τοξινών. Παράλληλα, η εν λόγω φυλή καταναλώνει ένα ιδιαίτερο είδος φιστικιών που περιέχουν κυκασίνη. Η κυκασίνη ρυθμίζει θετικά τη μεταγραφή των tau πρωτεϊνών και μειώνει την επιδιόρθωση του DNA. Σε αυτή την περίπτωση, πιθανολογείται η αλληλεπίδραση γενετικών και περιβαλλοντικών παραγόντων. Τέλος, διαφαίνεται πως υπάρχει κάποια γενετική συσχέτιση μεταξύ της ALS, της άνοιας και της νόσου του Parkinson, καθώς φέρουν πολυμορφισμούς σε κάποια κοινά γονίδια, οι οποίοι προδιαθέτουν στην εμφάνιση μίας από αυτές. Στατιστικά, μάλιστα, σε οικογένειες με ALS ασθενείς, εμφανίζεται άνοια ή η νόσος του Parkinson πιο συχνά συγκριτικά με οικογένειες υγιών (Majoor-Krakauer 2005). 14
15 Β.1.4 Μηχανισμοί παθογένειας Στοιχεία σχετικά με τους μηχανισμούς παθογένειας συλλέγονται από διάφορες πηγές, όπως (i) γονίδια που έχουν συσχετιστεί ισχυρά με τη βοήθεια μελετών σύνδεσης και συσχέτισης με τη FALS και SALS, αντίστοιχα, (ii) ευρήματα στο εγκεφαλονωτιαίο υγρό ασθενών και σε ιστούς που συλλέχθηκαν μετά θάνατο, καθώς και (iii) σε κυτταρικά ή/και ζωικά μοντέλα με μεταλλάξεις σε γονίδια που έχει εξακριβωθεί ότι ευθύνονται για τη νόσο. Καταστροφή κυττάρων λόγω αύξησης ενδοκυττάριου ασβεστίου Το γλουταμινικό οξύ, που απελευθερώνεται από την προσυναπτική απόληξη, ενεργοποιεί τον υποδοχέα γλουταμινικού στα μετασυναπτικά κύτταρα και έπειτα, απομακρύνεται από τη συναπτική σχισμή μέσω EAAT υποδοχέων. Αλλαγές σε αυτούς τους υποδοχείς δεν επιτρέπουν στο γλουταμινικό οξύ να απομακρυνθεί και αυτό συνεχίζει να ενεργοποιεί τους υποδοχείς του, όπως είναι οι υποδοχείς που συνδέονται με G πρωτεΐνες και κανάλια ιόντων NMDA και AMPA, οι οποίοι προκαλούν αύξηση του ενδοκυττάριου Ca 2+. Όταν το κύτταρο δεν μπορεί να ανταποκριθεί στην αύξηση του Ca 2+ και να επαναφέρει την ομοιόσταση, οδηγείται σε αύξηση του ΝΟ και επομένως, στον κυτταρικό θάνατο του νευρώνα. Αυτό το γεγονός ενισχύεται από την έλλειψη ασβεστιο - δεσμευτικών πρωτεϊνών (CBPs). Νίτρωση πρωτεϊνών Η συνδυασμένη αύξηση του ΝΟ και του Ο - 2 καταλήγουν στην παραγωγή ΟΝΟΟ -, το οποίο οδηγεί στη νιτροποίηση των πρωτεϊνών, πλήττοντας τη λειτουργία τους. Οι πρωτεΐνες που βλάπτονται μπορεί να είναι και συστατικά του κυτταροσκελετού, τα οποία παρέχουν την υποστήριξη για τη φυσιολογική ανάπτυξη του άξονα των νευρικών κυττάρων, οι λεγόμενες νευρικές ίνες (neurofilament). Η νιτροποίηση των πρωτεϊνών αυτών οδηγεί στη δημιουργία μη φυσιολογικών συσσωματωμάτων. Οι παραπάνω αντιδράσεις εξαρτώνται από τον ελεύθερο χαλκό. Το μεταλλαγμένο SOD1 μπορεί να εμπλέκεται και σε αυτές τις αντιδράσεις. Νευρικές ίνες Οι νευρικές ίνες με μήκος 10 νανομέτρων (10 nm) ονομάζονται ενδιάμεσα νημάτια και βρίσκονται αποκλειστικά στους νευρώνες. Αποτελούν ένα σημαντικό συστατικό του κυτταροσκελετού και παρέχουν την υποστήριξη για τη φυσιολογική αξονική ακτινική ανάπτυξη. Οι νευρικές ίνες παίζουν σημαντικό ρόλο στην αξονική μεταφορά και στην ανάπτυξη των κυττάρων και των αξόνων. Σε ασθενείς ALS, παρατηρείται αύξηση ή συσσωμάτωση αυτών. Ανώμαλες νευρικές ίνες ή ανώμαλη αύξηση αυτών οδηγεί σε αποδιοργάνωση και αποκλείει την μεταφορά χρήσιμων συστατικών, οδηγώντας τα νευρικά κύτταρα σε απόπτωση. Αυτή η διαδικασία ονομάζεται axonal strangulation. Κάποια από τα πιθανά αίτια αυτής της διαταραχής παρουσιάζονται ακόλουθα: o Δράση μεταλλαγμένης SOD1 o Μεταλλάξεις στα γονίδια που οδηγούν σε υπερέκφραση o Μεταλλάξεις στα γονίδια που οδηγούν σε μεταλλαγμένες υπομονάδες o Αύξηση από τραυματισμό ή κυτταροκίνες φλεγμονής o Ενίσχυση από την περιφερίνη Η περιφερίνη, ειδικότερα, είναι ένα ενδιάμεσο νημάτιο, συστατικό του κυτταροσκελετού των περιφερικών κινητικών νευρώνων, που αυξάνεται κατά την απόκριση σε τραυματισμό ή 15
16 φλεγμονή. Η περιφερίνη έχει βρεθεί ότι υπερπαράγεται παράλληλα με τον εκφυλισμό των κυττάρων σε κάποιες περιπτώσεις, όπως και σε ALS ασθενείς. Η περιφερίνη, τέλος, ενισχύει την αποδιοργάνωση των νευρικών ινών (neurofilaments). Ο μηχανισμός δράσης της, πιθανώς, σχετίζεται με τη σύνδεση σε μεσαίες και μεγάλες υπομονάδες των νευρικών ινών και τον σχηματισμό συσσωματωμάτων (Hand and Rouleau 2002). Προβλήματα στην μεταφορά μέσω των αξόνων Η αξονική μεταφορά βασίζεται στην κινησίνη και τα σύμπλοκα δυνακτίνης δυνεΐνης, τα οποία κινούνται με τη βοήθεια των μικροσωληνίσκων από το σώμα προς τους δενδρίτες του νευρικού κυττάρου και αντίστροφα, μεταφέροντας κυστίδια και πρωτεΐνες. Η ελαττωματική αξονική μεταφορά μπορεί να οφείλεται σε (i) μεταλλάξεις στα γονίδια δυνακτίνης (DCTN) και δυνεΐνης, (ii) δυσλειτουργία των μιτοχονδρίων ή (iii) αύξηση του παράγοντα νέκρωσης όγκων (TNF) και επακόλουθη μείωση της αξονικής μεταφοράς και (iv) μεταλλάξεις σε γονίδια της κατηγορία του ΜΑΡΤ, που σχετίζονται με τον κυτταροσκελετό. Η καταστροφή λόγω διέγερσης από το γλουταμινικό οξύ θα μπορούσε να επιφέρει πολύπλευρη ζημιά στου άξονες, μέσω των μιτοχονδρίων και της φωσφορυλίωσης των νευρικών ινών. Γενικότερα, οτιδήποτε μπορεί να επηρεάζει τη δομή και λειτουργία των νευρικών ινών και της αξονικής μεταφοράς μπορεί να οδηγήσει σε μια διαδικασία κατά την οποία το κύτταρο αποβιώνει από τους απομακρυσμένους άξονες προς τα πίσω (Εικόνα 1) (Ferraiuolo et al. 2011). Εικόνα 1: Επάνω, φυσιολογική λειτουργία του άξονα (Pasinelli and Brown 2006). Κάτω, «dying back process» (Coleman 2005). Τοξικότητα εξαρτώμενη από τα μιτοχόνδρια Η απότομη, μη αντισταθμιζόμενη αύξηση του ασβεστίου οδηγεί σε καταστροφή των μιτοχονδρίων. Τα μιτοχόνδρια, όμως, είναι απολύτως απαραίτητα για τα νευρικά κύτταρα, τα οποία έχουν μεγάλες ανάγκες σε ενέργεια λόγω του αυξημένου μεταβολισμού τους. Μεταλλάξεις στο γονίδιο SOD1 1. Τοξική συσσώρευση της πρωτεΐνης SOD1 2. Πρωτεϊνικά SOD1 συσσωματώματα, λόγω ατελούς αναδίπλωσης i. Συσσωματώματα τοξικά για τα μιτοχόνδρια 3. Κατάλυση απενεργοποίησης ΕΑΑΤ2 4. Τοξική δράση στις αξονικές νευρικές ίνες 5. Αύξηση περιφερίνης 6. Αύξηση ελεύθερου χαλκού από μεταλλαγμένες μορφές που δε δένουν Cu 2+ 16
17 7. Νίτρωση και οξείδωση τυροσινών, λόγω παραγωγής ελεύθερων ριζών αζώτου και οξυγόνου 8. Καταστροφή κυττάρων με την επίδραση του οξειδωτικού στρες i. Με πρόσδεση σε μη φυσιολογικά υποστρώματα ii. Με απώλεια της δυνατότητας να προσδένει ψευδάργυρο (απώλεια ειδικότητας) Το ένζυμο φυσιολογικά εξουδετερώνει τις ελεύθερες ρίζες, μέσω της αντίδραση που παρουσιάζεται στην Εικόνα 2. Οι μεταλλάξεις του SOD1, που καθιστούν το ένζυμο ανενεργό, - προκαλούν μεγάλη αύξηση των ελεύθερων ριζών Ο 2 από τα μιτοχόνδρια. Στα νευρικά κύτταρα, ήδη, παράγονται περισσότερες ελεύθερες ρίζες Ο 2, σε σχέση με άλλα είδη Εικόνα 2: Αντίδραση που λαμβάνει χώρα φυσιολογικά στα μιτοχόνδρια και εξασφαλίζει την εξουδετέρωση της περίσσειας ελευθέρων ριζών. κύτταρων. Η μεταλλαγμένη πρωτεΐνη SOD1, πιθανώς, οδηγεί και στη δημιουργία ριζών ΟΗ. και ΟΗ -, οι οποίες είναι υπεύθυνες για το οξειδωτικό στρες. Εναλλακτικά ή/και ταυτοχρόνως ενεργοποιούνται ένζυμα, όπως τα NOS, που επάγουν το σχηματισμό μονοξειδίου του αζώτου από την αργινίνη. Επιπλέον, η αύξηση ΝΟ από μόνη της οδηγεί σε περαιτέρω αύξηση ελεύθερων ριζών Ο 2 -, μέσω αναστολής της ροής των ηλεκτρονίων στα μιτοχόνδρια (Εικόνα 3). Τοξικότητα από χαλκό Ο χαλκός αποτελεί μαζί με τον ψευδάργυρο το βασικό συμπαράγοντα της πρωτεΐνης SOD1. Δομικές αλλαγές στην πρωτεΐνη αυτή, που μπορεί να οφείλονται σε μεταλλάγματα του γονιδίου και οδηγούν σε λανθασμένη αναδίπλωση της πρωτεΐνης, πιθανώς να αφήνουν ελεύθερο τον χαλκό να αλληλεπιδρά με άλλα μόρια μέσα στο κύτταρο, ο οποίος ως γνωστόν έχει νευροτοξική δράση. Η πιθανή τοξικότητα του χαλκού ενισχύεται από την παρατήρηση ότι τα χηλικά σύμπλοκα χαλκού αντιστρέφουν τις βλαπτικές δράσεις των SOD1 μεταλλαγμάτων. Σε αυτό το μηχανισμό παθογένειας, μέσω της απελευθέρωσης χαλκού, φαίνεται να είναι απαραίτητη και η συμμετοχή της πρωτεΐνης μεταφοράς του χαλκού του SOD (CCS - copper chaperone for SOD) (Hand and Rouleau 2002). Καταπόνηση ενδοπλασματικού δικτύου (ER stress) Η συσσώρευση λανθασμένα αναδιπλωμένων πρωτεϊνών στο κυτταρόπλασμα των νευρικών και μη κυττάρων είναι ένα συνηθισμένο εύρημα στην ALS. Η εσφαλμένη αναδίπλωση επάγει την ενεργοποίηση συνοδών πρωτεϊνών από το ενδοπλασματικό δίκτυο, οι οποίες έχουν ως στόχο τη σωστή επαναδίπλωση των πρωτεϊνών. Αν αυτό δεν είναι επιτυχές, το επόμενο στάδιο περιλαμβάνει την αναστολή της μετάφρασης και την αποικοδόμηση των πρωτεϊνών και τελικά, την ενεργοποίηση μηχανισμών απόπτωσης (Εικόνα 4). Πρωτεΐνες, οι οποίες σε μεμονωμένες περιπτώσεις συνδέθηκαν με το ALS, όπως η CHMP2B και η VAPB, σχετίζονται με τον προστατευτικό μηχανισμό της αυτοφαγίας, καθώς και διαδικασίες του ενδοπλασματικού δικτύου, αντίστοιχα. 17
18 Εικόνα 3: Μονοπάτια που εμπλέκονται στο θάνατο των νευρικών κυττάρων στην ALS. Το γλουταμινικό οξύ που εκλύεται από τις προσυναπτικές απολήξεις των νευρώνων, απομακρύνεται από τη συναπτική σχισμή με τη βοήθεια μεταφορέων του γλουταμινικού, όπως ο ΕΑΑΤ2. Ελλατωματικοί μεταφορείς του γλουταμινικού οξέος μπορεί να προκαλέσουν τη συνεχή ενεργοποίηση του υποδοχέα και τελικά, την αύξηση των επιπέδων ασβεστίου, ώστε να επηρεάζεται η λειτουργία των μιτοχονδρίων, καθώς και η ενεργοποίηση ενζύμων, όπως το NOS. Άλλο αίτιο της συσσώρευσης ασβεστίου είναι οι μη λειτουργικές ή δυσλειτουργικές ασβεστιο - δεσμευτικές πρωτείνες. Τα μιτοχόνδρια, με τη σειρά τους, είναι άφθονα στα νευρικά κύτταρα, λόγω των μεγάλων αναγκών των κυττάρων αυτών για ενέργεια. Όπως είναι αναμενόμενο, παράγονται μεγάλες ποσότητες ελεύθερων ριζών οξυγόνου, που φυσιολογικά αντισταθμίζονται με τη μετατροπή τους σε λιγότερο δραστικά μόρια από ένζυμα, όπως το SOD1. Μεταλλάξεις στο SOD1 οδηγούν σε αυξημένη οξειδωτική καταπόνηση, ενώ η ενεργοποίηση του NOS οδηγεί στην παραγωγή ΟΝΟΟ - και στη συνέχεια, μέσω μιας αντίδρασης νιτροζυλίωσης σε συσσωμάτωση των νευρονηματίων που είναι στόχοι των ελευθέρων ριζών (Hand and Rouleau 2002). 18
19 Τοξικότητα από διέγερση μέσω γλουταμινικού (Excitoxicity) Το γλουταμινικό οξύ, που εκλύεται από τις προσυναπτικές απολήξεις των νευρώνων, αποτελεί τον βασικότερο διεγερτικό νευροδιαβιβαστή του νευρικού συστήματος. Μεταξύ των κυριότερων μετασυναπτικών υποδοχέων που ενεργοποιεί συγκαταλέγεται ο υποδοχέας του α-αμινο-3-υδροξυ-5-μεθυλ-4-ισοξαζολπροπιονικού οξέος (ΑΜΡΑ). Ο υποδοχέας ΑΜΡΑ, με τη σειρά του, διαθέτει την υπομονάδα GLuR2, η οποία σε συνδυασμό με τις CBPs πρωτεΐνες, εξασφαλίζει την ομοιόσταση του Ca 2+. Ωστόσο, οι κινητικοί νευρώνες υποεκφράζουν αυτούς τους δύο παράγοντες ομοιόστασης, καθιστώντας το κύτταρο ευαίσθητο στη δράση των ενεργοποιημένων AMPA υποδοχέων. Οι παράγοντες που ευθύνονται για την υπερβολική δράση του γλουταμινικού οξέος, συνοψίζονται (i) στην αύξηση της ευαισθησίας ή στην υπερέκφραση των μετασυναπτικών υποδοχέων γλουταμινικού οξέος, (ii) στη μείωση της έκφρασης ή της λειτουργικότητας των προσυναπτικών μεταφορέων του γλουταμινικού οξέος, όπως ο ΕΑΑΤ2, (iii) στα μειωμένα επίπεδα της GluR2 υπομονάδας, λόγω απορρύθμισης των αστροκυττάρων ή/και (iv) στην υπερβολική προσυναπτική έκκριση γλουταμινικού οξέος και οδηγούν στην επονομαζόμενη «τοξικότητα από διέγερση». Η τοξικότητα από διέγερση περιλαμβάνει την υπέρμετρη αύξηση του ενδοκυττάριου Ca 2+, καθώς και των πρωτεολυτικών και προ - οξειδωτικών ενζύμων, αλλά και την ενεργοποίηση των μιτοχονδρίων για την παραγωγή ενέργειας (Εικόνες 3 και 4). Στοιχεία που επιβεβαιώνουν τον παραπάνω μηχανισμό είναι οι μεταλλάξεις, η μειωμένη έκφραση και λειτουργία του EAAT2 σε ασθενείς ALS, η αύξηση του γλουταμινικού οξέος στο εγκεφαλονωτιαίο υγρό ορισμένων από τους ασθενείς, η υπερδιέγερση του κινητικού συστήματος στο ηλεκτρονευρογράφημα σε πολύ πρώιμα στάδια της νόσου και τέλος, οι μεταλλάξεις στο γονίδιο DAO. Το DAO κωδικοποιεί ένα ένζυμο υπεύθυνο για την οξειδωτική απαμίνωση των D-αμινοξέων, μεταξύ των οποίων συγκαταλέγεται και η D-σερίνη. H D-σερίνη είναι συναγωνιστικός αγωνιστής των υποδοχέων NMDA (N-μεθυλ-D-ασπαρτικό οξύ) του νευρικού συστήματος (Ferraiuolo et al. 2011). Ανεπάρκεια αυξητικών παραγόντων νευρικής ανάπτυξης In vitro μοντέλα και μεταθανάτια δείγματα ασθενών, εμφανίζουν μείωση των νευροτροφικών παραγόντων, όπως οι CTNF, BDNF, GDNF και IGF-1. Επιπλέον, υπάρχουν ενδείξεις συσχέτισης του VEGF με τη SALS, που ωστόσο δεν επιβεβαιώθηκαν (Wijesekera and Leigh 2009). Οξειδωτική καταπόνηση Η υπέρμετρη αύξηση στις ενεργές ρίζες οξυγόνου (ROS) και η παράλληλη απώλεια της επιδιορθωτικής ικανότητας του κυττάρου έναντι στις ROS οδηγεί το κύτταρο σε συσσώρευση ζημιών στο επίπεδο DNA, RNA, λιπιδίων και πρωτεϊνών. Η επίδραση των ROS έχει μελετηθεί διεξοδικά σε μοντέλα τρωκτικών με μεταλλάξεις στο SOD1, που διαδραματίζει κρίσιμο ρόλο στον μεταβολισμό τους (όπως προαναφέρθηκε), αλλά και σε μεταλλάγματα του TDP-43. Ορισμένα mrna μόρια που συμμετέχουν σε κρίσιμες λειτουργίες του νευρικού κυττάρου - όπως η πρωτεϊνοσύνθεση, η αλυσίδα μεταφοράς ηλεκτρονίων των μιτοχονδρίων, η μυελίνωση, ο κυτταροσκελετός και η γλυκόλυση - είναι πιο ευαίσθητα στο οξειδωτικό στρες. Επιπρόσθετα, η οξειδωτική καταπόνηση συμμετέχει και σε άλλες διαδικασίες που οδηγούν στον νευροεκφυλισμό, όπως η υπερδιέγερση από το γλουταμινικό οξύ, η καταστροφή των μιτοχονδρίων, η συσσωμάτωση πρωτεϊνών, η καταπόνηση του ενδοπλασματικού δικτύου 19
20 και η εναλλακτική, αρνητική σηματοδότηση από τα συνοδά κύτταρα, όπως τα αστροκύτταρα και η μικρογλοία (Ferraiuolo et al. 2011, Rowland and Shneider 2001). Εικόνα 4: Μηχανισμοί παθογένειας στην ALS. Σε κίτρινο ορθογώνιο πλαίσιο φαίνονται οι πιθανές αιτίες ή αλλιώς, οι μηχανισμοί που δυσλειτουργούν και σε κόκκινο ορθογώνιο πλαίσιο το καταστροφικό για το κύτταρο αποτέλεσμα. Με πράσινο χρώμα απεικονίζεται το νευρικό κύτταρο με τον άξονα του. Με μοβ χρώμα απεικονίζονται τα αστροκύτταρα, τα οποία συμμετέχουν στη νευροεκφύλιση, μεσω διαφόρων μηχανισμών. Με μπλε - κίτρινο απεικονίζεται η μικρογλοία, η οποία διαδραματίζει σημαντικό ρόλο στον πιθανό μηχανισμό που εμπλέκει τη διαδικασία της φλεγμονής. ALS: amyotrophic lateral sclerosis, EAAT2: excitatory amino acid transporter 2, ER: endoplasmic reticulum, IL: interleukin, MCP-1: monocyte chemoattractant protein 1, NGF: nerve growth factor. NO: nitric oxide, PGE2: prostaglandin E2, ROS: reactive oxygen species (Ferraiuolo et al. 2011). 20
21 Τοξικότητα RNA-δεσμευτικών πρωτεϊνών Οι πρωτεΐνες που σχετίζονται με διαδικασίες επεξεργασίας του RNA και ταυτοχρόνως εμπλέκονται στην παθογένεια της ALS είναι οι FUS, TDP-43, ANG, SMN1 και SMN2. Πιο συγκεκριμένα για τα τελευταία μόρια, η παραλλαγή πολλαπλών αντιγράφων στο γονιδίο SMN1 και η διαγραφή στο SMN2 σχετίζονται με την ALS. Αυτές οι δύο πρωτεΐνες, υπό φυσιολογικές συνθήκες, αποτελούν συστατικά του σωματιδίου ματίσματος του mrna. Όσον αφορά το FUS, ο φυσιολογικός ρόλος του έγκειται στη ρύθμιση της μεταγραφής. Παρόμοια είναι και η δράση της αγγειογενίνης (ANG), η οποία ωστόσο δρα μέσω των ριβοσωμάτων, όπου διαδραματίζει ρόλο στην αποικοδόμηση του μεταφορικού trna και στη βιοσύνθεση του ριβοσωμικού rrna, επιπλέον είναι γνωστή η συμβολή της στην αγγειογένεση. Άγνωστος, ωστόσο, παραμένει ο τρόπος με τον οποίο η αγγειογενίνη εμπλέκεται στην παθογένεση της ALS. Η σεναξατίνη (SEXT) είναι ακόμα μια πρωτεΐνη που σχετίζεται με τα ριβοσώματα, καθώς αποτελεί στοιχείο των ριβονουκλεοτιδικών συμπλόκων και λειτουργικά είναι μια DNA - RNA ελικάση. Υποθέτοντας την ύπαρξη κοινών μονοπατιών στην παθογένεση της νόσου, αξίζει να αναφέρουμε τα κοινά λειτουργικά χαρακτηριστικά των FUS και TDP-43, τα οποία αποτελούν (i) η ρύθμιση της μεταγραφής, (ii) η συμμετοχή τους σε σύμπλοκα μεταφοράς RNA, και (iii) η επεξεργασία RNA και microrna. Μεταλλάξεις στα εξώνια του FUS αναστέλλουν την μετακίνηση του στον πυρήνα, γεγονός το οποίο οδηγεί στο σχηματισμό των «stress granules». Το φαινόμενο κατά το οποίο σχηματίζονται τα «stress granules» παρατηρείται και στην περίπτωση της TDP-43 πρωτεΐνης. Τα «stress granules» είναι στην ουσία κυτταροπλασματικά έγκλειστα των αντίστοιχων πρωτεϊνών (Εικόνα 5). Επιπλέον λειτουργίες του TDP-43 αφορούν τη ρύθμιση του εναλλακτικού ματίσματος και της αλληλεπίδρασης μεταξύ πρωτεϊνών. Στην τελική επικράτεια αλληλεπίδρασης πρωτεΐνης με πρωτεΐνη συναντώνται και οι περισσότερες μεταλλάξεις. Ένας σημαντικός mrna στόχος του οποίου η χωρική και χρονική μεταγραφή ρυθμίζεται από την πρόσδεσή του με την TDP-43 είναι αυτός της ελαφριάς αλυσίδας των νευρικών ινών (NFL). Προσφάτως δε, συσχετίστηκε το γονίδιο ELP3, που κωδικοποιεί ένα στοιχείο της RNA πολυμεράσης ΙΙ και συμμετέχει στην επιμήκυνση των μεταγράφων (Ferraiuolo et al. 2011, Chen et al. 2013). Συσσωματώματα πρωτεϊνών Τα συσσωματώματα πρωτεϊνών που εντοπίζονται μέσα σε ουβικουιτινιομένα έγκλειστα, σε ασθενείς ALS, αποτελούν χαρακτηριστικό εύρημα για τη νόσο. Με ποιο τρόπο, εντούτοις, μπορεί να σχετίζονται με τον μηχανισμό που οδηγεί στη νευροεκφύλιση παραμένει άγνωστο. Το είδος των πρωτεϊνών που συναντάμε στα έγκλειστα διαφέρει από κλινικό περιστατικό σε περιστατικό. Το μόριο TDP-43, φυσιολογικά εντοπίζεται στον πυρήνα του κυττάρου, ωστόσο σε ασθενείς με FALS αποτελεί βασικό πρωτεϊνικό συστατικό των κυτταροπλασματικών εγκλείστων, ενώ παρατηρείται σε νευρικά και μη κύτταρα. Συνεπώς, διαφαίνεται πως υπάρχει απώλεια, αν όχι όλης, μέρους της φυσιολογικής λειτουργίας που εκτελεί στους πυρήνες των κυττάρων αυτών. Συχνά απαντώνται, επίσης, έγκλειστα με FUS πρωτεΐνες ή λανθασμένα αναδιπλωμένα SOD1 ένζυμα στους κινητικούς νευρώνες ασθενών με FALS. Τα έγκλειστα υαλίνης, πλούσια σε νευρικές ίνες, επίσης φαίνεται να διαδραματίζουν κάποιο ρόλο στην παθογένεια της ALS. Τα έγκλειστα υαλίνης βρίσκονται στο περικάρυο ή στα συνοδά δενδριτικά κύτταρα των νευρώνων της σπονδυλικής στήλης. Η άποψη ότι συμμετέχουν στην παθογένεια της ALS ενισχύεται (i) λόγω της ύπαρξης τους σε ασθενείς με SOD1 μεταλλάξεις και (ii) λόγω της σημασίας των νευρικών ινών για τη δομή των 21
22 αξόνων και τη μεταφορά διαμέσου αυτών. Τα ηωσινοφιλικά σωμάτια Bunina, που περιέχουν κυστατίνη C, είναι τα πιο συχνά απαντώμενα και προσεγγίζουν το ποσοστό του 85 % των περιπτώσεων, ωστόσο ο ρόλος τους παραμένει εντελώς άγνωστος. Ο ρόλος των συσσωματωμάτων ενισχύεται (i) από τη συσχέτιση του γονιδίου VCP, το οποίο αναγνωρίζει ουβικουιτινιομένες πρωτεΐνες και τις οδηγεί στην αποικοδόμηση και (ii) του UBQLN2, το οποίο κωδικοποιεί μια κυτταροπλασματική πρωτεΐνη που προσομοιάζει της ουβικουιτίνης. Μικρογλοία, αστροκύτταρα και ολιγοδενδριτικά κύτταρα Σε πρώιμα ακόμη στάδια της νόσου βλέπουμε σημάδια φλεγμονής, όπως χημειοτακτικές πρωτεΐνες και IL-8 (ιντερλευκίνη 8) στο εγκεφαλονωτιαίο υγρό, καθώς και άλλες ενδείξεις ανοσοαπάντησης στο αίμα. Συσχέτιση, υπάρχει επίσης, μεταξύ ALS και ενεργοποίησης μικρογλοιακών και δενδριτικών κυττάρων, αλλά και αστροκυττάρων, τα οποία παράγουν κυτταροκίνες φλεγμονής, όπως προσταγλανδίνες Ε2 και λευκοτριένια Β4, ιντερλευκίνες COX1, TNFa και MCP1 (Wijesekera and Leigh 2009) (Εικόνα 4). Είναι φανερό ότι η φλεγμονή διαδραματίζει κάποιο ρόλο στην παθογένεια της νόσου. Ίσως η συσχέτιση αφορά την επίδραση των κυτταροκινών φλεγμονής με αποτέλεσμα την αύξηση των νευρικών πεπτιδικών νηματίων. Τα μικρογλοιακά, ολιγοδενδριτικά κύτταρα και τα αστροκύτταρα αποτελούν κατηγορίες κυττάρων που είναι συνοδά στα νευρικά κύτταρα (τα ολιγοδενδριτικά όσον αφορά τους νευράξονες) παρέχουν τη στήριξη και τους απαραίτητους αυξητικούς παράγοντες στο νευρικό κύτταρο. Ένας μηχανισμός που έχει προταθεί, αφορά τη συμβολή των αστροκυττάρων στη νευροεκφύλιση και περιλαμβάνει τη μείωση της απελευθέρωσης του γαλακτικού οξέος και της ενεργοποίησης του υποδοχέα του αυξητικού παράγοντα των προ - νευρικών κυττάρων, δηλαδή του p75 (Ferraiuolo et al. 2011) (Εικόνα 4). Επιπλέον, τα αστροκύτταρα φαίνεται να έχουν κάποια ανάμιξη και στη διεγερτική τοξικότητα του γλουταμινικού οξέος, καθώς σε πρώιμα στάδια παρατηρείται σε αυτά, μείωση του ΕΑΑΤ2 και ουβικουιτινιομένα έγκλειστα (Hand and Rouleau 2002). Απόπτωση (προγραμματισμένος κυτταρικός θάνατος) Εικάζεται ότι το αποτέλεσμα των παραπάνω μηχανισμών κυτταροτοξικότητας είναι τα νευρικά κύτταρα να οδηγηθούν σε θάνατο μέσω απόπτωσης, μια διαδικασία που εξαρτάται από τις κασπάσες (Wijesekera and Leigh 2009, Hand and Rouleau 2002, Ferraiuolo et al. 2011). 22
23 Β.1.5 Ευαισθησία των νευρικών κυττάρων Η επιλεκτική καταστροφή των νευρικών κυττάρων αποδίδεται κατά αρχήν στο μεγάλο μέγεθος τους (των αξόνων τους και των απολήξεών τους), που συνεπάγεται μεγάλες ενεργειακές ανάγκες, αυξημένο μεταβολισμό, έντονη κινητικότητα στα ενδοκυττάρια οργανίδια, αυξημένη λειτουργία των μιτοχονδρίων και του κυτταροσκελετού, καθώς επίσης τεταμένοι ρυθμοί μεταγραφής γονιδίων και πρωτεϊνοσύνθεσης. Επιπλέον, τα νευρικά κύτταρα εκφράζουν σε μεγάλο βαθμό AMPA υποδοχείς, στους οποίους απουσιάζει η GluR2 υπομονάδα, για τη διακίνηση του ασβεστίου και μειωμένα επίπεδα ασβεστιο-ρυθμιστικών πρωτεϊνών, γεγονός που τους προσδίδει ευαισθησία στις τοξικές δράσεις του γλουταμικού οξέος. Τέλος, πιθανολογείται ότι η ευαισθησία των νευρικών κυττάρων οφείλεται στην υψηλή ουδό απόκρισης στο θερμικό σοκ, στην καταπόνηση από ενεργοποίηση των οιστρογονικών υποδοχέων, στα χαρακτηριστικά των μιτοχονδρίων τα οποία διαθέτουν σε αφθονία και τέλος, στη συνεχή διέγερση των κυττάρων μέσω του ασβεστίου (Ferraiuolo et al. 2011) Εικόνα 5: Η πορεία του mrna από τη μεταγραφή στην αποικοδόμηση. Τα κοινά σημεία στο μηχανισμό FUS TARDBP αποδίδονται με κόκκινο. Η πορεία TARDBP απεικονίζεται με μπλε. Προτεινόμενα μονοπάτια παθογένειας, στην ALS (Strong and Volkening 2011). 23
24 Β.1.6 Κλινικά και Ιστοπαθολογικά Ευρήματα Η ALS είναι μια ασθένεια που παρουσιάζει μεγάλη ποικιλότητα όσον αφορά την έναρξη, την κλιμάκωση και το βαθμό εμφάνισης των συμπτωμάτων και των ευρημάτων που οφείλονται στους ανώτερους και κατώτερους κινητικούς νευρώνες (Εικονα 6). Αρχικά συμπτώματα Τα αρχικά συμπτώματα εμφανίζονται κυρίως ασύμμετρα, σε πόδια ή χέρια, στο 80 % των περιπτώσεων, ενώ στο 20 % των περιπτώσεων εμφανίζεται, αρχικά, δυσαρθρία ή δυσφαγία. Έτερα συμπτώματα αποτελούν η αδυναμία των αναπνευστικών μυών, η απώλεια βάρους με μυϊκή ατροφία, η πτώση της κεφαλής, η αδυναμία έκτασης του κορμού, οι ακούσιες μυϊκές συσπάσεις και οι κράμπες. Εικόνα 6: H κλασική ALS είναι η συχνότερη και πιο γρήγορα εξελισσόμενη μορφή της Νόσου του Κινητικού Νευρώνα. Παρουσιάζει ευρήματα από τους ανώτερους και κατώτερους κινητικούς νευρώνες, που μπορεί να εξελιχθούν, είτε με έναρξη από τους ανώτερους κινητικούς νευρώνες, είτε από τους κατώτερους. Με μπλε προσδιορίζονται οι ανώτεροι κινητικοί νευρώνες και με κόκκινο οι κατώτεροι. Κλινικά ευρήματα Στην πρωτογενή πλάγια σκλήρυνση, επηρεάζονται μόνο τα ανώτερα κινητικά νεύρα, παρόλο που και τα κατώτερα νεύρα έχουν υποστεί αλλοιώσεις. Τα νεύρα που επηρεάζονται βρίσκονται στον κινητικό φλοιό του εγκεφάλου, χωρίς να αποκλείονται ωστόσο άλλες περιοχές. Στο 80 % των περιπτώσεων, τα πρώτα συμπτώματα εμφανίζονται στα άκρα. Όσον αφορά τα χέρια, συνήθως, εμφανίζεται αδυναμία στους μυς του ώμου και έτσι, δυσχεραίνονται οι λεπτές κινήσεις. Αναφορικά με τα πόδια, οι πάσχοντες έχουν πιο συχνές πτώσεις, καθώς είτε έχει επηρεαστεί το άκρο του ποδιού, είτε οι μυϊκές ομάδες του μηρού. Άλλα συμπτώματα είναι η σπαστικότητα, οι υπερδραστήριοι τένοντες (σημείο Ηoffman), οι αιμωδίες των δακτύλων και η μη φυσιολογική αντίδραση στο πελματιαίο αντανακλαστικό (σημείο Babinski), τα οποία αποτελούν και διαγνωστικά σημεία. Το υπόλοιπο 20 % των περιπτώσεων, εμφανίζει προμηκική έναρξη με δυσφαγία και δυσαρθρία. Πιο σπάνια συμπτώματα της προμηκικής έναρξης είναι το ακούσιο γέλιο, κλάμα ή χασμουρητό, που δεν οφείλεται σε αλλαγές στη διάθεση, καθώς και ο αυξημένος τόνος κατά τη μάσηση, αλλά και η δυσκολία διάνοιξης του στόματος. Η εκφύλιση των ανώτερων κινητικών νεύρων του άξονα οδηγεί σε ακαμψία και έλλειψη ισορροπίας. Τα συμπτώματα από τα κατώτερα κινητικά νεύρα, δηλαδή τα νεύρα του εγκεφαλικού στελέχους και της σπονδυλικής στήλης, εμφανίζονται συνήθως κατά την εξέλιξη της νόσου. 24
25 Κατά κύριο λόγο, ο εκφυλισμός τους προκαλεί μυϊκή αδυναμία, μυϊκή ατροφία, μυϊκό σπασμό και κράμπες. Η εμφάνιση των συμπτωμάτων από τα κατώτερα κινητικά νεύρα έχει ως αποτέλεσμα την επιδείνωση των κινήσεων των άκρων και των στοματοφαρυγγικών μυών. Προοδευτικά, επηρεάζονται και άλλοι μύες του προσώπου, εμφανίζεται δύσπνοια λόγω διαφράγματος, καθώς και δυσκολία διατήρησης του κορμού και της κεφαλής σε όρθια θέση (Elman, LB and McCluskey, L, Uptodate. 2012). Ιστοπαθολογικά ευρήματα Η νόσος χαρακτηρίζεται από εκφυλισμό και απώλεια των κινητικών νευρώνων με αστροκυτταρική γλοίωση. Στα εκφυλιζόμενα νεύρα και στη γλοία παρατηρούνται ενδοκυτταρικά έγκλειστα. Αυτά τα έγκλειστα ανήκουν σε έναν ή περισσότερους από τους παρακάτω τύπους: 1. Σωμάτια bunina. Αυτά είναι ηωσινοφυλλικά ενδοκυττοπλασματικά σωμάτια υαλίνης, που περιέχουν τον αναστολέα της πρωτεάσης της κυστεΐνης. Τα σωμάτια bunina είναι χαρακτηριστικά της νόσου και εντοπίζονται κατά προσέγγιση στο 80 % των ασθενών. 2. Έγκλειστα ουβικουιτίνης. 3. Σωμάτια που μοιάζουν με Lewy και σε κάποιες περιπτώσεις περιέχουν νευρικές ίνες. 4. Έγκλειστα υαλίνης στα οποία εντοπίζονται, φωσφορυλιωμένες και μη, νευρικές ίνες. 5. Αδιάλυτες πολυγλυκοζυλιωμένες πρωτεΐνες σε έγκλειστα υαλίνης. Βρίσκονται σε ασθενείς με μετάλλαξη στο γονίδιο SOD1 και περιέχουν ουβικουιτίνη, φωσφορυλιωμένες νευρικές ίνες και SOD1. Επίσης, μια κοινή παρατήρηση σε ασθενείς με ALS είναι τα μη φυσιολογικά μιτοχόνδρια και η κατακερματισμένη συσκευή Golgi (Wijesekera and Leigh 2009). 25
26 Β.1.7 Κριτήρια Διάγνωσης και Διαφορική Διάγνωση Οι ασθενείς με κλινική εικόνα πλάγιας αμυοτροφικής σκλήρυνσης θα πρέπει να παραπέμπονται σε ηλεκτροφυσιολογικές διαγνωστικές εξετάσεις, ώστε αρχικά να καταγραφούν οι όποιες ενδείξεις εκφυλισμού των ανώτερων και κατώτερων κινητικών νευρώνων και δευτερευόντως, για να αποκλειστούν άλλες παθολογικές διεργασίες. Β Κριτήρια Διάγνωσης El Escorial Στην Awaji-shima (Ιαπωνία), τα αναθεωρημένα κριτήρια El Escorial διαφοροποιήθηκαν (Airlie House 1998) με την προσθήκη συναινετικών συστάσεων, όσον αφορά τις ηλεκτροφυσιολογικές εξετάσεις για τη διάγνωση της νόσου του ALS: Αρχές (από τα κριτήρια Airlie House). Η διάγνωση της αμυοτροφική πλευρικής σκλήρυνσης απαιτεί: (Α) παρουσία 1. στοιχείων από την κλινική, την ηλεκτροφυσιολογική εξέταση ή νευροπαθολογικά ευρήματα, που υποδεικνύουν εκφυλισμό του κάτω κινητικού νευρώνα (LMN) 2. στοιχείων από την κλινική εξέταση που υποδεικνύουν εκφυλισμό του ανώτερου κινητικού νευρώνα (UMN) 3. προοδευτική εξάπλωση των συμπτωμάτων σε μια περιοχή ή σε άλλες περιοχές, όπως καθορίζεται από το ιστορικό, τη φυσική εξέταση ή τα ηλεκτροφυσιολογικά τεστ (Β) απουσία 1. ηλεκτροφυσιολογικών ή παθολογικών ενδείξεων εκφυλισμού των LMN και / ή UMN, που θα μπορούσαν να αποδοθούν σε άλλη νόσο 2. νευροαπεικονιστικών στοιχείων, που υποδεικνύουν κάποια άλλη ασθένεια και που θα μπορούσαν να εξηγήσουν τα παρατηρούμενα κλινικά συμπτώματα και τις ηλεκτροφυσιολογικές εξετάσεις Β Διαγνωστικές κατηγορίες Η «Κλινικά οριστική ALS» ορίζεται από κλινικά ή ηλεκτροφυσιολογικά στοιχεία για την παρουσία εκφυλισμού ΑΚΝ, καθώς και σημάδια εκφυλισμού ΚΚΝ σε τρεις περιοχές. Η «Κλινικά πιθανή ALS» ορίζεται από κλινικά ή ηλεκτροφυσιολογικά στοιχεία για την παρουσία εκφυλισμού ΚΚΝ, καθώς και σημάδια εκφυλισμού ΑΚΝ σε τουλάχιστον δύο περιοχές με κάποια σημάδια εκφυλισμού ΑΚΝ ανωδικά των ΚΚΝ. Η «Κλινικά δυνατή ALS» ορίζεται από κλινικά ή ηλεκτροφυσιολογικά στοιχεία για την παρουσία δυσλειτουργίας ΑΚΝ και ΚΚΝ, τα οποία συνυπάρχουν σε μία μόνο περιοχή ή αποκλειστικά σημάδια εκφυλισμού των ΑΚΝ σε δύο ή περισσότερες περιοχές ή σημάδια εκφυλισμού από τους ΚΚΝ τα οποία βρέθηκαν να εκφύονται ανωδικά των σημείων από τους ΑΚΝ. Σημειώνεται, εδώ, πως η νευροαπεικόνιση και οι κλινικές εργαστηριακές μελέτες πρέπει να έχουν ήδη αποκλείσει άλλες νόσους. 26
27 Οι συστάσεις αυτές υπογραμμίζουν την ισοδυναμία των κλινικών και ηλεκτροφυσιολογικών δοκιμών. Η κατηγορία ''Κλινικά Πιθανή ALS Υποστηριζόμενη από εργαστηριακά ευρήματα'' καθίσταται περιττή (Wijesekera and Leigh 2009; Brooks, Β Διαφορική διάγνωση Ο αποκλεισμός των λοιπών νόσων γίνεται με διαγνωστικές εξετάσεις, που αφορούν κατά βάση τη μαγνητική τομογραφία (MRI - Magnetic resonance imaging) εγκεφάλου και αυχενικής μοίρας του νωτιαίου μυελού και το ηλεκτρομυογράφημα (EMG). 1. Ηλεκτροφυσιολογικές διαγνωστικές εξετάσεις Έλεγχος αγωγιμότητας κινητικών και αισθητικών νεύρων που αναμένεται φυσιολογικός ή σχεδόν φυσιολογικός εκτός λίγων περιπτώσεων Συμβατικό ηλεκτρομυογράφημα, το οποίο εκτιμάται βάση των κριτηρίων El Escorial Διακρανιακή μαγνητική διέγερση (TMS - Transcranial Magnetic Stimulation), που επιτρέπει μια μη επεμβατική αξιολόγηση των πυραμιδικών οδών και την ανίχνευση των UMN βλαβών Ο χρόνος αγωγής μέσω των κεντρικών κινητικών νεύρων προς τους μυς (CMCT - Central Motor Conduction Time), παρατείνεται τουλάχιστον σε ένα άκρο Ηλεκτρομυογράφημα, που παρέχει ποσοτική εκτίμηση του αριθμού των αξόνων που νευρώνουν ένα μυ ή μιας ομάδας μυών (MUNE - Motor Unit Number Estimation) 2. Νευροαπεικονιστικές μέθοδοι Αυτές δεν απαιτούνται στις περιπτώσεις που έχουμε κλινικά βέβαιη νόσο ή με προμηκική (βλάβη στον ΚΚΝ) ή ψευδοπρομηκική (βλάβες στις πυραμιδικές οδούς του ΑΚΝ) έναρξη Μαγνητική τομογραφία Βιοψία των σκελετικών μυών ή άλλων ιστών Δεν απαιτείται για τη διάγνωση, πέραν του αποκλεισμού ενός μιμητικού συνδρόμου (ενδεικτικά, μυοσίτιδα με έγκλειστα) Συνήθεις νόσοι, με τις οποίες συγχέεται η ALS: Α) Η πιο συχνή νόσος με την οποία συγχέεται η ALS η είναι η πολυεστιακή κινητική νευροπάθεια (MMN - Multifocal Motor Neuropathy) στην οποία, ωστόσο, κυριαρχούν ενδείξεις από τα κατώτερα κινητικά νεύρα και πολλαπλές ασυνέχειες κατά το ηλεκτρομυογράφημα. Η διάκριση γίνεται με έλεγχο των αντισωμάτων, αντανακλαστικών που δηλώνουν συμβολή του κεντρικού νευρικού συστήματος και της ανταπόκρισης στην κυκλοφωσφαμίδη και τη γλομπουλίνη. Η ανταπόκριση είναι θετική στην περίπτωση της πολυεστιακής κινητικής νευροπάθειας και ελέγχεται (i) με (MRS Magnetic Resonance Spectroscopy), μέτρηση του αριθμού των νευρώνων στον κινητικό φλοιό (μέτρηση μεταβολικής δραστηριότητας) και (ii) με μαγνητική διέγερση, ώστε να διαπιστωθεί η αγωγιμότητα στις φλοιονωτιαίες οδούς και (iii) με ηλεκτρομυογράφημα, για την καταμέτρηση των βιώσιμων κινητικών νευρώνων. 27
28 Β) H νωτιαία μυϊκή ατροφία (SMA - Spinal Muscular Atrophy ή Kennedy s syndrome) από τις κατώτερες κινητικές οδούς, που διακρίνεται από την ALS χάρη στη διαφορετική μοριακή παθολογία και την καλοήθη πορεία της ασθένειας. Γ) Η οικογενής σπαστική παραπληγία / παραπάρεση (HSP Hereditary Spastic Paraplegia / Paraparesis), η οποία κληρονομείται με αυτοσωμικό επικρατή ή υπολειπόμενο και φυλοσύνδετο τρόπο και χαρακτηρίζεται από σπαστική παραπάρεση και συμμετοχή κυρίως των ανώτερων κινητικών νευρώνων. Επιπροσθέτως, συνήθως παρατηρείται αργή εξέλιξη της νόσου. Οι παραπάνω νευροεκφυλιστικές ασθένειες, συμπεριλαμβανομένης της ALS ανήκουν στη νόσο του κινητικού νευρώνα (MND - Motor Neuron Disease) και διαθέτουν κοινό μοριακό μηχανισμό, αλλά διαφέρουν ως προς τα συμπτώματα, την πρόγνωση και την πρόοδο της νόσου. Ως πρόδρομες της ALS θεωρούνται: Α) Η πρωτογενής πλευρική σκλήρυνση (PLS - Primary lateral sclerosis) που εμφανίζεται αρχικά με συμπτώματα των ανώτερων κινητικών νευρώνων (σπαστικότητα, προβλήματα στην ομιλία και στην κατάποση και στο βάδισμα). Παρουσιάζει αργή πρόοδο και αυξημένη επιβίωση, ενώ η απώλεια βάρους δεν αποτελεί σύμπτωμα. Β) Η προοδευτική μυϊκή ατροφία (PMA - Progressive Muscular Atrophy) εμφανίζει αρχικά συμπτώματα που οφείλονται στους κατώτερους κινητικούς νευρώνες (αδυναμία, ατροφία μυών και μυϊκές συσπάσεις). Η διάγνωση της προμηνύει αυξημένη διάρκεια ζωής. Γ) Η σταδιακή προμηκική παράλυση (BPB - Progressive Bulbar Palsy), η οποία εμφανίζεται με διαταραχή των κρανιακών μυών και εκφυλισμό των ανώτερων και κατώτερων κινητικών νευρώνων. Τα πρώτα συμπτώματα είναι προβλήματα στην κίνηση της γλώσσας, στην κατάποση και την ομιλία. Δ) Το σύνδρομο πλήρης έλλειψης κινητικότητας και αίσθησης των άκρων (flail arm and flail leg syndrome), η αμυοτροφική διπληγία, εμφανίζεται με αδυναμία που κυρίως επηρεάζει τα άνω άκρα και εκφυλισμό των κατώτερων κινητικών νευρώνων. Η πρόοδος της νόσου είναι αργή, καθώς και η εξάπλωση των συμπτωμάτων στο σώμα και στους αναπνευστικούς μυς. Ε) Το «ALS plus syndrome» εκτός από τον εκφυλισμό των ανώτερων και κατώτερων κινητικών νευρώνων, που επηρεάζει μόνο τις ακούσιες κινήσεις, εμφανίζεται συγχρόνως με μια από τις παρακάτω νόσους: παρκινσονισμός, μετωποκροταφική άνοια, ανεπάρκεια αυτόνομου νευρικού συστήματος, αισθητική απώλεια ή υπερπυρηνική πάρεση βλέμματος (Elman, LB and McCluskey, L, Uptodate. 2012). 28
29 Β Παράγοντες πρόγνωσης Παράγοντες οι οποίοι παραπέμπουν σε λιγότερο ή περισσότερο επιθετική μορφή της νόσου και παρατεταμένη ή μειωμένη επιβίωση αντίστοιχα, είναι η ηλικία, η περιοχή έναρξης των συμπτωμάτων και τέλος, ορισμένα σύνδρομα (Πίνακας 1). Πίνακας 1: Προγνωστικοί παράγοντες της ALS (Hardiman, van den Berg, and Kiernan 2011) Ενθαρρυντικοί Προγνωστικοί παράγοντες Δυσμενείς Προγνωστικοί παράγοντες Ηλικία < 50 ετών Ηλικία > 65 ετών άκρα Έναρξη συμπτωμάτων από τα κάτω Έναρξη συμπτωμάτων από την αναπνευστική οδό Μεγάλο μεσοδιάστημα από την έναρξη των συμπτωμάτων ως τη διάγνωση Υπερλιπιδαιμία Φροντίδα σε καλή κλινική Σύνδρομο πλήρους έλλειψης κινητικότητας και αίσθησης των άνω ή κάτω άκρων (flail arm or flail leg syndrome) ή σημάδια εκφύλισης μόνο από τους κατώτερους ή τους ανώτερους κινητικούς νευρώνες. Προμηκική έναρξη Μικρό μεσοδιάστημα από την έναρξη των συμπτωμάτων ως τη διάγνωση Κακή διατροφή Επηρεασμένη εκτελεστική λειτουργία Χαμηλός κίνδυνος για το καρδιαγγειακό (καλή λιπιδική ισορροπία) Γρήγορη επιδείνωση Μειωμένη λειτουργία των πνευμόνων 29
30 Β.1.8 Θεραπεία και θεραπευτικές προσεγγίσεις Στόχος της θεραπείας στην ALS είναι η αύξηση του χρόνου επιβίωσης, η παράταση της περιόδου αυτονομίας του ασθενούς και η βελτίωση της ποιότητας της ζωής του. Ριλουζόλη Η ριλουζόλη αποτελεί την πρώτη εγκεκριμένη θεραπεία για την ALS από τον FDA και πλέον έχει λάβει έγκριση και από τον ΕΜΑ. Η ριλουζόλη δρα αυξάνοντας τον χρόνο επιβίωσης από 3 έως 6 μήνες, καθυστερώντας την εξέλιξη της νόσου. Τα αποτελέσματα της χρήσης της ριλουζόλης είναι καλύτερα κατά τους πρώτους 12 μήνες θεραπείας και στις περιπτώσεις που η έναρξη της ασθένειας εντοπίζεται στον προμήκη. Ο μηχανισμός δράσης της ριλουζόλης δεν είναι πλήρως τεκμηριωμένος. Ωστόσο, έχει βρεθεί ότι αναστέλλει προσυναπτικά την απελευθέρωση του γλουταμινικού οξέος και αυξάνει την επαναπρόσληψή του από τις προσυναπτικές απολήξεις. Μετασυναπτικά δρα ως έμμεσος ανταγωνιστής του γλουταμινικού οξέος, πιθανώς αλληλεπιδρώντας με τους τασεο εξαρτώμενους διαύλους νατρίου, σταθεροποιώντας τους σε ανενεργή μορφή ή με G πρωτεΐνες. Εμπλέκεται, επίσης, στις απαντήσεις ενεργοποίησης των NMDA υποδοχέων. Οι ανεπιθύμητες ενέργειες περιλαμβάνουν αδυναμία, δυσκινησία και γαστρεντερικές διαταραχές, ενώ η ανεπιθύμητη ενέργεια που πιθανόν να οδηγήσει στη διακοπή της φαρμακευτικής χορήγησης είναι η αύξηση των επιπέδων των τρανσαμινασών. Άλλοι αντι γλουταμικοί παράγοντες που διερευνήθηκαν, όπως η γκαπαπεντίνη, η λαμοτριγίνη, η τοπιραμάτη και η ταλαμπανέλη αποδείχτηκαν αναποτελεσματικοί. Tirasemtiv Πρόκειται για φάρμακο που σταμάτησε στη φάση ΙΙΒ των κλινικών μελετών, γιατί παρόλο που εμφάνισε ενθαρρυντικά αποτελέσματα, επιβραδύνοντας την επιδείνωση της αναπνευστικής λειτουργίας και την αποδυνάμωση των μυών, δε γίνεται καλά ανεκτό (Pflumm 2014c). Φάρμακα που στοχεύουν το SOD1 Η λανθασμένα αναδιπλωμένη SOD1 πρωτεΐνη είναι ο νέος στόχος των ερευνητών (Banci et al. 2008). Το αντινοηματικό ολιγονουκλεοτίδιο SOD1Rx, που αναπτύχθηκε από την ISIS Pharmaceuticals, είναι αυτή τη στιγμή σε κλινική φάση σταδίου Ι. Αντισώματα ενάντια σε SOD1 με λανθασμένη τους αναδίπλωση, αναπτύχθηκαν από την Neurimmune Therapeutics AG και την Biogen Idec και είναι σε προκλινικό στάδιο. Μικρά μόρια, που στοχεύουν το λανθασμένα αναδιπλωμένο SOD1 και αναπτύσσονται από τις ομάδες των Neil Cashman MD και Fernando Vieira MD, προσεγγίζουν το προκλινικό στάδιο. Τέλος, νανοσωματίδια λανθασμένα αναδιπλωμένου SOD1 από το Πανεπιστήμιο του Λούβεν, υπό την ηγεσία του Wim Robberecht MD PhD, βρίσκονται σε αρχικό ακόμα στάδιο ανάπτυξης (Pflumm 2014b). Φάρμακα νέας γενιάς για την προστασία των μιτοχονδρίων Το MitoQ, απόγονος του συνενζύμου Q10 (CoQ10), που αποδείχθηκε αναποτελεσματικό στη βελτίωση της κλινικής εικόνας της ALS, παρουσίασε ενθαρρυντικά αποτελέσματα, όταν δοκιμάστηκε σε μύες. Τα αποτελέσματα αποδίδονται στην αντιοξειδωτική του δράση έναντι των αζωτούχων ριζών, που παράγονται, λόγω δυσλειτουργίας των μιτοχονδρίων (Miguel 2014). 30
31 IL-2 Ο Gilbert Bensimon, αναμένεται να πραγματοποιήσει μια τυχαιοποιημένη κλινική δοκιμή, στην οποία θα συμμετέχουν 24 ασθενείς ALS, όπου θα μελετηθεί η ανοχή και αποτελεσματικότητα των χαμηλών δόσεων IL-2, με σκοπό την αύξηση των Τ ρυθμιστικών κυττάρων (Pflumm 2014a), που φέρονται να έχουν ευεργετική δράση στην εξέλιξη της νόσου (Henkel et al. 2013, Βeers 2011). Τροποποιητικά της νόσου φάρμακα Η γκαπαπεντίνη έδωσε ενθαρρυντικά αποτελέσματα σε ζωικά μοντέλα. Εκτός από τους ανταγωνιστές του γλουταμινικού οξέος, έχουν δοκιμαστεί αντιοξειδωτικά, νευροτροφικοί παράγοντες, όπως ορμόνες, αυξητικοί παράγοντες και εκλυτικοί παράγοντες νευροτροφικών παραγόντων. Έχουν δοκιμαστεί, επίσης, αντιικοί παράγοντες, όπως η τιλορόνη και η αμανταδίνη, καθώς και τροποποιητικοί παράγοντες του ανοσοποιητικού (Rowland and Shneider 2001). Ο μηχανισμός εκφυλισμού των νευρικών κυττάρων θεωρείται ότι είναι ο προγραμματισμένος κυτταρικός θάνατος και για αυτό το λόγο, δοκιμάστηκαν αναστολείς της απόπτωσης, όπως οι αναστολείς των κασπασών, η IL-1β και η αντιαποπτωτική πρωτεΐνη Bcl- 2. Επιπλέον, δοκιμάσθηκαν αντιφλεγμονώδεις παράγοντες, όπως η σελεκοξίμπη, η οποία δρα αναστολέας της κυκλοοξυγενάσης 2 (COX-2). Τέλος, διερευνήθηκαν χηλικές ενώσεις που δεσμεύουν τον χαλκό σε καλλιέργειες νευρικών κυττάρων. Τα ιόντα του χαλκού είναι απαραίτητα για την τοξικότητα που παρουσιάζει η μεταλλαγμένη SOD1. Άλλος μελλοντικός στόχος είναι μια σαπερόνη που μεταφέρει τα ιόντα χαλκού στη SOD1 (Wijesekera and Leigh 2009). Γονιδιακή θεραπεία Ιικοί ανασυνδυασμένοι φορείς δύνανται να δοκιμαστούν για τη μεταφορά και την έκφραση πολλών γονιδίων εφόσον αυτά είναι γνωστό ότι ευθύνονται για την ασθένεια. Μία εκδοχή είναι η χρήση γονιδιακής θεραπείας για να εκφραστούν νευροτροφικοί παράγοντες απευθείας στους νευρώνες με τη χρήση γενετικά ανασυνδυασμένων αδενοσχετιζόμενων ιών (AAV), τεχνική που έχει δοκιμαστεί με θετικά αποτελέσματα σε ζωικά μοντέλα με μεταλλάξεις σε κρίσιμα γονίδια. Με παρόμοια επιτυχία έχει δοκιμαστεί και η έκφραση της αντιαποπτωτικής πρωτεΐνης Bcl-2. Εναλλακτικά και εφόσον έχει βρεθεί ότι μια συγκεκριμένη γενετική βλάβη είναι υπεύθυνη για την εκδήλωση της νόσου, δύναται να αποδειχτεί ωφέλιμη η χρήση των τεχνικών της γονιδιακής θεραπείας για την εισαγωγή του γονιδίου της μη λειτουργικής πρωτεΐνης (Traub, Mitsumoto, and Rowland 2011). 31
32 Αποσιώπηση RNA Αυτή η τεχνική εξασφαλίζει την αναστολή της γονιδιακής έκφρασης σε επίπεδο mrna με τη χρήση sirna, γυμνού ή ενσωματωμένου σε κατάλληλο φορέα, συμπληρωματικού προς τμήμα του γονιδίου που επιθυμούμε να αποσιωπήσουμε. Η εν λόγω τεχνική απαιτεί το υπεύθυνο γονίδιο ή τμήμα του γονιδίου (τουλάχιστον 21 βάσεων στην περιοχή των εξωνίων) να είναι γνωστό. Σημαντική προϋπόθεση αποτελεί ο κατάλληλος φορέας. Στην περίπτωση του κεντρικού νευρικού συστήματος, οι ιικοί φορείς είναι πιο αποτελεσματικοί, αλλά τα αποτελέσματα της μακροχρόνιας χορήγησης δεν είναι γνωστά (Traub, Mitsumoto, and Rowland 2011). Η χρήση αντινοηματικών ολιγονουκλεοτιδίων ερευνάται στην περίπτωση της επέκτασης επανάληψης στο C9orf72, χωρίς επιτυχία μέχρι στιγμής (Lagier-Tourenne et al. 2013). Ανοσοθεραπεία Η ανοσοθεραπεία στηρίζεται στη χρήση ειδικών αντισωμάτων, τα οποία αναγνωρίζουν την μεταλλαγμένη πρωτεΐνη και συνδέονται ανταγωνιστικά μαζί της ή μειώνουν τη συγκέντρωσή της (Traub, Mitsumoto, and Rowland 2011). Η παθητική ανοσοποίηση έχει δοκιμαστεί σε ζωικά μοντέλα SOD1 με ενθαρρυντικά αποτελέσματα (Gros-Louis et al. 2010), ενώ σε κλινική δοκιμή βρίσκεται το μονοκλωνικό αντίσωμα οζανεζουμάβη (GSK ) έναντι του αναστολέα ανάπτυξης των νευρικών κυττάρων (Neurite Outgrowth Inhibitor, NOGO-A) ( =3). Μεταμόσχευση Βλαστοκυττάρων Η μεταμόσχευση βλαστοκυττάρων μπορεί να προσφέρει τη δυνατότητα μεταφοράς αυξητικών παραγόντων, αστροκυττάρων ή μικρογλοιακών κυττάρων με αντιφλεγμονώδη δράση, καθώς επίσης και ανοσορύθμιση. Ακόμα, τα βλαστοκύτταρα μπορούν να αντισταθμίσουν την απώλεια των νευρικών κυττάρων με αντικατάσταση ή με νευροτροφικά κύτταρα. 1. Μεταμόσχευση μεσεγχυματικών βλαστοκυττάρων (mesenchymal stem cells MSCs) (Mazzini et al. 2010) 2. Μεταμόσχευση μυελού των οστών, που περιέχει μεσεγχυματικά βλαστοκύτταρα και αιμοποιητικά βλαστοκύτταρα (hematopoietic stem cells HSCs). 3. Αυτόλογη μεταμόσχευση μεσεγχυματικών βλαστοκυττάρων και αιμοποιητικών βλαστοκυττάρων για τη ρύθμιση της ανοσοαπόκρισης και της φλεγμονής, αντίστοιχα (Papadeas and Maragakis 2009). 4. Μεταμόσχευση αντικατάστασης νευρικών κυττάρων με πρόδρομα νευρικά κύτταρα. 5. Μεταμόσχευση ινοβλαστών ενηλίκων που έχουν μετασχηματιστεί σε πολυδύναμα βλαστικά κύτταρα (Traub, Mitsumoto, and Rowland 2011). 6. Πρόδρομα νευρικά κύτταρα (Neural precursor cells NPCs) επεξεργασμένα με μεθόδους γενετικής μηχανικής, ώστε να μεταφέρουν νευροτροφικούς παράγοντες 7. Μεταμόσχευση διαφοροποιημένων συνοδών κυττάρων, όπως μικρογλοία και αστροκύτταρα (Papadeas and Maragakis 2009, Traub, Mitsumoto, and Rowland 2011) 32
33 NSI-566 Μεταμόσχευση ανθρώπινων βλαστοκυττάρων προερχόμενα από τη σπονδυλική στήλη εμφυτεύονται κατευθείαν στην φαιά ουσία της σπονδυλικής στήλης του ασθενούς σε κλινικές μελέτες φάσης Ι/ΙΙ (Neuralstem Inc 2014, καθώς τα αποτελέσματα από την πρώτη φάση ήταν ενθαρρυντικά (Glass et al. 2012) Αυτόλογη μεταμόσχευση μονοπύρηνων βλαστικών κυττάρων μυελού των οστών Στη φάση Ι/ΙΙ των κλινικών μελετών βρίσκεται και η αυτόλογη μεταμόσχευση, με απευθείας έγχυση στη σπονδυλική στήλη, μονοπύρηνων βλαστικών κυττάρων μυελού των οστών. Τα αποτελέσματα μέχρι ώρας δείχνουν ασφάλεια και νευροτροφική δράση (Blanquer et al. 2012). Άλλες κλινικές μελέτες Αυτή τη στιγμή λαμβάνουν χώρα κλινικές μελέτες φάσης ΙΙ/ΙΙΙ για το «Arimoclomol» το οποίο ενεργοποιεί ένα επιδιορθωτικό μονοπάτι, στο οποίο συμμετέχουν μοριακές σαπερόνες και φάσης Ι/ΙΙ για την πυριμεθαμίνη. Συμπτωματική αντιμετώπιση Στα πιο προχωρημένα και τελικά στάδια της ALS παρατηρούνται οι παρακάτω κρίσιμες καταστάσεις: I. Η αναπνευστική ανεπάρκεια λόγω αδυναμίας των μυών του αναπνευστικού εμφανίζεται με δύσπνοια, ορθόπνοια, ανορεξία, διαταραχές συγκέντρωσης και είναι εντονότερη κατά τη διάρκεια του ύπνου. II. Η δυσφαγία που οδηγεί σε αφυδάτωση, κακή θρέψη, απώλεια βάρους και εισροφητικές πνευμονίες. Η αντιμετώπιση γίνεται με παρεμβατικές ή μη τεχνικές. Σημαντική είναι και η φροντίδα της ψυχολογικής κατάστασης συγγενών, καθώς η ALS θεωρείται χρόνια και ανίατη νόσος. των ασθενών και των Για τη βελτίωση της ποιότητας της ζωής και την παράταση της αυτονομίας του ασθενούς αξιοποιείται η δυνατότητα συμπτωματικής θεραπείας. Η συμπτωματική θεραπεία στοχεύει τα βασικά συμπτώματα των ασθενών με ALS. Για τις κράμπες, συνήθως, χρησιμοποιείται καρβαμαζεπίνη και φαινυτοΐνη, ενώ για τη σπαστικότητα βακλοφένη, δανδρολένη και τιζανιδίνη, σε συνδυασμό με φυσιοθεραπεία και υδροθεραπεία. Για την σιελόρροια χρησιμοποιείται ατροπίνη, αμιτριπτυλίνη και υοσκιαμίνη, ενώ για τον λαρυγγόσπασμο, λοραζεπάμη και τέλος, αναλγητικά, οπιοειδή και ΜΣΑΦ για τον πόνο. Άλλα συμπτώματα, τα οποία πρέπει να αντιμετωπιστούν, είτε με φάρμακα, είτε με άλλες προσεγγίσεις, είναι οι επικοινωνιακές δυσκολίες, η δυσκοιλιότητα, η κατάθλιψη, το άγχος και η κόπωση (Wijesekera and Leigh 2009). 33
34 Β.1.9 Γενετικοί παράγοντες που σχετίζονται με την Πλάγια Αμυοτροφική Σκλήρυνση Β Ετερογένεια της νόσου Η γνώση μιας πληθώρας γενετικών τόπων και γονιδίων που έχουν συσχετισθεί με την ALS, μας οδηγούν στο συμπέρασμα ότι διαφορετικά γενετικά αίτια μπορούν να οδηγήσουν στην τελική εκδήλωση της νόσου, ενώ ταυτόχρονα τα κλινικοπαθολογικά χαρακτηριστικά της να είναι πανομοιότυπα. Στον αντίποδα, έχει παρατηρηθεί διαφορετικός βαθμός διεισδυτικότητας ή διαφορές σε άλλα φαινοτυπικά χαρακτηριστικά ως αποτέλεσμα διαφορετικών μεταλλάξεων στο ίδιο γονίδιο. Σε αυτή την κατηγορία ανήκει το παράδειγμα των μεταλλάξεων του SOD1 που είναι υπεύθυνο για την ALS1. Συγκεκριμένα, οι μεταλλάξεις Ι113Τ και D90A προσδίδουν μειωμένη διεισδυτικότητα στη νόσο σε σχέση με την Α4V. Επιπροσθέτως, η τελευταία έχει συσχετισθεί με τη ραγδαία εξέλιξη της νόσου, ενώ ταυτοχρόνως προκαλεί το 50 % της ALS1 στους Νοτιο - Αμερικάνους (Siddique and Siddique 2008). Β Γενετική στη διάγνωση της ALS Όσον αφορά τη διαγνωστική αξία των μεταλλάξεων αυτών, μόνο οι μεταλλάξεις στο γονίδιο SOD1 έχουν συμπεριληφθεί στα κριτήρια El Escorial και επομένως, έχουν διαγνωστική αξία. Ο εντοπισμός τους οδηγεί απευθείας σε διάγνωση «Σίγουρη ALS» (Siddique and Siddique 2008). Β Διερεύνηση της Γενετικής προδιάθεσης Μελέτες σύνδεσης Οι μελέτες σύνδεσης (Linkage studies) αφορούν κυρίως τη μελέτη οικογενειών στις οποίες υπάρχουν μέλη που πάσχουν από την Οικογενή μορφή της Πλαγίας Αμυοτροφικής Σκλήρυνσης. Στόχος αυτών των μελετών είναι η αναζήτηση των γονιδίων που σχετίζονται με την εμφάνιση της νόσου. Μια μελέτη σύνδεσης μπορεί να αφορά γονίδια που έχουν επιλεχτεί ως υποψήφια ή την αναζήτηση των υπεύθυνων γονιδίων σε ολόκληρο το γονιδίωμα. Η τελευταία προσέγγιση αφορά μεθόδους συσχέτισης ολόκληρου του γονιδιώματος, αλληλούχησης ολόκληρου του γονιδιώματος ή μόνο των εξωνίων. Μελέτες συσχέτισης Οι μελέτες συσχέτισης (Association studies) εξυπηρετούν την εύρεση γενετικών αιτίων, υπεύθυνων για τη Σποραδική Πλάγια Αμυοτροφική Σκλήρυνση. Κατά τις μελέτες συσχέτισης είναι απαραίτητη η επιλογή των γονιδίων, των γενετικών τόπων ή των πολυμορφισμών που θα μελετηθούν. Η συνηθέστερη διαδικασία περιλαμβάνει τη μελέτη των υποψήφιων γονιδίων σε δείγμα ασθενών έναντι υγιών. Στόχος της συγκεκριμένης προσέγγισης είναι η συσχέτιση ενός φαινοτύπου με ένα γονίδιο ή ένα αλληλόμορφο. 34
35 Τα κριτήρια επιλογής των υποψήφιων γονιδίων είναι κατά κύριο λόγο τα εξής (Beleza- Meireles and Al-Chalabi 2009): 1. Δομή πρωτεΐνης 2. Λειτουργία πρωτεΐνης 3. Ομοιότητα με γνωστά γονίδια, δομική ή λειτουργική 4. Κατηγορίες γονιδίων που έχουν ήδη συσχετισθεί (Εικόνα 7) VAPB, DAO, UBQLN2, OPTN, Neurofilaments, SOD1, FUS, TARDBP Συσσωμάτωση πρωτεϊνών FIG4, VAPB,DCTN1, VCP, Alsin, CHMP2B TARDBP, FUS, ANG, SETX, ATXN2,ELP3 PRPH, SOD1, DCTN, SPG11, Neurofilaments Ενδοκυττάρια μετακίνηση οργανιδίων Eπεξεργασία του RNA Δυσλειτουργία των αξόνων ΕΑΑΤ2, SOD1, DAO SOD1, PON, APEX1 Τοξικότητα υπερδιέγερσης από γλουταμικό Αντιoξειδωτική διαδικασία VCP, UBQLN2 SOD1, PGRN OPTN, VCP SOD1, PGRN DAO MAPT APEX1 SIGMAR1 Ομοιόσταση πρωτεϊνών Αποκοδόμηση πρωτεϊνών Φλεγμονή Αυτοφαγία Φαγοκυττάρωση (ενεργοποίησης της μικρογλοίας) Απόπτωση Κυτταροσκελετός Επιδιόρθωση DNA και πρόσδεση μεταγραφικών παραγόντων Δίαυλος ιόντων Εικόνα 7: Γονίδια που έχουν συσχετισθεί, είτε με την Οικογενή, ή με την Σποραδική ALS. Στην εικόνα παρατίθεται η κατηγοριοποίηση των μηχανισμών των γονιδίων. Η κατηγοριοποίηση δίνει μια εικόνα των μηχανισμών που πιθανώς ευθύνονται για την νευροεκφύλιση στην ALS (Chen et al. 2013, Schymick, Talbot, and Traynor 2007, Kunst 2004, Ferraiuolo et al. 2011). 5. Συσχέτιση με άλλες νευροεκφυλιστικές ασθένειες, όπως η νόσος του Parkinson, η νόσος του Alzheimer, η Άνοια και η Οικογενής σπαστική παραπληγία (Εικόνα 8) Οι μελέτες σύνδεσης και αλληλούχησης των εξωνίων στηρίζονται στην υπόθεση ότι κάποια μετάλλαξη ευθύνεται για τον φαινότυπο του ενδιαφέροντος. Παρομοίως, οι μελέτες συσχέτισης με την αλληλούχηση των υποψηφίων γονιδίων δεν είναι δυνατό να εξηγήσει το σύνολο των σποραδικών περιπτώσεων και σε αυτό το σημείο, εμφανίζεται η θεώρηση ότι «μια κοινή νόσος θα οφείλεται σε κοινά αλληλόμορφα». Η ALS μπορεί να θεωρηθεί κοινή νόσος, καθώς ο κίνδυνος για κάθε άτομο να εμφανίσει τη νόσο στη διάρκεια της ζωής του ανέρχεται στις 1/ (βασισμένο σε μελέτες στο Ηνωμένο Βασίλειο) (Wijesekera and Leigh 2009). Η παραπάνω θεώρηση συνεπάγεται μελέτες συσχέτισης με στόχο, κυρίως, συχνούς μονονουκλεοτιδικούς πολυμορφισμούς (SNPs), οι οποίοι λειτουργούν ως δείκτες, μέσω της γονοτύπησης των οποίων εξάγονται συμπεράσματα για άλλους, επίσης συχνούς, μονονουκλεοτιδικούς πολυμορφισμούς (tag SNPs). Αυτή η προσέγγιση είναι δυνατή χάρη στην ιδιότητα ορισμένων SNPs να συγκληρονομούνται. Το πλεονέκτημα αυτής της μεθόδου έγκειται στο ότι ένας μεγάλος αριθμός υποψηφίων γονιδίων και κοινών αλληλομόρφων 35
36 ελέγχονται ταυτόχρονα. Η εν λόγω προσέγγιση, ωστόσο, απέτυχε να δείξει ότι κοινά αλληλόμορφα ευθύνονται σημαντικά για την προδιάθεση στη SALS. Μελέτες συσχέτισης ολόκληρου του γονιδιώματος (GWAS - Genome-Wide Association Studies) Η διερεύνηση μονονουκλεοτιδικών πολυμορφισμών σε μεγάλη κλίμακα έγινε δυνατή με την εγκαθίδρυση της τεχνολογίας των μικροσυστοιχιών. Η τεχνολογία αυτή έδωσε τη δυνατότητα της παράλληλης γονοτύπησης πλήθους μονονουκλεοτιδικών πολυμορφισμών, ακόμα και στις περιοχές ανάμεσα στα γονίδια. Σε αυτή την περίπτωση, προτιμήθηκαν SNPs τα οποία βρίσκονται σε ανισορροπία σύνδεσης με άλλα SNPs, τα λεγόμενα «tag SNPs», όπως αναφέρθηκε και προηγουμένως. Με αυτόν τον τρόπο οι βασισμένες σε SNPs μελέτες συσχέτισης ολόκληρου του γονιδιώματος δίνουν μια εικόνα για κοινά αλληλόμορφα σε όλη την έκταση του γονιδιώματος. Η υπόθεση στην οποία στηρίζονται οι μελέτες συσχέτισης ολόκληρου του γονιδιώματος, σε δείγμα ασθενών έναντι υγιών, είναι ότι κοινά αλληλόμορφα ευθύνονται για κοινές ασθένειες. Πιο αναλυτικά, η παραπάνω υπόθεση σημαίνει ότι οι παράγοντες κινδύνου μιας πολύπλοκης ασθένειας, όπως η ALS, είναι κοινοί και αόρατοι στην εξελικτική επιλογή. Επιπλέον, υποθέτουμε πως υπάρχει μικρή ετερογένεια στα αλληλόμορφα ανά περιοχή του γονιδιώματος και ότι τα εν λόγω αλληλόμορφα έχουν μικρή διεισδυτικότητα. Μειονέκτημα αυτής της προσέγγισης είναι ότι αποκλείει σχεδόν τον εντοπισμό των σπάνιων αλληλομόρφων. Επιπλέον, τα αποτελέσματα από μελέτες συσχέτισης ολόκληρου του γονιδιώματος, συνήθως, δεν επαρκούν για τη σύνδεση ενός δείκτη με την προδιάθεση και την ασθένεια και απαιτείται επαλήθευση με μελέτες συσχέτισης και μελέτες έκφρασης, ιδιαίτερα στους ιστούς που μας ενδιαφέρουν (εγκέφαλος, σπονδυλική στήλη, κινητικοί νευρώνες). Τέτοιου είδους μελέτες έχουν αποδειχθεί χρήσιμες στον εντοπισμό της συσχέτισης γονιδίων, όπως τα ITPR2, DPP6, ELP3, UNC13A και της χρωμοσωμικής περιοχής 9p21 (Beleza-Meireles and Al-Chalabi 2009, Simpson et al. 2009, Chiò, Mora, et al. 2013, Cronin et al. 2008, DeJesus-Hernandez et al. 2010, van Es et al. 2007, van Es et al. 2008). Αλληλούχηση του συνόλου των εξωνίων (WES - Whole exome sequencing) Η συγκεκριμένη μέθοδος είναι χρήσιμη, όταν εφαρμόζεται σε οικογένειες για τον εντοπισμό μεταλλάξεων στην κωδική περιοχή. Το πλεονέκτημα της είναι ότι μπορεί να φανεί χρήσιμη, ακόμα και όταν η οικογένεια είναι πολύ μικρή για την πραγματοποίηση μελέτης σύνδεσης. Με αυτή τη μέθοδο έχουν βρεθεί νέες μεταλλάξεις στα γονίδια SOD1, SPG11 και UBQLN2. Επίσης, έχουν συσχετιστεί εκ νέου γονίδια με πιο πρόσφατη την περίπτωση του MATR3, VCP στο οποίο βρέθηκαν 4 μεταλλάξεις σε 5 οικογένειες, το PFN1 με 4 μεταλλάξεις σε 7 οικογένειες και 2 μεταλλάξεις του hnrnpa1. Με τον ίδιο τρόπο βρέθηκε μία μετάλλαξη στο hnrnpa2b1, αλλά εκτός από ALS, τα μέλη έπασχαν από μετωποκροταφική άνοια, νόσο του Paget και μυοπάθεια από έγκλειστα (Ferraiuolo et al. 2011, Leblond et al. 2014, Kim et al. 2013, Wu et al. 2012, Daoud et al. 2012, Johnson et al. 2014, Williams et al. 2012). Μία μόνο μελέτη είχε ως στόχο την εύρεση de novo μεταλλάξεων και πραγματοποιήθηκε από την ερευνητική ομάδα του (Chesi et al. 2013). 36
37 Μέθοδοι αλληλούχησης ολόκληρου του γονιδιώματος Η αλληλούχηση ολόκληρου του γονιδιώματος δεν είναι τόσο διαδεδομένη, όσον αφορά την αναζήτηση της γενετικής αιτίας της ALS. Μία μοναδική περίπτωση αφορά τη συσχέτιση του γονιδίου ERBB4, μεταλλάξεις στο οποίο οδηγούν στην οικογενή ALS19. Η κληρονομικότητα της ALS19 είναι αυτοσωμική επικρατής με ατελή διεισδυτικότητα. Εντοπίστηκαν δύο μεταλλάξεις, η p.arg927gln σε έναν Καναδό ασθενή FALS και η p.arg1275trp σε έναν Ιάπωνα ασθενή (Takahashi et al. 2013). Σήμερα, βρίσκεται σε εξέλιξη μια μεγάλη εκστρατεία αλληλούχησης ολόκληρου του γονιδιώματος, χιλιάδων ασθενών ALS και υγιών με τον τίτλο Project MinE ( και μια ακόμα που αφορά, κυρίως, μονοζυγωτικά δίδυμα. Εικόνα 8: Κοινές γενετικές αιτίες της ALS και άλλων ασθενειών με νευρολογική βάση. (Andersen and Al-Chalabi 2011) ALS: Amyotrophic Lateral Sclerosis (Πλάγια Αμυοτροφική Σκλήρυνση) FTD: Frontotemporal Dementia (Μετωποκροταφική Άνοια), HSP: Hereditary Spastic Paraplegia (Οικογενής Σπαστική Παραπληγία), PLS: Primary lateral sclerosis (Πρωτογενής Πλευρική Σκλήρυνση) Parkinsonism (Παρκινσονισμός), Cerebellar Ataxia (Παρεγκεφαλιδική Αταξία), AOA2: Oculomotor Apraxia type 2 (Οφθαλμοκινητική Απραξία τύπου 2), POAG: Primary Open Angle Glaucoma (Πρωτογενές Γλαύκωμα Ανοικτής Γωνίας) Motor Neuropathies (Κινητικές Νευροπάθειες), PMA: Progressive Muscular Atrophy (Προοδευτική Μυϊκή Ατροφία), SMA: Spinal Muscular Atrophy (Σπονδυλική Μυϊκή Ατροφία) Οι παραπάνω προσεγγίσεις είναι απαραίτητο να συνδυαστούν για την χαρτογράφηση των παραλλαγών, οι οποίες ευθύνονται για αυτήν την πολύπλοκη ασθένεια (Beleza-Meireles and Al-Chalabi 2009). Δομικές παραλλαγές Οι δομικές παραλλαγές, όπως προσθήκες, ελλείψεις και παραλλαγές αριθμού αντιγράφων των γονιδίων (CNV Copy Number Variants), φαίνεται να έχουν κάποιο ρόλο στην ασθένεια. Προσπάθεια επαλήθευσης της σημασία των CNV, κατέληξε στο συμπέρασμα ότι κοινά CNV, αλλά και η αλλαγή στο γενικότερο φορτίο των παραλλαγών αυτών δε σχετίζεται με την νόσο. Αντιθέτως, οι σπάνιες παραλλαγές του αριθμού αντιγράφων είναι πιθανό να σχετίζονται με την παθογένεια της ALS. Χαρακτηριστικό παράδειγμα αποτελεί το SMN1. Ένα ή τρία αντίγραφα του SMN1 σχετίζονται με την SALS, ενώ απουσία αυτού με τη SMA (Blauw et al. 2008, Leblond et al. 2014, Beleza-Meireles and Al-Chalabi 2009, Corcia, Khoris, et al. 2002, Corcia, Mayeux-Portas, et al. 2002). 37
38 Β H γενετική βάση της Οικογενούς Πλαγίας Αμυοτροφικής Σκλήρυνσης Το 5 % όλων των ασθενών ALS φέρει την οικογενή αυτοσωμική επικρατή μορφή (Byrne et al. 2011). Η ALS1 αποτελεί το 20 % όλων των FALS και οφείλεται σε μεταλλάξεις στο γονίδιο SOD1 (Beleza-Meireles and Al-Chalabi 2009). Συνολικά οι γνώσεις μας, μας επέτρεπαν να γνωρίζουμε τη γενετική αιτία στο 30 % περίπου των οικογενών περιπτώσεων, με πιο συχνές τις μεταλλάξεις στα γονίδια SOD1, TARDBP και FUS (Chen et al. 2013). Πρόσφατα, με την περιγραφή της εξανουκλεοτιδικής επέκτασης επαναλήψεων στη μη κωδική περιοχή του C90RF72, το τοπίο άλλαξε, καθώς η συγκεκριμένη παραλλαγή υπολογίζεται ότι ευθύνεται για το 37,6 % των οικογενών περιπτώσεων. Αξίζει να σημειωθεί ότι απαντάται και στο 6,3 % των σποραδικών περιπτώσεων, ενώ μέχρι ώρας την πρωτιά έφερε το SOD1, του οποίου οι μεταλλάξεις απαντώνται σε ποσοστό 1 % σε SALS ασθενείς (Leblond et al. 2014). Οι υπόλοιποι τύποι και τα αντίστοιχα γονίδια απεικονίζονται στον Πίνακα 2. Στην κατηγορία των RNA δεσμευτικών πρωτεϊνών, ξεχωρίζουν οι FUS και TDP-43. Τα γονίδια που τις κωδικοποιούν θεωρούνται υπεύθυνα για το 5 % της FALS και συγκαταλέγονται μεταξύ των τεσσάρων πιο συχνά σχετιζόμενων γονιδίων. Στις σπάνιες μορφές ALS έχουν βρεθεί μεταλλάξεις στα γονίδια UBQLN2 (Daoud et al. 2012, Williams et al. 2012), PFN1 (Wu et al. 2012), ERBB4 (Takahashi et al. 2013), HNRNPA1/B1 (Kim et al. 2013) και MATR3 (Johnson et al. 2014), τα οποία έχουν βρεθεί σε περιπτώσεις μεμονωμένων οικογενειών, είτε μέσα από μελέτες αλληλούχησης όλων των εξωνίων (WES - Whole Exome Sequencing), είτε μέσω αλληλούχησης ολόκληρου του γονιδιώματος (WGS - Whole Genome Sequencing). Πίνακας 2: Γονίδια που συνδέονται με την οικογενή ALS και τα βασικά φαινοτυπικά χαρακτηριστικά τους (Ferraiuolo et al., 2011; Leblond et al., 2014; Majoor-Krakauer, 2005; Wijesekera and Leigh, 2009) Τύπος Γονίδιο Χρωμοσωμική περιοχή Πρωτεΐνη Κληρονομικότητα/Ηλικία Έναρξης/Εξέλιξη ΤΥΠΙΚΗ ALS ALS1 SOD1 21q22 Cu/Zn δισμουτάση του ΑΕ/ΑΥ Ενήλικη AY: αργή υπεροξειδίου εξέλιξη ALS3 Άγνωστο 18q21 - ΑΕ Ενήλικη ALS6/ ALS- FTD FUS/TLS 16p11.2 Fused in sarcoma/translated in ΑΕ Ενήλικη liposarcoma ALS7 Άγνωστο 20ptel-p13 - ΑΕ Ενήλικη ALS9 ANG 14q11.2 Αγγειογεννίνη Angiogenin/ribonuclease ALS10 TARDBP 1p36.2 Tar-43 (tar-πρωτεΐνη που δεσμεύει DNA) ΑΤΥΠΗ ALS ΑΕ Ενήλικη ΑΕ Ενήλικη ALS2 ALS2 2q33 Alsin ΑΥ Παιδική ΑΚΝ ALS4 SETX 9q34 Senataxin ΑΕ Παιδική Αργή ALS5 15q15.1-q21.1 ΑΥ Παιδική ALS/HSP SPG11 15q21.1 Spatacsin (ορισμένες μεταλλάξεις) ΑΥ Παιδική 38
39 ALS8/SMA VAPB 20q13.32 VAMP πρωτεΐνη σχετιζόμενη με ΑΕ Ενήλικη τη μεμβρανική πρωτεΐνη B και C ALS11 FIG 4 6q21 Polyphosphoinositide ΑE Ενήλικη phosphatase (φωσφατάση πολυφωσφοϊνοσιτιδίων) ALS12 OPTN 10p13 Optineurin (Oπτινευρίνη) ΑΕ/ΑΥ Ενήλικη ALS13 ATXN2 12q24.12 Ataxin-2 (23-34 polyq επαναλήψεις) DAO 12q24.11 D-aminoacid oxidase(οξειδάση D αμινοξέων) ALS/LMND DCTN1 2p13.1 Dynactin (Δυνακτίνη, μονονουκλεοτιδική μετάλλαξη) Πρωτεΐνες νευρικών ινών (Neurofilaments) ALS-FTD ALS 14 με ή χωρίς FTD NEFH 22q12.2 Neurofilament NF-Lβ (πρωτεΐνες νευρικών ινών) PRPH 12q13.12 Peripherin Περιφερίνη/ type III intermediate filament protein ΑΕ Ενήλικη ΑΕ Ενήλικη ΑΕ Ενήλικη ΚΚΝ Ενήλικη VCP 9p13.3 Valosin-containing protein ΑΕ Ενήλικη ALS-FTD2 C90RF72 9q21.2 Μετάλλαξη επέκτασης επαναλαμβανόμενων αλληλουχιών ΑLS16 SIGMAR1 9p13.3 Non-opioid intracellular receptor 1/endoplasmic reticulum chaperone ALS-FTD ALS17/FTD3 CHMP2B 3p11.2 Multivesicular protein 2B (πρωτεΐνη πολυκυστιδίων 2Β) ή Chromatin-modifying protein 2B ALS-FTD Άγνωστο 9q21-q22 ΑΕ Ενήλικη ΑΥ Παιδική ΑΕ Ενήλικη AE Ενήλικη Μεμονωμένες περιπτώσεις όπου μεταλλάξεις σε HSP γονίδια προκαλούν ALS (Pyeritz, 2013) HSP SPG4 2p22.3 Spastin (c.304_309dupgcctcg στο εξώνιο 1) Silver syndrome HSP BSCL2/ SPG17 SPG39/PN PLA6 Νεαρή (Meyer et al. 2005) 11q13 Seipin ΑΕ Ενήλικη 19p13.2 Neuropathy target esterase/patatin-like phospholipase domaincontaining protein 6 (ορισμένες μεταλλάξεις) HSP SPG3Α 14q22.1 Atlastin (ορισμένες μεταλλάξεις) Taupathies ΑΥ Παιδική FTDP ΜΑΡΤ 17q21-22 Microtubule-associated tau ΑΕ Ενήλικη 39
40 ALS-PDC TRPM7 15q21.2 Πιθανώς ΑΕ με πλήρη διεισδυτικότητα στους άντρες και 50% στις γυναίκες. Δεν φαίνεται να ακολουθεί το Μενδελικό πρότυπο/ενήλικη και Παιδική ΣΠΑΝΙΕΣ ΜΟΡΦΕΣ ALS ALSX/ALS15 UBQLN2 Χp11.21 Ubiquilin 2 ΨΕ Ενήλικη και Παιδική ALS18 PFN1 17p13.3 Profilin1 ALS19 ERBB4 2q34 Receptor tyrosine-protein kinase erbb-4 ALS20 HNRNPA1 12q13 Heterogeneous nuclear ribonucleoprotein A1 ALS 21 MATR3 5q31 Matrin 3 AE AE: Αυτοσωμική Επικρατής Κληρονομικότητα, ΑΥ: Αυτοσωμική Υπολειπόμενη Κληρονομικότητα, ΨΕ: Ψευδοεπικρατής ή Χ-εξαρτώμενη κληρονομικότητα, ΑΚΝ: Συμβολή Ανώτερων Κινητικών Νευρώνων, ΚΚΝ: Συμβολή Κατώτερων Κινητικών Νευρώνων, ALS: Amyotrophic Lateral Sclerosis (Πλάγια Αμυοτροφική Σκλήρυνση) FTD: Frontotemporal Dementia (Μετωποκροταφική Άνοια), HSP: Hereditary Spastic Paraplegia (Οικογενής Σπαστική Παραπληγία), FTDP: Frontotemporal Dementia and Parkinsonism (Μετωποκροταφική Άνοια και Παρκινσονισμός), ALS-PDC: Amyotrophic Lateral Sclerosis-Parkinsonism / Dementia ή Complex of Guam (Σύνδρομο του Γκουάμ), Silver syndrome: Σπαστική παραπληγία με μυϊκή ατροφία των χεριών και ποδιών, Taupathies: Οι πάσχοντες εμφανίζουν Αμυοτροφία, Παρκινσονισμό, Μετωποκροταφική άνοια και ο μοριακός μηχανισμός τους οφείλεται στον σχηματισμό μικροσωληνίσκων. Β Από τη γενετική αιτία στην εκδήλωση του φαινοτύπου Όσον αφορά το φαινότυπο με τον οποίο σχετίζονται οι μεταλλάξεις σε κάθε γονίδιο, αυτός ποικίλει από μετάλλαξη σε μετάλλαξη (όπως περιγράφεται και στην παράγραφο «Β Ετερογένεια της νόσου») και ορισμένες φορές παρατηρούνται διαφορές, ακόμα και σε φορείς της ίδιας μετάλλαξης, όπως συμβαίνει με την εξανουκλεοτιδική επανάληψη του C9orf72. Μεταξύ των γονιδίων που έχουν καταχωρηθεί ως υπεύθυνα για την FALS μόνο οι μεταλλάξεις στα γονίδια SOD1, TARDBP, FUS, ANG και VCP έχουν συσχετισθεί με την τυπική ALS, ενώ τα υπόλοιπα γονίδια έχουν συσχετισθεί με ασυνήθεις φαινοτύπους ή έχουν εντοπιστεί σε μεμονωμένες περιπτώσεις (Hardiman, van den Berg, and Kiernan 2011). Σχετικά με τη διάρκεια της νόσου, επίσης, παρατηρούνται διακυμάνσεις. Η ALS12 (OPTN) και η ALS14 (VCP) εμφανίζουν τα πρώτα συμπτώματα στα άκρα, ωστόσο στην πρώτη η νόσος εξελίσσεται αργά και σχετίζεται με βλάβες στου ΑΚΝ, ενώ αντιθέτως η ALS14 εξελίσσεται ταχέως και σχετίζεται με βλάβες του ΚΚΝ. Η συμμετοχή των ΚΚΝ ή των ΑΚΝ δεν φαίνεται να σχετίζεται με την πορεία της νόσου, καθώς σε αντίθεση με την περίπτωση της ALS14, η ALS από μεταλλάξεις στο DCTN1 εκδηλώνεται με νευροπάθεια (συμμετοχή ΚΚΝ) και αργή πορεία. Η συνηθέστερη περιοχή έναρξης είναι τα άκρα, ενώ η προμηκική έναρξη είναι κυρίαρχη στην ALS11 (FIG4) (Chen et al. 2013). Η μέση ηλικία έναρξης κυμαίνεται από γονίδιο σε γονίδιο (Εικόνα 9). Επιπλέον, το εύρος των ηλικιών έναρξης διαφέρει σημαντικά, ακόμα και σε ασθενείς με μεταλλάξεις στο ίδιο γονίδιο. Η εμφάνιση της ασθένειας σε νεαρή ηλικία ως επί το πλείστον έχει συσχετισθεί με τη χρωμοσωμική περιοχή των ALS2 (Alsin) (Hadano et al. 2001) και SPG11 (Orlacchio et al. 2010). 40
41 Συγκεκριμένα, το γονίδιο Alsin σχετίζεται λειτουργικά με την ενδοκυττάρια μετακίνηση κυστιδίων, ενώ διαθέτει τρεις επικράτειες GTPάσης. Μεταλλάξεις στο Ν - τελικό άκρο καθιστούν μη λειτουργικά τα μικρά και τα μεγάλα μετάγραφα του γονιδίου και θεωρείται ότι η απώλεια της λειτουργίας της πρωτεΐνης οδηγεί στο φαινότυπο της υπολειπόμενης και με έναρξη στην παιδική ηλικία PLS ή παιδικής έναρξης ALS, με κυρίαρχη συμπτωματολογία από τους ΑΚΝ (Siddique and Siddique 2008). Η έναρξη της νόσου στην παιδική ηλικία χαρακτηρίζει και τις μεταλλάξεις του SEXT, αλλά είναι σπάνιες και σε ορισμένες περιπτώσεις, δεν μειώνουν το προσδόκιμο ζωής (Andersen and Al-Chalabi 2011). Άλλα παραδείγματα γονιδίων, που σχετίστηκαν πρόσφατα με τον αυξημένο κίνδυνο εμφάνισης της ALS, είναι το UNC13A (Unc-13 homologue A (Caenorhabditis elegans) στη χρωμοσωμική περιοχή 19p13.12, το TAF15 (TAF15 RNA polymerase II, TATA box binding protein (TBP)-associated factor, 68 kda) στη χρωμοσωμική περιοχή 17q11.1 q11.2 και το ELP3 (Elongator acetyltransferase complex subunit 3 ) στη χρωμοσωμική περιοχή 8p21.1. Εικόνα 9: Μέση ηλικία έναρξης των συμπτωμάτων ανά γονίδιο. ( et al. 2013)) Β Τα κυριότερα γονίδια SOD1 - Δισμουτάση του υπεροξειδίου 1 Η πρωτεΐνη SOD1 αποτελεί ένα ομοδιμερές 153 συντηρημένων αμινοξέων, το οποίο προσδένει ένα ιόν χαλκού και ένα ιόν ψευδαργύρου σε κάθε μονομερές και απαντάται, κυρίως, στο κυτταρόπλασμα. Σε 68 από τα αμινοξέα της, έχουν καταγραφεί πάνω από 150 μεταλλάξεις, κυρίως μη συνώνυμες. Έχουν βρεθεί, ωστόσο, και μεταλλάξεις που οδηγούν σε πρώιμο τερματισμό της μεταγραφής, προσθήκες και ελλείψεις. Η φυσιολογική λειτουργία του ισοενζύμου, η οποία έχει βρεθεί ότι διαταράσσεται με διάφορους πιθανούς μηχανισμούς, είναι η μείωση των καταστροφικών ελευθέρων ριζών, παραπροϊόντα της αναπνοής του κυττάρου και του κυτοχρώματος P450 (Siddique and Siddique 2008). Εντοπίστηκε, αρχικά, σε ασθενείς FALS, αλλά πλέον γνωρίζουμε ότι οι μεταλλάξεις του εν λόγω γονιδίου είναι και συχνή αιτία της SALS. Συνήθως, η έναρξη των συμπτωμάτων αφορά τα κάτω άκρα. Οι μεταλλάξεις σε αυτό το γονίδιο είναι χαρακτηριστικό παράδειγμα για την ετερογένεια μεταξύ ατόμων, ακόμα και με την ίδια μετάλλαξη και μας δίνει μια ισχυρή ένδειξη ότι κι άλλοι γενετικοί και περιβαλλοντικοί παράγοντες έχουν ρόλο στην εκδήλωση 41
42 του φαινοτύπου. Η μετάλλαξη D90A, παρόλο που παρουσιάζει κληρονομικότητα σε σκανδιναβικούς πληθυσμούς, παρουσιάζει επικρατή κληρονομικότητα σε άλλες ομάδες. Οι μεταλλάξεις D90A, Α89V και Ι113Τ εμφανίζουν ατελή διεισδυτικότητα, αντίθετα από την Α4V και κυμαινόμενη ηλικία έναρξης. Η Α89V εμφανίζει, επιπλέον, αισθητική νευροπάθεια. Στην περίπτωση της Ι113Τ μετάλλαξης, η κλινική εκδήλωση και η εξέλιξη από ασθενή σε ασθενή διαφέρουν σημαντικά (Chen et al. 2013). TARDBP - TAR DNA Δεσμευτική Πρωτεΐνη Η ανεύρεση κυτταροπλασματικών εγκλείστων TDP-43 σε ασθενείς με FTD έστρεψε την έρευνα προς το γονίδιο TARDBP. Μέχρι σήμερα, έχουν βρεθεί 43 παρανοηματικές μεταλλάξεις και μία μετάλλαξη που οδηγεί σε πρώιμο κωδικόνιο λήξης στο C-τελικό άκρο, σε ασθενείς FALS. Στις περισσότερες περιπτώσεις, ο φαινότυπος είναι τυπική ALS, αλλά έχει παρατηρηθεί και σε συνδυασμό με FTD, επηρεασμένη γνωστική λειτουργία και εξωπυραμιδικά συμπτώματα, πρόσφατα δε συσχετίσθηκε και με την τυπική νόσο του Parkinson. Οι μεταλλάξεις του γονιδίου αυτού που εντοπίστηκαν σε ALS ασθενείς είναι μη συνώνυμες και εντοπίζονται κυρίως στην πλούσια σε γλυκίνη καρβοξυτελική περιοχή, η οποία συμμετέχει στις αλληλεπιδράσεις με άλλες πρωτεΐνες (Εικόνα 10). Η ΤDP - 43 αλληλεπιδρά με πλήθος πρωτεϊνών, ακόμα και κάποιες οι Εικόνα 10: Μεταλλάξεις των FUS/TLS και TDP-43. (Liscic 2011) οποίες έχουν συσχετισθεί με την ALS, όπως οι VCP, FUS, PGRN και άλλες που σχετίζονται, επίσης, με τον μηχανισμό της νευροεκφύλισης ή με την επεξεργασία του RNA. Βασισμένοι σε δεδομένα από ζωικά μοντέλα υποθέτουμε ότι ο μηχανισμός της παθογένειας του TDP-43 οφείλεται, είτε σε αυξημένη λειτουργικότητα, είτε σε αυξημένη έκφραση, που - όπως έχει παρατηρηθεί στα μοντέλα - οδηγεί σε σπαστική παράλυση και εκφύλιση των ΚΚΝ. Εναλλακτικά, η απώλεια του TDP-43 οδηγεί σε μείωση της έκφρασης του Tbc1d1 και επακόλουθη αύξηση του μεταβολισμού (Chen et al. 2013, Andersen and Al-Chalabi 2011). FUS/TLS Fused in Sarcoma/Translated in Liposarcoma Η σύνδεση των RNA δεσμευτικών πρωτεϊνών με την ALS και της χρωμοσωμικής περιοχής 16q11.2 οδήγησε στη διερεύνηση του γονιδίου FUS, το οποίο αναγνωρίστηκε για πρώτη φορά το 2009, ως γονίδιο υπεύθυνο για την οικογενή μορφή ALS (Kwiatkowski et al. 2009). Έχουν παρατηρηθεί μεταλλάξεις στο συγκεκριμένο γονίδιο και σε ορισμένες περιπτώσεις SALS. Το FUS/TLS είναι ένα γονίδιο 11,68 χιλιάδων ζευγών βάσεων και αντιστοιχεί σε μια πρωτεΐνη 526 αμινοξέων, εκφράζεται στους περισσότερους ιστούς του σώματος και αφού 42
43 εκφραστεί μετατοπίζεται και στον πυρήνα και στο κυτταρόπλασμα. H FUS πρωτεΐνη εμπλέκεται στη ρύθμιση μεταγραφικών παραγόντων, στο μάτισμα και στη συντήρηση του γονιδιώματος (van Blitterswijk et al. 2013). Επιπρόσθετα, μέσω του Ν - τελικού άκρου της, η πρωτεΐνη, εικάζεται ότι εμπλέκεται στην ενεργοποίηση της μεταγραφής, όταν είναι παρούσα σε όγκους. Ολόκληρη η πρωτεΐνη ρυθμίζει τη δραστηριότητα δύο μεταγραφικών παραγόντων, των NFkB και Spi-1, ενώ το C -τελικό άκρο της περιέχει ένα μοτίβο αναγνώρισης RNA. Όσον αφορά τα παθολογικά ευρήματα σε ασθενείς με μετάλλαξη στο FUS/TLS παρατηρείται (i) μια κυρίαρχη πυρηνική επισήμανση στα νεύρα και στη γλοία, (ii) στα κατώτερα κινητικά νεύρα, παρατηρείται αυξημένη παρουσία FUS/TLS στο κυτταρόπλασμα με δομές «σαν κουβάρι» και (iii) κυτταροπλασματικά έγκλειστα στα κύτταρα γλοίας. Ασθενείς με FUS μεταλλάξεις παρουσιάζουν πρώιμη έναρξη των συμπτωμάτων, αλλά με μικρότερη διάρκεια. Υπάρχει, επίσης, μια μικρή συσχέτισή τους, με την ταυτόχρονη παρουσία μετωποκροταφικής άνοιας και άνοιας / Parkinson. Ως αιτία της ALS, έχουν εντοπιστεί μεταλλάξεις στα εξώνια 3, 5, 6, 14 και 15. Οι περισσότερες μη συνώνυμες μεταλλάξεις βρίσκονται στο C - τελικό άκρο, δηλαδή τα εξώνια 14 και 15 (Πίνακας 3) (Andersen and Al-Chalabi 2011). Έχουν παρατηρηθεί, ωστόσο, και μεταλλάξεις που οδηγούν σε αλλαγή του πλαισίου ανάγνωσης (Yan et al. 2010). Πρόσφατα, έχουν βρεθεί αλληλόμορφα και στην 3 αμετάφραστη περιοχή του γονιδίου, τα οποία έχουν συσχετιστεί με τη νόσο (Sabatelli et al. 2013). Πίνακας 3: Πίνακας με τις πιο συχνές FUS/TLS μεταλλάξεις που έχουν εντοπιστεί στο γονίδιο Θέση /Κωδικόνιο Είδος Μετάλλαξη 521 Αντικατάσταση Arg521His/Cys/Ser/Gly/Leu C τελικό άκρο Μετατόπιση πλαισίου ανάγνωσης Απώλεια 4 ή 7 αμινοξέων στο C άκρο C τελικό άκρο Μετατόπιση πλαισίου ανάγνωσης Προσθήκη 4 αμινοξέων στο C άκρο 514 Αντικατάσταση Arg514Gly/Ser C9orf72 - Ανοιχτό πλαίσιο ανάγνωσης 72 του χρωμοσώματος 9 Η συσχέτιση της περιοχής 9p21.3-p13.3. στο χρωμόσωμα 9p με την ALS και την FTD έχει πραγματοποιηθεί από το 2006 (Morita et al. 2006). Ωστόσο, μόνο πρόσφατα η εξανουκλεοτιδική επανάληψη στο πρώτο εσώνιο του C9orf72 συσχετίσθηκε με την ALS. Σύμφωνα με τους Renton et al (2011), η εξανουκλεοτιδική επέκταση (GGGGCC) βρίσκεται 63 ζεύγη βάσεων από το πρώτο εξώνιο, προς το κέντρο του γονιδίου. Η αλληλουχία αγρίου τύπου περιλαμβάνει μέχρι 20 επαναλήψεις, ενώ όταν εντοπιστούν πάνω από 30 επαναλήψεις, το αλληλόμορφο θεωρείται παθογόνο. Ο αριθμός των επαναλήψεων έχει συσχετισθεί με την παθογένεια της σποραδικής και της οικογενούς μορφής των ALS και FTD. Ο εντοπισμός της αλληλουχίας με τη μέθοδο FISH (Εικόνα 11) υποδεικνύει πως το μέγεθός της μπορεί να ξεπερνά τα 1,5kb (που είναι το όριο ανίχνευσης της μεθόδου), που αντιστοιχεί σε τουλάχιστον 250 επαναλήψεις της αλληλουχίας. Ο φθορισμός εντοπίζεται αποκλειστικά στο χρωμόσωμα 9p21 (Renton et al. 2011). Ο αριθμός των επαναλήψεων της αλληλουχίας GGGGCC κυμαίνεται. Η παρουσία μεγάλου αριθμού επαναλήψεων (>30) έχει συσχετισθεί με την ALS και στον ελληνικό πληθυσμό. Συγκεκριμένα, καταγράφηκε ένα μικρό ποσοστό, της 43
44 τάξεως του 2 % υγιών ατόμων με επαναλήψεις της αλληλουχίας (Mok et al. 2012). Ως πιθανοί μηχανισμοί της «δηλητηριώδους» παραλλαγής έχουν προταθεί (i) η μη φυσιολογική έκφραση της πρωτεΐνης, που κωδικοποιεί το C9orf72 και κατά συνέπεια, τοξικότητα λόγω μειωμένης λειτουργίας και (ii) η συσσώρευση RNA στον μετωπιαίο φλοιό και τη σπονδυλική στήλη και επακόλουθη τοξικότητα από τη συσσώρευση μη κωδικού RNA στους πυρήνες των κυττάρων (RNA foci), όπως συμβαίνει και με άλλες ασθένειες που οφείλονται σε τέτοιου είδους επεκτάσεις επαναλήψεων (DeJesus-Hernandez et al. 2011). Ο μηχανισμός που συνδέει την εξανουκλεοτιδική επέκταση του C9orf72, καθώς και την ακέραια πρωτεΐνη με την παθογένεια της νόσου παραμένει άγνωστος. Σε μια προσπάθεια εξακρίβωσης του μηχανισμού αυτού, η ερευνητική ομάδα του Kiskinis (2014), παρήγαγε επαγόμενα πολυδύναμα βλαστικά κύτταρα που έφεραν μεταλλάγματα του C9orf72 και στη συνέχεια, τα συνέκρινε με τις αντίστοιχες κυτταρικές σειρές που έφεραν μεταλλάγματα του SOD1. Βρέθηκε, ότι μετάγραφα της κινησίνης, KIF14, που υπερεκφράζονται σε μεγάλο βαθμό στα μεταλλάγματα του Εικόνα 11: Εικόνα SOD1, υπερεκφράζονται και στα μεταλλάγματα του C9orf72. φθορισμού με τη μέθοδο FISH, όπου Επιπλέον, οι διαφορές στα επίπεδα έκφρασης των δύο ειδών χρησιμοποιήθηκε μεταλλαγμένων κινητικών νευρώνων βρέθηκαν να συμπίπτουν σεσημασμένη η εξανουκλεοτιδική και για άλλα γονίδια, διαύλων ιόντων ή υπεύθυνων για την αλληλουχία GGGGCC. κινητικότητα και την αναδίπλωση των πρωτεϊνών (DNAJC12, (Renton et al. 2011). EIF2B3, SCN1A, και KCNN3). Τα επίπεδα των μεταγράφων, που σχετίζονται με τη διακίνηση των ηλεκτρονίων στα μιτοχόνδρια, παρέμειναν ανεπηρέαστα στα μεταλλάγματα του C9orf72. Όμως τα γονίδια του μιτοχονδριακού μεταφορέα, ΜΤΧ3 και της καταλάσης παρουσίασαν υπερέκφραση στα μεταλλάγματα σε σύγκριση με τους φυσιολογικούς νευρώνες, στοιχείο ενδεικτικό της οξειδωτικής καταπόνησης. Τα παραπάνω στοιχεία έκφρασης μας προσφέρουν κάποιες ενδείξεις σχετικά με το μηχανισμό της παραλλαγής στο C9orf72 και αποκαλύπτουν την ομοιότητά του με τον μηχανισμό του SOD1 (Kiskinis et al. 2014). Η εξανουκλεοτιδική επανάληψη του C9orf72 έχει συσχετιστεί και με την παρουσία Μετωποκροταφικής άνοιας (FTD) και Πλαγίας Αμυοτροφικής Σκλήρυνσης, τόσο της οικογενούς, όσο και της σποραδικής μορφής. Τα κλινικοπαθολογικά χαρακτηριστικά στην ALS εμφανίζουν μεγάλες διακυμάνσεις, με μέση ηλικία εμφάνισης τα 57 έτη και μέση διάρκεια 2-3 έτη, ενώ πολύ συχνά, η ALS συνυπάρχει με την FTD. Συνολικά, η παραπάνω παραλλαγή εξηγεί το 34 % της οικογενούς ALS και το 26 % της οικογενούς FTD, ενώ θεωρείται υπεύθυνη για το 6 % και 5 % των σποραδικών μορφών των προαναφερθέντων ασθενειών, αντίστοιχα (van Blitterswijk, DeJesus-Hernandez, and Rademakers 2012). Renton et al.,
45 Β Γενετική της Σποραδικής Πλάγιας Αμυοτροφικής Σκλήρυνσης Στην περίπτωση της σποραδικής ALS ο εντοπισμός των γενετικών αιτίων δεν είναι δυνατός και επομένως, εστιάζουμε στη γενετική προδιάθεση της νόσου. Η συνηθέστερη προσέγγιση είναι η πραγματοποίηση μελετών συσχέτισης σε επιλεγμένα υποψήφια γονίδια. Η επιλογή των υποψηφίων γονιδίων στηρίζεται σε κατάλληλα κριτήρια (Β.1.9.3) ή στη συσχέτισή τους με την οικογενή ALS. Το σύνολο των γονιδίων που έχει συσχετιστεί με τη νόσο καταγράφεται στον πίνακα 4. Μεταξύ των επιλεγμένων υποψήφιων γονιδίων βρίσκεται η απουρινική ενδονουκλεάση (APEX1 - apurinic endonuclease 1), λόγω της λειτουργίας της. Η APEX1 επιδιορθώνει το DNA και με αυτόν τον τρόπο, προστατεύει τα κύτταρα από το οξειδωτικό στρες. Στην ίδια χρωμοσωμική περιοχή, 229 χιλιάδες βάσεις πιο μακριά, βρίσκεται το γονίδιο της Αγγειογενίνης (ANG Angiogenin), το οποίο είναι ένας αγγειογενετικός αυξητικός παράγοντας σαν τον VEGF, ο οποίος έχει συσχετισθεί και παλαιότερα με την ALS (Lambrechts et al. 2003) και το ίδιο το γονίδιό του είχε επιλεγεί ως υποψήφιο, ύστερα από μελέτες σε μύες. Η προγκρανουλίνη (PGRN Progranulin) είναι επίσης ένας αυξητικός παράγοντας και θεωρήθηκε ως η αιτία του φαινοτύπου ALS σε μία μεμονωμένη οικογένεια κατά τη διάρκεια μιας μελέτης συσχέτισης (Mackenzie et al. 2006). Επιπροσθέτως, μελέτες σύνδεσης που πραγματοποιήθηκαν σε οικογένειες με ασθενείς ALS έφεραν στην επιφάνεια και άλλα υποψήφια γονίδια, όπως τα CHMP2B και DCTN1. Η λειτουργία τους που σχετίζεται με την ενδοσωμική μεταφορά και την αξονική μεταφορά μέσω των μικροσωληνίσκων, ενισχύουν την υποψηφιότητά τους, καθώς ένα πλήθος πρωτεϊνών με παρόμοιες λειτουργίες έχει συσχετισθεί με την ALS. Η συσχέτιση των τελευταίων, όμως, με την SALS και σύμφωνα με μελέτες ασθενών έναντι υγειών δεν επιβεβαιώθηκε και απομένει να αποδειχτεί. Στην κατηγορία των πρωτεϊνών που είναι υπεύθυνα για τη σωστή λειτουργία των αξόνων ανήκουν και τα ενδιάμεσα νευροϊνίδια, NEFH, NEFL, NEFM και PRPH. Η σχέση των παραπάνω με την SALS είναι ισχυρή. Έγκλειστα νευροϊνιδίων εντοπίζονται στους νευράξονες και το σώμα του νευρικού κυττάρου των ασθενών, ενώ στα συσσωματώματα πρωτεϊνών στη σπονδυλική στήλη εντοπίζεται και περιφερίνη. Ορισμένα γονίδια που έχουν συσχετισθεί με συγγενείς νόσους ερευνώνται και για τη σχέση των μεταλλάξεων σε αυτά με την ALS. Ενδεικτικό παράδειγμα αποτελεί το γονίδιο της αιμοχρωμάτωσης (HFE Haemochromatosis) το οποίο εμπλέκεται στον μεταβολισμό του σιδήρου και στη νόσο του Alzheimer ή τα SMN1 και SMN2 που ευθύνονται για την SMA, με έναρξη στην παιδική ηλικία. Αξίζει να σημειωθεί ότι στην τελευταία περίπτωση μόνο η παραλλαγή του αριθμού του SMN1 αντιγράφων έχει δώσει ως φαινότυπο τη SALS. Πίνακας 4: Τα 114 γονίδια που αναφέρονται στη βάση δεδομένων Alsod (6.0) (Abel et al. 2013) Σύμβολο Όνομα Γονιδίου Γονιδίου AGT angiotensinogen (serpin peptidase inhibitor, clade A, member 8) ALAD d-aminolevulinic Acid Dehydratase 45
46 ALS-FTD1 Unknown ALS2 amyotrophic lateral sclerosis 2 (juvenile) homolog (human). Alsin ALS3 Unknown ALS7 Unknown ANG Angiogenin APEX1 Apurinic endonuclease APOE Apolipoprotein E AR Androgen receptor ARHGEF28 Rho guanine nucleotide exchange factor (GEF) 28 ATXN2 ataxin 2 B4GALT6 UDP-Gal:betaGlcNAc beta 1,4- galactosyltransferase, polypeptide BCL11B B-cell CLL/lymphoma 11B (zinc finger protein) BCL6 B-cell CLL/lymphoma 6 C1orf27 chromosome 1 open reading frame 27 C9orf72 chromosome 9 open reading frame 72 CCS Copper chaperone for superoxide dismutase CDH13 cadherin 13, H-cadherin (heart) CDH22 cadherin 22, type 2 CHMP2B chromatin modifying protein 2B CNTF Ciliary neurotrophic factor CNTN4 contactin 4 CNTN6 DOC2B double C2-like domains, beta CRIM1 cysteine rich transmembrane BMP regulator 1 (chordin-like) CRYM crystallin, mu CSNK1G3 casein kinase 1, gamma 3 CST3 cystatin C CYP2D6 Cytochrome p450, subfamily IID, polypeptide 6 DAO D-amino-acid oxidase DCTN1 Dynactin DIAPH3 diaphanous homolog 3 (Drosophila) DISC1 disrupted in schizophrenia 1 DOC2B double C2-like domains, beta DPP6 dipeptidyl-peptidase 6 DYNC1H1 Dynein heavy chain EFEMP1 EGF-containing fibulin-like extracellular matrix protein 1 ELP3 elongation protein 3 homolog (S. cerevisiae) EPHA4 EPH receptor A4 ERBB4 v-erb-b2 avian erythroblastic leukemia viral oncogene homolog 4 EWSR1 Ewing sarcoma breakpoint region 1 FEZF2 FEZ family zinc finger 2 FGGY FGGY carbohydrate kinase domain containing FIG4 FIG4 homolog, SAC1 lipid phosphatase domain containing (S. cerevisiae) FUS fusion (involved in t(12;16) in malignant liposarcoma) GARS Glycyl trna synthetase GRB14 growth factor receptor-bound protein 14 GRN Granulin HEXA Hexosaminidase A HFE Haemochromatosis 46
47 HNRNPA1 HNRNPA2B1 heterogeneous nuclear ribonucleoprotein A1 heterogeneous nuclear ribonucleoprotein A2/B1 ITPR2 inositol 1,4,5-triphosphate receptor, type 2 KDR kinase insert domain receptor (a type III receptor tyrosine kinase) KIFAP3 kinesin-associated protein 3 LIF LIPC LMNB1 LOX LUM MAOB MAPT Leukaemia inhibitory factor lipase, hepatic lamin B1 Lysyl oxidase Lumican MATR3 matrin 3 Monoamine oxidase B Microtubule-associated protein tau MT-ND2 Subunit 2 of mitochondrial NADH dehydrogenase (Complex I) NAIP NEFH Neuronal apoptosis inhibitory protein neurofilament, heavy polypeptide 200kDa, heavy chain NETO1 neuropilin (NRP) and tolloid (TLL)-like 1 NT5C1A OGG1 OMA1 OPTN 5'-nucleotidase, cytosolic IA 8-oxoguanine DNA glycosylase OMA1 homolog, zinc metallopeptidase (S. cerevisiae) Optineurin PCP4 Purkinje cell protein 4 PFN1 profilin 1 PON1 paraoxonase 1 PON2 paraoxonase 2 PON3 paraoxonase 3 PRPH PSEN1 PVR Peripherin presenilin-1 Poliovirus receptor RAMP3 receptor (G protein-coupled) activity modifying protein 3 RBMS1 RNA binding motif, single stranded interacting protein 1 RNASE2 RNF19A SCN7A SELL SEMA6A SETX ribonuclease, RNase A family, 2 (liver, eosinophil-derived neurotoxin) ring finger protein 19A sodium channel, voltage-gated, type VII, alpha selectin L sema domain, transmembrane domain (TM), and cytoplasmic domain, (semaphorin) 6A Senataxin SIGMAR1 sigma non-opioid intracellular receptor 1 SLC1A2 Excitatory amino acid transporter 2 SLC39A11 solute carrier family 39 (metal ion transporter), member 11 SMN1 SMN2 SNCG SOD1 SOD2 Survival of motor neuron ½ survival of motor neuron 2, centromeric Persyn Cu/Zn superoxide dismutase 1, soluble (amyotrophic lateral sclerosis 1 (adult)) Manganese superoxide dismutase SOX5 SRY (sex determining region Y)-box 5 SPAST Spastin 47
48 SPG11 SPG7 SQSTM1 sequestosome 1 spastic paraplegia 11 (autosomal recessive) spastic paraplegia 7 (pure and complicated autosomal recessive) SUSD1 sushi domain containing 1 SYT9 TAF15 TARDBP synaptotagmin IX UBQLN2 ubiquilin 2 UNC13A VAPB VCP VDR VEGFA VPS54 ZFP64 ZNF512B TAF15 RNA polymerase II, TATA box binding protein (TBP)-associated factor, 68kDa TAR DNA binding protein unc-13 homolog A (C. elegans) Vesicle-associated membrane protein-associated protein B valosin-containing protein Vitamin D receptor Vascular endothelial growth factor vacuolar protein sorting 54 homolog (S. cerevisiae) zinc finger protein 64 homolog zinc finger protein 512B ZNF746 zinc finger protein 746 Α Τροποποιητικά της νόσου γονίδια Εκτός από τα κύρια γονίδια της οικογενούς μορφής και τα γονίδια που προσδίδουν προδιάθεση για την εμφάνιση της νόσου και έχουν συσχετισθεί με τη σποραδική μορφή, υπάρχουν και γονίδια που οι παραλλαγές σε αυτά θεωρούνται τροποποιητικές για τη νόσο. Ο γονότυπος ApoE ε4 του γονιδίου της απολιποπρωτεΐνης - Ε επηρεάζει την εξέλιξη της νόσου, μειώνοντας τον χρόνο επιβίωσης. Παρόμοιο είναι το εύρημα και αναφορικά με τις μηδενικές μεταλλάξεις του ακτινωτού νευροτροφικού παράγοντα (CNTF Ciliary Neurotrophic Factor). Τέλος, παρουσία κάποιων SNPs στο γονίδιο του αγγειακού ενδοθηλιακού αυξητικού παράγοντα (VEGF), αυξάνεται ο κίνδυνος εμφάνισης της ALS και παράλληλα, επισπεύδεται η εμφάνιση της νόσου, όπως διαπιστώθηκε σε πειράματα σε μύες. Επιπρόσθετες παραλλαγές, που έχουν συσχετιστεί με τον αυξημένο κίνδυνο εμφάνισης της νόσου ενώ συγχρόνως φέρονται να την επιδεινώνουν, είναι οι παραλλαγές στον αριθμό των αντιγράφων των SMN1 και 2, καθώς και παραλλαγές του RNA της GluR2 υπομονάδας, που έχει υποστεί διαφορετική επεξεργασία, αλλά και η μειωμένη έκφραση του EAAT2 ως αποτέλεσμα παραλλαγών στο γονίδιο (Kunst 2004). Στην κατηγορία των τροποποιητών της νόσου ανήκουν και τα γονίδια SOD1, PON1-3 και ANG (Al-Chalabi et al. 2013). 48
49 Γ. ΣΚΟΠΟΣ ΤΗΣ ΕΡΓΑΣΙΑΣ 49
50 Η παρούσα μεταπτυχιακή εργασία, αφορά την Πλάγια Αμυοτροφική Σκλήρυνση και τα γενετικά αίτια αυτής, στον ελληνικό πληθυσμό. Η Πλάγια Αμυοτροφική Σκλήρυνση είναι μια νόσος που παραμένει ανίατη και της οποίας η σύνθετη αιτιολογία δεν έχει πλήρως διαλευκανθεί. Στα πλαίσια της εν λόγω εργασίας, χρησιμοποιήθηκε μια νέα, εξελισσόμενη μέθοδος ανάλυσης ολόκληρου του γονιδιώματος, μέσω της οποίας ευελπιστούμε να εξακριβώσουμε νέους ή ήδη γνωστούς γενετικούς δείκτες, στους οποίους οφείλεται η εμφάνιση της ασθένειας στον ελληνικό πληθυσμό. Σήμερα, οι προσεγγίσεις που διερευνώνται στην πλειοψηφία τους αφορούν γνωστά γονίδια που έχουν συσχετιστεί με τη νόσο. Τι γίνεται, όμως, για όσους φέρουν ακέραια αυτά τα γονίδια και τις αντίστοιχες πρωτεΐνες και η εκδήλωση της νόσου τους οφείλεται σε διαφορετικά αίτια; Αναμένουμε αυτά τα αίτια να είναι γενετικά και η προσέγγισή μας να αποδώσει μια νέα κατεύθυνση προς όφελος του ελληνικού πληθυσμού. 50
51 Δ. ΥΛΙΚΑ ΚΑΙ ΜΕΘΟΔΟΙ 51
52 Δ.1 Επεξεργασία δεδομένων Αλληλούχησης Ολόκληρου του Γονιδιώματος Η πλατφόρμα που χρησιμοποιήθηκε για την αλληλούχηση ολόκληρου του γονιδιώματος ήταν η Complete Genomics (όπως περιγράφεται στο παράρτημα), με κάλυψη 116Χ. Τα δεδομένα που αναλύθηκαν, προήλθαν από την επεξεργασία των δεδομένων της αλληλούχησης με τη χρήση μεθόδων βιοπληροφορικής. Η επεξεργασία αυτή, πραγματοποιήθηκε εξ ολοκλήρου από τον Clint Mizzi, ο οποίος εργάζεται στο Πανεπιστήμιο της Μάλτας. Δ.1.1 Επιλογή πολυμορφισμών στόχων, 1 η προσέγγιση Τα γονίδια και οι πολυμορφισμοί επιλέχθηκαν μεταξύ 174 πολυμορφισμών που προέκυψαν από την αλληλούχηση ολόκληρου του γονιδιώματος 10 Ελλήνων ασθενών ALS και την επακόλουθη σύγκριση όλων των πολυμορφισμών που εντοπίστηκαν και στα 10 γονιδιώματα τους, με τους πολυμορφισμούς που βρέθηκαν στα γονιδιώματα 5 υγιών Ελλήνων. Από την προσέγγιση αυτή προέκυψαν μόνο οι 174 πολυμορφισμοί οι οποίοι απαντήθηκαν σε όλους τους ασθενείς και σε κανένα γονιδίωμα του δείγματος αναφοράς (Πίνακας 5): Πίνακας 5: Συνοπτικά αποτελέσματα 1 ης προσέγγισης Γονίδια 58 Πολυμορφισμοί 174 Πολυμορφισμοί Διαγονιδιακοί 144 Πολυμορφισμοί Σε εσώνια 23 Πολυμορφισμοί Ανοδικά του γονιδίου (upstream) 2 Πολυμορφισμοί 3 αμετάφραστη περιοχή (3 UTR) 2 Πολυμορφισμοί Καθοδικά του γονιδίου (downstream) 1 Πολυμορφισμοί σε Μη κωδικό RNA 2 Οι 174 πολυμορφισμοί ήταν όλοι κοινοί, με ελάχιστη συχνότητα στο γενικό πληθυσμό και στους ευρωπαίους (15% και 14%, αντίστοιχα), ενώ η πλειοψηφία αυτών έχει συχνότητες μεγαλύτερες του 20%. Σε 19 από αυτούς δεν βρέθηκαν καταχωρημένα δεδομένα συχνοτήτων. Αξίζει να σημειωθεί ότι αυτοί οι 174 πολυμορφισμοί σχετίζονται μόνο με 58 γονίδια. Στον πίνακα 6 φαίνονται όλα τα γονίδια, ο αριθμός των πολυμορφισμών που βρέθηκαν να σχετίζονται με αυτά και η σχετική τους θέση. Πίνακας 6: Κατηγοριοποίηση των 174 πολυμορφισμών με βάση τα σχετιζόμενα γονίδια. Χρωμόσωμα Γονίδιο/α Νο Θέση σε σχέση με το/α πολυμορφισμών γονίδιο/α chr1 PRDM2,KAZN 19 intergenic chr1 KAZN 1 intronic chr1 ESPNP 2 ncrna chr1 WNT4,ZBTB40 4 intergenic chr1 ZBTB4 6 intergenic 52
53 chr1 PLA2G4A,NONE 23 intergenic chr1 LOC440704,RGS18 2 intergenic chr2 KCNH7,FIGN 2 intergenic chr2 ERBB4,MIR intergenic chr2 C2orf62 1 upstream chr3 PPP4R2,PDZRN3 7 intergenic chr4 TBC1D1 1 intronic chr4 HSP90AB3P,SPP1 5 intergenic chr4 PDLIM3,SORBS2 1 intergenic chr4 LOC401164,HSP90AA4P 1 intergenic chr5 ISL1,PELO 4 intergenic chr5 OTP,TBCA 11 intergenic chr6 FAM46A,IBTK 4 intergenic chr7 UBE3C 2 intronic chr8 KBTBD11,MYOM2 1 intergenic chr8 MSRA 2 intronic chr9 TMEM215,APTX 7 intergenic chr10 LOC399708,PFKP 2 intergenic chr10 NONE,SFTA1P 4 intergenic chr10 PRKG1 5 intronic chr11 MIR4300,FAM181B 14 intergenic chr11 FAM181B 3 downstream, UTR3, upstream chr11 FAM181B,PRCP 16 intergenic chr12 SLC38A2,SLC38A4 1 intergenic chr13 PCCA 1 intronic chr13 A2LD1 intronic, UTR3 chr14 FSCB,C14orf28 7 intergenic chr15 SPATA8,LOC intergenic chr16 PRSS36,FUS 1 intergenic chr16 FTO 3 intronic chr17 GPR142,GPRC5C 1 intergenic chr18 YES1,ADCYAP1 1 intergenic chr19 CEACAM4,CEACAM7 2 intergenic chr19 CEACAM7 1 intronic chrx PTCHD1,PRDX4 1 intergenic Καθώς δεν ήταν δυνατή η επαλήθευση της σημαντικότητας όλων αυτών των πολυμορφισμών σε μεγαλύτερο δείγμα, η επιλογή, των προς μελέτη πολυμορφισμών, στηρίχθηκε στη θέση τους σε σχέση με τα γονίδια (Πίνακας 7) και στη συσχέτιση των ίδιων των γονιδίων, είτε με νευροεκφυλιστικές ασθένειες, είτε με το νευρικό σύστημα και τον εγκέφαλο, γενικότερα. Κάθε γονίδιο ξεχωριστά ελέγχθηκε για τη συσχέτιση με το νευρικό σύστημα με τη χρήση του προγράμματος Ingenuity pathway analysis (IPA) (IPA, QIAGEN Redwood City, Επίσης, έγινε πρόβλεψη των μεταγραφικών παραγόντων με τη χρήση του SNPinfo (Xu and Taylor 2009). 53
54 Πίνακας 7: Παραλλαγές που απέχουν έως 250bp από το πλησιέστερο γονίδιο. Γονίδιο intronic upstream (έως και 250bp) KAZN 1 ZBTB40 6 TBC1D1 1 UBE3C 2 MSRA 2 PRKG1 5 FAM181B 1 1 PCCA 1 A2LD1 1 1 FTO 3 CEACAM7 1 3 UTR (έως 50bp από το κωδικόνιο λήξης) Intronic: στα εσώνια, upstream: πριν από την 5 αμετάφραστη περιοχή, 3 UTR: 3 αμετάφραστη περιοχή Οι απορρέοντες πολυμορφισμοί κατηγοριοποιήθηκαν, επίσης και ως προς το χρωμόσωμα στο οποίο βρίσκονται (Πίνακας 8), με τα χρωμοσώματα 1 και 11 να περιέχουν την πλειοψηφία αυτών: Πίνακας 8: Πολυμορφισμοί ανά Χρωμόσωμα. chr1 57 chr2 5 chr3 7 chr4 8 chr5 15 chr6 4 chr7 2 chr8 3 chr9 7 chr10 11 chr11 33 chr12 1 chr13 3 chr14 7 chr15 1 chr16 4 chr17 1 chr18 1 chr19 3 chrx 1 chr: χρωμόσωμα Με έντονη γραφή φαίνονται τα χρωμοσώματα στα οποία αντιστοιχούν πάνω από 10 πολυμορφισμοί. 54
55 Ως προς τα γονίδια τα οποία υπερισχύουν, τα σχετικά στοιχεία δίδονται ακολούθως (Πίνακας 9): Πίνακας 9: Γονίδια με περισσότερους από 10 πολυμορφισμούς να σχετίζονται με αυτά - ποιοι πολυμορφισμοί βρίσκονται πλησιέστερα σε αυτά. Γονίδια Συνολικός αριθμός πολυμορφισμών 3 UTR (έως 50bp από το κωδικόνιο τερματισμού) Αριθμός πολυμορφισμών Εσωνικοί Έως 250bp πριν το γονίδιο KAZN rs ZBTB rs rs rs rs rs rs PLA2G4A TBCA 11 FAM181B rs3780 rs rs ID: Ταυτότητα rs, 3 UTR: 3 αμετάφραστη περιοχή του γονιδίου, bp: ζεύγη βάσεων. Με το κόκκινο συμβολίζονται όσα γονίδια έχουν πολυμορφισμούς που αντιστοιχούν στις στήλες 3, 4, 5. Το γονίδιο το οποίο σχετιζόταν με τους περισσότερους πολυμορφισμούς ήταν το FAM181B. Η σχετική θέση αυτών με το γονίδιο παρουσιάζεται στην Εικόνα 12. rs ID Εικόνα 12: Με συμπαγές κόκκινο φαίνεται η περιοχή του γονιδίου FAM181B και με βέλη οι πολυμορφισμοί που προέκυψαν από τη σύγκριση WGS ασθενών και υγιών, καθώς και η σχετική τους θέση ως προς το γονίδιο. Κάποια από τα γονίδια που παρουσιάζονται στον Πίνακα 6, έχουν συσχετιστεί με την ALS, όπως το FUS και το ERBB4 ή με άλλες νευροεκφυλιστικές ασθένειες, όπως το KBTD11 με τη νοητική υστέρηση και το APTX με την αταξία με οφθαλμοκινητική απραξία. Αξίζει να σημειωθεί πως κάποιοι πολυμορφισμοί οι οποίοι έχουν συσχετιστεί με την εμφάνιση της νόσου σε GWAS μελετες, εντοπίζονται σε διαγονιδιακές περιοχές, όπως την περιοχή ανάμεσα στο TBCA και το AP3B1 ή την περιοχή ανάμεσα στα LOC και HSP90AA4. 55
56 Η βιβλιογραφική αναζήτηση για κάθε ένα από τα παραπάνω γονίδια υπέδειξε τις παρακάτω συσχετίσεις, είτε με το νευρικό σύστημα, γενικότερα, είτε με κάποιους μηχανισμούς που έχουν κυρίαρχο ρόλο στην ALS. Όσον φορά τους μηχανισμούς της ALS, είναι γνωστή η συσχέτιση του κυτταροσκελετού και των γονιδίων που συσχετίζονται με αυτόν, όπως το MAPT, ομοίως και το γονίδιο KAZN, σχετίζεται με τη συναρμολόγηση των δεσμοσωμάτων, την κυτταρική προσκόλληση, την κυτταροσκελετική οργάνωση και την κυτταρική διαφοροποίηση. Με τον κυτταροσκελετό σχετίζεται και άλλο ένα γονίδιο της λίστας, το FIGN (fidgetin), το οποίο κωδικοποιεί μια πρωτεΐνη, η οποία αποκόπτει τους μικροσωληνίσκους και επάγει τον απο - πολυμερισμό τους, ιδιαίτερα από το ( ) άκρο, αποτρέποντας την προσκόλλησή τους στο κεντροσωμάτιο. Επιπλέον, η αποσιώπηση του τελευταίου έχει συσχετιστεί με την ανάπλαση του νευρικού ιστού. Το TBCA γονίδιο αντιστοιχεί σε μια συνοδό πρωτεΐνη, η οποία είναι υπεύθυνη για την αναδίπλωση της β-τουμπουλίνης. Με την ουβικουιτίνη και συγκεκριμένα, τη συναρμολόγηση των νέων αλυσίδων πολυουβικουιτίνης σχετίζεται το UBE3C (ubiquitin protein ligase E3C). Η πρωτεΐνη OTP, είναι ένας μεταγραφικός παράγοντας, που ίσως λειτουργεί κατά την ανάπτυξη του εγκεφάλου, καθώς η οικογένεια των πρωτεϊνών που κωδικοποιεί έχει ρόλο - κλειδί στον καθορισμό της διαφοροποίησης του κυττάρου. Το γονίδιο PRDM2 διαφαίνεται να σχετίζεται με το νευρικο - ενδοκρινικό σύστημα. Συγκεκριμένα, οι λειτουργίες που του αποδίδονται είναι (i) η ρύθμιση της μεταγραφής κατά τη νευρωνική διαφοροποίηση και την παθογένεση του ρετινοβλαστώματος, (ii) η ενεργοποίηση της μεταγραφής της οξυγενάσης της αίμης 1 και (iii) η δράση του ως μεσολαβητής ενεργοποίησης της οιστρογονικής δράσης. Επιπροσθέτως, το PPP4R2 θεωρείται ρυθμιστής της νευρωνικής διαφοροποίησης και επιβίωσης (ως απάντηση στην καταστροφή του DNA), ενώ το KCNH7 εκφράζει ένα δίαυλο καλίου που θεωρείται ρυθμιστής της νευροδιαβίβασης, του καρδιακού ρυθμού, της έκκρισης της ινσουλίνης, της νευρικής διεγερσιμότητας, της επιθηλιακής μεταφοράς των ηλεκτρολυτών, της σύσπασης των λείων μυών και του όγκου των κυττάρων. Το ADCYAP1 παρουσιάζει εξίσου ενδιαφέρον, καθώς είναι μια πρόδρομη εκκρινόμενη πρωτεΐνη της υπόφυσης, η οποία αποτελεί βασικό μεσολαβητή των νευροενδοκρινολογικών απαντήσεων στο στρες. Ο μηχανισμός δράσης του περιλαμβάνει τη διέγερση της αδενυλικής κυκλάσης και στη συνέχεια, σε αύξηση των επιπέδων της κυκλικής μονοφωσφορικής αδενοσίνης (camp), με αποτέλεσμα τη μεταγραφική ενεργοποίηση των γονιδίων - στόχων. Όσον αφορά το οξειδωτικό στρες, το MSRA είναι ένα αναγωγικό ένζυμο που υπάρχει σε όλους τους οργανισμούς και είναι έντονα συντηρημένο, ενώ παρουσιάζει υψηλότερο επίπεδο έκφρασης στους νεφρούς και το νευρικό σύστημα. Ακόμη ένα αναγωγικό ένζυμο είναι το PRDX4, πιθανώς και το FTO, το οποίο κωδικοποιεί μια πυρηνική πρωτεΐνη, της οποίας η ακριβής φυσιολογική λειτουργία δεν είναι γνωστή. Στον αντίποδα, είναι γνωστό πως άλλα μη - αιμικού σιδήρου ένζυμα λειτουργούν για να αντιστραφεί το αλκυλιωμένο DNA και RNA, βλάβες που προκαλούνται από την οξειδωτική απομεθυλίωση. Μελέτες σε ανθρώπους και μύες έδειξαν συσχέτιση με το νευρικό σύστημα, το καρδιαγγειακό, με τον δείκτη μάζας σώματος, την παχυσαρκία και τον διαβήτη τύπου 2. Αναφορικά με τα μιτοχόνδρια, το PCCA (propionyl CoA carboxylase, alpha polypeptide) αποτελεί την α - υπομονάδα του μιτοχονδριακού ενζύμου. Μεταλλάξεις του γονιδίου ή της β υπομονάδας, που προκαλούν έλλειψη του ενζύμου, οδηγούν σε προπιονική οξυαιμία. Τέλος, ο ρόλος του γονιδίου A2LD1 - ή αλλιώς GGACT (gammaglutamylamine cyclotransferase) - είναι ο καταβολισμός του L-gamma-glutamyl-L-epsilon- 56
57 lysine. Ο μεταβολισμός των αλκυλαμινών, στον οποίο και εμπλέκεται, έχει συσχετισθεί με νευροεκφυλιστικές διεργασίες. Πίνακας 10: Σημαντικότερα μονοπάτια για τα γονίδια που προέκυψαν από τη σύγκριση ολόκληρου του γονιδιώματος ασθενών και υγιών σύμφωνα με το πρόγραμμα ΙΡΑ. Ασθένεια ή Λειτουργία Κρίσιμη τιμή σημαντικότητας (p) Γονίδια Πολλαπλασιασμός των νευρικών κυττάρων Πολλαπλασιασμός των κινητικών νευρώνων Μη φυσιολογική λειτουργία των κινητικών νευρώνων 6,02 x10-5 ISL1, FTO, ADCYAP1, ΟΤΡ, SPP x10-5 ISL1, FTO 1,28 x10-3 ISL1, WNT4 Ανάπτυξη νευρομυϊκής σύναψης 1,65 x10-3 PDZRN3 Αντανακλαστικά καμπτύρων της σπονδυλικής στήλης, διακλάδωση και καθοδήγηση των αξόνων αισθητικών νευρώνων ALS 6, HET 4, ασθένεια με έγκλειστα ενδιαμέσων ινιδίων Ανάπτυξη Μ και Ρ κυττάρων του οπτικού νευρικού συστήματος Ανάπτυξη φλοιού παρεγκεφαλίδας, ρύθμιση των ανώτερων αυχενικών γαγγλίων 1,65 x10-3 PRKG1 1,65 x10-3 FUS 1,65 x10-3 ΟΤΡ 1,65 x10-3 ADCYAP1 Ανάπτυξη κρανιακού νεύρου 1,9 x10-3 ISL1, ERBB4 Ανάπτυξη εγκεφάλου 2,56 x10-3 ADCYAP1, ERBB4, FTO, ΟΤΡ, PRKG1 Ανάπτυξη συγκεκριμένων νεύρων του χεριού, περιοχή δενδριτικών δένδρων Μετακίνηση της κρανιακής νευρικής ακρολοφίας, συμμετοχή στη διαμόρφωση του κεντρικού νευρικού συστήματος, προσκόλληση αστροκυττάρων 3,3 x10-3 ISL1 3,3 x10-3 ERBB4 Αριθμός νευρικών κυττάρων 3,75 x10-3 ADCYAP1, ERBB4, WNT4, SPP1 Μορφολογίας του νευρικού Συστήματος 6,33 x10-3 ERBB4, FTO, ISL1, WNT4, SPP1, YES1, Σχηματισμός των διεγερτικών συνάψεων και των ολιγοδενδροκυττάρων 6,6 x10-3 ERBB4 Ανάπτυξη του κεντρικού νευρικού 7,4 x10-3 ERBB4, ADCYAP1 57
58 συστήματος, ανάπτυξη δενδριτών Επέκταση κινητικών νευρώνων 9,88 x10-3 FTO Επέκταση v3 κινητικών νευρώνων της σπονδυλικής στήλης 9,88 x10-3 FTO Μέγεθος μεσενγκεφάλου 9,88 x10-3 FTO Υπαναχώρηση των νευραξόνων 1,32 x10-2 WNT4 Μορφολογία εγκεφάλου 1,35 x10-2 ERBB4, FTO, SPP1, YES1 Διακλάδωση νευράξονα 1,58 x10-2 ERBB4, ADCYAP1, PRKG1 Επισκευή του DNA 1,65 x10-2 APTX, FTO, FUS Στον Πίνακα 10 απεικονίζονται τα αποτελέσματα του προγράμματος ΙΡΑ σχετικά με το πόσο ισχυρά σχετίζονται τα γονίδια μας με διάφορους κυτταρικούς μηχανισμούς. Από όλες τις λειτουργίες και τις ασθένειες με τις οποίες σχετίζονται τα παραπάνω γονίδια επιλέχθηκαν μόνο εκείνες που αφορούν την ανάπτυξη της μορφολογίας, των ιστών και των κυττάρων του νευρικού συστήματος, την μορφολογία των οργάνων, την εμβρυονική και κυτταρική ανάπτυξη και τις λειτουργίες του νευρικού συστήματος. Ύστερα από αυτήν την αρχική επιλογή, ακολούθησε περισσότερη και ενδελεχής βιβλιογραφική αναζήτηση σχετικά με τα γονίδια KAZN, ZBTB40, TBC1D1, UBE3C, MSRA, PRKG1, FAM181B, FTO, PCCA και A2LD1. Βασικό κριτήριο της επιλογής αυτών των γονιδίων αποτέλεσε το γεγονός ότι συμπεριελάμβαναν πολυμορφισμούς, είτε στα εσώνια τους, είτε καθοδικά ή ανοδικά της κωδικής περιοχής. Επιπλέον, στις περιοχές που συγκεντρώνουν περισσότερους από έναν πολυμορφισμούς, όπως στα εσώνια του PRKG1, ZBTB40, UBE3C, MSRA, PCCA, A2LD1, CEACAM7 και του FTO, πραγματοποιήθηκε έλεγχος για απλοτύπους. Ο έλεγχος αυτός περιελάμβανε τη χρήση του προγράμματος Haploview, με τα δεδομένα της βάσης δεδομένων HapMap, είτε του SNPinfo ώστε να διαπιστωθεί αν αυτοί βρίσκονται σε ανισορροπία σύνδεσης (LD Linkage Disequillibrium). Η ύπαρξη ανισορροπίας σύνδεσης μεταξύ δύο ή περισσότερων αλληλομόρφων σημαίνει ότι έχουν την τάση να συν - κληρονομούνται και ενδεχομένως, αν αυτό επιβεβαιωθεί, επηρεάζουν ως σύνολο την εμφάνιση της ασθένειας που μελετάμε, δηλαδή ως απλότυπος. Στην περίπτωση του PRKG1, ZBTB40, UBE3C, PCCA, A2LD1 και CEACAM7 οι πολυμορφισμοί δεν βρέθηκαν σε LD, αντίθετα στην περίπτωση του MSRA βρέθηκε πλήθος πολυμορφισμών σε LD με τους εσωνικούς πολυμορφισμού rs και rs οι οποίοι απαντώνται σε όλου τους ασθενείς. Επιπροσθέτως, στην περίπτωση του FTO, παρατηρήθηκε ότι πολύ κοντά στον πολυμορφισμό rs , ο οποίος περιλαμβάνεται στα δεδομένα μας, υπάρχει ένας άλλος πολυμορφισμός, ο rs , ο οποίος δεν περιλαμβάνεται στα δεδομένα μας. Σύμφωνα με τα δεδομένα του Hapmap o rs είναι σε LD με τους rs και rs στον πληθυσμό της κεντρικής Ευρώπης. Κατά αυτόν τον τρόπο, επειδή οι rs και rs βρίσκονται αρκετά κοντά, ώστε να ενισχυθούν με μία μοναδική αλυσιδωτή αντίδραση πολυμεράσης, θεωρήθηκε ότι γονοτύπηση του rs θα μας δώσει μια καλή εκτίμηση των 58
59 αλληλομόρφων στις θέσεις των rs και rs , οι οποίοι όπως και ο rs ήταν κοινοί για το σύνολο των 10 ασθενών. Η οριστική επιλογή των πολυμορφισμών για περαιτέρω ανάλυση καθορίστηκε από τον συνδυασμό των παραπάνω δεδομένων και των δεδομένων έκφρασης των γονιδίων στον εγκέφαλο. Καταλήξαμε στην επιλογή πέντε εξ αυτών, οι οποίοι αναγράφονται παρακάτω: για το γονίδιο FAM181B, ο rs (C>T) για το γονίδιο A2LD1, ο rs (7bp del) για το γονίδιο A2LD1, ο rs (C>T) για το γονίδιο FTO, ο rs (C>T) & o rs (G>C) για το γονίδιο TBC1D1, ο rs (C>A) για το γονίδιο KAZN, ο rs (C>T) Ο σχεδιασμός των πειραμάτων στηρίχθηκε στη γονοτύπηση των παραπάνω πολυμορφισμών. 59
60 Δ.1.2 Επιλογή πολυμορφισμών στόχων, 2 η προσέγγιση Η δεύτερη προσέγγιση που ακολουθήθηκε για την επεξεργασία των δεδομένων του WGS ήταν η σύγκριση των δεδομένων μας με βάσεις δεδομένων καταγραφής μικρών προσθηκών, ελλείψεων, αντικαταστάσεων ή SNPs. Τα αποτελέσματα αυτής της προσέγγισης, που ουσιαστικά ήταν μια αναζήτηση νέων παραλλαγών, ήταν τα εξής: To πλήθος των πραγματικά νέων παραλλαγών ήταν Το είδος των παραλλαγών φαίνεται στο διάγραμμα πίτας που ακολουθεί (Εικόνα 13). Νέες Παραλλαγές intrergenic intronic ncrna_intronic upstream 7 downstream 28 5UTR UTR exonic 43 ncrna_exonic splicing 2195 Εικόνα 13: Διάγραμμα πίτας όπου παρουσιάζεται η σύνοψη των αποτελέσματα της αναζήτησης νέων παραλλαγών, δηλαδή που έχουν παρατηρηθεί το πολύ μία φορά. Τα χρώματα της πίτας, αντιστοιχούν στα είδη των παραλλαγών ανάλογα με τη θέση τους ως προς το πλησιέστερο γονίδιο και οι αριθμοί στα αντίστοιχα κουτάκια αντιπροσωπεύουν τον πραγματικό αριθμό των παρατηρήσεων. Αυτή η προσέγγιση, όπως και η προηγούμενη, επικεντρώθηκε στις παραλλαγές που είναι πιο πιθανό να επηρεάζουν τη λειτουργία της πρωτεΐνης ή τη γονιδιακή ρύθμιση, δηλαδή στις παραλλαγές των εξωνίων (Πίνακας 11) και της 5 αμετάφραστης περιοχής, αντίστοιχα. Πίνακας 11: Αποτελέσματα WGS. Νέες εξωνικές παραλλαγές. Γονίδιο EPPK1 Πληροφορίες EPPK1:NM_031308:exon1:c.6637_6639ATG Έναρξη Λήξη θέσης στο χρωμόσωμα Αλληλουχία Αναφοράς Αλληλουχία αλληλομόρφου Συνέπεια GTC CAT Asp/Met 60
61 OR9G1, OR9G9 SARM1 HRNR MUC4 OR9G1:NM_ :exo n1:c.335_339gctta,or9g9 :NM_ :exon1:c.3 35_339GCTTA SARM1:NM_015077:exon3: c.546_550cgtgg HRNR:NM_ :exon 3:c.G4052A:p.R1351Q MUC4:NM_018406:exon2:c.A6344T:p.D2115V *Αυτή η αλληλουχία βρέθηκε στους ασθενείς ACCTG GCTTA CGTGG * TGGGT Καμία OR9G9: GCTTA είναι η αλληλουχία αναφοράς C T Arg/Gln T A Asp/Val Με τη βοήθεια βάσεων δεδομένων, όπως το Εnsembl ( ή την Expasy ( και συγκεκριμένα τη σελίδα UniProtKB/Swiss-Prot variant pages, αναλύθηκαν οι παραπάνω παραλλαγές. Για την εκτίμηση της βαρύτητας της αλλαγής χρησιμοποιήθηκε η μήτρα BLOSUM (BLOcks SUbstitution Matrix). Η μήτρα BLOSUM είναι μία μήτρα υποκατάστασης που χρησιμοποιείται για την ευθυγράμμιση αλληλουχιών πρωτεϊνών. Οι μήτρες BLOSUM χρησιμοποιούνται για να αποδοθεί ένα σκορ στις ευθυγραμμίσεις μεταξύ των εξελικτικά αποκλίνουσων ακολουθιών των πρωτεϊνών. Η βαθμολογία εντός μιας μήτρας BLOSUM για το αντίστοιχο άγριου τύπου προς το εναλλακτικό αμινοξύ, ισούται με τον λογάριθμο του λόγου των πιθανοτήτων δύο αμινοξέων να εμφανίζονται κατά τύχη. Στην παρούσα εργασία, χρησιμοποιείται η μήτρα Blosum62 (Styczynski et al. 2008). Αυτή η μήτρα περιλαμβάνει βαθμολογίες για όλες τις πιθανές ανταλλαγές ενός αμινοξέος με ένα άλλο. Η χαμηλότερη βαθμολογία είναι το -4 και μεταφράζεται ως χαμηλή πιθανότητα υποκατάστασης, ενώ η υψηλότερη βαθμολογία είναι το 11 και σημαίνει υψηλή πιθανότητα υποκατάστασης. Εφόσον δεν θεωρήθηκε σκόπιμο στην παρούσα φάση να γονοτυπηθεί κάποια από τις παραπάνω παραλλαγές, στραφήκαμε προς την 5 αμετάφραστη περιοχή, αναζητώντας αν κάποια από αυτές τις παραλλαγές βρίσκεται στον υποκινητή και επομένως, αν μπορεί να επηρεάζει τη ρύθμιση του αντίστοιχου γονιδίου. Στην 5 αμετάφραστη περιοχή βρέθηκαν οι εξής νέες παραλλαγές (Πίνακας 12): Πίνακας 12: Νέες παραλλαγές στην 5 αμετάφραστη περιοχή. FGF13 Γονίδιο Έναρξη Λήξη θέσης στο χρωμόσωμα chrχ: Απόσταση από το κωδικόνιο έναρξης 350bp Αλληλουχία Αναφοράς/ Αλληλουχία αλληλομόρφου AGTG*/GCT SLC36A1 Chr5: C2orf88 Chr2: *Αυτή η αλληλουχία βρέθηκε στους ασθενείς 79bp GCTG/ACGAGTT ATATCTGT/TTAGTGATTA 61
62 Εν τέλει, επιλέχθηκαν να αλληλουχηθούν οι 5 αμετάφραστες περιοχές του FGF13 και του SLC36A1. Οι 5 UTR αποτελούν ενδιαφέρουσες περιοχές του γονιδίου λόγο του ρυθμιστικού ρόλου που έχουν. Είναι πιθανό, κάποια παραλλαγή στην 5 UTR να επηρεάζει την πρόσδεση κάποιου μεταγραφικού παράγοντα, για παράδειγμα. Η επίλογή της παραλλαγής στο γονίδιο FGF13, στηρίχθηκε στην αυξημένη έκφραση του στον εγκέφαλο ( και στη σχέση του με την πόλωση, διακλάδωση και μετακίνηση των αξόνων στον φλοιό του εγκεφάλου και στον ιππόκαμπο. Η επιλογή του ενισχύθηκε λόγο της συσχέτισης του με την ανάπτυξη των νευρώνων (Hartung et al. 1997). Σχετικά με το SLC36A1, τα στοιχεία που έχουμε αφορούν κυρίως πειράματα σε μύες, στους οποίους ο εν λόγω μεταφορέας αμινοξέων, εντοπίζεται στα ενδοκυττάρια οργανίδια των νευρώνων. Η υποψηφιότητα του ενισχύθηκε, μετά από αναζήτηση μεταγραφικών παραγόντων με τη βοήθεια του διαδικτυακού προγράμματος rvista (2.0), το οποίο υπέδειξε την ακολουθία γύρω από την παραλλαγή, ως πιθανή θέση πρόσδεσης του μεταγραφικό παράγοντα ELK1 (θεωρείται ότι έχει νευροπροστατευτικό ρόλο). Δ.1.3 Επιλογή πολυμορφισμών στόχων, 3 η προσέγγιση Η τρίτη προσέγγιση των δεδομένων του WGS αφορά την σύγκριση των γονιδιωμάτων των Ελλήνων ασθενών ALS, με τη βάση δεδομένων HGMD (The Human Gene Mutation Database) (Cooper, Ball, and Krawczak 1998). Από την παρούσα προσέγγιση επιλέχθηκαν οι μεταλλάξεις που έχουν συσχετισθεί με ALS και παρουσιάζονται σε τουλάχιστον έναν ασθενή (Πίνακας 13). Πίνακας 13: Αποτελέσματα 3 ης προσέγγισης των δεδομένων του WGS. Γονίδιο Καταγραφή στο Περιγραφή dbsnp Πηγή TARDBP rs (C-T) to initiation codon (Luquin et al. 2009) ALAD rs Lys59Asn (Kamel et al. 2005) APEX1 rs Asp148Glu (Hayward et al. 1999) ANG rs11701 Gly110Gly (Greenway et al. 2004) FUS rs (G-A) +41 to termination codon (Brown et al. 2012, Sabatelli et al. 2013) ZNF512B rs (T-C) to initiation codon (Iida et al. 2011) NEFH rs ; rs del 18 bp codon 744/2232_2249del18 (Al-Chalabi et al. 1999) Παρόλο που κανένα από τα αποτελέσματα του παραπάνω πίνακα δεν κρίθηκε ιδιαίτερης σημασίας, η περιοχή 3 UTR του γονιδίου FUS επιλέχθηκε για ανάλυση σε περισσότερα δείγματα ασθενών. Η επιλογή στηρίχθηκε, στον ήδη γνωστό ρόλο του γονιδίου για την ασθένεια και στις εξελίξεις, οι οποίες στρέφουν το ενδιαφέρον προς μεταλλάξεις της 3 UTR περιοχής του γονιδίου, οι οποίες έχουν συχετισθεί με την ALS (Sabatelli et al. 2013). 62
63 Δ.1.4 Εντοπισμός της μετάλλαξης SPG7 O εντοπισμός της μετάλλαξης στο γονίδιο SPG7 και συγκεκριμένα στο εξώνιο 1 πραγματοποιήθηκε σε συνεργαζόμενο εργαστήριο του καθηγητή Guy A. Rouleau στο Μόντρεαλ, από τον ερευνητή Dr. Hussein Daoud, με τη χρήση μεθόδου Whole Exome Sequencing. Η παραπάνω μέθοδος εφαρμόστηκε σε 4 δείγματα ασθενών με διάγνωση «πιθανή ALS οικογενής σπαστική παραπληγία (HSP Hereditary Spastic Paraplegia/Paraparesis)». Οι ασθενείς είναι όλοι άτομα της ίδιας οικογένειας, οι τρεις είναι αδέρφια και η τέταρτη ασθενής είναι 1 η ξαδέρφη αυτών. Σε όλα τα δείγματα βρέθηκε μια νέα, ομόζυγη, έλλειψη 25 βάσεων στο γονίδιο SPG7, στην περιοχή του εξωνίου 1. Ακολούθησε επαλήθευση στα άτομα αυτά και σε κάποιους από τους συγγενείς 1 ου βαθμού τους, τα αποτελέσματα της οποίας παρατίθενται αναλυτικά στην ενότητα Ε.3 των αποτελεσμάτων. Επίσης, παράλληλα, διερευνήθηκε περαιτέρω η κλινική εικόνα των ασθενών. 63
64 Δ.2 Πληθυσμιακό δείγμα Στην παρούσα μελέτη έλαβαν μέρος δύο διαφορετικές ομάδες ατόμων: Υγιή άτομα (ομάδα αναφοράς), Έλληνες ή Σαρδήνιοι Ασθενείς με ALS, οικογενούς ή σποραδικής μορφής, Έλληνες ή Σαρδήνιοι Τα δείγματα, τόσο των ασθενών, όσο και των υγιών ατόμων που χρησιμοποιήθηκαν, προήλθαν από τους ίδιους τους ασθενείς, οι οποίοι ενημερώθηκαν για τη μελέτη μας μέσω του Ελληνικού συλλόγου ALS ( και προέρχονται αποκλειστικά από τον ελληνικό πληθυσμό ή από τον πληθυσμό των Σαρδηνίων. Από όλους τους ασθενείς που συμπεριελήφθησαν στη μελέτη ελήφθη γραπτή ενήμερη συγκατάθεση. Δ.3 Απομόνωση γενωμικού DNA Δ.3.1 Απομόνωση γενωμικού DNA από αίμα Η απομόνωση του γενωμικού DNA από αίμα έγινε με τη χρήση του προτυποποιημένου συστήματος QIAamp Blood Midi Kit (Spin Protocol). Το παρακάτω πρωτόκολλο εφαρμόστηκε για την απομόνωση του γενωμικού DNA από 2 ml περιφερικού, ολικού αίματος, στο οποίο είχε προστεθεί EDTA, ως αντιπηκτικό. Κατά την εφαρμογή της μεθόδου, χρησιμοποιήθηκαν στήλες χαλαζία. Η απομόνωση του DNA στηρίζεται στο γεγονός ότι τα νουκλεϊκά οξέα προσδένονται (προσροφώνται) στη στήλη, σε περιβάλλον υψηλής ιοντικής ισχύος και χαμηλού ph, που δημιουργείται από την προσθήκη χαοτροπικού παράγοντα, ενώ η έκλουση του γίνεται με νερό ή με ρυθμιστικό διάλυμα Tris-EDTA (TE) σε ph 8,3. Διαδικασία: Τα ακριβή στάδια της διαδικασίας απομόνωσης περιγράφονται αναλυτικά, παρακάτω: Προσθήκη 200 μl του αντιδραστηρίου QIAGEN Protease σε σωλήνα φυγοκέντρησης 15 ml. Προσθήκη 1 ml δείγματος αίματος και 1 ml PBS (Phosphate buffered saline) στο σωλήνα και ανάδευση. Προσθήκη 2,4 ml διαλύματος AL (διάλυμα λύσης) και έντονη ανάδευση για περίπου 1 min. Επώαση στο υδατόλουτρο στους 70 ο C για 10 min. Προσθήκη 2 ml αιθανόλης (96-100%) στο μίγμα και έντονη ανάδευση. Μεταφορά της μισής ποσότητας του μίγματος στην ειδική QIAamp Midi spin στήλη (τοποθετημένη σε σωλήνα φυγοκέντρησης 15 ml). Φυγοκέντρηση για 3 min, σε ταχύτητα 1850 x g, σε θερμοκρασία δωματίου (15-25 C). 64
65 Αφαίρεση της στήλης και απόρριψη του διηθήματος. Επανατοποθέτηση της στήλης στο σωλήνα φυγοκέντρησης και φόρτωση με το υπόλοιπο του μίγματος. Επανάληψη της προηγούμενης φυγοκέντρησης. Ακολουθεί προσθήκη 2 ml διαλύματος AW1 (διάλυμα πλύσης) στη στήλη και φυγοκέντρηση στα 4500 x g, για 1 min. Προσθήκη 2 ml διαλύματος AW2 (διάλυμα πλύσης) στη στήλη. Ακολουθεί πάλι φυγοκέντρηση στα 4500 x g, για 15 min. Τοποθέτηση της QIAamp Midi spin στήλης σε ένα καθαρό σωλήνα φυγοκέντρησης όγκου 15 ml. Προσθήκη 300 μl διαλύματος έκλουσης ΑΕ και επώαση, για 5 min, σε θερμοκρασία δωματίου. Φυγοκέντρηση στα 4500 x g, για 2 min. Για να επιτευχθεί μεγαλύτερη τελική συγκέντρωση DNA, το προηγούμενο βήμα επαναλαμβάνεται, κάνοντας μία δεύτερη έκλουση, περνώντας ξανά το διήθημα από τη στήλη κι επωάζοντας για 5 min, σε θερμοκρασία δωματίου. Φυγοκέντρηση στα 4500 x g, για 2 min. Τέλος, το διήθημα που προκύπτει και περιέχει το απομονωμένο DNA, συλλέγεται και αποθηκεύεται στους -20 o C. Δ.3.2 Απομόνωση γενωμικού DNA από σίελο Ο σίελος συλλέχθηκε με μία ώρα τουλάχιστον αποχή από φαγητό, ποτό και κάπνισμα σε σωληνάκια των 15 ml που περιείχαν 3 ml ΤΝΕ (Tris-HCl ph 8, 50 mm NaCl, 7 mm EDTA, diluredin 66% αιθανόλη). Ζητήθηκε από τα άτομα να τρίψουν τη γλώσσα στο εσωτερικό της στοματικής κοιλότητας και στα δόντια, δαγκώνοντας παράλληλα ελαφρά την εσωτερική επιφάνεια των παρειών για περίπου 30 δευτερόλεπτα και στη συνέχεια, να φτύσουν στο δοχείο συλλογής που τους δόθηκε. Η διαδικασία επαναλήφθηκε έως τη συλλογή σιέλου περίπου συνολικού όγκου 8 ml. Το δείγμα φυλάχθηκε στους 4 C για 1-2 εβδομάδες και στη συνέχεια, έγινε απομόνωση του ολικού γενωμικού DNA με βάση το εξής πρωτόκολλο (Aidar and Line 2007): Το σωληνάκι των 15 ml, όπου συλλέχθηκε ο σίελος, φυγοκεντρήθηκε για 10 λεπτά στα 3000 rpm, σε θερμοκρασία δωματίου, με απόρριψη του υπερκείμενου Το ίζημα επαναδιαλυτοποιήθηκε με 1 ml ΤΝΕ και ακολούθησε ανάδευση με τη χρήση συσκευής vortex Κατόπιν φυγοκέντρησης για 5 λεπτά στα 2000 rpm, ακολούθησε απόρριψη του υπερκειμένου. Διατηρήθηκαν περίπου 200μl διαλύματος, ώστε να ακολουθήσει επαναδιαλυτοποίηση και ανάδευση (συσκευή vortex) για 5 δευτερόλεπτα 65
66 Στη συνέχεια έγινε προσθήκη 1,3 ml διαλύματος λύσης των κυττάρων (10mM Tris- HCl ph 8, 0,5% SDS, 5mM EDTA, 10 μl πρωτεϊνάση Κ) και ακολούθησε ανάδευση (συσκευή vortex) για 5 δευτερόλεπτα Τα δείγματα επωάστηκαν σε θερμοκρασία 55 ο C καθ όλη τη διάρκεια της νύχτας (overnight) Την επομένη ημέρα, προστέθηκαν - σε κάθε δείγμα 500μl διαλύματος - 8Μ ammonium acetate, 1 mm EDTA και ακολούθησε ανάδευση (συσκευή vortex) για 5 δευτερόλεπτα Μετά την προσθήκη του ammonium acetate και του EDTA τα δείγματα φυγοκεντρήθηκαν για 10 λεπτά στα rpm και το υπερκείμενο μεταφέρθηκε σε άλλο σωληνάκι, όπου προστέθηκαν 1080 μl ισοπροπανόλης Ακολούθησε ελαφριά ανάδευση και φυγοκέντρηση για 5 λεπτά στα rpm, οπότε και το υπερκείμενο απορρίφθηκε Τα βήματα 7 και 8 επαναλήφθηκαν ακόμη μια φορά και το σωληνάκι αφέθηκε μέχρι πλήρους εξάτμισης της ισοπροπανόλης Έγιναν πλύσεις με προσθήκη 2 ml αιθανόλης 70%, φυγοκέντρηση για 5 λεπτά στα rpm και απόρριψη του υπερκείμενου (τρις) Τελικά, τα δείγματα αφήνονται να στεγνώσουν για 45 λεπτά τουλάχιστον και επαναιωρούνται σε 100 μl TE buffer (10 mm Tris-HCl ph 7,8, 1 mm EDTA) 66
67 Δ.4 Προσδιορισμός της συγκέντρωσης του DNA σε υδατικό διάλυμα Για να προσδιορίσουμε τη συγκέντρωση των δειγμάτων DNA, που προέκυψαν από την παραπάνω διαδικασία απομόνωσης, έγινε χρήση φωτόμετρου Nanodrop. Η λειτουργία της συσκευής στηρίζεται στην ιδιότητα των νουκλεϊκών οξέων να απορροφούν σε συγκεκριμένα μήκη κύματος. Η κλασική καμπύλη απορρόφησης παρουσιάζεται στην Εικόνα 14. Ο τρόπος λειτουργίας της συσκευής φαίνεται στο πάνω τμήμα της Εικόνας 15 και στο κάτω μέρος απεικονίζεται η μορφή με την οποία λαμβάνουμε το αποτέλεσμα της μέτρησης. Εικόνα 14: Κλασική καμπύλη μέτρησης απορρόφησης νουκλεικών οξέων. Απεικονίζονται τα μήκη κύματος από τα οποία προκύπτει η συγκέντρωση (260nm) και οι προσμίξεις (230nm και 280nm). Αναλυτικότερα, μηδενίζουμε τη συσκευή χρησιμοποιώντας ως τυφλό, το διάλυμα που χρησιμοποιήθηκε για την έκλουση του DNA κατά την απομόνωση. Στη συνέχεια, τοποθετούμε μία σταγόνα DNA δείγματος, όγκου 1 1,5 μl, στην ειδική βάση όταν ο βραχίονας είναι ανοιχτός. Όταν ο βραχίονας κλείνει, το δείγμα σχηματίζει μία στήλη. Ο βραχίονας αυτόματα μετακινείται προς τα κάτω και υπολογίζει τη συγκέντρωση του δείγματος με τη βοήθεια οπτικών ινών. Στο τέλος κάθε μέτρησης καθαρίζουμε με ένα κομμάτι χαρτί την κεφαλή για να εξασφαλίσουμε την ειδικότητα των μετρήσεων. Τα αποτελέσματα των μετρήσεων, καταγράφονται αυτόματα στον υπολογιστή που βρίσκεται σε σύνδεση με τη συσκευή. Η φωτομέτρηση για το DNA γίνεται σε μήκος κύματος 260nm και από την τιμή της οπτικής απορρόφησης (O.D.), το λογισμικό του συστήματος Nanodrop υπολογίζει αυτόματα τη συγκέντρωση του DNA. Παράλληλα, γίνεται μέτρηση του ίδιου δείγματος και στα 280 nm και 230 nm για τον έλεγχο προσμίξεων. O λόγος O.D. 260nm /O.D. 280nm εκφράζει την καθαρότητα του δείγματος DNA. Καθαρά δείγματα DNA δίνουν λόγο 1,8 2,0 ενώ εάν υπάρχουν προσμίξεις πρωτεΐνης, φαινόλης ή άλλων αλκοολών στο δείγμα, ο λόγος είναι μικρότερος από 1,8 και ο προσδιορισμός της συγκέντρωσης του DNA δε θεωρείται ακριβής. Λόγο μικρότερο του 1,8 είναι πιθανό να έχουμε και για πολύ μικρές συγκεντρώσεις του δείγματος. Επιπλέον, πραγματοποιείται και μία δεύτερη μέτρηση, στα 230 nm, για τον υπολογισμό της 67
68 καθαρότητας του δείγματος. Ο λόγος O.D. 260nm /O.D. 230nm ο οποίος κυμαίνεται μεταξύ 2,0 2,2 δηλώνει ότι το δείγμα είναι απαλλαγμένο από προσμίξεις. Τιμές μικρότερες του 2 υποδηλώνουν την ύπαρξη φαινόλης, γουανιδίνης, γλυκογόνου ή υδρογονανθράκων, ανάλογα με τη μέθοδο απομόνωσης, ενώ μεγαλύτερες τιμές υποδηλώνουν τη πιθανή χρήση λανθασμένου τυφλού διαλύματος. Κλάσμα καθαρότητας O.D.260nm/O.D.280nm Κλάσμα καθαρότητας O.D.260nm/O.D.230nm Συγκέντρωση σε ng/μl Εικόνα 15: Στο πάνω μέρος της εικόνα βλέπουμε τη διαδικασία λήψης μετρήσεων με τη συσκευή Nanpdrop. Στο κάτω μέρος βλέπουμε την μορφή εξαγωγής των δεδομένων στο υπολογιστή. 68
69 Δ.5 Σχεδιασμός εκκινητών (primers) Ο σχεδιασμός των εκκινητών έγινε με τη βοήθεια του προγράμματος Primer3 (v ) (Koressaar and Remm 2007) ( Αρχικά, εντοπίζεται η ακριβής θέση των υπό μελέτη παραλλαγών μέσω της βάσης δεδομένων Ensembl ( όπου δίδεται και μέρος της αλληλουχίας που περιβάλλει τον εκάστοτε πολυμορφισμό. Ο σχεδιασμός των εκκινητών έγινε έτσι, ώστε το προϊόν της PCR να περικλείει τον πολυμορφισμό περίπου στο κέντρο του. Επίσης, μέσω του Primer3 ελέγχονται βασικές παράμετροι, όπως η θερμοκρασία τήξης (Tm) των εκκινητών και η ποσοστιαία σύστασή τους σε βάσεις γουανίνης και κυτοσίνης (GC content). Συγκεκριμένα, δίδεται η δυνατότητα ελέγχου των ακόλουθων παραμέτρων: οι Tm των εκκινητών θα πρέπει να είναι παρόμοιες και μεταξύ ο C, το μήκος τους μεταξύ νουκλεοτίδια, ενώ η περιεκτικότητα σε GC να κυμαίνεται μεταξύ %. Επιπλέον, είναι απαραίτητο να ελεγχθεί ο κάθε εκκινητής ως προς το αν εμφανίζει συμπληρωματικότητα, είτε με τον εαυτό του (self-complementarity) ή με τον άλλο εκκινητή, με αποτέλεσμα να σχηματίζονται διμερή εκκινητών (primer dimers). Η προϋπόθεση αυτή εξετάστηκε μέσω του προγράμματος DNAMAN ή εναλλακτικά του DINAMELT two-state melting (hybridization), το οποίο εντοπίζεται στον σύνδεσμο ( Για τη χρήση του DINAMELT two-state melting (hybridization) εργαλείου, πληκτρολογώντας το σύμβολο «;», μπορούμε να διαχωρίσουμε τα ολιγονουκλεοτίδια μεταξύ τους και με αυτόν τον τρόπο να εισάγουμε περισσότερες από δύο αλληλουχίες εκκινητών προς σύγκριση. Επίσης, υπάρχει η δυνατότητα ρύθμισης των παραμέτρων ενέργειας (energy rules), έτσι ώστε να αφορούν DNA ολιγονουκλεοτίδια, περίπου στη θερμοκρασία υβριδοποίησης των εκκινητών (~60 ο C), με συγκέντρωση Na + 50 mm και τέλος, συγκέντρωση ολιγονουκλεοτιδίων (strand concentration), η οποία αφορά τη συγκέντρωση των εκκινητών στον τελικό όγκο της αντίδρασης PCR (πλην εξαιρέσεων ορίζεται στα 2 μμ). Μια ακόμη παράμετρος που διερευνάται είναι η ειδικότητα των εκκινητών ως προς το ανθρώπινο γονιδίωμα. Για το λόγο αυτό, χρησιμοποιήθηκε ο αλγόριθμος BLAST (Basic Local Alignment Tool) του Ensembl, όπου εξετάζουμε αν οι εκκινητές που σχεδιάστηκαν, είναι ειδικοί και συμπληρωματικοί με μικρό αριθμό αλληλουχιών στο ανθρώπινο γονιδίωμα, για την αποφυγή παραπροϊόντων στην PCR. Τέλος, με τη βοήθεια του DINAMELT two-state melting (folding) βλέπουμε τις δευτεροταγείς δομές του pcr προϊόντος στον ακριβή σύνδεσμο ( Στον τελευταίο έλεγχο ανασταλτικός παράγοντα της επιλογής των εκκινητών αποτελεί η δημιουργία βρόγχου στην περιοχή των εκκινητών και επιπλέον προτιμάμε προϊόντα με τιμές της διαφορά στην ελεύθερης ενέργεια Gibbs (ΔG) μεταξύ -1 και +1. Οι εκκινητές που σχεδιάστηκαν, σύμφωνα με τα παραπάνω, για τη διεξαγωγή των πειραμάτων της παρούσας μελέτης, αναφέρονται στον Πίνακα 14: 69
70 Πίνακας 14: Οι αλληλουχίες των εκκινητών για κάθε πολυμορφισμό. Δίνεται, επίσης, το μέγεθος του PCR προϊόντος που προκύπτει σε κάθε περίπτωση. Γονίδιο Πολυμορφισμοί Αλληλουχία εκκινητών 5 3 Μέγεθος Προϊόντων (bp) GGGGTCGCTTTAGTTTTTCT(F) 455 FAM181B rs (C>T) TGTCAAGGGCTTAGGAATGG(R) CTAGCGGCAACACCAAGTCT(F) 108/101 A2LD1 rs (7bp del) TGCCTAATTCTTCTTCCTCCTC(R) AGAAGGATGGCAAGGAGGTT(F) 423 A2LD1 rs (C>T) ACTGAAGGAGCGGTTTCTGA(R) rs ( C>T) & ACACTGTTTCTACACTTGCAGAA(F) 396 FTO rs (G>C) GGCCTTAACAAAGCAGGTGAAA(R) TGGTAGGGATCTGTGCAGTT(F) 378 TBC1D1 rs (C>A) AAGTCCTCAAAGTCCAGCCC(R) GGAGGCCTTCCTATGAAGCA(ARMS1) GGAGGCCTTCCTATGAAGCC(ARMS2) CTGGGAAGCGCTACAGTCT(F) 403 KAZN rs (C>T) TGGACAGGAGGCTCAGAGTA(R) chrx: CTTTGGTCTCCTTAGCCTGC (F) 484 FGF13 GCT/AGTG GGGCCAACTTTTCCCGATTA (R) rs AGCAAAGGAGGATGGCGAG(F) 291 SLC36A1 GCTG/ACGAGTT CGCTTCGCCCAATTCACAG (R) GCTTTCAGGCCAACATGG(F) 207 SPG7 exon 1 GGGGATTTACCTGCAGAGC(R) bp: base pairs (ζεύγη βάσεων), exon: εξώνιο Το ζεύγος εκκινητών GCTTTCAGGCCAACATGG(F) και GGGGATTTACCTGCAGAGC(R), που αφορά ο εξώνιο 1 του γονιδίου SPG7, λόγω της απαίτησης του πειράματος να είναι δυνατός ο διαχωρισμός 25 ζευγών βάσεων, πράγμα που απαιτεί την ενίσχυση μικρού σχετικά τμήματος της αλληλουχίας, δεν είναι ιδανικά σχεδιασμένο. Συγκεκριμένα ο εκκινητής R έχει 6 βάσεις συμπληρωματικότητα με τον εαυτό του και ΔG = -2.1, επιπλέον το μονόκλωνο προϊόν αναδιπλώνεται με τον εαυτό του σχηματίζοντας δομή λούπας στην περιοχή του εκκινητή. Αυτές οι αποκλίσεις του σχεδιασμού φαίνεται να έχουν αντίκτυπο στο πείραμα, δυσχεραίνοντας την παραγωγή ειδικών προϊόντων απαλλαγμένων από παραπροϊόντα. 70
71 Δ.6 Αλυσιδωτή Αντίδραση Πολυμεράσης (PCR Polymerase chain reaction) Δ.6.1 Αρχή της μεθόδου Η τεχνική της αλυσιδωτής αντίδρασης πολυμεράσης (PCR - Polymerase Chain Reaction) περιγράφηκε για πρώτη φορά από τον Kary Mullis στη δεκαετία του 1980 (Mullis et al. 1986). Η PCR βασίζεται στον εκθετικό πολλαπλασιασμό των μορίων DNA από μια πολυμεράση. Η σύγχρονη εκδοχή της PCR περιλαμβάνει μια θερμοσταθερή πολυμεράση, όπως αυτή του Thermus aquaticus (Taq) και λαμβάνει χώρα σε ειδικά μηχανήματα, τους θερμοκυκλοποιητές. Η DNA πολυμεράση προσθέτει νουκλεοτίδια στην 3'-OH ομάδα ενός ήδη υπάρχοντος νουκλεοτιδίου και γι' αυτό η πολυμεράση χρειάζεται την ύπαρξη ενός τμήματος στο οποίο θα αρχίσει να προσθέτει νουκλεοτίδια. Για αυτό το λόγο κατά την PCR χρησιμοποιείται ένα ζεύγος συνθετικών ολιγονουκλεοτιδικών εκκινητών, καθένας από τους οποίους υβριδοποιείται σε έναν κλώνο ενός δίκλωνου, αποδιαταγμένου μορίου DNA. Το ζεύγος των εκκινητών οριοθετεί την περιοχή που θα πολλαπλασιαστεί εκθετικά. Οι υβριδοποιημένοι εκκινητές λειτουργούν ως υπόστρωμα για την DNA πολυμεράση, η οποία καταλύει την επιμήκυνση της νέας αλυσίδας τοποθετώντας δεοξυνουκλεοτίδια συμπληρωματικά προς τον κλώνο - στόχο με κατεύθυνση από το 5 3. Όπως φαίνεται στην Εικόνα 16. Η διαδικασία της PCR συνήθως περιλαμβάνει τρία βήματα που επαναλαμβάνονται για n κύκλους (όπου ο αριθμός n ισούται με τον αριθμό των κύκλων): 1. Αποδιάταξη του DNA-στόχου στους 94 ο C ή 95 ο C (Denaturation of DNA template) 2. Πρόσδεση των εκκινητών (υβριδισμός) στις συμπληρωματικές τους ακολουθίες σε θερμοκρασία που εξαρτάται από το μήκος και την αλληλουχία των εκκινητών και την περιεκτικότητα τους σε γουανίνες και κυτοσίνες (primer annealing) 3. Επιμήκυνση των συνδεδεμένων εκκινητών στους 72 ο C με κατεύθυνση 5 προς 3 σχηματίζοντας έτσι τους νέους θυγατρικούς κλώνους DNA (elongation) Τα βήματα αυτά επαναλαμβάνονται για κύκλους, με αποτέλεσμα η αύξηση του αριθμού των αντιγράφων - κλώνων να είναι εκθετική και θεωρητικά να ισούται με 2n. Πρακτικά όμως, η πραγματική απόδοση είναι μικρότερη της θεωρητικής. Τα μόρια που παρήχθησαν στον προηγούμενο κύκλο χρησιμεύουν ως στόχοι για κάθε επόμενο κύκλο. Στην παρακάτω εικόνα (Εικόνα 16) απεικονίζονται τα τρία βασικά στάδια της και φαίνεται πως προκύπτει η εκθετική αύξηση των κλώνων-στόχων. Η αντίδραση πραγματοποιείται σε ειδικά όργανα που ονομάζονται θερμικοί κυκλοποιητές (thermal cyclers), οι οποίοι παρέχουν την δυνατότητα εκτέλεσης αντιδράσεων σε διαφορετικές συνθήκες θερμοκρασίας και χρόνων επώασης. Η συσκευή διαθέτει ένα σύστημα θερμαντικής πλάκας η οποία δέχεται σωλήνες τύπου eppendorf όγκου έως 0,2 ml. Η θερμοκρασία της θερμαντικής πλάκας μπορεί να αυξάνεται και να μειώνεται ανάλογα με τις ανάγκες του πειράματος. 71
72 Εικόνα 16: Απεικόνιση των σταδίων PCR και των τριών πρώτων κύκλων της, ενδεικτικούς της εκθετικής πορείας της. Με την ολοκλήρωση του 1 ου κύκλου, (1) αποδίάταξης, (2) υβριδοποίησης και (3) επιμήκυνσης, έχουν προκύψει 2 νέα δίκλωνα τμήματα από κάθε δίκλωνο μόριο DNAστόχο. Με την ολοκλήρωση του 2 ου κύκλου προκύπτουν 4 δίκλωνες αλυσίδες και η πορεία της αντίδρασης συνεχίζεται με εκθετικό ρυθμό. 72
73 Δ.6.2 Υλικά PCR Για την PCR χρησιμοποιήθηκε το προτυποποιημένο σύστημα (kit) KAPA2G Fast HotStart ReadyMix της εταιρίας KAPABIOSYSTEMS. Το συγκεκριμένο kit αποτελείται από ένα έτοιμο μίγμα που περιλαμβάνει όλα τα απαραίτητα αντιδραστήρια της PCR (Εικόνα 17) εκτός από τους εκκινητές και το υπόστρωμα. Περιλαμβάνει δηλαδή: Εικόνα 17: Απαραίτητα αντιδραστήρια της PCR. Από πάνω προς τα κάτω: Εκκινητές, dntps, πολυμεράση, DNA-στόχος. DNA πολυμεράση ρυθμιστικό διάλυμα ελεύθερα δεοξυνουκλεοτίδια (dntps) 0,2mM το καθένα σε αραίωση 1x MgCl 2 (1.5 mm σε αραίωση 1x) Σε ορισμένες περιπτώσεις, κατά την προετοιμασία της PCR προστίθεται επιπλέον MgCl 2, το οποίο ευνοεί τη σύνδεση των εκκινητών με το στόχο και ενισχύει τη δράση της πολυμεράσης, όπως επίσης και παράγοντες που διευκολύνουν την αποδιάταξη του δίκλωνου DNA, ιδιαίτερα σε περιπτώσεις όπου επιθυμούμε των πολλαπλασιασμό αλληλουχιών με υψηλό περιεχόμενο σε γουανίνη και κυτοσίνη, όπως το DMSO (Dimethyl sulfoxide) σε αναλογία 5-7,5%. Η KAPA2G Fast HotStart DNA πολυμεράση δρα με κατεύθυνση 5 3 και έχει επίσης δραστικότητα 5 3 εξωνουκλεάσης. Όμως, δε χαρακτηρίζεται από 3 5 δράση εξωνουκλεάσης, με αποτέλεσμα να μην μπορούν να απομακρυνθούν λανθασμένα νουκλεοτίδια τα οποία πιθανώς να ενσωματώθηκαν στο PCR προϊόν. Το ποσοστό σφάλματος αντιστοιχεί περίπου σε ένα λανθασμένο νουκλεοτίδιο ανά 1, ενσωματωμένα νουκλεοτίδια. Όσον αφορά τα αναλώσιμα πλαστικά, χρησιμοποιήθηκαν σωληνάκια PCR αντίδρασης (PCR tubes) strips 8 θέσεων χωρητικότητας 200 μl (Kisker Biotech GmbH & Co., Steinfurt). Για την ετοιμασία της PCR αντίδρασης χρησιμοποιήθηκαν αποκλειστικά ακρορύγχια με φίλτρο, (filter tips) της εταιρίας Greiner (Greiner Bio-One GmbH, Germany) και, με σκοπό την αποφυγή των επιμολύνσεων. Δόθηκε μεγάλη προσοχή στον καθαρισμό του χώρου προετοιμασίας και των αυτόματων πιπετών PCR, που επιτεύχθηκε με τη χρήση αιθανόλης 70 % και DNA-ExitusPlus της εταιρίας Applichem (πρόκειται για ένα ειδικό καθαριστικό κατά των επιμολύνσεων από DNA και RNA). Επιπλέον, ο εργαστηριακός πάγκος προετοιμασίας των αντιδράσεων απομονώνεται χωρικά από τους χώρους όπου γίνεται διαχείριση PCR προϊόντων για αποφυγή επιμολύνσεων. 73
74 Δ.6.3 Βελτιστοποίηση παραμέτρων PCR Για τη βελτιστοποίηση της PCR είναι απαραίτητη η ρύθμιση πολλών παραμέτρων, μεταξύ των οποίων η Tm των εκκινητών της αλληλουχίας - στόχου, οι συγκεντρώσεις των αλάτων και η χρονική διάρκεια κάθε επιμέρους βήματος. Η θερμοκρασία υβριδοποίησης των εκκινητών μίας αντίδρασης PCR πρέπει να είναι περίπου 5 C χαμηλότερη από την Tm των εκιννητών. Η Tm των εκκινητών θεωρητικά υπολογίζεται από των τύπο: Tm = (A+T) x 2 o C + (G+C) x 4 o C (< 20bp) (Α: αδενίνες, Τ: θυμίνες, G: γουανίνες, C: κυτοσίνες). Στην πραγματικότητα όμως αυτό δεν είναι απόλυτο. Για αυτό το λόγο, θα πρέπει να δοκιμάσουμε αρχικά διάφορες θερμοκρασίες υβριδισμού ώστε να καταλήξουμε στην πιο κατάλληλη, κατά την οποία η αντίδρασή μας έχει την καλύτερη απόδοση. Η gradient PCR αποτελεί ένα στάδιο της διαδικασίας βελτιστοποίησης των συνθηκών της PCR, καθώς μας επιτρέπει να δοκιμάσουμε διαφορετικές Τm σε ένα πείραμα. Τα αποτελέσματα της αντίδρασης είναι δυνατόν να ελεγχθούν με ηλεκτροφόρηση σε πήκτωμα αγαρόζης ή πολυακρυλαμίδης, για την επιβεβαίωση του αναμενόμενου μεγέθους και συγκέντρωσης. Δ.6.4 Πρωτόκολλα PCR αντιδράσεων Παρακάτω αναφέρονται τα πρωτόκολλα και οι συνθήκες που χρησιμοποιήθηκαν για την ανάλυση του κάθε πολυμορφισμού. Για κάθε ξεχωριστή αντίδραση PCR τα αντιδραστήρια που χρησιμοποιούνται αναμιγνύονται πάντοτε με τη συγκεκριμένη σειρά που αναφέρεται στον παρακάτω πίνακα (Πίνακας 15). Πίνακας 15: Η τυπική στερεοχημεία μιας PCR αντίδρασης. Αντιδραστήριο Αρχική συγκέντρωση Τελική συγκέντρωση Όγκος (μl) H2O (PCR - grade) KAPA2G Fast ,5 HotStart ReadyMix Ευθύς εκκινητής 10μΜ 0,5μΜ 1,25 (Forward Primer) Αντίστροφος εκκινητής (Reverse Primer) 10μΜ 0,5μΜ 1,25 DNA - στόχος 50ng/μl 50 ng/αντίδραση 1 Τελικός όγκος αντίδρασης Στην παρούσα εργασία, πραγματοποιήθηκαν 8 διαφορετικές αντιδράσεις συμβατικής PCR, μία για τον προσδιορισμό της έλλειψης rs στο γονίδιο A2LD1, το οποίο ακολούθως, ηλεκτροφορήθηκε σε πηκτή πολυακρυλαμιδίου, 5 για την ενίσχυση των αλληλουχιών που περικλείουν τους πολυμορφισμούς rs στο γονίδιο FAM181B, τον rs στο γονίδιο A2LD1, τους rs και rs στο FTO, τον rs στο γονίδιο KAZN και τον rs στο γονδίο SLC36A1 και μία που να περικλείει τη θέση του 74
75 χρωμοσώματος Χ, όπου απαντάται η αντικατάσταση GCT/AGTG εντός της περιοχής του γονιδίου FGF13. Στον πίνακα 16, παρουσιάζονται τα στάδια της αντίδρασης για τον πολλαπλασιασμό των παραπάνω τμημάτων. Ο μοναδικός παράγοντας που διαφέρει από το ένα ζεύγος εκκινητών στο άλλο είναι η θερμοκρασία υβριδοποίησης. Σε κάθε περίπτωση, χρησιμοποιήθηκε η θερμοκρασία υβριδοποίησης που κρίθηκε ως βέλτιστη, βάσει των αποτελεσμάτων της «PCR gradient». Οι διαφορετικές θερμοκρασίες υβριδοποίησης για κάθε αλληλουχία - στόχο που πολλαπλασιάστηκε συνοψίζονται στον Πίνακα 17. Πίνακας 16: Στάδια αντίδρασης συμβατικής PCR. Βήμα Θερμοκρασία Χρόνος (σε λεπτά) 1: Ενεργοποίηση του 95 ο C 2:00 ενζύμου 2:Αποδιάταξη 95 ο C 00:15 3: Υβριδοποίηση (Tm) ο C * 00:15 4: Επιμήκυνση 72 ο C 00:01 5: Επανάληψη των βημάτων 2-4 για 34 φορές 6: Τελική επιμήκυνση 72 ο C 00:30 7: Συντήρηση 4 ο C *η θερμοκρασία αυτή εξαρτάται από το εκάστοτε ζεύγος εκκινητών Πίνακας 17: Θερμοκρασίες υβριδοποίησης για κάθε αλληλουχία στόχο. Γονίδιο Πολυμορφισμοί Tm αντίδρασης FAM181B rs o C A2LD1 rs o C A2LD1 rs o C FTO rs & rs o C KAZN rs o C chrx: o C FGF13 GCT/AGTG SLC36A1 rs o C SPG7 Εξώνιο 1ο 66 o C Οι εκκινητές που χρησιμοποιήθηκαν στις παραπάνω PCR αναγράφονται στον Πίνακα 14. SPG7ex1 Ιδιαίτερη περίπτωση αποτέλεσε η ενίσχυση του τμήματος γύρω από το εξώνιο 1 του γονιδίου SPG7. Στη συγκεκριμένη περίπτωση, σημειώθηκαν ορισμένες αλλαγές στο κλασικό πρωτόκολλο, ώστε να γίνει δυνατή η ειδική ενίσχυση τμήματος 207bp σε αυτή την περιοχή. Όταν η συμβατική PCR δοκιμάστηκε σε διάφορες θερμοκρασίες και παρατηρήθηκαν τα αποτελέσματα στο πήκτωμα αγαρόζης, υπήρχαν παραπροϊόντα σε όλες τις αυξανόμενες θερμοκρασίες, τα οποία επέμειναν μέχρι που το προϊόν δεν φαινόταν πια. Για αυτό το λόγο δοκιμάστηκαν διάφορες συνθήκες θερμοκρασίας, προσθήκης MgCl 2 ή DMSO και καταλήξαμε 75
76 σε θερμοκρασία Tm 66 ο C, 40 επαναλήψεις των σταδίων 2, 3 και 4 από τον Πίνακα 16, ενώ τα υπόλοιπα στάδια του θερμικού κυκλοποιητή παρέμειναν ίδια. Η στερεοχημεία της αντίδρασης διέφερε επίσης από τη συμβατική και απεικονίζεται στον Πίνακα 18. Οι όγκοι στη στήλη Α αφορούν όλα τα δείγματα που απομονώθηκαν από αίμα. Για τα δείγματα από σίελο, που είχαν καλή εικόνα στο πήκτωμα όταν ηλεκτροφορήθηκε 1 μl γενωμικό DNA από αυτά, δηλαδή είχαν έντονη σχετικά ζώνη, μεγάλου μοριακού βάρους, χρησιμοποιήθηκε το πρωτόκολλο της στήλης Β. Όταν στο πήκτωμα είχαμε ενδείξεις εκτεταμένου κατακερματισμού του γενωμικού DNA, χρησιμοποιήθηκε το πρωτόκολλο της στήλης Γ. Πίνακας 18: Σύσταση αντίδρασης PCR για το τμήμα που περιβάλλει το εξώνιο 1 του SPG7. Αντιδραστήριο Α. Όγκος (μl) Β. Όγκος (μl) Γ. Όγκος (μl) H2O (PCR-grade) 8,25 8,5 5 KAPA2G Fast 12,5 12,5 12,5 HotStart ReadyMix Ευθύς εκκινητής 1,25 1,25 1,25 (Forward Primer) Αντίστροφος εκκινητής (Reverse Primer) 1,25 1,25 1,25 DMSO 0,75 (3%) 0 0 DNA-στόχος 1 1,5 5 Τελικός όγκος αντίδρασης
77 Δ.7 Ηλεκτροφόρηση σε πήκτωμα αγαρόζης Δ.7.1 Αρχή ηλεκτροφόρησης Η ηλεκτροφόρηση σε πήκτωμα αγαρόζης βασίζεται στη μετακίνηση ηλεκτρικά φορτισμένων μορίων μέσα στο πορώδες πήκτωμα που σχηματίζει η αγαρόζη, όταν πολυμεριστεί, υπό την επίδραση ηλεκτρικού πεδίου. Η ηλεκτροφόρηση σε πήκτωμα αγαρόζης είναι η πιο κλασσική μέθοδος που ακολουθείται για το διαχωρισμό και την απομόνωση κλασμάτων DNA. Το DNA αποτελείται από μόρια που έχουν αρνητικό φορτίο, λόγω των φωσφορικών ομάδων που περιέχουν στο σκελετό τους (Εικόνα 18), επομένως, όπως είναι φυσικό κινούνται προς τον θετικό πόλο της συσκευής ηλεκτροφόρησης. Η ταχύτητα με την οποία μετακινούνται τα τμήματα του DNA μέσα σε ένα πήκτωμα είναι συνάρτηση του μήκους τους, του φορτίου τους και του σχήματός τους. Η μέθοδος, συνήθως, χρησιμοποιείται για το διαχωρισμό του DNA με κριτήριο το μέγεθος. Γενικά, τα μικρά τμήματα κινούνται γρηγορότερα σε σχέση με τα μεγάλα στο πήκτωμα. Τα μικρά τμήματα διασχίζουν ευκολότερα το πήκτωμα, ενώ τα μεγαλύτερα καθυστερούν περισσότερο, καθώς περνούν μέσα από το πορώδες του πηκτώματος. Καθώς μετακινούνται, τα διαφορετικά μόρια DNA σχηματίζουν χαρακτηριστικές ζώνες σε διαφορετικές (ανάλογα με το μέγεθός τους) περιοχές του πηκτώματος. Οι ζώνες αυτές είναι αόρατες στο μάτι και καθίστανται ορατές με την προσθήκη βρωμιούχου αιθιδίου στο πήκτωμα και έκθεση σε υπεριώδη ακτινοβολία (UV). Το βρωμιούχο αιθίδιο παρεμβάλλεται ανάμεσα στις αύλακες της δίκλωνης αλυσίδας του DNA και φθορίζει, όταν διεγείρεται με UV. Σε περιπτώσεις που είναι απαραίτητο να διαχωριστούν μεταξύ τους μικρά τμήματα DNA, που διαφέρουν κατά λίγα νουκλεοτίδια, προτιμάται η χρήση πηκτωμάτων ενός άλλου πολυμερούς, της πολυακρυλαμίδης, διαδικασία που θα αναλυθεί σε επόμενη ενότητα. Εικόνα 18: Δομή DNA ( 77
78 Δ.7.2 Υλικά πηκτώματος αγαρόζης Ρυθμιστικό διάλυμα ΤΑΕ (Tris acetate EDTA) συγκέντρωσης 50 Αρχικά, χρειαζόμαστε διάλυμα EDTA (Ethylenediamine tetraacetic acid) συγκέντρωσης 0,5 Μ και ph 8. Για την παρασκευή 500 ml του παραπάνω διαλύματος ζυγίζουμε 93,05 δινάτριο άλας EDTA και το διαλυτοποιούμε σε 400 ml απιονισμένο νερό. Προκειμένου να διαλυτοποιηθεί, το ph πρέπει να προσαρμοστεί στο 8 κι αυτό επιτυγχάνεται με τη χρήση NaOH σε σφαιρίδια (pellet). Ο όγκος προσαρμόζεται στα 500 ml. Για την παρασκευή του 1 λίτρου ΤΑΕ 50x διαλυτοποιούμε 242 g Tris base σε 750 ml απιονισμένο νερό. Εν συνεχεία, προστίθενται - με προσοχή ml 0,5 M EDTA (ph 8,0) και 57,1 ml glacial acetic acid και γίνεται προσαρμογή του όγκου στο 1 L. Το διάλυμα φυλάσσεται σε θερμοκρασία δωματίου. Το διάλυμα ΤΑΕ το οποίο χρησιμοποιείται στο πήκτωμα αγαρόζης έχει τελική συγκέντρωση 1x Αγαρόζη (Molecular Biology Grade) Μάρτυρας 100 bp DNA Ladder (50μg/500ml) της εταιρίας Nippon Genetics Europe GmbH (Εικόνα 19) Εικόνα 19: Ο μάρτυρας μοριακών μεγεθών προστίθεται σε όγκο 3-4 μl και σκοπός του είναι να αποτελέσει σημείο αναφοράς για τον υπολογισμό του μεγέθους και της συγκέντρωσης των δειγμάτων μας. Βρωμιούχο αιθίδιο της εταιρίας Applichem (10 mg/ml) Διάλυμα φόρτωσης (Gel Loading Buffer) 6 Τα διαλύματα φόρτωσης που χρησιμοποιήθηκαν περιείχαν είτε χρωστική Orange G ή μπλε της βρωμοφαινόλης (Bromophenol Blue). 78
79 H σύσταση του διαλύματος φόρτωσης με μπλε της βρωμοφαινόλης (1 ) περιλαμβάνει: 2,5 % Ficoll 400 για αύξηση του ιξώδους (ώστε να καταβυθίζεται στα πηγαδάκια του πηκτώματος), 11 mm EDTA, 3,3 mm Tris-HCl, 0,017% SDS και 0,015% μπλε της βρωμοφαινόλης (ph 8 στους 25ºC). Η χρωστική Orange G ανήκει στην κατηγορία των παραγώγων των διιμιδίων βαφών. Η σύσταση του διαλύματος φόρτωσης Orange G (1x) περιλαμβάνει: 10mM Tris-HCl (ph 7.6), 0.15% orange G, 60% glycerol, 60mM EDTA ή 2ml 50X TAE, 0.15 g Orange G, 60 ml Glycerol και προσαρμογή σε τελικό όγκο 100 ml με νερό MQ (καθαρότητα απεσταγμένου). Η γλυκερόλη φέρει το ρόλο της αύξησης του ιξώδους, όπως και η φαινόλη. Η μετακίνηση των χρωστικών στο πήκτωμα αγαρόζης εξαρτάται από την ποσοστιαία σύσταση του πηκτώματος σε αγαρόζη και από το ρυθμιστικό διάλυμα ηλεκτροφόρησης (Running Buffer) και απεικονίζονται στην Εικόνα 20 και στον Πίνακα 19. Λάμπα υπεριώδους ακτινοβολίας (UV transluminator) Η UV ακτινοβολία έχει καταστροφικές ιδιότητες, καθώς προκαλεί βλάβες κυρίως στον ανθρώπινο αμφιβληστροειδή, το δέρμα και το DNA και για αυτό πρέπει να λαμβάνονται τα κατάλληλα μέτρα προφύλαξης. Η ίδια η συσκευή που χρησιμοποιήθηκε διαθέτει ειδικό πολυμερές προστατευτικό τζάμι (Εικόνα 21). Επίσης ο χρόνος έκθεσης του πηκτώματος πρέπει να μειώνεται στο ελάχιστο, ιδιαίτερα αν θέλουμε να απομονώσουμε το DNA και να το επαναχρησιμοποιήσουμε. Παρατεταμένη έκθεση κατακερματίζει το DNA. Εικόνα 20: Μετανάστευση χρωστικών σε πήκτωμα αγαρόζης 1% Πίνακας 19: Μετακίνηση χρωστικών σε πήκτωμα αγαρόζης. (Protocol Molecular Cell Physiology: Agarose concentration, % Xylene cyanol FF Bromophenol blue Orange G ~4000bp ~300bp ~50bp ~800bp ~100bp ~30bp 79
80 Δ.7.3 Η διαδικασία παρασκευής πηκτώματος αγαρόζης 1% Το πήκτωμα αγαρόζης που συνήθως χρησιμοποιείται στην ηλεκτροφόρηση των PCR προϊόντων έχει περιεκτικότητα 1-2% w/v. Ανάλογα με τον αριθμό των δειγμάτων, παρασκευάζουμε πήκτωμα όγκου 50 ή 100 ml και χρησιμοποιείται καλούπι ανάλογου μεγέθους. Ζυγίζονται 0,5-1 g αγαρόζης και διαλυτοποιούνται υπό θέρμανση σε 50 ή 100 ml ρυθμιστικού διαλύματος ΤΑΕ 1x, αντίστοιχα. Πριν προλάβει να πολυμεριστεί η αγαρόζη, προσθέτουμε 5 ή 10 μl βρωμιούχου αιθιδίου και μεταφέρουμε το υγρό στο καλούπι που θα δώσει την επιδιωκόμενη μορφή λεπτής πλάκας στο πήκτωμα, μετά τον πολυμερισμό. Επίσης, τοποθετούμε σε απόσταση περίπου 1 cm από την άκρη του καλουπιού μία πλαστική «χτένα», κάθετα στο υγρό, βυθισμένη σε αυτό, έτσι ώστε μετά τον πολυμερισμό, να δημιουργηθούν τα κατάλληλα μικρά «πηγαδάκια» στο πήκτωμα, σημεία στα οποία θα τοποθετηθούν τα προς διαχωρισμό δείγματα μας. Αφού πολυμεριστεί, το πήκτωμα εμβαπτίζεται σε διάλυμα TAE 1x (Running buffer). Τα δείγματα τοποθετούνται (φορτώνονται) στα «πηγαδάκια» με μια πιπέτα. Πριν τη φόρτωση, στα δείγματα προστίθεται μικρή ποσότητα loading buffer, το οποίο λόγω της φικόλης ή γλυκερόλης που περιέχει, είναι βαρύτερο του TAE και προκαλεί την επιθυμητή καθίζηση των δειγμάτων στα «πηγαδάκια». Στο αρχικό «πηγαδάκι», προσθέτουμε 4 μl από τον μάρτυρα μοριακών μεγεθών. Στη συνέχεια, με τη βοήθεια κατάλληλου τροφοδοτικού, εφαρμόζουμε ηλεκτρικό πεδίο στα δύο άκρα της δεξαμενής ηλεκτροφόρησης. Η ηλεκτροφορητική συσκευή ρυθμίζεται ανάλογα με τον διαχωρισμό και την ευκρίνεια των ζωνών που χρειαζόμαστε, μεταξύ 70 και 100 Volts (V). Όπως είναι προφανές, όσο λιγότερα τα V, τόσο πιο αργά μετακινούνται τα τμήματα DNA και διαχωρίζονται καλύτερα. Η πολύ μικρή ταχύτητα, ωστόσο, μπορεί να μην αποδώσει το καλύτερο αποτέλεσμα στην ηλεκτροφόρηση. Μετά την πάροδο του επιθυμητού χρόνου ηλεκτροφόρησης, διακόπτεται η παροχή ρεύματος και αφαιρείται προσεκτικά το πήκτωμα από τη συσκευή ηλεκτροφόρησης. Για την παρατήρηση του αποτελέσματος, τοποθετούμε το πήκτωμα πάνω σε λάμπα UV (UV transluminator), όπου μπορούμε να παρατηρήσουμε τα DNA μόρια ως πορτοκαλί ζώνες, λόγω απορρόφησης του βρωμιούχου αιθιδίου (Εικόνα 21). 80
81 προστατευτικό πολυμερές λάμπα ηλεκρική πηγή μπροστά όψη κάτοψη Εικόνα 21: Λάμπα υπεριώδους φωτός (UV transluminator) ( Ιδιαίτερη περίπτωση αποτέλεσε το πήκτωμα αγαρόζης σε ποσοστό 3,5% για την ηλεκτροφόρηση της PCR του εξωνίου 1 στο γονίδιο SPG7. Η σύσταση του πηκτώματος αγαρόζης 3,5% περιλαμβάνει: 60mL TAE 1x (Tris-acetate EDTA) 2,1gr (3,5%) αγαρόζη 8 λ βρωμιούχο αιθίδιο Το πήκτωμα αυτό εμφάνισε δυσκολία κατά την παρασκευή του, καθώς πολυμεριζόταν πολύ γρήγορα και σε υψηλή θερμοκρασία. Το πλεονέκτημα που προσέφερε ήταν ότι έγινε δυνατή η παρατήρηση μιας έλλειψης 25 βάσεων σε προϊόν μεγέθους 207 ζευγών βάσεων, μετά από ηλεκτροφόρηση 7 μl του PCR προϊόντος και 3 μl διαλύματος φόρτωσης για λεπτά στα 80-90V και επακόλουθη έκθεση σε ακτινοβολία UV. 81
82 Δ.8 PCR - ARMS (Amplification Refractory Mutation System) Δ.8.1 Η μέθοδος PCR-ARMS Το 1989 περιγράφηκε μία νέα εφαρμογή της PCR για την ανάλυση γνωστών σημειακών μεταλλάξεων στο DNA και για τη διάκριση μεταξύ γονοτύπων. Η προσέγγιση αυτή, γνωστή ως PCR - ARMS (Amplification Refractory Mutation System Σύστημα Ανίχνευσης Μεταλλάξεων Ανθεκτικών στην Ενίσχυση), περιγράφηκε αναλυτικά στο περιοδικό Current Protocols in Human Genetics (Little 2001). H PCR-ARMS στηρίζεται στο γεγονός ότι μία ασυμφωνία ζευγαρώματος ανάμεσα στο 3 νουκλεοτίδιο ενός εκκινητή της PCR και του DNAστόχου μειώνει ή εμποδίζει την επιμήκυνση του εκκινητή από την Taq πολυμεράση, πιθανότατα αναστέλλοντας την πρόσδεση της πολυμεράσης. Η αντίδραση της PCR έχει μικρή ή και μηδαμινή απόδοση, εάν δεν υπάρχει υβριδοποίηση ανάμεσα στο 3 - τελικό νουκλεοτίδιο του εκκινητή και της αντίστοιχης αλληλουχίας-στόχου. Εκμεταλλευόμαστε την κατά τα άλλα αδυναμία της Taq DNA πολυμεράσης, η οποία στερείται δράσης 3 5 εξωνουκλεάσης και επομένως, δεν μπορεί να επιδιορθώσει τυχόν ασυμφωνίες ζευγαρώματος στο 3 άκρο του εκκινητή. Το γεγονός ότι απαιτείται πλήρης συμπληρωματικότητα στο 3 άκρο του εκκινητή, προκειμένου να επιτευχθεί αποδοτική ενίσχυση, αποτελεί τη βάση της μεθόδου. Η ενίσχυση του φυσιολογικού και όχι του μεταλλαγμένου αλληλομόρφου επιτυγχάνεται με τη χρήση ενός εκκινητή, ο οποίος είναι συμπληρωματικός με το φυσιολογικό αλληλόμορφο και εμφανίζει μια ασυμφωνία ζευγαρώματος με το μεταλλαγμένο αλληλόμορφο στο 3 νουκλεοτίδιο. Αντίστοιχα, θα ενισχυθεί ειδικά το μεταλλαγμένο αλληλόμορφο, εάν το 3 νουκλεοτίδιο του εκκινητή είναι συμπληρωματικό με το μεταλλαγμένο και όχι το φυσιολογικό αλληλόμορφο (Εικόνα 22). Εικόνα 22: Απεικονίζεται η βασική αρχή της PCR ARMS χρησιμοποιώντας το παράδειγμα ενός πρόσθιου εκκινητή, συμπληρωματικού προς το μεταλλαγμένο αλληλόμορφο (πάνω). Παρατηρούμε ότι όταν συναντά ο ίδιος εκκινητής το φυσιολογικό αλληλόμορφο δεν συμβαίνει επιμήκυνση (κάτω) (Patrinos GP, Ansorge W, eds. Molecular Diagnostics 2nd edition, Elsevier/Academic Press, 2009) 82
83 Επομένως, για τη διεξαγωγή μιας PCR - ARMS αντίδρασης σχεδιάζονται τρείς εκκινητές. Ένας αντίστροφος και δύο ευθείς, ή το αντίστροφο. Οι ευθείς εκκινητές είναι ταυτόσημοι μεταξύ τους, με μόνη διαφορά στο 3 τελικό νουκλεοτίδιο τους, το οποίο στη μία περίπτωση είναι συμπληρωματικό με το φυσιολογικό αλληλόμορφο και στην άλλη με το μεταλλαγμένο. Η σχεδίαση τέτοιου είδους εκκινητών ενέχει ιδιαιτερότητες σε σχέση με την κλασική σχεδίαση. Ενδεικτικά, προτείνεται το μέγεθος τους να είναι σχετικά μεγάλο (ιδανικά, ζεύγη βάσεων), να μην έχουν καμία συμπληρωματικότητα στο 3 άκρο, ούτε με άλλους εκκινητές, ούτε με του εαυτούς τους, να φέρουν περίπου κατά 50% περιεχόμενο σε GC και τέλος, να οδηγούν σε ένα σχετικά μικρό προϊόν ζεύγη βάσεων. Ιδιαίτερη προσοχή δίδεται στο είδος της παραλλαγής, δηλαδή ποια βάση αντικαθίσταται από ποια, καθώς δεν δίνουν όλες οι μετατροπές το ίδιο σαφή αποτελέσματα με την παρούσα μέθοδο. Σε περιπτώσεις που οι βάσεις των αλληλομόρφων δεν είναι οι ιδανικές υπάρχει η δυνατότητα στοχευμένης αλλαγής και της 2ης βάσης των εκκινητών, μετρώντας από το 3 άκρο. Επίσης, σημαντική είναι η προετοιμασία της αντίδρασης στον πάγο ή εναλλακτικά, η χρήση Hot start πολυμεράσης, όπως στην περίπτωση μας, για την αποφυγή μη ειδικών προϊόντων. Εικόνα 23: Απεικόνιση από πάνω προς τα κάτω σε σειρά φθίνουσας ισχύος οι ασυμφωνίες των βάσεων. Πάνω βρίσκονται οι πιο ισχυρές ασυμφωνίες μεταξύ του 3 άκρου του εκκινητή και του DNA στόχου, και χαμηλά βλέπουμε όλο και λιγότερο ισχυρές ασυμφωνίες. (Little 2001) Η Εικόνα 23 υποδεικνύει ισχυρές ασυμφωνίες βάσεων μεταξύ εκκινητή και αλληλουχίας προς γονοτύπηση. Κατά την προετοιμασία της PCR, ετοιμάζονται δύο διαφορετικά μίγματα, τα οποία διαφέρουν μόνο ως προς τον έναν εκκινητή που περιέχουν και συγκεκριμένα, αυτόν που περιλαμβάνει τη θέση παραλλαγής. Συνεπώς, η αντίδραση PCR πραγματοποιείται δύο φορές για κάθε δείγμα DNA, προκειμένου να διαπιστωθεί σε ποια από τις δύο περιπτώσεις θα παραχθεί το PCR-προϊόν. Το μίγμα της κάθε αντίδρασης περιλαμβάνει και ένα δεύτερο ζεύγος εκκινητών, οι οποίοι μπορεί να είναι ειδικοί για έναν ετερόλογο ή έναν ομόλογο γενετικό τόπο, η ενίσχυση του οποίου αποτελεί τον θετικό μάρτυρα της αντίδρασης PCR. Τα αποτελέσματα της αντίδρασης ελέγχονται με ηλεκτροφόρηση πηκτώματος αγαρόζης ή πολυακρυλαμίδης. 83
84 Δ.8.2 Το πρωτόκολλο για τον πολυμορφισμό rs του TBC1D1 Ο πολυμορφισμός που μελετήθηκε με την PCR-ARMS είναι ο rs , ο οποίος εντοπίζεται στην εσωνική περιοχή του γονιδίου TBC1D1. Ως θετικός μάρτυρας της αντίδρασης στο πείραμα μας χρησιμοποιήθηκε μια ομόλογη αλληλουχία. Αρχικά, χρησιμοποιήθηκαν οι εκκινητές F και R για τη γονοτύπηση με αλληλούχηση και την εύρεση ενός τουλάχιστον δείγματος με τον κάθε γονότυπο. Το πρωτόκολλο PCR που ακολουθήθηκε σε αυτό το πρώτο στάδιο φαίνεται στον Πίνακα 16 και οι ποσότητες των αντιδραστηρίων ήταν αυτές της συμβατικής PCR (Πίνακας 15). Ακολούθησε καθαρισμός με στήλες (Δ.10.1) και αλληλούχηση κατά Sanger (Δ.11.2) Αφού εντοπίστηκαν οι γονότυποι (ομόζυγος ΑΑ, ομόζυγος CC και ετερόζυγος CT) ξεκίνησε η διαδικασία εύρεσης ενός πρωτοκόλλου κατάλληλου για όλα τα δείγματα DNA. Οι εκκινητές που χρειάστηκαν ήταν ένας συμπληρωματικός προς το αλληλόμορφο με τη μικρότερη συχνότητα Α (ARMS1), ένας συμπληρωματικός προς το αλληλόμορφο C (ARMS2) και o R που αναφέρθηκε προηγουμένως και ο οποίος δουλεύει εξίσου αποτελεσματικά, είτε σε συνδυασμό με τον ARMS1, είτε με τον ARMS2 (Πίνακας 21). Ως ομόλογη αλληλουχία, που λειτουργεί ως θετικός μάρτυρας, επιλέχθηκε η αλληλουχία που παράγεται από τον συνδυασμό του ευθύ αριστερού εκκινητή F και του αντίστροφου R. Σε όλες τις περιπτώσεις, ο R παραμένει κοινός εκκινητής για όλους τους πρόσθιους εκκινητές. Επίσης, απαιτείται να λαμβάνουμε υπόψη κάθε φορά ότι πραγματοποιούνται παράλληλα για καθε δείγμα δύο αντιδράσεις, μία που θα περιέχει τον εκκινητή ARMS1 και μία, τον ARMS2. Επομένως, η στερεοχημεία της αντίδρασης διαμορφώνεται ως εξής (Πίνακας 20). Πίνακας 20: Στερεοχημεία της αντίδρασης PCR-ARMS για τον rs Αντιδραστήρια 1 ης Όγκος (μl) Αντιδραστήρια 2 ης Όγκος (μl) αντίδρασης αντίδρασης H2O (PCR-grade) 7,5 H2O (PCR-grade) 7,5 KAPA2G Fast HotStart 12,5 KAPA2G Fast HotStart 12,5 ReadyMix ReadyMix Ευθής εκκινητής, ARMS 1 1 Ευθής εκκινητής, ARMS 2 1 Ευθύς εκκινητής, θετικός 1 Ευθύς εκκινητής, θετικός 1 μάρτυρας (F) μάρτυρας (F) Κοινός Αντίστροφος 2 Κοινός Αντίστροφος 2 εκκινητής (R) εκκινητής (R) DNA-στόχος 1 DNA-στόχος 1 Τελικός όγκος αντίδρασης 25 Τελικός όγκος αντίδρασης 25 84
85 Και σε αυτήν την περίπτωση, η αντίδραση της PCR πραγματοποιήθηκε με το kit KAPA2G Fast HotStart ReadyMix. Το πρωτόκολλο που ορίστηκε για τον θερμικό κυκλοποιητή παρατίθεται στον Πίνακα 22. Πίνακας 21: Εκκινητές που χρησιμοποιήθηκαν στην ARMS. Γονίδιο Πολυμορφισμός Αλληλουχία εκκινητων 5 3 Μέγεθος προϊόντος (σε bp) TBC1D1 rs (c>a) TGGTAGGGATCTGTGCAGTT(F) AAGTCCTCAAAGTCCAGCCC(R) GGAGGCCTTCCTATGAAGCA(ARMS1) GGAGGCCTTCCTATGAAGCC(ARMS2) 378 Πίνακας 22: Πρωτόκολλο αντίδρασης PCR για το τμήμα που περικλείει τον rs Βήμα Θερμοκρασία Χρόνος (σε λεπτά) 1: Ενεργοποίηση του 95 ο C 2:00 ενζύμου 2:Αποδιάταξη 95 ο C 00:15 3: Υβριδοποίηση (Tm) 63 ο C 00:15 4: Επιμήκυνση 72 ο C 00:01 5: Επανάληψη των βημάτων 2-4 για 34 φορές 6: Τελική επιμήκυνση 72 ο C 00:30 7: Συντήρηση 4 ο C Μετά την ολοκλήρωση της PCR αντίδρασης, ακολούθησε ηλεκτροφόρηση σε πήκτωμα αγαρόζης 2 % με 1 μg/ml βρωμιούχο αιθίδιο. Ηλεκτροφορήθηκαν 5 μl του προϊόντος στα 85V για 40 τουλάχιστον λεπτά σε πηκτώματα μήκους 10 εκατοστών. 85
86 Δ.9 PCR - RFLP (PCR - Restriction Fragment Length Polymorphism) Η τεχνική της PCR-RFLP χρησιμοποιείται για τη γονοτύπηση πολυμορφισμών που εδράζονται στις αλληλουχίες αναγνώρισης περιοριστικών ενδονουκλεασών. Δ.9.1 Αρχή μεθόδου PCR - RFLP Η μέθοδος βασίζεται στην ικανότητα των ενζύμων - περιοριστικές ενδονουκλεάσες (restriction enzymes) - να αναγνωρίζουν συγκεκριμένες δίκλωνες αλληλουχίες DNA, τις θέσεις περιορισμού (restriction sites), και να πέπτουν το μόριο μέσα ή κοντά στην αλληλουχία αναγνώρισης, υδρολύοντας τους φωσφοδιεστερικούς δεσμούς και δημιουργώντας περιοριστικά θραύσματα (restriction fragments). Οι θέσεις περιορισμού είναι ολιγονουκλεοτιδικές αλληλουχίες, μήκους συνήθως 4-8 bp και συχνά, είναι παλίνδρομες. Τα περισσότερα περιοριστικά ένζυμα έχουν απομονωθεί από βακτήρια και η φυσιολογική τους λειτουργία είναι να προστατεύουν από ιικές μολύνσεις, μέσω του συστήματος μετατροπής και μεθυλίωσης. Τα περιοριστικά ένζυμα χρησιμοποιούνται συχνά για τη γονοτύπηση συγκεκριμένων θέσεων μέσω κοψίματος των PCR προϊόντων στη θέση αναγνώρισής τους. Η αλλαγή της αλληλουχίας στο σημείο αναγνώρισης του ενζύμου, όπως για παράδειγμα η αντικατάσταση ή η απαλοιφή μιας βάσης, προκαλεί τον σχηματισμό θραυσμάτων διαφορετικών μεγεθών. Επομένως, σε περιπτώσεις που ένας SNP εντοπίζεται στη θέση περιορισμού μιας ενδονουκλεάσης, η γονοτύπηση για αυτόν τον πολυμορφισμό μπορεί να γίνει με την τεχνική της PCR - RFLP. Η δραστικότητα των περιοριστικών ενδονουκλεασών κατά την εφαρμογή τους επηρεάζεται από ποικίλους παράγοντες, στους οποίους περιλαμβάνονται το ph, η ιοντική συγκέντρωση στο ρυθμιστικό διάλυμα αντίδρασης (buffer) και η θερμοκρασία στην οποία λαμβάνει χώρα η αντίδραση πέψης. Η επιλογή της κατάλληλης θερμοκρασίας είναι αυστηρή, ενώ οι διαφορές στη σύσταση των διαλυμάτων επώασης είναι μικρές. Τα ρυθμιστικά διαλύματα μέσα στα οποία γίνεται η αντίδραση της επώασης περιέχουν συνήθως Mg 2+, που λειτουργεί ως συμπαράγοντας του ενζύμου, καθώς και Na +. Η προσθήκη BSA (αλβουμίνη ορού βοός) στην αντίδραση επώασης προφυλάσσει το ένζυμο από πρωτεάσες και άλλους παράγοντες, ωστόσο, η προσθήκη ή όχι BSA καθορίζεται από το ένζυμο. Οι αναλύσεις γονοτύπησης που γίνονται με PCR-RFLP περιλαμβάνουν τα εξής στάδια: 1. Πολλαπλασιασμός του τμήματος DNA που περικλείει τον πολυμορφισμό με PCR 2. Κατάτμηση των PCR προϊόντων με το κατάλληλο ένζυμο 3. Διαχωρισμός των θραυσμάτων με ηλεκτροφόρηση σε πηκτή αγαρόζης Δ.9.2 Διαδικασία πέψης Στην παρούσα μελέτη, εφαρμόστηκε η μέθοδος PCR - RFLP για τη γονοτύπηση των δειγμάτων DNA ασθενών και υγιών, ως προς τους πολυμορφισμούς: 86
87 rs (C>T) του KAZN με χρήση της περιοριστικής ενδονουκλεάσης AccI της εταιρίας New England Biolabs. rs (C>T) του FAM181B με χρήση της περιοριστικής ενδονουκλεάσης BsrI της εταιρίας New England Biolabs. rs (C>T) του A2LD1 με χρήση της περιοριστικής ενδονουκλεάσης XmnI της εταιρίας New England Biolabs. Η διαδικασία της πέψης λαμβάνει χώρα στον πάγο για τη διατήρηση του ενζύμου ως ανενεργό έως την προσθήκη των λοιπών αντιδραστηρίων και τη ρύθμιση της βέλτιστης θερμοκρασίας για τη δράση του ενζύμου. Τα ένζυμα, συνήθως, διατηρούνται για μεγάλο χρονικό διάστημα, κατά μέσο όρο ένα με δύο χρόνια, στους -20 ο C. O πάγος εξασφαλίζει περαιτέρω ότι το ένζυμο δεν θα καταστραφεί γρήγορα από την επαναλαμβανόμενη ψύξη και απόψυξη. Η στερεοχημεία της αντίδρασης είναι απλή, καθώς περιλαμβάνει το PCR προϊόν, το ένζυμο και το κατάλληλο ρυθμιστικό διάλυμα 1x, ως σταθεροποιητικό παράγοντα. H αποτελεσματικότητα της πέψης, ωστόσο, εξαρτάται από τη συγκέντρωση του PCR προϊόντος και κατά επέκταση της PCR αντίδρασης, τον τελικό όγκο της αντίδρασης, την ποσότητα του ενζύμου (σε Units), τη χρήση κατάλληλου ρυθμιστικού διαλύματος για το εκάστοτε ένζυμο, τη θερμοκρασία και τη διάρκεια της πέψης. Όλα τα ένζυμα που χρησιμοποιήθηκαν στην παρούσα εργασία είναι time saver, δηλαδή απαιτούν λιγότερο χρόνο για την κατάλυση της αντίδρασης (5-15 λεπτά) και δεν εμφανίζουν star activity μετά από 16 ώρες πέψης, γεγονός που σημαίνει ότι δε δίνουν μη ειδικά θραύσματα μετά από παρατεταμένη επώαση. Πριν την χρήση του ενζύμου, σε μεγάλη κλίμακα, απαιτείται η βελτιστοποίηση των συνθηκών με τη χρήση δειγμάτων γνωστών γονοτύπων (Οι γονότυποι εντοπίζονται με τη μέθοδο της αλληλούχησης του PCR προϊόντος, όπως θα περιγραφεί στην ενότητα Δ.10 και Δ.11). Δ.9.3 Αναλυτικά για κάθε πολυμορφισμό rs Για την ανάλυση χρησιμοποιήθηκε το ένζυμο AccI, προερχόμενο από στέλεχος του ανασυνδυασμένου βακτηρίου E. coli, το οποίο μεταφέρει το γονίδιο AccI του Acinetobacter calcoaceticus (R. Roberts). Οι συνθήκες της PCR αντίδρασης για τον πολυμορφισμό rs είναι όμοιες με της συμβατικής PCR. Στον Πίνακα 15 φαίνεται η στερεοχημεία της αντίδρασης και στον 16 τα στάδια του θερμοκυκλοποιητή, με θερμοκρασία υβριδοποίησης τους 57 ο C. Η αλληλουχία αναγνώρισης, καθώς και τα σημεία στα οποία το ένζυμο πέπτει τη δίκλωνη αλυσίδα, φαίνονται στην Εικόνα 24. Το αρχικό προϊόν της αντίδρασης PCR που προκύπτει έχει μήκος 403bp. Παρατηρούμε ότι το C αλληλόμορφο του rs δημιουργεί τη θέση περιορισμού του AccI, με αποτέλεσμα να προκύπτουν 2 θραύσματα, μεγέθους 116 και 287 ζευγών βάσεων, ενώ το Τ αλληλόμορφο καταστρέφει την αλληλουχία αναγνώρισης, με αποτέλεσμα να μην προκύπτει περιοριστικό θραύσμα. 87
88 Οι βέλτιστες συνθήκες που υπολογίστηκαν για το ένζυμο AccI αναγράφονται στον Πίνακα 23. Αρχικά προετοιμάστηκε μίγμα νερού, ρυθμιστικού Cut Smart buffer (Πίνακας 26) και ενζύμου και μοιράστηκε σε σωληνάκια eppendorf χωρητικότητας 1,5 ml, ενώ στη συνέχεια προστέθηκαν τα PCR προϊόντα. Οι συνθήκες της αντίδρασης κατάτμησης επιλέχθηκαν με βάση τη θερμοκρασία μέγιστης ενεργότητας του ενζύμου, δηλαδή τους 37 o C και η επώαση είχε διάρκεια 30 λεπτά. Ο χρόνος επώασης προσδιορίστηκε μετά από δοκιμή των 30 και 60 λεπτών. Εν συνεχεία, το ένζυμο απενεργοποιείται με ψύξη στους -20 ο C. Το πρώτο στάδιο, πραγματοποιήθηκε στο ειδικό όργανο Dry Block Heating Thermostat (Bio TDB-120) της εταιρίας Biosan ή σε συμβατικό υδατόλουτρο με τα ίδια αποτελέσματα. Ακολουθεί ψύξη σε πάγο ώστε να σταματήσει η αντίδραση του ενζύμου και ο διαχωρισμός των προϊόντων της κατάτμησης με ηλεκτροφόρηση σε πήκτωμα αγαρόζης. Τουλάχιστον 15 μl της αντίδρασης με 3 μl loading buffer, ηλεκτροφορούνται σε πηκτή αγαρόζης 2%. Με τη βοήθεια της πηκτής, η οποία περιέχει βρωμιούχο αιθίδιο σε συγκέντρωση 1 μl/ml και μετά την έκθεση αυτής σε ακτινοβολία UV γίνεται η ταυτοποίηση του γονοτύπου, ανάλογα με τον αριθμό των περιοριστικών θραυσμάτων. 5 G T A C A C 3 3 C A T G T G 5 Εικόνα 24: Αλληλουχία που αναγνωρίζει η περιοριστική ενδονουκλεάση AccI. Με βέλη υποδεικνύεται το σημείο κοπής και με κύκλο η βάση που αλλάζει στα αλληλόμορφα. Πίνακας 23: Πρωτόκολλο της αντίδρασης Αντιδραστήριο Όγκος (μl) Απεσταγμένο H2O 16,4 PCR προϊόν 10 NEBuffer 4 (10 ) 3 AccI (10 U/μl) 0,5 Τελικός όγκος 30 αντίδρασης rs Οι συνθήκες της PCR αντίδρασης για τον πολυμορφισμό rs είναι όμοιες με της συμβατικής PCR. Στον Πίνακα 15 φαίνεται η στερεοχημεία και στον Πίνακα 16 τα στάδια του θερμοκυκλοποιητή, με θερμοκρασία υβριδοποίησης 60 ο C. Το αρχικό PCR προϊόν έχει μέγεθος 455bp. Η αλληλουχία αναγνώρισης, 3 TGACCN 5, καθώς και τα σημεία στα οποία το ένζυμο πέπτει τη δίκλωνη αλυσίδα φαίνονται στην Εικόνα 25. Παρατηρούμε ότι το T αλληλόμορφο του rs δημιουργεί τη θέση περιορισμού του BsrI, με αποτέλεσμα να προκύπτουν 2 θραύσματα, μεγέθους, 320 και 134 ζευγών βάσεων, 88
89 ενώ το C αλληλόμορφο καταστρέφει την αλληλουχία αναγνώρισης με αποτέλεσμα να παρατηρούμε μόνο το ακέραιο αρχικό τμήμα. Οι βέλτιστες συνθήκες που υπολογίστηκαν για το ένζυμο BsrI αναγράφονται στον Πίνακα 24. Αρχικά προετοιμάστηκε μίγμα νερού, ρυθμιστικού Neb Buffer 3.1 (Πίνακας 26) και ενζύμου και μοιράστηκε σε σωληνάκια Eppendorf, χωρητικότητας 1,5 ml, ενώ στη συνέχεια προστέθηκαν τα PCR προϊόντα. Οι συνθήκες της αντίδρασης κατάτμησης επιλέχθηκαν με βάση τη θερμοκρασία μέγιστης ενεργότητας του ενζύμου, δηλαδή τους 65 o C και η επώαση είχε διάρκεια 20 λεπτά, όπως προσδιορίστηκε μετά από δοκιμή σε 10, 15, 20 και 30 λεπτά χρόνο επώασης. Εν συνεχεία, το ένζυμο απενεργοποιείται με ψύξη στους -20 ο C. Τo πρώτο στάδιο πραγματοποιήθηκε στο ειδικό όργανο Dry Block Heating Thermostat (Bio TDB-120) της εταιρίας Biosan. Ακολουθεί ο διαχωρισμός των προϊόντων της κατάτμησης με ηλεκτροφόρηση σε πήκτωμα αγαρόζης - τουλάχιστον 10 μl της αντίδρασης και 3 μl loading buffer, ηλεκτροφορούνται σε πηκτή αγαρόζης 1,7%. Με τη βοήθεια της πηκτής, η οποία περιέχει βρωμιούχο αιθίδιο σε συγκέντρωση 1 μl/ml και μετά την έκθεση αυτής σε ακτινοβολία UV, γίνεται η ταυτοποίηση του γονοτύπου, ανάλογα με τον αριθμό των περιοριστικών θραυσμάτων. 5 A C T G G N 3 3 T G A C C N 5 Εικόνα 25: Αλληλουχία που αναγνωρίζει η περιοριστική ενδονουκλεάση BsrI. Με βέλη υποδεικνύεται το σημείο κοπής και με κύκλο η βάση που αλλάζει στα αλληλόμορφα. Πίνακας 24: Πρωτόκολλο της αντίδρασης Αντιδραστήριο Όγκος (μl) Απεσταγμένο H 2 O 3,25 PCR προϊόν 10 NEBuffer 4 (10 ) 1,5 BsrI (10 U/μl) 0,25 Τελικός όγκος 15 αντίδρασης rs Οι συνθήκες της PCR αντίδρασης για τον πολυμορφισμό rs είναι όμοιες με της συμβατικής PCR. Στον Πίνακα 15 φαίνεται η στερεοχημεία και στον Πίνακα 16 τα στάδια του θερμοκυκλοποιητή, με θερμοκρασία υβριδοποίησης 57 ο C. Πραγματοποιήθηκαν 35 κύκλοι της αντίδρασης. Σε περισσότερους κύκλους αντίδρασης (40 45) παρατηρήθηκε ατελής πέψη των προϊόντων, καθώς και με τη χρήση 10 μl του PCR προϊόντος. 89
90 Η αλληλουχία αναγνώρισης, καθώς και τα σημεία στα οποία το ένζυμο πέπτει τη δίκλωνη αλυσίδα, φαίνονται στην Εικόνα 26. Οι βάσεις στην αλληλουχία του προϊόντος είναι: 5 GAACTTGTTC 3. Το αρχικό PCR προϊόν έχει μέγεθος 423 bp. Παρατηρούμε ότι το Τ αλληλόμορφο, του rs , δημιουργεί τη θέση περιορισμού του XmnI, με αποτέλεσμα να προκύπτουν 2 θραύσματα, μεγέθους 163bp και 253bp. Αντιθέτως, το C αλληλόμορφο καταργεί την αλληλουχία αναγνώρισης, με αποτέλεσμα να μην προκύπτει περιοριστικό θραύσμα. Οι βέλτιστες συνθήκες που υπολογίστηκαν για το ένζυμο XmnI αναγράφονται στον Πίνακα 25. Αρχικά προετοιμάστηκε μίγμα νερού, ρυθμιστικού Cut Smart buffer (Πίνακας 26) και ενζύμου και μοιράστηκε σε σωληνάκια Eppendorf, χωριτικότητας 1,5 ml, ενώ στη συνέχεια προστέθηκαν τα PCR προϊόντα. Οι συνθήκες της αντίδρασης κατάτμησης επιλέχθηκαν με βάση τη θερμοκρασία μέγιστης ενεργότητας του ενζύμου, δηλαδή τους 37 o C και η επώαση είχε διάρκεια 30 λεπτά. Εν συνεχεία, το ένζυμο απενεργοποιείται με ψύξη στους -20 ο C. Τo πρώτο στάδιο πραγματοποιήθηκε στο ειδικό όργανο Dry Block Heating Thermostat (Bio TDB- 120) της εταιρίας Biosan ή σε συμβατικό υδατόλουτρο με τα ίδια αποτελέσματα. Ακολουθεί ο διαχωρισμός των προϊόντων της κατάτμησης με ηλεκτροφόρηση σε πήκτωμα αγαρόζης, αφού πρώτα διακοπεί η αντίδραση στους -20 ο C. Τουλάχιστον 20 μl της αντίδρασης ηλεκτροφορούνται σε πηκτή αγαρόζης 2 %. Με τη βοήθεια της πηκτής, η οποία περιέχει βρωμιούχο αιθίδιο σε συγκέντρωση 1 μl/ml και μετά την έκθεση αυτής σε ακτινοβολία UV γίνεται η ταυτοποίηση του γονοτύπου, ανάλογα με τον αριθμό των περιοριστικών θραυσμάτων. 5 G A A C T T G T T C 3 3 C T T G A A C A A G 5 Εικόνα 26: Αλληλουχία που αναγνωρίζει η περιοριστική ενδονουκλεάση XmnI. Με βέλη υποδεικνύεται το σημείο κοπής και με κύκλο η βάση που αλλάζει στα αλληλόμορφα. 90
91 Πίνακας 25: Πρωτόκολλο της αντίδρασης Αντιδραστήριο Όγκος (μl) Απεσταγμένο H 2 O 21,5 Cut Smart buffer 3 (10 ) XmnI (20 U/μl) 0,5 PCR προϊόν 5 Τελικός όγκος 30 αντίδρασης Πίνακας 26: Σύσταση ρυθμιστικών διαλυμάτων των περιοριστικών ενδονουκλεασών CutSmart Buffer NEBuffer mM Potassium Acetate 100 mm NaCl 20mM Tris-acetate 50 mm Tris-HCl 10mM Magnesium Acetate 10 mm MgCl 2 100μg/ml BSA 100 μg/ml BSA ph C ph C Η ηλεκτροφόρηση 5μl PCR προϊόντος σε πήκτωμα αγαρόζης 1% προηγείται της γονοτύπησης με χρήση περιοριστικού ενζύμου για την επιβεβαίωση του αναμενόμενου μεγέθους, καθώς και της συγκέντρωσης. 91
92 Δ.10 Καθαρισμός των προϊόντων της PCR Δ.10.1 Καθαρισμός προϊόντων με στήλες, απευθείας μετά την PCR αντίδραση Για τον καθαρισμό των προϊόντων της PCR από υπολείμματα εκκινητών, δεοξυνουκλεοτιδίων, ενζύμων, ελαίων, αλάτων, μπεταΐνης, απορρυπαντικών και DMSO, χρησιμοποιήσαμε το προτυποποιημένο σύστημα αντιδραστηρίων NucleoSpin Gel and PCR Clean-up της εταιρίας Macherey-Nagel (Εικόνα 27). 1. Αρχικά, προσαρμόστηκε ο όγκος της αντίδρασης στα 50 μl και έγινε ρύθμιση των συνθηκών πρόσδεσης στο DNA προσθέτοντας Buffer NTI. 2. Έπειτα, δεσμεύτηκε το DNA στη στήλη NucleoSpin Gel and PCR Clean-up Column, η οποία είναι μια στήλη silica. Ακολούθησε φυγοκέντρηση στα 11,000 xg για 30 δευτερόλεπτα και απόρριψη του υπερκειμένου. 3. Ακολούθησαν 2 πλύσεις με 700μL Buffer NT3 και φυγοκέντρηση στα 11,000 xg για 30 δευτερόλεπτα μετά από κάθε πλύση. Μετά από κάθε φυγοκέντρηση ακολούθησε απόρριψη του υπερκειμένου. 4. Έπειτα, επαναφυγοκεντρήθηκαν για 1 λεπτό για να απομακρυνθεί τελείως το προστιθέμενο BufferNT3, τοποθετήθηκαν σε καινούριο μικροφυγοκεντρικό σωλήνα συλλογής των 1,7ml και αφέθηκαν για 5 λεπτά στους 70 ο C με ανοιχτά καπάκια για να εξατμιστεί η αιθανόλη που περιέχεται στο BufferΝΤ3. 5. Τέλος, στις NucleoSpin Gel and PCR Clean-up στήλες που συγκρατούν τα δίκλωνα μόρια DNA προστέθηκαν 30 μl ρυθμιστικού έκλουσης, Buffer NE. Στη συνέχεια φυγοκεντρήθηκαν για 1 λεπτό σε 11,000 xg αφού πρώτα επωάστηκαν σε θερμοκρασία δωματίου για 1 λεπτό. Στο σωληνάκι συλλογής παρελήφθησαν τα εκλούσματα, τα οποία διατηρήσαμε στους -20οC μέχρι την ώρα της ανάλυσης με αλληλούχηση. Τα στάδια της φυγοκέντρησης πραγματοποιήθηκαν στην επιτραπέζια φυγόκεντρο Hettich Mikro 120 που διαθέτει ρότορα 24 θέσεων μικροσωληναρίων. Εικόνα 27: Δεξιά, η διαδικασία καθαρισμού με στήλες περιλαμβάνει τα 3 βασικά στάδια που παρουσιάζονται στην εικόνα. 1. Πρόσδεση στη στήλη (Binding), 2. Πλύση (Washing) και 3. Έκλουση (Elution). Υπάρχει δυνατότα καθαρισμού PCR τμημάτων από δύο διαφορετικές πηγές (αριστερή πλευρά της εικόνας), την πηκτή αγαρόζη (arose gel) και το μίγμα τη PCR αντίδρασης. 92
93 Στην παρούσα εργασία, χρησιμοποιήθηκε η παραπάνω μέθοδος κυρίως για τον καθαρισμό των PCR προϊόντων από τα αντιδραστήρια της διαδικασίας, ώστε να γονοτυπηθούν στη συνέχεια με τη διαδικασία της αλληλούχησης κατά Sanger. Επομένως, η παρούσα τεχνική εφαρμόστηκε για τον καθαρισμό όλων των προϊόντων της PCR, ασθενών και υγιών δοτών, για τους πολυμορφισμούς του γονιδίου FTO, για τις παραλλαγές αντικατάστασης στα γονίδια FGF13 και SLC36A1 και για την επιβεβαίωση μιας μετάλλαξης στο πρώτο εξώνιο του γονιδίου SPG7 στους πάσχοντες μίας, μοναδικής, οικογένειας. Δ.10.2 Καθαρισμός προϊόντων της PCR με απομόνωση από το πήκτωμα αγαρόζης και με τη χρήση στηλών Η χρήση του πρωτοκόλλου απομόνωσης έγινε σε τρεις μόνο περιπτώσεις που αφορούσαν τον εντοπισμό της μετάλλαξης στο γονίδιο SPG7 και στο εξώνιο 1 και συγκεκριμένα τα δείγματα των συγγενών. Τα δείγματα αυτά προέρχονταν από συλλογή σιέλου σε σωλήνα και η απομόνωση των προϊόντων της PCR από την πηκτή αγαρόζης κατέστει αναγκαία, λόγω του πλήθους των μη ειδικών ζωνών που ήταν εμφανείς στο πήκτωμα και προέρχονταν από το κατακερματισμένο γενωμικό DNA. Η διαφορά του πρωτοκόλλου απομόνωσης από πήκτωμα έγκειται μόνο στο πρώτο στάδιο της διαδικασίας. Όσον αφορά τη σύγκριση με το πρωτόκολλο καθαρισμού προϊόντων PCR, παραλείπουμε μόνο το βήμα της προσαρμογής του όγκου της αντίδρασης και την απευθείας προσθήκη Buffer NTI, δηλαδή παραλείπετε το 1 ο βήμα και αντικαθίσταται με το παρακάτω: Το βήμα αυτό περιλαμβάνει την ηλεκτροφόρηση όλου του PCR προϊόντος κάθε δείγματος σε πηκτή αγαρόζης 2 %, ώστε να διαχωριστεί το τμήμα που μας ενδιαφέρει και περιέχει το εξώνιο 1 του SPG7 από τα υπόλοιπα μη ειδικά τμήματα. Στη συνέχεια, εμφανίζουμε τις ζώνες της πηκτής με τη βοήθεια του UV transluminator και κόβουμε με νυστέρι τη ζώνη που έχει το σωστό μήκος βάσεων. Έχουμε προζυγίσει ένα σωληνάκι του 1,5 ml και μέσα σε αυτό τοποθετούμε το απομονωμένο κομμάτι της πηκτής που περιέχει το DNA. Ζυγίζουμε το τμήμα της πηκτής που κόψαμε, το οποίο δεν πρέπει να ξεπερνάει 100 mg ανά σωληνάκι. Για κάθε 100 mg πηκτής προσθέτουμε 200μl Buffer NTI και θερμαίνουμε στους 50 ο C σε συσκευή ξηρής θέρμανσης για 5-10 λεπτά, ενώ στο μεσοδιάστημα αναδεύουμε. Όταν η πηκτή έχει διαλυτοποιηθεί πλήρως, συνεχίζουμε με το βήμα 2 και την πρόσδεση του DNA σε στήλες πυριτίου. Δ.10.3 Καθαρισμός PCR προϊόντων με το ένζυμο ExoSAP IT Για τον καθαρισμό των δειγμάτων που γονοτυπήθηκαν με τη μέθοδο αλληλούχησης κατά Sanger στο Κάλιαρι της Ιταλίας, χρησιμοποιήθηκε ένα εναλλακτικό εξίσου αποδοτικό πρωτόκολλο καθαρισμού, αυτό με τη χρήση του ενζύμου ExoSAP-IT For PCR Product Cleanup της εταιρίας Affymetrix. Το αντιδραστήριο ExoSAP-IT αποτελείται από δύο ένζυμα μια εξωνουκλεάση Ι και μια αλκαλική φωσφατάση, ο συνδυασμός των οποίων απομακρύνει την περίσσεια των εκκινητών και τα δεοξυριβονουκλεοτίδια, επιτρέποντας έτσι την περαιτέρω αλληλούχηση των PCR προϊόντων. Η εξωνουκλεάση διασπά τα μονόκλωνα μόρια DNA, καταστρέφοντας, έτσι, την περίσσεια εκκινητών. Η αλκαλική φωσφατάση, από την άλλη, 93
94 υδρολύει τις ελεύθερες φωσφορικές ομάδες από τα δεοξυριβονουκλεοτίδια, προσδίδοντας τους ουδέτερο φορτίο. Το πρωτόκολλο χρήσης είναι πολύ απλό. Το ένζυμο φυλάσσεται στους -20 ο C και υπόκειται στα ίδια προστατευτικά για τα ένζυμα μέτρα, όπως η πολυμεράση και τα περιοριστικά ένζυμα. Πρωτόκολλο ExoSAP-IT 1. 5μl PCR προϊόν αναμιγνύεται με 2μl ExoSAP IT σε καθαρό, στείρο και απαλλαγμένο από DNA και RNA μεμονωμένο σωληνάκι των 200μl ή strip 8 θέσεων των 200μl. 2. Το μίγμα αναδεύεται, φυγοκεντρείται και επωάζεται στου 37 ο C για 15 λεπτά για να αποικοδομηθούν τα νουκλεοτίδια και οι εκκινητές που περίσσεψαν από την αντίδραση. 3. Στη συνέχεια τα δείγματα επωάζονται σε θερμοκρασία 80 ο C για να απενεργοποιηθούν τα ένζυμα. Τα παραπάνω στάδια πραγματοποιήθηκαν σε θερμικό κυκλοποιητή. Τα προϊόντα αποθηκεύονται μακροπρόθεσμα στους -20 ο C. Το ένζυμο δεν επηρεάζει την αντίδραση αλληλούχησης. Το παραπάνω πρωτόκολλο χρησιμοποιήθηκε αποκλειστικά για την επεξεργασία των δειγμάτων Ελλήνων ασθενών και Σαρδηνών ασθενών με ALS στο εργαστήριο Biologia Molecolare, εντός του νοσοκομείου Ospedale Binaghi στο Κάλιαρι της Ιταλίας, για τη γονοτύπηση των πολυμορφισμών του γονιδίου FTO. Δ.10.4 Σύγκριση μεθόδων καθαρισμού Τα τρία πρωτόκολλα απαιτούν συνολικά τον ίδιο χρόνο, μόνο που στην περίπτωση του ενζύμου η προετοιμασία είναι πολύ πιο σύντομη και απλή, δηλαδή πρακτικά μειώνεται αισθητά ο χρόνος εργασίας. Την μεγαλύτερη διάρκεια έχει το πρωτόκολλο απομόνωσης από πήκτωμα, καθώς σε αυτήν συμπεριλαμβάνεται ο χρόνος ηλεκτροφόρησης των προϊόντων, απομόνωσης και διαλυτοποίησης του τμήματος του πηκτώματος που περιέχει το προϊόν. Επιπλέον, η τελευταία μέθοδος δίνει αισθητά μικρότερη συγκέντρωση προϊόντων και δεν προτιμάται. Όλες οι μέθοδοι που περιγράφηκαν δίνουν εξίσου καλά αποτελέσματα κατά την αλληλούχηση. Πριν και μετά τον καθαρισμό των προϊόντων, η ηλεκτροφόρηση 5μl PCR προϊόντος σε πήκτωμα αγαρόζης 1 % μας επιβεβαιώνει ότι τα προϊόντα μας είναι τα αναμενόμενα, απαλλαγμένα από προσμίξεις νουκλεϊκών οξέων και έχουν επαρκή συγκέντρωση. 94
95 Δ.11 Αλληλούχηση κατά Sanger (Sequencing). Η παρούσα μέθοδος έχει ως στόχο τη διευκρίνηση της πρωτοταγούς δομής της νουκλεοτιδικής αλληλουχίας. Η μέθοδος, που επινοήθηκε από τον Sanger (Sanger, Nicklen, and Coulson 1977), στηρίζεται στην ενζυμική δραστηριότητα της πολυμεράσης και στη συμπληρωματικότητα των βάσεων. Περιλαμβάνει τη χρήση νουκλεοτιδικών αναλόγων, των τριφωσφορικών 2', 3' διδεοξυνουκλεοτιδίων (ddntps), τα οποία προκαλούν τον τερματισμό της επιμήκυνσης της αλυσίδας του DNA. Αυτά τα ddntps ενσωματώνονται στην αναπτυσσόμενη αλυσίδα του DNA από την πολυμεράση, μέσω των 5' τριφωσφορικών ομάδων τους, αλλά δεν μπορούν να ενωθούν με το επόμενο τριφωσφορικό δεοξυνουκλεοτίδιο (dntp) που θα έρθει να προστεθεί στην αλυσίδα, επειδή δε διαθέτουν την 3 -ΟΗ ομάδα. Η 3 -ΟΗ ομάδα είναι απαραίτητη για τη δημιουργία φωσφοδιεστερικού δεσμού και επομένως, στο σημείο ενσωμάτωσης ενός ddntp τερματίζεται η επιμύκυνση. Κάθε θραύσμα τερματίζεται μη αντιστρεπτά με την ενσωμάτωση ενός φθορίζοντος επισημασμένου νουκλεοτιδίου, ddntp, στην αλυσίδα διδεοξυ-τερματισμού και κατά αυτόν τον τρόπο, παράγεται μία σειρά θραυσμάτων που διαφέρουν σε μήκος κατά μία βάση και φέρουν ετικέτα φθορισμού βάσης (Εικόνα 28C). Για την εύρεση της αλληλουχίας ενός μορίου πραγματοποιούνται τέσσερις αντιδράσεις, η καθεμία με διαφορετικό ddntp (ddatp, ddgtp, ddctp, ddttp) (Εικόνα 28B). Οι αλυσίδες DNA, που προκύπτουν από κάθε αντίδραση, διαχωρίζονται μεταξύ τους με ηλεκτροφόρηση σε πήκτωμα πολυακρυλαμίδης (Εικόνα 28D) και ανιχνεύονται μέσω αυτοραδιογραφίας, οπότε καθίσταται δυνατή η ανάγνωση της αλληλουχίας στην αρχική εκδοχή της διαδικασίας. Οι Michael Hunkapiller και Leroy Hood (Hunkapiller et al. 1991) ανέπτυξαν μία μέθοδο σήμανσης κάθε ddntp με χρωστική διαφορετικού χρώματος. Έτσι, στις σύγχρονες μεθόδους αλληλούχησης, τα προϊόντα εντοπίζονται συνήθως με ανίχνευση του φθορισμού που εκπέμπουν οι χρωστικές, οι οποίες είναι συζευγμένες με τα ddntp, συνεπώς με τη χρήση διαφορετικής χρωστικής για κάθε ddntp (Εικόνα 29). Η παραπάνω προσθήκη επιτρέπει την ολοκλήρωση της διαδικασίας σε μία μόνο αντίδραση με όλα τα ddntps. Επιπλέον, η ανάλυση μπορεί να γίνει σε μία μόνο στήλη του πηκτώματος. Σήμερα, το κλασικό πήκτωμα πολυακρυλαμιδίου έχει αντικατασταθεί από ηλεκτροφόρηση σε τριχοειδή σωληνάρια (capillary electrophoresis) για την ανάλυση των τμημάτων που παράγονται κατά την αντίδραση αλληλούχησης. Τα τριχοειδή έχουν υψηλή διαχωριστική ικανότητα, με αποτέλεσμα τμήματα με διαφορά μίας μόνο βάσης - ακόμα και σχετικά μεγάλων τμημάτων DNA, μεγαλύτερων και από 700 ζεύγη βάσεων - να εκλούονται από τη στήλη σε διαφορετικό χρόνο. Κάθε τμήμα που εκλούεται, ανιχνεύεται μέσω του φθορισμού του νουκλεοτιδίου λήξης του, αφού διεγερθεί από laser και παρουσιάζεται ως μία κορυφή συγκεκριμένου χρώματος. 95
96 Εικόνα 28: Η τεχνική αλληλούχησης κατά Sanger ( MLAB 2321 Molecular Diagnostics for Clinical Laboratory Science Last Update: Monday, June 23, :59 PM Web Author: Terry Kotrla, MS, MT(ASCP)BB. Εικόνα 29: Κύκλοι της αντίδρασης αλληλούχησης. 96
97 Δ.11.1 Εφαρμογή αλληλούχησης κατά Sanger, Διαδικασία 1 Στα πειράματά μας, για τον προσδιορισμό των γονοτύπων των αλληλομόρφων - για τους πολυμορφισμούς υπό μελέτη - εφαρμόστηκε η ενζυμική μέθοδος αλληλούχησης κατά Sanger σε καθαρισμένα PCR προϊόντα και ακολούθησε ηλεκτροφόρηση σε τριχοειδές. Η ανάλυση έγινε στο εργαστήριο Biologia Molecolare εντός του νοσοκομείου Ospedale Binaghi και υπό την επίβλεψη του του Dr. Sandro Orru, Ricercatore confermato του τμήματος Genetica Medica-Dipartimento di Scienze Mediche που ανήκει στο Πανεπιστήμιο του Κάλιαρι, στην Ιταλία. Χρησιμοποιήθηκε το προτυποποιημένο σύστημα αντιδραστηρίων BigDye Terminator v1.1 Cycle Sequencing kit της εταιρίας Applied Biosystems. Σε αυτό το σύστημα, η αλληλουχία γίνεται με το BigDye Terminator v1.1 το οποίο περιέχει τα dntps και τα ddntps με τις τέσσερις φθορίζουσες χρωστικές, μία για κάθε βάση. Στο μίγμα της αντίδρασης προστίθεται επίσης ρυθμιστικό διάλυμα ΑΒΙ buffer (5x) και τοποθετείται στο θερμοκυκλοποιητή. Το πρωτόκολλο του θερμοκυκλοποιητή παρουσιάζεται στον Πίνακα 28, ενώ στον Πίνακα 27 φαίνεται η σύσταση της αντίδρασης αλληλούχησης και οι ποσότητες ανά αντίδραση. Πριν την ηλεκτροφόρηση στα τριχοειδή, η αλληλουχία που παράχθηκε από την παραπάνω διαδικασία εκπλύθηκε με 30 μl ενέσιμου διαλύματος (injection solution). Αρχικά, συναρμολογείται η αντλία κενού (Εικόνα 30) και εξασφαλίζεται η παροχή ρεύματος. Η πίεση που δημιουργείται από την αντλία, κατά τη λειτουργία της, είναι mmhg. Η διαδικασία αυτή περιλαμβάνει την αραίωση των 10 μl που βρίσκονται στα σωληνάκια των 200 μl της αντίδρασης, προσθέτοντας 30 μl ενέσιμου διαλύματος. Ακολουθεί ανάδευση και μεταφορά όλου του όγκου σε ειδική μεμβράνη που τοποθετείται πάνω στην αντλία. Η αντλία τίθεται σε λειτουργία και το ενέσιμο διάλυμα διέρχεται από τη μεμβράνη, ενώ η αλληλουχία παραμένει πάνω σε αυτή. Η αντλία σβήνει και όταν μειωθεί η πίεση, απομακρύνεται το ενέσιμο διάλυμα, που διήλθε από τη μεμβράνη. Προστίθενται άλλα 30 μl ενέσιμου διαλύματος και επαναλαμβάνεται η διαδικασία. Μετά και τη 2 η πλύση, η αλληλουχία παραμένει πάνω στην μεμβράνη, επαναδιαλύεται σε 20 μl ενέσιμου διαλύματος και μεταφέρεται στην πλάκα 96 πηγαδιών του μηχανήματος. Στη συνέχεια, η πλάκα 96 πηγαδιών φυγοκεντρείται για 4 λεπτά στα 2400 rpm. ΡΥΘΜΙΣΗ ΠΙΕΣΗΣ Διακόπτης κενού ΕΔΩ ΤΟΠΟΘΕΤΕΙΤΑΙ Η ΜΕΜΒΡΑΝΗ mm Hg ΠΙΕΣΟΜΕΤΡΟ ΑΝΤΛΙΑ ΚΕΝΟΥ ΠΑΡΟΧΗ ΡΕΥΜΑΤΟΣ Εικόνα 30: Αντλιά κενού για καθαρισμό της ακολουθίας. 97
98 Ο ηλεκτροφορητικός διαχωρισμός έγινε με τη χρήση ενός πλήρως αυτοματοποιημένου αναλυτή DNA και πραγματοποιείται στη συσκευή 3500 Series Genetic Analyzer της ίδιας εταιρίας, ο οποίος διαθέτει 8 τριχοειδή σε κάθε συστοιχία, μήκους 50 cm το καθένα και laser μονοχρωματικής ακτινοβολίας 505nm και λειτουργεί με πολυμερές POP-7. Πίνακας 27: Αντιδραστήρια αντίδρασης Αλληλούχησης και ποσότητες ανά αντίδραση Αντιδραστήριο Ποσότητα (μl) Big Dye Terminator v.1.1 0,4 ABI Buffer 5x 3,6 Distilled (MilliQ) Η 2 Ο 3,6 Εκκινητής Forward ή Reverse 1,4 2.5μΜ Καθαρισμένο PCR προϊόν 1 Τελικός Όγκος αντίδρασης 10 Πίνακας 28: Θερμοκρασίες αντίδρασης αλληλούχησης (Διαδικασία1) Βήμα Θερμοκρασία Χρόνος (σε λεπτά) 1: Ενεργοποίηση του 96 o C 1:00 ενζύμου 2:Αποδιάταξη 96 ο C 00:10 3: Υβριδοποίηση (Tm) 50 ο C 00:05 4: Επιμήκυνση 60 ο C 04:00 5: Επανάληψη των βημάτων 2-4 για 24 φορές 6: Συντήρηση 4 ο C Η παραπάνω μέθοδος εφαρμόστηκε για την αλληλούχηση των προϊόντων της PCR που συνοψίζονται στον Πίνακα 29: Πίνακας 29: Οι αναγραφόμενοι πολυμορφισμοί εξακριβώθηκαν μετά από αλληλούχηση με τη διαδικασία 1 και τα προϊόντα καθαρίστηκαν με το πρωτόκολλο καθαρισμού με ένζυμο ExoSAP IT. Γονίδιο FTO (δείγματα Ελλήνων και Σαρδηνών ασθενών) Στόχος αλληλούχησης Ταυτόχρονη παρατήρηση των πολυμορφισμών rs (C>T) & rs (G>C) που περιλαμβάνονται σε προϊόν μήκους 396bp και με τη χρήση του ευθύ εκκινητή για την αντίδραση αλληλούχησης. 98
99 Δ.11.2 Εφαρμογή αλληλούχησης κατά Sanger Διαδικασία 2 Τα υλικά για την πραγματοποίηση του πρωτοκόλλου της αντίδρασης αλληλούχησης περιλαμβάνονται στο προτυποποιημένο σύστημα αλληλούχησης της Applied Biosystems, BigDye Terminator v3.1 Cycle Sequencing Kit Protocol, το οποίο αποτελεί διαφορετική έκδοση του συστήματος που χρησιμοποιήθηκε στη διαδικασία 1. Η πολυμεράση, τα dntps και τα ddntps περιλαμβάνονται στο αντιδραστήριο BDT v3.1 reaction mix των 100 αντιδράσεων. Για την αντίδραση απαιτούνται 3,2 pmol εκκινητή, πρόσθιου ή αντίστροφου και ο τελικός όγκος της αντίδρασης είναι τα 10 μl. Ακολουθεί ο πίνακας με τα αντιδραστήρια και τις ποσότητες τους (Πίνακας 30). Τα αντιδραστήρια προστίθενται με τη σειρά που παρουσιάζονται στον πίνακα και στη συνέχεια, ακολουθεί ανάδευση και φυγοκέντρηση. Για λόγους ασφάλειας και οικονομίας αναδεύουμε ελαφρώς και φυγοκεντρούμε τα αντιδραστήρια και πριν τη χρήση. Πίνακας 30: Αντιδραστήρια και ποσότητες για την αντίδραση αλληλούχησης (Διαδικασία 2) Αντιδραστήριο Ποσότητα (µl) dh 2 O 5,5 Seq Buffer (5x) 1,5 BigDye Terminator v3.1 1 Εκκινητής (10μΜ) 1 Καθαρισμένο PCR προϊόν 1 1,5 Τελικός όγκος αντίδρασης 10 Εν γένει, προσέχουμε τη διάρκεια έκθεσης των αντιδραστηρίων BigDye Terminator v3.1 και v1.1 στο φως καθώς είναι φωτοευαίσθητα. Το μείγμα της αντίδρασης, αφού παρασκευάστηκε σε strips 8 θέσεων, χωρητικότητας 200 μl το καθε σωληνάκι, τοποθετήθηκε στον θερμικό κυκλοποιητή και ακολουθήθηκε το παρακάτω πρωτόκολλο (Πίνακας 31). Πίνακας 31: Θερμοκρασίες αντίδρασης αλληλούχησης (Διαδικασία2) Βήμα Θερμοκρασία Χρόνος (σε λεπτά) 1:Αποδιάταξη 96 ο C 00:10 2: Υβριδοποίηση (Tm) 50 ο C 00:10 4: Επιμήκυνση 60 ο C Κυμαίνεται (-0,5οC/κύκλο) 5: Επανάληψη των βημάτων 2-4 για 24 φορές 6: Συντήρηση 15 ο C 99
100 Τη διαδικασία παρασκευής της αλληλουχίας, ακολούθησε o καθαρισμός με στήλες illustra MicroSpin G-50 Columns. Το υλικό των στηλών είναι Sephadex G-50 Grade, εξισορροπημένο σε ρυθμιστικό διάλυμα ΤΕ με 0,05 % Kathon CG/ICP Biocide. Η λειτουργία της στήλης στηρίζεται στην αρχή της χρωματογραφίας. Ο όγκος του δείγματος πρέπει να είναι μl. Το πρωτόκολλο είναι κατάλληλο για οποιοδήποτε προϊόν μεγαλύτερο των 20 bp. Το πρωτόκολλο καθαρισμού έχει ως εξής: 1. Η στήλη πακετάρεται με φυγοκέντρηση για 2 λεπτά στα 1600 xg 2. Έπειτα μεταφέρεται σε καθαρό σωληνάκι φυγοκέντρησης των 1,5 ml 3. Φυγοκεντρείται για 2 λεπτά στα 1300 xg 4. Προστίθενται 50 μl παγωμένης καθαρής αιθανόλης στο μέσο έκλουσης και φυγοκεντρείται η στήλη για 10 λεπτά στα xg 5. Τοποθετούμε τα δείγματα στους 80 ο C, ώστε να εξατμιστούν πλήρως οι διαλύτες και επαναδιαλύουμε σε 20 μl του αντιδραστηρίου Hi-Di Formamide (Applied Biosystem P/(Applied Biosystem P/N ) Η παραπάνω μέθοδος εφαρμόστηκε για την αλληλούχηση των εξής προϊόντων της PCR (Πίνακας 32): Πίνακας 32: Οι αναγραφόμενοι πολυμορφισμοί ή μεταλλάξεις εξακριβώθηκαν μετά από αλληλούχηση με τη διαδικασία 2 και τα προϊόντα καθαρίστηκαν με το πρωτόκολλο καθαρισμού με στήλες με εξαίρεση την έλλειψη στο SPG7, όπου σε κάποια από τα δείγματα χρησιμοποιήθηκε το πρωτόκολλο απομόνωσης από πήκτωμα. Γονίδιο FTO (δείγματα Ελλήνων ασθενών και υγιών και Σαρδηνών υγιών) SLC36A1 FGF13 SPG7 Στόχος αλληλούχησης Ταυτόχρονη παρατήρηση των πολυμορφισμών rs (C>T) & rs (G>C) που περιλαμβάνονται σε προϊόν μήκους 396bp και με τη χρήση του ευθύ εκκινητή για την αντίδραση αλληλούχησης. Για τη γονοτύπηση της αντικατάστασης GCTG/ACGAGTT με αριθμό rs σε προϊόν μήκους 291bp με τη χρήση του ευθύ εκκινητή Για την γονοτύπηση της αντικατάστασης GCT/AGTG που έχει έναρξη στη θέση του χρωμοσώματος X και για την οποία στις βάσεις δεδομένων υπήρχε μόνο μια καταγραφή. Επιπλέον την παρατήρηση της ακολουθίας που περιβάλει την αντικατάσταση. Το προϊόν είχε μήκος 484bp και για την αλληλούχηση χρησιμοποιήθηκε ο αντίστροφος εκκινητής. Επιβεβαίωση έλλειψης 25 βάσεων στο εξώνιο1 του γονιδίου. Το προϊόν είχε μήκος 207bp. Η ανάλυση των αποτελεσμάτων έγινε με το λογισμικό Sequencher 4.8 από την Genes Code. 100
101 Δ.12 Ανάλυση ετεροδιμερών (HDA Heteroduplex analysis) Η ανάλυση ετεροδιμερών ανήκει στις δημοφιλέστερες τεχνικές ανίχνευσης μεταλλάξεων που βασίζονται στην ηλεκτροφόρηση σε πήκτωμα. Η μέθοδος γονοτύπησης περιλαμβάνει τον σχηματισμό ετεροδιμερών και την επακόλουθη ελεκτροφόρηση αυτών σε πήκτωμα. Η HDA στηρίζεται στο γεγονός ότι η δίκλωνη έλικα του DNA δεν είναι ευθύγραμμη και επιπλέον, ακόμα και μικρές παραλλαγές στην έλικα, της τάξεως του ενός ή μερικών νουκλεοτιδίων προκαλούν αλλαγές στη διάταξη του μορίου στο χώρο. Αν λοιπόν προκαλέσουμε την αποδιάταξη του δίκλωνου μορίου και στη συνέχεια, τον επανυβριδισμό των κλώνων το αποτέλεσμα θα είναι το εξής: κάποιοι κλώνοι θα επανυβριδοποιηθούν με τους απόλυτα συμπληρωματικούς τους, δηλαδή θα Εικόνα 31: Ανάλυση ετεροδιμερών. Molecular Diagnostics, 2ndedition, Patrinos GP, Ansorgeeds, 2009 επιστρέψουν στην κατάσταση τους πριν την αποδιάταξη, σχηματίζοντας ομοδιμερή, ενώ άλλοι θα σχηματίσουν ετεροδιμερή. Τα ετεροδιμερή αποτελούνται από δύο κλώνους που είναι όμοιοι, πλην του σημείου της παραλλαγής στο οποίο διαφέρουν, όπου προκαλείται μια κάμψη στην δίκλωνη αλυσίδα, η οποία δεν υπάρχει στα ομοδιμερή. Οι διαμορφωτικές αυτές αλλαγές ανιχνεύονται βάσει της ταχύτητας με την οποία τα μόρια αυτά κινούνται μέσα στο πήκτωμα. Συγκεκριμένα, τα ομοδιμερή θα κινηθούν γρηγορότερα σε σχέση με τα ετεροδιμερή και επομένως, θα παρατηρηθούν πολλαπλές ζώνες (Εικόνα 31). Υπάρχουν δύο ειδών διαμορφωτικές αλλαγές που προκαλούνται από το σχηματισμό ετεροδιμερών. Οι πρώτες αφορούν την αντικατάσταση μίας βάσης που οδηγεί σε ετεροδιμερές τύπου «φούσκας» (bubble type) και οι δεύτερες αφορούν μικρές ελλείψεις ή προσθήκες και οδηγούν σε ετεροδιμερή τύπου «προεξοχής» (bulge type) (Garinis A.G., 2005). Η ανάλυση ετεροδιμερών είναι μια μέθοδος η οποία εύκολα χρησιμοποιείται σε μεγάλο αριθμό δειγμάτων. Για να εφαρμόσουμε τη μέθοδο για τη γονοτύπηση κάποιου SNP ή κάποιας μικρής έλλειψης ή προσθήκης προηγείται ενίσχυση της περιοχής που περιέχει την παραλλαγή με την διαδικασία της PCR και στη συνέχεια, ένας κύκλος αποδιάταξης και η σταδιακή μείωση της θερμοκρασίας θα οδηγήσει στον σχηματισμό των ετεροδιμερών, τα οποία στη συνέχεια ηλεκτροφορούνται σε μη αποδιατακτικό (native) πήκτωμα πολυακρυλαμιδίου 5 10 %, πάχους 0,8 1 mm και τουλάχιστον, 20 cm μήκος. Ακολουθεί χρώση με βρωμιούχο αιθίδιο και η εμφάνιση των ζωνών με έκθεση σε ακτινοβολία UV ή silver stain. Οι παράγοντες που επηρεάζουν την τεχνική είναι το μήκος του PCR προϊόντος, το στάδιο αποδιάταξης και επανυβριδοποίησης των κλώνων, το μήκος του πηκτώματος, η διάρκεια και η ταχύτητα της ηλεκτροφόρησης (δηλαδή η τάση ανά εκατοστό του πηκτώματος, Volts/cm), 101
102 η ιονική ισχύς του διαλύματος ηλεκτροφόρησης, τα συστατικά του πηκτώματος και η ποσοστιαία σύσταση του πηκτώματος σε ακρυλαμίδιο και Ν, Ν'-μεθυλενο-δις-ακρυλαμίδιο. Στην παρούσα εργασία χρησιμοποιήθηκε η συγκεκριμένη μέθοδος για να γονοτυπήθεί μια έλλειψη 7 bp στο γονίδιο A2LD1. Τα πηκτώματα πολυακριλαμιδίου 20 cm, όπως αυτό που χρησιμοποιήθηκε, είχε διακριτική ικανότητα έως 2 % του μήκους του τμήματος που ηλεκτροφορείται και για αυτό, επιλέξαμε εκκινητές με τη χρήση των οποίων προκύπτει μικρό προϊόν (108bp). Χρησιμοποιήσαμε την κλασική στερεοχημεία (Πίνακας 15), που αποφέρει τα καλύτερα αποτελέσματα με το μίγμα της πολυμεράσης που χρησιμοποιούμε. Το πρωτόκολλο της PCR αποτελείται από τα «συνήθη» στάδια, με θερμοκρασία υβριδοποίησης των εκκινητών για τη συγκεκριμένη αντίδραση τους 58 ο C. Ύστερα, είτε ακολούθησαν αμέσως τα στάδια σχηματισμού των ετεροδιμερών, δηλαδή ένα στάδιο αποδιάταξης και έπειτα σταδιακή μείωση της θερμοκρασίας, είτε το προϊόν φυλάχθηκε στους 4 ο C και σε δεύτερο χρόνο (1-2 ημέρες) πραγματοποιήθηκαν τα στάδια της HDA, ώστε να είμαστε σίγουροι για την ακεραιότητα των ετεροδιμερών. Στον ακόλουθο πίνακα καταγράφονται και οι δύο εναλλακτικές διαδικασίες (Πίνακας 33). Οι εκκινητές που χρησιμοποιήθηκαν είναι ο αριστερός, CTAGCGGCAACACCAAGTCT(F) και ο δεξιός, TGCCTAATTCTTCTTCCTCCTC(R). Πίνακας 33: Πρωτόκολλα HDA που χρησιμοποιήθηκαν PCR σε συνδυασμό με HDA PCR συμβατική 1: Ενεργοποίηση του ενζύμου 95 o C 2min 1: Ενεργοποίηση του ενζύμου 95 o C 2min 2:Αποδιάταξη 95 o C 15sec 2:Αποδιάταξη 95 o C 15sec 3: Υβριδοποίηση (Tm) 58 o C 15sec 3: Υβριδοποίηση (Tm) 58 o C 15sec 4: Επιμήκυνση 72 o C 1sec 4: Επιμήκυνση 72 o C 1sec 5: Επανάληψη των βημάτων 2-4 για 34 φορές Go to step 2 For 34 cycles 5: Επανάληψη των βημάτων 2-4 για 34 φορές Go to step 2 For 34 cycles 6: Τελική επιμήκυνση 72 o C 30 sec 6: Τελική επιμήκυνση 72 o C 30 sec 7: Αποδιάταξη προϊόντων PCR 8: Σχηματισμός ετεροδιμερών και ομοδιμερών 94 o C 6min 9: Συντήρηση 4 o C Forever 50 o C 30min Heteroduplex analysis (HDA) * 9: Συντήρηση 4 o C Forever 1: Αποδιάταξη προϊόντων PCR 2: Σχηματισμός ετεροδιμερών και ομοδιμερών 94 o C 6min 50oC 30min 3: Συντήρηση 4oC Forever *HDA: αυτά τα στάδια μπορούν να συνδυαστούν με την pcr, όπως περιγράφεται στον πίνακα αριστερά (πριν την ηλεκτροφόρηση) και κατόπιν την pcr, όπως περιγράφεται δεξιά. 102
103 Στο προϊόν συνυπάρχουν ομοδιμερή και ετεροδιμερή, μόνο στην περίπτωση των ετεροζυγωτών, οι οποίοι φέρουν ένα αλληλόμορφο με την έλλειψη και ένα με την προσθήκη (αλληλουχία αναφοράς), τα οποία ανασυνδυάζονται μεταξύ τους, δημιουργώντας ετεροδιμερή. Η αλληλουχία που απουσιάζει στα αλληλόμορφα με την έλλειψη είναι η 5 TATTTAT.3. Στο σημείο όπου διαφέρουν κατά 7 βάσεις σχηματίζονται δύο ειδών ετεροδιμερή, αυτά που φέρουν την προσθήκη σε κατεύθυνση 5 3 και αυτά που φέρουν την προσθήκη 3 5 (3 ΑΤΑΑΑΤΑ 5 ). Τα ετεροδιμερή αυτά, πιθανώς, λόγω των διαφορετικών βάσεων που περιέχουν, οδηγούν στον σχηματισμό δυο ετεροδιμερών με διαφορετική διαμόρφωση, τα οποία κινούνται με διαφορετική ταχύτητα στο πήκτωμα. Στις περιπτώσεις των ομόζυγων ατόμων, είτε για την έλλειψη, είτε για την προσθήκη παρατηρήθηκε ένα μοναδικό προϊόν. Στην περίπτωση της ομοζυγωτίας, για την έλλειψη το μοναδικό προϊόν κινείτο πιο γρήγορα στο πήκτωμα σε σχέση με το προϊόν που προέκυψε από το άτομο με την προσθήκη και στα δύο αλληλόμορφα. 103
104 Δ.13 Ηλεκτροφόρηση DNA σε πήκτωμα πολυακρυλαμιδίου (PAGE Polyacrylamide Gel Electrophoresis) Δ.13.1 Γενικά για τη μέθοδο ηλεκτροφόρησης DNA σε πήκτωμα πολυακρυλαμιδίου Η πολυακρυλαμίδη είναι ένα σταυρωτά συνδεδεμένο πολυμερές του ακρυλαμιδίου. Το μήκος των αλυσίδων του πολυμερούς καθορίζεται από τη συγκέντρωση του ακρυλαμιδίου που είναι συνήθως 3,5 20 %. Τα πηκτώματα πολυακρυλαμιδίου τοποθετούνται ανάμεσα σε δύο τζάμια που απέχουν μεταξύ τους 0,5-1,5 χιλιοστά, γιατί διαφορετικά το οξυγόνο θα προκαλούσε την αναστολή του πολυμερισμού. Ιδιαίτερη προσοχή πρέπει να δίδεται στο χειρισμό της ακρυλαμίδης, καθώς είναι νευροτοξική. Στον Πίνακα 34, όπως και στην Εικόνα 32, βλέπουμε το εύρος των τμημάτων που είναι δυνατό να αναλυθούν στα διάφορα ποσοστά του πηκτώματος σε ακρυλαμίδιο και αντίστοιχα, σε πηκτώματα αγαρόζης. Η σταυρωτή αντίδραση της ακρυλαμιδίου με το Ν, Ν -μεθυλενο-δις-ακρυλαμίδιο κατά τον πολυμερισμό οδηγεί στο σχηματισμό πορώδους. Ο πολυμερισμός αναστέλλεται από το υπερθειικό αμμώνιο (APS - ammonium persulfate) και καταλύεται από την τετραμεθυλαιθυλενοδιαμίνη (TEMED - N,N,N',N'-Tetramethylethylenediamine). Ανάλογα με το είδος των μορίων που επιθυμούμε να διαχωρίσουμε, χρησιμοποιούμε και την αντίστοιχη αναλογία σε ακρυλαμίδιο προς δις-ακρυλαμίδιο. Πιο ειδικά, για τον διαχωρισμό νουκλεϊκών οξέων ενδείκνυται η αναλογία 19:1, για DNA και πρωτεΐνες προτιμάται η αναλογία 29:1, ενώ χρησιμοποιούμε την αναλογία 37,5:1 αποκλειστικά για πρωτεΐνες. Τα πηκτώματα πολυακρυλαμιδίου έχουν τη δυνατότητα διαχωρισμού τμημάτων DNA τα οποία διαφέρουν έως και 0,2 % σε μήκος, ενώ η διαχωριστική ικανότητα των πηκτωμάτων αγαρόζης φτάνει μόνο το 2 % του μήκους του προϊόντος της PCR ( Τα PCR προϊόντα σε πηκτώματα πολυακρυλαμιδίου είναι προτιμότερο να ηλεκτροφορούνται σε χαμηλή τάση, της τάξεως των 1-8 V/cm ή 20 45mA και ως ρυθμιστικό χρησιμοποιείται ΤΑΕ 1x ή ΤΒΕ 1x (890 mm Tris-base, 89 mm Boric acid, 2 mm EDTA). Πίνακας 34: Ποσοστά του πηκτώματος σε ακρυλαμίδιο ή αγαρόζη ανάλογα με το μήκος του προς ανάλυση τμήματος Agarose Polyacrylamide % Εύρος μεγεθών DNA(kb) % Εύρος μεγεθών DNA (bp) Δ.13.2 Η χρήση της PAGE σε συνδυασμό με HDΑ. Στην παρούσα εργασία, η τεχνική της ηλεκτροφόρησης σε πήκτωμα πολυακρυλαμιδίου χρησιμοποιήθηκε για τον διαχωρισμό των ετεροδιμερών και τον ταυτόχρονο διαχωρισμό 104
105 των ομοδιμερών, του τμήματος που περιέχει την παραλλαγή έλλειψης rs (A2LD1). Η παραλλαγή αυτή αντιστοιχεί στην έλλειψη ή προσθήκη μόνο 7 βάσεων κι έτσι, ιδιαίτερα στην περίπτωση των ομοζυγωτών, από το DNA των οποίων προκύπτουν μόνο ομοδιμερή, είναι απαραίτητη η ηλεκτροφόρηση σε πήκτωμα υψηλής ευαισθησίας ανίχνευσης, όπως είναι το πήκτωμα πολυακρυλαμιδίου. Η ουσιαστικότερη διαφορά τους με τα πηκτώματα αγαρόζης, όσον αφορά την ηλεκτροφόρηση των νουκλεϊκών οξέων, είναι ότι παρέχουν τη δυνατότητα διάκρισης ελλείψεων σε λίγες μόνο βάσεις. Εικόνα 32: Αναλυτικός πίνακας των αναλογιών σε ακρυλαμίδιο / δις-ακρυλαμίδιο (1 η στήλη), των ποσοστών σε ακρυλαμίδιο / δις-ακρυλαμίδιο (2 η στήλη) ανάλογα με το μέγεθος των προϊόντων που επιθυμούμε να ηλεκτροφορήσουμε και την κατάσταση των νουκλεϊκών οξέων, δηλαδή αν είναι αποδιαταγμένα (3 η στήλη) ή μη αποδιαταγμένα (4 η στήλη). (Barril and Nates 2012) Δ.13.3 Στήσιμο της κάθετης συσκευής ηλεκτροφόρησης Μεγάλη προσοχή πρέπει να δίδεται στο χειρισμό των τζαμιών και των χτενακίων, διότι είναι ιδιαίτερα εύθραυστα. Έχουμε το μεγάλο τζάμι και το μικρό. Στην συσκευή μας, το μεγάλο τζάμι διαθέτει ενσωματωμένο «spacer», δηλαδή το διαχωριστικό το οποίο καθορίζει την απόσταση που έχουν τα τζάμια μεταξύ τους και κατά επέκταση, το πάχος του πηκτώματος. Τα spacer που χρησιμοποιήθηκαν ήταν του 1 mm. Τοποθετούμε το μικρό τζάμι πάνω στο μεγάλο. Με τις βίδες στερεώνουμε τα δύο τζάμια στη συσκευή, ώστε το μικρό τζάμι να βρίσκεται στην εσωτερική πλευρά. Προσέχουμε να μη σφίξουμε τις βίδες υπερβολικά και σπάσουμε τα τζάμια. Στη συνέχεια, στερεώνουμε τα τζάμια πάνω στην βάση (caster), όπου θα παρασκευασθεί το πήκτωμα και ταυτοχρόνως, θα οριοθετήσει την κατασκευή μας από το κάτω μέρος και θα 105
106 εμποδίσει το πήκτωμα διαχωρισμού (separating gel) να διαρρεύσει από την κατασκευή, πριν πολυμερισθεί. Σε αυτό το σημείο ελέγχουμε τη στεγανότητα. Δηλαδή, γεμίζουμε το χώρο ανάμεσα στα τζάμια με απιονισμένο νερό και περιμένουμε για μερικά λεπτά να δούμε αν υπάρχουν διαρροές. Στη συνέχεια, αδειάζουμε όλο το νερό και με λίγο χαρτί απορροφάμε όσο νερό έχει μείνει. Δ.13.4 Υλικά και Προετοιμασία πηκτώματος πολυακρυλαμιδίου 8% Η συσκευή που χρησιμοποιήθηκε είναι η omnipage Maxi, 20 x 20cm Dual with Glass Plates της εταιρίας Kisker. Για την προετοιμασία του πηκτώματος χρειαζόμαστε ένα σωληνάκι φυγοκέντρησης των 50 ml για ανάμιξη, τις κατάλληλες πιπέτες, σιφώνια και ακρορύγχια και τη συσκευή έτοιμη πάνω στον «caster», καθώς και τα παρακάτω διαλύματα: TAE 1x TAE 4x 10% APS Το APS 10 % διατηρείται καλύτερα στους -80 ο C κατανεμημένο σε διαλύματα μικρότερου όγκου. 30 % N,N-methyl-bis-acrylamide/ acrylamide (29:1) Χρησιμοποιήθηκε διάλυμα ακρυλαμιδίου / Ν,Ν μεθύλενο-δις-ακρυλαμιδίου 30 % σε αναλογία 29/1. Ζυγίστηκαν 29 gr ακρυλαμίδιο και 1 gr δις-ακρυλαμίδιο και διαλύθηκαν σε 80 ml απεσταγμένο νερό. Για να επιτευχθεί πλήρης διάλυση, το διάλυμα θερμάνθηκε στους 37 ο C και παρέμεινε υπό ανάδευση μέχρι την πλήρη διαλυτοποίηση του. Ο όγκος του προσαρμόστηκε στα 100 ml. Το διάλυμα, διήλθε διαμέσου φίλτρου με μέγεθος πόρων 0,45 μm. Το διάλυμα είναι ευαίσθητο στο φως και μετά την παρασκευή του, πρέπει να φυλάσσεται σε σκοτεινό μπουκάλι. Το ph του πρέπει να είναι μικρότερο του 7. Προσθέτουμε τα αντιδραστήρια με την σειρά που φαίνονται στον Πίνακα 35. Πίνακας 35: Συστατικά του πηκτώματος πολυακρυλαμιδίου 20x20, 8%. Αντιδραστήριο dh2o Ποσότητα 19,6ml 30% N,N-methyl-bis-acrylamide/ acrylamide (29:1) 10,7ml TAE 4x APS 10% (στους -80C) 10,05ml 400μl 106
107 TEMED Τελικός Όγκος μίγματος 40μl 40ml (35 ml + 5 ml επιπλέον) dh2o: απιονισμένο νερό, APS: ammonium persulfate, TEMED: N,N,N',N'-Tetramethylethylenediamine, TAE: Tris acetate EDTA Από τη στιγμή που θα προστεθεί το APS και ιδιαίτερα, όταν προστεθεί και το TEMED έχει ήδη αρχίσει ο πολυμερισμός, οπότε γρήγορα αναδεύουμε, αναποδογυρίζοντας το σωληνάκι φυγοκέντρησης που περιέχει το μίγμα και με ένα σιφώνι των 50 ml μεταφέρουμε το μίγμα ανάμεσα στα τζάμια. Κρατάμε το σιφώνι με κλίση, ώστε το υγρό ακόμα πήκτωμα να πέφτει μέσα από τη σχισμή που δημιουργούν τα δύο τζάμια. Τα αντιδραστήρια προστίθενται με τη σειρά που αναγράφονται. Στη συνέχεια, τοποθετούμε τα κατάλληλα χτενάκια (τα μικρότερα από αυτά που διατίθενται). Μέχρι να αρχίσει να πολυμερίζεται το ακρυλαμίδιο, φροντίζουμε να μην πέσει καθόλου η στάθμη του ανάμεσα στα τζάμια. Προτιμούμε να είναι υπερχειλισμένο για να σχηματιστούν σωστά τα «πηγαδάκια». Επομένως, αν χρειαστεί και αφού επιβεβαιώσουμε ότι δεν υπάρχει διαρροή, γεμίζουμε από το πλάι με την περίσσεια του πηκτώματος διαχωρισμού που βρίσκεται στο σωληνάκι. Το πήκτωμα χρειάζεται περίπου μια ώρα για να πολυμεριστεί πλήρως. Δ Ηλεκτροφόρηση πηκτώματος πολυακρυλαμιδίου Τα βέλτιστα αποτελέσματα έφερε η ηλεκτροφόρηση για 6 τουλάχιστον ώρες στα 75V. Τα 75V, ουσιαστικά, αντιστοιχούν στα 4,5 V/cm για 17 cm που είναι το πραγματικό μήκος του πηκτώματος. To χρησιμοποιημένο running buffer (TAE 1x) μπορεί να επαναχρησιμοποιηθεί έως τρεις φορές και απαιτούνται περίπου 2 L για την πλήρωση της δεξαμενής. Η πλήρωση ξεκινάει από μέσα, δηλαδή εκεί όπου βρίσκεται το πήκτωμα, προς τα έξω ώστε να είμαστε σίγουροι ότι το κάτω και το πάνω εκτεθειμένο μέρος του πηκτώματος βρίσκεται μέσα στο διάλυμα, ώστε να διέρχεται το ρεύμα. Για τη φόρτωση των δειγμάτων στα «πηγαδάκια» του πηκτώματος που σχηματίζονται όταν αφαιρέσουμε τα χτενάκια, απαιτούνται 3 μl loading buffer και 7 μl προϊόντος pcr, το οποίο έχει περάσει και το στάδιο της δημιουργίας ετεροδιμερών (HDA). Η επιλογή του loading buffer θα γίνει στη βάση του ποιο μας εξυπηρετεί στο συγκεκριμένο ποσοστό ακρυλαμιδίου και για το μέγεθος του συγκεκριμένου προϊόντος. Στο πήκτωμα 8 %, το διάλυμα φόρτωσης με χρωστική το μπλε της βρωμοφαινόλης σχηματίζει μέτωπο στα 45 bp. 107
108 Δ.13.6 Χρώση πηκτώματος πολυακρυλαμιδίου. Σε αντίθεση με το πήκτωμα αγαρόζης, στο πήκτωμα πολυακρυλαμιδίου δεν προσθέτουμε το βρωμιούχο αιθίδιο κατά την παρασκευή, αλλά μετά το πέρας της ηλεκτροφόρησης. Για την χρώση του DNA, το πήκτωμα τοποθετείται σε διάλυμα βρωμιούχου αιθιδίου, συγκέντρωσης 1 μg/ml σε ΤΑΕ 1x (περίπου ml) για 15 λεπτά. Το διάλυμα χρωματισμού μπορεί να φυλαχτεί μέσα σε σκούρο μπουκάλι και να επαναχρησιμοποιηθεί. Για την αραίωση χρησιμοποιούμε διάλυμα βρωμιούχου αιθιδίου 0,5 mg/ml. Από το νόμο της αραίωσης CαρχικόVαρχικό = CτελικόVτελικό (όπου C: συγκέντρωση V: όγκος) προκύπτει, 0,5mg/ml. x= 1μg/ml. 150 ml, άρα x=1/500 ml = 0,002 ml = 2μl Περιστασιακά, αναδεύουμε, αργά και προσεκτικά, με κυκλικές κινήσεις. Ο αποχρωματισμός διαρκεί 20 λεπτά σε καθαρό ΤΑΕ 1x (περίπου 150 ml). Όλη η διαδικασία λαμβάνει χώρα σε απαγωγό. Η προσεκτική τήρηση των χρόνων χρώσης και αποχρωματισμού είναι σημαντική για το αποτέλεσμα. Ο αποχρωματισμός εξυπηρετεί στη μείωση του θορύβου στο υπόβαθρο. Αντιθέτως, ο παρατεταμένος αποχρωματισμός μειώνει την ποιότητα των ζωνών στο πήκτωμα. Η παρατεταμένη χρώση οδηγεί σε αυξημένο θόρυβο. 108
109 Δ.14 Mέθοδοι στατιστικής επεξεργασίας των αποτελεσμάτων Ως πρώτο μέλημα κατά τη στατιστική ανάλυση των δεδομένων μας, απαιτείται να διερευνηθεί αν οι υπό μελέτη πληθυσμοί μας για τον γενετικό τόπο που μας ενδαφέρει βρίσκονται σε ισορροπία Hardy Weinberg. Είναι σημαντικό να επικρατούν συνθήκες τυχαίας διασταύρωσης (random mating), αναφορικά με τον υπό μελέτη γενετικό τόπο, διαφορετικά ας πούμε απλοϊκά πως τα δεδομένα μας και η απορρέουσα στατιστική ανάλυση θα είναι «μεροληπτική» (biased). Για το σκοπό αυτό, εφαρμόστηκε η δοκιμασία «chi square goodness of fit». Μόνο στην περίπτωση ικανοποίησης της ισορροπίας Hardy Weinberg, έπεται συνέχεια στη στατιστική ανάλυση των δεδομένων μας, εφαρμόζοντας τον αμφίπλευρο ακριβή έλεγχο του Fisher (two tailed Fisher s exact test), βάσει του μεγέθους των πληθυσμών μας. Η εν λόγω δοκιμασία θεωρείται «δοκιμασία ακρίβειας», διότι η σημαντικότητα της απόκλισης από τη «μηδενική υπόθεση» μπορεί να υπολογιστεί με ακρίβεια. Δ.14.1 Η ισορροπία Hardy-Weinberg Σύμφωνα με τη διατύπωση αυτού του νόμου, σε σχετικά μεγάλους πληθυσμούς όπου δεν υπάρχει ουσιαστικά μετανάστευση, τα ζευγαρώματα θα γίνονται τυχαία απουσία επιλογής και μεταλλαγής και οι συχνότητες των γονιδίων θα παραμένουν οι ίδιες. Η ποικιλομορφία θα μπορούσε να διατηρηθεί κατά τη διάρκεια των γενεών. Ο νόμος αυτός ήταν στην ουσία μια προσπάθεια του μαθηματικού G. Harold Hardy να αποδείξει την παραπάνω θεωρία που πρότειναν γιατροί και βιολόγοι στην αρχή του 19 ου αιώνα και αποτελέι μια προσπάθεια να συνδυαστούν η θεωρία της εξέλιξης του Δαρβίνου, η κληρονομικότητα κατά Mendel και οι σύγχρονες παρατηρήσεις για την εξέλιξη. Στις περιπτώσεις που εξετάζουμε την ισορροπία Hardy-Weinberg ακολουθούμε την εξής διαδικασία. Οι γονοτυπικές συχνότητες κατανέμονται ανάλογα με τις συχνότητες των αλληλομόρφων στον πληθυσμό και παραμένουν σταθερές από γενεά σε γενεά. Έτσι, εάν p είναι η συχνότητα ενός αλληλομόρφου και q η συχνότητα του άλλου, τότε οι συχνότητες των τριών γονοτύπων δίνονται από το ανάπτυγμα του διωνύμου (p+q) 2 = p 2 + 2pq + q 2, όπου p 2 : η συχνότητα εμφάνισης του ενός ομοζυγώτη, 2pq: η συχνότητα εμφάνισης του ετεροζυγώτη και q 2 : η συχνότητα εμφάνισης του έτερου ομοζυγώτη. Ο πληθυσμός p 2 : 2pq : q 2 θεωρείται ότι βρίσκεται σε ισορροπία. Η ισχύς του νόμου ελέγχθηκε με τη στατιστική δοκιμασία «Chi square Goodness of fit». Δ.14.2 Το κριτήριο χ2 Η διερεύνηση της ισχύος του νόμου πραγματοποιήθηκε με τη σύγκριση των παρατηρούμενων γονοτυπικών συχνοτήτων σε σχέση με τις αναμενόμενες υπό τις συνθήκες της ισορροπίας Hardy Weinberg. Το κριτήριο χ2 μας επέτρεψε να εκτιμήσουμε την απόκλιση ανάμεσα στις θεωρητικά αναμενόμενες συχνότητες και στις παρατηρούμενες και εν γένει, εκφράζεται από την εξίσωση: 109
110 χ 2 = Σ(Π-Α) 2 /Α όπου Π: οι παρατηρούμενες τιμές και Α: οι θεωρητικώς αναμενόμενες τιμές. Η τιμή χ2 δίνει για συγκεκριμένους βαθμούς ελευθερίας Β.Ε. (οι οποίοι εκφράζουν κατά πόσους τρόπους μπορεί να μεταβληθεί ένα σύστημα) την πιθανότητα (P) συμφωνίας των θεωρητικά αναμενόμενων τιμών με τις τιμές που παρατηρήθηκαν. Στην παρούσα εργασία, ορίστηκε ως επίπεδο σημαντικότητας το 5 % (όρια εμπιστοσύνης 95 %). Πιθανότητα μεγαλύτερη του επιπέδου σημαντικότητας σημαίνει συμφωνία, δηλαδή στην πράξη, τα αποτελέσματά μας δεν παρουσιάζουν στατιστικώς σημαντική διαφορά (η μηδενική υπόθεση είναι αποδεκτή - ο πληθυσμός για τον συγκεκριμένο γενετικό τόπο είναι σε ισορροπία Hardy Weinberg). Αντίθετα, όταν η τιμή p που υπολογίζουμε είναι μικρότερη του επιπέδου σημαντικότητας 0,05, αυτό σημαίνει πως υπάρχει στατιστικώς σημαντική διαφορά μεταξύ των θεωρητικών και πραγματικών τιμών (η μηδενική υπόθεση δεν γίνεται αποδεκτή). Αναφορικά με τον υπολογισμό των βαθμών ελευθερίας (d.f), αυτοί δίδονται από τη μαθηματική σχέση: d.f = k 1 m όπου k: ο αριθμός των τάξεων και m: ο αριθμός των ανεξάρτητων μεταβλητών. Για ένα σύστημα δυο αλληλομόρφων υπάρχουν τρεις τάξεις και μια ανεξάρτητη μεταβλητή και συνεπώς, έχουμε έναν βαθμό ελευθερίας. Η τιμή του κριτηρίου χ2 προκύπτει από το άθροισμα των επιμέρους τετραγώνων για κάθε τάξη, δηλαδή κάθε γονότυπο. Με βάση τον ακόλουθο μερικό πίνακα του κριτηρίου χ2 για τις κριτικές τιμές (upper tail), η κριτική τιμή που θα καθορίσει την αποδοχή ή την απόρριψη της μηδενικής μας υπόθεσης είναι ίση του (Πίνακας 36). Πίνακας 36: Πίνακας κρίσιμων τιμών του κριτηρίου χ 2 (upper tail) o d.f
111 Δ.14.3 Αμφίπλευρος ακριβής έλεγχος του Fisher Ο αμφίπλευρος ακριβής έλεγχος του Fisher (Fisher s exact test) είναι ένας μη παραμετρικός έλεγχος, ανεξαρτησίας και ομοιογένειας. Χρησιμοποιείται για την ανάλυση διακριτών δεδομένων, όταν τα δυο ανεξάρτητα δείγματα έχουν μικρό μέγεθος. Tα αποτελέσµατα αυτών των δειγµάτων αντιστοιχούν στη µια από τις δύο τυχαίες κατηγορίες και κάθε στοιχείο αυτών είναι δυνατό να έχει το ένα από τα δύο χαρακτηριστικά. Έστω n1, n2 δυο ανεξάρτητα τυχαία δείγµατα µε N = n1 + n2. Ο έλεγχος δεν εξετάζει µόνο την παρατηρούµενη περίπτωση, αλλά υπολογίζει την πιθανότητα πιο ακραίων περιπτώσεων µε τα ίδια περιθώρια αθροίσµατα. Έτσι, η τιμή p υπολογίζεται µε το άθροισµα των πιθανοτήτων όλων των ακραίων περιπτώσεων και του πίνακα της εικόνας 33 (στην παρούσα ανάλυση, της μορφής 3 x 2): Εικόνα 33: Υπόδειγμα εισαγωγής συχνοτήτων για την πραγματοποίηση αμφίπλευρου ακριβή ελέγχου του Fisher, επέκταση 2x3. Παρατηρήσεις (Observation), δηλαδή κατηγορία γονότυπου, στον άξονα του Υ και πληθυσμιακή κατηγορίας δείγματος (Group) στον άξονα του Χ. Ο εν λόγω έλεγχος είναι ιδανικός στις περιπτώσεις που στον πίνακα ενδεχοµένων έχουµε πολύ µικρά µεγέθη (δηλαδή έχω αριθµό µικρότερο του 5). Με τη χρήση του λαµβάνουµε μια πιο ακριβή τιμή p, αν και χαρακτηρίζεται από πιο πολύπλοκους υπολογισμούς, συγκριτικά με το κριτήριο χ 2 (το οποίο καταλήγει σε μια µόνο προσεγγιστική τιμή p). Οι υπολογισμοί έγιναν κάνοντας χρήση της πλατφόρμας in-silico.net ( Η μηδενική υπόθεση, εδώ, είναι ότι δεν υπάρχει συσχέτιση μεταξύ Χ και Υ, δηλαδή πληθυσμιακής κατηγορίας δείγματος και γονοτύπων. Το ερώτημα που ερευνούμε για την στατιστική του σημασία είναι συνεπώς το ακόλουθο: Αν η μηδενική υπόθεση ήταν αληθής και επομένως, οποιαδήποτε σχέση μεταξύ των χαρακτηριστικών Χ και Υ οφείλετο στην τύχη και μόνο, πόσο πιθανό είναι ότι θα καταλήξουμε σε ένα αποτέλεσμα, όπου εμπεριέχονται οι μεγαλύτερες δυνατές τιμές που μπορεί να παίρνουμε, αν καταγράφαμε όλους τους συνδυασμούς που οδηγούν στο 111
112 άθροισμα των δειγμάτων μας (δηλαδή, αν αθροίσουμε κάθε στήλη (Χ) και κάθε σειρά (Υ) και χρησιμοποιήσουμε αυτές τις τιμές ως όρια της στήλης και της σειράς, αντίστοιχα). Στην παρούσα εργασία εξετάσαμε τις συχνότητες των αλληλομόρφων και γονοτύπων ασθενών, αντιπαραθέτωντας τες, με τις αντίστοιχες συχνότητες σε υγιείς. Αναφορικά με τα αλληλόμορφα, χρησιμοποιήσαμε την συμβατική πλατφόρμα της ακριβούς δοκιμασίας του Fisher, δηλαδή εισάγαμε τα δεδομένα μας σε πίνακα 2x2. Στην περίπτωση των γονοτύπων, καταφύγαμε στην επέκταση του αμφίπλευρου ακριβή έλεγχου του Fisher, 2x3, εκτελώντας μια επέκταση Freeman-Halton της εν λόγω δοκιμασίας πιθανοτήτων, σε πίνακα με δύο γραμμές και τρεις στήλες. 112
113 Ε. ΑΠΟΤΕΛΕΣΜΑΤΑ 113
114 Ε.1 Αποτελέσματα γονοτύπησης ασθενών και υγιών για τους πολυμορφισμούς που επιλέγχθηκαν από την 1η προσέγγιση του WGS. Ε.1.1 Γονίδιο Α2LD1, πολυμορφισμός rs Ο πολυμορφισμός rs αντιστοιχεί στην έλλειψη της ακολουθίας ΤΑΤΤΤΑΤ από την 3 UTR του γονιδίου Α2LD1 (GGACT) και εντοπίζεται στις θέσεις 13: του χρωμοσώματος 13. Η γονοτυπική ανάλυση πραγματοποιήθηκε σε δείγματα 18 ασθενών ALS και 24 υγιών ελληνικής καταγωγής. Οι υγιείς που γονοτυπήθηκαν αποτέλεσαν τον πληθυσμό αναφοράς. Επιπλέον, για τον συγκεκριμένο πολυμορφισμό δεν βρέθηκαν δεδομένα συχνοτήτων στη βάση δεδομένων Ensembl, οπότε τα δείγματα που γονοτυπήσαμε αποτελούσαν και τη μοναδική μας ένδειξη για τις συχνότητες του συγκεκριμένου πολυμορφισμού στον ελληνικό πληθυσμό. Για την γονοτύπηση ακολουθήθηκε η μέθοδος HDA με συνδυασμό ηλεκτροφόρησης σε πήκτωμα πολυακριμιδίου 8%, όπως φαίνεται στην Εικόνα 34 και 35. Εικόνα 34: Ασπρόμαυρη άποψη του πηκτώματος πολυακρυλαμιδίου 8%. Απεικονίζονται δείγματα αθενών, ενισχυμένα με PCR HDA για τον πολυμορφσμό rs Τα δείγματα που βρίσκονται στις θέσεις 1, 3, 5, 6, 7, 8 και 9 ανήκουν σε άτομα ετερόζυγα ως προς την έλλειψη, δηλαδή διαθέτουν τον γονότυπο ΤΑΤΤΤΑΤ/-. Αντιθέτως τα δείγματα που βρίσκονται στις θέσεις 2 και 4 αντιστοιχούν σε άτομα ομόζυγα για την έλλειψη, δηλαδή διαθέτουν γονότυπο -/-. Σε συνεργασία με την Ελένη Νταλαμπύρα. 114
115 Εικόνα 35: Πήκτωμα πολυακρυλαμιδίου 8% με χρώση σε 1μg/ml EtBr μετά από ηλεκτροφόρηση 6 ωρών στα 75V. Απεικονίζονται δείγματα υγιών, όπου εφαρμόστηκε η μέθοδος PCR HDA, για τον πολυμορφσμό rs Τα δείγματα που βρίσκονται στις θέσεις 1, 2, 5, 6 και 7 ανήκουν σε άτομα με γονότυπο ΤΑΤΤΤΑΤ/-, τα δείγματα 3 και 4 ανήκουν σε άτομα ομόζυγα για την προςσθήκη, δηλαδή διαθέτουν γονότυπο ΤΑΤΤΤΑΤ/ΤΑΤΤΤΑΤ και στη θέση 8 το προϊόν αντιστοιχεί σε γονότυπο -/-. Σε συνεργασία με την Ειρήνη Πατμετζή και Μύριαμ Παπαναούμ. Οι συχνότητες της έλλειψης σε ασθενείς και υγιείς φαίνεται στον πίνακα που ακολουθεί (Πίνακας 37): Πίνακας 37: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό. Ελληνικός πληθυσμός Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) in/in, in/del, del/del in del Υγιείς Ασθενείς In (insertion): προσθήκη, del (deletion): έλλειψη Οι πληθυσμοί των υγιών και των ασθενών βρίσκονται σε ισορροπία Hardy Weinberg για τον εν λόγω γενετικό τόπο, επομένως, ακολούθως εφαρμόσαμε την ακριβή δοκιμασία του Fisher. Από τη στατιστική δοκιμασία που πραγματοποιήσαμε για τα δεδομένα του πίνακα 37, προέκυψε πως σε επίπεδο συχνοτήτων των γονοτύπων, η τιμή πιθανότητας (p) ισούται με 0,36 (όρια εμπιστοσύνης 95%) και σε επίπεδο συχνοτήτων των αλληλομόρφων η τιμή p ισούται με 0,89 (όρια εμπιστοσύνης 95%). Συμπερασματικά, από τις τιμές p που λάβαμε καταλαβαίνουμε ότι δεν υπάρχει στατιστικά σημαντική διαφορά ούτε σε επίπεδο αλληλομόρφων, αλλά ούτε σε επίπεδο γονοτύπων, μεταξύ των δύο πληθυσμών για τον SNP υπό μελέτη. 115
116 Ε.1.2 Γονίδιο TBC1D1, πολυμορφισμός rs Για τη γονοτύπηση του συγκεκριμένου πολυμορφισμού χρησιμοποιήθηκε η μέθοδος PCR ARMS. Εκτελέστηκαν δύο αντιδράσεις PCR για κάθε ένα από τα 27 δείγματα Ελλήνων ασθενών και τα 40 δείγματα Ελλήνων υγιών. Στην πρώτη αντίδραση χρησιμοποιήθηκε ο εκκινητής ARMS1 ως ειδικός για τη θέση του πολυμορφισμού και στη δεύτερη ο ARMS2. Οι δύο εκκινητές είναι πρόσθιοι. Ο ARMS1 φέρει στο 3 άκρο της μονόκλωνης αλυσίδας του, τη βάση Α και επομένως είναι συμπληρωματικός προς το αλληλόμορφο Τ, ενώ ο ARMS2 φέρει ως τελευταία βάση τη βάση C και επομένως είναι συμπληρωματικός προς το αλληλόμορφο G. Τα προϊόντα των αντιδράσεων ηλεκτροφορήθηκαν σε πήκτωμα αγαρόζης 1,2% (Εικόνα 36). Εικόνα 36: Απεικονίζεται πήκτωμα αγαρόζης 1,2%, όπου φαίνονται οι γονότυποι 15 υγιών για τον πολυμορφισμό rs Στο πάνω μέρος της εικόνας βλέπουμε τις αντιδράσεις που έγιναν με τον εκκινητή ARMS1 και στο κάτω μέρος τις αντιδράσεις που πραγματοποιήθηκαν για τα ίδια δείγματα με τον εκκινητή ARMS2. Στο τέλος κάθε σειράς υπάρχει Μάρτυρας μοριακών μεγεθών των 100bp. Κάθε κάθετη διαδρομή αντιστοιχεί στο ίδιο δείγμα. Τα άτομα 30, 36, 39 και είναι C/C ομόζυγα, τα 31 και 45 είναι Α/Α ομόζυγα και τα υπόλοιπα C/A ετερόζυγα. ΑΕ: Αρνητικός έλεγχος (τυφλό). Σε συνεργασία με την Meneka Rupasinghe. 116
117 Στις θέσεις όπου απεικονίζεται μόνο μία ζώνη, αυτή αντιστοιχεί στον θετικό έλεγχο της αντίδρασης, γεγονός που σημαίνει ότι δεν υπάρχει ειδικός πολλαπλασιασμός του αλληλομόρφου που εξετάζεται, δηλαδή το Α για την αντίδραση που περιέχει τον εκκινητή ARMS1 και το C για την αντίδραση που περιέχει τον ARMS2. Στις περιπτώσεις, όπου απεικονίζονται 3 ζώνες ανά θέση, η μεσαία, έντονη ζώνη αντιστοιχεί στον ομόλογο θετικό έλεγχο και η τρίτη από πάνω, στον ειδικό πολλαπλασιασμό με πρόσθιο εκκινητή ARMS1 ή ARMS2. Η ζώνη που βρίσκεται πάνω από τις άλλες δύο, το πιθανότερο είναι να αντιστοιχεί σε κάποια αλληλεπίδραση μεταξύ των δύο προϊόντων (ίσως κάποιο ετεροδιμερές), έχοντας αποκλείσει την ύπαρξη παραπροϊόντων. Σύμφωνα με το Chi Square Goodness-of-Fit Test τα δεδομένα μας τηρούν το κριτήριο Hardy Weinberg, τόσο στο δείγμα των ασθενών (C^2= 0,579) όσο και στο δείγμα των υγιών (C^2=1,407). Πίνακας 38: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό. Ελληνικός πληθυσμός Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) C/C C/A A/A C A* Υγιείς Ασθενείς *Το αλληλόμορφο με τη μικρότερη συχνότητα στο γενικό πληθυσμό και στους κεντρο - ευρωπαίους. Επομένως, ακολούθησε η στατιστική σύγκριση των συχνοτήτων των γονοτύπων και των αλληλομόρφων, 27 ασθενών και των 40 υγιών, ελληνικής καταγωγής (Πίνακας 38). Η στατιστική ανάλυση έδωσε το εξής αποτέλεσμα: η κρίσιμη τιμή σημαντικότητας p ισούται με 0,39 σε επίπεδο συχνοτήτων των αλληλομόρφων, πράγμα που σημαίνει ότι οι συχνότητες τους δεν διαφέρουν σημαντικά ανάμεσα στους δύο πληθυσμούς (υγιείς και ασθενείς). Αντιθέτως, όσον αφορά τις συχνότητες των γονοτύπων το p παίρνει τιμή 0,033, γεγονός που υποδηλώνει στατιστική σημαντικότητα, καθώς η τιμή p είναι μικρότερη του 0,05. Τα παραπάνω ευρήματα, μας προτρέπουν να εξετάσουμε τον πολυμορφισμό rs και σε έναν ακόμα πληθυσμό, αυτόν των Σαρδηνών. Μετά από γονοτύπηση με την ίδια μέθοδο 29 ασθενών ALS και 28 υγιών, οι οποίοι κατάγονται από τη Σαρδηνία καταλήξαμε στις ακόλουθες συχνότητες (Πίνακας 39): 117
118 Πίνακας 39: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών με καταγωγή από τη Σαρδηνία, της Ιταλίας. Σαρδηνοί Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) C/C C/A A/A C A* Υγιείς Ασθενείς *Το αλληλόμορφο με τη μικρότερη συχνότητα στο γενικό πληθυσμό και στους κεντρο - ευρωπαίους. Τα αποτελέσματα της στατιστικής ανάλυσης δεν έδειξαν καμία στατιστικά σημαντική διαφορά μεταξύ υγιών και αθενών με καταγωγή από την Σαρδηνία για τον εν λόγω SNP, ούτε για τις συχνότητες αλληλομόρφων (p=0,46) αλλά ούτε και για τις συχνότητες γονοτύπων (p=0,43). Ε.1.3 Αποτελέσματα πέψης με περιοριστικά ένζυμα. Η διαδικασία της πέψης με περιοριστικά ένζυμα, με σκοπό τη γονοτύπηση, ακολουθεί την αντίδραση PCR, που στοχεύει την ενίσχυση του τμήματος που περιέχει τον πολυμορφισμό. Κατά αυτόν τον τρόπο είναι δυνατό να διαπιστωθεί εάν η αντίδραση είναι απαλλαγμένη παραπροιόντων και επιμολύνσεων, τα οποία μπορεί να επηρεάσουν το τελικό αποτέλεσμα. Τα προϊόντα της PCR, πριν από κάθε πέψη με ένζυμο περιορισμού ηλεκτροφορήθηκαν σε πήκτωμα αγαρόζης 1%. Ως παράδειγμα, παρατίθεται η εικόνα της PCR, η οποία αποσκοπούσε σε ενίσχυση του τμήματος που περιβάλει τον πολυμορφισμό rs (Εικόνα 37). Εικόνα 37: Πήκτωμα αγαρόζης 1%. Οι ζώνες αντιστοιχούν σε PCR προϊόντα τμημάτων που περικλείουν τον πολυρφισμό rs , προέρχονται από 27 δείγματα ασθενών και 20 δείγματα υγιών. 118
119 Ε Γονίδιο A2LD1, πολυμορφισμός rs (C>T). Η διερεύνηση του πολυμορφισμού rs έγινε δυνατή με τη χρήση του ενζύμου XmnI. Χρησιμοποιήθηκαν 27 δείγματα ασθενών και 27 δείγματα υγιών, ελληνικής καταγωγής. Στις εικόνες 38 και 39 απεικονίζονται πηκτώματα όπου ηλεκτροφορήθηκαν προϊόντα πέψης με το ένζυμο XmnI και από τα οποία μπορούμε να συμεράνουμε τους γονοτύπου των δειγμάτων για τον πολυμορφισμό rs Στην εικόνα 38 τα δείγματα που χρησιμοποιήθηκαν αντιστοιχούν αποκλειστικά σε ασθενείς και στην εικόνα 39 σε υγιείς. A B Εικόνα 38: Πήκτωμα αγαρόζης, όπου παρουσιάζονται τα αποτελέσματα γονοτύπησης του rs , σε ασθενείς. Στο A μέρος του πηκτώματος και στις θέσεις 1, 10, 11, 12 όπως και στις θέσεις 4, 5, 9 και 11 στο B μέρος, βλέπουμε την εικόνα των C/C ομοζυγοτών. Στις θέσεις 2 και 4 της εικόνας A και στις θέσεις 1, 3, 10 και 12 της εικόνας Β, βλέπουμε την εικόνα των Τ/Τ ομοζυγοτών. Στις υπόλοιπες θέσεις, δηλαδή 3, 5 9 και της Α, καθώς επίσης και στις θέσεις 2, 5, 6 και 7 της Β, βλέπουμε την εικόνα που παρουσιάζουν στο πήκτωμα οι ετεροζυγώτες (C/T). Η θέση Β11 αντιστοιχεί σε PCR προϊόν, στο οποίο ωστόσο δεν χρησιμοποιήθηκε ένζυμο και λειτουργεί ως αρνητικός έλεγχος. Στη θέση Β12 χρησιμοποιήσαμε δείγμα γνωστού γονοτύπου, Τ/Τ, ως θετικό έλεγχο της αντίδρασης. 119
120 Εικόνα 39: Πήκτωμα αγαρόζης όπου παρουσιάζονται τα αποτελέσματα γονοτύπησης του rs , σε υγιείς. Όπως και προηγουμένως οι 3 ζώνες αντιστοιχούν σε ετεροζυγώτες C/T, οι δύο ζώνες σε ομοζυγώτες Τ/Τ, όπου έχει επέλθει πλήρης πέψη με το XmnI και όπου βλέπουμε μία ζώνη, αυτή αντιστοιχεί σε ομοζυγώττη C/C. Η τελευταία θέση αντιστοιχεί σε PCR προϊόν, στο οποίο ωστόσο δεν χρησιμοποιήθηκε ένζυμο και λειτουργεί ως αρνητικός έλεγχος. Στην προ - τελευταία θέση χρησιμοποιήσαμε δείγμα γνωστού γονοτύπου, Τ/Τ, ως θετικό έλεγχο της αντίδρασης. Σύμφωνα με το Chi Square Goodness-of-Fit Test, οι πληθυσμοί μας πληρούν το κριτήριο Hardy Weinberg, τόσο στο δείγμα των ασθενών (C^2= 1,053) όσο και στο δείγμα των υγιών (C^2= 0,338). Πίνακας 40: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό. Ελληνικός πληθυσμός Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) C/C C/Τ Τ/Τ C Τ* Υγιείς Ασθενείς *Το αλληλόμορφο με τη μικρότερη συχνότητα στο γενικό πληθυσμό και στους κεντρο - ευρωπαίους. Η στατιστική ανάλυση των συχνοτήτων του πίνακα 40, έδωσε τις ακόλουθες παρατηρούμενες τιμές σημαντικότητας (p). Για τα αλληλόμορφα, η τιμή p ισούται με 0,39, ενώ για τους γονοτύπους με 0,22. Στις δύο περιπτώσεις οι τιμες p δεν υποδεικνύουν σημαντικές διαφορές ανάμεσα στο δείγμα των υγιών και το δείγμα των ασθενών, όσον αφορά τον rs Ε Γονίδιο ΚΑΖΝ, πολυμορφισμός rs (C>T). Με τη χρήση περιοριστικής ενδονουκλεάσης AccI, πραγματοποιήθηκε η γονοτύπηση του πολυμορφισμού rs Γονοτυπήθηκαν 27 ασθενείς και 38 υγιείς και σε αυτή την περίπτωση τα δείγματα άνηκαν στον ελληνικό πληθυσμό. Οι συχνότητες που προέκυψαν καταγράφονται στον πίνακα 41, που ακολουθεί: 120
121 Πίνακας 41: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό. Ελληνικός πληθυσμός Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) C/C C/Τ Τ/Τ C Τ* Υγιείς Ασθενείς *Το αλληλόμορφο με τη μικρότερη συχνότητα στο γενικό πληθυσμό και στους κεντρο - ευρωπαίους. Στην εικόνα 40, παρουσιάζεται ένα χαρακτηριστικό δείγμα της μορφής με την οποία λάβαμε τα αποτελέσματα. Εικόνα 40: Εικόνα πέψης σε πήκτωμα αγαρόζης, του πολυμορφισμού rs , με την περιοριστική ενδονουκλεάση AccI. Οι ζώνες που απεικονίζονται, αντιστοιχούν σε 25 δειγμάτα υγιών. Η πλειοψηφία φέρει C/T γονότυπο (3 ζώνες). Με λευκό βέλος υποδεικνύεται το άκοπο προϊόν, δηλαδή με γονότυπο Τ/Τ. Επίσης παρατηρούμε ένα μοναδικό προϊόν που έχει υποστεί πλήρη πέψη και υποδεικνύεται με κίτρινο βέλος. Όταν επιχειρήσαμε να κάνουμε στατιστική ανάλυση στα δεδομένα γονοτύπησης του πολυμορφισμού rs , αυτό δεν ήταν δυνατό, καθώς το δείγμα των υγιών δεν βρίσκεται σε HWE. Συγκεκριμένα όταν πραγματοποιήσαμε Chi Square Goodness-of-Fit Test το C^2 που προέκυψε για το δείγμα των υγιών ήταν 17,000, δηλαδή πολύ μεγαλύτερο του 3,841, που βάση του πίνακα 41, καθορίζει το επίπεδο σημαντικότητας όπου p = 0,05. Η ερμηνεία του παραπάνω αποτελέσματος συνοψίζεται στο ότι υπάρχει σημαντική διαφορά μεταξύ αναμενόμενων και παρατηρούμενων τιμών και επομένως στο δείγμα που εξετάζουμε, υπάρχει 95% πιθανότητα οι συχνότητες στα αλληλόμορφα και τους γονοτύπους του εν λόγω πολυμορφισμού, να μην οφείλονται καθαρά και μόνο στην τύχη, αλλά να επηρεάζονται από κάποιον άλλον παράγοντα, ανεξάρτητου της νόσου που εξετάζουμε. Το C^2, για το δείγμα των ασθενών παραμένει μικρότερο του 3,841, αλλά μόνο οριακά (C^2 = 3,394). Σε κάθε περίπτωση, δεν είναι δυνατό να προχωρήσουμε σε στατιστική ανάλυση των αποτελεσμάτων. Πιθανώς, η αύξηση του δείγματος τόσο των υγιών όσο και των ασθενών να άλλαζε την ισορροπία και να μας δινόταν η δυνατότητα στατιστικής ανάλυσης από την οποία θα προέκυπταν αξιόπιστα αποτελέσματα. 121
122 Ε Γονίδιο FAM181B, πολυμορφισμός rs (C>T). Η γονοτύπηση του πολυμορφισμού rs πραγματοποιήθηκε με τη χρήση περιοριστικής ενδονουκλεάσης BsrI. Γονοτυπήθηκαν 23 ασθενείς και 48 υγιείς, ελληνικής καταγωγής και οι συχνότητες που προέκυψαν αναπαριστώνται στον πίνακα 42, που ακολουθεί: Πίνακας 42: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό. Ελληνικός πληθυσμός Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) Τ/Τ Τ/C C/C T C* Υγιείς Ασθενείς *Το αλληλόμορφο με τη μικρότερη συχνότητα στο γενικό πληθυσμό και στους κεντρο - ευρωπαίους. Τόσο ο πληθυσμός των ασθενών, όσο και των υγιών ατόμων βρίσκεται σε HWE. Επομένως, από την στατιστική ανάλυση των συχνοτήτων του πίνακα 42, προέκυψαν τιμές στατιστικής σημαντικότητας, p = 0,11 κατά την σύγκριση των γονοτύπων με την ακριβή δοκιμασία του Fisher και p = 0,39 κατά την σύγκριση των αλληλομόρφων με την ίδια δοκιμασία. Τα αποτελέσματα υποδεικνύουν ότι δεν υπάρχει στατιστικά σημαντική διαφορά, τόσο σε επίπεδο γονοτύπων, όσο και σε επίπεδο αλληλομόρφων, μεταξύ των πληθυσμών υπό μελέτη, για τον εν λόγω SNP. Τα αποτελέσματα της πέψης αξιολογήθηκαν με τη χρήση πηκτώματος αγαρόζης 1,7%. Στην εικόνα 41 παρουσιάζοντται ενδεικτικά κάποια αποτελέσματα Εικόνα 41: Εικόνα όπου φαίνεται η δράση της περιοριστικής ενδονουκλεάσης στα ενισχυμένα με PCR τμήματα υγιών ατόμων που περιέχουν τον πολυμορφισμό rs Στις θέσεις 1, 4, 6, 7, 8, 9 και 11 απεικονίζεται το αποτέλεσμα της πέψης δείγμαμτος ατόμου με ετερόζυγο γονότυπο (C/T). Το άκοπο δείγμα στη θέση 2, ανήκει σε άτομο με C/C ομόζυγο γονότυπο, ενώ στις θέσεις 3, 5 και 10 βλέπουμε Τ/Τ ομόζυγους γονοτύπους. Σε συνεργασία με την Κυριακή Χαραλαμπίδου και Κωνσταντίνα Μάτσκου. 122
123 Ε Γονίδιο FΤΟ, πολυμορφισμοί rs (C>T) και rs (G>C) Οι εν λόγω πολυμορφισμοί γονοτυπήθηκαν με τη μέθοδο της αλληλούχησης, όπως αυτή περιγράφεται στην ενότητα Δ.11. Τα δείγματα που χρησιμοποιήθηκαν αποτελούνταν από 27 δείγματα ασθενών ALS και 39 υγιών ατόμων, ελληικής καταγωγής. Τα αποτελέσματα που λάβαμε είχαν τη μορφή χρωματογραφήματος. Γνωρίζοντας εξ αρχής τις θέσεις των πολυμορφισμών στην αλληλουχία αναφοράς, η οποία οριοθετείται από τους εκκινητές που επιλέχθηκαν για την PCR και ευθυγραμίζοντας τις ακολουθίες που προέκυψαν από την αλληλούχηση με την αλληλουχία αναφοράς, εντοπίσαμε τις θέσεις των πολυμορφισμών στα χρωματογραφήματα. Ακολουθούν μερικά παραδείγματα (Εικόνα 42). Στη συνέχεια πραγματοποιήθηκε στατιστική ανάλυση των αποτελεσμάτων και των δύο πολυμορφισμών, αφού πρώτα εξακριβώθηκε ότι τόσο ο πληθυσμός των υγιών, όσο και των ασθενών βρίσκονται σε HWE. Όσον αφορά τον πολυμορφισμό rs , η διεξαγωγή της ακριβούς δοκιμασίας του Fisher για τη στατιστική ανάλυση των δεδομένων (Πίνακας 43) έδωσε τιμή p ίση με 1 σε επίπεδο συχνοτήτων αλληλομόρφων, υποδεικνύοντας ότι δεν υπάρχει διαφορά μεταξύ υγιών και ασθενών. Αντιθέτως, η τιμή p σε επίπεδο γονοτύπων ισούται με 0,002, γεγονός που φανερώνει στατιστικά σημαντική διαφορά μεταξύ των γονοτύπων υγιών και ασθενών. Η τιμή p στην προκειμένη περίπτωση είναι μικρότερη του 0,01 και υποδηλώνει ισχυρή συσχέτιση του rs με την ALS, σε άτομα ελληνικής καταγωγής. Πίνακας 43: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό. Ελληνικός πληθυσμός Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) Τ/Τ Τ/C C/C T* C Υγιείς Ασθενείς *Το αλληλόμορφο αυτό έχει ελαφρώς μικρότερη συχνότητα στους κεντρο - ευρωπαίους. Ομοίως, για τον πολυμορφισμό rs η τιμή p που προέκυψε από τη σύγκριση των συχνοτήτων των αλληλομόρφων (Πίνακας 44) ήταν 0,48, δηλαδη μεγαλύτερη του ορίου σημαντικότητας 0,05, ενώ η τιμή p από τη σύγκριση των συχνοτήτων γονοτύπων ήταν 0,001, που σημαίνει ότι υπάρχει στατιστικά σημαντική διαφορά μεταξύ των πληθυσμών ασθενών και υγιών ατόμων ελληνικής καταγωγής. 123
124 Πίνακας 44: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό. Ελληνικός πληθυσμός Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) G/G G/C C/C G C* Υγιείς Ασθενείς *Το αλληλόμορφο αυτό έχει ελαφρώς μικρότερη συχνότητα στους κεντρο - ευρωπαίους. Οι συχνότητες των πινάκων 43 και 44 αναπαριστώνται γραφικά στο Διάγραμμα 1. Διάγραμμα 1: Συχνότητες πολυμορφισμών rs και rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τον ελληνικό πληθυσμό Συχνότητες αλληλομόρφων (%) στον Ελληνικό πληθυσμό Υγιείς Ασθενείς 124
125 Εικόνα 42: Παραδείγματα για κάθε γονότυπο των πολυμορφισμών rs (C>T) και rs (G>C) 125
126 Ανάλυση των rs (C>T) και rs (G>C), σε δείγματα Σαρδηνών ασθενών και υγιών. Η ανάλυση των δειγμάτων των ασθενών ALS, που είχαν καταγωγή από τη Σαρδηνία, πραγματοποιήθηκε στο εργαστήριο Biologia Molecolare στη Σαρδηνία, σε συνεργασία με τον ερευνητή Nicola Orru, με τον αναλυτή 3500 Series Genetic Analyzer. Οι αλληλουχίες που προέκυψαν είχαν μικρές μόνο διαφορές με τις υπόλοιπες (Εικόνα 43). Εικόνα 43: Χρωματογραφήματα που προέκυψαν κατά τη γονοτύπηση του πολυμορφισμού rs του FTO σε σείγματα Σαρδηνών με ALS. Από πάνω προς τα κάτω βλέπουμε τη μορφή του ετερόζυγου C/T γονοτύπου, ακολούθως του ομόζυγου C/C γονοτύπου και τέλος του ομόζυγου Τ/Τ γονοτύπου. Η θέση του SNP υποδεικνύεται με βέλος. (Nicola Orru) Ομοίως, παρουσιάζονται και τα αποτελέσματα για το πολυμορφισμό rs , με τη διαφορά ότι η βάση G αλλάζει για τη βάση C, στη συγκεκριμένη περίπτωση. Τα δείγματα των υγιών από τη Σαρδηνία που χρησιμοποιήθηκαν ως δείγμα αναφοράς για τον συγκεκριμένο πληθυσμό γονοτυπήθηκαν με την ίδια μέθοδο που χρησιμοποιήθηκε και για τα δείγματα Ελλήνων. Οι συχνότητες που προέκυψαν από την ανάλυση του πληθυσμού από τη Σαρδηνία για τους πολυμορφισμούς του γονιδίου FTO, παρουσιάζονται στους πίνακες που ακολουθούν (Πίνακες 45 και 46): 126
127 Πίνακας 45: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τη Σαρδηνία. Σαρδηνοί Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) Τ/Τ Τ/C C/C T* C Υγιείς Ασθενείς *Το αλληλόμορφο αυτό έχει ελαφρώς μικρότερη συχνότητα στους κεντρο - ευρωπαίους. Πίνακας 46: Συχνότητες πολυμορφισμού rs που προέκυψαν από τη γονοτύπηση υγιών και ασθενών από τη Σαρδηνία. Σαρδηνοί Συχνότητες γονοτύπων (%) Συχνότητες αλληλομόρφων (%) G/G G/C C/C G C* Υγιείς Ασθενείς *Το αλληλόμορφο αυτό έχει ελαφρώς μικρότερη συχνότητα στους κεντρο - ευρωπαίους. Αφού πραγματοποίηθηκε η δοκιμασία «Chi square Goodness of fit» και διαπιστώθηκε ότι ισχύει το κριτήριο χ2 και επομένως τα δείγματα βρίσκονται σε HWE, ακολούθως πραγματοποήθηκε στατιστική ανάλυση. Από τη στατιστική ανάλυση των αλληλομόρφων και των γονοτύπων του rs προέκυψαν τιμές p=1 σε επίπεδο αλληλομόρφων και p=0,9 σε επίπεδο γονοτύπων. Αντίστοιχα, για τον rs υπολογίστηκαν τιμές παρατηρούμενης σημαντικότητας p=0,57 σε επίπεδο αλληλομόρφων και p=0,37 σε επίπεδο γονοτύπων. Σύμφωνα με τις παρατηρούμενες τιμές σημαντικότητας (p), οι διαφορές μεταξύ ασθενών και υγιών είναι απειροελάχιστες στον πληθυσμό των Σαρδηνών, τόσο για τον rs όσο και για τον rs Στα δεδομένα του WGS εκτός του rs , δύο ακόμα εσωνικοί πολυμορφισμοί του FTO, ήταν κοινοί σε όλους τους ασθενείς, οι rs και rs Οι τελευταίοι δεν αξιολογήθηκαν με τη διαδικασία της γονοτύπησης. Προβλεψη απλοτύπων Την ανάλυση των συχνοτήτων, ακολούθησε προβλεψη απλοτύπων για τα rs , rs , rs και rs με το SNAP v2.2 ( Johnson 2008). Τα αποτελέσματα που εξήχθησαν μέσω του Haploview, με τη χρήση των δεδομένων του Hapmap, επαληθέφθηκαν στην προκειμένη περίπτωση για το rs , κατά τη σύγκριση των πολυμορφισμών ανα δυο και επεκτάθηκαν και στο rs , όπως βλέπουμε στον πίνακα 47. Σε αυτή την περίπτωση, χρησιμοποιήθηκαν δεδομένα του 1000 Genomes Pilot 1 και ως πληθυσμός επιλέχθηκε CEU, δηλαδή οι κεντρο - ευρωπαίοι. 127
128 Πίνακας 47: Πολυμορφισμοί σε LD με τον rs και rs SNP LD SNP CEU r2 D' Συντεταγμένες στο χρωμόσωμα 16 (HG18) rs rs rs rs rs rs rs rs rs rs rs rs Από τον παραπάνω πίνακα συμπεραίνουμε ότι οι πολυμορφισμοί που γονοτυπήσαμε είναι σε LD μεταξύ τους αλλά και με τους rs και rs , οι οποίοι εντοπίζονται στα δεδομένα του WGS, σχηματίζοντας κατά αυτόν τον τρόπο έναν απλότυπο. Ε.2 Αποτελέσματα γονοτύπησης ασθενών και υγιών για τους πολυμορφισμούς που επιλέγχθηκαν από τη 2 η προσέγγιση του WGS Ε.2.1 Γονίδιο FGF13, 5 UTR. Η παρραλλαγή έχει έναρξη στη θέση και λήξη στη θέση του χρωμοσώματος Χ, κατά τα στοιχεία που μας δώθηκαν από το WGS, τα οποία αντιστοιχούν στην έκδοση του γονιδιώματος GRCh37. Η θέση αυτή εντάσεται στην 5 UTR περιοχή του γονιδίου FGF13. Γονοτυπήσαμε μεγάλο μέρος της 5 UTR περιοχής, στην οποία περιέχεται η πλειοψηφία των παραλλαγών της περιοχής. Στην 5 UTR έχουν βρεθεί μεταξύ άλλων, δύο παραλλαγές σε διπλανές θέσεις, την παραλλαγή rs ή αλλιώς c.-352 G>A, όπου Τ είναι το αρχέγονο αλληλόμορφο και η παραλλαγή rs ή αλλιώς c.-353 A>C, για την οποία το αρχέγονο αλληλόμορφο είναι G. Ο rs έχει μία προηγούμενη καταχώρηση, ομοίως και ο rs Πράγματι, η αλληλούχηση 37 δειγμάτων μετά από πολλαπλασιασμό της συγεκριμένης περιοχής με PCR, έδειξε ότι η αλληλουχία ΑGTG εντοπίζεται και σε όλα τα υγιή άτομα, ελληνικής καταγωγής αντί της αλληλουχίας GCT που φέρεται ως αλληλουχία αναφοράς (cdna, Exon στο Ensembl). Διαπιστώθηκε, ότι η ίδια ακολουθία (ΑGTG) που βρέθηκε στους ασθενείς υπάρχει και στους υγιείς και επομένως, η συγκεκριμένη παραλλαγή δε μελετήθηκε περαιτέρω. Αξίζει ωστόσο να σημειωθεί, ότι η προσθήκη της βάσης Α, καθώς και οι μονονουκλεοτιδικές ελλείψεις σε τρία επιπλέον σημεία της συγκεκριμένης αλληλουχίας που ελέγξαμε, εντοπίστηκαν σε όλα τα υγιή άτομα, ενώ συγχρόνως δεν υπήρχαν στην αλληλουχία αναφοράς, ούτε και ήταν καταγεγραμμένες στη βάση δεδομένων ensembl. Η 1 η έλλειψη εντοπίστηκε κάπου ανάμεσα 128
129 στις θέσεις , όπου απουσίαζε μία βάση C ή Τ. Εννιά βάσεις πιο μακριά, στη θέση απουσιάζει μία βάση Τ και στη θέση μία ακόμα βάση Τ. Η σύγκριση της αλληλουχίας με την αναφοράς φαίνεται στην Εικόνα 44. Εικόνα 44: Τμήμα της ακολουθίας της 5 UTR περιοχής του γονιδίου FGF13. Ανάμεσα στις αγκύλες βρίσκεται η εν λόγω αντικατάσταση. Σε όλους τα δείγματα αναφοράς που αλληλουχήθηκαν, η ακολουθία που βρέθηκε είναι η AGTG. Απεικονίζονται 3 επιπλέον ελλείψεις που εντοπίζονται σε όλα τα δείγματα αναφοράς (υποδεικνύονται με βέλη). Ε.2.2 Γονίδιο SLC36A1, Chr5: Η συγκεκριμένη παραλλαγή είναι μια αντικατάσταση της ακολουθίας GCTG προς την ακολουθία ACGAGTT και εντοπίζεται 79bp ανοδικά του κωδικονίου έναρξης του γονιδίου SLC36A1. Στην πραγματικότητα, η συγκεκριμένη παραλλαγή δεν αποτελεί μια νέα παραλλαγή, αλλά είναι καταγεγραμμένη ως rs Για τη γονοτύπηση ακολουθήθηκε η μέθοδος της αλληλούχησης κατά Sanger και ηλεκτροφόρηση σε τριχοειδή. Πριν τη γονοτύπηση, πραγματοποιήθηκε PCR, τα αποτελέσματα της οποίας ήταν ικανοποιητικά, δηλαδή αναμενόμενου μεγέθους προϊόντα (291bp), απαλλαγμένα μη ειδικών προϊόντων και επιμολύνσεων. Ο παραπάνω έλεγχος 129
130 πραγματοποιήθηκε σε πήκτωμα αγαρόζης. Στη συνέχεια, παρουσιάζεται χαρακτηριστική εικόνα των χρωματογραφημάτων που προέκυψαν (Εικόνα 45). A C G G G C 32 Βάσεις που φαίνονται στο χρωματογράφημα αλλά δεν ταυτοποιούνται. Αλληλουχία ατόμου που πάσχει, το οποίο διαθέτει γονότυπο ομόζυγο για τo αλληλόμορφο ACGAGTT. Ετερόζυγο άτομο, δηλαδή με γονότυπο GCTG/ACGAGTT. Λόγω της διαφοράς 2 βάσεων της αντικατάστασης τα χρωματογραφήματα περιπλέκονται, παρόλο που οι δύο αλληλουχίες παραμένουν ίδιες στη συνέχεια. Αλληλουχία υγιούς ατόμου, που φέρει γονότυπο ομόζυγο προς το αλληλόμορφο αναφοράς, δηλαδή το GCTG. Εικόνα 45: Παραδείγματα απεικόνισης των τριών πιθανών γονοτύπων για την αντικατάσταση GCTG/ACGAGTT. Από τον ελληνικό πληθυσμό, αλληλουχήθηκαν 25 δείγματα ασθενών και 15 δείγματα υγιών. Σε κάθε περίπτωση, το δείγμα ήταν πολύ μικρό για να γίνει στατιστική ανάλυση και ιδιαίτερα το δείγμα των υγιών. Ακολουθούν οι παρατηρήσεις που προέκυψαν από τη γονοτυπική ανάλυση (Πίνακας 48). Πίνακας 48: Παρατηρήσεις που εξάχθηκαν με τη διαδικασία της αλληλούχησης, της παραλλαγής rs Παρατηρήσεις GCTG/GCTG GCTG/ACGAGTT ACGAGTT/ACGAGTT γονοτύπων Υγιείς Ασθενείς
131 Ε.3 Αποτελέσματα επαλήθευσης μετάλλαξης στο εξώνιο 1 του γονιδίου SPG7 σε οικογένεια ασθενών με διάγνωση πιθανή ALS - οικογενής σπαστική παραπάρεση και στου υγιείς συγγενείς 1 ου βαθμού (Εικόνα 46). Εικόνα 46: Οικογενειακό δένδρο ασθενών με μετάλλαξη στο SPG7. Άντρας που πάσχει Υγιής Άντρας Μη καθορισμένο φύλο Γυναίκα που πάσχει Υγιής Γυναίκα? Μη καθορισμένος αριθμός ατόμων IV.5 και IV.6: 2 α ξαδέρφια V.6: περιστατικό αναφοράς (index case). V.4, V.6, V.8 και V.17: πάσχοντες IV.1: 2 θήλεις που απεβίωσαν IV.2: 2 άρρενες που απεβίωσαν. IV. 3: Δύο γυναίκες IV.4: Πέντε άντρες. IV.6 και V.15: αποβιώσαντες Τα άτομα που απεβίωσαν δεν εμφάνισαν συμπτώματα σχετικά με τη νόσο. 131
132 Η επαλήθευση της μετάλλαξης στο εξώνιο 1 του γονιδίου SPG7 έγινε με δύο τρόπους: Α) Σε πήκτωμα αγαρόζης 3,5%, όπου είναι εμφανής η διαφορά μεταξύ υγιών, ασθενών και συγγενών ατόμων. Από τα δείγματα των υγιών προέκυψε μία μόνο ζώνη στο πήκτωμα αγαρόζης, η οποία αντιστοιχούσε σε προϊόν 207 ζευγών βάσεων, όπως αναμενόταν από το σχεδιασμό των εκκινητών. Στην περίπτωση των ασθενών, οι οποίοι αναμενόταν να είναι ομόζυγοι για την μετάλλαξη, παρατηρήσαμε πάλι μία μόνο ζώνη, που αντιστοιχούσε σε ένα λίγο μικρότερο προϊόν σε σχέση με τους υγιείς. Τέλος, στην περίπτωση των συγγενών, γονέων και τέκνων, οι οποίοι δεν είχαν συμπτώματα της νόσου παρατηρήσαμε δύο ζώνες στο πήκτωμα, μία μεγέθους 207bp και μια μικρότερου μεγέθους ίσου με τον ασθενών. Όπως αναμενόταν, οι συγγενείς ήταν ετερόζυγοι προς την έλλειψη η οποία φαίνεται να ακολουθεί το υπολειπόμενο πρότυπο κληρονομικότητας. Όπως φαίνεται και από το γενεαλογικό δένδρο της οικογένειας, τα μοναδικά άτομα που νόσησαν ήταν εκείνα της 5 ης γενεάς. Τουλάχιστον στην περίπτωση των αδερφών που νοσούν είναι εμφανής η ύπαρξη συγγένειας μεταξύ των γονέων τους. Τα συγκεντρωτικά αποτελέσματα φαίνονται στην φωτογραφία του πηκτώματος μετά από έκθεση αυτού στο υπεριώδες φως (Εικόνα 47). Εικόνα 47:Πήκτωμα αγαρόζης 3,5%, προς επιβεβαίωση έλλειψης 25bp. ΘΕ: θετικός έλεγχος, ΑΕ: αρνητικός έλεγχος 132
133 Β) Με τη μέθοδο αλληλούχησης κατά Sanger και ηλεκτροφόρηση σε τριχοειδή. Ακολουθούν τα χρωματογραφήματα: Εικόνα 48: Στο πάνω μέρος της εικόνας φαίνεται ξεκάθαρα η έλλειψη 25 βάσεων στην αλληλουχία 3 από τους ασθενείς, ακολουθεί η αλληλουχία αναφοράς και 3 ακολουθίες συγγενών. Στο κάτω μέρος φαίνονται 3 από τα χρωματογραφήματα, το 1ο αντιπροσωπεύει την ακολουθία με ομόζυγη έλλειψη και το 2 ο και 3 ο αντιπροσωπεύει αλληλουχίες των συγγενών που διαθέτουν την έλλειψη σε ετερόζυγη κατάσταση. Στην Εικόνα 48, η πάνω αλληλουχία αντιστοιχεί στον «index case» της οικογένειας, ο οποίος - όπως και τα υπόλοιπα μέλη που νοσούν - φέρουν την έλλειψη σε ομόζυγη κατάσταση. Στο κάτω μέρος της ίδιας εικόνας βλέπουμε την αλληλουχία ενός από τους συγγενείς. Οι αλληλουχίες των υπόλοιπων ατόμων στην οικογένεια που δεν νοσούν είναι παρόμοιες. Στην Εικόνα 49 παρατηρούμε το χρωματογραφία του ασθενή αναφοράς (V.6, ομόζυγος για την έλλειψη) και ενός υγιή, μέλους της ίδιας οικογένειας (VI.4), ετερόζυγο για την έλλειψη. Στις δύο αυτές περιπτώσεις, σημειώνεται η αρχή της έλλειψης στο χρωματογράφημα. 133
134 ΕΝΑΡΞΗ ΕΛΛΕΙΨΗΣ 25 bp Εικόνα 49: Έλλειψη στο γονίδιο SPG7 (exon1). Στα σημεία που συμβολίζονται με τα βέλη σηματοδοτείται η αρχή της έλλειψης. 134
135 ΣΤ. ΣΥΜΠΕΡΑΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ 135
136 ΣΤ.1 Συζήτηση και συμπεράσματα επί των αποτελεσμάτων Το Ε.1 και Ε.2 σκέλος των αποτελεσμάτων βασίστηκε στην ανάλυση των γονιδιωμάτων που προέκυψαν από την αλληλούχηση ολόκληρου του γονιδιώματος με τη χρήση μιας WGS τεχνικής. Αναφορικά με τα αποτελέσματα της 1 ης προσέγγισης («Ε.1 Αποτελέσματα γονοτύπησης ασθενών και υγιών για τους πολυμορφισμούς που επιλέγχθηκαν από την 1η προσέγγιση του WGS»), αξίζει να σημειωθεί ότι παρόλο που το αρχικό δείγμα ήταν μικρό (αποτελούνταν από 10 Έλληνες ασθενείς) και ο φαινότυπος των ατόμων που συνιστούσε το δείγμα μας διέφερε σημαντικά, διατηρώντας ως μοναδικό κοινό χαρακτηριστικό την διάγνωση της ALS, μεταξύ των αποτελεσμάτων που προέκυψαν, όταν επεκτάθηκε το εν λόγω δείγμα, διαπιστώθηκαν ήδη δύο στατιστικά σημαντικές συσχετίσεις. Πρόκειται για εκείνες του rs στο TBC1D1 και των rs και rs στο FTO. Το δείγμα των ασθενών Το δείγμα των ασθενών στο οποίο πραγματοποιήθηκε η πλήρης αλληλούχηση, περιλαμβάνει πέντε άτομα που φέρουν τη σποραδική μορφή της ALS, με τη νόσο σε τρία εξ αυτών να εξελίσσεται ταχέως, ενώ στα άλλα δύο άτομα η επιδείνωση είναι αργή. Τα υπόλοιπα πέντε άτομα έχουν οικογενειακό ιστορικό και έχουν διαγνωστεί με πιθανή FALS. Τέσσερις στους πέντε ασθενείς με οικογενειακό ιστορικό έχουν συγγένεια 1 ου βαθμού. Στο σύνολο των πασχόντων, έξι είναι θήλεις και 4 άρρενες. Οι ηλικίες έναρξης των συμπτωμάτων κυμαίνονται από τα 52 έως τα 73 έτη, με μία εξαίρεση, όπου η ηλικία έναρξης είναι κατά μία εικοσαετία μικρότερη της ελάχιστης (αργή εξέλιξη). Στατιστικά σημαντικά αποτελέσματα Ο rs τοποθετείται στο εσώνιο 2, του γονιδίου TBC1D1 και στη θέση 4: του χρωμοσώματος 4. Εναλλακτικά του ονόματα αποτελoύν, τα c c>a, c c>a και c c>a. Οι συχνότητες των αλληλομόρφων σε διάφορους πληθυσμούς παρουσιάζονται στην εικόνα 50. Εικόνα 50: Συχνότητες αλληλομόρφων A και C σε διάφορους πληθυσμούς του πολυμορφισμού rs ( 136
137 Στον ελληνικό πληθυσμό, σύμφωνα με τα δεδομένα μας, καθώς και στον πληθυσμό των Σαρδηνίων, οι συχνότητες των αλληλομόρφων Α και C δεν είναι σημαντικά διαφορετικές σε σχέση με τις συχνότητες στον ευρωπαϊκό πληθυσμό και δεν διαφέρουν σημαντικά, ούτε μεταξύ ασθενών και υγιών και για τους δύο πληθυσμούς, ούτε μεταξύ Σαρδηνίων και Ελλήνων. Παρατηρώντας προσεκτικά τις παρατηρούμενες συχνότητες για τον εν λόγω πολυμορφισμό (Πίνακας 38 και Διάγραμμα 2), γίνεται προφανές ότι η διαφορά εντοπίζεται στις συχνότητες των ετερόζυγων ατόμων. Οι ασθενείς που φέρουν το Α αλληλόμορφο σε ετερόζυγη κατάσταση είναι σημαντικά περισσότεροι από τους υγιείς, κυρίως, εις βάρος του C/C γονοτύπου. Διάγραμμα 2: Διάγραμμα στηλών, όπου απεικονίζονται γραφικά οι διαφορές στις συχνότητες γονοτύπων στον πληθυσμό των υγιών και στον πληθυσμό των ασθενών ατομων Συχνότητες γονοτύπων rs (%) στον Ελληνικό πληθυσμό * CC CA AA Υγιείς Ασθενείς Ο rs βρίσκεται στο εσώνιο 1 του γονιδίου FTO και στη θέση 16: του χρωμοσώματος 16. Εναλλακτικά ονόματα αποτελούν τα c c>t και c c>t. Ακολουθεί η απεικόνιση των συχνοτήτων του (Εικόνα 51). Εικόνα 51: Συχνότητες αλληλομόρφων Τ και C σε διάφορους πληθυσμούς, του πολυμορφισμού rs ( 137
138 Ιδιαίτερα στην περίπτωση του πολυμορφισμού rs παρατηρούμε μια πολύ σημαντική συσχέτιση, με παρατηρούμενη τιμή σημαντικόντητας, που ξεπερνάει κατά πολύ το όριο p < 0,05, ακόμα και το όριο p < 0,01. Αυτό σημαίνει, με απλά λόγια, ότι οι πιθανότητες οι υποθέσεις μας να είναι λανθασμένες είναι πολύ μικρότερες του 1 %. Αναμφισβήτητα στην περίπτωση του παραπάνω πολυμορφισμού συνιστάται περαιτέρω διερεύνηση (ενδεικτικά, μελέτες λειτουργίας). Ενδιαφέρον, πιθανώς, να παρουσιάζουν και οι άλλοι δύο πολυμορφισμοί που βρίσκονται στη περιοχή του γονιδίου FTO και προέκυψαν από την 1 η προσέγγιση στα δεδομένα του WGS. Αυτοί είναι ο rs (c c>t, n c>t) και ο rs (c a>g, n a>g). Γνωρίζουμε, ήδη, ότι και οι πολυμορφισμοί rs και rs οι οποίοι φαίνεται να συσχετίζονται ισχυρά με την εμφάνιση της ALS στον ελληνικό πληθυσμό, βρίσκονται σε LD με τους rs και rs αλλά και μεταξύ τους. Με αυτόν τον τρόπο και υποθέτοντας ότι η ισορροπία σύνδεσης ισχύει και στον ελληνικό πληθυσμό, τον οποίο μελετάμε, τα αποτελέσματα μας υποδεικνύουν έναν πιθανό απλότυπο που συσχετίζεται με την συχνότερη εμφάνιση της ALS. Μένει να αποδειχθεί η ανισορροπία σύνδεσης μεταξύ των 4 πολυμορφισμών και η συσχέτιση όλων αυτών με την ασθένεια. Έλεγχος για αλληλόμορφα σε LD, με τους rs και rs πραγματοποιήθηκε με τη βοήθεια του προγράμματος SNPinfo, έδωσε τα αποτελέσματα του πίνακα 49 για το rs και καθόλου αποτελέσματα για το rs Στον πίνακα συμπεριλαμβάνονται επιπλέον δύο πολυμορφισμοί, οι rs και rs , με τους οποίους δεν είχαμε ασχοληθεί πρωτύτερα. Ο πληθυσμός που επιλέχθηκε ήταν ο CEU, δηλαδή οι κεντρο ευρωπαίοι και η βάση δεδομένων, που χρησιμοποιεί το SNPinfo, είναι η HapMap ( Xu and Taylor 2009). Πίνακας 49: Πίνακας πολυμορφισμών σε LD με το rs στους κεντρο ευρωπαίους. rs Θέση Αλληλόμορφα Πληθυσμός/LD RegPotential Συντήρηση Απόσταση (bp) rs : C/T CEU/ rs : T/C CEU/ rs : G/C rs : C/T CEU/ rs : A/G CEU/ Από τους παραπάνω, ο rs έχει συσχετιστεί με τον δείκτη μάζας σώματος και βρίσκεται στη θέση 16: Ο rs βρίσκεται στη θέση 16: Από τις θέσεις των πολυμορφισμών στο χρωμόσωμα συμπεραίνουμε ότι και αυτοί βρίσκονται στο 1ο εσώνιο του FTO στο χρωμόσωμα 16. Διερευνώντας τη σχέση των συχνοτήτων των αλληλομόρφων, στον ευρωπαϊκό πληθυσμό συγκριτικά με τους πληθυσμούς των Σαρδηνών και των Ελλήνων, για τους rs και 138
139 rs , παρατηρούμε ότι οι διαφορές δεν είναι σημαντικές, είτε συγκρίνουμε τους δύο πληθυσμούς που εξετάσαμε με τους Ευρωπαίους, είτε τους Σαρδηνούς με τους Έλληνες. Το γενικότερο συμπέρασμα, που προκύπτει από τον έλεγχο των παραπάνω πολυμορφισμών στον πληθυσμό των Σαρδηνίων είναι ότι οι πολυμορφισμοί αυτοί αφορούν αποκλειστικά την συσχέτιση της ALS με τον ελληνικό πληθυσμό. Ωστόσο, πρέπει να ληφθεί υπόψη ότι ο πληθυσμός των Σαρδηνίων είναι γενετικά συντηρημένος. Ώστε να επιβεβαιωθεί εάν τα αποτελέσματα αφορούν αποκλειστικά τον ελληνικό πληθυσμό, απαιτείται επαλήθευση των ευρημάτων και σε άλλους πληθυσμούς. Αν κατά αυτόν τον τρόπο αποδειχθεί η ειδική συσχέτιση των πολυμορφισμών rs , rs , rs και του απλοτύπου των δύο τελευταίων, με την ALS στον ελληνικό πληθυσμό, αυτομάτως δημιουργείται το ερώτημα: Ποιες αλληλεπιδράσεις οδηγούν στην συσχέτιση μιας νόσου με έναν πολυμορφισμό σε έναν πληθυσμό και σε έναν άλλο όχι. Επιπλέον, η συσχέτιση ενός κοινού αλληλομόρφου με τη νόσο δείχνει ότι δεν είναι ο μοναδικός παράγοντας και καθιστά απαραίτητο τον έλεγχο ύπαρξης τόσο απλοτύπου όσο και άλλων γενετικών αιτίων. Γονίδια Σχετικά με τα γονίδια FTO και TBC1D1, αν και βάσει της υπάρχουσας βιβλιογραφίας, δεν είχαν συσχετιστεί στο παρελθόν με την ALS, υπάρχουν ωστόσο κάποιες ενδείξεις συσχέτισης με το νευρικό σύστημα ή αλληλεπίδρασεις με πρωτεΐνες, οι οποίες εμπλέκονται στην ALS. Στην εικόνα που ακολουθεί παρουσιάζονται οι αλληλεπιδράσεις του πρωτεϊνικού μορίου του TBC1D1 με μόρια σχετικά με την SALS (Εικόνα 53). Συγκεκριμένα, το προϊόν του Tbc1d1, όπως αναφέρθηκε και στην εισαγωγή (Ενότητα Β.1.9.6), φαίνεται να αλληλεπιδρά με την πρωτεΐνη του Tardbp, σε μοντέλα μυών και εμβρυικών βλαστοκυττάρων (Chiang et al. 2010), γνωστή για την συμμετοχή της στον μηχανισμό παθογένειας της ALS. Επιπροσθέτως, καθώς φαίνεται υπάρχει και κάποια έμμεση αλληλεπίδραση (διακεκομμένες γραμμές στην εικόνα 53) με το προϊόν του FAS. Προτείνεται, ότι η FAS ρυθμίζει την έκφραση του TBC1D1, ταυτοχρόνως η ίδια η FAS έχει συσχετιστεί με τον κυτταρικό θάνατο στην ALS, μέσω μηχανισμού που περιλαμβάνει τα μιτοχόνδρια, την ενεργοποίηση των κασπασών και ένζυμα που ρυθμίζουν το ΝΟ, όπως το ΝΟS (Εικόνα 52). Εικόνα 52: Προτεινόμενος μηχανισμός με τον οποίον η Fas προκαλεί την απόπτωση στην ALS (Raoul, 2006). 139
140 SALS TBC1D1 NETWORK Shortest paths: 36 Εικόνα 53: Αλληλεπιδράσεις του προϊόντος του γονιδίου TBC1D1 με άλλα μόρια, τα οποία έχουν συσχετιστεί με SALS. Τα δεδομένα παράχθηκαν με τη βοήθεια του προγράμματος IPA (IPA, QIAGEN Redwood City, Με κόκκινο απεικονίζεται το μόριο TBC1D1. Σε κύκλο εντοπίζονται οι πιο ενδιαφέρουσες αλληλεπιδράσεις. Αναφορικά με το FTO, αν και οι παθήσεις με τις οποίες έχει συσχετιστεί μέχρι ώρας, είναι η παχυσαρκία, ο μελιταίος διαβήτης και η καθυστερημένη ανάπτυξη, ο μηχανισμός του ωστόσο παραπέμπει σε μηχανισμούς που αντιπροσωπεύονται στην ALS. Ειδικότερα, η FTO είναι μια πυρηνική πρωτεΐνη, που σύμφωνα με την οικογένεια σιδηρομεταφορικών ενζύμων χωρίς ομάδα αίμης στην οποία ανήκει, υποδηλώνεται ένας μηχανισμός δράσης που περιλαμβάνει την αντιστροφή της αλκυλίωσης του DNA και RNA που προκαλείται από οξειδωτική απομεθυλίωση. Μελέτες σε μύες, υποδεικνύουν ότι η πρωτεΐνη παίζει ρόλο στο νευρικό και καρδιαγγειακό σύστημα (Entrez Gene Summary). Πέρα από τα χαρακτηριστικά που ήδη γνωρίζουμε για τα παραπάνω γονίδια είναι εύλογο να αναρωτηθούμε ποιος μπορεί να είναι ο ρόλος τους στην ασθένεια που μελετάμε. Συγχρόνως, δεν πρέπει να αποκλείσουμε την συμμετοχή των πολυμορφισμών που συσχετίστηκαν σε κάποιο διαφορετικό μηχανισμό, παραδείγματος χάριν, στη ρύθμιση της έκφασης κάποιου απομακρυσμένου γονιδίου. Ήδη γνωρίζουμε ότι η μη κωδική περιοχή του γονιδίου αλληλεπιδρά άμεσα με την περιοχή του υποκινητή του γονιδίου IRX3. Σχετικά με τα αλληλόμορφα που καταγράφηκαν για πρώτη φορά (2 η προσέγγιση) Το πλήθος των νέων παραλλαγών που εντοπίστηκαν στα γονιδιώματα των ασθενών, οι οποίες ξεπερνούν τις 3000, εξηγείται με την παραδοχή ότι η χαρτογράφηση του ανθρώπινου γονιδιώματος δεν είναι ολοκληρωμένη. Επιπλέον, αναλύοντας τα αποτελέσματα παρατηρήθηκαν ασυμφωνίες με την αλληλουχία αναφοράς, η οποία αυτή τη στιγμή αναθεωρείται, όπως στην περίπτωση της αντικατάστασης στην 5 UTR του γονιδίου FGF
141 Άλλη πιθανή εξήγηση, για τις διαφορές μεταξύ αλληλουχίας αναφοράς και δείγματος αναφοράς, είναι η ποικιλότητα μεταξύ των πληθυσμών. Επιπροσθέτως, είναι προφανές ότι οι παραλλαγές με την μικρότερη εξελικτική πίεση φαίνεται να υπερισχύουν στην κατηγορία των νέων παραλλαγών. Από την άλλη, όσον αφορά τις περιοχές ανοδικά και καθοδικά των γονιδίων, ίσως ο σχετικά μικρός αριθμός παραλλαγών που εντοπίζεται εκεί να σχετίζεται, εν μέρει, με το ποσοστό του συνολικού γονιδιώματος το οποίο αντιπροσωπεύουν. Αξιοσημείωτη είναι και η μεγάλη αντιπροσώπευση των νέων παραλλαγών στα εσώνια. Οι 5 UTR παραλλαγές που επιλέχθηκαν προς μελέτη, έχουν παρατηρηθεί ξανά (έχουν rs number), αλλά για τους περισσότερους υπάρχει μία μόνο παρατήρηση. Η αντικατάσταση στο SLC36A1 είναι στην ουσία ο rs Οι παραλλαγές της 5 UTR απέχουν 350bp και 79bp από το πρώτο κωδικόνιο του FGF13 και του SLC36A1, αντίστοιχα. Το FGF13 εκφράζεται στον εγκέφαλο σε μεγαλύτερο βαθμό από ότι στους άλλους ιστούς και έχει συσχετιστεί στο παρελθόν με την ανάπτυξη του νευρικού συστήματος. To SLC36A1 εμφανίζει αυξημένη έκφραση στον εγκέφαλο καθώς επίσης στα λευκοκύτταρα, στα λεμφοκύτταρα και στους ινοβλάστες. Έλλειψη 25 ζευγών βάσεων στο εξώνιο 1 του γονιδίου SPG7 Η έλλειψη 25bp που εντοπίστηκε στο εξώνιο 1 του γονιδίου SPG7 στα πάσχοντα άτομα της οικογένειας σε ομόζυγη κατάσταση και σε ετερόζυγη κατάσταση στους υγιείς συγγενείς, αποτελεί μια νέα μετάλλαξη. Η οικογένεια προέρχεται από ορεινό χωριό της Ελλάδος και ο φαινότυπός τους παρουσιάζει πολλές ιδιατερότητες. Ενδεικτικά, οι πάσχοντες συνδυάζουν συμπτώματα λόγω εκφύλισης ανώτερων (δυσαρθρία) και κατώτερων κινητικών νευρώνων (περιφερική νευροπάθεια, όπως καταγράφεται στο ηλεκτρομυογράφημα), αλλά και ευρήματα στην μαγνητική τομογραφία εγκεφάλου και σπονδυλικής στήλης. Στην συγκεκριμένη περίπτωση, εκτός από τη μοναδικότητα του περιστατικού έχει ενδιαφέρον η δυνατότητα που μας δίνεται να συσχετιστούν κάποια φαινοτυπικά χαρακτηριστικά και κυρίως της ALS με τη μετάλλαξη στο γονίδιο SPG7. ΣΤ.2 Μελλοντικές προοπτικές και συμπληρωματικά δεδομένα 3 UTR του γονιδίου FUS Ως μέρος της παρούσας εργασίας, εντοπίστηκαν μερικές ενδιαφέρουσες περιπτώσεις που χρήζουν περαιτέρω διερεύνησης. Η ιδέα για την πρώτη, προέκυψε από την 3η προσέγγιση των δεδομένων του WGS. Τα πρώτα αποτελέσματα της προσέγγισης 3, παρουσιάζονται στον πίνακα 13. Ένας εκ των ασθενών, φέρει μια παραλλαγή G A, 41 βάσεις μετά το κωδικόνιο λήξης του γονιδίου FUS (Brown et al. 2012, Sabatelli et al. 2013). Ωστόσο εκ των αποτελεσμάτων της ίδιας δημοσίευσης υπογραμμίζεται η σημασία της 3 UTR. Ηδη η διαδικασία διερεύνησης της περιοχής 3 UTR, στο γονίδιο FUS, ξεκίνησε με τον σχεδιασμό εκκινητών που περιβάλλουν το εξώνιο 15 και την 3 UTR περιοχή. Η αλληλουχία του πρόσθιου εκκινητή είναι η 5 AGGTAGGAGGGGCAGATAGG 3 και του αντίστροφου 5 CACCATTAAAAGGGCCAAAAG 3. Χρησιμοποιήθηκαν οι συνθήκες της συμβατικής PCR 141
142 και η κλασική στερεοχημεία (Πίνακες 15 και 16), με θερμοκρασία υβριδοποίησης τους 59 ο C και 40 κύκλους αποδιάταξης, υβριδοποίησης και επιμήκυνσης. Το προϊόν που παράγεται αποδίδει ικανοποιητικά αποτελέσματα κατά την αλληλούχηση με τη διαδικασία 2. Ωστόσο, κατά την ηλεκτροφόρηση σε πήκτωμα αγαρόζης, υπήρχε υποψία μη ειδικού προϊόντος, οπότε συστήνεται η δοκιμασία της PCR σε λίγο υψηλότερες θερμοκρασίες υβριδοποίησης. FAM181B και rs Μεταξύ των δεδομένων εντοπίζεται ο πολυμορφισμός rs στο γονίδιο FAM181B. Γονοτυπήθηκαν 23 ασθενείς και 48 υγιείς και οι συχνότητες που προέκυψαν αναπαριστώνται γραφικά στο Διάγραμμα 3 που ακολουθεί: Διάγραμμα 3: Διάγραμμα στηλών όπου απεικονίζονται γραφικά οι διαφορές στις συχνότητες γονοτύπων στον πληθυσμό των υγιών και στον πληθυσμό των ασθενών Συχνότητες γονοτύπων rs (%) στον Ελληνικό πληθυσμό T/T C/T C/C Υγιείς Ασθενείς Στην περίπτωση του πολυμορφισμού rs , θεωρείται χρήσιμη η αύξηση του δείγματος, καθώς μικρές αλλαγές στην κατανομή των γονοτύπων θα μπορούσαν να οδηγήσουν σε μείωση της τιμής p, σε τιμές μικρότερες του 0,05. Αυτή η αλλαγή, θα σήμαινε ότι η υπόθεση μας, δηλαδή ότι οι συχνότητες των γονοτύπων διαφέρουν σημαντικά μεταξύ υγιών και ασθενών, έχει 95% πιθανότητα να είναι αληθής. Εξανουκλεοτιδική επέκταση στο 1 ο εσώνιο του C9orf72 Το γονίδιο C9orf72 και η σχέση του με την ALS, αναλύθηκε εκτενώς στην ενότητα «Β Τα κυριότερα γονίδια», της εισαγωγής. Σύμφωνα με τη βιβλιογραφία, αριθμός αντιγράφων της εξανουκλεοτιδικής αλληλουχίας GGGGCC μεγαλύτερος των 30 βρέθηκε στο 11 % των ασθενών με ALS και σε κανέναν υγιή. Αποφασίσαμε να ελέγξουμε και τα δείγματα των ασθενών που διαθέτουμε, ως προς τον αριθμό των επαναλήψεων. Η αρχική ιδέα του σχεδιασμού στηρίχθηκε στην παρατήρηση σε πήκτωμα αγαρόζης και πολυακρυλαμιδίου του κατά προσέγγιση μεγέθους της επέκτασης. Για τον σκοπό αυτό σχεδιάστηκαν εκκινητές 5 GGAAAGTAAAAATGCGTCGAG 3 και 5 GCTCTGGAACTCAGGAGTCG 3 οι οποίοι αντιστοιχούν στον πρόσθιο και αντίστροφο εκκινητή και με την διαδικασία της PCR παράγονται πολλαπλά αντίγραφα προϊόντος 260 βάσεων. Ο σχεδιασμός παρόλο το υψηλό περιεχόμενο σε GC της περιοχής, απέδωσε εκκινητές με αποδεκτό ποσοστό GC, αποδεκτή συμπληρωματικότητα μεταξύ του πρόσθιου και του αντίστροφου εκκινητή, αλλά και κάθε εκκινητή με τον εαυτό του, 1 ευθυγράμμιση κατά το BLAST μόνο με την επιθυμητή 142
Φυσικοθεραπευτική Αντιμετώπιση σε Πλάγια Αμυοτροφική Σκλήρυνση- Νόσος του Κινητικού Νευρώνα
 ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΙΔΡΥΜΑ ΔΥΤΙΚΗΣ ΕΛΛΑΔΑΣ ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ ΦΥΣΙΚΟΘΕΡΑΠΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Φυσικοθεραπευτική Αντιμετώπιση σε Πλάγια Αμυοτροφική Σκλήρυνση- Νόσος του Κινητικού
ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΙΔΡΥΜΑ ΔΥΤΙΚΗΣ ΕΛΛΑΔΑΣ ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ ΦΥΣΙΚΟΘΕΡΑΠΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Φυσικοθεραπευτική Αντιμετώπιση σε Πλάγια Αμυοτροφική Σκλήρυνση- Νόσος του Κινητικού
Αιμοσφαιρίνες. Αιμοσφαιρίνη Συμβολισμός Σύσταση A HbA α 2 β 2 F HbF α 2 γ 2 A 2 HbA 2 α 2 δ 2 s. Σύγκριση γονιδιακών και χρωμοσωμικών μεταλλάξεων
 A. ΔΙΑΓΡΑΜΜΑ Αιμοσφαιρίνες Αιμοσφαιρίνη Συμβολισμός Σύσταση A HbA α 2 β 2 F HbF α 2 γ 2 A 2 HbA 2 α 2 δ 2 S HbS s α 2 β 2 Σύγκριση γονιδιακών και χρωμοσωμικών μεταλλάξεων ΓΟΝΙΔΙΑΚΕΣ Αλλαγή σε αζωτούχες
A. ΔΙΑΓΡΑΜΜΑ Αιμοσφαιρίνες Αιμοσφαιρίνη Συμβολισμός Σύσταση A HbA α 2 β 2 F HbF α 2 γ 2 A 2 HbA 2 α 2 δ 2 S HbS s α 2 β 2 Σύγκριση γονιδιακών και χρωμοσωμικών μεταλλάξεων ΓΟΝΙΔΙΑΚΕΣ Αλλαγή σε αζωτούχες
Εργαστηριακη διάγνωση Νευροεκφυλιστικων νοσημάτων. Χρυσούλα Νικολάου
 Εργαστηριακη διάγνωση Νευροεκφυλιστικων νοσημάτων Χρυσούλα Νικολάου Νευροεκφυλιστικά Νοσήματα Νοσολογικές οντότητες, συχνά κληρονομικής αρχής, με προσβολή συγκεκριμένων ανατομικών δομών του Ν.Σ, (επηρεάζουν
Εργαστηριακη διάγνωση Νευροεκφυλιστικων νοσημάτων Χρυσούλα Νικολάου Νευροεκφυλιστικά Νοσήματα Νοσολογικές οντότητες, συχνά κληρονομικής αρχής, με προσβολή συγκεκριμένων ανατομικών δομών του Ν.Σ, (επηρεάζουν
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Α ΣΥΝΑΠΤΙΚΗ ΟΛΟΚΛΗΡΩΣΗ
 ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Α ΣΥΝΑΠΤΙΚΗ ΟΛΟΚΛΗΡΩΣΗ Όπως συμβαίνει με τη συναπτική διαβίβαση στη νευρομυϊκή σύναψη, σε πολλές μορφές επικοινωνίας μεταξύ νευρώνων στο κεντρικό νευρικό σύστημα παρεμβαίνουν άμεσα ελεγχόμενοι
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Α ΣΥΝΑΠΤΙΚΗ ΟΛΟΚΛΗΡΩΣΗ Όπως συμβαίνει με τη συναπτική διαβίβαση στη νευρομυϊκή σύναψη, σε πολλές μορφές επικοινωνίας μεταξύ νευρώνων στο κεντρικό νευρικό σύστημα παρεμβαίνουν άμεσα ελεγχόμενοι
Βιοτεχνολογία Φυτών. Μοριακοί Δείκτες (Εισαγωγή στη Μοριακή Βιολογία)
 Βιοτεχνολογία Φυτών ΔΠΘ / Τμήμα Αγροτικής Ανάπτυξης ΠΜΣ Αειφορικά Συστήματα Παραγωγής και Περιβάλλον στη Γεωργία Μοριακοί Δείκτες (Εισαγωγή στη Μοριακή Βιολογία) Αριστοτέλης Χ. Παπαγεωργίου Εργαστήριο
Βιοτεχνολογία Φυτών ΔΠΘ / Τμήμα Αγροτικής Ανάπτυξης ΠΜΣ Αειφορικά Συστήματα Παραγωγής και Περιβάλλον στη Γεωργία Μοριακοί Δείκτες (Εισαγωγή στη Μοριακή Βιολογία) Αριστοτέλης Χ. Παπαγεωργίου Εργαστήριο
Αρχές μοριακής παθολογίας. Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ
 Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Εργαλεία Μοριακής Γενετικής
 Εργαλεία Μοριακής Γενετικής Αρχές Μοριακής κλωνοποίησης Τα περιοριστικά ένζυμα: αναγνωρίζουν αλληλουχίες (θέσεις περιορισμού). 2 τύποι ενζύμων: -Τύπος I = Κόβουν κοντά στη θέση περιορισμού -σπάνια χρησιμοποιούνται.
Εργαλεία Μοριακής Γενετικής Αρχές Μοριακής κλωνοποίησης Τα περιοριστικά ένζυμα: αναγνωρίζουν αλληλουχίες (θέσεις περιορισμού). 2 τύποι ενζύμων: -Τύπος I = Κόβουν κοντά στη θέση περιορισμού -σπάνια χρησιμοποιούνται.
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ 1ο 1. γ 2. γ 3. β 4. α 5. δ
 ΘΕΜΑ 1ο 1. γ 2. γ 3. β 4. α 5. δ 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 9 ΣΕΠΤΕΜΒΡΙΟΥ 2009 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΒΙΟΛΟΓΙΑ
ΘΕΜΑ 1ο 1. γ 2. γ 3. β 4. α 5. δ 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 9 ΣΕΠΤΕΜΒΡΙΟΥ 2009 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΒΙΟΛΟΓΙΑ
Αρχές μοριακής παθολογίας. Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ
 Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Βασικά γάγγλια. Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017
 Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017 Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί
Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017 Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί
ΝΕΥΡΟΜΥΙΚΕΣ ΠΑΘΗΣΕΙΣ ΑΝΔΡΙΤΣΟΠΟΥΛΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΓΑΣΤΡΕΝΤΕΡΟΛΟΓΟΣ - ΗΠΑΤΟΛΟΓΟΣ
 ΝΕΥΡΟΜΥΙΚΕΣ ΠΑΘΗΣΕΙΣ ΑΝΔΡΙΤΣΟΠΟΥΛΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΓΑΣΤΡΕΝΤΕΡΟΛΟΓΟΣ - ΗΠΑΤΟΛΟΓΟΣ ΤΙ ΕΙΝΑΙ ΤΑ ΝΕΥΡΟΜΥΙΚΑ ΝΟΣΗΜΑΤΑ? Τα νευρομυϊκά νοσήματα είναι ασθένειες που ενώ εμφανίζουν μεγάλη ετερογένεια στην κλινική
ΝΕΥΡΟΜΥΙΚΕΣ ΠΑΘΗΣΕΙΣ ΑΝΔΡΙΤΣΟΠΟΥΛΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΓΑΣΤΡΕΝΤΕΡΟΛΟΓΟΣ - ΗΠΑΤΟΛΟΓΟΣ ΤΙ ΕΙΝΑΙ ΤΑ ΝΕΥΡΟΜΥΙΚΑ ΝΟΣΗΜΑΤΑ? Τα νευρομυϊκά νοσήματα είναι ασθένειες που ενώ εμφανίζουν μεγάλη ετερογένεια στην κλινική
ΠΑΝΕΛΛΗΝΙΕΣ Απαντήσεις Βιολογίας κατεύθυνσης (ΗΜΕΡΗΣΙΟ)
 ΠΑΝΕΛΛΗΝΙΕΣ 2016 Απαντήσεις Βιολογίας κατεύθυνσης (ΗΜΕΡΗΣΙΟ) Μιχάλης Χαλικιόπουλος ΘΕΜΑ Α Α1 β Α2 β Α3 δ Α4 γ Α5 γ ΘΕΜΑ Β Β1 Β2 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Τα μεταφασικά χρωμοσώματα ενός κυττάρου διαφέρουν
ΠΑΝΕΛΛΗΝΙΕΣ 2016 Απαντήσεις Βιολογίας κατεύθυνσης (ΗΜΕΡΗΣΙΟ) Μιχάλης Χαλικιόπουλος ΘΕΜΑ Α Α1 β Α2 β Α3 δ Α4 γ Α5 γ ΘΕΜΑ Β Β1 Β2 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Τα μεταφασικά χρωμοσώματα ενός κυττάρου διαφέρουν
Κεφάλαιο 15 (Ιατρική Γενετική) Προγεννητική διάγνωση
 Κεφάλαιο 15 (Ιατρική Γενετική) Προγεννητική διάγνωση Η προγεννητική διάγνωση Ενδείξεις: -Προχωρημένη ηλικία μητέρας (πιο συχνό: σύνδρομο Down) -Προγενέστερο παιδί με de novo χρωμοσωμική ανωμαλία -Ύπαρξη
Κεφάλαιο 15 (Ιατρική Γενετική) Προγεννητική διάγνωση Η προγεννητική διάγνωση Ενδείξεις: -Προχωρημένη ηλικία μητέρας (πιο συχνό: σύνδρομο Down) -Προγενέστερο παιδί με de novo χρωμοσωμική ανωμαλία -Ύπαρξη
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών
 Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ
 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 2 ο 1. Με ποιο μηχανισμό αντιγράφεται το DNA σύμφωνα με τους Watson και Crick; 2. Ένα κύτταρο που περιέχει ένα μόνο χρωμόσωμα τοποθετείται σε θρεπτικό υλικό που περιέχει ραδιενεργό
ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 2 ο 1. Με ποιο μηχανισμό αντιγράφεται το DNA σύμφωνα με τους Watson και Crick; 2. Ένα κύτταρο που περιέχει ένα μόνο χρωμόσωμα τοποθετείται σε θρεπτικό υλικό που περιέχει ραδιενεργό
Βασικά γάγγλια. Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας
 Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί η πρόθεση δράσης
Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί η πρόθεση δράσης
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
Η ΔΟΜΗ ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ ΚΥΡΙΑΚΗ ΒΑΣΙΛΙΚΟΥ Γ1
 Η ΔΟΜΗ ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ ΚΥΡΙΑΚΗ ΒΑΣΙΛΙΚΟΥ Γ1 ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΣ Τρισδιάστατο δίκτυο που αποτελείται από μικροσωληνίσκους, μικροϊνίδια και ενδιάμεσα ινίδια. Οι νηματοειδείς πρωτεΐνες του
Η ΔΟΜΗ ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ ΚΥΡΙΑΚΗ ΒΑΣΙΛΙΚΟΥ Γ1 ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΣ Τρισδιάστατο δίκτυο που αποτελείται από μικροσωληνίσκους, μικροϊνίδια και ενδιάμεσα ινίδια. Οι νηματοειδείς πρωτεΐνες του
ΜΕΤΑΓΡΑΦΗ ΤΟΥ DNA ΣΕ RNA
 ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ Β ΤΡΙΜΗΝΟΥ Γ 4 23.1.12 ΜΕΤΑΓΡΑΦΗ ΤΟΥ DNA ΣΕ RNA ΕΡΓΑΣΤΗΚΑΝ: ΑΛΕΞΑΝΔΡΟΣ ΔΕΛΗΜΙΧΑΛΗΣ ΑΡΤΕΜΗΣ ΑΝΑΣΤΑΣΙΑΔΗΣ 1 ΕΙΣΑΓΩΓΗ Το δεοξυριβονουκλεϊκό οξύ (Deoxyribonucleic acid -
ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ Β ΤΡΙΜΗΝΟΥ Γ 4 23.1.12 ΜΕΤΑΓΡΑΦΗ ΤΟΥ DNA ΣΕ RNA ΕΡΓΑΣΤΗΚΑΝ: ΑΛΕΞΑΝΔΡΟΣ ΔΕΛΗΜΙΧΑΛΗΣ ΑΡΤΕΜΗΣ ΑΝΑΣΤΑΣΙΑΔΗΣ 1 ΕΙΣΑΓΩΓΗ Το δεοξυριβονουκλεϊκό οξύ (Deoxyribonucleic acid -
ΝΟΣΟΣ PARKINSON : ΜΙΑ ΑΣΘΕΝΕΙΑ ΠΟΥ ΣΧΕΤΙΖΕΤΑΙ ΜΕ ΤΗ ΜΕΙΩΣΗ ΠΑΡΑΓΩΓΗΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΩΝ
 ΝΟΣΟΣ PARKINSON : ΜΙΑ ΑΣΘΕΝΕΙΑ ΠΟΥ ΣΧΕΤΙΖΕΤΑΙ ΜΕ ΤΗ ΜΕΙΩΣΗ ΠΑΡΑΓΩΓΗΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΩΝ Η νόσος του Parkinson είναι μια προοδευτικά εξελισσόμενη, εκφυλιστική νόσος του κεντρικού νευρικού συστήματος, είναι
ΝΟΣΟΣ PARKINSON : ΜΙΑ ΑΣΘΕΝΕΙΑ ΠΟΥ ΣΧΕΤΙΖΕΤΑΙ ΜΕ ΤΗ ΜΕΙΩΣΗ ΠΑΡΑΓΩΓΗΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΩΝ Η νόσος του Parkinson είναι μια προοδευτικά εξελισσόμενη, εκφυλιστική νόσος του κεντρικού νευρικού συστήματος, είναι
Καραπέτσας Θανάσης. Διπλωματική Εργασία:
 Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Εργασία Βιολογίας Α' Λυκείου με θέμα: Μάριος Μ., Α'2. Νόσος του Πάρκινσον
 Εργασία Βιολογίας Α' Λυκείου με θέμα: Μάριος Μ., Α'2 Νόσος του Πάρκινσον Τρόπος αντιμετώπισης νόσου Πάρκινσον. Η νόσος του Πάρκινσον (Parkinson) είναι νευροεκφυλιστική ασθένεια της μέλαινας ουσίας με συχνότητα
Εργασία Βιολογίας Α' Λυκείου με θέμα: Μάριος Μ., Α'2 Νόσος του Πάρκινσον Τρόπος αντιμετώπισης νόσου Πάρκινσον. Η νόσος του Πάρκινσον (Parkinson) είναι νευροεκφυλιστική ασθένεια της μέλαινας ουσίας με συχνότητα
Ενδεικτικές απαντήσεις βιολογίας κατεύθυνσης 2014
 Θέμα Α Α1. δ Α2. γ Α3. β Α4. γ Α5. β Θέμα Β ΑΓ.ΚΩΝΣΤΑΝΤΙΝΟΥ 11 -- ΠΕΙΡΑΙΑΣ -- 18532 -- ΤΗΛ. 210-4224752, 4223687 Ενδεικτικές απαντήσεις βιολογίας κατεύθυνσης 2014 Β1. 4 2 1 6 3 5 Β2. α. DNA πολυμεράση
Θέμα Α Α1. δ Α2. γ Α3. β Α4. γ Α5. β Θέμα Β ΑΓ.ΚΩΝΣΤΑΝΤΙΝΟΥ 11 -- ΠΕΙΡΑΙΑΣ -- 18532 -- ΤΗΛ. 210-4224752, 4223687 Ενδεικτικές απαντήσεις βιολογίας κατεύθυνσης 2014 Β1. 4 2 1 6 3 5 Β2. α. DNA πολυμεράση
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α A1. α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ Β Β1. ζ στ α
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α A1. α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ Β Β1. ζ στ α
1. Πού πραγματοποιούνται η αντιγραφή και η μεταγραφή; ΘΩΜΑΣ ΑΠΑΝΤΗΣΗ. 2. Ποιες είναι οι κατηγορίες γονιδίων με κριτήριο το προϊόν της μεταγραφής τους;
 Βιολογία Γ Ενιαίου Λυκείου / Θετική Κατεύθυνση κεφαλαιο 2ο: αντιγραφη, εκφραση και ρυθμιση τησ ΓενετικηΣ ΠληροφοριαΣ 1. Πού πραγματοποιούνται η αντιγραφή και η μεταγραφή; Ευκαρυωτικά κύτταρα: στον πυρήνα,
Βιολογία Γ Ενιαίου Λυκείου / Θετική Κατεύθυνση κεφαλαιο 2ο: αντιγραφη, εκφραση και ρυθμιση τησ ΓενετικηΣ ΠληροφοριαΣ 1. Πού πραγματοποιούνται η αντιγραφή και η μεταγραφή; Ευκαρυωτικά κύτταρα: στον πυρήνα,
Φάσμα group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι.
 σύγχρονο Φάσμα group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. µαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990
σύγχρονο Φάσμα group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. µαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990
ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις:
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΟΠ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 18/09/2016 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΝΟΤΑ ΛΑΖΑΡΑΚΗ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Η Χαρά
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΟΠ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 18/09/2016 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΝΟΤΑ ΛΑΖΑΡΑΚΗ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Η Χαρά
Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki M.
 10th Panhellenic Conference of Alzheimer's Disease and Related Disorders (PICAD) and 2nd Mediterranean Conference of Neurodegenerative Diseases (MeCOND) Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki
10th Panhellenic Conference of Alzheimer's Disease and Related Disorders (PICAD) and 2nd Mediterranean Conference of Neurodegenerative Diseases (MeCOND) Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki
ΜΟΡΙΑΚΗ ΒΑΣΗ ΓΕΝΕΤΙΚΩΝ ΑΣΘΕΝΕΙΩΝ ΘΕΜΑ: ΠΟΛΛΑΠΛΗ ΝΕΥΡΟΙΝΩΜΑΤΩΣΗ. Ομάδα ΑΡΕΑΛΗ ΑΝΤΩΝΙΑ ΜΠΑΗ ΙΩΑΝΝΑ ΠΑΤΕΡΑΚΗ ΕΛΕΝΗ
 ΜΟΡΙΑΚΗ ΒΑΣΗ ΓΕΝΕΤΙΚΩΝ ΑΣΘΕΝΕΙΩΝ ΘΕΜΑ: ΠΟΛΛΑΠΛΗ ΝΕΥΡΟΙΝΩΜΑΤΩΣΗ Ομάδα ΑΡΕΑΛΗ ΑΝΤΩΝΙΑ ΜΠΑΗ ΙΩΑΝΝΑ ΠΑΤΕΡΑΚΗ ΕΛΕΝΗ ΑΠΡΙΛΙΟΣ 2015 ΣΚΟΠΟΣ Σκοπός της εργασίας αυτής είναι η παρουσίαση των χαρακτηριστικών της
ΜΟΡΙΑΚΗ ΒΑΣΗ ΓΕΝΕΤΙΚΩΝ ΑΣΘΕΝΕΙΩΝ ΘΕΜΑ: ΠΟΛΛΑΠΛΗ ΝΕΥΡΟΙΝΩΜΑΤΩΣΗ Ομάδα ΑΡΕΑΛΗ ΑΝΤΩΝΙΑ ΜΠΑΗ ΙΩΑΝΝΑ ΠΑΤΕΡΑΚΗ ΕΛΕΝΗ ΑΠΡΙΛΙΟΣ 2015 ΣΚΟΠΟΣ Σκοπός της εργασίας αυτής είναι η παρουσίαση των χαρακτηριστικών της
Νικόλαος Σιαφάκας Λέκτορας Διαγνωστικής Ιολογίας Εργαστήριο Κλινικής Μικροβιολογίας ΠΓΝ «ΑΤΤΙΚΟΝ»
 Νικόλαος Σιαφάκας Λέκτορας Διαγνωστικής Ιολογίας Εργαστήριο Κλινικής Μικροβιολογίας ΠΓΝ «ΑΤΤΙΚΟΝ» DNA RNA: ΑΝΤΙΓΡΑΦΗ, ΜΕΤΑΓΡΑΦΗ, ΜΕΤΑΦΡΑΣΗ DNA RNA: Βασικά Χαρακτηριστικά Ρόλος Κεντικό Δόγμα της Βιολογίας:
Νικόλαος Σιαφάκας Λέκτορας Διαγνωστικής Ιολογίας Εργαστήριο Κλινικής Μικροβιολογίας ΠΓΝ «ΑΤΤΙΚΟΝ» DNA RNA: ΑΝΤΙΓΡΑΦΗ, ΜΕΤΑΓΡΑΦΗ, ΜΕΤΑΦΡΑΣΗ DNA RNA: Βασικά Χαρακτηριστικά Ρόλος Κεντικό Δόγμα της Βιολογίας:
ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΘΝΙΚΟΥ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΕΡΕΥΝΑΣ Β'ΠΡΟΠΑΙΔΕΥΤΙΚΗΣ ΠΑΘΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΚΑΘΗΓΗΤΗΣ Θ.
 ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΘΝΙΚΟΥ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΕΡΕΥΝΑΣ Β'ΠΡΟΠΑΙΔΕΥΤΙΚΗΣ ΠΑΘΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΚΑΘΗΓΗΤΗΣ Θ. ΟΙΚΟΝΟΜΟΠΟΥΛΟΣ 1 ΙΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΒΙΟΛΟΓΟΣ: ΕΡΙΦΥΛΗ ΚΥΡΙΑΖΗ
ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΘΝΙΚΟΥ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΕΡΕΥΝΑΣ Β'ΠΡΟΠΑΙΔΕΥΤΙΚΗΣ ΠΑΘΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΚΑΘΗΓΗΤΗΣ Θ. ΟΙΚΟΝΟΜΟΠΟΥΛΟΣ 1 ΙΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΒΙΟΛΟΓΟΣ: ΕΡΙΦΥΛΗ ΚΥΡΙΑΖΗ
Α2. Το αντικωδικόνιο είναι τριπλέτα νουκλεοτιδίων του α. mrna β. snrna γ. trna δ. rrna Μονάδες 5
 ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις Α1 έως Α5 και δίπλα στο γράμμα που αντιστοιχεί στη λέξη ή στη φράση, η οποία συμπληρώνει
ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις Α1 έως Α5 και δίπλα στο γράμμα που αντιστοιχεί στη λέξη ή στη φράση, η οποία συμπληρώνει
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο 1. β 2. γ 3. α 4. γ 5. δ ΘΕΜΑ 2ο 1. Σχολικό
1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο 1. β 2. γ 3. α 4. γ 5. δ ΘΕΜΑ 2ο 1. Σχολικό
Κεφάλαιο 1 ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΝΕΥΡΟΦΥΣΙΟΛΟΓΙΑΣ
 Κεφάλαιο 1 ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΝΕΥΡΟΦΥΣΙΟΛΟΓΙΑΣ 1.1. Εισαγωγή Ο ζωντανός οργανισµός έχει την ικανότητα να αντιδρά σε µεταβολές που συµβαίνουν στο περιβάλλον και στο εσωτερικό του. Οι µεταβολές αυτές ονοµάζονται
Κεφάλαιο 1 ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΝΕΥΡΟΦΥΣΙΟΛΟΓΙΑΣ 1.1. Εισαγωγή Ο ζωντανός οργανισµός έχει την ικανότητα να αντιδρά σε µεταβολές που συµβαίνουν στο περιβάλλον και στο εσωτερικό του. Οι µεταβολές αυτές ονοµάζονται
ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ
 27 Μαΐου 2016 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων (Νέο & Παλιό Σύστημα) ΘΕΜΑ Γ Γ.1 Ο χαρακτήρας της ομάδας αίματος στον άνθρωπο
27 Μαΐου 2016 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων (Νέο & Παλιό Σύστημα) ΘΕΜΑ Γ Γ.1 Ο χαρακτήρας της ομάδας αίματος στον άνθρωπο
ALS. Βασιλική-Ελευθερία Περδίου & Σοφία Ρεσίτη. Τμήμα: Α 5
 ALS Βασιλική-Ελευθερία Περδίου & Σοφία Ρεσίτη Τμήμα: Α 5 Τι είναι η Αμυοτροφική Πλάγια Σκλήρυνση (ALS)? Η πάθηση αυτή είναι γνωστή και ως αμυοτροφική πλάγια σκλήρυνση είναι μια προοδευτική νευροεκφυλιστική
ALS Βασιλική-Ελευθερία Περδίου & Σοφία Ρεσίτη Τμήμα: Α 5 Τι είναι η Αμυοτροφική Πλάγια Σκλήρυνση (ALS)? Η πάθηση αυτή είναι γνωστή και ως αμυοτροφική πλάγια σκλήρυνση είναι μια προοδευτική νευροεκφυλιστική
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1 δ Α2 γ Α3 β Α4 γ Α5 β ΘΕΜΑ Β Β1 Κατά σειρά τα βήματα που οδηγούν στην κατασκευή του καρυότυπου είναι τα ακόλουθα: 4 2 1 6 3 5 Β2 α DNA πολυμεράσες
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΘΕΜΑ Α Α1 δ Α2 γ Α3 β Α4 γ Α5 β ΘΕΜΑ Β Β1 Κατά σειρά τα βήματα που οδηγούν στην κατασκευή του καρυότυπου είναι τα ακόλουθα: 4 2 1 6 3 5 Β2 α DNA πολυμεράσες
 Νόσος Parkinson-Νέοι ορίζοντες Ξηροµερήσιου Γεωργία Νευρολόγος-Μέλος ερευνητικής οµάδας Νευρογενετικής Αίτια της νόσου Parkinson Περιβαλλοντικοί παράγοντες Γενετικοί παράγοντες Γενετική βλάβη (παθογόνα
Νόσος Parkinson-Νέοι ορίζοντες Ξηροµερήσιου Γεωργία Νευρολόγος-Μέλος ερευνητικής οµάδας Νευρογενετικής Αίτια της νόσου Parkinson Περιβαλλοντικοί παράγοντες Γενετικοί παράγοντες Γενετική βλάβη (παθογόνα
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 11 ΙΟΥΝΙΟΥ 2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 11 ΙΟΥΝΙΟΥ 2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. β Α2. γ Α3. α Α4. γ Α5. δ ΘΕΜΑ Β Β1.
1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 11 ΙΟΥΝΙΟΥ 2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. β Α2. γ Α3. α Α4. γ Α5. δ ΘΕΜΑ Β Β1.
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑ 1 Ο Α. Να επιλέξετε την ορθή πρόταση: ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1. Το κωδικόνιο του mrna που κωδικοποιεί το αµινοξύ µεθειονίνη είναι α. 5 GUA
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ο.Ε.Φ.Ε. 2004 ΘΕΜΑ 1 Ο Α. Να επιλέξετε την ορθή πρόταση: ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1. Το κωδικόνιο του mrna που κωδικοποιεί το αµινοξύ µεθειονίνη είναι α. 5 GUA
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Ετυμολογία του ακρωνύμου A.L.S
 Ετυμολογία του ακρωνύμου A.L.S Αμυοτροφική είναι ένα σύνθετο επίθετο Ελληνικής προέλευσης. Αποτελείται από το στερητικό Α που σημαίνει χωρίς ή άνευ ή μη. Επίσης, τη λέξη μύο που αναφέρεται στους μύες και
Ετυμολογία του ακρωνύμου A.L.S Αμυοτροφική είναι ένα σύνθετο επίθετο Ελληνικής προέλευσης. Αποτελείται από το στερητικό Α που σημαίνει χωρίς ή άνευ ή μη. Επίσης, τη λέξη μύο που αναφέρεται στους μύες και
αμινοξύ. Η αλλαγή αυτή έχει ελάχιστη επίδραση στη στερεοδιάταξη και τη λειτουργικότητα της πρωτεϊνης. Επιβλαβής
 Κεφάλαιο 6: ΜΕΤΑΛΛΑΞΕΙΣ -ΘΕΩΡΙΑ- Μεταλλάξεις είναι οι αλλαγές που συμβαίνουν στο γενετικό υλικό ενός οργανισμού, τόσο σε γονιδιακό επίπεδο (γονιδιακές μεταλλάξεις) όσο και σε χρωμοσωμικό επίπεδο (χρωμοσωμικές
Κεφάλαιο 6: ΜΕΤΑΛΛΑΞΕΙΣ -ΘΕΩΡΙΑ- Μεταλλάξεις είναι οι αλλαγές που συμβαίνουν στο γενετικό υλικό ενός οργανισμού, τόσο σε γονιδιακό επίπεδο (γονιδιακές μεταλλάξεις) όσο και σε χρωμοσωμικό επίπεδο (χρωμοσωμικές
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων. Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014. Απαντήσεις Θεμάτων
 Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Βιολογία Α Λυκείου Κεφ. 9. Νευρικό Σύστημα. Δομή και λειτουργία των νευρικών κυττάρων
 Βιολογία Α Λυκείου Κεφ. 9 Νευρικό Σύστημα Δομή και λειτουργία των νευρικών κυττάρων Νευρικό Σύστημα Το νευρικό σύστημα μαζί με το σύστημα των ενδοκρινών αδένων φροντίζουν να διατηρείται σταθερό το εσωτερικό
Βιολογία Α Λυκείου Κεφ. 9 Νευρικό Σύστημα Δομή και λειτουργία των νευρικών κυττάρων Νευρικό Σύστημα Το νευρικό σύστημα μαζί με το σύστημα των ενδοκρινών αδένων φροντίζουν να διατηρείται σταθερό το εσωτερικό
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου
 Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Η αναλογία Α+G/T+C στο γενετικό υλικό ενός ιού είναι ίση με 2/3. Ο ιός μπορεί να είναι: α. ο φάγος λ. β. ο ιός της πολιομυελίτιδας. γ. φορέας κλωνοποίησης
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Η αναλογία Α+G/T+C στο γενετικό υλικό ενός ιού είναι ίση με 2/3. Ο ιός μπορεί να είναι: α. ο φάγος λ. β. ο ιός της πολιομυελίτιδας. γ. φορέας κλωνοποίησης
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΤΟ DNA ΚΑΙ RNA. Θανος Εξαρχου Γ1
 ΤΟ DNA ΚΑΙ RNA Θανος Εξαρχου Γ1 ΤΟ DNA Το δε(σ)οξυριβο(ζο)νουκλεϊ(νι)κό οξu είναι νουκλεϊκό οξύ που περιέχει τις γενετικές πληροφορίες που καθορίζουν τη βιολογική ανάπτυξη όλων των κυτταρικών μορφών ζωής
ΤΟ DNA ΚΑΙ RNA Θανος Εξαρχου Γ1 ΤΟ DNA Το δε(σ)οξυριβο(ζο)νουκλεϊ(νι)κό οξu είναι νουκλεϊκό οξύ που περιέχει τις γενετικές πληροφορίες που καθορίζουν τη βιολογική ανάπτυξη όλων των κυτταρικών μορφών ζωής
ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ
 ΑΣΘΕΝΕΙΕΣ ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑΣ ΣΥΝΕΠΕΙΕΣ ΕΙΔΟΣ ΜΕΤΑΛΛΑΞΗΣ Οικογενή υπερχοληστερολαιμία Αυτοσωμική επικρατής κληρονομικότητα Σχετίζεται με αυξημένο
ΑΣΘΕΝΕΙΕΣ ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑΣ ΣΥΝΕΠΕΙΕΣ ΕΙΔΟΣ ΜΕΤΑΛΛΑΞΗΣ Οικογενή υπερχοληστερολαιμία Αυτοσωμική επικρατής κληρονομικότητα Σχετίζεται με αυξημένο
ΘΕΜΑ 1 Ο ΜΑΘΗΜΑ / ΤΑΞΗ : ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 01/12/2013
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 01/12/2013 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Τα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΑΠΑΝΤΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 01/12/2013 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Τα
Κληρονοµικά νοσήµατα και καταστάσεις που οφείλονται σε γονιδιακές µεταλλάξεις
 Κληρονοµικά νοσήµατα και καταστάσεις που οφείλονται σε γονιδιακές µεταλλάξεις ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΗΣΗΣ ΤΩΝ ΚΥΡΙΟΤΕΡΩΝ ΚΛΗΡΟΝΟΜΙΚΩΝ ΝΟΣΩΝ ΑΥΤΟΣΩΜΙΚΗ ΕΠΙΚΡΑΤΗΣ ΑΥΤΟΣΩΜΙΚΗ ΥΠΟΛΕΙΠΟΜΕΝΗ ΦΥΛΟΣΥΝ ΕΤΗ ΥΠΟΛΕΙΠΟΜΕΝΗ
Κληρονοµικά νοσήµατα και καταστάσεις που οφείλονται σε γονιδιακές µεταλλάξεις ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΗΣΗΣ ΤΩΝ ΚΥΡΙΟΤΕΡΩΝ ΚΛΗΡΟΝΟΜΙΚΩΝ ΝΟΣΩΝ ΑΥΤΟΣΩΜΙΚΗ ΕΠΙΚΡΑΤΗΣ ΑΥΤΟΣΩΜΙΚΗ ΥΠΟΛΕΙΠΟΜΕΝΗ ΦΥΛΟΣΥΝ ΕΤΗ ΥΠΟΛΕΙΠΟΜΕΝΗ
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Τρίτη 18 Ιουνίου 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ. (Ενδεικτικές Απαντήσεις)
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Τρίτη 18 Ιουνίου 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (Ενδεικτικές Απαντήσεις) ΘΕΜΑ Α Α1. α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ Β Β1. 1-ζ 2-στ
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Τρίτη 18 Ιουνίου 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (Ενδεικτικές Απαντήσεις) ΘΕΜΑ Α Α1. α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ Β Β1. 1-ζ 2-στ
ΦΡΟΝΤΙΣΤΗΡΙΟ «ΕΝΑ» ΓΙΟΜΠΛΙΑΚΗΣ ΛΑΖΑΡΟΣ ΠΕΤΡΟΜΕΛΙΔΗΣ ΒΑΣΙΛΗΣ
 ΦΡΟΝΤΙΣΤΗΡΙΟ «ΕΝΑ» ΓΙΟΜΠΛΙΑΚΗΣ ΛΑΖΑΡΟΣ ΠΕΤΡΟΜΕΛΙΔΗΣ ΒΑΣΙΛΗΣ ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Α. Να βάλετε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Ο µέγιστος αριθµός διαφορετικών
ΦΡΟΝΤΙΣΤΗΡΙΟ «ΕΝΑ» ΓΙΟΜΠΛΙΑΚΗΣ ΛΑΖΑΡΟΣ ΠΕΤΡΟΜΕΛΙΔΗΣ ΒΑΣΙΛΗΣ ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Α. Να βάλετε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Ο µέγιστος αριθµός διαφορετικών
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
3. Η μέθοδος αλυσιδωτής αντίδρασης πολυμεράσης (PCR) επιτρέπει την επιλεκτική αντιγραφή μορίων DNA, χωρίς τη μεσολάβηση ζωικών κυττάρων.
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΘΕΜΑ 1ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 3 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΤΕΣΣΕΡΙΣ (4) Α. Να γράψετε τον αριθμό της
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΘΕΜΑ 1ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 3 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΤΕΣΣΕΡΙΣ (4) Α. Να γράψετε τον αριθμό της
ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ 24 ΜΑΪΟΥ 2013
 ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ 24 ΜΑΪΟΥ 2013 ΘΕΜΑ Α Α1. γ Α2. β Α3. α Α4. δ Α5. α ΘΕΜΑ Β Β1. Σελ. 123 124 σχολ. βιβλίου: «Η διαδικασία που ακολουθείται παράγουν το ένζυμο ADA». Β2. Σελ. 133 σχολ.
ΑΠΑΝΤΗΣΕΙΣ ΣΤΗ ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ 24 ΜΑΪΟΥ 2013 ΘΕΜΑ Α Α1. γ Α2. β Α3. α Α4. δ Α5. α ΘΕΜΑ Β Β1. Σελ. 123 124 σχολ. βιβλίου: «Η διαδικασία που ακολουθείται παράγουν το ένζυμο ADA». Β2. Σελ. 133 σχολ.
ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2018
 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ
ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΔΕΥΤΕΡΑ 10 ΣΕΠΤΕΜΒΡΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΣΤΑ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 2014
 ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΣΤΑ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 2014 ΘΕΜΑ Α Α1. δ Α2. γ Α3. β Α4. γ Α5. β ΘΕΜΑ Β Β1. Η σειρά των βημάτων που οδηγούν στην κατασκευή καρυότυπου είναι: 4, 2, 1, 6, 3, 5 Β2. α.
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΣΤΑ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 2014 ΘΕΜΑ Α Α1. δ Α2. γ Α3. β Α4. γ Α5. β ΘΕΜΑ Β Β1. Η σειρά των βημάτων που οδηγούν στην κατασκευή καρυότυπου είναι: 4, 2, 1, 6, 3, 5 Β2. α.
Βιολογία Κατεύθυνσης Γ Λυκείου ΚΥΡΙΑΚΗ 9 ΜΑΡΤΙΟΥ 2014 ΑΠΑΝΤΗΣΕΙΣ
 Βιολογία Κατεύθυνσης Γ Λυκείου ΚΥΡΙΑΚΗ 9 ΜΑΡΤΙΟΥ 2014 ΑΠΑΝΤΗΣΕΙΣ Επιμέλεια: Δημήτρης Κοτρόπουλος ΘΕΜΑ Α Α1. γ Α2. γ Α3. γ Α4. δ Α5. δ ΘΕΜΑ B B1. Στήλη Ι Στήλη ΙΙ 1. στ 2. ζ 3. ε 4. α 5. δ 6. β 7. γ Β2.
Βιολογία Κατεύθυνσης Γ Λυκείου ΚΥΡΙΑΚΗ 9 ΜΑΡΤΙΟΥ 2014 ΑΠΑΝΤΗΣΕΙΣ Επιμέλεια: Δημήτρης Κοτρόπουλος ΘΕΜΑ Α Α1. γ Α2. γ Α3. γ Α4. δ Α5. δ ΘΕΜΑ B B1. Στήλη Ι Στήλη ΙΙ 1. στ 2. ζ 3. ε 4. α 5. δ 6. β 7. γ Β2.
ΓΕΝΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ. Μαντώ Κυριακού 2015
 ΓΕΝΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Μαντώ Κυριακού 2015 Ενεργειακό Στα βιολογικά συστήματα η διατήρηση της ενέργειας συμπεριλαμβάνει οξειδοαναγωγικές αντιδράσεις παραγωγή ATP Οξείδωση: απομάκρυνση e από ένα υπόστρωμα
ΓΕΝΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Μαντώ Κυριακού 2015 Ενεργειακό Στα βιολογικά συστήματα η διατήρηση της ενέργειας συμπεριλαμβάνει οξειδοαναγωγικές αντιδράσεις παραγωγή ATP Οξείδωση: απομάκρυνση e από ένα υπόστρωμα
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων. Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014. Απαντήσεις Θεμάτων
 Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Kυτταρική Bιολογία. Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος ΔIAΛEΞΗ 20 (9/5/2017) Δρ. Xρήστος Παναγιωτίδης, Τμήμα Φαρμακευτικής Α.Π.Θ.
 Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
Θεωρία - Εφαρμογές ΓΕΝΕΤΙΚΗ ΒΕΛΤΙΩΣΗ ΦΥΤΩΝ - ΜΟΡΙΑΚΟΙ ΔΕΙΚΤΕΣ 1
 ΜΟΡΙΑΚΟΙ ΔΕΙΚΤΕΣ Θεωρία - Εφαρμογές ΓΕΝΕΤΙΚΗ ΒΕΛΤΙΩΣΗ ΦΥΤΩΝ - ΜΟΡΙΑΚΟΙ ΔΕΙΚΤΕΣ 1 ΕΙΣΑΓΩΓΗ ΣΤΟΥΣ ΜΟΡΙΑΚΟΥΣ Έπιλογή με βάση: ΔΕΙΚΤΕΣ Φαινοτυπικοί δείκτες Γενετικοί δείκτες Μοριακοί δείκτες (Πρωτεϊνικοί &
ΜΟΡΙΑΚΟΙ ΔΕΙΚΤΕΣ Θεωρία - Εφαρμογές ΓΕΝΕΤΙΚΗ ΒΕΛΤΙΩΣΗ ΦΥΤΩΝ - ΜΟΡΙΑΚΟΙ ΔΕΙΚΤΕΣ 1 ΕΙΣΑΓΩΓΗ ΣΤΟΥΣ ΜΟΡΙΑΚΟΥΣ Έπιλογή με βάση: ΔΕΙΚΤΕΣ Φαινοτυπικοί δείκτες Γενετικοί δείκτες Μοριακοί δείκτες (Πρωτεϊνικοί &
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ Ημερομηνία: Τετάρτη 4 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ Ημερομηνία: Τετάρτη 4 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ. ΘΕΜΑ Β Β1. Στήλη Ι Στήλη ΙΙ 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ
 ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ 1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β) ΠΑΡΑΣΚΕΥΗ 27 ΜΑΪΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ ΣΥΣΤΗΜΑ) ΒΙΟΛΟΓΙΑ
ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ 1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β) ΠΑΡΑΣΚΕΥΗ 27 ΜΑΪΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ ΣΥΣΤΗΜΑ) ΒΙΟΛΟΓΙΑ
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ Α A1. β Α2. γ Α3. γ Α4. α Α5. δ
 ΘΕΜΑ Α A1. β Α2. γ Α3. γ Α4. α Α5. δ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΤΕΤΑΡΤΗ 15 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ
ΘΕΜΑ Α A1. β Α2. γ Α3. γ Α4. α Α5. δ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΤΕΤΑΡΤΗ 15 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΕΛΕΓΧΟΣ ΓΟΝΙΔΙΑΚΩΝ ΣΥΧΝΟΤΗΤΩΝ ACAA2 ΣΤΟ ΕΞΩΝΙΟ 10 ΣΤΑ ΠΡΟΒΑΤΑ ΧΙΟΥ Μύρια Χατζηκώστα Λεμεσός, 2013
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΕΛΕΓΧΟΣ ΓΟΝΙΔΙΑΚΩΝ ΣΥΧΝΟΤΗΤΩΝ ACAA2 ΣΤΟ ΕΞΩΝΙΟ 10 ΣΤΑ ΠΡΟΒΑΤΑ ΧΙΟΥ Μύρια Χατζηκώστα Λεμεσός, 2013
gr ΜΟΥΓΙΟΣ Β.
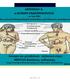 1ο Πανελλήνιο Συνέδριο ΙΒΙΣ «Βιολογία-Ιατρική Συστημάτων & Στρες» Άσκηση και μεταβολικόοξιδωτικό στρες Βασίλης Μούγιος Τμήμα Επιστήμης Φυσικής Αγωγής και Αθλητισμού με έδρα τη Θεσσαλονίκη Αριστοτέλειο
1ο Πανελλήνιο Συνέδριο ΙΒΙΣ «Βιολογία-Ιατρική Συστημάτων & Στρες» Άσκηση και μεταβολικόοξιδωτικό στρες Βασίλης Μούγιος Τμήμα Επιστήμης Φυσικής Αγωγής και Αθλητισμού με έδρα τη Θεσσαλονίκη Αριστοτέλειο
Ρευματολογία. Ψωριασική Αρθρίτιδα. Στέφανος Πατεράκης Φυσικοθεραπευτής, καθηγητής φυσ/πείας
 Ρευματολογία Ψωριασική Αρθρίτιδα Στέφανος Πατεράκης Φυσικοθεραπευτής, καθηγητής φυσ/πείας Τι είναι η ψωριασική αρθρίτιδα; Η ψωριασική αρθρίτιδα είναι μια χρόνια φλεγμονώδης πάθηση που προσβάλλει τις αρθρώσεις
Ρευματολογία Ψωριασική Αρθρίτιδα Στέφανος Πατεράκης Φυσικοθεραπευτής, καθηγητής φυσ/πείας Τι είναι η ψωριασική αρθρίτιδα; Η ψωριασική αρθρίτιδα είναι μια χρόνια φλεγμονώδης πάθηση που προσβάλλει τις αρθρώσεις
ΓΕΝΕΤΙΚΗ ΜΗΧΑΝΙΚΗ. Η τεχνολογία του ανασυνδυασμένου DNA και οι εφαρμογές της...
 ΓΕΝΕΤΙΚΗ ΜΗΧΑΝΙΚΗ Η τεχνολογία του ανασυνδυασμένου DNA και οι εφαρμογές της... Γενετική Μηχανική o Περιλαμβάνει όλες τις τεχνικές με τις οποίες μπορούμε να επεμβαίνουμε στο γενετικό υλικό των οργανισμών.
ΓΕΝΕΤΙΚΗ ΜΗΧΑΝΙΚΗ Η τεχνολογία του ανασυνδυασμένου DNA και οι εφαρμογές της... Γενετική Μηχανική o Περιλαμβάνει όλες τις τεχνικές με τις οποίες μπορούμε να επεμβαίνουμε στο γενετικό υλικό των οργανισμών.
Ελεύθερες ρίζες και αντιοξειδωτικά
 Ελεύθερες ρίζες και αντιοξειδωτικά Κατά τη διάρκεια των φυσιολογικών ανθρώπινων διεργασιών παραγωγή ενέργειας, αποτοξίνωση από τοξικές ουσίες και ανοσολογική απόκριση, παράγονται από τον οργανισµό ελεύθερες
Ελεύθερες ρίζες και αντιοξειδωτικά Κατά τη διάρκεια των φυσιολογικών ανθρώπινων διεργασιών παραγωγή ενέργειας, αποτοξίνωση από τοξικές ουσίες και ανοσολογική απόκριση, παράγονται από τον οργανισµό ελεύθερες
ΚΡΙΤΗΡΙΟ ΑΞΙΟΛΟΓΗΣΗΣ ΣΤΗ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΞΕΤΑΣΤΕΑ ΥΛΗ: ΚΕΦΑΛΑΙΑ 1, 2, 4, 5 και 6
 ΚΡΙΤΗΡΙΟ ΑΞΙΟΛΟΓΗΣΗΣ ΣΤΗ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΞΕΤΑΣΤΕΑ ΥΛΗ: ΚΕΦΑΛΑΙΑ 1, 2, 4, 5 και 6 ΦΡΟΝΤΙΣΤΗΡΙΟ: ΚΟΡΥΦΑΙΟ ΗΜΕΡΟΜΗΝΙΑ: 20 / 02 / 2016 ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΕΞΕΤΑΖΟΜΕΝΟΥ:. ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ
ΚΡΙΤΗΡΙΟ ΑΞΙΟΛΟΓΗΣΗΣ ΣΤΗ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΞΕΤΑΣΤΕΑ ΥΛΗ: ΚΕΦΑΛΑΙΑ 1, 2, 4, 5 και 6 ΦΡΟΝΤΙΣΤΗΡΙΟ: ΚΟΡΥΦΑΙΟ ΗΜΕΡΟΜΗΝΙΑ: 20 / 02 / 2016 ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΕΞΕΤΑΖΟΜΕΝΟΥ:. ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ
ΣΥΣΧΕΤΙΣΗ ΓΕΝΕΤΙΚΩΝ ΠΟΛΥΜΟΡΦΙΣΜΩΝ ΣΤΟ ΓΟΝΙ Ι0 MYD88 ΜΕ ΤΗΝ ΑΝΑΠΤΥΞΗ ΦΥΜΑΤΙΩΣΗΣ
 ΣΥΣΧΕΤΙΣΗ ΓΕΝΕΤΙΚΩΝ ΠΟΛΥΜΟΡΦΙΣΜΩΝ ΣΤΟ ΓΟΝΙ Ι MYD88 ΜΕ ΤΗΝ ΑΝΑΠΤΥΞΗ ΦΥΜΑΤΙΩΣΗΣ Φωτεινή Μάλλη 1, Ειρήνη Γερογιάννη 1 Καλλιόπη Αγγέλου 1, Βίκυ Μολλάκη 2, Φωτεινή Μπαρδάκα 1, Κωνσταντίνος Ι. Γουργουλιάνης
ΣΥΣΧΕΤΙΣΗ ΓΕΝΕΤΙΚΩΝ ΠΟΛΥΜΟΡΦΙΣΜΩΝ ΣΤΟ ΓΟΝΙ Ι MYD88 ΜΕ ΤΗΝ ΑΝΑΠΤΥΞΗ ΦΥΜΑΤΙΩΣΗΣ Φωτεινή Μάλλη 1, Ειρήνη Γερογιάννη 1 Καλλιόπη Αγγέλου 1, Βίκυ Μολλάκη 2, Φωτεινή Μπαρδάκα 1, Κωνσταντίνος Ι. Γουργουλιάνης
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Β ΔΙΑΒΙΒΑΣΗ ΣΤΗ ΝΕΥΡΟΜΥΪΚΗ ΣΥΝΑΨΗ
 ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Β ΔΙΑΒΙΒΑΣΗ ΣΤΗ ΝΕΥΡΟΜΥΪΚΗ ΣΥΝΑΨΗ Η νευρομυϊκή σύναψη αποτελεί ιδιαίτερη μορφή σύναψης μεταξύ του κινητικού νευρώνα και της σκελετικής μυϊκής ίνας Είναι ορατή με το οπτικό μικροσκόπιο Στην
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Β ΔΙΑΒΙΒΑΣΗ ΣΤΗ ΝΕΥΡΟΜΥΪΚΗ ΣΥΝΑΨΗ Η νευρομυϊκή σύναψη αποτελεί ιδιαίτερη μορφή σύναψης μεταξύ του κινητικού νευρώνα και της σκελετικής μυϊκής ίνας Είναι ορατή με το οπτικό μικροσκόπιο Στην
ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ
 1 ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ Οι δύο πολυνουκλεοτιδικές αλυσίδες του DNA αποτελούνται από νουκλεοτίδια τα οποία ενώνονται με φωσφοδιεστερικούς δεσμούς. Πιο συγκεκριμένα
1 ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ Οι δύο πολυνουκλεοτιδικές αλυσίδες του DNA αποτελούνται από νουκλεοτίδια τα οποία ενώνονται με φωσφοδιεστερικούς δεσμούς. Πιο συγκεκριμένα
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ
 ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α: Α1. δ Α2. γ Α3. β Α4. γ Α5. β ΘΕΜΑ Β: Β1. 4 2 1 6 3 5 Β2. α. DNA πολυμεράση β. Πριμόσωμα γ. DNA δεσμάση δ. DNA ελικάση ε. RNA πολυμεράση Β3.
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α: Α1. δ Α2. γ Α3. β Α4. γ Α5. β ΘΕΜΑ Β: Β1. 4 2 1 6 3 5 Β2. α. DNA πολυμεράση β. Πριμόσωμα γ. DNA δεσμάση δ. DNA ελικάση ε. RNA πολυμεράση Β3.
Γονιδιωματική. G. Patrinos
 Γονιδιωματική Η μεταγονιδιωματική εποχή... Σημαντικότερα επιτεύγματα POST GENOME ERA Ολοκλήρωση της αποκρυπτογράφησης της αλληλουχίας των γονιδιωμάτων πολλών οργανισμών. Προτύπωση μεθοδολογιών για προσδιορισμό
Γονιδιωματική Η μεταγονιδιωματική εποχή... Σημαντικότερα επιτεύγματα POST GENOME ERA Ολοκλήρωση της αποκρυπτογράφησης της αλληλουχίας των γονιδιωμάτων πολλών οργανισμών. Προτύπωση μεθοδολογιών για προσδιορισμό
Τελικό κείμενο της Μελέτης. Σύνδρομο Πολυκυστικών Ωοθηκών: Διατροφή και Υγεία
 Τελικό κείμενο της Μελέτης Σύνδρομο Πολυκυστικών Ωοθηκών: Διατροφή και Υγεία Τα τελικά προϊόντα προχωρημένης γλυκοζυλίωσης (Advanced Glycation End products, ) είναι μόρια υψηλής δραστικότητας, τα οποία
Τελικό κείμενο της Μελέτης Σύνδρομο Πολυκυστικών Ωοθηκών: Διατροφή και Υγεία Τα τελικά προϊόντα προχωρημένης γλυκοζυλίωσης (Advanced Glycation End products, ) είναι μόρια υψηλής δραστικότητας, τα οποία
Βιολογία προσανατολισμού
 Βιολογία προσανατολισμού Α. 1. β. 2. γ. 3. γ. 4. α. 5. δ. ΘΕΜΑ Α ΘΕΜΑ Β Β1. Σχολικό βιβλίο σελ. 131 «Το βακτήριο... στο σώμα των φυτών.» Β2.1 Ε, 2 Δ, 3 Α, 4 Β Β3. Σχολικό βιβλίο σελ. 108 «Η θερμοκρασία..
Βιολογία προσανατολισμού Α. 1. β. 2. γ. 3. γ. 4. α. 5. δ. ΘΕΜΑ Α ΘΕΜΑ Β Β1. Σχολικό βιβλίο σελ. 131 «Το βακτήριο... στο σώμα των φυτών.» Β2.1 Ε, 2 Δ, 3 Α, 4 Β Β3. Σχολικό βιβλίο σελ. 108 «Η θερμοκρασία..
Πανεπιστήμιο Θεσσαλίας Τμήμα βιοχημείας και βιοτεχνολογίας
 Πανεπιστήμιο Θεσσαλίας Τμήμα βιοχημείας και βιοτεχνολογίας Διδακτική με έμφαση στις βιοεπιστήμες Μαρία Ευαγγελία Βασιλογιάννη Στοιχεία Μαθήματος 1. Μάθημα : Βιολογία 2. Τίτλος ενότητας: Η ροή της γενετικής
Πανεπιστήμιο Θεσσαλίας Τμήμα βιοχημείας και βιοτεχνολογίας Διδακτική με έμφαση στις βιοεπιστήμες Μαρία Ευαγγελία Βασιλογιάννη Στοιχεία Μαθήματος 1. Μάθημα : Βιολογία 2. Τίτλος ενότητας: Η ροή της γενετικής
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΘΕΜΑ 1 Ο. 3. Το DNA των μιτοχονδρίων έχει μεγαλύτερο μήκος από αυτό των χλωροπλαστών.
 ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΘΕΜΑ 1 Ο Α. Να γράψετε τον αριθμό της καθεμιάς από τις παρακάτω προτάσεις 1-5 και δίπλα του τη λέξη Σωστό, αν η πρόταση είναι σωστή, ή Λάθος, αν η πρόταση
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΘΕΜΑ 1 Ο Α. Να γράψετε τον αριθμό της καθεμιάς από τις παρακάτω προτάσεις 1-5 και δίπλα του τη λέξη Σωστό, αν η πρόταση είναι σωστή, ή Λάθος, αν η πρόταση
ΓΕΝΕΤΙΚΗ ΒΕΛΤΙΩΣΗ ΦΥΤΩΝ
 ΓΕΝΕΤΙΚΗ ΒΕΛΤΙΩΣΗ ΦΥΤΩΝ Μοριακοί Δείκτες Επιμέλεια διαφανειών Τραντάς Μάνος 1 Μοριακοί Δείκτες είναι αλληλουχίες DNA (ή πρωτεϊνών) που μπορούν να συσχετιστούν με συγκεκριμένα χαρακτηριστικά ώστε να ανιχνευτούν
ΓΕΝΕΤΙΚΗ ΒΕΛΤΙΩΣΗ ΦΥΤΩΝ Μοριακοί Δείκτες Επιμέλεια διαφανειών Τραντάς Μάνος 1 Μοριακοί Δείκτες είναι αλληλουχίες DNA (ή πρωτεϊνών) που μπορούν να συσχετιστούν με συγκεκριμένα χαρακτηριστικά ώστε να ανιχνευτούν
Βιοπληροψορική, συσιημική βιολογία και εξατομικευμένη θεραπεία
 Βιοπληροψορική, συσιημική βιολογία και εξατομικευμένη θεραπεία Φραγκίσκος Κολίσης Καθηγητής Βιοτεχνολογίας, Σχολή Χημικών Μηχανικών ΕΜΠ, Διευθυντής Ινστιτούτου Βιολογικών Ερευνών και Βιοτεχνολογίας, EIE
Βιοπληροψορική, συσιημική βιολογία και εξατομικευμένη θεραπεία Φραγκίσκος Κολίσης Καθηγητής Βιοτεχνολογίας, Σχολή Χημικών Μηχανικών ΕΜΠ, Διευθυντής Ινστιτούτου Βιολογικών Ερευνών και Βιοτεχνολογίας, EIE
ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ, ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΕΙΚΟΝΑ 2.4 ΣΤΑΔΙΑ ΜΕΤΑΦΡΑΣΗΣ σ ε λ ί δ α 1 ΕΙΚΟΝΑ 4.2β ΕΡΩΤΗΣΕΙΣ 1. Να συμπληρώσετε τα κενά πλαίσια της εικόνας με την κατάλληλη λέξη ή φράση 2. Να γράψετε τον προσανατολισμό της μετακίνησης του ριβοσώματος
ΕΙΚΟΝΑ 2.4 ΣΤΑΔΙΑ ΜΕΤΑΦΡΑΣΗΣ σ ε λ ί δ α 1 ΕΙΚΟΝΑ 4.2β ΕΡΩΤΗΣΕΙΣ 1. Να συμπληρώσετε τα κενά πλαίσια της εικόνας με την κατάλληλη λέξη ή φράση 2. Να γράψετε τον προσανατολισμό της μετακίνησης του ριβοσώματος
ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΚΕΦΑΛΑΙΑ 1 ΚΑΙ 2
 ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΚΕΦΑΛΑΙΑ 1 ΚΑΙ 2 ΘΕΜΑ 1 ο Α. Στις ερωτήσεις 1-5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα του το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1. Το
ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΚΕΦΑΛΑΙΑ 1 ΚΑΙ 2 ΘΕΜΑ 1 ο Α. Στις ερωτήσεις 1-5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα του το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1. Το
ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΟΜΑΔΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Γ ΛΥΚΕΙΟΥ
 ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΟΜΑΔΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Γ ΛΥΚΕΙΟΥ Επιμέλεια: Βουδούρη Καλλιρρόη Ριζηνίας 69 & Λασαίας 21 τηλ.2810313170 www.kmathisi.com ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΟΝΟΜΑ:..
ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΟΜΑΔΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Γ ΛΥΚΕΙΟΥ Επιμέλεια: Βουδούρη Καλλιρρόη Ριζηνίας 69 & Λασαίας 21 τηλ.2810313170 www.kmathisi.com ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΟΝΟΜΑ:..
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ
 ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις 1 έως 5 και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή τη φράση, η οποία
Ποιες είναι οι ομοιότητες και οι διαφορές μεταξύ της αντιγραφής και της
 ΚΕΦ. 2 ο ΕΡΩΤΗΣΕΙΣ ΚΡΙΣΕΩΣ Ποιες είναι οι ομοιότητες και οι διαφορές μεταξύ της αντιγραφής και της μεταγραφής; Διαφορές Αντιγραφή Μεταγραφή 1. Διατηρείται και μεταβιβάζεται η 1. Μεταβιβάζεται η γενετική
ΚΕΦ. 2 ο ΕΡΩΤΗΣΕΙΣ ΚΡΙΣΕΩΣ Ποιες είναι οι ομοιότητες και οι διαφορές μεταξύ της αντιγραφής και της μεταγραφής; Διαφορές Αντιγραφή Μεταγραφή 1. Διατηρείται και μεταβιβάζεται η 1. Μεταβιβάζεται η γενετική
Συνιστώνται για... Οι δονήσεις είναι αποτελεσματικές...
 ΠΕΔΙΑ ΕΦΑΡΜΟΓΗΣ Εκφυλιστικές αλλοιώσεις Αγγειακές παθήσεις Παθολογίες των πνευμόνων Ουρο-γυναικολογικές διαταραχές Καρδιακές παθήσεις Παθολογίες σπονδυλικής στήλης Παθολογίες αρθρώσεων Παθολογίες συνδέσμων
ΠΕΔΙΑ ΕΦΑΡΜΟΓΗΣ Εκφυλιστικές αλλοιώσεις Αγγειακές παθήσεις Παθολογίες των πνευμόνων Ουρο-γυναικολογικές διαταραχές Καρδιακές παθήσεις Παθολογίες σπονδυλικής στήλης Παθολογίες αρθρώσεων Παθολογίες συνδέσμων
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων. Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 24 Μαΐου 2013. Απαντήσεις Θεμάτων
 Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 24 Μαΐου 2013 Απαντήσεις Θεμάτων ΘΕΜΑ Α Α1. Βασική μονάδα οργάνωσης αποτελεί το Γ. νουκλεόσωμα
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 24 Μαΐου 2013 Απαντήσεις Θεμάτων ΘΕΜΑ Α Α1. Βασική μονάδα οργάνωσης αποτελεί το Γ. νουκλεόσωμα
Παραγωγή, απομόνωση και καθαρισμός της φαρμακευτικής πρωτεΐνης.
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 1 ΙΟΥΝΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1o 1. δ 2. β 3. β 4. γ 5. δ ΘΕΜΑ 2o 1. Σχολικό βιβλίο, σελ.
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 1 ΙΟΥΝΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1o 1. δ 2. β 3. β 4. γ 5. δ ΘΕΜΑ 2o 1. Σχολικό βιβλίο, σελ.
ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ:ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019
 ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ:ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΘΕΜΑ 1 ο A1. α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ 2 ο Β1. 1-ζ 2-στ 3-α 4-ε 5-β 6-δ Β2. Απάντηση: Σύνθεση DNA θα πραγματοποιηθεί στο μοριο
ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ:ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΤΡΙΤΗ 18 ΙΟΥΝΙΟΥ 2019 ΘΕΜΑ 1 ο A1. α Α2. β Α3. γ Α4. γ Α5. β ΘΕΜΑ 2 ο Β1. 1-ζ 2-στ 3-α 4-ε 5-β 6-δ Β2. Απάντηση: Σύνθεση DNA θα πραγματοποιηθεί στο μοριο
Ποιος είναι ο ρόλος των πρωτεϊνών στα κύτταρα και ποιες είναι οι δομικές τους μονάδες;
 Ποιος είναι ο ρόλος των πρωτεϊνών στα κύτταρα και ποιες είναι οι δομικές τους μονάδες; Οι πρωτεΐνες αποτελούν δομικά ή λειτουργικά συστατικά των κυττάρων και δομούνται από απλούστερες ενώσεις, τα αμινοξέα.
Ποιος είναι ο ρόλος των πρωτεϊνών στα κύτταρα και ποιες είναι οι δομικές τους μονάδες; Οι πρωτεΐνες αποτελούν δομικά ή λειτουργικά συστατικά των κυττάρων και δομούνται από απλούστερες ενώσεις, τα αμινοξέα.
Βιολογία ομάδας προσανατολισμού θετικών σπουδών. Πανελλαδικές εξετάσεις
 Βιολογία ομάδας προσανατολισμού θετικών σπουδών Πανελλαδικές εξετάσεις 2015-2016 ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ ΘΕΜΑ Β Β1. 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Β2. Καρυότυπος ονομάζεται η απεικόνιση των μεταφασικών
Βιολογία ομάδας προσανατολισμού θετικών σπουδών Πανελλαδικές εξετάσεις 2015-2016 ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ ΘΕΜΑ Β Β1. 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ Β2. Καρυότυπος ονομάζεται η απεικόνιση των μεταφασικών
ΚΕΦΑΛΑΙΟ 11. Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα
 ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
Ενδεικτικές απαντήσεις στα Θέματα Βιολογίας Προσανατολισμού
 Ενδεικτικές απαντήσεις στα Θέματα Βιολογίας Προσανατολισμού Θέμα Α Α1) γ Α2) γ Α3) δ Α4) β Α5) β Θέμα Β Β1. Α = υδροξύλιο, Β = πρωταρχικό τμήμα, Γ = θέση έναρξης αντιγραφής, Δ = φωσφορική ομάδα, Ε = τμήμα
Ενδεικτικές απαντήσεις στα Θέματα Βιολογίας Προσανατολισμού Θέμα Α Α1) γ Α2) γ Α3) δ Α4) β Α5) β Θέμα Β Β1. Α = υδροξύλιο, Β = πρωταρχικό τμήμα, Γ = θέση έναρξης αντιγραφής, Δ = φωσφορική ομάδα, Ε = τμήμα
ΓΕΝΕΤΙΚΗ ΠΡΟΔΙΑΘΕΣΗ ΣΤΗΝ ΕΜΦΑΝΙΣΗ ΝΟΣΩΝ ΠΟΥ ΣΧΕΤΙΖΟΝΤΑΙ ΜΕ ΠΕΡΙΒΑΛΛΟΝΤΙΚΗ ΕΚΘΕΣΗ:
 ΓΕΝΕΤΙΚΗ ΠΡΟΔΙΑΘΕΣΗ ΣΤΗΝ ΕΜΦΑΝΙΣΗ ΝΟΣΩΝ ΠΟΥ ΣΧΕΤΙΖΟΝΤΑΙ ΜΕ ΠΕΡΙΒΑΛΛΟΝΤΙΚΗ ΕΚΘΕΣΗ: Ανάλυση γονιδιακών πολυμορφισμών Σταυροπούλου Χρύσα,PhD Εργαστήριο Υγειοφυσικής & Περιβαλλοντικής Υγείας Ινστιτούτο Πυρηνικής
ΓΕΝΕΤΙΚΗ ΠΡΟΔΙΑΘΕΣΗ ΣΤΗΝ ΕΜΦΑΝΙΣΗ ΝΟΣΩΝ ΠΟΥ ΣΧΕΤΙΖΟΝΤΑΙ ΜΕ ΠΕΡΙΒΑΛΛΟΝΤΙΚΗ ΕΚΘΕΣΗ: Ανάλυση γονιδιακών πολυμορφισμών Σταυροπούλου Χρύσα,PhD Εργαστήριο Υγειοφυσικής & Περιβαλλοντικής Υγείας Ινστιτούτο Πυρηνικής
φροντιστήρια Απαντήσεις Βιολογίας Γ λυκείου Προσανατολισμός Θετικών Σπουδών
 Απαντήσεις Βιολογίας Γ λυκείου Προσανατολισμός Θετικών Σπουδών Θέμα Α Α1. α. 2 β. 1 γ. 4 δ. 1 ε. 2 Θέμα Β Β1. α. 1-Γ, 2-Γ, 3-Β, 4-Β, 5-Α, 6-B, 7-Α β. 1. Σύμπλοκο έναρξης πρωτεϊνοσύνθεσης: Το σύμπλοκο που
Απαντήσεις Βιολογίας Γ λυκείου Προσανατολισμός Θετικών Σπουδών Θέμα Α Α1. α. 2 β. 1 γ. 4 δ. 1 ε. 2 Θέμα Β Β1. α. 1-Γ, 2-Γ, 3-Β, 4-Β, 5-Α, 6-B, 7-Α β. 1. Σύμπλοκο έναρξης πρωτεϊνοσύνθεσης: Το σύμπλοκο που
