Σελίδα 1. Institutional Repository - Library & Information Centre - University of Thessaly 06/09/ :10:17 EEST
|
|
|
- Ἀράμ Ελευθεριάδης
- 6 χρόνια πριν
- Προβολές:
Transcript
1 Σελίδα 1
2 ΤΡΙΜΕΛΗΣ ΕΠΙΤΡΟΠΗ Δημήτριος Στάγκος (επιβλέπων): Λέκτορας Φυσιολογίας Ζωικών Οργανισμών του Τμήματος Βιοχημείας & Βιοτεχνολογίας του Πανεπιστημίου Θεσσαλίας. Δημήτριος Κουρέτας: Καθηγητής Φυσιολογίας Ζωικών Οργανισμών του Τμήματος Βιοχημείας & Βιοτεχνολογίας του Πανεπιστημίου Θεσσαλίας. Κωνσταντίνος Πετρωτός: Αναπληρωτής Καθηγητής του Τμήματος Μηχανικής Βιοσυστημάτων του ΤΕΙ/Λάρισας. Σελίδα 2
3 ΠΡΟΛΟΓΟΣ - ΕΥΧΑΡΙΣΤΙΕΣ Η συγκεκριμένη διπλωματική εργασία πραγματοποιήθηκε στο Εργαστήριο Φυσιολογίας Ζωικών Οργανισμών του Τμήματος Βιοχημείας & Βιοτεχνολογίας του πανεπιστημίου Θεσσαλίας, υπό την επίβλεψη του Καθηγητή κ. Δημήτριου Κουρέτα και του Λέκτορα κ. Δημήτριου Στάγκου, τους οποίους θα ήθελα να ευχαριστήσω για την ευκαιρία που μου έδωσαν να εκπονήσω την πτυχιακή μου εργασία στο εργαστήριο τους. Επίσης, θα ήθελα να ευχαριστήσω τον υποψήφιο διδάκτορα, Νίκο Γκουτζουρέλα, και τον μεταδιδακτορικό ερευνητή, Γιάννη Καφαντάρη, για την ανεκτίμητη βοήθεια τους κατά τη διάρκεια της πειραματικής διαδικασίας.. Σελίδα 3
4 ΠΕΡΙΛΗΨΗ Για το σκοπό της συγκεκριμένης διπλωματικής εργασίας, πραγματοποιήθηκε εκτροφή στο στάδιο του απογαλακτισμού είκοσι οχτώ (28) προβάτων, της Ελληνικής φυλής «Χιώτικα», με πολυφαινολικά πρόσθετα από στέμφυλα και στη συνέχεια έγινε έλεγχος της αντιοξειδωτικής τους δράσης στον ιστό της σπλήνας και στο αίμα. Τα είκοσι οχτώ (28) πρόβατα που εκτράφηκαν χωρίστηκαν σε δύο (2) ομάδες. Σε αυτές τις δύο ομάδες χορηγήθηκε διαφορετικό σιτηρέσιο. Η πρώτη ομάδα αποτέλεσε την ομάδα ελέγχου ενώ η δεύτερη ομάδα αποτελούνταν από τα νεαρά πρόβατα στο σιτηρέσιο των οποίων, περιέχονταν επιπλέον στέμφυλα, τα οποία περιέχουν πολυφαινόλες. Τα πρόβατα εκτράφηκαν με το πειραματικό σιτηρέσιο για πενήντα (50) ημέρες, διότι τις πρώτες 15 ημέρες, τρέφονταν μόνο με το μητρικό γάλα. Πραγματοποιήθηκαν 3 ιστοληψίες αιμοληψίες. Η πρώτη αιμοληψία ιστοληψία πραγματοποιήθηκε δέκα πέντε (15) ημέρες μετά την γέννηση των προβάτων, από τέσσερα (4) ζώα, με σκοπό τον έλεγχο της αντιοξειδωτικής τους άμυνας σε πρόωρη ηλικία. Τα υπόλοιπα πρόβατα διαχωρίστηκαν σε δύο ισοδύναμες (2) ομάδες, των δώδεκα (12) ατόμων. Όπως αναφέρθηκε ήδη, η πρώτη ομάδα είναι η ομάδα ελέγχου που λαμβάνει το κανονικό σιτηρέσιο και η δεύτερη ομάδα λαμβάνει το πολυφαινολικό σιτηρέσιο απογαλακτισμού. Η δεύτερη αιμοληψία ιστοληψία πραγματοποιήθηκε σε δώδεκα (12) πρόβατα, έξι (6) από την κάθε ομάδα, ηλικίας σαράντα δύο (42) ημερών ενώ η τελευταία ιστοληψία έγινε σε δώδεκα (12) πρόβατα ηλικίας εξήντα πέντε (65) ημερών, έξι (6) από κάθε ομάδα. Εξετάστηκε εάν ο ιστός της σπλήνας και το αίμα θα παρουσίαζαν βελτίωση της οξειδοαναγωγικής κατάστασης των προβάτων τα οποία τρέφονταν με το σιτηρέσιο το οποίο περιείχε τα στέμφυλα. Οι δείκτες του οξειδωτικού στρες που ελέγχθηκαν ήταν: η ανηγμένη γλουταθειόνη (GSH) και η δραστικότητα της καταλάσης (CAT) για την αξιολόγηση της οξειδοαναγωγικής κατάστασης των ιστών, η ολική αντιοξειδωτική ικανότητα (TAC Total antioxidant capacity), οι ουσίες που αντιδρούν με θειοβαρβιτουρικό οξύ (TBARS- Thiobarbituric acid reactive substances), για τον προσδιορισμό της υπεροξείδωσης των λιπιδίων και τέλος τα πρωτεϊνικά καρβονύλια για τον προσδιορισμό της υπεροξείδωσης των πρωτεϊνών. Τα αποτελέσματα που καταγράφηκαν είναι τα εξής: Tα επίπεδα της GSH αυξήθηκαν στον ιστό της σπλήνας των 65 ημερών, από τις control στις πολυφαινολικές ομάδες, κατά 101,47%. Στις υπόλοιπες μετρήσεις, οι μεταβολές της GSH δεν ήταν στατιστικά σημαντικές. Τα TBARS παρουσιάζουν στον ιστό της σπλήνας των 65 ημερών μείωση, από τις control στις πολυφαινολικές ομάδες, κατά 26,34%. Επίσης, τα επίπεδα της καταλάσης παρουσιάστηκαν αυξημένα στο αίμα των 42 ημερών κατά 28,47%. Τα επίπεδα της TAC και των πρωτεινικών καρβονυλίων τόσο στο αίμα όσο και στον ιστό της σπλήνας δεν παρουσίασαν στατιστικά σημαντικές μεταβολές. Σελίδα 4
5 ABSTRACT The aim of the present study was to raise young sheeps with feed containing polyphenolic additives from grapes, in order to examine the effects on the redox status in spleen tissue and blood, using oxidative stress markers. For this purpose, feed containing polyphenolic additives was given to twenty eight (28) young sheeps at the stage of ablactation. The twenty eight (28) sheeps were divided into two (2) groups. In these two groups, different diets were given. The first group was the control group with the basic diet, while the other group was received special feed with polyphenolic additives from grapes. The sheeps were fed with the experimental diet for fifty (50) days. Tissues were collected from the experimental animals at 3 different time-points. The first time-point was fifteen (15) days after the birth of sheeps in order to check their antioxidant status at early age. The second time-points was at forty two (42) days after birth, and the last time-point was at sixty five (65) days after birth. The following oxidative stress biomarkers were assessed in tissues: reduced glutathione (GSH), catalase activity (CAT), total antioxidant capacity (TAC), thiobarbituric acid reactive substances (TBARS) and protein carbonyls. The observed results were: GSH levels in the 65 days polyphenolic group of spleen tissue was increased by 101,47% compared with the control. In TBARS assay, a reduction was found in spleen tissue of 65 days polyphenolic group by 26,34%, respectively compared with the control. The catalase activity was higher by 28,47% in blood of 42 days polyphenolic group. TAC changes and CARB changes were not statistically significant compared to control. Σελίδα 5
6 ΠΕΡΙΕΧΟΜΕΝΑ Πίνακας περιεχομένων ΤΡΙΜΕΛΗΣ ΕΠΙΤΡΟΠΗ... 2 ΠΕΡΙΛΗΨΗ... 4 ABSTRACT... 5 ΠΕΡΙΕΧΟΜΕΝΑ... 6 ΚΑΤΑΛΟΓΟΣ ΠΙΝΑΚΩΝ... 8 ΚΑΤΑΛΟΓΟΣ ΔΙΑΓΡΑΜΜΑΤΩΝ... 8 ΚΑΤΑΛΟΓΟΣ ΕΙΚΟΝΩΝ ΕΙΣΑΓΩΓΗ Οξειδωτικό στρες Ιστορική αναδρομή & ορισμός Ελεύθερες ρίζες και δραστικά είδη Ο Σχηματισμός ελευθέρων ριζών ) Οξειδωτική φωσφορυλίωση ) Μετατροπή της ξανθίνης σε ουρικό οξύ ) Κυτόχρωμα P ) Αυτοοξείδωση μορίων Εξωκυτταρικές πηγές Επιπτώσεις οξειδωτικού στρες στα βιομόρια Αντιοξειδωτική άμυνα Η υπεροξειδάση της δισμουτάσης (SOD) είναι ίσως το πιο σημαντικό ένζυμο του αντιοξειδωτικού μηχανισμού. Καταλύει την αντίδραση μετατροπής του O 2 - σε H 2 O 2 : SOD Οξειδωτικό στρες και διαταραχές της υγείας Οξειδωτικό στρες και διαταραχή της υγείας των ζώων Βιοδραστικές φυτοχημικές ενώσεις Βιολογικές ιδιότητες των σταφυλιών Ανατομία και χημική σύσταση σταφυλιών Στέμφυλα και περιβάλλον Πολυφαινόλες Ετυμολογία Ιστορικό Ορισμός Δομή και Tάξεις των Πολυφαινολών Σελίδα 6
7 1.3.5 Φυσικές Ιδιότητες Χημειοπροστατευτική Δράση Πολυφαινολών Επιδράσεις πολυφαινολών στην υγεία Γενικές πληροφορίες για τα πρόβατα Χαρακτηριστικά Εγκυμοσύνη Χιώτικο πρόβατο Σκοπός Υλικά και Μέθοδοι Γενικά Περιγραφή του σιτηρεσίου Παρασκευή βιολειτουργικών ζωοτροφών Παρασκευή βιολειτουργικών ζωοτροφών για τα πρόβατα ( Ελληνικής φυλής, «Χιώτικα») Παρασκευή ενσιρώματος στεμφύλων Αποτίμηση της αντιοξειδωτικής δράσης (in vitro) των ζωοτροφών Αποτίμηση της αντιοξειδωτικής ικανότητητας των παρασκευασμένων ζωοτροφών για τα πρόβατα Συσχέτιση των δύο μεθόδων κατά Spearman Συνολικά αποτελέσματα της αποτίμησης της αντιοξειδωτικής ικανότητας των ζωοτροφών Ομογενοποιήση ιστών Προσδιορισμός δεικτών οξειδωτικού στρες Γενικά Μέθοδοι Μέτρηση γλουταθειόνης Δραστικότητα της Καταλάσης Ολική Aντιοξειδωτική ικανότητα (Total Antioxidant Capacity, TAC) Ουσίες που αντιδρούν με το θειοβαρβιτουρικό οξύ (TBARS) ΟΥΣΙΕΣ ΠΟΥ ΑΝΤΙΔΡΟΥΝ ΜΕ ΤΟ ΘΕΙΟΒΑΡΒΙΤΟΥΡΙΚΟ ΟΞΥ (TBARS) ΣΤΟ ΠΛΑΣΜΑ Πρωτεϊνικά καρβονύλια Προσδιορισμός συνολικής ποσότητας πρωτεΐνης μέσω του αντιδραστηρίου Bradford ΑΠΟΤΕΛΕΣΜΑΤΑ Επίπεδα Γλουταθειόνης Επίπεδα TBARS Επίπεδα Καταλάσης Επίπεδα πρωτεινικών καρβονυλίων Επίπεδα ολικής αντιοξειδωτικής ικανότητας (TAC) ΣΥΖΗΤΗΣΗ Σελίδα 7
8 5.ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΑΤΑΛΟΓΟΣ ΠΙΝΑΚΩΝ Πίνακας 1: Συστηματική ταξινόμηση προβάτων Πίνακας 2: Σύσταση παρασκευασμένων σιτηρεσίων για την πολυφαινολική ομάδα Πίνακας 3: Σύσταση παρασκευασμένων σιτηρεσίων, ομάδα control Πίνακας 4: Τιμές IC50 των ζωοτροφών με τη μέθοδο DPPH και ABTS Πίνακας 5: Διαδοχική Σειρά Προσθήκης και οι Ποσότητες των Αντιδραστηρίων για τη Μέτρηση της GSH Πίνακας 6: Διαδοχική Σειρά Προσθήκης και οι Ποσότητες των Αντιδραστηρίων για τη Μέτρηση της GSH Πίνακας 7: Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της Καταλάσης Πίνακας 8: Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της Καταλάσης Πίνακας 9:Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της TAC Πίνακας 10 :Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της TAC Πίνακας 11 :Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων για τη μέτρηση της αιμοσφαιρίνης 62 ΚΑΤΑΛΟΓΟΣ ΔΙΑΓΡΑΜΜΑΤΩΝ Διάγραμμα 1: Στο διάγραμμα απεικονίζεται η % εξουδετέρωση τη ρίζας του DPPH σε συνάρτηση με τη συγκέντρωση της ζωοτροφής της ομάδας ελέγχου Διάγραμμα 2 :Στο διάγραμμα απεικονίζεται η % εξουδετέρωση της ρίζας DPPH σε συνάρτηση με τη συγκέντρωση της ζωοτροφής εμπλουτισμένη με στέμφυλα Διάγραμμα 3 :Στο διάγραμμα απεικονίζεται η % εξουδετέρωση της ρίζας του ABTS σε συνάρτηση με τη συγκέντρωση της ζωοτροφής της ομάδας ελέγχου Διάγραμμα 4 :Στο διάγραμμα απεικονίζεται η % εξουδετέρωση της ρίζας του ABTS σε συνάρτηση με τη συγκέντρωση της ζωοτροφής εμπλουτισμένη με στέμφυλα Διάγραμμα 5 :Στο διάγραμμα απεικονίζεται η συσχέτιση των τιμών IC50 της μεθόδου DPPH με τη μέθοδο του ABTS (r=0,991, p<0,05) Διάγραμμα 6 :Στο διάγραμμα απεικονίζεται η συσχέτιση των τιμών IC50 της μεθόδου DPPH με τη μέθοδο του ABTS (r=0,972, p<0,05) Διάγραμμα 7 :Πρότυπη καμπύλη Αλβουμίνης Διάγραμμα 8: Επίπεδα της γλουταθειόνης (GSH). * Στατιστικά σημαντική αύξηση στις πολυφαινολικές ομάδες των 65 ημερών σε σχέση με τις ομάδες ελέγχου κατά 101,47% στον ιστό της σπλήνας Σελίδα 8
9 Διάγραμμα 9 :τα επίπεδα της γλουταθειόνης, δεν παρουσιάζουν στατιστικά σημαντικές μεταβολές από τις 15 ημέρες στις 42 ημέρες, ούτε από της 42 στις 65 ημέρες Διάγραμμα 10: Επίπεδα TBARS. Στατιστικά σημαντική μείωση κατά 26,34% μεταξύ των ομάδων control 65 ημερών και polyphenol 65 ημερών Διάγραμμα 11: Επίπεδα TBARS Διάγραμμα 12 :Επίπεδα Καταλάσης Διάγραμμα 13: Επίπεδα Καταλάσης. Παρατηρείται στατιστικά σημαντική αύξηση της δραστικότητας της καταλάσης στις 42 ημέρες στην πολυφαινολική ομάδα κατά 28,47% Διάγραμμα 14 :Επίπεδα πρωτεϊνικών καρβονυλίων στον ιστό της σπλήνας Διάγραμμα 15 :Επίπεδα πρωτεινικών καρβονυλίων στο αίμα Διάγραμμα 16 :Επίπεδα TAC Διάγραμμα 17 :Επίπεδα της TAC στο πλάσμα του αίματος ΚΑΤΑΛΟΓΟΣ ΕΙΚΟΝΩΝ Εικόνα 1: Δραστικές μορφές οξυγόνου Εικόνα 2: Πηγές παραγωγής ελευθέρων ριζών Εικόνα 3 : Το DNA,οι πρωτεΐνες και τα λιπίδια αποτελούν τους στόχους των ΔΜΟ Εικόνα 4: Τρόποι σχηματισμού ελευθέρων ριζών Εικόνα 5 : Οξειδωτικό στρες Εικόνα 6 : Τρόπος δράσης αντιοξειδωτικών παραγόντων Εικόνα 7: Απεικόνιση δράσης των GR, GPx, SOD, CAT Εικόνα 8: Δομή γλουταθειόνης Εικόνα 9: Ασθένειες προκαλούμενες από οξειδωτικό στρες Εικόνα 10 : Ανατομία και σύσταση ράγας σταφυλιού Εικόνα 11: Χημικές Δομές Διαφορετικών Πολυφαινολικών Τάξεων Εικόνα 12:Πειραματικό πλάνο εκτροφής απογαλακτισμού των αναπτυσσόμενων αρνιών Εικόνα 13:Συσκευασία πακεταρίσματος σιτηρεσίων Εικόνα 14:Ομογενοποίηση α) με γουδί β) χρήση υπερήχων Εικόνα 15 :Συντακτικός τύπος γλουταθειόνης Σελίδα 9
10 Εικόνα 16 :Μονοπάτι αναγωγής του H 2 O 2 σε H 2 O Εικόνα 17 :Αντίδραση TBA (1) με MDA (2), που οδηγεί στην παραγωγή του μορίου TBA-MDA Εικόνα 18:Σύνδεση πρωτεΐνης με την DNPH (2,4-δίνιτριφαινυλυδραζίνη) και σχηματισμός του 2,4- δίνιτροφαινυλυδραζονίου Εικόνα 19 :Απεικόνιση του σπλήνα και οι βασικές λειτουργίες του Εικόνα 20 :Απεικόνιση αιμοσφαιρίνης και ερυθρών αιμοσφαιρίων Σελίδα 10
11 1.ΕΙΣΑΓΩΓΗ 1.1 Οξειδωτικό στρες Ιστορική αναδρομή & ορισμός Το 1775 ο Priestley ανέφερε ότι «η συνεχής έκθεση στο οξυγόνο μπορεί να σβήσει το κερί της ζωής πολύ γρήγορα». Η προφητική αυτή παρατήρηση από τον άνθρωπο που ανακάλυψε το οξυγόνο, έδωσε το έναυσμα για τη λύση ενός από τα σημαντικότερα προβλήματα της σύγχρονης επιστήμης: του «παράδοξου του οξυγόνου». Το Ο 2 είναι πολύ σημαντικό στοιχείο για τη διατήρηση της ζωής, αλλά κάτω από κάποιες περιπτώσεις μπορεί να γίνει τοξικό, καθώς η έκθεση του οργανισμού σε αυξημένες συγκεντρώσεις οξυγόνου προκαλεί ανεπιθύμητες αντιδράσεις για την υγεία. Τα αίτια των δηλητηριωδών ιδιοτήτων του οξυγόνου ήταν άγνωστα πριν τη δημοσίευση της θεωρίας των Gershman et al το 1954, σύμφωνα με την οποία η τοξικότητα του οξυγόνου οφειλόταν σε μερικώς αναχθείσες μορφές οξυγόνου. Λίγο αργότερα, ο Denham Harman το 1956 διατύπωσε την υπόθεση ότι οι δραστικές μορφές οξυγόνου (ΔΜΟ ROS) μπορεί να παίζουν ρόλο στην κυτταρική βλάβη, τη μεταλλαξιγένεση, τον καρκίνο και τις εκφυλιστικές διεργασίες της βιολογικής γήρανσης. Η ανακάλυψη του ενζύμου υπεροξειδική δισμουτάση (SOD) το 1969 σήμανε μια νέα εποχή για τη διερεύνηση των δράσεων των ελευθέρων ριζών στους ζώντες οργανισμούς. Μια τρίτη εποχή της έρευνας σχετικά με τις δράσεις των ελευθέρων ριζών ξεκίνησε όταν το 1977 εμφανίστηκαν οι πρώτες αναφορές που περιέγραφαν τις ευεργετικές βιολογικές δράσεις των ελευθέρων ριζών οξυγόνου. Έκτοτε, είναι πλέον σαφές ότι οι ζωντανοί οργανισμοί έχουν προσαρμοστεί στη συνύπαρξη με τις ελεύθερες ρίζες και έχουν αναπτύξει διάφορους μηχανισμούς για τη χρησιμοποίηση αυτών σε φυσιολογικές λειτουργίες. Είναι πλέον γνωστό, ότι οι ελεύθερες ρίζες αποτελούν προϊόντα του φυσικού κυτταρικού μεταβολισμού και παίζουν διπλό ρόλο: άλλοτε είναι ευεργετικές για τα κύτταρα και τους οργανισμούς και άλλοτε βλαπτικές (Valko, M., et al., 2007). Ο όρος οξειδωτικό στρες ορίστηκε για πρώτη φορά το 1985 ως «η διαταραχή της ισορροπίας των προ-οξειδωτικών και αντιοξειδωτικών μηχανισμών υπέρ των πρώτων» (Sies, H., et al., 1985). Τα τελευταία χρόνια ο ρόλος των ελευθέρων ριζών οξυγόνου στην παθογένεση πολλών ασθενειών κίνησε το ενδιαφέρον της επιστημονικής κοινότητας, με αποτέλεσμα να πληθαίνουν οι έρευνες για την κατανόηση των επιβλαβών δράσεων τους, αλλά και την επίλυση αυτών με τη μελέτη των αντιοξειδωτικών συστατικών του οργανισμού και των τροφίμων, τα οποία παρουσιάζουν σημαντική προστατευτική δράση Ελεύθερες ρίζες και δραστικά είδη Ο 2 Τα μόρια αποτελούνται από έναν ή περισσότερους ατομικούς πυρήνες, οι οποίοι περιβάλλονται από ηλεκτρόνια, τα οποία περιφέρονται γύρω από τον πυρήνα. Τα ηλεκτρόνια είναι διευθετημένα σε έναν αριθμό τροχιακών, τα οποία βρίσκονται σε διαφορετικές αποστάσεις από τον πυρήνα. Στα περισσότερα μόρια, τα ηλεκτρόνια που βρίσκονται σε κάθε τροχιακό, ζευγαρώνουν με ένα άλλο ηλεκτρόνιο. Τα δύο ηλεκτρόνια κάθε ζεύγους περιστρέφονται γύρω από τον εαυτό τους (spin) σε αντίθετες κατευθύνσεις. Τα ζευγαρωμένα ηλεκτρόνια διατηρούν το μόριο σχετικά σταθερό εμφανίζοντας μικρότερη ενεργειακή κατάσταση, με αποτέλεσμα να είναι λιγότερο δραστικό. 'Όταν ένα ή περισσότερα ηλεκτρόνια, ιδιαίτερα αυτά που βρίσκονται στα εξωτερικά τροχιακά του ατόμου, είναι ασύζευκτα, δεν έχουν δηλαδή ζευγάρι, τότε το μόριο γίνεται ασταθές, εμφανίζοντας μεγαλύτερη ενεργειακή κατάσταση, με αποτέλεσμα να είναι πιο δραστικό από άλλα μόρια. Άτομα ή μόρια με ασύζευκτα ηλεκτρόνια ονομάζονται παραμαγνητικά, ενώ όταν δεν διαθέτουν Σελίδα 11
12 τέτοια ηλεκτρόνια, διαμαγνητικά. Ένα ασύζευκτο ηλεκτρόνιο έχει τεράστια έλξη στα ηλεκτρόνια γειτονικών ατόμων με αποτέλεσμα την πρόκληση χημικών αντιδράσεων μεταξύ ατόμων ή μορίων, κατά τις οποίες έχουμε μεταφορά ηλεκτρονίων. Τέτοιες αντιδράσεις ονομάζονται οξειδοαναγωγικές (redox), εκ των οποίων κατά την οξείδωση έχουμε απώλεια ηλεκτρονίων, ενώ κατά την αναγωγή έχουμε απόκτηση ηλεκτρονίων από ένα άτομο. Ένα άτομο ή μόριο με ένα ή περισσότερα ασύζευκτα ηλεκτρόνια και ανεξάρτητη παρουσία λέγεται ελεύθερη ρίζα και συμμετέχει πολύ εύκολα σε αντιδράσεις οξειδοαναγωγής με γειτονικά μόρια (Gilbert, 2000, Halliwell & Gutteridge, 1990). Κατά τις αντιδράσεις αυτές όχι μόνο μεταβάλλονται σημαντικά τα γειτονικά μόρια στόχοι, αλλά μερικές φορές μεταβιβάζονται τα ασύζευκτα ηλεκτρόνια από στόχο σε στόχο, δημιουργώντας έτσι μία δεύτερη, τρίτη κ.ο.κ. ελεύθερη ρίζα υπό μορφή αλυσιδωτής αντίδρασης. (Halliwell & Gutteridge, 1990). Η πολύ μεγάλη βλαπτική επίδραση των ελευθέρων ριζών οφείλεται ακριβώς στον πολλαπλασιασμό των μεταβολών που προκαλούνται από παρόμοιες αλυσιδωτές αντιδράσεις. Αποτελούν προϊόντα του φυσικού κυτταρικού μεταβολισμού και έχουν διπλό ρόλο αφού ανάλογα με το ρυθμό παραγωγής τους μπορεί να είναι είτε ευεργετικές είτε επιβλαβείς. Οι πλέον σημαντικές ελεύθερες ρίζες είναι μοριακά είδη με κέντρο το οξυγόνο και μερικές φορές το άζωτο (Sengupta et al., 2004; Pani and Galeotti, 2010; AICR, 2007), το θείο (Battin et al., 2009; Pani and Galeotti, 2010) ή τον άνθρακα. Το ίδιο το οξυγόνο που αναπνέουμε αποτελεί μία ελεύθερη ρίζα, αφού περιέχει δύο ασύζευκτα ηλεκτρόνια, που βρίσκονται σε δύο διαφορετικά τροχιακά. Η μορφή όμως αυτή του Ο 2, που λέγεται οξυγόνο τριπλής κατάστασης (triplet state) και συμβολίζεται με 3Ο 2, δεν είναι ιδιαίτερα δραστική. Όμως, είναι δυνατή η ενεργοποίηση του μοριακού οξυγόνου, με αποτέλεσμα τα δύο ηλεκτρόνια να βρεθούν στο ίδιο τροχιακό. Η πολύ δραστική αυτή μορφή οξυγόνου ονομάζεται οξυγόνο μονής κατάστασης (singlet state) και συμβολίζεται με *Ο 2. Αν και το οξυγόνο μονής κατάστασης δεν αποτελεί ελεύθερη ρίζα, τα ηλεκτρόνια του βρίσκονται σε διεγερμένη κατάσταση, δηλαδή είναι πολύ δραστικά και ως εκ τούτου μπορεί να προκαλέσουν βλαπτικές αντιδράσεις παρόμοιες με αυτές των ελεύθερων ριζών οξυγόνου. Παρόμοιο μόριο το οποίο δεν είναι ελεύθερη ρίζα αλλά περιέχει δραστικό οξυγόνο αποτελεί και το υπεροξείδιο του υδρογόνου (Halliwell 2001). Συνολικά, όλα τα μοριακά είδη που περιλαμβάνουν οξυγόνο, είτε είναι ελεύθερες ρίζες είτε όχι, ονομάζονται δραστικά είδη οξυγόνου (ΔΕΟ) (Cheeseman et al,1993; Gutteridge, 1995). Τα κυριότερα ΔΕΟ (Aqil et al., 2012; Vainio et al., 1999; Weisburger, 2001; AICR, 2007) είναι: 1) Η ρίζα σουπεροξειδίου (O 2 - ) Το σουπεροξείδιο (Ο 2 - ) σχηματίζεται από την αναγωγή του οξυγόνου από ένα e - σύμφωνα με την ακόλουθη αντίδραση: Ο 2 + e- Ο 2 - Το σουπεροξείδιο έχει παραμαγνητικές ιδιότητες λόγω του ασύζευκτου ηλεκτρονίου. Ο σχηματισμός του σουπεροξειδίου πραγματοποιείται αυθόρμητα υπό αερόβιες συνθήκες στην εσωτερική μεμβράνη των μιτοχονδρίων κατά τη διάρκεια της λειτουργίας «της αλυσίδας μεταφοράς ηλεκτρονίων». Ένζυμα που παράγουν σουπεροξείδιο είναι η λιποξυγενάση, η κυκλοξυγενάση και η NADPH οξειδάση των φαγοκυττάρων που αποτελεί ένα παράδειγμα σκόπιμης παραγωγής Ο - 2. Η ρίζα του σουπεροξειδίου παίζει κεντρικό ρόλο στη βιοχημεία των ελευθέρων ριζών επειδή από τη ρίζα αυτή παράγονται πολλές - δραστικές μορφές οξυγόνου. Το Ο 2, όπως και όλες οι ρίζες, έχει τη φυσική τάση να ζευγαρώσει το - ασύζευκτό του ηλεκτρόνιο. Αυτό μπορεί να γίνει και αν αντιδράσουν δύο ρίζες Ο 2 μεταξύ τους. Σε υδατικά διαλύματα με ουδέτερο pη, δύο ρίζες Ο - 2 αντιδρούν μεταξύ τους και σχηματίζουν υπεροξείδιο του υδρογόνου, σύμφωνα με την αντίδραση: Σελίδα 12
13 2Η 2 Ο 2 2 Ο Η + Η 2 Ο 2 + Ο 2 2) Η ρίζα υδροξυλίου (OH ) Η ρίζα υδροξυλίου ΟΗ είναι πολύ δραστική, όπως έχει αποδειχθεί σε πολλές μελέτες (Bielski & Cabelli, 1995; Halliwell & Gutteridge, 1999; von Sonntag, 1987). Αυτή προκύπτει σύμφωνα με την αντίδραση Fenton-Haber-Weiss μεταξύ του ανιόντος του σουπεροξειδίου (Ο 2.- ) και του υπεροξειδίου του υδρογόνου (Η 2 Ο 2 ) παρουσία ενός μετάλλου μετάπτωσης, το οποίο επιταχύνει την αντίδραση. Στα βιολογικά συστήματα το μέταλλο αυτό είναι συνήθως ο σίδηρος (Mylonas & Kouretas, 1999). Η αντίδραση καταλύεται ως εξής: Ο Η + Ο 2. Η Ο2. Η + Ο2.- + Η + Fe 3+ + O2. - Η2Ο2 + Ο2 Fe 2+ + O2 Fe 2+ + H2O2 Fe 3+ + OH. + OH - Ο χαλκός και άλλα μεταλλικά ιόντα μπορούν επίσης να καταλύσουν την αντίδραση. Η ρίζα υδροξυλίου είναι ένας ισχυρός οξειδωτικός παράγοντας που αντιδρά με πολλά οργανικά και ανόργανα μόρια στο κύτταρο (DNA, πρωτεΐνες, λιπίδια, αμινοξέα και μέταλλα). Οι τρεις κύριες αντιδράσεις της ρίζας υδροξυλίου είναι: Η απόσπαση υδρογόνου, Η προσθήκη ηλεκτρονίου και Η μεταφορά ηλεκτρονίου (Halliwell & Gutteridge, 1999) 3) Υπεροξειδικές ρίζες (ROO - ) Οι υπεροξειδικές ρίζες ROO - σχηματίζονται από την προσθήκη μοριακού οξυγόνου (Ο 2 ) σε ελεύθερες οργανικές ρίζες. Είναι τοξικές για τα κύτταρα επειδή μπορούν να αφαιρέσουν άτομα υδρογόνου από τα λιπίδια και με αυτό τον τρόπο να προωθήσουν τη λιπιδική υπεροξείδωση (Παπαγεωργίου, 2005). 4) Ρίζα Υδροϋπεροξειδίου (HO 2 ) Η ρίζα υδροϋπεροξειδίου HO 2 προκύπτει από αναγωγή 1 e- στο οξυγόνο, σύμφωνα με την παρακάτω αντίδραση: Ο 2 + e- Ο 2 - ΗΟ 2 (pk=4,8) 5) Υπεροξείδιο του υδρογόνου (Η 2 Ο 2 ) Το υπεροξείδιο του υδρογόνου Η 2 Ο 2 παράγεται με αναγωγή του οξυγόνου με δύο ηλεκτρόνια, σύμφωνα με την αντίδραση: Σελίδα 13
14 Ο 2 + 2e - + 2Η + Η 2 Ο 2 Στο μόριο του το Η 2 Ο 2 δεν περιέχει ασύζευκτο ηλεκτρόνιο γι αυτό και δεν είναι ελεύθερη ρίζα. Υπό συγκεκριμένες συνθήκες (όπως είναι η παρουσία μεταλλικών ιόντων), διασπάται και σχηματίζει υδροξυλική ρίζα (ΗΟ ), που είναι ιδιαιτέρως δραστική και τοξική για τα κύτταρα. Η τοξικότητα του Η 2 Ο 2 στα κύτταρα διαφέρει, γεγονός που οφείλεται στην ικανότητα που έχουν τα διάφορα κύτταρα να απομακρύνουν το Η 2 Ο 2. Εκτός αυτού υπάρχουν τρία αντιοξειδωτικά συστήματα, τα οποία ενεργοποιούνται για να απομακρύνουν τα μόρια Η 2 Ο 2, μόλις αυτά παραχθούν (Παπαγεωργίου, 2005). 6) Υποχλωριώδες οξύ (ΗΟCl) Το υποχλωριώδες οξύ ΗΟCl είναι φορές πιο τοξικό από το Η 2 Ο 2 και το Ο 2.- και σχηματίζεται με την ενεργοποίηση των ουδετερόφιλων κυττάρων. Όταν ενεργοποιηθούν τα ουδετερόφιλα, η μυελο-υπεροξειδάση (ένζυμο που βρίσκεται στο κυτόπλασμα των φαγοκύτταρων), καταλύει την αντίδραση του υπεροξειδίου του υδρογόνου (Η 2 Ο 2 ) με το χλώριο (Cl), σύμφωνα με την παρακάτω αντίδραση: Η 2 Ο 2 + Cl - ΗΟCl+ ΟΗ Το υποχλωριώδες οξύ είναι ασθενές, εν τούτοις πολύ δραστικό χημικά. Ενοχοποιείται ότι οδηγεί σε κυτταρική νέκρωση μέσα σε σύντομο χρονικό διάστημα. Καταστρέφει τα αποθέματα ΑΤΡ που βρίσκονται στα μιτοχόνδρια, δυσχεραίνει το μηχανισμό παραγωγής ενέργειας του κυττάρου, προκαλείται «οίδημα» σ αυτά, απώλεια δυναμικού κυτταρικής μεμβράνης και απελευθέρωση κυτοχρώματος C, οπότε επέρχεται η κυτταρική απόπτωση. Εκτός αυτών, η έκθεση των βιομορίων (λιπίδια, DNA, πρωτεΐνες) καθώς και μικρότερων μορίων (ασκορβικό οξύ, νουκλεοτίδια) στο υποχλωριώδες οξύ είναι συνυφασμένη με πρόκληση οξειδωτικών βλαβών (Whiteman Matthew, 2005). 7) Υποβρωμιώδες Οξύ (HOBr) Το υποβρωμιώδες οξύ HOBr είναι ασθενές και ασταθές. Σε υδατικό διάλυμα, διίσταται εν μέρει στο ανιόν ΟΒr- και το κατιόν Η +. Όταν καθαρό βρώμιο προστίθεται σε νερό, σχηματίζει υποβρωμιώδες οξύ και υδροβρωμικό οξύ (HBr): Br 2 (l) + H 2 O(l) HOBr(aq) + HBr (aq) Το HOBr χρησιμοποιείται ως λευκαντικό, οξειδωτικό, αποσμητικό και απολυμαντικό, εξαιτίας της ικανότητάς του να σκοτώνει τα κύτταρα πολλών παθογόνων. Η ένωση παράγεται ιδίως από ηωσινόφιλα, τα οποία το παράγουν από τη δράση της υπεροξειδάσης ηωσινόφιλων, ένα ένζυμο που χρησιμοποιεί κατά προτίμηση βρωμίδιο. Το βρωμίδιο χρησιμοποιείται επίσης σε υδρομασάζ και ιαματικά λουτρά ως μικροβιοκτόνος παράγοντας, χρησιμοποιώντας τη δράση ενός οξειδωτικού παράγοντα για να παράγουν υποβρωμιώδες με παρόμοιο τρόπο με την υπεροξειδάση των ηωσινόφιλων. 8) Όζον (O 3 ) Το όζον Ο 3 βρίσκεται στα ανώτερα στρώματα της ατμόσφαιρας και έχει μεγάλη βιολογική σημασία επειδή απορροφά τις βλαβερές για τους ζωντανούς οργανισμούς, υπεριώδεις ακτινοβολίες. Σχηματίζεται Σελίδα 14
15 με φωτοδιάσπαση του Ο 2 από την υπεριώδη ακτινοβολία σε ατομικό οξυγόνο το οποίο εν συνεχεία αντιδρά με μοριακό οξυγόνο. Το όζον δεν είναι ελεύθερη ρίζα. Πρόκειται για οξειδωτικό αέριο στο μόριο του οποίου περιέχονται τρία άτομα οξυγόνου. Είναι διαμαγνητικό, έχει χαρακτηριστική οσμή και ιδιαίτερα περιορισμένη διαλυτότητα στο νερό (Παπαγεωργίου, 2005). 9) Μονήρες οξυγόνο ( 1 O 2 ) Το μονήρες οξυγόνο 1 Ο 2 (singlet oxygen) έχει όλα τα ηλεκτρόνιά του συζευγμένα, πράγμα που σημαίνει ότι ουσιαστικά δεν είναι ελεύθερη ρίζα. Το 1 Ο 2 σχηματίζεται μέσω μιας αλλαγής στην κατάσταση του spin, από παράλληλη σε αντιπαράλληλη. Αυτό αυξάνει πάρα πολύ τη δραστικότητά του, περισσότερο από το μοριακό οξυγόνο, επειδή αναιρείται ο περιορισμός του spin και παρουσιάζει αυξημένη οξειδωτική ικανότητα. Αυτό συμβαίνει επειδή το μονήρες οξυγόνο βρίσκεται σε διεγερμένη κατάσταση. Έχει μικρή διάρκεια ημιζωής και δυνατότητα να διαπερνά τα κύτταρα (Halliwell, How to charactirize an antioxidant: an update 1995). Αποτελεί το μεγαλύτερο καταλύτη για την έναρξη της υπεροξείδωσης των λιπιδίων, η οποία οδηγεί σε καταστροφή των μεμβρανών. Το 1 O 2 σχηματίζεται κατά την άμεση μεταφορά ενέργειας από φωτοευαίσθητα μόρια. Στα δραστικά αυτά μοριακά είδη συμπεριλαμβάνεται επίσης και η δραστική μορφή αζώτου, το μονοξείδιο του αζώτου (NO), το οποίο είναι ελεύθερη ρίζα (με τελεία συμβολίζεται η ελεύθερη ρίζα, ενώ με (-) συμβολίζεται το αρνητικό φορτίο της ρίζας και με R, ένα άτομο ή μία ομάδα ατόμων, κυρίως αλυσίδα ατόμων άνθρακα). Εικόνα 1: Δραστικές μορφές οξυγόνου. Οι ευεργετικές δράσεις των ΔΜΟ παρατηρούνται σε χαμηλές ή μέτριες συγκεντρώσεις και αφορούν σε φυσιολογικές διαδικασίες όπως στην κυτταρική απόκριση στο στρες, στη μεταγωγή σήματος, στην κυτταρική διαφοροποίηση, στη μεταγραφή γονιδίων, στον κυτταρικό πολλαπλασιασμό, στη φλεγμονή, στην απόπτωση, στη φαγοκυττάρωση κυττάρων του ανοσοποιητικού και στη σηματοδότηση για την πήξη του αίματος. Όπως συνάγεται από τις αντιδράσεις τους, οι ελεύθερες ρίζες και κυρίως οι πολύ δραστικές όπως η ρίζα υδροξυλίου μπορούν να προσβάλλουν μεγάλη ποικιλία μορίων όπως σάκχαρα, αμινοξέα, φωσφολιπίδια και γενικά λιπίδια, βάσεις DNA και οργανικά οξέα. Οι λιγότερο δραστικές ελεύθερες ρίζες μπορούν να οδηγήσουν στην παραγωγή δραστικότερων καταλήγοντας τελικά στο ίδιο αποτέλεσμα. Η παρουσία ασύζευκτου ηλεκτρονίου, προσδίδει στις ΔΜΟ ιδιαίτερη δραστικότητα, αφού μπορούν είτε να δώσουν είτε να λάβουν ένα ηλεκτρόνιο σε/από άλλα μόρια, συμπεριφερόμενες έτσι ως αναγωγικά ή οξειδωτικά μέσα αντίστοιχα (Durackova, Z., et al., 2010). Σελίδα 15
16 1.1.3 Σχηματισμός ελευθέρων ριζών Παράγονται μέσα από διάφορες εσωτερικές φυσιολογικές λειτουργίες του σώματος καθώς αποτελούν προϊόντα της φυσιολογικής λειτουργίας του μεταβολισμού του κυττάρου (ενδοκυτταρικές πηγές). Επίσης παράγονται και όταν το σώμα εκτίθεται σε συγκεκριμένης τοξικότητας περιβάλλον (εξωκυτταρικές πηγές). Οι ελεύθερες ρίζες είναι πολύ δραστικά μόρια και μπορούν να προκαλέσουν βλάβες σε διάφορα βιολογικά μακρομόρια και κατά συνέπεια σε κυτταρικές λειτουργίες. Μάλιστα, εκτός από τις επιβλαβείς συνέπειες που έχουν για το κύτταρο, έχουν σημαντική λειτουργία και στη μεταγωγή σήματος, τόσο ενδοκυτταρικά, όσο και διακυτταρικά. Σε γενικές γραμμές, δραστικές μορφές οξυγόνου παράγονται κατά: τις αντιδράσεις της αναπνευστικής αλυσίδας, τα προοξειδωτικά ενζυμικά συστήματα, τη λιπιδική οξείδωση, την ακτινοβολία, τη φλεγμονή, το κάπνισμα Ενδοκυτταρικές πηγές 1) Οξειδωτική φωσφορυλίωση Είναι μία διαδικασία, η οποία λαμβάνει χώρα στην εσωτερική μεμβράνη των μιτοχονδρίων και θεωρείται ίσως η σημαντικότερη ενδοκυτταρική πηγή ROS. Η πλειοψηφία των ROS παράγεται στην αλυσίδα μεταφοράς ηλεκτρονίων στα μιτοχόνδρια αφού το 0,1-1% του οξυγόνου μετατρέπεται σε ρίζα. Η αφυδρογονάση του ΝΑDH (σύμπλεγμα 1) και το σύμπλεγμα κυτοχρώματος bc1 (σύμπλεγμα 3), είναι γνωστές θέσεις παραγωγής O 2 - και H 2 O 2 (Chance et al., 1979). Το H 2 O 2 δημιουργείται με τη μεταφορά από το NADH και FADH 2 στην ουβικινόνη. Η ροή ηλεκτρονίων στο μοριακό οξυγόνο παράγει O 2 - (Chance et al., 1979). Το O 2 - ανάγεται σε H 2 O 2 από τη μιτοχονδριακή δισμουτάση του υπεροξειδίου (Mn-SOD). Ακόμα, μέσω της αντίδρασης Haber-Weiss ανάμεσα στο O 2 - και στο H 2 O 2 δημιουργείται OH. Αντίδραση Haber-Weiss: Fe 3+ + Ο 2.- Fe 2+ + Ο 2 Fe 2+ + Η 2 Ο 2 Fe 3+ + ΟΗ - + ΟΗ. Net Ο.- + Η 2 Ο 2 ΟΗ - + ΟΗ. + Ο 2 Στην εσωτερική μεμβράνη του μιτοχονδρίου παράγεται επίσης μονοξείδιο του αζώτου (NO) από τη συνθάση του NO. Το μονοξείδιο του αζώτου αντιδρά με το ανιόν σουπεροξειδίου (O 2 - ) και παράγει υπεροξυνιτρικό ανιόν (ONOO - ), το οποίο σε φυσιολογικό ph παράγει υπεροξυνιτρώδες οξύ (ONOOH) (Koppenol, 1998). Από αυτό τελικά σχηματίζονται οι ρίζες OH και NO 2. Η αντίδραση του μονοξειδίου του αζώτου (NO) με την ουβικινόλη (UQH 2 ) οδηγεί στο σχηματισμό ημικινόνης (UQH), η οποία λειτουργεί σαν σημείο παραγωγής σουπεροξειδίου (O 2 - ) (Boveris & Cadenas, 1997). Σελίδα 16
17 2) Ουδετερόφιλα και αναπνευστική «έκρηξη» Τα πολυμορφοπύρηνα ουδετερόφιλα (Polymorphonuclear neutrophil, PMN) είναι κύτταρα του ανοσοποιητικού που παίζουν σημαντικό ρόλο στην προστασία των ιστών από την προσβολή τους από ιούς και βακτήρια (Pyne, 1994). Η ενεργοποίηση των PMN τυπικά αρχίζει με την καταστροφή του ιστού που προκαλείται από ROS ή άλλους μηχανισμούς (Meydani & Evans, 1979). Στην οξεία φάση αντίδρασης, τα PMN μεταναστεύουν στην περιοχή τραυματισμού καθώς προσελκύονται από χημειοτακτικούς παράγοντες που προέρχονται από τα κατεστραμμένα κύτταρα και απελευθερώνουν τα λυτικά ένζυμα καθώς και το O 2 - κατά τη διάρκεια της φαγοκυττάρωσης. Τα λυτικά ένζυμα διευκολύνουν την καταστροφή των πρωτεϊνών που έχουν υποστεί βλάβες, ενώ το O 2 - παράγεται από τη μυελοϋπεροξειδάση και την NADPH οξειδάση (Petrone et al., 1992). Η κυτταροπλασματική δισμουτάση του υπεροξειδίου μετατρέπει το O 2 - σε H 2 O 2, το οποίο στη συνέχεια μετατρέπεται σε OH από ιόντα μετάλλων ή σε HOCl: Η 2 Ο 2 + Cl - HOCl +OH Αυτή η φλεγμονώδης αντίδραση θεωρείται σημαντική για την απομάκρυνση κατεστραμμένων πρωτεϊνών και την παρεμπόδιση βακτηριακής και ιϊκής μόλυνσης. Ωστόσο, ROS και άλλα οξειδωτικά μόρια που απελευθερώνονται από τα ουδετερόφιλα μπορούν να προκαλέσουν δευτερογενή βλάβη όπως υπεροξείδωση των λιπιδίων (Meydani & Evans, 1979; Meydani et al., 1992). Η φαγοκυττάρωση βακτηρίων ή ιών, προκαλεί το φαινόμενο που είναι γνωστό και ως αναπνευστική «έκρηξη». Χαρακτηρίζεται από αυξημένη κατανάλωση οξυγόνου και γλυκόζης από τα κύτταρα και έχει ως αποτέλεσμα την παραγωγή σουπεροξειδίου και εν τέλει HOCl. 3) Μετατροπή της ξανθίνης σε ουρικό οξύ Οι αντιδράσεις που καταλύονται από την οξειδάση της ξανθίνης αποτελούν σημαντική πηγή παραγωγής ελευθέρων ριζών (Downey, 1990; Kuppasamy & Zweier, 1989). Κατά τη διάρκεια της ισχαιμίας το ATP αποφωσφορυλιώνεται σε ADP και AMP εξαιτίας της ενέργειας που απαιτείται λόγω της σύσπασης του μυοκαρδίου. Αν τα αποθέματα οξυγόνου είναι ανεπαρκή το AMP μετατρέπεται σε υποξανθίνη, ξανθίνη και τελικά σε ουρικό οξύ. Η αντίδραση αυτή καταλύεται από την οξειδάση της ξανθίνης και συνοδεύεται από σχηματισμό του O 2 -. Η οξειδάση της ξανθίνης πρέπει να μετατραπεί από την ανηγμένη στην οξειδωμένη της μορφή από μία ενδοκυτταρική πρωτεάση που ενεργοποιείται από το Ca 2+ ενώ το μοριακό οξυγόνου είναι δέκτης ηλεκτρονίων. 4) Κυτόχρωμα P450 Κάτω από φυσιολογικές συνθήκες τα μικροσώματα των ηπατικών κυττάρων παράγουν ROS μέσου του κυτοχρώματος P 450 (Yu, 1994). Το NADPH υφίσταται οξείδωση δημιουργώντας O 2 - το οποίο στη συνέχεια μπορεί να μετατραπεί σε H 2 O 2 (Chance et al., 1979). Ο ρυθμός παραγωγής του H 2 O 2 είναι ανάλογος με την κατανάλωση οξυγόνου στο μικρόσωμα (Halliwell & Gutteridge, 1989). Παρουσία ADP και Fe 3+ η NADPH οξειδάση καταλύει τη μεταφορά ενός ηλεκτρονίου από το NADPH στο O 2 παράγοντας O 2 -. Σελίδα 17
18 5) Αυτοοξείδωση μορίων Ορισμένα μόρια όπως φλαβίνες, κατεχολαμίνες, θειόλες και η αιμογλοβίνη μπορούν να αυτοοξειδωθούν σχηματίζοντας ανιόν σουπεροξειδίου (O 2 - ). Εξωκυτταρικές πηγές Η ηλιακή και η ηλεκτρομαγνητική ακτινοβολία καθώς και το όζον, η ατμοσφαιρική ρύπανση, ο καπνός του τσιγάρου και τα βιομηχανικά απόβλητα είναι σημαντικοί οξειδωτικοί παράγοντες (Koren, 1995; Victoria, 1994). Επίσης, ελεύθερες ρίζες μπορούν να παραχθούν από τη δράση ορισμένων φαρμάκων (Naito et al., 1998; Rav et al., 2001) και άλλων ξενοβιοτικών όπως τοξίνες και εντομοκτόνα καθώς ακόμα και από το αλκοόλ (Elsayed et al., 1992; Jones et al., 2000; Obata et al., 2001; Wormser et al., 2000). Τέλος, σημαντική πηγή οξειδωτικών είναι και η διατροφή (Ames, 1986; Kanner & Labidot, 2001; Lijinsky, 1999). Εικόνα 2: Πηγές παραγωγής ελευθέρων ριζών. Όσο πιο σταθερή είναι μια ρίζα, τόσο πιο εύκολος είναι και ο σχηματισμός της (Valavanidis, 2006). Οι ρίζες εξουδετερώνονται είτε αλληλεπιδρώντας μεταξύ τους, είτε με άλλες ρίζες, είτε με άλλα συστατικά του κυττάρου. Αν μια ρίζα αλληλεπιδράσει με μια μη ρίζα, τότε το ασύζευκτο ηλεκτρόνιο θα μεταφερθεί στην δεύτερη, σχηματίζοντας μια νέα ρίζα. Αν όμως αλληλεπιδράσουν δυο ρίζες μεταξύ τους, τότε τα ασύζευκτα ηλεκτρόνια θα δημιουργήσουν ένα ζεύγος, με αποτέλεσμα το σχηματισμό μιας ένωσης που δε θα είναι ελεύθερη ρίζα. Υπάρχουν πολλοί τύποι ελεύθερων ριζών στο σώμα: Η ρίζα του υπεροξειδίου τείνει να προσλαμβάνει το απαραίτητο ηλεκτρόνιο από τα μιτοχόνδρια του κυττάρου. Όταν τα μιτοχόνδρια καταστρέφονται, το κύτταρο χάνει την ικανότητα να παράγει ενέργεια και πεθαίνει. Η ρίζα του υδροξυλίου μπορεί να αντιδρά με ένζυμα, πρωτεΐνες και λίπη στις κυτταρικές μεμβράνες. Η ρίζα του περοξυλίου λιπιδίων προκαλεί μια αλυσιδωτή αντίδραση υπεροξείδωσης των λιπιδίων, η οποία μπορεί να βλάψει την κυτταρική μεμβράνη, προκαλεί τη λύση του κυττάρου και την ελευθέρωση του περιεχομένου του. Σελίδα 18
19 Το μονήρες οξυγόνο δεν είναι ουσιαστικά ελεύθερη ρίζα, αλλά μπορεί να προκαλέσει την παραγωγή άλλων ελευθέρων ριζών. Εικόνα 3 : Το DNA,οι πρωτεΐνες και τα λιπίδια αποτελούν τους στόχους των ΔΜΟ. Εικόνα 4: Τρόποι σχηματισμού ελευθέρων ριζών Επιπτώσεις οξειδωτικού στρες στα βιομόρια Σε κυτταρικό επίπεδο, το οξειδωτικό στρες προκαλεί βλάβες σε όλα τα μακρομόρια (DNA, πρωτεΐνες και λιπίδια). Παράλληλα οι ελεύθερες ρίζες μπορούν να αλληλεπιδράσουν με σηματοδοτικά μονοπάτια του κυττάρου, αλλοιώνοντας έτσι τη σηματοδότηση, ενώ αν οι βλάβες είναι εκτεταμένες οδηγεί σε κυτταρικό θάνατο, είτε με απόπτωση είτε με νέκρωση. Ως προς τον κυτταρικό θάνατο το κύτταρο οδηγείται εκεί σε περίπτωση εκτεταμένων βλαβών είτε μέσω της νέκρωσης είτε μέσω της απόπτωσης. Κατά τη νέκρωση, το κύτταρο διογκώνεται και Σελίδα 19
20 διαρρηγνύεται απελευθερώνοντας το περιεχόμενό του στο περιβάλλον επηρεάζοντας και τα γειτονικά κύτταρα. Στην απόπτωση τα κύτταρα δεν απελευθερώνουν το περιεχόμενό τους και δεν προκαλούν βλάβες στα γειτονικά κύτταρα. Λιπίδια Όλες οι κυτταρικές μεμβράνες είναι ευάλωτες σε οξείδωση εξαιτίας των υψηλών συγκεντρώσεων σε ακόρεστα λιπαρά οξέα. Η υπεροξείδωση των λιπιδίων συμβαίνει σε τρία στάδια. Το πρώτο στάδιο περιλαμβάνει την επίθεση της ελεύθερης ρίζας, η οποία αποσπά ένα άτομο υδρογόνου από μια ομάδα μεθυλενίου στα λιπίδια. Η παρουσία ενός διπλού δεσμού γειτονικά της ομάδας μεθυλενίου εξασθενεί τον δεσμό μεταξύ των ατόμων υδρογόνου και άνθρακα έτσι ώστε να μπορεί να αποσπαστεί εύκολα από το μόριο. Μετά την απόσπαση του υδρογόνου το λιπαρό οξύ διατηρεί ένα ηλεκτρόνιο και σταθεροποιείται με επαναδιευθέτηση της μοριακής δομής για να σχηματίσει ένα συζυγές διένιο. Όταν το οξυγόνο είναι σε επαρκή ποσότητα στο περιβάλλον, το λιπαρό οξύ θα αντιδράσει με αυτό για να σχηματίσει ROO κατά τη διάρκεια της φάσης πολλαπλασιασμού. Αυτές οι ελεύθερες ρίζες είναι ικανές να αποσπάσουν κι άλλο άτομο υδρογόνου από ένα γειτονικό λιπαρό οξύ, το οποίο οδηγεί ξανά σε παραγωγή ριζών λιπαρών οξέων που υποβάλλονται στις ίδιες διαδικασίες- επαναδιευθέτησης και αλληλεπίδρασης με οξυγόνο (Halliwell & Gutteridge, 1999). Πρωτεΐνες Ανάμεσα στις διάφορες ROS, το OH, το RO και οι ενεργές ρίζες αζώτου προκαλούν πρωτεϊνική καταστροφή. Οι πρωτεΐνες υποβάλλονται σε άμεση και έμμεση καταστροφή μετά την αλληλεπίδραση με ROS όπως είναι οι αλλαγές στην τριτοταγή τους δομή, ο εκφυλισμός και η καταστροφή τους τους. Οι επιπτώσεις της πρωτεϊνικής καταστροφής είναι η απώλεια της ενζυμικής λειτουργίας, οι αλλαγμένες κυτταρικές λειτουργίες όπως παραγωγή ενέργειας και οι αλλαγές στον τύπο και στο επίπεδο των κυτταρικών πρωτεϊνών (Davis, 1987; Grune et al., 1997; Halliwell and Gutteridge, 1999; Levine et al., 2000; Stadtman, 1986). DNA Αν και το DNA είναι ένα σταθερό και καλά προστατευμένο μόριο, οι ROS μπορούν να αλληλεπιδράσουν με αυτό και να προκαλέσουν καταστροφές όπως η τροποποίηση των βάσεων, οι θραύσεις του DNA, η απώλεια πουρινών, η ζημιά στο σάκχαρο δεοξυριβόζης και η βλάβη στο σύστημα επιδιόρθωσης του DNA. Η ρίζα υδροξυλίου(oh ) προσβάλλει τη γουανίνη στη θέση C-8 και σχηματίζει ένα οξειδωτικό προϊόν, την 8-υδροξυγουανίνη (8-OHdG). Οι ρίζες υδροξυλίου μπορούν επίσης να επιτεθούν και σε άλλες βάσεις όπως η αδενίνη για να σχηματίσουν την 8-υδροξυαδενίνη. Η αλληλεπίδραση ανάμεσα στις πυριμιδίνες και στις ρίζες υδροξυλίου οδηγεί στο σχηματισμό υπεροξειδίου της θυμίνης, 5-ουρακίλης, γλυκολών της θυμίνης και άλλων παρεμφερών προϊόντων (Ames, 1986; Beckman and Koppenol, 1996; Dizdaroglu and Jaruga et al., 2002; Halliwell, 2001; Halliwell and Gutteridge, 1999; Helbock et al., 1999). Λιποειδή Υπεροξείδωση Ασθένειες Πρωτεΐνες Ένζυμα Μετουσίωση Απενεργοποίηση Βλάβες Νουκλεϊκά οξέα Μεταλλάξεις Γήρανση Σελίδα 20
21 1.1.5 Αντιοξειδωτική άμυνα Σε κάθε βιολογικό σύστημα, πρέπει να διατηρείται η ισορροπία μεταξύ του σχηματισμού και της απομάκρυνσης των ΔΕΟ. Η αύξηση των οξειδώσεων από τα ΔΕΟ οδηγεί τα κύτταρα σε μία κατάσταση που λέγεται οξειδωτικό στρες, ο οποίος όρος περιγράφει την κατάσταση ανισορροπίας, ανάμεσα στις συγκεντρώσεις των δραστικών μορφών οξυγόνου Reactive Oxygen Species - (ROS) και των αντιοξειδωτικών αμυντικών μηχανισμών ενός οργανισμού (Halliwel & Gutteridge, 1990; Dotan, et.al., 2004). Λόγω της συνεχούς έκθεσης σε ΔΕΟ και για την πρόληψη του οξειδωτικού στρες, ο οργανισμός μας, όπως όλα τα φυτά και τα ζώα, έχει αναπτύξει για προστασία διάφορους αντιοξειδωτικούς μηχανισμούς στους οποίους παίρνουν μέρος αντιοξειδωτικές ουσίες. Εικόνα 5 : Οξειδωτικό στρες. Γενικά χαρακτηρίζουμε ως αντιοξειδωτική ουσία κάθε ουσία η οποία βρίσκεται σε μικρές συγκεντρώσεις σε σύγκριση με το υπόστρωμα που οξειδώνεται και η οποία καθυστερεί σημαντικά ή αποτρέπει την οξείδωση του υποστρώματος αυτού. (Vaya J. and Aviram M., 2001) Ο Ρόλος Των Αντιοξειδωτικών Τα αντιοξειδωτικά παίρνουν μέρος σε μια σειρά από θετικές λειτουργίες στον ανθρώπινο οργανισμό, μερικές από τις οποίες αναφέρονται: Προστατεύουν τις κυτταρικές μεμβράνες, και συνεπώς το κύτταρο, εξουδετερώνοντας τις ελεύθερες ρίζες οξυγόνου. Δρουν καρδιοπροστατευτικά, αυξάνοντας την ανθεκτικότητα των αγγείων, περιορίζοντας τους φλεγμονώδεις παράγοντες, αποτρέποντας την οξείδωση της LDL χοληστερίνης και συμβάλλοντας στον έλεγχο των επιπέδων της αρτηριακής πίεσης και της οµοκυστεϊνης. Ασκούν αντικαρκινική δράση με το να μπλοκάρουν ή να εμποδίζουν την προσκόλληση επικίνδυνων ενζύµων στους ιστούς, αδρανοποιούν καρκινογόνες ουσίες που προκαλούν μεταλλάξεις σε υγιή κύτταρα κι επιβραδύνουν τους µηχανισµούς καρκινογένεσης. Βελτιώνουν τις πνευματικές ικανότητες και την ψυχική διάθεση, προστατεύοντας τους νευροδιαβιβαστές από την οξείδωση και βελτιώνοντας την εγκεφαλική µικροκυκλοφορία. Διατηρούν το δέρµα ελαστικό και το προφυλάσσουν από την πρόωρη γήρανση, περιορίζοντας τη διάσπαση του κολλαγόνου. Προστατεύουν οστά και αρθρώσεις, περιορίζοντας οιδήματα, φλεγμονές και εκφυλιστικές αλλοιώσεις. Σελίδα 21
22 Βελτιώνουν τη λειτουργική κατάσταση του αμφιβληστροειδούς χιτώνα των ματιών και ενισχύουν την όραση. Δρουν αντιαλλεργικά σε μεγάλο φάσµα αλλεργιών. Διαφυλάσσουν τα αποθέµατα άλλων απαραίτητων θρεπτικών ουσιών στον οργανισµό, αποτρέπουν την καταστροφή τους και, σε ορισμένες περιπτώσεις, ενισχύουν τη δράση τους. Εικόνα 6 : Τρόπος δράσης αντιοξειδωτικών παραγόντων Πηγές Αντιοξειδωτικών Ο ανθρώπινος οργανισμός διαθέτει αντιοξειδωτικά συστήματα (ενδογενή αντιοξειδωτικά) τα οποία μπορεί να είναι ενζυμικά ή μη ενζυμικά ή τα λαμβάνει εξωγενώς (εξωγενή αντιοξειδωτικά). Τα ενζυμικά αντιοξειδωτικά είναι το κυτόχρωμα C, η υπεροξειδική δισμουτάση (SOD), η υπεροξειδάση της γλουταθειόνης, η τρανσφεράση-s της γλουταθειόνης και η καταλάση. 1) Υπεροξειδική δισμουτάση (SOD) Η υπεροξειδάση της δισμουτάσης (SOD) είναι ίσως το πιο σημαντικό ένζυμο του αντιοξειδωτικού μηχανισμού. Καταλύει την αντίδραση μετατροπής του O 2 - σε H 2 O 2 : SOD 2 O H + H 2 O 2 + O 2 Το O 2 - παράγεται κατά την οξειδωτική φωσφορυλίωση στα μιτοχόνδρια και ανάγεται από τη μιτοχονδριακή SOD (Mn-SOD), ενώ όσο διαχέεται στο κυτταρόπλασμα ανάγεται από την κυτταροπλασματική SOD (Cu -SOD), η οποία βρίσκεται σε μεγάλα ποσά στα μυϊκά κύτταρα. Υπάρχουν διάφορες μορφές SOD στα βιολογικά συστήματα όπως η Cu,Zn-SOD στο εξωκυττάριο υγρό και η Fe- SOD στα βακτήρια και τα φυτά. 2) Καταλάση (CAT) Η καταλάση (CAT) εντοπίζεται στα υπεροξειδιοσώματα. Αποτελείται από τέσσερις πρωτεϊνικές υπομονάδες, άνω των 500 αμινοξέων, καθεμία από τις οποίες περιέχει και μία ομάδα αίμης στην ενεργό περιοχή τους. Επίσης, κάθε υπομονάδα φέρει ένα μόριο NADPH, το οποίο συμβάλλει στη σταθερότητα του ενζύμου. Τα υπεροξειδιοσώματα παίζουν ρόλο στην αποτοξίνωση του κυττάρου χρησιμοποιώντας οξυγόνο και παράγοντας Η 2 Ο 2 (Antunes et al., 2002). Η καταλάση καταλύει την αντίδραση μετατροπής Σελίδα 22
23 του Η 2 Ο 2 σε Η 2 Ο και Ο 2. 3) Υπεροξειδάση της γλουταθειόνης (GPX) CAT 2Η 2 Ο 2 2Η 2 Ο +Ο 2 Η υπεροξειδάση της γλουταθειόνης (GPX) είναι ένα ένζυμο που εντοπίζεται στα μιτοχόνδρια, το κυτταρόπλασμα αλλά και τον εξωκυττάριο χώρο και είναι άφθονο στην καρδιά, τους πνεύμονες και τον εγκέφαλο. Όπως και η καταλάση, έτσι και η GPX καταλύει την αντίδραση μετατροπής του Η 2 Ο 2 σε Η 2 Ο και Ο 2 χρησιμοποιώντας την ανηγμένη γλουταθειόνη, η οποία κατά τη διάρκεια της αντίδρασης οξειδώνεται: (Antunes et al., 2002) GPX H 2 O 2 + 2GSH 4) Αναγωγάση της γλουταθειόνης (GR) 2 H 2 O + GSSG Η αναγωγάση της γλουταθειόνης (GR) καταλύει την αναγωγή της GSSG σε GSH κι έτσι διατηρεί τη φυσιολογική αναλογία GSSG:GSH στο εσωτερικό του κυττάρου. Αποτελείται από δύο υπομονάδες, κάθε μία από τις οποίες περιέχει στην ενεργό περιοχή της ένα φλαβινο-αδενινο-δινουκλεοτίδιο (FAD). Το NADPH ανάγει το FAD, το οποίο στη συνέχεια μεταφέρει τα ηλεκτρόνιά του στη δισουλφιδική γέφυρα. Οι δύο σουλφυδρυλομάδες που σχηματίζονται αλληλεπιδρούν με την GSSG και την ανάγουν σε 2 μόρια GSH. Εικόνα 7: Απεικόνιση δράσης των GR, GPx, SOD, CAT. Στα μη ενζυμικά αντιοξειδωτικά συμπεριλαμβάνονται η α-τοκοφερόλη, το β-καροτένιο και το συνένζυμο Q10 τα οποία είναι προσαρμοσμένα στις μεμβράνες ενώ, υπάρχουν και το ασκορβικό οξύ, το ουρικό οξύ, η τρανσφερίνη, η χολερυθρίνη, η γλουταθειόνη, η λακτοφερίνη κ.α. τα οποία βρίσκονται έξω από τις μεμβράνες. 1) Γλουταθειόνη Η γλουταθειόνη είναι μία ένωση που κατατάσσεται στην κατηγορία των θειολών. Πρόκειται για ένα τριπεπτίδιο που αποτελείται από γλουταμινικό οξύ, κυστεΐνη και γλυκίνη και περιέχει μία σουλφυδρυλομάδα. Η σουλφυδρυλική κυστεΐνη λειτουργεί ως δότης ηλεκτρονίων και είναι υπεύθυνη για Σελίδα 23
24 τη βιολογική δραστηριότητα της γλουταθειόνης. Η κυστεΐνη είναι περιοριστικός παράγοντας στην κυτταρική σύνθεση της γλουταθειόνης, δεδομένου ότι αυτό το αμινοξύ είναι σχετικά σπάνιο στα τρόφιμα. Ωστόσο, σε ελεύθερη μορφή, η κυστεΐνη είναι τοξική και καταβολίζεται στο γαστρεντερικό σωλήνα και στο πλάσμα αίματος. Η γλουταθειόνη είναι ένα υδατοδιαλυτό μόριο, το οποίο συντίθεται στο ήπαρ και μέσω της κυκλοφορίας του αίματος μεταφέρεται στους ιστούς. Είναι ένα σημαντικό ενδοκυτταρικό αντιοξειδωτικό καθώς συμβάλλει στην προστασία από οξειδωτική βλάβη (Scholz RW et al, 1989). Αυτό οφείλεται στο γεγονός ότι μπορεί να ανακυκλώνεται διαρκώς από την οξειδωμένη (GSSG) προς την ανηγμένη μορφή (GSH) και το αντίστροφο. Η σύνθεσή της ελέγχεται από αυτή την επανατροφοδοτική αναστολή (feedback) του ενζύμου που την συνθέτει (συνθετάση της γ-γλουταμυλοκυστείνης). Η ανηγμένη μορφή είναι αυτή που έχει αντιοξειδωτικές ιδιότητες καθώς συμμετέχει σε αντιδράσεις που αναφέρθηκαν παραπάνω (Halliwell & Gutteridge,1998). Η ανηγμένη μορφή, συναντάται συχνότερα σε σχέση με την οξειδωμένη και συνήθως, η GSSG είναι το 10% της GSH. Ειδικότερα, ο λόγος της ανηγμένης προς την οξειδωμένη γλουταθειόνη στα κύτταρα χρησιμοποιείται συχνά σαν δείκτης της παρουσίας ελεύθερων ριζών, δηλαδή της ύπαρξης οξειδωτικού στρες. Εικόνα 8: Δομή γλουταθειόνης Η γλουταθειόνη δρα ενάντια του οξειδωτικού στρες απομακρύνοντας τις δραστικές μορφές του οξυγόνου (ROOH,H 2 O 2 ) και τις εξωγενείς ηλεκτρόνιοφιλες (πχ. κινόνες). Εκτός αυτού, η GSH συμβάλλει στην αναγωγή και άλλων αντιοξειδωτικών του κυττάρου (ασκορβικού οξέος, βιταμίνης Ε) συμμετέχοντας έτσι στη διατήρηση της ισορροπίας των επιπέδων των συγκεκριμένων βιταμινών (Παπαγεωργίου 2005). Ένα σημαντικό χαρακτηριστικό της συγκεκριμένης ένωσης, είναι οι αναγωγικές της ιδιότητες. Ειδικότερα, αυτές διαδραματίζουν σημαντικό ρόλο σε διάφορα μεταβολικά μονοπάτια, με χαρακτηριστικό παράδειγμα το αντιοξειδωτικό σύστημα των περισσότερων αερόβιων κυττάρων. Ένα ακόμα χαρακτηριστικό της γλουταθειόνης, είναι ότι χρησιμοποιείται από πολλά ένζυμα, όπως η υπεροξειδάση της γλουταθειόνης και η S-τρανσφεράση της γλουταθειόνης. Η κύρια αποστολή της είναι η διάσπαση και απομάκρυνση από το σώμα όλων των εν δυνάμει επικίνδυνων τοξινών που εισβάλλουν στο σώμα μας. Είναι ένα αντιοξειδωτικό που παρεμποδίζει την οξείδωση των λιπιδίων από τις ελεύθερες ρίζες στη γαστρεντερική οδό και προστατεύει τα κύτταρα από τις βλάβες που αυτές μπορεί να προκαλέσουν. Τα επίπεδα γλουταθειόνης στο αίμα ελαττώνονται κατά 17% από την ηλικία των σαράντα μέχρι την ηλικία των εξήντα. Σε χαμηλά επίπεδα γλουταθειόνης υπάρχει 33% μεγαλύτερος κίνδυνος για χρόνια νοσήματα. Στα χρόνια νοσήματα το 77% των ασθενών Σελίδα 24
25 έχουν ανεπάρκεια γλουταθειόνης. Η κατανάλωση λίπους αυξάνει τις ανάγκες του οργανισμού για γλουταθειόνη. Η αύξηση της γλουταθειόνης με χορήγηση πρόδρομων ουσιών για τη βιοσύνθεση της ή η ενδοφλέβια χορήγηση γλουταθειόνης είναι στρατηγικές που αναπτύχθηκαν για την αντιμετώπιση καταστάσεων όπως ανεπάρκεια του τριπεπτιδίου, υψηλό οξειδωτικό στρες και ανεπάρκεια του ανοσοποιητικού συστήματος. Συμπληρωματικά, η γλουταθειόνη είναι δυνατόν να επιτελεί και τις παρακάτω λειτουργίες: Μετέχει στον κύκλο μονοξειδίου του αζώτου που είναι κρίσιμος για τη ζωή. Χρησιμοποιείται σε μεταβολικές και βιοχημικές αντιδράσεις, όπως στη σύνθεση και επιδιόρθωση του DNA, την πρωτεϊνική σύνθεση, τη σύνθεση των προσταγλανδινών, τη μεταφορά αμινοξέων και την ενεργοποίηση ενζύμων. Έτσι, κάθε σύστημα του σώματος μπορεί να επηρεαστεί από τις συγκεντρώσεις της γλουταθειόνης, ιδιαίτερα το ανοσοποιητικό σύστημα, το νευρικό, το γαστρεντερικό και οι πνεύμονες. Παίζει ρόλο στο μεταβολισμό του σιδήρου. Διαδραματίζει σημαντικό ρόλο στο μεταβολισμό των φαρμάκων και του ασβεστίου. Βοηθά στη λειτουργία των αιμοπεταλίων και των κυτταρικών μεμβρανών. Συμμετέχει στην απομάκρυνση των ξενοβιοτικών ουσιών από τον οργανισμό. Απομακρύνει υπεροξείδια και ελεύθερες ρίζες. Βοηθά στη μεταφορά των αμινοξέων διαμέσου των μεμβρανών. 2) Βιταμίνες Οι βιταμίνες είναι αντιοξειδωτικά που λαμβάνονται μέσω της διατροφής και έχουν ευεργετική επίδραση στην υγεία. Είναι μη θερμιδικές ουσίες, απαραίτητες για το μεταβολισμό και συνήθως λειτουργούν ως συνένζυμα σε ενζυμικές αντιδράσεις. Ο οργανισμός δεν είναι σε θέση να τις παράγει γι αυτό το λόγο και λαμβάνονται μέσω της δίαιτας. Τα χαρακτηριστικά και οι λειτουργίες κάθε βιταμίνης ποικίλουν όπως ποικίλει και η απαιτούμενη διαιτητική πρόσληψη για κάθεμία. (Καλογιάννης 2010) 2.1) Βιταμίνη E Η βιταμίνη Ε είναι μια λιποδιαλυτή βιταμίνη, που αποτελείται από διάφορες τοκοφερόλες. Η πιο δραστική αλλά και πιο άφθονη είναι η α-τοκοφερόλη. Βρίσκεται στην κυττοπλασματική αλλά και τη μιτοχονδριακή μεμβράνη και προστατεύει τα λιπίδια από την υπεροξείδωση, που προκαλείται από τις ελεύθερες ρίζες. Επίσης, προστατεύει τη βιταμίνη Α από την οξείδωση (Halliwell & Gutteridge, 1998). 2.2) Βιταμίνη C Η βιταμίνη C ή αλλιώς, ασκορβικό οξύ είναι ένα υδατοδιαλυτό, ισχυρό αντιοξειδωτικό μόριο και μπορεί να εξουδετερώνει άμεσα τις ROS (Halliwell & Gutteridge, 1998). Η αναγωγική μορφή της βιταμίνης C είναι ένα σακχαρικό οξύ και κατατάσσεται στους μονοσακχαρίτες. Πολλοί οργανισμοί έχουν τη δυνατότητα να συνθέτουν τη βιταμίνη C. Είναι ένα απαραίτητο διατροφικό στοιχείο για τον άνθρωπο, ο οποίος δε μπορεί να τη βιοσυνθέσει, επειδή το ένζυμο οξειδάση της γουλονολακτόνης, που καταλύει τη τελευταία αντίδραση της βιοσύνθεσης του ασκορβικού οξέος από γλυκόζη απουσιάζει. Το ασκορβικό οξύ αποτελεί ένα συμπαράγοντα ή συνένζυμο οχτώ ενζυμικών αντιδράσεων που συμβαίνουν στον οργανισμό. Αυτές αφορούν τη βιοσύνθεση του κολλαγόνου, της καρτινίνης, το μεταβολισμό της τυροσίνης καθώς και είναι άκρως απαραίτητες στη σύνθεση ορμονών και την απελευθέρωσή τους από τα Σελίδα 25
26 επινεφρίδια. Ανήκει στα υδρόφιλα αντιοξειδωτικά και φαίνεται να βρίσκεται στη πρώτη γραμμή άμυνας κατά των οξειδωτικών βλαβών (Suvana Kimnite Wattanapitayakul, 2001). Το ασκορβικό οξύ είναι αναγωγικό αντιδραστήριο (δότης ηλεκτρονίων), πράγμα που σημαίνει ότι μπορεί να προμηθεύσει ηλεκτρόνια τόσο σε ένζυμα όσο και σε οξειδωτικές ενώσεις με τα οποία εξουδετερώνει ελεύθερες ρίζες. Έτσι, μπορεί να ανάγει το σουπεροξείδιο, τις υδροξυλικές ρίζες, το υποχλωριώδες οξύ καθώς και άλλες δραστικές μορφές οξυγόνου μέσα και έξω από τα κύτταρα. Στο κυτόπλασμα το ασκορβικό οξύ και η γλουταθεονίνη παρουσιάζουν συνεργό δράση για να προστατέψουν το κύτταρο από οξειδωτικές βλάβες. Εκτός του κυττάρου, το ασκορβικό οξύ πιθανώς να δρα σε σύζευξη με τη βιταμίνη Ε, η οποία βρίσκεται στις κυτταρικές μεμβράνες ώστε να τις προστατεύει από τη λιπιδική υπεροξείδωση, εξουδετερώνοντας τις ελεύθερες ρίζες. Στις μεμβράνες η φαινολική υδροξυλική ομάδα της βιταμίνης Ε βρίσκεται μεταξύ της μεμβράνης και της υδατικής φάσης, όπως συμβαίνει και με τις πολικές κεφαλές των φωσφολιπιδίων. Με ανάλογο τρόπο η βιταμίνη Ε προστατεύει και τις LDL από τη λιπιδική υπεροξείδωση και έτσι συμβάλλει στην πρόληψη του σχηματισμού αθηρωματικών πλακών (Παπαγεωργίου 2005). Το ασκορβικό οξύ μπορεί να ανάγει τόσο το Fe 3+ σε Fe 2+ όσο και το Cu 2+. Έτσι, μίγμα σιδήρου ή χαλκού με ασκορβικό οξύ παράγει in vitro την παραγωγή ελευθέρων ριζών και μπορεί να προκαλέσει βλάβες στο DNA, στις πρωτεΐνες και στα λιπίδια. Η συγκεκριμένη προ-οξειδωτική δράση, που εμφανίζει το ασκορβικό οξύ in vitro έχει μεγάλη σημασία επειδή σχετίζεται με την περιεκτικότητα του ασκορβικού στα τρόφιμα. Σε πολύ μεγάλες συγκεντρώσεις θα παρουσιάζει τοξική δράση. Η περίσσεια της βιταμίνης C αποβάλλεται μέσω των ούρων (Suvana Kimnite Wattanapitayakul, 2001). 3) Β-καροτίνη Η β-καροτίνη είναι λιποδιαλυτό μόριο και βρίσκεται στις κυτταρικές μεμβράνες. Μπορεί να μετατραπεί σε βιταμίνη Α. Πιστεύεται ακόμα, ότι και αυτή μπορεί να αδρανοποιήσει τις ελεύθερες ρίζες και να περιορίσει την υπεροξείδωση των λιπιδίων. Παίζει ρόλο στην ενίσχυση του ανοσοποιητικού συστήματος και αλληλεπιδρά με τις βιταμίνες C, Ε και το σελήνιο (Halliwell & Gutteridge, 1998). 4) Ουρικό οξύ Το ουρικό οξύ αποτελεί το τελικό προϊόν του μεταβολισμού των πουρινών. Κατά τη διάρκεια της άσκησης αυξάνονται τα επίπεδα του ουρικού οξέος στο πλάσμα του αίματος (Green & Fraser, 1988). Από εκεί μπορεί να διαχυθεί στα μυϊκά κύτταρα και με αυτό τον τρόπο τα προστατεύει από τις ROS. 5) Συνένζυμο Q10 Το συνένζυμο Q10 αποτελεί βασικό συστατικό των ενζύμων της οξειδωτικής φωσφορυλίωσης κατά την παραγωγή ATP. Έχει επίσης ισχυρή αντιοξειδωτική δράση και βοηθά στην αναγέννηση της α- τοκοφερόλης (Halliwell & Gutteridge,1998). 6) Σελήνιο Είναι ένα απαραίτητο μέταλλο που συγκαταλέγεται στα ιχνοστοιχεία. Φαίνεται ότι βοηθά στην πρόληψη διαφόρων ασθενειών. Λειτουργεί ως συμπαράγοντας της υπεροξειδάσης της γλουταθειόνης και με αυτό τον τρόπο συμμετέχει στους αντιοξειδωτικούς μηχανισμούς (Halliwell & Gutteridge, 1998). Σελίδα 26
27 Υπάρχουν πολλά τρόφιµα που περιέχουν αντιοξειδωτικές ουσίες, τα κυριότερα εκ των οποίων παραθέτονται παρακάτω: Βιταμίνη Α: αυγό, βούτυρο, γάλα και γαλακτοκομικά προϊόντα, συκώτι, ιχθυέλαια. Βιταμίνη C: φρούτα, κυρίως εσπεριδοειδή (πορτοκάλια, µανταρίνια, νεράντζια), φραγκοστάφυλα, φράουλες, ακτινίδια, κεράσια, µούρα, πεπόνι, ντοµάτα, λάχανο, πράσινη πιπεριά, πράσινα φυλλώδη λαχανικά (µαρούλι, σπανάκι), σταυρανθή (µπρόκολο, κουνουπίδι, λαχανάκια Βρυξελλών) (Χασαπίδου 1996). Β-καροτένιο: φρούτα, κυρίως εσπεριδοειδή, λαχανικά πράσινου, κίτρινου και πορτοκαλί χρώµατος, ντοµάτες, και επίσης (σε μικρότερες ποσότητες) βερίκοκα, γλυκοπατάτες, καρπούζι, κολοκύθα. Βιταμίνη E: φυτικά έλαια (ηλιέλαιο, αραβοσιτέλαιο, βαµβακέλαιο) και κυρίως ελαιόλαδο, δημητριακά ανεπεξέργαστα, σόγια, αμύγδαλα, καρύδια, φουντούκια, λαχανικά σκούρα πράσινα, λαχανικά φυλλώδη, φύτρα σταριού, αυγά. Σελήνιο: κρέας, συκώτι, θαλασσινά, αβοκάντο, ελιές, ξηροί καρποί, δημητριακά, σπόροι, φρούτα και λαχανικά που φυτρώνουν στο έδαφος. Φλαβονοειδή: αρακάς, βατόμουρα, εσπεριδοειδή, κόκκινο κρασί, κουµ κουάτ, κρεμμύδια, µέλι, µήλα, µπρόκολο, πικρή σοκολάτα, σόγια, σταφύλια, τσάι πράσινο και µαύρο, φασολάκια πράσινα και επίσης στους ανθούς λαχανικών και λουλουδιών και στα φύκια. Ψευδάργυρος: δημητριακά, συκώτι, όσπρια, θαλασσινά, σπόροι σιταριού, µαγιά µπύρας, αυγά. Ανθοκυανίνες: γογγύλια, κάρδαµο, κεράσια, κουνουπίδι, κραµβολάχανο, λάχανο κατσαρό, µούρα, µπρόκολο, µύρτιλλα, σπαράγγια, σταφύλια, φράουλες. Ελλαγικό οξύ: βατόμουρα, κεράσια, σταφύλια, φράουλες. Λυκοπένιο: ντοµάτες (φρέσκες, λιαστές και επεξεργασμένα προϊόντα ντοµάτας) και σε μικρότερο βαθμό γκρέιπφρουτ, καρπούζι και πιπεριές. Φαινόλες: ελαιόλαδο, ελιές, εσπεριδοειδή, κακάο, κρασί, λιναρόσπορος, µπρόκολο, σκόρδο, σοκολάτα πικρή, τσάι πράσινο. ΣυνένζυμοQ10: σαρδέλα, σκουµπρί, σόγια. Πυκνογενόλη: φρούτα,λαχανικά, ξηροί καρποί, κακάο, τσάι, και κρασί. Τα αντιοξειδωτικα γενικά λειτουργούν με δύο τρόπους: Είτε παρεμποδίζουν τη δημιουργία ΔΕΟ, είτε σταματούν τη διάδοση των ελεύθερων ριζών που προκαλείται από τις αλυσιδωτές αντιδράσεις. Το οξειδωτικό στρες προκαλείται συνήθως από: Μειωμένη δράση των αντιοξειδωτικών μηχανισμών. Αυτό μπορεί να συμβεί είτε εξαιτίας μεταλλάξεων ή τοξικών παραγόντων που επηρεάζουν τη δραστικότητα των αντιοξειδωτικών ενζύμων είτε από τη μείωση των διατροφικών αντιοξειδωτικών ουσιών. Αυξημένη παραγωγή ελευθέρων ριζών (ROS). Αυτό συμβαίνει είτε λόγω της έκθεσης των κυττάρων σε υψηλά επίπεδα ROS, λόγω της ύπαρξης παραγόντων που οδηγούν στην αυξημένη παραγωγή σε ROS. Σελίδα 27
28 1.1.6 Οξειδωτικό στρες και διαταραχές της υγείας Το οξειδωτικό στρες συμμετέχει σε πολλές παθολογικές καταστάσεις όπως είναι η αθηροσκλύρυνση, νευροεκφυλιστικές ασθένειες όπως Parkinson και Alzheimer, ο καρκίνος και η διαδικασία της γήρανσης (Vera, D., et al., 2013). Πιο συγκεκριμένα η περίσσεια ελευθέρων ριζών μπορεί να οδηγήσει σε αλλοίωση των κυτταρικών μεμβρανών (διακοπή της διακυτταρικής επικοινωνίας), των νουκλεϊκών οξέων (αυξημένος κίνδυνος καρκινογένεσης), των μιτοχονδρίων (αποσύζευξη ενεργειακής παραγωγής) και των πρωτεϊνών. Οι ασθένειες οι οποίες συνδέονται με τη ζημιά λόγω ελευθέρων ριζών είναι καρδιακές παθήσεις, νευρολογικές παθήσεις, αναπνευστικά προβλήματα, δερματικές παθήσεις, περιβαλλοντική ευαισθησία, φλεγμονώδης ασθένεια του εντέρου, χρόνιο σύνδρομο κόπωσης καθώς και AIDS ή παρεμφερείς ασθένειες (Poljsak, B., et al., 2011). Εικόνα 9: Ασθένειες προκαλούμενες από οξειδωτικό στρες Οξειδωτικό στρες και διαταραχή της υγείας των ζώων Αρκετές μελέτες έχουν δείξει ότι στα κτηνοτροφικά ζώα το οξειδωτικό στρες εμπλέκεται σε μία σειρά από παθολογικές καταστάσεις (σήψη, μαστίτιδα, εντερίτιδα, πνευμονία, παθήσεις των αρθρώσεων, φλεγμονή της αναπνευστικής οδού) στις οποίες συμπεριλαμβάνονται και καταστάσεις που σχετίζονται άμεσα με τη ζωική παραγωγή και την ευζωία (Lykkesfeldt and Svendsen 2007). Για παράδειγμα, κοινές ασθένειες όπως, πνευμονία (Lauritzen et al., 2003), εντερίτιδα (Miller et al., 1993), πυρετός (Kataria 2012b), σήψη στους χοίρους (Basu and Eriksson 2001) και υποτροπιάζουσα απόφραξη και φλεγμονή της αναπνευστικής οδού στα άλογα (Deaton et al., 2004a, 2005), προκαλούνται από διαταραχές της αντιοξειδωτικής ομοιόστασης των ζώων. Επιπλέον, έχει βρεθεί ότι μαστίτιδα (Weiss et al., 2004), πανώλη (Peste des petits ruminants) (PPR) (Kataria A. K 2012α), πνευμονία (Wessely-Szponder et al., 2004) και μολύνσεις από παράσιτα (Celi 2010) προκαλούνται στα μηρυκαστικά λόγω οξειδωτικού στρες, ενώ πολλές έρευνες έδειξαν ότι η χορήγηση αντιοξειδωτικών μπορεί να προστατεύσει τα ζώα από τέτοιες ασθένειες ή να μειώσει τα κλινικά συμπτώματά τους (Chaiyotwittayakan et al., 2004; Bouchard et al., 1999; Hogan et al., 1992; Deaton et al., 2004b). Έτσι, θεωρείται ότι η χορήγηση αντιοξειδωτικών μπορεί να αποτελέσει μια εναλλακτική και χαμηλού κόστους παρέμβαση για την αντιμετώπιση παθολογικών καταστάσεων των κτηνοτροφικών ζώων στις οποίες εμπλέκεται το οξειδωτικό στρες (Lykkesfeldt and Svendsen 2007). Επίσης, πρόσφατες μελέτες (Jain and Flora 2012; Chan et al., 2013; Campbell et al., 2013; van der Meulen 2010) έδειξαν ότι τα πολύ νεαρά ζώα λόγω παραγόντων στρες (στρες απογαλακτισμού) έχουν μειωμένους αντιοξειδωτικούς μηχανισμούς σε σύγκριση με τα ενήλικα άτομα και έτσι στα νεαρά άτομα είναι ακόμα πιο απαραίτητη η χορήγηση αντιοξειδωτικών για προστασία από ασθένειες. 1.2 Βιοδραστικές φυτοχημικές ενώσεις Ο όρος βιοδραστικές φυτοχημικές ενώσεις αναφέρεται σε ουσίες φυτικής προέλευσης που βρίσκονται στα τρόφιμα και έχουν ιδιότητες που τους προσδίδουν την ικανότητα να δρουν προστατευτικά σε χρόνιες παθήσεις (Bidlack et.al., 2000; Meskin et.al., 2002). Επιδημιολογικές μελέτες έχουν συσχετίσει Σελίδα 28
29 την κατανάλωση φρούτων και λαχανικών με ευεργετικές επιδράσεις σε χρόνιες παθήσεις, οι οποίες έχουν αποδοθεί στις περιεχόμενες φυτοχημικές ενώσεις (Kris- Etherton et. al., 2002) (Valko et.al., 2007). Οι πολυφαινολικές ενώσεις αποτελούν τις κυριότερες βιοδραστικές/ φυτοχημικές ενώσεις των τροφίμων και είναι εκείνες οι οποίες έχουν μελετηθεί εκτενέστερα για τις βιολογικές τους ιδιότητες (Bidlack και συν., 2000) Βιολογικές ιδιότητες των σταφυλιών Η άμπελος είναι ένα από τα φυτά του οποίου ο καρπός (τα σταφύλια) και το κύριο προϊόν του (το κρασί) παρουσιάζουν σημαντικές βιολογικές ιδιότητες. Η άμπελος ανήκει στην οικογένεια Vitaceae, με σημαντικότερο είδος το Vitis vinifera από το οποίο προέρχεται και το 90% της παγκόσμιας παραγωγής σταφυλιών (Soleas et.al., 1997). Το Vitis vinifera πιστεύεται ότι είναι ένα από τα πρώτα φυτά που άρχισε να καλλιεργεί ο άνθρωπος και υπάρχουν ιστορικές αποδείξεις που δείχνουν ότι η συστηματική καλλιέργειά του ξεκίνησε πριν από περίπου χρόνια (Soleas et.al., 1997). Από την αρχαιότητα ακόμα τα σταφύλια και το κρασί είχαν χρησιμοποιηθεί σε κοινωνικο-θρησκευτικές εκδηλώσεις καθώς και για θεραπευτικούς σκοπούς. Τα τελευταία χρόνια έχει δοθεί ιδιαίτερη σημασία στις βιολογικές ιδιότητες των σταφυλιών και του κρασιού κυρίως ύστερα από μία έρευνα (Renaud και de Lorgeril 1992) που πρότεινε ως εξήγηση στο λεγόμενο γαλλικό παράδοξο την κατανάλωση κρασιού. Γαλλικό παράδοξο έχει ονομαστεί η παρατήρηση ότι στη Γαλλία υπάρχουν μικρότερα ποσοστά καρδιακών παθήσεων σε σύγκριση με άλλες ανεπτυγμένες χώρες, αν και η κατανάλωση τροφών πλούσιων σε λιπαρά, το κάπνισμα, η έλλειψη σωματικής άσκησης καθώς και οι τιμές άλλων δεικτών υψηλού κινδύνου για καρδιοπάθειες δεν διαφέρουν σημαντικά ανάμεσα στη Γαλλία και στις άλλες χώρες. Η προστασία των σταφυλιών και του κρασιού έναντι των καρδιακών παθήσεων πιστεύεται ότι οφείλεται στην αντιαθηρωματική δράση τους βελτιώνοντας τη λειτουργία του ενδοθηλίου (Chou et.al., 2001), αυξάνοντας την αντιοξειδωτική ικανότητα του ορού και προστατεύοντας έτσι από οξείδωση τη λιποπρωτεΐνη χαμηλής πυκνότητας (LDL) (Day et.al., 1997), και ελαττώνοντας τη συσσωμάτωση των αιμοπεταλίων (Keevil et.al., 2000). Επιπλέον, επιδημιολογικές μελέτες έχουν δείξει ότι η μέτρια κατανάλωση κρασιού ίσως συνδέεται με προστασία από κάποιες μορφές καρκίνου (Boffetta και Garfinkel 1990; Renaud et.al., 1998)όπως ο καρκίνος του μαστού, του πνεύμονα και του στομάχου. Οι πολυφαινόλες οι οποίες απαντώνται σε αφθονία στα εκχυλίσματα ελληνικών ποικιλιών σταφυλιού, ήταν ισχυροί αναστολείς της τοποϊσομεράσης Ι, (που δείχνει ότι η αναστολή αυτού του ενζύμου μπορεί να αποτελεί ένα μηχανισμό για την αντικαρκινική δράση των ενώσεων αυτών). Επιπλέον, τα εκχυλίσματα σταφυλιού ανέστειλαν τη μιτομυκίνη C (αναστέλλει τη διαίρεση του DNA με το σχηματισμό συμπλόκου με αυτό, ασκώντας έτσι αντικαρκινική δράση), γεγονός που υποδηλώνει ότι θα μπορούσαν να εμποδίζουν βλάβες από τις ROS στο DNA. Οι φυτικές πολυφαινόλες ενισχύουν τη μιτομυκίνη C που δρα ως προοξειδωτικό (Στάγκος Δημήτρης 2005). Άλλοι μηχανισμοί που έχουν προταθεί για την αντικαρκινική δράση των σταφυλιών και του κρασιού είναι η διακοπή της κυτταρικής αύξησης μέσω τροποποίησης βιοχημικών μονοπατιών μεταγωγής σήματος που ρυθμίζουν τον κυτταρικό κύκλο καθώς και της δράσης διαφόρων κινασών, η επαγωγή της κυτταρικής διαφοροποίησης (Agarwal et.al., 2000β; Bagchi et.al., 2002), η αναστολή των κυκλοοξυγενασών (COX-1 και COX-2) (Waffo-Teguo et.al., 2001) και η αναστολή της αγγειογένεσης (Singh et,al., 2004). Το επίκεντρο του ενδιαφέροντος μετατοπίστηκε στη διερεύνηση της πιθανής χημειοπροστατευτικής δράσης των εκχυλισμάτων από σταφύλια, λόγω του υψηλού αντιοξειδωτικού περιεχομένου τους. Σε παλαιότερα πειράματα,σε μια σειρά από in vitro και in vivo μελέτες σε διάφορες ελληνικές ποικιλίες σταφυλιών διερευνήθηκε η δραστικότητα των ενζύμων που εμπλέκονται στη ρύθμιση του οξειδωτικού στρες, δηλαδή της οξειδάση της ξανθίνης (ΧΟ), της καταλάσης (CAT) και της δισμουτάσης του υπεροξειδίου (SOD).Τα αποτέλεσμα έδειξαν την ύπαρξη αντιοξειδωτικής δράση της Σελίδα 29
30 SOD ενώ η ΧΟ και η CAT φαίνεται ότι λειτουργούν ως προ-οξειδωτικά. Τα εκχυλίσματα φάνηκε να ασκούν προ-οξειδωτική δράση η οποία πιθανώς να εξαρτάται τόσο από τη σύνθεση όσο και από τη συγκέντρωση πολυφαινολικών συστατικών που περιέχουν (Spanou 2011). Άλλες βιολογικές ιδιότητες που έχουν αποδοθεί σε εκχυλίσματα σταφυλιών αντιμικροβιακές (Weisse et.al., 1995), δράση κατά του έλκους (Saito et.al., 1998) και αντιυπερτασικές (Soares De Moura et.al., 2002) Ανατομία και χημική σύσταση σταφυλιών Το σταφύλι και πιο συγκεκριμένα ο βότρυς του σταφυλιού απαρτίζεται από το ξυλώδες μέρος, που ονομάζεται βόστρυχας ή τσαμπί και τις ράγες, που αποτελούν το εδώδιμο και οινοποιήσιμο τμήμα του σταφυλιού. Τα στέμφυλα είναι το υπόλειμμα που μένει μετά την έκθλιψη των σταφυλιών και αποτελείται από τους βοστρύχους (κοτσάνια), τα γίγαρτα (κουκούτσια) και τους φλοιούς των σταφυλιών, ενώ περικλείει και κάποιο ποσοστό γλεύκους (αζύμωτου ή εν ζυμώσει) ή κρασιού ανάλογα με το βαθμό έκθλιψης / πίεσης τους. Η επί της εκατό αναλογία των δυο αυτών μερών του σταφυλιού δεν είναι σταθερή, αλλά εξαρτάται από την ποικιλία αυτού, τις κλιματολογικές συνθήκες, το έδαφος, την ηλικία των πρεμνών, το χρόνο του τρυγητού, την προσβολή από διάφορες ασθένειες και γενικά από κάθε παράγοντα που θα επηρέαζε το μέγεθος του βότρυ. Γενικά όσο μεγαλύτερος είναι ο βότρυς, τόσο μικρότερος είναι ο βόστρυχας, σε σχέση με το σύνολο των ραγών. Εικόνα 10 : Ανατομία και σύσταση ράγας σταφυλιού. Αν και τα τελευταία χρόνια έχει γίνει σημαντική πρόοδος όσον αφορά τη χημική σύσταση των σταφυλιών και του κρασιού, ωστόσο δεν είναι πλήρως γνωστή. Περισσότερες από 500 χημικές ουσίες έχουν αναγνωριστεί από τις οποίες οι 150 περίπου είναι εστέρες. Μεταξύ αυτών των ενώσεων περιλαμβάνονται το νερό (η συγκέντρωση του οποίου παίζει σημαντικό ρόλο στον καθορισμό των φυσικοχημικών χαρακτηριστικών), σάκχαρα (με κυριότερα τη γλυκόζη και τη φρουκτόζη ενώ η σουκρόζη συναντάται σπανιότερα), οργανικά οξέα και διάφορες αρωματικές ενώσεις. Οι περισσότερες ενώσεις βρίσκονται σε συγκεντρώσεις mg/lt ενώ υπάρχουν ορισμένες σε συγκέντρωση >100mg/lt οι οποίες καθορίζουν τη γεύση και το άρωμα των σταφυλιών. Η σημαντικότερη όμως κατηγορία χημικών ενώσεων που συναντάμε στα σταφύλια και το κρασί ιδιαίτερα όσον αφορά τη βιολογική τους δράση είναι οι φυτικές πολυφαινόλες (Jackson 1993) Στέμφυλα και περιβάλλον Τα στέμφυλα που θα χρησιμοποιηθούν για την παραγωγή των ζωοτροφών παράγονται ως υποπροϊόντα κατά την διαδικασία της οινοποίησης, τα οποία είναι ρυπογόνα λόγω της υψηλής περιεκτικότητάς τους σε οργανικές ενώσεις και η ανεξέλεγκτη απόρριψη τους προκαλεί τεράστια Σελίδα 30
31 προβλήματα στο οικοσύστημα. Συγκεκριμένα το οργανικό τους φορτίο διαθέτει σημαντική αντιμικροβιακή και φυτοτοξική δραστικότητα, η οποία περιορίζει σημαντικά τη δράση των μικροοργανισμών που συμμετέχουν στη διαδικασία της βιοαποικοδόμησης με αποτέλεσμα να επιβραδύνεται η βιοαποικοδόμηση και η ανεξέλεγκτη εναπόθεση των υποπροϊόντων να έχει ως επακόλουθο την εμφάνιση φαινόμενων φυτοτοξικότητας, που: επηρεάζει την ανάπτυξη των φυτών, μολύνει τον υδροφόρο ορίζοντα, υποβαθμίζοντας την ποιότητα του πόσιμου ύδατος. θανατώνει τους ευαίσθητους οργανισμούς των ποταμών και των θαλασσών. Με δεδομένο λοιπόν τα όσα αναφέρθηκαν παραπάνω, είναι αρκετά σημαντική η επεξεργασία των υποπροϊόντων των οινοποιείων κάτι το οποίο θα οδηγήσει στην εξάλειψη προβλημάτων ρύπανσης του περιβάλλοντος, στην αξιοποίηση των προϊόντων που θα προκύψουν και την περαιτέρω χρησιμοποίησή τους, μέσω της δημιουργίας βιολειτουργικών ζωοτροφών υψηλής προστιθέμενης αξίας. 1.3 Πολυφαινόλες Ετυμολογία Το όνομα τους προέρχεται από την αρχαία ελληνική λέξη «πολύς» και από τη λέξη φαινόλη η οποία αναφέρεται στη χημική δομή που σχηματίζεται με την προσάρτηση σε έναν αρωματικό βενζοειδή δακτύλιο μιας υδροξυλικής ομάδας (-OH) παρόμοια με εκείνη που βρέθηκε στις αλκοόλες Ιστορικό Υπάρχουν πολλοί λόγοι για να ερευνήσει κάποιος τις φυτικές πολυφαινόλες. Από τους βασικούς τύπους δομών τους μέχρι και τη συνεργασία τους για την περαιτέρω χημική τους μετατροπή και τη δημιουργία ολιγό-/πολυμερών συγκροτημάτων, οι φυτικές πολυφαινόλες παρουσιάζουν ένα εντυπωσιακό ευρύ φάσμα βιο-/φυσικό-χημικών ιδιοτήτων που τις καθιστά μάλλον μοναδικό και ενδιαφέρον φυσικό προϊόν. Η πρώτη ερώτηση που έρχεται στο μυαλό είναι γιατί τα φυτά επιλέγουν να βασίζονται σε τόσο μεγάλο βαθμό στην παραγωγή μεταβολιτών με πολλαπλές φαινολικές ομάδες. Η απάντηση στο ερώτημα αυτό εξακολουθεί να αποτελεί αντικείμενο συζήτησης και πιθανότατα είναι διαφορετική ανάλογα με το είδος της πολυφαινόλης. Σε γενικές γραμμές, οι φυτικές πολυφαινόλες έχουν εμπλακεί σε διάφορους λειτουργικούς ρόλους, συμπεριλαμβανομένης και της αντίστασης των φυτών έναντι παθογόνων μικροβίων και φυτοφάγων ζώων όπως είναι τα έντομα, την προστασία έναντι της ηλιακής ακτινοβολίας (έναντι της UV ακτινοβολίας που καταστρέφει το DNA), καθώς και την αναπαραγωγή, τη διατροφή και την ανάπτυξη, ιδίως μέσω αλληλεπιδράσεων με άλλους οργανισμούς πάνω και κάτω από το έδαφος (έντομα, μύκητες και συμβιωτικά βακτήρια) κατά τη διάρκεια της μακροπρόθεσμης εξέλιξης. Λόγω της υποχρεωτικής γρήγορης εποχικής προσαρμογής, τα φυτά έχουν μάθει να αντιμετωπίζουν τις μεταβαλλόμενες συνθήκες του περιβάλλοντος και τις πιέσεις επικαλούμενα το μεγάλο χημικό τους «οπλοστάσιο» μέσω του εξαιρετικά δυναμικού δευτερογενή μεταβολισμού τους. Φυσικά ανάμεσα στις κύριες ομάδες των δευτερογενών μεταβολιτών, άλλοι, όπως τα αλκαλοειδή και τα τερπενοειδή έχουν αποδείξει τη δυνατότητα τους στην προστασία των φυτών κατά τη διάρκεια της εξέλιξης τους, συμβάλλοντας στη διατήρηση της οικολογικής ισορροπίας μεταξύ των φυτών και άλλων ζωντανών οργανισμών, πολλοί εκ των οποίων τρέφονται από αυτούς, συμπεριλαμβανομένων και των ανθρώπων. Ωστόσο, οι φυτικές φαινόλες είναι ιδιαίτερα σημαντικές λόγω των λειτουργιών που προσφέρουν στα φυτά, οι οποίες είναι αποτέλεσμα των εγγενών φυσικοχημικών τους ιδιοτήτων. Αναμφισβήτητα το πιο πολυσυζητημένο χαρακτηριστικό των πολυφαινολών και γενικότερα των φαινολικών φυτών, είναι η αναγνωρισμένη ικανότητα τους να δεσμεύουν τις δραστικές ρίζες οξυγόνου Σελίδα 31
32 (ROS), όπως τις O 2 -., HO., NO., H 2 O 2,όπως επίσης και οξειδωτικές ελεύθερες ρίζες RO και ROO. Οι φυτικές πολυφαινολικές ενώσεις μπορούν να δρουν ως αντιοξειδωτικά με χηλίωση μεταλλικών ιόντων, όπως σιδήρου, χαλκού και σιδήρου και τα ιόντα που εμπλέκονται στην μετατροπή του Ο2-. και H 2 O 2 στο εξαιρετικά επιθετικό ΗΟ μέσω αντιδράσεων Haber-Weiss/Fenton. Μπορούν επίσης να εμποδίσουν τη δράση ορισμένων ενζύμων υπεύθυνων για την παραγωγή του Ο 2 όπως και την οξειδάση της ξανθίνης και της πρωτεϊνικής κινάσης (Prof. Stéphane Quideau et.al., 2011) Ορισμός Οι πολυφαινόλες είναι χημικές ενώσεις που απαντώνται στην φύση και βρίσκονται σε μεγάλες ποσότητες στα φρούτα, στα λαχανικά, στα δημητριακά και στα ποτά. Τα φρούτα όπως τα σταφύλια, τα μήλα, τα αχλάδια, τα κεράσια και τα μούρα περιέχουν μέχρι mg πολυφαινολών ανά 100 γραμμάρια νωπού βάρους. Τα προϊόντα που κατασκευάζονται από αυτά τα φρούτα, περιέχουν επίσης πολυφαινόλες σε σημαντικές ποσότητες. Στα τρόφιμα, οι πολυφαινόλες μπορούν να συμβάλλουν στην πικρή γεύση, στη στυφότητα, στο χρώμα, στη γεύση, στην οσμή και στην οξειδωτική σταθερότητα. Δεδομένου ότι οι φαινολικές ενώσεις στη διατροφή παρουσιάζουν ισχυρές ιδιότητες απομάκρυνσης των ελεύθερων ριζών ο κύριος ρόλος τους πιστεύεται ότι είναι η ικανότητα τους ως αντιοξειδωτικά που εμπλέκονται στην προστασία και την υπεροξείδωση των λιπιδίων. Ωστόσο την τελευταία δεκαετία, ο τρόπος δράσης αυτών των ενώσεων έχει αποδειχθεί ότι είναι πιο περίπλοκος από ότι αρχικά αναμενόταν. Στην πραγματικότητα οι πολυφαινόλες μπορούν να ασκούν και πολλές άλλες βιολογικές επιδράσεις. Μπορούν να αναστείλουν τον πολλαπλασιασμό των κυττάρων του καρκίνου και την πρόσληψη της χοληστερόλης, ρυθμίζουν διαφορετικά ένζυμα συμπεριλαμβανομένης της τελομεράσης, της κυκλοξυγενάσης και της λιποξυγενάσης, και να αλληλεπιδρούν με διάφορες οδούς της μεταγωγής σήματος. Επίσης οι πολυφαινόλες μπορούν να επηρεάσουν κασπασο-εξαρτώμενα μονοπάτια της ρύθμισης του κυτταρικού κύκλου και της ρύθμισης των αιμοπεταλίων και επίσης είναι σε θέση να αποτρέψουν ενδοθηλιακές δυσλειτουργίες (Massimo D Archivio et.al., 2010) Δομή και Tάξεις των Πολυφαινολών Περισσότερες από πολυφαινολικές ενώσεις έχουν εντοπιστεί σε διάφορα φυτικά είδη. Όλες οι φυτικές φαινολικές ενώσεις προκύπτουν από ένα κοινό ενδιάμεσο, την φαινυλαλανίνη, ή μια πρόδρoμη ένωση, το σικιμικό οξύ. Κυρίως απαντώνται σε συζευγμένες μορφές, με ένα ή περισσότερα υπολείμματα σακχάρων που συνδέονται με υδροξυλομάδες, αν και υπάρχουν επίσης άμεσες συζεύξεις του σακχάρου (πολυσακχαρίτη ή μονοσακχαρίτη) με έναν αρωματικό άνθρακα. Συσχέτιση με άλλες ενώσεις, όπως καρβοξυλικά και οργανικά οξέα, αμίνες, λιπίδια και σύνδεση με άλλες φαινόλες είναι επίσης κοινή. Οι πολυφαινόλες μπορούν να ταξινομηθούν σε διαφορετικές ομάδες σύμφωνα με τον αριθμό των δακτυλίων φαινόλης που περιέχουν και βάσει των δομικών στοιχείων τα οποία συνδέουν τους δακτυλίους μεταξύ τους. Οι κύριες κατηγορίες πολυφαινολών περιλαμβάνουν φαινολικά οξέα, φλαβονοειδή, στιλβένια και λιγνάνες. Οι πολυφαινόλες χωρίζονται στις εξής κατηγορίες ανάλογα με την χημική τους δομή: Φλαβονοειδή Τα φλαβονοειδή είναι μια μεγάλη κατηγορία οργανικών ενώσεων που μπορεί να υπάρχουν είτε ως μονομερή είτε πολυμερίζονται αντιδρώντας με άλλα φλαβονοειδή, με σάκχαρα, με μη φλαβονοειδή ή με συνδυασμούς αυτών των ενώσεων. Τα φλαβονοειδή είναι η καλύτερα μελετημένη κατηγορία Σελίδα 32
33 πολυφαινολών, περιλαμβάνει περισσότερες από 5000 ενώσεις και χωρίζεται σε 13 υποκατηγορίες. Χαρακτηριστικό των φλαβονοειδών είναι οι δύο αρωματικοί δακτύλιοι που συνδέονται μέσω ενός πυρανικού δακτυλίου που περιέχει οξυγόνο. Τα φλαβονοειδή διακρίνονται κυρίως σε 6 κατηγορίες: τις φλαβονόλες (π.χ. κερκετίνη, ρουτίνη, καμπφερόλη και μυρικετίνη), τις φλαβόνες (π.χ. απιγενίνη και λουτεολίνη), τις ισοφλαβόνες (π.χ. γενιστεΐνη και δαϊντζεΐνη), τις φλαβανόνες (π.χ. ναριγενίνη και εσπεριτίνη), τις ανθοκυανιδίνες (π.χ. κυανιδίνη, δελφινιδίνη και μαλβιδίνη) και τις φλαβανόλες (π.χ. κατεχίνη, επικατεχίνη και γαλλοκατεχίνη). Τα φλαβονοειδή περιέχονται σε σχεδόν όλα τα τρόφιμα και ποτά φυτικής προέλευσης. Ο ρόλος των ενώσεων αυτών, έχει χαρακτήρα προστατευτικό ενάντια των βλαβών που προκαλούνται στα κύτταρα από τη δράση των ελευθέρων ριζών. Τα φλαβονοειδή φαίνεται να συμβάλλουν στη χαμηλή συχνότητα εμφάνισης στεφανιαίας νόσου, γεγονός που προέκυψε με αφορμή το γαλλικό παράδοξο (υψηλή κατανάλωση κόκκινου κρασιού, κάπνισμα, μειωμένη φυσική δραστηριότητα, υψηλή κατανάλωση λιπαρών και παραδόξως ο πληθυσμός είχε μικρά ποσοστά εμφάνισης καρδιαγγειακών). Επίσης, τα φλαβονοειδή μπορεί να αντιδρούν με σάκχαρα όπως η D-γλυκόζη, η L-ραμνόζη, η γαλακτόζη, η αραβινόζη και η λιγνίνη και να σχηματίζουν γλυκοσυλιωμένες μορφές (Lea et al., 1979; Soleas et al., 1997; Ferguson 2001; Cooke and Samman 1996). Εν τούτοις, τα φλαβονοειδή δεν είναι αμιγώς αντιοξειδωτικές ενώσεις αλλά παρουσιάζουν και προοξειδωτική δράση. Αυτό το φαινόμενο εξηγείται με βάση την in vivo τοξικότητα ορισμένων φλαβονοειδών. Ακόμα και σε αυτή τη περίπτωση, η δράση τους μπορεί να είναι ωφέλιμη, δεδομένου ότι μια ήπιου βαθμού αύξηση του οξειδωτικού στρες θα ενεργοποιήσει ταυτόχρονα και την αύξηση της αντιοξειδωτικής άμυνας του οργανισμού (D. Procházková a 2011). Φλαβανόλες Χαρακτηριστικό παράδειγμα φλαβανολών είναι οι κατεχίνες (μονομερή) και οι προκυανιδίνες (πολυμερή), βρίσκονται σε πολλά φρούτα (π.χ. βερύκοκα και σταφύλια) και στο κρασί αλλά οι σημαντικότερες πηγές είναι το πράσινο τσάι και η σοκολάτα. Μάλιστα, κατά τη ζύμωση του πράσινου τσαγιού παράγονται πολύπλοκες πολυφαινόλες όπως είναι οι ταννίνες. Κύρια πηγή των φλαβανολών αποτελούν τα εσπεριδοειδή που περιέχουν την εσπεριδίνη. Στην ίδια κατηγορία πολυφαινολών συναντούμε τη ναρινγενίνη και τη ταξιφολίνη. Φλαβόνες Οι φλαβόνες απαντώνται στο σέλινο (λουτεολίνη) καθώς επίσης και στο κόκκινο γλυκό πιπέρι (απιγενίνη). Ακόμα, στο μαϊντανό, στα δημητριακά (κυρίως σε γλυκοσυλιωμένη μορφή) και στα εσπεριδοειδή (κυρίως σε πολυμεθοξυλιωμένες μορφές) (Shahidi and Naczk 1995). Φλαβονόλες Η κυριότερη φλαβονόλη είναι η κερκιτίνη, κατατάσσονται επίσης, η καμφερόλη, μυρικετίνη, και η φισετίνη. Οι φλαβονόλες βρίσκονται στις περισσότερες φυτικές τροφές που καταναλώνονται από τον άνθρωπο και οι σημαντικότερες πηγές τους είναι τα κρεμμύδια, τα πράσσα, τα μπρόκολα, τα βατόμουρα, το κρασί και το τσάι (Manach et al., 2004). Φλαβανόνες Σελίδα 33
34 Οι φλαβανόνες βρίσκονται στις τομάτες, σε αρωματικά φυτά όπως η μέντα και σε μεγάλες συγκεντρώσεις στα εσπεριδοειδή (Tomas-Barberan and Clifford 2000). Ισοφλαβόνες Οι ισοφλαβόνες βρίσκονται στη σόγια και αντιπροσωπεύονται από τη γενιστεϊνη και τη δαϊντζεΐνη. Η δομή τους είναι παρόμοια με εκείνη των οιστρογόνων. Oι ισοφλαβόνες υποστηρίζεται ότι ασκούν μια καρδιοπροστατευτική δράση. Επίσης συμβάλλουν και στη βελτίωση λειτουργίας του ενδοθηλίου. Όμως αυτή η θεωρία απορρέει από περιορισμένες μελέτες. Η πιθανή ευεργετική επίδραση των ισοφλαβονών στον ανθρώπινο οργανισμό δεν έχει αποσαφηνιστεί πλήρως και απαιτεί περαιτέρω έρευνα. Εκτός αυτού, έχει την ικανότητα να μειώνει την ενδοθηλιακή σύνθεση και δράση του μονοξειδίου του αζώτου (ΝΟ ) (Wendy L. Halli 2005). Ανθοκυανιδίνες Στις ανθοκυανιδίνες οφείλεται το κόκκινο και το μπλε χρώμα πολλών φρούτων και λαχανικών (κόκκινο λάχανο, μελιτζάνες, κόκκινα κρεμμύδια, φράουλες) (Clifford 2000).Οι προ-ανθοκυανιδίνες φαίνεται να μειώνουν στον ορό του αίματος, τα επίπεδα της γλυκόζης, της γλυκοζυλιωμένης πρωτεΐνης καθώς και της ουρίας. Επίσης, συμβάλλουν στην καταστολή της παραγωγής των δραστικών μορφών οξυγόνου ενώ παράλληλα αυξάνουν το λόγο GSH/GSSG. Επιπλέον, επιδρούν στην υπερλιπιδαιμία, μειώνοντας σημαντικά τα επίπεδα των τριγλυκεριδίων, της ολικής χοληστερόλης και των μη απαραίτητων λιπαρών οξέων. Οι προανθοκυανιδίνες (και συγκεκριμένα τα ολιγομερή αυτών) ασκούν προστατευτική δράση έναντι της υπεργλυκαιμίας και της υπερλιπιδαιμίας που παρουσιάζουν οι διαβητικοί ασθενείς (και του διαβήτη τύπου Ι και τύπουιι) και λειτουργούν ως ρυθμιστές σε φλεγμονώδεις καταστάσεις που προκαλούνται από το οξειδωτικό στρες (Τakako Yokozama 2012). Φαινολικά Οξέα Η δεύτερη μεγαλύτερη κατηγορία πολυφαινολών μετά τα φλαβονοειδή αποτελούν τα πολυφαινολικά οξέα, τα οποία είναι παράγωγα του υδροξυβενζοϊκού και του υδροξυκινναμικού οξέος. Τα υδροξυβενζοϊκά οξέα (π.χ. γαλλικό οξύ, πρωτοκατεχοϊκό οξύ) βρίσκονται σε μικρές συγκεντρώσεις στα μέρη των φυτών που μπορούν να καταναλωθούν από τον άνθρωπο με εξαίρεση ορισμένων φυτών (π.χ. τσάι), ενώ αποτελούν συνήθως υπομονάδες πολυμερών όπως οι υδρολυόμενες ταννίνες (Clifford και Scalbert 2000). Τα υδροξυκινναμικά οξέα βρίσκονται περισσότερο συχνά στα φυτά από τα υδροξυβενζοϊκά, και τα κυριότερα μέλη τους είναι το καφεϊκό οξύ, το κουμαρικό οξύ, το φερουλικό οξύ και τα σιναπικά οξέα. Συνήθως τα υδροξυκινναμικά οξέα γλυκοσυλιώνονται ή σχηματίζουν εστέρες με το κουινικό οξύ, το σικιμικό οξύ και το ταρταρικό οξύ. Το καφεϊκό οξύ και το κουινικό οξύ σχηματίζουν το χλωρογενικό οξύ που συναντάται σε πολλά φρούτα καθώς και στον καφέ (Clifford 1999). Το καφεϊκό οξύ, γενικά, είναι το πιο κοινό πολυφαινολικό οξύ και αντιπροσωπεύει το % των συνολικών υδροξυκινναμικών οξέων που υπάρχουν στα περισσότερα φυτά. Το φερουλικό οξύ είναι το πιο άφθονο πολυφαινολικό οξύ των δημητριακών σπόρων, που αποτελούν και την κύρια πηγή πρόσληψής του από τον άνθρωπο (Lempereur et al., 1997). Σελίδα 34
35 Στιλβένια Στην κατηγορία των στιλβενίων αντιπροσωπευτική χημική ένωση είναι η ρεσβερατρόλη. Είναι λιγότερο διαδεδομένη στη διατροφή σε σχέση με άλλες πολυφαινόλες. Βρίσκεται γενικά στο κρασί και ειδικά δε στο κόκκινο. Έρευνες έχουν δείξει την αντιοξειδωτική της δράση, κυρίως όσον αφορά τα καρδιαγγειακά νοσήματα (Παπαγεωργίου 2005). Τα στιλβένια (π.χ. ρεσβερατρόλη, αστρινγίνη, πικεΐδη) αποτελούν ένα μικρό ποσοστό των πολυφαινολών που προσλαμβάνονται μέσω της δίαιτας. Το σημαντικότερο μέλος τους είναι η ρεσβερατρόλη που αποτελείται από δύο αρωματικούς δακτυλίους ενωμένους με μία γέφυρα μεθυλενίου και βρίσκεται κυρίως στα σταφύλια και το κρασί (Βertelli et al., 1998). Είναι μια από τις καλύτερα μελετημένες πολυφαινόλες γιατί έχει παρουσιάσει σημαντική αντικαρκινική δράση. Η ρεσβερατρόλη στα σταφύλια βρίσκεται είτε ως μονομερές είτε πολυμερίζεται σχηματίζοντας τις βινιφερίνες (Soleas et al., 1997). Λιγνάνες Οι λιγνάνες σχηματίζονται από δύο φαινυλπροπανικές ομάδες, το λινέλαιο και το λιναρόσπορο. H κυριότερη πηγή τους είναι ο λιναρόσπορος, ενώ δημητριακά, φρούτα και λαχανικά περιέχουν μικρές ποσότητες λιγνανών (Adlercreutz and Mazur 1997). Η διαφορετικότητα τους έγκειται στο υδροξυλικό τους πρότυπο και μπορεί να είναι γλυκοσυλιωμένες ή/και ακετυλιωμένες. Το μέγεθος τους ποικίλει από μικρά μόρια (όπως η φαινόλη), έως πολυμερή (όπως οι ταννίνες) μεγάλου μοριακού βάρους (Perez- Jimenez et al., 2010) Εικόνα 11: Χημικές Δομές Διαφορετικών Πολυφαινολικών Τάξεων Φυσικές Ιδιότητες. Οι πολυφαινόλες είναι συνήθως μόρια μικρού μοριακού βάρους και βρίσκονται σε υγρή μορφή ή σε στερεή με χαμηλό σημείο τήξεως. Λόγω των δεσμών υδρογόνου, οι φαινόλες μικρού μοριακού βάρους, είναι υδατοδιαλυτές. Τείνουν να έχουν υψηλότερα σημεία βρασμού από τις αλκοόλες ιδίου μοριακού βάρους, λόγω του ισχυρότερου δεσμού υδρογόνου που έχουν Χημειοπροστατευτική Δράση Πολυφαινολών. Από την αρχαιότητα ακόμη, σε πολιτισμούς όπως ο Ελληνικός, ο Αιγυπτιακός, ο Ρωμαϊκός, ο Κινέζικος και ο Ινδικός, ήταν γνωστές οι δράσεις κάποιων φυτών για την αντιμετώπιση διαφόρων Σελίδα 35
36 ασθενειών (Klein et. al., 2011; Chang et. al.; 2012, Wells et. al., 2008). Εκατοντάδες χρόνια μετά, πληθώρα ερευνών αποδεικνύει μέρα με τη μέρα πως βιοδραστικά συστατικά των τροφών μπορούν να επηρεάσουν όλες τις καρκινικές διαδικασίες σε όλα τα στάδια του καρκίνου (Kushi et. al., 2011; Lee et al., 2005; Kloetzel et al. 2013; Bidinotto et al., 2012; Chang et al., 2012; Arcidiacono et al., 2012; Pauwels, 2010; La Vecchia, 2004; La Vecchia, 2009). Η χημειοπροστασία ως όρος χρησιμοποιήθηκε πριν 35 χρόνια από τον Lee Wattenberg και είναι η χρήση φυσικών ή συνθετικών ουσιών για την πρόληψη ασθενειών και μολύνσεων (Kushi et al., 2011; Kiani et al., 2005; Lee et al., 2005; Klein et al., 2011; Baliga et al., 2011; Brownell and Warner, 2009; Wang et al., 2012). Η χημειοπροστατευτική δράση των φυτικών τροφών οφείλεται στα φυτοχημικά τους συστατικά, τα οποία είναι μη θρεπτικά συστατικά που έχουν σημαντική βιολογική δράση, όπως η ρύθμιση της κυτταρικής σηματοδότησης, η ενίσχυση του ανοσοποιητικού, η γονιδιακή ρύθμιση, η κυτταρική διαφοροποίηση, ο κυτταρικός πολλαπλασιασμός και η απόπτωση (Karpi et al., 2012) και δρουν ως αντιοξειδωτικά, ενώ θεωρούνται φυτοοιστρογόνα, γιατί έχουν παρόμοια δράση με τις ορμόνες. Παίζουν ρόλο στον καθορισμό της γεύσης, του αρώματος, των χρωμάτων και άλλων χαρακτηριστικών των φυτικών τροφών. Τα τελευταία χρόνια, όλο και περισσότερες μελέτες αποδεικνύουν πως μόνο ένα συστατικό της τροφής δε φτάνει για να μειώσει τον κίνδυνο εμφάνισης καρκίνου, αλλά είναι ο συνδυασμός των συστατικών που βρίσκονται σε όλη την υγιεινή διατροφή που εμφανίζουν αυτή την ικανότητα (Banerjee et al., 2006, Baliga et al., 2011; Alexander and Cushing, 2009; Kumar et al., 2012; Cristensen et al., 2012; Kontou et al., 2012; Giacosa et al., 2012). Επίσης, οι πολυφαινόλες παίζουν σημαντικό ρόλο και στα φυτά καθώς μπορεί να έχουν αρκετές επιπτώσεις στους φυτικούς ιστούς όπως είναι η καταστολή αυξητικών ορμονών, η προστασία από την UV ακτινοβολία, η προσθήκη χρώματος, η πρόληψη μικροβιακών μολύνσεων και η συμμετοχή σε διαδικασίες ανάπτυξης (Huber., Β., et al., 2003), είναι υπεύθυνες επίσης για το φωτεινό χρώμα των φρούτων και των λαχανικών (Manach C. et al. 2004), συμβάλλοντας έτσι στη γονιμοποίηση των φυτών προσελκύοντας τα έντομα επικονιαστές και στη διασπορά των σπερμάτων μετά την κατανάλωση των καρπών από τα ζώα. Επιπλέον, λειτουργούν ως αναστολείς ενζύμων, ως χηλικές ενώσεις δεσμεύοντας μέταλλα που είναι τοξικά για τα φυτά και ως ρυθμιστές της έκφρασης γονιδίων ενώ εμπλέκονται στις διαδικασίες της μορφογένεσης, του καθορισμού του φύλου και της φωτοσύνθεσης (Manach et.al., 2004; Di Carlo et.al., 1999; Harborne 1986).. Επιπλέον, σε ορισμένα είδη φυτών οι πολυφαινόλες μπορούν να παρέχουν προφύλαξη έναντι της σήψης (John Hart., H., et al., 1974) Επιδράσεις πολυφαινολών στην υγεία. Στην περίπτωση των καρδιαγγειακών διαταραχών, το οξειδωτικό στρες και οι ΔΜΟ εμπλέκονται σε ενδοθηλιακές βλάβες, σε δημιουργία αρτηριοσκλήρυνσης και σε παρατεταμένη ζημιά η οποία μπορεί να οδηγήσει σε έμφραγμα του μυοκαρδίου, καθώς και σε ισχαιμική επανέγχυση. Πολυάριθμες μελέτες έχουν δείξει τη σημασία των φυσικών διατροφικών πολυφαινολών στη βελτίωση της καρδιαγγειακής υγείας και έχει τονιστεί ο σημαντικός ρόλος που παίζουν αυτές οι ουσίες στον περιορισμό των επιπτώσεων της κυτταρικής γήρανσης. Πολυφαινόλες όπως η ρεσβερατρόλη, επιγαλλοκατεχίνη (EGCG) και η κουρκουμίνη έχουν αναγνωριστεί και έχουν ευεργετικά αποτελέσματα στην καρδιαγγειακή υγεία, ενώ ορισμένες έχουν επίσης δειχθεί ότι είναι προστατευτικές ενάντια στη γήρανση (Sandhya, K., et al., 2013). H προστατευτική δράση των πολυφαινολών αποδίδεται στην αντιοξειδωτική τους δράση ως δεσμευτές ελευθέρων ριζών ή ως αναστολείς των αλυσιδωτών οξειδωτικών αντιδράσεων. Οι φαινολικές Σελίδα 36
37 τους ομάδες δρουν σαν ισχυροί δέκτες ηλεκτρονίων, σχηματίζοντας σταθερές φαινοξυλικές ρίζες. Αυτό έχει ως αποτέλεσμα οι ελεύθερες ρίζες που έρχονται σε επαφή μαζί τους να δίνουν το ηλεκτρόνιο τους και να αδρανοποιούνται. Η φαινολική ρίζα που παράγεται είναι σταθερή και έχει την ικανότητα να μετατοπίζει το ηλεκτρόνιο έτσι ώστε να μην είναι δραστικό. Με τον τρόπο αυτό αποφεύγονται οι αλυσιδωτές αντιδράσεις, γεγονός το οποίο προσαυξάνει την αντιοξειδωτική δράση των πολυφαινολών. Η ρίζα αυτή μπορεί επιπλέον να αδρανοποιήσει και την αρχική ρίζα η οποία οδήγησε στην παραγωγή της οδηγώντας στη δημιουργία ενός μη δραστικού μορίου (Ferguson et al., 2001). 1.4 Γενικές πληροφορίες για τα πρόβατα Το οικόσιτο πρόβατο (Ovis aries - Πρόβατον ο κριός), το πιο κοινό μέλος της οικογένειας των προβάτων (Πρόβατον - Ovis), είναι ένα μηρυκαστικό, τετράποδο ζώο, που πιθανότατα κατάγεται από τα άγρια πρόβατα mouflon της Νότιας και Νοτιοδυτικής Ασίας. Για την εξημέρωση των προβάτων υπάρχουν τεκμήρια στο Ιράκ που χρονολογούνται από το π.χ. Τα πρόβατα συνδέθηκαν με πολλούς πολιτισμούς, κυρίως στη Βρετανία και τη Μεσόγειο, όπου αποτελούν το πιο κοινό αντικείμενο της κτηνοτροφίας. Έχουν μεγάλη οικονομική σημασία, καθώς η απόδοση εισοδήματος που προσφέρουν σε σχέση με το κόστος της εκτροφής τους είναι γύρω στο 40%. Ο παγκόσμιος πληθυσμός των προβάτων υπολογίζεται γύρω στο ένα δισεκατομμύριο. Συστηματική ταξινόμηση Βασίλειο Ζώα (Animalia) Συνομοταξία Χορδωτά (Chordata) Ομοταξία Θηλαστικά (Mammalia) Τάξη Αρτιοδάκτυλα (Artiodactyla) Οικογένεια Βοοειδή (Bovidae) Υποοικογένεια Αιγώδη (Caprinae) Γένος Πρόβατον (Ovis) Είδος O. aries Πίνακας 1: : Συστηματική ταξινόμηση προβάτων Χαρακτηριστικά Ανάλογα με την ηλικία και το φύλο τους, ονομάζονται αρνιά μέχρι δυο μηνών, ζυγούρια μέχρι ενός έτους, κριάρια τα ώριμα αρσενικά και προβατίνες τα θηλυκά. Έχουν μέτριο σώμα που καλύπτεται από πυκνό τρίχωμα, απαλό στην αφή, σγουρό ή ίσιο, μακρύ ή κοντό, λευκό, μαύρο, καστανό ή γκρίζο. Ζουν 10 έως 14 χρόνια, ανάλογα με τις συνθήκες διαβίωσής τους. Τρέφονται με νωπά χόρτα, τα οποία καταπίνουν σχεδόν αμάσητα, ώστε να εξασφαλιστούν κατά τη διάρκεια της ημερήσιας βοσκής οι μεγάλες ποσότητες που απαιτούνται - αργότερα όταν αναπαύονται, η τροφή επανέρχεται στο στόμα και αναμασάται Εγκυμοσύνη Τα πρόβατα θεωρούνται πολυγαμικά ζώα. Έτσι, στο κοπάδι, σε κάθε κριάρι πρέπει να αντιστοιχούν γύρω στις προβατίνες. Η εγκυμοσύνη διαρκεί κατά μέσο όρο 150 μέρες. Ο πρώτος τοκετός γίνεται σε ηλικία μηνών ή 2 ετών. Τα θηλυκά γεννούν 1-2 ή σπανιότερα 3-4 μικρά, ύστερα από κύηση 5 μηνών. Οι προβατίνες γεννούν μόνο μια φορά τον χρόνο, αν και βιολογικά έχουν τη δυνατότητα να γεννούν κάθε 6-7 μήνες. Αξίζει να αναφερθεί ότι κάθε προβατίνα αναγνωρίζει το δικό της μικρό, Σελίδα 37
38 ανάμεσα σε πλήθος άλλων, βάσει της μυρωδιάς των μικρών της. Τα πρόβατα ενηλικιώνονται σε 2 χρόνια αν είναι αρσενικά, και σε ένα χρόνο αν είναι θηλυκά Χιώτικο πρόβατο Το Χιώτικο πρόβατο προήλθε από το ομώνυμο νησί της Χίου, στην περιοχή του Βορειοανατολικού Αιγαίου. Αποτελεί διασταύρωση ομοιόμαλλου λεπτόουρου ελληνικού πρόβατου με παχύουρο αναμικτόμαλλου μικρασιάτικου πρόβατου. Τελικά, κατατάσεται στα ομοιόμαλλα παχύουρα πρόβατα. Λέγεται ότι παλαιότερα κτηνοτρόφοι της νήσου Χίου και της Ανατολίας, περιοχής της Μικράς Ασίας προχώρησαν σε προσμίξεις μεταξύ των ντόπιων φυλών και των φυλών Kivircik και Daglic. Το Χιώτικο πρόβατο είναι σχετικά μεγαλόσωμο με σωματικό βάρος προβατίνων κιλά ( λίβρες) και κριαριών κιλά ( λίβρες). Θεωρείται η καλύτερη ελληνική φυλή λόγω της υψηλής γαλακτοπαραγωγής και αμνοπαραγωγής. Ο χρωματισμός του είναι λευκός με χαρακτηριστικές κηλίδες μαύρου χρώματος στο κεφάλι γύρω από τα αυτιά, τα μάτια, στην κοιλιά και στα πόδια. Τα αρσενικά διαθέτουν κέρατα με μεγάλη σπείρα ενώ τα θηλυκά, όταν έχουν κέρατα, είναι μικρά σαν ένα εξόγκωμα. Το Χιώτικο πρόβατο έχει χρησιμοποιηθεί σε ευρεία κλίμακα για τη γενετική βελτίωση άλλων ελληνικών και ξένων φυλών με πολύ καλά αποτελέσματα ως προς την αύξηση της γαλακτοπαραγωγής και αμνοπαραγωγής. 1.5 Σκοπός Ο σκοπός της συγκεκριμένης εργασίας είναι να προσδιοριστεί η επίδραση εκχυλισμάτων στέμφυλων, στους δείκτες οξειδωτικού στρες (GSH, CAT, TBARS, TAC, CARBONYLS) σε αίμα και ιστό σπλήνας νεαρών προβάτων. Για το σκοπό αυτό εκτράφηκαν 28 πρόβατα της Ελληνικής φυλής Χιώτικα, τα οποία, τράφηκαν για 65 ημέρες με ζωοτροφή εμπλουτισμένη με στέμφυλα. Έγιναν συνολικά τρεις ιστοληψίες και αιμοληψίες, στις 15 ημέρες όπου τα ζώα τρεφόντουσαν αποκλειστικά με το γάλα της μητέρας τους, στις 42 ημέρες όπου τα μισά πρόβατα λάμβαναν πολυφαινολικό σιτηρέσιο και γάλα, και τα άλλα μισά κανονικό σιτηρέσιο και γάλα και στις 65 ημέρες όπου οι δύο ομάδες τρεφόντουσαν αποκλειστικά με ζωοτροφή (control και πολυφαινολικό σιτηρέσιο). Σελίδα 38
39 2.Υλικά και Μέθοδοι 2.1 Γενικά Για την παρούσα εργασία εκτράφηκαν 28 πρόβατα. Η εκτροφή των προβάτων πραγματοποιήθηκε στο Ινστιτούτο Επιστήμης και Ζωικής Παραγωγής των Γιαννιτσών. Κατά τον μήνα Δεκέμβριο γεννήθηκαν 28 αρνιά Ελληνικής φυλής «Χιώτικης» τα οποία μετά το πέρας των 15 ημερών από την γέννησή τους χωρίστηκαν σε δύο (2) ομάδες (Α, Β ομάδα, 12 αρνιά ανά ομάδα) η οποίες λάμβαναν τις πειραματικές ζωοτροφές. Κανονικό σιτηρέσιο (ομάδα Α, ελέγχου), σιτηρέσιο εμπλουτισμένο με ενσίρωμα καλαμποκιού-στεμφύλων (ομάδα Β). Η εκτροφή πραγματοποιήθηκε σύμφωνα με το παρακάτω πειραματικό πλάνο. Εικόνα 12 :Πειραματικό πλάνο εκτροφής απογαλακτισμού των αναπτυσσόμενων αρνιών Μετά το πέρας των 15 ημερών από την γέννηση, τα αρνιά βρίσκονταν με τις μητέρες τους. Στο διάστημα ημερών τα αρνιά θήλαζαν και ταυτόχρονα έτρωγαν τις πειραματικές ζωοτροφές. Μια ώρα το πρωί και μια ώρα το απόγευμα τα αρνιά απομακρύνονταν από τις μητέρες τους, με σκοπό να τραφούν οι μητέρες. Τις υπόλοιπες ώρες της ημέρας όπως προαναφέρθηκε τα αρνιά θήλαζαν και τρέφονταν με τις πειραματικές ζωοτροφές οι οποίες είχαν τοποθετηθεί σε ειδικές ταΐστρες όπου παραβρίσκονταν στο διπλανό χώρο, ο οποίος ήταν ξεχωριστός και τα αρνιά εισέρχονταν μέσω μιας μικρής πόρτας. Παράλληλα με τις πειραματικές ζωοτροφές και τον θηλασμό τα αρνιά τρέφονταν με μηδική (τριφύλλι). Στο διάστημα μεταξύ των 42 και 65 ημερών, στο οποίο ολοκληρώθηκε ο πειραματισμός, απομακρύνθηκαν οι μητέρες και τα αρνιά τρέφονταν αποκλειστικά με τις πειραματικές ζωοτροφές καθώς και με μηδική τροφή. Σελίδα 39
40 2.2. Περιγραφή του σιτηρεσίου Παρασκευή βιολειτουργικών ζωοτροφών Είναι γενικά αποδεκτό ότι η διατροφή σήμερα αποτελεί καθοριστικό παράγοντα στη ζωική παραγωγή καθώς δεν επηρεάζει μόνο την υγεία και την παραγωγικότητα των αγροτικών ζώων, αλλά και το κόστος παραγωγής των παραγόμενων κτηνοτροφικών προϊόντων. Γενικά, ως ζωοτροφή, ορίζεται κάθε ύλη η οποία μετά την πρόσληψή και την πέψη της μπορεί να απορροφηθεί και να χρησιμοποιηθεί από τον οργανισμό του ζώου. Η ορθή επιλογή και κατάρτιση των ζωοτροφών απαιτεί την ακριβή γνώση της θρεπτικής τους αξίας, ώστε να καλύπτουν επαρκώς τις διατροφικές ανάγκες των ζώων, συμπιέζοντας παράλληλα το κόστος παραγωγής. Αυτό ουσιαστικά προϋποθέτει τον ακριβή καθορισμό των αναγκών των ζώων σε ενέργεια και θρεπτικά συστατικά αλλά και την ακριβή γνώση της θρεπτικής αξίας των ζωοτροφών. Για την κατάρτιση των παρακάτω βιολειτουργικών ζωοτροφών, χρησιμοποιήθηκαν συστατικά που περιέχουν όλες τις απαραίτητες θρεπτικές ουσίες που πληρούν τις ενεργειακές ανάγκες και εξασφαλίζουν την υγεία των προβάτων καθώς επίσης ενσωματώθηκαν, ως πρόσθετες ύλες, βιοδραστικά συστατικά φυτικής προέλευσης με αποδεδειγμένη αντιοξειδωτική δράση. Όπως αναφέρθηκε και στην εισαγωγή τα συγκεκριμένα βιοδραστικά συστατικά, δηλαδή οι πολυφαινόλες που εμπεριέχονται στο εκχύλισμα στεμφύλων έχουν μεγάλη ποικιλία ευεργετικών και θεραπευτικών ωφελειών. Η διατροφή των προβάτων με τις συγκεκριμένες βιολειτουργικές ζωοτροφές αναμένουμε να βοηθήσει σημαντικά ειδικότερα στην ηλικία απογαλακτισμού όπου τα νεαρά ζώα είναι επιρρεπή σε ασθένειες λόγω της μειωμένης αντιοξειδωτικής τους άμυνας και εξαιτίας του στρες απογαλακτισμού Παρασκευή βιολειτουργικών ζωοτροφών για τα πρόβατα ( Ελληνικής φυλής, «Χιώτικα»). Παρασκευάστηκαν 2 είδη σιτηρεσίων. Κανονικό σιτηρέσιο (χορήγηση σε ομάδα Α, ελέγχουcontrol) και σιτηρέσιο εμπλουτισμένο με ενσίρωμα στεμφύλων (χορήγηση σε ομάδα Β). Ομάδα (Β): καλαμπόκι (ενσιρωμένο με εκχύλισμα στεμφύλων), γάλα φυράματος, σογιάλευρο, πίτυρα, ισορροπιστής αρνιών, μονοφωσφορικό ασβέστιο, μαρμαρόσκονη, άλας. Πίνακας 2: Σύσταση παρασκευασμένων Πίνακας 3 :Σύσταση παρασκευασμένων σιτηρεσίων, σιτηρεσίων, ομάδα στεμφύλων. ΣΙΤΗΡΕΣΙΟ ΜΕ ΕΝΣΙΡΩΜΑ ΣΤΕΜΦΥΛΩΝ (ΟΜΑΔΑ Β) ΖΩΟΤΡΟΦΗ % ΕΝΣΙΡΩΜΑ ΣΤΕΜΦΥΛΩΝ 45 ΠΙΤΥΡΑ ΣΙΤΟΥ 9 ΣΟΓΙΑΛΕΥΡΟ 21 ΓΑΛΑ 20 ΙΣΟΡΡΟΠΙΣΤΗΣ 2,5 ΑΛΑΣ 0,5 ΜΑΡΜΑΡΟΣΚΟΝΗ 1,2 ΦΩΣΦ. ΜΟΝΟΑΣΒΕΣΤΙΟ 0,8 ΣΥΝΟΛΟ 100 ομάδα control. ΣΙΤΗΡΕΣΙΟ ΕΛΕΓΧΟΥ (ΟΜΑΔΑ Α) ΖΩΟΤΡΟΦΗ % ΑΡΑΒΟΣΙΤΟΣ 45 ΠΙΤΥΡΑ ΣΙΤΟΥ 9 ΣΟΓΙΑΛΕΥΡΟ 21 ΓΑΛΑ 20 ΙΣΟΡΡΟΠΙΣΤΗΣ 2,5 ΑΛΑΣ 0,5 ΜΑΡΜΑΡΟΣΚΟΝΗ 1,2 ΦΩΣΦ. ΜΟΝΟΑΣΒΕΣΤΙΟ 0,8 ΣΥΝΟΛΟ 100 Σελίδα 40
41 2.2.3 Παρασκευή ενσιρώματος στεμφύλων Το ενσίρωμα στεμφύλων παρασκευάστηκε πριν την δημιουργία των ζωοτροφών και η σύστασή του αποτελείται από: καλαμπόκι (άλευρο), στέμφυλα (ποικιλία μοσχάτο - κόκκινο) και νερό. Η αναλογία των συστατικών ήταν τέτοια έτσι ώστε στο τελικό ενσίρωμα να έχουμε ποσοστό 60% στερεών και έτσι γι αυτόν τον σκοπό πριν την ανάμιξη συνυπολογίστηκαν τα ποσοστά υγρασίας του καλαμποκιού και των στεμφύλων. Κατά την παρασκευή του ενσιρώματος προστέθηκαν και βακτήρια (Lactobacillus) τα οποία σε αναερόβιες συνθήκες προκαλούν ζύμωση. Το ενσιρωμένο καλαμπόκι περιέχει μεγάλα ποσοστά υγρασίας, οργανικά οξέα, όπως γαλακτικό οξύ και χορηγείται στα ζώα σαν χονδροειδής ζωοτροφή. Η ενσίρωση είναι η διαδικασία ζύμωσης φυτικών προϊόντων με υψηλό ποσοστό υγρασίας και υπό αναερόβιες συνθήκες, με σκοπό τη διατήρηση του προϊόντος αλλά και τη βελτίωση της θρεπτικής του αξίας, για χρήση ως ζωοτροφή. Κατά την ενσίρωση δημιουργούνται όξινες συνθήκες που εξασφαλίζουν την διατήρηση της υγρασίας και της γεύσης τους. Μετά την ανάμειξη των συστατικών το ενσίρωμα τοποθετήθηκε σε σακούλες κενού αέρος και παρακολουθήθηκε η διαδικασία της ζύμωσης. Μετά το πέρας 2-4 ημερών (ανάλογα με τη θερμοκρασία του περιβάλλοντος), ήταν αναγκαίο οι σακούλες να ανοίγονται και να κλείνουν ξανά αεροστεγώς. Αυτή η διαδικασία που εκτελέστηκε τέσσερις (4) φορές, είναι απαραίτητη λόγω του ότι παράγεται διοξείδιο του άνθρακα κατά τη διάρκεια της αντίδρασης που πραγματοποιούν τα βακτήρια, με αποτέλεσμα αν δεν αφαιρεθεί ο αέρας οι σακούλες να ανοίξουν και να έρθουν σε επαφή με το ατμοσφαιρικό οξυγόνο. Λόγω του ότι η αντίδραση που πραγματοποιείται για την ενσίρωση του καλαμποκιού απαιτεί αναερόβιες συνθήκες, η επαφή του ενσιρώματος με τον ατμοσφαιρικό αέρα θα έχει ως αποτέλεσμα την αναστολή της αντίδρασης. Κατά την διάρκεια της παραπάνω διαδικασίας λαμβάνονταν δείγματα έτσι ώστε να γίνεται ο έλεγχος του ph του ενσιρώματος. Το ph το οποίο πρέπει να έχει το τελικό ενσίρωμα πρέπει να είναι μικρότερο του 4,1. Επίσης το τελικό προϊόν της ενσίρωσης έχει πιο σκούρο χρώμα από το αρχικό και τα βακτήρια σταματούν την αντίδραση με αποτέλεσμα να μην παρατηρείται ύπαρξη διοξειδίου του άνθρακα μέσα στην σακούλα που βρίσκεται το τελικό προϊόν. Η μέτρηση του ph έγινε με 2 μεθόδους. Στην πρώτη μέθοδο γίνεται αραίωση 1/10 του ενσιρώματος. Δηλαδή σε 1 γραμμάριο ενσιρώματος προστίθενται 9 ml απεσταγμένου νερού. Το μίγμα αναδεύεται έντονα σε vortex για τουλάχιστον 20 λεπτά. Τέλος μετρήθηκε το ph το οποίο ήταν 3,82. Με την δεύτερη μέθοδο γίνεται αραίωση 1/2 του ενσιρώματος. Δηλαδή σε 5 γραμμάρια ενσιρώματος προστίθενται 5 ml απεσταγμένου νερού. Έπειτα ακολουθεί έντονη ανάδευση σε vortex για τουλάχιστον 20 λεπτά και τέλος μετρήθηκε το ph. Το ph του ενσιρώματος με την δεύτερη μέθοδο ήταν 3,80. Όπως φαίνεται και οι δύο μέθοδοι έδωσαν παρόμοιες τιμές ph και συνεπώς η διαδικασία της γαλακτικής ζύμωσης στο ενσίρωμα είχε ολοκληρωθεί και ήταν πλέον έτοιμο για να προστεθεί στο σιτηρέσιο. Σελίδα 41
42 Εικόνα 13 :Συσκευασία πακεταρίσματος σιτηρεσίων Αποτίμηση της αντιοξειδωτικής δράσης (in vitro) των ζωοτροφών. Η αποτίμηση της αντιοξειδωτικής δράσης των πειραματικών ζωοτροφών πραγματοποιήθηκε σύμφωνα με τις εξής μεθόδους: Ι. Προσδιορισμός της εξουδετέρωσης της ρίζας του DPPH H μέθοδος του DPPH βασίζεται στη χρήση της ρίζας του DPPH (1,1-diphenyl-2-picrylhydrazyl). Παρουσία μιας αντιοξειδωτικής ένωσης που λειτουργεί ως δότης ιόντων υδρογόνου, η παραπάνω ρίζα (DPPH ) ανάγεται προς σχηματισμό της αντίστοιχης υδραζίνης (1,1-diphenyl-2-picrylhydrazine). Η μετατροπή της ρίζας υπολογίζεται με φωτομέτρηση στα 520 nm (Apostolou et al., 2013). ΙΙ. Προσδιορισμός της εξουδετέρωσης της ρίζας του ΑΒΤS H μέθοδος του ABTS βασίζεται στη χρήση του ενζύμου horseradish peroxidase κατά την οποία η ένωση του ABTS μετατρέπεται στη ρίζα ABTS +. Η προσθήκη μιας αντιοξειδωτικής ουσίας στο διάλυμα της ρίζας ABTS + έχει ως αποτέλεσμα την αναγωγή της ρίζας με τη μεταφορά ιόντων υδρογόνου. Η μετατροπή της ρίζας υπολογίζεται με φωτομέτρηση στα 730 nm (Apostolou et al., 2013). Μέσω των παραπάνω μεθόδων προσδιορίζεται η τιμή IC 50, δηλαδή η συγκέντρωση των εξεταζόμενων ουσιών η οποία εξουδετερώνει την ρίζα (DPPH, ABTS) κατά 50%. Όσο μικρότερη είναι η τιμή του IC 50 τόσο ισχυρότερη είναι η αντιοξειδωτική δράση της ουσίας. Έτσι υπολογίζοντας το IC 50 των ζωοτροφών μπορούμε να εκτιμήσουμε την δραστικότητα και την αντιοξειδωτική τους ικανότητα. Σελίδα 42
43 2.2.5 Αποτίμηση της αντιοξειδωτικής ικανότητητας των παρασκευασμένων ζωοτροφών για τα πρόβατα Διάγραμμα 1:Στο διάγραμμα απεικονίζεται η % εξουδετέρωση τη ρίζας του DPPH σε συνάρτηση με τη συγκέντρωση της ζωοτροφής της ομάδας ελέγχου. Διάγραμμα 2: Στο διάγραμμα απεικονίζεται η % εξουδετέρωση της ρίζας DPPH σε συνάρτηση με τη συγκέντρωση της ζωοτροφής εμπλουτισμένη με στέμφυλα Σελίδα 43
44 Διάγραμμα 3 :Στο διάγραμμα απεικονίζεται η % εξουδετέρωση της ρίζας του ABTS σε συνάρτηση με τη συγκέντρωση της ζωοτροφής της ομάδας ελέγχου. Διάγραμμα 4 :Στο διάγραμμα απεικονίζεται η % εξουδετέρωση της ρίζας του ABTS σε συνάρτηση με τη συγκέντρωση της ζωοτροφής εμπλουτισμένη με στέμφυλα. Από τις γραφικές παραστάσεις παρατηρείται ότι με την μέθοδο της εξουδετέρωσης της ρίζας του DPPH, η ζωοτροφή εμπλουτισμένη με τα υποπροϊόντα οινοποιίας (στέμφυλα) (IC 50 = 11,9 mg/ml) παρουσιάζει διπλάσια αντιοξειδωτική ικανότητα σε σχέση με την ζωοτροφή της ομάδας ελέγχου (IC 50 = 25,5 mg/ml) Με την μέθοδο της εξουδετέρωσης της ρίζας του ABTS, οι τιμές IC 50 είναι πιο χαμηλές (IC 50 =12 mg/ml και IC 50 =5,6 mg/ml), κάτι που οφείλεται στο ότι τα βιοδραστικά συστατικά των ζωοτροφών εξουδετερώνουν με διαφορετικό τρόπο την ρίζα του ABTS σε σχέση με εκείνη του DPPH. Ωστόσο, και στη μέθοδο του ABTS η δραστικότητα της ζωοτροφής που είναι εμπλουτισμένη με τα στέμφυλα είναι περίπου διπλάσια σε σχέση με την ζωοτροφή της ομάδας ελέγχου Συσχέτιση των δύο μεθόδων κατά Spearman Για τον υπολογισμό του συντελεστή συσχέτισης r κατά Spearman χρησιμοποιήθηκε το πρόγραμμα στατιστικής SPSS18. Παρακάτω παρατίθενται τα αποτελέσματα της στατιστικής ανάλυσης. Ζωοτροφή ομάδας ελέγχου (control) Σελίδα 44
45 Διάγραμμα 5: Στο διάγραμμα απεικονίζεται η συσχέτιση των τιμών IC50 της μεθόδου DPPH με τη μέθοδο του ABTS (r=0,991, p<0,05). Ζωοτροφή εμπλουτισμένη με ενσίρωμα στεμφύλων Διάγραμμα 6 :Στο διάγραμμα απεικονίζεται η συσχέτιση των τιμών IC50 της μεθόδου DPPH με τη μέθοδο του ABTS (r=0,972, p<0,05). Υπολογίζοντας τον συντελεστή γραμμικής συσχέτισης κατά Spearman, ανάμεσα στις τιμές IC 50 που προέκυψαν από τις δύο μεθόδους (DPPH, ABTS), τόσο στην ζωοτροφή της ομάδας ελέγχου (r=0,99) όσο και στην ζωοτροφή εμπλουτισμένη με το ενσίρωμα στεμφύλων (r=0,97), παρατηρείται μια μεγάλη συσχέτιση που σημαίνει ότι τα ίδια πιθανώς βιοδραστικά συστατικά των ζωοτροφών εξουδετερώνουν και τις δύο ρίζες. Σελίδα 45
46 2.2.7 Συνολικά αποτελέσματα της αποτίμησης της αντιοξειδωτικής ικανότητας των ζωοτροφών Ζωοτροφές DPPH(IC 50 ) mg/ml ABTS(IC 50 ) mg/ml Ελέγχου (πρόβατα) 25,5 12 Στέμφυλα (πρόβατα) 11,9 5,6 Πίνακας 4 :Τιμές IC50 των ζωοτροφών με τη μέθοδο DPPH και ABTS. Παρατηρώντας τον παραπάνω πίνακα των συνολικών αποτελεσμάτων διαπιστώνουμε ότι τα βιοδραστικά συστατικά των στεμφύλων (πολυφαινόλες) προσδίδουν στις ζωοτροφές μεγαλύτερη αντιοξειδωτική ικανότητα κάτι το οποίο αναμένουμε να παρατηρήσουμε και στους δείκτες ευζωίας των προβάτων. Τα αποτελέσματα εκφράστηκαν ως μέση τιμή ± SEM. Εκτελέστηκε μονόδρομη ανάλυση διασποράς (one way ANOVA), με το πρόγραμμα PASW Statistics 18 (πρώην SPSS Statistics), κατά Tukey και Dunett. Το επίπεδο σημαντικότητας προσδιορίστηκε σε *p<0, Ομογενοποιήση ιστών Τα δείγματα του ιστού της σπλήνας και του αίματος τοποθετήθηκαν σε eppendorf tubes 1,5mL, ψύχθηκαν αμέσως σε υγρό άζωτο και διατηρήθηκαν στους C μέχρι τη βιοχημική τους ανάλυση. Ο ιστός ομογενοποιήθηκε με αναλογία 1 προς 2 σε ρυθμιστικό διάλυμα PBS ph 7,4 που περιείχε 138mM NaCL, 2,7mM KCL και 1mM EDTA καθώς και ένα μίγμα αναστολέων πρωτεασών (Complete Mini Protease Inhibitor Cocktail Tablets - Roche Diagnostics GmbH). Κατά την προετοιμασία για τη βιοχημική ανάλυση του ιστού τα δείγματα ομογενοποιήθηκαν με γουδί και γουδοχέρι χρησιμοποιώντας υγρό άζωτο. Ακολούθως, το ομογενοποίημα υπέστη επεξεργασία με υπερήχους για την απελευθέρωση της μεγαλύτερης δυνατής ποσότητας πρωτεΐνης και φυγοκεντρήθηκε( g - 5 min - 4 o C). Εικόνα 14: Ομογενοποίηση α) με γουδί β) χρήση υπερήχων. Σελίδα 46
47 2.4 Προσδιορισμός δεικτών οξειδωτικού στρες Γενικά Για την αξιολόγηση της οξειδοαναγωγικής κατάστασης των ιστών προσδιορίζεται η συγκέντρωση της ανηγμένης γλουταθειόνης καθώς και η δραστικότητα της καταλάσης. Για την εκτίμηση της αντιοξειδωτικής ικανότητας συχνά προσδιορίζεται η ολική αντιοξειδωτική ικανότητα των ιστών. Για την αξιολόγηση του οξειδωτικού στρες, ένας από τους δείκτες που χρησιμοποιούνται για τον προσδιορισμό της υπεροξείδωσης των λιπιδίων, είναι οι ουσίες που αντιδρούν με το θειοβαρβιτουρικό οξύ, ενώ για την καταστροφή των πρωτεϊνών χρησιμοποιούνται τα πρωτεϊνικά καρβονύλια. Εκτός από το πλάσμα και το ερυθροκυτταρικό αιμόλυμα οι παραπάνω δείκτες μπορούν να προσδιοριστούν σε αιώρημα κυττάρων που έχουν διαρρηχθεί με υπερήχους. Επεξεργασία αιμολύματος: Χρησιμοποιούμε: Ολικό αίμα για τον προσδιορισμό αιματολογικών παραμέτρων, όπως ο αιματοκρίτης και η αιμοσφαιρίνη. Ερυθροκυτταικό αιμόλυμα για τον προσδιορισμό της ανηγμένης και της οξειδωμένης γλουταθειόνης (GSH και GSSG), της καταλάσης των πρωτεϊνικών καρβονυλίων και των TBARS. Πλάσμα για τον προσδιορισμό των TBARS, των πρωτεϊνικών καρβονυλίων και της ολικής αντιοξειδωτικής ικανότητας. Προετοιμασία ολικού αίματος Βάζουμε περίπου 1 ml αίματος σε σωληνάρια με EDTA (αντιπηκτικό), το ανακινούμε και το βάζουμε στο ψυγείο ως τη χρησιμοποίησή του για τους αιματολογικούς προσδιορισμούς. Συλλογή πλάσματος και ερυθροκυτταρικού αιμολύματος 1. Συλλέγουμε το αίμα σε σωληνάρια falcon (15 ml) με 200 μl EDTA 7,5% και το ανακινούμε μερικές φορές (20 μl 7,5% EDTA για κάθε 1mL αίματος). 2. Φυγοκεντρούμε στα 1370 g, για 10 λεπτά, στους 4 o C. 3. Συλλέγουμε το υπερκείμενο (πλάσμα) και το χωρίζουμε σε φιαλίδια eppendorf, ανάλογα με τις μετρήσεις που θα γίνουν. 4. Προσθέτουμε απιονισμένο νερό (1:1 v/v) στα ερυθροκύτταρα, τα οποία μετά τη φυγοκέντρηση βρίσκονται στο κάτω μέρος του falcon. 5. Ανακινούμε βίαια. 6. Φυγοκεντρούμε στα 4020 g, για 15 λεπτά, στους 4 o C. 7. Συλλέγουμε το υπερκείμενο, που είναι το ερυθροκυτταρικό αιμόλυμα. Οι μεμβράνες των ερυθροκυττάρων μένουν ως ίζημα πολύ μικρού όγκου (10-20 μl). Σελίδα 47
48 8. Χωρίζουμε σε eppendorf το αιμόλυμα ανάλογα με τις μετρήσεις που θα γίνουν. Διατήρηση στους -20 o C. Καθαρισμός αιμολύματος για την προσδιορισμό της ανηγμένης και οξειδωμένης γλουταθειόνης 1. Προσθέτουμε 500 μl αιμολύματος σε 500 μl 5% TCA σε eppendorf. Ανακινούμε στο vortex. 2. Φυγοκεντρούμε στα g (16000 rpm) για 5 min στους 5 o C. 3. Συλλέγουμε το υπερκείμενο σε eppendorf και προσθέτουμε 5% TCA με την εξής αναλογία: 300 μl αιμολύματος / 90 μl 5% TCA ή 260 μl αιμολύμτος / 60 μl 5% TCA. Ανακινούμε στο vortex. 4. Φυγοκεντρούμε στα g (16000 rpm) για 5 min στους 5 o C. 5. Μεταφέρουμε το καθαρό υπερκείμενο σε eppendorf. 100 μl για την GSH και 50 μl για την GSSG. Διατήρηση στους -20 o C Μέθοδοι 1. Μέτρηση γλουταθειόνης Η γλουταθειόνη (γ-γλουταμυλοκυστεϊνογλυκίνη) είναι η πιο άφθονη θειόλη (SH) στους ιστούς των ζώων και του ανθρώπου, με ενδοκυτταρική συγκέντρωση 1-15 mμ. Είναι ένα τριπεπτίδιο που αποτελείται από γλουταμινικό οξύ, γλυκίνη και κυστεΐνη. Οι αναγωγικές (αντιοξειδωτικές) της ιδιότητες παίζουν σημαντικό ρόλο σε διάφορα μεταβολικά μονοπάτια όπως και στο αντιοξειδωτικό σύστημα των περισσότερων αερόβιων κυττάρων. Η γλουταθειόνη απαντάται κυρίως στην ανηγμένη (GSH) και λιγότερο στην οξειδωμένη της μορφή (δισουλφίδιο της γλουταθειόνης, GSSG). Συνήθως, η GSSG είναι το 10% της GSH. Η GSH χρησιμοποιείται ως δείκτης της αντιοξειδωτικής ικανότητας (Pastore., A., et al., 2003). Εικόνα 15: Συντακτικός τύπος γλουταθειόνης. Η GSH λειτουργεί ως συνένζυμο σε πολλά ένζυμα. Ενδεικτικά αναφέρονται η υπεροξειδάση της γλουταθειόνης, η S-τρανσφεράση της γλουταθειόνης και η θειολτρανσφεράση (Battinetal, 2009). Παίζει επίσης σημαντικό ρόλο στο μεταβολισμό των φαρμάκων και του ασβεστίου καθώς και στη λειτουργία των αιμοπεταλίων και των κυτταρικών μεμβρανών. Είναι επίσης ζωτική η συμμετοχή της στην απομάκρυνση των ξενοβιοτικών ουσιών από τον οργανισμό, στην απομάκρυνση των υπεροξειδίων και των ελεύθερων ριζών αλλά και στη μεταφορά των αμινοξέων διαμέσου των μεμβρανών (Sengupta, A., et al., 2004). Σελίδα 48
49 ΑΝΗΓΜΕΝΗ ΓΛΟΥΤΑΘΕΙΟΝΗ (GSH) ΣΤΟ ΕΡΥΘΡΟΚΥΤΤΑΡΙΚΟ ΑΙΜΟΛΥΜΑ Αρχή της μεθόδου Το πειραματικό πρωτόκολλο βασίζεται στην οξείδωση της GSH από το διθειοδυο νιτροβενζοϊκό οξύ (DTNB) και μετριέται σε αιμόλυμα. Η GSH αντιδρά με το DTNB παράγοντας GSSG και 2-νιτρο-5- θειοβενζοΐκό οξύ σύμφωνα με την παρακάτω αντίδραση, το οποίο είναι έγχρωμο προϊόν που απορροφάει στα 412 nm. 2 GSH + DTNB GSSG + 2-nitro-5- thiobenzoic acid.η GSH παράγεται από την GSSG μέσω της δράσης της αναγωγάσης της γλουταθειόνης. Εικόνα 19: Ανακύκλωση και αρχή προσδιορισμού της γλουταθειόνης. Αντιδραστήρια Phosphate buffer 67 mm (ph 7,95). ΜΒ (KH 2 PO 4 ): 136 ΜΒ (Na 2 HPO 4 ): 178. Για να δημιουργήσουμε 500 ml από το phosphate buffer φτιάχνουμε 25 mlkh 2 PO 4 (67 mm) και 500 mlna 2 HPO 4 (67 mm). Για το KH 2 PO 4 ζυγίζουμε 0,227 g και τα διαλύουμε σε 25 ml νερού. Για το Na 2 HPO 4 ζυγίζουμε 5,94 g και τα διαλύουμε σε 475 ml νερού. Σε ένα ποτήρι ζέσεως αναμιγνύουμε τα δύο διαλύματα. Διορθώνουμε με NaOH or HCl, 1 N μέχρι το ph να φτάσει την τιμή 7,95. DTNB (1mM) σε 1% κιτρικό νάτριο (sodium citrate) σε νερό. (39,6 mg DTNB σε 100 ml του 1% διαλύματος του κιτρικού νατρίου, για να δώσει μία συγκέντρωση του 1 mm). DTNB [5,5 -Dithiobis (2-nitrobenzoic acid)], ΜΒ:396,35 Κιτρικό Νάτριο. (C 6 H 5 Na 3 O 7 *2H 2 O, διένυδρο τρινάτριο, tri-sodium dihydrate), ΜΒ: 294,10. Το DTNB διαλύεται σε κιτρικό νάτριο το οποίο εμποδίζει σημαντικές αλλαγές στο ph. Πειραματικό πρωτόκολλο Προθέτουμε τις παρακάτω ποσότητες σε φιαλίδια Εppendorf Σελίδα 49
50 Blank Sample Phosphate buffer 67 mm, ph μl 660 μl DTNB 1 mm 330 μl 330 μl Απεσταγμένο νερό 20 μl Αιμόλυμα 20 μl Πίνακας 5 : Διαδοχική Σειρά Προσθήκης και οι Ποσότητες των Αντιδραστηρίων για τη Μέτρηση της GSH Αναδεύουμε τα eppendorfs και τα επωάζουμε στο σκοτάδι σε θερμοκρασία δωματίου για 45 λεπτά. Η διατήρησή τους στο σκοτάδι έχει ως στόχο την πραγματοποίηση της αντίδρασης μεταξύ του DTNB και της GSH. Μεταφέρουμε το περιεχόμενό τους σε μια πλαστική κυψελίδα και μετράμε την απορρόφηση στα 412 nm. Υπολογισμοί Δραστικότητα της GSH (mmol/l) = (Αbs δείγματος ΔAbs τυφλού / 13,6) * 262,6, όπου το 262,6 είναι ο συντελεστής αραίωσης, που προκύπτει διαιρώντας τον τελικό όγκο (1010 μl) με τον όγκο του αιμολύματος (20 μl) (1010 / 20 = 50,5), πολλαπλασιάζοντας με 2 για να συνυπολογίσουμε την 1:1 αραίωση που έγινε για τη λύση των ερυθροκυττάρων και με 2 * 1,3 για να συνυπολογίσουμε την πρώτη (500 μl αιμολ. / 500 μl 5% TCA) και τη δεύτερη αραίωση (390 μl / 300 μl ή 260 μl / 200 μl) που έγιναν από το TCA 5%. Το 13,6 είναι ο συντελεστής μοριακής απόσβεσης του DTNB. Ο συντελεστής μοριακής απόσβεσης μιας ουσίας ισούται με την απορρόφηση της ουσίας αυτής σε συγκέντρωση 1 mol/l. Ο υπολογισμός της συγκέντρωσης της GSH εκφράζεται ως προς την αιμοσφαιρίνη. Η αιμοσφαιρίνη υπολογίζεται με τη βοήθεια ενός kit και πρέπει να εκφραστεί σε g/l ώστε η μονάδα αυτή να είναι σε συμφωνία με τη συγκέντρωση της GSH που υπολογίστηκε προηγουμένως (mmol/l). Έτσι, μετά τη φωτομέτρηση η τιμή της αιμοσφαιρίνης υπολογίζεται σε g/dl. Πολλαπλασιάζοντας την τιμή αυτή με 10X2, τη μετατρέπουμε σε g/l και ταυτόχρονα λαμβάνουμε υπόψη την 1:1 αραίωση κατά τη λύση των ερυθροκυττάρων. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΗΣ ΑΝΗΓΜΕΝΗΣ ΓΛΟΥΤΑΘΕΙΟΝΗΣ ΣΕ ΙΣΤΟ Η αρχή της μεθόδου και τα αντιδραστήρια είναι ίδια με εκείνα του προσδιορισμού της ανηγμένης γλουταθειόνης στο αιμόλυμα. Πειραματικό πρωτόκολλο Αρχικά, 100μL ιστού προστέθηκαν σε 100μL TCA 5% και φυγοκεντρήθηκαν στα g για 5 min στους 5 o C. Το υπερκείμενο συλλέχτηκε και διατηρήθηκε σε ένα φιαλίδιο eppendorf. 20 μl ιστού, αραιωμένου 1/2 αναμίχθηκαν με 660 μl ρυθμιστικού διαλύματος 67mM (ph 8,0) και 330μL DTNB. Προθέτουμε τις παρακάτω ποσότητες σε φιαλίδια eppendorf: Σελίδα 50
51 Blank Sample Phosphate buffer 67 mm, ph μl 660 μl DTNB 1 mm 330 μl 330 μl Απεσταγμένο νερό 20 μl - Ομογενοποιημένος Ιστός - 20 μl Πίνακας 6: Διαδοχική Σειρά Προσθήκης και οι Ποσότητες των Αντιδραστηρίων για τη Μέτρηση της GSH Αναδεύουμε τα αντιδραστήρια και τα επωάζουμε στο σκοτάδι σε θερμοκρασία δωματίου για 45 λεπτά. Η διατήρησή τους στο σκοτάδι έχει ως στόχο την πραγματοποίηση της αντίδρασης μεταξύ του DTNB και της GSH. Φυγοκεντρούμε στα g για 5 min στους 5 o C και τέλος μεταφέρουμε το περιεχόμενό τους σε μια πλαστική κυψελίδα και μετράμε την απορρόφηση στα 412 nm (Roland., F., et al., 1952). Εικόνα 20: Φάσμα απορρόφησης του 2-νιτρο-5-θειοβενζοϊκού οξέος (Dojindo Molecular Technologies). Υπολογισμοί Δραστικότητα GSH (μmol/mg total prot.) = (Absδείγματος - Δabsτυφλού/13,6) 2 3 ή 4 (λόγω αραιώσεων) 50,5 / Συγκ. πρωτεΐνης (mg/ml). Όπου το 50,5 είναι ο συντελεστής αραίωσης που προκύπτει διαιρώντας τον τελικό όγκο (1010μL) με τον όγκο του ιστού (20μL) (1010/20=50,5), πολλαπλασιάζουμε με 2 και την πρώτη αραίωση που έγινε από το TCA 5% (1:1), πολλαπλασιάζουμε με 3 για τον ιστό της σπλήνας, για να συνυπολογίσουμε την αραίωση που έγινε κατά τη διάρκεια της ομογενοποίησης. To 13,6 είναι ο συντελεστής μοριακής απόσβεσης του DTNB. Η συγκέντρωση της πρωτεΐνης, υπολογίστηκε βάσει της πρότυπης καμπύλης της αλβουμίνης, με εξίσωση y=0,0002x + 0,0705 και R 2 = 0,9935, όπου ο άξονας y = Abs στα 595 nm και ο x = Συγκέντρωση (μg/ml). Κατόπιν, με το Bradford test, λαμβάνονταν η τιμή της απορρόφησης και υπολογίζονταν αντίστοιχα η συγκέντρωση της ολικής πρωτεΐνης. Σελίδα 51
52 2. Δραστικότητα της Καταλάσης. Διάγραμμα 7: Πρότυπη καμπύλη Αλβουμίνης Αρχή της μεθόδου Η καταλάση είναι ένα κοινό ένζυμο, το οποίο απαντάται σε όλους σχεδόν τους ζωντανούς οργανισμούς που έρχονται σε επαφή με το οξυγόνο. Το υπεροξείδιο του υδρογόνου διαμορφώνεται ως προϊόν μεταβολισμού σε πολλούς οργανισμούς. Είναι τοξικό και πρέπει να μετατραπεί γρήγορα σε άλλο, λιγότερο επικίνδυνη χημική ουσία. Για να διαχειριστεί αυτό το πρόβλημα, η ενζυμική καταλάση καταλύει γρήγορα την αποσύνθεση του υπεροξειδίου υδρογόνου, σε αβλαβή οξυγόνο και νερό. Chelikani P, et. al., (2004). Ένα μόριο καταλάσης μπορεί να μετατρέψει μόρια H 2 O 2 το δευτερόλεπτο σε νερό και οξυγόνο. Βρίσκεται στα υπεροξεισώματα, στα μιτοχόνδρια και το κυτταρόπλασμα. Είναι ένα τεραμερές με 4 πολυπεπτιδικές αλυσίδες μεγέθους τουλάχιστον 500 αμινοξέων. Boon EM, et. al. (2007). Στο τετραμερές αυτό υπάρχουν 4 πορφυρινικές ομάδες αίμης, οι οποίες επιτρέπουν στην καταλάση να αντιδρά με το H 2 O 2. Το ιδανικό της ph είναι το ουδέτερο. Η αντίδραση διάσπασης του H 2 O 2 από την καταλάση είναι η ακόλουθη: 2 H 2 O 2 2 H 2 O + O 2 Η αντίδραση πραγματοποιείται σε 2 στάδια: H 2 O 2 + Fe(III)-E H 2 O + O=Fe(IV)-E H 2 O 2 + O=Fe(IV)-E H 2 O + Fe(III)-E + O 2 (Όπου το σύμπλοκο Fe-E αντιπροσωπεύει το κέντρο με το σίδηρο της ομάδας της αίμης που είναι προσδεδεμένη στο ένζυμο). Εικόνα 16 :Μονοπάτι αναγωγής του H 2 O 2 σε H 2 O Σελίδα 52
53 Επίσης η καταλάση μπορεί να χρησιμοποιήσει το H 2 O 2 για την απομάκρυνση τοξικών ουσιών (Η 2 Α) με τη χρησιμοποίηση υποστρώματος (αιθανόλη), σύμφωνα με την ακόλουθη αντίδραση: CAT H 2 O 2 + H 2 A (substrate) 2 H 2 O + A. Για τον προσδιορισμό της δραστικότητας της καταλάσης χρησιμοποιήθηκε η μέθοδος του Aebi et al., (1984). Διαλύματα Phosphate buffer 67mM (ph 7,4) ΜΒ (KH 2 PO 4 ): 136 και ΜΒ (Na 2 HPO 4 ): 178. Για να παρασκευάσουμε 500 ml του phosphate buffer ξεκινάμε πρώτα με 100 ml KH 2 PO 4 (67 mm) και 400 ml Na 2 HPO 4 (67 mm). Για το KH 2 PO 4 ζυγίζουμε 0,91 g και τα διαλύουμε σε 100 ml νερού. Για το Na 2 HPO 4 ζυγίζουμε 4,77 g και τα διαλύουμε σε 400 ml νερού. Σε ένα ποτήρι ζέσεως αναμιγνύουμε τα διαλύματα. Αν χρειαστεί προσθέτουμε NaOH ή HCl, 1 N ώστε το ph του παραγόμενου διαλύματος να είναι 7,4. 30% υπεροξείδιο του υδρογόνου (H 2 O 2 ). Το διάλυμα H 2 O 2 είναι έτοιμο προς χρήση. Πειραματικό πρωτόκολλο Προσθέτουμε τους παρακάτω όγκους σε πλαστικούς δοκιμαστικούς σωλήνες: Δείγμα Phosphate buffer 67 mm, ph μl Ομογενοποιημένος Ιστός 40 μl Πίνακας 7 : Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της Καταλάσης. Αναδεύουμε στο vortex και επωάζουμε στον κλίβανο στους 37 o C για 10 λεπτά. Είναι πιο πρακτικό να επωάζουμε 2 δείγματα κάθε φορά ώστε να είμαστε σίγουροι ότι τα δείγματα φωτομετρούνται αμέσως μετά την επώαση. Κατόπιν, μεταφέρουμε το περιεχόμενο του πλαστικού κυλίνδρου σε μία κυψελίδα για μέτρηση στο υπεριώδες (UV). Τέλος, προσθέτουμε 5 μl 30% H 2 O 2 στην κυψελίδα, την ανακινούμε τρεις φορές χρησιμοποιώντας παραφίλμ στην κορυφή της και μετράμε την απορρόφηση στα 240 nm για 130 δευτερόλεπτα. Υπολογισμοί Δραστικότητα της καταλάσης (U/mg Hb) = (ΔΑbs sample per min / 40) x(75 x 1000 x 3 ή 4 x 2) / Conc. Protein (mg/ml). Όπου, το 40 (mol/l) είναι ο συντελεστής μοριακής απόσβεσης του H 2 O 2 πολλαπλασιαζόμενος με 1000 για τη μετατροπή του σε μmol/ml. Το 75 είναι ο παράγοντας αραίωσης που προκύπτει από τη διαίρεση του τελικού όγκου του κυλίνδρου (3000μL) με τον όγκο του δείγματος (40μL) (3000/40=75). Πολλαπλασιάζουμε με 3 για τον ιστό της σπλήνας, για να συνυπολογίσουμε την αραίωση που έγινε κατά τη διάρκεια της ομογενοποίησης. Ο υπολογισμός της δραστικότητας της καταλάσης εκφράζεται ως προς την συγκέντρωση της ολικής πρωτεΐνης. Δ Αbs = η μεταβολή της απορρόφησης σε ένα λεπτό. Η συγκέντρωση του H 2 O 2 στην κυψελίδα είναι περίπου16 mm. U = μmol/min. ΔAbs blank είναι πάντοτε μηδέν και έτσι δεν απαιτείται μέτρηση του τυφλού (One Unit decomposes one micromole of hydrogen peroxide per minute at 25 o C ph 7,0). Σελίδα 53
54 ΚΑΤΑΛΑΣΗ ΣΤΟ ΕΡΥΘΡΟΚΥΤΤΑΡΙΚΟ ΑΙΜΟΛΥΜΑ Η αρχή της μεθόδου και τα αντιδραστήρια είναι ίδια με εκείνα του προσδιορισμού της καταλάσης στον ιστό. Πειραματικό πρωτόκολλο Προσθέτουμε τους παρακάτω όγκους σε πλαστικούς δοκιμαστικούς σωλήνες και ακολουθείται η διαδικασία που αναφέρθηκε προηγουμένως: Δείγμα Phosphate buffer 67 mm, ph 7.4 Αιμόλυμα αραιωμένο 1/ μl 4 μl Πίνακας 8: Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της Καταλάσης. Υπολογισμοί Δραστικότητα της καταλάσης (U/mg Hb) = (ΔΑbs sample per min / 40) * (750 *1000 *10 *2) / Conc. Hb (mg/ml). Όπου, το 40 (mol/l) είναι ο συντελεστής μοριακής απόσβεσης του H 2 O 2 πολλαπλασιαζόμενος με 1000 για τη μετατροπή του σε μmol/ml. Το 750 είναι ο παράγοντας αραίωσης που προκύπτει από τη διαίρεση του τελικού όγκου του κυλίνδρου (3000 μl) με τον όγκο του αιμολύματος (4 μl) (3000 / 4 = 750), το 10 προκύπτει από την 1:10 αραίωση του δείγματος και το 2 από την 1:1 λύση των ερυθροκυττάρων. Ο υπολογισμός της δραστικότητας της καταλάσης εκφράζεται ως προς την αιμοσφαιρίνη. Η αιμοσφαιρίνη υπολογίζεται με τη βοήθεια ενός kit και πρέπει να εκφραστεί σε g/l ώστε η μονάδα αυτή να είναι σε συμφωνία με τη συγκέντρωση των TBARS που υπολογίστηκε προηγουμένως (μmol/l). Έτσι, μετά τη φωτομέτρηση η τιμή της αιμοσφαιρίνης υπολογίζεται σε g/dl. Πολλαπλασιάζοντας την τιμή αυτή με 10x2, τη μετατρέπουμε σε g/l και ταυτόχρονα λαμβάνουμε υπόψη την 1:1 αραίωση κατά τη λύση των ερυθροκυττάρων. Δ Αbs (min) = η μεταβολή της απορρόφησης σε ένα λεπτό. Η συγκέντρωση του H 2 O 2 στην κυψελίδα είναι 16 mm. 3.Ολική Aντιοξειδωτική ικανότητα (Total Antioxidant Capacity, TAC). Ο όρος ολική αντιοξειδωτική ικανότητα (TAC) αναφέρεται στην ικανότητα των συστατικών των ιστών να εξουδετερώνουν τις ελεύθερες ρίζες. Κάθε συστατικό έχει αντιοξειδωτική δράση. Ωστόσο, κάθε ένα συνεισφέρει με διαφορετικό τρόπο στην ολική αντιοξειδωτική ικανότητα του πλάσματος, η οποία είναι γενικά ένα μέτρο της αντιοξειδωτικής κατάστασης ολόκληρου του οργανισμού. Υπάρχουν δύο διαφορετικοί τρόποι προσέγγισης της ποσοτικοποίησης της αντιοξειδωτικής ικανότητας. Ο πρώτος είναι το άθροισμα της αντιοξειδωτικής ικανότητας του κάθε συστατικού ξεχωριστά. Αυτός είναι ο πιο επίπονος τρόπος επειδή υπάρχουν πολλά μόρια που συνεισφέρουν στην αντιοξειδωτική ικανότητα. Ο δεύτερος τρόπος είναι η μέτρηση της TAC ως σύνολο. Σελίδα 54
55 Αρχή της μεθόδου Η TAC των ιστών στη συγκεκριμένη μέθοδο υπολογίζεται χρησιμοποιώντας το DPPH (1,1-diphenyl- 2-picrylhydrazyl). Παρουσία ενός δότη υδρογόνων που υπάρχει στον ορό, η παραπάνω ρίζα (DPPH ) ανάγεται προς σχηματισμό της αντίστοιχης υδραζίνης (1,1-diphenyl-2-picrylhydrazine). Ο προσδιορισμός της TAC βασίστηκε στη μέθοδο των Janaszweska και Bartosz, (2002). Η μετατροπή της ρίζας υπολογίζεται με φωτομέτρηση στα 520 nm. Διαλύματα Phosphate buffer 10 mm (ph 7,4). ΜΒ (KH 2 PO 4 ): 136 και ΜΒ (Na 2 HPO 4 ): 178. Για να φτιάξουμε 500 ml του phosphate buffer φτιάχνουμε 100 ml KH 2 PO 4 (10 mm) και 400 ml Na 2 HPO 4 (10 mm). Για το KH 2 PO 4 ζυγίζουμε 0,136 g και τα διαλύουμε σε 100 ml νερό. Για το Na 2 HPO 4 ζυγίζουμε 0,712 g και τα διαλύουμε σε 400 ml νερό. Σε ένα ποτήρι ζέσεως χύνουμε τα διαλύματα και προσθέτουμε NaOH ή HCl, 1 N μέχρι το ph να φτάσει την τιμή 7,4. DPPH 0,1 mm. ΜΒ: 394,32 Διαλύουμε 0,02 g DPPH σε 5 ml μεθανόλης και τα αναμειγνύουμε με μαγνητάκι (10 mm). Μετά αραιώνουμε 100 φορές με μεθανόλη και τα αναμειγνύουμε ξανά με μαγνητάκι. Για παράδειγμα, αραιώνουμε 200 μl του 10 mm διαλύματος του DPPH σε 19,8 ml μεθανόλης (ποσό αρκετό για 10 δείγματα, συν το τυφλό και τον θετικό έλεγχο). Εξαιτίας της αραίωσης, ο αρχικός όγκος των 5 ml είναι πάντα αρκετός για πολλούς προσδιορισμούς. Καλύπτουμε με αλουμινόχαρτο το ποτήρι ζέσεως, στο οποίο φτιάχνουμε το DPPH για να αποφύγουμε τη φωτόλυση. Το συγκεκριμένο διάλυμα φτιάχνεται τη μέρα του πειράματος. Ασκορβικό οξύ 10 mm. Είναι έτοιμο προς χρήση.φυσιολογικά, η τιμή της απορρόφησης για το δείγμα που περιέχει το ασκορβικό οξύ (Positive Control) θα πρέπει να είναι χαμηλότερη και από την τιμή των δειγμάτων αλλά και του τυφλού. Ο λόγος είναι η συγκέντρωση του ασκορβικού οξέος (ένα ισχυρό αντιοξειδωτικό μόριο) που έχουμε επιλέξει. Η τιμή της απορρόφησης των δειγμάτων, θα πρέπει να βρίσκεται ανάμεσα στις τιμές του τυφλού (η μεγαλύτερη τιμή) και του θετικού ελέγχου (η μικρότερη τιμή). Πειραματικό πρωτόκολλο Προσθέτουμε τις ακόλουθες ποσότητες στα Εppendorfs: Blank Θετικός control Δείγμα Phosphate buffer 10 mm, ph μl 495 μl 460 μl DPPH 0.1 mm 500 μl 500 μl 500 μl Ασκορβικό Οξύ 10 mm - 5 μl - Ιστός (Αραίωση 1/5) μl Πίνακας 9 :Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της TAC Ανακινούμε τα Eppendorfs μερικές φορές και τα επωάζουμε στο σκοτάδι για 60 λεπτά. Κατά τη διάρκεια της επώασης η αντιοξειδωτικές ουσίες του ιστού, εξουδετερώνουν τη ρίζα DPPH μετατρέποντάς τη στην πιο σταθερή ένωση υδραζίνη. Φυγοκεντρούμε για 3 λεπτά στα g στους 25 o C (για την καταβύθιση σωματιδίων που θα αυξήσουν την απορρόφηση). Μεταφέρουμε 900 ml από το υπερκείμενο με πιπέτα σε πλαστική κυψελίδα και μετράμε την απορρόφηση στα 520 nm. Επειδή είναι πιθανό η απορρόφηση του τυφλού να αυξάνεται με την πάροδο του χρόνου, είναι σκόπιμη η επανάληψη της μέτρησης του τυφλού κάθε 5 περίπου δείγματα. Σελίδα 55
56 Υπολογισμοί Τα αποτελέσματα μπορούν να εκφραστούν ως: i) % μείωση της απορρόφησης (Abs) σε σχέση με το τυφλό, πχ, % Abs μείωση = (Abs τυφλού Abs δείγματος) / Abs τυφλού x 100 ii) μmol DPPH που απομακρύνθηκαν / ml πλάσματος = [(% Abs μείωση / 100) x 50 x 25 x 3 ή 4 x 5] / α) Διαιρούμε με το 100 με σκοπό να μετατρέψουμε την ποσοστιαία μείωση της απορρόφησης σε απλή μείωση της απορρόφησης. β) Πολλαπλασιάζουμε με το 50 διότι η συγκέντρωση του DPPH στην κυψελίδα είναι 50 μmol/l της κυψελίδας. γ) Πολλαπλασιάζουμε με το 25 διότι η αραίωση του ιστού στην κυψελίδα είναι 25 πλάσια (1000 μl στην κυψελίδα / 40 μl ιστού του δείγματος στην κυψελίδα = 25). δ) Πολλαπλασιάζουμε με 3 για τον ιστό της σπλήνας, για να συνυπολογίσουμε την αραίωση που έγινε κατά τη διάρκεια της ομογενοποίησης και με 5 επειδή το δείγμα αραιώνεται 1/5 κατά τη μέτρηση. ε) Διαιρούμε με το 1000 για να μετατρέψουμε τα L σε ml. Η διόρθωση με βάση την ολική πρωτεΐνη έγινε σύμφωνα με τον ακόλουθο τρόπο: mmol DPPH / mg total prot. ΟΛΙΚΗ ΑΝΤΙΟΞΕΙΔΩΤΙΚΗ ΙΚΑΝΟΤΗΤΑ ΤΟΥ ΠΛΑΣΜΑΤΟΣ Το ουρικό οξύ φαίνεται να είναι το μόριο που έχει τον πιο ισχυρό ρόλο στον καθορισμό της τιμής της TAC στο πλάσμα (55-60%) προκαλώντας μεγάλη αύξησή της όταν η συγκέντρωσή του αυξάνεται. Το ουρικό οξύ βρίσκεται σε πολύ πιο υψηλές συγκεντρώσεις στο πλάσμα σε σχέση με άλλα μόρια με εξαίρεση τις θειόλες. Η βιταμίνη C (ασκορβικό οξύ) είναι το δεύτερο πιο ισχυρό μόριο στον καθορισμό της τιμής της TAC και ακολουθούν κατά σειρά οι βιταμίνες E και A. Οι βιταμίνες C και E μάλιστα είναι πιθανό να αποτελούν το 25 % της συνολικής αντιοξειδωτικής ικανότητας του πλάσματος. Η αρχή της μεθόδου και τα αντιδραστήρια είναι τα ίδια με εκείνα που χρησιμοποιήθηκαν για τον προσδιορισμό της ολικής αντιοξειδωτικής ικανότητας σε ιστό. Πειραματικό πρωτόκολλο Προσθέτουμε τις ακόλουθες ποσότητες στα Εppendorfs και ακολουθείται η διαδικασία που αναφέρθηκε προηγουμένως: Blank Θετικός control Δείγμα Phosphate buffer 10 mm, ph μl 495 μl 480 μl DPPH 0.1 mm 500 μl 500 μl 500 μl Ασκορβικό Οξύ 10 mm 5 μl Πλάσμα 20 μl Σελίδα 56
57 Πίνακας 10 :Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων, για την μέτρηση της TAC. Υπολογισμοί Τα αποτελέσματα μπορούν να εκφραστούν ως: i) % μείωση της απορρόφησης (Abs) σε σχέση με το τυφλό, πχ % Abs μείωση = (Abs τυφλού Abs δείγματος) / Abs τυφλού * 100 ii) μmol DPPH που απομακρύνθηκαν / ml πλάσματος = [(% Abs μείωση / 100) *50 * 50] / 1000 α) Διαιρούμε με το 100 με σκοπό να μετατρέψουμε την ποσοστιαία μείωση της απορρόφησης σε απλή μείωση της απορρόφησης. β) Πολλαπλασιάζουμε με το 50 διότι η συγκέντρωση του DPPH στην κυψελίδα είναι 50 μmol/l της κυψελίδας. γ) Πολλαπλασιάζουμε με το 50 διότι η αραίωση του πλάσματος στην κυψελίδα είναι 50-πλάσια (1000 μl στην κυψελίδα / 20 μl πλάσματος του δείγματος στην κυψελίδα = 50). δ) Διαιρούμε με το 1000 για να μετατρέψουμε τα L του πλάσματος σε ml ορού. 4.Ουσίες που αντιδρούν με το θειοβαρβιτουρικό οξύ (TBARS). Αρχή της μεθόδου Το οξειδωτικό στρες στο κυτταρικό περιβάλλον έχει ως αποτέλεσμα το σχηματισμό άκρως ενεργών και ασταθών υπεροξειδίων των λιπιδίων από τα πολυακόρεστα λιπαρά οξέα. Προϊόν της διάσπασης αυτών των ασταθών μορίων είναι η μαλονδιαλδεΰδη. Η μαλονδιαλδεΰδη μπορεί να προσδιοριστεί μέσω της αντίδρασής της με το θειοβαρβιτουρικό οξύ. Έτσι, τα TBARS εκφράζονται σαν ισοδύναμα της μαλονδιαλδεΰδης, η οποία σχηματίζει μία ένωση με το θειοβαρβιτουρικό οξύ με αναλογία μαλονδιαλδεΰδης προς θειοβαρβιτουρικό οξύ 1/2. Η μέτρηση της μαλονδιαλδεΰδης είναι μία φωτομετρική μέθοδος για τον προσδιορισμό του βαθμού υπεροξείδωσης των λιπιδίων. Εικόνα 17 :Αντίδραση TBA (1) με MDA (2), που οδηγεί στην παραγωγή του μορίου TBA-MDA Για τον προσδιορισμό των TBARS χρησιμοποιήθηκε μια ελαφρά τροποποιημένη μέθοδος του Keles et al., (2001). Πριν ξεκινήσει η πειραματική διαδικασία ρυθμίζουμε το υδατόλουτρο σε θερμοκρασία 95 o C. Σελίδα 57
58 Διαλύματα Tris-HCl 200 mm (ph 7,4). ΜΒ (Tris): 121,14. ΜΒ (HCl): 36,46 (stock 37%) [10,1 N]. Για να παρασκευάσουμε 100 ml του Tris-HCl buffer φτιάχνουμε 25 ml Tris (200 mm) και 42 ml HCl (0,1 N). Για το Tris ζυγίζουμε 0,61 g και τα διαλύουμε σε 25 ml νερού. Για το HCl διαλύουμε 0,42 ml του stock 37% HCl (10,1 N) σε 42 ml νερού. Σε ένα ποτήρι ζέσεως ρίχνουμε τα 25 ml από το Tris και προσθέτουμε αργά τα 42 ml του HCl και μετά προσθέτουμε νερό ως τα 100 ml. Ελέγχουμε το ph αν είναι στο 7,4.Το Tris είναι συντομογραφία του τρισυδροξυμεθυλαμινομεθάνιου (trishydroxymethylaminomethane). Το Tris είναι κατάλληλο για τη δημιουργία ρυθμιστικών διαλυμάτων με ph από 6,5 μέχρι 9,7. Διάλυμα Na 2 SO 4 (2 M) TBA (55 mm). ΜΒ (TBA): 144,1 και ΜΒ (Na 2 SO 4 ): 142,04. Για την παρασκευή10 ml διαλύματος, ζυγίζουμε 2,84 g Na 2 SO 4 και 0,08 g θειοβαρβιτουρικό οξύ (TBA). Τα μεταφέρουμε σε ένα ποτήρι ζέσεως και προσθέτουμε 10 ml νερού. Θερμαίνουμε και ανακατεύουμε με το μαγνητάκι μέχρι να διαλυθούν τα συστατικά πλήρως. Το συγκεκριμένο διάλυμα πρέπει να φτιάχνεται πάντοτε την ημέρα του πειράματος. TCA 35%: Ζυγίζουμε 35 g TCA και τα διαλύουμε σε απεσταγμένο νερό ώστε ο τελικός όγκος να φτάσει τα 100 ml νερού (σε θερμοκρασία δωματίου). TCA 70%: Ζυγίζουμε 70 g TCA και τα διαλύουμε σε απεσταγμένο ώστε ο τελικός όγκος να φτάσει τα 100 ml νερού (σε θερμοκρασία δωματίου). Πειραματικό Πρωτόκολλο Σε δοκιμαστικούς σωλήνες Falcon (15 ml) προσθέτουμε 100 μl ομογενοποιημένου ιστού (για τα δείγματα) ή απεσταγμένο νερό (για το τυφλό). Προσθέτουμε 500 μl TCA 35% και 500 μl Tris-HCl και αναδεύουμε. Επωάζουμε για 10 min σε θερμοκρασία δωματίου. Προσθέτουμε 1 ml Na 2 SO 4 TBA και επωάζουμε στους 95 o C για 45 min στο υδατόλουτρο. Κατόπιν, μεταφέρουμε τους Falcon στον πάγο και τους αφήνουμε να κρυώσουν για 5 min. Προσθέτουμε 1 ml TCA 70% και αναδεύουμε. Μεταφέρουμε 1 ml σε eppendorfs και φυγοκεντρούμε στα g (10000 rpm) στους 25 o C για 3 min. Τέλος, μεταφέρουμε με πιπέτα 900 μl από το υπερκείμενο σε κυψελίδα και μετράμε την απορρόφηση στα 530 nm. Υπολογισμοί Η συγκέντρωση των TBARS (nmol/mg total protein) = (Abs δείγματος Abs τυφλού) / 0,156 x 31 x 2 ή 3 x 3, όπου το 31 είναι ο συντελεστής αραίωσης, που προέρχεται από τη διαίρεση του τελικού όγκου (3100 μl) με τον όγκο του ομογενοποιημένου ιστού (100 μl) (3100 / 100 = 31). Το 0,156 προέρχεται από το συντελεστή μοριακής απόσβεσης* της MDA που είναι 156 (mol/l) διαιρούμενου με 10-6 με σκοπό να μετατραπούν τα mol/l σε μmol/l. Πολλαπλασιάζουμε με 3 για τον ιστό της σπλήνας για να συνυπολογίσουμε την αραίωση που έγινε κατά τη διάρκεια της ομογενοποίησης και με 3 επειδή το δείγμα αραιώνεται 3 φορές κατά τη μέτρηση. * Ο συντελεστής μοριακής απόσβεσης μιας ουσίας ισούται με την απορρόφηση της ουσίας αυτής σε συγκέντρωση 1 mol/l. ΟΥΣΙΕΣ ΠΟΥ ΑΝΤΙΔΡΟΥΝ ΜΕ ΤΟ ΘΕΙΟΒΑΡΒΙΤΟΥΡΙΚΟ ΟΞΥ (TBARS) ΣΤΟ ΠΛΑΣΜΑ Η αρχή της μεθόδου, τα αντιδραστήρια και το πειραματικό πρωτόκολλο είναι τα ίδια με εκείνα που χρησιμοποιηθήκαν για τον προσδιορισμό της μεθόδου στον ιστό. Σελίδα 58
59 Υπολογισμοί Η συγκέντρωση των TBARS (μmol/l) = (Abs δείγματος Abs τυφλού) / 0,156 *31, όπου το 31 είναι ο συντελεστής αραίωσης, που προέρχεται από τη διαίρεση του τελικού όγκου (3100 μl) με τον όγκο του πλάσματος (100 μl) (3100 / 100 = 31). Το 0,156 προέρχεται από το συντελεστή μοριακής απόσβεσης* της MDA που είναι (mol/l) διαιρούμενου με 10-6 με σκοπό να μετατραπούν τα mol/l to μmol/l. *Ο συντελεστής μοριακής απόσβεσης μιας ουσίας ισούται με την απορρόφηση της ουσίας αυτής σε συγκέντρωση 1 mol/l 5.Πρωτεϊνικά καρβονύλια Αρχή της μεθόδου Οι πρωτεΐνες και τα αμινοξέα είναι ευαίσθητα σε βλάβες προκαλούμενες από τις ελεύθερες ρίζες. Τα πρωτεϊνικά καρβονύλια είναι ένας δείκτης της οξείδωσης ων πρωτεϊνών και χρησιμοποιείται ευρέως. Οι καρβονυλικές ομάδες (αλδεΰδες και κετόνες) που αποτελούνται από ένα άτομο άνθρακα σε διπλό δεσμό με ένα άτομο οξυγόνου C = O, ως συνήθως αποτελούν μέρος σε άλλες μεγαλύτερες λειτουργικές ομάδες. Παράγονται κυρίως στις προσθετικές ομάδες της προλίνης (pro), της αργινίνης (arg), της λυσίνης (lys) και της θρεονίνης (thr). Είναι ένας αξιόπιστος δείκτης οξείδωσης των πρωτεϊνών καθώς τα καρβονύλια είναι σταθερά μόρια. Οι πρωτεΐνες που καρβονυλιώνοται υφίστανται μη αναστρέψιμες βλάβες καθώς εκτρέπονται από τη φυσιολογική τους λειτουργία. Οι καρβονυλιωμένες πρωτείνες σε μέτριο βαθμό, διασπώνται από το πρωτεόσωμα αλλά αν υποστούν πολύ δριμείες βλάβες τότε δεν μπορούν να διασπαστούν και συγκεντρώνονται σε συσσωματώματα υψηλού μοριακού βάρους. Η καρβονυλίωση των πρωτεϊνών όχι μόνο επηρεάζει τη δική τους λειτουργία αλλά και τον τρόπο με τον οποίο λειτουργούν και άλλα βιομόρια. Για παράδειγμα, αν υποστούν καρβονυλίωση ένζυμα όπως εκείνα που επισκευάζουν το DNA ή οι DNA πολυμεράσες, το DNA δε θα επιδιορθώνεται ούτε θα αντιγράφεται με την απαραίτητη πιστότητα. Ο σχηματισμός των καρβονυλίων συνήθως ανιχνεύεται με την αντίδρασή τους με το DNPH (2,4-δίνιτριφαινυλυδραζίνη) προς σχηματισμό του 2,4-δίνιτροφαινυλυδραζονίου. Ο προσδιορισμός των καρβονυλίων βασίστηκε στη μέθοδο Patsoukis et. al., (2004). Εικόνα 18 :Σύνδεση πρωτεΐνης με την DNPH (2,4-δίνιτριφαινυλυδραζίνη) και σχηματισμός του 2,4- δίνιτροφαινυλυδραζονίου Διαλύματα Διάλυμα HCl 2,5 N. HCl: ΜΒ 36,46; stock 37% (10,1 N)Για να παρασκευάσουμε 100 ml διαλύματος 2,5 N HCl, προσθέτουμε αργά 24,6 ml του 37% HCl (ίσο με 10,1 N HCl) σε 70 ml απεσταγμένου νερού και το φέρνουμε σε τελικό όγκο 100 ml με απεσταγμένο Σελίδα 59
60 νερό. Κατά την παρασκευή του διαλύματος του 2,5 N HCl χρειάζεται ιδιαίτερη προσοχή επειδή το διάλυμα του 37 % είναι πολύ καυστικό. Πάντα η παρασκευή γίνεται κάτω από τον απαγωγό και φορώντας γάντια. DNPH 14 mm. (ΜΒ: 198,1). Για να φτιάξουμε 100 ml 14 mm DNPH διαλύουμε 0,2833 g DNPH σε 100 ml 2,5 N HCl. Το διάλυμα αυτό φτιάχνεται πάντα τη μέρα του πειράματος. Όταν το ετοιμάσουμε το καλύπτουμε με αλουμινόχαρτο γιατί είναι φωτοευαίσθητο. Απαιτούνται 0,5 ml για κάθε δείγμα. Φτιάχνουμε και ένα τυφλό για κάθε δείγμα. Ουρία 5 M (ph 2,3). (ΜΒ: 60,06). Για να φτιάξουμε 100 ml 5 M ουρίας (ph 2,3, το οποίο ρυθμίζεται με 2N HCl), διαλύουμε 30 g ουρίας in 70 ml απεσταγμένου νερού και το φέρνουμε σε τελικό όγκο 100 ml με απεσταγμένο νερό. Πειραματικό πρωτόκολλο Σε 50 μl ομογενοποιημένου ιστού προσθέτουμε 50 μl 20% TCA σε eppendorfs και αναδεύουμε στο vortex (κάθε δείγμα έχει το τυφλό του)*. Το 20% TCA προστίθεται με σκοπό να κατακρημνιστούν οι πρωτεΐνες του πλάσματος. Το TCA (τριχλωροοξικό οξύ) χρησιμοποιείται ευρέως στη βιοχημεία για την κατακρήμνιση μακρομορίων όπως πρωτεΐνες, DNA και RNA. Επωάζουμε στον πάγο για 15 λεπτά και φυγοκεντρούμε στα g για 5 λεπτά στους 4 o C και απομακρύνουμε το υπερκείμενο. Κατόπιν, προσθέτουμε στο ίζημα (πελέτα) 0,5 ml του 14 mm DNPH (διαλυμένο σε 2,5 N HCL) για τα δείγματα ή 0,5 ml 2,5 N HCL για τα τυφλά (κάθε δείγμα έχει το δικό του τυφλό), διαλύουμε με την πιπέτα το ίζημα, αναδεύουμε και επωάζουμε στο σκοτάδι σε θερμοκρασία δωματίου για 1 ώρα με ενδιάμεση ανάδευση στο vortex κάθε 15 λεπτά. Μετά την πάροδο της μίας ώρας, φυγοκεντρούμε στα g για 5 λεπτά στους 4 o C. Απομακρύνουμε το υπερκείμενο και προσθέτουμε 1 ml από το 10% TCA, αναδεύουμε (διαλύουμε με την πιπέτα το ίζημα αν χρειάζεται) και φυγοκεντρούμε στα g για 5 λεπτά στους 4 o C. Απομακρύνουμε το υπερκείμενο και προσθέτουμε 0,5 ml αιθανόλης και 0,5 ml οξικού ειθυλεστέρα (αναλογία μίγματος, 1:1 v/v), κάνουμε vortex και φυγοκεντρούμε στα g για 5 λεπτά στους 4 o C. Το ίζημα πλένεται με 10% TCA και με μίγμα αιθανόλης και οξικού αιθυλεστέρα για να απομακρυνθεί το DNPH που δεν έχει αντιδράσει. Αυτήν την διαδικασία την επαναλαμβάνουμε άλλες δύο (2) φορές και απομακρύνουμε το υπερκείμενο. Προσθέτουμε 1 ml 5 M ουρία (ph 2,3), αναδεύουμε και επωάζουμε στους 37 o C για 15 λεπτά. Η ουρία προκαλεί μετουσίωση των πρωτεϊνών (διασπώντας τους ομοιoπολικούς δεσμούς) αυξάνοντας έτσι τη διαλυτότητά τους. Φυγοκεντρούμε στα g για 3 λεπτά στους 4 o C. Τέλος, μεταφέρουμε με την πιπέτα 900 ml σε μία κυψελίδα και μετράμε την απορρόφηση στα 375 nm. *(Το τυφλό περιέχει τα πάντα εκτός από τα 0,5 ml DNPH, τα οποία αντικαθίστανται 0,5 ml HCL 2,5 N). Υπολογισμοί Συγκέντρωση πρωτεϊνικών καρβονυλίων (nmol/mg total prot.)= Aδείγματος- Ατυφλού/ /50 x 2 ή 3 x 2/Συγκ. πρωτεΐνης (mg/ml). Ο συντελεστής μοριακής απόσβεσης του DNPH είναι 22 mm x cm -1. Το 1000/50 είναι ο συντελεστής αραίωσης (1000 μl στην κυψελίδα /50 μl δείγματος). Πολλαπλασιάζουμε με 3 για τον ιστό της σπλήνας, για να συνυπολογίσουμε την αραίωση που έγινε κατά τη διάρκεια της ομογενοποίησης και με 2 επειδή το δείγμα αραιώνεται 2 φορές κατά τη μέτρηση, διότι προσθέτουμε TCA 20% αρχικά). Σελίδα 60
61 ΠΡΩΤΕΙΝΙΚΑ ΚΑΡΒΟΝΥΛΙΑ ΣΤΟ ΠΛΑΣΜΑ Η αρχή της μεθόδου, τα αντιδραστήρια και το πειραματικό πρωτόκολλο είναι τα ίδια με εκείνα που χρησιμοποιηθήκαν για τον προσδιορισμό της μεθόδου στον ιστό. Υπολογισμοί Συγκέντρωση πρωτεϊνικών καρβονυλίων (nmol/ml) = A δείγματος A τυφλού / * 1000/50. Ο συντελεστής μοριακής απόσβεσης του DNPH είναι 22 mm cm -1. Το 1000/50 είναι ο συντελεστής αραίωσης (1000 μl στην κυψελίδα /50 μl δείγματος). Ο υπολογισμός της συγκέντρωσης των πρωτεϊνικών καρβονυλίων ανά πρωτεΐνη πλάσματος μπορεί να γίνει μέσω της εξίσωσης:συγκ. πρωτ. καρβ. (nmol/mg) = συγκ. πρωτ. καρβ. nmol/ml / συγκ. πρωτ mg/ml.συγκέντρωση πρωτεϊνών = 70 mg/ml 6.Προσδιορισμός συνολικής ποσότητας πρωτεΐνης μέσω του αντιδραστηρίου Bradford Ο προσδιορισμός συνολικής ποσότητας πρωτεΐνης των δειγμάτων έγινε μέσω της πρότυπης καμπύλης της πρωτεΐνης αλβουμίνης, μέσω του αντιδραστηρίου Bradford. Το αντιδραστήριο Bradford χρησιμοποιείται συχνά για τον ποσοτικό προσδιορισμό συνολικής ποσότητας πρωτεΐνης. Η μέθοδος βασίζεται στην αλληλεπίδραση της χρωστικής Coomassie Briliant Blue G-250 του αντιδραστηρίου με τα αμινοξέα των πρωτεϊνών, οδηγώντας στο σχηματισμό χρωμογόνου προϊόντος με μπλε χρώμα το οποίο έχει οπτική απορρόφηση στα 595 nm (Bradford M.M 1976 A rapid sensitive method for the quantification of microgram of protein utilizing the principle of protein- Dye Binding. Anal Biochem 72: ). 7. Ποσοτικός προσδιορισμός της αιμοσφαιρίνης του αίματος. Αντιδραστήρια που χρησιμοποιήθηκαν: Potassium ferricyanide Potassium cyanide Dihydrogen potassium phosphate 0,60 mmol/l 0,90 mmol/l 2 mmol/l Αρχή της μεθόδου Η αιμοσφαιρίνη οξειδώνεται από το potassium ferricyanide σε μεθαιμοσφαιρίνη η οποία μετατρέπεται σε κυανομεθαιμοσφαιρίνη από το potassium cyanide. Η ένταση του χρώματος που σχηματίζεται, είναι ανάλογη της συγκέντρωσης της αιμοσφαιρίνης στο δείγμα. Πειραματικό πρωτόκολλο 1) Προσθέτουμε τα ακόλουθα αντιδραστήρια και αναδεύουμε τα eppendorfs με vortex. Sample Kit αντιδραστήριο 1000 μl Σελίδα 61
62 Αιμόλυμα 4 μl Πίνακας 11 :Διαδοχική σειρά προσθήκης και οι ποσότητες των αντιδραστηρίων για τη μέτρηση της αιμοσφαιρίνης. Περιμένουμε δέκα λεπτά και κατόπιν μετρούμε την απορρόφηση στα 540 nm. 3.ΑΠΟΤΕΛΕΣΜΑΤΑ 3.1 Επίπεδα Γλουταθειόνης * Διάγραμμα 8: Επίπεδα της γλουταθειόνης (GSH). * Στατιστικά σημαντική αύξηση στις πολυφαινολικές ομάδες των 65 ημερών σε σχέση με τις ομάδες ελέγχου κατά 101,47% στον ιστό της σπλήνας. Σύγκριση των ομάδων control Στις ομάδες control, τα επίπεδα της γλουταθειόνης αυξάνονται στατιστικά σημαντικά από τις 15 στις 65 ημέρες κατά 99,93%±0,007. Επίσης, παρατηρείται στατιστικά σημαντική αύξηση από τις 42 στις 65 ημέρες κατά 99,93%±0,007. Σύγκριση των πολυφαινολικών ομάδων Συγκρίνοντας τις δύο πολυφαινολικές ομάδες των 42 και 65 ημερών, παρατηρούμε ότι τα επίπεδα της GSH αυξάνονται στατιστικά σημαντικά από τις 42 ημέρες στις 65 ημέρες κατά 99,87%±0,011. Σελίδα 62
63 Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα παρατηρούμε ότι: A. Στις 42 ημέρες παρατηρείται αύξηση της GSH από τα control ζώα στα πολυφαινολικά κατά 27,02%, ωστόσο η αύξηση αυτή δεν είναι στατιστικά σημαντική. B. Στις 65 ημέρες παρατηρείται στατιστικά σημαντική αύξηση της GSH από τα control στα πολυφαινολικά ζώα κατά 101,47% ±0,011. Διάγραμμα 9: Επίπεδα γλουταθειόνης. Σύγκριση των ομάδων control Στις ομάδες control του αίματος, τα επίπεδα της γλουταθειόνης αυξάνονται στατιστικά σημαντικά από τις 15 στις 42 ημέρες κατά 114,50% ± 0,118 καθώς επίσης και από τις 15 στις 65 ημέρες κατά 96,186% ±0,422. Στατιστικά σημαντική αύξηση παρατηρείται και από τις 42 στις 65 ημέρες κατά 281,4% ± 0,422. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες του αίματος, τα επίπεδα της γλουταθειόνης, αυξάνονται στατιστικά σημαντικά από τις 42 στις 65 ημέρες κατά 95,23% ±0,428. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα παρατηρούμε ότι: Α. Στις 42 ημέρες δεν υπάρχουν στατιστικά σημαντικές διαφορές της GSH από τα control ζώα στα πολυφαινολικά καθώς τα επίπεδα της γλουταθειόνης παραμένουν περίπου ίδια. Β. Στις 65 ημέρες παρατηρείται αύξηση στα επίπεδα της γλουταθειόνης από τα control στα πολυφαινολικά ζώα κατά 25,09%, ωστόσο η αύξηση αυτή δεν είναι στατιστικά σημαντική. Σελίδα 63
64 3.2 Επίπεδα TBARS * Διάγραμμα 10: Επίπεδα TBARS. Στατιστικά σημαντική μείωση κατά 26,34% μεταξύ των ομάδων control 65 ημερών και polyphenol 65 ημερών. Σύγκριση των ομάδων control Από το διάγραμμα, παρατηρούμε ότι τα επίπεδα των TBARS μειώνονται στατιστικά σημαντικά από τις 15 στις 42 ημέρες κατά 89,74%±0,415. Επιπλέον, παρατηρείται στατιστικά σημαντική μείωση από τις 15 στις 65 ημέρες κατά 92,01% ± 0,485. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες παρατηρούμε στατιστικά σημαντική μείωση των επιπέδων των TBARS από τις 42 στις 65 ημέρες κατά 99,15% ± 0,789. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα παρατηρούμε ότι: A. Στις 42 ημέρες δεν υπάρχει στατιστικά σημαντική μεταβολή των TBARS από τα control ζώα στα πολυφαινολικά. B. Στις 65 ημέρες τα TBARS μειώνονται στατιστικά σημαντικά κατά 26,34% ± 0,789 από τα control στα πολυφαινολικά ζώα. Σελίδα 64
65 Διάγραμμα 11: Επίπεδα TBARS. Σύγκριση των ομάδων control Από το διάγραμμα, παρατηρούμε ότι τα επίπεδα των TBARS μειώνονται στατιστικά σημαντικά από τις 15 στις 42 ημέρες κατά 96,05% ± 0,415. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες δεν παρατηρούνται στατιστικά σημαντικές μεταβολές. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα, παρατηρούμε ότι: A. Στις 42 ημέρες υπάρχει μείωση κατά 14,80% των TBARS από τα control ζώα στα πολυφαινολικά,ωστόσο η μείωση αυτή δεν είναι στατιστικά σημαντική. B. Στις 65 ημέρες τα TBARS αυξάνονται κατά 17,45% από τα control στα πολυφαινολικά ζώα χωρίς όμως η αύξηση αυτή να είναι στατιστικά σημαντική. Σελίδα 65
66 3.3 Επίπεδα Καταλάσης Διάγραμμα 12: Επίπεδα Καταλάσης Σύγκριση των ομάδων control Από το διάγραμμα, παρατηρούμε ότι τα επίπεδα της καταλάσης μειώνονται στατιστικά σημαντικά από τις 42 στις 65 ημέρες κατά 52,41%±11,388. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες παρατηρούμε μείωση των επιπέδων της καταλάσης από τις 42 στις 65 ημέρες κατά 65,92% ± 22,889. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα, παρατηρούμε ότι: A. Στις 42 ημέρες δεν υπάρχει στατιστικά σημαντική μεταβολή στα επίπεδα της καταλάσης από τα πολυφαινολικά ζώα στα control. B. Στις 65 ημέρες δεν υπάρχουν στατικά σημαντικές μεταβολές. Σελίδα 66
67 * Διάγραμμα 13: Επίπεδα Καταλάσης. Παρατηρείται στατιστικά σημαντική αύξηση της δραστικότητας της καταλάσης στις 42 ημέρες στην πολυφαινολική ομάδα κατά 28,47%. Σύγκριση των ομάδων control Από το διάγραμμα, παρατηρούμε στατιστικά σημαντική αύξηση από τις 42 στις 65 ημέρες κατά 37,23%±7,015. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες δεν παρατηρούνται στατιστικά σημαντικές μεταβολές. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα παρατηρούμε ότι: A. Στις 42 ημέρες παρατηρείται στατιστικά σημαντική αύξηση στις πολυφαινολικές ομάδες σε σχέση με τις ομάδες ελέγχου κατά 28,47% ±5,866. B. Στις 65 ημέρες δεν υπάρχουν στατιστικά σημαντικές μεταβολές στα επίπεδα της καταλάσης από τα control στα πολυφαινολικά ζώα. Σελίδα 67
68 3.4 Επίπεδα πρωτεινικών καρβονυλίων Διάγραμμα 14: Επίπεδα πρωτεϊνικών καρβονυλίων στον ιστό της σπλήνας. Σύγκριση των ομάδων control Τα επίπεδα των καρβονυλίων αυξάνονται στατιστικά σημαντικά από τις 15 στις 42 ημέρες κατά 53,36%±6,849 και από τις 15 στις 65 ημέρες κατά 53,60%±2,520. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες παρατηρούμε ότι οι τιμές των καρβονυλίων στις 42 ημέρες και στις 65 ημέρες δεν είναι στατιστικά σημαντικές. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα, παρατηρούμε ότι: A. Στις 42 ημέρες υπάρχει μείωση των καρβονυλίων κατά 18,75% από τα control ζώα στα πολυφαινολικά η οποία όμως δεν είναι στατιστικά σημαντική. B. Στις 65 ημέρες υπάρχει μείωση των καρβονυλίων από τα control στα πολυφαινολικά ζώα κατά 4,93% η οποία όμως δεν είναι στατιστικά σημαντική. Σελίδα 68
69 CARBS In Plasma Διάγραμμα 15: Επίπεδα πρωτεινικών καρβονυλίων στο αίμα. Σύγκριση των ομάδων control Για τις ομάδες control, τα επίπεδα των καρβονυλίων μειώθηκαν στατιστικά σημαντικά κατά 99,65% ± 0,021 από τις 15 στις 42 ημέρες και κατά 99,71% ± 0,036 από τις 15 στις 65 ημέρες. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες δεν παρατηρήθηκαν στατιστικά σημαντικές μεταβολές ούτε στις 42 ούτε στις 65 ημέρες. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα παρατηρούμε ότι: A. Στις 42 ημέρες δεν υπάρχει στατιστικά σημαντική μεταβολή των καρβονυλίων από τα control ζώα στα πολυφαινολικά. B. Στις 65 ημέρες δεν παρατηρείται στατιστικά σημαντική μεταβολή των καρβονυλίων από τα control στα πολυφαινολικά ζώα. Σελίδα 69
70 3.5 Επίπεδα ολικής αντιοξειδωτικής ικανότητας (TAC) Διάγραμμα 16: Επίπεδα TAC. Σύγκριση των ομάδων control Από το διάγραμμα, παρατηρούμε ότι τα επίπεδα της TAC αυξάνονται στατιστικά σημαντικά κατά 99,07% ± 0,028 από τις 15 στις 42 ημέρες και κατά 99,05% ± 0,027 από τις 42 στις 65 ημέρες. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες δεν παρατηρούμε στατιστικά σημαντικές μεταβολές. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα, παρατηρούμε ότι: A. Στις 42 ημέρες παρατηρήθηκε αύξηση στα επίπεδα της TAC κατά 2,70% από τα control στα πολυφαινολικά ζώα η οποία δεν είναι στατιστικά σημαντική. B. Στις 65 ημέρες παρατηρήθηκε αύξηση στα επίπεδα της TAC κατά 14,27% από τα control στα πολυφαινολικά ζώα η οποία δεν είναι στατιστικά σημαντική. Σελίδα 70
71 Διάγραμμα 17: Επίπεδα της TAC στο πλάσμα του αίματος. Σύγκριση των ομάδων control Από το διάγραμμα, παρατηρούμε στατιστικά σημαντική αύξηση των επιπέδων TAC από τις 15 στις 42 ημέρες κατά 99,4% ±0,026, από τις 42 στις 65 ημέρες κατά 99,2%±0,020 και από τις 15 στις 65 ημέρες κατά 99,2%±0,026. Σύγκριση των πολυφαινολικών ομάδων Στις πολυφαινολικές ομάδες παρατηρούμε στατιστικά σημαντική αύξηση των επιπέδων TAC από τις 42 στις 65 ημέρες κατά 99,15%±0,024. Σύγκριση των ομάδων control με τις πολυφαινολικές ομάδες Από το παραπάνω διάγραμμα, παρατηρούμε ότι: A. Στις 42 ημέρες δεν υπάρχουν στατιστικά σημαντικές διαφορές καθώς παρατηρείται αύξηση κατά 9,16% η οποία δεν είναι στατιστικά σημαντική. B. Στις 65 ημέρες δεν υπάρχουν στατιστικά σημαντικές διαφορές καθώς παρατηρείται αύξηση κατά 6,35% η οποία δεν είναι στατιστικά σημαντική.. Σελίδα 71
72 4.ΣΥΖΗΤΗΣΗ Η παρούσα διπλωματική εργασία πραγματοποιήθηκε με σκοπό να αξιολογηθεί η οξειδοαναγωγική κατάσταση νεαρών προβάτων κρεατοπαραγωγής, Ελληνικής φυλής «Χιώτικα», τα οποία, ανάλογα με την ομάδα στην οποία ανήκαν, εκτρέφονταν με διαφορετικό σιτηρέσιο. H πρώτη ομάδα που αποτελούσε την ομάδα ελέγχου, τρέφονταν με το βασικό σιτηρέσιο ενώ η δεύτερη τρέφονταν με σιτηρέσιο που περιλάμβανε πολυφαινολικά πρόσθετα από στέμφυλα. Συνολικά είκοσι οχτώ (28) πρόβατα χρησιμοποιήθηκαν στα οποία έγιναν τρείς (3) ιστοληψίες σε διαφορετικές χρονικές στιγμές της ανάπτυξής τους, συγκεκριμένα: στις δέκα πέντε (15), σαράντα δύο (42) και εξήντα πέντε (65) ημέρες από τη γέννησή τους. Μέχρι και τις δέκα πέντε (15) ημέρες από τη γέννηση τους, τα πρόβατα τρέφονταν μόνο με μητρικό γάλα. Από εκείνη τη μέρα και μέχρι την τεσσαρακοστή δεύτερη (42) ημέρα, η τροφή τους εκτός από γάλα περιείχε και το σιτηρέσιο απογαλακτισμού. Τέλος, ο πλήρης απογαλακτισμός πραγματοποιήθηκε από την τεσσαρακοστή δεύτερη (42) ημέρα μέχρι και την εξηκοστή πέμπτη (65) ημέρα από τη γέννηση τους. Τα τελευταία χρόνια έντονο ερευνητικό ενδιαφέρον έχει στραφεί προς τις ευεργετικές ιδιότητες εκχυλισμάτων από στέμφυλα λόγω της αντιοξειδωτικής δράσης η οποία βασίζεται κυρίως στην σημαντικά υψηλή περιεκτικότητα τους σε πολυφαινόλες (κατεχίνη, επικατεχίνη, ουριδίνη, γενιστεϊνη, γενιστίνη, τυροσόλη, γαλλικό οξύ, πρωτοκατεχικό οξύ, συριγκικό οξύ, μηλικό οξύ, π-μεθόξυκουμαρικό οξύ, π-κουμαρικό οξύ, τρυγικό οξύ), (Soquet et al., 2000; Vivas et al., 2004; Apostolou et al., 2013). Έρευνες για την ανάκτηση πολυφαινολών από τα υποπροϊόντα της οινοποίησης έχουν κυρίως επικεντρωθεί στα στέμφυλα των κόκκινων σταφυλιών, τα οποία χαρακτηρίζονται από σχετικά υψηλή περιεκτικότητα σε φαινολικές ενώσεις (Nile et al., 2013; Ju and Howard 2005; Kammerer et al., 2005; Spingo et al., 2007). Τα στέμφυλα τα οποία αποτελούνται από τα στερεά μέρη του σταφυλιού, δηλαδή τους βόστρυχους, τους φλοιούς, και τα κουκούτσια (γίγαρτα), είναι η φυτική βιομάζα που προκύπτει κατά τη διαδικασία οινοποίησης, μετά από την πίεση των σταφυλιών για την παραλαβή του μούστου και είναι το κύριο από άποψη όγκου και απομένουσας αξίας υποπροϊόν της οινοποιΐας. Μελέτες που πραγματοποιήθηκαν σε κυτταροκαλλιέργειες έδειξαν ότι εκχύλισμα στεμφύλων, πλούσιο σε πολυφαινόλες, ενισχύει τους ενδοκυττάριους αντιοξειδωτικούς μηχανισμούς όπως αύξηση των επιπέδων της γλουταθειόνης (GSH), επιδρώντας στην οξειδοαναγωγική κατάσταση των κυττάρων, ενώ προσφέρει προστασία υπό την παρουσία του οξειδωτικού παράγοντα t-bhp (Tert-butylhydroperoxide) (Goutzourelas et al., 2014). Οι πολυφαινόλες που εμπεριέχονται στο εκχύλισμα στεμφύλων, διαθέτουν όπως αναφέρθηκε αντιοξειδωτική δράση παρεμποδίζοντας την υπερβολική συσσώρευση των ελεύθερων ριζών. Έτσι, θεωρείται ιδιαίτερα σημαντική η πιθανή συμβολή των αντιοξειδωτικών ουσιών στην ευζωία των ζωικών οργανισμών σε όλα τα στάδια του κύκλου της ζωής τους και είναι ιδιαίτερης σημασίας η δημιουργία βιολειτουργικών ζωοτροφών και η εισαγωγή τους στην καθημερινή διατροφή ειδικότερα στα πρωταρχικά στάδια μετά την γέννηση όπου η φυσική άμυνα του οργανισμού δεν επαρκεί για να διατηρήσει την ισορροπία μεταξύ του οξειδωτικού στρες και των αντιοξειδωτικών μηχανισμών. Στην παρούσα εργασία μελετήθηκαν οι αντιοξειδωτικές επιδράσεις των εκχυλισμάτων στεμφύλων στον ιστό της σπλήνας και στο αίμα νεαρών προβάτων. Ο σπλήνας είναι ένα λεμφοειδές όργανο των ζώων. Αποτελεί αιμοποιητικό όργανο κατά την εμβρυική ζωή καθώς συμμετέχει στην παραγωγή ερυθρών αιμοσφαιρίων ενώ λειτουργεί και ως ηθμός που καθαρίζει το αίμα από γηρασμένα ή παθολογικά ερυθρά αιμοσφαίρια, από έγκλειστα που υπάρχουν εντός των ερυθροκυττάρων και από αντιγόνα και μικροοργανισμούς. Επίσης παίζει σημαντικό ρόλο στη μη ειδική και ειδική ανοσία του οργανισμού, συμμετέχει στο μεταβολισμό του σιδήρου και λειτουργεί ως αποθήκη λευκών αιμοσφαιρίων και αιμοπεταλίων. Σε ορισμένα είδη ζώων, όπως στον ίππο, στο πρόβατο και στο σκύλο, η ικανότητα του σπλήνα για αποθήκευση ερυθροκυττάρων είναι σημαντικά μεγάλη. Έτσι σε περίπτωση έντονης μυικής προσπάθειας, ο σπλήνας συσπάται ελευθερώνοντας στην κυκλοφορία του αίματος μια συμπυκνωμένη μάζα ερυθροκυττάρων. Επιπλέον, ο σπλήνας είναι τόπος καταστροφής των ερυθροκυττάρων και συμμετέχει στο σχηματισμό χολοχρωστικών. Ο σπλήνας, όμως, δεν είναι ένα Σελίδα 72
73 τελείως απαραίτητο για τη ζωή όργανο. Στους ενήλικους οργανισμούς (όχι όμως και στους νεαρούς) μπορεί να αφαιρεθεί χωρίς σημαντικές επιπτώσεις στον οργανισμό καθώς οι λειτουργίες του αναλαμβάνονται από άλλους ιστούς. Στα μηρυκαστικά υπάρχουν ορισμένα γάγγλια (αιμογάγγλια) με ιστολογική δομή και ίσως και λειτουργία όμοια με εκείνη του σπλήνα. Στα γάγγλια αυτά παράγονται ερυθροκύτταρα κατά την εμβρυική ζωή και ουδετερόφιλα, εωσινόφιλα και βασεόφιλα κατά τη μετεμβρυική ζωή (Αθ.Σμοκοβίτη: Φυσιολογία, έκδοση 2007). Εικόνα 19: Απεικόνιση του σπλήνα και οι βασικές λειτουργίες του. Το αίμα αποτελείται από το πλάσμα (άμορφο συστατικό), μέσα στο οποίο εναιωρούνται τα ερυθρά αιμοσφαίρια, τα λευκά αιμοσφαίρια και τα αιμοπετάλια. Το αίμα περιέχει αέρια όπως το οξυγόνο, το διοξείδιο του άνθρακα και το άζωτο και μεταφέρει επίσης σε μικρές ποσότητες μια μεγάλη ποικιλία διαλυμένων χημικών ουσιών, στις οποίες περιλαμβάνονται υδατάνθρακες (γλυκόζη), πρωτεΐνες (λευκώματα), ορμόνες, λίπη και αζωτούχες ενώσεις. Το αίμα αποτελείται κατά 22 % από στερεά και κατά 78 % από νερό. Το πιο σημαντικό από τα λευκώματα που μεταφέρει το αίμα είναι η αιμοσφαιρίνη, η οποία είναι μια είναι μεταλλοπρωτεΐνη με σίδηρο, που περιέχεται στα ερυθρά αιμοσφαίρια. Η λειτουργία που επιτελεί στα περισσότερα θηλαστικά είναι αυτή της μεταφοράς οξυγόνου από τους πνεύμονες στο υπόλοιπο σώμα και διοξειδίου του άνθρακα από το σώμα στους πνεύμονες. (Αθ.Σμοκοβίτη: Φυσιολογία, έκδοση 2007). Εικόνα 20 : Απεικόνιση αιμοσφαιρίνης και ερυθρών αιμοσφαιρίων. Σελίδα 73
Οξειδωτικό Stress, άσκηση και υπερπροπόνηση
 Οξειδωτικό Stress, άσκηση και υπερπροπόνηση Τζιαμούρτας Ζ. Αθανάσιος Επίκουρος Καθηγητής Βιοχημείας της Άσκησης, ΠΘ Ερευνητής, Ινστιτούτο Σωματικής Απόδοσης και Αποκατάστασης Οξειδωτικό στρες Γενικός όρος
Οξειδωτικό Stress, άσκηση και υπερπροπόνηση Τζιαμούρτας Ζ. Αθανάσιος Επίκουρος Καθηγητής Βιοχημείας της Άσκησης, ΠΘ Ερευνητής, Ινστιτούτο Σωματικής Απόδοσης και Αποκατάστασης Οξειδωτικό στρες Γενικός όρος
Ελεύθερες ρίζες και αντιοξειδωτικά
 Ελεύθερες ρίζες και αντιοξειδωτικά Κατά τη διάρκεια των φυσιολογικών ανθρώπινων διεργασιών παραγωγή ενέργειας, αποτοξίνωση από τοξικές ουσίες και ανοσολογική απόκριση, παράγονται από τον οργανισµό ελεύθερες
Ελεύθερες ρίζες και αντιοξειδωτικά Κατά τη διάρκεια των φυσιολογικών ανθρώπινων διεργασιών παραγωγή ενέργειας, αποτοξίνωση από τοξικές ουσίες και ανοσολογική απόκριση, παράγονται από τον οργανισµό ελεύθερες
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΦΥΣΙΚΗΣ ΑΓΩΓΗΣ & ΑΘΛΗΤΙΣΜΟΥ. 9η Διάλεξη: «Άσκηση και ελεύθερες ρίζες»
 ΕΠΕΑΕΚ ΑΝΑΜΟΡΦΩΣΗ ΤΟΥ ΠΡΟΓΡΑΜΜΑΤΟΣ ΣΠΟΥΔΩΝ ΤΟΥ Τ.Ε.Φ.Α.Α.ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΙΑΣ - ΑΥΤΕΠΙΣΤΑΣΙΑ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΦΥΣΙΚΗΣ ΑΓΩΓΗΣ & ΑΘΛΗΤΙΣΜΟΥ ΚΕ 0918 «Βιοχημική Αξιολόγηση Αθλητών»
ΕΠΕΑΕΚ ΑΝΑΜΟΡΦΩΣΗ ΤΟΥ ΠΡΟΓΡΑΜΜΑΤΟΣ ΣΠΟΥΔΩΝ ΤΟΥ Τ.Ε.Φ.Α.Α.ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΙΑΣ - ΑΥΤΕΠΙΣΤΑΣΙΑ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΦΥΣΙΚΗΣ ΑΓΩΓΗΣ & ΑΘΛΗΤΙΣΜΟΥ ΚΕ 0918 «Βιοχημική Αξιολόγηση Αθλητών»
Institutional Repository - Library & Information Centre - University of Thessaly 28/12/ :57:59 EET
 ΤΡΙΜΕΛΗΣ ΕΠΙΤΡΟΠΗ 1. Δημήτριος Κουρέτας (επιβλέπων): Καθηγητής Φυσιολογίας Ζωικών Οργανισμών - Τοξικολογίας του Τμήματος Βιοχημείας & Βιοτεχνολογίας του Πανεπιστημίου Θεσσαλίας. 2. Δημήτριος Στάγκος: Επίκουρος
ΤΡΙΜΕΛΗΣ ΕΠΙΤΡΟΠΗ 1. Δημήτριος Κουρέτας (επιβλέπων): Καθηγητής Φυσιολογίας Ζωικών Οργανισμών - Τοξικολογίας του Τμήματος Βιοχημείας & Βιοτεχνολογίας του Πανεπιστημίου Θεσσαλίας. 2. Δημήτριος Στάγκος: Επίκουρος
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ: «ΜΕΛΕΤΗ ΔΕΙΚΤΩΝ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΜΥΙΚΑ ΚΥΤΤΑΡΑ ΠΟΝΤΙΚΟΥ, ΕΠΕΙΤΑ ΑΠΟ ΧΟΡΗΓΗΣΗ ΕΚΧΥΛΙΣΜΑΤΩΝ ΑΠΟ ΒΟΣΤΡΥΧΟΥΣ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ: «ΜΕΛΕΤΗ ΔΕΙΚΤΩΝ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΜΥΙΚΑ ΚΥΤΤΑΡΑ ΠΟΝΤΙΚΟΥ, ΕΠΕΙΤΑ ΑΠΟ ΧΟΡΗΓΗΣΗ ΕΚΧΥΛΙΣΜΑΤΩΝ ΑΠΟ ΒΟΣΤΡΥΧΟΥΣ
ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΕΙΣΑΓΩΓΗ. Θερινό εξάμηνο ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων
 ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΕΙΣΑΓΩΓΗ Θερινό εξάμηνο 2015 Αριστοτέλης Χ. Παπαγεωργίου Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων
ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΕΙΣΑΓΩΓΗ Θερινό εξάμηνο 2015 Αριστοτέλης Χ. Παπαγεωργίου Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ
 ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-CoA Αναπνευστική Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-CoA Αναπνευστική Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική
Πηγή: ΑΠΟΛΥΜΑΝΣΗ ΤΟΥ ΠΟΣΙΜΟΥ ΝΕΡΟΥ : ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΤΟΥ ΧΛΩΡΙΟΥ, ΘΕΟΔΩΡΑΤΟΥ ΑΓΓΕΛΙΚΗ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ, ΜΥΤΙΛΗΝΗ 2005
 Πηγή: ΑΠΟΛΥΜΑΝΣΗ ΤΟΥ ΠΟΣΙΜΟΥ ΝΕΡΟΥ : ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΤΟΥ ΧΛΩΡΙΟΥ, ΘΕΟΔΩΡΑΤΟΥ ΑΓΓΕΛΙΚΗ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ, ΜΥΤΙΛΗΝΗ 2005 ΠΡΟΧΩΡΗΜΕΝΕΣ ΤΕΧΝΙΚΕΣ ΟΞΕΙΔΩΣΗΣ 1 ΕΙΣΑΓΩΓΗ Οι προχωρημένες τεχνικές
Πηγή: ΑΠΟΛΥΜΑΝΣΗ ΤΟΥ ΠΟΣΙΜΟΥ ΝΕΡΟΥ : ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΤΟΥ ΧΛΩΡΙΟΥ, ΘΕΟΔΩΡΑΤΟΥ ΑΓΓΕΛΙΚΗ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ, ΜΥΤΙΛΗΝΗ 2005 ΠΡΟΧΩΡΗΜΕΝΕΣ ΤΕΧΝΙΚΕΣ ΟΞΕΙΔΩΣΗΣ 1 ΕΙΣΑΓΩΓΗ Οι προχωρημένες τεχνικές
ΟΞΕΙΔΩΤΙΚΗ ΦΩΣΦΟΡΥΛΙΩΣΗ Ι Η ΑΝΑΠΝΕΥΣΤΙΚΗ ΑΛΥΣΙΔΑ
 ΟΞΕΙΔΩΤΙΚΗ ΦΩΣΦΟΡΥΛΙΩΣΗ Ι Η ΑΝΑΠΝΕΥΣΤΙΚΗ ΑΛΥΣΙΔΑ Σύνοψη: Οξειδωτική Φωσφορυλίωση Σύνοψη: Αναπνευστική αλυσίδα (μεταφοράς ηλεκτρονίων) Οξειδωτική φωσφορυλίωση Τι είναι; Οξειδωτική φωσφορυλίωση Τι είναι;
ΟΞΕΙΔΩΤΙΚΗ ΦΩΣΦΟΡΥΛΙΩΣΗ Ι Η ΑΝΑΠΝΕΥΣΤΙΚΗ ΑΛΥΣΙΔΑ Σύνοψη: Οξειδωτική Φωσφορυλίωση Σύνοψη: Αναπνευστική αλυσίδα (μεταφοράς ηλεκτρονίων) Οξειδωτική φωσφορυλίωση Τι είναι; Οξειδωτική φωσφορυλίωση Τι είναι;
Τμήμα Βιοχημείας & Βιοτεχνολογίας Πανεπιστήμιο Θεσσαλίας
 Τμήμα Βιοχημείας & Βιοτεχνολογίας Πανεπιστήμιο Θεσσαλίας ΜΕΛΕΤΗ ΤΗΣ ΕΠΙΔΡΑΣΗΣ ΠΟΛΥΦΑΙΝΟΛΙΚΟΥ ΕΚΧΥΛΙΣΜΑΤΟΣ ΣΤΕΜΦΥΛΩΝ ΣΕ ΔΕΙΚΤΕΣ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΜΥΙΚΑ ΚΑΙ ΕΝΔΟΘΗΛΙΑΚΑ ΚΥΤΤΑΡΑ ΜΕ ΚΥΤΤΑΡΟΜΕΤΡΙΑΣ ΡΟΗΣ
Τμήμα Βιοχημείας & Βιοτεχνολογίας Πανεπιστήμιο Θεσσαλίας ΜΕΛΕΤΗ ΤΗΣ ΕΠΙΔΡΑΣΗΣ ΠΟΛΥΦΑΙΝΟΛΙΚΟΥ ΕΚΧΥΛΙΣΜΑΤΟΣ ΣΤΕΜΦΥΛΩΝ ΣΕ ΔΕΙΚΤΕΣ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΜΥΙΚΑ ΚΑΙ ΕΝΔΟΘΗΛΙΑΚΑ ΚΥΤΤΑΡΑ ΜΕ ΚΥΤΤΑΡΟΜΕΤΡΙΑΣ ΡΟΗΣ
Άσκηση, Οξειδωτικό στρες και ανοσιακό σύστημα. Θανάσης Ζ. Τζιαμούρτας Αναπληρωτής Καθηγητής Βιοχημείας της Άσκησης
 Άσκηση, Οξειδωτικό στρες και ανοσιακό σύστημα Θανάσης Ζ. Τζιαμούρτας Αναπληρωτής Καθηγητής Βιοχημείας της Άσκησης Θέματα παρουσίασης Λοιμώξεις του ανώτερου αναπνευστικού συστήματος (URTI) και άσκηση (γιατί;)
Άσκηση, Οξειδωτικό στρες και ανοσιακό σύστημα Θανάσης Ζ. Τζιαμούρτας Αναπληρωτής Καθηγητής Βιοχημείας της Άσκησης Θέματα παρουσίασης Λοιμώξεις του ανώτερου αναπνευστικού συστήματος (URTI) και άσκηση (γιατί;)
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C.
 Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Κεφαλαίο 3 ο. Μεταβολισμός. Ενέργεια και οργανισμοί
 Κεφαλαίο 3 ο Μεταβολισμός Ενέργεια και οργανισμοί Η ενέργεια είναι απαρέτητη σε όλους τους οργανισμούς και την εξασφαλίζουν από το περιβάλλον τους.παρόλα αυτά, συνήθως δεν μπορούν να την χρησιμοποιήσουν
Κεφαλαίο 3 ο Μεταβολισμός Ενέργεια και οργανισμοί Η ενέργεια είναι απαρέτητη σε όλους τους οργανισμούς και την εξασφαλίζουν από το περιβάλλον τους.παρόλα αυτά, συνήθως δεν μπορούν να την χρησιμοποιήσουν
Συνδυάζοντας το πρώτο και το δεύτερο θερμοδυναμικό αξίωμα προκύπτει ότι:
 Συνδυάζοντας το πρώτο και το δεύτερο θερμοδυναμικό αξίωμα προκύπτει ότι: Για να είναι μια αντίδραση αυθόρμητη, πρέπει η μεταβολή της ελεύθερης ενέργειας της αντίδρασης να είναι αρνητική. Η μεταβολή της
Συνδυάζοντας το πρώτο και το δεύτερο θερμοδυναμικό αξίωμα προκύπτει ότι: Για να είναι μια αντίδραση αυθόρμητη, πρέπει η μεταβολή της ελεύθερης ενέργειας της αντίδρασης να είναι αρνητική. Η μεταβολή της
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Μελέτη επίδρασης της αιγοπρόβειας πρωτεΐνης ορού γάλακτος σε δείκτες οξειδωτικού στρες σε ενδοθηλιακά κύτταρα EA.hy926
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Μελέτη επίδρασης της αιγοπρόβειας πρωτεΐνης ορού γάλακτος σε δείκτες οξειδωτικού στρες σε ενδοθηλιακά κύτταρα EA.hy926
ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ASSESSMENT OF OXIDATIVE STRESS MARKERS IN TISSUES ( LIVER-SPLEEN) FROM SHEEPS CONSUMED FEED WITH OLIVE MILL WASTEWATERS ΣΑΒΒΑ ΣΑΛΩΜΗ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΔΕΙΚΤΩΝ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΙΣΤΟΥΣ (ΗΠΑΡ ΚΑΙ ΣΠΛΗΝΑ) ΑΠΟ ΝΕΑΡΑ ΠΡΟΒΑΤΑΚΡΕΑΤΟΠΑΡΑΓΩΓΗΣ ΜΕΤΑ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΔΕΙΚΤΩΝ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΙΣΤΟΥΣ (ΗΠΑΡ ΚΑΙ ΣΠΛΗΝΑ) ΑΠΟ ΝΕΑΡΑ ΠΡΟΒΑΤΑΚΡΕΑΤΟΠΑΡΑΓΩΓΗΣ ΜΕΤΑ
BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι. ΒΙΟΧΗΜΕΙΑ (Lubert Stryer)
 BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 17.1 Η πυροσταφυλική αφυδρογονάση συνδέει τη γλυκόλυση με τον κύκλο του κιτρικού οξέος 17.2 O κύκλος του κιτρικού οξέος οξειδώνει μονάδες δύο ατόμων
BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 17.1 Η πυροσταφυλική αφυδρογονάση συνδέει τη γλυκόλυση με τον κύκλο του κιτρικού οξέος 17.2 O κύκλος του κιτρικού οξέος οξειδώνει μονάδες δύο ατόμων
Καθηγητής Δ. Μόσιαλος
 Μικροβιολογία-Ιολογία Επίκουρος Καθηγητής Καθηγητής Δ. Μόσιαλος Βιοενεργητική μικροβίων Βακτηριακή Γενετική Επισκόπηση Βακτηριοφάγων Προκαρυωτική ποικιλότητα (Βακτήρια) Προκαρυωτική ποικιλότητα (Αρχαία)
Μικροβιολογία-Ιολογία Επίκουρος Καθηγητής Καθηγητής Δ. Μόσιαλος Βιοενεργητική μικροβίων Βακτηριακή Γενετική Επισκόπηση Βακτηριοφάγων Προκαρυωτική ποικιλότητα (Βακτήρια) Προκαρυωτική ποικιλότητα (Αρχαία)
ΒΙΟΧΗΜΕΙΑ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ. Στοιχείο O C H N Ca P K S Na Mg περιεκτικότητα % ,5 1 0,35 0,25 0,15 0,05
 ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ
 ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΚΕΦΑΛΑΙΟ 4. Κυτταρική αναπνοή: Ο διαχειριστής της ενέργειας και των σκελετών άνθρακα
 ΚΕΦΑΛΑΙΟ 4 Κυτταρική αναπνοή: Ο διαχειριστής της ενέργειας και των σκελετών άνθρακα Η πορεία σχηματισμού του αμύλου στους χλωροπλάστες και της σακχαρόζης στο κυτταρόπλασμα Η πορεία σχηματισμού του αμύλου
ΚΕΦΑΛΑΙΟ 4 Κυτταρική αναπνοή: Ο διαχειριστής της ενέργειας και των σκελετών άνθρακα Η πορεία σχηματισμού του αμύλου στους χλωροπλάστες και της σακχαρόζης στο κυτταρόπλασμα Η πορεία σχηματισμού του αμύλου
BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ
 BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 1. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 2. BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ Ι. ΑΤΟΜΑ ΚΑΙ ΜΟΡΙΑ ΙΙ. ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΙΙΙ. ΜΑΚΡΟΜΟΡΙΑ ΣΤΑ ΚΥΤΤΑΡΑ
BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 1. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 2. BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ Ι. ΑΤΟΜΑ ΚΑΙ ΜΟΡΙΑ ΙΙ. ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΙΙΙ. ΜΑΚΡΟΜΟΡΙΑ ΣΤΑ ΚΥΤΤΑΡΑ
BIOΛ154 ΒΙΟΧΗΜΕΙΑ. ΒΙΟΧΗΜΕΙΑ (Lubert Stryer)
 BIOΛ154 ΒΙΟΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 18.1 H οξειδωτική φωσφορυλίωση στους ευκαρυωτικούς οργανισμούς λαμβάνει χώρα στα μιτοχόνδρια. 18.2 H οξειδωτική φωσφορυλίωση εξαρτάται από τη μεταφορά
BIOΛ154 ΒΙΟΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 18.1 H οξειδωτική φωσφορυλίωση στους ευκαρυωτικούς οργανισμούς λαμβάνει χώρα στα μιτοχόνδρια. 18.2 H οξειδωτική φωσφορυλίωση εξαρτάται από τη μεταφορά
ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΟΞΕΙΔΩΤΙΚΗΣ ΔΡΑΣΗΣ ΤΗΣ ΑΙΓΟΠΡΟΒΕΙΑΣ ΠΡΩΤΕΪΝΗΣ ΤΥΡΟΓΑΛΑΚΤΟΣ IN VITRO KAI ΣΤΗΝ ΚΥΤΤΑΡΙΚΗ ΣΕΙΡΑ C2C12
 Τμήμα Βιοχημείας & Βιοτεχνολογίας Πανεπιστήμιο Θεσσαλίας ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΟΞΕΙΔΩΤΙΚΗΣ ΔΡΑΣΗΣ ΤΗΣ ΑΙΓΟΠΡΟΒΕΙΑΣ ΠΡΩΤΕΪΝΗΣ ΤΥΡΟΓΑΛΑΚΤΟΣ IN VITRO KAI ΣΤΗΝ ΚΥΤΤΑΡΙΚΗ ΣΕΙΡΑ C2C12 Ευθαλία Κερασιώτη, Αλέξανδρος
Τμήμα Βιοχημείας & Βιοτεχνολογίας Πανεπιστήμιο Θεσσαλίας ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΟΞΕΙΔΩΤΙΚΗΣ ΔΡΑΣΗΣ ΤΗΣ ΑΙΓΟΠΡΟΒΕΙΑΣ ΠΡΩΤΕΪΝΗΣ ΤΥΡΟΓΑΛΑΚΤΟΣ IN VITRO KAI ΣΤΗΝ ΚΥΤΤΑΡΙΚΗ ΣΕΙΡΑ C2C12 Ευθαλία Κερασιώτη, Αλέξανδρος
9/5/2015. Απαραίτητα θρεπτικά στοιχεία για τα φυτά
 Δηµοκρίτειο Πανεπιστήµιο Θράκης Τµήµα Αγροτικής Ανάπτυξης ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ «Θρεπτικά στοιχεία» Θρεπτικές ουσίες Απαραίτητα θρεπτικά στοιχεία για την αύξηση των φυτών: Μακροστοιχεία: C, H, O, N, P, S, K,
Δηµοκρίτειο Πανεπιστήµιο Θράκης Τµήµα Αγροτικής Ανάπτυξης ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ «Θρεπτικά στοιχεία» Θρεπτικές ουσίες Απαραίτητα θρεπτικά στοιχεία για την αύξηση των φυτών: Μακροστοιχεία: C, H, O, N, P, S, K,
Hans Krebs ( ) Κύκλος του κιτρικού οξέος και οξειδωτική φωσφορυλίωση
 Hans Krebs (1900-1981) Κύκλος του κιτρικού οξέος και οξειδωτική φωσφορυλίωση 10.1. Μ σημασία του κύκλου του κιτρικού οξέος Όπως είδαμε στο προηγούμενο κεφάλαιο κατά τη γλυκολυτική πορεία η γλυκόζη μετατρέπεται
Hans Krebs (1900-1981) Κύκλος του κιτρικού οξέος και οξειδωτική φωσφορυλίωση 10.1. Μ σημασία του κύκλου του κιτρικού οξέος Όπως είδαμε στο προηγούμενο κεφάλαιο κατά τη γλυκολυτική πορεία η γλυκόζη μετατρέπεται
ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΠΕΡΙΛΗΨΗ ΚΕΦΑΛΑΙΟΥ 3
 ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΠΕΡΙΛΗΨΗ ΚΕΦΑΛΑΙΟΥ 3 Το θέμα που απασχολεί το κεφάλαιο σε όλη του την έκταση είναι ο μεταβολισμός και χωρίζεται σε τέσσερις υποκατηγορίες: 3.1)Ενέργεια και οργανισμοί,
ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΠΕΡΙΛΗΨΗ ΚΕΦΑΛΑΙΟΥ 3 Το θέμα που απασχολεί το κεφάλαιο σε όλη του την έκταση είναι ο μεταβολισμός και χωρίζεται σε τέσσερις υποκατηγορίες: 3.1)Ενέργεια και οργανισμοί,
Β. ΚΑΜΙΝΕΛΛΗΣ ΒΙΟΛΟΓΙΑ. Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα).
 ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ. π. Αναστάσιος Ισαάκ Λύκειο Παραλιμνίου Δεκέμβριος 2013 www.biomathia.webnode.gr
 π. Αναστάσιος Ισαάκ Λύκειο Παραλιμνίου Δεκέμβριος 2013 www.biomathia.webnode.gr EΞΕΤΑΣΤΕΑ ΥΛΗ: ΕΝΟΤΗΤΑ 8: Η ελευθέρωση της ενέργειας, σελ. 155-168 ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ Η κυτταρική αναπνοή είναι η διαδικασία
π. Αναστάσιος Ισαάκ Λύκειο Παραλιμνίου Δεκέμβριος 2013 www.biomathia.webnode.gr EΞΕΤΑΣΤΕΑ ΥΛΗ: ΕΝΟΤΗΤΑ 8: Η ελευθέρωση της ενέργειας, σελ. 155-168 ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ Η κυτταρική αναπνοή είναι η διαδικασία
Ο ρόλος της οξειδάσης της ξανθίνης. στην οξειδοαναγωγική κατάσταση κατά την άσκηση
 Ο ρόλος της οξειδάσης της ξανθίνης στην οξειδοαναγωγική κατάσταση κατά την άσκηση Αριστείδης Σ. Βεσκούκης, PhD Βιοχημικός - Βιοτεχνολόγος Πανεπιστήμιο Θεσσαλίας Τμήμα Βιοχημείας & Βιοτεχνολογίας Εργαστήριο
Ο ρόλος της οξειδάσης της ξανθίνης στην οξειδοαναγωγική κατάσταση κατά την άσκηση Αριστείδης Σ. Βεσκούκης, PhD Βιοχημικός - Βιοτεχνολόγος Πανεπιστήμιο Θεσσαλίας Τμήμα Βιοχημείας & Βιοτεχνολογίας Εργαστήριο
ΕΝΟΤΗΤΑ 8: Η ΕΛΕΥΘΕΡΩΣΗ ΤΗΣ ΕΝΕΡΓΕΙΑΣ 8.2 AΕΡΟΒΙΑ ΑΝΑΠNOH
 1 ΕΝΟΤΗΤΑ 8: Η ΕΛΕΥΘΕΡΩΣΗ ΤΗΣ ΕΝΕΡΓΕΙΑΣ 8.2 AΕΡΟΒΙΑ ΑΝΑΠNOH Οι οργανισμοί για να επιβιώσουν χρειάζονται ενέργεια η οποία παράγεται μέσω μιας διαδικασίας που ονομάζεται κυτταρική αναπνοή. Οι ουσίες που
1 ΕΝΟΤΗΤΑ 8: Η ΕΛΕΥΘΕΡΩΣΗ ΤΗΣ ΕΝΕΡΓΕΙΑΣ 8.2 AΕΡΟΒΙΑ ΑΝΑΠNOH Οι οργανισμοί για να επιβιώσουν χρειάζονται ενέργεια η οποία παράγεται μέσω μιας διαδικασίας που ονομάζεται κυτταρική αναπνοή. Οι ουσίες που
Φ ΣΙ Σ Ο Ι Λ Ο Ο Λ Γ Ο Ι Γ Α
 Δηµοκρίτειο Πανεπιστήµιο Θράκης Τµήµα Αγροτικής Ανάπτυξης ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ «Θρεπτικά στοιχεία» Ορεστιάδα 2017 Απαραίτητο θεωρείται ένα στοιχείο όταν: 1. Η έλλειψη του εµποδίζει την ολοκλήρωση του φυτικού
Δηµοκρίτειο Πανεπιστήµιο Θράκης Τµήµα Αγροτικής Ανάπτυξης ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ «Θρεπτικά στοιχεία» Ορεστιάδα 2017 Απαραίτητο θεωρείται ένα στοιχείο όταν: 1. Η έλλειψη του εµποδίζει την ολοκλήρωση του φυτικού
ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΑΝΟΜΟΙΩΣΗ
 ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΑΝΟΜΟΙΩΣΗ Θερινό εξάμηνο 2011 Καταβολισμός ή ανομοίωση Καταβολισμός ή ανομοίωση η σταδιακή και ελεγχόμενη διάσπαση των
ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΑΝΟΜΟΙΩΣΗ Θερινό εξάμηνο 2011 Καταβολισμός ή ανομοίωση Καταβολισμός ή ανομοίωση η σταδιακή και ελεγχόμενη διάσπαση των
Περίληψη Βιολογίας Κεφάλαιο 3
 Περίληψη Βιολογίας Κεφάλαιο 3 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Η σημασία της ενέργειας στους οργανισμούς. Η ενέργεια είναι ένας παράγοντας σημαντικός για τους οργανισμούς γιατί όλες οι λειτουργίες τους απαιτούν
Περίληψη Βιολογίας Κεφάλαιο 3 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Η σημασία της ενέργειας στους οργανισμούς. Η ενέργεια είναι ένας παράγοντας σημαντικός για τους οργανισμούς γιατί όλες οι λειτουργίες τους απαιτούν
3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί οργανισμοί μετατρέπουν την ηλιακή ενέργεια με τη διαδικασία
3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί οργανισμοί μετατρέπουν την ηλιακή ενέργεια με τη διαδικασία
3.1 Ενέργεια και οργανισμοί
 Δημήτρης Η. Β 1 25.3.14 3 Ο Κεφάλαιο 3.1 Ενέργεια και οργανισμοί Η ενέργεια έχει κεντρική σημασία για έναν οργανισμό, γιατί ό,τι και να κάνουμε χρειαζόμαστε ενέργεια. Ο κλάδος της βιολογίας που ασχολείται
Δημήτρης Η. Β 1 25.3.14 3 Ο Κεφάλαιο 3.1 Ενέργεια και οργανισμοί Η ενέργεια έχει κεντρική σημασία για έναν οργανισμό, γιατί ό,τι και να κάνουμε χρειαζόμαστε ενέργεια. Ο κλάδος της βιολογίας που ασχολείται
Εργασία για το μάθημα της Βιολογίας. Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου
 Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
ΟΞΕΙΔΩΤΙΚΟ ΣΤΡΕΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ
 ΟΞΕΙΔΩΤΙΚΟ ΣΤΡΕΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ ΕΛΕΥΘΕΡΕΣ ΡΙΖΕΣ ΩΣ ΕΛΕΥΘΕΡΗ ΡΙΖΑ ΟΡΙΖΕΤΑΙ ΕΝΑ ΜΟΡΙΟ Ή ΑΤΟΜΟ ΠΟΥ ΕΧΕΙ ΕΝΑ Ή ΠΕΡΙΣΣΟΤΕΡΑ ΑΣΥΖΕΥΚΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΟΙΒΑΔΑ ΣΘΕΝΟΥΣ. Αυτό μπορεί να γίνει είτε με
ΟΞΕΙΔΩΤΙΚΟ ΣΤΡΕΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ ΕΛΕΥΘΕΡΕΣ ΡΙΖΕΣ ΩΣ ΕΛΕΥΘΕΡΗ ΡΙΖΑ ΟΡΙΖΕΤΑΙ ΕΝΑ ΜΟΡΙΟ Ή ΑΤΟΜΟ ΠΟΥ ΕΧΕΙ ΕΝΑ Ή ΠΕΡΙΣΣΟΤΕΡΑ ΑΣΥΖΕΥΚΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΟΙΒΑΔΑ ΣΘΕΝΟΥΣ. Αυτό μπορεί να γίνει είτε με
Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου
 Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Τ. ΘΕΟΔΩΡΑ ΤΜΗΜΑ Β3 ΚΕΦΑΛΑΙΟ ΤΡΙΤΟ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Ο όρος ενέργεια σημαίνει δυνατότητα παραγωγής έργου.
Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Τ. ΘΕΟΔΩΡΑ ΤΜΗΜΑ Β3 ΚΕΦΑΛΑΙΟ ΤΡΙΤΟ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Ο όρος ενέργεια σημαίνει δυνατότητα παραγωγής έργου.
1. Να οξειδωθούν και να παράγουν ενέργεια. (ΚΑΤΑΒΟΛΙΣΜΟΣ)
 Θάνος Α. Β1 ΠΕΡΙΛΗΨΗ ΚΕΦΑΛΑΙΟ ΤΡΙΤΟ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί οργανισμοί μετατρέπουν
Θάνος Α. Β1 ΠΕΡΙΛΗΨΗ ΚΕΦΑΛΑΙΟ ΤΡΙΤΟ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί οργανισμοί μετατρέπουν
Εφαρμοσμένη Διατροφική Ιατρική
 Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
gr ΜΟΥΓΙΟΣ Β.
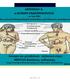 1ο Πανελλήνιο Συνέδριο ΙΒΙΣ «Βιολογία-Ιατρική Συστημάτων & Στρες» Άσκηση και μεταβολικόοξιδωτικό στρες Βασίλης Μούγιος Τμήμα Επιστήμης Φυσικής Αγωγής και Αθλητισμού με έδρα τη Θεσσαλονίκη Αριστοτέλειο
1ο Πανελλήνιο Συνέδριο ΙΒΙΣ «Βιολογία-Ιατρική Συστημάτων & Στρες» Άσκηση και μεταβολικόοξιδωτικό στρες Βασίλης Μούγιος Τμήμα Επιστήμης Φυσικής Αγωγής και Αθλητισμού με έδρα τη Θεσσαλονίκη Αριστοτέλειο
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2016-2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1) Δίνονται τα αμινοξέα σερίνη, αλανίνη, γλουταμικό, κυστεΐνη, λυσίνη, αργινίνη, διαχωρίστε τα
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2016-2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1) Δίνονται τα αμινοξέα σερίνη, αλανίνη, γλουταμικό, κυστεΐνη, λυσίνη, αργινίνη, διαχωρίστε τα
Ασκησιογενές οξειδωτικό και αναγωγικό στρες: το ζήτημα των βιοδεικτών Αριστείδης Βεσκούκης, Ph.D Βιοχημικός & Βιοτεχνολόγος
 Ασκησιογενές οξειδωτικό και αναγωγικό στρες: το ζήτημα των βιοδεικτών Αριστείδης Βεσκούκης, Ph.D Βιοχημικός & Βιοτεχνολόγος Email: veskoukis@uth.gr Προσωπική ιστοσελίδα: http://veskoukis.weebly.com Θεσσαλονίκη,
Ασκησιογενές οξειδωτικό και αναγωγικό στρες: το ζήτημα των βιοδεικτών Αριστείδης Βεσκούκης, Ph.D Βιοχημικός & Βιοτεχνολόγος Email: veskoukis@uth.gr Προσωπική ιστοσελίδα: http://veskoukis.weebly.com Θεσσαλονίκη,
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΔΕΙΚΤΩΝ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΙΣΤΟΥΣ (ΚΑΡΔΙΑ- ΗΠΑΡ) ΑΠΟ ΝΕΑΡΑ ΠΡΟΒΑΤΑ ΚΡΕΑΤΟΠΑΡΑΓΩΓΗΣ ΜΕΤΑ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΔΕΙΚΤΩΝ ΟΞΕΙΔΩΤΙΚΟΥ ΣΤΡΕΣ ΣΕ ΙΣΤΟΥΣ (ΚΑΡΔΙΑ- ΗΠΑΡ) ΑΠΟ ΝΕΑΡΑ ΠΡΟΒΑΤΑ ΚΡΕΑΤΟΠΑΡΑΓΩΓΗΣ ΜΕΤΑ
Θρέψη Φυτών. Ενότητα 9 η Οι ενεργές μορφές οξυγόνου στα φυτά
 Θρέψη Φυτών Ενότητα 9 η Οι ενεργές μορφές οξυγόνου στα φυτά Όνομα καθηγητή: Δ. Μπουράνης Όνομα καθηγητή: Σ. Χωριανοπούλου Τμήμα: Επιστήμης Φυτικής Παραγωγής Στόχοι ενότητας 1. Ποιες είναι οι ενεργές μορφές
Θρέψη Φυτών Ενότητα 9 η Οι ενεργές μορφές οξυγόνου στα φυτά Όνομα καθηγητή: Δ. Μπουράνης Όνομα καθηγητή: Σ. Χωριανοπούλου Τμήμα: Επιστήμης Φυτικής Παραγωγής Στόχοι ενότητας 1. Ποιες είναι οι ενεργές μορφές
CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010
 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 Μεγεθυντική ικανότητα και διακριτική ικανότητα ή ανάλυση Μέγιστη ανάλυση
CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 Μεγεθυντική ικανότητα και διακριτική ικανότητα ή ανάλυση Μέγιστη ανάλυση
3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί με εξαίρεση τους φωτοσυνθετικούς εξασφαλίζουν την απαραίτητη ενέργεια διασπώντας θρεπτικές ουσίες που
 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί με εξαίρεση τους φωτοσυνθετικούς εξασφαλίζουν την απαραίτητη ενέργεια διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Αντίθετα οι φωτοσυνθετικοί,
3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί με εξαίρεση τους φωτοσυνθετικούς εξασφαλίζουν την απαραίτητη ενέργεια διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Αντίθετα οι φωτοσυνθετικοί,
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου. Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση:
 KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
ΦΡΟΝΤΙΣΤΗΡΙΟ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΗΡΑΚΛΕΙΤΟΣ
 ΚΩΛΕΤΤΗ 19-21 -10681 210 3824614 210 3847670 www.irakleitos.gr ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β') ΤΕΤΑΡΤΗ 4 ΙΟΥΝΙΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ
ΚΩΛΕΤΤΗ 19-21 -10681 210 3824614 210 3847670 www.irakleitos.gr ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β') ΤΕΤΑΡΤΗ 4 ΙΟΥΝΙΟΥ 2014 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ
ΓΕΝΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ. Μαντώ Κυριακού 2015
 ΓΕΝΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Μαντώ Κυριακού 2015 Ενεργειακό Στα βιολογικά συστήματα η διατήρηση της ενέργειας συμπεριλαμβάνει οξειδοαναγωγικές αντιδράσεις παραγωγή ATP Οξείδωση: απομάκρυνση e από ένα υπόστρωμα
ΓΕΝΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ Μαντώ Κυριακού 2015 Ενεργειακό Στα βιολογικά συστήματα η διατήρηση της ενέργειας συμπεριλαμβάνει οξειδοαναγωγικές αντιδράσεις παραγωγή ATP Οξείδωση: απομάκρυνση e από ένα υπόστρωμα
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01%
 ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΒΙΟΤΕΧΝΟΛΟΓΙΑ - ΠΟΙΟΤΗΤΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΠΕΡΙΒΑΛΛΟΝΤΟΣ»
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΒΙΟΤΕΧΝΟΛΟΓΙΑ - ΠΟΙΟΤΗΤΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΠΕΡΙΒΑΛΛΟΝΤΟΣ» «ΕΠΊΔΡΑΣΗ ΤΗΣ ΠΡΩΤΕΪΝΗΣ ΤΥΡΟΓΆΛΑΚΤΟΣ ΣΤΗΝ ΈΚΦΡΑΣΗ ΤΟΥ ΜΕΤΑΓΡΑΦΙΚΟΎ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΒΙΟΤΕΧΝΟΛΟΓΙΑ - ΠΟΙΟΤΗΤΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΠΕΡΙΒΑΛΛΟΝΤΟΣ» «ΕΠΊΔΡΑΣΗ ΤΗΣ ΠΡΩΤΕΪΝΗΣ ΤΥΡΟΓΆΛΑΚΤΟΣ ΣΤΗΝ ΈΚΦΡΑΣΗ ΤΟΥ ΜΕΤΑΓΡΑΦΙΚΟΎ
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ. 3.1 Ενέργεια και οργανισμοί
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ ΚΕΦΑΛΑΙΟ 3 3.1 Ενέργεια και οργανισμοί Την ενέργεια και τα υλικά που οι οργανισμοί εξασφαλίζουν από το περιβάλλον τους συνήθως δεν μπορούν να τα αξιοποίησουν άμεσα. Η αξιοποίησή τους
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ ΚΕΦΑΛΑΙΟ 3 3.1 Ενέργεια και οργανισμοί Την ενέργεια και τα υλικά που οι οργανισμοί εξασφαλίζουν από το περιβάλλον τους συνήθως δεν μπορούν να τα αξιοποίησουν άμεσα. Η αξιοποίησή τους
Μεταβολισμός του γλυκογόνου. Μεταβολισμός των υδατανθράκων κατά την άσκηση. Από που προέρχεται το μυϊκό και ηπατικό γλυκογόνο;
 Μεταβολισμός των υδατανθράκων κατά την άσκηση Μεταβολισμός του γλυκογόνου Το γλυκογόνο είναι ο αφθονότερος υδατάνθρακας των ζώων Το γλυκογόνο αποθηκεύεται κυρίως στο ήπαρ (3-7% κατά βάρος) και στους μύες
Μεταβολισμός των υδατανθράκων κατά την άσκηση Μεταβολισμός του γλυκογόνου Το γλυκογόνο είναι ο αφθονότερος υδατάνθρακας των ζώων Το γλυκογόνο αποθηκεύεται κυρίως στο ήπαρ (3-7% κατά βάρος) και στους μύες
CO 2 H 2 O O 2 C 6 H 12 O 6 ATP ADP DNA NADPH - TAC AAA CAT CCC GGG TTT ATT
 ΘΕΜΑ ο Α. (Μ 5) Ποιο φαινόµενο ονοµάζεται «µετουσίωση των πρωτεινών»; Να αναφέρεις ένα παράδειγµα. Β. (Μ 5) Να περιγράψεις το φαινόµενο της «ενδοκύττωσης» Γ. (Μ 5) Στις παρακάτω ερωτήσεις -5 να γράψεις
ΘΕΜΑ ο Α. (Μ 5) Ποιο φαινόµενο ονοµάζεται «µετουσίωση των πρωτεινών»; Να αναφέρεις ένα παράδειγµα. Β. (Μ 5) Να περιγράψεις το φαινόµενο της «ενδοκύττωσης» Γ. (Μ 5) Στις παρακάτω ερωτήσεις -5 να γράψεις
KΕΦΑΛΑΙΟ 3ο Μεταβολισμός. Ενότητα 3.1: Ενέργεια και Οργανισμοί Ενότητα 3.2: Ένζυμα - Βιολογικοί Καταλύτες
 KΕΦΑΛΑΙΟ 3ο Μεταβολισμός Ενότητα 3.1: Ενέργεια και Οργανισμοί Ενότητα 3.2: Ένζυμα - Βιολογικοί Καταλύτες Να συμπληρώσετε με τους κατάλληλους όρους τα κενά στις παρακάτω προτάσεις: 1. Ο καταβολισμός περιλαμβάνει
KΕΦΑΛΑΙΟ 3ο Μεταβολισμός Ενότητα 3.1: Ενέργεια και Οργανισμοί Ενότητα 3.2: Ένζυμα - Βιολογικοί Καταλύτες Να συμπληρώσετε με τους κατάλληλους όρους τα κενά στις παρακάτω προτάσεις: 1. Ο καταβολισμός περιλαμβάνει
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 2 Η ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ ΚΑΙ ΟΞΕΙΔΩΤΙΚΗ ΦΩΣΦΟΡΥΛΙΩΣΗ 1 Κυτταρική αναπνοή Ως κυτταρική αναπνοή αναφέρεται η διαδικασία στα κύτταρα κατά την οποία πολύπλοκα οργανικά μόρια,
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 2 Η ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ ΚΑΙ ΟΞΕΙΔΩΤΙΚΗ ΦΩΣΦΟΡΥΛΙΩΣΗ 1 Κυτταρική αναπνοή Ως κυτταρική αναπνοή αναφέρεται η διαδικασία στα κύτταρα κατά την οποία πολύπλοκα οργανικά μόρια,
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ ΕΝΟΤΗΤΑ: ΕΝΖΥΜΑ ΚΑΘΗΓΗΤΗΣ: ΠΑΤΗΡ ΑΝΑΣΤΑΣΙΟΣ ΙΣΑΑΚ 1. Να εξηγήσετε γιατί πολλές βιταμίνες, παρά τη μικρή συγκέντρωσή τους στον οργανισμό, είναι πολύ σημαντικές για
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ ΕΝΟΤΗΤΑ: ΕΝΖΥΜΑ ΚΑΘΗΓΗΤΗΣ: ΠΑΤΗΡ ΑΝΑΣΤΑΣΙΟΣ ΙΣΑΑΚ 1. Να εξηγήσετε γιατί πολλές βιταμίνες, παρά τη μικρή συγκέντρωσή τους στον οργανισμό, είναι πολύ σημαντικές για
Τα χημικά στοιχεία που είναι επικρατέστερα στους οργανισμούς είναι: i..
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
Β α σ ι κ έ ς α ρ χ έ ς μ ε τ α β ο λ ι σ μ ο ύ
 Β α σ ι κ έ ς α ρ χ έ ς μ ε τ α β ο λ ι σ μ ο ύ 7.1. Εισαγωγή Εάν παρατηρήσουμε τις δραστηριότητες των διάφορων ειδών του ζωικού βασιλείου, μπορούμε εύκολα να καταλήξουμε στο συμπέρασμα ότι όλα τα είδη
Β α σ ι κ έ ς α ρ χ έ ς μ ε τ α β ο λ ι σ μ ο ύ 7.1. Εισαγωγή Εάν παρατηρήσουμε τις δραστηριότητες των διάφορων ειδών του ζωικού βασιλείου, μπορούμε εύκολα να καταλήξουμε στο συμπέρασμα ότι όλα τα είδη
Χαλκός Cu. Στοιχείο µετάπτωσης, µέταλλο. Στο κυτταρικό περιβάλλον βρίσκεται σε δύο µορφές οξείδωσης. Cu + ανηγµένος χαλκός. Cu 2+ οξειδωµένος χαλκός
 Χαλκός Cu Στοιχείο µετάπτωσης, µέταλλο Στο κυτταρικό περιβάλλον βρίσκεται σε δύο µορφές οξείδωσης Cu + ανηγµένος χαλκός Cu 2+ οξειδωµένος χαλκός Είναι µαλακό οξύ προτιµά να προσαρτάται σε µαλακούς υποκαταστάτες
Χαλκός Cu Στοιχείο µετάπτωσης, µέταλλο Στο κυτταρικό περιβάλλον βρίσκεται σε δύο µορφές οξείδωσης Cu + ανηγµένος χαλκός Cu 2+ οξειδωµένος χαλκός Είναι µαλακό οξύ προτιµά να προσαρτάται σε µαλακούς υποκαταστάτες
Θέματα Διάλεξης. James Bond και Ελεύθερες Ρίζες. Το οξυγόνο στη γη. Το Ο 2 είναι τοξικό. Οξειδωτικό στρες. Επίδραση της άσκησης στο οξειδωτικό Stress
 Επίδραση της άσκησης στο οξειδωτικό Stress Θέματα Διάλεξης James Bond και Ελεύθερες Ρίζες Το οξυγόνο στη γη Επίπεδα 2 οξυγόνου στην ατμόσφαιρα % Ραγδαία αύξηση της συγκέντρωσης του ατμοσφαιρικού οξυγόνου
Επίδραση της άσκησης στο οξειδωτικό Stress Θέματα Διάλεξης James Bond και Ελεύθερες Ρίζες Το οξυγόνο στη γη Επίπεδα 2 οξυγόνου στην ατμόσφαιρα % Ραγδαία αύξηση της συγκέντρωσης του ατμοσφαιρικού οξυγόνου
Κεφάλαιο 4. Copyright The McGraw-Hill Companies, Inc Utopia Publishing, All rights reserved
 Κεφάλαιο 4 Copyright The McGraw-Hill Companies, Inc. Οι νόμοι της Θερμοδυναμικής 1 ος Νόμος της θερμοδυναμικής (αρχή διατήρησης της ενέργειας) Η ενέργεια δεν δημιουργείται ούτε καταστρέφεται Αλλάζει μορφή
Κεφάλαιο 4 Copyright The McGraw-Hill Companies, Inc. Οι νόμοι της Θερμοδυναμικής 1 ος Νόμος της θερμοδυναμικής (αρχή διατήρησης της ενέργειας) Η ενέργεια δεν δημιουργείται ούτε καταστρέφεται Αλλάζει μορφή
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ. Χημεία της ζωής 1
 ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
Είναι σχεδόν βέβαιο, είτε να γνωρίζετε κάποιον που πάσχει από μια τέτοια ασθένεια είτε να έχετε μια εσείς οι ίδιοι.
 Γράφει: Δημήτρης Τσουκαλάς, Ιατρός Φυσικής Υγείας Τα αυτοάνοσα νοσήματα είναι ασθένειες που προκύπτουν γιατί το σώμα μας επιτίθεται και καταστρέφει τα δικά του κύτταρα και όργανα. Γνωρίζετε ότι ένας στους
Γράφει: Δημήτρης Τσουκαλάς, Ιατρός Φυσικής Υγείας Τα αυτοάνοσα νοσήματα είναι ασθένειες που προκύπτουν γιατί το σώμα μας επιτίθεται και καταστρέφει τα δικά του κύτταρα και όργανα. Γνωρίζετε ότι ένας στους
Οξειδωτική καταπόνηση
 Οξειδωτική καταπόνηση Δημιουργία ενεργών μορφών οξυγόνου Ο ρόλος του μοριακού οξυγόνου ως τελικού αποδέκτη των ηλεκτρονίων στην αλυσίδα μεταφοράς ηλεκτρονίων της αναπνευστικής λειτουργίας των αερόβιων
Οξειδωτική καταπόνηση Δημιουργία ενεργών μορφών οξυγόνου Ο ρόλος του μοριακού οξυγόνου ως τελικού αποδέκτη των ηλεκτρονίων στην αλυσίδα μεταφοράς ηλεκτρονίων της αναπνευστικής λειτουργίας των αερόβιων
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική αναπνοή.
 5ο ΓΕΛ ΧΑΛΑΝΔΡΙΟΥ Μ. ΚΡΥΣΤΑΛΛΙΑ 2/4/2014 Β 2 ΚΕΦΑΛΑΙΟ 3 ΒΙΟΛΟΓΙΑΣ 3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική
5ο ΓΕΛ ΧΑΛΑΝΔΡΙΟΥ Μ. ΚΡΥΣΤΑΛΛΙΑ 2/4/2014 Β 2 ΚΕΦΑΛΑΙΟ 3 ΒΙΟΛΟΓΙΑΣ 3.1 Ενέργεια και οργανισμοί..σελίδα 2 3.2 Ένζυμα βιολογικοί καταλύτες...σελίδα 4 3.3 Φωτοσύνθεση..σελίδα 5 3.4 Κυτταρική
Εργασία Βιολογίας 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ ΜΕΤΑΒΟΛΙΣΜΟΣ
 Εργασία Βιολογίας Καθηγητής: Πιτσιλαδής Β. Μαθητής: Μ. Νεκτάριος Τάξη: Β'2 Υλικό: Κεφάλαιο 3 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ ΜΕΤΑΒΟΛΙΣΜΟΣ Την ενέργεια και τα υλικά που οι οργανισμοί εξασφαλίζουν από το περιβάλλον
Εργασία Βιολογίας Καθηγητής: Πιτσιλαδής Β. Μαθητής: Μ. Νεκτάριος Τάξη: Β'2 Υλικό: Κεφάλαιο 3 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ ΜΕΤΑΒΟΛΙΣΜΟΣ Την ενέργεια και τα υλικά που οι οργανισμοί εξασφαλίζουν από το περιβάλλον
Μεταβολισμός πρωτεϊνών και των αμινοξέων
 Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
Μελέτη δεικτών οξειδωτικού στρες σε ενδοθηλιακά κύτταρα υπό την επίδραση μίγματος πολυφαινολών από στέμφυλα
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΣΧΟΛΗ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΠΟΙΟΤΗΤΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΠΕΡΙΒΑΛΛΟΝΤΟΣ» Μελέτη δεικτών οξειδωτικού στρες σε ενδοθηλιακά
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΣΧΟΛΗ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΠΟΙΟΤΗΤΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΠΕΡΙΒΑΛΛΟΝΤΟΣ» Μελέτη δεικτών οξειδωτικού στρες σε ενδοθηλιακά
Βιταμίνες/ Συμπληρώματα Διατροφής
 Βιταμίνες/ Συμπληρώματα Διατροφής e-catalogue 2012 Βιταμίνες Μέταλλα & Ιχνοστοιχεία Αμινοξέα & Πρωτεΐνες Απαραίτητα Λιπαρά Οξέα Πεπτικά/Προβιοτικά Βοηθήματα Βιταμίνες Οι βιταμίνες είναι απαραίτητες για
Βιταμίνες/ Συμπληρώματα Διατροφής e-catalogue 2012 Βιταμίνες Μέταλλα & Ιχνοστοιχεία Αμινοξέα & Πρωτεΐνες Απαραίτητα Λιπαρά Οξέα Πεπτικά/Προβιοτικά Βοηθήματα Βιταμίνες Οι βιταμίνες είναι απαραίτητες για
ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ. Καρβουντζή Ηλιάνα Βιολόγος
 ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ Η τροφή αποτελείται και από ουσίες μεγάλου μοριακού βάρους (πρωτεΐνες, υδατάνθρακες, λιπίδια, νουκλεϊνικά οξέα). Οι ουσίες αυτές διασπώνται (πέψη) σε απλούστερες (αμινοξέα, απλά σάκχαρα,
ΚΥΤΤΑΡΙΚΗ ΑΝΑΠΝΟΗ Η τροφή αποτελείται και από ουσίες μεγάλου μοριακού βάρους (πρωτεΐνες, υδατάνθρακες, λιπίδια, νουκλεϊνικά οξέα). Οι ουσίες αυτές διασπώνται (πέψη) σε απλούστερες (αμινοξέα, απλά σάκχαρα,
Β. Μαμαρέλη 1, Μ. Κυριακίδου 2, Ο. Τάνης 2, Ι. Μαμαρέλης 1, Χ. Κωτούλας 3, Ε. Κουτουλάκης 4, Ι. Κασσικού 1, Ι. Αναστασοπούλου 5
 Β. Μαμαρέλη 1, Μ. Κυριακίδου 2, Ο. Τάνης 2, Ι. Μαμαρέλης 1, Χ. Κωτούλας 3, Ε. Κουτουλάκης 4, Ι. Κασσικού 1, Ι. Αναστασοπούλου 5 1 Καρδιολογική Κλινική ΝΙΜΤΣ, 2 Σχολή Χημικών Μηχανικών, Πολυτεχνειούπολη
Β. Μαμαρέλη 1, Μ. Κυριακίδου 2, Ο. Τάνης 2, Ι. Μαμαρέλης 1, Χ. Κωτούλας 3, Ε. Κουτουλάκης 4, Ι. Κασσικού 1, Ι. Αναστασοπούλου 5 1 Καρδιολογική Κλινική ΝΙΜΤΣ, 2 Σχολή Χημικών Μηχανικών, Πολυτεχνειούπολη
Θέµατα Χηµείας - Βιοχηµείας Τεχνoλογικής Κατεύθυνσης Γ Λυκείου 2000
 Θέµατα Χηµείας Βιοχηµείας Τεχνoλογικής Κατεύθυνσης Γ Λυκείου 000 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: 1.1. Ένα υδατικό διάλυµα χαρακτηρίζεται ουδέτερο
Θέµατα Χηµείας Βιοχηµείας Τεχνoλογικής Κατεύθυνσης Γ Λυκείου 000 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: 1.1. Ένα υδατικό διάλυµα χαρακτηρίζεται ουδέτερο
Θέματα πριν τις εξετάσεις. Καλό διάβασμα Καλή επιτυχία
 Θέματα πριν τις εξετάσεις Καλό διάβασμα Καλή επιτυχία 2013-2014 Θέματα πολλαπλής επιλογής Μετουσίωση είναι το φαινόμενο α. κατά το οποίο συνδέονται δύο αμινοξέα για τον σχηματισμό μιας πρωτεΐνης β. κατά
Θέματα πριν τις εξετάσεις Καλό διάβασμα Καλή επιτυχία 2013-2014 Θέματα πολλαπλής επιλογής Μετουσίωση είναι το φαινόμενο α. κατά το οποίο συνδέονται δύο αμινοξέα για τον σχηματισμό μιας πρωτεΐνης β. κατά
Μελέτη επίδρασης της αιγοπρόβειας πρωτεΐνης τυρογάλακτος σε δείκτες οξειδωτικού στρες σε μυοβλάστες ποντικού (C2C12)
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Μελέτη επίδρασης της αιγοπρόβειας πρωτεΐνης τυρογάλακτος σε δείκτες οξειδωτικού στρες σε μυοβλάστες ποντικού (C2C12) Effect
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Μελέτη επίδρασης της αιγοπρόβειας πρωτεΐνης τυρογάλακτος σε δείκτες οξειδωτικού στρες σε μυοβλάστες ποντικού (C2C12) Effect
Θέµατα Χηµείας - Βιοχηµείας Τεχνoλογικής Κατεύθυνσης Γ Λυκείου 2000. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 Ζήτηµα 1ο Θέµατα Χηµείας - Βιοχηµείας Τεχνoλογικής Κατεύθυνσης Γ Λυκείου 000 Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: 1.1. Ένα υδατικό διάλυµα χαρακτηρίζεται ουδέτερο στους
Ζήτηµα 1ο Θέµατα Χηµείας - Βιοχηµείας Τεχνoλογικής Κατεύθυνσης Γ Λυκείου 000 Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: 1.1. Ένα υδατικό διάλυµα χαρακτηρίζεται ουδέτερο στους
ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ Η άσκηση, επιφέρει ευεργετικά αποτελέσματα στα διάφορα συστήματα του οργανισμού. Τα αποτελέσματα αυτά ενδέχεται να είναι παροδικά ή μόνιμα ανάλογα
ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ Η άσκηση, επιφέρει ευεργετικά αποτελέσματα στα διάφορα συστήματα του οργανισμού. Τα αποτελέσματα αυτά ενδέχεται να είναι παροδικά ή μόνιμα ανάλογα
ΦΡΟΝΤΙΣΤΗΡΙΑ ΠΡΟΟΠΤΙΚΗ
 Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
ΠΑΡΑΓΩΓΑ ΑΜΙΝΟΞΕΩΝ & ΑΙΜΗ
 ΠΑΡΑΓΩΓΑ ΑΜΙΝΟΞΕΩΝ & ΑΙΜΗ Ανασκόπηση μεταβολισμού πρωτεϊνών & αμινοξέων Ιστοί ΤΡΟΦΗ Αλανίνη & Γλουταμίνη Αμινοξέα Κυκλοφορία Πρωτεΐνες Αμινοξέα Βιοσύνθεση (Νουκλεοτίδια κλπ) ΝΗ 4 + + Κετοξέα ΗΠΑΡ Ακέτυλο-CoA
ΠΑΡΑΓΩΓΑ ΑΜΙΝΟΞΕΩΝ & ΑΙΜΗ Ανασκόπηση μεταβολισμού πρωτεϊνών & αμινοξέων Ιστοί ΤΡΟΦΗ Αλανίνη & Γλουταμίνη Αμινοξέα Κυκλοφορία Πρωτεΐνες Αμινοξέα Βιοσύνθεση (Νουκλεοτίδια κλπ) ΝΗ 4 + + Κετοξέα ΗΠΑΡ Ακέτυλο-CoA
Μικροοργανισμοί. Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς
 Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ. Διπλωματική εργασία
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Διπλωματική εργασία Προσδιορισμός δεικτών οξειδωτικού στρες σε αθλητές υπερμαραθωνίου βουνού Assessment of oxidative stress
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ & ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Διπλωματική εργασία Προσδιορισμός δεικτών οξειδωτικού στρες σε αθλητές υπερμαραθωνίου βουνού Assessment of oxidative stress
Εργασία Βιολογίας. Β. Γιώργος. Εισαγωγή 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ. Μεταφορά ενέργειας στα κύτταρα
 Εργασία Βιολογίας Β. Γιώργος Εισαγωγή Η ενεργεια εχει πολυ μεγαλη σημασια για εναν οργανισμο, γιατι για να κανει οτιδηποτε ενας οργανισμος ειναι απαραιτητη. Ειναι απαραιτητη ακομη και οταν δεν κανουμε
Εργασία Βιολογίας Β. Γιώργος Εισαγωγή Η ενεργεια εχει πολυ μεγαλη σημασια για εναν οργανισμο, γιατι για να κανει οτιδηποτε ενας οργανισμος ειναι απαραιτητη. Ειναι απαραιτητη ακομη και οταν δεν κανουμε
ΒΙΟΧΗΜΕΙΑ Ι. ΚΕΦΑΛΑΙΟ 2 ο Βιοχημική εξέλιξη
 ΒΙΟΧΗΜΕΙΑ Ι ΚΕΦΑΛΑΙΟ 2 ο Βιοχημική εξέλιξη ΣΥΝΔΕΣΗ ΜΕ ΤΑ ΠΡΟΗΓΟΥΜΕΝΑ Τι είναι ΒΙΟΧΗΜΕΙΑ DNA ΠΡΩΤΕΙΝΕΣ ΑΛΛΑ ΣΥΝΔΕΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΧΗΜΕΙΑΣ (Δεσμοί, ενέργεια, δομή) ΕΞΕΛΙΞΗ ΤΗΣ ΖΩΗΣ Υπάρχει μια συνεχή εξελικτική
ΒΙΟΧΗΜΕΙΑ Ι ΚΕΦΑΛΑΙΟ 2 ο Βιοχημική εξέλιξη ΣΥΝΔΕΣΗ ΜΕ ΤΑ ΠΡΟΗΓΟΥΜΕΝΑ Τι είναι ΒΙΟΧΗΜΕΙΑ DNA ΠΡΩΤΕΙΝΕΣ ΑΛΛΑ ΣΥΝΔΕΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΧΗΜΕΙΑΣ (Δεσμοί, ενέργεια, δομή) ΕΞΕΛΙΞΗ ΤΗΣ ΖΩΗΣ Υπάρχει μια συνεχή εξελικτική
σελ 1 από 8 Τμήμα Τεχνολογίας Τροφίμων ΤΕΙ Αθήνας Εαρινό Εξάμηνο a 2 η Εξέταση στην Βιοχημεία
 Τμήμα Τεχνολογίας Τροφίμων ΤΕΙ Αθήνας Εαρινό Εξάμηνο 2006 2007 a 2 η Εξέταση στην Βιοχημεία σελ 1 από 8 Ονοματεπώνυμο : Τυπικό εξάμηνο : Αριθμός Μητρώου : Σε κάθε ερώτηση αντιστοιχούν πέντε απαντήσεις
Τμήμα Τεχνολογίας Τροφίμων ΤΕΙ Αθήνας Εαρινό Εξάμηνο 2006 2007 a 2 η Εξέταση στην Βιοχημεία σελ 1 από 8 Ονοματεπώνυμο : Τυπικό εξάμηνο : Αριθμός Μητρώου : Σε κάθε ερώτηση αντιστοιχούν πέντε απαντήσεις
Μονάδες 3 β. Ποιο από τα παραπάνω ζεύγη, στο ίδιο υδατικό διάλυμα, μπορεί να αποτελέσει ρυθμιστικό διάλυμα; Μονάδες 2
 ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 12 ΙΟΥΝΙΟΥ 2000 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο Να γράψετε στο τετράδιό
ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 12 ΙΟΥΝΙΟΥ 2000 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο Να γράψετε στο τετράδιό
ΟΡΓΑΝΙΚΕΣ ΟΥΣΙΕΣ. 1. (α) Ποιο μόριο απεικονίζεται στο σχεδιάγραμμα; (β) Ποια είναι η απλούστερη μορφή του R;
 ΟΡΓΑΝΙΚΕΣ ΟΥΣΙΕΣ 1. (α) Ποιο μόριο απεικονίζεται στο σχεδιάγραμμα; (β) Ποια είναι η απλούστερη μορφή του R; (γ) Ποιο μέρος του μορίου προσδίδει σε αυτό όξινες ιδιότητες; (δ) Ποιο μέρος του μορίου προσδίδει
ΟΡΓΑΝΙΚΕΣ ΟΥΣΙΕΣ 1. (α) Ποιο μόριο απεικονίζεται στο σχεδιάγραμμα; (β) Ποια είναι η απλούστερη μορφή του R; (γ) Ποιο μέρος του μορίου προσδίδει σε αυτό όξινες ιδιότητες; (δ) Ποιο μέρος του μορίου προσδίδει
ΣΤΕΡΟΕΙΔΗ ΟΡΜΟΝΕΣ - ΒΙΤΑΜΙΝΕΣ. ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου
 ΣΤΕΡΟΕΙΔΗ ΟΡΜΟΝΕΣ - ΒΙΤΑΜΙΝΕΣ ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου 1 Στεροειδή Τα στεροειδή, είναι μια κατηγορία μη υδρολυόμενων λιπιδίων με χαρακτηριστική
ΣΤΕΡΟΕΙΔΗ ΟΡΜΟΝΕΣ - ΒΙΤΑΜΙΝΕΣ ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου 1 Στεροειδή Τα στεροειδή, είναι μια κατηγορία μη υδρολυόμενων λιπιδίων με χαρακτηριστική
ΕΡΓΑΣΙΑ ΣΤΗ ΒΙΟΛΟΓΙΑ
 ΕΡΓΑΣΙΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΕΠΙΜΕΛΕΙΑ: Κ. ΔΗΜΗΤΡΙΟΣ ΤΜΗΜΑ:Β 1 ΚΕΦΑΛΑΙΟ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Είναι γνωστό πως οποιοσδήποτε οργανισμός, για να λειτουργήσει χρειάζεται ενέργεια. Η ενέργεια αυτή βρίσκεται
ΕΡΓΑΣΙΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΕΠΙΜΕΛΕΙΑ: Κ. ΔΗΜΗΤΡΙΟΣ ΤΜΗΜΑ:Β 1 ΚΕΦΑΛΑΙΟ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Είναι γνωστό πως οποιοσδήποτε οργανισμός, για να λειτουργήσει χρειάζεται ενέργεια. Η ενέργεια αυτή βρίσκεται
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Θέµατα ιάλεξης ΜΕΤΑΒΟΛΙΣΜΟΣ ΛΙΠΩΝ. Λίπη. Ταξινόµηση λιπών. Τριακυλογλυκερόλες ή τριγλυκερίδια. Λιπαρά οξέα
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΜΕΤΑΒΟΛΙΣΜΟΣ ΛΙΠΩΝ Θέµατα ιάλεξης οµή και ρόλος των λιπών στην άσκηση ιαδικασία διάσπασης των ελεύθερων λιπαρών
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΜΕΤΑΒΟΛΙΣΜΟΣ ΛΙΠΩΝ Θέµατα ιάλεξης οµή και ρόλος των λιπών στην άσκηση ιαδικασία διάσπασης των ελεύθερων λιπαρών
Kυτταρική Bιολογία. Μιτοχόνδρια & Χλωροπλάστες - Τα Ενεργειακά Κέντρα των Ευκαρυωτικών Κυττάρων ΔIAΛEΞΕΙΣ 24 & 25 (27 /5/2016)
 Kυτταρική Bιολογία ΔIAΛEΞΕΙΣ 24 & 25 (27 /5/2016) Μιτοχόνδρια & Χλωροπλάστες - Τα Ενεργειακά Κέντρα των Ευκαρυωτικών Κυττάρων Τα κύρια σημεία των διαλέξεων 24 & 25 Αποικοδόμηση & οξείδωση μακρομορίων,
Kυτταρική Bιολογία ΔIAΛEΞΕΙΣ 24 & 25 (27 /5/2016) Μιτοχόνδρια & Χλωροπλάστες - Τα Ενεργειακά Κέντρα των Ευκαρυωτικών Κυττάρων Τα κύρια σημεία των διαλέξεων 24 & 25 Αποικοδόμηση & οξείδωση μακρομορίων,
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ
 ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
