ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
|
|
|
- Ευστοργιος Βλαβιανός
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FUDESIX 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά Κάθε 5ML πόσιµου διαλύµατος περιέχουν 20mg ή 40mg Furosemide 3. ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ Πόσιµο διάλυµα 4. ΚΛΙΝΙΚΑ ΣΤΟΙΧΕΙΑ 4.1 Θεραπευτικές ενδείξεις Οιδήµατα οφειλόµενα σε συµφορητική καρδιακή ανεπάρκεια, κίρρωση ήπατος ή νεφρική βλάβη. Αρτηριακή υπέρταση, ως µονοθεραπεία ή σε συνδυασµό µε κάποιο αντιϋπερτασικό. 4.2 οσολογία και τρόπος χορήγησης Ενήλικες Θεραπεία οιδήµατος: mg ηµερησίως. Αν χρειασθεί, αύξηση της δόσης κατά 20 ή 40mg ανά διαστήµατα 8 ωρών, ωσότου επιτευχθεί η επιθυµητή διούρηση. Η αποτελεσµατική δόση δίδεται εφάπαξ ή σε δύο τµήµατα την ηµέρα. Θεραπεία αρτηριακής υπέρτασης: 40 mg δύο φορές την ηµέρα. Η δόση ρυθµίζεται ανάλογα µε την ανταπόκριση. Βρέφη και παιδιά Αρχική δόση 2 mg/kg σωµατικού βάρους. Μέγιστη ηµερήσια δόση 6 mg/kg σωµατικού βάρους όση συντήρησης η ελάχιστη αποτελεσµατική. Χορήγηση Τα δισκία λαµβάνονται αµάσητα µε πολλά υγρά, σε άδειο στοµάχι. Η διάρκεια της αγωγής καθορίζεται από τον ιατρό. Προσδιορίζεται ανάλογα µε το είδος και τη βαρύτητα της νόσου. 4.3 Αντενδείξεις Το φάρµακο δεν πρέπει να χορηγείται σε ασθενείς υπερευαίσθητους στη φουροσεµίδη ή σε κάποιο από τα έκδοχα. Ασθενείς αλλεργικοί στις σουλφοναµίδες (π.χ. σουλφοναµιδικά αντιµικροβιακά ή σουλφονυλουρίες) και γενικά στις θειαζίδες µπορεί να εµφανίσουν διασταυρούµενη ευαισθησία στη φουροσεµίδη, ασθενείς µε υποογκαιµία ή αφυδάτωση, ασθενείς µε ανουρία λόγω νεφρικής ανεπάρκειας οι οποίοι δεν ανταποκρίνονται στη φουροσεµίδη, ασθενείς µε βαριάς µορφής υποκαλιαιµία, ασθενείς µε βαριάς µορφής υπονατριαιµία,
2 ασθενείς σε κωµατώδη και προκωµατώδη κατάσταση που έχει σχέση µε ηπατική εγκεφαλοπάθεια, θηλάζουσες. Όσον αφορά στην κύηση, βλ. κεφ. "Κύηση και γαλουχία". 4.4 Ιδιαίτερες προειδοποιήσεις και ιδιαίτερες προφυλάξεις κατά τη χρήση Θα πρέπει να διασφαλίζεται η εκροή των ούρων. Σε ασθενείς µε µερική απόφραξη της εκροής των ούρων απαιτείται προσεκτική παρακολούθηση και ειδικότερα κατά τα αρχικά στάδια της αγωγής. Η αγωγή µε το φάρµακο απαιτεί τακτική ιατρική παρακολούθηση. Ιδιαίτερα προσεκτική παρακολούθηση απαιτείται σε: ασθενείς µε υπόταση, ασθενείς οι οποίοι βρίσκονται σε ιδιαίτερο κίνδυνο, λόγω έντονης πτώσης της αρτηριακής πιέσεως, π.χ. ασθενείς µε σηµαντική στένωση των στεφανιαίων αρτηριών ή των αιµοφόρων αγγείων που εφοδιάζουν τον εγκέφαλο, ασθενείς µε λανθάνοντα ή έκδηλο σακχαρώδη διαβήτη, ασθενείς µε ουρική αρθρίτιδα, ασθενείς µε ηπατονεφρικό σύνδροµο, π.χ. νεφρική βλάβη λειτουργικής αιτιολογίας συνοδευόµενη από βαριάς µορφής νόσο του ήπατος, ασθενείς µε υποπρωτεϊναιµία συνοδευόµενη π.χ. από νεφρωσικό σύνδροµο (δυνατόν να εξασθενήσει η δράση της φουροσεµίδης και να ενισχυθεί η ωτοτοξικότητά της). Απαιτείται προσεκτική τιτλοποίηση της δόσης, πρόωρα νεογνά (πιθανή εµφάνιση νεφρασβέστωσης/νεφρολιθίασης θα πρέπει να παρακολουθείται η νεφρική λειτουργία και να διεξάγεται υπερηχογράφηµα των νεφρών). Επίσης αυξάνει τη συχνότητα παραµονής ανοικτού του βοταλείου πόρου και επιπλέκει το σύνδροµο αναπνευστικής δυσχέρειας των νεογνών. Στη διάρκεια της θεραπείας συνιστάται ο προσεκτικός και τακτικός έλεγχος των ηλεκτρολυτών και ιδιαίτερα του καλίου, του ασβεστίου, των χλωριδίων και του δικαρβονικοι) και του ισοζυγίου υγρών. Ακόµη είναι απαραίτητος ο τακτικός έλεγχος κρεατινίνης και ουρίας στο αίµα. Πρέπει επίσης να ελέγχεται ο µεταβολισµός-τωνυδατανθράκων. Ιδιαίτερα στενός έλεγχος απαιτείται σε ασθενείς που βρίσκονται σε υψηλό κίνδυνο να εκδηλώσουν διαταραχές στην ισορροπία των ηλεκτρολυτών ή ακόµη σε περίπτωση σηµαντικής επιπλέον απώλειας υγρών (π.χ. λόγω εµέτων, διάρροιας ή έντονης εφίδρωσης). Πρέπει να γίνεται αποκατάσταση της υποογκαιµίας ή της αφυδάτωσης, καθώς επίσης και οποιασδήποτε σηµαντικής διαταραχής των ηλεκτρολυτών και της οξεοβασικής ισορροπίας. Αυτό δυνατόν να απαιτήσει παροδική διακοπή της φουροσεµίδης. Λόγω της περιεχόµενης Λακτόζης το προϊόν δεν χορηγείται σε ασθενείς που πάσχουν από γαλακτοζαιµία, σύνδροµο δυσαπορρόφησης γλυκόζης και γαλακτόζης ή ανεπάρκεια λακτάσης (βλ. επίσης κεφ. 4.3) 4.5 Αλληλεπιδράσεις µε άλλα φάρµακα και άλλες µορφές αλληλεπιδράσεων Τροφή Αν και σε ποιο βαθµό η απορρόφηση της φουροσεµίδης επηρεάζεται από τη λήψη της µε την τροφή φαίνεται να εξαρτάται από τη φαρµακοτεχνική µορφή. Συνιστάται οι από του
3 στόµατος χορηγούµενες φαρµακοτεχνικές µορφές του φάρµακο να λαµβάνονται µε άδειο στοµάχι. Μη συνιστώµενοι συνδυασµοί Σε µεµονωµένες περιπτώσεις µετά από ενδοφλέβια χορήγηση φουροσεµίδης και εντός 24 ωρών από τη λήψη ένυδρης χλωράλης µπορεί να εµφανισθούν αίσθηµα καύσου, εφίδρωση, ανησυχία, ναυτία, αύξηση της αρτηριακής πίεσης και ταχυκαρδία. Η φουροσεµίδη δυνατόν να ενισχύσει την ωτοτοξικότητα των αµινογλυκοσιδών και των άλλων ωτοτοξικών φαρµακευτικών προϊόντων. Επειδή µπορεί να προκληθεί µη ανατάξιµη βλάβη, τα φάρµακα αυτά πρέπει να χορηγούνται µόνον εφόσον επιβάλλεται από ιατρικής πλευράς. Προφυλάξεις κατά τη χρήση Κατά τη συγχορήγηση της φουροσεµίδης µε σισπλατίνη υπάρχει κίνδυνος ωτοτοξικής επίδρασης. Επιπλέον δυνατόν να ενισχυθεί η νεφροτοξικότητα της σισπλατίνης στην περίπτωση που η φουροσεµίδη δεν χορηγείται σε χαµηλές δόσεις (π.χ. 40 mg σε ασθενείς µε φυσιολογική νεφρική λειτουργία) και µε θετικό ισοζύγιο υγρών, όταν χορηγείται για να επιτευχθεί έντονη διούρηση κατά τη διάρκεια της αγωγής µε σισπλατίνη. Η από του στόµατος χορηγούµενη φουροσεµίδη και η σουκραλφάτη δεν θα πρέπει να χορηγούνται εντός 2 ωρών µεταξύ της λήψης των δύο ουσιών, επειδή η σουκραλφάτη µειώνει την απορρόφηση της φουροσεµίδης από το έντερο και έτσι εξασθενεί η δράση της. Η φουροσεµίδη ελαττώνει την αποβολή των αλάτων λιθίου και πιθανόν να προκαλέσει αυξηµένα επίπεδα λιθίου στον ορό, καταλήγοντας σε αυξηµένη τοξικότητα από το λίθιο. Γι αυτό συνιστάται όπως παρακολουθούνται προσεκτικά τα επίπεδα λιθίου των ασθενών οι οποίοι λαµβάνουν το συνδυασµό. Σε ασθενείς στους οποίους χορηγούνται διουρητικά µπορεί να εµφανισθεί βαριάς µορφής υπόταση και επιδείνωση της νεφρικής λειτουργίας όταν χορηγηθεί για πρώτη φορά αναστολέας του ΜΕΑ ή για πρώτη φορά αυξηµένη δόση ("υποτασικό φαινόµενο της πρώτης δόσης"). Γι αυτό, πρέπει να εξεταστεί η διακοπή της χορήγησης της φουροσεµίδης παροδικά ή τουλάχιστον η µείωση της δόσης για 3 ηµέρες πριν από την έναρξη της αγωγής µε κάποιο αναστολέα του ΜΕΑ ή την αύξηση της δόσης αυτού. Να λαµβάνονται υπόψη Η ταυτόχρονη χορήγηση µε µη στεροειδή αντιφλεγµονώδη φάρµακα, περιλαµβανοµένου και του ακετυλοσαλικυλικού οξέος µπορεί να µειώσει τη δράση της φουροσεµίδης. Σε ασθενείς µε αφυδάτωση ή υποογκαιµία τα µη στεροειδή αντιφλεγµονώδη φάρµακα δυνατόν να προκαλέσουν οξεία νεφρική βλάβη. Η τοξικότητα των σαλικυλικών είναι δυνατόν να αυξηθεί από τη φουροσεµίδη. Κατά τη συγχορήγηση µε φαινυτοϊνη παρατηρήθηκε εξασθένηση της δράσης της φουροσεµίδης. Η βλαπτική επίδραση των νεφροτοξικών αντιβιοτικών στο νεφρό µπορεί να αυξηθεί. Τα κορτικοστεροειδή ή ACTH, η καρβενοξολόνη, η γλυκύρριζα σε µεγάλη ποσότητα, καθώς και η παρατεταµένη χρήση καθαρτικών πιθανόν να αυξήσει τον κίνδυνο υποκαλιαιµίας.
4 Ορισµένες ηλεκτρολυτικές διαταραχές (π.χ. υποκαλιαιµία, υποµαγνησιαιµία) δυνατόν να αυξήσουν την τοξικότητα συγκεκριµένων άλλων φαρµάκων (π.χ. σκευάσµατα δακτυλίτιδας και φάρµακα που προκαλούν το σύνδροµο επιµήκυνσης του διαστήµατος QT). Στην περίπτωση που συγχορηγηθεί η φουροσεµίδη µε αντιϋπερτασικά φάρµακα ή άλλες ουσίες µε υποτασική δράση θα πρέπει να ληφθεί υπόψη η πιο έντονη µείωση της αρτηριακής πιέσεως. Η προβενεσίδη, η µεθοτρεξάτη και άλλες ουσίες, όπως η φουροσεµίδη, που υφίσταται σηµαντική απέκκριση από τα σωληνάρια των νεφρών πιθανόν να µειώνουν τη δράση της φουροσεµίδης. Αντιθέτως, η φουροσεµίδη µπορεί να µειώσει την αποβολή αυτών των φαρµάκων από τους νεφρούς. Σε περίπτωση αγωγής µε υψηλές δόσεις (ιδιαίτερα κατά τη συγχορήγηση φουροσεµίδης µε τα άλλα φάρµακα) µπορεί να προκληθούν αυξηµένα επίπεδα στον ορό και αυξηµένος κίνδυνος ανεπιθύµητων ενεργειών λόγω της φουροσεµίδης ή εξαιτίας της συγχορηγούµενης αγωγής. Η δράση των αντιδιαβητικών και των συµπαθητικοµιµητικών που αυξάνει την αρτηριακή πίεση (π.χ. αδρεναλίνη, νοραδρεναλίνη) µπορεί να µειωθεί. Η φουροσεµίδη ανταγωνίζεται τη δράση των µυοχαλαρωτικών τύπου κουραρίου και ενισχύει τη δράση της σουκινυλχολίνης. Επίσης αυξάνει τις φαρµακολογκές ενέργειες της θεοφυλλίνης. Η µετολαζόνη δρα συνεργικά µε τη φουροσεµίδη και µπορεί να προκαλέσει έντονη διούρηση σε ασθενείς, που δεν ανταποκρίνονται στη φουροσεµίδη µόνη της. Ο κίνδυνος πρόκλησης ορθοστατικής υπότασης αυξάνει µε σύγχρονη χορήγηση αλκοόλης, βαρβιτουρικών και ναρκωτικών. Απουσία φαρµακοκινηπκής αλληλεπίδρασης του φαρµάκου Καµιά πληροφορία µέχρι σήµερα δεν θεωρήθηκε απαραίτητη. Αλληλεπίδραση µε εργαστηριακές ή διαγνωστικές δοκιµασίες Καµιά πληροφορία µέχρι σήµερα δεν θεωρήθηκε απαραίτητη. 4.6 Κύηση και γαλουχία Κύηση Η φουροσεµίδη διαπερνά το φραγµό του πλακούντα. εν πρέπει να χορηγείται κατά την κύηση, εκτός και αν συντρέχουν σοβαροί ιατρικοί λόγοι και για µικρό χρονικό διάστηµα. Η αγωγή κατά την κύηση απαιτεί παρακολούθηση της ανάπτυξης του εµβρύου. Γαλουχία Η φουροσεµίδη περνά στο µητρικό γάλα και αναστέλλει τη γαλουχία. Οι γυναίκες στις οποίες χορηγείται φουροσεµίδη, δεν πρέπει να θηλάζουν. 4.7 Επίδραση στην ικανότητα οδήγησης και χειρισµού µηχανηµάτων Κάποιες ανεπιθύµητες αντιδράσεις (π.χ. ανεπιθύµητα έντονη πτώση της αρτηριακής πίεσης) είναι δυνατόν να επηρεάσουν την ικανότητα των ασθενών να συγκεντρωθούν και να αντιδράσουν και γι' αυτό αποτελούν κίνδυνο σε καταστάσεις, οπου αυτές οι ικανότητες είναι ιδιαίτερης σηµασίας (π.χ." χειρισµός µηχανηµάτων ή αυτοκινήτου). Αυτό έχει ιδιαίτερη σηµασία στην αρχή της αγωγής ή όταν γίνεται αλλαγή του φαρµάκου ή σε συνδυασµό µε λήψη οινοπνεύµατος.
5 4.8 Ανεπιθύµητες ενέργειες Η φουροσεµίδη προκαλεί αυξηµένη απέκκριση νατρίου και χλωρίου και ακολούθως ύδατος. Επιπλέον αυξάνεται η απέκκριση και άλλων ηλεκτρολυτών (ειδικότερα καλίου, ασβεστίου και µαγνησίου). Είναι δυνατόν να εκδηλωθούν συµπτωµατικές διαταραχές των ηλεκτρολυτών και µεταβολική αλκάλωση µε τη µορφή βαθµιαία αυξανόµενου ελλείµµατος των ηλεκτρολυτών ή π.χ. όταν χορηγούνται υψηλότερες δόσεις φουροσεµίδης σε ασθενείς µε φυσιολογική νεφρική λειτουργία, οξεία, βαριάς µορφής απώλεια ηλεκτρολυτών. Ως σηµεία προειδοποιητικά για διαταραχές των ηλεκτρολυτών αναφέρονται δίψα, κεφαλαλγία, σύγχυση, µυϊκές κράµπες, τετανία, µυϊκή αδυναµία, διαταραχές του καρδιακού ρυθµού και γαστρεντερικά συµπτώµατα. Η εκδήλωση διαταραχών των ηλεκτρολυτών επηρεάζεται από παράγοντες όπως υποκείµενα νοσήµατα (π.χ. κίρρωση του ήπατος, καρδιακή ανεπάρκεια), συγχορήγηση φαρµάκων (βλέπε επίσης "Αλληλεπιδράσεις µε άλλα φάρµακα και άλλες µορφές αλληλεπιδράσεων") και διατροφή. Ειδικότερα µπορεί να παρουσιασθεί ανεπάρκεια καλίου ως αποτέλεσµα του εµέτου ή της διάρροιας. Η διουρητική δράση της φουροσεµίδης µπορεί να οδηγήσει ή να συµβάλλει σε υποογκαιµία και αφυδάτωση, ειδικότερα σε ηλικιωµένους ασθενείς. Βαριάς µορφής απώλεια υγρών µπορεί να προκαλέσει αιµοσυµπύκνωση µε τάση εµφάνισης θροµβώσεων. Η φουροσεµίδη µπορεί να προκαλέσει µείωση στην αρτηριακή πίεση, η οποία, αν είναι έντονη, µπορεί να οδηγήσει σε σηµεία και συµπτώµατα τέτοια όπως µείωση της συγκέντρωσης και αντιδράσεις, όπως αίσθηµα κενού στο κεφάλι, αίσθηµα πίεσης στο κεφάλι, κεφαλαλγία, ζάλη, νυσταγµός, αδυναµία, διαταραχές της όρασης, ξηροστοµία, ορθοστατική δυσανεξία. Αυξηµένη απέκκριση των ούρων δυνατόν να εγκαταστήσει ή να επιδεινώσει τα ενοχλήµατα σε ασθενείς µε απόφραξη της εκροής των ούρων. Γι αυτό δυνατόν να παρουσιασθεί οξεία κατακράτηση των ούρων µε πιθανές δευτεροπαθείς επιπλοκές, όπως για παράδειγµα σε ασθενείς µε διαταραχές κένωσης της ουροδόχου κύστης, υπερτροφία του προστάτη ή στένωση της ουρήθρας. Η χορήγηση φουροσεµίδης µπορεί να προκαλέσει παροδικά αύξηση στα επίπεδα κρεατινίνης και ουρικού οξέος στο αίµα καθώς επίσης και αύξηση των επιπέδων χοληστερίνης και τριγλυκεριδίων. υνατόν να αυξηθούν τα επίπεδα του ουρικού οξέος στον ορό και µπορεί να εµφανισθεί κρίση ουρικής αρθρίτιδας. Η φουροσεµίδη µπορεί να µειώσει την ανοχή στη γλυκόζη. Στους ασθενείς µε σακχαρώδη διαβήτη µπορεί να προκαλέσει επιδείνωση του µεταβολισµού. Ο λανθάνων σακχαρώδης διαβήτης µπορεί να γίνει έκδηλος. Σε σπάνιες περιπτώσεις µπορεί να παρουσιασθούν γαστρεντερικές αντιδράσεις, όπως ναυτία, έµετος ή διάρροια. Σε µεµονωµένες περιπτώσεις µπορεί να εκδηλωθεί ενδοηπατική χολόσταση, αύξηση των τρανσαµινασών του ήπατος ή οξεία παγκρεατίτιδα. Σε σπάνιες περιπτώσεις µπορεί να εµφανισθούν διαταραχές της ακοής και εµβοές των ώτων, παρ' όλο που συνήθως είναι παροδικές, ιδιαίτερα σε ασθενείς µε νεφρική βλάβη, υποπρωτεϊναιµία (π.χ. σε νεφρωσικό σύνδροµο) ή/και όταν η ενδοφλέβια χορήγηση φουροσεµίδης γίνεται πολύ γρήγορα. Παροδικά δυνατόν να παρουσιασθούν αντιδράσεις του δέρµατος και των βλεννογόνων, π.χ. κνησµός, κνίδωση, άλλα εξανθήµατα ή φυσαλλιδώδεις αλλοιώσεις, πολύµορφο ερύθηµα, αποφολιδωτική δερµατίτις, πορφύρα.
6 Σπάνια εµφανίζονται βαριάς µορφής αναφυλακτικές ή αναφυλακτικού τύπου αντιδράσεις (π.χ. µε shock). Σπάνιες είναι η διάµεση νεφρίτις, νεκρωτική αγγειίτις ή ηωσινοφιλία. Σε σπάνιες περιπτώσεις µπορεί να παρουσιαστούν πυρετός ή παραισθησίες και παροδικά οωτοευαισθησία. Παροδικά µπορεί να εµφανισθεί θροµβοκυτοπενία. υνατόν να εκδηλωθεί σε σπάνιες περιπτώσεις λευκοπενία και σε µεµονωµένες περιπτώσεις ακοκκιοκυτταραιµία, απλαστική αναιµία ή αιµολυτική αναιµία. Στα πρόωρα νεογνά η φουροσεµίδη δυνατόν να επισπεύσει τη νεφρασβέστωση/νεφρολιθίαση. Στην περίπτωση που η φουροσεµίδη χορηγηθεί στα πρόωρα νεογνά κατά τις πρώτες εβδοµάδες της ζωής τους, µπορεί να αυξηθεί ο κίνδυνος παραµονής ανοικτού του βοταλείου πόρου. Ο συστηµατικός ερυθηµατώδης λύκος µπορεί να ενεργοποιηθεί ή να παρουσιάσει έξαρση µε τη φουροσεµίδη. Στο ηπατικό κώµα και στην ηπατική ανεπάρκεια η αιφνίδια διαταραχή ισορροπίας ύδατος και ηλεκτρολυτών µπορεί να προκαλέσει ηπατική εγκεφαλοπάθεια και να επιφέρει το θάνατο. Γι' αυτό επιβάλλεται τακτική παρακολούθηση της διούρησης και των ηλεκτρολυτών και ανάλογη διόρθωση τυχόν διαταραχών. Ξανθοψία, θροµβοφλεβίτις, υπερουριχαιµία, αζωθαιµία. Επίσης συχνή, ιδιαίτερα στους υπερήλικες και τους καλοκαιρινούς µήνες, είναι η αφυδάτωση. 4.9 Υπερδοσολογία Η κλινική εικόνα της οξείας ή χρόνιας υπερδοσολογίας αρχικά εξαρτάται από το µέγεθος και τις συνέπειες της απώλειας υγρών και ηλεκτρολυτών π.χ. υποογκαιµία, αφυδάτωση, αιµοσυµπύκνωση, καρδιακές αρρυθµίες (συµπεριλαµβάνεται ο κολποκοιλιακός αποκλεισµός και η κοιλιακή µαρµαρυγή). Τα συµπτώµατα αυτών των διαταραχών αφορούν σε βαριάς µορφής νεφρική υπόταση (εξελισσόµενη µέχρι και shock), οξεία νεφρική βλάβη, θρόµβωση, καταστάσεις παραληρήµατος, χαλαρή παράλυση, απάθεια και σύγχυση. εν είναι γνωστό κάποιο ειδικό αντίδοτο για τη φουροσεµίδη. Στην περίπτωση που η λήψη έγινε µόλις προ ολίγου, απαιτείται προσπάθεια για να ελαχιστοποιηθεί η περαιτέρω συστηµατική απορρόφηση του δραστικού συστατικού λαµβάνοντας µέτρα, τέτοια όπως πλύση στοµάχου ή αυτά που συνιστώνται για τη µείωση της απορρόφησης (π.χ. ενεργοποιηµένος άνθρακας). Θα πρέπει να γίνει αποκατάσταση των κλινικά σηµαντικών διαταραχών στο ισοζύγιο υγρών και ηλεκτρολυτών. Εκτός από την πρόληψη και θεραπευτική αντιµετώπιση των σοβαρών επιπλοκών που προέρχονται από τέτοιες διαταραχές και από άλλες επιδράσεις στον οργανισµό, πιθανόν η διορθωτική αυτή ενέργεια να απαιτήσει ειδική εντατική ιατρική παρακολούθηση και να ληφθούν τα θεραπευτικά µέτρα αντιµετώπισης.
7 5. ΦΑΡΜΑΚΟΛΟΓΙΚΕ! Ι ΙΟΤΗΤΕΣ Κωδικός ATC: C03CA Φαρµακοδυναµικές ιδιότητες Τρόπος δράσης Η φουροσεµίδη {χηµική ονοµασία: 5-(aminosulfonyl)-4-chloro-2-[(2-furanylmethyl) amino] benzoic acid; 4-chloro-N-furfuryl-5-sulfamoyl-anthranilic acid) είναι ένα διουρητικό της αγκύλης που δηµιουργεί µια συγκριτικά ισχυρή και βραχείας διάρκειας διούρηση µε ταχεία έναρξη. Η φουροσεµίδη παρεµποδίζει το σύστηµα συν-µεταφοράς του Na + Κ + 2CI - το οποίο είναι παρόν στην κυτταρική µεµβράνη του αυλού στο ευρύ ανιόν σκέλος της αγκύλης του Henle: ως εκ τούτου η αποτελεσµατικότητα της αλατοδιουρητικής δράσης της φουροσεµίδης εξαρτάται από τη συγκέντρωση της ουσίας που φθάνει στον αυλό του σωληνάριου µέσω της αντλίας οργανικών οξέων. Η διουρητική δράση επιτυγχάνεται µε αναστολή της επαναπορρόφησης χλωριούχου νατρίου σε αυτό το τµήµα της αγκύλης του Henle. Ως επακόλουθο αυτού, η κλασµατική αποβολή νατρίου µπορεί να φθάσει στο 35% της σπειραµατικής διήθησης νατρίου.τα δευτεροπαθή αποτελέσµατα της αυξηµένης αποβολής νατρίου είναι η αυξηµένη απέκκριση ούρων (λόγω του ωσµωτικά δεσµευµένου ύδατος) και η αυξηµένη απέκκριση καλίου από το αθροιστικό σωληνάριο. Επίσης αυξηµένη είναι και η αποβολή ιόντων ασβεστίου και µαγνησίου. Η φουροσεµίδη διακόπτει το µηχανισµό παλίνδροµης αλληλορύθµισης του σπειράµατος στο εγγύς εσπειραµένο σωληνάριο, µε αποτέλεσµα να µην υπάρχει εξασθένιση της αλατοδιουρητικής δραστηριότητας. Η φουροσεµίδη προκαλεί δοσοεξαρτώµενη διέγερση του συστήµατος ρενίνης-αγγειοτασίνης-αλδοστερόνης. Σε καρδιακή ανεπάρκεια, η φουροσεµίδη προκαλεί οξεία κατακράτηση του προφορτίου της καρδιάς µέσω διαστολής των αγγείων των φλεβών. Αυτή η πρώιµη αγγειακή δράση φαίνεται ότι έχει σχέση µε τις προσταγλανδίνες και προϋποθέτει επαρκή νεφρική λειτουργία µε δραστηριοποίηση του συστήµατος ρενίνης-αγγειοτασίνης και δεν επηρεάζεται η σύνθεση προσταγλανδινών. Επιπλέον η φουροσεµίδη λόγω της νατριουρητικής της δράσης ελαττώνει την αγγειακή αντιδραστικότητα στις κατεχολαµίνες, που εµφανίζεται αυξηµένη στους υπερτασικούς ασθενείς. Το αντιϋπερτασικό αποτέλεσµα της φουροσεµίδης αποδίδεται στην αυξηµένη αποβολή νατρίου, στον ελαττωµένο όγκο αίµατος και στη µειωµένη ανταπόκριση των λείων µυϊκών ινών των αγγείων στα αγγειοσυσταλτικά ερεθίσµατα. Φαρµακοδυναµικά χαρακτηριστικά Η έναρξη της διούρησης µετά την ενδοφλέβια χορήγηση φουροσεµίδης επέρχεται εντός 15 λεπτών και µετά την από του στόµατος χορήγηση εµφανίζεται εντός 1 ώρας. Σε υγιή άτοµα που έλαβαν φουροσεµίδη σε δόσεις mg εντοπίσθηκε δοσοεξαρτώµενη αύξηση στη διούρηση και νατριούρηση. Η διάρκεια δράσης είναι περίπου 3 ώρες µετά από ενδοφλέβια χορήγηση 20 mg φουροσεµίδης ενώ µετά από του στόµατος χορήγηση 40 mg σε υγιή άτοµα είναι 3-6 ώρες. Σε ασθενείς, η σχέση των ενδοσωληναριακών συγκεντρώσεων της αδέσµευτης (ελεύθερης) φουροσεµίδης (προσδιορίζεται χρησιµοποιώντας το ρυθµό απέκκρισης της φουροσεµίδης µε τα ούρα) µε το νατριουρητικό του αποτέλεσµα έχει τη µορφή καµπύλης τύπου S µε ελάχιστο ρυθµό αποτελεσµατικής απέκκρισης της φουροσεµίδης περίπου 10 µg ανά λεπτό. Γι αυτό, η συνεχής έγχυση φουροσεµίδης είναι πιο αποτελεσµατική από ότι οι επαναλαµβανόµενες
8 ενέσεις bolus. Επιπλέον, πέρα από τη συγκεκριµένη δόση bolus του φαρµάκου, δεν υπάρχει σηµαντική αύξηση στο αποτέλεσµα. Η δράση της φουροσεµίδης µειώνεται, εφόσον είναι µειωµένη η σωληναριακή απέκκριση ή η ενδοσωληναριακή δέσµευση του φαρµάκου µε τη λευκωµατίνη. 5.2 Φαρµακοκινητικές ιδιότητες Η φουροσεµίδη απορροφείται ταχέως από το γαστρεντερικό σωλήνα. Ο χρόνος επίτευξης της µέγιστης συγκέντρωσης µετά τη χορήγηση (t max ) των δισκίων 40 mg ανέρχεται σε 1-1,5 ώρες. Η απορρόφηση του φαρµάκου παρουσιάζει µεγάλη µεταβλητότητα τόσο από άτοµο σε άτοµο όσο και στο ίδιο άτοµο. Στους υγιείς εθελοντές η βιοδιαθεσιµότητα της φουροσεµίδης ανέρχεται περίπου σε 50%- 70% για τα δισκία. Η βιοδιαθεσιµότητα του φαρµάκου στους ασθενείς προσδιορίζεται από διάφορους παράγοντες συµπεριλαµβανόµενων και των συνοδών νόσων και µπορεί να µειωθεί σε ποσοστό µικρότερο από 30% (π.χ. σε νεφρωσικό σύνδροµο). Αν και σε ποιο µέγεθος η απορρόφηση της φουροσεµίδης επηρεάζεται από τη λήψη τροφής φαίνεται ότι εξαρτάται από τη φαρµακοτεχνική µορφή. Ο όγκος κατανοµής της φουροσεµίδης είναι 0,1-0,2 l/kg βάρους σώµατος. Ο όγκος κατανοµής µπορεί να είναι µεγαλύτερος σε σχέση µε το συνοδό νόσηµα. Η φουροσεµίδη συνδέεται εκτεταµένα µε τις πρωτείνες του πλάσµατος σε ποσοστό µεγαλύτερο από 98% και κυρίως µε τη λευκωµατίνη. Η φουροσεµίδη αποβάλλεται βασικά αναλλοίωτη, αρχικά µέσω απέκκρισης από το εγγύς σωληνάριο. Μετά από την ενδοφλέβια χορήγηση φουροσεµίδης ποσοστό 60%-70% της δόσης εκκρίνεται µε τον ίδιο τρόπο. Ο γλυκουρονικός µεταβολίτης της φουροσεµίδης ο οποίος ανιχνεύεται στα ούρα ανέρχεται σε ποσοστό περίπου 10%-20%. Η εναποµείνασα δόση αποβάλλεται µε τα κόπρανα, πιθανώς µετά από χολική έκκριση. Ο τελικός χρόνος ηµίσειας ζωής της φουροσεµίδης µετά από ενδοφλέβια χορήγηση ανέρχεται περίπου σε 1-1,5 ώρα. Η φουροσεµίδη εκκρίνεται στο µητρικό γάλα. Η φουροσεµίδη διαπερνά τον πλακουντιακό φραγµό και µεταφέρεται αργά στο έµβρυο. Στο έµβρυο ή στο νεογνό ανευρίσκεται στις ίδιες συγκεντρώσεις όπως και στη µητέρα. Νεφρική νόσος Η βιοδιαθεσιµότητα των δισκίων 500 mg δεν διαφοροποιείται σε ασθενείς µε νεφρική ανεπάρκεια τελικού σταδίου. Σε νεφρική ανεπάρκεια, η αποβολή της φουροσεµίδης επιβραδύνεται και ο χρόνος ηµιζωής επιµηκύνεται. Ο τελικός χρόνος ηµίσειας ζωής σε ασθενείς µε βαριάς µορφής νεφρική ανεπάρκεια ανέρχεται µέχρι και 24 ώρες. Σε νεφρωσικό σύνδροµο οι µειωµένες συγκεντρώσεις πρωτείνης στο πλάσµα οδηγούν σε αυξηµένες συγκεντρώσεις αδέσµευτης (ελεύθερης) φουροσεµίδης. Από την άλλη πλευρά, η δραστικότητα της φουροσεµίδης µειώνεται σε αυτούς τους ασθενείς λόγω δέσµευσης µε την ενδοσωληναριακή λευκωµατίνη και την ελαττωµένη σωληναριακή απέκκριση. Η φουροσεµίδη αποµακρύνεται ελάχιστα µέσω αιµοδιύλισης, περιτοναϊκής διύλισης και CAPD.
9 Ηπατική ανεπάρκεια Σε ηπατική ανεπάρκεια, ο χρόνος ηµίσειας ζωής της φουροσεµίδης αυξάνεται σε ποσοστό 30% -90% βασικά λόγω του µεγαλύτερου όγκου κατανοµής. Επιπλέον, σε αυτή την οµάδα ασθενών υπάρχει ευρεία παρέκκλιση σε όλες τις φαρµακοκινητικές παραµέτρους. Συµφορηπκή καρδιακή ανεπάρκεια, βαριάς µορφής υπέρταση, ηλικιωµένοι Η αποβολή της φουροσεµίδης επιβραδύνεται λόγω της µειωµένης νεφρικής λειτουργίας σε ασθενείς µε συµφορητική καρδιακή ανεπάρκεια, βαριάς µορφής υπέρταση ή σε ηλικιωµένους. Πρόωρα και πλήρους κυήσεως νεογνά Η αποβολή της φουροσεµίδης δυνατόν να επιβραδυνθεί σε εξάρτηση µε την ωρίµανση των νεφρών. Ο µεταβολισµός του φαρµάκου µειώνεται επίσης στην περίπτωση που είναι µειωµένη η ικανότητα γλουκουρογένεσης του εµβρύου. Στα βρέφη ο τελικός χρόνος ηµίσειας ζωής είναι λιγότερο από 12 ώρες σε ηλικία µεγαλύτερη των 33 εβδοµάδων µετά τη γονιµοποίηση. Σε βρέφη ηλικίας 2 µηνών και µεγαλύτερα, η τελική κάθαρση είναι η ίδια µε αυτή των ενηλίκων. 5.3 Προκλινικά στοιχεία για την ασφάλεια (τοξικολογικά στοιχεία) Οξεία τοξικότητα Από µελέτες τοξικότητας όπου χορηγήθηκε η φουροσεµίδη είτε από το στόµα είτε ενδοφλεβίως σε διάφορα είδη τρωκτικών και σκύλους εντοπίσθηκε µικρή οξεία τοξικότητα. Η από του στόµατος LD 5 o της φουροσεµίδης κυµαίνεται µεταξύ 1050 και 4600 mg/kg σωµατικού βάρους στα ποντίκια και στους αρουραίους, ενώ στα ινδικά χοιρίδια είναι 243 mg/kg βάρουςσώµατος. Σε σκύλους η από του στόµατος LD 5 o είναι περίπου 2000 mg/kg βάρους σώµατος και η ενδοφλέβια LD 5 o είναι περισσότερο από 400 mg/kg σωµατικού βάρους. Χρόνια τοξικότητα Σε αρουραίους και σκύλους µετά από 6 και 12 µηνών χορήγηση οι νεφρικές αλλοιώσεις συµπεριλαµβανόµενης της τοπικής ινώσεως, αποτιτανώσεως έγιναν αντιληπτές στις οµάδες που είχαν λάβει την ανώτατη δόση (10-20 φορές µεγαλύτερη από τη θεραπευτική δόση που χορηγείται στον άνθρωπο). Ωτοτοξικότητα Η φουροσεµίδη δυνατόν να παρέµβει στη διαδικασία µεταφοράς στο αγγειώδες πέταλο του έσω ωτός και πιθανόν να προκαλέσει ακουστικές διαταραχές οι οποίες γενικά είναι αναστρέψιµες. Μεταλλαξιογόνος δράση In vitro δοκιµές που διεξήχθησαν σε βακτηρίδια και κύτταρα θηλαστικών εντόπισαν τόσο θετικά όσο και αρνητικά αποτελέσµατα. Επαγωγή παρ' όλα αυτά των γονιδιακών και χρωµοσωµικών µεταλλάξεων παρατηρήθηκε µόνο όταν επιτεύχθηκαν κυτταροτοξικές συγκεντρώσεις από τη φουροσεµίδη. Καρκινογόνος δράση Η φουροσεµίδη χορηγήθηκε σε ποσότητα περίπου 200 mg/kg σωµατικού βάρους ( ppm) την ηµέρα µαζί µε την τροφή σε θηλυκά ποντίκια και αρουραίους για χρονικό διάστηµα περισσότερο από 2 χρόνια. Παρουσιάσθηκε αυξηµένη συχνότητα αδενοκαρκινώµατος των µαστών σε ποντικούς, όχι όµως σε αρουραίους. Η δόση αυτή είναι σηµαντικά µεγαλύτερη από τη θεραπευτική δόση
10 που χορηγείται σε ασθενείς ανθρώπους. Επιπλέον, οι όγκοι αυτοί µορφολογικά ήταν ίδιοι µε τους όγκους που εµφανίσθηκαν αυτόµατα και εντοπίσθηκαν σε ποσοστό 2% - 8% των υπό έλεγχο ευρισκοµένων ζώων. Παρ' όλα αυτά η συχνότητα αυτή των όγκων θεωρείται απίθανο να σχετίζεται µε την αγωγή που χορηγείται στον άνθρωπο. Πράγµατι δεν υπάρχει µαρτυρία αυξηµένης συχνότητας αδενοκαρκινώµατος των µαστών στον άνθρωπο µετά τη χορήγηση φουροσεµίδης. Με βάση τις επιδηµιολογικές µελέτες, η ταξινόµηση της καρκινογένεσης λόγω της φουροσεµίδης σε ανθρώπους δεν είναι δυνατή. Σε µια µελέτη ως προς την καρκινογένεση χορηγήθηκε σε αρουραίους φουροσεµίδη σε ηµερήσιες δόσεις των 15 και 30 mg/kg σωµατικού βάρους. Οι άρρενες αρουραίοι στη δόση των 15 mg/kg αλλά όχι στη δόση των 30 mg/kg εµφάνισαν οριακή αύξηση σε ασυνήθεις όγκους. Θεωρείται ότι τα ευρήµατα αυτά ήταν τυχαία. Η καρκινογένεση της ουροδόχου κύστεως που προκαλείται από τη νιτροζαµίνη σε αρουραίους δεν έδωσε στοιχεία από τα οποία να υποδηλώνεται ότι η φουροσεµίδη είναι παράγοντας προαγωγής. Τοξικότητα κατά την αναπαραγωγή Η φουροσεµίδη δεν επέδρασε στη γονιµότητα των αρρένων και θηλέων αρουραίων όταν χορηγήθηκε σε ηµερήσιες δόσεις των 90 mg/kg βάρους σώµατος όπως και στα άρρενα και θηλυκά ποντίκια σε ηµερήσιες από του στόµατος χορηγούµενες δόσεις 200 mg/kg βάρους σώµατος. Μετά από χορήγηση φουροσεµίδης σε διάφορα είδη θηλαστικών συµπεριλαµβανόµενων του ποντικού, αρουραίου, γάτας, κουνελιού και σκύλου δεν παρατηρήθηκε κάποια σχετική εµβρυοτοξική ή τερατογόνος δράση. Περιγράφηκε καθυστερηµένη νεφρική ωρίµανση - µείωση στον αριθµό των διαφοροποιηµένων σπειραµάτων - στους απογόνους των αρουραίων που αντιµετωπίσθηκαν θεραπευτικά µε 75 mg φουροσεµίδης ανά kg βάρους σώµατος κατά τις ηµέρες της κυήσεως, ήτοι από 7η-11η και 14η-18η ηµέρα. Η φουροσεµίδη διαπερνά τον πλακούντα και στον οµφάλιο λώρο επιτυγχάνει 100% συγκεντρώσεις ορού στη µητέρα. Μέχρι σήµερα δεν ανιχνεύθηκαν κάποιες δυσµορφίες στον άνθρωπο που µπορεί να συνδέονται µε την έκθεση στη φουροσεµίδη. Παρ' όλα αυτά, δεν υπάρχει αρκετή εµπειρία προκειµένου να υπάρξει αδιαµφισβήτητη εκτίµηση των πιθανών βλαβερών επιδράσεων στο έµβρυο. Η παραγωγή ούρων στο έµβρυο µπορεί να διεγερθεί στη µήτρα Παρατηρήθηκε ουρολιθίαση και νεφρασβέστωση µετά από χορήγηση φουροσεµίδης σε πρόωρα νεογνά. εν διεξήχθησαν µελέτες προκειµένου να αξιολογηθεί η δράση της φουροσεµίδης σε νεογνά, όταν εισάγεται µε το µητρικό γάλα. 6. ΦΑΡΜΑΚΕΥΤΙΚΑ ΣΤΟΙΧΕΙΑ 6.1 Κατάλογος εκδόχων Ethanol, Sodium Hydroxide, Propylene Glycol, Liquid Maltitol, Disodium Phosphate, Citric Acid Monohydrate, Cherry Flavour, Purified Water 6.2 Ασυµβατότητες εν εφαρµόζεται.
11 6.3 ιάρκεια ζωής 24 Μήνες 6.4 Ιδιαίτερες προφυλάξεις κατά τη φύλαξη του προϊόντος Το προϊον φυλάσσεται σε θερµοκρασία <25 C. 6.5 Φύση και συστατικά του περιέκτη Σκουρόχρωµο γυάλινο φιαλίδιο που περιέχει 150ml του πόσιµου διαλύµατος µε βιδωτό πώµα ασφαλείας και επιπλέον δοσοµετρική πιπέτα. 6.6 Οδηγίες χρήσης/χειρισµού εν εφαρµόζεται. 7. ΚΑΤΟΧΟΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ HELP Α.Β.Ε.Ε. ΒΑΛΑΩΡΙΤΟΥ ΜΕΤΑΜΟΡΦΩΣΗ ΑΤΤΙΚΗ Τηλ: ΑΡΙΘΜΟΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ Fudesix 20mg/5ml Πόσιµο ιάλυµα: 28224/ Fudesix 40mg/5ml Πόσιµο ιάλυµα: 28225/ ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΣΤΗΝ ΕΛΛΑ Α Fudesix 20mg/5ml Πόσιµο ιάλυµα: Fudesix 40mg/5ml Πόσιµο ιάλυµα: ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ
ΠΑΡΕΝΤΕΡΙΚΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ
 ΠΑΡΕΝΤΕΡΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ https://users.auth.gr/epontiki Ελένη Ποντίκη Θεσσαλονίκη 2018 Παρεντερικά διαλύματα Αποστειρωμένα διαλύματα που προορίζονται: για την στοιχείων αναπλήρωση
ΠΑΡΕΝΤΕΡΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ https://users.auth.gr/epontiki Ελένη Ποντίκη Θεσσαλονίκη 2018 Παρεντερικά διαλύματα Αποστειρωμένα διαλύματα που προορίζονται: για την στοιχείων αναπλήρωση
1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ:
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ INFLABION. ( ιακετυλρεΐνη)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ INFLABION ( ιακετυλρεΐνη) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ INFLABION 50 mg σκληρά καψάκια 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε καψάκιο περιέχει 50 mg διακετυλρεΐνη.
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ INFLABION ( ιακετυλρεΐνη) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ INFLABION 50 mg σκληρά καψάκια 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε καψάκιο περιέχει 50 mg διακετυλρεΐνη.
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, Wednesday, 19 December :05 -
 SUPERAMIN ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία Προϊόντος: SUPERAMIN α) Πόσιμο διάλυμα σε συσκευασία μιας δόσης 1 g/10ml FL & g/10ml FL β) Ενέσιμο διάλυμα 1 g/5ml AMP & 2g/5ml AMP 1.2 Σύνθεση: Δραστική
SUPERAMIN ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία Προϊόντος: SUPERAMIN α) Πόσιμο διάλυμα σε συσκευασία μιας δόσης 1 g/10ml FL & g/10ml FL β) Ενέσιμο διάλυμα 1 g/5ml AMP & 2g/5ml AMP 1.2 Σύνθεση: Δραστική
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8%
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8% 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Νάτριο Ανθρακικό Όξινο/DEMO (Sodium Bicarbonate/DEMO) 2. ΠΟΙΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8% 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Νάτριο Ανθρακικό Όξινο/DEMO (Sodium Bicarbonate/DEMO) 2. ΠΟΙΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ERRKES. Οφθαλμικές σταγόνες, διάλυμα
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
Mometasone/Target Mometasone furoate
 Mometasone/Target Mometasone furoate ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1. Ονοµασία: Mometasone/Target 1.2. Σύνθεση: ραστική ουσία: Mometasone furoate. Έκδοχα: α) Κρέµα: White
Mometasone/Target Mometasone furoate ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1. Ονοµασία: Mometasone/Target 1.2. Σύνθεση: ραστική ουσία: Mometasone furoate. Έκδοχα: α) Κρέµα: White
Ο νεφρώνας είναι το πιο σημαντικο μερος των νεφρων υγρα και ηλεκτρολυτες
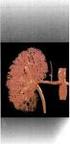 ΔΙΟΥΡΗΤΙΚΑ Ο νεφρώνας είναι το πιο σημαντικο μερος των νεφρων υγρα και ηλεκτρολυτες Σχηματισμος ουρων: 1. Σπειραματικη διηθηση (GFR) = 180L/day 2. Σωληναριακη επαναρροφηση(περιπου 98%) 3. Σωληναριακη απεκκριση
ΔΙΟΥΡΗΤΙΚΑ Ο νεφρώνας είναι το πιο σημαντικο μερος των νεφρων υγρα και ηλεκτρολυτες Σχηματισμος ουρων: 1. Σπειραματικη διηθηση (GFR) = 180L/day 2. Σωληναριακη επαναρροφηση(περιπου 98%) 3. Σωληναριακη απεκκριση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ MAG-2 διάλυµα πόσιµο σε συσκευασία µιας δόσης 1,5 g / 10 ml VIAL (ORAL) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 10 ml περιέχουν
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ MAG-2 διάλυµα πόσιµο σε συσκευασία µιας δόσης 1,5 g / 10 ml VIAL (ORAL) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 10 ml περιέχουν
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SmPC) NEPHROTECT. 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Nephrotect, διάλυµα για έγχυση
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SmPC) NEPHROTECT 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Nephrotect, διάλυµα για έγχυση 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1000 ml περιέχουν: L-isoleucine
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SmPC) NEPHROTECT 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Nephrotect, διάλυµα για έγχυση 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1000 ml περιέχουν: L-isoleucine
ROIPLON (Etofenamate)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΙΟΝΤΟΣ ROIPLON (Etofenamate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ ROIPLON 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ 5% ή 10% Etofenamate. 3. ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΙΟΝΤΟΣ ROIPLON (Etofenamate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ ROIPLON 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ 5% ή 10% Etofenamate. 3. ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ
AMINOPLASMAL HEPA-10%
 AMINOPLASMAL HEPA-10% ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1.ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Αminoplasmal Hepa 10% 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 1000ml διαλύματος περιέχουν: L-Isoleucin
AMINOPLASMAL HEPA-10% ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1.ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Αminoplasmal Hepa 10% 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 1000ml διαλύματος περιέχουν: L-Isoleucin
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ. T r a v o g e n (Isoconazole)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ T r a v o g e n (Isoconazole) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Travogen 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 g κολπικής κρέµας Travogen περιέχει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ T r a v o g e n (Isoconazole) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Travogen 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 g κολπικής κρέµας Travogen περιέχει
Κανένα για αυτήν την παρουσίαση. Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini,
 Κανένα για αυτήν την παρουσίαση Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini, 2 Κυκλοσπορίνη-θεραπευτικές ενδείξεις 3 Θεραπεία σοβαρών μορφών
Κανένα για αυτήν την παρουσίαση Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini, 2 Κυκλοσπορίνη-θεραπευτικές ενδείξεις 3 Θεραπεία σοβαρών μορφών
Ανακούφιση των συμπτωμάτων ήπιας έως μέτριας οστεοαρθρίτιδας των γονάτων.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Panadol 120 mg/5 ml πόσιμο εναιώρημα Παρακεταμόλη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Panadol 120 mg/5 ml πόσιμο εναιώρημα Παρακεταμόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Panadol 120 mg/5 ml πόσιμο εναιώρημα Παρακεταμόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,
Tormis 5 mg δισκία Tormis 10 mg δισκία Tορασεμίδη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 5 mg δισκία Tormis 10 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 5 mg δισκία Tormis 10 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ CLIMYCEN 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κλινδαµυκίνη φωσφορική 23,800mg που ισοδυναµεί µε 20mg κλινδαµυκίνη
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ CLIMYCEN 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κλινδαµυκίνη φωσφορική 23,800mg που ισοδυναµεί µε 20mg κλινδαµυκίνη
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 Depon â (Paracetamol) (Bristol Myers Squibb) ΑΝΑΛΓΗΤΙΚΟ -ΑΝTIΠΥΡΕΤIΚΟ ΜΟΡΦΕΣ ΕΝΗΛΙΚΩΝ ΔΙΣΚΙΑ ΑΠΛΑ, ΑΝΑΒΡΑΖΟΝΤΑ 500mg, ΑΝΑΒΡΑΖΟΝΤΑ 1000mg (MAXIMUΜ) ΚΑΙ ΥΠΟΘΕΤΑ ΔΡΑΣΗ: Το DEPON περιέχει σαν δραστική ουσία
Depon â (Paracetamol) (Bristol Myers Squibb) ΑΝΑΛΓΗΤΙΚΟ -ΑΝTIΠΥΡΕΤIΚΟ ΜΟΡΦΕΣ ΕΝΗΛΙΚΩΝ ΔΙΣΚΙΑ ΑΠΛΑ, ΑΝΑΒΡΑΖΟΝΤΑ 500mg, ΑΝΑΒΡΑΖΟΝΤΑ 1000mg (MAXIMUΜ) ΚΑΙ ΥΠΟΘΕΤΑ ΔΡΑΣΗ: Το DEPON περιέχει σαν δραστική ουσία
Ηλεκτρολυτικές διαταραχές των αλκοολικών. Γεώργιος Τουλκερίδης, Νεφρολόγος, Γενικό Νοσοκομείο Λάρνακας, Κύπρος
 Ηλεκτρολυτικές διαταραχές των αλκοολικών Γεώργιος Τουλκερίδης, Νεφρολόγος, Γενικό Νοσοκομείο Λάρνακας, Κύπρος Αλκοολισμός Διαταραχή από χρήση αλκοόλ (αιθανόλη C 2 H 6 O) 208.000.000 αλκοολικοί σε όλο τον
Ηλεκτρολυτικές διαταραχές των αλκοολικών Γεώργιος Τουλκερίδης, Νεφρολόγος, Γενικό Νοσοκομείο Λάρνακας, Κύπρος Αλκοολισμός Διαταραχή από χρήση αλκοόλ (αιθανόλη C 2 H 6 O) 208.000.000 αλκοολικοί σε όλο τον
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ Ι.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ORBIMAG 300 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε αναβράζον δισκίο περιέχει : 498 mg οξείδιο του μαγνησίου (ισοδύναμο με 300 Mg
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ Ι.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ORBIMAG 300 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε αναβράζον δισκίο περιέχει : 498 mg οξείδιο του μαγνησίου (ισοδύναμο με 300 Mg
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
Καταπράυνση της φλεγμονής και ανακούφιση του πόνου, τόσο σε οξείες, όσο και σε χρόνιες μυοσκελετικές διαταραχές σε άλογα.
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 15 mg/ml πόσιμο εναιώρημα για άλογα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη Έκδοχα: Sodium benzoate
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 15 mg/ml πόσιμο εναιώρημα για άλογα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη Έκδοχα: Sodium benzoate
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ HIDRASEC ΓΙΑ ΒΡΕΦΗ 10 mg κοκκία για πόσιμο εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει 10 mg
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ HIDRASEC ΓΙΑ ΒΡΕΦΗ 10 mg κοκκία για πόσιμο εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει 10 mg
Γάτες: Μείωση του μετεγχειρητικού πόνου μετά από ωοθηκυστερεκτομή και δευτερεύουσες επεμβάσεις στους μαλακούς ιστούς.
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για σκύλους και γάτες 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό(ά) συστατικό(ά): Μελοξικάμη 5 mg Έκδοχα:
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για σκύλους και γάτες 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό(ά) συστατικό(ά): Μελοξικάμη 5 mg Έκδοχα:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
O S T E O V I L E (Alfacalcidol)
 O S T E O V I L E (Alfacalcidol) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OSTEOVILE 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ OSTEOVILE 0,25 mcg/cap: Περιέχει 0,25 mcg/cap alfacalcidol
O S T E O V I L E (Alfacalcidol) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OSTEOVILE 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ OSTEOVILE 0,25 mcg/cap: Περιέχει 0,25 mcg/cap alfacalcidol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ (SPC) 2. ΠΟΙΟΤΙΚΗ &ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ (SPC) 1. ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ALDACTONE 2. ΠΟΙΟΤΙΚΗ &ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά Κάθε δισκίο περιέχει Spironolactone 25 mg ή 100 mg
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ (SPC) 1. ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ALDACTONE 2. ΠΟΙΟΤΙΚΗ &ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά Κάθε δισκίο περιέχει Spironolactone 25 mg ή 100 mg
ΠΑΙΔΙΑ ΚΑΙ ΦΑΡΜΑΚΑ. Γεώργιος Ι. Πανουτσόπουλος Δρ. Φυσιολογίας του Ανθρώπου Τμήμα Νοσηλευτικής Πανεπιστήμιο Πελοποννήσου
 ΠΑΙΔΙΑ ΚΑΙ ΦΑΡΜΑΚΑ Γεώργιος Ι. Πανουτσόπουλος Δρ. Φυσιολογίας του Ανθρώπου Τμήμα Νοσηλευτικής Πανεπιστήμιο Πελοποννήσου 1 Ο πρώτος χρόνος μετά τη γέννηση έχει τις μεγαλύτερες και ταχύτερες φυσιολογικές
ΠΑΙΔΙΑ ΚΑΙ ΦΑΡΜΑΚΑ Γεώργιος Ι. Πανουτσόπουλος Δρ. Φυσιολογίας του Ανθρώπου Τμήμα Νοσηλευτικής Πανεπιστήμιο Πελοποννήσου 1 Ο πρώτος χρόνος μετά τη γέννηση έχει τις μεγαλύτερες και ταχύτερες φυσιολογικές
ROIPLON Ενέσιμο διάλυμα 1g/2ml vial (Etofenamate)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial (Etofenamate) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 φύσιγγα
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial (Etofenamate) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 φύσιγγα
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ FORTEKOR FLAVOUR 5 mg Δισκία επικαλυμμένα με υμένιο για γάτες και σκύλους
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Δισκία επικαλυμμένα με υμένιο για γάτες και σκύλους 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Δισκία επικαλυμμένα με υμένιο για γάτες και σκύλους 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 2 mg/ml ενέσιμο διάλυμα για γάτες 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό(ά) συστατικό(ά): Μελοξικάμη 2 mg Έκδοχα: Αιθανόλη
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 2 mg/ml ενέσιμο διάλυμα για γάτες 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό(ά) συστατικό(ά): Μελοξικάμη 2 mg Έκδοχα: Αιθανόλη
Tormis 2,5 mg δισκία Tορασεμίδη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 2,5 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει σημαντικές
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 2,5 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει σημαντικές
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS, 500 mg / 400 IU Μασώμενα Δισκία 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστικές ουσίες Aσβέστιο..500 mg που αντιστοιχεί
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS, 500 mg / 400 IU Μασώμενα Δισκία 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστικές ουσίες Aσβέστιο..500 mg που αντιστοιχεί
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AIR SALONPAS 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 100 ml του αερολύµατος για τοπική χρήση περιέχουν: Methyl salicylate 1.75g
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AIR SALONPAS 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 100 ml του αερολύµατος για τοπική χρήση περιέχουν: Methyl salicylate 1.75g
Καταπράυνση της φλεγμονής και του πόνου τόσο στις οξείες όσο και στις χρόνιες μυοσκελετικές διαταραχές σε σκύλους.
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 0,5 mg/ml πόσιμο εναιώρημα για σκύλους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 0,5 mg (ισοδυναμεί με
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 0,5 mg/ml πόσιμο εναιώρημα για σκύλους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 0,5 mg (ισοδυναμεί με
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό + επινεφρίνη ή νορεπινεφρίνη
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ III 1 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 4. ΚΛΙΝΙΚΑ ΣΤΟΙΧΕΙΑ 4.1 Θεραπευτικές ενδείξεις Θεραπεία του οξέος πόνου (βλ. παράγραφο 4.2). Συµπτωµατική θεραπεία της επώδυνης οστεοαρθρίτιδας
ΠΑΡΑΡΤΗΜΑ III 1 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 4. ΚΛΙΝΙΚΑ ΣΤΟΙΧΕΙΑ 4.1 Θεραπευτικές ενδείξεις Θεραπεία του οξέος πόνου (βλ. παράγραφο 4.2). Συµπτωµατική θεραπεία της επώδυνης οστεοαρθρίτιδας
ΙΑΤΡΙΚΗ ΦΑΡΜΑΚΟΛΟΓΙΑ ΑΥΤΟΧΘΟΝΑ ΒΙΟ ΡΑΣΤΙΚΑ ΜΟΡΙΑ. Π. Παππάς
 ΙΑΤΡΙΚΗ ΦΑΡΜΑΚΟΛΟΓΙΑ ΑΥΤΟΧΘΟΝΑ ΒΙΟ ΡΑΣΤΙΚΑ ΜΟΡΙΑ Π. Παππάς ΑΥΤΟΧΘΟΝΑ ΒΙΟ ΡΑΣΤΙΚΑ ΜΟΡΙΑ Κατηγορίες ιστικών ορµονών Αποκαρβοξυλιωµένα αµινοξέα (ισταµίνη, σεροτονίνη) Πολυπεπτίδια (κινίνες, ουσία Ρ) Εικοσανοειδή
ΙΑΤΡΙΚΗ ΦΑΡΜΑΚΟΛΟΓΙΑ ΑΥΤΟΧΘΟΝΑ ΒΙΟ ΡΑΣΤΙΚΑ ΜΟΡΙΑ Π. Παππάς ΑΥΤΟΧΘΟΝΑ ΒΙΟ ΡΑΣΤΙΚΑ ΜΟΡΙΑ Κατηγορίες ιστικών ορµονών Αποκαρβοξυλιωµένα αµινοξέα (ισταµίνη, σεροτονίνη) Πολυπεπτίδια (κινίνες, ουσία Ρ) Εικοσανοειδή
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ. 1.1 Ονομασία: PLATAMINE Ενέσιμο διάλυμα 10mg/20ml vial και 50mg/100ml vial.
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. Προσδιορισμός φαρμακευτικού προϊόντος 1.1 Ονομασία: PLATAMINE Ενέσιμο διάλυμα 10mg/20ml vial και 50mg/100ml vial. 1.2 Σύνθεση: Δραστική ουσία: Σισπλατίνη (Cisplatin) Έκδοχα:
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. Προσδιορισμός φαρμακευτικού προϊόντος 1.1 Ονομασία: PLATAMINE Ενέσιμο διάλυμα 10mg/20ml vial και 50mg/100ml vial. 1.2 Σύνθεση: Δραστική ουσία: Σισπλατίνη (Cisplatin) Έκδοχα:
Εφαρμογές αρχών φαρμακολογίας
 Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g macrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g macrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ XATRAL OD 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο Χatral OD παρατεταμένης αποδέσμευσης περιέχει 10 mg υδροχλωρικής
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ XATRAL OD 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο Χatral OD παρατεταμένης αποδέσμευσης περιέχει 10 mg υδροχλωρικής
Καταπράυνση της φλεγμονής και του πόνου τόσο στις οξείες όσο και στις χρόνιες μυοσκελετικές διαταραχές σε σκύλους.
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 1 mg μασώμενα δισκία για σκύλους Metacam 2,5 mg μασώμενα δισκία για σκύλους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα μασώμενο δισκίο περιέχει: Δραστικό(ά)
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 1 mg μασώμενα δισκία για σκύλους Metacam 2,5 mg μασώμενα δισκία για σκύλους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα μασώμενο δισκίο περιέχει: Δραστικό(ά)
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης
 Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
Παράρτημα ΙΙΙ. Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης
 Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης Σημείωση : Οι τροποποιήσεις στην Περίληψη των Χαρακτηριστικών του Προϊόντος
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης Σημείωση : Οι τροποποιήσεις στην Περίληψη των Χαρακτηριστικών του Προϊόντος
1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ RIMADYL injectable solution 2. ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΟ( Α) ΚΑΙ ΑΛΛΕΣ ΟΥΣΙΕΣ Δραστικό( ά) συστατικό( ά ) : Το προϊόν περιέχει 50 mg καρπροφένης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ RIMADYL injectable solution 2. ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΟ( Α) ΚΑΙ ΑΛΛΕΣ ΟΥΣΙΕΣ Δραστικό( ά) συστατικό( ά ) : Το προϊόν περιέχει 50 mg καρπροφένης
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g Μacrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g Μacrogol
ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ. Λειτουργία των νεφρών. Συμπτώματα της χρόνιας νεφρικής ανεπάρκειας
 ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ Η χρόνια νεφρική ανεπάρκεια είναι η προοδευτική, μη αναστρέψιμη μείωση της νεφρικής λειτουργίας, η οποία προκαλείται από βλάβη του νεφρού ποικίλης αιτιολογίας. Η χρόνια νεφρική ανεπάρκεια
ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ Η χρόνια νεφρική ανεπάρκεια είναι η προοδευτική, μη αναστρέψιμη μείωση της νεφρικής λειτουργίας, η οποία προκαλείται από βλάβη του νεφρού ποικίλης αιτιολογίας. Η χρόνια νεφρική ανεπάρκεια
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE. Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ:
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: MEGACE 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: MEGACE 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann, Μασώμενα δισκία, (100 + 0,350) mg/δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ (σε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Ferrum Fol Hausmann, Μασώμενα δισκία, (100 + 0,350) mg/δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ (σε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Afluon nasal spray SPC 13 EMA (GR120306) 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AFLUON 0,1% w/v ρινικό εκνέφωμα, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Διάλυμα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Afluon nasal spray SPC 13 EMA (GR120306) 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AFLUON 0,1% w/v ρινικό εκνέφωμα, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Διάλυμα
Περιεχόμενα. 1. Εισαγωγή Εισαγωγή Σημασία των νεφρών στη ζωή Βιβλιογραφία Δομή και λειτουργία των νεφρών...
 Περιεχόμενα 1. Εισαγωγή... 1 1. Εισαγωγή... 1 2. Σημασία των νεφρών στη ζωή... 4 3. Βιβλιογραφία... 6 2. Δομή και λειτουργία των νεφρών... 7 1. Εισαγωγή... 8 2. Νεφρικά αγγεία... 9 3. Νεφρικό σπείραμα...
Περιεχόμενα 1. Εισαγωγή... 1 1. Εισαγωγή... 1 2. Σημασία των νεφρών στη ζωή... 4 3. Βιβλιογραφία... 6 2. Δομή και λειτουργία των νεφρών... 7 1. Εισαγωγή... 8 2. Νεφρικά αγγεία... 9 3. Νεφρικό σπείραμα...
Φαρμακοκινητική. Χρυσάνθη Σαρδέλη
 Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
Αμέσως δρώντα αγγειοδιασταλτικά, α-αποκλειστές, νιτρώδη: πού, πότε, πώς
 Αμέσως δρώντα αγγειοδιασταλτικά, α-αποκλειστές, νιτρώδη: πού, πότε, πώς Ηρακλής Αβραμόπουλος Παθολόγος Ιατρείο Υπέρτασης Νοσοκομείο Υγεία Αμέσως δρώντα αγγειοδιασταλτικά ΒΒ Χάλαση των αγγείων Δραστηριότητα
Αμέσως δρώντα αγγειοδιασταλτικά, α-αποκλειστές, νιτρώδη: πού, πότε, πώς Ηρακλής Αβραμόπουλος Παθολόγος Ιατρείο Υπέρτασης Νοσοκομείο Υγεία Αμέσως δρώντα αγγειοδιασταλτικά ΒΒ Χάλαση των αγγείων Δραστηριότητα
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Cetirizine Dihydrochloride
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
Trileptal Oxcarbazepine (οξκαρβαζεπίνη) Αντιεπιληπτικό ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ. Trileptal δισκία των 300 mg και 600 mg. Oxcarbazepine (Οξκαρβαζεπίνη).
 Oxcarbazepine (οξκαρβαζεπίνη) Αντιεπιληπτικό ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ δισκία των 300 mg και 600 mg. Oxcarbazepine (Οξκαρβαζεπίνη). ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστική ουσία: 10,11 - Dihydro-10-οχο-5Η-dibenz
Oxcarbazepine (οξκαρβαζεπίνη) Αντιεπιληπτικό ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ δισκία των 300 mg και 600 mg. Oxcarbazepine (Οξκαρβαζεπίνη). ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστική ουσία: 10,11 - Dihydro-10-οχο-5Η-dibenz
Διουρητικά και νεφροπάθειες
 Διουρητικά και νεφροπάθειες Μελεξοπούλου Χριστίνα Νεφρολόγος Γ.Ν.Α. Λαϊκό Μαθήματα Φυσιολογίας 2017 Διουρητικά: ουσίες που προκαλούν αύξηση του ρυθμού παραγωγής των ούρων Δρουν με ελάττωση του ρυθμού της
Διουρητικά και νεφροπάθειες Μελεξοπούλου Χριστίνα Νεφρολόγος Γ.Ν.Α. Λαϊκό Μαθήματα Φυσιολογίας 2017 Διουρητικά: ουσίες που προκαλούν αύξηση του ρυθμού παραγωγής των ούρων Δρουν με ελάττωση του ρυθμού της
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά : α) Κάθε φιαλίδιο πόσιμου διαλύματος
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SUPERAMIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά : α) Κάθε φιαλίδιο πόσιμου διαλύματος
Νεφρική ρύθμιση Καλίου, Ασβεστίου, Φωσφόρου και Μαγνησίου. Βασίλης Φιλιόπουλος Νεφρολόγος Γ.Ν.Α «Λαϊκό»
 Νεφρική ρύθμιση Καλίου, Ασβεστίου, Φωσφόρου και Μαγνησίου Βασίλης Φιλιόπουλος Νεφρολόγος Γ.Ν.Α «Λαϊκό» Κάλιο Το 98% του ολικού Κ + του σώματος βρίσκεται στο εσωτερικό των κυττάρων Το 2% στο εξωκυττάριο
Νεφρική ρύθμιση Καλίου, Ασβεστίου, Φωσφόρου και Μαγνησίου Βασίλης Φιλιόπουλος Νεφρολόγος Γ.Ν.Α «Λαϊκό» Κάλιο Το 98% του ολικού Κ + του σώματος βρίσκεται στο εσωτερικό των κυττάρων Το 2% στο εξωκυττάριο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) WARTEC 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) WARTEC 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ WARTEC 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά Οξινο αιθανολικό διάλυμα Podophyllotoxin
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) WARTEC 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ WARTEC 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά Οξινο αιθανολικό διάλυμα Podophyllotoxin
FLORKEM 300 mg/ml ενέσιµο διάλυµα για βοοειδή και χοίρους
 FLORKEM 300 mg/ml ενέσιµο διάλυµα για βοοειδή και χοίρους ΣΥΝΘΕΣΗ 1 ml περιέχει: Florfenicol.300 mg Ωχρο-κίτρινο έως διαυγές κίτρινο διάλυµα. ΕΝ ΕΙΞΕΙΣ Λοιµώξεις που οφείλονται σε βακτήρια ευαίσθητα στη
FLORKEM 300 mg/ml ενέσιµο διάλυµα για βοοειδή και χοίρους ΣΥΝΘΕΣΗ 1 ml περιέχει: Florfenicol.300 mg Ωχρο-κίτρινο έως διαυγές κίτρινο διάλυµα. ΕΝ ΕΙΞΕΙΣ Λοιµώξεις που οφείλονται σε βακτήρια ευαίσθητα στη
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ FYSIOFOL 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: FYSIOFOL
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ FYSIOFOL 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: FYSIOFOL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Iron proteinsuccinylate + calcium folinate
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ FYSIOFOL 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: FYSIOFOL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Iron proteinsuccinylate + calcium folinate
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 4g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει: Macrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 4g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει: Macrogol
Νεφρική ρύθμιση όγκου αίματος και εξωκυτταρίου υγρού. Βασίλης Φιλιόπουλος Νεφρολόγος Γ.Ν.Α «Λαϊκό»
 Νεφρική ρύθμιση όγκου αίματος και εξωκυτταρίου υγρού Βασίλης Φιλιόπουλος Νεφρολόγος Γ.Ν.Α «Λαϊκό» Διαμερίσματα σωματικών υγρών 28,0 L Νεφρικοί μηχανισμοί ρύθμισης εξωκυτταρίου υγρού Ο όγκος του εξωκυτταρίου
Νεφρική ρύθμιση όγκου αίματος και εξωκυτταρίου υγρού Βασίλης Φιλιόπουλος Νεφρολόγος Γ.Ν.Α «Λαϊκό» Διαμερίσματα σωματικών υγρών 28,0 L Νεφρικοί μηχανισμοί ρύθμισης εξωκυτταρίου υγρού Ο όγκος του εξωκυτταρίου
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, Thursday, 20 December :49 -
 Ζιρτέκ (Ζirtek) Cetirizine Dihydrochloride Δισκία επικαλυμένα με λεπτό υμένιο ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΠΑΤΟ ΧΡΗΣΤΗ 1. Προσδιορισμός φαρμακευτικού προϊόντος 1.1 Εμπορική ονομασία φαρμάκου: ΖΙΡΤΕΚ 1.2 Σύνθεση Δραστική
Ζιρτέκ (Ζirtek) Cetirizine Dihydrochloride Δισκία επικαλυμένα με λεπτό υμένιο ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΠΑΤΟ ΧΡΗΣΤΗ 1. Προσδιορισμός φαρμακευτικού προϊόντος 1.1 Εμπορική ονομασία φαρμάκου: ΖΙΡΤΕΚ 1.2 Σύνθεση Δραστική
Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών
 Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών Οι ρευματικές παθήσεις είναι συχνές στην αναπαραγωγική ηλικία των γυναικών. Στην πρόσφατη πανελλήνια επιδημιολογική έρευνα για τις ρευματικές παθήσεις στο γενικό
Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών Οι ρευματικές παθήσεις είναι συχνές στην αναπαραγωγική ηλικία των γυναικών. Στην πρόσφατη πανελλήνια επιδημιολογική έρευνα για τις ρευματικές παθήσεις στο γενικό
VOMEX A ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. Ονομασία, μορφή : VOMEX A. Ενέσιμο διάλυμα: 100 mg/2ml ΑΜP
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Ονομασία, μορφή : Ενέσιμο διάλυμα: 100 mg/2ml ΑΜP Σιρόπι: 16.5 mg/5 ml Σύνθεση -Δραστικά συστατικά : Διμενυδρινάτη (Dimenhydrinate)
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Ονομασία, μορφή : Ενέσιμο διάλυμα: 100 mg/2ml ΑΜP Σιρόπι: 16.5 mg/5 ml Σύνθεση -Δραστικά συστατικά : Διμενυδρινάτη (Dimenhydrinate)
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FYSIOFER 800 (40 Fe +3 ) mg/15ml VIAL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Κάθε φιαλίδιο FYSIOFER
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FYSIOFER 800 (40 Fe +3 ) mg/15ml VIAL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Κάθε φιαλίδιο FYSIOFER
2.2 Ποσοτική σύνθεση 100ml διαλύματος περιέχουν 25g πρωτεΐνης πλάσματος με τουλάχιστον το 95% ανθρώπινη λευκωματίνη.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Plasbumin 25 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 2.1 Ποιοτική σύνθεση Ανθρώπινη λευκωματίνη από ανθρώπινο πλάσμα 2.2 Ποσοτική
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Plasbumin 25 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 2.1 Ποιοτική σύνθεση Ανθρώπινη λευκωματίνη από ανθρώπινο πλάσμα 2.2 Ποσοτική
Συγκέντρωση Ηλεκτρολυτών (m Eq/L) : Sodium 140, Potassium 10, Calcium 5, Magnesium 3, Chloride 103, Acetate 47, Citrate 8.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ELECTROLYTE/FRESENIUS, διάλυµα για ενδοφλέβια έγχυση. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 1000 ml περιέχουν : Sodium Acetate
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ELECTROLYTE/FRESENIUS, διάλυµα για ενδοφλέβια έγχυση. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 1000 ml περιέχουν : Sodium Acetate
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 1. ΟΝΟΜΑΣΙΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 1. ΟΝΟΜΑΣΙΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ
Ο ρόλος της υπερδιήθησης στο Καρδιονεφρικό Σύνδροµο.! Ιωάννης Μακρής Νοσηλευτής MSc Μ.Τ.Ν. ΓΝΑ «Ιπποκράτειο»
 Ο ρόλος της υπερδιήθησης στο Καρδιονεφρικό Σύνδροµο Ιωάννης Μακρής Νοσηλευτής MSc Μ.Τ.Ν. ΓΝΑ «Ιπποκράτειο» Καρδιονεφρικό Σύνδροµο (CRS) Ορισµός Οι διαταραχές της καρδιάς και των νεφρών, όπου οξεία ή χρόνια
Ο ρόλος της υπερδιήθησης στο Καρδιονεφρικό Σύνδροµο Ιωάννης Μακρής Νοσηλευτής MSc Μ.Τ.Ν. ΓΝΑ «Ιπποκράτειο» Καρδιονεφρικό Σύνδροµο (CRS) Ορισµός Οι διαταραχές της καρδιάς και των νεφρών, όπου οξεία ή χρόνια
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1/5 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1/5 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Postinor 1500 1500 µικρογραµµάρια ισκίο 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1500 µικρογραµµάρια λεβονοργεστρέλης
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Postinor 1500 1500 µικρογραµµάρια ισκίο 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1500 µικρογραµµάρια λεβονοργεστρέλης
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ MESTINON 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε επικαλυμμένο δισκίο περιέχει 60 mg της δραστικής ουσιάς βρωμιούχος πυριδοστιγμίνη
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ MESTINON 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε επικαλυμμένο δισκίο περιέχει 60 mg της δραστικής ουσιάς βρωμιούχος πυριδοστιγμίνη
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. 194.1μg 99μg
 1 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VITALIPID ( ADULT ) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1ml VITALIPID ADULT περιέχει: Δραστικά συστατικά Retinopalmitate
1 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VITALIPID ( ADULT ) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1ml VITALIPID ADULT περιέχει: Δραστικά συστατικά Retinopalmitate
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLUTAMOL
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLUTAMOL 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ GLUTAMOL, Πυκνό διάλυμα για παρασκευή διαλύματος προς έγχυση 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLUTAMOL 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ GLUTAMOL, Πυκνό διάλυμα για παρασκευή διαλύματος προς έγχυση 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙOΝΤΟΣ: duphalac 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Το υδατικό πόσιμο διάλυμα (σιρόπι) LACTULOSE περιέχει 3,335 g λακτουλόζης ανά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙOΝΤΟΣ: duphalac 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Το υδατικό πόσιμο διάλυμα (σιρόπι) LACTULOSE περιέχει 3,335 g λακτουλόζης ανά
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΞΕΝΟΒΙΟΤΙΚΩΝ ΟΥΣΙΩΝ ΣΤΑ ΒΙΟΛΟΓΙΚΑ ΔΕΙΓΜΑΤΑ
 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΞΕΝΟΒΙΟΤΙΚΩΝ ΟΥΣΙΩΝ ΣΤΑ ΒΙΟΛΟΓΙΚΑ ΔΕΙΓΜΑΤΑ ΞΕΝΟΒΙΟΤΙΚΗ ΟΥΣΙΑ χημική ουσία που δεν παράγεται στον οργανισμό και εισαγόμενη στον οργανισμό δεν αξιοποιείται για την εξασφάλιση ενέργειας ή σύνθεση
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΞΕΝΟΒΙΟΤΙΚΩΝ ΟΥΣΙΩΝ ΣΤΑ ΒΙΟΛΟΓΙΚΑ ΔΕΙΓΜΑΤΑ ΞΕΝΟΒΙΟΤΙΚΗ ΟΥΣΙΑ χημική ουσία που δεν παράγεται στον οργανισμό και εισαγόμενη στον οργανισμό δεν αξιοποιείται για την εξασφάλιση ενέργειας ή σύνθεση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1.ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: ARTHROLOC 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά: Crystalline glucosamine sulphate 1,884 g / SACHET
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1.ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: ARTHROLOC 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά: Crystalline glucosamine sulphate 1,884 g / SACHET
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:100000 ARTICAINE HYDROCHLORIDE & ADRENALINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:100000 ARTICAINE HYDROCHLORIDE & ADRENALINE
ΤΡΕΧΟΥΣΕΣ Ο ΗΓΙΕΣ ΓΙΑ ΤΗ ΧΡΗΣΗ ΑΝΤΙ-ΙΙΚΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΑΣΘΕΝΩΝ ΜΕ ΓΡΙΠΗ ΑΠΟ ΤΟ ΝΕΟ ΙΟ Α/Η1Ν1 ΚΑΙ ΤΩΝ ΣΤΕΝΩΝ ΕΠΑΦΩΝ ΤΟΥΣ
 ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ ΤΡΕΧΟΥΣΕΣ Ο ΗΓΙΕΣ ΓΙΑ ΤΗ ΧΡΗΣΗ ΑΝΤΙ-ΙΙΚΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΑΣΘΕΝΩΝ ΜΕ ΓΡΙΠΗ ΑΠΟ ΤΟ ΝΕΟ ΙΟ Α/Η1Ν1 ΚΑΙ ΤΩΝ ΣΤΕΝΩΝ ΕΠΑΦΩΝ ΤΟΥΣ Ιούλιος 2009 Το παρόν έγγραφο
ΥΠΟΥΡΓΕΙΟ ΥΓΕΙΑΣ ΚΑΙ ΚΟΙΝΩΝΙΚΗΣ ΑΛΛΗΛΕΓΓΥΗΣ ΤΡΕΧΟΥΣΕΣ Ο ΗΓΙΕΣ ΓΙΑ ΤΗ ΧΡΗΣΗ ΑΝΤΙ-ΙΙΚΩΝ ΓΙΑ ΤΗΝ ΑΝΤΙΜΕΤΩΠΙΣΗ ΑΣΘΕΝΩΝ ΜΕ ΓΡΙΠΗ ΑΠΟ ΤΟ ΝΕΟ ΙΟ Α/Η1Ν1 ΚΑΙ ΤΩΝ ΣΤΕΝΩΝ ΕΠΑΦΩΝ ΤΟΥΣ Ιούλιος 2009 Το παρόν έγγραφο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DOLAL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ DOLAL SYR 125MG/5ML: Κάθε 1 ml προϊόντος περιέχει 25mg παρακεταμόλης.
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DOLAL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ DOLAL SYR 125MG/5ML: Κάθε 1 ml προϊόντος περιέχει 25mg παρακεταμόλης.
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 of 7 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Calcioral D 3 1000 mg + 20 µg (800 IU) µασώµενο δισκίο 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα δισκίο περιέχει: Ασβέστιο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 of 7 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Calcioral D 3 1000 mg + 20 µg (800 IU) µασώµενο δισκίο 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα δισκίο περιέχει: Ασβέστιο
SALONPAS HOT â (Capsicum extract)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â (Capsicum extract) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε έµπλαστρο SALONPAS HOT â, µεγέθους
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â (Capsicum extract) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε έµπλαστρο SALONPAS HOT â, µεγέθους
PANADOL ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 PANADOL ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Panadol Δισκία επικαλυμμένα με λεπτό υμένιο 500mg/TAB, δισκία αναβράζοντα 500mg/E.F. TAB, πόσιμο διάλυμα 160mg/5ml,
PANADOL ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Panadol Δισκία επικαλυμμένα με λεπτό υμένιο 500mg/TAB, δισκία αναβράζοντα 500mg/E.F. TAB, πόσιμο διάλυμα 160mg/5ml,
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 Πολυσακχαριδικό πολυδύναμο εμβόλιο ττνευμονιόκοκκου 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 PNEUMO 23* Ενέσιμο διάλυμα 25 mcg χ 23 / 0,5 ml P.F.Syringe (1 Dose) 1.2 Σύνθεση Δραστική ουσία: Purified
Πολυσακχαριδικό πολυδύναμο εμβόλιο ττνευμονιόκοκκου 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 PNEUMO 23* Ενέσιμο διάλυμα 25 mcg χ 23 / 0,5 ml P.F.Syringe (1 Dose) 1.2 Σύνθεση Δραστική ουσία: Purified
