ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
|
|
|
- Ναθαναήλ Παχής
- 6 χρόνια πριν
- Προβολές:
Transcript
1 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord lihtsustamise või eelduse abil lahendamine on mitte ainult mõistlik, vaid ka ainus võimalus Tavaliselt on olemas ka üldisem lahendamise võimalus, mis on aeganõudev, kuid samal ajal kindlaim See on viidud kõikide võrrandi muutujate süstemaatilisele loendamisele: M(E)= m n ω(e) 1 ω(e) M(E* ) Samas on ilmtingimata vaja kontrollida kõikvõimalikud m ja n väärtused valemiga * E n E m, kus E * võib olla nii aatomite grupp, näiteks C Soovitatav on koostada mustandis tulemuste tabel Tabel aitab aega kokku hoida lahenduste kontrollimisel olukorras, kus õiget vastust pole õnnestunud leida mõne vea tõttu Seepärast tuleb ka mustand koostada hoolikalt, kuid samal ajal selle vormistamisele liigset aega kulutamata Süstemaatiline lähenemine võib tunduda ebavajalik piirkondlike ja vabariiklike voorude ülesannete lahendamisel, kuid see on ilmtingimata vajalik rahvusvaheliste olümpiaadide ülesannete lahendamisel ÜLESANNE 1 Stabiilse soola kristallhüdraat sisaldab 2,79% H; 9,97% C ja 38,48% elementi A Kristallhüdraadi kuumutamisel 800 o C juures moodustub oksiid hapnikusisaldusega 14,73% Kuumutamisel madalamal temperatuuril moodustub ühend, mis sisaldab 5,80% C; 67,13% elementi A ja 27,07% Leidke kristallhüdraadi valem LAHENDUS: Elemendi A molaarmassi oksiidis koostisega A x y võib leida valemiga: M(A)= y x ω(a) ω() 16,00 g mol = y x 85,27% 14,73% 16,00 g mol 1
2 Kui x=2 ja y=3 saame A molaarmassiks 138,9, molaarmassile Lantaanoksiid on La 2 3 g mol mis vastab La (lantaani) Kristallhüdraadi ja vahesaaduse empiirilised valemid võib leida elementide protsendilise sisalduse järgi: (La C 3 11 H 10 ) m ja (La 2 C 2 7 ) n Tõenäoliselt on kristallhüdraat mingisuguse orgaanilise happe sool, vahesaadus on aga karbonaat Sobiv orgaaniline hape on oblikhape, sellele vastab soola La 2 (C 2 4 ) 3 10H 2 Vahesaaduse valem on La 2 (C 3 Nüüd vaatame ülesandeid, milles on aine protsendilise koostise asemel antud aine mass ÜLESANNE 2 0,300 g lihtainet A soojendati kloori voolus; jahutamisel jääga koguti vastuvõtjasse 1,06 g roosakat tahket ainet В Valge ühend С, mis saadi ühendi В kuumutamisel, lahustati väikeses koguses vees Lahus aurutati kuivaks ja saadi tahke aine D Ühendit D kuumutati temperatuuril üle 400 C ja saadi 0,403 g valget tahket ainet F Ainet F kuumutati vesiniku voolus ja saadi 0,300 g esialgset ühendit А LAHENDUS: Määrake ained A F Ülesande tekstis lähtuvalt on lihtaine A metall, B kloriid ning F oksiid ksiidide puhul on valem M( A) arvutamiseks järgmine: Kirjutame valemi ümber: M(A)= y x ω(a) ω() 16,00 g mol 2
3 0,300 M(A)= y x 0,403 16,00 g 0,403 0,300 mol = y x 0,300 0,403 0,300 16,00 g mol 0,403 Kui x=2, y=3, M(A)=69,9 g mol Kloriidide puhul on valem M(A) arvutamiseks järgmine: Taaskord kirjutame valemi kujul: M(A)= y x ω(a) ω(cl) 35,45 g mol 0,300 M(A)= y x 1,06 35,45 g 1,06 0,300 mol = y x 0,300 1,06 0,300 35,45 g mol 0,403 Kui x=1, y=5, M(A)=70,0 g mol Järelikult on element A gallium, ühend B on kloriid GaCl 5 ; ühend C on kloriid GaCl 3 ; ühend D on hüdroksiid Ga(H) 3 ; ühend F on oksiid, Ga 2 3 Pole üllatav, et galliumi oksüdatsiooniaste on 5 See on võimalik tänu doonoraktseptor sidemele Sarnaselt NH 3 -ga, mis moodustab [H 3 N:H] +, moodustab GaCl 3 -ga ühendit Cl 3 Ga: Cl 2, kus Cl on doonor ja Ga on aktseptor Viimase ülesande näitel on näha, et mida kõrgem on olümpiaadi tase, seda keerulisemad võivad olla nii lahendus kui ka ülesande andmed Kusjuures keeruline on see just keemia seisukohast, ning seda ülesannet pole võimalik lihtsasti lahendada pelgalt keemiaalaseid süllogisme kasutades Sellisel juhul on lahenduse võtmeks kõige "lihtsama" aine, tavaliselt oksiidi või elemendi, valemi leidmine Nüüd, kui te teate, et selle "võtme" leidmiseks on vajalik süstemaatiline 3
4 HAPNIK lähenemine ja oskate teha lihtsustusi ja eeldusi, on lootust, et rasked ülesanded saavad teile jõukohasteks Alljärgneva eesmärk on tutvustada olümpiaadiülesannetes enim kasutustleidvate elementide mõningaid reaktsioone ning ühendeid selleks, et osata leida arvutuste tulemusel saadud elementide valikust just see, mis on antud ülesande jaoks sobivaim Hapnik on aktiivne mittemetall, mis oma elektronegatiivsuse poolest jääb alla ainult fluorile Enamasti ühendites oa -II, kuid esineb ka erandeid Näiteks: Na naatriumperoksiid, H vesinikperoksiid (oa -I), K 2 - kaaliumsuperoksiid (oa -0,5) ja mõningad hapniku fluoriidid nagu F 2 - hapnikdifluoriid (oa II) ning 2 F 2 - dihapnikdifluoriid (oa I) Lihtainena on 2 suhteliselt püsiv kaksiksideme ja väikeste mõõtmete tõttu See on ka põhjuseks, miks on hapniku keemiline aktiivsus palju väiksem, kui elektronegatiivsuse järgi võiks arvata Kuumutamisel on hapnik tugev oksüdeerija, mis reageerib enamiku lihtainetega Hapnikku on võimalik saada mõningate soolade kuumutamisel: 2KN to C 3 2KN KCl to C,kat 3 2KCl+32 2KMn to C 4 K 2 Mn 4 +Mn Ba 700o C 2 = 2Ba+ 2 Samuti ka vesinikperoksiidi lagunemisel: 2H 2 2 2H Hapnikule on iseloomulik moodustada binaarseid ühendeid oksiide IA ja IIA rühma metallide oksiidid ja superoksiidid on valged Erinevaid värvusi võivad omada d-metallide ja teiste A-rühma elementide oksiidid Mittemetallioksiididest esinevad tavatingimustel gaasilises olekus süsiniku, lämmastiku ja väävli oksiidid ning samuti osa halogeenioksiidid Gaasid pole räni, fosfori, boori, arseeni oksiidid, lisaks veel mõningad halogeenioksiidid ksiide võib saada: Metall/mittemetall+hapnik: 2Na+ 2 =Na 2 2 (naatriumperoksiidcu+ 2 =2Cu 2Mg+ 2 =2Mg K+ 2 =K 2 (kaltsiumsuperoksiid) 4 P+5 2 =P 4 10 S+ 2 =S 2 4
5 NB! Ioonilise sideme esinemisel hapnikuühendeis (IA ja IIA rühm) eristatakse: oksiidioone 2-2- ( Ca, K 2, Mg ) peroksiidioone 2 ( Ba 2, Na 2 2 ), superoksiidioone 2 - ( K 2, Rb 2 ) Binaarsete ühendite kuumutamisel hapniku juuresolekul: 2CuS+3 2 = to C2Cu+2S 2 Nitraatide, nitritite ja karbonaatide (va leelismetallide karbonaadid) termilisel lagunemisel: CaC 3 = to C Ca+C 2 2Cu(N 3 = to C 2 Cu+4N NH 4 N 2 = to CN 2 Lisaks lagunevad osa hüdroksiide (mitte LEELISMETALLID alates naatriumist) ja happed kuumutades: 4 HN 3 =4 N Ca(H =Ca 2 Al(H) 3 =Al 2 3 ksiididest reageerivad veega tugevalt aluselised ning paljud happelised oksiidid Neutraalsed ja amfoteersed oksiidid veega EI reageeri: Al 2 3 =EI REAGEERI S 3 =H 2 S 4 Ca =Ca(H Tugevalt aluseliste oksiidide (leelis- ja leelismuldmetallide oksiidid) reaktsioonil veega tekib hüdroksiid Nõrgalt aluselised oksiidid (näiteks Mn, Fe ja Cu) veega ei reageeri Happeliste oksiidide (va Si 2 ) reaktsioonil veega tekib hape Aluselised oksiidid reageerivad happega andes soola: Ca S 4 =CaS 4 Happelised oksiidid reageerivad alusega andes soola: S 3 +2NaH=Na 2 S 4 Amfoteersed oksiidid reageerivad kuumutamisel nii aluste kui hapetega: Al HCl = to C2 AlCl 3 Al 2 3 +konts 2NaH = to C2Na 3 [Al(H) 6 ] (kompleksühend) Tuntumad amfoteersed oksiidid on Al 2 3 ja Zn Mõningad oksiidid, kus teisel elemendil on tavapärasest kõrgem oksüdatsiooniaste, võivad käituda tugevate oksüdeerijatena nt Pb 2 ja Mn 2 : 5
6 Pb 2 +4HCl=PbCl 2 +Cl 2 VÄÄVEL Väävel on suhteliselt aktiivne mittemetall, mis võib käituda nii oksüdeerijana kui redutseerijana Peamised oksüdatsiooniastmed on -II, 0, (II), IV, VI Lihtainena esineb mitme allotroobina, millest kõige püsivamad koosnevad S 8 molekulidest Lihtainena vees praktiliselt ei lahustu ega reageeri Looduses leidub väävlit ehedana, kuid laboris on võimalik saada reaktsioonil: 2H 2 S+S 2 =3 S Väävel käitub oksüdeerijana kuumutamisel mitmete metallide ja vähemaktiivsete mittemetallidega H 2 +S=H 2 S Cu+S CuS Fe+S t o C FeS Redutseerijana käitub väävel kuumutamisel aktiivsemate mittemetallidega ning reaktsioonil tugevate oksüdeerijatega: S+ 2 =S 2 S+2Cl 2 =SCl 4 S+2konts H 2 S 4 =3S 2 3S+2KCl 3 =2KCl+3S 2 Vääveldioksiid S 2 terava lõhnaga happeliste omadustega mürgine gaas, mis on termiliselt väga püsiv Tekib väävli põletamisel Laboris saadakse sulfitile kontsentreeritud väävelhappe lisamisel: K 2 S 3 +2kontsH 2 S 4 =2KHS 4 +S 2 Ülekaalus redutseerivad omadused: S 2 +Cl 2 =S 2 Cl 2 Väävlishape H 2 S 3 on ebapüsiv hape, mis laguneb kuumutamisel: H 2 S 3 H2 +S 2 Väävlishape oksüdeerub kergesti, minnes juba õhuhapniku toimel aeglaselt üle väävelhappeks: 2H 2 S =2H 2 S 4 Samal ajal väga tugevate redutseerijate nt HI või H 2 S juuresolekul on oksüdeerija: H 2 S 3 S=3S Vääveltrioksiid S 3 tugev oksüdeerija, mida saadakse S 2 oksüdeerumisel kõrgel temperatuuril, kasutades katalüsaatorina Pt või V 2 5 6
7 Väävelhape H 2 S 4 viskoosne õlitaoline vedelik Kontsentreeritult väga tugev oksüdeerija, mis redoksreaktsiooni käigus läheb üle S 2, S või H 2 S Mida aktiivsem on reaktsioonil osalev metall ning mida kõrgem temperatuur, seda madalama oksüdatsiooniastmega saadus tekib Näiteks: 4 Zn+5 kontsh 2 S 4 4ZnS4 S+4H 2 Cu+2konts H 2 S 4 =CuS 4 +S 2 +2 H 2 Kontsentreeritud väävelhape oksüdeerib kuumutamisel ka mitmeid mittemetalle ning Br - ja I - vabaks halogeniidiks: C+2 kontsh 2 S 4 =C 2 +2S 2 2KI+konts2 H 2 S 4 =I 2 +K 2 S 4 +S 2 Lahjendatud väävelhappe reageerimisel metalliga käitub oksüdeerijana H + ioon: Ca+lahjH 2 S 4 =CaS 4 Divesiniksulfiid H 2 S väga tugev redutseerija Väga mürgine ning iseloomuliku mädamunalõhnaga H 2 S+Br 2 =2HBr +S H 2 S 2 =S Tioväävelhape H 2 S 2 3 suhteliselt tugev hape, mis on tavatingimustel väga ebapüsiv Tioväävelhappe soolad on kasutusel nii fotograafias, meditsiinis kui ka jodomeetrias Tiosulfaatidel on ülekaalus redutseerivad omadused, kuid omab ka oksüdeerivaid omadusi: Na 2 S Cl 2 +5 H 2 =2NaHS 4 +8HCl Saadakse sulfitite keetmisel väävli segus: Na 2 S 3 +S=Na 2 S 2 3 Lagunevad kergesti: Na 2 S HCl=S+S 2 +2 NaCl Na 2 S 2 3 S 4 =H 2 +S 2 +S+Na 2 S 4 Naatriumtiosulfaati kasutatakse jodomeetrias: 2Na 2 S 2 3 +I 2 =Na 2 S NaI (naatriumtetrationaat) RÄNI Kristalliline räni on hõbehall metallilise läikega kõva ja habras aine Amorfne räni on pruunikas pulber Põhiline looduslik mineraal Si 2 on liiva põhikomponent Räni tihedus on vedelas olekus suurem kui tahkes ning toatemperatuuril on keemiliselt passiivne pooljuht 7
8 Räni saadakse kõrgel temperatuuril ränidioksiidist: Si 2 +C=Si+2C või magneesiumit redutseerijana kasutades: Si 2 +2Mg=2Mg+Si Enamasti reaktsioonides käitub redutseerijana Toatemperatuuril reageerib räni ainult fluoriga: Si+2F 2 =SiF 4 Räni halogeniidühendite reaktsioonil veega tekib metaränihape: SiCl 4 +3 H 2 =H 2 Si 3 +4 HCl Väga kõrgetel temperatuuridel reageerib nii lämmastiku kui süsinikuga: Si+C=SiC 2N 2 +3 Si=Si 3 N 4 Räni reageerib energiliselt leelistega, mille tulemusena tekivad silikaadid Si +2KH=K 2 Si 3 või Si+4KH=K 4 Si 4 Räni reageerib ka lämmastikhappe ja vesinikfluoriidhappe segus: 3Si+4 HN 3 +18HF=3H 2 SiF 6 +4N+8H 2 Heksafluororänihapet saab ka reaktsioonil: SiF 4 +2HF=H 2 SiF 6 Heksafluororänihapete sooli on võimalik saada reaktsiooni: 2NaF+SiF 4 =Na 2 SiF 6 Aktiivsete metallidega reageerides on räni oksüdeerija, tekivad silitsiidid: Räni moodustab hüdriidi SiH 4 : 2Mg+Si=Mg 2 Si 1) sänihalogeniidi reaktsioonil liitiumalumiiniumhüdriidiga SiCl 4 +LiAlH 4 =SiH 4 +LiCl+AlCl 3 2) silitsiidide (räni oa -IV) lagundamisel hapete või leelistega Mg 2 Si+4HCl=SiH 4 +2MgCl 2 SiH 4 süttib õhus : SiH =Si 2, kuid aluselistes lahustes moodustab silikaadi SiH 4 +2KH =K 2 Si 3 +4H 2 Leeliste reageerimisel Si 2 -ga sulas olekus tekivad silikaadid, mis tekivad aeglaselt ka kuuma kontsentreeritud leeliste korral: Si 2 +4NaH Na4 Si 4 või Si 2 +2NaH Na2 Si 3 8
9 Silikaate saab ka soolade reageerimisel sulaolekus ränidioksiidiga, avalduvad ränidioksiidi happelised omadused ning gaasina eraldub soola aniooni kuulunud element: LÄMMASTIK CaC 3 +Si 2 = to CCaSi 3 +C 2 2K 2 S 4 +2Si 2 +C = to C 2Na2 Si 3 +2S 2 +C 2 Lämmastik on tüüpiline mittemetalliline element, mis jääb elektronegatiivsuselt alla ainult hapnikule ja fluorile ning on võrreldav klooriga Tavaliselt moodustab ühendeid, kus sidemete arv on 3 Erandiks on ammooniumühendid, kus lämmastikul on neli sidet Looduslikest mineraalidest on olulisemad tšiili salpeeter ( NaN 3 ), india salpeeter ( KN 3 ) ning norra salpeeter ( Ca(N 3 ) Lihtainena on lämmastik värvusetu, lõhnata gaas N 2 on vähe polariseeritav ning kolmiksideme tõttu on erakordselt püsiv Saamine: Laboris NH 4 N 2 kuumutamisel: NH 4 N 2 =N 2 Täiendavalt: (NH 4 Cr 2 7 Cr 2 3 +N 2 +4H 2 3Cu+2NH 3 N2 +3Cu 2N 2 2N2 + 2 NaN 3 2Na+3N2 Lämmastiku sidumine lihtainest teistesse ühenditesse on keerukas: o Haberi protsess: N 2 +3H to C, kat 2 = 2NH 3 o Tsüaanamiidi meetod: CaC 2 +N 2 C+CaCN2 CaCN 2 CaC3 +2NH 3 Kõrgel temperatuuril oksüdeerib lämmastik paljusid metalle ning mittemetalle, tekivad nitriidid (lämmastiku oa -III): 3Mg+N 2 =Mg 3 N 2 2B+N 2 =2BN 3H 2 +N 2 =2 NH 3 Aktiivse metalli nitriidi reageerimisel veega tekib vastav hüdroksiid ja ammoniaak: Li 3 N =3 LiH+NH 3 Aktiivse mittemetalli nitriidi reaktsioonil veega tekib hape ja ammoniaak: 9
10 NCl 3 =3HCl+NH 3 Amfoteersed ning vähemaktiivsete mittemetallide nitriidid on keemiliselt püsivad ja veega ei reageeri Ammoniaak NH 3 terava hingematva lõhnaga gaas Kõige paremini vees lahustuv gaas Väga hea elektronipaari doonor Tüüpiline ligand kompleksühendites: CuS 4 +4NH 3 H 2 =[Cu(NH 3 ) 4 ]S 4 +4 H 2 Hapetega ning happeliste oksiididega reageerimisel tekivad ammooniumsoolad: NH 3 +HBr=NH 4 Br Ammooniumsoolad lagunevad kuumutamisel: NH 4 Cl NH3 +HCl Ammoniaak oksüdeerub väga aeglaselt hapniku mõjul: Tugev redutseerija: 4 NH = to C 2N2 +6 H 2 2NH 3 +2Cr 3 =N 2 +Cr 2 3 2NH 3 +3Cu=N 2 +3Cu 8NH 3 +3Br 2 =N 2 +6NH 4 Br Hüdrasiin N 2 H 4 õhus suitsev, värvusetu sööbiv vedelik Nõrgem alus kui ammoniaak, kuid on kahe elektronipaari doonor Saamine: 2NH 3 +NaCl=N 2 H 4 +NaCl Tugev redutseerija: N 2 H 4 2 =N 2 +4H 2 N 2 H 4 +CuS 4 =N 2 +Cu S 4 Dilämmastikoksiid N 2 värvusetu meeldiva lõhnaga gaas, ei reageeri veega Tekitab eufooriat Segu vesinikuga on plahvatusohtlik: N 2 =N 2 Laboratoorselt saadakse ammooniumnitraadist: NH 4 N 3 N2 Nõrk oksüdeerija, kuid tugevate oksüdeerijate juures käitub redutseerijana: 2N 2 +S=S 2 +2N 2 5N 2 +8KMn 4 +7H 2 S 4 =5 Mn(N 3 +3MnS 4 +4K 2 S 4 +7H 2 Lämmastikoksiid N värvusetu mürgine gaas, neutraalne oksiid, paaritu elektronide arvuga, võib vaadelda kui radikaali 10
11 Saamine tööstuses: N 2 + to C, Pt 2 2N 4 NH3 +5 to C,Pt 2 4N+6H2 Saamine laboris: 3Cu+ lahj 8HN 3 =3Cu(N 3 +2N+4H 2 ksüdeerub kergesti, isegi õhuhapniku juures praktiliselt koheselt Reageerimisel Cl 2 -ga tekib nitrosüülkloriid: 2N+Cl 2 =2NCl Redutseerijate juuresolekul võib ka käituda oksüdeerijana: 2N S=N 2 +2S Lämmastikdioksiid N 2 punakaspruun mürgine gaas, vedelikuna pruunikaskollane Paaritu elektronide arvuga ning seetõttu võib vaadelda kui radikaali Keemiliselt aktiivne ning reageerib isegi külma veega: 2N 2 =HN 2 +HN 3 Kuumas vees tekkiv lämmastikushape laguneb ning tekib N: 3N 2 =2HN 3 +N Laboris saadakse N 2 : Cu+konts 4HN 3 =Cu(N 3 +2N 2 Keskmiste või väheaktiivsete metallide nitraatide kuumutamisel: 2Pb(N 3 4 N2 +2Pb+ 2 S+konts6 HN 3 =H 2 S 4 +6N 2 Lämmastikdioksiid on tugev oksüdeerija: 2S+2N 2 =2S 2 +N 2 8K+2N 2 =4K 2 +N 2 S 2 +N 2 =S 3 +N 2KI+2N 2 =I 2 +2 KN 2 Lämmastikushape HN 2 ebapüsiv hape, mis eksisteerib vaid vesilahustes Laguneb seismisel ja kuumutamisel: 3HN 2 =HN 3 +2N Lämmastikushappe soolad on püsivamad ning seetõttu saadakse lämmastikushapet nendest: KN 2 +HCl=HN 2 +KCl AgN 2 +HCl=HN 2 +AgCl Laboris saadakse lämmastikushapet aktiivsete metallide nitraatidest, tekib vastav nitrit: 2KN 3 2KN2 + 2 Nitritid on eelkõige redutseerijad, oksüdeerudes nitraatioonideks: 2KMn 4 +5NaN 2 S 4 =2MnS 4 +5 NaN 3 +K 2 S 4 11
12 NaN 2 +Pb 2 S 4 =NaN 3 +PbS 4 HN 2 +Br 2 =HN 3 +2HBr Redutseerijate toimel redutseerub ja tekib N : 2NaN 2 +2KI S 4 =I 2 +2N+K 2 S 4 +Na 2 S 4 Na 2 S+2NaN 2 S 4 =S+2N+2Na 2 S 4 Lämmastikhape HN 3 värvusetu suitsev vedelik, mis on kollakas N 2 tekke tõttu Vesilahuses tugev hape 4 HN 3 =4 N Reageerib aluste ning aluseliste oksiididega: Ba+2HN 3 =Ba(N 3 NaH+HN 3 =NaN 3 Lämmastikhape on tugev oksüdeerija Sõltuvalt kontsentratsioonist on saadused: N 2, N, N 2, N 2, NH 3 Konts HN 3 -ga tekib N 2 : Cu+konts 4HN 3 =Cu(N 3 +2N 2 Tugevalt lahjendatud HN 3 redutseerub aktiivsemate redusteerijate toimel NH 4 + -ks: 4 Mg+väga lahj10 HN 3 =4 Mg(N 3 +NH 4 N 3 Kergelt lahjendatud HN 3 redutseerub N -ks Saadused sõltuvad samuti metalli aktiivsusest: aktiivsete metallidega tekivad madalama oksüdatsiooniastmega saadused Kontsentreeritud lämmastikhappes passiveeruvad Fe, Al, Cr, Mn, Ni jmt Konts lämmastikhape oksüdeerib ka paljusid liitaineid: H 2 S+k 2HN 3 =S+2N 2 Fe+k 4HN 3 =Fe(N 3 ) 3 +N 2 +3 H 2 PbS+k8HN 3 Pb S4 +8N 2 +4H 2 Nitraadid lagunevad kuumutamisel erinevalt: o Aktiivsed metallid magneesiumist vasakul tekib hapnik ja vastav nitrit: 2NaN 3 2NaN2 + 2 o Enamiku metallide (magneesiumist vaseni) nitraatidest tekib metallioksiid ja N 2 : 2Cu(N 3 2Cu+4N
13 o Väga väheaktiivsete metallide nitraadid (vasest väheaktiivsemad väärismetallid ja elavhõbe) - tekib vaba metall: 2 AgN 3 2 Ag+N2 + 2 Kuna eraldub hapnik ja N 2, käituvad nitraadid tugeva oksüdeerijana ka kuumutamisel: Mn 2 +KN 3 +2KH K2 Mn 4 +KN 2 H 2 C 2 4 +KN 3 =2C 2 +KN 2 FSFR 4 Zn+KN 3 +7KH 4K 2 Zn 2 +NH 3 Fosfor on lämmastiku elektronanaloog Põhiline oksüdatsiooniaste on V Teistes ühendites, kuis fosfori oksüdatsiooniaste on väiksem kui V käitub redutseerijana Lihtainena omab mitmeid allotroope, tuntumad on: valge fosfor( P 4 ), mis tekib fosfori aurude kondenseerumisel, oksüdeerub kergesti ning võib süttida ka juba noaga lõigates, kihilise struktuuriga punane fosfor ( P 2 ), mis tekib valge fosfori kuumutamisel õhu juurdepääsuta ja on palju stabiilsem kui valge fosfor Tööstuses saadakse: Ca 3 (P 4 +3Si 2 +5 C 1500o C P2 +5 C+3CaSi 3 Redutseerijana käitub halogeniidide, hapniku, väävli ja kuuma konts H 2 S 4 ning HN 3 toimel Kui oksüdeerijat on liias, tekivad P(V) ühendid, kui oksüdeerijat on vähe, siis P(III) ühendid: 2P+3Cl 2 =2PCl 3 3P+5 HN 3 =3H 3 P 4 +5 N 6P+5KCl 3 =5 KCl+3P 2 5 Fosfori halogeniidide reaktsioonil veega tekib vastava oa-ga hape: PCl 3 =H 3 P 3 +3HCl PCl 5 +4H 2 =H 3 P 4 +5HCl Reaktsioonil kuumutamisel metallidega tekivad fosfiidid: 3Mg+2P Mg3 P 2 3Na+P Na3 P Fosfaan PH 3 väga mürgine küüslaugulõhnaline gaas, mille vesilahus on praktiliselt neutraalne Saadakse valge fosfori kuumutamisel kontsentreeritud leelises: 13
14 4 P+3KH+3 H 2 =3 K H 2 P 2 +PH 3 või Ca 3 P 2 +6H 2 =3Ca(H +2PH 3 Tugev redutseerija: PH 3 +4I 2 +4H 2 =H 3 P 4 +8HI PH =H 3 P 4 PH 3 +4Cu(N 3 +4 H 2 =4Cu+H 3 P 4 +8HN 3 Hüpofosforihape H 3 P 2 väga tugev redutseerija ning keskmise tugevusega hape, mis laguneb kuumutamisel: 3H 3 P 2 PH3 +2H 3 P 3 ksiidid: Tetrafosforheksaoksiid P 4 6 valge kristalliline ebameeldiva lõhnaga aine, õhus kuumutamisel süttib P =P 4 10, veega reageerides moodustab fosforishappe: P H 2 =4 H 3 P 3 Tetrafosfordekaoksiid P 4 10 valge tahke aine, väga efektiivne kuivatusagent, mis seob vett nii ühenditest kui ka vaba vett 6H 2 S 4 +P 4 10 =6S 3 +4 H 3 P 4 Veega reageerides tekivad fosforhapped: P H 2 =4HP 3 (metafosforhape) P H 2 =4H 3 P 4 (ortofosforhape) Fosforishape H 3 P 3 värvusetu hügroskoopne tahkis, mis lahustub vees hästi Tegu on kaheprootoni happega: P NaH=4Na 2 HP 3 Üsna tugev redutseerija, mis oksüdeerub kergesti: 2H 3 P 3 +AgN 3 =Ag+2H 3 P 4 +N Kuumutamisel laguneb: 4 H 3 P 3 PH3 +3H 3 P 4 (autoredoksreatsioon) Fosforhape H 3 P 4 keskmise tugevusega hape, mis dissotsieerub kolmes astmes Kuumutamisel toimub vee eraldumine, kuid oksiidi ei teki: H 3 P 4 HP3 Fosforhape ei ole oksüdeerija, laboris saadakse valge fosfori reag lämmastikhappega Reageerib aktiivsemate metallidega Samuti reageerib aluste ja aluseliste oksiididega: Ca+2H 3 P 4 =Ca 3 (P 4 3KH+H 3 P 4 =K 3 P 4 Vees lahustuvad leelismetallide fosfaadid, ammooniumfosfaadid ning divesinikfosfaadid 14
15 HALGEENID Mittemetallid, mille aktiivsused oksüdeerijatena vähenevad rühmas ülevalt alla Fluor ja kloor on rohekat värvi gaasid Broom on punakaspruun vedelik ning jood on tahke must metalliläikeline aine Halogeenid on väga reaktsioonivõimelised mittemetallid Nende reaktsioonid on samuti väga sarnased Fluori saadakse sulatatud KHF 2 +HF segu elektrolüüsil Kloori, broomi ja joodi saadakse laboris oksüdeerijate abil: või aktiivsema halogeeniga: Mn 2 +4HCl=MnCl 2 +Cl 2 2NaBr +Cl 2 =2NaCl+Br 2 Kontsentreeritud H 2 S 4 toimel oksüdeeruvad HBr ja HI, kuid mitte HF ja HCl: 2HBr +kh 2 S 4 =Br 2 +S 2 Reaktsioonil veega tekib hüpohalogeenishape ja vesinikhalogeniidhape: Cl 2 =HCl+HCl, kus tasakaal on nihutatud tugevalt vasakule, erandiks on fluor, mis tõrjub toatemp hapniku veest välja: 2F 2 +2 H 2 =4HF+ 2 Halogeenide reageerimisel leelistega jahutamisel tekib halogeniid ja hüpohalogenit: Cl 2 +2KH=KCl+KCl Kuuma leelisega tekib halogenaat ja halogeniid: 3Cl 2 +6KH 5KCl+KCl3 Reageerimisel metallidega tekivad vastavad halogeniidid: 2Fe+3Cl 2 =2FeCl 3, kuid Fe+I 2 =FeI 2 Halogeenide ühendid hapnikuga on head oksüdeerijad: HCl S=HCl +S KCl 3 +3KN 2 =3KN 3 +KCl KCl 3 +6 KH+3Mn 2 =3K 2 Mn 4 +KCl Halogeniidide redutseerivad omadused, kasvavad rühmas ülevalt alla ning avalduvad märgatavalt joodi korral 8HI+kH 2 S 4 =4I 2 S+4H 2 K 2 Cr KI+7 H 2 S 4 =Cr 2 (S 4 ) 3 +3I 2 +4K 2 S 4 +7H 2 15
16 Halogeenide oksohapete soolad lagunevad kuumutamisel Ilma katalüsaatorita: 3KCl 2KCl+KCl3 4 KBr 3 KBr+3KBr4 Mn 2 juuresolekul vabaneb hapnik: 2KCl 2KCl+2 2KBr 3 2KBr+32 Mittemetallide halogeniidide reageerimisel veega tekib vesinikhalogeniid: PBr 3 =H 3 P 3 +3HBr NCl 3 =3HCl+NH 3 Halogeniidioonide tõestamine: Reagent Fluoriidioon F - Kloriidioon Cl - Bromiidioon Br - Jodiidioon I - Pb(N 3 PbF 2 Valge sade PbCl 2 Valge sade PbBr 2 Kreemjas sade PbI 2 Kollane sade AgN 3 AgCl Valge sade Lahustub lahjas ammoniaagi lahuses [Ag(NH 3 ]Cl AgBr Kollakas sade Lahustub konts ammoniaagi lahuses [Ag(NH 3 ]Br AgI Kollane sade Ei lahustu ammoniaagi lahuses Kasutatud kirjandus: Karik, H, & Truus, K (2003) Elementide keemia Tallinn: Kirjastus Ilo Terje Raudseppa anorgaanilise keemia konspekt Ahmetov, N (1974) Anorgaaniline keemia Tallinn: Valgus 16
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut
 Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat
 Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Leelismetallid, I A Li liitium, Na naatrium, K kaalium, Rb, Cs, Fr
 Leelismetallid, I A Li liitium, Na naatrium, K kaalium, Rb, Cs, Fr Li Na K Z 3 11 19 A r 6.941 22.990 39.098 El.neg. 1.0 0.97 0.8 st, C 180.5 97.8 63.2 kt, C 1317 890 753.8 ρ, g/cm 3 0.534 0.971 0.862
Leelismetallid, I A Li liitium, Na naatrium, K kaalium, Rb, Cs, Fr Li Na K Z 3 11 19 A r 6.941 22.990 39.098 El.neg. 1.0 0.97 0.8 st, C 180.5 97.8 63.2 kt, C 1317 890 753.8 ρ, g/cm 3 0.534 0.971 0.862
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
13.2 C 161 C 232 C α-sn β-sn γ-sn sulametall
 Tähtsamate metallide keemia Leelismetallid: Li, Na, K, Rb, Cs, Fr Leelismuldmetallid: Ca, Sr, Ba, Ra (ei kuulu Be, Mg) Siirdeelemendid (d-alakiht täitmata), 1. rida: Sc, Ti, V, Cr, Mn, Co, Ni, Cu (ei kuulu
Tähtsamate metallide keemia Leelismetallid: Li, Na, K, Rb, Cs, Fr Leelismuldmetallid: Ca, Sr, Ba, Ra (ei kuulu Be, Mg) Siirdeelemendid (d-alakiht täitmata), 1. rida: Sc, Ti, V, Cr, Mn, Co, Ni, Cu (ei kuulu
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
Lokaalsed ekstreemumid
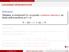 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
1998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
ΠΑΡΑΡΤΗΜΑ V. Πρότυπα δυναμικά αναγωγής ( ) ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΑΝΑΓΩΓΗΣ ΣΤΟΥΣ 25 o C. Ημιαντιδράσεις αναγωγής , V. Antimony. Bromine. Arsenic.
 ΠΑΡΑΡΤΗΜΑ V. ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΑΝΑΓΩΓΗΣ ΣΤΟΥΣ 5 o C ΠΑΡΑΡΤΗΜΑ V. Πρότυπα δυναμικά αναγωγής ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΑΝΑΓΩΓΗΣ ΣΤΟΥΣ 5 o C, V, V Auminum Bervium A ( H ) e A H. 0 Be e Be H. 1 ( ) [ ] e A F. 09 AF
ΠΑΡΑΡΤΗΜΑ V. ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΑΝΑΓΩΓΗΣ ΣΤΟΥΣ 5 o C ΠΑΡΑΡΤΗΜΑ V. Πρότυπα δυναμικά αναγωγής ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΑΝΑΓΩΓΗΣ ΣΤΟΥΣ 5 o C, V, V Auminum Bervium A ( H ) e A H. 0 Be e Be H. 1 ( ) [ ] e A F. 09 AF
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ
 23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
Θέμα Α. Ονοματεπώνυμο: Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
ΓΗ ΚΑΙ ΣΥΜΠΑΝ. Εικόνα 1. Φωτογραφία του γαλαξία μας (από αρχείο της NASA)
 ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2019 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Δίνεται στοιχείο Χ το οποίο έχει οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα.
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) ( ) ΘΕΜΑ Α Α1.
 Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΠΤΙΚΟ ΔΙΑΓΩΝΙΣΜΑ (ΚΕΦΑΛΑΙΑ 2-3) (5 2 2017) ΘΕΜΑ Α Α1. Επιλέξτε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις : 1. Σε ποια από τις επόμενες ενώσεις το χλώριο έχει μεγαλύτερο αριθμό
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
2005/2006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. = 52,5 g/mol
 005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor
Παραδοχές στις οποίες στις οποίες στηρίζεται ο αριθμός οξείδωσης
 Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
Χ ΗΜΙΚΕΣ Α Ν Τ ΙΔΡΑΣΕΙΣ
 53 Χ ΗΜΙΚΕΣ Α Ν Τ ΙΔΡΑΣΕΙΣ Χημική αντίδραση ονομάζουμε κάθε χημικό φαινόμενο. Δηλαδή, κάθε φαινόμενο στο οποίο έχουμε αναδιάταξη των ηλεκτρονίων ( e ) της εξωτερικής στιβάδας των ατόμων που παίρνουν μέρος
53 Χ ΗΜΙΚΕΣ Α Ν Τ ΙΔΡΑΣΕΙΣ Χημική αντίδραση ονομάζουμε κάθε χημικό φαινόμενο. Δηλαδή, κάθε φαινόμενο στο οποίο έχουμε αναδιάταξη των ηλεκτρονίων ( e ) της εξωτερικής στιβάδας των ατόμων που παίρνουν μέρος
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ ΕΚΦΩΝΗΣΕΙΣ ÏÅÖÅ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ
 ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΑΡΙΘΜΟΣ ΟΞΕΙΔΩΣΗΣ - ΓΡΑΦΗ ΧΗΜΙΚΩΝ ΤΥΠΩΝ- ΟΝΟΜΑΤΟΛΟΓΙΑ Τι είναι ο αριθμός οξείδωσης Αριθμό οξείδωσης ενός ιόντος σε μια ετεροπολική ένωση ονομάζουμε το πραγματικό φορτίο του ιόντος. Αριθμό οξείδωσης ενός
ΚΕΦΑΛΑΙΟ 5: ΟΞΕΙΟΑΑΝ ΑΓΩΓΗ - ΗΑΕΚΤΡΟΛΥΣΗ
 45 ΚΕΦΑΛΑΙΟ 5: ΟΞΕΙΟΑΑΝ ΑΓΩΓΗ - ΗΑΕΚΤΡΟΛΥΣΗ 1-12. Οι απαντήσεις προκύπτουν εύκολα από τη θεωρία. Ερωτήσεις - ασκήσεις - προβλήματα 13. Η3ΡΟ4: 3 + χ + (-8) = 0 ή χ = +5 Ρ 4 : ο Α.Ο. στα ελεύθερα στοιχεία
45 ΚΕΦΑΛΑΙΟ 5: ΟΞΕΙΟΑΑΝ ΑΓΩΓΗ - ΗΑΕΚΤΡΟΛΥΣΗ 1-12. Οι απαντήσεις προκύπτουν εύκολα από τη θεωρία. Ερωτήσεις - ασκήσεις - προβλήματα 13. Η3ΡΟ4: 3 + χ + (-8) = 0 ή χ = +5 Ρ 4 : ο Α.Ο. στα ελεύθερα στοιχεία
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
ΙΑΦΑ Φ ΝΕΙ Ε ΕΣ Ε ΧΗΜΕ Μ Ι Ε ΑΣ ΓΥΜΝ Μ ΑΣΙΟΥ H
 Hταξινόµηση των στοιχείων τάξη Γ γυµνασίου Αναγκαιότητα ταξινόµησης των στοιχείων Μέχρι το 1700 µ.χ. ο άνθρωπος είχε ανακαλύψει µόνο 15 στοιχείακαι το 1860 µ.χ. περίπου 60στοιχεία. Σηµαντικοί Χηµικοί της
Hταξινόµηση των στοιχείων τάξη Γ γυµνασίου Αναγκαιότητα ταξινόµησης των στοιχείων Μέχρι το 1700 µ.χ. ο άνθρωπος είχε ανακαλύψει µόνο 15 στοιχείακαι το 1860 µ.χ. περίπου 60στοιχεία. Σηµαντικοί Χηµικοί της
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
Funktsiooni diferentsiaal
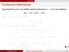 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ. β) Να βρεθεί σε ποια οµάδα και σε ποια περίοδο του Περιοδικού Πίνακα ανήκουν.
 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΤΕΤΑΡΤΗ 29 ΜΑΪΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΤΕΤΑΡΤΗ 9 ΜΑΪΟΥ 01 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ Α1. γ Α. β Α. δ Α4. β Α5. α) Μπορεί ενδεικτικά
ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΤΕΤΑΡΤΗ 9 ΜΑΪΟΥ 01 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ Α1. γ Α. β Α. δ Α4. β Α5. α) Μπορεί ενδεικτικά
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Matemaatiline analüüs I iseseisvad ülesanded. Leidke funktsiooni y = log( ) + + 5 määramispiirkond.. Leidke funktsiooni y = + arcsin 5 määramispiirkond.. Leidke funktsiooni y = sin + 6 määramispiirkond.
Κανόνες διαλυτότητας για ιοντικές ενώσεις
 Κανόνες διαλυτότητας για ιοντικές ενώσεις 1. Ενώσεις των στοιχείων της Ομάδας 1A και του ιόντος αμμωνίου (Ιόντα: Li +, Na +, K +, Rb +, Cs +, NH 4+ ) είναι ευδιάλυτες, χωρίς εξαίρεση: πχ. NaCl, K 2 S,
Κανόνες διαλυτότητας για ιοντικές ενώσεις 1. Ενώσεις των στοιχείων της Ομάδας 1A και του ιόντος αμμωνίου (Ιόντα: Li +, Na +, K +, Rb +, Cs +, NH 4+ ) είναι ευδιάλυτες, χωρίς εξαίρεση: πχ. NaCl, K 2 S,
KARBOKSÜÜLHAPPED. Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COOH). Üldvalem R-COOH või HOOC-R
 KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
KARBOKSÜÜLAPPED Karboksüülhapped on orgaanilised aineid, mis sisaldavad üht või mitut karboksüülrühma (-COO). Üldvalem R-COO või OOC-R Karboksüülhapete nimetused tuletatakse süsivesinike nimetustest ja
Ημερομηνία: Τρίτη 18 Απριλίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
Μετά το τέλος της μελέτης του 3ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει ποιες ενώσεις είναι οξέα, βάσεις, άλατα και οξείδια.
 Μετά το τέλος της μελέτης του 3ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει ποιες ενώσεις είναι οξέα, βάσεις, άλατα και οξείδια. Να ονομάζει ανόργανες ενώσεις, όταν δίνεται ο μοριακός
Μετά το τέλος της μελέτης του 3ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει ποιες ενώσεις είναι οξέα, βάσεις, άλατα και οξείδια. Να ονομάζει ανόργανες ενώσεις, όταν δίνεται ο μοριακός
ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ. Χημεία
 ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ Χημεία Λύσεις Ασκήσεων Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Ομάδας Προσανατολισμού Θετικών Σπουδών ΙΝΣΤΙΤΟΥΤΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΠΟΛΟΓΙΣΤΩΝ ΚΑΙ
ΥΠΟΥΡΓΕΙΟ ΠΟΛΙΤΙΣΜΟΥ, ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΙΝΣΤΙΤΟΥΤΟ ΕΚΠΑΙΔΕΥΤΙΚΗΣ ΠΟΛΙΤΙΚΗΣ Χημεία Λύσεις Ασκήσεων Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Ομάδας Προσανατολισμού Θετικών Σπουδών ΙΝΣΤΙΤΟΥΤΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΠΟΛΟΓΙΣΤΩΝ ΚΑΙ
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
SÜSIVESINIKUD. Kaido Viht
 SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
SÜSIVSINIKUD Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2016 Süsivesinike struktuurid Käesolevas materjalis selgitame mõningaid süsivesinikele iseloomulikke reaktsioone. Süsivesinikud, nagu
3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης
 3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης 1. Στόχοι του μαθήματος Οι μαθητές να γνωρίσουν:i) πότε πραγματοποιείται μια αντίδραση απλής αντικατάστασης, με βάση τη σειρά δραστικότητας των μετάλλων και
3 o Μάθημα : Αντιδράσεις απλής αντικατάστασης 1. Στόχοι του μαθήματος Οι μαθητές να γνωρίσουν:i) πότε πραγματοποιείται μια αντίδραση απλής αντικατάστασης, με βάση τη σειρά δραστικότητας των μετάλλων και
Χημικές Αντιδράσεις. Εισαγωγική Χημεία
 Χημικές Αντιδράσεις Εισαγωγική Χημεία Κατηγορίες Χημικών Αντιδράσεων Πέντε κυρίως κατηγορίες: Σύνθεσης Διάσπασης Απλής αντικατάστασης Διπλής αντικατάστασης Καύσης Αντιδράσεις σύνθεσης Ένωση δύο ή περισσότερων
Χημικές Αντιδράσεις Εισαγωγική Χημεία Κατηγορίες Χημικών Αντιδράσεων Πέντε κυρίως κατηγορίες: Σύνθεσης Διάσπασης Απλής αντικατάστασης Διπλής αντικατάστασης Καύσης Αντιδράσεις σύνθεσης Ένωση δύο ή περισσότερων
Κεφάλαιο 1. Έννοιες και παράγοντες αντιδράσεων
 Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Κεφάλαιο 1 Έννοιες και παράγοντες αντιδράσεων Σύνοψη Το κεφάλαιο αυτό είναι εισαγωγικό του επιστημονικού κλάδου της Οργανικής Χημείας και περιλαμβάνει αναφορές στους πυλώνες της. Ειδικότερα, εδώ παρουσιάζεται
Ca +2 K + Mg +2 H + Al +3 Na + Zn +2 S -2 NO 3. ΑΣΚΗΣΗ 1-Συμπληρώστε κατάλληλα, τα κενά του πίνακα με τα ονόματα και τους χημικούς τύπους των ενώσεων.
 Σελίδα: 1 Φ.Εργασίας Χημεία Α Λυκείου Κεφ. 2 ΤΟΛΟΓΙΑ / ΑΟ /ΧΗΜΙΚΟΙ ΤΥΠΟΙ / Mr - Επιμέλεια: Παναγιώτης Κουτσομπόγερας Όνομα & Επώνυμο : Τάξη: Ημερομηνία: ΤΥΠΟΣ Cl -1 CaCl 2 ΑΣΚΗΣΗ 1-Συμπληρώστε κατάλληλα,
Σελίδα: 1 Φ.Εργασίας Χημεία Α Λυκείου Κεφ. 2 ΤΟΛΟΓΙΑ / ΑΟ /ΧΗΜΙΚΟΙ ΤΥΠΟΙ / Mr - Επιμέλεια: Παναγιώτης Κουτσομπόγερας Όνομα & Επώνυμο : Τάξη: Ημερομηνία: ΤΥΠΟΣ Cl -1 CaCl 2 ΑΣΚΗΣΗ 1-Συμπληρώστε κατάλληλα,
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
ΟΝΟΜΑΣΙΑ F - HF Υδροφθόριο S 2- H 2 S Υδρόθειο Cl - HCl Υδροχλώριο OH - H 2 O Οξείδιο του Υδρογόνου (Νερό) NO 3 HNO 3. Νιτρικό οξύ SO 3 H 2 SO 3
 1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
Αλληλεπίδραση ακτίνων-χ με την ύλη
 Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ
 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ ΘΕΜΑ Α Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το ιόν 56 Fe +2 περιέχει:
ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ ΘΕΜΑ Α Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το ιόν 56 Fe +2 περιέχει:
Ονοματεπώνυμο: Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
Θέματα Ανόργανης Χημείας Γεωπονικής ΓΟΜΗ ΑΣΟΜΩΝ
 Θέματα Ανόργανης Χημείας Γεωπονικής 1 ΓΟΜΗ ΑΣΟΜΩΝ 1. α) Γχζηε ηζξ ααζζηέξ ανπέξ μζημδυιδζδξ ημο δθεηηνμκζημφ πενζαθήιαημξ ηςκ αηυιςκ Mg (Z=12), K (Z=19), ηαζ Ag (Ε=47). Δλδβήζηε ιε ηδ εεςνία ηςκ ιμνζαηχκ
Θέματα Ανόργανης Χημείας Γεωπονικής 1 ΓΟΜΗ ΑΣΟΜΩΝ 1. α) Γχζηε ηζξ ααζζηέξ ανπέξ μζημδυιδζδξ ημο δθεηηνμκζημφ πενζαθήιαημξ ηςκ αηυιςκ Mg (Z=12), K (Z=19), ηαζ Ag (Ε=47). Δλδβήζηε ιε ηδ εεςνία ηςκ ιμνζαηχκ
Matemaatiline analüüs I iseseisvad ülesanded
 Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
Matemaatiline analüüs I iseseisvad ülesanded Leidke funktsiooni y = log( ) + + 5 määramispiirkond Leidke funktsiooni y = + arcsin 5 määramispiirkond Leidke funktsiooni y = sin + 6 määramispiirkond 4 Leidke
FUNKTSIONAALSED RÜHMAD I osa. Kaido Viht
 FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ. Η 2 SO 4 + BaCl 2 2HCl + BaSO 4. 2HCl + Na 2 CO 3 CO 2 + H 2 O + 2NaCl. 2HCl + Na 2 SO 3 SO 2 + H 2 O + 2NaCl
 ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ Οι αντιδράσεις διπλής αντικατάστασης γίνονται ανάµεσα σε ηλεκτρολύτες µε ανταλλαγή ιόντων. Για να πραγµατοποιηθεί µια αντίδραση διπλής αντικατάστασης πρέπει ένα τουλάχιστον από τα προϊόντα
ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ Οι αντιδράσεις διπλής αντικατάστασης γίνονται ανάµεσα σε ηλεκτρολύτες µε ανταλλαγή ιόντων. Για να πραγµατοποιηθεί µια αντίδραση διπλής αντικατάστασης πρέπει ένα τουλάχιστον από τα προϊόντα
ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ
 Κεφάλαιο 1ο-ΟΞΕΙΔΩΑΝΑΓΩΓΗ 1 ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το
Κεφάλαιο 1ο-ΟΞΕΙΔΩΑΝΑΓΩΓΗ 1 ΓΕΝΙΚΑ ΓΙΑ ΤΗΝ ΟΞΕΙΔΩΣΗ ΚΑΙ ΤΗΝ ΑΝΑΓΩΓΗ Ορισμοί : -Αριθμός οξείδωσης: I)Σε μία ιοντική ένωση ο αριθμός οξείδωσης κάθε στοιχείου είναι ίσος με το ηλεκτρικό φορτίο που έχει το
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Ιωάννα Βασιλείου, Σταυρούλα Γκιτάκου
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 12 02-2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Ιωάννα Βασιλείου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 12 02-2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Ιωάννα Βασιλείου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε
Κεφάλαιο 3 Χημικές Αντιδράσεις
 Κεφάλαιο 3 Χημικές Αντιδράσεις Οι χημικές αντιδράσεις μπορούν να ταξινομηθούν σε δύο μεγάλες κατηγορίες, τις οξειδοαναγωγικές και τις μεταθετικές. Α. ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Στις αντιδράσεις αυτές
Κεφάλαιο 3 Χημικές Αντιδράσεις Οι χημικές αντιδράσεις μπορούν να ταξινομηθούν σε δύο μεγάλες κατηγορίες, τις οξειδοαναγωγικές και τις μεταθετικές. Α. ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Στις αντιδράσεις αυτές
ÖÑÏÍÔÉÓÔÇÑÉÏ ÏÑÏÓÇÌÏ ÅËÁÓÓÏÍÁ
 ΘΕΜΑ Α ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 2 ΜΑΪΟΥ 2011 ΑΠΑΝΤΗΣΕΙΣ Α1. β, Α2. α, Α. δ, Α4. β, Α5. α. Σ, β. Σ, γ. Λ, δ. Λ, ε. Σ ΘΕΜΑ Β Β1.α. β. Β2.α. 12 15 19 26 Mg : 1s 2s 2p 2+ 2 2 6 P : 1s 2s 2p s p
ΘΕΜΑ Α ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 2 ΜΑΪΟΥ 2011 ΑΠΑΝΤΗΣΕΙΣ Α1. β, Α2. α, Α. δ, Α4. β, Α5. α. Σ, β. Σ, γ. Λ, δ. Λ, ε. Σ ΘΕΜΑ Β Β1.α. β. Β2.α. 12 15 19 26 Mg : 1s 2s 2p 2+ 2 2 6 P : 1s 2s 2p s p
ph< 8,2 : άχρωμη ph> 10 : ροζ-κόκκινη
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2016 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΑΝΙΧΝΕΥΣΗ ΟΞΕΟΣ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ 2. ΟΓΚΟΜΕΤΡΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2016 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΑΝΙΧΝΕΥΣΗ ΟΞΕΟΣ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ 2. ΟΓΚΟΜΕΤΡΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 23 ΜΑΪΟΥ 2011 ΑΠΑΝΤΗΣΕΙΣ
 ΘΕΜΑ Α ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 2 ΜΑΪΟΥ 2011 ΑΠΑΝΤΗΣΕΙΣ Α1. β, Α2. α, Α. δ, Α4. β, Α5. α. Σ, β. Σ, γ. Λ, δ. Λ, ε. Σ ΘΕΜΑ Β Β1.α. β. Β2.α. 12 15 19 26 Mg : 1s 2s 2p 2+ 2 2 6 P : 1s 2s 2p s p
ΘΕΜΑ Α ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ 2 ΜΑΪΟΥ 2011 ΑΠΑΝΤΗΣΕΙΣ Α1. β, Α2. α, Α. δ, Α4. β, Α5. α. Σ, β. Σ, γ. Λ, δ. Λ, ε. Σ ΘΕΜΑ Β Β1.α. β. Β2.α. 12 15 19 26 Mg : 1s 2s 2p 2+ 2 2 6 P : 1s 2s 2p s p
Άσκηση. Ισχυρό οξύ: Η 2 SeO 4 Ασθενές οξύ: (CH 3 ) 2 CHCOOH Ισχυρή βάση: KOH Ασθενής βάση: (CH 3 ) 2 CHNH 2
 Ασκήσεις κεφ. 1-3 Άσκηση Κατατάξτε τις παρακάτω ενώσεις ως ισχυρά και ασθενή οξέα ή ισχυρές και ασθενείς βάσεις α) Η 2 SeO 4, β) (CH 3 ) 2 CHCOOH γ) KOH, δ) (CH 3 ) 2 CHNH 2 Ισχυρό οξύ: Η 2 SeO 4 Ασθενές
Ασκήσεις κεφ. 1-3 Άσκηση Κατατάξτε τις παρακάτω ενώσεις ως ισχυρά και ασθενή οξέα ή ισχυρές και ασθενείς βάσεις α) Η 2 SeO 4, β) (CH 3 ) 2 CHCOOH γ) KOH, δ) (CH 3 ) 2 CHNH 2 Ισχυρό οξύ: Η 2 SeO 4 Ασθενές
ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ ΤΜΗΜΑ ΟΧΗΜΑΤΩΝ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΔΙΑΒΡΩΣΗ ΚΑΙ ΠΡΟΣΤΑΣΙΑ ΤΩΝ ΥΛΙΚΩΝ Η ΠΕΡΙΠΤΩΣΗ ΤΩΝ ΧΑΛΥΒΩΝ ΣΤΑ ΑΥΤΟΚΙΝΗΤΑ.
 ΑΝΩΤΑΤΟ ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΙΔΡΥΜΑ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ ΤΜΗΜΑ ΟΧΗΜΑΤΩΝ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΔΙΑΒΡΩΣΗ ΚΑΙ ΠΡΟΣΤΑΣΙΑ ΤΩΝ ΥΛΙΚΩΝ Η ΠΕΡΙΠΤΩΣΗ ΤΩΝ ΧΑΛΥΒΩΝ ΣΤΑ ΑΥΤΟΚΙΝΗΤΑ των ΦΑΡΛΕΚΑ ΓΕΩΡΓΙΟΥ
ΑΝΩΤΑΤΟ ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΙΔΡΥΜΑ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ ΤΜΗΜΑ ΟΧΗΜΑΤΩΝ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΔΙΑΒΡΩΣΗ ΚΑΙ ΠΡΟΣΤΑΣΙΑ ΤΩΝ ΥΛΙΚΩΝ Η ΠΕΡΙΠΤΩΣΗ ΤΩΝ ΧΑΛΥΒΩΝ ΣΤΑ ΑΥΤΟΚΙΝΗΤΑ των ΦΑΡΛΕΚΑ ΓΕΩΡΓΙΟΥ
1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία
 1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία Ημ. Παράδοσης: Δευτέρα 25/11/2013 11 πμ 1. Οι αντιδράσεις οξειδοαναγωγής σώζουν ζωές!!! Οι αερόσακοι στα αυτοκίνητα, όταν ανοίγουν γεμίζουν με άζωτο το
1 η Σειρά προβλημάτων στο μάθημα Εισαγωγική Χημεία Ημ. Παράδοσης: Δευτέρα 25/11/2013 11 πμ 1. Οι αντιδράσεις οξειδοαναγωγής σώζουν ζωές!!! Οι αερόσακοι στα αυτοκίνητα, όταν ανοίγουν γεμίζουν με άζωτο το
3. Να συμπληρωθούν οι παρακάτω αντιδράσεις:
 1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
SUPPLEMENTAL INFORMATION. Fully Automated Total Metals and Chromium Speciation Single Platform Introduction System for ICP-MS
 Electronic Supplementary Material (ESI) for Journal of Analytical Atomic Spectrometry. This journal is The Royal Society of Chemistry 2018 SUPPLEMENTAL INFORMATION Fully Automated Total Metals and Chromium
Electronic Supplementary Material (ESI) for Journal of Analytical Atomic Spectrometry. This journal is The Royal Society of Chemistry 2018 SUPPLEMENTAL INFORMATION Fully Automated Total Metals and Chromium
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ ΙΠΛΗΣ ΑΝΤΙΚΑΤΑΣΤΑΣΗΣ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ ΙΠΛΗΣ ΑΝΤΙΚΑΤΑΣΤΑΣΗΣ Για να πραγµατοποιηθεί µία αντίδραση διπλής αντικατάστασης πρέπει να δηµιουργείται χηµική ένωση που είναι δυσδιάλυτη ή αέρια ή ελάχιστα ιονιζόµενη, έτσι
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ ΙΠΛΗΣ ΑΝΤΙΚΑΤΑΣΤΑΣΗΣ Για να πραγµατοποιηθεί µία αντίδραση διπλής αντικατάστασης πρέπει να δηµιουργείται χηµική ένωση που είναι δυσδιάλυτη ή αέρια ή ελάχιστα ιονιζόµενη, έτσι
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Πανελλαδικές Εξετάσεις Ηµερησίων Γενικών Λυκείων
 Πανελλαδικές Εξετάσεις Ηµερησίων Γενικών Λυκείων Παρασκευή 14 06 2019 Εξεταζόµενο µάθηµα: Χηµεία Προσανατολισµού Θετικών Σπουδών Θέµα A Α1. β Α2. γ Α3. α Α4. γ Α5. β Θέµα B Β1. α) CH C CH 3 H 2 β) ph =
Πανελλαδικές Εξετάσεις Ηµερησίων Γενικών Λυκείων Παρασκευή 14 06 2019 Εξεταζόµενο µάθηµα: Χηµεία Προσανατολισµού Θετικών Σπουδών Θέµα A Α1. β Α2. γ Α3. α Α4. γ Α5. β Θέµα B Β1. α) CH C CH 3 H 2 β) ph =
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
C M. V n: n =, (D): V 0,M : V M P = ρ ρ V V. = ρ
 »»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
»»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015)
 Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
Ερωτήσεις πολλαπλης επιλογής στην οξειδοαναγωγή (1ο κεφάλαιο Γ Θετική 2015) 1. Σε ποια απο τις παρακάτω ενώσεις το Ν έχει αριθμό οξέιδωσης +5 A. ΗΝΟ 2 C ΚΝΟ 3 B. ΝΗ 3 D Ν 2 Ο 3 2. Σε ποια απο τις παρακάτω
Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα
 Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα Βοηθητικές Σημειώσεις Αγγελική Απ. Γαλάνη, Χημικός Ph.D. Εργαστηριακό Διδακτικό Προσωπικό, (Ε.ΔΙ.Π.) Χημείας Γραφή
Ονοματολογία ανόργανων χημικών ενώσεων Γραφή ανόργανων χημικών ενώσεων Οξέα, βάσεις, άλατα Βοηθητικές Σημειώσεις Αγγελική Απ. Γαλάνη, Χημικός Ph.D. Εργαστηριακό Διδακτικό Προσωπικό, (Ε.ΔΙ.Π.) Χημείας Γραφή
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
