Molekulid ei esine üksikuna vaid suurearvuliste kogumitena.
|
|
|
- Ήρα Κορωναίος
- 6 χρόνια πριν
- Προβολές:
Transcript
1 2. AGREGAATOLEKUD Intramolekulaarsed jõud - tugevatoimelised jõud aatomite vahel molekulides - keemiline side. Nendega on seotud ainete keemilised omadused Intermolekulaarsed jõud - nõrgad elektrostaatilised vastasmõjud molekulide vahel - van der Waalsi jõud. Nendega on seotud ainete füüsikalised omadused 2.1. Molekulidevahelised jõud Molekulid ei esine üksikuna vaid suurearvuliste kogumitena. Jõududest molekulide vahel olenevad ainete füüsikalised omadused (agregaatolek, sulamis- ja keemistemp., pindade ja vedelike vastastoime, lahustumine - hüdraatide teke lahustes) Neutraalsete molekulide vahel toimivaid jõudusid nimet. van der Waalsi jõududeks nõrgad elektrostaatilise iseloomuga jõud Orientatsioonijõud jõud püsiva dipoolmomendiga polaarsete molekulide vahel või ioon-dipool vastastoime 2µ 2 E or = - r 3 kus µ - dipoolmoment r - kaugus ioonide-dipoolide tsentrite vahel Induktsioonijõud jõud polaarsete ja mittepolaarsete molekulide vahel (polaarne molekul tekitab teises samuti dipoolmomendi) 2αµ 2 E ind = - r 6 kus α - polariseeritavus (näitab kui kergesti on elektronpilv deformeeritav) Reeglina - mida suurem on elektronide arv, seda kaugemal on nad tuumast, seda suurem polariseeritavus Dispersioonijõud elektronide liikumisel tekkivate hetkdipoolide nõrk vastastikune mõju Iα 2 E disp = - 3/4 r 6 kus I - ionisatsioonienergia (suureneb molaarmassi kasvuga) 2.1 KKY3031 Üldine keemia
2 Van der Waalsi jõud kahanevad kaugusega väga kiiresti, eriti olulised on nad tugevasti kokkusurutud gaasides, vedelikes, aga ka molekulvõrega kristallides Vesinikside Dipool-dipool tüüpi vastastoime, mis esineb polaarse sidemega seotud H aatomi ja elektronegatiivse O, N või F aatomi vahel A H B A H A kus tähistab vesiniksidet ja A ning B on kas O, F või N Need kolm aatomit paiknevad kas ühel sirgel või kuni 30 -se nurga all sirgjoonest Vesinikside põhjustab nende vesinikühendite keemis- ja sulamistemperatuuride olulist erinevust, võrreldes teiste sama rühma elementidega: H 2 O +100 C HF +20 C H 2 S C HCl -85 C H 2 Se -42 C HBr -67 C peaks alanema Erinevate vastasmõjude energiate võrdlus Vastastoime tüüp Energia, kj/mol Keemiline side ~ Vesinikside ~20-40 Orientatsioonitoime ~1-5 Induktsioonitoime ~ Dispersioonitoime ~ Gaasid Gaasilises olekus aine molekulid täidavad ühtlaselt kogu ruumi, molekulid on pidevas korrapäratus soojusliikumises, molekulidevahelised jõud on väikesed. Gaaside maht sõltub oluliselt temperatuurist ning rõhust. Mahtu väljend. tavaliselt kokkuleppelistel tingimustel - nn. normaaltingimustel: temperatuur rõhk 273,15 K (0 C) Pa (1 atm, 760 mm Hg) 2.2 A.Trikkel, 2002
3 Põhilised seadused Boyle'i - Mariotte'i seadus. Konstantsel temperatuuril on kindla koguse gaasi maht pöördvõrdelises sõltuvuses rõhuga. P * V = const P 1 V 2 = P 2 V 1 Gay Lussac'i seadus. Konstantsel rõhul on kindla koguse gaasi maht võrdelises sõltuvuses temperatuuriga. V = const T V 1 V 2 = T 1 T 2 Kombineerides saame: P 1 V 1 P 2 V 2 P 0 V 0 = = T 1 T 2 T 0 P V = const = R T universaalne gaasikonstant Kui ühikuteks on rõhk P [Pa]; mass m [g]; moolide arv n [mol], maht V [m 3 ]; temperatuur T [K] siis R = J/mol K ja kehtib seos: P V = n R T ehk m P V = R T M 2.3 KKY3031 Üldine keemia
4 Muude ühikute korral võib R väärtuseks olla näiteks R = atm L/mol K R = mm Hg cm 3 /mol K Daltoni seadus. Gaaside segu üldrõhk võrdub segu moodustavate gaaside osarõhkude summaga. Osarõhk - rõhk mida avaldaks gaas kui teisi gaase segus poleks. P üld = p 1 + p = Σp i p i = P üld * X i, kus X i - vastava gaasi moolimurd segus Moolimurd - ühe komponendi moolide arv jagatud kõikide komponentide moolide arvude summaga n i X i = Σn Gaasilise aine molekulid liiguvad alati suunas, kus antud gaasi osarõhk on väiksem - difusioon. Toimub osarõhu ühtlustumine kogu süsteemis. Gaasi suhteline tihedus. Ühe gaasi massi suhe teise gaasi massi samadel tingimustel (V, P, T); ühikuta suurus m 1 M 1 D = = m 2 M 2 väljendatakse tavaliselt õhu suhtes või vesiniku suhtes M gaas D õhk = 29 M gaas D H2 = 2 Gaasi absoluutne tihedus normaaltingimustel e. 1 liitri gaasi mass normaaltingimustelt M gaas ρ 0 =, [g/dm 3 ] A.Trikkel, 2002
5 Näit. õhu tihedus: ρ 0 = 29/22.4 = 1.29 g/l 2.3. Vedelikud veeauru tihedus: ρ 0 = 18/22.4 = 0.80 g/l Vedelikud - ained, mis omandavad raskusjõu mõjul voolavuse. Voolavus - vedelike omadus muuta oma väliskuju (võtta anuma kuju), tingitud pidevast molekulide ümberpaiknemisest soojusliikumise tagajärjel. Raskusjõu mõjul toimub molekulide suunatud liikumine. Viskoossus (η, kg / m s) - vedelikukihtide omadus takistada vastastikku üksteise või vedelikku asetatud keha liikumist. Väheneb t kasvuga. Mida väiksem viskoosus, seda voolavam vedelik 20 C juures: vesi H 2 O atsetoon oliivõli 1.00 kg/m s ( C juures) 0.32 kg/m s 84.0 kg/m s Pindpinevus (γ, N/m)- energiahulk, mis on vajalik vedeliku pinna suurendamiseks või vähendamiseks ühe pinnaühiku võrra. Põhjustatud pinnal asuvate molekulide energiaülejäägist, võrreldes vedeliku sees asuvate molekulidega. Kuna pinnakihi molekulidele mõjuvad jõud on suunatud vedeliku sisse, võtab vedelikupiisk kera kuju. 20 C juures: vesi atsetoon elavhõbe 72.7 N/m 23.7 N/m 487 N/m Pindaktiivsed ained - ühendid, mille lisamisel vähaneb vedeliku pindpinevus (tensiidid, näit. seep) Märguvad pinnad - hüdrofiilsed pinnad (ioonvõrega mineraalid - silikaadid, sulfaadid, metallioksiidid ja hüdroksiidid) Mittemärguvad pinnad - hüdrofoobsed pinnad (metallid, enamik molekulaarse struktuuriga orgaanilisi ühendeid) 2.5 KKY3031 Üldine keemia
6 Θ < 90 Θ > 90 Θ 0 märguv pind mittemärguv pind täielik märgumine hüdrofiilne hüdrofoobne Kui vedelik märgab pinda, tõuseb ta kapillaarides ja poorides üles. Vedelikusamba kõrgus on määratud kapillari raadiuse, vedeliku tiheduse, ja pindpinevusega. Kohesioon - vastastoimed vedeliku sees sarnaste molekulide vahel. Kohesioonijõud F koh Adhesioon - vedeliku molekulide ja tahke materjali pinna vaheline vastastoime (vesiklaas). Adhesioonijõud F adh Pindaktiivsed ained ja nende toime Pindaktiivsed ained - pika süsinikuahelaga molekulid, mille ühes otsas on aktiivne rühm, näit. happerühm (-COOH), sulfonaatrühm (-SO 3 H). C 18 H 28 SO 3 Na - Nadodetsüülbenseensulfonaat. Üks ahela ots on vett tõrjuv (hüdrofoobne), teine veelembene (hüdrofiilne) Alandavad pindpinevust - hüdrofiilne molekuliosa seostub vee molekulidega, nõrgenevad jõud vee molekulide vahel, seega ka pindpinevus vee molekulid saavad tungida väiksematesse lõhedesse ja pooridesse Eemaldavad mustust - hüdrofiilne ots seostub vee molekulidega, hüdrofoobne ots mustusekübekesega, nii viiakse mustus pesulahusesse Takistavad mustuse tagasisadenemist - tensiidi molekulid ümbritsevad kohe mustuseosakese - tekivad mitsellid. Nii takistatakse mustuseosakeste ühinemist ja tagasisadenemist 2.4. Vesi Üldised omadused Levinuim vesinikuühend (ookeanid, jõed, järved, veeaur atmosfääris, lumi ja jää). Vesi osaleb kõikides eluprotsessides % elusorganismide massist (2/3 inimese massist) külmumistemperatuur 0 C keemistemperatuur 100 C (760 mm Hg juures) tihedus 1,00 g/cm 3 (+4 C juures suurim) jää tihedus ~0,9 g/cm 3 Looduslik vesi sisaldab alati lahustunud ja suspendeeritud lisandeid: ookeanivesi sooladesisaldus kuni 4% magevesi % 2.6 A.Trikkel, 2002
7 Vesi on hea lahusti ioonilistele ja polaarsetele ühenditele Veel on kõrge soojusmahtuvus neelab palju soojust, samas temperatuur palju ei tõuse temperatuuri stabiliseerimine looduses Tahkes olekus tihedus väiksem kui vedelas jäätumine toimub veekogu pinnalt alates Vee keemis-ja sulamistemperatuur oluliselt kõrgemad kui sarnastel ühenditel (H 2 S, H 2 Te) Need omadused seotud suhteliselt tugevate molekulidevaheliste jõudude nn. vesiniksideme olemasoluga vee molekulide vahel. Ühe vee molekuli hapnikuaatomi ja kahe teise vee molekuli vesinikuaatomite vahel tekib tugev elektrostaatiline vastasmõju, mistõttu vee molekulid moodustavad ulatusliku kolmemõõtmelise võrgustiku, kus iga vee molekul on seotud nelja lähedalasuva vee molekuliga (vt. molekulidevahelised jõud) Nende täiendavate sidemete lõhkumiseks on vaja oluliselt enam energiat kui nende ühendite korral, milles vesiniksidet ei esine Keemiliselt on vesi aktiivne ühend reageerib paljude metallidega, mittemetallidega, sooladega (hüdrolüüs) ja oksiididega. Leelismetallidega 2 Na + 2 H 2 O 2 NaOH + H 2 Happeliste oksiididega SO 2 + H 2 O H 2 SO 3 Aluseliste oksiididega CaO + H 2 O Ca(OH) 2 Vähedissotsieeruva ühendina on paljude ioonvahetusreaktsioonide saaduseks. Loodusliku vee puhastamine Koagulantide (Fe ja Al soolade) lisamine tekivad Fe(OH) 3 ja Al(OH) 3 kolloidosakesed, mille laeng on vastasmärgiline vees leiduvate orgaaniliste osakeste laenguga. Toimub koagulatsioon ning tekkivad suuremad osakesed eraldatakse filtrimisega (läbi kruusa ja liiva) Aereerimine gaasilise hapniku juhtimine läbi vee. Hapniku kontsentratsiooni kasv soodustab orgaaniliste ühendite oksüdeerumist CO 2 -ks ja veeks Osoneerimine ja kloreerimine bakterite hävitamiseks. Cl 2 + H 2 O H + + Cl - + HOCl (tugev oksüdeerija) basseinides lisatakse sageli tahket NaOCl või Ca(OCl) KKY3031 Üldine keemia
8 Vee karedus Vee karedus iseloomustab Ca ja Mg soolade sisaldust vees. Mööduv karedus on tingitud Ca(HCO 3 ) 2 ja Mg(HCO 3 ) 2 sisaldusest Püsiv karedus Ca ja Mg kloriididest ning sulfaatidest Kareduse mõõtühikud mg-ekv/l 1 mg-ekv/l on mg/l Ca 2+ -ioone või mg/l Mg 2+ -ioone Saksa kareduskraad ( dh) 1 dh on 10 mg/l CaO või ekvivalentne hulk muid Ca, Mg ühendeid Eriti pehme vesi < 1.5 mg-ekv/l 0-2 dh Pehme vesi mg-ekv/l 2-5 dh Mõõdukalt kare vesi mg-ekv/l 5-10 dh Kare vesi mg-ekv/l dh Väga kare vesi > 9.0 mg-ekv/l > 21 dh Kare vesi raskendab pesemist ning tekitab kuumutamisel katlakivi Ca(HCO 3 ) 2 CaCO 3 + H 2 O + CO 2 Mg(HCO 3 ) 2 Mg(OH) 2 + 2CO 2 2C 17 H 35 COONa + Ca(HCO 3 ) 2 (C 17 H 35 COO) 2 Ca + 2NaHCO 3 seep lahustumatu lubjaseep Vett pehmendavad lisandid karbonaadid, silikaadid, ortofosfaadid moodustavad Ca 2+ ioonidega sademe polüfosfaadid ja orgaanilised kompleksimoodustajad seovad Ca ja Mg ioonid püsivateks kompleksühenditeks, näiteks etüleendiammiintetraäädikhappe (EDTA) Na-sool (NaOOCH 2 C) 2 -N-CH 2 -CH 2 -N-(CH 2 COONa) 2 Vee pehmendamiseks kasutatakse: kuumutamist ja filtrimist kõrvaldab mööduva kareduse ioonvahetust Ca ja Mg ioonid vahetatakse välja Na ioonidega kuna Na-soolad on hästilahustuvad siis selline vesi katlakivi ei tekita 2.8 A.Trikkel, 2002
9 Soolade kõrvaldamine veest ioniitidega Ioniidid teatud kõrgmolekulaarsed ühendid või Ca, Al silikaadid (näit. tseoliidid), millel on võime adsorbeerida oma pinnale lahustest anioone või katioone. Kationiidid adsorbendid, mis seovad lahustest katioone Anioniidid adsorbendid, mis seovad lahustest anioone Osaline puhastamine Na-kationiidiga CaSO 4, MgSO 4 Ca Na 2 SO 4 2Na-kat + (kat) 2 + CaCl 2, MgCl 2 Mg 2NaCl Täielik puhastamine järjestikuste H-kationiidi ja OH-anioniidiga 1) vee läbijuhtimine H-kationiidiga kolonnist CaSO 4, MgSO 4 Ca H 2 SO 4 2 H-kat + (kat) 2 + CaCl 2, MgCl 2 Mg 2HCl 2) vee läbijuhtimine OH-anioniidiga kolonnist H 2 SO 4 (an) 2 SO 4 2 an-oh H 2 O 2 HCl 2 (an)cl saadakse puhas vesi samane destilleeritud veega 2.5. Tahked ained Tahkesse olekusse üleminekul suureneb osakeste korrapärase paigutuse aste ja suurenevad jõud osakeste vahel. Energia, mis eraldub kristallide tekkimisel ioonidest, aatomitest või molekulidest - võreenergia (kj/mol). Mida suurem võreenergia, seda püsivam on ühend (kõrgem sulamis t ). Amorfsed ühendid - ühendid, millel puudub korrapärane 3-mõõtmeline struktuur ja mis võivad võtta suvalise kuju (lõpmatult suure viskoossusega vedelikud, näit. klaas). Amorfsete ainete omadused (tugevus, elektrijuhtivus) on ühesugused igas suunas - nad on isotroopsed Klaas - optiliselt läbipaistev anorgaaniliste materjalide sulamisprodukt, mida on jahutatud kristallumata. 2.9 KKY3031 Üldine keemia
10 puhas kvartsklaas 100% SiO 2 optika termokindel klaas 60-80% SiO 2 väike soojuspaisumine 10-25% B 2 O 5 laborinõud Al 2 O 3 tavaline klaas 75% SiO 2 aknad, pudelid, 15% Na 2 O tundlik t löökidele 10% CaO ja kemikaalidele Kristalsed ühendid - ühendid, millel on korrapärane perioodiliselt korduv osakeste (ioonide, aatomite, molekulide) paigutus. Osakesed moodustavad kristallivõre, mille sõlmedes nad paiknevad. Osakesi iseloomustab soojuslik võnkumine, mis on seda intensiivsem, mida kõrgem on t. Omadused sõltuvad sageli suunast - anisotroopsed ühendid. Elementaarrakk - kristallivõre korduv element, millel on antud kristalli kõik sümmeetriaelemendid. Iseloomustatakse sümmeetriatelgedega (a, b, c) ja nurkadega telgede vahel (α, β, γ) Eristatakse 7 kristallisüsteemi: kuubiline, tetragonaalne, rombiline, heksagonaalne, monokliinne, trigonaalne ja trikliinne. Süsteemid jaotuvad omakorda klassideks (>30) ja tüüpideks (>200). Näit.kuubilise võre puhul a=b=c ja α=β=γ=90. Kuubiline Kuubiline Kuubiline mahttsentreeritud tahktsentreeritud Polümorfism - ühe aine esinemine erinevates kristallmodifikatsioonides. C - teemant, grafiit, fullereenid; S monokliinne, rombiline Isomorfism - erinevad ühendid, sarnase kristallvõrega. Ca 5 (PO 4 ) 6 F, Sr 5 (PO 4 ) 6 OH 2.10 A.Trikkel, 2002
11 Kristallvõrede iseloomustus Jaotamise aluseks jõud, mis hoiavad osakesi koos. Kristallvõred Ioonilised NaCl, LiF, MgO Kovalentsed C teemant, grafiit, SiO 2 kvarts Molekulaarsed Ar, CO 2, I 2, H 2 O Metallilised kõik metallid Na, Mg, Cu, Fe Võresõlmedes positiivsed ja negatiivsed ioonid Jõud osakeste vahel elektrostaatilised tõmbejõud; tihe pakkimine, kõrge võreenergia Omadused kõvad, sädeleved, kõrge st, halvad elektri- ja soojusjuhid aatomid kovalentne side kõvad, kõrge st, halvad soojus- ja elektrijuhid molekulid või aatomid aatomid nõrgad el.staatil. iseloomuga jõud (vesinikside, van der Waals'i jõud); hõre võre,madal võreenergia metalliline side, elektronid tugevalt delokaliseeritud pehmed, madal st, halvad soojus- ja elektrijuhid varieeruv kõvadus ja st, head soojusja elektrijuhid Vedelkristallid Ained, mis on ka vedelas olekus anisotroopsed st. omadused (näit. elektrijuhtivus) sõltuvad suunast Nende ühendite osakesed võivad üksteise suhtes ümber paikneda, kuid nad säilitavad oma orientatsiooni (näit. teljed paigutunud niidikujuliselt ühes suunas). Struktuur muutub kuumutamisel või voolu läbijuhtimisel, selle tulemusel muutuvad ka omadused (värvus) Adsorptsioon Adsorptsioon süsteemi mingi komponendi isevooluline kogunemine faaside (tahke-gaas, vedelik-gaas) eralduspinnale Kui adsorptsioon kandub edasi faasi sisemusse (gaasi neeldumine vedelikes), nimet nähtust absorptsiooniks Aine, mille pinnal toimub adsorptsioon adsorbent (aktiivsüsi, silikogeel), adsorbeeruv aine - adsorbaat. Adsorbendi pinnal on teatav lisaenergia (pinnaenergia), vastastoimel adsorbaadi osakestega see pinnaenergia väheneb KKY3031 Üldine keemia
12 Adsorbeerunud aine hulk väheneb t kasvuga ja suureneb t alanemisel Adsorptsiooniisotermid - adsorbeerunud aine hulga sõltuvus tema kontsentratsioonist või osarõhust antud temperatuuril (vt joonis) Adsorptsioon läheneb piirväärtusele, kuna adsorbaadi osakesed katavad kogu pinna ja edasine sidumine pole enam võimalik. Adsorptsioonil tekib side adsorbendi pinna ja adsorbaadi osakese vahel. Vastavalt selle sideme iseloomule eristatakse füüsikaline adsorptsioon põhjustatud van der Waalsi jõududest ei toimu elektronide üleminekut adsorbendi ja adsorbaadi vahel, seotud väikeste energiahulkadega, toimub kiiresti ka madalal temperatuuril keemiline adsorptsioon tekib keemiline side adsorbaadi ja pinna vahel, selektiivne protsess seotud keemiliste omadustega, keemiline side on seotud elektronide üleminekuga, sõltub aktivatsioonienergiast ja kulgeb kiiresti vaid kõrgematel temperatuuridel Kromatograafia analüüsimeetod kus uuritav segu juhitakse läbi sobivat adsorbenti sisaldava kolonni, milles segu komponendid jaotuvad adsorptsioonivõime erinevuste tõttu piki kolonni tsoonidesse Faasisiirded Vedel - gaas Iga vedeliku kohale tekib selle vedeliku aur. Osa vedeliku molekule mille kineetiline energia on piisav läheb gaasifaasi, osa molekule gaasifaasis, mille kineetiline energia kahaneb, seotakse uuesti vedelikuga. Suletud süsteemis saavad kindlal temperatuuril ja rõhul aurustumise ja kondenseerumise kiirused võrdseks süsteem jõuab tasakaaluolekusse. See on nn dünaamiline tasakaal vastassuunaliste protsesside kiirused võrdsustuvad. Tasakaalne aururõhk - vedeliku auru (gaasifaasis oleva vedeliku) rõhk vedeliku kohal tasakaaluolekus. Temperatuuri tõusuga molekulide keskmine kineetiline energia kasvab, seega suureneb ka auru rõhk vedeliku kohal (veeauru rõhk vee kohal 20 C juures 17.5 mm Hg, 100 C juures 760 mm Hg). Aurustumissoojus ( H a, kj/mol) - energiahulk, mis on vajalik ühe mooli vedeliku aurustamiseks keemistemperatuuril Keemistemperatuur - temperatuur, mille juures vedeliku aururõhk saab võrdseks välisrõhuga (rõhul 760 mm Hg, keeb vesi 100 C juures). Järelikult sõltub keemistemperatuur välisrõhust. Mida madalam on rõhk, seda madalam on keemistemperatuur A.Trikkel, 2002
13 Gaasi veeldamiseks on vaja alandada temperatuuri ja/või tõsta rõhku. Kriitiline temperatuur (T k ) - temperatuur, millest kõrgemal pole võimalik antud gaasi veeldada. Vedel - tahke Sulamistemperatuur - temperatuur, mille juures tahke ja vedel faas on tasakaalus rõhul 1 atm. Sulamissoojus ( H s, kj/mol) - energiahulk, mis on vajalik 1 mooli aine sulatamiseks sulamistemperatuuril. Üldjuhul samale ainele H s < H a vesi: H s = 6.01 kj/mol H a = 40.8 kj/mol Tahke - gaas Sublimatsioon - tahke aine üleminek gaasifaasi vedelfaasi läbimata (näit. I 2, CO 2 ). H sub = H s + H a Olekudiagrammid Seovad kõikide faaside (tahke, vedel, gaas) püsivuspiirid. Võimaldavad määrata aine agregaatolekut erinevatel temperatuuridel ja rõhkudel, samuti keemis- ja sulamistemperatuuri erinevatel rõhkudel. Olekudiagrammid on kolmemõõtmelised teljestikus P-V-T, sagedamini kasutatakse tasapinnalist P-T diagrammi Pinnad (alad) diagrammil kujutavad ühe faasi eksisteerimistingimusi (rõhk ja temperatuur). Kõverad diagrammil kujutavad neid T ja P tingimusi mille juures kaks erinevat faasi on omavahel tasakaalus KKY3031 Üldine keemia
14 Pressure 218 atm C Pcr, Tcr D BD - keemiskõver tasakaalus V-G BC - sulamiskõver tasakaalus V-T 760 mmhg liquid BA - sublimatsioonikõver, tasakaalus T-G solid B B kolmikpunkt tasakaalus T-V-G 4.58 mmhg A gas H 2 O: 0.01 C, 4.6 mm Hg CO 2 : -57 C, 5.2 atm 0 C 0.01 C 100 C 374 C Temperature Kõver BD lõpeb alati kriitilises punktis T kr, P kr. Sellest temperatuurist kõrgemal ei saa antud aine eksisteerida vedelas olekus (olenemata rõhust). H 2 O: C ja atm 2.14 A.Trikkel, 2002
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
Vedelikud ja tahkised. Aine olekud. Molekulidevahelised jõud E P
 Molekulidevahelised jõud Vedelike struktuur ja omadused Viskoossus ja pindpinevus Vedelike vastasmõju tahkisega Tahkised Kristalli struktuur Metallid Sulamid Ioonilised tahkised Molekulaarsed tahkised
Molekulidevahelised jõud Vedelike struktuur ja omadused Viskoossus ja pindpinevus Vedelike vastasmõju tahkisega Tahkised Kristalli struktuur Metallid Sulamid Ioonilised tahkised Molekulaarsed tahkised
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014. ÄÉÁÍüÇÓÇ
 ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
8. Faasid ja agregaatolekud.
 Soojusõpetus 8a 1 8. Faasid ja agregaatolekud. 8.1. Faasi ja agregaatoleku mõisted. Faas = süsteemi homogeenne ja mehaaniliselt eraldatav osa. Keemiliselt heterogeense süsteemi näide: õli + vesi. Keemiliselt
Soojusõpetus 8a 1 8. Faasid ja agregaatolekud. 8.1. Faasi ja agregaatoleku mõisted. Faas = süsteemi homogeenne ja mehaaniliselt eraldatav osa. Keemiliselt heterogeense süsteemi näide: õli + vesi. Keemiliselt
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 2016
 Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
Temperatuur ja soojus. Temperatuuri mõõtmise meetodid. I. Bichele, 016 Soojuseks (korrektselt soojushulgaks) nimetame energia hulka, mis on keha poolt juurde saadud või ära antud soojusvahetuse käigus
http://ekfe.chi.sch.gr ΙΑΝΟΥΑΡΙΟΣ 2010 Πειράματα Χημείας Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων
 http://ekfe.chi.sch.g 5 η - 6 η Συνάντηση ΙΑΝΟΥΑΡΙΟΣ 010 Πειράματα Χημείας Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων Παρασκευή διαλύματος ορισμένης συγκέντρωσης αραίωση διαλυμάτων Παρασκευή και ιδιότητες
http://ekfe.chi.sch.g 5 η - 6 η Συνάντηση ΙΑΝΟΥΑΡΙΟΣ 010 Πειράματα Χημείας Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων Παρασκευή διαλύματος ορισμένης συγκέντρωσης αραίωση διαλυμάτων Παρασκευή και ιδιότητες
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
Lokaalsed ekstreemumid
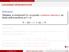 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
ΟΝΟΜΑΣΙΑ F - HF Υδροφθόριο S 2- H 2 S Υδρόθειο Cl - HCl Υδροχλώριο OH - H 2 O Οξείδιο του Υδρογόνου (Νερό) NO 3 HNO 3. Νιτρικό οξύ SO 3 H 2 SO 3
 1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
1 Να συμπληρωθεί ο παρακάτω πίνακα οξέων: ΟΝΟΜΑΣΙΑ F HF Υδροφθόριο S 2 H 2 S Υδρόθειο Cl HCl Υδροχλώριο OH H 2 O Υδρογόνου (Νερό) NO 3 HNO 3 οξύ SO 3 H 2 SO 3 Θειώδε οξύ Br HBr Υδροβρώμιο 2 SO 4 H 2 SO
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ
 23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
23 3. ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ 1. Βλέπε θεωρία σελ. 83. 2. α) (χημική εξίσωση) β) (δύο μέλη) (ένα βέλος >) γ) (αντιδρώντα) δ) (τμήμα ύλης ομογενές που χωρίζεται από το γύρω του χώρο με σαφή όρια). ε) (που οδηγούν
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
Funktsiooni diferentsiaal
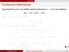 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Κανόνες διαλυτότητας για ιοντικές ενώσεις
 Κανόνες διαλυτότητας για ιοντικές ενώσεις 1. Ενώσεις των στοιχείων της Ομάδας 1A και του ιόντος αμμωνίου (Ιόντα: Li +, Na +, K +, Rb +, Cs +, NH 4+ ) είναι ευδιάλυτες, χωρίς εξαίρεση: πχ. NaCl, K 2 S,
Κανόνες διαλυτότητας για ιοντικές ενώσεις 1. Ενώσεις των στοιχείων της Ομάδας 1A και του ιόντος αμμωνίου (Ιόντα: Li +, Na +, K +, Rb +, Cs +, NH 4+ ) είναι ευδιάλυτες, χωρίς εξαίρεση: πχ. NaCl, K 2 S,
Lahused ja lahustumisprotsess konserveerimises
 Lahused ja lahustumisprotsess konserveerimises Lektor: Heige Peets Ennistuskoda Kanut, 6 44 25 63 esemed@kanut.ee Tallinn-Tartu 2004 Loengu eesmärgiks on anda ülevaade ja lühike selgitus kõige üldisematest
Lahused ja lahustumisprotsess konserveerimises Lektor: Heige Peets Ennistuskoda Kanut, 6 44 25 63 esemed@kanut.ee Tallinn-Tartu 2004 Loengu eesmärgiks on anda ülevaade ja lühike selgitus kõige üldisematest
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
AATOMI EHITUS KEEMILINE SIDE
 TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Molekulaarfüüsika - ja termodünaamika alused
 Molekulaarfüüsika - ja termodünaamika alused Ettevalmistus kontrolltööks 1. Missugustel väidetel põhineb molekulaarkineetiline teooria? Aine koosneb molekulidest Osakesed on pidevas liikumises Osakestele
Molekulaarfüüsika - ja termodünaamika alused Ettevalmistus kontrolltööks 1. Missugustel väidetel põhineb molekulaarkineetiline teooria? Aine koosneb molekulidest Osakesed on pidevas liikumises Osakestele
1. Õppida tundma kalorimeetriliste mõõtmiste põhimõtteid ja kalorimeetri ehitust.
 Kaorimeetriised mõõtmised LABORATOORNE TÖÖ NR. 3 KALORIMEETRILISED MÕÕTMISED TÖÖ EESMÄRGID 1. Õppida tundma aorimeetriiste mõõtmiste põhimõtteid ja aorimeetri ehitust. 2. Määrata jää suamissoojus aorimeetriise
Kaorimeetriised mõõtmised LABORATOORNE TÖÖ NR. 3 KALORIMEETRILISED MÕÕTMISED TÖÖ EESMÄRGID 1. Õppida tundma aorimeetriiste mõõtmiste põhimõtteid ja aorimeetri ehitust. 2. Määrata jää suamissoojus aorimeetriise
3. Να συμπληρωθούν οι παρακάτω αντιδράσεις:
 1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
1. Να συμπληρωθούν οι παρακάτω αντιδράσεις: 2N 2 + 3H 2 2NH 3 4Na + O 2 2Να 2 Ο Fe + Cl 2 FeCl 2 Zn + Br 2 ZnBr 2 2K + S K 2 S 2Ca + O 2 2CaO Na + Ca -------- C + O 2 CO 2 H 2 + Br 2 2HBr CaO + H 2 O Ca(OH)
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2015 Β ΦΑΣΗ Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Κυριακή 26 Απριλίου 2015 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα
ORGAANILISE KEEMIA LABORIJUHEND ABISTAV MATERJAL
 TALLINNA ÜLIKL Matemaatika ja Loodusteaduste Instituut RGAANILISE KEEMIA LABRIJUEND ABISTAV MATERJAL Marju Robal ja Rando Tuvikene Tallinn 2008 SISUKRD 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME...3
TALLINNA ÜLIKL Matemaatika ja Loodusteaduste Instituut RGAANILISE KEEMIA LABRIJUEND ABISTAV MATERJAL Marju Robal ja Rando Tuvikene Tallinn 2008 SISUKRD 1. RGAANILISTE AINETE LAUSTUVUS JA LAUSTAMISVÕIME...3
ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ. Η 2 SO 4 + BaCl 2 2HCl + BaSO 4. 2HCl + Na 2 CO 3 CO 2 + H 2 O + 2NaCl. 2HCl + Na 2 SO 3 SO 2 + H 2 O + 2NaCl
 ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ Οι αντιδράσεις διπλής αντικατάστασης γίνονται ανάµεσα σε ηλεκτρολύτες µε ανταλλαγή ιόντων. Για να πραγµατοποιηθεί µια αντίδραση διπλής αντικατάστασης πρέπει ένα τουλάχιστον από τα προϊόντα
ΙΠΛΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗ Οι αντιδράσεις διπλής αντικατάστασης γίνονται ανάµεσα σε ηλεκτρολύτες µε ανταλλαγή ιόντων. Για να πραγµατοποιηθεί µια αντίδραση διπλής αντικατάστασης πρέπει ένα τουλάχιστον από τα προϊόντα
Vektoralgebra seisukohalt võib ka selle võrduse kirja panna skalaarkorrutise
 Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
Jõu töö Konstanse jõu tööks lõigul (nihkel) A A nimetatakse jõu mooduli korrutist teepikkusega s = A A ning jõu siirde vahelise nurga koosinusega Fscos ektoralgebra seisukohalt võib ka selle võrduse kirja
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
3. Solvendiefektide mõju ainete omadustele ja keemilistele protsessidele. 3.1 Solvendiefektid happe-aluse protsessidele. Tasakaal ja kiirus
 3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
3. olvendiefektide mõju ainete omadustele ja keemilistele protsessidele Põhiallikas: Tasakaal ja kiirus Lahusti mõju tasakaalule ilmneb seeläbi, et erinevad lahustid solvateerivad erineva intensiivsusega
MEHAANIKA. s t. kogu. kogu. s t
 MLR 700 Üldfüüsika süvakursus: Katrin Teras Ettevalmistus Üldfüüsika eksamiks Aine kood: MLR 700 Eksami aeg: 05.0.006 Kell:.00 Ruum: P-5 Konsultatsiooni aeg: 04.0.006 Kell:.00 Ruum: P-5. Ainepunkti mõiste.
MLR 700 Üldfüüsika süvakursus: Katrin Teras Ettevalmistus Üldfüüsika eksamiks Aine kood: MLR 700 Eksami aeg: 05.0.006 Kell:.00 Ruum: P-5 Konsultatsiooni aeg: 04.0.006 Kell:.00 Ruum: P-5. Ainepunkti mõiste.
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ORGAANILINE KEEMIA ANDRES TALVARI
 ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
ORGAANILINE KEEMIA ANDRES TALVARI Käesolev õppevahend on koostatud mitmete varem väljaantud kõrgkooli õpikute abil ja on mõeldud Sisekaitseakadeemia päästeteenistuse eriala üliõpilastele õppeaine RAKENDUSKEEMIA
Χ ΗΜΙΚΕΣ Α Ν Τ ΙΔΡΑΣΕΙΣ
 53 Χ ΗΜΙΚΕΣ Α Ν Τ ΙΔΡΑΣΕΙΣ Χημική αντίδραση ονομάζουμε κάθε χημικό φαινόμενο. Δηλαδή, κάθε φαινόμενο στο οποίο έχουμε αναδιάταξη των ηλεκτρονίων ( e ) της εξωτερικής στιβάδας των ατόμων που παίρνουν μέρος
53 Χ ΗΜΙΚΕΣ Α Ν Τ ΙΔΡΑΣΕΙΣ Χημική αντίδραση ονομάζουμε κάθε χημικό φαινόμενο. Δηλαδή, κάθε φαινόμενο στο οποίο έχουμε αναδιάταξη των ηλεκτρονίων ( e ) της εξωτερικής στιβάδας των ατόμων που παίρνουν μέρος
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat
 Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
ORGAANILINE KEEMIA I osa
 ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
Ημερομηνία: Τρίτη 18 Απριλίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
ΑΠΟ 10/04/017 ΕΩΣ /04/017 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ XHMEIA Ημερομηνία: Τρίτη 18 Απριλίου 017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις παρακάτω προτάσεις Α1 Α5 να επιλέξετε τη σωστή απάντηση.
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Materjalide omadused. kujutatud joonisel Materjalide mehaanikalised omadused määratakse tavaliselt otsese testimisega,
 Peatükk 7 Materjalide omadused 1 Materjalide mehaanikalised omadused määratakse tavaliselt otsese testimisega, mis sageli lõpevad katsekeha purunemisega, näiteks tõmbekatse, väändekatse või löökkatse.
Peatükk 7 Materjalide omadused 1 Materjalide mehaanikalised omadused määratakse tavaliselt otsese testimisega, mis sageli lõpevad katsekeha purunemisega, näiteks tõmbekatse, väändekatse või löökkatse.
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
C M. V n: n =, (D): V 0,M : V M P = ρ ρ V V. = ρ
 »»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
»»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
Ecophon Line LED. Süsteemi info. Mõõdud, mm 1200x x x600 T24 Paksus (t) M329, M330, M331. Paigaldusjoonis M397 M397
 Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
Ecophon Line LED Ecophon Line on täisintegreeritud süvistatud valgusti. Kokkusobiv erinevate Focus-laesüsteemidega. Valgusti, mida sobib kasutada erinevates ruumides: avatud planeeringuga kontorites; vahekäigus
Deformeeruva keskkonna dünaamika
 Peatükk 4 Deformeeruva keskkonna dünaamika 1 Dünaamika on mehaanika osa, mis uurib materiaalsete keskkondade liikumist välismõjude (välisjõudude) toimel. Uuritavaks materiaalseks keskkonnaks võib olla
Peatükk 4 Deformeeruva keskkonna dünaamika 1 Dünaamika on mehaanika osa, mis uurib materiaalsete keskkondade liikumist välismõjude (välisjõudude) toimel. Uuritavaks materiaalseks keskkonnaks võib olla
1. Arrhenius. Ion equilibrium. ก - (Acid- Base) 2. Bronsted-Lowry *** ก - (conjugate acid-base pairs) HCl (aq) H + (aq) + Cl - (aq)
 Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
Ion equilibrium ก ก 1. ก 2. ก - ก ก ก 3. ก ก 4. (ph) 5. 6. 7. ก 8. ก ก 9. ก 10. 1 2 สารล ลายอ เล กโทรไลต (Electrolyte solution) ก 1. strong electrolyte ก HCl HNO 3 HClO 4 NaOH KOH NH 4 Cl NaCl 2. weak
TMR praktikum. Teooria: Aatomituuma varjestatus
 TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
TMR praktikum Praktikum toimub 2-l praktikumipäeval ning koosneb kahest tööst. Tööde eesmärk on ühendite TMR spektrite interpreteerimine ning ainete identifitseerimine nii struktuurvalemi kui brutovalemi
Κεφάλαιο 3 Χημικές Αντιδράσεις
 Κεφάλαιο 3 Χημικές Αντιδράσεις Οι χημικές αντιδράσεις μπορούν να ταξινομηθούν σε δύο μεγάλες κατηγορίες, τις οξειδοαναγωγικές και τις μεταθετικές. Α. ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Στις αντιδράσεις αυτές
Κεφάλαιο 3 Χημικές Αντιδράσεις Οι χημικές αντιδράσεις μπορούν να ταξινομηθούν σε δύο μεγάλες κατηγορίες, τις οξειδοαναγωγικές και τις μεταθετικές. Α. ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Στις αντιδράσεις αυτές
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut
 Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
Penteelid, VA Lämmastik (nitrogen, typpi), fosfor, arseen, antimon, vismut N P As Sb Bi Z 7 15 33 51 83 A r 14.00674 30.97376 74.9216 121.76(1) 208.9804 El. neg. 3.0 2.1 2.0 1.9 1.9 T s, C 210.1 44.2 817
ATMOSFÄÄRI- JA MEREFÜÜSIKA ALUSED. Loengukonspekt. I osa
 ARU ÜLIKOOL KESKKONNAFÜÜSIKA INSIUU AMOSFÄÄRI- JA MEREFÜÜSIKA ALUSED Loengukonspekt I osa Koostanud H. Ohvril Aprill 2005 artu Konspekt on koostatud toetamaks Füüsika õppekava magistriõppe loengukursust
ARU ÜLIKOOL KESKKONNAFÜÜSIKA INSIUU AMOSFÄÄRI- JA MEREFÜÜSIKA ALUSED Loengukonspekt I osa Koostanud H. Ohvril Aprill 2005 artu Konspekt on koostatud toetamaks Füüsika õppekava magistriõppe loengukursust
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ
 ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ 1 η : A) 9,8g H 3 PO 4 αντιδρούν με την κατάλληλη ποσότητα NaCl σύμφωνα με την χημική εξίσωση: H 3 PO 4 + 3NaCl Na 3 PO 4 + 3HCl. Να υπολογίσετε πόσα λίτρα αέριου HCl παράγονται,
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ ΑΣΚΗΣΗ 1 η : A) 9,8g H 3 PO 4 αντιδρούν με την κατάλληλη ποσότητα NaCl σύμφωνα με την χημική εξίσωση: H 3 PO 4 + 3NaCl Na 3 PO 4 + 3HCl. Να υπολογίσετε πόσα λίτρα αέριου HCl παράγονται,
Διαγώνισμα Χημείας Α Λυκείου Οξέα Βάσεις Αλατα, και Χημικές αντιδράσεις. Θέμα 1 ο...
 Διαγώνισμα Χημείας Α Λυκείου Οξέα Βάσεις Αλατα, και Χημικές αντιδράσεις. Θέμα 1 ο.... Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις, 1.1. Από τις ενώσεις: HCl, H 2 O, NH 3, H 2 SO
Διαγώνισμα Χημείας Α Λυκείου Οξέα Βάσεις Αλατα, και Χημικές αντιδράσεις. Θέμα 1 ο.... Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις, 1.1. Από τις ενώσεις: HCl, H 2 O, NH 3, H 2 SO
1. Στο παρακάτω διάγραμμα τα γράμματα Α, Β, Γ, Δ, Ε, Ζ, Θ, Κ, Λ
 Επαναληπτικά δέντρα.. Ανόργανης στο ph. Στο παρακάτω διάγραμμα τα γράμματα Α, Β, Γ, Δ, Ε, Ζ, Θ, Κ, Λ αναφέρονται σε υδατικά διαλύματα. Το διάλυμα Α έχει όγκο 00mL και ph = HCl 00mL Ca(OH) 2 900mLH2O 0,448L
Επαναληπτικά δέντρα.. Ανόργανης στο ph. Στο παρακάτω διάγραμμα τα γράμματα Α, Β, Γ, Δ, Ε, Ζ, Θ, Κ, Λ αναφέρονται σε υδατικά διαλύματα. Το διάλυμα Α έχει όγκο 00mL και ph = HCl 00mL Ca(OH) 2 900mLH2O 0,448L
Θέμα Α. Ονοματεπώνυμο: Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Διαγώνισμα εφ όλης της ύλης Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες ερωτήσεις.
Teaduskool. Alalisvooluringid. Koostanud Kaljo Schults
 TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
TARTU ÜLIKOOL Teaduskool Alalisvooluringid Koostanud Kaljo Schults Tartu 2008 Eessõna Käesoleva õppevahendi kasutajana on mõeldud eelkõige täppisteaduste vastu huvi tundvaid gümnaasiumi õpilasi, kes on
4. KEHADE VASTASTIKMÕJUD. JÕUD
 4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
4. KEHADE VASTASTIKMÕJUD. JÕUD Arvatavasti oled sa oma elus kogenud, et kõik mõjud on vastastikused. Teiste sõnadega: igale mõjule on olemas vastumõju. Ega füüsikaski teisiti ole. Füüsikas on kehade vastastikuse
HAPNIKUTARBE INHIBEERIMISE TEST
 HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
HAPNIKUTABE INHIBEEIMISE TEST 1. LAHUSED JA KEMIKAALID 1.1 Üldised põhimõtted Lahuste valmistamiseks kasutada analüütiliselt puhtaid kemikaale. Kasutatav vesi peab olema destilleeritud või deioniseeritud
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
SOOJUSFÜÜSIKA ALUSED. Tehniline termodünaamika Soojusläbikanne ANDRES TALVARI
 SOOJUSFÜÜSIKA ALUSED Tehniline termodünaamika Soojusläbikanne ANDRES TALVARI Õppevahend on mõeldud kasutamiseks Sisekaitseakadeemia päästekolledži üliõpilastele õppeaine Soojusfüüsika omandamisel, kuid
SOOJUSFÜÜSIKA ALUSED Tehniline termodünaamika Soojusläbikanne ANDRES TALVARI Õppevahend on mõeldud kasutamiseks Sisekaitseakadeemia päästekolledži üliõpilastele õppeaine Soojusfüüsika omandamisel, kuid
Ασκήσεις Προβλήματα. Μετρήσεις Μονάδες Γνωρίσματα της Ύλης
 Ασκήσεις Προβλήματα Μετρήσεις Μονάδες Γνωρίσματα της Ύλης 19. Ποιες μονάδες χρησιμοποιούν συνήθως οι χημικοί για την πυκνότητα των: α) στερεού, β) υγρού και γ) αερίου σώματος; Να εξηγήσετε τη διαφορά.
Ασκήσεις Προβλήματα Μετρήσεις Μονάδες Γνωρίσματα της Ύλης 19. Ποιες μονάδες χρησιμοποιούν συνήθως οι χημικοί για την πυκνότητα των: α) στερεού, β) υγρού και γ) αερίου σώματος; Να εξηγήσετε τη διαφορά.
Vedelikkromatograafilise meetodi optimeerimine. Näited ajakirja LC&GC Europe erinevatest numbritest
 Vedelikkromatograafilise meetodi optimeerimine Näited ajakirja LC&GC Europe erinevatest numbritest 1 Eesmärgid? Arenda meetodit kuni see on piisav sinu vajadustele, siis lõpeta Iga meetodit saab teha paremaks
Vedelikkromatograafilise meetodi optimeerimine Näited ajakirja LC&GC Europe erinevatest numbritest 1 Eesmärgid? Arenda meetodit kuni see on piisav sinu vajadustele, siis lõpeta Iga meetodit saab teha paremaks
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 4
 ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
ΚΕΦΑΛΑΙΟ 4 ΣΤΟΙΧΕΙΟΜΕΤΡΙΑ ΕΡΩΤΗΣΕΙΣ ΜΕ ΤΙΣ ΑΠΑΝΤΗΣΕΙΣ: 1. Τι είναι ατομικό και τί μοριακό βάρος; Ατομικό βάρος είναι ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη η μάζα του ατόμου από το 1/12 της
Παραδοχές στις οποίες στις οποίες στηρίζεται ο αριθμός οξείδωσης
 Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
Αριθμός Οξείδωσης ή τυπικό σθένος Είναι ένας αριθμός που εκφράζει την ενωτική ικανότητα των στοιχείων με βάση ορισμένες παραδοχές. Η χρησιμοποίηση του επιβλήθηκε για τους πιο κάτω λόγους : Χρησιμεύει στη
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4
 ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4 ΘΕΜΑ Α Α1. Στον σύγχρονο Περιοδικό Πίνακα τα χημικά στοιχεία έχουν ταξινομηθεί: α. κατ αύξοντα ατομικό
ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4 ΘΕΜΑ Α Α1. Στον σύγχρονο Περιοδικό Πίνακα τα χημικά στοιχεία έχουν ταξινομηθεί: α. κατ αύξοντα ατομικό
MATERJALI VALIK JA KONSTRUEERIMINE
 MATERJALI VALIK JA KONSTRUEERIMINE 1 Tabel: MATERJALIDE OMADUSED üüsikalised Mehaanilised Tehnoloogilised Keemilised Muud mittemeh. om.-d Majanduslikud Esteetilised Tihedus, sulamistemperatuur, kõvadus,
MATERJALI VALIK JA KONSTRUEERIMINE 1 Tabel: MATERJALIDE OMADUSED üüsikalised Mehaanilised Tehnoloogilised Keemilised Muud mittemeh. om.-d Majanduslikud Esteetilised Tihedus, sulamistemperatuur, kõvadus,
Energiabilanss netoenergiavajadus
 Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Kujutise saamine MAGNETRESONANTSTOMOGRAAFIAS (MRT) Magnetic Resonance Imaging - MRI
 Kujutise saamine MAGNETRESONANTSTOMOGRAAFIAS (MRT) Magnetic Resonance Imaging - MRI Mait Nigul MRT kool, 2011, ERÜ MRT baseerub füüsikalisel nähtuse tuumamagnetresonants avastasid /kirjeldasid1945 aastal
Kujutise saamine MAGNETRESONANTSTOMOGRAAFIAS (MRT) Magnetic Resonance Imaging - MRI Mait Nigul MRT kool, 2011, ERÜ MRT baseerub füüsikalisel nähtuse tuumamagnetresonants avastasid /kirjeldasid1945 aastal
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
Kordamine 2. osa Jõud looduses, tihedus, rõhk, kehad vedelikus ja gaasis. FÜÜSIKA 8. KLASSILE
 Kordamine 2. osa Jõud looduses, tihedus, rõhk, kehad vedelikus ja gaasis. FÜÜSIKA 8. KLASSILE AINE TIHEDUS AINE TIHEDUSEKS nimetatakse füüsikalist suurust, mis võrdub keha (ainetüki) massi ja selle keha
Kordamine 2. osa Jõud looduses, tihedus, rõhk, kehad vedelikus ja gaasis. FÜÜSIKA 8. KLASSILE AINE TIHEDUS AINE TIHEDUSEKS nimetatakse füüsikalist suurust, mis võrdub keha (ainetüki) massi ja selle keha
2 η ΕΞΕΤΑΣΤΙΚΗ ΠΕΡΙΟΔΟΣ. Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 4 Μαΐου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Α1. Να βρεθεί η δομή των παρακάτω ατόμων: 23 11 Na, 40 20 Ca, 33 16 S, 127 53 I, 108
REAKTSIOONIKINEETIKA
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE II REAKTSIOONIKINEETIKA Vello Past Õppevahend TK õpilastele Tartu 008 REAKTSIOONIKINEETIKA. Keemilise reatsiooni võrrand, tema võimalused ja
Το Η 2 διότι έχει το μικρότερο Mr επομένως τα περισσότερα mol ή V=αx22,4/Mr V ( H2) =11,2α...
 Λύσεις Ολυμπιάδας Β Λυκείου 2012 ΜΕΡΟΣ Α (20 μονάδες) Ερώτηση 1 (2 μονάδες) Το Η 2 διότι έχει το μικρότερο Mr επομένως τα περισσότερα mol ή V=αx22,4/Mr V ( H2) =11,2α... Ερώτηση 2 (4 μονάδες) -3 +5 i.nh
Λύσεις Ολυμπιάδας Β Λυκείου 2012 ΜΕΡΟΣ Α (20 μονάδες) Ερώτηση 1 (2 μονάδες) Το Η 2 διότι έχει το μικρότερο Mr επομένως τα περισσότερα mol ή V=αx22,4/Mr V ( H2) =11,2α... Ερώτηση 2 (4 μονάδες) -3 +5 i.nh
ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ. β) Να βρεθεί σε ποια οµάδα και σε ποια περίοδο του Περιοδικού Πίνακα ανήκουν.
 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ: 03490 ΗΜΕΡΟΜΗΝΙΑ: 27/5/2014 ΟΙ ΚΑΘΗΓΗΤΕΣ: ΜΑΞΙΜΟΣ ΚΟΤΕΛΙΔΑΣ ΕΚΦΩΝΗΣΕΙΣ Θέμα 2ο Α) Για τα στοιχεία: 12 Μg και 8 Ο α) Να κατανεµηθούν τα ηλεκτρόνιά τους σε στιβάδες. (µονάδες 2) β)
28. Sirgvoolu, solenoidi ja toroidi magnetinduktsiooni arvutamine koguvooluseaduse abil.
 8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ
 ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΤΑΞΗ: ΜΑΘΗΜΑ: A ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 14 Απριλίου 2018 Διάρκεια Εξέτασης: 2 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ)
 ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ) ΘΕΜΑ 1 Ο Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές και να διορθώσετε τις λανθασµένες: 1. Τα άτοµα όλων των στοιχείων είναι διατοµικά.. Το 16 S έχει ατοµικότητα
ΙΑΓΩΝΙΣΜΑ 1 Ο ( 1 Ο ΚΕΦΑΛΑΙΟ) ΘΕΜΑ 1 Ο Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές και να διορθώσετε τις λανθασµένες: 1. Τα άτοµα όλων των στοιχείων είναι διατοµικά.. Το 16 S έχει ατοµικότητα
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
