«ΑΛΛΗΛΕΠΙΔΡΑΣΗ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΑΔΕΝΟΣΙΝΗΣ ΚΑΙ ΓΛΟΥΤΑΜΙΝΙΚΟΥ ΟΞΕΟΣ ΣΕ ΔΙΑΔΙΚΑΣΙΕΣ ΝΕΥΡΩΝΙΚΗΣ ΠΛΑΣΤΙΚΟΤΗΤΑΣ ΣΤΟΝ ΙΠΠΟΚΑΜΠΟ ΕΠΙΜΥΟΣ»
|
|
|
- Σοφοκλής Καζαντζής
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΕΦΑΡΜΟΓΕΣ ΣΤΙΣ ΒΑΣΙΚΕΣ ΙΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ» ΜΕΤΑΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ «ΑΛΛΗΛΕΠΙΔΡΑΣΗ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΑΔΕΝΟΣΙΝΗΣ ΚΑΙ ΓΛΟΥΤΑΜΙΝΙΚΟΥ ΟΞΕΟΣ ΣΕ ΔΙΑΔΙΚΑΣΙΕΣ ΝΕΥΡΩΝΙΚΗΣ ΠΛΑΣΤΙΚΟΤΗΤΑΣ ΣΤΟΝ ΙΠΠΟΚΑΜΠΟ ΕΠΙΜΥΟΣ» ΤΣΙΑΜΑΚΗ ΕΙΡΗΝΗ ΙΑΤΡΟΣ ΠΑΤΡΑ 2012 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ
2 ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΕΦΑΡΜΟΓΕΣ ΣΤΙΣ ΒΑΣΙΚΕΣ ΙΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ» ΜΕΤΑΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ «ΑΛΛΗΛΕΠΙΔΡΑΣΗ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΑΔΕΝΟΣΙΝΗΣ ΚΑΙ ΓΛΟΥΤΑΜΙΝΙΚΟΥ ΟΞΕΟΣ ΣΕ ΔΙΑΔΙΚΑΣΙΕΣ ΝΕΥΡΩΝΙΚΗΣ ΠΛΑΣΤΙΚΟΤΗΤΑΣ ΣΤΟΝ ΙΠΠΟΚΑΜΠΟ ΕΠΙΜΥΟΣ» ΤΣΙΑΜΑΚΗ ΕΙΡΗΝΗ ΙΑΤΡΟΣ Επιβλέπουσα Καθηγήτρια: Φεβρωνία Αγγελάτου Καθηγήτρια Τμήμα Ιατρικής Πανεπιστήμιο Πατρών ΠΑΤΡΑ
3 Τριμελής συμβουλευτική επιτροπή Αγγελάτου Φεβρωνία Καθηγήτρια Τμήμα Ιατρικής Πανεπιστήμιο Πατρών Κωστόπουλος Γεώργιος Καθηγητής Τμήμα Ιατρικής Πανεπιστήμιο Πατρών Μητσάκου Αδαμαντία Καθηγήτρια Τμήμα Ιατρικής Πανεπιστήμιο Πατρών 3
4 ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ.7 ΠΕΡΙΛΗΨΗ..8 1.ΕΙΣΑΓΩΓΗ Ιππόκαμπος Φυλογενετική εξέλιξη Ανατομία-Δομή-Συνδέσεις Ο ιπποκάμπειος σχηματισμός Λειτουργικός ρόλος του Ιπποκάμπου: Η Μνήμη και η Μάθηση Μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος Μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος Δομή μεταβοτροπικών υποδοχέων Αμινοτελικό άκρο- περιοχή δέσμευσης γλουταμινικού Οι εφτά διαμεμβρανικές έλικες των mglurs Καρβοξυ-τελικά άκρο Τοπογραφική και κυτταρική κατανομή των μεταβοτροπικών υποδοχέων στο κεντρικό νευρικό σύστημα Κατανομή των Group I Μεταβοτροπικών υποδοχέων Κατανομή των Group I I Μεταβοτροπικών υποδοχέων Κατανομή των Group I I I Μεταβοτροπικών υποδοχέων Κυτταρική εντόπιση των μεταβοτροπικών υποδοχέων Μεταγωγή σήματος Αλληλεπιδρώσες πρωτεΐνες με τους mglurs Κυτταρική σηματοδότηση μέσω του group I μεταβοτροπικών υποδοχέων Ενεργοποίηση των G πρωτεϊνών από τους group Ι mglur Αλληλεπίδραση των group Ι mglur με τους NMDA υποδοχείς Σηματοδοτικό μονοπάτι ενεργοποίησης του group Ι mglur, ανεξάρτητο από την ενεργοποίηση των G- πρωτεϊνών Αλληλεπίδραση των group I mglur με Homer πρωτεΐνες Φαρμακολογία του group I μεταβοτροπικών υποδοχέων mglur5:σημαντικός ο ρόλος τους στις γνωστικές λειτουργίες NMDA Υποδοχείς: Δομή και λειτουργία Συναπτική λειτουργία Υπότυποι Δομή Λειτουργική Ρύθμιση των NMDA Υποδοχέων από Φωσφορυλίωση σε Θέσεις Σερίνης/ Θρεονίνης Ρύθμιση της φωσφορυλίωσης της NR1 υπομονάδας σε 4
5 κατάλοιπα σερίνης Ρύθμιση της φωσφορυλίωσης των NR2 υπομονάδων σε κατάλοιπα σερίνης Λειτουργική Ρύθμιση των NMDA Υποδοχέων από Φωσφορυλίωση σε Κατάλοιπα Τυροσίνης Διαταραχή λειτουργίας των NMDA υποδοχέων Αδενοσίνη Παραγωγή, απελευθέρωση και μεταβολισμός της αδενοσίνης Υποδοχείς αδενοσίνης A1 υποδοχείς A2 υποδοχείς A3 υποδοχείς Αλληλεπιδράσεις μεταξύ των υποδοχέων A1/A 2A αδενοσίνης Αλληλεπιδράσεις μεταξύ των υποδοχέων A 2A υποδοχέων αδενοσίνης και της γλουταμινεργικής δραστηριότητας Το σηματοδοτικό μονοπάτι των MARK κινασών (ERK ½) και η συμβολή του στη συναπτική πλαστικότητα Η συμμετοχή της ERK1/2 κινάσης στο LTP Η συμμετοχή της ERK1/2 κινάσης στην μνήμη και στην μάθηση Η συμμετοχή της ERK1/2 κινάσης στη συναπτική νευροδιαβίβαση Οι πρωτεΐνες της μετασυναπτικής πυκνότητας και οι ιοντικοί δίαυλοι K V 4.2 αποτελούν στόχους της ERK1/2 κινάσης Οι μεταγραφικοί παράγοντες αποτελούν στόχους της ERK1/2 κινάσης ΣΤΟΧΟΣ ΥΛΙΚΑ ΚΑΙ ΜΕΘΟΔΟΙ Πειραματόζωα Προετοιμασία του ιστού για τα «in vitro» πειράματα «In vitro» ενεργοποίηση των mglur5 υποδοχέων γλουταμινικού οξέος, καθώς και των Α2Α υποδοχέων αδενοσίνης στις φέτες ιππόκαμπου Ομογενοποίηση των δειγμάτων Μέτρηση συγκέντρωσης πρωτεϊνών SDS ηλεκτροφόρηση σε πήκτωμα πολυακρυλαμιδίου (SDS-PAGE) Ανοσοαποτύπωμα (Western blot) Πειραματική Πορεία ΑΠΟΤΕΛΕΣΜΑΤΑ Αποτελέσματα 127 5
6 3.2 Επίδραση της ενεργοποίησης των υποδοχέων mglur5 του γλουταμινικού οξέως στα επίπεδα φωσφορυλίωσης των υπομονάδων του NMDA υποδοχέα του γλουταμινικού οξέος στον ιππόκαμπο Η ενεργοποίηση των Α2Α υποδοχέων Αδενοσίνης, δεν είχε επίδραση στα επίπεδα φωσφορυλίωσης των υπομονάδων του NMDA υποδοχέα του γλουταμινικού οξέος στον ιππόκαμπο επίμυος Επίδραση της ταυτόχρονης διέγερσης των Α2A και mglur5 υποδοχέων στο επίπεδο φωσφορυλίωσης των υπομονάδων των NMDA υποδοχέων στον ιππόκαμπο Η αναστολή των Α2Α υποδοχέων αδενοσίνης με τον ανταγωνιστή ΖΜ μειώνει σημαντικά την mglur5 επαγώμενη φωσφορυλίωση των NMDA υπομονάδων στον ιππόκαμπο Η διέγερση των υποδοχέων mglur5 του γλουταμινικού οξέως ενεργοποιεί το σηματοδοτικό μονοπάτι της ERK ½ κινάσης στον ιππόκαμπο επίμυος Η διέγερση των υποδοχέων Α2Α αδενοσίνης δεν έχει καμία επίδραση στην ενεργοποίηση του σηματοδοτικού μονοπατιού της ERK ½ κινάσης στον ιππόκαμπο επίμυος Η συγχορήγηση του ZM και του CHPG, δεν έχει επίδραση στο σηματοδοτικό μονοπάτι της ERK ½ κινάσης στον ιππόκαμπο ΣΥΖΗΤΗΣΗ Η ενεργοποίηση των mglur5 υποδοχέων γλουταμινικού οξέος προκαλεί ισχυρή αύξηση της φωσφορυλίωσης του καταλοίπου τυροσίνη-1472 της NR2B υπομονάδας, η οποία παίζει σημαντικό ρόλο στη μετακίνηση του NMDA υποδοχέα και στη σταθεροποίηση του στη κυτταρική μεμβράνη (trafficking) Η ενεργοποίηση των Α2Α υποδοχέων αδενοσίνης δεν επηρεάζει άμεσα τη φωσφορυλίωση των υπομονάδων του NMDA υποδοχέα, δεν παρουσιάζει συνεργιστική αλληλεπίδραση με τους mglur5 υποδοχείς, αλλά δρα αδειοδοτικά στην ικανότητα των mglur5 υποδοχέων να ρυθμίζουν τη λειτουργία των NMDA υποδοχέων Η μεταγωγή σήματος μέσω των mglur5 υποδοχέων στον ιππόκαμπο του επίμυος επάγει το μονοπάτι των ΜΑΡ κινασών ΒΙΒΛΙΟΓΡΑΦΙΑ
7 ΠΡΟΛΟΓΟΣ Σε αυτό το σημείο και με την ολοκλήρωση της μεταπτυχιακής μου εργασίας θα ήθελα να ευχαριστήσω όλους εκείνους που συνέβαλαν στην ολοκλήρωσή της. Αρχικά, θα ήθελα να ευχαριστήσω από καρδιάς την επιβλέπουσα καθηγήτριά μου Φεβρωνία Αγγελάτου, γιατί χωρίς την πολύτιμη συμβολή της δεν θα ήταν δυνατή η περάτωση αυτού του έργου. Την ευχαριστώ θερμά για τις πολύτιμες συμβουλές, αλλά και για την αμέριστη στήριξή της σε όλη τη διάρκεια αυτού του όμορφου ταξιδιού. Επιπλέον, θα ήθελα να ευχαριστήσω τα μέλη της τριμελούς συμβουλευτικής επιτροπής μου, τον καθηγητή κ. Γεώργιο Κωστόπουλο και την καθηγήτρια κ. Αδαμαντία Μητσάκου, που με τις πολύτιμες συμβουλές τους υπήρξαν καθοδηγητές σε κάθε μου βήμα. Θα ήθελα να ευχαριστήσω επίσης όλα τα μέλη του εργαστηρίου φυσιολογίας για το φιλικό κλίμα εντός και εκτός εργαστηρίου και ιδιαίτερα τον Κώστα Σαράντη γιατί οι συμβουλές του υπήρξαν χρήσιμες για την ολοκλήρωση των πειραμάτων. Τέλος, θα ήθελα να ευχαριστήσω ιδιαίτερα τους γονείς μου, Γρηγόρη και Αρετή και την αδερφή μου, Δήμητρα, γιατί η αγάπη και συμπαράστασή τους σε κάθε μου βήμα, επαγγελματικό ή μη, μου δίνουν δύναμη να συνεχίσω να προσπαθώ. 7
8 ΠΕΡΙΛΗΨΗ Το γλουταμινικό οξύ αποτελεί τον κύριο διεγερτικό νευροδιαβιβαστή στο Κεντρικό Νευρικό Σύστημα των θηλαστικών, παίζοντας σημαντικό ρόλο σε διαδικασίες μάθησης και μνήμης, αλλά και σε διεργασίες διεγερσιμοτοξικότητας. Το γλουταμινικό οξύ ασκεί τις δράσεις του μέσω δύο ομάδων υποδοχέων, των ιοντοτρόπων και των μεταβοτροπικών υποδοχέων. Οι ιοντοτρόποι υποδοχείς είναι δίαυλοι ιόντων, των οποίων η ενεργοποίηση προκαλεί ταχεία διεγερτική νευροδιαβίβαση και διακρίνονται σε δύο μεγάλες υποομάδες,τους NMDA και τους μη- NMDA υποδοχείς. Οι μεταβοτροπικοί υποδοχείς, συνδέονται με G-πρωτεΐνες και προκαλούν αργή συναπτική νευροδιαβίβαση μέσω ενεργοποίησης δεύτερων αγγελιοφόρων. Διακρίνονται σε τρεις μεγάλες ομάδες: το Group I που περιλαμβάνει τους mglur1 και mglur5, οι οποίοι ενεργοποιούν την Φωσφολιπάση C (PLC), το Group II που περιλαμβάνει τους mglur 2 και 3 και το Group III που περιλαμβάνει τους mglurs 4, 6, 7και 8, οι οποίοι ρυθμίζουν αρνητικά την αδενυλική κυκλάση. Οι μεταβοτροπικοί υποδοχείς διαδραματίζουν σημαντικό νευροτροποποιητικό ρόλο σε ολόκληρο τον εγκέφαλο και αποτελούν στόχο για θεραπευτική αγωγή διαφόρων ψυχιατρικών και νευρολογικών διαταραχών όπως το άγχος, η κατάθλιψη, το σύνδρομο του εύθραυστου Χ και η σχιζοφρένεια. Στον ιππόκαμπο, μια δομή όπου διενεργούνται διεργασίες μάθησης και μνήμης, οι mglur5 υποδοχείς είναι οι πλέον άφθονοι από την οικογένεια των Group I Μεταβοτροπικών υποδοχέων και παίζουν ρόλο στη ρύθμιση της συναπτικής πλαστικότητας και χωρικής μάθησης. Όπως έχει δειχθεί από ηλεκτροφυσιολογικές μελέτες, μια από τις πιο αξιοσημείωτες επιδράσεις των mglur5 υποδοχέων είναι η ενίσχυση των NMDA-εξαρτώμενων ρευμάτων. Η δράση τους αυτή φαίνεται να παίζει ρόλο στη δημιουργία του LTP ( μακροχρόνια συναπτική ενίσχυση), καθώς η χορήγηση του ειδικού ανταγωνιστή των mglur5 υποδοχέων (ΜΡΕΡ) σε ιππόκαμπειους νευρώνες επίμυος, αναστέλλει την επαγωγή του LTP. Στο ραβδωτό σώμα, οι mglur5 υποδοχείς βρίσκονται υπό τον έλεγχο των Α 2Α υποδοχέων αδενοσίνης, με τους οποίους σχηματίζουν ετεροδιμερή συμπλέγματα Α 2Α -mglur5 υποδοχέων. Στον ιππόκαμπο, οι Α 2Α υποδοχείς αδενοσίνης εκφράζονται σε πολύ χαμηλά επίπεδα, ενώ είναι ελάχιστα τα βιβλιογραφικά δεδομένα για την πιθανή αλληλεπίδρασή τους με τους mglur5 υποδοχείς. 8
9 Προκειμένου να διερευνήσουμε το μοριακό μηχανισμό μέσω του οποίου οι mglur5 υποδοχείς του γλουταμινικού οξέος ενισχύουν τα ρεύματα των NMDA υποδοχέων στον ιππόκαμπο επίμυος, εξετάσαμε την in vitro επίδραση της ενεργοποίησης των mglur5, στο επίπεδο φωσφορυλίωσης της NR2B υπομονάδας του NMDA υποδοχέα, στα κατάλοιπα τυροσίνη-1472 και σερίνη Εν συνεχεία, διερευνήσαμε in vitro, την ενδεχόμενη αλληλεπίδραση των mglur5 και υποδοχέων στον ιππόκαμπο, μελετώντας την επίδραση της διέγερσης ή της αναστολής τους στην mglur5-επαγόμενη φωσφορυλίωση των NMDA υποδοχέων. Τέλος, προκειμένου να ανιχνεύσουμε το ενδοκυττάριο μονοπάτι μεταγωγής σήματος των mglur5 υποδοχέων στον ιππόκαμπο, εξετάσαμε την επίδραση της ενεργοποίησης των mglur5 υποδοχέων στο επίπεδο φωσφορυλίωσης της ERK ½ κινάσης καθώς και την επίδραση της διέγερσης των Α 2Α υποδοχέων αδενοσίνης στην ενεργοποίηση αυτή. Τα αποτελέσματά μας δείχνουν ότι η διέγερση των mglur5 υποδοχέων του γλουταμινικού οξέος με τον ειδικό αγωνιστή τους, CHPG, επάγει μια ισχυρή φωσφορυλίωση του καταλοίπου τυροσίνη της NR2B υπομονάδας, η οποία είναι εξειδικευμένη στη θέση αυτή δεδομένου ότι δεν εμφανίζονται στο κατάλοιπο σερίνη Σύμφωνα με τα υπάρχοντα βιβλιογραφικά δεδομένα, η φωσφορυλίωση του καταλοίπου τυροσίνη της NR2B υπομονάδας, παίζει ρόλο στη μετακίνηση του υποδοχέα στη μεμβράνη και στην ορθή τοποθέτηση του στη σύναψη (trafficking). Συγκεκριμένα, η φωσφορυλίωση στη θέση αυτή καταστέλλει την κλαθρίνη-εξαρτώμενη ενδοκυττάρωση των NMDA υποδοχέων, με αποτέλεσμα τη συσσώρευσή τους στη συναπτική μεμβράνη. Η συσσώρευση των NR2B-NMDA υποδοχέων και η σωστή τοποθέτηση τους στη συναπτική μεμβράνη προάγει τις NMDA εξαρτώμενες αποκρίσεις. Το γεγονός αυτό, συμφωνεί με τα ηλεκτροφυσιολογικά δεδομένα που δείχνουν ότι η διέγερση των mglur5, ενισχύει τα ρεύματα των NMDA υποδοχέων και προάγει την επαγωγή του LTP στον ιππόκαμπο. Σύμφωνα με τα αποτελέσματά μας, θεωρούμε ότι η φωσφορυλίωση στη τυροσίνη-1472, αποτελεί το μοριακό μηχανισμό ( ή μέρος αυτού), μέσω του οποίου η ενεργοποίηση των mglur5 υποδοχέων προάγει τα ρεύματα των NMDA διαύλων. Είναι ενδιαφέρον ότι, οι mglur5 υποδοχείς του γλουταμινικού οξέος φαίνεται να βρίσκονται υπό τον έλεγχο των Α 2Α υποδοχέων αδενοσίνης και στον ιππόκαμπο, όπως και στο ραβδωτό σώμα, καθώς τα αποτελέσματά μας δείχνουν ότι φαρμακευτική αναστολή των Α 2Α υποδοχέων εξασθενεί σημαντικά την 9 Α 2Α
10 ικανότητα των ιπποκάμπειων mglur5 να ελέγχουν τις NMDA-επαγόμενες απαντήσεις. Άρα στον ιππόκαμπο φαίνεται ότι οι Α 2Α υποδοχείς δρουν αδειοδοτικά για τη λειτουργία των mglur5 υποδοχέων ως προς τη ρύθμιση των NMDAεπαγόμενων απαντήσεων. Τέλος, τα αποτελέσματά μας καταδεικνύουν ότι η ενεργοποίηση των mglur5 υποδοχέων, με το ειδικό αγωνιστή τους CHPG, στον ιππόκαμπο, επάγει τη φωσφορυλίωση της ERK 1/2 κινάσης με τρόπο δοσοεξαρτώμενο. Η επαγωγή αυτή δεν υπόκειται στον έλεγχο των Α 2Α υποδοχέων αδενοσίνης, καθώς η φαρμακευτική αναστολή τους δεν είχε επίδραση στα επίπεδα φωσφορυλίωσης της ERK 1/2 κινάσης. Η λειτουργική σημασία της ενεργοποίησης αυτής δεν είναι ακόμα γνωστή και αποτελεί στόχο μελλοντικών πειραμάτων μας. 10
11 1.ΕΙΣΑΓΩΓΗ 11
12 1.ΙΠΠΟΚΑΜΠΟΣ Ο ιππόκαμπος αποτελεί μια από τις πιο καλά μελετημένες δομές του Κεντρικού Νευρικού Συστήματος. Η πρώτη περιγραφή του προέρχεται από τον Ενετό ανατόμο Julius Caesar Aranzi ( 1587) ο οποίος του έδωσε την ονομασία του ομώνυμου θαλάσσιου οργανισμού καθώς προσομοιάζουν στο σχήμα ( Εικόνα 1). Εικόνα 1: Παρασκεύασμα ανθρώπινου ιππόκαμπου και ψαλίδας (αριστερά), που προσομοιάζει με τον θαλάσσιο οργανισμό, από όπου πήρε και το όνομά του. Στον άνθρωπο βρίσκεται στον έσω κροταφικό λοβό και αποτελεί μια εν τω βάθει εγκεφαλική δομή σχήματος C, συμμετρική ως προς τη μέση γραμμή και εκτεινόμενη από το οπίσθιο τμήμα της υπομεσολόβιας περιοχής μέχρι το κάτω κέρας της πλάγιας κοιλίας (Εικ. 2). Στον επίμυ αποτελεί μια επιμήκη δομή που εκτείνεται επίσης σε σχήμα C από τους πυρήνες του διαφράγματος προσθιοραχιαία, πάνω και πίσω από το διεγκέφαλο προς τον κροταφικό λοβό οπισθοκοιλιακά (Johnston and Amaral, 1998) (Εικόνα 3). 12
13 Εικόνα 2: (αριστερά) Σχηματική παράσταση της μορφής και της θέσης του ιππόκαμπου ανθρώπινου εγκέφαλου(από συλλογή Carol Donner, τροποποιημένη).(δεξιά )Η ανατομική θέση του ιπποκάμπου όπως φαίνεται σε στεφανιαία τομή Μαγνητική; Τομογραφίας εγκεφάλου. Εικόνα 3: Η θέση του ιππόκαμπου στον εγκέφαλο του επίμυος, όπου διακρίνονται οι δύο πόλοι του: ο διαφραγματικός ή ραχιαίος πόλος (μπλε) και ο κροταφικός ή κοιλιακός πόλος (κόκκινο) (Από Bear et al., 2001). 1.1 Φυλογενετική Εξέλιξη Ο ιππόκαμπος αποτελεί μία από τις πολυπλοκότερες δομές και φυλογενετικά αρχαιότερες του εγκεφάλου. Μια από τις πρώτες περιοχές του τοιχώματος του πρόσθιου εγκέφαλου των πρωτόγονων σπονδυλωτών διαφοροποιείται σχηματίζοντας τον αρχαιοφλοιό (archicortex). Οι λειτουργίες του φαίνεται να βασίζονται στο 13
14 παρακείμενο διάφραγμα, με το οποίο συνδέεται στενά. Καθώς ο πρόσθιος εγκέφαλος επεκτείνεται κατά τη διάρκεια της εξέλιξης, ο ιππόκαμπος (αρχαιοφλοιός) πιέζεται και προβάλλεται προς το εσωτερικό του εγκεφάλου και συνάπτεται με τον κροταφικό λοβό. Έτσι, καθώς αυτός ο λοβός επιμηκύνεται, ο ιππόκαμπος σύρεται σχηματίζοντας μια καμπυλωτή δομή από το ραχιαίο πρόσθιο εγκέφαλο προς τον κροταφικό λοβό και τελικά καταλήγει εξολοκλήρου μέσα σε αυτόν το λοβό στα πρωτεύοντα, στριμωγμένος απέναντι από την αμυγδαλή. Ο ιππόκαμπος διατηρεί την πρωτόγονη σύνδεσή του με το διάφραγμα μέσω μιας παχιάς ταινίας, που ονομάζεται ψαλίδα (fornix), της οποίας το σχήμα περιγράφει την τροχιά της εξέλιξης του ιππόκαμπου. 1.2 Aνατομία- Δομή- Συνδέσεις Ο ιππόκαμπος αποτέλεσε σημαντικό πεδίο ενδιαφέροντος των νευροανατόμων από τα πρώτα στάδια των μελετών του νευρικού συστήματος. Το εσωτερικό κύκλωμά του παρουσιάζει εξαιρετική στρωμάτωση. Το μεγαλύτερο μέρος των αξόνων των πυραμιδικών κυττάρων έχει παράλληλο προσανατολισμό με κατεύθυνση σχεδόν κάθετη ως προς τον επιμήκη άξονα του ιππόκαμπου. Το σύνολο των κυττάρων και των νευρικών ινών ενός στρώματος θεωρήθηκε ότι αποτελεί μια λειτουργική μονάδα του ιππόκαμπου (Andersen et al., 1971). Ένα μεγάλο ποσοστό της πληροφορίας σχετικά με την κυτταρική οργάνωση και τις διασυνδέσεις των διαφόρων περιοχών του ιπποκάμπειου σχηματισμού χρονολογείται από τις μελέτες των Ramόn y Cajal και Lorente de Nό (Ramon y Cajal 1911; Lorente de No 1933; Lorente de No 1934) οι οποίοι με τη χρήση της τεχνικής του Golgi ανέδειξαν ένα μεγάλο μέρος της ανατομικής οργάνωσης του ιππόκαμπου (Amaral and Witter, 1995) (Εικόνα 4). 14
15 Εικόνα 4: Αριστερά φαίνεται μια σχηματική παράσταση εγκάρσιας τομής ιππόκαμπου μετά από χρώση Golgi (από αρχείο Camillo Golgi). Δεξιά απεικονίζεται μία πραγματική τομή ιππόκαμπου με χρώση Golgi (Institute of Pathology of the University of Pavia original Golgi s lab preparation). Μεγάλη ώθηση στην μελέτη του ιππόκαμπου έδωσε, στη δεκαετία του 1950, η αναγνώριση του σημαντικού ρόλου του σε συγκεκριμένους τύπους μνήμης και μάθησης. Σημείο αναφοράς αποτελεί η περίπτωση του ασθενούς Η.Μ. (Scoville and Milner, 1957) ο οποίος αποτελεί το πιο εκτενώς μελετημένο υποκείμενο στην έρευνα για τη μνήμη. Ο Η.Μ. υποβλήθηκε σε χειρουργείο για την αμφίπλευρη αφαίρεση του ιππόκαμπου, με σκοπό την θεραπεία βαριάς μορφής επιληψίας. Αυτή η επέμβαση είχε ως συνέπεια την αδυναμία κωδικοποίησης νέων πληροφοριών σε μακρόχρονη μνήμη. Έκτοτε η έρευνα σχετικά με τους μηχανισμούς μνήμης και μάθησης και το ρόλο των περιοχών του ιππόκαμπου συνεχίζεται σε μεγάλη κλίμακα. Νευροφυσιολογικές μελέτες έχουν δείξει ότι ο ιππόκαμπος παίζει σημαντικό ρόλο στη λειτουργία της βραχυπρόθεσμης λειτουργικής μνήμης και της μάθησης (Nadel and Moscovitch, 1997; Fell et al., 2001; Small et al., 2001; Eichenbaum 2004; Jeffery and Hayman, 2004). Πρόσφατες επίσης μελέτες έχουν δείξει ότι οι δυο πόλοι του ιππόκαμπου συμμετέχουν με διαφορετικό τρόπο στις διαδικασίες της μνήμης και της μάθησης (Moser et al. 1993; Becker et al., 1997; Moser and Moser, 1998; Bannerman et al., 2004; Giovanello et al. 2004; Pothuizen et al., 2004; Rudy and Matus-Amat, 2005; Hobin et al., 2006). Επιπλέον η μακρόχρονη ενδυνάμωση της σύναψης (Long Term Potentiation) που παρατηρήθηκε από τους Bliss και Lomo στον ιππόκαμπο (Bliss and Lomo, 1973), αποτελεί ένα τύπο πλαστικότητας των νευρωνικών συνάψεων που παίζει σημαντικό ρόλο στις διαδικασίες της μνήμης και της μάθησης (Bliss and Collingridge, 1993). 15
16 1.3 Ο ιπποκάμπειος σχηματισμός Ο ιπποκάμπειος σχηματισμός των τρωκτικών αποτελεί μια επιμήκη δομή σχήματος C, που εκτείνεται προσθιοραχιαία από το διαφραγματικό πυρήνα του βασικού πρόσθιου εγκέφαλου, πάνω και πίσω από το διεγκέφαλο μέχρι τον αρχόμενο κροταφικό λοβό οπισθιοκοιλιακά (Εικόνα 2,3). Ο επιμήκης άξονας του ιπποκάμπειου σχηματισμού αναφέρεται ως διαφραγμοκροταφικός άξονας (με τον διαφραγματικό πόλο να βρίσκεται πρόσθια) και ο κατακόρυφος άξονας αναφέρεται ως εγκάρσιος άξονας (Εικόνα 3). Στην εικόνα 3 διακρίνονται οι δύο πόλοι του ιπποκάμπου, οι οποίοι περιλαμβάνουν το ραχιαίο ή διαφραγματικό πόλο και τον κοιλιακό ή κροταφικό πόλο. Στον άνθρωπο, ο ιπποκάμπειος σχηματισμός αποτελεί μια πτυχωμένη δομή, η οποία εντοπίζεται κεντρικά της πλάγιας κοιλίας (Εικόνες 2, 3). Ο ραχιαίος πόλος του ιπποκάμπου των τρωκτικών αντιστοιχεί στον οπίσθιο ιππόκαμπο στον άνθρωπο, ενώ ο κοιλιακός ιππόκαμπος των τρωκτικών αντιστοιχεί στον πρόσθιο ιππόκαμπο στον άνθρωπο. Εικόνα 5: Σχηματικές παραστάσεις στεφανιαίων τομών από τον διαφραγματικό ιππόκαμπο, στις οποίες φαίνονται περιοχές, στοιβάδες και οδοί ινών του ιπποκάμπειου σχηματισμού επίμυος. Α) so:stratum oriens: πολυμορφική στιβάδα; pcl:pyramidal cell layer: στιβάδα πυραμιδικών κυττάρων; sl:stratum lucidum: διαυγαστική στιβάδα; sr:stratum radiatum: ακτινωτή στιβάδα; s l-m:stratum lacunosum-moleculare: βοθριώδης-μοριώδης στιβάδα; alv:alveus:σκάφη; ab:angular bundle: τοξοειδής δεσμίδα; PaS:parasubiculum: παραυπόθεμα; PrS:presubiculum:προ-υπόθεμα; ML,GL and PoDG: molecular, granule cell and polymorphic layers, respectively, of the dentate gyrus: μοριώδης, κοκκιώδης και πολυμορφική στιβάδα οδοντωτής έλικας; S:subiculum: υπόθεμα 16
17 Β) Περιγραφή των 3 ζωνών της μοριώδους στιβάδας της οδοντωτής έλικας. Η έξω ζώνη δείχνει την πλευρική οδό perforant (lpp), η κεντρική περιοχή αντιστοιχεί στην τελική ζώνη της κεντρικής οδού perforant (mpp) και η εσωτερική ζώνη αντιστοιχεί στη ζώνη τερματισμού της συνειρμικής/συναρθρωτικής προβολής της οδοντωτής έλικας. fr: fribia: παρυφή; sl:stratum lucidum: διαυγαστική στιβάδα; mmp: medial perforant pathway: έσω διατιτραίνουσα οδός; lpp: lateral perforant path: έξω διατιτραίνουσα οδός; com/assoc: commissural/associational:συνδεσμική/συνδετική (Amaral and Witter, 1995). Ο ιπποκάμπειος σχηματισμός συγκροτείται από έξι κυταρροαρχιτεκτονικά διακριτές περιοχές, που περιλαμβάνουν την οδοντωτή έλικα (dentate gyrus), τον ιππόκαμπο (hippocampus), ο οποίος υποδιαιρείται σε 3 πεδία (CA1, CA2 και CA3), το υπόθεμα (subiculum), το προϋπόθεμα (presubiculum), το παραϋπόθεμα (parasubiculum) και τον ενδορινικό φλοιό (entorhinal cortex), ο οποίος περιέχει δύο ή περισσότερες υποδιαιρέσεις. Το υπόθεμα, το προϋπόθεμα και το παραϋπόθεμα αναφέρονται συνήθως μαζί και ως υποθεματικό σύμπλοκο (Amaral and Witter, 1995) (Εικόνες 5, 6). 17
18 Εικόνα 6: (α) Πλευρική και κεντρική άποψη της θέσης του ιππόκαμπου στον κροταφικό λοβό του εγκεφάλου του ανθρώπου, (β) Στεφανιαία τομή του εγκεφάλου του ανθρώπου, όπου διακρίνονται οι διακριτές περιοχές του ιπποκάμπειου σχηματισμού (Από Bear et al., 2001). Σε επίπεδα του ιπποκάμπειου σχηματισμού κοντά στο διαφραγματικό πυρήνα, μόνο η οδοντωτή έλικα και οι CA1-CA3 υποδιαιρέσεις είναι εμφανείς. Περίπου στο 1/3 του ιπποκάμπειου σχηματισμού, εμφανίζεται πρώτα το υπόθεμα και στη συνέχεια εμφανίζεται το προϋπόθεμα και το παραϋπόθεμα σε επίπεδα πιο κοντά στον κροταφικό λοβό. Ο ενδορινικός φλοιός βρίσκεται κοιλιακά στην πιο ουριαία μοίρα του φλοιϊκού μανδύα. Έτσι, η κύρια μοίρα του ενδορινικού φλοιού βρίσκεται ουριαία και κοιλιακά σε σχέση με τις άλλες περιοχές του ιπποκάμπειου σχηματισμού. Τα πλευρικά όρια του ενδορινικού φλοιού βρίσκονται περίπου στην ρινική αύλακα, η οποία αποτελεί μια απ τις κυριότερες αύλακες του εγκεφαλικού φλοιού (Amaral and Witter, 1995). 18
19 Το βασικό κύκλωμα λειτουργίας του ιπποκάμπου είναι το τρισυναπτικό κύκλωμα, το οποίο επαναλαμβάνεται σε όλο τον επιμήκη άξονα του ιπποκάμπου (Εικόνα 7). Ο ενδορινικός φλοιός προβάλει στην οδοντωτή έλικα μέσω νευρικών ινών, που συνιστούν τη διαιτιτραίνουσα οδό (perforant pathway, PP). Οι προβολές του ενδορινικού φλοιού στην οδοντωτή έλικα δεν είναι αμοιβαίες και αυτό, γιατί κανένα από τα κύτταρα της οδοντωτής έλικας δεν προβάλει πίσω στον ενδορινικό φλοιό. Τα κοκκιώδη κύτταρα της οδοντωτής έλικας προβάλουν μέσω των διακριτών βρυωδών ινών τους (mossy fibers, MF) στα πυραμιδικά κύτταρα της CA3 περιοχής του ιππόκαμπου. Αν και κάποια κύτταρα της CA3 περιοχής του ιππόκαμπου συνιστούν άξονες στην πολυμορφική στοιβάδα της οδοντωτής έλικας, αυτοί οι άξονες δεν νευρώνουν τα κοκκιώδη κύτταρα. Τα πυραμιδικά κύτταρα της CA3 περιοχής προβάλλουν μέσω των παράλληλων ινών schaffer (schaffer collaterals, SC) στα πυραμιδικά κύτταρα της CA1 περιοχής του ιπποκάμπου. Τα τελευταία προβάλλουν μέσω του υποθέματος πίσω στον ενδορινικό φλοιό (Εικόνα 4) (Amaral and Witter, 1995). Εικόνα 7: Το ενδογενές τρισυναπτικό ιπποκάμπειο κύκλωμα. PP: Perforant Pathway- Διαιτιτραίνουσα οδός, MF: Mossy Fibers- Βρυώδεις Ινες, SC: Scaffer Collaterals- Παράλληλες Ινες Scaffer (Από Centre for Synaptic Plasticity, University of Bristol) Οι βαθιές ή κοιλιακές επιφάνειες του ιππόκαμπου και του υποθέματος καλύπτονται από ένα λεπτό στρώμα από κυρίως εμμύελες, προσαγωγές και απαγωγές, νευρικές ίνες, που ονομάζεται χοάνη (alveus). Εν μέρει, οι ίνες αυτές προέρχονται από τα πυραμιδικά κύτταρα του ιππόκαμπου και από το υπόθεμα, με κατεύθυνση προς υποφλοιϊκές δομές ή προς τον αντίπλευρο ιπποκάμπειο σχηματισμό. Οι ίνες εκτείνονται πλάγια, πάνω από την επιφάνεια του ιππόκαμπου και 19
20 συγκεντρώνονται σε μια αυξανόμενα παχύτερη νευρική δέσμη, που βρίσκεται στο ακραίο πλευρικό τμήμα του ιππόκαμπου και ονομάζεται κροσσός (fimbria). Καθώς οι ίνες αφήνουν τον ιππόκαμπο και κατανέμονται στον πρόσθιο εγκέφαλο, αναφέρονται συνήθως ως οι κίονες της ψαλίδας (columns of fornix). Η ψαλίδα (fornix) διχάζεται γύρω από τον πρόσθιο σύνδεσμο (anterior commissure), ώστε να διαμορφώνει ένα πρόσθια κατευθυνόμενο προσυναρθρωτικό σύμπλοκο, το οποίο νευρώνει τον διαφραγματικό πυρήνα και άλλες βασικές δομές του πρόσθιου εγκεφάλου και ένα ουριαία κατευθυνόμενο προσυναρθρωτικό σύμπλοκο, το οποίο κατευθύνεται προς το διεγκέφαλο. Καθώς η μετασυναρθρωτική ψαλίδα αρχίζει την πορεία της στο διεγκέφαλο (ώστε τελικά να φτάσει στην περιοχή των μαστίων του οπίσθιου υποθαλάμου), χωρίζεται σε δύο μικρότερες δέσμες. Η μια, που ονομάζεται κεντρικό φλοιοϋποθαλαμικό δέμα (medial corticohypothalamic tract), εκτείνεται κεντρικά νευρώνοντας έναν αριθμό περιοχών του πρόσθιου υποθαλάμου. Η άλλη, που καλείται υποθεμοθαλαμικό δέμα, παρέχει ίνες προς τον πρόσθιο θαλαμικό πυρήνα (Amaral and Witter, 1995). Όσον αφορά στον κροσσό (fimbria), ένας μεγάλος αριθμός ινών διαπερνά τη κεντρική γραμμή, πριν εισέλθει στους κίονες της ψαλίδας. Αυτές οι ίνες σε μια θέση ακριβώς κοιλιακά της διαφραγματικής περιοχής διαπερνούν στην κοιλιακή ιπποκάμπεια σύμφυση. Πολλές από αυτές τις ίνες είναι πραγματικές συναρθρωτικές ίνες και κατευθύνονται σε περιοχές του αντίπλευρου ιπποκάμπειου σχηματισμού. Ένας μικρότερος αριθμός ινών κατευθύνεται στον αντίπλευρο κατιών κίονα της ψαλίδας και τελικά νευρώνει τις ίδιες δομές, που λαμβάνουν ίνες από την προσυναρθρωτική και την μετασυναρθρωτική ψαλίδα. Η ψαλίδα (fornix) και ο κροσσός (fimbria) περιέχουν απαγωγές ίνες από τον ιπποκάμπειο σχηματισμό και προσαγωγές ίνες από υποφλοιϊκές δομές προς τον ιπποκάμπειο σχηματισμό. Ένα δεύτερο συναρθρωτικό δέμα αποτελεί η ραχιαία ιπποκάμπεια σύμφυση, η οποία διαπερνά τη μέση γραμμή ακριβώς πρόσθια και κοιλιακά του σπληνίου του μεσολόβιου (splenium of corpus callosum). Αυτό περιέχει ίνες, οι οποίες προέρχονται ή προβάλουν κυρίως στο προϋπόθεμα, στο παραϋπόθεμα και στον ενδορινικό φλοιό. Οι ίνες της ραχιαίας ιπποκάμπειας σύμφυσης συνεχίζουν πλευρικά με ένα δέμα ινών, το οποίο παρεμβάλλεται μεταξύ του προϋποθέματος και του παραϋποθέματος και του ενδορινικού φλοιού. Αυτή η συνάρθρωση ινών αναφέρεται ως γωνιακό δέμα (angular bundle), το οποίο, εκτός της μεταφοράς συναρθρωτικών ινών ενδορινικής και προϋποθεματικής και παραϋποθεματικής προέλευσης, αποτελεί το κύριο πέρασμα, 20
21 μέσω του οποίου ίνες από τον κοιλιακά τοποθετημένο ενδορινικό φλοιό μεταφέρονται σε όλα τα διαφραγμοκροταφικά επίπεδα των υπόλοιπων ιπποκάμπειων περιοχών και ιδιαίτερα στην οδοντωτή έλικα, στον ιππόκαμπο και στο υπόθεμα (Amaral and Witter, 1995). 1.4 Λειτουργικός Ρόλος του Ιπποκάμπου: Η Μνήμη και Μάθηση Ο ιππόκαμπος διαδραματίζει κυρίαρχο ρόλο σε διάφορες γνωστικές λειτουργίες, κυρίως στην μνήμη και στην μάθηση. Η έννοια της μάθησης χαρακτηρίζει την διαδικασία απόκτησης νέων πληροφοριών, ενώ η αποθήκευση αυτών των πληροφοριών χαρακτηρίζει την έννοια της μνήμης. Σε νευρωνικό επίπεδο, η μνήμη και η μάθηση χαρακτηρίζονται από μακροχρόνιες προσαρμοστικές μεταβολές των νευρωνικών κυκλωμάτων του εγκεφάλου ως απόκριση στο περιβάλλον. Οι προσαρμοστικές αυτές μεταβολές των νευρωνικών κυκλωμάτων του εγκεφάλου δίνουν τη δυνατότητα στον οργανισμό να μπορεί να αντιδρά κατάλληλα σε αλλαγές του περιβάλλοντός του, με βάση προηγούμενες εμπειρίες, που έχουν αποθηκευτεί στον εγκέφαλο ως μνήμη (Bear et al., 2001). Από καιρό ήταν γνωστό, ότι ο ιππόκαμπος και οι σχετιζόμενες με αυτόν περιοχές του κροταφικού λοβού είναι σημαντικές για τη διαμόρφωση της μνήμης. Οι μελέτες της εμπλοκής του κροταφικού λοβού στις διαδικασίες της μνήμης ξεκίνησαν από την περίπτωση του ασθενούς H.M., ο οποίος υπέφερε από επιληπτικές κρίσεις. Μετά την αμφοτερόπλευρη αφαίρεση της έσω μοίρας του κροταφικού λοβού (συμπεριλαμβανομένου του ιπποκάμπου), οι επιληπτικές κρίσεις του ασθενούς Η.Μ. μειώθηκαν σημαντικά, αλλά διαπιστώθηκε μεγάλη απώλεια μνήμης, καθώς ο ασθενής έχασε την ικανότητα να σχηματίζει νέες μακροχρόνιες μνήμες (Scoville and Milner, 1957). Ενώ η βραχύχρονη μνήμη του ήταν άθικτη, εκείνο που έλειπε σε σημαντικό βαθμό από τον ασθενή ήταν η ικανότητα να μεταφέρει τους περισσότερους τύπους μάθησης από τη βραχύχρονη μνήμη, που διαρκεί μερικά δευτερόλεπτα ή λεπτά, στη μακρόχρονη μνήμη που διαρκεί ημέρες, μήνες ή και περισσότερο (Kandel et al., 2000). Παρόμοια αποτελέσματα παρουσιάστηκαν αργότερα από μελέτες σε ασθενείς με βλάβες περιορισμένες αποκλειστικά στον ιππόκαμπο (Zola-Morgan et al., 1986; Rempel-Clowe et al., 1996), υποδηλώνοντας ότι αυτή η εγκεφαλική περιοχή είναι υπεύθυνη για πολλές από τις διαδικασίες της μνήμης. Επιπλέον μελέτες σε φυσιολογικούς ανθρώπους επιβεβαιώνουν την άποψη 21
22 αυτή, υποδηλώνοντας ενεργοποίηση της περιοχής του ιπποκάμπου, κατά την κωδικοποίηση οπτικών και λεκτικών πληροφοριών (Squire, 1992; Nyberg et al., 1996; Stern et al., 1996; Rombouts et al., 1997; Fernadez et al., 1998). Εικόνα 8: Δραστηριότητα του ανθρώπινου εγκεφάλου, που σχετίζεται με τη χωρική μάθηση. (Α) Μια εικονική πόλη δείχνεται σε μια οθόνη υπολογιστή και άτομα, υπό τη συσκευή ΡΕΤ, χρησιμοποιούν κουμπιά για να εξερευνήσουν το εικονικό περιβάλλον, (Β) Σ αυτήν την στεφανιαία τομή του εγκεφάλου ανθρώπου, παρατηρείται αυξημένη ενεργοποίηση του δεξιού ιπποκάμπου και της αριστερής ουράς του κελύφους (Από Bear et al., 2001). Επίσης, στον άνθρωπο έχει παρατηρηθεί ότι ο ιππόκαμπος ενεργοποιείται σε καταστάσεις που σχετίζονται με εικονική πλοήγηση στο περιβάλλον. Έτσι, μόλις τα άτομα μάθουν το εικονικό περιβάλλον, καταγράφεται η εγεκεφαλική τους δραστηριότητα με τη βοήθεια της τεχνικής της τομογραφίας εκπομπής ποζιτρονίων (ΡΕΤ), καθώς μετακινούνται νοερά από ένα αρχικό σημείο σε ένα άλλο τελικό σημείο του περιβάλλοντος. Όπως φαίνεται και στην Εικόνα 8, όταν το άτομο εξερευνά το περιβάλλον, παρατηρείται αυξημένη ενεργοποίηση του δεξιού ιππόκαμπου, καθώς και της αριστερής ουράς του κελύφους. Αυτό υποδηλώνει την εμπλοκή του ιπποκάμπου στη χωρική μνήμη και μάθηση. Η συμμετοχή του ιππόκαμπου στις λειτουργίες τις μνήμης (κωδικοποίησηανάκτηση) προκύπτει και από πειράματα σε ζώα, τα οποία χρησιμοποιούν την χωρική μνήμη για πλοήγηση στο χώρο (Black et al., 1977; Olton et al., 1978; Nadel, 1991; Maguire et al., 1997; Morris and Frey, 1997). Για παράδειγμα, η ικανότητα εκμάθησης του υδάτινου λαβύρινθου (Morris water maze), μια συμπεριφορική δοκιμασία της χωρικής μνήμης και της μάθησης, μειώνεται σημαντικά μετά από βλάβες στον ιππόκαμπο (Hughes, 1965; Sinnamon et al., 1978; Moser et al., 1993, 22
23 1995). Επίσης, έχει αναφερθεί ότι η χωρική μνήμη μειώνεται με την απώλεια των νευρώνων της CA1 περιοχής του ιπποκάμπου, μετά από προσωρινή ισχαιμία του πρόσθιου εγκεφάλου (Volpe et al., 1992). Ο ρόλος του ιπποκάμπου στη χωρική μνήμη και στη μάθηση έχει δειχθεί και σε άλλα συμεριφορικά μοντέλα, όπως στην περίπτωση του ακτινωτού λαβυρίνθου, όπου το πειραματόζωο μαθαίνει τη θέση της τροφής ακολουθώντας συγκεκριμένη διαδρομή (Davidson and Jarrard, 1993; Alvarado and Rudy, 1995; Bunsey and Eichenbaum, 1995) (Εικόνα 6). Ο ρόλος του ιππόκαμπου στη χωρική μνήμη έγινε περισσότερο σαφής με την ανακάλυψη των «κυττάρων θέσης» (place cells) (O'Keefe and Dostrovsky, 1971). Η θέση ενός πειραματόζωου σε ένα συγκεκριμένο χώρο κωδικοποιείται από ένα πρότυπο εκφόρτισης ενός πυραμιδικού κυττάρου του ιπποκάμπου. Όταν ένα ζώο κινείται στο χώρο, διαφορετικά «κύτταρα θέσης» πυροδοτούν στον ιππόκαμπο και επομένως, οι διαφορετικές θέσεις του πειραματόζωου στο χώρο σηματοδοτούνται από την εκφόρτιση ενός συγκεκριμένου πληθυσμού «κυττάρων θέσης». Με αυτό τον τρόπο, διαμορφώνεται στον ιππόκαμπο ένας «χωρικός χάρτης» (place field), μια ενδογενή αναπαράσταση του χώρου στον οποίο κινείται το πειραματόζωο. Όταν το ζώο εισέρχεται σε ένα νέο περιβάλλον, διαμορφώνονται νέοι «χωρικοί χάρτες» μέσα σε λίγα λεπτά, οι οποίοι παραμένουν σταθεροί για λίγες εβδομάδες έως και μήνες. Τα ίδια πυραμιδικά κύτταρα πιθανώς σηματοδοτούν διαφορετικές πληροφορίες σε διαφορετικά περιβάλλοντα και επομένως μπορούν να χρησιμοποιηθούν σε περισσότερους από ένα «χωρικούς χάρτες» (Eichenban et al., 1999; Kandel et al., 2000; McHugh et al, 2007). Σε συμφωνία με τα παραπάνω, ηλεκτοροφυσιολογικές καταγραφές από τον ιππόκαμπο επίμυων υποδεικνύουν τον συντονισμό της πυροδότησης των «κυττάρων θέσης» του ιπποκάμπου στη συχνότητα του θ- ρυθμού (theta oscillations) κατά την διάρκεια της εξερευνητικής κίνησης του ζώου που έχει ως αποτέλεσμα αλλάγες της θέσης του στο χώρο (O'Keefe and Recce, 1993; Harvey et al., 2009; Lever et al., 2010). Η μνήμη μπορεί να διακριθεί γενικά σε έκδηλη (declarative) και άδηλη (nondeclarative memory) μνήμη. Κατά τη διάρκεια της ζωής μας διδασκόμαστε πολλά, όπως για παράδειγμα ότι «η πρωτεύουσα της Ελλάδας είναι η Αθήνα». Επιπλέον, αποθηκεύουμε μνήμες από αυτοβιογραφικά γεγονότα και καταστάσεις της ζωής μας, όπως για παράδειγμα «παντρεύτηκα πέρυσι το χειμώνα» ή «πήγα στο σινεμά χθες» (Εικόνα 10). Η μνήμη για γεγονότα, καταστάσεις και πραγματικότητες, όπως τα παραπάνω, χαρακτηρίζεται ως έκδηλη μνήμη, η οποία απαιτεί συνειδητή 23
24 γνωστική επεξεργασία. Ο ιππόκαμπος, κυρίως, αλλά και άλλες δομές του κροταφικού λοβού είναι υπεύθυνες για τη διαμόρφωση της έκδηλης μνήμης (Bear et al., 2001). Η άδηλη μνήμη διακρίνεται σε διάφορα είδη. Ένα είδος της είναι η λεγόμενη διαδικαστική μνήμη (procedural memory) ή μνήμη που σχετίζεται με συνήθειες, συμπεριφορές ή εμπειρίες και δεν προϋποθέτει συνειδητή γνωστική επεξεργασία. Το να παίζουμε βιολί, να δένουμε τα κορδόνια των παπουτσιών μας ή να οδηγούμε είναι γεγονότα που τα κάνουμε ασυναίσθητα και αποτελούν είδη διαδικαστικής, άδηλης μάθησης (Εικόνα 7). Άλλο είδος άδηλης μνήμης είναι η μνήμη που σχετίζεται με το φόβο στην οποία εμπλέκεται, κυρίως, η αμυγδαλή (Εικόνα 10). Εικόνα 9: (α) Δοκιμασία μνήμης στον ακτινωτό λαβύρινθο (radial arm maze), (β) H διαδρομή που ακολουθείται από το πειραματόζωο όταν και οι οκτώ βραχίονες περιέχουν στο άκρο τους τροφή, (γ) Η διαδρομή που ακολουθείται από το πειραματόζωο όταν μάθει ότι μόνο οι τέσσερις από τους οκτώ βραχίονες περιέχουν τροφή. Τους άλλους τέσσερις τους αγνοεί και δεν τους επισκέπτεται (Από Bear et al., 2001). Γενικά, η έκδηλη μνήμη είναι δυνατόν να ανακληθεί ενσυνείδητα, ενώ η άδηλη μνήμη όχι. Αντίθετα, τα αντανακλαστικά και οι συναισθηματικές συσχετίσεις που έχουμε διαμορφώσει εκδηλώνονται, χωρίς ενσυνείδητη ανάκληση. Για παράδειγμα, ποτέ δεν ξεχνούμε πώς να κάνουμε ποδήλατο. Μπορεί να μην θυμόμαστε πότε ακριβώς κάναμε για πρώτη φορά ποδήλατο (η έκδηλη μορφή της μνήμης), αλλά ο εγκέφαλος «θυμάται τι να κάνει» όταν βρεθούμε πάνω σε ένα ποδήλατο (η άδηλη μορφή της μνήμης). Η άδηλη μνήμη αποκαλείται πολλές φορές 24
25 και ενδεχόμενη ή συνεπαγόμενη μνήμη (implicit memory), επειδή είναι αποτέλεσμα άμεσων εμπειριών, ενώ η έκδηλη μνήμη χαρακτηρίζεται και ως σαφής ή ρητή μνήμη (explicit memory), επειδή προέρχεται από ενσυνείδητη διαδικασία (Bear et al., 2001). Εικόνα 10: Τύποι έκδηλης και άδηλης μνήμης. Επίσης, υποδεικνύονται οι εγκεφαλικές περιοχές που σχετίζονται με κάθε τύπο μνήμης (Από Bear et al., 2001). Ένας άλλος διαχωρισμός της έννοιας της μνήμης είναι η βραχύχρονη (shortterm) και η μακρόχρονη μνήμη (long-term memory). Η μακρόχρονη μνήμη μπορεί να ανακληθεί για ημέρες, μήνες ή και χρόνια από τη στιγμή που αποθηκεύτηκε στον εγκέφαλο. Παρόλ αυτά, δεν μετατρέπονται όλες οι μνήμες σε μακρόχρονες. Για παράδειγμα, σχετικά εύκολα μπορούμε να θυμηθούμε τι γευματίσαμε χθες. Αλλά δεν είναι το ίδιο εύκολο να θυμηθούμε τι γευματίσαμε πριν μια εβδομάδα. Είναι πολύ πιθανό αυτή η μνήμη να έχει εξαλείφει οριστικά. Έτσι, είναι χρήσιμη η διάκριση της βραχύχρονης (το γεύμα της χθεσινής ημέρας) από τη μακρόχρονη μνήμη. Η βραχύχρονη μνήμη διαρκεί από μερικά δευτερόλεπτα έως λίγες ώρες και είναι επιδεκτική στην εξάλειψη. Για παράδειγμα, οι βραχύχρονες μνήμες μπορούν να εξαλειφθούν μετά από εγκεφαλικό τραύμα ή από ηλεκτρικό σοκ. Αλλά αυτές οι διαδικασίες δεν επηρεάζουν την μακρόχρονη μνήμη (π.χ. μνήμες της παιδικής ηλικίας), οι οποίες έχουν αποθηκευτεί αρκετό καιρό πριν. Αυτές οι παρατηρήσεις οδήγησαν στο συμπέρασμα ότι οι μνήμες αποθηκεύονται αρχικά ως βραχύχρονες μνήμες και βαθμιαία μετατρέπονται σε μόνιμες, μέσω μιας διαδικασίας που ονομάζεται μνημονική εδραίωση (memory consolidation). Ο χώρος αποθήκευσης της βραχύχρονης μνήμης εντοπίζεται στον 25
26 ιππόκαμπο. Η πληροφορία από φλοιϊκές συνειρμικές περιοχές φτάνει στον ιππόκαμπο, μέσω του ενδορινικού και περιρινικού φλοιού (Εικόνες 11, 12). Εκεί η πληροφορία αποθηκεύεται προσωρινά ως βραχύχρονη μνήμη και στη συνέχεια μεταφέρεται στον συνειρμικό φλοιό, όπου μετατρέπεται σε μακροκρόχρονη μνήμη με τη διαδικασία της μνημονικής εδραίωσης και μπορεί να διαρκέσει ακόμα και χρόνια από τη στιγμή που αποθηκεύτηκε (Bear et al., 2001). Εικόνα 11: Η ροή της πληροφορίας μέσω των δομών του κεντρικού κροταφικού λοβού (Από Bear et al., 2001). Εικόνα 12 Βραχύχρονη και μακρόχρονη μνήμη. Η αισθητική πληροφορία μπορεί να συγκρατηθεί προσωρινά ως βραχύχρονη μνήμη. Η μόνιμη αποθήκευση, όμως, ως μακρόχρονη μνήμη απαιτεί εδραίωση (consolidation). (Από Bear et al., 2001). 26
27 2. ΜΕΤΑΒΟΤΡΟΠΙΚΟΙ ΥΠΟΔΟΧΕΙΣ ΤΟΥ ΓΛΟΥΤΑΜΙΝΙΚΟΥ ΟΞΕΟΣ Το γλουταμινικό οξύ έχει πλέον αναγνωρισθεί ως ο κύριος διεγερτικός νευροδιαβιβαστής στο Κεντρικό Νευρικό Σύστημα των θηλαστικών, καθώς φαίνεται ότι συμμετέχει σε μια πληθώρα νευρωνικών και νευρογλοιακών διαδικασιών (Fonnum, 1984). Εκτός από την καλά χαρακτηρισμένη συμμετοχή του σε γνωστικές διαδικασίες μάθησης κ μνήμης, το γλουταμινικό οξύ, δρα δυνητικά ως ένας ισχυρός, ενδογενής, νευροτοξικός παράγοντας με σημαντική συμβολή στην ανάπτυξη ή/και εξέλιξη πληθώρας νευρολογικών διαταραχών. Μέχρι τα μέσα του 1980, υπήρχε η πεποίθηση ότι το γλουταμινικό οξύ ασκούσε τις δράσεις του αποκλειστικά διαμέσου ενός αριθμού υποδοχέων που ελέγχουν άμεσα διαύλους ιόντων και ονομάζονται Ιοντοτρόποι υποδοχείς. Ιοντοτρόποι υποδοχείς είναι δίαυλοι ιόντων, των οποίων η ενεργοποίηση προκαλεί ταχεία διεγερτική νευροδιαβίβαση και διακρίνονται σε δύο μεγάλες υποομάδες,τους NMDA και τους μη- NMDA υποδοχείς, ανάλογα με τους αγωνιστές που τους ενεργοποιούν ή τους ανταγωνιστές που αναστέλλουν την δράση τους. Οι υποδοχείς μη-nmda ενεργοποιούνται από τις φαρμακευτικές ουσίες α- αμινο-3-υδροξυ-5- μεθυλο-ισοξαζολο-προπιονικό οξύ (AMPA), καϊνικό οξύ και κισκαλικό οξύ ( Kandel et al, 2000) ( Εικόνα 13). To γλουταμινικό οξύ, όμως, όπως και πολλοί άλλοι νευροδιαβιβαστές, ασκεί τις πλειοτροπικές του δράσεις μέσω πολλαπλών πρωτεϊνικών υποδοχέων. Έτσι, εκτός από τους Ιοντοτροπικούς υποδοχείς, αλληλεπιδρά και με τους Μεταβοτροπικούς υποδοχείς (mglurs), οι οποίοι συνδεόμενοι με G-πρωτεΐνες, προκαλούν αργή συναπτική νευροδιαβίβαση μέσω ενεργοποίησης δεύτερων αγγελιοφόρων (Nakanishi et al.1998). Η ικανότητα του γλουταμινικού οξέος να ενεργοποιεί υποδοχείς που συνδέονται με G- πρωτεΐνες, διαπιστώθηκε αρχικά Οι στα μέσα του 1980, όπου παρατηρήθηκε ότι προκαλεί τον σχηματισμό κ την αύξηση μονο, δι- και τρι- φωσφο ινοσιτόλης σε κυτταροκαλλιέργειες από νευρώνες ραβδωτού (Sladeczek et al.1985). Η έρευνα για την μοριακή ταυτότητα των υποδοχέων αυτών, που ανήκουν στην κατηγορία των GPCRs ( G-protein coupled receptors), οδήγησε πρώτα στην ανακάλυψη του mglur1α υποδοχέα, ο οποίος μπορεί να συνδεθεί με την φωσφολιπάση C ( PLC) και άλλους παράγοντες μέσω G- πρωτεϊνών. Εν συνεχεία, 27
28 κατά τη διάρκεια της περιόδου , η κλωνοποίηση 7 επιπλέον mglurs πραγματοποιήθηκε στα θηλαστικά. Οι υποδοχείς αυτοί, μοιράζονται ομοιότητα 35-60% με τον mglur1α υποδοχέα και μπορούν να διακριθούν σε τρεις ομάδες, με βάση ομοιότητες αλληλουχίας, προτιμώμενα σηματοδοτικά μονοπάτια και φαρμακολογικά κριτήρια ( Εικόνα 13). Οι Μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος (mglurs), με τους οποίους και θα ασχοληθούμε στο κεφάλαιο αυτό, αποτελούν νευροτροποποιητές μέσω των οποίων το γλουταμινικό οξύ ρυθμίζει την κυτταρική διεγερσιμότητα και τη συναπτική διαβίβαση, ενεργοποιώντας σηματοδοτικά μονοπάτια δεύτερων αγγελιοφόρων. Η ευρεία εξάπλωση των mglurs πρωτεϊνών, τους καθιστά ικανούς στόχους για θεραπευτικές παρεμβάσεις σε πληθώρα διαταραχών του ΚΝΣ, καθώς φαίνεται ότι συμμετέχουν σε πολλές λειτουργίες του. Εικόνα 13: Μοριακές οικογένειες υποδοχέων γλουταμινκού οξέος. Οι δύο κύριες οικογένειες υποδοχέων του γλουταμινικού οξέος είναι οι Ιοντοτρόποι και οι Μεταβοτροπικοί υποδοχείς, και κάθε μία από αυτές διακρίνεται σε τρεις υποοικογένειες. Οι υποοικογένειες των γλουταμινικών υποδοχέων αποτελούνται από πληθώρα επιμέρους υπομονάδων, κάθε μία από τις οποίες κωδικοποιείται από διαφορετικό γονίδιο.( Basic Neurochemistry, 2006) 28
29 2.1 Μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος Οι Μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος (mglurs), είναι μέλη της υπεροικογένειας των υποδοχέων που συνδέονται με G πρωτείνες ( G-protein coupled receptors, GPCRs), της πιο εξαπλωμένης γονιδιακής οικογένειας υποδοχέων στο ανθρώπινο γονιδίωμα. Οι GPCRs είναι διαμεμβρανικοί υποδοχείς που ενεργοποιούνται από εξωκυττάριους προσδέτες, όπως πεπτίδια ή νευροδιαβιβαστές, και αλληλεπιδρώντας με G-πρωτεΐνες, ενεργοποιούν ενδοκυττάρια σηματοδοτικά μονοπάτια. Οι G- πρωτεΐνες, είναι ετεροτριμερή σύμπλοκα αποτελούμενα από τις α, β και γ υπομονάδες, και στην ανενεργή τους μορφή είναι συνδεδεμένες με ένα μόριο 5 -διφωσφορικής γουανοσίνης ( guanosine 5 diphosphate, GDP). Η αλληλεπίδραση του υποδοχέα με τον προσδέτη, συνεπάγεται τη μεταβολή της στερεοδιάταξης της G-πρωτεΐνης και την ανταλλαγή της GDP με την 5 -τριφωσφορική γουανοσίνη (guanosine 5 -triphosphate, GTP), γεγονός που προκαλεί διάσταση της υπομονάδας α από το σύμπλοκο αβγ. Οι ενεργοποιημένες G- πρωτεΐνες στη συνέχεια ρυθμίζουν την λειτουργία πληθώρας δραστικών παραγόντων. Η υδρόλυση του GTP σε GDP από την υπομονάδα α επαναφέρει την υπομονάδα στην αρχική της χωροδιάταξη και την σύνδεσή της με το σύμπολοκο βγ ( Kandel et al., 2000, C.M. Niswenwder and P.J.Conn, 2010) ( Εικόνα 14). Εικόνα 14: Η σύνδεση του προσδέτη ( γλουταμινικό οξύ) στους μεταβοτροπικούς υποδοχείς, αλλάζει τη στερεοδιάταξη του συμπλόκου των G- πρωτεϊνών και η ανταλλαγή της GDP με την GTP, προκαλεί διάσταση της υπομονάδας α από το σύμπλοκο αβγ. Οι ενεργοποιημένες G- πρωτεΐνες στη συνέχεια ρυθμίζουν την λειτουργία πληθώρας δραστικών παραγόντων όπως της PLC. 29
30 Η οικογένεια των GPCR περιλαμβάνει αρκετές υποοικογένειες υποδοχέων και οι Μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος (mglurs) ανήκουν στην C οικογένεια των GPCRs, μαζί με τους υποδοχείς GABA B, τους υποδοχείς ανίχνευσης ασβεστίου (Ca ++ -sensing receptors), τους υποδοχείς φερορμονών και τους υποδοχείς γεύσης (Pin JP et al.,2003). Οι mglurs, χαρακτηρίζονται από την ομολογία των επτά διαμεμβρανικών ελίκων τους, το μεγάλο εξωκυττάριο αμινοτελικό άκρο τους που περιλαμβάνει το σημείο δέσμευσης του αγωνιστή και από την δημιουργία διμερών (Εικόνα 15). Η ενεργοποίησή τους, πυροδοτεί έναν μηχανισμό μέσω του οποίου το γλουταμινικό οξύ μπορεί να ρυθμίσει την κυτταρική διεγερσιμότητα και την συναπτική διαβίβαση με την ενεργοποίηση σηματοδοτικών μονοπατιών δεύτερων αγγελιοφόρων. Εικόνα 15: Μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος: αποτελούνται από 7 διαμεμβρανικές έλικες, ένα μεγάλο εξωκυττάριο αμινοτελικό άκρο που περιλαμβάνει την θέση δέσμευσης του γλουταμινικού οξέος και ένα ενδοκυττάριο καρβοξυτελικό άκρο το οποίο περιλαμβάνει τη θέση δέσμευσης των G-πρωτεϊνών. 30
31 Γονίδια τα οποία κωδικοποιούν την έκφραση 8 διαφορετικών υποτύπων mglurs έχουν χαρακτηριστεί και εκφράζονται με διαφορετικό τρόπο στα διάφορα κύτταρα του ΚΝΣ( Πίνακας 1). Με βάση την ομολογία των αλληλουχιών των αμινοξέων και την ενεργοποίηση διαφορετικών σηματοδοτικών μηχανισμών, οι mglurs διακρίνονται σε τρεις μεγάλες ομάδες: το Group I που περιλαμβάνει τους mglur1 και mglur5, οι οποίοι κατά κύριο λόγο ενεργοποιούν την Φωσφολιπάση C (PLC) μέσω των Ga q/11 - πρωτεϊνών και την απελευθέρωση Ca ++ από τις κυτταραπλασματικές αποθήκες. Η ικανότητα αύξησης του ενδοκυττάριου Ca ++ ποικίλει στα διάφορα μέλη αυτής της ομάδας και εξαρτάται από τη διαφορετική συγγένεια τους με τις G-πρωτεΐνες. Η ενεργοποίηση της Φωσφολιπάσης C (PLC) οδηγεί όχι μόνο στο σχηματισμό τριφωσφορικής ινοσιτόλης ( inositol-1,4,5- triphosphate, IP 3 ), αλλά και της διακυλογλυκερόλης ( diacylglycerol, DAG), η οποία με τη σειρά της ενενργοποιεί την Πρωτεϊνική κινάση C ( protein kinase C, PKC). Οι άλλες δύο ομάδες των μεταβοτροπικών υποδοχέων περιλαμβάνουν, το Group II που περιλαμβάνει τους mglur 2 και 3 και το Group III που περιλαμβάνει τους mglurs 4, 6, 7και 8, οι οποίοι ρυθμίζουν αρνητικά την Αδενυλική κυκλάση μέσω Ga i πρωτεϊνών ( Schoepp et al.,2001, Siegel et al.,1999) ( Εικόνα 16). 31
32 Εικόνα 16: Σχηματική αναπαράσταση των τεσσάρων τύπων υποδοχέων του γλουταμινικού οξέος και των σηματοδοτικών μονοπατιών που ενεργοποιούν. Και οι δύο ομάδες των Μεταβοτροπικών υποδοχέων που απεικονίζονται συνδέονται μέσω G- πρωτεινών στα ενδοκυττάρια ένζυμα, φωσφολιπάση C (PLC) για το Group I και Αδενυλική κυκλάση για το Group II. Η ενεργοποίηση της PLC καταλύει το σχηματισμό της IP 3 και της DAG από το PIP 2 ( phosphatidylinositol-4,5-biphosphate). Το αποτέλεσμα της αύξησης του κυτταροπλασματικού IP 3 πυροδοτεί την απελευθέρωση Ca ++ από ενδοκυττάριες πηγές. Η ενεργοποίηση των Group III μεταβοτροπικών υποδοχέων, τυπικά, έχει ως αποτέλεσμα την αναστολή της αδενυλικής κυκλάσης. Οι κυτταροπλασματικές πρωτεΐνες PSD-95, GRIP και Homer αγκυστρώνουν τους υποδοχείς στην κυτταροπλασματική μεμβράνη ενδεχομένως με το να δημιουργούν γέφυρες μεταξύ των υποδοχέων κ των σχηματισμών του κυτταροσκελετού. Η ποικιλότητα των mglurs μπορεί να αυξηθεί περαιτέρω από την ύπαρξη προϊόντων εναλλακτικού ματίσματος. Το εναλλακτικό προ-mrna μάτισμα έχει πράγματι προκύψει τα τελευταία χρόνια ως ένα από τους πιο σημαντικούς και ευρέως διαδεδομένους μηχανισμούς που συμμετέχουν στη γένεση μεταγραφικής και πρωτεϊνικής ποικιλότητας. Το εναλλακτικό μάτισμα συμβαίνει κατά βάση στο καρβοξυτελικό άκρο, πλην όμως έχουν χαρακτηριστεί και προϊόντα στα οποία λείπει ολόκληρο το διαμεμβρανικό τμήμα. 32
33 Έτσι, το γονίδιο για τον mglur1a, κωδικοποιεί τέσσερα προϊόντα εναλλακτικού ματίσματος με διαφορετικά καρβοξυτελικά άκρα: mglur1a, b, c και d, εκ των οποίων ο mglur1a έχει τη μακρύτερη καρβοξυτελική ουρά. Ο mglur1e, κωδικοποιεί μια ανενεργή μορφή του mglur1( Pin JP et al.,1995), ενώ ο mglur1f κωδικοποιεί μια πρωτεΐνη με πανομοιότυπη αλληλουχία με τον mglur1b, όπως έχει δειχθεί σε επίμυες ( Soloviev MM et al., 1999). Για τον mglur5, υπάρχουν δύο κύρια προϊόντα εναλλακτικού ματίσματος: mglur5a και mglur5b (Joly C et al.,1995).ενώ δεν έχουν παρατηρηθεί φαινόμενα εναλλακτικού ματίσματος για τον mglur2, για τον mglur3 έχουν διαπιστωθεί τουλάχιστον τέσσερα προϊόντα εναλλακτικού ματίσματος: πλήρους μήκους mglur3, GRM3A2 ( λείπει το εξόνιο 2), GRM3A4 ( λείπει το εξόνιο 4), GRMA2A3 ( λείπουν τα εξόνια 2 και 3). Το προϊόν GRM3A4 είναι το πιο συχνά εμφανιζόμενο και παρότι λείπει το διαμεμβρανικό του τμήμα, μπορεί να μεταφραστεί σε κυτταρικές σειρές και in vivo, γεγονός που υποδηλώνει ότι μπορεί να λειτουργεί ως ενιαίος γλουταμινεργικός υποδοχέας. Ομοίως και για τον mglur6, υπάρχουν 3 προϊόντα εναλλακτικού ματίσματος, εκ των οποίων τα mglur6b και mglur6c, τερματίζουν στο αμινοτελικό άκρο. Το καρβοξυτελικό άκρο των mglurs 7 και 8, αποτελεί επίσης σημαντική περιοχή για εναλλακτικό μάτισμα. Για παράδειγμα, έχουν χαρακτηριστεί πέντε ισομορφές του mglur7 (mglur7 a-e ) καθώς και δύο mglur8 (mglur8a και mglur8b) ( Corti,1998) ( Εικόνα 17). 33
34 Εικόνα 17: Σχηματική αναπαράσταση των mglur προϊόντων εναλλακτικού ματίσματος. Οι αριθμοί δεξιά αντιπροσωπεύουν το μήκος των καταλοίπων των αμινοξέων στις διάφορες ισομορφές. Οι διαφορετικοί χρωματικοί συνδυασμοί στα καρβοξυτελικά άκρα, υποδεικνύουν τις μεταβολές στην αλληλουχία των αμινοξέων στις διάφορες ισομορφές που αναλογούν στα προϊόντα του εναλλακτικού ματίσματος. 2.2 Δομή μεταβοτροπικών υποδοχέων Αμινοτελικό άκρο- περιοχή δέσμευσης γλουταμινικού Σε αντίθεση με την πλειονότητα των GPCRs, οι Μεταβοτροπικοί Υποδοχείς του γλουταμινικού οξέος υπάρχουν ως λειτουργικά ομοδιμερή, όπου περιοχές πλούσιες σε κυστεΐνη συνδέουν τα δύο μονομερή του υποδοχέα. Οι Μεταβοτροπικοί Υποδοχείς του γλουταμινικού οξέος ( mglurs), όπως έχει ήδη αναφερθεί, αποτελούνται από εφτά διαμεμβρανικές έλικες, με ένα μεγάλο εξωκυττάριο αμινοτελικό άκρο, το οποίο περιλαμβάνει την περιοχή δέσμευσης του γλουταμινικού οξέος, το Venus Flytrap Domain (VFD,) ( Pin JP, 2003). Όπως φαίνεται σε μελέτες κρυσταλλογραφίας, κάθε VFD αποτελείται. από δύο λοβούς που είναι τοποθετημένοι ο ένας δίπλα στον άλλο και στη σχισμή που δημιουργείται μεταξύ τους δεσμεύεται το γλουταμινικό οξύ ( Muto T et al., 2007) ( Εικόνα 18). Η πρόσδεση του γλουταμινικού 34
35 ή των αγωνιστών, στον έναν ή και στους δύο λοβούς των VFD υπομονάδων, επιφέρει μεγάλες χωροταξικές αλλαγές στα διμερή VFD με τέτοιο τρόπο ώστε οι δύο λοβοί να κλείνουν γύρω από τον νευροδιαβιβαστή. Τρεις διαφορετικές καταστάσεις των VFD διμερών υπάρχουν: ανοιχτή-ανοιχτή, ανοιχτή κλειστή και κλειστή κλειστή και η ισορροπία μεταξύ τους καθορίζεται από τη δέσμευση του γλουταμινικού. Η πρώτη χωροδιάταξη, ανοιχτή-ανοιχτή, καθιστά το διμερές ανενεργό και μπορεί να σταθεροποιηθεί από ανταγωνιστές, ενώ οι δύο άλλες διατάξεις (ανοιχτό κλειστό ή κλειστό κλειστό) δημιουργούνται από την πρόσδεση του προσδέτη στον ένα ή στον άλλο λοβό( Εικόνα 19). Οι αλλαγές στη διαμόρφωση των VFD διμερών που πραγματοποιούνται με την σύνδεσή τους με τον προσδέτη, διαδίδονται διαμέσω τμημάτων πλούσιων στο αμινοξύ κυστείνη ( cysteine- rich domains,crds ) στις εφτά διαμεμβρανικές έλικες του υποδοχέα και στο καρβοξυ- τελικό άκρο του ( Εικόνα 19). Η CRD περιοχή του υποδοχέα, περιέχει εννέα σημαντικά αμινοξέα, οχτώ από τα οποία είναι συνδεδεμένα σε δισουλφιδικές γέφυρες (Muto et al, 2007). Μελέτες κρυσταλλογραφίας και μεταλλαξιγένεσης, έχουν δείξει ότι το σήμα που δημιουργείται από τη δέσμευση του υποδοχέα στις VFD υπομονάδες μεταδίδεται διαμέσω των CRD, κυρίως εξαιτίας της δισουλφιδικής γέφυρας που δημιουργείται μεταξύ του 9 ου αμινοξέος της CRD και της κυστείνης στον λοβό 2 των VFD (Muto et al, 2007, Rondard et al.,2006). Ενδεχομένως οι δισουλφιδικές γέφυρες που συνδέουν τα CRD και τα VFD μετέχουν στην διάδοση των σημάτων από την σύνδεση ορθοστερικού αγωνιστή στους mglurs. 35
36 Εικόνα 18: Περιοχή Δέσμευσης του Γλουταμινικού: στο μεγάλο εξωκυττάριο αμινοτελικό άκρο του υποδοχέα, βρίσκεται η περιοχή δέσμευσης του γλουταμινικού και άλλων αγωνιστών, Venus Flytrap Domain (VFD), η οποία αποτελείται από δύο λοβούς κ στην σχισμή που δημιουργείται μεταξύ τους δεσμεύεται ο νευροδιαβιβαστής. Στην εικόνα απεικονίζονται επίσης κ τα άλλα μέρη του υποδοχέα, δηλαδή οι 7 διαμεμβρανικές έλικες και το ενδοκυττάριο, καρβοξυτελικό άκρο. Εικόνα 19: Σχηματικό διάγραμμα των mglurs διμερών σε διαφορετικές καταστάσεις δραστηριότητας: Η κατάσταση ανοικτό-ανοικτό ( open-open state) του υποδοχέα, (αριστερά) είναι μια αδρανής κατάσταση που μπορεί επίσης να σταθεροποιηθεί με τους ανταγωνιστές του υποδοχέα. Στη συνέχεια, η δέσμευση του γλουταμινικού στη μία ή/και στις δυο υπομονάδες της περιοχής δέσμευσης, VFD, του γλουταμινικού, έχει ως αποτέλεσμα την μετατροπή του υποδοχέα σε ενεργή μορφή. Περιοχές πλούσιες στο αμινοξύ κυστείνη (cysteine- rich domains,crds) συνδέουν την περιοχή δέσμευσης του γλουταμινικού (VFD), με το εφταμερές διαμεμβρανικό τμήμα του και το καρβοξυτελικό άκρο του υποδοχέα, το οποίο κ αποτελεί συχνά έδαφος για εναλλακτικό μάτισμα. 36
37 2.2.2 Οι εφτά διαμεμβρανικές έλικες των mglurs Όπως προαναφέρθηκε, οι mglurs αποτελούνται από ένα σύστημα εφτά διαμεμβρανικών ελίκων εκ των οπoίων η 3 η ενδοκυττάρια έλικα ρυθμίζει την ειδικότητα δέσμευσης των G πρωτεϊνών (Gomeza J.et al, 1996, Pin JP et al.,1994), ενώ η 2 η ενδοκυττάρια έλικα αποτελεί επίσης περιοχή ρύθμισης από κινάσες ( Dhami et al,2005) (Εικόνα 20). Η πλειονότητα των αλλοστερικών ρυθμιστών (allosteric modulators) των mglurs που ρυθμίζουν θετικά ή αρνητικά την δραστηριότητα του γλουταμινκού οξέος δεσμεύονται στις εφτά διαμεμβρανικές έλικες του υποδοχέα Καρβοξυ-τελικό άκρο Το καρβοξυ-τελικό άκρο των mglurs αποτελεί σημαντική περιοχή για τη ρύθμιση της δέσμευσης των G-πρωτεϊνών. Η περιοχή αυτή για την πλειονότητα των μεταβοτροπικών υποδοχέων, αποτελεί σημείο εναλλακτικού ματίσματος, ρύθμισης με φωσφορυλίωση και ρυθμιστικών αλληλεπιδράσεων πρωτεΐνης - πρωτεΐνης. 37
38 Εικόνα 20: Αμινοξέα του αμινοτελικού άκρου των μεταβοτροπικών υποδοχέων που συμμετέχουν στην αναγνώριση του γλουταμινικού οξέος απεικονίζονται με μπλε. Σε αυτή την περιοχή του υποδοχέα εντοπίζεται ο σχηματισμός των δύο λοβών, Venus Flytrap Domain (VFD), που δημιουργεί την περιοχή δέσμευσης του γλουταμινικού οξέος. Η περιοχή αυτή, διαχωρίζεται από το διαμεμβρανικό τμήμα των 7 ελίκων μέσω περιοχής πλούσιας σε αμινοξέα κυστείνης. Ανάμεσα στην πληθώρα των καταλοίπων κυστείνης που υπάρχουν στην περιοχή αυτή ( κόκκινα, ανοιχτά σύμβολα), η Cys 140 ( και ενδεχομένως οι Cys 67 και Cys 109 ) (κλειστά κόκκινα σύμβολα), είναι απαραίτητη για τον διμερισμό του υποδοχέα. Αμφότερες οι 2 η και η 3 η έλικα συμμετέχουν στην δέσμευση και στην ενεργοποίηση των G-πρωτεϊνών. Σημαντικά κατάλοιπα που καθορίζουν την δέσμευση με τις G-πρωτείνες φαίνονται στα πράσινα κουτιά. Μία ομάδα από 4 σημαντικά κατάλοιπα του καρβοξυτελικού άκρου που απεικονίζονται με το κόκκινο κουτί συμμετέχουν στην ενεργοποίηση της PLC. 38
39 2.3 Τοπογραφική και κυτταρική κατανομή των μεταβοτροπικών υποδοχέων στο κεντρικό νευρικό σύστημα Ενώ η ταχεία διεγερτική νευροδιαβίβαση που διαμεσολαβείται μέσω των ιοντοτροπικών υποδοχέων του γλουταμινικού οξέος, απαιτεί την εντόπισή τους κατά κύριο λόγο στη μετασυναπτική μεμβράνη των γλουταμινεργικών συνάψεων, οι μεταβοτροπικοί υποδοχείς, mglurs, κατανέμονται ευρέως στα μεμβρανικά διαμερίσματα, τόσο των νευρικών όσο και των κυττάρων της γλοίας. Η ενεργοποίηση των mglurs, από το απελευθερωμένο στη σύναψη γλουταμινικό οξύ, συχνά απαιτεί υψηλής συχνότητας ή επαναλαμβανόμενη διέγερση ( Fiorillo and Williams, 1998), λόγω της περισυναπτικής τοποθέτησης των μεταβοτροπικών υποδοχέων στους δενδρίτες και στους άξονες. Με αυτόν τον τρόπο, επιτυγχάνεται η μετάδοση του σήματος ανάμεσα σε διαφορετικές συνάψεις ( ετεροσυναπτική διαβίβαση) ή σε μεταβοτροπικούς απελευθέρωσης του γλουταμινικού υποδοχείς απομακρυσμένους από τα σημεία οξέος, μέσω ενεργοποίησης διαφορετικών σηματοδοτικών μονοπατιών από το γλουταμινικό οξύ που διαχέεται ( Wada et al,1998, Vogt and Nicoll, 1999). Για να κατανοηθούν οι φυσιολογικές δράσεις του γλουταμινικού οξέος είναι απαραίτητη η γνώση της μοριακής ταυτότητας των μεταβοτροπικών υποδοχέων που εκφράζονται στους διαφορετικούς υποπληθυσμούς νευρώνων, τα μεμβρανικά διαμερίσματα των νευρώνων που εντοπίζονται και η χωρική σχέση ανάμεσα στους μεταβοτροπικούς υποδοχείς και στις θέσεις απελευθέρωσης του γλουταμινικού οξέος. Μελέτες με in situ υβριδισμό και ανοστοιστοχημικές μεθόδους, έχουν αναδείξει τις θέσεις κατανομής των οχτώ υποτύπων των μεταβοτροπικών υποδοχέων ( Εικόνα 21) που αν και μερικώς αλληλοεπικαλυπτόμενες, είναι κατά βάση διαφορετικές στο ΚΝΣ τόσο των τρωκτικών όσο και των πρωτευόντων. Η κατανομή των mglur1, mglur3, mglur5 και mglur7, είναι εκτενής σε όλο τον εγκέφαλο, ενώ αυτή των mglur2, mglur4 και mglur8 είναι περισσότερο εντοπισμένη σε συγκεκριμένες περιοχές του εγκεφάλου. Η έκφραση του mglur6 έχει διαπιστωθεί αποκλειστικά στον αμφιβληστροειδή και όχι στον εγκέφαλο ή στην σπονδυλική στήλη ( Nakajima et al., 1993; Nomura et al.,1994, Schools and Kimelberg, 1999). Στον εγκέφαλο του ενήλικου επίμυος, οι μεταβοτροπικοί υποδοχείς εκφράζονται κυρίως στα νευρωνικά κύτταρα, με εξαίρεση τον mglur3, ο οποίος φαίνεται ότι εκφράζεται ευρέως στα κύτταρα της γλοίας κατά μήκος του εγκεφάλου. Επίσης, η έκφραση των mglur3 και 39
40 mglur5, είναι αυξημένη σε ενεργοποιημένα αστροκύτταρα, ενώ τα κύτταρα αυτά εκφράζουν και τους mglur4. Επίσης, κύτταρα μικρογλοίας σε κυτταροκαλλιέργειες φαίνεται ότι εκφράζουν τους mglur2, mglur4, mglur5, mglur6 και mglur Κατανομή των Group I Μεταβοτροπικών υποδοχέων Οι mglur1 κατανέμονται ευρέως στο ΚΝΣ και φαίνεται ότι η έκφρασή τους είναι ισχυρή στα κύτταρα Purkinjie και στα κύτταρα του εγκεφαλικού φλοιού (Shigemoto et al.,1992). Διαφορετική έκφραση του mrna έχει παρατηρηθεί ανάμεσα στα προϊόντα εναλλακτικού ματίσματος των mglur1 στον εγκέφαλο τρωκτικών και θηλαστικών ( Berthele et al., 1998,1999). Έτσι, ισχυρή έκφραση των mglur1a έχει διαπιστωθεί στα κύτταρα Purkinjie, στους ιπποκάμπειους ενδονευρώνες, στους θαλαμικούς νευρώνες και στους νευρώνες της μέλαινας ουσίας ( Martin et al., 1992, Fotuhy et al.,1993), ενώ οι mglur1β εκφράζονται ισχυρά στους πυραμιδικούς νευρώνες της CA3 περιοχής του ιππόκαμπου, στα κοκκιώδη κύτταρα της οδοντωτής έλικας και στον πλευρικό υποθάλαμο ( Ferraguti et al., 1998, Mateos et al.,1998). Στο επίπεδο του ηλεκτρονικού μικροσκοπίου, οι mglur1 μεταβοτροπικοί υποδοχείς έχουν κυρίως παρατηρηθεί στα μετασυναπτικά νευρωνικά στοιχεία του εγκεφαλικού φλοιού, στον ιππόκαμπο, στο ραβδωτό, στον θάλαμο, στον υποθάλαμο και στον εγκεφαλικό φλοιό. Η κατανομή του άλλου μέλους του Group I των μεταβοτροπικών υποδοχέων, των mglur5 στο ΚΝΣ είναι συμπληρωματική με αυτή των mglur1. Η έκφρασή τους είναι ισχυρή σε τελεγκεφαλικές περιοχές συμπεριλαμβανομένων του εγκεφαλικού φλοιού, του ιπποκάμπου, του subiculum, του ραβδωτού και του επικλινή πυρήνα ( Abe et al., 1992, Shigemoto et al., 1993, Romano et al., 1995). Στον ιππόκαμπο, οι mglur5 κυρίως εκφράζονται στα δενδριτικά πεδία των πυραμιδικών και κοκκώδων κυττάρων ( Shigemoto et al., 1997). Ισχυρή έκφραση έχει επίσης διαπιστωθεί σε κάποιους GABAεργικούς ενδονευρώνες του νεοφλοιού και του ιπποκάμπου ( Kerner et al., 1997). Αν και η κατανομή των mglur5a και των mglur5b, εμφανίζει ομοιότητες, φαίνεται ότι οι mglur5a είναι πιο συχνοί σε νεαρούς επίμυες ενώ η έκφραση των mglur5b, υπερισχύει σε ενήλικους επίμυες (Joly et al., 1995, Romano et al., 1996). Στο επίπεδο του ηλεκτρονικού μικροσκοπίου, οι mglur5, εντοπίζονται κυρίως στις σωματικές και δενδριτικές περιοχές του 40
41 ιπποκάμπου, στα βασικά γάγγλια, στον θάλαμο, στον υποθάλαμο, στον εγκεφαλικό φλοιό και στην σπονδυλική στήλη Κατανομή των Group I I Μεταβοτροπικών υποδοχέων Η κατανομή των mglur2, είναι περισσότερο περιορισμένη στο ΚΝΣ σε σχέση με αυτή των mglur1, mglur3 και mglur5. Η πιο ισχυρή έκφραση των mglur2, διαπιστώνεται στον εγκεφαλικό φλοιό ( Ohishi et al.,1994), ενώ φαίνεται ότι δεν εκφράζονται μόνο στις σωματο-δενδριτικές περιοχές αλλά και στις αξονικές περιοχές των νευρώνων. Στον ιππόκαμπο, ανοσοδραστικότητα των mglur2, έχει διαπιστωθεί στις προσυναπτικές κατασκευές των βρυώδων ινών. Αντίθετα οι mglur3, εκφράζονται ισχυρά κατά μήκος του ΚΝΣ ( Tamaru et al.,2001). Σε εικόνες ηλεκτρονικού μικροσκοπίου φαίνεται ότι οι mglur3 εντοπίζονται όχι μόνον μετασυναπτικά αλλά και προσυναπτικά, καθώς και σε κύτταρα γλοίας στον ιππόκαμπο, στον εγκεφαλικό φλοιό και στο ραβδωτό (Tamaru et al., 2001) Κατανομή των Group I I I Μεταβοτροπικών υποδοχέων Από τους υποδοχείς που περιλαμβάνονται στην τρίτη οικογένεια των μεταβοτροπικών υποδοχέων οι mglur7 είναι οι πιο συχνοί, ενώ οι mglur6 εντοπίζονται αυστηρά στον αμφιβληστροειδή και δεν υπάρχουν δεδομένα που να αποδεικνύουν την έκφρασή τους σε άλλες εγκεφαλικές περιοχές ( Nakajima et al., 1993, Kinoshita et al.,1998 ). Έκφραση των mglur7, έχει διαπιστωθεί στον νεοφλοιό, στον ιππόκαμπο συμπεριλαμβανομένων των CA1-CA3 περιοχών και της οδοντωτής έλικας, στο ραβδωτό, στο δίκτυο της αμυγδαλής, στον υποθάλαμο, στο θάλαμο και στην σπονδυλική στήλη ( Shigemoto et al., 1997, Corti et al., 1998, Wada et al., 1998). Όσον αφορά στην κατανομή των προϊόντων εναλλακτικού ματίσματος των mglur7, φαίνεται ότι η κατανομή των mglur7b είναι περιορισμένη σε σχέση με αυτή των mglur7a (Corti et al., 1998) και ότι οι περισσότερες περιοχές που εκφράζουν mglur7b εκφράζουν και mglur7a (Shigemoto et al., 1997). Η έκφραση των mglur4, είναι πιο ισχυρή στα εγκεφαλικά κοκκιώδη κύτταρα (Kinoshita et al.,1996a) έχει όμως διαπιστωθεί και στον ιππόκαμπο και σε άλλες εγκεφαλικές περιοχές, όπως στον θάλαμο, στην αμυγδαλή και στο ραβδωτό ( Corti et al., 2002 ). Η έκφραση των mglur8 είναι περιορισμένη σε σχέση με αυτή των mglur7 (Corti 41
42 et al., 1998). Ισχυρή έκφρασή τους παρουσιάζεται στους οσφρητικούς βολβούς, στον οσφρητικό φλοιό και στον προμήκη μυελό. Στον ιππόκαμπο οι mglur8a εντοπίζονται στην CA1 περιοχή ( Ferraguti et al., 2005) και στα κύτταρα της οδοντωτής έλικας (Shigemoto et al., 1997). Εικόνα 21: Κατανομή των μεταβοτροπικών υποδοχέων στον εγκέφαλο ενήλικα επίμυος (από Shigemoto and Mizuno, 2000) : Ανοσοδραστικότητα των 8 μεταβοτροπικών υποδοχέων στις διaφορετικές περιοχές του εγκεφάλου ( AOB accessory olfactory bulb, Acb accumbens nucleus, Cb cerebellum, Cx neocortex, GP globus pallidus, Hi hippocampus, IC inferior colliculus, LS lateral septum, MOB main olfactory bulb, Ot olfactory tubercle, Pir piriform cortex, SC superioir colliculus, SN substantia nigra, SpV spinal vestibular nucleus, St neostriatum, Th thalamus, VP ventral pallidum) Κυτταρική εντόπιση των μεταβοτροπικών υποδοχέων Εικόνες του ηλεκτρονικού μικροσκοπίου αναδεικνύουν τα διαφορετικά μοτίβα κατανομής των μεταβοτροπικών υποδοχέων σε σχέση με τις περιοχές κατανομής του γλουταμινικού οξέος. Έτσι, οι μεταβοτροπικοί υποδοχείς του Group I εντοπίζονται κυρίως στις σωματοδενδριτικές περιοχές των νευρώνων, κοντά στις περιοχές της πρωτεϊνικής σύνθεσης, ενώ οι μεταβοτροπικοί υποδοχείς του Group II παρατηρούνται όχι μόνον στις περιοχές αυτές, αλλά και στις περιοχές των αξόνων. 42
43 Αντίθετα, οι μεταβοτροπικοί υποδοχείς που ανήκουν στην τρίτη κατηγορία, πλην των mglur6, είναι κατά κύριο λόγο παρόντες στις προσυναπτικές περιοχές των αξόνων. Πιο συγκεκριμένα, οι Group I mglurs, εντοπίζονται κατά κύριο λόγο στην περιφέρεια των μετασυναπτικών περιοχών των ασύμμετρων συνάψεων, σε πολλές περιοχές του εγκεφάλου συμπεριλαμβανομένων του εγκεφαλικού φλοιού και του ιπποκάμπου ( Baude et al., 1993, Nusser et al., 1994, Lujan et al., 1996,1997). Η ενεργοποίησή τους συχνά οδηγεί στε κυτταρική εκπόλωση και αυξάνει την κυτταρική διεγερσιμότητα ( Πίνακας 1, εικόνα 10). Η άποψη περί περισυναπτικής θέσης της πρώτης ομάδας των μεταβοτροπικών υποδοχέων, ενισχύθηκε μετά την ανακάλυψη πρωτεϊνών που συνδέονται στις συνάψεις ( Tu et al. 1999), οπότε και αποκαλύφθηκε η λειτουργική σύνδεσή τους, με τους, μετασυναπτικούς, NMDA υποδοχείς καθώς και η ρύθμιση των ρευμάτων των NMDA υποδοχέων από τους mglu1/5 σε κυτταροκαλλιέργειες φλοιϊκών νευρώνων ( Yu et al. 1997). Αντίθετα, οι Group II και Group III μεταβοτροπικοί υποδοχείς κατά βάση εντοπίζονται στους προσυναπτικούς νευρώνες και σε γενικές γραμμές αναστέλλουν την απελευθέρωση του γλουταμινκού οξέος ( Εικόνα 22). Τα γεγονότα αυτά παρατηρούνται στις διεγερτικές (γλουταμινεργικές), στις ανασταλτικές (GABAεργικές) και νευροτροποποιητικές ( μονοαμίνες, πεπτίδια, ακετυλοχολίνη) συνάψεις. Στις προσυναπτικές περιοχές οι μεταβοτροπικοί υποδοχείς της δεύτερης και τρίτης ομάδας κατανέμονται με διαφορετικό τρόπο κοντά στις θέσεις απελευθέρωσης του γλουταμινικού οξέος ( Shigemoto et al., 1997, Wada et al., 1998). Οι Group III μεταβοτροπικοί υποδοχείς εντοπίζονται κατά κύριο λόγο στην προσυναπτική ενεργό ζώνη, ενώ οι μεταβοτροπικοί υποδοχείς του Group II συχνά εντοπίζονται σε περιοχές πριν από το τελικό τμήμα των αξόνων και ενεργοποιούνται από το απελευθερούμενο γλουταμινικό οξύ. Οι διαφορετικές περιοχές κατανομής των Group II και Group III μεταβοτροπικών υποδοχέων, ενδεχομένως υποδεικνύουν διαφορετικές πηγές γλουταμινικού που ενεργοποιεί αυτούς τους υποδοχείς και διαφορετικούς δραστικούς παράγοντες με τους οποίους συνδέονται. Έτσι, φαίνεται ότι οι Group III δρουν ως αυτουποδοχείς, ενώ οι Group II πιθανόν ενεργοποιούνται από την διάχυση του γλουταμινικού οξέος από απομακρυσμένες συνάψεις στο ίδιο ή σε άλλο προσυναπτικό στοιχείο ( Vogt and Nicoll, 1999). Μολονότι έχουν αναφερθεί παρόμοιοι δραστικοί μηχανισμοί με ειδικούς αγωνιστές για τους Group II και Group III μεταβοτροπικούς υποδοχείς, η λειτουργική διαφοροποίηση τους που αφορά στην 43
44 διαφορετική προσυναπτική κατανομή τους, έχει αναφερθεί (Capogna 2004) (Εικόνα 22). στον ιππόκαμπο. Εικόνα 22: Σχηματική αναπαράσταση των μεταβοτροπικών υποδοχέων στη σύναψη. Γενικά, οι Group I mglurs ( πράσινοι) εντοπίζονται μετασυναπτικά και οι Group II ( μπλε) και οι Group III ( κόκκινοι ) υποδοχείς, εντοπίζονται προσυναπτικά, παρότι υπάρχουν και εξαιρέσεις. Στις προσυναπτικές περιοχές οι mglur 2,3,4, και 8 βασικά εμφανίζουν εξτρασυναπτικές εντοπίσεις και ο mglur7 εκφράζεται σημαντικά στην ενεργό ζώνη. Οι Group II και οι Group III αναστέλλουν την απελευθέρωση του γλουταμινικού ( αριστερά, κίτρινοι κύκλοι),ή του GABA ( δεξιά, κόκκινοι κύκλοι), ενώ οι Group I όταν είναι παρόντες προσυναπτικά ενεργοποιούν την απελευθέρωση του γλουταμινικού. Στην προσυναπτική περιοχή ιοντικοί δίαυλοι, όπως οι NMDA και οι AMPA, απαντούν στην απελευθέρωση του γλουταμινικού αυξάνοντας το ενδοκυττάριο ασβέστιο με αποτέλεσμα την νευρωνική διεγερσιμότητα. Group I mglurs, μέσω της σύνδεσής τους με G-πρωτεΐνες, αυξάνουν το ενδοκυττάριο αβσέστιο, ενώ οι mglur5 και οι NMDA, φαίνεται ότι αλληλεπιδρούν μέσω μηχανισμών που επάγουν την φωσφορυλίωσή τους. 44
45 ΠΙΝΑΚΑΣ Μεταγωγή σήματος Οι mglurs όπως και τα άλλα μέλη της οικογένειας C των GPCR, δρουν ως εν δυνάμει διμερή. Από τα μέχρι τώρα βιβλιογραφικά δεδομένα δεν καθίσταται σαφές εάν το γλουταμινικό οξύ που δεσμεύεται σε ένα από τα μέρη του διμερούς είναι ικανό να ενεργοποιήσει ολόκληρο το σύμπλοκο. Για παράδειγμα, το γλουταμινικό οξύ δεν ήταν ικανό να ενεργοποιήσει διμερή τα οποία σχηματίζονταν από ένα wildtype και από ένα μεταλλαγμένο στέλεχος των mglur1 όταν δεσμευόταν σε έναν από τους δύο υποκινητές ( Kammermeier et al., 2005). Αντίθετα, οι Kniazeff et al, έδειξαν ότι ένα μόριο γλουταμινικού είναι αρκετό ώστε να ενεργοποιήσει mglur5 ομοδιμερή, αλλά η σύνδεση και των δύο VFD με τον προσδέτη είναι περισσότερο αποτελεσματική. Oι Suzuki et al, έδειξαν ότι η σύνδεση του γλουταμινικού στον έναν υποκινητή προκαλεί αρνητική συνενεργοποίηση για δέσμευση και στον άλλο υποκινητή (Suzuki et al., 2004) γεγονός που υποδεικνύει ότι το γλουταμινικό 45
46 δεσμεύεται και στα δυο διμερή, η σύνδεση όμως αυτή μπορεί να παρουσιάζει ποικιλότητα στην φαρμακολογία του υποδοχέα. Γενικά, οι group I mglurs δεσμεύονται στις G q / G 11 πρωτεΐνες και ενεργοποιούν την φωσφολιπάση C β, με αποτέλεσμα την υδρόλυση των φωσφοινοσιτιδών και την δημιουργία της τριφωσφορικής ινοσιτόλης (IP 3 ) και της διακυλογλυκερόλης ( Πίνακας 1). Αυτό το μονοπάτι οδηγεί στην απελευθέρωση του ενδοκυττάριου ασβεστίου ( από το ενδοπλασματικό δίκτυο) και στην ενεργοποίηση της πρωτεϊνικής κινάσης C (PKC). Βέβαια, είναι πλέον γνωστό ότι αυτοί οι υποδοχείς μπορούν ενεργοποίησουν και σηματοδοτικά μονοπάτια που δεν εξαρτώνται από την ενεργοποίηση G- πρωτεϊνών, όπως αναφέρεται παρακάτω (Hermans et al., 2001). Ανάλογα με τον κυτταρικό τύπο ή τον τύπο του νευρικού πληθυσμού, οι group I mglurs μπορούν να ενεργοποίησουν μια πληθώρα από ενδοκυττάριους παράγοντες, συμπεριλαμβανομένων της φωσφολιπάσης D, μονοπατιών πρωτεινικών κινασών όπως της casein kinase 1, της πρωτεϊνικής κινάσης 5, της JUN κινάσης, του μονοπατιού των ΜΑΡ-κινασών καθώς και του στόχου της rapamycin (MTOR)/p70 S6 kinase μονοπατιού. Τα δύο τελευταία ενδοκυττάρια μονοπάτια, φαίνεται ότι είναι ιδιαίτερα σημαντικά μονοπάτια στη ρύθμιση της συναπτικής πλαστικότητας από τους group I mglurs. Σε αντίθεση με τους group I mglurs, οι group II και III mglurs δεσμεύονται κατά κύριο λόγο σε G i/o πρωτεΐνες. Οι υποδοχείς που δεσμεύονται σε G i/o πρωτεΐνες, προκαλούν αναστολή της αδενυλικής κυκλάσης και άμεσα ρυθμίζουν διαύλους ιόντων και άλλους ενδοκυττάριους παράγοντες. Όπως και στην περίπτωση των group I mglurs, και οι group II και III mglurs ενεργοποιούν και άλλα ενδοκυττάρια σηματοδοτικά μονοπάτια, όπως αυτά των MAPK και IP3 κινασών (Iacovelli et al.,2002), γεγονός που υποδεικνύει ότι υπάρχει πολυπλοκότητα στους μηχανισμούς μέσω των οποίων αυτοί οι υποδοχείς μπορούν να ρυθμίσουν την συναπτική διαβίβαση Αλληλεπιδρώσες πρωτεΐνες με τους mglurs Πολλαπλές πρωτεΐνες αλληλεπιδρούν άμεσα με το καρβοξυτελικό άκρο καθενός από τους mglurs υποτύπους και παίζουν σημαντικό ρόλο στη ρύθμιση της σηματοδότησης μέσω των μεταβοτροπικών υποδοχέων. Αυτό γίνεται μέσω αλληλεπιδράσεων πρωτεϊνών- πρωτεϊνών. Από τις πιο καλά χαρακτηρισμένες 46
47 πρωτεΐνες που αλληλεπιδρούν με τους μεταβοτροπικούς υποδοχείς είναι οι Homer πρωτεΐνες, οι οποίες περιέχουν τη PDZ 1 περιοχή ( post synaptic density 95, dics large, zona occludens) που αλληλεπιδρά με τα τελευταία αμινοξέα, PPxxF των GluR1a και mglur5a, b, όπως θα δούμε παρακάτω ( Εικόνα 23). Μολονότι αλληλεπιδράσεις ανάμεσα στους μεταβοτροπικούς υποδοχείς του group II με πρωτεΐνες, δεν είναι καλά χαρακτηρισμένες όπως οι αντίστοιχες του group I, η καλμοδουλίνη και η πρωτεϊνική φωσφατάση 2 C, σύμφωνα με νεότερα βιβλιογραφικά δεδομένα, αλληλεπιδρούν με το καρβοξυτελικό άκρο των mglur3 (Flajolet et al., 2003). Το καρβοξυτελικό άκρο του GluR7 και των προϊόντων εναλλακτικού ματίσματος, επίσης αλληλεπιδρά με πληθώρα πρωτεϊνών όπως η PDZ περιοχή και συγκεκριμένα με την πρωτεΐνη PICK1 ( protein interacting with C kinase 1). H PICK1 δεσμεύεται στην πρωτεϊνική κινάση Ca ( PKCa ), οπότε σχηματίζεται ένα τριμερές πρωτεϊνικό σύμπλοκο στις ενεργές ζώνες των προσυναπτικών νευρώνων ( Boudin et al., 2000, El Far O et al., 2000). Εικόνα 23: group Ι mglur και αλληλεπιδρώσες πρωτεΐνες 47
48 2.5 Κυτταρική σηματοδότηση μέσω του group I μεταβοτροπικών υποδοχέων Οι μεταβοτροπικοί υποδοχείς του γλουταμινικού οξέος που ανήκουν στην πρώτη κατηγορία (group I mglurs), έχουν ενοχοποιηθεί για πληθώρα εγκεφαλικών νοσημάτων. Καλύτερη κατανόηση των σηματοδοτικών μονοπατιών που ενεργοποιούνται από αυτούς, μπορεί να συμβάλλει στην κατανόηση των μοριακών μηχανισμών διαφόρων νευρολογικών νοσημάτων και άρα στην ανάπτυξη νέων μορφών θεραπείας. Τα σηματοδοτικά μονοπάτια ( Εικόνα 24) ( Πίνακας 2) που ενεργοποιούνται από τους group I mglurs, είναι πολύπλοκα και περιλαμβάνουν την ενεργοποίηση ενός καταρράκτη ενδοκυττάριων γεγονότων. Έχει ενδιαφέρον ότι κάθε ένα από αυτά τα διαφορετικά σηματοδοτικά μονοπάτια που ενεργοποιούνται μπορούν να ρυθμιστούν με ξεχωριστούς μηχανισμούς και με διαφορετική ένταση, γεγονός που επιτρέπει την ειδική ρύθμιση στην σηματοδότηση των μεταβοτροπικών υποδοχέων με βάση την παθολογία της νόσου. Μολονότι, η πρόοδος όσον αφορά στην κατανόηση του τρόπου ενεργοποίησης των σηματοδοτικών μονοπατιών των mglurs είναι σημαντική, παραμένει νεφελώδης ο τρόπος μέσω του οποίου η ενεργοποίηση τους μπορεί να πυροδοτήσει την παθογένεση των περισσοτέρων νευρολογικών νοσημάτων στις οποίες εμπλέκονται. Μελλοντικές μελέτες πάνω στα μοριακά μονοπάτια που ενεργοποιούνται από τους mglurs μπορεί να καθορίσουν την ανάπτυξη θεραπειών για πολυπαραγοντικά και πολύπλοκα νευρολογικά νοσήματα Ενεργοποίηση των G πρωτεϊνών από τους group Ι mglur Οι group I mglurs μπορούν να ρυθμίσουν τη δραστηριότητα πολλαπλών ενδοκυττάριων σηματοδοτικών μονοπατιών μέσω λειτουργικής δέσμευσής τους με ποικιλία G- πρωτεϊνών (Εικόνα 24). Αυτή η σηματοδοτική δέσμευση, η οποία και έχει ευρέως χαρακτηριστεί σε ανασυνδυασμένα συστήματα, στα οποία ένας μοναδικός υποδοχέας μπορεί να εκφραστεί, παρατηρείται επίσης και στο Κεντρικό Νευρικό Σύστημα και είναι πιθανόν να εξαρτάται από τη φύση των σηματοδοτικών μορίων που είναι παρόντα στο κύτταρο και από την άμεση γειτνίαση του υποδοχέα με αυτά. Αυτά τα διαφορετικά σηματοδοτικά μονοπάτια ενδεχομένως συμμετέχουν (θετικά ή αρνητικά) στο ίδιο βιοχημικό γεγονός, δηλαδή στη ρύθμιση ( finetunning ) της κυτταρικής απόκρισης στο γλουταμινικό οξύ. Συγχρόνως, η ενεργοποίηση αυτών των διαφορετικών μονοπατιών ρυθμίζεται από πληθώρα 48
49 παραγόντων, γεγονός που ενισχύει την άποψη περί πολυπλοκότητας της σηματοδότησης του γλουταμινικού μέσω των mglurs υποδοχέων. Είναι επίσης πιθανό ότι οι αλληλεπιδράσεις μεταξύ των mglurs υποδοχέων και άλλων σηματοδοτικών μονοπατιών μπορούν να συνεισφέρουν στην πολύπλοκη διαμόρφωση των υποδοχέων αυτών. Όπως προαναφέρθηκε, οι group Ι mglurs δεσμεύονται κατά κύριο λόγο σε Ga q/11 πρωτεΐνες οπότε ενεργοποιείται το PLC/InsP3/Ca ++ σηματοδοτικό μονοπάτι. Η ενεργοποίηση της φωσφολιπάσης C β1 (PLC β1 ), συνεπάγεται το σχηματισμό της διακυλογλυκερόλης ( DAG) και τριφωσφοτικής ινοσιτόλης (IP 3 ), η δέσμευση της οποίας στον υποδοχέα της προκαλεί απελευθέρωση ασβεστίου από τις ενδοκυττάριες αποθήκες (Εικόνα 24). Η κινητική της σηματοδότησης των IP3 και του ασβεστίου, ως απάντηση της ενεργοποίησης των group I mglurs είναι πιθανό να ρυθμίζεται με διαφορετικό τρόπο στους διάφορους κυτταρικούς πληθυσμούς, γεγονός που εξαρτάται από την αλληλεπίδραση των group I mglurs με πρωτεΐνες όπως η Homer (Tu J.C et al.,1998 ) και η NHERF-2 ( Paquet M.et al., 2006). Τόσο το Ca ++ όσο και η DAG οδηγούν στην ενεργοποίηση της PKC, η οποία έχει προταθεί ότι οδηγεί στην ενεργοποίηση των PLD, PLA 2 και του σηματοδοτικού μονοπατιού των MAPK κινασών, καθώς και στην ενεργοποίηση πληθώρας ιοντικών διαύλων (Εικόνα 24) (Hermans, E.; Challiss, R.A, 2001). Μολονότι ο κύριος σηματοδοτικός μηχανισμός ενεργοποίησης των G- πρωτεϊνών μέσω των group Ι mglurs περιλαμβάνει την ενεργοποίηση των Gaq /11 πρωτεϊνών, αυτοί οι υποδοχείς μπορούν να ενεργοποιήσουν και άλλες G- πρωτεΐνες συμπεριλαμβανομένων των Gas και Ga i/0, άρα μπορούν να ενεργοποιήσουν τα μονοπάτια φωσφοινοσιτόλης και camp ταυτόχρονα ( Εικόνα 24). Όταν ο mglur1a υπερεκφράζεται σε κύτταρα βατράχου (CHO cells), οδηγεί στο σχηματισμό του camp και στην απελευθέρωση αραχιδονικού οξέος (Aramori et al., 1992). Ομοίως και σε άλλα ανασυνδυασμένα συστήματα όπως σε κύτταρα ωοθηκών (Aramori I et al., 1992), σε BΗK κύτταρα ( Thomsen et al., 1996) ή σε κύτταρα HEK 293 (Francesconi et al.,1998, Parmentier et al., 1998) η έκφραση του συγκεκριμένου υποδοχέα, συνεπάγεται το σχηματισμό του camp. Αντίθετα, η έκφραση των προϊόντων εναλλακτικού ματίσματος mglur1b, mglur1c και mglur1d δεν προκαλεί τον σχηματισμό του camp ( Joly et al., 1995, Hiltscher et al., 1998, Mary et al., 1997). Από την άλλη, η ενεργοποίηση του mglur5, όταν εκφράζεται ετερογενώς, αυξάνει την αναγέννηση του camp σε κύτταρα ωοθηκών και σε LLC- 49
50 PK1 κύτταρα ( Joly C. et al., 1995), όχι όμως σε CHO κύτταρα ή αστροκύτταρα, σε πρωτογενείς κυτταροκαλλιέργειες ( Abe T. et al.,1992, Balazs, R. et al., 1997). Έχει επίσης δειχθεί ότι η ενεργοποίηση του mglur1a σε ΒΗΚ κύτταρα, μπορεί να αναστείλει την ενεργοποίηση της αδενυλικής κυκλάσης μέσω δέσμευσης του υποδοχέα με Ga i/0 πρωτεΐνες ( Hermans, E.; Challiss, R.A, 2001, Hermans E. et al.,2000 ). Όμως, η mglur1a- Ga i/0 δέσμευση δεν παρατηρείται όταν χαμηλά επίπεδα του υποδοχέα εκφράζονται σε CHO κύτταρα ( Selkirk J.V. et al.,2001). Έτσι δεν είναι ακόμα τελείως ξεκάθαρο εάν ο mglur1 υποδοχέας δεσμεύεται σε Ga i/0 πρωτεΐνες. Το ερώτημα εάν ο σχηματισμός της αδενυλικής κυκλάσης μετά την ενεργοποίηση των mglur1/5, είναι μέσω άμεσης δέσμευσης των υποδοχέων αυτών με Gs πρωτεΐνη ή έμμεσης, από την ενεργοποίηση της PLC, έχει τεθεί σε πληθώρα μελετών. Η απουσία μιας mglur5- εξαρτώμενης απάντησης, όσον αφορά στην ενεργοποίηση της αδενυλικής κυκλάσης, σε κυτταρικά υποστρώματα όπου ο mglur1a είναι δραστικός, υποδεικνύει ότι η PLC και η αδενυλική κυκλάση ρυθμίζονται με διαφορετικό τρόπο ( Aramori,I. and Nakanishi, S., 1992 ). Οι Francenson and Duvoision ( 1998) έδειξαν ότι σε διαφορετικές περιοχές οι mglurs συμμετέχουν στη λειτουργική ενεργοποίηση διαφορετικών σηματοδοτικών μονοπατιών. Οι group I mglurs, συμμετέχουν στη λειτουργική ρύθμιση πληθώρας ιοντικών διαύλων. Σε ιπποκάμπειους νευρώνες, οι mglur1/5, μέσω αλληλεπίδρασής τους με ενεργοποιημένες G-πρωτεΐνες μπορούν να ρυθμίσουν την αναστολή τασεοελεγχόμενων διαύλων Ca ++ ( Lester, R.A.; Jahr, C.E,1990, Swartz, K.J.; Bean, B.P,1992 ). Σε HEΚ 293 κύτταρα έχει δειχθεί ότι η αναστολή των καναλιών Ca ++ από την ενεργοποίηση των mglur1/5 πιθανόν γίνεται μέσω των βγ υπομονάδων των Ga 1/0 πρωτεϊνών (McCool. et al.,1998). Έχει ενδιαφέρον ότι ένα G- πρωτεϊνοεξαρτώμενο μονοπάτι σηματοδότησης, αλλά ανεξάρτητο από την ενεργοποίηση του InsP3/PKC μονοπατιού, ενοχοποιείται για την mglur1 εξαρτώμενη ρύθμιση των L-type τασεοελεγχόμενων καναλιών Ca ++ και εξαρτάται από τους Ryanodine receptors (RyRs), που αποτελούν τους κύριους μεσολαβητές απελευθέρωσης ασβεστίου στα ζωικά κύτταρα ( Chavis, P et al 1996, Fagni, L. et al.,2000). Πληθώρα διαύλων K + μπορεί επίσης να ρυθμιστούν μέσω του group I mglurs. Για παράδειγμα, έχει δειχθεί ότι οι group I mglurs επηρεάζουν την αγωγιμότητα Ca ++ - εξαρτώμενων καναλιών K + σε κοκκιώδη κύτταρα παρεγκεφαλίδας (Fagni et al 1991). 50
51 Σε συνδυασμό με τη ρύθμιση του PLC/AC μονοπατιού και με τη ρύθμιση των ιοντικών διαύλων, οι group I mglurs έχει δειχθεί ότι αλληλεπιδρούν με άλλους ρυθμιστικούς παράγοντες. Έτσι, ο mglur1a υποδοχέας μέσω ενεργοποίησης του σηματοδοτικού μονοπατιού της PLC-β ρυθμίζει την παραγωγή αραχιδονικού οξέος, πιθανόν μέσω ενεργοποίησης της δραστηριότητας της φωσφολιπάσης Α2 (PLΑ2) (Aramori, et al 1992). Πληθώρα μελετών επίσης έχει δείξει την εξαρτώμενη από την ενεργοποίηση των μεταβοτροπικών υποδοχέων, ρύθμιση της έκφρασης της φωσφολιπάσης D (PLD), τόσο σε νευρωνικά όσο και σε κύτταρα γλοίας. Ως επί το πλείστον, θεωρείται ότι η ενεργοποίηση της PLD γίνεται μέσω PKC( Boss, et al 1992, Pellegrini-Giampietro et al., 1996, Pellegrini-Giampietro et al., 2000). 51
52 Εικόνα 24: Τα πολλαπλά σηματοδοτικά μονοπάτια που ενεργοποιούνται μέσω της δέσμευσης των group Ι mglurs με διαφορετικές G-πρωτείνες. Οι group Ι mglurs κατά κύριο λόγο δεσμεύονται με Ga q/11 πρωτεΐνες, γεγονός που οδηγεί στην ενεργοποίηση του PLC/InsP3 σημετοδοτικού μονοπατιού, με αποτέλεσμα την αύξηση του ενδοκυττάριου Ca ++ και την απελευθέρωση της διακυλογλυκερόλης ( DAG). Η PKC, φαίνεται ότι συμμετέχει στην ενεργοποίηση των PLΑ2 και PLD και ενδεχομένως στην ενεργοποίηση του σηματοδοτικού μονοπατιού των ΜΑΡΚ κινασών Αλληλεπίδραση των group Ι mglur με τους NMDA υποδοχείς Η γειτονική κατανομή των μεταβοτροπικών υποδοχέων με τους ιοντοτρόπους υποδοχείς του γλουταμινικού οξέος στις μετασυναπτικές μεμβράνες των διεγερτικών συνάψεων (Takumi et al., 1999), έχει ως συνέπεια την αλληλεπίδρασή τους. Η ενεργοποίηση των group I mglurs, και κυρίως του υποτύπου τους 52
53 mglur5, φαίνεται ότι προκαλεί ισχυρή ρυθμιστική επίδραση στις NMDAεπαγόμενες απαντήσεις μέσω της πρωτεϊνικής κινάσης C (PKC) (Doherty et al., 1997, Awad et al., 2000, Kelso et al., 1992, Fitzjohn et al.,1996, Pisani et al., 1997, Skeberdis et al., 2001, Aoki et al., 2004) ( Εικόνα 25). Η ενεργοποίηση της PKC ενεργοποιεί τους NMDA υποδοχείς και αυξάνει την πιθανότητα διάνοιξης των διαύλων τους ( Lu et al., 1999) καθώς αυξάνεται η εισροή ασβεστίου εντός του κυττάρου ( Lan et al., 2001). Συγχρόνως, φαίνεται ότι τα διεγερτικά μετασυναπτικά δυναμικά είναι μειωμένα στον ιππόκαμπο mglur5- knockout μυών, και ότι οι μύες αυτοί εμφανίζουν ελλείμματα στην NMDA εξαρτώμενη πλαστικότητα και μάθηση (Lu et al., 1997, Jia et al., 1998). Έχει ενδιαφέρον ότι η ενεργοποίηση της PKC, είτε από τους mglur5 είτε από άλλους GPCRs, μπορεί να οδηγήσει στην PKCεπαγόμενη απευαισθητοποίηση των mglur5, η οποία αντιστρέφεται από την ενεργοποίηση των NMDA υποδοχέων. Το φαινόμενο αυτό διαμεσολαβείται μέσω μιας ασβεστιοεξαρτώμενης φωσφατάσης, της καλσινευρίνης (Alagarsamy S et al 1999). Με άλλα λόγια, οι mglur5 και NMDA υποδοχείς, είναι στενοί συνεργάτες, οπότε η ρύθμιση της δραστηριότητας των mglur5 υποδοχέων επηρεάζει τις NMDA-επαγόμενες απαντήσεις Ο Heidinger και οι συνεργάτες του έχουν επίσης προτείνει ότι η αύξηση των ρευμάτων των NMDA υποδοχέων από την ενεργοποίηση των mglur1 σε φλοιώδεις νευρώνες, περιλαμβάνει την Ca++-καλμοδουλίνη και Src- εξαρτώμενη ενεργοποιήση της PyK2 ( proline-nch tyrocine kinase 2) (Heidinger et al., 2002). Με άλλα λόγια, οι mglur5 και NMDA υποδοχείς, είναι στενοί συνεργάτες, οπότε η ρύθμιση της δραστηριότητας των mglur5 υποδοχέων επηρεάζει τις NMDA-επαγόμενες απαντήσεις. 53
54 . Εικόνα 25: Σχηματική να αναπαράσταση της κατασκευής των μεταβοτροπικών υποδοχέων του γλουταμινικού οξέος ( mglur5) και του πιθανού μοντέλου ενδοκυττάριας αλληλεπίδρασής τους με N-methyl-D-aspartate (NMDA) υποδοχείς και με την πρωτεϊνική κινάση C (PKC) Σηματοδοτικό μονοπάτι ενεργοποίησης του group Ι mglur, ανεξάρτητο από την ενεργοποίηση των G- πρωτεϊνών Αν και η πλειονότητα των ενδοκυττάριων σηματοδοτικών γεγονότων που συμβαίνουν από την ενεργοποίηση των μεταβοτροπικών υποδοχέων εξαρτάται από τη ρύθμιση της ανταλλαγής των GTP/GDP στις ετερομερείς G-πρωτεΐνες, έχει γίνει γνωστό ότι οι υποδοχείς αυτοί, μπορούν να δεσμεύονται και με άλλους ενδοκυττάριους παράγοντες, γεγονός που μπορεί να οδηγήσει σε ορισμένες περιπτώσεις σε σηματοδοτικά μονοπάτια διαφορετικά από αυτά που ενεργοποιούνται από τις G- πρωτεΐνες ( Hall et al., 1999, Hall et al., 2000). Ένας τέτοιος πιθανός μηχανισμός σε ιπποκάμπειους πυραμιδικούς νευρώνες έχει πρόσφατα χαρακτηριστεί. Μια ανάλυση των σηματοδοτικών μηχανισμών που συνδέει την ενεργοποίηση των mglur1 με τη ρύθμιση των διεγερτικών μετασυναπτικών ρευμάτων, παρουσιάζει αποδείξεις της συμμετοχής της οικογένειας 54
55 των Src-non receptor tyrocine kinase. Oι mgiu1a, mglur5a και mglu5b υποδοχείς, περιλαμβάνουν μέσα στις μεγάλες τους καρβοξυτελικές ουρές, περιοχές πλούσιες στο αμινοξύ προλίνη, στις οποίες οι c-src κινάνες μπορούν να επιδράσουν (Heuss and Gerber, 2000). Ένα από πρώτα σηματοδοτικά μονοπάτια που διαπιστώθηκε ότι ενεργοποιούνται από τους GPCRs και είναι ανεξάρτητα από την ενεργοποίηση των G- πρωτεϊνών, ήταν αυτό των GRKs ( G-protein-coupled receptor kinases). Συγκεκριμένα έχει δηχθεί ότι, η φωσφορυλίωση των μεταβοτροπικών υποδοχέων από τις κινάσες των υποδοχέων των G-πρωτεινών και εν συνεχεία από τη β- αρεστίνη (β-arrestin), όχι μόνο εμποδίζει την περαιτέρω ενεργοποίηση των μεταβοτροπικών υποδοχέων από τις G- πρωτεΐνες, αλλά μπορεί να οδηγήσει και στην ενεργοποίηση ενός εναλλακτικού σηματοδοτικού μονοπατιού ενεργοποίησης των ΜΑΡΚ κινασών ( mitogen-activated protein kinases, ΜΑΡΚ) (Lefkowitz,1998 ). H σύνδεση των μεταβοτροπικών υποδοχέων με το σηματοδοτικό μονοπάτι των ΜΑΡΚ κινασών ενδεχομένως γίνεται μέσω του σηματοδοτικού μονοπατιού των c- Src κινασών, όπως και σε άλλα μέλη της οικογένειας των GPCRs ( Luttrell et al., 1999). Έτσι, φαίνεται ότι οι group Ι mglurς ενεργοποιούν το μονοπάτι της ΕRK ½ κινάσης ( Peavy and Conn,1998, Schinkmann et al., 2000, Karim et al., 2001) και αλληλεπιδρούν με αρεστίνες (Mundell et al., 2001). Παρότι άλλα σηματοδοτικά μονοπάτια, μέσω ενεργοποίησης των G (i) πρωτεινών, έχουν ενοχοποιηθεί για την ενεργοποίηση του μονοπατιού των ΜΑΡΚ κινασών από τους group Ι mglurs (Ferraguti et al.,1999), έχει ενδιαφέρον η μελέτη ανεξάρτητων από G- πρωτεΐνες, σηματοδοτικών μονοπατιών Αλληλεπίδραση των group I mglur με Homer πρωτεΐνες Μια διαφορετική οικογένεια πρωτεϊνών έχει χαρακτηρισθεί με τα μέλη της να περιλαμβάνουν μία ή περισσότερες PDZ (post synaptic density (PSD)- 95, Discslarge, Zona occludens-1) περιοχές. Οι PDZ περιοχές, διαμεσολαβούν ώστε να πραγματοποιηθούν αλληλεπιδράσεις ανάμεσα σε πρωτεΐνες που περιλαμβάνουν PDΖ-περιοχές και σε μια σειρά πρωτεϊνών που περιλαμβάνουν κοντές αλληλουχίες αμινοξέων, συχνά εμφανιζόμενες στα ακραία καρβοξυτελικά τους άκρα. Στους νευρώνες, οι πρωτεΐνες που περιλαμβάνουν PDΖ περιοχές, συχνά εντοπίζονται στο μετασυναπτικό ικρίωμα (PSD), όπου πιστεύεται ότι διαδραματίζουν κεντρικό ρόλο στην οργάνωση διαφόρων διακυτταρικών σηματοδοτικών μηχανισμών, με το να 55
56 σχηματίζουν άμεσους ή έμμεσους φυσικούς συνδαιτυμόνες ανάμεσα σε επιφανειακούς υποδοχείς, σε ιοντικούς διαύλους και σε διάφορα καίρια σηματοδοτικά σημεία ( Scannevin and Huganir, 2000). Αυτή η αλληλεπίδραση φαίνεται ότι είναι σημαντική όχι μόνο για τη συναπτική κατανομή και χαρακτηρισμό των NMDA-υποδοχέων, αλλά και για τη φυσική αλληλεπίδραση τους με άλλες πρωτεΐνες (Kim et al.,1996). Όπως έχει προαναφερθεί, οι group I mglurs φαίνεται ότι εμφανίζουν χαρακτηριστική μετασυναπτική κατανομή στη μεμβράνη των γλουταμινεργικών συνάψεων. Μια ιδέα για το πώς μπορούν να ασκούν οι υποδοχείς αυτοί τις μετασυναπτικές τους δράσεις, δόθηκε από την ανακάλυψη των Homer πρωτεϊνών (Brakeman et al., 1997, Kato et al.,1998). Ο χαρακτηρισμός του πρώτου μέλους της οικογένειας (Homer 1a) ακολουθήθηκε ταχέως από την κλωνοποίηση τριών διαφορετικών γονιδίων (Homer 1-3), τα οποία μπορούν να οδηγήσουν στη γένεση πολλών ισομορφών του Homer. Οι πρωτεΐνες Homer διακρίνονται σε δύο ομάδες: α) στην μακριά κατασκευή όπου υπάρχουν coiled-coil δομές (cc) που επιτρέπουν ομοκαι έτερο-διμερισμό και β) στις κοντές μορφές όπου λείπει η cc κατασκευή ( Xiao et al.,1998, Soloviev et al., 2000). Στους νευρώνες οι cc Homer εκφράζονται σημαντικά ως Homer1 b/ c, Cupidin/ Homer2a/d, Homer3a/b, ενώ η κοντύτερη μορφή που ελέγχεται από το πρώιμο γονίδιο IEG ρυθμίζεται από την νευρωνική δραστηριότητα (Shiraishi et al., 2004). Οι Homer πρωτεΐνες διαθέτουν μια PDΖ περιοχή και μια EVH1 (Ena/VasP homology) περιοχή, που όπως φαίνεται αλληλεπιδρούν με τους group I μεταβοτροπικούς υποδοχείς ( εικόνα 26). Έτσι, οι Homer πρωτεΐνες δεσμεύονται σε μια περιοχή πλούσια στο αμινοξύ προλίνη των μακριών καροξυτελικών ουρών των mglur1/5 υποδοχέων. Η αλληλουχία δέσμευσης των Homer πρωτεϊνών, όπως αυτή έχει αναδειχθεί από γενετικές μελέτες είναι η PPXXFR (Tu et al., 1997) και είναι παρούσα στους mglur5 υποδοχείς (και στα δύο προϊόντα εναλλακτικού ματίσματος) και στον mglur1a αλλά είναι απούσα στα «κοντά» προϊόντα εναλλακτικού ματίσματος των mglur1 ισομορφών. Αν και οι Homer πρωτεΐνες περιλαμβάνουν μια μοναδική EVH1 περιοχή στο αμινοτελικό τους άκρο που επιτρέπει μια μοναδική επαφή με την αλληλεπιδρώσα πρωτεΐνη, η πλειοψηφία των Homer ισομορφών περιλαμβάνει επίσης μια coiled-coil περιοχή στο καρβοξυτελικό άκρο, που επιτρέπει την αυτοένωσή τους ( Solovievet al., 2000, Xiao et al., 1998). Αυτή η ένωση φαίνεται ότι διαδραματίζει σημαντικό ρόλο και επιτρέπει τον ομο-και-ετερο διμερισμό των 56
57 Homer πρωτεϊνών και έτσι την αλληλεπίδραση των μεταβοτροπικών υποδοχέων με άλλες ενδοκυττάριες πρωτεΐνες ( Πίνακας 3). Οι διμερισμένες Homer πρωτεΐνες έχει δειχθεί ότι δεσμεύουν τους group I mglurs στους InSP3 υποδοχείς και έτσι συμμετέχουν στην ενδοκυττάρια ρύθμιση της απελευθέρωσης των Ca ++ από το ενδοπλασματικό δίκτυο ( Tu et al., 1998) ( εικόνα 26). Η ικανότητα λοιπόν, των cc- Homer πρωτεϊνών να πολυμερίζονται και του Homer 1a να διακόπτει τις cc-homer αλληλεπιδράσεις με τους συνεργάτες του, καθορίζει το σημαντικό ρόλο των Homer πρωτεϊνών στη ρύθμιση των mglur-εξαρτώμενων καναλιών Ca ++. Οι Homer πρωτεΐνες μπορούν επίσης να συνδέουν τους μεταβοτροπικούς υποδοχείς με τους NMDA μέσω συμμετοχής των Shank πρωτεϊνών (Tu et al., 1999, Husi et al., 2000)( Εικόνα 26). Οι Homer πρωτεΐνες ρυθμίζουν τις κυτταρικές απαντήσεις από την ενεργοποίηση των mglur5 υποδοχέων, ρυθμίζοντας την ικανότητα του υποδοχέα να δεσμεύεται σε N-type κανάλια Ca ++ και Μ-type κανάλια Κ + ( Kammermeier et al., 2000). Επιπλέον, οι Homer πρωτεΐνες δεσμεύουν τους mglur5 στις Akt πρωτεΐνες μέσω ενός μηχανισμού που περιλαμβάνει την ενεργοποίηση της φωσφοινοσιτόλη κινάση-3 ( phosphoinosited 3-kinase, Pl3K), φωσφοινοσιτόλη- εξαρτώμενη κινάση 1 (phosphoinosited-dependent kinase 1, PDK1) και του P13K ενεργοποιητή ( PIKE ) ( Rong et al., 2003, Hou et al., 2004). Η ενεργοποίηση του mglur1 συνεπάγεται το σχηματισμό του λειτουργικού συμπλόκου mglur1-homer-iplke που οδηγεί στην ενεργοποίηση της Akt και αναστέλλει την κυτταρική απόπτωση (Rong et al., 2003). 57
58 Εικόνα 26: Οι πρωτεΐνες Homer συνδέουν τους group ImGluRs με μία πληθώρα ενδοκυττάριων σηματοδοτικών μονοπατιών. Οι Homer πρωτείνες είναι σημαντικές ως αλληλεπιδρώντες παράγοντες με τους group I mglurs, καθώς πολυμερίζονται και συνδέουν τους μεταβοτροπικούς υποδοχείς με διαφορετικά σηματοδοτικά μονοπάτια. Συγκεκριμένα η δέσμευσή τους με IP3 και με Ryanodine receptors, επηρεάζει την κινητική του ασβεστίου. Επίσης, συμβάλλουν στην αλληλεπίδραση των mglurs με τους NMDA υποδοχείς, καθώς οι Homer πρωτείνες αλληλεπιδρούν με Shank πρωτεΐνες, και πρωτεΐνες του μετασυναπτικού ικριώματος όπως οι GKAP, PSD 95, mglurs και NMDA. Σε συνδυασμό με τα παραπάνω, η ενεργοποίηση των mglur1/5 μπορεί να οδηγήσει στην ενεργοποίηση του σηματοδοτικού μονοπατιού της ERK1/2 κινάσης, το οποίο είναι σημαντικό για τη κυτταρική ανάπτυξη, διαφοροποίηση και επιβίωση (Choe et al., 2001, Mao et al., 2005 ). Η mglur5 επαγόμενη ενεργοποίηση της ERK1/2 κινάσης σε νευρώνες ραβδωτού πραγματοποιείται σαν συνέπεια της InSP3- εξαρτώμενης απελευθέρωσης Ca ++, της ενεργοποίησης των Homer πρωτεϊνών και της Pyk2 (Mao et al., 2005, Nicodemo et al., 2010). O ακριβής μηχανισμός μέσω του οποίου ο Homer συνδέει τους mglurs με το σηματοδοτικό μονοπάτι της ERK ½ κινάσης είναι αγνωστος, έχει όμως δειχθεί ότι η συνενεργοποίηση των NMDA και mglur5 υποδοχεών στους νευρώνες, οδηγεί στην συνεργιστική ενεργοποίηση του μονοπατιού της ERK1/2 κινάσης, μέσω μηχανισμού που περιλαμβάνει τη αλληλεπίδραση μεταξύ του PSD-95 των NMDA υποδοχέων και του Homer των mglur1/5 και είναι ανεξάρτητος από το ασβέστιο (Yang et al., 2004). Το 58
59 ενδιαφέρον είναι ότι ο Homer είναι σημαντικός για την mglur5-επαγόμενη ενεργοποίηση του μονοπατιού της ERK1/2 στο ραβδωτό, αλλά όχι στον ιππόκαμπο (Tappe et al., 2006, Ronesi et al., 2008). Σε CHO κύτταρα, η ενεργοποίηση των mglur5 ενεργοποιεί την ERK1/2 κινάση μέσω μηχανισμού που εξαρτάται από το Ca ++ ( Thandi et al., 2002). Σε αστροκύτταρα φλοιού, η δέσμευση των mglur5 στον επιδερμικό αυξητικό παράγοντα (Epidermal Growth Factor, EGF) συνεπάγεται την ενεργοποίηση της ERK ½ ( Peavy et al., 2001). Αυτό το σηματοδοτικό μονοπάτι περιλαμβάνει την ενεργοποίηση των Cβγ υπομονάδων και των Src κινασών τυροσίνης και είναι ανεξάρτητο της ενεργοποίησης των σηματοδοτικού μονοπατιού των PLC/PKC/ Ca ++ ( Luttrell et al., 1997). Επιπλέον, η ενεργοποίηση των mglur1/5 οδηγεί στη φωσφορυλίωση και αναστολή της πρωτεϊνικής φωσφατάσης PP2A η οποία είναι υπεύθυνη για την αποφωσφορυλίωση και την απενεργοποίηση της ERK ½ κινάσης ( Μao et al., 2005 ). Αυτός φαίνεται ότι είναι ο μηχανισμός ενεργοποίησης της ERK μέσω των mglur1/5. Προσφάτως έχει παρατηρηθεί ότι η PyK2 δέσμευση στην δεύτερη ενδοκυττάρια αγκύλη και στο καρβοξυτελικό άκρο των mglur1α προκαλεί την αποδέσμευση του υποδοχέα από την ασβεστιοεξαρτώμενο InSP3 μονοπάτι (Nicodemo et al., 2010). Το σηματοδοτικό μονοπάτι που ενεργοποιείται στην περίπτωση αυτή και συνεπάγεται τη φωσφορυλίωση της ERK1/2 κινάσης, είναι εξαρτώμενο από την ενεργοποίηση των Src κινασών, της καλμοδουλίνης και της PKC (Meli et al., 2005). 59
60 ΠΙΝΑΚΑΣ 3: Ενδοκυττάριες πρωτεΐνες που αλληλεπιδρούν με τους group I mglur 2.6 Φαρμακολογία του group I μεταβοτροπικών υποδοχέων Οι φαρμακολογικοί προσδέτες των mglurs μπορούν να διακριθούν σε ανταγωνιστικούς (competitive) και μη-ανταγωνιστικούς ( non- competitive) προσδέτες. Οι ανταγωνιστικοί προσδέτες, αλληλεπιδρούν με την ορθοστερική περιοχή δέσμευσης, που αποτελεί την περιοχή δέσμευσης του ενδογενούς γλουταμινικού και εντοπίζεται στο αμινοτελικό άκρο των mglurs. Οι μη ανταγωνιστικοί προσδέτες, ή όπως αλλιώς ονομάζονται αλλοστερικοί προσδέτες, δεσμεύονται σε διαφορετικές θέσεις στους mglurs υποδοχείς, που εντοπίζονται στο εξωκυττάριο τμήμα των εφτά διαμεμβρανικών περιοχών. Οι αλλοστερικοί πρόσδετες, εμφανίζουν εγγενή αποτελεσματικότητα, ανεξάρτητα από την παρουσία των ορθοστερικών αγωνιστών και ρυθμίζουν την απάντηση του υποδοχέα σε αυτούς. Διακρίνονται σε θετικούς αλλοστερικούς τροποποιητές ( positive allosteric modulators, PAMs) και αρνητικούς αλλοστερικούς τροποποιητές (negative allosteric modulators, NAMs) ανάλογα με το αν ρυθμίζουν θετικά ή αρνητικά τον υποδοχέα. Δεδομένου ότι οι mglurs, αποτελούν θεραπευτικούς στόχους για πληθώρα 60
61 ψυχιατρικών και νευρολογικών διαταραχών, η αλλοστερική λειτουργίας τους αποτελεί αντικείμενο εκτεταμένης έρευνας. ρύθμιση της 2.7 mglur5:σημαντικός ο ρόλος τους στις γνωστικές λειτουργίες Οι mglur5 εντοπίζονται κατά κύριο λόγο στις περιοχές που ελέγχουν ανώτερες γνωστικές λειτουργίες όπως ο προμετωπιαίος φλοιός, η έλικα του προσαγωγίου, ο ιππόκαμπος, το ραβδωτό, ο διαφραγματικός πυρήνας και ο πλευρικός πυρήνας της αμυγδαλής (Abe et al., 1992, Bell et al., 2002, Romano et al., 1995, Shigemoto et al.,1993). Ο συνδυασμός της κατανομής τους και της αργής ενεργοποίησής τους από G-πρωτεΐνες, φαίνεται ότι αποτελεί τη βάση για την εκλεκτική συμμετοχή τους σε συγκεκριμένες μορφές συναπτικής πλαστικότητας (Lu et al., 1997, Jia et al., 1998, Huber et al., 2000, Bikbaev et al., 2008) και μάθησης (Lu et al., 1997, Chiamulera et al., 2001, Balschun and Wetzel, 2002), ενώ έχει προταθεί η χρησιμοποίησή τους ως θεραπευτικούς παράγοντες σε πληθώρα νευρολογικών διαταραχών ( Brody et al., 2004, Slassi et al., 2005, Marino and Conn, 2006, Dolen et al., 2007). Μελέτες έχουν αναδείξει τον ρόλο των mglur5 σε δύο διαφορετικές μορφές μάθησης, που εντοπίζονται στον ιππόκαμπο και στην αμυγδαλή. Συγκεκριμένα, ενδοφλέβια ( Schulz et al., 2001) ή απευθείας ( Rodrigues et al., 2002) έγχυση στην αμυγδαλή, φαρμακολογικών ανταγωνιστών των mglur5 σε μύες, διαταράσσει την απόκτηση της «απάντησης του φόβου» ( fear response) στους μύες αυτούς σε ανάλογες δοκιμασίες. Oι μύες αυτοί διατηρούσαν την ικανότητα ανάκλησης μνημών φόβου ( Xu et al., 2009), γεγονός που υποδηλώνει ότι είχαν έλλειμμα στην απόκτηση των μνημών αυτών και όχι στη αποθήκευση ή ανάκλησή τους. Ομοίως, knockout μύες για τους mglu5 υποδοχείς, παρουσιάζουν ελλείμματα στη χωρική μάθηση, που εντοπίζεται στον ιππόκαμπο, όπως διαπιστώθηκε σε δοκιμασίες στον υδάτινο λαβύρινθο του Morris ( Lu et al., 1997, Xu et al., 2009 ). Στο πλαίσιο αυτό, φαρμακολογικοί ανταγωνιστές των mglur5, προκαλούν δοσοεξαρτώμενη εξασθένιση της ενεργού μνήμης και χωρικής μάθησης, ( Balschun and Wetzel, 2002, Homayoun et al., 2004, Manahan-vaughan and Schuetz, 2002, Naie and Manahanvaughan, 2004). Πιο πρόσφατες μελέτες, στις οποίες οι mglur5 ρυθμίζονται μέσω αλλοστερικών τροποποίητων τους, ανέδειξαν βελτίωση της γνωστικής επίδοσης των πειραματόζωων σε δοκιμασίες όπως ο υδάτινος λαβύρινθος του Morris, η 61
62 αναγνώριση νέου αντικειμένου (novel object recognition) και η δοκιμασία ελέγχου του χρόνου αντίδρασης σε μια σειρά πέντε επιλογών (five-choise serial reaction time test) ( Ayala et al., 2009, Balschun et al., 2006, Liu et al., 2008). Η συμμετοχή των mglur5 στη ρύθμιση γνωστικών λειτουργιών τους καθιστά αδιαμφισβήτητους θεραπευτικούς στόχους για ένα ευρύ φάσμα ψυχιατρικών και νευρολογικών διαταραχών. Για το λόγο αυτό, η φαρμακολογία τους αποτελεί αντικείμενο έρευνας που στοχεύει κυρίως στους αλλοστερικoύς ρυθμιστές τους (Bear et al., 2004, Kewn et al., 2004, Shipe et al.,2005). Δηλαδή σε παράγοντες που ενισχύουν ή εμποδίζουν την δράση των ορθοστερικών αγωνιστών των mglur5. Αρκετές ηλεκτροφυσιολογικές μελέτες έχουν καταδείξει στοιχεία για τον τρόπο με τον οποίο οι mglur5 υποδοχείς μπορούν να ρυθμίσουν τις γνωστικές λειτουργίες. Καταρχάς, η ενεργοποίηση των mglur5 υποδοχέων προκαλεί άμεση διεγερτική νευροδιαβίβαση, καθώς παράγονται διεγερτικά μετασυναπτικά δυναμικά ( EPSPs) σε in vitro πειράματα, στον υποθάλαμο ( Awad et al.,2000), στον ιππόκαμπο ( Fitzjohn et al.,1999) και στη μέλαινα ουσία ( Marino et al.,2001). Η ικανότητα των mglur5 υποδοχέων να επάγουν διεγερσιμότητα έχει συνδεθεί με την ασβέστιο-εξαρτώμενη μείωση της αγωγιμότητας των ιόντων Καλίου και τη συσσώρευση ενδοκυττάριου ασβεστίου στον ιππόκαμπο ( Μannaioni et al., 2001). Μια άλλη άμεση διεγερτική επίδραση των mglur5 υποδοχέων έχει περιγραφεί σε τομές ιπποκάμπου που έχουν παρασκευαστεί με ανταγωνιστές του γ- αμινοβουτυρικού οξέος (GABA), όπου η δραστηριότητα τους οδηγεί σε συνεχή ρυθμό διέγερσης των νευρώνων (Lee et al.,2002, Merlin,2002, Stoop et al.,2002). Νεώτερα βιβλιογραφικά δεδομένα υποδεικνύουν τη συμμετοχή των mglur5 υποδοχέων στην παράταση της διεγερτικής δραστηριότητας. Η δράση τους αυτή είναι πιθανό να συμβάλλει στη ρύθμιση των γνωστικών λειτουργιών υπό φυσιολογικές συνθήκες, όπου ο τετανικός ερεθισμός ( bursting) αποτελεί σημαντική μορφή διαβίβασης της πληροφορίας ανάμεσα στα νευρωνικά δίκτυα. Η διαταραχή του μηχανισμού που ρυθμίζει την δραστηριότητα των mglur5 οδηγεί σε σοβαρά γνωστικά ελλείμματα όπως υποδεικνύεται από πρόσφατα προκλινικά και κλινικά δεδομένα. Χαρακτηριστικό παράδειγμα αποτελεί το σύνδρομο του εύθραυστου Χ (Fragile X syndrome) που οδηγεί σε βαριάς μορφής νοητική υστέρηση εξαιτίας υπερβολικής διεγερσιμότητας των mglur5 από εξασθένιση του ρυθμιστικού μηχανισμού τους ( Bear, 2005, Chuang et al., 2005). 62
63 Οι mglur5 υποδοχείς φαίνεται να συμμετέχουν και στους μηχανισμούς συναπτικής πλαστικότητας που αποτελούν τα κυτταρικά υποστρώματα για τις διαδικασίες μάθησης και μνήμης. Πλέον, η συμμετοχή τους σε μορφές συναπτικής πλαστικότητας όπως η μακροχρόνια ενδυνάμωση ( long-term potentiation, LTP) ή καταστολή ( long-term depression,ltd), είναι καλά χαρακτηρισμένη σε διάφορες περιοχές του εγκεφάλου. Στον ιππόκαμπο, η δράση των mglur5 είναι σημαντική για την παραγωγή του LTP όπως φαίνεται σε in vitro ( Behnisch and Reymann,1993, Camodeca et al., 1999, Jia et al.,1998, Lu et al., 1997, Νeyman and Manahan- Vaughan, 2008) και in vivo πειράματα ( Balschun and Wetzel, 2002, Bikbaev et al., 2008, Manahan Vaughan and Braunewell, 2005, Naie and Manahan-Vaughan, 2004). Έτσι, οι mglur5-knockout μύες παρουσιάζουν εξασθένιση του LTP στην CΑ1 περιοχή του ιπποκάμπου, όπως φαίνεται στις διάφορες διαγνωστικές δοκιμασίες ( Lu et al.,1997). Η χορήγηση ανταγωνιστών των mglur5 υποδοχέων οδηγεί στην εξασθένηση της χωρικής μνήμης και της μνήμης ενεργείας, ως αποτέλεσμα της εξασθένισης του ιπποκάμπειου LTP και του μειωμένου επιπέδου έκφρασης των υποδοχέων αυτών (Manahan Vaughan and Braunewell, 2005). Βέβαια, οι mglur5 υποδοχείς φαίνεται ότι διαδραματίζουν καθοριστικό ρόλο και στην επαγωγή του ιπποκάμπειου LTD ( Faas et al.,2002, Gasparini et al., 1999, Huang and Hsu, 2006, Huber et al., 2001). Στην αμυγδαλή η επαγωγή του LTP και ο επακόλουθος σχηματισμός των μνημών του φόβου, εξαρτώνται από την τονική ενεργοποίηση των mglur5 υποδοχέων ( Fendt and Schhmid, 2002, Rodrigues et al., 2002). Άλλωστε, μια νέα μορφή LTP έχει προσφάτως χαρακτηριστεί στον νεοφλοιό που είναι ανεξάρτητη από την ενεργοποίηση των NMDA υποδοχέων και εξαρτάται κατά κύριο λόγο από την ενεργοποίηση των mglur5 υποδοχέων (Sourdet et al, 2003, Wang and Daw, 2003). Στην εξασθένιση αυτού του μηχανισμού φαίνεται να οφείλεται η έκπτωση των γνωστικών λειτουργιών που παρατηρείται σε knockout μύες για την πρωτεΐνη FMRP, που αποτελούν τα πειραματικά μοντέλα για το σύνδρομο του εύθραυστου Χ ( Wilson and Cox, 2007). Ο ρόλος των mglur5 στη συναπτική πλαστικότητα φαίνεται να διαμεσολαβείται τουλάχιστον εν μέρει, από μοριακά μονοπάτια όπως αυτά των ΕPΚ1/2 κινασών και του CREB ( Liu et al.,2006, 2008, Mao et al., 2008). Η ρύθμιση των μονοπατιών αυτών, που είναι σημαντική για τις διαδικασίες μνήμης και μάθησης, ενδεχομένως να υπόκειται στην ομαλή λειτουργία των mglur5 υποδοχέων. 63
64 Εκτός από την άμεση επίδραση των mglur5 υποδοχέων στην συναπτική διεγερσιμότητα, in vitro μελέτες αναδεικνύουν τον καθοριστικό τους ρόλο στην ρύθμιση των NMDA εξαρτώμενων απαντήσεων ( Pisani et al., 1997). Σε τομές ραβδωτού, ο ειδικός αγωνιστής των mglur5, CHPG ρυθμίζει την NMDAεπαγόμενη εκπόλωση της μεμβράνης. Η επίδραση του CHPG είναι απούσα σε τομές όπου έχουν προ-παρασκευαστεί με τον μη ειδικό ανταγωνιστή των mglur5, ΜΡΕΡ και σε mglur5-knockout μύες (Pisani et al., 2001). Έτσι οι mglur5 αγωνιστές μειώνουν, ενώ οι ανταγωνιστές ενισχύουν τις NMDA-επαγόμενες εκπολώσεις ( Attucci et al., 2001). Οι mglur5 φαίνεται να συμμετέχουν επίσης στην επαγωγή των NMDA-εξαρτώμενων ρευμάτων στον ιππόκαμπο ( Doherty et al.,1997, Mannaioni et al., 2001). Η αλληλεπίδραση λοιπόν των mglur5 και NMDA υποδοχέων είναι αδιαμφισβήτητη και φαίνεται να περιλαμβάνει πολλαπλά ενδοκυττάρια μονοπάτια. Σε αυτά συμπεριλαμβάνονται το μονοπάτι της πρωτεϊνικής κινάσης C (Alagarsamy et al, 1999, Mao and Wang, 2002a,b), της ERK1/2 κινάσης (Yang et al., 2004) και του CREB ( Mao and Wang, 2002a). Συγχρόνως η λειτουργική αλληλεπίδραση των υποδοχέων αυτήν μπορεί να περιλαμβάνει cross talk μεταξύ πρωτεϊνών όπως οι homer, στο μετασυναπτικό ικρίωμα ( Ango et al., 2000, 2001, Yang et al., 2004.) H πληθώρα των επιδράσεων των mglur5 στην τονική διεγερσιμότητα, στην συναπτική πλαστικότητα και στη λειτουργία των NMDA υποδοχέων, τους καθιστά απαραίτητους στη διατήρηση της νευρωνικής δραστηριότητας. Έτσι η ρύθμιση της λειτουργίας τους μπορεί να οδηγήσει σε θεραπευτικές προσεγγίσεις για τη σχιζοφρένεια και για άλλες καταστάσεις που σχετίζονται με παθολογική γλουταμινεργική δραστηριότητα. 64
65 3. NMDA ΥΠΟΔΟΧΕΙΣ: ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ Όπως έχει ήδη αναφερθεί, οι ιοντοτρόποι υποδοχείς του γλουταμινικού οξέος με βάση το διαφορετικό φαρμακολογικό τους προφίλ, μπορούν να διακριθούν στους N-methyl-D-aspartate (NMDA) υποδοχείς, a-amino-3-hydroxy-5-methyl-4-isoxazole propionate (AMPA) υποδοχείς και στους υποδοχείς του καϊνικού οξέος ( Dingledine et al., 1999) (Εικόνα 27). Οι υποδοχείς αυτοί, πραγματοποιούν την πλειονότητα της διεγερτικής νευρωνικής νευροδιαβίβασης στον εγκέφαλο και παίζουν σημαντικό ρόλο στη ρύθμιση της συναπτικής δραστηριότητας. Εικόνα 27: Οι τρεις κατηγορίες ιοντοτροπικών υποδοχέων του γλουταμινικού οξέος: N- methyl-d-aspartate (NMDA) υποδοχείς, υποδοχείς του καϊνικού οξέος και a-amino-3- hydroxy-5-methyl-4-isoxazole propionate (AMPA) υποδοχείς ( Bear et al,2007). Οι NMDA υποδοχείς είναι δίαυλοι ιόντων με υψηλή διαπερατότητα στο ασβέστιο, που παίζουν σημαντικό ρόλο σε πολλούς τομείς της βιολογίας των ανώτερων οργανισμών. Είναι σημαντικοί για την ανάπτυξη του ΚΝΣ, για τις διαδικασίες που συμμετέχουν στην μνήμη και τη μάθηση και στην πλαστικότητα του εγκεφάλου. Εξαιτίας της σημαντικής δράσης των υποδοχέων αυτών, φαίνεται ότι η διαταραχή στην έκφραση ή στην λειτουργία τους, εμπλέκεται σε μια πληθώρα νευρολογικών διαταραχών και παθολογικών νοσημάτων. Η υπολειτουργία των NMDA υποδοχέων σχετίζεται με γνωστικά ελλείμματα, ενώ η υπερλειτουργία τους προκαλεί τοξικότητα και εκφυλισμό των νευρώνων του ΚΝΣ. Για το λόγο αυτό, οι NMDA υποδοχείς αποτελούν θεραπευτικούς στόχους για πλήθος νευρολογικών 65
66 διαταραχών όπως η νόσος Alzheimer, η νόσος Parkinson και η σχιζοφρένεια (Cull- Candy et al., 2001; Waxman and Lynch,2005), ενώ φαίνεται ότι εμπλέκονται επίσης στην παθοφυσιολογία του αγγειακού εγκεφαλικού επεισοδίου, της ισχαιμίας, σε αγχώδεις διαταραχές και αλλού. Μολονότι προς το παρόν η χρησιμοποίηση των NMDA υποδοχέων σαν θεραπευτικούς στόχους ( Farlow MR, 2004), είναι περιορισμένη εξαιτίας των πολλαπλών παρενεργειών που συνεπάγεται η χορήγηση τους, όπως ψευδαισθήσεις, κατατονία,αταξία, διαταραχές μνήμης, εφιάλτες, εντούτοις η φαρμακολογία των NMDA υποδοχέων αποτελεί ένα πεδίο στο οποίο η έρευνα συνεχίζεται ( Kemp JA et al., 2002, Wood PL, 2005). Η κατανόηση των μηχανισμών ενεργοποίησής τους και των βιολογικών γεγονότων που αυτή συνεπάγεται, μπορεί να οδηγήσει στην παραγωγή φαρμακευτικών σκευασμάτων που στοχεύουν ειδικά τους υποτύπους των NMDA υποδοχέων και μεταβάλλουν τη λειτουργία τους σε ένα καλά καθορισμένο βαθμό. Οι υποδοχείς NMDA έχουν τέσσερις μοναδικές ιδιότητες. Πρώτον, ο δίαυλος αυτός είναι ο μοναδικός ανάμεσα στους διαύλους που ελέγχονται από νευροδιαβιβαστές που εκτός από χημειοελεγχόμενος, είναι ταυτόχρονα και τασεοελεγχόμενος. Στο δυναμικό ηρεμίας, το στόμιο του διαύλου- υποδοχέα NMDA φράσσεται από ένα μαγνήσιο (Mg 2+ ) του εξωκυτταρικού χώρου, με αποτέλεσμα να μην συμβάλλει σχεδόν καθόλου στο φυσιολογικό συναπτικό δυναμικό (Εικόνα 28). Όταν όμως η μεμβράνη εκπολώνεται με παρουσία γλουταμινικού, το Mg 2+ εκτινάσσεται από το στόμιο του διαύλου με ηλεκτροστατική απώθηση, επιτρέποντας την είσοδο ιόντων Na + και Ca 2+ (Cull-Candy et al., 2001). Δεύτερον, ο υποδοχέας ελέγχει ένα δίαυλο κατιόντων μεγάλης αγωγιμότητας, ο οποίος είναι διαπερατός από τα Ca 2+, Na + και Κ +. Τρίτον, η είσοδος ιόντων ασβεστίου διαμέσου του διαύλου που ενεργοποιείται από το NMDA ενεργοποιεί ασβεστιοεξαρτώμενους καταρράκτες μεταγωγής σήματος. Τέταρτον, ο δίαυλος λειτουργεί μόνο με παρουσία γλυκίνης, της οποίας η πρόσδεση στον υποδοχέα γίνεται πριν την ενεργοποίησή του. 66
67 Εικόνα 28: NMDA υποδοχέας: περιλαμβάνει θέσεις δέσμευσης για το γλουταμινικό οξύ και για την γλυκίνη, όπως επίσης και για ιόντα Mg 2+ εντός του διαύλου. Όταν η μεμβράνη είναι υπερπολωμένη, η ηλεκτρική κινητήριος δύναμη σπρώχνει το κατιόν του Mg 2+ μέσα στον δίαυλο, μπλοκάροντας τον υποδοχέα. 3.1 Συναπτική λειτουργία Κατά τη διάρκεια της φυσιολογικής συναπτικής διαβίβασης απελευθερώνεται γλουταμινικό οξύ από τις προσυναπτικές απολήξεις, ενεργοποιώντας τους μη- NMDA υποδοχείς (AMPA, καϊνικού οξέος), με αποτέλεσμα ιόντα Na + και Κ + να διέρχονται διαμέσου των μη- NMDA υποδοχέων, εκπολώνοντας την μετασυναπτική μεμβράνη ( Εικόνα 29). Η ενεργοποίηση των AMPA υποδοχέων είναι ταχεία και παροδική, προκαλώντας σύντομες εκπολώσεις που δεν διαρκούν περισσότερο από μερικά κλάσματα του δευτερολέπτου. Δεν συμβαίνει το ίδιο και με τους NMDA υποδοχείς, οι οποίοι βρίσκονται κοντά με τους AMPA υποδοχείς στις δενδριτικές άκανθες (Kandel et al., 2000) ( Εικόνα 29), διότι το Mg 2+ αποκλείει τους διαύλους αυτούς, όταν το δυναμικό βρίσκεται σε κατάσταση ηρεμίας. Τα ιόντα Mg 2+ ιόντα είναι παρόντα στο εξωτερικό περιβάλλον των νευρώνων, σε μεγαλύτερες 67
68 συγκεντρώσεις σε σχέση με το ενδοκυττάριο περιβάλλον, με αποτέλεσμα την καθαρή προς τα έσω κινητήρια δύναμη των ιόντων σε κατάσταση ηρεμίας. Όταν, όμως, η μετασυναπτική μεμβράνη εκπολώνεται από τις δράσεις των μη- NMDA υποδοχέων, το Mg 2+ απομακρύνεται από το δίαυλο του NMDA υποδοχέα, με αποτέλεσμα να επιτρέπεται η δίοδος ιόντων Na + και Κ +, αλλά κυρίως Ca 2+ μέσω του διαύλου (Kandel et al., 2000) ( Εικόνα 30). Έτσι, μέσω της αργής απόκρισής τους στο γλουταμινικό οξύ οι NMDA υποδοχείς παράγουν ένα αργό, καθυστερημένο συναπτικό ρεύμα, το οποίο παρατείνει την διάρκεια του διεγερτικού μετασυναπτικού δυναμικού. Θα λέγαμε λοιπόν ότι οι NMDA υποδοχείς λειτουργούν ως μοριακοί ανιχνευτές δύο ξεχωριστών γεγονότων, που πρέπει όμως να συμβούν ταυτόχρονα ώστε να ενεργοποιηθεί ο υποδοχέας και να επιτραπεί η είσοδος ιόντων στο κύτταρο, της συναπτικής απελευθέρωσης του γλουταμινικού και της εκπόλωσης της μετασυναπτικής μεμβράνης. Αυτή η διπλή απαίτηση εισόδου, σε συνδυασμό με την αργή ενεργοποίησή και απενεργοποίησης τους, επιτρέπει στους NMDA υποδοχείς να ενσωματώσουν και να αποκωδικοποιούν τα εισερχόμενα στη σύναψη μηνύματα (Antonius M Van Dongen., 2009). Το γεγονός της εισόδου Ca 2+ στο μετασυναπτικό νευρώνα, είναι ιδιαίτερα σημαντικό καθώς έχει ως αποτέλεσμα την ενεργοποίηση ασβέστιο-εξαρτώμενων μονοπατιών μεταγωγής σήματος που συντελούν στο φαινόμενο της μακροχρόνιας ενδυνάμωσης της συναπτικής δύναμης (LTP) ( Εικόνα 30). Το φαινόμενο αυτό μπορεί να επιτευχθεί με τη σύντομη και έντονη συναπτική ενεργοποίηση και πρωτοπεριγράφθηκε στον ιππόκαμπο (Bliss and Lomo, 1973). Στην επαγωγή του φαινομένου αυτού κρίσιμο ρόλο παίζουν οι NMDA υποδοχείς, εξαιτίας της εισροής των ιόντων Ca 2+, το οποίο προκαλεί τη διαρκή ενίσχυση της συναπτικής διαβίβασης, μέσω της ενεργοποίησης ασβέστιο-εξαρτώμενων σηματοδοτικών μονοπατιών (Kandel et al., 2000). 68
69 Εικόνα 29: Οι υποδοχείς του γλουταμινικού οξέος στις διεγερτικές συνάψεις. Εικόνα 30: Ο ιοντικός δίαυλος των NMDA υποδοχέων μπορεί να ανοίξει μόνον εφόσον εκπολωθεί η μετασυναπτική μεμβράνη από τους AMPA υποδοχείς. Η εκπόλωση αυτή απομακρύνει τα ιόντα Mg 2+ επιτρέποντας έτσι τη ροή ρεύματος στο μετασυναπτικό κύτταρο. Το γεγονός αυτό επιτρέπει την είσοδο Ca 2+ στο μετασυναπτικό νευρώνα που πυροδοτεί την παραγωγή LTP ( Nicoll et al, 1988) 69
70 3.2 Υπότυποι Πολλοί ξεχωριστοί υπότυποι του υποδοχέα NMDA έχουν αναγνωριστεί στους νευρώνες του κεντρικού νευρικού συστήματος, οι οποίοι διαφέρουν όσον αφορά στην ευαισθησία τους σε ενδογενή και εξωγενή προσδέματα, στην διαπερατότητα και τον αποκλεισμό από δισθενή ιόντα, στις κινητικές ιδιότητες και στην αλληλεπίδραση με ενδοκυττάριες πρωτεΐνες. Μέχρι σήμερα έχουν χαρακτηριστεί τρεις οικογένειες γονιδίων (NR1, NR2 και NR3), οι οποίες κωδικοποιούν υπομονάδες του NMDA υποδοχέα (Cull -Candy et al., 2001). Η υπομονάδα NR1 υπάρχει σε οκτώ διαφορετικές ισομορφές εξαιτίας της ύπαρξης τριών διαφορετικών θέσεων εναλλακτικού ματίσματος, μία στο αμινοτελικό και δύο στο καρβοξυτελικό άκρο της πρωτεΐνης. Η υπομονάδα αυτή ανευρίσκεται σε όλον τον εγκέφαλο και είναι απαραίτητη για να δημιουργηθεί λειτουργικός δίαυλος καθώς οι μύες knock-out για την NR1 δεν επιβιώνουν. Στην δεύτερη κατηγορία, ανήκουν τέσσερις υπομονάδες NR2 (Α, Β, C, D). Οι υπομονάδες αυτής της κατηγορίας είναι υπεύθυνες για τις λειτουργικές ιδιότητες του υποδοχέα. Στην τρίτη κατηγορία ανήκουν οι δύο υπομονάδες NR3, οι οποίες δεν έχουν μελετηθεί σε βάθος ( Εικόνα 31). Εικόνα 31. Η ποικιλία των υπομονάδων του υποδοχέα NMDA. (a) Διάγραμμα των υπομονάδων του υποδοχέα NMDA. (b) Αναπαράσταση των πολυπεπτιδίων των υπομονάδων του υποδοχέα NMDA. Τα μαύρα κουτιά υποδεικνύουν τις διαμεμβρανικές περιοχές και τα γκρι την θηλιά επανεισόδου Μ2. Οι C1 και C2 περιοχές αποτελούν σημεία εναλλακτικού ματίσματος. 70
71 Οι λειτουργικοί NMDA υποδοχείς αποτελούν τετραμερείς δομές που αποτελούνται από 2 απαραίτητες για τη λειτουργία του υποδοχέα NR1 υπομονάδες σε συνδυασμό με δύο NR2 υπομονάδες ή σε ορισμένες περιπτώσεις, μια NR2 και μια NR3 υπομονάδα (Cull-Candy and Leszkiewicz, 2004) (Εικόνα 32). Κρυσταλλογραφικά δεδομένα σε συνδυασμό με βιοχημικές και ηλεκτροφυσιολογικές μελέτες υποδεικνύουν ότι το ετεροδιμερές NR1-NR2 αποτελεί τη λειτουργική μονάδα στους τετραμερείς NMDA υποδοχείς ( Furukawa et al., 2005) (Εικόνα 33). Όπως αναφέρθηκε, μια μοναδική ιδιότητα των NMDA υποδοχέων είναι ότι η ενεργοποίηση του υποδοχέα απαιτεί και τη σύνδεση της γλυκίνης, που αποτελεί και συναγωνιστή του γλουταμινικού οξέος ( Erreger et al., 2004). Επομένως, οι λειτουργικοί NMDA υποδοχείς απαιτούν, μια NR1 υπομονάδα, η οποία περιέχει τη θέση δέσμευσης της γλυκίνης και μια NR2 υπομονάδα, στην οποία δεσμεύεται το γλουταμινικό οξύ (Εικόνες 32,33). Επιπλέον του σχηματισμού ετεροδιμερών υποδοχέων (π.χ. NR1/ NR2Β), υπάρχουν ενδείξεις για την ύπαρξη ετεροτριμερών NMDA υποδοχέων (π.χ. NR1/ NR2Α/ NR2Β) (Cull-Candy and Leszkiewicz, 2004). Πολλές ηλεκτροφυσιολογικές μελέτες έχουν δείξει ότι οι NR2 και οι NR3 υπομονάδες προσδίδουν διακριτές ηλεκτροφυσιολογικές ιδιότητες στους NMDA υποδοχέων (Cull-Candy and Leszkiewicz, 2004). Επομένως, διακυμάνσεις στη σύνθεση των υπομονάδων του NMDA υποδοχέα αποτελεί μια σημαντική πηγή ποικιλίας για τη λειτουργική ρύθμιση των NMDA υποδοχέων. Η ακριβής σύνθεση των υπομονάδων του NMDA υποδοχέα ποικίλει στις διάφορες συνάψεις σε διαφορετικά αναπτυξιακά στάδια. Η NR1 υπομονάδα είναι ένα μοναδικό γονιδιακό προϊόν και ως μια ουσιώδης υπομονάδα εκφράζεται ευρέως στον εγκέφαλο. Αντίθετα, οι NR2 υπομονάδες (NR2Α-D) κωδικοποιούνται από τέσσερα διαφορετικά γονίδια που εκφράζονται διαφορετικά στις διάφορες περιοχές του εγκεφάλου, αλλά και κατά την ανάπτυξη. Η ταυτότητα της NR2 υπομονάδας καθορίζει πολλές από τις βιοφυσικές και φαρμακολογικές ιδιότητες των NMDA υποδοχέων και μπορεί επίσης να επηρεάσει το ενδοκυτταρικό μονοπάτι μεταγωγής του σήματος, καθώς και τη διακίνηση των υποδοχέων στην επιφάνεια της μεμβράνης του νευρώνα (trafficking) ( Cull-Candy and Leszkiewicz, 2004). Ανάμεσα στις NR2 υπομονάδες, τα πρότυπα έκφρασης της NR2Α και της NR2Β είναι σχετικά υψηλά και αναπτυξιακά ρυθμιζόμενα, με μια παράλληλη μείωση της έκφρασης της NR2Β και αύξηση της έκφρασης της NR2Α υπομονάδας, καθώς οι νευρώνες ωριμάζουν. Η NR2A υπομονάδα προσδίδει χαμηλότερη συγγένεια για το γλουταμινικό οξύ, 71
72 γρηγορότερη κινητική, μεγαλύτερη πιθανότητα ανοίγματος (open probability) του ιοντικού διαύλου και μεγαλύτερη ασβεστιοεξαρτώμενη απευαισθητοποίηση απ ότι η NR2B υπομονάδα, η οποία προσδίδει πιο αργή κινητική του ιοντικού διαύλου και μειωμένη πιθανότητα ανοίγματος του διαύλου. Η έκφραση της NR2C υπομονάδας περιορίζεται κυρίως στην παρεγκεφαλίδα και εκφράζεται αργότερα κατά την ανάπτυξη. Αντίθετα, η NR2D εκφράζεται κυρίως νωρίς κατά την ανάπτυξη και εντοπίζεται κυρίως στους θαλαμικούς και υποθαλαμικούς πυρήνες, καθώς και στο εγκεφαλικό στέλεχος (Monyer et al., 1994). Οι NR2C και NR2D υπομονάδες χαρακτηρίζονται από χαμηλής αγωγιμότητας ανοίγματα του διαύλου και μειωμένη ευαισθησία στο μπλοκάρισμα από τα ιόντα μαγνησίου ( Cull-Candy and Leszkiewicz, 2004). H NR3A υπομονάδα εκφράζεται ισχυρά νωρίς κατά την ανάπτυξη (Ciabarra et al., 1995; Sucher et al., 1995), ενώ η έκφραση της NR3Β υπομονάδας περιορίζεται κυρίως στους κινητικούς νευρώνες (Chatterton et al., 2002). Οι NR3 υπομονάδες προσδίδουν μειωμένη διαπερατότητα στα ιόντα ασβεστίου και μικρότερη επιφανειακή έκφραση (Cull-Candy and Leszkiewicz, 2004). Οι τυπικοί ενδογενείς NMDA υποδοχείς περιέχουν NR1 και NR2 υπομονάδες, με τις NR3 υπομονάδες να απαντούν μόνο σε υποπληθυσμούς των NMDA υποδοχέων, διαδραματίζοντας ρυθμιστικό ρόλο (Cull-Candy and Leszkiewicz, 2004). 72
73 Εικόνα 32. Η δομή του NMDA υποδοχέα. 3.3 Δομή Οι υπομονάδες του NMDA υποδοχέα περιέχουν μια μακριά, εξωκυττάρια, αμινοτελική περιοχή, από τέσσερα υδρόφοβα τμήματα (Μ1-Μ4) περίπου στο μέσο του μορίου και ένα ενδοκυττάριο, καρβοξυτελικό τμήμα μεταβλητού μήκους (Εικόνες 32, 33). Από τα τέσσερα υδρόφοβα τμήματα μόνο τα τρία διασχίζουν την μεμβράνη (Μ1, Μ3, Μ4). Το τμήμα Μ2 δε φαίνεται να διασχίζει την μεμβράνη, αλλά να σχηματίζει μια θηλιά μέσα σε αυτήν. Σε όλες τις υπομονάδες το τμήμα Μ2 περιέχει μια ασπαραγίνη, που είναι η πιο πιθανή θέση δέσμευσης του Mg2+. Η αντικατάσταση της ασπαραγίνης από γλουταμίνη οδηγεί στην απώλεια της ευαισθησίας στον έλεγχο από το Mg2+ ( Mori and Mishina, 1995). γλουταμινικού Όπως συμβαίνει και στις υπόλοιπες υποομάδες υποδοχέων του οξέος, η περιοχή πρόσδεσης του αγωνιστή καθορίζεται από τα πολυπεπτιδικά τμήματα S1 και S2 (πρωτεϊνική ιοντική θηλιά) ( Furukawa and Gouaux, 2003). Το αμινοτελικό άκρο προσδιορίζεται από τα πρώτα 400 αμινοξέα και ενώ δεν εμπλέκεται άμεσα στην πρόσδεση του αγωνιστή, παίζει ρόλο στο 73
74 σχηματισμό της υπομονάδας καθώς και στην τροποποίηση του υποδοχέα από πρωτόνια, πολυαμίνες, Zn και φάρμακα. Η καρβοξυτελική ουρά ρυθμίζει τις αλληλεπιδράσεις του υποδοχέα με μια πληθώρα κυτταροπλασματικών πρωτεϊνών. Εικόνα 33: α) Kατασκευή της NR υπομονάδας, η οποία σχηματίζεται από το αμινοτελικό άκρο ( amino terminal Domain,ATD), τα διαμεμβρανικά τμήματα ( Μ1-Μ4) και την καρβοξυτελική ουρά ( carboxy terminal domain, CTD). Η περιοχή δέσμευσης του γλουταμινικού οξέος σχηματίζεται από τις δύο S περιοχές (S1 και S2). β) οι περισσότεροι NMDA υποδοχείς αποτελούνται από δύο NR1 και δύο NR2 υπομονάδες. Αυτές οι αλληλεπιδράσεις πρωτεΐνης-πρωτεΐνης ελέγχουν τη διακίνηση των NMDA υποδοχέων στην επιφάνεια της μεμβράνης του νευρώνα (trafficking). Επιπλέον, διαφορετικές υπομονάδες του NMDA υποδοχέα μπορούν να συζεύξουν υποδοχείς σε ένα διακριτό σύμπλοκο ενδοκυτταρικής μεταγωγής σήματος. Για παράδειγμα, η NR2B υπομονάδα αλληλεπιδρά ειδικά με την πρωτεΐνη SynGAP, η οποία είναι μια Ras πρωτεΐνη με ενεργότητα GTPάσης, και έχει δειχθεί ότι αναστέλλει επιλεκτικά το επαγόμενο από τους NMDA υποδοχείς σηματοδοτικό μονοπάτι της ERK κινάσης ( Kim et al., 2005) (Εικόνα 34). Επιπλέον, οι NR2Α και NR2Β δεσμεύουν την ασβέστιο/καλμοδουλίνη-εξαρτώμενη πρωτεϊνική κινάση ΙΙ (CaMKII) με διαφορετική χημική συγγένεια (Strack and Colbran, 1998), η οποία έχει ως αποτέλεσμα διαφορετικές μορφές της συναπτικής πλαστικότητας (Barria and Molinow, 2005). Τέλος, τα καρβοξυτελικά άκρα των υπομονάδων του NMDA 74
75 υποδοχέα αποτελούν υποστρώματα μετα-μεταφραστικών τροποποιήσεων, όπως είναι η φωσφορυλίωση (Πίνακας 4). Άμεση φωσφορυλίωση των ιοντοτροπικών NMDA υποδοχέων του γλουταμινικού οξέος αποτελεί ένα μηχανισμό-κλειδί για τη ρύθμιση της λειτουργίας του διαύλου και της διακίνησης των υποδοχέων στις συνάψεις (Lee, 2006) (Πίνακας 4). Εικόνα 34. Οργάνωση των πρωτεϊνικών συμπλόκων στη μετασυναπτική πυκνότητα (PostSynaptic Density- PSD). Η μετασυναπτική πυκνότητα αποτελείται από μεμβρανικούς υποδοχείς και ιοντικούς διαύλους, πρωτεΐνες του ικριώματος, πρωτεΐνες- συνδέτες, σηματοδοτικές πρωτεΐνες, πρωτεϊνικές κινάσες και φωσφατάσες, καθώς και μόρια του κυτταροσκελετού. Οι NMDA υποδοχείς βρίσκονται κυρίως στο κέντρο της μετασυναπτικής μεμβράνης, ενώ οι AMPA υποδοχείς πιο περιφερειακά. AKAP: adenylate-kinase anchoring protein; CaCh: Ca2+ channel; CaMKII: calcium/calmodulin-dependent protein kinase II; CRIPT: cysteine-rich PDZ-binding protein;; IP3:, inositol-1,4,5-trisphosphate receptor; KCh: K+ channel mglur: metabotropic glutamate receptor; nnos: neuronal nitric oxide synthase; PICK: protein interacting with PRKCA1;; SyNGAP: synaptic Ras GTPaseactivating protein; 75
76 Οι συναπτικοί NMDA υποδοχείς εντοπίζονται στις μετασυναπτικές πυκνότητες ( PostSynaptic Densities, PSD), όπου οργανώνονται δομικά σε μεγάλα μακρομοριακά σηματοδοτικά σύμπλοκα συναπτικών πρωτεϊνών του ικριώματος (scaffolding) και πρωτεϊνών-συνδετών (adaptor), οι οποίες συνδέουν τους υποδοχείς με κινάσες, φωσφατάσες και άλλες σηματοδοτικές πρωτεΐνες, καθώς και με τους μεταβολοτροπικούς υποδοχείς τύπου Ι του γλουταμινικού οξέος (mglurs) ( Lau and Zukin, 2007) (Εικόνα 34). H πρωτεΐνη SAP-90 (γνωστή και ως synapse associated protein-90, SAP-90), καθώς και η synapse associated protein-102 (SAP-102) είναι συναπτικές πρωτεΐνες του ικριώματος και μέλη της μεγάλης οικογένειας πρωτεϊνών PSD-95 των ρυθμιστικών πρωτεϊνών που περιέχουν τη PDZ περιοχή και προσδένουν τους NMDA υποδοχείς στο PSD ( Kim and Sheng, 2004) (Εικόνα 34). Επιπλέον του ρόλου τους ως προσδέτες πρωτεϊνών στις συνάψεις, οι PDZ πρωτεΐνες είναι σημαντικές και στο ενδοκυτταρικό trafficking των NMDA υποδοχέων ( Lau and Zukin, 2007). Η ενδοκυτταρική μεταγωγή σήματος μέσω των NMDA υποδοχέων πιθανώς πραγματοποιείται από πρωτεΐνες που συνδέονται στενά με αυτούς, διαμορφώνοντας ένα μεγάλο δίκτυο μεταγωγής σήματος, το οποίο συχνά αναφέρεται ως «πολυπρωτεϊνικό (ή μακρομοριακό) σύμπλοκο των NMDA υποδοχέων» (NMDA receptor multiprotein or macromelecular complex,nrc) ( Husi et al., 2000) ή ως «Hebbosome» ( Husi and Grant, 2001). 76
77 Πίνακας 4. Θέσεις φωσφορυλίωσης των υπομονάδων του NMDA υποδοχέα (Από Lee, 2006). 3.4 Λειτουργική Ρύθμιση των NMDA Υποδοχέων από Φωσφορυλίωση σε Θέσεις Σερίνης/ Θρεονίνης Οι υποδοχείς NMDA μπορούν να φωσφορυλιωθούν από την c-amp εξαρτώμενη πρωτεϊνική κινάση A (PKA), από την πρωτεϊνική κινάση C (PKC), από την ασβεστιοεξαρτώμενη πρωτεϊνική κινάση της καλμοδουλίνης ΙΙ (CaMKII) και από κινάσες της τυροσίνης (π.χ. Scr και Fyn) ( Dingledine et al., 1999). Η φωσφορυλίωση χρησιμεύει στην αύξηση της μοριακής και λειτουργικής ετερογένειας των υποδοχέων NMDA. Η κατάσταση φωσφορυλίωσης των NMDA υποδοχέων μπορεί να μεταβάλει την πιθανότητα ανοίγματος του διαύλου, την ενεργοποίηση του υποδοχέα, την υποκυτταρική κατανομή και την συναπτική στόχευση των υποδοχέων Μέχρι τώρα έχουν χαρακτηριστεί πολλές θέσεις φωσφορυλίωσης σε κατάλοιπα σερίνης/ θρεονίνης των υπομονάδων του NMDA υποδοχέα, οι οποίες αποτελούν υποστρώματα της camp-εξαρτώμενης πρωτεϊνικής κινάσης (PKA), της πρωτεϊνικής κινάσης C (PKC), της πρωτεϊνικής κινάσης Β (PKΒ), της CaMKII, της εξαρτώμενης από την κυκλίνη κινάσης-5 (Cdk5) και της CKII (casein kinase II) 77
78 (Εικόνα 35). Αυτές οι κινάσες μπορούν να ρυθμίσουν το ενδοκυτταρικό trafficking ή τις ιδιότητες το διαύλου του NMDA υποδοχέα με αποτέλεσμα αλλαγές στη συναπτική δύναμη, γεγονός που χαρακτηρίζει πολλές μορφές συναπτικής πλαστικότητας ( Lee, 2006). Εικόνα 35. Θέσεις φωσφορυλίωσης των κυτταροπλασματικών τμημάτων των υπομονάδων του NMDA υποδοχέα. Οι κυτταροπλασματικές ουρές των NR1, NR2A, NR2B και NR2C υπομονάδων του NMDA υποδοχέα περιέχουν περίπου 100, 630, 640 και 400 αμινοξέα, αντίστοιχα. Κάθε ουρά φωσφορυλιώνεται σε κατάλοιπα σερίνης/ θρεονίνης και/ ή κατάλοιπα τυροσίνης από πληθώρα κινασών. Ανάμεσα στις χαρακτηρισμένες θέσεις φωσφορυλίωσης: η NR2A υπομονάδα είναι η μόνη που φωσφορυλιώνεται από τη Cdk5, η NR2Β υπομονάδα είναι η μόνη που φωσφορυλιώνεται από τη CKII και η NR2C υπομονάδα είναι η μόνη που φωσφορυλιώνεται από την PKΒ (Από Chen and Roche, 2007). 78
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ Συγκριτική μελέτη των φαρμακολογικών ιδιοτήτων του συμπλόκου του υποδοχέα GABA A /Βενζοδιαζεπινών μεταξύ του διαφραγματικού
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ Συγκριτική μελέτη των φαρμακολογικών ιδιοτήτων του συμπλόκου του υποδοχέα GABA A /Βενζοδιαζεπινών μεταξύ του διαφραγματικού
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
Η βιολογία της μάθησης και της μνήμης: Μακρόχρονη ενδυνάμωση/αποδυνάμωση
 Η βιολογία της μάθησης και της μνήμης: Μακρόχρονη ενδυνάμωση/αποδυνάμωση 1 Τι λέμε μνήμη? Η ικανότητα να καταγράφουμε, να αποθηκεύουμε και να ανακαλούμε πληροφορίες Είναι ένας πολύπλοκος συνδυασμός υποσυστημάτων
Η βιολογία της μάθησης και της μνήμης: Μακρόχρονη ενδυνάμωση/αποδυνάμωση 1 Τι λέμε μνήμη? Η ικανότητα να καταγράφουμε, να αποθηκεύουμε και να ανακαλούμε πληροφορίες Είναι ένας πολύπλοκος συνδυασμός υποσυστημάτων
Εσωτερική Κατασκευή των Εγκεφαλικών Ηµισφαιρίων. Μεταιχµιακό Σύστηµα
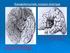 Εσωτερική Κατασκευή των Εγκεφαλικών Ηµισφαιρίων Μεταιχµιακό Σύστηµα Στο εσωτερικό των ηµισφαιρίων υπάρχου πλάγιες κοιλίες λευκή ουσία Βασικά Γάγγλια µεταιχµιακό (στεφανιαίο) σύστηµα διάµεσος εγκέφαλος
Εσωτερική Κατασκευή των Εγκεφαλικών Ηµισφαιρίων Μεταιχµιακό Σύστηµα Στο εσωτερικό των ηµισφαιρίων υπάρχου πλάγιες κοιλίες λευκή ουσία Βασικά Γάγγλια µεταιχµιακό (στεφανιαίο) σύστηµα διάµεσος εγκέφαλος
Μνήμη και μάθηση. Συμπεριφορικό επίπεδο Κυτταρικό επίπεδο. Παρασκευή, 5 Απριλίου 13
 Μνήμη και μάθηση Συμπεριφορικό επίπεδο Κυτταρικό επίπεδο Κατηγορίες μνήμης Βραχύχρονη/Μακρόχρονη μνήνη Έκδηλη μνήμη (ιππόκαμπος/φλοιός) Άδηλη μνήμη (αμυγδαλή, παρεγκεφαλίδα) Συνειρμική Μη συνειρμική Διαδικαστική
Μνήμη και μάθηση Συμπεριφορικό επίπεδο Κυτταρικό επίπεδο Κατηγορίες μνήμης Βραχύχρονη/Μακρόχρονη μνήνη Έκδηλη μνήμη (ιππόκαμπος/φλοιός) Άδηλη μνήμη (αμυγδαλή, παρεγκεφαλίδα) Συνειρμική Μη συνειρμική Διαδικαστική
ΠΑΝΔΠΗΣΖΜΗΟ ΠΑΣΡΧΝ ΥΟΛΖ ΔΠΗΣΖΜΧΝ ΤΓΔΗΑ ΣΜΖΜΑ ΗΑΣΡΗΚΖ ΔΡΓΑΣΖΡΗΟ ΦΤΗΟΛΟΓΗΑ ΓΗΔΤΘΤΝΣΖ: ΓΔΧΡΓΗΟ ΚΧΣΟΠΟΤΛΟ
 ΠΑΝΔΠΗΣΖΜΗΟ ΠΑΣΡΧΝ ΥΟΛΖ ΔΠΗΣΖΜΧΝ ΤΓΔΗΑ ΣΜΖΜΑ ΗΑΣΡΗΚΖ ΔΡΓΑΣΖΡΗΟ ΦΤΗΟΛΟΓΗΑ ΓΗΔΤΘΤΝΣΖ: ΓΔΧΡΓΗΟ ΚΧΣΟΠΟΤΛΟ «In vitro ειεθηξνθπζηνινγηθή κειέηε ησλ κεραληζκώλ δηαθνξνπνίεζεο κεηαμύ δηαθξαγκαηηθνύ θαη θξνηαθηθνύ
ΠΑΝΔΠΗΣΖΜΗΟ ΠΑΣΡΧΝ ΥΟΛΖ ΔΠΗΣΖΜΧΝ ΤΓΔΗΑ ΣΜΖΜΑ ΗΑΣΡΗΚΖ ΔΡΓΑΣΖΡΗΟ ΦΤΗΟΛΟΓΗΑ ΓΗΔΤΘΤΝΣΖ: ΓΔΧΡΓΗΟ ΚΧΣΟΠΟΤΛΟ «In vitro ειεθηξνθπζηνινγηθή κειέηε ησλ κεραληζκώλ δηαθνξνπνίεζεο κεηαμύ δηαθξαγκαηηθνύ θαη θξνηαθηθνύ
ΜΑΘΗΜΑ 7ο ΜΕΡΟΣ Α Η ΔΟΜΗ ΤΩΝ ΗΜΙΣΦΑΙΡΙΩΝ
 ΜΑΘΗΜΑ 7ο ΜΕΡΟΣ Α Η ΔΟΜΗ ΤΩΝ ΗΜΙΣΦΑΙΡΙΩΝ Η ΛΕΥΚΗ ΟΥΣΙΑ ΤΩΝ ΗΜΙΣΦΑΙΡΙΩΝ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Η λευκή ουσία συντίθεται από εμύελες νευρικές ίνες διαφόρων διαμέτρων και νευρογλοία Οι νευρικές ίνες κατατάσσονται
ΜΑΘΗΜΑ 7ο ΜΕΡΟΣ Α Η ΔΟΜΗ ΤΩΝ ΗΜΙΣΦΑΙΡΙΩΝ Η ΛΕΥΚΗ ΟΥΣΙΑ ΤΩΝ ΗΜΙΣΦΑΙΡΙΩΝ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Η λευκή ουσία συντίθεται από εμύελες νευρικές ίνες διαφόρων διαμέτρων και νευρογλοία Οι νευρικές ίνες κατατάσσονται
«In vivo και in vitro μελέτες της φυσιολογίας και της φαρμακολογίας της GABA-εργικής συναπτικής αναστολής στον εγκέφαλο μυών και επίμυων.
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ ΚΑΙ ΖΩΩΝ «In vivo και in vitro μελέτες της φυσιολογίας και της φαρμακολογίας της GABA-εργικής συναπτικής αναστολής
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ ΚΑΙ ΖΩΩΝ «In vivo και in vitro μελέτες της φυσιολογίας και της φαρμακολογίας της GABA-εργικής συναπτικής αναστολής
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Γ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ
 ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Γ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ Ορίζουμε ως διαβιβαστή μια ουσία που απελευθερώνεται από έναν νευρώνα σε μια σύναψη και που επηρεάζει ένα άλλο κύτταρο, είτε έναν νευρώνα είτε ένα κύτταρο
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Γ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ Ορίζουμε ως διαβιβαστή μια ουσία που απελευθερώνεται από έναν νευρώνα σε μια σύναψη και που επηρεάζει ένα άλλο κύτταρο, είτε έναν νευρώνα είτε ένα κύτταρο
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών
 Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΒΙΟ492: ΝΕΥΡΟΒΙΟΛΟΓΙΑ
 ΒΙΟ492: ΝΕΥΡΟΒΙΟΛΟΓΙΑ Δρ. Κυριακή Σιδηροπούλου Λέκτορας Νευροφυσιολογίας Γραφείο: Γ316δ ΤΗΛ: 28103940871 (γραφείο) E- MAIL: sidirop@imbb.forth.gr Εισαγωγή Σιδηροπούλου - Νευροβιολογία 1 Δομή μαθήματος
ΒΙΟ492: ΝΕΥΡΟΒΙΟΛΟΓΙΑ Δρ. Κυριακή Σιδηροπούλου Λέκτορας Νευροφυσιολογίας Γραφείο: Γ316δ ΤΗΛ: 28103940871 (γραφείο) E- MAIL: sidirop@imbb.forth.gr Εισαγωγή Σιδηροπούλου - Νευροβιολογία 1 Δομή μαθήματος
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
Εσωτερική Κατασκευή των Εγκεφαλικών Ηµισφαιρίων
 Εσωτερική Κατασκευή των Εγκεφαλικών Ηµισφαιρίων Διάµεσος Εγκέφαλος (Θάλαµος) Ελίζαµπεθ Τζόνσον Εργαστήριο Ανατοµίας Ιατρική Σχολή Στο εσωτερικό των ηµισφαιρίων υπάρχου πλάγιες κοιλίες λευκή ουσία Βασικά
Εσωτερική Κατασκευή των Εγκεφαλικών Ηµισφαιρίων Διάµεσος Εγκέφαλος (Θάλαµος) Ελίζαµπεθ Τζόνσον Εργαστήριο Ανατοµίας Ιατρική Σχολή Στο εσωτερικό των ηµισφαιρίων υπάρχου πλάγιες κοιλίες λευκή ουσία Βασικά
ΦΑΡΜΑΚΟ ΥΝΑΜΙΚΗ ΙΙ. Γενικές έννοιες (Θεωρία υποδοχέων - Αγωνιστής ανταγωνιστής) Σηµεία ράσης Μοριακοί Μηχανισµοί ράσης Φαρµάκων
 ΦΑΡΜΑΚΟ ΥΝΑΜΙΚΗ ΙΙ Γενικές έννοιες (Θεωρία υποδοχέων - Αγωνιστής ανταγωνιστής) Σηµεία ράσης Μοριακοί Μηχανισµοί ράσης Φαρµάκων Υποδοχείς (φαρµάκων) και ενδοκυττάριες σηµατοδοτικές πορείες - Συστήµατα Μεταγωγής
ΦΑΡΜΑΚΟ ΥΝΑΜΙΚΗ ΙΙ Γενικές έννοιες (Θεωρία υποδοχέων - Αγωνιστής ανταγωνιστής) Σηµεία ράσης Μοριακοί Μηχανισµοί ράσης Φαρµάκων Υποδοχείς (φαρµάκων) και ενδοκυττάριες σηµατοδοτικές πορείες - Συστήµατα Μεταγωγής
Απ. Χατζηευθυμίου Αν Καθηγήτρια Ιατρικής Φυσιολογίας
 Απ. Χατζηευθυμίου Αν Καθηγήτρια Ιατρικής Φυσιολογίας Το 80% περίπου της γεύσης του φαγητού παρέχεται στην πραγματικότητα από την αίσθηση της όσφρησης. Η μυρωδιά μιας ουσίας σχετίζεται άμεσα με τη χημική
Απ. Χατζηευθυμίου Αν Καθηγήτρια Ιατρικής Φυσιολογίας Το 80% περίπου της γεύσης του φαγητού παρέχεται στην πραγματικότητα από την αίσθηση της όσφρησης. Η μυρωδιά μιας ουσίας σχετίζεται άμεσα με τη χημική
ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΕΦΑΡΜΟΓΕΣ ΣΤΙΣ ΒΙΟΪΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ»
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΕΦΑΡΜΟΓΕΣ ΣΤΙΣ ΒΙΟΪΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ» ΜΕΤΑΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ "Η ΣΥΝΕΡΓΙΣΤΙΚΗ ΔΡΑΣΗ ΤΩΝ mglur5
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΕΦΑΡΜΟΓΕΣ ΣΤΙΣ ΒΙΟΪΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ» ΜΕΤΑΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ "Η ΣΥΝΕΡΓΙΣΤΙΚΗ ΔΡΑΣΗ ΤΩΝ mglur5
ΦΥΣΙΟΛΟΓΙΑ ΝΕΥΡΙΚΩΝ ΚΥΤΤΑΡΩΝ ΣΥΝΑΠΤΙΚΗ ΔΙΑΒΙΒΑΣΗ ΗΛΕΚΤΡΙΚΕΣ ΣΥΝΑΨΕΙΣ ΧΗΜΙΚΕΣ ΣΥΝΑΨΕΙΣ
 ΦΥΣΙΟΛΟΓΙΑ ΝΕΥΡΙΚΩΝ ΚΥΤΤΑΡΩΝ ΣΥΝΑΠΤΙΚΗ ΔΙΑΒΙΒΑΣΗ ΗΛΕΚΤΡΙΚΕΣ ΣΥΝΑΨΕΙΣ ΧΗΜΙΚΕΣ ΣΥΝΑΨΕΙΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ ΑΠΕΛΕΥΘΕΡΩΣΗ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΩΝ ΥΠΟΔΟΧΕΙΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΩΝ 1 Ηλεκτρικές και Χημικές Συνάψεις 2 Ηλεκτρικές
ΦΥΣΙΟΛΟΓΙΑ ΝΕΥΡΙΚΩΝ ΚΥΤΤΑΡΩΝ ΣΥΝΑΠΤΙΚΗ ΔΙΑΒΙΒΑΣΗ ΗΛΕΚΤΡΙΚΕΣ ΣΥΝΑΨΕΙΣ ΧΗΜΙΚΕΣ ΣΥΝΑΨΕΙΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ ΑΠΕΛΕΥΘΕΡΩΣΗ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΩΝ ΥΠΟΔΟΧΕΙΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΩΝ 1 Ηλεκτρικές και Χημικές Συνάψεις 2 Ηλεκτρικές
Οι Κυριότερες Νευρικές Οδοί
 Οι Κυριότερες Νευρικές Οδοί Κατιόντα (φυγόκεντρα) δεµάτια Ελίζαµπεθ Τζόνσον Εργαστήριο Ανατοµίας Ιατρική Σχολή φυσιολογικά δεµάτια (κατά τον επιµήκη άξονα) έχουν κοινή έκφυση πορεία απόληξη λειτουργία
Οι Κυριότερες Νευρικές Οδοί Κατιόντα (φυγόκεντρα) δεµάτια Ελίζαµπεθ Τζόνσον Εργαστήριο Ανατοµίας Ιατρική Σχολή φυσιολογικά δεµάτια (κατά τον επιµήκη άξονα) έχουν κοινή έκφυση πορεία απόληξη λειτουργία
Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος
 MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Α ΣΥΝΑΠΤΙΚΗ ΟΛΟΚΛΗΡΩΣΗ
 ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Α ΣΥΝΑΠΤΙΚΗ ΟΛΟΚΛΗΡΩΣΗ Όπως συμβαίνει με τη συναπτική διαβίβαση στη νευρομυϊκή σύναψη, σε πολλές μορφές επικοινωνίας μεταξύ νευρώνων στο κεντρικό νευρικό σύστημα παρεμβαίνουν άμεσα ελεγχόμενοι
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Α ΣΥΝΑΠΤΙΚΗ ΟΛΟΚΛΗΡΩΣΗ Όπως συμβαίνει με τη συναπτική διαβίβαση στη νευρομυϊκή σύναψη, σε πολλές μορφές επικοινωνίας μεταξύ νευρώνων στο κεντρικό νευρικό σύστημα παρεμβαίνουν άμεσα ελεγχόμενοι
Κεφάλαιο 1 ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΝΕΥΡΟΦΥΣΙΟΛΟΓΙΑΣ
 Κεφάλαιο 1 ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΝΕΥΡΟΦΥΣΙΟΛΟΓΙΑΣ 1.1. Εισαγωγή Ο ζωντανός οργανισµός έχει την ικανότητα να αντιδρά σε µεταβολές που συµβαίνουν στο περιβάλλον και στο εσωτερικό του. Οι µεταβολές αυτές ονοµάζονται
Κεφάλαιο 1 ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΝΕΥΡΟΦΥΣΙΟΛΟΓΙΑΣ 1.1. Εισαγωγή Ο ζωντανός οργανισµός έχει την ικανότητα να αντιδρά σε µεταβολές που συµβαίνουν στο περιβάλλον και στο εσωτερικό του. Οι µεταβολές αυτές ονοµάζονται
ΜΑΘΗΜΑ 6ο ΜΕΡΟΣ Β ΤΑ ΕΓΚΕΦΑΛΙΚΑ ΗΜΙΣΦΑΙΡΙΑ
 ΜΑΘΗΜΑ 6ο ΜΕΡΟΣ Β ΤΑ ΕΓΚΕΦΑΛΙΚΑ ΗΜΙΣΦΑΙΡΙΑ ΤΑ ΕΓΚΕΦΑΛΙΚΑ ΗΜΙΣΦΑΙΡΙΑ Τα εγκεφαλικά ημισφαίρια διακρίνονται σε δεξιό και αριστερό Διαχωρίζονται μεταξύ τους με μια βαθιά σχισμή, την επιμήκη σχισμή Εντός
ΜΑΘΗΜΑ 6ο ΜΕΡΟΣ Β ΤΑ ΕΓΚΕΦΑΛΙΚΑ ΗΜΙΣΦΑΙΡΙΑ ΤΑ ΕΓΚΕΦΑΛΙΚΑ ΗΜΙΣΦΑΙΡΙΑ Τα εγκεφαλικά ημισφαίρια διακρίνονται σε δεξιό και αριστερό Διαχωρίζονται μεταξύ τους με μια βαθιά σχισμή, την επιμήκη σχισμή Εντός
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Μεμβρανική Βιοφυσική. Δίαυλοι: απο το γονίδιο στην εξέλιξη Διδάσκων: Λεκ. Χαράλαμπος Λαμπρακάκης
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μεμβρανική Βιοφυσική Δίαυλοι: απο το γονίδιο στην εξέλιξη Διδάσκων: Λεκ. Χαράλαμπος Λαμπρακάκης Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μεμβρανική Βιοφυσική Δίαυλοι: απο το γονίδιο στην εξέλιξη Διδάσκων: Λεκ. Χαράλαμπος Λαμπρακάκης Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
Νευροβιολογία των Μνημονικών Λειτουργιών
 Νευροβιολογία των Μνημονικών Λειτουργιών Ενότητα 2: Κατηγοριοποιήσεις Μάθησης & Μνήμης Κωνσταντίνος Παπαθεοδωρόπουλος Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Σκοποί ενότητας Ανάλυση των γενικών αξόνων που
Νευροβιολογία των Μνημονικών Λειτουργιών Ενότητα 2: Κατηγοριοποιήσεις Μάθησης & Μνήμης Κωνσταντίνος Παπαθεοδωρόπουλος Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Σκοποί ενότητας Ανάλυση των γενικών αξόνων που
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΟΡΜΟΝΕΣ ΚΑΙ ΑΣΚΗΣΗ. ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΟΡΜΟΝΕΣ ΚΑΙ ΑΣΚΗΣΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Αδένες Έκκρισης Ορμονών Υπόφυση Θυρεοειδής Αδένας Παραθυροειδείς
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΟΡΜΟΝΕΣ ΚΑΙ ΑΣΚΗΣΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Αδένες Έκκρισης Ορμονών Υπόφυση Θυρεοειδής Αδένας Παραθυροειδείς
ΜΑΘΗΜΑ 10ο ΜΕΡΟΣ Γ ΜΑΘΗΣΗ ΚΑΙ ΜΝΗΜΗ
 ΜΑΘΗΜΑ 10ο ΜΕΡΟΣ Γ ΜΑΘΗΣΗ ΚΑΙ ΜΝΗΜΗ ΜΑΘΗΣΗ ΚΑΙ ΜΝΗΜΗ Πρόσφατες εργασίες έχουν αποδείξει ότι στη μνήμη παρεμβαίνουν πολλές περιοχές του εγκεφάλου Παρ όλα αυτά, υπάρχουν διαφορετικοί τύποι μνήμης και ορισμένες
ΜΑΘΗΜΑ 10ο ΜΕΡΟΣ Γ ΜΑΘΗΣΗ ΚΑΙ ΜΝΗΜΗ ΜΑΘΗΣΗ ΚΑΙ ΜΝΗΜΗ Πρόσφατες εργασίες έχουν αποδείξει ότι στη μνήμη παρεμβαίνουν πολλές περιοχές του εγκεφάλου Παρ όλα αυτά, υπάρχουν διαφορετικοί τύποι μνήμης και ορισμένες
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
Μοριακή Βιολογία. Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
Συστήματα αισθήσεων. Αισθητικοί υποδοχείς Νευρικές αισθητικές οδοί Συνειρμικός φλοιός και διαδικασία αντίληψης Πρωτοταγής αισθητική κωδικοποίηση
 Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας 2018 Συστήματα αισθήσεων Αισθητικοί υποδοχείς Νευρικές αισθητικές οδοί Συνειρμικός φλοιός και διαδικασία αντίληψης Πρωτοταγής αισθητική κωδικοποίηση
Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας 2018 Συστήματα αισθήσεων Αισθητικοί υποδοχείς Νευρικές αισθητικές οδοί Συνειρμικός φλοιός και διαδικασία αντίληψης Πρωτοταγής αισθητική κωδικοποίηση
Γνωστική-Πειραµατική Ψυχολογία
 Γνωστική-Πειραµατική Ψυχολογία ΕΑΡΙΝΟ ΕΞΑΜΗΝΟ 2018 Γνωστική λειτουργία & φλοιός. Γνωστική λειτουργία & φλοιός. Γνωστικές λειτουργίες à επεξεργασία πληροφοριών από διαφορετικές περιοχές (µεγαλύτερη ( αποκλειστική)
Γνωστική-Πειραµατική Ψυχολογία ΕΑΡΙΝΟ ΕΞΑΜΗΝΟ 2018 Γνωστική λειτουργία & φλοιός. Γνωστική λειτουργία & φλοιός. Γνωστικές λειτουργίες à επεξεργασία πληροφοριών από διαφορετικές περιοχές (µεγαλύτερη ( αποκλειστική)
Νευροβιολογία των Μνημονικών Λειτουργιών
 Νευροβιολογία των Μνημονικών Λειτουργιών Ενότητα 3: Ιππόκαμπος και Μνήμη Στυλιανός Κούβαρος Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Σκοποί ενότητας Μνημονικά Συστήματα Ιππόκαμπος και Μνήμη Πειραματική Μεθοδολογία
Νευροβιολογία των Μνημονικών Λειτουργιών Ενότητα 3: Ιππόκαμπος και Μνήμη Στυλιανός Κούβαρος Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Σκοποί ενότητας Μνημονικά Συστήματα Ιππόκαμπος και Μνήμη Πειραματική Μεθοδολογία
Εγκέφαλος και Έλεγχος της Κίνησης
 Παρεγκεφαλίδα Εγκέφαλος και Έλεγχος της Κίνησης 3 4 Γενικά Cerebellum = Little brain 10% όγκου εγκεφάλου, >50% του συνόλου των νευρώνων του εγκεφάλου Κανονικότητα στη διάταξη των νευρώνων και τις διασυνδέσεις
Παρεγκεφαλίδα Εγκέφαλος και Έλεγχος της Κίνησης 3 4 Γενικά Cerebellum = Little brain 10% όγκου εγκεφάλου, >50% του συνόλου των νευρώνων του εγκεφάλου Κανονικότητα στη διάταξη των νευρώνων και τις διασυνδέσεις
Γνωστική-Πειραµατική Ψυχολογία
 Γνωστική-Πειραµατική Ψυχολογία ΕΑΡΙΝΟ ΕΞΑΜΗΝΟ 2018 Μηχανισµοί της ΣΔ à Βάση διεργασιών όπως η αντίληψη, µάθηση, εκούσια κίνηση. 10.000 à Μέσος νευρώνας à 1000 (1011 1014). 2 θεµελιώδεις µηχανισµοί ΣΔς:
Γνωστική-Πειραµατική Ψυχολογία ΕΑΡΙΝΟ ΕΞΑΜΗΝΟ 2018 Μηχανισµοί της ΣΔ à Βάση διεργασιών όπως η αντίληψη, µάθηση, εκούσια κίνηση. 10.000 à Μέσος νευρώνας à 1000 (1011 1014). 2 θεµελιώδεις µηχανισµοί ΣΔς:
Συστήματα αισθήσεων. Αισθητικοί υποδοχείς Νευρικές αισθητικές οδοί Συνειρμικός φλοιός και διαδικασία αντίληψης Πρωτοταγής αισθητική κωδικοποίηση
 Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017 Συστήματα αισθήσεων Αισθητικοί υποδοχείς Νευρικές αισθητικές οδοί Συνειρμικός φλοιός και διαδικασία αντίληψης Πρωτοταγής αισθητική κωδικοποίηση
Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017 Συστήματα αισθήσεων Αισθητικοί υποδοχείς Νευρικές αισθητικές οδοί Συνειρμικός φλοιός και διαδικασία αντίληψης Πρωτοταγής αισθητική κωδικοποίηση
Αμυγδαλή (ΑΜΥ)* Ι. Εισαγωγή ΙΙ. Ανατομική οργάνωση
 Αμυγδαλή (ΑΜΥ)* Ι. Εισαγωγή Η αμυγδαλή είναι μια σύνθετη δομή που εμπλέκεται σε μια πληθώρα φυσιολογικών συμπεριφορικών λειτουργιών αλλά και ψυχιατρικών καταστάσεων. Για πολύ καιρό η αμυγδαλή αποτελούσε
Αμυγδαλή (ΑΜΥ)* Ι. Εισαγωγή Η αμυγδαλή είναι μια σύνθετη δομή που εμπλέκεται σε μια πληθώρα φυσιολογικών συμπεριφορικών λειτουργιών αλλά και ψυχιατρικών καταστάσεων. Για πολύ καιρό η αμυγδαλή αποτελούσε
Σκοπός του μαθήματος είναι ο συνδυασμός των θεωρητικών και ποσοτικών τεχνικών με τις αντίστοιχες περιγραφικές. Κεφάλαιο 1: περιγράφονται οι βασικές
 Εισαγωγή Ασχολείται με τη μελέτη των ηλεκτρικών, η λ ε κ τ ρ ο μ α γ ν η τ ι κ ώ ν κ α ι μ α γ ν η τ ι κ ώ ν φαινομένων που εμφανίζονται στους βιολογικούς ιστούς. Το αντικείμενο του εμβιοηλεκτρομαγνητισμού
Εισαγωγή Ασχολείται με τη μελέτη των ηλεκτρικών, η λ ε κ τ ρ ο μ α γ ν η τ ι κ ώ ν κ α ι μ α γ ν η τ ι κ ώ ν φαινομένων που εμφανίζονται στους βιολογικούς ιστούς. Το αντικείμενο του εμβιοηλεκτρομαγνητισμού
Σύναψη µεταξύ της απόληξης του νευράξονα ενός νευρώνα και του δενδρίτη ενός άλλου νευρώνα.
 ΟΙ ΝΕΥΡΩΝΕΣ ΕΠΙΚΟΙΝΩΝΟΥΝ ΜΕΣΩ ΤΗΣ ΣΥΝΑΨΗΣ Άντα Μητσάκου Αναπληρώτρια Καθηγήτρια, Ιατρική Σχολή, Πανεπιστήµιο Πατρών Γνωρίζουµε ότι είµαστε ικανοί να εκτελούµε σύνθετες νοητικές διεργασίες εξαιτίας της
ΟΙ ΝΕΥΡΩΝΕΣ ΕΠΙΚΟΙΝΩΝΟΥΝ ΜΕΣΩ ΤΗΣ ΣΥΝΑΨΗΣ Άντα Μητσάκου Αναπληρώτρια Καθηγήτρια, Ιατρική Σχολή, Πανεπιστήµιο Πατρών Γνωρίζουµε ότι είµαστε ικανοί να εκτελούµε σύνθετες νοητικές διεργασίες εξαιτίας της
Ανατοµία του Εγκεφάλου
 Ανατοµία του Εγκεφάλου Κύριες Σχισµές & Αύλακες: 1. Η επιµήκης σχισµή 2. Η εγκάρσια σχισµή 3. Η πλάγια σχισµή (του Sylvius) πρόσθιο οριζόντιο κλαδο πρόσθιο ανιόντα κλάδο οπίσθιο κλάδο 4. Κεντρική αύλακα
Ανατοµία του Εγκεφάλου Κύριες Σχισµές & Αύλακες: 1. Η επιµήκης σχισµή 2. Η εγκάρσια σχισµή 3. Η πλάγια σχισµή (του Sylvius) πρόσθιο οριζόντιο κλαδο πρόσθιο ανιόντα κλάδο οπίσθιο κλάδο 4. Κεντρική αύλακα
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΑΣΚΗΣΗ: MΕΤΡΗΣΗ ΜΕΤΑΣΥΝΑΠΤΙΚΩΝ ΔΥΝΑΜΙΚΩΝ ΣΕ ΤΟΜΕΣ ΙΠΠΟΚΑΜΠΟΥ ΑΡΟΥΡΑΙΟΥ.
 ΑΣΚΗΣΗ: MΕΤΡΗΣΗ ΜΕΤΑΣΥΝΑΠΤΙΚΩΝ ΔΥΝΑΜΙΚΩΝ ΣΕ ΤΟΜΕΣ ΙΠΠΟΚΑΜΠΟΥ ΑΡΟΥΡΑΙΟΥ. Η μετάδοση σημάτων μεταξύ των νευρώνων επιτυγχάνεται μέσω χημικών συνάψεων. Κατά τη χημική συναπτική διαβίβαση απελευθερώνεται από
ΑΣΚΗΣΗ: MΕΤΡΗΣΗ ΜΕΤΑΣΥΝΑΠΤΙΚΩΝ ΔΥΝΑΜΙΚΩΝ ΣΕ ΤΟΜΕΣ ΙΠΠΟΚΑΜΠΟΥ ΑΡΟΥΡΑΙΟΥ. Η μετάδοση σημάτων μεταξύ των νευρώνων επιτυγχάνεται μέσω χημικών συνάψεων. Κατά τη χημική συναπτική διαβίβαση απελευθερώνεται από
Βασικά γάγγλια. Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας
 Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί η πρόθεση δράσης
Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί η πρόθεση δράσης
ΚΛΙΝΙΚΗ ΠΕΡΙΠΤΩΣΗ Μνήμη και Μάθηση Νόσος του Alzheimer
 ΚΛΙΝΙΚΗ ΠΕΡΙΠΤΩΣΗ Μνήμη και Μάθηση Νόσος του Alzheimer Περιγραφή της περίπτωσης (Ι) Γυναίκα 43 ετών διακομίσθηκε στο τμήμα επειγόντων περιστατικών από την οικογένειά της λόγω διαταραχών μνήμης. Η ασθενής
ΚΛΙΝΙΚΗ ΠΕΡΙΠΤΩΣΗ Μνήμη και Μάθηση Νόσος του Alzheimer Περιγραφή της περίπτωσης (Ι) Γυναίκα 43 ετών διακομίσθηκε στο τμήμα επειγόντων περιστατικών από την οικογένειά της λόγω διαταραχών μνήμης. Η ασθενής
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Β ΔΙΑΒΙΒΑΣΗ ΣΤΗ ΝΕΥΡΟΜΥΪΚΗ ΣΥΝΑΨΗ
 ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Β ΔΙΑΒΙΒΑΣΗ ΣΤΗ ΝΕΥΡΟΜΥΪΚΗ ΣΥΝΑΨΗ Η νευρομυϊκή σύναψη αποτελεί ιδιαίτερη μορφή σύναψης μεταξύ του κινητικού νευρώνα και της σκελετικής μυϊκής ίνας Είναι ορατή με το οπτικό μικροσκόπιο Στην
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Β ΔΙΑΒΙΒΑΣΗ ΣΤΗ ΝΕΥΡΟΜΥΪΚΗ ΣΥΝΑΨΗ Η νευρομυϊκή σύναψη αποτελεί ιδιαίτερη μορφή σύναψης μεταξύ του κινητικού νευρώνα και της σκελετικής μυϊκής ίνας Είναι ορατή με το οπτικό μικροσκόπιο Στην
ΗΛΕΚΤΡΙΚΑ ΣΗΜΑΤΑ ΑΠΟ ΤΟ ΣΩΜΑ (I)
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΙΑΤΡΙΚΗΣ ΦΥΣΙΚΗΣ ΗΛΕΚΤΡΙΚΑ ΣΗΜΑΤΑ ΑΠΟ ΤΟ ΣΩΜΑ (I) Γιάννης Τσούγκος ΓΕΝΙΚΑ:...πολλούς αιώνες πριν μελετηθεί επιστημονικά ο ηλεκτρισμός οι άνθρωποι γνώριζαν
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΙΑΤΡΙΚΗΣ ΦΥΣΙΚΗΣ ΗΛΕΚΤΡΙΚΑ ΣΗΜΑΤΑ ΑΠΟ ΤΟ ΣΩΜΑ (I) Γιάννης Τσούγκος ΓΕΝΙΚΑ:...πολλούς αιώνες πριν μελετηθεί επιστημονικά ο ηλεκτρισμός οι άνθρωποι γνώριζαν
ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ 7-8/ Π.Παπαζαφείρη ΣΥΝΑΨΕΙΣ
 ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ 7-8/02-03-2016 Π.Παπαζαφείρη ΣΥΝΑΨΕΙΣ Νευροδιαβιβαστές α) παραγωγή, είδη β) αναγνώριση γ) σηματοδότηση Σε πρώτη προσέγγιση, ο ορισμός του διαβιβαστή είναι: Διαβιβαστής είναι μια ουσία που
ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ 7-8/02-03-2016 Π.Παπαζαφείρη ΣΥΝΑΨΕΙΣ Νευροδιαβιβαστές α) παραγωγή, είδη β) αναγνώριση γ) σηματοδότηση Σε πρώτη προσέγγιση, ο ορισμός του διαβιβαστή είναι: Διαβιβαστής είναι μια ουσία που
Κυτταροαρχιτεκτονική Ελίζαµπεθ Τζόνσον Εργαστήριο Ανατοµίας Ιατρική Σχολή
 Κυτταροαρχιτεκτονική Ελίζαµπεθ Τζόνσον Εργαστήριο Ανατοµίας Ιατρική Σχολή Τελικός Εγκ Εγκεφαλικά ηµισφαίρια Διάµεσος εγκ & Βασικά γάγγλια Διαίρεση του ΚΝΣ Στέλεχος του εγκέφαλου Μέσος εγκ Γέφυρα Προµήκης
Κυτταροαρχιτεκτονική Ελίζαµπεθ Τζόνσον Εργαστήριο Ανατοµίας Ιατρική Σχολή Τελικός Εγκ Εγκεφαλικά ηµισφαίρια Διάµεσος εγκ & Βασικά γάγγλια Διαίρεση του ΚΝΣ Στέλεχος του εγκέφαλου Μέσος εγκ Γέφυρα Προµήκης
Οπτική οδός. Έξω γονατώδες σώµα. Οπτική ακτινοβολία
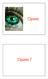 Όραση Γ Όραση Οπτική οδός Έξω γονατώδες σώµα Οπτική ακτινοβολία Οπτικό χίασµα: Οι ίνες από το ρινικό ηµιµόριο περνούν στην αντίπλευρη οπτική οδό ενώ τα κροταφικά ηµιµόρια δεν χιάζονται. Εποµένως κάθε οπτική
Όραση Γ Όραση Οπτική οδός Έξω γονατώδες σώµα Οπτική ακτινοβολία Οπτικό χίασµα: Οι ίνες από το ρινικό ηµιµόριο περνούν στην αντίπλευρη οπτική οδό ενώ τα κροταφικά ηµιµόρια δεν χιάζονται. Εποµένως κάθε οπτική
ΕΙΣΑΓΩΓΗ ΣΤΟ ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ
 ΕΙΣΑΓΩΓΗ ΣΤΟ ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ Νευρικό Σύστημα 2 Ανατομία ΝΣ ΝΣ ΚΝΣ (εγκέφαλος + ΝΜ) ΠΝΣ Προσαγωγό (αισθητικό) Απαγωγό Κινητικοί νευρώνες ΑΝΣ Συμπαθητικό Παρασυμπαθητικό 3 Οι διαταραχές της λειτουργίας
ΕΙΣΑΓΩΓΗ ΣΤΟ ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ Νευρικό Σύστημα 2 Ανατομία ΝΣ ΝΣ ΚΝΣ (εγκέφαλος + ΝΜ) ΠΝΣ Προσαγωγό (αισθητικό) Απαγωγό Κινητικοί νευρώνες ΑΝΣ Συμπαθητικό Παρασυμπαθητικό 3 Οι διαταραχές της λειτουργίας
Θάλαμος, Φλοιός του Εγκεφάλου & Δικτυωτός Σχηματισμός. Α. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας
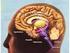 Θάλαμος, Φλοιός του Εγκεφάλου & Δικτυωτός Σχηματισμός Α. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Θάλαμος Ο θάλαμος: «πύλη προς τον εγκέφαλο» Είναι μια μεγάλη συλλογή νευρώνων στο διεγκέφαλο Παίρνει
Θάλαμος, Φλοιός του Εγκεφάλου & Δικτυωτός Σχηματισμός Α. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Θάλαμος Ο θάλαμος: «πύλη προς τον εγκέφαλο» Είναι μια μεγάλη συλλογή νευρώνων στο διεγκέφαλο Παίρνει
Πως ο Νους Χειρίζεται το Φόβο
 Πως ο Νους Χειρίζεται το Φόβο Σύμφωνα με δύο σχετικά πρόσφατες έρευνες, οι μνήμες φόβου και τρόμου διαφέρουν σημαντικά από τις συνηθισμένες μνήμες. Οι διαφορές αυτές δεν συνίστανται μόνο στις εμφανείς
Πως ο Νους Χειρίζεται το Φόβο Σύμφωνα με δύο σχετικά πρόσφατες έρευνες, οι μνήμες φόβου και τρόμου διαφέρουν σημαντικά από τις συνηθισμένες μνήμες. Οι διαφορές αυτές δεν συνίστανται μόνο στις εμφανείς
Συναπτική ολοκλήρωση. Η διαδικασία της άθροισης όλων των εισερχόμενων διεγερτικών και ανασταλτικών σημάτων σε ένα νευρώνα. Τετάρτη, 20 Μαρτίου 13
 Συναπτική ολοκλήρωση Η διαδικασία της άθροισης όλων των εισερχόμενων διεγερτικών και ανασταλτικών σημάτων σε ένα νευρώνα http://www.mpg.de/13795/learning_memory_perception?print=yes 2 Τοποθεσία συνάψεων
Συναπτική ολοκλήρωση Η διαδικασία της άθροισης όλων των εισερχόμενων διεγερτικών και ανασταλτικών σημάτων σε ένα νευρώνα http://www.mpg.de/13795/learning_memory_perception?print=yes 2 Τοποθεσία συνάψεων
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ Εργαστήριο Φυσιολογίας Καθηγητής: Ηλίας Κούβελας
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ Εργαστήριο Φυσιολογίας Καθηγητής: Ηλίας Κούβελας Συγκριτική Μελέτη της Έκφρασης των Υποµονάδων του GABA A Υποδοχέα και των Πρώιµων Γονιδίων c-fos
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ Εργαστήριο Φυσιολογίας Καθηγητής: Ηλίας Κούβελας Συγκριτική Μελέτη της Έκφρασης των Υποµονάδων του GABA A Υποδοχέα και των Πρώιµων Γονιδίων c-fos
ΚΕΦΑΛΑΙΟ 15. Κυτταρική ρύθμιση. Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1
 ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
Δομή των μυϊκών κυττάρων.
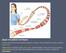 Δομή των μυϊκών κυττάρων. Οι μύες αποτελούνται από δεμάτια μεγάλων κυττάρων (που ονομάζονται μυϊκά κύτταρα ή μυϊκές ίνες). Κάθε μυϊκή ίνα περιέχει πολλά μυϊκά ινίδια, δηλαδή δεμάτια ινιδίων ακτίνης και
Δομή των μυϊκών κυττάρων. Οι μύες αποτελούνται από δεμάτια μεγάλων κυττάρων (που ονομάζονται μυϊκά κύτταρα ή μυϊκές ίνες). Κάθε μυϊκή ίνα περιέχει πολλά μυϊκά ινίδια, δηλαδή δεμάτια ινιδίων ακτίνης και
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής
 Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
Νευροβιολογία των Μνημονικών Λειτουργιών. Ενότητα 4: Βιωματική Μνήμη Κωνσταντίνος Παπαθεοδωρόπουλος Σχολή Επιστημών Υγείας Τμήμα Ιατρικής
 Νευροβιολογία των Μνημονικών Λειτουργιών Ενότητα 4: Βιωματική Μνήμη Κωνσταντίνος Παπαθεοδωρόπουλος Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Σκοποί ενότητας Ορισμός της βιωματικής μνήμης μέσα από μια ιστορική
Νευροβιολογία των Μνημονικών Λειτουργιών Ενότητα 4: Βιωματική Μνήμη Κωνσταντίνος Παπαθεοδωρόπουλος Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Σκοποί ενότητας Ορισμός της βιωματικής μνήμης μέσα από μια ιστορική
Βασικά γάγγλια. Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017
 Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017 Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί
Βασικά γάγγλια Απ. Χατζηευθυμίου Αν. Καθηγήτρια Ιατρικής Φυσιολογίας Μάρτιος 2017 Ιεραρχία κινητικού ελέγχου ΠΡΟΘΕΣΗ Αναμετάδοση της πληροφορίας Εξειδίκευση της θέσης και της κίνησης για να εκτελεστεί
ηδιεργασία µε την οποία αποκτούµε γνώσεις για τον κόσµο η οποία θα οδηγήσει στην τροποποίηση µιας συµπεριφοράς
 Μάθηση και Μνήµη Μάθηση Μνήµη Μάθηση: Μνήµη: ηδιεργασία µε την οποία αποκτούµε γνώσεις για τον κόσµο η οποία θα οδηγήσει στην τροποποίηση µιας συµπεριφοράς ηαποθήκευσητωνπληροφοριώναυτών η ικανότητα να
Μάθηση και Μνήµη Μάθηση Μνήµη Μάθηση: Μνήµη: ηδιεργασία µε την οποία αποκτούµε γνώσεις για τον κόσµο η οποία θα οδηγήσει στην τροποποίηση µιας συµπεριφοράς ηαποθήκευσητωνπληροφοριώναυτών η ικανότητα να
Η Λευκή Ουσία του Νωτιαίου Μυελού
 Η Λευκή Ουσία του Νωτιαίου Μυελού λκλλκλκλλκκκκ Εισαγωγή Ανιόντα Δεµάτια του Νωτιαίου Μυελού Ανιόντα Δεµάτια της Πρόσθιας Δέσµης Ανιόντα Δεµάτια της Πλάγιας Δέσµης Ανιόντα Δεµάτια της Οπίσθιας Δέσµης Κατιόντα
Η Λευκή Ουσία του Νωτιαίου Μυελού λκλλκλκλλκκκκ Εισαγωγή Ανιόντα Δεµάτια του Νωτιαίου Μυελού Ανιόντα Δεµάτια της Πρόσθιας Δέσµης Ανιόντα Δεµάτια της Πλάγιας Δέσµης Ανιόντα Δεµάτια της Οπίσθιας Δέσµης Κατιόντα
Μόρια κυτταρικής πρόσφυσης
 Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
M.Sc. Bioinformatics and Neuroinformatics
 M.Sc. Bioinformatics and Neuroinformatics Recording and Processing Brain Signals Μαρία Σαγιαδινού Ο ανθρώπινος εγκέφαλος Πιο πολύπλοκο δημιούργημα της φύσης Προιόν βιολογικής εξέλιξης εκατομμυρίων ετών
M.Sc. Bioinformatics and Neuroinformatics Recording and Processing Brain Signals Μαρία Σαγιαδινού Ο ανθρώπινος εγκέφαλος Πιο πολύπλοκο δημιούργημα της φύσης Προιόν βιολογικής εξέλιξης εκατομμυρίων ετών
Νευροδιαβιβαστές και συμπεριφορά
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Νευροδιαβιβαστές και συμπεριφορά Νευροβιολογία της λήψης τροφής Διδάσκοντες: Καθ. Α. Ψαρροπούλου, Λεκ. Χ. Λαμπρακάκης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Νευροδιαβιβαστές και συμπεριφορά Νευροβιολογία της λήψης τροφής Διδάσκοντες: Καθ. Α. Ψαρροπούλου, Λεκ. Χ. Λαμπρακάκης Άδειες Χρήσης Το παρόν εκπαιδευτικό
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Ιππόκαμπος: Ανατομία, Φυσιολογία, Παθολογία
 Ιππόκαμπος: Ανατομία, Φυσιολογία, Παθολογία Άννα Σιατούνη Νευρολόγος Εφαρμοσμένη Νευροανατομία ΙΙΙ: Εν τω βάθει δομές του εγκεφάλου Πρόγραμμα Μεταπτυχιακών Σπουδών «ΕΦΑΡΜΟΣΜΕΝΗ ΝΕΥΡΟΑΝΑΤΟΜΙΑ» Αρχαιοφλοιός
Ιππόκαμπος: Ανατομία, Φυσιολογία, Παθολογία Άννα Σιατούνη Νευρολόγος Εφαρμοσμένη Νευροανατομία ΙΙΙ: Εν τω βάθει δομές του εγκεφάλου Πρόγραμμα Μεταπτυχιακών Σπουδών «ΕΦΑΡΜΟΣΜΕΝΗ ΝΕΥΡΟΑΝΑΤΟΜΙΑ» Αρχαιοφλοιός
ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΣΤΙΣ ΒΑΣΙΚΕΣ ΙΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ. Διπλωματική Εργασία
 ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΣΤΙΣ ΒΑΣΙΚΕΣ ΙΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ Διπλωματική Εργασία «Φαρμακολογικές επιδράσεις επί των in vitro Οξέων Κυμάτων σε λεπτές τομές ιπποκάμπου επίμυος» Γιαννόπουλος Παναγιώτης Α.Μ.
ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΣΤΙΣ ΒΑΣΙΚΕΣ ΙΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ Διπλωματική Εργασία «Φαρμακολογικές επιδράσεις επί των in vitro Οξέων Κυμάτων σε λεπτές τομές ιπποκάμπου επίμυος» Γιαννόπουλος Παναγιώτης Α.Μ.
ΜΑΘΗΜΑ 9ο ΜΕΡΟΣ Α Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ
 ΜΑΘΗΜΑ 9ο ΜΕΡΟΣ Α Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Ο εγκέφαλος αρδεύεται από : 1. Τις δύο έσω καρωτίδες και τους κλάδους τους 2. Τις δύο σπονδυλικές αρτηρίες και τους κλάδους τους Οι τέσσερις
ΜΑΘΗΜΑ 9ο ΜΕΡΟΣ Α Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Ο εγκέφαλος αρδεύεται από : 1. Τις δύο έσω καρωτίδες και τους κλάδους τους 2. Τις δύο σπονδυλικές αρτηρίες και τους κλάδους τους Οι τέσσερις
Κεφ. 4 DNA, RNA και η ροή των γενετικών πληροφοριών
 Κεφ. 4 DNA, RNA και η ροή των γενετικών πληροφοριών Η οικογενειακή ομοιότητα, οφείλεται στα κοινά γονίδια. Τα γονίδια πρέπει να εκφραστούν για να έχουν αποτέλεσμα, και η έκφραση αυτή ρυθμίζεται από πρωτεΐνες.
Κεφ. 4 DNA, RNA και η ροή των γενετικών πληροφοριών Η οικογενειακή ομοιότητα, οφείλεται στα κοινά γονίδια. Τα γονίδια πρέπει να εκφραστούν για να έχουν αποτέλεσμα, και η έκφραση αυτή ρυθμίζεται από πρωτεΐνες.
Πρώτα μηνύματα: ορμόνες, νευροδιαβιβαστές, παρακρινείς/αυτοκρινείς παράγοντες που φθάνουν στηνκμαπότονεξωκυττάριοχώροκαιδεσμεύονται με ειδικούς
 Πρώτα μηνύματα: ορμόνες, νευροδιαβιβαστές, παρακρινείς/αυτοκρινείς παράγοντες που φθάνουν στηνκμαπότονεξωκυττάριοχώροκαιδεσμεύονται με ειδικούς κυτταρικούς υποδοχείς Δεύτερα μηνύματα: μη-πρωτεϊνικές ουσίες
Πρώτα μηνύματα: ορμόνες, νευροδιαβιβαστές, παρακρινείς/αυτοκρινείς παράγοντες που φθάνουν στηνκμαπότονεξωκυττάριοχώροκαιδεσμεύονται με ειδικούς κυτταρικούς υποδοχείς Δεύτερα μηνύματα: μη-πρωτεϊνικές ουσίες
Ομαδες μοριων κυτταρικης προσφυσης
 Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
ΓΕΝΙΚΗ ΦΥΣΙΟΛΟΓΙΑ. Γιώργος Ανωγειανάκις Εργαστήριο Πειραματικής Φυσιολογίας 2310-999054 (προσωπικό) 2310-999185 (γραμματεία) anogian@auth.
 ΓΕΝΙΚΗ ΦΥΣΙΟΛΟΓΙΑ Γιώργος Ανωγειανάκις Εργαστήριο Πειραματικής Φυσιολογίας 2310-999054 (προσωπικό) 2310-999185 (γραμματεία) anogian@auth.gr Σύνοψη των όσων εξετάσαμε για τους ιοντικούς διαύλους: 1. Διαπερνούν
ΓΕΝΙΚΗ ΦΥΣΙΟΛΟΓΙΑ Γιώργος Ανωγειανάκις Εργαστήριο Πειραματικής Φυσιολογίας 2310-999054 (προσωπικό) 2310-999185 (γραμματεία) anogian@auth.gr Σύνοψη των όσων εξετάσαμε για τους ιοντικούς διαύλους: 1. Διαπερνούν
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης
 Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
3. Να συμπληρώσετε κατάλληλα τα μέρη από τα οποία αποτελείται ένας νευρώνας.
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 9 ο ΚΕΦΑΛΑΙΟ «ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ» ΜΕΡΟΣ Α: ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΝΕΥΡΙΚΩΝ ΚΥΤΤΑΡΩΝ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Να συμπληρώσετε το παρακάτω διάγραμμα. 2. Ποιος είναι ο ρόλος του
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 9 ο ΚΕΦΑΛΑΙΟ «ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ» ΜΕΡΟΣ Α: ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΝΕΥΡΙΚΩΝ ΚΥΤΤΑΡΩΝ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Να συμπληρώσετε το παρακάτω διάγραμμα. 2. Ποιος είναι ο ρόλος του
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
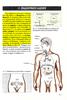 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ. ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
Ν Ε Υ Ρ Ο Ψ Υ Χ Ο Λ Ο Γ Ι Κ Ο Ι Π Α Ρ Α Γ Ο Ν Τ Ε Σ Π Ο Υ Ε Π Η Ρ Ε Α Ζ Ο Υ Ν Τ Η Μ Α Θ Η Σ Η
 Ν Ε Υ Ρ Ο Ψ Υ Χ Ο Λ Ο Γ Ι Κ Ο Ι Π Α Ρ Α Γ Ο Ν Τ Ε Σ Π Ο Υ Ε Π Η Ρ Ε Α Ζ Ο Υ Ν Τ Η Μ Α Θ Η Σ Η 2 ΤΙ ΕΙΝΑΙ ΣΥΝΑΙΣΘΗΜΑ; Μηχανισμός επικοινωνίας που διατηρούν την κοινωνική τάξη / δομή Μαθημένη συμπεριφορά
Ν Ε Υ Ρ Ο Ψ Υ Χ Ο Λ Ο Γ Ι Κ Ο Ι Π Α Ρ Α Γ Ο Ν Τ Ε Σ Π Ο Υ Ε Π Η Ρ Ε Α Ζ Ο Υ Ν Τ Η Μ Α Θ Η Σ Η 2 ΤΙ ΕΙΝΑΙ ΣΥΝΑΙΣΘΗΜΑ; Μηχανισμός επικοινωνίας που διατηρούν την κοινωνική τάξη / δομή Μαθημένη συμπεριφορά
Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος
 Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Κυτταρική επικοινωνία Τύποι επικοινωνίας
Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Κυτταρική επικοινωνία Τύποι επικοινωνίας
Τι θα προτιμούσατε; Γνωστική Ψυχολογία Ι (ΨΧ32) 25/4/2012. Διάλεξη 5 Όραση και οπτική αντίληψη. Πέτρος Ρούσσος. Να περιγράψετε τι βλέπετε στην εικόνα;
 Γνωστική Ψυχολογία Ι (ΨΧ32) Διάλεξη 5 Όραση και οπτική αντίληψη Πέτρος Ρούσσος Να περιγράψετε τι βλέπετε στην εικόνα; Τι θα προτιμούσατε; Ή να αντιμετωπίσετε τον Γκάρι Κασπάροβ σε μια παρτίδα σκάκι; 1
Γνωστική Ψυχολογία Ι (ΨΧ32) Διάλεξη 5 Όραση και οπτική αντίληψη Πέτρος Ρούσσος Να περιγράψετε τι βλέπετε στην εικόνα; Τι θα προτιμούσατε; Ή να αντιμετωπίσετε τον Γκάρι Κασπάροβ σε μια παρτίδα σκάκι; 1
Γονιμοποίηση αναγνώριση και συνένωση ωαρίου-σπερματοζωαρίου φραγμός στην πολυσπερμία μετα μετ βολική ενεργο ενεργο ο π ίηση
 Γονιμοποίηση αναγνώριση και συνένωση ωαρίου-σπερματοζωαρίου φραγμός στην πολυσπερμία μεταβολική ενεργοποίηση του αυγού ανακατατάξεις στα συστατικά του αυγού σχηματισμός του διπλοειδή πυρήνα του ζυγωτού
Γονιμοποίηση αναγνώριση και συνένωση ωαρίου-σπερματοζωαρίου φραγμός στην πολυσπερμία μεταβολική ενεργοποίηση του αυγού ανακατατάξεις στα συστατικά του αυγού σχηματισμός του διπλοειδή πυρήνα του ζυγωτού
Μάθηση και Μνήμη. Ε. Παρασκευά Αναπλ. Καθηγήτρια Κυτταρικής Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 2018
 Μάθηση και Μνήμη Ε. Παρασκευά Αναπλ. Καθηγήτρια Κυτταρικής Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 2018 Μάθηση: η διεργασία µε την οποία αποκτούµε γνώσεις για τον κόσµο η οποία θα οδηγήσει στην τροποποίηση µιας
Μάθηση και Μνήμη Ε. Παρασκευά Αναπλ. Καθηγήτρια Κυτταρικής Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 2018 Μάθηση: η διεργασία µε την οποία αποκτούµε γνώσεις για τον κόσµο η οποία θα οδηγήσει στην τροποποίηση µιας
Καραπέτσας Θανάσης. Διπλωματική Εργασία:
 Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών
 Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Διαφώτιση των διαμορφωτικών αλλαγών της
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Διαφώτιση των διαμορφωτικών αλλαγών της
Ρύθµιση κυτταρικής λειτουργίας. Μεταγωγή σήµατος
 Ρύθµιση κυτταρικής λειτουργίας Μεταγωγή σήµατος 1 Εισαγωγή Η διαδικασία εξέλιξης των πολυκύτταρων οργανισµών (πρίν 2.5 δις χρόνια) άρχισε πολύ πιο αργά από την ύπαρξη των µονοκύτταρων οργανισµών (πρίν
Ρύθµιση κυτταρικής λειτουργίας Μεταγωγή σήµατος 1 Εισαγωγή Η διαδικασία εξέλιξης των πολυκύτταρων οργανισµών (πρίν 2.5 δις χρόνια) άρχισε πολύ πιο αργά από την ύπαρξη των µονοκύτταρων οργανισµών (πρίν
ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ
 ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ Εγκέφαλος Μεγάλη αιµάτωση, πολύ σηµαντική για την λειτουργία του Επικοινωνία µε το περιβάλλον Χρησιµοποιεί το 20% του Ο 2 και ως πηγή ενέργειας γλυκόζη Στις χειρουργικές επεµβάσεις
ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ Εγκέφαλος Μεγάλη αιµάτωση, πολύ σηµαντική για την λειτουργία του Επικοινωνία µε το περιβάλλον Χρησιµοποιεί το 20% του Ο 2 και ως πηγή ενέργειας γλυκόζη Στις χειρουργικές επεµβάσεις
Κεφάλαιο 1: Βασικές αρχές ανατοµίας και οργάνωσης του νευρικού συστήµατος
 Κεφάλαιο 1: Βασικές αρχές ανατοµίας και οργάνωσης του νευρικού συστήµατος Περίληψη Σε αυτό το πρώτο κεφάλαιο, θα παρουσιαστεί η βασική οργάνωση του νευρικού συστήµατος, δηλαδή ο διαχωρισµός σε κεντρικό
Κεφάλαιο 1: Βασικές αρχές ανατοµίας και οργάνωσης του νευρικού συστήµατος Περίληψη Σε αυτό το πρώτο κεφάλαιο, θα παρουσιαστεί η βασική οργάνωση του νευρικού συστήµατος, δηλαδή ο διαχωρισµός σε κεντρικό
«ΚΑΤΑΝΟΜΗ GABA ΝΕΥΡΩΝΩΝ ΣΤΗ ΡΑΧΙΑΙΑ ΚΑΙ ΚΟΙΛΙΑΚΗ ΜΟΙΡΑ ΤΟΥ ΙΠΠΟΚΑΜΠΟΥ»
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΚΛΙΝΙΚΕΣ ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΜΟΡΙΑΚΗΣ ΙΑΤΡΙΚΗΣ» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ «ΚΑΤΑΝΟΜΗ GABA ΝΕΥΡΩΝΩΝ ΣΤΗ ΡΑΧΙΑΙΑ ΚΑΙ ΚΟΙΛΙΑΚΗ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΚΛΙΝΙΚΕΣ ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΜΟΡΙΑΚΗΣ ΙΑΤΡΙΚΗΣ» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ «ΚΑΤΑΝΟΜΗ GABA ΝΕΥΡΩΝΩΝ ΣΤΗ ΡΑΧΙΑΙΑ ΚΑΙ ΚΟΙΛΙΑΚΗ
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης
 ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
ΕΠΙΔΡΑΣΕΙΣ ΤΗΣ ΙΝΔΙΚΗΣ ΚΑΝΑΒΗΣ ΣΤΗΝ ΜΝΗΜΗ ΚΩΝΣΤΑΝΤΙΝΟΣ ΛΥΣΙΤΣΑΣ ΝΕΥΡΟΛΟΓΟΣ ΜΕΤΕΚΠΑΙΔΕΥΘΕΙΣ ΣΤΟ ST THOMAS HOSPITAL TΟΥ ΛΟΝΔΙΝΟΥ
 ΕΠΙΔΡΑΣΕΙΣ ΤΗΣ ΙΝΔΙΚΗΣ ΚΑΝΑΒΗΣ ΣΤΗΝ ΜΝΗΜΗ ΚΩΝΣΤΑΝΤΙΝΟΣ ΛΥΣΙΤΣΑΣ ΝΕΥΡΟΛΟΓΟΣ ΜΕΤΕΚΠΑΙΔΕΥΘΕΙΣ ΣΤΟ ST THOMAS HOSPITAL TΟΥ ΛΟΝΔΙΝΟΥ Η μαριχουάνα και το χασίς είναι ψυχοτρόπες ουσίες που παράγονται από το φυτό
ΕΠΙΔΡΑΣΕΙΣ ΤΗΣ ΙΝΔΙΚΗΣ ΚΑΝΑΒΗΣ ΣΤΗΝ ΜΝΗΜΗ ΚΩΝΣΤΑΝΤΙΝΟΣ ΛΥΣΙΤΣΑΣ ΝΕΥΡΟΛΟΓΟΣ ΜΕΤΕΚΠΑΙΔΕΥΘΕΙΣ ΣΤΟ ST THOMAS HOSPITAL TΟΥ ΛΟΝΔΙΝΟΥ Η μαριχουάνα και το χασίς είναι ψυχοτρόπες ουσίες που παράγονται από το φυτό
ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ - ΜΕΡΟΣ Α. Ο ηλεκτρονικός υπολογιστής του οργανισμού μας
 ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ - ΜΕΡΟΣ Α Ο ηλεκτρονικός υπολογιστής του οργανισμού μας Ρόλος του νευρικού συστήματος Το νευρικό σύστημα (Ν.Σ.) ελέγχει, ρυθμίζει και συντονίζει όλες τις λειτουργίες του οργανισμού ανάλογα
ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ - ΜΕΡΟΣ Α Ο ηλεκτρονικός υπολογιστής του οργανισμού μας Ρόλος του νευρικού συστήματος Το νευρικό σύστημα (Ν.Σ.) ελέγχει, ρυθμίζει και συντονίζει όλες τις λειτουργίες του οργανισμού ανάλογα
Κλινική Νευροψυχολογία του παιδιού
 Κλινική Νευροψυχολογία του παιδιού Α εξάμηνο Διδάσκων : Α. Β. Καραπέτσας Ακαδημαϊκό έτος 2015-2016 1 ΜΟΥΣΙΚΗ ΚΑΙ ΜΝΗΜΗ 2 Μία από τις πρώτες έρευνες που μελετούν και επιβεβαιώνουν ότι τα άτομα με μουσική
Κλινική Νευροψυχολογία του παιδιού Α εξάμηνο Διδάσκων : Α. Β. Καραπέτσας Ακαδημαϊκό έτος 2015-2016 1 ΜΟΥΣΙΚΗ ΚΑΙ ΜΝΗΜΗ 2 Μία από τις πρώτες έρευνες που μελετούν και επιβεβαιώνουν ότι τα άτομα με μουσική
Κινητικό σύστηµα. Κινητικός φλοιός
 Κινητικό σύστηµα Κινητικός φλοιός Κινητικός φλοιός Όλες οι εκούσιες κινήσεις ελέγχονται από τον εγκέφαλο Μια από τις περιοχές του εγκεφάλου που εµπλέκονται στον έλεγχο των εκούσιων κινήσεων είναι ο κινητικός
Κινητικό σύστηµα Κινητικός φλοιός Κινητικός φλοιός Όλες οι εκούσιες κινήσεις ελέγχονται από τον εγκέφαλο Μια από τις περιοχές του εγκεφάλου που εµπλέκονται στον έλεγχο των εκούσιων κινήσεων είναι ο κινητικός
Βασικοί μηχανισμοί προσαρμογής
 ΣΥΓΚΡΙΤΙΚΗ ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ 23-24, 18/4/2016 Π.Παπαζαφείρη Βασικοί μηχανισμοί προσαρμογής Προσαρμογή σε μοριακό και γονιδιακό επίπεδο Επίπεδα ελέγχου 1. Πρωτεïνική δράση 2. Πρωτεïνοσύνθεση 3. Ρύθμιση της
ΣΥΓΚΡΙΤΙΚΗ ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ 23-24, 18/4/2016 Π.Παπαζαφείρη Βασικοί μηχανισμοί προσαρμογής Προσαρμογή σε μοριακό και γονιδιακό επίπεδο Επίπεδα ελέγχου 1. Πρωτεïνική δράση 2. Πρωτεïνοσύνθεση 3. Ρύθμιση της
«Η ομορφιά εξαρτάται από τα μάτια εκείνου που τη βλέπει»
 «Η ομορφιά εξαρτάται από τα μάτια εκείνου που τη βλέπει» Γνωστική Νευροεπιστήμη Πώς γίνεται αντιληπτή η αισθητική πληροφορία; Πώς σχηματίζονται οι μνήμες; Πώς μετασχηματίζονται σε λόγο οι αντιλήψεις και
«Η ομορφιά εξαρτάται από τα μάτια εκείνου που τη βλέπει» Γνωστική Νευροεπιστήμη Πώς γίνεται αντιληπτή η αισθητική πληροφορία; Πώς σχηματίζονται οι μνήμες; Πώς μετασχηματίζονται σε λόγο οι αντιλήψεις και
Οι Κυριότερες Νευρικές Οδοί. Ανιόντα (Κεντροµόλα) Δεµάτια
 Οι Κυριότερες Νευρικές Οδοί Ανιόντα (Κεντροµόλα) Δεµάτια φυσιολογικά δεµάτια (κατά τον επιµήκη άξονα) έχουν κοινή έκφυση πορεία απόληξη λειτουργία Κατιόντα (φυγόκεντρα) δεµάτια Ανιόντα (κεντροµόλα) δεµάτια
Οι Κυριότερες Νευρικές Οδοί Ανιόντα (Κεντροµόλα) Δεµάτια φυσιολογικά δεµάτια (κατά τον επιµήκη άξονα) έχουν κοινή έκφυση πορεία απόληξη λειτουργία Κατιόντα (φυγόκεντρα) δεµάτια Ανιόντα (κεντροµόλα) δεµάτια
