Numele și prenumele elevului: Unitatea de învățământ:
|
|
|
- Τιτάνια Αρβανίτης
- 6 χρόνια πριν
- Προβολές:
Transcript
1 clasa 9 Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a IV-a Formular de concurs Clasa a IX-a Toate subiectele sunt obligatorii, un singur răspuns este corect la fiecare item. Pentru fiecare subiect, completați răspunsul pe care îl considerați corect, cu simbolul în grila de evaluare, și pe foaia cu subiectele. Barem: Subiectele 1-15 sunt cotate cu 2 puncte Subiectele sunt cotate cu 4 puncte Subiectele sunt cotate cu 6 puncte Punctaj maxim 100 puncte. Timp de lucru 80 minute. Succes! 1. Sarcina electrică a nucleului este: a) pozitivă și egală cu numărul b) pozitivă și egală cu de neutroni. numărul de protoni. c) negativă și egală cu numărul de neutroni. 2. Conține doar 3 electroni pe ultimul strat: a) N (Z = 7) b) Al (Z = 13) c) Cl (Z = 17) 3. Precizați care dintre ionii de mai jos au configurație de gaz inert: a) S 2-, Cl -, Mg 2+, P 3- b) S 2-, Br +, Sc 3+, Mg 2+ c) P 2-, Cl -, Mg 2+, Sc 3+ (Z: Br=35, Cl=17; Mg=12; P=15, Sc=21, S=16) 4. Se prepară două soluții: soluția I (care conține 12 grame substanță la 150 grame soluție) și soluția II (care conține 20 grame de substanță la 350 grame de soluție). Care dintre următoarele afirmații este adevărată?: a) soluția II este mai diluată decât soluția I b) soluțiile I și II au concentrații procentuale egale c) soluția II este mai concentrată decât soluția I 5. Care este afirmația falsă privind razele ionice: a) raza ionilor pozitivi b) raza ionilor pozitivi (cationilor) este mai mică (cationilor) este egală cu decât raza atomilor din care raza atomilor din care provin provin c) raza ionilor negativi (anionilor) este mai mare decât raza atomilor din care provin 1 / 4
2 Plumbul se găsește în natură sub forma izotopilor naturali: 82Pb (1,36%); 82Pb (25,12%); 82Pb 208 (21,25%); 82Pb (52,57%). Precizați masa atomică relativă a plumbului, poziția în sistemul periodic și numărul electronilor de valență: a) 208,23; grupa 4, b) 207,85; grupa 14, c) 207,85; grupa 14, perioada a 6-a; 2; perioada a 6-a; 4 perioada a 5-a; 4 7. Elementele chimice din grupa 13 (IIIA) au electronul distinctiv situat în : a) substratul de tip d b) substratul de tip s c) substratul de tip p 8. Reacția de disociere termică a oxidului mercuric: HgO Hg+1/2 O2 prezintă interes istoric, ea fiind folosită de Priestley în anul 1774, pentru a prepara pentru prima dată oxigen pur. Știind că s-au obținut 0,025 mmoli de oxigen, cantitatea de oxid mercuric supusă analizei este: (AHg=200,6, AO=16). a) 10,83 mg b) 10,83 g c) 21,66 mg 9. Seria care cuprinde simbolurile unor elemente chimice cu caracter metalic este: a) Ru, Rb, Rh, Rn b) Ra, Rb, Rh, Rn c) Ru, Rb, Rh, Ra 10. Sulful se găsește în grupa 16, perioada a III-a. Configurația electronică a ionului sulfură este: a) 1s 2 2s 2 2p 6 3s 2 3p 4 b) 1s 2 2s 2 2p 6 3s 2 3p 2 c) 1s 2 2s 2 2p 6 3s 2 3p Care dintre cele trei configurații respectă regulile de completare a învelișului electronic: a) 1s 2 2s 1 2p 6 3s 2 3d 10 3p 2 b) 1s 2 2s 2 2p 8 3s 2 3p 6 4s 2 c) 1s 2 2s 2 2p 6 3s 2 3p Ionul E 3- are configurația electronică a kriptonului (Z=36). Elementul E are configurația electronică: a) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 3 b) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 c) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 7 4p Speciile izoelectronice cu 10Ne sunt: a) NaCl, H2O, NH3, CH4; b) C 4-, N 3-, O 2-, F - ; c) Na +, Mg 2+, Al 3+, C 4+ (Z: Na=11, H=1, O=8, C=6, N=7, F=9, Mg=12, Al=13, Cl=17) 14. Se găsesc 32 protoni în: ( O, 1H, 16S) a) o moleculă de O2 b) 16 molecule de H2 c) un atom de S 15. Caracterul chimic al elementului cu Z=37 este : a) metalic b) nemetalic c) semimetalic 2 / 4
3 16. Andreea are un medalion din argint marca 925 (92,5%Ag) care cântărește 2,95 g. Fiind curioasă, a calculat că medalionul are: a) 1,08 moli de argint pur b) 0,250 moli Ag pur c) 0,025 moli Ag pur (AAg = 108) 17.Se neutralizează 100 g de soluție de NaOH de concentrație 40% cu 100 g de soluție HCl de concentrație 16,25%. În soluția finală culoarea fenolftaleinei este: a) Albastră b) Roză c) Incoloră 18. Pentru dublarea concentrației a 200 g de soluție de NaOH 15% este necesară: a) adăugarea a 100 g de NaOH b) evaporarea a 30 g de apă c) adăugarea a 0,3 kg de soluție NaOH 40% 19. Un amestec format din 12 g pilitură de Mg şi 20 g pulbere de S se încălzește pentru a forma MgS; în exces s-au luat: a) 16 g S b) 4 g S c) 3 g Mg (AS=32, AMg=24) 20. Un balon de 200 ml este umplut până la semn cu o soluție de NaOH de concentrație 40% cu ρ= 2,5 g/cm 3. Numărul de moli de substanță dizolvată în această soluție este? a) 5 b) 200 c) 40 (ANa=23, AH=1, AO=16) 21. Câte grame de hidroxid de sodiu tehnic (care conține 97 % NaOH) sunt necesare pentru a prepara 250 g de soluție de NaOH 15%? a) 37,5 g b) 38,6 g c) 3,86 g 22. Pentru conservarea lemnului este utilizată o soluție de clorură de zinc 30%. Masa de zinc necesară preparării a 25 kg dintr-o astfel de soluție este: a) 7,17 kg b) 3,6 kg c) 3,26 kg (AZn=65,38, ACl=35,5, AH=1, Ao=16) 23. Rivanolul, soluție pentru dezinfectat rănile, are formula C18H21N3O4. Câte molecule de rivanol se găsesc în 25 g soluție de concentrație 1%? a) 4, molecule b) 1, molecule c) 1, molecule (AC=12, AH=1, AO=16, AN=14) 3 / 4
4 24. Într-un termometru se află 1,48 ml Hg (ρ = 13,53g/cm 3 ). La ora de chimie, elevii au calculat că în termometrul respectiv se află: a) 0,1 moli Hg b) 0,2 moli Hg c) 2 mg Hg (AHg=200,6) 25. În acumulatorul cu plumb se utilizează soluție de H2SO4 38% (ρ = 1,29 g/ml). Volumul de soluție de acid sulfuric 98% (ρ = 1,84 g/ml) necesar obținerii a 2 litri soluție pentru acumulator este: a) 0,98 L b) 0,54 L c) 1,05 L 26. Puritatea pietrei de var pentru care prin descompunere termică completă (impuritățile sunt stabile termic), masa acesteia scade cu 33% este: a) 90% b) 75% c) 66% (ACa=40, AO=16, AC=12). 27. Într-un vas cu 100 g apă se introduc 25 g sodiu. Concentrația procentuală a bazei obținute este: a) 35,08% b) 34,78% c) 20% (ANa=23, AH=1, AO=16) 28. Galbenul de zinc este un pigment de culoare galbenă folosit în industria coloranților și are formula 3(ZnCrO4) K2CrO4. Să se determine raportul masic al elementelor din moleculă (Zn:Cr:K:O), numărul de atomi existent într-un mol de pigment și cât cântărește o moleculă de pigment. (AZn=65; ACr=52; AK=39; AO=16). a) 1,5 : 2 : 1 : 8; 1, atomi; 1, g b) 2,5 : 2,67 : 1 : 3,28; 1, atomi; 1, g c) 1,5 : 2 : 1 : 8; 1, atomi; 122, g 29. Pe eticheta unui flacon cu 90 ml sirop expectorant (ρsirop = 1,111 g/ml) se precizează că acesta conține 0,1% NH4Cl. Ana a calculat câte molecule de NH4Cl i se administrează într-o zi frățiorului ei dacă acesta primește la fiecare 8 ore câte 5 ml sirop și numărul de zile în care acesta va termina flaconul cu sirop. (ACl=35,5, AN=14, AH=1). a) 1, molecule, 6 zile b) 1, molecule, 6 zile c) 1, molecule, 9 zile 30. Un precipitat umed de AgCl conține 56% apă și 1,01% impurități. Puritatea produsului uscat va fi: a) 9,70% b) 58,5% c) 97,7% 4 / 4
5 clasa 10 Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a IV-a Formular de concurs Clasa a X-a Toate subiectele sunt obligatorii, un singur răspuns este corect la fiecare item. Pentru fiecare subiect, completați răspunsul pe care îl considerați corect, cu simbolul în grila de evaluare, și pe foaia cu subiectele. Barem: Subiectele 1-15 sunt cotate cu 2 puncte Subiectele sunt cotate cu 4 puncte Subiectele sunt cotate cu 6 puncte Punctaj maxim 100 puncte. Timp de lucru 80 minute. Succes! 1. Unul dintre primele parfumuri sintetice introduse de Coco Chanel în 1921 conținea compusul cu structura de mai jos. Numărul de atomi de carbon primari din structură sunt: A) 1 B) 2 C) 3 2. Care dintre compușii de mai jos prezintă atât o grupare funcțională acidă cât și o grupare funcțională alcoolică? A) acid lactic B) Acid benzoic C) Acid acetic 3. Câți izomeri are compusul cu formula C5H10: A) 10 B) 6 C) 5 4. Polietena, polimer obținut în industria chimică prin reacţia de polimerizare a etenei, este folosită la fabricarea foliilor pentru ambalaje, pungi, saci și pentru izolarea cablurilor electrice. Ştiind că în urma reacției de polimerizare se obține polietena cu masa molară de g/ mol, gradul de polimerizare este: A) 1000 B) 1200 C) / 4
6 5. Compusul organic de mai jos este un medicament utilizat pentru tratamentul tuberculozei şi are formula structurală: Procentul masic de azot din compus este: A) 9,15 % B) 10,28 % C) 16,76 %. 6. Pentru sinteza unui monomer utilizat în obținerea fibrelor sintetice se folosește HCN, care este un lichid incolor, extrem de toxic, care în cantități foarte mici poate produce moartea. Acidul cianhidric se obține din: A) C3H4 B) CH4 C) C6H6 7. Ce relație există între structurile de mai jos? A) izomeri de catenă B) reprezintă același compus C) au puncte de fierbere diferite 8. Radicalul vinil are formula: A) CH2=CH-CH2- B) CH2=CH- C) CH3-CH=CH-CH2-9. Un inginer chimist a determinat experimental, în condiții normale, punctele de fierbere ale butanului, cis-2-butenei și trans-2-butenei, obținând următoarele date: 3,7 C; 0,96 C și -0,5 C. Punctul de fierbere corespunzător fiecărui compus este: A) butan: 3,7 C, cis-2-butena: 0,96 C, trans-2-butena: -0,5 C. B) butan: 3,7 C, cis-2-butena: -0,5 C, trans-2-butena: 0,96 C. C) butan: -0,5 C, cis-2-butena: 3,7 C, trans-2-butena: 0,96 C. 10. Ordinea creșterii punctului de fierbere pentru seria de alcani este: A) 2-metilheptan, B) 2,2,4-trimetilpentan, octan, 2-metilheptan, 2,2,4-trimetilpentan octan C) octan, 2-metilheptan, 2,2,4-trimetilpentan. 11. n-butanul este un gaz inflamabil care intră în compoziția gazului de sondă, având efect narcotic. În molecula sa se găsesc: A) legături σ B) legături π C) legături π și legături σ 12. Care dintre denumirile IUPAC de mai jos este cea corectă: A) 2-metil-5-izopropilheptan B) 2,2-dimetil-4-etilheptan C) 3,5-dietil-3-izopropil-2,2,6- trimetilheptan 2 / 4
7 13. Acetatul de izopentil este compusul chimic responsabil de aroma de banană, formula structurală fiind redată mai jos. Formula moleculară a acestuia este: A) C7H14O2 B) C6H11O2 C) C5H14O2 14. Tetradecanul (C14H30) are punctul de topire 5,9 C și punctul de fierbere 254 C. Starea sa de agregare la temperatura camerei este: A) solidă B) lichidă C) gazoasă 15. Denumirea corespunzătoare structurii de mai jos este: A) 2-metil-2-butena B) 2-metil-3-butena C) izobutena 16. Polietilena este un polimer cu aplicabilitate în ambalaje, implanturi medicale, echipamente sportive etc. care se obține prin polimerizarea etenei. Care este compoziția în procente de masă a etenei? A) 74,21%C; 26,8%H B) 85,71%C; 14,28%H C) 89%C; 11%H 17. Care dintre alchenele de mai jos prezintă izomerie cis-trans? A) 3-hexena B) 2-metil-2-hexena C) 2,3-dimetil-2-hexena 18. O hidrocarbură saturată aciclică, obținută la rafinarea țițeiului, este o componentă importantă din benzină și are masa molară M= 86 g/mol. Determinați formula moleculară a hidrocarburii și numărul izomerilor posibili. A) C6H14, 5 izomeri B) C6H14, 6 izomeri C) C5H12, 4 izomeri 19. Negrul de fum, unul dintre cei mai folosiți pigmenți anorganici, în special la colorarea cauciucului, se obține prin arderea incompletă a metanului. Cantitatea de aer necesară arderii incomplete a 10 moli de metan în condiții normale este: A) 2240 litri B) 1220 litri C) 1120 litri 20. Alchena care prin oxidare cu permanganat de potasiu si acid sulfuric formează un mol de acid acetic și un mol de acetonă este: A) 2-pentenă B) 2-metil-2-butenă C) 2-metil-1-butenă 21. Prin halogenarea la 300 C a unui alcan cu formula moleculară C5H12 rezultă un singur derivat monohalogenat. Alcanul este: A) izopentan B) n-pentan C) neopentan 22. Într-un cilindru se găsesc 80 kg metan la 100 atm. Folosind o parte din gaz, presiunea din cilindru scade la 30 atm. Cantitatea de metan rămasă în cilindru este: A) 24 kg B) 42 kg C) 34 kg 3 / 4
8 23. Prin arderea cu oxigen a unei substanțe organice se formează 19,8 g dioxid de carbon, 4,725 g apă și 840 ml azot gazos. Formula moleculară a substanței supuse arderii este: A) C6H8N2 B) C7H9N C) C6H7N 24. Se consideră o alchenă care prezintă în structură un singur atom de C primar. Dacă la 5,6 g de alchenă se adiţionează brom (20 g soluţie de concentraţie 80 %), alchena este: A) 1-butena B) 2-butena C) 1-pentena 25. Alcanul cu structura de mai jos are denumirea: A) 7-etil-4,8-dimetil-6-propildecan B) 4-etil-3,7-dimetil-6-propildecan C) 4-etil-3-metil-6-butilundecan 26. Un amestec de metan și etenă ocupă un volum de 100 L. Prin combustia completă a celor două gaze rezultă 175 L CO2. Compoziția amestecului în volume este: A) 75 L metan și 25 L etenă B) 25 L metan și 75 L etenă C) 50 L metan și 50 L etenă 27. Prin arderea unui amestec de două alchene A (M= 42 g/mol) și B (M= 56 g/mol), conținând 40% (v/v) hidrocarbură A, se obțin 40 g CO2. Volumele de alchene luate în lucru sunt: A) 3,39 L butenă B) 1,13 L propenă C) 2,26 L propenă și 2,26 L etenă și 1,69 L butenă și 3,39 L butenă 28. Prin descompunerea termică a propanului se obține un amestec gazos care conține 25% C2H4, 15% C3H6, restul H2, CH4 și propan netransformat. Procentul de propan transformat în C3H6 este: A) 25 % B) 15 % C) 37,5 % 29. Ce volume de metan și clor sunt necesare pentru obținerea a 80 kmoli cloroform, știind că raportul molar al produșilor de reacție este CH3Cl : CH2Cl2 : CHCl3 : CCl4 = 1: 3 : 4 : 2? A) 4480 m 3 metan, m 3 clor B) 1344 m 3 metan, 3584 m 3 clor C) 3136 m 3 metan, 5376 m 3 clor 30. Butanul este materia primă în industria chimică pentru obţinerea maselor plastice, a cauciucului sintetic, a săpunurilor şi detergenţilor. Un amestec de butan și metan cu un conținut de 75% metan (v/v), prin ardere formează 23,52 L CO2. Numărul de moli de butan și metan este: A) 0,5 moli butan și 1,5 moli metan B) 1,5 moli butan și 3,5 moli metan C) 0,15 moli butan și 0,45 moli metan Notă! Se dau masele atomice: C = 12, H = 1, N = 14, O = 16, S = 32, Br = 80, Cl = 35,5. Aerul conține 20% O2; 760 torri = 1 atm, R = 0,0821 atm L/kmol 4 / 4
9 clasa 11 Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a IV-a Formular de concurs Clasa a XI-a Toate subiectele sunt obligatorii, un singur răspuns este corect la fiecare item. Pentru fiecare subiect, completați răspunsul pe care îl considerați corect, cu simbolul în grila de evaluare, și pe foaia cu subiectele. Barem: Subiectele 1-15 sunt cotate cu 2 puncte Subiectele sunt cotate cu 4 puncte Subiectele sunt cotate cu 6 puncte Punctaj maxim 100 puncte. Timp de lucru 80 minute. Succes! 1. Compușii cu structura de mai jos se deosebesc prin mirosul degajat: (1) are aromă de mentă, iar (2) are aromă de semințe de chimen. Cele două structuri se găsesc în relația de: A) izomeri de catenă B) enantiomeri C) nici una 2. Colesterolul, o lipidă cu structură steroidică întâlnită în organismele animale prezintă 8 centre chirale. Numărul de stereoizomeri posibili pentru o substanță cu 8 centre chirale este: A) 16 B) 256 C) Bronopolul este un derivat halogenat care nu prezintă toxicitate, fiind utilizat ca agent antimicrobian în servețelele umede pentru copii. Numărul de enantiomeri pe care îi prezintă sunt: A) 0 B) 2 C) 4 4. Diclordifeniltricoloroetanul (DDT) a fost utilizat pentru prima dată în 1930, fiind primul insecticid folosit pentru distrugerea țânțarilor și eradicarea malariei. Numărul de carboni asimetrici pe care îi prezintă în structură sunt în număr de: A) 0 B) 1 C) 2 1 / 4
10 5. Denumirea corectă pentru următoarea structură este: A) 3-cloro-3-propilhexan B) 4-cloro-4-propilhexan C) 4-cloro-4-etilheptan 6. Amfetamina este un compus utilizat în tratarea copiilor cu deficiență de atenție (cunoscută sub denumirea de ADHD) și a sindromului oboselii cronice. În timpul celui de-al doilea război mondial a fost utilizată de către soldați pentru reducerea oboselii și creșterea vigilenței. Numărul de enantiomeri pe care îi prezintă sunt: A) 2 B) 4 C) 6 7. Prin încălzirea 2-cloropropanului cu o soluție apoasă de NaOH rezultă ca produs principal: A) Alcool propilic B) Alcool izopropilic C) Propenă 8. Prin hidroliza unui derivat dihalogenat, în care atomii de halogen sunt legați de atomi de carbon diferiți, se obțin: A) Dioli B) Aldehide sau cetone C) Acizi carboxilici 9. Cu ce alchenă trebuie alchilat benzenul pentru a obţine o hidrocarbură cu raportul masic C : H = 9 : 1? A) etena B) butena C) propena 10. Toluenul, o hidrocarbură aromatică din seria benzenului, este utilizat ca solvent industrial, la prepararea unor coloranți și a unor medicamente. Tratarea acestuia cu clor în prezenţă de clorură de aluminiu anhidră (AlCl3) conduce la: A) clorură de benzil B) meta-clorotoluen C) un amestec de ortoşi para-clorotoluen 11. Perechile de compuși de mai jos se găsesc în relația: A) enantiomeri B) diastereoizomeri C) amestec racemic 12. Capsaicina este compusul responsabil de gustul arzător al ardeiului iute. Aplicată pe piele în doze moderate determină o senzația de căldură, iar în doze mari provoacă arsuri. Capsaicina este optic inactivă? A) nu B) da C) nu poate fi determinat 13. O hidrocarbură cu formula moleculară C4H8 nu reacționează cu clorul la întuneric, însă la lumina solară formează un singur derivat monoclorurat. Identificați hidrocarbura. A) 2-butena B) ciclobutan C) metilciclopropenă 2 / 4
11 14. Într-o instalație de fabricare a clorobenzenului s-au introdus 800 kg clor și s-au obținut 1125 kg derivat monohalogenat. Randamentul de transformare al clorului este: A) 100 % B) 90,75 % C) 88,75 % 15. Prin clorurarea propilenei se obține 1,2-dicloropropan, un solvent inflamabil, care afectează sistemul nervos central și cel respirator. Conținutul procentual de clor din formula 1,2-dicloropropanului este: A) 85,2% B) 77,25% C) 62,83% 16. Viteza de dehidrohalogenare pentru următorii derivați halogenați scade în ordinea: A) 1 > 2 > 3 B) 3 > 2 > 1 C) 2 > 1 > Indicați produșii obținuți în fiecare dintre reacțiile următoare: a) A: 2-bromobutan, B: bromură de 1-butilmagneziu C: butan b) A: 2-bromobutan, B: bromură de sec-butilmagneziu C: butan c) A: 2-bromobutan, B: bromură de butilmagneziu C: pentan 18. Tetraclorura de carbon, folosită la stingerea incendiilor la instalațiile electrice, se obține prin clorurarea metanului. Dacă s-a lucrat cu un randament de 86,5%, ce volum de metan s-a consumat pentru fabricarea unei cantități de 200 kg CCl4? A) 33,3 m 3 B) 33,6 m 3 C) 36,6 m O hidrocarbură cu formula moleculară C5H10 formează prin clorurare cu Cl2 la 500ºC un singur compus monoclorurat, iar prin oxidare cu K2Cr2O7/H2SO4 formează acidul 2-metilpropionic. Hidrocarbura este: A) 1-pentenă B) 3-metil-1-butenă C) izopren 20. Prin tratarea cu apă a 20 kg carbură de calciu tehnică (carbid) s-au obținut 4480 litri acetilenă, măsurați în condiții normale. Puritatea carburii de calciu este: A) 64% B) 56% C) 46% 21. Stirenul se fabrică din benzen prin intermediul etilbenzenului. Știind că randamentul etapei intermediare este de 95% și a celei finale de 90%, randamentul global este: A) 88,5% B) 85,5% C) 58,8% 22. Prin dehidrohalogenarea unui derivat halogenat optic activ rezultă două alchene izomere cu formula moleculară C6H12, în proporții diferite. Alchena rezultată ca produs majoritar prezintă izomerie geometrică, în timp ce alchena rezultată ca produs secundar nu prezintă izomerie geometrică. Derivatul halogenat este: A) 2-cloro-2-metilpentan B) 2-cloro-3-metilpentan C) 3-cloro-2-metilpentan 23. Compusul aromatic monoclorurat A, cu un conţinut de 28,06% clor, suferă următoarea transformare: Compusul A este: a) clorobenzen b) clorura de benzil c) clorotoluen 3 / 4
12 24. Alchena cu structura de mai jos poate fi obținută prin dehidrohalogenarea a doi derivați halogenați achirali diferiți. Structurile derivaților halogenați sunt : A) 2-cloro-2-metilpropan B) 1-cloro-2-metilpropan și 1-cloropropan și 2-cloro-2-metilpropan C) 2-cloro-2-metilpropan și 1-cloro-1-metilpropan 25. Produsul majoritar de eliminare care se formează prin tratarea 2-bromo-3-metilbutanului cu KOH/etanol este: A) 3-metil-1-butena B) 2-metil-2-butena C) 3-metil-2-butanol 26. Se fabrică acetilenă prin procedeul în arc electric. Din 1000 m 3 metan, măsurat în condiții normale, se obține în cuptorul electric un amestec volumetric de gaze ce conține 20% acetilenă, 20% metan netransformat și restul hidrogen. Conversia la o trecere a materiei prime prin cuptor este: A) 33,33% B) 66,67 % C) 85% 27. Se hidrogenează cu un randament de 89,8% benzenul în prezență de Ni-Raney drept catalizator, obținându-se produsul ciclic saturat Y. Știind că se lucrează cu un exces de 15% hidrogen, volumul de gaz necesar pentru fabricarea a 156 tone produs Y de puritate 91% este: A) 123, m 3 H2 B) 145, m 3 H2 C) 191, m 3 H2 28. Hidrocarburile alifatice pot fi utilizate drept combustibili, materii prime pentru obţinerea de macromolecule sau pot fi transformate în compuși cu aplicații practice pentru industriile cosmetică și farmaceutică. Un amestec de etenă, propan, propenă și hidrogen în raport molar 4:1:2:8 se trece peste un catalizator de platină, sub presiune și la temperatură ridicată. Raportul dintre numărul de moli din amestecul inițial și numărul de moli după reacție și compoziția în procente de moli a amestecului final sunt: A) raport = 3:1; compoziție: 44,44% etan, 22,33% propan, 33,22% hidrogen B) raport = 5:3; compoziție: 44,44% etan, 33,33% propan, 22,22% hidrogen C) raport = 4:3; compoziție: 40 % etan, 20 % propan, 30 % hidrogen 29. Clorobenzenul este folosit ca intermediar în sinteza insecticidului DDT. Halogenarea benzenului cu o conversie totală de 70%, conduce la un amestec de produși mono-, di- și trihalogenați, în raport molar de 4:2:1. Dacă halogenul s-a consumat în totalitate, raportul molar inițial clor : benzen este: A) 1,1 : 1 B) 1 : 2 C) 2 : Prin clorurarea în condiții normale a 0,6 m 3 metan s-au obținut numai primii doi derivați halogenați ai acestuia. Având în vedere că s-a utilizat 1 m 3 Cl2 și că acesta s-a transformat integral, raportul molar între produșii de reacție este: A) 1 : 2 B) 2 : 1 C) 1 : 3 Notă! Se dau masele atomice: C = 12, H = 1, N = 14, O = 16, Ca = 40, Cl = 35,5. 4 / 4
13 clasa 12 Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a IV-a Formular de concurs Clasa a XII-a Toate subiectele sunt obligatorii, un singur răspuns este corect la fiecare item. Pentru fiecare subiect, completați răspunsul pe care îl considerați corect, cu simbolul în grila de evaluare, și pe foaia cu subiectele. Barem: Subiectele 1-15 sunt cotate cu 2 puncte Subiectele sunt cotate cu 4 puncte Subiectele sunt cotate cu 6 puncte Punctaj maxim 100 puncte. Timp de lucru 80 minute. Succes! 1. Arderea combustibililor solizi, necesară pentru obținerea agentului termic în halele de producție este un proces: a) endoterm, care nu necesită oxigen b) exoterm, care necesită oxigen c) nu este însoțit de efecte termice 2. Neutralizarea reprezintă o etapă importantă în procesele de tratare ale apelor uzate industriale. Reacția de neutralizare care stă la baza acestei etape are loc: a) cu formare de precipitat b) cu degajare de căldură c) nu este însoțit de efect termic 3. Precizați care proces este endoterm: a) adăugarea de apă în H2SO4 b) topirea unui cub de gheață c) adăugarea unor granule de KOH în apă 4. În condiții standard, valoarea căldurii de neutralizare a unui acid tare cu o bază tare cu o bază tare este de: a) 57,33 kj/mol, indiferent de acidul tare sau baza tare b) 17,35 kcal/mol, indiferent de acidul tare sau baza tare c) depinde de natura acidului tare 5. Selectați răspunsul corect: a) Într-o reacție chimică, valoarea efectului termic nu depinde de starea inițială a reactanților și de cea finală a produșilor și nu depinde de etapele intermediare. b) Într-o reacție chimică, valoarea efectului termic depinde numai de starea inițială a reactanților și de cea finală a produșilor și nu depinde de etapele intermediare. c) Într-o reacție chimică, valoarea efectului termic depinde de starea inițială a reactanților, de cea finală a produșilor și de etapele intermediare. 6. Cunoscând entalpiile standard de formare pentru următorii dioxizi, precizați care este cel mai stabil: SO2(g): = -296,61 kj/mol, SiO2(s): = -858,57 kj/mol, NO2(g): = 33,82 J/mol H f a) SiO2 b) NO2 c) SO2 H f H f 1 / 4
14 7. Dacă într-o reacție chimică variația de entalpie este H = -95 J putem afirma că: a) sistemul primește 95 J, în timp ce mediul înconjurător cedează 95 J b) sistemul cedează 95 J, în timp ce mediul înconjurător primește 95 J c) atât sistemul cât și mediul exterior pierd 95 J 8. Comparați entalpiile următorilor oxizi și aranjați-i în ordinea descrescătoare a stabilități: Substanța CO2 (g) CO (g) NO(g) SO2 (g), -393,2-110,4 +90, o H f kj / mol a) CO2 (g) > CO (g) > > SO2 (g) > NO(g) b) NO(g) > CO(g) > > SO2(g) > CO2(g) c) CO2 (g) > SO2 (g) > > CO (g) > NO(g) 9. Se dau următoarele ecuații termochimice. Care dintre acestea sunt endoterme? C(s) + O2(g) Q1 CO2(g) H2(g) + I2(g) +Q2 2HI(g) SeO2(s) + 2C(s) + Q3 Se(s) +2CO(g) a) reacțiile și b) reacțiile și c) reacțiile și 10. Puterea calorică a unui combustibil lichid sau solid este dată de: a) Cantitatea de căldura b) Cantitatea de căldură degajată degajată la arderea completă a la arderea completă a unei mase unei mase de 1 kg de 10 kg c) Cantitatea de căldură degajată la arderea completă a unei mase de 1 t 11. Entalpia molară de formare a unui compus: a) este entalpia reacției de b) este entalpia reacției de formare a unui mol de formare a unui kilogram de substanță din elementele substanță din elementele componente componente c) este căldura degajată sau absorbită în reacția la care participă un kg de substanță 12. Prin arderea combustibililor fosili se formează cantități semnificative de CO și CO2 care ajung în atmosferă, contribuind astfel la fenomenul de încălzire globală. Știind că entalpia de formare a CO este de -110,5 kj/mol, iar cea a CO2 este de -393,5 kj/mol, se poate spune: a) CO2 este mai stabil decât CO, și se formează în cantități mai mari b) CO este mai stabil decât CO2, și se formează în cantități mai mari c) CO şi CO2 au stabilități comparabile, și se formează în cantități egale 13. Emisiile de CO2 și alte gaze poluante sunt reglementate de norme internaționale de tipul EURO I, II, V. O anumită mașină prin arderea benzinei produce 120 g CO2/km (ardere totală). Presupunând că benzina (ρbenzen = 740 kg/m 3 ) conține doar un alcan cu 7 atomi de carbon să se calculeze consumul de combustibil al acestei mașini în litri carburant pentru 100 km parcurși. a) 5,26 litri b) 3,86 litri c) 2,86 litri 14. Pentru încălzirea unei hale de producție se consumă zilnic 5 gigacalorii ( calorii). Știind că prin arderea unui mol de CH4(g) se produce o cantitate de căldură de 212,8 kcal, volumul de gaz metan necesar pentru încălzirea halei timp de 5 zile este: a) 657,8 m 3 b) 1315,6 m 3 c) 2631,5 m La neutralizarea a 250 ml soluție NaOH 2M cu o soluție diluată de HBr se degajă o cantitate de căldură de 28,63 kj. Calculați căldura degajată la neutralizarea a 2,5 moli NaOH. a) 114,52 kj b) 143,15 kj c) 57,26 kj 2 / 4
15 16. La scară industrială, alcoolul etilic se obține prin fermentația anaerobă a glucozei în prezența unor enzime, conform reacției:c6h12o6(aq) 2 C2H5OH(aq) + 2 CO2(g) Știind că: Hf(C6H12O6(aq)) = kj/mol; Hf(C2H5OH(aq)) = - 277,7 kj/mol şi Hf(CO2(g)) = - 393,5 kj/mol, căldura degajată la fermentația 10 moli de glucoză este de: a) -82,4 kj b) -824 kj c) -412 kj 17. Să se calculeze căldura de condensare a 72 g apă, cunoscând: o H f (H2O (l)) = -68,3 kcal/mol. o H f a) -126,1 kcal/mol b) 10,5 kcal/mol c) -42 kcal/mol (H2O (g)) = -57,8 kcal/mol; 18. Se dă ecuația termochimică: H2S(g) + 3/2O2(g) SO2(g) + H2O(g) + 558,66 kj o o şi căldurile de formare pentru H f (SO2(g)) = -297 kj/mol, H f (H2O(g)) = -241,6 kj/mol. Știind că 1 cal = 4,18 J, căldura de formare pentru H2S (în kcal/mol) este: a) 5,12 kcal/mol b) 3,26 kcal/mol c) 4,79 kcal/mol 19. O piesă de 50g de fier care are temperatura inițială de 225 C este pusă în contact direct cu o piesă de 50g de aur care are temperatura inițială de 25 C. (Căldura specifică pentru fier este 0,449 J/g C, iar pentru aur 0,128 J/g C ). Temperatura finală de echilibru a celor două metale, dacă se consideră că nu sunt pierderi de căldură în mediul exterior este: a) 172 C b) 191 C c) 181 C 20. Industrial, prelucrarea pieselor metalice necesită carbură de wolfram (WCsolid) pentru finisare. Determinați variația de entalpie exprimată în kj a reacției de formare a carburii de wolfram (sau carbura de tungsten): W(s) + C(grafit) WC(s), utilizând următoarele date termochimice: 2W(s) + 3O2(g) 2WO3(s) ΔHa = -1680,6 kj C(grafit) + O2(g) CO2(g) ΔHb = -393,5 kj 2WC(s) + 5O2(g) 2WO3(s) +2CO2(g) ΔHc = -2391,6 kj a) -38 kj b) -22 kj c) -35 kj 21. Pe baza următoarelor ecuații termochimice determinați căldura de formare a C5H12 (g): (1) C(s) + O2 (g) CO2 (g), (2) H2(g) + 1/2 O2 (g) H2O (g), o H f = -393,2 kj/mol o H f = -241,6 kj/mol o (3) C5H12 (g) + 8O2 (g) 5CO2 (g) + 6H2O(g), H r = -3269,3 kj/mol. a) -126 kj b) -146,3 kj c) 126 kj 22. Să se calculeze căldura care se degajă la fermentația completă a 200 kg de must dulce cu concentrația de 45% glucoză (M=180 g/mol), știind că: C6H12O6(aq) 2C2H5OH(l) +2 CO2(g) H = -108,68 KJ a) J b) J c) J 23. Etanolul (C2H5OH) poate fi folosit drept combustibil alternativ. Acesta se poate obține ușor din culturile de trestie de zahăr şi porumb. Dacă temperatura de fierbere a etanolului este de 78 C, ce cantitate de căldură exprimată în kj este necesară pentru a încălzi 105 g de etanol de la 25 C până la temperatura de fierbere? (căldură specifică etanol = 2,44 J/g C). a) 12,33 kj b) 13,58 kj c) 14,04 kj 3 / 4
16 24. Să se calculeze variația de entalpie corespunzătoare arderii unui mol de benzen lichid la 298 K, știind că valoarea căldurii degajate la combustia sa într-o incintă de volum constant este de 3275,5 kj/mol. a) 3275,50 kj/mol b) 3260,15 kj/mol c) 3271,78 kj/mol 25. Alama este unul dintre cele mai vechi aliaje descoperite de către om și care își găsește și în prezent aplicații industriale. Aceasta are densitatea de 8,40 g/cm 3 și căldura specifică de 0,385 J/g C. Dacă un lingou de alamă de 14,5 cm 3 are temperatura inițială de 152 C și este introdus într-un recipient izolat în care se găsesc 138 g de apă cu o temperatură inițială de 23,7 C, care va fi temperatura finală în recipient? (Căldura specifică a apei este 4,18 J/g C). a) 43,23 C b) 33,34 C c) 36,22 C 26. Puterea calorică a unui amestec echimolecular format din alcool metilic (MCH3OH=32 g/mol) și benzen (MC6H6)=78 g/mol) utilizat ca solvent în industria de lacuri și vopsele este kj/kg. Știind că prin arderea unui mol de benzen se degajă de 4,5 ori mai multă energie decât la arderea unui mol de alcool metilic, precizați căldura care se eliberează prin combustia unui amestec obținut din 64g alcool și 39g benzen? a) 4200,552 kj b) 3068,585 kj c) 1444,041 kj 27. Deoarece F-21 (CHFCl2) este un agent frigorific inclus în categoria gazelor cu efect de seră, a cărui emisie este restricționată, se impune înlocuirea lui cu agentul frigorific F-32 (CH2F2 ). Știind că F-21 (CHFCl2) are căldura latentă de vaporizare de 24,4 kj/mol iar F-32 (CH2F2) de 360,24 kj/kg, calculați raportul dintre masa F-21 : F-32 știind că în timpul funcționării unui frigider se degajă o cantitate de căldură de 100 kcal. Se dă masa molară pentru F-21 = g/mol și 1 kcal = 4184 J. a) 1,50 b) 2,50 c) 3, Energia solară poate fi utilizată pentru a genera energie termică. Pentru un consum mediu zilnic de 200 kg de apă caldă, să se calculeze numărul de panouri solare necesare creșterii temperaturii apei de la 10 C la 50 C, în 6 ore de funcționare, știind că puterea instalată a unui panou este de 400 J/s, și nu există pierderi de căldură. Să se calculeze temperatura finală a apei în condițiile mai sus menționate dacă se consideră un timp de funcționare al panourilor solare de 8 ore. Căldura specifică a apei este 4,18 J/g C. a) 4 panouri, temperatura finală 65,12 C b) 3 panouri, temperatura finală 51,05 C c) 4 panouri, temperatura finală 51,25 C 29. O probă de 92,22 g de bicarbonat de sodiu (M = 84,01g/mol) se descompune conform reacției termochimice: 2NaHCO3(s) kj Na2CO3(s) + H2O(g) + CO2(g). În cazul în care căldura necesară pentru a descompune bicarbonatul de sodiu provine din răcirea a 498 g de argint (căldura specifică este 0,235 J/g C), variația temperaturii în proba de argint este: a) 502 C b) 558 C c) 605 C 30. Se dau următoarele ecuații termochimice: 4PCl5(g) P4(s) + 10Cl2(g) Ha = 1222 kj PCl5(g) PCl3(g) + Cl2(g) Hb = 89 kj Calculați cantitatea de apă exprimată în grame care se încălzește de la 10 C la 90 C (căldura specifică a apei este 4,18 J/g C), pe baza căldurii degajate în reacția de obținere a 754g triclorură de fosfor (M = 137,32 g/mol): P4(s) + 6Cl2(g) 4PCl3(g). a) 4325 g b) 3555 g c) 5355g 4 / 4
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu
 Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
a. 11 % b. 12 % c. 13 % d. 14 %
 1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Aplicaţii ale principiului I al termodinamicii la gazul ideal
 Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare.
 Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 2-HIDROCARBURI-2.2.-ALCHENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Liceul de Ştiinţe ale Naturii Grigore Antipa Botoşani
 Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
Fişă de lucru RANDAMENT. CONVERSIE UTILĂ. CONVERSIE TOTALĂ 1. Randament A. Hidrocarburile alifatice pot fi utilizate drept combustibili, sau pot fi transformate în compuşi cu aplicaţii practice. 1. Scrieţi
Capitolul 2-HIDROCARBURI-2.3.-ALCHINE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Capitolul 1-INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme
 Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Valori limită privind SO2, NOx şi emisiile de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili
 Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Capitolul 2-HIDROCARBURI-2.5.-ARENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
3. Care este afirmația adevărată referitoare la energia de ionizare: b) rămâne constantă în perioada a IV-a
 Numele și prenumele: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Editia a III-a - 215 Formular de concurs Clasa a IX-a Toate subiectele sunt obligatorii, un singur răspuns este
Numele și prenumele: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Editia a III-a - 215 Formular de concurs Clasa a IX-a Toate subiectele sunt obligatorii, un singur răspuns este
1 C L A S A a I X - a
 9 Clasa Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a V-a, 2017 Formular de concurs Clasa a IX-a, CHIMIE APLICATĂ ÎN PROTECȚIA MEDIULUI Toate
9 Clasa Numele și prenumele elevului: Unitatea de învățământ: Concurs "Academician Cristofor Simionescu" - Ediția a V-a, 2017 Formular de concurs Clasa a IX-a, CHIMIE APLICATĂ ÎN PROTECȚIA MEDIULUI Toate
II. 5. Probleme. 20 c 100 c = 10,52 % Câte grame sodă caustică se găsesc în 300 g soluţie de concentraţie 10%? Rezolvare m g.
 II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
Subiectul II (30 puncte) Varianta 001
 Subiectul II (30 puncte) Varianta 001 Compuşii cloruraţi obţinuţi din hidrocarburile alifatice au importante aplicaţii practice. 1. Scrieţi ecuaţiile reacţiilor chimice, prin care se obţin din metan: monoclorometan,
Subiectul II (30 puncte) Varianta 001 Compuşii cloruraţi obţinuţi din hidrocarburile alifatice au importante aplicaţii practice. 1. Scrieţi ecuaţiile reacţiilor chimice, prin care se obţin din metan: monoclorometan,
CLASA a X a PROBA TEORETICĂ Filiera tehnologică toate profilurile/specializările/calificările
 CLASA a X a PROBA TEORETICĂ Filiera tehnologică toate profilurile/specializările/calificările Subiectul I 20 Fiecare item are un singur răspuns corect. Notaţi în tabel cu X numai răspunsul corect. Pentru
CLASA a X a PROBA TEORETICĂ Filiera tehnologică toate profilurile/specializările/calificările Subiectul I 20 Fiecare item are un singur răspuns corect. Notaţi în tabel cu X numai răspunsul corect. Pentru
Reactia de amfoterizare a aluminiului
 Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
5.1. Noţiuni introductive
 ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
a. 0,1; 0,1; 0,1; b. 1, ; 5, ; 8, ; c. 4,87; 6,15; 8,04; d. 7; 7; 7; e. 9,74; 12,30;1 6,08.
 1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II)
 Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Examenul de bacalaureat naţional 2015 Proba E. d) Chimie organică (nivel I/ nivel II) Varianta 9 Toate subiectele sunt obligatorii. Se acordă din oficiu. Timpul de lucru efectiv este de 3 ore. SUBIECTUL
Concurs Acad. Cristofor Simionescu Clasa a IX-a - chimie Toate subiectele sunt obligatorii, 1 singur răspuns corect.
 oncurs Acad. ristoor Simionescu lasa a IX-a - chimie Toate subiectele sunt obligatorii, 1 singur răspuns corect. 1. Într-un atom de magneziu, care are Z = 12 şi A = 24: a) numărul protonilor = b) numărul
oncurs Acad. ristoor Simionescu lasa a IX-a - chimie Toate subiectele sunt obligatorii, 1 singur răspuns corect. 1. Într-un atom de magneziu, care are Z = 12 şi A = 24: a) numărul protonilor = b) numărul
Subiecte Clasa a VII-a
 lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ
 Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2015 DISCIPLINA: CHIMIE ORGANICĂ CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE CONCURS DE ADMITERE LA
14. Se dă următorul compus:
 CLASA a XI-a 1. Care din următorii compuşi este un derivat halogenat vicinal: a) 1,2-dicloropropanul; b) 1,1-dicloropropanul; c) 1-bromopropanul; d) 2-bromo-2-metilpropanul; e) 1,3,5-tricloropropanul.
CLASA a XI-a 1. Care din următorii compuşi este un derivat halogenat vicinal: a) 1,2-dicloropropanul; b) 1,1-dicloropropanul; c) 1-bromopropanul; d) 2-bromo-2-metilpropanul; e) 1,3,5-tricloropropanul.
ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli
 LIEUL TEORETI GRIGORE ANTIPA BOTOŞANI - ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli Subiectul A: Indicaţi care dintre afirmaţiile de mai jos sunt adevărate şi care sunt false, completând cu litera
LIEUL TEORETI GRIGORE ANTIPA BOTOŞANI - ITEMI MODEL PENTRU UNITATEA DE ÎNVĂŢARE: Alcooli Subiectul A: Indicaţi care dintre afirmaţiile de mai jos sunt adevărate şi care sunt false, completând cu litera
Capitolul 4-COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ-
 Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM 1 electronica.geniu.ro
 Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ. Capitolul Hidrocarburi
 Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ Capitolul Hidrocarburi CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE
Universitatea Dunărea de Jos din Galaţi CULEGERE DE TESTE PENTRU ADMITEREA 2014 DISCIPLINA: CHIMIE ORGANICĂ Capitolul Hidrocarburi CULEGEREA DE TESTE ESTE RECOMANDATĂ PENTRU CANDIDAȚII CARE VOR SUSȚINE
Examenul de bacalaureat naţional 2016 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d)
 Examenul de bacalaureat naţional 2016 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
Examenul de bacalaureat naţional 2016 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
MARCAREA REZISTOARELOR
 1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
Unitatea atomică de masă (u.a.m.) = a 12-a parte din masa izotopului de carbon
 ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
Studiu privind soluţii de climatizare eficiente energetic
 Studiu privind soluţii de climatizare eficiente energetic Varianta iniţială O schemă constructivă posibilă, a unei centrale de tratare a aerului, este prezentată în figura alăturată. Baterie încălzire/răcire
Studiu privind soluţii de climatizare eficiente energetic Varianta iniţială O schemă constructivă posibilă, a unei centrale de tratare a aerului, este prezentată în figura alăturată. Baterie încălzire/răcire
Metoda rezolvării problemelor de determinare a formulelor chimice
 inisterul Educaţiei şi Tineretului al Republicii oldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă etoda rezolvării problemelor de determinare a formulelor chimice Autor Postolache
inisterul Educaţiei şi Tineretului al Republicii oldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă etoda rezolvării problemelor de determinare a formulelor chimice Autor Postolache
Planul determinat de normală şi un punct Ecuaţia generală Plane paralele Unghi diedru Planul determinat de 3 puncte necoliniare
 1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
5. FUNCŢII IMPLICITE. EXTREME CONDIŢIONATE.
 5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
COLEGIUL NATIONAL CONSTANTIN CARABELLA TARGOVISTE. CONCURSUL JUDETEAN DE MATEMATICA CEZAR IVANESCU Editia a VI-a 26 februarie 2005.
 SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
REACŢII DE ADIŢIE NUCLEOFILĂ (AN-REACŢII) (ALDEHIDE ŞI CETONE)
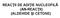 EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
CLASA a X-a. 3. Albastrul de Berlin are formula: a) PbS; b) [Cu(NH 3 ) 4 ](OH); c) Na 4 [Fe(CN) 6 ]; d) Ag(NH 3 ) 2 OH; e) Fe 4 [Fe(CN) 6 ] 3.
; c) Na 4 [Fe(CN) 6 ]; d) Ag(NH 3 ) 2 OH; e) Fe 4 [Fe(CN) 6 ] 3. CLASA a X-a. 3. Albastrul de Berlin are formula: a) PbS; b) [Cu(NH 3 ) 4 ](OH); c) Na 4 [Fe(CN) 6 ]; d) Ag(NH 3 ) 2 OH; e) Fe 4 [Fe(CN) 6 ] 3.](/thumbs/54/33993973.jpg) CLASA a X-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea solubilităţii;
CLASA a X-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea solubilităţii;
CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM
 LICEUL TEORETIC TRAIAN CONSTANŢA CLAS a X-a VARIANTA II CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 La întrebările de la 1-20, alege un singur răspuns: 1. Sunt adevarate urmatoarele afirmații cu
LICEUL TEORETIC TRAIAN CONSTANŢA CLAS a X-a VARIANTA II CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 La întrebările de la 1-20, alege un singur răspuns: 1. Sunt adevarate urmatoarele afirmații cu
EXAMENUL DE BACALAUREAT Proba E/F
 EXAMENUL DE BACALAUREAT - 2009 Proba E/F Toate subiectele A-F sunt obligatorii. Subiectul G1 este obligatoriu numai pentru NIVELUL I. Subiectul G2 este obligatoriu numai pentru NIVELUL II. Timpul efectiv
EXAMENUL DE BACALAUREAT - 2009 Proba E/F Toate subiectele A-F sunt obligatorii. Subiectul G1 este obligatoriu numai pentru NIVELUL I. Subiectul G2 este obligatoriu numai pentru NIVELUL II. Timpul efectiv
CAP. 4. ALCHENE 10. Despre adiţia apei la alchene nesimetrice sunt adevărate afirmaţiile: 1. Referitor la alchene sunt adevărate afirmaţiile:
 CAP. 4. ALCHENE 1. Referitor la alchene sunt adevărate afirmaţiile: A. se mai numesc şi parafine B. se mai numesc şi olefine C. au formula generală C nh 2n D. se mai numesc şi acetilene E. au structură
CAP. 4. ALCHENE 1. Referitor la alchene sunt adevărate afirmaţiile: A. se mai numesc şi parafine B. se mai numesc şi olefine C. au formula generală C nh 2n D. se mai numesc şi acetilene E. au structură
Subiecte Clasa a VIII-a
 Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE
 DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
MODEL DE SUBIECT Chimie organică (nivel I / nivel II)
 Bun venit dragi elevi! Am speranţa, că ciclul de emisiuni destinate pregătirii examenului de Bacalaureat-proba de Chimie organică sau Chimie anorganică şi generală, va fi util pentru alegerea voastră.
Bun venit dragi elevi! Am speranţa, că ciclul de emisiuni destinate pregătirii examenului de Bacalaureat-proba de Chimie organică sau Chimie anorganică şi generală, va fi util pentru alegerea voastră.
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate.
 Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
OLIMPIADA NAȚIONALĂ DE CHIMIE
 MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
R R, f ( x) = x 7x+ 6. Determinați distanța dintre punctele de. B=, unde x și y sunt numere reale.
 5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
CONCURSUL DE CHIMIE CORIOLAN DRĂGULESCU 2017
 Universitatea Politehnica Timişoara Facultatea de Chimie Industrială şi Ingineria Mediului Clasa a IX-a Chimie anorganică CONCURSUL DE CHIMIE CORIOLAN DRĂGULESCU 2017 1. (2 p) Precizaţi poziţia în sistemul
Universitatea Politehnica Timişoara Facultatea de Chimie Industrială şi Ingineria Mediului Clasa a IX-a Chimie anorganică CONCURSUL DE CHIMIE CORIOLAN DRĂGULESCU 2017 1. (2 p) Precizaţi poziţia în sistemul
CHIMIE ORGANICĂ CLASA a XII-a
 CHIMIE ORGANICĂ CLASA a XII-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea
CHIMIE ORGANICĂ CLASA a XII-a 1. Puritatea unei substanţe organice se verifică prin: a) efectuarea analizei elementare calitative; b) invariabilitatea constantelor fizice la repetarea purificării; c) testarea
1. PROPRIETĂȚILE FLUIDELOR
 1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
5.5. REZOLVAREA CIRCUITELOR CU TRANZISTOARE BIPOLARE
 5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
ANALIZE FIZICO-CHIMICE MATRICE APA. Tip analiza Tip proba Metoda de analiza/document de referinta/acreditare
 ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25
 Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25 LAGĂRELE CU ALUNECARE!" 25.1.Caracteristici.Părţi componente.materiale.!" 25.2.Funcţionarea lagărelor cu alunecare.! 25.1.Caracteristici.Părţi componente.materiale.
Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25 LAGĂRELE CU ALUNECARE!" 25.1.Caracteristici.Părţi componente.materiale.!" 25.2.Funcţionarea lagărelor cu alunecare.! 25.1.Caracteristici.Părţi componente.materiale.
Tema 5 (S N -REACŢII) REACŢII DE SUBSTITUŢIE NUCLEOFILĂ. ŞI DE ELIMINARE (E - REACŢII) LA ATOMULDE CARBON HIBRIDIZAT sp 3
 Tema 5 REACŢII DE SUBSTITUŢIE NUCLEOFILĂ (S N -REACŢII) ŞI DE ELIMINARE (E - REACŢII) LA ATOMULDE CARBON IBRIDIZAT sp 3 1. Reacții de substituție nucleofilă (SN reacții) Reacţiile de substituţie nucleofilă
Tema 5 REACŢII DE SUBSTITUŢIE NUCLEOFILĂ (S N -REACŢII) ŞI DE ELIMINARE (E - REACŢII) LA ATOMULDE CARBON IBRIDIZAT sp 3 1. Reacții de substituție nucleofilă (SN reacții) Reacţiile de substituţie nucleofilă
Metode iterative pentru probleme neliniare - contractii
 Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Curs 14 Funcţii implicite. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi"
 Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
TEST VI CHIMIE ORGANICA
 TEST VI CHIMIE ORGANICA 1. AlegeŃi afirmańia adevărată: A. prin analiza elementală calitativă nu se pot determina elementele prezente într-un compus organic B. în compuşii organici sunt preponderente legăturile
TEST VI CHIMIE ORGANICA 1. AlegeŃi afirmańia adevărată: A. prin analiza elementală calitativă nu se pot determina elementele prezente într-un compus organic B. în compuşii organici sunt preponderente legăturile
OLIMPIADA DE CHIMIE etapa judeţeană
 Clasa a VIII-a OLIMPIADA DE CHIMIE etapa judeţeană Str. General Berthelot nr. 28-30, Sector 1, Cod 010168, Bucureşti Tel: +40 (0)21 405 62 21 Fax: +40 (0)21 313 55 47 www.edu.ro DIRECȚIA GENERALĂ EDUCAȚIE
Clasa a VIII-a OLIMPIADA DE CHIMIE etapa judeţeană Str. General Berthelot nr. 28-30, Sector 1, Cod 010168, Bucureşti Tel: +40 (0)21 405 62 21 Fax: +40 (0)21 313 55 47 www.edu.ro DIRECȚIA GENERALĂ EDUCAȚIE
Modele de teste grilă pentru examenul de admitere la Facultatea de Medicină şi Farmacie, specializarea Farmacie*
 Universitatea UNIVERSITATEA DUNĂREA DE JOS din GALAŢI Facultatea de Medicină şi Farmacie, Specializarea Farmacie Modele de teste grilă pentru examenul de admitere la Facultatea de Medicină şi Farmacie,
Universitatea UNIVERSITATEA DUNĂREA DE JOS din GALAŢI Facultatea de Medicină şi Farmacie, Specializarea Farmacie Modele de teste grilă pentru examenul de admitere la Facultatea de Medicină şi Farmacie,
Fig Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36].
![Fig Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36]. Fig Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36].](/thumbs/72/67648751.jpg) Componente şi circuite pasive Fig.3.85. Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36]. Fig.3.86. Rezistenţa serie echivalentă pierderilor în funcţie
Componente şi circuite pasive Fig.3.85. Impedanţa condensatoarelor electrolitice SMD cu Al cu electrolit semiuscat în funcţie de frecvenţă [36]. Fig.3.86. Rezistenţa serie echivalentă pierderilor în funcţie
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor X) functia f 1
 Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
 4. CIRCUITE LOGICE ELEMENTRE 4.. CIRCUITE LOGICE CU COMPONENTE DISCRETE 4.. PORŢI LOGICE ELEMENTRE CU COMPONENTE PSIVE Componente electronice pasive sunt componente care nu au capacitatea de a amplifica
4. CIRCUITE LOGICE ELEMENTRE 4.. CIRCUITE LOGICE CU COMPONENTE DISCRETE 4.. PORŢI LOGICE ELEMENTRE CU COMPONENTE PSIVE Componente electronice pasive sunt componente care nu au capacitatea de a amplifica
Esalonul Redus pe Linii (ERL). Subspatii.
 Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
CULEGERE DE PROBLEME pentru Concursul de Chimie Organică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVERSITATEA POLITEHNICA
 Sabina-Violeta NIȚU Sorina RAN CULGR PRLM pentru Concursul de Chimie rganică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVRSITATA PLITHNICA TIMIȘARA Timișoara 2014 1 CUPRINS I.
Sabina-Violeta NIȚU Sorina RAN CULGR PRLM pentru Concursul de Chimie rganică din cadrul Facultății de Chimie Industrială și Ingineria Mediului UNIVRSITATA PLITHNICA TIMIȘARA Timișoara 2014 1 CUPRINS I.
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor
 Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
III. Serii absolut convergente. Serii semiconvergente. ii) semiconvergentă dacă este convergentă iar seria modulelor divergentă.
 III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
Curs 1 Şiruri de numere reale
 Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Problema a II - a (10 puncte) Diferite circuite electrice
 Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
Seminariile Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reziduurilor
 Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Aplicaţii ale principiului I al termodinamicii în tehnică
 Aplicaţii ale principiului I al termodinamicii în tehnică Sisteme de încălzire a locuinţelor Scopul tuturor acestor sisteme, este de a compensa pierderile de căldură prin pereţii locuinţelor şi prin sistemul
Aplicaţii ale principiului I al termodinamicii în tehnică Sisteme de încălzire a locuinţelor Scopul tuturor acestor sisteme, este de a compensa pierderile de căldură prin pereţii locuinţelor şi prin sistemul
Examenul naţional de bacalaureat 2014 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d)
 Examenul naţional de bacalaureat 2014 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
Examenul naţional de bacalaureat 2014 PROBĂ SCRISĂ LA CHIMIE ORGANICĂ (NIVEL I / NIVEL II) PROBA E.d) FILIERĂ TEHNOLOGICĂ profil tehnic, profil resurse naturale şi protecţia mediului SUBIECTUL I (30 puncte)
(a) se numeşte derivata parţială a funcţiei f în raport cu variabila x i în punctul a.
 Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
V O. = v I v stabilizator
 Stabilizatoare de tensiune continuă Un stabilizator de tensiune este un circuit electronic care păstrează (aproape) constantă tensiunea de ieșire la variaţia între anumite limite a tensiunii de intrare,
Stabilizatoare de tensiune continuă Un stabilizator de tensiune este un circuit electronic care păstrează (aproape) constantă tensiunea de ieșire la variaţia între anumite limite a tensiunii de intrare,
Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling.
 Cursul 8 3.5.4. Electronegativitatea Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling. Cantitativ, ea se exprimă prin coeficienţii de electronegativitate
Cursul 8 3.5.4. Electronegativitatea Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling. Cantitativ, ea se exprimă prin coeficienţii de electronegativitate
V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile
 Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Curs 4 Serii de numere reale
 Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
CAP. 3. ALCANI. B. clorura de metil C. bromura de metil D. iodura de metilen E. cloroformul
 CAP. 3. ALCANI 1. Despre alcani sunt adevărate afirmaţiile: A. n-alcanii şi izoalcanii au aceeaşi formulă moleculară B. izoalcanii au temperaturi de fierbere mai mici decât n- alcanii C. n-alcanii sunt
CAP. 3. ALCANI 1. Despre alcani sunt adevărate afirmaţiile: A. n-alcanii şi izoalcanii au aceeaşi formulă moleculară B. izoalcanii au temperaturi de fierbere mai mici decât n- alcanii C. n-alcanii sunt
CURSUL 3 ECHILIBRE DE DIZOLVARE
 CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
Rezolvarea problemelor la chimie prin metoda algebrică
 Ministerul Educaţiei şi Tineretului al Republicii Moldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă Rezolvarea problemelor la chimie prin metoda algebrică Autor: Postolache Ion,
Ministerul Educaţiei şi Tineretului al Republicii Moldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă Rezolvarea problemelor la chimie prin metoda algebrică Autor: Postolache Ion,
Tranzistoare bipolare şi cu efect de câmp
 apitolul 3 apitolul 3 26. Pentru circuitul de polarizare din fig. 26 se cunosc: = 5, = 5, = 2KΩ, = 5KΩ, iar pentru tranzistor se cunosc următorii parametrii: β = 200, 0 = 0, μa, = 0,6. a) ă se determine
apitolul 3 apitolul 3 26. Pentru circuitul de polarizare din fig. 26 se cunosc: = 5, = 5, = 2KΩ, = 5KΩ, iar pentru tranzistor se cunosc următorii parametrii: β = 200, 0 = 0, μa, = 0,6. a) ă se determine
Subiectul III (30 puncte) Varianta 001
 Subiectul III (30 puncte) Varianta 001 Proteinele şi zaharidele sunt compuşi organici cu acţiune biologică. 1. Scrieţi formula de structură pentru o tripeptidă P care conţine glicină, valină şi serină
Subiectul III (30 puncte) Varianta 001 Proteinele şi zaharidele sunt compuşi organici cu acţiune biologică. 1. Scrieţi formula de structură pentru o tripeptidă P care conţine glicină, valină şi serină
CONCURSUL DE MATEMATICĂ APLICATĂ ADOLF HAIMOVICI, 2017 ETAPA LOCALĂ, HUNEDOARA Clasa a IX-a profil științe ale naturii, tehnologic, servicii
 Clasa a IX-a 1 x 1 a) Demonstrați inegalitatea 1, x (0, 1) x x b) Demonstrați că, dacă a 1, a,, a n (0, 1) astfel încât a 1 +a + +a n = 1, atunci: a +a 3 + +a n a1 +a 3 + +a n a1 +a + +a n 1 + + + < 1
Clasa a IX-a 1 x 1 a) Demonstrați inegalitatea 1, x (0, 1) x x b) Demonstrați că, dacă a 1, a,, a n (0, 1) astfel încât a 1 +a + +a n = 1, atunci: a +a 3 + +a n a1 +a 3 + +a n a1 +a + +a n 1 + + + < 1
Seminar 5 Analiza stabilității sistemelor liniare
 Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
2. STATICA FLUIDELOR. 2.A. Presa hidraulică. Legea lui Arhimede
 2. STATICA FLUIDELOR 2.A. Presa hidraulică. Legea lui Arhimede Aplicația 2.1 Să se determine ce masă M poate fi ridicată cu o presă hidraulică având raportul razelor pistoanelor r 1 /r 2 = 1/20, ştiind
2. STATICA FLUIDELOR 2.A. Presa hidraulică. Legea lui Arhimede Aplicația 2.1 Să se determine ce masă M poate fi ridicată cu o presă hidraulică având raportul razelor pistoanelor r 1 /r 2 = 1/20, ştiind
Componente şi Circuite Electronice Pasive. Laborator 3. Divizorul de tensiune. Divizorul de curent
 Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Continue. Answer: a. Logout. e-desc» Concurs Phi» Quizzes» Setul 1 - Clasa a X-a» Attempt 1. 1 of 2 4/14/ :27 PM. Marks: 0/1.
 Concurs Phi: Setul 1 - Clasa a X-a 1 of 2 4/14/2008 12:27 PM Logout e-desc» Concurs Phi» Quizzes» Setul 1 - Clasa a X-a» Attempt 1 1 Un termometru cu lichid este gradat intr-o scara de temperatura liniara,
Concurs Phi: Setul 1 - Clasa a X-a 1 of 2 4/14/2008 12:27 PM Logout e-desc» Concurs Phi» Quizzes» Setul 1 - Clasa a X-a» Attempt 1 1 Un termometru cu lichid este gradat intr-o scara de temperatura liniara,
CHIMIE. Asistență Medicală Generală. Varianta A
 CHIMIE Asistență Medicală Generală Varianta A 1. Un alcool primar se poate obține prin: 1. hidroliza oleatului de etil 2. hidroliza clorurii de benzoil 3. hidroliza clorurii de metilen 4. hidroliza clorurii
CHIMIE Asistență Medicală Generală Varianta A 1. Un alcool primar se poate obține prin: 1. hidroliza oleatului de etil 2. hidroliza clorurii de benzoil 3. hidroliza clorurii de metilen 4. hidroliza clorurii
PROBLEME DE CHIMIE ORGANICĂ
 FNDUL SCIAL EURPEAN Programul peraţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară: 1 Educaţia şi formarea profesională în sprijinul creşterii economice şi dezvoltării societăţii
FNDUL SCIAL EURPEAN Programul peraţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară: 1 Educaţia şi formarea profesională în sprijinul creşterii economice şi dezvoltării societăţii
Examenul de bacalaureat național 2014 Proba E. d) Chimie organică (nivel I/ nivel II)
 Ministerul Educației Naționale Centrul Național de Evaluare şi Examinare Examenul de bacalaureat național 2014 Proba E. d) Chimie organică (nivel I/ nivel II) Filiera teoretică profil real, specializarea
Ministerul Educației Naționale Centrul Național de Evaluare şi Examinare Examenul de bacalaureat național 2014 Proba E. d) Chimie organică (nivel I/ nivel II) Filiera teoretică profil real, specializarea
SEMINAR 14. Funcţii de mai multe variabile (continuare) ( = 1 z(x,y) x = 0. x = f. x + f. y = f. = x. = 1 y. y = x ( y = = 0
 Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
1. Completati caseta, astfel incat propozitia obtinuta sa fie adevarata lg 4 =.
 Copyright c ONG TCV Scoala Virtuala a Tanarului Matematician Ministerul Educatiei al Republicii Moldova Agentia de Evaluare si Examinare Examenul de bacalaureat la matematica, 4 iunie Profilul real Timp
Copyright c ONG TCV Scoala Virtuala a Tanarului Matematician Ministerul Educatiei al Republicii Moldova Agentia de Evaluare si Examinare Examenul de bacalaureat la matematica, 4 iunie Profilul real Timp
ALGEBRĂ ŞI ELEMENTE DE ANALIZĂ MATEMATICĂ FIZICĂ
 Sesiunea august 07 A ln x. Fie funcţia f : 0, R, f ( x). Aria suprafeţei plane delimitate de graficul funcţiei, x x axa Ox şi dreptele de ecuaţie x e şi x e este egală cu: a) e e b) e e c) d) e e e 5 e.
Sesiunea august 07 A ln x. Fie funcţia f : 0, R, f ( x). Aria suprafeţei plane delimitate de graficul funcţiei, x x axa Ox şi dreptele de ecuaţie x e şi x e este egală cu: a) e e b) e e c) d) e e e 5 e.
RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii transversale, scrisă faţă de una dintre axele de inerţie principale:,
 REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
Acizi carboxilici heterofuncționali.
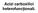 Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
Ministerul Educa iei i Cercet rii Serviciul Na ional de Evaluare i Examinare. EXAMENUL DE BACALAUREAT Prob scris la CHIMIE ORGANIC I Proba E/F
 Ministerul Educa iei i Cercet rii Serviciul Na ional de Evaluare i Examinare EXAMENUL DE BACALAUREAT - 2007 Prob scris la CHIMIE ORGANIC I Proba E/F Toate subiectele sunt obligatorii. Se acord din oficiu.
Ministerul Educa iei i Cercet rii Serviciul Na ional de Evaluare i Examinare EXAMENUL DE BACALAUREAT - 2007 Prob scris la CHIMIE ORGANIC I Proba E/F Toate subiectele sunt obligatorii. Se acord din oficiu.
LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM
 LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 Clasa a XI-a Varianta 2 La întrebările de la 1-30, alege un singur răspuns: 1.Câți enantiomeri prezintă 4,5 dimetil
LICEUL TEORETIC TRAIAN CONSTANŢA CONCURSUL DE CHIMIE ORGANICĂ MARGARETA AVRAM - 2017 Clasa a XI-a Varianta 2 La întrebările de la 1-30, alege un singur răspuns: 1.Câți enantiomeri prezintă 4,5 dimetil
