Δομή και δεσμικότητα των οργανικών ενώσεων. Αδαμαντοειδή: πενταμαντάνιο
|
|
|
- Τελαμών Ρόκας
- 8 χρόνια πριν
- Προβολές:
Transcript
1 Δομή και δεσμικότητα των οργανικών ενώσεων Αδαμαντοειδή: πενταμαντάνιο
2 Δομή και δεσμικότητα των οργανικών ενώσεων Σχεδόν οτιδήποτε βλέπετε στην εικόνα αυτή είναι φτιαγμένο από οργανικές χημικές ενώσεις.
3 Δομή και δεσμικότητα των οργανικών ενώσεων
4 Μία αντίδραση χλωρίωσης Ενέργεια CH 4 + Cl 2 CH 3 Cl + HCl Μία αντίδραση υποκατάστασης CH 3 Cl + K + I - CH 3 I + K + Cl - Μία αντίδραση απόσπασης
5 Σύνθεση ουρίας κατά Wöhler
6 Το άτομο
7 Σχήμα 1-1. Οι μεταβολές στην ενέργεια, Ε, που προκύπτουν όταν δύο άτομα πλησιάζουν μεταξύ τους. Στην απόσταση που ορίζεται ως μήκος δεσμού επιτυγχάνεται η μέγιστη δεσμικότητα.
8 Νόμος του Coulomb Νόμος του Coulomb Ελκτική δύναμις = σταθερά ( + ) φορτίο ( ) φορτίο απόσταση 2
9 Σχήμα 1-2 Ομοιοπολική σύνδεση. Ελκτικές (συνεχής γραμμή) και απωθητικές (διακεκομμένη γραμμή) δυνάμεις κατά τη σύνδεση μεταξύ δύο ατόμων. Οι μεγάλες σφαίρες αντιπροσωπεύουν περιοχές του χώρου στις οποίες βρίσκονται τα ηλεκτρόνια γύρω από τον πυρήνα. Οι μικροί κύκλοι γύρω από το σημείο συν αντιπροσωπεύουν τον πυρήνα. Σχήμα 1-3 Ιοντική σύνδεση. Ένας διαφορετικός τύπος σύνδεσης προκύπτει από την πλήρη μεταφορά ενός ηλεκτρονίου από το άτομο 1 στο άτομο 2, δημιουργώντας έτσι δύο ιόντα. Τα αντίθετα φορτία τους συντελούν ώστε τα ιόντα να έλκονται μεταξύ τους.
10 1-3 Ιοντικοί και ομοιοπολικοί δεσμοί: Ο κανόνας της οκτάδας 1. Ένας ομοιοπολικός δεσμός σχηματίζεται με συμμετοχή των ηλεκτρονίων (όπως φαίνεται στο Σχήμα 1-2). 2. Ένας ιοντικός δεσμός βασίζεται στην ηλεκτροστατική έλξη δύο ιόντων με αντίθετα φορτία (όπως φαίνεται στο Σχήμα 1-3).
11 Πίνακας1-1 Μερικός περιοδικός πίνακας Περίοδος Αλογόνα Ευγενή αέρια Πρώτη Η 1 He 2 Δεύτερη Li 2,1 Be 2,2 B 2,3 C 2,4 N 2,5 O 2,6 F 2,7 Ne 2,8 Τρίτη Na 2,8,1 Mg 2,8,2 Al 2,8,3 Si 2,8,4 P 2,8,5 S 2,8,6 Cl 2,8,7 Ar 2,8,8 Τέταρτη K 2,8,8,1 Br 2,8,18,7 Kr 2,8,18,8 Πέμπτη I 2,8,18,18,7 Xe 2,8,18,18,8 Σημείωση: Οι αριθμοί στα σύμβολα των ατόμων αντιστοιχούν στον αριθμό των ηλεκτρονίων που βρίσκονται σε κάθε μία από τις κύριες στιβάδες του ατόμου.
12 1-3 Ιοντικοί και ομοιοπολικοί δεσμοί: Ο κανόνας της οκτάδας
13 Δυναμικό ιονισμού (Ionization potential, IP) Ηλεκτρονική συγγένεια (Electron affinity, EA) Na 2,8,1 1 e [Na 2,8 ] + IP = 119 kcal mol 1 (498 kj mol 1 ) Κατιόν νατρίου (Διαμόρφωση νέου) Απαιτούμενη προσφορά ενέργειας + 1 e Cl 2,8,7 [Cl 2,8,8 ] EA = 83 kcal mol 1 ( 347 kj mol 1 ) Ανιόν χλωριδίου (Διαμόρφωση αργού) Ελευθερούμενη ενέργεια Na + Cl Na + + Cl Σύνολο = = 36 kcal mol 1 (151 kj mol 1 )
14 Σχηματισμός ιοντικών δεσμών με μεταφορά ηλεκτρονίων ηλεκτροστατική έλξη 120 kcal mol-1 (2,8Å) =84 kcal mol-1 Na 2,8,1 + Cl 2,8,7 [Na 2,8 ] + [Cl 2,8,8 ] ή NaCl ( 84 kcal mol 1 ) Χάρτης ηλεκτροστατικού δυναμικού
15 Ηλεκτρόνια σθένους ως ηλεκτρόνιατελείες
16 Απεικόνιση αλάτων με ηλεκτρόνια-τελείες
17 Το άτομο του υδρογόνου είναι μοναδικό γιατί μπορεί είτε να χάσει ένα ηλεκτρόνιο και να μετατραπεί σε έναν γυμνό πυρήνα, το πρωτόνιο, είτε να δεχθεί ένα ηλεκτρόνιο και να σχηματισθεί ένα ιόν υδριδίου, [Η, δηλαδή, Η:]
18 Στους ομοιοπολικούς δεσμούς τα ηλεκτρόνια διαμοιράζονται γιαναεπιτευχθείδιαμόρφωσηοκτάδας
19 Απεικόνιση απλών ομοιοπολικών δεσμών με ηλεκτρόνια-τελείες
20 Απεικόνιση απλών ομοιοπολικών δεσμών με ηλεκτρόνιατελείες
21 Αυξανόμενη ηλεκτραρνητικότητα
22 Στους περισσότερους οργανικούς δεσμούς τα ηλεκτρόνια δεν μοιράζονται εξίσου: πολικοί ομοιοπολικοί δεσμοί
23
24 Η άπωση μεταξύ των ηλεκτρονίων σθένους καθορίζει το σχήμα των μορίων
25 1 4 Απεικόνιση δεσμών με ηλεκτρόνια τελείες: Δομές Lewis Οι δομές Lewis γράφονται ακολουθώντας απλούς κανόνες Κανόνας 1. Γράψτε τον (δοθέντα ή επιθυμητό) μοριακό σκελετό. Πάρτε παράδειγμα το μεθάνιο. Το μόριο έχει τέσσερα άτομα υδρογόνου συνδεδεμένα σε ένα κεντρικό άτομο άνθρακα. H H C H H Σωστό H H C H H Λάθος
26 Δομές Lewis Κανόνας 2. Μετρήστε τον αριθμό των διαθεσίμων ηλεκτρονίων σθένους. CH 4 4H 4 1 ηλεκτρόνιο = 4 ηλεκτρόνια HBr 1H 1 1 ηλεκτρόνιο = 1 ηλεκτρόνιο C 1 4 ηλεκτρόνια = 4 ηλεκτρόνια 1Br 1 7 ηλεκτρόνια = 7 ηλεκτρόνια Σύνολο 8 ηλεκτρόνια Σύνολο 8 ηλεκτρόνια H 3 O + 3H 3 1 ηλεκτρόνιο = 3 ηλεκτρόνια ΝΗ 2 2Η 2 1 ηλεκτρόνιο = 2 ηλεκτρόνια 1O 1 6 ηλεκτρόνια = 6 ηλεκτρόνια 1Ν 1 5 ηλεκτρόνια = 5 ηλεκτρόνια Φορτίο +1 = 1 ηλεκτρόνιο Φορτίο 1 = +1 ηλεκτρόνιο Σύνολο 8 ηλεκτρόνια Σύνολο 8 ηλεκτρόνια
27 Κανόνας 3. (Κανόνας της οκτάδας) Γράψτε όλους τους ομοιοπολικούς δεσμούς με δύο κοινά, για τα δύο άτομα, ηλεκτρόνια, δίνοντας, γύρω από όσο περισσότερα άτομα γίνεται, οκτάδα ηλεκτρονίων, εκτός από τα άτομα του Η, τα οποία χρειάζονται μόνο ένα ζεύγος.
28
29 ΟρθέςκαιλανθασμένεςδομέςLewis Κανόνας 3. (Κανόνας της οκτάδας)
30 Απεικόνιση δομών Lewis Κανόνας 4. Προσδιορίστε τα (τυπικά) φορτία στα άτομα του μορίου. Τυπικό φορτίο = αριθμός ηλεκτρονίων εξωτερεικής στιβάδας στο ελεύθερο, ουδέτερο μόριο αριθμός μη κοινών ηλεκτρονίων στο 1 άτομο του μορίου 2 αριθμός δεσμικών ηλεκτρονίων γύρω από το άτομο στο μόριο ή Τυπικό φορτίο = αριθμός ηλεκτρονίων σθένους αριθμός ηλεκτρονίων των ελευθέρων ζευγών ηλεκτρονίων ½ αριθμός δεσμικών ηλεκτρονίων
31 Απεικόνιση δομών Lewis Κανόνας 4. Ιόν υδροξωνίου Τυπικό φορτίο = αριθμός ηλεκτρονίων σθένους αριθμός ηλεκτρονίων των ελευθέρων ζευγών ηλεκτρονίων ½ αριθμός δεσμικών ηλεκτρονίων
32 Ο κανόνας της οκτάδας δεν ισχύει πάντοτε Εξαίρεση 1. Περιπτώσεις με περιττό αριθμό ηλεκτρονίων. Εξαίρεση 2. έλλειψη ηλεκτρονίων σθένους
33
34 Ο κανόνας της οκτάδας δεν ισχύει πάντοτε Εξαίρεση 3. Επέκταση της στιβάδας σθένους (valence-shell expansion)
35 Οι ομοιοπολικοί δεσμοί μπορούν να παρασταθούν ως ευθείες γραμμές Δομές Kekulé Απεικόνιση του ομοιοπολικού δεσμού με ευθείες γραμμές
36 1-5 Δομές συντονισμού Το ανθρακικό ιόν έχει περισσότερες από μία ορθές δομές Lewis Δομές συντονισμού του ανθρακικού ιόντος
37 1-5 Δομές συντονισμού Ποια όμως είναι η αληθινή δομή; απεντοπισμένο υβρίδιο συντονισμού
38 1-5 Δομές συντονισμού
39 1-5 Δομές συντονισμού
40 1-5 Δομές συντονισμού Δεν είναι ισοδύναμες όλες οι δομές συντονισμού Οι δύο μη ισοδύναμες δομές συντονισμού του ενολικού ιόντος
41 1-5 Δομές συντονισμού Δεν είναι ισοδύναμες όλες οι δομές συντονισμού Οδηγία 1. Οι δομές με τον μεγαλύτερο αριθμό οκτάδων είναι οι πιο σημαντικές.
42 1-5 Δομές συντονισμού Δεν είναι ισοδύναμες όλες οι δομές συντονισμού Οδηγία 2. Τα φορτία πρέπει κατά προτίμηση να τοποθετούνται στα άτομα σε αντιστοιχία με την ηλεκτραρνητικότητά τους.
43 1-5 Δομές συντονισμού Δεν είναι ισοδύναμες όλες οι δομές συντονισμού Οδηγία 3. Οι δομές με μικρότερο διαχωρισμό των αντιθέτων φορτίων έχουν μεγαλύτερη συνεισφορά στον συντονισμό απ ό,τι εκείνες με μεγαλύτερο διαχωρισμό.
44 1-6 Ατομικά τροχιακά: Μια κβαντομηχανική περιγραφή των ηλεκτρονίων γύρω από τον πυρήνα Μήκος κύματος de Broglie λ = h mν Σύμφωνα με τη σχέση του de Broglie, σωματίδιο μάζας m που κινείται με ταχύτατα v έχει μήκος κύματος λ. Το ηλεκτρόνιο περιγράφεται με κυματικές εξισώσεις οι λύσεις των εξισώσεων ονομάζονται κυματικές συναρτήσεις (ψ) ή ατομικά τροχιακά
45 1-6 Ατομικά τροχιακά: Μια κβαντομηχανική περιγραφή των ηλεκτρονίων γύρω από τον πυρήνα Το ηλεκτρόνιο περιγράφεται με κυματικές εξισώσεις Σχήμα 1 4 (Α) Ένα κύμα. Τα πρόσημα του πλάτους τέθηκαν αυθαίρετα. Στα σημεία μηδενικής έντασης, που ονομάζονται κόμβοι, τα κύματα αλλάζουν πρόσημο. (Β) Κύματα με πλάτη του ίδιου πρόσημου (της αυτής φάσεως) ενισχύουν το ένα το άλλο, σχηματίζοντας ένα μεγαλύτερο κύμα. (Γ) Κύματα εκτός φάσεως αφαιρούνται μεταξύ τους, σχηματίζοντας ένα μικρότερο κύμα.
46 Τα ατομικά τροχιακά έχουν χαρακτηριστικά σχήματα Σχήμα 1 5 Απεικονίσεις ενός 1s τροχιακού. (Α) Το τροχιακό στις τρεις διαστάσεις έχει σφαιρική συμμετρία. (Β) Μια απλουστευμένη παράσταση δυο διαστάσεων. Το σημείο συν δηλώνει το μαθηματικό πρόσημο της κυματικής συνάρτησης και δεν είναι φορτίο. Σχήμα 1 6 Απεικονίσεις ενός 2s τροχιακού. Σημειώστε ότι είναι μεγαλύτερο από το 1s τροχιακό και ότι υπάρχει ένας κόμβος. Τα σημεία + και δηλώνουν τα πρόσημα της κυματικής συνάρτησης. (Α) Το τροχιακό σε τρεις διαστάσεις, με ένα τμήμα αποσπασμένο για να γίνει οπτικά διακριτός ο κόμβος. (Β) Μια πιο συμβατική δύο διαστάσεων παράσταση του τροχιακού.
47 Τα ατομικά τροχιακά έχουν χαρακτηριστικά σχήματα Σχήμα 1 7 Απεικονίσεις των 2p τροχιακών (Α) σε τρεις διαστάσεις και (Β) σε δύο διαστάσεις. Να θυμάστε ότι τα σημεία + και αναφέρονται στις κυματικές συναρτήσεις και όχι σε ηλεκτρικά φορτία. Οι λοβοί με τα αντίθετα πρόσημα χωρίζονται με ένα κομβικό επίπεδο, το οποίο είναι κάθετο στον άξονα του τροχιακού. Για παράδειγμα, το 2p x τροχιακό χωρίζεται με ένα κόμβο στο επίπεδο yz. Λύσεις με ίση ενέργεια ονομάζονται εκφυλισμένες.
48 Η αρχή δόμησης (Aufbau Prinzip) καθορίζει την τοποθέτηση των ηλεκτρονίων στα τροχιακά Κατά προσέγγιση σχετικές ενέργειες των ατομικών τροχιακών Σχήμα 1-8 Κατά προσέγγιση σχετικές ενέργειες των ατομικών τροχιακών, που χονδρικά αντιστοιχούν στη σειρά με την οποία αυτά συμπληρώνονται στα άτομα. Πρώτα συμπληρώνονται τα τροχιακά με χαμηλότερη ενέργεια τα εκφυλισμένα τροχιακά συμπληρώνονται σύμφωνα με τον κανόνα του Hund.
49 Η αρχή δόμησης (Aufbau Prinzip) καθορίζει την τοποθέτηση των ηλεκτρονίων στα τροχιακά Σταθερές ηλεκτρονικές διαμορφώσεις για τον άνθρακα, το άζωτο, το οξυγόνο και το φθόριο Σχήμα 1 9 Οι πιο σταθερές ηλεκτρονικές διαμορφώσεις για τον άνθρακα, (1s) 2 (2s) 2 (2p) 2, το άζωτο, (1s) 2 (2s) 2 (2p) 3, το οξυγόνο, (1s) 2 (2s) 2 (2p) 4 και το φθόριο (1s) 2 (2s) 2 (2p) 5. Σημειώστε ότι τα spin των μονήρων ηλεκτρονίων στα p τροχιακά είναι σύμφωνα με τον κανόνα του Hund, και τα spin των ζευγών των ηλεκτρονικών στα συμπληρωμένα 1s και 2s τροχιακά είναι σύμφωνα με την αρχή του Pauli και τον κανόνα Hund. Η σειρά της συμπλήρωσης των p τροχιακών επελέγη τυχαία ως p x, p y και τέλος p z. Οποιαδήποτε άλλη σειράθαήτανεξίσουκαλή.
50 Η αρχή δόμησης (Aufbau Prinzip) καθορίζει την τοποθέτηση των ηλεκτρονίων στα τροχιακά Διαμορφώσεις κλειστής στιβάδας των ευγενών αερίων Σχήμα 1 10 Διαμορφώσεις κλειστής στιβάδας των ευγενών αερίων ηλίου, νέου και αργού.
51 1-7 Μοριακά τροχιακά και ομοιοπολική δεσμικότητα Eν φάσει(δεσμικός) και εκτός φάσεως (αντιδεσμικός) συνδυασμός των 1s ατομικών τροχιακών. Σχήμα 1 11 Eν φάσει(δεσμικός) και εκτός φάσεως (αντιδεσμικός) συνδυασμός των 1s ατομικών τροχιακών. Τα σημεία + και δηλώνουν το πρόσημο της κυματικής συνάρτησης και όχι φορτία. Στα δεσμικά μοριακά τροχιακά, τα ηλεκτρόνια έχουν μεγάλη πιθανότητα να καταλαμβάνουν τον μεταξύ των ατομικών πυρήνων χώρο, όπως απαιτείται για να υπάρχει καλή δεσμικότητα, (συγκρίνετε το Σχήμα 1 2). Το αντιδεσμικό μοριακό τροχιακό έχει ένα κομβικό επίπεδο, όπου η πιθανότητα να βρεθούν τα ηλεκτρόνια είναι μηδέν. Τα ηλεκτρόνια σε αντιδεσμικά μοριακά τροχιακά έχουν τη μεγαλύτερη πιθανότητα να βρίσκονται εκτός του μεταξύ των πυρήνων χώρου και κατά συνέπεια δεν συνεισφέρουν στη δεσμικότητα.
52 Η επικάλυψη των ατομικών τροχιακών δημιουργεί σίγμα και πι δεσμούς Σχήμα 1 12 Σχηματική απεικόνιση της αλληλεπίδρασης δύο (Α) απλώς κατεχόμενων (όπως στο Η 2 ) και (Β) διπλώς κατεχόμενων (όπως στο He 2 ) συμπληρωμένων ατομικών τροχιακών που σχηματίζουν δύο μοριακά τροχιακά (ΜΟ, Molecular Orbitals). (Δε δίνονται σε κλίμακα). Ο σχηματισμός του δεσμού Η Η ευνοείται, γιατί σταθεροποιεί δύο ηλεκτρόνια. Ο σχηματισμός δεσμού He He σταθεροποιεί δυο ηλεκτρόνια (στο δεσμικό ΜΟ) αλλά αποσταθεροποιεί δύο άλλα (στο αντιδεσμικό ΜΟ). Έτσι, ο δεσμός μεταξύ He και He δεν προκαλεί τελικά σταθεροποίηση. Για τον λόγο αυτόν το ήλιο είναι μονατομικό.
53 Σχηματισμός δεσμών μεταξύ ατομικών τροχιακών. Σχήμα 1 13 Σχηματισμός δεσμών μεταξύ ατομικών τροχιακών. (Α) 1s και 1s (π.χ. Η 2 ), (Β) 1s και 2p (π.χ. HF), (Γ) 2p και 2p (π.χ. F 2 ), (Δ) 2p και 3p (π.χ. FCl) τοποθετημένα σε ευθεία κατά μήκος του διαπυρηνικού άξονα, σ δεσμοί (Ε) 2p και 2p τοποθετημένα κάθετα προς τον διαπυρηνικό άξονα (π.χ. H 2 C=CH 2 ), ένας π δεσμός. Σημειώστε την τυχαία χρήση των σημείων + και για να δειχθούν οι εν φάσει αλληλεπιδράσεις των κυματικών συναρτήσεων. Σημειώστε επίσης στο (Δ) τη σε «σχήμα 8 εντόςενόςσχήματος8», ανάλογη προς τα βαράκια γυμναστικής, μορφή και την εμφάνιση μεγαλύτερης διάχυσης του 3p τροχιακού σε σχέση με το αντίστοιχό 2p.
54 1-8 Υβριδικά τροχιακά: Δεσμικότητα σε σύνθετα μόρια Σχήμα 1-14 Μετακίνηση ενός ηλεκτρονίου βηρυλλίου σε υψηλότερο ενεργειακό επίπεδο, ώστε να μπορέσουν να χρησιμοποιηθούν και τα δύο ηλεκτρόνια σθένους στον σχηματισμό δεσμών.
55 1-8 Υβριδικά τροχιακά: Δεσμικότητα σε σύνθετα μόρια Σχήμα 1-15 Πιθανή αλλά λανθασμένη σύνδεση στο BeH 2, με τη χρησιμοποίηση ξεχωριστά ενός 2s και ενός 2p τροχιακού του βηρυλλίου. Δεν δείχνεται ο κόμβος στο πρώτο (2s) τροχιακό. Επιπλέον, για λόγους απλότητας, παραλείπονται τα δύο κενά 2p και το συμπληρωμένο 1s τροχιακό. Οι τελείες δηλώνουν τα ηλεκτρόνια σθένους.
56 Τα sp υβρίδια σχηματίζουν γραμμικές δομές Σχήμα 1 16 Υβριδισμός στο βηρύλλιο για τη δημιουργία δύο sp υβριδίων. (Α) Οι δεσμοί που δημιουργούνται δίνουν στο BeH 2 γραμμική δομή. Και πάλι, τα υπόλοιπα δύο p τροχιακά και το 1s τροχιακό παραλείπονται για λόγους ευκρίνειας. Το σημείο της κυματικής συνάρτησης για τους μεγαλύτερους sp λοβούς είναι αντίθετο προς αυτό των μικρότερων λοβών. (Β) Οι ενεργειακές μεταβολές που παρατηρούνται κατά τον υβριδισμό. Το 2s τροχιακό και ένα από τα 2p τροχιακά συνενώνονται σε δύο sp τροχιακά ενδιάμεσης ενέργειας. Οι ενέργειες του 1s και των υπόλοιπων 2p τροχιακών παραμένουν αμετάβλητες.
57 Τα sp 2 υβρίδια δημιουργούν τριγωνικές δομές Σχήμα 1 17 Ο υβριδισμός στο βόριο δημιουργεί τρία sp 2 υβρίδια. Οι δεσμοί που προκύπτουν δίνουν στο ΒH 3 επίπεδη τριγωνική δομή. Υπάρχουν τρεις εμπρόσθιοι λοβοί με ένα σημείο και τρείς οπίσθιοι λοβοί με αντίθετο σημείο. Το p τροχιακό που απομένει (p z ) είναι κάθετο στο μοριακό επίπεδο (το επίπεδο της σελίδας ο ένας p z λοβός βρίσκεται επάνω και ο άλλος κάτω απ αυτό το επίπεδο) και έχει παραλειφθεί. Σε αναλογία προς το Σχήμα 1 16Β, το ενεργειακό διάγραμμα για το υβριδισμένο βόριο εμφανίζει τρία απλώς κατεχόμενα, ίσης ενέργειας, sp 2 επίπεδα και ένα κενό 2p επίπεδο, επιπλέον του συμπληρωμένου 1s τροχιακού.
58 Ο sp 3 υβριδισμός εξηγεί το σχήμα των τετραεδρικών ενώσεων του άνθρακα Σχήμα 1 18 Ο υβριδισμός στον άνθρακα δημιουργεί τέσσερα sp 3 υβρίδια. Οι δεσμοί που προκύπτουν δίνουν στο CH 4 και στις άλλες ενώσεις του άνθρακα τετραεδρικές δομές. Τα sp 3 υβρίδια έχουν μικρούς οπίσθιους λοβούς με σημείο αντίθετο προς αυτό των εμπρόσθιων λοβών. Σε αναλογία με το Σχήμα 1-16Β, το ενεργειακό διάγραμμα του sp 3 υβριδισμένου άνθρακα περιέχει τέσσερα απλώς κατεχόμενα, ίσης ενέργειας sp 3 επίπεδα, επιπλέον του συμπληρωμένου 1s τροχιακού
59 Σχηματισμός του δεσμού άνθρακα άνθρακα στο αιθάνιο Σχήμα 1 19 Επικάλυψη δύο sp 3 τροχιακών για τον σχηματισμό του δεσμού άνθρακα άνθρακα στο αιθάνιο
60 Τα υβριδικά τροχιακά μπορούν να περιέχουν ελεύθερα ζεύγη ηλεκτρονίων: αμμωνία και νερό Σχήμα 1 20 Δεσμικότητα και άπωση ηλεκτρονίων στην αμμωνία και στο νερό. Τα τόξα δηλώνουν αυξημένη άπωση ηλεκτρονίων από τα ελεύθερα ζεύγη που βρίσκονται κοντά στον κεντρικό πυρήνα.
61 Επικάλυψη τροχιακών στο νερό
62 Οι πι δεσμοί είναι παρόντες στο αιθένιο (αιθυλένιο) και στο αιθύνιο (ακετυλένιο) Σχήμα 1 21 Οδιπλόςδεσμόςστοαιθένιο (αιθυλένιο) και ο τριπλός δεσμός στο αιθύνιο (ακετυλένιο).
63 1-9 Δομές και συντακτικοί τύποι των οργανικών μορίων Για να καθορίσουμε την ταυτότητα ενός μορίου, προσδιορίζουμε τη δομή του Συντακτικά ή δομικά ισομερή-διαφέρουν ως προς τη σειρά που συνδέονται τα άτομα ενώ έχουν τον ίδιο εμπειρικό τύπο
64 1-9 Δομές και συντακτικοί τύποι των οργανικών μορίων Συντακτικά ισομερή C20Η32Ο5
65 1-9 Δομές και συντακτικοί τύποι των οργανικών μορίων Απεικονίσεις τριών διαστάσεων (Α) αιθανόλης και (Β) μεθοξυμεθανίου Σχήμα 1 22 Απεικονίσεις τριών διαστάσεων (Α) αιθανόλης και (Β) μεθοξυμεθανίου, αναπαριστώμενες με μοριακά μοντέλα σφαίρας-ράβδου (ball- and-sick). Τα μήκη των δεσμών δίνονται σε μονάδες angstrom, οι γωνίες των δεσμών σε βαθμούς. (Γ) Απόδοση του μεθοξυμεθανίου με μοντέλα πλήρωσης χώρου (space-filling), όπου λαμβάνεται υπ όψιν το αποτελεσματικό μέγεθος των ηλεκτρονικών «νεφών» γύρω από τους πυρήνες που συνθέτουν το μόριο.
66 Για την απεικόνιση των μοριακών δομών χρησιμοποιούνται διάφοροι τρόποι σχεδιασμού Kekulé Συμπυκνωμένοι Δομή γραμμών-δεσμών
67 Απεικόνιση των δεσμών με διακεκομμένες (κόκκινες) και σφηνοειδείς (μπλε) γραμμές Σχήμα 1 23 Απεικόνιση των δεσμών με διακεκομμένες (κόκκινες) και σφηνοειδείς (μπλε) γραμμές για (Α) ανθρακική αλυσίδα (Β) μεθάνιο (Γ) αιθάνιο (Δ) αιθανόλη και (Ε) μεθοξυμεθάνιο. Τα άτομα που ενώνονται με κανονικές ευθείες γραμμές βρίσκονται στο επίπεδο της σελίδας. Οι ομάδες στα άκρα των διακεκομμένων γραμμών βρίσκονται κάτω απ αυτό το επίπεδο οι ομάδες στα άκρα των σφηνοειδών γραμμών βρίσκονται πάνω απ αυτό.
68 Άσκηση 1-7
69 Άσκηση 1-10
70 Άσκηση 1-14
71 ΠΡΟΒΛΗΜΑΤΑ ΑΦΟΜΟΙΩΣΗΣ ΚΕΦΑΛΑΙΟΥ
72 ΠΡΟΒΛΗΜΑΤΑ ΑΦΟΜΟΙΩΣΗΣ ΚΕΦΑΛΑΙΟΥ
73
74 Ένας αρχιτέκτων οργανικών μορίων στη δουλειά του
75 H 3 C CH 3 Αιθάνιο
76
77 Αποτέλεσμα αζωτούχων λιπασμάτων: σιτηρά με λίπασμα (αριστερά) χωρίς λίπασμα (δεξιά
78 Κβαντικό κοράλλι
79
80
81
82
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Οργανική Χημεία. Κεφάλαιο 1: Δομή και δεσμοί
 Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη. Ιοντικός χαρακτήρας δεσμών. Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
 Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού
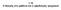 1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
Χημεία είναι επιστήμη που ερευνά τις ιδιότητες της ύλης σε σχέση με τη μοριακή δομή της. Με άλλα λόγια: μοριακής δομής της ύλης με τις ιδιότητές της
 Τι είναι Χημεία; Χημεία είναι επιστήμη που ερευνά τις ιδιότητες της ύλης σε σχέση με τη μοριακή δομή της Με άλλα λόγια: Αντικείμενο της Χημείας είναι η συσχέτιση της μοριακής δομής της ύλης με τις ιδιότητές
Τι είναι Χημεία; Χημεία είναι επιστήμη που ερευνά τις ιδιότητες της ύλης σε σχέση με τη μοριακή δομή της Με άλλα λόγια: Αντικείμενο της Χημείας είναι η συσχέτιση της μοριακής δομής της ύλης με τις ιδιότητές
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
Περίληψη 1 ου Κεφαλαίου
 Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Θεωρία δεσµού σθένους - Υβριδισµός. Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης. Αντιδράσεις υποκατάστασης Πολυµερισµός
 11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΠΑΡΑΔΕΙΓΜΑ
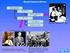 ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
κυματικής συνάρτησης (Ψ) κυματική συνάρτηση
 Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ
 ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
Μάθημα 10 ο. Ο Περιοδικός Πίνακας και ο Νόμος της Περιοδικότητας. Μέγεθος ατόμων Ενέργεια Ιοντισμού Ηλεκτρονιακή συγγένεια Ηλεκτραρνητικότητα
 Μάθημα 10 ο Ο Περιοδικός Πίνακας και ο Νόμος της Περιοδικότητας Μέγεθος ατόμων Ενέργεια Ιοντισμού Ηλεκτρονιακή συγγένεια Ηλεκτραρνητικότητα Σχέση σειράς συμπλήρωσης τροχιακών και ΠΠ Μνημονικός κανόνας
Μάθημα 10 ο Ο Περιοδικός Πίνακας και ο Νόμος της Περιοδικότητας Μέγεθος ατόμων Ενέργεια Ιοντισμού Ηλεκτρονιακή συγγένεια Ηλεκτραρνητικότητα Σχέση σειράς συμπλήρωσης τροχιακών και ΠΠ Μνημονικός κανόνας
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις
 Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
Μάθημα 21 ο. Το σχήμα των μορίων. Θεωρία VSEPR. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΕΣΜΟΥ
 ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
1o Kριτήριο Αξιολόγησης
 1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί
 1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
O 3,44 S 2,58 N 3,04 P 2,19
 Περιοδικός Πίνακας (Σύστημα) των Ατόμων Περιοδικό σύστημα είναι ο πίνακας στον οποίο κατατάσσονται όλα τα άτομα με βάση τον αριθμό των πρωτονίων (θετικά φορτισμένα σωματίδια) που ευρίσκονται στον πυρήνα
Περιοδικός Πίνακας (Σύστημα) των Ατόμων Περιοδικό σύστημα είναι ο πίνακας στον οποίο κατατάσσονται όλα τα άτομα με βάση τον αριθμό των πρωτονίων (θετικά φορτισμένα σωματίδια) που ευρίσκονται στον πυρήνα
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό
 Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
ΑΤΟΜΙΚΑ ΤΟΜΙΚΑ ΠΡΟΤΥΠΑ
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
Διάλεξη 7: Μοριακή Δομή
 Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ. Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών. Να εξηγούν το σχηματισμό του ιοντικού ομοιοπολικού δεσμού.
 ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση
 5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι μια πρώτη προσέγγιση των κυματομηχανικών θεωριών του ομοιοπολικού δεσμού και η ανακάλυψη του πώς οι θεωρίες αυτές δημιουργούν
5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι μια πρώτη προσέγγιση των κυματομηχανικών θεωριών του ομοιοπολικού δεσμού και η ανακάλυψη του πώς οι θεωρίες αυτές δημιουργούν
Μάθημα 22 ο. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 22 ο Θεωρία Δεσμού Σθένους- Υβριδισμός Linus Pauling Έγραψε τη μονογραφία : Nature of the chemical bond Τιμήθηκε για το έργο του με το βραβείο Nobel το 1954 Εισήγαγε την ιδέα του υβριδισμού Υβριδισμένα
Μάθημα 22 ο Θεωρία Δεσμού Σθένους- Υβριδισμός Linus Pauling Έγραψε τη μονογραφία : Nature of the chemical bond Τιμήθηκε για το έργο του με το βραβείο Nobel το 1954 Εισήγαγε την ιδέα του υβριδισμού Υβριδισμένα
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ
 ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
Οργανική Χημεία 24 4
 Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
 http://mathesis.cup.gr/courses/physics/phys1.1/2016_t3/about http://mathesis.cup.gr/courses/course-v1:physics+phys1.2+2016_t4/about f atomic orbitals http://www.orbitals.com/orb/orbtable.htm g atomic orbitals
http://mathesis.cup.gr/courses/physics/phys1.1/2016_t3/about http://mathesis.cup.gr/courses/course-v1:physics+phys1.2+2016_t4/about f atomic orbitals http://www.orbitals.com/orb/orbtable.htm g atomic orbitals
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις
 1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων
 Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων Κβαντικοί αριθμοί Κύριος κβαντικός αριθμός (n) Αζιμουθιακός κβαντικός αριθμός (l) Μαγνητικός κβαντικός αριθμός (ml) Στροφορμή (Spin) ηλεκτρονίου κβαντικός
Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων Κβαντικοί αριθμοί Κύριος κβαντικός αριθμός (n) Αζιμουθιακός κβαντικός αριθμός (l) Μαγνητικός κβαντικός αριθμός (ml) Στροφορμή (Spin) ηλεκτρονίου κβαντικός
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
Γεωμετρία Μορίων Θεωρία VSEPR
 Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Ασκήσεις. Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3
 Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
 Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
Μοριακή δομή Ο2 σύμφωνα με VB διαμαγνητικό
 Μοριακή δομή Ο 2 σύμφωνα με VB? διαμαγνητικό Θεωρία Μοριακών Τροχιακών Μolecular Orbital Theory (MO) Τα μοριακά τροχιακά (molecular orbital) είναι κυματοσυναρτήσεις οι οποίες προκύτπουναπότογραμμικόσυνδυασμότωνκυματοσυναρτήσεωντωναο.
Μοριακή δομή Ο 2 σύμφωνα με VB? διαμαγνητικό Θεωρία Μοριακών Τροχιακών Μolecular Orbital Theory (MO) Τα μοριακά τροχιακά (molecular orbital) είναι κυματοσυναρτήσεις οι οποίες προκύτπουναπότογραμμικόσυνδυασμότωνκυματοσυναρτήσεωντωναο.
Κεφάλαιο 9. Ιοντικός και Ομοιοπολικός Δεσμός
 Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
Ομοιοπολικός εσμός Θεωρία Lewis
 Ομοιοπολικός εσμός Θεωρία Lewis Oμοιοπολικός δεσμός: αμοιβαία συνεισφορά ηλεκτρονίων σθένους κοινά ζεύγη ηλεκτρονίων δομή ευγενούς αερίου (κανόνας της οκτάδας) Πλεονεκτήματα: η πληρέστερη προ-κβαντική
Ομοιοπολικός εσμός Θεωρία Lewis Oμοιοπολικός δεσμός: αμοιβαία συνεισφορά ηλεκτρονίων σθένους κοινά ζεύγη ηλεκτρονίων δομή ευγενούς αερίου (κανόνας της οκτάδας) Πλεονεκτήματα: η πληρέστερη προ-κβαντική
Ζαχαριάδου Φωτεινή Σελίδα 1 από 21. Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου
 Ζαχαριάδου Φωτεινή Σελίδα 1 από 21 Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου Θέµατα Σωστού/Λάθους και Πολλαπλής επιλογής Πανελληνίων, ΟΕΦΕ, ΠΜ Χ Το 17Cl σχηµατίζει ενώσεις µε ένα µόνο
Ζαχαριάδου Φωτεινή Σελίδα 1 από 21 Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου Θέµατα Σωστού/Λάθους και Πολλαπλής επιλογής Πανελληνίων, ΟΕΦΕ, ΠΜ Χ Το 17Cl σχηµατίζει ενώσεις µε ένα µόνο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ένωση Χ 3 το κεντρικό άτομο Χ φέρει δύο μονήρη ζεύγη ηλεκτρονίων σθένους, ενώ στην ένωση Υ 2 το κεντρικό άτομο Υ φέρει τρία μονήρη ζεύγη ηλεκτρονίων σθένους.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ένωση Χ 3 το κεντρικό άτομο Χ φέρει δύο μονήρη ζεύγη ηλεκτρονίων σθένους, ενώ στην ένωση Υ 2 το κεντρικό άτομο Υ φέρει τρία μονήρη ζεύγη ηλεκτρονίων σθένους.
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί
 1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων. Περιοδικός πίνακας. Σταυρακαντωνάκης Γιώργος Λύκειο Γαζίου Page 1
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
Γενική & Ανόργανη Χημεία
 Γενική & Ανόργανη Χημεία 2017-18 1 Ηλεκτρονιακή Συγγένεια (Electron Affinity) Η πρόβλεψη ορισμένων χημικών ιδιοτήτων, προϋποθέτει τη γνώση του τρόπου μεταβολής της ενέργειας κατά την προσθήκη ηλεκτρονίων
Γενική & Ανόργανη Χημεία 2017-18 1 Ηλεκτρονιακή Συγγένεια (Electron Affinity) Η πρόβλεψη ορισμένων χημικών ιδιοτήτων, προϋποθέτει τη γνώση του τρόπου μεταβολής της ενέργειας κατά την προσθήκη ηλεκτρονίων
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
Ομοιοπολικός Δεσμός. Ασκήσεις
 Ασκήσεις Ομοιοπολικός Δεσμός 1. Δίνεται η οργανική ένωση CH 3 -CH 2 -C CH της οποίας τα άτομα αριθμούνται από 1 έως 4, όπως φαίνεται παραπάνω. Πόσοι και τι είδους σ δεσμοί και π δεσμοί υπάρχουν στην ένωση;
Ασκήσεις Ομοιοπολικός Δεσμός 1. Δίνεται η οργανική ένωση CH 3 -CH 2 -C CH της οποίας τα άτομα αριθμούνται από 1 έως 4, όπως φαίνεται παραπάνω. Πόσοι και τι είδους σ δεσμοί και π δεσμοί υπάρχουν στην ένωση;
Μοριακά Πρότυπα (Μοντέλα)
 Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
Ιοντικός Δεσμός Πολωσιμότητα ιόντος Κανόνες Fajans
 Ιοντικός Δεσμός Πολωσιμότητα ιόντος: εκφράζει την παραμόρφωση που υφίσταται το ηλεκτρονιακό νέφος από ένα γειτονικό ιόν αντιθέτου φορτίου. Η ιοντική αυτή παραμόρφωση αυξάνει τον ομοιοπολικό χαρακτήρα του
Ιοντικός Δεσμός Πολωσιμότητα ιόντος: εκφράζει την παραμόρφωση που υφίσταται το ηλεκτρονιακό νέφος από ένα γειτονικό ιόν αντιθέτου φορτίου. Η ιοντική αυτή παραμόρφωση αυξάνει τον ομοιοπολικό χαρακτήρα του
ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου. Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη
 Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2
 Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
5. Να βρείτε τον ατομικό αριθμό του 2ου μέλους της ομάδας των αλογόνων και να γράψετε την ηλεκτρονιακή δομή του.
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.
![ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας. ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.](/thumbs/102/153828250.jpg) ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
ΛΥΣΕΙΣ ΑΣΚΗΣΕΩΝ ΚΕΦΑΛΑΙΟΥ 2 Α
 ΛΥΣΕΙΣ ΑΣΚΗΣΕΩΝ ΚΕΦΑΛΑΙΟΥ 2 Α Άσκηση 1: Εξηγείστε με την κλασσική θεωρία Lewis τη δομή των παρακάτω ιοντικών ενώσεων MgF 2, CaF 2 και ZrO 2. Σε ποια από τις αυτές τις ενώσεις οι ιοντικοί δεσμοί είναι ισχυρότεροι;
ΛΥΣΕΙΣ ΑΣΚΗΣΕΩΝ ΚΕΦΑΛΑΙΟΥ 2 Α Άσκηση 1: Εξηγείστε με την κλασσική θεωρία Lewis τη δομή των παρακάτω ιοντικών ενώσεων MgF 2, CaF 2 και ZrO 2. Σε ποια από τις αυτές τις ενώσεις οι ιοντικοί δεσμοί είναι ισχυρότεροι;
Σχ. 1: Τυπική μορφή μοριακού δυναμικού.
 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-1 Κεφάλαιο 6. Μόρια Εδάφια: 6.a. Μόρια και μοριακοί δεσμοί 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού 6.c. Περιστροφή και ταλάντωση μορίων 6.d. Μοριακά φάσματα 6.a.
ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-1 Κεφάλαιο 6. Μόρια Εδάφια: 6.a. Μόρια και μοριακοί δεσμοί 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού 6.c. Περιστροφή και ταλάντωση μορίων 6.d. Μοριακά φάσματα 6.a.
Μάθημα 16 ο. Γραφή Χημικών Τύπων κατά Lewis. Ο Χημικός Δεσμός Τυπικό φορτίο
 Μάθημα 16 ο Γραφή Χημικών Τύπων κατά Lewis. Ο Χημικός Δεσμός Τυπικό φορτίο Δεσμός στο μοριακό υδρογόνο ( 2 ) Το υδρογόνο σχηματίζει έναν ομοιοπολικό δεσμό. Όταν δύο άτομα υδρογόνου συνδέονται μεταξύ τους,
Μάθημα 16 ο Γραφή Χημικών Τύπων κατά Lewis. Ο Χημικός Δεσμός Τυπικό φορτίο Δεσμός στο μοριακό υδρογόνο ( 2 ) Το υδρογόνο σχηματίζει έναν ομοιοπολικό δεσμό. Όταν δύο άτομα υδρογόνου συνδέονται μεταξύ τους,
Βασικά σωματίδια της ύλης
 1 Βασικά σωματίδια της ύλης Τα βασικά σωματίδια της ύλης είναι τα άτομα, τα μόρια και τα ιόντα. «Άτομο ονομάζουμε το μικρότερο σωματίδιο της ύλης που μπορεί να πάρει μέρος στο σχηματισμό χημικών ενώσεων».
1 Βασικά σωματίδια της ύλης Τα βασικά σωματίδια της ύλης είναι τα άτομα, τα μόρια και τα ιόντα. «Άτομο ονομάζουμε το μικρότερο σωματίδιο της ύλης που μπορεί να πάρει μέρος στο σχηματισμό χημικών ενώσεων».
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ. Παππάς Χρήστος Επίκουρος Καθηγητής
 ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Είδη Δεσμών Ιοντικός δεσμός (Ionic bond), σχηματίζεται πάντα μεταξύ ηλεκτροθετικών
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Είδη Δεσμών Ιοντικός δεσμός (Ionic bond), σχηματίζεται πάντα μεταξύ ηλεκτροθετικών
ηλεκτρονιακές Κατανοµή
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΧΗΜΙΚΟΙ ΕΣΜΟΙ 1. ίνεται ο πίκας: Σύµβολο Στοιχείου Να Ηλεκτρονιακή Κατανοµή X K (2) L(4) Ψ K (2) L(8) M(7) Ζ K (2) L(7) αντιγράψετε τον πίκα Οµάδα Π.Π. στη κόλλα Περίοδος Π.Π. σας τον
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΧΗΜΙΚΟΙ ΕΣΜΟΙ 1. ίνεται ο πίκας: Σύµβολο Στοιχείου Να Ηλεκτρονιακή Κατανοµή X K (2) L(4) Ψ K (2) L(8) M(7) Ζ K (2) L(7) αντιγράψετε τον πίκα Οµάδα Π.Π. στη κόλλα Περίοδος Π.Π. σας τον
ΧΗΜΕΙΑ» ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ. Διδάσκουσα: ΣΟΥΠΙΩΝΗ Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ)
 ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ ΧΗΜΕΙΑ» Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ) ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ Διδάσκουσα: ΣΟΥΠΙΩΝΗ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΡΙΑ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ ΧΗΜΕΙΑ» Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ) ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ Διδάσκουσα: ΣΟΥΠΙΩΝΗ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΡΙΑ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
Μοριακή δομή. Απλοϊκή εικόνα του μορίου του νερού. Ηλεκτρονιακοί τύποι κατά Lewis. Δημόκριτος π.χ.
 Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
Μεταβολή ορισμένων περιοδικών ιδιοτήτων
 Μεταβολή ορισμένων περιοδικών ιδιοτήτων 1. Ερώτηση: Ποια θεωρούνται θεμελιώδη χαρακτηριστικά του ατόμου και γιατί; Θεμελιώδη χαρακτηριστικά του ατόμου είναι: η ατομική ακτίνα, η ενέργεια ιοντισμού και
Μεταβολή ορισμένων περιοδικών ιδιοτήτων 1. Ερώτηση: Ποια θεωρούνται θεμελιώδη χαρακτηριστικά του ατόμου και γιατί; Θεμελιώδη χαρακτηριστικά του ατόμου είναι: η ατομική ακτίνα, η ενέργεια ιοντισμού και
) σχηματίζονται : α. Ένας σ και δύο π δεσμοί β. Τρεις σ δεσμοί γ. Ένας π και δύο σ δεσμοί δ. Τρεις π δεσμοί.
 ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
Κομβικές επιφάνειες. Από τη γνωστή σχέση: Ψ(r, θ, φ) = R(r).Θ(θ).Φ(φ) για Ψ = 0 θα πρέπει είτε R(r) = 0 ή Θ(θ).Φ(φ) = 0
 Κομβικές επιφάνειες Από τα σχήματα των ατομικών τροχιακών αλλά και από τις μαθηματικές εκφράσεις είναι φανερό ότι υπάρχουν επιφάνειες όπου το Ψ 2 μηδενίζεται, πάνω στις οποίες δηλαδή είναι αδύνατο να βρεθεί
Κομβικές επιφάνειες Από τα σχήματα των ατομικών τροχιακών αλλά και από τις μαθηματικές εκφράσεις είναι φανερό ότι υπάρχουν επιφάνειες όπου το Ψ 2 μηδενίζεται, πάνω στις οποίες δηλαδή είναι αδύνατο να βρεθεί
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Σύγxρονη Φυσική II. Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΠΕΡΙΟΔΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΑΤΟΜΙΚΗ ΑΚΤΙΝΑ ΕΝΕΡΓΕΙΑ ΙΟΝΤΙΣΜΟΥ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΠΕΡΙΟΔΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΑΤΟΜΙΚΗ ΑΚΤΙΝΑ ΕΝΕΡΓΕΙΑ ΙΟΝΤΙΣΜΟΥ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Η ηλεκτρονιακή δομή και κυρίως τα ηλεκτρόνια σθένους (τελευταία ηλεκτρόνια) προσδίδουν στο άτομο τη χημική
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΠΕΡΙΟΔΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΑΤΟΜΙΚΗ ΑΚΤΙΝΑ ΕΝΕΡΓΕΙΑ ΙΟΝΤΙΣΜΟΥ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Η ηλεκτρονιακή δομή και κυρίως τα ηλεκτρόνια σθένους (τελευταία ηλεκτρόνια) προσδίδουν στο άτομο τη χημική
Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις
 Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις Ακολουθώντας τους κανόνες δόμησης των πολυηλεκτρονιακών ατόμων που αναπτύχθηκαν παραπάνω, θα διαπιστώσουμε ότι σε ορισμένες περιπτώσεις παρατηρούνται αποκλίσεις
Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις Ακολουθώντας τους κανόνες δόμησης των πολυηλεκτρονιακών ατόμων που αναπτύχθηκαν παραπάνω, θα διαπιστώσουμε ότι σε ορισμένες περιπτώσεις παρατηρούνται αποκλίσεις
Χημικοί Χημικ σμ σμ & Μοριακά Τροχιακά
 Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
ΜΕΡΟΣ Α' (Διάρκεια εξέτασης: 15 min)
 ΣΕΜΦΕ ΕΜΠ Γενική Χημεία Διαγώνισμα 11/02/20 1 ΜΕΡΟΣ Α' (Διάρκεια εξέτασης: 15 min) 1.Σημειώστε τη σωστή ηλεκτρονική διαμόρφωση του 28 Ni +2, [ 18 Ar]=1s 2 2s 2 2p 6 3s 2 3p 6 a. [Ar] 4s 2 3d 6 b. [Ar]
ΣΕΜΦΕ ΕΜΠ Γενική Χημεία Διαγώνισμα 11/02/20 1 ΜΕΡΟΣ Α' (Διάρκεια εξέτασης: 15 min) 1.Σημειώστε τη σωστή ηλεκτρονική διαμόρφωση του 28 Ni +2, [ 18 Ar]=1s 2 2s 2 2p 6 3s 2 3p 6 a. [Ar] 4s 2 3d 6 b. [Ar]
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (6): Τροχιακά και υβριδισμός Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (6): Τροχιακά και υβριδισμός Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
Οι δομές, οι οποίες δεν περιέχουν τυπικά φορτία υψηλά (δηλαδή είναι 2) είναι:
 Answers to Homework Set 3 12162016 1. Πριν από μερικά χρόνια δημοσιεύθηκε η σύνθεση του ιόντος 5 +. Ποια είναι η πλέον πιθανή α) γεωμετρία ηλεκτρονικών ζευγών, και β) μοριακή γεωμετρική δομή του ιόντος
Answers to Homework Set 3 12162016 1. Πριν από μερικά χρόνια δημοσιεύθηκε η σύνθεση του ιόντος 5 +. Ποια είναι η πλέον πιθανή α) γεωμετρία ηλεκτρονικών ζευγών, και β) μοριακή γεωμετρική δομή του ιόντος
Ομοιοπολικοί δεσμοί. Δύο μοριακές ενώσεις. Το ιωδοφόρμιο, CHI 3, είναι ένα εύτηκτο, κίτρινο στερεό (σημείο τήξεως 120 ο C).
 μοιοπολικοί δεσμοί μοιοπολικός δεσμός: χημικός δεσμός που σχηματίζεται με το μοίρασμα ενός ζεύγους e μεταξύ δύο ατόμων (π.χ. Η 2 ) Μοριακές ενώσεις: ενώσεις αποτελούμενες από μόρια (π.χ. 2 O) Δύο μοριακές
μοιοπολικοί δεσμοί μοιοπολικός δεσμός: χημικός δεσμός που σχηματίζεται με το μοίρασμα ενός ζεύγους e μεταξύ δύο ατόμων (π.χ. Η 2 ) Μοριακές ενώσεις: ενώσεις αποτελούμενες από μόρια (π.χ. 2 O) Δύο μοριακές
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, S = 32,066 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Σχετική ισχύς οξέων (ελάττωση από αριστερά προς τα δεξιά):
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, S = 32,066 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Σχετική ισχύς οξέων (ελάττωση από αριστερά προς τα δεξιά):
Ατομική Ακτίνα ατομική ακτίνα δραστικού μείωση δραστικό πυρηνικό φορτίο και ο κύριος κβαντικός αριθμός των εξωτ. ηλεκτρονίων
 ATOMIKH AKTINA Ατομική Ακτίνα ορίζεται ως το μισό της απόστασης μεταξύ δύο γειτονικών ατόμων, όπως αυτά διατάσσονται στο κρυσταλλικό πλέγμα του στοιχείου. Η ατομική ακτίνα ενός στοιχείου: Κατά μήκος μιας
ATOMIKH AKTINA Ατομική Ακτίνα ορίζεται ως το μισό της απόστασης μεταξύ δύο γειτονικών ατόμων, όπως αυτά διατάσσονται στο κρυσταλλικό πλέγμα του στοιχείου. Η ατομική ακτίνα ενός στοιχείου: Κατά μήκος μιας
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός.
 2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ (Valence bond theory) Οιβασικές αρχές της θεωρίας δεσµού σθένους είναι:
 ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ (Valence bond theory) Οιβασικές αρχές της θεωρίας δεσµού σθένους είναι: Κατάτην ανάπτυξη οµοιοπολικού δεσµού ανάµεσα σε δύο άτοµα, τροχιακά της στιβάδας σθένους του ενός ατόµου επικαλύπτουν
ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ (Valence bond theory) Οιβασικές αρχές της θεωρίας δεσµού σθένους είναι: Κατάτην ανάπτυξη οµοιοπολικού δεσµού ανάµεσα σε δύο άτοµα, τροχιακά της στιβάδας σθένους του ενός ατόµου επικαλύπτουν
1. (α) Ποιες είναι οι τιμές των κβαντικών αριθμών για το ηλεκτρόνιο. (β) Ποια ουδέτερα άτομα ή ιόντα μπορεί να έχουν αυτή την ηλεκτρονική διάταξη;
 1 η ΔΟΚΙΜΑΣΙΑ ΠΡΟΟΔΟΥ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ : ΑΡΙΘΜΟΣ ΜΗΤΡΩΟΥ : ΗΜΕΡΟΜΗΝΙΑ : 1. (α) Ποιες είναι οι τιμές των κβαντικών αριθμών για το ηλεκτρόνιο (β) Ποια ουδέτερα άτομα ή ιόντα μπορεί να έχουν
1 η ΔΟΚΙΜΑΣΙΑ ΠΡΟΟΔΟΥ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ : ΑΡΙΘΜΟΣ ΜΗΤΡΩΟΥ : ΗΜΕΡΟΜΗΝΙΑ : 1. (α) Ποιες είναι οι τιμές των κβαντικών αριθμών για το ηλεκτρόνιο (β) Ποια ουδέτερα άτομα ή ιόντα μπορεί να έχουν
και να υπολογίσετε την ενωτική ενέργεια του κρυσταλλικού πλέγματος του. ίνονται: Ενθαλπία σχηματισμού SrCl 2
 Ποιά από τις ενώσεις NaCl και CaCl 2 είναι περισσότερο ιοντική και γιατί; Να σχεδιαστεί ο κύκλος Born-Haber για την ένωση AlF 3 Να σχεδιάσετε τον κύκλο Born-Haber της ένωσης SrCl 2 και να υπολογίσετε την
Ποιά από τις ενώσεις NaCl και CaCl 2 είναι περισσότερο ιοντική και γιατί; Να σχεδιαστεί ο κύκλος Born-Haber για την ένωση AlF 3 Να σχεδιάσετε τον κύκλο Born-Haber της ένωσης SrCl 2 και να υπολογίσετε την
Πρωτόνια, νετρόνια και ηλεκτρόνια. πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1
 Πρωτόνια, νετρόνια και ηλεκτρόνια. σχετική μάζα σχετικό φορτίο πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1 Ο πυρήνας βρίσκεται στο κέντρο του ατόμου και περιέχει
Πρωτόνια, νετρόνια και ηλεκτρόνια. σχετική μάζα σχετικό φορτίο πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1 Ο πυρήνας βρίσκεται στο κέντρο του ατόμου και περιέχει
ΥΒΡΙ ΙΣΜΟΣ υβριδισµός
 ΥΒΡΙ ΙΣΜΟΣ Οσχηµατισµός δεσµών µε απλή επικάλυψη ατοµικών τροχιακών, σε πολλές περιπτώσεις, αδυνατεί να ερµηνεύσει τη δοµή των µορίων, όπως π.χ. των οργανικών ενώσεων. Μια προωθηµένη αντίληψη για την ερµηνεία
ΥΒΡΙ ΙΣΜΟΣ Οσχηµατισµός δεσµών µε απλή επικάλυψη ατοµικών τροχιακών, σε πολλές περιπτώσεις, αδυνατεί να ερµηνεύσει τη δοµή των µορίων, όπως π.χ. των οργανικών ενώσεων. Μια προωθηµένη αντίληψη για την ερµηνεία
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού
 7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ. ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ 1 ου ΚΕΦΑΛΑΙΟΥ
 ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1 ο ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ-ΚΟΡΔΕΛΙΟΥ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ 1 ου ΚΕΦΑΛΑΙΟΥ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: 1 2 1. ΣΩΣΤΟ (Σ) ή ΛΑΘΟΣ (Λ); Αιτιολογήστε σύντομα. 1.1 Ένα ηλεκτρόνιο σθένους του ατόμου
ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 1 ο ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ-ΚΟΡΔΕΛΙΟΥ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ 1 ου ΚΕΦΑΛΑΙΟΥ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: 1 2 1. ΣΩΣΤΟ (Σ) ή ΛΑΘΟΣ (Λ); Αιτιολογήστε σύντομα. 1.1 Ένα ηλεκτρόνιο σθένους του ατόμου
ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ
 Αρχές δόµησης πολυηλεκτρονιακών ατόµων 39. 2 o Αρχές δόµησης Πολυηλεκτρονιακών ατόµων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Η συµπλήρωση των τροχιακών ενός ατόµου µε ηλεκτρόνια γίνεται µε βάση την αρχή ηλεκτρονιακής
Αρχές δόµησης πολυηλεκτρονιακών ατόµων 39. 2 o Αρχές δόµησης Πολυηλεκτρονιακών ατόµων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Η συµπλήρωση των τροχιακών ενός ατόµου µε ηλεκτρόνια γίνεται µε βάση την αρχή ηλεκτρονιακής
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ο άργυρος εμφανίζεται στη φύση υπό τη μορφή δύο ισοτόπων τα οποία έχουν ατομικές μάζες 106,905 amu και 108,905 amu. (α) Γράψτε το σύμβολο για καθένα ισότοπο του αργύρου
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ο άργυρος εμφανίζεται στη φύση υπό τη μορφή δύο ισοτόπων τα οποία έχουν ατομικές μάζες 106,905 amu και 108,905 amu. (α) Γράψτε το σύμβολο για καθένα ισότοπο του αργύρου
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΣΗΜΕΙΩΣΕΙΣ ΚΕΦΑΛΑΙΟΥ 1 ΣΤΗ ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟ ΚΕΦΑΙΛΑΙΟ 1. Α) Μηχανική συνθήκη ( βελάκι σελ 3) Β) Οπτική συνθήκη (1 ο βελάκι σελ 4 )
 ΣΗΜΕΙΩΣΕΙΣ ΚΕΦΑΛΑΙΟΥ 1 ΣΤΗ ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟ ΚΕΦΑΙΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚOΣ ΠΙΝΑΚΑΣ 1)Ατομικό πρότυπο του Bohr ( πυρήνας,..., περιστρεφόμενα ηλεκτρόνια) περιγράφεται
ΣΗΜΕΙΩΣΕΙΣ ΚΕΦΑΛΑΙΟΥ 1 ΣΤΗ ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟ ΚΕΦΑΙΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚOΣ ΠΙΝΑΚΑΣ 1)Ατομικό πρότυπο του Bohr ( πυρήνας,..., περιστρεφόμενα ηλεκτρόνια) περιγράφεται
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, Ca = 40,078 amu, N = 14,0067 amu, H = 1,00794 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Γράφετε ευανάγνωστα και
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, Ca = 40,078 amu, N = 14,0067 amu, H = 1,00794 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Γράφετε ευανάγνωστα και
Κατανομή μετάλλων και αμετάλλων στον Π.Π.
 Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια.
 ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
Διαγώνισμα στη Χημεία Γ Λυκείου.
 Διαγώνισμα στη Χημεία Γ Λυκείου. 1 ο Κεφάλαιο: μέχρι και Ηλ. τύποι Lewis. 5 ο Κεφάλαιο μέχρι πολυμερισμός Ενδεικτικές Απαντήσεις Θέμα 1 ο.... Σημειώστε τη σωστή απάντηση στις ερωτήσεις 1.1 έως 1.5 1.1.
Διαγώνισμα στη Χημεία Γ Λυκείου. 1 ο Κεφάλαιο: μέχρι και Ηλ. τύποι Lewis. 5 ο Κεφάλαιο μέχρι πολυμερισμός Ενδεικτικές Απαντήσεις Θέμα 1 ο.... Σημειώστε τη σωστή απάντηση στις ερωτήσεις 1.1 έως 1.5 1.1.
Περιοδικό Σύστημα Ιστορική Εξέλιξη
 Περιοδικό Σύστημα Ιστορική Εξέλιξη Newlands (1864): ταξινόμηση στοιχείων κατά αύξουσα ατομική μάζα και σε οκτάβες H Li Be B C N O F Na Mg Al Si P S Cl K Ca Cr Ti Mn Fe Meyer (1865): σχέση ιδιοτήτων και
Περιοδικό Σύστημα Ιστορική Εξέλιξη Newlands (1864): ταξινόμηση στοιχείων κατά αύξουσα ατομική μάζα και σε οκτάβες H Li Be B C N O F Na Mg Al Si P S Cl K Ca Cr Ti Mn Fe Meyer (1865): σχέση ιδιοτήτων και
Μάθημα 14ο. Περιοδικότητα των ιδιοτήτων των ατόμων των στοιχείων
 Μάθημα 14ο Περιοδικότητα των ιδιοτήτων των ατόμων των στοιχείων Ηλεκτρονιακή συγγένεια Το αντίθετο της ενέργειας ιοντισμού. Μεταβολή της ενέργειας όταν τα άτομα στην αέρια φάση κερδίζουν ηλεκτρόνια και
Μάθημα 14ο Περιοδικότητα των ιδιοτήτων των ατόμων των στοιχείων Ηλεκτρονιακή συγγένεια Το αντίθετο της ενέργειας ιοντισμού. Μεταβολή της ενέργειας όταν τα άτομα στην αέρια φάση κερδίζουν ηλεκτρόνια και
1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα
 1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα Θεωρία 3.1. Ποια είναι τα δομικά σωματίδια της ύλης; Τα άτομα, τα μόρια και τα ιόντα. 3.2. SOS Τι ονομάζεται άτομο
1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα Θεωρία 3.1. Ποια είναι τα δομικά σωματίδια της ύλης; Τα άτομα, τα μόρια και τα ιόντα. 3.2. SOS Τι ονομάζεται άτομο
Ερωτήσεις Σωστού Λάθους
 Ερωτήσεις Σωστού Λάθους Να χαρακτηρίσετε τις παρακάτω προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ) και να αιτιολογήσετε την απάντησή σας. 1. Το ιόν του νατρίου, 11 Na +, προκύπτει όταν το άτομο του Na προσλαμβάνει
Ερωτήσεις Σωστού Λάθους Να χαρακτηρίσετε τις παρακάτω προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ) και να αιτιολογήσετε την απάντησή σας. 1. Το ιόν του νατρίου, 11 Na +, προκύπτει όταν το άτομο του Na προσλαμβάνει
