( ) ( ) 2008/2009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
|
|
|
- Αποστόλης Αγγελοπούλου
- 6 χρόνια πριν
- Προβολές:
Transcript
1 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) ρ ( A ) = 5,5 ρ( ) ( A ) = ( A ) = 5,5 ( ) = 5,5 g/mol = 7g/mol ( A) = = A, kloor / V 5,5 / V m m r 7/ 5,5 b) X Fe, raud A, kloor B Fe, raud(iii)kloriid Fe, raud(ii)kloriid D Fe(), raud(iii)hüdroksiid E Fe(), raud(ii)hüdroksiid c) Fe + = Fe Fe + = Fe + t Fe = Fe + Fe + K = Fe() + K Fe + K = Fe() + K Fe() + + = Fe() II III Fe e = Fe 0 -II + e =. a) Ag = Ag n = n Ag ( ) g mol n = mg = 0,00mol 000 mg g 5,5 g m ( g ) = 0,00mol = 0,055 g m lahus = 0 cm = 0 g mol cm - 0,055 g %( ) = 00 = 0,55 0,6 0 g b) n, g mol ( Ag ) = cm 0, cm 70 g =0,00 mol > 0,00mol c) g + + P - = g (P ) a + + P = a (P ) 000 cm 0,00mol n (,poriloigus) =,5 dm = 0,5 mol dm 0cm n ( P ) = 0,5 mol = 0,07 mol 0 6 g m ( ap ) = 0,07 mol =, 8 g g mol. a) äädikas, etaanhape 5 piiritus, etanool etüleen, eteen ( ) 7 parafiin, nonadekaan b) + = = + + = + ( ) = c) Iga aine korral tuleb leida süsinikdioksiidi ruumala, kuna veeaur kondenseerub toatemperatuuril. mol,dm V () = g = 0,75 dm 60g mol mol, dm V (5) = g = 0,97 dm 6g mol mol, dm V ( ) = g =,6 dm 8g mol 9 mol, dm V (( ) 7 ) = g =,6 dm 68 g mol Kõige suurema õhupalli saaksime,0 g etüleeni ja parafiini põletamisest.. a) emulsioon b) Pentaan aurustub, oktaan jääb vee pinnale. m ( 5) = 500 t 0,5 = 50 t 6 m 0 g mol 6 n ( 5) = = 50 t =,5 0 mol t 7g 6, dm m V ( 5 ) = nv m =,5 0 mol = 7,7 0 m mol 000 dm 8 0 m c) erepinnale jääb oktaan, seega: m ( 88) = 500 t 0,5 = 50 t m 0 kg dm 5 = 50 t =,6 0 dm 5 V 8 8 = 0 dm ρ t 0,70kg 5 ha 5 5 S ( 8 8 ) =,6 0 dm =, 0 ha 0 ha dm d) Pentaani jaoks: V mol molekuli ( 5,g) = n A = A = dm 6,0 0 = Vm, dm mol =,7 0 molekuli 0 molekuli m ρ V 000 cm 0,69 g mol 5 A A A dm (,v) = n = = = dm cm 7g molekuli 6,0 0 = 5, 0 molekuli 5 0 molekuli mol
2 ktaani jaoks: m ρ V 000 cm 0,70 g mol 8 8 A A A dm (,v) = n = = = dm cm g molekuli 6,0 0 =,7 0 molekuli 0 molekuli mol 5. a) Tselluloos on (polü)sahhariid. Ühes lülis peab paiknema kolm hüdroksüülrühma, sest üks hapniku aatom on tsükli sees ja iga tsükli kohta tuleb ka üks tsükleid ühendav hapniku aatom. () = = 6 r 6 7 b) mol -0 n = =,0 0 mol 6,0 0 c) ( 6 7 ) n r( 67 ) = = 97 d) Lülide arv tselluloosi molekulis ei ole selle arvutuse jaoks oluline ja kogu arvutuse võib sooritada ühe molekuli korduva osa kohta. 97 m = 50 g 0,9 = 578 g 580 g 6 r Z = 58 0, = 8 ) X Si, ränidioksiid (liiv, r ( X ) = 58 0,65 = 60 ) Q võib keemiliste omaduste alusel olla kas Al (0 g/mol) või Fe (60 g/mol), sest alumiinium ja raud passiveeruvad kontsentreeritud väävelhappe toimel. Täpsemalt saame tuvastada mineraali A kaudu: r ( Q ) = 58 0,95 = 0 Q Al, alumiiniumoksiid mineraal A Al Si ehk Al Si 9 mineraal B Al Si ehk Al Si 7 mineraal D Al Si ehk Al Si mineraal E Al Si ehk Al 6 Si b) Al Si 9 t = Al Si 7 + Al Si t 7 = Al Si + Si Al Si t = Al 6 Si + 5Si 6. a) Z, vesi (vesi eraldus mineraalist A,
3 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused 0. klass. a) () b) ( ) = ( D ) = V, ,999 g/mol = 8,05 g/mol 8,0 g / mol,0 + 5,999 g/mol = 0,07 g/mol 0,0 g/mol 8,0 g cm = = 8,05 cm / mol mol 0,998 g m 0,0 g cm V m( D ) = = 8, cm / mol mol,06 g 8,05 cm mol dm -6 dm V ( ) = =,997 0 mol 6,0 0 molek. 0 cm molek. 8,cm mol dm -6 dm V ( D ) = =,007 0 mol 6,0 0 molek. 0 cm molek. -8 c) V =,0 μm π (0,5 μm) =,57 μm =,6 0 m -8 kg 0,5,57 0 m 00 mol -6 mol c = m = 0,007 =,7 0 =,7 μ -8 kg,57 0 m m dm mol. a) A a (söögisool nii maitseaine kui ka säilitusaine) B ( r ( ) = 7) F ( ja F on mõlemad VIIA rühmas) D F (binaarne ühend, o.a() = +III) E F (binaarne ühend, o.a() = +I) F F (binaarne ühend) G (hape) (hape) I (hape) J ( r ( ) = 7 0,95 = 5,5 + 6 = 67,5) b) a + n + S = a S + ns + + F + = F + F F + = F + + S = + S c) hν = III V e = III IV e = III -I + e = d) < < g mol m e = dm = 0,79 g mol, dm 9 g mol m ( õhk ) = dm =,9 g mol, dm b) Kuna tihedused on võrdelised molaarmassidega (ρ = /V m ), siis heeliumi tihedus on 9,00 g/mol g/mol = 7,5 korda väiksem. Et tihedused oleksid võrdsed, peab samas ruumalaühikus olema 7,5 korda rohkem heeliumi, seega 7,5 atmosfääri. m ρv ρ c) pv = nrt = RT = RT => p = RT Kui p = const, ρ = const ja R = const, siis T T = / 9,00 g/mol T ( õhk ) = 7 K = 979 K = 70,00 g/mol g/mol d) ω = 5, ppm = 0,7 ppm 9 g/mol. a). a) etallihüdriidi üldine valem on n, kus n on metalli o.a. Reaktsioon veega: n + n = () n + n. Kui ühe mooli hüdriidi reaktsioonil tekib üks mool vesinikku, siis n =. ksüdatsiooniaste, aktiivsus ja hüdroksiidi tugev aluseline reaktsioon viitavad leelismetallile. Ülesande tingimustega on kooskõlas Li. b) Li -I + I = Li + 0 üdriidi koostises olev vesinik käitub redutseerijana ja vees olev vesinik oksüdeerijana mol, dm V (Li) = g =,8 dm 8 g mol c) Li + = Li liitiumoksiid Li + = Li liitiumhüdriid Li + = Li + liitiumhüdroksiid 6Li + = Li liitiumnitriid Li + = Li Li = Li + liitiumkarbonaat
4 5. a) 0 + = g mol 655 kj 6 Q ( butaan ) =,0 kg =,5 0 kj kg 58,g mol b) + = + 6, kj n( ) = =,88 0 mol 80 kj/mol dm 6 K dm i) V m(talvel) =, =,6 mol 7 K mol,6 dm m V (, talvel ) =,88 0 mol =, m mol 000 dm 0,98 dm 9 K dm ii) V m(suvel) =, =,0 mol 7 K mol dm m V (, suvel ) =,88 0 mol = 6,0 m mol 000 dm 0,98 6. a) A i B o Fe D s E Ir F Rh b) Fe 0 + i III () = i II () + Fe II () c) Aatomnumbri erinevus võrra viitab sellele, et elemendid D ja F on perioodis. Arvestades aatomnumbrite erinevust 9 jõuame järeldusele, et B on., F 5. ja D 6. perioodis. Elementide D ja E aatommasside väikene erinevus ning see, et B ja E asuvad samas rühmas määrab ära elemendi E asendi. Aatommasside erinevus,0 amü viitab, et D s ja A/ o /A E Ir. Seega F Rh ja B o. A ja võivad olla kas Rh raud või nikkel s Ir Koobalt(III)hüdroksiid on tugevam oksüdeerija kui raud(iii)hüdroksiid. Raud-nikkel elemendi töötamisel raud oksüdeerub ja i() redutseerub. Seega A i ja Fe. D D B F B F E
5 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused. klass π ( 0,% lahus ) = 7,5atm/=,5 atm < atm 0,% a lahuses toimub hemolüüs.. a) A B D. a) V( 0,9% a lahus) V( 0,% a lahus) = = = cm dm 5 g 0,005 dm g 000 cm = 0,9% lahuse valmistamine: m a = 5 g 0,009 = 0,05 g E b) eksanitrodifenüülamiin moodustab vastavaid soolasid, sest kahe aktseptorrühma mõju tõttu on aminorühma vesinikuaatom happeliste omadustega. X m ( % lahus ) = 0,05 g =,5 g m ( vesi ) = ( 5,5) g= 0,5 g 0,0 c n mol ( 0,9% lahus ) = 0,05 g 0,5 V = 58, g 0,005 dm = = 0,5 0,% lahuse valmistamine: m a = 5 g 0,00 = 0,05 g 0,05 g 0,0 m ( % lahus ) = =,5 g m ( vesi ) = c ( 0,9% lahus ) = 0,05 / = 0,05 = 0,05 b) T = ( + 7) K = 9 K 0,5 mol 0,08 dm atm 5,5 g=,5 g π 0,9% lahus = 9K atm dm molk = 7,5 atm > 0,9% a lahuses ei toimu hemolüüsi. +. a) X Si, räni A Si, räni(iv)oksiid ehk kvarts (piesoefekt) B F, vesinikfluoriidhape Si 8, trisilaan D [( ) Si] n ((R Si) n ), silikoon a Al X 8 5 a Al Si 9, alumosilikaat ehk tseoliit X Z Si, räninitriid b) Si + = Si, Si + 6F = SiF 6 + Si + a = a Si + Si = Si + Si + F = SiF 6 + F. a) + A B vaheühend V Y b) etadooni (R)-enantiomeer Z Br + gbr W + etadooni vesinikkloriidhappe sool a + X
6 5. a) aatriumuraadi lahustuvus puhtas vees: С 5 Н a a KL = a 5 + s = a = 5 KL = s s = s s = KL s = 6,0 0 5 =0,00777 Dinaatriumuraadi lahustuvus puhtas vees: С 5 Н a a KL = a 5 a + 5 s = = KL KL = s s = s s = 7 7,8 0 s = = 0,0058 b) Leiame a kontsentratsiooni peale lahuste kokku valamist 0,5 0 cm ca = = 0,05 ( ) cm aatriumuraadi lahustuvus 0,05 a vesilahuses: С 5 Н a a KL = a 5 a a a = ca + s 5 = s KL = ( ca + s) s = cas + s s + c s K = s = 0,5c ± 0,5c + K a L 0 a a L s = 0,05 ± 0,06 s = 0,00 Lahustuvuste erinevus on 0,00777 /0,00 = 6,6 korda Dinaatriumuraadi lahustuvus 0,05 a vesilahuses: С 5 Н a a KL = a 5 a a a = ca + s 5 = s K L = ca + s s Teeme lihtsustuse ca s ca + s ca KL ca s 7 KL 7,8 0 s = =, 0 (Täpne lahend on, ) ca 0,05 Lahustuvuste erinevus on 0,0058 /0,000 = 9 korda c) Kolme käiguga:. (.). (.). (.). (.) 5. (.) 6. (.) 7. (.) Jörgen Andres Jörgen Andres Jörgen Andres Jörgen I n II Br III Re IV I V s VI K n KBr Re KI K s Jörgen võitis, sest nimetatud on kõik elemendid, mis võivad esineda o.a-s +VII. d) Kolme käiguga:. (.). (.). (.). (.) 5. (.) 6. (.) 7. (.) 8. (.) Jörgen Andres Jörgen Andres Jörgen Andres Jörgen Andres Li I Xe II Br III s IV I V Ru VI n VII LiF XeF KBr s KI K Ru Kn Andres võitis, sest nimetatud on kõik elemendid, mis võivad esineda o.a-s +VIII. e) Elemendid oksüdatsiooniastmega 8: Xe, Ru, s käiku Elemendid oksüdatsiooniastmega 7:, Br, I, n, Re veel 7 käiku Summaarselt käiku. 6. a) mitte radioaktiivne Bi, vismut (õigeks võib lugeda ka Pb, plii Kuigi vismutit on kaua aega peetud mitteradioaktiivseks, on hiljuti leitud, et vismut on siiski radioaktiivne ülipika poolestusajaga,9 0 9 aastat) radioaktiivsed Tc, tehneetsium ja Pm, promeetium b) +VII (, Br, I, n, Re) ja +VIII (Xe, Ru, s)
7 008/009 õ.a. keemiaolümpiaadi lõppvooru ülesannete lahendused. klass. а) = b) A, sinihape + [ ][ ] c) K = a [] ( + + ) Soola hüdrolüüs: + = + [] = [ ] [ ] = c(a) [ ] [ + ] = K w /[ ] ( + + ) K ( c(a) [ ]) W K = a [ ] K a [ ] + K w [ ] K W c(a) = 0 0,mol ( c ( a) = 0,5 dm = 0,8 ) [] = [ ] =,7 0 (Võib ka lihtsustada: c(a) >> [ ], [ ] c(a) KW 0 [ ] = = c ( a) = 0,8 =,7 0 ) 9, Ka 0 d) n(amügdaliin) = n(, 0 7 hüdrol.) = n(, a hüdrol.) 57 g kirsikivid =,7 0 0,5 dm = 7 mol 0,008 g (Amügdaliini hüdrolüüsil tekkinud sinihape on praktiliselt kõik dissotsieerumata kujul). a) mol D, mol D ja 6 mol ja D aatomid on vedelikus vahetuvad ja kombineeruvad seetõttu statistiliselt (eeldame, et vee ioonkorrutis ei muutu K w = const ). (80 mol) + + (0 mol) D D + + D Vesiniku ja deuteeriumi leidumise tõenäosused on vastavalt: 80 P () = = 0,8 0 P (D) = = 0, Leiame kombinatsioonide D, D, D ja esinemise tõenäosused kerge ja raske vee segus: P (D) = 0, 0, = 0,0 P(D) = P(D) = 0,8 0, = 0,6 P () = 0,8 0,8 = 0,6 Arvutame segu lõppkoostise: n (D ) = 00 mol 0,0 = mol n (D) = 00 mol 0,6 + 0,6 = mol n () = 00 mol 0,6 = 6 mol b) T (A) ja T (B). ( A) ( B) > 6/ Suhe on 6/ suurem, sest A derivaat on lisaks veel steeriliselt eelistatum, kuna metüülrühmad (- ) on triitiumile kergemini kätte saadavad. D с) A, D D, D D D D B D, E DD, D D D D, F D D, D + (I) D D või R + R + (II) R + R + R (III) R R + R + R (IV) R R
8 Kui esimeses reaktsioonis osaleb, siis reaktsioonides (II-IV) tekib ainult ühend A. Ühendid B-F tekivad, siis kui I reaktsioonis osalevad nii kui ka D. B tekkimisel vahetatakse välja D vastu. etapis. tekkimisel vahetatakse välja D vastu. etapis. D tekkimisel vahetatakse välja D vastu. etapis (kordub korda). E tekkimisel vahetatakse välja D vastu. ja. etapis. F tekkimisel vahetatakse välja D vastu. (kordub korda) ja. etapis. IV. a) A, nurk 0 ; B V VII b), nurgad (): ja 06 (keskm. 09,5 ) c) K + S = K S + () = + + () a + S = + a S () a + () + S = + a S + + () a + = + a. a) R metüülrühm [ ] r ( R ) = ( ) / = 5 R etüülrühm [ ] R -metüülpropüülrühm [ ( ) ] R -karboksüetüülrühm [ ( )] Et molekulis oleks kiraalne tsenter, peab liitumine toimuma etüülrühma esimesse asendisse + I - alus- - I - r = 76 + r (R) - + I - I - - alus ( ) Br - alus- - Br ( ) Br - Br - - alus- + - alus Ibuprofeen + = 06 b) (R)--[-(-metüülpropüül)fenüül]propaanhape c) (0,8) = 0,5. Summaarne saagis on 50%. d) Kuna karboksüülhape on märksa tugevam hape, deprotoneerub esimesena karboksüülrühm ja moodustub liitiumatsetaat. + 9 Li= Li a) Fe + = Fe + V RT 8,J/(mol K) (7,5 + 5)K m dm b) V = = = = 0 = m 5 n p 0 Pa mol mol 000 g mol,0 dm V ( ) = kg = 858 dm 0,86 m kg 55,85 g mol 0 c) Δ = ( 0 0) kj mol = kj mol 0 Δ S = + 7 ( 78 + ) J ( mol K) = 6 J ( mol K) J 6 J J Δ G = Δ TΔ S = ( ) K = 56 mol mol K mol exp ΔG exp 56 K = = = RT 8, 7,66 d) i) Rõhk praktiliselt ei mõjuta tasakaalu, sest gaasimolekulide arv mõlemal pool võrrandit on võrdne. ii) Kõrgemal temperatuuril reaktsiooni tasakaalukonstant väheneb (Δ 0 < 0). Tasakaal on nihutatud rohkem reagentide tekke suunas.
9 e) Õhu keskmine molaarmass on 9 g/mol.,0 dm mol 000 g m V ( ) = 00 kg = 78 m (9 ) g mol kg 000 dm 78 m ( püssitorud ) = 07 0,859 m = 0 V RT 8,J/(mol K) (7,5 + )K dm f) V = = = = 9, m 5 n p 0,78 0 Pa mol 9, dm mol 000 g m V ( ) = 00 kg = 7 m (9 ) g mol kg 000 dm 6. a) A P, divesinikfosfaatioon B a (P ), kaltsiumfosfaat, kloriidioon 58,9 D o, koobalt(ii)kloriid %( o) = 00 = 5,9 9,8 E o (P ), koobalt(iii)fosfaat Y o, koobalt b) ATP + ADP ATP-aas + P P + a = a (P ) ( KL = 0 L = 70 ) a (P ) + o = o (P ) + a 5 8 ( KL = 0 L = 50 ) ( ) S + o (P ) = os + ( ) P ( K L (α os) 0 L = = 6 0 ) c) Lihaskiudude tumedaksvärvumine näitab suure hulga ATP-aasi olemasolu neis kiududes, seega on need kiud võimelised kiiresti lagundama ATP-d ja saama lühikese aja jooksul palju energiat. Tumedaks värvuvad on nn. tüüpi ehk sprinterikiud. Kuna opossumil neid eriti palju ei olnud, sobiks ilmselt pikamaajooks talle paremini ning sprinteriks saamise unistus on veidi ebareaalne.
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 16. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja 0. klass) 6. november 2002. a.. ) 2a + 2 = a 2 2 2) 2a + a 2 2 = 2a 2 ) 2a + I 2 = 2aI 4) 2aI + Cl 2 = 2aCl + I 2 5) 2aCl = 2a + Cl 2 (sulatatud
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Nooem aste (9. ja 10. klass) Tallinn, Tatu, Kuessaae, Nava, Pänu, Kohtla-Jäve 11. novembe 2006 Ülesannete lahendused 1. a) M (E) = 40,08 / 0,876 = 10,2 letades,
HAPE-ALUS TASAKAAL. Teema nr 2
 PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
PE-LUS TSL Teema nr Tugevad happed Tugevad happed on lahuses täielikult dissotiseerunud + sisaldus lahuses on võrdne happe analüütilise kontsentratsiooniga Nt NO Cl SO 4 (esimeses astmes) p a väärtused
Eesti koolinoorte 43. keemiaolümpiaad
 Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Eesti koolinoorte 4. keeiaolüpiaad Koolivooru ülesannete lahendused 9. klass. Võrdsetes tingiustes on kõikide gaaside ühe ooli ruuala ühesugune. Loetletud gaaside ühe aarruuala ass on järgine: a 2 + 6
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 18. november a.
 Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
Keemia lahtise võistluse ülesannete lahendused oorem rühm (9. ja. klass) 8. november 2. a.. a) X C, vingugaas, Q Cl 2, Z CCl 2, fosgeen b) Z on õhust raskem, sest Q on õhust raskem, Z molekulmass on aga
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused klass
 2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
2017/2018. õa keemiaolümpiaadi piirkonnavooru lahendused 11. 12. klass 18 g 1. a) N = 342 g/mol 6,022 1023 molekuli/mol = 3,2 10 22 molekuli b) 12 H 22 O 11 + 12O 2 = 12O 2 + 11H 2 O c) V = nrt p d) ΔH
I. Keemiline termodünaamika. II. Keemiline kineetika ja tasakaal
 I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
I. Keemiline termdünaamika I. Keemiline termdünaamika 1. Arvutage etüüni tekke-entalpia ΔH f lähtudes ainete põlemisentalpiatest: ΔH c [C(gr)] = -394 kj/ml; ΔH c [H 2 (g)] = -286 kj/ml; ΔH c [C 2 H 2 (g)]
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
217/218. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 11. 12. klass 1. a) Vee temperatuur ei muutu. (1) b) A gaasiline, B tahke, C vedel Kõik õiged (2), üks õige (1) c) ja d) Joone õige asukoht
Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 10. klass) 15. november a.
 . a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
. a) A mutant E.coli B β galaktosidaas C allolaktoos D laktoos b) N = 2 aatomit Keemia lahtise võistluse ülesannete lahendused Noorem rühm (9. ja 0. klass) 5. november 200. a. molekulis 6 prootonit + aatomit
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED, ÜLESANDED LEA PALLAS VII OSA SISUKORD 57 Joone uutuja Näited 8 58 Ülesanded uutuja võrrandi koostamisest 57 Joone uutuja Näited Funktsiooni tuletisel on
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
2012/2013 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Meie keha valgud koosnevad aminohapetest, Aminohape R- rühm mida ühendavad peptiidsidemed. Peptiidside Glütsiin -H tekib ühe aminohappe karboksüülrühma
Kompleksarvu algebraline kuju
 Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
Kompleksarvud p. 1/15 Kompleksarvud Kompleksarvu algebraline kuju Mati Väljas mati.valjas@ttu.ee Tallinna Tehnikaülikool Kompleksarvud p. 2/15 Hulk Hulk on kaasaegse matemaatika algmõiste, mida ei saa
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass
 2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
2004/2005 õa keemiaolümpiaadi lõppvooru ülesanded 10. klass 1. Andresele anti analüüsiks kolm tahket metalli, millest kaks olid väliselt väga sarnased, kolmas oli pisut tuhmim. Andres leidis, et antud
5. a) ρ (g/cm 3 ) = 0,119 = 11,9% 12% 2 p
 201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
201/2014 õ.a keemiaolümpiaadi piirkonnavooru ülesanded 8. klass Ülesannete lahendused 1. a) Alumiinium 1 p b) Broom 1 p c) Füüsikalised nähtused: muna vahustamine; sahharoosi lahustumine; katseklaasi purunemine,
1998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass
 998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
998/99 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) S ii) S iii) S S S b) i) S 9 ii)m(s 9 ) = g/mol + 9 6 g/mol = 40 g/mol c) i) m(s ) = amü + 6 amü = 44 amü ii) 96 = 5, iii) 80
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass
 2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
2001/2002 õa keemiaolümpiaadi piirkonnavooru ülesanded 8. klass 1. Justus von Liebig sündis 1803. aastal Saksamaal. Koolist visati ta paugutamise pärast välja, mille järel asus tööle apteekri abina. Kui
Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design
 Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Supplemental Material for Estimation of grain boundary segregation enthalpy and its role in stable nanocrystalline alloy design By H. A. Murdoch and C.A. Schuh Miedema model RKM model ΔH mix ΔH seg ΔH
Funktsiooni diferentsiaal
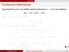 Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Diferentsiaal Funktsiooni diferentsiaal Argumendi muut Δx ja sellele vastav funktsiooni y = f (x) muut kohal x Eeldusel, et f D(x), saame Δy = f (x + Δx) f (x). f (x) = ehk piisavalt väikese Δx korral
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Νόµοςπεριοδικότητας του Moseley:Η χηµική συµπεριφορά (οι ιδιότητες) των στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού. Περιοδικός πίνακας: α. Είναι µια ταξινόµηση των στοιχείων κατά αύξοντα
Ruumilise jõusüsteemi taandamine lihtsaimale kujule
 Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Kodutöö nr.1 uumilise jõusüsteemi taandamine lihtsaimale kujule Ülesanne Taandada antud jõusüsteem lihtsaimale kujule. isttahuka (joonis 1.) mõõdud ning jõudude moodulid ja suunad on antud tabelis 1. D
Keemiliste elementide perioodilisustabel
 Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O 2, Si, H 2 ) (HCl) (KOH) (Na 2 SO 4 ) Happelised oksiidid Aluselised oksiidid (SO 2, CO 2,
Ehitusmehaanika harjutus
 Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
Ehitusmehaanika harjutus Sõrestik 2. Mõjujooned /25 2 6 8 0 2 6 C 000 3 5 7 9 3 5 "" 00 x C 2 C 3 z Andres Lahe Mehaanikainstituut Tallinna Tehnikaülikool Tallinn 2007 See töö on litsentsi all Creative
b) Täpne arvutus (aktiivsete kontsentratsioonide kaudu) ph arvutused I tugevad happed ja alused
 ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
ph arvutused I tugevad happed ja alused Tugevad happed: HCl, HBr, HI, (NB! HF on nõrk hape) HNO 3, H 2SO 4, H 2SeO 4, HClO 4, HClO 3, HBrO 4, HBrO 3, HMnO 4, H 2MnO 4 Tugevad alused: NaOH, OH, LiOH, Ba(OH)
Lokaalsed ekstreemumid
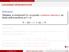 Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
Lokaalsed ekstreemumid Öeldakse, et funktsioonil f (x) on punktis x lokaalne maksimum, kui leidub selline positiivne arv δ, et 0 < Δx < δ Δy 0. Öeldakse, et funktsioonil f (x) on punktis x lokaalne miinimum,
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA
 MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
MATEMAATIKA TÄIENDUSÕPE MÕISTED, VALEMID, NÄITED LEA PALLAS XII OSA SISUKORD 8 MÄÄRAMATA INTEGRAAL 56 8 Algfunktsioon ja määramata integraal 56 8 Integraalide tabel 57 8 Määramata integraali omadusi 58
gaas-tahke Lahustumisprotsess:
 5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
5. LAHUSED Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Ainete agregaatolekute baasil saab eristada järgmisi lahuseid: gaas-gaas gaas-vedelik gaas-tahke
=217 kj/mol (1) m Ühe mooli glükoosi sünteesil lihtainetest vabaneb footoneid: Δ H f, glükoos n (glükoos) =5,89 mol (1) E (footon)
 KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
KEEMIAÜLESANNETE LAHENDAMISE LAHTINE VÕISTLUS Vanem rühm (11. ja 12. klass) Kohtla-Järve, Kuressaare, Narva, Pärnu, Tallinn ja Tartu 6. oktoober 2018 1. a) 1 p iga õige ühendi eest. (4) b) Võrrandist ():
2005/2006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. = 52,5 g/mol
 005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
005/006 õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. klass. a) i) Zn Hl = Znl H ii) Na H = NaH H iii) Al 6NaH 6H = Na [Al(H) 6 ] H b) i) HN ii) sool, oksiid ja vesi c) H = H d) Vesinikku on 00
ΝΟΜΟΣ ΤΗΣ ΠΕΡΙΟ ΙΚΟΤΗΤΑΣ : Οι ιδιότητες των χηµικών στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
ETTEVALMISTUS KEEMIAOLÜMPIAADIKS II
 ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
ETTEVALMISTUS KEEMIALÜMPIAADIKS II ÜLESANDED VALEMITE MÄÄRAMISE KHTA III SÜSTEMAATILINE LÄHENEMINE LAHENDAMISELE Kõikvõimalikud lihtsustamised ja eeldused on eelkõige vajalikud aja säästmiseks Mõnikord
,millest avaldub 21) 23)
 II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
II kursus TRIGONOMEETRIA * laia matemaatika teemad TRIGONOMEETRILISTE FUNKTSIOONIDE PÕHISEOSED: sin α s α sin α + s α,millest avaldu s α sin α sα tan α, * t α,millest järeldu * tα s α tα tan α + s α Ülesanne.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ. Εικόνα 1. Φωτογραφία του γαλαξία μας (από αρχείο της NASA)
 ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
ΓΗ ΚΑΙ ΣΥΜΠΑΝ Φύση του σύμπαντος Η γη είναι μία μονάδα μέσα στο ηλιακό μας σύστημα, το οποίο αποτελείται από τον ήλιο, τους πλανήτες μαζί με τους δορυφόρους τους, τους κομήτες, τα αστεροειδή και τους μετεωρίτες.
Graafiteooria üldmõisteid. Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid
 Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Graafiteooria üldmõisteid Graaf G ( X, A ) Tippude hulk: X={ x 1, x 2,.., x n } Servade (kaarte) hulk: A={ a 1, a 2,.., a m } Orienteeritud graafid Orienteerimata graafid G(x i )={ x k < x i, x k > A}
Et mingit probleemi hästi uurida, katsuge enne alustamist sellest põhjalikult aru saada!
 EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
EESSÕNA Käesolev juhendmaterjal on abiks eelkõige harjutustundides ning laboratoorsete tööde tegemisel. Esimene peatükk sisaldab põhimõisteid ja mõningaid arvutamisjuhiseid, peatüki lõpus on valik anorgaanilise
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
rgaanilise keemia õpiku küsimuste vastused 8. KARBNÜÜLÜENDID (LK 15 16) II osa 1. Butaani ja propanooni (atsetooni) molekulid omavahel vesiniksidemeid ei moodusta, sellest nende madal keemistemperatuur.
Geomeetrilised vektorid
 Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
Vektorid Geomeetrilised vektorid Skalaarideks nimetatakse suurusi, mida saab esitada ühe arvuga suuruse arvulise väärtusega. Skalaari iseloomuga suurusi nimetatakse skalaarseteks suurusteks. Skalaarse
ITI 0041 Loogika arvutiteaduses Sügis 2005 / Tarmo Uustalu Loeng 4 PREDIKAATLOOGIKA
 PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
PREDIKAATLOOGIKA Predikaatloogika on lauseloogika tugev laiendus. Predikaatloogikas saab nimetada asju ning rääkida nende omadustest. Väljendusvõimsuselt on predikaatloogika seega oluliselt peenekoelisem
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused klass
 2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
2017/2018. õa keemiaolümpiaadi lõppvooru ülesannete lahendused 9. 10. klass 1. a) Mg 2+ + 2OH = Mg(OH) 2 (1) b) c(karedus) = 19,25 cm3 0,02000 mol/dm 3 100 cm 3 = 0,003850 M c(karedus) = 3,850 mmol/dm
TÄIENDAVAID TEEMASID KOOLIKEEMIALE I
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE I LAHUSED Natalia Nekrassova Õppevahend TK õpilastele Tartu 008 LAHUSED Looduses ja tehnikas lahused omavad suurt tähtsust. Taimed omandavad
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ Περίοδοι περιοδικού πίνακα Ο περιοδικός πίνακας αποτελείται από 7 περιόδους. Ο αριθμός των στοιχείων που περιλαμβάνει κάθε περίοδος δεν είναι σταθερός, δηλ. η περιοδικότητα
Αλληλεπίδραση ακτίνων-χ με την ύλη
 Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Άσκηση 8 Αλληλεπίδραση ακτίνων-χ με την ύλη Δ. Φ. Αναγνωστόπουλος Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Ιωάννινα 2013 Άσκηση 8 ii Αλληλεπίδραση ακτίνων-χ με την ύλη Πίνακας περιεχομένων
Orgaanilise keemia õpiku küsimuste vastused
 rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
rgaanilise keemia õpiku küsimuste vastused 1. SÜSINIKU KEEMIA (LK 24) I osa 3. Tasapinnaline struktuurivalem Ruumiline struktuurivalem C C C C C C 4. a) b) c) 5. a) b) c) C C C C C C C C C C C C C C C
9. AM ja FM detektorid
 1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
1 9. AM ja FM detektorid IRO0070 Kõrgsageduslik signaalitöötlus Demodulaator Eraldab moduleeritud signaalist informatiivse osa. Konkreetne lahendus sõltub modulatsiooniviisist. Eristatakse Amplituuddetektoreid
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks
 4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
4.2.5 Täiustatud meetod tuletõkestusvõime määramiseks 4.2.5.1 Ülevaade See täiustatud arvutusmeetod põhineb mahukate katsete tulemustel ja lõplike elementide meetodiga tehtud arvutustel [4.16], [4.17].
Το άτομο του Υδρογόνου
 Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
Το άτομο του Υδρογόνου Δυναμικό Coulomb Εξίσωση Schrödinger h e (, r, ) (, r, ) E (, r, ) m ψ θφ r ψ θφ = ψ θφ Συνθήκες ψ(, r θφ, ) = πεπερασμένη ψ( r ) = 0 ψ(, r θφ, ) =ψ(, r θφ+, ) π Επιτρεπτές ενέργειες
Vektorid II. Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale
 Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Vektorid II Analüütiline geomeetria 3D Modelleerimise ja visualiseerimise erialale Vektorid Vektorid on arvude järjestatud hulgad (s.t. iga komponendi väärtus ja positsioon hulgas on tähenduslikud) Vektori
Koduseid ülesandeid IMO 2017 Eesti võistkonna kandidaatidele vol 4 lahendused
 Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Koduseid ülesandeid IMO 017 Eesti võistkonna kandidaatidele vol 4 lahendused 17. juuni 017 1. Olgu a,, c positiivsed reaalarvud, nii et ac = 1. Tõesta, et a 1 + 1 ) 1 + 1 ) c 1 + 1 ) 1. c a Lahendus. Kuna
Kehade soojendamisel või jahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks.
 KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
KOOLIFÜÜSIKA: SOOJUS 3 (kaugõppele) 6. FAASISIIRDED Kehade sooendamisel või ahutamisel võib keha minna ühest agregaatolekust teise. Selliseid üleminekuid nimetatakse faasisiireteks. Sooendamisel vaaminev
Compress 6000 LW Bosch Compress LW C 35 C A ++ A + A B C D E F G. db kw kw /2013
 55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
55 C 35 C A A B C D E F G 50 11 12 11 11 10 11 db kw kw db 2015 811/2013 A A B C D E F G 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi
Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika
 Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
Operatsioonsemantika Kirjeldab kuidas toimub programmide täitmine Tähendus spetsifitseeritakse olekuteisendussüsteemi abil Loomulik semantika kirjeldab kuidas j~outakse l~oppolekusse Struktuurne semantika
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass
 2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
2013/2014 õ.a keemiaolümpiaadi lõppvooru ülesanded 9. klass 1. Ained A on oksiidid. Tuntud metalli X võib saada vedelal kujul, kui süüdata segu, mis koosneb metalli Y ja musta oksiidi A pulbritest, kõrvalsaadusena
Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ. Παππάς Χρήστος Επίκουρος Καθηγητής
 ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
ΗΛΕΚΤΡΟΝΙΚΗ ΟΜΗ ΚΑΙ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΑΤΟΜΩΝ Παππάς Χρήστος Επίκουρος Καθηγητής ΤΟ ΜΕΓΕΘΟΣ ΤΩΝ ΑΤΟΜΩΝ Ατομική ακτίνα (r) : ½ της απόστασης μεταξύ δύο ομοιοπυρηνικών ατόμων, ενωμένων με απλό ομοιοπολικό δεσμό.
CaCO 3(s) --> CaO(s) + CO 2(g) H = kj. Näide
 3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
3. KEEMILINE TERMODÜNAAMIKA Keemiline termodünaamika uurib erinevate energiavormide vastastikuseid üleminekuid keemilistes ja füüsikalistes protsessides. 3.1. Soojuslikud muutused keemilistes reaktsioonides
28. Sirgvoolu, solenoidi ja toroidi magnetinduktsiooni arvutamine koguvooluseaduse abil.
 8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
8. Sigvoolu, solenoidi j tooidi mgnetinduktsiooni vutmine koguvooluseduse il. See on vem vdtud, kuid mitte juhtme sees. Koguvooluseduse il on sed lihtne teh. Olgu lõpmt pikk juhe ingikujulise istlõikeg,
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi
 Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
Eesti koolinoorte XLVIII täppisteaduste olümpiaadi lõppvoor MATEMAATIKAS Tartus, 9. märtsil 001. a. Lahendused ja vastused IX klass 1. Vastus: x = 171. Teisendame võrrandi kujule 111(4 + x) = 14 45 ning
ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ ο Γυμνάσιο Αγ. Παρασκευής
 ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ04.01 5 ο Γυμνάσιο Αγ. Παρασκευής Όπως συμβαίνει στη φύση έτσι και ο άνθρωπος θέλει να πετυχαίνει σπουδαία αποτελέσματα καταναλώνοντας το λιγότερο δυνατό
ΠΕΡΙΟΔΙΚΟ ΣΥΣΤΗΜΑ ΤΩΝ ΣΤΟΙΧΕΙΩΝ (1) Ηλία Σκαλτσά ΠΕ04.01 5 ο Γυμνάσιο Αγ. Παρασκευής Όπως συμβαίνει στη φύση έτσι και ο άνθρωπος θέλει να πετυχαίνει σπουδαία αποτελέσματα καταναλώνοντας το λιγότερο δυνατό
Επιμέλεια: Φροντιστήρια «ΟΜΟΚΕΝΤΡΟ ΦΛΩΡΟΠΟΥΛΟΥ»
 Τρίτη 27 Μαΐου 2014 Α ΛΥΚΕΙΟΥ ΝΕΟ ΕΞΕΤΑΣΤΙΚΟ ΣΥΣΤΗΜΑ ΧΗΜΕΙΑ Επιμέλεια: Φροντιστήρια «ΟΜΟΚΕΝΤΡΟ ΦΛΩΡΟΠΟΥΛΟΥ» ΧΗΜΕΙΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1-Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και
Τρίτη 27 Μαΐου 2014 Α ΛΥΚΕΙΟΥ ΝΕΟ ΕΞΕΤΑΣΤΙΚΟ ΣΥΣΤΗΜΑ ΧΗΜΕΙΑ Επιμέλεια: Φροντιστήρια «ΟΜΟΚΕΝΤΡΟ ΦΛΩΡΟΠΟΥΛΟΥ» ΧΗΜΕΙΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1-Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και
Andmeanalüüs molekulaarbioloogias
 Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
Andmeanalüüs molekulaarbioloogias Praktikum 3 Kahe grupi keskväärtuste võrdlemine Studenti t-test 1 Hüpoteeside testimise peamised etapid 1. Püstitame ENNE UURINGU ALGUST uurimishüpoteesi ja nullhüpoteesi.
DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud.
 Kolmnurk 1 KOLMNURK DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud. Kolmnurga tippe tähistatakse nagu punkte ikka
Kolmnurk 1 KOLMNURK DEF. Kolmnurgaks nim hulknurka, millel on 3 tippu. / Kolmnurgaks nim tasandi osa, mida piiravad kolme erinevat punkti ühendavad lõigud. Kolmnurga tippe tähistatakse nagu punkte ikka
HULGATEOORIA ELEMENTE
 HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
HULGATEOORIA ELEMENTE Teema 2.2. Hulga elementide loendamine Jaan Penjam, email: jaan@cs.ioc.ee Diskreetne Matemaatika II: Hulgateooria 1 / 31 Loengu kava 2 Hulga elementide loendamine Hulga võimsus Loenduvad
Μάθημα 12ο. O Περιοδικός Πίνακας Και το περιεχόμενό του
 Μάθημα 12ο O Περιοδικός Πίνακας Και το περιεχόμενό του Γενική και Ανόργανη Χημεία 201-17 2 Η χημεία ΠΠΠ (= προ περιοδικού πίνακα) μαύρο χάλι από αταξία της πληροφορίας!!! Καμμία οργάνωση των στοιχείων.
Μάθημα 12ο O Περιοδικός Πίνακας Και το περιεχόμενό του Γενική και Ανόργανη Χημεία 201-17 2 Η χημεία ΠΠΠ (= προ περιοδικού πίνακα) μαύρο χάλι από αταξία της πληροφορίας!!! Καμμία οργάνωση των στοιχείων.
τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n, l)
 ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
ΑΤΟΜΙΚΑ ΤΡΟΧΙΑΚΑ Σχέση κβαντικών αριθµών µε στιβάδες υποστιβάδες - τροχιακά Η στιβάδα καθορίζεται από τον κύριο κβαντικό αριθµό (n) Η υποστιβάδα καθορίζεται από τους δύο πρώτους κβαντικούς αριθµούς (n,
3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE
 3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE 3.1. Loendamise põhireeglid Kombinatoorika on diskreetse matemaatika osa, mis uurib probleeme, kus on tegemist kas diskreetse hulga mingis mõttes eristatavate osahulkadega
3. LOENDAMISE JA KOMBINATOORIKA ELEMENTE 3.1. Loendamise põhireeglid Kombinatoorika on diskreetse matemaatika osa, mis uurib probleeme, kus on tegemist kas diskreetse hulga mingis mõttes eristatavate osahulkadega
AATOMI EHITUS KEEMILINE SIDE
 TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
TALLINNA TEHNIKAÜLIKOOL Keemiainstituut Vambola Kallast AATOMI EHITUS KEEMILINE SIDE Õppevahend Tallinn 1997 ISBN 9789949483112 (pdf) V. Kallast, 1997 TTÜ,1997,300,223 Kr. 12.20 Sisukord Eessõna... 4 I.
Answers to practice exercises
 Answers to practice exercises Chapter Exercise (Page 5). 9 kg 2. 479 mm. 66 4. 565 5. 225 6. 26 7. 07,70 8. 4 9. 487 0. 70872. $5, Exercise 2 (Page 6). (a) 468 (b) 868 2. (a) 827 (b) 458. (a) 86 kg (b)
Answers to practice exercises Chapter Exercise (Page 5). 9 kg 2. 479 mm. 66 4. 565 5. 225 6. 26 7. 07,70 8. 4 9. 487 0. 70872. $5, Exercise 2 (Page 6). (a) 468 (b) 868 2. (a) 827 (b) 458. (a) 86 kg (b)
2.2.1 Geomeetriline interpretatsioon
 2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
2.2. MAATRIKSI P X OMADUSED 19 2.2.1 Geomeetriline interpretatsioon Maatriksi X (dimensioonidega n k) veergude poolt moodustatav vektorruum (inglise k. column space) C(X) on defineeritud järgmiselt: Defineerides
KEEMIA ÜLESANNETE LAHENDAMINE II
 KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
KEEMIA ÜLESANNETE LAHENDAMINE II ÜLESANDED JA LAHENDUSED Ülesanne 1 Ülesanne Ülesanne Vana münt diameetria, cm ja paksusea,0 mm on tehtud puhtast kullast (ρ = 1900 k m ). Kulla hind on 410$ ühe untsi eest
p A...p D - gaasiliste ainete A...D osarõhud, atm K p ja K c vahel kehtib seos
 LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
LABO RATOO RNE TÖÖ 3 Keemiline tasakaal ja reaktsioonikiirus Keemilised rotsessid võib jagada öörduvateks ja öördumatuteks. Pöördumatud rotsessid kulgevad ühes suunas raktiliselt lõuni. Selliste rotsesside
Eesti koolinoorte 51. täppisteaduste olümpiaad
 Eesti koolinoorte 5 täppisteaduste olümpiaad Füüsika lõppvoor 7 märts 2004 a Põhikooli ülesannete lahendused ülesanne (KLAASTORU) Plaat eraldub torust siis, kui petrooleumisamba rõhk saab võrdseks veesamba
Eesti koolinoorte 5 täppisteaduste olümpiaad Füüsika lõppvoor 7 märts 2004 a Põhikooli ülesannete lahendused ülesanne (KLAASTORU) Plaat eraldub torust siis, kui petrooleumisamba rõhk saab võrdseks veesamba
STM A ++ A + A B C D E F G A B C D E F G. kw kw /2013
 Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
Ι 47 d 11 11 10 kw kw kw d 2015 811/2013 Ι 2015 811/2013 Toote energiatarbe kirjeldus Järgmised toote andmed vastavad nõuetele, mis on esitatud direktiivi 2010/30/ täiendavates määrustes () nr 811/2013,
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat
 Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
Halogeenid, VIIA Fluor, kloor, broom, jood, astaat F Cl Br I At Z 9 17 35 53 85 A r 18.9984 35.4527 79.904 126.9045 [210] El. neg. 4.0 3.0 2.8 2.5 2.2 T s, C -219.6-101.5-7.3 113.7 302 T k, C -188.1-34.0
..,..,.. ! " # $ % #! & %
 ..,..,.. - -, - 2008 378.146(075.8) -481.28 73 69 69.. - : /..,..,... : - -, 2008. 204. ISBN 5-98298-269-5. - -,, -.,,, -., -. - «- -»,. 378.146(075.8) -481.28 73 -,..,.. ISBN 5-98298-269-5..,..,.., 2008,
..,..,.. - -, - 2008 378.146(075.8) -481.28 73 69 69.. - : /..,..,... : - -, 2008. 204. ISBN 5-98298-269-5. - -,, -.,,, -., -. - «- -»,. 378.146(075.8) -481.28 73 -,..,.. ISBN 5-98298-269-5..,..,.., 2008,
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Βιολογία Γ Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΚΩΣΤΑΣ ΓΚΑΤΖΕΛΑΚΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Βιολογία Γ Λυκείου Επιμέλεια: ΚΩΣΤΑΣ ΓΚΑΤΖΕΛΑΚΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 2010 2011 µ..., µ..,... 2011. 1:, 19-21
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Βιολογία Γ Λυκείου Επιμέλεια: ΚΩΣΤΑΣ ΓΚΑΤΖΕΛΑΚΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 2010 2011 µ..., µ..,... 2011. 1:, 19-21
Ασκήσεις Προβλήματα. Μετρήσεις Μονάδες Γνωρίσματα της Ύλης
 Ασκήσεις Προβλήματα Μετρήσεις Μονάδες Γνωρίσματα της Ύλης 19. Ποιες μονάδες χρησιμοποιούν συνήθως οι χημικοί για την πυκνότητα των: α) στερεού, β) υγρού και γ) αερίου σώματος; Να εξηγήσετε τη διαφορά.
Ασκήσεις Προβλήματα Μετρήσεις Μονάδες Γνωρίσματα της Ύλης 19. Ποιες μονάδες χρησιμοποιούν συνήθως οι χημικοί για την πυκνότητα των: α) στερεού, β) υγρού και γ) αερίου σώματος; Να εξηγήσετε τη διαφορά.
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2012. Ηµεροµηνία: Τετάρτη 18 Απριλίου 2012 ΕΚΦΩΝΗΣΕΙΣ
 ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 0 Ε_.ΧλΘ(ε) ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 8 Απριλίου
Kontekstivabad keeled
 Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
Kontekstivabad keeled Teema 2.1 Jaan Penjam, email: jaan@cs.ioc.ee Rekursiooni- ja keerukusteooria: KV keeled 1 / 27 Loengu kava 1 Kontekstivabad grammatikad 2 Süntaksipuud 3 Chomsky normaalkuju Jaan Penjam,
sin 2 α + cos 2 sin cos cos 2α = cos² - sin² tan 2α =
 KORDAMINE RIIGIEKSAMIKS III TRIGONOMEETRIA ) põhiseosed sin α + cos sin cos α =, tanα =, cotα =, cos sin + tan =, tanα cotα = cos ) trigonomeetriliste funktsioonide täpsed väärtused α 5 6 9 sin α cos α
KORDAMINE RIIGIEKSAMIKS III TRIGONOMEETRIA ) põhiseosed sin α + cos sin cos α =, tanα =, cotα =, cos sin + tan =, tanα cotα = cos ) trigonomeetriliste funktsioonide täpsed väärtused α 5 6 9 sin α cos α
TÄIENDAVAID TEEMASID KOOLIKEEMIALE III
 TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
TARTU ÜLIKOOL TEADUSKOOL TÄIENDAVAID TEEMASID KOOLIKEEMIALE III KEEMILINE TASAKAAL Vello Past Õppevahend TK õpilastele Tartu 007 KEEMILINE TASAKAAL 1. Keemilise tasakaalu mõiste. Tasakaalu mõiste on laialt
Jätkusuutlikud isolatsioonilahendused. U-arvude koondtabel. VÄLISSEIN - COLUMBIA TÄISVALATUD ÕÕNESPLOKK 190 mm + SOOJUSTUS + KROHV
 U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
U-arvude koondtabel lk 1 lk 2 lk 3 lk 4 lk 5 lk 6 lk 7 lk 8 lk 9 lk 10 lk 11 lk 12 lk 13 lk 14 lk 15 lk 16 VÄLISSEIN - FIBO 3 CLASSIC 200 mm + SOOJUSTUS + KROHV VÄLISSEIN - AEROC CLASSIC 200 mm + SOOJUSTUS
PÕLEVAINETE OMADUSED. Andres Talvari
 PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
PÕLEVAINETE OMADUSED Andres Talvari Õppevahend on koostatud kõrgkooli õpikute alusel ja mõeldud kasutamiseks SKA Päästekolledzi rakenduskõrgharidusõppe päästeteenistuse erialal õppeaines Põlemiskeemia
5. TUGEVUSARVUTUSED PAINDELE
 TTÜ EHHTROONKNSTTUUT HE00 - SNTEHNK.5P/ETS 5 - -0-- E, S 5. TUGEVUSRVUTUSE PNELE Staatika üesandes (Toereaktsioonide eidmine) vaadatud näidete ause koostada taade sisejõuepüürid (põikjõud ja paindemoment)
TTÜ EHHTROONKNSTTUUT HE00 - SNTEHNK.5P/ETS 5 - -0-- E, S 5. TUGEVUSRVUTUSE PNELE Staatika üesandes (Toereaktsioonide eidmine) vaadatud näidete ause koostada taade sisejõuepüürid (põikjõud ja paindemoment)
Κατανομή μετάλλων και αμετάλλων στον Π.Π.
 Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
Planeedi Maa kaardistamine G O R. Planeedi Maa kõige lihtsamaks mudeliks on kera. Joon 1
 laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
laneedi Maa kaadistamine laneedi Maa kõige lihtsamaks mudeliks on kea. G Joon 1 Maapinna kaadistamine põhineb kea ümbeingjoontel, millest pikimat nimetatakse suuingjooneks. Need suuingjooned, mis läbivad
Ερωηήζεις Πολλαπλής Επιλογής
 Ερωηήζεις Θεωρίας 1. Ππθλφηεηα: α) δηαηχπσζε νξηζκνχ, β) ηχπνο, γ) είλαη ζεκειηψδεο ή παξάγσγν κέγεζνο;, δ) πνηα ε κνλάδα κέηξεζήο ηεο ζην Γηεζλέο Σχζηεκα (S.I.); ε) πνηα ε ρξεζηκφηεηά ηεο; 2. Γηαιπηφηεηα:
Ερωηήζεις Θεωρίας 1. Ππθλφηεηα: α) δηαηχπσζε νξηζκνχ, β) ηχπνο, γ) είλαη ζεκειηψδεο ή παξάγσγν κέγεζνο;, δ) πνηα ε κνλάδα κέηξεζήο ηεο ζην Γηεζλέο Σχζηεκα (S.I.); ε) πνηα ε ρξεζηκφηεηά ηεο; 2. Γηαιπηφηεηα:
20. SIRGE VÕRRANDID. Joonis 20.1
 κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
κ ËÁÊ Â Ì Ë Æ Á 20. SIRGE VÕRRANDID Sirget me võime vaadelda kas tasandil E 2 või ruumis E 3. Sirget vaadelda sirgel E 1 ei oma mõtet, sest tegemist on ühe ja sama sirgega. Esialgu on meie käsitlus nii
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ. Γενικής Παιδείας Χημεία Α Λυκείου ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ. Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ
 ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
ΗΛΙΑΣΚΟΣ ΦΡΟΝΤΙΣΤΗΡΙΑ ΥΠΗΡΕΣΙΕΣ ΠΑΙΔΕΙΑΣ ΥΨΗΛΟΥ ΕΠΙΠΕΔΟΥ Γενικής Παιδείας Χημεία Α Λυκείου Επιμέλεια: ΒΑΣΙΛΗΣ ΛΟΓΟΘΕΤΗΣ e-mail: info@iliaskos.gr www.iliaskos.gr 1 57 1.. 1 kg = 1000 g 1 g = 0,001 kg 1
C M. V n: n =, (D): V 0,M : V M P = ρ ρ V V. = ρ
 »»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
»»...» -300-0 () -300-03 () -3300 3.. 008 4 54. 4. 5 :.. ;.. «....... :. : 008. 37.. :....... 008.. :. :.... 54. 4. 5 5 6 ... : : 3 V mnu V mn AU 3 m () ; N (); N A 6030 3 ; ( ); V 3. : () 0 () 0 3 ()
Eesti koolinoorte XLIX täppisteaduste olümpiaad
 Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
Eesti koolinoorte XLIX täppisteaduste olümpiaad MATEMAATIKA PIIRKONDLIK VOOR 26. jaanuaril 2002. a. Juhised lahenduste hindamiseks Lp. hindaja! 1. Juhime Teie tähelepanu sellele, et alljärgnevas on 7.
ORGAANILINE KEEMIA. Lühikonspekt gümnaasiumile. Koostaja: Kert Martma
 ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
ORGAANILINE KEEMIA Lühikonspekt gümnaasiumile Koostaja: Kert Martma Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline
2.2 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΕΡΙΩΝ
 2.2 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΕΡΙΩΝ Έστω ότι μια ποσότητα αερίου έχει όγκο V, πίεση P και απόλυτη θερμοκρασία Τ. Διατηρώντας σταθερή τη θερμοκρασία Τ του αερίου, μεταβάλλουμε τον όγκο μέχρι την τιμή V,
2.2 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΕΡΙΩΝ Έστω ότι μια ποσότητα αερίου έχει όγκο V, πίεση P και απόλυτη θερμοκρασία Τ. Διατηρώντας σταθερή τη θερμοκρασία Τ του αερίου, μεταβάλλουμε τον όγκο μέχρι την τιμή V,
Energiabilanss netoenergiavajadus
 Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
Energiabilanss netoenergiajadus 1/26 Eelmisel loengul soojuskadude arvutus (võimsus) φ + + + tot = φ φ φ juht v inf φ sv Energia = tunnivõimsuste summa kwh Netoenergiajadus (ruumis), energiakasutus (tehnosüsteemis)
ΛΥΣΕΙΣ. 1. Χαρακτηρίστε τα παρακάτω στοιχεία ως διαµαγνητικά ή. Η ηλεκτρονική δοµή του 38 Sr είναι: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 2
 ΛΥΣΕΙΣ 1. Χαρακτηρίστε τα παρακάτω στοιχεία ως διαµαγνητικά ή παραµαγνητικά: 38 Sr, 13 Al, 32 Ge. Η ηλεκτρονική δοµή του 38 Sr είναι: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 2 Η ηλεκτρονική δοµή του
ΛΥΣΕΙΣ 1. Χαρακτηρίστε τα παρακάτω στοιχεία ως διαµαγνητικά ή παραµαγνητικά: 38 Sr, 13 Al, 32 Ge. Η ηλεκτρονική δοµή του 38 Sr είναι: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 2 Η ηλεκτρονική δοµή του
4. ELECTROCHEMISTRY - II
 4. ELETROHEMISTRY - II Molar coductace, Equivalet coductace, cell cetat ad Kohlraush Law :. Give : l 0.98 cm a.3 cm cell cost. cell cost. a l cell cost. a l 0.98.3 0.7538 cm As : ell costat for the cell
4. ELETROHEMISTRY - II Molar coductace, Equivalet coductace, cell cetat ad Kohlraush Law :. Give : l 0.98 cm a.3 cm cell cost. cell cost. a l cell cost. a l 0.98.3 0.7538 cm As : ell costat for the cell
FUNKTSIONAALSED RÜHMAD I osa. Kaido Viht
 FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
FUNKTSINAALSED ÜMAD I osa Kaido Viht Õppematerjal TÜ teaduskooli õpilastele Tartu 2018 aliid al : halorühm Alkohol, fenool ( = Ar) hüdroksüülrühm Eeter ' alkoksürühm, arüüloksürühm (' = Ar) Peroksiid,
PLASTSED DEFORMATSIOONID
 PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
PLAED DEFORMAIOONID Misese vlavustingimus (pinegte ruumis) () Dimensineerimisega saab kõrvaldada ainsa materjali parameetri. Purunemise (tugevuse) kriteeriumid:. Maksimaalse pinge kirteerium Laminaat puruneb
ORGAANILINE KEEMIA I osa
 ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
ORGAANILINE KEEMIA I osa (Pildiallikas: http://www.indigo.com/models/gphmodel/molymod-d-glucose.jpg ) 1. SISSEJUHATUS Orgaaniliseks keemiaks nimetatakse keemia haru, mis käsitleb orgaanilisi ühendeid ja
T~oestatavalt korrektne transleerimine
 T~oestatavalt korrektne transleerimine Transleerimisel koostatakse lähtekeelsele programmile vastav sihtkeelne programm. Transleerimine on korrektne, kui transleerimisel programmi tähendus säilib. Formaalsemalt:
T~oestatavalt korrektne transleerimine Transleerimisel koostatakse lähtekeelsele programmile vastav sihtkeelne programm. Transleerimine on korrektne, kui transleerimisel programmi tähendus säilib. Formaalsemalt:
Eesti koolinoorte XLI täppisteaduste olümpiaad
 Eesti koolinoorte XLI täppisteaduste olümpiaad MATEMAATIKA III VOOR 6. märts 994. a. Lahendused ja vastused IX klass.. Vastus: a) neljapäev; b) teisipäev, kolmapäev, reede või laupäev. a) Et poiste luiskamise
Eesti koolinoorte XLI täppisteaduste olümpiaad MATEMAATIKA III VOOR 6. märts 994. a. Lahendused ja vastused IX klass.. Vastus: a) neljapäev; b) teisipäev, kolmapäev, reede või laupäev. a) Et poiste luiskamise
2004/2005 õa keemiaolümpiaadi piirkonnavooru ülesannete lahendused 8. klass
 . a) i) ii) km 0 000 m 00 cl L L 2004/2005 õa keemiaolümpiaadi piirkonnavooru ülesannete lahendused 8. klass 5 = 050 km 2 = 200 cl m iii) 000 kg/m = kg/dm 000 dm b) i) keemiliste nähtuste korral molekulide
. a) i) ii) km 0 000 m 00 cl L L 2004/2005 õa keemiaolümpiaadi piirkonnavooru ülesannete lahendused 8. klass 5 = 050 km 2 = 200 cl m iii) 000 kg/m = kg/dm 000 dm b) i) keemiliste nähtuste korral molekulide
7.7 Hii-ruut test 7.7. HII-RUUT TEST 85
 7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
7.7. HII-RUUT TEST 85 7.7 Hii-ruut test Üks universaalsemaid ja sagedamini kasutust leidev test on hii-ruut (χ 2 -test, inglise keeles ka chi-square test). Oletame, et sooritataval katsel on k erinevat
