7.Separarea clorurii de sodiu (sare de bucătărie) dintr-un amestec se realizează prin: a. decantarea; b. filtrare;
|
|
|
- Ευρώπη Κοντολέων
- 6 χρόνια πριν
- Προβολές:
Transcript
1 MINISTERUL EDUCAŢIEI, CERCETĂRII, TINERETULUI SI SPORTULUI INSPECTORATUL ŞCOLAR AL JUDEŢULUI SUCEAVA COLEGIUL NAŢIONAL EUDOXIU HURMUZACHI RĂDĂUŢI, Calea Bucovinei 5, Cod: , Tel: 0230/561522, Fax:0230/ yahoo.com COD FISCAL Nr. 317/13 martie 2013 Anexa 4 PROBLEME PROPUSE 1.Un cui de fier este supus unor transformări chimice prin; a. îndoire, b. magnetizare; c. rupere; d. ruginire. 2.Substanţele obţinute în urma vaporizăriii: a. îşi modifică compoziţia; b. îşi modifică starea de agregare, c. au aceeaşi compoziţie cu cele iniţiale; d. se transformă în substanţe cu proprietăţi noi. 3.Stingerea varului reprezintă: a. un fenomen fizic; b. un fenomen chimic; c. o transformare a unei substanţe în alta cu proprietăţi noi; d. o transformare ce lasă nemodificată compoziţia substanţelor. 4.Care din exemplele următoare reprezintă o substanţă simplă: a. apă; b. aer; c. oxigen, d. alcool. 5.Care din exemplele de mai jos reprezintă o substanţă compusă: a. azot; b. pilitură de fier; c. oţet; d. aer. 6.Care din exemplele următoare reprezintă un amestec: a. mina de creion; b. aer; c. apă distilată; d. piatra de var. 7.Separarea clorurii de sodiu (sare de bucătărie) dintr-un amestec se realizează prin: a. decantarea; b. filtrare; 1
2 c. sublimare; d. alte metode. 8.Într-un pahar Berzelius cu apă se adaugă o spatulă de pilitură de fer şi una de zahăr. Separarea celor două substanţe se realizează prin: a. decantare urmată de filtrare; b. filtrare urmată de cristalizare; c. filtrare urmată de distilare; d. distilare urmată de cristalizare. 9.Purificarea sării extrase din saline se realizează prin: a. distilare; b. decantare; c. filtrare; d. cristalizare. 10.Într-un pahar Berzelius găseşte un amestec de apă, pulbere de cărbune şi iod. Care din următoarele metode de separare a componenţilor, în ordinea aplicării lor, sunt valabile: a. filtrare şi sublimare; b. sublimare şi filtrare; c. decantare şi cristalizare; d. filtrare şi cristalizare. 11.Soluţiile sunt: a. combinaţii chimice obţinute din 2 substanţe; b. amestecuri eterogene de 2 sau mai multe substanţe; c. amestecuri omogene de 2 sau mai multe substanţe; d. amestecuri neomogene de 2 sau mai multe substanţe. 12.Soluţiile sunt amestecuri omogene formate din 2 sau mai multe substanţe între care: a. se produc fenomene fizice şi chimice; b. se produc numai fenomene fizice; c. nu se produc fenomene fizice şi chimice; d. se produc numai fenomene chimice. 13.Soluţiile sunt amestecuri: a. neomogene de lichide; b. omogene gazoase şi solide; c. omogene de lichide sau gaze; d. eterogene de solide si lichide. 14.Componenţii unei soluţii sunt: a. dizolvantul şi solventul; b. solvatul şi dizolvatul; c. dizolvantul şi dizolvatul; d. solvatul şi sarea. 15.Prin amestecarea căror substanţe se obţine o soluţie: a. nisip şi apă; b. iod si alcool; 2
3 c. alcool şi sare de bucătărie; d. iod şi apă. 16.Soluţiile saturate sunt soluţiile care: a. conţin o cantitate minimă de substanţă dizolvată, la o anumită temperatură; b. conţin o cantitate maximă de substanţă dizolvată, la o anumită temperatură; c. conţin o cantitate mare de substanţă; d. mai pot dizolva noi cantităţi de substanţă. 17.Solubilitatea substanţelor este influenţată de: a. presiune; b. agitarea componenţilor; c. natura dizolvatului şi dizolvantului; d. creşterea cantităţii de solvent. 18.Concentraţia procentuală reprezintă: a. cantitatea de substanţă dizolvată în 1000 g soluţie; b. cantitatea de substanţă conţinută într-o soluţie; c. cantitatea de substanţă dizolvată într-o soluţie concentrată; d. cantitatea de substanţă conţinută în 100 g soluţie. 19.O soluţie ce conţine 50 g piatră vânătă dizolvata în 250 g apa are concentraţia procentuală: a. 5%; b. 20%; c. 16,6%; d. 10,6%. 20.Masa unei soluţii de concentraţie c este m. Cantitatea de apă care trebuie adăugată pentru a scădea concentraţia de n ori este: a. m/n; b. n m; c. n/m; d. 2m. 21.Prin amestecarea a 20 g sodă caustică la 100g soluţie de concentraţie 10%, concentraţia soluţiei devine: a. 30%; b. 15%; c. 25%; d. 20%. 22.Concentraţia procentuală a soluţiei obţinută prin dizolvarea a 2 moli NaCl în 200 ml H 2 O este: a. 11,7%; b. 58,5%; c. 36,91%; d. 10%. 23.Ce cantitate de NaOH (solidă) trebuie adăugată la 200 g soluţie de NaOH 10% pentru a dubla concentraţia acesteia: a. 10 g; 3
4 b. 40 g; c. 37,5 g; d. 20 g. 24.Se amestecă 150 g H 2 SO 4 10% cu 50g H 2 SO 4 40% şi 10g H 2 SO 4 94%. Concentraţia procentuală a soluţiei finale va fi: a. 48%; b. 16,67%; c. 24%; d. 21,14%. 25.Ce concentraţie procentuală are o soluţie obţinută prin dizolvarea a 5 g CuSO 4 5H 2 O în 50 ml H 2 O: a. 10%; b. 5,82%; c. 5%; d. 11%. 26.Ce volum de apă distilată trebuie adăugată la 50 ml soluţie HCl 36 % (ρ=1,18 g/ml), pentru a scădea concentraţia soluţiei la jumătate: a. 50 ml; b. 36 ml; c. 59 ml; d. 118 ml. 27.Câţi moli de Na 2 CO 3 sunt necesari pentru a prepara 1 L soluţie de concentraţie 10% (ρ=1,15 g/ml): a. 0,94; b. 2,16; c. 1,80; d. 1, Câţi mililitri de soluţie de KOH 30% (ρ=1,29 g/ml) trebuie adăugaţi la 1 L soluţie KOH 10% (ρ=1,09 g/ml) pentru a obţine o soluţie de concentraţie 20% (ρ=1,19 g/ml): a ml; b. 549 ml; c. 845 ml; d. 632 ml. 29.Soluţia de H 2 SO 4 obţinută prin dizolvarea a 22,4 ml soluţie H 2 SO 4 94% (ρ = 1,84 g/ml), în 100 ml H 2 O, va avea concentraţia procentuală: a. 18,30%; b. 27,93%; c. 49,49%; d. 29,19%. 30.Se amestecă 30g KOH 40% cu 50 g KOH 20% şi 100 g H2O. Concentraţia procentuală a soluţiei finale va fi: a. 30%; b. 27,5%; 4
5 c. 12,22%; d. 10,7%. 31. Ştiind că masa atomică a azotului este egală cu masa moleculara a unui oxid al carbonului, atunci valenţa carbonului în oxidul respectiv este : a. 1; b. 2; c. 3; d Care dintre perechile de substanţe de mai jos sunt săruri? a. Al 2 O 3 ; FeS; b. KCI; KOH; c. NaCl: CuSO 4 ; d. KNO3; H 2 SO Care dintre ecuaţiile reacţiilor de mai jos reprezintă o reacţie de combinare? a. 2 Na + S = Na 2 S; b. MgCO 3 = MgO + CO 2 ; c. FeCl KOH = Fe(OH) KCl; d. Na 2 CO 3 + HCl = NaCl + H 2 O + CO Care din exemplele următoare: oxigen, cărămidă, Luna, azot, fular, aur, sticlă, eprubetă, reprezintă substanţe: a. cărămidă, Luna, fular; b. oxigen, azot,aur; c. oxigen, azot, sticlă; d. fular, sticlă, eprubetă. 35. Identifică din următoarele cuvinte pe acelea care reprezintă substanţe: granit, hârtie, cui, sare, cană, sticlă, piatră, alcool, cuier, dulap,cântar, zahăr, baghetă, aur: a. granit, hârtie, cui; b. alcool, cuier, dulap; c. sare, alcool, aur; d. sticlă, zahăr, aur. 36. Identifică din următoarele cuvinte pe acelea care reprezintă materiale: granit, hârtie, cui, sare, cană, sticlă, piatră, alcool, cuier, dulap,cântar, zahăr, baghetă, aur: a. cană, sticlă; b. dulap, cântar; c. sare, aur; d. granit, hârtie. 37.Cilindrul gradat se foloseşte pentru: a. cântărirea substanţelor; b. dizolvarea substanţelor; c. măsurarea volumelor; d. arderea substanţelor. 5
6 38.Prepararea soluţiilor se realizează în: a. cilindrul gradat; b. biuretă; c. mojar; d. pahar Berzelius. 40.Proprietăţile fizice care pot fi observate cu ajutorul organelor de simţ, pot fi: a. duritate, strălucire; b. densitate, duritate; c. miros, gust; d. punct de topire, culoare. 41. Sunt proprietăţi fizice: a. Alcoolul arde; b. Cauciucul este elastic; c. Vinul se oţeteşte; d. Gazul metan arde. 42. Sunt proprietăţi chimice: a. Densitatea plumbului este mare; b. Zahărul se sfărâmă; c. Fierul este cenuşiu; d. Cuprul cocleşte. 43. Care din următoarele substanţe sunt folosite în gospodărie: a. apă distilată, calcar, acid sulfuric; b. sodă caustică, dioxid de carbon, acid sulfuric; c. oţet, oxigen, cărbune; d. soda de rufe, zahăr, sare de bucătărie. 44.Fenomenele chimice reprezintă: a. transformări care modifică compoziţia substanţelor; b. transformări de stare pe care le suferă corpurile, compoziţia rămânând constantă; c. transformări de poziţie pe care le suferă corpurile, compoziţia rămânând constantă; d. transformări care nu modifică compoziţia substanţelor. 45.Se consideră următoarele elemente din perioada a 3-a: Na, Mg, Al, Si, P, S, Cl. Dintre acestea, sunt metale: a. Mg, Al, S; b. Na, Mg, Al; c. Al, Si, P; d. Si, P, S. 46.O masă x de hidrogen reacţionează cu 2 moli de oxigen rezultând apă. Care este valoarea lui x? a. 6 grame; b. 4 grame; c. 2 grame; d. 8 grame. 6
7 47.Substanţele care intră într-o reacţie chimică se numesc: a. mediu de reacţie; b. condiţii de reacţie; c. produşi de reacţie; d. reactanţi. 48. În care din ecuaţiile de mai jos trebuie adăugat semnul "? a. Fe + S = FeS; b. Zn + H 2 SO 4 = ZnSO 4 + H 2; c. FeCl KOH = Fe(OH) KCl; d. 2 Na + S = Na 2 S. 49. Care din materialele de mai jos sunt de provenienţă naturală: a. hârtia şi betonul; b. porţelanul şi mortarul; c. sticla şi marmura; d. ceara de albine şi lemnul. 50.Determină cantitatea de apă care trebuie evaporată pentru a obţine o soluţie cu concentraţia 50% din 500 g de soluţie 25% de sodă caustică a. 300 grame; b. 250 grame; c. 200 grame; d. 150 grame. 51. Refrigerentul se foloseşte pentru: a. distilare; b. dizolvare; c. încălzire; d. mojarare. 52.Care din următoarele transformări reprezintă o proprietate fizică: a. coclirea unui vas de cupru; b. ruginirea unui cui de fier; c. fierberea apei; d. acrirea laptelui. 53.În ce masă de apă trebuie să dizolvăm 50 g de sare de bucătărie pentru a obţine o soluţie de concentraţie 20%? a. 100 grame; b. 150 grame; c. 200 grame; d. 250 grame. 54. Următoarele procese de ionizare pot avea loc: a. S = S e-; b. Al + 3e = Al +3 ; c. Cl + 1e = Cl - ; d. Ar = Ar + 4e -. 7
8 55. Ştiind că substanţa se numeşte sulfură acidă de magneziu, raportul atomic între numărul de atomi din fiecare element chimic component, în ordinea apariţiei în formula substanţei respective, este: a. 2 : 1 : 1; b. 1 : 1 : 1; c. 1 : 1 : 2; d. 1 : 2 : Atomul unui element are numărul atomic, Z = x şi numărul de masă. A = 2x + 1. Numărul neutronilor din nucleul atomului este: a. x + 1; b. x; c. 2x; d. x Care din următoarele situaţii corespund unor fenomene fizice: a. în corp hrana se transformă în alte substanţe; b. laptele nefiert se acreşte; c. cuiul de fier rugineşte în timp; d. apa îngheaţă la 0 ºC. 58. Care din următoarele substanţe se găsesc în fază lichidă : a. soda caustică, gheaţă, piatră vânătă; b. alcool, azot (din aer), fier; c. oxigen, dioxid de carbon, gaz metan; d. cupru, aur, iod. 59 Culoarea unei substanţe este o proprietate: a. chimică; b. biologică; c. fizică; d. fiziologică. 60. Substanţele obţinute în urma fierberii: a. îşi modifică starea de agregare; b. îşi modică compoziţia; c. se transformă în substanţe cu proprietăţi noi; d. îşi păstrează starea de agregare. 61. Care din următoarele exemple reprezintă proprietăţi chimice: a. lămâia are gust acru; b. şinele de tramvai se dilată la cald; c. alcoolul arde la apropierea de un băţ de chibrit aprins; d. esenţele din fructe au miros plăcut. 62. Arderea zahărului reprezintă: a. un fenomen chimic; b. un fenomen fizic; c. un fenomen biologic; d. o proprietate fizică a zahărului. 8
9 63. Fenomenele chimice reprezintă: a. transformări de fază pe care suferă corpurile, compoziţia rămânând constantă; b. transformări care modifică compoziţia substanţelor; c. transformări care nu modifică compoziţia; d. transformări de poziţie pe care le suferă corpurile. 64. Ruginirea fierului reprezintă: a. o transformare ce lasă nemodificată compoziţia substanţelor; b. un fenomen chimic; c. un fenomen fizic; d. un fenomen biologic. 65. Care din următoarele amestecuri sunt omogene: a. apă + piatră vânătă; b. apă + nisip; c. apă + mercur; d. azot + alcool. 66. Sunt amestecuri eterogene: a. detergent + apă; b. apă + oţet; c. alcool + apă; d. lapte praf + apă. 67 Aerul este un amestec gazos alcătuit din 78 % azot, 21 % oxigen şi 1 % alte gaze. Pentru separarea componenţilor din aer se foloseşte metoda: a. sublimare; b. comprimare; c. evaporare, d. cristalizare. 68 De ce iarna, dacă amestecăm zăpada cu sare gemă (grunjoasă) provocăm topirea ei? a. pentru că amestecul format are un punct de topire mai mare decât cel al apei; b. pentru că amestecul format are un punct de fierbere mai mic de 0 ºC; c. pentru că zăpada în amestec cu sarea formează o soluţie cu punctul de topire mai coborât decât cel al apei; d. pentru că zăpada în amestec cu sarea se transformă într-o altă substanţă chimică cu alte proprietăţi. 69. Indicaţi metodele de separare pentru amestecul: naftalină + nisip + pilitură de fier: a. crisalizare şi sublimare; b. distilare şi evaporare; c. sublimare şi separare magnetică; d. sublimare şi filtrare. 70. Ce fenomen produce apariţia florilor de gheaţă pe geamuri iarna? a. sublimarea; b. desublimarea; c. vaporizarea; d. condensarea. 9
10 71. Alege răspunsul corect, indicandu-l prin eliminarea uneia din optiunile Da sau Nu : a. Reacţia chimică este un fenomen fizic) Da Nu b. Reactanţii sunt substanţe simple sau compuse ce rezultă din reacţie. Da Nu c. Legea care se aplică în calcularea coeficienţiilor este Legea Conservării Atomilor. Da Nu d. Reacţia de combinare este reacţia chimică dintre două substanţe compuse. Da Nu e. Reacţia dintre o substanţă simplă şi o substanţă compusă este reacţia de combinare Da Nu 72. Arată corespondenţa între informaţiile din coloana stângă, notate cu cifre de la 1 la 4 şi ecuaţiile din coloana dreaptă, notate cu litere de la a la d), prin completarea cu săgeți intre cifra și litera corespunzătoare: 1. Reacţia de descompunere a) AgNO 3 +HCl=AgCl +HNO 3 ; 2. Reacţia de combinare b) 2 KclO 3 = 2 KCl+3O 2 (t ); 3. Reacţia de substituţie c) K 2 O+H 2 O=2KOH; 4. Reacţia de schimb d) Zn+Pb(NO 3 ) 2 =Zn(NO 3 ) 2 +Pb ; 73. Comletează spaţiile libere din schemele de reacţii chimice de mai jos: 900 C a. CaCO 3...+CO 2 ; b....+h2o var stins; c. Var stins + CO 2 CaCO ; d. CO H 2 CO 3 ; e. CaCO 3 + BaCl CaCl Elementul E cu Z=7 şi A=14 formează cu hidrogenul un compus de tipul : a. EH; b. EH 2 ; c. EH 3 ; d. EH 4 ; e. EH Au molecule diatomice: a. sulful, hidrogenul; b. hidrogenul, carbonul; c. oxigenul, carbonul; d. oxigenul, hidrogenul. 76.Care configuraţie electronică corespunde elementelor grupei a VI-a A: a. K -2e; L -4e; b. K- 2e; L- 8e; M- 2e; c. K -2e; L- 6e; d. K- 2e; L- 8e; M- 4e. 77. În cazul în care apreciezi că informaţia este adevărată, încercuieşte litera A (adevărat), dacă apreciezi că informaţia este falsă încercuieşte litera F (fals): a. Sulful se uneşte cu oxigenul la rece şi formează SO 2. A / F; b. Sulful arde şi formează SO 2. A / F; c. Prin descompunerea apei oxigenate se degajă hidrogen. A / F; d. În oxigen ard atât metalele cât şi nemetalele. A / F. 10
11 78. Citiţi afirmaţiile de mai jos. Dacă apreciaţi că afirmaţiile sunt corecte, încercuiţi litera A. Dacă o afirmaţie este falsă încercuiţi litera F. a. A, F. La formarea legăturii covalente atomii îşi realizează configuraţii electronice stabile prin transfer de electroni; b. A, F. Legătura ionică se formează prin punere în comun de electroni de la atomii elementelor cu caracter chimic opus. 79.Care este proprietatea comună pentru moleculele:h 2, F 2, N 2 : a. atomii sunt legaţi prin legături covalente simple; b. dubletul comun de electroni aparţine în egală măsură celor doi atomi; c. prezintă electroni neparticipanţi; d. legătura covalentă se realizeză prin întrepătrunderea orbitalilor de tip p; e. molecula este alungită. 80. Cel mai răspîndit nemetal din natură este: a. hidrogenul; b. carbonul; c. oxigenul; d. siliciul; e. azotul. 81.Nemetalele cunoscute sunt în număr de: a. 20; b. 22; c. 24; d. 18; e Pot dezlocui hidrogenul din acizi, următoarele metale: a. Zn şi Mg; b. Cu şi Pt; c. Al şi Fe; d. Ag şi Hg. 83. În reacţia Zn cu 73 g soluţie de HCl 20%: a. se formează 0,4 moli ZnCl 2 ; b. se degajă 0,2 moli H 2 ; c. nu se degajă H 2 ; d. Se degajă 2 moli H În molecula de oxigen legătura oxigen-oxigen este: a. ionică; b. covalentă nepolară; c. covalentă polară; d. coordinativă. 85. Oxigenul se poate obţine din apă prin:; a. descompunerea apei la încălzire; b. reacţia apei cu sodiul metalic; c. electroliza apei acidulate; d. cu ajutorul unui catalizator. 11
12 86. Raportul atomic H:O în molecula de apă este: a.1:2; b.2:3; c.2:1; d.1: Apa chimic pură este: a.apa potabilă; b.apa reziduală; c.apa regală; d.apa distilată. 88. Nemetalele tind să accepte electroni pe stratul de valenţă, devenind: a. ioni pozitivi; b. ioni negativi; c. atomi cu N.O. egal cu numărul grupei; d. ioni cu sarcina egală cu numărul grupei; e. molecule. 89.Caracterul nemetalic este determinat de: a. numărul atomic Z; b. numărul grupei; c. tăria acizilor formaţi, d. capacitatea de combinare cu nemetalele. 90. Hidrogenul se poate prepara prin reacţia acizilor cu: a. cupru; b. carbon; c. zinc; d. fer. 91. Indicaţi care dintre transformările următoare sunt fizice: a. gheaţa se topeşte; b. fierul rugineşte; c. gazul metan arde; d. apa fierbe la 100 C. 91. Indicaţi care dintre afirmaţiile următoare se referă la transformări chimice: a. benzina îngheaţă"; b. frunza îngălbeneşte; c. iodul sublimează; d. vinul se oţeteşte. 92. Atomul este format din: a. nucleu şi înveliş electronic; b. din protoni şi electroni; c. din protoni şi neutroni; d. neutroni şi electroni. 93. Elementele Li, Na, K sunt monovalente deoarece: a. sunt metale; b. sunt nemetale; 12
13 c. prezintă atât caracter metalic cât şi nemetalic; d. sunt în grupa I şi conţin un electron de valenţă. 94. Se consideră elementul sodiu, pentru care Z=11. Care din următoarele afirmaţii este adevărată: a. este situat în grupa a III-a, perioada 1; b. este situat în grupa I, perioada a 3-a; c. este situat în grupa I, perioada 1; d. este situa în grupa a III-a, perioada a 3-a. 95. Care din următoarele afirmaţii privitoare la hidrogen este adevărată: a. are cel mai mare număr de izotopi; b. este cel mai uşor element chimic; c. se afla situat în grupa a II-a; d. se află situa în perioada a 2-a. 96. Elementele grupe a II-a formează: a. cationi; b. anioni; c. cationi şi anioni; d. nu ionizează. 97. Halogenii formează ioni monovalenţi deoarece: a. cedează 7 electroni; b. acceptă 2 electroni; c. cedează un electron; d. acceptă un electron. 98. Un kilomol de Ca conţine: a. 6, atomi; b. 3, atomi; c. 6, atomi; d. 6, atomi. 99. Elementul cu Z= 11 poate forma în anumite condiţii o combinaţie chimică cu elementul pentru care Z= 17. Această combinaţie va fi: a. KF; b. KCl; c. NaCl; d. NaF Într-o incintă se află doi moli de hidrogen molecular. Câţi atomi de hidrogen se află în respectiva incintă? a. 3, atomi; b. 6, atomi; c. 1, atomi; d. 2, atomi O specie chimică ce conţine 11 protoni în nucleu şi 10 electroni în învelişul electronic reprezintă: a. un atom; b. un ion pozitiv; c. un ion negativ; d. un izotop. 13
14 102. Care dintre următoarele afirmaţii nu este corectă: a. valenţa caracterizează capacitatea de combinare a unui atom cu alt atom; b. valenţa este dată de numărul electronilor cu care atomul participă la formarea legăturilor chimice; c. numărul grupei principale indică valenţa minimă a elementelor; d. valenţa variază în funcţie de atom şi de gruparea chimică Care dintre următoarele afirmaţii este corectă: a. legătura electrovalentă se stabileşte între ioni cu sarcini electrice de semn contrar; b. electrovalenţa se formează prin punerea în comun de electroni; c. combinaţiile formate între ioni pozitivi şi negativi se numesc combinaţii covalente; d. legătura electrovalentă se stabileşte între ioni cu sarcini electrice de acelaşi semn Numărul de masă se notează cu: a. A; b. Z; c. N; d. M Daca masa atomică a aluminiului este 27 u.a.m. iar cea a clorului 35,5 u.a.m., masa moleculară a clorurii de aluminiu va fi: a. 133,5 u.a.m.; b. 98 u.a.m.; c. 62,5 u.a.m.; d. 169 u.a.m Daca un element are Z= 12, în ce perioadă se va afla situat acel element? a. Întâia; b. a doua; c. a treia; d. a patra Daca un element are Z= 12, în ce grupă se va afla situat acel element? a. Întâia; b. a doua; c. a treia; d. a patra Un milimol de substanţă conţine: a. 6, atomi; b. 3, atom;i c. 6, atomi; d. 6, atomi Concentraţia procentuală a soluţiei finale obţinute prin amestecarea a 25 g soluţie acid sulfuric de concentraţie 30 % şi 36 g soluţie acid sulfuric de concentraţie 65 % este: a. 50,65 %; b. 45,9 %; c. 38,6 %; d. 76,4 %. 14
15 110. Concentraţia soluţiei obţinute prin amestecarea a 150 g soluţie sodă caustică de concentraţie 15 % cu 80 g soluţie de concentraţie 25 % din aceeaşi substanţă este: a) 18,5 % ; b) 25,7 %; c) 45,8 %; d) 74,7 % g soluţie acid clorhidric de concentraţie necunoscută este diluată cu 300 g apă. Concentraţia procentuală este: a. 40 %; b. 14,5 %; c. 36,5 %; d. 26,5 % Dacă se introduc 4 g NaOH în 32 g soluţie NaOH de concentraţie necunoscută, se obţine o nouă soluţie de concentraţie 20 %. Concentraţia procentuală a soluţiei iniţiale este: a. 10 %; b. 15 %; c. 23,5 %; d. 34 % Se introduc 2,3 g Na în 200 g soluţie NaOH 4,6 %. Concentraţia procentuală a soluţiei finale este: a. 6,53 % b. 3,76 %; c. 7,5 %; d. 10 %. 15
Probleme clasa a VII-a
 Probleme clasa a VII-a 1.Un cui de fier este supus unor transformări chimice prin; a) îndoire b) magnetizare c) rupere d) ruginire 2.Substanţele obţinute în urma vaporizăriii: a) îşi modifică compoziţia
Probleme clasa a VII-a 1.Un cui de fier este supus unor transformări chimice prin; a) îndoire b) magnetizare c) rupere d) ruginire 2.Substanţele obţinute în urma vaporizăriii: a) îşi modifică compoziţia
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.2 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Radicalul C 6 H 5 - se numeşte fenil. ( fenil/
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE TEST 2.3.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Acetilena poate participa la reacţii de
5.1. Noţiuni introductive
 ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
ursul 13 aitolul 5. Soluţii 5.1. oţiuni introductive Soluţiile = aestecuri oogene de două sau ai ulte substanţe / coonente, ale căror articule nu se ot seara rin filtrare sau centrifugare. oonente: - Mediul
I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare.
 Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
Capitolul 3 COMPUŞI ORGANICI MONOFUNCŢIONALI 3.2.ACIZI CARBOXILICI TEST 3.2.3. I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Reacţia dintre
II. 5. Probleme. 20 c 100 c = 10,52 % Câte grame sodă caustică se găsesc în 300 g soluţie de concentraţie 10%? Rezolvare m g.
 II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
II. 5. Problee. Care ete concentraţia procentuală a unei oluţii obţinute prin izolvarea a: a) 0 g zahăr în 70 g apă; b) 0 g oă cautică în 70 g apă; c) 50 g are e bucătărie în 50 g apă; ) 5 g aci citric
Aplicaţii ale principiului I al termodinamicii la gazul ideal
 Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Aplicaţii ale principiului I al termodinamicii la gazul ideal Principiul I al termodinamicii exprimă legea conservării şi energiei dintr-o formă în alta şi se exprimă prin relaţia: ΔUQ-L, unde: ΔU-variaţia
Capitolul 2 - HIDROCARBURI 2.5.ARENE
 Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
Capitolul 2 - HIDROCARBURI 2.5.ARENE TEST 2.5.3 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. 1. Sulfonarea benzenului este o reacţie ireversibilă.
a. 11 % b. 12 % c. 13 % d. 14 %
 1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
1. Un motor termic funcţionează după ciclul termodinamic reprezentat în sistemul de coordonate V-T în figura alăturată. Motorul termic utilizează ca substanţă de lucru un mol de gaz ideal având exponentul
Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling.
 Cursul 8 3.5.4. Electronegativitatea Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling. Cantitativ, ea se exprimă prin coeficienţii de electronegativitate
Cursul 8 3.5.4. Electronegativitatea Electronegativitatea = capacitatea unui atom legat de a atrage electronii comuni = concept introdus de Pauling. Cantitativ, ea se exprimă prin coeficienţii de electronegativitate
MARCAREA REZISTOARELOR
 1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
1.2. MARCAREA REZISTOARELOR 1.2.1 MARCARE DIRECTĂ PRIN COD ALFANUMERIC. Acest cod este format din una sau mai multe cifre şi o literă. Litera poate fi plasată după grupul de cifre (situaţie în care valoarea
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE TEST 2.4.1 I. Scrie cuvântul / cuvintele dintre paranteze care completează corect fiecare dintre afirmaţiile următoare. Rezolvare: 1. Alcadienele sunt hidrocarburi
Metode iterative pentru probleme neliniare - contractii
 Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Metode iterative pentru probleme neliniare - contractii Problemele neliniare sunt in general rezolvate prin metode iterative si analiza convergentei acestor metode este o problema importanta. 1 Contractii
Capitolul 1-INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme
 Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Capitolul 1- INTRODUCERE ÎN STUDIUL CHIMIEI ORGANICE Exerciţii şi probleme ***************************************************************************** 1.1. Care este prima substanţă organică obţinută
Unitatea atomică de masă (u.a.m.) = a 12-a parte din masa izotopului de carbon
 ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
ursul.3. Mării şi unităţi de ăsură Unitatea atoică de asă (u.a..) = a -a parte din asa izotopului de carbon u. a.., 0 7 kg Masa atoică () = o ărie adiensională (un nuăr) care ne arată de câte ori este
III. Serii absolut convergente. Serii semiconvergente. ii) semiconvergentă dacă este convergentă iar seria modulelor divergentă.
 III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
III. Serii absolut convergente. Serii semiconvergente. Definiţie. O serie a n se numeşte: i) absolut convergentă dacă seria modulelor a n este convergentă; ii) semiconvergentă dacă este convergentă iar
(a) se numeşte derivata parţială a funcţiei f în raport cu variabila x i în punctul a.
 Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Definiţie Spunem că: i) funcţia f are derivată parţială în punctul a în raport cu variabila i dacă funcţia de o variabilă ( ) are derivată în punctul a în sens obişnuit (ca funcţie reală de o variabilă
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE
 Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Capitolul 2 - HIDROCARBURI 2.4.ALCADIENE Exerciţii şi probleme E.P.2.4. 1. Scrie formulele de structură ale următoarele hidrocarburi şi precizează care dintre ele sunt izomeri: Rezolvare: a) 1,2-butadiena;
Planul determinat de normală şi un punct Ecuaţia generală Plane paralele Unghi diedru Planul determinat de 3 puncte necoliniare
 1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
1 Planul în spaţiu Ecuaţia generală Plane paralele Unghi diedru 2 Ecuaţia generală Plane paralele Unghi diedru Fie reperul R(O, i, j, k ) în spaţiu. Numim normala a unui plan, un vector perpendicular pe
Activitatea A5. Introducerea unor module specifice de pregătire a studenţilor în vederea asigurării de şanse egale
 POSDRU/156/1.2/G/138821 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
POSDRU/156/1.2/G/138821 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
OLIMPIADA NAȚIONALĂ DE CHIMIE
 MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
MINISTERUL EDUCAȚIEI ȘI CERCETĂRII ȘTIINȚIFICE INSPECTORATUL ȘCOLAR JUDEȚEAN GALAȚI OLIMPIADA NAȚIONALĂ DE CHIMIE EDIȚIA a XLIX-a GALAȚI 5-10 APRILIE 2015 Proba teoretică Clasa a VIII-a Subiectul I (20
Subiecte Clasa a VIII-a
 Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Subiecte lasa a VIII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate.
 Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Curs 10 Funcţii reale de mai multe variabile reale. Limite şi continuitate. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie p, q N. Fie funcţia f : D R p R q. Avem următoarele
Curs 1 Şiruri de numere reale
 Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
Bibliografie G. Chiorescu, Analiză matematică. Teorie şi probleme. Calcul diferenţial, Editura PIM, Iaşi, 2006. R. Luca-Tudorache, Analiză matematică, Editura Tehnopress, Iaşi, 2005. M. Nicolescu, N. Roşculeţ,
ŞTIINŢA ŞI INGINERIA. conf.dr.ing. Liana Balteş curs 7
 ŞTIINŢA ŞI INGINERIA MATERIALELOR conf.dr.ing. Liana Balteş baltes@unitbv.ro curs 7 DIAGRAMA Fe-Fe 3 C Utilizarea oţelului în rândul majorităţii aplicaţiilor a determinat studiul intens al sistemului metalic
ŞTIINŢA ŞI INGINERIA MATERIALELOR conf.dr.ing. Liana Balteş baltes@unitbv.ro curs 7 DIAGRAMA Fe-Fe 3 C Utilizarea oţelului în rândul majorităţii aplicaţiilor a determinat studiul intens al sistemului metalic
Teoria mecanic-cuantică a legăturii chimice - continuare. Hibridizarea orbitalilor
 Cursul 10 Teoria mecanic-cuantică a legăturii chimice - continuare Hibridizarea orbitalilor Orbital atomic = regiunea din jurul nucleului în care poate fi localizat 1 e - izolat, aflat într-o anumită stare
Cursul 10 Teoria mecanic-cuantică a legăturii chimice - continuare Hibridizarea orbitalilor Orbital atomic = regiunea din jurul nucleului în care poate fi localizat 1 e - izolat, aflat într-o anumită stare
In cazul sistemelor G-L pentru care nu se aplica legile amintite ale echilibrului de faza, relatia y e = f(x) se determina numai experimental.
 ECHILIBRUL FAZELOR Este descris de: Legea repartitiei masice Legea fazelor Legea distributiei masice La echilibru, la temperatura constanta, raportul concentratiilor substantei dizolvate in doua faze aflate
ECHILIBRUL FAZELOR Este descris de: Legea repartitiei masice Legea fazelor Legea distributiei masice La echilibru, la temperatura constanta, raportul concentratiilor substantei dizolvate in doua faze aflate
Esalonul Redus pe Linii (ERL). Subspatii.
 Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
Seminarul 1 Esalonul Redus pe Linii (ERL). Subspatii. 1.1 Breviar teoretic 1.1.1 Esalonul Redus pe Linii (ERL) Definitia 1. O matrice A L R mxn este in forma de Esalon Redus pe Linii (ERL), daca indeplineste
a. 0,1; 0,1; 0,1; b. 1, ; 5, ; 8, ; c. 4,87; 6,15; 8,04; d. 7; 7; 7; e. 9,74; 12,30;1 6,08.
 1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
1. În argentometrie, metoda Mohr: a. foloseşte ca indicator cromatul de potasiu, care formeazǎ la punctul de echivalenţă un precipitat colorat roşu-cărămiziu; b. foloseşte ca indicator fluoresceina, care
 4. CIRCUITE LOGICE ELEMENTRE 4.. CIRCUITE LOGICE CU COMPONENTE DISCRETE 4.. PORŢI LOGICE ELEMENTRE CU COMPONENTE PSIVE Componente electronice pasive sunt componente care nu au capacitatea de a amplifica
4. CIRCUITE LOGICE ELEMENTRE 4.. CIRCUITE LOGICE CU COMPONENTE DISCRETE 4.. PORŢI LOGICE ELEMENTRE CU COMPONENTE PSIVE Componente electronice pasive sunt componente care nu au capacitatea de a amplifica
Integrala nedefinită (primitive)
 nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
nedefinita nedefinită (primitive) nedefinita 2 nedefinita februarie 20 nedefinita.tabelul primitivelor Definiţia Fie f : J R, J R un interval. Funcţia F : J R se numeşte primitivă sau antiderivată a funcţiei
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor X) functia f 1
 Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Functii definitie proprietati grafic functii elementare A. Definitii proprietatile functiilor. Fiind date doua multimi X si Y spunem ca am definit o functie (aplicatie) pe X cu valori in Y daca fiecarui
Subiecte Clasa a VII-a
 lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
lasa a VII Lumina Math Intrebari Subiecte lasa a VII-a (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor
 Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
Functii definitie, proprietati, grafic, functii elementare A. Definitii, proprietatile functiilor. Fiind date doua multimi si spunem ca am definit o functie (aplicatie) pe cu valori in daca fiecarui element
V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile
 Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Metode de Optimizare Curs V.7. Condiţii necesare de optimalitate cazul funcţiilor diferenţiabile Propoziţie 7. (Fritz-John). Fie X o submulţime deschisă a lui R n, f:x R o funcţie de clasă C şi ϕ = (ϕ,ϕ
Capitolul 2-HIDROCARBURI-2.3.-ALCHINE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
Capitolul 2 - HIDROCARBURI 2.3.ALCHINE Exerciţii şi probleme E.P.2.3. 1. Denumeşte conform IUPAC următoarele alchine: Se numerotează catena cea mai lungă ce conţine şi legătura triplă începând de la capătul
R R, f ( x) = x 7x+ 6. Determinați distanța dintre punctele de. B=, unde x și y sunt numere reale.
 5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
5p Determinați primul termen al progresiei geometrice ( b n ) n, știind că b 5 = 48 și b 8 = 84 5p Se consideră funcția f : intersecție a graficului funcției f cu aa O R R, f ( ) = 7+ 6 Determinați distanța
5.5. REZOLVAREA CIRCUITELOR CU TRANZISTOARE BIPOLARE
 5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
5.5. A CIRCUITELOR CU TRANZISTOARE BIPOLARE PROBLEMA 1. În circuitul din figura 5.54 se cunosc valorile: μa a. Valoarea intensității curentului de colector I C. b. Valoarea tensiunii bază-emitor U BE.
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM 1 electronica.geniu.ro
 Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Analiza în curent continuu a schemelor electronice Eugenie Posdărăscu - DCE SEM Seminar S ANALA ÎN CUENT CONTNUU A SCHEMELO ELECTONCE S. ntroducere Pentru a analiza în curent continuu o schemă electronică,
Sisteme diferenţiale liniare de ordinul 1
 1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
1 Metoda eliminării 2 Cazul valorilor proprii reale Cazul valorilor proprii nereale 3 Catedra de Matematică 2011 Forma generală a unui sistem liniar Considerăm sistemul y 1 (x) = a 11y 1 (x) + a 12 y 2
REACŢII DE ADIŢIE NUCLEOFILĂ (AN-REACŢII) (ALDEHIDE ŞI CETONE)
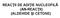 EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
EAŢII DE ADIŢIE NULEFILĂ (AN-EAŢII) (ALDEIDE ŞI ETNE) ompușii organici care conțin grupa carbonil se numesc compuși carbonilici și se clasifică în: Aldehide etone ALDEIDE: Formula generală: 3 Metanal(formaldehida
a n (ζ z 0 ) n. n=1 se numeste partea principala iar seria a n (z z 0 ) n se numeste partea
 Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
Serii Laurent Definitie. Se numeste serie Laurent o serie de forma Seria n= (z z 0 ) n regulata (tayloriana) = (z z n= 0 ) + n se numeste partea principala iar seria se numeste partea Sa presupunem ca,
CURSUL 3 ECHILIBRE DE DIZOLVARE
 CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
CURSUL 3 ECHILIBRE DE DIZOLVARE Soluţii: ţ definiţie, ţ compoziţie, ţ exemple Soluţia mediu dispersant (solvent) fază dispersată (solut, solvit) Importanţa soluţiilor: olocul de desfăşurare a majorităţii
SEMINAR 14. Funcţii de mai multe variabile (continuare) ( = 1 z(x,y) x = 0. x = f. x + f. y = f. = x. = 1 y. y = x ( y = = 0
 Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
Facultatea de Hidrotehnică, Geodezie şi Ingineria Mediului Matematici Superioare, Semestrul I, Lector dr. Lucian MATICIUC SEMINAR 4 Funcţii de mai multe variabile continuare). Să se arate că funcţia z,
ΦΡΟΝΤΙΣΤΗΡΙΟ Μ.Ε. ΣΥΜΒΟΛΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ Α ΛΥΚΕΙΟΥ ΑΝΤΙ ΡΑΣΕΙΣ Όλες οι αντιδράσεις που ζητούνται στη τράπεζα θεµάτων πραγµατοποιούνται. Στην πλειοψηφία των περιπτώσεων απαιτείται αιτιολόγηση της πραγµατοποίησης των αντιδράσεων.
ANALIZE FIZICO-CHIMICE MATRICE APA. Tip analiza Tip proba Metoda de analiza/document de referinta/acreditare
 ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
ph Conductivitate Turbiditate Cloruri Determinarea clorului liber si total Indice permanganat Suma Ca+Mg, apa de suprafata, apa, apa grea, apa de suprafata, apa grea, apa de suprafata, apa grea, apa de
Curs 4 Serii de numere reale
 Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Curs 4 Serii de numere reale Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Criteriul rădăcinii sau Criteriul lui Cauchy Teoremă (Criteriul rădăcinii) Fie x n o serie cu termeni
Seminar 5 Analiza stabilității sistemelor liniare
 Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
Seminar 5 Analiza stabilității sistemelor liniare Noțiuni teoretice Criteriul Hurwitz de analiză a stabilității sistemelor liniare În cazul sistemelor liniare, stabilitatea este o condiție de localizare
5. FUNCŢII IMPLICITE. EXTREME CONDIŢIONATE.
 5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
5 Eerciţii reolvate 5 UNCŢII IMPLICITE EXTREME CONDIŢIONATE Eerciţiul 5 Să se determine şi dacă () este o funcţie definită implicit de ecuaţia ( + ) ( + ) + Soluţie ie ( ) ( + ) ( + ) + ( )R Evident este
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE
 DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
DISTANŢA DINTRE DOUĂ DREPTE NECOPLANARE ABSTRACT. Materialul prezintă o modalitate de a afla distanţa dintre două drepte necoplanare folosind volumul tetraedrului. Lecţia se adresează clasei a VIII-a Data:
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu
 Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
Modele de subiecte propuse pentru concursul Acad. Cristofor Simionescu Ediția a-5-a, 18 noiembrie 2017, Iași Clasa a XII-a, secțiunea a-2-a: Chimie Aplicată în Protecția Mediului Alegeţi răspunsul corect
ECHILIBRE ACIDO BAZICE - 1
 ECHILIBRE ACIDO-BAZICE 1 DISOCIEREA APEI 2 H 2 O H 3 O + + OH - H 3 O + H + PRODUS IONIC AL APEI: + c P H K = [ H ] [ OH ] = 2 O P H O = 2 = 10 14 M 2 (25 o C ) ÎN APA PURĂ + [ H ] = [ OH ] = PH 2 O =
ECHILIBRE ACIDO-BAZICE 1 DISOCIEREA APEI 2 H 2 O H 3 O + + OH - H 3 O + H + PRODUS IONIC AL APEI: + c P H K = [ H ] [ OH ] = 2 O P H O = 2 = 10 14 M 2 (25 o C ) ÎN APA PURĂ + [ H ] = [ OH ] = PH 2 O =
UNITĂŢI Ţ DE MĂSURĂ. Măsurarea mărimilor fizice. Exprimare în unităţile de măsură potrivite (mărimi adimensionale)
 PARTEA I BIOFIZICA MOLECULARĂ 2 CURSUL 1 Sisteme de unităţiţ de măsură. Atomi şi molecule. UNITĂŢI Ţ DE MĂSURĂ Măsurarea mărimilor fizice Exprimare în unităţile de măsură potrivite (mărimi adimensionale)
PARTEA I BIOFIZICA MOLECULARĂ 2 CURSUL 1 Sisteme de unităţiţ de măsură. Atomi şi molecule. UNITĂŢI Ţ DE MĂSURĂ Măsurarea mărimilor fizice Exprimare în unităţile de măsură potrivite (mărimi adimensionale)
CUPRINS ATOM. ELEMENT CHIMIC. IZOTOPI 2 STRATURI. SUBSTRATURI. ORBITALI 5 PROPRIETĂŢILE ELEMENTELOR ŞI LOCUL ÎN SISTEMUL PERIODIC 7 TESTUL 1 8
 CUPRINS ATOM. ELEMENT CHIMIC. IZOTOPI 2 STRATURI. SUBSTRATURI. ORBITALI 5 PROPRIETĂŢILE ELEMENTELOR ŞI LOCUL ÎN SISTEMUL PERIODIC 7 TESTUL 1 8 CRITERII PENTRU STABILIREA NUMERELOR DE OXIDARE 9 ETAPELE
CUPRINS ATOM. ELEMENT CHIMIC. IZOTOPI 2 STRATURI. SUBSTRATURI. ORBITALI 5 PROPRIETĂŢILE ELEMENTELOR ŞI LOCUL ÎN SISTEMUL PERIODIC 7 TESTUL 1 8 CRITERII PENTRU STABILIREA NUMERELOR DE OXIDARE 9 ETAPELE
2. CONDENSATOARE 2.1. GENERALITĂŢI PRIVIND CONDENSATOARELE DEFINIŢIE UNITĂŢI DE MĂSURĂ PARAMETRII ELECTRICI SPECIFICI CONDENSATOARELOR SIMBOLURILE
 2. CONDENSATOARE 2.1. GENERALITĂŢI PRIVIND CONDENSATOARELE DEFINIŢIE UNITĂŢI DE MĂSURĂ PARAMETRII ELECTRICI SPECIFICI CONDENSATOARELOR SIMBOLURILE CONDENSATOARELOR 2.2. MARCAREA CONDENSATOARELOR MARCARE
2. CONDENSATOARE 2.1. GENERALITĂŢI PRIVIND CONDENSATOARELE DEFINIŢIE UNITĂŢI DE MĂSURĂ PARAMETRII ELECTRICI SPECIFICI CONDENSATOARELOR SIMBOLURILE CONDENSATOARELOR 2.2. MARCAREA CONDENSATOARELOR MARCARE
CHIMIE. clasa a IX-a frecvenţă redusă Semestrul al II - lea. prof. Bucaciuc Camelia
 CHIMIE clasa a IX-a frecvenţă redusă Semestrul al II - lea prof. Bucaciuc Camelia REACTII PROTOLITICE Teoria protolitica a acizilor si bazelor. Cuplul Acid-baza conjugata Teoria lui Arrhenius a insemnat
CHIMIE clasa a IX-a frecvenţă redusă Semestrul al II - lea prof. Bucaciuc Camelia REACTII PROTOLITICE Teoria protolitica a acizilor si bazelor. Cuplul Acid-baza conjugata Teoria lui Arrhenius a insemnat
Definiţia generală Cazul 1. Elipsa şi hiperbola Cercul Cazul 2. Parabola Reprezentari parametrice ale conicelor Tangente la conice
 1 Conice pe ecuaţii reduse 2 Conice pe ecuaţii reduse Definiţie Numim conica locul geometric al punctelor din plan pentru care raportul distantelor la un punct fix F şi la o dreaptă fixă (D) este o constantă
1 Conice pe ecuaţii reduse 2 Conice pe ecuaţii reduse Definiţie Numim conica locul geometric al punctelor din plan pentru care raportul distantelor la un punct fix F şi la o dreaptă fixă (D) este o constantă
Activitatea A5. Introducerea unor module specifice de pregătire a studenţilor în vederea asigurării de şanse egale
 Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
Investeşte în oameni! FONDUL SOCIAL EUROPEAN Programul Operaţional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educaţiaşiformareaprofesionalăînsprijinulcreşteriieconomiceşidezvoltăriisocietăţiibazatepecunoaştere
Capitolul 4-COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ-
 Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
Capitolul 4 COMPUŞI ORGANICI CU ACŢIUNE BIOLOGICĂ 4.1.ZAHARIDE.PROTEINE. Exerciţii şi probleme E.P.4.1. 1. Glucoza se oxidează cu reactivul Tollens [Ag(NH 3 ) 2 ]OH conform ecuaţiei reacţiei chimice. Această
CLASIFICAREA REACŢIILOR CHIMICE
 CLASIFICAREA REACŢIILOR CHIMICE 1. Reacţii de combinare Reacţia de combinare este reacţia chimică ce are loc între două sau mai multe substanţe chimice, simple sau compuse, cu obţinerea unei singure substanţe
CLASIFICAREA REACŢIILOR CHIMICE 1. Reacţii de combinare Reacţia de combinare este reacţia chimică ce are loc între două sau mai multe substanţe chimice, simple sau compuse, cu obţinerea unei singure substanţe
Reactia de amfoterizare a aluminiului
 Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
Problema 1 Reactia de amfoterizare a aluminiului Se da reactia: Al (s) + AlF 3(g) --> AlF (g), precum si presiunile partiale ale componentelor gazoase in functie de temperatura: a) considerand presiunea
Subiecte Clasa a V-a
 (40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul numarului intrebarii
(40 de intrebari) Puteti folosi spatiile goale ca ciorna. Nu este de ajuns sa alegeti raspunsul corect pe brosura de subiecte, ele trebuie completate pe foaia de raspuns in dreptul numarului intrebarii
COLEGIUL NATIONAL CONSTANTIN CARABELLA TARGOVISTE. CONCURSUL JUDETEAN DE MATEMATICA CEZAR IVANESCU Editia a VI-a 26 februarie 2005.
 SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
SUBIECTUL Editia a VI-a 6 februarie 005 CLASA a V-a Fie A = x N 005 x 007 si B = y N y 003 005 3 3 a) Specificati cel mai mic element al multimii A si cel mai mare element al multimii B. b)stabiliti care
5.4. MULTIPLEXOARE A 0 A 1 A 2
 5.4. MULTIPLEXOARE Multiplexoarele (MUX) sunt circuite logice combinaţionale cu m intrări şi o singură ieşire, care permit transferul datelor de la una din intrări spre ieşirea unică. Selecţia intrării
5.4. MULTIPLEXOARE Multiplexoarele (MUX) sunt circuite logice combinaţionale cu m intrări şi o singură ieşire, care permit transferul datelor de la una din intrări spre ieşirea unică. Selecţia intrării
Curs 14 Funcţii implicite. Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi"
 Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Curs 14 Funcţii implicite Facultatea de Hidrotehnică Universitatea Tehnică "Gh. Asachi" Iaşi 2014 Fie F : D R 2 R o funcţie de două variabile şi fie ecuaţia F (x, y) = 0. (1) Problemă În ce condiţii ecuaţia
Metoda rezolvării problemelor de determinare a formulelor chimice
 inisterul Educaţiei şi Tineretului al Republicii oldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă etoda rezolvării problemelor de determinare a formulelor chimice Autor Postolache
inisterul Educaţiei şi Tineretului al Republicii oldova Colegiul Pedagogic Ion Creangă, Bălţi Liceul Teoretic Ion Creangă etoda rezolvării problemelor de determinare a formulelor chimice Autor Postolache
Componente şi Circuite Electronice Pasive. Laborator 3. Divizorul de tensiune. Divizorul de curent
 Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Laborator 3 Divizorul de tensiune. Divizorul de curent Obiective: o Conexiuni serie şi paralel, o Legea lui Ohm, o Divizorul de tensiune, o Divizorul de curent, o Implementarea experimentală a divizorului
Laborator 11. Mulţimi Julia. Temă
 Laborator 11 Mulţimi Julia. Temă 1. Clasa JuliaGreen. Să considerăm clasa JuliaGreen dată de exemplu la curs pentru metoda locului final şi să schimbăm numărul de iteraţii nriter = 100 în nriter = 101.
Laborator 11 Mulţimi Julia. Temă 1. Clasa JuliaGreen. Să considerăm clasa JuliaGreen dată de exemplu la curs pentru metoda locului final şi să schimbăm numărul de iteraţii nriter = 100 în nriter = 101.
Capitolul 2-HIDROCARBURI-2.2.-ALCHENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Capitolul 2 - HIDROCARBURI 2.2.ALCHENE Exerciţii şi probleme E.P.2.2.1. Denumeşte conform IUPAC următoarele alchene: A CH 3 CH 3 CH 2 C 3 C 4 H C 5 CH 3 C 2 H CH 3 C 6 H 2 C 1 H 3 C 7 H 3 3-etil-4,5,5-trimetil-2-heptenă
Capitolul 2-HIDROCARBURI-2.5.-ARENE Exerciţii şi probleme
 Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
Capitolul 2 - HIDROCARBURI 2.5.ARENE Exerciţii şi probleme E.P.2.5. 1. Denumeşte conform IUPAC următoarele hidrocarburi aromatice mononucleare: Determină formula generală a hidrocarburilor aromatice mononucleare
Valori limită privind SO2, NOx şi emisiile de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili
 Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Anexa 2.6.2-1 SO2, NOx şi de praf rezultate din operarea LPC în funcţie de diferite tipuri de combustibili de bioxid de sulf combustibil solid (mg/nm 3 ), conţinut de O 2 de 6% în gazele de ardere, pentru
Activitatea A5. Introducerea unor module specifice de pregătire a studenților în vederea asigurării de șanse egale
 Investește în oameni! FONDUL SOCIAL EUROPEAN Programul Operațional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educația și formarea profesională în sprijinul creșterii
Investește în oameni! FONDUL SOCIAL EUROPEAN Programul Operațional Sectorial pentru Dezvoltarea Resurselor Umane 2007 2013 Axa prioritară nr. 1 Educația și formarea profesională în sprijinul creșterii
Capitolul I NOŢIUNI FUNDAMENTALE
 Capitolul I NOŢIUNI FUNDAMENTALE 1.1. Materia. Universul este format din materie, prezentă sub două forme: substanţă şi energie radiantă. Materia este în continuă transformare. Substanţa reprezintă o formă
Capitolul I NOŢIUNI FUNDAMENTALE 1.1. Materia. Universul este format din materie, prezentă sub două forme: substanţă şi energie radiantă. Materia este în continuă transformare. Substanţa reprezintă o formă
V O. = v I v stabilizator
 Stabilizatoare de tensiune continuă Un stabilizator de tensiune este un circuit electronic care păstrează (aproape) constantă tensiunea de ieșire la variaţia între anumite limite a tensiunii de intrare,
Stabilizatoare de tensiune continuă Un stabilizator de tensiune este un circuit electronic care păstrează (aproape) constantă tensiunea de ieșire la variaţia între anumite limite a tensiunii de intrare,
CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC Clasa a VII-a
 FACULTATEA DE CHIMIE, BIOLOGIE, GEOGRAFIE Departamentul de Chimie Str. Petalozzi 6, Timişoara 3005, Tel/Fax: 056/5960 CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC 7.0.007 Claa a VII-a. Proprietăţi
FACULTATEA DE CHIMIE, BIOLOGIE, GEOGRAFIE Departamentul de Chimie Str. Petalozzi 6, Timişoara 3005, Tel/Fax: 056/5960 CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC 7.0.007 Claa a VII-a. Proprietăţi
Acizi carboxilici heterofuncționali.
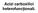 Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
Acizi carboxilici heterofuncționali. 1. Acizi carboxilici halogenați. R R 2 l l R 2 R l Acizi α-halogenați Acizi β-halogenați l R 2 2 l Acizi γ-halogenați Metode de obținere. 1. alogenarea directă a acizilor
Conice. Lect. dr. Constantin-Cosmin Todea. U.T. Cluj-Napoca
 Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
Conice Lect. dr. Constantin-Cosmin Todea U.T. Cluj-Napoca Definiţie: Se numeşte curbă algebrică plană mulţimea punctelor din plan de ecuaţie implicită de forma (C) : F (x, y) = 0 în care funcţia F este
LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ ISBN
 Raluca Pop Mihaiela Andoni LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ ISBN 978-606-8456-56-0 1 Editura Victor Babeş Piaţa Eftimie Murgu 2, cam. 316, 300041 Timişoara Tel./ Fax 0256 495 210 e-mail:
Raluca Pop Mihaiela Andoni LUCRĂRI PRACTICE DE CHIMIE GENERALĂ ŞI ANORGANICĂ ISBN 978-606-8456-56-0 1 Editura Victor Babeş Piaţa Eftimie Murgu 2, cam. 316, 300041 Timişoara Tel./ Fax 0256 495 210 e-mail:
Structura sistemului periodic... 9
 Cuprins Structura atomului Atomul. Particula. Molecula... 1 Modele atomice... 4 A.) Modelul lui J.J. Thomson... 4 B.) Modelul lui Rutherford sau modelul planetar al atomului... 4 C.) Modelul lui Bohr...
Cuprins Structura atomului Atomul. Particula. Molecula... 1 Modele atomice... 4 A.) Modelul lui J.J. Thomson... 4 B.) Modelul lui Rutherford sau modelul planetar al atomului... 4 C.) Modelul lui Bohr...
panagiotisathanasopoulos.gr
 . Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
. Παναγιώτης Αθανασόπουλος Χηµικός ιδάκτωρ Παν. Πατρών. Οξειδοαναγωγή Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών 95 Χηµικός ιδάκτωρ Παν. Πατρών 96 Χηµικός ιδάκτωρ Παν. Πατρών. Τι ονοµάζεται
 10. STABILIZATOAE DE TENSIUNE 10.1 STABILIZATOAE DE TENSIUNE CU TANZISTOAE BIPOLAE Stabilizatorul de tensiune cu tranzistor compară în permanenţă valoare tensiunii de ieşire (stabilizate) cu tensiunea
10. STABILIZATOAE DE TENSIUNE 10.1 STABILIZATOAE DE TENSIUNE CU TANZISTOAE BIPOLAE Stabilizatorul de tensiune cu tranzistor compară în permanenţă valoare tensiunii de ieşire (stabilizate) cu tensiunea
CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC EDIŢIA a III-a
 CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC EDIŢIA a III-a 27.01.2008 SUBIECTE PROPUSE Adrian Chiriac, Delia Isac, Otilia Bizerea, Horia Popovici, Daniela Dascălu, Titus Vlase, Dana Vlascici,
CONCURSUL DE CHIMIE GENERALĂ ŞI ANORGANICĂ VERONICA CHIRIAC EDIŢIA a III-a 27.01.2008 SUBIECTE PROPUSE Adrian Chiriac, Delia Isac, Otilia Bizerea, Horia Popovici, Daniela Dascălu, Titus Vlase, Dana Vlascici,
Lectia 4 proiect-17.10.2010 Clasa a VIII-a Grupa de performanta. Mulaje, chituri pentru geamuri FeSO 4.7H 2 0 Calaican Mordant in vopsitorie
 Lectia 4 proiect-17.10.2010 Clasa a VIII-a Grupa de performanta COMPOZITIA PROCENTUALA A UNUI AMESTEC.SOLUTII.CRISTALOHIDRATI. REGULA DREPTUNGIULUI O serie de substante retin un numar de molecule de apa,
Lectia 4 proiect-17.10.2010 Clasa a VIII-a Grupa de performanta COMPOZITIA PROCENTUALA A UNUI AMESTEC.SOLUTII.CRISTALOHIDRATI. REGULA DREPTUNGIULUI O serie de substante retin un numar de molecule de apa,
Chimie Anorganică. e Chimie
 Chimie Anorganică Contribuţii autori Cap. 1 Cap. 2 Cap. 3 Cap. 4 Cap. 5 conf. dr. ing. Anca Răzvan conf. dr. ing. Cristian Matei conf. dr. ing. Daniela Cristina Berger conf. dr. ing. Daniela Raluca Isopescu
Chimie Anorganică Contribuţii autori Cap. 1 Cap. 2 Cap. 3 Cap. 4 Cap. 5 conf. dr. ing. Anca Răzvan conf. dr. ing. Cristian Matei conf. dr. ing. Daniela Cristina Berger conf. dr. ing. Daniela Raluca Isopescu
Universitatea de Stat de Medicină și Farmacie Nicolae Testemițanu
 Universitatea de Stat de Medicină și Farmacie Nicolae Testemițanu Programul analitic pentru examenul de admitere. Chimie Introducere Cunoștințele în chimie sunt necesare pentru a înțelege concepțiile bazice
Universitatea de Stat de Medicină și Farmacie Nicolae Testemițanu Programul analitic pentru examenul de admitere. Chimie Introducere Cunoștințele în chimie sunt necesare pentru a înțelege concepțiile bazice
1. PROPRIETĂȚILE FLUIDELOR
 1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
1. PROPRIETĂȚILE FLUIDELOR a) Să se exprime densitatea apei ρ = 1000 kg/m 3 în g/cm 3. g/cm 3. b) tiind că densitatea glicerinei la 20 C este 1258 kg/m 3 să se exprime în c) Să se exprime în kg/m 3 densitatea
Noțiuni termodinamice de bază
 Noțiuni termodinamice de bază Alexandra Balan Andra Nistor Prof. Costin-Ionuț Dobrotă COLEGIUL NAȚIONAL DIMITRIE CANTEMIR ONEȘTI Septembrie, 2015 http://fizicaliceu.wikispaces.com Noțiuni termodinamice
Noțiuni termodinamice de bază Alexandra Balan Andra Nistor Prof. Costin-Ionuț Dobrotă COLEGIUL NAȚIONAL DIMITRIE CANTEMIR ONEȘTI Septembrie, 2015 http://fizicaliceu.wikispaces.com Noțiuni termodinamice
Ecuatii trigonometrice
 Ecuatii trigonometrice Ecuatiile ce contin necunoscute sub semnul functiilor trigonometrice se numesc ecuatii trigonometrice. Cele mai simple ecuatii trigonometrice sunt ecuatiile de tipul sin x = a, cos
Ecuatii trigonometrice Ecuatiile ce contin necunoscute sub semnul functiilor trigonometrice se numesc ecuatii trigonometrice. Cele mai simple ecuatii trigonometrice sunt ecuatiile de tipul sin x = a, cos
Bazele Chimiei Organice
 Bazele Chimiei Organice An universitar 2017-2018 Lector dr. Adriana Urdă Partea 1. Scurt istoric; definiții; principii de bază în purificarea și investigarea compușilor organici. Obiectivele acestei părți:
Bazele Chimiei Organice An universitar 2017-2018 Lector dr. Adriana Urdă Partea 1. Scurt istoric; definiții; principii de bază în purificarea și investigarea compușilor organici. Obiectivele acestei părți:
4. ELEMENTE DE CALCUL ÎN CHIMIE. 4.1 Introducere. Chimie Anorganică
 4. ELEMENTE DE CALCUL ÎN CHIMIE 4.1 Introducere În acest capitol vor fi prezentate câteva dintre cele mai importante elemente ale calculelor chimice. Dacă în capitolele anterioare s-au introdus principalele
4. ELEMENTE DE CALCUL ÎN CHIMIE 4.1 Introducere În acest capitol vor fi prezentate câteva dintre cele mai importante elemente ale calculelor chimice. Dacă în capitolele anterioare s-au introdus principalele
SERII NUMERICE. Definiţia 3.1. Fie (a n ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0
 SERII NUMERICE Definiţia 3.1. Fie ( ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0 şirul definit prin: s n0 = 0, s n0 +1 = 0 + 0 +1, s n0 +2 = 0 + 0 +1 + 0 +2,.......................................
SERII NUMERICE Definiţia 3.1. Fie ( ) n n0 (n 0 IN) un şir de numere reale şi (s n ) n n0 şirul definit prin: s n0 = 0, s n0 +1 = 0 + 0 +1, s n0 +2 = 0 + 0 +1 + 0 +2,.......................................
Mecanica fluidelor. F 12 Forta ascensionala la lichide. Materiale : Prezentare experiment
 F 12 Forta ascensionala la lichide Sina cu profil, 180 mm 2 1 Pereche talpi sina 3 Calaret 4 Tija stativa, 330 mm 5 Mufa dubla 7 Sfoara 10 Cilindru de masura 24 Dinamometru 32 Garnitura cilindru metalic
F 12 Forta ascensionala la lichide Sina cu profil, 180 mm 2 1 Pereche talpi sina 3 Calaret 4 Tija stativa, 330 mm 5 Mufa dubla 7 Sfoara 10 Cilindru de masura 24 Dinamometru 32 Garnitura cilindru metalic
BARAJ DE JUNIORI,,Euclid Cipru, 28 mai 2012 (barajul 3)
 BARAJ DE JUNIORI,,Euclid Cipru, 8 mi 0 (brjul ) Problem Arătţi că dcă, b, c sunt numere rele cre verifică + b + c =, tunci re loc ineglitte xy + yz + zx Problem Fie şi b numere nturle nenule Dcă numărul
BARAJ DE JUNIORI,,Euclid Cipru, 8 mi 0 (brjul ) Problem Arătţi că dcă, b, c sunt numere rele cre verifică + b + c =, tunci re loc ineglitte xy + yz + zx Problem Fie şi b numere nturle nenule Dcă numărul
RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii transversale, scrisă faţă de una dintre axele de inerţie principale:,
 REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
REZISTENTA MATERIALELOR 1. Ce este modulul de rezistenţă? Exemplificaţi pentru o secţiune dreptunghiulară, respectiv dublu T. RĂSPUNS Modulul de rezistenţă este o caracteristică geometrică a secţiunii
2. STATICA FLUIDELOR. 2.A. Presa hidraulică. Legea lui Arhimede
 2. STATICA FLUIDELOR 2.A. Presa hidraulică. Legea lui Arhimede Aplicația 2.1 Să se determine ce masă M poate fi ridicată cu o presă hidraulică având raportul razelor pistoanelor r 1 /r 2 = 1/20, ştiind
2. STATICA FLUIDELOR 2.A. Presa hidraulică. Legea lui Arhimede Aplicația 2.1 Să se determine ce masă M poate fi ridicată cu o presă hidraulică având raportul razelor pistoanelor r 1 /r 2 = 1/20, ştiind
Problema a II - a (10 puncte) Diferite circuite electrice
 Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
Olimpiada de Fizică - Etapa pe judeţ 15 ianuarie 211 XI Problema a II - a (1 puncte) Diferite circuite electrice A. Un elev utilizează o sursă de tensiune (1), o cutie cu rezistenţe (2), un întrerupător
STRUCTURA MOLECULELOR
 STRUCTURA MOLECULELOR Legătura chimică - ansamblu de interacţiuni care se exercită între atomi, ioni sau molecule care conduce la formarea unor specii moleculare independente. Legături chimice: - tari
STRUCTURA MOLECULELOR Legătura chimică - ansamblu de interacţiuni care se exercită între atomi, ioni sau molecule care conduce la formarea unor specii moleculare independente. Legături chimice: - tari
Seminariile Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reziduurilor
 Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Facultatea de Matematică Calcul Integral şi Elemente de Analiă Complexă, Semestrul I Lector dr. Lucian MATICIUC Seminariile 9 20 Capitolul X. Integrale Curbilinii: Serii Laurent şi Teorema Reiduurilor.
Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25
 Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25 LAGĂRELE CU ALUNECARE!" 25.1.Caracteristici.Părţi componente.materiale.!" 25.2.Funcţionarea lagărelor cu alunecare.! 25.1.Caracteristici.Părţi componente.materiale.
Capitolul ASAMBLAREA LAGĂRELOR LECŢIA 25 LAGĂRELE CU ALUNECARE!" 25.1.Caracteristici.Părţi componente.materiale.!" 25.2.Funcţionarea lagărelor cu alunecare.! 25.1.Caracteristici.Părţi componente.materiale.
