ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ. Απορρόφηση 1
|
|
|
- Ευδοκία Αθανασιάδης
- 6 χρόνια πριν
- Προβολές:
Transcript
1 ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ 1. Ισορροπία αερίων- υγρού 2. Ανάλυση διεργασίας Απορρόφησης 3. Απορρόφηση Πολυσύνθετων Μιγμάτων 4. Στήλες Απορρόφησης με πληρωτικά υλικά Απορρόφηση 1
2 Απορρόφηση Απορρόφηση Αερίων (Gas adsorption) είναι ο διαχωρισμός ενός μίγματος αερίων μέσω της επαφής του με ένα υγρό, το οποίο διαλύει ένα ή περισσότερα συστατικά του μίγματος, με αποτέλεσμα να το (τα( διαχωρίζει από το αρχικό τμήμα. Η διεργασία αυτή γίνεται σε παρόμοιες εγκαταστάσεις όπως αυτές των στηλών απόσταξης. Μεταφορά Μάζας- Ισορροπία Αερίων- Υγρού Η αντίστροφη διεργασία, δηλ. η απομάκρυνση ενός ή περισσοτέρων αερίων από το διάλυμα ονομάζεται εκρόφηση ή εξάντληση (stripping). Βασίζεται στην διαβίβαση ενός αδρανούς αερίου μέσω του διαλύματος το οποίο απομακρύνει το εκροφούμενο αέριο. Απορρόφηση 2
3 Απορρόφηση Ισορροπία Αερίων Υγρού Διαλυτότητα ενός αερίου σε ένα υγρό: βάρος του αερίου σε 100 μ. β. διαλύτη, για δεδομένη P και T Νόμος του Henry p i =H i x i, p i :είναι μερική πίεση του αερίου στην αέρια φάση x i :είναι το γραμ/κό κλάσμα του αερίου i στην υγρή φάση H i : σταθερά του Henry Διαλυτότητα= f(t, P) (συνήθης διαλύτης: Νερό) Απορρόφηση 3
4 Απορρόφηση Τέλεια διαλύματος αερίου σε υγρό p i =p io x i, (Νόμος του Raoult) p io : η τάση ατμών του καθαρού i, στην θερμοκρασία του διαλύματος H i = p i o p i i = H x i y i = mx i ( p : ολικη πιεση) p p Η εξίσωση παριστάνει ευθεία γραμμή με κλίση m στο διάγραμμα ισορροπίας y-x Σε περίπτωση που δεν ισχύει ο νόμος του Henry ή του Raoult τότε η αναπαράσταση της ισορροπίας στο διάγραμμα δεν είναι γραμμική. Απορρόφηση 4
5 Απορρόφηση Διαλύτες -Νερό -Διαλύματα αλκάλεων -Διαλύματα αμινών -Διάφορα ορυκτέλαια Βασικές απαιτήσεις για την εκλογή του διαλύτη Α) Να διαλύει σημαντικά τα προς διαχωρισμό αέρια και να μπορεί να τα εκροφήσει Β) Να μην είναι πτητικός ή τοξικός Γ) Να έχει χαμηλό ιξώδες Δ) Να είναι χημικά σταθερός και φτηνός Απορρόφηση 5
6 Απορρόφηση Ανάλυση Διεργασίας Απορρόφησης Ισοζύγια Μάζας και γραμμές λειτουργίας Α) Αραιά μίγματα [Ποσότητα διαλυμένου αερίου <<ποσότητα υπολειπόμενου αερίου (αδρανούς) και του διαλύτη] Ολικό Ισοζύγιο: G 1 =G 2 =G και L 1 =L 2 =L Ισοζ. Προσρ. Συστ.: G (y 1 -y 2 )= L (x 1 -x 2 ) (ΓΡΑΜΜΗ ΛΕΙΤΟΥΡΓΙΑΣ ΤΟΥ ΠΥΡΓΟΥ ΑΠΟΡΡΟΦΗΣΗΣ) Αν y 2 δεδομένο και y 1 άγνωστο τότε L L y = x+ y x G G 2 2 Απορρόφηση 6
7 B) Πυκνά μίγματα Απορρόφηση [ Ποσότητα του απορροφούμενου αερίου είναι σημαντική με αποτέλεσμα να μεταβάλλεται ο ρυθμός ροής των δύο ρευμάτων, (G 1 >G 2, και L 1 > L 2 )] Αδρανές αέριο, G, διαλύτης, L (G, L σταθερά σε όλο το μήκος): G (1-y)= G και L(1-x)= L Ισοζύγιο μάζας του προς απορρόφηση Υγρού: G y y x x ' 1 2 ' ( ) = L( 1 2 ) 1 y1 1 y2 1 x1 1 x2 Απορρόφηση 7
8 Απορρόφηση ' ' G ( Y1 Y2) = L( X1 X2) οπου x y Χ= και Υ= 1 x 1 y Χ, Υ λόγοι μοριακών κλασμάτων και εκφράζουν τους λόγους του μοριακού κλάσματος του απορροφούμενου αερίου στην υγρή ή την αέρια φάση προς το μοριακό κλάσμα του αδρανούς υγρού ή αερίου αντίστοιχα. Η ανωτέρω εξίσωση αντιπροσωπεύει μια ευθεία γραμμή στο «τροποποιημένο» διάγραμμα ισορροπίας Χ, Υ (κλίση L /G ). Απορρόφηση 8
9 Απορρόφηση Εύρεση ελαχίστου λόγου ροής Υγρού/Αερίου Δεδομένα: G, y 1, y 2 και x 2 Ζητούμενα: L, x 1 με βάση την οικονομική και πρακτική λειτουργία της στήλης Ελάχιστος λόγος ροής υγρού/αερίου, (L/G) min : Άπειρος αριθμός θεωρητικών βαθμίδων ή άπειρο ύψος του πύργου απορρόφησης (L/G) min : Η οδηγούσα δύναμη για μεταφορά μάζας από το υγρό στο αέριο μηδενίζεται. Στο διάγραμμα ισορροπίας x-y αυτό θα συμβαίνει στο σημείο τομής της γραμμής λειτουργίας με την καμπύλη ισορροπίας. Απορρόφηση 9
10 Απορρόφηση Ελάχιστος λόγος ροής υγρού/αερίου L y1 y2 ( ) min = G x x 1,max 2 Πραγματικός λόγος ροής υγρού/αερίου (L/G)=β (L/G) min, Τυπικές τιμές του β: 1.25< β <1.5 Η επίτευξη καλής επαφής μεταξύ υγρού και αερίου (αποτελεσματική απορρόφηση) γίνεται συχνά με την χρήση «δίσκων», όπως στην διεργασία της απόσταξης. Απορρόφηση 10
11 Απορρόφηση Μέθοδος McCabe Thiele (θεωρούμε ότι επιτυγχάνεται ισορροπία μεταξύ υγρού και αερίου σε κάθε βαθμίδα) Βήμα 1 ον : Κατασκευάζουμε την γραμμή λειτουργίας (ΑΒ) με βάση των δεδομένων και του απαιτούμενου (L/G) Βήμα 2 ον : Κατασκευάζουμε τις θεωρητικές βαθμίδες ξεκινώντας από την κορυφή του πύργου (Β) κατά τον γνωστό τρόπο, έχοντας σαν όρια την γραμμή λειτουργίας (ΑΒ) και την καμπύλη ισορροπίας, y e = f(x) Απορρόφηση 11
12 Απορρόφηση Αναλυτικές λύσεις για τον υπολογισμό των θεωρητικών βαθμίδων, Ν (Αραιά μίγματα, νόμος του Raoult): Εξισώσεις Kremser, Souders and Brown A A N + 1 y1 y2 0 0 = N y mx A N 1 y mx 1 1 = + ln( A ) y mx A A 1 2 ln[( )(1 ) ] m: η κλίση της εξ. ισορροπίας (y e =m x) και Α 0 : ο παράγοντας απορρόφησης, Α 0 =L/(m G) Απορρόφηση 12
13 Απορρόφηση Πολυσύνθετων Μιγμάτων Αραιά μίγματα αερίων πολλών συστατικών, τα οποία σχηματίζουν ιδανικά (τέλεια) διαλύματα με τον διαλύτη (ισχύει ο νόμος του Henry): Sherwood, Pigford and Wilke s L ( X X ) = G ( Y Y ) M 0 2 M 2 L X X = G Y Y s 0 M( 1 ) M( M ) Όπου L 0 Μ: ρυθμός ροής του διαλύτη, G 0 M: ρυθμός ροής αερίου μίγματος στην είσοδο, Χ: moles του ενός αερίου συστατικού/mole καθαρού υγρού διαλύτη (είσοδο), Υ: moles του ενός συστατικού στην αέρια φάση/mole τροφοδοσίας του προς επεξεργασία αερίου μίγματος, 1:πυθμένας, 2: κορυφή Απορρόφηση 13
14 Απορρόφηση Πολυσύνθετων Μιγμάτων Περίπτωση αραιών διαλυμάτων (νόμος του Henry) Y=K X K= mg ( G )/( L / L ) 0 S M M M M Όπου m=y/x (σταθερά ισορροπίας), για αραιά διαλύματα Κ=m Συστατικό κλειδί (λιγότερο διαλυτό στο αέριο τροφοδοσίας) s 0 L / G M M επιλέγεται βάσει της διαλυτότητας του λιγότερου διαλυτού συστατικού Το κάθε συστατικό έχει την δική του γραμμή λειτουργίας αλλά με την s 0 ίδια κλίση L (παράλληλες γραμμές) M / GM Τα λιγότερα πτητικά απορροφώνται πλήρως ενώ τα πτητικότερα απορροφώνται μερικώς Απορρόφηση 14
15 Απορρόφηση Πολυσύνθετων Μιγμάτων Απαιτούμενος αριθμός θεωρητικών βαθμίδων για την επίτευξη συγκεκριμένου βαθμού απόδοσης Βήμα 1 ον : Κατασκευάζονται οι γραμμές ισορροπίας των διαφόρων συστατικών Βήμα 2 ον : Επιλέγετε το συστατικό κλειδί (γραμμή ισορροπίας // με την γραμμή λειτουργίας [Κ (ή m) = L s M/G 0 M]. Ζωγραφίζουμε τις γραμμές λειτουργίας των υπολοίπων συστατικών (// με του συστατικού κλειδί). ΑΒ από δεδομένα στην είσοδο και έξοδο του πύργου Βήμα 3 ον : McCabe-Thiele αριθμός θεωρητικών βαθμίδων Βήμα 4 ον : Γραμμές λειτουργίας άλλων συστ. // γραμμή λειτ. Σ.Κ. Ακόμη ο αριθμός των θεωρητικών στιβάδων πρέπει να είναι ο ίδιος για όλες τις περιπτώσεις. Απορρόφηση 15
16 Απορρόφηση Πολυσύνθετων Μιγμάτων Αναλυτική μέθοδος (Kremser) N + 1 Y1 Y2 A0 A0 s 0 = οπου A 1 0 = LM / mg N + M Y mx A 1 και m = y / x Όταν A 0 <<1 και Ν μεγάλο η άνω εξ. : (Υ 1 -Υ 2 )/(Υ 1 -mχ 2 )=A 0 Πρώτη εκτίμηση του βαθμού απορρόφησης των πλέον πτητικών συστατικών Όταν A 0 >>1 και Ν μεγάλο η άνω εξ. 1. Το αέριο εγκαταλείπει τον πύργο σε κατάσταση ισορροπίας με το υγρό απορρόφησης (διαλύτη) Αν Α 0 =1 η άνω εξίσωση καταλήγει σε αοριστία. (Y 1 -Y 2 )/(Y 1 -mx 2 )=N/(N+1) Απορρόφηση 16
17 Απορρόφηση με πληρωτικά υλικά Αύξηση επιφάνειας επαφής μεταξύ των δύο φάσεων (αέριας και υγρής) καλύτερη μεταφορά μάζας από την αέρια φάση στην υγρή. Είδη πληρωτικών υλικών - Δακτύλιοι Rashing (απλοί και σταυρωτοί) - Δακτύλιοι Lessing - Δακτύλιοι Pal - Σάγματα Intralox Απορρόφηση 1
18 Απορρόφηση με πληρωτικά υλικά Επιλογή υλικών Αύξηση επιφάνειας επαφής Χαμηλό κόστος Ανθεκτικότητα στις διαβρώσεις Καλή διαβρεξιμότητα και καλή κατανομή του ρευστού Αποτελούνται από: Πλαστικά, κεραμικά, ανοξείδωτος χάλυβας Τοποθέτηση: Με τυχαίο τρόπο Απορρόφηση 2
19 Απορρόφηση με πληρωτικά υλικά Σχεδιασμός στηλών απορρόφησης με πληρωτικά υλικά Ειδική επιφάνεια, α, του πληρωτικού υλικού: «η επιφάνεια του πληρωτικού υλικού ανά μονάδα όγκου κλίνης πληρωτικού υλικού. Πορώδες, ε, της πληρωμένης κλίνης: «το κλάσμα κενού χώρου κλίνης, δηλαδή ο όγκος κενού χώρου προς τον ολικό όγκο κλίνης= (όγκος κλίνηςόγκος πληρωτικού υλικού)/ όγκος κλίνης) Διάμετρος πληρωτικού υλικού, d: 15<D/d<20 Φαινόμενη ταχύτητα αερίου, U G : ~1 m/s Απορρόφηση 3
20 Απορρόφηση με πληρωτικά υλικά Ταχύτητα πλημμυρίσης, U G,Π : «η ταχύτητα εκείνη του αερίου που εμποδίζει σχεδόν εντελώς το υγρό να κατέλθει, με αποτέλεσμα την απότομη αύξηση της πτώσης πίεσης της στήλης» U a L ( )( )( ) exp[ 4( ) ( ) ] g 2 G, Π ρg ηl 2 m 1/4 ρg 1/8 = 3 ε ρl ηw Gm ρl Όπου U G,Π : ταχύτητα πλημμύρισης, α: ειδική επιφάνεια, ε: πορώδες, ρ G, ρ L4 : πυκνότητες αερίου και υγρού αντίστοιχα, G M, L M : μαζικές παροχές αερίου και υγρού αντίστοιχα, n L, n W : ιξώδες του υγρού και νερού αντίστοιχα, g: συντελεστής βαρύτητας Συνήθως U G ~ ( ) U G,Π Απορρόφηση 4
21 Απορρόφηση με πληρωτικά υλικά Μεταφορά μάζας μεταξύ των δύο φάσεων Συστατικό i μεταφέρεται από την αέρια φάση προς την υγρή λόγω διαφοράς συγκέντρωσης μέσω της διεπιφάνειας αερίου- υγρού Ρυθμός μεταφοράς μάζας, Ni (kmol/m 2 s) NA = kg( y yδ ) N = k ( x x) A L δ Όπου k G, k L «μερικοί συντελεστές μεταφοράς μάζας» και αναφέρονται σε μεταφορά μάζας σε μια μόνο καθαρή φάση. Παραδοχές: 1. Αμελητέα αντίσταση στην διεπιφάνεια 2. Μη- συσσώρευση μάζας σε αυτήν 3. Θερμοδυναμική ισορροπία στην διεπιφάνεια 4. Αντιστάσεις στην μεταφορά μάζας μόνο στους δύο υμένες Απορρόφηση 5
22 Απορρόφηση με πληρωτικά υλικά Ολικοί συντελεστές μεταφοράς μάζας N = k ( y y ) A G, ΟΛ e N = k ( x x) A L, ΟΛ e Όπου k G,ΟΛ, k L,ΟΛ «ολικοί συντελεστές μεταφοράς μάζας» ως προς την αέρια και υγρή φάση, αντίστοιχα. και y e, x e γραμμομοριακά κλάσματα του συστατικού i, στην αέρια και υγρή φάση σε θερμοδυναμική ισορροπία με τις συστάσεις y και x, αντίστοιχα στις δύο φάσεις. Απορρόφηση 6
23 Απορρόφηση με πληρωτικά υλικά ( y y ) = ( y y ) + ( y y ) e ( x x) = ( x x ) + ( x x) e οποτε e δ δ 1 1 m ( y ye) m και k k k ( x x) 1 δ = + οπου 1 = L, ΟΛ G L e ( y yδ ) = + οπου m = k k m k ( x x ) 2 L, ΟΛ L 2 G e δ δ e δ Απορρόφηση 7
24 Απορρόφηση με πληρωτικά υλικά Σε περίπτωση που ισχύει ο νόμος του Henry Τότε m 1 =m 2 =m=h i /P και 1 1 m = + k k k L, ΟΛ G L = + k k mk L, ΟΛ L G και Οι εξισώσεις αυτές συνδέουν τους μερικούς συντελεστές μεταφοράς μάζας με τους ολικούς. Απορρόφηση 8
25 Απορρόφηση με πληρωτικά υλικά Αραιά μίγματα 1. Οι γραμ/κές ροές αερίου και υγρού σταθερές σε όλο το ύψος της στήλης 2. Η μέση πίεση του αδρανούς αερίου είναι σταθερή και ίση με την ολική πίεση του συστήματος 3. Οι συντελεστές μεταφοράς μάζας είναι σταθεροί σε όλο το ύψος της στήλης 4. Μεταβολές ενθαλπίας αμελητέες Απορρόφηση 9
26 Απορρόφηση με πληρωτικά υλικά Αναλυτική λύση (όταν ισχύει ο νόμος του Henry) Gy ( y) = Lx ( x) G G Gy ( y) = Lx ( x) x= y+ x y L L (4.6) G G ye = mx y ye = y mx y ye = y m y mx2 + m y2 L L G G y ye = (1 m ) y mx ( 2 y2) L L G οπου C = m( x2 y2) : const,( x2, y2, G, L, m : καθορισµενα ) L Απορρόφηση 10
27 N OG? Απορρόφηση με πληρωτικά υλικά N N OG OG y dy y dy y2 ( y y ) y2 G e (1 m ) y+ C L G (1 m ) y C = ln[ L ] G G 1 m (1 m ) y2 + C L L 1 1 = = Απορρόφηση 11
28 Απορρόφηση με πληρωτικά υλικά Πυκνά μίγματα (σημαντική μεταβολή στις γραμμομοριακές παροχές υγρού, αερίου) Βάση: Παροχή αδρανούς αερίου, G και διαλύτη, L. G (Υ 1 -Υ 2 )=L (Χ 1 -Χ 2 ), Χ,Υ: λόγοι γραμμομοριακών κλασμάτων Διαφορικό Ισοζύγιο Μάζας Ad(Gy)=Ad(Lx)=N A ds και G(1-y)=G και L(1-x)=L Απορρόφηση 12
29 Απορρόφηση με πληρωτικά υλικά ' Gy x L Ad( ) = Ad( ) = N AdS 1 y 1 x dy dx (1 y) (1 x) ' ' AG = AL = N 2 2 AdS ( y y ) (1 y) (1 ye) NA = k οπου (1 y) = (1 y) ln[(1 y) /(1 y )] dy e G, ΟΛ ln ln ' e G = k 2 G, ΟΛα dz (1 y) (1 y) ln dz = G, ΟΛ ( y y ) ' G (1 y) ln dy k α(1 y) (1 y)( y y ) e e Απορρόφηση 13
30 Απορρόφηση με πληρωτικά υλικά Z = y (1 y) ln dy (1 )( ) 1 OG y 2 y y ye Αν (1 y) [(1 y) + (1 y )]/2 N OG H y ln dy 1 y ( y y ) 2 1 y 1 = + y2 e 1 ln[ 2 ] 1 e Απορρόφηση 14
31 Απορρόφηση με πληρωτικά υλικά Απόδοση Στήλης Απορρόφησης, η 0 : η 0 =(πραγματικός διαχωρισμός/διαχωρισμός σε στήλη άπειρου ύψους) η 0 Όπου y 2,e είναι η σύσταση του αερίου που θα ήταν σε ισορροπία με το υγρό σύστασης x 2. Αν x2=0 (καθαρός διαλύτης) τότε: Ακόμη: = y y y y ,e 1 2 Αν ισχύει ο νόμος του Henry (y e =mx) τότε y 1 =m x 1,max L y y 1 L = βm = βmη η = ( ) G y1 β m G Απορρόφηση 15 η 0 = L L y y y y = β( ) min = β = β G G x x x ,max 2 1,max y y 1 y
32 Πανεπιστήμιο Πατρών Τμήμα: Διαχείρισης Περιβάλλοντος και Φυσικών Πόρων 2015 Φυσικές Διεργασίες Απορρόφηση Αερίων Καθηγητής: Ευάγγελος Παπαδάκης Ομάδα: Διακάκης Σταύρος Καραβούλιας Γιώργος Κεντρωτής Γιάννης
33 Περίληψη Η εργασία ασχολείται με την φυσική διεργασία της απορρόφησης των αερίων. Περιέχονται ο ορισμός της απορρόφησης καθώς και οι βασικές αρχές πάνω στις οποίες στηρίζεται η φυσική διεργασία. Γίνεται παρουσίαση των βασικών μηχανισμών μεταφοράς μάζας από τους οποίους εξαρτάται η διεργασία καθώς και οι νόμοι στους οποίους υπακούει. Επιπλέον αναφέρονται οι βασικές εξισώσεις επίλυσης αλλά και σχεδιασμού της διεργασίας της απορρόφησης. Όλα τα παραπάνω επεξηγούνται με σχήματα. Τέλος, γίνεται αναφορά των εφαρμογών αυτής της φυσικής διεργασίας στην βιομηχανία και στο περιβάλλον, με την παρουσίαση των συσκευών για κάθε περίπτωση.
34 Ιστορική αναδρομή Η χρήση της ψύξεως ξεκινά από την προϊστορική εποχή από φυλές όπως οι Κινέζοι, οι Εβραίοι, οι Έλληνες, οι Ρωμαίοι και οι Πέρσες. Τα υλικά αποθηκεύονταν σε σπηλιές και κλειστούς χώρους με σκοπό την διατήρηση των τροφίμων. Αυτή η τεχνική με ορισμένες διαφοροποιήσεις έδρασε πολύ καλά μέχρι τον 20 ο αιώνα όπου και έχουμε μια ριζική απομάκρυνση αυτής. Λίγο πιο πριν και συγκεκριμένα τον 16 ο αιώνα η ανακάλυψη του Νιτρικού άλατος του νατρίου (ΝαΝΟ3) και του Νιτρικού άλατος του καλίου (ΚΝΟ3) έδωσε σημαντική ώθηση προς την κατεύθυνση των τεχνιτών ψυκτικών.
35 Το δε χρονοδιάγραμμα εξέλιξης έχει ως εξής: 1748: Ο William Cullen στο παν/μιο της Γλασκόβης πραγματοποιεί το πρώτο πείραμα με δημιουργία κενού και αιθυλικό αιθέρα που έχει πρακτική εφαρμογή 1805: Ο Oliver Evans σχεδιάζει, αλλά δεν κατασκευάζει, μηχανή βασισμένη στον κύκλο συμπιέσεως ατμού. 1820: Ο Michael Faraday υγροποιεί την αμμωνία και άλλα αέρια χρησιμοποιώντας χαμηλές θερμοκρασίες και μεγάλες πιέσεις. 1834: Ο Jacob Perkins κατοχυρώνει την πρώτη πατέντα και κατασκευάζει το πρωτότυπο μηχανισμό συμπιέσεων ατμού. 1842: Ο John Gorrie σχεδιάζει σύστημα ψύξης του νερού με σκοπό την δημιουργία πάγου και παράλληλα συλλαμβάνει την ιδέα του κλιματιστικού εσωτερικών χώρων. 1850: Ο Alexander Twining πειραματίζεται με τον κύκλο συμπιέσεως του ατμού και καταφέρνει μέχρι το 1856 να αρχίσει εμπορικές προσπάθειες στην Αμερική. 1860: Ο Ferdinand Carre εξελίσσειτην πρώτη μηχανήαπορρόφησης. 1861: Ο James Harrison εισάγει την ψύξη με μηχανική συμπίεση ατμού σε επιχειρήσεις. 1915: Η Kelvinator κατασκευάζει τις πρώτες μηχανές οικιακής ψύξεως.
36 Εισαγωγή Απορρόφηση: είναι η επιλεκτική μεταφορά μιας αέριας ουσίας από ένα αέριο ρεύμα σε ένα υγρό, κυρίως με νερό, με το οποίο έρχεται σε επαφή. Βασίζεται στην διαλυτότητα ενός αερίου στο υγρό και αποτελεί διεργασία μεταφοράς μάζας. Η διαλυτότητα ενός αερίου είναι πολύ σημαντική παράμετρος η οποία επηρεάζει την ποσότητα του ρύπου που μπορεί να απορροφηθεί. Είναι συνάρτηση κυρίως της θερμοκρασίας και λιγότερο της πίεσης. Η πιο κοινή μέθοδος ανάλυσης των δεδομένων διαλυτότητας είναι το διάγραμμα ισορροπίας.
37 Η διεργασία περιλαμβάνει τα εξής: Διάχυση της ουσίας από την αέρια φάση μέσω της διεπιφάνειας αερίου υγρού και τη διασπορά της στην υγρή φάση. Μπορεί να πραγματοποιηθεί με χημική αντίδραση στο υγρό Η μεταφορά μάζας επιτελείται τόσο με μοριακά μέσα όσο και με συναγωγή. Μπορεί να ελέγχεται είτε από την αντίσταση στην αέρια φάση είτε από την αντίσταση στην υγρή.
38 Θεωρητικό Υπόβαθρο Ρόλος της Θερμοκρασίας Όταν αυξάνεται η θερμοκρασία σε ένα αέριο μίγμα, τότε δημιουργείται αυξημένη κινητικότητα των μορίων και η διαλυτότητα μειώνεται. Όταν η διαδικασία της απορρόφησης είναι εξώθερμη, τότε δυσχεραίνεται η συνέχισή της. Η συγκέντρωση του αερίου στο υγρό για δεδομένη μερική πίεση αυξάνει με την μείωση της θερμοκρασίας. Αυτό το γεγονός αποτελεί ένα γενικότερο χαρακτηριστικό της απορρόφησης.
39 Μεταφορά μάζας Ο ρυθμός μεταφοράς μάζας ανάμεσα σε δύο φάσεις ρευστών εξαρτάται από τις φυσικές ιδιότητες που έχουν οι 2 φάσεις, τη διαφορά συγκέντρωσης, το εμβαδό της διεπιφάνειας και τον βαθμό στροβιλισμού. Στις περισσότερες όμως βιομηχανικές περιπτώσεις η μορφή της ροής είναι τόσο σύνθετη, ώστε είναι πρακτικά αδύνατον να δοθεί με μια μαθηματική έκφραση και το εμβαδό της διεπιφάνειας δεν είναι γνωστό. Έχουν δοθεί λοιπόν τρεις γνωστές θεωρίες για να αναπαραστήσουν τις συνθήκες που επικρατούν στην περιοχή της διεπιφάνειας.
40 Θεωρία δύο λεπτών στοιβάδων Η πρώτη θεωρία είναι του Whitman. Δεν παράγει αρκετά πιστά τις συνθήκες που επικρατούν στις περισσότερες πρακτικές συσκευές αλλά μας δίνει εκφράσεις για να τις χρησιμοποιήσουμε σε πειραματικά δεδομένα. Με βάση την θεωρία, ο στροβιλισμός εξαφανίζεται κοντά στην διεπιφάνεια, και σε κάθε ρευστό υπάρχει νηματώδης στοιβάδα. Έξω από την στοιβάδα, οι δίνες συμπληρώνουν την δράση που προκαλείται από την τυχαία κίνηση των μορίων, και η αντίσταση στη μεταφορά μειώνεται. Όταν λοιπόν έχουμε ισομοριακή αντιδιάχυση, η κλίση της συγκέντρωσης είναι γραμμική κοντά στην διεπιφάνεια και σταδιακά σε μεγαλύτερες αποστάσεις μειώνεται.
41 Οι διακεκομμένες γραμμές AGC και DHF δείχνουν την υποθετική κατανομή της συγκέντρωσης και το πάχος των στοιβάδων είναι αντίστοιχα L 1 και L 2.
42 Θεωρία της διείσδυσης Η δεύτερη θεωρία είναι του Higbie. Την διατύπωσε καθώς εξέταζε την ύπαρξη ή μη αντίστασης στη μεταφορά στην διεπιφάνεια, όταν το καθαρό αέριο απορροφάται σε ένα υγρό. Σύμφωνα με την θεωρία, οι στροβιλισμοί φέρνουν ένα στοιχείο του ρευστού στη διεπιφάνεια, όπου εκτίθεται για λίγο, και μετά αναμιγνύεται πάλι με την κύρια μάζα του ρευστού. Υποτίθεται επίσης, πως η ισορροπία στις επιφανειακές στοιβάδες αποκαθίσταται αμέσως και πως συμβαίνει μια λειτουργία μοριακής διάχυσης μη σταθερής κατάστασης. Ακόμα, δεν υπάρχει η κλίση της ταχύτητας στα δύο ρευστά, και το ρευστό σε όλα τα βάθη θεωρείται πως κινείται με την ίδια ταχύτητα όπως στην διεπιφάνεια.
43 Διείσδυση διαλυτού συστατικού σε διαλύτη
44 Θεωρία λεπτής στοιβάδας διείσδυσης Η θεωρία διατυπώθηκε από τους Toor & Marchello. Σύμφωνα με την θεωρία όλη η αντίσταση στη μεταφορά θεωρείται ότι βρίσκεται μέσα σε μια νηματώδη λεπτή στοιβάδα κοντά στην διεπιφάνεια, αλλά η μεταφορά μάζας θεωρείται σαν μία λειτουργία μη σταθερής κατάστασης. Μετά, συμβαίνει μεταφορά μάζας, με την εξαίρεση ότι η αντίσταση είναι περιορισμένη στην καθορισμένη λεπτή στοιβάδα και ότι το υλικό που διασχίζει τη στοιβάδα αμέσως αναμιγνύεται πλήρως με την κύρια μάζα του ρευστού.
45 Μεταφορά μάζας στην διεπιφάνεια Μπορούμε να θεωρήσουμε πως η μεταφορά ενός αερίου σε ένα υγρό γίνεται σε τρία στάδια: Διάχυση από την αέρια φάση στην υγρή επιφάνεια Διάλυση στο υγρό Διάχυση από την επιφάνεια του υγρού στην κύρια μάζα αυτού
46 Οι ατομικοί επιφανειακοί συντελεστές μεταφοράς μάζας ορίζονται ως εξής: N A : ταχύτητα μεταφοράς k G = N A /(P A P i ) k L = N A /(C i C A ) k G : ο επιφανειακός συντελεστής της αέριας στοιβάδας k L : ο συντελεστής της υγρής Οι ολικοί συντελεστές που κανονικά γράφονται με βάση την αέρια φάση ως Κ G και ως Κ L για την υγρή φάση, δίνονται από τις εξισώσεις: P e : η μερική πίεση σε ισορροπία με τη C A Κ G = N A /(P A P e ) K L = N A /(C e C A ) C e : η μοριακή συγκέντρωση σε ισορροπία με την P Α.
47 Μεταφορά κατά αντιρροή Η περίπτωση της αντιρροής είναι η ποιο συνηθισμένη. Μερικές φορές η ομορροή παρουσιάζει πλεονεκτήματα. Παρουσιάζονται 3 παραδείγματα αντιρροής: Σε αποστακτική στήλη με πληρωτικό υλικό. Σε μια απορροφητική στήλη με πληρωτικό υλικό. Σε μια στήλη υγρής-υγρής εκχύλισης.
48 Νόμος του Henry Όταν αυξήσουμε την πίεση ενός αερίου Α πάνω από ένα διάλυμα αυτού σε έναν διαλύτη S, τότε θα αυξηθεί και το ποσοστό των μορίων του αερίου τα οποία εισέρχονται στο διάλυμα και κατά συνέπεια το μοριακό κλάσμα του, x, στο διάλυμα. Το x για μικρές πιέσεις θα είναι και αυτό μικτό και θα αυξάνεται γραμμικά, ανάλογα με την πίεση. Δηλαδή, μπορούμε να γράψουμε την σχέση: P A = H A x A x A : το μοριακό κλάσμα του συστατικού Α που διαλύεται Η Α : η σταθερά αναλογίας (σταθερά Henry) P A : η μερική πίεση του αερίου Α πάνω από το διάλυμα
49 Νόμος του Raoult Έστω ότι έχουμε το συστατικό Α σε υγρή κατάσταση και σε ισορροπία με ατμούς του ίδιου συστατικού. Με αυτή την υπόθεση, η πίεση που επικρατεί είναι η τάση των ατμών του καθαρού Α την οποία την συμβολίζουμε με P 0,A. Αν τώρα, διαλυθούν και μερικά μόρια διαλύτη S που έχει πολύ μικρή πτητικότητα, τότε το κλάσμα το Α από 1 θα γίνει x. Τότε η τάση των ατμών του Α μεταβάλλεται ανάλογα με το x και θα γίνει P A = P A,0 X A. Προσοχή! Αν και οι νόμοι Henry και Raoult μοιάζουν στην μαθηματική τους έκφραση, η σταθερά Η Α ΔΕΝ ισούται με την τάση ατμών P A,0!
50
51 Εξοπλισμός Σχεδιασμός Οι κύριες συσκευές απορρόφησης είναι: Με διακριτές βαθμίδες Με πληρωτικό υλικό Υπάρχουν και άλλα είδη συσκευών όπως διασκόρπισης αερίου και διασκόρπισης υγρού, οι οποίες λειτουργούν με ψεκασμό, ώστε τα σωματίδια τα οποία ψεκάζονται και έχουν την μεγαλύτερη ειδική επιφάνεια να απορροφήσουν το άεριο πιο αποτελεσματικά.
52 Πληρωτικός πύργος Θεωρούμε έναν πληρωτικό πύργο αντιρροής. Αποδεικνύεται πως ισχύουν οι παρακάτω σχέσεις: Y = y/(1 y) = P/(P T P) ή y = Y/(1 + Y) P T : η ολική πίεση y & Y: αναφέρονται στο αέριο ρεύμα x & X: στο υγρό Επίσης Χ = x/(1 x) G- s = G(1 y) = G/(1 + Y) L s = L(1 x) = L/(1 + X) L και G: είναι οι μοριακές παροχές ο δείκτης s: συμβολίζει τη διαλυτή ουσία * Με κεφαλαία συμβολίζεται η αναλογία των γραμμομορίων και με πεζά είναι τα μοριακά κλάσματα.
53 Ένα ισοζύγιο μάζας στο κάτω μέρος της στήλης (συμβολίζεται ως 1) είναι δυνατό να εκφρασθεί είτε με τον όρο της αναλογίας των γραμμομορίων είτε με τα μοριακά κλάσματα * G s (Y 1 Y) = L s (X 1 X) * G(y 1 y) = L(x 1 x) Είτε με την μορφή των ροών και των μοριακών κλασμάτων της διαλυτής ουσίας * Gs[y1/(1 - y 1 ) y/(1 y)] = G s [P 1 /(P T P 1 ) P/(P T P)] = L s [x 1 /(1 x 1 ) x/(1 x)]
54 Αραιά Μίγματα Όταν έχουμε να εξετάσουμε αραιά αέρια μίγματα τα οποία απορροφούνται σε ένα υγρό, γίνεται συνήθως μια υπόθεση ότι η λειτουργία είναι ισόθερμη. Υπάρχουν όμως και αρκετές περιπτώσεις που στην διεργασία περιλαμβάνονται μεγάλες επιδράσεις θερμότητας. Το παρακάτω ισοζύγιο ενέργειας επιτρέπει τον υπολογισμό του φορτίου θερμότητας: H L2 L 2 + H G G = G G2 G 2 + H L L + Q Η L και Η G : είναι οι μοριακές ενθαλπίες του υγρού και του αέριου ρεύματος Η ενθαλπία του διαλύματος σύστασης Χ και θερμοκρασίας t L υπολογίζεται από την παρακάτω εξίσωση: Η L = C L (t L t 0 )M av + ΔH s C L : είναι η ειδική θερμότητα του υγρού t L, t 0 : οι θερμοκρασίες του διαλύματος και της αναφοράς για το υγρό M av : το μέσο μοριακό βάτος του διαλύματος ΔH s : η θερμότητα ανάμιξης (είναι ίσιο με το μηδέν για ιδανικά διαλύματα και η έκλυση θερμότητας σε αυτή την περίπτωση οφείλεται μόνο στην λανθάνουσα θερμότητα συμπύκνωσης της απορροφούμενης διαλυτής ουσίας.)
55 Πυκνά διαλύματα Χρησιμοποιούμε μια τροποποιημένη έκφραση για τα μοριακά κλάσματα. Για το υγρό σε μία τυχαία διατομή, αν S είναι η ροή του διαλύτη, τότε θα ισχύει: xl = XS = X(1 x)l X = x/(1 x) και παρομοίως, για το άεριο, το τροποποιημένο κλάσμα είναι: Y = y/(1 y)
56 Στον σχεδιασμό λαμβάνονται υπόψη, επίσης, τα εξής: Περίπτωση ομορροής Σχέση γραμμής λειτουργίας και γραμμής ισορροπίας Σημασία κλίσης γραμμής λειτουργίας
57 * Η διαλυτότητα του αερίου πρέπει να είναι υψηλή στον επιλεγέντα διαλύτη * Ο διαλύτης πρέπει να είναι φθηνός, μη διαβρωτικός, μη τοξικός και μη εύφλεκτος * Ο ελάχιστον λόγος αερίου/υγρού υπολογίζεται από την σύσταση του εισερχόμενου αερίου και τη διαλυτότητά του στο υγρό εξόδου
58
59 Εφαρμογές Στην βιομηχανία αναψυκτικών Απομάκρυνση αερίων από αέρια μίγματα Ανάκτηση αμμωνίας στη βιομηχανία λιπασμάτων Απομάκρυνση HF από τα απαέρια του φούρνου υάλου Έλεγχος H-- 2 S από την αποθείωση απαερίων (FGD) Ανάκτηση διαλυτών (μεθανόλη, ακετόνη) Έλεγχος οσμών
60 Βιβλιογραφία n/chap03_aporrofisi.pdf 8/matis_askisi_absorption.pdf DIAXEIRISH-AERION-RYPON-PP-31-Y-1998-EIS10.pdf Ζουμπούλης Α., Καραπάντσιος Θ., Μάτης Κ., Μαύρος Π., Στοιχεία Φυσικών Διεργασιών, Αθήνα, Μούρσιας Χρήστος, Πτυχιακή Εργασία με Θέμα: Συστήματα ψύξης με απορρόφηση, Καβάλα 2014, pdf
Energy resources: Technologies & Management
 Πανεπιστήμιο Δυτικής Μακεδονίας Energ resources: echnologies & Management Τεχνολογίες άνθρακα Σχεδιασμός Στηλών Απορρόφησης Αερίων Δρ. Γεώργιος Σκόδρας Αν. Καθηγητής Περιεχόμενα Η διάλεξη που ακολουθεί
Πανεπιστήμιο Δυτικής Μακεδονίας Energ resources: echnologies & Management Τεχνολογίες άνθρακα Σχεδιασμός Στηλών Απορρόφησης Αερίων Δρ. Γεώργιος Σκόδρας Αν. Καθηγητής Περιεχόμενα Η διάλεξη που ακολουθεί
Φυσικές Διεργασίες Πέμπτη Διάλεξη
 Φυσικές Διεργασίες Πέμπτη Διάλεξη Δευτέρα, 12 Μαΐου 2008 Απορρόφηση αερίων 1. Ορισμός Τι είναι απορρόφηση; Είναι μεταφορά μέσω της διεπιφάνειας αερίου-υγρού ενός συστατικού από αέριο μίγμα σε έναν υγρό
Φυσικές Διεργασίες Πέμπτη Διάλεξη Δευτέρα, 12 Μαΐου 2008 Απορρόφηση αερίων 1. Ορισμός Τι είναι απορρόφηση; Είναι μεταφορά μέσω της διεπιφάνειας αερίου-υγρού ενός συστατικού από αέριο μίγμα σε έναν υγρό
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens. ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Gas Absorption
 Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Gas Absorption Παράγοντες που Επηρεάζουν Διεργασία Απορρόφησης Συνήθως δίνονται: Ρυθμός
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Gas Absorption Παράγοντες που Επηρεάζουν Διεργασία Απορρόφησης Συνήθως δίνονται: Ρυθμός
Απορρόφηση Αερίων. 1. Εισαγωγή
 1. Εισαγωγή Απορρόφηση Αερίων Πρόκειται για διαχωρισμό συστατικών από μείγμα αερίου με τη βοήθεια υγρού διαλύτη. Κινητήρια δύναμη είναι η διαφορά διαλυτότητας στο διαλύτη. Στη συνέχεια θα ασχοληθούμε με
1. Εισαγωγή Απορρόφηση Αερίων Πρόκειται για διαχωρισμό συστατικών από μείγμα αερίου με τη βοήθεια υγρού διαλύτη. Κινητήρια δύναμη είναι η διαφορά διαλυτότητας στο διαλύτη. Στη συνέχεια θα ασχοληθούμε με
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens. ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Liquid Liquid Extraction
 Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Liquid Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Περιοχές
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Liquid Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Περιοχές
Απορρόφηση (Absorption)
 Απορρόφηση (Absorption) Απορρόφηση: η επιλεκτική μεταφορά μιας αέριας ουσίας (απορροφήσιμο μέσο-absorbate) από ένα αέριο ρεύμα σε ένα υγρό (απορροφητικό μέσοabsorbent) με το οποίο βρίσκεται σε επαφή. Βασίζεται
Απορρόφηση (Absorption) Απορρόφηση: η επιλεκτική μεταφορά μιας αέριας ουσίας (απορροφήσιμο μέσο-absorbate) από ένα αέριο ρεύμα σε ένα υγρό (απορροφητικό μέσοabsorbent) με το οποίο βρίσκεται σε επαφή. Βασίζεται
5.3 Υπολογισμοί ισορροπίας φάσεων υγρού-υγρού
 5.3 Υπολογισμοί ισορροπίας φάσεων υγρού-υγρού Η αρχική εξίσωση που χρησιμοποιείται για τους υπολογισμούς της ΙΦΥΥ είναι η ικανοποίηση της βασικής θερμοδυναμικής απαίτησης της ισότητας των τάσεων διαφυγής
5.3 Υπολογισμοί ισορροπίας φάσεων υγρού-υγρού Η αρχική εξίσωση που χρησιμοποιείται για τους υπολογισμούς της ΙΦΥΥ είναι η ικανοποίηση της βασικής θερμοδυναμικής απαίτησης της ισότητας των τάσεων διαφυγής
ΦΥΣΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ ΜΕΤΑΦΟΡΑΣ ΜΑΖΑΣ. -Απορρόφηση - Απόσταξη - Εκχύλιση - Κρυστάλλωση - Ξήρανση
 ΦΥΣΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ ΜΕΤΑΦΟΡΑΣ ΜΑΖΑΣ -Απορρόφηση - Απόσταξη - Εκχύλιση - Κρυστάλλωση - Ξήρανση Απορρόφηση αερίων φυσική και χημική Παραδείγματα βιομηχανικών εφαρμογών ) Απορρόφηση SΟ 3 κατά την παραγωγή
ΦΥΣΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ ΜΕΤΑΦΟΡΑΣ ΜΑΖΑΣ -Απορρόφηση - Απόσταξη - Εκχύλιση - Κρυστάλλωση - Ξήρανση Απορρόφηση αερίων φυσική και χημική Παραδείγματα βιομηχανικών εφαρμογών ) Απορρόφηση SΟ 3 κατά την παραγωγή
ΕΦΑΡΜΟΓΕΣ ΑΠΟΡΡΟΦΗΣΗΣ ΑΕΡΙΩΝ Κ. Μάτης
 ΕΦΑΡΜΟΓΕΣ ΑΠΟΡΡΟΦΗΣΗΣ ΑΕΡΙΩΝ Κ. Μάτης Πρόβληµα 1. Ένα µίγµα αερίων που περιέχει 65% του Α, 5% Β, 8% C και % D βρίσκεται σε ισορροπία µ' ένα υγρό στους 350 Κ και 300 kn/m. Αν η τάση ατµών των καθαρών συστατικών
ΕΦΑΡΜΟΓΕΣ ΑΠΟΡΡΟΦΗΣΗΣ ΑΕΡΙΩΝ Κ. Μάτης Πρόβληµα 1. Ένα µίγµα αερίων που περιέχει 65% του Α, 5% Β, 8% C και % D βρίσκεται σε ισορροπία µ' ένα υγρό στους 350 Κ και 300 kn/m. Αν η τάση ατµών των καθαρών συστατικών
Απορρόφηση Αερίων (2)
 Απορρόφηση Αερίων (2) Λεπτομερής Ανάλυση Θεωρούμε έναν πύργο απορρόφησης που μπορεί να περιέχει δίσκους ή να είναι τύπου πληρωτικού υλικού ή άλλου τύπου. Τελικός σκοπός είναι να βρούμε το μέγεθος του πύργου.
Απορρόφηση Αερίων (2) Λεπτομερής Ανάλυση Θεωρούμε έναν πύργο απορρόφησης που μπορεί να περιέχει δίσκους ή να είναι τύπου πληρωτικού υλικού ή άλλου τύπου. Τελικός σκοπός είναι να βρούμε το μέγεθος του πύργου.
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens. ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ- ΥΓΡΟΥ Liquid- Liquid Extraction
 Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ- ΥΓΡΟΥ Liquid- Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Τριγωνικές
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ- ΥΓΡΟΥ Liquid- Liquid Extraction ΕΚΧΥΛΙΣΗ ΙΣΟΡΡΟΠΙΑΣ ΓΙΑ ΜΕΡΙΚΩΣ ΑΝΑΜΙΞΙΜΑ ΣΥΣΤΗΜΑΤΑ Τριγωνικές
σχηματική αναπαράσταση των βασικών τμημάτων μίας βιομηχανικής εγκατάστασης
 σχηματική αναπαράσταση των βασικών τμημάτων μίας βιομηχανικής εγκατάστασης Αρχές μεταφοράς μάζας Αρχές σχεδιασμού συσκευών μεταφοράς μάζας Διεργασίες μεταφοράς μάζας - Απορρόφηση - Απόσταξη - Εκχύλιση
σχηματική αναπαράσταση των βασικών τμημάτων μίας βιομηχανικής εγκατάστασης Αρχές μεταφοράς μάζας Αρχές σχεδιασμού συσκευών μεταφοράς μάζας Διεργασίες μεταφοράς μάζας - Απορρόφηση - Απόσταξη - Εκχύλιση
Βασικές Διεργασίες Μηχανικής Τροφίμων
 Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
ΠΑΡΑΔΕΙΓΜΑΤΑ ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ
 ΠΑΡΑΔΕΙΓΜΑΤΑ ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Παράδειγμα 1 Σε μονάδα εκχύλισης μιας μόνο βαθμίδας πραγματοποιείται εκχύλιση οξικού οξέος από νερό με χρήση βουτανόλης. Η τροφοδοσία παροχής F= 100 kg/h περιέχει οξικό
ΠΑΡΑΔΕΙΓΜΑΤΑ ΕΚΧΥΛΙΣΗ ΥΓΡΟΥ ΥΓΡΟΥ Παράδειγμα 1 Σε μονάδα εκχύλισης μιας μόνο βαθμίδας πραγματοποιείται εκχύλιση οξικού οξέος από νερό με χρήση βουτανόλης. Η τροφοδοσία παροχής F= 100 kg/h περιέχει οξικό
ΑΠΟΡΡΟΦΗΣΗ (absorption)
 Εισαγωγή ΑΠΟΡΡΟΦΗΣΗ (absorption) Απορρόφηση: η επιλεκτική μεταφορά μιας αέριας ουσίας (απορροφήσιμο μέσοabsorbate ή solute) από ένα αέριο ρεύμα σε ένα υγρό (απορροφητικό μέσο - absorbent), με το οποίο
Εισαγωγή ΑΠΟΡΡΟΦΗΣΗ (absorption) Απορρόφηση: η επιλεκτική μεταφορά μιας αέριας ουσίας (απορροφήσιμο μέσοabsorbate ή solute) από ένα αέριο ρεύμα σε ένα υγρό (απορροφητικό μέσο - absorbent), με το οποίο
ΥΤΙΚΕ ΔΙΕΡΓΑΙΕ ΜΕΣΑΥΟΡΑ ΜΑΖΑ. - Απορρόφηση - Απόσταξη - Εκχύλιση - Κρυστάλλωση - Ξήρανση
 ΥΤΙΚΕ ΔΙΕΡΓΑΙΕ ΜΕΣΑΥΟΡΑ ΜΑΖΑ - Απορρόφηση - Απόσταξη - Εκχύλιση - Κρυστάλλωση - Ξήρανση Εκχύλιση : εκχύλιση υγρών εκχύλιση στερεών διαχωρισμός αναμίξιμων υγρών παραπλήσια σ.ζ. ή α ΑΒ =1 έκπλυση ή διαλυτοποίηση
ΥΤΙΚΕ ΔΙΕΡΓΑΙΕ ΜΕΣΑΥΟΡΑ ΜΑΖΑ - Απορρόφηση - Απόσταξη - Εκχύλιση - Κρυστάλλωση - Ξήρανση Εκχύλιση : εκχύλιση υγρών εκχύλιση στερεών διαχωρισμός αναμίξιμων υγρών παραπλήσια σ.ζ. ή α ΑΒ =1 έκπλυση ή διαλυτοποίηση
Σφαιρικές συντεταγμένες (r, θ, φ).
 T T r e r 1 T e r Σφαιρικές συντεταγμένες (r, θ, φ). 1 T e. (2.57) r sin u u e u e u e, (2.58) r r οπότε το εσωτερικό γινόμενο u.t γίνεται: T u T u T u. T ur. (2.59) r r r sin 2.5 Η ΑΡΧΗ ΔΙΑΤΗΡΗΣΗΣ ΤΗΣ
T T r e r 1 T e r Σφαιρικές συντεταγμένες (r, θ, φ). 1 T e. (2.57) r sin u u e u e u e, (2.58) r r οπότε το εσωτερικό γινόμενο u.t γίνεται: T u T u T u. T ur. (2.59) r r r sin 2.5 Η ΑΡΧΗ ΔΙΑΤΗΡΗΣΗΣ ΤΗΣ
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ
 Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
ΒΙΟΜΗΧΑΝΙΚΗ ΑΠΟΣΤΑΚΤΙΚΗ ΣΤΗΛΗ : Ερωτήσεις πολλαπλής επιλογής. Σκεφθείτε και δικαιολογήσετε τη σωστή απάντηση κάθε φορά)
 ΒΙΟΜΗΧΑΝΙΚΗ ΑΠΟΣΤΑΚΤΙΚΗ ΣΤΗΛΗ : Ερωτήσεις πολλαπλής επιλογής (Σηµείωση: Σκεφθείτε και δικαιολογήσετε τη σωστή απάντηση κάθε φορά) Η απόσταξη στηρίζεται στη διαφορά που υπάρχει στη σύσταση ισορροπίας των
ΒΙΟΜΗΧΑΝΙΚΗ ΑΠΟΣΤΑΚΤΙΚΗ ΣΤΗΛΗ : Ερωτήσεις πολλαπλής επιλογής (Σηµείωση: Σκεφθείτε και δικαιολογήσετε τη σωστή απάντηση κάθε φορά) Η απόσταξη στηρίζεται στη διαφορά που υπάρχει στη σύσταση ισορροπίας των
ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Κ. Α. Μάτης
 3 ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Κ. Α. Μάτης 3. ΕΙΣΑΓΩΓΗ Η γενική θεωρητική επεξεργασία που αναπτύσσεται στα φαινόµενα µεταφοράς συχνά έχει σχέση µε τη µεταφορά µάζας σε µια µοναδική φάση που δεν έχει ασυνέχειες. Αλλά
3 ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Κ. Α. Μάτης 3. ΕΙΣΑΓΩΓΗ Η γενική θεωρητική επεξεργασία που αναπτύσσεται στα φαινόµενα µεταφοράς συχνά έχει σχέση µε τη µεταφορά µάζας σε µια µοναδική φάση που δεν έχει ασυνέχειες. Αλλά
Κεφάλαιο 6 Απορρόφηση
 Κεφάλαιο 6 Απορρόφηση Σύνοψη Απορρόφηση αεριών ονομάζεται η φυσική διεργασία απομάκρυνσης ενός ή περισσοτέρων συστατικών ενός αερίου ρεύματος προς ένα μη πτητικό υγρό, το οποίο διαλύει αυτό(α) το(α) συστατικό(α).
Κεφάλαιο 6 Απορρόφηση Σύνοψη Απορρόφηση αεριών ονομάζεται η φυσική διεργασία απομάκρυνσης ενός ή περισσοτέρων συστατικών ενός αερίου ρεύματος προς ένα μη πτητικό υγρό, το οποίο διαλύει αυτό(α) το(α) συστατικό(α).
Λύση Παραδείγματος 1. Διάγραμμα ροής διεργασίας. Εκρόφηση χλωριούχου βινυλίου από νερό στους 25 C και 850 mmhg. Είσοδος υγρού.
 Παράδειγμα 1 Μια εγκατάσταση καθαρισμού νερού απομακρύνει χλωριούχο βινύλιο (vinyl cloride) από μολυσμένα υπόγεια ύδατα σε θερμοκρασία 25 C και πίεση 850 mmhg χρησιμοποιώντας στήλη εκρόφησης κατ αντιρροή.
Παράδειγμα 1 Μια εγκατάσταση καθαρισμού νερού απομακρύνει χλωριούχο βινύλιο (vinyl cloride) από μολυσμένα υπόγεια ύδατα σε θερμοκρασία 25 C και πίεση 850 mmhg χρησιμοποιώντας στήλη εκρόφησης κατ αντιρροή.
ΠΡΟΒΛΗΜΑΤΑ Υ/Υ ΕΚΧΥΛΙΣΗΣ Κ. Μάτης
 ΠΡΟΒΛΗΜΑΤΑ Υ/Υ ΕΚΧΥΛΙΣΗΣ Κ. Μάτης Πρόβληµα 36. Μια υγρή τροφοδοσία 3,5 kg/s, που περιέχει µια διαλυτή ουσία Β διαλυµένη σε συστατικό Α, πρόκειται να διεργαστεί µε ένα διαλύτη S σε µια µονάδα επαφής καθ
ΠΡΟΒΛΗΜΑΤΑ Υ/Υ ΕΚΧΥΛΙΣΗΣ Κ. Μάτης Πρόβληµα 36. Μια υγρή τροφοδοσία 3,5 kg/s, που περιέχει µια διαλυτή ουσία Β διαλυµένη σε συστατικό Α, πρόκειται να διεργαστεί µε ένα διαλύτη S σε µια µονάδα επαφής καθ
ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ. Σχεδιασµός της Στήλης µε Χρήση ενός Προσοµοιωτή. K.A. Μάτης
 ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Σχεδιασµός της Στήλης µε Χρήση ενός Προσοµοιωτή K.A. Μάτης Εισαγωγή Στη διεργασία της απορρόφησης ένα αέριο µίγµα έρχεται σε επαφή µε ένα υγρό (το διαλύτη ή απορροφητικό) ώστε να διαλυθεί
ΑΠΟΡΡΟΦΗΣΗ ΑΕΡΙΩΝ Σχεδιασµός της Στήλης µε Χρήση ενός Προσοµοιωτή K.A. Μάτης Εισαγωγή Στη διεργασία της απορρόφησης ένα αέριο µίγµα έρχεται σε επαφή µε ένα υγρό (το διαλύτη ή απορροφητικό) ώστε να διαλυθεί
Enrico Fermi, Thermodynamics, 1937
 I. Θερµοδυναµικά συστήµατα Enrico Feri, herodynaics, 97. Ένα σώµα διαστέλλεται από αρχικό όγκο. L σε τελικό όγκο 4. L υπό πίεση.4 at. Να υπολογισθεί το έργο που παράγεται. W - -.4 at 5 a at - (4..) - -
I. Θερµοδυναµικά συστήµατα Enrico Feri, herodynaics, 97. Ένα σώµα διαστέλλεται από αρχικό όγκο. L σε τελικό όγκο 4. L υπό πίεση.4 at. Να υπολογισθεί το έργο που παράγεται. W - -.4 at 5 a at - (4..) - -
ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΙΙ. Διδάσκων: Παπασιώπη Νυμφοδώρα Αναπληρώτρια Καθηγήτρια Ε.Μ.Π. Ενότητα 9 η : Μεταφορά Μάζας
 ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΙΙ Διδάσκων: Παπασιώπη Νυμφοδώρα Αναπληρώτρια Καθηγήτρια Ε.Μ.Π. Ενότητα 9 η : Μεταφορά Μάζας Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creatve Coons. Για εκπαιδευτικό
ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΙΙ Διδάσκων: Παπασιώπη Νυμφοδώρα Αναπληρώτρια Καθηγήτρια Ε.Μ.Π. Ενότητα 9 η : Μεταφορά Μάζας Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creatve Coons. Για εκπαιδευτικό
Βασικές Διεργασίες Μηχανικής Τροφίμων
 Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
Συστήματα Ανάκτησης Θερμότητας
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργαστήριο Θερμοδυναμικής & Φαινομένων Μεταφοράς Συστήματα Ανάκτησης Θερμότητας Εισαγωγή Σκοπός των συστημάτων ανάκτησης θερμότητας είναι η αξιοποίηση
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργαστήριο Θερμοδυναμικής & Φαινομένων Μεταφοράς Συστήματα Ανάκτησης Θερμότητας Εισαγωγή Σκοπός των συστημάτων ανάκτησης θερμότητας είναι η αξιοποίηση
ΣΥΝΔΥΑΣΜΟΣ ΤΗΣ ΑΝΤΙΣΤΑΣΗΣ ΔΙΑΧΥΣΗΣ ΣΤΟΥΣ ΠΟΡΟΥΣ ΜΕ ΚΙΝΗΤΙΚΗ ΕΠΙΦΑΝΕΙΑΚΗΣ ΑΝΤΙΔΡΑΣΗΣ
 ΣΥΝΔΥΑΣΜΟΣ ΤΗΣ ΑΝΤΙΣΤΑΣΗΣ ΔΙΑΧΥΣΗΣ ΣΤΟΥΣ ΠΟΡΟΥΣ ΜΕ ΚΙΝΗΤΙΚΗ ΕΠΙΦΑΝΕΙΑΚΗΣ ΑΝΤΙΔΡΑΣΗΣ Παράγοντας Αποτελεσματικότητας Ειδικά για αντίδραση πρώτης τάξης, ο παράγοντας αποτελεσματικότητας ισούται προς ε = C
ΣΥΝΔΥΑΣΜΟΣ ΤΗΣ ΑΝΤΙΣΤΑΣΗΣ ΔΙΑΧΥΣΗΣ ΣΤΟΥΣ ΠΟΡΟΥΣ ΜΕ ΚΙΝΗΤΙΚΗ ΕΠΙΦΑΝΕΙΑΚΗΣ ΑΝΤΙΔΡΑΣΗΣ Παράγοντας Αποτελεσματικότητας Ειδικά για αντίδραση πρώτης τάξης, ο παράγοντας αποτελεσματικότητας ισούται προς ε = C
ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ. Μ. Κροκίδα
 ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ Μ. Κροκίδα ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓ. ΣΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Στόχος: Επεξεργασία συγκεκριμένης τροφοδοσίας (ροή
ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ Μ. Κροκίδα ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓ. ΣΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Στόχος: Επεξεργασία συγκεκριμένης τροφοδοσίας (ροή
Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων
 Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
Η ψύξη ενός αερίου ρεύματος είναι δυνατή με αδιαβατική εκτόνωση του. Μπορεί να συμβεί:
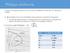 Ψύξη με εκτόνωση Η ψύξη ενός αερίου ρεύματος είναι δυνατή με αδιαβατική εκτόνωση του. Μπορεί να συμβεί: A. Mε ελεύθερη εκτόνωση σε βαλβίδα στραγγαλισμού: ισενθαλπική διεργασία σε χαμηλές θερμοκρασίες,
Ψύξη με εκτόνωση Η ψύξη ενός αερίου ρεύματος είναι δυνατή με αδιαβατική εκτόνωση του. Μπορεί να συμβεί: A. Mε ελεύθερη εκτόνωση σε βαλβίδα στραγγαλισμού: ισενθαλπική διεργασία σε χαμηλές θερμοκρασίες,
1. ΔΙΕΡΓΑΣΙΕΣ ΔΙΑΧΩΡΙΣΜΟΥ (γενική περιγραφή και αναγκαιότητα) 17
 ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ 13 1. ΔΙΕΡΓΑΣΙΕΣ ΔΙΑΧΩΡΙΣΜΟΥ (γενική περιγραφή και αναγκαιότητα) 17 1.1 Φυσικές Διεργασίες Διαχωρισμού 20 1.1.1 Μια γενική εποπτεία της παραγωγικής Χημικής Βιομηχανίας 21 1.1.2 Σύντομος
ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ 13 1. ΔΙΕΡΓΑΣΙΕΣ ΔΙΑΧΩΡΙΣΜΟΥ (γενική περιγραφή και αναγκαιότητα) 17 1.1 Φυσικές Διεργασίες Διαχωρισμού 20 1.1.1 Μια γενική εποπτεία της παραγωγικής Χημικής Βιομηχανίας 21 1.1.2 Σύντομος
Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ
 Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 poulios@chem.auth.gr photocatalysisgroup.web.auth.gr ΚΡΑΜΑΤΑ Χρώμα κραμάτων αποτελούμενα από Χρυσό (Au),
Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 poulios@chem.auth.gr photocatalysisgroup.web.auth.gr ΚΡΑΜΑΤΑ Χρώμα κραμάτων αποτελούμενα από Χρυσό (Au),
ΘΕΡΜΟΔΥΝΑΜΙΚΗ. Χαροκόπειο Πανεπιστήμιο. 11 Μαΐου 2006
 ΘΕΡΜΟΔΥΝΑΜΙΚΗ Χαροκόπειο Πανεπιστήμιο 11 Μαΐου 2006 Κλάδοι της Θερμοδυναμικής Χημική Θερμοδυναμική: Μελετά τις μετατροπές ενέργειας που συνοδεύουν φυσικά ή χημικά φαινόμενα Θερμοχημεία: Κλάδος της Χημικής
ΘΕΡΜΟΔΥΝΑΜΙΚΗ Χαροκόπειο Πανεπιστήμιο 11 Μαΐου 2006 Κλάδοι της Θερμοδυναμικής Χημική Θερμοδυναμική: Μελετά τις μετατροπές ενέργειας που συνοδεύουν φυσικά ή χημικά φαινόμενα Θερμοχημεία: Κλάδος της Χημικής
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Χημική Κινητική Γενικές Υποδείξεις 1. Τάξη Αντίδρασης 2. Ενέργεια Ενεργοποίησης
 Χημική Κινητική Γενικές Υποδείξεις 1. Τάξη Αντίδρασης Γενικά, όταν έχουμε δεδομένα συγκέντρωσης-χρόνου και θέλουμε να βρούμε την τάξη μιας αντίδρασης, προσπαθούμε να προσαρμόσουμε τα δεδομένα σε εξισώσεις
Χημική Κινητική Γενικές Υποδείξεις 1. Τάξη Αντίδρασης Γενικά, όταν έχουμε δεδομένα συγκέντρωσης-χρόνου και θέλουμε να βρούμε την τάξη μιας αντίδρασης, προσπαθούμε να προσαρμόσουμε τα δεδομένα σε εξισώσεις
Δ' Εξάμηνο ΦΥΣΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ. Ερωτήσεις Επανάληψης
 Δ' Εξάμηνο ΦΥΣΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ Ερωτήσεις Επανάληψης 1 0.8 0.6 x D = 0.95 y 0.4 x F = 0.45 0.2 0 0 0.2 0.4 0.6 0.8 1 x B = 0.05 Σχήμα 1. Δεδομένα ισορροπίας y-x για δυαδικό μίγμα συστατικών Α και Β και οι
Δ' Εξάμηνο ΦΥΣΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ Ερωτήσεις Επανάληψης 1 0.8 0.6 x D = 0.95 y 0.4 x F = 0.45 0.2 0 0 0.2 0.4 0.6 0.8 1 x B = 0.05 Σχήμα 1. Δεδομένα ισορροπίας y-x για δυαδικό μίγμα συστατικών Α και Β και οι
Ειδική Ενθαλπία, Ειδική Θερµότητα και Ειδικός Όγκος Υγρού Αέρα
 θερµοκρασία που αντιπροσωπεύει την θερµοκρασία υγρού βολβού. Το ποσοστό κορεσµού υπολογίζεται από την καµπύλη του σταθερού ποσοστού κορεσµού που διέρχεται από το συγκεκριµένο σηµείο. Η απόλυτη υγρασία
θερµοκρασία που αντιπροσωπεύει την θερµοκρασία υγρού βολβού. Το ποσοστό κορεσµού υπολογίζεται από την καµπύλη του σταθερού ποσοστού κορεσµού που διέρχεται από το συγκεκριµένο σηµείο. Η απόλυτη υγρασία
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ
 ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ
 . ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ ΣΩΤΗΡΗΣ ΤΣΙΒΙΛΗΣ, Καθ. ΕΜΠ 135 ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ 1 2 3 4 1 στερεό (solid) 2 υγρό (liquid) 3 ατμός (vapor) 4 αέριο (gas) A 1+2+3
. ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΟΛΥΦΑΣΙΚΑ ΣΥΣΤΗΜΑΤΑ ΣΩΤΗΡΗΣ ΤΣΙΒΙΛΗΣ, Καθ. ΕΜΠ 135 ΔΙΑΓΡΑΜΜΑΤΑ ΦΑΣΕΩΝ 1 2 3 4 1 στερεό (solid) 2 υγρό (liquid) 3 ατμός (vapor) 4 αέριο (gas) A 1+2+3
Χημικές Διεργασίες: Εισαγωγή
 : Εισαγωγή Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση - Αφυδρογόνωση - Πυρόλυση - Ενυδάτωση κλπ Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση
: Εισαγωγή Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση - Αφυδρογόνωση - Πυρόλυση - Ενυδάτωση κλπ Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση
ΜΗΧΑΝΙΚΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΔΙΕΡΓΑΣΙΩΝ
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΜΗΧΑΝΙΚΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΔΙΕΡΓΑΣΙΩΝ ΟΔΗΓΙΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΥΓΡΗΣ ΕΚΧΥΛΙΣΗΣ Ελένη Παντελή, Υποψήφια Διδάκτορας Γεωργία Παππά, Δρ. Χημικός Μηχανικός
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΜΗΧΑΝΙΚΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΔΙΕΡΓΑΣΙΩΝ ΟΔΗΓΙΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΥΓΡΗΣ ΕΚΧΥΛΙΣΗΣ Ελένη Παντελή, Υποψήφια Διδάκτορας Γεωργία Παππά, Δρ. Χημικός Μηχανικός
Παράδειγμα 2-1. Διαχωρισμός νερού- αιθανόλης
 Παράδειγμα 2-1. Διαχωρισμός νερού- αιθανόλης Μια αποστακτική στήλη που λειτουργεί σε πίεση 101,3 kpa, διαχωρίζει ένα μίγμα νερούαιθανόλης. Η σύσταση του μίγματος αποτελείται 40 mol% αιθανόλη και η τροφοδοσία
Παράδειγμα 2-1. Διαχωρισμός νερού- αιθανόλης Μια αποστακτική στήλη που λειτουργεί σε πίεση 101,3 kpa, διαχωρίζει ένα μίγμα νερούαιθανόλης. Η σύσταση του μίγματος αποτελείται 40 mol% αιθανόλη και η τροφοδοσία
ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΕΤΑΔΟΣΗ ΘΕΡΜΟΤΗΤΑΣ
 ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΕΤΑΔΟΣΗ ΘΕΡΜΟΤΗΤΑΣ Η Επιστήμη της Θερμοδυναμικής ασχολείται με την ποσότητα της θερμότητας που μεταφέρεται σε ένα κλειστό και απομονωμένο σύστημα από μια κατάσταση ισορροπίας σε μια άλλη
ΕΙΣΑΓΩΓΗ ΣΤΗ ΜΕΤΑΔΟΣΗ ΘΕΡΜΟΤΗΤΑΣ Η Επιστήμη της Θερμοδυναμικής ασχολείται με την ποσότητα της θερμότητας που μεταφέρεται σε ένα κλειστό και απομονωμένο σύστημα από μια κατάσταση ισορροπίας σε μια άλλη
ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ. Μ. Κροκίδα
 ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ Μ. Κροκίδα ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓ. ΣΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διαφορική (batch) Rectifying column Stripping column
ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΙΙ Μ. Κροκίδα ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓ. ΣΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διαφορική (batch) Rectifying column Stripping column
M V n. nm V. M v. M v T P P S V P = = + = σταθερή σε παραγώγιση, τον ορισµό του συντελεστή διαστολής α = 1, κυκλική εναλλαγή 3
 Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος εκεµβρίου 04- (//04. ίνονται οι ακόλουθες πληροφορίες για τον διθειάνθρακα (CS. Γραµµοµοριακή µάζα 76.4 g/mol, κανονικό σηµείο ζέσεως 46 C, κανονικό
Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος εκεµβρίου 04- (//04. ίνονται οι ακόλουθες πληροφορίες για τον διθειάνθρακα (CS. Γραµµοµοριακή µάζα 76.4 g/mol, κανονικό σηµείο ζέσεως 46 C, κανονικό
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ
 ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ 2 Διεργασίες Πολυφασικών συστημάτων Πολλές διεργασίες στη Χημική Μηχανική στηρίζονται στη μεταφορά μάζας μεταξύ διαφορετικών φάσεων (αέρια, υγρή, στερεή) Εξάτμιση-Εξάχνωση
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΚΑΙ ΤΑΣΗ ΑΤΜΩΝ 2 Διεργασίες Πολυφασικών συστημάτων Πολλές διεργασίες στη Χημική Μηχανική στηρίζονται στη μεταφορά μάζας μεταξύ διαφορετικών φάσεων (αέρια, υγρή, στερεή) Εξάτμιση-Εξάχνωση
ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΙΔΑΝΙΚΩΝ ΑΝΤΙΔΡΑΣΤΗΡΩΝ ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΙΔΑΝΙΚΩΝ ΑΝΤΙΔΡΑΣΤΗΡΩΝ
 Εισαγωγή Διαδικασία σχεδιασμού αντιδραστήρα: Καθορισμός του τύπου του αντιδραστήρα και των συνθηκών λειτουργίας. Εκτίμηση των χαρακτηριστικών για την ομαλή λειτουργία του αντιδραστήρα. μέγεθος σύσταση
Εισαγωγή Διαδικασία σχεδιασμού αντιδραστήρα: Καθορισμός του τύπου του αντιδραστήρα και των συνθηκών λειτουργίας. Εκτίμηση των χαρακτηριστικών για την ομαλή λειτουργία του αντιδραστήρα. μέγεθος σύσταση
ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΚΑΙ ΕΝΕΡΓΕΙΑΣ. Στην βιομηχανία τροφίμων προκύπτουν ερωτήματα για:
 ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΚΑΙ ΕΝΕΡΓΕΙΑΣ Στην βιομηχανία τροφίμων προκύπτουν ερωτήματα για: Πληροφορίες για τις απαιτήσεις σε υλικά και πρώτες ύλες Πληροφορίες για τον όγκο παραγωγής Πληροφορίες
ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΚΑΙ ΕΝΕΡΓΕΙΑΣ Στην βιομηχανία τροφίμων προκύπτουν ερωτήματα για: Πληροφορίες για τις απαιτήσεις σε υλικά και πρώτες ύλες Πληροφορίες για τον όγκο παραγωγής Πληροφορίες
ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ Equilibrium or Flash Distillation
 Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ Equilibrium or Flash Distillation ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ 1. ΟΡΙΣΜΟΣ ΣΚΟΠΟΣ ΔΙΕΡΓΑΣΙΑΣ
Associate. Prof. M. Krokida School of Chemical Engineering National Technical University of Athens ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ Equilibrium or Flash Distillation ΑΠΟΣΤΑΞΗ ΙΣΟΡΡΟΠΙΑΣ 1. ΟΡΙΣΜΟΣ ΣΚΟΠΟΣ ΔΙΕΡΓΑΣΙΑΣ
Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου (21/6/2017)
 Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου -7 (//7). Δίνεται η θεμελιώδης εξίσωση για την εσωτερική ενέργεια ενός συστήματος ενός συστατικού όπου κατάλληλη σταθερά. Να προσδιορίσετε
Τμήμα Χημείας Μάθημα: Φυσικοχημεία Ι Εξέταση: Περίοδος Ιουνίου -7 (//7). Δίνεται η θεμελιώδης εξίσωση για την εσωτερική ενέργεια ενός συστήματος ενός συστατικού όπου κατάλληλη σταθερά. Να προσδιορίσετε
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας
 Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
panagiotisathanasopoulos.gr
 Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΔΙΕΡΓΑΣΙΩΝ ΔΙΑΧΩΡΙΣΜΟΥ ΜΑΔ, 2013
 ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΔΙΕΡΓΑΣΙΩΝ ΔΙΑΧΩΡΙΣΜΟΥ ΜΑΔ, 2013 1 Ισορροπία Φάσεων Ανάλογα με τη φύση των συστατικών του μίγματος (ή της ολικής πίεσης του συστήματος) οι τάσεις διαφυγής υπολογίζονται - ανάλογα
ΑΝΑΛΥΣΗ ΚΑΙ ΣΧΕΔΙΑΣΜΟΣ ΔΙΕΡΓΑΣΙΩΝ ΔΙΑΧΩΡΙΣΜΟΥ ΜΑΔ, 2013 1 Ισορροπία Φάσεων Ανάλογα με τη φύση των συστατικών του μίγματος (ή της ολικής πίεσης του συστήματος) οι τάσεις διαφυγής υπολογίζονται - ανάλογα
ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι
 ΦΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 6 η - Β ΜΕΡΟΣ ΔΙΑΛΜΑΤΑ Όνομα καθηγητή: ΕΑΓΓΕΛΙΟ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟ ΜΑΘΗΜΑΤΟΣ Στόχος (): Κατανόηση των εννοιών: υγρά διαλύματα,
ΦΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 6 η - Β ΜΕΡΟΣ ΔΙΑΛΜΑΤΑ Όνομα καθηγητή: ΕΑΓΓΕΛΙΟ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟ ΜΑΘΗΜΑΤΟΣ Στόχος (): Κατανόηση των εννοιών: υγρά διαλύματα,
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις. Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι
 Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
Ανάλυση Τροφίμων. Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Διαλύματα Τα ομοιογενή μίγματα
Ανάλυση Τροφίμων Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Διαλύματα Τα ομοιογενή μίγματα
Είδη ΙΦΥΥ δυαδικών μιγμάτων
 Είδη ΙΦΥΥ δυαδικών μιγμάτων T A X 1 X 1 ΙΦΥΥ τριαδικών μιγμάτων Τριγωνικά διαγράμματα C 0.1 0.2 0.3 0.4 0.5 P 0.9 0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 0.6 0.7 0.8 0.9 κλάσμα βάρους του B κλάσμα βάρους του C
Είδη ΙΦΥΥ δυαδικών μιγμάτων T A X 1 X 1 ΙΦΥΥ τριαδικών μιγμάτων Τριγωνικά διαγράμματα C 0.1 0.2 0.3 0.4 0.5 P 0.9 0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 0.6 0.7 0.8 0.9 κλάσμα βάρους του B κλάσμα βάρους του C
ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ (ΣΤΕΦ) ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΚΑΙ ΜΗΧΑΝΙΚΩΝ ΑΝΤΙΡΡΥΠΑΝΣΗΣ ΚΑΤΕΥΘΥΝΣΗ ΜΗΧΑΝΙΚΩΝ ΑΝΤΙΡΡΥΠΑΝΣΗΣ Τ.Ε.
 ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ (ΣΤΕΦ) ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΚΑΙ ΜΗΧΑΝΙΚΩΝ ΑΝΤΙΡΡΥΠΑΝΣΗΣ ΚΑΤΕΥΘΥΝΣΗ ΜΗΧΑΝΙΚΩΝ ΑΝΤΙΡΡΥΠΑΝΣΗΣ Τ.Ε. ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΣ, 2016 Μάθημα: «Αντιρρυπαντική Τεχνολογία
ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΚΩΝ ΕΦΑΡΜΟΓΩΝ (ΣΤΕΦ) ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΚΑΙ ΜΗΧΑΝΙΚΩΝ ΑΝΤΙΡΡΥΠΑΝΣΗΣ ΚΑΤΕΥΘΥΝΣΗ ΜΗΧΑΝΙΚΩΝ ΑΝΤΙΡΡΥΠΑΝΣΗΣ Τ.Ε. ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΣ, 2016 Μάθημα: «Αντιρρυπαντική Τεχνολογία
Ακρίβεια αποτελεσμάτων σχεδιασμού διεργασιών ΜΑΔ, 2013
 Ακρίβεια αποτελεσμάτων σχεδιασμού διεργασιών ΜΑΔ, 2013 1 ΣΚΟΠΟΣ και ΑΝΤΙΚΕΙΜΕΝΟ ΘΧΜ Σκοπός της θερμοδυναμικής χημικής μηχανικής είναι η παροχή των κατάλληλων θεωρητικών γνώσεων και των απαραίτητων υπολογιστικών-μεθοδολογικών
Ακρίβεια αποτελεσμάτων σχεδιασμού διεργασιών ΜΑΔ, 2013 1 ΣΚΟΠΟΣ και ΑΝΤΙΚΕΙΜΕΝΟ ΘΧΜ Σκοπός της θερμοδυναμικής χημικής μηχανικής είναι η παροχή των κατάλληλων θεωρητικών γνώσεων και των απαραίτητων υπολογιστικών-μεθοδολογικών
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
Υπολογισµοί του Χρόνου Ξήρανσης
 Η πραγµατική επιφάνεια ξήρανσης είναι διασπαρµένη και ασυνεχής και ο µηχανισµός από τον οποίο ελέγχεται ο ρυθµός ξήρανσης συνίσταται στην διάχυση της θερµότητας και της µάζας µέσα από το πορώδες στερεό.
Η πραγµατική επιφάνεια ξήρανσης είναι διασπαρµένη και ασυνεχής και ο µηχανισµός από τον οποίο ελέγχεται ο ρυθµός ξήρανσης συνίσταται στην διάχυση της θερµότητας και της µάζας µέσα από το πορώδες στερεό.
ΚΕΦΑΛΑΙΟ 4 ΑΠΟΡΡΟΦΗΣΗ- ΕΚΡΟΦΗΣΗ ΑΕΡΙΩΝ
 ΚΕΦΑΛΑΙΟ 4 ΑΠΟΡΡΟΦΗΣΗ- ΕΚΡΟΦΗΣΗ ΑΕΡΙΩΝ Η απορρόφηση αερίων είναι η διεργασία κατά την οποία μία ή περισσότερες συνιστώσες ενός αέριου μείγματος διαλύονται κατά την επαφή με ένα υγρό (Beet & Mers, 96).
ΚΕΦΑΛΑΙΟ 4 ΑΠΟΡΡΟΦΗΣΗ- ΕΚΡΟΦΗΣΗ ΑΕΡΙΩΝ Η απορρόφηση αερίων είναι η διεργασία κατά την οποία μία ή περισσότερες συνιστώσες ενός αέριου μείγματος διαλύονται κατά την επαφή με ένα υγρό (Beet & Mers, 96).
ΑΝΑΛΥΣΗ ΣΥΣΤΗΜΑΤΩΝ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ
 ΑΝΑΛΥΣΗ ΣΥΣΤΗΜΑΤΩΝ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ 2015-2016 2 Ο ΕΞΑΜΗΝΟ Ε. ΠΑΥΛΑΤΟΥ ΑΝ. ΚΑΘΗΓΗΤΡΙΑ ΕΜΠ ΜΟΝΑΔΕΣ ΒΑΣΙΚΕΣ ΚΑΙ ΠΑΡΑΓΟΜΕΝΕΣ ΔΙΑΣΤΑΣΕΙΣ 3 ΒΑΣΙΚΕΣ ΚΑΙ ΠΑΡΑΓΟΜΕΝΕΣ ΔΙΑΣΤΑΣΕΙΣ 4 ΠΑΡΑΓΟΜΕΝΕΣ ΔΙΑΣΤΑΣΕΙΣ 5 Επιφάνεια
ΑΝΑΛΥΣΗ ΣΥΣΤΗΜΑΤΩΝ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ 2015-2016 2 Ο ΕΞΑΜΗΝΟ Ε. ΠΑΥΛΑΤΟΥ ΑΝ. ΚΑΘΗΓΗΤΡΙΑ ΕΜΠ ΜΟΝΑΔΕΣ ΒΑΣΙΚΕΣ ΚΑΙ ΠΑΡΑΓΟΜΕΝΕΣ ΔΙΑΣΤΑΣΕΙΣ 3 ΒΑΣΙΚΕΣ ΚΑΙ ΠΑΡΑΓΟΜΕΝΕΣ ΔΙΑΣΤΑΣΕΙΣ 4 ΠΑΡΑΓΟΜΕΝΕΣ ΔΙΑΣΤΑΣΕΙΣ 5 Επιφάνεια
ΘΕΡΜΟΧΗΜΕΙΑ. Είδη ενέργειας ΘΕΡΜΟΔΥΝΑΜΙΚΟΙ ΟΡΙΣΜΟΙ
 ΘΕΡΜΟΧΗΜΕΙΑ Όλες οι χημικές αντιδράσεις περιλαμβάνουν έκλυση ή απορρόφηση ενέργειας υπό μορφή θερμότητας. Η γνώση του ποσού θερμότητας που συνδέεται με μια χημική αντίδραση έχει και πρακτική και θεωρητική
ΘΕΡΜΟΧΗΜΕΙΑ Όλες οι χημικές αντιδράσεις περιλαμβάνουν έκλυση ή απορρόφηση ενέργειας υπό μορφή θερμότητας. Η γνώση του ποσού θερμότητας που συνδέεται με μια χημική αντίδραση έχει και πρακτική και θεωρητική
v = 1 ρ. (2) website:
 Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Τμήμα Φυσικής Μηχανική Ρευστών Βασικές έννοιες στη μηχανική των ρευστών Μαάιτα Τζαμάλ-Οδυσσέας 17 Φεβρουαρίου 2019 1 Ιδιότητες των ρευστών 1.1 Πυκνότητα Πυκνότητα
Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Τμήμα Φυσικής Μηχανική Ρευστών Βασικές έννοιες στη μηχανική των ρευστών Μαάιτα Τζαμάλ-Οδυσσέας 17 Φεβρουαρίου 2019 1 Ιδιότητες των ρευστών 1.1 Πυκνότητα Πυκνότητα
ΜΑΘΗΜΑ: Τεχνολογία Μετρήσεων ΙΙ
 ΜΑΘΗΜΑ: Τεχνολογία Μετρήσεων ΙΙ ΔΙΔΑΣΚΩΝ: Αν. Καθ. Δρ Μαρία Α. Γούλα ΤΜΗΜΑ: Μηχανικών Περιβάλλοντος & Μηχανικών Αντιρρύπανσης 1 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΜΑΘΗΜΑ: Τεχνολογία Μετρήσεων ΙΙ ΔΙΔΑΣΚΩΝ: Αν. Καθ. Δρ Μαρία Α. Γούλα ΤΜΗΜΑ: Μηχανικών Περιβάλλοντος & Μηχανικών Αντιρρύπανσης 1 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Κεφάλαιο 5 Eναλλάκτες Θερμότητας
 Κεφάλαιο 5 Eναλλάκτες Θερμότητας 5. Εισαγωγή Σε πολλές εφαρμογές απαιτείται η μετάδοση θερμότητας μεταξύ δύο ρευστών. Οι διεργασίες αυτές λαμβάνουν χώρα σε συσκευές που αποκαλούνται εναλλάκτες θερμότητας
Κεφάλαιο 5 Eναλλάκτες Θερμότητας 5. Εισαγωγή Σε πολλές εφαρμογές απαιτείται η μετάδοση θερμότητας μεταξύ δύο ρευστών. Οι διεργασίες αυτές λαμβάνουν χώρα σε συσκευές που αποκαλούνται εναλλάκτες θερμότητας
Παρασκευαστικό διαχωρισμό πολλών ουσιών με κατανομή μεταξύ των δύο διαλυτών.
 1. ΕΚΧΥΛΙΣΗ Η εκχύλιση είναι μία από τις πιο συνηθισμένες τεχνικές διαχωρισμού και βασίζεται στην ισορροπία κατανομής μιας ουσίας μεταξύ δύο φάσεων, που αναμιγνύονται ελάχιστα μεταξύ τους. Η ευρύτητα στη
1. ΕΚΧΥΛΙΣΗ Η εκχύλιση είναι μία από τις πιο συνηθισμένες τεχνικές διαχωρισμού και βασίζεται στην ισορροπία κατανομής μιας ουσίας μεταξύ δύο φάσεων, που αναμιγνύονται ελάχιστα μεταξύ τους. Η ευρύτητα στη
4.2 Παρα γοντες που επηρεα ζουν τη θε ση χημικη ς ισορροπι ας - Αρχη Le Chatelier
 Χημικός Διδάκτωρ Παν. Πατρών 4.2 Παρα γοντες που επηρεα ζουν τη θε ση χημικη ς ισορροπι ας - Αρχη Le Chatelier Τι ονομάζεται θέση χημικής ισορροπίας; Από ποιους παράγοντες επηρεάζεται η θέση της χημικής
Χημικός Διδάκτωρ Παν. Πατρών 4.2 Παρα γοντες που επηρεα ζουν τη θε ση χημικη ς ισορροπι ας - Αρχη Le Chatelier Τι ονομάζεται θέση χημικής ισορροπίας; Από ποιους παράγοντες επηρεάζεται η θέση της χημικής
ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ
 Θέματα Πανελλ. Εξετάσεων Χημείας Προσανατολισμού Β Λυκείου 1 ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1984 2004 (Περιέχει όσα από τα θέματα αναφέρονται στην ύλη της
Θέματα Πανελλ. Εξετάσεων Χημείας Προσανατολισμού Β Λυκείου 1 ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1984 2004 (Περιέχει όσα από τα θέματα αναφέρονται στην ύλη της
Σχεδιασμός Χημικών Διεργασιών και Βιομηχανιών Διάλεξη 6
 Σχεδιασμός Χημικών Διεργασιών και Βιομηχανιών Διάλεξη 6 Δευτέρα, 14 Απριλίου 008 Οικονομική Ανάλυση Βιομηχανιών και Διεργασιών 1 Εισαγωγή Αριστοποίηση: ενός κριτηρίου (αντικειμενικής συνάρτησης) πολυκριτηριακή
Σχεδιασμός Χημικών Διεργασιών και Βιομηχανιών Διάλεξη 6 Δευτέρα, 14 Απριλίου 008 Οικονομική Ανάλυση Βιομηχανιών και Διεργασιών 1 Εισαγωγή Αριστοποίηση: ενός κριτηρίου (αντικειμενικής συνάρτησης) πολυκριτηριακή
ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Ι & ΙΙ Εργαστηριακή Άσκηση 4: ΚΛΑΣΜΑΤΙΚΗ ΑΠΟΣΤΑΞΗ
 Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
1. Στοιχεία Μεταφοράς Μάζας και Εξισώσεις Διατήρησης
 Εθνικό Μετσόβιο Πολυτεχνείο Σχολή Μηχανολόγων Μηχανικών Ετερογενή Μείγματα & Συστήματα Καύσης 1. Στοιχεία Μεταφοράς Μάζας και Εξισώσεις Διατήρησης Δ. Κολαΐτης Μ. Φούντη Δ.Π.Μ.Σ. «Υπολογιστική Μηχανική»
Εθνικό Μετσόβιο Πολυτεχνείο Σχολή Μηχανολόγων Μηχανικών Ετερογενή Μείγματα & Συστήματα Καύσης 1. Στοιχεία Μεταφοράς Μάζας και Εξισώσεις Διατήρησης Δ. Κολαΐτης Μ. Φούντη Δ.Π.Μ.Σ. «Υπολογιστική Μηχανική»
Φυσικοί μετασχηματισμοί καθαρών ουσιών
 Φυσικοί μετασχηματισμοί καθαρών ουσιών Ή εξάτμιση, η τήξη και η μετατροπή του γραφίτη σε διαμάντι αποτελούν συνηθισμένα παραδείγματα αλλαγών φάσης χωρίς μεταβολή της χημικής σύστασης. Ορισμός φάσης: Μια
Φυσικοί μετασχηματισμοί καθαρών ουσιών Ή εξάτμιση, η τήξη και η μετατροπή του γραφίτη σε διαμάντι αποτελούν συνηθισμένα παραδείγματα αλλαγών φάσης χωρίς μεταβολή της χημικής σύστασης. Ορισμός φάσης: Μια
ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΙΙ. Διδάσκων: Παπασιώπη Νυμφοδώρα Αναπληρώτρια Καθηγήτρια Ε.Μ.Π. Ενότητα 9 η : Μεταφορά Μάζας. Διάχυση Νόμος Fick
 ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΙΙ Διδάσκων: Παπασιώπη Νυμφοδώρα Αναπληρώτρια Καθηγήτρια Ε.Μ.Π. Ενότητα 9 η : Μεταφορά Μάζας. Διάχυση Νόμος Fck Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creatve
ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΙΙ Διδάσκων: Παπασιώπη Νυμφοδώρα Αναπληρώτρια Καθηγήτρια Ε.Μ.Π. Ενότητα 9 η : Μεταφορά Μάζας. Διάχυση Νόμος Fck Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creatve
Για την επίλυση αυτής της άσκησης, αλλά και όλων των παρόμοιων χρησιμοποιούμε ιδιότητες των αναλογιών (χιαστί)
 ΜΕΘΟΔΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΔΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυμάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούμε ή
ΜΕΘΟΔΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΔΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυμάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούμε ή
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου /3
 Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΚΑΙ ΕΝΕΡΓΕΙΑΣ. Προσδιορισµός ισοζυγίων µάζας
 ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΚΑΙ ΕΝΕΡΓΕΙΑΣ Προσδιορισµός ισοζυγίων µάζας Κατά τον προσδιορισµό των ισοζυγίων µάζας γίνεται εφαρµογή του νόµου διατήρησης της µάζας στην επίλυση προβληµάτων που αναφέρονται:
ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΚΑΙ ΕΝΕΡΓΕΙΑΣ Προσδιορισµός ισοζυγίων µάζας Κατά τον προσδιορισµό των ισοζυγίων µάζας γίνεται εφαρµογή του νόµου διατήρησης της µάζας στην επίλυση προβληµάτων που αναφέρονται:
Χειμερινό εξάμηνο
 Μεταβατική Αγωγή Θερμότητας: Ανάλυση Ολοκληρωτικού Συστήματος Τμήμα Μηχανολόγων Μηχανικών και Μηχανικών Παραγωγής 1 Μεταβατική Αγωγή (ranen conducon Πολλά προβλήματα μεταφοράς θερμότητας εξαρτώνται από
Μεταβατική Αγωγή Θερμότητας: Ανάλυση Ολοκληρωτικού Συστήματος Τμήμα Μηχανολόγων Μηχανικών και Μηχανικών Παραγωγής 1 Μεταβατική Αγωγή (ranen conducon Πολλά προβλήματα μεταφοράς θερμότητας εξαρτώνται από
ΕΡΓΑΣΤΗΡΙΟ 8 (ΦΡΟΝΤΙΣΤΗΡΙΟ) ΦΑΣΜΑΤΟΦΩΤΟΜΕΤΡΙΚΗ ΑΝΑΛΥΣΗ
 ΕΡΓΑΣΤΗΡΙΟ 8 (ΦΡΟΝΤΙΣΤΗΡΙΟ) ΦΑΣΜΑΤΟΦΩΤΟΜΕΤΡΙΚΗ ΑΝΑΛΥΣΗ Με τον όρο αυτό ονοµάζουµε την τεχνική ποιοτικής και ποσοτικής ανάλυσης ουσιών µε βάση το µήκος κύµατος και το ποσοστό απορρόφησης της ακτινοβολίας
ΕΡΓΑΣΤΗΡΙΟ 8 (ΦΡΟΝΤΙΣΤΗΡΙΟ) ΦΑΣΜΑΤΟΦΩΤΟΜΕΤΡΙΚΗ ΑΝΑΛΥΣΗ Με τον όρο αυτό ονοµάζουµε την τεχνική ποιοτικής και ποσοτικής ανάλυσης ουσιών µε βάση το µήκος κύµατος και το ποσοστό απορρόφησης της ακτινοβολίας
ΕΞΑΤΜΙΣΗ Θοδωρής Καραπάντσιος
 ΕΞ ΕΞΑΤΜΙΣΗ Θοδωρής Καραπάντσιος ΕΞ.1 Εισαγωγή Αντικείµενο της συµπύκνωσης είναι κατά κύριο λόγο η αποµάκρυνση νερού, µε εξάτµιση, από ένα υδατικό διάλυµα που περιέχει µια ή περισσότερες διαλυµένες ουσίες,
ΕΞ ΕΞΑΤΜΙΣΗ Θοδωρής Καραπάντσιος ΕΞ.1 Εισαγωγή Αντικείµενο της συµπύκνωσης είναι κατά κύριο λόγο η αποµάκρυνση νερού, µε εξάτµιση, από ένα υδατικό διάλυµα που περιέχει µια ή περισσότερες διαλυµένες ουσίες,
Τ, Κ Η 2 Ο(g) CΟ(g) CO 2 (g) Λύση Για τη συγκεκριμένη αντίδραση στους 1300 Κ έχουμε:
 ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ - ΑΣΚΗΣΕΙΣ 5-6 (Α. Χημική Θερμοδυναμική) η Άσκηση Η αντίδραση CO(g) + H O(g) CO (g) + H (g) γίνεται σε θερμοκρασία 3 Κ. Να υπολογιστεί το κλάσμα των ατμών του
ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ - ΑΣΚΗΣΕΙΣ 5-6 (Α. Χημική Θερμοδυναμική) η Άσκηση Η αντίδραση CO(g) + H O(g) CO (g) + H (g) γίνεται σε θερμοκρασία 3 Κ. Να υπολογιστεί το κλάσμα των ατμών του
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΚΑΙ ΒΙΟΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ
 ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΚΑΙ ΒΙΟΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Διδάσκοντες:Ν. Καλογεράκης Π. Παναγιωτοπούλου Γραφείο: K.9 Email: ppanagiotopoulou@isc.tuc.gr Μέρες/Ώρες διδασκαλίας: Δευτέρα (.-3.)-Τρίτη (.-3.) ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΚΑΙ ΒΙΟΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Διδάσκοντες:Ν. Καλογεράκης Π. Παναγιωτοπούλου Γραφείο: K.9 Email: ppanagiotopoulou@isc.tuc.gr Μέρες/Ώρες διδασκαλίας: Δευτέρα (.-3.)-Τρίτη (.-3.) ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
ΑΣΚΗΣΕΙΣ ΣΥΣΚΕΥΩΝ ΘΕΡΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ. 1η ενότητα
 1η ενότητα 1. Εναλλάκτης σχεδιάζεται ώστε να θερμαίνει 2kg/s νερού από τους 20 στους 60 C. Το θερμό ρευστό είναι επίσης νερό με θερμοκρασία εισόδου 95 C. Οι συντελεστές συναγωγής στους αυλούς και το κέλυφος
1η ενότητα 1. Εναλλάκτης σχεδιάζεται ώστε να θερμαίνει 2kg/s νερού από τους 20 στους 60 C. Το θερμό ρευστό είναι επίσης νερό με θερμοκρασία εισόδου 95 C. Οι συντελεστές συναγωγής στους αυλούς και το κέλυφος
6.2. ΤΗΞΗ ΚΑΙ ΠΗΞΗ, ΛΑΝΘΑΝΟΥΣΕΣ ΘΕΡΜΟΤΗΤΕΣ
 45 6.1. ΓΕΝΙΚΑ ΠΕΡΙ ΦΑΣΕΩΝ ΜΕΤΑΤΡΟΠΕΣ ΦΑΣΕΩΝ Όλα τα σώµατα,στερεά -ά-αέρια, που υπάρχουν στη φύση βρίσκονται σε µια από τις τρεις φάσεις ή σε δύο ή και τις τρεις. Όλα τα σώµατα µπορεί να αλλάξουν φάση
45 6.1. ΓΕΝΙΚΑ ΠΕΡΙ ΦΑΣΕΩΝ ΜΕΤΑΤΡΟΠΕΣ ΦΑΣΕΩΝ Όλα τα σώµατα,στερεά -ά-αέρια, που υπάρχουν στη φύση βρίσκονται σε µια από τις τρεις φάσεις ή σε δύο ή και τις τρεις. Όλα τα σώµατα µπορεί να αλλάξουν φάση
1 ΦΥΣΙΚΟ ΦΥΣΙΚ ΧΗΜΕΙΑ Ο ΣΥΣΤΗΜΑΤΩΝ
 1 ΦΥΣΙΚΟΧΗΜΕΙΑ ΣΥΣΤΗΜΑΤΩΝ Φυσικοχημεία συστημάτων 2 «Όμοιος Ό αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη είναι δύο ουσίες τόσο μεγαλύτερη είναι η αμοιβαία διαλυτότητά τους. Οι ανόργανες ενώσεις διαλύονται
1 ΦΥΣΙΚΟΧΗΜΕΙΑ ΣΥΣΤΗΜΑΤΩΝ Φυσικοχημεία συστημάτων 2 «Όμοιος Ό αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη είναι δύο ουσίες τόσο μεγαλύτερη είναι η αμοιβαία διαλυτότητά τους. Οι ανόργανες ενώσεις διαλύονται
Εφαρμοσμένη Θερμοδυναμική: Εξετάζει σχέσεις θερμότητας,
 Στοιχεία Χημικής Θερμοδυναμικής Κλάδοι της Θερμοδυναμικής Θερμοδυναμική: Ο κλάδος της επιστήμης που μελετά τις μετατροπές ενέργειας. Στην πραγματικότητα μετρά μεταβολές ενέργειας. Μελετά τη σχέση μεταξύ
Στοιχεία Χημικής Θερμοδυναμικής Κλάδοι της Θερμοδυναμικής Θερμοδυναμική: Ο κλάδος της επιστήμης που μελετά τις μετατροπές ενέργειας. Στην πραγματικότητα μετρά μεταβολές ενέργειας. Μελετά τη σχέση μεταξύ
Κεφάλαιο 5: Διεργασίες απόσταξης
 92 Κεφάλαιο 5: Διεργασίες απόσταξης Σύνοψη Το κεφάλαιο αυτό συνιστά την πρώτη ολοκληρωμένη ανάλυση μίας διεργασίας. Παρουσιάζονται στην αρχή οι απλές αποστάξεις και στη συνέχεια αναλύεται διεξοδικά η κλασματική
92 Κεφάλαιο 5: Διεργασίες απόσταξης Σύνοψη Το κεφάλαιο αυτό συνιστά την πρώτη ολοκληρωμένη ανάλυση μίας διεργασίας. Παρουσιάζονται στην αρχή οι απλές αποστάξεις και στη συνέχεια αναλύεται διεξοδικά η κλασματική
3 Η ΣΕΙΡΑ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΑΝΑΠΤΥΞΗΣ ΔΙΕΡΓΑΣΙΩΝ - PC-LAB ΗΜΕΡΟΜΗΝΙΑ ΠΑΡΑΔΟΣΗΣ: ΑΣΚΗΣΗ 1 ΠΡΟΣΟΜΟΙΩΣΗ ΜΟΝΑΔΑΣ ΦΥΣΙΚΟΥ ΑΕΡΙΟΥ
 3 Η ΣΕΙΡΑ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΑΝΑΠΤΥΞΗΣ ΔΙΕΡΓΑΣΙΩΝ - PC-LAB ΗΜΕΡΟΜΗΝΙΑ ΠΑΡΑΔΟΣΗΣ: 23.12.2015 ΑΣΚΗΣΗ 1 ΠΡΟΣΟΜΟΙΩΣΗ ΜΟΝΑΔΑΣ ΦΥΣΙΚΟΥ ΑΕΡΙΟΥ Ένα τυπικό φυσικό αέριο έχει την ακόλουθη σύσταση σε % mol: 0.5% Ν 2,
3 Η ΣΕΙΡΑ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΑΝΑΠΤΥΞΗΣ ΔΙΕΡΓΑΣΙΩΝ - PC-LAB ΗΜΕΡΟΜΗΝΙΑ ΠΑΡΑΔΟΣΗΣ: 23.12.2015 ΑΣΚΗΣΗ 1 ΠΡΟΣΟΜΟΙΩΣΗ ΜΟΝΑΔΑΣ ΦΥΣΙΚΟΥ ΑΕΡΙΟΥ Ένα τυπικό φυσικό αέριο έχει την ακόλουθη σύσταση σε % mol: 0.5% Ν 2,
ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 31 ΜΑΪΟΥ 2000 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ
 ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 31 ΜΑΪΟΥ 2000 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΘΕΜΑ 1ο Στις ερωτήσεις 1-3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 31 ΜΑΪΟΥ 2000 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΘΕΜΑ 1ο Στις ερωτήσεις 1-3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης
Σκοπός: Περιγραφή της συμπεριφοράς των νευρικών κυττάρων και ποσοτικά και ποιοτικά.
 Σκοπός: Περιγραφή της συμπεριφοράς των νευρικών κυττάρων και ποσοτικά και ποιοτικά. Τα νευρικά κύτταρα περιβάλλονται από μία πλασματική μεμβράνη της οποίας κύρια λειτουργία είναι να ελέγχει το πέρασμα
Σκοπός: Περιγραφή της συμπεριφοράς των νευρικών κυττάρων και ποσοτικά και ποιοτικά. Τα νευρικά κύτταρα περιβάλλονται από μία πλασματική μεμβράνη της οποίας κύρια λειτουργία είναι να ελέγχει το πέρασμα
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες
 Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις
 Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση 4: Μερικός γραμμομοριακός όγκος Αθανάσιος Τσεκούρας Τμήμα Χημείας . Θεωρία... 3. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 5 4. Τελικά αποτελέσματα... 7 Σελίδα
Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση 4: Μερικός γραμμομοριακός όγκος Αθανάσιος Τσεκούρας Τμήμα Χημείας . Θεωρία... 3. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 5 4. Τελικά αποτελέσματα... 7 Σελίδα
Ε. Παυλάτου, 2017 ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΜΕ ΑΝΤΙΔΡΑΣΗ
 1 ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΜΕ ΑΝΤΙΔΡΑΣΗ 2 ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΜΕ ΑΝΤΙΔΡΑΣΗ Βασικές έννοιες Στοιχειομετρία-Στοιχειομετρικοί συντελεστές-στοιχειομετρική αναλογία Περιοριστικό αντιδρών Αντιδρών σε περίσσεια Μετατροπή (κλάσμα,
1 ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΜΕ ΑΝΤΙΔΡΑΣΗ 2 ΙΣΟΖΥΓΙΑ ΜΑΖΑΣ ΜΕ ΑΝΤΙΔΡΑΣΗ Βασικές έννοιες Στοιχειομετρία-Στοιχειομετρικοί συντελεστές-στοιχειομετρική αναλογία Περιοριστικό αντιδρών Αντιδρών σε περίσσεια Μετατροπή (κλάσμα,
Μηχανική και Ανάπτυξη Διεργασιών
 Μηχανική και Ανάπτυξη Διεργασιών Κωστής Μαγουλάς, Καθηγητής Επαμεινώνδας Βουτσάς, Επ. Καθηγητής 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ . ΟΡΙΣΜΟΣ Οι διαχωρισμοί είναι οι πιο συχνά παρατηρούμενες διεργασίες
Μηχανική και Ανάπτυξη Διεργασιών Κωστής Μαγουλάς, Καθηγητής Επαμεινώνδας Βουτσάς, Επ. Καθηγητής 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ . ΟΡΙΣΜΟΣ Οι διαχωρισμοί είναι οι πιο συχνά παρατηρούμενες διεργασίες
ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ. Καθηγητής Δ. Ματαράς
 ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Καθηγητής Δ. Ματαράς image url 0.Μεταφορά Θερμότητας σε Ρευστά Εναλλάκτης Κελύφους-Αυλών E 2 Β 2 Ατμός F C K Εξαέρωση Β Θερμό Υγρό J E D 2 Α D H Ψυχρό Υγρό Eικόνα
ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Καθηγητής Δ. Ματαράς image url 0.Μεταφορά Θερμότητας σε Ρευστά Εναλλάκτης Κελύφους-Αυλών E 2 Β 2 Ατμός F C K Εξαέρωση Β Θερμό Υγρό J E D 2 Α D H Ψυχρό Υγρό Eικόνα
