PAU XUÑO 2014 QUÍMICA. Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
|
|
|
- Ἁλκυόνη Διαμαντόπουλος
- 6 χρόνια πριν
- Προβολές:
Transcript
1 PAU Código: 27 XUÑO 2014 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A Dados os seguintes elementos: B, O, C e F, ordéneos en orde crecente segundo o primeiro potencial de ionización. Razoe a resposta Agrupe as especies que son isoelectrónicas: O², C, F, Na+, Ge²+, B, Zn. Razoe a resposta Formule: benceno, etanoato de metilo, 2-butanol e nomee: CH₃-CH₂-CH₂-CHO y CH₃-O-CH₃ Razoe o tipo de isomería que presenta o composto 2-hidroxipropanoico, de fórmula química: CH₃-CH(OH)- COOH. Sinale e indique o nome dos grupos funcionais que presenta Considere a seguinte reacción: Br₂(g) 2 Br(g). Cando 1,05 moles de Br₂ colócanse nun matraz de 0,980 L a unha temperatura de 1873 K disóciase o 1,20 % de Br₂. Calcule a constante de equilibrio K da reacción Calcule a masa de cobre que se pode obter ao reaccionar 200 ml de disolución de sulfato de cobre(ll) ao 20 % en peso e densidade 1,10 g ml ¹ co suficiente ferro, tendo en conta que na reacción tamén se produce sulfato de ferro(li) Sabendo que a 25 a K (BaSO₄) é 1,1 10 ¹⁰, determine a solubilidade do sal en g L ¹ Se 250 ml de BaCl₂ 0,0040 M engádense a 500 ml de K₂SO₄ 0,0080 M e supoñendo que os volumes son aditivos, indique se se formará precipitado ou non. 5. A 25 e empregando un eléctrodo de prata e outro de cinc, disolucións de Zn²+(1,0 M) e Ag+(1,0 M) e unha disolución de KNO₃ 2,0 M como ponte salina, constrúese no laboratorio a seguinte pila: Zn(s) Zn²+(aq) Ag+(aq) Ag(s). Datos: E (Zn²+/Zn) = -0,76 V e E (Ag+/Ag) = +0,80 V Escribir as semirreaccións que ocorren en cada eléctrodo e a ecuación da reacción iónica global, calculando tamén a forza electromotriz da pila Faga un debuxo-esquema detallado da pila, indique o ánodo e cátodo, e o sentido no que circulan os electróns, así como os ións da ponte salina. OPCIÓN B Considere o seguinte proceso en equilibrio: N₂F₄(g) 2 NF₂(g); H = 38,5 kj. Razoe que lle ocorre ao equilibrio si diminúese a presión da mestura de reacción a temperatura constante Especifique que orbitais híbridos utiliza o carbono no eteno (C₂H₄), así como o tipo de enlaces que se forman na molécula. Razoe a resposta. 2. Xustifique si estas afirmacións son correctas: 2.1. O produto da constante de ionización dun ácido e a constante de ionización da súa base conxugada é igual á constante do produto iónico do auga A presenza dun ión común diminúe a solubilidade dun sal lixeiramente soluble. 3. No laboratorio pódese preparar cloro gas facendo reaccionar permanganato do potasio sólido con ácido clorhídrico concentrado No transcurso desta reacción redox fórmase cloro, cloruro de manganeso(ll), cloruro de potasio e auga. Escriba e axuste a reacción molecular mediante o método do ión-electrón Calcule o volume de cloro gas, a 20 e 1 atm (101,3 kpa), que se obtén ao facer reaccionar 10 ml de ácido clorhídrico concentrado do 35,2 % en masa e densidade 1,175 g ml ¹ cun exceso de permanganato de potasio. Datos: R = 0,082 atm L K ¹ mol ¹ = 8,31 J K ¹ mol ¹. 4. O nafaleno (C₁₀H₈) é un composto aromático sólido que se vende para combater a couza. A combustión completa deste composto para producir CO₂(g) e H₂O(l) a 25 e 1 atm (101,3 kpa) desprende 5154 kj mol ¹ Escriba as reaccións de formación do nafaleno e a reacción de combustión Calcule a entalpía estándar de formación do nafaleno e interprete o seu signo. Datos: H (CO₂(g)) = -393,5 kj mol ¹; H (H₂O(l)) = -285,8 kj mol ¹ Cantos ml dunha disolución de NaOH 0,610 M necesítanse para neutralizar 20,0 ml dunha disolución de H₂SO₄ 0,245 M? Indique a reacción que ten lugar e xustifique o ph no punto de equivalencia Nomee o material necesario e describa o procedemento experimental para levar a cabo a valoración.
2 Solucións OPCIÓN A 1.- a) Dados os seguintes elementos: B, O, C e F, ordénaos en orde crecente segundo o primeiro potencial de ionización. Razoa a resposta. b) Agrupa as especies que son isoelectrónicas: O², C, F, Na+, Ge²+, B, Zn. Razoa a resposta. a) A enerxía de ionización é a enerxía necesaria para arrincar o electrón máis externo a cada átomo dun mol de átomos dun elemento en fase gasosa e en estado fundamental. Corresponde á entalpía do proceso: A(g) A+(g) + e ΔH = I (= Enerxía de ionización) É unha propiedade periódica. Aumenta a medida que se avanza no período ata facerse máxima para os gases nobres, debido ao aumento da carga nuclear efectiva e a diminución do radio atómico. I(B) < I(C) < I(O) < I(F) b) As especies isoelectrónicas son as que teñen o mesmo número de electróns. Para un átomo neutro, o número de electróns é igual ao número de protóns que se indica no número atómico. Os ións positivos perderon tantos electróns como indica a súa carga e os negativos gañaron electróns. Os números atómicos e número de electróns de cada especie móstrase na seguinte táboa: Especie O² C F Na+ Ge²+ B Zn Número atómico Número de electróns Por tanto son isoelectrónicos: Os ións óxido (O² ), fuoruro (F ) e sodio (Na+) con 10 electróns. O carbono (C) e o ión boruro(1-) (B ), con 6 electróns. O cinc (Zn) e o ión xermanio(ii) (Ge²+) con 30 electróns. 2.- a) Formula: benceno, etanoato de metilo, 2-butanol e nomea: CH₃-CH₂-CH₂-CHO y CH₃-O-CH₃. b) Razoa o tipo de isomería que presenta o composto 2-hidroxipropanoico, de fórmula química: CH₃- CH(OH)-COOH. Sinala e indica o nome dos grupos funcionais que presenta. Rta.: a) Benceno: ; etanoato de metilo: CH₃ COO CH₃; 2-butanol: CH₃ CHOH CH₂ CH₃ CH₃-CH₂-CH₂-CHO: butanal; CH₃-O-CH₃: dimetiléter (ou metoximetano). b) Isomería óptica (o carbono 2 é asimétrico). Grupo ácido COOH e grupo alcol OH. 3. a) Considera a seguinte reacción: Br₂(g) 2 Br(g). Cando 1,05 moles de Br₂ colócanse nun matraz de 0,980 dm³ a unha temperatura de 1873 K disóciase o 1,20 % de Br₂. Calcula a constante de equilibrio K da reacción. b) Calcula a masa de cobre que se pode obter ao reaccionar 200 ml de disolución de sulfato de cobre(ii) ao 20 % en peso e densidade 1,10 g/cm³ co suficiente ferro, tendo en conta que na reacción tamén se produce sulfato de ferro(ii). Rta.: a) K = 6,25 10 ⁴; b) m(cu) = 17,5 g Cu Datos Cifras signifcativas: 3 Gas: Volume V = 0,980 dm³ Temperatura Cantidade inicial de Br₂ T = 1873 K n₀(br₂) = 1,05 mol Br₂ Grao de disociación α = 1,20 % = 0,0120 Incógnitas Constante do equilibrio K K
3 Outros símbolos Cantidade de Br₂ que se ha disociado Ecuacións Concentración da substancia X Grao de disociación Constantes do equilibrio: a A + b B c C + d D n (Br₂) [X] =n(x) / V α = n d n 0 K c = [C] c d e [D] e b [ A] ea [ B] e A ecuación de disociación química do bromo é: Disociáronse: Br₂(g) 2 Br(g) n (Br₂) = α n₀(br₂) = 0,0120 1,05 [mol Br₂] = 0,01206 mol Br₂ disociados Pola estequiometría da reacción, as cantidades de bromo atómico formado e en equilibrio son: Br₂ 2 Br Cantidade inicial n₀ 1,05 0 mol Cantidade que reacciona ou se forma n 0, ,02502 mol Cantidade no equilibrio nₑ 1,05 0,01 = 1,04 0,02502 mol Concentración no equilibrio [X]ₑ 1,04 / 0,980 = 1,06 0,02507 mol/dm³ A expresión da constante de equilibrio en función das concentracións é: K c = [ Br] 2 e (0,0250 7)2 = =6, (concentracións en mol/dm³) [ Br 2 ] e 1,06 Datos Cifras signifcativas: 3 Disolución de sulfato de cobre(ii) : Volume V = 200 cm³ Riqueza r = 20,0 % = 0,200 Densidade ρ = 1,10 g/cm³ Masa molar: Sulfato de cobre(ii) M(CuSO₄) = 159,6 g/mol Incógnitas Masa de cobre Ecuacións Cobre Cantidade (número de moles) Concentración dunha disolución M(Cu) = 63,5 g/mol m(cu) n = m / M [soluto] =n(s) /V(D) a) A cantidade de sulfato de cobre(ii) que hai en 200 cm³ de disolución é: n(cuso 4 )=200 cm 3 D 1,10 g D 1 cm 3 D 20,0 g CuSO g D 1 mol CuSO 4 159,6 g CuSO 4 =0,276 mol CuSO 4
4 Da ecuación axustada: A cantidade do cobre que se obtén é a mesma: que corresponde a unha masa de: CuSO₄(aq)+ Fe(s) Cu(s) + FeSO₄(aq) m(cu)=0,276 mol Cu n(cu) = 0,276 mol Cu 63,5 g Cu =17,5 g Cu 1 mol Cu 4.- a) Sabendo que a 25 a K (BaSO₄) é 1,1 10 ¹⁰, determina a solubilidade do sal en g/dm³. b) Se 250 cm³ de BaCl₂ de concentración 0,0040 mol/dm³ engádense a 500 cm³ de K₂SO₄ de concentración 0,0080 mol/dm³ e supoñendo que os volumes son aditivos, indica se se formará precipitado ou non. Rta.: a) s = 2,4 10 ³ g/dm³; b) Si. 1,3 10 ³ 5,3 10 ³ > K Datos Cifras signifcativas: 2 Produto de solubilidade do BaSO₄ Volume disolución de BaCl₂ Volume disolución K₂SO₄ Concentración da disolución do BaCl₂ Concentración do K₂SO₄ Masa molar do sulfato de bario Incógnitas Solubilidade do sulfato de bario en g/dm³ s Se se formará precipitado Outros símbolos Solubilidade do sulfato de bario en mol/dm³ Ecuacións Concentración molar (mol/dm³) Produto de solubilidade do equilibrio: B Aₐ(s) b B β +(aq) + a A α (aq) Kₛ = 1,1 10 ¹⁰ V₁ = 250 cm³ = 0,25 dm³ V₂ = 500 cm³ = 0,50 dm³ [BaCl₂]₀ = 0,0040 mol/dm³ [K₂SO₄]₀ = 0,0080 mol/dm³ M(BaSO₄) = 233 g/mol Q s s = n / V = s / M Kₛ = [A α ]ᵃ [B β +]ᵇ a) O equilibrio de solubilidade é BaSO₄(s) Ba²+(aq) + SO₄² (aq) A constante de equilibrio Kₛ é: A solubilidade do sulfato de bario é que se pode expresar en g/dm³: BaSO₄ Ba²+ SO₄² Concentración no equilibrio [X]ₑ s s mol/dm³ Kₛ = [Ba²+]ₑ [SO₄² ]ₑ = s s = s² = 1,1 10 ¹⁰ s= K s = 1, =1, mol BaSO 4 / dm 3 D s'=1, mol BaSO 4 /dm 3 D 233 g BaSO 1 mol BaSO =2, g/dm 3 D
5 b) Os sales das disolucións están totalmente disociados. As concentracións iniciais dos ións son: BaCl₂(s) Ba²+(aq) + 2 Cl (aq) K₂SO₄(s) SO₄² (aq) + 2 K+(aq) [Ba²+]₀ = [BaCl₂]₀ = 0,0040 mol/dm³ [SO₄² ]₀ = [BaSO₄]₀ = 0,0080 mol/dm³ Ao mesturar ambas as disolucións, dilúense. Supoñendo volumes aditivos, as novas concentracións son: [Ba 2+ ]= n(ba2+ ) V T = 0,25 dm3 0,0040 0mol Ba 2+ /dm 3 (0,25+0,50) dm 3 =1, mol Ba 2+ /dm 3 [SO 2 4 ]= n (SO 2 4 ) = 0,50 dm3 0,0080 0mol SO 2 4 /dm 3 =5, mol SO V T (0,25+0,50) dm 3 4 Formarase precipitado se Q = [Ba²+] [SO₄² ] > Kₛ e, por tanto, fórmase precipitado. [Ba²+] [SO₄² ] = 1,3 10 ³ 5,3 10 ³ = 7,1 10 ⁶ > 1,1 10 ¹⁰ 2 /dm A 25 e empregando un eléctrodo de prata e outro de cinc, disolucións de Zn²+(1,0 mol/dm³) e Ag+(1,0 mol/dm³) e unha disolución de KNO₃ de concentración 2,0 mol/dm³ como ponte salina, constrúese no laboratorio a seguinte pila: Zn(s) Zn²+(aq) Ag+(aq) Ag(s). Datos: E (Zn²+/Zn) = -0,76 V e E (Ag+/Ag) = +0,80 V. a) Escribe as semirreaccións que ocorren en cada eléctrodo e a ecuación da reacción iónica global, calculando tamén a forza electromotriz da pila. b) Fai un debuxo-esquema detallado da pila, indica o ánodo e cátodo, e o sentido no que circulan os electróns, así como os ións da ponte salina. Material: Vasos de precipitados de 100 cm³ (2), tubo en O, cables con pinzas, voltímetro. Reactivos: láminas de prata e cinc puídas, disolucións de sulfato de cinc de concentración 1 mol/dm³ e nitrato de prata de concentración 1 mol/dm³. Disolución de nitrato de potasio de concentración 2 mol/dm³ para a ponte salina. (Cátodo +) redución: 2 Ag+ + 2 e 2 Ag E = 0,80 V (Ánodo ) oxidación: Zn Zn²+ + 2 e E = 0,76 V Reacción global: Zn + 2 Ag+ Zn²+ + 2 Ag E = 1,56 V e Zn NO₃ Zn²+ K+ Ag+ Ag Os electróns circulan do polo negativo (ánodo Zn) ao polo positivo (cátodo Ag). Na ponte salina, os catións K+ circulan cara á disolución que contén ións prata (para compensar a perda de ións prata que se depositaron) e os anións NO₃ diríxense cara á disolución que contén ións cinc (que están en exceso). OPCIÓN B 1. a) Considera o seguinte proceso en equilibrio: N₂F₄(g) 2 NF₂(g); H = 38,5 kj. Razoa que lle ocorre ao equilibrio si diminúese a presión da mestura de reacción a temperatura constante. b) Especifica que orbitais híbridos utiliza o carbono no eteno (C₂H₄), así como o tipo de enlaces que se forman na molécula. Razoa a resposta.
6 A constante de equilibrio en función das presións pode escribirse así: K p = p 2 e(nf 2 ) p e (N 2 F 4 ) =(x (NF ) p e 2 t )2 = x 2 e(nf 2 ) x e (N 2 F 4 ) p t x 2 e (N 2 F 4 ) p t onde x(gas) é a fracción molar de cada gas e p é a presión total no interior do recipiente. A constante de equilibrio só depende da temperatura. Non varía aínda que cambien as cantidades de reactivos ou produtos, o volume ou a presión. Se se diminúe a presión total, para que K permaneza constante, ou ben deberá aumentar a fracción molar do NF₂ que aparece no numerador, ou ben diminuír a fracción molar de N₂F₄ no denominador. O equilibrio desprazarase (cara á dereita) ata alcanzar un novo estado de equilibrio no que haberá máis NF₂ e menos N₂F₄. b) A confguración fundamental do carbono Z = 6 é (1s)² (2s)² (2pₓ)¹ (2p )¹ Pero, debido a que a formación de dúas enlaces máis compensa a enerxía de excitación, antes de formar enlaces pasa á confguración excitada, [He] (2s)¹ (2pₓ)¹ (2p )¹ (2p )¹, con catro electróns desapareados que poden formar catro enlaces covalentes. Prodúcese unha hibridación sp²: aparecen tres híbridos 1 s sp² p sp² formados por combinación dun orbital s e dous orbitais p, (pₓ e p ) e queda sen hibridar o orbital p. Haberá un electrón desapareado en cada híbrido e tamén no orbital p. Estes híbridos están dirixidos cara aos vértices dun triángulo equilátero. H Nos enlaces C H, superpóñense un orbital híbrido sp² do carbono co C C orbital 1s do hidróxeno dando lugar a un enlace σ. No enlace C C superpóñense dous orbitais híbridos, un de cada átomo de carbono, para H dar lugar a outro enlace σ. Pero tamén superpóñense os dous orbitais p dos dous carbonos, dando lugar a un enlace π fóra da liña que une os enlace π dous átomos de carbono. H H 2.- Xustifica si estas afirmacións son correctas: a) O produto da constante de ionización dun ácido e a constante de ionización da súa base conxugada é igual á constante do produto iónico do auga. b) A presenza dun ión común diminúe a solubilidade dun sal lixeiramente soluble. a) Verdadeira. Cando un ácido HA débil disólvese en auga, ionízase parcialmente en ións A e H+. O ión hidróxeno únese a unha molécula de auga para formar o ión oxonio H₃O+. HA(aq) + H₂O(l) A (aq) + H₃O+(aq) A constante de acidez do ácido AH débil, en función das concentracións, é: K a = [ A ] e [H + ] e [H A ] e A base conxugada, segundo a teoría de Brönsted e Lowry, é o ión A. En disolucións dos sales do ácido HA, o ión A atópase en equilibrio que se pode expresar por A constante de basicidade desta base é Se multiplicamos ambas as constantes, obtemos A (aq) + H₂O(l) HA(aq) + OH (aq) K b = [HA] e [OH ] e [ A ] e
7 K a K b = [A ] e [H + ] e [ HA] e [HA ] e [OH ] e [A ] e =[ H + ] e [OH ] e =K w a constante de ionización da auga que vale K = 1 10 ¹⁴ b) Verdadeira. A solubilidade diminúe en presenza dun ión común. Para un sal pouco soluble, por exemplo o cloruro de prata, o sólido atópase en equilibrio cos ións disoltos. AgCl(s) Ag+(aq) + Cl (aq) A solubilidade s (concentración da disolución saturada), pódese calcular da expresión da constante de equilibrio: AgCl Cl Ag+ Concentración no equilibrio [X]ₑ s s mol/dm³ Kₛ = [Cl ] [Ag+] = s s = s² O cloruro de sodio é un electrólito forte que, en disolucións diluídas, está totalmente disociado. NaCl(aq) Na+(aq) + Cl (aq) Ao engadir a unha disolución de cloruro de prata en equilibrio unha cantidade de cloruro de sodio, que se disolve totalmente, o equilibrio desprázase, seguindo a lei de Le Chatelier, no sentido de consumir o ión cloruro extra e de formar maior cantidade de precipitado de cloruro de prata, deixando menos ións prata na disolución. 3.- No laboratorio pódese preparar cloro gas facendo reaccionar permanganato do potasio sólido con ácido clorhídrico concentrado. a) No transcurso desta reacción redox fórmase cloro, cloruro de manganeso(ll), cloruro de potasio e auga. Escribe e axusta a reacción molecular mediante o método do ión-electrón. b) Calcula o volume de cloro gas, a 20 e 1 atm (101,3 kpa), que se obtén ao facer reaccionar 10 ml de ácido clorhídrico concentrado do 35,2 % en masa e densidade 1,175 g ml ¹ cun exceso de permanganato de potasio. Datos: R = 0,082 atm L K ¹ mol ¹ = 8,31 J K ¹ mol ¹. Rta.: a) 2 KMnO₄ + 16 HCl 2 MnCl₂ + 2 KCl + 5 Cl₂ + 8 H₂O; b) V = 0,853 dm³ Cl₂ Datos Cifras signifcativas: 3 Disolución de ácido clorhídrico: Volume V (HCl) = 10,0 cm³ Riqueza r = 35,2 % Densidade ρ = 1,175 g/cm³ Gas cloro: Temperatura T = 20 = 293 K Presión Constante dos gases ideais Masa molar do ácido clorhídrico Incógnitas Volume de cloro a 20 e 1 atm Ecuacións De estado dos gases ideais a) As semirreaccións iónicas son: Oxidación: 2 Cl Cl₂ + 2 e p = 101,3 kpa = 1,013 10⁵ Pa R = 8,31 J mol ¹ K ¹ M(HCl) = 36,5 g/mol V(Cl₂) p V = n R T
8 Redución: MnO₄ + 8 H+ + 5 e Mn²+ + 4 H₂O Multiplicando a primeira por 5 e a segunda por 2 e sumando, obtense a reacción iónica axustada. 10 Cl + 2 MnO₄ + 16 H+ 5 Cl₂ + 2 Mn²+ + 8 H₂O Sumando 2 K+ e 6 Cl a cada lado da ecuación e xuntando os ións de signos opostos obtense a reacción global: 2 KMnO₄(aq) + 16 HCl(aq) 2 MnCl₂(aq) + 2 KCl(aq) + 5 Cl₂(g) + 8 H₂O(l) b) A cantidade de ácido clorhídrico que hai en 10 cm³ de disolución é: n(hcl)=10,0 cm 3 D HCl 1,175 g D HCl 1,00 cm 3 D HCl A cantidade de gas cloro que se obtén na reacción é n(cl 2 )=0,113 mol HCl Supoñendo comportamento ideal, ocuparán un volume de: V = n R T p 35,2 g HCl 100 g D HCl 5 mol Cl 2 16 mol HCl =0,0350 4mol Cl 2 1 mol HCl =0,113 mol HCl 36,5 g HCl = 0,0350 4mol Cl 2 8,31 J mol 1 K K =8, m 3 =0,853 dm 3 Cl 1, Pa 4.- O nafaleno (C₁₀H₈) é un composto aromático sólido que se vende para combater a couza. A combustión completa deste composto para producir CO₂(g) e H₂O(l) a 25 e 1 atm (101,3 kpa) desprende 5154 kj mol ¹. a) Escribe as reaccións de formación do nafaleno e a reacción de combustión. b) Calcula a entalpía estándar de formación do nafaleno e interprete o seu signo. Datos: H (CO₂(g)) = -393,5 kj mol ¹; H (H₂O(l)) = -285,8 kj mol ¹ Rta.: b) H (C₁₀H₈) = 75,8 kj/mol C₁₀H₈ Datos Cifras signifcativas: 4 C₁₀H₈(s) + 12 O₂(g) 10 CO₂(g) + 4 H₂O(l) C(s) + O₂(g) CO₂(g) H₂(g) + ½ O₂(g) H₂O(l) Incógnitas Entalpía de formación do nafaleno Ecuacións Lei de Hess a) Ecuación de combustión do nafaleno: H (C₁₀H₈) = kj/mol H (CO₂) = -393,5 kj/mol H (H₂O) = -285,8 kj/mol H (C₁₀H₈) C₁₀H₈(s) + 12 O₂(g) 10 CO₂(g) + 4 H₂O(l) H = kj/mol H = H (prod.) H (react.) A ecuación de combustión do carbono sólido (grafto) coincide coa ecuación de formación do CO₂(g). Ecuacións de formación: 10 C(s) + 4 H₂(g) C₁₀H₈(s) H (C₁₀H₈) C(s) + O₂(g) CO₂(g) H (CO₂) = -393,5 kj/mol H₂(g) + ½ O₂(g) H₂O(l) H (H₂O) = -285,5 kj/mol b) Pola lei de Hess, H (C₁₀H₈) = 10 H (CO₂) + 4 H (H₂O) ( H (C₁₀H₈) + 12 H (O₂)) [kj] = (10 [mol CO₂] ( 393,5 [kj/mol CO₂] + 4 [mol H₂O] (-285,8 [kj/mol H₂O])) ( H (C₁₀H₈)) H (C₁₀H₈) = 75,8 kj/mol C₁₀H₈ O signo positivo indica que a reacción de formación é endotérmica.
9 5. a) Cantos cm³ dunha disolución de NaOH de concentración 0,610 mol/dm³ necesítanse para neutralizar 20,0 cm³ dunha disolución de H₂SO₄ de concentración 0,245 mol/dm³? Indica a reacción que ten lugar e xustifica o ph no punto de equivalencia. b) Nomea o material necesario e describe o procedemento experimental para levar a cabo a valoración. Rta.: a) V = 16,1 cm³ D a) A reacción axustada é H₂SO₄(aq) + 2 NaOH(aq) Na₂SO₄(aq) + 2 H₂O(l) Cálculos: Para neutralizar 20,0 cm³ de H₂SO₄ de concentración 0,245 mol/dm³ necesitaranse: V =20,0 cm 3 D H 2 SO 4 0,245 mol H 2 SO cm 3 D H 2 SO 4 2 mol NaOH 1 mol H 2 SO cm 3 D NaOH 0,610 mol NaOH =16,1 cm3 D NaOH O ph no punto de equivalencia será 7, xa que teoricamente* todo o ácido foi neutralizado e só haberá sulfato de sodio disolto e auga. O produto iónico da auga é: H₂O(l) H+(aq) + OH (aq) K = [H+] [OH ] = 1,00 10 ¹⁴ Cando non hai exceso de ácido nin de base, as concentracións dos ións hidróxeno e hidróxido son iguais e a concentración de ións hidróxeno é: [H+] = [OH ] [H + ]= K w = 1, =1, mol /dm 3 polo que o ph = -log[h`+] = 7,0 (* Na práctica o indicador ácido-base vira ao redor do punto de equivalencia cunha marxe de 1 unidade de ph, polo que se usamos o indicador adecuado, azul de bromotimol, só podemos dicir que o ph estará comprendido entre 6 e 8) Procedemento de valoración: Cunha pipeta mídense 20,0 cm³ de disolución de H₂SO₄ e vértense nun matraz erlenmeyer de 100 cm³. Engádense dúas pingas de azul de bromotimol e a disolución volverase de cor amarela. Énchese unha bureta de 25 cm³ con disolución de NaOH de concentración 0,610 mol/dm³ por encima do cero. Ábrese a chave ata que o pico da bureta estea cheo e o nivel en cero. Déixanse caer 15 cm³ sobre o erlenmeyer e axítase. Ábrese a chave da bureta para deixar caer a disolución de NaOH en pequenos chorros mentres se imprime un movemento circular ao erlenmeyer ata que a cor do contido do erlenmeyer pase a azul. Anótase o volume de NaOH gastado (p. ex. 16,9 cm³) e tírase o contido do erlenmeyer e lávase o matraz. Vólvese a encher a bureta con NaOH ata o cero. Mídense outros 20,0 cm³ de H₂SO₄ coa pipeta, vértense no erlenmeyer (lavado pero non necesariamente seco) e engádense dúas pingas de azul de bromotimol. Colócase o erlenmeyer baixo a bureta e ábrese a chave ata deixar caer case todo o volume medido antes (p. ex. 16,5 cm³). Agora déixase caer o NaOH pinga a pinga mentres se fai rotar ao erlenmeyer, ata que o indicador vire de cor. Anótase este valor. Repítese outras dúas veces e tómase como volume correcto o valor medio das medidas que máis se aproximan. Material: Bureta (1) de 25 cm³ (graduada en 0,1 cm³), pipeta (1) de 20 cm³ con aspirador, matraz erlenmeyer (1) de 100 cm³, disolución de azul de bromotimol. A bureta é un tubo estreito graduado cunha boca superior algo máis ancha para enchelo e unha chave de paso na parte inferior para poder baleirala. A pipeta é tamén un tubo estreito que pode ser graduado ou ter unha marca de aforo. Énchese ao aspirar cunha especie de xiringa cando a boca inferior máis estreita está mergullada na disolución. O matraz erlenmeyer é un recipiente con forma de tronco de cono, coa boca máis estreita que o fondo, para non salpicar ao removelo cun movemento circular. Cuestións e problemas das Probas de Acceso á Universidade (P.A.U.) en Galicia. Respostas e composición de Alfonso J. Barbadillo Marán.
10 Algúns cálculos fxéronse cunha folla de cálculo OpenOfce (ou LibreOfce) do mesmo autor. Algunhas ecuacións e as fórmulas orgánicas construíronse coa extensión CLC09 de Charles Lalanne-Cassou. A tradución ao/desde o galego realizouse coa axuda de traducindote, de Óscar Hermida López. Procurouse seguir as recomendacións do Centro Español de Metrología (CEM)
PAU XUÑO QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
 PAU XUÑO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. 1.1. Dados os seguintes elementos: B, O, C e F, ordéneos en
PAU XUÑO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. 1.1. Dados os seguintes elementos: B, O, C e F, ordéneos en
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amonuíaco de concentración 0,01 mol/dm³ está ionizada nun 4,2 %. a) Escribe a reacción de disociación e calcula
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amonuíaco de concentración 0,01 mol/dm³ está ionizada nun 4,2 %. a) Escribe a reacción de disociación e calcula
PAU. Código: 27 SETEMBRO QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualifcarase con 2 puntos.
 PAU Código: 27 SETEMBRO 2012 QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualifcarase con 2 puntos. OPCIÓN A 1. Os elementos A, B, C e D teñen números atómicos 10, 15,
PAU Código: 27 SETEMBRO 2012 QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualifcarase con 2 puntos. OPCIÓN A 1. Os elementos A, B, C e D teñen números atómicos 10, 15,
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
PAU. Código: 27 SETEMBRO QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualifcarase con 2 puntos.
 PAU Código: 27 SETEMBRO 2013 QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualifcarase con 2 puntos. OPCIÓN A 1. Complete as seguintes reaccións ácido-base e identifique
PAU Código: 27 SETEMBRO 2013 QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualifcarase con 2 puntos. OPCIÓN A 1. Complete as seguintes reaccións ácido-base e identifique
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA
 Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. O nafaleno (C₁₀H₈) é un composto aromático sólido que se vende para combater a traza. A combustión completa deste composto para producir
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. O nafaleno (C₁₀H₈) é un composto aromático sólido que se vende para combater a traza. A combustión completa deste composto para producir
Proba de Avaliación do Bacharelato para o Acceso á Universidade XUÑO 2018
 Proba de Avaliación do Bacharelato para o Acceso á Universidade Código: 24 XUÑO 2018 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1.
Proba de Avaliación do Bacharelato para o Acceso á Universidade Código: 24 XUÑO 2018 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1.
EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm³ contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm³ contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
Código: 27 PAU XUÑO 2012 QUÍMICA OPCIÓN A OPCIÓN B
 PAU Código: 27 XUÑO 2012 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Cos seguintes datos E (Fe²+/Fe) = -0,44 e E (Ag+/Ag) = +0,80,
PAU Código: 27 XUÑO 2012 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Cos seguintes datos E (Fe²+/Fe) = -0,44 e E (Ag+/Ag) = +0,80,
Química 2º Bacharelato Equilibrio químico 11/02/08
 Química º Bacharelato Equilibrio químico 11/0/08 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: PROBLEMAS 1. Nun matraz de,00 litros introdúcense 0,0 10-3 mol de pentacloruro de fósforo sólido. Péchase, faise
Química º Bacharelato Equilibrio químico 11/0/08 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: PROBLEMAS 1. Nun matraz de,00 litros introdúcense 0,0 10-3 mol de pentacloruro de fósforo sólido. Péchase, faise
Proba de Avaliación de Bacharelato para o Acceso á Universidade XUÑO 2017
 Proba de Avaliación de Bacharelato para o Acceso á Universidade ódigo: 24 XUÑO 2017 QUÍMIA ualificación: O alumno elixirá UNA das dúas opcións. ada pregunta cualificarase con 2 puntos. OPIÓN A 1. 1.1.
Proba de Avaliación de Bacharelato para o Acceso á Universidade ódigo: 24 XUÑO 2017 QUÍMIA ualificación: O alumno elixirá UNA das dúas opcións. ada pregunta cualificarase con 2 puntos. OPIÓN A 1. 1.1.
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2 %. a) Escriba a reacción de disociación e calcule
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2 %. a) Escriba a reacción de disociación e calcule
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
PAU XUÑO QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
 PAU XUÑO 2012 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Cos seguintes datos E (Fe 2+ /Fe) = -0,44 e E (Ag + /Ag) =
PAU XUÑO 2012 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Cos seguintes datos E (Fe 2+ /Fe) = -0,44 e E (Ag + /Ag) =
Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA
 Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA PROBLEMAS REACCIÓNS 1. Por oxidación do ión bromuro con ión permanganato [tetraoxomanganato(vii)] no medio ácido, obtense bromo (Br 2) e o sal de manganeso(ii):
Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA PROBLEMAS REACCIÓNS 1. Por oxidación do ión bromuro con ión permanganato [tetraoxomanganato(vii)] no medio ácido, obtense bromo (Br 2) e o sal de manganeso(ii):
Proba de Avaliación de Bacharelato para o Acceso á Universidade SETEMBRO 2017
 Proba de Avaliación de Bacharelato para o Acceso á Universidade Código: 24 SETEMBRO 2017 QUÍMICA Cualificación: O alumno elixirá UNA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
Proba de Avaliación de Bacharelato para o Acceso á Universidade Código: 24 SETEMBRO 2017 QUÍMICA Cualificación: O alumno elixirá UNA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
PAU SETEMBRO QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos.
 PAU SETEMBRO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Indique razoadamente, si son verdadeiras ou falsas as seguintes
PAU SETEMBRO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Indique razoadamente, si son verdadeiras ou falsas as seguintes
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA
 Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA PROBLEMAS REACCIÓNS 1. No laboratorio pódese preparar cloro gas facendo reaccionar permanganato do potasio sólido con ácido clorhídrico concentrado. a) No
Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA PROBLEMAS REACCIÓNS 1. No laboratorio pódese preparar cloro gas facendo reaccionar permanganato do potasio sólido con ácido clorhídrico concentrado. a) No
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA
 Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. Para o proceso Fe 2O 3 (s) + 2 Al (s) Al 2O 3 (s) + 2 Fe (s), calcule: a) A entalpía da reacción en condicións estándar e a calor desprendida
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. Para o proceso Fe 2O 3 (s) + 2 Al (s) Al 2O 3 (s) + 2 Fe (s), calcule: a) A entalpía da reacción en condicións estándar e a calor desprendida
PAU SETEMBRO 2014 OPCIÓN A
 PAU Código: 27 SETEMBRO 2014 QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opficións. Cada pregunta ficualifficarase ficon 2 puntos. OPCIÓN A 1. Indique razoadamente, si son verdadeiras ou falsas
PAU Código: 27 SETEMBRO 2014 QUÍMICA Cualifficafición: O alumno elixirá UNHA das dúas opficións. Cada pregunta ficualifficarase ficon 2 puntos. OPCIÓN A 1. Indique razoadamente, si son verdadeiras ou falsas
PROBLEMAS E CUESTIÓNS DE SELECTIVIDADE
 PROBLEMAS E CUESTIÓNS DE SELECTIVIDADE O KMnO en presenza de H SO transforma o FeSO en Fe (SO ), formándose tamén K SO, MnSO e auga: a) Axusta a reacción molecular. b) Cantos cm de disolución de KMnO 0,5
PROBLEMAS E CUESTIÓNS DE SELECTIVIDADE O KMnO en presenza de H SO transforma o FeSO en Fe (SO ), formándose tamén K SO, MnSO e auga: a) Axusta a reacción molecular. b) Cantos cm de disolución de KMnO 0,5
ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS
 Química P.A.U. ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS CUESTIÓNS NÚMEROS CUÁNTICOS. a) Indique o significado dos números cuánticos
Química P.A.U. ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS CUESTIÓNS NÚMEROS CUÁNTICOS. a) Indique o significado dos números cuánticos
CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA
 QQuímica P.A.U. CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA 1 CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA PROBLEMAS GASES 1. Nun matraz de 10 dm³ introdúcense 2,0 g de hidróxeno; 8,4 g de nitróxeno e 4,8 g de
QQuímica P.A.U. CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA 1 CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA PROBLEMAS GASES 1. Nun matraz de 10 dm³ introdúcense 2,0 g de hidróxeno; 8,4 g de nitróxeno e 4,8 g de
QUÍMICA. Cualificación: Cuestións =2 puntos cada unha; problemas: 2 puntos cada un; práctica: 2 puntos
 31 QUÍMICA Cualificación: Cuestións =2 puntos cada unha; problemas: 2 puntos cada un; práctica: 2 puntos CUESTIÓNS (Responda SAMENTE a DÚAS das seguintes cuestións) 1 Indique xustificando a resposta, se
31 QUÍMICA Cualificación: Cuestións =2 puntos cada unha; problemas: 2 puntos cada un; práctica: 2 puntos CUESTIÓNS (Responda SAMENTE a DÚAS das seguintes cuestións) 1 Indique xustificando a resposta, se
Tema: Enerxía 01/02/06 DEPARTAMENTO DE FÍSICA E QUÍMICA
 Tema: Enerxía 01/0/06 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: 1. Unha caixa de 150 kg descende dende o repouso por un plano inclinado por acción do seu peso. Se a compoñente tanxencial do peso é de 735
Tema: Enerxía 01/0/06 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: 1. Unha caixa de 150 kg descende dende o repouso por un plano inclinado por acción do seu peso. Se a compoñente tanxencial do peso é de 735
Química 2º Bacharelato Cálculos elementais e Termoquímica 14/01/08
 Química 2º Bacharelato álculos elementais e Termoquímica 14/1/8 DEPARTAMENTO DE FÍSIA E QUÍMIA Nome: UALIFIAIÓN: UESTIÓNS =2 PUNTOS ADA UNHA; PROBLEMAS: 2 PUNTOS ADA UN; PRÁTIA: 2 PUNTOS PROBLEMAS (Responda
Química 2º Bacharelato álculos elementais e Termoquímica 14/1/8 DEPARTAMENTO DE FÍSIA E QUÍMIA Nome: UALIFIAIÓN: UESTIÓNS =2 PUNTOS ADA UNHA; PROBLEMAS: 2 PUNTOS ADA UN; PRÁTIA: 2 PUNTOS PROBLEMAS (Responda
PAU XUÑO 2011 QUÍMICA OPCIÓN A
 AU XUÑO 011 Código: 7 QUÍMICA Cualificación: O alumno elixirá UNA das dúas opcións. Cada pregunta cualificarase con puntos OCIÓN A 1. 1.1. Que sucedería se utilizase unha culler de aluminio para axitar
AU XUÑO 011 Código: 7 QUÍMICA Cualificación: O alumno elixirá UNA das dúas opcións. Cada pregunta cualificarase con puntos OCIÓN A 1. 1.1. Que sucedería se utilizase unha culler de aluminio para axitar
PROBLEMAS DE SELECTIVIDADE: EQUILIBRIO QUÍMICO
 PROBLEMAS DE SELECTIVIDADE: EQUILIBRIO QUÍMICO 3013 2. Para a seguinte reacción: 2NaHCO 3(s) Na 2 CO 3(s) + CO 2(g) + H 2 O (g) ΔH
PROBLEMAS DE SELECTIVIDADE: EQUILIBRIO QUÍMICO 3013 2. Para a seguinte reacción: 2NaHCO 3(s) Na 2 CO 3(s) + CO 2(g) + H 2 O (g) ΔH
TEMA 5. O EQUILIBRIO QUÍMICO
 TEMA 5. O EQUILIBRIO QUÍMICO 1. Para a reacción: N (g) + 3 H (g) NH 3 (g), a constante de equilibrio, K c, a certa temperatura, é,38 10 3. Calcula a constante de equilibrio, á mesma temperatura, para as
TEMA 5. O EQUILIBRIO QUÍMICO 1. Para a reacción: N (g) + 3 H (g) NH 3 (g), a constante de equilibrio, K c, a certa temperatura, é,38 10 3. Calcula a constante de equilibrio, á mesma temperatura, para as
EXERCICIOS DE REFORZO: RECTAS E PLANOS
 EXERCICIOS DE REFORZO RECTAS E PLANOS Dada a recta r z a) Determna a ecuacón mplícta do plano π que pasa polo punto P(,, ) e é perpendcular a r Calcula o punto de nterseccón de r a π b) Calcula o punto
EXERCICIOS DE REFORZO RECTAS E PLANOS Dada a recta r z a) Determna a ecuacón mplícta do plano π que pasa polo punto P(,, ) e é perpendcular a r Calcula o punto de nterseccón de r a π b) Calcula o punto
PAU XUÑO 2013 QUÍMICA OPCIÓN A
 PAU Código: 7 XUÑO 01 QUÍICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con puntos OPCIÓN A 1. Indique razoadamente se son verdadeiras ou falsas as afirmacións seguintes:
PAU Código: 7 XUÑO 01 QUÍICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con puntos OPCIÓN A 1. Indique razoadamente se son verdadeiras ou falsas as afirmacións seguintes:
Exercicios das PAAU clasificados por temas
 Exercicios das PAAU clasificados por temas. 1996-2008 Índice: Unidade 1: CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA... 1 Unidade 2: ESTRUCTURA DA MATERIA... 4 Unidade 3: ENLACE QUÍMICO... 6 Unidade 4: TERMOQUÍMICA...
Exercicios das PAAU clasificados por temas. 1996-2008 Índice: Unidade 1: CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA... 1 Unidade 2: ESTRUCTURA DA MATERIA... 4 Unidade 3: ENLACE QUÍMICO... 6 Unidade 4: TERMOQUÍMICA...
ENLACE QUÍMICO CUESTIÓNS ENLACE IÓNICO. 1. Considerando o elemento alcalinotérreo do terceiro perquíodo e o segundo elemento do grupo dos halóxenos.
 QQuímica P.A.U. ELACE QUÍMICO 1 ELACE QUÍMICO CUESTIÓS ELACE IÓICO 1. Considerando o elemento alcalinotérreo do terceiro perquíodo e o segundo elemento do grupo dos halóxenos. a) Escribe as súas configuracións
QQuímica P.A.U. ELACE QUÍMICO 1 ELACE QUÍMICO CUESTIÓS ELACE IÓICO 1. Considerando o elemento alcalinotérreo do terceiro perquíodo e o segundo elemento do grupo dos halóxenos. a) Escribe as súas configuracións
REACCIÓNS DE TRANSFERENCIA DE PROTÓNS
 REACCIÓNS DE TRANSFERENCIA DE PROTÓNS 1. Concepto de ácido e base segundo as teorías de Arrhenius e Brönsted-Lowry. 2. Concepto de par ácido-base conxugado. 3. Forza relativa dos ácidos e bases. Grao de
REACCIÓNS DE TRANSFERENCIA DE PROTÓNS 1. Concepto de ácido e base segundo as teorías de Arrhenius e Brönsted-Lowry. 2. Concepto de par ácido-base conxugado. 3. Forza relativa dos ácidos e bases. Grao de
QUÍMICA EXERCICIOS RESOLTOS. Segundo Curso de Bacharelato. Manuela Domínguez Real
 QUIMICA º BACHARELATO QUÍMICA Segundo Curso de Bacharelato Manuela Domínguez Real 1ª Edición Setembro 003 003 Manuela Domínguez Real 003 BAÍA Edicións Polígono de Pocomaco, ª Avda. Parcela G18 Nave posterior
QUIMICA º BACHARELATO QUÍMICA Segundo Curso de Bacharelato Manuela Domínguez Real 1ª Edición Setembro 003 003 Manuela Domínguez Real 003 BAÍA Edicións Polígono de Pocomaco, ª Avda. Parcela G18 Nave posterior
Física P.A.U. ELECTROMAGNETISMO 1 ELECTROMAGNETISMO. F = m a
 Física P.A.U. ELECTOMAGNETISMO 1 ELECTOMAGNETISMO INTODUCIÓN MÉTODO 1. En xeral: Debúxanse as forzas que actúan sobre o sistema. Calcúlase a resultante polo principio de superposición. Aplícase a 2ª lei
Física P.A.U. ELECTOMAGNETISMO 1 ELECTOMAGNETISMO INTODUCIÓN MÉTODO 1. En xeral: Debúxanse as forzas que actúan sobre o sistema. Calcúlase a resultante polo principio de superposición. Aplícase a 2ª lei
PAU XUÑO 2016 QUÍMICA
 PAU Código: 7 XUÑO 016 QUÍICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con puntos. Todas as cuestións teóricas deberán ser razoadas. OPCIÓN A 1. 1.1. Xustifique,
PAU Código: 7 XUÑO 016 QUÍICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con puntos. Todas as cuestións teóricas deberán ser razoadas. OPCIÓN A 1. 1.1. Xustifique,
EXERCICIOS AUTOAVALIABLES: RECTAS E PLANOS. 3. Cal é o vector de posición da orixe de coordenadas O? Cales son as coordenadas do punto O?
 EXERCICIOS AUTOAVALIABLES: RECTAS E PLANOS Representa en R os puntos S(2, 2, 2) e T(,, ) 2 Debuxa os puntos M (, 0, 0), M 2 (0,, 0) e M (0, 0, ) e logo traza o vector OM sendo M(,, ) Cal é o vector de
EXERCICIOS AUTOAVALIABLES: RECTAS E PLANOS Representa en R os puntos S(2, 2, 2) e T(,, ) 2 Debuxa os puntos M (, 0, 0), M 2 (0,, 0) e M (0, 0, ) e logo traza o vector OM sendo M(,, ) Cal é o vector de
EQUILIBRIOS ÁCIDO-BASE
 EQUILIBRIOS ÁCIDO-BASE 1- ÁCIDOS E BASES. DEFINICIÓN SEGUNDO AS TEORÍAS DE ARRHENIUS E BRÖNSTED-LOWRY. Arrhenius.- Ácido. substancia que en disolución acuosa disóciase producindo ións H. ( auga) AH H (aq.)
EQUILIBRIOS ÁCIDO-BASE 1- ÁCIDOS E BASES. DEFINICIÓN SEGUNDO AS TEORÍAS DE ARRHENIUS E BRÖNSTED-LOWRY. Arrhenius.- Ácido. substancia que en disolución acuosa disóciase producindo ións H. ( auga) AH H (aq.)
Procedementos operatorios de unións non soldadas
 Procedementos operatorios de unións non soldadas Técnicas de montaxe de instalacións Ciclo medio de montaxe e mantemento de instalacións frigoríficas 1 de 28 Técnicas de roscado Unha rosca é unha hélice
Procedementos operatorios de unións non soldadas Técnicas de montaxe de instalacións Ciclo medio de montaxe e mantemento de instalacións frigoríficas 1 de 28 Técnicas de roscado Unha rosca é unha hélice
Tema 3. Espazos métricos. Topoloxía Xeral,
 Tema 3. Espazos métricos Topoloxía Xeral, 2017-18 Índice Métricas en R n Métricas no espazo de funcións Bólas e relacións métricas Definición Unha métrica nun conxunto M é unha aplicación d con valores
Tema 3. Espazos métricos Topoloxía Xeral, 2017-18 Índice Métricas en R n Métricas no espazo de funcións Bólas e relacións métricas Definición Unha métrica nun conxunto M é unha aplicación d con valores
Química P.A.U. ENLACE QUÍMICO 1 ENLACE QUÍMICO
 Química P.A.U. ENLAE QUÍMI ENLAE QUÍMI UESTIÓNS ENLAE IÓNI. Razoa cal dos seguintes compostos terá maior punto de fusión: fluoruro de sodio ou bromuro de potasio. (P.A.U. Xuño 96) luoruro de sodio. punto
Química P.A.U. ENLAE QUÍMI ENLAE QUÍMI UESTIÓNS ENLAE IÓNI. Razoa cal dos seguintes compostos terá maior punto de fusión: fluoruro de sodio ou bromuro de potasio. (P.A.U. Xuño 96) luoruro de sodio. punto
CRITERIOS DE AVALIACIÓN. QUÍMICA (Cód. 27)
 CRITERIOS DE AVALIACIÓN QUÍMICA (Cód. 7) CRITERIOS XERAIS DE AVALIACIÓ DO EXAME DE QUÍMICA - As respostas deben axustarse ao enunciado da pregunta. - Terase en conta a claridade da exposición dos conceptos,
CRITERIOS DE AVALIACIÓN QUÍMICA (Cód. 7) CRITERIOS XERAIS DE AVALIACIÓ DO EXAME DE QUÍMICA - As respostas deben axustarse ao enunciado da pregunta. - Terase en conta a claridade da exposición dos conceptos,
Parte científico-técnica TECNOLOXÍA [CM.PC.002]
![Parte científico-técnica TECNOLOXÍA [CM.PC.002] Parte científico-técnica TECNOLOXÍA [CM.PC.002]](/thumbs/89/97642488.jpg) Parte científico-técnica TENOLOÍ [M.P.002] 1. Formato da proba Formato proba constará de cinco problemas e nove cuestións tipo test, distribuídos así: Problema 1: tres cuestións. Problema 2: dúas cuestións.
Parte científico-técnica TENOLOÍ [M.P.002] 1. Formato da proba Formato proba constará de cinco problemas e nove cuestións tipo test, distribuídos así: Problema 1: tres cuestións. Problema 2: dúas cuestións.
CALCULOS ELEMENTAIS EN QUIMICA. (I)
 CALCULOS ELEMENTAIS EN QUIMICA. (I) 1. 10 ml de hidróxido potásico neutralízanse con 35,4 ml dunha disolución 0,07 M de ácido sulfúrico. a/ Escriba e axuste a reacción de neutralización. b/ Calcule os
CALCULOS ELEMENTAIS EN QUIMICA. (I) 1. 10 ml de hidróxido potásico neutralízanse con 35,4 ml dunha disolución 0,07 M de ácido sulfúrico. a/ Escriba e axuste a reacción de neutralización. b/ Calcule os
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO. Datos Cifras significativas: 3 Gas: Volume V = 2,00 dm³. Ecuación de estado dos gases ideais
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un rcipint d 2 dm³ contén unha mstura gasosa n quilibrio d 0,003 mols d hidróxno, 0,003 mols d iodo 0,024 mols d ioduro
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un rcipint d 2 dm³ contén unha mstura gasosa n quilibrio d 0,003 mols d hidróxno, 0,003 mols d iodo 0,024 mols d ioduro
VALORACIÓN DOS RESULTADOS DAS PAU DE QUÍMICA (ENQUISAS RESPONDIDAS POLOS CORRECTORES/AS DA MATERIA) XUÑO 2011
 VALORACIÓN DOS RESULTADOS DAS PAU DE QUÍMICA (ENQUISAS RESPONDIDAS POLOS CORRECTORES/AS DA MATERIA) XUÑO 2011 A) AVALIACIÓN DOS RESULTADOS DA PROBA nº alumnado presentado Porcentaxe aptos/as Nota media
VALORACIÓN DOS RESULTADOS DAS PAU DE QUÍMICA (ENQUISAS RESPONDIDAS POLOS CORRECTORES/AS DA MATERIA) XUÑO 2011 A) AVALIACIÓN DOS RESULTADOS DA PROBA nº alumnado presentado Porcentaxe aptos/as Nota media
PAU XUÑO 2011 MATEMÁTICAS II
 PAU XUÑO 2011 MATEMÁTICAS II Código: 26 (O alumno/a debe responder só os exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio 2= 3 puntos, exercicio
PAU XUÑO 2011 MATEMÁTICAS II Código: 26 (O alumno/a debe responder só os exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio 2= 3 puntos, exercicio
EXERCICIOS DE ÁLXEBRA. PAU GALICIA
 Maemáicas II EXERCICIOS DE ÁLXEBRA PAU GALICIA a) (Xuño ) Propiedades do produo de marices (só enuncialas) b) (Xuño ) Sexan M e N M + I, onde I denoa a mariz idenidade de orde n, calcule N e M 3 Son M
Maemáicas II EXERCICIOS DE ÁLXEBRA PAU GALICIA a) (Xuño ) Propiedades do produo de marices (só enuncialas) b) (Xuño ) Sexan M e N M + I, onde I denoa a mariz idenidade de orde n, calcule N e M 3 Son M
Química prácticas (selectividad)
 Departamento de Ciencias Páxina 1 material de laboratorio Embudo Buchner conectado a un matraz Kitasato y a una bomba de vacío Embudo Buchner Departamento de Ciencias Páxina 2 Nome Usos Vaso de precipitados
Departamento de Ciencias Páxina 1 material de laboratorio Embudo Buchner conectado a un matraz Kitasato y a una bomba de vacío Embudo Buchner Departamento de Ciencias Páxina 2 Nome Usos Vaso de precipitados
PAU XUÑO 2016 QUÍMICA OPCIÓN A
 PAU Código: 7 XUÑO 016 QUÍMICA Calificación: El alumno elegirá UNA de las dos opciones. Cada pregunta se calificará con puntos. Todas las cuestiones teóricas deberán ser razonadas. OPCIÓN A 1. 1.1. Justifique,
PAU Código: 7 XUÑO 016 QUÍMICA Calificación: El alumno elegirá UNA de las dos opciones. Cada pregunta se calificará con puntos. Todas las cuestiones teóricas deberán ser razonadas. OPCIÓN A 1. 1.1. Justifique,
PAU XUÑO 2010 MATEMÁTICAS II
 PAU XUÑO 010 MATEMÁTICAS II Código: 6 (O alumno/a deber responder só aos eercicios dunha das opcións. Punuación máima dos eercicios de cada opción: eercicio 1= 3 punos, eercicio = 3 punos, eercicio 3 =
PAU XUÑO 010 MATEMÁTICAS II Código: 6 (O alumno/a deber responder só aos eercicios dunha das opcións. Punuación máima dos eercicios de cada opción: eercicio 1= 3 punos, eercicio = 3 punos, eercicio 3 =
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS
 Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS INTRODUCIÓN MÉTODO 1. En xeral: a) Debúxanse as forzas que actúan sobre o sistema. b) Calcúlase cada forza. c) Calcúlase a resultante polo principio
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS INTRODUCIÓN MÉTODO 1. En xeral: a) Debúxanse as forzas que actúan sobre o sistema. b) Calcúlase cada forza. c) Calcúlase a resultante polo principio
Ano 2018 FÍSICA. SOL:a...máx. 1,00 Un son grave ten baixa frecuencia, polo que a súa lonxitude de onda é maior.
 ABAU CONVOCAT ORIA DE SET EMBRO Ano 2018 CRIT ERIOS DE AVALI ACIÓN FÍSICA (Cód. 23) Elixir e desenvolver unha das dúas opcións. As solución numéricas non acompañadas de unidades ou con unidades incorrectas...
ABAU CONVOCAT ORIA DE SET EMBRO Ano 2018 CRIT ERIOS DE AVALI ACIÓN FÍSICA (Cód. 23) Elixir e desenvolver unha das dúas opcións. As solución numéricas non acompañadas de unidades ou con unidades incorrectas...
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS
 Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS PROBLEMAS M.H.S.. 1. Dun resorte elástico de constante k = 500 N m -1 colga unha masa puntual de 5 kg. Estando o conxunto en equilibrio, desprázase
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS PROBLEMAS M.H.S.. 1. Dun resorte elástico de constante k = 500 N m -1 colga unha masa puntual de 5 kg. Estando o conxunto en equilibrio, desprázase
ln x, d) y = (3x 5 5x 2 + 7) 8 x
 EXERCICIOS AUTOAVALIABLES: CÁLCULO DIFERENCIAL. Deriva: a) y 7 6 + 5, b) y e, c) y e) y 7 ( 5 ), f) y ln, d) y ( 5 5 + 7) 8 n e ln, g) y, h) y n. Usando a derivada da función inversa, demostra que: a)
EXERCICIOS AUTOAVALIABLES: CÁLCULO DIFERENCIAL. Deriva: a) y 7 6 + 5, b) y e, c) y e) y 7 ( 5 ), f) y ln, d) y ( 5 5 + 7) 8 n e ln, g) y, h) y n. Usando a derivada da función inversa, demostra que: a)
A proba constará de vinte cuestións tipo test. As cuestións tipo test teñen tres posibles respostas, das que soamente unha é correcta.
 Páxina 1 de 9 1. Formato da proba Formato proba constará de vinte cuestións tipo test. s cuestións tipo test teñen tres posibles respostas, das que soamente unha é correcta. Puntuación Puntuación: 0.5
Páxina 1 de 9 1. Formato da proba Formato proba constará de vinte cuestións tipo test. s cuestións tipo test teñen tres posibles respostas, das que soamente unha é correcta. Puntuación Puntuación: 0.5
PAU Setembro 2010 FÍSICA
 PAU Setembro 010 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU Setembro 010 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
Física P.A.U. ELECTROMAGNETISMO 1 ELECTROMAGNETISMO
 Física P.A.U. ELECTROMAGNETISMO 1 ELECTROMAGNETISMO PROBLEMAS CAMPO ELECTROSTÁTICO 1. Dúas cargas eléctricas de 3 mc están situadas en A(4, 0) e B(-4, 0) (en metros). Calcula: a) O campo eléctrico en C(0,
Física P.A.U. ELECTROMAGNETISMO 1 ELECTROMAGNETISMO PROBLEMAS CAMPO ELECTROSTÁTICO 1. Dúas cargas eléctricas de 3 mc están situadas en A(4, 0) e B(-4, 0) (en metros). Calcula: a) O campo eléctrico en C(0,
Física P.A.U. GRAVITACIÓN 1 GRAVITACIÓN
 Física P.A.U. GRAVITACIÓN 1 GRAVITACIÓN PROBLEMAS SATÉLITES 1. O período de rotación da Terra arredor del Sol é un año e o radio da órbita é 1,5 10 11 m. Se Xúpiter ten un período de aproximadamente 12
Física P.A.U. GRAVITACIÓN 1 GRAVITACIÓN PROBLEMAS SATÉLITES 1. O período de rotación da Terra arredor del Sol é un año e o radio da órbita é 1,5 10 11 m. Se Xúpiter ten un período de aproximadamente 12
PAU XUÑO 2012 MATEMÁTICAS II
 PAU Código: 6 XUÑO 01 MATEMÁTICAS II (Responder só aos exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio = 3 puntos, exercicio 3= puntos, exercicio
PAU Código: 6 XUÑO 01 MATEMÁTICAS II (Responder só aos exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio = 3 puntos, exercicio 3= puntos, exercicio
Exame tipo. C. Problemas (Valoración: 5 puntos, 2,5 puntos cada problema)
 Exame tipo A. Proba obxectiva (Valoración: 3 puntos) 1. - Un disco de 10 cm de raio xira cunha velocidade angular de 45 revolucións por minuto. A velocidade lineal dos puntos da periferia do disco será:
Exame tipo A. Proba obxectiva (Valoración: 3 puntos) 1. - Un disco de 10 cm de raio xira cunha velocidade angular de 45 revolucións por minuto. A velocidade lineal dos puntos da periferia do disco será:
VALORACIÓN DOS RESULTADOS DAS ABAU DE QUÍMICA (ENQUISAS RESPOSTADAS POLOS CORRECTORES DA MATERIA) XUÑO nº alumnos presentados OPCIÓNS
 VALORACIÓN DOS RESULTADOS DAS ABAU DE QUÍMICA (ENQUISAS RESPOSTADAS POLOS CORRECTORES DA MATERIA) XUÑO 2017 A) AVALIACIÓN DOS RESULTADOS DA PROBA Total Acceso Bacharelato Opción A Elixida por un 71,6%
VALORACIÓN DOS RESULTADOS DAS ABAU DE QUÍMICA (ENQUISAS RESPOSTADAS POLOS CORRECTORES DA MATERIA) XUÑO 2017 A) AVALIACIÓN DOS RESULTADOS DA PROBA Total Acceso Bacharelato Opción A Elixida por un 71,6%
Exercicios de Física 02a. Campo Eléctrico
 Exercicios de Física 02a. Campo Eléctrico Problemas 1. Dúas cargas eléctricas de 3 mc están situadas en A(4,0) e B( 4,0) (en metros). Caalcula: a) o campo eléctrico en C(0,5) e en D(0,0) b) o potencial
Exercicios de Física 02a. Campo Eléctrico Problemas 1. Dúas cargas eléctricas de 3 mc están situadas en A(4,0) e B( 4,0) (en metros). Caalcula: a) o campo eléctrico en C(0,5) e en D(0,0) b) o potencial
Volume dos corpos xeométricos
 11 Volume dos corpos xeométricos Obxectivos Nesta quincena aprenderás a: Comprender o concepto de medida do volume e coñecer e manexar as unidades de medida do S.M.D. Obter e aplicar expresións para o
11 Volume dos corpos xeométricos Obxectivos Nesta quincena aprenderás a: Comprender o concepto de medida do volume e coñecer e manexar as unidades de medida do S.M.D. Obter e aplicar expresións para o
Código: 25 PAU XUÑO 2014 FÍSICA OPCIÓN A OPCIÓN B
 PAU XUÑO 2014 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU XUÑO 2014 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
Física P.A.U. ÓPTICA 1 ÓPTICA
 Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10¹⁴ Hz incide cun ángulo de incidencia de 30 sobre unha lámina de vidro de caras plano-paralelas de espesor 10
Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10¹⁴ Hz incide cun ángulo de incidencia de 30 sobre unha lámina de vidro de caras plano-paralelas de espesor 10
Física A.B.A.U. GRAVITACIÓN 1 GRAVITACIÓN
 Física A.B.A.U. GRAVITACIÓN 1 GRAVITACIÓN PROBLEMAS 1. A luz do Sol tarda 5 10² s en chegar á Terra e 2,6 10³ s en chegar a Xúpiter. a) O período de Xúpiter orbitando arredor do Sol. b) A velocidade orbital
Física A.B.A.U. GRAVITACIÓN 1 GRAVITACIÓN PROBLEMAS 1. A luz do Sol tarda 5 10² s en chegar á Terra e 2,6 10³ s en chegar a Xúpiter. a) O período de Xúpiter orbitando arredor do Sol. b) A velocidade orbital
PAU XUÑO Código: 25 FÍSICA OPCIÓN A OPCIÓN B
 PAU XUÑO 013 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU XUÑO 013 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
MATEMÁTICAS. (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 puntos)
 21 MATEMÁTICAS (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 Dada a matriz a) Calcula os valores do parámetro m para os que A ten inversa.
21 MATEMÁTICAS (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 Dada a matriz a) Calcula os valores do parámetro m para os que A ten inversa.
TRIGONOMETRIA. hipotenusa L 2. hipotenusa
 TRIGONOMETRIA. Calcular las razones trigonométricas de 0º, º y 60º. Para calcular las razones trigonométricas de º, nos ayudamos de un triángulo rectángulo isósceles como el de la figura. cateto opuesto
TRIGONOMETRIA. Calcular las razones trigonométricas de 0º, º y 60º. Para calcular las razones trigonométricas de º, nos ayudamos de un triángulo rectángulo isósceles como el de la figura. cateto opuesto
Física P.A.U. ÓPTICA 1 ÓPTICA
 Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10 14 Hz incide, cun ángulo de incidencia de 30, sobre unha lámina de vidro de caras plano-paralelas de espesor
Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10 14 Hz incide, cun ángulo de incidencia de 30, sobre unha lámina de vidro de caras plano-paralelas de espesor
NÚMEROS COMPLEXOS. Páxina 147 REFLEXIONA E RESOLVE. Extraer fóra da raíz. Potencias de. Como se manexa k 1? Saca fóra da raíz:
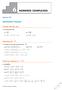 NÚMEROS COMPLEXOS Páxina 7 REFLEXIONA E RESOLVE Extraer fóra da raíz Saca fóra da raíz: a) b) 00 a) b) 00 0 Potencias de Calcula as sucesivas potencias de : a) ( ) ( ) ( ) b) ( ) c) ( ) 5 a) ( ) ( ) (
NÚMEROS COMPLEXOS Páxina 7 REFLEXIONA E RESOLVE Extraer fóra da raíz Saca fóra da raíz: a) b) 00 a) b) 00 0 Potencias de Calcula as sucesivas potencias de : a) ( ) ( ) ( ) b) ( ) c) ( ) 5 a) ( ) ( ) (
Código: 25 XUÑO 2014 PAU FÍSICA OPCIÓN A OPCIÓN B
 PAU Código: 25 XUÑO 204 FÍSICA Puntuación máxima: Cuestións 4 puntos ( cada cuestión, teórica ou práctica). Problemas 6 puntos ( cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU Código: 25 XUÑO 204 FÍSICA Puntuación máxima: Cuestións 4 puntos ( cada cuestión, teórica ou práctica). Problemas 6 puntos ( cada apartado). Non se valorará a simple anotación dun ítem como solución
Resorte: estudio estático e dinámico.
 ESTUDIO DO RESORTE (MÉTODOS ESTÁTICO E DINÁMICO ) 1 Resorte: estudio estático e dinámico. 1. INTRODUCCIÓN TEÓRICA. (No libro).. OBXECTIVOS. (No libro). 3. MATERIAL. (No libro). 4. PROCEDEMENTO. A. MÉTODO
ESTUDIO DO RESORTE (MÉTODOS ESTÁTICO E DINÁMICO ) 1 Resorte: estudio estático e dinámico. 1. INTRODUCCIÓN TEÓRICA. (No libro).. OBXECTIVOS. (No libro). 3. MATERIAL. (No libro). 4. PROCEDEMENTO. A. MÉTODO
PAAU (LOXSE) Setembro 2006
 PAAU (LOXSE) Setembro 2006 Código: 22 FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (,5 cada apartado). Cuestións 4 puntos ( cada cuestión, teórica
PAAU (LOXSE) Setembro 2006 Código: 22 FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (,5 cada apartado). Cuestións 4 puntos ( cada cuestión, teórica
FÍSICA OPCIÓN 1. ; calcula: a) o período de rotación do satélite, b) o peso do satélite na órbita. (Datos R T. = 9,80 m/s 2 ).
 22 Elixir e desenrolar unha das dúas opcións propostas. FÍSICA Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Non se valorará a simple
22 Elixir e desenrolar unha das dúas opcións propostas. FÍSICA Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Non se valorará a simple
XEOMETRÍA NO ESPAZO. - Se dun vector se coñecen a orixe, o módulo, a dirección e o sentido, este está perfectamente determinado no espazo.
 XEOMETRÍA NO ESPAZO Vectores fixos Dos puntos do espazo, A e B, determinan o vector fixo AB, sendo o punto A a orixe e o punto B o extremo, é dicir, un vector no espazo é calquera segmento orientado que
XEOMETRÍA NO ESPAZO Vectores fixos Dos puntos do espazo, A e B, determinan o vector fixo AB, sendo o punto A a orixe e o punto B o extremo, é dicir, un vector no espazo é calquera segmento orientado que
IX. ESPAZO EUCLÍDEO TRIDIMENSIONAL: Aplicacións ao cálculo de distancias, áreas e volumes
 IX. ESPAZO EUCLÍDEO TRIDIMENSIONAL: Aplicacións ao cálculo de distancias, áreas e volumes 1.- Distancia entre dous puntos Se A e B son dous puntos do espazo, defínese a distancia entre A e B como o módulo
IX. ESPAZO EUCLÍDEO TRIDIMENSIONAL: Aplicacións ao cálculo de distancias, áreas e volumes 1.- Distancia entre dous puntos Se A e B son dous puntos do espazo, defínese a distancia entre A e B como o módulo
PAAU (LOXSE) Xuño 2002
 PAAU (LOXSE) Xuño 00 Código: FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica).
PAAU (LOXSE) Xuño 00 Código: FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica).
FISICA 2º BAC 27/01/2007
 POBLEMAS 1.- Un corpo de 10 g de masa desprázase cun movemento harmónico simple de 80 Hz de frecuencia e de 1 m de amplitude. Acha: a) A enerxía potencial cando a elongación é igual a 70 cm. b) O módulo
POBLEMAS 1.- Un corpo de 10 g de masa desprázase cun movemento harmónico simple de 80 Hz de frecuencia e de 1 m de amplitude. Acha: a) A enerxía potencial cando a elongación é igual a 70 cm. b) O módulo
EQUILIBRIO QUÍMICO. 2 HI (g)
 EQUILIBRIO QUÍMICO 1- EQUILIBRIO QUÍMICO APLICADO A REACCIÓNS EN FASE GASOSA EN CONDICIÓNS IDEAIS. Se itroducimos H 2 (g) e I 2 (g) u recipiete pechado e matemos a temperatura costate podemos apreciar
EQUILIBRIO QUÍMICO 1- EQUILIBRIO QUÍMICO APLICADO A REACCIÓNS EN FASE GASOSA EN CONDICIÓNS IDEAIS. Se itroducimos H 2 (g) e I 2 (g) u recipiete pechado e matemos a temperatura costate podemos apreciar
PAU Xuño Código: 25 FÍSICA OPCIÓN A OPCIÓN B
 PAU Xuño 00 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos ( cada cuestión, teórica ou práctica). Problemas 6 puntos ( cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU Xuño 00 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos ( cada cuestión, teórica ou práctica). Problemas 6 puntos ( cada apartado). Non se valorará a simple anotación dun ítem como solución
Física e Química 4º ESO
 Física e Química 4º ESO DEPARTAMENTO DE FÍSICA E QUÍMICA Física: Temas 1 ao 6. 01/03/07 Nome: Cuestións 1. Un móbil ten unha aceleración de -2 m/s 2. Explica o que significa isto. 2. No medio dunha tormenta
Física e Química 4º ESO DEPARTAMENTO DE FÍSICA E QUÍMICA Física: Temas 1 ao 6. 01/03/07 Nome: Cuestións 1. Un móbil ten unha aceleración de -2 m/s 2. Explica o que significa isto. 2. No medio dunha tormenta
PROGRAMACIÓN 2º BACHARELATO QUÍMICA 1
 PROGRAMACIÓN 2º BACHARELATO QUÍMICA 1 PROGRAMACIÓN 2º BACHARELATO QUÍMICA 2 1. OBXECTIVOS. O Departamento seguirá as recomendacións da CIuG, e en aplicación do Decreto 231/2002 do 6 de xuño(dog do 15 de
PROGRAMACIÓN 2º BACHARELATO QUÍMICA 1 PROGRAMACIÓN 2º BACHARELATO QUÍMICA 2 1. OBXECTIVOS. O Departamento seguirá as recomendacións da CIuG, e en aplicación do Decreto 231/2002 do 6 de xuño(dog do 15 de
Código: 25 PAU XUÑO 2012 FÍSICA OPCIÓN A OPCIÓN B
 PAU XUÑO 2012 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU XUÑO 2012 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
Profesor: Guillermo F. Cloos Física e química 1º Bacharelato O enlace químico 3 1
 UNIÓNS ENTRE ÁTOMOS, AS MOLÉCULAS E OS CRISTAIS Até agora estudamos os átomos como entidades illadas, pero isto rara vez ocorre na realidade xa que o máis frecuente é que os átomos estea influenciados
UNIÓNS ENTRE ÁTOMOS, AS MOLÉCULAS E OS CRISTAIS Até agora estudamos os átomos como entidades illadas, pero isto rara vez ocorre na realidade xa que o máis frecuente é que os átomos estea influenciados
Problemas xeométricos
 Problemas xeométricos Contidos 1. Figuras planas Triángulos Paralelogramos Trapecios Trapezoides Polígonos regulares Círculos, sectores e segmentos 2. Corpos xeométricos Prismas Pirámides Troncos de pirámides
Problemas xeométricos Contidos 1. Figuras planas Triángulos Paralelogramos Trapecios Trapezoides Polígonos regulares Círculos, sectores e segmentos 2. Corpos xeométricos Prismas Pirámides Troncos de pirámides
Alumna/o Medida-unidades Erro absoluto. Valor medio: Erro relativo: EXPERIENCIA 2: DETERMINACION DE SUPERFICIES POR MEDIDA DIRECTA
 PRÁCTICA 1 REALIZACIÓN DE MEDIDAS OBXECTIVOS: 1. Construír táboas de datos 2. Expresar correctamente o resultado das medidas 3. Aplicar a noción de que o valor medio é o que mais se aproxima ó valor verdadeiro.
PRÁCTICA 1 REALIZACIÓN DE MEDIDAS OBXECTIVOS: 1. Construír táboas de datos 2. Expresar correctamente o resultado das medidas 3. Aplicar a noción de que o valor medio é o que mais se aproxima ó valor verdadeiro.
Sistemas e Inecuacións
 Sistemas e Inecuacións 1. Introdución 2. Sistemas lineais 2.1 Resolución gráfica 2.2 Resolución alxébrica 3. Método de Gauss 4. Sistemas de ecuacións non lineais 5. Inecuacións 5.1 Inecuacións de 1º e
Sistemas e Inecuacións 1. Introdución 2. Sistemas lineais 2.1 Resolución gráfica 2.2 Resolución alxébrica 3. Método de Gauss 4. Sistemas de ecuacións non lineais 5. Inecuacións 5.1 Inecuacións de 1º e
VII. RECTAS E PLANOS NO ESPAZO
 VII. RETS E PLNOS NO ESPZO.- Ecuacións da recta Unha recta r no espao queda determinada por un punto, punto base, e un vector v non nulo que se chama vector director ou direccional da recta; r, v é a determinación
VII. RETS E PLNOS NO ESPZO.- Ecuacións da recta Unha recta r no espao queda determinada por un punto, punto base, e un vector v non nulo que se chama vector director ou direccional da recta; r, v é a determinación
ELECTROTECNIA. BLOQUE 1: ANÁLISE DE CIRCUÍTOS (Elixir A ou B) A.- No circuíto da figura determinar o valor da intensidade na resistencia R 2
 36 ELECTROTECNIA O exame consta de dez problemas, debendo o alumno elixir catro, un de cada bloque. Non é necesario elixir a mesma opción (A ou B ) de cada bloque. Todos os problemas puntúan igual, é dicir,
36 ELECTROTECNIA O exame consta de dez problemas, debendo o alumno elixir catro, un de cada bloque. Non é necesario elixir a mesma opción (A ou B ) de cada bloque. Todos os problemas puntúan igual, é dicir,
Código: 25 MODELO DE EXAME ABAU FÍSICA OPCIÓN A OPCIÓN B
 ABAU Código: 25 MODELO DE EXAME FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como
ABAU Código: 25 MODELO DE EXAME FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como
Código: 25 XUÑO 2012 PAU FÍSICA OPCIÓN A OPCIÓN B
 PAU Código: 25 XUÑO 2012 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU Código: 25 XUÑO 2012 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU XUÑO 2012 FÍSICA
 PAU XUÑO 2012 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica) Problemas 6 puntos (1 cada apartado) Non se valorará a simple anotación dun ítem como solución
PAU XUÑO 2012 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica) Problemas 6 puntos (1 cada apartado) Non se valorará a simple anotación dun ítem como solución
2.6 Teoría atómica (unha longa historia)
 2.6 Teoría atómica (unha longa historia) Milleiros de resultados experimentais avalan a idea de que as partículas que forman os gases, os sólidos e os líquidos, en todo o universo, están constituídas por
2.6 Teoría atómica (unha longa historia) Milleiros de resultados experimentais avalan a idea de que as partículas que forman os gases, os sólidos e os líquidos, en todo o universo, están constituídas por
PAU Xuño 2011 FÍSICA OPCIÓN A
 PAU Xuño 20 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos ( cada cuestión, teórica ou práctica). Problemas 6 puntos ( cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU Xuño 20 Código: 25 FÍSICA Puntuación máxima: Cuestións 4 puntos ( cada cuestión, teórica ou práctica). Problemas 6 puntos ( cada apartado). Non se valorará a simple anotación dun ítem como solución
PAAU (LOXSE) Xuño 2006
 PAAU (LOXSE) Xuño 006 Código: FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica).
PAAU (LOXSE) Xuño 006 Código: FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica).
