Σχ. 1: Τυπική μορφή μοριακού δυναμικού.
|
|
|
- Σωστράτη Γεννάδιος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-1 Κεφάλαιο 6. Μόρια Εδάφια: 6.a. Μόρια και μοριακοί δεσμοί 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού 6.c. Περιστροφή και ταλάντωση μορίων 6.d. Μοριακά φάσματα 6.a. Μόρια και μοριακοί δεσμοί Μόριο ονομάζουμε ένα σύνολο ατόμων που είναι ενωμένα με χημικούς δεσμούς. Τα μόρια υπάρχουν στη φύση γιατί είναι ενεργειακά συμφερότερες καταστάσεις από ό,τι τα μεμονωμένα άτομά τους. Οι ιδιότητες του κάθε μορίου εξαρτώνται από τα άτομα που το αποτελούν και από το είδος των δεσμών μεταξύ τους. Οι δεσμοί αυτοί, όπως θα γίνει φανερό στη συνέχεια, οφείλονται στα εξωτερικά ηλεκτρόνια, τα οποία ονομάζονται και ηλεκτρόνια σθένους (υπεύθυνα για το "σθενος" των ατόμων στο να σχηματίζουν δεσμούς). Οι δεσμοί ανάμεσα στα άτομα του μορίου οφείλονται σε ηλεκτροστατικές δυνάμεις μεταξύ των ατόμων αυτών. Οι δυνάμεις αυτές είναι συνδυασμός απωστικών και ελκτικών δυνάμεων (λόγω άπωσης των ομώνυμων φορτίων και έλξης των ετερώνυμων φορτίων των ατόμων). Το δυναμικό σε ένα διατομικό μόριο, ως συνάρτηση της απόστασης των πυρήνων, μπορεί να προσεγγιστεί από την έκφραση (1) (άθροισμα ενός ελκτικού και ενός απωστικού όρου), και έχει τη μορφή που δείχνεται στο Σχ. 1. Στην (1) r είναι η απόσταση μεταξύ των πυρήνων, n και m είναι μικροί ακέραιοι και Α κα Β σταθερές. Σχ. 1: Τυπική μορφή μοριακού δυναμικού. Το δυναμικό U είναι αρνητικό (ελκτικό) ή θετικό (απωστικό) ανάλογα με την απόσταση ανάμεσα στα άτομα. Η θέση ισορροπίας του μορίου (απόσταση ισορροπίας των ατόμων του) είναι στο ελάχιστο του δυναμικού (τότε η συνολική δύναμη (=παράγωγος του δυναμικού)
2 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-2 είναι μηδέν). Παρατηρήστε την ομοιότητα του μοριακού δυναμικού κοντά στο ελάχιστό του με το δυναμικό αρμονικού ταλαντωτή. Η λεπτομερής περιγραφή των δεσμών (μηχανισμών σύνδεσης) των ατόμων για το σχηματισμό μορίου είναι πολύπλοκο πρόβλημα που εμπεριέχει αλληλεπιδράσεις πολλών σωματιδίων. Μπορούμε παρόλα αυτά να περιγράψουμε τους δεσμούς χρησιμοποιώντας μερικά απλοποιημένα μοντέλα, που αναπαράγουν αρκετά ικανοποιητικά τα βασικά χαρ/κά των διαφόρων ειδών δεσμού. Οι μοριακοί δεσμοί μπορούν να καταταγούν σε μια από τις παρακάτω κατηγορίες: 1. Ιοντικός ή ετεροπολικός δεσμός 2. Ομοιοπολικός δεσμός 3. Δεσμός Υδρογόνου 4. Δεσμός Van der Waals Στον ιοντικό δεσμό ένα εξωτερικό ηλεκτρόνιο ενός ατόμου, το οποίο είναι χαλαρά δέσμιο (βλέπει τον πυρήνα ισχυρά θωρακισμένο από το νέφος των εσωτερικότερων ηλεκτρονίων), προσχωρεί σε ένα άλλο άτομο (το οποίο το δέχεται ευχαρίστως γιατί έτσι συμπληρώνει τις στοιβάδες του και γίνεται σταθερότερο). Τα δύο αυτά άτομα γίνονται έτσι ιόντα και κρατιούνται ενωμένα λόγω της ηλεκτροστατικής τους έλξης. Παράδειγμα ιοντικού δεσμού έχουμε στο NaCl, για το σχηματισμό του οποίου το τελευταίο ηλεκτρόνιο του Na (Ζ=11) (σε ποια στοιβάδα βρίσκεται;) συλλαμβάνεται από το Cl (Ζ=17), συμπληρώνοντας την τελευταία ημικατειλημμένη στάθμη του. Η απόσταση ισορροπίας (απόσταση πυρήνων) του μορίου του NaCl είναι 0,24 nm και η ενέργεια διάσπασής του (ίση με την ενέργεια που κερδίζεται κατά το σχηματισμό του μορίου) είναι 4,2 ev. Στον ομοιοπολικό δεσμό δεν έχουμε προσχώρηση των ηλεκτρονίων σθένους από το ένα άτομο στο άλλο, αλλά έχουμε μάλλον μοίρασμα των ηλεκτρονίων μεταξύ των ατόμων (κοινοκτημοσύνη). Τα ηλεκτρόνια, π.χ. σε ένα διατομικό μόριο, έλκονται ταυτόχρονα από τους πυρήνες και των δύο ατόμων και αυτή η έλξη είναι που κρατάει τα άτομα ενωμένα. Το γεγονός ότι τα ηλεκτρόνια αξιοποιούν την έλξη και των δύο πυρήνων ταυτόχρονα κάνει το μόριο είναι ενεργειακά συμφερότερη κατάσταση (περισσότερη έλξη περισσότερο αρνητική (χαμηλότερη) ενέργεια). Παράδειγμα ομοιοπολικού δεσμού είναι ο δεσμός μεταξύ όμοιων ατόμων, π.χ. στο μόριο H 2, βλ. Σχ. 2. Σχ. 2: Ομοιοπολικός δεσμός στο μόριο του H 2. Για την καλύτερη κατανόηση του ομοιοπολικού δεσμού κοιτάτε και το επόμενο εδάφιο, «Κβαντομηχανική περιγραφή του χημικού δεσμού». Ο δεσμός Υδρογόνου είναι εξαιρετικά ασθενής αλλά με πολύ μεγάλη βιολογική σημασία, επειδή είναι ο δεσμός που συνδέει τμήματα πολύ βασικών βιολογικών μορίων (π.χ. στο DNA
3 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-3 τις στροφές της έλικας). Στο δεσμό Υδρογόνου δύο αρνητικά ιόντα κρατιούνται ενωμένα μέσω της έλξης και των δύο με το πρωτόνιο του ατόμου του Η. Π.χ. στο ιόν του HF 2 -, βλ. Σχ. 3. Σχ. 3: Ο δεσμός Υδρογόνου στο ιόν του HF 2 -. Η ενέργεια σύνδεσης του ιόντος είναι 0.1 ev. Οι δεσμοί Van der Waals είναι ασθενέστεροι από όλους τους παραπάνω δεσμούς. Είναι κυρίως δεσμοί μεταξύ μορίων (ή ατόμων που δεν συνδέονται με ιοντικούς ή ομοιοπολικούς δεσμούς) για το σχηματισμό της στερεάς, υγρής ή αέριας ύλης. Οφείλονται στις αδύναμες ηλεκτροστατικές έλξεις ανάμεσα στα ουδέτερα αυτά μόρια. Οι δυνάμεις Van der Waals είναι τριών ειδών: Δύναμη διπόλου-διπόλου: Αλληλεπίδραση μορίων με μόνιμη διπολική ροπή (λόγω της ανομοιόμορφης κατανομής φορτίου στο κάθε μόριο). Το μόριο αλληλεπιδρά με το ηλεκτρικό πεδίο που δημιουργείται από το άλλο μόριο. Η εξάρτηση της δύναμης αυτής από την απόσταση μεταξύ των μορίων είναι της μορφής. Δύναμη διπόλου - διπόλου εξ επαγωγής: Το ηλεκτρικό πεδίο του ενός μορίου-διπόλου πολώνει το δεύτερο μόριο αλληλεπίδραση διπόλου-διπόλου εξ επαγωγής. Η εξάρτηση της δύναμης αυτής από την απόσταση μεταξύ των μορίων είναι της μορφής. Δύναμη διασποράς: Δύναμη μεταξύ μη πολικών μορίων. Λόγω της ανομοιόμορφης κατανομής φορτίου στο κάθε μόριο τα φορτία του ενός, όταν τα μόρια έλθουν κοντά, "βλέπουν" τα φορτία του άλλου. Οι δεσμοί Van der Waals είναι αυτοί που καθορίζουν αν μια ουσία θα είναι υγρή ή αέρια σε θερμοκρασία περιβάλλοντος. Μια ουσία που αποτελείται από μη πολικά μόρια περιμένουμε να είναι αέρια (π.χ. H 2 ) ενώ μια ουσία που αποτελείται από πολικά μόρια θα είναι υγρή (π.χ. H 2 Ο). 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού Σε κάθε μεμονωμένο άτομο τα ηλεκτρόνια σθένους έλκονται από το "ενεργό" πυρηνικό φορτίο του ατόμου, παραμένοντας δέσμια στο άτομο. Άρα τα ηλεκτρόνια μπορούν να προσεγγιστούν με σωματίδια παγιδευμένα σε ένα πηγάδι δυναμικού (το οποίο για ποιοτική περιγραφή μπορεί να θεωρηθεί τετραγωνικό). Θα χρησιμοποιήσουμε την προσέγγιση αυτή για να μελετήσουμε κβαντομηχανικά το σχηματισμό του μορίου του Η 2. Κατά το σχηματισμό του Η 2 δύο πηγάδια δυναμικού έρχονται κοντά το ένα στο άλλο. Στην περίπτωση αυτή δίδεται η δυνατότητα στα ηλεκτρόνια του ενός ατόμου να μεταπηδήσουν και στο άλλο άτομο (γιατί;). Η επιπλέον ηλεκτροστατική έλξη που δέχονται τα ηλεκτρόνια του κάθε ατόμου από το δεύτερο άτομο έχει ως αποτέλεσμα την τροποποίηση του δυναμικού
4 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-4 του συστήματος και άρα και των ενεργειακών του καταστάσεων, σε σχέση με τις καταστάσεις των δύο μεμονωμένων ατόμων. Η τροποποίηση αυτή φαίνεται στο Σχ. 4. Σχ. 4: Η ένωση δύο ατόμων Η για το σχηματισμό του Η 2. Φαίνονται οι ενεργειακές στάθμες που προκύπτουν καθώς και οι αντίστοιχες κυματοσυναρτήσεις. Οι δύο νέες καταστάσεις (μοριακές στάθμες) που προκύπτουν από τις στάθμες Ε 1 (Σχ. 4) έχουν ενέργεια Ε 1 -δε και Ε 1 +δε, όπου το δε (θετικό) είναι τόσο μεγαλύτερο όσο μεγαλύτερη είναι η δυνατότητα μεταπήδησης του ηλεκτρονίου από το ένα άτομο στο άλλο (ή, πιο μαθηματικά, όσο μεγαλύτερη είναι η επικάλυψη των κυματοσυναρτήσεων των δύο ατομικών σταθμών, για τη δεδομένη απόσταση των ατόμων). Ο εποικισμός των μοριακών σταθμών από τα ηλεκτρόνια των ατόμων γίνεται και εδώ χρησιμοποιώντας την αρχή του Pauli. Στο Σχ. 5 φαίνεται ο εποικισμός αυτός για το μόριο του Η 2. Σχ. 5: Ο εποικισμός των μοριακών σταθμών στο μόριο του Η 2. Από το Σχ. 5 φαίνεται γιατί ο σχηματισμός του μορίου του Η 2 είναι συμφερότερη κατάσταση σε σχέση με δύο μεμονωμένα άτομα Η. Γιατί; Εν γένει, σε ένα μόριο, από κάθε ατομική στάθμη προκύπτουν τόσες μοριακές στάθμες όσος είναι και ο αριθμός των ατόμων που αποτελούν το μόριο. Η κατάληψη των σταθμών γίνεται με βάση την αρχή του Pauli. Όταν η προκύπτουσα κατάσταση δεν συμφέρει ενεργειακά τα άτομα δεν σχηματίζουν μόριο. Ερωτήσεις Χρησιμοποιώντας τα παραπάνω εξηγήστε γιατί τα εσωτερικά ηλεκτρόνια των ατόμων δεν παίζουν ρόλο στο σχηματισμό μορίων. Εξηγήστε γιατί τα ευγενή αέρια δεν σχηματίζουν μόρια. Χρησιμοποιήστε την αρχή της αβεβαιότητας για να εξηγήσετε γιατί συμφέρει ενεργειακά το κάθε ηλεκτρόνιο του μορίου να "χρησιμοποιεί" και τα δύο άτομα. Με βάση αυτά που είχαμε πει στο φαινόμενο σήραγγας εξηγήστε γιατί όταν δύο άτομα έλθουν κοντά τα ηλεκτρόνιά τους μπορούν να μεταπηδούν από το ένα στο άλλο. Στο μόριο του Η 2 έχουμε τη συνένωση δύο όμοιων ατόμων, δηλαδή δύο όμοιων πηγαδιών δυναμικού. Στην περίπτωση αυτή έχουμε ίση πιθανότητα να βρούμε το κάθε ηλεκτρόνιο
5 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-5 σθένους κοντά στο ένα ή το άλλο άτομο και άρα το μόριό μας είναι μη πολικό, δηλαδή το κέντρο "βάρους" τόσο του αρνητικού όσο και του θετικού φορτίου είναι στο κέντρο του μορίου. Ο δεσμός στην περίπτωση αυτή είναι ομοιοπολικός, γιατί τα ηλεκτρόνια σθένους τα "μοιράζονται εξίσου" και τα δύο άτομα. Στις περιπτώσεις όπου το μόριο αποτελείται από ανόμοια άτομα έχουμε συνένωση δύο πηγαδιών δυναμικού διαφορετικού βάθους. Στην περίπτωση αυτή, βλ. Σχ. 6, τα ηλεκτρόνια θα έχουν την τάση να περνούν τον περισσότερο χρόνο της ζωής τους κοντά στο βαθύτερο πηγάδι (στο ισχυρότερο ελκτικό κέντρο). Ως αποτέλεσμα θα έχουμε ένα πολικό μόριο (ανομοιόμορφη κατανομή φορτίου στον όγκο του μορίου, αφού τα ηλεκτρόνια σθένους θα βρίσκονται κατά το πλείστον στη γειτονιά του βαθύτερου πηγαδιού, αφήνοντας το πιο ρηχό πηγάδι με περίσσεια θετικού φορτίου). Ο δεσμός στην περίπτωση αυτή είναι κυρίως ετεροπολικός. Σχ. 6: Ο σχηματισμός των σταθμών μορίου που αποτελείται από δύο διαφορετικά άτομα (δείχνονται μόνο οι μοριακές στάθμες που προκύπτουν από τις τελευταίες εποικισμένες ατομικές στάθμες). Εν γένει, η ενέργεια της χαμηλότερης από τις δύο μοριακές στάθμες είναι λίγο μικρότερη από Ε 2 και της υψηλότερης λίγο μεγαλύτερη από Ε 1. Εφαρμογή Αναλύστε κβαντομηχανικά τη δομή του μορίου του νερού (H 2 O) και εξηγήστε το τριγωνικό σχήμα του, την ικανότητά του να διαλύει τις πολικές ενώσεις (π.χ. αλάτι), τη μεγάλη θερμοχωρητικότητά του και το γεγονός ότι ο πάγος επιπλέει στο νερό. Όσον αφορά τώρα τη μορφή των μοριακών κυματοσυναρτήσεων στο χώρο: Αν οι ατομικές καταστάσεις που "ενώνονται" για να σχηματίσουν τον χημικό δεσμό (ατομικά τροχιακά σθένους) είναι καταστάσεις τύπου s, ή καταστάσεις τύπου p που ενώνονται όπως φαίνεται στο πάνω από τα Σχ. 7 (μετωπικά), η προκύπτουσα κατάσταση έχει συμμετρία περιστροφής γύρω από τον άξονα του μορίου. Ένας τέτοιος δεσμός λέγεται τύπου σ και είναι εξαιρετικά ισχυρός. Αν τα ατομικά τροχιακά σθένους ενώνονται "πλευρικά", δηλ. όπως στο κάτω από τα Σχ. 7, ο δεσμός είναι ασθενέστερος και λέγεται τύπου π.
6 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-6 Σχ. 7: Δεσμός τύπου σ (πάνω) και τύπου π (κάτω). Μια άλλη έννοια που συμπληρώνει και επεκτείνει την παραπάνω κβαντομηχανική περιγραφή του δεσμού και που εξηγεί τη δομή, τη γεωμετρία και τις ενέργειες των οργανικών (κυρίως) μορίων είναι η έννοια του υβριδισμού. Υβριδισμός είναι η "τροποποίηση" (ανάμιξη) των ατομικών τροχιακών των ατόμων που συμμετέχουν στον χημικό δεσμό προκειμένου να αξιοποιήσουν καλύτερα την ένωσή τους με το άλλο άτομο (ή τα άλλα άτομα). Τα τροποποιημένα αυτά ατομικά τροχιακά (υβριδικά τροχιακά) αλληλεπιδρούν ισχυρότερα (αλληλοεπικαλύπτονται περισσότερο) κατά το σχηματισμό μορίου, με αποτέλεσμα η προκύπτουσα κατάσταση (μόριο) να έχει χαμηλότερη ενέργεια. Ο υβριδισμός εμφανίζεται κυρίως στον άνθρακα (Ζ=6) και ερμηνεύει τη μεγάλη ποικιλία των δεσμών του. Τα υβριδικά τροχιακά προκύπτουν από "ανάμιξη" (γραμμικό συνδυασμό των κυματοσυναρτήσεων) των τροχιακών τύπου s και τύπου p. Η διαδικασία αυτή για τον άνθρακα δείχνεται στο Σχ. 8 και η μορφή των υβριδικών τροχιακών στο Σχ. 9. Σχ. 8: Υβριδισμός στο άτομο του άνθρακα (Ζ=6). Πρώτο βήμα είναι η μετάβαση ενός ηλεκτρονίου από τη στάθμη 2s στη 2p. Αυτό συνεπάγεται δαπάνη ενέργειας (για αυτό και δεν συμβαίνει στην συνήθη, ατομική κατάσταση), η οποία όμως είναι μικρή μπροστά στο μεγαλύτερο ενεργειακό κέρδος που προκύπτει από τον δεσμό (βλέπε και επόμενο σχήμα). Έπειτα, υπάρχει η δυνατότητα είτε μία είτε δύο είτε τρεις p στάθμες να "αναμιχθούν" με την s και τα ηλεκτρόνια σθένους να καταλάβουν τις νέες στάθμες που προέκυψαν από την ανάμιξη (κόκκινες στάθμες στο σχήμα). Ο υβριδισμός λέγεται αντίστοιχα sp 1, sp 2, sp 3.
7 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-7 Σχ. 9: Αριστερά: Υβριδισμένα τροχιακά που προκύπτουν από τη συνένωση s και p. Τα τροχιακά αυτά, λόγω της μεγάλης κατευθυντικότητάς τους, επικαλύπτονται περισσότερο με τα τροχιακά του ατόμου με το οποίο γίνεται ο δεσμός (άρα προσφέρουν μεγαλύτερη δυνατότητα μεταπήδησης ηλεκτρονίων από το ένα άτομο στο άλλο), με αποτέλεσμα μεγαλύτερο ενεργειακό κέρδος κατά τη χημική ένωση από το κέρδος που θα προέκυπτε από μη υβρισμένα τροχιακά. Δεξιά: Η μορφή των υβριδισμένων τροχιακών μορίου με υβριδισμό sp 1, sp 2 και sp 3. Παράδειγμα sp 3 έχουμε στο μεθάνιο (CH 4 ), η γεωμετρία του οποίου επίσης δείχνεται. 6.c. Περιστροφή και ταλάντωση μορίων Όταν σε ένα μόριο (το οποίο δεν κινείται ως σύνολο) δίδεται ενέργεια, η ενέργεια αυτή μπορεί να χρησιμοποιηθεί είτε για να διεγείρει τα ηλεκτρόνιά του, φέρνοντάς τα σε υψηλότερες στάθμες, είτε για να το περιστρέψει (Σχ αριστερά), είτε για να το θέσει σε ταλάντωση (Σχ δεξιά), δηλαδή για να του αλλάξει είτε ηλεκτρονική, είτε περιστροφική, είτε ταλαντωτική κατάσταση. Σχ. 10: περιστροφή και ταλάντωση διατομικού μορίου. Όπως είδαμε πιο πάνω, οι ηλεκτρονικές καταστάσεις των μορίων, οι οποίες προκύπτουν από τις αντίστοιχες ατομικές, είναι κβαντισμένες. Οι ηλεκτρονικές ενέργειες είναι της τάξης των μερικών ev και έτσι τα μόρια σε συνήθεις θερμοκρασίες βρίσκονται στη θεμελιώδη στάθμη τους (γιατί;). Στα επόμενα θα εξετάσουμε τις περιστροφικές και τις ταλαντωτικές ενέργειες και θα δείξουμε ότι είναι επίσης κβαντισμένες.
8 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-8 Μοριακή περιστροφή: Η κβάντωση των περιστροφικών ενεργειών απορρέει από την κβάντωση της στροφορμής, σε συνδυασμό με τη σχέση ενέργειας-στροφορμής,, l=0,1,2,... (2) H ποσότητα ονομάζεται ροπή αδράνειας του μορίου (m i είναι οι μάζες των ατόμων (i=1,2) και r i οι αποστάσεις τους από τον άξονα περιστροφής), και είναι ένα μέτρο της δυσκολίας να τεθεί το σώμα σε περιστροφή, δηλ. το ανάλογο της μάζας για την περιστροφική κίνηση (αναφερόμαστε, χάριν απλότητας, σε διατομικά μόρια). Αν η περιστροφή γίνεται ως προς άξονα που περνάει από το κέντρο μάζας, τότε Ι=Ι cm, με,. (3). Στις σχέσεις (3) R είναι η απόσταση ισορροπίας των ατόμων του μορίου και το μ λέγεται ανηγμένη μάζα του μορίου. Η μετάβαση του μορίου από τη μια περιστροφική κατάσταση στην άλλη με εκπομπή φωτονίου γίνεται υπακούοντας στον κανόνα επιλογής (γιατί;). Η τάξη μεγέθους των περιστροφικών ενεργειών (δηλαδή των ενεργειών των φωτονίων που προέρχονται από μεταβολές της περιστροφικής κατάστασης του μορίου, ή αλλιώς από μεταπτώσεις μεταξύ περιστροφικών επιπέδων) είναι (4). (E el είναι οι ηλεκτρονικές ενέργειες - μερικά ev, m p και m e οι μάζες πρωτονίου και ηλεκτρονίου αντίστοιχα.) Μοριακή ταλάντωση: Στο σύστημα κέντρου μάζας ένα διατομικό μόριο, όσον αφορά την ταλαντωτική του συμπεριφορά, μπορεί να περιγραφεί ως ένα σωμάτιο μάζας μ που κινείται στο δυναμικό του Σχήματος 1 (εκτελεί μικρές ταλαντώσεις γύρω από το ελάχιστο του δυναμικού, όπου, r είναι η απόσταση των ατόμων). (Αποδείξτε το.) Πρόκειται δηλαδή για έναν μονοδιάστατο ταλαντωτή μάζας μ και σταθεράς ελατηρίου. (Η σταθερά k εξαρτάται από την ισχύ του ηλεκτροστατικής φύσης μοριακού δεσμού.) Ένας τέτοιος ταλαντωτής, όπως έχουμε δει σε προηγούμενα κεφάλαια, έχει διακριτό φάσμα, και οι δυνατές ενέργειές του δίδονται από, ν=0,1,2,... (5). Σημειώστε ότι ακόμα και στη χαμηλότερη ταλαντωτική κατάσταση, ν=0, το μόριο δεν ηρεμεί. Η ενέργεια της κατάστασης αυτής λέγεται ενέργεια μηδενικού σημείου.
9 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-9 Για τις μεταβάσεις μεταξύ ταλαντωτικών καταστάσεων ισχύει ο κανόνας επιλογής. Η τάξη μεγέθους των ταλαντωτικών ενεργειών (ενέργειες από μεταπτώσεις μεταξύ ταλαντωτικών επιπέδων, ή, ισοδύναμα, αλλαγές στην ταλαντωτική κατάσταση του μορίου) είναι (Αποδείξτε το). (6). Άσκηση: Αποδείξτε το πρώτο μέλος της (2), την (3), την (4) και την (6). 6.d. Μοριακά φάσματα Με τον όρο μοριακό φάσμα εννοούμε το σύνολο των συχνοτήτων των φωτονίων που εκπέμπονται κατά τις μεταβάσεις του μορίου από μια κατάσταση σε άλλη. Επειδή στις συνηθισμένες θερμοκρασίες τα ηλεκτρόνια του μορίου είναι "παγωμένα" στη θεμελιώδη τους κατάσταση, οι μεταβάσεις που συνήθως γίνονται θα είναι μεταξύ περιστροφικών και ταλαντωτικών καταστάσεων. Από τη σχέση που δίνει τις ταλαντωτικές και περιστροφικές επιτρεπτές ενέργειες, σε συνδυασμό με τους κανόνες επιλογής, (7),, (8) μπορεί κανείς να συμπεράνει ότι δεν υπάρχουν μοριακές μεταβάσεις που να είναι αμιγώς ταλαντωτικές ή αμιγώς περιστροφικές (θα αντιστοιχούσαν σε Δl=0 ή Δν=0). Τα φωτόνια των μοριακών φασμάτων εκπομπής τα οποία προέρχονται από μεταπτώσεις μεταξύ ταλαντωτικών και περιστροφικών καταστάσεων θα έχουν ενέργειες (l=1,2,..), Ένα τυπικό μοριακό φάσμα δείχνεται στο Σχ. 11. (l=0,1,2,..).
10 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ Σχ. 11: Μοριακό φάσμα (απορρόφησης) του HCl. Εφαρμογή: Σχεδιάστε τις πρώτες περιστροφικές και ταλαντωτικές στάθμες διατομικού μορίου και δείξτε με βέλη τις επιτρεπτές αποδιεγέρσεις του μορίου.
Διάλεξη 7: Μοριακή Δομή
 Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Σύγxρονη Φυσική II. Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Μοριακή δομή. Απλοϊκή εικόνα του μορίου του νερού. Ηλεκτρονιακοί τύποι κατά Lewis. Δημόκριτος π.χ.
 Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
Μοριακή Φυσική Γενικές αρχές
 Μοριακή Φυσική Γενικές αρχές. Στην ατομική δομή διακρίναμε τα ηλεκτρόνια σε ηλεκτρόνια σθένους και ηλεκτρόνια εσωτερικών στοιβάδων. Ο λόγος βέβαια είναι ότι τα ηλεκτρόνια σθένους είναι υπεύθυνα για τον
Μοριακή Φυσική Γενικές αρχές. Στην ατομική δομή διακρίναμε τα ηλεκτρόνια σε ηλεκτρόνια σθένους και ηλεκτρόνια εσωτερικών στοιβάδων. Ο λόγος βέβαια είναι ότι τα ηλεκτρόνια σθένους είναι υπεύθυνα για τον
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ
 ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
Κεφάλαια (από το βιβλίο Serway-Jewett) και αναρτημένες παρουσιάσεις
 Ύλη μαθήματος «Σύγχρονη Φυσική» Κεφάλαια (από το βιβλίο Serway-Jewett) και αναρτημένες παρουσιάσεις Σ2-Σελίδες: 673-705, (όλο το κεφάλαιο από το βιβλίο) και η παρουσίαση Σ2 που έχει αναρτηθεί στο e-class
Ύλη μαθήματος «Σύγχρονη Φυσική» Κεφάλαια (από το βιβλίο Serway-Jewett) και αναρτημένες παρουσιάσεις Σ2-Σελίδες: 673-705, (όλο το κεφάλαιο από το βιβλίο) και η παρουσίαση Σ2 που έχει αναρτηθεί στο e-class
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
κυματικής συνάρτησης (Ψ) κυματική συνάρτηση
 Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Μοριακή Φασματοσκοπία I. Παραδόσεις μαθήματος Θ. Λαζαρίδης
 Μοριακή Φασματοσκοπία I Παραδόσεις μαθήματος Θ. Λαζαρίδης 2 Τι μελετά η μοριακή φασματοσκοπία; Η μοριακή φασματοσκοπία μελετά την αλληλεπίδραση των μορίων με την ηλεκτρομαγνητική ακτινοβολία Από τη μελέτη
Μοριακή Φασματοσκοπία I Παραδόσεις μαθήματος Θ. Λαζαρίδης 2 Τι μελετά η μοριακή φασματοσκοπία; Η μοριακή φασματοσκοπία μελετά την αλληλεπίδραση των μορίων με την ηλεκτρομαγνητική ακτινοβολία Από τη μελέτη
Περίληψη 1 ου Κεφαλαίου
 Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων
 Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων Περιεχόμενα Κεφαλαίου 39 Τα άτομα από την σκοπιά της κβαντικής μηχανικής Το άτομο του Υδρογόνου: Η εξίσωση του Schrödinger και οι κβαντικοί αριθμοί ΟΙ κυματοσυναρτήσεις
Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων Περιεχόμενα Κεφαλαίου 39 Τα άτομα από την σκοπιά της κβαντικής μηχανικής Το άτομο του Υδρογόνου: Η εξίσωση του Schrödinger και οι κβαντικοί αριθμοί ΟΙ κυματοσυναρτήσεις
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Σύγxρονη Φυσική II. Μοριακή Δομή ΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική Μοριακή Δομή ΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Ceative Coons. Για
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική Μοριακή Δομή ΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Ceative Coons. Για
Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
Το άτομο του Υδρογόνου- Υδρογονοειδή άτομα
 Το άτομο του Υδρογόνου- Υδρογονοειδή άτομα Το πιο απλό κβαντομηχανικό ρεαλιστικό σύστημα, το οποίο λύνεται ακριβώς, είναι το άτομο του Υδρογόνου (1 πρωτόνιο και 1 ηλεκτρόνιο) Το δυναμικό στην περίπτωση
Το άτομο του Υδρογόνου- Υδρογονοειδή άτομα Το πιο απλό κβαντομηχανικό ρεαλιστικό σύστημα, το οποίο λύνεται ακριβώς, είναι το άτομο του Υδρογόνου (1 πρωτόνιο και 1 ηλεκτρόνιο) Το δυναμικό στην περίπτωση
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
Μια πρόταση παρουσίασης με
 Διαμοριακές δυνάμεις Μια πρόταση παρουσίασης με το PowerPoint Διαμοριακές δυνάμεις Είναι οι ελκτικές δυνάμεις ηλεκτροστατικής φύσης (ασθενέστερες από τις ενδομοριακές) που ασκούνται μεταξύ μορίων (του
Διαμοριακές δυνάμεις Μια πρόταση παρουσίασης με το PowerPoint Διαμοριακές δυνάμεις Είναι οι ελκτικές δυνάμεις ηλεκτροστατικής φύσης (ασθενέστερες από τις ενδομοριακές) που ασκούνται μεταξύ μορίων (του
Μοντέρνα Φυσική. Κβαντική Θεωρία. Ατομική Φυσική. Μοριακή Φυσική. Πυρηνική Φυσική. Φασματοσκοπία
 Μοντέρνα Φυσική Κβαντική Θεωρία Ατομική Φυσική Μοριακή Φυσική Πυρηνική Φυσική Φασματοσκοπία ΚΒΑΝΤΙΚΗ ΘΕΩΡΙΑ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης:
Μοντέρνα Φυσική Κβαντική Θεωρία Ατομική Φυσική Μοριακή Φυσική Πυρηνική Φυσική Φασματοσκοπία ΚΒΑΝΤΙΚΗ ΘΕΩΡΙΑ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης:
Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR
 Φασματοσκοπία Ερμηνεία & εφαρμογές : Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR Ποια φαινόμενα παράγουν τα
Φασματοσκοπία Ερμηνεία & εφαρμογές : Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR Ποια φαινόμενα παράγουν τα
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ. Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών. Να εξηγούν το σχηματισμό του ιοντικού ομοιοπολικού δεσμού.
 ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
(Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου )
 Δυνάμεις διπόλου διπόλου (Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου ) Τα πολικά μόρια μπορούν να έλκονται αμοιβαία μέσω δυνάμεων διπόλου διπόλου. Η δύναμη διπόλου
Δυνάμεις διπόλου διπόλου (Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου ) Τα πολικά μόρια μπορούν να έλκονται αμοιβαία μέσω δυνάμεων διπόλου διπόλου. Η δύναμη διπόλου
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
Χημικοί Χημικ σμ σμ & Μοριακά Τροχιακά
 Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
Μάθημα 21 ο. Το σχήμα των μορίων. Θεωρία VSEPR. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
ηλεκτρόνια που αποβάλλονται από τα 2 άτομα του Na τα παίρνει το S και γίνεται S 2-.
 1. Το στοιχείο Β είναι ευγενές αέριο, άρα έχει 8 ηλεκτρόνια στην εξωτερική του στιβάδα. Κατά συνέπεια το Α έχει 7 και το Γ 1 (Ανήκει στην 1 Η ομάδα της επόμενης περιόδου του Β). Θα ενωθούν με ετεροπολικό
1. Το στοιχείο Β είναι ευγενές αέριο, άρα έχει 8 ηλεκτρόνια στην εξωτερική του στιβάδα. Κατά συνέπεια το Α έχει 7 και το Γ 1 (Ανήκει στην 1 Η ομάδα της επόμενης περιόδου του Β). Θα ενωθούν με ετεροπολικό
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ Ένα σημαντικό αποτέλεσμα της κβαντομηχανικής θεωρίας είναι ότι τα μόρια, όχι μόνο βρίσκονται σε διακριτές ενεργειακές
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ Ένα σημαντικό αποτέλεσμα της κβαντομηχανικής θεωρίας είναι ότι τα μόρια, όχι μόνο βρίσκονται σε διακριτές ενεργειακές
6. ιαμοριακές δυνάμεις
 6. ιαμοριακές δυνάμεις ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τα είδη των ελκτικών δυνάμεων που αναπτύσσονται μεταξύ των μορίων των ομοιοπολικών ενώσεων και την επίδραση που ασκούν οι δυνάμεις
6. ιαμοριακές δυνάμεις ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τα είδη των ελκτικών δυνάμεων που αναπτύσσονται μεταξύ των μορίων των ομοιοπολικών ενώσεων και την επίδραση που ασκούν οι δυνάμεις
Οργανική Χημεία. Κεφάλαιο 1: Δομή και δεσμοί
 Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που
 ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
1o Kριτήριο Αξιολόγησης
 1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
ΦΑΣΜΑΤΑ ΕΚΠΟΜΠΗΣ ΑΠΟΡΡΟΦΗΣΗΣ
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ. Χημεία της ζωής 1
 ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
Ασκήσεις. Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3
 Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό
 Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2
 Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Διατομικά μόρια- Περιστροφική ενέργεια δονητικά - περιστροφικά φάσματα
 Διατομικά μόρια- Περιστροφική ενέργεια δονητικά - περιστροφικά φάσματα Πολυατομικά μόρια περιστροφική ενέργεια περιστροφικά φάσματα Σκέδαση φασματοσκοπία n συνεισφορά του πυρηνικού σπιν Δονητικά περιστροφικά
Διατομικά μόρια- Περιστροφική ενέργεια δονητικά - περιστροφικά φάσματα Πολυατομικά μόρια περιστροφική ενέργεια περιστροφικά φάσματα Σκέδαση φασματοσκοπία n συνεισφορά του πυρηνικού σπιν Δονητικά περιστροφικά
Χημικοί Χημικ σμ σμ & Μοριακά Τροχιακά
 Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που
 ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΠΕΡΙΟΔΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΑΤΟΜΙΚΗ ΑΚΤΙΝΑ ΕΝΕΡΓΕΙΑ ΙΟΝΤΙΣΜΟΥ
 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΠΕΡΙΟΔΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΑΤΟΜΙΚΗ ΑΚΤΙΝΑ ΕΝΕΡΓΕΙΑ ΙΟΝΤΙΣΜΟΥ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Η ηλεκτρονιακή δομή και κυρίως τα ηλεκτρόνια σθένους (τελευταία ηλεκτρόνια) προσδίδουν στο άτομο τη χημική
ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΠΕΡΙΟΔΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΑΤΟΜΙΚΗ ΑΚΤΙΝΑ ΕΝΕΡΓΕΙΑ ΙΟΝΤΙΣΜΟΥ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Η ηλεκτρονιακή δομή και κυρίως τα ηλεκτρόνια σθένους (τελευταία ηλεκτρόνια) προσδίδουν στο άτομο τη χημική
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη. Ιοντικός χαρακτήρας δεσμών. Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
 Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΕΣΜΟΥ
 ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1
 ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1 Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΝΙΚΟΛΑΟΣ ΚΟΥΤΡΟΥΜΑΝΗΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 5 Μαρτίου 2015 2 ο Φροντιστήριο 1) Ποια είναι τα ηλεκτρόνια σθένους και ποιός ο ρόλος τους;
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1 Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΝΙΚΟΛΑΟΣ ΚΟΥΤΡΟΥΜΑΝΗΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 5 Μαρτίου 2015 2 ο Φροντιστήριο 1) Ποια είναι τα ηλεκτρόνια σθένους και ποιός ο ρόλος τους;
14 ο VIDEO 21/11/2013 Από 1ω,5λ έως το τέλος
 ΚΕΦΑΛΑΙΟ 0: ΜΟΡΙΑ Η ΕΝΟΤΗΤΑ: ΕΝΕΡΓΕΙΑ ΔΥΟ ΑΤΟΜΩΝ, Σελ. 4-46 του βιβλίου ΚΣ 4 ο VIDEO //0 Από ω,5λ έως το τέλος Η η ενότητα αναφέρεται στο γράφημα που παριστά την αλληλεπίδραση δύο ουδέτερων ατόμων καθώς
ΚΕΦΑΛΑΙΟ 0: ΜΟΡΙΑ Η ΕΝΟΤΗΤΑ: ΕΝΕΡΓΕΙΑ ΔΥΟ ΑΤΟΜΩΝ, Σελ. 4-46 του βιβλίου ΚΣ 4 ο VIDEO //0 Από ω,5λ έως το τέλος Η η ενότητα αναφέρεται στο γράφημα που παριστά την αλληλεπίδραση δύο ουδέτερων ατόμων καθώς
ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 11-11-2012
 ΘΕΜΑ Α ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 11-11-2012 Για τις ερωτήσεις Α.1 έως Α.5 να γράψετε το γράμμα που αντιστοιχεί στη σωστή απάντηση δίπλα στον αριθμό της ερώτησης. Α.1 Τα χημικά στοιχεία μιας κύριας ομάδας
ΘΕΜΑ Α ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 11-11-2012 Για τις ερωτήσεις Α.1 έως Α.5 να γράψετε το γράμμα που αντιστοιχεί στη σωστή απάντηση δίπλα στον αριθμό της ερώτησης. Α.1 Τα χημικά στοιχεία μιας κύριας ομάδας
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Spin του πυρήνα Μαγνητική διπολική ροπή Ηλεκτρική τετραπολική ροπή. Τάσος Λιόλιος Μάθημα Πυρηνικής Φυσικής
 Spin του πυρήνα Μαγνητική διπολική ροπή Ηλεκτρική τετραπολική ροπή Τάσος Λιόλιος Μάθημα Πυρηνικής Φυσικής Εξάρτηση του πυρηνικού δυναμικού από άλλους παράγοντες (πλην της απόστασης) Η συνάρτηση του δυναμικού
Spin του πυρήνα Μαγνητική διπολική ροπή Ηλεκτρική τετραπολική ροπή Τάσος Λιόλιος Μάθημα Πυρηνικής Φυσικής Εξάρτηση του πυρηνικού δυναμικού από άλλους παράγοντες (πλην της απόστασης) Η συνάρτηση του δυναμικού
Άτομο: Η μικρότερη μονάδα ενός στοιχείου που διατηρεί τις χημικές του ιδιότητες
 Άτομο: Η μικρότερη μονάδα ενός στοιχείου που διατηρεί τις χημικές του ιδιότητες 1 Πυρήνας: Περιβάλλων: χώρος - πρωτόνια - νετρόνια - ηλεκτρόνια 2 fm (femtometre) = 10 15 m nm (nanometre) = 10-9 m Όνομα
Άτομο: Η μικρότερη μονάδα ενός στοιχείου που διατηρεί τις χημικές του ιδιότητες 1 Πυρήνας: Περιβάλλων: χώρος - πρωτόνια - νετρόνια - ηλεκτρόνια 2 fm (femtometre) = 10 15 m nm (nanometre) = 10-9 m Όνομα
ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΠΑΡΑΔΕΙΓΜΑ
 ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ
 ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
Μοριακά φάσματα. Όσον αφορά τα ενεργειακά επίπεδα των ηλεκτρονίων σε ένα μόριο, αυτά μελετήθηκαν σε μια πρώτη προσέγγιση μέσω της μεθόδου LCAO.
 Μοριακά φάσματα Η ολική ενέργεια που αποθηκεύει εσωτερικά ένα μόριο δίνεται από το άθροισμα: α) της ενέργειάς του λόγω μεταφορικής κίνησης β) της ενέργειας των ηλεκτρονίων του γ) της περιστροφικής ενέργειας
Μοριακά φάσματα Η ολική ενέργεια που αποθηκεύει εσωτερικά ένα μόριο δίνεται από το άθροισμα: α) της ενέργειάς του λόγω μεταφορικής κίνησης β) της ενέργειας των ηλεκτρονίων του γ) της περιστροφικής ενέργειας
Γεωμετρία Μορίων Θεωρία VSEPR
 Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
7.a. Οι δεσμοί στα στερεά
 ΤΕΤΥ Σύγχρονη Φυσική Κεφ. 7-1 Κεφάλαιο 7. Στερεά Εδάφια: 7.a. Οι δεσμοί στα στερεά 7.b. Η θεωρία των ενεργειακών ζωνών 7.c. Νόθευση ημιαγωγών και εφαρμογές 7.d. Υπεραγωγοί 7.a. Οι δεσμοί στα στερεά Με
ΤΕΤΥ Σύγχρονη Φυσική Κεφ. 7-1 Κεφάλαιο 7. Στερεά Εδάφια: 7.a. Οι δεσμοί στα στερεά 7.b. Η θεωρία των ενεργειακών ζωνών 7.c. Νόθευση ημιαγωγών και εφαρμογές 7.d. Υπεραγωγοί 7.a. Οι δεσμοί στα στερεά Με
ΠΩΣ ΙΑΤΑΣΣΟΝΤΑΙ ΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΙΒΑ Α
 1 ΠΩΣ ΙΑΤΑΣΣΟΝΤΑΙ ΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΙΒΑ Α Πριν προχωρήσουµε στον τρόπο που συνδέονται τα άτοµα σκέψου τα παρακάτω και επιστράτευσε τη φαντασία σου για να µπορέσεις να καταλάβεις καλύτερα πως
1 ΠΩΣ ΙΑΤΑΣΣΟΝΤΑΙ ΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΙΒΑ Α Πριν προχωρήσουµε στον τρόπο που συνδέονται τα άτοµα σκέψου τα παρακάτω και επιστράτευσε τη φαντασία σου για να µπορέσεις να καταλάβεις καλύτερα πως
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
διατήρησης της μάζας.
 6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.
![ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας. ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.](/thumbs/102/153828250.jpg) ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
Ατομική Φυσική. Η Φυσική των ηλεκτρονίων και των ηλεκτρομαγνητικών δυνάμεων.
 Ατομική Φυσική Η Φυσική των ηλεκτρονίων και των ηλεκτρομαγνητικών δυνάμεων. Μικρόκοσμος Κβαντική Φυσική Σωματιδιακή φύση του φωτός (γενικότερα της ακτινοβολίας) Κυματική φύση των ηλεκτρονίων (γενικότερα
Ατομική Φυσική Η Φυσική των ηλεκτρονίων και των ηλεκτρομαγνητικών δυνάμεων. Μικρόκοσμος Κβαντική Φυσική Σωματιδιακή φύση του φωτός (γενικότερα της ακτινοβολίας) Κυματική φύση των ηλεκτρονίων (γενικότερα
Κεφάλαιο 37 Αρχική Κβαντική Θεωρία και Μοντέλα για το Άτομο. Copyright 2009 Pearson Education, Inc.
 Κεφάλαιο 37 Αρχική Κβαντική Θεωρία και Μοντέλα για το Άτομο Περιεχόμενα Κεφαλαίου 37 Η κβαντική υπόθεση του Planck, Ακτινοβολία του μέλανος (μαύρου) σώματος Θεωρία των φωτονίων για το φως και το Φωτοηλεκτρικό
Κεφάλαιο 37 Αρχική Κβαντική Θεωρία και Μοντέλα για το Άτομο Περιεχόμενα Κεφαλαίου 37 Η κβαντική υπόθεση του Planck, Ακτινοβολία του μέλανος (μαύρου) σώματος Θεωρία των φωτονίων για το φως και το Φωτοηλεκτρικό
ΑΤΟΜΙΚΑ ΤΟΜΙΚΑ ΠΡΟΤΥΠΑ
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
Ασκήσεις Φασµατοσκοπίας
 Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός.
 2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
Κεφάλαιο 9. Ιοντικός και Ομοιοπολικός Δεσμός
 Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα:
 ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΧΑΡΑΛΑΜΠΟΣ ΔΡΙΒΑΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 1 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 1. Τι τάξη μεγέθους είναι οι ενδοατομικές αποστάσεις και ποιες υποδιαιρέσεις του
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΧΑΡΑΛΑΜΠΟΣ ΔΡΙΒΑΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 1 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 1. Τι τάξη μεγέθους είναι οι ενδοατομικές αποστάσεις και ποιες υποδιαιρέσεις του
ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (11): Ομοιοπολικός Δεσμός Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (11): Ομοιοπολικός Δεσμός Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
ΙΟΝΤΙΚΟΣ Η ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ (ΙΟΝΙC BOND)
 ΙΟΝΤΙΚΟΣ Η ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ (ΙΟΝΙC BOND) Ο χημικός δεσμός που δημιουργείται λόγω των ελκτικών δυνάμεων αντιθέτως φορτισμένων ιόντων λέγεται ετεροπολικός ή ιοντικός δεσμός, αφού η δημιουργία του oφείλεται
ΙΟΝΤΙΚΟΣ Η ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ (ΙΟΝΙC BOND) Ο χημικός δεσμός που δημιουργείται λόγω των ελκτικών δυνάμεων αντιθέτως φορτισμένων ιόντων λέγεται ετεροπολικός ή ιοντικός δεσμός, αφού η δημιουργία του oφείλεται
ΠΥΡΗΝΙΚΟΣ ΜΑΓΝΗΤΙΚΟΣ ΣΥΝΤΟΝΙΣΜΟΣ ΚΑΙ ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ. Του Αλέκου Χαραλαμπόπουλου ΕΙΣΑΓΩΓΗ
 ΠΥΡΗΝΙΚΟΣ ΜΑΓΝΗΤΙΚΟΣ ΣΥΝΤΟΝΙΣΜΟΣ ΚΑΙ ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ Του Αλέκου Χαραλαμπόπουλου ΕΙΣΑΓΩΓΗ Ένα επαναλαμβανόμενο περιοδικά φαινόμενο, έχει μία συχνότητα επανάληψης μέσα στο χρόνο και μία περίοδο. Επειδή κάθε
ΠΥΡΗΝΙΚΟΣ ΜΑΓΝΗΤΙΚΟΣ ΣΥΝΤΟΝΙΣΜΟΣ ΚΑΙ ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ Του Αλέκου Χαραλαμπόπουλου ΕΙΣΑΓΩΓΗ Ένα επαναλαμβανόμενο περιοδικά φαινόμενο, έχει μία συχνότητα επανάληψης μέσα στο χρόνο και μία περίοδο. Επειδή κάθε
Κυματική φύση της ύλης: ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ. Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης:
 Κυματική φύση της ύλης: ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης: Κινούμενα ηλεκτρόνια συμπεριφέρονται σαν κύματα (κύματα de Broglie)
Κυματική φύση της ύλης: ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης: Κινούμενα ηλεκτρόνια συμπεριφέρονται σαν κύματα (κύματα de Broglie)
Κεφάλαιο 2 Ο Χημικός Δεσμός
 Κεφάλαιο 2 Ο Χημικός Δεσμός Σύνοψη O Χημικός Δεσμός εξηγεί τον τρόπο με τον οποίο δημιουργούνται οι ενώσεις. Υπάρχουν οι ιοντικές ενώσεις στις οποίες ιόντα αντίθετου φορτίου ενώνονται μεταξύ τους προς
Κεφάλαιο 2 Ο Χημικός Δεσμός Σύνοψη O Χημικός Δεσμός εξηγεί τον τρόπο με τον οποίο δημιουργούνται οι ενώσεις. Υπάρχουν οι ιοντικές ενώσεις στις οποίες ιόντα αντίθετου φορτίου ενώνονται μεταξύ τους προς
1 p p a y. , όπου H 1,2. u l, όπου l r p και u τυχαίο μοναδιαίο διάνυσμα. Δείξτε ότι μπορούν να γραφούν σε διανυσματική μορφή ως εξής.
 ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ Ασκήσεις Κεφαλαίου V Άσκηση : Οι θεμελιώδεις σχέσεις μετάθεσης της στροφορμής επιτρέπουν την ύπαρξη ακέραιων και ημιπεριττών ιδιοτιμών Αλλά για την τροχιακή στροφορμή L r p γνωρίζουμε ότι
ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ Ασκήσεις Κεφαλαίου V Άσκηση : Οι θεμελιώδεις σχέσεις μετάθεσης της στροφορμής επιτρέπουν την ύπαρξη ακέραιων και ημιπεριττών ιδιοτιμών Αλλά για την τροχιακή στροφορμή L r p γνωρίζουμε ότι
ηλεκτρονιακές Κατανοµή
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΧΗΜΙΚΟΙ ΕΣΜΟΙ 1. ίνεται ο πίκας: Σύµβολο Στοιχείου Να Ηλεκτρονιακή Κατανοµή X K (2) L(4) Ψ K (2) L(8) M(7) Ζ K (2) L(7) αντιγράψετε τον πίκα Οµάδα Π.Π. στη κόλλα Περίοδος Π.Π. σας τον
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΧΗΜΙΚΟΙ ΕΣΜΟΙ 1. ίνεται ο πίκας: Σύµβολο Στοιχείου Να Ηλεκτρονιακή Κατανοµή X K (2) L(4) Ψ K (2) L(8) M(7) Ζ K (2) L(7) αντιγράψετε τον πίκα Οµάδα Π.Π. στη κόλλα Περίοδος Π.Π. σας τον
ΙΑΤΡΙΚΗ ΦΥΣΙΚΗ eclass: MED808 Π. Παπαγιάννης
 ΙΑΤΡΙΚΗ ΦΥΣΙΚΗ eclass: MED808 Π. Παπαγιάννης Επικ. Καθηγητής, Εργαστήριο Ιατρικής Φυσικής, Ιατρική Σχολή Αθηνών. Γραφείο 21 210-746 2442 ppapagi@phys.uoa.gr Τις προσεχείς ώρες θα συζητήσουμε τα πέντε πρώτα
ΙΑΤΡΙΚΗ ΦΥΣΙΚΗ eclass: MED808 Π. Παπαγιάννης Επικ. Καθηγητής, Εργαστήριο Ιατρικής Φυσικής, Ιατρική Σχολή Αθηνών. Γραφείο 21 210-746 2442 ppapagi@phys.uoa.gr Τις προσεχείς ώρες θα συζητήσουμε τα πέντε πρώτα
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού
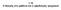 1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
O 3,44 S 2,58 N 3,04 P 2,19
 Περιοδικός Πίνακας (Σύστημα) των Ατόμων Περιοδικό σύστημα είναι ο πίνακας στον οποίο κατατάσσονται όλα τα άτομα με βάση τον αριθμό των πρωτονίων (θετικά φορτισμένα σωματίδια) που ευρίσκονται στον πυρήνα
Περιοδικός Πίνακας (Σύστημα) των Ατόμων Περιοδικό σύστημα είναι ο πίνακας στον οποίο κατατάσσονται όλα τα άτομα με βάση τον αριθμό των πρωτονίων (θετικά φορτισμένα σωματίδια) που ευρίσκονται στον πυρήνα
Κυματική φύση της ύλης: ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ. Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης:
 Κυματική φύση της ύλης: ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης: Κινούμενα ηλεκτρόνια συμπεριφέρονται σαν κύματα (κύματα de Broglie)
Κυματική φύση της ύλης: ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης: Κινούμενα ηλεκτρόνια συμπεριφέρονται σαν κύματα (κύματα de Broglie)
Διάλεξη 6: Ατομική Δομή Συμμετρία Εναλλαγής
 Συμμετρία Εναλλαγής Σε μονοηλεκτρονιακά άτομα ιόντα η κατάσταση του ηλεκτρονίου καθορίζεται από τέσσερις κβαντικούς αριθμούς {n, l, m l, m s } ή {n, l, j, m j }. Σε πολυηλεκτρονιακά άτομα πόσα ηλεκτρόνια
Συμμετρία Εναλλαγής Σε μονοηλεκτρονιακά άτομα ιόντα η κατάσταση του ηλεκτρονίου καθορίζεται από τέσσερις κβαντικούς αριθμούς {n, l, m l, m s } ή {n, l, j, m j }. Σε πολυηλεκτρονιακά άτομα πόσα ηλεκτρόνια
Προβλήματα Κεφαλαίου 2
 Άνοιξη 2013 5/3/2013 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 3, 4, 5 * να παραδοθούν μέχρι τις 22/3/2013 Οι λύσεις των προβλημάτων 8 * και 20 να παραδοθούν μέχρι τις 28/3/2013 1. Για να κερδίσουμε
Άνοιξη 2013 5/3/2013 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 3, 4, 5 * να παραδοθούν μέχρι τις 22/3/2013 Οι λύσεις των προβλημάτων 8 * και 20 να παραδοθούν μέχρι τις 28/3/2013 1. Για να κερδίσουμε
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
( J) e 2 ( ) ( ) x e +, (9-14) = (9-16) ω e xe v. De = (9-18) , (9-19)
 Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια.
 ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
ΕΙΣΑΓΩΓΗ ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ IV. ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ
 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ IV. ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Στο ατομικό πρότυπο του Bohr ο κύριος κβαντικός αριθμός (n) εισάγεται αυθαίρετα, για τον καθορισμό
ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Η ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ IV. ΟΙ ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΚΑΙ ΤΑ ΤΡΟΧΙΑΚΑ Ν. ΜΠΕΚΙΑΡΗΣ ΕΙΣΑΓΩΓΗ Στο ατομικό πρότυπο του Bohr ο κύριος κβαντικός αριθμός (n) εισάγεται αυθαίρετα, για τον καθορισμό
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί
 1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
 Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ
 ΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ Χρήστος Παππάς Επίκουρος Καθηγητής 1 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΠΟΛΙΚΗ ΡΟΠΗ δ+ δ- Α------------Β μ Aν μ ΟΛ 0 πολική Aν μ ΟΛ =0 άπολη 2 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΑΤΟΜΙΚΑ ΜΟΡΙΑ Αν τα άτομα
ΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ Χρήστος Παππάς Επίκουρος Καθηγητής 1 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΠΟΛΙΚΗ ΡΟΠΗ δ+ δ- Α------------Β μ Aν μ ΟΛ 0 πολική Aν μ ΟΛ =0 άπολη 2 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΑΤΟΜΙΚΑ ΜΟΡΙΑ Αν τα άτομα
Δομή ενεργειακών ζωνών
 Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
ΜΑΘΗΜΑ / ΤΑΞΗ : ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013 ΘΕΜΑ Α Οδηγία: Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις Α1-Α4 και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013 ΘΕΜΑ Α Οδηγία: Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις Α1-Α4 και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ: ΔΙΑΓΩΝΙΣΜΑ ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ:
 ΜΑΘΗΜΑ / ΤΑΞΗ: ΔΙΑΓΩΝΙΣΜΑ ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10-11-2013 ΘΕΜΑ Α Οδηγία: Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις Α1-Α4 και δίπλα
ΜΑΘΗΜΑ / ΤΑΞΗ: ΔΙΑΓΩΝΙΣΜΑ ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ/Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10-11-2013 ΘΕΜΑ Α Οδηγία: Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις Α1-Α4 και δίπλα
1.1 Ηλεκτρονικές ιδιότητες των στερεών. Μονωτές και αγωγοί
 1. Εισαγωγή 1.1 Ηλεκτρονικές ιδιότητες των στερεών. Μονωτές και αγωγοί Από την Ατομική Φυσική είναι γνωστό ότι οι επιτρεπόμενες ενεργειακές τιμές των ηλεκτρονίων είναι κβαντισμένες, όπως στο σχήμα 1. Σε
1. Εισαγωγή 1.1 Ηλεκτρονικές ιδιότητες των στερεών. Μονωτές και αγωγοί Από την Ατομική Φυσική είναι γνωστό ότι οι επιτρεπόμενες ενεργειακές τιμές των ηλεκτρονίων είναι κβαντισμένες, όπως στο σχήμα 1. Σε
Ο Πυρήνας του Ατόμου
 1 Σκοποί: Ο Πυρήνας του Ατόμου 15/06/12 I. Να δώσει μία εισαγωγική περιγραφή του πυρήνα του ατόμου, και της ενέργειας που μπορεί να έχει ένα σωματίδιο για να παραμείνει δέσμιο μέσα στον πυρήνα. II. III.
1 Σκοποί: Ο Πυρήνας του Ατόμου 15/06/12 I. Να δώσει μία εισαγωγική περιγραφή του πυρήνα του ατόμου, και της ενέργειας που μπορεί να έχει ένα σωματίδιο για να παραμείνει δέσμιο μέσα στον πυρήνα. II. III.
Κεφάλαιο 4 Καταστάσεις της Ύλης: Αέρια, Υγρά και Στερεά
 Κεφάλαιο 4 Καταστάσεις της Ύλης: Αέρια, Υγρά και Στερεά Σύνοψη Η ύλη χαρακτηρίζεται από μεγάλη ποικιλία φυσικών καταστάσεων όπως αέρια, υγρή, στερεή. Οι διάφορες αυτές φάσεις που μπορεί να έχει μία ουσία
Κεφάλαιο 4 Καταστάσεις της Ύλης: Αέρια, Υγρά και Στερεά Σύνοψη Η ύλη χαρακτηρίζεται από μεγάλη ποικιλία φυσικών καταστάσεων όπως αέρια, υγρή, στερεή. Οι διάφορες αυτές φάσεις που μπορεί να έχει μία ουσία
Παράγοντες που εξηγούν τη διαλυτότητα. Είδη διαλυμάτων
 Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
6. Το Μόριο Ετεροπολικός δεσμός. Χρήστος Ελευθεριάδης, Ελένη Καλδούδη
 6. Το Μόριο Χρήστος Ελευθεριάδης, Ελένη Καλδούδη Διαφορετικά άτομα είναι δυνατό να συνδυαστούν και να σχηματίσουν σταθερές δομές, τα μόρια. Οι χημικές και φυσικές ιδιότητες των μορίων οφείλονται στα επιμέρους
6. Το Μόριο Χρήστος Ελευθεριάδης, Ελένη Καλδούδη Διαφορετικά άτομα είναι δυνατό να συνδυαστούν και να σχηματίσουν σταθερές δομές, τα μόρια. Οι χημικές και φυσικές ιδιότητες των μορίων οφείλονται στα επιμέρους
