ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ CO-RENITEC R 1 ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
|
|
|
- Λευί Βλαστός
- 9 χρόνια πριν
- Προβολές:
Transcript
1 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ CO-RENITEC R 1 ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ CO-RENITEC R 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Κάθε δισκίο περιέχει 20 mg μηλεϊνική εναλαπρίλη και 12,5 mg υδροχλωροθειαζίδη. Κάθε δισκίο περιέχει 141,0 mg μονοϋδρική λακτόζη. Για τον πλήρη κατάλογο των εκδόχων, βλέπε παράγραφο ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ Δισκία 4. ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ 4.1 Θεραπευτικές ενδείξεις Το CO-RENITEC ενδείκνυται για τη θεραπεία της υπέρτασης σε ασθενείς στους οποίους η συνδυασμένη θεραπεία είναι κατάλληλη. 4.2 Δοσολογία και τρόπος χορήγησης Το CO-RENITEC διατίθεται σε δισκία για χορήγηση από το στόμα. Το CO-RENITEC περιέχει μηλεϊνική εναλαπρίλη 20mg και υδροχλωροθειαζίδη 12,5mg Υπέρταση Στην υπέρταση η συνήθης δοσολογία είναι ένα δισκίο χορηγούμενο μία φορά την ημέρα. Εάν είναι απαραίτητο, η δόση μπορεί να αυξηθεί σε δύο δισκία χορηγούμενα μία φορά την ημέρα. Προηγούμενη διουρητική θεραπεία Συμπτωματική υπόταση μπορεί να εμφανιστεί μετά την αρχική δόση του CO- RENITEC. Αυτό είναι πιο πιθανό να συμβεί σε ασθενείς με μειωμένο όκγο υγρών ή άλατος σαν αποτέλεσμα προηγούμενης διουρητικής θεραπείας. Η θεραπεία με διουρητικά θα πρέπει να διακόπτεται για 2-3 ημέρες πριν την έναρξη της θεραπείας με CO-RENITEC. Δοσολογία σε νεφρική ανεπάρκεια: Οι θειαζίδες μπορεί να μην είναι τα κατάλληλα διουρητικά για χορήγηση σε ασθενείς με νεφρική ανεπάρκεια και δεν είναι αποτελεσματικά εάν οι τιμές κάθαρσης κρεατινίνης είναι 30ml/min ή λιγότερο (π.χ. μέτρια ή βαριά νεφρική ανεπάρκεια). Σε ασθενείς με τιμές κάθαρσης κρεατινίνης μεγαλύτερες των 30 και μικρότερες των 80ml/min, το CO-RENITEC θα πρέπει να χρησιμοποιείται μόνο μετά από τιτλοποίηση καθενός των συστατικών του. Η συνιστώμενη αρχική δόση μηλεϊνική εναλαπρίλη όταν χορηγείται μόνο του στην ήπια νεφρική ανεπάρκεια είναι 5 έως 10mg.
2 Παιδιατρικός πληθυσμός Το CO-RENITEC 6 δεν συνιστάται για χρήση σε παιδιά ηλικίας κάτω των 18 ετών λόγω έλλειψης κατάλληλων στοιχείων ασφάλειας και αποτελεσματικότητας. 4.3 Αντενδείξεις Υπερευαισθησία στην δραστκή ουσία, ή σε οποιοδήποτε από τα έκδοχα που αναφέρονται στην παράγραφο 6.1. Σοβαρή νεφρική δυσλειτουργία ( κάθαρση κρεατινίνης 30ml/min). Ανουρία Ιστορικό αγγειονευρωτικού οιδήματος που έχει σχέση με προηγούμενη θεραπεία με έναν αναστολέα ΜΕΑ. Κληρονομικό ή ιδιοπαθές αγγειοοίδημα Υπερευαισθησία σε άλλα φάρμακα παράγωγα των σουλφοναμιδών Δεύτερο και τρίτο τρίμηνο της κύησης (βλέπε παράγραφο 4.4 και 4.6). Σοβαρή ηπατική δυσλειτουργία Αμφοτερόπλευρη στένωση νεφρικής αρτηρίας Το CO-RENITEC δεν πρέπει να χορηγείται με προϊόντα που περιέχουν αλισκιρένη σε ασθενείς με διαβήτη ή με νεφρική δυσλειτουργία (GFR<60ml/min/1.73 m 2 ) 4.4 Ιδιαίτερες προειδοποιήσεις και προφυλάξεις κατά τη χρήση Μηλεϊνική εναλαπρίλη -Υδροχλωροθειαζίδη Υπόταση και διαταραχή των ηλεκτρολυτών/υγρών: Έχει σπάνια παρατηρηθεί συμπτωματική υπόταση σε ανεπίπλεκτους υπερτασικούς ασθενείς. Σε υπερτασικούς ασθενείς που λαμβάνουν CO-RENITEC, συμπτωματική υπόταση είναι πιο πιθανόν να εμφανισθεί εάν ο ασθενής έχει μειωμένο όγκο υγρών, π.χ. από θεραπεία με διουρητικά, περιορισμό άλατος στη διατροφή, διάρροια ή έμετο (βλέπε παράγραφο 4.5 και 4.8 ). Θα πρέπει να γίνεται τακτικός προσδιορισμός των ηλεκτρολυτών του ορού σε κατάλληλα διαστήματα σ αυτούς τους ασθενείς. Ιδιαίτερη προσοχή απαιτείται στους ασθενείς με ισχαιμική καρδιακή ή αγγειοεγκεφαλική νόσο στους οποίους μία σημαντική πτώση της αρτηριακής πίεσης μπορεί να οδηγήσει σε έμφραγμα του μυοκαρδίου ή αγγειοεγκεφαλικό επεισόδιο. Σε υπερτασικούς ασθενείς με καρδιακή ανεπάρκεια, με ή χωρίς σχετιζόμενη νεφρική ανεπάρκεια, έχει παρατηρηθεί συμπτωματική υπόταση. Εάν εμφανισθεί υπόταση, ο ασθενής θα πρέπει να τοποθετηθεί σε ύπτια θέση και εάν κριθεί αναγκαίο, να του χορηγηθεί ενδοφλεβίως διάλυμα φυσιολογικού ορού. Παροδικό υποτασικό φαινόμενο δεν είναι αντένδειξη για περαιτέρω χορήγηση που μπορεί να δοθεί συνήθως χωρίς δυσκολία μόλις η πίεση αυξηθεί μετά την αύξηση του αγγειακού όγκου. Διαταραχή της νεφρικής λειτουργίας Το CO-RENITEC δεν πρέπει να χορηγείται σε ασθενείς με νεφρική ανεπάρκεια (κάθαρση κρεατινίνης 80 ml/min και 30 ml/min) έως ότου η τιτλοποίηση της εναλαπρίλης καταδείξει ότι η απαιτούμενη δόση υπάρχει στο παρόν δισκίο συνδυασμού (βλέπε παράγραφο 4.2).
3 Μερικοί υπερτασικοί ασθενείς χωρίς εμφανή προϋπάρχουσα νεφρική νόσο ανέπτυξαν αυξήσεις της ουρίας του αίματος και της κρεατινίνης όταν η εναλαπρίλη χορηγήθηκε μαζί με ένα διουρητικό (βλέπε Ιδιαίτερες προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Μηλεϊνική εναλαπρίλη, Νεφρική δυσλειτουργία, Υδροχλωροθειζίδη, Διαταραχή της νεφρικής λειτουργίας στην παράγραφο 4.4). Αν αυτό εμφανισθεί, η θεραπεία με CO-RENITEC πρέπει να διακοπεί. Αυτή η κατάσταση εγείρει το ενδεχόμενο υποκείμενης στένωσης της νεφρικής αρτηρίας (βλέπε Ιδιαίτερες προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Εnalapril maleate, Νεφραγγειακή Υπέρταση στην παράγραφο 4.4). Διπλός αποκλεισμός του συστήματος ρενίνης-αγγειοτασίνης-αλδοστερόνης (ΣΡΑΑ) Έχουν αναφερθεί υπόταση, συγκοπή, εγκεφαλικό επεισόδιο, υπερκαλιαιμία, και αλλαγές της νεφρικής λειτουργίας (συμπεριλαμβανομένης της οξείας νεφρικής ανεπάρκειας) σε ευαίσθητα άτομα, ιδιαίτερα με συνδυασμό φαρμακευτικών προϊόντων που επηρεάζουν αυτό το σύστημα (βλέπε παράγραφο 4.5). Ο διπλός αποκλεισμός του συστήματος ρενίνης-αγγειοτασίνης-αλδοστερόνης σε συνδυασμό με ένα αναστολέα-μεα με ένα ανταγωνιστή αποκλειστών των υποδοχέων της αγγειοτασίνης ΙΙ (ΑΥΑ), ή αλισκιρένη δεν συνιστάται. Ο διπλός αποκλεισμός του ΣΡΑΑ σε συνδυασμό CO-RENITEC με αλισκιρένη δεν συνιστάται. Ο συνδυασμός με αλισκιρένη αντενδείκνυται σε ασθενείς με σακχαρώδη διαβήτη ή με νεφρική δυσλειτουργία (GFR<60ml/min/1.73 m 2 (βλέπε παράγραφο 4.3). Υπερκαλιαιμία Ο συνδυασμός της εναλαπρίλης και η χαμηλή δόση διουρητικού δεν μπορεί να αποκλείσει την πιθανότητα εμφάνισης υπερκαλιαιμίας (βλέπε Ιδιαίτερες προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Μηλεϊνική εναλαπρίλη, Υπερκαλιαιμία στην παράγραφο 4.4). Λίθιο Ο συνδυασμός λιθίου με εναλαπρίλη και διουρητικά, γενικά δεν συνιστάται (βλέπε παράγραφο 4.5). Λακτόζη Το CO-RENITEC περιέχει λιγότερο από 200 mg λακτόζης σε κάθε δισκίο. Οι ασθενείς με σπάνια κληρονομικά προβλήματα δυσανεξίας της γαλακτόζης, ανεπάρκεια της Lapp λακτάσης ή δυσαπορρόφησης της γλυκόζης-γαλακτόζης δεν πρέπει να πάρουν αυτό το φάρμακο. Μηλεϊνική εναλαπρίλη Αορτική στένωση / Υπερτροφική καρδιομυοπάθεια Όπως όλοι οι αγγειοδιαστολείς, οι αναστολείς ΜΕΑ πρέπει να χρησιμοποιούνται με προσοχή σε ασθενείς με υπερτροφική καρδιομυοπάθεια και να αποφεύγεται σε περιπτώσεις καρδιογενούς σοκ και αιμοδυναμικά σημαντικής απόφραξης. Διαταραχή νεφρικής λειτουργίας Έχει αναφερθεί νεφρική ανεπάρκεια που σχετίζεται με την εναλαπρίλη, κυρίως σε ασθενείς με σοβαρή καρδιακή ανεπάρκεια ή με υποκείμενη νεφρική νόσο, συμπεριλαμβανομένης της στένωσης νεφρικής αρτηρίας. Αν διαγνωσθεί έγκαιρα και θεραπευθεί κατάλληλα η νεφρική ανεπάρκεια, όταν σχετίζεται με θεραπεία με εναλαπρίλη, είναι συνήθως αναστρέψιμη (βλέπε παράγραφο 4.2 και 4.4 Ειδικές προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Μηλεϊνική εναλαπρίλη-
4 Υδροχλωροθειαζίδη, Νεφρική δυσλειτουργία, Υδροχλωροθειαζίδη, Διαταραχή νεφρικής λειτουργίας στην παράγραφο 4.4. Νεφραγγειακή υπέρταση Υπάρχει αυξημένος κίνδυνος για υπόταση και νεφρική ανεπάρκεια όταν ασθενείς με αμφοτερόπλευρη στένωση της νεφρικής αρτηρίας ή στένωση της αρτηρίας μονήρους νεφρού λάβουν αγωγή με αναστολείς ΜΕΑ. Η απώλεια της νεφρικής λειτουργίας μπορεί να παρουσιαστεί και με ήπιες μεταβολές της κρεατινίνης του πλάσματος. Στους ασθενείς αυτούς η θεραπεία πρέπει να αρχίζει κάτω από στενή ιατρική παρακολούθηση με χαμηλές δόσεις και προσεκτική τιτλοποίηση της δόσης και παρακολούθηση της νεφρικής λειτουργίας. Μεταμόσχευση νεφρού Δεν υπάρχει εμπειρία σχετικά με τη χορήγηση εναλαπρίλης σε ασθενείς με πρόσφατη μεταμόσχευση νεφρού. Επομένως δεν συνιστάται η θεραπεία με εναλαπρίλη. Ασθενείς που υποβάλλονται σε αιμοδιύλυση Δεν ενδείκνυται η χορήγηση της εναλαπρίλης σε ασθενείς στους οποίους απαιτείται αιμοδιύλυση λόγω νεφρικής ανεπάρκειας. Έχουν αναφερθεί αναφυλακτοειδείς αντιδράσεις σε ασθενείς που υποβάλλονται σε αιμοδιύλιση με υψηλής ροής μεμβράνες (π.χ ΑΝ 69 ) και ταυτόχρονα βρίσκονται σε αγωγή με αναστολείς ΜΕΑ. Σε αυτούς τους ασθενείς συνιστάται να χρησιμοποιείται μία εναλλακτική μεμβράνη ή ένα αντιϋπερτασικό φάρμακο άλλης κατηγορίας. Ηπατική ανεπάρκεια Σπάνια, οι αναστολείς ΜΕΑ έχουν συσχετισθεί με ένα σύνδρομο που αρχίζει με χολοστατικό ίκτερο ή ηπατίτιδα και εξελίσσεται σε κεραυνοβόλο ηπατική νέκρωση και (μερικές φορές) σε θάνατο. Ο μηχανισμός αυτού του συνδρόμου δεν είναι κατανοητός. Οι ασθενείς που λαμβάνουν αναστολείς ΜΕΑ που ανέπτυξαν ίκτερο ή σημαντικές αυξήσεις των ηπατικών ενζύμων θα πρέπει να διακόψουν τον αναστολέα ΜΕΑ και να έχουν την κατάλληλη ιατρική παρακολούθηση (βλέπε Ιδιαίτερες προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Υδροχλωροθειαζίδη, Ηπατική νόσος στην παράγραφο.4.4). Ουδετεροπενία/Ακοκκιοκυτάρωση Έχουν αναφερθεί ουδετεροπενία/ακοκκιοκυτάρωση, θρομβοκυτοπενία και αναιμία σε ασθενείς που λαμβάνουν αναστολείς ΜΕΑ. Σε ασθενείς με φυσιολογική νεφρική λειτουργία και χωρίς άλλους παράγοντες επιπλοκών, σπάνια εμφανίζεται ουδετεροπενία. Η εναλαπρίλη θα πρέπει να χρησιμοποιηθεί με ιδιαίτερη προσοχή σε ασθενείς με κολλαγονική αγγειακή νόσο, ανοσοκατασταλτική θεραπεία, θεραπεία με αλλοπουρινόλη ή προκαϊναμίδη ή ένα συνδυασμό αυτών των περίπλοκων παραγόντων, ιδιαίτερα όταν προϋπάρχει διαταραχή της νεφρικής λειτουργίας. Μερικοί από αυτούς τους ασθενείς ανέπτυξαν σοβαρές λοιμώξεις οι οποίες σε μερικές περιπτώσεις, δεν ανταποκρίθηκαν στην εντατική θεραπεία με αντιβιοτικά. Εάν χορηγείται εναλαπρίλη σε τέτοιους ασθενείς, ενδείκνυται περιοδικός έλεγχος των λευκών αιμοσφαιρίων και οι ασθενείς θα πρέπει να καθοδηγούνται να αναφέρουν οποιοδήποτε σημείο λοίμωξης. Υπερκαλιαιμία Αυξήσεις στο κάλιο του ορού παρατηρήθηκαν σε μερικούς ασθενείς που έλαβαν θεραπεία με αναστολείς ΜΕΑ, συμπεριλαμβανομένης της εναλαπρίλης. Παράγοντες κινδύνου για την εμφάνιση υπερκαλιαιμίας, συμπεριλαμβάνουν αυτούς με νεφρική ανεπάρκεια, επιδείνωση της νεφρικής λειτουργίας, ηλικίας( 70 ετών), με σακχαρώδη διαβήτη, παρεμπίπτοντα επεισόδια, ιδιαίτερα αφυδάτωση, οξεία καρδιακή μη αντιρροπούμενη ανεπάρκεια, μεταβολική οξέωση και ταυτόχρονη
5 χρήση καλιοσυντηρητικών διουρητικών (π.χ. σπιρονολακτόνη, επλερενόνη, τριαμτερένη, ή αμιλορίδη), υποκατάστατα καλίου ή υποκατάστατα αλάτων, που περιέχουν κάλιο, ή εκείνους τους ασθενείς που λαμβάνουν άλλα φάρμακα που σχετίζονται με αυξήσεις στο κάλιο το ορού (π.χ. ηπαρίνη). Η χρήση συμπληρωμάτων καλίου, καλιοσυντηρητικών διουρητικών ή υποκατάστατων αλάτων, που περιέχουν κάλιο ιδιαίτερα σε ασθενείς με επηρεασμένη νεφρική λειτουργία μπορεί να οδηγήσει σε σημαντική αύξηση του καλίου του ορού. Η υπερκαλιαιμία μπορεί να προκαλέσει σοβαρές και μερικές φορές θανατηφόρες αρρυθμίες. Αν θεωρηθεί απαραίτητη η ταυτόχρονη χορήγηση της εναλαπρίλης και οποιουδήποτε από τα παραπάνω αναφερθέντα σκευάσματα, πρέπει να χρησιμοποιούνται με προσοχή και συχνή παρακολούθηση του καλίου του ορού (βλέπε Ιδιαίτερες προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Μηλεϊνική εναλαπρίλη - Υδροχλωροθειαζίδη, Υπερκαλιαιμία, Υδροχλωροθειαζίδη, Μεταβολικές και Ενδοκρινικές Επιδράσεις παράγραφο.4.4 και 4.5). Υπογλυκαιμία Οι διαβητικοί ασθενείς που λαμβάνουν από το στόμα χορηγούμενα αντιδιαβητικά σκευάσματα ή ινσουλίνη, όταν αρχίζουν την θεραπεία με ένα αναστολέα ΜΕΑ, θα πρέπει να ενημερώνονται ώστε να παρακολουθούνται στενά για υπογλυκαιμία, ιδιαίτερα κατά τη διάρκεια του πρώτου μηνός της συνδυασμένης θεραπείας (βλέπε παράγραφο. 4.4 Ιδιαίτερες προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Υδροχλωροθειαζίδη, Μεταβολικές και Ενδοκρινικές Επιδράσεις στην παράγραφο 4.4 και παράγραφο 4.5). Υπερευαισθησία/Αγγειονευρωτικό οίδημα Έχει αναφερθεί αγγειονευρωτικό οίδημα του προσώπου, των άκρων, των χειλέων, της γλώσσας, της γλωττίδας και/ή του λάρυγγα σε ασθενείς που βρίσκονται σε αγωγή με αναστολείς του μετατρεπτικού ενζύμου της αγγειοτασίνης, συμπεριλαμβανομένης της εναλαπρίλης. Αυτό μπορεί να συμβεί καθ' όλη τη διάρκεια της θεραπείας. Σε αυτές τις περιπτώσεις το CO-RENITEC πρέπει να διακόπτεται αμέσως και να γίνεται απαραίτητος έλεγχος για να εξασφαλισθεί πλήρης εξάλειψη των συμπτωμάτων πριν τη διακοπή της θεραπείας. Ακόμη και σε εκείνες τις περιπτώσεις όπου στο οίδημα εμπλέκεται μόνο η γλώσσα, χωρίς δυσχέρεια του αναπνευστικού, μπορεί να απαιτηθεί παρατεταμένη παρακολούθηση των ασθενών, επειδή η θεραπεία με αντιϊσταμινικά και κορτικοστεροειδή μπορεί να μην είναι επαρκής. Πολύ σπάνια, έχουν αναφερθεί θάνατοι λόγω αγγειοοιδήματος, που σχετίζεται με οίδημα του λάρυγγα ή οίδημα της γλώσσας. Ασθενείς, με εμπλοκή της γλώσσας, της γλωττίδας ή του λάρυγγα στο οίδημα, είναι πιθανόν να παρουσιάσουν απόφραξη του αεραγωγού, ιδιαίτερα σ αυτούς με ιστορικό χειρουργικής επέμβασης των αεραγωγών. Όπου υπάρχει εμπλοκή της γλώσσας, της γλωττίδας ή του λάρυγγα, ώστε να προκαλείται απόφραξη των αεροφόρων οδών, θα πρέπει να χορηγηθεί αμέσως κατάλληλη θεραπεία, η οποία μπορεί να περιλαμβάνει, άμεση υποδόρια χορήγηση διαλύματος επινεφρίνης σε αναλογία 1:1.000 (0.3 ml έως 0.5 ml) και/ή μέτρα ώστε να εξασφαλισθεί ανοικτός αεραγωγός. Έχει αναφερθεί ότι οι ασθενείς που ανήκουν στην μαύρη φυλή που λαμβάνουν αναστολείς ΜΕΑ παρουσιάζουν μεγαλύτερη συχνότητα εμφάνισης αγγειοοιδήματος σε σύγκριση με εκείνους που ανήκουν στην λευκή φυλή. Ωστόσο, γενικά φαίνεται ότι οι ασθενείς που ανήκουν στην μαύρη φυλή βρίσκονται σε αυξημένο κίνδυνο αγγειοοιδήματος.
6 Οι ασθενείς με ιστορικό αγγειοοιδήματος μη σχετιζόμενο με θεραπεία με αναστολείς ΜΕΑ, μπορεί να βρίσκονται σε αυξημένο κίνδυνο αγγειοοιδήματος, ενώ λαμβάνουν θεραπεία με ένα αναστολέα ΜΕΑ (βλέπε επίσης 4.3). Αναφυλακτοειδείς αντιδράσεις κατά τη διάρκεια απευαισθητοποίησης έναντι υμενοπτέρων Σπάνια, ασθενείς που ελάμβαναν αναστολείς ΜΕΑ, παρουσίασαν αναφυλακτοειδείς αντιδράσεις απειλητικές για τη ζωή κατά τη διάρκεια απευαισθητοποίησης από δηλητήριο υμενοπτέρων. Αυτές οι αντιδράσεις αποφεύχθηκαν με την προσωρινή διακοπή του αναστολέα ΜΕΑ πριν από κάθε διαδικασία απευαισθητοποίησης. Αναφυλακτοειδείς αντιδράσεις κατά τη διάρκεια LDL αφαίρεσης Σπάνια, ασθενείς που ελάμβαναν αναστολείς ΜΕΑ κατά τη διάρκεια αφαίρεσης της χαμηλής πυκνότητας λιποπρωτεΐνης (LDL) με θειικό δεξτράνιο παρουσίασαν αναφυλακτικές αντιδράσεις απειλητικές για τη ζωή. Αυτές οι αντιδράσεις είχαν αποφευχθεί με την προσωρινή διακοπή της θεραπείας με τον αναστολέα ΜΕΑ πριν από κάθε θεραπεία αφαίρεσης. Βήχας Έχει αναφερθεί βήχας με τη χρήση αναστολέων ΜΕΑ. Χαρακτηριστικά, ο βήχας είναι μη παραγωγικός βήχας, επίμονος και εξαφανίζεται μετά τη διακοπή της αγωγής. Ο βήχας που σχετίζεται με αναστολέα ΜΕΑ πρέπει να λαμβάνεται υπόψη στη διαφορική διάγνωση του βήχα. Χειρουργική επέμβαση/αναισθησία Η εναλαπρίλη αναστέλλει την παραγωγή αγγειοτασίνης II και με αυτόν τον τρόπο μειώνει την ικανότητα των ασθενών, που υποβάλλονται σε μεγάλη χειρουργική επέμβαση ή αναισθησία με φάρμακα που προκαλούν υπόταση, να αντιρροπίσουν μέσω του μηχανισμού του συστήματος ρενίνης-αγγειοτασίνης. Η υπόταση που οφείλεται σε αυτόν τον μηχανισμό μπορεί να διορθωθεί με αύξηση του κυκλοφορούντος όγκου.( βλέπε παράγραφο 4.5). Κύηση Οι αναστολείς ΜΕΑ δεν πρέπει να χορηγούνται κατά την διάρκεια της κύησης. Εάν η θεραπεία με αναστολείς ΜΕΑ θεωρηθεί απαραίτητη, οι ασθενείς που προγραμματίζουν εγκυμοσύνη πρέπει να αλλάξουν θεραπεία και να λάβουν εναλλακτική αντιυπερτασική θεραπεία που έχει ένα τεκμηριωμένο προφίλ ασφάλειας για χορήγηση κατά την εγκυμοσύνη. Εάν έχει διαγνωσθεί εγκυμοσύνη, η θεραπεία με αναστολείς ΜΕΑ πρέπει να σταματήσει αμέσως και, εάν θεωρηθεί απαραίτητο, πρέπει να ξεκινήσει μία εναλλακτική θεραπεία (βλέπε παραγράφους 4.3 και 4.6). Εθνοτικές διαφορές Όπως με άλλους αναστολείς του μετατρεπτικού ενζύμου αγγειοτασίνης η εναλαπρίλης είναι προφανώς λιγότερο αποτελεσματική στη μείωση της αρτηριακής πίεσης σε άτομα της μαύρης φυλής από ότι στους μη μαύρους, πιθανόν λόγω του μεγαλύτερου επιπολασμού χαμηλής ρενίνης στους μαύρους υπερτασικούς ασθενείς. Υδροχλωροθειαζίδη Διαταραχή νεφρικής λειτουργίας Οι θειαζίδες μπορεί να μην είναι τα κατάλληλα διουρητικά για χρήση σε ασθενείς με νεφρική διαταραχή και δεν είναι αποτελεσματικά εάν οι τιμές κάθαρσης της κρεατινίνης είναι 30ml/min ή λιγότερο (π.χ. μέτρια ή βαριά νεφρική ανεπάρκεια, (βλέπε παράγραφο 4.2 και Ειδικές προειδοποιήσεις και προφυλάξεις κατά τη χρήση,
7 Μηλεϊνική εναλαπρίλη- Υδροχλωροθειαζίδη, Διαταραχή νεφρικής λειτουργίας, Μηλεϊνική εναλαπρίλη, Διαταραχή νεφρικής λειτουργίας στην παράγραφο 4.4 ). Ηπατική Νόσος Οι θειαζίδες θα πρέπει να χορηγούνται με προσοχή σε ασθενείς με διαταραχή της ηπατικής λειτουργίας ή προοδευτικά επιδεινούμενη ηπατική νόσο, επειδή μικρές μεταβολές στο ισοζύγιο των υγρών και των ηλεκτρολυτών μπορεί να επισπεύσουν την εμφάνιση ηπατικού κώματος ( βλέπε Ειδικές προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Μηλεϊνική εναλαπρίλη, Ηπατική ανεπάρκεια στην παράγραφο 4.4). Μεταβολικές και Ενδοκρινικές Επιδράσεις Η θεραπεία με θειαζίδη μπορεί να επηρεάσει την ανοχή στη γλυκόζη. Μπορεί να χρειασθεί αναπροσαρμογή της δοσολογίας των αντιδιαβητικών σκευασμάτων συμπεριλαμβανομένης της ινσουλίνης (βλέπε Ειδικές προειδοποιήσεις και προφυλάξεις κατά τη χρήση, Μηλεϊνική εναλαπρίλη, Διαβητικοί Ασθενείς στην παράγραφο 4.4). Αυξήσεις της χοληστερόλης και επιπέδων τριγλυκεριδίων μπορεί να σχετίζονται με τη διουρητική θεραπεία με θειαζίδη. Ωστόσο, με τη δόση 12.5 mg υδροχλωροθειαζίδης έχει αναφερθεί ελάχιστη ή καθόλου επίδραση. Επιπλέον, σε κλινικές μελέτες με υδροχλωροθειαζίδη 6 mg δεν αναφέρθηκαν κλινικά σημαντικές κλινικές επιδράσεις στη γλυκόζη, χοληστερόλη, τριγλυκερίδια, νάτριο, μαγνήσιο ή κάλιο. Σε ορισμένους ασθενείς η θεραπεία με θειαζίδη μορεί να προκαλέσει την εμφάνιση υπερουριχαιμίας και/ή ουρικής αρθρίτιδας. Η επίδραση στην υπερουριχαιμία φαίνεται ότι είναι δοσοεξαρτώμενη. Επιπλέον, η εναλαπρίλη μπορεί να αυξήσει το ουρικό οξύ των ούρων και έτσι να μειώσει την υπερουριχαιμική δράση της υδροχλωροθειαζίδης. Όπως για κάθε ασθενή που λαμβάνει διουρητική θεραπεία, θα πρέπει να γίνεται περιοδικός έλεγχος των ηλεκτρολυτών του ορού σε κατάλληλα διαστήματα. Οι θειαζίδες (συμπεριλαμβανομένης της υδροχλωροθειαζίδης ) μπορεί να προκαλέσουν ανισορροπία υγρών και ηλεκτρολυτών (υποκαλιαιμία, υπονατριαιμία και υποχλωραιμική αλκάλωση). Προειδοποιητικά σημεία της ανισορροπίας υγρών και ηλεκτρολυτών είναι ξηροστομία, δίψα, αδυναμία, λήθαργος, υπνηλία, ανησυχία, μυϊκό πόνο ή κράμπες, μυϊκή κόπωση, υπόταση, ολιγουρία, ταχυκαρδία και γαστρεντερικές διαταραχές όπως ναυτία και έμετος. Μολονότι μπορεί να εμφανισθεί υποκαλιαιμία κατά την χορήγηση θειαζιδικών διουρητικών, ταυτόχρονη θεραπεία με εναλαπρίλη μπορεί να μειώσει την υποκαλιαιμία που προκλήθηκε από το διουρητικό. Ο κίνδυνος υποκαλιαιμίας είναι πιο μεγάλος σε ασθενείς με κίρρωση του ήπατος, σε ασθενείς που παρουσίασαν γρήγορη διούρηση, σε ασθενείς με ανεπαρκή λήψη ηλετρολυτών από του στόματος και σε ασθενείς που λαμβάνουν ταυτόχρονη θεραπεία με κορτικοστεροειδή ή ACTH (βλέπε παράγραφο 4.5). Μπορεί να εμφανισθεί υπονατριαιμία σε ασθενείς με οίδημα σε συνθήκες καύσωνα. Το έλλειμμα χλωριούχων ενώσεων είναι γενικά μέτριο και δεν απαιτεί συνήθως θεραπεία. Οι θειαζίδες μπορεί να ελαττώσουν την απέκκριση ασβεστίου από τα ούρα και να προκαλέσουν μία διαλείπουσα και ελαφρά αύξηση του ασβεστίου στον ορό όταν δεν υπάρχουν διαπιστωμένες διαταραχές του μεταβολισμού του ασβεστίου.
8 Εκσεσημασμένη υπερασβεστιαιμία μπορεί να αποτελεί ένδειξη λανθάνοντος υπερπαραθυροειδισμού. Οι θειαζίδες θα πρέπει να διακόπτονται πριν τη διεξαγωγή εξετάσεων σχετικών με τη λειτουργία του παραθυροειδούς. Οι θειαζίδες έχουν δείξει ότι αυξάνουν την απέκκριση του μαγνησίου από τα ούρα που μπορεί να οδηγήσει σε υπομαγνησαιμία. Έλεγχος anti-doping Η υδροχλωροθειαζίδη που περιέχεται σ αυτό το φαρμακευτικό προϊόν μπορεί να προκαλέσει θετικό αναλυτικό αποτέλεσμα σε έλεγχο anti-doping. Υπερευαισθησία Σε ασθενείς που λαμβάνουν θειαζίδες, μπορεί να εμφανισθούν αντιδράσεις υπερευαισθησίας με ή χωρίς ιστορικό αλλεργίας ή βρογχικού άσθματος. Έχει αναφερθεί έξαρση ή ενεργοποίηση του ερυθηματώδους λύκου με την χρήση θειαζιδών. 4.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης Μηλεϊνική εναλαπρίλη Υδροχλωροθειαζίδη Διπλός αποκλεισμός του συστήματος ρενίνης-αγγειοτασίνης-αλδοστερόνης (ΣΡΑΑ) Ο διπλός αποκλεισμός (π.χ. με τον συνδυασμό ενός αναστολέα ΜΕΑ με ένα ανταγωνιστή των υποδοχέων της αγγειοτασίνης ΙΙ ή αλισκιρένη) θα πρέπει να περιορίζεται σε συγκεκριμένες εξατομικευμένες περιπτώσεις με στενή παρακολούθηση της νεφρικής λειτουργίας, των ηλεκρολυτών, και της αρτηριακής πίεσης. Μερικές μελέτες έδειξαν ότι σε ασθενείς με τεκμηριωμένη αθηροσκληρωτική νόσο, καρδιακή ανεπάρκεια, ή με διαβήτη με τελική βλάβη οργάνου, ο διπλός αποκλεισμός σχετίζεται με μεγαλύτερη συχνότητα υπότασης, συγκοπής, υπερκαλιαιμίας, και επιδείνωσης της νεφρικής λειτουργίας (συμπεριλαμβανομένης της οξείας νεφρικής ανεπάρκειας) σε σύγκριση με τη χρήση μεμονωμένου παράγοντα του συστήματος ρενίνης-αγγειοτασίνης-αλδοστερόνης. Να μην συγχορηγείται αλισκιρένη με CO- RENITEC σε ασθενείς με διαβήτη ή σε ασθενείς με νεφρική δυσλειτουργία (GFR<60ml/min/1.73 m 2 (βλέπε παράγραφο 4.3 και 4.4). Άλλοι αντιυπερτασικοί παράγοντες Η ταυτόχρονη χορήγηση αυτών των σκευασμάτων μπορεί να αυξήσει το υποτασικό αποτέλεσμα της εναλαπρίλης και της υδροχλωροθειαζίδης. Η ταυτόχρονη χορήγηση με νιτρογλυκερίνη ή άλλα νιτρώδη, ή άλλους αγγειοδιαστολείς, μπορεί να μειώσουν περαιτέρω την αρτηριακή πίεση. Λίθιο Αναστρέψιμες αυξήσεις του λιθίου στον ορό και της τοξικότητας έχουν αναφερθεί κατά τη διάρκεια ταυτόχρονης χορήγησης του λιθίου με αναστολείς ΜΕΑ. Η ταυτόχρονη χορήγηση θειαζιδικών διουρητικών, μπορεί να αυξήσει περαιτέρω τα επίπεδα του λιθίου και να αυξήσει τον κίνδυνο της τοξικότητας του λιθίου με αναστολείς ΜΕΑ. Η χορήγηση του CO-RENITEC με λίθιο δεν συνιστάται, αλλά εάν ο συνδυασμός κριθεί απαραίτητος, θα πρέπει να γίνεται προσεκτικός έλεγχος των επιπέδων λιθίου στον ορό. (βλέπε παράγραφο 4.4).
9 Μη στεροειδή αντιφλεγμονώδη φάρμακα συμπεριλαμβανομένων των εκλεκτικών αναστολέων της κυκλοοξυγενάσης-2 (COX-2) Τα μη στεροειδή αντιφλεγμονώδη φάρμακα συμπεριλαμβανομένων των εκλεκτικών αναστολέων της κυκλοοξυγενάσης-2 (αναστολέων COX-2) μπορεί να μειώσουν την δράση των διουρητικών και άλλων αντιυπερτασικών φαρμάκων. Επομένως, η αντιυπερτασική δράση των ανταγωνιστών των υποδοχέων της αγγειοτασίνης ΙΙ, των αναστολέων ΜΕΑ ή των διουρητικών μπορεί να εξασθενίσει μέσω των ΜΣΑΦ συμπεριλαμβανομένων των εκλεκτικών αναστολέων της κυκλοοξυγενάσης-2 (COX-2). Η συγχορήγηση των ΜΣΑΦ (συμπεριλαμβανομένων των αναστολέων COX-2) και των ανταγωνιστών των υποδοχέων της αγγειοτασίνης ΙΙ ή των αναστολέων ΜΕΑ επιφέρουν ένα επιπρόσθετο αποτέλεσμα στην αύξηση του καλίου του ορού, και μπορεί να οδηγήσουν στην επιδείνωση της νεφρικής λειτουργίας. Αυτές οι επιδράσεις είναι συνήθως αναστρέψιμες. Σπάνια, μπορεί να παρουσιασθεί οξεία νεφρική ανεπάρκεια, ιδιαίτερα σε ασθενείς με επηρεασμένη νεφρική λειτουργία (όπως οι ηλικιωμένοι ή ασθενείς με μειωμένο όγκο υγρών, συμπεριλαμβανομένων αυτών που λαμβάνουν διουρητική αγωγή). Επομένως, ο συνδυασμός θα πρέπει να χορηγείται με προσοχή σε ασθενείς με επηρεασμένη νεφρική λειτουργία. Μηλεϊνική εναλαπρίλη Καλιοσυντηρητικά διουρητικά, ή συμπληρώματα καλίου. Οι αναστολείς ΜΕΑ μετριάζουν την προκαλούμενη από τα διουρητικά απώλεια καλίου. Τα καλιοσυντηρητικά διουρητικά (π.χ σπιρονολακτόνη, τριαμτερένη, ή αμιλορίδη), τα συμπληρώματα καλίου, ή τα υποκατάστατα αλάτων που περιέχουν κάλιο μπορεί να οδηγήσουν σε σημαντική αύξηση του καλίου του ορού. Εάν η ταυτόχρονη χορήγηση ενδείκνυται λόγω αποδεδειγμένης υποκαλιαιμίας, πρέπει να χρησιμοποιούνται με προσοχή και συχνή παρακολούθηση του καλίου του ορού (βλέπε παράγραφο 4.4) Διουρητικά (θειαζιδικά ή διουρητικά της αγκύλης) Προϋπάρχουσα θεραπεία με μεγάλες δόσεις διουρητικών μπορεί να οδηγήσει σε μειωμένο όγκο υγρών και σε κίνδυνο για υπόταση, εάν αρχίσει η θεραπεία με εναλαπρίλη (βλέπε παράγραφο 4.2 και 4.4). Τα υποτασικά αποτελέσματα μπορεί να μειωθούν με τη διακοπή του διουρητικού ή με την αύξηση του όγκου υγρών ή την λήψη άλατος. Τρικυκλικά αντικαταθλιπτικά/αντιψυχωσικά/αναισθητικά Η ταυτόχρονη χορήγηση ορισμένων αναισθητικών φαρμακευτικών προϊόντων τρικυκλικών αντικαταθλιπτικών και αντιψυχωσικών με αναστολείς ΜΕΑ μπορεί να οδηγήσει σε περαιτέρω μείωση της αρτηριακής πίεσης. (βλέπε παράγραφο 4.4) Συμπαθομιμητικά Τα συμπαθομιμητικά μπορεί να μειώνουν τις αντιυπερτασικές επιδράσεις των αναστολέων ΜΕΑ Αντιδιαβητικά Επιδημιολογικές μελέτες υποστηρίζουν ότι η ταυτόχρονη χορήγηση αναστολέων ΜΕΑ και αντιδιαβητικών φαρμακευτικών σκευασμάτων (ινσουλίνης, από το στόμα χορηγούμενων υπογλυκαιμικών σκευασμάτων), μπορεί να προκαλέσουν αυξημένη αποτελεσματικότητα στη μείωση της γλυκόζης του αίματος με κίνδυνο υπογλυκαιμίας. Αυτό το γεγονός, φαίνεται ότι είναι πιθανότερο να συμβεί κατά τη διάρκεια των πρώτων εβδομάδων της συνδυασμένης θεραπείας και σε ασθενείς με νεφρική βλάβη (βλέπε παράγραφο 4.5 και 4.8)
10 Αλκοόλ Το αλκοόλ αυξάνει το υποτασικό αποτέλεσμα των αναστολέων ΜΕΑ. Ακετυλοσαλικυλικό οξύ, θρομβολυτικά και β-αναστολείς Η εναλαπρίλη μπορεί να χορηγηθεί με ασφάλεια ταυτόχρονα με ακετυλοσαλικυλικό οξύ (σε καρδιολογική δοσολογία), θρομβολυτικά και β-αναστολείς). Ενώσεις χρυσού Αντιδράσεις παρόμοιες με αυτές των νιτριτοειδών ενώσεων (συμπτώματα που περιλαμβάνουν έξαψη του προσώπου, ναυτία, έμετο και υπόταση) έχουν αναφερθεί σπάνια σε ασθενείς που λαμβάνουν θεραπεία με ενώσεις χρυσού ενέσιμης μορφής (νάτριο θειομηλικού χρυσού) και ταυτόχρονη θεραπεία με αναστολέα ΜΕΑ συμπεριλαμβανομένης της εναλαπρίλης. Υδροχλωροθειαζίδη Μη αποπολωτικά μυοχαλαρωτικά: Οι θειαζίδες μπορεί να αυξήσουν την ανταπόκριση στην τουβοκουραρίνη. Αλκοόλ, βαρβιτουρικά ή οπιοειδή αναλγητικά Μπορεί να εμφανισθεί ενίσχυση της ορθοστατικής υπότασης. Αντιδιαβητικά φάρμακα (σκευάσματα χορηγούμενα από το στόμα και ινσουλίνη) Μπορεί να απαιτηθεί αναπροσαρμογή της δοσολογίας του αντιδιαβητικού φαρμάκου (βλέπε παράγραφο 4.8). Ρητίνες χολεστυραμίνης και κολεστιπόλης Η απορρόφηση της υδροχλωροθειαζίδης παραβλάπτεται με την παρουσία ρητινών ανταλλαγής ανιόντων. Εφάπαξ δόσεις ρητινών είτε χολεστυραμίνης ή κολεστιπόλης δεσμεύουν την υδροχλωροθειαζίδη και μειώνουν την απορρόφηση από το γαστρεντερικό σωλήνα κατά 85% και 43% αντίστοιχα. Αύξηση του διαστήματος QT (π.χ. κινιδίνη, προκαϊναμίδη, αμιωδαρόνη σολοτόλη ) Aυξημένος κίνδυνος για κοιλιακή ταχυκαρδία δίκην ριπιδίου ( torsades de pointes) Γλυκοζίδες της δακτυλίτιδας Η υποκαλιαιμία μπορεί να ευαισθητοποιήσει ή να επιτείνει την ανταπόκριση της καρδιάς στις τοξικές επιδράσεις της δακτυλίτιδας (π.χ αυξημένη κοιλιακή ευερεθιστότητα) Κορτικοστεροειδή, ACTH Έντονη μείωση των ηλεκτρολυτών, ειδικότερα υποκαλιαιμία Καλιοσυντηρητικά διουρητικά (π.χ φουροσεμίδη), καρβενοξολόνη ή κατάχρηση καθαρτικών Η υδροχλωροθειαζίδη μπορεί να αυξήσει την απώλεια καλίου και/ή μαγνησίου Αγγειοσυσπαστικές αμίνες (π.χ νοραδρεναλίνη) Η επίδραση των αγγειοσυσπαστικών αμινών μπορεί να μειωθεί Κυτταροστατικά (π.χ κυκλοφωσφαμίδη, μεθοτρεξάτη Oι θειαζίδες μπορεί να μειώσουν τη νεφρική απέκκριση κυτταροστατικών φαρμάκων και να αυξήσουν τις μυελοκατασταλτικές επιδράσεις.
11 Παιδιατρικός πληθυσμός Μελέτες αλληλεπίδρασης έχουν διεξαχθεί μόνο σε ενήλικες. 4.6 Γονιμότητα, κύηση και γαλουχία Κύηση Αναστολείς ΜΕΑ: Η χρήση των αναστολέων ΜΕΑ δεν συνιστάται κατά το πρώτο τρίμηνο της κύησης (βλέπε παράγραφο 4.4). Η χρήση των αναστολέων ΜΕΑ αντενδείκνυται κατά το δεύτερο και τρίτο τρίμηνο της κύησης (βλέπε παραγράφους 4.3 και 4.4). Δεν υπάρχει οριστική απόδειξη μέσω επιδημιολογικής μελέτης σχετικά με τον κίνδυνο για τερατογένεση κατόπιν έκθεσης σε αναστολείς ΜΕΑ κατά το πρώτο τρίμηνο της κύησης. Ωστόσο, δεν μπορεί να αποκλεισθεί μία μικρή αύξηση του κινδύνου. Εάν η θεραπεία με αναστολείς ΜΕΑ θεωρηθεί απαραίτητη, οι ασθενείς που προγραμματίζουν εγκυμοσύνη πρέπει να αλλάξουν θεραπεία και να λάβουν εναλλακτική αντιυπερτασική θεραπεία που έχει ένα τεκμηριωμένο προφίλ ασφάλειας για χορήγηση κατά την εγκυμοσύνη. Εάν έχει διαγνωσθεί εγκυμοσύνη, η θεραπεία με αναστολείς ΜΕΑ πρέπει να σταματήσει αμέσως και, εάν κριθεί απαραίτητο, πρέπει να ξεκινήσει μία εναλλακτική θεραπεία. Είναι γνωστό ότι η έκθεση στους αναστολείς ΜΕΑ κατά τη διάρκεια του δεύτερου και τρίτου τριμήνου της κύησης, προκαλεί εμβρυοτοξικότητα στον άνθρωπο (μειωμένη νεφρική λειτουργία, ολιγοϋδράμνιο, καθυστέρηση της οστεοποίησης του κρανίου ) και νεογνική τοξικότητα (νεφρική ανεπάρκεια, υπόταση, υπερκαλιαιμία) (Βλέπε παράγραφο 5.3) Εάν υπάρχει έκθεση στους αναστολείς ΜΕΑ από το δεύτερο τρίμηνο της κύησης, συνιστάται να γίνει έλεγχος μέσω υπερηχογραφήματος της νεφρικής λειτουργίας και του κρανίου. Τα βρέφη των οποίων οι μητέρες έλαβαν αναστολείς ΜΕΑ, πρέπει να παρακολουθούνται προσεκτικά για υπόταση (βλέπε παραγράφους 4.3 και 4.4). Yδροχλωροθειαζίδη: Υπάρχει περιορισμένη εμπειρία από τη χρήση υδροχλωροθειαζίδης κατά την εγκυμοσύνη, ιδιαίτερα κατά το πρώτο τρίμηνο. Μελέτες σε πειραματόζωα δεν είναι επαρκείς. Η υδροχλωροθειαζίδη διαπερνά τον πλακουντιακό φραγμό. Βάσει του φαρμακολογικού μηχανισμού δράσης της υδροχλωροθειαζίδης, η χρήση της κατά το δεύτερο και τρίτο τρίμηνο μπορεί να επηρεάσει τη διήθηση μέσω του πλακούντα στο έμβρυο και να προκαλέσει εμβρυϊκές και νεογνικές επιδράσεις, όπως ίκτερο, διαταραχές ηλεκτρολυτών και θρομβοκυτοπενία. Η υδροχλωροθειαζίδη δεν πρέπει να χορηγείται επι οιδήματος της κυήσεως, υπέρτασης της κυήσεωςή προεκλαμψίας λόγω του κινδύνου μείωσης του όγκου του πλάσματος και πλακουντιακής υποδιήθησης, χωρίςευεργετικά αποτελέσματα όσον αφορά την πορεία της νόσου. Η υδροχλωροθειαζίδη δεν πρέπει να χορηγείται για την ιδιοπαθή υπέρταση σε έγκυες γυναίκες, εκτός από σπάνιες περιπτώσεις, όπου δεν μπορεί να χρησιμοποιηθεί καμία άλλη εναλλακτική θεραπεία. Θηλασμός Εναλαπρίλη:
12 Περιορισμένος αριθμός στοιχείων φαρμακοκινητικής δείχνει πολύ μικρές συγκεντρώσεις στο μητρικό γάλα (βλέπε παράγραφο 5.2). Παρόλο που αυτές οι συγκεντρώσεις δεν φαίνεται ότι είναι κλινικά σχετιζόμενες, η χρήση του CO- RENITEC κατά την γαλουχία δεν συνιστάται για τα πρόωρα νεογνά και για τις λίγες πρώτες εβδομάδες μετά την γέννησή τους, λόγω του υποθετικού κινδύνου για καρδιαγγειακές και νεφρικές επιδράσεις και λόγω του ότι δεν υπάρχει επαρκής κλινική εμπειρία. Στην περίπτωση ενός μεγαλύτερου βρέφους, η χρήση του CO-RENITEC από την μητέρα που θηλάζει μπορεί να εξετασθεί ως ενδεχόμενο, εάν αυτή η θεραπεία είναι αναγκαία για την μητέρα και το παιδί παρακολουθείται για οποιαδήποτε ανεπιθύμητη ενέργεια. Υδροχλωροθειαζίδη: Η υδροχλωροθειαζίδη εκκρίνεται στο μητρικό γάλα σε μικρές ποσότητες. Οι θειαζίδες σε μεγάλες δόσεις που προκαλούν έντονη διούρηση μπορεί να εμποδίσουν την παραγωγή γάλακτος. Η χρήση του CO-RENITEC κατά τη διάρκεια της γαλουχίας δεν συνιστάται. Εάν το CO-RENITEC χρησιμοποιηθεί κατά τη διάρκεια της γαλουχίας, οι δόσεις πρέπει να παραμείνουν όσο το δυνατόν χαμηλότερες. 4.7 Επίδραση στην ικανότητα οδήγησης και χειρισμού μηχανών Θα πρέπει να λαμβάνεται υπόψη ότι κατά την οδήγηση οχημάτων ή το χειρισμό μηχανών μπορεί να εμφανισθεί περιστασιακά ζάλη ή κόπωση( βλέπε παράγραφο 4.8).
13 4.8 Ανεπιθύμητες ενέργειες Το CO RENITEC είναι συνήθως καλά ανεκτό. Σε κλινικές μελέτες, οι ανεπιθύμητες ενέργειες ήταν συνήθως ήπιες και παροδικές, και στις περισσότερες περιπτώσεις δεν απαιτήθηκε διακοπή της θεραπείας. Οι πιο συχνές ανεπιθύμητες ενέργειες που αναφέρθηκαν κατά την διάρκεια κλινικής μελέτης με το CO RENITEC ήταν κεφαλαλγία και βήχας. Οι ακόλουθες ανεπιθύμητες ενέργειες έχουν αναφερθεί για το CO RENITEC, μόνο με την εναλαπρίλη ή μόνο με την υδροχλωροθειαζίδη, είτε κατά την διάρκεια κλινικών μελετών ή μετά την κυκλοφορία του φαρμάκου. Κατηγορία οργανικό σύστημα Πολύ συχνές (> 1/10) Συχνές ( 1/100 έως <1/10) Όχι συχνές ( 1/1.000 έως <1/100) Σπάνιες ( 1/ έως <1/1.000) Πολύ σπάνιες (<1/ ) Μη γνωστές (δεν μπορούν να εκτιμηθούν με βάση τα διαθέσιμα δεδομένα) Διαταραχές του αίματος και του λεμφικού συστήματος Αναιμία (συμπεριλαμ βανομένης απλαστικής και της αιμολυτικής) Ουδετεροπεν ία, μείωση αιμοσφαιρίνη ς, μείωση του αιματοκρίτη, θρομβοκυτοπ ενία, ακοκιοκυττά ρωση, καταστολή του μυελού των οστών, λευκοπενία, πανκυτοπενία, λεμφαδενοπά θεια,αυτοάνο σοι νόσοι. Διαταραχές του ενδοκρινικού συστήματος σύνδρομο απρόσφορης έκκρισης αντιδιουρητικής ορμόνης (SIADH) Διαταραχές του μεταβολισμού και της θρέψης Υποκαλιαιμ ία, αύξηση χοληστερόλ ης, αύξηση τριγλυκεριδί ων,υπερουρι χαιμία Υπογλυκαιμί α (βλέπε παράγραφο 4.4),υπομαγν η σαιμία, ουρική αρθρίτιδα** Αύξηση γλυκόζης αίματος Υπερασβεσ τ αιμία(βλέπ ε παράγραφο. 4.4).
14 Κατηγορία οργανικό σύστημα Πολύ συχνές (> 1/10) Συχνές ( 1/100 έως <1/10) Όχι συχνές ( 1/1.000 έως <1/100) Σπάνιες ( 1/ έως <1/1.000) Πολύ σπάνιες (<1/ ) Μη γνωστές (δεν μπορούν να εκτιμηθούν με βάση τα διαθέσιμα δεδομένα) Διαταραχές του νευρικού συστήματος και ψυχιατρικές διαταραχές: Κεφαλαλγία, κατάθλιψη, συγκοπή, διαταραχές γεύσης Σύγχυση, υπνηλία, αϋπνία, νευρικότητα, παραισθησία, ίλιγγος, μειωμένη libido** Ανώμαλα όνειρα, διαταραχές ύπνου, πάρεση (λόγω υποκαλιαιμία ς) Οφθαλμικές διαταραχές Θάμβος όρασης Διαταραχές των ώτων και του λαβυρίνθου Εμβοές Καρδιακές και αγγειακές διαταραχές Ζάλη Υπόταση, ορθοστατικ ή υπόταση, διαταραχές του καρδιακού ρυθμού, ασταθή στηθάγχη, ταχυκαρδία. Έξαψη, αίσθημα παλμών, έμφραγμα του μυοκαρδίου ή αγγειοεγκεφα λικό επεισόδιο* πιθανόν δευτερογενώ ς λόγω εκσεσημαμέ νης υπότασης σε ασθενείς υψηλού κινδύνου (βλέπε παράγραφο 4.4) Φαινόμενο Raynaud s
15 Κατηγορία οργανικό σύστημα Πολύ συχνές (> 1/10) Συχνές ( 1/100 έως <1/10) Όχι συχνές ( 1/1.000 έως <1/100) Σπάνιες ( 1/ έως <1/1.000) Πολύ σπάνιες (<1/ ) Μη γνωστές (δεν μπορούν να εκτιμηθούν με βάση τα διαθέσιμα δεδομένα) Διαταραχές του αναπνευστικού συστήματος, του θώρακα και του μεσοθωράκιου Βήχας Δύσπνοια Ρινόρροια, κυνάγχη, βράχνος φωνής, βρογχόσπα σμος/άσθμα Πνευμονικές διηθήσεις, αναπνευστικ ή δυσχέρεια, (συμπεριλαμ βανομένης της πνευμονίτιδα ς και του πνευμονικού οιδήματος), ρινίτις, αλλεργική κυψελίτιδα/ ηωσινοφιλικ η πνευμονία.
16 Κατηγορία οργανικό σύστημα Πολύ συχνές (> 1/10) Συχνές ( 1/100 έως <1/10) Όχι συχνές ( 1/1.000 έως <1/100) Σπάνιες ( 1/ έως <1/1.000) Πολύ σπάνιες (<1/ ) Μη γνωστές (δεν μπορούν να εκτιμηθούν με βάση τα διαθέσιμα δεδομένα) Διαταραχές του γαστρεντερικού Διαταραχές του ήπατος και των χοληφόρων Ναυτία Διάρροια, κοιλιακό άλγος Ειλεός, παγκρεατίτιδ α, έμετος, δυσπεψία, δυσκοιλιότητ α, ανορεξία, γαστρικοί ερεθισμοί, ξηροστομία, πεπτικό έλκος, μετεωρισμός ** Στοματίτιδα/ άφθώδη έλκη, γλωσσίτιδα Ηπατική ανεπάρκεια, ηπατική νέκρωση, (μπορεί να αποβεί θανατηφόρα), ηπατίτιδα είτε ηπατοκυτταρι κή ή χολοστατική, ίκτερος, χολοκυστίτιδ α (ειδικότερα σε ασθενείς με προϋπάρχουσ α χολολιθίαση). Εντερικό αγγειοοίδη μα
17 Κατηγορία οργανικό σύστημα Πολύ συχνές (> 1/10) Συχνές ( 1/100 έως <1/10) Όχι συχνές ( 1/1.000 έως <1/100) Σπάνιες ( 1/ έως <1/1.000) Πολύ σπάνιες (<1/ ) Μη γνωστές (δεν μπορούν να εκτιμηθούν με βάση τα διαθέσιμα δεδομένα) Διαταραχές του δέρματος και του υποδόρριου ιστού Εξάνθημα (exanthema). υπερευαισθ ησία/αγγειο νευρωτικό οίδημα: αγγειονευρ ω τικό οίδημα του προσώπου, των άκρων, των χειλέων, της γλώσσας, γλωττίδας και/ή του λάρυγγα (βλέπε παράγραφο 4.4 ) Εφίδρωση, κνίδωση, κνησμός, αλωπεκία Πολύμορφο ερύθημα, σύνδρομο Stevens- Johnson, αποφολιδωτι κή δερματίτιδα, τοξική επιδερμική νεκρόλυση, πορφύρα, δερματικός ερυθυματώδη ς λύκος, ερυθρόδερμα, πέμφιγ Έχει αναφερθεί ένα σύμπλεγμα συμπτωμάτων που μπορεί να περιλαμβάνει μερικά ή όλα από τα ακόλουθα: πυρετός, ορογονίτιδα, αγγειίτιδα, μυαλγία/μυοσίτι δα, αρθραλγία/αρθρί τι δα, θετικά ΑΝΑ, αυξημένη ΤΚΕ, ηωσινοφιλία και λευκοκυττάρωσ η. Εξάνθημα, φωτοευαισθησία ή άλλες δερματολογικές εκδηλώσεις μπορεί να εμφανισθούν. Διαταραχές του μυοσκελετικού συστήματος και του συνδετικού ιστού μυϊκές κράμπες*** αρθραλγία** Διαταραχές των νεφρών και του ουροποιητικού συστήματος Νεφρική δυσλειτουρ γία, νεφρική ανεπάρκεια, πρωτεϊνουρία Ολιγουρία, διάμεση νεφρίτις Αναπαραγωγικό σύστημα και διαταραχές των μαστών Ανικανότητα Γυναικο μαστία
18 Κατηγορία οργανικό σύστημα Πολύ συχνές (> 1/10) Συχνές ( 1/100 έως <1/10) Όχι συχνές ( 1/1.000 έως <1/100) Σπάνιες ( 1/ έως <1/1.000) Πολύ σπάνιες (<1/ ) Μη γνωστές (δεν μπορούν να εκτιμηθούν με βάση τα διαθέσιμα δεδομένα) Γενικές διαταραχές και ενοχλήσεις στη θέση χορήγησης Εξασθένι ση Θωρακικό άλγος, κόπωση Κακουχία, πυρετός Παρακλινικές εξετάσεις Υπερκαλιαι μία, αυξήσεις της κρεατινίνης του ορού Αυξήσεις στην ουρία του αίματος, υπονατριαιμί α Αυξήσεις των ηπατικών ενζύμων, αυξήσεις της χολερυθρίνης του ορού Στις κλινικές μελέτες οι συχνότητες επίπτωσης ήταν συγκρίσιμες μεταξύ των ομάδων του placebo και αυτών της ενεργού θεραπείας. παρατηρήθηκε μόνο με δόσεις υδροχλωροθειαζίδης 12.5mg και 25mg, όπως βρέθηκε στο CO-RENITEC Η συχνότητα των μυϊκών κραμπών ως συχνή προκύπτει από τις δόσεις υδροχλωροθειαζίδης 12.5mg και 25mg, όπως βρέθηκε στο CO-RENITEC, ενώ η συχνότητα του συμβάματος είναι όχι συχνή όπως προκύπτει από τη δόση των 6 mg υδροχλωροθειαζίδης που βρίσκεται στο CO-RENITEC 6. Αναφορά πιθανολογούμενων ανεπιθύμητων ενεργειών Η αναφορά πιθανολογούμενων ανεπιθύμητων ενεργειών μετά από τη χορήγηση άδειας κυκλοφορίας του φαρμακευτικού προϊόντος είναι σημαντική. Επιτρέπει τη συνεχή παρακολούθηση της σχέσης οφέλους/κινδύνου του φαρμακευτικού προϊόντος. Ζητείται από τους επαγγελματίες του τομέα της υγειονομικής περίθαλψης να αναφέρουν οποιεσδήποτε πιθανολογούμενες ανεπιθύμητες ενέργειες απευθείας στον Εθνικό Οργανισμό Φαρμάκων (Μεσογείων 284, Χολαργός, Υπερδοσολογία Δεν υπάρχουν ειδικές πληροφορίες για την αντιμετώπιση της υπερδοσολογίας με CO- RENITEC. Η θεραπεία είναι συμπτωματική και υποστηρικτική. Η θεραπεία με CO- RENITEC πρέπει να διακόπτεται και ο ασθενής να παρακολουθείται στενάτα προτεινόμενα μέτρα περιλαμβάνουν την πρόκληση εμέτου, χορήγηση ενεργού άνθρακα και καθαρτικών εάν η λήψη είναι πρόσφατη και διόρθωση της αφυδάτωσης, της διαταραχής των ηλεκτρολυτών και της υπότασης με τις καθιερωμένες μεθόδους. Μηλεϊνική εναλαπρίλη Τα πλέον προεξέχοντα χαρακτηριστικά υπερδοσολογίας που έχουν αναφερθεί μέχρι σήμερα είναι εκσεσημασμένη υπόταση εμφανιζόμενη περίπου 6 ώρες μετά τη λήψη των δισκίων, ταυτόχρονα με τον αποκλεισμό του συστήματος ρενίνης-αγγειοτενσίνης και λήθαργος. Συμπτώματα που σχετίζονται με υπερδοσολογία των α-μεα μπορεί να
19 περιλαμβάνουν κυκλοφορικό σοκ, διαταραχές ηλεκτρολυτών, νεφρική ανεπάρκεια, υπεραερισμό, ταχυκαρδία, αίσθημα παλμών, βραδυκαρδία, ζάλη, ανησυχία και βήχα. Επίπεδα του άλατος της εναλαπρίλης στον ορό, 100 και 200 φορές μεγαλύτερα από τα συνήθη θεραπευτικά επίπεδα έχουν αναφερθεί μετά τη λήψη 300 mg και 440 mg μηλεϊνικής εναλαπρίλης, αντίστοιχα. Η συνιστώμενη θεραπευτική αντιμετώπιση της υπερδοσολογίας είναι η ενδοφλέβια έγχυση φυσιολογικού ορού. Αν εμφανισθεί υπόταση, ο ασθενής θα πρέπει να τοποθετηθεί στην κατάλληλη θέση για την αντιμετώπιση του σοκ. Εάν είναι διαθέσιμη, μπορεί να εξετασθεί η χορήγηση αγγειοτασίνης ΙΙ με έγχυση και/ή ενδοφλέβια χορήγηση κατεχολαμινών. Αν η λήψη είναι πρόσφατη,θα πρέπει να ληφθούν μέτρα για την αποβολή της μηλεϊνικής εναλαπρίλης ( π.χ. έμετος, γαστρική πλύση, χορήγηση απορροφητικών σκευασμάτων, και θειικό νάτριο). Το άλας της εναλαπρίλης μπορεί να απομακρυνθεί από την κυκλοφορία με αιμοδιύλυση (βλέπε παράγραφο 4.4). Η θεραπεία με βηματοδότη ενδείκνυται για ανθιστάμενη στη θεραπεία βραδυκαρδία. Θα πρέπει να παρακολουθούνται προσεκτικά τα ζωτικά σημεία και οι συγκεντρώσεις των ηλεκτρολυτών και της κρεατινίνης στον ορό. Υδροχλωροθειαζίδη Τα πιο κοινά σημεία και συμπτώματα που έχουν παρατηρηθεί είναι εκείνα που προκαλούνται από την απώλεια των ηλεκτρολυτών (υποκαλιαιμία, υποχλωριαιμία, υπονατριαιμία) και αφυδάτωση σαν αποτέλεσμα της υπερβολικής διούρησης. Εάν επίσης έχει δοθεί δακτυλίτιδα, η υποκαλιαιμία μπορεί να επιδεινώσει τις καρδιακές αρρυθμίες. 5. ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 5.1 Φαρμακοδυναμικές Ιδιότητες Φαρμακοθεραπευτική κατηγορία: Εναλαπρίλη και διουρητικά, Κωδικός ATC: C09 B02 Το CO-RENITEC (εναλαπρίλη maleate & hydrochlorothiazide, MSD) είναι ένας συνδυασμός ενός αναστολέα του μετατρεπτικού ενζύμου της αγγειοτασίνης (εναλαπρίλη maleate) και ενός διουρητικού (hydrochlorothiazide). Το μετατρεπτικό ένζυμο της αγγειοτασίνης είναι μία πεπτιδιλική διπεπτιδάση που καταλύει τη μετατροπή της αγγειοτασίνης Ι στην αγγειοσυσπαστική ουσία αγγειοτασίνη ΙΙ. Μετά την απορρόφηση, η εναλαπρίλη υδρολύεται σε εναλαπριλάτη που αναστέλλει το μετατρεπτικό ένζυμο της αγγειοτασίνης. Η αναστολή του μετατρεπτικού ενζύμου της αγγειοτασίνης έχει σαν αποτέλεσμα τη μείωση της αγγειοτασίνης ΙΙ στο πλάσμα, που οδηγεί σε αύξηση της δραστικότητας της ρενίνης στο πλάσμα (επειδή δεν υπάρχει πλέον η παλίνδρομος αναστολή της απελευθέρωσης της ρενίνης) και μειώνει την έκκριση αλδοστερόνης. Το μετατρεπτικό ένζυμο της αγγειοτασίνης είναι ταυτόσημο με την κινινάση ΙΙ. Ετσι η εναλαπρίλη μπορεί επίσης να εμποδίσει την αποδόμηση της βραδυκινίνης, ένα ισχυρό αγγειοδιασταλτικό πεπτίδιο. Εντούτοις, ο ρόλος που παίζει στη θεραπευτική δράση η εναλαπρίλη εξακολουθεί να είναι αδιευκρίνιστος. Ενώ ο μηχανισμός μέσω του οποίου η εναλαπρίλη μειώνει την αρτηριακή πίεση πιστεύεται ότι οφείλεται κυρίως στην καταστολή του συστήματος ρενίνης - αγγειοτασίνης - αλδοστερόνης, που παίζει σημαντικό ρόλο στη ρύθμιση της αρτηριακής πίεσης, η εναλαπρίλη είναι αποτελεσματική ακόμη και σε υπερτασικούς ασθενείς με χαμηλή ρενίνη.
20 Η υδροχλωροθειαζίδη είναι ένα διουρητικό και αντιυπερτασικό φάρμακο που αυξάνει τη δραστικότητα της ρενίνης στο πλάσμα. Αν και η εναλαπρίλη χορηγούμενη ως μονοθεραπεία είναι αντιυπερτασικό ακόμη και σε υπερτασικούς ασθενείς με χαμηλή ρενίνη, η ταυτόχρονη χορήγηση της υδροχλωροθειαζίδης σε αυτούς τους ασθενείς οδηγεί σε μεγαλύτερη μείωση της αρτηριακής πίεσης. Ο μηχανισμός της αντιυπερτασικής δράσης των θειαζιδών είναι άγνωστος. Η υδροχλωροθειαζίδη συνήθως δεν επηρεάζει τη φυσιολογική πίεση του αίματος. Χορήγηση μηλεϊνικής εναλαπρίλης σε ασθενείς με υπέρταση έχει σαν αποτέλεσμα τη μείωση της αρτηριακής πίεσης τόσο σε ύπτια όσο και σε όρθια θέση, χωρίς σημαντική αύξηση της καρδιακής συχνότητας. Η συμπτωματική ορθοστατική υπόταση δεν είναι συχνή. Σε μερικούς ασθενείς η επίτευξη της επιθυμητής μείωσης της αρτηριακής πίεσης μπορεί να απαιτεί μερικές εβδομάδες θεραπείας. Απότομη διακοπή της μηλεϊνικής εναλαπρίλης δεν έχει συνδυαστεί με ταχεία αύξηση της αρτηριακής πίεσης. Αποτελεσματική αναστολή της δραστικότητας του μετατρεπτικού ενζύμου της αγγειοτασίνης συνήθως συμβαίνει 2 έως 4 ώρες μετά τη λήψη από το στόμα μιας μόνο δόσης εναλαπρίλης. Εναρξη της αντιυπερτασικής δράσης συνήθως παρατηρείται σε μία ώρα με το μέγιστο της μείωσης της αρτηριακής πίεσης σε 4 έως 6 ώρες μετά τη χορήγηση. Η διάρκεια δράσης είναι δοσοεξαρτώμενη. Ωστόσο, στις συνιστώμενες δόσεις η αντιυπερτασική και η αιμοδυναμική δράση έχει αποδειχθεί ότι διατηρείται τουλάχιστον 24 ώρες. Σε αιμοδυναμικές μελέτες σε ασθενείς με ιδιοπαθή υπέρταση, η μείωση της αρτηριακής πίεσης συνοδεύτηκε με μείωση των περιφεριακών αγγειακών αντιστάσεων με ελαφρά αύξηση της καρδιακής παροχής και μικρή ή καμία μεταβολή της καρδιακής συχνότητας. Μετά τη χορήγηση της μηλεϊνικής εναλαπρίλης υπήρξε αύξηση στη νεφρική ροή του αίματος. Ο ρυθμός σπειραματικής διήθησης ήταν αμετάβλητος. Όμως, σε ασθενείς με χαμηλό ρυθμό σπειραματικής διήθησης προ της θεραπείας συνήθως παρατηρήθηκε αύξηση του ρυθμού. Σε κλινικές μελέτες το μέγεθος της μείωσης της αρτηριακής πίεσης που παρατηρείται από το συνδυασμό μηλεϊνικής εναλαπρίλης και υδροχλωροθειαζίδης ήταν μεγαλύτερο από αυτό που παρατηρήθηκε εάν χορηγούνται τα συστατικά μεμονωμένα. Επιπλέον, η αντιυπερτασική δράση του CO-RENITEC διατηρείται για 24 ώρες τουλάχιστον. 5.2 Φαρμακοκινητικές ιδιότητες Το CO-RENITEC έχει αντιυπερτασική και διουρητική δράση. Η μηλεϊνική εναλαπρίλη και η υδροχλωροθειαζίδη έχουν χρησιμοποιηθεί χωριστά και από κοινού για τη θεραπεία της υπέρτασης. Οι αντιυπερτασικές ενέργειες αυτών των δύο φαρμάκων είναι αθροιστικές και διαρκούν 24 ώρες τουλάχιστον. Η μηλεϊνική εναλαπρίλη συστατικό του CO-RENITEC έχει αποδειχθεί ότι μειώνει την απώλεια καλίου που σχετίζεται με την υδροχλωροθειαζίδη. Η μηλεϊνική εναλαπρίλη και η υδροχλωροθειαζίδη έχουν παρόμοια δοσολογικά σχήματα. Έτσι, το CO-RENITEC προσφέρεται σαν κατάλληλο σκεύμασμα για την ταυτόχρονη χορήγηση της μηλεϊνικής εναλαπρίλης και της υδροχλωροθειαζίδης. Απορρόφηση Η μηλεϊνική εναλαπρίλη χορηγούμενη από το στόμα απορροφάται γρήγορα και οι μέγιστες συγκεντρώσεις στον ορό, εμφανίζονται μέσα σε μια ώρα. Με βάση την
21 ανάκτηση από τα ούρα, ο βαθμός της απορρόφησης της εναλαπρίλης χορηγούμενης ως μηλεϊνικής εναλαπρίλης από το στόμα είναι περίπου 60%. Μετά την από του στόματος απορρόφηση, η εναλαπρίλη υδρολύεται γρήγορα και εκτεταμένα σε εναλαπριλάτη ένα ισχυρό αναστολέα του μετατρεπτικού ενζύμου της αγγειοτασίνης. Οι μέγιστες συγκεντρώσεις της εναλαπριλάτης at στον ορό εμφανίζονται 3 με 4 ώρες μετά τη χορήγηση τηςμηλεϊνικής εναλαπρίλης από το στόμα. Η απέκκριση της εναλαπρίλης είναι κυρίως νεφρική. Τα κύρια συστατικά στα ούρα είναι εναλαπριλάτη σε ποσοστό περίπου 40% της δόσης και αυτούσια εναλαπρίλη. Εκτός από την μετατροπή σε εναλαπριλάτη δεν υπάρχει ένδειξη για σημαντικό μεταβολισμό της εναλαπρίλης. Το προφίλ της συγκέντρωσης τηςεναλαπρίλης στον ορό παρουσιάζει μία παρατεταμένη τελική φάση, προφανώς σχετιζόμενη με τη σύνδεση με το μετατρεπτικό ένζυμο της αγγειοτασίνης. Σε άτομα με φυσιολογική νεφρική λειτουργία σταθερές συγκεντρώσεις της εναλαπριλάτης στον ορό επιτεύχθηκαν την τέταρτη ημέρα της αγωγής Η έκταση απορρόφησης και υδρόλυσης της εναλαπρίλης είναι παρόμοια για διαφορετικές δόσεις εντός του συνιστώμενου θεραπευτικού εύρους. Ο αποτελεσματικός χρόνος για τη συρώρευση των συγκεντρώσεων του άλατος εναλαπρίλης κατά το ήμισυ μετά χορήγησης πολλαπλών δόσεων μηλεϊνικής εναλαπρίλης από το στόμα είναι 11 ώρες. Οταν τα επίπεδα του πλάσματος παρακολουθούνται για 24 τουλάχιστον ώρες, η ημίσεια ζωή στο πλάσμα έχει παρατηρηθεί ότι κυμαίνεται μεταξύ 5,6 και 14,8 ωρών. Η υδροχλωροθειαζίδη δε μεταβολίζεται αλλά αποβάλλεται γρήγορα από τα νεφρά. Τουλάχιστον 61% της δοσολογίας από το στόμα αποβάλλεται αναλλοίωτο μέσα σε 24 ώρες. Η υδροχλωροθειαζίδη διαπερνά τον πλακούντα αλλά όχι το φραγμό αίματος - εγκεφάλου. Μηλεϊνική εναλαπρίλη και υδροχλωροθειαζίδη Η από κοινού χορήγηση πολλαπλών δόσεων μηλεϊνικής εναλαπρίλης και υδροχλωροθειαζίδης έχουν μικρή ή καμία επίδραση στη βιοδιαθεσιμότητα αυτών των φαρμάκων. Το συνδυασμένο δισκίο είναι βιολογικά ισοδύναμο με την ταυτόχρονη χορήγηση των ουσιών μεμονωμένα. Κατανομή Για το εύρος των θεραπευτικών συγκεντρώσεων, το ποσοστό σύνδεσης της εναλαπριλάτης που συνδέεται με τις πρωτεϊνες του πλάσματος δεν ξεπερνά το 60 %. Βιομετατροπή Εκτός από τη μετατροπή σε εναλαπριλάτη, δεν υπάρχουν ενδείξεις για σημαντικό μεταβολισμό της εναλαπρίλης. Η υδροχλωροθειαζίδη δεν μεταβολίζεται αλλά απεκκρίνεται ταχέως από τους νεφρούς. Αποβολή Η απέκκριση της εναλαπριλάτης είναι κυρίως νεφρική. Τα κύρια συστατικά στα ούρα είναι εναλαπριλάτη που αντιστοιχεί στο 40% περίπου της δόσης και άθικτη εναλαπρίλη (περίπου 20 %). Η υδροχλωροθειαζίδη δεν μεταβολίζεται αλλά απεκκρίνεται ταχέως από τους νεφρούς. Τουλάχιστον το 61% της από του στόματος χορηγούμενης δόσης απεκκρίνεται άθικτο εντός 24 ωρών. Νεφρική δυσλειτουργία
22 Η έκθεση στην εναλαπρίλη και την εναλαπριλάτη είναι αυξημένη σε ασθενείς με νεφρική ανεπάρκεια. Σε ασθενείς με μέτρια έως ήπια νεφρική ανεπάρκεια (κάθαρση κρεατινίνης ml/min) η ΑUC της εναλαπριλάτης σε σταθερή κατάσταση ηταν περίπου δύο φορές υψηλότερη από οτι σε ασθενείς με φυσιολογική νεφρική λειτουργία μετά από χορήγηση 5 mg ημερησίως. Σε σοβαρή νεφρική ανεπάρκεις (κάθαρση κρεατινίνης <30 ml/min) η AUC αυξήθηκε περίπου 8 φορές. Ο αποτελεσματικός χρόνος ημιζωής της εναλαπριλάτης μετά από πολλαπλές δόσεις μηλεϊνικής εναλαπρίλης παρατείνεται σε αυτό το επίπεδο νεφρικής ανεπάρκειας και ο χρόνος για την κατάσταση ισορροπίας καθυστερεί (βλέπε παράγραφο 4.2). Η εναλαπριλάτη μπορεί να απομακρυνθεί από τη γενική κυκλοφορία με αιμοδιύλιση. Η κάθαρση της αιμοδιύλισης είναι 62 ml/min. Γαλουχία Μετά από μια εφάπαξ δόση των 20mg χoρηγούμενη από το στόμα σε πέντε γυναίκες μετά τον τοκετό ο μέσος όρος του μέγιστου επιπέδου εναλαπρίλης στο γάλα ήταν 1.7μg/l (εύρος 0.54 έως 5.9 μg/l) σε 4 έως 6 ώρες μετά την δόση. Ο μέσος όρος του μέγιστου επιπέδου του άλατος εναλαπρίλης ήταν 1.7μg/l (εύρος 1.2 έως 2.3 μg/l. Μέγιστα επίπεδα παρατηρήθηκαν σε διαφορετικούς χρόνους στο διάστημα των 24 ωρών. Μέσω των στοιχείων των μέγιστων επιπέδων του γάλακτος, η υπολογισθείσα μέγιστη λήψη ενός αποκλειστικά θηλάζοντος βρέφους ήταν περίπου 0.16 % της δοσολογίας που προσαρμόσθηκε με το βάρος της μητέρας. Μια γυναίκα που έχει λάβει εναλαπρίλη 10mg χορηγούμενη από το στόμα ημερησίως για 11 μήνες είχε μέγιστα επίπεδα εναλαπρίλης στο γάλα 2 μg/l 4 ώρες μετά την δόση και μέγιστα επίπεδα άλατος εναλαπρίλης στο γάλα 0.75 μg/l περίπου 9 ώρες μετά την δόση. Η συνολική ποσότητα εναλαπρίλης και άλατος εναλαπρίλης που μετρήθηκε στο γάλα στην περίοδο 24 ωρών ήταν 1.44 μg/l και 0.63 μg/l του γάλακτος αντίστοιχα. Τα επίπεδα του άλατος εναλαπρίλης στο γάλα δεν ήταν ανιχνεύσιμα ( 0.2 μg/l) 4 ώρες μετά από μια εφάπαξ δόση εναλαπρίλης 5mg σε μία μητέρα και 10mg σε 2 δύο μητέρες. Τα επίπεδα εναλαπρίλης δεν προσδιορίσθηκαν. 5.3 Προκλινικά στοιχεία για την ασφάλεια Τα προκλινικά δεδομένα δεν αποκαλύπτουν ιδιαίτερο κίνδυνο για τους ανθρώπους με βάση συμβατικέ μελέτες φαρμακολογικής ασφάλειας, επαναλαμβανομένης τοξικότητας, γονοτοξικότητας ενδεχόμενης καρκινογένεσης. Οι μελέτες αναπαραγωγικής τοξικότητας υποδεικνύουν ότι η εναλαπρίλη δεν επιδρά στην γονιμότητα και αναπαραγωγική ιδιότητα των αρουραίων και οτι δεν είναι τερατογόνος. Σε μία μελέτη, κατά την οποία θηλυκοί αρουραίοι έλαβαν το φάρμακο πριν το ζευγάρωμα και κατά την διάρκεια της κυοφορίας, παρατηρήθηκε αυξημένη επίπτωση θανάτων των νεογνών αρουραίων κατά τη γαλουχία. Η δραστική διαπερνά τον πλακούντα και εκκρίνεται στο γάλα. Οι αναστολείς του μετατρεπτικού ενζύμου της αγγειοτασίνης, ως κατηγορία, έχει δειχθεί ότι είναι εμβρυοτοξικοί (προκαλούν βλάβη και/ή θάνατο του εμβρύου), όταν χορηγούνται στο δεύτερο ή τρίτο τρίμηνο. Η υδροχλωροθειαζίδη περνά τον πλακούντα αλλά όχι τον αιματοεγκεφαλικό φραγμό. Μηλεϊνική εναλαπρίλη: Η ασφάλεια της εναλαπρίλης διερευνήθηκε λεπτομερώς σε ποντίκια, αρουραίους, σκύλους και πιθήκους ώστε να αξιολογηθεί η γενική τοξικότητα. Το σκεύασμα αυτό έχει μία χαμηλή συχνότητα οξείας τοξικότητας. Η από του στόματος LD 50 της
CO-RENITEC R. (enalapril maleate & hydrochlorothiazide, MSD) ΔΙΣΚΙΑ ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ ΧΡΗΣΗΣ ΣΤΑΘΕΡΩΝ ΣΥΝΔΥΑΣΜΩΝ ΔΙΟΥΡΗΤΙΚΩΝ ΜΕ ΑΛΛΑ ΥΠΟΤΑΣΙΚΑ ΦΑΡΜΑΚΑ
 CO-RENITEC R CRN-GR-3296 (enalapril maleate & hydrochlorothiazide, MSD) ΔΙΣΚΙΑ ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ ΧΡΗΣΗΣ ΣΤΑΘΕΡΩΝ ΣΥΝΔΥΑΣΜΩΝ ΔΙΟΥΡΗΤΙΚΩΝ ΜΕ ΑΛΛΑ ΥΠΟΤΑΣΙΚΑ ΦΑΡΜΑΚΑ Δεν ενδείκνυται γενικά ευθύς εξ αρχής η χορήγηση
CO-RENITEC R CRN-GR-3296 (enalapril maleate & hydrochlorothiazide, MSD) ΔΙΣΚΙΑ ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ ΧΡΗΣΗΣ ΣΤΑΘΕΡΩΝ ΣΥΝΔΥΑΣΜΩΝ ΔΙΟΥΡΗΤΙΚΩΝ ΜΕ ΑΛΛΑ ΥΠΟΤΑΣΙΚΑ ΦΑΡΜΑΚΑ Δεν ενδείκνυται γενικά ευθύς εξ αρχής η χορήγηση
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Enapral 5 mg, δισκία Enapral 20 mg, δισκία Παρακαλείσθε να διαβάσετε προσεκτικά αυτό το φυλλάδιο ακόμη και αν έχετε ξαναχρησιμοποιήσει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Enapral 5 mg, δισκία Enapral 20 mg, δισκία Παρακαλείσθε να διαβάσετε προσεκτικά αυτό το φυλλάδιο ακόμη και αν έχετε ξαναχρησιμοποιήσει
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
Penopril (Enalapril maleate 20mg + Hydrochlorothiazide 12,5mg)
 Penopril (Enalapril maleate 20mg + Hydrochlorothiazide 12,5mg) 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Penopril. 1.2 Σύνθεση Δραστικές ουσίες: Enalapril maleate + hydrochlorothiazide
Penopril (Enalapril maleate 20mg + Hydrochlorothiazide 12,5mg) 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Penopril. 1.2 Σύνθεση Δραστικές ουσίες: Enalapril maleate + hydrochlorothiazide
1.1 Enalapril HEXAL comp 10/25: Δισκία 10 mg enalapril maleate και 25 mg hydrochlorodiazide
 Φύλλο Οδηγιών Χρήσης. Παρακαλώ διαβάστε προσεκτικά! Αγαπητοί ασθενείς, Παρακαλώ διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης. Περιέχει σημαντικές πληροφορίες για σας. Εάν έχετε περαιτέρω απορίες
Φύλλο Οδηγιών Χρήσης. Παρακαλώ διαβάστε προσεκτικά! Αγαπητοί ασθενείς, Παρακαλώ διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης. Περιέχει σημαντικές πληροφορίες για σας. Εάν έχετε περαιτέρω απορίες
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΣΗΜΕΙΩΣΗ: ΤΟ ΠΑΡΟΝ SPC (ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ) ΑΠΟΤΕΛΟΥΣΕ ΠΑΡΑΡΤΗΜΑ ΤΗΣ ΑΠΟΦΑΣΗΣ ΤΗΣ ΕΠΙΤΡΟΠΗΣ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΠΑΡΑΠΕΜΠΤΙΚΟ ΓΙΑ ΙΑΙΤΗΣΙΑ. ΤΑ ΚΕΙΜΕΝΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΣΗΜΕΙΩΣΗ: ΤΟ ΠΑΡΟΝ SPC (ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ) ΑΠΟΤΕΛΟΥΣΕ ΠΑΡΑΡΤΗΜΑ ΤΗΣ ΑΠΟΦΑΣΗΣ ΤΗΣ ΕΠΙΤΡΟΠΗΣ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΠΑΡΑΠΕΜΠΤΙΚΟ ΓΙΑ ΙΑΙΤΗΣΙΑ. ΤΑ ΚΕΙΜΕΝΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ FORTEKOR FLAVOUR 5 mg Δισκία επικαλυμμένα με υμένιο για γάτες και σκύλους
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Δισκία επικαλυμμένα με υμένιο για γάτες και σκύλους 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Δισκία επικαλυμμένα με υμένιο για γάτες και σκύλους 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΑΡΕΝΤΕΡΙΚΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ
 ΠΑΡΕΝΤΕΡΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ https://users.auth.gr/epontiki Ελένη Ποντίκη Θεσσαλονίκη 2018 Παρεντερικά διαλύματα Αποστειρωμένα διαλύματα που προορίζονται: για την στοιχείων αναπλήρωση
ΠΑΡΕΝΤΕΡΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΝΤΕΡΙΚΗ ΔΙΑΤΡΟΦΗ / ΣΥΜΠΛΗΡΩΜΑΤΑ https://users.auth.gr/epontiki Ελένη Ποντίκη Θεσσαλονίκη 2018 Παρεντερικά διαλύματα Αποστειρωμένα διαλύματα που προορίζονται: για την στοιχείων αναπλήρωση
Ο νεφρώνας είναι το πιο σημαντικο μερος των νεφρων υγρα και ηλεκτρολυτες
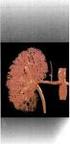 ΔΙΟΥΡΗΤΙΚΑ Ο νεφρώνας είναι το πιο σημαντικο μερος των νεφρων υγρα και ηλεκτρολυτες Σχηματισμος ουρων: 1. Σπειραματικη διηθηση (GFR) = 180L/day 2. Σωληναριακη επαναρροφηση(περιπου 98%) 3. Σωληναριακη απεκκριση
ΔΙΟΥΡΗΤΙΚΑ Ο νεφρώνας είναι το πιο σημαντικο μερος των νεφρων υγρα και ηλεκτρολυτες Σχηματισμος ουρων: 1. Σπειραματικη διηθηση (GFR) = 180L/day 2. Σωληναριακη επαναρροφηση(περιπου 98%) 3. Σωληναριακη απεκκριση
To Zestoretic κυκλοφορεί σε δισκία που περιέχουν δύο δραστικά συστατικά. Κάθε δισκίο περιέχει 20 mg lisinopril και 12.5 mg hydrochlorothiazide.
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ZESTORETIC TABLETS ΤΙ ΠΡΕΠΕΙ ΝΑ ΓΝΩΡΙΖΕΤΕ ΓΙΑ ΤΟ ZESTORETIC. Οι πληροφορίες που περιέχονται σ αυτό το φυλλάδιο αφορούν μόνο το φάρμακό σας, το Zestoretic. Διαβάστε το προσεκτικά. Παρέχει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ZESTORETIC TABLETS ΤΙ ΠΡΕΠΕΙ ΝΑ ΓΝΩΡΙΖΕΤΕ ΓΙΑ ΤΟ ZESTORETIC. Οι πληροφορίες που περιέχονται σ αυτό το φυλλάδιο αφορούν μόνο το φάρμακό σας, το Zestoretic. Διαβάστε το προσεκτικά. Παρέχει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8%
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8% 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Νάτριο Ανθρακικό Όξινο/DEMO (Sodium Bicarbonate/DEMO) 2. ΠΟΙΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΝΑΤΡΙΟ ΑΝΘΡΑΚΙΚΟ ΟΞΙΝΟ/DEMO Ενέσιμο διάλυμα 4% και 8% 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Νάτριο Ανθρακικό Όξινο/DEMO (Sodium Bicarbonate/DEMO) 2. ΠΟΙΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΣΗΜΕΙΩΣΗ: ΤΟ ΠΑΡΟΝ SPC (ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ) ΑΠΟΤΕΛΟΥΣΕ ΠΑΡΑΡΤΗΜΑ ΤΗΣ ΑΠΟΦΑΣΗΣ ΤΗΣ ΕΠΙΤΡΟΠΗΣ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΠΑΡΑΠΕΜΠΤΙΚΟ ΓΙΑ ΙΑΙΤΗΣΙΑ. ΤΑ ΚΕΙΜΕΝΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΣΗΜΕΙΩΣΗ: ΤΟ ΠΑΡΟΝ SPC (ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ) ΑΠΟΤΕΛΟΥΣΕ ΠΑΡΑΡΤΗΜΑ ΤΗΣ ΑΠΟΦΑΣΗΣ ΤΗΣ ΕΠΙΤΡΟΠΗΣ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΠΑΡΑΠΕΜΠΤΙΚΟ ΓΙΑ ΙΑΙΤΗΣΙΑ. ΤΑ ΚΕΙΜΕΝΑ
ΤΙ ΕΙΝΑΙ ΤΟ ΦΑΡΜΑΚΟ ΣΑΣ; To Zestril κυκλοφορεί σε χάπια που περιέχουν 5 mg, 10 mg ή 20 mg lisinopril.
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ZESTRIL TABLETS ΤΙ ΠΡΕΠΕΙ ΝΑ ΓΝΩΡΙΖΕΤΕ ΓΙΑ ΤΟ ZESTRIL. Οι πληροφορίες που περιέχονται σ αυτό το φυλλάδιο αφορούν μόνο το φάρμακό σας, το Zestril. Διαβάστε το προσεκτικά. Παρέχει σημαντικές
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ZESTRIL TABLETS ΤΙ ΠΡΕΠΕΙ ΝΑ ΓΝΩΡΙΖΕΤΕ ΓΙΑ ΤΟ ZESTRIL. Οι πληροφορίες που περιέχονται σ αυτό το φυλλάδιο αφορούν μόνο το φάρμακό σας, το Zestril. Διαβάστε το προσεκτικά. Παρέχει σημαντικές
Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών
 Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών Οι ρευματικές παθήσεις είναι συχνές στην αναπαραγωγική ηλικία των γυναικών. Στην πρόσφατη πανελλήνια επιδημιολογική έρευνα για τις ρευματικές παθήσεις στο γενικό
Από: Ελληνικό Ίδρυμα Ρευματολογικών Ερευνών Οι ρευματικές παθήσεις είναι συχνές στην αναπαραγωγική ηλικία των γυναικών. Στην πρόσφατη πανελλήνια επιδημιολογική έρευνα για τις ρευματικές παθήσεις στο γενικό
Empirol ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ
 NORMA HELLAS S.A. EMPIROL VERSION: PIL-2060601-03 DATE: 14-12-2012 Empirol ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Empirol 1.2 ΣΥΝΘΕΣΗ ΔΡΑΣΤΙΚΕΣ ΟΥΣΙΕΣ: Καπτοπρίλη,
NORMA HELLAS S.A. EMPIROL VERSION: PIL-2060601-03 DATE: 14-12-2012 Empirol ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Empirol 1.2 ΣΥΝΘΕΣΗ ΔΡΑΣΤΙΚΕΣ ΟΥΣΙΕΣ: Καπτοπρίλη,
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης
 Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
Παράρτημα III. Τροποποιήσεις στις σχετικές παραγράφους των πληροφοριών προϊόντος
 Παράρτημα III Τροποποιήσεις στις σχετικές παραγράφους των πληροφοριών προϊόντος Σημείωση: Οι αλλαγές στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών Προϊόντος και του Φύλλου Οδηγιών Χρήσης
Παράρτημα III Τροποποιήσεις στις σχετικές παραγράφους των πληροφοριών προϊόντος Σημείωση: Οι αλλαγές στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών Προϊόντος και του Φύλλου Οδηγιών Χρήσης
Tormis 5 mg δισκία Tormis 10 mg δισκία Tορασεμίδη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 5 mg δισκία Tormis 10 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 5 mg δισκία Tormis 10 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι
Παράρτημα ΙΙ. Τροποποιήσεις στις αντίστοιχες παραγράφους των περιλήψεων χαρακτηριστικών προϊόντος και του φύλλου οδηγιών χρήσης
 Παράρτημα ΙΙ Τροποποιήσεις στις αντίστοιχες παραγράφους των περιλήψεων χαρακτηριστικών προϊόντος και του φύλλου οδηγιών χρήσης 7 Για προϊόντα που περιέχουν τους αναστολείς του μετατρεπτικού ενζύμου της
Παράρτημα ΙΙ Τροποποιήσεις στις αντίστοιχες παραγράφους των περιλήψεων χαρακτηριστικών προϊόντος και του φύλλου οδηγιών χρήσης 7 Για προϊόντα που περιέχουν τους αναστολείς του μετατρεπτικού ενζύμου της
ΠΑΙΔΙΑ ΚΑΙ ΦΑΡΜΑΚΑ. Γεώργιος Ι. Πανουτσόπουλος Δρ. Φυσιολογίας του Ανθρώπου Τμήμα Νοσηλευτικής Πανεπιστήμιο Πελοποννήσου
 ΠΑΙΔΙΑ ΚΑΙ ΦΑΡΜΑΚΑ Γεώργιος Ι. Πανουτσόπουλος Δρ. Φυσιολογίας του Ανθρώπου Τμήμα Νοσηλευτικής Πανεπιστήμιο Πελοποννήσου 1 Ο πρώτος χρόνος μετά τη γέννηση έχει τις μεγαλύτερες και ταχύτερες φυσιολογικές
ΠΑΙΔΙΑ ΚΑΙ ΦΑΡΜΑΚΑ Γεώργιος Ι. Πανουτσόπουλος Δρ. Φυσιολογίας του Ανθρώπου Τμήμα Νοσηλευτικής Πανεπιστήμιο Πελοποννήσου 1 Ο πρώτος χρόνος μετά τη γέννηση έχει τις μεγαλύτερες και ταχύτερες φυσιολογικές
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 ALTAXA ΠΕΡΙΛΗΨΗ ΤΟΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ α. α)sumatriptan succinate 50mg/δισκίο β). Sumatriptan succinate 100mg/ δισκίο Για τα έκδοχα βλίπε 'Φαρμακευτικά
ALTAXA ΠΕΡΙΛΗΨΗ ΤΟΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ α. α)sumatriptan succinate 50mg/δισκίο β). Sumatriptan succinate 100mg/ δισκίο Για τα έκδοχα βλίπε 'Φαρμακευτικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
ANASTOL Captopril + Hydrochlorothiazide
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) ANASTOL Captopril + Hydrochlorothiazide 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ : ANASTOL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) ANASTOL Captopril + Hydrochlorothiazide 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ : ANASTOL 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά:
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Edarbi 20 mg δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 20 mg μεδοξομιλικής αζιλσαρτάνης
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Edarbi 20 mg δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 20 mg μεδοξομιλικής αζιλσαρτάνης
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΑΝΤΙΣΤΟΙΧΕΣ ΠΑΡΑΓΡΑΦΟΙ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΑΝΤΙΣΤΟΙΧΕΣ ΠΑΡΑΓΡΑΦΟΙ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Σημείωση: Οι εν λόγω τροποποιήσεις της περίληψης των χαρακτηριστικών του προϊόντος και
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΑΝΤΙΣΤΟΙΧΕΣ ΠΑΡΑΓΡΑΦΟΙ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Σημείωση: Οι εν λόγω τροποποιήσεις της περίληψης των χαρακτηριστικών του προϊόντος και
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία: Flodil Kαψάκια, σκληρά 5 και 10 mg Αmlodipine 1.2 Σύνθεση: Δραστική ουσία:αmlodipine ( ως Amlodipine besylate ) Έκδοχα: Cellulose microcrystalline, Starch maize
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία: Flodil Kαψάκια, σκληρά 5 και 10 mg Αmlodipine 1.2 Σύνθεση: Δραστική ουσία:αmlodipine ( ως Amlodipine besylate ) Έκδοχα: Cellulose microcrystalline, Starch maize
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ. Panadol 250 mg υπόθετα Παρακεταμόλη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Panadol 250 mg υπόθετα Παρακεταμόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι περιλαμβάνει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Panadol 250 mg υπόθετα Παρακεταμόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι περιλαμβάνει
ROIPLON Ενέσιμο διάλυμα 1g/2ml vial (Etofenamate)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial (Etofenamate) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 φύσιγγα
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial (Etofenamate) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ROIPLON Ενέσιμο διάλυμα 1g/2ml vial 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 φύσιγγα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό + επινεφρίνη ή νορεπινεφρίνη
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE. Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ:
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: MEGACE 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) MEGACE Οξική Μεγεστρόλη (Megestrol Acetate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: MEGACE 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g macrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g macrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g Μacrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 10g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει 10g Μacrogol
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩN ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩN ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Pentatec 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΟ ΣΥΣΤΑΤΙΚΟ Κάθε δισκίο περιέχει 50mg καπτοπρίλη και 25mg υδροχλωροθειαζίδη.
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩN ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Pentatec 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΟ ΣΥΣΤΑΤΙΚΟ Κάθε δισκίο περιέχει 50mg καπτοπρίλη και 25mg υδροχλωροθειαζίδη.
Tormis 2,5 mg δισκία Tορασεμίδη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 2,5 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει σημαντικές
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Tormis 2,5 mg δισκία Tορασεμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει σημαντικές
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ IRBEPRESS 75 mg, 150 mg, 300 mg δισκία Ιρβεσαρτάνη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ IRBEPRESS 75 mg, 150 mg, 300 mg δισκία Ιρβεσαρτάνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ IRBEPRESS 75 mg, 150 mg, 300 mg δισκία Ιρβεσαρτάνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. Φυλάξτε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ III 1 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 4. ΚΛΙΝΙΚΑ ΣΤΟΙΧΕΙΑ 4.1 Θεραπευτικές ενδείξεις Θεραπεία του οξέος πόνου (βλ. παράγραφο 4.2). Συµπτωµατική θεραπεία της επώδυνης οστεοαρθρίτιδας
ΠΑΡΑΡΤΗΜΑ III 1 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 4. ΚΛΙΝΙΚΑ ΣΤΟΙΧΕΙΑ 4.1 Θεραπευτικές ενδείξεις Θεραπεία του οξέος πόνου (βλ. παράγραφο 4.2). Συµπτωµατική θεραπεία της επώδυνης οστεοαρθρίτιδας
Παράρτημα ΙΙΙ. Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης
 Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης Σημείωση : Οι τροποποιήσεις στην Περίληψη των Χαρακτηριστικών του Προϊόντος
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών του Προϊόντος και τα Φύλλα Οδηγιών Χρήσης Σημείωση : Οι τροποποιήσεις στην Περίληψη των Χαρακτηριστικών του Προϊόντος
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη. CYTOTEC 200 mcg Δισκία Μισοπροστόλη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CYTOTEC 200 mcg Δισκία Μισοπροστόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε αυτό το
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CYTOTEC 200 mcg Δισκία Μισοπροστόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε αυτό το
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ERRKES. Οφθαλμικές σταγόνες, διάλυμα
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
Ανακούφιση των συμπτωμάτων ήπιας έως μέτριας οστεοαρθρίτιδας των γονάτων.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Αμέσως δρώντα αγγειοδιασταλτικά, α-αποκλειστές, νιτρώδη: πού, πότε, πώς
 Αμέσως δρώντα αγγειοδιασταλτικά, α-αποκλειστές, νιτρώδη: πού, πότε, πώς Ηρακλής Αβραμόπουλος Παθολόγος Ιατρείο Υπέρτασης Νοσοκομείο Υγεία Αμέσως δρώντα αγγειοδιασταλτικά ΒΒ Χάλαση των αγγείων Δραστηριότητα
Αμέσως δρώντα αγγειοδιασταλτικά, α-αποκλειστές, νιτρώδη: πού, πότε, πώς Ηρακλής Αβραμόπουλος Παθολόγος Ιατρείο Υπέρτασης Νοσοκομείο Υγεία Αμέσως δρώντα αγγειοδιασταλτικά ΒΒ Χάλαση των αγγείων Δραστηριότητα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Aflen 300 mg καψάκια σκληρά Triflusal Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Aflen 300 mg καψάκια σκληρά Triflusal Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο,
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Αυτές οι μεταβολές στη ΠΧΠ και το φύλλο οδηγιών χρήσης θα είναι εν ισχύ κατά την έκδοση της Κοινοτικής
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Αυτές οι μεταβολές στη ΠΧΠ και το φύλλο οδηγιών χρήσης θα είναι εν ισχύ κατά την έκδοση της Κοινοτικής
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Zaneril 10 mg/10 mg επικαλυμμένα με λεπτό υμένιο δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε επικαλυμμένο με λεπτό υμένιο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Zaneril 10 mg/10 mg επικαλυμμένα με λεπτό υμένιο δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε επικαλυμμένο με λεπτό υμένιο
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
ΠΑΡΑΡΤΗΜΑ III Τροποποιήσεις των σχετικών παραγράφων της περίληψης χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης
 ΠΑΡΑΡΤΗΜΑ III Τροποποιήσεις των σχετικών παραγράφων της περίληψης χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης 36/44 A. Περίληψη Χαρακτηριστικών του Προϊόντος 4.1 Θεραπευτικές ενδείξεις
ΠΑΡΑΡΤΗΜΑ III Τροποποιήσεις των σχετικών παραγράφων της περίληψης χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης 36/44 A. Περίληψη Χαρακτηριστικών του Προϊόντος 4.1 Θεραπευτικές ενδείξεις
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ HIDRASEC ΓΙΑ ΒΡΕΦΗ 10 mg κοκκία για πόσιμο εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει 10 mg
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ HIDRASEC ΓΙΑ ΒΡΕΦΗ 10 mg κοκκία για πόσιμο εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει 10 mg
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ (SPC) 2. ΠΟΙΟΤΙΚΗ &ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ (SPC) 1. ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ALDACTONE 2. ΠΟΙΟΤΙΚΗ &ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά Κάθε δισκίο περιέχει Spironolactone 25 mg ή 100 mg
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ (SPC) 1. ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ALDACTONE 2. ΠΟΙΟΤΙΚΗ &ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά Κάθε δισκίο περιέχει Spironolactone 25 mg ή 100 mg
LOROTENS (Losartan potassium)
 LOROTENS (Losartan potassium) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LOROTENS 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ To LOROTENS 50mg περιέχει 50mg losartan potassium. To LOROTENS
LOROTENS (Losartan potassium) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LOROTENS 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ To LOROTENS 50mg περιέχει 50mg losartan potassium. To LOROTENS
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 Depon â (Paracetamol) (Bristol Myers Squibb) ΑΝΑΛΓΗΤΙΚΟ -ΑΝTIΠΥΡΕΤIΚΟ ΜΟΡΦΕΣ ΕΝΗΛΙΚΩΝ ΔΙΣΚΙΑ ΑΠΛΑ, ΑΝΑΒΡΑΖΟΝΤΑ 500mg, ΑΝΑΒΡΑΖΟΝΤΑ 1000mg (MAXIMUΜ) ΚΑΙ ΥΠΟΘΕΤΑ ΔΡΑΣΗ: Το DEPON περιέχει σαν δραστική ουσία
Depon â (Paracetamol) (Bristol Myers Squibb) ΑΝΑΛΓΗΤΙΚΟ -ΑΝTIΠΥΡΕΤIΚΟ ΜΟΡΦΕΣ ΕΝΗΛΙΚΩΝ ΔΙΣΚΙΑ ΑΠΛΑ, ΑΝΑΒΡΑΖΟΝΤΑ 500mg, ΑΝΑΒΡΑΖΟΝΤΑ 1000mg (MAXIMUΜ) ΚΑΙ ΥΠΟΘΕΤΑ ΔΡΑΣΗ: Το DEPON περιέχει σαν δραστική ουσία
Amlopen (Amlodipine) Δ
 Amlopen (Amlodipine) 5500567Δ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Amlopen 1.2 Σύνθεση Δραστική ουσία: Amlodipine (ως besylate). Έκδοχα: Microcrystalline cellulose, magnesium stearate,
Amlopen (Amlodipine) 5500567Δ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Amlopen 1.2 Σύνθεση Δραστική ουσία: Amlodipine (ως besylate). Έκδοχα: Microcrystalline cellulose, magnesium stearate,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Panadol 120 mg/5 ml πόσιμο εναιώρημα Παρακεταμόλη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Panadol 120 mg/5 ml πόσιμο εναιώρημα Παρακεταμόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Panadol 120 mg/5 ml πόσιμο εναιώρημα Παρακεταμόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,
ΠΑΡΑΡΤΗΜΑ ΙII ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣHΣ
 ΠΑΡΑΡΤΗΜΑ ΙII ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣHΣ 14 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 15 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Vascace Plus και οι
ΠΑΡΑΡΤΗΜΑ ΙII ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣHΣ 14 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 15 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Vascace Plus και οι
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 1. ΟΝΟΜΑΣΙΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 1. ΟΝΟΜΑΣΙΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ΑΜΙΝΟΦΥΛΛΙΝΗ ΕΝΕΣΙΜΟ ΔΙΑΛΥΜΑ / DEMO 250mg/10ml AMP 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ XATRAL OD 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο Χatral OD παρατεταμένης αποδέσμευσης περιέχει 10 mg υδροχλωρικής
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ XATRAL OD 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο Χatral OD παρατεταμένης αποδέσμευσης περιέχει 10 mg υδροχλωρικής
Γενική περίληψη της επιστημονικής αξιολόγησης του Kytril και των λοιπών εμπορικών ονομασιών του (βλ. Παράρτημα Ι)
 ΠΑΡΑΡΤΗΜΑ ΙΙ ΕΠΙΣΤΗΜΟΝΙΚΑ ΠΟΡΙΣΜΑΤΑ ΚΑΙ ΛΟΓΟΙ ΓΙΑ ΤΗΝ ΤΡΟΠΟΠΟΙΗΣΗ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΤΗΣ ΕΠΙΣΗΜΑΝΣΗΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΠΟΥ ΠΑΡΟΥΣΙΑΣΤΗΚΑΝ ΑΠΟ ΤΟΝ ΕΥΡΩΠΑΪΚΟ ΟΡΓΑΝΙΣΜΟ
ΠΑΡΑΡΤΗΜΑ ΙΙ ΕΠΙΣΤΗΜΟΝΙΚΑ ΠΟΡΙΣΜΑΤΑ ΚΑΙ ΛΟΓΟΙ ΓΙΑ ΤΗΝ ΤΡΟΠΟΠΟΙΗΣΗ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΤΗΣ ΕΠΙΣΗΜΑΝΣΗΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΠΟΥ ΠΑΡΟΥΣΙΑΣΤΗΚΑΝ ΑΠΟ ΤΟΝ ΕΥΡΩΠΑΪΚΟ ΟΡΓΑΝΙΣΜΟ
1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ:
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 4g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει: Macrogol
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TANILAS 4g, σκόνη για πόσιμο διάλυμα σε φακελλίσκο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ: Κάθε φακελλίσκος περιέχει: Macrogol
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, Thursday, 20 December :49 -
 Ζιρτέκ (Ζirtek) Cetirizine Dihydrochloride Δισκία επικαλυμένα με λεπτό υμένιο ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΠΑΤΟ ΧΡΗΣΤΗ 1. Προσδιορισμός φαρμακευτικού προϊόντος 1.1 Εμπορική ονομασία φαρμάκου: ΖΙΡΤΕΚ 1.2 Σύνθεση Δραστική
Ζιρτέκ (Ζirtek) Cetirizine Dihydrochloride Δισκία επικαλυμένα με λεπτό υμένιο ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΠΑΤΟ ΧΡΗΣΤΗ 1. Προσδιορισμός φαρμακευτικού προϊόντος 1.1 Εμπορική ονομασία φαρμάκου: ΖΙΡΤΕΚ 1.2 Σύνθεση Δραστική
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 ACCUPRON Δισκία επικαλυμμένα με λεπτό υμένιο 5, 20 ή 40 mg/tab. Υδροχλωρική κιναπρίλη. 1.2 Σύνθεση : Δραστική ουσία : Quinapril Hydrochloride (υδροχλωρική κιναπρίλη) Εκδοχα
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 ACCUPRON Δισκία επικαλυμμένα με λεπτό υμένιο 5, 20 ή 40 mg/tab. Υδροχλωρική κιναπρίλη. 1.2 Σύνθεση : Δραστική ουσία : Quinapril Hydrochloride (υδροχλωρική κιναπρίλη) Εκδοχα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:100000 ARTICAINE HYDROCHLORIDE & ADRENALINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:100000 ARTICAINE HYDROCHLORIDE & ADRENALINE
Trileptal Oxcarbazepine (οξκαρβαζεπίνη) Αντιεπιληπτικό ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ. Trileptal δισκία των 300 mg και 600 mg. Oxcarbazepine (Οξκαρβαζεπίνη).
 Oxcarbazepine (οξκαρβαζεπίνη) Αντιεπιληπτικό ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ δισκία των 300 mg και 600 mg. Oxcarbazepine (Οξκαρβαζεπίνη). ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστική ουσία: 10,11 - Dihydro-10-οχο-5Η-dibenz
Oxcarbazepine (οξκαρβαζεπίνη) Αντιεπιληπτικό ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ δισκία των 300 mg και 600 mg. Oxcarbazepine (Οξκαρβαζεπίνη). ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστική ουσία: 10,11 - Dihydro-10-οχο-5Η-dibenz
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS, 500 mg / 400 IU Μασώμενα Δισκία 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστικές ουσίες Aσβέστιο..500 mg που αντιστοιχεί
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ IDEOS, 500 mg / 400 IU Μασώμενα Δισκία 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Δραστικές ουσίες Aσβέστιο..500 mg που αντιστοιχεί
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. Σπειρονολακτόνη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1. Ονομασία: 1.2. Σύνθεση: ALDACTONE Επικαλυμμένα με λεπτό υμένιο δισκία 25 mg/tab & 100 mg/tab Σπειρονολακτόνη Δραστική ουσία: Σπειρονολακτόνη
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1. Ονομασία: 1.2. Σύνθεση: ALDACTONE Επικαλυμμένα με λεπτό υμένιο δισκία 25 mg/tab & 100 mg/tab Σπειρονολακτόνη Δραστική ουσία: Σπειρονολακτόνη
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DUSPATALIN 200mg/cap καψάκιο παρατεταμένης αποδέσμευσης, σκληρό 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε σκληρό καψάκιο παρατεταμένης
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DUSPATALIN 200mg/cap καψάκιο παρατεταμένης αποδέσμευσης, σκληρό 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε σκληρό καψάκιο παρατεταμένης
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 Νurofen Μαλακές κάψουλες - Liquid Soft Capsules ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ TO ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ 1.1 Ονομασία Nurofen Capsules. Μαλακή κάψουλα 200 mg / Cap Iβουπροφαίνη 1.2 Σύνθεση
Νurofen Μαλακές κάψουλες - Liquid Soft Capsules ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ TO ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ 1.1 Ονομασία Nurofen Capsules. Μαλακή κάψουλα 200 mg / Cap Iβουπροφαίνη 1.2 Σύνθεση
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ 1.1 CARDURA Δισκία 2 & 4 mg/τab 1.2 Σύνθεση Δραστική ουσία: Doxazosin mesylate Έκδοχα: Άμυλο καρβοξυμεθυλιωμένο νατριούχο, κυτταρίνη μικροκρυσταλλική, λακτόζη,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ 1.1 CARDURA Δισκία 2 & 4 mg/τab 1.2 Σύνθεση Δραστική ουσία: Doxazosin mesylate Έκδοχα: Άμυλο καρβοξυμεθυλιωμένο νατριούχο, κυτταρίνη μικροκρυσταλλική, λακτόζη,
Κάθε επικαλυμένο με λεπτό υμένιο δισκίο περιέχει 5 mg levocetirizine dihydrochloride.
 Xozal 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Xozal 5 mg επικαλυμένα με λεπτό υμένιο δισκία 1.2 Σύνθεση Δραστική ουσία: Ievocetiiizine dihydrochloride Έκδοχα: microcrystalline cellulose,
Xozal 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία Xozal 5 mg επικαλυμένα με λεπτό υμένιο δισκία 1.2 Σύνθεση Δραστική ουσία: Ievocetiiizine dihydrochloride Έκδοχα: microcrystalline cellulose,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Cetirizine Dihydrochloride
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1/5 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1/5 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
Κανένα για αυτήν την παρουσίαση. Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini,
 Κανένα για αυτήν την παρουσίαση Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini, 2 Κυκλοσπορίνη-θεραπευτικές ενδείξεις 3 Θεραπεία σοβαρών μορφών
Κανένα για αυτήν την παρουσίαση Εκπαιδευτικές-ερευνητικές-συμβουλευτικές επιχορηγήσεις την τελευταία διετία: Abbvie,Novartis, MSD, Angelini, 2 Κυκλοσπορίνη-θεραπευτικές ενδείξεις 3 Θεραπεία σοβαρών μορφών
Παράρτημα I. Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας
 Παράρτημα I Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας 1 Επιστημονικά πορίσματα Λαμβάνοντας υπόψη την έκθεση αξιολόγησης της PRAC σχετικά με την PSUR για τη rivastigmine,
Παράρτημα I Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας 1 Επιστημονικά πορίσματα Λαμβάνοντας υπόψη την έκθεση αξιολόγησης της PRAC σχετικά με την PSUR για τη rivastigmine,
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. Ονομασία του φαρμακευτικού προϊόντος QUINAPRIL/GENERICS 5 mg Επικαλυμμένα με λεπτό υμένιο δισκία QUINAPRIL/GENERICS 20 mg Επικαλυμμένα με λεπτό υμένιο δισκία
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. Ονομασία του φαρμακευτικού προϊόντος QUINAPRIL/GENERICS 5 mg Επικαλυμμένα με λεπτό υμένιο δισκία QUINAPRIL/GENERICS 20 mg Επικαλυμμένα με λεπτό υμένιο δισκία
O S T E O V I L E (Alfacalcidol)
 O S T E O V I L E (Alfacalcidol) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OSTEOVILE 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ OSTEOVILE 0,25 mcg/cap: Περιέχει 0,25 mcg/cap alfacalcidol
O S T E O V I L E (Alfacalcidol) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OSTEOVILE 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ OSTEOVILE 0,25 mcg/cap: Περιέχει 0,25 mcg/cap alfacalcidol
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: LACIPIL 1.2 Σύνθεση: Δραστική ουσία: Lacidipine (λασιδιπίνη) Έκδοχα: Lactose monohydrate, lactose spray-dried, polividone,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: LACIPIL 1.2 Σύνθεση: Δραστική ουσία: Lacidipine (λασιδιπίνη) Έκδοχα: Lactose monohydrate, lactose spray-dried, polividone,
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣIΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤIΚΟΥ ΠΡΟΪΟΝΤΟΣ DICETEL, δισκία επικαλυμμένα με λεπτό υμένιο 50 MG DICETEL, δισκία επικαλυμμένα με λεπτό υμένιο 100 MG 2. ΠΟIΟΤIΚΗ ΚΑI
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣIΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤIΚΟΥ ΠΡΟΪΟΝΤΟΣ DICETEL, δισκία επικαλυμμένα με λεπτό υμένιο 50 MG DICETEL, δισκία επικαλυμμένα με λεπτό υμένιο 100 MG 2. ΠΟIΟΤIΚΗ ΚΑI
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή INOTREX 250mg/20ml διάλυμα για ενδοφλέβια χορήγηση Υδροχλωρική δοβουταμίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή INOTREX 250mg/20ml διάλυμα για ενδοφλέβια χορήγηση Υδροχλωρική δοβουταμίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lacipil 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 4mg ή 6mg lacidipine. 3. ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ Επικαλυμμένο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lacipil 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 4mg ή 6mg lacidipine. 3. ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ Επικαλυμμένο
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Riprazo 150 mg επικαλυμμένα με λεπτό υμένιο δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε επικαλυμμένο με
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Riprazo 150 mg επικαλυμμένα με λεπτό υμένιο δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε επικαλυμμένο με
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AIR SALONPAS 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 100 ml του αερολύµατος για τοπική χρήση περιέχουν: Methyl salicylate 1.75g
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AIR SALONPAS 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 100 ml του αερολύµατος για τοπική χρήση περιέχουν: Methyl salicylate 1.75g
Έκδοχα: microcrystalline cellulose, lactose monohydrate, povidone Κ 24-27, magnesium stearate.
 BRIVIR 125 mg Δισκία [Brivudin] Σύνθεση : Δαστικές ουσίες : Brivudin Έκδοχα: microcrystalline cellulose, lactose monohydrate, povidone Κ 24-27, magnesium stearate. Φαρμακοτεχνική μορφή : Δισκία. Περιεκτικότητα
BRIVIR 125 mg Δισκία [Brivudin] Σύνθεση : Δαστικές ουσίες : Brivudin Έκδοχα: microcrystalline cellulose, lactose monohydrate, povidone Κ 24-27, magnesium stearate. Φαρμακοτεχνική μορφή : Δισκία. Περιεκτικότητα
Παράρτημα ΙII. Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών
 Παράρτημα ΙII Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών Σημείωση: Όπου εφαρμόζεται, η περίληψη των χαρακτηριστικών του προϊόντος και
Παράρτημα ΙII Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών Σημείωση: Όπου εφαρμόζεται, η περίληψη των χαρακτηριστικών του προϊόντος και
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
AΣΘΜΑ ΚΑΙ ΕΓΚΥΜΟΣΥΝΗ ΑΛΛΗΛΕΠΙΔΡΑΣΕΙΣ ΑΣΘΜΑΤΟΣ & ΚΥΗΣΗΣ
 AΣΘΜΑ ΚΑΙ ΕΓΚΥΜΟΣΥΝΗ Το άσθμα είναι ένα από τις πιο συχνές νόσους που περιπλέκει την εγκυμοσύνη. Πρόσφατες μελέτες δείχνουν πως περίπου 8-10% των εγκύων έχουν άσθμα και μπορεί να επηρεάσει την εγκυμοσύνη
AΣΘΜΑ ΚΑΙ ΕΓΚΥΜΟΣΥΝΗ Το άσθμα είναι ένα από τις πιο συχνές νόσους που περιπλέκει την εγκυμοσύνη. Πρόσφατες μελέτες δείχνουν πως περίπου 8-10% των εγκύων έχουν άσθμα και μπορεί να επηρεάσει την εγκυμοσύνη
ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ. Λειτουργία των νεφρών. Συμπτώματα της χρόνιας νεφρικής ανεπάρκειας
 ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ Η χρόνια νεφρική ανεπάρκεια είναι η προοδευτική, μη αναστρέψιμη μείωση της νεφρικής λειτουργίας, η οποία προκαλείται από βλάβη του νεφρού ποικίλης αιτιολογίας. Η χρόνια νεφρική ανεπάρκεια
ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ Η χρόνια νεφρική ανεπάρκεια είναι η προοδευτική, μη αναστρέψιμη μείωση της νεφρικής λειτουργίας, η οποία προκαλείται από βλάβη του νεφρού ποικίλης αιτιολογίας. Η χρόνια νεφρική ανεπάρκεια
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Micardis 20 mg, δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 20 mg telmisartan. Έκδοχα με
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Micardis 20 mg, δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 20 mg telmisartan. Έκδοχα με
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. Micardis 40 mg, δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ. Κάθε δισκίο περιέχει 40 mg telmisartan
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Micardis 40 mg, δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 40 mg telmisartan Έκδοχα με γνωστή επίδραση: Κάθε δισκίο περιέχει 169 mg σορβιτόλη (E420).
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Micardis 40 mg, δισκία 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 40 mg telmisartan Έκδοχα με γνωστή επίδραση: Κάθε δισκίο περιέχει 169 mg σορβιτόλη (E420).
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 ACCUPRON Δισκία επικαλυμμένα με λεπτό υμένιο 5, 20 ή 40 mg/tab. Υδροχλωρική κιναπρίλη. 1.2 Σύνθεση: Δραστική ουσία: Quinapril Hydrochloride (υδροχλωρική κιναπρίλη) Εκδοχα:
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 ACCUPRON Δισκία επικαλυμμένα με λεπτό υμένιο 5, 20 ή 40 mg/tab. Υδροχλωρική κιναπρίλη. 1.2 Σύνθεση: Δραστική ουσία: Quinapril Hydrochloride (υδροχλωρική κιναπρίλη) Εκδοχα:
Κηφισού 132, 121 31 Αθήνα. Τηλ.: 210-5702199 FAX: 210-5728215. Ισλανδία Β. KLEVA ΑΦΒΕΕ Λεωφ. Πάρνηθος 189 13675 Αχαρναί, Αττική Τηλ.
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ QUIMEA Quinapril + Hydrochlorothiazide Σύνθεση : Δραστικά Συστατικά : Quinapril (ως Quinapril hydrochloride) και Hydrochlorothiazide Έκδοχα : Magnesium carbonate heavy, Calcium
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ QUIMEA Quinapril + Hydrochlorothiazide Σύνθεση : Δραστικά Συστατικά : Quinapril (ως Quinapril hydrochloride) και Hydrochlorothiazide Έκδοχα : Magnesium carbonate heavy, Calcium
