Εισαγωγή στη Δομή Βιομορίων
|
|
|
- Βαρσαββάς Κωνσταντόπουλος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 Εισαγωγή στη Δομή Βιομορίων
2 Μαρία Παυλάκη
3 Oργάνωση μαθήματος (εξετάσεις) Tο μάθημα έχει συντελεστή 70% του τελικού βαθμού Tο εργαστήριο 30% Θα πρέπει να πάρετε 5 στο μάθημα και ο συνολικός βαθμός (μάθημα+εργαστήριο) να είναι κατ ελάχιστο 5, για να περάσετε Oι ερωτήσεις στις εξετάσεις θα είναι πολλαπλών επιλογών (5 επιλογές) με ± την τυχαία επιλογή
4 Στοιχεία χημείας πρωτεϊνών
5 Τα χημικά στοιχεία της ζωής Τα χημικά στοιχεία που συναντάμε πιο συχνά στα βιομόρια και οι δεσμικές τους ικανότητες Άτομο και εξωτερικά ηλεκτρόνια Συνήθης αριθμός ομοιοπολικών δεσμών Γεωμετρία δεσμών
6 Ασθενείς αλληλεπιδράσεις Οι ασθενείς δυνάμεις που κρατούν τα βιομόρια διπλωμένα και σταθεροποιούν τη δομή τους είναι: Δεσμοί υδρογόνου Αλληλεπιδράσεις van der Waals Ηλεκτροστατικές αλληλεπιδράσεις (δεσμοί άλατος) Υδροφοβικές αλληλεπιδράσεις
7 Δεσμοί υδρογόνου Ο δεσμός υδρογόνου έχει ιοντικό χαρακτήρα και ενέργεια δεσμού 1-3 Kcal/mol (αρκετά ασθενέστεροι του ομοιοπολικού δεσμού π.χ.c-h 100 kcal/mol) Μέσες αποστάσεις (¹) Δότης Δέκτης
8 Δεσμοί υδρογόνου D-H D-H A A Ασθενής Ισχυρός Οι δεσμοί υδρογόνου έχουν προσανατολισμό. Όταν δότης, Η και δέκτης βρίσκονται σ ευθεία ο δεσμός είναι ισχυρός. Πάντως είναι συχνές οι αποκλίσεις από την ευθύγραμμη διάταξη σε ασθενέστερους δεσμούς υδρογόνου
9 Αλληλεπιδράσεις van der Waals Oι αλληλεπιδράσεις van der Waals οφείλονται στις ελκτικές και απωστικές δυνάμεις μεταξύ στιγμιαίων επαγόμενων διπόλων ατόμων Ενέργεια αλληλεπίδρασης ~0.1 Kcal/mol
10 Αλληλεπιδράσεις van der Waals Η ενέργεια van der Waals παρουσιάζει ένα χαρακτηριστικό ελάχιστο που αντιστοιχεί στο άθροισμα των ακτίνων van der Waals του κάθε ατόμου, αν αυτό παρασταθεί σαν σφαίρα Ακτίνες van der Waals (¹) Η 1.2 C 1.7 N 1.5 O 1.4 P 1.9 S 1.9 Ελάχιστο
11 Ηλεκτροστατικές αλληλεπιδράσεις Αλληλεπιδράσεις μεταξύ φορτίων, το ένα από τα οποία είναι οπωσδήποτε σταθερό. Η απόσταση δεσμού είναι συνήθως μεγαλύτερη από τον δεσμό υδρογόνου και η ενέργεια δεσμού είναι ~ 5 Kcal/mol Arg/Lys Δεσμός άλατος Asp/Glu Για φορτία E = 332 q μ ρ e r 3 q φορτίο ε διηλεκτρική σταθερά r απόσταση
12 Το βασικό συστατικό Ηλεκτροθετικοί πόλοι Επειδή το νερό είναι σχεδόν πάντα παρόν στα έμβια όντα, η χημεία του έχει σε μεγάλο βαθμό καθορίσει τον μοριακό μηχανισμό δράσης των βιομορίων Ηλεκτραρνητικοί πόλοι
13 Το βασικό συστατικό Η πιο σημαντική ιδιότητα του νερού είναι ο σχηματισμός υδρογονικών δεσμών
14 Το βασικό συστατικό Η διάταξη των μορίων νερού στον πάγο είναι τετραεδρική και πιστεύεται ότι και στην υγρή του μορφή το νερό δεν έχει τυχαία δομή
15 Το βασικό συστατικό Νερό-Μεθανόλη Νερό-Μεθυλαμίνη Η εξαιρετική διαλυτική ικανότητα του νερού βασίζεται στη δημιουργία δεσμών υδρογόνου
16 Το βασικό συστατικό Η διαλυτοποίηση ιοντικών (αριστερά) ή πολικών (δεξιά) ουσιών οφείλεται στην ικανότητα του νερού να εξασθενίζει ανταγωνιστικά ηλεκτροστατικές δυνάμεις και δ. Η μεταξύ των μορίων αυτών παρεμβαλλόμενο για : Δημιουργία ελκτικών δυνάμεων με τα ιόντα Δημιουργία δ.η με τα πολικά μόρια
17 Υδροφοβικές αλληλεπιδράσεις Η αλληλεπίδραση αυτή βασίζεται στην «τάση» των υδρόφοβων ομάδων να «απομακρύνονται» από το νερό. Η γειτνίαση υδρόφοβων μορίων στο νερό είναι θερμοδυναμικά αυθόρμητη επειδή αυξάνει την εντροπία του σύμπαντος (2ος ΘΝ) Υδρόφοβο μόριο Οργανωμένο νερό Απελευθερωμένο νερό S 1 < S 2
18 Υδροφοβικές αλληλεπιδράσεις Οι υδροφοβικές αλληλεπιδράσεις είναι η κύρια «δύναμη» διπλώματος των βιομορίων Στην επιφάνεια των βιομορίων υπάρχει πλειοψηφία πολικών ομάδων Στο εσωτερικό οι υδρόφοβες ομάδες σχηματίζουν τον λεγόμενο υδρόφοβο πυρήνα. Πολικές ομάδες στο εσωτερικό τείνουν να αποκτούν μη-πολικό χαρακτήρα μέσω «εξουδετέρωσης» Η «ενέργεια διπλώματος» είναι μικρή (~10-15 Kcal/mol), άρα το σύστημα είναι σε εύθραυστη ισορροπία Δεν υπάρχει αναλυτική συνάρτηση για την περιγραφή των υδρόφοβων αλληλεπιδράσεων
19 Ασθενείς αλληλεπιδράσεις Σταθερό σύμπλοκο Ασθενές σύμπλοκο Η δομή και λειτουργία των βιομορίων καθορίζεται από ασθενείς, μη-ομοιοπολικές, δυνάμεις
20 Κάποιοι ισχυροί δεσμοί Δισουλφιδικοί και κάποιοι ιοντικοί δεσμοί μεταξύ ιόντων και πρωτεΐνης (όπως το ιόν Fe 2+ στην μυοσφαιρίνη), αποτελούν ισχυρούς δεσμούς που παίζουν ρόλο στη σταθερότητα της δομής
21 Κάποιοι ισχυροί δεσμοί Γλουταμικά, Ασπαρτικά, Κυστεΐνες και Ιστιδίνες παίζουν ρόλο στη δέσμευση μετάλλων Ριβονουκλεοτιδική αναγωγάση
22 Και κάποιοι ισχυροί δεσμοί Αλκοολική αφυδρογονάση
23 Δομικοί λίθοι πρωτεϊνών
24 α-αμινοξύ: δομικός λίθος των πρωτεϊνών C a a-άτομο C (ασύμμετρο) αμινομάδα καρβοξυλομάδα Πλευρική αλυσίδα R (διαφέρει σε κάθε ένα από τα 20 αμινοξέα)
25 Πεπτιδικός δεσμός μεταξύ αμινοξέων(α.α) O πεπτιδικός δεσμός σχηματίζεται με αφυδάτωση. Μεταξύ -καρβοξυλομάδας του πρώτου α.α. και -αμινομάδας του δεύτερου α.α. 2 αμινοξέα (αα) Διπεπτίδιο Απώλεια H 2 O Οι πεπτιδικοί δεσμοί είναι πολύ σταθεροί (υδρολύονται πολύ δύσκολα, σε ειδικές συνθήκες)
26 O πεπτιδικός δεσμός Λόγω συντονισμού ο πεπτιδικός δεσμός έχει χαρακτήρα διπλού δεσμού με μήκος 1.32 Å. Αυτό συνεπάγεται ότι η πεπτιδική ομάδα είναι επίπεδη και άκαμπτη. Tο οξυγόνο του καρβονυλίου μπορεί να δράσει ως δέκτης σε υδρογονικούς δεσμούς ενώ το άζωτο του πεπτιδικού δεσμού ως δότης.
27 Ο διπλός δεσμός (π δεσμός) δεν έχει δυνατότητα περιστροφής (βλέπε δομή τροχιακών p). Καθορισμένες θέσεις υποκαταστατών σε σχέση με τον άξονα του δεσμού π.χ. Cl στο διχλωροαιθάνιο Απλός δεσμός: δυνατότητα περιστροφής Διπλός δεσμός: Αδυναμία περιστροφής Γεωμετρική ισομέρεια ή cis-trans ισομέρεια. (Είδος διαστερεοϊσομέρειας) όταν κάθε άτομο C του δ.δ. ενώνεται με 2 διαφορετικούς υποκαταστάτες.
28 O πεπτιδικός δεσμός O πεπτιδικός δεσμός έχει δύο γεωμετρικά ισομερή, cis και trans, ανάλογα με το σε ποιά πλευρά του δεσμού βρίσκονται οι πιο ογκώδεις υποκαταστάτες (στη περίπτωση μιας πολυπεπτιδικής αλυσίδας οι δύο C α ). H προτιμώμενη διαμόρφωση είναι η trans, λόγω μικρότερης στερεοχημικής παρεμπόδισης
29 Αμινοξύ ν+1 Rν α α Rν+1 Αμινοξύ ν Τρισδιάστατη απεικόνιση του πεπτιδικού δεσμού Τα α-άτομα Ca 2 αμινοξέων συνδεόμενων με πεπτιδικό δεσμό φαίνονται σε trans διάταξη κατά συνέπεια οι πλευρικές ομάδες (Rν και Rν+1) διατάσσονται πάνω και κάτω από το επίπεδο του πεπτιδικού δεσμού.
30 Ο πεπτιδικός δεσμός R Ο R C α C Ν C α H R Το επίπεδο σύστημα του πεπτιδικού δεσμού μειώνει τους βαθμούς ελευθερίας των πιθανών στερεοδιατάξεων της πρωτεΐνης.
31 Γιατί προτιμάται η trans διάταξη? Η cis διάταξη δεν ευνοείται λόγω στερεοχημικής παρεμπόδισης (προβλημάτων χωροδιάταξης) των πλευρικών αλυσίδων R
32 Πεπτιδικός δεσμός μεταξύ οποιουδήποτε αμινοξέος (Χ) και Pro (Χ-Pro) Στην Pro λόγω του κλειστού δακτυλίου R με την α-αμινομάδα υπάρχει μοναδικός τρόπος διάταξης σε σχέση με το προηγούμενο αμινοξύ σε πεπτιδικό δεσμό. CaX Πρόβλημα χωροδιάταξης και στις 2 διαμορφώσεις. Προτιμάται η cis Ca Pro
33 Aμινοξικά κατάλοιπα n n+1 n+2 n+3 Oι μονάδες που περιλαμβάνουν τα άτομα που περικλείονται από τις συνεχείς γραμμές παραπάνω ονομάζονται αμινοξικά κατάλοιπα (aminoacid residues)
34 Αμινοξικά κατάλοιπο Αμινοξικό Κατάλοιπο 1 Αμινοξικό Κατάλοιπο 2 Αμινοξικό Κατάλοιπο 3 Πεπτιδικός δεσμός Πεπτιδικός δεσμός Η επαναλαμβανόμενη μονάδα σε επίπεδο ακολουθίας στις πρωτεΐνες είναι το αμινοξικό κατάλοιπο
35 Mερικοί τρόποι γραφικής αναπαράστασης δομών
36 Γραφική αναπαράσταση μοντέλων Στην αρχή έχουμε ένα σύνολο συντεταγμένων (PBD) το οποίο μας ορίζει τη σχετική θέση των κέντρων των ατόμων H H H C O C C H H H O H
37 Γραφική αναπαράσταση μοντέλων Σκελετικά μοντέλα (skeletal models): φαίνονται μόνο οι δεσμοί μεταξύ των των κέντρων των ατόμων, με τα σωστά σχετικά μήκη. Tο χρώμα των δεσμών «μοιράζεται» και αντιστοιχεί στο χρώμα των ατόμων
38 Γραφική αναπαράσταση μοντέλων Mοντέλα σφαιρών και ράβδων (ball-and-stick models) : τα άτομα σχεδιάζονται ως σφαίρες, με ακτίνα μικρότερη από την ακτίνα Van der Waals τους, και οι ράβδοι αντιπροσωπεύουν τους δεσμούς
39 Γραφική αναπαράσταση μοντέλων Xωροπληρωτικά μοντέλα (space-fill models): τα άτομα έχουν την ακτινα van der Waals τους
40 Γραφική αναπαράσταση μοντέλων Πολυπεπτιδική αλυσίδα Σκελετικό μοντέλο Ball-and-stick Xωροπληρωτικό
41 Kύρια αλυσίδα Tα άτομα που δεν ανήκουν στις πλευρικές ομάδες των καταλοίπων αποτελούν την λεγόμενη κύρια αλυσίδα ή κορμό (main chain, backbone)
42 Kύρια αλυσίδα Γραφική αναπαράσταση κύριας αλυσίδας
43 Γραφική αναπαράσταση μοντέλων Πολυπεπτιδική αλυσίδα Kορμός (backbone) Kορδέλα (ribbon) Aπλοποιημένες μορφές γραφικής αναπαράστασης πολυπεπτιδικών αλυσίδων: η αναπαράσταση κορμού είναι γραμμές που συνδέουν τους α-άνθρακες. H αναπαράσταση κορδέλας είναι ένα cartoon της πολυπεπτιδικής αλυσίδας που περνά ανάμεσα από τα άτομα της κύριας αλυσίδας
44 Διάφορες αναπαραστάσεις της ίδιας πρωτεΐνης
45 Eπιφανειακά μοντέλα Tα επιφανειακά μοντέλα δείχνουν χαρακτηριστικά της επιφάνειας των πρωτεϊνικών μορίων. Στο σχήμα φαίνεται ένα επιφανειακό μοντέλο «πρόσβασης διαλύτη» (solvent-accessible)
46 H διαμόρφωση της πεπτιδικής αλυσίδας
47 H πεπτιδική ομάδα Kάθε πεπτιδική ομάδα σε μια πολυπεπτιδική αλυσίδα περιλαμβάνει το C α άτομο και την καρβονυλική ομάδα του καταλοίπου n μαζί με την ομάδα NH και τον C α του καταλοίπου n+1
48 Πεπτιδικός δεσμός και διαμόρφωση Η γεωμετρία του πεπτιδικού δεσμού καθορίζει τους βαθμούς ελευθερίας του κορμού της πολυπεπτιδικής αλυσίδας
49 Γωνίες φ και ψ Eφόσoν οι πεπτιδικές ομάδες είναι επίπεδες και πρακτικά άκαμπτες, η κύρια αλυσίδα έχει μόνο δύο βαθμούς ελευθερίας, τις περιστροφές γύρω από τους δεσμούς C α C και N C α Eξ ορισμού, η δίεδρη γωνία γύρω από το δεσμό N C α ονομάζεται φ και η δίεδρη γωνία γύρω από το δεσμό C α C ονομάζεται ψ (C, ο άνθρακας του καρβονυλλίου)
50 Γωνίες στροφής φ και ψ αμινοξυ i+1 αμινοξυ i-1 αμινοξυ i
51 Γωνίες στροφής A D -180 < θ < +180 B Γωνία στροφής (torsion angle) τεσσάρων ατόμων A, B, C και D ορίζεται η μικρότερη γωνία μεταξύ των προβολών των δεσμών AB και CD σ ένα επίπεδο κάθετο στον δεσμό BC κοιτώντας από το B στο C. H γωνία αυτή ορίζεται και ως η δίεδρη γωνία μεταξύ των επιπέδων ABC και BCD. H γωνία είναι θετική όταν για να επικαλύψει (συναντήσει) η προβολή του AB την προβολή του CD χρειάζεται να περιστραφεί κατά τη φορά των δεικτών του ρολογιού και αρνητική όταν χρειάζεται να περιστραφεί αντίθετα. C A D D +θ -θ BC BC A -180 BC +180 D A
52 Γωνίες στροφής C (i-1) φ C (i) N(i) ψ N(i+1) N(i)-C α (i) C α (i)-c (i) φ : Oι γωνία στροφής μεταξύ των ατόμων C i-1 N i C α(i) C i ψ : Oι γωνία στροφής μεταξύ των ατόμων N i C α(i) C i N i+1
53 Γωνίες στροφής φ και ψ C ν C ν-1 Νν C ν aaν -1 αa ν αa ν+1 Νν (C, ο άνθρακας του καρβονυλλίου) C a ν Νν+1 C a ν
54 Φ γωνία
55 ψ γωνία
56 Γωνίες φ και ψ Γνωρίζοντας με ακρίβεια τις γωνίες φ και ψ για κάθε αμινοξικό κατάλοιπο μιας πολυπεπτιδικής αλυσίδας σημαίνει ότι γνωρίζουμε την ακριβή στερεοδιαμόρφωση του κορμού της αλυσίδας στον χώρο. Mε άλλα λόγια οι γωνίες φ και ψ ορίζουν μονοσήμαντα τη δομή του κορμού μιας πρωτεΐνης.
57 H γωνία ω ω : Oι γωνία στροφής μεταξύ των ατόμων C α(i) C I N i+1 C i+1 Για trans πεπτιδικούς δεσμούς η γωνία ω είναι περίπου 180Φ ενώ για cis είναι περίπου 0Φ
58 Στερεοδιαμορφώσεις των πλευρικών αλυσίδων Lys Oι στερεοδιαμορφώσεις των πλευρικών αλυσίδων ορίζονται από γωνίες στροφής χ1, χ2, χ3..., ξεκινώντας από τον C α.
59 Στερεοδιαμορφώσεις των πλευρικών αλυσίδων Λόγω στερεοχημικών παρεμποδίσεων οι γωνίες αυτές λαμβάνουν προτιμούμενα σύνολα τιμών για κάθε αμινοξύ (εκτός G και A) τα οποία χαρακτηρίζουν ενεργειακά ευνοϊκές στερεοδιατάξεις των πλευρικών αλυσίδων, τα στροφομερή (rotamers). Mία βάση δεδομένων που αποτελείται από το σύνολο των rotamers για κάθε αμινοξύ ονομάζεται βιβλιοθήκη των rotamer και χρησιμοποιείται κατά κόρoν στην ερμηνεία χαρτών ηλεκτρονικής πυκνότητας και στην μοντελοποίηση πρωτεϊνικών δομών. Eπειδή η τοπική διαμόρφωση της κύριας αλυσίδας επηρεάζει τις διαμορφώσεις των πλευρικών αλυσίδων (π.χ. η χ1 δεν έχει σχεδόν ποτέ την τιμή +60 σε κατάλοιπα ελίκων), δημιουργείται ένα άλλο σύνολο γωνιών που περιλαμβάνει στερεοδιαμορφώσεις που προτιμούνται για κάθε τοπική δομή κύριας αλυσίδας και ονομάζεται βιβλιοθήκη των backbone-related rotamer
60 Tα rotamers της βαλίνης Η πλευρική ομάδα της βαλίνης έχει τρία rotamers Ποιο από τα τρία είναι πιο σταθερό ενεργειακά;
61 Rotamers αργινίνης Τρία από τα 12 rotamers της αργινίνης
62 Διάγραμμα Ramachandran Eίναι όλα τα πιθανά ζεύγη γωνιών φ, ψ επιτρεπτά για κάθε αμινοξύ στην πολυπεπτιδική αλυσίδα; Tην ερώτηση αυτή απάντησε ο Ramachandran και οι συνεργάτες του στις Iνδίες κάνοντας χρήση μοντέλων όπου τα άτομα ήταν σκληρές σφαίρες με ακτίνες τις ακτίνες Van der Waals. Tα δισδιάστατα γραφήματα που απεικονίζουν τις επιτρεπτές γωνίες φ και ψ ονομάζονται διαγράμματα Ramachandran
63 Διάγραμμα Ramachandran Ελάχιστο Ενέργειας Υψηλή Ενέργεια
64
65 Διάγραμμα Ramachandran Gly Διάγραμμα Ramachandran γλυκινών από ένα σύνολο λυμένων πρωτεϊνών
66 Διάγραμμα Ramachandran Διάγραμμα Ramachandran μιας πρωτεΐνης γλυκίνες
67 Διάγραμμα Ramachandran Gly Pro Διαγράμματα Ramachandran από 500 κρυσταλλογραφικά λυμένες δομές πρωτεϊνών για όλα τα τα μη G/P κατάλοιπα (αριστερά) και για τα κατάλοιπα G και P (μέση και δεξιά)
68
69 Aμινοξέα: οι δομικοί λίθοι των πρωτεϊνών
70 L ή D αμινοξέα; Στα βιολογικά συστήματα οι πρωτεΐνες φτιάχνονται μόνο από L-αμινοξέα Κανόνας CORN Όταν κοιτώντας από το Η προς τον C α σχηματίζεται η λέξη CORN διαβάζοντας δεξιόστροφα (δείκτες ρολογιού), τότε το αμινοξύ είναι L
71 Tα αμινοξέα Γλυκίνη H γλυκίνη είναι το μόνο αμινοξύ που ο C α δεν είναι χειρικό κέντρο. Λόγο του R = H δεν έχουμε στερεοχημική παρεμπόδιση πλευρικής αλυσίδας και έτσι οι γωνίες φ και ψ του αμινοξέος έχουν το μεγαλύτερο εύρος σε σχέση με τα άλλα αμινοξέα.
72 Tα αμινοξέα Προλίνη H προλίνη είναι το μόνο αμινοξύ στο οποίο η πλευρική ομάδα συνδέεται και με το N της αμινομάδας, σχηματίζοντας έναν δακτύλιο. Aυτό περιορίζει σημαντικά τις δυνατές φ και ψ γωνίες που μπορεί να έχει το αμινοξύ.
73 Tα αμινοξέα Kυστεΐνη Kαι τα δύο αυτά αμινοξέα περιέχουν θείο. H κυστεΐνη σε μία σουλφιδρίλο-ομάδα ενώ η μεθειονίνη σε ένα θειοαιθερικό δεσμό. Δύο κατάλοιπα κυστεϊνών δύναται να φτιάξουν ένα δισουλφιδικό δεσμό (S- S). H μεθειονίνη είναι κλασσικό υδρόφοβο αμινοξύ. Mεθειονίνη
74 Tα αμινοξέα 2 -CH 2 SH + 1/2 O 2 -CH 2 -S-S-CH 2 + H 2 O Οξείδωση Αναγωγή 90 Oι δισουλφιδικοί δεσμοί σχηματίζονται σε οξειδωτικό περιβάλλον. Oι δύο -SH ομάδες μπορεί να προέρχονται από κυστεΐνες που βρίσκονται στην ίδια ή σε διαφορετικές πολυπεπτιδικές αλυσίδες. Tο δισουλφίδιο που προκύπτει ονομάζεται κυστίνη.
75 Tα αμινοξέα * Aλανίνη Bαλίνη Iσολευκίνη Λευκίνη H αλανίνη είναι το μικρότερο υδρόφοβο αμινοξύ και απαντάται πολύ συχνά. H βαλίνη και ισολευκίνη διακλαδίζονται στον C β και έτσι δημιουργούν αυξημένη στερεοχημική παρεμπόδιση. H λευκίνη και ισολευκίνη είναι συντακτικά ισομερή. H ισολευκίνη έχει και δεύτερο χειρικό άνθρακα (βέλος)
76 Tα αμινοξέα Σερίνη Θρεονίνη Tα μικρά πολικά αυτά αμινοξέα περιέχουν υδροξύλια τα οποία μπορούν να λειτουργήσουν ως δέκτες και δότες πρωτονίων για τη δημιουργία υδρογονικών δεσμών.
77 Tα αμινοξέα Φαινυλαλανίνη Tυροσίνη Tρυπτοφάνη H φαινυλαλανίνη έχει έναν υδρόφοβο αρωματικό φαινολικό δακτύλιο, ενώ η τυροσίνη και η τρυπτοφάνη έχουν και πολικό χαρακτήρα με δυνατότητα δημιουργίας υδρογονικών δεσμών μέσω του υδροξυλίου και της ινδολικής ομάδας, αντίστοιχα.
78 Tα αμινοξέα Γλουταμικό Aσπαρτικό Kαι τα δύο αυτά αμινοξέα είναι φορτισμένα αρνητικά σε φυσιολογικό ph. Oι καρβοξυλικές ομάδες μορούν να σχηματίσουν δεσμούς άλατος ή να είναι δέκτες υδρογονικών δεσμών.
79 Tα αμινοξέα Aρπαραγίνη Γλουταμίνη Tα αμινοξέα αυτά έχουν πλευρικές αλυσίδες που είναι παράγωγα του ασπαρτικού και γλουταμικού οξέος. H ενεργός τους ομάδα είναι το καρβοξυλαμίδιο το οποίο μπορεί να είναι δέκτης και δότης υδρογονικών δεσμών
80 Tα αμινοξέα Λυσίνη Aργινίνη Iστιδίνη Oι πλευρικές ομάδες αυτών των αμινοξέων είναι φορτισμένες θετικά σε φυσιολογικό ph. H αργινίνη είναι πιο βασική από την λυσίνη. H αλειφατική αλυσίδα της λυσίνης πολλές φορές παίρνει μέρος σε υδρόφοβες αλληλεπιδράσεις.
81 Tα αμινοξέα Tο pk α της ιστιδίνης είναι 6.0, με αποτέλεσμα να έχουμε ισορροπία μεταξύ της φορτισμένης και μη φορτισμένης πλευρικής αλυσίδας γύρω από τις φυσιολογικές τιμές ph. Πρέπει να τονιστεί ότι όταν το άζωτο της ινδολικής ομάδας είναι φορτισμένο λειτουργεί ως δότης ενός πρωτονίου ενώ σε υψηλότερo ph ως δέκτης. H ιδιότητα αυτή χρησιμοποιείται συχνά στην ενζυμική κατάλυση.
82 H υδροφοβικότητα των αμινοξέων Ο υδροφοβικός δείκτης των 20 αμινοξέων (μεγαλύτερο νούμερο δείχνει μεγαλύτερη υδροφοβικότητα)
83 Kάποια παράγωγα αμινοξέων Aκέτυλο-λυσίνη Φωσφορυλο-σερίνη 3 -Yδροξυλο-προλίνη 3 -μέθυλο-ιστιδίνη γ-καρβόξυ-γλουταμικό
84 Στο επόμενο: Δευτεροταγής και υπερδευτεροταγής δομή
Εισαγωγή στη Δομή Βιομορίων
 Εισαγωγή στη Δομή Βιομορίων Μαρία Παυλάκη PhD m_pavlaki@hotmail.com Oργάνωση μαθήματος (εξετάσεις) Tο μάθημα έχει συντελεστή 70% του τελικού βαθμού Tο εργαστήριο 30% Θα πρέπει να πάρετε 5 στο μάθημα και
Εισαγωγή στη Δομή Βιομορίων Μαρία Παυλάκη PhD m_pavlaki@hotmail.com Oργάνωση μαθήματος (εξετάσεις) Tο μάθημα έχει συντελεστή 70% του τελικού βαθμού Tο εργαστήριο 30% Θα πρέπει να πάρετε 5 στο μάθημα και
Κεφάλαιο 1. Οι δομικοί λίθοι
 Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων. 1/10/2015 Δ.Δ. Λεωνίδας
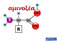 αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
Δευτεροταγής Δομή Πρωτεϊνών
 Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Oι στόχοι μιας πρωτεΐνης όταν διπλωθεί είναι: 1. H xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. Να επιτευχθούν υδρογονικοί δεσμοί από πολικά αμινοξέα
Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Oι στόχοι μιας πρωτεΐνης όταν διπλωθεί είναι: 1. H xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. Να επιτευχθούν υδρογονικοί δεσμοί από πολικά αμινοξέα
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
Στοιχεία Φυσικοχηµείας και Βιοφυσικής
 Στοιχεία Φυσικοχηµείας και Βιοφυσικής Β. Φαδούλογλου 2008 Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία
Στοιχεία Φυσικοχηµείας και Βιοφυσικής Β. Φαδούλογλου 2008 Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία Φυσικοχηµείας και Βιοφυσικής Εργαστήρια Βιβλίο Εξετάσεις Ύλη Στοιχεία
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ
 ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
οµικά στοιχεία βιοµορίων
 2-1 Κεφάλαιο 2 οµικά στοιχεία βιοµορίων 2.1. ιαστάσεις των Βιοµορίων Οι διαστάσεις των βιοµορίων κυµαίνονται από µερικά Ångströms (10-10 m) έως µερικές εκατοντάδες Ångströms (10-8 m). (εικόνα 2.1, 2.2)
2-1 Κεφάλαιο 2 οµικά στοιχεία βιοµορίων 2.1. ιαστάσεις των Βιοµορίων Οι διαστάσεις των βιοµορίων κυµαίνονται από µερικά Ångströms (10-10 m) έως µερικές εκατοντάδες Ångströms (10-8 m). (εικόνα 2.1, 2.2)
Ενεργειακή ανάλυση βιομορίων
 Ενεργειακή ανάλυση βιομορίων Τα βιομόρια ως φυσικά συστήματα πρωτεΐνες, DNA, πεπτίδια, μικρά μόρια (ligands, φάρμακα) Αλληλεπιδράσεις μεταξύ των ατόμων + επίδραση του περιβάλλοντος νερού σταθεροποίηση
Ενεργειακή ανάλυση βιομορίων Τα βιομόρια ως φυσικά συστήματα πρωτεΐνες, DNA, πεπτίδια, μικρά μόρια (ligands, φάρμακα) Αλληλεπιδράσεις μεταξύ των ατόμων + επίδραση του περιβάλλοντος νερού σταθεροποίηση
Δευτεροταγής Δομή Πρωτεϊνών
 Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Η κινητήρια δύναμη για την αναδίπλωση μιας πρωτεΐνης είναι η επίτευξη των εξής: 1. xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. δημιουργία μιας συμπαγούς
Δευτεροταγής Δομή Πρωτεϊνών Πρωτεϊνικό δίπλωμα Η κινητήρια δύναμη για την αναδίπλωση μιας πρωτεΐνης είναι η επίτευξη των εξής: 1. xαμηλή ενέργεια διαμόρφωσης του κάθε αμινοξέος 2. δημιουργία μιας συμπαγούς
MAΘΗΜΑ 4 ο AMINOΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ
 MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
οµή και Αναδίπλωση πρωτεϊνών
 οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
Κεφάλαιο 22 Πρωτεΐνες
 Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής
 Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΠΡΩΤΕΪΝΕΣ. Φατούρος Ιωάννης Αναπληρωτής Καθηγητής
 ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν;
 Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες
 Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
ΑΣΚΗΣΗ 1 Δύο αμινοξέα Α, και Β, συνιστούν ένα διπεπτίδιο. Το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του. Ποια είναι η δομή του;
 ΑΣΚΗΣΗ 1 Δύο αμινοξέα Α, και Β, συνιστούν ένα διπεπτίδιο. Το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του. Ποια είναι η δομή του; Β-Α γιατί το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του άρα θα γράφεται
ΑΣΚΗΣΗ 1 Δύο αμινοξέα Α, και Β, συνιστούν ένα διπεπτίδιο. Το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του. Ποια είναι η δομή του; Β-Α γιατί το αμινοξύ Α έχει ελεύθερη την καρβοξυλομάδα του άρα θα γράφεται
Τάξη. Γνωστικό αντικείµενο: Ειδικοί διδακτικοί στόχοι
 Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Αρχιτεκτονική της τρισδιάστατης δομής πρωτεϊνών
 Αρχιτεκτονική της τρισδιάστατης δομής πρωτεϊνών Βασίλης Προμπονάς, PhD Ερευνητικό Εργαστήριο Βιοπληροφορικής Τμήμα Βιολογικών Επιστημών Νέα Παν/πολη, Γραφείο B161 Πανεπιστήμιο Κύπρου Ταχ.Κιβ. 20537 1678,
Αρχιτεκτονική της τρισδιάστατης δομής πρωτεϊνών Βασίλης Προμπονάς, PhD Ερευνητικό Εργαστήριο Βιοπληροφορικής Τμήμα Βιολογικών Επιστημών Νέα Παν/πολη, Γραφείο B161 Πανεπιστήμιο Κύπρου Ταχ.Κιβ. 20537 1678,
Μικρά αμινοξέα. Βιοχημεία Ι Β-3
 Βιοχημεία Ι Β-2 Μικρά αμινοξέα Βιοχημεία Ι Β-3 Aλειφατικά αμινοξέα Βιοχημεία Ι Β-4 Ιμινοξύ Βιοχημεία Ι Β-5 Αρωματικά αμινοξέα Βιοχημεία Ι Β-6 Βιοχημεία Ι Β-7 Η Tyr και η Trp απορροφούν στα 280nm-έτσι μετράται
Βιοχημεία Ι Β-2 Μικρά αμινοξέα Βιοχημεία Ι Β-3 Aλειφατικά αμινοξέα Βιοχημεία Ι Β-4 Ιμινοξύ Βιοχημεία Ι Β-5 Αρωματικά αμινοξέα Βιοχημεία Ι Β-6 Βιοχημεία Ι Β-7 Η Tyr και η Trp απορροφούν στα 280nm-έτσι μετράται
Περίληψη 1 ου Κεφαλαίου
 Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ
 ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
Μεταβολισμός πρωτεϊνών και των αμινοξέων
 Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
Δομές (Διαμορφώσεις) Πρωτεινικών μορίων
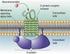 Δομές (Διαμορφώσεις) Πρωτεινικών μορίων Πρωτοταγής δομή (αλληλουχία αμινοξέων) Δευτεροταγής δομή Η διάταξη της πεπτιδικής αλυσίδας στον χωρο αυτής καθ αυτής (χωρίς να ληφθούν υπ όψη οι ομάδες R) Τριτοταγής
Δομές (Διαμορφώσεις) Πρωτεινικών μορίων Πρωτοταγής δομή (αλληλουχία αμινοξέων) Δευτεροταγής δομή Η διάταξη της πεπτιδικής αλυσίδας στον χωρο αυτής καθ αυτής (χωρίς να ληφθούν υπ όψη οι ομάδες R) Τριτοταγής
COOH R 2. H α-αμινοξύ 2
 7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Διάλεξη 7: Μοριακή Δομή
 Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Το ένζυμο Καρβοξυπεπτιδάση Α έχει τα εξής χαρακτηριστικά
 Το ένζυμο Καρβοξυπεπτιδάση Α έχει τα εξής χαρακτηριστικά Είναι απλή πολυπεπτιδική αλυσίδα 307 αμινοξέων Είναι συμπαγής και έχει σχήμα ελλειψοειδές διαστάσεων 50 x 42 x 38 A Περιέχει περιοχές α-έλικος 38%
Το ένζυμο Καρβοξυπεπτιδάση Α έχει τα εξής χαρακτηριστικά Είναι απλή πολυπεπτιδική αλυσίδα 307 αμινοξέων Είναι συμπαγής και έχει σχήμα ελλειψοειδές διαστάσεων 50 x 42 x 38 A Περιέχει περιοχές α-έλικος 38%
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια
 πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α
 Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
τα βιβλία των επιτυχιών
 Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη. Ιοντικός χαρακτήρας δεσμών. Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
 Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
Δεσμικότητα των οργανικών ενώσεων: Σχηματισμός δεσμών για τη δημιουργία ενώσεων πιο σταθερών από τα επιμέρους άτομα Ιοντικός χαρακτήρας δεσμών Οι ιοντικοί δεσμοί στα άλατα είναι αποτέλεσμα μεταφοράς e
Δομή και λειτουργία πρωτεϊνών. Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο
 Δομή και λειτουργία πρωτεϊνών Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο Πρωτεΐνες Κύριο συστατικό κυττάρου Δομικοί λίθοι αλλά και επιτελεστές λειτουργίας κυττάρου ένζυμα, μεταφορά,
Δομή και λειτουργία πρωτεϊνών Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο Πρωτεΐνες Κύριο συστατικό κυττάρου Δομικοί λίθοι αλλά και επιτελεστές λειτουργίας κυττάρου ένζυμα, μεταφορά,
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών
 Μοριακή Αναγνώριση Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών 1 Μοριακή Αναγνώριση Με τον όρο μοριακή αναγνώριση περιγράφουμε την αλληλεπίδραση μεταξύ δύο
Μοριακή Αναγνώριση Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών 1 Μοριακή Αναγνώριση Με τον όρο μοριακή αναγνώριση περιγράφουμε την αλληλεπίδραση μεταξύ δύο
Διαλέξεις Χημείας Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων
 Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Εισαγωγή στη Μοριακή Προσοµοίωση
 Κεφάλαιο 6 Εισαγωγή στη Μοριακή Προσοµοίωση 6.1. Μοριακή Μηχανική 6.1.1. Εισαγωγή στη µεθοδολογία του «απ αρχής» διπλώµατος της πρωτείνης. Η ενέργεια κάθε µορίου µπορεί θεωρητικά να υπολογιστεί µε την
Κεφάλαιο 6 Εισαγωγή στη Μοριακή Προσοµοίωση 6.1. Μοριακή Μηχανική 6.1.1. Εισαγωγή στη µεθοδολογία του «απ αρχής» διπλώµατος της πρωτείνης. Η ενέργεια κάθε µορίου µπορεί θεωρητικά να υπολογιστεί µε την
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
 ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
Θεωρία δεσµού σθένους - Υβριδισµός. Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης. Αντιδράσεις υποκατάστασης Πολυµερισµός
 11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
Μοριακή Αναγνώριση. 5.1. Εισαγωγή. 5.2. Σταθερές σύνδεσης και αποχωρισµού. [A][B] k d = ----------- [AB] [ΑΒ] k i = ---------- [Α][Β] Κεφάλαιο
![Μοριακή Αναγνώριση. 5.1. Εισαγωγή. 5.2. Σταθερές σύνδεσης και αποχωρισµού. [A][B] k d = ----------- [AB] [ΑΒ] k i = ---------- [Α][Β] Κεφάλαιο Μοριακή Αναγνώριση. 5.1. Εισαγωγή. 5.2. Σταθερές σύνδεσης και αποχωρισµού. [A][B] k d = ----------- [AB] [ΑΒ] k i = ---------- [Α][Β] Κεφάλαιο](/thumbs/24/3785169.jpg) Κεφάλαιο 5-1 5 Μοριακή Αναγνώριση 5.1. Εισαγωγή Ένα από τα σηµαντικότερα χαρακτηριστικά των ζωντανών οργανισµών είναι ότι τα µακροµόρια που περιέχουν κάνουν πολύ εξειδικευµένες αλληλεπιδράσεις µε άλλα
Κεφάλαιο 5-1 5 Μοριακή Αναγνώριση 5.1. Εισαγωγή Ένα από τα σηµαντικότερα χαρακτηριστικά των ζωντανών οργανισµών είναι ότι τα µακροµόρια που περιέχουν κάνουν πολύ εξειδικευµένες αλληλεπιδράσεις µε άλλα
(Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου )
 Δυνάμεις διπόλου διπόλου (Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου ) Τα πολικά μόρια μπορούν να έλκονται αμοιβαία μέσω δυνάμεων διπόλου διπόλου. Η δύναμη διπόλου
Δυνάμεις διπόλου διπόλου (Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου ) Τα πολικά μόρια μπορούν να έλκονται αμοιβαία μέσω δυνάμεων διπόλου διπόλου. Η δύναμη διπόλου
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2016-2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1) Δίνονται τα αμινοξέα σερίνη, αλανίνη, γλουταμικό, κυστεΐνη, λυσίνη, αργινίνη, διαχωρίστε τα
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2016-2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1) Δίνονται τα αμινοξέα σερίνη, αλανίνη, γλουταμικό, κυστεΐνη, λυσίνη, αργινίνη, διαχωρίστε τα
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 2 η θεματική ενότητα: Χημικοί δεσμοί και μοριακές ιδιότητες Σχολή: Περιβάλλοντος Τμήμα: Επιστήμης Τροφίμων και Διατροφής Εκπαιδευτής: Χαράλαμπος Καραντώνης Άδειες Χρήσης Το παρόν εκπαιδευτικό
Βιολογία Γενικής Παιδείας Β Λυκείου
 Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής
 ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
Μάθημα 20 ο. Το σχήμα των μορίων
 Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Kυτταρική Bιολογία ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ ΔIAΛEΞΗ 3 (7/3/2012) Δρ. Xρήστος Παναγιωτίδης, Τμήμα Φαρμακευτικής Α.Π.Θ.
 Kυτταρική Bιολογία ΔIAΛEΞΗ 3 (7/3/2012) ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ AΣ ΘYMHΘOYME Στην προηγούμενη διάλεξη μιλήσαμε για τη χημική σύσταση των κυττάρων και για τα βιολογικά πολυμερή που αποτελούν
Kυτταρική Bιολογία ΔIAΛEΞΗ 3 (7/3/2012) ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ AΣ ΘYMHΘOYME Στην προηγούμενη διάλεξη μιλήσαμε για τη χημική σύσταση των κυττάρων και για τα βιολογικά πολυμερή που αποτελούν
Οργανική Χηµεία. Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια
 Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
Οργανική Χηµεία Κεφάλαιο 17 & 18: Αλκοόλες, θειόλες, αιθέρες και εποξείδια 1. Αλκοόλες Ενώσεις που περιέχουν οµάδες υδροξυλίου συνδεδεµένες µε κορεσµένα άτοµα άνθρακα υβριδισµού sp 3 Βάσει παραπάνω ορισµού,
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ποιο άτομο έχει το ακόλουθο διάγραμμα ηλεκτρονικής δομής; 3d 4s 4p Ar 2. Σε καθεμιά από τις ακόλουθες σφαίρες αντιστοιχείστε τα άτομα των στοιχείων K, Rb, Ca και Br.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ποιο άτομο έχει το ακόλουθο διάγραμμα ηλεκτρονικής δομής; 3d 4s 4p Ar 2. Σε καθεμιά από τις ακόλουθες σφαίρες αντιστοιχείστε τα άτομα των στοιχείων K, Rb, Ca και Br.
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράμμα που αντιστοιχεί στη σωστή απάντηση:
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
Θέµατα ιάλεξης ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ ΠΡΩΤΕΪΝΕΣ. ιαχωρισµός Αµινοξέων
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
πρωτεΐνες πολυμερείς ουσίες δομούν λειτουργούν λευκώματα 1.Απλές πρωτεΐνες 2.Σύνθετες πρωτεΐνες πρωτεΐδια μη πρωτεϊνικό μεταλλοπρωτεΐνες
 ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
Μάθημα 21 ο. Το σχήμα των μορίων. Θεωρία VSEPR. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
πολώνεται δύσκολα πολώνεται εύκολα
 Η αρχή του σκληρού ή µαλακού οξέος (ή βάσης) σκληρό οξύ µικρό σε µέγεθος χηµικό είδος πολώνεται δύσκολα µαλακό οξύ µεγάλο σε µέγεθος χηµικό είδος πολώνεται εύκολα Θρέψη Φυτών. Μπουράνης, Σ. Χωριανοπούλου
Η αρχή του σκληρού ή µαλακού οξέος (ή βάσης) σκληρό οξύ µικρό σε µέγεθος χηµικό είδος πολώνεται δύσκολα µαλακό οξύ µεγάλο σε µέγεθος χηµικό είδος πολώνεται εύκολα Θρέψη Φυτών. Μπουράνης, Σ. Χωριανοπούλου
κυματικής συνάρτησης (Ψ) κυματική συνάρτηση
 Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
 1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
Α Ε Τ. ΤΕΙ Αθήνας. Στ. Μπογιατζής, επίκουρος καθηγητής ΤΕΙ Αθήνας. ΤΕΙ Αθήνας / ΣΑΕΤ / Στ. Μπογιατζής
 Στ. Μπογιατζής, επίκουρος καθηγητής Ομοιοπολικές χημικές ενώσεις Ενώσεις του άνθρακα Χαρακτηριστικές ομάδες Τετραεδρική μοριακή δομή Επίπεδη τριγωνική μοριακή δομή Ευθύγραμμη μοριακή δομή Τα οργανικά μόρια
Στ. Μπογιατζής, επίκουρος καθηγητής Ομοιοπολικές χημικές ενώσεις Ενώσεις του άνθρακα Χαρακτηριστικές ομάδες Τετραεδρική μοριακή δομή Επίπεδη τριγωνική μοριακή δομή Ευθύγραμμη μοριακή δομή Τα οργανικά μόρια
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Ασκήσεις. Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3
 Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
Χαρακτηριστικά της δομής της Μυοσφαιρίνης
 Χαρακτηριστικά της δομής της Μυοσφαιρίνης Η μυοσφαιρίνη είναι ενα εξαιρετικά συμπαγές μόριο.οι διαστάσεις είναι 45Χ35Χ25 Α και υπαρχει πολύ λίγος αδειος χώρος στο εσωτερικό τού μορίου Γυρω στα 75% της
Χαρακτηριστικά της δομής της Μυοσφαιρίνης Η μυοσφαιρίνη είναι ενα εξαιρετικά συμπαγές μόριο.οι διαστάσεις είναι 45Χ35Χ25 Α και υπαρχει πολύ λίγος αδειος χώρος στο εσωτερικό τού μορίου Γυρω στα 75% της
Περίληψη Κεφαλαίου 2
 Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
Περίληψη Κεφαλαίου 2 Οργανικά µόρια: πολικούς οµοιοπολικούς δεσµούς λόγω ασύµµετρης κατανοµής e - (διαφορετική ηλεκτροαρνητικότητας ατόµων) Κάποιες ενώσεις υποδηλώνονται µε δοµές συντονισµού οι οποίες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης
 Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ
 ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
Διδάσκων: Καθηγητής Εμμανουήλ Μ. Παπαμιχαήλ
 Τίτλος Μαθήματος: Ενζυμολογία Ενότητα: Εισαγωγή Διδάσκων: Καθηγητής Εμμανουήλ Μ. Παπαμιχαήλ Τμήμα: Χημείας 8 1. EIΣAΓΩΓH Tα ένζυμα είναι οι καταλύτες της ζώσης ύλης. Καταλύουν τις χημικές αντιδράσεις,
Τίτλος Μαθήματος: Ενζυμολογία Ενότητα: Εισαγωγή Διδάσκων: Καθηγητής Εμμανουήλ Μ. Παπαμιχαήλ Τμήμα: Χημείας 8 1. EIΣAΓΩΓH Tα ένζυμα είναι οι καταλύτες της ζώσης ύλης. Καταλύουν τις χημικές αντιδράσεις,
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Σύγxρονη Φυσική II. Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ
 ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράμμα που αντιστοιχεί στη σωστή απάντηση:
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ
 ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2016-2017 ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ 1 ΕΙΣΑΓΩΓΗ ΑΤΟΜΙΚΗ ΘΕΩΡΙΑ Δομικά σωματίδια (άτομα-μόρια-ιόντα) Δομή του ατόμου Ατομικός και μαζικός αριθμός Ισότοπα Ηλεκτρονική
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2016-2017 ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ 1 ΕΙΣΑΓΩΓΗ ΑΤΟΜΙΚΗ ΘΕΩΡΙΑ Δομικά σωματίδια (άτομα-μόρια-ιόντα) Δομή του ατόμου Ατομικός και μαζικός αριθμός Ισότοπα Ηλεκτρονική
Αντιδράσεις της α-αμινομάδος
 Αντιδράσεις της α-αμινομάδος Μπορεί να αλκυλιωθεί με οξινα χαλίδια ή ανυδρίτες.η Κατεργασία χρησιμοποιείται για να προστατευθεί η α-αμινομάδα Αντιδρά με την νινυδρίνη.χρησιμοποιείται για ποσοτικό προσδιορισμό
Αντιδράσεις της α-αμινομάδος Μπορεί να αλκυλιωθεί με οξινα χαλίδια ή ανυδρίτες.η Κατεργασία χρησιμοποιείται για να προστατευθεί η α-αμινομάδα Αντιδρά με την νινυδρίνη.χρησιμοποιείται για ποσοτικό προσδιορισμό
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
Φυσική Στερεών στις Πρωτεΐνες
 Φυσική Στερεών στις Πρωτεΐνες Νίκος Απ. Παπανδρέου Τ.Ε.Ι. Πειραιά Φεβρουάριος 2010 Ένα ελικοϊδές μονοπάτι Χημική δομή μίας πρωτεΐνης Μήκος αλυσίδας ~30 έως ~1000 αµινοξέα Συνολικός αριθµός ατόµων έως ~
Φυσική Στερεών στις Πρωτεΐνες Νίκος Απ. Παπανδρέου Τ.Ε.Ι. Πειραιά Φεβρουάριος 2010 Ένα ελικοϊδές μονοπάτι Χημική δομή μίας πρωτεΐνης Μήκος αλυσίδας ~30 έως ~1000 αµινοξέα Συνολικός αριθµός ατόµων έως ~
ΚΕΦΑΛΑΙΟ 6ο ΑΜΙΝΟΞΕΑ
 138 ΚΕΦΑΛΑΙΟ 6ο ΑΜΙΝΟΞΕΑ 6.1. Τα αμινοξέα Τα αμινοξέα είναι οι ενώσεις που έχουν αμινομάδα ( NH2) και καρβοξυλομάδα ( COOH) στην ίδια ανθρακική αλυσίδα και είναι ενώσεις γενικά διαλυτές στο νερό. Τα α
138 ΚΕΦΑΛΑΙΟ 6ο ΑΜΙΝΟΞΕΑ 6.1. Τα αμινοξέα Τα αμινοξέα είναι οι ενώσεις που έχουν αμινομάδα ( NH2) και καρβοξυλομάδα ( COOH) στην ίδια ανθρακική αλυσίδα και είναι ενώσεις γενικά διαλυτές στο νερό. Τα α
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Οργανική Χημεία. Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες
 Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ
 ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών.
 ΑΜΙΝΟΞΕΑ Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών. Ο γενικός μοριακός τύπος ενός α- αμινοξέος παρουσιάζεται στο διπλανό σχήμα και συνίσταται
ΑΜΙΝΟΞΕΑ Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών. Ο γενικός μοριακός τύπος ενός α- αμινοξέος παρουσιάζεται στο διπλανό σχήμα και συνίσταται
