ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
|
|
|
- Ευαδνη Κουβέλης
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1
2 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml εναιωρήματος περιέχει 10 mg βρινζολαμίδης και 5 mg τιμολόλης (ως μηλεϊνική τιμολόλη). Έκδοχα: Ένα ml εναιωρήματος περιέχει 0,10 mg βενζαλκώνιο χλωριούχο. Για τον πλήρη κατάλογο των εκδόχων, βλ. παράγραφο ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ Οφθαλμικές σταγόνες, εναιώρημα (οφθαλμικές σταγόνες) Λευκό έως υπόλευκο ομοιογενές εναιώρημα, ph 7,2 (κατά προσέγγιση). 4. ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ 4.1 Θεραπευτικές ενδείξεις Μείωση της ενδοφθάλμιας πίεσης (ΕΟΠ) σε ενήλικες ασθενείς με γλαύκωμα ανοικτής γωνίας ή οφθαλμική υπέρταση για τους οποίους η μονοθεραπεία παρέχει ανεπαρκή μείωση της ΕΟΠ (βλ. παράγραφο 5.1). 4.2 Δοσολογία και τρόπος χορήγησης Χρήση σε ενήλικες, συμπεριλαμβανομένων των ηλικιωμένων Η δόση είναι μία σταγόνα AZARGA στο κόλπωμα του επιπεφυκότα του πάσχοντος οφθαλμού-ών δύο φορές την ημέρα. Συνιστάται η απόφραξη της ρινοδακρυϊκής οδού ή το απαλό κλείσιμο των βλεφάρων μετά την ενστάλαξη. Έτσι μπορεί να ελαττωθεί η συστηματική απορρόφηση των φαρμακευτικών προϊόντων που χορηγούνται μέσω της οφθαλμικής οδού με αποτέλεσμα τη μείωση των συστηματικών ανεπιθύμητων ενεργειών. Εάν χρησιμοποιούνται περισσότερα του ενός τοπικά οφθαλμικά φαρμακευτικά προϊόντα, αυτά θα πρέπει να χορηγούνται με διαφορά τουλάχιστον 5 λεπτών. Αν παραλειφθεί μία δόση, η θεραπεία θα πρέπει να συνεχιστεί με την επόμενη δόση, όπως είναι προγραμματισμένο. Η δόση δε θα πρέπει να ξεπερνά τη μία σταγόνα στον πάσχοντα οφθαλμό-ούς δύο φορές την ημέρα. Όταν αντικαθιστάτε έναν άλλο οφθαλμικό αντιγλαυκωματικό παράγοντα με AZARGA, διακόψτε τη χορήγηση του άλλου παράγοντα και αρχίστε την επόμενη ημέρα το AZARGA. Παιδιατρικοί ασθενείς Το AZARGA δεν συνιστάται για χρήση σε παιδιά κάτω των 18 ετών λόγω έλλειψης στοιχείων για την ασφάλεια και την αποτελεσματικότητα. 2
3 Χρήση επί ηπατικής και νεφρικής δυσλειτουργίας Δεν έχουν πραγματοποιηθεί μελέτες με το AZARGA ή με οφθαλμικές σταγόνες τιμολόλης 5 mg/ml σε ασθενείς με ηπατική ή νεφρική δυσλειτουργία. Δεν απαιτείται ρύθμιση της δοσολογίας σε ασθενείς με ηπατική δυσλειτουργία ή σε ασθενείς με ήπια ή μέτρια νεφρική δυσλειτουργία. Το AZARGA δεν έχει μελετηθεί σε ασθενείς με σοβαρή νεφρική δυσλειτουργία (κάθαρση κρεατινίνης <30 ml/λεπτό) ή σε ασθενείς με υπερχλωραιμική οξέωση. Επειδή η βρινζολαμίδη και ο κύριος μεταβολίτης της απεκκρίνονται κυρίως από το νεφρό, το AZARGA αντενδείκνυται σε ασθενείς με σοβαρή νεφρική δυσλειτουργία (βλ. παράγραφο 4.3). Τρόπος χορήγησης Για οφθαλμική χρήση. Δώστε οδηγίες στους ασθενείς να ανακινούν τη φιάλη πριν από τη χρήση. Για να προληφθεί η επιμόλυνση του σταγονομετρικού ρύγχους και του διαλύματος, πρέπει να δίνεται προσοχή ώστε να μην αγγίζονται τα βλέφαρα, οι γύρω περιοχές ή άλλες επιφάνειες με το σταγονομετρικό ρύγχος της φιάλης. Δώστε οδηγίες στους ασθενείς να κρατούν σφιχτά κλειστή τη φιάλη, όταν δε χρησιμοποιείται. 4.3 Αντενδείξεις Υπερευαισθησία στις δραστικές ουσίες ή σε κάποιο από τα έκδοχα. Βρογχικό άσθμα, ιστορικό βρογχικού άσθματος ή σοβαρή χρόνια αποφρακτική πνευμονοπάθεια. Φλεβοκομβική βραδυκαρδία, κολποκοιλιακός αποκλεισμός δεύτερου ή τρίτου βαθμού, έκδηλη καρδιακή ανεπάρκεια ή καρδιογενής καταπληξία. Σοβαρή αλλεργική ρινίτιδα και βρογχική υπεραντιδραστικότητα, υπερευαισθησία σε άλλους β-αναστολείς. Υπερχλωραιμική οξέωση (βλ. παράγραφο 4.2) Σοβαρή νεφρική δυσλειτουργία. Υπερευαισθησία στις σουλφοναμίδες (βλ. παράγραφο 4.4). 4.4 Ειδικές προειδοποιήσεις και προφυλάξεις κατά τη χρήση Συστηματικές επιδράσεις Όπως και άλλοι οφθαλμικοί παράγοντες που εφαρμόζονται τοπικά, η βρινζολαμίδη και η τιμολόλη απορροφώνται συστηματικά. Λόγω του β-αδρενεργικού συστατικού, της τιμολόλης, ενδέχεται να εμφανιστούν οι ίδιοι τύποι καρδιαγγειακών και πνευμονικών ανεπιθύμητων ενεργειών που παρατηρούνται με τους β-αδρενεργικούς αναστολείς που χορηγούνται συστηματικά. Η καρδιακή ανεπάρκεια θα πρέπει να έχει τεθεί επαρκώς υπό έλεγχο πριν την έναρξη θεραπείας με τιμολόλη. Ασθενείς με ιστορικό σοβαρής καρδιοπάθειας πρέπει να παρακολουθούνται για σημεία καρδιακής ανεπάρκειας και να ελέγχεται ο σφυγμός τους. Αναπνευστικές και καρδιακές αντιδράσεις, συμπεριλαμβανομένου του θανάτου λόγω βρογχόσπασμου σε ασθενείς με άσθμα και, σπανίως, του θανάτου που συνδέεται με καρδιακή ανεπάρκεια, έχουν αναφερθεί μετά τη χορήγηση μηλεϊνικής τιμολόλης. Οι β-αδρενεργικοί αναστολείς πρέπει να χορηγούνται με προσοχή σε ασθενείς για τους οποίους υπάρχει το ενδεχόμενο αυθόρμητης υπογλυκαιμίας ή σε ασθενείς με ασταθή ινσουλινοεξαρτώμενο διαβήτη, καθώς οι β-αδρενεργικοί αναστολείς ενδέχεται να συγκαλύψουν τα σημεία και τα συμπτώματα οξείας υπογλυκαιμίας. Αυτοί ενδέχεται επίσης να συγκαλύψουν τα σημεία υπερθυρεοειδισμού και να προκαλέσουν επιδείνωση στηθάγχης Prinzmetal, σοβαρές περιφερικές και κεντρικές κυκλοφορικές διαταραχές και υπόταση. 3
4 Το AZARGA περιέχει βρινζολαμίδη, μια σουλφοναμίδη. Οι ίδιοι τύποι ανεπιθύμητων ενεργειών, που μπορούν να αποδοθούν στις σουλφοναμίδες, ενδέχεται να εμφανιστούν με την τοπική χορήγηση. Οξεο-βασικές διαταραχές έχουν αναφερθεί με αναστολείς της καρβονικής ανυδράσης που λαμβάνονται από το στόμα. Αν εμφανιστούν σημεία σοβαρών αντιδράσεων ή υπερευαισθησίας, διακόψτε τη χρήση αυτού του φαρμακευτικού προϊόντος. Υπάρχει το ενδεχόμενο προσθετικής επίδρασης στις γνωστές συστηματικές δράσεις αναστολής της καρβονικής ανυδράσης σε ασθενείς που λαμβάνουν έναν από του στόματος αναστολέα της καρβονικής ανυδράσης και AZARGA. Η ταυτόχρονη χορήγηση AZARGA και από του στόματος αναστολέων της καρβονικής ανυδράσης δεν έχει μελετηθεί και δε συνιστάται (βλ. παράγραφο 4.5). Αναφυλακτικές αντιδράσεις Κατά τη λήψη β-αδρενεργικών αναστολέων, ασθενείς με ιστορικό ατοπίας ή ιστορικό σοβαρής αναφυλακτικής αντίδρασης σε διάφορα αλλεργιογόνα ενδέχεται να μην αντιδρούν στις συνήθεις δόσεις αδρεναλίνης που χρησιμοποιούνται για την αντιμετώπιση αναφυλακτικών αντιδράσεων. Ταυτόχρονη θεραπεία Η τιμολόλη ενδέχεται να αλληλεπιδράσει με άλλα φαρμακευτικά προϊόντα (βλ. παράγραφο 4.5). Η επίδραση στην ενδοφθάλμια πίεση ή οι γνωστές επιδράσεις της συστηματικής β-αδρενεργικής αναστολής ενδέχεται να ενισχυθούν όταν το AZARGA χορηγείται σε ασθενείς που ήδη λαμβάνουν ένα β-αδρενεργικό αναστολέα από το στόμα. Δε συνιστάται η χρήση δύο τοπικών β-αδρενεργικών αναστολέων ή δύο τοπικών αναστολέων της καρβονικής ανυδράσης. Οφθαλμικές επιδράσεις Υπάρχει περιορισμένη εμπειρία με το AZARGA στη θεραπεία ασθενών με ψευδοαποφολιδωτικό γλαύκωμα ή μελαγχρωστικό γλαύκωμα. Θα πρέπει να δίδεται προσοχή στην αντιμετώπιση αυτών των ασθενών και συνιστάται στενή παρακολούθηση της ΕΟΠ. Το AZARGA δεν έχει μελετηθεί σε ασθενείς με γλαύκωμα στενής γωνίας και δε συνιστάται η χρήση του σε αυτούς τους ασθενείς. Οι από τους στόματος αναστολείς της καρβονικής ανυδράσης ενδέχεται να επηρεάσουν την εκτέλεση εργασιών που απαιτούν νοητική εγρήγορση ή/και σωματικό συντονισμό σε ηλικιωμένους ασθενείς. Το AZARGA απορροφάται συστηματικά και, επομένως, αυτό ενδέχεται να συμβεί με την τοπική χορήγηση. Ο πιθανός ρόλος της βρινζολαμίδης στην ενδοθηλιακή λειτουργία του κερατοειδούς δεν έχει διερευνηθεί σε ασθενείς με πρόβλημα στους κερατοειδείς (ιδιαίτερα σε ασθενείς με χαμηλό αριθμό ενδοθηλιακών κυττάρων). Συγκεκριμένα, δεν έχουν γίνει μελέτες για ασθενείς που φοράνε φακούς επαφής και συνιστάται προσεκτική παρακολούθηση αυτών των ασθενών, όταν χρησιμοποιούν βρινζολαμίδη, επειδή οι αναστολείς της καρβονικής ανυδράσης μπορεί να επηρεάσουν την ενυδάτωση του κερατοειδούς και το γεγονός ότι οι ασθενείς φοράνε φακούς επαφής μπορεί να αυξήσει τον κίνδυνο για τον κερατοειδή. Συνιστάται προσεκτική παρακολούθηση των ασθενών με πρόβλημα στους κερατοειδείς, όπως ασθενείς με σακχαρώδη διαβήτη ή δυστροφίες του κερατοειδούς. Το βενζαλκώνιο χλωριούχο, το οποίο συνήθως χρησιμοποιείται ως συντηρητικό σε οφθαλμικά προϊόντα, έχει αναφερθεί ότι προκαλεί στικτή κερατοειδοπάθεια ή/και τοξική ελκώδη κερατοειδοπάθεια. Επειδή το AZARGA περιέχει βενζαλκώνιο χλωριούχο, απαιτείται στενή παρακολούθηση με τη συχνή ή την παρατεταμένη χρήση. Το AZARGA περιέχει βενζαλκώνιο χλωριούχο, το οποίο μπορεί να προκαλέσει ερεθισμό στους οφθαλμούς και είναι γνωστό ότι αποχρωματίζει τους μαλακούς φακούς επαφής. Η επαφή με μαλακούς φακούς επαφής πρέπει να αποφεύγεται. Πρέπει να συμβουλεύετε τους ασθενείς να βγάζουν τους φακούς επαφής πριν την εφαρμογή του AZARGA και να περιμένουν 15 λεπτά μετά την ενστάλαξη της δόσης πριν φορέσουν και πάλι τους φακούς επαφής. 4
5 4.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης Δεν έχουν πραγματοποιηθεί μελέτες αλληλεπιδράσεων με το AZARGA. Το AZARGA περιέχει βρινζολαμίδη, έναν αναστολέα της καρβονικής ανυδράσης και, παρότι χορηγείται τοπικά, απορροφάται συστηματικά. Όξεο-βασικές διαταραχές έχουν αναφερθεί με αναστολείς της καρβονικής ανυδράσης που λαμβάνονται από το στόμα. Το ενδεχόμενο αλληλεπιδράσεων πρέπει να λαμβάνεται υπόψη σε ασθενείς που λαμβάνουν AZARGA. Στα ισοένζυμα του κυτοχρώματος P-450 που είναι υπεύθυνα για το μεταβολισμό της βρινζολαμίδης περιλαμβάνονται τα CYP3A4 (κύριο), CYP2A6, CYP2B6, CYP2C8 και CYP2C9. Είναι αναμενόμενο ότι αναστολείς του CYP3A4 όπως η κετοκοναζόλη, η ιτρακοναζόλη, η κλοτριμαζόλη, η ριτοναβίρη και η τρολεανδομυκίνη θα αναστείλουν το μεταβολισμό της βρινζολαμίδης από το CYP3A4. Συνιστάται προσοχή αν χορηγούνται ταυτόχρονα αναστολείς του CYP3A4. Ωστόσο, είναι απίθανη η συσσώρευση της βρινζολαμίδης αφού η αποβολή από τους νεφρούς αποτελεί την κύρια οδό. Η βρινζολαμίδη δεν είναι αναστολέας των ισοενζύμων του κυτοχρώματος P-450. Υπάρχει ενδεχόμενο για προσθετικές επιδράσεις που οδηγούν σε υπόταση και/ή σαφή βραδυκαρδία όταν χορηγούνται οφθαλμικές σταγόνες με τιμολόλη ταυτόχρονα με αναστολείς διαύλων ασβεστίου που χορηγούνται από το στόμα, γουανεθιδίνη ή β-αναστολείς, αντιαρρυθμικά, δακτυλιδικές γλυκοσίδες ή παρασυμπαθομιμητικά. Η υπερτασική αντίδραση σε αιφνίδια διακοπή κλονιδίνης ενδέχεται να ενισχυθεί όταν λαμβάνονται β-αναστολείς. Ενισχυμένος συστηματικός β-αποκλεισμός (π.χ. μειωμένος καρδιακός ρυθμός) έχει αναφερθεί κατά τη διάρκεια συνδυασμένης θεραπείας με αναστολείς του CYP2D6 (π.χ. κινιδίνη, σιμετιδίνη) και τιμολόλη. Οι β-αναστολείς ενδέχεται να αυξήσουν την υπογλυκαιμική επίδραση των αντιδιαβητικών παραγόντων. Οι β-αναστολείς ενδέχεται να συγκαλύψουν τα σημεία και τα συμπτώματα υπογλυκαιμίας (βλ. παράγραφο 4.4). 4.6 Κύηση και γαλουχία Κύηση Δεν υπάρχουν επαρκή στοιχεία από τη χρήση της βρινζολαμίδης σε έγκυες γυναίκες. Μελέτες σε ζώα κατέδειξαν τοξικότητα στην αναπαραγωγική ικανότητα (βλ. παράγραφο 5.3). Ο ενδεχόμενος κίνδυνος για τον άνθρωπο είναι άγνωστος. Καλά ελεγχόμενες επιδημιολογικές μελέτες με συστηματική χρήση β-αναστολέων δεν κατέδειξαν επιδράσεις δυσπλασίας, αλλά παρατηρήθηκαν σε έμβρυα ή νεογνά κάποιες φαρμακολογικές επιδράσεις, όπως βραδυκαρδία. Τα δεδομένα σχετικά με περιορισμένο αριθμό περιπτώσεων έκθεσης κατά την εγκυμοσύνη στην τιμολόλη σε οφθαλμικές σταγόνες, δεν καταδεικνύουν ανεπιθύμητες ενέργειες στην εγκυμοσύνη ή στην υγεία του εμβρύου/νεογέννητου, αλλά σε μία περίπτωση, αναφέρθηκαν βραδυκαρδία και αρρυθμία στο έμβρυο μιας γυναίκας που υποβλήθηκε σε θεραπεία με οφθαλμικές σταγόνες τιμολόλης. Έως σήμερα δεν διατίθενται άλλα σχετικά επιδημιολογικά δεδομένα. Το AZARGA δεν πρέπει να χρησιμοποιείται κατά τη διάρκεια της εγκυμοσύνης εκτός εάν είναι σαφώς απαραίτητο. 5
6 Γαλουχία Δεν είναι γνωστό εάν η βρινζολαμίδη εκκρίνεται στο ανθρώπινο μητρικό γάλα. Μελέτες σε ζώα κατέδειξαν ότι η βρινζολαμίδη εκκρίνεται στο μητρικό γάλα Η τιμολόλη εμφανίζεται στο ανθρώπινο μητρικό γάλα. Ωστόσο, σε θεραπευτικές δόσεις του AZARGA, δεν αναμένονται επιδράσεις στα νεογέννητα/βρέφη που θηλάζουν. Το AZARGA μπορεί να χρησιμοποιηθεί κατά τη διάρκεια του θηλασμού. 4.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών Όπως ισχύει με οποιεσδήποτε άλλες οφθαλμικές σταγόνες, παροδικά θαμπή όραση ή άλλες οπτικές διαταραχές μπορεί να επηρεάσουν την ικανότητα οδήγησης ή χειρισμού μηχανών. Αν παρουσιαστεί θαμπή όραση κατά την ενστάλαξη, ο ασθενής θα πρέπει να περιμένει μέχρις ότου καθαρίσει η όρασή του πριν οδηγήσει ή χρησιμοποιήσει μηχανές. Οι από τους στόματος αναστολείς της καρβονικής ανυδράσης ενδέχεται να επηρεάσουν την ικανότητα των ηλικιωμένων ασθενών να εκτελούν εργασίες που απαιτούν νοητική εγρήγορση ή/και σωματικό συντονισμό (βλ. παράγραφο 4.4). 4.8 Ανεπιθύμητες ενέργειες Περίληψη του προφίλ ασφαλείας Σε δύο κλινικές δοκιμές διάρκειας 6 και 12 μηνών που περιλάμβαναν 394 ασθενείς, οι οποίοι υποβλήθηκαν σε θεραπεία με το AZARGA, η πιο συχνά αναφερόμενη ανεπιθύμητη ενέργεια ήταν παροδική θαμπή όραση κατά την ενστάλαξη (3,6%), που διαρκούσε από μερικά δευτερόλεπτα μέχρι μερικά λεπτά. Περίληψη ανεπιθύμητων ενεργειών σε μορφή πίνακα Οι ακόλουθες ανεπιθύμητες ενέργειες ταξινομούνται χρησιμοποιώντας τον εξής κανόνα: πολύ συχνές ( 1/10), συχνές ( 1/100 έως <1/10), όχι συχνές ( 1/1.000 έως <1/100), σπάνιες ( 1/ έως <1/1.000) ή πολύ σπάνιες (<1/10.000). Εντός κάθε κατηγορίας συχνότητας εμφάνισης, οι ανεπιθύμητες ενέργειες παρατίθενται κατά φθίνουσα σειρά σοβαρότητας. Κατηγορία οργανικού συστήματος Ψυχιατρικές διαταραχές Διαταραχές του νευρικού συστήματος Οφθαλμικές διαταραχές Αγγειακές διαταραχές Διαταραχές του αναπνευστικού συστήματος, του θώρακα και του μεσοθωρακίου Διαταραχές του δέρματος και του υποδόριου ιστού Όχι συχνές: αϋπνία Συχνές: δυσγευσία Προτιμώμενη ορολογία MedDRA Συχνές: θαμπή όραση, πόνος του οφθαλμού, ερεθισμός του οφθαλμού, αίσθηση ξένου σώματος στους οφθαλμούς Όχι συχνές: διάβρωση του κερατοειδούς, στικτή κερατίτιδα, ξηροφθαλμία, οφθαλμικό έκκριμα, κνησμός του οφθαλμού, υπεραιμία του οφθαλμού, βλεφαρίτιδα, αλλεργική επιπεφυκίτιδα, διαταραχή του κερατοειδούς, ερύθημα του προσθίου θαλάμου, υπεραιμία του επιπεφυκότα, εφελκίδα του χείλους του βλεφάρου, ασθενωπία, μη φυσιολογικό αίσθημα στον οφθαλμό, κνησμός βλεφάρων, αλλεργική βλεφαρίτιδα, ερύθημα βλεφάρου Όχι συχνές: μειωμένη αρτηριακή πίεση Όχι συχνές: χρόνια αποφρακτική πνευμονοπάθεια, φαρυγγολαρυγγικό άλγος, ρινόρροια, βήχας Όχι συχνές: διαταραχή του τριχώματος, ομαλός λειχήνας 6
7 Περιγραφή επιλεγμένων ανεπιθύμητων ενεργειών Η δυσγευσία (πικρή ή ασυνήθιστη γεύση στο στόμα μετά την ενστάλαξη) ήταν μια συχνά αναφερόμενη συστηματική ανεπιθύμητη ενέργεια συνδεδεμένη με τη χρήση του AZARGA κατά τη διάρκεια των κλινικών δοκιμών. Είναι πιθανό να προκαλείται από το πέρασμα των οφθαλμικών σταγόνων στο ρινοφάρυγγα μέσω του ρινοδακρυϊκού πόρου και μπορεί να αποδοθεί στη βρινζολαμίδη. Η ρινοδακρυϊκή απόφραξη ή το απαλό κλείσιμο του βλεφάρου μετά την ενστάλαξη μπορεί να βοηθήσει στην ελάττωση της εμφάνισης αυτής της επίδρασης (βλ. παράγραφο 4.2). Το AZARGA περιέχει βρινζολαμίδη, η οποία είναι ένας σουλφοναμιδικός αναστολέας της καρβονικής ανυδράσης με συστηματική απορρόφηση. Οι γαστρεντερικές επιδράσεις, οι επιδράσεις στο νευρικό σύστημα, οι αιματολογικές, νεφρικές και μεταβολικές επιδράσεις συνδέονται γενικά με τους συστηματικούς αναστολείς της καρβονικής ανυδράσης. Οι ίδιοι τύποι ανεπιθύμητων ενεργειών, που μπορούν να αποδοθούν σε από του στόματος αναστολείς της καρβονικής ανυδράσης, ενδέχεται να εμφανιστούν και με την τοπική χορήγηση. Το AZARGA περιέχει βρινζολαμίδη και τιμολόλη (ως μηλεϊνική τιμολόλη). Στις επιπρόσθετες ανεπιθύμητες ενέργειες που συνδέονται με τη χρήση των μεμονωμένων συστατικών, οι οποίες παρατηρήθηκαν σε κλινικές δοκιμές και από την εμπειρία μετά την κυκλοφορία του φαρμάκου και που ενδέχεται να εμφανιστούν με το AZARGA, περιλαμβάνονται: 7
8 Κατηγορία οργανικού συστήματος Λοιμώξεις και παρασιτώσεις Διαταραχές του αιμοποιητικού και του λεμφικού συστήματος Διαταραχές του ανοσοποιητικού συστήματος Διαταραχές του μεταβολισμού και της θρέψης Ψυχιατρικές διαταραχές Διαταραχές του νευρικού συστήματος Οφθαλμικές διαταραχές Διαταραχές του ωτός και του λαβυρίνθου Βρινζολαμίδη 10 mg/ml Προτιμώμενη ορολογία MedDRA ρινοφαρυγγίτιδα, φαρυγγίτιδα, κολπίτιδα, ρινίτιδα μειωμένος αριθμός ερυθροκυττάρων, αυξημένα χλωριούχα αίματος υπερευαισθησία απάθεια, κατάθλιψη, καταθλιπτική διάθεση, μειωμένη γενετήσια ορμή, εφιάλτες, νευρικότητα υπνηλία, κινητική δυσλειτουργία, αμνησία, επηρεασμένη μνήμη, ζάλη, παραισθησία, τρόμος, κεφαλαλγία, υπαισθησία, αγευσία Κερατίτιδα, κερατοειδοπάθεια, αυξημένη σχέση θηλής/δίσκου οπτικού νεύρου, έλλειμμα του επιθηλίου του κερατοειδούς, διαταραχή του επιθηλίου του κερατοειδούς, αυξημένη ενδοφθάλμια πίεση, οφθαλμικές εναποθέσεις, χρώση κερατοειδούς, οίδημα κερατοειδούς, επιπεφυκίτιδα, φλεγμονή των μεϊβομιανών αδένων, διπλωπία, θάμβος των οφθαλμών από το ισχυρός φως, φωτοφοβία, φωτοψία, μειωμένη οπτική οξύτητα, πτερύγιο, δυσφορία του οφθαλμού, ξηρή κερατοεπιπεφυκίτιδα, υπαισθησία του οφθαλμού, μελάγχρωση στο σκληρό, κύστη υπό τον επιπεφυκότα, αυξημένη δακρύρροια, οπτική διαταραχή, οίδημα του οφθαλμού, αλλεργία του οφθαλμού, μαδάρωση, διαταραχή του βλεφάρου, οίδημα του βλεφάρου εμβοές, ίλιγγος Τιμολόλη 5 mg/ml υπογλυκαιμία κατάθλιψη εγκεφαλική ισχαιμία, αγγειακό εγκεφαλικό επεισόδιο, συγκοπή, μυασθένεια gravis, παραισθησία, κεφαλαλγία, ζάλη επιπεφυκίτιδα, διπλωπία, βλεφαρόπτωση, κερατίτιδα, οπτική διαταραχή 8
9 Καρδιακές διαταραχές Αγγειακές διαταραχές Διαταραχές του αναπνευστικού συστήματος, του θώρακα και του μεσοθωρακίου Διαταραχές του γαστρεντερικού συστήματος Διαταραχές του ήπατος και των χοληφόρων Διαταραχές του δέρματος και του υποδόριου ιστού Διαταραχές του μυοσκελετικού συστήματος και του συνδετικού ιστού Διαταραχές των νεφρών και των ουροφόρων οδών Διαταραχές του αναπαραγωγικού συστήματος και του μαστού Γενικές διαταραχές και καταστάσεις της οδού χορήγησης Κακώσεις, δηλητηριάσεις και επιπλοκές θεραπευτικών χειρισμών καρδιοαναπνευστική δυσχέρεια, στηθάγχη, βραδυκαρδία, ανώμαλος καρδιακός ρυθμός, αρρυθμία, αίσθημα παλμών, ταχυκαρδία, αυξημένος καρδιακός ρυθμός αυξημένη αρτηριακή πίεση, υπέρταση δύσπνοια, άσθμα, βρογχική υπερδραστηριότητα, επίσταξη, ερεθισμός του λαιμού, ρινική συμφόρηση, συμφόρηση της ανώτερης αναπνευστικής οδού, οπισθορρινική καταρροή, πταρμός, ξηρότητα ρινικού βλεννογόνου ξηροστομία, οισοφαγίτιδα, έμετος, διάρροια, ναυτία, δυσπεψία, άλγος άνω κοιλιακής χώρας, κοιλιακή δυσφορία, δυσφορία του στομάχου, συχνές κενώσεις, διαταραχή του γαστρεντερικού συστήματος, υπαισθησία στόματος, παραισθησία στοματική, μετεωρισμός μη φυσιολογικές δοκιμασίες ηπατικής λειτουργίας κνίδωση, κηλιδοβλατιδώδες εξάνθημα, εξάνθημα, γενικευμένος κνησμός, αλωπεκία, τάση δέρματος, δερματίτιδα, ερύθημα οσφυαλγία, μυϊκοί σπασμοί, μυαλγία, αρθραλγία, πόνος στα άκρα άλγος νεφρού, πολλακιουρία στυτική δυσλειτουργία άλγος, εξασθένιση, θωρακική δυσφορία, κόπωση, αίσθηση μη φυσιολογική, αίσθηση εκνευρισμού, ευερεθιστότητα, θωρακικό άλγος, περιφερικό οίδημα, αίσθημα κακουχίας, υπόλειμμα φαρμακευτικής αγωγής ξένο σώμα στον οφθαλμό καρδιακή ανακοπή, καρδιακή ανεπάρκεια, αρρυθμία, κολποκοιλιακός αποκλεισμός, βραδυκαρδία, αίσθημα παλμών υπόταση αναπνευστική ανεπάρκεια, βρογχόσπασμος, δύσπνοια, ρινική συμφόρηση διάρροια, ναυτία αλωπεκία, εξάνθημα εξασθένιση, θωρακικό άλγος 9
10 Παιδιατρικός πληθυσμός Το AZARGA δε συνιστάται για χρήση σε παιδιά κάτω των 18 ετών λόγω έλλειψης στοιχείων για την ασφάλεια και την αποτελεσματικότητα. 4.9 Υπερδοσολογία Δεν αναφέρθηκε καμία περίπτωση υπερδοσολογίας. Σε περίπτωση υπερδοσολογίας με τις οφθαλμικές σταγόνες AZARGA, η θεραπεία θα πρέπει να είναι συμπτωματική και υποστηρικτική. Ενδέχεται να υπάρξουν ηλεκτρολυτικές διαταραχές, ανάπτυξη οξειδωτικής κατάστασης και ενδεχομένως επιδράσεις στο κεντρικό νευρικό σύστημα. Θα πρέπει να παρακολουθούνται τα επίπεδα ηλεκτρολυτών στον ορό (ιδιαίτερα του καλίου) και τα επίπεδα ph του αίματος. Μελέτες έχουν δείξει ότι η διαπίδυση της τιμολόλης δεν είναι άμεση. 5. ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 5.1 Φαρμακοδυναμικές ιδιότητες Φαρμακοθεραπευτική κατηγορία: Aντιγλαυκωματικό σκεύασμα και μυωτικά Κωδικός ATC: S01ED51 Μηχανισμός δράσης Το AZARGA περιέχει δύο δραστικές ουσίες: τη βρινζολαμίδη και τη μηλεϊνική τιμολόλη. Αυτά τα δύο συστατικά ελαττώνουν την αυξημένη ΕΟΠ κυρίως ελαττώνοντας την έκκριση του υδατοειδούς υγρού, αλλά αυτό το κάνουν με διαφορετικούς μηχανισμούς δράσης. Η συνδυασμένη δράση αυτών των δύο δραστικών ουσιών έχει ως αποτέλεσμα την επιπλέον ελάττωση της ΕΟΠ σε σύγκριση με την κάθε μια ένωση μόνη της. Η βρινζολαμίδη είναι ένας ισχυρός αναστολέας της ανθρώπινης καρβονικής ανυδράσης II (CA-II), του κυρίαρχου ισοενζύμου στον οφθαλμό. Η αναστολή της καρβονικής ανυδράσης στις εξεργασίες του ακτινωτού σώματος του οφθαλμού ελαττώνει την έκκριση του υδατοειδούς υγρού, πιθανώς επιβραδύνοντας τη δημιουργία διττανθρακικών ιόντων με παρεπόμενη ελάττωση στη μεταφορά νατρίου και υγρών. Η τιμολόλη είναι ένας μη εκλεκτικός αδρενεργικός αναστολέας που δεν έχει ενδογενή, συμπαθομιμητική, άμεση κατασταλτική δράση στο μυοκάρδιο ή σταθεροποιητική δράση στις μεμβράνες. Μελέτες τονογραφίας και φθοριοφωτομετρίας στον άνθρωπο υποδηλώνουν ότι η κύρια δράση της συνδέεται με τον ελαττωμένο σχηματισμό υδατοειδούς υγρού και μια ελαφρά αύξηση στην ευκολία της εκροής. Φαρμακοδυναμικές επιδράσεις Κλινικές επιδράσεις: Σε μία ελεγχόμενη κλινική δοκιμή δώδεκα μηνών με ασθενείς με γλαύκωμα ανοιχτής γωνίας ή οφθαλμική υπέρταση, οι οποίοι, κατά τη γνώμη του ερευνητή, θα μπορούσαν να ωφεληθούν από μια θεραπεία συνδυασμού, και οι οποίοι είχαν μέση ενδοφθάλμια πίεση αναφοράς από 25 έως 27 mmhg, το αποτέλεσμα ελάττωσης της μέσης ενδοφθάλμιας πίεσης με AZARGA που χορηγείτο δύο φορές ημερησίως ήταν 7 έως 9 mm Hg. Η μη κατωτερότητα του AZARGA σε σύγκριση με τη δορζολαμίδη 20 mg/ml + τιμολόλη 5 mg/ml ως προς την ελάττωση της μέσης ΕΟΠ αποδείχθηκε σε όλα τα χρονικά σημεία σε όλες τις επισκέψεις. 10
11 Σε μια ελεγχόμενη κλινική μελέτη έξι μηνών με ασθενείς με γλαύκωμα ανοιχτής γωνίας ή οφθαλμική υπέρταση και μέση ενδοφθάλμια πίεση αναφοράς από 25 έως 27 mm Hg, το αποτέλεσμα ελάττωσης της μέσης ενδοφθάλμιας πίεσης με AZARGA που χορηγείτο δύο φορές την ημέρα ήταν 7 έως 9 mmhg και ήταν έως 3 mmhg μεγαλύτερο από εκείνο της βρινζολαμίδης 10 mg/ml που χορηγείτο δύο φορές ημερησίως και έως 2 mmhg μεγαλύτερο από εκείνο της τιμολόλης 5 mg/ml που χορηγείτο δύο φορές ημερησίως. Μια στατιστικά μεγαλύτερη ελάττωση της μέσης ΕΟΠ παρατηρήθηκε σε σύγκριση τόσο με τη βρινζολαμίδη όσο και με την τιμολόλη σε όλα τα χρονικά σημεία και επισκέψεις καθ όλη τη διάρκεια της μελέτης. Σε τρεις ελεγχόμενες κλινικές δοκιμές, η δυσφορία του οφθαλμού κατά την ενστάλαξη του AZARGA ήταν κατά πολύ μικρότερη από εκείνη της δορζολαμίδης 20 mg/ml + τιμολόλης 5 mg/ml. 5.2 Φαρμακοκινητικές ιδιότητες Απορρόφηση Μετά από τοπική οφθαλμική χορήγηση, η βρινζολαμίδη και η τιμολόλη απορροφώνται μέσω του κερατοειδούς και περνούν στη συστηματική κυκλοφορία. Σε μια φαρμακοκινητική μελέτη, υγιή υποκείμενα λάμβαναν από του στόματος βρινζολαμίδη (1 mg) δύο φορές ημερησίως για 2 εβδομάδες για να μειωθεί ο χρόνος επίτευξης σταθερής κατάστασης πριν την έναρξη της χορήγησης του AZARGA. Μετά από τη χορήγηση δύο φορές ημερησίως του AZARGA επί 13 εβδομάδες, οι συγκεντρώσεις της βρινζολαμίδης στα ερυθρά αιμοσφαίρια (RBC) ήταν κατά μέσο όρο 18,8 ± 3,29 µm, 18,1 ± 2,68 µm και 18,4 ± 3,01 µm στις εβδομάδες 4, 10 και 15, αντίστοιχα, υποδηλώνοντας ότι διατηρούνταν οι συγκεντρώσεις σταθερής κατάστασης της βρινζολαμίδης στα RBC. Στη σταθερή κατάσταση, μετά τη χορήγηση του AZARGA, οι μέσες τιμές C max και AUC 0-12h της τιμολόλης στο πλάσμα ήταν κατά 27% και 28% χαμηλότερες (C max : 0,824 ± 0,453 ng/ml, AUC 0-12h : 4,71 ± 4,29 ng h/ml), αντίστοιχα, σε σύγκριση με τη χορήγηση τιμολόλης 5 mg/ml (C max : 1,13 ± 0,494 ng/ml, AUC 0-12h : 6,58 ± 3,18 ng h/ml). Η χαμηλότερη συστηματική έκθεση στην τιμολόλη μετά τη χορήγηση του AZARGA δεν είναι κλινικά σχετική. Μετά τη χορήγηση του AZARGA, η μέση C max της τιμολόλης επιτεύχθηκε σε 0,79 ± 0,45 ώρες. Κατανομή Η δέσμευση της βρινζολαμίδης στις πρωτεΐνες του πλάσματος είναι μέτρια (περίπου 60%). Η βρινζολαμίδη διαχωρίζεται στα RBC λόγω της δέσμευσής της για λόγους υψηλής συγγένειας στη CA-II και σε μικρότερη έκταση στη CA-I. Ο δραστικός N-desethyl μεταβολίτης της επίσης συσωρρεύεται στα RBC όπου δεσμεύεται κυρίως στη CA-I. Η συγγένεια της βρινζολαμίδης και του μεταβολίτη με τα RBC και τη CA ιστών έχει ως αποτέλεσμα χαμηλές συγκεντρώσεις στο πλάσμα. Τα δεδομένα κατανομής στους οφθαλμικούς ιστούς σε κουνέλια έδειξαν ότι η τιμολόλη μπορεί να μετρηθεί στο υδατοειδές υγρό μέχρι 48 ώρες μετά τη χορήγηση του AZARGA. Σε σταθερή κατάσταση, η τιμολόλη ανιχνεύεται στο ανθρώπινο πλάσμα για μέχρι 12 ώρες από τη χορήγηση του AZARGA. Μεταβολισμός Οι μεταβολικές οδοί για το μεταβολισμό της βρινζολαμίδης περιλαμβάνουν N-απαλκυλίωση, O-απαλκυλίωση και οξείδωση της N-propyl πλευρικής αλυσίδας της. Η N-desethyl βρινζολαμίδη είναι ένας κύριος μεταβολίτης της βρινζολαμίδης που σχηματίζεται στους ανθρώπους, ο οποίος δεσμεύεται επίσης στη CA-I παρουσία βρινζολαμίδης και συσωρρεύεται στα RBC. Μελέτες in vitro δείχνουν ότι ο μεταβολισμός της βρινζολαμίδης περιλαμβάνει κυρίως το CYP3A4 καθώς και τουλάχιστον τέσσερα άλλα ισοένζυμα (CYP2A6, CYP2B6, CYP2C8 και CYP2C9). Η τιμολόλη μεταβολίζεται μέσω δύο οδών. Η μια οδός δίνει μια πλευρική αλυσίδα αιθανολαμίνης στο δακτύλιο θειαδιαζόλης και η άλλη δίνει μια αιθανολική πλευρική αλυσίδα στο άζωτο μορφολίνης και μια δεύτερη παρόμοια πλευρική αλυσίδα με μια καρβονυλομάδα παρακείμενη στο άζωτο. Ο μεταβολισμός της τιμολόλης διαμεσολαβείται κυρίως από το CYP2D6. 11
12 Απέκκριση Η βρινζολαμίδη αποβάλλεται κυρίως με νεφρική απέκκριση (περίπου 60%). Περίπου το 20% της δόσης υπολογίζεται ότι είναι στα ούρα ως μεταβολίτης. Η βρινζολαμίδη και η N-desethyl-βρινζολαμίδη είναι τα κυρίαρχα συστατικά που βρίσκονται στα ούρα μαζί με ίχνη (<1%) των N-desmethoxypropyl και O-desmethyl μεταβολιτών. Η τιμολόλη και οι μεταβολίτες της απεκκρίνονται κυρίως από τους νεφρούς. Περίπου 20% μιας δόσης τιμολόλης απεκκρίνεται στα ούρα αναλλοίωτη και το υπόλοιπο απεκκρίνεται στα ούρα ως μεταβολίτες. Η τιμή t 1/2 τιμολόλης του πλάσματος είναι 4,8 ώρες μετά τη χορήγηση του AZARGA. 5.3 Προκλινικά δεδομένα για την ασφάλεια Βρινζολαμίδη Τα μη κλινικά δεδομένα δεν αποκαλύπτουν ιδιαίτερο κίνδυνο με τη βρινζολαμίδη για τον άνθρωπο με βάση τις συμβατικές μελέτες φαρμακολογικής ασφάλειας, τοξικότητας επαναλαμβανόμενων δόσεων, γονοτοξικότητας και ενδεχόμενης καρκινογόνου δράσης. Μελέτες τοξικότητας επί της ανάπτυξης σε κουνέλια με από του στόματος δόσεις βρινζολαμίδης έως και 6 mg/kg/ημέρα (214 φορές μεγαλύτερη από τη συνιστώμενη ημερήσια κλινική δόση των 28 µg/kg/ημέρα) δεν αποκάλυψαν επίδραση στην ανάπτυξη του εμβρύου παρ ολη τη σημαντική τοξικότητα επί της μητέρας. Παρόμοιες μελέτες σε αρουραίους είχαν σαν αποτέλεσμα ελαφρά μειωμένη οστεοποίηση του κρανίου και του στερνιδίου των εμβρύων των οποίων οι μητέρες λάμβαναν βρινζολαμίδη σε δόσεις των 18 mg/kg/ημέρα (642 φορές μεγαλύτερη της συνιστώμενης ημερήσιας κλινικής δόσης), αλλά όχι στη δόση των 6 mg/kg/ημέρα. Αυτά τα ευρήματα παρουσιάστηκαν σε δόσεις που προκάλεσαν μεταβολική οξέωση με ελαττωμένη αύξηση σωματικού βάρους για τις μητέρες και μειωμένο βάρος στα έμβρυα. Παρατηρήθηκαν δοσοεξαρτώμενες μειώσεις του βάρους των εμβρύων των οποίων οι μητέρες λάμβαναν βρινζολαμίδη από το στόμα και κυμαίνονταν από μια ελαφρά μείωση (περίπου 5-6%) στα 2 mg/kg/ημέρα έως περίπου 14% στα 18 mg/kg/ημέρα. Κατά τη γαλουχία, το επίπεδο χωρίς ανεπιθύμητες ενέργειες για τα νεογνά ήταν 5 mg/kg/ ημέρα. Τιμολόλη Τα μη κλινικά δεδομένα δεν αποκαλύπτουν ιδιαίτερο κίνδυνο με την τιμολόλη για τον άνθρωπο με βάση τις συμβατικές μελέτες φαρμακολογικής ασφάλειας, τοξικότητας επαναλαμβανόμενων δόσεων, γονοτοξικότητας και ενδεχόμενης καρκινογόνου δράσης. Μελέτες τοξικότητας στην αναπαραγωγική ικανότητα με την τιμολόλη έδειξαν καθυστερημένη οστεοποίηση του εμβρύου σε αρουραίους χωρίς ανεπιθύμητες ενέργειες στη μεταγεννητική ανάπτυξη (στα 50 mg/kg/ημέρα ή φορές μεγαλύτερη από την ημερήσια κλινική δόση των 14 μg/kg/ημέρα) και αυξημένες απορροφήσεις εμβρύων σε κουνέλια (στα 90 mg/kg/ημέρα ή φορές μεγαλύτερη από την ημερήσια κλινική δόση). 6. ΦΑΡΜΑΚΕΥΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ 6.1 Κατάλογος εκδόχων Βενζαλκώνιο χλωριούχο Μαννιτόλη (E421) Καρβοπόλη 974P Τυλοξαπόλη Αιθυλενοδιαμινοτετραοξικό δινάτριο άλας Νάτριο χλωριούχο Υδροχλωρικό οξύ και/ή νατρίου υδροξείδιο (για ρύθμιση του ph) Κεκαθαρμένο ύδωρ 12
13 6.2 Ασυμβατότητες Δεν εφαρμόζεται. 6.3 Διάρκεια ζωής 2 χρόνια. 4 εβδομάδες μετά το πρώτο άνοιγμα. 6.4 Ιδιαίτερες προφυλάξεις κατά την φύλαξη του προϊόντος Δεν υπάρχουν ειδικές οδηγίες διατήρησης για το προϊόν αυτό. 6.5 Φύση και συστατικά του περιέκτη Στρογγυλές, αδιαφανείς φιάλες των 5 ml από πολυαιθυλένιο χαμηλής πυκνότητας με σταγονομετρικό ρύγχος και λευκό βιδωτό πώμα από πολυπροπυλένιο (DROP-TAINER) που περιέχει 5 ml εναιωρήματος. Τα κουτιά περιέχουν 1 ή 3 φιάλες. Μπορεί να μη κυκλοφορούν όλες οι συσκευασίες. 6.6 Ιδιαίτερες προφυλάξεις απόρριψης Καμία ειδική υποχρέωση. 7. ΚΑΤΟΧΟΣ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ Alcon Laboratories (UK) Ltd. Pentagon Park Boundary Way Hemel Hempstead Herts HP2 7UD Ηνωμένο Βασίλειο 8. ΑΡΙΘΜΟΣ(ΟΙ) ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 9. ΗΜΕΡΟΜΗΝΙΑ ΠΡΩΤΗΣ ΕΓΚΡΙΣΗΣ/ΑΝΑΝΕΩΣΗΣ ΤΗΣ ΑΔΕΙΑΣ 10. ΗΜΕΡΟΜΗΝΙΑ ΑΝΑΘΕΩΡΗΣΗΣ ΤΟΥ ΚΕΙΜΕΝΟΥ Λεπτομερή πληροφοριακά στοιχεία για το προϊόν είναι διαθέσιμα στην ιστοσελίδα του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMEA): 13
14 ΠΑΡΑΡΤΗΜΑ ΙΙ Α. ΚΑΤΟΧΟΣ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ ΤΩΝ ΠΑΡΤΙΔΩΝ Β. ΟΙ ΟΡΟΙ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 14
15 Α. ΚΑΤΟΧΟΣ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ ΤΩΝ ΠΑΡΤΙΔΩΝ Όνομα και διεύθυνση του παραγωγού που είναι υπεύθυνος για την αποδέσμευση των παρτίδων S.A. Alcon-Couvreur N.V. Rijksweg 14 B-2870 Puurs Βέλγιο Β. ΟΙ ΟΡΟΙ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΟΙ ΟΡΟΙ ΚΑΙ ΟΙ ΠΕΡΙΟΡΙΣΜΟΙ ΣΧΕΤΙΚΑ ΜΕ ΤΗ ΔΙΑΘΕΣΗ ΚΑΙ ΤΗ ΧΡΗΣΗ ΠΟΥ ΒΑΡΥΝΟΥΝ ΤΟΝ ΚΑΤΟΧΟ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ Φαρμακευτικό προϊόν για το οποίο απαιτείται ιατρική συνταγή. ΟΡΟΙ Η ΠΕΡΙΟΡΙΣΜΟΙ ΟΣΟΝ ΑΦΟΡΑ ΤΗΝ ΑΣΦΑΛΗ ΚΑΙ ΑΠΟΤΕΛΕΣΜΑΤΙΚΗ ΧΡΗΣΗ ΤΟΥ ΦΑΡΜΑΚΟΥ Δεν εφαρμόζεται. ΑΛΛΟΙ ΟΡΟΙ Σύστημα φαρμακοεπαγρύπνησης Ο Kάτοχος της Άδειας Κυκλοφορίας πρέπει να διασφαλίσει ότι διαθέτει και εφαρμόζει ένα σύστημα φαρμακοεπαγρύπνησης πριν και κατά τη διάρκεια της κυκλοφορίας του προϊόντος, όπως περιγράφεται στην έκδοση 4, ημερομηνίας 21 Ιουνίου 2007, που παρουσιάζεται στην Ενότητα της Αίτησης για Χορήγηση Αδείας Κυκλοφορίας. Σχέδιο Διαχείρισης Κινδύνου Ο κάτοχος της άδειας κυκλοφορίας δεσμεύεται ότι θα διεξαγάγει τις μελέτες και τις πρόσθετες δραστηριότητες φαρμακοεπαγρύπνησης που λεπτομερώς αναφέρονται στο Σχέδιο Φαρμακοεπαγρύπνησης όπως συμφωνήθηκε στην έκδοση 1, ημερομηνίας 30 Σεπτεμβρίου 2007 (με ημερομηνία εφαρμογής την 16 η Μαϊου 2008), του Σχεδίου Διαχείρισης Κινδύνου (ΣΔΚ) που παρουσιάζεται στην Ενότητα της Αίτησης για Χορήγηση Αδείας Κυκλοφορίας και σε οποιεσδήποτε μετέπειτα αναθεωρήσεις του ΣΔΚ που συμφωνούνται με την CHMP. Σύμφωνα με την κατευθεντήρια γραμμή της CHMP αναφορικά με τα Συστήματα Διαχείρισης Κινδύνου για φαρμακευτικά προϊόντα ανθρώπινης χρήσης, το αναθεωρημένο ΣΔΚ πρέπει να υποβάλλεται ταυτόχρονα με την επόμενη Έκθεση Περιοδικής Παρακολούθησης Ασφάλειας (ΕΠΠΑ). Επιπρόσθετα, ένα αναθεωρημένο ΣΔΚ πρέπει να υποβάλλεται: Όταν λαμβάνονται νέες πληροφορίες που δυνατόν να επηρεάσουν τις υπάρχουσες προδιαγραφές ασφάλειας, το σχέδιο φαρμακοεπαγρύπνησης ή τις δραστηριότητες ελαχιστοποίησης κινδύνου. Μέσα σε 60 ημέρες από την επίτευξη ενός σημαντικού ορόσημου (φαρμακοεπαγρύπνησης ή ελαχιστοποίησης κινδύνου) Κατόπιν αιτήματος του EMEA 15
16 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 16
17 Α. ΕΠΙΣΗΜΑΝΣΗ 17
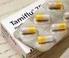
18 ΕΝΔΕΙΞΕΙΣ ΠΟΥ ΠΡΕΠΕΙ ΝΑ ΑΝΑΓΡΑΦΟΝΤΑΙ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΥΣΚΕΥΑΣΙΑ ΚΟΥΤΙ ΓΙΑ ΕΝΑ ΜΟΝΟ ΦΙΑΛΙΔΙΟ ΤΩΝ 5 ml + ΚΟΥΤΙ ΓΙΑ 3 ΦΙΑΛΙΔΙΑ ΤΩΝ 5 ml 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, εναιώρημα Βρινζολαμίδη/Τιμολόλη 2. ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΗ ΟΥΣΙΑ 1 ml εναιωρήματος περιέχει 10 mg βρινζολαμίδης και 5 mg τιμολόλης (ως μηλεϊνική τιμολόλη). 3. ΚΑΤΑΛΟΓΟΣ ΕΚΔΟΧΩΝ Περιέχει: βενζαλκώνιο χλωριούχο, μαννιτόλη (Ε421), καρβοπόλη 974P, τυλοξαπόλη, αιθυλενοδιαμινοτετραοξικό δινάτριο άλας, νάτριο χλωριούχο, υδροχλωρικό οξύ και/ή νατρίου υδροξείδιο (για ρύθμιση του ph), κεκαθαρμένο ύδωρ. Βλέπε το φύλλο οδηγιών χρήσης για περισσότερες πληροφορίες. 4. ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ KAI ΠEPIEXOMENO Οφθαλμικές σταγόνες, εναιώρημα 1 x 5 ml 3 x 5 ml 5. ΤΡΟΠΟΣ ΚΑΙ ΟΔΟΣ ΧΟΡΗΓΗΣΗΣ Οφθαλμική χρήση. Ανακινήστε καλά πριν τη χρήση. Διαβάστε το φύλλο οδηγιών χρήσης πριν από τη χορήγηση. 6. ΕΙΔΙΚΗ ΠΡΟΕΙΔΟΠΟΙΗΣΗ ΣΥΜΦΩΝΑ ΜΕ ΤΗΝ ΟΠΟΙΑ ΤΟ ΦΑΡΜΑΚEYTIKΟ ΠPOΪON ΠPEΠEI NA ΦYΛAΣΣETAI ΣE ΘEΣH, THN OΠOIA ΔEN BΛEΠOYN KAI ΔEN ΠPOΣEΓΓIZOYN TA ΠAIΔIA Να φυλάσσεται σε θέση την οποία δε βλέπουν και δεν προσεγγίζουν τα παιδιά. 7. ΑΛΛΗ(ΕΣ) ΕΙΔΙΚΗ(ΕΣ) ΠΡΟΕΙΔΟΠΟΙΗΣΗ(ΕΙΣ), ΕΑΝ ΕΙΝΑΙ ΑΠΑΡΑΙΤΗΤH(ΕΣ) 18
19 8. ΗΜΕΡΟΜΗΝΙΑ ΛΗΞΗΣ ΛΗΞΗ: Απορρίπτεται 4 εβδομάδες μετά το πρώτο άνοιγμα. Ανοίχθηκε: 9. ΕΙΔΙΚΕΣ ΣΥΝΘΗΚΕΣ ΦYΛAΞΗΣ 10. ΙΔΙΑΙΤΕΡΕΣ ΠΡΟΦΥΛΑΞΕΙΣ ΓΙΑ ΤΗΝ ΑΠΟΡΡΙΨΗ ΤΩΝ ΜΗ ΧΡΗΣΙΜΟΠΟΙHΘENTΩΝ ΦΑΡΜΑΚΕΥΤΙΚΩΝ ΠΡΟΪΟΝΤΩΝ Ή ΤΩΝ ΥΠΟΛΕΙΜΜΑΤΩΝ ΠΟΥ ΠΡΟΕΡΧΟΝΤΑΙ ΑΠΟ AYΤΑ, ΕΦΟΣΟΝ ΑΠΑΙΤΕΙΤΑΙ 11. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ Alcon Laboratories (UK) Ltd. Pentagon Park Boundary Way Hemel Hempstead Herts HP2 7UD Ηνωμένο Βασίλειο 12. ΑΡΙΘΜΟΣ(ΟΙ) ΚΥΚΛΟΦΟΡΙΑΣ EU/0/00/000/001 1 x 5 ml EU/0/00/000/002 3 x 5 ml 13. ΑΡΙΘΜΟΣ ΠΑΡΤΙΔΑΣ Παρτίδα: 14. ΓΕΝΙΚΗ ΚΑΤΑΤΑΞΗ ΓΙΑ ΤΗ ΔΙΑΘΕΣΗ Φαρμακευτικό προϊόν για το οποίο απαιτείται ιατρική συνταγή. 15. OΔHΓIEΣ XPHΣHΣ 16 ΠΛΗΡΟΦΟΡΙΕΣ ΣΕ BRAILLE azarga 19
20 ΕΛΑΧΙΣΤΕΣ ΕΝΔΕΙΞΕΙΣ ΠΟΥ ΠΡΕΠΕΙ ΝΑ ΑΝΑΓΡΑΦΟΝΤΑΙ ΣΤΙΣ ΜΙΚΡΕΣ ΣΤΟΙΧΕΙΩΔΕΙΣ ΣΥΣΚΕΥΑΣΙΕΣ ΕΤΙΚΕΤΑ ΦΙΑΛΗΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΟΔΟΣ ΧΟΡΗΓΗΣΗΣ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες Βρινζολαμίδη/Τιμολόλη Οφθαλμική χρήση 2. ΤΡΟΠΟΣ ΧΟΡΗΓΗΣΗΣ Διαβάστε το φύλλο οδηγιών χρήσης πριν από τη χορήγηση. 3. ΗΜΕΡΟΜΗΝΙΑ ΛΗΞΗΣ ΛΗΞΗ: Απορρίπτεται 4 εβδομάδες μετά το πρώτο άνοιγμα. Ανοίχθηκε: 4. ΑΡΙΘΜΟΣ ΠΑΡΤΙΔΑΣ Παρτίδα: 5. ΠΕΡΙΕΧΟΜΕΝΟ ΚΑΤΑ ΒΑΡΟΣ, ΚΑΤ ΟΓΚΟ Ή ΚΑΤΑ ΜΟΝΑΔΑ 5 ml 6 ΑΛΛΑ ΣΤΟΙΧΕΙΑ 20
21 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 21
22 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, εναιώρημα Βρινζολαμίδη/Τιμολόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο. - Φυλάξτε αυτό το φύλλο οδηγιών χρήσης. Ίσως χρειαστεί να το διαβάσετε ξανά. - Εάν έχετε περαιτέρω απορίες, ρωτήστε το γιατρό ή το φαρμακοποιό σας. - Η συνταγή για αυτό το φάρμακο χορηγήθηκε για σας. Δεν πρέπει να δώσετε το φάρμακο σε άλλους. Μπορεί να τους προκαλέσει βλάβη, ακόμα και όταν τα συμπτώματά τους είναι ίδια με τα δικά σας. - Αν κάποια ανεπιθύμητη ενέργεια γίνεται σοβαρή ή αν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια που δεν αναφέρεται στο παρόν φύλλο οδηγιών, παρακαλείσθε να ενημερώσετε το γιατρό ή το φαρμακοποιό σας. Το παρόν φύλλο οδηγιών χρήσης περιέχει: 1. Τι είναι το AZARGA και ποια είναι η χρήση του 2. Τι πρέπει να γνωρίζετε προτού χρησιμοποιήσετε το AZARGA 3. Πώς να χρησιμοποιήσετε το AZARGA 4. Πιθανές ανεπιθύμητες ενέργειες 5. Πώς να φυλάσσεται το AZARGA 6. Λοιπές πληροφορίες 1. ΤΙ ΕΙΝΑΙ ΤΟ AZARGA ΚΑΙ ΠΟΙΑ ΕΙΝΑΙ Η ΧΡΗΣΗ ΤΟΥ Το AZARGA χρησιμοποιείται για την αντιμετώπιση της υψηλής πίεσης των ματιών. Η πίεση αυτή μπορεί να οδηγήσει σε μια ασθένεια που ονομάζεται γλαύκωμα. Το AZARGA αποτελεί ένα συνδυασμό θεραπειών για το γλαύκωμα. Περιέχει δύο δραστικές ουσίες που συνεργάζονται για να μειώνουν την πίεση μέσα στο μάτι. 2. ΤΙ ΠΡΕΠΕΙ ΝΑ ΓΝΩΡΙΖΕΤΕ ΠΡΟΤΟΥ ΧΡΗΣΙΜΟΠΟΙΗΣΕΤΕ ΤΟ AZARGA Μη χρησιμοποιήσετε το AZARGA Σε περίπτωση αλλεργίας σε οποιοδήποτε από τα συστατικά του AZARGA. Για ένα πλήρη κατάλογο των συστατικών, βλ. παράγραφο 6. Σε περίπτωση που έχετε αναπνευστικά προβλήματα όπως άσθμα, βρογχίτιδα ή άλλους τύπους αναπνευστικών προβλημάτων. Σε περίπτωση που έχετε αργό καρδιακό παλμό, καρδιακή ανεπάρκεια ή διαταραχές στον καρδιακό ρυθμό. Σε περίπτωση που έχετε υπερβολική οξύτητα στο αίμα σας (μια κατάσταση που ονομάζεται υπερχλωραιμική οξέωση). Σε περίπτωση που έχετε σοβαρά προβλήματα με τα νεφρά σας. Προσέξτε ιδιαιτέρως με το AZARGA εάν έχετε στηθάγχη (πόνους στο στήθος), προβλήματα στην κυκλοφορία ή χαμηλή πίεση. Το AZARGA μπορεί να επιδεινώσει οποιαδήποτε από τις καταστάσεις αυτές. Αν ανησυχείτε για τυχόν αλλαγές στα συμπτώματα αυτά, ζητήστε τη συμβουλή του γιατρού σας το συντομότερο δυνατό. 22
23 εάν εμφανίσετε οποιαδήποτε σοβαρή αλλεργική αντίδραση ενώ χρησιμοποιείτε το AZARGA, όποια κι αν είναι η αιτία, η θεραπεία με αδρεναλίνη ενδέχεται να μην είναι αποτελεσματική. Επομένως, όταν λαμβάνετε οποιαδήποτε άλλη θεραπεία, ενημερώστε τον επαγγελματία υγείας ότι λαμβάνετε το AZARGA. εάν έχετε διαβήτη. Το AZARGA μπορεί να συγκαλύψει συμπτώματα χαμηλού σακχάρου στο αίμα (υπογλυκαιμία) όπως τρεμούλα και ζάλη, επομένως θα πρέπει να το χρησιμοποιείτε προσεκτικά. σε περίπτωση που έχετε προβλήματα με το συκώτι σας. Μιλήστε με το γιατρό σας. σε περίπτωση που έχετε ξηροφθαλμία ή προβλήματα κερατοειδούς. Μιλήστε με το γιατρό σας. To AZARGA δεν συνιστάται για χρήση σε παιδιά κάτω των 18 ετών. Χρήση άλλων φαρμάκων Το AZARGA μπορεί να επηρεάσει άλλα φάρμακα που παίρνετε ή να επηρεαστεί από αυτά, συμπεριλαμβανομένων οφθαλμικών σταγόνων για τη θεραπεία του γλαυκώματος. Ενημερώστε το γιατρό σας αν παίρνετε ή σκοπεύετε να πάρετε φάρμακα για ελάττωση της πίεσης του αίματος, φάρμακα για την καρδιά, φάρμακα για την αντιμετώπιση του διαβήτη ή φάρμακα για τη θεραπεία του έλκους του στομάχου ή αντιμυκητιασικά φάρμακα, αντιιικά ή αντιβιοτικά. Παρακαλείσθε να ενημερώσετε το γιατρό ή το φαρμακοποιό σας εάν παίρνετε ή έχετε πάρει πρόσφατα οποιαδήποτε άλλα φάρμακα, ακόμα και αυτά που δεν σας έχουν χορηγηθεί με συνταγή. Κύηση και θηλασμός Δεν πρέπει να χρησιμοποιείτε το AZARGA αν είστε έγκυος ή πιστεύετε ότι μπορεί να μείνετε έγκυος. Μιλήστε με το γιατρό σας πριν να χρησιμοποιήσετε το AZARGA. Εάν θηλάζετε, μπορείτε να χρησιμοποιήσετε το AZARGA. Ζητήστε τη συμβουλή του γιατρού σας προτού πάρετε οποιοδήποτε φάρμακο. Οδήγηση και χειρισμός μηχανών Μην οδηγείτε ή μη χρησιμοποιείτε μηχανές μέχρι να είναι καθαρή η όρασή σας. Μπορεί να αντιληφθείτε ότι η όρασή σας είναι θολή για λίγη ώρα ακριβώς μετά τη χρήση του AZARGA. Ένα από τα δραστικά συστατικά ενδέχεται να επηρεάσει την ικανότητα ηλικιωμένων ασθενών για εκτέλεση εργασιών που απαιτούν νοητική εγρήγορση ή/και σωματικό συντονισμό. Αν έχετε επηρεαστεί, προσέξτε όταν οδηγείτε ή χρησιμοποιείτε μηχανές. Σημαντικές πληροφορίες σχετικά με ορισμένα συστατικά του AZARGA Στο AZARGA υπάρχει ένα συντηρητικό (βενζαλκώνιο χλωριούχο) που μπορεί να αποχρωματίσει τους μαλακούς φακούς επαφής και μπορεί να προκαλέσει ερεθισμό στα μάτια. Επομένως, μη φοράτε φακούς επαφής ενώ χρησιμοποιείτε το AZARGA. Περιμένετε 15 λεπτά, αφού χρησιμοποιήσετε το AZARGA, πριν ξαναφορέσετε τους φακούς σας. 3. ΠΩΣ ΝΑ ΧΡΗΣΙΜΟΠΟΙΗΣΕΤΕ ΤΟ AZARGA Πάντοτε να χρησιμοποιείτε το AZARGA αυστηρά σύμφωνα με τις οδηγίες του γιατρού σας. Εάν έχετε αμφιβολίες, ρωτήστε τον γιατρό ή τον φαρμακοποιό σας. 23
24 Η συνήθης δόση είναι Ενήλικες: Μια σταγόνα στον(στους) πάσχοντα(ες) οφθαλμό(ούς), δύο φορές την ημέρα, το πρωί και το βράδυ. Να χρησιμοποιείτε το AZARGA και στα δύο μάτια μόνον αν σας το έχει πει ο γιατρός σας. Να χρησιμοποιείτε το φάρμακο για όσο χρονικό διάστημα σας έχει πει ο γιατρός σας Πάρτε τη φιάλη με το AZARGA και έναν καθρέπτη. Πλύνετε τα χέρια σας. Ανακινήστε καλά πριν τη χρήση. Ξεβιδώστε το πώμα της φιάλης. Κρατήστε τη φιάλη, με το ρύγχος προς τα κάτω, μεταξύ του αντίχειρα και των δακτύλων σας. Κρατήστε το κεφάλι σας γερμένο προς τα πίσω. Τραβήξτε προς τα κάτω το βλέφαρό σας με ένα καθαρό δάχτυλο, μέχρι να δημιουργηθεί μια "τσέπη" μεταξύ του βλεφάρου και του ματιού σας. Η σταγόνα θα πέσει μέσα εδώ (εικόνα 1). Φέρτε το ρύγχος της φιάλης κοντά στο μάτι. Χρησιμοποιήστε τον καθρέφτη, αν βοηθάει. Μην αγγίζετε το μάτι ή το βλέφαρό σας, τις γύρω περιοχές ή άλλες επιφάνειες με το ρύγχος. Μπορεί να μολυνθούν οι σταγόνες. Πιέστε απαλά στη βάση της φιάλης για να απελευθερώνετε μία σταγόνα AZARGA τη φορά. Μην σφίγγετε υπερβολικά τη φιάλη. Είναι σχεδιασμένη με τέτοιο τρόπο ώστε να χρειάζεται μόνο μια απαλή πίεση στο κάτω μέρος του (εικόνα 2). Μετά τη χρήση του AZARGA, πιέστε με το δάχτυλό σας τη γωνία του ματιού σας που είναι κοντά στη μύτη σας (εικόνα 3). Αυτό εμποδίζει το AZARGA να περάσει στο υπόλοιπο σώμα. Αν βάζετε σταγόνες και στα δύο μάτια, επαναλάβετε τη διαδικασία για το άλλο σας μάτι. Βιδώστε καλά το πώμα στη φιάλη αμέσως μετά τη χρήση. Χρησιμοποιήστε ολόκληρη τη μία φιάλη πριν ανοίξετε την επόμενη. Αν μια σταγόνα ξεφύγει από το μάτι σας, προσπαθήστε πάλι. Αν χρησιμοποιήσετε μεγαλύτερη ποσότητα AZARGA από την κανονική, ξεπλύνετε το μάτι σας με ζεστό νερό. Μη βάζετε άλλες σταγόνες μέχρι να έρθει η ώρα της επόμενης τακτικής σας δόσης. Αν ξεχάσετε να χρησιμοποιήσετε το AZARGA, συνεχίστε με την επόμενη δόση σύμφωνα με το κανονικό πρόγραμμά σας. Μην πάρετε διπλή δόση για να αναπληρώσετε τη δόση που ξεχάσατε. Να μη χρησιμοποιείτε πάνω από μία σταγόνα στον πάσχοντα οφθαλμό (ή οφθαλμούς) δύο φορές την ημέρα. Αν σταματήσετε να χρησιμοποιείτε το AZARGA χωρίς να μιλήσετε με το γιατρό σας, η πίεση στο μάτι σας δε θα είναι υπό έλεγχο, κάτι που μπορεί να οδηγήσει σε απώλεια της όρασης. Αν χρησιμοποιείτε άλλες οφθαλμικές σταγόνες, αφήστε διάστημα τουλάχιστον 5 λεπτών μεταξύ της ενστάλαξης του AZARGA και των άλλων σταγόνων. Εάν έχετε περισσότερες ερωτήσεις σχετικά με τη χρήση αυτού του προϊόντος, ρωτήστε το γιατρό ή το φαρμακοποιό σας. 24
25 4. ΠΙΘΑΝΕΣ ΑΝΕΠΙΘΥΜΗΤΕΣ ΕΝΕΡΓΕΙΕΣ Όπως όλα τα φάρμακα, έτσι και το AZARGA μπορεί να προκαλέσει ανεπιθύμητες ενέργειες αν και δεν παρουσιάζονται σε όλους τους ανθρώπους. Συνήθως μπορείτε να συνεχίσετε να βάζετε τις σταγόνες, εκτός αν οι αντιδράσεις είναι σοβαρές. Αν ανησυχείτε, μιλήστε με το γιατρό ή το φαρμακοποιό σας. Οι ακόλουθες ανεπιθύμητες ενέργειες έχουν παρατηρηθεί με το AZARGA: Συχνές ανεπιθύμητες ενέργειες (επηρεάζουν 1 έως 10 χρήστες στους 100) Αντιδράσεις στο μάτι: θολή όραση, ερεθισμός του ματιού, πόνος στο μάτι, μη φυσιολογική αίσθηση στα μάτια Γενικές ανεπιθύμητες ενέργειες: άσχημη γεύση Όχι συχνές ανεπιθύμητες ενέργειες (επηρεάζουν 1 έως 10 χρήστες στους 1.000) Αντιδράσεις στο μάτι: φλεγμονή στην επιφάνεια του ματιού με επιφανειακή βλάβη, φλεγμονή μέσα στο μάτι, κόκκινο μάτι, φαγούρα στο μάτι, φαγούρα στο βλέφαρο, ερυθρότητα, πρήξιμο ή δημιουργία κρούστας, εκκρίσεις από το μάτι, αλλεργία στο μάτι, ξηροφθαλμία, κουρασμένα μάτια Γενικές ανεπιθύμητες ενέργειες: χρόνια πνευμονοπάθεια, ελαττωμένη πίεση αίματος, ερεθισμός του λαιμού, βήχας, δυσκολία στον ύπνο, φλεγμονή στο δέρμα, ερυθρότητα ή φαγούρα, ρινική καταρροή, διαταραχή τριχοφυΐας Επιπλέον: Το AZARGA είναι ένας συνδυασμός 2 φαρμάκων που κυκλοφορούν στην αγορά. Ανεπιθύμητες ενέργειες που έχουν παρατηρηθεί με τα μεμονωμένα φάρμακα και οι οποίες μπορεί να προκύψουν με το AZARGA είναι οι ακόλουθες: Αντιδράσεις στο μάτι: βλάβη στο οπτικό νεύρο, αυξημένη πίεση στο μάτι, ιζήματα στην επιφάνεια του ματιού, διαταραχή του κερατοειδούς, μειωμένη αίσθηση στο μάτι, φλεγμονή ή λοίμωξη του επιπεφυκότα, μη φυσιολογική, διπλή ή μειωμένη όραση, αυξημένη μελάγχρωση του ματιού, ανάπτυξη στην επιφάνεια του ματιού, αυξημένη παραγωγή δακρύων, πρήξιμο του ματιού, ευαισθησία στο φως, μειωμένη ανάπτυξη ή αριθμός βλεφαρίδων, πτώση βλεφάρων, φλεγμονή των αδένων του βλεφάρου Γενικές ανεπιθύμητες ενέργειες: Καρδιά και κυκλοφορικό: αλλαγές στον καρδιακό παλμό ή ρυθμό, πόνος στο στήθος, ελαττωμένη καρδιακή λειτουργία, σταμάτημα της καρδιάς, αυξημένη πίεση αίματος, μειωμένη ροή του αίματος προς τον εγκέφαλο, αγγειακό εγκεφαλικό επεισόδιο, πρήξιμο των άκρων Αναπνευστικό: αγκομαχητό ή δυσκολία στην αναπνοή, συμπτώματα κρυολογήματος, συμφόρηση στο στήθος, λοίμωξη στην κοιλότητα της μύτης, φτέρνισμα, μπουκωμένη μύτη, ξηρότητα μύτης, αιμορραγία της μύτης, άσθμα Νευρικό σύστημα και γενικές διαταραχές: κατάθλιψη, δυσκολία με τη μνήμη, πονοκέφαλος, νευρικότητα, ευερεθιστότητα, κούραση, τρεμούλα, μη φυσιολογική διάθεση, λιποθυμία, ζάλη, υπνηλία, γενικευμένη ή σοβαρή αδυναμία. 25
26 Γαστρεντερικό: ναυτία, έμετος, διάρροια, αέρια από τα έντερα ή κοιλιακός πόνος, φλεγμονή στο λαιμό, ξηροστομία ή μη φυσιολογική αίσθηση στο στόμα, μειωμένη αίσθηση γεύσης, βαρυστομαχιά, πόνος στο στομάχι. Αίμα: μη φυσιολογικές εξετάσεις αίματος για τη λειτουργία του συκωτιού, αυξημένα επίπεδα χλωρίου στο αίμα, ή μειωμένος αριθμός ερυθρών αιμοσφαιρίων στις αιματολογικές εξετάσεις Αλλεργία: αυξημένα αλλεργικά συμπτώματα Αυτί: κουδούνισμα στα αυτιά, αίσθημα στροβιλισμού ή ζάλης Δέρμα: φαγούρα, εξάνθημα, μη φυσιολογική ή μειωμένη αίσθηση στο δέρμα, απώλεια τριχών Μυϊκό: γενικευμένος πόνος στην πλάτη, στις αρθρώσεις ή στους μύες, μυϊκοί σπασμοί, πόνος στα άκρα, μυική αδυναμία Νεφρά: πόνος νεφρών όπως ο πόνος χαμηλά στην πλάτη, συχνή ούρηση Αναπαραγωγή: μειωμένη σεξουαλική επιθυμία, δυσκολία στη σεξουαλική λειτουργία στους άνδρες Μεταβολισμός: χαμηλή περιεκτικότητα σακχάρου στο αίμα Αν κάποια ανεπιθύμητη ενέργεια γίνεται σοβαρή ή αν παρατηρήσετε κάποια ανεπιθύμητη ενέργεια που δεν αναφέρεται στο παρόν φύλλο οδηγιών, παρακαλείσθε να ενημερώσετε το γιατρό ή το φαρμακοποιό σας. 5. ΠΩΣ ΝΑ ΦΥΛΑΣΣΕΤΑΙ ΤΟ AZARGA Να φυλάσσεται σε μέρη που δεν το φθάνουν και δεν το βλέπουν τα παιδιά. Να μη χρησιμοποιείτε το AZARGA μετά την ημερομηνία λήξης που αναφέρεται στη φιάλη και το κουτί μετά τη ΛΗΞΗ. Η ημερομηνία λήξης είναι η τελευταία ημέρα του μήνα που αναφέρεται. Δεν υπάρχουν ειδικές οδηγίες διατήρησης για το προϊόν αυτό. Πρέπει να πετάτε τη φιάλη 4 εβδομάδες μετά το πρώτο άνοιγμά της, για να αποφύγετε τις μολύνσεις και να χρησιμοποιείτε μία νέα φιάλη. Σημειώστε την ημερομηνία που την ανοίξατε στον κατάλληλο χώρο της ετικέτας της φιάλης και του κουτιού. Τα φάρμακα δεν πρέπει να απορρίπτονται στο νερό της αποχέτευσης ή στα σκουπίδια. Ρωτήστε το φαρμακοποιό σας πώς να πετάξετε τα φάρμακα που δεν χρειάζονται πια. Αυτά τα μέτρα θα βοηθήσουν στην προστασία του περιβάλλοντος. 6. ΛΟΙΠΕΣ ΠΛΗΡΟΦΟΡΙΕΣ Τι περιέχει το AZARGA Οι δραστικές ουσίες είναι η βρινζολαμίδη και η τιμολόλη. Ένα ml εναιωρήματος περιέχει 10 mg βρινζολαμίδης και 5 mg τιμολόλης. Τα άλλα συστατικά είναι βενζαλκώνιο χλωριούχο, καρβοπόλη 974P, αιθυλενοδιαμινοτετραοξικό δινάτριο άλας, μαννιτόλη (E421), κεκαθαρμένο νερό, νάτριο χλωριούχο, τυλοξαπόλη, υδροχλωρικό οξύ και/ή νατρίου υδροξείδιο. 26
27 Προστίθενται ελάχιστες ποσότητες υδροχλωρικού οξέος και/ή νατρίου υδροξείδιο για διατήρηση της οξύτητας (επίπεδα ph) σε φυσιολογικά επίπεδα. Εμφάνιση του AZARGA και περιεχόμενο της συσκευασίας Το AZARGA είναι ένα υγρό (λευκό έως υπόλευκο ομοιογενές εναιώρημα) που παρέχεται σε συσκευασία η οποία περιλαμβάνει μία πλαστική φιάλη των 5 ml με βιδωτό πώμα ή σε συσκευασία που περιλαμβάνει τρεις φιάλες των 5 ml. Ενδέχεται να μη διατίθενται όλα τα μεγέθη συσκευασίας στην αγορά. Κάτοχος άδειας κυκλοφορίας Alcon Laboratories (UK) Ltd. Pentagon Park Boundary Way Hemel Hempstead Herts HP2 7UD Ηνωμένο Βασίλειο Παραγωγός S.A. Alcon-Couvreur N.V Rijksweg 14 B-2870 Puurs Βέλγιο 27
28 Για οποιαδήποτε πληροφορία σχετικά με το παρόν φαρμακευτικό προϊόν, παρακαλείστε να απευθυνθείτε στον τοπικό αντιπρόσωπο του κατόχου της άδειας κυκλοφορίας. België/Belgique/Belgien Luxembourg/Luxemburg SA Alcon-Couvreur NV + 32 (0) (België/Belgique/Belgien) България Алкон България ЕООД Česká republika Alcon Pharmaceuticals (Czech Republic) s.r.o Danmark Alcon Danmark A/S Deutschland Alcon Pharma GmbH + 49 (0) Ελλάδα Κύπρος Άλκον Λαμποράτορις Ελλάς ΑΕΒΕ (Ελλάδα) Eesti Alcon Eesti España Alcon Cusí, S.A France Laboratoires Alcon + 33 (0) Ireland Malta United Kingdom Alcon Laboratories (UK) Ltd (0) (United Kingdom) Ísland K. Pétursson ehf Lietuva Alcon Pharmaceuticals Ltd. atstovybė Magyarország Alcon Hungária Gyógyszerkereskedelmi Kft Nederland Alcon Nederland BV + 31 (0) Norge Alcon Norge AS Österreich Alcon Ophthalmika GmbH + 43 (0) Polska Alcon Polska Sp. z o.o Portugal Alcon Portugal Produtos e Equipamentos Oftalmológicos, Lda România S.C. Alcon Romania S.R.L. : Slovenija Alcon d.o.o Slovenská Republika Alcon Pharmaceuticals Ltd oz Suomi/Finland Alcon Finland Oy (0)
29 Italia Alcon Italia S.p.A Sverige Alcon Sverige AB + 46 (0) E-post: receptionen@alconlabs.com Latvija Alcon Pharmaceuticals Ltd Το παρόν φύλλο οδηγιών χρήσης εγκρίθηκε για τελευταία φορά στις Λεπτομερή πληροφοριακά στοιχεία για το προϊόν είναι διαθέσιμα στην ιστοσελίδα του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMEA): 29
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Nasoxyl 0.05% nasal drops Ξυλομεταζολίνη HCl
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Nasoxyl 0.05% nasal drops Ξυλομεταζολίνη HCl Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, διότι περιέχει πληροφορίες που είναι σημαντικές για σας.
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Nasoxyl 0.05% nasal drops Ξυλομεταζολίνη HCl Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, διότι περιέχει πληροφορίες που είναι σημαντικές για σας.
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml εναιωρήματος
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml εναιωρήματος
ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ Α. ΕΠΙΣΗΜΑΝΣΗ 1 ΕΞΩΤΕΡΙΚΗ ΣΥΣΚΕΥΑΣΙΑ, 5 ml EMADINE 0,05% β/ο Οφθαλμικές Σταγόνες, Διάλυμα Emedastine 0,05% β/ο (ως difumarate). 5 ml Χλωριούχο βενζαλκόνιο
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ Α. ΕΠΙΣΗΜΑΝΣΗ 1 ΕΞΩΤΕΡΙΚΗ ΣΥΣΚΕΥΑΣΙΑ, 5 ml EMADINE 0,05% β/ο Οφθαλμικές Σταγόνες, Διάλυμα Emedastine 0,05% β/ο (ως difumarate). 5 ml Χλωριούχο βενζαλκόνιο
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Nasoxyl 0.1% nasal spray Ξυλομεταζολίνη HCl
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Nasoxyl 0.1% nasal spray Ξυλομεταζολίνη HCl Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, διότι περιέχει πληροφορίες που είναι σημαντικές για σας.
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Nasoxyl 0.1% nasal spray Ξυλομεταζολίνη HCl Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, διότι περιέχει πληροφορίες που είναι σημαντικές για σας.
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Cetirizine Dihydrochloride
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Pevison (1% + 0,1%) κρέμα Econazole nitrate + triamcinolone acetonide Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Pevison (1% + 0,1%) κρέμα Econazole nitrate + triamcinolone acetonide Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Aflen 300 mg καψάκια σκληρά Triflusal Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Aflen 300 mg καψάκια σκληρά Triflusal Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5mg/ml πόσιμες σταγόνες, διάλυμα Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5mg/ml πόσιμες σταγόνες, διάλυμα Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ PEVARYL Kρέμα 1% w/w Νιτρική εκοναζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ PEVARYL Kρέμα 1% w/w Νιτρική εκοναζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 TOBREX 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Τ Ο Β R Ε Χ Οφθαλμικές σταγόνες, διάλυμα 0,3% 1.2 Σύνθεση: Δραστική ουσία: Tobramycin (Τομπραμυκίνη) Έκδοχα: Benzalkonium chloride, Boric acid,
TOBREX 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Τ Ο Β R Ε Χ Οφθαλμικές σταγόνες, διάλυμα 0,3% 1.2 Σύνθεση: Δραστική ουσία: Tobramycin (Τομπραμυκίνη) Έκδοχα: Benzalkonium chloride, Boric acid,
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ERRKES. Οφθαλμικές σταγόνες, διάλυμα
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CromoHEXAL eye drops Νατριούχος Χρωμογλυκίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CromoHEXAL eye drops Νατριούχος Χρωμογλυκίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CromoHEXAL eye drops Νατριούχος Χρωμογλυκίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ IRBEPRESS 75 mg, 150 mg, 300 mg δισκία Ιρβεσαρτάνη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ IRBEPRESS 75 mg, 150 mg, 300 mg δισκία Ιρβεσαρτάνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ IRBEPRESS 75 mg, 150 mg, 300 mg δισκία Ιρβεσαρτάνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. Φυλάξτε
B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 29 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Parsabiv 2,5 mg ενέσιμο διάλυμα Parsabiv 5 mg ενέσιμο διάλυμα Parsabiv 10 mg ενέσιμο διάλυμα etelcalcetide Το φάρμακο αυτό τελεί
B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 29 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Parsabiv 2,5 mg ενέσιμο διάλυμα Parsabiv 5 mg ενέσιμο διάλυμα Parsabiv 10 mg ενέσιμο διάλυμα etelcalcetide Το φάρμακο αυτό τελεί
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Vasexten 10, 10 mg καψάκια ελεγχόμενης αποδέσμευσης Vasexten 20, 20 mg καψάκια ελεγχόμενης αποδέσμευσης βαρνιδιπίνη υδροχλωρική Διαβάστε προσεκτικά ολόκληρο
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Vasexten 10, 10 mg καψάκια ελεγχόμενης αποδέσμευσης Vasexten 20, 20 mg καψάκια ελεγχόμενης αποδέσμευσης βαρνιδιπίνη υδροχλωρική Διαβάστε προσεκτικά ολόκληρο
ΦΥΛΛΟ Ο ΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ. ΒΕΤΑVΕRΤ 24 mg δισκία. ιϋδροχλωρική Βηταϊστίνη
 ΦΥΛΛΟ Ο ΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ ΒΕΤΑVΕRΤ 24 mg δισκία ιϋδροχλωρική Βηταϊστίνη ιαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, προτου αρχίσετε να λαµβάνετε αυτό το φάρµακo. Φυλάξτε αυτό το φύλλο οδηγιών
ΦΥΛΛΟ Ο ΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ ΒΕΤΑVΕRΤ 24 mg δισκία ιϋδροχλωρική Βηταϊστίνη ιαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, προτου αρχίσετε να λαµβάνετε αυτό το φάρµακo. Φυλάξτε αυτό το φύλλο οδηγιών
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Vimpat 10 mg/ml διάλυμα προς έγχυση Λακοσαμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Vimpat 10 mg/ml διάλυμα προς έγχυση Λακοσαμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ FLECARDIA 50, 100, 150 και 200 mg καψάκια παρατεταμένης αποδέσμευσης, σκληρά flecainide acetate Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ FLECARDIA 50, 100, 150 και 200 mg καψάκια παρατεταμένης αποδέσμευσης, σκληρά flecainide acetate Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο.
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ (120+75+30 ) mg Καψάκιο ελεγχόμενης αποδέσμευσης, σκληρό Dimenhydrinate + Nicotinicacid + Pyridoxinehydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ (120+75+30 ) mg Καψάκιο ελεγχόμενης αποδέσμευσης, σκληρό Dimenhydrinate + Nicotinicacid + Pyridoxinehydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 10 mg δισκία Λοραταδίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 10 mg δισκία Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει σημαντικές
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 10 mg δισκία Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει σημαντικές
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 14 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ OMNIC TOCAS 0,4 mg δισκία παρατεταμένηςαποδέσμευσης Υδροχλωρική Ταμσουλοζίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 14 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ OMNIC TOCAS 0,4 mg δισκία παρατεταμένηςαποδέσμευσης Υδροχλωρική Ταμσουλοζίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Fortrans 74g, σκόνη για πόσιμο διάλυμα
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Fortrans 74g, σκόνη για πόσιμο διάλυμα Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι περιλαμβάνει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Fortrans 74g, σκόνη για πόσιμο διάλυμα Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι περιλαμβάνει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ. Zodin 1000 mg μαλακά καψάκια Αιθυλεστέρες των ω 3 λιπαρών οξέων 90
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Zodin 1000 mg μαλακά καψάκια Αιθυλεστέρες των ω 3 λιπαρών οξέων 90 Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Zodin 1000 mg μαλακά καψάκια Αιθυλεστέρες των ω 3 λιπαρών οξέων 90 Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό
Β. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 Β. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1/5 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη DAFLON 500 mg επικαλυμμένα με λεπτό υμένιο δισκία Micronized purified flavonoid fraction Διαβάστε προσεκτικά ολόκληρο το φύλλο
Β. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1/5 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη DAFLON 500 mg επικαλυμμένα με λεπτό υμένιο δισκία Micronized purified flavonoid fraction Διαβάστε προσεκτικά ολόκληρο το φύλλο
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. HYPNOMIDATE 20 mg/10 ml ενέσιμο διάλυμα Ετομιδάτη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ HYPNOMIDATE 20 mg/10 ml ενέσιμο διάλυμα Ετομιδάτη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ HYPNOMIDATE 20 mg/10 ml ενέσιμο διάλυμα Ετομιδάτη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5 mg επικαλυμμένα με λεπτό υμένιο δισκία Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5 mg επικαλυμμένα με λεπτό υμένιο δισκία Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
Pre-formed Bottle ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟN ΧΡΗΣΤΗ
 Pre-formed Bottle ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟN ΧΡΗΣΤΗ Xalatan 50 μικρογραμμάρια/ml Οφθαλμικές σταγόνες, Διάλυμα Latanoprost Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
Pre-formed Bottle ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟN ΧΡΗΣΤΗ Xalatan 50 μικρογραμμάρια/ml Οφθαλμικές σταγόνες, Διάλυμα Latanoprost Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Skinoren 15% Γέλη Aζελαϊκό οξύ Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Skinoren 15% Γέλη Aζελαϊκό οξύ Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml εναιωρήματος
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZARGA 10 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml εναιωρήματος
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη. CYTOTEC 200 mcg Δισκία Μισοπροστόλη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CYTOTEC 200 mcg Δισκία Μισοπροστόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε αυτό το
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CYTOTEC 200 mcg Δισκία Μισοπροστόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε αυτό το
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZOPT 10 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml εναιωρήματος περιέχει
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZOPT 10 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml εναιωρήματος περιέχει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. XOZAL 5 mg/ml πόσιμες σταγόνες, διάλυμα Λεβοσετιριζίνη διυδροχλωρική
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5 mg/ml πόσιμες σταγόνες, διάλυμα Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5 mg/ml πόσιμες σταγόνες, διάλυμα Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ VASTAREL 35 mg, δισκία ελεγχόμενης αποδέσμευσης Trimetazidine Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ VASTAREL 35 mg, δισκία ελεγχόμενης αποδέσμευσης Trimetazidine Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OPATANOL 1 mg/ml οφθαλμικές σταγόνες, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml διαλύματος περιέχει
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OPATANOL 1 mg/ml οφθαλμικές σταγόνες, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml διαλύματος περιέχει
ΠΑΡΑΡΤΗΜΑ ΙΙ Α. ΚΑΤΟΧΟΙ ΤΗΣ Α ΕΙΑΣ ΠΑΡΑΓΩΓΗΣ, ΥΠΕΥΘΥΝΟΙ ΓΙΑ ΤΗΝ ΑΠΟ ΕΣΜΕΥΣΗ ΤΩΝ ΠΑΡΤΙ ΩΝ Β. ΟΡΟΙ ΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙ Α. ΚΑΤΟΧΟΙ ΤΗΣ Α ΕΙΑΣ ΠΑΡΑΓΩΓΗΣ, ΥΠΕΥΘΥΝΟΙ ΓΙΑ ΤΗΝ ΑΠΟ ΕΣΜΕΥΣΗ ΤΩΝ ΠΑΡΤΙ ΩΝ Β. ΟΡΟΙ ΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 1 Α. ΚΑΤΟΧΟΙ ΤΗΣ Α ΕΙΑΣ ΠΑΡΑΓΩΓΗΣ, ΥΠΕΥΘΥΝΟI ΓΙΑ ΤΗΝ ΑΠΟ ΕΣΜΕΥΣΗ ΤΩΝ ΠΑΡΤΙ ΩΝ Όνοµα
ΠΑΡΑΡΤΗΜΑ ΙΙ Α. ΚΑΤΟΧΟΙ ΤΗΣ Α ΕΙΑΣ ΠΑΡΑΓΩΓΗΣ, ΥΠΕΥΘΥΝΟΙ ΓΙΑ ΤΗΝ ΑΠΟ ΕΣΜΕΥΣΗ ΤΩΝ ΠΑΡΤΙ ΩΝ Β. ΟΡΟΙ ΤΗΣ Α ΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ 1 Α. ΚΑΤΟΧΟΙ ΤΗΣ Α ΕΙΑΣ ΠΑΡΑΓΩΓΗΣ, ΥΠΕΥΘΥΝΟI ΓΙΑ ΤΗΝ ΑΠΟ ΕΣΜΕΥΣΗ ΤΩΝ ΠΑΡΤΙ ΩΝ Όνοµα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Afluon nasal spray SPC 13 EMA (GR120306) 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AFLUON 0,1% w/v ρινικό εκνέφωμα, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Διάλυμα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Afluon nasal spray SPC 13 EMA (GR120306) 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AFLUON 0,1% w/v ρινικό εκνέφωμα, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Διάλυμα
B. ΕΣΩΚΛΕΙΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ
 B. ΕΣΩΚΛΕΙΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ NAXCEL 100 mg/ml ενέσιμο εναιώρημα για χοίρους 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ
B. ΕΣΩΚΛΕΙΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ NAXCEL 100 mg/ml ενέσιμο εναιώρημα για χοίρους 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DuoTrav 40 µικρογραµµάρια/ml + 5 mg/ml οφθαλµικές σταγόνες, διάλυµα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 ml
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DuoTrav 40 µικρογραµµάρια/ml + 5 mg/ml οφθαλµικές σταγόνες, διάλυµα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 ml
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Cerenia 10mg ανά ml ενέσιμο διάλυμα για σκύλους και γάτες
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Cerenia 10mg ανά ml ενέσιμο διάλυμα για σκύλους και γάτες 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Cerenia 10mg ανά ml ενέσιμο διάλυμα για σκύλους και γάτες 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Salofalk 1 g υπόθετα Mεσαλαζίνη
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Salofalk 1 g υπόθετα Mεσαλαζίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε αυτό το φύλλο
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Salofalk 1 g υπόθετα Mεσαλαζίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε αυτό το φύλλο
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ProMeris Spot/on για γάτες
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ProMeris Spot/on για γάτες 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ ΠΑΡΤΙΔΩΝ ΣΤΟΝ ΕΟΧ,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ProMeris Spot/on για γάτες 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ ΠΑΡΤΙΔΩΝ ΣΤΟΝ ΕΟΧ,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη Carbosylane (140+45) mg καψάκια, σκληρά Carbosylane (140+45) mg γαστροανθεκτικά καψάκια, σκληρά Ενεργός άνθρακας & σιμεθικόνη Διαβάστε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη Carbosylane (140+45) mg καψάκια, σκληρά Carbosylane (140+45) mg γαστροανθεκτικά καψάκια, σκληρά Ενεργός άνθρακας & σιμεθικόνη Διαβάστε
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣHΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣHΣ 1 Β. ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 2 ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ AZOPT 10 mg/ml οφθαλµικές σταγόνες, εναιώρηµα Brinzolamide ιαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣHΣ 1 Β. ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 2 ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ AZOPT 10 mg/ml οφθαλµικές σταγόνες, εναιώρηµα Brinzolamide ιαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών
Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη Diacerein/Norma 50mg καψάκια σκληρά Διασερεΐνη
 REGULATORY AFFAIRS DEPARTMENT DIACEREIN/NORMA VERSION: PIL-2626801-04 DATE: 18-02-2016 Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη Diacerein/Norma 50mg καψάκια σκληρά Διασερεΐνη Διαβάστε προσεκτικά
REGULATORY AFFAIRS DEPARTMENT DIACEREIN/NORMA VERSION: PIL-2626801-04 DATE: 18-02-2016 Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη Diacerein/Norma 50mg καψάκια σκληρά Διασερεΐνη Διαβάστε προσεκτικά
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Xalatan 50 μικρογραμμάρια/ml Οφθαλμικές σταγόνες, διάλυμα Λατανοπρόστη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Xalatan 50 μικρογραμμάρια/ml Οφθαλμικές σταγόνες, διάλυμα Λατανοπρόστη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε
Φύλλο οδηγιών xρήσης: Πληροφορίες για τον ασθενή. Lopexal 2mg, σκληρά καψάκια. Υδροχλωρική Λοπεραμίδη
 Φύλλο οδηγιών xρήσης: Πληροφορίες για τον ασθενή Lopexal 2mg, σκληρά καψάκια Υδροχλωρική Λοπεραμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι
Φύλλο οδηγιών xρήσης: Πληροφορίες για τον ασθενή Lopexal 2mg, σκληρά καψάκια Υδροχλωρική Λοπεραμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣHΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣHΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Ζιρτέκ 10 mg/ml πόσιμες σταγόνες, διάλυμα Σετιριζίνη διϋδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣHΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Ζιρτέκ 10 mg/ml πόσιμες σταγόνες, διάλυμα Σετιριζίνη διϋδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ EMADINE 0,5 mg/ml, Οφθαλμικές σταγόνες, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 ml διαλύματος περιέχει
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ EMADINE 0,5 mg/ml, Οφθαλμικές σταγόνες, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 ml διαλύματος περιέχει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Pevison (1% + 0,1%) κρέμα Νιτρική εκοναζόλη + ακετονίδιο τριαμσινολόνης Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Pevison (1% + 0,1%) κρέμα Νιτρική εκοναζόλη + ακετονίδιο τριαμσινολόνης Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ Onsior 6 mg δισκία για γάτες
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ Onsior 6 mg δισκία για γάτες 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΕΛΕΥΘΕΡΩΣΗ ΠΑΡΤΙΔΩΝ, ΕΦΟΣΟΝ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ Onsior 6 mg δισκία για γάτες 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΕΛΕΥΘΕΡΩΣΗ ΠΑΡΤΙΔΩΝ, ΕΦΟΣΟΝ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5 mg επικαλυμμένα με λεπτό υμένιο δισκία Λεβοσετιριζίνη διυδροχλωρική
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5 mg επικαλυμμένα με λεπτό υμένιο δισκία Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ XOZAL 5 mg επικαλυμμένα με λεπτό υμένιο δισκία Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης
 Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
Παράρτημα ΙΙΙ Τροποποιήσεις στις σχετικές παραγράφους της περίληψης των χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης Σημείωση: Αυτές οι τροποποιήσεις στις σχετικές παραγράφους της περίληψης
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
Φύλλο Οδηγιών Χρήσης: Πληροφορίες για τον Χρήστη. Xalacom 50 μικρογραμμάρια/ml και 5 mg/ml Οφθαλμικές Σταγόνες, Διάλυμα Λατανοπρόστη + Τιμολόλη
 Φύλλο Οδηγιών Χρήσης: Πληροφορίες για τον Χρήστη Xalacom 50 μικρογραμμάρια/ml και 5 mg/ml Οφθαλμικές Σταγόνες, Διάλυμα Λατανοπρόστη + Τιμολόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
Φύλλο Οδηγιών Χρήσης: Πληροφορίες για τον Χρήστη Xalacom 50 μικρογραμμάρια/ml και 5 mg/ml Οφθαλμικές Σταγόνες, Διάλυμα Λατανοπρόστη + Τιμολόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή. Vimpat 10 mg/ml διάλυμα προς έγχυση Λακοσαμίδη
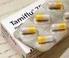 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Vimpat 10 mg/ml διάλυμα προς έγχυση Λακοσαμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Vimpat 10 mg/ml διάλυμα προς έγχυση Λακοσαμίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
Φύλλο Οδηγιών Χρήσης: Πληροφορίες για τον χρήστη. Travogen 1% κολπική κρέμα Isoconazole nitrate
 . Φύλλο Οδηγιών Χρήσης: Πληροφορίες για τον χρήστη Travogen 1% κολπική κρέμα Isoconazole nitrate Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
. Φύλλο Οδηγιών Χρήσης: Πληροφορίες για τον χρήστη Travogen 1% κολπική κρέμα Isoconazole nitrate Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη. Pivmecillinam hydrochloride
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Selexid 200 mg Δισκία επικαλυμένα με υμένιο Pivmecillinam hydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Selexid 200 mg Δισκία επικαλυμένα με υμένιο Pivmecillinam hydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ SKINOREN, κρέμα 20% Azelaic Acid Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,διότι
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ SKINOREN, κρέμα 20% Azelaic Acid Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,διότι
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 10 mg δισκία Λοραταδίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 10 mg δισκία Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι περιλαμβάνει
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον Χρήστη CLARITYNE 10 mg δισκία Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι περιλαμβάνει
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Dacogen 50 mg κόνις για πυκνό σκεύασμα για παρασκευή διαλύματος προς έγχυση δεσιταβίνη Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Dacogen 50 mg κόνις για πυκνό σκεύασμα για παρασκευή διαλύματος προς έγχυση δεσιταβίνη Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό + επινεφρίνη ή νορεπινεφρίνη
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή XOZAL 5 mg/ml πόσιμες σταγόνες, διάλυμα Για ενήλικες και παιδιά ηλικίας 2 ετών και άνω Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή XOZAL 5 mg/ml πόσιμες σταγόνες, διάλυμα Για ενήλικες και παιδιά ηλικίας 2 ετών και άνω Λεβοσετιριζίνη διυδροχλωρική Διαβάστε προσεκτικά ολόκληρο το φύλλο
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ GANFORT 0,3 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml διαλύματος
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ GANFORT 0,3 mg/ml + 5 mg/ml οφθαλμικές σταγόνες, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml διαλύματος
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 / 5 Φύλλο Οδηγιών Χρήσης: Πληροφορίες Για Τον Χρήστη DONAROT 1500 mg κόνις για πόσιμο διάλυμα Θειική Γλυκοσαμίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 / 5 Φύλλο Οδηγιών Χρήσης: Πληροφορίες Για Τον Χρήστη DONAROT 1500 mg κόνις για πόσιμο διάλυμα Θειική Γλυκοσαμίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΟΝΟΜΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BETOPTIC S 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Betaxolol Hydrochloride 2,8mg/ml ισοδύναμο με 2,5mg/ml betaxolol
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΟΝΟΜΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BETOPTIC S 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Betaxolol Hydrochloride 2,8mg/ml ισοδύναμο με 2,5mg/ml betaxolol
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. SKINOREN, κρέμα 20% Δραστικό συστατικό: Azelaic Acid
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ SKINOREN, κρέμα 20% Δραστικό συστατικό: Azelaic Acid Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ SKINOREN, κρέμα 20% Δραστικό συστατικό: Azelaic Acid Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο,
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DuoTrav 40 μικρογραμμάρια/ml+ 5 mg/ ml οφθαλμικές σταγόνες, διάλυμα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DuoTrav 40 μικρογραμμάρια/ml+ 5 mg/ ml οφθαλμικές σταγόνες, διάλυμα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZOPT 10 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Brinzolamide 10 mg/ml Για
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AZOPT 10 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Brinzolamide 10 mg/ml Για
Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
Φύλλο οδηγιών χρήσης: Πληροφορίες για το χρήστη CLARITYNE 1 mg/ml σιρόπι Λοραταδίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Vermox 100 mg μασώμενα δισκία Vermox 100 mg/5 ml πόσιμο εναιώρημα Mebendazole Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Vermox 100 mg μασώμενα δισκία Vermox 100 mg/5 ml πόσιμο εναιώρημα Mebendazole Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή. Integrilin 0,75 mg/ml διάλυμα για ενδοφλέβια έγχυση επτιφιμπατίδη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Integrilin 0,75 mg/ml διάλυμα για ενδοφλέβια έγχυση επτιφιμπατίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Integrilin 0,75 mg/ml διάλυμα για ενδοφλέβια έγχυση επτιφιμπατίδη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ PEVARYL 1% w/w κολπική κρέμα PEVARYL 150 mg κολπικά υπόθετα Νιτρική εκοναζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ PEVARYL 1% w/w κολπική κρέμα PEVARYL 150 mg κολπικά υπόθετα Νιτρική εκοναζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ. VASTAREL 20 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. Trimetazidine
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ VASTAREL 20 mg, επικαλυμμένο με λεπτό υμένιο δισκίο Trimetazidine Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ VASTAREL 20 mg, επικαλυμμένο με λεπτό υμένιο δισκίο Trimetazidine Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή. Τalcid 500 mg/tab μασώμενα δισκία Yδροταλκίτης
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Τalcid 500 mg/tab μασώμενα δισκία Yδροταλκίτης Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Τalcid 500 mg/tab μασώμενα δισκία Yδροταλκίτης Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να παίρνετε αυτό το φάρμακο, διότι περιλαμβάνει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. Έκδοχα με γνωστή δράση: χλωριούχο βενζαλκόνιο 0,2 mg/ml.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Vicks Sinex 0,5 mg/ml, διάλυμα ρινικού εκνεφώματος 2 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Οξυμεταζολίνη υδροχλωρική 0,5 mg/ml
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Vicks Sinex 0,5 mg/ml, διάλυμα ρινικού εκνεφώματος 2 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Οξυμεταζολίνη υδροχλωρική 0,5 mg/ml
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη. Dacogen 50 mg κόνις για πυκνό σκεύασμα για παρασκευή διαλύματος προς έγχυση δεσιταβίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Dacogen 50 mg κόνις για πυκνό σκεύασμα για παρασκευή διαλύματος προς έγχυση δεσιταβίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Dacogen 50 mg κόνις για πυκνό σκεύασμα για παρασκευή διαλύματος προς έγχυση δεσιταβίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Vermox 100 mg μασώμενα δισκία Vermox 100 mg/5 ml πόσιμο εναιώρημα Μεβενδαζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Vermox 100 mg μασώμενα δισκία Vermox 100 mg/5 ml πόσιμο εναιώρημα Μεβενδαζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ AFLUON 0,1% (w/v) ρινικό εκνέφωμα, διάλυμα Αζελαστίνη υδροχλωρική/azelastine hydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ AFLUON 0,1% (w/v) ρινικό εκνέφωμα, διάλυμα Αζελαστίνη υδροχλωρική/azelastine hydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο
Τι είναι το γλαύκωμα;
 Τι είναι το γλαύκωμα; Το γλαύκωμα περιλαμβάνει μια ομάδα παθήσεων που βλάπτουν το οπτικό νεύρο, προκαλώντας διαταραχές όρασης, οι οποίες, αν δεν αντιμετωπιστούν έγκαιρα, μπορούν να εξελιχθούν και να επιφέρουν
Τι είναι το γλαύκωμα; Το γλαύκωμα περιλαμβάνει μια ομάδα παθήσεων που βλάπτουν το οπτικό νεύρο, προκαλώντας διαταραχές όρασης, οι οποίες, αν δεν αντιμετωπιστούν έγκαιρα, μπορούν να εξελιχθούν και να επιφέρουν
ΠΑΡΑΡΤΗΜΑ III Τροποποιήσεις των σχετικών παραγράφων της περίληψης χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης
 ΠΑΡΑΡΤΗΜΑ III Τροποποιήσεις των σχετικών παραγράφων της περίληψης χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης 36/44 A. Περίληψη Χαρακτηριστικών του Προϊόντος 4.1 Θεραπευτικές ενδείξεις
ΠΑΡΑΡΤΗΜΑ III Τροποποιήσεις των σχετικών παραγράφων της περίληψης χαρακτηριστικών του προϊόντος και του φύλλου οδηγιών χρήσης 36/44 A. Περίληψη Χαρακτηριστικών του Προϊόντος 4.1 Θεραπευτικές ενδείξεις
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Vimpat 50 mg δισκία επικαλυμμένα με λεπτό υμένιο Vimpat 100 mg δισκία επικαλυμμένα με λεπτό υμένιο Vimpat 150 mg δισκία επικαλυμμένα
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Vimpat 50 mg δισκία επικαλυμμένα με λεπτό υμένιο Vimpat 100 mg δισκία επικαλυμμένα με λεπτό υμένιο Vimpat 150 mg δισκία επικαλυμμένα
Ανακούφιση των συμπτωμάτων ήπιας έως μέτριας οστεοαρθρίτιδας των γονάτων.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΑΝΤΙΣΤΟΙΧΕΣ ΠΑΡΑΓΡΑΦΟΙ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΑΝΤΙΣΤΟΙΧΕΣ ΠΑΡΑΓΡΑΦΟΙ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Σημείωση: Οι εν λόγω τροποποιήσεις της περίληψης των χαρακτηριστικών του προϊόντος και
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΑΝΤΙΣΤΟΙΧΕΣ ΠΑΡΑΓΡΑΦΟΙ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Σημείωση: Οι εν λόγω τροποποιήσεις της περίληψης των χαρακτηριστικών του προϊόντος και
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. AFLUON 0,1% (w/v) ρινικό εκνέφωμα, διάλυμα. Αζελαστίνη υδροχλωρική/azelastine hydrochloride
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ AFLUON 0,1% (w/v) ρινικό εκνέφωμα, διάλυμα Αζελαστίνη υδροχλωρική/azelastine hydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ AFLUON 0,1% (w/v) ρινικό εκνέφωμα, διάλυμα Αζελαστίνη υδροχλωρική/azelastine hydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε
