Εκλεκτική Καταλυτική Υδρογόνωση Ανανεώσιμων Μεθυλεστέρων Φυτικών Ελαίων σε Υδατικό Περιβάλλον
|
|
|
- Ευμελια Μιχαλολιάκος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «ΧΗΜΕΙΑΣ» ΕΙΔΙΚΕΥΣΗ «ΚΑΤΑΛΥΣΗ ΚΑΙ ΕΦΑΡΜΟΓΕΣ ΤΗΣ» ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ ΔΙΠΛΩΜΑΤΟΣ ΕΙΔΙΚΕΥΣΗΣ Εκλεκτική Καταλυτική Υδρογόνωση Ανανεώσιμων Μεθυλεστέρων Φυτικών Ελαίων σε Υδατικό Περιβάλλον ΔΗΜΗΤΡΑ ΣΤΑΥΡΟΥΛΑΚΗ ΧΗΜΙΚΟΣ ΑΘΗΝΑ ΙΟΥΝΙΟΣ 2015
2
3 ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ ΔΙΠΛΩΜΑΤΟΣ ΕΙΔΙΚΕΥΣΗΣ Εκλεκτική Καταλυτική Υδρογόνωση Ανανεώσιμων Μεθυλεστέρων Φυτικών Ελαίων σε Υδατικό Περιβάλλον ΔΗΜΗΤΡΑ ΣΤΑΥΡΟΥΛΑΚΗ Α.Μ.: ΕΠΙΒΛΕΠΩΝ ΚΑΘΗΓΗΤΗΣ: Γεώργιος Παπαδογιαννάκης, Αναπληρωτής Καθηγητής ΕΚΠΑ ΤΡΙΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ Χριστιάνα Μητσοπούλου, Καθηγήτρια ΕΚΠΑ Ερμόλαος Ιατρού, Καθηγητής ΕΚΠΑ Γεώργιος Παπαδογιαννάκης, Αναπληρωτής Καθηγητής ΕΚΠΑ ΗΜΕΡΟΜΗΝΙΑ ΕΞΕΤΑΣΗΣ 29/06/2015
4
5 ΠΕΡΙΛΗΨΗ Σε αυτήν τη διατριβή μελετούμε την εκλεκτική υδρογόνωση των πολυακόρεστων μεθυλεστέρων φυτικών ελαίων προς μονοακόρεστους λιπαρούς μεθυλεστέρες με χαμηλή περιεκτικότητα σε trans-ισομερή καταλυόμενη από υδατοδιαλυτά καταλυτικά συστήματα μετάλλων μετάπτωσης τροποποιημένα με αζωτούχους υποκαταστάτες σε υδατικά/οργανικά διφασικά συστήματα. Η μερική υδρογόνωση των μεθυλεστέρων του λινέλαιου (MELO) καταλυόμενη από σύμπλοκα Na 2 PtCl 6 6H 2 O/BPhDS έδωσε τα καλύτερα αποτελέσματα όσον αφορά τη δραστικότητα, εκλεκτικότητα και σταθερότητα του καταλύτη. Υπό ήπιες συνθήκες (T = 70 0 C, P H2 = 10 bar) εντός 20 min αντίδρασης η δραστικότητα αυτού του καταλύτη ανέρχεται σε TOF = 2000 h -1, και η εκλεκτικότητα ως προς το σύνολο των C18:1 εστέρων σε 36 mol%, με τα ανεπιθύμητα trans-c18:1 ισομερή να παράγονται σε ποσοστό μόλις 0.7 mol%. Η αντίστοιχη αντίδραση υδρογόνωσης των μεθυλεστέρων του ηλιέλαιου (MESO) απαιτεί δραστικότερες συνθήκες (T = C, P H2 = 40 bar) και δίνει υψηλά ποσοστά trans-c18:1 εστέρων (7.1 mol%). Η υδρογόνωση του MESO καταλυόμενη από συστήματα του Pd/Νυποκαταστάτες δίνει ικανοποιητικά αποτελέσματα με τους υποκαταστάτες BPhDS, EDTA Na 2 2H 2 O, NTPA και 3-PSA να εμφανίζουν τις υψηλότερες δραστικότητες (> 6000 TOF s ανά ώρα) και εκλεκτικότητες (85.9 mol% σύνολο C18:1 εστέρων). Αντίθετα, η υδρογόνωση του MESO καταλυόμενη από Ni/TPPTS και από σύμπλοκα Cu/Ν-υποκαταστάτες απαιτεί υψηλές θερμοκρασίες (> C) και οδηγεί σε παραγωγή κυρίως του κορεσμένου μεθυλεστέρα (MS) με πολύ χαμηλές δραστικότητες ( TOF s ανά ώρα). Παρόμοια αποτελέσματα παρουσιάζει και η μερική υδρογόνωση των μεθυλεστέρων του σογιέλαιου (MESBO) καταλυόμενη από διάφορα σύμπλοκα του Fe τροποποιημένα με αζωτούχους υποκαταστάτες. Επίσης, η υδρογόνωση με Fe/Sυποκαταστάτες έδειξε ότι η φύση του καταλύτη πιθανότατα είναι ετερογενής. Η υδρογόνωση του MESBO καταλυόμενη από σύμπλοκα του σιδήρου τροποποιημένα με αζωτούχους υποκαταστάτες οδήγησε στο σχηματισμό μικρής ποσότητας λιπαρών αλκοολών της τάξεως του 0.6 mol%. ΘΕΜΑΤΙΚΗ ΠΕΡΙΟΧΗ: Υδρογόνωση ανανεώσιμων μεθυλεστέρων φυτικών ελαίων ΛΕΞΕΙΣ ΚΛΕΙ ΙΑ: Υδρογόνωση, μεθυλεστέρες φυτικών ελαίων, trans-ισομερή, υδατοδιαλυτά καταλυτικά συστήματα μετάλλων μετάπτωσης με αζωτούχους και θειούχους υποκαταστάτες, υδατικά/οργανικά διφασικά συστήματα
6
7 ABSTRACT In this thesis we study the selective hydrogenation of polyunsaturated methyl esters of vegetable oils into their monounsaturated counterparts with a low content of transisomers catalyzed by water-soluble transition metal complexes modified with nitrogencontaining ligands in aqueous/organic two-phase systems. The best results were obtained in the partial hydrogenation of methyl esters of linseed oil (MELO) using Na 2 PtCl 6 6H 2 O /BPhDS complexes in terms of activity, selectivity and catalyst stability. Catalytic activity achieved with such complexes was 2000 TOF s per hour with a selectivity towards C18:1 esters of 36 mol%, and a low content of undesired trans- C18:1 isomers of 0.7 mol%. The Pt/BPhDS-catalyzed hydrogenation of methyl esters of sunflower oil (MESO) requires more drastic conditions (T = C, P H2 = 40 bar) with however high contents of trans-c18:1 esters (7.1 mol%). In the hydrogenation of MESO catalyzed by Pd/N-ligands the best results were obtained with BPhDS, EDTA Na 2 2H 2 O, NTPA and 3-PSA ligands to achieve high catalytic activities (TOF > 6000 h -1 ) and selectivities (85.9 mol% of total C18:1 esters). In sharp contrast, the hydrogenation of MESO catalyzed by Ni/TPPTS and Cu/N-ligand systems require high temperatures (>170 0 C) to gine mainly the saturated methyl ester product (MS), with low catalytic activities ( TOF s per hour). Similar results were obtained in the partial hydrogenation of methyl esters of soybean oil (MESBO) catalyzed by different complexes of Fe modified with N-containing ligands. Moreover the hydrogenation with Fe/S-ligands demonstrated that the nature of this catalyst is highly probable heterogeneous. Furthermore, in the hydrogenation of MESBO catalyzed by iron complexes modified with nitrogen-containing ligands a small amount of fatty alcohols (0.6 mol%) was formed. SUBJECT AREA: Hydrogenation of renewable methyl esters of vegetable oils KEYWORDS: Hydrogenation, methyl esters of vegetable oils, trans-isomers, watersoluble transition metal catalytic complexes with nitrogen- and sulfurcontaining ligands, aqueous/organic two-phase systems
8
9 Στους γονείς μου, που είναι δίπλα μου κάθε στιγμή της ζωής μου
10 ΕΥΧΑΡΙΣΤΙΕΣ Ολοκληρώνοντας την διπλωματική μου εργασία θα ήθελα να ευχαριστήσω όλα εκείνα τα πρόσωπα, που με την αμέριστη συμπαράσταση και κατανόηση που έδειξαν, με βοήθησαν να εκπονήσω την εργασία αυτή. Αρχικά, για τη διεκπεραίωση της παρούσας ερευνητικής εργασίας, θα ήθελα να ευχαριστήσω τον επιβλέποντα καθηγητή μου κ. Γεώργιο Παπαδογιαννάκη για τη συνεργασία και την πολύτιμη συμβολή του στην ολοκλήρωση της. Θα ήθελα επίσης να ευχαριστήσω την κα. Νίκη Κάϊκα και τον κ. Παναγιώτη Στάθη για το κλίμα συνεργασίας, συναδελφικότητας και φιλίας που αναπτύξαμε στον εργαστηριακό χώρο και το οποίο με βοήθησε να διατελέσω ευχάριστα την ερευνητική μου εργασία. Θα ήθελα να πω ένα μεγάλο ευχαριστώ, μέσα από την καρδιά μου, στους δικούς μου ανθρώπους, στους φίλους μου, κα. Ζωή Μοδιανάκη, κα. Δήμητρα Φωτοπούλου, κα. Ιωάννα Αντζουλάτου, κα. Παναγιώτα Περλεπέ, κ. Γιώργο Παλυβό, οι οποίοι με στήριξαν ο καθένας ξεχωριστά, με το δικό του μοναδικό τρόπο και με όλη την αγάπη τους. Ιδιαίτερως θέλω ολόψυχα να ευχαριστήσω τον κ. Κωνσταντίνο Σκαρλάτο για την συμπαράσταση και την αγάπη του όλο αυτό το διάστημα καθώς και για την πολύτιμη βοήθειά του στην τελειοποίηση αυτής της εργασίας. Τέλος και πάνω από όλα, θέλω να ευχαριστήσω και να αφιερώσω την εργασία αυτή στους γονείς μου και την αδελφή μου, οι οποίοι όλα αυτά τα χρόνια μου παρέχουν τόσο ηθική και συναισθηματική στήριξη, όσο και υλική, και με βοηθούν να πραγματοποιώ κάθε όνειρο και στόχο μου. Κυρίως όμως, τους ευχαριστώ για την αγάπη που μου έδωσαν και που με έμαθαν να την ανταποδίδω σε καθετί με το οποίο καταπιάνομαι.
11 ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ ΚΕΦΑΛΑΙΟ 1 ΕΙΣΑΓΩΓΗ ΚΕΦΑΛΑΙΟ 2 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Ορισμός κατάλυσης Είδη καταλυτικών αντιδράσεων Σύγκριση ομογενούς-ετερογενούς κατάλυσης Καταλυτική δραστικότητα Ετερογενοποίηση ομογενών καταλυτών Ετερογενοποίηση ομογενών καταλυτών με τη χρήση υδατικών/οργανικών διφασικών συστημάτων Υδατοδιαλυτοί υποκαταστάτες Μικυλλιακή κατάλυση Κατάλυση με νανοσωματίδια Υδρογόνωση Υδρογονοεπεξεργασία (Hydrotreating) Υδρογονοεπεξεργασία φυτικών ελαίων για παραγωγή βιοντίζελ 2 ης γενιάς Υδρογονοδιάσπαση (Hydrocracking) Υδρογόνωση βενζολίου Υδρογόνωση της D-γλυκόζης προς D-σορβιτόλη Υδρογόνωση του αζώτου (σύνθεση της αμμωνίας) Υδρογόνωση αδιπονιτριλίου προς εξαμεθυλενοδιαμίνη: Υδρογόνωση ολεφινών Υδρογόνωση εδώδιμων φυτικών ελαίων Υδρογόνωση φυτικών ελαίων καταλυόμενη από λευκόχρυσο... 52
12 Καταλύτες παλλαδίου στην υδρογόνωση φυτικών ελαίων όπως και των αλκυλεστέρων τους Υδρογόνωση φυτικών ελαίων καταλυόμενη από νικέλιο Υδρογόνωση φυτικών ελαίων και παραγώγων τους καταλυόμενη από χαλκό Καταλυτική υδρογόνωση παρουσία σιδήρου Εναντιοεκλεκτική υδρογόνωση προχειρόμορφων ολεφινών για την παραγωγή του φαρμάκου L-dopa (Διεργασία Monsanto) Υδρογονόλυση λιπαρών μεθυλεστέρων προς λιπαρές αλκοόλες Υδρογόνωση σε υδατικά/οργανικά διφασικά συστήματα ΚΕΦΑΛΑΙΟ 3 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Πειραματική διαδικασία αντίδρασης μετεστεροποίησης Πειραματική διαδικασία αντίδρασης υδρογόνωσης Παρασκευή απαερωμένου νερού Αντιδραστήρας Αέρια χρωματογραφία Ανάλυση μεθυλεστέρων φυτικών ελαίων Ερμηνεία χρωματογραφήματος του υποστρώματος και των προϊόντων της υδρογόνωσης Αντιδραστήρια ΚΕΦΑΛΑΙΟ 4 ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Εκλεκτική υδρογόνωση των μεθυλεστέρων του λινέλαιου (MELO) καταλυόμενη από το υδατοδιαλυτό καταλυτικό σύστημα Na 2 PtCl 6 6H 2 O/BPhDS σε υδατικό περιβάλλον Εκλεκτική υδρογόνωση των μεθυλεστέρων του ηλιέλαιου (MESO) καταλυόμενη από το υδατοδιαλυτό καταλυτικό σύστημα Na 2 PtCl 6 6H 2 O/BPhDS σε υδατικό περιβάλλον Εκλεκτική υδρογόνωση του MESO καταλυόμενη από το υδατοδιαλυτό καταλυτικό σύστημα Pd(O 2 CCF 3 ) 2 /BPhDS σε υδατικό περιβάλλον... 94
13 4.4 Εκλεκτική υδρογόνωση του MESO καταλυόμενη από το υδατοδιαλυτά σύμπλοκα Pd(O 2 CCF 3 ) 2 τροποποιημένα με διάφορους αζωτούχους υποκαταστάτες σε υδατικό περιβάλλον Εκλεκτική υδρογόνωση του MESO καταλυόμενη από υδατοδιαλυτά σύμπλοκα του νικελίου σε υδατικό περιβάλλον Εκλεκτική υδρογόνωση του MESO καταλυόμενη από υδατοδιαλυτά σύμπλοκα του χαλκού σε υδατικό περιβάλλον Εκλεκτική υδρογόνωση των μεθυλεστέρων του σογιέλαιου (MESBO) καταλυόμενη από σύμπλοκα του σιδήρου σε υδατικό περιβάλλον Μελέτη της υδρογόνωσης των μεθυλεστέρων του σογιέλαιου MESBO προς αλκόολες καταλυόμενη από το υδατοδιαλυτό σύστημα FeSO 4 7H 2 O/BPhDS ΚΕΦΑΛΑΙΟ 5 ΣΥΜΠΕΡΑΣΜΑΤΑ ΠΙΝΑΚΑΣ ΟΡΟΛΟΓΙΑΣ ΣΥΝΤΜΗΣΕΙΣ ΑΡΚΤΙΚΟΛΕΞΑ ΑΚΡΩΝΥΜΙΑ ΑΝΑΦΟΡΕΣ
14 ΚΑΤΑΛΟΓΟΣ ΣΧΗΜΑΤΩΝ Σχήμα 1: Ενεργειακό διάγραμμα μιας εξώθερμης αντίδρασης που δείχνει την ενέργεια ενεργοποίησης α) χωρίς καταλύτη και β) με καταλύτη Σχήμα 2: Το μετά νατρίου άλας της τρισουλφονικής τριφαινυλοφωσφίνης (TPPTS) Σχήμα 3: Επιφανειοδραστική φωσφίνη με δομή βεταΐνης Σχήμα 4: Δομή κανονικού μικυλλίου Σχήμα 5: "Ηλεκτροστερεοχημική" (ηλεκτρονιακή και στερεοχημική) Σχήμα 6: Υδρογόνωση του βενζολίου προς κυκλοεξάνιο και η μη επιθυμητή αντίδραση της ισομερείωσης του κυκλοεξανίου προς μεθυλοκυκλοπεντάνιο Σχήμα 7: Υδρογόνωση D-γλυκόζης προς D-σορβιτόλη καταλυόμενη από Ni/Raney σε υδατικό περιβάλλον Σχήμα 8: Υδρογόνωση αδιπονιτριλίου προς εξαμεθυλενοδιαμίνη Σχήμα 9: Ομογενής υδρογόνωση του οκτενίου-1 παρουσία του καταλύτη του Wilkinson Σχήμα 10: Καταλυτικός κύκλος της υδρογόνωσης ολεφινών παρουσία του καταλύτη RhCl(PPh 3 ) 3 σύμφωνα με τον μηχανισμό Halpern Σχήμα 11: Απλοποιημένες πορείες της βιομηχανικής διεργασίας της μερικής και πλήρους υδρογόνωσης φυτικών ελαίων καταλυόμενη από νικέλιο στο παράδειγμα του τριλινελαϊκού τριγλυκερινεστέρα προς τον ενδιάμεσο τριελαϊκό τριεστέρα και ακολούθως προς το πλήρες υδρογονωμένο προϊόν τον τριστεατικό τριγλυκερινεστέρα όπως και η παράπλευρη αντίδραση της ισομερίωσης που δίνει τα διάφορα γεωμετρικά cis/transισομερή όπως και τοπο-ισομερή (regiomers), δηλαδή ισομερή θέσης των C=C ομάδων C18:2 και C18:1 τριγλυκερινεστέρων Σχήμα 12: Η αντίδραση υδρογόνωσης του 1-εξενίου υπό ήπιες συνθήκες με τη χρήση του συμπλόκου ( ipr PDI)Fe(N 2 ) 2, σε τολουόλιο σε θερμοκρασία δωματίου Σχήμα 13: Τα πρόδρομα καταλυτικά συστήματα του τύπου [PhBPiPr 3 ]Fe-R (Α) και [PhBPiPr 3 ]Fe(H) 3 (PR 3 ) (Β) τα οποία έχουν χρησιμοποιηθεί στην υδρογόνωση ολεφινών
15 Σχήμα 14: Η αντίδραση υδρογόνωσης της κινναμαλδεΰδης Σχήμα 15: Τα σύμπλοκα του σιδήρου-pnp, pincer τύπου για την υδρογόνωση εστέρων προς αλκοόλες Σχήμα 16: Εναντιοεκλεκτική υδρογόνωση παραγώγων του ακεταμιδιοκινναμωμικού οξέος προς L-dopa καταλυόμενη από χειρομορφικούς καταλύτες Rh/DIPAMP σύμφωνα με την διεργασία Monsanto (o-an = C 6 H 4 -o-och 3, S = μεθανόλη). Στο 2 ο στάδιο παρουσία H 3 O + πραγματοποιείται η υδρόλυση του εστέρα προς L-dopa Σχήμα 17: Οι αντιδράσεις που συντελούνται στη βιομηχανική διεργασία της καταλυτικής υδρογονόλυσης ανανεώσιμων λιπαρών μεθυλεστέρων προς λιπαρές αλκοόλες στο παράδειγμα της υδρογονόλυσης μίγματος μεθυλεστέρων του φοινικικού πυρηνέλαιου προς τις αντίστοιχες λιπαρές αλκοόλες υπεράνω ετερογενών καταλυτικών συστημάτων τύπου Adkins Σχήμα 18: Πορείες της διεργασίας της υδρογονόλυσης του μονοακόρεστου ελαϊκού μεθυλεστέρα: (α) πορεία υδρογονόλυσης και υδρογόνωσης υπεράνω CuO/Cr 2 O 3 /Al 2 O 3 προς στεατική αλκοόλη και (β) πορεία υδρογονόλυσης υπεράνω ZnO/Cr 2 O 3 /Al 2 O 3 ή CdO/Cr 2 O 3 /Al 2 O 3 προς ελαϊκή αλκοόλη Σχήμα 19: Φάσμα των προϊόντων υδρογονόλυσης και υδρογόνωσης των C18 συστατικών των μεθυλεστέρων του φοινικικού πυρηνέλαιου όπου φαίνονται οι ενδιάμεσοι κηρώδεις εστέρες ο ελαϊκός ελαϋλεστέρας και ο στεατικός στεαρυλεστέρας και τα τελικά προϊόντα η ελαϊκή και στεατική αλκοόλη Σχήμα 20: Η απλοποιημένη πορεία της μερικής υδρογόνωσης των μεθυλεστέρων του λινελαίου (ΜΕLO), καταλυόμενη από υδατοδιαλυτά σύμπλοκα μετάλλων μετάπτωσης σε υδατικό/οργανικό διφασικό σύστημα Σχήμα 21: Μετά νατρίου άλας του δισουλφονικού οξέος της βαθοφαινανθρολίνης (BPhDS) Σχήμα 22: Επίδραση του μοριακού λόγου L/Pt στην καταλυτική δραστικότητα του συμπλόκου Na 2 PtCl 6 6H 2 O/ BPhDS στην αντίδραση υδρογόνωσης του MELO Σχήμα 23: Επίδραση της θερμοκρασίας στη σύσταση του MELO, μετά την αντίδραση υδρογόνωσής του με καταλύτη Na 2 PtCl 6 6H 2 O/ BPhDS
16 Σχήμα 24: Σχηματισμός των trans-c18:1 εστέρων συναρτήσει της θερμοκρασίας, στην αντίδραση υδρογόνωσης του MELO, καταλυόμενη από Na 2 PtCl 6 6H 2 O/ BPhDS Σχήμα 25: Επίδραση της θερμοκρασίας στην καταλυτική δραστικότητα του συμπλόκου Na 2 PtCl 6 6H 2 O/ BPhDS, στην αντίδραση υδρογόνωσης του MESO Σχήμα 26: Μεταβολή των trans-c18:1 συστατικών συναρτήσει της θερμοκρασίας, στην αντίδραση υδρογόνωσης του MESO, καταλυόμενη από Na 2 PtCl 6 6H 2 O/ BPhDS Σχήμα 27: Επίδραση της θερμοκρασίας στην καταλυτική δραστικότητα του συμπλόκου Pd(O 2 CCF 3 ) 2 / BPhDS, στην αντίδραση υδρογόνωσης του MESO Σχήμα 28: Μεταβολή των trans-c18:1 συστατικών συναρτήσει της θερμοκρασίας, στην αντίδραση υδρογόνωσης του MESO, καταλυόμενη από Pd(O 2 CCF 3 ) 2 / BPhDS Σχήμα 29: Επίδραση της θερμοκρασίας στη σύσταση των λιπαρών μεθυλεστέρων, μετά την αντίδραση υδρογόνωσής του με καταλύτη Pd(O 2 CCF 3 ) 2 / BPhDS Σχήμα 30: Επίδραση του μοριακού λόγου L/Pd στην καταλυτική δραστικότητα του συμπλόκου Pd(O 2 CCF 3 ) 2 / BPhDS, στην αντίδραση υδρογόνωσης του MESO Σχήμα 31: Επίδραση του χρόνου στην καταλυτική δραστικότητα του συμπλόκου Pd(O 2 CCF 3 ) 2 / BPhDS, στην αντίδραση υδρογόνωσης του MESO Σχήμα 32: Μεταβολή των trans-c18:1 συστατικών συναρτήσει του χρόνου, στην αντίδραση υδρογόνωσης του MESO, καταλυόμενη από Pd(O 2 CCF 3 ) 2 / BPhDS Σχήμα 33: Οι δομές των αζωτούχων υδατοδιαλυτών υποκαταστατών: το μετά νατρίου άλας του δισουλφονικού οξέος της βαθοκουπροΐνης (BCDS), το μετά καλίου άλας της 2,2-δικινολίνης-4,4-δικαρβοξυλικού οξέος (BQC), το 2,2-διπυριδίνη-4,4 - δικαρβοξυλικό οξύ (BPyDCA), το μετα τετρανατρίου άλας του αιθυλενοδιαμινοτετραοξικού οξέος (EDTA Na 4 ), το αιθυλενοδιαμινοτετραοξικό οξύ (EDTA), το μετα δινατρίου άλας του αιθυλενοδιαμινοτετραοξικού οξέος (EDTA Na 2 ), το trans-1,2-διαμινοκυκλοεξανο- Ν,Ν,Ν,Ν-τετραοξικό οξύ (CyDTA), το διαιθυλενοτριαμινο πεντάκις μεθυλοφωσφονικό οξύ (DTPPA), το μετα πεντανατρίου άλας του διαιθυλενοτριαμινοπενταοξικού οξέος (DTPA Na 5 ), το νιτριλο-τρι(μεθυλοφωσφονικό) οξύ (NTPA), το μετα τρινατρίου άλας του νιτριλοτριοξικού οξέος (NTA Na 3 ), η ταυρίνη (Taurine), το 2,6-πυριδινοδικαρβοξυλικό οξύ (2,6-PyDCA), το 3,4- πυριδινοδικαρβοξυλικό οξύ (3,4-PyDCA), το μετα νατρίου άλας του σουλφανιλικού οξέος (SANa), το 3-πυριδίνη σουλφονικό οξύ (3-PSA)
17 Σχήμα 34: Επίδραση της θερμοκρασίας στην καταλυτική δραστικότητα του συμπλόκου NiCl 2 6H 2 O/ TPPTS στην αντίδραση υδρογόνωσης του MESO Σχήμα 35: Μεταβολή των trans-c18:1 και C18:0 συστατικών συναρτήσει της θερμοκρασίας, στην αντίδραση υδρογόνωσης του MESO, καταλυόμενη από NiCl 2 6H 2 O/ TPPTS Σχήμα 36: Επίδραση της θερμοκρασίας στην καταλυτική δραστικότητα του συμπλόκου FeSO 4 7H 2 O/ BPhDS, στην αντίδραση υδρογόνωσης του MESBO Σχήμα 37: Μεταβολή των C18:1 και C18:0 συστατικών συναρτήσει της θερμοκρασίας, στην αντίδραση υδρογόνωσης του MESBO, καταλυόμενη από FeSO 4 7H 2 O/ BPhDS Σχήμα 38: Μεταβολή των C18:1 και C18:0 συστατικών συναρτήσει του χρόνου, στην αντίδραση υδρογόνωσης του MESBO, καταλυόμενη από FeSO 4 7H 2 O/ BPhDS Σχήμα 39: Οι δομές των Ν,Ο-, S,O-, και S,N,O-υποκατασττών: Ν,Ν δι(σαλικυλιδενιο)αιθυλενοδιαμίνη (Salen), Ν,Ν -δι(σαλικυλιδενιο)-1,3-προπυλενοδιαμίνη (Saloprop), 6,6 -διθειοδινικοτινικό οξύ (DThNA), 2,2 -διθειοσαλικυλικό οξύ (DThSA). 124
18
19 ΚΑΤΑΛΟΓΟΣ ΕΙΚΟΝΩΝ Εικόνα 1: Πειραματική διάταξη της αντίδρασης μετεστεροποίησης του σογιέλαιου με μεθανόλη Εικόνα 2: Το υδατικό/οργανικό διφασικό σύστημα που προκύπτει μετά την αντίδρασης υδρογόνωσης Εικόνα 3: Η πειραματική διάταξη για την παρασκευή απαερωμένου νερού Εικόνα 4: Ο αντιδραστήρας της εταιρείας Autoclave Engineers Εικόνα 5: Ο πύργος ελέγχου του αντιδραστήρα (Universal Reactor Controller) Εικόνα 6: Το μεταλλικό δοχείο του αντιδραστήρα Εικόνα 7: Διάταξη αέριου χρωματογράφου Εικόνα 8: Αέριο χρωματογράφημα του υποστρώματος MESBO Εικόνα 9: Χρωματογραφική ανάλυση των προϊόντων υδρογόνωσης του MESBO
20
21 ΚΑΤΑΛΟΓΟΣ ΠΙΝΑΚΩΝ Πίνακας 1: Επίδραση του μοριακού λόγου υποκαταστάτη/μετάλλου και της θερμοκρασίας στην αντίδραση εκλεκτικής υδρογόνωσης του MELO καταλυόμενη από Na 2 PtCl 6 6H 2 O/BPhDS σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 2: Επίδραση της θερμοκρασίας στην αντίδραση εκλεκτικής υδρογόνωσης του MESO καταλυόμενη από Na 2 PtCl 6 6H 2 O/BPhDS σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 3: Επίδραση του μοριακού λόγου υποκαταστάτη/μετάλλου, της θερμοκρασίας και του χρόνου στην αντίδραση εκλεκτικής υδρογόνωσης του MESO καταλυόμενη από Pd(O 2 CCF 3 ) 2 /BPhDS σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 4: Επίδραση διαφόρων αζωτούχων υποκαταστατών στις καταλυτικές ιδιότητες του Pd(O 2 CCF 3 ) 2 όπως και του μοριακού λόγου αζώτου/μετάλλου και της θερμοκρασίας στην αντίδραση εκλεκτικής υδρογόνωσης του MESO σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 5: Επίδραση της θερμοκρασίας στην αντίδραση εκλεκτικής υδρογόνωσης του MESO καταλυόμενη από NiCl 2 6H 2 O/TPPTS σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 6: Επίδραση του πρόδρομου καταλυτικού συστήματος και της θερμοκρασίας στην αντίδραση εκλεκτικής υδρογόνωσης του MESO καταλυόμενη από υδατοδιαλυτά σύμπλοκα Ni/TPPTS σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 7: Επίδραση διαφόρων υποκαταστατών καθώς και του μοριακού λόγου Cu/L στην αντίδραση εκλεκτικής υδρογόνωσης του MESO καταλυόμενη από υδατοδιαλυτά σύμπλοκα του χαλκού σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 8: Επίδραση του πρόδρομου καταλυτικού συστήματος Fe στην αντίδραση εκλεκτικής υδρογόνωσης του MESBO καταλυόμενη από υδατοδιαλυτά σύμπλοκα Fe/BPhDS σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 9: Επίδραση της θερμοκρασίας και του χρόνου στην αντίδραση εκλεκτικής υδρογόνωσης του MESBO καταλυόμενη από το υδατοδιαλυτό σύμπλοκο FeSO 4 7H 2 O /BPhDS σε υδατικό/οργανικό διφασικό σύστημα
22 Πίνακας 10: Μελέτη της επίδρασης διαφόρων αζωτούχων υποκαταστατών στην αντίδραση εκλεκτικής υδρογόνωσης του MESBO καταλυόμενη από υδατοδιαλυτά σύμπλοκα του σιδήρου σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 11: Μελέτη της επίδρασης χηλικών N,O-, S,O-, S,N,O-υποκαταστατών στην αντίδραση εκλεκτικής υδρογόνωσης του MESBO παρουσία υδατοδιαλυτών καταλυτικών συμπλόκων του σιδήρου σε υδατικό/οργανικό διφασικό σύστημα Πίνακας 12: Πίνακας ορολογίας με τις αντιστοιχίσεις των ελληνικών και ξενόγλωσσων όρων
23 ΠΡΟΛΟΓΟΣ Το πειραματικό μέρος της παρούσας εργασίας εκπονήθηκε στο εργαστήριο Βιομηχανικής Χημείας, του Τμήματος Χημείας της Σχολής Θετικών Επιστημών του Εθνικού Καποδιστριακού Πανεπιστημίου Αθηνών. Για την ολοκλήρωση του Μεταπτυχιακού Προγράμματος Σπουδών «Κατάλυση και Εφαρμογές της» καθώς και για την διεκπεραίωση της ερευνητικής μου εργασίας θα ήθελα να ευχαριστήσω εκτός από τον επιβλέποντα καθηγητή μου και όλους τους υπόλοιπους καθηγητές που συμμετέχουν στο Πρόγραμμα αυτό και που μας μετέδωσαν πολύτιμες γνώσεις κατά την διάρκεια των μαθημάτων. 23
24 1. ΚΕΦΑΛΑΙΟ 1 ΕΙΣΑΓΩΓΗ Η χρήση καταλυτικών συστημάτων στις χημικές αντιδράσεις είναι ιδιαίτερα σημαντική καθώς μειώνουν την ενέργεια ενεργοποίησης και αυξάνουν την ταχύτητά τους. Έτσι αντιδράσεις που υπό άλλες συνθήκες θα απαιτούσαν μεγαλύτερο χρονικό διάστημα να ολοκληρωθούν ή που θα ήταν αδύνατο να πραγματοποιηθούν λόγω της κινητικής τους, παρουσία καταλυτών δεν αντιμετωπίζουν τέτοιου είδους προβλήματα. Στη χημική βιομηχανία η κατάλυση εξασφαλίζει πολλές φορές χαμηλότερο ενεργειακό αλλά και οικονομικό κόστος σε συνδυασμό με διαδικασίες περισσότερο φιλικές προς το περιβάλλον. Γι αυτούς τους λόγους βρίσκει μεγάλη εφαρμογή σε διάφορους τομείς όπως στην παραγωγή φαρμάκων, καυσίμων, πολυμερών, τροφίμων κ.λπ. Μία από τις αντιδράσεις όπου χρησιμοποιούνται καταλυτικά συστήματα και στην οποία θα επικεντρωθούμε στο υπόλοιπο της εργασίας είναι η αντίδραση υδρογόνωσης για την παραγωγή βιοκαυσίμων ανώτερης ποιότητας και εδώδιμων λιπών. Ήδη, από τις αρχές του προηγούμενου αιώνα αναπτύχθηκε η βιομηχανική διεργασία υδρογόνωσης φυτικών ελαίων για την παραγωγή εδώδιμων λιπών. Όμως την τελευταία δεκαετία παρατηρείται μια εκθετική μείωση της χωρητικότητας παραγωγής των υδρογονωμένων λιπών εξαιτίας της παρουσίας trans ισομερών λιπαρών οξέων, τα οποία συνδέονται με αρνητικές επιπτώσεις στην ανθρώπινη υγεία. Έτσι, τα τελευταία χρόνια διεξάγεται έντονη έρευνα πάνω στην ανάπτυξη καινοτόμων εκλεκτικών καταλυτικών συστημάτων στην αντίδραση υδρογόνωσης εδώδιμων φυτικών ελαίων, τα οποία δεν παρουσιάζουν δραστικότητα στην παράπλευρη αντίδραση της cis/trans-ισομερείωσης και οδηγούν στην παραγωγή ημιστερεών λιπών με επιθυμητές οργανοληπτικές και θρεπτικές ιδιότητες με χαμηλά έως μηδαμινά ποσοστά σε trans λιπαρά. Η παρούσα εργασία εκπονήθηκε με σκοπό να μελετήσει την εκλεκτική υδρογόνωση ανανεώσιμων πολυακόρεστων μεθυλεστέρων φυτικών ελαίων προς τους αντίστοιχους μονοακόρεστους λιπαρούς μεθυλεστέρες χωρίς το 24
25 σχηματισμό trans-ισομερών η οποία λειτουργεί ως ένα μοντέλο αντίδρασης της υδρογόνωσης των φυτικών ελαίων προς λίπη παρουσία υδατοδιαλυτών καταλυτικών συμπλόκων των στοιχείων μετάπτωσης τροποποιημένα με αζωτούχους υποκαταστάτες σε υδατικά/οργανικά διφασικά συστήματα τα οποία εκτός από τη δυνατότητα ανάκτησης του καταλύτη παρουσιάζουν ιδιαίτερο περιβαλλοντικό ενδιαφέρον λόγω της χρήσης του υδατικού διαλύτη. 25
26 2. ΚΕΦΑΛΑΙΟ 2 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ 2.1 Ορισμός κατάλυσης Κατάλυση είναι το φαινόμενο κατά το οποίο ορισμένες ουσίες, που τις ονομάζουμε καταλύτες, μεταβάλλουν το ρυθμό μιας χημικής αντίδρασης, κατά κανόνα τον αυξάνουν, χωρίς οι ίδιες να καταναλίσκονται και χωρίς να μεταβάλλουν το σημείο της χημικής ισορροπίας που προβλέπεται από τη χημική θερμοδυναμική κάτω από ορισμένες συνθήκες. Με την χρήση καταλυτών στις χημικές αντιδράσεις παρέχεται ένας εναλλακτικός μηχανισμός, με διαφορετική μεταβατική κατάσταση και χαμηλότερη ενέργεια ενεργοποίησης (Σχήμα 1). [1] Σχήμα 1: Ενεργειακό διάγραμμα μιας εξώθερμης αντίδρασης που δείχνει την ενέργεια ενεργοποίησης α) χωρίς καταλύτη και β) με καταλύτη. 2.2 Είδη καταλυτικών αντιδράσεων Διακρίνουμε την κατάλυση σε ομογενή, ετερογενή και ενζυματική. Στην πρώτη, ο καταλύτης και οι αντιδρώσες ουσίες βρίσκονται στην ίδια φάση, συνήθως μέσα σε διαλύματα. Στη δεύτερη, ο καταλύτης είναι συνήθως στερεό σώμα, ενώ οι αντιδρώσες ουσίες βρίσκονται στην υγρή ή στην αέρια φάση. 26
27 Στην ομογενή κατάλυση ο καταλύτης είναι κάποιο καλά καθορισμένο είδος (μόριο, ιόν, σύμπλοκο ιόν, ένζυμο). Στην ενζυματική κατάλυση ο καταλύτης είναι ένα ένζυμο και το υπόστρωμα βρίσκεται στην υγρή ή στην στερεή φάση. [1] 2.3 Σύγκριση ομογενούς-ετερογενούς κατάλυσης Οι μηχανισμοί των ομογενών καταλυτικών αντιδράσεων μπορούν να μελετηθούν με NMR, IR, MS, UV, ESR κ.α. υπό συνθήκες αντίδρασης και να γίνουν κατανοητοί σε μοριακό επίπεδο. Αντίθετα, η μελέτη του μηχανισμού ετερογενών καταλυτικών συστημάτων είναι πάρα πολύ δύσκολη, σχεδόν αδύνατη. Τα ομογενή καταλυτικά συστήματα έχουν υψηλότερη δραστικότητα και εκλεκτικότητα υπό ήπιες συνθήκες σε σύγκριση με τα ετερογενή. Αυτό συμβαίνει επειδή στο ομογενές σύστημα υπάρχει η δυνατότητα διαμόρφωσης και τροποποίησης της σφαίρας σύνταξης του καταλύτη, καθώς επίσης τα ενεργά κέντρα του ομογενούς καταλύτη είναι προσιτά και μπορούν να λάβουν μέρος στην κατάλυση. Αντίθετα, στην ετερογενή η καταλυτική δράση εκδηλώνεται σε ορισμένες μόνο θέσεις της καταλυτικής επιφάνειας, τις δραστικές θέσεις, των οποίων η συγκέντρωση, και πολύ περισσότερο η φύση, προσδιορίζονται πολύ δύσκολα. Οι ομογενείς καταλύτες δίνουν τη δυνατότητα διαμόρφωσης στερεοχημικών παραμέτρων και άρα της υψηλής περίσσειας εναντιομερών. Λόγω της διαφορετικής φύσης των ενεργών κέντρων σε μια ετερογενή καταλυτική επιφάνεια, η ασύμμετρη σύνθεση καθίσταται δύσκολη. Στην ετερογενή κατάλυση τα φαινόμενα της διάχυσης και μπορεί να είναι καθοριστικά και δύνανται να επηρεάσουν την συνολική ταχύτητα της αντίδρασης. Τέτοιου είδους φαινόμενα δεν παρουσιάζονται συνήθως στα ομογενή καταλυτικά συστήματα, στα οποία η μεταφορά μάζας των αντιδρώντων ουσιών στα ενεργά κέντρα του καταλύτη είναι απρόσκοπτη. Τα ομογενή καταλυτικά συστήματα έχουν μικρότερο χρόνο ζωής σε σύγκριση με τα ετερογενή παρά την μεγάλη ευαισθησία των τελευταίων στα δηλητήρια. 27
28 Στις ομογενείς καταλυτικές αντιδράσεις η αναπαραγωγιμότητα των αποτελεσμάτων είναι εφικτή, εν αντιθέσει με τις ετερογενείς. Στην ομογενή κατάλυση ο διαχωρισμός του καταλύτη από τα προϊόντα της αντίδρασης καθώς και η ποσοτική του ανάκτηση σε ενεργό μορφή είναι δύσκολη. Αυτό δεν συμβαίνει στα ετερογενή καταλυτικά συστήματα. Για αυτόν τον λόγο έχουν γίνει προσπάθειες ετερογενοποίησης ομογενών καταλυτών. [2] 2.4 Καταλυτική δραστικότητα Ο πιο απλός τρόπος για να προσδιοριστεί η δραστικότητα ενός καταλύτη είναι η έννοια της συχνότητας επανάληψης (αναστροφής) του καταλυτικού κύκλου TOF (turnover frequency), που χρησιμοποιείται ευρύτατα στη βιομηχανική κατάλυση. Ο αριθμός TOF δηλώνει πόσες φορές πραγματοποιείται η συνολική καταλυτική αντίδραση ανά ενεργό κέντρο του καταλύτη στη μονάδα του χρόνου υπό καθορισμένες συνθήκες αντίδρασης (θερμοκρασία, πίεση ή συγκέντρωση, αναλογία των αντιδρώντων, ποσοστό μετατροπής των αντιδρώντων): Η ελάχιστη δραστικότητα που θα πρέπει να έχει ένας καταλύτης για να χρησιμοποιηθεί σε μια βιομηχανική καταλυτική διεργασία καθορίζεται από έναν κανόνα που είναι γενικά παραδεκτός. Ο κανόνας αυτός ορίζει ότι για την παραγωγή χημικών προϊόντων μεγάλης κλίμακας (bulk chemicals) το καταλυτικό σύστημα θα πρέπει να έχει μια μέση δραστικότητα TOF average >2.000 h -1. Για την παραγωγή προϊόντων μικρότερης κλίμακας (fine chemicals) και/ή ακριβών προϊόντων (π.χ. φαρμακευτικών υλών) η TOF μπορεί να είναι χαμηλότερη. Εκτός από την έννοια TOF υπάρχει και η έννοια TON (turnover number) που δηλώνει τον αριθμό επανάληψης του καταλυτικού κύκλου και ορίζεται ως εξής: TON = αριθμός μορίων ενός προϊόντος/ αριθμός ενεργών κέντρων του καταλύτη. Ο TON προσδιορίζει την παραγωγικότητα ενός καταλυτικού 28
29 συστήματος και επομένως το κόστος του καταλύτη. Είναι γενικά παραδεκτό ότι ο ΤΟΝ ενός καταλύτη που χρησιμοποιείται στην παραγωγή χημικών προϊόντων μεγάλης κλίμακας θα πρέπει να είναι της τάξης των με Τέλος, στη βιομηχανική κατάλυση χρησιμοποιείται συχνά η έννοια space-timeyield που είναι η απόδοση του καταλύτη, και ορίζεται ως η ποσότητα ενός προϊόντος σε Kg, ανά λίτρο καταλύτη, ανά ώρα (Kg x l -1 x h -1 ). [2] 2.5 Ετερογενοποίηση ομογενών καταλυτών Όπως αναφέρθηκε προηγουμένως τα ομογενή καταλυτικά συστήματα υπερτερούν έναντι των ετερογενών σε ότι αφορά στην καταλυτική δραστικότητα και εκλεκτικότητα. Εντούτοις το μειονέκτημα της ανακτησιμότητας των ομογενών καταλυτών και του δύσκολου διαχωρισμού τους από το μίγμα της αντίδρασης δεν είναι διόλου ευκαταφρόνητο. Η χρήση καταλυτών σε βιομηχανική κλίμακα προϋποθέτει εκτός από δραστικότητα και εκλεκτικότητα, σταθερότητα και εύκολη ανάκτηση, προκειμένου ο καταλύτης να μπορεί να επαναχρησιμοποιηθεί και να διατηρήσει την ενεργότητά του σε περισσότερους από έναν καταλυτικούς κύκλους, μειώνοντας έτσι το κόστος παραγωγής. Γι αυτόν ακριβώς το λόγο, έχουν γίνει προσπάθειες ετερογενοποίησης ομογενών οργανομεταλλικών καταλυτικών συμπλόκων πάνω σε οργανικούς ή ανόργανους στερεούς φορείς, ή περίκλεισης τους μέσα σε υπερθύλακες ζεόλιθων (ship-in-a-bottle). Κανένα σύστημα μέχρι τώρα δεν έχει βρει εφαρμογή ως καταλύτης σε μια βιομηχανική διεργασία για διάφορους λόγους, όπως οι χαμηλές καταλυτικές δραστικότητες και εκλεκτικότητες, η έκπλυση μετάλλου από το φορέα, η μη αναπαραγωγιμότητα της δραστικότητας και εκλεκτικότητας, η αποικοδόμηση του οργανικού φορέα και συχνά η μεγαλύτερη ευαισθησία αυτών των συστημάτων στο οξυγόνο του αέρα, κ.α. Εξαίρεση αποτελεί μια βιομηχανική διεργασία η οποία συντελείται σε πιλοτική κλίμακα και χρησιμοποιεί μεμβράνες για των διαχωρισμό προϊόντων από τον ομογενή καταλύτη. Η διεργασία αυτή περιλαμβάνει την αντίδραση υδροφορμυλίωσης του δικυκλοπενταδιενίου σε τρικυκλοδεκάνιο διαλδεΰδη σε οργανικούς διαλύτες. [3] 29
30 Μια άλλη προσέγγιση για να διαχωρίσουμε τα προϊόντα της αντίδρασης από τον ομογενή καταλύτη είναι να χρησιμοποιήσουμε ένα υγρό διφασικό σύστημα. Μια χαρακτηριστική αντίδραση που χρησιμοποιεί αυτήν την μέθοδο διαχωρισμού και ανάκτησης του καταλύτη είναι η αντίδραση ολιγομερισμού για παραγωγή γραμμικών α-ολεφινών, γνωστή και ως διεργασία SHOP (Shell Higher Olefins Process). Στην αντίδραση ολιγομερισμού αυτής της διεργασίας, ο πολικός καταλύτης νικελίου που περιέχει χηλικούς υποκαταστάτες P-O διαλύεται σε έναν πολικό διαλύτη π.χ. 1,4-βουτανοδιόλη. Με αυτόν τον τρόπο ο καταλύτης καθίσταται μη αναμίξιμος με το επιθυμητό προϊόν, δηλαδή τις α-ολεφίνες, και με έναν απλό διαχωρισμό δύο φάσεων καθίσταται εύκολη η ανάκτησή του. Πιο πρόσφατες εφαρμογές των υγρών/υγρών διαφασικών συστημάτων αποτελούν τα φθοριωμένα διφασικά συστήματα (fluorous biphase system FBS) και η χρήση ιοντικών υγρών ως διαλύτες. Επίσης η κατάλυση σε υπερκρίσιμα ρευστά αποτελεί μια άλλη περιβαλλοντικά ελκυστική προσέγγιση. Η ιδέα των φθοριωμένων διφασικών συστημάτων στηρίζεται στην περιορισμένη αναμιξιμότητα των κοινών οργανικών διαλυτών και προϊόντων με την φθοριωμένη φάση, η οποία αποτελείται από έναν καταλύτη διαλυτοποιημένο σε φθοριωμένο διαλύτη όπως για παράδειγμα ένα φθοριωμένο αλκάνιο ή αμίνη. Στην περίπτωση των ιοντικών υγρών, όπως π.χ. τα διαλκυλο ιμιδαζόλια που είναι μη αναμίξιμα με τους περισσότερους οργανικούς διαλύτες και μπορούν να διαλυτοποιήσουν τους καταλύτες είτε μέσω του ιοντικού τους χαρακτήρα, είτε με τη χρήση πολικών υποκαταστατών. [3] Ετερογενοποίηση ομογενών καταλυτών με τη χρήση υδατικών/οργανικών διφασικών συστημάτων Η χρήση του νερού ως δεύτερη φάση στο διφασικό διαχωρισμό αποτελεί μια εναλλακτική προσέγγιση αυτής της μεθόδου ανάκτησης του καταλύτη, προσδίδοντάς της περιβαλλοντικό χαρακτήρα. Το νερό ως πολικός διαλύτης είναι μη αναμίξιμο με τα περισσότερα οργανικά προϊόντα. Η αρχή της μεθόδου περιλαμβάνει την χρήση ενός υδατοδιαλυτού καταλύτη ο οποίος μετά το πέρας της αντίδρασης παραμένει στην υδατική φάση και απομακρύνεται από τα οργανικά προϊόντα με έναν απλό διφασικό 30
31 διαχωρισμό. Η ιδέα των δύο μη αναμίξιμων υγρών φάσεων προτάθηκε αρχικά από τον J. Manassen το 1972 και άρχισε να αποκτά μεγαλύτερο ενδιαφέρον όταν το 1975 ο J.C. Bailar δημοσίευσε ένα άρθρο ανασκόπησης με τίτλο: «Ετερογενοποιώντας Ομογενείς Καταλύτες». Τον ίδιο χρόνο ο Kuntz από την Rhône-Poulenc παρασκεύασε το μετά νατρίου άλας της τρισουλφονικής τριφαινυλοφωσφίνης TPPTS, και υδροφορμυλίωσε το προπένιο με τη χρήση του υδατοδιαλυτού καταλύτη RhH(CO)(TPPTS) 3 σε υδατικό/οργανικό διφασικό σύστημα. Στη συνέχεια ο Cornils και οι συνεργάτες του της εταιρίας Ruhrchemie AG, (γνωστή σήμερα ως Hoechst AG Werk Ruhrchemie), βελτίωσαν την σύνθεση και την καθαρότητα του TPPTS και ανέπτυξαν μια βιομηχανική διεργασία για την υδροφορμυλίωση του προπενίου σε διφασικό σύστημα. Η διεργασία αυτή των εταιρειών Ruhrchemie/ Rhône-Poulenc (RCH/RP) αποτελεί προπύργιο στον τομέα της οργανομεταλλικής κατάλυσης σε υδατικό περιβάλλον και η επιτυχία της κινητοποίησε την εφαρμογή αυτής της μεθόδου σε ένα ευρύ φάσμα καταλυτικών αντιδράσεων. Και αυτό γιατί η μέθοδος αυτή συνδυάζει τα πλεονεκτήματα της ομογενούς κατάλυσης με το προτέρημα της ετερογενούς, δηλαδή την εύκολη ανάκτηση και ανακύκλωση του καταλύτη που επιτυγχάνεται με έναν απλό διαχωρισμό των δύο φάσεων στο διφασικό σύστημα. [3] Τα πλεονεκτήματα ενός διφασικού υδατικού/οργανικού συστήματος είναι τα εξής: I. Εύκολη ανάκτηση του καταλύτη σε σχέση με τα κλασικά ομογενή καταλυτικά συστήματα. II. Χρησιμοποίηση του νερού ως διαλύτη το οποίο είναι ασφαλές, μη τοξικό, ευρέως διαδεδομένο, φτηνό και φιλικό ως προς το περιβάλλον, με αποτέλεσμα να πληροί τις απαιτήσεις της πράσινης χημείας. III. Απλοποίηση της χημικής μηχανικής στις χημικές βιομηχανικές διεργασίες IV. Εξοικονόμηση χρόνου, χρήματος και ενέργειας. Επιπλέον, το νερό παρουσιάζει ξεχωριστές ιδιότητες οι οποίες το καθιστούν ιδανικό ως διαλύτη: 31
32 1. To νερό είναι πολικό και εύκολα ανακτήσιμο από άπολους διαλύτες και προϊόντα. Η υψηλή πολικότητά του μπορεί να αυξάνει την καταλυτική δραστικότητα του συστήματος. 2. Είναι μη αναφλέξιμο και σε αφθονία και δεν χρειάζεται ιδιαίτερη επεξεργασία για τη χρήση του. 3. Είναι άοσμο και άχρωμο και επομένως οποιαδήποτε πρόσμιξη από άλλη ουσία είναι ευκολότερα ανιχνεύσιμη. 4. Επηρεάζει την διαλυτότητα των ενώσεων μέσω του σχηματισμού εξαγωνικής δισδιάστατης δομής της επιφάνειας και τετραεδρικού τρισδιάστατου μοριακού πλέγματος. Οι χαοτροπικές ενώσεις αυξάνουν την εντροπία μέσω σχάσης δεσμών υδρογόνου. 5. Η παράμετρος Hildebrand του νερού είναι πολύ υψηλή (μονάδα διαλυτότητας μη ηλεκτρολυτών σε οργανικούς διαλύτες). 6. Έχει πυκνότητα 1g/cm 3, η οποία το διαφοροποιεί από τις περισσότερες οργανικές ενώσεις. 7. Έχει υψηλή διηλεκτρική σταθερά, υψηλή θερμική αγωγιμότητα, υψηλή ειδική θερμοχωρητικότητα, υψηλή ενθαλπία εξάτμισης και χαμηλό δείκτη διάθλασης. 8. Υψηλή διαλυτότητα αερίων σε αυτό, ειδικά του CO Σχηματίζει ένυδρα άλατα και επιδιαλυτωμένα σωματίδια. 10. Διαχέεται εύκολα και έχει μεγάλη τάση σχηματισμού μικυλλίων, ώστε να γίνεται σταθεροποίηση ενώσεων και μέσω προσθέτων. 11. Έχει αμφοτερική συμπεριφορά κατά Brønsted. 12. Η χρήση του σε βιομηχανικές μονάδες παραγωγής συνοδεύεται από χαμηλότερες εκπομπές ρύπων. [3,4] Υδατοδιαλυτοί υποκαταστάτες Αναφέρθηκε προηγουμένως ότι η εφαρμογή της μεθόδου ανάκτησης και διαχωρισμού ενός ομογενούς καταλύτη από υδατικό/οργανικό διφασικό σύστημα απαιτεί την διαλυτοποίηση του καταλύτη αυτού στην υδατική φάση 32
33 του συστήματος. Έτσι κρίνεται αναγκαία η χημική τροποποίηση των κλασσικών οργανομεταλλικών συμπλόκων, που χρησιμοποιούνται ως καταλύτες, προκειμένου να γίνουν υδατοδιαλυτά. Η τροποποίηση αυτή μπορεί να επιτευχθεί με την εισαγωγή υδατοδιαλυτών υποκαταστατών στα σύμπλοκα αυτά. Οι υδατοδιαλυτοί υποκαταστάτες διακρίνονται στις εξής κατηγορίες: σουλφουρωμένες φωσφίνες, καρβοξυλιωμένες φωσφίνες, φωσφίνες με αιθερικές και υδροξυλικές ομάδες, φωσφίνες με άμινο, αμμώνιο, φωσφορικές και φωσφονικές ομάδες ή με κατιόν φωσφονίου. Επίσης υπάρχουν συστήματα όπως σουλφουρωμένες αμίνες, φθαλοκυανίνες, πορφυρίνες, τριφαινυλοαρσίνες, θειοαιθερικές ή σουλφονικές φωσφίνες και αζωτούχοι υποκαταστάτες. Από τους υδατοδιαλυτούς υποκαταστάτες που παρουσιάστηκαν, ξεχωριστό ενδιαφέρον έχουν οι σουλφουρωμένες φωσφίνες εξαιτίας της καλής αναλογίας κόστος/διαλυτότητα που εμφανίζουν. Το TPPTS, δηλαδή το μετα νατρίου άλας της τρισουλφονικής τριφαινυλοφωσφίνης αποτελεί τον πιο αντιπροσωπευτικό υποκαταστάτη αυτής της κατηγορίας. Επιπλέον, θεωρείται μακράν ο καλύτερος υδατοδιαλυτός υποκαταστάτης αν λάβουμε υπόψη το χαμηλό του κόστος σε σχέση με την αποδοτικότητά του, την διαθεσιμότητά του, καθώς επίσης και την μεγάλη του σταθερότητα στη οξείδωση και την θερμοκρασία. Το TPPTS έχει διαλυτότητα 1100g/L στους 20 0 C και η δομή του φαίνεται στο σχήμα 2. Σχήμα 2: Το μετά νατρίου άλας της τρισουλφονικής τριφαινυλοφωσφίνης (TPPTS). Κλείνοντας, πρέπει να αναφέρουμε ότι τα τελευταία χρόνια γίνεται λόγος για μία νέα τάξη πολικών υποκαταστατών, τους σουλφουρωμένους φωσφίτες. Αυτού του είδους οι ενώσεις δείχνουν αξιοσημείωτη σταθερότητα στο νερό, συγκρινόμενοι με τους συμβατικούς φωσφίτες όπως ο P(OPh) 3. Έχει 33
34 αποδειχθεί επίσης ότι καταλύτες ροδίου που έχουν τροποποιηθεί με σουλφουρωμένους φωσφίτες δείχνουν μεγαλύτερη καταλυτική δραστικότητα σε χαμηλότερη θερμοκρασία στην υδροφορμυλίωση του 1-τετραδεκενίου, σε σύγκριση με τον συμβατικό καταλύτη Rh/ P(OPh) 3. [3] Μικυλλιακή κατάλυση Η μικυλλιακή κατάλυση αποτελεί μια εναλλακτική προσέγγιση στο πρόβλημα της διαλυτότητας ανώτερων ολεφινών στα διφασικά συστήματα, όπου λαμβάνουν χώρα οι αντιδράσεις τους. Αυτή η μέθοδος τονίζει έμμεσα ότι η αντίδραση πραγματοποιείται στην μεσεπιφάνεια ενός διφασικού συστήματος. Η πρώτη ένωση που σχεδιάστηκε για να πραγματοποιήσει μικυλλιακή κατάλυση, σε υδατικό μέσο με αδιάλυτο σε αυτό υπόστρωμα και με τη χρήση συμπλόκων στοιχείων μετάπτωσης ως καταλύτη, είναι μία φωσφίνη με δομή βεταΐνης (διιόντος). Αυτό το μόριο συνδυάζει διπλή λειτουργία και ως υποκαταστάτης και ως επιφανειοδραστική ουσία. Η δομή των ενώσεων αυτών που είναι συστήματα σουλφοαλκυλιωμένης τρις(2-πυριδυλο)-φωσφίνης παρουσιάζονται στο σχήμα 3. Σχήμα 3: Επιφανειοδραστική φωσφίνη με δομή βεταΐνης. Η προσθήκη των επιφανειοδραστικών ουσιών γίνεται με σκοπό να δημιουργηθούν μικύλλια σε συγκεντρώσεις πάνω από την κρίσιμη μικυλλιακή συγκέντρωση (Critical Micellar Concentration, CMC). Κινητήρια δύναμη της μικυλλιακής κατάλυσης είναι οι διαμοριακές δυνάμεις Van der Waals, οι οποίες τείνουν με υδρόφοβες αλληλεπιδράσεις να μειώσουν την επαφή του άπολου τμήματος με τον πολικό διαλύτη, οπότε προκύπτουν συσσωματώματα μικυλλίων. Ένα απλοποιημένο μοντέλο ενός σφαιρικού μικυλλίου παρουσιάζεται στο σχήμα 4. 34
35 Σχήμα 4: Δομή κανονικού μικυλλίου. Ο πυρήνας του μικυλλίου αποτελείται από την υδρόφοβη αλυσίδα της επιφανειοδραστικής ουσίας, π.χ. της φωσφίνης, στην οποία είναι διαλυτοποιημένη η ανώτερη ολεφίνη, π.χ. το 1-τετραδεκένιο. Ο πυρήνας περιβάλλεται από την στοιβάδα του Stern στην οποία βρίσκονται οι φορτισμένες ομάδες (SO - 3 ), καθώς και τα αντισταθμιστικά κατιόντα νατρίου (Na + ) του ιοντικού μικυλλίου. Τα άτομα του μετάλλου μετάπτωσης, π.χ. του ροδίου, είναι πιθανόν να βρίσκονται στην πολική βαθμίδωση μεταξύ της στοιβάδας του Stern και του πυρήνα του μικυλλίου. Η ακριβής θέση των ατόμων του μετάλλου καθορίζεται από την τιμή του λόγου υδρόφιλη/λιπόφιλη ισορροπία, (Hydrophilic/Lipophilic balance, HLB), της επιφανειοδραστικής ουσίας. Στο παράδειγμα του σχήματος 3 το ιδανικό μέγεθος της υδρογονανθρακικής αλυσίδας είναι n=5 για να επιτευχθεί μέγιστη καταλυτική δραστικότητα. Για n<5 ο υποκαταστάτης έχει πολύ μικρό μοριακό βάρος για να διαλυτοποιήσει την ολεφίνη, και για n>5 το ρόδιο βρίσκεται πολύ μακριά από την πολική βαθμίδωση μεταξύ της στοιβάδας του Stern και του πυρήνα του μυκυλλίου, οπότε μειώνεται η καταλυτική δραστικότητα. Εκτός από τα κανονικά μικύλλια είναι δυνατόν να σχηματιστούν αντίστροφα μικύλλια το οποίο συμβαίνει στην περίπτωση όπου η οργανική φάση είναι περισσότερη από την υδατική. Κλείνοντας πρέπει να αναφερθεί ότι η μικυλλιακή κατάλυση έχει παραλληλιστεί από πολλούς συγγραφείς με την ετερογενή κατάλυση σε στερεά επιφάνεια. Και αυτό γιατί η διαλυτοποίηση του υποστρώματος στον πυρήνα του μικυλλίου που περιέχει τα ενεργά κέντρα του καταλύτη προσομοιάζει με την προσρόφησή του στην επιφάνεια ενός ετερογενούς 35
36 καταλύτη και ο αριθμός των σχηματιζόμενων μικυλλίων με τον αριθμό των ενεργών κέντρων στην επιφάνεια του καταλύτη. [3] 2.6 Κατάλυση με νανοσωματίδια Τα νανοσωματίδια θεωρούνται ως το όριο μεταξύ ομογενούς και ετερογενούς κατάλυσης και συνδυάζουν τα πλεονεκτήματα και των δύο. Ως νανοσωματίδια ορίζονται τα διακριτά στερεά σωματίδια μετάλλων μεγέθους nm. Τα νανοσωματίδια (Nanoparticles ΝPs, μερικές φορές καλούνται τεράστιες πλειάδες, πλειάδες ή κολλοειδή) εμφανίζουν πολύ υψηλή δραστικότητα υπό ήπιες συνθήκες εξαιτίας της μεγάλης τους επιφάνειας. Η σταθεροποίησή τους μπορεί να γίνει μέσω ηλεκτροστατικών, στερεοχημικών ή ηλεκτροστερεοχημικών (συνδυασμός στερεοχημικών και ηλεκτροστατικών) παραγόντων ή με συμπλοκοποίηση παρουσία υποκαταστατών. Η κλασσική δομή ενός νανοσωματιδίου που σταθεροποιείται μέσω ηλεκτροστερεοχημικών παραγόντων -συνηθέστερη περίπτωση- δίδεται στο σχήμα 5. Σχήμα 5: "Ηλεκτροστερεοχημική" (ηλεκτρονιακή και στερεοχημική) σταθεροποίηση νανοσωματιδίων μετάλλων μέσω αναγωγής ενός χλωριούχου άλατος του μετάλλου παρουσία τεταρτοταγών αλκυλαμμωνιακών κατιόντων. Εκτός από μονομεταλλικά σωματίδια έχουν συντεθεί και διμεταλλικά και τριμεταλλικά. Η σύνθεση των νανοσωματιδίων γίνεται συνήθως μέσω αντίδρασης κάποιων πρόδρομων καταλυτικών συστημάτων. Αυτά περιλαμβάνουν ένα άλας μετάλλου, ένα μοριακό σταθεροποιητή και ένα αναγωγικό (κάποιο αέριο, π.χ. CO ή H 2 ή κάποιο υδρίδιο, π.χ. NaBH 4 ). Οι 36
37 κυριότεροι τρόποι σύνθεσης καταλυτικά ενεργών νανοσωματιδίων είναι οι εξής: Διαβροχή, εμποτισμός, Συγκαταβύθιση, συγκατακάθιση, επικάθιση, καταβύθιση, χρήση γελών, οργανομεταλλική απόθεση αέριας φάσης, χρήση υπερήχων, σχηματισμός μικρογαλακτωμάτων, ακτινοβόλιση με laser (φωτοχημικά), ηλεκτροχημικά και cross- linking (σχηματισμός πλεγμάτων). Η ανάκτησή τους επιτυγχάνεται συνήθως μέσω ακινητοποίησής τους σε ανόργανους ή οργανικούς πολυμερικούς φορείς. Μερικοί από τους βασικότερους φορείς είναι οι εξής: πολυμερή, δενδριμερή, υποκαταστάτες, σταθεροποίηση χωρίς υποκαταστάτες, μικύλλια, γαλακτώματα και επιφανειοδραστικές ουσίες, ιοντικά υγρά, οξείδια, άνθρακας. Εξαιτίας της εύκολης σύνθεσής τους, της δυνατότητας ρύθμισης των ιδιοτήτων τους και όλων των άλλων πλεονεκτημάτων που συγκεντρώνουν τα νανοσωματίδια ως καταλύτες έχουν βρει πληθώρα καταλυτικών εφαρμογών. Μερικές από τις αντιδράσεις είναι οι εξής: υδρογονώσεις, αμινώσεις, καρβονυλιώσεις, αντιδράσεις οξείδωσης, αντιδράσεις σύζευξης, και διάφορες άλλες αντιδράσεις. Η ταυτοποίηση των νανοσωματιδίων γίνεται αρχικά με φυγοκέντρηση (δημιουργία ιζήματος) και ο προσδιορισμός της διαμέτρου τους με δυναμική σκέδαση φωτός. Για την ταυτοποίηση τριμεταλλικών ή διμεταλλικών νανοσωματιδίων χρησιμοποιείται και η φασματοσκοπία υπεριώδους-ορατού (UV-vis spectroscopy). Άλλες τεχνικές που επιτρέπουν την διερεύνηση έκπλυσης ή όχι του μετάλλου από το φορέα προς το διάλυμα είναι η ηλεκτρονιακή μικροσκοπία μεταφοράς (transmission electron microscopy, TEM), η ενεργειακή σκέδαση ακτίνων Χ (Energy dispersion X-ray analysis, EDX) και η περίθλαση ακτίνων Χ (X-ray diffraction). [5] 2.7 Υδρογόνωση Η υδρογόνωση αποτελεί μία από τις σημαντικότερες διεργασίες στη χημική βιομηχανία. Η πορεία αυτή, που συνήθως είναι καταλυτική, εκτός από ελάχιστες εξαιρέσεις στις οποίες η αντίδραση προάγεται θερμικά με την χρήση υψηλής θερμοκρασίας, βρίσκει εφαρμογές σε πολλούς και διαφορετικούς τομείς της βιομηχανικής δραστηριότητας. Έτσι η αντίδραση της υδρογόνωσης 37
38 εφαρμόζεται κατά κύριο λόγο στην βιομηχανία καυσίμων, τροφίμων και λιπασμάτων, ενώ η χρήση της στη φαρμακοβιομηχανία, στα πολυμερή και τα λιπαντικά δεν είναι αμελητέα Υδρογονοεπεξεργασία (Hydrotreating) Όπως αναφέρθηκε προηγουμένως η υδρογονοεπεξεργασία των κλασμάτων της απόσταξης του πετρελαίου κατέχει εξέχουσα θέση στην χημική βιομηχανία. Με τον όρο υδρογονοεπεξεργασία εννοούμε το σύνολο των αντιδράσεων υδρογονόλυσης οργανικών θειούχων, αζωτούχων και οξυγονούχων ενώσεων προς τα αντίστοιχα ουδέτερα οργανικά παράγωγα με σύγχρονη παραγωγή H 2 S, NH 3 και H 2 O τα οποία διαχωρίζονται εύκολα από το μίγμα υγρών καυσίμων. Έτσι, ανάλογα με το ποιό ετεροάτομο απομακρύνεται από το πετρελαϊκό κλάσμα, δηλαδή το S,N και Ο οι επιμέρους αντιδράσεις υδρογονοεπεξεργασίας χαρακτηρίζονται ως εξής: υδρογονοαποθείωση (hydrodesulfurization, HDS), υδρογονοαποαζώτωση (hydrodenitrogenation, HDN), υδρογονοαποξυγόνωση (hydrodeoxygenation, HDO), υδρογονοαπομετάλλωση (hydrodemetallization, HDM). Επιπλέον, αυτή η διεργασία περιλαμβάνει και ορισμένες αντιδράσεις υδρογόνωσης αρωματικών ενώσεων, αλκενίων, αλκινίων και διενίων. Η υδρογονοεπεξεργασία των πετρελαϊκών κλασμάτων συντελείται για κάποιους βασικούς λόγους, όπως είναι η προστασία των καταλυτών στις διεργασίες που ακολουθούν (π.χ. η καταλυτική αναμόρφωση της νάφθας) από ενώσεις που περιέχουν κοινά δηλητήρια καταλυτών, δηλαδή τα ετεροάτομα S,N,O. Επίσης, με την υδρογονοεπεξεργασία αποφεύγεται ο πολυμερισμός των ολεφινών, επιτυγχάνεται ανώτερη ποιότητα των καυσίμων όσον αφορά την οσμή, το χρώμα, την σταθερότητα και την διάβρωση και ταυτόχρονα προστατεύεται το περιβάλλον. Κλείνοντας, πρέπει να ειπωθεί ότι η υδρογονοεπεξεργασία εφαρμόζεται σε ευρεία κλίμακα από το τέλος της δεκαετίας του Οι συνήθεις καταλύτες που χρησιμοποιούνται στη μετατροπή της νάφθας (συνθήκες αντίδρασης T= C, P=15-40 bar), είναι ετερογενή συστήματα του τύπου CoS-MoS 2 / γ-al 2 O 3 ή NiS- MoS 2 / γ- Al 2 O 3, ενώ στην υδρογονοεπεξεργασία του αεριελαίου (συνθήκες αντίδρασης 38
39 T= C, P= bar), η κατάλυση γίνεται με συστήματα του τύπου CoMoS /γ-al 2 O 3. [2] Υδρογονοεπεξεργασία φυτικών ελαίων για παραγωγή βιοντίζελ 2 ης γενιάς Το βιοντίζελ 2 ης γενιάς αποτελεί μίγμα γραμμικών αλκανίων από C 12 έως και C 18 το οποίο προέρχεται από την υδρογονοεπεξεργασία φυτικών ελαίων. Η διεργασία αυτή πραγματοποιείται σήμερα σε βιομηχανική κλίμακα και συντελείται υπεράνω θειούχων καταλυτών NiMo/γ-Al 2 O 3 σε θερμοκρασίες C και μερικές πιέσεις υδρογόνου atm. Τα βιοκαύσιμα 2 ης γενιάς πλεονεκτούν έναντι των βιοκαυσίμων 1 ης γενιάς (τα οποία προέρχονται από την μετεστεροποίηση φυτικών ελαίων με μεθανόλη, αφού εμφανίζουν τα εξής χαρακτηριστικά: Χαμηλότερο κατά 50 % κόστος παραγωγής Συμβατότητα με την υπάρχουσα υποδομή των εγκαταστάσεων υδρογονοεπεξεργασίας των πετρελαϊκών κλασμάτων. Συμβατότητα με τον κινητήρα. Ευελιξία στην πρώτη ύλη. Η Ευρωπαϊκή Ένωση έχει προγραμματίσει την πλήρη ανάπτυξη της βιομηχανικής κλίμακας παραγωγής του βιοντίζελ 2 ης γενιάς ως το έτος 2020 οπότε το ποσοστό των βιοκαυσίμων στα καύσιμα κίνησης θα ανέρχεται τουλάχιστον στο 10%. [2] Υδρογονοδιάσπαση (Hydrocracking) Μια άλλη καταλυτική διεργασία που χρησιμοποιεί υδρογόνο για την αναβάθμιση της ποιότητας των υγρών καυσίμων στα διυλιστήρια πετρελαίου είναι η υδρογονοδιάσπαση. Στη διεργασία αυτή το βαρύ αεριέλαιο και το αεριέλαιο της απόσταξης μετατρέπονται παρουσία υδρογόνου προς ελαφρύτερα προϊόντα όπως η νάφθα, η κηροζίνη και το ντίζελ. Η υδρογονοδιάσπαση διαχωρίζεται από την καταλυτική διάσπαση στο ότι στη δεύτερη, δηλαδή στη διεργασία FCC δεν παρέχεται υδρογόνο. Έτσι οι δύο αντιδράσεις δεν είναι ανταγωνιστικές αλλά αλληλοεξαρτώμενες. Επίσης η υδρογονοδιάσπαση διαφοροποιείται από την υδρογονοεπεξεργασία στο 39
40 γεγονός ότι στη δεύτερη δεν διασπώνται δεσμοί C-C. Η υδρογόνωση και η απομάκρυνση των ετεροατόμων απαιτεί έναν καταλύτη υδρογόνωσης, ενώ η διάσπαση έναν όξινο καταλύτη. Επομένως, στην υδρογονοδιάσπαση χρησιμοποιούνται μικτά θειούχα μέταλλα όπως π.χ. NiS/MoS 2 και Ni/WS 2 ή ευγενή μέταλλα, ενώ η δραστικότητα αυτών των καταλυτικών συστημάτων αυξάνεται με περισσότερο όξινους φορείς όπως π.χ. φορείς οξειδίου του πυριτίου και του αργιλίου ή ζεόλιθοι. Οι τυπικές συνθήκες της αντίδρασης υδρογονοδιάσπασης είναι C και πιέσεις bar. [2] Υδρογόνωση βενζολίου Το βασικό πετροχημικό βενζόλιο υφίσταται καταλυτική υδρογόνωση προς παραγωγή κυκλοεξανίου, με χωρητικότητα παγκόσμιας παραγωγής περίπου 3 x 10 6 τόννους το χρόνο. Σ αυτήν τη διεργασία βασίζονται οι βιομηχανικές πορείες της παραγωγής του Nylon 6 και του Nylon 6,6. Η υδρογόνωση του βενζολίου προς κυκλοεξάνιο μπορεί να πραγματοποιηθεί στην υγρή φάση (T = ~ C, P H2 = 50 bar) ή στην αέρια φάση (T = C, P H2 = 30 bar). Εκτός από την αντίδραση αυτή, είναι δυνατόν να λάβει χώρα η παράπλευρη και ανεπιθύμητη αντίδραση της ισομερείωσης του κυκλοεξανίου προς μεθυλοκυκλοπεντάνιο (σχήμα 6), η οποία μπορεί να αποφευχθεί σε χαμηλές θερμοκρασίες ή σε μικρότερους χρόνους επαφής. Σχήμα 6: Υδρογόνωση του βενζολίου προς κυκλοεξάνιο και η μη επιθυμητή αντίδραση της ισομερείωσης του κυκλοεξανίου προς μεθυλοκυκλοπεντάνιο. Το Ινστιτούτο Πετρελαίου της Γαλλίας (Institut Français du Pétrole, IFP) ανέπτυξε μια βιομηχανική μέθοδο υδρογόνωσης του βενζολίου στην υγρή φάση υπεράνω ετερογενών καταλυτικών συστημάτων του νικελίου του Raney, στους C και μερική πίεση υδρογόνου 50 bar, όπου στην τροφοδοσία του βενζολίου επιτρέπεται μια περιεκτικότητα θείου < 1 ppm. Στην διεργασία IFP η μετατροπή του βενζολίου είναι < 95% και η ποσοτική του μετατροπή 40
41 επιτυγχάνεται σε έναν δεύτερο αντιδραστήρα στην αέρια φάση. Εκτός από την ετερογενή διεργασία το IFP ανέπτυξε και μια ομογενή διεργασία υδρογόνωσης του βενζολίου προς κυκλοεξάνιο καταλυόμενη από συστήματα τύπου Ziegler που βασίζονται σε άλατα του Ni (II) και Co (II) σε συνδυασμό με τριαιθυλοαργίλιο υπό ήπιες συνθήκες (T = C, P H2 = 10 bar). [2] Υδρογόνωση της D-γλυκόζης προς D-σορβιτόλη Οι υδατάνθρακες που αποτελούν το 95% της ανανεώσιμης βιομάζας θεωρούνται η σημαντικότερη τάξη οργανικών ενώσεων όσον αφορά τη χωρητικότητα παραγωγής τους. Η ανανεώσιμη βιομάζα έχει συνολική χωρητικότητα παραγωγής 200 Gt το χρόνο από την οποία μόνο το 7% χρησιμοποιείται από τον άνθρωπο και το υπόλοιπο διασπάται και ανακυκλώνεται με φυσικές μεθόδους. Από αυτά τα μεγέθη συμπεραίνουμε ότι οι ανανεώσιμοι υδατάνθρακες έχουν πολλές προοπτικές να χρησιμοποιηθούν μελλοντικά ως εναλλακτικές πρώτες ύλες της χημικής βιομηχανίας. Η υδρογόνωση της D-γλυκόζης προς D-σορβιτόλη η οποία είναι το πρώτο στάδιο της κλασικής συνθετικής πορείας της παραγωγής της βιταμίνης C χρησιμοποιεί ανανεώσιμους υδρογονάνθρακες ως πρώτη ύλη (σχήμα 7). Η υδρογόνωση πραγματοποιείται συνήθως με διεργασίες ασυνεχούς λειτουργίας (batch) σε υδατικό διάλυμα 50% D-γλυκόζης, ph = 5-6, παρουσία του καταλύτη Ni/Raney σε θερμοκρασίες C και μερικές πιέσεις υδρογόνου bar. Η μετατροπή της D-γλυκόζης προς D-σορβιτόλη είναι ποσοτική εντός 2-4 ωρών. Σχήμα 7: Υδρογόνωση D-γλυκόζης προς D-σορβιτόλη καταλυόμενη από Ni/Raney σε υδατικό περιβάλλον. 41
42 Η D-σορβιτόλη έχει μεγάλη χωρητικότητα παραγωγής περίπου 300 x 10 3 τόννοι ετησίως και εκτός από την παραγωγή της βιταμίνης C χρησιμοποιείται σε πολλούς άλλους τομείς όπως π.χ. στα καλλυντικά, στην παραγωγή επιφανειοδραστικών ουσιών, στη διατροφή κ.α. [2] Υδρογόνωση του αζώτου (σύνθεση της αμμωνίας) Η σύνθεση της αμμωνίας έγινε για πρώτη φορά τον Μάρτιο του Τότε ο F. Haber (βραβείο Nobel Χημείας, 1918) κατάφερε να συνθέσει αμμωνία δεσμεύοντας άζωτο με υδρογόνο. Η διεργασία αρχικά διεξαγόταν παρουσία καταλυτών που βασίζονταν στο ευγενές μέταλλο όσμιο Os. Η αντίδραση είναι εξώθερμη και συνοδεύεται από ελάττωση του όγκου (καταναλώνονται δύο μόρια προς σχηματισμό ενός), οπότε η θέση ισορροπίας μετατοπίζεται προς τα δεξιά σε χαμηλές θερμοκρασίες και υψηλές πιέσεις. Το καταλυτικό σύστημα που χρησιμοποιείται σχεδόν το ίδιο μέχρι σήμερα στην χημική βιομηχανία για την σύνθεση της αμμωνίας είναι το ετερογενές σύστημα Fe/Al 2 O 3 /CaO/K 2 O και αναπτύχθηκε ύστερα από επίπονη έρευνα από τον Mittasch και τους συνεργάτες του στην BASF. Μέχρι τις μέρες μας η απόδοση της αμμωνίας είναι %, επομένως η ανάπτυξη δραστικότερων καταλυτών είναι αναγκαία, αλλά ταυτόχρονα εξαιρετικά δύσκολη. [2] Υδρογόνωση αδιπονιτριλίου προς εξαμεθυλενοδιαμίνη: Η εξαμεθυλενοδιαμίνη, η οποία χρησιμοποιείται μαζί με το αδιπικό οξύ για την παραγωγή του nylon 6,6 λαμβάνεται ως προϊόν από τη διεργασία υδρογόνωσης του αδιπονιτριλίου (σχήμα 8) παρουσία καταλυτικών συστημάτων που βασίζονται στο κοβάλτιο με χαλκό υπό υψηλή πίεση 600 bar ή υπό ήπιες συνθήκες χαμηλής πίεσης 30 bar παρουσία καταλυτών νικελίου. [6] 42
43 Σχήμα 8: Υδρογόνωση αδιπονιτριλίου προς εξαμεθυλενοδιαμίνη Υδρογόνωση ολεφινών Η πρώτη ετερογενής υδρογόνωση ολεφινών στην αέρια φάση καταλυόμενη από νικέλιο αναπτύχθηκε το 1905 από τον Paul Sabatier (βραβείο Nobel Χημείας, 1912) και θεωρείται ως η αρχή της οργανικής ετερογενούς κατάλυσης. Στις ετερογενείς αντιδράσεις υδρογόνωσης καταλυόμενες από συστήματα που βασίζονται σε στοιχεία μετάπτωσης, όπως π.χ. Ni/Raney, Pd/C και Pt/Al 2 O 3, η ανάκτηση του καταλύτη από το προϊόν της αντίδρασης είναι εύκολη. To 1965 αναπτύχθηκε η ομογενής υδρογόνωση ολεφινών καταλυόμενη από το σύστημα RhCl(PPh 3 ) 3, το οποίο είναι γνωστό ως «Καταλύτης του Wilkinson». Το σύστημα αυτό είναι ένας πολύ δραστικός καταλύτης ομογενούς υδρογόνωσης ολεφινών και αλκινίων υπό ήπιες συνθήκες (θερμοκρασία περιβάλλοντος και ατμοσφαιρική πίεση). Παρά το γεγονός ότι μέχρι τότε ήταν γνωστοί ορισμένοι ομογενείς καταλύτες υδρογόνωσης, με την ανακάλυψη του καταλύτη RhCl(PPh 3 ) 3 από τον Wilkinson ενεργοποιήθηκε σε παγκόσμιο επίπεδο η έρευνα στο πεδίο της ομογενούς καταλυτικής υδρογόνωσης και έχει μελετηθεί σε μεγάλο βαθμό ίσως όσο καμία άλλη αντίδραση καταλυόμενη από σύμπλοκα των στοιχείων μετάπτωσης στο ομογενές σύστημα. Σχήμα 9: Ομογενής υδρογόνωση του οκτενίου-1 παρουσία του καταλύτη του Wilkinson. Ο μηχανισμός της υδρογόνωσης ολεφινών καταλυόμενη από RhCl(PPh 3 ) 3 μελετήθηκε από τον Halpern και τους συνεργάτες του, των οποίων η εργασία οδήγησε στην ταυτοποίηση των ενδιάμεσων σωματιδίων της αντίδρασης και 43
44 στον προσδιορισμό της κινητικής των διαφόρων σταδίων. Ο μηχανισμός Halpern θεωρείται ο γενικά παραδεκτός μηχανισμός αυτής της αντίδρασης. Η έρευνα για την κατανόηση του μηχανισμού αφορούσε απομόνωση, χαρακτηρισμό και ταυτοποίηση ορισμένων σωματιδίων του ροδίου και προσδιορισμό των ταχυτήτων των διαφόρων σταδίων υπό συνθήκες όμως στοιχειομετρικών αντιδράσεων. Σύμφωνα με τον μηχανισμό Halpern (σχήμα 10) πρώτα αποσπάται ένας υποκαταστάτης PPh 3 από το σύμπλοκο (I) σχηματίζοντας το συμπλεκτικά ακόρεστο σωματίδιο RhCl(PPh 3 ) 2 (II). Στη σφαίρα σύνταξης του συστήματος (II) είναι πιθανότατα ένα μόριο ή μόρια διαλύτη που είναι υποκαταστάτες ασθενούς σύμπλεξης. Με οξειδωτική προσθήκη διυδρογόνου Η 2 στο σύστημα (ΙΙ) προκύπτει το ενδιάμεσο σωματίδιο τρισθενούς ροδίου RhCl(H) 2 (PPh 3 ) 2 (III), το οποίο έχει επίσης μια κενή θέση στη σφαίρα σύνταξης, όπου συμπλέκεται η ολεφίνη σχηματίζοντας το π-σύμπλοκο (IV). Με μετανάστευση υδριδίου, πιθανότατα διαμέσου μιας μεταβατικής κατάστασης τεσσάρων κέντρων (και ισομερείωσης), προκύπτει το αλκυλοσύμπλοκο (V). Η αναγωγική απόσπαση αλκανίου από το ενδιάμεσο σωματίδιο του τρισθενούς ροδίου (V) ολοκληρώνει τον καταλυτικό κύκλο με αναγέννηση του αρχικού σωματιδίου κλειδί (ΙΙ) το οποίο είναι έτοιμο να δεχθεί ένα άλλο μόριο διυδρογόνου για τον επόμενο κύκλο. [2] 44
45 Σχήμα 10: Καταλυτικός κύκλος της υδρογόνωσης ολεφινών παρουσία του καταλύτη RhCl(PPh 3 ) 3 σύμφωνα με τον μηχανισμό Halpern Υδρογόνωση εδώδιμων φυτικών ελαίων Η καταλυτική υδρογόνωση φυτικών ελαίων αποτελεί μια παγιωμένη τεχνολογία στην βιομηχανία τροφίμων. Η τεχνολογία αυτή έχει ως κύριο στόχο την υδρογόνωση των ευαίσθητων στην αυτό-οξείδωση πολυακόρεστων λιπαρών οξέων, προκειμένου να σταθεροποιηθούν μέσω αυτής της διεργασίας τα φυτικά έλαια. Τα υδρογονωμένα έλαια βρίσκουν εφαρμογή στις κρύες σάλτσες, στα μαγειρικά έλαια κ.λπ. Εμβαθύνοντας λίγο, η μερική υδρογόνωση μετατρέπει τα φυτικά έλαια σε (ημί-) στερεά λιπαρά προϊόντα με διαφορετικά οργανοληπτικά χαρακτηριστικά για χρήση σε ποικίλες εφαρμογές στα τρόφιμα, όπως ως μαργαρίνες και μαγειρικά λίπη. Αυτή η βιομηχανική διεργασία έχει μία πολύ μακρά ιστορία. Η πρώτη αντίδραση υδρογόνωσης λιπαρών ελαίων στην υγρή φάση κατοχυρώθηκε το 1902 από τον γερμανό χημικό Wilhelm Normann ( ). Λίγο νωρίτερα ο Paul Sabatier είχε αναπτύξει την υδρογόνωση ακόρεστων οργανικών ενώσεων στην αέρια φάση με καταλύτη Ni. Το 1906 η διαδικασία της υδρογόνωσης λιπαρών ελαίων εφαρμόστηκε βιομηχανικά στην Αγγλία από την εταιρεία Joseph Crossfield and Sons για την επεξεργασία του λίπους της φάλαινας. Αρχικά σκοπός ήταν η παραγωγή σάπωνα, αργότερα όμως η 45
46 τεχνολογία της υδρογόνωσης χρησιμοποιήθηκε για παρασκευή λιπαρών προϊόντων στην βιομηχανία τροφίμων. Με αυτή την τεχνική, τα ασταθή φυτικά έλαια και ιχθυέλαια μετατρέπονταν σε σταθερές στην οξείδωση και εύγευστες μαργαρίνες και μαγειρικά λίπη. To πρώτο υδρογονωμένο προϊόν από φυτικό έλαιο με το όνομα Crisco, δημιουργήθηκε το 1911 από την εταιρεία Procter & Gamble, η οποία απέκτησε τα δικαιώματα από την πατέντα του Normann το Το όνομα Crisco αποτελεί ακρωνύμιο των λέξεων crystallized cottonseed oil, δηλαδή κρυσταλλωμένο βαμβακέλαιο. Το προϊόν αυτό παρουσιάζει παρόμοιες φυσικές ιδιότητες με το λαρδί, δηλαδή το ζωικό λίπος, που ως τότε ήταν το πλέον χρησιμοποιούμενο εδώδιμο λιπαρό. Το Crisco χαρακτηρίστηκε πιο υγιεινό μαγειρικό λίπος σε σύγκριση με το συμβατικό ζωικό και αποτέλεσε σημείο καμπής για την μετάβαση από την μαζική κατανάλωση ζωικών λιπών, στην κατανάλωση λιπαρών προϊόντων φυτικής προέλευσης. Καθώς η ζήτηση αυτών των φτηνών υποκατάστατων των ζωικών λιπών ολοένα και αυξανόταν τις πρώτες δεκαετίες του 20 ου αιώνα, το ποσό των υδρογονωμένων λιπαρών στα τρόφιμα αυξανόταν κι αυτό. Η δημοτικότητα των υδρογονωμένων προϊόντων για χρήση τους στα εδώδιμα είχε ως συνέπεια την σταδιακή σύγκρουση πατεντών. Το 1920 το Ανώτατο Δικαστήριο των ΗΠΑ αποφάσισε ότι οι δύο πρώτες αξιώσεις (claims) της πατέντας της εταιρείας Procter & Gamble δεν ήταν έγκυρες, ανοίγωντας, με αυτόν τον τρόπο, τον δρόμο σε άλλες εταιρείες να εφαρμόσουν τη διαδικασία της υδρογόνωσης στα εδώδιμα φυτικά έλαια. [6, 12] Η μεγάλη απήχηση της διεργασίας της υδρογόνωσης εδώδιμων φυτικών ελαίων από τις αρχές του προηγούμενου αιώνα, έως και σήμερα οφείλεται όχι μόνο σε οικονομικούς παράγοντες, αλλά και σε ευρήματα που σχετίζονται με την θρεπτική αξία των υδρογονωμένων ελαίων. Τα υδρογονωμένα λίπη αποτελούν την κύρια πηγή των κορεσμένων λιπών. Από τη δεκαετία του 1950 έρευνες έδειξαν ότι η κατανάλωση σε κορεσμένα λίπη συνδέεται άμεσα με υψηλότερα επίπεδα συγκέντρωσης LDL (low density lipoproteins, λιποπρωτεΐνες χαμηλής πυκνότητας) χοληστερόλης στο αίμα και αυξάνεται ο κίνδυνος για καρδιαγγειακές νόσους. Γι αυτόν τον λόγο η βιομηχανία 46
47 εδώδιμων ελαίων αναγκάστηκε να αναπροσαρμόσει τη διεργασία υδρογόνωσης φυτικών ελαίων, ώστε να υπάρχει ένας υψηλότερος λόγος πολυακόρεστων/κορεσμένων λιπών στο τελικό προϊόν. Έτσι από ένα επίπεδο μερικής υδρογόνωσης ανέπτυξε διάφορα επίπεδα υδρογόνωσης και το τελικό προϊόν αποτελείτο από ένα μίγμα διαφόρων επιπέδων υδρογόνωσης μαζί με ένα ποσοστό από το αρχικό φυτικό έλαιο. Στην περίπτωση π.χ. του σογιέλαιου με αριθμό ιωδίου IV = 130 (IV, iodine value, g I 2 /100g) όλα σχεδόν τα λιπαρά τελικά προϊόντα μπορούσαν να παραχθούν με μίγματα τριών επιπέδων υδρογονωμένου σογιέλαιου (IV = 80, IV = 65, πλήρης υδρογόνωση) μαζί με σογιέλαιο σε διάφορα ποσοστά το καθένα, ανάλογα με τη χρήση του τελικού προϊόντος. Το υψηλότερο ποσοστό των ακόρεστων λιπαρών καθιστούσε τα προϊόντα πιο υγιεινά και πολλοί καταναλωτές προτιμούσαν πλέον αντί του βουτύρου τη μαργαρίνη. Από την δεκαετία του 1950 έως την δεκαετία του 1980 η καταλυτική υδρογόνωση αποτελούσε την κύρια διεργασία της βιομηχανίας επεξεργασίας και αξιοποίησης φυτικών ελαίων. [6, 12, 13] Η βιομηχανική διεργασία της υδρογόνωσης εδώδιμων φυτικών ελαίων χρησιμοποιούσε σχεδόν αποκλειστικά ετερογενείς καταλύτες Ni οι οποίοι παρουσίαζαν υψηλή εκλεκτικότητα στην υδρογόνωση των διπλών δεσμών C=C στα τμήματα των καρβοξυλικών οξέων των τριγλυκεριδίων σε υψηλές θερμοκρασίες (Τ = C) υπό χαμηλές πιέσεις (P H2 < 15 bar) και συγκεντρώσει του νικελίου [Ni] = % (σχήμα 15). Το υδρογόνο που χρησιμοποιείται για την παραγωγή της μαργαρίνης προέρχεται από την ηλεκτρόλυση του ύδατος και έχει πολύ υψηλή καθαρότητα. Το τριγλυκερίδιο π.χ. του λινελαϊκού οξέος (cis-9, cis-12-δεκαοκταδιενοϊκό οξύ, linoleic acid) που περιέχει δύο διπλούς δεσμούς C=C σε κάθε τμήμα του καρβοξυλικού οξέος (σχήμα 15) υδρογονώνεται υπεράνω Ni αρχικά ποσοτικά προς το τριγλυκερίδιο του ελαϊκού οξέος (cis-9-δεκαοκτενoϊκό οξύ, oleic acid) που περιέχει έναν διπλό δεσμό C=C σε κάθε ανθρακική αλυσίδα του τμήματος του καρβοξυλικού οξέος και μετά ξεκινά η ποσοτική υδρογόνωση του τριελαϊκού τριγλυκερινεστέρα προς τον κορεσμένο τριστεατικό τριγλυκερινεστέρα (δεκαοκτανοϊκό οξύ, στεατικό οξύ, stearic acid) (σχήμα 11). [6] 47
48 Σχήμα 11: Απλοποιημένες πορείες της βιομηχανικής διεργασίας της μερικής και πλήρους υδρογόνωσης φυτικών ελαίων καταλυόμενη από νικέλιο στο παράδειγμα του τριλινελαϊκού τριγλυκερινεστέρα προς τον ενδιάμεσο τριελαϊκό τριεστέρα και ακολούθως προς το πλήρες υδρογονωμένο προϊόν τον τριστεατικό τριγλυκερινεστέρα όπως και η παράπλευρη αντίδραση της ισομερίωσης που δίνει τα διάφορα γεωμετρικά cis/trans-ισομερή όπως και τοπο-ισομερή (regiomers), δηλαδή ισομερή θέσης των C=C ομάδων C18:2 και C18:1 τριγλυκερινεστέρων. Όμως μαζί με την αντίδραση της υδρογόνωσης σε αυτήν την βιομηχανική διεργασία συντελείται και η παράπλευρη αντίδραση της cis/transισομερείωσης των ομάδων C=C των εδώδιμων φυτικών ελαίων προς transλίπη. Με ετερογενή καταλυτικά συστήματα Ni παράγονται μεγάλες ποσότητες trans-λιπαρών σε ποσοστό έως 50%. Τα πιο γνωστά trans-ισομερή που σχηματίζονται είναι ο C18:1 trans-9 (τριελαϊδικός τριγλυκερινεστέρας) και ο C18:1 trans-10 τριεστέρας (σχήμα 11). Η παρουσία αυτών των γεωμετρικών ισομερών πιθανόν αποτελεί συνέπεια του μηχανισμού υδρογόνωσης των Horiuti-Polanyi. Αυτός ο μηχανισμός περιγράφει την σταδιακή και αντιστρεπτή προσθήκη των προσροφημένων ατόμων υδρογόνου στον προσροφημένο διπλό δεσμό στην επιφάνεια του καταλύτη. Μετά την αντίδραση με ένα προσροφημένο άτομο υδρογόνου, σχηματίζεται ένα ημι-υδρογονωμένο ενδιάμεσο προϊόν. Αυτό το ενδιάμεσο είτε ανάγεται από την αντίδραση με το 48
49 δεύτερο άτομο υδρογόνου, οπότε σχηματίζεται κορεσμένος δεσμός, είτε χάνει ένα άτομο υδρογόνου πριν την εκρόφηση, οδηγώντας σταδιακά στον σχηματισμό γεωμετρικών trans-ισομερών και ισομερών θέσης του αρχικού ακόρεστου λιπαρού μείγματος των φυτικών ελαίων. [12] Παρόλο που τα τριγλυκερίδια που περιέχουν trans λιπαρά οξέα έχουν ιδανικά χαρακτηριστικά ως προς την υφή και την ρευστότητά τους, συνδέονται με αρνητικές επιπτώσεις στην ανθρώπινη υγεία, οι οποίες μεταφράζονται σε υψηλότερο κίνδυνο για καρδιοπάθειες. Το γεγονός αυτό μπορεί να ερμηνευθεί ως εξής: Η υδρογόνωση μπορεί να επιφέρει αλλαγές στη διαμορφωση μερικών λιπαρών οξέων. Αυτές οι δομικές αλλαγές σχετίζονται με τη διαφορετική τοποθέτηση των ανθρακικών αλυσίδων και των ατόμων υδρογόνου σε κάθε πλευρά του διπλού δεσμού. Στην κανονική ή cisδιαμόρφωση, οι ανθρακικές αλυσίδες είναι στη μία πλευρά του διπλού δεσμού, ενώ τα άτομα υδρογόνου στην άλλη. Σε συνθήκες υδρογόνωσης, η δομή των λιπαρών οξέων αλλάζει έτσι ώστε να σχηματιστεί η transδιαμόρφωση. Tα άτομα υδρογόνου είναι σε αντίθετες πλευρές στον διπλό δεσμό και παρομοίως και οι ανθρακικές αλυσίδες. Αυτά τα λιπαρά οξέα καλούνται trans-λιπαρά οξέα. Εκτός από τη γεωμετρική ισομέρεια που λαμβάνει χώρα κατά τη διάρκεια της υδρογόνωσης πραγματοποιούνται αλλαγές στο σχήμα των λιπαρών οξέων. Ένα cis-λιπαρό οξύ έχει κλήση στο διπλό δεσμό, ενώ ένα trans-λιπαρό οξύ είναι ευθύγραμμο. Αυτή η σχηματική διαφοροποίηση έχει αντίκτυπο στην μοριακή στοίβαξη των λιπιδίων (molecular packing) σε έναν περιορισμένο χώρο όπως είναι η μεμβράνη. Εάν τα φωσφολιπίδια των μεμβρανών έχουν trans- ακόρεστα λιπαρά οξέα στη δομή τους μπορούν να «πακεταριστούν» εγγύτερα, σε σύγκριση με το αν είχαν cis- ακόρεστα λιπαρά οξέα στη δομή τους. Αυτό με τη σειρά του επηρεάζει την ρευστότητα των μεμβρανών και την ευκολία με την οποία τα υλικά κινούνται μέσα ή διαμέσου αυτής. Η ρευστότητα επίσης επηρεάζει την κινητικότητα των πρωτεϊνών όπως των υποδοχέων και των μεταφορέων που είναι ενσωματωμένοι είτε εσωτερικά, είτε εξωτερικά, είτε διαμέσου των μεμβρανών. Επιπλέον, έρευνες που δημοσιεύτηκαν από το 1990 έχουν δείξει ότι η κατανάλωση trans-λιπών έχει ως συνέπεια την αύξηση της «κακής 49
50 χοληστερίνης» (LDL) και την μείωση της «καλής» (HDL), καθώς και την αύξηση των τριγλυκεριδίων στο πλάσμα του αίματος και της λιποπρωτεϊνης α, με αποτέλεσμα να υπάρχει κίνδυνος για καρδιαγγειακά επεισόδια και ασθένειες όπως η στεφανιαία νόσος. Μάλιστα οι αρνητικές αυτές επιπτώσεις στην υγεία είναι πιθανότατα σε μεγαλύτερο βαθμό από όταν γίνεται κατανάλωση σε κορεσμένα λίπη. Τέλος, υπάρχουν ενδείξεις ότι μερικοί τύποι καρκίνου καθώς και η υπογονιμότητα στις γυναίκες είναι δυνατόν να σχετίζονται με την πρόσληψη trans λιπαρών οξέων από τις τροφές. [4, 12, 14] Από τις αρχές της δεκαετίας του 1990 έχει γίνει αναφορά στην επίδραση των trans-λιπαρών οξέων, που προέρχονται από τα υδρογονωμένα λίπη της βιομηχανίας, στις μεμβράνες των αιμοφόρων αγγείων. Επομένως, οι κυβερνήσεις έχουν «πιέσει» την βιομηχανία να μειώσει την ποσότητα των trans-λιπαρών στα εδώδιμα προϊόντα. Η Δανία ήταν το πρώτο κράτος που με νομοθεσία έθεσε σε ισχύ από τον Ιανουάριο του 2004 ένα όριο έως 2% κ.β. στην περιεκτικότητα των trans-λιπαρών στα τρόφιμα με σκοπό οι άνθρωποι να καταναλώνουν λιγότερο από 1g trans-λιπών την ημέρα. Όμως στην Ευρωπαϊκή Ένωση δεν έχουν ληφθεί ακόμα αποφάσεις ώστε να ισχύουν ενιαία σε όλη την επικράτειά της όσον αφορά το επίμαχο ζήτημα των transλιπαρών και η Επιτροπή δεσμεύτηκε τον Δεκέμβριο του 2014 να δώσει στη δημοσιότητα μια έκθεση που αφορά στην παρουσία των trans-λιπαρών στα τρόφιμα. Στις ΗΠΑ η Διεύθυνση Ελέγχου Τροφίμων και Φαρμάκων (Food and Drug Administration, FDA) αποφάσισε την 1 η Ιανουαρίου του 2006 να δηλώνεται πάνω στην πινακίδα του τροφίμου το ποσοστό των trans-λιπών μέσα στο συγκεκριμένο προϊόν. [6, 12] Η επισήμανση όμως αυτή των trans-λιπών επηρεάζει άμεσα την ψυχολογία των καταναλωτών, όπως αυτό αντικατοπτρίζεται στις πωλήσεις των εδώδιμων φυτικών ελαίων. Πριν από δέκα περίπου χρόνια το σογιέλαιο συνιστούσε το 80 % της κατανάλωσης στις ΗΠΑ και από τότε έχει μειωθεί στο 65%. Επιπλέον το 2004 ο σύμβουλος και συνεργάτης της AOCS, Walter Farr σημείωσε: «Πάντα θα υπάρχει η ανάγκη για υδρογόνωση πολλών προϊόντων, αλλά ο όγκος των ελαίων που πρόκειται να υδρογονωθούν μειώνεται». [13] Για αυτόν τον λόγο, από το 2003, η βιομηχανία εδώδιμων ελαίων 50
51 αναγκάστηκε, λόγω των προβλημάτων που σχετίζονται με τα επιβλαβή για την υγεία trans-λίπη, να αναπροσαρμόσει τις διεργασίες υδρογόνωσης φυτικών ελαίων και από βαριά υδρογονωμένα λίπη να στραφεί προς τα ελαφρώς υδρογονωμένα έλαια, όπου τα τελευταία χρόνια σημειώνεται μια συνεχής αύξηση της χωρητικότητας παραγωγής τους. Τροπικά έλαια αντικατέστησαν τα trans-λίπη για την παραγωγή τροφίμων επειδή τα τροπικά έλαια περιέχουν σε ένα πολύ υψηλό ποσοστό (μέχρι ~ 90%) κορεσμένα λιπαρά. Έλαια αυτού του τύπου είναι π.χ. το φοινικέλαιο (palm oil), το φοινικικό πυρηνέλαιο (palm kernel oil) και το έλαιο καρύδας (coconut oil). Μια άλλη ευρύτατα διαδεδομένη μέθοδος για τη αποφυγή του σχηματισμού των trans-λιπαρών σήμερα είναι η πορεία της πλήρους υδρογόνωσης των εδώδιμων ελαίων προς το κορεσμένο προϊόν τον τριστεατικό τριγλυκερινεστέρα (σχήμα 11) συνδυασμένη με την αντίδραση της διαεστεροποίησης (interesterification) του κορεσμένου τριστεατικού τριεστέρα με το εδώδιμο έλαιο προς ένα τελικό προϊόν με ενδιάμεσες φυσικές ιδιότητες αλλά με μηδενικά ποσοστά σε trans-λίπη. Σήμερα, η παραγωγή σογιελαίου και φοινικέλαιου αποτελούν το ~ 60% της παγκόσμιας χωρητικότητας παραγωγής εδώδιμων ελαίων. Εδώ πρέπει να αναφερθεί ότι πολύ πρόσφατες μελέτες δείχνουν ότι η κατανάλωση σε κορεσμένα λίπη δεν σχετίζεται άμεσα με έναν αυξημένο κίνδυνο καρδιαγγειακών νόσων. [12] Εν κατακλείδι, η βιομηχανία επεξεργασίας εδώδιμων ελαίων ήταν πάντα ευέλικτη και ικανή να καινοτομήσει με βελτιωμένες τεχνολογίες και προϊόντα προσαρμοσμένα στις ανάγκες των καταναλωτών. Όπως αναφέρει και ο G.R. List [13] η υδρογόνωση των φυτικών ελαίων αν και δεν είναι πλέον ακμάζουσα, μπορεί όμως ακόμα να προσφέρει υπηρεσίες στο πεδίο της παραγωγής τροφίμων υψηλής ποιότητας. 51
52 Υδρογόνωση φυτικών ελαίων καταλυόμενη από λευκόχρυσο Όπως αναφέρθηκε ανωτέρω, η μερική υδρογόνωση εδώδιμων φυτικών ελαίων οδηγεί στον σχηματισμό ανεπιθύμητων trans λιπαρών οξέων, η κατανάλωση των οποίων διαμέσου των τροφών έχει αρνητικές επιπτώσεις στην ανθρώπινη υγεία. Έτσι, τα τελευταία χρόνια πραγματοποιούνται συνεχώς έρευνες προκειμένου να βελτιωθούν οι συνθήκες και τα καταλυτικά συστήματα υδρογόνωσης και να μειωθεί το παραγόμενο ποσοστό των transλιπαρών οξέων. Πολλές ερευνητικές ομάδες συγκλίνουν στο γεγονός ότι η χρήση του λευκόχρυσου ως καταλύτη, στην αντίδραση υδρογόνωσης εδώδιμων φυτικών ελαίων, μειώνει αισθητά τα επίπεδα των trans-λιπών σε σύγκριση με τους συμβατικούς καταλύτες νικελίου Ni. Ο Pierre Jacobs και η ομάδα του [12, 15-17], το έτος 2010 ανέπτυξαν τη μερική υδρογόνωση του σογιέλαιου με την χρήση δύο διαφορετικών ετερογενών καταλυτών λευκοχρύσου, στηριγμένο σε μικροπορώδες ζεόλιθο ZSM-5 και Pt στηριγμένο σε μεσοπορώδη φορέα Al 2 O 3. Και οι δύο αυτοί καταλύτες οδηγούσαν στον σχηματισμό σχεδόν αμελητέας ποσότητας transισομερών στο υδρογονωμένο προϊόν. Συγκεκριμένα, η χρήση του καταλύτη Pt/ZSM-5 είχε ως αποτέλεσμα την ύπαρξη μόνο ενός ποσοστού της τάξεως του 2 κ.β% trans-c18:1 τριεστέρων, στην σύσταση του τελικού προϊόντος, ενώ ο καταλύτης ήταν ιδιαίτερα εκλεκτικός αφού μετά το πέρας της αντίδρασης δεν είχε μείνει σχεδόν καθόλου ποσότητα λινολενικού οξέος (0.2 κ.β%) και ο σχηματισμός του πλήρως κορεσμένου τριστεατικού τριγλυκερινεστέρα ήταν ιδιαίτερα χαμηλός. Ο καταλύτης Pt/Al 2 O 3 δίνει ακόμη χαμηλότερο ποσοστό σε trans-ισομερή, 0.8 κ.β% trans-c18:1 τριεστέρες, ωστόσο δεν εμφανίζει ικανοποιητική εκλεκτικότητα όσον αφορά το σχηματισμό του κορεσμένου τριστεατικού τριγλυκερινεστέρα ο οποίος λαμβάνεται σε υψηλά ποσοστά. [12, 15-17] Η ερευνητική ομάδα του J.J Leahy [18] ανέφερε το 2010 την ετερογενή καταλυτική υδρογόνωση του ηλιέλαιου με την χρήση καταλυτών Pt στηριγμένους σε μεσοπορώδη SiO 2. Η ομάδα χρησιμοποίησε διαφορετικά πρόδρομα συστήματα λευκοχρύσου όπως H 2 PtCl 6 και Pt(acac) 2 και έκανε 52
53 σύγκριση της καταλυτικής δραστικότητας και εκλεκτικότητας ως προς τον σχηματισμό των trans ισομερών των λιπαρών οξέων. Τα αποτελέσματα έδειξαν ότι το σύστημα H 2 PtCl 6 παρουσίαζε μεγαλύτερη καταλυτική δραστικότητα από το σύστημα Pt(acac) 2, η οποία είναι δυνατόν να οφείλεται στην ύπαρξη του χλωριδίου στο φορέα του ετερογενούς καταλύτη που θεωρείται ότι βελτιώνει τη διάχυση υδρογόνου από το μέταλλο στο φορέα (spillover) σε αυτόν και πιθανόν την καταλυτική δραστικότητα. [18] Το 2009 η ομάδα του P.H. Pfromm [19] ανέφερε την μερική υδρογόνωση του σογιέλαιου χρησιμοποιώντας έναν υψηλής απόδοσης καταλύτη ο οποίος αποτελείτο από πολυαιθεραμιδική μεμβράνη με διασπαρμένο πάνω σε αυτήν λευκόχρυσο. Η αντίδραση της υδρογόνωσης με την χρήση αυτού του καταλυτικού συστήματος μέταλλο/πολυμερές, οδηγούσε στην παραγωγή μόνο 4 κ.β% trans-λιπαρών προϊόντων, σε σύγκριση με τα συμβατικά ετερογενή συστήματα Pt/C στα οποία το ποσοστό των trans-λιπαρών οξέων ξεπερνούσε το 10 κ.β%. Αξίζει να αναφερθεί ότι η αντίδραση διεξαγόταν σε σχετικά ήπιες συνθήκες, P H2 = 65 psi και θερμοκρασία περίπου 70 0 C. [19] Ο D.E. Damiani και οι συνεργάτες του [20], το 2008 πραγματοποίησαν πειράματα για να συγκρίνουν την ετερογενή με την ομογενή κατάλυση σε υπερκρίσιμο προπάνιο στην αντίδραση υδρογόνωσης ηλιέλαιου με τη χρήση Pt στηριγμένου σε TiO 2. Η προσθήκη προπανίου ως υπερκρίσιμος διαλύτης στο μίγμα αντίδρασης επέτρεπε την διεξαγωγή της αντίδρασης σε ομογενές σύστημα το οποίο βρισκόταν σε επαφή με τον στερεό καταλύτη. Έτσι, παρατηρήθηκε σημαντική αύξηση της ταχύτητας της αντίδρασης στο ομογενές σύστημα. Όσον αφορά την εκλεκτικότητα, ο σχηματισμός trans ισομερών ήταν υψηλότερος στο συμβατικό ετερογενές σύστημα, ενώ στο ομογενές σύστημα η ευνοείται η παραγωγή κορεσμένων ενώσεων. [20] Καταλύτες παλλαδίου στην υδρογόνωση φυτικών ελαίων όπως και των αλκυλεστέρων τους Παρόμοια με τον λευκόχρυσο, το παλλάδιο αποτελεί έναν εναλλακτικό καταλύτη υδρογόνωσης εδώδιμων φυτικών ελαίων σε σύγκριση με τον συμβατικό καταλύτη νικελίου που χρησιμοποιήθηκε πρώτα στη διεργασία 53
54 αυτή. Έτσι, πολλές ερευνητικές ομάδες ασχολούνται με την ανάπτυξη και βελτίωση ετερογενών κυρίως καταλυτών παλλαδίου. Το 2005 ο J. Barbier και οι συνεργάτες του [21] ανέφεραν την εκλεκτική υδρογόνωση αιθυλεστέρων του ηλιέλαιου, σε χαμηλή θερμοκρασία (40 0 C), σε αιθανόλη ως διαλύτη, παρουσία στηριγμένων καταλυτών παλλαδίου σε διάφορους φορείς οξειδίων. Η ομάδα αυτή παρατήρησε ότι η προσθήκη αμινών στο μέσο αντίδρασης τροποποιεί τις καταλυτικές ιδιότητες του Pd/SiO 2. Ανάλογα με την ποσότητα και την φύση των προστιθέμενων αμινών (αλειφατικές, με γραμμική ή διακλαδισμένη αλυσίδα και κυκλικές ενώσεις) η καταλυτική δραστικότητα μπορεί είτε να μην μεταβληθεί, είτε να ανασταλεί. Αυτή η καταλυτική συμπεριφορά είναι αποτέλεσμα ενός ηλεκτρονικού φαινομένου, που λειτουργεί ως προωθητής και οφείλεται στην παρουσία των αμινών και ενός γεωμετρικού φαινομένου, που λειτουργεί ως αναστολέας και σχετίζεται με την προσρόφοση αυτών των αζωτούχων ενώσεων στην επιφάνεια του παλλαδίου. Οποιαδήποτε κι αν είναι όμως η φύση των αμινών επάγει την αύξηση της εκλεκτικότητας σε cis-c18:1 εστέρες, που είναι τα επιθυμητά προϊόντα. [21] Ο D.E. Damiani και η ομάδα του [22], το 2006 υδρογόνωσαν ηλιέλαιο με την χρήση καταλύτη παλλαδίου στηριγμένου σε γ-al 2 O 3. Η ομάδα αυτή διαφοροποιήθηκε ως προς την χρήση υπερκρίσιμου διαλύτη προπανίου, οπότε η αντίδραση τελικά πραγματοποιήθηκε στην ομογενή φάση, η οποία βρισκόταν σε επαφή με τον στερεό καταλύτη. [22] Η ίδια ομάδα, το 2009, συνέθεσε έξι καταλύτες παλλαδίου χρησιμοποιώντας διαφορετικά πρόδρομα συστήματα όπως π.χ. ακετυλοακετονικό παλλάδιο, νιτρικό παλλάδιο και νιτρικό τετρααμινοπαλλάδιο και διαφορετικούς φορείς (α- Al 2 O 3, γ-al 2 O 3, ZSM- 5, MCM-22). Η καταλυτική δραστικότητα και εκλεκτικότητα αυτών των καταλυτών εξετάστηκε στην αντίδραση υδρογόνωσης ηλιέλαιου και συγκρίθηκε με αυτήν των εμπορικών καταλυτών νικελίου. Οι καταλύτες Pd παρουσίασαν υψηλότερη δραστικότητα, μεγαλύτερη εκλεκτικότητα ως προς τον σχηματισμό μονοακόρεστων εστέρων και παρόμοια μετατροπή όσον αφορά στην παραγωγή των trans-ισομερών, σε σύγκριση με τον συμβατικό καταλύτη Ni. [23] 54
55 Μία αντίδραση υδρογόνωσης ακόρεστων μεθυλεστέρων ή ακόρεστων λιπαρών οξέων με καταλυτικό σύστημα νανοσωματιδίων παρουσιάστηκε από τον Α. Behr και τους συνεργάτες του [24]. Η ομάδα αυτή ανέπτυξε ένα καταλυτικό σύστημα που αποτελούνταν από σταθεροποιημένα κολλοειδή συστήματα παλλαδίου προκειμένου να υδρογονώσει μονοακόρεστα ή πολυακόρεστα λιπαρά οξέα σε κορεσμένα οξέα σε ήπιες συνθήκες θερμοκρασίας και πίεσης με ικανότητα ανάκτησης του καταλύτη. [24] Το 2014 στο εργαστήριο μας [11] επιτεύχθηκαν ιδιαίτερα υψηλές καταλυτικές δραστικότητες (TOF = h -1 ) στην υδρογόνωση ανανεώσιμων πολυακόρεστων μεθυλεστέρων του σογιέλαιου προς μονοακόρεστους εστέρες, σε υδατικό/οργανικό διφασικό, μικυλλιακό σύστημα καταλυόμενη από νανοσωματίδια Pd 0 σταθεροποιημένα από υδατοδιαλυτούς αζωτούχους υποκαταστάτες. Το πρόδρομο καταλυτικό σύστημα χλωρίδιο του Pd ΙΙ παρουσίασε υψηλή καταλυτική δραστικότητα με τους ποικίλους αζωτούχους υποκαταστάτες. Συγκεκριμένα, η καταλυτική δραστικότητα του παλλαδίου με το δινάτριο άλας της δισουλφονικής βαθοφαινανθρολίνης (BPhDS), έφτασε τα TOF = h -1 και με το τετρανάτριο άλας του αιθυλενοδιαμινοτετραοξικού οξέος (EDTA Na 4 ) τα TOF = h -1. Η δραστικότητα αυτή είναι σημαντικά μεγαλύτερη, συγκρινόμενη με εκείνη του συστήματος Pd/TPPTS (TOF = h -1 ). Πειράματα με Hg απέδειξαν την ετερογενή φύση του καταλύτη Pd/BPhDS, ενώ ένα πείραμα ανακύκλωσης που πραγματοποιήθηκε στους C έδειξε ότι η δραστικότητα του καταλυτικού συστήματος παρέμεινε αρκετά υψηλή, υποδεικνύοντας ένα σταθερό καταλυτικό νανασωματίδιο Pd (0). [11] Υδρογόνωση φυτικών ελαίων καταλυόμενη από νικέλιο Οι ετερογενείς καταλύτες νικελίου ήταν οι πρώτοι που χρησιμοποιήθηκαν στην βιομηχανική διεργασία υδρογόνωσης εδώδιμων ελαίων. Η υδρογόνωση λιπαρών ελαίων στην υγρή φάση με καταλύτη νικελίου έγινε πατέντα από τον W. Normann το 1902, ενώ λίγο νωρίτερα ο P. Sabatier είχε αναφέρει την υδρογόνωση ακόρεστων οργανικών ενώσεων στην αέρια φάση από μεταλλικό νικέλιο. Το 1906 καθιερώθηκε βιομηχανικά η διεργασία της 55
56 υδρογόνωσης από την εταιρεία Joseph Crossfield and Sons, στην επεξεργασία ιχθυέλαιου φάλαινας με τη χρήση νικελίου. Το 1911 η εταιρεία Procter & Gamble παρήγαγε το πρώτο υδρογονωμένο προϊόν φυτικής προέλευσης με την επωνυμία Crisco. Έκτοτε, σχεδόν όλες οι βιομηχανικές διεργασίες μερικής υδρογόνωσης εδώδιμων φυτικών ελαίων διεξάγονται με τη χρήση εμπορικών, ετερογενών καταλυτών Ni, οι οποίοι παράγουν έως και 50 % trans-λιπαρά οξέα. [12] Ενδεικτικά, αναφέρουμε μερικές εργασίες διαφόρων ερευνητικών ομάδων, οι οποίες χρησιμοποίησαν ετερογενείς καταλύτες Ni στην υδρογόνωση φυτικών ελαίων και πολλές από αυτές έκαναν κινητική μελέτη της αντίδρασης υδρογόνωσης. Το 1979 ο Schuerch και οι συνεργάτες του [25] πραγματοποίησαν κινητικές μελέτες στην αντίδραση υδρογόνωσης και ισομερείωσης του ηλιέλαιου στην υγρή φάση, με καταλύτες νικελίου. Το 1990 οι S.M. Echeverria και V.M. Andres [26] εξέτασαν την επίδραση της μεθόδου σύνθεσης πάνω στην καταλυτική δραστικότητα των καταλυτών Ni σε γη διατόμων, στην αντίδραση υδρογόνωσης φυτικών ελαίων. Δύο χρόνια αργότερα ο S. Mendioroz και η ομάδα του [27] ερεύνησαν την δραστικότητα και εκλεκτικότητα καταλυτών Ni στηριγμένων σε πυριτία, στην αντίδραση υδρογόνωσης ηλιέλαιου. Το 2006 και το 2008 ο R.J. Grau και οι συνεργάτες του [28,29] πρότειναν κινητικά μοντέλα στην αντίδραση υδρογόνωσης του ελαϊκού μεθυλεστέρα υπεράνω καταλύτη Ni/α-Al 2 O 3 στην υγρή φάση. Τέλος το 2007 ο D.E. Damiani και η ομάδα του [30] επανεξέτασαν την αντίδραση υδρογόνωσης του ηλιέλαιου υπεράνω καταλυτών νικελίου σε διαφορετικές συνθήκες αντίδρασης. Πρέπει επίσης να γίνει αναφορά στην χρήση του καταλύτη νικελίου στην διεργασία SHOP (Shell Higher Olefin Process). Η αντίδραση ολιγομερισμού του αιθυλενίου και η ακόλουθη ισομερείωση και μετάθεση σχεδιάστηκε για να καλύψει τις ανάγκες της αγοράς για γραμμικές α-ολεφίνες για απορρυπαντικά κ.λπ. Το πρώτο εργοστάσιο φτιάχτηκε στο Geismar του LA το 1977 από τη Shell και στο Stanlow, UK το 1982, και σήμερα παράγουν 1 εκατομμύριο τόνους ολεφινών το έτος. Η αντίδραση του ολιγομερισμού λαμβάνει χώρα σε έναν πολικό διαλύτη, συνήθως 1,4-βουτανοδιόλη, στον οποίο είναι διαλυτός ο 56
57 καταλύτης Ni και η α-ολεφίνη σχεδόν αδιάλυτη. Πρόκειται για ένα διφασικό σύστημα υγρού/υγρού και μάλιστα του πρώτου που χρησιμοποιήθηκε. Ως καταλύτης χρησιμοποιείται ένα χηλικό (P-O) σύμπλοκο του νικελίου, το οποίο ελέγχει την εκλεκτικότητα της αντίδρασης. Τα σύμπλοκα αυτά ολιγομερίζουν το αιθυλένιο στο τολουόλιο στους 80 0 C και πίεση 5 MPa μέχρι 99% γραμμικής ολεφίνης και μάλιστα 98% α-ολεφίνης. [31] Κλείνοντας πρέπει να αναφέρουμε ότι πολλές ερευνητικές ομάδες έχουν κάνει σύγκριση μεταξύ των συμβατικών ετερογενών καταλυτών νικελίου και των εναλλακτικών καταλυτών λευκοχρύσου και παλλαδίου στην αντίδραση υδρογόνωσης εδώδιμων φυτικών ελαίων. Όλα τα αποτελέσματα συγκλίνουν στο γεγονός ότι οι καταλύτες παλλαδίου συνήθως εμφανίζουν τη μεγαλύτερη καταλυτική δραστικότητα έναντι των δύο άλλων μετάλλων. Σε αντιδιαστολή, οι καταλύτες λευκοχρύσου δίνουν το μικρότερο ποσοστό στην παραγωγή των ανεπιθύμητων trans-λιπαρών και είναι πιο δραστικοί από τους καταλύτες Ni. [30] Υδρογόνωση φυτικών ελαίων και παραγώγων τους καταλυόμενη από χαλκό Ο χαλκός είναι ένα ακόμη μέταλλο που χρησιμοποιείται ως εναλλακτικός καταλύτης στην αντίδραση υδρογόνωσης εδώδιμων φυτικών ελαίων. Η χρήση και αυτού του καταλύτη σκοπό έχει την υδρογόνωση των πολυακόρεστων χωρίς ικανότητα υδρογόνωσης των μονοακόρεστων λιπαρών εστέρων προς τον τριστεατικό τριγλυκερινεστέρα. Το 1965 η ερευνητική ομάδα του C. Okkerse δημοσίευσε στο Nature [32] μία εργασία στην οποία συνέκρινε τις ιδιότητες του νικελίου και του χαλκού ως καταλύτες στην αντίδραση υδρογόνωσης του σογιέλαιου. Τα πειράματα έδειξαν ότι παρουσία του καταλύτη χαλκού το λινολενικό οξύ (C18:3) υδρογονώνεται εκλεκτικά προς το λινολεϊκό οξύ (C18:2) και ακολούθως προς ελαϊκό οξύ (C18:1), ενώ αυτό δεν συμβαίνει όσον αφορά την αναγωγή του C18:1 προς στεατικό οξύ και σε αντίθεση με την παρουσία καταλυτών νικελίου. Σε ότι αφορά το ποσοστό των trans-c18:1 ισομερών δεν παρατηρήθηκαν σημαντικές διαφορές μεταξύ των δύο καταλυτών. [32] 57
58 Η N. Ravasio και η ομάδα της [33], το 2002, ανέφεραν την εκλεκτική υδρογόνωση φυτικών ελαίων και των μεθυλεστέρων τους με την χρήση ετερογενών καταλυτών χαλκού. H ομάδα παρατήρησε ότι όταν οι καταλύτες ήταν προ-ανηγμένοι ex situ, ήταν πιο δραστικοί από εκείνους που ανάγονταν μέσα στο μίγμα αντίδρασης. Επιπλέον, ανέφερε ότι με την χρήση του καταλύτη Cu/SiO 2 το λινολενικό οξύ (C18:3) μπορεί να περιοριστεί και το λινολεϊκό οξύ (C18:2) μειώνεται από 22% σε 3-5%, χωρίς να αυξάνεται το ποσοστό του στεατικού οξέος (C18:0). Επίσης, με την χρήση αυτού του καταλύτη περιορίζεται η cis/trans ισομερείωση του ολεϊκού οξέος (C18:1). Η ίδια ομάδα [34], το 2009 δημοσίευσε μια σειρά πειραμάτων στα οποία με την χρήση του ίδιου καταλύτη κατάφερε να υδρογονώσει πολυακόρεστους μεθυλεστέρες ποικίλων μη εδώδιμων ελαίων εκλεκτικά προς τους μονοακόρεστους μεθυλεστέρες με σκοπό να συνθέσει πρώτες ύλες κατάλληλες για παραγωγή βιοντίζελ. [33, 34] Καταλυτική υδρογόνωση παρουσία σιδήρου Ο σίδηρος θα έπρεπε να είναι ένας από τους δημοφιλείς καταλύτες της ομογενούς κατάλυσης, αφού παρουσιάζει πολλά πλεονεκτήματα, όπως μη τοξικότητα, διαθεσιμότητα και χαμηλή τιμή. Όπως αναφέρει ο M. Beller και η ομάδα του [36], το πεδίο της ομογενούς κατάλυσης με σύμπλοκα του σιδήρου έχει πολύ μεγάλο ενδιαφέρον και αποτελεί «φλέγον ζήτημα». Έτσι τις τελευταίες δύο δεκαετίες οι αντιδράσεις αναγωγής καταλυόμενες από σύμπλοκα του Fe έχουν διερευνηθεί διεξοδικά, όπως αυτό αντανακλάται από το πλήθος των εργασιών πάνω σε αυτό το πεδίο. Ιδιαίτερη όμως προσοχή έχει δοθεί στην υδρογόνωση ολεφινών και καρβονυλο-ενώσεων και στην υδροπυριτίωση. H πρώτη καταλυτική υδρογόνωση ολεφινών παρουσία του συμπλόκου πεντακαρβονυλίου του σιδήρου χρονολογείται το 1960 [35, 36]. Ο Ε.Ν. Frankel και οι συνεργάτες του ασχολήθηκαν με την υδρογόνωση των μεθυλεστέρων του λινολεϊκού και λινολενικού οξέος καταλυόμενη από πεντακαρβονύλιο του σιδήρου υπό δραστικές συνθήκες (T = C, P H2 = 30 bar). Τα προϊόντα της αντίδρασής τους ήταν κυρίως μονοακόρεστοι εστέρες 58
59 με μια αμελητέα ποσότητα του πλήρως κορεσμένου στεατικού μεθυλεστέρα [36]. Πιο πρόσφατες έρευνες πάνω στο πεδίο έχουν διεξαχθεί από τον P.J. Chiric και τους συνεργάτες του [38] στην υδρογόνωση ολεφινών υπό ήπιες συνθήκες με τη χρήση του συμπλόκου του σιδήρου με τρισχιδή υποκαταστάτη πυριδινοδιιμίνης ( ipr PDI)Fe(N 2 ) 2, σε τολουόλιο σε θερμοκρασία δωματίου (σχήμα 12), του οποίου η καταλυτική δραστικότητα στην υδρογόνωση του 1- εξενίου φτάνει τα 1814 h -1 TOF. Αυτή η δραστικότητα υπερβαίνει μακράν την αποδοτικότητα, στις ίδιες συνθήκες, του καταλύτη Pd πάνω σε C TOF = 366 h -1, του καταλύτη του Wilkinson (PPh 3 ) 3 RhCl TOF = 12 h -1, και του καταλύτη του Crabtree [(cod)ir(pcy 3 )py]pf 6 TOF = 75 h -1. [35-38] Οι J.C. Peters και E.J. Daida [35, 36] περιέγραψαν ένα πρόδρομο καταλυτικό σύστημα του τύπου [PhBP ipr 3]Fe-R (Α) και [PhBP ipr 3]Fe(H) 3 (PR 3 ) (Β) τα οποία έχουν χρησιμοποιηθεί στην υδρογόνωση ολεφινών και συγκεκριμένων αλκινίων (σχήμα 13). Τα σύμπλοκα του τύπου Α ήταν πιο δραστικά TOF = 1.5 h -1 από εκείνα του τύπου Β TOF = 0.5 h -1 για την υδρογόνωση του στυρενίου σε θερμοκρασία δωματίου υπό ατμοσφαιρική πίεση υδρογόνου. Το οξειδοαναγωγικό ζεύγος Fe (II)/(IV) είναι πιθανώς υπεύθυνο για την καταλυτική λειτουργία των συμπλόκων. [35, 36] Σχήμα 12: Η αντίδραση υδρογόνωσης του 1-εξενίου υπό ήπιες συνθήκες με τη χρήση του συμπλόκου ( ipr PDI)Fe(N 2 ) 2, σε τολουόλιο σε θερμοκρασία δωματίου. 59
60 Σχήμα 13: Τα πρόδρομα καταλυτικά συστήματα του τύπου [PhBPiPr 3 ]Fe-R (Α) και [PhBPiPr 3 ]Fe(H) 3 (PR 3 ) (Β) τα οποία έχουν χρησιμοποιηθεί στην υδρογόνωση ολεφινών. Ο J. G. de Vries και οι συνεργάτες του [35, 36] έδειξαν ότι τα νανοσωματίδια σιδήρου είναι αποτελεσματικοί καταλύτες στην υδρογόνωση αλκενίων και αλκινίων. Η αντίδραση λαμβάνει χώρα σε THF σε θερμοκρασία δωματίου και σε τυπική πίεση υδρογόνου 20 bar. Επιπλέον, νανοσωματίδια Fe στηριγμένα σε γραφένιο έχουν χρησιμοποιηθεί ως καταλύτες για την υδρογόνωση πολλών α- και κυκλικών ολεφινών και του 1-φαινυλο-προπινίου. Ο καταλύτης μπορεί να απομακρυνθεί με απόχυση της υγρής φάσης, κατά τη διάρκεια της οποίας τα νανοσωματίδια σιδήρου συγκρατώνται με μαγνήτη. Έτσι, ο καταλύτης μπορεί να ξαναχρησιμοποιηθεί χωρίς σημαντική απώλεια της δραστικότητάς του. [35, 36] Πιο πρόσφατα ο B.M. Bhanage και η ομάδα του [39] πραγματοποίησαν εκλεκτική υδρογόνωση διπλών δεσμών C=C, α,β-ακόρεστων καρβονυλοενώσεων, σε διφασικό σύστημα, χρησιμοποιώντας το υδατοδιαλυτό σύμπλοκο Fe II /Na 2 EDTA, ως καταλύτη. Τα δύο υποστρώματα που υδρογονώθηκαν ήταν η κινναμαλδεΰδη και η κιτράλη (σχήμα 14). [39] 60
61 Σχήμα 14: Η αντίδραση υδρογόνωσης της κινναμαλδεΰδης. Το 2014 τρεις ανεξάρτητες ερευνητικές ομάδες του D. Milstein [41], των H. Guan και N.T. Fairweather [43], και του M. Beller [42] ανέφεραν τα πρώτα παραδείγματα ομογενούς κατάλυσης με σύμπλοκα του σιδήρου ως καταλύτες στην υδρογόνωση εστέρων προς αλκοόλες υπό σχετικά ήπιες συνθήκες. Οι τρεις ομάδες χρησιμοποίησαν παρόμοια στη δομή σύμπλοκα σιδήρου, δηλαδή θραύσματα [Fe(H) 2 (CO)] ή [Fe(H)(HBH 3 )(CO)], τα οποία συμπλέκονται με τρισχιδή υποκαταστάτη φωσφόρου (Ρ)/αζώτου (Ν) (PNP), τύπου λαβίδας (pincer-type ligand) (σχήμα 15). [40] Ο D. Milstein και οι συνεργάτες του [41], ήταν οι πρώτοι που ανέφεραν την υδρογόνωση τριφθοροοξικών εστέρων προς αλκοόλες με τη χρήση του καταλυτικού συμπλόκου σιδήρου-pnp (σχήμα 15) παρουσία ισχυρής βάσης. Οι συνθήκες αντίδρασης ήταν σχετικά ήπιες P H2 = 5-25 bar και θερμοκρασία 40 0 C. Η ομάδα του Μ. Beller [42] ήταν η πρώτη που ανέφερε την αναγωγή εστέρων προς αλκοόλες καταλυόμενη από σύμπλοκα του τύπου Fe-PNP (σχήμα 15) χωρίς την προσθήκη βάσης. Το ίδιο έτος η ομάδα του H. Guan σε συνεργασία με την εταιρεία Procter & Gamble Co [43, 44] ανέπτυξαν τη διεργασία ομογενούς υδρογόνωσης λιπαρών μεθυλεστέρων του καρυδέλαιου προς λιπαρές αλκοόλες με τη χρήση συμπλόκων του τύπου Fe-PNP (σχήμα 15). Αυτοί οι καταλύτες λειτουργούν σε ουδέτερες συνθήκες, χωρίς την παρουσία διαλυτών και βάσεων. Τα 61
62 αντίστοιχα καταλυτικά συστήματα του ρουθηνίου παρουσιάζουν υψηλή παραγωγικότητα που φτάνει ως τα 1860 ΤΟΝs, μεταβαίνοντας εύκολα από την κλίμακα των γραμμαρίων σε αυτή των κιλών, ενώ τα συστήματα που βασίζονται στο σίδηρο (σχήμα 15) παρουσιάζουν χαμηλότερες παραγωγικότητες. Σχήμα 15: Τα σύμπλοκα του σιδήρου-pnp, pincer τύπου για την υδρογόνωση εστέρων προς αλκοόλες Εναντιοεκλεκτική υδρογόνωση προχειρόμορφων ολεφινών για την παραγωγή του φαρμάκου L-dopa (Διεργασία Monsanto) Το L-dopa [3-(3,4-διυδροξυφαινυλο)αλανίνη] είναι ένα εξαιρετικά αποτελεσματικό φάρμακο για την θεραπεία των συμπτωμάτων της νόσου του Parkinson. Το φάρμακο αυτό προέρχεται από την εναντιοεκλεκτική υδρογόνωση παραγώγων του ακεταμιδιοκινναμωμικού οξέος που ανέπτυξε η εταιρεία Monsanto το 1971 σε βιομηχανική κλίμακα παραγωγής. Στη διεργασία αυτή εφαρμόζεται για πρώτη φορά ομογενής καταλυτική υδρογόνωση και συντίθεται για πρώτη φορά χειρόμορφη φαρμακευτική ύλη με ασύμμετρη κατάλυση παρουσία χειρόμορφων συμπλόκων. Η διεργασία χρησιμοποιεί καταλύτες τύπου Wilkinson δηλαδή συστήματα ροδίου τροποποιημένα με την χειρόμορφη διφωσφίνη {o-ch 3 O-C 6 H 4 (C 6 H 5 )P-(CH 2 ) 2 - P(C 6 H 5 )C 6 H 4 -o-o CH 3 } (γνωστή ως DIPAMP), η οποία αναπτύχθηκε από τον W.S. Knowless (βραβείο Nobel Χημείας, 2001). Το προϊόν L-dopa σχηματίζεται με 99% ee και η χωρητικότητα παραγωγής του είναι 200 τόννοι το χρόνο (σχήμα 16). [2] 62
63 Σχήμα 16: Εναντιοεκλεκτική υδρογόνωση παραγώγων του ακεταμιδιοκινναμωμικού οξέος προς L-dopa καταλυόμενη από χειρομορφικούς καταλύτες Rh/DIPAMP σύμφωνα με την διεργασία Monsanto (o-an = C 6 H 4 -o-och 3, S = μεθανόλη). Στο 2 ο στάδιο παρουσία H 3 O + πραγματοποιείται η υδρόλυση του εστέρα προς L-dopa Υδρογονόλυση λιπαρών μεθυλεστέρων προς λιπαρές αλκοόλες Η καταλυτική αντίδραση της υδρογονόλυσης λιπαρών μεθυλεστέρων προς λιπαρές αλκοόλες ανακαλύφθηκε από διάφορες ερευνητικές ομάδες όπως π.χ. από την ομάδα του Adkins και Sauer μεταξύ των ετών και αναπτύχθηκε τη δεκαετία του 1930 από τον τότε όμιλο Deutsche Hydrierwerke (Σήμερα: Cognis GmbH - BASF) στη βιομηχανική κλίμακα παραγωγής. Οι λιπαρές αλκοόλες είναι μια σπουδαία τάξη χημικών ενώσεων με μια ετήσια χωρητικότητα παραγωγής περίπου 1 x 10 6 τόννους το χρόνο, έχουν ένα μήκος ανθρακικής αλυσίδας C 10 - C 18, είναι πρωτοταγείς αλκοόλες και χρησιμοποιούνται στην παραγωγή ενώσεων με εξειδικευμένες χρήσεις (specialties) όπως είναι οι επιφανειοδραστικές ουσίες, οι γαλακτωματοποιητές, τα λιπαντικά, οι πλαστικοποιητές, οι βιομηχανικοί διαλύτες και παίζουν επίσης ένα ρόλο στη βιομηχανία καλλυντικών και τροφίμων. Το μίγμα τροφοδοσίας της υδρογονόλυσης, οι λιπαροί μεθυλεστέρες λαμβάνονται από τη μετεστεροποίηση τροπικών ελαίων όπως είναι π.χ. το φοινικικό πυρηνέλαιο και το έλαιο καρύδας (προφίλ λιπαρών οξέων όμοιο με το φοινικικό πυρηνέλαιο) ή φυτικών ελαίων με μεθανόλη παρουσία βάσεων ως καταλύτες. Η βιομηχανική διεργασία της καταλυτικής υδρογονόλυσης λιπαρών εστέρων προς λιπαρές αλκοόλες (σχήμα 17) συντελείται υπό δραστικές συνθήκες που είναι υψηλές θερμοκρασίες, T =
64 350 ºC, και πολύ υψηλές πιέσεις υδρογόνου, P H2 = bar, υπεράνω ετερογενών καταλυτικών συστημάτων CuO/Cr 2 O 3 /Al 2 O 3 που ονομάζονται καταλύτες τύπου Adkins. Σχήμα 17: Οι αντιδράσεις που συντελούνται στη βιομηχανική διεργασία της καταλυτικής υδρογονόλυσης ανανεώσιμων λιπαρών μεθυλεστέρων προς λιπαρές αλκοόλες στο παράδειγμα της υδρογονόλυσης μίγματος μεθυλεστέρων του φοινικικού πυρηνέλαιου προς τις αντίστοιχες λιπαρές αλκοόλες υπεράνω ετερογενών καταλυτικών συστημάτων τύπου Adkins. Τα καταλυτικά συστήματα CuO/Cr 2 O 3 /Al 2 O 3 δεν παρουσιάζουν εκλεκτικότητα στις αντιδράσεις υδρογονόλυσης και υδρογόνωσης ώστε οι ανανεώσιμοι ακόρεστοι λιπαροί μεθυλεστέρες υπό τις δραστικές συνθήκες που συντελείται η βιομηχανική διεργασία υπεράνω αυτού του τύπου καταλυτικών συστημάτων να υδρογονολύονται στην εστερομάδα προς την αλκοόλη αλλά και να υδρογονώνονται σε όλους τους διπλούς δεσμούς C=C που υπάρχουν στο υπόστρωμα της αντίδρασης. Στη διεργασία της υδρογονόλυσης του μονοακόρεστου ελαϊκού μεθυλεστέρα και του διακόρεστου λινελαϊκού μεθυλεστέρα καταλυόμενη από CuO/Cr 2 O 3 /Al 2 O 3 λαμβάνουν χώρα αντιδράσεις υδρογονόλυσης των εστερομάδων και αντιδράσεις υδρογόνωσης 64
65 των C=C ομάδων ώστε το προϊόν που λαμβάνεται είναι η κορεσμένη στεατική αλκοόλη (σχήμα 18, πορεία α και σχήμα 19). Εάν χρησιμοποιηθούν καταλυτικά συστήματα ZnO/Cr 2 O 3 /Al 2 O 3 ή CdO/Cr 2 O 3 /Al 2 O 3 υπό όμοιες θερμοκρασίες και μερικές πιέσεις υδρογόνου που κυριαρχούν στη βιομηχανική διεργασία της υδρογονόλυσης ακόρεστων λιπαρών εστέρων τότε υδρογονολύεται εκλεκτικά μόνον η ομάδα του εστέρα προς την αλκοόλη ενώ ο διπλός δεσμός C=C παραμένει ανέπαφος. Στην αντίδραση π.χ. του ελαϊκού μεθυλεστέρα με υδρογόνο καταλυόμενη από ZnO/Cr 2 O 3 /Al 2 O 3 ή CdO/Cr 2 O 3 /Al 2 O 3 υπό υψηλές θερμοκρασίες T = ºC και πιέσεις PH2 = bar το προϊόν που σχηματίζεται είναι η ακόρεστη ελαϊκή αλκοόλη (σχήμα 18, πορεία β). Η ακόρεστη ελαϊκή αλκοόλη είναι ένα πολύ χρήσιμο υπόστρωμα αντίδρασης για την παραγωγή εξειδικευμένων επιφανειοδραστικών με ξεχωριστές εφαρμογές. Σχήμα 18: Πορείες της διεργασίας της υδρογονόλυσης του μονοακόρεστου ελαϊκού μεθυλεστέρα: (α) πορεία υδρογονόλυσης και υδρογόνωσης υπεράνω CuO/Cr 2 O 3 /Al 2 O 3 προς στεατική αλκοόλη και (β) πορεία υδρογονόλυσης υπεράνω ZnO/Cr 2 O 3 /Al 2 O 3 ή CdO/Cr 2 O 3 /Al 2 O 3 προς ελαϊκή αλκοόλη. Εκτός από τις αντιδράσεις της απευθείας υδρογονόλυσης/υδρογόνωσης των λιπαρών μεθυλεστέρων προς κορεσμένες/ακόρεστες λιπαρές αλκοόλες συντελούνται επίσης και αντιδράσεις μετεστεροποίησης μεταξύ μεθυλεστέρων και λιπαρών αλκοολών προς ενδιάμεσα προϊόντα που είναι κηρώδεις εστέρες οι οποίοι επίσης αντιδρούν προς τα αντίστοιχα κορεσμένα ή ακόρεστα τελικά προϊόντα των λιπαρών αλκοολών. Στο σχήμα 19 παρουσιάζεται το προφίλ των ενδιάμεσων και τελικών προϊόντων που σχηματίζονται στη διεργασία της 65
66 υδρογονόλυσης του κλάσματος των C18 λιπαρών μεθυλεστέρων του φοινικικού πυρηνελαίου. Σχήμα 19: Φάσμα των προϊόντων υδρογονόλυσης και υδρογόνωσης των C18 συστατικών των μεθυλεστέρων του φοινικικού πυρηνέλαιου όπου φαίνονται οι ενδιάμεσοι κηρώδεις εστέρες ο ελαϊκός ελαϋλεστέρας και ο στεατικός στεαρυλεστέρας και τα τελικά προϊόντα η ελαϊκή και στεατική αλκοόλη. Η Procter & Gamble είναι μια άλλη βιομηχανική η εταιρεία η οποία επίσης δραστηριοποιείται στο πεδίο της υδρογονόλυσης ανανεώσιμων λιπαρών μεθυλεστέρων προς λιπαρές αλκοόλες καταλυόμενη από ετερογενή καταλυτικά συστήματα υπό δραστικές συνθήκες. Όσον αφορά την παραγωγή επιφανειοδραστικών ουσιών οι λιπαρές αλκοόλες χρησιμοποιούνται κυρίως για την παραγωγή μη ιοντικών επιφανειοδραστικών ουσιών όπως π.χ. [RO(CH 2 CH 2 O)n H] μετά από την μετατροπή τους με αιθυλενοξείδιο και/ή προπυλενοξείδιο. Ακόμη, οι λιπαρές αλκοόλες χρησιμοποιούνται για την παραγωγή ανιοντικών επιφανειοδραστικών ουσιών όπως π.χ. αλκυλοθειικών αλάτων (ROSO 3 Na) κατόπιν αντίδρασης των λιπαρών αλκοολών με SO 3 ή ατμίζον θειικό οξύ (SO 3 /H 2 SO 4 ). Το πρώτο συνθετικό απορρυπαντικό, ελεύθερο από σάπωνες, (FEWA, 1932) περιείχε ως επιφανειοδραστικές ουσίες αλκυλοθειικά άλατα. Η βιομηχανική διεργασία της καταλυτικής υδρογονόλυσης ανανεώσιμων λιπαρών μεθυλεστέρων προς λιπαρές αλκοόλες είναι ένα από τα ελάχιστα παραδείγματα διεργασιών που ήδη συντελούνται σε ένα βιοδιυλιστήριο και αφορούν τον τομέα παραγωγής 66
67 ενδιάμεσων χημικών προϊόντων από βασικά χημικά που λαμβάνονται από την ανανεώσιμη πρώτη ύλη βιομάζα. [2,6] Υδρογόνωση σε υδατικά/οργανικά διφασικά συστήματα Τα πλεονεκτήματα της κατάλυσης σε υδατικό/οργανικό διφασικό σύστημα ενέπνευσαν την ερευνητική ομάδα του εργαστηρίου μας στο να διεξάγει καταλυτικές αντιδράσεις ανανεώσιμων μεθυλεστέρων σε υδατικό περιβάλλον με την βοήθεια υδατοδιαλυτών καταλυτών. Η υδρογόνωση της ανανεώσιμης φρουκτόζης με την χρήση ομογενούς υδατοδιαλυτού καταλύτη ρουθηνίου, τροποποιημένου με τον υποκαταστάτη μετά νατρίου άλας της τρισουλφονικής τριφαινυλοφωσφίνης (TPPTS, P(m- C 6 H 4 SO 3 Na) 3 ) συντελείται υπό ήπιες συνθήκες σε μονοφασικό υδατικό περιβάλλον. [7] Η ομάδα του εργαστηρίου μας ανέφερε την πρώτη καταλυτική αντίδραση μερικής υδρογόνωσης των ανανεώσιμων πολυακόρεστων μεθυλεστέρων του λινέλαιου και του ηλιέλαιου σε υδατικό/οργανικό διφασικό σύστημα. Η αντίδραση αυτή καταλυόταν από το υδατοδιαλυτό σύμπλοκο Rh/TPPTS με σκοπό την παραγωγή μονοακόρεστων λιπαρών μεθυλεστέρων, οι οποίοι αποτελούν βιοντίζελ 1 ης γενιάς βελτιωμένης οξειδωτικής σταθερότητας και ενεργειακής απόδοσης, φιλικό προς το περιβάλλον, με χαμηλό σημείο ροής. Ο καταλύτης αυτός έδειξε ασυνήθιστη καταλυτική δραστικότητα (TOF = h -1 ) σε σύγκριση με τους μέχρι τότε γνωστούς ρυθμούς αντίδρασης που προέκυπταν από την εφαρμογή αυτού του καταλύτη σε βιομηχανικές αντιδράσεις με μεγάλου μοριακού βάρους υποστρώματα. [8] Εν συνεχεία, η διεργασία αυτή βελτιστοποιήθηκε χρησιμοποιώντας διαφορετικά ανανεώσιμα υποστρώματα όπως π.χ. τους μεθυλεστέρες του σογιέλαιου με την εκλεκτικότητα προς τον επιθυμητό μονοακόρεστο μεθυλεστέρα (C18:1) που χρησιμοποιείται ως βιοντίζελ 1 ης γενιάς υψηλής ποιότητας να ανέρχεται στο 79.8 mol%. Επίσης στην εργασία αυτή, μελετήθηκε η εκλεκτική υδρογόνωση μη εδώδιμων φυτικών ελαίων για παραγωγή βιοντίζελ 2 ης γενιάς. [9] Η καταλυτική υδρογόνωση των μεθυλεστέρων του μη εδώδιμου και χαμηλού κόστους ελαίου της αγριαγκινάρας (cynara cardunculus oil) 67
68 πραγματοποιήθηκε επίσης σε υδατικό/οργανικό διφασικό σύστημα με την χρήση του υδατοδιαλυτού συμπλόκου Ru/TPPTS και αποτέλεσε μία καλή εναλλακτική πορεία της παραγωγής βιοντίζελl 2 ης γενιάς. [10] Υψηλές καταλυτικές δραστικότητες της τάξεως των TOF = h -1 επιτεύχθηκαν στην αντίδραση υδρογόνωσης των μεθυλεστέρων του σογιέλαιου καταλυόμενη από νανοσωματίδια Pd 0 σταθεροποιημένα από αζωτούχους υποκαταστάτες σε υδατικό περιβάλλον. [11] Τέλος, η πιο πρόσφατη εργασία που διεξήχθη σε αυτό το πεδίο αφορούσε στην εκλεκτική υδρογόνωση πολυακόρεστων μεθυλεστέρων του λινέλαιου καταλυόμενη από το υδατοδιαλυτό σύμπλοκο Pt/TPPTS. Σκοπός της εργασίας αυτής ήταν η μελέτη της εκλεκτικής υδρογόνωσης των μεθυλεστέρων του λινέλαιου προς τον μονοακόρεστο ελαϊκό μεθυλεστέρα (C18:1) και η αποφυγή της cis/trans ισομερείωσης αυτού, ώστε να χρησιμοποιηθεί ως ένα μοντέλο αντίδρασης για την υδρογόνωση εδώδιμων φυτικών ελαίων με χαμηλή περιεκτικότητα σε trans-λίπη για την βιομηχανία τροφίμων. 68
69 3. ΚΕΦΑΛΑΙΟ 3 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ 3.1 Πειραματική διαδικασία αντίδρασης μετεστεροποίησης Η διαδικασία μετεστεροποίησης των φυτικών ελαίων είναι απαραίτητη προκειμένου να παραχθούν οι λιπαροί αλκυλεστέρες και να απομακρυνθούν τυχόν προσμίξεις του αρχικού ακατέργαστου ελαίου, οι οποίες πιθανόν θα προκαλούσαν προβλήματα κατά την διάρκεια της αντίδρασης υδρογόνωσης. Η αντίδραση μετεστεροποίησης φυτικών ελαίων με μεθανόλη περιλαμβάνει κάποια τυπικά στάδια τα οποία ακολουθούνται κάθε φορά και ανεξάρτητα από το είδος του ελαίου που υπόκειται σε αυτήν την διαδικασία. Ακολούθως, θα γίνει ενδεικτικά η περιγραφή της πειραματικής πορείας μετεστεροποίησης του σογιέλαιου. Με παρόμοιο τρόπο προηγήθηκαν οι αντιδράσεις μετεστεροποίησης των δύο άλλων φυτικών ελαίων, του λινέλαιου και του ηλιέλαιου, που χρησιμοποιήθηκαν στην παρούσα εργασία, με την μόνη διαφοροποίηση να έγκειται στις ποσότητες των αντιδραστηρίων που καταναλώθηκαν. Η πειραματική διάταξη της αντίδρασης περιλαμβάνει μία τρίλαιμη σφαιρική φιάλη των ml, στην οποία ενσωματώνονται ένας μηχανικός αναδευτήρας, ένα θερμόμετρο και ένας ψυκτήρας (εικόνα 1). Αρχικά, στην σφαιρική φιάλη προστίθεται συγκεκριμένη ποσότητα φυτικού ελαίου (323,6 g σογιέλαιου). Στη συνέχεια, προστίθεται σιγά σιγά υπό ανάδευση διάλυμα μεθανόλης (220,315 g) με υδροξείδιο του νατρίου (3,243 g). Το μίγμα αντίδρασης αναδεύεται για 70 λεπτά στους C και έπειτα ψύχεται για περίπου 2 ώρες σε θερμοκρασία δωματίου, ενώ βρίσκεται υπό ανάδευση, έως ότου αποκτήσει θερμοκρασία περίπου 25 0 C. Μετά την ψύξη του, το αντιδρών μίγμα μεταφέρεται σε διαχωριστική χοάνη όπου πραγματοποιείται ο διαχωρισμός των μεθυλεστέρων του σογιέλαιου (ανώτερη φάση, ανοιχτό κίτρινο χρώμα) από την κατώτερη φάση της γλυκερίνης (σκούρο κόκκινο χρώμα). Η φάση της γλυκερίνης φυλάσσεται σε μία άλλη διαχωριστική χοάνη, 69
70 με σκοπό η ποσότητα των μεθυλεστέρων που θα ανακτηθεί από αυτήν να ενωθεί με την ήδη διαχωρισθείσα ποσότητα και να αποφευχθεί τυχόν απώλεια επιθυμητού προϊόντος. Από την άλλη πλευρά, στη φάση των μεθυλεστέρων του σογιέλαιου προστίθεται απιονισμένο νερό, γίνεται εκχύλιση και το μίγμα αφήνεται σε ηρεμία να διαχωριστεί όλο το βράδυ (περίπου 20 ώρες). Την επόμενη μέρα, ακολουθεί διαχωρισμός της υδατικής από την οργανική φάση και στην δεύτερη προστίθεται η φάση των μεθυλεστέρων του σογιέλαιου που έχουν προκύψει από τον δεύτερο διαχωρισμό τους από την γλυκερόλη. Η διαδικασία των εκχυλίσεων των μεθυλεστέρων με απιονισμένο νερό και ο διαχωρισμός τους από αυτό επαναλαμβάνεται 7 ακόμη φορές, έως ότου το ph της υδατικής φάσης να είναι ουδέτερο. Στη διάρκεια των εκχυλίσεων λαμβάνονται μετρήσεις του ph των διαφόρων δειγμάτων και παρατηρείται ότι το ph μεταβάλλεται από πολύ βασικό μέχρι ουδέτερο. Τελικά, μετά και την τελευταία πλύση η υδατική φάση έχει ph = 6,36. Η οργανική φάση υπόκειται σε ξήρανση υπεράνω άνυδρου Na 2 SO 4 και η ποσότητα που παραμένει ζυγίζεται και μεταφέρεται σε σκουρόχρωμη υάλινη φιάλη. Η τελική απόδοση σε μεθυλεστέρες του σογιέλαιου είναι 254,0 g και η ακριβής του σύσταση διαπιστώνεται με την βοήθεια της αέριας χρωματογραφίας. Εικόνα 1: Πειραματική διάταξη της αντίδρασης μετεστεροποίησης του σογιέλαιου με μεθανόλη. 70
71 3.2 Πειραματική διαδικασία αντίδρασης υδρογόνωσης Σε ένα τυπικό πείραμα υδρογόνωσης μεθυλεστέρων οποιουδήποτε φυτικού ελαίου, είτε του λινέλαιου, είτε του ηλιέλαιου, είτε του σογιέλαιου ακολουθείται η εξής διαδικασία: Αρχικά σε αναλυτικό ζυγό ζυγίζουμε τα mg του εκάστοτε πρόδρομου άλατος μετάλλου καθώς και του υποκαταστάτη. Το πρόδρομο αυτό καταλυτικό σύστημα τοποθετείται σε αυτόκλειστο αντιδραστήρα όγκου 100ml της Autoclave Engineers τον οποίο προηγουμένως έχουμε απαερώσει με αδρανές αέριο αργό. Στον αντιδραστήρα προστίθενται και 20 ml απαερωμένου, απιονισμένου νερού υπό ατμόσφαιρα αργού. Έτσι, προκύπτει in situ το υδατικό διάλυμα του καταλύτη. Πολλές φορές, αντί αυτού λαμβάνει χώρα συμπλοκοποίηση του μετάλλου με τον υποκαταστάτη σε υδατικό περιβάλλον για λίγα λεπτά υπό ανάδευση και ακολούθως το διάλυμα αυτό τοποθετείται στον αντιδραστήρα. Στη συνέχεια, στο υδατικό διάλυμα προστίθεται η ποσότητα των μεθυλεστέρων του εκάστοτε ελαίου και έτσι προκύπτει ένα διφασικό υδατικό/οργανικό σύστημα. Ακολούθως το μεταλλικό δοχείο αντίδρασης προσαρμόζεται στον αντιδραστήρα και ξεκινά η ανάδευση του μίγματος, η οποία ρυθμίζεται πάντα στα 820 rpm (στροφές το λεπτό). Πριν ξεκινήσει η αντίδραση πραγματοποιούνται ορισμένες συμπιέσεις και εκτονώσεις με σκοπό την απομάκρυνση της ποσότητας του ατμοσφαιρικού οξυγόνου από τον αντιδραστήρα. Μετά από αυτό τοποθετείται ο θερμαντικός μανδύας γύρω από το μεταλλικό δοχείο και ρυθμίζεται η επιθυμητή θερμοκρασία αντίδρασης. Η μέτρηση του χρόνου αντίδρασης ξεκινά από τη στιγμή που το αντιδρών μίγμα φτάσει στην επιθυμητή θερμοκρασία που έχουμε ορίσει. Μετά το τέλος της αντίδρασης, ο αντιδραστήρας ψύχεται και όταν η θερμοκρασία είναι C το αέριο υδρογόνο εκτονώνεται. Επίσης, το μίγμα αντίδρασης μεταφέρεται σε διαχωριστική χοάνη προς διαχωρισμό των δύο φάσεων. Η εκχύλιση γίνεται με τη χρήση οργανικού διαλύτη διαιθυλαιθέρα, ο οποίος είναι μη αναμίξιμος με το νερό, ενώ ταυτόχρονα διαλύει πλήρως τους μεθυλεστέρες των φυτικών ελαίων. Στη χοάνη, η κατώτερη φάση είναι η υδατική η οποία περιέχει το καταλυτικό σύστημα, ενώ η ανώτερη στοιβάδα είναι η οργανική και αποτελείται από το μίγμα των προϊόντων της αντίδρασης (εικόνα 2). Μετά τον διαχωρισμό μετριέται το ph 71
72 της υδατικής φάσης και η οργανική υπόκειται σε ξήρανση υπεράνω Na 2 SO 4. Τα προϊόντα της αντίδρασης αναλύονται με αεριοχρωματογραφία με τη μέθοδο όπως αναφέρεται στο Ως εσωτερικό πρότυπο προστίθεται μετά το τέλος της αντίδρασης δεκαεπτανοϊκός μεθυλεστέρας. Εικόνα 2: Το υδατικό/οργανικό διφασικό σύστημα που προκύπτει μετά την αντίδρασης υδρογόνωσης. Στο σημείο αυτό πρέπει να αναφέρουμε ότι όλες οι αντιδράσεις έλαβαν χώρα απουσία επιφανειοδραστικών ουσιών. Οι επιφανειοδραστικές ουσίες βοηθούν τα αντιδρώντα σώματα να ξεπεράσουν τα προβλήματα μεταφοράς μάζας και με σχηματισμό μικυλλίων να έρθουν πιο εύκολα σε επαφή όταν η αντίδραση γίνεται σε υδατικά/οργανικά διφασικά συστήματα. Η εξήγηση αρχικά βρίσκεται στο γεγονός ότι τα αρχικά μίγματα των μεθυλεστέρων όλων των φυτικών ελαίων έχουν μία μικρή ικανότητα να δρουν από μόνα τους ως επιφανειοδραστικές ουσίες. Επίσης τα αρχικά ακατέργαστα έλαια άρα και οι παραγόμενοι από την μετεστεροποίηση μεθυλεστέρες τους περιέχουν σε μικρές ποσότητες κάποια συστατικά όπως η λεκιθίνη που δρουν ως επιφανειοδραστικές ουσίες. 72
73 3.3 Παρασκευή απαερωμένου νερού Σε όλα τα πειράματα που πραγματοποιήθηκαν, χρησιμοποιήθηκε απιονισμένο και απαερωμένο νερό, με σκοπό να ελαχιστοποιηθεί όσο το δυνατόν περισσότερο η επαφή των καταλυτών των μετάλλων μετάπτωσης με το ατμοσφαιρικό οξυγόνο. Η πειραματική πορεία που ακολουθήθηκε για την παρασκευή απαερωμένου νερού είναι η εξής: Σε μία τρίλαιμη σφαιρική φιάλη των 1000 ml προστίθενται περίπου 500 ml απιονισμένου νερού. Η φιάλη τοποθετείται σε λουτρό υπερήχων και συνδέεται με μια παγίδα η οποία ψύχεται σε δοχείο dewar με την βοήθεια υγρού αζώτου (εικόνα 3) και ενώνεται σε υψηλό κενό. Η διαδικασία της αποοξυγόνωσης διαρκεί περίπου δύο ώρες και κατά την διάρκειά της η φιάλη αποσυνδέεται από το κενό, και ο υδατικός διαλύτης υπόκειται σε κορεσμό με αργό. Αυτό επαναλαμβάνεται σε τακτά χρονικά διαστήματα, περίπου επτά με οκτώ φορές και τελικά το νερό θεωρείται απαερωμένο όταν μετά και την τελευταία προσθήκη αργού, σταματήσει η παραγωγή φυσαλίδων στην επιφάνεια του ύδατος. Εικόνα 3: Η πειραματική διάταξη για την παρασκευή απαερωμένου νερού. 73
74 3.4 Αντιδραστήρας Όλα τα πειράματα έλαβαν χώρα σε αντιδραστήρα ασυνεχούς λειτουργίας με ανάδευση της εταιρείας Autoclave Engineers. Το μοντέλο του αντιδραστήρα που χρησιμοποιήθηκε περιλάμβανε συστήματα εισαγωγής και εξαγωγής αερίων, μηχανική ανάδευση, και θερμαντικό μανδύα για ρύθμιση της επιθυμητής θερμοκρασίας αντίδρασης (εικόνα 4). Εικόνα 4: Ο αντιδραστήρας της εταιρείας Autoclave Engineers. Η ρύθμιση της θερμοκρασίας και της ταχύτητας ανάδευσης μέσα στον αντιδραστήρα γινόταν με την βοήθεια ενός πύργου ελέγχου που ήταν συνδεδεμένο με αυτόν, της ίδιας εταιρείας και πιο συγκεκριμένα του μοντέλου Universal Reactor Controller (εικόνα 5). Το μίγμα της αντίδρασης τοποθετούνταν σε ένα μεταλλικό δοχείο το οποίο προσαρμοζόταν στον αντιδραστήρα μέσω ενός δακτυλίου με έξι βίδες (εικόνα 6). Επειδή το μεταλλικό αυτό δοχείο είχε χρησιμοποιηθεί σε προγενέστερα πειράματα είχε ενεργοποιηθεί από μέταλλα προηγούμενων καταλυτών. Για να αποφευχθούν αυτά τα memory effects του αντιδραστήρα, τα αρχικά πειράματά μας διεξήχθησαν σε υάλινη επένδυση (glass liner), δηλαδή σε υάλινο δοχείο που 74
75 κατασκευάστηκε ώστε να έχει τις ίδιες διαστάσεις με το μεταλλικό δοχείο και να προσαρμόζεται εύκολα μέσα σε αυτό. Μετά το πέρας όμως αρκετών πειραμάτων παρατηρήθηκε ο σχηματισμός μαύρων στιγμάτων στο εσωτερικό του υάλινου αντιδραστήρα, τα οποία δεν απομακρύνονταν εύκολα μετά από καθαρισμό. Η εναπόθεση μεταλλικών στοιχείων στην εσωτερική επιφάνεια της υάλινης επένδυσης δημιουργούσε και αυτό με την σειρά του memory effects. Ετσι, κρίθηκε αναγκαία η επαναχρησιμοποίηση απ ευθείας του μεταλλικού αντιδραστήρα, τον οποίο μπορούσαμε μετά από κάθε πείραμα να τον καθαρίσουμε καλύτερα και να τον ενεργοποιήσουμε πολλές φορές με το επιθυμητό καταλυτικό σύμπλοκο των μετάλλων μετάπτωσης πριν την διεξαγωγή των αντίστοιχων πειραμάτων, προκειμένου να ελαχιστοποιήσουμε την επίδραση των προγενέστερων μετάλλων. Εικόνα 5: Ο πύργος ελέγχου του αντιδραστήρα (Universal Reactor Controller). 75
76 Εικόνα 6: Το μεταλλικό δοχείο του αντιδραστήρα. 3.5 Αέρια χρωματογραφία Η χρωματογραφία είναι μια πανίσχυρη τεχνική διαχωρισμού, η οποία βρίσκει εφαρμογές σε κάθε κλάδο της επιστήμης. Με τον όρο χρωματογραφία εννοούμε όλες εκείνες τις μεθόδους που χρησιμοποιούνται ώστε να διαχωριστούν ουσίες με παραπλήσιες χημικές ιδιότητες από σύνθετα μίγματα. Η τεχνική της χρωματογραφίας διέπεται από μια γενική αρχή: Το δείγμα κινείται σε μια κινητή φάση, η οποία μπορεί να είναι ένα αέριο, ένα υγρό ή ένα υπερκρίσιμο ρευστό. Στη συνέχεια, η κινητή φάση εξαναγκάζεται να διέλθει μέσω μιας στατικής φάσης η οποία είναι καθηλωμένη σε μια στήλη ή σε μια στερεά επιφάνεια. Οι δύο φάσεις επιλέγονται έτσι, ώστε τα συστατικά του δείγματος να κατανέμονται μεταξύ της κινητής και της στατικής φάσης σε διαφορετικό βαθμό. Τα συστατικά τα οποία κατακρατούνται ισχυρότερα από τη στατική φάση κινούνται αργά κατά τη ροή της κινητής φάσης. Το αντίθετο συμβαίνει με τα συστατικά τα οποία κατακρατούνται ασθενέστερα από την στατική φάση. Οι διαφορές αυτές στην ευκινησία έχουν ως αποτέλεσμα τα συστατικά του δείγματος να διαχωρίζονται καταλαμβάνοντας το καθένα ξεχωριστές ζώνες, και έπειτα να είναι δυνατός ο ποιοτικός και ο ποσοτικός προσδιορισμός τους. Στην αέρια χρωματογραφία η έκλουση πραγματοποιείται με ροή αδρανούς αερίου (φέρον αέριο), το οποίο αποτελεί την κινητή φάση. Υπάρχουν δύο τύποι αέριας χρωματογραφίας: η χρωματογραφία αερίου-στερεού (gas-solid 76
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «ΧΗΜΕΙΑΣ» ΕΙΔΙΚΕΥΣΗ «ΚΑΤΑΛΥΣΗ ΚΑΙ ΕΦΑΡΜΟΓΕΣ ΤΗΣ» ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ ΔΙΠΛΩΜΑΤΟΣ ΕΙΔΙΚΕΥΣΗΣ
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «ΧΗΜΕΙΑΣ» ΕΙΔΙΚΕΥΣΗ «ΚΑΤΑΛΥΣΗ ΚΑΙ ΕΦΑΡΜΟΓΕΣ ΤΗΣ» ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ ΔΙΠΛΩΜΑΤΟΣ ΕΙΔΙΚΕΥΣΗΣ
Βιοκαύσιμα υποκατάστατα του πετρελαίου Ντίζελ
 Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών - Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων Βιοκαύσιμα υποκατάστατα του πετρελαίου Ντίζελ Ν. Παπαγιαννάκος Καθηγητής
Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών - Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων Βιοκαύσιμα υποκατάστατα του πετρελαίου Ντίζελ Ν. Παπαγιαννάκος Καθηγητής
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ
 ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2016-2017 ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ 1 ΕΙΣΑΓΩΓΗ ΑΤΟΜΙΚΗ ΘΕΩΡΙΑ Δομικά σωματίδια (άτομα-μόρια-ιόντα) Δομή του ατόμου Ατομικός και μαζικός αριθμός Ισότοπα Ηλεκτρονική
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2016-2017 ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ 1 ΕΙΣΑΓΩΓΗ ΑΤΟΜΙΚΗ ΘΕΩΡΙΑ Δομικά σωματίδια (άτομα-μόρια-ιόντα) Δομή του ατόμου Ατομικός και μαζικός αριθμός Ισότοπα Ηλεκτρονική
ΠΑΡΑΓΩΓΗ ΒΙΟΚΑΥΣΙΜΩΝ ΥΠΟΚΑΤΑΣΤΑΤΩΝ ΤΟΥ ΝΤΙΖΕΛ ΑΠΟ ΧΡΗΣΙΜΟΠΟΙΗΜΕΝΑ ΦΥΤΙΚΑ ΕΛΑΙΑ
 ΠΑΡΑΓΩΓΗ ΒΙΟΚΑΥΣΙΜΩΝ ΥΠΟΚΑΤΑΣΤΑΤΩΝ ΤΟΥ ΝΤΙΖΕΛ ΑΠΟ ΧΡΗΣΙΜΟΠΟΙΗΜΕΝΑ ΦΥΤΙΚΑ ΕΛΑΙΑ ΑΝΔΡΕΑΣ ΒΟΝΟΡΤΑΣ ΝΙΚΟΣ ΠΑΠΑΓΙΑΝΝΑΚΟΣ ΦΥΤΙΚΑ ΕΛΑΙΑ ΩΣ ΚΑΥΣΙΜΑ Φυτικά έλαια ή ζωικά λίπη ή παράγωγά τους Μετεστεροποίηση Υδρογονοαποξυγόνωση
ΠΑΡΑΓΩΓΗ ΒΙΟΚΑΥΣΙΜΩΝ ΥΠΟΚΑΤΑΣΤΑΤΩΝ ΤΟΥ ΝΤΙΖΕΛ ΑΠΟ ΧΡΗΣΙΜΟΠΟΙΗΜΕΝΑ ΦΥΤΙΚΑ ΕΛΑΙΑ ΑΝΔΡΕΑΣ ΒΟΝΟΡΤΑΣ ΝΙΚΟΣ ΠΑΠΑΓΙΑΝΝΑΚΟΣ ΦΥΤΙΚΑ ΕΛΑΙΑ ΩΣ ΚΑΥΣΙΜΑ Φυτικά έλαια ή ζωικά λίπη ή παράγωγά τους Μετεστεροποίηση Υδρογονοαποξυγόνωση
Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των
 124 Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των καταλυτών των μετάλλων μεταπτώσεως στην οργανική σύνθεση.
124 Εισαγωγή στις βασικές έννοιες που αφορούν τις οργανομεταλλικές ενώσεις, την κατάλυση και τις βασικές αρχές της, καθώς και τη χρησιμότητα των καταλυτών των μετάλλων μεταπτώσεως στην οργανική σύνθεση.
Τεχνολογίες Εκμετάλλευσης και Αξιοποίησης Υδρογονανθράκων
 Τεχνολογίες Εκμετάλλευσης και Αξιοποίησης Υδρογονανθράκων Μάθημα 4 ο Υδρογονοκατεργασία > Υδρογονοεπεξεργασία > Υδρογονοπυρόλυση Δρ. Στέλλα Μπεζεργιάννη Υδρογονοκατεργασία (Hydroprocessing) Υδρογονοκατεργασία
Τεχνολογίες Εκμετάλλευσης και Αξιοποίησης Υδρογονανθράκων Μάθημα 4 ο Υδρογονοκατεργασία > Υδρογονοεπεξεργασία > Υδρογονοπυρόλυση Δρ. Στέλλα Μπεζεργιάννη Υδρογονοκατεργασία (Hydroprocessing) Υδρογονοκατεργασία
Φυσικό αέριο. Ορισμός: Το φυσικό αέριο είναι μίγμα αέριων υδρογονανθράκων με κύριο συστατικό το μεθάνιο, CH 4 (μέχρι και 90%).
 Φυσικό αέριο Ορισμός: Το φυσικό αέριο είναι μίγμα αέριων υδρογονανθράκων με κύριο συστατικό το μεθάνιο, CH 4 (μέχρι και 90%). Το φυσικό αέριο χρησιμοποιείται ως καύσιμο και παρουσιάζει δύο βασικά πλεονεκτήματα
Φυσικό αέριο Ορισμός: Το φυσικό αέριο είναι μίγμα αέριων υδρογονανθράκων με κύριο συστατικό το μεθάνιο, CH 4 (μέχρι και 90%). Το φυσικό αέριο χρησιμοποιείται ως καύσιμο και παρουσιάζει δύο βασικά πλεονεκτήματα
2 ο Κεφάλαιο: Πετρέλαιο - Υδρογονάνθρακες
 2 ο Κεφάλαιο: Πετρέλαιο - Υδρογονάνθρακες Δημήτρης Παπαδόπουλος, χημικός Βύρωνας, 2015 Καύσιμα - καύση Τα καύσιμα είναι υλικά που, όταν καίγονται, αποδίδουν σημαντικά και εκμεταλλεύσιμα ποσά θερμότητας.
2 ο Κεφάλαιο: Πετρέλαιο - Υδρογονάνθρακες Δημήτρης Παπαδόπουλος, χημικός Βύρωνας, 2015 Καύσιμα - καύση Τα καύσιμα είναι υλικά που, όταν καίγονται, αποδίδουν σημαντικά και εκμεταλλεύσιμα ποσά θερμότητας.
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
ΚΕΦΑΛΑΙΟ 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ
 ΚΕΦΑΛΑΙΟ 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανικές ενώσεις Οργανική Χημεία είναι ο κλάδος της Χημείας που ασχολείται με τις ενώσεις του άνθρακα (C). Οργανικές ενώσεις ονομάζονται οι χημικές ενώσεις που
ΚΕΦΑΛΑΙΟ 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Οργανικές ενώσεις Οργανική Χημεία είναι ο κλάδος της Χημείας που ασχολείται με τις ενώσεις του άνθρακα (C). Οργανικές ενώσεις ονομάζονται οι χημικές ενώσεις που
Χημική Κινητική. Κωδ. Μαθήματος 718 Τομέας Φυσικοχημείας, Τμήμα Χημείας, ΕΚΠΑ. Μάθημα 12. Βίκη Νουσίου
 Χημική Κινητική Κωδ. Μαθήματος 718 Τομέας Φυσικοχημείας, Τμήμα Χημείας, ΕΚΠΑ Μάθημα 12 Βίκη Νουσίου Εαρινό εξάμηνο 2019 Ένζυμα 2 3 4 Ένζυμα Ένζυμα: Βιολογικοί καταλύτες Μακρομόρια ΜΒ 10 4-10 6 Πρωτεΐνες
Χημική Κινητική Κωδ. Μαθήματος 718 Τομέας Φυσικοχημείας, Τμήμα Χημείας, ΕΚΠΑ Μάθημα 12 Βίκη Νουσίου Εαρινό εξάμηνο 2019 Ένζυμα 2 3 4 Ένζυμα Ένζυμα: Βιολογικοί καταλύτες Μακρομόρια ΜΒ 10 4-10 6 Πρωτεΐνες
Χημικές Διεργασίες: Εισαγωγή
 : Εισαγωγή Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση - Αφυδρογόνωση - Πυρόλυση - Ενυδάτωση κλπ Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση
: Εισαγωγή Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση - Αφυδρογόνωση - Πυρόλυση - Ενυδάτωση κλπ Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση
ΠΑΡΑΓΩΓΗ ΒΙΟΝΤΙΖΕΛ ΑΠΟ ΑΠΟΒΛΗΤΕΣ ΕΛΑΙΟΥΧΕΣ ΥΛΕΣ ΜΕ ΤΗ ΧΡΗΣΗ ΕΤΕΡΟΓΕΝΟΥΣ ΒΑΣΙΚΟΥ ΚΑΤΑΛΥΤΗ
 Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων ΠΑΡΑΓΩΓΗ ΒΙΟΝΤΙΖΕΛ ΑΠΟ ΑΠΟΒΛΗΤΕΣ ΕΛΑΙΟΥΧΕΣ ΥΛΕΣ ΜΕ ΤΗ ΧΡΗΣΗ ΕΤΕΡΟΓΕΝΟΥΣ ΒΑΣΙΚΟΥ
Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων ΠΑΡΑΓΩΓΗ ΒΙΟΝΤΙΖΕΛ ΑΠΟ ΑΠΟΒΛΗΤΕΣ ΕΛΑΙΟΥΧΕΣ ΥΛΕΣ ΜΕ ΤΗ ΧΡΗΣΗ ΕΤΕΡΟΓΕΝΟΥΣ ΒΑΣΙΚΟΥ
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ
 Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
Ανάλυση Τροφίμων. Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ
 ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ B ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ 1. Ταξινόμηση
ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ B ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ 1. Ταξινόμηση
ΠΕΤΡΕΛΑΙΟ ΥΔΡΟΓΟΝΑΝΘΡΑΚΕΣ ΚΑΥΣΗ και ΚΑΥΣΙΜΑ
 ΠΕΤΡΕΛΑΙΟ ΥΔΡΟΓΟΝΑΝΘΡΑΚΕΣ ΚΑΥΣΗ και ΚΑΥΣΙΜΑ Καύση ονομάζεται η αντίδραση μιας οργανικής ή ανόργανης ουσίας με το Ο 2, κατά την οποία εκλύεται θερμότητα στο περιβάλλον και παράγεται φως. Είδη καύσης Α.
ΠΕΤΡΕΛΑΙΟ ΥΔΡΟΓΟΝΑΝΘΡΑΚΕΣ ΚΑΥΣΗ και ΚΑΥΣΙΜΑ Καύση ονομάζεται η αντίδραση μιας οργανικής ή ανόργανης ουσίας με το Ο 2, κατά την οποία εκλύεται θερμότητα στο περιβάλλον και παράγεται φως. Είδη καύσης Α.
panagiotisathanasopoulos.gr
 Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
ΧΗΜΕΙΑ Β ΓΥΜΝΑΣΙΟΥ ΕΝΟΤΗΤΑ: 1.2
 ΕΝΟΤΗΤΑ: 1.2 Η ύλη συναντάται σε τρεις φυσικές καταστάσεις: Στερεή: έχει καθορισμένη μάζα, σχήμα και όγκο. Υγρή: έχει καθορισμένη μάζα και όγκο, ενώ σχήμα κάθε φορά παίρνει το σχήμα του δοχείου που το
ΕΝΟΤΗΤΑ: 1.2 Η ύλη συναντάται σε τρεις φυσικές καταστάσεις: Στερεή: έχει καθορισμένη μάζα, σχήμα και όγκο. Υγρή: έχει καθορισμένη μάζα και όγκο, ενώ σχήμα κάθε φορά παίρνει το σχήμα του δοχείου που το
Τεχνολογία παραγωγής βιοντίζελ 2 ης γενιάς από τηγανέλαια
 Τεχνολογία παραγωγής βιοντίζελ 2 ης γενιάς από τηγανέλαια Δρ. Στέλλα Μπεζεργιάννη Χημικός Μηχανικός - Ερευνήτρια ΕΚΕΤΑ Εθνικό Κέντρο Έρευνας & Τεχνολογικής Ανάπτυξης (ΕΚΕΤΑ) Ινστιτούτο Τεχνικής Χημικών
Τεχνολογία παραγωγής βιοντίζελ 2 ης γενιάς από τηγανέλαια Δρ. Στέλλα Μπεζεργιάννη Χημικός Μηχανικός - Ερευνήτρια ΕΚΕΤΑ Εθνικό Κέντρο Έρευνας & Τεχνολογικής Ανάπτυξης (ΕΚΕΤΑ) Ινστιτούτο Τεχνικής Χημικών
Εθνικόν και Καποδιστριακόν Πανεπιστήμιον Αθηνών ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Τομέας Φαρμακευτικής Χημείας. Ιωάννης Ντότσικας. Επικ.
 Εθνικόν και Καποδιστριακόν Πανεπιστήμιον Αθηνών ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Τομέας Φαρμακευτικής Χημείας Ιωάννης Ντότσικας Επικ. Καθηγητής 1 Οι κυκλοδεξτρίνες (Cyclodextrins, CDs) είναι κυκλικοί ολιγοσακχαρίτες
Εθνικόν και Καποδιστριακόν Πανεπιστήμιον Αθηνών ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Τομέας Φαρμακευτικής Χημείας Ιωάννης Ντότσικας Επικ. Καθηγητής 1 Οι κυκλοδεξτρίνες (Cyclodextrins, CDs) είναι κυκλικοί ολιγοσακχαρίτες
Κατάλυση σε διαλύµατα Συµπλόκων των Στοιχείων Μετάπτωσης. Βασίλης Ταγκούλης
 Κατάλυση σε διαλύµατα Συµπλόκων των Στοιχείων Μετάπτωσης Βασίλης Ταγκούλης vtango@upatras.gr στοιχειώδεις έννοιες στην κατάλυση η κατάλυση και η σπουδαιότητά της η έννοια της κατάλυσης καταλυτικός κύκλος
Κατάλυση σε διαλύµατα Συµπλόκων των Στοιχείων Μετάπτωσης Βασίλης Ταγκούλης vtango@upatras.gr στοιχειώδεις έννοιες στην κατάλυση η κατάλυση και η σπουδαιότητά της η έννοια της κατάλυσης καταλυτικός κύκλος
ΠΑΡΑΓΩΓΗ ΒΙΟΝΤΙΖΕΛ ΑΠΟ ΟΞΙΝΟ ΒΑΜΒΑΚΕΛΑΙΟ ΜΕ ΤΗ ΧΡΗΣΗ ΕΤΕΡΟΓΕΝΟΥΣ ΒΑΣΙΚΟΥ ΚΑΤΑΛΥΤΗ
 Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων ΠΑΡΑΓΩΓΗ ΒΙΟΝΤΙΖΕΛ ΑΠΟ ΟΞΙΝΟ ΒΑΜΒΑΚΕΛΑΙΟ ΜΕ ΤΗ ΧΡΗΣΗ ΕΤΕΡΟΓΕΝΟΥΣ ΒΑΣΙΚΟΥ
Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων ΠΑΡΑΓΩΓΗ ΒΙΟΝΤΙΖΕΛ ΑΠΟ ΟΞΙΝΟ ΒΑΜΒΑΚΕΛΑΙΟ ΜΕ ΤΗ ΧΡΗΣΗ ΕΤΕΡΟΓΕΝΟΥΣ ΒΑΣΙΚΟΥ
ΕΤΕΡΟΓΕΝΗΣ ΚΑΤΑΛΥΤΙΚΗ ΜΕΤΑΤΡΟΠΗ ΕΛΕΥΘΕΡΩΝ ΛΙΠΑΡΩΝ ΟΞΕΩΝ ΟΞΙΝΩΝ ΕΛΑΙΩΝ ΣΕ ΒΙΟΝΤΙΖΕΛ
 Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων ΕΤΕΡΟΓΕΝΗΣ ΚΑΤΑΛΥΤΙΚΗ ΜΕΤΑΤΡΟΠΗ ΕΛΕΥΘΕΡΩΝ ΛΙΠΑΡΩΝ ΟΞΕΩΝ ΟΞΙΝΩΝ ΕΛΑΙΩΝ ΣΕ
Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χημικών Μηχανικών Τομέας ΙΙ Μονάδα Μηχανικής Διεργασιών Υδρογονανθράκων και Βιοκαυσίμων ΕΤΕΡΟΓΕΝΗΣ ΚΑΤΑΛΥΤΙΚΗ ΜΕΤΑΤΡΟΠΗ ΕΛΕΥΘΕΡΩΝ ΛΙΠΑΡΩΝ ΟΞΕΩΝ ΟΞΙΝΩΝ ΕΛΑΙΩΝ ΣΕ
Χημική Κινητική. Κωδ. Μαθήματος 718 Τομέας Φυσικοχημείας, Τμήμα Χημείας, ΕΚΠΑ. Μάθημα 11. Βίκη Νουσίου
 Χημική Κινητική Κωδ. Μαθήματος 718 Τομέας Φυσικοχημείας, Τμήμα Χημείας, ΕΚΠΑ Μάθημα 11 Βίκη Νουσίου Εαρινό εξάμηνο 2019 Κατάλυση Καταλύτης: Επιταχύνει μια αντίδραση χωρίς να υφίσταται συνολικά χημική μεταβολή
Χημική Κινητική Κωδ. Μαθήματος 718 Τομέας Φυσικοχημείας, Τμήμα Χημείας, ΕΚΠΑ Μάθημα 11 Βίκη Νουσίου Εαρινό εξάμηνο 2019 Κατάλυση Καταλύτης: Επιταχύνει μια αντίδραση χωρίς να υφίσταται συνολικά χημική μεταβολή
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 13: Χημική κινητική
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 13: Χημική κινητική Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 13: Χημική κινητική Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
ΧΗΜΕΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Σε κάθε μία από τις επόμενες ερωτήσεις να επιλέξετε τη σωστή απάντηση
 Κανάρη 36, Δάφνη Τηλ. 210 9713934 & 210 9769376 ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ ΧΗΜΕΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑ Α Σε κάθε μία από τις επόμενες ερωτήσεις να επιλέξετε τη σωστή απάντηση Α1. Σε δοχείο σταθερού όγκου
Κανάρη 36, Δάφνη Τηλ. 210 9713934 & 210 9769376 ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ ΧΗΜΕΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑ Α Σε κάθε μία από τις επόμενες ερωτήσεις να επιλέξετε τη σωστή απάντηση Α1. Σε δοχείο σταθερού όγκου
ΕΤΚΛ ΕΜΠ. Τεχνολογία Πετρελαίου και Και Λιπαντικών ΕΜΠ
 Φυσικού Αερίου Στόχοι Απομάκρυνση Ανεπιθύμητων Συστατικών Νερό Βαρείς Υδρογονάνθρακες Υδρόθειο Διοξείδιο του Άνθρακα Στοιχειακό Θείο Άλλα Συστατικά Ανάκτηση Συστατικών με Οικονομική Αξία Ήλιο Υδρογονάνθρακες
Φυσικού Αερίου Στόχοι Απομάκρυνση Ανεπιθύμητων Συστατικών Νερό Βαρείς Υδρογονάνθρακες Υδρόθειο Διοξείδιο του Άνθρακα Στοιχειακό Θείο Άλλα Συστατικά Ανάκτηση Συστατικών με Οικονομική Αξία Ήλιο Υδρογονάνθρακες
ÁÎÉÁ ÅÊÐÁÉÄÅÕÔÉÊÏÓ ÏÌÉËÏÓ
 ΘΕΜΑ Α ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ ΣΥΣΤΗΜΑ) 14 ΙΟΥΝΙΟΥ 2017 ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθµό της πρότασης και δίπλα το γράµµα που αντιστοιχεί στη σωστή
ΘΕΜΑ Α ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ ΣΥΣΤΗΜΑ) 14 ΙΟΥΝΙΟΥ 2017 ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθµό της πρότασης και δίπλα το γράµµα που αντιστοιχεί στη σωστή
Απώλειες των βιταμινών κατά την επεξεργασία των τροφίμων
 Απώλειες των βιταμινών κατά την επεξεργασία των τροφίμων Αποφλοίωση και καθαρισμός Πολλά φυτικά προϊόντα π.χ, μήλα, πατάτες χρειάζονται αποφλοίωση ή καθαρισμό μερικών τμημάτων τους πριν από την κατεργασία.
Απώλειες των βιταμινών κατά την επεξεργασία των τροφίμων Αποφλοίωση και καθαρισμός Πολλά φυτικά προϊόντα π.χ, μήλα, πατάτες χρειάζονται αποφλοίωση ή καθαρισμό μερικών τμημάτων τους πριν από την κατεργασία.
Παραγωγή Καυσίµου Ντίζελ από Ανανεώσιµες Πρώτες Ύλες
 Ο ΠΕΤΡΕΛΑΪΚΟΣ ΤΟΜΕΑΣ ΣΤΗΝ ΕΛΛΑ Α 29-30 Μαΐου 2009, Αλεξανδρούπολη Παραγωγή Καυσίµου Ντίζελ από Ανανεώσιµες Πρώτες Ύλες Νίκος Παπαγιαννάκος Εθνικό Μετσόβιο Πολυτεχνείο Σχολή Χηµικών Μηχανικών 1 ΒΙΟΚΑΥΣΙΜΑ
Ο ΠΕΤΡΕΛΑΪΚΟΣ ΤΟΜΕΑΣ ΣΤΗΝ ΕΛΛΑ Α 29-30 Μαΐου 2009, Αλεξανδρούπολη Παραγωγή Καυσίµου Ντίζελ από Ανανεώσιµες Πρώτες Ύλες Νίκος Παπαγιαννάκος Εθνικό Μετσόβιο Πολυτεχνείο Σχολή Χηµικών Μηχανικών 1 ΒΙΟΚΑΥΣΙΜΑ
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες
 Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
ΚΗΡΟΙ- ΛΙΠΗ- ΕΛΑΙΑ- ΣΑΠΩΝΕΣ ΑΠΟΡΡΥΠΑΝΤΙΚΑ- ΦΩΣΦΟΛΙΠΙΔΙΑ. ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου
 ΚΗΡΟΙ- ΛΙΠΗ- ΕΛΑΙΑ- ΣΑΠΩΝΕΣ ΑΠΟΡΡΥΠΑΝΤΙΚΑ- ΦΩΣΦΟΛΙΠΙΔΙΑ ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου ΚΗΡΟΙ Κηροί είναι μίγματα εστέρων καρβοξυλικών οξέων και
ΚΗΡΟΙ- ΛΙΠΗ- ΕΛΑΙΑ- ΣΑΠΩΝΕΣ ΑΠΟΡΡΥΠΑΝΤΙΚΑ- ΦΩΣΦΟΛΙΠΙΔΙΑ ΓΕΩΠΟΝΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Γενικό Τμήμα Εργαστήριο Χημείας, Καθηγητής Μόσχος Πολυσίου ΚΗΡΟΙ Κηροί είναι μίγματα εστέρων καρβοξυλικών οξέων και
3. Βασικές αρχές-b Σύμπλοκα Κινητική αντιδράσεων μεταλλικών συμπλόκων Σύμπλοκα μεταλλικών ιόντων στα φυσικά ύδατα
 . Βασικές αρχές-b Σύμπλοκα Κινητική αντιδράσεων μεταλλικών συμπλόκων Σύμπλοκα μεταλλικών ιόντων στα φυσικά ύδατα Αντιδράσεις σχηματισμού συμπλόκων και χηλικών ενώσεων Τα µεταλλικά ιόντα αντιδρούν µε δότες
. Βασικές αρχές-b Σύμπλοκα Κινητική αντιδράσεων μεταλλικών συμπλόκων Σύμπλοκα μεταλλικών ιόντων στα φυσικά ύδατα Αντιδράσεις σχηματισμού συμπλόκων και χηλικών ενώσεων Τα µεταλλικά ιόντα αντιδρούν µε δότες
Χημεία Β ΓΕΛ 21 / 04 / 2019
 Β ΓΕΛ 21 / 04 / 2019 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. A1. Από την προσθήκη HBr στο
Β ΓΕΛ 21 / 04 / 2019 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. A1. Από την προσθήκη HBr στο
Εξεταστέα ύλη (από το ΥΠΕΠΘ)
 39 th ICHO 21 ος Πανελλήνιος Μαθητικός Διαγωνισμός Χημείας Τάξη Α Εξεταστέα ύλη 2006-2007 (από το ΥΠΕΠΘ) 1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1) ΑΝΤΙΚΕΙΜΕΝΟ ΤΗΣ ΧΗΜΕΙΑΣ Με τι ασχολείται η χημεία Ποια είναι η σημασία της
39 th ICHO 21 ος Πανελλήνιος Μαθητικός Διαγωνισμός Χημείας Τάξη Α Εξεταστέα ύλη 2006-2007 (από το ΥΠΕΠΘ) 1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1) ΑΝΤΙΚΕΙΜΕΝΟ ΤΗΣ ΧΗΜΕΙΑΣ Με τι ασχολείται η χημεία Ποια είναι η σημασία της
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
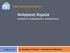 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Πείραμα 2 Αν αντίθετα, στο δοχείο εισαχθούν 20 mol ΗΙ στους 440 ºC, τότε το ΗΙ διασπάται σύμφωνα με τη χημική εξίσωση: 2ΗΙ(g) H 2 (g) + I 2 (g)
 Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Βιοµηχανική παραγωγή βιοντίζελ στην Θεσσαλία. Κόκκαλης Ι. Αθανάσιος Χηµικός Μηχ/κός, MSc Υπεύθυνος παραγωγής
 Βιοµηχανική παραγωγή βιοντίζελ στην Θεσσαλία Κόκκαλης Ι. Αθανάσιος Χηµικός Μηχ/κός, MSc Υπεύθυνος παραγωγής Ορισµοί 1. Βιοµάζα : το βιοαποικοδοµήσιµο κλάσµα προϊόντων, αποβλήτων και καταλοίπων που προέρχονται
Βιοµηχανική παραγωγή βιοντίζελ στην Θεσσαλία Κόκκαλης Ι. Αθανάσιος Χηµικός Μηχ/κός, MSc Υπεύθυνος παραγωγής Ορισµοί 1. Βιοµάζα : το βιοαποικοδοµήσιµο κλάσµα προϊόντων, αποβλήτων και καταλοίπων που προέρχονται
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΘΕΜΑ Α ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 14 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Για τις προτάσεις
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΘΕΜΑ Α ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 14 ΙΟΥΝΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Για τις προτάσεις
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 11 η : Χημική ισορροπία. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 11 η : Χημική ισορροπία Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Η Κατάσταση Ισορροπίας 2 Πολλές αντιδράσεις δεν πραγματοποιούνται
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 11 η : Χημική ισορροπία Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Η Κατάσταση Ισορροπίας 2 Πολλές αντιδράσεις δεν πραγματοποιούνται
ΧΗΜΕΙΑ Α ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ
 ΧΗΜΕΙΑ Α ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 1: ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1.3. «Δομικά σωματίδια της ύλης Δομή του ατόμου Ατομικός αριθμός Μαζικός αριθμός Ισότοπα» Παρατήρηση: Από τον πίνακα 1.4: Μάζα και φορτίο
ΧΗΜΕΙΑ Α ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 1: ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1.3. «Δομικά σωματίδια της ύλης Δομή του ατόμου Ατομικός αριθμός Μαζικός αριθμός Ισότοπα» Παρατήρηση: Από τον πίνακα 1.4: Μάζα και φορτίο
Μηχανική Βιομηχανικών Αντιδραστήρων Υπολογιστικό θέμα
 EΘNIKO ΜEΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Ανάλυσης, Σχεδιασμού & Ανάπτυξης Διεργασιών & Συστημάτων Μηχανική Βιομηχανικών Αντιδραστήρων Υπολογιστικό θέμα Μάθημα κατεύθυνσης 8 ου εξαμήνου
EΘNIKO ΜEΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Ανάλυσης, Σχεδιασμού & Ανάπτυξης Διεργασιών & Συστημάτων Μηχανική Βιομηχανικών Αντιδραστήρων Υπολογιστικό θέμα Μάθημα κατεύθυνσης 8 ου εξαμήνου
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
Επιμέλεια: Καρνάβα Σοφία
 Επιμέλεια: Καρνάβα Σοφία Τι είναι λοιπόν η Oργανοκατάλυση Ως Oργανοκατάλυση ορίζεται το είδος κατάλυσης, όπου η ταχύτητα και η απόδοση μιας αντίδρασης αυξάνεται από κάποιο οργανικό μόριο που χαρακτηρίζεται
Επιμέλεια: Καρνάβα Σοφία Τι είναι λοιπόν η Oργανοκατάλυση Ως Oργανοκατάλυση ορίζεται το είδος κατάλυσης, όπου η ταχύτητα και η απόδοση μιας αντίδρασης αυξάνεται από κάποιο οργανικό μόριο που χαρακτηρίζεται
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
2. ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΧΟΜΕΝΑ
 2. ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΧΟΜΕΝΑ Τύποι διαλυμάτων Διαλυτότητα και η διαδικασία διάλυσης Επιδράσεις θερμοκρασίας και πίεσης πάνω στη διαλυτότητα Τρόποι έκφρασης της συγκέντρωσης Τάση ατμών διαλύματος Ανύψωση σημείου
2. ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΧΟΜΕΝΑ Τύποι διαλυμάτων Διαλυτότητα και η διαδικασία διάλυσης Επιδράσεις θερμοκρασίας και πίεσης πάνω στη διαλυτότητα Τρόποι έκφρασης της συγκέντρωσης Τάση ατμών διαλύματος Ανύψωση σημείου
ΟΙ ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΟΞΙΝΗΣ ΒΡΟΧΗΣ ΣΤΟ ΠΕΡΙΒΑΛΛΟΝ
 !Unexpected End of Formula l ΟΙ ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΟΞΙΝΗΣ ΒΡΟΧΗΣ ΣΤΟ ΠΕΡΙΒΑΛΛΟΝ ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Παραδεισανός Αδάμ ΠΡΟΛΟΓΟΣ Η εργασία αυτή εκπονήθηκε το ακαδημαϊκό έτος 2003 2004 στο μάθημα «Το πείραμα στη
!Unexpected End of Formula l ΟΙ ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΟΞΙΝΗΣ ΒΡΟΧΗΣ ΣΤΟ ΠΕΡΙΒΑΛΛΟΝ ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Παραδεισανός Αδάμ ΠΡΟΛΟΓΟΣ Η εργασία αυτή εκπονήθηκε το ακαδημαϊκό έτος 2003 2004 στο μάθημα «Το πείραμα στη
ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΠΡΟΣΘΗΚΗΣ ΤΟΥ ΒΙΟΝΤΙΖΕΛ FAME ΣΤΗΝ ΠΟΙΟΤΗΤΑ ΤΟΥ ΠΕΤΡΕΛΑΙΟΥ ΚΙΝΗΣΗΣ
 ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΠΡΟΣΘΗΚΗΣ ΤΟΥ ΒΙΟΝΤΙΖΕΛ FAME ΣΤΗΝ ΠΟΙΟΤΗΤΑ ΤΟΥ ΠΕΤΡΕΛΑΙΟΥ ΚΙΝΗΣΗΣ Αθηνά Τουµπέλη Ελληνικά Πετρέλαια Α.Ε. Βιοµηχανικές Εγκαταστάσεις Θεσσαλονίκης Π Ε Ρ Ι Ε Χ Ο Μ Ε Ν Α Σκοπός της µελέτης
ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΠΡΟΣΘΗΚΗΣ ΤΟΥ ΒΙΟΝΤΙΖΕΛ FAME ΣΤΗΝ ΠΟΙΟΤΗΤΑ ΤΟΥ ΠΕΤΡΕΛΑΙΟΥ ΚΙΝΗΣΗΣ Αθηνά Τουµπέλη Ελληνικά Πετρέλαια Α.Ε. Βιοµηχανικές Εγκαταστάσεις Θεσσαλονίκης Π Ε Ρ Ι Ε Χ Ο Μ Ε Ν Α Σκοπός της µελέτης
Ονοματεπώνυμο: Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Αριθμός Οξείδωσης Ονοματολογία Απλή Αντικατάσταση Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ
 ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
καρβοξυλικά οξέα μεθυλοπροπανικό οξύ
 112 4.1. Κορεσμένα μονο - Αιθανικό οξύ Γενικά Τα κορεσμένα μονο προκύπτουν θεωρητικά από τα αλκάνια, αν αντικαταστήσουμε ένα άτομο υδρογόνου με τη ρίζα καρβοξύλιο -COOH. Έχουν το γενικό τύπο: C ν H 2ν+1
112 4.1. Κορεσμένα μονο - Αιθανικό οξύ Γενικά Τα κορεσμένα μονο προκύπτουν θεωρητικά από τα αλκάνια, αν αντικαταστήσουμε ένα άτομο υδρογόνου με τη ρίζα καρβοξύλιο -COOH. Έχουν το γενικό τύπο: C ν H 2ν+1
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ
 ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
Παράγοντες που εξηγούν τη διαλυτότητα. Είδη διαλυμάτων
 Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Η µελέτη αυτή είναι µέρος του έργου BIOFUELS-2G που χρηµατοδοτείται από το Ευρωπαϊκό Πρόγραµµα LIFE+ (LIFE08 ENV/GR/000569)
 Παραγωγή Βιοκαυσίµων µε Υδρογονοπεξεργασία Χρησιµοποιηµένων Τηγανελαίων ρ. Στέλλα Μπεζεργιάννη Χηµικός Μηχανικός Ερευνήτρια ΕΚΕΤΑ Εθνικό Κέντρο Έρευνας & Τεχνολογικής Ανάπτυξης (ΕΚΕΤΑ) Ινστιτούτο Τεχνικής
Παραγωγή Βιοκαυσίµων µε Υδρογονοπεξεργασία Χρησιµοποιηµένων Τηγανελαίων ρ. Στέλλα Μπεζεργιάννη Χηµικός Μηχανικός Ερευνήτρια ΕΚΕΤΑ Εθνικό Κέντρο Έρευνας & Τεχνολογικής Ανάπτυξης (ΕΚΕΤΑ) Ινστιτούτο Τεχνικής
ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ
 ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της πρότασης και, δίπλα, το γράμμα που αντιστοιχεί στη σωστή επιλογή. Α1. Ποια
ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της πρότασης και, δίπλα, το γράμμα που αντιστοιχεί στη σωστή επιλογή. Α1. Ποια
Xημεία β γυμνασίου. Ερωτήσεις πολλαπλής επιλογής
 Xημεία β γυμνασίου Ερωτήσεις πολλαπλής επιλογής 1. Ένα υγρό βρέθηκε με τη βοήθεια του ζυγού ότι έχει μάζα 22g και με τη βοήθεια ογκομετρικού κυλίνδρου ότι έχει όγκο 20 ml. Η πυκνότητά του είναι: α. 1,1
Xημεία β γυμνασίου Ερωτήσεις πολλαπλής επιλογής 1. Ένα υγρό βρέθηκε με τη βοήθεια του ζυγού ότι έχει μάζα 22g και με τη βοήθεια ογκομετρικού κυλίνδρου ότι έχει όγκο 20 ml. Η πυκνότητά του είναι: α. 1,1
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (3) ΣΧΗΜΑΤΙΣΜΟΣ ΙΖΗΜΑΤΩΝ. ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (3) ΣΧΗΜΑΤΙΣΜΟΣ ΙΖΗΜΑΤΩΝ ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΠΟΙΗΣΗ ΙΖΗΜΑΤΟΣ (1) I.P = [M α+ ] m [X β- ] x < K sp (M m X x ) 1. Σχηµατισµός
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (3) ΣΧΗΜΑΤΙΣΜΟΣ ΙΖΗΜΑΤΩΝ ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΠΟΙΗΣΗ ΙΖΗΜΑΤΟΣ (1) I.P = [M α+ ] m [X β- ] x < K sp (M m X x ) 1. Σχηµατισµός
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων. Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης
 Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ. Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια.
 ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
ΠΑΡΑΓΩΓΗ ΒΙΟΚΑΥΣΙΜΟΥ 2 ΗΣ ΓΕΝΙΑΣ
 ΠΑΡΑΓΩΓΗ ΒΙΟΚΑΥΣΙΜΟΥ 2 ΗΣ ΓΕΝΙΑΣ ΑΠΟ ΧΡΗΣΙΜΟΠΟΙΗΜΕΝΟ ΤΗΓΑΝΕΛΑΙΟ Δρ. Στέλλα Μπεζεργιάννη ΕΚΕΤΑ Εθνικό Κέντρο Έρευνας & Τεχνολογικής Ανάπτυξης (ΕΚΕΤΑ) Ινστιτούτο Τεχνικής Χημικών Διεργασιών (ΙΤΧΗΔ) Εργαστήριο
ΠΑΡΑΓΩΓΗ ΒΙΟΚΑΥΣΙΜΟΥ 2 ΗΣ ΓΕΝΙΑΣ ΑΠΟ ΧΡΗΣΙΜΟΠΟΙΗΜΕΝΟ ΤΗΓΑΝΕΛΑΙΟ Δρ. Στέλλα Μπεζεργιάννη ΕΚΕΤΑ Εθνικό Κέντρο Έρευνας & Τεχνολογικής Ανάπτυξης (ΕΚΕΤΑ) Ινστιτούτο Τεχνικής Χημικών Διεργασιών (ΙΤΧΗΔ) Εργαστήριο
Ε. Μαλαμίδου-Ξενικάκη
 Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Ε. Μαλαμίδου-Ξενικάκη Θεσσαλονίκη 2015 ΑΛΚΥΝΙΑ: C ν H 2ν-2 Ο τριπλός δεσμός άνθρακα άνθρακα Τριπλός δεσμός αλκυνίου ΑΛΚΥΝΙΑ Μόρια πρότυπα για «μοριακούς διακόπτες» Μικροσκοπία σάρωσης σήραγγας (Scanning
Αντιδράσεις οξείδωσης αναγωγής οργανικών ενώσεων.
 Αντιδράσεις οξείδωσης αναγωγής οργανικών ενώσεων. Οξείδωση είναι η αύξηση του αριθμού οξείδωσης ατόμου ή ιόντος. Αναγωγή είναι η ελάττωση του αριθμού οξείδωσης ατόμου ή ιόντος. Στην οργανική οξείδωση είναι
Αντιδράσεις οξείδωσης αναγωγής οργανικών ενώσεων. Οξείδωση είναι η αύξηση του αριθμού οξείδωσης ατόμου ή ιόντος. Αναγωγή είναι η ελάττωση του αριθμού οξείδωσης ατόμου ή ιόντος. Στην οργανική οξείδωση είναι
ΕΤΕΡΟΓΕΝΗΣ ΚΑΤΑΛΥΤΙΚΗ ΜΕΤΑΤΡΟΠΗ ΣΕ ΒΙΟΝΤΙΖΕΛ. Μονάδα Μηχανικής ιεργασιών Υδρογονανθράκων και Βιοκαυσίµων
 Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χηµικών Μηχανικών Τοµέας ΙΙ Μονάδα Μηχανικής ιεργασιών Υδρογονανθράκων και Βιοκαυσίµων ΕΤΕΡΟΓΕΝΗΣ ΚΑΤΑΛΥΤΙΚΗ ΜΕΤΑΤΡΟΠΗ ΕΛΕΥΘΕΡΩΝ ΛΙΠΑΡΩΝ ΟΞΕΩΝ ΟΞΙΝΩΝ ΕΛΑΙΩΝ ΣΕ ΒΙΟΝΤΙΖΕΛ
Εθνικό Μετσόβιο Πολυτεχνείο (ΕΜΠ) Σχολή Χηµικών Μηχανικών Τοµέας ΙΙ Μονάδα Μηχανικής ιεργασιών Υδρογονανθράκων και Βιοκαυσίµων ΕΤΕΡΟΓΕΝΗΣ ΚΑΤΑΛΥΤΙΚΗ ΜΕΤΑΤΡΟΠΗ ΕΛΕΥΘΕΡΩΝ ΛΙΠΑΡΩΝ ΟΞΕΩΝ ΟΞΙΝΩΝ ΕΛΑΙΩΝ ΣΕ ΒΙΟΝΤΙΖΕΛ
ΔΙΔΑΚΤΕΑ ΥΛΗ ΧΗΜΕΙΑΣ Β ΓΥΜΝΑΣΙΟΥ 2015-16
 ΔΙΔΑΚΤΕΑ ΥΛΗ ΧΗΜΕΙΑΣ Β ΓΥΜΝΑΣΙΟΥ 205-6 ΔΕΙΚΤΕΣ ΕΠΙΤΥΧΙΑΣ Οι μαθητές και οι μαθήτριες θα πρέπει να είναι σε θέση: ΔΕΙΚΤΕΣ ΕΠΑΡΚΕΙΑΣ Διδ. περ. Σύνολο διδ.περ.. Η συμβολή της Χημείας στην εξέλιξη του πολιτισμού
ΔΙΔΑΚΤΕΑ ΥΛΗ ΧΗΜΕΙΑΣ Β ΓΥΜΝΑΣΙΟΥ 205-6 ΔΕΙΚΤΕΣ ΕΠΙΤΥΧΙΑΣ Οι μαθητές και οι μαθήτριες θα πρέπει να είναι σε θέση: ΔΕΙΚΤΕΣ ΕΠΑΡΚΕΙΑΣ Διδ. περ. Σύνολο διδ.περ.. Η συμβολή της Χημείας στην εξέλιξη του πολιτισμού
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 7 ΣΕΛΙΔΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΣΑΒΒΑΤΟ 8 ΣΕΠΤΕΜΒΡΙΟΥ 018 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΣΑΒΒΑΤΟ 8 ΣΕΠΤΕΜΒΡΙΟΥ 018 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ
ΓΥΜΝΑΣΙΟ ΑΡΑΔΙΠΠΟΥ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ ΧΡΟΝΟΣ: 2 Ώρες (Χημεία + Φυσική)
 ΓΥΜΝΑΣΙΟ ΑΡΑΔΙΠΠΟΥ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2014-2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ: XHMEIA (35/100) ΤΑΞΗ: Β Γυμνασίου ΗΜΕΡΟΜΗΝΙΑ: 8/6/2015. ΧΡΟΝΟΣ: 2 Ώρες (Χημεία + Φυσική) ΒΑΘΜΟΛΟΓΙΑ Αριθμητικά:.
ΓΥΜΝΑΣΙΟ ΑΡΑΔΙΠΠΟΥ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2014-2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ: XHMEIA (35/100) ΤΑΞΗ: Β Γυμνασίου ΗΜΕΡΟΜΗΝΙΑ: 8/6/2015. ΧΡΟΝΟΣ: 2 Ώρες (Χημεία + Φυσική) ΒΑΘΜΟΛΟΓΙΑ Αριθμητικά:.
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
Χαρακτηρισμός των στερεών ιζημάτων ανάκτησης φωσφόρου Μελέτη βιοδιαθεσιμότητας του παραγόμενου προϊόντος
 ΠΡΑΞΗ ΕΘΝΙΚΗΣ ΕΜΒΕΛΕΙΑΣ «Πρόγραμμα Ανάπτυξης Βιομηχανικής Έρευνας και Τεχνολογίας (ΠΑΒΕΤ) 2013» Δευτέρα 25 Μαΐου, 2015 Ημερίδα - Κ.Ε.Δ.Ε.Α. Θεσσαλονίκη Χαρακτηρισμός των στερεών ιζημάτων ανάκτησης φωσφόρου
ΠΡΑΞΗ ΕΘΝΙΚΗΣ ΕΜΒΕΛΕΙΑΣ «Πρόγραμμα Ανάπτυξης Βιομηχανικής Έρευνας και Τεχνολογίας (ΠΑΒΕΤ) 2013» Δευτέρα 25 Μαΐου, 2015 Ημερίδα - Κ.Ε.Δ.Ε.Α. Θεσσαλονίκη Χαρακτηρισμός των στερεών ιζημάτων ανάκτησης φωσφόρου
Στοιχειμετρικοί υπολογισμοί σε διαλύματα
 Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Πολυτεχνείο Κρήτης Σχολή Μηχανικών Περιβάλλοντος. Υδατική Χηµεία. Σηµειώσεις
 110 Πολυτεχνείο Κρήτης Σχολή Μηχανικών Περιβάλλοντος Υδατική Χηµεία Σηµειώσεις Κεφάλαιο : Τύχη των µετάλλων στο περιβάλλον Υδρόλυση και συµπλοκοποίηση µετάλλων Σταθερές συµπλοκοποίησης Οργανική συµπλοκοποίηση
110 Πολυτεχνείο Κρήτης Σχολή Μηχανικών Περιβάλλοντος Υδατική Χηµεία Σηµειώσεις Κεφάλαιο : Τύχη των µετάλλων στο περιβάλλον Υδρόλυση και συµπλοκοποίηση µετάλλων Σταθερές συµπλοκοποίησης Οργανική συµπλοκοποίηση
Χημεία. ΘΕΜΑ Α A1. α - 5 μονάδες
 Β ΓΕΛ 21 / 04 / 2019 Χημεία ΘΕΜΑ Α A1. α - 5 μονάδες A2. β - 5 μονάδες A3. α - 5 μονάδες A4. δ - 5 μονάδες A5. α - 5 μονάδες ΘΕΜΑ Β Β1. Σε ένα χημικό εργαστήριο διαθέτουμε ισοπροπυλική αλκοόλη (δευτεροταγής
Β ΓΕΛ 21 / 04 / 2019 Χημεία ΘΕΜΑ Α A1. α - 5 μονάδες A2. β - 5 μονάδες A3. α - 5 μονάδες A4. δ - 5 μονάδες A5. α - 5 μονάδες ΘΕΜΑ Β Β1. Σε ένα χημικό εργαστήριο διαθέτουμε ισοπροπυλική αλκοόλη (δευτεροταγής
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ
 ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της πρότασης και, δίπλα, το γράμμα που αντιστοιχεί στη σωστή επιλογή. Α1. Δίνεται
ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α5 να γράψετε στο τετράδιό σας τον αριθμό της πρότασης και, δίπλα, το γράμμα που αντιστοιχεί στη σωστή επιλογή. Α1. Δίνεται
1.5 Αλκένια - αιθένιο ή αιθυλένιο
 19 1.5 Αλκένια - αιθένιο ή αιθυλένιο Γενικά Αλκένια ονομάζονται οι άκυκλοι ακόρεστοι υδρογονάνθρακες, οι οποίοι περιέχουν ένα διπλό δεσμό στο μόριο. O γενικός τύπος των αλκενίων είναι C ν Η 2ν (ν 2). Στον
19 1.5 Αλκένια - αιθένιο ή αιθυλένιο Γενικά Αλκένια ονομάζονται οι άκυκλοι ακόρεστοι υδρογονάνθρακες, οι οποίοι περιέχουν ένα διπλό δεσμό στο μόριο. O γενικός τύπος των αλκενίων είναι C ν Η 2ν (ν 2). Στον
ΚΑΤΑΛΥΤΙΚΆ ΥΛΙΚΆ. 1. Παρασκευή Στηριγμένων Καταλυτών. 2. Χαρακτηρισμός Καταλυτών
 ΚΑΤΑΛΥΤΙΚΆ ΥΛΙΚΆ 1. Παρασκευή Στηριγμένων Καταλυτών 2. Χαρακτηρισμός Καταλυτών Παρασκευή Στηριγμένων Καταλυτών Τεχνικές Εμποτισμού Ξηρός Εμποτισμός Υγρός Εμποτισμός Απλός Εμποτισμός Εναπόθεση - Καθίζηση
ΚΑΤΑΛΥΤΙΚΆ ΥΛΙΚΆ 1. Παρασκευή Στηριγμένων Καταλυτών 2. Χαρακτηρισμός Καταλυτών Παρασκευή Στηριγμένων Καταλυτών Τεχνικές Εμποτισμού Ξηρός Εμποτισμός Υγρός Εμποτισμός Απλός Εμποτισμός Εναπόθεση - Καθίζηση
Αιωρήματα & Γαλακτώματα
 Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2014-15 Μάθημα 2ο 25 February 2015 Αιωρήματα Γαλακτώματα 1 Παρασκευή αιωρημάτων Οι μέθοδοι παρασκευής αιωρημάτων κατατάσσονται σε δύο μεγάλες κατηγορίες
Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2014-15 Μάθημα 2ο 25 February 2015 Αιωρήματα Γαλακτώματα 1 Παρασκευή αιωρημάτων Οι μέθοδοι παρασκευής αιωρημάτων κατατάσσονται σε δύο μεγάλες κατηγορίες
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ ΧΗΜΕΙΑ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Η σωστή τετράδα κβαντικών αριθμών για το μονήρες
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Η σωστή τετράδα κβαντικών αριθμών για το μονήρες
Γ.Κονδύλη 1 & Όθωνος-Μ αρούσι Τ ηλ. Κέντρο: , /
 Γ.Κονδύλη 1 & Όθωνος-Μ αρούσι Τ ηλ. Κέντρο:210-61.24.000, http:/ / www.akadimos.gr ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ 2016 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ Επιμέλεια θεμάτων: Βελαώρας Βασίλειος, Χημικός ΘΕΜΑ Α Για
Γ.Κονδύλη 1 & Όθωνος-Μ αρούσι Τ ηλ. Κέντρο:210-61.24.000, http:/ / www.akadimos.gr ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ 2016 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ Επιμέλεια θεμάτων: Βελαώρας Βασίλειος, Χημικός ΘΕΜΑ Α Για
ΚΑΥΣΙΜΑ-ΚΑΥΣΗ ΠΕΤΡΕΛΑΙΟ
 ΚΑΥΣΙΜΑ-ΚΑΥΣΗ Τα καύσιμα είναι υλικά που, όταν καίγονται, αποδίδουν σημαντικά και εκμεταλλεύσιμα ποσά θερμότητας. Τα καύσιμα που παίρνουμε έτοιμα από τη φύση λέγονται φυσικά, ενώ αυτά που παρασκευάζουμε
ΚΑΥΣΙΜΑ-ΚΑΥΣΗ Τα καύσιμα είναι υλικά που, όταν καίγονται, αποδίδουν σημαντικά και εκμεταλλεύσιμα ποσά θερμότητας. Τα καύσιμα που παίρνουμε έτοιμα από τη φύση λέγονται φυσικά, ενώ αυτά που παρασκευάζουμε
Ι. Ντότσικας, Επ. Καθηγητής Φαρμακευτικής ΕΚΠΑ. Οι κυκλοδεξτρίνες (cyclodextrins, CDs)
 Οι κυκλοδεξτρίνες (cyclodextrins, CDs) Οι κυκλοδεξτρίνες είναι μία οικογένεια κυκλικών ολιγοσακχαριτών αποτελούμενες από μονομερή σακχάρων (α-d-γλυκοπυρανόζη) συνδεδεμένων μεταξύ τους με α - [1,4] γλυκοσιδικούς
Οι κυκλοδεξτρίνες (cyclodextrins, CDs) Οι κυκλοδεξτρίνες είναι μία οικογένεια κυκλικών ολιγοσακχαριτών αποτελούμενες από μονομερή σακχάρων (α-d-γλυκοπυρανόζη) συνδεδεμένων μεταξύ τους με α - [1,4] γλυκοσιδικούς
13. Μεταλλοκένια. Μεταλλοκένια: Ενώσεις σάντουιτς (σημαντικότερο το φερροκένιο) Τύποι διαμόρφωσης (conformations) φερροκενίου. Καλυπτική (eclipsed)
 13. εταλλοκένια εταλλοκένια: Ενώσεις σάντουιτς (σημαντικότερο το φερροκένιο) Τύποι διαμόρφωσης (conformations) φερροκενίου ιαβαθμισμένη (staggered) Καλυπτική (eclipsed) Ετεροκλινής (skew) Ανακάλυψη: Kealy
13. εταλλοκένια εταλλοκένια: Ενώσεις σάντουιτς (σημαντικότερο το φερροκένιο) Τύποι διαμόρφωσης (conformations) φερροκενίου ιαβαθμισμένη (staggered) Καλυπτική (eclipsed) Ετεροκλινής (skew) Ανακάλυψη: Kealy
BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ
 BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 1. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 2. BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ Ι. ΑΤΟΜΑ ΚΑΙ ΜΟΡΙΑ ΙΙ. ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΙΙΙ. ΜΑΚΡΟΜΟΡΙΑ ΣΤΑ ΚΥΤΤΑΡΑ
BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ ΕΝΕΡΓΕΙΑ ΚΑΙ ΜΕΤΑΒΟΛΙΣΜΟΣ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 1. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΚΥΤΤΑΡΩΝ 2. BΑΣΙΚΕΣ ΑΡΧΕΣ ΒΙΟΧΗΜΕΙΑΣ Ι. ΑΤΟΜΑ ΚΑΙ ΜΟΡΙΑ ΙΙ. ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΙΙΙ. ΜΑΚΡΟΜΟΡΙΑ ΣΤΑ ΚΥΤΤΑΡΑ
Βασικές έννοιες και κατάρτιση φακέλου, Μέρος III
 Βασικές έννοιες και κατάρτιση φακέλου, Μέρος III Ουσίες UVCB Gabriele CHRIST http://echa.europa.eu 1 Ουσίες UVCB Άγνωστης (U) ή Ασταθούς σύνθεσης (V) Προϊόντα πολύπλοκων αντιδράσεων (C) ή Βιολογικά υλικά
Βασικές έννοιες και κατάρτιση φακέλου, Μέρος III Ουσίες UVCB Gabriele CHRIST http://echa.europa.eu 1 Ουσίες UVCB Άγνωστης (U) ή Ασταθούς σύνθεσης (V) Προϊόντα πολύπλοκων αντιδράσεων (C) ή Βιολογικά υλικά
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 7 ΣΕΛΙΔΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΠΑΡΑΣΚΕΥΗ 6 ΣΕΠΤΕΜΒΡΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΠΑΡΑΣΚΕΥΗ 6 ΣΕΠΤΕΜΒΡΙΟΥ 2019 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 7 ΣΕΛΙΔΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΚΑΙ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΣΕΠΤΕΜΒΡΙΟΥ 018 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΚΑΙ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΣΕΠΤΕΜΒΡΙΟΥ 018 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ. + SO 4 Βάσεις είναι οι ενώσεις που όταν διαλύονται σε νερό δίνουν ανιόντα υδροξειδίου (ΟΗ - ). NaOH Na
 ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ ΙΔΙΟΤΗΤΕΣ ΟΞΕΩΝ Αλλάζουν το χρώμα των δεικτών. Αντιδρούν με μέταλλα και παράγουν αέριο υδρογόνο (δες απλή αντικατάσταση) Αντιδρούν με ανθρακικά άλατα και παράγουν αέριο CO2. Έχουν όξινη
ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ ΙΔΙΟΤΗΤΕΣ ΟΞΕΩΝ Αλλάζουν το χρώμα των δεικτών. Αντιδρούν με μέταλλα και παράγουν αέριο υδρογόνο (δες απλή αντικατάσταση) Αντιδρούν με ανθρακικά άλατα και παράγουν αέριο CO2. Έχουν όξινη
ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ
 ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΜΟΝΤΕΛΑ ΜΕΜΒΡΑΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ 1. Μονοστιβάδες 2. Διπλοστιβάδες 3. Λιποσώματα 1.1 ΜΟΝΟΣΤΙΒΑΔΕΣ Σχηματίζονται από μη-πολικά μόρια στη μεσόφαση αέρα/νερού Συσκευή
ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΜΟΝΤΕΛΑ ΜΕΜΒΡΑΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ 1. Μονοστιβάδες 2. Διπλοστιβάδες 3. Λιποσώματα 1.1 ΜΟΝΟΣΤΙΒΑΔΕΣ Σχηματίζονται από μη-πολικά μόρια στη μεσόφαση αέρα/νερού Συσκευή
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΤΩΝ ΟΞΕΙΔΙΩΝ ΤΟΥ ΑΖΩΤΟΥ (NO X
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΤΩΝ ΟΞΕΙΔΙΩΝ ΤΟΥ ΑΖΩΤΟΥ (NO X
22 ος Πανελλήνιος Μαθητικός ιαγωνισµός Χηµείας (για την 40 η ICHO) Εξεταστέα ύλη (από το ΥΠΕΠΘ)
 22 ος Πανελλήνιος Μαθητικός ιαγωνισµός Χηµείας (για την 40 η ICHO) Εξεταστέα ύλη 2007-2008 (από το ΥΠΕΠΘ) Οι µαθητές της Β τάξης του Ενιαίου Λυκείου και των ΕΠΑ.Λ. εξετάζονται σε θέµατα σχετικά µε την
22 ος Πανελλήνιος Μαθητικός ιαγωνισµός Χηµείας (για την 40 η ICHO) Εξεταστέα ύλη 2007-2008 (από το ΥΠΕΠΘ) Οι µαθητές της Β τάξης του Ενιαίου Λυκείου και των ΕΠΑ.Λ. εξετάζονται σε θέµατα σχετικά µε την
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
ΘΕΜΑ 1 0 Να επιλέξετε τη σωστή απάντηση σε κάθε μία από τις επόμενες ερωτήσεις:
 Άνω Γλυφάδα 21/10/2017 ΔΙΑΓΩΝΙΣΜΑ Μάθημα: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Καθηγητής/τρια: Αυγερινού Χρόνος: 3 ώρες Ονοματεπώνυμο: Τμήμα: Γ ΘΕΜΑ 1 0 Να επιλέξετε τη σωστή απάντηση σε κάθε μία από τις επόμενες ερωτήσεις:
Άνω Γλυφάδα 21/10/2017 ΔΙΑΓΩΝΙΣΜΑ Μάθημα: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ Καθηγητής/τρια: Αυγερινού Χρόνος: 3 ώρες Ονοματεπώνυμο: Τμήμα: Γ ΘΕΜΑ 1 0 Να επιλέξετε τη σωστή απάντηση σε κάθε μία από τις επόμενες ερωτήσεις:
Θρεπτικές ύλες Τρόφιµα - Τροφή
 ΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ 1 Θρεπτικές ύλες Τι καλούµε θρεπτικές ύλες; Ποιες είναι; Τρόφιµα Τι καλούµε τρόφιµο; Χηµεία Τροφίµων Θρεπτικές ύλες Τρόφιµα - Τροφή Προϋπόθεση για να χαρακτηριστεί ένα προϊόν τρόφιµο; 2
ΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ 1 Θρεπτικές ύλες Τι καλούµε θρεπτικές ύλες; Ποιες είναι; Τρόφιµα Τι καλούµε τρόφιµο; Χηµεία Τροφίµων Θρεπτικές ύλες Τρόφιµα - Τροφή Προϋπόθεση για να χαρακτηριστεί ένα προϊόν τρόφιµο; 2
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
ΜΙΑ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΔΟΣ ΤΗ ΒΔΟΜΑΔΑ ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΠΡΩΤΗ ΕΝΟΤΗΤΑ
 ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ Γ ΤΑΞΗ ΓΥΜΝΑΣΙΟΥ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΜΙΑ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΔΟΣ ΤΗ ΒΔΟΜΑΔΑ ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ
ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ Γ ΤΑΞΗ ΓΥΜΝΑΣΙΟΥ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΜΙΑ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΔΟΣ ΤΗ ΒΔΟΜΑΔΑ ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ
