ΒΙΟΛΟΓΙΚΗ ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΦΥΣΙΚΩΝ ΚΑΙ ΤΕΧΝΗΤΩΝ ΙΣΤΩΝ
|
|
|
- Λυσιμάχη Δουμπιώτης
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΒΙΟΛΟΓΙΚΗ ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΦΥΣΙΚΩΝ ΚΑΙ ΤΕΧΝΗΤΩΝ ΙΣΤΩΝ Ροκίδη Σταματία Χημικός Μηχανικός Πανεπιστήμιο Πατρών, Τμήμα Χημικών Μηχανικών Εργαστήριο Ανόργανης και Αναλυτικής Χημείας Πάτρα, 2011
2 ΒΙΟΛΟΓΙΚΗ ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΦΥΣΙΚΩΝ ΚΑΙ ΤΕΧΝΗΤΩΝ ΙΣΤΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Υποβληθείσα στο Τμήμα Χημικών Μηχανικών του Πανεπιστημίου Πατρών Υπό ΡΟΚΙΔΗ ΣΤΑΜΑΤΙΑΣ Χημικού Μηχανικού Για την απόκτηση του τίτλου της Διδάκτορος του Πανεπιστημίου Πατρών ΠΑΤΡΑ, 2011
3 Η έγκριση της Διδακτορικής Διατριβής από το Τμήμα Χημικών Μηχανικών της Πολυτεχνικής Σχολής του Πανεπιστημίου Πατρών δεν υποδηλώνει αποδοχή των γνωμών του συγγραφέα. (Ν. 5343/1932, Άρθρο 202)
4
5 Στη μητέρα μου
6
7 ΠΡΟΛΟΓΟΣ Η παρούσα διδακτορική διατριβή εκπονήθηκε στο εργαστήριο Ανόργανης και Αναλυτικής Χημείας, του Τμήματος Χημικών Μηχανικών του Πανεπιστημίου Πατρών κατά το χρονικό διάστημα Οκτωβρίου Οκτωβρίου 2010, υπό την επίβλεψη του Καθηγητή κ. Πέτρου Κουτσούκου, προς τον οποίο εκφράζω τις θερμότατες ευχαριστίες μου, τόσο για την επιστημονική του καθοδήγηση, όσο και για την αμέριστη συμπαράστασή του καθ όλη τη διάρκεια της συνεργασίας μας. Τον ευχαριστώ για τις πολύτιμες συμβουλές του σε επιστημονικό και προσωπικό επίπεδο. Το ήθος και η ευγένεια της ψυχής του αποτέλεσαν εξαιρετικό παράδειγμα. Είναι για μένα πραγματικός δάσκαλος και του χρωστώ ευγνωμοσύνη για το χρόνο που αφιέρωσε και την ψυχολογική στήριξη που μου προσέφερε κατά την ερευνητική και συγγραφική πορεία της διατριβής μου. Ευχαριστώ θερμά τον Επίκουρο Καθηγητή του τμήματος Μηχανολόγων και Αεροναυπηγών Μηχανικών κ. Δημοσθένη Μαυρίλα, μέλος της Τριμελούς Συμβουλευτικής Επιτροπής, για το ότι μου μετέδωσε τις γνώσεις και την εμπειρία του στη βιολογική ασβεστοποίηση ιστών, για το συνεχές ενδιαφέρον του και για την συνεργασία του. Θα ήθελα επίσης να εκφράσω τις ευχαριστίες μου προς τον κ. Χρίστο Κοντογιάννη, Καθηγητή του Τμήματος Φαρμακευτικής, μέλος της Τριμελούς Συμβουλευτικής Επιτροπής, για τις εύστοχες παρατηρήσεις και υποδείξεις του κατά το σεμινάριο προόδου μου καθώς και για την πρόσβαση που μου παρείχε στο εργαστήριό του. Ιδιαιτέρως ευχαριστώ τον κ. Παύλο Κλεπετσάνη, Επίκουρο Καθηγητή του Τμήματος Φαρμακευτικής, για την ενθάρρυνσή του και την πολύτιμη βοήθεια σε επιστημονικά και τεχνικά θέματα. Θα ήθελα επίσης να ευχαριστήσω τον Επίκουρο Καθηγητή του Τμήματος Επιστήμης Υλικών κ. Νικόλαο Μπουρόπουλο, για την επιστημονική συνεργασία του και την πρόσβαση που μου παρείχε στο εργαστήριό του. Επιπλέον, θα ήθελα να ευχαριστήσω τον κ. Συμεών Αγαθόπουλο, Επίκουρο Καθηγητή του Τμήματος Μηχανικών Επιστήμης Υλικών του Πανεπιστημίου Ιωαννίνων για τη συμμετοχή του στην Επταμελή Εξεταστική Επιτροπή καθώς και για τις επιστημονικές συμβουλές που μου έδωσε κατά τη διάρκεια του 1 ου κοινού συνεδρίου Ελληνικής Εταιρείας Βιοϋλικών & Τμήματος Ορθοπαιδικής Έρευνας και του 4 ου συνεδρίου Ελληνικής Εμβιομηχανικής Εταιρείας. Ευχαριστώ τον Επίκουρο Καθηγητή του Τμήματος Χημικών Μηχανικών κ. Χριστάκη Παρασκευά για τη συμμετοχή του στην Επταμελή Εξεταστική Επιτροπή, για το ενδιαφέρον που έδειξε όλα αυτά τα χρόνια και την απρόσκοπτη πρόσβαση που μου παρείχε στο εργαστήριο Φαινομένων Μεταφοράς και Φυσικοχημικής Υδροδυναμικής. i
8 Οφείλω ακόμα να εκφράσω τις ευχαριστίες μου στον Αναπληρωτή Καθηγητή της σχολής Θετικών Επιστημών και Τεχνολογίας του Ελληνικού Ανοιχτού Πανεπιστημίου κ. Νικόλαο Σπανό για την επιστημονική καθοδήγηση και την πολύτιμη βοήθειά του στη μελέτη του ηλεκτροστατικού δυναμικού των επιφανειών με τη μέθοδο του ρευματικού δυναμικού (streaming potential). Ευχαριστώ την Prof. Christèle Combes του CIRIMAT, UPS-INPT-CNRS, ENSIACET, του Πολυτεχνείου της Τουλούζης για την φιλοξενία και την υποστήριξή της κατά την διάρκεια της παραμονής μου στο εργαστήριό της. Επίσης, θα ήθελα να ευχαριστήσω τον Καθηγητή κ. Στεφάνο Φούσσα και την ομάδα του από την καρδιοχειρουργική κλινική του Τζάννειου Νοσοκομείου Πειραιώς για την παραχώρηση των ασβεστοποιημένων ιστών από ανθρώπινες φυσικές βαλβίδες καρδιάς. Ευχαριστίες επίσης οφείλονται και στην εταιρεία Synovis Surgical Innovations (SSI) για την διάθεση δειγμάτων βόειου περικαρδίου για τη μελέτη της ασβεστοποίησής τους. Τις ειλικρινείς ευχαριστίες μου θα ήθελα να εκφράσω προς την Δήμητρα Κανελλοπούλου, την Κατερίνα Κοφινά και την Μαριάννα Λιόλιου για τη βοήθεια που μου προσέφεραν στα πρώτα μου βήματα καθώς και για την φιλία τους. Ευχαριστώ, επίσης, τους συναδέλφους του εργαστηρίου Κατερίνα Βαβουράκη και Στάθη Νταφαλιά για την συνεργασία, καθώς και τον Γιάννη Μπούντα για την συμπαράστασή του και την φιλία του. Επιπλέον, ένα ευχαριστώ σε όλους τους φοιτητές που εκπόνησαν τις διπλωματικές τους εργασίες σε επιμέρους θέματα της διατριβής. Θα ήθελα, ακόμη, να εκφράσω τις ευχαριστίες μου προς το Ερευνητικό Ινστιτούτο Χημικής Μηχανικής και Χημικών Διεργασιών Υψηλής Θερμοκρασίας (ΕΙΧΗΜΥΘ/ΙΤΕ) για την υποτροφία που μου παρείχε όλα αυτά τα χρόνια καθώς και την δυνατότητα να χρησιμοποιήσω τον άρτιο εξοπλισμό του. Επιπλέον, ευχαριστώ την Γενική Γραμματεία Έρευνας και Τεχνολογίας (Γ.Γ.Ε.Τ.) για την μερική οικονομική υποστήριξη του έργου (ΕΠΑΝ). Τέλος, ένα μεγάλο ευχαριστώ στην οικογένειά μου για την αγάπη, την αμέριστη συμπαράσταση, τη φροντίδα και την στήριξη που μου προσέφερε σε όλη την διάρκεια των σπουδών μου. Σταματία Ροκίδη Πάτρα, Οκτώβριος 2011 ii
9 iii
10 ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ ΠΕΡΙΕΧΟΜΕΝΑ ΠΕΡΙΛΗΨΗ ΑBSTRACT i iv x xvi ΚΕΦΑΛΑΙΟ 1. ΕΙΣΑΓΩΓΗ Βιοϋλικά Βιολογική Ασβεστοποίηση Ασβεστοποίηση σε βαλβίδες καρδιάς Η καρδιά Οι βαλβίδες της καρδιάς Περί Αορτικής Βαλβίδας Προσθετικές Βαλβίδες Καρδιάς Στόχοι Διδακτορικής Διατριβής 13 Βιβλιογραφία Κεφαλαίου 1 15 ΚΕΦΑΛΑΙΟ 2. ΘEΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ Κρυστάλλωση Διαλυτότητα Διάγραμμα Διαλυτότητας Γινόμενο Διαλυτότητας Ενεργότητα και Συντελεστές Ενεργότητας Υπερκορεσμός Επίτευξη Υπερκορεσμού Πυρηνογένεση Ομογενής Πυρηνογένεση Ετερογενής Πυρηνογένεση Δευτερογενής Πυρηνογένεση Επιταξία Κρυσταλλική Ανάπτυξη Θεωρίες Επιφανειακής Ενέργειας Θεωρίες Προσρόφησης Στρώματος 51 iv
11 2.4.3 Θεωρίες Διάχυσης Καθορισμός Μηχανισμού Ελέγχου Κρυσταλλικής Ανάπτυξης Επίδραση Θερμοκρασίας Επίδραση Παρουσίας Ξένων Ιόντων ή Ενώσεων (Επιμολύνσεις) Δευτερογενείς Διεργασίες Διάλυση Μηχανισμοί διάλυσης κρυσταλλικών αλάτων 69 Βιβλιογραφία Κεφαλαίου 2 71 ΚΕΦΑΛΑΙΟ 3. ΤΟ ΣΥΣΤΗΜΑ ΤΟΥ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ Εισαγωγή Υδροξυαπατίτης (ΗΑΡ), Ca 5 (PO 4 ) 3 OH Φωσφορικό οκτασβέστιο (ΟCP), Ca 8 H 2 (PO 4 ) 6 5H 2 O Διένυδρο φωσφορικό διασβέστιο (DCPD), CaHPO 4 2H 2 O 81 Βιβλιογραφία Κεφαλαίου 3 82 ΚΕΦΑΛΑΙΟ 4. ΦΥΣΙΚΟΧΗΜΙΚΟΣ ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΑΣΒΕΣΤΟΥΧΩΝ ΕΝΑΠΟΘΕΣΕΩΝ ΑΠΟ ΒΑΛΒΙΔΕΣ ΚΑΡΔΙΑΣ 84 Βιβλιογραφία Κεφαλαίου 4 95 ΚΕΦΑΛΑΙΟ 5. ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΒΙΟΛΟΓΙΚΩΝ ΙΣΤΩΝ IN VITRO Εισαγωγή Μεθοδολογία Πειραματικό μέρος Αντιδραστήρια Κατεργασία ιστών Πειραματική διάταξη και διαδικασία Αποτελέσματα και συζήτηση 110 Βιβλιογραφία Κεφαλαίου ΚΕΦΑΛΑΙΟ 6. ΜΕΤΡΗΣΕΙΣ ΕΠΙΦΑΝΕΙΑΚΟΥ ΦΟΡΤΙΟΥ ΒΙΟΛΟΓΙΚΩΝ ΙΣΤΩΝ ΜΕ ΤΗ ΜΕΘΟΔΟ ΤΟΥ ΔΥΝΑΜΙΚΟΥ ΡΟΗΣ (STREAMING POTENTIAL) Εισαγωγή Θεωρητικό μέρος 133 v
12 6.2.1 Ηλεκτρική διπλοστιβάδα Ρευματικό δυναμικό Πειραματικό μέρος Αντιδραστήρια και υποστρώματα Πειραματική Διάταξη και Διαδικασία Αποτελέσματα και συζήτηση 142 Βιβλιογραφία Κεφαλαίου ΚΕΦΑΛΑΙΟ 7. MEΛETH ΤΗΣ ΚΡΥΣΤΑΛΛΙΚΗΣ ΑΝΑΠΤΥΞΗΣ ΑΛΑΤΩΝ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ ΣΕ ΑΝΟΡΓΑΝΑ ΥΠΟΣΤΡΩΜΑΤΑ ΓΙΑ ΤΗΝ ΑΝΑΠΤΥΞΗ ΒΙΟΫΛΙΚΩΝ Κρυστάλλωση υδροξυαπατίτη σε βιοτσιμέντα φωσφορικού ασβεστίου Εισαγωγή Πειραματικό μέρος Αντιδραστήρια Παρασκευή και χαρακτηρισμός βιοτσιμέντων φωσφορικού ασβεστίου Σύνθεση & χαρακτηρισμός συνθετικών κρυστάλλων ΗΑΡ Πειραματική διάταξη και διαδικασία Αποτελέσματα και συζήτηση Κρυστάλλωση φωσφορικού οκτασβεστίου (OCP) σε βιοτσιμέντα ανθρακικού φωσφορικού ασβεστίου (CaCO 3 -CaP) Εισαγωγή Πειραματικό μέρος Αντιδραστήρια Παρασκευή και χαρακτηρισμός βιοτσιμέντων ανθρακικού-φωσφορικού ασβεστίου Σύνθεση και χαρακτηρισμός συνθετικών κρυστάλλων OCP Πειραματική διάταξη και διαδικασία Αποτελέσματα και συζήτηση Ετερογενής σχηματισμός φωσφορικού οκτασβεστίου (OCP) σε υποστρώματα ανθρακικού ασβεστίου (CaCO 3 ) Εισαγωγή To σύστημα του ανθρακικού ασβεστίου 205 vi
13 7.3.2 Πειραματικό μέρος Αντιδραστήρια Παρασκευή και χαρακτηρισμός συνθετικών κρυστάλλων ανθρακικού ασβεστίου CaCO Πειραματική διάταξη και διαδικασία Αποτελέσματα και συζήτηση Κρυσταλλική ανάπτυξη αλάτων φωσφορικού ασβεστίου παρουσία ιόντων στροντίου (Sr 2+ ) Εισαγωγή Πειραματικό μέρος Αντιδραστήρια Πειραματική διάταξη και διαδικασία Αποτελέσματα και συζήτηση 222 Βιβλιογραφία Κεφαλαίου ΚΕΦΑΛΑΙΟ 8. ΜΕΛΕΤΗ ΤΗΣ ΚΙΝΗΤΙΚΗΣ ΤΗΣ ΔΙΑΛΥΣΗΣ ΑΣΒΕΣΤΟΥΧΩΝ ΕΝΑΠΟΘΕΣΕΩΝ ΑΠΟ ΦΥΣΙΚΕΣ ΒΑΛΒΙΔΕΣ ΚΑΡΔΙΑΣ Εισαγωγή Πειραματική διάταξη και διαδικασία Αποτελέσματα και συζήτηση 253 Βιβλιογραφία Κεφαλαίου ΚΕΦΑΛΑΙΟ 9. ΓΕΝΙΚΑ ΣΥΜΠΕΡΑΣΜΑΤΑ - ΜΕΛΛΟΝΤΙΚΕΣ ΠΡΟΕΚΤΑΣΕΙΣ 9.1 Γενικά συμπεράσματα Μελλοντικές προεκτάσεις 266 ΠΑΡΑΡΤΗΜΑ Ι. ΧΗΜΙΚΕΣ ΙΣΟΡΡΟΠΙΕΣ ΚΑΙ ΣΤΑΘΕΡΕΣ ΙΣΟΡΡΟΠΙΑΣ ΣΕ ΥΠΕΡΚΟΡΑ ΔΙΑΛΥΜΑΤΑ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ 269 ΠΑΡΑΡΤΗΜΑ ΙΙ. ΑΝΑΛΥΤΙΚΕΣ ΤΕΧΝΙΚΕΣ 277 ΙΙ.1 Ποτενσιομετρία 278 ΙΙ.1.1 Βασικές Αρχές 278 ΙΙ.1.2 Ηλεκτρόδιο Υάλου και Μέτρηση ph 280 ΙΙ.2 Φασματομετρία Μοριακής Απορρόφησης Υπεριώδους/Ορατού (UV/VIS) 282 vii
14 ΙΙ.2.1 Αρχή Μεθόδου 282 ΙΙ.2.2 Οργανολογία 284 ΙΙ.2.3 Μέτρηση Συγκέντρωσης Φωσφορικών Ιόντων 286 ΙΙ.3 Φασματοσκοπία Ατομικής Απορρόφησης (AAS) 287 ΙΙ.3.1 Αρχή Τεχνικής 287 ΙΙ.3.2 Οργανολογία 288 ΙΙ.3.3 Μέτρηση Ασβεστίου, Μαγνησίου και Στροντίου σε διαλύματα 291 ΙΙ.4 Περίθλαση Ακτίνων Χ (XRD) 292 ΙΙ.4.1 Αρχή Μεθόδου 292 ΙΙ.4.2 Οργανολογία 294 ΙΙ.4.3 Ταυτοποίηση Κρυσταλλικών Στερεών 297 ΙΙ.5 Φασματοσκοπία απορρόφησης υπέρυθρης ακτινοβολίας (FTIR) 297 ΙΙ.5.1 Γενική Αρχή 297 ΙΙ.5.2 Οργανολογία 299 ΙΙ.6 Ηλεκτρονική Μικροσκοπία Σάρωσης (SEM) 301 ΙΙ.6.1 Αλληλεπιδράσεις Ηλεκτρονίων - Στερεού Δείγματος 301 ΙΙ.6.2 Οργανολογία 304 ΙΙ.6.3 Λειτουργικές Συνθήκες 307 ΙΙ.7 Θερμοσταθμική Ανάλυση (TGA) 308 ΙΙ.7.1 Γενικές Αρχές 308 ΙΙ.7.2 Οργανολογία 309 ΙΙ.8 Μέτρηση Ειδικής Επιφάνειας (BET) 311 ΙΙ.8.1 Ρόφηση Αερίου σε Στερεό Ισόθερμοι Ρόφησης 311 ΙΙ.8.2 Οργανολογία 314 ΙΙ.8.3 Υπολογισμός Ειδικής Επιφάνειας 315 Βιβλιογραφία Παραρτημάτων 317 ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ 320 viii
15 ix
16 ΠΕΡΙΛΗΨΗ Κατά την επαφή επιφανειών, όπως οι βαλβίδες καρδιάς ή και άλλοι ιστοί, με βιολογικά υγρά, υπό προϋποθέσεις, εναποτίθενται άλατα φωσφορικού ασβεστίου, λόγω του υφιστάμενου υπερκορεσμού με αποτέλεσμα τη μείωση της λειτουργικότητάς τους. Οι αυξημένες περιπτώσεις ασβεστοποίησης αορτικών αλλά και βιοπροσθετικών βαλβίδων καρδιάς, έχει καταστήσει επιτακτική ανάγκη τη μελέτη και τη κατανόηση του μηχανισμού του σχηματισμού των εναποθέσεων. Στην παρούσα διατριβή, έγινε φυσικοχημικός χαρακτηρισμός παθολογικών εναποθέσεων που απομονώθηκαν από ανθρώπινες φυσικές και βιοπροσθετικές βαλβίδες καρδιάς. Ο χαρακτηρισμός έδειξε ότι οι εναποθέσεις αποτελούνται από κρυσταλλικές φάσεις φωσφορικού ασβεστίου. Έγινε ταυτοποίηση της κρυσταλλικής φάσης που είχε εναποτεθεί στις φυσικές και βιοπροσθετικές βαλβίδες ασθενών με χρήση αναλυτικών μεθόδων (XRD, FT-IR, SEM) και συγκρίθηκαν τα αποτελέσματα. Η μορφολογική εξέταση έδειξε κυρίως την παρουσία απατιτικών (υδροξυαπατίτης με υποκαταστάσεις ανθρακικών ιόντων και ιόντων νατρίου) πρισματικών μικροκρυστάλλων. Επίσης, ταυτοποιήθηκε η παρουσία του θερμοδυναμικά ασταθέστερου φωσφορικού οκτασβεστίου (OCP). Η χημική σύσταση των εναποθέσεων στις ασβεστοποιημένες βαλβίδες ασθενών προσδιορίστηκε διαλύοντας συγκεκριμένη ποσότητα στερεού σε διάλυμα HCl 0.1Ν. Έγινε ανάλυση ιόντων ασβεστίου, νατρίου, μαγνησίου με ατομική απορρόφηση και φωσφορικών ιόντων φασματοφωτομετρικά. Οι λόγοι των γραμμομοριακών συγκεντρώσεων Ca/P των στερεών υπολογίστηκαν από τη χημική ανάλυση. Οι γραμμομοριακοί λόγοι των βιοπροσθετικών βαλβίδων βρέθηκαν Ca/P~1.55 ± 0.25, ενώ οι γραμμομοριακοί λόγοι των φυσικών βαλβίδων βρέθηκαν Ca/P ~ 1.80 ± Στα πλαίσια της εκπόνησης της παρούσας διατριβής, μελετήθηκε η κινητική της ασβεστοποίησης in vitro σε χοίρειες αορτικές βαλβίδες καρδιάς (γλωχίνες & τοιχώματα) και σε βόειο περικάρδιο. Έγινε μελέτη του σχηματισμού των εναποθέσεων φωσφορικού ασβεστίου σε υπέρκορα διαλύματά του. Όλα τα πειράματα στην παρούσα εργασία έγιναν σε θερμοκρασία 37 ο C, ph 7.4 ± 0.1 και ιοντική ισχύ 0.15 Μ ρυθμισμένη με ΝaCl. Για την μέτρηση του ρυθμού κρυσταλλικής ανάπτυξης και άλλων παραμέτρων όπως ο χρόνος επαγωγής, η μορφολογία και η στοιχειομετρική σύσταση των σχηματιζόμενων κρυστάλλων χρησιμοποιήθηκε η μέθοδος του σταθερού υπερκορεσμού (σταθερή σύσταση υπέρκορων διαλυμάτων). O ρυθμός κρυστάλλωσης του φωσφορικού x
17 οκτασβεστίου (Ca 4 H(PO 4 ) 3 2.5H 2 O, OCP) στις γλωχίνες βρέθηκε ότι ήταν μεγαλύτερος σε σύγκριση με τον αντίστοιχο ρυθμό σχηματισμού του ιδίου άλατος στα αορτικά τοιχώματα και στο βόειο περικάρδιο. Η πρώτης τάξεως εξάρτηση του ρυθμού κρυστάλλωσης από τον σχετικό υπερκορεσμό έδειξε ότι το καθορίζον την ταχύτητα στάδιο είναι η επιφανειακή διάχυση. Η κρυσταλλική φάση που σχηματίσθηκε με ετερογενή πυρηνογένεση στους ιστούς ταυτοποιήθηκε με τη βοήθεια αναλυτικών μεθόδων όπως η περίθλαση ακτίνων Χ (XRD) και η ηλεκτρονική μικροσκοπία σάρωσης (SEM). Η μορφολογική εξέταση των εναποθέσεων στους ιστούς έδειξε τον σχηματισμό πλακoειδών και φυλλόμορφων κρυστάλλων φωσφορικού οκτασβεστίου (OCP) καθώς και πρισματικών μικροκρυστάλλων του θερμοδυναμικά σταθερότερου υδροξυαπατίτη (Ca 5 (PO 4 ) 3 OH, HAP), ο σχηματισμός των οποίων αποδόθηκε στην υδρόλυση του OCP. Η σχέση υποστρώματος (ιστών) και της κρυσταλλικής φάσης η οποία κρυσταλλώθηκε στην επιφάνειά τους, διερευνήθηκε και με τη μελέτη του ηλεκτροστατικού δυναμικού των επιφανειών. Οι αντίστοιχες μετρήσεις έγιναν με τη μέθοδο του δυναμικού ροής (streaming potential) σε ειδική κυψελλίδα η οποία κατασκευάσθηκε για τον σκοπό αυτό. Στις μετρήσεις που έγιναν, οι ιστοί, τόσο άνευ αλλά και με εναποθέσεις φωσφορικού ασβεστίου, αποτέλεσαν την σταθερή φάση ενώ κινουμένη φάση ήταν ηλεκτρολυτικό διάλυμα ΚΝΟ 3 ή NaCl. Πραγματοποιήθηκαν για πρώτη φορά σε συστήματα αυτού του είδους, μετρήσεις δυναμικού ροής και υπολογίσθηκαν οι τιμές των αντιστοίχων επιφανειακών δυναμικών (δυναμικά ζ) σε ιστούς, προ και μετά την ασβεστοποίησή τους με άλατα του φωσφορικού ασβεστίου. Η αύξηση της ιονικής ισχύος είχε ως αποτέλεσμα τη μείωση του δυναμικού επιφάνειας ιστών που εξετάστηκαν. Το δυναμικό ροής ήταν ανάλογο της εφαρμοζόμενης πίεσης και από τα διαγράμματα δυναμικού ροής-πίεσης συμπεραίνεται ότι η επιφάνεια των ιστών (περικαρδίου και γλωχίνων) έχει αρνητικό επιφανειακό φορτίο ενώ ασβεστοποίηση των ιστών αυτών έδωσε αρνητικότερες τιμές του ζ δυναμικού τους. Με δεδομένο ότι στην τιμή του ph ισορροπίας που έγιναν οι μετρήσεις, τόσο η επιφάνεια του υποστρώματος όσο και η κρυσταλλική φάση έχουν μικρό αρνητικό φορτίο και δεν φαίνεται οι ηλεκτροστατικές δυνάμεις κρυστάλλων-υποστρωμάτων που εξετάσθηκαν να παίζουν σημαντικό ρόλο. Οι μετρήσεις που έγιναν σε υψηλές τιμές της ιοντικής ισχύος, έδειξαν αύξηση του αρνητικού επιφανειακού φορτίου για το σύνθετο υλικό υπόστρωμα- ΗΑΡ. Η συνάφεια υποστρώματος-κρυσταλλικής φάσης είναι πιθανώς δομικής φύσης. Οι συνεχώς αυξανόμενες απαιτήσεις για την παρασκευή βιοϋλικών έχουν ως αποτέλεσμα το συνεχώς αυξανόμενο ενδιαφέρον για τη σύνθεση και τη μελέτη xi
18 βιοτσιμέντων, στα συστατικά των οποίων περιλαμβάνονται άλατα φωσφορικού ασβεστίου ή και ανθρακικού ασβεστίου. Tα βιοτσιμέντα έχουν πολλαπλές βιο-ιατρικές εφαρμογές λόγω της δυνατότητας απορρόφησης ή και τροποποίησης με την ενσωμάτωσή τους στα οστά. Μεταξύ των κρυσταλλικών φάσεων του φωσφορικού ασβεστίου, η θερμοδυναμικά σταθερότερη είναι ο HAP, ο οποίος είναι βασικό ανόργανο συστατικό των σκληρών ιστών των ανώτερων θηλαστικών και αποτελεί ένα πολύ καλό βιοσυμβατό υλικό. Παρασκευάστηκαν απατιτικά τσιμέντα φωσφορικού ασβεστίου με ανάμειξη α-φωσφορικού τριασβεστίου (α-ca 3 (PO 4 ) 2, a-tcp) με υδατικό διάλυμα Na 2 HPO 4 και μελετήθηκε η κινητική της κρυστάλλωσης ΗΑP στα απατιτικά τσιμέντα σε υπέρκορα διαλύματα φωσφορικού ασβεστίου, σε συνθήκες σταθερού υπερκορεσμού. Έγινε σειρά πειραμάτων στα οποία μετρήθηκε πρώτα η κινητική της κρυστάλλωσης συνθετικών καλά χαρακτηρισμένων κρυσταλλιτών HAP. Η σειρά αυτή των πειραμάτων ήταν το σύστημα αναφοράς. Πρόσθετες σειρές πειραμάτων έγιναν σε υπέρκορα διαλύματα με σύσταση τροποποιημένων προσομοιωμένων βιολογικών ρευστών (msbf). Ο ρυθμός κρυστάλλωσης HAP σε φύτρα ΗΑΡ σε ηλεκτρολυτικό διάλυμα, ήταν μεγαλύτερος σε σύγκριση με τον αντίστοιχο ρυθμό σε προσομοιωμένο βιολογικό ρευστό (SBF), της αυτής ιοντικής ισχύος και υπερκορεσμού. Η εξάρτηση του ρυθμού κρυστάλλωσης από τον σχετικό υπερκορεσμό, βρέθηκε ότι ήταν πρώτης τάξεως, οδηγώντας και σε αυτή την περίπτωση στο συμπέρασμα, ότι η κρυστάλλωση και στις δύο περιπτώσεις ηλεκτρολυτικών διαλυμάτων γίνεται με μηχανισμό επιφανειακής διάχυσης. Κατά την σπορά των υπέρκορων διαλυμάτων με κρυσταλλίτες των βιοτσιμέντων το συμπέρασμα ως προς τον μηχανισμό κρυσταλλικής ανάπτυξης ήταν το ίδιο. Ο φυσικοχημικός χαρακτηρισμός τόσο των τσιμέντων όσο και της εναποτεθείσας κρυσταλλικής φάσης έγινε με αναλυτικές μεθόδους χαρακτηρισμού στερεών (XRD, FT-IR, SEM). Τα αποτελέσματα έδειξαν ότι τα τσιμέντα αποτελούνταν κατά κύριο λόγο από απατίτη με ποικίλη μορφολογία. Βρέθηκαν απατιτικοί κρύσταλλοι της τάξης μερικών δεκάδων nm, μεγάλοι πρισματικοί κρύσταλλοι ( nm) καθώς και φυλλόμορφες πλάκες 1-2 μm. Παράλληλα, διερευνήθηκε η επίδραση και άλλων ανόργανων υποστρωμάτων που χρησιμοποιούνται ως βιοϋλικά, όπως είναι τα βιοτσιμέντα τα οποία παρασκευάζονται από μιγμάτα ανθρακικού και φωσφορικού ασβεστίου. Έγινε μελέτη της κινητικής της κρυστάλλωσης φωσφορικού οκτασβεστίου (ΟCP) με τη μέθοδο σταθερού υπερκορεσμού στους 37 o C σε ph 7.40 ± 0.1 και σε ιοντική ισχύ 0.15 Μ NaCl. Για την εκκίνηση της κρυσταλλικής ανάπτυξης σε σταθερά υπέρκορα διαλύματα xii
19 φωσφορικού ασβεστίου χρησιμοποιήθηκαν το βιοτσιμέντο τύπου Α (μίγμα βατερίτη (CaCO 3 ) και διένυδρου φωσφορικού ασβεστίου (CaHPO 4 2H 2 O, DCPD)), και το βιοτσιμέντο τύπου Β (μίγμα βατερίτη (CaCO 3 ), διένυδρου φωσφορικού ασβεστίου (CaHPO 4 2H 2 O, DCPD) και 20% ανθρακικού στροντίου (SrCO 3 ). Επιπλέον, για τη μελέτη της κινητικής της κρυστάλλωσης χρησιμοποιήθηκαν συνθετικοί κρύσταλλοι υδροξυαπατίτη (HAP) και φωσφορικού οκτασβεστίου (OCP), ως υλικά αναφοράς. Η παρουσία ανθρακικών ιόντων έδειξε πως επηρεάζει το ρυθμό κρυστάλλωσης και από την εξάρτηση του ρυθμού κρυστάλλωσης από τον σχετικό υπερκορεσμό συμπεραίνεται ότι η κρυστάλλωση γίνεται με μηχανισμό επιφανειακής διάχυσης. Η μορφολογική εξέταση στις περιπτώσεις κρυστάλλωσης OCP σε φύτρα κρυστάλλων OCP και βιοτσιμέντων (μίγμα CaCO 3 και DCPD) έδειξε φυλλόμορφους σχηματισμούς φωσφορικού οκτασβεστίου (OCP), ενώ πλακοειδείς κρύσταλλοι φωσφορικού οκτασβεστίου (OCP) αναπτύχθηκαν σε φύτρα ΗΑΡ. Η συνάφεια μεταξύ ανθρακικών και φωσφορικών αλάτων του ασβεστίου είναι σημαντική για την κατανόηση της συμπεριφοράς και των ιδιοτήτων νέων βιοϋλικών που βασίζονται σ αυτά τα υλικά. Έτσι, έγινε διερεύνηση της δυνατότητα χρήσεως διαφόρων πολυμορφικών φάσεων ανθρακικού ασβεστίου (CaCO 3 ) ως βάσεων για την παρασκευή νέων βιοϋλικών. Μελετήθηκε ο ετερογενής σχηματισμός του φωσφορικού οκτασβεστίου (OCP) σε υποστρώματα ανθρακικού ασβεστίου, σε συνθήκες σταθερού υπερκορεσμού στους 37 o C σε ph 7.40 ± 0.1 και σε ιοντική ισχύ 0.15 Μ NaCl, χρησιμοποιώντας ως φύτρα σποράς κρυστάλλους ασβεστίτη καθώς και μίγμα κρυστάλλων αραγωνίτη-ασβεστίτη. H κρυστάλλωση του φωσφορικού οκτασβεστίου έλαβε χώρα μετά την πάροδο χρόνου επαγωγής, τ, στα δυο υποστρώματα CaCO 3 που μελετήθηκαν και οι αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης ανά μονάδα επιφάνειας βρέθηκαν ότι ήσαν ανεξάρτητοι της ποσότητας των κρυσταλλικών φύτρων, γεγονός που υποδηλώνει την επιλεκτική πυρηνογένεση του σχηματιζόμενου στερεού (ΟCP) στα υποστρώματα που εξετάσθηκαν (CaCO 3 ). Η μορφολογική εξέταση της σχηματιζόμενης φάσης στα δυο υποστρώματα CaCO 3 επιβεβαίωσε τον αποκλειστικό σχηματισμό χαρακτηριστικών φυλλόμορφων κρυσταλλιτών OCP, ενώ ο σταθερότερος θερμοδυναμικά υδροξυαπατίτης (HAP) δε σχηματίστηκε ούτε κατευθείαν, ούτε και μέσω υδρόλυσης του θερμοδυναμικά ασταθέστερου OCP, ο οποίος έδειξε να σταθεροποιείται αναπτυσσόμενος ετερογενώς σε ανθρακικά άλατα του ασβεστίου. Είναι γνωστό, ότι η παρουσία ξένων ουσιών ή ιόντων στα υπέρκορα διαλύματα παίζει σημαντικό ρόλο τόσο στην κινητική σχηματισμού του φωσφορικού ασβεστίου xiii
20 όσο και στα χαρακτηριστικά του κρυσταλλικού στερεού το οποίο αναπτύσσεται. Ιδιαίτερο ενδιαφέρον παρουσιάζει ο ρόλος του στροντίου στην κινητική της βιολογικής ασβεστοποίησης, αφού όπως αναφέρεται στη βιβλιογραφία ενισχύει τη βιοενεργότητα και τη βιοσυμβατότητα των βιοϋλικών και μπορεί να βοηθήσει στην αντιμετώπιση της οστεοπόρωσης (π.χ. ρανελικό στρόντιο). Έγινε διερεύνηση της επίδρασης ιόντων στροντίου (Sr 2+ ) στην κινητική κρυσταλλικής ανάπτυξης αλάτων φωσφορικού ασβεστίου σε υποστρώματα συνθετικών κρυστάλλων φωσφορικού οκτασβεστίου (OCP) και υδροξυαπατίτη (HAP) σε υπέρκορα διαλύματα φωσφορικού ασβεστίου. Η παρουσία των ιόντων στροντίου στα υπέρκορα διαλύματα φωσφορικού ασβεστίου έδειξε ότι ενσωματώθηκαν στο κρυσταλλικό πλέγμα τόσο του OCP όσο και του HAP, ενώ κινητικά επιβράδυνε τους ρυθμούς κρυστάλλωσης και των δύο αλάτων. Μεγαλύτερη μείωση του ρυθμού κρυσταλλικής ανάπτυξης μετρήθηκε στην περίπτωση του HAP. Επίσης, παρατηρήθηκαν αλλαγές στη μορφολογία των κρυστάλλων ενώ η παρουσία των ιόντων Sr 2+ είχε ως αποτέλεσμα την επιβράδυνση της υδρολυτικής μετατροπής του θερμοδυναμικά ασταθέστερου OCP προς τον θερμοδυναμικά σταθερό HAP. Τέλος, μελετήθηκε η κινητική της διάλυσης των εναποθέσεων φωσφορικού ασβεστίου που απομονώθηκαν από ασβεστοποιημένες φυσικές βαλβίδες ασθενών, αλλά και συνθετικών καλά χαρακτηρισμένων κρυσταλλιτών HAP ως υλικού αναφοράς, σε ακόρεστα διαλύματα. Τα πειράματα έγιναν στους 37 o C, ιοντική ισχύ 0.15 Μ NaCl, σε ph 7.4 ± 0.1 και σε συνθήκες σταθερής ακορεστότητας. Η εξάρτηση του ρυθμού διάλυσης από την σχετική ακορεστότητα των διαλυμάτων εργασίας, η οποία βρέθηκε ότι ήταν δευτέρας τάξεως, έδειξε ότι η διάλυση και στα δύο υποστρώματα ελέγχεται από επιφανειακή διάχυση των δομικών μονάδων. Η διάλυση των παθολογικών εναποθέσεων σε φυσικές βαλβίδες καρδιάς σε συνθήκες σταθερής ακορεστότητας έδωσε σταθερές ταχύτητας σημαντικά μεγαλύτερες σε σύγκριση με τις αντίστοιχες τιμές που ελήφθησαν για συνθετικούς κρυστάλλους ΗΑΡ. Από τη μορφολογική εξέταση τόσο των κρυστάλλων των ασβεστούχων εναποθέσεων όσο και του ΗAP μετά τη διάλυση παρατηρήθηκαν διαφορές μόνο ως προς το μέγεθος των κρυσταλλιτών. Μετά την διάλυση, οι πρισματικοί κρυσταλλίτες του ΗΑΡ είχαν μικρότερο μέγεθος τόσο ως προς το μήκος τους όσο και ως προς το πάχος. xiv
21 xv
22 ABSTRACT The formation of calcium phosphate deposits upon contact of biological fluids which are supersaturated with respect to a number of calcium phosphate phases, with tissues (e.g. heart valves, artery walls etc) is detrimental to the function of vital organs or of bioprosthetic materials replacing for damaged tissues. Understanding of the mechanisms underlying the formation of the calcium phosphate deposits, adhering tenaciously to functional tissues is of prime importance not only for the amelioration of health but also for the development of efficient and functional biomaterials. Ιn the present work pathological formations of native and bioprosthetic heart valves removed from patients were examined and showed that were consisted of calcium phosphate phases. The calcific deposits formed on native and bioprosthetic heart valves were characterized using solid characterization analytical methods (XRD, FT-IR, SEM) and the results were compared. The morphological examination showed mainly the presence of apatitic (HAP substituted by carbonate and sodium ions) nano-crystals. Τhe presence of the thermodynamically unstable OCP was, also, identified. The chemical composition of calcific deposits was determined by dissolving an amount of solid in solution of HCl 0.1N. The molar Ca/P ratios in the solids were calculated and found to be Ca/P ~ 1.55 ± 0.25 for bioprosthetic heart valves whereas for native heart valves Ca/P ~ 1.80 ± This difference may be attributed to the different maturation of the solids in contact with the respective biological fluids. It seems that the longer the exposure of the solids with solutions containing ions which may replace for calcium in the crystal lattice, the higher the respective Ca/P molar ratio. Another purpose of the present work was the investigation of the heterogeneous nucleation of calcium phosphates on heart valve tissues and on synthetic biomaterials. The mechanistic investigation was done through the correlation of the measured rates of crystal growth as a function of the solution supersaturation and in relation with the substrates on which nucleation took place. The kinetics of calcification of porcine aortic valves (leaflets & walls) and bovine pericardium was investigated in vitro. More specifically, the formation of calcium phosphate deposits was studied at 37 0 C, ph 7.4 ± 0.1 and ionic strength 0.15 M adjusted with NaCl, from supersaturated solutions. The solution composition was selected to simulate the respective conditions in plasma serum. These conditions were maintained throughout the experiments done in the present work. The kinetic was xvi
23 measured with the method of constant supersaturation. The rate of crystal growth of OCP on heart valve leaflets was higher in comparison with the respective rate on aortic walls and on bovine pericardium. The dependence of the rate of OCP crystal growth on the relative supersaturation was first order, suggesting a surface diffusion controlled process. The crystalline phase formed was characterized by physicοchemical solid characterization methods (XRD, SEM). The mineralogical analysis confirmed the exclusive formation of the transient OCP phase, which was stabilized kinetically because of the maintenance of the solution supersaturation. The morphological examination showed the formation of plate like OCP crystallites (Ca 4 H(PO 4 ) 3 2.5H 2 O, OCP), which hydrolyzed with time yielding prismatic nano-crystals of the thermodynamically more stable hydroxyapatite (Ca 5 (PO 4 ) 3 OH, HAP). Moreover, the effect of the formation of deposits on the tissues investigated on their surface potential was investigated, through measurements the streaming potential of the surfaces with and without deposits. To our knowledge it is the first time this electrokinetic methodology was applied to investigate mineralized tissues. A home made apparatus was used after the appropriate modifications. A special cell was prepared in which the electrolyte solution was forced to flow over the immobile tissue surface. The surface potentials (zeta potential) of non calcified and calcified tissues were calculated from the electrokinetic measurements. The measurements were conducted over a wide range of concentrations of potassium nitrate (KNO 3 ) and sodium chloride (NaCl) electrolyte solutions. The increase in ionic strength resulted to the decrease in the zeta potential values of the examined tissues. The potential flow was proportional to the applied pressure and from the graph of potential flow as a function of the applied pressure it was concluded that the surfaces of tissues (pericardium and leaflets) were negatively charged. The presence of calcific deposits resulted to more negative values of zeta potential. The fast growing demand for the development of biomaterials has led to increased interest for the development and study of calcium phosphate and/or calcium carbonate biocements. Biocements have multiple bio-medical applications due to their resorbability and/or bioactivity and biocompatibility properties. Among calcium phosphates, the thermodynamically most stable HAP is the major component of hard tissues of higher mammals and an excellent biocompatible material. Apatitic cements of calcium phosphate were prepared by mixing a- tricalcium phosphate (α-ca 3 (PO 4 ) 2, a- TCP) with aqueous disodium hydrogen phosphate solution (Na 2 HPO 4 ). The kinetics of xvii
24 crystal growth of HAP from calcium phosphate supersaturated solutions on the apatitic cements was investigated at conditions of constant solution supersaturation. Synthetic HAP crystals were used as reference materials. In addition, experiments were carried out in supersaturated solutions of modified simulated body fluid (m-sbf). The crystal growth rate of HAP was found to be higher in the aqueous solutions than in the m-sbf solution. The kinetics measurements showed that in both cases the crystal growth of HAP was a surface diffusion controlled process. The physicochemical characterization of the cements and the crystal growth phase was examined by solid phase characterization methods (XRD, FT-IR, SEM). The morphological examination showed that the cements consisted mainly of apatite with variable morphology. Small apatitic nano-crystals, larger prismatic crystals ( nm) and leaf-like plates 1-2μm. The effect of another type of inorganic substrates, suggested for use as biomaterials was, also, investigated. These included biocements of mixtures of calcium phosphate and calcium carbonate. The investigation of the kinetics of crystal growth of OCP was carried out at conditions of constant solution supersaturation. The crystal growth was initiated by introduction of different types of inoculating solids. Specifically, biocement A refers to a mixture of vaterite (CaCO 3 ) and dicalcium dihydrogen phosphate dihydrate (CaHPO 4 2H 2 O) and biocement B to vaterite (CaCO 3 ), dicalcium dihydrogen phosphate (CaHPO 4 2H 2 O) and 20% of SrCO 3 mixture. Synthetic HAP and OCP crystals were used as reference materials. The presence of carbonate ions showed that they had a significant effect on the rate of crystal growth of OCP. From the growth rate dependence on the relative supersaturation, it was concluded that in all cases the mechanism was the same for all substrates and it was surface diffusion controlled. The morphological examination of the deposits on the OCP seed crystals and on biocements showed the formation of the leaf-like OCP crystallites, while plate-like OCP crystals were formed on the HAP seed crystals. The compatibility between minerals like calcium carbonate and calcium phosphate is an issue of key importance for understanding the behavior and properties of implants and for the design of new materials with desired properties. Thus, it was investigated the possibility of using different polymorphs of calcium carbonate (CaCO 3 ) as basis for the development of new biomaterials. The kinetics of heterogeneous nucleation of OCP on calcium carbonate substrates was studied at conditions of constant supersaturation. Stable calcium phosphate solutions, supersaturated with respect to OCP and HAP were inoculated with well characterized calcite seed crystals and mixed xviii
25 aragonite and calcite seed crystals. Past the suspension of the seed crystals in the supersaturated calcium phosphate solutions, OCP crystal growth started past induction time, τ, and the initial crystal growth rates per unit area were found to be independent on the amount of the seeds, suggesting that OCP nucleation occurs selectively on the inoculating solids of CaCO 3. The morphological examination of the precipitating phase on both CaCO 3 substrates confirmed the exclusive formation of typical leaf-like OCP crystals, while the thermodynamically stable (HAP) did not grow directly on the substrates neither through the hydrolysis of the unstable OCP. The role of strontium on the kinetics of biological calcification is of particular interest, since it is reported in literature that it enhances the bioactivity and biocompatibility of biomaterials and may have a potential use in the treatment of osteoporosis (e.g. strontium ranelate). The effect of the presence of strontium ions in supersaturated calcium phosphate solutions on the rates of crystal growth of OCP and HAP was investigated at constant solution supersaturation, taking care to account only for the dilution of the strontium in the supersaturated solutions. It was found that Sr 2+ ions entered the crystal lattice of both HAP and OCP probably substituting for calcium ions. The inhibitory effect of strontium on the crystallization rate of both calcium phosphates was evident, although in the case of OCP inhibition was exhibited a less extent in comparison with HAP. The presence of strontium during the crystal growth of OCP and HAP induced morphology changes and seemed that it retarded the transformation of the unstable OCP into the thermodynamically more stable HAP. Finally, the dissolution kinetics of apatitic deposits from pathological formations on native heart valves removed from patients was investigated in vitro at conditions of constant undersaturation. The dissolution of synthetic HAP was studied as a reference material. The dependence of the dissolution rates on the relative undersaturation of both substrates was second order suggested a surface diffusion controlled process. A marked difference was found however in the rates of dissolution of the two materials tested. The heart valve calcific deposits dissolved with rates 10 fold faster than the corresponding value of the synthetic HAP crystals. Crystallites of smaller size were observed from the morphological examination of both calcific deposits and HAP crystals after dissolution. xix
26
27 ΚΕΦΑΛΑΙΟ 1 ΕΙΣΑΓΩΓΗ 1
28 1.1 ΒΙΟΫΛΙΚΑ Η επιστήμη των βιοϋλικών μελετά υλικά φυσικής ή τεχνητής προέλευσης τα οποία μπορούν να χρησιμοποιηθούν σε ένα ζωντανό οργανισμό ως πρόσθετα υλικά ή ως εμφυτεύματα για αντικατάσταση ιστών στο ανθρώπινο σώμα. Για τον όρο βιοϋλικά δεν έχει δοθεί κάποιος επίσημος ορισμός. Ένας εκ των ορισμών που έτυχε ευρείας αποδοχής από επιστήμονες του αντίστοιχου τομέα έχει ως εξής: Βιοϋλικά είναι μη έμβια υλικά που χρησιμοποιούνται στην ιατρική και τα οποία τείνουν να αλληλεπιδράσουν με τα βιολογικά συστήματα [Williams, 1987]. Σύμφωνα με τον ορισμό που έδωσε το National Institutes of Health Consensus Development Conference, ως βιοϋλικό ορίζεται: Κάθε ουσία ή συνδυασμός υλικών, συνθετική ή φυσική, που μπορεί να χρησιμοποιηθεί είτε ενιαίο, είτε ως τμήμα ενός συστήματος το οποίο θεραπεύει, ενισχύει ή αντικαθιστά έναν ιστό, ένα όργανο ή μια λειτουργία του σώματος [Boretos and Eden, 1984]. Η μελέτη των βιοϋλικών εξελίσσεται τα τελευταία πενήντα χρόνια, όμως, η χρήση τους έχει τις ρίζες της σε αρχαίους ακόμα πολιτισμούς. Με το πέρασμα των αιώνων και με τη βελτίωση των σύνθετων υλικών και των ιατρικών μεθόδων, η χρήση των βιοϋλικών βρίσκει ολοένα και περισσότερες εφαρμογές. Τα βιοϋλικά χρησιμοποιούνται σε όλους τους τομείς της ιατρικής ως εμφυτεύματα, όπως βαλβίδες καρδιάς, μοσχεύματα αρτηριών, ενδοφθάλμιους φακούς, οδοντικά εμφυτεύματα, αντικαταστάτες συνδέσμων ισχύου, γονάτου και ώμου, ενθεμάτων αισθητικής χειρουργικής κ.ά. Επιπλέον, τα βιοϋλικά χρησιμοποιούνται και με τη μορφή ιατρικών συσκευών, όπως τεχνητές καρδιές, τεχνητά νεφρά, καθετήρες, συσκευές αιμοκάθαρσης κ.ά. [Ratner et al., 2004] Για να μπορέσει να χρησιμοποιηθεί ένα υλικό ως βιοϋλικό θα πρέπει να είναι ασφαλές μέσα στον οργανισμό και να μην προκαλεί την αντίδραση των περιβαλλόντων ιστών. Προκειμένου να μην υπάρξει αλληλεπίδραση ανάμεσα στο υλικό και στον ξενιστή, θα πρέπει το υλικό να είναι μη τοξικό και βιοσυμβατό, έτσι ώστε το βιοϋλικό να γίνει δεκτό από τον οργανισμό και να υπάρξει αρμονική συμβίωση μεταξύ αυτού και του ζώντος οργανισμού [Ratner et al., 2004]. 2
29 Τα βιοϋλικά κατατάσσονται σε τέσσερις κατηγορίες με βάση το υλικό που είναι κατασκευασμένα: (i) μεταλλικά (ανοξείδωτος χάλυβα, ο χρυσός, ή λευκόχρυσος και κράματα τιτανίου και κοβαλτίου-χρωμίου), (ii) κεραμικά (υδροξυαπατίτης, τσιμέντα φωσφορικού ασβεστίου, αλούμινα και βιοενεργά γυαλιά), (iii) πολυμερικά (πολυαιθυλένιο, πολυμεθακρυλικός μεθυλεστέρας, πολυβινυλοχλωρίδιο, σιλικόνη πολυουραιθάνη κ.ά) και (iv) σύνθετα (συνδυασμός τριών πρώτων κατηγοριών, ενίσχυση αυτών με ίνες κ.ά) [Park, 2000]. Βασικές εφαρμογές τους εντοπίζονται στους τομείς της Ορθοπεδικής, της Αγγειοχειρουργικής, της Καρδιολογίας, της Ουρολογίας, της Πλαστικής Χειρουργικής και της Οδοντιατρικής. Από τα κεραμικά βιοϋλικά, τα άλατα του φωσφορικού ασβεστίου, όπως ο υδροξυαπατίτης (Ca 5 (PO 4 ) 3 OH, HAP), όντας το κύριο ανόργανο συστατικό των οστών και των δοντιών [Weiner and Wagner, 1998], έχουν παρουσιάσει εξαιρετική βιοσυμβατότητα, έχοντας δείξει πως είναι αποδεκτά από τον οργανισμό, πως ενσωματώνονται καλά και επάγουν την οστεοσύνθεση [Rueger et al., 1998]. Ως εκ τούτου, έχουν σημαντικές εφαρμογές ως βιοϋλικά στην ορθοπεδική και στην οδοντιατρική, συγκεντρώνοντας αυξημένο ερευνητικό ενδιαφέρον ως προς τη δυνατότητα χρήσης τους ως χειρουργικών οστικών και οδοντικών εμφυτευμάτων [LeGeros, 1991 ; Hong et al., 1991]. Τα τσιμέντα φωσφορικού ασβεστίου προτάθηκαν για πρώτη φορά τη δεκαετία του 80 [LeGeros et al., 1982 ; Brown and Chow, 1983]. Τρεις δεκαετίες αργότερα, το ενδιαφέρον για αυτά τα βιοϋλικά παραμένει ακόμα αυξημένο. Τα τσιμέντα φωσφορικού ασβεστίου παρασκευάζονται με ανάμιξη μιας στερεάς φάσης φωσφορικού ασβεστίου ή και περισσοτέρων με υδατικό διάλυμα. Από την ανάμιξη προκύπτει μια πάστα η οποία σκληραίνει σταδιακά. Το πρώτο εμπορικό προϊόν τσιμέντου χρησιμοποιήθηκε πριν 16 χρόνια για τη θεραπεία κατάγματος [Constantz et al., 1995]. Τα πλεονεκτήματά τους είναι η υψηλή βιοσυμβατότητα, η μη τοξικότητα, η βιοενεργότητα (σχηματίζονται χημικοί δεσμοί με τον περιβάλλοντα ιστό που τα σταθεροποιούν) [Dorozhkin, 2010] και η δημιουργία ευνοϊκών συνθηκών για οστεοσύνθεση [Driessens et al., 1998 ; Frayssinet et al., 1998 ; Combes et al., 2006]. Η δυνατότητά τους για μορφοποίηση, τα καθιστά ικανά να ενσωματώνονται καλύτερα στη γεωμετρία του οστικού ελλείματος και να πληρούν τις ατέλειες στα οστά αφού δεν εμφυτεύονται ως συμπαγή στερεά. Ωστόσο, μειονεκτήματα αποτελούν τα χαμηλά ποσοστά απορρόφησής τους από τους ιστούς, το γεγονός ότι δεν αποδομούνται με τον ίδιο ρυθμό ανακατασκευής του ιστού και η 3
30 σχετικά μικρή μηχανική αντοχή τους [Dorozhkin, 2010 ; Braye et al., 1996 ; Ikenaga et al., 1998]. 1.2 ΒΙΟΛΟΓΙΚΗ ΑΣΒΕΣΤΟΠΟΙΗΣΗ Βιολογική ασβεστοποίηση ή αλλιώς αποτιτάνωση (αρχαία λέξη τίτανος = ασβεστόπετρα) είναι η εναπόθεση αλάτων φωσφορικού ασβεστίου σε σκληρούς ιστούς όπως είναι τα οστά (οστεοποίηση ή οστεογένεση) και τα δόντια (ενασβέστωση αδαμαντίνης και οδοντίνης), σε μαλακούς ιστούς, όπως οι αρτηρίες (αθηρωματικές πλάκες), οι βαλβίδες καρδιάς και τα τοιχώματα των αγγείων, καθώς επίσης και σε ξένες επιφάνειες που έρχονται σε χρόνια επαφή με τα βιολογικά ρευστά, όπως είναι τα εμφυτεύματα (βιοπροσθετικές βαλβίδες καρδιάς, stents κ.ά.) [Bonucci, 2007]. Κατά την επαφή μιας τέτοιας επιφάνειας, είτε αυτή είναι βιολογική είτε τεχνητή, με βιολογικά ρευστά, όπως το αίμα, ενδέχεται να δημιουργηθούν εναποθέσεις φωσφορικού ασβεστίου, αφού το αίμα όπως και όλα σχεδόν τα βιολογικά ρευστά είναι υπέρκορα ως προς τις κρυσταλλικές φάσεις του φωσφορικού ασβεστίου [Nancollas, 1992]. Η μελέτη του φαινομένου της βιολογικής ασβεστοποίησης κρίνεται αναγκαία, καθώς μπορεί να βοηθήσει αποτελεσματικά στην αντιμετώπιση καρδιαγγειακών προβλημάτων που σχετίζονται με την ασβεστοποίηση αλλά και στην ανάπτυξη κατάλληλων βιοϋλικών για εμφυτεύσεις στο ανθρώπινο σώμα. 1.3 ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΣΕ ΒΑΛΒΙΔΕΣ ΚΑΡΔΙΑΣ Η ασβεστοποίηση του καρδιαγγειακού συστήματος αναφέρεται στην παθολογική εναπόθεση φωσφορικού ασβεστίου σε αιμοφόρα αγγεία, στο μυοκάρδιο και σε καρδιακές βαλβίδες [Speer and Giachelli, 2004]. Τον 19 ο αιώνα, ο παθολογοανατόμος Rudolph Virchow πρώτος αναγνώρισε τη συμμετοχή της ασβεστοποίησης των ιστών στην παθοβιολογία της καρδιαγγειακής νόσου. Οι κυριότερες ιστοπαθολογικές μορφές ασβεστοποίησης αφορούν στις καρδιακές βαλβίδες και στα αγγεία [Vattikuti and Towler, 2004]. Η εκφυλιστική νόσος της αορτικής βαλβίδας έχει γίνει η συνηθέστερη αιτία βαλβιδοπάθειας στον δυτικό κόσμο προκαλώντας σημαντική νοσηρότητα και θνησιμότητα [Goldbarg et al., 2007 ; Schoen and Levy, 1999]. 4
31 1.3.1 Η καρδιά Η καρδιά είναι το κεντρικό όργανο του κυκλοφορικού συστήματος. Είναι ένας κοίλος μυϊκός σάκος που γεμίζει με αίμα, συστέλλεται και διαστέλλεται 70 φορές το λεπτό περίπου και σε έναν ενήλικα έχει το μέγεθος μιας μεγάλης γροθιάς ενώ ζυγίζει γραμμάρια περίπου. Η καρδιά βρίσκεται μέσα στη θωρακική κοιλότητα ανάμεσα στους δύο πνεύμονες. Περιβάλλεται από ένα λεπτό υμένα, το περικάρδιο, ενώ οι εσωτερικές της κοιλότητες καλύπτονται από μια λεπτή μεμβράνη, το ενδοκάρδιο. Ανάμεσα στο περικάρδιο και το ενδοκάρδιο βρίσκεται το παχύτερο τοίχωμα της καρδιάς που ονομάζεται μυοκάρδιο και αποτελείται από δυνατές μυϊκές ίνες. Από τη βάση της καρδιάς ξεκινούν οι μεγάλες αρτηρίες (αορτή και πνευμονική αρτηρία) και στη βάση επιστρέφουν και οι μεγάλες φλέβες (άνω και κάτω κοίλη φλέβα, πνευμονικές φλέβες). Η καρδιά παίζει το ρόλο μυϊκής αντλίας, που παίρνει αίμα από το φλεβικό σύστημα και το προωθεί μέσα στο αρτηριακό σύστημα (Σχήμα 1.1). Σχήμα 1.1: Η ανατομία της καρδιάς [Νetter, 2010]. Εσωτερικά η καρδιά διαιρείται σε δύο τμήματα, ένα δεξιό και ένα αριστερό, τα οποία χωρίζονται μεταξύ τους με ένα μυώδες διάφραγμα που ονομάζεται μεσοκοιλιακό διάφραγμα. Καθένα από τα τμήματα αυτά αποτελείται από δύο κοιλότητες: την επάνω, πού λέγεται κόλπος (δεξιός και αριστερός) και την κάτω, που λέγεται κοιλία (δεξιά και αριστερή). Ο κόλπος και η κοιλία συγκοινωνούν μεταξύ τους με μια βαλβίδα [Νetter, 1998]. 5
32 1.3.2 Οι βαλβίδες της καρδιάς Η καρδιά διαθέτει τέσσερις βαλβίδες που χρησιμεύουν στο να επιτρέπουν την δίοδο του αίματος προς μία μόνο κατεύθυνση και να εμποδίζουν την παλινδρόμησή του κατά τη διάρκεια της καρδιακής συστολής. Αυτές οι βαλβίδες είναι: (i) η τριγλώχινη (ii) η πνευμονική, (iii) η μιτροειδής ή διγλώχινη και (iv) η αορτική (Σχήμα 1.2). Σχήμα 1.2: Οι τέσσερις βαλβίδες της καρδιάς [Νetter, 2010]. Η τριγλώχινη βαλβίδα παρεμβάλλεται μεταξύ του δεξιού κόλπου και της δεξιάς κοιλίας. Το φυσιολογικό εμβαδό της είναι 6-7cm² και είναι η μεγαλύτερη βαλβίδα του σώματος. Η πνευμονική βαλβίδα βρίσκεται μεταξύ της πνευμονικής αρτηρίας και της δεξιάς κοιλίας και έχει εμβαδό 4-5 cm². Η μιτροειδής βαλβίδα είναι τοποθετημένη μεταξύ των δύο αριστερών κοιλοτήτων της καρδιάς, δηλαδή μεταξύ του αριστερού κόλπου και της αριστερής κοιλίας. Τα δύο φύλλα της μιτροειδούς, οι γλωχίνες, σε κάθε καρδιακό κύκλο (συστολή - διαστολή) κλείνουν και ανοίγουν. Το φυσιολογικό εμβαδό της είναι 5-6 cm². Η αορτική βαλβίδα παρεμβάλλεται μεταξύ της αριστερής κοιλίας και της αορτής και θα αναφερθώ εκτενέστερα για αυτή στην επόμενη υποενότητα. Η μιτροειδής και η τριγλώχινη βαλβίδα αποτρέπουν την προς τα πίσω διαφυγή του αίματος από τις κοιλίες προς τους κόλπους όταν συστέλλονται η δεξιά και η αριστερή κοιλία, ενώ η αορτική και η πνευμονική βαλβίδα αποτρέπουν την προς τα 6
33 πίσω διαφυγή του αίματος από την αορτή προς την αριστερή κοιλία και από την πνευμονική αρτηρία προς τη δεξιά κοιλία κατά τη διαστολή (Σχήμα 1.3) [Netter, 1998]. Σχήμα 1.3: Οι τέσσερις βαλβίδες καρδιάς σε κατάσταση συστολής (αριστερά) και διαστολής (δεξιά) [Netter, 1998]. Στην καρδιολογία, ο όρος στένωση μιας βαλβίδας σημαίνει ότι η βαλβίδα δεν μπορεί να ανοίξει πλήρως, ενώ ανεπάρκεια σημαίνει ότι η βαλβίδα δεν μπορεί να κλείσει υδατοστεγώς. Πιο συχνά παρατηρείται στένωση ή ανεπάρκεια της αορτικής και της μιτροειδούς βαλβίδας. Το μεγαλύτερο βάρος από πλευράς πιέσεων το δέχονται οι βαλβίδες που βρίσκονται στο αριστερό μέρος της καρδιάς (μιτροειδής και αορτική) και αυτό συνάδει με το ότι οι βαλβίδες αυτές προσβάλλονται από στένωση ή ανεπάρκεια, ενώ οι στενώσεις της πνευμονικής και της τριγλώχινης είναι σπανιότερες. Στην περίπτωση της αορτικής βαλβίδας η εκφυλιστική στένωση, η οποία εμφανίζεται σε ηλικίες μεγαλύτερες των 65 ετών, είναι αποτέλεσμα προοδευτικής ασβεστοποίησης και ίνωσης των βαλβιδικών πτυχών λόγω της μειωμένης αντοχής της βαλβίδας κατά τη μηχανική καταπόνηση με αποτέλεσμα να δημιουργείται στένωση της τρίπτυχης βαλβίδας. Η ρευματική στένωση αορτικής βαλβίδας συμβαίνει είτε λόγω εκτεταμένης συγκόλλησης είτε λόγω δευτερογενούς εναπόθεσης αλάτων ασβεστίου εξαιτίας του ρευματικού πυρετού. Η στένωση μιτροειδούς βαλβίδας συνήθως οφείλεται σε ρευματικό πυρετό που προκαλεί συγκόλληση και ασβεστοποίηση των πτυχών της βαλβίδας. Ο ρευματικός πυρετός προκαλείται από φλεγμονή που οφείλεται στο β- αιμολυτικό στρεπτόκοκκο της ομάδας Α. Ο στρεπτόκοκκος προσβάλλει συνήθως τον φάρυγγα και τις αμυγδαλές και μετά από τη στρεπτοκοκκική λοίμωξη εκδηλώνεται ο 7
34 ρευματικός πυρετός. Η νόσος προσβάλλει κατά κύριο λόγο την καρδιά και οι καρδιακές βλάβες οφείλονται σε ανοσολογική αντίδραση του οργανισμού έναντι αντιγόνων του στρεπτόκοκκου. Παλαιότερα, ο ρευματικός πυρετός ήταν η πρώτη αιτία που κατέστρεφε τις βαλβίδες της καρδιάς. Σήμερα με τη βελτίωση των συνθηκών διαβίωσης ελαττώθηκαν οι πιθανότητες προσβολής από στρεπτόκοκκο, ιδίως στις οικονομικά αναπτυγμένες χώρες όπου ο ρευματικός πυρετός δεν υφίσταται [Netter, 2010] Περί Αορτικής Βαλβίδας Η αορτική βαλβίδα αποτελεί μέρος της αορτικής ρίζας. Η αορτική ρίζα συνδέει την καρδιά με τη συστηματική κυκλοφορία και εξασφαλίζει τη βέλτιστη αιμάτωση στα στεφανιαία αγγεία. Η φυσιολογική αορτική βαλβίδα έχει εμβαδό 4-5 cm2 και αποτελείται από τρείς μηνοειδείς πτυχές που ονομάζονται γλωχίνες, τη δεξιά, την αριστερή και την οπίσθια ή μη στεφανιαία. Από τη δεξιά και την αριστερή εκφύονται τα στόμια των ομώνυμων στεφανιαίων αρτηριών (Σχήμα 1.4) [Netter, 1998]. Σχήμα 1.4: Η ανατομία της αορτικής βαλβίδας [Netter, 2010]. Κάθε μια από τις γλωχίνες περιλαμβάνει τρεις στοιβάδες, την κοιλιακή, την ινώδη και τη σπογγώδη, οι οποίες διακρίνονται στο σχήμα 1.5 [Vesely, 1998]. Η κοιλιακή (ventricularis) στοιβάδα, προς την κοιλιακή επιφάνεια της γλωχίνας, 8
35 αποτελείται κυρίως από ελαστικές ίνες με ακτινική κατεύθυνση, κάθετη προς τα χείλη της γλωχίνας. Η ινώδης (fibrosa) στοιβάδα, στην αορτική πλευρά της γλωχίνας, αποτελείται κυρίως από ινοβλάστες και ίνες κολλαγόνου σε μια κυκλοτερή διάταξη, παράλληλα προς τα χείλη της γλωχίνας. Η σπογγώδης (spongiosa) είναι μια στοιβάδα με χαλαρό συνδετικό ιστό στη βάση της γλωχίνας, μεταξύ της ινώδους και της κοιλιακής, που αποτελείται από ινοβλάστες, μεσεγχυματικά κύτταρα και διάμεση ουσία πλούσια σε βλεννοπολυσακχαρίτες [Vesely and Noseworthy, 1992]. Σχήμα 1.5: Η διαμόρφωση των στοιβάδων της γλωχίνας [Vesely, 1998]. Η συνεργασία αυτών των στοιβάδων παρέχει την κατάλληλη αντοχή και ευκαμψία που είναι απαραίτητες για τις χρονίως επαναλαμβανόμενες κινήσεις των γλωχίνων [Freeman and Otto, 2005]. Mέσω της διάνοιξης των μηνοειδών πτυχών προωθείται το αίμα, κατά τη συστολική φάση του καρδιακού κύκλου, από την αριστερή κοιλία στην αορτή και από εκεί στη συστηματική κυκλοφορία. Η σύγκλειση των μηνοειδών πτυχών κατά τη διαστολική φάση του καρδιακού κύκλου, αφενός μεν επιτρέπει την πλήρωση με αίμα της αριστερής κοιλίας, αφετέρου δε συγκρατεί το αίμα στην αορτή, παρεμποδίζοντας την παλινδρόμηση του στην αριστερή κοιλία εξασφαλίζοντας έτσι τη συνεχή άρδευση των ιστών. Η βλάβη των ενδοθηλιακών κυττάρων που καλύπτουν τις γλωχίνες μπορεί να είναι ένα από τα σημαντικότερα αρχικά βήματα στην παθογένεση διαφόρων καταστάσεων [Taylor et al., 2003 ; Leskelä et al., 2006]. Τα δομικά και λειτουργικά συστατικά του ενδοθηλίου των βαλβίδων συμμετέχουν στις εκφυλιστικές διαδικασίες. Η 9
36 αορτική βαλβίδα είναι χρονίως εκτεθειμένη σε δυνάμεις διατμητικού στρες. Η ασβεστοποίηση λαμβάνει χώρα κυρίως στην αορτική πλευρά των γλωχίνων όπου η ροή του αίματος είναι πιο στροβιλώδης υποδεικνύοντας ότι οι διατμητικές δυνάμεις επιδρούν στο ενδοθήλιο με συνέπεια την έναρξη εκφυλιστικών διεργασιών [Goldbarg et al., 2007]. Η ασβεστοποίηση της αορτικής βαλβίδας είναι μια βραδέως εξελισσόμενη διαταραχή με ένα φάσμα που εκτείνεται από μια ήπια πάχυνση της βαλβίδας χωρίς απόφραξη της ροής του αίματος, η οποία ονομάζεται σκλήρυνση, μέχρι την έντονη ασβεστοποίηση των γλωχίνων με περιορισμό της κίνησής τους ή την αορτική στένωση (Σχήμα 1.6) [Freeman and Otto, 2005]. H διεργασία αυτή θεωρείται «εκφυλιστική» λόγω χρόνιων μικροτραυματισμών των γλωχίνων και παθητικής εναπόθεσης ασβεστίου. Ωστόσο πρόσφατες μελέτες έχουν δείξει ότι η ασβέστοποίηση των βαλβίδων οφείλεται σε στενά ρυθμιζόμενες διαδικασίες με αρκετές ομοιότητες με το σχηματισμό των οστών κάτι που τις καθιστά κατάλληλες για θεραπευτικούς χειρισμούς [Farzaneh-Far et al., 2001 ; Rajamannan et al., 2003]. Υπάρχουν ιστοπαθολογικές και κλινικές πληροφορίες που δείχνουν πως η ασβεστοποίηση της αορτικής βαλβίδας είναι μια ενεργητική διεργασία παρόμοια με την αθηροσκλήρυνση, με εναπόθεση λιποπρωτεϊνών, χρόνια φλεγμονή και ενεργό ασβέστωση των γλωχίνων [Freeman and Otto, 2005]. Η αντιμετώπιση της ασβεστοποίησης των καρδιακών βαλβίδων σχετίζεται με μία συνολική θεώρηση και αντιμετώπιση των υπεύθυνων παθογενετικών μηχανισμών, όπου οι θεμελιώδεις παθογενετικοί μηχανισμοί της παραμένουν ακόμα αδιευκρίνιστοι. Σχήμα 1.6: Μακροσκοπικά δείγματα φυσιολογικής (αριστερά) και ασβεστοποιημένης αορτικής βαλβίδας (δεξιά) [Freeman and Otto, 2005]. 10
37 Οι μηχανικές πιέσεις στην αορτική βαλβίδα είναι υψηλότερες στην αορτική πλευρά των γλωχίνων, στην περιοχή κάμψης κοντά στη συμβολή με το αορτικό τοίχωμα. Η τάση στο ενδοθήλιο της μη στεφανιαίας πτυχής είναι μικρότερη από αυτή της αριστερής και δεξιάς στεφανιαίας πτυχής, λόγω της απουσίας διαστολικής στεφανιαίας ροής, και έτσι εξηγείται γιατί η μη στεφανιαία πτυχή είναι αυτή που επηρεάζεται πρώτη. Ενδεικτικό του σημαντικού ρόλου που παίζουν οι πιέσεις που ασκούνται στις βαλβιδικές γλωχίνες είναι και το γεγονός ότι ο μέσος όρος ηλικίας εμφάνισης των βλαβών είναι κατά δυο περίπου δεκαετίες νωρίτερα στους ασθενείς με δίπτυχη αορτική βαλβίδα, όπου οι μηχανικές πιέσεις που υφίστανται οι γλωχίνες είναι ισχυρότερες, σε σύγκριση με αυτές των ασθενών με τρίπτυχη βαλβίδα [Beppu et al., 1993 ; Pachulski et al., 1993]. Σχεδόν όλοι οι ασθενείς με δίπτυχη αορτική βαλβίδα αναπτύσσουν με το χρόνο σημαντική απόφραξη στο χώρο εξόδου, ενώ ένα σχετικά μικρό ποσοστό ασθενών με τρίπτυχη βαλβίδα θα εξελίξουν σημαντική στένωση της βαλβίδας. Η εκφυλιστική νόσος της αορτικής βαλβίδας λόγω ασβεστοποίησης χαρακτηρίζεται από πάχυνση και αποτιτάνωση των πτυχών σε απουσία ρευματικής καρδιακής νόσου. Διακρίνεται λειτουργικά στην αορτική σκλήρυνση στην οποία οι πτυχές δεν αποφράσσουν το χώρο εξόδου και την αορτική στένωση όπου παρατηρείται απόφραξη [O'Brien, 2006]. Στην περίπτωση της αορτικής στένωσης, μεγάλη συμβολή στην εξέλιξη της νόσου έχει η ασβεστοποίηση με την προοδευτική πάχυνση και ακαμψία των γλωχίνων και τη στένωση του χώρου εξόδου [Warren et al., 1997]. Η ασβεστοποίηση της αορτικής βαλβίδας σχετίζεται με την αυξημένη νοσηρότητα και θνητότητα, ιδιαίτερα στους ηλικιωμένους. Σε πληθυσμιακή μελέτη του Cardiovascular Health Study, που συμπεριέλαβε ενήλικες άνω των 65 ετών, οι κλινικοί παράγοντες που σχετίζονταν με την ασβεστοποίηση της αορτικής βαλβίδας ήταν η αυξημένη ηλικία, το κάπνισμα, ο δείκτης μάζας σώματος, η αρτηριακή υπέρταση, η υπερλιπιδαιμία και ο σακχαρώδης διαβήτης [Stewart et al., 1997] Προσθετικές Βαλβίδες Καρδιάς Η πιο κοινή θεραπεία που εφαρμόζεται για τις ασβεστοποιημένες ή εκφυλισμένες βαλβίδες είναι η χειρουργική αντικατάσταση της βαλβίδας. Οι βαλβίδες που συνήθως χειρουργούνται είναι η αορτική και η μιτροειδής. 11
38 Οι προσθετικές βαλβίδες διακρίνονται σε δύο κατηγορίες, τις μηχανικές και τις βιοπροσθετικές. Οι μηχανικές βαλβίδες είναι κατασκευασμένες εξ ολοκλήρου από μηχανικά μέρη, από υλικά συμβατά με τον οργανισμό και έχουν τη μορφή μονόφυλλης ή δίφυλλης βαλβίδας. H εισαγωγή του άνθρακα στην κατασκευή των βαλβίδων κατέστησε εφικτό τον σχεδιασμό εξελιγμένων τύπων βαλβίδων που επιτρέπουν ικανοποιητική δίοδο του αίματος και παρουσιάζουν πολύ χαμηλούς δείκτες επιπλοκών. Oι μηχανικές βαλβίδες είναι εξαιρετικά ανθεκτικές και αντέχουν στο χρόνο. Αυτού του είδους οι βαλβίδες όμως, έχουν αυξημένες επιπλοκές σε σχέση με τις βιοπροσθετικές. H συχνότερη επιπλοκή είναι ο θρομβοεμβολισμός και συνίσταται στην πήξη του αίματος στη βαλβίδα που μπορεί να προκαλέσει δυσλειτουργία του βαλβιδικού μηχανισμού από τον σχηματιζόμενο θρόμβο ή μπορεί να συμβεί απόσπαση μικρών τεμαχίων του θρόμβου που δρουν ως έμβολα, που μπορεί να αποφράξουν μικρές αρτηρίες και να προκαλέσουν εμφράγματα των διαφόρων οργάνων με δυσάρεστα αποτελέσματα. H ανάγκη αντιπηκτικής αγωγής είναι το κύριο πρόβλημα που συνοδεύει τις εμφυτεύσεις μηχανικών βαλβίδων [Senthilnathan et al., 1999]. Οι βιοπροσθετικές βαλβίδες είναι κατασκευασμένες είτε από ζωϊκούς ιστούς (xenograft) που υπόκεινται χημική κατεργασία, όπως χοίρειες αορτικές βαλβίδες ή βόειο περικάρδιο, είτε από πτωματικό ιστό δότη (hοmograft - allograft). Επιπλέον, έχουν ξεκινήσει νέες έρευνες κατασκευής βιοπροσθετικών βαλβίδων από ιστό φώκιας που αποσκοπούν σε καλύτερα αποτελέσματα σε σύγκριση με τους χοίρειους ή βόειους ιστούς [Agathos et al., 2011]. Οι βιοπροσθετικές βαλβίδες είναι καλύτερες από πλευράς επιπλοκών και ποιότητας ζωής του ασθενή και δε χρειάζεται λήψη αντιπηκτικών φαρμάκων παρά μόνο τους πρώτους μήνες μετά την εμφύτευση. Ωστόσο, η συμπεριφορά των βιοπροσθετικών βαλβίδων διαφέρει από τις φυσικές βαλβίδες, για παράδειγμα με το άνοιγμα και το κλείσιμό τους κατά τη λειτουργία τους, αφού έχουν υποστεί χημική κατεργασία. Το βασικό τους μειονέκτημα είναι ο περιορισμένος χρόνος ανθεκτικότητάς τους, λόγω εκφυλιστικών αλλοιώσεων που αναπτύσσουν από αντίδραση του οργανισμού και η ανάγκη για αντικατάστασή τους μετά από ορισμένο χρονικό διάστημα. O χρόνος διάρκειας των βιοπροσθετικών βαλβίδων κυμαίνεται από 8-15 έτη ανάλογα με την ηλικία του ασθενούς και τον τύπο της βαλβίδας [Schoen and Levy, 1999]. Εκτός από τις φυσικές βαλβίδες, οι εναποθέσεις αλάτων φωσφορικού ασβεστίου εμφανίζονται και στις βιοπροσθετικές και μάλιστα αποτελούν μείζονα αιτία 12
39 πρωτοπαθούς ανεπάρκειάς τους. Η αύξηση των ασβεστούχων εναποθέσεων συμβάλλει στην ακινησία των γλωχίνων. Ωστόσο, σε αντίθεση με τις φυσικές βαλβίδες, η επίπτωση της ασβεστοποίησης των βιοπροσθετικών, φαίνεται να μειώνεται με την αύξηση της ηλικίας. Σε μια μελέτη 196 ασθενών με βιοπροσθετική αορτική βαλβίδα, 18 από τα 20 περιστατικά πρωτοπαθούς βαλβιδικής ανεπάρκειας συνέβησαν σε ασθενείς ηλικίας κάτω των 65 ετών [Hammermeister et al., 2000]. Σε μια άλλη μελέτη 653 ασθενών, που υποβλήθηκαν σε αντικατάσταση αορτικής βαλβίδας, ο μόνος δείκτης βαλβιδικής ανεπάρκειας και επανάληψης του χειρουργείου ήταν το νεαρό της ηλικίας [Ruel et al, 2004]. Αυτό δηλώνει ότι η διαδικασία της ασβεστοποίησης της βιοπροσθετικής βαλβίδας μπορεί να είναι διαφορετική από αυτή της φυσικής [David et al., 2003]. Η ανάπτυξη in vitro μοντέλων αποτελεί ένα βήμα για την κατανόηση του μηχανισμού σε μοριακό επίπεδο, και του ρόλου που παίζουν διάφοροι παράγοντες, κατά κύριο λόγο χημικοί, στο φαινόμενο της εναπόθεσης αλάτων φωσφορικού ασβεστίου στους ιστούς. 1.4 ΣΤΟΧΟΙ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ Ο σκοπός της παρούσας διατριβής ήταν η διερεύνηση του μηχανισμού σχηματισμού κρυσταλλικών αλάτων φωσφορικού ασβεστίου τα οποία αποτελούν το ανόργανο συστατικό των παθολογικών σχηματισμών της βιολογικής ασβεστοποίησης. Απαραίτητη προϋπόθεση για την μηχανιστική διερεύνηση ετερογενών διεργασιών όπως η κρυσταλλική ανάπτυξη σε υπέρκορα διαλύματα, είναι η κατά το δυνατόν ακριβέστερη μέτρηση της αντίστοιχης κινητικής. Η ακρίβεια αυτή, ιδιαίτερα στην περίπτωση της κινητικής της κρυσταλλικής ανάπτυξης αλάτων του φωσφορικού ασβεστίου σε ιστούς και βιοϋλικά απαιτεί κατάλληλες και αξιόπιστες μεθόδους, οι οποίες εξασφαλίζουν ακρίβεια των μετρούμενων κινητικών παραμέτρων και υψηλή επαναληψιμότητα. Ο στόχος αυτός μπορεί να επιτευχθεί με την προσαρμογή της πειραματικής μεθοδολογίας μετρήσεως ρυθμών κρυσταλλικής ανάπτυξης σε συνθήκες σταθερού υπερκορεσμού, σε συστήματα ιστών τα οποία παρουσιάζουν προβλήματα στην μελέτη τους λόγω της μικρής τους (γεωμετρικής) επιφάνειας. Η προσαρμογή αυτή της πειραματικής μεθοδολογίας και η λήψη αξιόπιστων και επαναλήψιμων αποτελεσμάτων απετέλεσε βασικό στόχο της παρούσας εργασίας. Για την ανάπτυξη αξιόπιστου μοντέλου σχεδιάσθηκε συλλογή παθολογικών εναποθέσεων, προκειμένου να χαρακτηρισθούν οι παθολογικοί σχηματισμοί ανοργάνων αλάτων και να συγκριθούν με τα άλατα μοντέλα 13
40 (ΗΑΡ και OCP) τα οποία χαρακτηρίζονται από υψηλή καθαρότητα και σταθερή και συγκεκριμένη στοιχειομετρία. Ιδιαίτερης σημασίας ήταν η διερεύνηση του ρόλου ενδιάμεσων μεταβατικών φάσεων του φωσφορικού ασβεστίου όπως το OCP. Οι μελέτες αυτές, πλην της ασβεστοποιήσεως βιολογικών ιστών ή ιστών που έχουν ανπτυχθεί για χρήση ως εμφυτεύματα για την αποκατάσταση ή αντικατάσταση ιστών που έχουν υποστεί βλάβες, έχουν σημασία για την αξιολόγηση και ανόργανων βιοϋλικών, όπως τα βιοτσιμέντα. Η επέκταση των μελετών από τα κατά κύριο λόγο οργανικά υποστρώματα (γλωχίνες, περικάρδιο κ.τ.λ.) σε ανόργανα τα οποία βασίζονται σε ανθρακικά και φωσφορικά άλατα του ασβεστίου ήταν ένας ακόμα στόχος, ο οποίος αποσκοπούσε στην διευκρίνιση των ιδιαίτερων χαρακτηριστικών των υποστρωμάτων και του ρόλου που διαδραματίζουν στην βιολογική ασβεστοποίηση. Ένα χαρακτηριστικό ωστόσο των ανόργανων υποστρωμάτων είναι η συνύπαρξη σε ισορροπία ιόντων όπως τα ανθρακικά ή ιόντα μετάλλων όπως το στρόντιο, ο ρόλος της παρουσίας των οποίων θα πρέπει να διερευνηθεί στα πλαίσια της παρούσας εργασίας. Δεδομένου δε του ότι η κρυσταλλική ανάπτυξη είναι διεργασία, η οποία λαμβάνει χώρα στη διεπιφάνεια υποστρώματος/υπέρκορου διαλύματος σχεδιάσθηκε η διερεύνηση του ρόλου της διεπιφάνειας στερεού - υγρού στην κρυσταλλική ανάπτυξη των εναποθέσεων σε ιστούς με την κατασκευή ειδικής προς τούτο κυψελίδας η οποία θα επέτρεπε μετρήσεις του επιφανειακού δυναμικού με την μέθοδο του δυναμικού ροής. Τέλος, η μελέτη του μηχανισμού διάλυσης εναποθέσεων φωσφορικού ασβεστίου, και μετά την διευκρίνιση της σχέσεως μεταξύ αλάτων μοντέλων και παθολογικών εναποθέσεων, αποτελεί αναπόσπαστο στόχο προκειμένου να είναι δυνατή η υπόδειξη μεθόδων όχι μόνο παρεμπόδισης του σχηματισμού αλλά και της διερεύνησης της αναστρεψιμότητας του φαινομένου της βιολογικής ασβεστοποίησης σε περιπτώσεις παθολογικές, όπου και είναι ανεπιθύμητη. 14
41 ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟΥ 1 Agathos E.A., Shen M., Katsiboulas M., Koutsoukos P., Gloustianou G., In Vivo Calcification of Glutaraldehyde-Fixed Cardiac Valve and Pericardium of Phoca groenlandica, American Society of Artificial Internal Organs, 57, pp , (2011) Beppu S., Suzuki S., Matsuda H., Ohmori F., Nagata S. and Miyatake K., Rapidity of progression of aortic stenosis in patients with congenital bicuspid aortic valves, The American Journal of Cardiology, 71, pp , (1993) Bonucci E., Biological Calcification: Normal and Pathological Processes in the Early Stages, Springer-Verlag: Berlin, (2007) Boretos J.W and Eden M., Contemporary Biomaterials, Noyes Publ: Park Ridge, NJ, (1984) Bostr M.K., Insights into the mechanism of vascular calcification, The American Journal of Cardiology, 88, pp , (2001) Braye F., Irigaray J.L., Jallot E., Oudadesse H., Weber G., Deschamps N., Deschamps C., Frayssinet P., Tourenne P., Tixier H., Terver S., Lefaivre J. and Amirabadi A., Resorption kinetics of osseous substitute: Natural coral and synthetic hydroxyapatite, Biomaterials, 17, pp , (1996) Brown W.E. and Chow L.C., A new calcium phosphate setting cement, J Dental Res, 62, p. 672, (1983) Combes C., Bareille R. and Rey C., Calcium carbonate-calcium phosphate mixed cement compositions for bone reconstruction, J. Biomed. Mater. Res. A, 79, pp , (2006) Constantz B.R., Ison I.C., Fulmer M.T., Poser R.D, Smith S.T., VanWagonerM., Ross J., Goldstein S.A., Jupiter J.B. and Rosenthal D.I., Skeletal repair by in situ formation of the mineral phase of bone, Science 267, pp , (1995) 15
42 David T.E. and Ivanov J., Is degenerative calcification of the native aortic valve similar to calcification of bioprosthetic heart valves?, J Thorac Cardiovasc Surg., 126, pp , (2003) Dorozhkin S.V., Calcium Orthophosphate Cements and Concretes, Materials, 2, pp , (2009) Dorozhkin S.V., Calcium Orthophosphates as Bioceramics: State of the Art, J. Funct. Biomater., 1, , (2010) Driessens F.C.M., Planell J.A., Boltong M.G., Khairoun I. and Ginebra, M.P., Osteotransductive bone cements, Proc. Inst. Mech. Eng. H: J. Eng. Med., 212, pp , (1998) Farzaneh-Far A., Proudfoot D., Shanahan C. and Weissberg P.L., Vascular and Valvar Calcification: Recent Advances, British Medical Journal, 85, pp , (2001) Frayssinet P., Gineste L., Conte P., Fages J.and Rouquet N., Short-term implantation effects of a DCPD-based calcium phosphate cement, Biomaterials, 19, pp , (1998) Freeman R.V. and Otto C.M., Spectrum of calcific aortic valve disease: pathogenesis, disease progression, and treatment strategies, Circulation, 111 (24), pp , (2005) Goldbarg S.H., Elmariah S., Miller M.A. and Fuster V., Insights into degenerative aortic valve disease, Journal of the American College of Cardiology, 50, pp , (2007) Hammermeister K., Sethi G.K., Henderson W.G., Grover F.L., Oprian C. and Rahimtoola S.H., Outcomes 15 years after valve replacement with a mechanical versus a bioprosthetic valve: final report of the Veterans Affairs randomized trial, Journal of the American College of Cardiology, 36, pp , (2000) 16
43 Hong Y.C., Wang J.T., Hong C.Y., Brown W.E. and Chow L.C., The periapical tissue reactions to a calcium phosphate cement in the teeth of monkeys, J. Biomed. Mater. Res., 25 (4), pp , (1991) Ikenaga M., Hardouin P., Lemaître J., Andrianjatovo H. and Flautre B., Biomechanical characterization of a biodegradable calcium phosphate hydraulic cement: A comparison with porous biphasic calcium phosphate ceramics, J Biomed Mater Res 40, pp , (1998) LeGeros R.Z., Chohayeb A. and Shulman A., Apatitic calcium phosphates: possible dental restorative materials, J Dental Res, 61 p. 343, (1982) LeGeros R.Z., Calcium Phosphates in Oral Biology and Medicine, Monographs in Oral Sciences, 15 Myers H. (ed), Karger: Basel, (1991) Leskelä H.V., Satta J., Oiva J., Eriksen H., Juha R., Korkiamäki P., Ivaska K.K., Soini Y. and Lehenkari P., Calcification and cellularity in human aortic heart valve tissue determine the differentiation of bone-marrow-derived cells, Journal of molecular and cellular cardiology, 41, pp , (2006) Nancollas G.H., The involvement of calcium phosphates in biological mineralization and demineralization processes, Pure & Appl. Chern., 64 (11), pp , (1992) Netter H.F., Atlas of Human Anatomy, 2nd Edition, Elsevier Health Sciences, (1998) Νetter H.F., Παθολογία: Καρδιαγγειακό Σύστημα, Ιατρικές Εκδόσεις: Π.Χ. Πασχαλίδης, (2010) O'Brien K.D., Kuusisto J., Reichenbach D.D., Ferguson M., Giachelli C., Alpers C.E. and Otto C.M., Osteopontin is expressed in human aortic valvular lesions, Circulation, 92, pp , (1995) 17
44 O'Brien K.D., Pathogenesis of calcific aortic valve disease: a disease process comes of age (and a good deal more), Arteriosclerosis, thrombosis, and vascular biology, 26, p. 1721, (2006) Pachulski R.T and Chan K.L., Progression of aortic valve dysfunction in 51 adult patients with congenital bicuspid aortic valve: assessment and follow-up by Doppler echocardiography, British Heart Journal, 69, pp , (1993) Park J.B., The Biomedical Engineering Handbook, Section IV: Biomaterials, 1, 2 nd edition, (ed.) Bronzino J.D, CRC Press and Springer Verlag GmbH, (2000) Rajamannan N.M., Subramaniam M., Rickard D., Stock S.R., Donovan J., Springett M., Orszulak T., Fullerton D.A., Tajik A.J., Bonow R.O., Spelsberg T., Human aortic valve calcification is associated with an osteoblast phenotype, Circulation, 107, pp , (2003) Ratner B., Hoffman A., Schoen F., and Lemons J., Biomaterials science: An Introduction to Materials in Medicine, 2 nd edition, Elsevier Academic Press: San Diego, (2004) Rueger J.M., Linhart W. and Sommerfeldt D., Biological reactions to calcium phosphate ceramic implants. Results of animal experiments, Orthopäde, 27, pp , (1998) Ruel M., Kulik A., Rubens F.D., Bedard P., Masters R.G., Pipe A.L. and Mesana T.G., Late incidence and determinants of reoperation in patients with prosthetic heart valves, Eur J Cardiothorac Surg, 25, pp , (2004) Schoen F.J. and Levy R.J., Tissue Heart Valves: Current Challenges and Future Research Perspectives, Journal of Biomedical Materials Research, 47, pp , (1999) Senthilnathan V., Treasure T., Grunkemeier G. and Starr A., Heart valves: which is the best choice?, Cardiovascular surgery, 7, pp , (1999) 18
45 Speer M.Y. and Giachelli C.M., Regulation of cardiovascular calcification, Cardiovascular Pathology, 13, pp , (2004) Stewart B.F., Siscovick D., Lind B.K., Gardin J.M., Gottdiener J.S., Smith V.E., Kitzman D.W. and Otto C.M. Clinical factors associated with calcific aortic valve disease. Cardiovascular Health Study, Journal of the American College of Cardiology, 29, pp , (1997) Taylor P.M., Batten P., Brand N.J., Thomas P.S. and Yacoub M.H., The cardiac valve interstitial cell, International Journal of Biochemistry and Cell Biology, 35, pp , (2003) Vattikuti R. and Towler D.A., Osteogenic regulation of vascular calcification: an early perspective, Am J Physiol Endocrinol Metab., 286, pp , (2004) Vesely I. and Noseworthy R., Micromechanics of the fibrosa and the ventricularis in aortic valve leaflets, Journal of Biomechanics, 25 (1), pp , (1992) Vesely I., The role of elastin in aortic valve mechanics, Journal of Biomechanics, 31, pp , (1998) Warren B.A. and Yong J.L.C., Calcification of the aortic valve: its progression and grading, Pathology, 29, pp , (1997) Weiner S. and Wagner H.D., The material bone: Structure - mechanical function relations, Annu Rev Mater Sci, 28, pp , (1998) Williams D.E., Definition in Biomaterials, Progress in Biomedical Engineering, 4 Elsevier: Amsterdam, (1987) 19
46 20
47 Κ Ε Φ Α Λ Α Ι Ο 2 ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 21
48 2.1 ΚΡΥΣΤΑΛΛΩΣΗ Η κρυστάλλωση είναι μια χημική διεργασία η χρήση της οποίας απαντάται σε όλες σχεδόν τις βιομηχανίες, είτε ως μέθοδος παραγωγής κρυσταλλικών στερεών, είτε ως μέθοδος καθαρισμού, διαχωρισμού και ανάκτησης υλικών από διαλύματα. Επιπλέον, η κρυστάλλωση ως διεργασία έχει το πλεονέκτημα ότι τα τελικά προϊόντα είναι δυνατόν να σχεδιαστούν έτσι ώστε να αποκτήσουν επιθυμητές ιδιότητες όπως είναι το σχήμα και το μέγεθος των σωματιδίων, οι οποίες διευκολύνουν την περαιτέρω χρήση τους. Εφαρμογές των μεθόδων και των αρχών της κρυστάλλωσης γίνονται στις βιομηχανίες παραγωγής χημικών προϊόντων, φαρμάκων, κεραμικών, χρωμάτων, πολυμερών υλικών, στη μεταλλουργία, στη σύνθεση ημιαγωγών, στην παρασκευή καταλυτών, στις βιομηχανίες τροφίμων, λιπασμάτων και πετρελαίου [Söhnel and Garside, 1992]. Πέραν όμως των βιομηχανικών εφαρμογών, η κρυστάλλωση είναι σημαντική διεργασία τόσο για ζωντανούς οργανισμούς όσο και για φύση. Ο σχηματισμός των σκληρών ιστών των ανώτερων θηλαστικών (οστά και δόντια) αλλά και οι παθολογικοί σχηματισμοί λίθων στη χολή, τους νεφρούς και αλάτων ασβεστίου σε βαλβίδες καρδιάς και σε αρτηρίες, αποτελούν χαρακτηριστικά παραδείγματα βιολογικής ασβεστοποίησης (φυσιολογικής ή παθολογικής) δηλαδή, κρυσταλλικής ανάπτυξης αλάτων του ασβεστίου [Dorozhkin and Epple, 2002]. Στη φύση ο ρόλος της κρυστάλλωσης είναι επίσης σημαντικός στο σχηματισμό διαφόρων ορυκτών και πετρωμάτων όπως ο ασβεστόλιθος, το μάρμαρο, και οι σταλακτίτες. Ο σχηματισμός οστράκων, κοχυλιών και κοραλλιογενών αποθέσεων γίνεται με διεργασίες κρυστάλλωσης [Lowenstamm and Weiner, 1989]. Η κρυστάλλωση περιλαμβάνει μια σειρά διεργασιών το τελικό αποτέλεσμα των οποίων είναι ο σχηματισμός νέας φάσης, θερμοδυναμικά σταθερής μέσα σε ομογενές διάλυμα. Αναγκαία, αλλά όχι ικανή συνθήκη για τον σχηματισμό της νέας φάσης είναι η ύπαρξη υπερκορεσμού. Ο υπερκορεσμός είναι μία θερμοδυναμικά ασταθής κατάσταση στην οποία σε τυχαία σημεία του διαλύματος οι δομικές μονάδες της διαλυμένης ουσίας αρχίζουν να διατάσσονται με τρόπο που από δομική άποψη, είναι χαρακτηριστικός της νέας φάσης. Υπό συγκεκριμένες προϋποθέσεις, σχηματίζεται μια νέα διαχωριστική επιφάνεια μεταξύ του διαλύματος και της νέας, στερεάς φάσης. Η νέα φάση εμφανίζεται πρώτα με τη μορφή κρυσταλλικών εμβρύων (πλειάδες δομικών μονάδων) μέσα στο υπέρκορο διάλυμα. Τα έμβρυα, μόλις ξεπεράσουν ένα κρίσιμο μέγεθος, αναπτύσσονται ανεμπόδιστα μέχρι το υπέρκορο διάλυμα να φτάσει την κατάσταση ισορροπίας η οποία 22
49 αντιστοιχεί στον σχηματισμό κορεσμένου διαλύματος. Οι πλειάδες (clusters) των δομικών μονάδων γνωστές και ως έμβρυα ή πυρήνες (nuclei) [Mullin, 2001] είτε επαναδιαλύονται στο διάλυμα, είτε ξεπερνώντας ένα ενεργειακό φράγμα, αναπτύσσονται περαιτέρω σχηματίζοντας την νέα φάση. Η κινητήρια δύναμη για το σχηματισμό της νέας φάσης είναι η μεταβολή της ελεύθερης ενέργειας Gibbs για την μετάβαση από την θερμοδυναμικά ασταθή κατάσταση του υπερκορεσμού στην σταθερή κατάσταση του κορεσμού. Το ενεργειακό φράγμα που απαιτείται να ξεπεραστεί για το σχηματισμό των πρώτων μικροσκοπικών κρυσταλλιτών της νέας φάσης αντιστοιχεί στην επιφανειακή τους ενέργεια. Οι διεργασίες που οδηγούν στο σχηματισμό της νέας φάσης είναι: (i) η επίτευξη του υπερκορεσμού, (ii) η πυρηνογένεση, (iii) η κρυσταλλική ανάπτυξη και (iv) οι δευτερογενείς διεργασίες, όπως η συσσωμάτωση, η ωρίμανση, η επαναδιάλυση και η ανακρυστάλλωση. Η πυρηνογένεση προηγείται χρονικά της κρυσταλλικής ανάπτυξης. Είναι δυνατό όμως, κατά την διάρκεια της κρυσταλλικής ανάπτυξης σε διαφορετική περιοχή του διαλύματος να λαμβάνει χώρα ταυτόχρονα σχηματισμός νέων πυρήνων και ανάπτυξη των όσων ήδη προϋπάρχουν. Συχνά οι διεργασίες της κρυστάλλωσης συμβαίνουν σχεδόν ταυτόχρονα, γεγονός που καθιστά δύσκολη τη μελέτη των επιμέρους μηχανισμών και αναγκαία την παράλληλη διερεύνησή τους Διαλυτότητα Με τον όρο διαλυτότητα χαρακτηρίζεται η ικανότητα μιας στερεής χημικής ουσίας να διαλυθεί σε έναν υγρό διαλύτη. Αυτή η ικανότητα προσδιορίζεται από την μέγιστη ποσότητα της ουσίας που μπορεί να διαλυθεί σε καθορισμένη ποσότητα διαλύτη και ορισμένη θερμοκρασία και πίεση. Το διάλυμα που περιέχει αυτή τη μεγαλύτερη δυνατή ποσότητα διαλυτής ουσίας καλείται κορεσμένο διάλυμα. Το ποσό της διαλυμένης ουσίας το οποίο απαιτείται για τον σχηματισμό κορεσμένου διαλύματος σε δεδομένες συνθήκες, ονομάζεται διαλυτότητα της ουσίας. Οι διαλυτότητες των δυσδιάλυτων αλάτων εξαρτώνται από την θερμοκρασία και (σε μικρότερο βαθμό) από την πίεση και εκφράζονται ως γινόμενα διαλυτότητας από τα οποία υπολογίζονται οι συγκεντρώσεις των επιμέρους χημικών ειδομορφών (species) που βρίσκονται στο κορεσμένο διάλυμα. 23
50 2.1.2 Διάγραμμα Διαλυτότητας Διάγραμμα διαλυτότητας ενός δυσδιάλυτου άλατος είναι το διάγραμμα στο οποίο, σε σταθερή πίεση, παρίσταται γραφικά η συγκέντρωση του άλατος η οποία βρίσκεται σε ισορροπία με την στερεά φάση, συναρτήσει της θερμοκρασίας σε σταθερό pη ή συναρτήσει του pη για σταθερή θερμοκρασία. Σε ένα διάγραμμα διαλυτότητας, όπως αυτό του σχήματος 2.1, διακρίνονται τρεις περιοχές η φυσική σημασία των οποίων καθορίζεται από τις καμπύλες διαλυτότητας και "υπερδιαλυτότητας". α) Σταθερή περιοχή: Είναι η περιοχή που βρίσκεται κάτω από την καμπύλη διαλυτότητας. Στην περιοχή αυτή το διάλυμα είναι ακόρεστο, η μόνη φάση που υπάρχει είναι η υδατική και σε περίπτωση προσθήκης του αντίστοιχου στερεού, λαμβάνει χώρα η διεργασία της διάλυσής του. Η καμπύλη διαλυτότητας περιγράφει την ισορροπία μεταξύ υγρής και στερεής φάσης. Η καμπύλη διαλυτότητας αντιστοιχεί στον γεωμετρικό τόπο των σημείων που ικανοποιούν την συνθήκη του γινομένου διαλυτότητας. β) Μετασταθής - Σταθερή περιοχή: Είναι η περιοχή του διαγράμματος πάνω από την καμπύλη διαλυτότητας και χαρακτηρίζεται από το ότι τα αντίστοιχα διαλύματα είναι υπέρκορα μεν, αλλά μπορεί να είναι πρακτικά σταθερά έπ άπειρον. Σε διαλύματα τα οποία αντιστοιχούν στην περιοχή αυτή, κρυστάλλωση λαμβάνει χώρα μόνον όταν εισάγονται πυρήνες κρυστάλλωσης. Η καμπύλη υπερδιαλυτότητας αποτελεί το άνω όριο της μετασταθούς περιοχής. Η καμπύλη υπερδιαλυτότητας είναι μια σχετικά ασαφής περιοχή μετάβασης από την «σταθερά μετασταθή» στην ασταθή (labile) περιοχή, η οποία επηρεάζεται σημαντικά από παράγοντες όπως η παρουσία ξένων σωματιδίων ή ακαθαρσιών στο διάλυμα, η ύπαρξη ανωμαλιών στα τοιχώματα του δοχείου και ο βαθμός αναταράξεως του διαλύματος. Η καμπύλη υπερδιαλυτότητας καθορίζεται από την κινητική του σχηματισμού της στερεάς φάσης, δηλαδή προσδιορίζεται μόνο πειραματικά. Τα σημεία της καμπύλης υπερδιαλυτότητας, αντιστοιχούν σε διαλύματα στα οποία η έναρξη της καταβύθισης γίνεται με την πάροδο ενός χρονικού διαστήματος που ονομάζεται χρόνος επαγωγής (induction time). Ο χρόνος αυτός είναι αντιστρόφως ανάλογος του υπερκορεσμού του διαλύματος. γ) Μετασταθής - Ασταθής περιοχή: Είναι η περιοχή πέρα από την μετασταθή περιοχή όπου τα διαλύματα είναι αρκετά υπέρκορα. Στην ασταθή περιοχή συμβαίνει αυθόρμητη 24
51 καταβύθιση του δυσδιάλυτου άλατος με την δημιουργία πυρήνων κρυστάλλωσης αυθόρμητα στο υπέρκορο διάλυμα. Σχήμα 2.1: Διάγραμμα διαλυτότητας ενός δυσδιάλυτου άλατος Γινόμενο Διαλυτότητας Η θερμοδυναμική ισορροπία μεταξύ της κρυσταλλικής φάσης και υδατικού της διαλύματος, ορίζεται με την βοήθεια του γινομένου διαλυτότητας. Δυσδιάλυτα άλατα της μορφής Α m Β n διΐστανται σύμφωνα με την: Α m Β n(s) ma n+ + nb m- το χημικό δυναμικό των ιόντων στο διάλυμα δίνεται από τις σχέσεις: 0 n n A kt lna n (2-1) A A 0 m m B kt ln a m (2-2) B B όπου 0 n A και 0 m n B είναι τα πρότυπα χημικά δυναμικά και A ενεργότητες των πλεγματικών ιόντων αντίστοιχα. Όμοια για την στερεά φάση: m n n A και a και m a B οι m B στην κατάσταση ισορροπίας 0 A B Am Bn kt ln a A B (2-3) m n όπου a A m B n η μέση ιοντική ενεργότητα του διαλελυμένου άλατος η οποία είναι: 25
52 a A B m n 1 m n a a mn A m B n (2-4) Η μεταβολή του χημικού δυναμικού κατά την κρυστάλλωση, οπότε από το υπέρκορο διάλυμα η διεργασία χωρεί μέχρις της καταστάσεως ισορροπίας (κορεσμός ως προς το άλας) είναι: ( ) ( ) (2-5) Am B n s Am B n όπου οι δείκτες s και υποδηλώνουν το υπέρκορο διάλυμα και την ισορροπία αντίστοιχα. Αντικατάσταση της Εξ. 2-3 στην εξ. 2-5, δίνει: 0 A B m 0 A B m n n kt ( A ln ( m) ( n) ( kt IP ln K 0 s m B A B m n n ) ) s (2-6) όπου ν=m- + n+, IP = a A m a B n n m και 0 K s η τιμή του ΙΡ σε άπειρη αραίωση (θερμοδυναμικό γινόμενο διαλυτότητας). Το θερμοδυναμικό γινόμενο διαλυτότητας εξαρτάται από την θερμοκρασία, την πίεση και από τη φύση του διαλύματος. Κατά τον ακριβή υπολογισμό των ενεργοτήτων των πλεγματικών ιόντων του δυσδιάλυτου άλατος στο διάλυμα, απαιτείται να λαμβάνονται υπόψη όλα τα χημικά είδη (ιόντα ή μόρια) πέραν των πλεγματικών ιόντων. Οι τιμές της ενεργότητας των ελεύθερων ιόντων στα διαλύματα, επηρεάζονται είτε λόγω σχηματισμού συμπλόκων, είτε λόγω της υδρόλυσής τους με αποτέλεσμα αναλόγως της παρουσίας διαφόρων χημικών ειδών να μεταβάλλεται τόσο η ιοντική ισχύς των διαλυμάτων όσο και η ενεργότητα των ελευθέρων ιόντων στα διαλύματα. Αν τα ιόντα ή τα μόρια ενσωματωθούν στο κρυσταλλικό πλέγμα ή καταβυθίζεται και νέα φάση μαζί με το δυσδιάλυτο άλας τότε ο υπολογισμός των ενεργοτήτων και του γινομένου διαλυτότητας γίνονται ακόμη πιο πολύπλοκος καθώς σε αυτή την περίπτωση η ενεργότητα του στερεού είναι διαφορετική της μονάδας [Zemaitis et al., 1986]. Δυσκολίες αυτού του είδους, επιλύονται με υπολογιστικά προγράμματα, στα οποία λαμβάνονται υπόψη όλες οι χημικές ισορροπίες στο διάλυμα καθώς και τα ισοζύγια μάζας και φορτίου για κάθε χημικό είδος. 26
53 2.1.4 Ενεργότητα και Συντελεστές Ενεργότητας Τα διάφορα χημικά είδη σε ένα διάλυμα αλληλεπιδρούν μεταξύ τους όπως και με τα μόρια του διαλύτη. Προκειμένου να διακριθεί η αναλυτική συγκέντρωση μιας διαλυμένης ουσίας, η οποία προσδιορίζεται με χημική ανάλυση από τη δραστική (effective) συγκέντρωση, εισήχθη ο όρος της ενεργότητας. Η έκφραση που συνδέει την ενεργότητα ενός χημικού είδους i, i, με την αναλυτική συγκέντρωση, C i, είναι: a i C (2-7) i Ο συντελεστής ενεργότητας αποτελεί μέτρο της απομάκρυνσης του διαλύματος από την ιδανική συμπεριφορά λόγω ηλεκτροστατικών αλληλεπιδράσεων μεταξύ των διαφόρων χημικών ειδών στο ηλεκτρολυτικό διάλυμα. Σε πολύ αραιά διαλύματα, οι αλληλεπιδράσεις θεωρούνται αμελητέες οπότε τα διαλύματα συμπεριφέρονται ιδανικά. Στην περίπτωση αυτή ο συντελεστής ενεργότητας ισούται με τη μονάδα οπότε η ενεργότητα και η συγκέντρωση του χημικού είδους i είναι ίσες. Αντίθετα για πιο πυκνά διαλύματα η ενεργότητα θα είναι διαφορετική από την συγκέντρωση και ο συντελεστής ενεργότητας μικρότερος από την μονάδα. Τα διαλύματα στην περίπτωση αυτή παρουσιάζουν απόκλιση από την ιδανική συμπεριφορά. Στην πράξη είναι αδύνατο να μετρηθεί πειραματικά ο συντελεστής ενεργότητας από ένα μόνο χημικό είδος σε ένα διάλυμα. Ορίζεται ο μέσος ιοντικός συντελεστής ενεργότητας i, ο οποίος μπορεί να υπολογιστεί και θεωρητικά και να μετρηθεί πειραματικά [Robinson, 1970]. Ο μέσος ιοντικός συντελεστής ενεργότητας ενός ηλεκτρολύτη Α m Β n ο οποίος διΐσταται στα ιόντα n A και m B δίνεται από την (2-8): mn ) m n B ( (2-8) Ο μέσος ιοντικός συντελεστής ενεργότητας εξαρτάται τόσο από την συγκέντρωση του ηλεκτρολύτη Α m Β n όσο και από την συγκέντρωση και το φορτίο όλων των ιόντων του διαλύματος. Για την περιγραφή αυτής της εξάρτησης εισήχθη η έννοια της ιοντικής ισχύος του διαλύματος, Ι, η οποία ισούται με το ημιάθροισμα των γινομένων των αναλυτικών συγκεντρώσεων όλων των ιόντων του διαλύματος επί τα φορτία τους. I C z i i (2-9) 27
54 όπου zi το φορτίο του χημικού είδους i στο διάλυμα. Ο μέσος ιοντικός συντελεστής ενεργότητας με βάση το φορτίο και το μέγεθος των ιόντων μπορεί να υπολογισθεί από τον οριακό νόμο Debye-Hückel [Robinson and Stokes, 1970] σύμφωνα με τον οποίο: log A z z I (2-10) όπου Α σταθερά που περιλαμβάνει την διηλεκτρική σταθερά του διαλύματος, τη σταθερά Boltzmann, την απόλυτη θερμοκρασία, το φορτίο του ηλεκτρονίου και τον αριθμό Avogardo [Aylward and Findlay, 2002]. A Ο οριακός νόμος ισχύει για πολύ αραιά διαλύματα με τιμή ιοντικής ισχύος μέχρι 0.001Μ. Για μεγαλύτερες τιμές ιοντικής ισχύος τα φορτία δεν θεωρούνται πλέον σημειακά αλλά έχουν ορισμένο μέγεθος το οποίο αντιστοιχεί στο ιοντικό μέγεθος a. Ο οριακός νόμος Debye-Hückel διορθώνεται για το ιοντικό μέγεθος, με την βοήθεια της παραμέτρου μεγέθους, α, και γίνεται: B A z AzB I log (2-11) 1 Ba I όπου Β σταθερά που σχετίζεται με την ακτίνα κ -1 της ιονικής ατμόσφαιρας της θεωρίας των ηλεκτρολυτικών διαλυμάτων Debye-Hückel, η οποία περιλαμβάνει επίσης την διηλεκτρική σταθερά του διαλύματος, τη σταθερά Boltzmann, την απόλυτη θερμοκρασία, το φορτίο του ηλεκτρονίου και τον αριθμό Avogardo. Η διορθωμένη έκφραση του οριακού νόμου Debye-Hückel ισχύει για διαλύματα με ιοντική ισχύ μέχρι 0.05Μ. Για διαλύματα με μεγαλύτερες τιμές ιοντικής ισχύος και λαμβάνοντας υπόψη όλες τις αλληλεπιδράσεις των ιόντων με τα μόρια του διαλύτη χρησιμοποιούνται ημιεμπειρικές σχέσεις όπως η (2-12): A z AzB I log bi (2-12) 1 Ba I όπου b σταθερά, η οποία αντιστοιχεί στις αλληλεπιδράσεις των ιόντων και λαμβάνει τιμές που ικανοποιούν πειραματικά δεδομένα. Για ηλεκτρολύτες 1:1 με ιονική ισχύ μέχρι 0.3Μ ισχύει η ημιεμπειρική έκφραση της εξίσωσης Davies [Davies, 1962]: 2 A z I log 0.3I (2-13) 1 I 28
55 2.1.5 Υπερκορεσμός Επίτευξη Υπερκορεσμού Ο υπερκορεσμός ενός διαλύματος ως προς ένα άλας, για ορισμένη θερμοκρασία και πίεση, είναι το μέτρο της απομάκρυνσης του διαλύματος από την κατάσταση ισορροπίας. Το μέτρο του υπερκορεσμού, ανάλογα με τη φύση της διαλελυμένης ουσίας ορίζεται με διάφορους τρόπους. Έτσι για μοριακές ενώσεις είναι η διαφορά μεταξύ της γραμμομοριακής συγκέντρωσης της ένωσης στο υπέρκορο διάλυμα, C, από την συγκέντρωση ισορροπίας, δηλαδή από την διαλυτότητα, C : Υπερκορεσμός ΔC = C-C (2-14) Ο σχετικός υπερκορεσμός, σ x, για την ίδια μοριακή ένωση ορίζεται ως: C C και ο βαθμός ή λόγος υπερκορεσμού, S : C x (2-15) C C C S 1 (2-16) C Θα πρέπει να σημειωθεί, ότι στις παραπάνω εκφράσεις υποτίθεται ότι πρόκειται περί αραιών διαλυμάτων με αποτέλεσμα οι ενεργότητες να αντικαθίστανται από τις αντίστοιχες αναλυτικές συγκεντρώσεις. Κατά κανόνα, τα ηλεκτρολυτικά διαλύματα είναι μη ιδανικά οπότε αντί των συγκεντρώσεων πρέπει ο υπερκορεσμός να εκφράζεται συναρτήσει των ενεργοτήτων των ιόντων. Η εξίσωση (2-6) μετά την αντικατάσταση των ενεργοτήτων από τις αντίστοιχες αναλυτικές συγκεντρώσεις και τους συντελεστές ενεργότητας γίνεται: kt C ln C s ( ) kt kt ( ) ln ln ( ) ( ) s kt ( C ln ( C s n A m n A m C C m Bn m Bn ) ) s kt ( ) ln ( ) s (2-17) όπου ( ) s και ( ) οι μέσοι ιοντικοί συντελεστές ενεργότητας της διαλυμένης ένωσης στο υπέρκορο διάλυμα και στην κατάσταση ισορροπίας αντίστοιχα και Ω, ο βαθμός υπερκορεσμού κατ αναλογία του ορισμού από την εξίσωση (2-16). Ο υπερκορεσμός, Ω, για διαλύματα ηλεκτρολυτών, σύμφωνα με την εξίσωση (2-6) είναι ο λόγος του ιοντικού γινομένου των ενεργοτήτων προς το θερμοδυναμικό γινόμενο διαλυτότητας. Στην ισορροπία, δηλαδή πάνω στην καμπύλη διαλυτότητας, το ιοντικό γινόμενο των ενεργοτήτων ισούται με το θερμοδυναμικό γινόμενο διαλυτότητας οπότε ισχύει Ω=1 και συνεπώς το διάλυμα λέγεται κορεσμένο. Για Ω>1 το διάλυμα 29
56 είναι υπέρκορο και είναι δυνατή η καταβύθιση του άλατος ενώ για Ω<1, το διάλυμα είναι ακόρεστο και είναι δυνατή η διάλυση του άλατος. Ο σχετικός υπερκορεσμός (κατ αναλογία με την (2-15)) συνδέεται με τον υπερκορεσμό με την σχέση: 1/ 1 (2-18) όπου ν ο αριθμός των ιόντων του άλατος που καταβυθίζεται. Η επίτευξη του υπερκορεσμού είναι το πρώτο στάδιο στην διεργασία της κρυστάλλωσης. Η δημιουργία ενός υπέρκορου διαλύματος μπορεί να γίνει με αρκετούς τρόπους όπως με αλλαγή στην θερμοκρασία, εξάτμιση του διαλύτη, αλλαγή της σύστασης του διαλύτη ή με χημική αντίδραση. Η διαλυτότητα κάποιων ενώσεων, αντίθετα με τον γενικό κανόνα, μειώνεται αυξανομένης της θερμοκρασίας. Στην περίπτωση αυτή αυξανομένης της θερμοκρασίας αυξάνεται και ο υπερκορεσμός των διαλυμάτων ως προς το αντίστοιχο άλας. Η εξάτμιση του διαλύτη είναι μια από τις τεχνικές επίτευξης υπερκορεσμού η οποία χρησιμοποιείται σε μη υδατικούς διαλύτες με σχετικά υψηλή τάση ατμών του κορεσμένου διαλύματος. Με την εξάτμιση απομακρύνεται ο διαλύτης με αποτέλεσμα να αυξάνεται η συγκέντρωση του διαλυμένου συστατικού. Όταν η διαδικασία αυτή γίνεται σε σταθερή θερμοκρασία το σύστημα γίνεται αρχικά κορεσμένο και στη συνέχεια υπέρκορο ως προς το αντίστοιχο άλας. Στην τρίτη τεχνική, γνωστή ως εξαλάτωση η σύσταση του διαλύτη αλλάζει με προσθήκη ενός δεύτερου διαλύτη πλήρως αναμίξιμου με τον κύριο διαλύτη αλλά μη αναμίξιμου με την διαλυμένη ουσία. Η τεχνική αυτή εφαρμόζεται στην κρυστάλλωση οργανικών ουσιών. Η δημιουργία ενός υδατικού υπέρκορου διαλύματος για την σύνθεση ανόργανων δυσδιάλυτων αλάτων σε δεδομένη θερμοκρασία, γίνεται με τον έλεγχο της σύστασης του διαλύματος. Στην περίπτωση αυτή χρησιμοποιούνται δύο ευδιάλυτα άλατα τα οποία αναμιγνύονται με αποτέλεσμα την δημιουργία άλατος με χαμηλή διαλυτότητα. Καθώς η σύσταση του διαλύματος, υπερβαίνει το γινόμενο διαλυτότητας του άλατος, το διάλυμα γίνεται υπέρκορο ως προς το άλας αυτό και καθίσταται δυνατή η πυρηνογένεση και στην συνέχεια η κρυσταλλική ανάπτυξη του άλατος. 30
57 2.2 ΠΥΡΗΝΟΓΕΝΕΣΗ Ο σχηματισμός μιας νέας, στερεάς φάσης σε ένα ομογενές υπέρκορο διάλυμα εκτός από την επίτευξη του υπερκορεσμού προϋποθέτει την δημιουργία τρισδιάστατων πυρήνων κρυστάλλωσης. Ο σχηματισμός αυτός, λαμβάνει χώρα στο το στάδιο της πυρηνογένεσης και συνοδεύεται από μεταβολή της ελεύθερης ενέργειας του συστήματος. Παρόλα αυτά είναι δυνατό σε απόλυτα καθαρά ομογενή συστήματα να μην σχηματίζονται πυρήνες νέας φάσης ακόμα και αν ευνοούνται θερμοδυναμικά. Στις περιπτώσεις αυτές η εισαγωγή φύτρων της νέας φάσης ή ακόμα και τοπικές μηχανικές αναταράξεις οδηγούν στην δημιουργία της νέας φάσης. Από τα παραπάνω γίνεται κατανοητό ότι η πυρηνογένεση μπορεί να γίνει είτε αυθόρμητα είτε να προκληθεί εξωγενώς. Ανάλογα με τις συνθήκες που επικρατούν στο υπέρκορο διάλυμα, η πυρηνογένεση διακρίνεται στα ακόλουθα είδη, τα οποία παρουσιάζονται στο σχήμα 2.2. Σχήμα 2.2: Τα είδη της πυρηνογένεσης που προηγείται του σχηματισμού στερεών σε υπέρκορα διαλύματά τους. Κατά την πρωτογενή πυρηνογένεση απουσιάζουν οι κρύσταλλοι της σχηματιζόμενης νέας φάσης ενώ η δευτερογενής πυρηνογένεση εξαρτάται από την παρουσία τέτοιων κρυστάλλων. Η πρωτογενής πυρηνογένεση διακρίνεται στην ομογενή και στην ετερογενή. 31
58 Η ομογενής πυρηνογένεση λαμβάνει χώρα σε απολύτως καθαρά διαλύματα απουσία ξένων σωματιδίων ή επιφανειών. Πρόκειται για το αποτέλεσμα διμοριακών αντιδράσεων ανάμεσα σε μόρια ή ιόντα της διαλυμένης ουσίας που δημιουργούν μοριακές πλειάδες ή έμβρυα. Για να γίνει αυθόρμητος σχηματισμός κρυστάλλων, θα πρέπει το διάλυμα να είναι επαρκώς υψηλού υπερκορεσμού. Αντίθετα, κατά την ετερογενή πυρηνογένεση οι νέοι πυρήνες σχηματίζονται σε συγκεκριμένες θέσεις, όπου ευνοείται ο σχηματισμός της νέας φάσης και είναι το είδος της πυρηνογένεσης, το οποίο συναντάται κατά κανόνα στην πράξη. Τέτοιες θέσεις αποτελούν εισαχθέντες κρύσταλλοι διαφορετικού υλικού από την σχηματιζόμενη νέα φάση, σωματίδια σκόνης ή άλλων ακαθαρσιών ή ανωμαλίες στα τοιχώματα του δοχείου που περιέχει το υπέρκορο διάλυμα και λαμβάνει χώρα η διεργασία. Η ενέργεια ενεργοποίησης στην ετερογενή πυρηνογένεση είναι μικρότερη από την αντίστοιχη της ομογενούς και λαμβάνει χώρα σε χαμηλότερες τιμές υπερκορεσμού συγκριτικά με την ομογενή πυρηνογένεση. Κατά την δευτερογενή πυρηνογένεση προϋπάρχουν στο διάλυμα κρύσταλλοι της ίδιας φάσης με τους σχηματιζόμενους πυρήνες της νέας φάσης. Οι κρύσταλλοι της σχηματιζόμενης νέας φάσης είτε εισάγονται στο υπέρκορο διάλυμα είτε δημιουργούνται από θραύση των κρυστάλλων λόγω ανάδευσης και δρουν ως πρόσθετα κέντρα κρυστάλλωσης στα υπέρκορα διαλύματα. Αυτό συνεπάγεται τον σχηματισμό των πυρήνων πάνω στην επιφάνεια των εισαγόμενων κρυστάλλων Ομογενής Πυρηνογένεση Ο σχηματισμός του κρίσιμου πυρήνα είναι μια διαδικασία, κατά την οποία οι δομικές μονάδες πρέπει να συσσωματωθούν με σχηματισμό δομής ανάλογης με εκείνη του κρυσταλλικού πλέγματος του στερεού το οποίο σχηματίζεται. Οι αλληλεπιδράσεις μεταξύ των ιόντων ή μορίων οδηγούν στο σχηματισμό αρχικά ενός πυρήνα αρκετά μεγάλου, έτσι ώστε το μέγεθος του να φθάσει ένα κρίσιμο μέγεθος. Η αύξηση ως προς το μέγεθος των μικρών αυτών πυρήνων, τελικά οδηγεί στην ανάπτυξη του κρυστάλλου. Για να υπάρξει κρυσταλλική ανάπτυξη θα πρέπει πρώτα να υπερνικηθεί το ενεργειακό φράγμα της πυρηνογένεσης. Σύμφωνα με την κλασσική θεωρία της πυρηνογένεσης, ο σχηματισμός ενός σταθερού πυρήνα είναι το αποτέλεσμα μιας σειράς αυτοκαταλυόμενων διμοριακών αντιδράσεων μεταξύ πλειάδων δομικών μονάδων. Αποτέλεσμα της σειράς αυτής των αντιδράσεων, οι οποίες σχηματικά αποδίδονται στο σχήμα 2.3, είναι ο σχηματισμός 32
59 διαδοχικά μεγαλύτερου μεγέθους πλειάδων, οι οποίες είτε επαναδιαλύονται είτε αυξάνουν σε μέγεθος μέχρι του σχηματισμού μιας πλειάδας δομικών μονάδων η οποία έχει ένα κρίσιμο μέγεθος (critical nucleus). Η κρίσιμη αυτή πλειάδα αναπτύσσεται περαιτέρω ως κρύσταλλος με την προσθήκη νέων δομικών μονάδων [Walton, 1967]. Η διαδικασία αυτή δημιουργίας του πυρήνα κρίσιμου μεγέθους γίνεται ταχύτατα και σε τιμές υψηλού υπερκορεσμού. Σχήμα 2.3: Διμοριακές αντιδράσεις προσθήκης μορίων διαλυμένης ουσίας κατά τον σχηματισμό κρίσιμου πυρήνα. Η δομή του κρίσιμου πυρήνα δεν είναι γνωστή καθώς το μέγεθός τους είναι αρκετά μικρό για απευθείας παρατήρηση. Ο κρίσιμος πυρήνας θεωρείται ότι είναι είτε ένας μικροσκοπικός κρύσταλλος με σχεδόν τέλεια μορφή ή ένα μάλλον διάχυτο σωματίδιο με μη σαφώς καθορισμένη επιφάνεια. Οι ιδιότητες των εμβρύων είναι οι αυτές με τις αντίστοιχες ιδιότητες της συνεχούς φάσεως και η επιφανειακή τους ενέργεια είναι η αυτή με την αντίστοιχη τιμή μιας άπειρης έκτασης επίπεδης στερεάς επιφάνειας. Οι εργασίες των Gibbs, Volmer, Becker και Doring [Nielsen, 1964] αποτέλεσαν τη βάση για την κατανόηση της πυρηνογένεσης δημιουργώντας το υπόβαθρο για την κλασική θεωρία της πυρηνογένεσης. Η δημιουργία των πυρήνων συνοδεύεται από μεταβολή της ελεύθερης ενέργειας του συστήματος. Στη μεταβολή αυτή συνεισφέρουν δύο όροι: ο ένας όρος αντιστοιχεί στην δημιουργία του όγκου της νέας φάσης, ενέργειας που αντιστοιχεί στο σχηματισμό της νέας επιφάνειας, Gv και ο δεύτερος στη μεταβολή της Gs. G G v G s (2-19) Η μεταβολή της ελεύθερης ενέργειας η οποία αντιστοιχεί στη δημιουργία του όγκου της νέας φάσης, Gv, είναι πάντοτε αρνητική, αφού το πλήθος των ελεύθερα κινούμενων 33
60 δομικών μονάδων υποχρεώνονται να βρεθούν σε ολοένα και μικρότερο χώρο. Η μεταβολή αυτή οφείλεται σε μετάβαση από μια ασταθή σε μια σταθερή κατάσταση και έχει τη μορφή: G v al V m 3 (2-20) όπου α ο παράγοντας σχήματος με βάση των όγκο βασισμένο στο χαρακτηριστικό μήκος L, V m ο γραμμομοριακός όγκος της ουσίας που κρυσταλλώνεται και Δμ η μεταβολή του χημικού δυναμικού κατά το σχηματισμό του πυρήνα η οποία δίνεται από την: C kt ln kt ln S (2-21) C o Η μεταβολή της ελεύθερης ενέργειας η οποία αντιστοιχεί στο σχηματισμό της επιφάνειας του πυρήνα, Gs, είναι πάντα θετική αφού για την μεταφορά μιας δομικής μονάδας από το κυρίως διάλυμα στην επιφάνεια του πυρήνα απαιτείται ενέργεια. Η μεταβολή αυτή εξαρτάται από την επιφανειακή τάση και δίνεται από την έκφραση: G bl 2 (2-22) s s όπου b ο παράγοντας σχήματος με βάση την επιφάνεια βασισμένο στο χαρακτηριστικό μήκος L και γ s η διεπιφανειακή τάση. Η μεταβολή της ελεύθερης ενέργειας του συστήματος (2-19) μέσω των (2-20) και (2-22) γίνεται: 3 2 al G bl s V m (2-23) Για πυρήνα σφαιρικού σχήματος, ακτίνας r, η μεταβολή της ελεύθερης ενέργειας του συστήματος γράφεται: G 4r 4r s 3V 2 m 3 (2-24) Εξαιτίας των πολύ μικρών διαστάσεων των σχηματιζόμενων πυρήνων η σχετική μεταβολή της επιφάνειάς τους είναι μεγαλύτερη σε σχέση με την αλλαγή του όγκου 34
61 τους, με συνέπεια ο όρος της μεταβολής της ελεύθερης ενέργειας η οποία αντιστοιχεί στο σχηματισμό της επιφάνειας του πυρήνα, Gs, συνεισφέρει πολύ περισσότερο. Οι εξισώσεις (2-23) και (2-24) παρουσιάζουν την εξάρτηση της μεταβολής της ελεύθερης ενέργειας του συστήματος ως συνάρτηση του χαρακτηριστικού μεγέθους του σχηματιζόμενου πυρήνα. Η εξάρτηση αυτή αναπαρίσταται γραφικά στο σχήμα 2.4. Λόγω της εξάρτησης της μεταβολής της ελεύθερης ενέργειας από δύο όρους, ο ένας των οποίων τείνει να αυξήσει την τιμή της αυξάνει και ο δεύτερος τείνει να την μειώνει, η συνολική μεταβολή της ελεύθερης ενέργειας, ΔG, θα έχει ένα μέγιστο. Η μέγιστη αυτή τιμή της μεταβολής της ελεύθερης ενέργειας του συστήματος αντιστοιχεί στην ακτίνα r cr του κρίσιμου πυρήνα. Ο σχηματισμός πυρήνα με μέγεθος μικρότερο από το κρίσιμο δεν ευνοείται θερμοδυναμικά αφού η μεταβολή της ελεύθερης ενέργειας είναι θετική. Στην περίπτωση αυτή ο σχηματιζόμενος πυρήνας είναι ασταθής και επαναδιαλύεται. Αντίθετα αν ο πυρήνας έχει μέγεθος μεγαλύτερο από το κρίσιμο, ο πυρήνας μπορεί να αναπτυχθεί περισσότερο καθώς η αύξηση του μεγέθους συνοδεύεται με μείωση της ελεύθερης ενέργειας. Δημιουργία επιφάνειας Ελεύθερη Ενέργεια Gibbs, ΔG ΔG cr r cr Σχηματισμός Όγκου G s G Σύνολική Ελεύθερη Ενέργεια G Ακτίνα σχηματιζόμενου πυρήνα, r Σχήμα 2.4: Μεταβολή της ελεύθερης ενέργειας του συστήματος συναρτήσει της ακτίνας του σχηματιζόμενου πυρήνα. Η τιμή της ακτίνας, η οποία αντιστοιχεί στην μέγιστη τιμή της ελεύθερης ενέργειας, η οποία αντιστοιχεί στην αντίστοιχη ακτίνα του κρίσιμου πυρήνα προκύπτει 35
62 από την παραγώγιση της (2-23) ως προς το χαρακτηριστικό μέγεθος, L ή για την περίπτωση σφαιρικού πυρήνα την (2-24) ως προς την ακτίνα, r και εξίσωση της τιμής της παραγώγου με μηδέν (συνθήκη μεγίστου). ( G) L 0 2bL s 3aL V m 2 0 ή ( G) r 0 8r s 12r 3V m 2 0 Με τον τρόπο αυτό, προκύπτει το χαρακτηριστικό μέγεθος ή η ακτίνα του κρίσιμου πυρήνα: 2b svm svm L ή r 2 3a (2-25) Αντικατάσταση στις (2-23) και (2-24) δίνει την τιμή της μεταβολής της ελεύθερης ενέργειας, η οποία αντιστοιχεί στο απαιτούμενο ενεργειακό φράγμα για την πυρηνογένεση: 3 s 2 m 2 3 s 2 m s Vm 2 3 4b V V 16 G crit ή G 2 crit (2-26) 27a 3 όπου β ο παράγοντας σχήματος ο οποίος εξαρτάται από την επιφάνεια και τον όγκο του σχηματιζόμενου πυρήνα. Για σφαιρικούς πυρήνες β=16π/3, για πυρήνες κυβικού σχήματος β=32, για πυρήνες σχήματος ράβδου β=110 και για πυρήνες σχήματος πλάκας β=205 [Nývlt et al., 1985]. Από τη στιγμή που θα δημιουργηθεί ο κρίσιμος πυρήνας, σύμφωνα με το σχήμα 2.4 είναι αναμενόμενη η συμπεριφορά του η οποία σκοπό έχει την ελάττωση της ελεύθερης ενέργειας του συστήματος. Η ελεύθερη ενέργεια η οποία απαιτείται για την δημιουργία και σταθεροποίηση του κρίσιμου πυρήνα, οφείλεται σε στατιστικές διακυμάνσεις της συγκέντρωσης της διαλυμένης ουσίας σε ορισμένα σημεία του διαλύματος. Έτσι σε περιοχές όπου η τιμή του υπερκορεσμού είναι κατάλληλη και στις οποίες παρατηρείται μια προσωρινή αύξηση της ενέργειας ευνοείται η πυρηνογένεση [Garner, 1975]. Ως ταχύτητα πυρηνογένεσης, J, ορίζεται ο αριθμός των σχηματιζόμενων πυρήνων ανά μονάδα όγκου και ανά μονάδα χρόνου και εκφράζεται από μια εξίσωση τύπου Arrhenius: 36
63 G J A0 exp (2-27) k T όπου Α ο ένας προεκθετικός παράγοντας εξαρτώμενος από την θερμοκρασία, k η σταθερά Boltzmann και Τ η απόλυτη θερμοκρασία. Η (2-27) με αντικατάσταση της μεταβολής της ελεύθερης ενέργειας, ΔG, από την (2-26) και αντικαθιστώντας σε αυτή τη μεταβολή του χημικού δυναμικού, Δμ, από την (2-21) γράφεται: J 3 2 exp s Vm 3 3 k T (ln S) A0 2 (2-28) Η εξίσωση (2-28) δείχνει ότι η ταχύτητα πυρηνογένεσης εξαρτάται από τον υπερκορεσμό, S, την θερμοκρασία, T και την διεπιφανειακή ενέργεια, γ s. Η ταχύτητα πυρηνογένεσης αυξάνεται με αύξηση του υπερκορεσμού και της θερμοκρασίας ενώ μειώνεται με αύξηση της διεπιφανειακής ενέργειας. Η εξίσωση (2-28) στη λογαριθμική της μορφή έχει επιβεβαιωθεί και πειραματικά [Turnbull, 1956]. Στο σχήμα 2.5 φαίνεται G η εξάρτηση του παράγοντα exp και της ταχύτητας πυρηνογένεσης, J, από το kt λόγο υπερκορεσμού, S. Σχήμα 2.5: Εξάρτηση της ταχύτητας πυρηνογένεσης, J, από τον λόγο υπερκορεσμού, S. Παράλληλα με την κλασσική θεωρία της πυρηνογένεσης έχουν αναπτυχθεί και μια σειρά από εμπειρικές θεωρίες οι οποίες βασίζονται σε μεγέθη που μπορούν να μετρηθούν ή να παρατηρηθούν κατά την διεργασία της πυρηνογένεσης. Μια σημαντική 37
64 παράμετρος που χρησιμοποιείται για την περιγραφή του σχηματισμού των πυρήνων είναι ο χρόνος επαγωγής, τ. Χρόνος επαγωγής είναι το χρονικό διάστημα που μεσολαβεί ανάμεσα στην χρονική στιγμή στην οποία επιτυγχάνεται ο υπερκορεσμός και την χρονική στιγμή στην οποία ανιχνεύεται ο σχηματισμός νέας φάσης με κάποια φυσικοχημική μέθοδο. Ο χρόνος επαγωγής επηρεάζεται από τον υπερκορεσμό, την θερμοκρασία, τον τρόπο ανάδευσης, το ιξώδες του συστήματος, την παρουσία ακαθαρσιών κ.α. Η παράμετρος αυτή, μετρείται όπως προαναφέρθηκε με διαθέσιμες φυσικοχημικές μεθόδους, π.χ. με οπτική μέθοδο, με παρακολούθηση της συγκέντρωσης στο υπέρκορο διάλυμα ενός από τα χημικά είδη τα οποία σχετίζονται άμεσα ή έμμεσα με το καταβυθιζόμενο στερεό, αλλά εξαρτάται πάντα από την μέθοδο με την οποία προσδιορίζεται, διότι κάθε μέθοδος έχει ορισμένη ευαισθησία έναντι της παρατηρούμενης μεταβολής. Μία γενική έκφραση του χρόνου επαγωγής συναρτήσει της χρονικά εξαρτώμενης ταχύτητας πυρηνογένεσης, J, για καταβύθιση σε διαλύματα [Kashchiev and van Rosmalen, 2003] δίνεται από την: 1/( q1) K B ( S) exp q 2 (2-29) SG ( S) ( q 1)ln S όπου q παράμετρος, Κ κινητικός παράγοντας, Β θερμοδυναμική σταθερά και G χρονικά εξαρτώμενη συνάρτηση του ρυθμού ανάπτυξης των υπερκρίσιμων πυρήνων. Η παράμετρος q και ο κινητικός παράγοντας Κ, λαμβάνουν διαφορετικές τιμές ανάλογα με την τεχνική μέτρησης του χρόνου επαγωγής που χρησιμοποιείται. Για μέτρηση του 1 χρόνου επαγωγής με βάση έναν υπερκρίσιμο πυρήνα q = 0 και K, ενώ με βάση AV πολλούς υπερκρίσιμους πυρήνες και μετρήσεις της συγκέντρωσης στο υπέρκορο 3av διάλυμα ενός από τα πλεγματικά ιόντα q = 3 και K όπου a v το ανιχνεύσιμο A κλάσμα του όγκου της σχηματιζόμενης νέας φάσης στο υπέρκορο διάλυμα. Ο χρόνος επαγωγής αντιστοιχεί στον χρόνο που χρειάζονται οι σχηματιζόμενοι πυρήνες να φτάσουν στο κρίσιμο μέγεθος και θεωρείται ότι αποτελείται από τρεις επιμέρους χρόνους: α) τον χρόνο χαλάρωσης t r που χρειάζεται για να επιτευχθεί στο σύστημα μια ημισταθερή κατανομή των πλειάδων, β) τον χρόνο πυρηνογένεσης, t n, που απαιτείται για τον σχηματισμό του σταθερού πυρήνα και γ) τον χρόνο ανάπτυξης, t g, που απαιτείται για την ανάπτυξη του πυρήνα σε ανιχνεύσιμο μέγεθος. Ο χρόνος επαγωγής ισούται με το άθροισμα των επιμέρους χρόνων: 38
65 t t t (2-30) r n Πειραματικά προσδιορίζεται ο συνολικός χρόνος επαγωγής, τ γιατί ο ακριβής προσδιορισμός κάθε επιμέρους χρόνου είναι αδύνατος. Στις εμπειρικές θεωρίες ο χρόνος επαγωγής θεωρείται αντιστρόφως ανάλογος της ταχύτητας πυρηνογένεσης και το μέγεθος των κρίσιμων πυρήνων ανεξάρτητο του υπερκορεσμού. Η (2-28) μπορεί κατ αναλογία να γραφεί: 3 2 Vm A exp s 3 3 k T (ln S) 2 (2-31) Για δεδομένη θερμοκρασία η γραφική παράσταση του λογαρίθμου του χρόνου επαγωγής έναντι του αντιστρόφου τετραγώνου του λογαρίθμου του υπερκορεσμού δίνει ευθεία γραμμή από την κλίση της οποίας υπολογίζεται η διεπιφανειακή ενέργεια, γ s, με την προϋπόθεση ότι τα δεδομένα αναφέρονται σε ομογενή πυρηνογένεση [Mullin, 2001]. Στην πράξη, όμως, τα πειραματικά δεδομένα μπορεί να προσαρμόζονται σε δύο διαφορετικές ευθείες με διαφορετικές κλίσεις. Ο υπολογισμός της διεπιφανειακής ενέργειας πραγματοποιείται από την κλίση της ευθείας στην περιοχή υψηλότερων τιμών υπερκορεσμού, περιοχή η οποία αντιστοιχεί στην ομογενή πυρηνογένεση. Η αλλαγή στην κλίση των δύο ευθειών σε συγκεκριμένη τιμή υπερκορεσμού αντιστοιχεί στην μετάβαση από την ομογενή στην ετερογενή πυρηνογένεση [Söhnel and Mullin, 1978 ; Mullin and Ang, 1976]. Οι τυπικές τιμές της διεπιφανειακής ενέργειας για δυσδιάλυτα άλατα κυμαίνονται μεταξύ mj m -2 ενώ για πιο ευδιάλυτα άλατα οι τιμές της διεπιφανειακής ενέργειας είναι αρκετά μικρότερες. Οι Christiansen και Nielsen [Christiansen and Nielsen, 1951 ; Nielsen, 1964] θεώρησαν ότι ο χρόνος επαγωγής για την ανάπτυξη των κρίσιμων πυρήνων, οι οποίοι αποτελούνται από p δομικές μονάδες εξαρτάται από την αρχική συγκέντρωση, C 0, της καταβυθιζόμενης στο υπέρκορο διάλυμα: C 1 p 0 g p k (2-32) όπου p είναι ο αριθμός των δομικών μονάδων που απαρτίζουν τον κρίσιμο πυρήνα και k p μια σταθερά. Η εξ. (2-32) ισχύει για υδατικά διαλύματα και στη λογαριθμική της μορφή δίνει ευθεία γραμμή με κλίση (1-p) από την τιμή της οποίας, υπολογίζεται ο αριθμός των δομικών μονάδων οι οποίες συγκροτούν τον κρίσιμο πυρήνα. 39
66 Γενικά ο χρόνος επαγωγής μειώνεται αυξανομένου του υπερκορεσμού, με αύξηση της θερμοκρασίας για δεδομένη τιμή του υπερκορεσμού, με την παρουσία ξένης φάσης που οδηγεί σε ετερογενή πυρηνογένεση και με αύξηση της ταχύτητας ανάδευσης Ετερογενής Πυρηνογένεση Ετερογενής πυρηνογένεση είναι αυτή που προκαλείται από ξένη επιφάνεια που τυχόν υπάρχει στο υπέρκορο διάλυμα. Η ετερογενής πυρηνογένεση είναι αυτή που συνήθως λαμβάνει χώρα στα πραγματικά συστήματα γιατί ο σχηματισμός πυρήνων κρυστάλλωσης με μια καθαρά ομογενή διαδικασία είναι εφικτός κάτω από ειδικές και απόλυτα ελεγχόμενες συνθήκες. Οι ξένες αυτές επιφάνειες μπορεί να παρεμποδίζουν την πυρηνογένεση σε κάποιο σύστημα ενώ να την επιταχύνουν σε ένα άλλο. Η συμπεριφορά τους αυτή δεν καθορίζεται από κάποιο γενικό κανόνα, αλλά ερμηνεύεται κατά περίπτωση μετά από σχετική πειραματική εργασία. Ένας από τους τρόπους αλλά όχι ο μοναδικός, με τον οποίο μπορεί να αρχίσει η κρυστάλλωση σε ένα σύστημα είναι η εισαγωγή κρυσταλλιτών του υλικού που πρόκειται να κρυσταλλωθεί σε υπέρκορα διαλύματά του. Πολλές φορές χρησιμοποιούνται ισόμορφα υλικά με αυτό που πρόκειται να κρυσταλλωθεί για την έναρξη της διεργασίας, ενώ επίσης χρησιμοποιούνται και υλικά τα οποία δεν παρουσιάζουν ομοιότητα πλέγματος με τα προς κρυστάλλωση υλικά αλλά προκαλούν πυρηνογένεση και κρυστάλλωση. Στην περίπτωση αυτή ιδιότητες όπως το επιφανειακό φορτίο, η δομή της επιφάνειας ή η συνάφεια του κρυσταλλικού πλέγματος των αναπτυσσόμενων κρυστάλλων με αυτό του υποστρώματος, παίζουν καθοριστικό ρόλο. Πυρηνογένεση παρουσιάζεται σε σημεία του δοχείου κρυστάλλωσης όπου παρατηρείται τοπική αύξηση του βαθμού υπερκορεσμού, όπως δίπλα σε μια ψυχόμενη ή θερμαινόμενη επιφάνεια, στην επιφάνεια ενός υγρού, ενώ δεν είναι ασυνήθιστο η πυρηνογένεση να ξεκινά πάνω στα τοιχώματα του δοχείου ή στον αναδευτήρα, λόγω των μικροσκοπικών ατελειών των επιφανειών τους. Ο μηχανισμός με τον οποίο λαμβάνει χώρα η ετερογενής πυρηνογένεση είναι αποτέλεσμα αλληλεπιδράσεων των ιόντων του διαλύματος και του στερεού υποστρώματος στην επιφάνεια επαφής υποστρώματος - διαλύματος. Οι θεωρίες για την ετερογενή πυρηνογένεση στηρίζονται στις αντίστοιχες που αναπτύχθηκαν για την ομογενή, υιοθετώντας την ιδέα της προσρόφησης των δομικών μονάδων του σχηματιζόμενου πυρήνα πάνω στο υπόστρωμα. Με ανάλογο τρόπο όταν ένας ικανός αριθμός δομικών μονάδων συγκεντρωθεί στην επιφάνεια του υποστρώματος θα 40
67 δημιουργηθεί ο πυρήνας ο οποίος μόλις ξεπεράσει το κρίσιμο μέγεθος θα αναπτυχθεί περαιτέρω. Η ετερογενής πυρηνογένεση λαμβάνει χώρα σε χαμηλότερες τιμές υπερκορεσμού από τις αντίστοιχες τιμές της ομογενούς πυρηνογένεσης με αποτέλεσμα το πλάτος της μετασταθούς περιοχής να είναι μικρότερο από το πλάτος της μετασταθούς περιοχής για την ομογενή πυρηνογένεση [Tavare, 1995 ; Kashchiev, 2000]. Το όριο της μετασταθούς περιοχής, ως προς τον αντίστοιχο υπερκορεσμό, καθορίζεται από την τιμή του κρίσιμου υπερκορεσμού. Κάτω από το όριο αυτό, το διάλυμα παραμένει υπέρκορο για μεγαλύτερο διάστημα από έναν αυθαίρετο χρόνο αναμονής. Η ελεύθερη ενέργεια η οποία σχετίζεται με το σχηματισμό του πυρήνα κρίσιμου μεγέθους κατά την ετερογενή πυρηνογένεση, GET, είναι μικρότερη της αντίστοιχης για ομογενή πυρηνογένεση,, κατά ένα παράγοντα ( 0 1): GOM G (2-33) ET G OM Όπως έχει ήδη αναφερθεί η διαφασική επιφανειακή ενέργεια είναι ένας από τους παράγοντες που επηρεάζουν την πυρηνογένεση. Στο σχήμα 2.6 απεικονίζονται σχηματικά τα διανύσματα των διαφασικών επιφανειακών ενεργειών στο σύστημα επιφάνεια υποστρώματος σχηματιζόμενος κρύσταλλος διάλυμα. Σχήμα 2.6: Επιφανειακές ενέργειες στις διεπιφάνειες των τριών φάσεων διαλύματος, κρυστάλλου και στερεού υποστρώματος. Οι τρεις διαφασικές επιφανειακές ενέργειες που φαίνονται στο σχήμα 2.6 είναι: cl η διαφασική επιφανειακή ενέργεια μεταξύ του διαλύματος και της κρυσταλλικής 41
68 φάσης που δημιουργείται, sl η διαφασική επιφανειακή ενέργεια μεταξύ της στερεής επιφάνειας του υποστρώματος και του διαλύματος και cs η διαφασική επιφανειακή ενέργεια μεταξύ της κρυσταλλικής φάσης και της στερεάς επιφάνειας του υποστρώματος. Διανυσματική ανάλυση των τριών διαφασικών επιφανειακών ενεργειών, δίνει: sl cs cl sl cs cos cos (2-34) cl Η γωνία θ είναι η γωνία επαφής μεταξύ της κρυσταλλικής φάσης και της στερεάς επιφάνειας και η τιμή της καθορίζει την διαβροχή σε συστήματα υγρούστερεού. Έτσι, ο παράγοντας της εξίσωσης (2-33) μπορεί να εκφραστεί συναρτήσει της γωνίας επαφής, θ: Σύμφωνα με την εξίσωση (2-35): Για θ=180 0, 1 οπότε: GET GOM 2 (2 cos ) (1 cos ) (2-35) 4. Υπάρχει δηλαδή πλήρης κρυσταλλική ασυμβατότητα μεταξύ υποστρώματος και νέας φάσης και η ελεύθερη ενέργεια για ετερογενή πυρηνογένεση είναι η ίδια με αυτή για ομογενή πυρηνογένεση. Η παρουσία του ξένου υποστρώματος στην περίπτωση αυτή δεν μπορεί να προκαλέσει ετερογενή πυρηνογένεση. Για 0<θ<180 0, 1 οπότε: GET GOM. Υπάρχει δηλαδή μερική κρυσταλλική συμβατότητα ενώ η πυρηνογένεση είναι πιθανότερη όσο μικρότερη η τιμή του παράγοντα. Η ξένη φάση μειώνει το ενεργειακό φράγμα για τη δημιουργία του κρίσιμου πυρήνα, λειτουργώντας καταλυτικά για την πυρηνογένεση. Τέλος για θ=0, 0 οπότε G 0 ET. Υπάρχει δηλαδή πλήρης κρυσταλλική συμβατότητα μεταξύ υποστρώματος και νέας κρυσταλλικής φάσης. Η περίπτωση αυτή αντιστοιχεί στη σπορά του υπέρκορου διαλύματος με κρυσταλλικά φύτρα της φάσης η οποία κρυσταλλώνεται. Έτσι, δεν χρειάζεται να δημιουργηθούν νέοι πυρήνες και η ελεύθερη ενέργεια πυρηνογένεσης μηδενίζεται. Στο σχήμα 2.7 φαίνεται η σχέση μεταξύ του παράγοντα φ και της γωνίας επαφής, θ. 42
69 Σχήμα 2.7: Εξάρτηση του παράγοντα φ από τη γωνία επαφής θ κατά τον σχηματισμό νέας φάσης με ετερογενή πυρηνογένεση. Στην έως τώρα ανάλυση θεωρήθηκε επίπεδη επιφάνεια του υποστρώματος, γεγονός που στην πράξη δεν υφίσταται. Η επιφάνεια του υποστρώματος περιλαμβάνει ατέλειες στις οποίες οι πυρήνες της νέας φάσης σχηματίζονται και σταθεροποιούνται ευκολότερα σε σύγκριση με τα αναμενόμενα για εντελώς λείες επιφάνειες [Turnbull, 1950]. Η μέγιστη διάμετρος μιας κυλινδρικής ατέλειας η οποία είναι ικανή να σταθεροποιήσει ένα πυρήνα, δίνεται από την έκφραση της μορφής: όπου 4 cl cos dmax (2-36) G G η ελεύθερη ενέργεια για το σχηματισμό ενός πυρήνα ορισμένου όγκου. Παρόμοιες εκφράσεις έχουν εξαχθεί και για ατέλειες διαφορετικής γεωμετρίας. Η ταχύτητα της ετερογενούς πυρηνογένεσης υπολογίζεται συναρτήσει της μεταβολής της ελεύθερης ενέργειας κατά την ετερογενή πυρηνογένεση, GET, όπως και στην περίπτωση της ομογενούς από αντίστοιχη εξίσωση τύπου Arrhenius [Söhnel and Garside, 1992]: J J ET ET A A ET ET G exp k T ET 3 2 s Vm exp k T (ln S) (2-37) 43
70 Επίσης κατά αντιστοιχία με την ομογενή πυρηνογένεση ο χρόνος επαγωγής θα είναι αντιστρόφως ανάλογος της ταχύτητας πυρηνογένεσης Δευτερογενής Πυρηνογένεση Όταν ο σχηματισμός νέων πυρήνων σε υπέρκορο διάλυμα είναι αποτέλεσμα της παρουσίας θραυσμάτων κρυστάλλων της στερεάς φάσης που κρυσταλλώνεται, τότε η πυρηνογένεση καλείται δευτερογενής. Η παρουσία αυτών των κρυστάλλων παίζει καταλυτικό ρόλο στην πυρηνογένεση, η οποία πραγματοποιείται σε μικρότερους υπερκορεσμούς σε σύγκριση με την αυθόρμητη. Οι μηχανισμοί της δευτερογενούς πυρηνογένεσης χωρίζονται σε τρεις κύριες κατηγορίες [Botsaris, 1976]: (i) τη φαινόμενη δευτερογενή πυρηνογένεση, όπου οι πυρήνες κρυστάλλωσης εισάγονται στο σύστημα μαζί με τους κρυστάλλους οι οποίοι χρησιμοποιούνται. Στην περίπτωση αυτή δεν συμβαίνει σχηματισμός νέων πυρήνων, (ii) την αληθή δευτερογενή πυρηνογένεση, όπου οι νέοι πυρήνες είναι αποτέλεσμα αλληλεπιδράσεων των κρυστάλλων που προϋπάρχουν στο σύστημα με το διάλυμα και (iii) τη δευτερογενή πυρηνογένεση επαφής, όπου οι νέοι πυρήνες σχηματίζονται μετά από συγκρούσεις των κρυστάλλων μεταξύ τους ή με επιφάνειες του δοχείου κρυστάλλωσης. Η δευτερογενής πυρηνογένεση εξαρτάται πέραν του υπερκορεσμού, από την θερμοκρασία, την ταχύτητα ανάδευσης, το μέγεθος, το σχήμα και η ανθεκτικότητα των κρυστάλλων καθώς και την παρουσία προσμίξεων. Η ταχύτητα της δευτερογενούς πυρηνογένεσης συνήθως δίνεται από εμπειρικές εκφράσεις της μορφής [Myerson, 2002]: j T i n B k M W ( C ) (2-38) b όπου W η ταχύτητα ανάδευσης, M T η μάζα των κρυστάλλων ανά μονάδα όγκου του διαλύματος και k b μια σταθερά η οποία εξαρτάται από την θερμοκρασία, την υδροδυναμική, την παρουσία προσμίξεων και τις ιδιότητες των κρυστάλλων. Η δευτερογενής πυρηνογένεση είναι σημαντική στην κρυστάλλωση ευδιάλυτων αλάτων, στα οποία οι σχηματιζόμενοι κρύσταλλοι είναι κατά κανόνα μεγάλου μεγέθους (αρκετές δεκάδες ή εκατοντάδες μm). Αντίθετα, κατά την καταβύθιση δυσδιάλυτων αλάτων, δευτερογενής πυρηνογένεση δεν λαμβάνει χώρα γιατί τα σχηματιζόμενα σωματίδια είναι πολύ μικρά για να συμμετάσχουν στους μηχανισμούς της δευτερογενής 44
71 πυρηνογένεσης. Στις περισσότερες περιπτώσεις καταβύθισης η δευτερογενής πυρηνογένεση δεν λαμβάνεται υπόψη, αλλά μπορεί να είναι σημαντική στα τελευταία στάδια της αυθόρμητης καταβύθισης αν ο αρχικός υπερκορεσμός είναι χαμηλός [Söhnel and Garside, 1992]. 2.3 Επιταξία Επιταξία ή προσανατολισμένη ανάπτυξη, είναι μια ειδική περίπτωση της ετερογενούς πυρηνογένεσης και αναφέρεται στην προσανατολισμένη κρυσταλλική ανάπτυξη ενός στερεού πάνω σε ένα άλλο στερεό υπόστρωμα, όπου τα άτομα του αναπτυσσόμενου κρυστάλλου ακολουθούν την κρυσταλλική διάταξη του πλέγματος του υποστρώματος [Herman, 1994]. Περαιτέρω κρυσταλλική ανάπτυξη στρωμάτων δύναται να οδηγήσει (i) σε διατήρηση της κρυσταλλικής συμμετρίας του υποστρώματος από το επιταξιακά αναπτυσσόμενο στερεό [Turnbull and Vonnegut, 1952], (ii) στην υιοθέτηση μιας νέας συμμετρίας διαφορετικής από αυτήν του υποστρώματος, αλλά και από αυτή που θα είχε ο κρύσταλλος αν ήταν σε καθαρή μορφή και (iii) σε κατάργηση της επίδρασης του υποστρώματος μετά από κάποια στρώματα, οπότε το στερεό αναπτύσσεται όπως στην περίπτωση που το υπόστρωμα ήταν ο ίδιος ο κρύσταλλος. Ο όρος επιταξία χρησιμοποιήθηκε για πρώτη φορά στη βιβλιογραφία το 1928 προκειμένου να περιγράψει την προσανατολισμένη ανάπτυξη ενός κρυστάλλου πάνω σε κάποια άλλη επιφάνεια [Palatnik and Papinov, 1971]. Διακρίνονται τρεις περιπτώσεις: (i) αυτοεπιταξία, κατά την οποία ο κρύσταλλος αναπτύσσεται με υπόστρωμα τον ίδιο κρύσταλλο, (ii) ετεροεπιταξία, όπου ο αναπτυσσόμενος κρύσταλλος και το υπόστρωμα έχουν διαφορετικές κρυσταλλικές συμμετρίες και διαστάσεις πλέγματος και (iii) προσανατολισμένη κρυσταλλική ανάπτυξη επάνω σε άμορφο υλικό. Στην τελευταία περίπτωση, ο αναπτυσσόμενος κρύσταλλος μπορεί να είναι μερικά προσανατολισμένος, δηλαδή η συμμετρία και οι διαστάσεις του κρίσιμου πυρήνα δε διατηρούνται σταθερές σε όλη την έκταση του αναπτυσσόμενου κρυστάλλου. Για την εξήγηση του μηχανισμού του φαινομένου της επιταξίας υπάρχουν δύο προσεγγίσεις. Σύμφωνα με την πρώτη, κρίσιμο παράγοντα αποτελεί η μορφολογία και ειδικότερα η γεωμετρία της επιφάνειας, ενώ σύμφωνα με τη δεύτερη δίνεται έμφαση σε ενεργειακούς παράγοντες και στην ταχύτητα σχηματισμού του κρίσιμου πυρήνα [Sheftal, 1976]. Η επιφάνεια του υποστρώματος παίζει πολύ σημαντικό ρόλο στο φαινόμενο της επιταξιακής κρυσταλλικής ανάπτυξης, επειδή επηρεάζει τη διάταξη των ατόμων ή των 45
72 ιόντων του αναπτυσσόμενου κρυστάλλου. Υπάρχει, δηλαδή, μια αλληλεπίδραση μεταξύ του πλέον επιφανειακού επιπέδου του υποστρώματος με τις δομικές μονάδες του αναπτυσσόμενου κρυστάλλου. Η αλληλεπίδραση αυτή εντοπίζεται σε συγκεκριμένες θέσεις πάνω στην επιφάνεια του υποστρώματος. Προκειμένου να επιτευχθεί προσανατολισμένη ανάπτυξη μιας νέας κρυσταλλικής φάσης πάνω σε ένα κρυσταλλικό υπόστρωμα πρέπει αρχικά να σχηματιστεί ένα μονόστρωμα με καθορισμένη διευθέτηση ατόμων στη δομή του, πάνω στο οποίο στη συνέχεια θα σχηματιστεί ένα καινούριο μονόστρωμα διατηρώντας τον ίδιο προσανατολισμό. Ικανή αλλά όχι και αναγκαία συνθήκη για επιταξία αποτελεί η ύπαρξη συμβατότητας μεταξύ των κρυσταλλικών πλεγμάτων υποστρώματος, s, και υπερκείμενης κρυσταλλικής φάσης, ο. Ως μέτρο της συμβατότητας μεταξύ δύο κρυσταλλικών πλεγμάτων χρησιμοποιείται ο δείκτης κρυσταλλικής ασυμβατότητας (lattice misfit), δ, ο οποίος ορίζεται ως: όπου as και a a a s o (2-39) s ao οι παράμετροι πλέγματος του υποστρώματος και της νέας κρυσταλλικής φάσης αντίστοιχα [Royer, 1934]. Όταν χρησιμοποιούνται ως υπόστρωμα κρύσταλλοι του υλικού που πρόκειται να κρυσταλλωθεί θα ισχύει a s = a o, δηλαδή θα υπάρχει πλήρης κρυσταλλική συμβατότητα αφού δ=0. Σε κάθε άλλη περίπτωση ο δείκτης κρυσταλλικής ασυμβατότητας θα είναι διαφορετικός από το μηδέν. Όσο ο δείκτης κρυσταλλικής ασυμβατότητας πλησιάζει προς το μηδέν, λόγω της μεγάλης συμβατότητας των κρυσταλλικών πλεγμάτων, το πλέγμα της νέας κρυσταλλικής φάσης που αναπτύσσεται δεν παρουσιάζει παραμορφώσεις λόγω τάσεων από το υπόστρωμα. Τέτοιες παραμορφώσεις δημιουργούνται όσο οι τιμές του δείκτη κρυσταλλικής συμβατότητας αυξάνουν. Στο σχήμα 2.8 παρουσιάζονται δύο περιπτώσεις, όπου τα πλέγματα της κρυσταλλικής φάσης και του υποστρώματος παρουσιάζουν μεγάλη και μικρή συμβατότητα. 46
73 Σχήμα 2.8: Επιταξιακή ανάπτυξη μιας φάσης ( ) πάνω σε υπόστρωμα ( ) με α) μεγάλη και β) με μικρή κρυσταλλική συμβατότητα. Για δημιουργία επιταξίας απαιτείται ο δείκτης κρυσταλλικής ασυμβατότητας, δ να παίρνει τιμές μέχρι 0.09, ενώ για τιμές μέχρι 0.14 επιτυγχάνεται επιταξία μόνο αν ξεπερασθεί ορισμένο ενεργειακό φράγμα. Γενικά, είναι παραδεκτό ότι αναγκαία συνθήκη για να υπάρξει προσανατολισμένη ανάπτυξη είναι ο δείκτης κρυσταλλικής ασυμβατότητας, δ να παίρνει τιμές μικρότερες ή ίσες από 0.1 ή 0.2. Σε διαλύματα υψηλού υπερκορεσμού έχει αναφερθεί επιταξία και για τιμές δ ίσες με 0.5 [Turnbull and Vonnegut, 1952]. Όσον αφορά στο μηχανισμό που ακολουθείται κατά την επιταξιακή κρυσταλλική ανάπτυξη λεπτών μονοστρωμάτων σε κρυσταλλικό υπόστρωμα, έχουν προταθεί τρεις περιπτώσεις [Bauer, 1958]: (α) Ο σχηματισμός και η κρυσταλλική ανάπτυξη απομονωμένων τρισδιάστατων κρυσταλλιτών (μηχανισμός Volmer-Weber ή μηχανισμός μέσω ανάπτυξης νησίδων). Αυτός ο μηχανισμός ακολουθείται όταν η αλληλεπίδραση του υποστρώματος με την αναπτυσσόμενη κρυσταλλική φάση είναι ασθενής. (β) Ο σχηματισμός και η κρυσταλλική ανάπτυξη μονοστρωμάτων (μηχανισμός Frankvan der Merwe). Ο μηχανισμός αυτός εμφανίζεται όταν η αλληλεπίδραση του υποστρώματος με την αναπτυσσόμενη κρυσταλλική φάση είναι ισχυρότερη από αυτή της νέας φάσης για τον εαυτό της. (γ) Η κρυσταλλική ανάπτυξη ξεκινά με τη δημιουργία και την ανάπτυξη μονοστρωμάτων που συνοδεύονται από το σχηματισμό τρισδιάστατων κρυσταλλιτών (μηχανισμός Stranskii-Krastanov) [Sranskii and Krastanov, 1938]. Ο μηχανισμός αυτός αποτελεί συνδυασμό των δύο προηγούμενων και απαντάται στις περιπτώσεις που υπάρχει ισχυρή αλληλεπίδραση μεταξύ υποστρώματος και αναπτυσσόμενου κρυστάλλου. 47
74 2.4 ΚΡΥΣΤΑΛΛΙΚΗ ΑΝΑΠΤΥΞΗ Το επόμενο στάδιο στη διεργασία της κρυστάλλωσης είναι η κρυσταλλική ανάπτυξη. Στο στάδιο αυτό οι νεοσχηματιζόμενοι πυρήνες κατά το στάδιο της πυρηνογένεσης αναπτύσσονται μέχρι τη δημιουργία του κρυστάλλου. Οι συνθήκες και ο ρυθμός της κρυσταλλικής ανάπτυξης επηρεάζουν τα χαρακτηριστικά του κρυστάλλου και του τελικού προϊόντος της διεργασίας. Για την εξήγηση του μηχανισμού της κρυσταλλικής ανάπτυξης και για την διατύπωση εκφράσεων του ρυθμού της, έχουν αναπτυχθεί σημαντικές θεωρίες. Οι θεωρίες αυτές περιγράφουν την κρυσταλλική ανάπτυξη τόσο από θερμοδυναμική άποψη όσο και από κινητική και κατατάσσονται σε τρεις βασικές κατηγορίες: Τις θεωρίες επιφανειακής ενέργειας Τις θεωρίες προσρόφησης στρώματος Τις θεωρίες διάχυσης Στις θεωρίες επιφανειακής ενέργειας η δόμηση των κρυστάλλων γίνεται με βάση κρυσταλλογραφικά και δομικά δεδομένα με στόχο την ελαχιστοποίηση της επιφανειακής ενέργειας. Στις θεωρίες προσρόφησης στρώματος άτομα ή μόρια από ένα συνεχές μέσον, ενσωματώνονται στον κρύσταλλο συμβάλλοντας έτσι στην ανάπτυξή του. Η διαδικασία είναι ασυνεχής και πραγματοποιείται με προσρόφηση κατά στρώματα επάνω στην κρυσταλλική επιφάνεια. Τέλος, στις θεωρίες διάχυσης ακολουθείται η διαδικασία της μεταφοράς της δομικής μονάδας στην επιφάνεια του κρυστάλλου από την κύρια μάζα του διαλύματος με διάχυση. Γενικά, δυο διαδικασίες παίζουν σημαντικό ρόλο κατά την κρυσταλλική ανάπτυξη: (i) τα φαινόμενα μεταφοράς από το διάλυμα προς την επιφάνεια του κρυστάλλου και (ii) η ενσωμάτωση των δομικών μονάδων στο κρυσταλλικό πλέγμα του στερεού, φαινόμενο που αναφέρεται ως επιφανειακή αντίδραση και που περιλαμβάνει δύο στάδια. Αρχικά, η δομική μονάδα προσεγγίζει την επιφάνεια του κρυστάλλου και αφυδατώνεται και κατόπιν, είτε προσεγγίζει το σημείο που θα ενσωματωθεί με επιφανειακή διάχυση, είτε εκροφείται και επιστρέφει στο διάλυμα. Η επιφάνεια ενός κρυστάλλου περιέχει ατέλειες όπως βαθμίδες, ακμές, κόγχες και οπές, όπως φαίνεται και στο σχήμα 2.9 (μοντέλο κρυστάλλου κατά Kossel). Οι 48
75 ακμές, οι κόγχες και οι οπές, αποτελούν τα ενεργά κέντρα κρυστάλλωσης, δηλαδή τα σημεία στα οποία μπορούν να ενσωματωθούν οι δομικές μονάδες ώστε να αναπτυχθεί ο κρύσταλλος. Οι θέσεις αυτές χαρακτηρίζονται από το πλήθος των σημείων συγκράτησης των δομικών μονάδων με την επιφάνεια του κρυστάλλου. Θέσεις με περισσότερα σημεία συγκράτησης, ευνοούνται ενεργειακά. Έτσι από ενεργειακή άποψη, η πιθανότητα συγκράτησης μιας δομικής μονάδας, Δ, στην θέση Κ είναι πολύ μεγαλύτερη από την πιθανότητα συγκράτησης στη θέση Α και από την αντίστοιχη στην θέση Β, η οποία θεωρείται αμελητέα. Κ Ο Α Δ Β Σχήμα 2.9: Η επιφάνεια ενός αναπτυσσόμενου κρυστάλλου σύμφωνα με το μοντέλο Kossel και οι πιθανές θέσεις ενσωμάτωσης των δομικών μονάδων (Δ): Βαθμίδα (Β), Ακμή (Α), Κόγχη (Κ), Οπή (Ο). Η ταχύτητα ανάπτυξης των κρυστάλλων περιγράφεται με αρκετούς τρόπους μεταξύ των οποίων η μεταβολή μιας διάστασης του κρυστάλλου ή της μάζας του κρυστάλλου στη μονάδα του χρόνου [Matuchová and Nývlt, 1976]. Η μακροσκοπική ταχύτητα κρυσταλλικής ανάπτυξης, R ορίζεται ως το ποσό του καταβυθιζόμενου στερεού στη μονάδα του χρόνου, έχει μονάδες mol l -1 sec -1 όταν η καταβύθιση γίνεται αυθόρμητα και mol m -2 sec -1 όταν το καταβυθιζόμενο στερεό αποτίθεται σε υπόστρωμα κρυσταλλικής επιφάνειας, Α. Η ταχύτητα αυτή, για πολυκρυσταλλικά συστήματα, σχετίζεται με τη συνολική ανάπτυξη όλων των εδρών του κρυστάλλου και έχει ιδιαίτερη πρακτική σημασία, μιας και είναι εύκολα μετρήσιμη. 49
76 2.4.1 Θεωρίες Επιφανειακής Ενέργειας Οι θεωρίες επιφανειακής ενέργειας είναι από τις παλαιότερες όσον αφορά στην κρυσταλλική ανάπτυξη. Αναπτύχθηκαν από τον Gibbs [Gibbs 1948] και βασίζονται στην ιδέα ότι υπάρχει συσχέτιση μεταξύ του σχήματος του αναπτυσσόμενου κρυστάλλου και της επιφανειακής ενέργειας των εδρών του. Η ολική ελεύθερη ενέργεια ενός κρυστάλλου σε ισορροπία με το περιβάλλον του, υπό σταθερή θερμοκρασία και πίεση, είναι ελάχιστη για δεδομένο όγκο. Επομένως, το σχήμα ενός κρυστάλλου σε ισορροπία με το περιβάλλον του, σε σταθερή θερμοκρασία και πίεση είναι το μικρότερο δυνατό για ένα δεδομένο όγκο. Γεγονός που σημαίνει ότι το σχήμα ενός κρυστάλλου ο οποίος αναπτύσσεται μέσα σε υπέρκορο ρευστό είναι το σχήμα ισορροπίας και η ανάπτυξη των εδρών του γίνεται με τρόπο ώστε η ολική επιφανειακή του ενέργεια να είναι ελάχιστη. Σύμφωνα με τις θεωρίες επιφανειακής ενέργειας οι διάφορες κρυσταλλικές έδρες αναπτύσσονται με ταχύτητες ανάλογες των αντίστοιχων επιφανειακών τους ενεργειών. Εκτός από την ειδική περίπτωση ενός γεωμετρικά ομοιόμορφου κρυστάλλου η ταχύτητα ανάπτυξης είναι διαφορετική για κάθε κρυσταλλική έδρα. Στο σχήμα 2.10 (a) απεικονίζεται κρύσταλλος ο οποίος αναπτύσσεται ιδανικά, δηλαδή κατά την ανάπτυξη του κρυστάλλου το σχήμα του παραμένει ίδιο με το αρχικό. Στην περίπτωση αυτή οι τρεις όμοιες έδρες Α αναπτύσσονται με τον ίδιο ρυθμό, ενώ οι μικρότερες έδρες Β, αναπτύσσονται ταχύτερα. Η ακόμα μικρότερη έδρα C αναπτύσσεται ταχύτερα όλων. Στην πραγματικότητα, ένας κρύσταλλος δεν διατηρεί πάντα το ίδιο γεωμετρικό σχήμα κατά την ανάπτυξή του. Στην περίπτωση αυτή, η οποία απεικονίζεται στο σχήμα 2.10 (b), οι μικρότερες έδρες Β, αναπτύσσονται πιο γρήγορα. Οι έδρες αυτές όσο αναπτύσσεται ο κρύσταλλος γίνονται ολοένα και μικρότερες έως ότου τελικά εξαφανίζονται. Αντίθετα, οι μεγαλύτερες έδρες Α, αναπτύσσονται με μικρότερες ταχύτητες και ολοένα και μεγαλώνουν. 50
77 Σχήμα 2.10: Ταχύτητες ανάπτυξης κρυσταλλικών εδρών, (α) για κρύσταλλο μη μεταβλητού σχήματος και (β) για κρύσταλλο μεταβλητού σχήματος (περίπτωση επικαλυπτόμενης κρυσταλλικής ανάπτυξης). Μειονέκτημα των θεωριών αυτών είναι ότι αντιλαμβάνονται την κρυσταλλική ανάπτυξη μακροσκοπικά και περιορίζονται σε θερμοδυναμική μελέτη του φαινομένου, χωρίς να διατυπώνονται εκφράσεις του ρυθμού κρυσταλλικής ανάπτυξης. Αδυνατούν επίσης να εξηγήσουν την εξάρτηση του ρυθμού κρυσταλλικής ανάπτυξης από τον υπερκορεσμό Θεωρίες Προσρόφησης Στρώματος Ο Volmer [Volmer, 1939] υπήρξε ο πρώτος που υποστήριξε την ιδέα ότι η κρυσταλλική ανάπτυξη είναι μια συνεχής διαδικασία, η οποία λαμβάνει χώρα κατά στρώματα προσροφημένων ατόμων ή μορίων της διαλυμένης ουσίας επάνω στην κρυσταλλική επιφάνεια. Σύμφωνα με το σχήμα 2.9 για την επιφάνεια του κρυστάλλου, η κρυσταλλική ανάπτυξη επιτυγχάνεται με διαδοχικές ενσωματώσεις δομικών μονάδων σε κόγχες και βαθμίδες [Kossel, 1934]. Καθώς η αναπτυσσόμενη βαθμίδα φτάνει στο όριο της επιφάνειας, η ενσωμάτωση νέων δομικών μονάδων σταματά, γιατί πλέον δεν υπάρχουν άλλες ευνοϊκές θέσεις κρυστάλλωσης. Η κρυσταλλική ανάπτυξη συνεχίζεται με την ανάπτυξη ενός μηχανισμού επιφανειακής δισδιάστατης πυρηνογένεσης, όπως φαίνεται στο σχήμα
78 Σχήμα 2.11: Κρυσταλλική ανάπτυξη: (α) μεταφορά της δομικής μονάδας στο σημείο ενσωμάτωσής της στο κρυσταλλικό πλέγμα (β) ολοκλήρωση του μονομοριακού στρώματος (γ) επιφανειακή πυρηνογένεση. Όταν ένα κρυσταλλικό επίπεδο ολοκληρώνεται, δομικές μονάδες μεταφέρονται στην επιφάνεια του κρυστάλλου και καθώς κινούνται τυχαία, συγκρούονται μεταξύ τους. Αν αυτές οι συγκρούσεις είναι μη ελαστικές, τότε δημιουργούνται επιφανειακά δισδιάστατα έμβρυα τα οποία οδηγούν στο σχηματισμό κρίσιμων πυρήνων. Προκειμένου να σταθεροποιηθεί ο πυρήνας αυτός θα πρέπει ένας ικανός αριθμός δομικών μονάδων που είναι προσροφημένες στην επιφάνεια να σχηματίσουν ένα δισδιάστατο πυρήνα, γεγονός που προϋποθέτει τη δημιουργία δεσμών μεταξύ των δομικών μονάδων αλλά και με την επιφάνεια του κρυστάλλου. Κατόπιν υπολογισμών, αντίστοιχων με αυτών του μεγέθους του κρίσιμου πυρήνα κατά την ομογενή πυρηνογένεση, αποδείχθηκε ότι η κρίσιμη ακτίνα του δισδιάστατου πυρήνα και η αντίστοιχη κρίσιμη ελεύθερη ενέργεια πυρηνογένεσης δίνονται από τις σχέσεις: D svm r 2 crit (2-40) G 2D crit 2 hn s V m (2-41) όπου h N το ύψος του δισδιάστατου πυρήνα. Η ταχύτητα πυρηνογένεσης δίδεται από μια σχέση τύπου Arrhenius [Ohara and Reid, 1973]: J B 2 hn s V exp 2 2 k BT ln S 2D 2D m (2-42) 52
79 όπου D B 2 προεκθετικός παράγοντας συνάρτηση της τετραγωνικής ρίζας του lns. H ταχύτητα ανάπτυξης του κρυστάλλου δίδεται από την εξίσωση [Freche, 1989]: R 2 2 hn s V (ln S) 1/ exp 2 2 kbt ln S 2D 2D 2D M J A hn A hnc1 m (2-43) όπου Α το εμβαδόν της επιφάνειας του κρυστάλλου και C 1 σταθερά η οποία εξαρτάται από τον γραμμομοριακό όγκο, το ύψος του δισδιάστατου πυρήνα, την μέση ταχύτητα των προσροφημένων δομικών μονάδων και την συγκέντρωση των μονομερών στην επιφάνεια του κρυστάλλου. Το πρότυπο αυτό της κρυσταλλικής ανάπτυξης αναφέρεται πολλές φορές και ως πρότυπο μονοπυρηνικής ανάπτυξης, το οποίο σχηματικά δίνεται από το σχήμα 2.12 (α). Συνήθως στην επιφάνεια του κρυστάλλου σχηματίζονται περισσότεροι πυρήνες οι οποίοι αναπτύσσονται με μεγάλη ταχύτητα καλύπτοντας την έδρα. Ο απαιτούμενος χρόνος για να δημιουργηθεί το μονόστρωμα παραμένει μικρότερος από το χρόνο που χρειάζεται για να δημιουργηθούν οι πυρήνες. Η επιφανειακή διάχυση των δομικών μονάδων και η διευθέτησή τους στα ενεργά κέντρα είναι το καθορίζον την ταχύτητα στάδιο. Ο μηχανισμός ανάπτυξης ονομάζεται πολυπυρηνικός, σχηματικά φαίνεται στο σχήμα 2.12 (β) και η ταχύτητα ανάπτυξης του κρυστάλλου δίνεται από την σχέση [Hilling, 1966]: R όπου C 2 σταθερά και και δίνεται από την σχέση: 2 4 / 3 2D 2 2D 2D s Vm ( rcrit ) hn J C2 f S exp 2 (2-44) 3 ( k T ) ln S 2D P f S είναι μια συνάρτηση που εξαρτάται από τον υπερκορεσμό f 6 3 1/ 6 S S 7 / ( S 1) 2 / (ln S) (2-45) Εκτός από τις δύο προηγούμενες περιπτώσεις υπάρχει και μια ενδιάμεση, η οποία μοιάζει περισσότερο πιθανή. Όταν ο χρόνος σχηματισμού ενός πυρήνα είναι σχετικά μικρότερος από το χρόνο σχηματισμού του μονοστρώματος τότε νέοι πυρήνες, και άρα καινούργια επίπεδα, αρχίζουν να σχηματίζονται πριν τελειώσει ο σχηματισμός των προηγούμενων. Ο μηχανισμός αυτός ανάπτυξης των κρυστάλλων ονομάζεται μηχανισμός γέννησηςεξάπλωσης ή πρότυπο NAN ( birth-spread model ή nuclei above nuclei model ) και 53
80 σχηματικά παρουσιάζεται στο σχήμα 2.12 (γ). Η ταχύτητα κρυσταλλικής ανάπτυξης με βάση αυτόν το μηχανισμό δίδεται από τη σχέση: 2 2D 2D 3 3 2D 2D 6 hn s V RBS hn ( J ) 1/ u 2 / s C C (ln S) 5 / 1 3 exp 2 3 m kt ln S (2-46) όπου u s η ταχύτητα εξάπλωσης του πυρήνα και D C 2 3 σταθερά. (α) (α) (β) (β) (γ) (γ) Σχήμα 2.12: Πρότυπα κρυσταλλικής ανάπτυξης με δισδιάστατη πυρηνογένεση: (α) Μονοπυρηνικό πρότυπο, (β) Πολυπυρηνικό πρότυπο, (γ) πρότυπο Γέννεσης και Εξάπλωσης. Κάθε ένα από τα τρία παραπάνω πρότυπα δίνει μια ένδειξη για την κρυσταλλική ανάπτυξη συναρτήσει του υπερκορεσμού, της θερμοκρασίας και της κρυσταλλικής έδρας στον ρυθμό της ανάπτυξης της οποίας αναφέρεται. Από το μονοπυρηνικό πρότυπο και την (2-43) ο ρυθμός κρυσταλλικής ανάπτυξης μιας έδρας είναι ευθέως ανάλογος της επιφάνειας της έδρας. Κατά το πρότυπο αυτό οι μεγαλύτερες έδρες αναπτύσσονται πιο γρήγορα σε σχέση με τις μικρότερες, γεγονός που αντιτίθεται στην παρατήρηση ότι οι γρηγορότερα αναπτυσσόμενες έδρες ενός κρυστάλλου έχουν 54
81 μικρότερες επιφάνειες. Αυτό το γεγονός καθιστά το μονοπυρηνικό πρότυπο μη ρεαλιστικό για τις περισσότερες των περιπτώσεων. Το πολυπυρηνικό πρότυπο, σύμφωνα με την εξίσωση (2-44) υποδεικνύει, ότι ο ρυθμός κρυσταλλικής ανάπτυξης αυξάνεται αυξανομένου του ρυθμού πυρηνογένεσης, εν τούτοις ελαττώνεται με μείωση του μεγέθους του κρίσιμου πυρήνα. Το μέγεθος του κρίσιμου πυρήνα ελαττώνεται με αύξηση του υπερκορεσμού, μετατρέποντας την έκφραση του ρυθμού κρυσταλλικής ανάπτυξης σε πολύπλοκη συνάρτηση του υπερκορεσμού. Από την εξίσωση (2-44), ο ρυθμός κρυσταλλικής ανάπτυξης φαίνεται ότι δεν αυξάνεται συνεχώς με τον υπερκορεσμό. Αντίθετα υπάρχει μια τιμή υπερκορεσμού, για την οποία ο ρυθμός γίνεται μέγιστος, ενώ ελαττώνεται με περαιτέρω αύξηση ή μείωση του υπερκορεσμού. Ένα τέτοιο αποτέλεσμα φαίνεται απίθανο και δεν έχει επαληθευθεί πειραματικά. Κατά το πρότυπο γέννησης-εξάπλωσης ο ρυθμός κρυσταλλικής ανάπτυξης αυξάνεται με αύξηση του υπερκορεσμού και της θερμοκρασίας. Η εξάρτηση του ρυθμού από τις μεταβλητές αυτές δεν είναι απλή συνάρτηση του υπερκορεσμού και το πρότυπο αυτό δεν φαίνεται να παρουσιάζει τα προβλήματα των δύο απλούστερων μοντέλων. Μια επιπλέον δυσκολία που αντιμετωπίζουν τα παραπάνω πρότυπα, τα οποία στηρίζονται στην επιφανειακή δισδιάστατη πυρηνογένεση, είναι ότι αν δεν χρησιμοποιηθεί μια πολύ μικρή τιμή επιφανειακής ενέργειας κάθε πρότυπο αποτυγχάνει να ερμηνεύσει την παρουσία κρυσταλλικής ανάπτυξης σε χαμηλές τιμές υπερκορεσμού. Κρυσταλλική ανάπτυξη όμως παρατηρείται και σε χαμηλότερες τιμές υπερκορεσμού από αυτούς που προβλέπονται για περιπτώσεις επιφανειακής πυρηνογένεσης σύμφωνα με την κλασσική θεωρία και μάλιστα με ρυθμούς σημαντικούς σε ορισμένες περιπτώσεις. Η εξήγηση αυτής της συμπεριφοράς ορισμένων υπέρκορων διαλυμάτων δόθηκε από τους Burton, Cabrera και Frank [Burton et al., 1951] οι οποίοι και συνέδεσαν το όνομα τους με την ομώνυμη θεωρία. Σύμφωνα με τη θεωρία αυτή, μόνο ένας μικρός αριθμός κρυστάλλων αναπτύσσονται στρωματικά. Στην πραγματικότητα, στην επιφάνεια των αναπτυσσόμενων κρυστάλλων δημιουργούνται γραμμοαταξίες έλικας (screw dislocations) οι οποίες παρέχουν μόνιμα κέντρα κρυστάλλωσης χωρίς να είναι απαραίτητη η δισδιάστατη πυρηνογένεση. Δομικές μονάδες προσροφούνται στην επιφάνεια του κρυστάλλου και διαχέονται στην κορυφή του βήματος των γραμμοαταξιών έλικας. Αυτές οι γραμμοαταξίες έλικας 55
82 έχουν το ένα άκρο τους σε κάποιο σημείο της επιφάνειας του κρυστάλλου και δημιουργούν ένα βήμα, το οποίο στη συνέχεια αυτοπεριστρέφεται και αναπτύσσεται σε σπείρα γύρω από το σταθερό σημείο. Στο σχήμα 2.13 παρουσιάζεται η σπειροειδής ανάπτυξη σύμφωνα με το πρότυπο Burton, Cabrera και Frank (BCF). Η καλύτερη προσέγγιση για την κατεύθυνση της σπείρας είναι αυτή της αρχιμήδειας σπείρας, υπό την προϋπόθεση ότι τα βήματα ισαπέχουν και δεν είναι πολύ κοντά στο κέντρο της. Συχνό είναι επίσης το φαινόμενο να αναπτύσσονται παράλληλα πολλές έλικες της ίδιας φοράς κυρίως όταν υπάρχουν πολλές γραμμοαταξίες έλικας στην επιφάνεια του κρυστάλλου. (α) (α) (β) (β) (γ) (γ) Σχήμα 2.13: Κρυσταλλική ανάπτυξη σύμφωνα με το πρότυπο Burton, Cabrera και Frank. Η γραμμοαταξία έλικας της επιφάνειας αυτοπεριστρέφεται και δημιουργεί μια έλικα. Σύμφωνα με το πρότυπο BCF η επιφανειακή διάχυση είναι το καθορίζον τον μηχανισμό βήμα. Η σχέση μεταξύ του ρυθμού κρυστάλλωσης, υπερκορεσμού δίνεται από την εξίσωση: BCF R, και του σχετικού R BCF B 2 j A j tanh (2-47) 56
83 όπου Aj και B j σταθερές οι οποίες εξαρτώνται από την θερμοκρασία και το μέγεθος των βημάτων στην επιφάνεια των κρυστάλλων. Για χαμηλούς υπερκορεσμούς από την εξίσωση (2-46) προκύπτει ότι η ποσότητα B tanh j 1 και συνεπώς η ταχύτητα κρυστάλλωσης είναι ανάλογη του τετράγωνου του σχετικού υπερκορεσμού: BCF 2 R A j (2-48) B j B j Αντίθετα για υψηλές τιμές υπερκορεσμού η ποσότητα tanh περίπτωση αυτή η ταχύτητα κρυστάλλωσης είναι ανάλογη του υπερκορεσμού:. Στην BCF R A B (2-49) j j Σύμφωνα με την θεωρία των Burton, Cabrera και Frank οι ρυθμοί κρυσταλλικής ανάπτυξης μεταβάλλονται από παραβολική εξάρτηση με τον υπερκορεσμό σε γραμμική εξάρτηση καθώς ο υπερκορεσμός αυξάνεται. Η μεταβολή αυτή παρίσταται γραφικά στο σχήμα Σχήμα 2.14: Εξάρτηση της ταχύτητας κρυσταλλικής ανάπτυξης από τον σχετικό υπερκορεσμό σύμφωνα με το πρότυπο ΒCF, (I) Παραβολική, (ΙΙ) Γραμμική. 57
84 2.4.3 Θεωρίες Διάχυσης Η παλαιότερη θεωρία διάχυσης διετυπώθη αρχικά από τους Noyes και Whitney το 1897 και σύμφωνα με αυτή, η διαλυμένη ουσία μεταφέρεται από το υπέρκορο διάλυμα προς την επιφάνεια του αναπτυσσόμενου κρυστάλλου και ενσωματώνεται στο κρυσταλλικό πλέγμα. Σύμφωνα με την θεωρία αυτή η διάλυση είναι διεργασία, αντίστροφη της κρυστάλλωσης. Θεωρώντας ότι υπάρχει ένα λεπτό στάσιμο στρώμα υγρού γύρω από τον αναπτυσσόμενο κρύσταλλο στο οποίο διαχέονται οι δομικές μονάδες θα ισχύει: dm D A C C s (2-50) dt όπου m η μάζα του στερεού που εναποτίθεται σε χρόνο t, D ο συντελεστής διάχυσης του μητρικού υγρού, δ το πάχος του στρώματος διάχυσης, Α το εμβαδόν της επιφάνειας του κρυστάλλου, C η συγκέντρωση του διαλυμένου σώματος στο διάλυμα και συγκέντρωση ισορροπίας (διαλυτότητα). C s η Το πάχος του στρώματος διάχυσης εξαρτάται από την ταχύτητα ανάδευσης του διαλύματος, δηλαδή την σχετική ταχύτητα στερεού υγρού. Έχει βρεθεί ότι το πάχος του στρώματος αυτού κυμαίνεται από 20 έως 150 μm σε μη αναδευόμενα διαλύματα, ενώ σε ισχυρά αναδευόμενα σχεδόν μηδενίζεται. Η αδυναμία της θεωρίας αυτής να ερμηνεύσει πειραματικά δεδομένα έγκειται στο γεγονός ότι θα έπρεπε σε αναδευόμενα διαλύματα να παρατηρούνται θεωρητικά σχεδόν άπειρες ταχύτητες ανάπτυξης των κρυστάλλων, καθώς και στο γεγονός ότι εν τέλει η διάλυση ενός κρυστάλλου δεν αποτελεί την αντίστροφη διεργασία της κρυστάλλωσης. Ακολούθησε τροποποίηση της αρχικής θεώρησης, υποθέτοντας ότι τα στάδια της κρυσταλλικής ανάπτυξης είναι δύο: μια διεργασία διάχυσης, κατά την οποία οι δομικές μονάδες μεταφέρονται από το μητρικό υγρό στην επιφάνεια του αναπτυσσόμενου κρυστάλλου και μια αντίδραση πρώτης τάξης κατά την οποία οι δομικές μονάδες ενσωματώνονται στο κρυσταλλικό πλέγμα. Κινητήρια δύναμή στα δυο αυτά στάδια είναι η διαφορά συγκέντρωσης και οι αντίστοιχοι ρυθμοί μεταφοράς μάζας περιγράφονται από τις ακόλουθες εξισώσεις: dm K d AC C in (διάχυση) (2-51) dt 58
85 dm Kr AC in Cs (αντίδραση) (2-52) dt όπου K d ο συντελεστής μεταφοράς μάζας λόγω διάχυσης, K r η σταθερά ταχύτητας για την αντίδραση και C in η συγκέντρωση της διαλυμένης ουσίας στη διεπιφάνεια στερεούυγρού. Η εξάρτηση της συγκέντρωσης συναρτήσει της απόστασης από την επιφάνεια του κρυστάλλου παρουσιάζεται στο σχήμα c c c-c in κινούσα δύναμη για τη μεταφορά μάζας λόγω διαχύσεως c-c s c in κρύσταλλος c in -c s κινούσα δύναμη για την αντίδραση c s ακίνητο στρώμα υγρού επιφάνεια επαφής στερεού - υγρού δ μάζα διαλύματος x Σχήμα 2.15: Μεταβολής της συγκέντρωσης συναρτήσει της απόστασης από την επιφάνεια ενός αναπτυσσόμενου κρυστάλλου. Λόγω της πρακτικής δυσκολίας στη μέτρηση του όρου C in, γίνεται απαλοιφή του από τις δύο εξισώσεις χρησιμοποιώντας μια συνολική διαφορά συγκέντρωσης C-C s, οπότε ο ρυθμός μεταφοράς μάζας δίδεται από τη σχέση: dm dt n G A C C s K (2-53) και η ταχύτητα της κρυσταλλικής ανάπτυξης αντίστοιχα από την: dm R 1 K n G C C s (2-54) A dt 59
86 όπου K G ο ολικός συντελεστής κρυσταλλικής ανάπτυξης και n η τάξη της αντίδρασης. Στην περίπτωση που n = 1 και η επιφανειακή ενσωμάτωση των δομικών μονάδων είναι επίσης πρώτης τάξης αντίδραση, τότε η συγκέντρωση C in απαλείφεται από τις παραπάνω εξισώσεις δίνοντας: οπότε προκύπτει ότι: dm dt A C C 1 1 K K d r sc s (2-55) 1 K G 1 K d 1 K r K G K d K r K K d r (2-56) Στην περίπτωση που η επιφανειακή αντίδραση είναι πάρα πολύ γρήγορη, δηλαδή το K r λαμβάνει αρκετά μεγάλη τιμή θα ισχύει K G K d οπότε το ρυθμίζον την ταχύτητα της διεργασίας στάδιο είναι η διάχυση των δομικών μονάδων. Αντίστοιχα, σε περίπτωση που το K d πάρει αρκετά μεγάλη τιμή, δηλαδή υπάρχει χαμηλή αντίσταση στην διάχυση των δομικών μονάδων από το μητρικό υγρό, τότε K G K r και το καθορίζον την ταχύτητα στάδιο είναι η επιφανειακή αντίδραση. Η σταθερά της ταχύτητας διάχυσης, K d, υπολογίζεται από την σχέση: K d D / (2-57) όπου D ο μοριακός συντελεστής διάχυσης και δ το πάχος του οριακού στρώματος διάχυσης, το οποίο δίνεται από την έκφραση (2-58) [Nielsen, 1980]: ( m ) r ( ) (2-58) όπου r η ακτίνα των σωματιδίων που διαλύονται σε [μm] και Δρ η διαφορά πυκνότητας μεταξύ του στερεού και του διαλύματος σε [g/cm 3 ]. Η μετατροπή της μακροσκοπικής ταχύτητας διάλυσης σε γραμμική ταχύτητα δίνεται από την (2-59) R L 1 b R (2-59) 3a όπου R η ταχύτητα διάλυσης σε [mol/min m 2 ], ρ s η πυκνότητα του στερεού και b, a οι παράγοντες σχήματος με βάση την επιφάνεια και τον όγκο αντίστοιχα. Για σφαίρες ή κύβους b/3a =2 και για οκτάεδρα b/3a =2.45 [Mullin, 2001]. s Καθορισμός Μηχανισμού που Ελέγχει την Κρυσταλλική Ανάπτυξη Πέρα από τις θερμοδυναμικές προσεγγίσεις για την εξήγηση των μηχανισμών της κρυσταλλικής ανάπτυξης αναπτύχθηκαν ημιεμπειρικές σχέσεις για την προσέγγιση 60
87 των πολλών πειραματικών δεδομένων. Μια εκτίμηση για το είδος του μηχανισμού σε ένα σύστημα κρυστάλλωσης προκύπτει από την πιο συχνά απαντώμενη ημιεμπειρική σχέση η οποία εκφράζει την εξάρτηση του ρυθμού καταβύθισης από τον σχετικό υπερκορεσμό και δίνεται από την εξίσωση (2-60) [Nancollas and Reddy, 1971]: R p n K s (2-60) όπου n η φαινόμενη τάξη της ταχύτητας καταβύθισης, σ ο σχετικός υπερκορεσμός ως προς την καταβυθιζόμενη φάση, K μια σταθερά εξαρτώμενη από τη θερμοκρασία και s μια συνάρτηση του αριθμού των ενεργών κέντρων των κρυστάλλων. Η φαινόμενη τάξη της καταβύθισης σχετίζεται άμεσα με τον μηχανισμό που καθορίζει την ταχύτητα ανάπτυξης του κρυστάλλου [Freche, 1989 ; Sangwal, 1994]. Συγκεκριμένα για: n = 1 η ταχύτητα καταβύθισης των κρυστάλλων καθορίζεται είτε από την διάχυση των δομικών μονάδων από το κυρίως διάλυμα (μεταφορά μάζας), είτε από διάχυση των δομικών μονάδων στην αναπτυσσόμενη κρυσταλλική επιφάνεια και ενσωμάτωση τους στα ενεργά κέντρα αυτής, είτε από ελικοειδή μετατόπιση βήματος σύμφωνα με γραμμική εξάρτηση της ταχύτητας από τον σχετικό υπερκορεσμό κατά το πρότυπο BCF n = 2 οι κρύσταλλοι αναπτύσσονται σύμφωνα με τον μηχανισμό ελικοειδούς ανάπτυξης-μοντέλο B.C.F.(παραβολική εξάρτηση) n > 2 οι κρύσταλλοι αναπτύσσονται μέσω επιφανειακής πυρηνογένεσης (πολυπυρηνικό πρότυπο). Συνήθως σε μια διαδικασία κρυσταλλικής ανάπτυξης συμμετέχουν περισσότεροι του ενός μηχανισμοί. Αν οι μηχανισμοί αυτοί συμβαίνουν παράλληλα τότε ο ταχύτερος εξ αυτών καθορίζει τον ρυθμό της διεργασίας. Αν οι μηχανισμοί πραγματοποιούνται σε σειρά τότε ο βραδύτερος είναι αυτός ο οποίος καθορίζει τον ρυθμό κρυστάλλωσης Επίδραση Θερμοκρασίας Η θερμοκρασία είναι ένας από εκείνους τους παράγοντες που επηρεάζουν τον ρυθμό κρυσταλλικής ανάπτυξης. Ο ρυθμός καταβύθισης συνήθως αυξάνεται σε υψηλότερες θερμοκρασίες, ενώ το σχήμα το μέγεθος και η μορφολογία των κρυστάλλων επίσης επηρεάζονται από την θερμοκρασία. 61
88 Κατά την κρυστάλλωση η σχέση μεταξύ της σταθεράς ταχύτητας της καταβύθισης, k p και της απόλυτης θερμοκρασίας Τ, δίνεται από εξίσωση τύπου Arrhenius, κατ αναλογία προς τις ομογενείς χημικές αντιδράσεις : d ln k p E 2 (2-61) dt RT όπου Ε η ενέργεια ενεργοποίησης για την αντίδραση καταβύθισης. Ολοκληρώνοντας την (2-61) προκύπτει η πιο συνηθισμένη μορφή της εξίσωσης: k p E Aexp( ) (2-62) RT όπου Α η σταθερά Arrhenius. Λογαριθμίζοντας την εξίσωση (2-62) προκύπτει η: E 1 ln k p ln A (2-63) R T Από την (2-63) προσδιορίζεται η ενέργεια ενεργοποίησης της αντίδρασης. Η γραφική παράσταση του λογαρίθμου της σταθεράς ταχύτητας της αντίδρασης k p έναντι της αντίστροφης απόλυτης θερμοκρασίας δίνει ευθεία γραμμή με κλίση E. Η ενέργεια R ενεργοποίησης η οποία προσδιορίζεται έτσι είναι φαινόμενη και παρέχει πληροφορίες για τον μηχανισμό της κρυσταλλικής ανάπτυξης που ακολουθείται αναλόγως της τάξεως μεγέθους της. Επιπλέον η ενέργεια ενεργοποίησης υπολογίζεται όταν είναι διαθέσιμες δύο σταθερές ταχύτητας k 1 και k 2 σε δυο διαφορετικές θερμοκρασίες Τ 1 και Τ 2. E T T T T 1 2 ln 1 ( ) R (2-64) 1 2 Όταν το καθορίζον την αντίδραση στάδιο είναι η μεταφορά μάζας από το διάλυμα προς την επιφάνεια του κρυστάλλου με διάχυση, τότε η τιμή της ενέργειας ενεργοποίησης κυμαίνεται μεταξύ KJ mol -1. Όταν η επιφανειακή διάχυση είναι αυτή που καθορίζει την ταχύτητα τότε η τιμή της ενέργειας ενεργοποίησης κυμαίνεται μεταξύ KJ mol -1 [Liu and Nancollas, 1970]. Καθώς ο ρυθμός της επιφανειακής διάχυσης αυξάνεται πιο γρήγορα με την θερμοκρασία σε σχέση με τον ρυθμό διάχυσης από το διάλυμα, ο ρυθμός κρυσταλλικής ανάπτυξης ελέγχεται από τη διάχυση σε υψηλές θερμοκρασίες και από την επιφανειακή διάχυση σε χαμηλές θερμοκρασίες [Rumford and Bain, 1960]. k k 2 62
89 2.4.6 Επίδραση Παρουσίας Ξένων Ιόντων ή Ενώσεων (Επιμολύνσεις) Η διεργασία της κρυστάλλωσης επηρεάζεται σημαντικά από την παρουσία ξένων ιόντων ή ενώσεων στα υπέρκορα διαλύματα. Η παρουσία των επιμολύνσεων αυτών ακόμα και σε πολύ μικρές συγκεντρώσεις μεταβάλλει την ταχύτητα πυρηνογένεσης, τον ρυθμό κρυσταλλικής ανάπτυξης αλλά και την μορφολογία, το σχήμα ή το μέγεθος των σχηματιζόμενων κρυστάλλων. Κάθε ουσία διαφορετική από αυτή που κρυσταλλώνεται μπορεί να θεωρηθεί ως επιμόλυνση. Οι επιμολύνσεις επηρεάζουν τους ρυθμούς της κρυστάλλωσης είτε αλλάζοντας τις φυσικοχημικές ιδιότητες του διαλύματος αλλά και του στερεού προϊόντος, είτε μεταβάλλοντας τα χαρακτηριστικά της ηλεκτρικής διπλοστιβάδας που περιβάλλει τα σωματίδια των κρυστάλλων [Khamskii, 1979]. Οι επιμολύνσεις μπορούν επίσης να προσροφηθούν στα ενεργά κέντρα ή ακόμα και να σχηματίσουν ένα ξεχωριστό στρώμα στην επιφάνεια των αναπτυσσομένων κρυστάλλων το οποίο έχει ορισμένο προσανατολισμό και κρυσταλλογραφική συνάφεια με το υπόστρωμα. Σύμφωνα με το πρότυπο του Kossel υπάρχουν τρεις πιθανές θέσεις όπου οι επιμολύνσεις μπορούν να προσροφηθούν επιφέροντας αποδιοργάνωση στην κρυσταλλική ανάπτυξη του κρυστάλλου και μείωση του ρυθμού κρυσταλλικής ανάπτυξης [Davey, 1979]. Μερικές επιμολύνσεις προσροφούνται μη αντιστρεπτά ενώ τα προσροφούμενα μόρια παραμένουν στην επιφάνεια πρακτικώς ακίνητα. Σε άλλες περιπτώσεις τα προσροφούμενα μόρια διατηρούν ευκινησία και μπορούν να εκροφηθούν από την επιφάνεια. Έτσι λοιπόν, διακρίνονται δυο ακραίες περιπτώσεις αναλόγως των θέσεων προσροφήσεως: ευκίνητες επιμολύνσεις, οι οποίες προσροφούνται στις κόγχες ή στις ακμές και ακίνητες επιμολύνσεις οι οποίες προσροφούνται σε επίπεδες επιφάνειες των βαθμίδων. 63
90 Σχήμα 2.16: Θέσεις προσρόφησης επιμολύνσεων στην επιφάνεια του κρυστάλλου σύμφωνα με το πρότυπο του Kossel: (a) σε Κόγχη, (b) σε Ακμή και (c) σε Βαθμίδα. Η παρουσία επιμολύνσεων στο σύστημα επηρεάζει και την πυρηνογένεση είτε επιταχύνοντάς την, αν δράσουν ως ετερογενή υποστρώματα, είτε ανασταλτικά [Sarig and Kahara, 1976]. Στην δεύτερη περίπτωση η μείωση της ταχύτητας πυρηνογένεσης οφείλεται στον σχηματισμό σύμπλοκων ενώσεων με κάποιο από τα συστατικά του πυρήνα, ή στην προσρόφηση των επιμολύνσεων στην επιφάνεια του υποκρίσιμου πυρήνα αλλάζοντας την δομή του ή στην στερεοχημική παρεμπόδιση συστατικών που ενσωματώνονται στον πυρήνα. Οι μεταβολές στην ταχύτητα πυρηνογένεσης γίνονται αντιληπτές από ανάλογες μεταβολές στον χρόνο επαγωγής [Verdoes et al., 1992]. Τόσο στην πυρηνογένεση όσο και στην κρυσταλλική ανάπτυξη η διεπιφανειακή ενέργεια, γ s, μεταξύ σχηματιζόμενου κρυστάλλου και διαλύματος είναι εκείνη η θερμοδυναμική παράμετρος, η οποία εμφανίζεται σε όλα τα κινητικά πρότυπα και επηρεάζεται από φαινόμενα προσρόφησης. Η προσρόφηση μιας ένωσης στην επιφάνεια του κρυστάλλου μειώνει την διεπιφανειακή ενέργεια. Η μείωση της διεπιφανειακής ενέργειας έχει ως συνέπεια την μείωση του μεγέθους του κρίσιμου πυρήνα ή του δισδιάστατου πυρήνα ή της ακτίνας της σπείρας και τη μείωση της ελεύθερης ενέργειας Gibbs. Αποτέλεσμα της μείωσης της ελεύθερης ενέργειας είναι η αύξηση της ταχύτητας πυρηνογένεσης ή της κρυσταλλικής ανάπτυξης αντίστοιχα. Από τα παραπάνω προκύπτει ότι τα θεωρητικά πρότυπα της κρυσταλλικής αναπτύξεως προβλέπουν αντίθετες τάσεις των επιμολύνσεων στην κινητική της 64
91 κρυσταλλικής ανάπτυξης. Από θερμοδυναμική άποψη η ταχύτητα κρυσταλλικής ανάπτυξης τείνει να αυξηθεί ενώ από κινητική η προσρόφηση μειώνει την ταχύτητα. Η επιφανειακή συγκέντρωση της επιμόλυνσης, Γ μπορεί να προσδιοριστεί από την εξίσωση [Lyklema, 1995]: V ( Co Ceq ) W SSA (2-65) όπου V ο όγκος του διαλύματος, C o η συγκέντρωση της επιμόλυνσης πριν την προσρόφηση, C eq η συγκέντρωση της επιμόλυνσης στην ισορροπία δηλαδή μετά την προσρόφηση, W το βάρος και SSA η ειδική επιφάνεια του υποστρώματος. Η γραφική παράσταση της επιφανειακής συγκέντρωσης, Γ, έναντι της συγκέντρωσης ισορροπίας στο διάλυμα, C eq, σε σταθερή θερμοκρασία, δίνει την ισόθερμο προσρόφησης της επιμόλυνσης στο δεδομένο υπόστρωμα. Ανάλογα με τη θέση που καταλαμβάνουν τα προσροφημένα μόρια ή ιόντα στην διαφασική επιφάνεια κρυστάλλου διαλύματος καθώς και την συμπεριφορά τους στην θέση αυτή υπάρχουν αρκετά πρότυπα τα οποία ερμηνεύουν τα φαινόμενα προσρόφησης. Για την ερμηνεία των κινητικών αποτελεσμάτων και δεδομένου του ότι, η δράση των επιμολύνσεων εντοπίζεται στην προσρόφησή τους στην επιφάνεια των κρυστάλλων μπορεί να υιοθετηθεί το πρότυπο προσρόφησης Langmuir. Σύμφωνα με το πρότυπο αυτό, τα προσροφημένα μόρια σχηματίζουν επιφανειακό μονόστρωμα, δεν αλληλεπιδρούν μεταξύ τους, τα ενεργά κέντρα προσρόφησης του υποστρώματος είναι ενεργειακά ισοδύναμα και η προσρόφηση θεωρείται αντιστρεπτή. Οι ταχύτητες προσρόφησης και εκρόφησης δίνονται αντίστοιχα από τις εξισώσεις (2-66) και (2-67): J ad k C C C ) (2-66) ad ( m a J k C (2-67) des des a όπου k ad η σταθερά ταχύτητας προσρόφησης, C η συγκέντρωση της επιμόλυνσης στο διάλυμα, C m η συγκέντρωση που απαιτείται για να γίνει ένα μονόστρωμα, C α η εκάστοτε πραγματική συγκέντρωση της επιμόλυνσης και k des η σταθερά ταχύτητας εκρόφησης. 65
92 Στην κατάσταση ισορροπίας οι δύο ταχύτητες είναι ίσες οπότε προκύπτει: C C a kdes k C k m 1 ad aff C (2-68) Το κλάσμα των ενεργών θέσεων της επιφάνειας του κρυστάλλου που καλύπτεται από τις επιμολύνσεις, θ και η σταθερά συνάφειας, k aff ορίζεται από την εξ.(2-68). Η ταχύτητα της κρυσταλλικής ανάπτυξης, R i παρουσία επιμόλυνσης η οποία προσροφείται στην επιφάνεια του κρυστάλλου είναι μικρότερη από την ταχύτητα κρυσταλλικής ανάπτυξης, R ο, απουσία επιμόλυνσης λόγω δέσμευσης ορισμένων ενεργών κέντρων κρυστάλλωσης και δίνεται από έκφραση της μορφής [Nancollas and Zawacki, 1984]: R R R ( 1 b) (2-69) i o όπου b σταθερά (0<b<1). Συνδυάζοντας τις (2-69) και (2-68) προκύπτει το κινητικό πρότυπο για την κρυσταλλική ανάπτυξη με προσρόφηση Langmuir: R R R i o o 1 1 b k aff 1 (1 b) C o 1 (2-70) Η γραφική παράσταση του Ro R R i o συναρτήσει του αντιστρόφου της συγκέντρωσης της 1 1 επιμόλυνσης στο υπέρκορο διάλυμα,, δίνει ευθεία γραμμή με κλίση C k aff (1 b) και τεταγμένη επί την αρχή 1, από όπου υπολογίζεται η τιμή της σταθεράς συνάφειας 1 b k aff, η οποία αποτελεί μέτρο της συνάφειας της προσροφημένης επιμόλυνσης προς το υπόστρωμα [Koutsoukos, 1980]. Αν η τεταγμένη επί την αρχή είναι μεγαλύτερη της μονάδας τότε η επιμόλυνση προκαλεί μερική παρεμπόδιση της κρυσταλλικής ανάπτυξης ακόμα και σε υψηλές συγκεντρώσεις. Στην περίπτωση αυτή είναι δυνατόν να παρατηρηθούν αλλαγές στην μορφολογία του αναπτυσσόμενου κρυστάλλου καθώς αναπτύσσονται οι έδρες εκείνες με τις οποίες οι αλληλεπιδράσεις της επιμόλυνσης είναι μικρότερες. Αν η τεταγμένη επί την αρχή είναι μικρότερη της μονάδας τότε η επιμόλυνση προκαλεί πλήρη παρεμπόδιση της κρυσταλλικής ανάπτυξης ακόμα και σε συγκεντρώσεις μικρότερες από την απαιτούμενη για πλήρη μονοστρωματική κάλυψη της κρυσταλλικής επιφάνειας. 66
93 Εκτός από το πρότυπο προσρόφησης Langmuir χρησιμοποιούνται επίσης τα πρότυπα Freundlich και Temkin. Η υπόθεση εργασίας στο πρότυπο προσρόφησης Freundlich είναι, ότι οι επιφάνειες είναι ετερογενείς και ότι η ενέργεια ρόφησης μειώνεται με αύξηση της κάλυψης της επιφάνειας. Η γραμμικοποιημένη της μορφή είναι αυτή που χρησιμοποιείται συνήθως και δίνεται από την: 1 log log K logc eq (2-71) n Το πρότυπο προσρόφησης Temkin λαμβάνει υπόψη και την μείωση της ενέργειας ρόφησης με την κάλυψη της επιφάνειας, καθώς η εμφάνιση μεγίστου στην προσρόφηση αντιστοιχεί στον σχηματισμό μονοστρώματος και εκφράζεται από την εξίσωση: A ln C B (2-72) eq 2.5 ΔΕΥΤΕΡΟΓΕΝΕΙΣ ΔΙΕΡΓΑΣΙΕΣ Αρκετές δευτερογενείς διεργασίες, οι οποίες ακολουθούν την πυρηνογένεση και την κρυσταλλική ανάπτυξη, επιδρούν σημαντικά στις τελικές φυσικές και χημικές ιδιότητες της καταβυθιζόμενης φάσης κατά την παραμονή της στο μητρικό υγρό. Στις κυριότερες δευτερογενείς διεργασίες συγκαταλέγονται, η ωρίμανση, η ανακρυστάλλωση και η συσσωμάτωση [Söhnel and Garside, 1992]. Η ωρίμανση επιφέρει μικροσκοπικές ή και μακροσκοπικές αλλαγές στην καταβυθιζόμενη φάση και είναι από τις πιο αργές δευτερογενείς διεργασίες. Κατά την ωρίμανση αλλάζουν τα μορφολογικά χαρακτηριστικά των κρυστάλλων, η ειδική επιφάνεια και πολλές φορές και η χημική σύσταση του στερεού. Η ανακρυστάλλωση επιφέρει αλλαγές στο μέγεθος και στο σχήμα των κρυστάλλων μέσω του μηχανισμού της επιφανειακής αντίδρασης ή της μεταφοράς μάζας από την υγρή φάση. Ανάλογα με τις συνθήκες διακρίνεται σε ισοθερμική και μη ισοθερμική ανακρυστάλλωση. Η ισοθερμική χαρακτηρίζεται από μετατόπιση της κατανομής του μεγέθους των κρυστάλλων. Έτσι μεγαλύτεροι κρύσταλλοι αναπτύσσονται εις βάρος των μικρότερων οι οποίοι βαθμιαία διαλύονται ώσπου τελικά εξαφανίζονται. Η διαδικασία της ανακρυστάλλωσης λαμβάνει χώρα σχετικά γρήγορα. Κατά την συσσωμάτωση, μεμονωμένα μικρά σωματίδια συσσωρεύονται σε πλειάδες και σχηματίζουν μεγαλύτερα σωματίδια. Ο ρυθμός με τον οποίο 67
94 συσσωματώνονται τα σωματίδια και συνεπώς η σταθερότητα του συστήματος εξαρτώνται από το είδος των δυνάμεων μεταξύ των σωματιδίων. Ο συνολικός αριθμός των σωματιδίων και η ειδική επιφάνεια του αντίστοιχου πολυκρυσταλλικού υλικού, μειώνονται κατά την συσσωμάτωση. Για ορισμένες εφαρμογές η κύρια απαίτηση για τα συσσωματωμένα σωματίδια είναι να συγκροτούν μια χαλαρή διάταξη η οποία να μπορεί εύκολα να διαλύεται, όπως απαιτείται σε φαρμακευτικά παρασκευάσματα, ενώ σε άλλες εφαρμογές μια πιο πυκνή δομή απαιτείται η οποία παρέχει μια πιο αργή αποδέσμευση αυτών, όπως στα λιπάσματα [Jones, 2002]. 2.6 ΔΙΑΛΥΣΗ Η διάλυση θεωρείται η αντίστροφη διεργασία της κρυστάλλωσης, κατά την οποία οι δομικές μονάδες του κρυσταλλικού στερεού αποδομούνται, παρέχοντας στο διάλυμα ιόντα, αυξάνοντας συνεχώς την συγκέντρωσή τους, μέχρι κορεσμού του διαλύματος, δηλαδή, έως ότου η συγκέντρωση του διαλυμένου στερεού εξισωθεί με τη διαλυτότητά του. Στο διάγραμμα διαλυτότητας του σχήματος 2.1, διακρίνεται η σταθερή περιοχή, κάτω από την καμπύλη διαλυτότητας, όπου το διάλυμα είναι ακόρεστο. Στην περιοχή αυτή υπάρχει μόνο η υγρή φάση, ενώ η εισαγωγή κρυσταλλικού στερεού ενεργοποιεί τη διαδικασία της διάλυσης. Η κινητήρια δύναμη για τη διάλυση είναι η μεταβολή της ελεύθερης ενέργειας Gibbs, για την μετάβαση του διαλύματος από την ακόρεστη κατάσταση στην κατάσταση ισορροπίας, δηλαδή στο κορεσμένο διάλυμα. Η κινητήρια δύναμη ισούται με τη διαφορά των χημικών δυναμικών της διαλυμένης ουσίας στο υδατικό ακόρεστο διάλυμα και της αντίστοιχης στο κορεσμένο διάλυμα. Κατ αναλογία με την διεργασία της κρυστάλλωσης ορίζεται η ακορεστότητα, Ω, ως ο λόγος του ιοντικού γινομένου των ενεργοτήτων προς το θερμοδυναμικό γινόμενο διαλυτότητας: IP K και η σχετική ακορεστότητα δίνεται αντίστοιχα από την σχέση: 0 sp 1/ (2-73) 1/ 1 (2-74) Η ακορεστότητα Ω αποτελεί μέτρο της απόκλισης από την κατάσταση ισορροπίας. Όταν Ω < 1 το διάλυμα είναι ακόρεστο. Όσο πιο μακριά από την 68
95 κατάσταση ισορροπίας, δηλαδή όσο πιο μικρή η τιμή της ακορεστότητας Ω, τόσο πιο έντονο είναι το φαινόμενο της διάλυσης και τόσο μεγαλύτερη η ταχύτητά του Μηχανισμοί διάλυσης κρυσταλλικών αλάτων Όπως προαναφέρθηκε, η διάλυση είναι δυνατόν να θεωρηθεί ως διεργασία, αντίστροφη της κρυστάλλωσης. Κατά την διάλυση, οι κρύσταλλοι χάνουν δομικές μονάδες (διαλύονται). Στην πράξη, οι σχετικές μετρήσεις έχουν δείξει ότι οι κρύσταλλοι αποδομούνται με ταχύτερους ρυθμούς σε σύγκριση με τους αντίστοιχους ρυθμούς ανάπτυξής τους [Mullin, 2001]. Οι θεωρίες οι οποίες αναπτύχθηκαν για την κρυσταλλική ανάπτυξη εφαρμόζονται και στην περίπτωση της διάλυσης. Έτσι κατά την αποδόμηση/ διάλυση ενός κρυστάλλου, αποκολλώνται αρχικά οι δομικές μονάδες από τα ενεργά κέντρα και αφού ενυδατωθούν μερικώς, διαχέονται στο επιφανειακό στρώμα προσρόφησης. Στη συνέχεια, ακολουθεί εκρόφηση από το στρώμα προσρόφησης και διάχυση των μορίων του διαλύτη προς την επιφάνεια και ολική ενυδάτωση της δομικής μονάδας. Τέλος, μεταφέρεται η διαλυμένη ουσία στην κύρια μάζα του διαλύματος μέσω του οριακού στρώματος που περιβάλλει τον κρύσταλλο. Η διεργασία της διάλυσης αρχίζει σε εκείνα τα σημεία του κρυστάλλου στα οποία υπάρχουν ατέλειες. Κατά τις θεωρίες ελαχιστοποίησης της επιφανειακής ενέργειας οι έδρες με υψηλότερες τιμές δεικτών Miller διαλύονται ταχύτερα και αποκτούν μεγαλύτερη επιφάνεια. Σύμφωνα με τις θεωρίες προσρόφησης στρώματος, κατά την διάλυση, η αποδόμηση γίνεται με τη συνεχή απομάκρυνση δομικών μονάδων από τα ενεργά κέντρα. Όταν ένα κρυσταλλικό επίπεδο εξαφανίζεται, υπάρχει πιθανότητα από το επόμενο στρώμα να αποκολληθεί μια δομική μονάδα δημιουργώντας μια οπή. Η οπή αυτή έχει την πιθανότητα να αναπτυχθεί περισσότερο με περαιτέρω αποκόλληση δομικών μονάδων ακολουθώντας τα πρότυπα της κρυσταλλικής ανάπτυξης, κατ αντίστροφο τρόπο. 69
96 Σχήμα 2.17: Σχηματική αναπαράσταση αποδόμησης / διάλυσης ενός κρυστάλλου, δομική μονάδα, μόρια νερού. Όταν η μεταφορά και η διάχυση των δομικών μονάδων στο στρώμα προσρόφησης είναι το καθορίζον τη διάλυση στάδιο, τότε η κινητική της διάλυση ελέγχεται από την διάχυση. Όταν τα υπόλοιπα στάδια της διάλυσης που αναφέρθηκαν, καθορίζουν την ταχύτητά της, τότε η κινητική της διάλυσης χαρακτηρίζεται ως ελεγχόμενη από διαδικασίες επιφανειακών αντιδράσεων. Η εξίσωση που περιγράφει την κινητική της διάλυσης ενός κρυστάλλου, διαλυτότητας C s, σε ακόρεστα διαλύματά του, έχει την γενική μορφή: dc dt K C C s n dis ( ) (2-75) Ο ρυθμός διάλυσης συναρτήσει της σχετικής ακορεστότητας είναι : R n diss Kdiss s (2-76) όπου n η φαινόμενη τάξη της ταχύτητας διάλυσης, σ η σχετική ακορεστότητα, K diss η σταθερά διάλυσης και s μια συνάρτηση του αριθμού των ενεργών κέντρων των κρυστάλλων. Οι σταθερές διάχυσης και αντίδρασης υπολογίζονται σύμφωνα με την θεωρία διάχυσης, η οποία αναπτύχθηκε στην 2.4. Από την τάξη της αντίδρασης αντλούνται πληροφορίες για τον μηχανισμό της διάλυσης. Συγκεκριμένα για: n = 1 η διάλυση ελέγχεται από διάχυση n > 1 ελέγχεται από επιφανειακή αντίδραση. 70
97 ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟΥ 2 Aylward G. and Findlay T., SI Chemical Data, 5 th Edition, John Wiley and Sons: Australia, (2002) Bauer E., Phänomenologische Theorie der Kristallabscheidung an Oberflächen I-II, Zeitschrift für Kristallographie, 110, pp , (1958) Botsaris G.D., Industrial Crystallization, J.W. Mullin (ed.), Plenum Press: New York (1976) Burton W.K., Cabrera N. and Frank F.C., The growth of crystals and the equilibrium structure of their surfaces, Phil. Trans. A, 243, pp , (1951) Christiansen J.A. and Nielsen A.E., Kinetic determination of the size of crystal germs, Acta Chemica Scandinavica, 5, pp , (1951) Davey R.J., The control of Crystal Habit: In Industrial Crystallization 1978, S.J. Jancic, E.J. de Jong (eds.), North Holland Pub. Co: Amsterdam, (1979) Davies C.W., Ion Association, Butterworths: Washington, (1962) Dorozhkin S.V. and Epple M., Review: Biological and Medical Significance of Calcium Phosphates, Angew. Chem. Int. Ed., 41, pp , (2002) Freche M., PhD thesis, Institute Nationale Polytechnique de Toulouse, (1989) Gardner G.L., Nucleation and crystal growth of calcium oxalate trihydrate, Journal of Crystal Growth, 30, pp , (1975) Gibbs J.W., Collected Works: Thermodynamics, vol. I, Yale University Press: New Haven, (1948) Herman M.A., Crystallization of epitaxial layers: Fundamentals in elementary crystal growth, K. Sangwal ed., Saan Publishers: Lublin, chap. 12, pp , (1994) Hillig W.B., A derivation of classical two-dimensional nucleation kinetics and the associated crystal growth laws, Acta Metallurgica, 14, pp , (1966) Jones A.G., Crystallization Process Systems, Butterworths-Heinemann Ltd.: Oxford, (2002). Kashchiev D., Nucleation Basic Theory with Applications, Butterworths-Heinemann Ltd.: Oxford, (2000) Kashchiev D. and van Rosmalen G.M., Review: Nucleation in solutions revisited, Crystal Research Technology, 38, pp , (2003) Khamskii E.V., In Industrial Crystallization 1978, S.J. Jancic, E.J. de Jong (eds.), North Holland Pub. Co: Amsterdam, (1979) 71
98 Kossel W., Zur Energetik von Oberflächenvorgängen, Annalen der Physik, 21, pp , (1934) Koutsoukos P.G., Kinetics of precipitation of hydroxyapatite from aqueous solutions, PhD. Thesis, State University of New York at Buffalo, New York, (1980) Liu S-T and Nancollas G.H. The kinetics of crystal growth of calcium sulfate dehydrate. Journal of Crystal Growth, 6, pp , (1970) Lowenstamm H. and Weiner S., Biomineralization, Oxford Univ. Press: New York (1989) Lyklema J., Fundamentals of Interface and Colloid Science, Vol. 2, Academic Press: London, (1995) Matuchová M. and Nývlt J., Determination of linear growth rates of crystals. (I). Calculation of linear growth rates of individual crystal faces from overall rates, Kristall und Technik, 11, pp , (1976) Mullin J.W. and Ang H-M., Nucleation Characteristics of aqueous nickel ammonium sulphate solutions, Faraday Society Discussions, 61, pp , (1976) Mullin J.W., Crystallization, 4 th Edition, Butterworths-Heinemann Ltd.: Oxford (2001) Myerson A.S., Handbook of Industrial Crystallization, 2 nd Heinemann Ltd: Boston, (2002) Edition, Butterworths- Nancollas G.H. and Reddy M.M., The crystallization of calcium carbonate: II. Calcite growth mechanism, Journal of Colloid and Interface Science, 37, pp , (1971) Nancollas G.H. and Zawacki S.J., In Industrial Crystallization, vol. 84, S.J. Jancic, E.J. de Jong (eds.), Elsevier: Amsterdam, (1984) Nielsen A.E., Kinetics of Precipitation, Pergamon Press: Oxford, (1964) Nielsen A.E., Transport control in crystal growth from solution, Croatica Chemica Acta, 53, pp , (1980) Nývlt J., Söhnel O., Matuchova M. and Broul M., The kinetics of Industrial Crystallization, Elsevier: Amsterdam, (1985) Ohara M. and Reid R.C., Modeling Crystal Growth Rates from Solutions, Prentice-Hall, Englewood Cliffs: New Jersey, (1973) Palatnik L.S. and Papinov I.I., Epitaxial Films, Nauka Publisher: Moscow (1971) Robinson R.A and Stokes R.H., Electrolyte Solutions, 2 nd London, (1970) Edition, Butterworths: Royer L., Recherches expérimentales sur l epitaxie ou orientation muttuelle de cristaux d espés differentes, Bulletin Societe Francaise Mineralle, 51, pp , (1934) 72
99 Rumford F. and Bain J., The Controlled Crystallization of Sodium Chloride, Trans. Inst. Chem. Engrs London, 38, p. 10, (1960) Sangwal K., Kinetics and Mechanisms of Crystal Growth In Elementary Crystal Growth, K. Sangwal (ed.), Saan Publishers: Lublin, (1994) Sarig S. and Kahara F., On the association between sparingly soluble carbonates and polyelectrolytes, Journal of Crystal Growth, 35, pp , (1976) Sheftal N.N., Growth of crystals, Consultant Bureau: New York and London, vol. 10, pp , (1976) Söhnel O. and Mullin J.W., A method for the determination of precipitation induction periods, Journal of Crystal Growth, 44, pp , (1978) Söhnel O. and Garside G., Precipitation: Basic Principles and Industrial Applications, Butterworths-Heinemann: London, (1992) Stranskii I.N. and Krastanov L., Theory of orientation separation of ionic crystals, Sitzungsberichte der Kaiserlichen Akademie der Wissenschaften in Wien, 146, pp , (1938) Tavare N.S., Industrial Crystallization: Process Simulation Analysis and Design, Plenum Press: New York, (1995) Turnbull D., Kinetics of heterogeneous nucleation, Journal of Chemical Physics, 18, pp , (1950) Turnbull D. and Vonnegut B., Nucleation Catalysis, Industrial and Engineering Chemistry, 44, pp , (1952) Turnbull D., Solid State Physics, 3, p. 225, (1956) Verdoes D., Kashchiev D and van Rosmalen G.M., Determination of nucleation and growth rates from induction times in seeded and unseeded precipitation of calcium carbonate, Journal of Crystal Growth, 118, pp , (1992) Volmer M., Kinetik der Phasenbildung, T. Steinköpf Vlg: Leipsig and Dresden, (1939) Walton A.G., The Formation and Properties of Precipitates, Interscience Publishers: New York, (1967) Zemaitis J.F.Jr., Clark D.M., Rafal M. and Scrivner N.C., Handbook of Aqueous Electrolyte Thermodynamics, American Institute of Chemical Engineers: New York, (1986) 73
100 74
101 ΚΕΦΑΛΑΙΟ 3 ΤΟ ΣΥΣΤΗΜΑ ΤΟΥ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ 75
102 3.1 Εισαγωγή Το σύστημα του φωσφορικού ασβεστίου παρουσιάζει μεγάλο ενδιαφέρον και ταυτόχρονα πρόκειται για ένα πολύπλοκο σύστημα, αφού περιλαμβάνει περισσότερες της μιας φάσεις. Στο τριαδικό σύστημα Ca(OH) 2 -H 3 PO 4 -H 2 O, παρουσιάζονται στον πίνακα 3.1 έξι κρυσταλλικές φάσεις του φωσφορικού ασβεστίου καθώς και μία μη κρυσταλλική με διαφορετική γραμμομοριακή αναλογία ασβεστίου-φωσφόρου. Πίνακας 3.1: Φάσεις των αλάτων του φωσφορικού ασβεστίου: γραμμομοριακός λόγος ασβεστίου προς φωσφορικά και γινόμενα διαλυτότητας. Ονομασία Χημικός τύπος Συντομογραφία Ca/P K sp Άνυδρο δισόξινο φωσφορικό ασβέστιο CaHPO 4 DCPA 1,00 9.2x10-7 (mol L -1 ) 2 Διένυδρο δισόξινο φωσφορικό ασβέστιο CaHPO 4 2H 2 O DCPD 1, x10-7 (mol L -1 ) 2 β- φωσφορικό τριασβέστιο β-ca 3 (PO 4 ) 2 β-τcp 1,50 2.8x10-9 (mol L -1 ) 5 Φωσφορικό Οκτασβέστιο Ca 8 H 2 (PO 4 ) 6 5H 2 O OCP 1,33 2.5x10-99 (mol L -1 ) 16 Υδροξυαπατίτης Ca 10 (PO 4 ) 6 (OH) 2 ΗΑP 1,67 5.5x (moll -1 ) 18 Aνθρακικός απατίτης Ca 10 (PO4) 6-X (CO3) X (OH) 2 CAP Άμορφο Φωσφορικό Ασβέστιο Ca 10-u (HPO4) u (PO4) 6-u (OH) 2-u O<u<2 ΑCP Το DCPA, DCPD, β-tcp και το OCP αποτελούν πρόδρομες φάσεις του HAP, οι οποίες είναι δυνατόν να συμμετέχουν στη διαδικασία κρυστάλλωσης σύμφωνα με τον κανόνα του Ostwald. Οι φάσεις αυτές είναι θερμοδυναμικά ασταθείς και υδρολύονται 76
103 προς τον θερμοδυναμικά σταθερότερο HAP. Το άμορφο φωσφορικό ασβέστιο (ACP) είναι φάση του φωσφορικού ασβεστίου το χαρακτηριστικό της οποίας είναι η απουσία κρυσταλλικότητας ως προς τις ακτίνες Χ. Σε ένα υπέρκορο διάλυμα φωσφορικού ασβεστίου μπορούν να καταβυθιστούν μία ή και περισσότερες φάσεις αναλόγως των συνθηκών του διαλύματος. Η καταβυθιζόμενη φάση εξαρτάται από τη θερμοκρασία, τις συγκεντρώσεις των ιόντων φωσφόρου και ασβεστίου, το ph του διαλύματος καθώς επίσης και από την παρουσία ή όχι ξένων ιόντων στο διάλυμα. Στο διάγραμμα του σχήματος 3.1 που ακολουθεί, παρουσιάζονται οι ισόθερμες καμπύλες διαλυτότητας των διαφόρων κρυσταλλικών φάσεων του φωσφορικού ασβεστίου. Από τα διαγράμματα αυτά φαίνεται ότι το ποσό που διαλύεται στην ισορροπία εξαρτάται τόσο από το θερμοδυναμικό γινόμενο διαλυτότητος της ένωσης όσο και από το ph του διαλύματος. Όταν οι ισόθερμοι δύο στερεών τέμνονται, στο σημείο αυτό τα δύο στερεά είναι σε ισορροπία το ένα με το άλλο DCPD OCP βtcp HAP DCPA DCPD log [Ca] -3 DCPA -4 OCP HAP β-tcp ph Σχήμα 3.1: Διαγράμμα διαλυτότητας κρυσταλλικών φάσεων του φωσφορικού ασβεστίου για το τριαδικό σύστημα, Ca(OH) 2 H 3 PO 4 H 2 O, στους 37 o C. Μεταβολή του λογαρίθμου της συγκέντρωσης του ασβεστίου συναρτήσει του ph του διαλύματος. Η τιμή του ph, η θερμοκρασία και ο υπερκορεσμός του διαλύματος έχει βρεθεί ότι επηρεάζει τον σχηματισμό των διαφόρων φάσεων [Tung et al., 1988]. Σε διαλύματα 77
104 με τιμές ph μεταξύ 4 και 6 έχει βρεθεί πειραματικά ότι καταβυθίζεται κυρίως DCPD ενώ σε ph μεταξύ 6 και 7 η φάση που υπερισχύει είναι αυτή του OCP. Για ακόμα μεγαλύτερες τιμές του ph ( ) η φάση που καταβυθίζεται είναι αυτή του HAP. Επειδή το DCPD και το OCP είναι θερμοδυναμικά ασταθείς φάσεις, την δημιουργία των κρυστάλλων τους ακολουθεί η υδρόλυσή τους σε κρυσταλλικό HAP. Παρ όλ αυτά υπάρχουν ουσίες οι οποίες αναστέλλουν την διεργασία μετασχηματισμού με χαρακτηριστικό παράδειγμα το μαγνήσιο, το οποίο παρεμποδίζει την υδρόλυση του OCP. Κατά την κρυστάλλωση του φωσφορικού ασβεστίου έχει επίσης διαπιστωθεί αντικατάσταση των ιόντων του κρυσταλλικού πλέγματος από ξένα ιόντα. Έτσι είναι πιθανή η αντικατάσταση του ΟΗ - από ιόντα Cl - ή F -, των φωσφορικών από ανθρακικά η θειïκά ιόντα και του Ca 2+ από ιόντα Sr 2+, Mg 2+ και Na + [Salimi et al., 1984]. Το μέγεθος και η μορφολογία των κρυστάλλων των διαφόρων φάσεων του φωσφορικού ασβεστίου διαφέρoυν σημαντικά. Οι κρύσταλλοι DCPD διακρίνονται για το πλακοειδές σχήμα τους και για το μεγάλο τους μέγεθος το οποίο κυμαίνεται συνήθως μεταξύ των 10 έως 100 μm και το πάχος τους είναι της τάξης των 2-10 μm. Η μορφολογία των κρυστάλλων ΗΑΡ είναι συνήθως πρισματικοί επιμήκεις κατά τον άξονα c και είναι οι μικρότεροι σε μέγεθος, το οποίο μπορεί να κυμαίνεται από 200 nm έως 1 μm. Οι κρύσταλλοι του OCP παρουσιάζουν φυλλόμορφο ή πλακοειδές σχήμα και το μέγεθος τους κυμαίνεται μεταξύ του 1 έως 4 μm, ενώ το πάχος τους δεν ξεπερνά τα nm. Πολλά βιολογικά στερεά, όπως τα οστά και τα δόντια, καθώς επίσης και οι παθολογικές εναποθέσεις σε βαλβίδες καρδιάς και αρτηρίες, περιέχουν άλατα φωσφορικού ασβεστίου ως κύριο συστατικό τους. Μεγάλη σημασία έχουν οι βιολογικοί απατίτες αφού, με εξαίρεση κάποιους μικρούς σχηματισμούς σκληρών ιστών στα αυτιά, όλοι οι υπόλοιποι φυσικοί σκληροί ιστοί είναι κυρίως απατιτικοί [Dorozhkin and Epple, 2002]. Στην παρούσα εργασία, μεταξύ των κρυσταλλικών φάσεων του φωσφορικού ασβεστίου, το ενδιαφέρον επικεντρώθηκε κατά κύριο λόγο στο φωσφορικό οκτασβέστιο (OCP), στον υδροξυαπατίτη (HAP) και σε βιολογικούς απατίτες, άλατα μεγάλου βιολογικού ενδιαφέροντος λόγω της παρουσίας τους σε ιστούς και βιολογικούς σχηματισμούς. 78
105 3.2 Υδροξυαπατίτης (ΗΑΡ), Ca 5 (PO 4 ) 3 OH O υδροξαπατίτης αποτελεί τη θερμοδυναμικά σταθερότερη φάση των αλάτων του φωσφορικού ασβεστίου. Είναι ελάχιστα διαλυτός και κρυσταλλώνεται στο εξαγωνικό σύστημα, όπως φαίνεται και στο σχήμα 3.2. Από βιολογικής άποψης, αποτελεί ένωση με μεγάλο ενδιαφέρον δεδομένου του ότι συνιστά το κύριο ανόργανο συστατικό των σκληρών ιστών των ανώτερων θηλαστικών. Εκτός της ευεργετικής λειτουργικής δημιουργίας του, υπάρχει και ο παθολογικός σχηματισμός του ΗΑΡ, όπως στις περιπτώσεις των νεφρικών λίθων και των εναποθέσεων στις βαλβίδες καρδιάς. Θα πρέπει να σημειωθεί ότι άλατα του φωσφορικού ασβεστίου, και σε πολλές περιπτώσεις αναλόγως των τοπικών συνθηκών με την μορφή του ΗΑΡ αποτελούν στα εδάφη την πηγή του φωσφόρου, απαραίτητη για τα φυτά. Διαστάσεις μοναδιαίας κυψελίδας: a=9.360, b=9.360, c=6.860 Å u z u y y x x Σχήμα 3.2: Το κρυσταλλογραφικό σύστημα του ΗΑΡ με τα στοιχεία συμμετρίας σε (i)προοπτική, (ii) στερεογραφική προβολή και (iii) ένα σχέδιο του κρυστάλλου με τους δείκτες Miller των κυριότερων εδρών. 79
106 3.3 Φωσφορικό οκτασβέστιο (ΟCP), Ca 8 H 2 (PO 4 ) 6 5H 2 O Το φωσφορικό οκτασβέστιο αποτελεί θερμοδυναμικά ασταθή και πρόδρομη φάση του φωσφορικού ασβεστίου, η οποία υδρολύεται προς τον θερμοδυναμικά σταθερότερο ΗΑΡ, ενώ κρυσταλλώνεται στο τρικλινές σύστημα. Διαστάσεις μοναδιαίας κυψελίδας: a=19.715, b=9.534, c=6.839 Å Σχήμα 3.3. Απεικόνιση του τρικλινούς συστήματος: (α) τρισδιάστατη απεικόνιση, (β) διδιάστατη απεικόνιση (ο κύκλος παριστάνει το κατοπτρικό επίπεδο), (γ) ένα σχέδιο του κρυστάλλου με τους δείκτες Miller των κυριότερων εδρών. Σχηματισμοί ΟCP εμφανίζονται, κυρίως ως αποτέλεσμα παθολογικής ασβεστοποίησης σε βαλβίδες καρδιάς, και ως το βασικό κρυσταλλικό συστατικό της πέτρας των δοντιών όπου και συνήθως συνυπάρχει με τον ΗΑΡ. Η μετατροπή του ΟCP σε ΗΑΡ, αποτελεί μια εξήγηση της μη ανίχνευσής του στην οδοντίνη, στην αδαμαντίνη και στο ανόργανο τμήμα του οστού. Ένας επιπλέον παράγοντας που συμβάλει στη σπανιότερη εύρεσή του στα βιολογικά συστήματα αποτελεί η ομοιότητα των κρυστάλλων του με τους κρυστάλλους του υδροξυαπατίτη, καθιστώντας την παρουσία μικρής ποσότητας κρυστάλλων ΟCP, μη ανιχνεύσιμη [Βrown et al., 1962 ; Βrown et al., 1979]. Οι κρύσταλλοι του ΟCP αποτελούνται από δύο ευδιάκριτα εναλλασσόμενα στρώματα, εκ των οποίων το ένα έχει δομή παρόμοια με αυτή του ΗΑΡ και το άλλο αποτελείται από πιο ευρέως διατεταγμένα ιόντα ασβεστίου και φωσφορικά ανιόντα με διεσπαρμένα μόρια νερού. Η ομοιότητα μεταξύ της δομής των κρυστάλλων του OCP και του HAP ενισχύει την άποψη σύμφωνα με την οποία το OCP αποτελεί πρόδρομη φάση στην καταβύθιση του HAP στο σχηματισμό πολλών αλάτων φωσφορικού ασβεστίου σε βιολογικούς σχηματισμούς και εναποθέσεις [Brown et al., 1987]. 80
107 3.4 Διένυδρο Φωσφορικό διασβέστιο (DCPD), CaHPO 4 2H 2 O Το Διένυδρο Φωσφορικό Διασβέστιο (DCPD) είναι γνωστό και με το όνομα βρουσίτης, και αποτελεί την πιο ευδιάλυτη φάση από τα άλατα του φωσφορικού ασβεστίου. Η δομή του DCPD είναι σχεδόν η ίδια με αυτή του γύψου, με παρόμοιες διαστάσεις μοναδιαίας κυψελίδας, και κρυσταλλώνεται στο μονοκλινές σύστημα. Το DCPD αποτελείται από παράλληλα συνδεδεμένες αλυσίδες ομάδων CaPO 4 επίπεδα διατεταγμένες, με μόρια νερού μεταξύ των επιπέδων. Η παρουσία του έχει διαπιστωθεί σε δείγματα πέτρας των δοντιών (ηλικίας 3 ημερών), σε οστά ηλικίας 800 ετών καθώς και σε οστά εμβρύων [Roufosse et al.,1979]. Το DCPD αποτελεί ασταθή θερμοδυναμικά και πρόδρομη φάση του φωσφορικού ασβεστίου η οποία μετατρέπεται σε υδροξυαπατίτη. Έχει μάλιστα διατυπωθεί η άποψη ότι αποτελεί τον κρίσιμο πυρήνα για τον σχηματισμό φωσφορικών και οξαλικών νεφρικών λίθων [Pak et al., 1971]. Επίσης, έχουν αναφερθεί χρήσεις του DCPD ως συστατικού σε φάρμακα και οδοντόπαστες ως πηγής χορήγησης ασβεστίου σε ασθενείς [Ohta and Tsutsumi, 1982]. Διαστάσεις μοναδιαίας κυψελίδας: a=5.812, b=15.180, c=6.239 Å Σχήμα 3.4: Απεικόνιση του μονοκλινούς συστήματος: (α) τρισδιάστατη απεικόνιση, (β) διδιάστατη απεικόνιση (ο κύκλος παριστάνει το κατοπτρικό επίπεδο) και (γ) ένα σχέδιο του κρυστάλλου με τους δείκτες Miller των κυριότερων εδρών. 81
108 ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟΥ 3 Brown W.E., Smith J.P., Lehr J.R. and Frazier A.W., Octacalcium phosphate and hydroxyapatite, Nature, 196, pp , (1962) Brown W.E., Schroeder L.W. and Ferris J.S., Interlayering of crystalline octacalcium phosphate and hydroxyapatite, Journal of Physical Chemistry, 83, pp , (1979) Brown W. E., N. Eidelman and B. B. Tomazic, Octacalcium Phosphate as a Precursor in Biomineral Formation, Adv. Dent. Res, 1, pp , (1987) Dorozhkin S.V. and Epple M., Review: Biological and Medical Significance of Calcium Phosphates, Angew. Chem. Int. Ed., 41, pp , (2002) Ohta M. and Tsutsumi M., The relationship between the morphology of brushite crystals grown rapidly in silica gel and its structure, Journal of Crystal Growth, 56, pp , (1982) Pak C.Y.C., Eanes E.D. and Ruskin B., Spontaneous precipitation of brushite in urine: evidence that brushite is the nidus of renal stones originating as calcium phosphate, Proc Natl Acad Sci USA, 68, pp , (1971) Roufosse A.H., Landis W.J., Sabine W.K. and Glimcher M.J., Identification of brushite in newly deposited bone mineral from embryonic chicks, Journal of Ultrastructure Research, 68, pp , (1979) Salimi M.H., Heughebaert J.C. and Nancollas G.H, Crystal Growth of Calcium Phosphates in the presence of Magnesium Ions, Langmuir, 1, pp , (1985) Tung M.S., Eidelman N., Sieck B. and Brown W.E., Octacalcium phosphate solubility product from 4 to 37 o C, Journal of Research of the National Bureau of Standards, 93, pp , (1988) 82
109 83
110 ΚΕΦΑΛΑΙΟ 4 ΦΥΣΙΚΟΧΗΜΙΚΟΣ ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΑΣΒΕΣΤΟΥΧΩΝ ΕΝΑΠΟΘΕΣΕΩΝ ΑΠΟ ΒΑΛΒΙΔΕΣ ΚΑΡΔΙΑΣ 84
111 Όπως αναφέρθηκε και στο Κεφάλαιο 1, η βιολογική ασβεστοποίηση σε καρδιακές βαλβίδες αποτελεί μείζονα αιτία πρωτοπαθούς ανεπάρκειας τόσο των φυσικών όσο και των βιοπροσθετικών βαλβίδων καρδιάς που οδηγεί στην αναγαία χειρουργική αντικατάστασή τους (Σχήμα 4.1). Σχήμα 4.1: Ασβεστοποιημένες βαλβίδες ασθενών: (α) φυσική και (β) βιοπροσθετική. Στην παρούσα μελέτη εξετάστηκαν παθολογικές εναποθέσεις που απομονώθηκαν από 20 ανθρώπινες φυσικές και 9 βιοπροσθετικές βαλβίδες καρδιάς. Οι ασβεστοποιημένοι ιστοί από ανθρώπινες φυσικές βαλβίδες παραχωρήθηκαν από την 85
112 καρδιοχειρουργική κλινική του Τζάννειου Νοσοκομείου Πειραιώς από την ομάδα του Καθηγητού κ. Στεφάνου Φούσσα και οι βιοπροσθετικές βαλβίδες καρδιάς από το πρόγραμμα COST 537 (SEPA). Αρχικά πραγματοποιήθηκε κατεργασία των βαλβίδων καρδιάς με χρήση υδραζίνης για την απομάκρυνση του οργανικού μέρους [Τermine et al., 1973]. Στη συνέχεια οι εναποθέσεις που απομονώθηκαν (ανόργανο μέρος), ξεπλύθηκαν πολύ καλά με ορό, ξηράνθηκαν και κονιοποιήθηκαν. Ακολούθησε ταυτοποίηση της κρυσταλλικής φάσης που είχε εναποτεθεί τόσο στις φυσικές όσο και στις και βιοπροσθετικές βαλβίδων καρδιάς με περίθλαση ακτίνων Χ (XRD) και φασματοσκοπία υπερύθρου (FT-IR) καθώς και μορφολογική εξέταση με ηλεκτρονική μικροσκοπία σάρωσης (SEM). Στο σχήμα 4.2 απεικονίζεται το περιθλασιόγραμμα ακτίνων-χ της κρυσταλλικής εναπόθεσης βιοπροσθετικής βαλβίδας ασθενούς και το περιθλασιόγραμμα ακτίνων-χ συνθετικού OCP το οποίο ελήφθη από την κρυσταλλογραφική βάση δεδομένων Search Match (Αρ. Κάρτας ). Από την ταύτιση των κύριων χαρακτηριστικών ανακλάσεων του OCΡ, εξήχθη το συμπέρασμα ότι η εναπόθεση αποτελείτο από φωσφορικό οκτασβέστιο Intensity/ a.u Σχήμα 4.2: Περιθλασιογράμματα κόνεως ακτίνων-χ 1: κρυσταλλικής εναπόθεσης σε βιοπροσθετική βαλβίδα ασθενούς και 2: συνθετικού φωσφορικού οκτασβεστίου (OCΡ) (Αρ. Κάρτας ). 86
113 Στην περίπτωση εναποθέσεων σε φυσική βαλβίδα η φάση που ταυτοποιήθηκε ήταν αυτή του υδροξυαπατίτη, όπως φαίνεται και στο σχήμα Intensity/ a.u Σχήμα 4.3: Περιθλασιογράμματα κόνεως ακτίνων-χ 1: κρυσταλλικής εναπόθεσης σε φυσική βαλβίδα ασθενούς και 2: συνθετικού υδροξυαπατίτη (ΗΑΡ) (Αρ. Κάρτας 9-432). Ο χαρακτηρισμός των παθολογικών εναποθέσεων πραγματοποιήθηκε και με φασματοσκοπία υπερύθρου. Στο πρώτο φάσμα (σχήμα 4.4 (α)) επιβεβαιώθηκε η παρουσία OCP στις εναποθέσεις που απομονώθηκαν από βιοπροσθετική βαλβίδα, αφού, όπως φαίνεται και σε μεγέθυνση στο σχήμα 4.4 (β), ήταν δυνατή η διάκριση της χαρακτηριστικής ζώνης απορρόφησής του στα 917 cm -1 [Fowler et al, 1993]. Στο φάσμα διακρίνονται, επίσης, οι ζώνες απορρόφησης στα 560 cm -1 και 600 cm -1, οι οποίες αντιστοιχούν στην εκφυλισμένη δόνηση κάμψης (ν 4 ) των δεσμών Ο-Ρ-Ο. Η κορυφή στα 861 cm -1 αποδίδεται στη συμμετρική δόνηση τάσης (ν 5 ) του δεσμού Ρ-Ο(Η) της όξινης φωσφορικής ομάδας, ενώ η κορυφή στα 962 cm -1 οφείλεται στη συμμετρική δόνηση τάσης (ν 1 ) του δεσμού Ρ-Ο της φωσφορικής ομάδας ΡΟ 4. Οι ζώνες απορρόφησης στα 1642 cm -1 και 3400 cm -1 αποδίδονται σε δόνηση κάμψης και δόνηση τάσης του υδρογόνου των μορίων του Η 2 Ο αντίστοιχα[fowler et al, 1993]. Στην περίπτωση των παθολογικών εναποθέσεων σε φυσική βαλβίδα καρδιάς ταυτοποιήθηκε η ύπαρξη ανθρακικών ιόντων από τις ζώνες απορρόφησης στα 1420 cm - 1 και 1465 cm -1, χαρακτηριστικές στους ανθρακικούς απατίτες τύπου Β, καθώς και η 87
114 ζώνη απορρόφησης στα 873 cm -1 η οποία εμφανίζεται σε ανθρακικούς απατίτες (σχήμα 4.4 (γ)) [Χu et al., 2001]. Οι ζώνες απορρόφησης στα 565 cm -1 και 602 cm -1 αποδίδονται στην τριπλώς εκφυλισμένη δόνηση κάμψης (ν 4 ) των δεσμών Ο-Ρ-Ο, ενώ αυτή στα 1046 cm -1 οφείλεται στην τριπλώς εκφυλισμένη ασύμμετρη δόνηση τάσης (ν 3 ) του δεσμού Ρ- Ο της φωσφορικής ομάδας. Οι κορυφές απορρόφησης στα 1642 cm -1 και 3440 cm -1 οφείλονται στη δόνηση κάμψης ν 2, μορίων νερού και σε προσροφημένα μόρια ύδατος, αντίστοιχα [Fowler, 1974]. ιαπερατότητα % HPO 2_ OH- OH- PO 3-4 PO Κυματάριθμος/ cm -1 ιαπερατότητα % Κυματάριθμος/ cm -1 88
115 ιαπερατότητα % CO 2-3 CO 2-3 OH - OH - PO 3-4 PO Κυματάριθμος/ cm -1 Σχήμα 4.4: Φάσματα υπερύθρου παθολογικών εναποθέσεων (α) σε βιοπροσθετική βαλβίδα καρδιάς, (β) μεγέθυνση φάσματος και (γ) σε φυσική βαλβίδα καρδιάς. Επιπλέον, πραγματοποιήθηκε θερμική ανάλυση των παθολογικών εναποθέσεων με την θερμοσταθμική μέθοδο (TGA), με ρυθμό θέρμανσης 2 o C min -1 και σε ατμόσφαιρα αζώτου. Οι μεταβολές του βάρους των δειγμάτων συναρτήσει της θερμοκρασίας, επιβεβαίωσαν την παρουσία ανθρακικών ιόντων στις εναποθέσεις. Στο σχήμα 4.5 παρουσιάζεται ενδεικτικά ένα γράφημα της θερμοσταθμικής ανάλυσης εναποθέσεων από ασβεστοποιημένη φυσική βαλβίδα καρδιάς. Στη θερμοκρασιακή περιοχή o C συμβαίνει απώλεια νερού, ενώ στην περιοχή θερμοκρασιών o C καίγεται το οργανικό μέρος που μπορεί να έχει παραμείνει. Από τους 400 o C o C χάνονται τα ανθρακικά ιόντα που πιθανόν υπάρχουν στο στερεό [Tadic and Epple, 2004]. Η ανάλυση των δειγμάτων έδειξε στους 75 o C ποσοστό απώλειας της παρουσίας υγρασίας 6%, στους 302 o C απώλεια οργανικού μέρους ποσοστού 8% και στους 740 o C ποσοστό απώλειας ανθρακικών 2%. Το ποσοστό περιεκτικότητας σε ανθρακικά από την εξέταση όλων των δειγμάτων κυμάνθηκε μεταξύ 2-4%. Στη βιβλιογραφία έχουν αναφερθεί παρόμοιες τιμές για την περιεκτικότητα σε ανθρακικά (2-6%) και αναφέρεται πως όλοι οι βιολογικοί απατίτες είναι ανθρακικοί απατίτες [Dorozhkin and Epple, 2002]. 89
116 % Βάρος T/ O C Σχήμα 4.5: Γράφημα θερμοσταθμικής ανάλυσης εναποθέσεων από ασβεστοποιημένη φυσική βαλβίδα καρδιάς. Στη συνέχεια παρουσιάζονται φωτογραφίες ηλεκτρονικού μικροσκοπίου σάρωσης, των παθολογικών εναποθέσεων που απομονώθηκαν από τις ασβεστοποιημένες βαλβίδες καρδιάς. Στις φωτογραφίες του σχήματος 4.6 φαίνεται η μορφολογία των εναποθέσεων των βιοπροσθετικών βαλβίδων, στις οποίες φαίνεται παρατηρήθηκε ο σχηματισμός πλάκας DCPD μεγέθους > 10 μm (σχήμα 4.6 (α)) καθώς και πλακοειδείς σχηματισμοί OCP μεγέθους 3-4 μm (σχήμα 4.6 (β)) οι οποίοι, όπως φαίνεται στο σχήμα 7.6 (γ), συνυπήρχαν με απατιτικούς και ανθρακικούς απατιτικούς μικροκρυστάλλους (σχήμα 4.6 (δ)). Επιπλέον, παρατηρήθηκε η υδρόλυση πλακών OCP προς απατιτικούς πρισματικούς κρυστάλλους μεγέθους nm (σχήμα 4.6 (ε)-(ζ)). 90
117 91
118 Σχήμα 4.6: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης των εναποθέσεων που απομονώθηκαν από ασβεστοποιημένες βιοπροσθετικές βαλβίδες καρδιάς; (α) εμφάνιση πλακοειδούς κρυστάλλου DCPD, (β), (γ) πλακοειδείς σχηματισμοί OCP, (δ) απατιτικοί μικροκρυσταλλικοί σχηματισμοί και (ε), (στ), (ζ) υδρόλυση πλακών OCP προς απατιτικούς πρισματικούς κρυστάλλους. Όσον αφορά στις παθολογικές εναποθέσεις των φυσικών βαλβίδων καρδιάς, η μορφολογική τους εξέταση έδειξε το σχηματισμό πρισματικών απατιτικών κρυστάλλων μεγέθους nm (σχήμα 4.7 (α), (β)) καθώς και την ύπαρξη μη πρισματικών μικροκρυστάλλων ανθρακικού απατίτη (σφαιρικού σχήματος) μεγέθους nm (σχήμα 4.7 (γ), (δ)). Αξίζει να σημειωθεί ότι στις εναποθέσεις των ασβεστοποιημένων φυσικών βαλβίδων καρδιάς δεν παρατηρήθηκαν κρυσταλλίτες OCP. Στην περίπτωση αυτή, επειδή ο χρόνος παραμονής με τα βιολογικά ρευστά ήταν σαφώς μεγαλύτερος, είναι δυνατόν να υποτεθεί ότι, ακόμα και αν σχηματίσθηκε το ασταθέστερο OCP, υδρολύθηκε προς βιοαπατίτη. 92
119 Σχήμα 4.7: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης των εναποθέσεων που απομονώθηκαν από ασβεστοποιημένες φυσικές βαλβίδες καρδιάς; (α), (β) πρισματικοί απατιτικοί κρύσταλλοι και (γ), (δ) μη πρισματικοί απατιτικοί μικροκρυσταλλικοί σχηματισμοί. Οι τιμές της ειδικής επιφάνειας των παθολογικών εναποθέσεων, υπολογίσθηκαν από μετρήσεις ρόφησης αζώτου από τις ισοθέρμους BET. Οι τιμές που βρέθηκαν έδειξαν μεγάλες μεταβολές και ήσαν: 9 m 2 g -1, 15.4 m 2 g -1, 21 m 2 g -1, 29.5 m 2 g -1, 39.5 m 2 g -1, 46.7 m 2 g -1, 51 m 2 g -1, 63 m 2 g -1, 71 m 2 g -1. Η αιτία για την διακύμανση αυτή των τιμών, θα πρέπει να αναζητηθεί στο ιστορικό του σχηματισμού κάθε εναπόθεσης το οποίο δυστυχώς δεν ήταν διαθέσιμο. Από τη χημική ανάλυση των εναποθέσεων υπολογίστηκε ο λόγος των γραμμομοριακών συγκεντρώσεων Ca/P, ενώ ταυτοποιήθηκε η παρουσία ιόντων νατρίου αλλά όχι μαγνησίου. Στις βιοπροσθετικές βαλβίδες η τιμή του λόγου Ca/P = ήταν 1.55 ± 0.25, ενώ στην περίπτωση των φυσικών βαλβίδων ο λόγος των γραμμομοριακών συγκεντρώσεων ήταν υψηλότερος, Ca/P = 1.80 ± Οι χαμηλές τιμές του λόγου 93
120 Ca/P των βιοπροσθετικών βαλβίδων θα μπορούσαν να εξηγηθούν από τη μεγαλύτερη συνεισφορά των όξινων φάσεων, ενώ οι υψηλότερες τιμές του λόγου Ca/P των φυσικών βαλβίδων πιθανόν οφείλεται στο γεγονός ότι παρέμειναν στους ανθρώπινους οργανισμούς μεγαλύτερο χρονικό διάστημα με αποτέλεσμα την υδρόλυση των θερμοδυναμικά ασταθέστερων φάσεων προς απατιτικά στερεά. Επιπλέον, η παρουσία των ανθρακικών απατιτικών κρυστάλλων κυρίως στις εναποθέσεις των φυσικών βαλβίδων, όπως φάνηκε και από τον χαρακτηρισμό τους, δικαιολογεί τις υψηλές, τιμές του λόγου Ca/P και την απόκλισή τους από την τιμή του στοιχειομετρικού ΗΑΡ (1.67) λόγω της υποκατάστασης των φωσφορικών ιόντων από τα ανθρακικά στο κρυσταλλικό πλέγμα. Συμπερασματικά, από τα αποτελέσματα της φυσικοχημικής μελέτης των εναποθέσεων που απομονώθηκαν από ασβεστοποιημένες βαλβίδες καρδιάς προέκυψε ότι στην περίπτωση των φυσικών βαλβίδων οι παθολογικές εναποθέσεις απετελούντο από ανθρακικό απατίτη, ενώ στις βιοπροσθετικές βαλβίδες ήταν έντονη η παρουσία πρόδρομων φάσεων (DCPD και κυρίως OCP) καθώς και απατιτικών μικροκρυσταλλικών σχηματισμών. 94
121 ΒIΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟΥ 4 Dorozhkin S.V., Epple M., Biological and medical significance of calcium phosphates, Angew Chem Int Ed Engl, 41, pp , (2002) Tadic D., Epple Μ., A thorough physicochemicalcharacterisation of 14 calcium phosphate-based bone substitution materials in comparison to natural bone, Biomaterials, 25, pp , (2004) Τermine J.D., Eanes E.D., Greenfield D.J., Nylen M.U., Harper R.A., Hydrazinedeproteinated bone mineral. Physical and chemical properties, Calcif. Tiss. Res., 12, pp , (1973) 95
122 96
123 ΚΕΦΑΛΑΙΟ 5 ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΒΙΟΛΟΓΙΚΩΝ ΙΣΤΩΝ IN VITRO 97
124 5.1 ΕΙΣΑΓΩΓΗ Ο σχηματισμός δυσδιάλυτων αλάτων φωσφορικού ασβεστίου σε επιφάνειες βαλβίδων καρδιάς και βιοπροσθετικών εμφυτευμάτων αποτελεί ένα από τα κυριότερα προβλήματα στον καρδιαγγειακό τομέα αλλά και στην ανάπτυξη βιοπροσθετικών βαλβίδων καρδιάς. Για το λόγο αυτό, η μελέτη του μηχανισμού του σχηματισμού των εναποθέσεων σε βιολογικούς ιστούς κρίνεται αναγκαία. Έτσι, στο κεφάλαιο αυτό, προκειμένου να διερευνηθεί η κινητικής της ασβεστοποίησης in vitro σε χοίρειες αορτικές βαλβίδες καρδιάς και σε βόειο περικάρδιο, έγινε μελέτη του σχηματισμού των εναποθέσεων φωσφορικού ασβεστίου σε υπέρκορα διαλύματά του και σε συνθήκες 37 ο C, ph 7.4 ± 0.1, ιοντική ισχύ 0.15Μ ΝaCl και χρησιμοποιήθηκε η μέθοδος του σταθερού υπερκορεσμού (σταθερή σύσταση υπέρκορων διαλυμάτων). Η φάση του φωσφορικού ασβεστίου που κρυσταλλώθηκε ήταν το φωσφορικού οκτασβεστίο (Ca 4 H(PO 4 ) 3 2.5H 2 O, OCP). Παρ όλο που το φωσφορικό οκτασβέστιο (OCP) είναι πρόδρομη και θερμοδυναμικά ασταθής φάση του φωσφορικού ασβεστίου, σημαντικός αριθμός βιβλιογραφικών μελετών αναφέρουν την παρουσία του σε παθολογικές εναποθέσεις [Höhling et al., 1968 ; Rokita et al., 1992]. 5.2 ΜΕΘΟΔΟΛΟΓΙΑ Η πειραματική τεχνική που χρησιμοποιήθηκε για τη μελέτη της κινητικής της κρυστάλλωσης του φωσφορικού οκτασβεστίου σε ιστούς ήταν η μέθοδος κρυστάλλωσης με σπορά κρυσταλλικών φυτρών (seeded growth). Η μέθοδος κρυστάλλωσης με σπορά κρυσταλλικών φυτρών χρησιμοποιείται για την μελέτη της κρυσταλλικής ανάπτυξης πάνω σε καλά χαρακτηρισμένους κρυστάλλους σε σταθερά υπέρκορα διαλύματα των ιόντων του καταβυθιζόμενου στερεού [Nancollas and Purdie, 1964]. Ως φύτρα, χρησιμοποιούνται είτε κρύσταλλοι του άλατος του οποίου η καταβύθιση μελετάται ή οποιοδήποτε άλλο στερεό το οποίο μπορεί να χρησιμεύσει ως υπόστρωμα για κρυσταλλική ανάπτυξη [Koutsoukos and Nancollas, 1981 ; Nancollas and Wefel, 1976]. Η μελέτη της κινητικής της κρυστάλλωσης του φωσφορικού ασβεστίου πραγματοποιήθηκε παρακολουθώντας το ph και την χημική σύσταση των υπέρκορων διαλυμάτων, με τη χρήση μιας μεθόδου σύμφωνα με την οποία τα χημικά δυναμικά όλων των ειδών του διαλύματος παραμένουν σταθερά κατά την καταβύθιση και την 98
125 κρυσταλλική ανάπτυξη. Η μέθοδος αυτή καλείται μέθοδος σταθερής σύστασης (constant composition method) [Tomson and Nancollas, 1978]. Σύμφωνα με τη μέθοδο αυτή, οι ενεργότητες των πλεγματικών ιόντων του καταβυθιζόμενου στερεού παραμένουν σταθερές με τη προσθήκη διαλυμάτων τιτλοδότησης (titrants) τα οποία έχουν τη στοιχειομετρική αναλογία της καταβυθιζόμενης φάσης. Τα διαλύματα τιτλοδότησης περιέχουν και κατάλληλη ποσότητα βάσης για την διατήρηση του ph στην επιθυμητή τιμή καθώς και τον ηλεκτρολύτη, ο οποίος χρησιμοποιείται στα υπέρκορα διαλύματα για τη διατήρηση της ιοντικής ισχύος του διαλύματος. Με την μέθοδο σταθερού υπερκορεσμού διατηρούνται σταθερά τόσο το ph όσο και η χημική σύσταση των συστατικών του διαλύματος εργασίας κατά την πρόοδο της καταβύθισης του άλατος. Στα πλεονεκτήματα της μεθόδου περιλαμβάνονται η ακρίβεια και η επαναληψιμότητα στην μέτρηση των ρυθμών της καταβύθισης σε ένα εύρος τιμών υπερκορεσμού καθώς και το ότι είναι δυνατόν να διεξάγονται μετρήσεις σε συνθήκες πολύ κοντά στην κατάσταση ισορροπίας, σε συνθήκες μόνιμης κατάστασης. Ο ρυθμός ανάπτυξης των κρυστάλλων με τη μέθοδο σταθερού υπερκορεσμού υπολογίζεται από τον όγκο των προστιθέμενων διαλυμάτων τιτλοδότησης. Με τη διατήρηση του υπερκορεσμού σε σταθερή τιμή και με τη συνεχή αναπλήρωση στο υπέρκορο διάλυμα των πλεγματικών ιόντων που καταβυθίζονται, επιτυγχάνεται η συνεχόμενη παραγωγή της καταβυθιζόμενης φάσης σε μεγάλες ποσότητες. Η μέθοδος σταθερού υπερκορεσμού είναι κατάλληλη για τη μελέτη της καταβύθισης μιας συγκεκριμένης κρυσταλλικής φάσης σε συστήματα όπου μπορούν να καταβυθιστούν περισσότερες από μια φάσεις, εφόσον τα διαλύματα τιτλοδότησης είναι υπέρκορα ως προς την επιθυμητή φάση [Koutsoukos et al., 1980]. Επιπλέον, μπορεί να εφαρμοστεί επιτυχώς για τη μελέτη της επίδρασης ξένων ιόντων στο διάλυμα εργασίας χωρίς να μεταβάλλεται η σύσταση με την εξέλιξη της αντίδρασης καθώς και για τη μελέτη της συνεισφοράς διαφορετικών παραμέτρων ξεχωριστά. 5.3 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Αντιδραστήρια Για την παρασκευή όλων των διαλυμάτων χρησιμοποιήθηκαν αντιδραστήρια αναλυτικής καθαρότητας, Pro Analisi, τα οποία είτε ήσαν πρότυπα γνωστής στοιχειομετρίας είτε μπορούσαν να προτυποποιηθούν με συνήθεις αναλυτικές τεχνικές. 99
126 Το νερό που χρησιμοποιήθηκε ήταν απομεταλλωμένο και τριπλά απεσταγμένο, προερχόμενο από το νερό του δικτύου υδροδότησης. Πρότυπα πυκνά διαλύματα διένυδρου χλωριούχου ασβεστίου, CaCl 2 2H 2 O (Μerck), δισόξινου φωσφορικού καλίου, KH 2 PO 4 (Μerck) συγκέντρωσης 0.1Μ και χλωριούχου νατρίου, ΝaCl (Merck) συγκέντρωσης 1Μ παρασκευάστηκαν με ζύγιση και αραίωση της απαιτούμενης ποσότητας. Στη συνέχεια διηθήθηκαν υπό κενό με φίλτρα μεμβράνης διαμέτρου πόρων 0.2μm (Millipore) και αποθηκεύτηκαν σε πλαστικά δοχεία. Παρασκευάστηκε επίσης πρότυπο διάλυμα καυστικού νατρίου, NaOH (Merck, Titrisol) συγκέντρωσης 0.1Ν από σφραγισμένη πλαστική φύσιγγα πρότυπου πυκνού διαλύματος μετά από αραίωση στο 1 L. Το πρότυπο πυκνό διαλύμα του ασβεστίου (CaCl 2 2H 2 O) προτυποποιήθηκε με συμπλοκομετρική τιτλοδότηση με πρότυπο διάλυμα EDTA (Fluka) συγκέντρωσης 0.1M. Χρησιμοποιήθηκε δείκτης calmagite (Sigma) για την εμφάνιση ροζ χρώματος και ρυθμιστικό διάλυμα NH 3 /NH 4 Cl για τη ρύθμιση του ph μεταξύ Η συγκέντρωση του πρότυπου διαλύματος EDTA είχε προσδιοριστεί με ακρίβεια με τον ίδιο τρόπο χρησιμοποιώντας πρότυπο διάλυμα ασβεστίου, Ca 1000mg L -1, από πυκνό πρότυπο διάλυμα σε σφραγισμένη πλαστική φύσιγγα (Merck, Titrisol). Το διάλυμα των φωσφορικών προτυποποιήθηκε με ποτενσιομετρική τιτλοδότηση με πρότυπο διάλυμα NaOH 0.1Μ [Skoog, 1996]. Το διάλυμα καυστικού νατρίου (NaOH) προτυποποιήθηκε με διάλυμα όξινου φθαλικού καλίου, C 8 H 5 KO 4 (Merck), το οποίο είχε παρασκευαστεί από το αντίστοιχο κρυσταλλικό στερεό το οποίο είχε προηγουμένως ξηρανθεί για μία νύχτα στους 105 o C. Για τις ποτενσιομετρικές τιτλοδοτήσεις χρησιμοποιήθηκε συνδυασμένο ηλεκτρόδιο υάλου Ag/AgCl για τις μετρήσεις της μεταβολής του ph του διαλύματος συναρτήσει του προστιθέμενου όγκου της βάσης. Παρασκευάστηκαν πρότυπα ρυθμιστικά διαλύματα [Bates, 1973] με τιμές ph 6.84 και στους 37 o C τα οποία απαιτούνται για την βαθμονόμηση του ηλεκτροδίου μέτρησης του ph. Για την παρασκευή τους χρησιμοποιήθηκαν τα κρυσταλλικά στερεά KH 2 PO 4 (Merck) και Na 2 HPO 4 (Merck), τα οποία πριν τη ζύγισή τους είχαν ξηρανθεί για 24 h στους 105 o C. Τα πρότυπα πυκνά διαλύματα και τα ρυθμιστικά διαλύματα μετά την παρασκευή τους διηθούνταν υπό κενό με χρήση φίλτρων μεμβράνης διαμέτρου πόρων 0.2μm (Millipore). Το πρότυπο διάλυμα των φωσφορικών και τα ρυθμιστικά διαλύματα φυλάσσονταν στο ψυγείο στους 4 o C, για να αποφευχθεί η ανάπτυξη μικροβιακής δράσης, η οποία είναι πολύ πιθανή σε θερμοκρασία περιβάλλοντος [Taylor, 1989]. 100
127 5.3.2 Κατεργασία ιστών Στα πειράματα χρησιμοποιήθηκαν χοίρειες τριγλώχινες αορτικές βαλβίδες και βόειο περικάρδιο, τα οποία αποτέλεσαν υπόστρωματα για τη μελέτη της κινητικής της κρυστάλλωσης του φωσφορικού οκτασβεστίου (ΟCP). Οι βαλβίδες καρδιάς υποβάλονταν σε κατεργασία πριν την εισαγωγή τους στον αντιδραστήρα ώστε να αποτελέσουν υπόστρωμα για την κρυσταλλική ανάπτυξη. Συγκεκριμένα, καρδιές από χοίρους, αλλά και βόειο περικάρδιο προσκομίζονταν από το τοπικό σφαγείο αμέσως μετά τη σφαγή των ζώων, μεταφέρονταν στο εργαστήριο μέσα σε δοχεία με πάγο και σε φυσιολογικό ορό και στη συνέχεια γινόταν ο διαμελισμός της καρδιάς και η εξαγωγή της αορτικής βαλβίδας. Ακολουθούσε ο καθαρισμός τους από περίσσεια μυοκαρδίου και λιπαρό ιστό και στη συνέχεια οι καθαρισμένες αορτικές βαλβίδες και το βόειο περικάρδιο αποθηκεύονταν σε φυσιολογικό ορό στους 4 ο C το πολύ για 24 ώρες. Ο φυσιολογικός ορός είναι ένα διάλυμα ΝaCl 0.9%, ισοτονικό και αποστειρωμένο. Την επόμενη ημέρα οι βαλβίδες και το βόειο περικάρδιο εισάγονταν σε ρυθμιστικό διάλυμα φωσφορικών 0.15 Μ (ΚΗ 2 PO 4 ), ph 7.40 και στη συνέχεια γινόταν προσθήκη 0.625% γλουταραλδεΰδης (25% w/v, Serva Feinbiochemica) ως στερεωτικό μέσο για την προετοιμασία των ιστών [Broom and Thomson, 1979] έτσι ώστε να παρεμποδιστεί η αποσύνθεση του κολλαγόνου με την ανάπτυξη διαμοριακών διασυνδέσεων (cross-linking). Η χρήση της γλουταραλδεΰδης ως μέσου κατεργασίας βαλβίδων εισήχθη για πρώτη φορά από τον Carpentier και εξακολουθεί να χρησιμοποιείται και σήμερα με αρκετές παραλλαγές ως μέθοδος κατεργασίας βαλβίδων. Με τη χρήση της επιτυγχάνεται η μονιμοποίηση των ιστών, έτσι ώστε να διατηρείται σταθερή η δομή τους και η μορφολογική και χημική σύνθεσή τους, καθώς αυξάνει την ανθεκτικότητα, σταθεροποιώντας τους σταυροδεσμούς του κολλαγόνου και επίσης, καταστρέφει την ανοσο-δράση τους [Carpentier et al., 1969]. Οι βαλβίδες και το περικάρδιο παρέμεναν στο διάλυμα αυτό για περίπου μία ώρα σε θερμοκρασία δωματίου. Στο διάστημα αυτό ασκούταν στις βαλβίδες μικρός μηχανικός εφελκυσμός έτσι ώστε να διατηρούνται οι γλωχίνες κλειστές. Η υποκίτρινη απόχρωση στους ιστούς ήταν χαρακτηριστική της δράσης της γλουταραλδεΰδης. Τέλος, ακολουθούσε καλό ξέπλυμά τους με φυσιολογικό ορό και αποθήκευση των βαλβίδων και του βοείου περικαρδίου σε διάλυμα φορμαλδεΰδης 4% (40% Formaldehyde, Sigma-Aldrich) σε ph 5.60 στους 4 ο C [Ο Brien, 1967]. Με τη χρήση φορμαλδεΰδης ως συντηρητικού μέσου 101
128 διατηρείται η δομή του ιστού στην κατάσταση που εξάγεται από τον οργανισμό. Η κατεργασία αυτή, όμως, προκαλεί συρρίκνωση και δυσκαμψία του ιστού [Βlack et al., 1983]. Ένα άλλο είδος ιστού που αποτέλεσε υλικό μελέτης για την κρυστάλλωση του OCP ήταν βόειο περικάρδιο που προήλθε από την εταιρεία Synovis Surgical Innovations (SSI) η οποία εδρεύει στη Μινεσότα της Αμερικής από το 1985 και είναι ευρέως γνωστή για την ανάπτυξη και κατασκευή βιοϋλικών τα οποία χρησιμοποιούνται ως εμφυτεύματα. Το πρώτο εμφυτεύσιμο βιοϋλικό προϊόν της εταιρείας ήταν το Supple Peri-Guard, ενώ το τελευταίο προϊόν τους, το Veritas Collagen Matrix, έχει ήδη ξεκινήσει να χρησιμοποιείται και αυτό ως εμφυτεύσιμο υλικό από το Και τα δύο αυτά προϊόντα αποτέλεσαν υποστρώματα για τη μελέτη του σχηματισμού εναποθέσεων φωσφορικού οκτασβεστίου σε υπέρκορα διαλύματα. Το βόειο περικάρδιο Supple Peri-Guard αναφέρεται πως έχει υποστεί κατεργασία με γλουταραλδεΰδη (ανάπτυξη σταυροδεσμών- cross linked). Ο ιστός, είχε αποστειρωθεί χημικά χρησιμοποιώντας γλουταραλδεΰδη, αιθανόλη και προπυλενοξείδιο. Επιπλέον, είχε υποστεί επεξεργασία με διάλυμα υδροξειδίου του νατρίου, NaOH 1Μ, για λεπτά σε θερμοκρασία C. Το βόειο περικάρδιο Supple Peri-Guard ήταν συσκευασμένο σε έναν περιέκτη γεμάτο με στείρο, μη πυρετογόνο νερό που περιείχε προπυλενοξείδιο και είχε διαστάσεις cm 2. Το βόειο περικάρδιο Veritas Collagen Matrix είχε υποστεί αποκυταρροποίηση δίχως να έχει γίνει χρήση γλουταραλδεΰδης (non-cross-linked), ήταν συσκευασμένο σε εσωτερικά αποστειρωμένη σακούλα και είχε διαστάσεις 4 7 cm 2. Στα πειράματα δεν χρησιμοποιήθηκε ποτέ ολόκληρη η αορτική βαλβίδα. Γινόταν διαμελισμός αυτής και διαχωρισμός των τριών γλωχίνων από το αορτικό τοίχωμα. Έτσι, ήταν δυνατή η μελέτη του σχηματισμού των εναποθέσεων OCP τόσο σε γλωχίνες όσο και σε αορτικά τοιχώματα. Ο διαχωρισμός των γλωχίνων από το αορτικό τοίχωμα γινόταν με χειρουργική λεπίδα πριν από κάθε πείραμα. Οι επιφάνειες των ιστών που χρησιμοποιήθηκαν ήσαν διαφορετικές, όμως, για τη σωστή σύγκριση των ρυθμών κρυστάλλωσης ήταν επιθυμητό οι επιφάνειες να είναι όμοιες. Έγινε, λοιπόν, γεωμετρική θεώρηση των επιφανειών και χρησιμοποιούνταν δώδεκα γλωχίνες και δύο αορτικά τοιχώματα με συνολικό εμβαδόν 54 cm 2 περίπου για το καθένα. Στην περίπτωση των βόεϊων περικαρδίων, κόβονταν 2 κομμάτια συνολικής επιφάνειας 54 cm
129 Πριν από κάθε πείραμα, οι προς χρήση ιστοί ξεπλένονταν με άφθονο τριπλά απεσταγμένο νερό και ακολουθούσε η ραφή των ιστών με χειρουργικά ράμματα πάνω σε ορθογώνια πλαίσια. Τα πλαίσια αυτά εφαρμόζονταν στο πώμα του αντιδραστήρα ο οποίος έφερε κατάλληλες οπές Πειραματική Διάταξη και Διαδικασία Η πειραματική διάταξη που χρησιμοποιήθηκε για τα πειράματα κρυστάλλωσης OCP σε υποστρώματα ιστών με τη μέθοδο της σταθερής σύστασης παρουσιάζεται στο σχήμα 5.1. Σχήμα 5.1: Πειραματική διάταξη για πειράματα κρυστάλλωσης φωσφορικού ασβεστίου με τη μέθοδο σταθερού υπερκορεσμού. Τα πειράματα πραγματοποιήθηκαν σε ένα θερμοστατούμενο διπλότοιχο δοχείο, κατασκευασμένο από γυαλί (Pyrex), τελικού όγκου 0.5L. Κυκλοφορία νερού μέσω αντλίας, στο χώρο μεταξύ των τοιχωμάτων του διπλότοιχου δοχείου, διατηρούσε τη θερμοκρασία στο εσωτερικό του αντιδραστήρα σταθερή στους 37 ± 0.5 o C. Το νερό 103
130 προερχόταν από θερμοστατούμενο υδατόλουτρο, η θερμοκρασία του οποίου παρέμενε σταθερή μέσω θερμαντικής αντίστασης και ηλεκτρονικού θερμοστάτη για τον έλεγχο της θερμοκρασίας. Ο αντιδραστήρας σφραγιζόταν με ειδικά σχεδιασμένο και κατασκευασμένο καπάκι από πολυαμίδιο το οποίο διέθετε πέντε οπές. Η πρώτη χρησιμοποιούταν για την είσοδο του ηλεκτροδίου στο διάλυμα εργασίας και η δεύτερη για τη σταθερή παροχή κορεσμένου σε υδρατμούς αζώτου, N 2, που διερχόταν πρώτα από αφυγραντήρα, μέσα στο διάλυμα εργασίας με σκοπό την απομάκρυνση του διοξειδίου του άνθρακα. Η τρίτη οπή χρησιμοποιούταν για την είσοδο του σωλήνα δειγματοληψίας και οι υπόλοιπες δύο για τους σωλήνες τριχοειδούς διαμέτρου, για τη μεταφορά των διαλυμάτων τιτλοδότησης από τις μηχανικά συνδεδεμένες σύριγγες στο διάλυμα εργασίας. Η ανάδευση του διαλύματος εργασίας γινόταν με συσκευή μαγνητικής ανάδευσης και με μαγνητική ράβδο καλυμμένη από Teflon έτσι ώστε το διάλυμα εργασίας να διατηρείται ομογενές. Το συνδυασμένο ηλεκτρόδιο υάλου, το οποίο χρησιμοποιήθηκε για τη μέτρηση ph του διαλύματος εργασίας, ήταν συνδεδεμένο με μία μονάδα ελέγχου (controller). Η μονάδα ελέγχου ήταν συνδεδεμένη με έναν κινητήρα, ο οποίος κινούσε τις δύο μηχανικά συνδεδεμένες βαθμονομημένες σύριγγες (αυτόματος τιτλοδότης) και με έναν ηλεκτρονικό υπολογιστή, ο οποίος διέθετε κατάλληλη κάρτα συλλογής των δεδομένων. Μεταβολή της τιμής του ph του διαλύματος μεγαλύτερη από μονάδες είχε ως αποτέλεσμα η μονάδα ελέγχου να ενεργοποιήσει τον κινητήρα με τις δύο μηχανικά συνδεδεμένες σύριγγες και να γίνονται με παλμικό ρυθμό κατάλληλες προσθήκες των διαλυμάτων τιτλοδότησης στο διάλυμα εργασίας. Πριν την έναρξη του κάθε πειράματος γινόταν πλήρωση των δύο μηχανικά συζευγμένων συρίγγων με τα διαλύματα τιτλοδότησης. Η σύστασή τους διαμορφωνόταν ανάλογα με τις συνθήκες του πειράματος. Τα διαλύματα τιτλοδότησης (titrants) παρασκευάζονταν από τα πρότυπα διαλύματα ασβεστίου (0.1Μ CaCl 2 2H 2 O), φωσφορικών (0.1Μ KΗ 2 PO 4 ), χλωριούχου νατρίου (1Μ NaCl) και καυστικού νατρίου (0.1Ν NaOH) με τις απαραίτητες αραιώσεις με τριπλά απεσταγμένο νερό. Η πρώτη σύριγγα περιείχε το διάλυμα του CaCl 2 2H 2 O και το διάλυμα του αδρανούς ηλεκτρολύτη NaCl, ενώ η δεύτερη το διάλυμα του KΗ 2 PO 4 και το διάλυμα του NaOH. Ο υπολογισμός των συγκεντρώσεων των τιτλοδοτικών διαλυμάτων ήταν σημαντικός για τη σωστή διεξαγωγή των πειραμάτων κρυστάλλωσης με τη μέθοδο της σταθερής σύστασης. Η προσθήκη των τιτλοδοτικών διαλυμάτων με την αυτή 104
131 στοιχειομετρική αναλογία με το καταβυθιζόμενο άλας έχει ως στόχο την αναπλήρωση των ιόντων που καταναλώνονται στο διάλυμα για τον σχηματισμό της κρυσταλλικής φάσης, τη διατήρηση σταθερής ιοντικής ισχύος (σταθεροί συντελεστές ενεργότητας όλων των ιόντων) και την αποφυγή περαιτέρω αραίωσης στο διάλυμα, έτσι ώστε να παραμένει σταθερή η σύσταση στο διάλυμα εργασίας. Οι συγκεντρώσεις των τιτλοδοτικών διαλυμάτων προέκυψαν από ισοζύγια μάζας για κάθε ιόν που συμμετέχει στην αντίδραση ως ακολούθως: Το υδατικό διάλυμα εργασίας περιέχει διαλύματα CaCl 2 2H 2 O, KΗ 2 PO 4, NaCl και NaOH, όπου Ca ws, P ws, NaCl ws, NaOH ws οι αντίστοιχες συγκεντρώσεις τους στο διάλυμα εργασίας. Το πρώτο τιτλοδοτικό διάλυμα (Τ Α ) περιέχει διαλύματα CaCl 2 2H 2 O και NaCl, όπου TA TA Ca και NaCl οι συγκεντρώσεις τους στο τιτλοδοτικό διάλυμα αντίστοιχα, ενώ το δεύτερο τιτλοδοτικό διάλυμα (Τ Β ) περιέχει ΚΗ 2 PO 4 και NaOH, με συγκεντρώσεις TB TB P και ενεργότητες όλων των πλεγματικών ιόντων σταθερές. NaOH αντιστοίχως, έτσι ώστε να διατηρούνται οι Έστω ότι καταναλώνονται m Ca moles ιόντων ασβεστίου σε τελικό όγκο υπέρκορου διαλύματος V και dv ο στοιχειώδης όγκος του διαλύματος τιτλοδότησης ο οποίος προστίθεται από κάθε σύριγγα. Έτσι ώστε να διατηρηθεί η ενεργότητα των ιόντων Ca 2+ σταθερή, από το ακόλουθο ισοζύγιο μάζας, προσδιορίζεται η συγκέντρωση του ασβεστίου στο διάλυμα τιτλοδότησης, TA Ca : Ca ws ws ws T A T A T B T B Ca V Ca dv Ca dv mca ws T A T B V dv dv T A T B T A T A T B T B Ca ws ( V ws dv dv ) Ca ws V ws Ca dv Ca dv m Ca TA TB T dv =dv =dv και Ca B=0 ws ws ws ws T A Ca ( V 2 dv ) Ca V Ca dv m Ca T A ws T A ws mca Ca dv 2Ca dv mca Ca 2Ca dv T A ws Ca 2Ca m όπου, mca dv m είναι ένα μέτρο της καταβυθιζόμενης ποσότητας ανά μονάδα όγκου. Η παράμετρος αυτή καθορίζεται εμπειρικά, μέσω μιας σειράς προκαταρκτικών 105
132 πειραμάτων και εκφράζει πόσο πιο πυκνά πρέπει να είναι τα διαλύματα τιτλοδότησης για να αναπληρώνεται ότι καταβυθίζεται. Ομοίως, για να διατηρηθεί η ενεργότητα των φωσφορικών ιόντων PO 4 3- σταθερή, από το ακόλουθο ισοζύγιο μάζας, προσδιορίζεται η συγκέντρωση των φωσφορικών στο διάλυμα τιτλοδότησης, TB P : P ws ws ws T A T A T B T B P V P dv P dv mp ws T A T B V dv dv TA TB T dv =dv =dv και P A =0 T A T B T A T A T B T B P ws ( V ws dv dv ) P ws V ws P dv P dv m P ws ws ws ws T B P ( V 2 dv) P V P dv m P T B ws T B ws mp P dv 2P dv mp P 2P dv P T B ws 2P n Με όμοιο τρόπο από το ισοζύγιο μάζας για τα ιόντα Cl -, προσδιορίζεται η συγκέντρωσή τους στο τιτλοδοτικό διάλυμα, TA Cl : 106
133 Cl ws ws ws T A T A T B T B Cl V Cl dv Cl dv - m ws T A T B V dv dv Cl dv TA =dv TB =dv και Cl TB =0 και m Cl =0 T A T B T A T A T B T B Cl ws ( V ws dv dv ) Cl ws V ws Cl dv Cl dv -m Cl ws ws ws ws T A ws T A Cl ( V 2 dv ) Cl V Cl dv Cl 2dV Cl dv T A ws TA TA ws ws CaCl2 NaCl CaCl2 NaCl T A TA ws ws NaCl CaCl2 NaCl ws TA ws ws Ca m ClNaCl ClCaCl ClNaCl 2 T A ws Ca =2Ca + m ws ws Ca = ClCaCl 2 T T Ca A = Cl A CaCl 2 Cl 2Cl 2 Cl Cl 2 2 Cl Cl 2 Ca Cl 2 2 Cl Cl ws TA ws ws 4Ca 2m Cl 2 2 Ca Cl NaCl NaCl TA ws Cl 2Cl -2m NaCl NaCl Παρόμοια από το ισοζύγιο μάζας για τα ιόντα νατρίου Να + και καλίου Κ + έχουμε: ws ws A T A ws T T B T B Na K V Na K dv Na K dv mnak ws T A T B Na K V dv dv ws ws ws T A T ws T B A T A Na K V dv dv Na K V Na K dv T T B A B B dv = dv = dv και m Na+K = 0 2 T T ws ws ws ws NaK Na K dv m Na K V dv Na K V T A B ws Na K dv Na K 2 2 T ws ws ws ws dv Na K V Na K dv Na K V T A T B ws T A T B Na K dv Na K dv Na K dv Na K dv Na K dv 2 NaCl NaOH KH PO NaCl NaOH KH PO ws ws ws T A T B T B NaCl 2NaOH 2KH PO NaCl NaOH KH PO ws ws ws T A T B T B ws ws T T ws ws Τ Τ ws KH2PO 4 = P και NaCl A = Cl A Β Β NaCl = 2ClNaCl -2m = 2NaCl και KH2PO 4 = P = 2P +n ws ws 2NaCl 2NaOH TB 2P ws 2NaCl ws 2mNaOH 2P ws n TB ws NaOH 2NaOH 2m n 107
134 Συγκεντρωτικά, λοιπόν, οι συγκεντρώσεις όλων των ειδών που πρέπει να περιέχονται στα τιτλοδοτικά διαλύματα, έτσι ώστε κατά τη διάρκεια των πειραμάτων ο υπερκορεσμός στο διάλυμα εργασίας να διατηρείται σταθερός έχουν ως εξής: TA ws Ca 2 Ca m (5-1) PO 2 PO n (5-2) TB ws 4 4 NaCl T A ws 2NaCl -2 m (5-3) T B ws NaOH 2NaOH 2m - n (5-4) όπου για την περίπτωση καταβύθισης υδροξυαπατίτη (ΗΑP) ισχύει: 3 HAP Ca5PO4 OH n m 3 5 ενώ στην περίπτωση που καταβυθίζεται OCP ισχύει: 3 OCP Ca4H PO4 n m 3 4 Για τον προσδιορισμό της τιμής m έγιναν προκαταρκτικά πειράματα, με την τεχνική της δοκιμής και σφάλματος. Επιλέγονταν πολλαπλάσια της συγκέντρωσης ασβεστίου του διαλύματος εργασίας (Ca ws ) και εξεταζόταν αν τα διαλύματα τιτλοδότησης ήταν ικανά να διατηρούν το ph και την χημική σύσταση του διαλύματος σταθερή στην διάρκεια της αντίδρασης. Έτσι, από τα προκαταρκτικά πειράματα προσδιορίστηκε ότι στην περίπτωση καταβύθισης ΗΑP: m =10 Ca ws Ceff, ενώ στην περίπτωση καταβύθισης OCP: m =3 Ca ws Ceff, όπου eff C η συγκέντρωση αποτελεσματικότητας και η οποία αποτελεί μέτρο της ποσότητας του στερεού που καταβυθίζεται. Οι εξισώσεις που προέκυψαν για τις συγκεντρώσεις των διαλυμάτων τιτλοδότησης αποτελούνται από δύο όρους και ο κάθε ένας έχει την φυσική του σημασία. Ο πρώτος όρος αντιστοιχεί στην αποφυγή της αραίωσης των συγκεντρώσεων των ιόντων στο διάλυμα με τις προσθήκες που πραγματοποιούνται και ο δεύτερος σχετίζεται με την ποσότητα που μεταφέρεται στο καταβυθιζόμενο στερεό. 108
135 Εν τέλει, οι συγκεντρώσεις των τιτλοδοτικών διαλυμάτων ανάλογα με το άλας που καταβυθίζεται έχουν ως εξής: Για ΗΑΡ: TA ws Ca 2 Ca C (5-1α) eff T 3 B ws PO4 2 PO4 Ceff (5-2α) 5 TA ws NaCl 2NaCl - 2 C (5-3α) T 7 B ws NaOH 2 NaOH Ceff (5-4α) 5 ws όπου C 10 Ca (5-5α) eff eff Για OCP: TA ws Ca 2 Ca C (5-1β) eff T 3 B ws PO4 2 PO4 Ceff (5-2β) 4 TA ws NaCl 2NaCl - 2 C (5-3β) T 5 B ws NaOH 2 NaOH Ceff (5-4β) 4 ws όπου C 3 Ca (5-5β) eff eff Στον αντιδραστήρα, το διάλυμα εργασίας παρασκευαζόταν με προσθήκη κατάλληλης ποσότητας τριπλά απεσταγμένου νερού έτσι ώστε με την προσθήκη όλων των αντιδρώντων ο τελικός όγκος του διαλύματος εργασίας να είναι 0.4L, κατάλληλων συγκεντρώσεων του αδρανούς ηλεκτρολύτη ΝaCl και του διαλύματος των φωσφορικών KH 2 PO 4. Στη συνέχεια γινόταν εισαγωγή των ιστών στον αντιδραστήρα. Οι ιστοί ήταν ραμμένοι πάνω σε ορθογώνια πλαίσια με τέτοιο τρόπο, ώστε να βρίσκεται όσο το δυνατόν μεγαλύτερη επιφάνεια τους σε επαφή με το υπέρκορο διάλυμα εργασίας. Το διάλυμα αναδευόταν και διοχετευόταν άζωτο κορεσμένο σε υδρατμούς. Έπειτα ρυθμιζόταν το ph του διαλύματος εργασίας στην επιθυμητή τιμή, ανάλογα με τις συνθήκες του πειράματος με προσθήκη κατάλληλης ποσότητας βάσης ΝαΟΗ 0.1Ν. Τέλος, ακολουθούσε η προσθήκη της απαιτούμενης ποσότητας, από την συγκέντρωση του εκάστοτε πειράματος, του διαλύματος CaCl. 2 2H 2 O. Η χρονική αυτή στιγμή της επίτευξης του υπερκορεσμού ουσιαστικά σηματοδοτούσε την έναρξη της διεργασίας της καταβύθισης. Από εκείνη τη χρονική στιγμή ξεκινούσε η καταγραφή της μεταβολής του ph του διαλύματος με το χρόνο και η συλλογή των δεδομένων στον ηλεκτρονικό υπολογιστή. Η τελευταία τιμή του ph του διαλύματος πριν την πρώτη μείωσή της, οριζόταν ως set point. Η τιμή του set point αντιστοιχούσε στην τιμή ph η οποία όταν μειωνόταν περισσότερο από μονάδες ενεργοποιούσε μέσω της μονάδας ελέγχου τις μηχανικά συνδεδεμένες σύριγγες με τα διαλύματα τιτλοδότησης. Μόλις ξεκινούσε η καταβύθιση του στερεού, σύμφωνα με την αντίδραση (5-6), απελευθερώνονταν πρωτόνια στο διάλυμα τα οποία γίνονταν αντιληπτά με μείωση στην 109
136 τιμή του ph του διαλύματος και την έναρξη των προσθηκών των διαλυμάτων τιτλοδότησης με στοιχειομετρική αναλογία του καταβυθιζόμενου άλατος (ΟCP). 4Ca 3HPO 2.5 H O Ca H ( PO ) 2.5H O 2 H (5-6) ( s) Σε τακτά χρονικά διαστήματα, συλλέγονταν δείγματα από το διάλυμα εργασίας με συχνότητα ανάλογη με τον ρυθμό της αντίδρασης, έτσι ώστε ο όγκος του διαλύματος εργασίας να παραμένει όσο το δυνατό σταθερός. Τα δείγματα διηθούνταν από ηθμούς μεμβράνης 0.2μm (Millipore) και αναλύονταν για ασβέστιο με φασματοσκοπία ατομικής απορρόφησης και για φωσφορικά φασματοφωτομετρικά με την μέθοδο των βαναδομολυβδαινικών. Τα πειράματα διαρκούσαν έως και 6 ημέρες, ανάλογα με τις πειραματικές συνθήκες, έτσι ώστε να εναποτίθεται κάθε φορά όσο το δυνατόν περισσότερη ποσότητα της καταβυθιζόμενης φάσης στους ιστούς. Μετά το πέρας του πειράματος, οι ιστοί ξεπλένονταν για την απομάκρυνση ποσότητας χλωριούχου νατρίου και ακολουθούσε η ξήρανσή τους σε λυοφιλοποιητή (Cryodos, Telestar). Οι ιστοί τοποθετούνταν σε ειδικές φιάλες στη συσκευή λυοφιλοποίησης υπό πίεση 0.053mbar και σε θερμοκρασία ο C για 24 ώρες. Στη συνέχεια ακολουθούσε χαρακτηρισμός τους με περίθλαση ακτίνων-χ (XRD) και με ηλεκτρονική μικροσκοπία σάρωσης (SEM). 5.4 ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Από τη συλλογή των δεδομένων στον ηλεκτρονικό υπολογιστή, με την βοήθεια της ψηφιακής κάρτας συλλογής (A/D, D/A Advantech PCL 812) προέκυπταν τα διαγράμματα της μεταβολής του ph του διαλύματος και του προστιθέμενου όγκου των διαλυμάτων τιτλοδότησης συναρτήσει του χρόνου, όπως φαίνεται στα σχήματα 5.2 (α) και 5.2 (β). Από το διάγραμμα της μεταβολής του ph με τον χρόνο επιβεβαιωνόταν η σταθερότητα του ph του διαλύματος εργασίας. 110
137 V/ ml t/ sec () ph 7,50 7,48 7,46 7,44 7,42 7,40 7,38 7,36 7,34 7,32 7, t/ sec () Σχήμα 5.2: Γραφική παράσταση (α) του ph του διαλύματος εργασίας συναρτήσει του χρόνου και (β) του προστιθέμενου όγκου διαλυμάτων τιτλοδότησης έναντι του χρόνου. Από τις αναλύσεις των διηθημάτων των δειγμάτων προέκυπταν τα διαγράμματα της μεταβολής της συγκέντρωσης των πλεγματικών ιόντων με το χρόνο, από τα οποία ελεγχόταν η σταθερότητα της χημικής σύστασης του διαλύματος εργασίας. Τα διαγράμματα αυτά είχαν τη μορφή που φαίνονται στα σχήματα 5.3 (α) και 5.3 (β). 1,6x10-3 1,5x10-3 () 1,2x10-3 1,1x10-3 () 1,4x10-3 1,3x10-3 1,0x10-3 1,2x10-3 9,0x10-4 [Ca] total / M 1,1x10-3 1,0x10-3 [P] total / M 8,0x10-4 7,0x10-4 9,0x10-4 8,0x10-4 6,0x10-4 7,0x10-4 5,0x10-4 6,0x10-4 4,0x t/ hr t/ hr Σχήμα 5.3: Διάγραμμα μεταβολής ολικής συγκέντρωσης (α) ασβεστίου και (β)φωσφορικών σε πειράματα σταθερού υπερκορεσμού. Ο ρυθμός κρυσταλλικής ανάπτυξης του OCP ανά μονάδα επιφάνειας, σε αρχικό dv στάδιο της κρυστάλλωσης, υπολογιζόταν από την εξίσωση (5-7), όπου ο όρος dt προσδιοριζόταν από την κλίση της εφαπτόμενης ευθείας της καμπύλης του 111
138 διαγράμματος του προστιθέμενου όγκου των διαλυμάτων τιτλοδότησης συναρτήσει του χρόνου. g R mol dv ml sec lt mol Ca 1 mol OCP C 3 eff 1 2 dt sec min ml lt 4 mol Ca OCP min m (5-7) m ό ιστού cm 10 2 cm Η κινητήρια δύναμη για το σχηματισμό του OCP είναι η διαφορά μεταξύ του χημικού δυναμικού του στερεού στο υπέρκορο διάλυμα, από το αντίστοιχο στην ισορροπία. Θεωρώντας ότι τα πρότυπα χημικά δυναμικά στο υπέρκορο διάλυμα και στην ισορροπία είναι ίσα η διαφορά στα χημικά δυναμικά είναι: s o 1/8 o 1/8 kt ln( a a a ) kt ln( a a a ) 2 3 s 2 3 Ca H PO s 4 Ca H PO4 1/8 ( a 2 a a 3) Ca H PO 4 kt 1/8 ( a a a ) Ca H PO s 8 kt ln ln (5-8) όπου k η σταθερά Boltzmann, Τ η απόλυτη θερμοκρασία και Ω ο υπερκορεσμός που ορίζεται από την ακόλουθη σχέση: a a a Ca H PO (5-9) K 0 s όπου Κ s 0 το θερμοδυναμικό γινόμενο διαλυτότητας του OCP. Ο υπερκορεσμός είναι ένα μέτρο της απόκλισης του συστήματος από την ισορροπία και αποτελεί μέτρο της κινητήριας δύναμης για την καταβύθιση. Ο σχετικός υπερκορεσμός ως προς ΟCP ορίζεται ως : 112
139 1/8 1 (5-10) Οι συγκεντρώσεις των χημικών ειδών του διαλύματος και ο υπερκορεσμός ως προς ΟCP υπολογίσθηκαν με την βοήθεια του λογισμικού MINEQL+ [Schecher, 1998], λαμβάνοντας υπ όψη όλες τις δυνατές χημικές ισορροπίες στα υπέρκορα διαλύματα σε συνδυασμό με τις εξισώσεις ισοζυγίου μάζας και φορτίου. Τα αποτελέσματα των υπολογισμών είναι ενδεικτικά για το τι μπορεί να συμβεί από θερμοδυναμική άποψη. Οι χημικές ισορροπίες και οι τιμές των σταθερών οι οποίες χρησιμοποιήθηκαν στους υπολογισμούς παρουσιάζονται στο Παράρτημα I. Στον πίνακα 5.1 που ακολουθεί συνοψίζονται οι αρχικές πειραματικές συνθήκες και τα αποτελέσματα των μετρήσεων της κινητικής στα πειράματα κρυστάλλωσης του OCP στα διάφορα υποστρώματα ιστών που δοκιμάσθηκαν σε συνθήκες σταθερού υπερκορεσμού. 113
140 Πίνακας 5.1 Πειραματικές συνθήκες και αποτελέσματα μετρήσεων της κινητικής της κρυσταλλικής ανάπτυξης: ολική συγκέντρωση ασβεστίου, C Ca, σχετικός υπερκορεσμός ως προς OCP, σ OCP, και αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης R g, για την κρυστάλλωση του φωσφορικού οκτασβεστίου (OCP) σε διάφορους τύπους ιστών (υποστρώματα) σε υπέρκορα διαλύματα και σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, θερμοκρασία, θ = 37.0 ± 0.1 o C και C Ca /C P = 1.33, όπου C P η ολική συγκέντρωση των φωσφορικών. Υποστρώματα C Ca / 10-3 M σ OCP σ HAP R g / 10-5 mol OCP min -1 m -2 Γλωχίνες Αορτικά Τοιχώματα Βόειο Περικάρδιο Βόειο Περικάρδιο Supple Peri-Guard Βόειο Περικάρδιo Veritas Collagen Matrix
141 Η ημιεμπειρική σχέση η οποία συσχετίζει την ταχύτητα ανάπτυξης των κρυστάλλων, R g, σε υπέρκορα διαλύματά τους, συναρτήσει του σχετικού υπερκορεσμού του διαλύματος ως προς το άλας που κρυσταλλώνεται είναι: R g n k g (5-11) όπου, k g και n, η αντίστοιχη φαινόμενη σταθερά ταχύτητας και η φαινόμενη τάξη της κρυστάλλωσης στα υπό μελέτη υποστρώματα, αντίστοιχα. Η προσαρμογή των πειραματικών αποτελεσμάτων στην εξίσωση (5-11) από τα πειράματα κρυστάλλωσης OCP σε υπέρκορα διαλύματα σε υποστρώματα ιστών, μπορεί να δώσει πληροφορίες για το μηχανισμό της κρυσταλλικής ανάπτυξης, όπως έχει αναφερθεί και στο Κεφάλαιο 2. Η γραφική παράσταση του λογαρίθμου του ρυθμού κρυσταλλικής ανάπτυξης συναρτήσει του λογαρίθμου του σχετικού υπερκορεσμού ως προς OCP, από τα δεδομένα του πίνακα 5.1 φαίνεται στο σχήμα 5.4. Γραμμική προσαρμογή των δεδομένων έδωσε ευθεία γραμμή από την τεταγμένη επί την αρχή και την κλίση της οποίας υπολογίσθηκε η τιμή της φαινόμενης σταθεράς της ταχύτητας και η φαινόμενη τάξη της κρυστάλλωσης αντίστοιχα για κάθε υπόστρωμα. -3,2 log (R g / mol OCP min -1 m -2 ) -3,6-4,0-4,4-4,8-5,2-0,2 0,0 0,2 0,4 log OCP Σχήμα 5.4: Κινητική κρυστάλλωσης OCP στα διάφορα υποστρώματα ιστών σε συνθήκες σταθερού υπερκορεσμού. Διαγράμματα του λογαρίθμου του αρχικού ρυθμού κρυσταλλικής ανάπτυξης OCP συναρτήσει του λογαρίθμου του αντίστοιχου σχετικού υπερκορεσμού. θ= 37 C, ph 7.40, 0.15 M NaCl: ( ) γλωχίνες; ( ) αορτικά τοιχώματα; ( ) βόειο περικάρδιο; ( ) βόειο περικάρδιο Supple Peri Guard; ( ) βόειο περικάρδιο Veritas Collagen Matrix. 115
142 Στον πίνακα 5.2 παρουσιάζονται οι τιμές που υπολογίστηκαν για τη φαινόμενη σταθερά ταχύτητας και για τη φαινόμενη τάξη της κρυστάλλωσης του OCP στα διαφορετικά υποστρώματα των ιστών. Πίνακας 5.2 Τιμές της φαινόμενης τάξης και της φαινόμενης σταθεράς κρυσταλλικής ανάπτυξης του φωσφορικού οκτασβεστίου (OCP) στους διάφορους τύπους ιστών (υποστρώματα) που υπολογίσθηκαν με γραμμική προσαρμογή της λογαριθμισμένης εξίσωσης (5-11), σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, θερμοκρασία θ = 37.0 ± 0.1 o C, ΝaCl 0.15 M Υποστρώματα Φαινόμενη Τάξη n Φαινόμενη Κινητική Σταθερά k g / 10-5 mol min -1 m -2 Γλωχίνες Αορτικά Τοιχώματα Βόειο Περικάρδιο Βόειο Περικάρδιο Supple Peri-Guard Βόειο Περικάρδιο Veritas Collagen Matrix Από την τιμή της φαινόμενης τάξης (περίπου 1), προέκυψε το συμπέρασμα ότι ο μηχανισμός της ανάπτυξης των κρυστάλλων ελέγχεται από επιφανειακή διάχυση, των δομικών μονάδων στα ενεργά κέντρα κρυστάλλωσης. Η τιμή της φαινόμενη τάξης που υπολογίστηκε για την κρυστάλλωση OCP σε υποστρώματα αορτικών βαλβίδων και βοείου περικαρδίου από υπέρκορα διαλύματα, βρίσκεται σε συμφωνία με αντίστοιχες 116
143 τιμές που έχουν αναφερθεί σε ανάλογες εργασίες [Kapolos et al., 1997 ; Mavrilas et al, 2006]. Ωστόσο, υπάρχουν και βιβλιογραφικές αναφορές από μελέτες κρυστάλλωσης OCP σε υπόστρωμα κολλαγόνου στις οποίες αναφέρονται υψηλότερες τιμές (n = 3.5, n = 4) [Combes et al., 1999 ; Koutsoukos and Nancollas, 1987]. Οι υψηλότερες αυτές της φαινόμενης τάξης έχουν ερμηνευθεί ως ενδεικτικές πολυπυρηνικού μηχανισμού ανάπτυξης, ο οποίος και στην περίπτωση αυτή ελέγχεται από την επιφανειακή διάχυση των δομικών μονάδων (καθορίζον την ταχύτητα στάδιο). Από το συγκριτικό διάγραμμα των ρυθμών κρυσταλλικής ανάπτυξης του OCP στα διάφορα υποστρώματα ιστών, ενδεικτικά σε μια τιμή σχετικού υπερκορεσμού σ OCP = 1.38 (σχήμα 5.5), φαίνεται ότι ταχύτεροι ρυθμοί προέκυψαν κατά την κρυστάλλωση OCP στις γλωχίνες και στα αορτικά τοιχώματα. Το βόειο περικάρδιο έδειξε, ότι σε αντίστοιχα υπέρκορα διαλύματα ασβεστοποιείται με μικρότερους ρυθμούς (μια τάξης μεγέθους) σε σχέση με τις αορτικές βαλβίδες. Παρόμοια συμπεριφορά έχει παρατηρηθεί και κατά την ασβεστοποίηση αορτικών βαλβίδων και βοείου περικαρδίου τόσο in vitro όσο και in vivo [Mavrilas et al., 2004]. 5,0x10-4 4,0x10-4 R g / mol OCP min -1 m -2 3,0x10-4 2,0x10-4 1,0x10-4 1,0x10-5 OCP = 1.38 Σχήμα 5.5: Γραφική απεικόνιση του ρυθμού κρυσταλλικής ανάπτυξης OCP σε διάφορα υποστρώματα ιστών συνθήκες σταθερού υπερκορεσμού σε 37 C, ph 7.40, 0.15 M NaCl σ OCP = 1.38: (α) γλωχίνες; (β) αορτικά τοιχώματα; (γ) βόειο περικάρδιο; (δ) βόειο περικάρδιο Supple Peri Guard; (ε) βόειο περικάρδιο Veritas Collagen Matrix. 117
144 Αξιοσημείωτη, επίσης, είναι η διαφορά των ρυθμών κρυστάλλωσης OCP μεταξύ των δύο υποστρωμάτων βοείου περικαρδίου, Supple Peri-Guard και Veritas Collagen Matrix, τα οποία έχουν υποστεί διαφορετική χημική επεξεργασία. Το crosslinked Supple Peri-Guard το οποίο έχει υποστεί επεξεργασία με γλουταραλδεΰδη, έδωσε σημαντικά ταχύτερους ρυθμούς κρυσταλλικής ανάπτυξης καθώς και μεγαλύτερες τιμές εναπόθεσης OCP σε σχέση με το αποκυτταροποιημένο, (non-cross-linked) βόειο περικάρδιο χωρίς σταυροδεσμούς Veritas Collagen Matrix, στις ίδιες πειραματικές συνθήκες. Υπάρχουν αρκετές τόσο in vitro όσο και in vivo μελέτες που αναφέρονται στον επιβαρυντικό ρόλο της γλουταραλδεΰδης κατά την ασβεστοποίηση των βιοπροσθετικών βαλβίδων [Grabenwöger et al., 1996 ; Levy, 1994 ; Schoen et al., 1986]. Βόειο περικάρδιο το οποίο δεν είχε προηγουμένως υποστεί επεξεργασία με γλουταραλδεΰδη, έδειξε ότι ασβεστοποιήθηκε σε μικρότερο βαθμό σε σχέση με αντίστοιχο ιστό ο οποίος είχε υποβληθεί σε επεξεργασία με γλουταραλδεΰδη [Abolhoda et al., 1996]. Επιπλέον, έχουν γίνει μελέτες που αναφέρουν τη χρήση άλλων μεθόδων επεξεργασίας βιοπροσθετικών βαλβίδων, πέρα από αυτή με γλουταραλδεΰδη, οι οποίες έχουν δώσει ικανοποιητικά αποτελέσματα όσον αφορά στο μειωμένο βαθμό ασβεστοποίησής τους [Pathak et al., 1990 ; Vyavahare et al., 1997 ; Xi et al., 1992]. Η σημαντική διαφορά που παρουσιάζεται στους ρυθμούς κρυστάλλωσης του OCP στους ιστούς που ασβεστοποιήθηκαν και οι οποίοι υπέστησαν την ίδια χημική κατεργασία με γλουταραλδεΰδη, μπορεί να εξηγηθεί από τη γωνία επαφής, θ, μεταξύ της κρυσταλλικής φάσης και της στερεής επιφάνειας, όπως αναφέρθηκε και στο θεωρητικό υπόβαθρο της ετερογενούς πυρηνογένεσης στο Κεφάλαιο 2. Η γωνία επαφής, θ, η οποία καθορίζει τη διαβροχή σε συστήματα υγρού στερεού, όσο μικρότερη τιμή έχει τόσο μεγαλύτερη κρυσταλλική συμβατότητα υπάρχει μεταξύ του υποστρώματος και της κρυσταλλικής φάσης και τόσο μεγαλύτερος ο ρυθμός κρυσταλλικής ανάπτυξης. Λογαριθμίζοντας την εξίσωση (2-37) και προσαρμόζοντας τα πειραματικά δεδομένα του πίνακα 5.1, προέκυψε ευθεία γραμμή της λογαριθμικής παράστασης του αρχικού ρυθμού κρυσταλλικής ανάπτυξης συναρτήσει του αντιστρόφου του τετραγώνου του υπερκορεσμού, από την κλίση της οποίας υπολογίστηκε η τιμή του όρου γ s φ 1/3 (όπου β=32 και V m = m 3 ). Επιπλέον, από την εξίσωση (2-33) και λαμβάνοντας από τη βιβλιογραφία ως τιμή για την επιφανειακή ενέργεια του OCP κατά την ομογενή κρυστάλλωση (γ hom = 60 mj m -2 ) [Boistelle R. and Lopez-Valero, 1990] υπολογίστηκε ο παράγοντας φ για το κάθε υπόστρωμα. Έτσι από τη σχέση (2-35) βρέθηκε η τιμή της γωνίας επαφής για την 118
145 κρυστάλλωση OCP σε γλωχίνες, θ=13.48 ο, σε αορτικά τοιχώματα θ=13.7 ο, σε βόειο περικάρδιο θ=13.95 ο, σε βόειο περικάρδιο Supple Peri Guard θ=14.04 ο και σε βόειο περικάρδιο Veritas Collagen Matrix θ=14.2 ο, όπου επιβεβαιώνεται η καλή κρυσταλλική συμβατότητα μεταξύ των ιστών και του OCP που κρυσταλλώθηκε. Στη βιβλιογραφία κατά την κρυστάλλωση OCP σε κολλαγόνο σε συνθήκες σταθερού υπερκορεσμού έχει αναφερθεί τιμή γωνίας επαφής, θ=35 ο [Combes et al., 1999]. Συνεπώς, κατά την ασβεστοποίηση των ιστών σημαντικό ρόλο δεν έχει μόνο η χημική επεξεργασία του ιστού αλλά και η επιφάνειά του. Επομένως, η φύση του υποστρώματος και η τροποποίηση της επιφάνειας είναι καθοριστική για τη διεργασία της κρυσταλλικής ανάπτυξης φάσεων του φωσφορικού ασβεστίου. Ο χαρακτηρισμός της κρυσταλλικής φάσης που αναπτύχθηκε στα υποστρώματα που δοκιμάσθηκαν, κατά την εισαγωγή τους στα αντίστοιχα υπέρκορα διαλύματα, έγινε με περιθλασιμετρία ακτίνων-χ (XRD) και με ανάλυση της μορφολογίας με ηλεκτρονική μικροσκοπία σάρωσης (SEM). Στο σχήμα 5.6 απεικονίζονται τα περιθλασιογράμματα ακτίνων-χ της φάσης που κρυσταλλώθηκε στους ιστούς, συγκεκριμένα σε γλωχίνα και βόειο περικάρδιο, και το περιθλασιόγραμμα ακτίνων-χ συνθετικού OCP το οποίο ελήφθη από την κρυσταλλογραφική βάση δεδομένων Search Match (Αρ. Κάρτας ) [Crystallographica-Search Match, 1996]. Θα πρέπει να σημειωθεί ότι τα περιθλασιογράμματα των ασβεστοποιημένων ιστών παρουσίασαν αρκετό θόρυβο. Παρόλα αυτά, ήταν δυνατή η διάκριση της χαρακτηριστικής (κύριας) ανάκλασης (010) του OCP (4,73 ο σε 2θ) και στις δύο περιπτώσεις. 260 ( Intensity/a.u
146 010 Intensity/a.u Σχήμα 5.6: Περιθλασιογράμματα ακτίνων-χ (α) 1: φωσφορικού οκτασβεστίου (OCP) που κρυσταλλώθηκε σε γλωχίνες σε συνθήκες σταθερού υπερκορεσμού; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.51 (β) 2: φωσφορικού οκτασβεστίου (OCP) που κρυσταλλώθηκε σε βόειο περικάρδιο σε συνθήκες σταθερού υπερκορεσμού; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.51 και 3: συνθετικού φωσφορικού οκτασβεστίου (OCP) (Αρ ). Από τη σύγκριση των περιθλασιογραμμάτων όπου φαίνεται η ταύτιση των ανακλάσεων που ελήφθησαν λόγω της παρουσίας του στερεού που σχηματίσθηκε με τις αντίστοιχες ανακλάσεις του OCP της βάσης δεδομένων, εξήχθη το συμπέρασμα ότι το στερεό που σχηματίσθηκε ήταν το θερμοδυναμικά ασταθές (σε σχέση με τον ΗΑΡ) OCP. Στο σχήμα 5.7, παρουσιάζονται φωτογραφίες, οι οποίες ελήφθησαν με το ηλεκτρονικό μικροσκόπιο σάρωσης, της φάσης που κρυσταλλώθηκε σε γλωχίνες. 120
147 Σχήμα 5.7: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε γλωχίνες; (α), (β) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.16, (γ) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.51, (δ) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 0.69 και (ε) φάσμα μικροανάλυσης ακτίνων Χ (ΕDS) για στοιχειακή ανάλυση του δείγματος. Όπως φαίνεται και στις φωτογραφίες, παρατηρήθηκαν ποικίλες μορφολογίες του OCP, όπως φυλλόμορφοι πυκνοσχηματισμένοι κρύσταλλοι OCP, οι οποίοι είχαν μεγέθη χαρακτηριστικά των κρυσταλλιτών απατίτη (περίπου 200 nm, σχήμα 5.7 (α),(β)), πλάκες OCP μεγέθους 2-3 μm οι οποίες είναι δεμένεςˮ με τις ίνες του κολλαγόνου (σχήμα 5.7 (γ)) καθώς και πλακοειδείς σχηματισμούς OCP μεγέθους 1-2 μm, οι οποίοι υδρολύονται προς το θερμοδυναμικά σταθερότερο HAP (σχήμα 5.7 (δ)). Από το φάσμα ποιοτικής μικροανάλυσης (σχήμα 5.7 (ε)) στο δείγμα που εξετάστηκε, στο οποίο εμφανίζονται υψηλής έντασης κορυφές του ασβεστίου και του φωσφόρου, επιβεβαιώθηκε ο σχηματισμός του φωσφορικού ασβεστίου στις γλωχίνες. Στην περίπτωση κρυστάλλωσης OCP σε αορτικά τοιχώματα, σχηματίστηκαν επιμέρους πλάκες OCP μεγέθους 1-3 μm (σχήμα 5.8 (α)-(γ)) καθώς παρατηρήθηκε και 121
148 η συνύπαρξη μικροκρυστάλλων HAP με πλάκες OCP, οι οποίοι δημιουργήθηκαν από την μερική υδρόλυση του OCP (σχήμα 5.8 (δ)), η οποία πιθανώς να οφείλεται στην επεξεργασία του δείγματος και την διατήρησή του μέχρι την λήψη των φωτογραφιών. Σχήμα 5.8: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε αορτικό τοίχωμα; (α), (β) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.51, (γ) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.16 και (δ) ph 7.40, 37 C, 0.15 M NaCl, σ OCP =0.69. Η μορφολογική εξέταση στην περίπτωση κρυστάλλωσης OCP σε βόειο περικάρδιο έδειξε το σχηματισμό πλακών OCP μεγέθους 2-3 μm δεμένων με τις ίνες του κολλαγόνου (σχήμα 5.9 (α), (β)). Επιπλέον, όπως φαίνεται και στο σχήμα 5.9 (γ), παρατηρήθηκε να συνυπάρχουν οι φυλλόμορφοι πυκνοσχηματισμένοι κρύσταλλοι OCP μεγέθους 200 nm με πλάκες OCP μεγέθους περίπου 2μm, οι οποίες υδρολύονται προς λεπτούς πρισματικούς κρυστάλλους HAP μεγέθους περίπου 200 nm (σχήμα 5.9 (δ)). 122
149 Σχήμα 5.9: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε βόειο περικάρδιο; (α), (β) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.51 και (γ), (δ) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = Στις φωτογραφίες του σχήματος 5.10 που ακολουθούν, απεικονίζεται η μορφολογία της φάσης που κρυσταλλώθηκε σε βόειο περικάρδιο Supple Peri-Guard. 123
150 Σχήμα 5.10: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε βόειο περικάρδιο Supple Peri-Guard; (α), (β) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.51, (γ) γραμμική σαρωτική μικροανάλυση του δείγματος και (δ), (ε) ph 7.40, 37 C, 0.15 M NaCl, σ OCP =0.69. Παρατηρήθηκε ο σχηματισμός πλάκας OCP μεγέθους 3 μm η οποία ήταν τυλιγμένη στις ίνες του κολλαγόνου (σχήμα 5.10 (α), (β)). Η γραμμική σαρωτική μικροανάλυση έδειξε τη σταθερή συγκέντρωση ασβεστίου και φωσφόρου κατά μήκος της πλάκας OCP (σχήμα 5.10 (γ)). Επιπλέον, στα σχήματα 5.10 (δ) και 5.10 (ε) διακρίνονται η υδρολυόμενη πλάκα OCP μεγέθους 4 μm και οι πρισματικοί κρύσταλλοι HAP, της υδρολυόμενης πλάκας, μεγέθους nm, αντίστοιχα. 124
151 Η μορφολογική εξέταση της φάσης που εναποτέθηκε στην περίπτωση κρυστάλλωσης του OCP σε βόειο περικάρδιο Veritas Collagen Matrix, έδειξε το σχηματισμό πλακών OCP μεγέθους 2-4 μm (σχήμα 5.11 (α), (β)), οι οποίες όπως φαίνεται και στο σχήμα 5.11 (γ) και 5.11 (δ), υδρολύονται προς απατιτικούς μικροκρυστάλλους. Σχήμα 5.11: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε βόειο περικάρδιο Veritas Collagen Matrix; (α) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.16, (β) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.51 και (γ), (δ) ph 7.40, 37 C, 0.15 M NaCl, σ OCP = Θα πρέπει ωστόσο να σημειωθεί, ότι σε συνθήκες σταθερού υπερκορεσμού, σταθεροποιήθηκε σε όλα τα υποστρώματα η φάση του OCP ενώ η παρουσία των κρυσταλλιτών ΗΑΡ που ταυτοποιήθηκε, οφείλεται πιθανώς στον χρόνο που μεσολάβησε μεταξύ λήψεως και μορφολογικής εξετάσεως των δειγμάτων, δεδομένου του ότι, στα υπέρκορα διαλύματα η σύσταση διατηρείτο σταθερή εντός των αναλυτικών 125
152 σφαλμάτων. Σε περίπτωση κατά την οποία η υδρόλυση λάμβανε χώρα σε σημαντικό βαθμό, ταυτόχρονα με την κρυσταλλική ανάπτυξη δεν θα ήταν δυνατή η διατήρηση σταθερής της σύστασης του διαλύματος, κάτι το οποίο επιτυγχάνεται με την προσθήκη αντιδραστηρίων με την στοιχειομετρική αναλογία μόνον του καταβυθιζόμενου OCP. 126
153 ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟΥ 5 Abolhoda Α., Yu S., Oyarzun J.R, McCormick J.R., Bogden J.D., Gabbay S., Calcification of Bovine Pericardium: Glutaraldehyde Versus No-React Biomodification, Ann Thorac Surg, 62, pp , (1996) Black M.M., Drury P.J. and Tindale W.B., Twenty five years of heart valve substitutes: A review, Journal of the Royal Society of Medicine, 76, pp , (1983) Boistelle R. and Lopez-Valero I., Growth units and nucleation: The case of calcium phosphates, Journal of Crystal Growth, 102, pp , (1990) Broom N.D. and Thomson F.G., Influence of fixation conditions on the performance of glutaraldehyde-treatedporcine aortic valves: Towards a more scientific basis, Thorax., 34, pp , (1979) Carpentier A., Lemaigre G., Robert L., Carpentier S., Dubost C., Biological factors affecting long-term results of valvular heterografts, J Thorac Cardiovasc Surg, 58, pp , (1969) Combes C., Rey C., Freche M., In vitro crystallization of octacalcium phosphate on type I collagen: influence of serum albumin, Journal of Materials Science: Materials in Medicine, 10, pp , (1999) Crystallographica, Search-Match version 2,0,3,1. A computer database, Oxford: Cryosystems, (1996) Grabenwöger M. MD, Sider J. MD, Fitzal F. MD, Zelenka C. MD, Windberger U. MD, Grimm M. MD, Moritz A. MD, Böck P. MD, Wolner E. MD, Impact of Glutaraldehyde on Calcification of Pericardial Bioprosthetic Heart Valve Material, Ann Thorac Surg, 62, pp , (1996) 127
154 Höhling H.J., Fearnhead R.W., Lotter G., The mineral components in aortic calcification studied by x-ray and electron diffraction combined with electron microscopy, Ger Med Mon., 13, pp , (1968) Kapolos J., Mavrilas D., Missirlis Y., Koutsoukos P.G., Model Experimental System for Investigation of Heart Valve Calcification In Vitro, J Biomed Mater Res (Appl Biomater), 38, pp , (1997) Koutsoukos P.G, Amjad Z., Tomson M.B., Nancollas G.H., Crystallization of calcium phosphates. A constant composition study, J Am Chem Soc., 102, pp , (1980) Koutsoukos P.G. and Nancollas G.H., Crystal growth of calcium phosphates - epitaxial considerations, Journal of Crystal Growth, 53, pp , (1981) Koutsoukos P.G., Nancollas G.H., The Mineralization of Collagen In Vitro, Colloids and Surfaces, 28, pp , (1987) Levy R.J., Glutaraldehyde and the calcification mechanism of bioprosthetic heart valves, J Heart Valve Dis, 3, pp , (1994) Mavrilas D., Kapolos J., Koutsoukos P.G., Dougenis D., Screening biomaterials with a new in vitro method for potential calcification: Porcine aortic valves and bovine pericardium, Journal of Materials Science: Materials in Medicine, 15, pp , (2004) Mavrilas D., Koutsoukos P.G., Koletsis E.N., Apostolakis E. and Dougenis D., In Vitro Evaluation for Potential Calcification of Biomaterials Used for Staple Line Reinforcement in Lung Surgery, Exp Biol Med, 231, pp , (2006) Nancollas G.H. and Purdie N., The kinetics of crystal growth, Quarterly Reviews of the Chemical Society, 18, pp. 1-20, (1964). 128
155 Nancollas G.H. and Wefel J.S., Seeded Growth of Calcium Phosphates: Effect of Different Calcium Phosphate Seed Material, Journal of Dental Research, 55, pp , (1976) O'Brien M.F., Heterograft aortic valves for human use: Valve bank, techniques of measurement and implantation, J. Thorac. Cardiovasc. Surg., 53, pp , (1967) Pathak Y.V., Boyd J., Levy R.J. and Schoen F.J., Prevention of calcification of glutaraldehyde pretreated bovine pericardium through controlled release polymeric implants: studies of Fe 3+, A1 3+, protamine, sulphate and levamisole, Biomaterials, 11, pp , (1990) Rokita E., Cichocki T., Heck D., Jarczyk L., Milos A., Ryczek J., Strzałkowski A., Szytuła A., Physicochemical characterization of the inorganic phases in the aortic wall of young individuals, Pathologica, 84, pp , (1992) Schoen F.J., Tsao J.W. and Levy R.J., Calcification of bovine pericardium used in cardiac valve bioprostheses: implications for the mechanisms of bioprosthetic tissue mineralization, Am J Pathol, 123, pp , (1986) Tomson M.B. and Nancollas G.H., Mineralization kinetics: A constant composition approach, Science, 200, pp , (1978) Vyavahare N., Hirsch D., Lerner E., Baskin J.Z., Schoen F.J., Bianco R., Kruth H.S., Zand R., Levy R.J., Prevention of Bioprosthetic Heart Valve Calcification by Ethanol Preincubation, Circulation, 95, pp , (1997) Xi Τ., Ma J., Tian W., Lei X., Long S. and Xi B., Prevention of tissue calcification on bioprosthetic heart valve by using epoxy compounds: A study of calcification tests in vitro and in vivo, Journal of Biomedical Materials Research, 26, pp , (1992) 129
156 130
157 ΚΕΦΑΛΑΙΟ 6 ΜΕΤΡΗΣΕΙΣ ΕΠΙΦΑΝΕΙΑΚΟΥ ΦΟΡΤΙΟΥ ΒΙΟΛΟΓΙΚΩΝ ΙΣΤΩΝ ΜΕ ΤΗ ΜΕΘΟΔΟ ΤΟΥ ΔΥΝΑΜΙΚΟΥ ΡΟΗΣ (STREAMING POTENTIAL) 131
158 6.1 ΕΙΣΑΓΩΓΗ Κατά την επαφή επιφανειών ή σωματιδίων με ηλεκτρολυτικό διάλυμα, δημιουργείται ηλεκτρική διπλοστιβάδα (ή ιονοστιβάδα), δηλαδή μια συγκεκριμένη διαμόρφωση των ηλεκτρικών φορτίων μεταξύ φορτισμένου ηλεκτρικά υποστρώματος και ηλεκτρολυτικού διαλύματος. Οι βιολογικοί ιστοί, μεταξύ άλλων, περιλαμβάνουν ιονιζόμενες χαρακτηριστικές ομάδες, οι οποίες θα μπορούσαν θεωρούνται υπεύθυνες για την δημιουργία του επιφανειακού φορτίου, το οποίο είναι καθοριστικής σημασίας, τόσο για τις ροφητικές ικανότητες των αντίστοιχων ιστών, και πιθανώς και για την ασβεστοποίησή τους. Οι μετρήσεις του επιφανειακού φορτίου είναι δυσχερείς και μπορούν να επιτευχθούν μόνο με μεθόδους κατά τις οποίες το υπόστρωμα παραμένει σταθερό, ενώ κινείται το ηλεκτρολυτικό διάλυμα (μετρήσεις δυναμικού ροής, streaming potential). Οι κυριότερες παράμετροι που αφορούν στο χαρακτηρισμό της συμπεριφοράς των υλικών σε συνθήκες επαφής με ηλεκτρολυτικό διάλυμα, είναι το ζ-δυναμικό και η επιφανειακή αγωγιμότητα. Το ζ-δυναμικό είναι μία πολύ σημαντική παράμετρος καθώς καθορίζει το μέγεθος του φορτίου στο επίπεδο ολίσθησης της ηλεκτρική διπλοστοιβάδα η οποία σχηματίζεται στη διεπιφάνεια υποστρώματος ηλεκτρολυτικού διαλύματος. Η μέθοδος μέτρησης δυναμικού επιφανειών με μετρήσεις του δυναμικού ροής, xρησιμοποιείται ευρέως για το χαρακτηρισμό του επιφανειακού φορτίου μεμβρανών μικροδιήθησης, νανοδιήθησης και αντίστροφης ώσμωσης, κυρίως για την αντιμετώπιση του φαινομένου της απόφραξης (fouling) των μεμβρανών λόγω της συσσώρευσης αιωρούμενων στην υγρή φάση σωματιδίων. Στις περιπτώσεις αυτές, κατάλληλη τροποποίηση των επιφανειών των μεμβρανών βελτιώνει την συμπεριφορά τους ως προς την απόφραξη λόγω προσκολλήσως αιωρουμένων σωματιδίων [Chapman Wilbert et al., 1998 ; Lawrence et al., 2006]. Στο κεφάλαιο αυτό, παρουσιάζονται για πρώτη φορά, μετρήσεις δυναμικού ροής και υπολογισμοί του αντίστοιχου επιφανειακού δυναμικού (ζ- δυναμικό) ιστών, πρό και μετά την ασβεστοποίησή τους με άλατα του φωσφορικού ασβεστίου. Οι μετρήσεις έγιναν με την τεχνική της μέτρησης του δυναμικού ροής με ηλεκτρολυτικά διαλύματα NaCl και KNO 3. Τα δύο διαφορετικά ηλεκτρολυτικά διαλύματα χρησιμοποιήθηκαν για λόγους σύγκρισης επειδή το KNO 3 θεωρείται αδρανής ηλεκτρολύτης σε σύγκριση με το NaCl, όπου υπάρχει πιθανότητα ειδικής προσρόφησης των ιόντων του στις μετρούμενες 132
159 επιφάνειες, η οποία έχει ως αποτέλεσμα την διαφοροποίηση των μετρούμενων τιμών του δυναμικού ζ. 6.2 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Ηλεκτρική Διπλοστιβάδα Όταν στερεά σωματίδια ή επιφάνεια έρχονται σε επαφή με κάποιο πολικό μέσο το επιφανειακό ηλεκτρικό τους φορτίο υφίσταται αναδιάταξη. Οι ιοντικές ουσίες αποκτούν επιφανειακό φορτίο λόγω της άνισης διάλυσης στο πολικό μέσο των αντίθετα φορτισμένων ιόντων από τα οποία αποτελούνται. Η εμφάνιση επιφανειακού φορτίου προκαλείται επίσης από προσρόφηση ιόντων ή φορτισμένων μορίων στην επιφάνεια, από προσρόφηση και προσανατολισμό διπόλων στην επιφάνεια ή από ιονισμό επιφανειακών ομάδων. Η παρουσία του επιφανειακού φορτίου επηρεάζει την κατανομή των ιόντων στο πολικό μέσο. Ιόντα αντίθετου φορτίου (counter-ions) έλκονται προς την επιφάνεια, ενώ ιόντα με ίδιο φορτίο (co-ions) απωθούνται από την επιφάνεια. Δημιουργείται έτσι μια ιονική ατμόσφαιρα γύρω από το φορτισμένο σωματίδιο, η οποία καλείται ηλεκτρική διπλοστιβάδα ή ιονοστιβάδα [Κουτσούκος, 1996 ; Lyklema, 1995]. Το ηλεκτρικό φορτίο στην επιφάνεια ενός σωματιδίου κατανέμεται ομοιόμορφα και αντισταθμίζεται από ιόντα αντιθέτου φορτίου, η συγκέντρωση των οποίων μειώνεται εκθετικά αυξανομένης της απόστασης από την επιφάνεια. Σε όλες τις περιπτώσεις, το σύνολο σωματίδιο-ηλεκτρική διπλοστιβάδα είναι αφόρτιστο ηλεκτρικά. Οι πρώτες προσπάθειες περιγραφής της ηλεκτρικής διπλοστιβάδας έγιναν από τους Helmholtz, Gouy και Chapman σύμφωνα με τους οποίους η ηλεκτρική διπλοστιβάδα αποτελείται από δύο βασικές περιοχές. Την εσωτερική ή συμπαγής περιοχή, η οποία περιλαμβάνει προσροφημένα ιόντα και την διάχυτη περιοχή, στην οποία τα ιόντα κατανέμονται υπό την επίδραση ηλεκτροστατικών δυνάμεων και της τυχαίας θερμικής κίνησης. Το επίπεδο που διαχωρίζει τις δύο αυτές περιοχές ονομάζεται διατμητικό ή επίπεδο ολίσθησης (shear ή slipping plane). Ο Stern πρότεινε ένα μοντέλο κατά το οποίο η διπλοστιβάδα χωρίζεται σε δύο μέρη με το επίπεδο Stern, το οποίο βρίσκεται σε απόσταση περίπου ίση με την ακτίνα των αφυδατωμένων ιόντων. Το μοντέλο του Stern λαμβάνει υπόψη του και τα ειδικά προσροφημένα ιόντα στην επιφάνεια. Ο Grahame πρότεινε μια βελτιωμένη έκδοση του μοντέλου Stern σύμφωνα με την οποία γίνεται διάκριση μεταξύ ενός εξωτερικού και ενός εσωτερικού επιπέδου 133
160 Helmholtz. Το εξωτερικό ταυτίζεται με το επίπεδο Stern, ενώ το εσωτερικό αποτελεί τον γεωμετρικό τόπο των κέντρων των ιόντων τα οποία αφυδατώνονται κατά την προσρόφηση. Η μεταβολή του δυναμικού στην ηλεκτρική διπλοστιβάδα είναι συνάρτηση της απόστασης από την φορτισμένη επιφάνεια. Το δυναμικό μεταβάλλεται γραμμικά στην συμπαγή περιοχή και εκθετικά στην διάχυτη περιοχή της ηλεκτρικής διπλοστιβάδας. Το δυναμικό του σωματιδίου είναι το δυναμικό στο εξώτατο όριο της διαχωριστικής στιβάδας σωματιδίου / μέσου, που δεν είναι άλλο από το επίπεδο ολίσθησης. Το δυναμικό στο επίπεδο αυτό ονομάζεται ηλεκτροκινητικό ή ζ-δυναμικό. Το ζ-δυναμικό σχετίζεται με τις ηλεκτροστατικές αλληλεπιδράσεις μεταξύ σωματιδίων. Σχήμα 6.1: Η δομή της ηλεκτρικής διπλοστοιβάδας κατά τη θεωρία Stern. Τα ηλεκτροκινητικά φαινόμενα διακρίνονται ως εξής [Lyklema, 1995]: (α) ηλεκτροφόρηση (electrophoresis). Κατά την ηλεκτροφόρηση η σχετική κίνηση της φορτισμένης επιφάνειας ως προς τον θεωρούμενο στάσιμο διαλύτη γίνεται εξ αιτίας του εφαρμοζόμενου ηλεκτρικού πεδίου, (β) ηλεκτροώσμωση (electro osmosis), όπου η σχετική κίνηση του διαλύτη ως προς την θεωρούμενη στάσιμη επιφάνεια γίνεται εξ 134
161 αιτίας του εφαρμοζόμενου ηλεκτρικού πεδίου. Δηλαδή, αποτελεί συμπληρωματικό της ηλεκτροφόρησης φαινόμενο, (γ) δυναμικό ροής (streaming potential). Με τον όρο αυτό χαρακτηρίζεται το ηλεκτρικό πεδίο που δημιουργείται όταν ένα ρευστό αναγκάζεται να κινηθεί κατά μήκος μιας στάσιμης φορτισμένης επιφάνειας. Πρόκειται, δηλαδή, για αντίθετο της ηλεκτροώσμωσης φαινόμενο, και (δ) δυναμικό καθίζησης (sedimentation potential), κατά το οποίο ηλεκτρικό πεδίο δημιουργείται από την σχετική κίνηση φορτισμένων σωματιδίων ως προς ένα στάσιμο ρευστό. Αποτελεί, δηλαδή, το αντίθετο της ηλεκτροφόρησης φαινόμενο. Τα ηλεκτροκινητικά φαινόμενα εξαρτώνται από την ίδια τη φύση της ηλεκτρικής διπλοστοιβάδας και όλες οι πληροφορίες που μπορούν να αντληθούν από την μελέτη τους σχετίζονται με τις ιδιότητες της επιφάνειας. Από τα τέσσερα αυτά ηλεκτροκινητικά φαινόμενα, η ηλεκτροφόρηση παρουσιάζει την μεγαλύτερη πρακτική εφαρμογή και συγκεντρώνει το μεγαλύτερο ενδιαφέρον, ενώ σε μικρότερη έκταση έχουν μελετηθεί η ηλεκτροώσμωση και το δυναμικό ροής Ρευματικό Δυναμικό Σε τριχοειδή αγγεία Η εξαγωγή των κλασικών εξισώσεων που συνδέουν το ρευματικό δυναμικό ή δυναμικό ροής (streaming potential) με το ζ δυναμικό, βασίζεται σε δυο σημαντικές παραδοχές: α) Θεώρηση γραμμικής ροής: Αυτή η συνθήκη επαληθεύεται εύκολα στην πράξη καθώς, σε ίσιους σωλήνες, όπως είναι και τα τριχοειδή αγγεία, εκδηλώνονται στροβιλισμοί για αριθμούς Reynolds περίπου ίσους με 2000 [Hunter, 1981], μια τιμή δηλαδή, η οποία είναι αρκετά υψηλή για τις σχετικά χαμηλές ταχύτητες ροής που απαιτούνται στις μετρήσεις ρευματικού δυναμικού. β) Θεώρηση πως η ηλεκτρική διπλοστοιβάδα είναι πολύ λεπτή σε σχέση με την ακτίνα του τριχοειδούς (κr>>1), του οποίου η επιφάνεια επομένως, μπορεί να θεωρηθεί επίπεδη. Όπου, κ το αντίστροφο μήκος Debye, το οποίο καθορίζει το πάχος της ηλεκτρικής διπλοστοιβάδας και r η ακτίνα του σωματιδίου. Έστω P η ασκούμενη διαφορά πίεσης στα άκρα τριχοειδούς αγγείου ακτίνας, r, και μήκους, l (σχήμα 6.2). 135
162 Σχήμα 6.2: Προφίλ ταχυτήτων υγρού σε τριχοειδές. Όπως έχει ήδη ειπωθεί η ροή είναι γραμμική, οπότε η ταχύτητα του υγρού σε απόσταση y από τον άξονα του αγγείου δίνεται από την Eξίσωση του Poiseuille : 2 ( y) P( r 2 y ) / 4l (6-1) z όπου, η το ιξώδες. Επίσης, θεωρείται ως δεδομένο ότι το συνολικό ηλεκτρικό φορτίο, το οποίο μεταφέρει το κινούμενο υγρό, βρίσκεται περιορισμένο στη διπλοστοιβάδα, η οποία είναι μια λεπτή περιοχή κοντά στο τοίχωμα του αγγείου. Αυτό σημαίνει ότι, σε απομακρυσμένη από τη διπλοστοιβάδα περιοχή (κυρίως διάλυμα), το υγρό δε μεταφέρει φορτίο και επομένως μόνο τιμές του y πολύ κοντά στην περιοχή όπου y r παίζουν ρόλο στον προσδιορισμό του ρεύματος, I s, το οποίο οφείλεται στη μεταφορά φορτίου από την κινούμενη φάση (streaming current). Ως εκ τούτου, το y μπορεί να θεωρηθεί περίπου ίσο με το r και η εξίσωση (6-1) να μετασχηματισθεί ως εξής [Hunter, 1993] : ( y) P( r y)2r / 4 l (6-2) z 136
163 ή ( x) Pr x / 2 l (6-3) z όπου, x = r y. Το ρεύμα, I s, το οποίο δεν είναι άλλο από το συνολικό ηλεκτρικό φορτίο που μεταφέρεται από το κινούμενο υγρό ανά μονάδα χρόνου, δίνεται από την εξίσωση : r I s 2 y z (y) ( y) dy (6-4) o ή I o Prx 2 ( r x) ( x dx (6-5) 2l s ) r όπου, ρ η πυκνότητα φορτίου. Επειδή για τον προσδιορισμό του I s, οι τιμές εκείνες του x που έχουν σημασία περιορίζονται στη διπλοστοιβάδα, θεωρούνται αμελητέες σε σχέση με την ακτίνα του τριχοειδούς, δηλαδή ισχύει r x r και η εξίσωση (6-5) γίνεται : 2 o r P I s x( x) dx l r (6-6) Με αντικατάσταση της πυκνότητας φορτίου ρ(x), η οποία σχετίζεται με το δυναμικό ψ, ψ x = ψ ο exp (-κx) (6-7) όπου, ψ ο το δυναμικό στην επιφάνεια, από την εξίσωση του Poisson (εξίσωση 6-8) για τη μεταβολή της πυκνότητας φορτίου σε μία μόνο διάσταση 2 d x x (6-8) 2 4 dx 137
164 και ολοκληρώνοντας, προκύπτει: I s 2 r P l o r x o d 2 dx dx 2 r 2 P o l d x dx xo xr o r d dx dx r o o 2 d r P l (6-9) l 2 P o όπου, ε η διηλεκτρική σταθερά του μέσου και ε ο η διηλεκτρική σταθερά του κενού. Ο πρώτος όρος της αγκύλης είναι ίσος με το μηδέν καθώς το δυναμικό για x = r είναι επίσης μηδέν και επομένως dψ/dx = 0. Όσον αφορά στο ρεύμα, το οποίο οφείλεται στην κίνηση των ιόντων υπό την επίδραση του αναπτυσσόμενου στα άκρα του τριχοειδούς δυναμικού (conduction current), κανένα σημαντικό σφάλμα δεν υπεισέρχεται στους υπολογισμούς, κάνοντας την παραδοχή πως η συνεισφορά του φαινομένου της ηλεκτροώσμωσης είναι αμελητέα. Επομένως, η ολική αντίθετη ροή ιόντων λαμβάνει χώρα αποκλειστικά και μόνο λόγω της αγωγιμότητας (ρεύμα αγωγιμότητας, conduction current). Το ρεύμα αγωγιμότητας, I c, δίδεται εξ ορισμού από την παρακάτω εξίσωση στην οποία, E, είναι το αναπτυσσόμενο δυναμικό στα άκρα του τριχοειδούς και, K L, η αγωγιμότητα του κυρίως διαλύματος : I c 2 L rek (6-10) l Όταν το φαινόμενο φτάσει σε μόνιμη κατάσταση, το συνολικό ρεύμα είναι ίσο με μηδέν, δηλαδή, I s + I c = 0, και το αναπτυσσόμενο στα άκρα του τριχοειδούς δυναμικό είναι το ρευματικό δυναμικό, E str, και επομένως : or l 2 P r E l 2 str K L 0 (6-11) ή 138
165 E str P o (6-12) L K Η εξίσωση (6-12) είναι γνωστή ως εξίσωση Smoluchowski. 6.3 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Αντιδραστήρια και Υποστρώματα Το νερό που χρησιμοποιήθηκε στα πειράματα και στην παρασκευή διαλυμάτων ήταν τριπλά αποσταγμένο (αγωγιμότητα < 2.5 μs cm -1 ). Ηλεκτρολυτικά διαλύματα χλωριούχου νατρίου, ΝaCl (Merck) και νιτρικού καλίου, ΚΝΟ 3 (Merck) συγκέντρωσεων 0.3mΜ, 1mΜ, 3mM, 10mM και 100mΜ παρασκευάζονταν με ζύγιση και αραίωση των απαιτούμενων ποσοτήτων. Με σκοπό να είναι τα ηλεκτρολυτικά διαλύματα NaCl και KNO 3 κορεσμένα ως προς υδροξυαπατίτη (HAP), προς αποφυγή τυχόν διάλυσης των εναποθέσεων στους ασβεστοποιημένους ιστούς κατά την εισροή ηλεκτρολύτη διαμέσου αυτών, γινόταν προσθήκη μικρής ποσότητας συνθετικών κρυστάλλων HAP και αφήνονταν για μια ημέρα υπό ανάδευση. Την επομένη διηθούνταν υπό κενό με φίλτρα μεμβράνης διαμέτρου πόρων 0.2μm (Millipore) και αποθηκεύονταν σε πλαστικά δοχεία. Τα υποστρώματα που χρησιμοποιήθηκαν για τις μετρήσεις ήσαν βιολογικοί ιστοί. Συγκεκριμένα, μελετήθηκαν γλωχίνες από χοίρειες αορτικές βαλβίδες καρδιάς και βόειο περικάρδιο, πρό και μετά την ασβεστοποίησή τους, όπως αναφέρθηκε στο Κεφάλαιο Πειραματική Διάταξη και Διαδικασία Στο σχήμα 6.3 παρουσιάζεται η πειραματική διάταξη που χρησιμοποιήθηκε για τη μέτρηση του δυναμικού ροής (ή ρευματικό δυναμικό) σε ιστούς κατά την εισροή ηλεκτρολύτη διαμέσου αυτών. 139
166 Σχήμα 6.3: Πειραματική διάταξη της συσκευής μέτρησης ρευματικού δυναμικού. Η συσκευή, η οποία κατασκευάστηκε στο εργαστήριο, αποτελείτο από δύο φιάλες με ηλεκτρολυτικό διάλυμα, οι οποίες επικοινωνούσαν με σωλήνα στον οποίο ήταν τοποθετημένο το κελί μέτρησης που περιείχε κατάλληλα στερεωμένο τον υπό 140
167 μελέτη ιστό (σχήμα 6.4 (β)). Το σύστημα ήταν συνδεδεμένο με μία φιάλη αερίου αζώτου, που χρησιμοποιείτο για την εφαρμογή διαφοράς πίεσης προς εξαναγκασμό του υγρού να ρεύσει διαμέσου του κελιού. Η εφαρμοζόμενη αυτή διαφορά ελεγχόταν από μία βαλβίδα, ενώ ένα μανόμετρο έδειχνε την τιμή της. Στα δύο άκρα του κελιού, προσαρμόζονταν τα ηλεκτρόδια πλατίνας στις θέσεις 1 και 2, όπως φαίνεται στο σχήμα 6.4 (β), τα οποία διέθεταν και λεπτό σύρμα πλατίνας το οποίο προεκτεινόταν μέσα από μικρή οπή έξω από το κελί. (α) 1 2 (β) Σχήμα 6.4: (α) το κελί μέτρησης, (β) το κελί μέτρησης που περιείχε στερεωμένο τον υπό μελέτη ιστό και τα ηλεκτρόδια Pt στις θέσεις 1 και
168 Η διαφορά δυναμικού (δυναμικό ροής, Ε s ) στα άκρα των δύο ηλεκτροδίων εμετρείτο με ένα βολτόμετρο υψηλής αντίστασης εισόδου, ενώ η αγωγιμότητα του μέσου (ηλεκτρολύτη /ιστού), Κ *, μεταξύ των δύο ηλεκτροδίων με ένα αγωγιμόμετρο (Metrohm, 712). Ταυτόχρονα εμετρείτο και η ηλεκτρική αγωγιμότητα των ηλεκτρολυτικών διαλυμάτων, K L. Το σύστημα ήταν συνδεδεμένο και με έναν ηλεκτρονικό υπολογιστή, όπου καταγράφονταν οι μετρήσεις. Το ρευματικό δυναμικό μετρήθηκε σε επτά διαφορετικές πιέσεις, μεταξύ 0 και 0.35 x 10 5 N/m 2. Όλες οι μετρήσεις πραγματοποιήθηκαν στους 25 C και σε ph ισορροπίας, ph = Η μέτρηση του ph του διαλύματος γινόταν και πριν και μετά τις μετρήσεις. Κατά τη διεξαγωγή των μετρήσεων, δε σημειώθηκαν σημαντικές μεταβολές στις τιμές ph των διαλυμάτων που διέρχονταν μέσω των ασβεστοποιημένων ιστών, που σημαίνει πως δεν υπήρξε διάλυση των ασβεστούχων εναποθέσεων. Αυτό επιβεβαιώθηκε και από τις αναλύσεις των διαλυμάτων αυτών, για μετρήσεις ασβεστίου με φασματοσκοπία ατομικής απορρόφησης και φωσφορικών φασματοφωτομετρικά με την μέθοδο των βαναδομολυβδαινικών. Οι μετρήσεις ρευματικού δυναμικού έγιναν για όλα τα υποστρώματα ασβεστοποιημένων και μη βιολογικών ιστών, που προαναφέθηκαν, και στα δύο ηλεκτρολυτικά διαλύματα, NaCl και KNO 3, συγκεντρώσεων 0.3mΜ, 1mΜ, 3mM, 10mM και 100mΜ. Πριν από τη λήψη των μετρήσεων ρευματικού δυναμικού και σε κάθε αλλαγή ηλεκτρολύτη, εφαρμοζόταν στο σύστημα πίεση 0.35 bar για ένα χρονικό διάστημα έως ότου να εξισορροπηθεί και παρατηρείτο η τιμή της αγωγιμότητας του μέσου (ηλεκτρολύτη/ιστού), Κ *, συναρτήσει του χρόνου. Μετά την επίτευξη ισορροπίας, εφαρμόζοταν διαφορά πίεσης ώστε να αρχίσει η ροή του διαλύματος διαμέσου του ιστού και καταγράφοταν η εκάστοτε διαφορά δυναμικού στα άκρα των ηλεκτροδίων. 6.4 ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Από τη διαφορά δυναμικού μεταξύ των ηλεκτροδίων συναρτήσει του χρόνου, το ρευματικό δυναμικό (Ε str ) προσδιοριζόταν από την «αναπήδηση» του δυναμικού όταν εφαρμοζόταν ή όταν έπαυε να εφαρμόζεται η διαφορά πίεσης, όπως φαίνεται στο σχήμα
169 0,05 0,04 0,03 E/ mv 0,02 0,01 E str 0,00-0,01-0, t/ sec Σχήμα 6.5: Τυπικό διάγραμμα μεταβολής της διαφοράς δυναμικού με το χρόνο, στα άκρα του κελιού κατά την εφαρμογή-παύση διαφοράς πίεσης στα άκρα του. Από τη γραφική απεικόνιση των μετρούμενων τιμών ρευματικού δυναμικού, E str, συναρτήσει της εκάστοτε διαφοράς πίεσης, προέκυπτε ευθεία γραμμή, από την κλίση της οποίας, προσδιοριζόταν ο παράγοντας E str ΔP (σχήμα 6.6). 0,8 Equation y = a + b*x Adj. R-Square 0,99603 Value Standard Error I Intercept 0, ,01716 I Slope -2,8711 0,07397 E str /mv 0,4 0,0 0,0 0,1 0,2 0,3 0,4 P/ bar Σχήμα 6.6: Μεταβολή του ρευματικού δυναμικού ασβεστοποιημένου βοείου περικαρδίου συνάρτησει της εφαρμοζόμενης διαφοράς πίεσης σε 10 mm NaCl. 143
170 Από τα διαγράμματα συσχέτισης του μετρούμενου ρευματικού δυναμικού με την εφαρμοζόμενη διαφορά πίεσης προέκυψαν παρόμοιες ευθείες, με πολύ καλή γραμμική προσαρμογή για όλους τους ιστούς και σε όλες τις τιμές της ιοντικής ισχύος των ηλεκτρολυτών που μελετήθηκαν. Τα επιφανειακά δυναμικά (ζ- δυναμικά) υπολογίστηκαν για όλους τους ιστούς σε κάθε ιονική ισχύ ηλεκτρολύτη, με χρήση της εξίσωσης Smoluchowski (εξίσωση 6-12) και των αποτελεσμάτων που προέκυψαν από τις κλίσεις των διαγραμμάτων μεταβολής ρευματικού δυναμικού συναρτήσει της εφαρμοζόμενης διαφοράς πίεσης (Ε str /ΔP) και τις μετρούμενες τιμές αγωγιμότητας ηλεκτρολύτη, Κ L, Estr P o L K (6-12) Στους υπολογισμούς χρησιμοποιήθηκαν οι εξής τιμές: για τη διηλεκτρική σταθερά του κενού ε ο = A s V -1 m -1, τη διηλεκτρική σταθερά απιονισμένου νερού σε 25.0 o C, ε = [Drake et al., 1930] και το ιξώδες νερού σε 25.0 o C, η = Ν m -2 s. Επιπλέον, λήφθηκαν υπ όψιν και οι μετατροπές των μονάδων στο S.I. και για τον όρο (Ε str /ΔP), σε V N -1 m 2 και για την αγωγιμότητα Κ L, σε S m -1. Στους πίνακες 6.1 και 6.2 που ακολουθούν, συνοψίζονται οι πειραματικές συνθήκες και τα αποτελέσματα που προέκυψαν από τις μετρήσεις δυναμικού ροής σε ιστούς σε ηλεκτρολυτικά διαλύματα NaCl και KNO 3, αντίστοιχα. 144
171 Πίνακας 6.1 Πειραματικές συνθήκες και αποτελέσματα: συγκέντρωση ηλεκτρολυτικού διαλύματος, C ΝaCl, μετρούμενη αγωγιμότητα του ηλεκτρολύτη, Κ L, υπολογιζόμενη κλίση της ευθείας της γραφικής παράστασης του μετρούμενου ρευματικού δυναμικού συναρτήσει της διαφοράς πίεσης, Ε str /P, και επιφανειακό δυναμικό ιστού (ζ- δυναμικό), για τις μετρήσεις δυναμικού ροής σε ιστούς, πρό και μετά την ασβεστοποίησή τους, σε συνθήκες θερμοκρασίας θ = 25.0 o C και ph = Ιστοί πρό ασβεστοποίησης Τύπος ιστού C NaCl / mm Κ L Ε str /ΔP ζ- δυναμικό / μs cm -1 / mv bar -1 / mv Γλωχίνες Βόειο Περικάρδιο Ασβεστοποιημένοι ιστοί Τύπος ιστού C NaCl / mm Κ L Ε str /ΔP ζ- δυναμικό / μs cm -1 / mv bar -1 / mv Γλωχίνες Βόειο Περικάρδιο
172 Πίνακας 6.2 Πειραματικές συνθήκες και αποτελέσματα: συγκέντρωση ηλεκτρολυτικού διαλύματος, C KNO3, μετρούμενη αγωγιμότητα του ηλεκτρολύτη, Κ L, υπολογιζόμενη κλίση της ευθείας της γραφικής παράστασης του μετρούμενου ρευματικού δυναμικού συναρτήσει της διαφοράς πίεσης, Ε str /P, και επιφανειακό δυναμικό ιστού (ζ- δυναμικό), για τις μετρήσεις δυναμικού ροής σε ιστούς, πρό και μετά την ασβεστοποίησή τους, σε συνθήκες θερμοκρασίας θ = 25.0 o C και ph = Ιστοί πρό ασβεστοποίησης Τύπος ιστού C KNO3 / mm Κ L Ε str /ΔP ζ- δυναμικό / μs cm -1 / mv bar -1 / mv Γλωχίνες Βόειο Περικάρδιο Ασβεστοποιημένοι ιστοί Τύπος ιστού C KNO3 / mm Κ L Ε str /ΔP ζ- δυναμικό / μs cm -1 / mv bar -1 / mv Γλωχίνες Βόειο Περικάρδιο Στα σχήματα 6.7 και 6.8, που ακολουθούν, παρουσιάζεται η μεταβολή του επιφανειακού δυναμικού των ιστών που μελετήθηκαν συναρτήσει της ιοντικής ισχύος των ηλεκτρολυτικών διαλυμάτων ΝaCl και KNO 3, αντίστοιχα. 146
173 5 0-5 ζ δυναμικό/ mv Iοντική ισχύς/ mm 1 () 0-1 ζ δυναμικό/ mv Iοντική ισχύς/ mm Σχήμα 6.7: Μεταβολή του ζ- δυναμικού συναρτήσει της ιοντικής ισχύος ηλεκτρολυτικού διαλύματος NaCl συγκεντρώσεων (α) 0.3 mμ 100 mμ και (β) 0.3 mμ 10 mμ, σε θ = 25.0 o C και ph = : ( )γλωχίνων ; ( ) ασβεστοποιημένων γλωχίνων ; ( )βοείου περικαρδίου ; ( ) ασβεστοποιημένου βοείου περικαρδίου. 147
174 5 0-5 ζ δυναμικό/ mv Iοντική ισχύς/ mm 1 () 0-1 ζ δυναμικό/ mv Iοντική ισχύς/ mm Σχήμα 6.8: Μεταβολή του ζ- δυναμικού συναρτήσει της ιοντικής ισχύος ηλεκτρολυτικού διαλύματος KNO 3 συγκεντρώσεων (α) 0.3 mμ 100 mμ και (β) 0.3 mμ 10 mμ, σε θ = 25.0 o C και ph = : ( )γλωχίνων ; ( ) ασβεστοποιημένων γλωχίνων ; ( )βοείου περικαρδίου ; ( ) ασβεστοποιημένου βοείου περικαρδίου. Η επιφάνεια των προ ασβεστοποιημένων γλωχίνων και βοείου περικαρδίου βρέθηκε πως έχει αρνητικό επιφανειακό φορτίο, ενώ ασβεστοποίηση των ιστών αυτών έδωσε αρνητικότερες τιμές του ζ δυναμικού τους. Σε τιμή ιοντικής ισχύος 0.1Μ, η αύξηση του αρνητικού δυναμικού ζ, των ιστών ήταν θεαματική με την ανάπτυξη των εναποθέσεων. Τα επιφανειακά δυναμικά των γλωχίνων ήσαν λιγότερο αρνητικά σε σύγκριση με τα αντίστοιχα του βοείου περικαρδίου. Σε όλες τις περιπτώσεις, όπως 148
175 φαίνεται και στα σχήματα 6.7 και 6.8, η αύξηση της ιοντικής ισχύος οδήγησε σε αρνητικότερες τιμές ζ δυναμικού των ιστών που εξετάστηκαν. Συγκρίνοντας τους δύο ηλεκτρολύτες που χρησιμοποιήθηκαν, φαίνεται πως δεν υπάρχουν μεγάλες διαφορές στις τιμές του ζ δυναμικού των ιστών γεγονός το οποίο υποδηλώνει την απουσία σημαντικής ειδικής προσρόφησης λόγω του ηλεκτρολύτη. Η ασβεστοποίηση των διαφόρων ιστών δεν φαίνεται να συσχετίζεται με το επιφανειακό ηλεκτρικό φορτίο. Το εύρημα αυτό είναι σε συμφωνία με αναφορές στην βιβλιογραφία ότι όλα τα πολυμερή, τόσο τα θετικά όσο και αρνητικά φορτισμένα (είτε μόνα τους είτε διαμορφωμένα σε πολυστοιβαδική διάταξη) είναι δυνατόν να προκαλέσουν την ετερογενή πυρηνογένεση του φωσφορικού ασβεστίου. Για την κρυσταλλική φάση όμως αλλά και για την μορφολογία των σχηματιζόμενων κρυσταλλιτών σημασία έχει η σύσταση στο τελικό στρώμα του πολυμερούς [Ngankam et al., 2000]. Μελέτη μέτρησης δυναμικού ροής σε εμπορικές μεμβράνες αντίστροφης ώσμωσης, έδειξε πως η επίδραση της γλουταραλδεΰδης στο ζ δυναμικό της μεμβράνης δεν είναι σημαντική. Συγκέντρωση γλουταραλδεΰδης 0.2% έδειξε πως είχε αμελητέα μεταβολή στο επιφανειακό δυναμικό της μεμβράνης, ενώ σε συγκέντρωση γλουταραλδεΰδης 0.4%, σημειώθηκε πολύ μικρή μεταβολή του ζ δυναμικού, οδηγώντας σε λιγότερο αρνητική τιμή [Deshmukh and Childress, 2001]. Μετρήσεις ζ δυναμικού σε κρυστάλλους φωσφορικού οκτασβεστίου (OCP) σε ηλεκτρολύτες 0.15 Μ ΝaCl και 0.15 Μ KNO 3, σε διαφορετικούς γραμμομοριακούς λόγους Ca/P και για εύρος τιμών ph , αναφέρουν για ph 6.50 και γραμμομοριακό λόγο Ca/P = 0.1, τιμή ζ δυναμικού 4 mv και 2 mv, αντίστοιχα, ενώ για λόγο Ca/P = 1.33 και ph 6.50, θετικές τιμές ζ δυναμικού +12 mv και +15 mv, αντιστοίχως [Burke and Nancollas, 1999]. Η επιφάνεια του ΗΑΡ είναι αρνητικά φορτισμένη. Υψηλές τιμές ζ δυναμικού όπως, -25 mv και -12 mv έχουν αναφερθεί από μετρήσεις σε 0.01 Μ φωσφορικό ρυθμιστικό διάλυμα σε ph 7.0, χρησιμοποιώντας την τεχνική της μέτρησης του ρευματικού δυναμικού σε πλακοειδείς κρυστάλλους ΗΑΡ [Matsumura et al., 2003] και της μικροηλεκτροφόρησης για σωματίδια ΗΑΡ σε ph 6.50, στους 25 o C και σε ηλεκτρολύτη 0.01 Μ NaΝΟ 3 [Spanos and Koutsoukos, 2001], αντίστοιχα. Ενώ, μετρήσεις δυναμικού ροής σε πακτωμένα σωματίδια HAP, αναφέρονται σε τιμή ζ δυναμικού -4 mv, σε 0.01 Μ KCl για ph 7.0 [Skartsila and Spanos, 2006]. Η πολύ αρνητική τιμή του ζ δυναμικού παρουσία του φωσφορικού ρυθμιστικού διαλύματος, 149
176 πιθανόν οφείλεται στην ειδική προσρόφηση των αρνητικά φορτισμένων φωσφορικών ειδών. Η απόκλιση των τιμών του επιφανειακού δυναμικού για τον ΗΑP από την τεχνική του ρευματικού δυναμικού και της μικροηλεκτροφόρησης, προφανώς οφείλεται στο ότι κατά τον υπολογισμό του ζ δυναμικού από τις πειραματικές μετρήσεις του ρευματικού δυναμικού, δεν ελήφθει υπʼ όψιν η επιφανειακή αγωγιμότητα, όπου σε χαμηλές τιμές ιοντικής ισχύος είναι σημαντική. Σε κάθε περίπτωση λόγω των σχετικά χαμηλών τιμών του δυναμικού ζ (<50 mv), μπορεί να γίνει η προσέγγιση ότι το δυναμικό ζ είναι ανάλογο του ηλεκτρικού φορτίου στο επίπεδο ολίσθησης. Η αύξηση του αρνητικού ηλεκτρικού φορτίου συνεπεία της ανάπτυξης του OCP μπορεί να αποδοθεί στην μετατόπιση του επιπέδου ολίσθησης λόγω της ανάπτυξης του επιστρώματος του άλατος το οποίο έχει ομόσημο φορτίο με την επιφάνεια του πολυμερικού υλικού στο οποίο αναπτύσσεται. 150
177 ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟΥ 6 Burke E.M., Nancollas G.H., Relation of lattice ion solution composition to octacalcium phosphate dissolution kinetics, Colloids and Surfaces A: Physicochemical and Engineering Aspects, 150, pp , (1999) Chapman Wilbert M., Pellegrino J., Zydney A., Bench scale testing of surfactantmodified reverse osmosis/nanofiltration membranes, Desalination, 115, pp , (1998) Deshmukh S.S. and Childress A.E., Zeta potential of commercial RO membranes: influence of source water type and chemistry, Desalination, 140, pp , (2001) Drake F.H., Pierce G.W., Dow M.T., Measurement of the Dielectric Constant and Index of Refraction of Water and Aqueous Solutions of KCl at High Frequencies, Physical Review, 35, pp , (1930) Hunter, R.J., The Calculation of Zeta Potential, in Zeta Potential in Colloid Science, Ottewill R.H., Rowell R.L. (eds.), Academic Press: London, pp , (1981) Hunter R. J., Measuring Surface Charge and Potential, in Introduction to Modern Colloid Science, 1 st Edition, Oxford Science Publications: New York, pp , (1993) Lawrence N.D., Perera J.M., Iyer M., Hickey M.W., Stevens G.W., The use of streaming potential measurements to study the fouling and cleaning of ultrafiltration membranes, Separation and Purification Technology, 48, pp , (2006) Lyklema J. Fundamentals of Interface and Colloid Science, 2, Academic Press: London, (1995) 151
178 Matsumura H., Kawasaki K., Okumura N., Kambara M., Norde W., Characterization of the surface of protein-adsorbed dental materials by wetting and streaming potential measurements, Colloid Surface B, 32, pp , (2003) Ngankam P.A., Lavalle Ph., Voegel J.C., Szyk L., Decher G., Schaaf P. and Cuisinier F.J.G., Influence of Polyelectrolyte Multilayer Films on Calcium Phosphate Nucleation, J. Am. Chem. Soc., 122, pp , (2000) Skartsila Κ. and Spanos Ν., Physicochemical Characterization of Variously Packed Porous Plugs of Hydroxyapatite: Streaming Potential Coupled with Conductivity Measurements, Langmuir, 22, pp , (2006) Spanos N. and Koutsoukos P.G., Model Studies of the Effect of Orthophospho-L-serine on Biological Mineralization, Langmuir, 17, pp , (2001) Κουτσούκος Π.Γ., Χημεία Κολλοειδών, Εκδόσεις Πανεπιστημίου Πατρών: Πάτρα, (1996) 152
179 153
180 ΚΕΦΑΛΑΙΟ 7 MEΛETH ΤΗΣ ΚΡΥΣΤΑΛΛΙΚΗΣ ΑΝΑΠΤΥΞΗΣ ΑΛΑΤΩΝ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ ΣΕ ΑΝΟΡΓΑΝΑ ΥΠΟΣΤΡΩΜΑΤΑ ΓΙΑ ΤΗΝ ΑΝΑΠΤΥΞΗ ΒΙΟΫΛΙΚΩΝ 154
181 7.1 ΚΡΥΣΤΑΛΛΩΣΗ ΥΔΡΟΞΥΑΠΑΤΙΤΗ (ΗΑΡ) ΣΕ ΒΙΟΤΣΙΜΕΝΤΑ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ ΕΙΣΑΓΩΓΗ H κρυσταλλική ανάπτυξη αλάτων φωσφορικού ασβεστίου αποτελεί σημαντική διεργασία της βιολογικής ασβεστοποίησης. Παρότι τα το ανόργανο συστατικό των σκληρών ιστών των ανώτερων θηλαστικών αποτελείται κυρίως από βιολογικό απατίτη (μη στοιχειομετρικό υδροξυαπατίτη) είναι δυνατή η συμμετοχή και των υπολοίπων πρόδρομων κρυσταλλικών φάσεων του φωσφορικού ασβεστίου στο σχηματισμό τους [Nancollas, 1982]. Λόγω της συμβατότητας των αλάτων φωσφορικού ασβεστίου με τους βιολογικούς απατίτες, έχει αναπτυχθεί μέγαλος αριθμός βιοτσιμέντων, τα οποία σε πολλές περιπτώσεις περιέχουν συνδυασμό διαφορετικών φάσεων φωσφορικού ασβεστίου, και χρησιμοποιούνται ευρέως ως οστικά εμφυτεύματα [Dorozhkin, 2010 ; LeGeros, 1991]. Το οστό αποτελείται από οργανικό και ανόργανο υλικό. Το οργανικό μέρος, περιλαμβάνει τα κύτταρα και τη θεμέλια ουσία, η οποία αποτελείται κυρίως από κολλαγόνο και κατά ένα μικρό ποσοστό από πρωτεΐνες. Η διαδικασία σχηματισμού του οστού περιλαμβάνει την φυσιολογική ανάπτυξή του, τον επανασχηματισμό του και την ανάπλασή του [Weiner and Wagner, 1998]. Ο ιστός του οστού ή οστίτης ιστός αποτελείται από τρεις τύπους κυττάρων: (α) τους οστεοβλάστες, οι οποίοι παράγουν τα οργανικά στοιχεία της οστικής ουσίας (πχ. κολλαγόνο) στα οποία εναποτίθενται άλατα ασβεστίου με την μεσολάβηση ενζύμων, (β) τους οστεοκλάστες, οι οποίοι αποσυνθέτουν το οστό, με την έκκριση ενζύμων τα οποία διαλύουν την οστική μάζα και απαντώνται εκεί που συντελείται απορρόφηση οστίτη ιστού από τον οργανισμό, και (γ) τα οστεοκύτταρα τα οποία είναι οστεοβλάστες που περιβάλλονται με οστική μάζα από την παραγωγή του οστικού ιστού [Fetter, 1985]. Το ανόργανο μέρος του οστού αποτελείται κυρίως από υδροξυαπατίτη, στον οποίο έχουν επέλθει ιοντικές υποκαταστάσεις (Na +, Mg 2+, K +, CO 2-3, Cl - ). Αυτό το είδος απατίτη είναι γνωστό και ως μη στοιχειομετρικός υδροξυαπατίτης [Nancollas, 1982]. Οστικά ελλείμματα είναι δυνατόν να επέλθουν από κατάγματα, όπου συμβαίνει θραύση του οστού, ή από παθολογικές καταστάσεις, όπως είναι η οστεοπόρωση κατά την οποία μειώνεται η οστική πυκνότητα με αποτέλεσμα το κίνδυνο εμφάνισης κατάγματος. Σε αυτές τις περιπτώσεις μπορούν να χρησιμοποιηθούν υλικά οστικής 155
182 αποκατάστασης, για τα οποία έχει γίνει ήδη αναφορά στην ενότητα 1.1, με σκοπό να υποκαταστήσουν την οστική μάζα. Βασικά χαρακτηριστικά των βιοϋλικών οστικής αποκατάστασης, εκτός από την βιοσυμβατότητα, αποτελούν: (α) η οστεοενσωμάτωση, δηλαδή η ικανότητα ανάπτυξης χημικών δεσμών με την επιφάνεια του οστού χωρίς την παρέμβαση στρώματος από ινώδη ιστό, (β) η οστεοαγωγιμότητα, που παρέχει τη δυνατότητα στο οστό να αναπτύσσεται πάνω στην επιφάνεια του υλικού, (γ) η οστεοεπαγωγή, δηλαδή η ικανότητα να προκαλούν τη διαφοροποίηση των βλαστικών κυττάρων από τους ιστούς και (δ) η οστεογένεση, κατά την οποία μορφοποιείται το νέο οστό από οστεοαναπαραγωγικά κύτταρα που είναι ενσωματωμένα στο υλικό [Khan et al., 2005]. Για τα βιοτσιμέντα φωσφορικού ασβεστίου, όπως ο ΗΑΡ και το β-τcp που χρησιμοποιούνται ως οστικά υποκατάστατα, έχει αναφερθεί πως αποτελούν βιοσυμβατά υλικά με ικανότητα οστεοαγωγιμότητας, χωρίς να εμποδίζουν την οστεοβλαστική διαφοροποίηση των κυττάρων [Ηeise et al., 1990 ; LeGeros, 2002]. Στην παρούσα μελέτη, παρασκευάστηκαν βιοτσιμέντα φωσφορικού ασβεστίου με ανάμειξη α-φωσφορικού τριασβεστίου (α-ca 3 (PO 4 ) 2, a-tcp) με υδατικό διάλυμα Na 2 HPO 4. Έγινε φυσικοχημικός χαρακτηρισμός των στερεών και διερευνήθηκε η κινητική της κρυστάλλωσης του HAP στα απατιτικά βιοτσιμέντα σε υπέρκορα διαλύματα φωσφορικού ασβεστίου σε συνθήκες σταθερού υπερκορεσμού, στους 37 o C, σε ph 7.40 τόσο σε υδατικά διαλύματα ιοντικής ισχύος 0.15 Μ σε NaCl όσο και σε διαλύματα προσομοιωμένων βιολογικών ρευστών (m-sbf). Επιπλέον, μετρήθηκε και η κινητική της κρυστάλλωσης φωσφορικού ασβεστίου σε κρυστάλλους HAP, οι οποίοι είχαν παρασκευασθεί συνθετικά και είχαν χαρακτηρισθεί. Η μελέτη αυτή χρησιμοποιήθηκε ως σύστημα αναφοράς για την σύγκριση των αποτελεσμάτων με τα νέα υλικά ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Αντιδραστήρια Για την παρασκευή των υπέρκορων διαλυμάτων χρησιμοποιήθηκαν πυκνά πρότυπα διαλύματα ασβεστίου, CaCl 2 2H 2 O, και φωσφορικών, KH 2 PO 4, συγκεντρώσεων 0.1Μ, ενώ για την πρώτη σειρά πειραμάτων, η ιοντική ισχύς των υπέρκορων διαλυμάτων εργασίας ρυθμιζόταν στην τιμή 0.15Μ με στοκ διάλυμα 156
183 χλωριούχου νατρίου, ΝaCl, συγκέντρωσης 1Μ. Η δεύτερη σειρά πειραμάτων έγινε σε υπέρκορα διαλύματα με σύσταση τροποποιημένων προσομοιωμένων βιολογικών ρευστών (modified simulated body fluid, m-sbf), χρησιμοποιήθηκαν επιπλέον πυκνά πρότυπα διαλύματα εξαένυδρου χλωριούχου μαγνησίου, MgCl 2 6H 2 O (Merck), θειικού νατρίου, Na 2 SO 4 (Merck), και όξινου ανθρακικού νατρίου, NaHCO 3 (Merck), συγκεντρώσεων 0.1Μ, και χλωριούχου καλίου, KCl (Merck), συγκέντρωσης 1Μ. Η χημική σύσταση του τροποποιημένου προσομοιωμένου βιολογικού ρευστού (m-sbf) που χρησιμοποιήθηκε στα πειράματα κρυστάλλωσης ΗΑΡ σε συνθήκες σταθερού υπερκορεσμού, καθώς και η χημική σύσταση του προσομοιωμένου βιολογικού ρευστού (SBF) και των βιολογικών ρευστών στο πλάσμα του αίματος, παρουσιάζονται στον πίνακα 7.1. Πίνακας 7.1 Η χημική σύσταση του τροποποιημένου προσομοιωμένου βιολογικού ρευστού (m-sbf) για τα πειράματα κρυστάλλωσης ΗΑΡ σε απατιτικά τσιμέντα και σε συνθετικούς κρυστάλλους ΗΑΡ σε συνθήκες σταθερού υπερκορεσμού, του προσομοιωμένου βιολογικού ρευστού (SBF) και των βιολογικών ρευστών στο πλάσμα του αίματος. Συγκέντρωση Na + K + Mg 2+ Ca 2+ HCO 3 - Cl - HPO 4 2- SO 4 2- / mm Πλάσμα αίματος SBF m-sbf H συγκέντρωση των ανθρακικών στο m-sbf ήταν χαμηλότερη από την αντίστοιχη στο SBF, διότι σε υψηλότερες συγκεντρώσεις ανθρακικών δεν ήταν δυνατή η διατήρηση του ph στην επιθυμητή τιμή χωρίς τη χρήση ρυθμιστικών διαλυμάτων. Προκαταρκτικές μελέτες στο εργαστήριο, έδειξαν ότι το ρυθμιστικό διάλυμα που συνήθως χρησιμοποιείται (tris-buffer) δρα παρεμποδιστικά στην κρυσταλλική ανάπτυξη του φωσφορικού ασβεστίου με αποτέλεσμα να προκαλεί διαφοροποίηση των 157
184 κινητικών δεδομένων. Το διάλυμα του m-sbf, λόγω της παρουσίας ανθρακικών, παρασκευαζόταν εκ νέου πριν από κάθε πείραμα σε ποσότητα μέχρι 2L και καταναλωνόταν άμεσα. Όλα τα πρότυπα πυκνά διαλύματα που χρησιμοποιήθηκαν, παρασκευάστηκαν με τον τρόπο που αναφέρθηκε και στην ενότητα Παρασκευή και χαρακτηρισμός βιο τσιμέντων φωσφορικού ασβεστίου Αρχικά, παρασκευάστηκε το α-tcp (Ca 3 (PO 4 ) 2 ), το οποίο αποτελεί τη στερεή φάση του τσιμέντου με βάση την αντίδραση: CaCO 3 + γ-ca 2 P 2 O 7 Ca 3 (PO 4 ) 2 + CO 2 (7-1) Σε ισομοριακή αναλογία, τα αντιδρώντα: ανθρακικό ασβέστιο (CaCO 3 ) και πυροφωσφορικό ασβέστιο (Ca 2 P 2 O 7 ) κονιορτοποιήθηκαν σε γουδί. Στη συνέχεια, για να επιτευχθεί ομοιόμορφη διασπορά των σωματιδίων προστέθηκε καθαρή αιθανόλη και το αιώρημα αφέθηκε με ανάδευση με μαγνητικό αναδευτήρα για δεκαπέντε λεπτά. Στη συνέχεια, με συμπύκνωση υπό κενό, απομακρύνθηκε η αιθανόλη και ακολούθησε η πλήρης αποξήρανσή του αιωρήματος με θέρμανση στους 80 ο C για δύο ώρες περίπου, έτσι ώστε να εξατμιστούν τα υπολείμματα αιθανόλης ή νερού. Τέλος, τα στερεά θερμάνθηκαν στους 1300 ο C και ψύχθηκε απότομα σε θερμοκρασία δωματίου προκειμένου να ληφθεί το τελικό προϊόν. Το στερεό προϊόν αλέσθηκε σε σφαιρόμυλο για μία ώρα ώστε να συνθλιβούν τα συσσωματώματα του α-tcp που δημιουργήθηκαν λόγω της υψηλής θερμοκρασίας και να επιτευχθεί το επιθυμητό μέγεθος κόκκων, το οποίο σύμφωνα με τη βιβλιογραφία πρέπει να είναι μικρότερο των 100 μm [Komath et al, 2000]. Μετά την παραγωγή και την άλεση του α-tcp το προϊόν αποθηκεύθηκε σε θερμοκρασία δωματίου και μέσα σε ξηραντήρα υπό κενό. Η διασφάλιση ξηρού περιβάλλοντος αποθήκευσης του α-tcp ήταν σημαντική, διότι το προϊόν έχει την τάση να δεσμεύει μόρια νερού από την ατμόσφαιρα με αποτέλεσμα το μετασχηματισμό του σε απατίτη. Το στερεό, πλέον, α-tcp αναμείχθηκε με υδατικό διάλυμα Na 2 HPO 4 με αναλογία υγρού/στερεού ίση με 0.32 ml/g. Στη συνέχεια, με τη βοήθεια σπάτουλας, το μείγμα ομογενοποιήθηκε και τοποθετήθηκε σε καλούπια διαστάσεων 6 cm x 1.5 cm και αφέθηκε για σκλήρυνση (setting) σε κλειστό δοχείο με συνθήκες υγρασίας 100% για
185 ώρες. Κατόπιν, τα δοκίμια αφαιρέθηκαν από τα καλούπια και τοποθετήθηκαν σε πλαστικά δοχεία περιέχοντα διάλυμα Ringer σε θερμοκρασία 37 o C έτσι ώστε να μετατραπεί το α-tcp σε ΗΑΡ. Το διάλυμα Ringer είναι εμπλουτισμένος ορρός, η σύσταση του οποίου παρουσιάζεται στον πίνακα 7.2. Πίνακας 7.2 Σύσταση του διαλύματος Ringer Όνομα Χημικός τύπος Ποσότητα g/ 100 ml Γαλακτικό νάτριο CH 3 CH(OH)COONa 0.31 Χλωριούχο Νάτριο NaCl 0.60 Χλωριούχο κάλιο KCl 0.03 Χλωριούχο Ασβέστιο CaCl 0.02 Τα δείγματα παρέμειναν σε θερμοκρασία 37 ο C έτσι ώστε να αρχίσει η διαδικασία μετασχηματισμού του TCP σε απατίτη. Σε χρονικά διαστήματα 24 h, 31 h, 48 h και 380 h αφαιρέθηκαν δοκίμια από το διάλυμα, λυοφιλοποιήθηκαν (freeze drying) και χαρακτηρίστηκαν με περιθλασιμετρία ακτίνων-χ (XRD) και με ηλεκτρονική μικροσκοπία σάρωσης (SEM). Η στερεά φάση που παρασκευάστηκε (βιοτσιμέντο) χαρακτηρίστηκε με περιθλασιμετρία ακτίνων-χ. Στο σχήμα 7.1 παρουσιάζεται το περιθλασιόγραμμα της στερεάς φάσης σε σύγκριση με πρότυπα περιθλασιογράμματα ακτίνων-χ συνθετικού α- TCP, β-tcp και υδροξυαπατίτη (ΗΑΡ), τα οποία ελήφθησαν από την κρυσταλλογραφική βάση δεδομένων Search-Match (Αρ. Κάρτας 9-348, και 9-432, αντίστοιχα). 159
186 Intensity/ a.u Σχήμα 7.1: Περιθλασιογράμματα ακτίνων-χ 1: στερεάς φάσης που παρασκευάστηκε (βιοτσιμένο), 2: συνθετικού α-tcp (Αρ ), 3: συνθετικού β-tcp (Αρ ) και 4: συνθετικού ΗΑΡ (Αρ ). Όπως προέκυψε από τη σύγκριση των περιθλασιογραμμάτων ακτίνων-χ, το υλικό που παρασκευάστηκε εκτός από το α-tcp περιείχε και ανιχνεύσιμη ποσότητα β- TCP. Οι κύριες ανακλάσεις (1 7 0) για το α-tcp (30,8 ο σε 2θ) και (0 2 10) για το β- TCP (31,04 ο σε 2θ) είναι χαρακτηριστικές στο τσιμέντο που παρασκευάστηκε. Επιπλέον, στη στερεά φάση που παρασκευάστηκε, δεν διαπιστώθηκε η παρουσία υδροξυαπατίτη (ΗΑΡ) [Κατσαμένης, 2006]. Μετά την τοποθέτηση των δοκιμίων σε διάλυμα Ringer σε τακτά χρονικά διαστήματα γινόταν αφαίρεση δειγμάτων από το διάλυμα με σκοπό τη μελέτη της μετατροπής της στερεάς φάσης που παρασκευάστηκε σε υδροξυαπατίτη (ΗΑΡ). Στο σχήμα 7.2 παρουσιάζονται συγκριτικά τα περιθλασιογράμματα ακτίνων-χ δειγμάτων που ελήφθησαν σε 24, 54, και 380 ώρες. Επιπλέον, παρουσιάζονται και τα περιθλασιογράμματα ακτίνων-χ της στερεάς φάσης που παρασκευάστηκε και του συνθετικού υδροξυαπατίτη (ΗΑΡ). 160
187 Intensity/ a.u Σχήμα 7.2: Περιθλασιογράμματα ακτίνων-χ 1: στερεάς φάσης που παρασκευάστηκε (βιοτσιμένο), 2: στερεάς φάσης που παρασκευάστηκε μετά από παραμονή 24 h σε διάλυμα Ringer, 3: στερεάς φάσης που παρασκευάστηκε μετά από παραμονή 54 h σε διάλυμα Ringer, 4: στερεάς φάσης που παρασκευάστηκε μετά από παραμονή 380 h σε διάλυμα Ringer και 5: συνθετικού υδροξυαπατίτη (ΗΑΡ) (Αρ ). Όπως φαίνεται, ο μετασχηματισμός της στερεάς φάσης σε ΗΑΡ ήταν αρκετά έντονος στις πρώτες 24 ώρες. Αυτό διακρίνεται από την εμφάνιση των χαρακτηριστικών ανακλάσεων (0 0 2), (2 1 1), (1 1 2) και (3 0 0) του ΗΑΡ (25,9 ο ; 31,8 ο ; 32,23 ο και 32,93 ο σε 2θ, αντίστοιχα). Στο διάστημα των 380 ωρών που έγιναν οι μετρήσεις 161
188 παρατηρήθηκε πλήρης μετατροπή του α-tcp σε απατίτη. Ωστόσο, η κύρια ανάκλαση (0 2 10) του β-tcp (31,04 ο σε 2θ) παρέμεινε σχεδόν αναλλοίωτη, γεγονός που δείχνει την παραμονή ενός ποσοστού β-tcp στο τελικό προϊόν [Κατσαμένης, 2006]. Ο χαρακτηρισμός του βιοτσιμέντου πραγματοποιήθηκε και με φασματοσκοπία υπερύθρου FT-IR, όπως παρουσιάζεται στο σχήμα 7.3. ιαπερατότητα % PO 3-4 PO 3-4 OH - OH - OH Κυματάριθμος/ cm -1 Σχήμα 7.3: Φάσμα υπερύθρου του βιοτσιμέντου που παρασκευάστηκε. Οι κορυφές απορρόφησης στα 565 cm -1 και 602 cm -1 αποδίδονται στην τριπλώς εκφυλισμένη δόνηση κάμψης (ν 4 ) των δεσμών Ο-Ρ-Ο του ΗΑΡ [Fowler, 1974], ενώ η κορυφή στα 1040 cm -1 οφείλεται στη φωσφορική ομάδα του β-tcp [Shibata et al., 2005]. Οι κορυφές απορρόφησης στα 1645 cm -1 και στα 3440 cm -1, αποδίδονται σε προσροφημένα μόρια νερού, όπου διακρίνεται και η μικρή κορυφή στα 3570 cm -1 που αποδίδεται σε δόνηση τάσης (ν s ) της υδροξυλομάδας του ΗΑΡ [Ashok et al., 2003 ; Fowler, 1974]. Στη συνέχεια, παρουσιάζονται φωτογραφίες, οι οποίες ελήφθησαν με το ηλεκτρονικό μικροσκόπιο σάρωσης, της αρχικής στερεάς φάσης που παρασκευάστηκε και των δειγμάτων αυτής μετά από διαφορετικούς χρόνους παραμονής σε διάλυμα Ringer. 162
189 163
190 Σχήμα 7.4: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης της στερεάς φάσης που παρασκευάστηκε (α) πρό εμβαπτίσεως σε διάλυμα Ringer, (β), (γ) μετά από παραμονή 24 h σε διάλυμα Ringer, (δ), (ε) μετά από παραμονή 48 h σε διάλυμα Ringer και (στ), (ζ) μετά από παραμονή 380 h σε διάλυμα Ringer. Στο σχήμα 7.4 (α) φαίνεται η στερεά φάση που παρασκευάστηκε (τσιμέντο) μετά την κατεργασία της σε σφαιρόμυλο και προ της εμβαπτίσεώς της σε διάλυμα Ringer, όπου παρατηρείται μια ανομοιόμορφη κατανομή κρυστάλλων, το μέγεθος των οποίων δεν υπερβαίνει τα 10 μm. Η μορφολογία του τσιμέντου μετά από 24 h παραμονής σε διάλυμα Ringer παρουσιάζεται στο σχήμα 7.4 (β) και (γ), όπου παρατηρείται αλλαγή της μορφολογίας με την παρουσία φυλλόμορφων κρυστάλλων στην επιφάνεια του τσιμέντου. Αυτοί οι φυλλοειδείς σχηματισμοί των κρυστάλλων οφείλονται πιθανώς στο σχηματισμό φωσφορικού οκτασβεστίου (OCP), από τη διάλυση του α-tcp προς σχηματισμό του OCP. Ωστόσο, η χαρακτηριστική ανάκλαση (010) του OCP (4,73 ο σε 2θ) δεν ανιχνεύτηκε με την εξέταση των αντίστοιχων δειγμάτων με περιθλασιμετρία ακτίνων-χ. Στα σχήματα 7.4 (δ) και (ε) παρουσιάζεται η διαφορετική και πάλι μορφολογία του τσιμέντου μετά από 48 h παραμονής σε διάλυμα Ringer. Διακρίνονται βελονοειδείς σχηματισμοί απατιτικών κρυστάλλων με μήκος της τάξης των 300 nm και πάχος μικρότερο από 50 nm. Επιπλέον, στο σχήμα 7.4 (ε) φαίνεται η συνύπαρξη των φυλλόμορφων κρυστάλλων με τους βελονοειδείς σχηματισμούς. Πιθανόν σε αυτό το στάδιο να λαμβάνει χώρα υδρόλυση του OCP προς ΗΑΡ. Μετά την πάροδο 380 h, η μορφολογία του τσιμέντου χαρακτηρίζεται από την ύπαρξη βελονοειδών κρυστάλλων, υποδηλώνοντας την παρουσία απατίτη, γεγονός το 164
191 οποίο βρίσκεται σε συμφωνία και με το προηγούμενο περιθλασιόγραμμα ακτίνων-χ (σχήμα 7.2). Στο σημείο αυτό πρέπει να αναφερθεί πως η παρασκευή και ο φυσικοχημικός χαρακτηρισμός του βιο τσιμέντου, έγινε από τον κ. Ορ. Κατσαμένη υπό την επίβλεψη του Επίκ. Καθηγητή Ν. Μπουρόπουλου, από το Τμήμα Επιστήμης των Υλικών [Κατσαμένης, 2006]. Ωστόσο, τα τσιμέντα που παρασκευάστηκαν, προτού αποτελέσουν υποστρώματα για τη μελέτη της κινητικής της κρυστάλλωσης ΗΑΡ σε υπέρκορα διαλύματα, εξετάστηκαν μορφολογικά για άλλη μία φορά. Από τις φωτογραφίες που ελήφθησαν με το ηλεκτρονικό μικροσκόπιο σάρωσης, παρατηρήθηκε ποικιλία στη μορφολογία των τσιμέντων (σχήμα 7.5). 165
192 Σχήμα 7.5: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης των τσιμέντων που παρασκευάστηκαν και χρησιμοποιήθηκαν για τη μελέτη της κινητικής κρυστάλλωσης ΗΑΡ σε υπέρκορα διαλύματα με τη μέθοδο της σταθερής σύστασης υπέρκορων διαλυμάτων. Συγκεκριμένα, στο σχήμα 7.5 (α) διακρίνεται καλοσχηματισμένος κρύσταλλος ΤCP, που φαίνεται να έχει παραμείνει στο τελικό στερεό, και ο οποίος υδρολύεται προς φυλλόμορφους κρυστάλλους OCP μεγέθους 1-2 μm, όπου και αυτοί με τη σειρά τους δείχνουν να υδρολύονται προς απατιτικούς μικροκρυστάλλους (σχήμα 7.5 (β)). Η παρουσία των πλακών του TCΡ συνάδει και με το περιθλασιόγραμμα του σχήματος 6.2, από το οποίο φάνηκε να παραμένει ποσότητα β-tcp στο τελικό προϊόν. Επιπλέον, εκτός από φυλλόμορφους σχηματισμούς OCP (σχήμα 7.5 (γ)), παρατηρήθηκαν και πρισματικοί απατιτικοί μικροκρύσταλλοι μεγέθους περίπου nm και πάχους nm, όπως φαίνεται και στο σχήμα 7.5 (δ). Τέλος, όπως παρουσιάζεται στο σχήμα 7.5 (ε) και (στ), παρατηρήθηκαν και βελονοειδείς απατιτικοί κρύσταλλοι μεγέθους περίπου μm. Όπως φάνηκε και από τα αποτελέσματα της μορφολογικής εξέτασης των τσιμέντων που παρασκευάστηκαν, ο σχηματισμός του απατίτη είναι μια αρκετά πολύπλοκη διαδικασία και χρειάζεται περαιτέρω διερεύνηση καθώς περιλαμβάνει το σχηματισμό ενδιάμεσων, θερμοδυναμικά ασταθέστερων κρυσταλλικών φάσεων του φωσφορικού ασβεστίου. Παράγοντες όπως το ph και η περίσσεια ιόντων ασβεστίου είναι πολύ σημαντικοί. Η υδρόλυση του α-tcp σε OCP έχει μελετηθεί σε αραιά διαλύματα φωσφορικού οξέος και έχει βρεθεί ότι υδρολύεται σε 24 ώρες σύμφωνα με την αντίδραση [Bigi et al., 2002]: 8α Ca 3 (PO 4 ) 2 +2H 3 PO 4 +15H 2 O 3Ca 8 H 2 (PO 4 ) 6 5H 2 O (7-2) 166
193 Σε μία άλλη μελέτη περίσσειας ασβεστίου, η μετατροπή του OCP προς ΗΑΡ ήταν δυνατή σύμφωνα με τις αντιδράσεις [Xin et al., 2006]: Ca 8 H 2 (PO 4 ) 6 5H 2 O + 2Ca 2+ Ca 10 (PO 4 ) 6 (OH) 2 + 3H 2 O + 4H + (7-3) 5Ca 8 H 2 (PO 4 ) 6 5H 2 O 4Ca 10 (PO 4 ) 6 (OH) 2 + 6H 3 PO H 2 O (7-4) H ειδική επιφάνεια των παρασκευασμένων απατιτικών τσιμέντων μετρήθηκε με τη μέθοδο ρόφησης αζώτου (BET) και βρέθηκε ίση με 16 m 2 g Σύνθεση και χαρακτηρισμός συνθετικών κρυστάλλων ΗΑΡ Οι κρύσταλλοι του υδροξυαπατίτη παρασκευάστηκαν με ανάμιξη ίσων όγκων διαλυμάτων CaCl M και ΚH 2 PO M. Το διάλυμα ΚH 2 PO 4 αναδευόταν σε θερμοστατούμενο αντιδραστήρα στους 70 o C, όπου γίνονταν προσθήκες του διαλύματος CaCl 2 στάγδην, ενώ το ph διατηρούταν στην περιοχή 9-10 με προσθήκες πυκνού διαλύματος καυστικού νατρίου ΝaOH [Nancollas and Mohan, 1970]. Μετά το πέρας της διαδικασίας ακολουθούσε ωρίμανση του αιωρήματος για 5 μέρες στους 40 o C, διήθηση υπό κενό διαμέσου φίλτρου 0.22 μm, πλύσιμο με τριπλά απεσταγμένο νερό, ξήρανση σε ξηραντήρα και τέλος κονιοποίηση του στερεού με γουδί. Το κονιοποιημένο στερεό χαρακτηρίσθηκε με τις συνήθεις για τα στερεά φυσικοχημικές μεθόδους. Η ταυτοποίηση των συνθετικών κρυστάλλων ΗΑΡ που παρασκευάστηκαν πραγματοποιήθηκε με περιθλασιμετρία κόνεως ακτίνων-χ. Το λαμβανόμενο περιθλασιόγραμμα ακτίνων-χ παρουσιάζεται στο σχήμα 7.6 το οποίο και συγκρίθηκε με πρότυπο περιθλασιόγραμμα ακτίνων-χ συνθετικού υδροξυαπατίτη από την κρυσταλλογραφική βάση δεδομένων Search-Match (Αρ. Κάρτας 9-432). Συγκρίνοντας τα δύο περιθλασιογράμματα ακτίνων-χ, από την ταύτιση των κύριων χαρακτηριστικών ανακλάσεων (0 0 2), (2 1 1), (1 1 2) και (3 0 0) του ΗΑΡ (25,9 ο ; 31,8 ο ; 32,23 ο και 32,93 ο σε 2θ, αντίστοιχα), προέκυψε πως οι συνθετικά παρασκευασμένοι κρύσταλλοι ήσαν στοιχειομετρικός ΗΑΡ. 167
194 Intensity/ a.u Σχήμα 7.6: Περιθλασιογράμματα κόνεως ακτίνων-χ 1: συνθετικά παρασκευασμένου υδροξυαπατίτη (ΗΑΡ) και 2: συνθετικού υδροξυαπατίτη (ΗΑΡ) (Αρ. Κάρτας 9-432). Ο χαρακτηρισμός των συνθετικών κρυστάλλων του υδροξυαπατίτη πραγματοποιήθηκε και με φασματοσκοπία υπερύθρου FT-IR. Όπως φαίνεται στο σχήμα 7.7 οι ζώνες απορρόφησης στα 565 cm -1 και 602 cm -1 αποδίδονται στην τριπλώς εκφυλισμένη δόνηση κάμψης (ν 4 ) των δεσμών Ο-Ρ-Ο [Fowler, 1974]. Οι ζώνες στα 3570 cm -1, 1645 cm -1 και 631 cm -1, αποδίδονται σε δόνηση τάσης (ν s ), δόνηση κάμψης (ν 2 ) μορίων νερού και περιστροφικής ταλάντωσης (ν L ) της υδροξυλομάδας, αντίστοιχα, ενώ αυτή στα 870 cm -1 είναι χαρακτηριστική των όξινων φωσφορικών [Arends et al., 1987 ; Ashok et al., 2003]. Η ζώνη απορρόφησης στην περιοχή cm -1 οφείλεται στην τριπλώς εκφυλισμένη ασύμμετρη δόνηση τάσης (ν 3 ) του δεσμού Ρ-Ο της φωσφορικής ομάδας, ενώ η κορυφή στα 962 cm -1 αποδίδεται στη μη εκφυλισμένη συμμετρική δόνηση τάσης (ν 1 ) των δεσμών Ρ-Ο της φωσφορικής ομάδας [Fowler, 1974]. 168
195 4 ιαπερατότητα % PO 3-4 HPO 2- OH - PO 3-4 OH - OH Κυματάριθμος/ cm -1 Σχήμα 7.7: Φάσμα υπερύθρου συνθετικά παρασκευασμένου υδροξυαπατίτη (ΗΑΡ). Στο σχήμα 7.8 που ακολουθεί, παρουσιάζεται η μορφολογία των συνθετικά παρασκευασμένων κρυστάλλων ΗΑΡ. Πρόκειται για πρισματικούς κρυστάλλους μήκους nm και πάχους nm περίπου. Σχήμα 7.8: Φωτογραφία ηλεκτρονικής μικροσκοπίας σάρωσης των συνθετικών κρυστάλλων υδροξυαπατίτη (ΗΑΡ). 169
196 Τέλος, μετρήθηκε και η ειδική επιφάνεια των συνθετικά παρασκευασμένων κρυστάλλων ΗΑΡ με τη μέθοδο ρόφησης αζώτου (BET). Η τιμή της ειδικής επιφάνειας υπολογίστηκε 40 m 2 g Πειραματική Διάταξη και Διαδικασία Η πειραματική διάταξη που χρησιμοποιήθηκε για τα πειράματα κρυστάλλωσης ΗΑΡ σε απατιτικά τσιμέντα και συνθετικούς κρυστάλλους ΗΑΡ, με τη μέθοδο της σταθερής σύστασης, παρουσιάζεται στο σχήμα 7.9. Σχήμα 7.9: Πειραματική διάταξη για τα πειράματα κρυστάλλωσης φωσφορικού ασβεστίου με τη μέθοδο σταθερού υπερκορεσμού. 170
197 Η κρυστάλλωση σε σταθερά υπέρκορα διαλύματα, οφειλόταν στην εισαγωγή και την παρουσία των κρυσταλλικών φύτρων ή των βιοτσιμέντων στο διάλυμα εργασίας. Η σύσταση των διαλυμάτων τιτλοδότησης διαμορφωνόταν ανάλογα με τις συνθήκες του πειράματος. Για την πρώτη σειρά πειραμάτων σε ηλεκτρολυτικό διάλυμα ΝaCl, τα διαλύματα τιτλοδότησης (titrants) παρασκευάζονταν από τα πρότυπα στοκ διαλύματα ασβεστίου (0.1Μ CaCl 2 2H 2 O), φωσφορικών (0.1Μ KΗ 2 PO 4 ), χλωριούχου νατρίου (1Μ NaCl) και καυστικού νατρίου (0.1Ν NaOH) με τις απαραίτητες αραιώσεις με τριπλά απεσταγμένο νερό. Η πρώτη σύριγγα περιείχε το διάλυμα του CaCl 2 2H 2 O και το διάλυμα του αδρανούς ηλεκτρολύτη NaCl, ενώ η δεύτερη το διάλυμα του KΗ 2 PO 4 και το διάλυμα του NaOH. Ενώ για τη δεύτερη σειρά πειραμάτων σε τροποποιημένο προσομοιωμένο βιολογικό ρευστό (m-sbf), τα διαλύματα τιτλοδότησης (titrants) παρασκευάζονταν από τα πρότυπα διαλύματα ασβεστίου (0.1Μ CaCl 2 2H 2 O), φωσφορικών (0.1Μ KΗ 2 PO 4 ) και καυστικού νατρίου (0.1Ν NaOH) με τις απαραίτητες αραιώσεις με διάλυμα m-sbf, το οποίο δεν περιείχε ιόντα ασβεστίου και φωσφορικών. Οι συγκεντρώσεις των διαλυμάτων τιτλοδότησης για τα πειράματα μελέτης της κινητικής της κρυστάλλωσης ΗΑΡ τόσο σε απατιτικά τσιμέντα όσο και σε φύτρα συνθετικών κρυστάλλων ΗΑΡ, υπολογίστηκαν από τις εξισώσεις (5-1α) έως (5-5α), οι οποίες προέκυψαν από τα ισοζύγια μάζας για κάθε ιόν που συμμετέχει στην αντίδραση, όπως φάνηκε αναλυτικά στην ενότητα Στον αντιδραστήρα, το διάλυμα εργασίας παρασκευαζόταν με προσθήκη κατάλληλης ποσότητας τριπλά απεσταγμένου νερού έτσι ώστε με την προσθήκη όλων των αντιδρώντων ο τελικός όγκος του διαλύματος εργασίας να είναι 0.4L, κατάλληλων συγκεντρώσεων του αδρανούς ηλεκτρολύτη ΝaCl και του διαλύματος των φωσφορικών KH 2 PO 4. Για τη δεύτερη σειρά πειραμάτων που έγινε σε υπέρκορα διαλύματα με σύσταση τροποποιημένων προσομοιωμένων βιολογικών ρευστών (m-sbf), το διάλυμα εργασίας παρασκευαζόταν με προσθήκη κατάλληλης ποσότητας του διαλύματος m-sbf (απουσία ασβεστίου και φωσφορικών) και διαλύματος των φωσφορικών KH 2 PO 4. Στη συνέχεια γινόταν εισαγωγή των τσιμέντων στον αντιδραστήρα, τα οποία ήταν στερεωμένα πάνω σε ορθογώνια πλαίσια, όπως φαίνεται και στο σχήμα 7.9, ή εισαγόταν στο διάλυμα προζυγισμένη ποσότητα των συνθετικών κρυσταλλικών φύτρων ΗΑΡ. Το διάλυμα αναδευόταν και διοχετευόταν άζωτο κορεσμένο σε υδρατμούς προκειμένου να εξασφαλισθεί αδρανής ατμόσφαιρα. Στην περίπτωση των υπέρκορων διαλύματων με σύσταση m-sbf, η διοχέτευση του αζώτου γινόταν πάνω από το διάλυμα εργασίας με σκοπό την αποφυγή εισόδου του διοξειδίου του άνθρακα από την ατμόσφαιρα ή την 171
198 αποφυγή έκλυσής του από τα διαλελυμένα ανθρακικά. Στη συνέχεια, ρυθμιζόταν το ph του διαλύματος εργασίας στην επιθυμητή τιμή, ανάλογα με τις συνθήκες του πειράματος με προσθήκη κατάλληλης ποσότητας βάσης ΝαΟΗ 0.1Ν, και όχι με tris buffer. Τέλος, ακολουθούσε η προσθήκη της απαιτούμενης ποσότητας, από την συγκέντρωση του εκάστοτε πειράματος, του διαλύματος CaCl. 2 2H 2 O. Από εκείνη τη χρονική στιγμή γινόταν η έναρξη της διεργασίας της καταβύθισης και ξεκινούσε η καταγραφή της μεταβολής του ph του διαλύματος συναρτήσει του χρόνου. Η τελευταία τιμή του ph του διαλύματος πριν την πρώτη μείωσή της, οριζόταν ως η τιμή η οποία διετηρείτο σταθερή καθόλη τη διάρκεια της κρυσταλλικής ανάπτυξης (set point). Μείωση της τιμής του ph κατά μονάδες από το set point ενεργοποιούσε τις μηχανικές σύριγγες, με αποτέλεσμα την προσθήκη των τιτλοδοτικών διαλυμάτων στο διάλυμα εργασίας. Μόλις ξεκινούσε η καταβύθιση του στερεού, σύμφωνα με την αντίδραση (7-5), απελευθερώνονταν πρωτόνια στο διάλυμα τα οποία γίνονταν αντιληπτά με μείωση στην τιμή του ph του διαλύματος και την έναρξη των προσθηκών των διαλυμάτων τιτλοδότησης με στοιχειομετρική αναλογία του καταβυθιζόμενου άλατος (ΗΑP). 5Ca 3 HPO H O Ca ( PO ) OH 4 H (7-5) ( s) Σε τακτά χρονικά διαστήματα, συλλέγονταν δείγματα από το διάλυμα εργασίας με συχνότητα ανάλογη με τον ρυθμό της κρυστάλλωσης, έτσι ώστε ο όγκος του διαλύματος εργασίας να παραμένει όσο το δυνατό σταθερός. Τα δείγματα διηθούνταν από ηθμούς μεμβράνης 0.2μm (Millipore) και αναλύονταν για ασβέστιο και μαγνήσιο με φασματοσκοπία ατομικής απορρόφησης και για φωσφορικά φασματοφωτομετρικά με την μέθοδο των βαναδομολυβδαινικών. Επιπλέον, έγινε διάλυση των σχηματιζόμενων στερών σε διάλυμα ΗCl 0.1 Ν με σκοπό τον προσδιορισμό του γραμμομοριακού λόγου ασβεστίου προς φωσφόρο. Τα πειράματα διαρκούσαν τόσο ώστε να επιτυγχανόταν όσο το δυνατόν υψηλότερο ποσοστό κρυστάλλωσης του ΗΑΡ στα υποστρώματα. Μετά το πέρας του πειράματος, τα υποστρώματα ξεπλένονταν με τριπλά απεσταγμένο νερό για την απομάκρυνση ποσότητας χλωριούχου νατρίου και ακολουθούσε χαρακτηρισμός τους με περίθλαση ακτίνων-χ (XRD), φασματοσκοπία υπερύθρου (FT IR) και με ηλεκτρονική μικροσκοπία σάρωσης (SEM). 172
199 7.1.3 ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Όπως αναφέρθηκε και στην ενότητα 5.4, από τη συλλογή των δεδομένων στον ηλεκτρονικό υπολογιστή, προέκυπταν τα διαγράμματα της μεταβολής του ph του διαλύματος, όπου επιβεβαιωνόταν η σταθερότητα του ph του διαλύματος εργασίας, και του προστιθέμενου όγκου των διαλυμάτων τιτλοδότησης συναρτήσει του χρόνου, μέσω του οποίου υπολογιζόταν ο ρυθμού κρυσταλλικής ανάπτυξης, ενώ από τις αναλύσεις των διηθημάτων των δειγμάτων επιβεβαιωνόταν η σταθερότητα της χημικής σύστασης των υπέρκορων διαλυμάτων εργασίας. Ο ρυθμός κρυσταλλικής ανάπτυξης του ΗΑP ανά μονάδα επιφάνειας, σε ποσοστό κρυστάλλωσης 2%, υπολογιζόταν από την εξίσωση (7-6), όπου ο όρος προσδιοριζόταν από την κλίση της εφαπτόμενης ευθείας της καμπύλης του διαγράμματος του προστιθέμενου όγκου των διαλυμάτων τιτλοδότησης συναρτήσει του χρόνου, όπου SSA η ειδική επιφάνεια των κρυσταλλικών φύτρων, και m η μάζα των εισαγόμενων κρυσταλλικών φύτρων στο διάλυμα εργασίας. dv dt R mol HAP min m g 1 2 dv ml sec 3 lt mol Ca 1 mol HAP Ceff dt sec min ml lt 5 mol Ca 2 m SSA mg g (7-6) O υπερκορεσμός για τον ΗΑΡ ορίζεται από την ακόλουθη σχέση: a 2 a 3 a Ca PO 4 OH (7-7) 0 K όπου Κ 0 s το θερμοδυναμικό γινόμενο διαλυτότητας του ΗΑP. Ο σχετικός υπερκορεσμός ως προς ΗΑP ορίζεται ως : s 1/9 1 (7-8) Οι χημικές ισορροπίες και οι τιμές των σταθερών οι οποίες χρησιμοποιήθηκαν στους υπολογισμούς παρουσιάζονται στο Παράρτημα Ι. 173
200 Οι πειραματικές συνθήκες και τα κινητικά αποτελέσματα, τα οποία προέκυψαν από την πρώτη σειρά πειραμάτων κρυστάλλωσης ΗΑΡ σε συνθήκες σταθερού υπερκορεσμού στους 37 o C, σε ph 7.40, ΝaCl 0.15 Μ σε υπέρκορα διαλύματα, παρουσιάζονται στον πίνακα 7.3. Πίνακας 7.3 Πειραματικές συνθήκες και αποτελέσματα μετρήσεων της κινητικής της κρυσταλλικής ανάπτυξης: ολική συγκέντρωση ασβεστίου, C Ca, σχετικός υπερκορεσμός ως προς ΗΑP, σ ΗΑP, και αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης R g, για την κρυστάλλωση του υδροξυαπατίτη (HAP) στα δύο υποστρώματα, σε υπέρκορα διαλύματα ηλεκτρολυτικού διαλύματος ΝaCl 0.15 Μ και σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, θερμοκρασία, θ = 37.0 ± 0.1 o C και C Ca /C P = 1.67, όπου C P η ολική συγκέντρωση των φωσφορικών. Υποστρώματα C Ca / 10-3 M σ ΗΑΡ σ OCΡ σ ΤCΡ R g / 10-8 mol min -1 m Βιοτσιμέντο Κρυσταλλικά φύτρα ΗΑΡ Στον πίνακα 7.4 που ακολουθεί, συνοψίζονται οι πειραματικές συνθήκες και τα κινητικά αποτελέσματα για τη δεύτερη σειρά πειραμάτων, στην οποία μελετήθηκε η κρυστάλλωση του ΗΑΡ σε υπέρκορα διαλύματα με σύσταση τροποποιημένων προσομοιωμένων βιολογικών ρευστών (m-sbf). 174
201 Πίνακας 7.4 Πειραματικές συνθήκες και αποτελέσματα μετρήσεων της κινητικής της κρυσταλλικής ανάπτυξης: ολική συγκέντρωση ασβεστίου, C Ca, σχετικός υπερκορεσμός ως προς ΗΑP, σ ΗΑP, και αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης R g, για την κρυστάλλωση του υδροξυαπατίτη (HAP) στα δύο υποστρώματα, σε υπέρκορα διαλύματα με σύσταση τροποποιημένων προσομοιωμένων βιολογικών ρευστών (m-sbf) και σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, θερμοκρασία, θ = 37.0 ± 0.1 o C και C Ca /C P = 1.67, όπου C P η ολική συγκέντρωση των φωσφορικών. Υποστρώματα Βιοτσιμέντο C Ca / 10-3 M σ ΗΑP σ OCP σ TCP R g / 10-8 mol min -1 m Κρυσταλλικά φύτρα ΗΑΡ Ένα συγκριτικό διάγραμμα των ρυθμών κρυσταλλικής ανάπτυξης του HAP στα δύο υποστρώματα φωσφορικού ασβεστίου για τις δύο περιπτώσεις ηλεκτρολυτικών διαλυμάτων παρουσιάζεται στο σχήμα 7.10 που ακολουθεί, ενδεικτικά σε μια τιμή σχετικού υπερκορεσμού σ ΗΑP =
202 1,0x10-7 R g / mol HAP min -1 m -2 8,0x10-8 6,0x10-8 4,0x10-8 2,0x10-8 σ HAP = 7.1 Σχήμα 7.10: Γραφική απεικόνιση του ρυθμού κρυσταλλικής ανάπτυξης ΗΑP στα δύο υποστρώματα φωσφορικού ασβεστίου σε συνθήκες σταθερού υπερκορεσμού, 37 C, ph 7.40, 0.15 M NaCl, σ OCP = 7.1: (α) κρυσταλλικά φύτρα ΗΑΡ; (β) βιοτσιμέντο και 37 C, ph 7.40, m-sbf, σ OCP = 7.1: (γ) κρυσταλλικά φύτρα ΗΑΡ; (δ) βιοτσιμέντο. Όπως φαίνεται από το διάγραμμα, στο ηλεκτρολυτικό διάλυμα NaCl 0.15 M μετρήθηκαν ταχύτεροι ρυθμοί κατά την κρυστάλλωση ΗΑP στα κρυσταλλικά φύτρα ΗΑΡ. Συγκεκριμένα, σημειώθηκε ποσοστό μείωσης 20-25% κατά την κρυσταλλική ανάπτυξη ΗΑΡ στο βιοτσιμέντο. Παρόμοια συμπεριφορά παρατηρήθηκε και κατά την κρυσταλλική ανάπτυξη ΗΑΡ μεταξύ των δύο υποστρωμάτων σε προσομοιωμένο βιολογικό ρευστό (m-sbf), όπου το βιοτσιμέντο έδειξε, ότι σε αντίστοιχα υπέρκορα διαλύματα κρυσταλλώνεται με μικρότερους ρυθμούς (ποσοστό μείωσης 25-30%) σε σχέση με τα κρυσταλλικά φύτρα ΗΑΡ. Οι αρχικοί ρυθμοί κρυστάλλωσης HAP τόσο σε φύτρα κρυστάλλων ΗΑΡ όσο και στο βιοτσιμέντο παρουσία ηλεκτρολυτικού διαλύματος ΝaCl, βρέθηκαν μεγαλύτεροι σε σύγκριση με τους αντίστοιχους ρυθμούς σε προσομοιωμένο βιολογικό ρευστό (m-sbf), της ίδιας ιοντικής ισχύος και υπερκορεσμού. Και για τα δύο υποστρώματα η κρυστάλλωση του ΗΑΡ σε υπέρκορα διαλύματα με σύσταση m-sbf οδήγησε σε ποσοστό μείωσης περίπου 50-55% σε σχέση με τους αντίστοιχους ρυθμούς σε υπέρκορα διαλύματα παρουσία ηλεκτρολύτη NaCl. Η μείωση αυτή πιθανόν οφείλεται στην ύπαρξη ανθρακικών ιόντων, τα οποία ενσωματώνονται στο κρυσταλλικό πλέγμα του ΗΑΡ. Αυτή η συμπεριφορά βρίσκεται σε συμφωνία με παρόμοιες βιβλιογραφικές μελέτες που έγιναν σε συνθήκες σταθερού 176
203 υπερκορεσμού, οι οποίες έδειξαν πως σε υδατικά υπέρκορα διαλύματα φωσφορικού ασβεστίου η παρουσία ανθρακικών ιόντων επιβραδύνει σημαντικά τους ρυθμούς κρυσταλλικής ανάπτυξης ΗΑΡ σε φύτρα κρυστάλλων ΗΑΡ [Campbell et al., 1991 ; Κapolos and Koutsoukos, 1999]. Επιπλέον, η μείωση του ρυθμού κρυσταλλικής ανάπτυξης στην περίπτωση κρυστάλλωσης ΗΑΡ σε m-sbf διάλυμα θα μπορούσε να οφείλεται και στην ύπαρξη των ιόντων μαγνησίου στο υπέρκορο διάλυμα. Μελέτες αναφέρονται στην επιβραδυντική δράση των ιόντων μαγνησίου στην κινητική κρυστάλλωσης αλάτων φωσφορικού ασβεστίου, ιδιαιτέρως κατά την κρυστάλλωση υδροξυαπατίτη σε κρυσταλλικά φύτρα HAP, λόγω της προσρόφησης των ιόντων στην επιφάνεια των αναπτυσσόμενων κρυστάλλων, και όχι λόγω της ενσωμάτωσή τους στο κρυσταλλικό πλέγμα, με αποτέλεσμα τη μείωση των ενεργών κέντρων και την παρεμπόδιση της κρυσταλλικής ανάπτυξης του ΗΑΡ [Amjad et al., 1984 ; Campbell et al., 1991 ; Salimi et al., 1985]. Στην παρούσα μελέτη τα αποτελέσματα των χημικών αναλύσεων των σχηματιζόμενων στερεών δεν έδειξαν την παρουσία ιόντων μαγνησίου, ενώ ο γραμμομοριακός λόγος ασβεστίου προς φωσφόρο υπολογίστηκε Ca/P = , υποδηλώνοντας πως η μείωση στους ρυθμούς κρυσταλλικής ανάπτυξης οφείλεται στην ενσωμάτωση ανθρακικών ιόντων στο κρυσταλλικό πλέγμα του ΗΑΡ. Για την πρώτη σειρά πειραμάτων ο γραμμομοριακός λόγος ασβεστίου προς φωσφόρο του στερεού που κρυσταλλώθηκε βρέθηκε Ca/P = Στο σχήμα 7.11 απεικονίζεται η λογαριθμική εξάρτηση των αρχικών ρυθμών κρυσταλλικής ανάπτυξης από τον σχετικό υπερκορεσμό ως προς ΗΑΡ για την κρυστάλλωση HAP σε υπέρκορα διαλύματα παρουσία ηλεκτρολυτικού διαλύματος ΝaCl 0.15 Μ με βάση τα δεδομένα του πίνακα
204 -6,4-6,6 log (R g / mol HAP min -1 m -2 ) -6,8-7,0-7,2-7,4 0,8 0,9 1,0 1,1 1,2 logσ HAP Σχήμα 7.11: Κινητική της κρυστάλλωσης του υδροξυαπατίτη (ΗΑP) στα δύο υποστρώματα σε συνθήκες σταθερού υπερκορεσμού. Μεταβολή του λογαρίθμου του αρχικού ρυθμού κρυσταλλικής ανάπτυξης ΗΑP συναρτήσει του λογαρίθμου του σχετικού υπερκορεσμού. θ= 37 C, ph 7.40, 0.15 M NaCl: ( )βιοτσιμέντο και ( ) κρυσταλλικά φύτρα ΗΑΡ. Από τη γραμμμική προσαρμογή των πειραματικών αποτελεσμάτων στην ημιεμπειρική εξίσωση (5-11) υπολογίσθηκε η φαινόμενη τάξη της κρυστάλλωσης και η τιμή της φαινόμενης σταθεράς της ταχύτητας για κάθε υπόστρωμα. Για την κρυστάλλωση ΗΑP στο βιοτσιμέντο η φαινόμενη τάξη της αντίδρασης βρέθηκε ίση με n = 1.4 ( 0.05) και η φαινόμενη σταθερά ταχύτητας k g = ( ) mol min -1 m -2, ενώ οι αντίστοιχες τιμές που προέκυψαν στην περίπτωση κρυστάλλωσης σε φύτρα ΗΑΡ ήταν n = 1.32 ( 0.02) και k g = ( ) mol min -1 m -2, η οποία βρίσκεται σε σχετική συμφωνία με αντίστοιχη τιμή φαινόμενης τάξης σε ανάλογη εργασία (n = ) [Koutsoukos et al., 1980]. Από την τιμή της φαινόμενης τάξης προέκυψε το συμπέρασμα ότι ο μηχανισμός της ανάπτυξης των κρυστάλλων ελέγχεται από επιφανειακή διάχυση των δομικών μονάδων στα ενεργά κέντρα κρυστάλλωσης. Ακολούθως, βάσει των δεδομένων του πίνακα 7.4, προέκυψε το λογαριθμικό διάγραμμα των αρχικών ρυθμών κρυσταλλικής ανάπτυξης συναρτήσει του σχετικού υπερκορεσμού ως προς ΗΑΡ (σχήμα 7.12) από το οποίο με γραμμική προσαρμογή υπολογίσθηκαν οι τιμές της φαινόμενης τάξης και της φαινόμενης σταθεράς της 178
205 ταχύτητας για την κρυστάλλωση HAP σε υπέρκορα διαλύματα με σύσταση τροποποιημένων προσομοιωμένων βιολογικών ρευστών (m-sbf) για τα δύο υποστρώματα. -6,8 log (R g / mol HAP min -1 m -2 ) -7,0-7,2-7,4-7,6 0,8 0,9 1,0 1,1 1,2 logσ HAP Σχήμα 7.12: Κινητική της κρυστάλλωσης του υδροξυαπατίτη (ΗΑP) στα δύο υποστρώματα σε συνθήκες σταθερού υπερκορεσμού. Μεταβολή του λογαρίθμου του αρχικού ρυθμού κρυσταλλικής ανάπτυξης ΗΑP συναρτήσει του λογαρίθμου του σχετικού υπερκορεσμού. θ= 37 C, ph 7.40, m-sbf: ( ) βιοτσιμέντο και ( ) κρυσταλλικά φύτρα ΗΑΡ. Στην περίπτωση κρυστάλλωσης ΗΑΡ στο βιοτσιμέντο βρέθηκε n = 1.53 ( 0.04) και k g = ( ) mol min -1 m -2, ενώ στα φύτρα ΗΑΡ n = 1.57 ( 0.07) και k g = ( ) mol min -1 m -2, υποδηλώνοντας ότι το καθορίζον την ταχύτητα στάδιο είναι η διάχυση των δομικών μονάδων πάνω στην επιφάνεια των υποστρωμάτων και η ενσωμάτωσή τους στα ενεργά κρυσταλλικά κέντρα. Το συμπέρασμα που προέκυψε από την συγκριτική μελέτη ήταν ότι δεν υφίσταται αλλαγή στο μηχανισμό ανάπτυξης των κρυστάλλων παρουσία m-sbf. Σε παρόμοια εργασία που μελετήθηκε η κρυστάλλωση ΗΑΡ σε φύτρα κρυστάλλων ΗΑΡ σε υπέρκορα διαλύματα σε προσομοιωμένο βιολογικό ρευστό (SBF) [Spanos et al., 2006], βρέθηκε παραβολική εξάρτηση των αρχικών ρυθμών κρυσταλλικής ανάπτυξης ΗΑΡ από τον σχετικό υπερκορεσμό και υπολογίστηκε υψηλότερη τιμή της φαινόμενης τάξης (n=4), 179
206 οδηγώντας στο συμπέρασμα πως πρόκειται για πολυπυρηνικό μηχανισμό ανάπτυξης, ο οποίος, όμως, και σε αυτήν την περίπτωση ελέγχεται από την επιφανειακή διάχυση των δομικών μονάδων. Η διαφορά ως προς την τιμή της φαινόμενης τάξης (n=1.5 έναντι n=4), που προέκυψε συγκρίνοντας τις δύο μελέτες, μπορεί να οφείλεται στο γεγονός ότι η συγκέντρωση των ανθρακικών ιόντων ([CO 2-3 ] = 4.2 mm) στη μελέτη σε SBF ήταν υψηλότερη σε σχέση με την αντίστοιχη στο m-sbf ([CO 2-3 ] = 1.0 mm). To ενδεχόμενο της ενσωμάτωσης ανθρακικών ιόντων στο κρυσταλλικό πλέγμα του ΗΑΡ κατά την κρυστάλλωση ΗΑΡ στα δύο κρυσταλλικά υποστρώματα σε διάλυμα SBF, διερευνήθηκε με εξέταση των σχηματιζόμενων στερεών με φασματοσκοπία υπερύθρου, τα αποτελέσματα της οποίας παρουσιάζονται στη συνέχεια. 1 ιαπερατότητα % PO 3-4 PO 3-4 CO 2-3 CO 2-3 PO 3-4 PO 3-4 CO 2-3 CO 2-3 OH - OH - OH - OH Κυματάριθμος/ cm -1 Σχήμα 7.13: Φάσματα υπερύθρου κρυστάλλωσης ΗΑΡ σε υπέρκορα διαλύματα με σύσταση m-sbf 1: στο βιοτσιμέντο και 2: σε φύτρα κρυστάλλων υδροξυαπατίτη (ΗΑP). Όπως φαίνεται στο σχήμα 7.13 οι κορυφές απορρόφησης στα 1413 cm -1 και 1455 cm -1 αποδίδονται στην παρουσία ανθρακικών, οι οποίες είναι χαρακτηριστικές σε ανθρακικούς απατίτες τύπου Β (υποκατάσταση φωσφορικών) και τύπου Α (υποκατάσταση υδροξυλομάδας), αντίστοιχα, και επιπλέον η κορυφή στα 875 cm -1 αντιστοιχεί στη δόνηση κάμψης (ν 2 ) σε ανθρακικούς απατίτες [LeGeros, 1991 ; Xu et al., 2000]. Οι ζώνες απορρόφησης στα 565 cm -1 και 602 cm -1 αποδίδονται στην τριπλώς εκφυλισμένη δόνηση κάμψης (ν 4 ) των δεσμών Ο-Ρ-Ο, ενώ η ζώνη απορρόφησης
207 1110 cm -1 οφείλεται στην τριπλώς εκφυλισμένη ασύμμετρη δόνηση τάσης (ν 3 ) του δεσμού Ρ-Ο της φωσφορικής ομάδας [Fowler, 1974]. Οι ζώνες απορρόφησης στα 1645 cm -1 και 3440 cm -1 οφείλονται στη δόνηση κάμψης ν 2, μορίων νερού και σε προσροφημένα μόρια ύδατος [Ashok et al., 2003 ; Fowler, 1974]. Από τον χαρακτηρισμό των σχηματιζόμενων στερεών με περιθλασιμετρία ακτίνων-χ, ταυτοποιήθηκε πως σε όλες τις περιπτώσεις η φάση που κρυσταλλώθηκε ήταν υδροξυαπατίτης (σχήμα 7.14), χωρίς να ταυτοποιηθεί η παρουσία κάποιας άλλης φάσης του φωσφορικού ασβεστίου. Intensity/ a.u Σχήμα 7.14: Περιθλασιογράμματα ακτίνων-χ 1: της φάσης που κρυσταλλώθηκε στο βιοτσιμένο, 2: της φάσης που κρυσταλλώθηκε σε φύτρα κρυστάλλων ΗΑΡ, 3: συνθετικού β-tcp (Αρ ) και 4: συνθετικού ΗΑΡ (Αρ ). Ο χαρακτηρισμός της κρυσταλλικής φάσης που αναπτύχθηκε στα υποστρώματα που μελετήθηκαν έγινε και με ανάλυση της μορφολογίας με ηλεκτρονική μικροσκοπία σάρωσης. Στις φωτογραφίες του σχήματος 7.15 φαίνονται οι μικροκρυσταλλικοί πρισματικοί απατίτες μεγέθους nm, που εναποτέθηκαν στο βιοτσιμέντο καλύπτοντας και τις υδρολυόμενες πλάκες ΟCP που έχουν απομείνει από τη διάλυση του TCP, όπως είχε φανεί και από την μορφολογική εξέταση του βιοτσιμέντου (ενότητα ). 181
208 Σχήμα 7.15: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης υδροξυαπατίτη (ΗΑP) στο βιοτσιμέντο σε συνθήκες σταθερού υπερκορεσμού σε NaCl 0.15 M; ph 7.40, 37 C, σ HAP =7.60. H μορφολογική εξέταση της φάσης που σχηματίστηκε κατά την κρυστάλλωση ΗΑΡ στα φύτρα ΗΑΡ, έδειξε το σχηματισμό πρισματικών κρυστάλλων ΗΑΡ μεγέθους nm και πάχους nm (σχήμα 7.16), οι οποίοι ήσαν αρκετά μεγαλύτεροι σε μέγεθος σε σχέση με τα φύτρα κρυστάλλων ΗΑΡ. Σχήμα 7.16: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης υδροξυαπατίτη (ΗΑP) σε συνθετικούς κρυστάλλους ΗΑΡ σε συνθήκες σταθερού υπερκορεσμού σε NaCl 0.15 M; ph 7.40, 37 C, σ HAP =
209 Στις φωτογραφίες από το ηλεκτρονικό μικροσκόπιο σάρωσης του σχήματος 7.17, απεικονίζεται η μορφολογία της φάσης που κρυσταλλώθηκε σε υπέρκορα διαλύματα με σύσταση m-sbf στα δύο υποστρώματα. Πρόκειται για μη πρισματικούς απατιτικούς και σφαιρικούς μικροκρυσταλλίτες, οι οποίοι μοιάζουν με τη μορφολογία ανθρακικών απατιτικών μικροκρυστάλλων [Dorozhkina and Dorozhkin, 2002]. Σχήμα 7.17: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης υδροξυαπατίτη (ΗΑP) (α) στο βιοτσιμέντο και (β) σε συνθετικούς κρυστάλλους ΗΑΡ σε συνθήκες σταθερού υπερκορεσμού σε υπέρκορα διαλύματα με σύσταση m-sbf; ph 7.40, 37 C, σ HAP = Kατά την κρυστάλλωση ΗΑΡ σε υπέρκορα διαλύματα με σύσταση τροποποιημένων προσομοιωμένων βιολογικών ρευστών (m-sbf) φάνηκε πως επηρεάζεται και η μορφολογία των σχηματιζόμενων κρυστάλλων ΗΑΡ, η οποία άλλαξε δραματικά συγκρινόμενη με την αντίστοιχη σε ηλεκτρολυτικό διάλυμα NaCl, ενισχύοντας το γεγονός της ενσωμάτωσης των ανθρακικών ιόντων στο κρυσταλλικό πλέγμα. 7.2 ΚΡΥΣΤΑΛΛΩΣΗ ΦΩΣΦΟΡΙΚΟΥ ΟΚΤΑΣΒΕΣΤΙΟΥ (OCP) ΣΕ ΒΙΟΤΣΙΜΕΝΤΑ ΑΝΘΡΑΚΙΚΟΥ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ (CaCO 3 -CaP) ΕΙΣΑΓΩΓΗ Τo φωσφορικό οκτασβέστιο (OCP) παίζει σημαντικό ρόλο στα βιολογικά συστήματα, όπως φυσικά και ο HAP, λόγω των ενδείξεων οι οποίες έχουν παρουσιασθεί 183
210 στην διεθνή βιβλιογραφία, σύμφωνα με τις οποίες βάσιμα πιστεύεται ότι συμμετέχει ως πρόδρομη φάση στα αρχικά στάδια της βιολογικής ασβεστοποίησης ιστών [Brown et al.,, 1987]. Πρόσφατες έρευνες αναφέρουν πως κρύσταλλοι OCP που είχαν συντεθεί στο εργαστήριο, προκαλούσαν την οστεοβλαστική διαφοροποίηση των κυττάρων in vitro [Anada et al., 2008 ; Suzuki et al., 2006]. Επιπλέον, in vivo μελέτες έδειξαν ότι συνθετικό OCP μετατράπηκε σε απατιτικό υλικό σε μύες και σε διάφορα οστέωδη μέρη [Ban et al., 1992 ; Suzuki et al., 1991]. Διαπιστώθηκε, επίσης, ότι την απορρόφηση του OCP ακολουθεί ο σχηματισμός νέου οστού [Barrere et al., 2003 ; Imaizumi et al., 2006 Sugihara et al., 1995], ενώ επιστρώσεις OCP σε μεταλλικά εμφυτεύματα έδειξαν πως η κρυσταλλική αυτή φάση, δίνει τη δυνατότητα ανάπτυξης οστού στην επιφάνειά του (οστεοαγωγιμότητα) [Barrere et al., 1999]. Από την πρώτη φορά που αναπτύχθηκαν τα βιοτσιμέντα φωσφορικού ασβεστίου μέχρι σήμερα, έχουν διερευνηθεί διάφοροι συνδυασμοί τους [Dorozhkin et al., 2008]. Οι συνεχείς απαιτήσεις για την παρασκευή βιοϋλικών έχουν οδηγήσει σε αυξημένο ενδιαφέρον για τη σύνθεση και τη μελέτη βιοτσιμέντων φωσφορικού ασβεστίου ή και μίγματων ανθρακικού και φωσφορικού ασβεστίου [Bermudez, 1994 ; Combes et al., 2006; LeGeros, 1993 ; Markovic and Chow, 2010]. Η συνάφεια μεταξύ ανθρακικών και φωσφορικών αλάτων του ασβεστίου είναι σημαντική για την κατανόηση της συμπεριφοράς και των ιδιοτήτων νέων βιοϋλικών που βασίζονται σ αυτά τα υλικά. Ο στόχος της μελέτης που παρουσιάζεται σε αυτήν την ενότητα ήταν η παρασκευή βιοτσιμέντων ανθρακικού-φωσφορικού ασβεστίου με σκοπό να αποτέλεσουν υποστρώματα για την εκκίνηση της κρυσταλλικής ανάπτυξης του ΟCP σε σταθερά υπέρκορα διαλύματα φωσφορικού ασβεστίου. Η μελέτη, και στην περίπτωση αυτή, έγινε με τη μέθοδο σταθερού υπερκορεσμού στους 37 o C, ph 7.40 ± 0.1 και ιοντική ισχύ 0.15 Μ NaCl. Επιπλέον, για τη μελέτη της κινητικής της κρυστάλλωσης του ΟCP χρησιμοποιήθηκαν συνθετικοί κρύσταλλοι HAP και OCP, ως υλικά αναφοράς ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Αντιδραστήρια Για τα πειράματα χρησιμοποιήθηκαν πρότυπα πυκνά διαλύματα διένυδρου χλωριούχου ασβεστίου, CaCl 2 2H 2 O, και δισόξινου φωσφορικού καλίου, KH 2 PO 4, συγκέντρωσης 0.1Μ, καθώς και διάλυμα χλωριούχου νατρίου, ΝaCl, συγκέντρωσης 184
211 1Μ ενώ η ρύθμιση του ph γινόταν με πρότυπο διάλυμα καυστικού νατρίου, NaOH, συγκέντρωσης 0.1Ν Παρασκευή και χαρακτηρισμός βιοτσιμέντων ανθρακικού-φωσφορικού ασβεστίου Παρασκευάστηκαν δύο τύποι βιοτσιμέντων ανθρακικού-φωσφορικού ασβεστίου (CaCO 3 -CaP). Το βιοτσιμέντο Α παρασκευάστηκε με ανάμιξη βατερίτη (CaCO 3 ) και διένυδρου φωσφορικού ασβεστίου (CaHPO 4 2H 2 O, DCPD) με τριπλά απεσταγμένο νερό. Το βιοτσιμέντο Β παρασκευάστηκε με ισομοριακή ανάμιξη βατερίτη, DCPD και 20% ανθρακικού στροντίου (SrCO 3 ) με τριπλά απεσταγμένο νερό. Το μείγμα παρέμεινε σε θερμοκρασία 37 ο C για 2 ημέρες, έτσι ώστε να σκληρύνουν οι αντίστοιχες πάστες, σε κορεσμένη σε υδρατμούς ατμόσφαιρα και στη συνέχεια κονιοποιήθηκαν με γουδί. Ο λόγος που χρησιμοποιήθηκε το SrCO 3 είναι ότι είναι αδιαφανές στις ακτίνες Χ και είναι σαν δείκτηςˮ στο τσιμέντο για τις ακτινογραφίες. Επιπλέον, δε συμμετέχει στην αντίδραση και δεν σχηματίζεται Sr-HAP [Combes et al., 2006]. Οι δύο τύποι βιοτσιμέντων που παρασκευάστηκαν χαρακτηρίστηκαν με περίθλαση κόνεως ακτίνων-χ, φασματοσκοπία υπερύθρου και με ηλεκτρονικό μικροσκόπιο σάρωσης. Στο σχήμα 7.18 παρουσιάζονται τα περιθλασιογράμματα των δύο βιοτσιμέντων, τα οποία συγκρίθηκαν με τα πρότυπα φάσματα υδροξυαπατίτη (Αρ. Κάρτας 9-432), βατερίτη (Αρ. Κάρτας ) και ανθρακικού στροντίου (Αρ. Κάρτας 5-418) από την κρυσταλλογραφκή βάση δεδομένων Search Match. Συγκρίνοντας τα φάσματα προέκυψε από τη σύμπτωση των χαρακτηριστικών ανακλάσεων (0 0 2), (2 1 1), (1 1 2), (3 0 0) του ΗΑΡ (25,9 ο ; 31,8 ο ; 32,23 ο ; 32,93 ο σε 2θ, αντίστοιχα) και των (1 1 0), (1 1 2), (1 1 4), (3 0 0) του βατερίτη (CaCO 3 ) (24,91 ο ; 27,06 ο ; 32,8 ο ; 43,87 ο σε 2θ, αντίστοιχα), ότι το βιοτσιμέντο Α αποτελείτο από απατίτη και βατερίτη, ο οποίος δεν είχε αντιδράσει. Επιπλέον, για το φάσμα του βιοτσιμέντου Β, λόγω της ταύτισης των αντιστοίχων ανακλάσεων με τις χαρακτηριστικές ανακλάσεις (1 1 1), (0 0 2), (1 1 2), (1 3 0), (1 1 3) του SrCO 3 (25,2 ο ; 29,6 ο ; 36,2 ο ; 36,5 ο ; 49,9 ο σε 2θ, αντίστοιχα), προέκυψε πως το βιοτσιμέντο Β ήταν απατίτης που περιείχε επιπλέον βατερίτη και ανθρακικό στρόντιο, τα οποία δεν αντέδρασαν. 185
212 Intensity/ a.u Intensity/ a.u Σχήμα 7.18: Περιθλασιογράμματα ακτίνων-χ κρυσταλλικών φύτρων 1: βιοτσιμέντου A, 2: βιοτσιμέντου B, ( ): συνθετικού υδροξυαπατίτη (HAP) (Αρ ), ( ): συνθετικού βατερίτη (CaCO 3 ) (Αρ ) και ( ): συνθετικού ανθρακικού στροντίου (SrCO 3 ) (Αρ ). Ο χαρακτηρισμός των δύο βιοτσιμέντων που παρασκευάστηκαν, έγινε και με φασματοσκοπία υπερύθρου. Στο σχήμα 7.19 παρουσιάζονται τα φάσματα υπερύθρου των βιοτσιμέντων Α και Β. 186
213 ιαπερατότητα % PO 3-4 CO 2-3 PO 3-4 CO 2-3 PO 3-4 PO 3-4 CO 2-3 CO 2-3 OH - OH - OH - OH Κυματάριθμος/ cm -1 Σχήμα 7.19: Φάσματα υπερύθρου κρυσταλλικών φύτρων 1: βιοτσιμέντου Α και 2: βιοτσιμέντου Β. Οι ζώνες απορρόφησης στα 565 cm -1 και 602 cm -1 αποδόθηκαν στην τριπλώς εκφυλισμένη δόνηση κάμψης (ν 4 ) των δεσμών Ο-Ρ-Ο, ενώ αυτή στα 1046 cm -1 οφείλεται στην τριπλώς εκφυλισμένη ασύμμετρη δόνηση τάσης (ν 3 ) του δεσμού Ρ-Ο της φωσφορικής ομάδας [Fowler, 1974]. Η κορυφή στα 1430 cm -1 αποδίδεται στη δόνηση τάσης (ν 1 ), η οποία είναι χαρακτηριστική στους ανθρακικούς απατίτες τύπου Β, και οι κορυφές στα 875 cm -1 και 1500 cm -1 στις δόνησεις κάμψης (ν 2 ) και (ν 3 ) αντίστοιχα, οι οποίες εμφανίζονται σε ανθρακικούς απατίτες [Nelson and Featherstone, 1982]. Οι ζώνες απορρόφησης στα 1645 cm -1 και 3440 cm -1 οφείλονται στη δόνηση κάμψης ν 2, μορίων νερού και σε προσροφημένα μόρια ύδατος, αντίστοιχα [Ashok et al., 2003 ; Fowler, 1974]. H ύπαρξη του βατερίτη στα βιοτσιμέντα Α και Β ταυτοποιήθηκε από τη χαρακτηριστική ζώνη απορρόφησης στα 745 cm -1 [Vagenas et al., 2003], ενώ για το βιοτσιμέντο Β πιστοποιήθηκε και η ύπαρξη ανθρακικού στροντίου από την ζώνη απορρόφησης στα 704 cm -1 [Zhagn et al., 2008]. Η θερμική ανάλυση των βιοτσιμέντων έγινε με την θερμοσταθμική μέθοδο (TGA), τα αποτελέσματα της οποίας παρουσιάζονται στη συνέχεια (Σχήμα 7.20). 187
214 100 ( % Βάρος % απώλεια CO T/ 0 C 100 () 90 % Βάρος 18% απώλεια CO T/ 0 C Σχήμα 7.20: Γράφημα θερμοσταθμικής ανάλυσης (α) βιοτσιμέντου A, (β) βιοτσιμέντου B. Η θερμοσταθμική ανάλυση έγινε με ρυθμό θέρμανσης 2 o C min -1 και σε ατμόσφαιρα αζώτου. Η ανάλυση έδειξε ότι το βιοτσιμέντο Α και το βιοτσιμέντο Β είχαν 12% και 18% συνολική απώλεια βάρους αντίστοιχα, λόγω της περιεκτικότητάς τους σε ανθρακικά. Κατά τη θέρμανση απατιτικών στερεών τα οποία περιέχουν ανθρακικά, σε ατμόσφαιρα αζώτου, εκλύονται τα ανθρακικά, όπως έχει αναφερθεί και σε άλλες βιβλιογραφικές μελέτες, στην περιοχή θερμοκρασιών o C, ενώ σε ατμόσφαιρα αέρα, η αντίστοιχη απομάκρυνση γίνεται στην περιοχή o C [Joschek et al., 2000 ; Murugan et al., 2006]. Από την παραγώγιση των θερμοσταθμικών γραφημάτων των 188
215 δύο βιοτσιμέντων πρέκυψε πως η απομάκρυνση των ανθρακικών στην περίπτωση του βιοτσιμέντου Α συνέβη στους 650 o C και 800 o C, ενώ για το βιοτσιμέντο Β στους 640 o C και 810 o C. Στη βιβλιογραφία, για τη θερμική ανάλυση του ΗΑΡ αναφέρεται πως στη θερμοκρασιακή περιοχή o C διακρίνεται απώλεια βάρους που οφείλεται στην απομάκρυνση επιφανειακών ΗΡΟ 2-4 λόγω του σχηματισμού πυροφωσφορικών και στη συνέχεια σε ορθοφωσφορικά [Arends et al., 1987 ; Fowler et al., 1966]. Κατά τη θερμική ανάλυση του ανθρακικού ασβεστίου αναφέρεται ότι η διάσπαση ανθρακικού ασβεστίου λαμβάνει χώρα στην θερμοκρασιακή περιοχή o C στους 700 o C περίπου [Οniyama and Wahlbeck, 1995 ; Tiwari, 2008]. Στο σχήμα 7.21 παρουσιάζονται φωτογραφίες που ελήφθησαν με ηλεκτρονικό μικροσκόπιο σάρωσης, όπου διακρίνονται μικροκρυσταλλικοί ( nm), μη πρισματικοί, απατίτες (σχήμα 7.21 (α)), καθώς και κρύσταλλοι βατερίτη μεγέθους 1-2 μm να συνυπάρχουν με τους απατιτικούς σχηματισμούς (σχήμα 7.21 (β)). Σχήμα 7.21: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης του παρασκευασμένου βιοτσιμέντου Α. Η μορφολογική εξέταση του βιοτσιμέντου Β έδειξε ομοίως απατιτικούς μικροκρυστάλλους (σχήμα 7.22 (α)), κρυστάλλους βατερίτη 1 μm καθώς και πλάκοειδείς κρυσταλλίτες ανθρακικού στροντίου, το οποίο δεν αντέδρασε, μεγέθους 3-4 μm, (σχήμα 7.22 (β),(γ)). 189
216 Σχήμα 7.22: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης του παρασκευασμένου βιοτσιμέντου Β και μικροανάλυση με σάρωση γραμμής (δ). Το γεγονός πως πρόκειται για πλάκες ανθρακικού στροντίου και όχι φωσφορικού στροντίου ή φωσφορικού ασβεστίου (π.χ. DCPD), επιβεβαιώθηκε από τη γραμμική σάρωση του δείγματος (σχήμα 7.22 (δ)), όπου διακρίνεται η διαφοροποιημένη περιοχή που κυριαρχεί μόνο το στρόντιο. Τέλος, με τη μέθοδο ρόφησης αζώτου (BET), υπολογίστηκε η ειδική επιφάνεια των δύο βιοτσιμέντων και βρέθηκε 65 m 2 g -1 για το βιοτσιμέντο Α και 54.5 m 2 g -1 για το βιοτσιμέντο Β. 190
217 Σύνθεση και χαρακτηρισμός συνθετικών κρυστάλλων OCP Οι κρύσταλλοι του OCP παρασκευάστηκαν με ανάμιξη ίσων όγκων διαλυμάτων οξικού ασβεστίου (Ca(CH 3 COO) 2 ) 0.02 M και δισόξινου φωσφορικού νατρίου (NaH 2 PO 4 ) 0.02 M. Το διάλυμα ΝaH 2 PO 4 αναδευόταν σε θερμοστατούμενο αντιδραστήρα στους 60 o C, όπου γίνονταν προσθήκες στάγδην του διαλύματος Ca(CH 3 COO) 2, ενώ το ph διατηρούταν στην περιοχή 5-6 [LeGeros, 1985]. Μετά το πέρας της διαδικασίας ακολουθούσε διήθηση υπό κενό διαμέσου φίλτρου 0.22 μm, καλό πλύσιμο με τριπλά απεσταγμένο νερό, ξήρανση σε λυοφιλοποιητή και τέλος κονιοποίηση του στερεού σε γουδί από αχάτη. Οι κρύσταλλοι του OCP που παρασκευάστηκαν, ταυτοποιήθηκαν με περιθλασιμετρία κόνεως ακτίνων-χ. Στο σχήμα 7.23 απεικονίζονται τα περιθλασιογράμματα ακτίνων-χ των παρασκευασμένων κρυστάλλων του OCP και του προτύπου OCP από την κρυσταλλογραφική βάση δεδομένων Search Match (Αρ. Κάρτας ). Από την ταύτιση των κύριων χαρακτηριστικών ανακλάσεων (010), (002) και (260) του OCΡ (4,73 ο ; 26,0 ο και 31,58 ο σε 2θ, αντίστοιχα), επιβεβαιώθηκε πως οι κρύσταλλοι που παρασκευάστηκαν ήσαν φωσφορικό οκτασβέστιο Intensity/ a.u Σχήμα 7.23: Περιθλασιογράμματα κόνεως ακτίνων-χ 1: παρασκευασμένων κρυστάλλων φωσφορικού οκτασβεστίου (OCΡ) και 2: φωσφορικού οκτασβεστίου (OCΡ) (Αρ. Κάρτας ). 191
218 4 Στο σχήμα 7.24 παρουσιάζεται το φάσμα υπερύθρου των συνθετικών κρυστάλλων φωσφορικού οκτασβεστίου (OCP). ιαπερατότητα % HPO 2_ OH - OH - PO 3-4 PO Κυματάριθμος/ cm -1 Σχήμα 7.24: Φάσμα υπερύθρου συνθετικών κρυστάλλων φωσφορικού οκτασβεστίου (OCP). Στο φάσμα διακρίνονται οι ζώνες απορρόφησης στα 560 cm -1 και 600 cm -1, οι οποίες αντιστοιχούν στην εκφυλισμένη δόνηση κάμψης (ν 4 ) των δεσμών Ο-Ρ-Ο. Η κορυφή στα 861 cm -1 αποδίδεται στη συμμετρική δόνηση τάσης (ν 5 ) του δεσμού Ρ-Ο(Η) της όξινης φωσφορικής ομάδας, ενώ η κορυφή στα 962 cm -1 οφείλεται στη συμμετρική δόνηση τάσης (ν 1 ) του δεσμού Ρ-Ο της φωσφορικής ομάδας ΡΟ 4. Οι κορυφές απορρόφησης στα 1642 cm -1 και 3400 cm -1 αποδίδονται σε δόνηση κάμψης και δόνηση τάσης του υδρογόνου των μορίων του Η 2 Ο [Fowler et al, 1966 ; Fowler et al., 1993 ; Rey et al., 1990]. Η μορφολογική εξέταση με το ηλεκτρονικό μικροσκόπιο σάρωσης των κρυστάλλων OCP που παρασκευάσθηκαν, έδειξε ότι οι κρύσταλλοι ήταν φυλλόμορφοι και ήσαν μεγέθους περίπου 2 μm (σχήμα 7.25). 192
219 Σχήμα 7.25: Φωτογραφία ηλεκτρονικής μικροσκοπίας σάρωσης συνθετικά παρασκευασμένων κρυστάλλων φωσφορικού οκτασβεστίου (OCΡ). Η ειδική επιφάνεια των κρυστάλλων του φωσφορικού οκτασβεστίου (OCP) μετρήθηκε με τη μέθοδο ρόφησης αζώτου (BET) και υπολογίστηκε ίση προς 30.6 m 2 g -1. Όσον αφορά στους συνθετικούς κρυστάλλους ΗΑΡ, η παρασκευή και ο χαρακτηρισμός τους έχουν περιγραφεί στην παράγραφο Πειραματική Διάταξη και Διαδικασία Η πειραματική διάταξη που χρησιμοποιήθηκε για τα πειράματα ήταν ίδια με αυτή του σχήματος 7.9. Οι συγκεντρώσεις των διαλυμάτων τιτλοδότησης για την διατήρηση σταθερής σύστασης κατά την διάρκεια της καταβύθισης του OCP στα υποστρώματα ανθρακικού ασβεστίου υπολογίστηκαν βάσει των εξισώσεων (5-1β) - (5-4β), όπου για την κρυστάλλωση του OCP στα κρυσταλλικά φύτρα των βιοτσιμέντων και του ΗΑΡ ήταν C eff = 3 Ca ws, ενώ στα φύτρα κρυστάλλων OCP ήταν C eff = 10 Ca ws. Στον αντιδραστήρα ο συνολικός όγκος των υπέρκορων διαλυμάτων ήταν 0.2L. Η έναρξη της κρυσταλλικής ανάπτυξης γινόταν με την εισαγωγή στα υπέρκορα διαλύματα προζυγισμένης ποσότητα των κρυσταλλικών φύτρων. Το διάλυμα αναδευόταν και διοχετευόταν άζωτο κορεσμένο σε υδρατμούς. Στην περίπτωση που τα υποστρώματα περιείχαν ανθρακικά (βιοτσιμέντα), η διοχέτευση του αζώτου γινόταν πάνω από το διάλυμα εργασίας με σκοπό την αποφυγή εισόδου του διοξειδίου του άνθρακα από την ατμόσφαιρα. Στη συνέχεια, ρυθμιζόταν το ph του διαλύματος εργασίας στην επιθυμητή τιμή, ανάλογα με τις συνθήκες του πειράματος με προσθήκη κατάλληλης ποσότητας βάσης ΝαΟΗ 0.1Ν. Τέλος, ακολουθούσε η προσθήκη της 193
220 απαιτούμενης ποσότητας, από την συγκέντρωση του εκάστοτε πειράματος, του διαλύματος CaCl. 2 2H 2 O, σηματοδοτώντας την έναρξη της διεργασίας της καταβύθισης. Η διαδικασία αυτή ακολουθήθηκε προκειμένου να προηγείται η εξισορρόπηση των κρυσταλλικών υποστρωμάτων που χρησιμοποιήθηκαν με τα συστατικά των διαλυμάτων. Η διάλυση των στερεών ήταν αμελητέα, αν ληφθεί υπόψη η επίδραση του κοινού ιόντος ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Οι χημικές ισορροπίες και οι τιμές των σταθερών οι οποίες χρησιμοποιήθηκαν για τους υπολογισμούς των συγκεντρώσεων των χημικών ειδών του διαλύματος και των υπερκορεσμών παρουσιάζονται στο Παράρτημα Ι, ενώ οι εξισώσεις ορισμού του υπερκορεσμού και του σχετικού υπερκορεσμού ως προς OCP έχουν ήδη δοθεί στην ενότητα 5.4. Και στα πειράματα της μελέτης αυτής, οι ρυθμοί κρυσταλλικής ανάπτυξης του OCP ανά μονάδα επιφάνειας, υπολογίστηκαν σε ποσοστό κρυστάλλωσης 2%, από την εξίσωση (7-9). R mol OCP min m g 1 2 dv ml sec 3 lt mol Ca 1 mol OCP Ceff dt sec min ml lt 4 mol Ca 2 m SSA mg g (7-9) Οι πειραματικές συνθήκες και τα αποτελέσματα των μετρήσεων για τη μελέτη της κινητικής της κρυστάλλωσης του OCP σε κρυσταλλικά φύτρα βιοτσιμέντων (CaCO 3 -CaP), OCP και ΗΑΡ, παρουσιάζονται συγκεντρωτικά στον πίνακα
221 Πίνακας 7.5 Πειραματικές συνθήκες και αποτελέσματα μετρήσεων της κινητικής της κρυσταλλικής ανάπτυξης: ολική συγκέντρωση ασβεστίου, C Ca, υπερκορεσμός ως προς OCP, Ω ΟCP, σχετικοί υπερκορεσμοί ως προς OCP και HAP, σ OCP και σ HAP, χρόνος επαγωγής, τ, και αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης, R g, για την κρυστάλλωση του φωσφορικού οκτασβεστίου (OCP) στα διάφορα υποστρώματα κρυσταλλικών φύτρων σε υπέρκορα διαλύματα και σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, θ = 37.0 ± 0.1 o C και C Ca /C P = 1.33, όπου C P η ολική συγκέντρωση των φωσφορικών. C Ca Ω OCP σ OCP σ HAP τ Υπόστρωμα R g / 10-3 M s / 10-5 mol min -1 m OCP HAP Βιοτσιμέντο Α Βιοτσιμέντο Β OCP HAP Βιοτσιμέντο Α Βιοτσιμέντο Β OCP HAP Βιοτσιμέντο Α Βιοτσιμέντο Β OCP HAP Βιοτσιμέντο Α Βιοτσιμέντο Β 0.90 Όπως φαίνεται και στον πίνακα, το διάλυμα εργασίας ήταν υπέρκορο και ως προς ΗΑΡ, ενώ στην περίπτωση των βιοτσιμέντων, η κρυσταλλική ανάπτυξη ξεκίνησε μετά την πάροδο χρόνου επαγωγής, τ, ο οποίος και μετρήθηκε από τον χρόνο που μεσολάβησε μεταξύ της παρασκευής των υπέρκορων διαλυμάτων και της έναρξης της προσθήκης αντιδραστηρίων. Για την ίδια τιμή σχετικού υπερκορεσμού, μετρήθηκαν μεγαλύτεροι χρόνοι επαγωγής για το βιοτσιμέντο Β. Η κρυστάλλωση του OCP στα υποστρώματα ανθρακικού-φωσφορικού ασβεστίου (βιοτσιμέντο Α και Β) έλαβε χώρα μετά την πάροδο χρόνου επαγωγής, τ, ο 195
222 οποίος ήταν αντιστρόφως ανάλογος του σχετικού υπερκορεσμού του διαλύματος, όπως φαίνεται και στο σχήμα 7.26, στο οποίο παρίσταται γραφικά η εξάρτηση του χρόνου επαγωγής που μετρήθηκε, συναρτήσει του σχετικού υπερκορεσμού του διαλύματος ως προς OCP (καμπύλη σχηματισμού) Χρόνος Επαγωγής, τ/s Υπερκορεσμός, Ω OCP Σχήμα 7.26: Μεταβολή του χρόνου επαγωγής, τ, συναρτήσει του υπερκορεσμού, Ω, για την κρυστάλλωση του ΟCP σε υποστρώματα φωσφορικού-ανθρακικού ασβεστίου σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, 37 C, 0.15 M NaCl: ( ) φύτρα κρυστάλλων βιοτσιμέντου A ; ( ) φύτρα κρυστάλλων βιοτσιμέντου B. Η εξάρτηση του λογαρίθμου του χρόνου επαγωγής, log από το αντίστροφο του τετραγώνου του λογαρίθμου του υπερκορεσμού ως προς το αντίστοιχο άλας, 1 / log 2 σύμφωνα με την κλασσική θεωρία της ομογενούς πυρηνογένεσης δίνεται από την εξίσωση: 2 3 V 1 log m s (7-10) 3 2 (2.303 kt ) log Η προσαρμογή των πειραματικών δεδομένων στην εξίσωση (7-10), έδωσε ευθεία γραμμή από την κλίση της οποίας υπολογίστηκε η επιφανειακή ενέργεια, γ s, για την 196
223 κάθε περίπτωση (σχήμα 7.27). Η τιμή της επιφανειακής ενέργειας του OCP που προέκυψε μετά τους υπολογισμούς ήταν 9 mj m -2 (γ s = 9.1 mj m -2 για την κρυστάλλωση OCP στα κρυσταλλικά φύτρα βιοτσιμέντου Α και γ s = 8.6 mj m -2 στα κρυσταλλικά φύτρα βιοτσιμέντου Β). Επειδή η κρυστάλλωση είναι ετερογενής, είναι αναμενόμενη η μικρή τιμή της επιφανειακής ενέργειας. 4,0 3,5 log(τ/s) 3,0 2,5 2,0 0,05 0,10 0,15 0,20 (logω OCP ) -2 Σχήμα 7.27: Μεταβολή του λογαρίθμου του χρόνου επαγωγής, log τ, συναρτήσει του του αντίστροφου του τετραγώνου του λογαρίθμου του υπερκορεσμού, (log Ω) -2, για την κρυστάλλωση του ΟCP σε υποστρώματα φωσφορικού-ανθρακικού ασβεστίου σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, 37 C, 0.15 M NaCl: ( ) φύτρα κρυστάλλων βιοτσιμέντου A ; ( ) φύτρα κρυστάλλων βιοτσιμέντου B. Στο σχήμα 7.28 φαίνεται η λογαριθμική εξάρτηση των αρχικών ρυθμών κρυσταλλικής ανάπτυξης από τον σχετικό υπερκορεσμό. Από την κλίση της κάθε ευθείας, η οποία προέκυψε από την προσαρμογή των δεδομένων με την μέθοδο της γραμμικής παλινδρόμησης των ελαχίστων τετραγώνων και από την τεταγμένη επί την αρχή, υπολογίστηκαν οι τιμές της φαινόμενης τάξης της αντίδρασης, n, και της σταθεράς της ταχύτητας κρυσταλλικής ανάπτυξης, k g, αντιστοίχως, και οι οποίες συνοψίζονται στον πίνακα
224 -5,0 log (R g / mol OCP min -1 m -2 ) -5,5-6,0-6,5 0,0 0,1 0,2 0,3 0,4 logσ OCP Σχήμα 7.28: Κινητική της κρυστάλλωσης του OCP σε διάφορα υποστρώματα σε συνθήκες σταθερού υπερκορεσμού. Διαγράμματα του λογαρίθμου του αρχικού ρυθμού κρυσταλλικής ανάπτυξης OCP συναρτήσει του λογαρίθμου του αντίστοιχου σχετικού υπερκορεσμού. θ= 37 C, ph 7.40, 0.15 M NaCl: ( ) κρυσταλλικά φύτρα OCP; ( ) κρυσταλλικά φύτρα ΗΑΡ; ( ) κρυσταλλικά φύτρα βιοτσιμέντου A; ( ) κρυσταλλικά φύτρα βιοτσιμέντου B. Πίνακας 7.6 Τιμές της φαινόμενης τάξης και της φαινόμενης σταθεράς κρυσταλλικής ανάπτυξης του φωσφορικού οκτασβεστίου (OCP) στους διάφορους τύπους κρυσταλλικών φύτρων σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, θερμοκρασία θ = 37.0 ± 0.1 o C, ΝaCl 0.15 M Κρυσταλλικά φύτρα Φαινόμενη Τάξη n Φαινόμενη Σταθερά Ταχύτητας k g / 10-7 mol min -1 m -2 Βιοτσιμέντο Α Βιοτσιμέντο Β ΗΑΡ OCP
225 Aπό την τιμή της φαινόμενης τάξης, η οποία είναι σύμφωνη με βιβλιογραφικές αναφορές σε αντίστοιχες εργασίες [Heughebaert and Nancollas, 1984], εξήχθη το συμπέρασμα ότι ο μηχανισμός της ανάπτυξης των κρυστάλλων ΟCP σε όλα τα υποστρώματα ήταν ο αυτός, ενώ η κρυσταλλική ανάπτυξη στα υποστρώματα που δοκιμάσθηκαν καθορίζεται από την επιφανειακή διάχυση των δομικών μονάδων στην αναπτυσσόμενη κρυσταλλική επιφάνεια. Επιπλέον, από το γεγονός ότι ο ρυθμός κρυστάλλωσης ήταν ανεξάρτητος του ρυθμού ανάδευσης των υπέρκορων διαλυμάτων, επιβεβαιώθηκε ότι η μεταφορά μάζας δεν συνεισφέρει σημαντικά στην [Nielsen and Toft, 1964]. Στο σχήμα 7.29 παρουσιάζεται γραφικά, η σύγκριση των ρυθμών κρυσταλλικής ανάπτυξης του OCP στα διάφορα κρυσταλλικά υποστρώματα, σε μια τιμή σχετικού υπερκορεσμού σ OCP = ,0x10-6 5,0x10-6 R g / mol OCP min -1 m -2 4,0x10-6 3,0x10-6 2,0x10-6 1,0x10-6 OCP Σχήμα 7.29: Γραφική απεικόνιση του ρυθμού κρυσταλλικής ανάπτυξης OCP σε διάφορα υποστρώματα σε συνθήκες σταθερού υπερκορεσμού: 37 C, ph 7.40, 0.15 M NaCl, σ OCP = (α) κρυσταλλικά φύτρα OCP; (β) κρυσταλλικά φύτρα ΗΑΡ; (γ) κρυσταλλικά φύτρα βιοτσιμέντου A; (δ) κρυσταλλικά φύτρα βιοτσιμέντου B. Από το διάγραμμα φαίνεται ότι ταχύτεροι ρυθμοί προέκυψαν κατά την κρυστάλλωση OCP σε κρυστάλλους OCP, ενώ σχεδόν μία τάξη μεγέθους μικρότερη, 199
226 ήσαν οι ρυθμοί κρυστάλλωσης του OCP στα βιοτσιμέντα (CaCO 3 -CaP) και επιπλέον, ο ρυθμός κρυστάλλωσής του σε φύτρα HAP, βρέθηκε ότι ήταν σχεδόν διπλάσιος από τον αντίστοιχο στα βιοτσιμέντα. Η παρουσία ανθρακικών ιόντων έδειξε πως επηρεάζει το ρυθμό κρυστάλλωσης και όσο μεγαλύτερη ήταν η περιεκτικότητα του στερεού σε ανθρακικά, τόσο βραδύτερη έδειξε να είναι η κρυστάλλωση. Η επιβράδυνση της κρυσταλλικής ανάπτυξης του OCP στην περίπτωση των βιοτσιμέντων (CaCO 3 -CaP) προφανώς οφείλεται στην παρουσία των ανθρακικών ιόντων ισορροπίας που υπάρχουν στα υπέρκορα διαλύματα και τα οποία, όπως έχει ήδη αναφερθεί, προκαλούν αναστολή της ανάπτυξης των κρυστάλλων [Kapolos and Koutsoukos, 1999]. Από τα περιθλασιογράμματα ακτίνων-χ του στερεού που κρυσταλλώθηκε στα διάφορα υποστρώματα, προέκυψε ότι η φάση που σχηματίστηκε σε όλες τις περιπτώσεις των κρυσταλλικών φύτρων ήταν το φωσφορικό οκτασβέστιο (σχήμα 7.30) Intensity/ a.u
227 Intensity/ a.u Σχήμα 7.30: Περιθλασιογράμματα ακτίνων-χ (α) 1: κρυστάλλωσης OCP σε φύτρα κρυστάλλων βιοτσιμέντου Α, 2: κρυστάλλωσης OCP σε φύτρα κρυστάλλων βιοτσιμέντου Β, (β) 1: κρυστάλλωσης OCP σε κρυσταλλικά φύτρα φωσφορικού οκτασβεστίου (OCP), 2: κρυστάλλωσης OCP σε κρυσταλλικά φύτρα υδροξυαπατίτη (ΗΑP) και ( ): συνθετικού φωσφορικού οκτασβεστίου (OCP) (Αρ ). Το γεγονός ότι η φάση που κρυσταλλώθηκε στα υποστρώματα ήταν το φωσφορικό οκτασβέστιο, επιβεβαιώθηκε και από την εξέταση των στερεών με υπέρυθρη φασματοσκοπία. Στο σχήμα 7.31 παρουσιάζονται τα φάσματα υπερύθρου των στερεών που προέκυψαν από την κρυστάλλωση του OCP στα διάφορα κρυσταλλικά φύτρα, όπου διακρίνονται δύο χαρακτηριστικές ζώνες απορρόφησης του OCP στα 560 cm -1 και 600 cm -1 [Rey et al., 1990]. 201
228 1 ιαπερατότητα (%) PO Κυματάριθμος/ cm -1 Σχήμα 7.31: Φάσματα υπερύθρου 1: κρυστάλλωσης OCP σε φύτρα κρυστάλλων βιοτσιμέντου Α, 2: κρυστάλλωσης OCP σε φύτρα κρυστάλλων βιοτσιμέντου B, 3: κρυστάλλωσης OCP σε φύτρα κρυστάλλων υδροξυαπατίτη (ΗΑP) και 4: κρυστάλλωσης OCP σε φύτρα κρυστάλλων φωσφορικού οκτασβεστίου (OCP). Στα σχήματα 7.32 και 7.33 παρουσιάζονται φωτογραφίες που ελήφθησαν με ηλεκτρονικό μικροσκόπιο σάρωσης, στις οποίες είναι εμφανείς οι φυλλόμορφοι πυκνοσχηματισμένοι κρύσταλλοι, μεγέθους μm, του OCP που κρυσταλλώθηκε στα βιοτσιμέντα Α και Β, αντίστοιχα. Σχήμα 7.32: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων βιοτσιμέντου A; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.70 & σ HAP =
229 Σχήμα 7.33: Μικροφωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων βιοτσιμέντου Β; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.70 & σ HAP = Η μορφολογική εξέταση της φάσης που εναποτέθηκε στην περίπτωση κρυστάλλωσης OCP σε κρυσταλλικά φύτρα ΗΑΡ, έδειξε την παρουσία πλακοειδών σχηματισμών OCP μεγέθους περίπου 0.5 μm (σχήμα 7.34). Σχήμα 7.34: Μικροφωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε κρυσταλλικά φύτρα ΗΑΡ; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.70 & σ HAP =
230 Στο σχήμα 7.35 που ακολουθεί, διακρίνονται οι φυλλόμορφοι κρύσταλλοι OCP, μεγέθους 1-2 μm, οι οποίοι κρυσταλλώθηκαν στα φύτρα κρυστάλλων OCP. Σχήμα 7.35: Μικροφωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε κρυσταλλικά φύτρα ΟCP; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.70 & σ HAP = Όπως φάνηκε και από τη μορφολογική εξέταση, η φάση του OCP που ταυτοποιήθηκε, σταθεροποιήθηκε σε όλα τα υποστρώματα που εξετάστηκαν κατά τη μελέτη της κρυστάλλωσης OCP με σπορά κρυσταλλικών φύτρων σε υπέρκορα διαλύματα με τη μέθοδο σταθερής σύστασης. 7.3 ΕΤΕΡΟΓΕΝΗΣ ΣΧΗΜΑΤΙΣΜΟΣ ΦΩΣΦΟΡΙΚΟΥ ΟΚΤΑΣΒΕΣΤΙΟΥ (OCP) ΣΕ ΥΠΟΣΤΡΩΜΑΤΑ ΑΝΘΡΑΚΙΚΟΥ ΑΣΒΕΣΤΙΟΥ (CaCO 3 ) ΕΙΣΑΓΩΓΗ Στα βιολογικά συστήματα, εκτός από τον σχηματισμό των αλάτων φωσφορικού ασβεστίου, σημαντικό μέρος αποτελούν και τα άλατα του ανθρακικού ασβεστίου. Στα πλαίσια της βελτίωσης των φυσικών και χημικών ιδιοτήτων των τσιμέντων που χρησιμοποιούνται στα βιοϋλικά, την προσοχή των ερευνητών έχει ελκύσει η ανάπτυξη βιοτσιμέντων ανθρακικού ασβεστίου. Παρότι παρασκευάζονται και χρησιμοποιούνται σε μεγάλη κλίμακα βιοτσιμέντα αποκλειστικά φωσφορικού ασβεστίου ή και με μικρή περιεκτικότητα σε ανθρακικό ασβέστιο, όπως έχει αναφερθεί και στις προηγούμενες ενότητες, η δυνατότητα χρήσεως διαφόρων πολυμορφικών φάσεων ανθρακικού 204
231 ασβεστίου ως βάσεων για την παρασκευή νέων βιοϋλικών παρουσιάζει εξαιρετικό ενδιαφέρον [Combes et al., 2006]. To ανθρακικό ασβέστιο, το οποίο υπάρχει σε αφθονία στη φύση (πχ. σκελετός κοραλλιών), έχει χρησιμοποιηθεί ως εμφυτεύσιμο υλικό [Guillemin et al., 1995 ; Souyris et al., 1985]. Στη βιβλιογραφία έχει αναφερθεί, ότι το ανθρακικό ασβέστιο είναι βιοσυμβατό, βιοδραστικό, αφομοιώνεται εύκολα από το οστό και το γεγονός πως είναι περισσότερο απορροφήσιμο σε σχέση με τον ΗΑΡ [Braye et al., 1996], λόγω της μεγαλύτερης διαλυτότητάς του, το καθιστά ιδανικό υλικό για την παρασκευή βιοτσιμέντων. Επιπλέον, έχει αναφερθεί ως πιθανή πρόδρομη φάση για τη σύνθεση οστού [Kim and Park, 2010]. Στην παρούσα ενότητα μελετήθηκε ο ετερογενής σχηματισμός του OCP σε υποστρώματα ανθρακικού ασβεστίου, σε συνθήκες σταθερού υπερκορεσμού στους 37 o C σε ph 7.40 ± 0.1 και σε ιοντική ισχύ 0.15Μ NaCl, χρησιμοποιώντας ως φύτρα σποράς κρυστάλλους ασβεστίτη καθώς και μία νέα σύνθεση βιοτσιμέντου ανθρακικού ασβεστίου To σύστημα του ανθρακικού ασβεστίου Το ανθρακικό ασβέστιο (CaCO 3 ) είναι μια χημική ένωση, η οποία απαντάται τόσο στο φυσικό περιβάλλον όσο και στους ζωντανούς οργανισμούς. Η παρουσία των διαφόρων μορφών του ανθρακικού ασβεστίου στη φύση αποτελεί χαρακτηριστικό παράδειγμα πολυμορφισμού του συστήματος. Υπάρχουν τρεις άνυδρες, μία άμορφη και δύο ένυδρες (διένυδρη και εξαένυδρη) μορφές του ανθρακικού ασβεστίου. Οι τρεις κύριες άνυδρες μορφές του ανθρακικού ασβεστίου είναι κρυσταλλικές και χαρακτηρίζονται από την συχνή τους εμφάνιση στη φύση καθώς και στους ζωντανούς οργανισμούς, ενώ η άμορφη και οι δύο ένυδρες μορφές είναι πιο σπάνιες στην εμφάνιση τους λόγω κυρίως της χημικής τους αστάθειας [Lowenstam and Weiner, 1989]. Οι σχηματισμοί του ανθρακικού ασβεστίου έχουν βρεθεί στο φυσικό περιβάλλον τόσο στον στερεό φλοιό της γης ως συστατικά ορυκτών όσο και στον πυθμένα λιμνών και θαλασσών καθώς και στα σπήλαια με τη μορφή σταλαγμιτών-σταλακτιτών. Στους ζωντανούς οργανισμούς το ανθρακικό ασβέστιο εμφανίζεται τόσο ως αποτέλεσμα φυσιολογικής ασβεστοποίησης όσο και σε παθολογικές περιπτώσεις. Παραδείγματα φυσιολογικής ασβεστοποίησης αποτελούν οι ωτόλιθοι που βρίσκονται στο εσωτερικό των αυτιών των ψαριών, όπου το ανόργανο τμήμα του σκληρού αυτού ιστού αποτελείται από ανθρακικό ασβέστιο. Επίσης, αρκετοί θαλάσσιοι οργανισμοί όπως τα 205
232 κοχύλια, τα μαλάκια, τα κοράλλια καθώς και οι ακανθωτοί σκελετοί (π.χ. αχινοί) αποτελούνται από ανθρακικό ασβέστιο [Mann, 1989]. Περιπτώσεις παθολογικής ασβεστοποίησης αποτελούν οι σχηματισμοί χολικών και νεφρικών λίθων. Παρότι οι νεφρικοί λίθοι αποτελούνται κυρίως από οξαλικό ασβέστιο, έχουν αναφερθεί στη βιβλιογραφία περιπτώσεις λίθων, οι οποίοι αποτελούνται μεταξύ άλλων και από ανθρακικό ασβέστιο [Prien and Frondel, 1947]. Οι τρεις κύριες πολυμορφικές κρυσταλλικές φάσεις του ανθρακικού ασβεστίου κατά σειρά αύξουσας θερμοδυναμικής σταθερότητας είναι οι ακόλουθες: ο βατερίτης, ο αραγωνίτης και ο ασβεστίτης. Ο βατερίτης αποτελεί την πιο ευδιάλυτη και θερμοδυναμικά ασταθέστερη φάση του ανθρακικού ασβεστίου. Από κρυσταλλογραφική άποψη, ο βατερίτης κρυσταλλώνεται στο εξαγωνικό σύστημα με διαστάσεις μοναδιαίας κυψελίδας a o = Å, c o = Å [Αρ. κάρτας ]. Η μορφολογία των κρυστάλλων βατερίτη είναι κυρίως σφαιρική, διαμέτρου μm περίπου. Η ύπαρξη του βατερίτη έχει ανιχνευθεί σε ωτολίθους, σε κελύφη μαλακίων και σπανιότερα σε πετρώματα. Η θερμοδυναμική αστάθεια του βατερίτη και η μετατροπή του στις άλλες δύο σταθερότερες φάσεις του ανθρακικού ασβεστίου, αποτελεί μια εξήγηση της σπάνιας εμφάνισής του στη φύση. Ο αραγωνίτης αποτελεί τη δεύτερη κατά σειρά θερμοδυναμικής σταθερότητας φάση του ανθρακικού ασβεστίου και από κρυσταλλογραφική άποψη κατατάσσεται στο ορθορομβικό σύστημα με διαστάσεις μοναδιαίας κυψελίδας a o = Å, b o = Å, c o = Å [Αρ. κάρτας 5-453]. Η μορφολογία των κρυστάλλων του αραγωνίτη είναι κυρίως πρισματική. Ο αραγωνίτης απαντάται σε κοράλλια, σε κελύφη οστρακόδερμων, σε ωτολίθους και σπανιότερα σε πετρώματα. Ο ασβεστίτης θεωρείται η θερμοδυναμικά σταθερότερη κρυσταλλική φάση του ανθρακικού ασβεστίου, είναι ελάχιστα διαλυτός σε υδατικό περιβάλλον και κρυσταλλώνεται στο ρομβοεδρικό σύστημα με διαστάσεις μοναδιαίας κυψελίδας a o = Å, c o = Å [Aρ. Κάρτας 5-586]. Ο ασβεστίτης απαντάται στο σκελετό των ζωντανών θαλάσσιων οργανισμών, ενώ αποτελεί περίπου το 7% του γήινου φλοιού με τη μορφή ορυκτών ασβεστολιθικών πετρωμάτων ή με τη μορφή του μαρμάρου. Επιπροσθέτως, ασβεστίτης βρίσκεται στους πυθμένες των θαλασσών λόγω της διαλυτοποίησης των πετρωμάτων [Mann, 1989]. 206
233 7.3.2 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Αντιδραστήρια Για την παρασκευή των υπέρκορων διαλυμάτων εργασίας και των διαλυμάτων τιτλοδότησης χρησιμοποιήθηκαν τα αντιδραστήρια που αναφέρθηκαν στην ενότητα Παρασκευή και χαρακτηρισμός συνθετικών κρυστάλλων CaCO 3 Το βιοτσιμέντο με βάση το ανθρακικό ασβέστιο παρασκευάστηκε με ανάμιξη αμόρφου ανθρακικού ασβεστίου και βατερίτη με τριπλά απεσταγμένο νερό. Η πάστα που παρασκευάστηκε, παρέμεινε στους 37 ο C για 2 ημέρες, ώστε να σκληρυνθεί, σε κορεσμένη σε υδρατμούς ατμόσφαιρα και στη συνέχεια κονιοποιήθηκε με γουδί [Combes et al., 2006]. Ο φυσικοχημικός χαρακτηρισμός των κρυστάλλων του βιοτσιμέντου CaCO 3 που παρασκευάστηκε και παρουσιάζεται στη συνέχεια, έδειξε πως πρόκειται για μίγμα κρυστάλλων αραγωνίτη-ασβεστίτη. Επιπλέον, παρασκευάστηκαν στο εργαστήριο κρύσταλλοι ασβεστίτη με στάγδην προσθήκη 1L διαλύματος χλωριούχου ασβεστίου (CaCl 2 ) συγκεντρώσεως 0.2 M σε 1L διαλύματος ανθρακικού νατρίου (Νa 2 CO 3 ) συγκεντρώσεως 0.2 M, το οποίο ήταν υπό συνεχή ανάδευση σε θερμοκρασία 25 ο C [Reddy and Nancollas, 1971]. Μετά από περίοδο ωρίμανσης των κρυστάλλων για τρεις εβδομάδες στο μητρικό υγρό υπό συνεχή ανάδευση και σε θερμοκρασία δωματίου, ακολούθησε διήθηση υπό κενό διαμέσου φίλτρου 0.22 μm, ξήρανση σε ξηραντήρα και κονιοποίηση του στερεού με γουδί. Η ειδική επιφάνεια των κρυστάλλων μίγματος αραγωνίτη-ασβεστίτη (βιοτσιμέντου CaCO 3 ) και των συνθετικά παρασκευασμένων κρυστάλλων ασβεστίτη μετρήθηκε με τη μέθοδο ρόφησης αζώτου (BET) και υπολογίστηκε 4.15 m 2 g -1 και 0.32 m 2 g -1, αντιστοίχως. Η ταυτοποίηση και των δύο τύπων κρυστάλλων ανθρακικού ασβεστίου που παρασκευάστηκαν, πραγματοποιήθηκε με περιθλασιμετρία κόνεως ακτίνων-χ. Στο περιθλασιόγραμμα ακτίνων-χ που παρουσιάζεται στο σχήμα 7.36, διακρίνεται το φάσμα των κρυστάλλων του βιοτσιμέντου CaCO 3, το οποίο και συγκρίνεται με πρότυπα περιθλασιογράμματα ακτίνων-χ συνθετικού αραγωνίτη και ασβεστίτη από την κρυσταλλογραφική βάση δεδομένων Search Match. Συγκρίνοντας τα περιθλασιογράμματα ακτίνων-χ, από την ταύτιση των κύριων χαρακτηριστικών 207
234 ανακλάσεων (1 1 1), (0 2 1), (0 1 2), και (2 2 1) του αραγωνίτη (26,2 ο ; 27,2 ο ; 33,1 ο και 45,9 ο σε 2θ, αντίστοιχα), και της χαρακτηριστικής ανάκλασης (1 0 4) του ασβεστίτη (29,42 ο σε 2θ), προέκυψε πως οι κρύσταλλοι του παρασκευασμένου βιοτσιμέντου CaCO 3, ήταν μίγμα αραγωνίτη-ασβεστίτη Intensity/ a.u Σχήμα 7.36: Περιθλασιογράμματα ακτίνων-χ κρυσταλλικών φύτρων (α) 1: βιοτσιμέντου ανθρακικού ασβεστίου (CaCO 3 ), 2: συνθετικού αραγωνίτη από (Αρ ) και 3: συνθετικού ασβεστίτη (Αρ ). Επιπλέον, από το περιθλασιόγραμμα ακτίνων-χ του σχήματος 7.37 ταυτοποιήθηκαν και οι κρύσταλλοι του ασβεστίτη που παρασκευάστηκαν. 208
235 104 Intensity/ a.u Σχήμα 7.37: Περιθλασιογράμματα ακτίνων-χ κρυσταλλικών φύτρων 1: ασβεστίτη και 2: συνθετικού ασβεστίτη (Αρ ). Η ταυτοποίηση των κρυσταλλικών φάσεων του ανθρακικού ασβεστίου που παρασκευάστηκαν πραγματοποιήθηκε και με τη χρήση υπέρυθρης φασματοσκοπίας. Στο σχήμα 7.38 παρουσιάζονται τα φάσματα υπερύθρου των κρυστάλλων του βιοτσιμέντου CaCO 3 και των κρυστάλλων του ασβεστίτη που παρασκευάστηκαν. Για το βιοτσιμέντο CaCO 3 επιβεβαιώθηκε πως πρόκειται για μίγμα αραγωνίτη-ασβεστίτη από την ταύτιση των ζωνών απορρόφησής του με τις τέσσερις χαρακτηριστικές κορυφές απορρόφησης του αραγωνίτη 700 cm -1, 713 cm -1, 856 cm -1 και 1080 cm -1 και τις δύο χαρακτηριστικές ζώνες απορρόφησης του ασβεστίτη 713 cm -1 και 876 cm
236 ιαπερατότητα Κυματάριθμος/ cm -1 Σχήμα 7.38: Φάσματα υπερύθρου 1: κρυσταλλικών φύτρων βιοτσιμέντου CaCO 3 και 2: κρυσταλλικών φύτρων ασβεστίτη. Στο σχήμα 7.39 που ακολουθεί, παρουσιάζονται φωτογραφίες που ελήφθησαν με το ηλεκτρονικό μικροσκόπιο σάρωσης, στις οποίες φαίνεται η μορφολογία των κρυστάλλων του ανθρακικού ασβεστίου που παρασκευάστηκαν. Συγκεκριμένα, στο σχήμα 7.39 (α) παρουσιάζεται η μορφολογία των κρυστάλλων του βιοτσιμέντου (CaCO 3 ), όπου διακρίνεται ένα μίγμα κρυστάλλων αραγωνίτη μεγέθους περίπου 2 μm και ασβεστίτη, ενώ στο σχήμα 7.39 (β) φαίνονται οι καλοσχηματισμένες ρομβοεδρικές επιφάνειες των κρύσταλλων του ασβεστίτη. Σχήμα 7.39: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλων ανθρακικού ασβεστίου (α) βιοτσιμέντου και (β) ασβεστίτη. 210
237 Πειραματική διάταξη και διαδικασία Η προετοιμασία των σταθερών υπέρκορων διαλυμάτων εργασίας, των διαλυμάτων τιτλοδότησης, η περιγραφή της πειραματικής διάταξης καθώς και η πειραματική διαδικασία ήταν όμοια με βάση αυτών που περιγράφηκαν στην προηγούμενη ενότητα ( ). Οι συγκεντρώσεις των διαλυμάτων τιτλοδότησης για την διατήρηση σταθερής σύστασης κατά την διάρκεια της καταβύθισης του OCP στα υποστρώματα ανθρακικού ασβεστίου υπολογίστηκαν βάσει των εξισώσεων (5-1β) (5-5β), ενώ οι χημικές ισορροπίες και οι τιμές των σταθερών οι οποίες χρησιμοποιήθηκαν στους υπολογισμούς των υπερκορεσμών παρουσιάζονται στο Παράρτημα Ι ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Στον πίνακα 7.7 που ακολουθεί παρουσιάζονται οι πειραματικές συνθήκες και τα αποτελέσματα των μετρήσεων της κινητικής στα πειράματα κρυστάλλωσης του OCP σε κρυσταλλικά φύτρα ανθρακικού ασβεστίου (μίγμα αραγωνίτη-ασβεστίτη και ασβεστίτη) σε συνθήκες σταθερού υπερκορεσμού. Πίνακας 7.7 Πειραματικές συνθήκες και αποτελέσματα μετρήσεων της κινητικής της κρυσταλλικής ανάπτυξης: ολική συγκέντρωση ασβεστίου, C Ca, υπερκορεσμός ως προς OCP, Ω ΟCP, σχετικοί υπερκορεσμοί ως προς OCP και HAP, σ OCP και σ HAP, χρόνος επαγωγής, τ, και αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης, R g, για την κρυστάλλωση του φωσφορικού οκτασβεστίου (OCP) στα διάφορα υποστρώματα ανθρακικού ασβεστίου (CaCO 3 ) σε υπέρκορα διαλύματα και σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, θ = 37.0 ± 0.1 o C και C Ca /C P = 1.33, όπου C P η ολική συγκέντρωση των φωσφορικών. C Ca / 10-3 M Ω OCP σ OCP σ HAP τ /s Υπόστρωμα αραγωνίτης-ασβεστίτης ασβεστίτης αραγωνίτης-ασβεστίτης ασβεστίτης αραγωνίτης-ασβεστίτης ασβεστίτης αραγωνίτης-ασβεστίτης ασβεστίτης R g / 10-5 mol min -1 m
238 Όπως διακρίνεται και στον πίνακα, σε όλα τα πειράματα που πραγματοποιήθηκαν, τα διαλύματα ήσαν υπέρκορα και ως προς ΗΑΡ. Παρόλα αυτά δεν παρατηρήθηκε ο σχηματισμός της φάσης αυτής. Θα πρέπει να αναφερθεί πως τα πειράματα επεκτάθηκαν και σε χαμηλότερες τιμές υπερκορεσμού από αυτές που παρουσιάζονται στον πίνακα 7.7 (σ OCP = ), ωστόσο σε αυτές τις συνθήκες δεν έλαβε χώρα κρυσταλλική ανάπτυξη OCP για χρονικές περιόδους μεγαλύτερες των 72 ωρών. Η κρυστάλλωση του OCP στα υποστρώματα του ανθρακικού ασβεστίου έλαβε χώρα μετά την πάροδο χρόνου επαγωγής, τ, ο οποίος ήταν αντιστρόφως ανάλογος του σχετικού υπερκορεσμού του διαλύματος, όπως φαίνεται και στο σχήμα Kαι για τους δύο τύπους κρυσταλλικών φύτρων ανθρακικού ασβεστίου, που χρησιμοποιήθηκαν ως υποστρώματα κρυσταλλικής ανάπτυξης OCP, μετρήθηκαν οι ίδιοι χρόνοι επαγωγής, στην ίδια τιμή σχετικού υπερκορεσμού Χρόνος Επαγωγής, / s Υπερκορεσμός, OCP Σχήμα 7.40: Μεταβολή του χρόνου επαγωγής, τ, συναρτήσει του υπερκορεσμού ως προς OCP, Ω, για την κρυστάλλωση ΟCP σε φύτρα κρυστάλλων ανθρακικού ασβεστίου (CaCO 3 ) σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, 37 C, 0.15 M NaCl: ( ) μίγμα αραγωνίτη-ασβεστίτη; ( ) φύτρα ασβεστίτη. 212
239 Από την εξίσωση (7-10) και από την κλίση της ευθείας της λογαριθμικής παράστασης του χρόνου επαγωγής συναρτήσει του αντιστρόφου του τετραγώνου του υπερκορεσμού (σχήμα 7.41), υπολογίστηκε η τιμή της επιφανειακής ενέργειας, γ s, του OCP και βρέθηκε ίση με 10 mj m -2. 3,2 3,0 log/s) 2,8 2,6 0,06 0,08 0,10 (log OCP ) -2 Σχήμα 7.41: Μεταβολή του λογαρίθμου του χρόνου επαγωγής, log τ, συναρτήσει του αντίστροφου του τετραγώνου του λογαρίθμου του υπερκορεσμού, (log Ω) -2, για την κρυστάλλωση του ΟCP σε φύτρα κρυστάλλων ανθρακικού ασβεστίου (CaCO 3 ) σε συνθήκες σταθερού υπερκορεσμού, ph 7.40, 37 C, 0.15 M NaCl: ( ) μίγμα αραγωνίτηασβεστίτη; ( ) φύτρα ασβεστίτη. Η χαμηλή τιμή της επιφανειακής ενέργειας του OCP ήταν αναμενόμενη λόγω της ετερογενούς πυρηνογένεσης, όμως, είναι σε καλή συμφωνία με αντίστοιχες τιμές από μελέτες για την κρυσταλλική ανάπτυξη OCP σε σωματίδια TiO 2 (14 mj m -2 ) [Wu and Nancollas, 1997] και σε TCP (17 mj m -2 ) [Heughebaert et al., 1983]. Στο σχήμα 7.42 δίδεται η λογαριθμική εξάρτηση των αρχικών ρυθμών κρυσταλλικής ανάπτυξης OCP ως συνάρτηση του σχετικού υπερκορεσμού για τα πειράματα με σπορά κρυσταλλικών φύτρων ανθρακικού ασβεστίου. 213
240 -3,0-3,5 log (R g / mol min -1 m -2 ) -4,0-4,5-5,0-5,5 0,16 0,24 0,32 0,40 log OCP Σχήμα 7.42: Κινητική της κρυστάλλωσης του OCP σε φύτρα κρυστάλλων ανθρακικού ασβεστίου (CaCO 3 ) σε συνθήκες σταθερού υπερκορεσμού. Διαγράμματα του λογαρίθμου του αρχικού ρυθμού κρυσταλλικής ανάπτυξης OCP συναρτήσει του λογαρίθμου του αντίστοιχου σχετικού υπερκορεσμού. θ= 37 C, ph 7.40, 0.15 M NaCl: ( ) μίγμα αραγωνίτη-ασβεστίτη; ( ) φύτρα ασβεστίτη. Από την τεταγμένη επί την αρχή και τη κλίση της ευθείας του σχήματος 7.42 υπολογίσθηκε η τιμή της φαινόμενης σταθεράς της ταχύτητας και η φαινόμενη τάξη της κρυστάλλωσης αντίστοιχα, για κάθε υπόστρωμα. Οι τιμές που προέκυψαν από τους υπολογισμούς ήταν k g = ( ) mol min -1 m -2 και n = 1.11 ( 0.15) για την κρυστάλλωση OCP σε κρυσταλλικά φύτρα μίγματος αραγωνίτη-ασβεστίτη, και k g = ( ) mol min -1 m -2 και n = 1.14 ( 0.1) για την κρυστάλλωση OCP σε κρυσταλλικά φύτρα ασβεστίτη. Η τιμή αυτή είναι σε συμφωνία με βιβλιογραφικές αναφορές σχετικά με την κρυστάλλωση του φωσφορικού οκτασβεστίου σε διάφορα υποστρώματα σε τιμές υψηλού υπερκορεσμού (σ OCP > 0.6) [Nancollas, 1989]. Από την τιμή της φαινόμενης τάξης προέκυψε το συμπέρασμα πως ο μηχανισμός της ανάπτυξης των κρυστάλλων ελέγχεται από επιφανειακή διάχυση των δομικών μονάδων στα ενεργά κέντρα κρυστάλλωσης. Για το μηχανισμό αυτό συνηγορεί και το γεγονός ότι οι μετρούμενοι ρυθμοί κρυσταλλικής ανάπτυξης ήσαν ευθέως ανάλογοι της ολικής επιφάνειας των εισαγόμενων κρυσταλλικών φύτρων. Όπως φαίνεται και στο σχήμα 7.43 οι αρχικές ταχύτητες κρυσταλλικής ανάπτυξης εκφρασμένες σε mol ανά 214
241 μονάδα χρόνου βρέθηκαν ανάλογες της ποσότητας των κρυστάλλων CaCO 3 που χρησιμοποιήθηκαν για την σπορά των σταθερών υπέρκορων διαλυμάτων. Η διαπίστωση αυτή αποτελεί ένδειξη ότι η κρυστάλλωση πραγματοποιείται πάνω στα ενεργά κέντρα και δεν λαμβάνει χώρα δευτερογενής πυρηνογένεση [Nancollas and Koutsoukos, 1980 ; Spanos and Koutsoukos, 1998]. 3,0x10-6 2,4x10-6 R g / mol OCP min -1 1,8x10-6 1,2x10-6 6,0x ,5 23 Ποσότητα κρυσταλλικών φύτρων CaCO 3 / mg Σχήμα 7.43: Επίδραση της ποσότητας των κρυσταλλικών φύτρων ανθρακικού ασβεστίου (CaCO 3 ) στον αρχικό ρυθμό κρυσταλλικής ανάπτυξης του OCP. Η κρυσταλλική συμβατότητα μεταξύ φωσφορικού οκτασβεστίου-ασβεστίτη και φωσφορικού οκτασβεστίου-αραγωνίτη, υπολογίστηκε από την εξίσωση (2-39) και με βάση τις διαστάσεις πλέγματος του OCP για τα επίπεδα (100) και (010) (19.26 (Å) x (Å) (89.3) και (Å) x (Å) (92.2) αντίστοιχα) με το επίπεδο (10-10) του ασβεστίτη (14.97 (Å) x (Å) (90.0)) και το επίπεδο (001) του αραγωνίτη (Å) x (Å) (90.0) [Londsale, 1968]. Προέκυψε πως ο βαθμός κρυσταλλικής συμβατότητας για το ζεύγος OCP-ασβεστίτη ήταν 28% και 39% αντίστοιχα για τις δύο διαστάσεις, ενώ η τιμή της κρυσταλλικής συμβατότητας για το ζεύγος OCP και αραγωνίτη υπολογίστηκε 29% και 37% αντίστοιχα για τις δύο διαστάσεις πλέγματος. Για να ικανοποιείται η συνθήκη της συμβατότητας αναγκαία συνθήκη είναι να έχει τιμές μεταξύ του 10-20%. Ωστόσο, στη βιβλιογραφία αναφέρεται πως σε διαλύματα 215
242 υψηλού υπερκορεσμού, μπορεί να υπάρξει επιταξία και για τιμές έως 50% [Turnbull and Vonnegut, 1952]. Έτσι, ικανοποιείται η συνθήκη για την επιταξιακή ανάπτυξη του OCP σε υποστρώματα ανθρακικού ασβεστίου. Από τα περιθλασιογράμματα ακτίνων-χ της φάσης που κρυσταλλώθηκε στα κρυσταλλικά φύτρα ανθρακικού ασβεστίου και το περιθλασιόγραμμα ακτίνων-χ συνθετικού OCP από την κρυσταλλογραφική βάση δεδομένων Search Match (Aρ. Κάρτας ) που απεικονίζονται στο σχήμα 7.44, ταυτοποιήθηκε ο σχηματισμός του θερμοδυναμικά ασταθούς OCP, αφού ήταν δυνατή η διάκριση της χαρακτηριστικής κύριας ανάκλασης (0 1 0) του OCP (4,73 ο σε 2θ) παρότι ήταν αρκετά μικρής έντασης. 104 Intensity/ a.u Σχήμα 7.44: Περιθλασιογράμματα ακτίνων-χ 1: κρυστάλλωσης OCP σε φύτρα κρυστάλλων ασβεστίτη, 2: κρυστάλλωσης OCP σε φύτρα κρυστάλλων μίγματος αραγωνίτη-ασβεστίτη και 3: σε κρυσταλλικά φύτρα OCP (Αρ ). Το γεγονός ότι η φάση που κρυσταλλώθηκε στα κρυσταλλικά φύτρα μίγματος αραγωνίτη-ασβεστίτη αλλά και στους κρυστάλλους ασβεστίτη ήταν το ΟCP, επιβεβαιώθηκε και από τα φάσματα υπερύθρου των στερεών που εξετάστηκαν μετά την κρυστάλλωση του OCP στα δύο υποστρώματα ανθρακικού ασβεστίου. Στο σχήμα 7.45 διακρίνονται δύο χαρακτηριστικές ζώνες απορρόφησης του φωσφορικού οκτασβεστίου στα 560 cm -1 και 600 cm -1 και για τις δύο περιπτώσεις. 216
243 ιαπερατότητα Κυματάριθμος/ cm -1 Σχήμα 7.45: Φάσματα υπερύθρου κρυστάλλωσης OCP 1: σε φύτρα μίγματος αραγωνίτηασβεστίτη και 2: σε φύτρα ασβεστίτη. Στο σχήμα 7.46 που ακολουθεί, απεικονίζεται η μορφολογία των κρυστάλλων της φάσης που σχηματίστηκε κατά την κρυστάλλωση OCP σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων μίγματος αραγωνίτη-ασβεστίτη. 217
244 Σχήμα 7.46: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης OCP σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων μίγματος αραγωνίτη-ασβεστίτη; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.80 & σ HAP = Στις φωτογραφίες SEM που ελήφθησαν, παρατηρήθηκαν χαρακτηριστικοί φυλλόμορφοι, πυκνοσχηματισμένοι κρυσταλλίτες OCP μεγέθους περίπου 200 nm, οι οποίοι συνυπήρχαν με τα κρυσταλλικά φύτρα μίγματος αραγωνίτη ασβεστίτη. Η ίδια μορφολογία παρατηρήθηκε και για το στερεό που σχηματίστηκε στην περίπτωση κρυστάλλωσης OCP σε φύτρα ασβεστίτη. Στις φωτογραφίες του σχήματος 7.47 φαίνονται οι φυλλόμορφοι κρυσταλλίτες OCP μεγέθους nm που σχηματίστηκαν στις ρομβοεδρικές επιφάνειες των κρυστάλλων ασβεστίτη. 218
245 Σχήμα 7.47: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης φωσφορικού οκτασβεστίου (OCP) σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων ασβεστίτη; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 1.80 & σ HAP = Ο φυσικοχημικός χαρακτηρισμός και η μορφολογική εξέταση των στερεών που σχηματίστηκαν κατά την κρυστάλλωση του OCP σε συνθήκες σταθερού υπερκορεσμού, έδειξαν ότι στα υποστρώματα ανθρακικού ασβεστίου εναποτέθηκαν αποκλειστικά κρύσταλλοι του θερμοδυναμικά ασταθούς OCP. Αξίζει να σημειωθεί, παρότι τα πειράματα διήρκεσαν για σχετικά μεγάλο χρονικό διάστημα, δεν υπήρξαν ενδείξεις για την υδρόλυση του OCP προς το θερμοδυναμικά σταθερότερο ΗΑΡ, γεγονός που υποδηλώνει τη σταθεροποίηση του ασταθούς OCP από τα υποστρώματα των αλάτων του ανθρακικού ασβεστίου. Η απουσία-παρεμπόδιση της κρυσταλλικής ανάπτυξης του ΗΑΡ σε διαλύματα είτε υπέρκορα μόνο ως προς τη φάση του ΗΑΡ είτε ελαφρώς υπέρκορα ως προς OCP, προφανώς οφείλεται στην αναστολή της ανάπτυξης κρυστάλλων ΗΑΡ λόγω των ανθρακικών που υπάρχουν σε ισορροπία στο διάλυμα εργασίας με τα υποστρώματα ανθρακικού ασβεστίου. Παρόμοια συμπεριφορά έχει αναφερθεί και για το θαλάσσιο 219
246 περιβάλλον, όπου φάνηκε να παρεμποδίζεται ο σχηματισμός HAP από υπέρκορα διαλύματα όπου λαμβάνει χώρα κρυστάλλωση του ΟCP [Gunnars et al., 2004]. 7.4 ΚΡΥΣΤΑΛΛΙΚΗ ΑΝΑΠΤΥΞΗ ΑΛΑΤΩΝ ΦΩΣΦΟΡΙΚΟΥ ΑΣΒΕΣΤΙΟΥ ΠΑΡΟΥΣΙΑ ΙΟΝΤΩΝ ΣΤΡΟΝΤΙΟΥ (Sr 2+ ) ΕΙΣΑΓΩΓΗ O ρόλος του στροντίου στη βιολογική ασβεστοποίηση παρουσιάζει ιδιαίτερο ενδιαφέρον. Το στρόντιο χρησιμοποιείται στην παρασκευή φαρμάκων για την αντιμετώπιση της οστεοπόρωσης με σκοπό τη μείωση των καταγμάτων (π.χ. ρανελικό στρόντιο). Κατά τη δράση τέτοιων φαρμακευτικών ουσιών, αποδεσμεύεται το στρόντιο το οποίο απορροφάται από τα οστά, διεγείροντας το σχηματισμό των οστών και περιορίζοντας έτσι την αποδόμησή τους [McCaslin and Janes, 1959 ; Reginster et al., 2005]. Στην βιβλιογραφία αναφέρεται, ότι η παρουσία του στροντίου αυξάνει τον αριθμό των ενεργών οστεοβλαστών, οδηγώντας σε αύξηση της παραγωγής νέου οστίτη ιστού από τα κύτταρα αυτά [Ammann et al., 2004 ; Meunier et al., 2004]. Απόδειξη της δράσης του στροντίου στην οστική παραγωγή αποτελεί και η αύξηση της παραγωγής κολλαγόνου [Canalis et al., 1996]. Επιπλέον, αναφέρεται πως η παρουσία στροντίου μπορεί να οδηγήσει σε μείωση της οστικής απορρόφησης από τους οστεοκλάστες [Marie, 2006]. Το γεγονός ότι η αλληλεπίδραση του στροντίου με τα οστά είναι παρόμοια με αυτή του ΗΑΡ [Neuman et al., 1963] και το ότι η δράση του στροντίου στα οστά είναι ευεργετική, όπως προαναφέρθηκε, έχει οδηγήσει σε αυξημένο ενδιαφέρον για την παρασκευή και τη χρήση βιοτσιμέντων και βιοκεραμικών υλικών φωσφορικού ασβεστίου ως εμφυτεύματα, αφού η παρουσία του στροντίου μπορεί να ενισχύσει τη βιοενεργότητα και τη βιοσυμβατότητα των βιοϋλικών [Alkhraisat et al., 2011 ; Landi et al., 2007 ; Leroux and Lacout, 2001 ; Saint-Jean et al., 2005]. To στρόντιο, ως χημικό στοιχείο που υπάρχει στα οστά, λόγω της χημικής ομοιότητας και της εγγύτητας μεγέθους που έχει με το ασβέστιο (r Sr2+ = 1.12 Å, r Ca2+ = 0.99 Å) μπορεί να καταλάβει τη θέση του ασβεστίου και να ενσωματωθεί στο κρυσταλλικό πλέγμα του υδροξυαπατίτη και του φωσφορικού οκτασβεστίου [Boanini et al., 2010 ; Bracci et al., 2009 ; Li et al., 2007]. In vitro μελέτες αναφέρουν, επίσης, την παρεμποδιστική δράση του στροντίου κατά την κρυστάλλωση του υδροξυαπατίτη [Christoffersen et al., 1997; Koutsoukos and Nancollas, 1981]. Θεωρητικοί υπολογισμοί που έγιναν οδήγησαν στο συμπέρασμα, ότι τα ιόντα στροντίου μπορούν να 220
247 υποκαταστήσουν το ασβέστιο στο κρυσταλλικό πλέγμα του OCP μέσω ιοντοανταλλαγής και να οδηγήσουν στη σταθεροποίησή του [Matsunaga and Murata, 2009]. Η παρουσία ξένων ουσιών ή ιόντων στα υπέρκορα διαλύματα παίζει σημαντικό ρόλο τόσο στην κινητική σχηματισμού του φωσφορικού ασβεστίου όσο και στα χαρακτηριστικά του κρυσταλλικού στερεού το οποίο αναπτύσσεται, αφού πιθανή ενσωμάτωση των ξένων ιόντων στο στερεό θα μπορούσε να επιφέρει σημαντικές αλλαγές στις ιδιότητές του [Matsumoto et al., 2010]. Έτσι, στην ενότητα αυτή διερευνήθηκε η επίδραση των ιόντων στροντίου (Sr 2+ ) στην κινητική κρυσταλλικής ανάπτυξης αλάτων φωσφορικού ασβεστίου σε υποστρώματα συνθετικών κρυστάλλων OCP και HAP σε υπέρκορα διαλύματα φωσφορικού ασβεστίου με τη μέθοδο της σταθερής σύστασης υπέρκορων διαλυμάτων ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Αντιδραστήρια Για την παρασκευή των υπέρκορων διαλυμάτων εργασίας και των διαλυμάτων τιτλοδότησης για την διατήρηση σταθερού υπερκορεσμού, χρησιμοποιήθηκαν τα αντιδραστήρια που αναφέρθηκαν στην ενότητα Επιπλέον, ως πηγή ιόντων στροντίου χρησιμοποιήθηκε διάλυμα εξαένυδρου χλωριούχου στροντίου, SrCl 2 6H 2 O, συγκέντρωσης 0.1 Μ. Ως κρυσταλλικά φύτρα χρησιμοποιήθηκαν οι κρύσταλλοι HAP και OCP, οι οποίοι παρασκευάστηκαν και χαρακτηρίστηκαν όπως περιγράφηκε στις ενότητες και , αντίστοιχα Πειραματική διάταξη και διαδικασία Τα πειράματα της μελέτης αυτής πραγματοποιήθηκαν με χρήση της ίδιας πειραματική διάταξης και ακολουθώντας την ίδια πειραματική διαδικασία, όπως έχει ήδη αναφερθεί στις δύο πρώτες ενότητες του κεφαλαίου, με τη μόνη διαφορά ότι γινόταν και προσθήκη του διαλύματος SrCl 2 6H 2 O, πριν την εισαγωγή των κρυσταλλικών φύτρων στο διάλυμα εργασίας. Οι συγκεντρώσεις των διαλυμάτων που προσετίθεντο για την διατήρηση σταθερού υπερκορεσμού κατά την κρυστάλλωση ΗΑΡ και OCP στα αντίστοιχα υποστρώματα, υπολογίστηκαν με χρήση των εξισώσεων (5-1α) (5-4α) και (5-1β) (5-4β), αντιστοίχως, όπου C eff = 10 Ca ws. Στο πρώτο από τα δύο διαλύματα τα οποία προσετίθεντο στο διάλυμα από τις αντίστοιχες σύριγγες, προσετίθετο και η κατάλληλη 221
248 συγκέντρωση SrCl 2 6H 2 O, έτσι ώστε να μην γίνεται αραίωσή του στο υπέρκορο διάλυμα. Η συγκέντρωση του στροντίου στο προστιθέμενο διάλυμα ήταν: όπου TA Sr και T A ws Sr =2 Sr (7-11) ws Sr οι συγκεντρώσεις του στροντίου στο προστιθέμενο διάλυμα και στο διάλυμα εργασίας, αντίστοιχα. Οι χημικές ισορροπίες και οι τιμές των σταθερών οι οποίες χρησιμοποιήθηκαν στους υπολογισμούς των υπερκορεσμών παρουσιάζονται στο Παράρτημα Ι. Επιπλέον, έγινε διάλυση συγκεκριμένης ποσότητας των στερεών που σχηματίστηκαν κατά την κρυστάλλωση σε διάλυμα ΗCl 0.1 N και από τη χημική τους ανάλυση ως προς ασβέστιο, στρόντιο και φωσφορικά, υπολογίστηκαν οι γραμμομοριακοί τους λόγοι στο στερεό. Ο χαρακτηρισμός της φάσης που κρυσταλλώθηκε έγινε με περίθλαση ακτίνων-χ (XRD) και με ηλεκτρονική μικροσκοπία σάρωσης (SEM) ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Οι πειραματικές συνθήκες και τα αποτελέσματα τα οποία προέκυψαν από τα πειράματα κρυστάλλωσης ΟCP και HAP στα αντίστοιχα κρυσταλλικά φύτρα παρουσία στροντίου παρουσιάζονται στους πίνακες 7.8 και 7.9 Πίνακας 7.8 Πειραματικές συνθήκες και αποτελέσματα για την κρυστάλλωση του OCP σε κρυσταλλικά φύτρα OCP, παρουσία στροντίου σε υδατικά διαλύματα σε συνθήκες σταθερού υπερκορεσμού σε ph 7.40, θ = 37.0 ± 0.1 o C, ΝaCl 0.15Μ: ολική συγκέντρωση ασβεστίου, C Ca, ολική συγκέντρωση φωσφορικών, C Ρ, ολική συγκέντρωση στροντίου, C Sr, σχετικός υπερκορεσμός ως προς OCP, σ OCP, αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης, R g, γραμμομοριακός λόγος στροντίου προς ασβέστιο στο διάλυμα εργασίας και στο σχηματιζόμενο στερεό, (Sr/Ca) διάλυμα και (Sr/Ca) στερεό, αντίστοιχα. C Ca / 10-3 M C P / 10-3 M C Sr / 10-3 M σ OCP R g (Sr/Ca) διάλυμα (Sr/Ca) στερεό / 10-7 mol min -1 m
249 Πίνακας 7.9 Πειραματικές συνθήκες και αποτελέσματα για την κρυστάλλωση του υδροξυαπατίτη (HAP) σε κρυσταλλικά φύτρα HAP, παρουσία στροντίου σε υδατικά διαλύματα σε συνθήκες σταθερού υπερκορεσμού σε ph 7.40, θ = 37.0 ± 0.1 o C, ΝaCl 0.15 Μ: ολική συγκέντρωση ασβεστίου, C Ca, ολική συγκέντρωση φωσφορικών, C Ρ, ολική συγκέντρωση στροντίου, C Sr, σχετικός υπερκορεσμός ως προς ΗΑP, σ ΗΑP, αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης, R g, γραμμομοριακός λόγος στροντίου προς ασβέστιο στο διάλυμα εργασίας και στο σχηματιζόμενο στερεό, (Sr/Ca) διάλυμα και (Sr/Ca) στερεό, αντίστοιχα. C Ca / 10-3 M C P / 10-3 M C Sr / 10-3 M σ ΗΑP R g (Sr/Ca) διάλυμα (Sr/Ca) στερεό / 10-8 mol min -1 m Η παρουσία των ιόντων στροντίου στο διάλυμα εργασίας φάνηκε ότι επηρεάζει την κινητική της κρυσταλλικής ανάπτυξης του OCP και του HAP. Όπως φαίνεται και στο σχήμα 7.48, αυξανομένης της συγκέντρωσης στροντίου στο διάλυμα εργασίας σημειώθηκε μείωση του αρχικού ρυθμού κρυσταλλικής ανάπτυξης του OCP. Συγκεκριμένα, η παρουσία στροντίου συγκέντρωσης 1 mμ στο υπέρκορο διάλυμα οδήγησε σε μείωση του ρυθμού κρυσταλλικής ανάπτυξης κατά 40%. 223
250 1,0x10-3 Ρυθμός/ moles OCP m -2 5,0x10-4 0, Χρόνος/ min Σχήμα 7.48: Διαγράμματα του ρυθμού κρυσταλλικής ανάπτυξης OCP σε κρυσταλλικά φύτρα OCP παρουσία στροντίου συναρτήσει του χρόνου: θ = 37 C, ph 7.40, 0.15 M NaCl; ( ) απουσία στροντίου; ( ) 0.25 mm C Sr ; ( ) 0.5 mm C Sr ; ( ) 1.0 mm C Sr. Ανάλογη συμπεριφορά παρατηρήθηκε και στην περίπτωση της κρυσταλλικής ανάπτυξης ΗΑΡ σε φύτρα κρυστάλλων ΗΑΡ (σχήμα 7.49), όπου παρουσία στροντίου συγκέντρωσης 1 mμ ο ρυθμός κρυσταλλικής ανάπτυξης μειώθηκε κατά 60-70%. 224
251 1,4x10-4 Ρυθμός/ moles HAP m -2 7,0x Χρόνος/ min Σχήμα 7.49: Διαγράμματα των ρυθμών κρυσταλλικής ανάπτυξης ΗΑP σε κρυσταλλικά φύτρα ΗΑΡ παρουσία στροντίου συναρτήσει του χρόνου: θ = 37 C, ph 7.40, 0.15 M NaCl; ( ) απουσία στροντίου; ( ) 0.1 mm C Sr ; ( ) 0.25 mm C Sr ; ( ) 0.5 mm C Sr ; ( ) 1.0 mm C Sr. Μεγαλύτερο ποσοστό μείωσης του ρυθμού κρυσταλλικής ανάπτυξης ΗΑΡ παρουσία στροντίου, παρατηρήθηκε στην υψηλότερη τιμή σχετικού υπερκορεσμού, όπως φαίνεται και στο σχήμα
252 % (R g / R g,0 ) C Sr =0 C Sr =0.1mM C Sr =0.25mM C Sr =0.5mM C Sr =1mM Σχήμα 7.50: Ποσοστό μείωσης (%) του ρυθμού κρυσταλλικής ανάπτυξης του HAP σε κρυσταλλικά φύτρα HAP παρουσία στροντίου. R g και R g,0, οι αρχικοί ρυθμοί κρυσταλλικής ανάπτυξης (mol min -1 m -2 ) παρουσία και απουσία στροντίου, αντίστοιχα, για δύο διαφορετικές τιμές υπερκορεσμού: ( ) σ HAP = 6.35 και ( ) σ HAP = 9.94; ph 7.40, 37 C, 0.15 M NaCl. Με σκοπό να ελεγχθεί η επίδραση του στροντίου και στα κρυσταλλικά σχηματιζόμενα στερεά, έγινε χημική ανάλυση των στερεών που κρυσταλλώθηκαν στα φύτρα κρυστάλλων OCP και HAP παρουσία στροντίου και τα αποτελέσματα συνοψίζονται στον πίνακα Πίνακας 7.10 Αποτελέσματα από τη χημική ανάλυση των στερεών που κρυσταλλώθηκαν στα φύτρα κρυστάλλων OCP και HAP παρουσία στροντίου. C Sr / 10-3 M (Ca/P) στερεό [(Ca+Sr)/P] στερεό (%Sr) στερεό Σχηματιζόμενο στερεό ΟCP ΟCP ΟCP ΟCP HAP HAP HAP HAP HAP 226
253 Όπως φαίνεται και από τα αποτελέσματα, δύναται να υπάρχει υποκατάσταση του ασβεστίου από το στρόντιο στη κρυσταλλική δομή των στερεών. Επιπλέον, το ποσοστό του στροντίου στο κρυσταλλικό πλέγμα του ΗΑΡ βρέθηκε ότι ήταν μεγαλύτερο από το αντίστοιχο στο πλέγμα του OCP, για την ίδια συγκέντρωση στροντίου στα υπέρκορα διαλύματα. Στο σχήμα 7.51 και 7.52 παρουσιάζεται το διάγραμμα του γραμμομοριακού λόγου στροντίου προς ασβέστιο στο σχηματιζόμενο στερεό, (Sr/Ca) στερεό, συναρτήσει του αντίστοιχου λόγου στο υπέρκορο διάλυμα, (Sr/Ca) διάλυμα, για την κρυστάλλωση του OCP και του ΗΑΡ, αντίστοιχα. 0,040 0,032 (Sr/Ca) στερεό 0,024 0,016 0,008 0,000 0,0 0,2 0,4 0,6 0,8 (Sr/Ca) διάλυμα Σχήμα 7.51: Διάγραμμα του γραμμομοριακού λόγου στροντίου προς ασβέστιο στο σχηματιζόμενο στερεό, (Sr/Ca) στερεό, συναρτήσει του αντίστοιχου λόγου στο διάλυμα εργασίας, (Sr/Ca) διάλυμα, για την κρυστάλλωση του OCP σε κρυσταλλικά φύτρα OCP, σε υδατικά διαλύματα παρουσία στροντίου σε συνθήκες σταθερού υπερκορεσμού και σε ph 7.40, θ = 37.0 ± 0.1 o C, ΝaCl 0.15Μ. 227
254 2,5x10-2 2,0x10-2 (Sr/Ca) στερεό 1,5x10-2 1,0x10-2 5,0x10-3 0,0 0,00 0,25 0,50 0,75 1,00 1,25 (Sr/Ca) διάλυμα 1,5x10-1 1,0x10-1 (Sr/Ca) στερεό 5,0x10-2 0,0 0,0 0,2 0,4 0,6 0,8 (Sr/Ca) διάλυμα Σχήμα 7.52: Διάγραμμα του γραμμομοριακού λόγου στροντίου προς ασβέστιο στο σχηματιζόμενο στερεό, (Sr/Ca) στερεό, συναρτήσει του αντίστοιχου λόγου στο διάλυμα εργασίας, (Sr/Ca) διάλυμα, για την κρυστάλλωση του ΗΑP σε κρυσταλλικά φύτρα ΗΑΡ, σε υδατικά διαλύματα παρουσία στροντίου σε συνθήκες σταθερού υπερκορεσμού και σε ph 7.40, θ = 37.0 ± 0.1 o C, ΝaCl 0.15 Μ: (α) σε χαμηλή τιμή υπερκορεσμού σ HAP = 6.35; (β) σε υψηλή τιμή υπερκορεσμού σ HAP =
255 Από τα διαγράμματα παρατηρήθηκε πως αυξανόμενου γραμμομοριακού λόγου στροντίου προς ασβέστιο στο υπέρκορο διάλυμα, (Sr/Ca) διάλυμα, σημειώθηκε αύξηση του αντίστοιχου λόγου στο σχηματιζόμενο στερεό. Στην περίπτωση του OCP αλλά και του ΗΑΡ για χαμηλή τιμή υπερκορεσμού, το διάγραμμα που φαίνεται η ενσωμάτωση του στροντίου στο κρυσταλλικό πλέγμα, παρουσίασε τάση σταθεροποίησης, ενώ στην περίπτωση της ενσωμάτωσης του στροντίου στον ΗΑΡ σε υψηλότερη τιμή υπερκορεσμού ήταν πιο έντονη (σχήμα 7.52 (β)). Αξίζει να σημειωθεί, πως στην περίπτωση αυτή και η μείωση του ρυθμού κρυστάλλωσης ήταν δραματική, όπως έχει ήδη αναφερθεί. Στο σχήμα 7.53 απεικονίζονται τα περιθλασιογράμματα των στερεών που σχηματίσθηκαν κατά την κρυστάλλωση OCP με σπορά κρυσταλλικών φύτρων OCP απουσία και παρουσία στροντίου. Από τη σύγκριση των περιθλασιογραμμάτων και μεγεθύνοντας γύρω από τις δύο χαρακτηριστικές ανακλάσεις (0 1 0) (4,73 ο σε 2θ) και (0 0 2) (26 ο σε 2θ) του OCP (σχήμα 7.53 (β), (γ)), παρατηρήθηκε μόνο για την (0 0 2) ανάκλαση, μετατόπιση των περιθλασιογραμμάτων παρουσία στροντίου προς μικρότερη γωνία 2θ (από 26 ο σε ο ). 229
256 ( 3 Intensity/a.u ( 3 Intensity/ a.u
257 002 ( 3 Intensity/ a.u ,8 25,6 26,4 27,2 2 Σχήμα 7.53: Περιθλασιογράμματα ακτίνων-χ (α) OCP που κρυσταλλώθηκε σε φύτρα κρυστάλλων OCP: 1 απουσία στροντίου; 2: παρουσία 0.5 mm C Sr ; 3: παρουσία 1.0 mm C Sr, και (β), (γ) μεγέθυνση των περιθλασιογραμμάτων στις χαρακτηριστικές ανακλάσεις (0 1 0) και (0 0 2), αντίστοιχα. Παρομοίως, η σύγκριση των περιθλασιογραμμάτων ακτίνων-χ των στερεών που κρυσταλλώθηκαν σε κρυσταλλικά φύτρα ΗΑΡ απουσία και παρουσία στροντίου (σχήμα 7.54), έδειξε πως υπάρχει μετατόπιση των περιθλασιογραμμάτων του ΗΑΡ που κρυσταλλώθηκε παρουσία στροντίου στην ανάκλαση (0 0 2) του ΗΑΡ προς μικρότερη γωνία 2θ (από 25.9 ο σε ο ). 231
258 002 3 Intensity/ a.u Intensity/ a.u Σχήμα 7.54: Περιθλασιογράμματα ακτίνων-χ (α) ΗΑP που κρυσταλλώθηκε σε φύτρα κρυστάλλων ΗΑP: 1 απουσία στροντίου; 2: παρουσία 0.5 mm C Sr ; 3: παρουσία 1.0 mm C Sr, και (β) μεγέθυνση των περιθλασιογραμμάτων στη χαρακτηριστική ανάκλαση (002). Η μετατόπιση αυτή υποδηλώνει αλλαγές των παραμέτρων της μοναδιαίας κυψελίδας του κρυσταλλικού πλέγματος των στερεών, αλλά και μείωση του μεγέθους των κρυστάλλων [Koutsoukos and Nancollas, 1981]. Αυτό συνάδει με τα αποτελέσματα 232
259 που προέκυψαν από τη χημική ανάλυση των καταβυθιζόμενων στερεών, τα οποία παρουσιάστηκαν παραπάνω, και με παρόμοιες μελέτες [Boanini et al., 2010]. Στο σχήμα 7.55 που ακολουθεί, παρουσιάζονται φωτογραφίες από το ηλεκτρονικό μικροσκόπιο σάρωσης, στις οποίες απεικονίζεται η μορφολογία των καταβυθιζόμενων κρυστάλλων OCP με σπορά κρυσταλλικών φύτρων OCP σε συνθήκες σταθερού υπερκορεσμού, απουσία και παρουσία στροντίου. Απουσία στροντίου παρατηρήθηκαν οι συνήθεις φυλλόμορφοι κρύσταλλοι OCP μεγέθους περίπου 2 μm, ενώ παρουσία στροντίου συγκέντρωσης 1 mμ, οι σχηματιζόμενοι φυλλόμορφοι κρύσταλλοι OCP ήταν μικρότερου μεγέθους. Σχήμα 7.55: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης OCP σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων OCP; (α) απουσία στροντίου, (β) παρουσία 1 mm [Sr 2+ ]; ph 7.40, 37 C, 0.15 M NaCl, σ OCP = 0.90 & σ HAP = Η μορφολογική εξέταση του σχηματιζόμενου στερεού από την κρυστάλλωση του ΗΑΡ σε κρυσταλλικά φύτρα ΗΑΡ απουσία στροντίου, έδειξε πρισματικούς κρυστάλλους ΗΑΡ μεγέθους nm (σχήμα 7.56 (α)). Η διαφοροποίηση στη μορφολογία των καταβυθιζόμενων κρυστάλλων ΗΑΡ παρουσία στροντίου συγκέντρωσης 1 mμ ήταν έντονη, αφού όπως φαίνεται και στο σχήμα 7.56 (β), παρατηρήθηκαν απατιτικοί μη πρισματικοί μικροκρυσταλλίτες μεγέθους nm. 233
260 Σχήμα 7.56: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης ΗΑΡ σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων ΗΑΡ; (α) απουσία στροντίου, (β) παρουσία 1 mm [Sr 2+ ]; ph 7.40, 37 C, 0.15 M NaCl, σ HAP = 6.35 & σ OCP = Κατά την κρυστάλλωση HAP με σπορά κρυσταλλικών φύτρων HAP σε υψηλότερη τιμή σχετικού υπερκορεσμού και απουσία στροντίου, εναποτέθηκαν εκτός των πρισματικών απατιτικών κρυστάλλων μεγέθους nm και φυλλόμορφοι κρύσταλλοι OCP μεγέθους περίπου 0.5 μm (σχήμα 7.57). Παρουσία στροντίου η μορφολογία και το μέγεθος των σχηματιζόμενων κρυστάλλων OCP δεν άλλαξαν δραματικά, ενώ οι σχηματιζόμενοι κρύσταλλοι του ΗΑΡ είχαν και πάλι διαφορετική μορφολογία και μέγεθος (σχήμα 7.57 (β)). 234
261 Σχήμα 7.57: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλωσης υδροξυαπατίτη (ΗΑΡ) σε συνθήκες σταθερού υπερκορεσμού σε φύτρα κρυστάλλων ΗΑΡ; (α) απουσία στροντίου, (β) παρουσία 1 mm [Sr 2+ ]; ph 7.40, 37 C, 0.15 M NaCl, σ HAP = 9.94 & σ OCP = Η παρουσία των ιόντων στροντίου (Sr 2+ ) εκτός από τις αλλαγές που προκάλεσε στο μέγεθος και τη μορφολογία των σχηματιζόμενων κρυστάλλων, είχε ως αποτέλεσμα την επιβράδυνση της υδρολυτικής μετατροπής του θερμοδυναμικά ασταθέστερου OCP προς τον θερμοδυναμικά σταθερό HAP και πιθανόν και τη σταθεροποίησή του, υποδηλώνοντας την επιβράδυνση ή παρεμπόδιση της μετατροπής του OCP προς ΗΑΡ. Τα αποτελέσματα αυτά, βρίσκονται αντίθεση σε αναφορά στην βιβλιογραφία στην οποία παρουσιάσθηκε μελέτη της επίδρασης ξένων ιόντων, μεταξύ αυτών και του στροντίου, σε OCP και HAP σε συνθήκες μεταβαλλόμενου ph. Στην αναφορά αυτή δεν διαπιστώθηκε κανενός είδους επίδραση της παρουσίας των ιόντων κατά την υδρόλυση του OCP προς απατιτικό στερεό [Bigi et al., 1988]. Η διαφωνία αυτή, κατά πάσα πιθανότητα οφείλεται στο γεγονός ότι κατά την μελέτη αυτή, η μεταβολή του υπερκορεσμού κατά την διάρκεια της κρυσταλλικής ανάπτυξης ήταν σημαντική. Κατά την κρυσταλλική ανάπτυξη, όμως μεταβολές του υπερκορεσμού του διαλύματος, επιταχύνει την υδρόλυση των ασταθών κρυσταλλικών φάσεων που σχηματίζονται αρχικά, προς θερμοδυναμικά σταθερότερες [Spanos and Koutsoukos, 1998(b)]. Το γεγονός ότι η επίδραση των ιόντων στροντίου στην κρυσταλλική ανάπτυξη αλάτων φωσφορικού ασβεστίου μελετήθηκε με τη μέθοδο του σταθερού υπερκορεσμού, έδωσε μια ακριβή εικόνα του ρόλου που έχει το στρόντιο στην κρυσταλλική ανάπτυξη του OCP. 235
262 ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟΥ 7 Alkhraisat M.H., Rueda C. and Cabarcos E.L., Strontium Ions Substitution in Brushite Crystals: The Role of Strontium Chloride, J. Funct. Biomater., 2, pp , (2011) Ammann P., Shen V., Robin B., Mauras Y., Bonjour J.P., Rizzoli R., Strontium ranelate improves bone resistance by increasing bone mass and improving architecture in intact female rats, Journal of Bone and Mineral Research, 19, pp , (2004) Amjad Z., Koutsoukos P.G. and Nancollas G.H., The crystallization of hydroxyapatite and fluorapatite in the presence of magnesium ions, J Colloid Interface Sci, 101, pp , (1984) Anada T., Kumagai T., Honda Y., Masuda T., Kamijo R., Kamakura S., Yoshihara N., Koriyagama T., Shimauchi H., and Suzuki O., Dose-Dependent Osteogenic Effect of Octacalcium Phosphate on Mouse Bone Marrow Stromal Cells, Tissue Eng. Part A, 14, pp , (2008) Arends J., Christoffersen J., Christoffersen M.R., Eckert H., Fowler B.O, Heughebaert J.C., Nancollas G.H., Yesinowski J.P., Zawacki S.J., A calcium hydroxyapatite precipitated from an aqueous solution: An international multimethod analysis, Journal of Crystal Growth, 84, pp , (1987) Ashok M., Sundaram N.M., Narayana Kalkura S.N., Crystallization of hydroxyapatite at physiological temperature, Materials Letters, 57, pp , (2003) Ban S., Jinde T., and Hasegawa J., Phase Transformation of Octacalcium Phosphate in vivo and in vitro, Dent. Mater. J., 11, pp , (1992) Barrere F., Layrolle P., van Blitterswijk C.A., de Groot K., Biomimetic Calcium Phosphate Coatings on Ti6Al4V: A Crystal Growth Study of Octacalcium Phosphate and Inhibition by Mg 2+ and HCO 3 -, Bone, 25, pp , (1999) 236
263 Barrere F., van der Valk C.M., Dalmeijer R.A.J., Meijer G., van Blitterswijk C.A., de Groot K., and Layrolle P., Osteogenecity of Octacalcium Phosphate Coatings Applied on Porous Metal Implants, J. Biomed. Mater. Res. Part A, 66, pp , (2003) Bermudez O., Boltong M.G., Driessens F.C.M. and Planell J.A., Development of an Octacalcium Phosphate Cement, J. Mater. Sci. Mater. Med., 5, pp , (1994) Bigi A., Boanini E., Botter R., Panzavolta S. and Rubini K., α-tricalcium phosphate hydrolysis to octacalcium phosphate: effect of sodium polyacrylate, Biomaterials, 23, pp , (2002) Bigi A., Gazzano M., Ripamonti A., Roveri N., Effect of foreign ions on the conversion of brushite and octacalcium phosphate into hydroxyapatite, Journal of Inorganic Biochemistry, 32, pp , (1988) Boanini E., Gazzano M., Rubini K. and Bigi A., Collapsed Octacalcium Phosphate Stabilized by Ionic Substitutions, Crystal Growth & Design, 10, pp , (2010) Bracci B., Torricelli P., Panzavolta S., Boanini E., Giardino R., Bigi A., Εffect of Mg 2+, Sr 2+, and Mn 2+ on the chemico-physical and in vitro biological properties of calcium phosphate biomimetic coatings, Journal of Inorganic Biochemistry, 103, pp , (2009) Braye F., Irigaray J.L., Jallot E., Oudadesse H., Weber G., Deschamps N., Deschamps C., Frayssinet P., Tourenne P., Tixier H., Terver S., Lefaivre J., Amirabaldi A., Resorption kinetics of osseous substitute: natural coral and synthetic hydroxyapatite, Biomaterials, 17, pp , (1996) Brown W.E., Eidelman N. and Tomazic B., Octacalcium Phosphate as a Precursor in Biomineral Formation, Adv. Dent. Res., 1, pp , (1987) Campbell Α.Α, LoRe Μ. and Nancollas G.H., The influence of carbonate and magnesium ions on the growth of hydroxyapatite, carbonated apatite and human powdered enamel, Colloids and Surfaces, 54, pp , (1991) 237
264 Canalis E., Hott M., Deloffre P., Tsouderos Y., Marie, P.J., The divalent strontium salts enhances bone cell replication and bone formation in vitro, Bone, 18, pp , (1996) Christoffersen J., Christoffersen M.R., Kolthoff N., Bärenholdt O., Effects of strontium ions on growth and dissolution of hydroxyapatite and on bone mineral detection, Bone, 20, pp , (1997) Combes C., Bareille R., Rey C., Calcium carbonate calcium phosphate mixed cement compositions for bone reconstruction, J Biomed Mater Res 79A, pp , (2006) Combes C., Miao B., Bareille R., Rey C., Preparation, physical chemical characterisation and cytocompatibility of calcium carbonate cements, Biomaterials, 27, pp , (2006) Dorozhkina Ε.Ι and Dorozhkin S.V., Surface mineralisation of hydroxyapatite in modified simulated body fluid (m-sbf) with higher amounts of hydrogencarbonate ions, Colloids and Surfaces A: Physicochemical and Engineering Aspects, 210, pp , (2002) Dorozhkin S.V., Calcium Orthophosphate Cements for Biomedical Application, J. Mater. Sci., 43, pp , (2008) Dorozhkin S.V., Calcium Orthophosphates as Bioceramics: State of the Art, J. Funct. Biomater., 1, pp , (2010) Fetter A.W., Structure and function of bone, in Textbook of Orthopaedics, Newton C.D. and Nunamaker D.M (eds.), J.B. Lippincott Co: Philadelphia, (1985) Fowler B.O., Infrared studies of apatites. I. Vibrational assignments for calcium, strontium, and barium hydroxyapatites utilizing isotopic substitution, Inorg. Chem., 13, pp , (1974) 238
265 Fowler B.O., Markovic J.M. and Brown W.E., Octacalcium Phosphate: Infrared and Raman Vibrational Spectra, Chem. Mater., 5, pp , (1993) Fowler B.O., Moreno E.C. and Brown W.E., Infra-red spectra of hydroxyapatite, octacalcium phosphate and pyrolysed octacalcium phosphate, Arch. Oral Bid., 11, pp , (1966) Guillemin G., Patat J.L., Meunier A., Natural corals used as bone graft substitutes, Bulletin de l'institut Océanographique de Monaco, 14, pp , (1995) Gunnars A., Blomqvist S., Martinsson C., Inorganic formation of apatite in brackish seawater from the Baltic Sea: An experimental approach, Marine Chemistry, 91, pp , (2004) Heise U., Osborn J.F., Duwe F., Hydroxyapatite ceramic as a bone substitute, Int Orthop, 14, pp , (1990) Heughebaert J.C., Nancollas G.H., Kinetics of crystallization of octacalcium phosphate, J. Phys. Chem., 88, pp , (1984) Heughebaert J.C., Zawacki S.J., Nancollas G.H., The growth of octacalcium phosphate on beta tricalcium phosphate, J. Crystal Growth, 63, pp , (1983) Imaizumi H., Sakurai M., Kashimoto O., Kikawa T., and Suzuki O., Comparative Study on Osteoconductivity by Synthetic Octacalcium Phosphate and Sintered Hydroxyapatite in Rabbit Bone Marrow, Calcif. Tissue Int. 78, pp , (2006) Joschek S., Nies B., Krotz R. and Gopferich A., Chemical and physicochemical characterization of porous hydroxyapatite ceramics made of natural bone, Biomaterials, 21, pp , (2000) Kapolos J., Koutsoukos P.G., Formation of Calcium Phosphates in Aqueous Solutions in the Presence of Carbonate Ions, Langmuir, 15, pp , (1999) 239
266 Khan S.N. MD, Cammisa F.P. MD, Sandhu H.S. MD, Diwan A.D. MD, Girardi F.P. MD, Lane J.M. MD, The Biology of Bone Grafting, J Am Acad Orthop Surg, 13, pp , (2005) Kim S., Park C.B., Mussel-inspired transformation of CaCO 3 to bone minerals, Biomaterials, 31, pp , (2010) Komath Μ., Varma Η., Sivakumar R., On the development of an apatitic calcium phosphate bone cement, Bulletin of Materials Science, 23, pp , (2000) Koutsoukos P.G., Amjad Z., Tomson M.B., Nancollas G.H., Crystallization of calcium phosphates. A constant composition study, J. Am. Chem. Soc., 102, pp , (1980) Koutsoukos P.G., Nancollas G.H., Influence of strontium ion on the crystallization of hydroxyapatite from aqueous solution, Journal of Physical Chemistry, 85, pp , (1981) Landi E., Tampieri A., Celotti G., Sprio S., Sandri M., Logroscino G., Sr-substituted hydroxyapatites for osteoporotic bone replacement, Acta Biomaterialia, 3, pp , (2007) LeGeros RZ., Biodegradation and bioresorption of calcium phosphate ceramics, Clin. Mater., 14, pp , (1993) LeGeros R.Z, Biological and synthetic apatites, in Hydroxyapatite and Related Materials, Brown P.W. and Constanz B. (eds.), CRC Press: Roca-Batton, (1994) LeGeros R.Z., Calcium Phosphates in Oral Biology and Medicine, Monographs in Oral Sciences, 15, Myers H. (ed), Karger: Basel, (1991) 240
267 LeGeros R.Z., Preparation of Octacalcium Phosphate (OCP): A Direct Fast Method, Calcif Tissue Int, 37, pp , (1985) LeGeros R.Z., Properties of osteoconductive biomaterials: calcium phosphates, Clin Orthop Relat Res, 395, pp , (2002) Leroux L. and Lacout J.L., Preparation of calcium strontium hydroxyapatites by a new route involving calcium phosphate cements, J. Mater. Res., 16, pp , (2001) Lonsdale K., Epitaxy as a growth factor in urinary calculi and gallstones, Nature, 217, pp , (1968) Lowenstam H. and Weiner S., Biomineralization, Oxford Univ. Press: New York, (1989) Mann S., Biomineralization, VCH: New York, (1989) Marie P.J., Strontium ranelate: a novel mode of action optimizing bone formation and resorption, Bone, 38, pp , (2006) Markovic M. and Chow L.C., An Octacalcium Phosphate Forming Cement, J. Res. Natl. Inst. Stand. Technol., 115, pp , (2010) Matsumoto N., Yoshida K., Hashimoto K., Toda Y., Dissolution mechanisms of β- tricalcium phosphate doped with monovalent ions, Journal of the Ceramic Society of Japan, 118, pp , (2010) Matsunaga K., Murata H., Strontium substitution in bioactive calcium phosphates: A first-principles study, Journal of Physical Chemistry B, 113, pp , (2009) McCaslin F.E.Jr., Janes J.M., The effect of strontium lactate in the treatment of osteoporosis, Proceedings of the Staff Meetings of the Mayo Clinic, 34, pp , (1959) 241
268 Meunier P.J., Roux C., Seeman E., Ortolani S., Badurski J.E., Spector T.D., The effects of strontium ranelate on the risk of vertebral fracture in women with postmenopausal osteoporosis, New England Journal of Medicine, 350, pp , (2004) Murugan R., Ramakrishna S., Panduranga Rao K., Nanoporous hydroxy-carbonate apatite scaffold made of natural bone, Materials Letters, 60, pp , (2006) Nancollas G.H., Biological Mineralization and Demineralization, Springer-Verlag: Heidelberg, (1982) Nancollas G.H., In Biomineralization, Mann S., Webb J., Williams R.T.P. (eds.), VCH: Weinheim, pp , (1989) Nancollas G.H. and Koutsoukos P.G., Calcium phosphate nucleation and growth in solution. Prog. Crystal Growth Charact., 3, pp , (1980) Nancollas G.H. and Mohan M.S., The growth of hydroxyapatite crystals, Arch. Oral Biol., 15, , (1970) Nelson D.G. and Featherstone J.D., Preparation, analysis, and characterization of carbonated apatites, Calcif Tissue Int, 34, pp , (1982) Neuman W.F., Bjornerstedt R., Mulrvan B.J., Synthetic hydroxyapatite crystals. II. Aging and strontium incorporation, Archives of Biochemistry and Biophysics, 101, pp , (1963) Nielsen A.E. and Toft J.M., Electrolyte crystal growth kinetics, J. Crystal Growth, 67, pp , (1964) Oniyama E., Wahlbeck P.G., Application of transpiration theory to TGA data: Calcium carbonate and zinc chloride, Thermochimica Acta, 250, pp , (1995) 242
269 Prien E. and Frondel C., Studies in Urolithiasis: Composition of Urinary Calculi, J. Urology, 57, pp , (1947) Reddy M.M. and Nancollas G.H., The Crystallization of Calcium Carbonate Part I. Isotopic Exchange and Kinetics, J. Colloid Interface Sci., 36, pp , (1971) Reginster J.Y., Seeman E., De Vernejoul M.C., Adami S., Compston J., Phenekos C., Devogelaer J.P., Curiel M.D., Sawicki A., Goemaere S., Sorensen O.H., Felsenberg D., Meunier P.J., Strontium ranelate reduces the risk of nonvertebral fractures in postmenopausal women with osteoporosis: Treatment of Peripheral Osteoporosis study, J Clin Endocrinol Metab, 90, pp , (2005) Rey C., Shimizu M., Collins B., Glimcher M.J., Resolution-enhanced fourier transform infrared spectroscopy study of the environment of phosphate ions in the early deposits of a solid phase of calcium-phosphate in bone and enamel, and their evolution with age. I: Investigations in the v 4 PO 4 domain, Calcif Tiss Int, 46, pp , (1990) Saint-Jean S.J., Camire C.L., Nevsten P., Hansen S., Ginebra M.P., Study of the reactivity and in vitro bioactivity of Sr-substituted alpha-tcp cements, Journal of Materials Science: Materials in Medicine, 16, pp , (2005) Salimi Μ.Η, Heughebaert J.C. and Nancollas G.H., Crystal Growth of Calcium Phosphates in the Presence of Magnesium Ions, Langmuir, 1, pp , (1985) Shibata Υ., Yamamoto Η. and Miyazaki Τ., Colloidal b-tricalcium Phosphate Prepared by Discharge in a Modified Body Fluid Facilitates Synthesis of Collagen Composites, J Dent Res, 84, pp , (2005) 243
270 Souyris F., Pellequer C., Payrot C., Servera C., Coral: A new biomedical material. Experimental and first clinical investigations on Madreporaria, J. Maxillofac. Surg., 13, pp , (1985) Spanos N. and Koutsoukos P.G., Kinetics of precipitation of calcium carbonate in alkaline ph at constant supersaturation. Spontaneous and Seeded Growth., J. Phys. Chem. B, 102, pp , (1998 (a)) Spanos N. and Koutsoukos P.G., The transformation of vaterite to calcite: effect of the conditions of the solutions in contact with the mineral phase, Journal of Crystal Growth, 191, pp , (1998 (b)) Spanos N., Misirlis D.Y., Kanellopoulou D.G., Koutsoukos P.G., Seeded growth of hydroxyapatite in simulated body fluid, J Mater Sci, 41, pp , (2006) Sugihara F., Onishi H., Kushitani S., Iwaki N., Mandai K., Minamigawa K., Tshuji E., Yoshikawa M., Toda T., Bone Tissue Reaction of Octacalcium Phosphate, in Bioceramics, Wilson J., Hench L.L. and D. Greenspan (eds.), Pergamon Press: Oxford, England, (1995) Suzuki Ο., Kamakura S., Katagiri T., Nakamura M., Zhao B., Honda Y., Kamijo R., Bone Formation Enhanced by Implanted Octacalcium Phosphate Involving Conversion into Ca-deficient Hydroxyapatite, Biomaterials, 27, pp , (2006) Suzuki O., Nakamura M., Miyasaka Y., Kagayama M., and Sakurai M., Bone Formation on Synthetic Precursors of Hydroxyapatite, Tohoku J. Exp. Med., 164, pp , (1991) Tiwari R., Special Report/ Instrumentation: Thermal Techniques for Material Characterization, in Ceramic Industry, (2008) Turnbull D. and Vonnegut B., Nucleation Catalysis, Industrial and Engineering Chemistry, 44, pp , (1952) 244
271 Vagenas N.V., Gatsouli A., Kontoyannis C.G., Quantitative analysis of synthetic calcium carbonate polymorphs using FT-IR spectroscopy, Talanta, 59, pp , (2003) Weiner S. and Wagner H.D., The material bone: Structure-Mechanical Function Relations, Annual Review Material Science, 28, pp , (1998) Wu W., Nancollas G.H., Crystal growth of octacalcium phosphate on titanium oxide surfaces, Langmuir, 13, pp , (1997) Xin R., Leng Y. and Wang N., In situ TEM examinations of octacalcium phosphate to hydroxyapatite transformation, Journal of Crystal Growth, 289, pp , (2006) Xu G., Aksay I.A. and Groves J.T., Continuous Crystalline Carbonate Apatite Thin Films. A Biomimetic Approach, J. Am. Chem. Soc., 123, pp , (2001) Zhagn M.X., Huo J.C., Yu Y.S., Cui C.P., Lei Y.L., Morphology Control of SrCO3 Crystals using Complexons as Modifiers in the Ethanol-water mixtures, Chinese J. Struct. Chem., 27, pp , (2008) Κατσαμένης Ορ. Σύνθεση και χαρακτηρισμός οστεϊκών τσιμέντων φωσφορικού ασβεστίου, Διπλωματική Εργασία, Τμήμα Επιστήμης Υλικών, Πανεπιστήμιο Πατρών, (2006) 245
272 246
273 ΚΕΦΑΛΑΙΟ 8 ΜΕΛΕΤΗ ΤΗΣ ΚΙΝΗΤΙΚΗΣ ΤΗΣ ΔΙΑΛΥΣΗΣ ΑΣΒΕΣΤΟΥΧΩΝ ΕΝΑΠΟΘΕΣΕΩΝ ΑΠΟ ΦΥΣΙΚΕΣ ΒΑΛΒΙΔΕΣ ΚΑΡΔΙΑΣ 247
274 8.1 ΕΙΣΑΓΩΓΗ Στην παρούσα εργασία έγινε μελέτη της κινητικής της διάλυσης των εναποθέσεων φωσφορικού ασβεστίου που απομονώθηκαν από τις ασβεστοποιημένες φυσικές βαλβίδες ασθενών σε ακόρεστα διαλύματα με τη μέθοδο σταθερής σύστασης. Επιπλέον, για τη μελέτη της κινητικής της διάλυσης χρησιμοποιήθηκαν συνθετικοί κρύσταλλοι υδροξυαπατίτη (HAP), ως υλικό αναφοράς. Τα πειράματα πραγματοποιήθηκαν στους 37 o C, σε ιοντική ισχύ 0.15Μ NaCl, σε ph 7.4 ± 0.1 και σε συνθήκες σταθερής ακορεστότητας. 8.2 ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΤΑΞΗ ΚΑΙ ΔΙΑΔΙΚΑΣΙΑ Τα πειράματα διάλυσης σε συνθήκες σταθερής ακορεστότητας, έγιναν στην ίδια πειραματική διάταξη στην οποία πραγματοποιήθηκαν και τα πειράματα κρυστάλλωσης φωσφορικού ασβεστίου (σχήμα 7.9). Για την παρασκευή των ακόρεστων διαλυμάτων χρησιμοποιήθηκαν πυκνά πρότυπα διαλύματα ασβεστίου, CaCl 2 2H 2 O, και φωσφορικών, ΚH 2 PO 4, συγκέντρωσης 0.01 Μ. Τα διαλύματα τιτλοδότησης για την διατήρηση σταθερού κορεσμού στα διαλύματα (titrants) παρασκευάζονταν από τα πρότυπα διαλύματα ασβεστίου (0.01Μ CaCl 2 2H 2 O), φωσφορικών (0.01Μ KΗ 2 PO 4 ), χλωριούχου νατρίου (1Μ NaCl) και υδροχλωρικού οξέος (0.01Ν HCl) με τις απαραίτητες αραιώσεις με τριπλά απεσταγμένο νερό. Χρησιμοποιήθηκαν δύο διαλύματα τα οποία περιείχοντο στις αντίστοιχες σύριγγες του τροποποιημένου αυτόματου τιτλοδότη. Η πρώτη σύριγγα περιείχε το διάλυμα του CaCl 2 2H 2 O και το διάλυμα του αδρανούς ηλεκτρολύτη NaCl, ενώ η δεύτερη το διάλυμα του KΗ 2 PO 4 και το διάλυμα του HCl. Ο υπολογισμός των συγκεντρώσεων των διαλυμάτων που προσετίθεντο κατά την διάρκεια της ήταν σημαντικός για τη σωστή διεξαγωγή των πειραμάτων της διάλυσης με τη μέθοδο της σταθερής σύστασης. Η προσθήκη των τιτλοδοτικών διαλυμάτων με την στοιχειομετρική αναλογία του στερεού που διαλύεται έχει ως στόχο τη συνεχή αραίωση του διαλύματος εργασίας έτσι ώστε να αντισταθμίζεται η αύξηση της συγκέντρωσης των ιόντων που προκαλείτο λόγω διάλυσης του στερεού και τη διατήρηση σταθερής ιοντικής ισχύος (σταθεροί συντελεστές ενεργότητας όλων των ιόντων). Οι συγκεντρώσεις των τιτλοδοτικών διαλυμάτων προέκυψαν από ισοζύγια μάζας για κάθε ιόν που συμμετέχει στην αντίδραση ως ακολούθως: Το υδατικό ακόρεστο διάλυμα εργασίας περιείχε διαλύματα CaCl 2 2H 2 O, KΗ 2 PO 4, NaCl, ΝaΟΗ και HCl, και Ca ws, P ws, NaCl ws, ΝaΟΗ ws και HCl ws ήσαν οι 248
275 αντίστοιχες συγκεντρώσεις. Το πρώτο τιτλοδοτικό διάλυμα (Τ Α ) περιλάμβανε διαλύματα CaCl 2 2H 2 O και NaCl, των οποίων οι συγκεντρώσεις ήσαν TA Ca T NaCl A αντίστοιχα, ενώ το δεύτερο τιτλοδοτικό διάλυμα (Τ Β ) περιείχε ΚΗ 2 PO 4 και ΗCl, με συγκεντρώσεις TB TB P και και HCl αντιστοίχως, έτσι ώστε να διατηρούνται οι ενεργότητες όλων των πλεγματικών ιόντων στο ακόρεστο διάλυμα σταθερές. Αν υποτεθεί ότι διαλύονται m Ca moles ιόντων ασβεστίου σε τελικό όγκο υπέρκορου διαλύματος V και dv ο στοιχειώδης όγκος του διαλύματος τιτλοδότησης ο οποίος προστίθεται από κάθε σύριγγα έτσι ώστε να διατηρηθεί η ενεργότητα των ιόντων Ca 2+ σταθερή, από το ακόλουθο ισοζύγιο μάζας, υπολογίζεται η συγκέντρωση του ασβεστίου στο διάλυμα τιτλοδότησης, TA Ca : Ca ws ws ws T A T A T B T B Ca V Ca dv Ca dv mca ws T A T B V dv dv T A T B T A T A T B T B Ca ws ( V ws dv dv ) Ca ws V ws Ca dv Ca dv m Ca TA TB T dv =dv =dv και Ca B=0 ws ws ws ws T A Ca ( V 2 dv ) Ca V Ca dv m Ca T A ws T A ws mca Ca dv 2Ca dv mca Ca 2Ca dv T A ws Ca 2Ca m όπου, mca dv m είναι ένα μέτρο της ποσότητας του στερεού που διαλύεται ανά μονάδα όγκου του διαλύματος. Η παράμετρος αυτή καθορίζεται εμπειρικά, μέσω μιας σειράς προκαταρκτικών πειραμάτων και εκφράζει πόσο πιο αραιά πρέπει να είναι τα διαλύματα τιτλοδότησης για να αντισταθμίζεται η αύξηση της συγκέντρωσης στο διάλυμα εργασίας. Ομοίως, για να διατηρηθεί η ενεργότητα των φωσφορικών ιόντων PO 4 3- σταθερή, από το ακόλουθο ισοζύγιο μάζας, προσδιορίζεται η συγκέντρωση των φωσφορικών στο διάλυμα τιτλοδότησης, TB P : 249
276 P ws ws ws T A T A T B T B P V P dv P dv mp ws T A T B V dv dv TA TB T dv =dv =dv και P A =0 T A T B T A T A T B T B P ws ( V ws dv dv ) P ws V ws P dv P dv m P ws ws ws ws T B P ( V 2 dv) P V P dv m P T B ws T B ws mp P dv 2P dv mp P 2P dv P T B ws 2P n Με όμοιο τρόπο από το ισοζύγιο μάζας για τα ιόντα νατρίου Να + και καλίου Κ + έχουμε: ws ws A T A ws T T B T B Na K V Na K dv Na K dv mnak ws T A T B Na K V dv dv ws ws ws T A T ws T B A T A Na K V dv dv Na K V Na K dv T T B A B B dv = dv = dv και m Na+K = 0 2 T T ws ws ws ws NaK Na K dv m Na K V dv Na K V T A B ws Na K dv Na K 2 2 T ws ws ws ws dv Na K V Na K dv Na K V T A T B ws T A T B NaK dv NaK dv NaK dv NaK dv NaK dv 2 NaCl NaOH KH PO NaCl KH PO ws ws ws T A T B NaCl 2NaOH 2KH PO NaCl KH PO ws ws ws T A T B ws ws Τ Τ ws KH2PO 4 = P και KH2PO Β Β 4 = P = 2P -n T A 2NaCl ws 2NaOH ws 2P ws NaCl 2P ws n T A ws ws NaCl 2NaCl 2NaOH n Παρόμοια από το ισοζύγιο μάζας για τα ιόντα Cl - έχουμε: 250
277 Cl ws ws ws T A T A T B T B Cl V Cl dv Cl dv mcl ws T A T B V dv dv dv TA =dv TB =dv και m Cl =0 T A T B T A T A T B T B Cl ws ( V ws dv dv ) Cl ws V ws Cl dv Cl dv m Cl T A T B T A T B Cl ws ( V ws 2 dv ) Cl ws V ws Cl dv Cl dv Cl ws 2dV Cl dv Cl dv ws T A T B ws ws ws TA TA TB CaCl2 NaCl HCl CaCl2 NaCl HCl T TA T T Ca A = Cl A A CaCl και NaCl = Cl 2 NaCl 2Cl Cl Cl 2 2 Cl Cl Cl 2 Cl Cl Cl 4Cl 2Cl 2Cl 2 Ca NaCl HCl ws ws ws CaCl2 NaCl HCl T A TA TB T A ws T ws ws Ca =2Ca - m και NaCl A =2NaCl 2NaOH n ws ws ws ws ws ws TB 4 ClCaCl 2 Cl NaCl ClHCl Ca m NaCl NaOH n HCl ws ws ws ws ws ws TB 4Ca 2NaCl 2HCl 4Ca 2m 2NaCl 2NaOH n HCl n TB ws ws HCl 2 HCl 2 NaOH 2 m Συγκεντρωτικά, λοιπόν, οι συγκεντρώσεις όλων των ειδών που πρέπει να περιέχονται στα τιτλοδοτικά διαλύματα, έτσι ώστε να διατηρείται σταθερή η ακορεστότητα στο διάλυμα εργασίας έχουν ως εξής: TA ws Ca 2 Ca m (8-1) PO 2 PO n (8-2) TB ws 4 4 NaCl TA ws ws 2NaCl 2 NaOH +n (8-3) TB ws ws HCl 2HCl 2NaOH 2m - n (8-4) 3 όπου για την διάλυση υδροξυαπατίτη (ΗΑP) ισχύει: Ca5PO4 OH n m 3 5 Για τον προσδιορισμό της τιμής m έγιναν προκαταρκτικά πειράματα, με δοκιμή και σφάλμα έτσι ώστε να διατηρείται το ph και η χημική σύσταση του διαλύματος σταθερή στην διάρκεια της διάλυσης. Από τα προκαταρκτικά πειράματα προσδιορίστηκε ότι για τη διάλυση ΗΑP: m =1 Ca ws Ceff, όπου eff C η συγκέντρωση αποτελεσματικότητας που αποτελεί μέτρο της ποσότητας του στερεού που διαλύεται. 251
278 Έτσι, οι συγκεντρώσεις των τιτλοδοτικών διαλυμάτων που χρησιμοποιήθηκαν για τη μελέτη της κινητικής της διάλυσης του ΗΑΡ σε σταθερή ακορεστότητα είχαν ως εξής: TA ws Ca 2 Ca C (8-1α) eff T 3 B ws PO4 2 PO4 Ceff 5 ( 8-2α) T 3 A ws ws NaCl 2NaCl 2 NaOH Ceff 5 (8-3α) T 7 B ws ws HCl 2HCl 2 NaOH Ceff 5 (8-4α) C ws 1 Ca eff Στον αντιδραστήρα, τα ακόρεστα διαλύματα παρασκευάζονταν με προσθήκη κατάλληλης ποσότητας τριπλά απεσταγμένου νερού έτσι ώστε με την προσθήκη όλων των αντιδρώντων ο τελικός όγκος του διαλύματος εργασίας να είναι 0.2L. Επίσης, προσετίθεντο κατάλληλες συγκεντρώσεις αδρανούς ηλεκτρολύτη ΝaCl και διαλύματος φωσφορικών KH 2 PO 4. Στη συνέχεια εισαγόταν στο διάλυμα προζυγισμένη ποσότητα των κρυσταλλικών φύτρων των οποίων μελετήθηκε η διάλυση. Το διάλυμα αναδευόταν και διοχετευόταν άζωτο κορεσμένο σε υδρατμούς. Στην περίπτωση των εναποθέσεων φωσφορικού ασβεστίου που απομονώθηκαν από τις ασβεστοποιημένες φυσικές βαλβίδες, η διοχέτευση του αζώτου γινόταν πάνω από το διάλυμα εργασίας με σκοπό την αποφυγή εισόδου του διοξειδίου του άνθρακα από την ατμόσφαιρα. Έπειτα ρυθμιζόταν το ph του διαλύματος εργασίας στην επιθυμητή τιμή με προσθήκη κατάλληλης ποσότητας βάσης ή οξέος ΝαΟΗ ή HCl 0.01Ν. Τέλος, ακολουθούσε η προσθήκη της απαιτούμενης ποσότητας του διαλύματος CaCl. 2 2H 2 O, σηματοδοτώντας την έναρξη της διεργασίας της διάλυσης. Κατά τη διάλυση του στερεού, σύμφωνα με την αντίδραση (8-5), το ph αυξανόταν, καθώς, δεσμεύονταν πρωτόνια από το διάλυμα: Ca 5 (PO 4 ) 3 ΟΗ (s) + 4Η + 5Ca ΗPO Η 2 Ο (8-5) Αύξηση της τιμής του ph μεγαλύτερη από μονάδες, οδηγούσε στην έναρξη των προσθηκών των διαλυμάτων τιτλοδότησης με στοιχειομετρική αναλογία του στερεού που διαλύεται, δηλαδή του ΗΑΡ. Σε τακτά χρονικά διαστήματα, συλλέγονταν δείγματα από το διάλυμα εργασίας με συχνότητα ανάλογη με τον ρυθμό της διάλυσης, έτσι ώστε ο όγκος του διαλύματος 252
279 εργασίας να παραμένει όσο το δυνατό σταθερός. Τα δείγματα διηθούνταν από ηθμούς μεμβράνης 0.2μm (Millipore) και αναλύονταν για ασβέστιο με φασματοσκοπία ατομικής απορρόφησης και για φωσφορικά φασματοφωτομετρικά με την μέθοδο των βαναδομολυβδαινικών. Τα πειράματα διαρκούσαν τόσο ώστε να επιτευχθεί όσο το δυνατόν υψηλότερο ποσοστό διάλυσης του ΗΑΡ στα δύο υποστρώματα. Μετά το πέρας του πειράματος, τα κρυσταλλικά φύτρα ξεπλένονταν με τριπλά απεσταγμένο νερό για την απομάκρυνση ποσότητας χλωριούχου νατρίου και ακολουθούσε η μορφολογική τους εξέταση με ηλεκτρονική μικροσκοπία σάρωσης (SEM). 8.3 ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΗΤΗΣΗ Το ποσοστό διάλυσης του ΗΑΡ σε σύγκριση με την αρχική ποσότητα των κρυσταλλικών φύτρων που εισαγόταν στο ακόρεστο διάλυμα υπολογιζόταν από τον προστιθέμενο όγκο των τιτλοδοτικών διαλυμάτων, σύμφωνα με την εξίσωση: titr mol Ca 1 mol HAP g 3 mg V ( lt) Ceff MWHAP 10 lt 5 mol Ca mol HAP g % ά 100% mseeds mg (8-6) όπου ΜW HAP = g mol -1. Από τις αναλύσεις των δειγμάτων που συλλέγονταν κατά τη διάρκεια της διάλυσης, προέκυπταν τα διαγράμματα της μεταβολής των συγκεντρώσεων των πλεγματικών ιόντων με το χρόνο, για να ελεγχόταν η σταθερότητα της χημικής σύστασης του διαλύματος. Ένα τέτοιο διάγραμμα παρουσιάζεται στο σχήμα
280 4,2x10-5 2,5x10-5 [Ca] total / M 4,0x10-5 [P] total / M 2,4x10-5 2,3x10-5 3,8x t/ hr t/ hr Σχήμα 8.1: Διάγραμμα μεταβολής ολικής συγκέντρωσης (α) ασβεστίου και (β)φωσφορικών σε πειράματα διάλυσης σε σταθερή ακορεστότητα. Ο ρυθμός διάλυσης του ΗΑP ανά μονάδα επιφάνειας, υπολογιζόταν σε αρχικό dv στάδιο διάλυσης (5%) από την εξίσωση (8-7), όπου ο όρος προσδιοριζόταν από την dt κλίση της εφαπτόμενης ευθείας της καμπύλης του διαγράμματος του προστιθέμενου όγκου των διαλυμάτων τιτλοδότησης συναρτήσει του χρόνου (σχήμα 8.2). R mol HAP min m diss 1 2 dv ml sec 3 lt mol Ca 1 mol HAP Ceff dt sec min ml lt 5 mol Ca 2 m SSA mg g (8-7) όπου SSA η ειδική επιφάνεια των κρυστάλλων και m η ποσότητα των κρυσταλλικών φύτρων που εισάγονταν στο διάλυμα εργασίας. 254
281 8 6 V titr / ml t/ sec Σχήμα 8.2: Γραφική παράσταση του προστιθέμενου όγκου των διαλυμάτων τιτλοδότησης στο ακόρεστο διάλυμα, προκειμένου να διατηρηθεί σταθερή η ακορεστότητα των διαλυμάτων, συναρτήσει του χρόνου; διάλυση κρυσταλλικών φύτρων ΗΑΡ σε συνθήκες σταθερής ακορεστότητας, ΝaCl 0.15 M, ph 7.40, 37 C, σ HAP =0.38. Αξίζει να σημειωθεί, ότι αρχικά, η διάλυση γινόταν γρήγορα, ενώ στη συνέχεια ο ρυθμός της μειωνόταν. Το μέγιστο ποσοστό διάλυσης ΗΑΡ που επιτεύχθηκε στα πειράματα ήταν 60%. Κάτι τέτοιο έρχεται σε αντίθεση με τη γενική θεώρηση της σταθερής σύστασης για μέτρηση της κινητικής της διάλυσης του φωσφορικού ασβεστίου σε συνθήκες μόνιμης κατάστασης. Αυτή η συμπεριφορά έχει αναφερθεί και σε άλλες εργασίες για τη μελέτη της κινητικής της διάλυσης του φωσφορικού ασβεστίου [Budz and Nancollas, 1988 ; Tang and Nancollas, 2000 ; Zhang and Nancollas, 1992]. Μία εξήγηση θα μπορούσε να είναι η λείανση των κρυστάλλων στην αρχή της διάλυσης, αφού έχει βρεθεί πως οι τραχείες επιφάνειες διαλύονται γρηγορότερα ή λόγω απενεργοποίησης των ενεργών κέντρων η οποία έχει ως συνέπεια την μείωση του ρυθμού διάλυσης των κρυστάλλων. Ένας ακόμη λόγος θα μπορούσε να είναι η αλλαγή της μορφολογίας της επιφάνειας του κρυστάλλου κατά την εξέλιξη της διάλυσης. Η εμφάνιση οπών και βημάτων κατά τη διάλυση ενός στερεού, όπως έχει αναφερθεί από αρκετούς εραυνητές, πιθανόν οδηγεί στην τροποποίηση της επιφάνειας επηρεάζοντας την ταχύτητα της διάλυσης [Wang et al., 2005]. Όπως έχει ήδη αναφερθεί στην ενότητα 2.6, η κινητήριος δύναμη για τη διάλυση είναι η διαφορά μεταξύ του χημικού δυναμικού του στερεού στο ακόρεστο διάλυμα, 255
282 από το αντίστοιχο στην ισορροπία και η ακορεστότητα είναι ένα μέτρο της απόκλισης του συστήματος από την ισορροπία που αποτελεί μέτρο της κινητήριας δύναμης για τη διάλυση. Η ακορεστότητα του ΗΑΡ ορίζεται ως το πηλίκο του γινομένου των ενεργοτήτων των ιόντων του προς το θερμοδυναμικό γινόμενο διαλυτότητάς του και δίνεται από την ακόλουθη εξίσωση: a 2 a 3 a Ca PO4 OH (8-8) K 0 s Η σχετική ακορεστότητα ως προς ΗΑP ορίζεται ως : 1/9 1 (8-9) Στον πίνακα 8.1 παρουσιάζονται οι πειραματικές συνθήκες και τα κινητικά αποτελέσματα της διάλυσης του ΗΑΡ στα δύο υποστρώματα. Να σημειωθεί ότι οι τιμές της ακορεστότητας του ΗΑΡ υπολογίσθηκαν με το λογισμικό MINEQL +. Πίνακας 8.1 Πειραματικές συνθήκες και αποτελέσματα της κινητικής της διάλυσης ΗΑΡ και απατιτικών εναποθέσεων σε βαλβίδες καρδιάς: ολική συγκέντρωση ασβεστίου, C Ca, σχετική ακορεστότητα ως προς ΗΑP, σ ΗΑP, και αρχικοί ρυθμοί διάλυσης, R diss, για τη διάλυση του υδροξυαπατίτη (HAP) στα δύο υποστρώματα, σε ακόρεστα διαλύματα και σε συνθήκες σταθερής ακορεστότητας, θ = 37.0 ± 0.1 o C, ph 7.40, ΝaCl 0.15 Μ και C Ca /C P = 1.67, όπου C P η ολική συγκέντρωση των φωσφορικών. Υποστρώματα Ασβεστούχες εναποθέσεις C Ca / 10-5 M σ ΗΑP σ ΟCP R diss / 10-7 mol min -1 m Κρυσταλλικά φύτρα ΗΑΡ
283 Όπως φαίνεται από τις τιμές των αποτελεσμάτων του πίνακα, παρά τη μικρή περιεκτικότητα των εναποθέσεων σε ανθρακικά (2-4%) οι ρυθμοί διάλυσής τους έδειξαν σημαντική διαφορά σε σχέση με τους αντίστοιχους του ΗΑΡ. Ενδεικτικά στο σχήμα 8.3 παρουσιάζεται ένα συγκριτικό διάγραμμα των ρυθμών διάλυσης του HAP στα δύο υποστρώματα φωσφορικού ασβεστίου σε μια τιμή σχετικής ακορεστότητας σ ΗΑP = Όπως φαίνεται ο ρυθμός διάλυσης των απατιτικών εναποθέσεων από ασβεστοποιημένες φυσικές βαλβίδες ήταν ταχύτερος (μία τάξη μεγέθους) σε σύγκριση με τον αντίστοιχο ρυθμό των συνθετικών κρυστάλλων ΗΑP. Η ίδια συμπεριφορά έχει αναφερθεί σε παρόμοια μελέτη [Budz et al., 1987]. Η διαφορά αυτή προφανώς οφείλεται στην μεγαλύτερη διαλυτότητα των παθολογικών εναποθέσεων. 4,5x10-7 4,0x10-7 3,5x10-7 R diss / mol HAP min -1 m -2 3,0x10-7 2,5x10-7 2,0x10-7 1,5x10-7 1,0x10-7 5,0x10-8 σ HAP = 0.48 Σχήμα 8.3: Γραφική απεικόνιση του ρυθμού διάλυσης ΗΑP στα δύο υποστρώματα φωσφορικού ασβεστίου σε συνθήκες σταθερής ακορεστότητας, 37 C, ph 7.40, 0.15 M NaCl, σ ΗΑP = 0.48 : ( ) παθολογικές εναποθέσεις και ( )κρυσταλλικά φύτρα ΗΑΡ. Ο αρχικός ρυθμός διάλυσης περιγράφεται από την εξίσωση (2-76) του θεωρητικού μέρους της παρούσας εργασίας. Η λογαριθμική μορφή της δίνεται από την εξίσωση (8-10): log R log K nlog (8-10) diss diss 257
284 όπου n η φαινόμενη τάξη της ταχύτητας καταβύθισης, σ η σχετική ακορεστότητα και K dis η σταθερά διάλυσης. Η προσαρμογή των πειραματικών αποτελεσμάτων του πίνακα 8.1 στην εξίσωση (8-10) φαίνεται στο διάγραμμα του σχήματος ,5-6,0 log (R diss / mol HAP min -1 m -2 ) -6,5-7,0-7,5-8,0-0,4-0,3-0,2-0,1 logσ HAP Σχήμα 8.4: Κινητική της διάλυσης του υδροξυαπατίτη (ΗΑP) στα δύο υποστρώματα σε συνθήκες σταθερής ακορεστότητας. Μεταβολή του λογαρίθμου του αρχικού ρυθμού διάλυσης ΗΑP συναρτήσει του λογαρίθμου της σχετικής ακορεστότητας. θ= 37 C, ph 7.40, ΝaCl 0.15 M: ( ) παθολογικές εναποθέσεις και ( ) κρυσταλλικά φύτρα ΗΑΡ. Η φαινόμενη τάξη και η αντίστοιχη σταθερά της διάλυσης του ΗΑΡ για τις παθολογικές εναποθέσεις και τα κρυσταλλικά φύτρα ΗΑΡ που μελετήθηκαν ήταν n=2.0 ( 0.1), K diss = ( ) mol min -1 m -2 και n=3.0 ( 0.1), K diss = ( ) mol min -1 m -2, αντίστοιχα. Οι τιμές αυτές της φαινόμενης τάξης οδηγούν στο συμπέρασμα ότι η επιφανειακή διάχυση αποτελεί το καθορίζον την ταχύτητα της διάλυσης στάδιο και για τα δύο υποστρώματα που μελετήθηκαν. Τα αποτελέσματα είναι σε συμφωνία με παρόμοιες μελέτες διάλυσης υδροξυαπατίτη, ανθρακικού απατίτη και αδαμαντίνης [Christoffersen, 1981 ; Tang et al., 2003]. Στη συνέχεια παρατίθενται τα αποτελέσματα της μορφολογικής εξέταση των στερεών, τα οποία προέκυψαν από τη διάλυση με ηλεκτρονική μικροσκοπία σάρωσης. Στις φωτογραφίες του σχήματος 8.5 διακρίνονται οι κρύσταλλοι των ασβεστούχων εναποθέσεων από βαλβίδες καρδιάς μετά τη διάλυσή τους σε συνθήκες 258
285 σταθερής ακορεστότητας, όπου είναι εμφανές το πόσο δραματικά έχει αλλάξει το μέγεθός των κρυσταλλιτών και κυρίως το πάχος τους. Όπως φαίνεται και στη φωτογραφία του σχήματος 8.5 (β) και στην περίπτωση των μικροκρυσταλλικών σφαιρικών σχηματισμών ανθρακικού απατίτη ήταν φανερή η επίδραση της διάλυσης στους κρυστάλλους αυτούς. Σχήμα 8.5: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυσταλλιτών ΗΑP από εναποθέσεις βαλβίδων καρδιάς, οι οποίοι υπεβλήθησαν σε διάλυση σε ακόρεστα διαλύματα φωσφορικού ασβεστίου σε συνθήκες σταθερής ακορεστότητας; ΝaCl 0.15 M; ph 7.40, 37 C, (α) σ HAP =0.38 και (β) σ HAP =
286 Η ίδια συμπεριφορά παρατηρήθηκε και κατά τη διάλυση ΗΑΡ σε συνθετικά κρυσταλλικά φύτρα ΗΑΡ, όπου στο σχήμα 8.6 φαίνονται οι λεπτοσχηματισμένοι πρισματικοί κρύσταλλοι ΗΑΡ. Σχήμα 8.6: Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης κρυστάλλων ΗΑP οι οποίοι έχουν υποβληθεί σε διάλυση σε ακόρεστα διαλύματα φωσφορικού ασβεστίου σε συνθήκες σταθερής ακορεστότητας; ΝaCl 0.15 M; ph 7.40, 37 C, (α) σ HAP =0.38 και (β) σ HAP =
Γεώργιος Τρανταλής. Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική
 Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Η αορτική
Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Η αορτική
ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ. Κάντε κλικ για να επεξεργαστείτε τον υπότιτλο του υποδείγματος
 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κάντε κλικ για να επεξεργαστείτε τον υπότιτλο του υποδείγματος ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κυκλοφορικό σύστημα Αιμοφόρο 1. 2. Καρδιά Αιμοφόρα αγγεία Λεμφοφόρο Αρτηρίες Λεμφικά τριχοειδή Φλέβες
ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κάντε κλικ για να επεξεργαστείτε τον υπότιτλο του υποδείγματος ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κυκλοφορικό σύστημα Αιμοφόρο 1. 2. Καρδιά Αιμοφόρα αγγεία Λεμφοφόρο Αρτηρίες Λεμφικά τριχοειδή Φλέβες
Βιολογία Α Λυκείου Κεφ. 3. Κυκλοφορικό Σύστημα. Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα
 Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ ΠΡΟΪΟΝ
 Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ
Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ
ΒΙΟΣΥΜΒΑΤΟΤΗΤΑ ΒΙΟΫΛΙΚΩΝ: Η ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΙΣΤΩΝ ΚΑΙ ΒΙΟΫΛΙΚΩΝ
 ΒΙΟΣΥΜΒΑΤΟΤΗΤΑ ΒΙΟΫΛΙΚΩΝ: Η ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΙΣΤΩΝ ΚΑΙ ΒΙΟΫΛΙΚΩΝ Στ. Ροκίδη, Π.Κουτσούκος Πανεπιστήμιο Πατρών, Τμήμα Χημικών Μηχανικών και ΙΤΕ/ΙΕΧΜΗ, Πάτρα Δημ. Μαυρίλας Πανεπιστήμιο Πατρών, Τμήμα Μηχανολόγων
ΒΙΟΣΥΜΒΑΤΟΤΗΤΑ ΒΙΟΫΛΙΚΩΝ: Η ΑΣΒΕΣΤΟΠΟΙΗΣΗ ΙΣΤΩΝ ΚΑΙ ΒΙΟΫΛΙΚΩΝ Στ. Ροκίδη, Π.Κουτσούκος Πανεπιστήμιο Πατρών, Τμήμα Χημικών Μηχανικών και ΙΤΕ/ΙΕΧΜΗ, Πάτρα Δημ. Μαυρίλας Πανεπιστήμιο Πατρών, Τμήμα Μηχανολόγων
Εύη Καραγιαννίδου Χημικός Α.Π.Θ. ΟΙ ΕΠΟΞΕΙΔΙΚΕΣ ΚΟΛΛΕΣ ΣΤΗΝ ΑΠΟΚΑΤΑΣΤΑΣΗ ΕΡΓΩΝ ΤΕΧΝΗΣ ΑΠΟ ΓΥΑΛΙ ή ΚΕΡΑΜΙΚΟ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ Εύη Καραγιαννίδου Χημικός Α.Π.Θ. ΟΙ ΕΠΟΞΕΙΔΙΚΕΣ ΚΟΛΛΕΣ ΣΤΗΝ ΑΠΟΚΑΤΑΣΤΑΣΗ ΕΡΓΩΝ ΤΕΧΝΗΣ ΑΠΟ ΓΥΑΛΙ ή ΚΕΡΑΜΙΚΟ ΜΕΛΕΤΗ ΤΗΣ ΚΙΝΗΤΙΚΗΣ
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ Εύη Καραγιαννίδου Χημικός Α.Π.Θ. ΟΙ ΕΠΟΞΕΙΔΙΚΕΣ ΚΟΛΛΕΣ ΣΤΗΝ ΑΠΟΚΑΤΑΣΤΑΣΗ ΕΡΓΩΝ ΤΕΧΝΗΣ ΑΠΟ ΓΥΑΛΙ ή ΚΕΡΑΜΙΚΟ ΜΕΛΕΤΗ ΤΗΣ ΚΙΝΗΤΙΚΗΣ
ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΜΕΛΕΤΗ ΤΡΟΠΟΠΟΙΗΜΕΝΩΝ ΥΛΙΚΩΝ ΚΑΤΑΛΛΗΛΩΝ ΓΙΑ ΑΚΙΝΗΤΕΣ ΠΡΟΣΘΕΤΙΚΕΣ ΑΠΟΚΑΤΑΣΤΑΣΕΙΣ, ΜΕ ΔΥΝΑΤΟΤΗΤΕΣ ΑΝΑΠΤΥΞΗΣ
 ΞΑΝΘΙΠΠΗ ΧΑΤΖΗΣΤΑΥΡΟΥ ΦΥΣΙΚΟΣ ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΜΕΛΕΤΗ ΤΡΟΠΟΠΟΙΗΜΕΝΩΝ ΥΛΙΚΩΝ ΚΑΤΑΛΛΗΛΩΝ ΓΙΑ ΑΚΙΝΗΤΕΣ ΠΡΟΣΘΕΤΙΚΕΣ ΑΠΟΚΑΤΑΣΤΑΣΕΙΣ, ΜΕ ΔΥΝΑΤΟΤΗΤΕΣ ΑΝΑΠΤΥΞΗΣ ΣΥΝΘΕΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΔΟΜΩΝ. Σκοπός της παρούσας έρευνας
ΞΑΝΘΙΠΠΗ ΧΑΤΖΗΣΤΑΥΡΟΥ ΦΥΣΙΚΟΣ ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΜΕΛΕΤΗ ΤΡΟΠΟΠΟΙΗΜΕΝΩΝ ΥΛΙΚΩΝ ΚΑΤΑΛΛΗΛΩΝ ΓΙΑ ΑΚΙΝΗΤΕΣ ΠΡΟΣΘΕΤΙΚΕΣ ΑΠΟΚΑΤΑΣΤΑΣΕΙΣ, ΜΕ ΔΥΝΑΤΟΤΗΤΕΣ ΑΝΑΠΤΥΞΗΣ ΣΥΝΘΕΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΔΟΜΩΝ. Σκοπός της παρούσας έρευνας
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5
 ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
ΗΚΑΡΔΙΑ ΗΚΑΡΔΙΑ. Ροβίθης Μιχαήλ
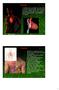 ΗΚΑΡΔΙΑ Η καρδιά που το μέγεθός της είναι λίγο μεγαλύτερο από μία γροθιά, είναι μία διπλή αυτόνομη μυώδης αντλία. Ενώ το βάρος της κυμαίνεται από 280 340 γραμμάρια. Είναι η κεντρική αντλία του κυκλοφορικού
ΗΚΑΡΔΙΑ Η καρδιά που το μέγεθός της είναι λίγο μεγαλύτερο από μία γροθιά, είναι μία διπλή αυτόνομη μυώδης αντλία. Ενώ το βάρος της κυμαίνεται από 280 340 γραμμάρια. Είναι η κεντρική αντλία του κυκλοφορικού
3. Με ποιο άλλο σύστημα είναι συνδεδεμένο το κυκλοφορικό σύστημα;
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ. 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε.
 ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε. Αμανατίδης ΤΡΙΤΗ 24/10/2017 ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Κατηγορίες
ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε. Αμανατίδης ΤΡΙΤΗ 24/10/2017 ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Κατηγορίες
Η δομή και λειτουργία της φυσιολογικής καρδιάς και των αγγείων
 Η δομή και λειτουργία της φυσιολογικής καρδιάς και των αγγείων Η μεταφορά των θρεπτικών ουσιών στα κύτταρα των ιστών και η απομάκρυνση από αυτά των αχρήστων γίνεται από το κυκλοφορικό σύστημα, το οποίο
Η δομή και λειτουργία της φυσιολογικής καρδιάς και των αγγείων Η μεταφορά των θρεπτικών ουσιών στα κύτταρα των ιστών και η απομάκρυνση από αυτά των αχρήστων γίνεται από το κυκλοφορικό σύστημα, το οποίο
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΜΕΤΑΤΡΟΠΗ ΑΝΘΡΑΚΑ (ΚΑΡΒΟΥΝΟ) ΣΕ ΕΝΕΡΓΟ ΑΝΘΡΑΚΑ ΜΕΣΩ ΧΗΜΙΚΗΣ ΚΑΙ ΘΕΡΜΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΜΕΤΑΤΡΟΠΗ ΑΝΘΡΑΚΑ (ΚΑΡΒΟΥΝΟ) ΣΕ ΕΝΕΡΓΟ ΑΝΘΡΑΚΑ ΜΕΣΩ ΧΗΜΙΚΗΣ ΚΑΙ ΘΕΡΜΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΥΔΡΟΠΟΝΙΚΗ ΚΑΛΛΙΕΡΓΕΙΑ ΔΥΟΣΜΟΥ ΣΕ ΔΙΑΦΟΡΕΤΙΚΑ ΘΡΕΠΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΡΑΤΩ ΝΙΚΟΛΑΪΔΟΥ Λεμεσός 2014
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΥΔΡΟΠΟΝΙΚΗ ΚΑΛΛΙΕΡΓΕΙΑ ΔΥΟΣΜΟΥ ΣΕ ΔΙΑΦΟΡΕΤΙΚΑ ΘΡΕΠΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΕΡΑΤΩ ΝΙΚΟΛΑΪΔΟΥ Λεμεσός 2014
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η ΣΥΓΚΕΝΤΡΩΣΗ ΤΩΝ ΒΑΡΕΩΝ ΜΕΤΑΛΛΩΝ ΣΤΟ ΕΔΑΦΟΣ ΚΑΙ ΜΕΘΟΔΟΙ ΠΡΟΣΔΙΟΡΙΣΜΟΥ ΤΟΥΣ Μιχαήλ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η ΣΥΓΚΕΝΤΡΩΣΗ ΤΩΝ ΒΑΡΕΩΝ ΜΕΤΑΛΛΩΝ ΣΤΟ ΕΔΑΦΟΣ ΚΑΙ ΜΕΘΟΔΟΙ ΠΡΟΣΔΙΟΡΙΣΜΟΥ ΤΟΥΣ Μιχαήλ
 ΚΑΡΔΙΑ ΚΑΡΔΙΑ Ινομυώδες κοίλο όργανο Εντόπιση: στο θώρακα - λοξή θέση Κορυφή: προς τα κάτω, εμπρός και αριστερά Βάση: προς τα πίσω, άνω και δεξιά Δεξιές κοιλότητες: δεξιός κόλπος - δεξιά κοιλία Αριστερές
ΚΑΡΔΙΑ ΚΑΡΔΙΑ Ινομυώδες κοίλο όργανο Εντόπιση: στο θώρακα - λοξή θέση Κορυφή: προς τα κάτω, εμπρός και αριστερά Βάση: προς τα πίσω, άνω και δεξιά Δεξιές κοιλότητες: δεξιός κόλπος - δεξιά κοιλία Αριστερές
ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ ΚΑΡΔΙΑ
 1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Αποτελείται από την καρδιά και τα αγγεία( αρτηρίες, φλέβες, τριχοειδή αγγεία). Η καρδιά με τους παλμικούς ρυθμούς στέλνει το αίμα στο σώμα. Οι αρτηρίες παίρνουν το αίμα από την καρδιά
1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Αποτελείται από την καρδιά και τα αγγεία( αρτηρίες, φλέβες, τριχοειδή αγγεία). Η καρδιά με τους παλμικούς ρυθμούς στέλνει το αίμα στο σώμα. Οι αρτηρίες παίρνουν το αίμα από την καρδιά
ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ
 ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ ΧΡΙΣΤΙΝΑ ΚΑΛΟΓΕΡΟΠΟΥΛΟΥ ΑΘΗΝΑ 2010 1 ΣΚΟΠΟΣ Η ανάλυση και μελέτη της μοριακής δομής των καρωτίδων αρτηριών με υπέρυθρη φασματοσκοπία. Η εξαγωγή συμπερασμάτων
ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ ΧΡΙΣΤΙΝΑ ΚΑΛΟΓΕΡΟΠΟΥΛΟΥ ΑΘΗΝΑ 2010 1 ΣΚΟΠΟΣ Η ανάλυση και μελέτη της μοριακής δομής των καρωτίδων αρτηριών με υπέρυθρη φασματοσκοπία. Η εξαγωγή συμπερασμάτων
Πτυχιακή διατριβή. Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN) στην ατμόσφαιρα
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN)
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN)
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Επιβλέπων Καθηγητής: Δρ. Νίκος Μίτλεττον Η ΣΧΕΣΗ ΤΟΥ ΜΗΤΡΙΚΟΥ ΘΗΛΑΣΜΟΥ ΜΕ ΤΗΝ ΕΜΦΑΝΙΣΗ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 2 ΣΤΗΝ ΠΑΙΔΙΚΗ ΗΛΙΚΙΑ Ονοματεπώνυμο: Ιωσηφίνα
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Επιβλέπων Καθηγητής: Δρ. Νίκος Μίτλεττον Η ΣΧΕΣΗ ΤΟΥ ΜΗΤΡΙΚΟΥ ΘΗΛΑΣΜΟΥ ΜΕ ΤΗΝ ΕΜΦΑΝΙΣΗ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 2 ΣΤΗΝ ΠΑΙΔΙΚΗ ΗΛΙΚΙΑ Ονοματεπώνυμο: Ιωσηφίνα
Η ΦΥΣΙΟΛΟΓΙΚΗ ΚΑΡ ΙA ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΗΣ
 Η ΦΥΣΙΟΛΟΓΙΚΗ ΚΑΡ ΙA ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΗΣ 1 Η φυσιολογική καρδιά είναι µία πολύ δυνατή αντλία φτιαγµένη από µυϊκό ιστό, που λειτουργεί εντατικά και συνεχώς. Έχει περίπου τις διαστάσεις µιας ανθρώπινης
Η ΦΥΣΙΟΛΟΓΙΚΗ ΚΑΡ ΙA ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΗΣ 1 Η φυσιολογική καρδιά είναι µία πολύ δυνατή αντλία φτιαγµένη από µυϊκό ιστό, που λειτουργεί εντατικά και συνεχώς. Έχει περίπου τις διαστάσεις µιας ανθρώπινης
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΘΟΔΟΙ ΠΡΟΕΠΕΞΕΡΓΑΣΙΑΣ ΤΩΝ ΛΙΠΩΝ ΚΑΙ ΕΛΕΩΝ ΠΡΟΣ ΠΑΡΑΓΩΓΗ ΒΙΟΑΕΡΙΟΥ Ανδρέας Φράγκου Λεμεσός 2015
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΘΟΔΟΙ ΠΡΟΕΠΕΞΕΡΓΑΣΙΑΣ ΤΩΝ ΛΙΠΩΝ ΚΑΙ ΕΛΕΩΝ ΠΡΟΣ ΠΑΡΑΓΩΓΗ ΒΙΟΑΕΡΙΟΥ Ανδρέας Φράγκου Λεμεσός 2015
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΟΥ ΚΛΙΜΑΤΟΣ ΑΣΦΑΛΕΙΑΣ ΤΩΝ ΑΣΘΕΝΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΟ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΟΥ ΚΛΙΜΑΤΟΣ ΑΣΦΑΛΕΙΑΣ ΤΩΝ ΑΣΘΕΝΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΟ ΑΝΔΡΕΑΣ ΛΕΩΝΙΔΟΥ Λεμεσός, 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΟΥ ΚΛΙΜΑΤΟΣ ΑΣΦΑΛΕΙΑΣ ΤΩΝ ΑΣΘΕΝΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΟ ΑΝΔΡΕΑΣ ΛΕΩΝΙΔΟΥ Λεμεσός, 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ
Βιολογικές δοκιμές σε Βιοϋλικά
 Βιολογικές δοκιμές σε Βιοϋλικά Γενικές έννοιες (κυτο)τοξικότητας In vitro αποτίμηση ιστών Δοκιμές (assays) Μορφολογία κυττάρων α) Μέθοδος άμεσης επαφής (direct contact) Ζωντανά-νεκρά κύτταρα (βαφή με αιματοξυλίνη
Βιολογικές δοκιμές σε Βιοϋλικά Γενικές έννοιες (κυτο)τοξικότητας In vitro αποτίμηση ιστών Δοκιμές (assays) Μορφολογία κυττάρων α) Μέθοδος άμεσης επαφής (direct contact) Ζωντανά-νεκρά κύτταρα (βαφή με αιματοξυλίνη
ΑΡΤΗΡΙΑΚΗ ΠΙΕΣΗ (Α.Π.)
 ΥΠΕΡΤΑΣΗ Η καρδιά προωθεί το αίμα στον οργανισμό μέσω των αρτηριών, με αποτέλεσμα οι αρτηρίες να βρίσκονται υπό πίεση. Η πίεση αυξάνει όταν είμαστε αναστατωμένοι, όταν τρομάζουμε, όταν καταβάλουμε κάποια
ΥΠΕΡΤΑΣΗ Η καρδιά προωθεί το αίμα στον οργανισμό μέσω των αρτηριών, με αποτέλεσμα οι αρτηρίες να βρίσκονται υπό πίεση. Η πίεση αυξάνει όταν είμαστε αναστατωμένοι, όταν τρομάζουμε, όταν καταβάλουμε κάποια
Β. Μαμαρέλη 1, Μ. Κυριακίδου 2, Ο. Τάνης 2, Ι. Μαμαρέλης 1, Χ. Κωτούλας 3, Ε. Κουτουλάκης 4, Ι. Κασσικού 1, Ι. Αναστασοπούλου 5
 Β. Μαμαρέλη 1, Μ. Κυριακίδου 2, Ο. Τάνης 2, Ι. Μαμαρέλης 1, Χ. Κωτούλας 3, Ε. Κουτουλάκης 4, Ι. Κασσικού 1, Ι. Αναστασοπούλου 5 1 Καρδιολογική Κλινική ΝΙΜΤΣ, 2 Σχολή Χημικών Μηχανικών, Πολυτεχνειούπολη
Β. Μαμαρέλη 1, Μ. Κυριακίδου 2, Ο. Τάνης 2, Ι. Μαμαρέλης 1, Χ. Κωτούλας 3, Ε. Κουτουλάκης 4, Ι. Κασσικού 1, Ι. Αναστασοπούλου 5 1 Καρδιολογική Κλινική ΝΙΜΤΣ, 2 Σχολή Χημικών Μηχανικών, Πολυτεχνειούπολη
Εφαρμοσμένη Διατροφική Ιατρική
 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Σημείωση: Το κείμενο αποτελεί απόσπασμα του κεφαλαίου «Χοληστερίνη και φλεγμονή». Έχει αναπαραχθεί λόγω των πολύτιμων πληροφοριών
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Σημείωση: Το κείμενο αποτελεί απόσπασμα του κεφαλαίου «Χοληστερίνη και φλεγμονή». Έχει αναπαραχθεί λόγω των πολύτιμων πληροφοριών
Όταν χρειάζεται ρύθμιση της ποσότητας των χορηγούμενων υγρών του ασθενή. Όταν θέλουμε να προλάβουμε την υπερφόρτωση του κυκλοφορικού συστήματος
 Ερωτήσεις Αξιολόγησης Εργαστηριακού Μαθήματος Θέμα: «Κεντρική Φλεβική Πίεση» 1. Τι είναι η Κεντρική Φλεβική Πίεση (ΚΦΠ); Είναι η υδροστατική πίεση των μεγάλων φλεβών που είναι πλησιέστερα στην καρδιά,
Ερωτήσεις Αξιολόγησης Εργαστηριακού Μαθήματος Θέμα: «Κεντρική Φλεβική Πίεση» 1. Τι είναι η Κεντρική Φλεβική Πίεση (ΚΦΠ); Είναι η υδροστατική πίεση των μεγάλων φλεβών που είναι πλησιέστερα στην καρδιά,
ΙΑΦΡΑΓΜΑΤΙΚΑ ΕΛΛΕΙΜΜΑΤΑ
 7 ΙΑΦΡΑΓΜΑΤΙΚΑ ΕΛΛΕΙΜΜΑΤΑ Σε µια καρδιά που λειτουργεί φυσιολογικά, το αίµα µε χαµηλή περιεκτικότητα σε οξυγόνο ρέει από το σώµα στη δεξιά πλευρά της καρδιάς (στο δεξιό κόλπο και από εκεί στη δεξιά κοιλία).
7 ΙΑΦΡΑΓΜΑΤΙΚΑ ΕΛΛΕΙΜΜΑΤΑ Σε µια καρδιά που λειτουργεί φυσιολογικά, το αίµα µε χαµηλή περιεκτικότητα σε οξυγόνο ρέει από το σώµα στη δεξιά πλευρά της καρδιάς (στο δεξιό κόλπο και από εκεί στη δεξιά κοιλία).
ΜΕΛΕΤΗ ΜΟΡΦΟΛΟΓΙΑΣ ΣΤΕΡΕΩΝ ΥΜΕΝΙΩΝ ΓΙΑ ΦΩΤΟΝΙΟΕΝΕΡΓΕΙΑΚΗ ΑΝΑΒΑΘΜΙΣΗ
 Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΜΕΛΕΤΗ ΜΟΡΦΟΛΟΓΙΑΣ ΣΤΕΡΕΩΝ ΥΜΕΝΙΩΝ ΓΙΑ ΦΩΤΟΝΙΟΕΝΕΡΓΕΙΑΚΗ ΑΝΑΒΑΘΜΙΣΗ Βασιλική Ζήνωνος Λεμεσός, Μάϊος 2017 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ
Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΜΕΛΕΤΗ ΜΟΡΦΟΛΟΓΙΑΣ ΣΤΕΡΕΩΝ ΥΜΕΝΙΩΝ ΓΙΑ ΦΩΤΟΝΙΟΕΝΕΡΓΕΙΑΚΗ ΑΝΑΒΑΘΜΙΣΗ Βασιλική Ζήνωνος Λεμεσός, Μάϊος 2017 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ
Φυσιολογία της Άσκησης
 ΕΛΛΗΝΙΚΟ ΜΕΣΟΓΕΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΩΝ ΔΙΑΤΡΟΦΗΣ & ΔΙΑΙΤΟΛΟΓΙΑΣ Φυσιολογία της Άσκησης Λειτουργία καρδιαγγειακού συστήματος Καρδιαγγειακός έλεγχος κατά τη διάρκεια της
ΕΛΛΗΝΙΚΟ ΜΕΣΟΓΕΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΩΝ ΔΙΑΤΡΟΦΗΣ & ΔΙΑΙΤΟΛΟΓΙΑΣ Φυσιολογία της Άσκησης Λειτουργία καρδιαγγειακού συστήματος Καρδιαγγειακός έλεγχος κατά τη διάρκεια της
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή Εργασία. Κόπωση και ποιότητα ζωής ασθενών με καρκίνο.
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Κόπωση και ποιότητα ζωής ασθενών με καρκίνο Μαργαρίτα Μάου Λευκωσία 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Κόπωση και ποιότητα ζωής ασθενών με καρκίνο Μαργαρίτα Μάου Λευκωσία 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ
ΑΠΟΦΡΑΚΤΙΚΕΣ ΠΑΘΗΣΕΙΣ (ΣΤΕΝΩΣΕΙΣ) ΤΗΣ ΚΑΡ ΙΑΣ Ή ΤΩΝ ΑΓΓΕΙΩΝ
 8 ΑΠΟΦΡΑΚΤΙΚΕΣ ΠΑΘΗΣΕΙΣ (ΣΤΕΝΩΣΕΙΣ) ΤΗΣ ΚΑΡ ΙΑΣ Ή ΤΩΝ ΑΓΓΕΙΩΝ Μία παρακώλυση της ροής του αίµατος οφείλεται συχνά σε στένωση και µπορεί να σταµατήσει τη ροή του αίµατος µερικώς ή τελείως. Κάθε µία από
8 ΑΠΟΦΡΑΚΤΙΚΕΣ ΠΑΘΗΣΕΙΣ (ΣΤΕΝΩΣΕΙΣ) ΤΗΣ ΚΑΡ ΙΑΣ Ή ΤΩΝ ΑΓΓΕΙΩΝ Μία παρακώλυση της ροής του αίµατος οφείλεται συχνά σε στένωση και µπορεί να σταµατήσει τη ροή του αίµατος µερικώς ή τελείως. Κάθε µία από
Σχολή Μηχανικής και Τεχνολογίας. Πτυχιακή διατριβή
 Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή διατριβή ΠΕΙΡΑΜΑΤΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗΣ ΜΕΡΟΥΣ ΤΟΥ ΚΑΥΣΙΜΟΥ ΠΟΥ ΚΑΤΑΝΑΛΩΝΕΙ ΒΕΝΖΙΝΟΚΙΝΗΤΗΡΑΣ ΜΕ ΥΔΡΟΓΟΝΟ ΤΟ ΟΠΟΙΟ ΘΑ ΠΑΡΑΓΕΤΑΙ ΜΕ ΑΝΑΚΤΗΣΗ ΕΝΕΡΓΕΙΑΣ ΚΑΤΑ
Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή διατριβή ΠΕΙΡΑΜΑΤΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΑΝΤΙΚΑΤΑΣΤΑΣΗΣ ΜΕΡΟΥΣ ΤΟΥ ΚΑΥΣΙΜΟΥ ΠΟΥ ΚΑΤΑΝΑΛΩΝΕΙ ΒΕΝΖΙΝΟΚΙΝΗΤΗΡΑΣ ΜΕ ΥΔΡΟΓΟΝΟ ΤΟ ΟΠΟΙΟ ΘΑ ΠΑΡΑΓΕΤΑΙ ΜΕ ΑΝΑΚΤΗΣΗ ΕΝΕΡΓΕΙΑΣ ΚΑΤΑ
Πτυχιακή εργασία. Ελένη Κυριάκου
 Σχολή Γεωπονικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία Βιοδιάσπαση Ιοντικών Υγρών σε Διαφορετικές Θερμοκρασίες από τον Sphingomonas sp. VITPTHJ Ελένη Κυριάκου Λεμεσός, Μάιος 2017 ΤΕΧΝΟΛΟΓΙΚΟ
Σχολή Γεωπονικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία Βιοδιάσπαση Ιοντικών Υγρών σε Διαφορετικές Θερμοκρασίες από τον Sphingomonas sp. VITPTHJ Ελένη Κυριάκου Λεμεσός, Μάιος 2017 ΤΕΧΝΟΛΟΓΙΚΟ
Κυκλοφορικό σύστημα. Από μαθητές και μαθήτριες του Στ 1
 Κυκλοφορικό σύστημα Από μαθητές και μαθήτριες του Στ 1 Η καρδία Χτύπα 2 δισεκατομμύρια φορές σε όλη μας τη ζωή. Βρίσκεται στο θώρακα, κέντρο προς αριστερά. Έχει το μέγεθος μιας γροθιάς. Αλεξάνδρα, Αναστασία,
Κυκλοφορικό σύστημα Από μαθητές και μαθήτριες του Στ 1 Η καρδία Χτύπα 2 δισεκατομμύρια φορές σε όλη μας τη ζωή. Βρίσκεται στο θώρακα, κέντρο προς αριστερά. Έχει το μέγεθος μιας γροθιάς. Αλεξάνδρα, Αναστασία,
Θέμα: Παχυσαρκία και κύηση:
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜ Α ΝΟΣΗΛΕΥΤΙΚΗΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Θέμα: Παχυσαρκία και κύηση: επιπτώσεις στην έκβαση της κύησης και στο έμβρυο Ονοματεπώνυμο: Στέλλα Ριαλά Αριθμός
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜ Α ΝΟΣΗΛΕΥΤΙΚΗΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Θέμα: Παχυσαρκία και κύηση: επιπτώσεις στην έκβαση της κύησης και στο έμβρυο Ονοματεπώνυμο: Στέλλα Ριαλά Αριθμός
ΜΗΤΡΙΚΟΣ ΘΗΛΑΣΜΟΣ ΚΑΙ ΓΝΩΣΤΙΚΗ ΑΝΑΠΤΥΞΗ ΜΕΧΡΙ ΚΑΙ 10 ΧΡΟΝΩΝ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΜΗΤΡΙΚΟΣ ΘΗΛΑΣΜΟΣ ΚΑΙ ΓΝΩΣΤΙΚΗ ΑΝΑΠΤΥΞΗ ΜΕΧΡΙ ΚΑΙ 10 ΧΡΟΝΩΝ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Ονοματεπώνυμο Κεντούλλα Πέτρου Αριθμός Φοιτητικής Ταυτότητας 2008761539 Κύπρος
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΜΗΤΡΙΚΟΣ ΘΗΛΑΣΜΟΣ ΚΑΙ ΓΝΩΣΤΙΚΗ ΑΝΑΠΤΥΞΗ ΜΕΧΡΙ ΚΑΙ 10 ΧΡΟΝΩΝ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Ονοματεπώνυμο Κεντούλλα Πέτρου Αριθμός Φοιτητικής Ταυτότητας 2008761539 Κύπρος
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΤΩΝ ΟΞΕΙΔΙΩΝ ΤΟΥ ΑΖΩΤΟΥ (NO X
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΤΩΝ ΟΞΕΙΔΙΩΝ ΤΟΥ ΑΖΩΤΟΥ (NO X
Τεχνικές παρασκευής ζεόλιθου ZSM-5 από τέφρα φλοιού ρυζιού με χρήση φούρνου μικροκυμάτων και τεχνικής sol-gel
 Τεχνικές παρασκευής ζεόλιθου ZSM-5 από τέφρα φλοιού ρυζιού με χρήση φούρνου μικροκυμάτων και τεχνικής sol-gel Δέσποινα Στεφοπούλου Επιβλέπων: Κωνσταντίνος Κορδάτος Στην παρούσα διπλωματική εργασία παρασκευάστηκαν
Τεχνικές παρασκευής ζεόλιθου ZSM-5 από τέφρα φλοιού ρυζιού με χρήση φούρνου μικροκυμάτων και τεχνικής sol-gel Δέσποινα Στεφοπούλου Επιβλέπων: Κωνσταντίνος Κορδάτος Στην παρούσα διπλωματική εργασία παρασκευάστηκαν
ΑΠΟΜΟΝΩΣΗ, ΤΑΥΤΟΠΟΙΗΣΗ ΜΕΘΑΝΟΤΡΟΦΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΚΑΙ ΒΙΟΛΟΓΙΚΗ ΜΕΤΑΤΡΟΠΗ ΜΕΘΑΝΙΟΥ ΣΕ ΜΕΘΑΝΟΛΗ
 Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΟΝΩΣΗ, ΤΑΥΤΟΠΟΙΗΣΗ ΜΕΘΑΝΟΤΡΟΦΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΚΑΙ ΒΙΟΛΟΓΙΚΗ ΜΕΤΑΤΡΟΠΗ ΜΕΘΑΝΙΟΥ ΣΕ ΜΕΘΑΝΟΛΗ Ιρένα Κυπριανίδου Λεμεσός, Μάιος
Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΟΝΩΣΗ, ΤΑΥΤΟΠΟΙΗΣΗ ΜΕΘΑΝΟΤΡΟΦΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΚΑΙ ΒΙΟΛΟΓΙΚΗ ΜΕΤΑΤΡΟΠΗ ΜΕΘΑΝΙΟΥ ΣΕ ΜΕΘΑΝΟΛΗ Ιρένα Κυπριανίδου Λεμεσός, Μάιος
Πτυχιακή Εργασία ΓΝΩΣΕΙΣ KAI ΣΤΑΣΕΙΣ ΤΩΝ ΕΠΑΓΓΕΛΜΑΤΙΩΝ ΥΓΕΙΑΣ ΓΙΑ ΤΗΝ ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΚΘΕΣΗ ΣΤΟΝ HIV. Στυλιανού Στυλιανή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία ΓΝΩΣΕΙΣ KAI ΣΤΑΣΕΙΣ ΤΩΝ ΕΠΑΓΓΕΛΜΑΤΙΩΝ ΥΓΕΙΑΣ ΓΙΑ ΤΗΝ ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΚΘΕΣΗ ΣΤΟΝ HIV Στυλιανού Στυλιανή Λευκωσία 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία ΓΝΩΣΕΙΣ KAI ΣΤΑΣΕΙΣ ΤΩΝ ΕΠΑΓΓΕΛΜΑΤΙΩΝ ΥΓΕΙΑΣ ΓΙΑ ΤΗΝ ΕΠΑΓΓΕΛΜΑΤΙΚΗ ΕΚΘΕΣΗ ΣΤΟΝ HIV Στυλιανού Στυλιανή Λευκωσία 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΣΥΓΓΕΝΕΙΣ ΚΑΡΔΙΟΠΑΘΕΙΕΣ ΠΟΥ ΔΕΝ ΧΡΕΙΑΖΟΝΤΑΙ ΑΝΤΙΜΕΤΩΠΙΣΗ
 8 Η ΕΠΙΣΤΗΜΟΝΙΚΗ ΣΥΝΑΝΤΗΣΗ ΠΑΙΔΙΑΤΡΩΝ-ΚΑΡΔΙΟΛΟΓΩΝ 8/12/2018 ΣΥΓΓΕΝΕΙΣ ΚΑΡΔΙΟΠΑΘΕΙΕΣ ΠΟΥ ΔΕΝ ΧΡΕΙΑΖΟΝΤΑΙ ΑΝΤΙΜΕΤΩΠΙΣΗ Κων/νος Κ. Θωμαϊδης Γ.Ν. «Γ. ΠΑΠΑΝΙΚΟΛΑΟΥ» Σκοπός της διόρθωσης μίας συγγενούς καρδιακής
8 Η ΕΠΙΣΤΗΜΟΝΙΚΗ ΣΥΝΑΝΤΗΣΗ ΠΑΙΔΙΑΤΡΩΝ-ΚΑΡΔΙΟΛΟΓΩΝ 8/12/2018 ΣΥΓΓΕΝΕΙΣ ΚΑΡΔΙΟΠΑΘΕΙΕΣ ΠΟΥ ΔΕΝ ΧΡΕΙΑΖΟΝΤΑΙ ΑΝΤΙΜΕΤΩΠΙΣΗ Κων/νος Κ. Θωμαϊδης Γ.Ν. «Γ. ΠΑΠΑΝΙΚΟΛΑΟΥ» Σκοπός της διόρθωσης μίας συγγενούς καρδιακής
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΣΥΜΒΟΛΗ ΤΟΥ ΤΕΧΝΗΤΟΥ ΘΗΛΑΣΜΟΥ ΣΤΗ ΔΙΑΤΡΟΦΗ ΤΩΝ ΑΜΝΩΝ ΦΥΛΗΣ ΧΙΟΥ ΓΙΑΝΝΟΣ ΜΑΚΡΗΣ Λεμεσός 2014 ii
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΣΥΜΒΟΛΗ ΤΟΥ ΤΕΧΝΗΤΟΥ ΘΗΛΑΣΜΟΥ ΣΤΗ ΔΙΑΤΡΟΦΗ ΤΩΝ ΑΜΝΩΝ ΦΥΛΗΣ ΧΙΟΥ ΓΙΑΝΝΟΣ ΜΑΚΡΗΣ Λεμεσός 2014 ii
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ
 ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή διατριβή ΟΙ ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΣΧΕΤΙΖΟΜΕΝΗ ΜΕ ΤΗΝ ΥΓΕΙΑ ΣΕ ΗΛΙΚΙΩΜΕΝΟΥΣ ΜΕ ΚΑΡΔΙΑΚΗ ΑΝΕΠΑΡΚΕΙΑ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή διατριβή ΟΙ ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΣΧΕΤΙΖΟΜΕΝΗ ΜΕ ΤΗΝ ΥΓΕΙΑ ΣΕ ΗΛΙΚΙΩΜΕΝΟΥΣ ΜΕ ΚΑΡΔΙΑΚΗ ΑΝΕΠΑΡΚΕΙΑ
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Φυσιολογία του καρδιαγγειακού συστήματος. Κλειώ Μαυραγάνη
 Φυσιολογία του καρδιαγγειακού συστήματος Κλειώ Μαυραγάνη Σύνοψη I. Γενικές αρχές καρδιαγγειακού συστήματος- Δομή και ρόλος II. III. IV. Προέλευση του καρδιακού ρυθμού και της ηλεκτρικής δραστηριότητας
Φυσιολογία του καρδιαγγειακού συστήματος Κλειώ Μαυραγάνη Σύνοψη I. Γενικές αρχές καρδιαγγειακού συστήματος- Δομή και ρόλος II. III. IV. Προέλευση του καρδιακού ρυθμού και της ηλεκτρικής δραστηριότητας
Διπλωματική Εργασία. Μελέτη των μηχανικών ιδιοτήτων των stents που χρησιμοποιούνται στην Ιατρική. Αντωνίου Φάνης
 Διπλωματική Εργασία Μελέτη των μηχανικών ιδιοτήτων των stents που χρησιμοποιούνται στην Ιατρική Αντωνίου Φάνης Επιβλέπουσες: Θεοδώρα Παπαδοπούλου, Ομότιμη Καθηγήτρια ΕΜΠ Ζάννη-Βλαστού Ρόζα, Καθηγήτρια
Διπλωματική Εργασία Μελέτη των μηχανικών ιδιοτήτων των stents που χρησιμοποιούνται στην Ιατρική Αντωνίου Φάνης Επιβλέπουσες: Θεοδώρα Παπαδοπούλου, Ομότιμη Καθηγήτρια ΕΜΠ Ζάννη-Βλαστού Ρόζα, Καθηγήτρια
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ. Πτυχιακή Εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή Εργασία ΣΥΜΠΛΗΡΩΜΑΤΙΚΕΣ ΚΑΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΘΕΡΑΠΕΙΕΣ ΩΣ ΠΡΟΣ ΤΗ ΔΙΑΧΕΙΡΙΣΗ ΤΟΥ ΠΟΝΟΥ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΚΑΡΚΙΝΟ. Ονοματεπώνυμο:
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή Εργασία ΣΥΜΠΛΗΡΩΜΑΤΙΚΕΣ ΚΑΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΘΕΡΑΠΕΙΕΣ ΩΣ ΠΡΟΣ ΤΗ ΔΙΑΧΕΙΡΙΣΗ ΤΟΥ ΠΟΝΟΥ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΚΑΡΚΙΝΟ. Ονοματεπώνυμο:
Βιοϊατρική τεχνολογία
 Τμήμα Μηχανικών Πληροφορικής & Τηλεπικοινωνιών Βιοϊατρική τεχνολογία Ενότητα 7: Φυσιολογία της καρδιάς Αν. καθηγητής Αγγελίδης Παντελής e-mail: paggelidis@uowm.gr ΕΕΔΙΠ Μπέλλου Σοφία e-mail: sbellou@uowm.gr
Τμήμα Μηχανικών Πληροφορικής & Τηλεπικοινωνιών Βιοϊατρική τεχνολογία Ενότητα 7: Φυσιολογία της καρδιάς Αν. καθηγητής Αγγελίδης Παντελής e-mail: paggelidis@uowm.gr ΕΕΔΙΠ Μπέλλου Σοφία e-mail: sbellou@uowm.gr
ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΑΞΙΟΛΟΓΗΣΗ ΑΠΟΔΟΣΗΣ ΠΡΟΣΩΠΙΚΟΥ: ΜΕΛΕΤΗ ΠΕΡΙΠΤΩΣΗΣ ΙΔΙΩΤΙΚΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΠΑΡΑΓΙΟΥΔΑΚΗ ΜΑΓΔΑΛΗΝΗ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ ΤΜΗΜΑ ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΑΞΙΟΛΟΓΗΣΗ ΑΠΟΔΟΣΗΣ ΠΡΟΣΩΠΙΚΟΥ: ΜΕΛΕΤΗ ΠΕΡΙΠΤΩΣΗΣ ΙΔΙΩΤΙΚΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΠΑΡΑΓΙΟΥΔΑΚΗ ΜΑΓΔΑΛΗΝΗ Διπλωματική
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ ΤΜΗΜΑ ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΑΞΙΟΛΟΓΗΣΗ ΑΠΟΔΟΣΗΣ ΠΡΟΣΩΠΙΚΟΥ: ΜΕΛΕΤΗ ΠΕΡΙΠΤΩΣΗΣ ΙΔΙΩΤΙΚΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΠΑΡΑΓΙΟΥΔΑΚΗ ΜΑΓΔΑΛΗΝΗ Διπλωματική
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Χαμηλά επίπεδα βιταμίνης D σχετιζόμενα με το βρογχικό άσθμα στα παιδιά και στους έφηβους Κουρομπίνα Αλεξάνδρα Λεμεσός [2014] i ΤΕΧΝΟΛΟΓΙΚΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Χαμηλά επίπεδα βιταμίνης D σχετιζόμενα με το βρογχικό άσθμα στα παιδιά και στους έφηβους Κουρομπίνα Αλεξάνδρα Λεμεσός [2014] i ΤΕΧΝΟΛΟΓΙΚΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή εργασία ΑΓΧΟΣ ΚΑΙ ΚΑΤΑΘΛΙΨΗ ΣΕ ΓΥΝΑΙΚΕΣ ΜΕ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΜΕΤΑ ΑΠΟ ΜΑΣΤΕΚΤΟΜΗ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΑΓΧΟΣ ΚΑΙ ΚΑΤΑΘΛΙΨΗ ΣΕ ΓΥΝΑΙΚΕΣ ΜΕ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΜΕΤΑ ΑΠΟ ΜΑΣΤΕΚΤΟΜΗ ΧΡΥΣΟΒΑΛΑΝΤΗΣ ΒΑΣΙΛΕΙΟΥ ΛΕΜΕΣΟΣ 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΑΓΧΟΣ ΚΑΙ ΚΑΤΑΘΛΙΨΗ ΣΕ ΓΥΝΑΙΚΕΣ ΜΕ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΜΕΤΑ ΑΠΟ ΜΑΣΤΕΚΤΟΜΗ ΧΡΥΣΟΒΑΛΑΝΤΗΣ ΒΑΣΙΛΕΙΟΥ ΛΕΜΕΣΟΣ 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ. Πτυχιακή εργασία ΟΛΙΣΘΗΡΟΤΗΤΑ ΚΑΙ ΜΑΚΡΟΥΦΗ ΤΩΝ ΟΔΟΔΤΡΩΜΑΤΩΝ ΚΥΚΛΟΦΟΡΙΑΣ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ Πτυχιακή εργασία ΟΛΙΣΘΗΡΟΤΗΤΑ ΚΑΙ ΜΑΚΡΟΥΦΗ ΤΩΝ ΟΔΟΔΤΡΩΜΑΤΩΝ ΚΥΚΛΟΦΟΡΙΑΣ Χριστοδούλου Αντρέας Λεμεσός 2014 2 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ Πτυχιακή εργασία ΟΛΙΣΘΗΡΟΤΗΤΑ ΚΑΙ ΜΑΚΡΟΥΦΗ ΤΩΝ ΟΔΟΔΤΡΩΜΑΤΩΝ ΚΥΚΛΟΦΟΡΙΑΣ Χριστοδούλου Αντρέας Λεμεσός 2014 2 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
Άσκηση και Καρδιοπάθειες
 Συμμαχία για την υγεία - Άσκηση Άσκηση και Καρδιοπάθειες Συγγραφική ομάδα: Φλουρής Ανδρέας, Ερευνητής Βογιατζής Ιωάννης, Αναπληρωτής Καθηγητής ΤΕΦΑΑ, ΕΚΠΑ Σταυρόπουλος- Καλίνογλου Αντώνης, Ερευνητής Σύγχρονες
Συμμαχία για την υγεία - Άσκηση Άσκηση και Καρδιοπάθειες Συγγραφική ομάδα: Φλουρής Ανδρέας, Ερευνητής Βογιατζής Ιωάννης, Αναπληρωτής Καθηγητής ΤΕΦΑΑ, ΕΚΠΑ Σταυρόπουλος- Καλίνογλου Αντώνης, Ερευνητής Σύγχρονες
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή Εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Γνώση και στάση νοσηλευτών στη διαχείριση του πόνου καρκινοπαθών που νοσηλεύονται Παναγιώτης Χαραλάμπους Λεμεσός, 2014 i ΤΕΧΝΟΛΟΓΙΚΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Γνώση και στάση νοσηλευτών στη διαχείριση του πόνου καρκινοπαθών που νοσηλεύονται Παναγιώτης Χαραλάμπους Λεμεσός, 2014 i ΤΕΧΝΟΛΟΓΙΚΟ
ΠΕΡΙΕΧΟΜΕΝΑ ΠΕΡΙΛΗΨΗ ΤΗΣ ΠΑΡΟΥΣΑΣ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ 1.2 ΕΙΣΑΓΩΓΗ ΣΤΑ ΒΙΟΥΛΙΚΑ ΤΙΤΑΝΙΟΥ-ΥΔΡΟΞΥΑΠΑΤΙΤΗ 3
 ΠΕΡΙΛΗΨΗ ΤΗΣ ΠΑΡΟΥΣΑΣ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΚΕΦΑΛΑΙΟ 1. ΒΙΒΛΙΟΓΡΑΦΙΚΗ ΑΝΑΣΚΟΠΗΣΗ 1.1 ΕΙΣΑΓΩΓΗ ΣΤΑ ΒΙΟΥΛΙΚΑ 1 1.2 ΕΙΣΑΓΩΓΗ ΣΤΑ ΒΙΟΥΛΙΚΑ ΤΙΤΑΝΙΟΥ-ΥΔΡΟΞΥΑΠΑΤΙΤΗ 3 1.3 ΤΟ ΤΙΤΑΝΙΟ ΣΤΗΝ ΚΑΤΑΣΚΕΥΗ ΒΙΟΥΛΙΚΩΝ
ΠΕΡΙΛΗΨΗ ΤΗΣ ΠΑΡΟΥΣΑΣ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΚΕΦΑΛΑΙΟ 1. ΒΙΒΛΙΟΓΡΑΦΙΚΗ ΑΝΑΣΚΟΠΗΣΗ 1.1 ΕΙΣΑΓΩΓΗ ΣΤΑ ΒΙΟΥΛΙΚΑ 1 1.2 ΕΙΣΑΓΩΓΗ ΣΤΑ ΒΙΟΥΛΙΚΑ ΤΙΤΑΝΙΟΥ-ΥΔΡΟΞΥΑΠΑΤΙΤΗ 3 1.3 ΤΟ ΤΙΤΑΝΙΟ ΣΤΗΝ ΚΑΤΑΣΚΕΥΗ ΒΙΟΥΛΙΚΩΝ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
ΕΡΓΑΣΙΑ ΣΤΗ ΒΙΟΛΟΓΙΑ. Μαθήτρια: Κ. Σοφία. Καθηγητής: κ. Πιτσιλαδής
 ΕΡΓΑΣΙΑ ΣΤΗ ΒΙΟΛΟΓΙΑ Μαθήτρια: Κ. Σοφία Καθηγητής: κ. Πιτσιλαδής Σχολ. Έτος: 2015-2016 ΑΓΓΕΙΟΠΛΑΣΤΙΚΗ-BYPASS Αορτοστεφανιαία παράκαμψη είναι η χειρουργική διαδικασία της παράκαμψης των θρομβώσεων ή των
ΕΡΓΑΣΙΑ ΣΤΗ ΒΙΟΛΟΓΙΑ Μαθήτρια: Κ. Σοφία Καθηγητής: κ. Πιτσιλαδής Σχολ. Έτος: 2015-2016 ΑΓΓΕΙΟΠΛΑΣΤΙΚΗ-BYPASS Αορτοστεφανιαία παράκαμψη είναι η χειρουργική διαδικασία της παράκαμψης των θρομβώσεων ή των
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΔΙΑΤΡΙΒΗ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΔΙΑΤΡΙΒΗ Ο ΠΡΟΩΡΟΣ ΤΟΚΕΤΟΣ ΚΑΙ Η ΣΥΣΧΕΤΙΣΗ ΤΟΥ ΜΕ ΤΟ ΣΥΝΔΡΟΜΟ ΑΝΑΠΝΕΥΣΤΙΚΗΣ ΔΥΣΧΕΡΕΙΑΣ Όνομα Φοιτήτριας: Χρυσοστομή Αγαθοκλέους Αριθμός φοιτητικής
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΔΙΑΤΡΙΒΗ Ο ΠΡΟΩΡΟΣ ΤΟΚΕΤΟΣ ΚΑΙ Η ΣΥΣΧΕΤΙΣΗ ΤΟΥ ΜΕ ΤΟ ΣΥΝΔΡΟΜΟ ΑΝΑΠΝΕΥΣΤΙΚΗΣ ΔΥΣΧΕΡΕΙΑΣ Όνομα Φοιτήτριας: Χρυσοστομή Αγαθοκλέους Αριθμός φοιτητικής
Εκτίµηση της στεφανιαίας µικροκυκλοφορίας µε διοισοφάγειο υπερηχοκαρδιογραφία Doppler στους διαβητικούς τύπου ΙΙ
 37 ο Πανελλήνιο Καρδιολογικό Συνέδριο Εκτίµηση της στεφανιαίας µικροκυκλοφορίας µε διοισοφάγειο υπερηχοκαρδιογραφία Doppler στους διαβητικούς τύπου ΙΙ Σ. Λαγουδάκου, Π. Δερµάτης, Μ. Μαριόλης, Γ. Αρµατάς,
37 ο Πανελλήνιο Καρδιολογικό Συνέδριο Εκτίµηση της στεφανιαίας µικροκυκλοφορίας µε διοισοφάγειο υπερηχοκαρδιογραφία Doppler στους διαβητικούς τύπου ΙΙ Σ. Λαγουδάκου, Π. Δερµάτης, Μ. Μαριόλης, Γ. Αρµατάς,
ΠΡΟΛΗΨΗ ΣΧΗΜΑΤΙΣΜΟΥ ΕΝΑΠΟΘΕΣΕΩΝ ΤΟΥ ΑΝΘΡΑΚΙΚΟΥ ΑΣΒΕΣΤΙΟΥ ΣΕ ΕΝΑΛΛΑΚΤΕΣ ΘΕΡΜΟΤΗΤΑΣ
 ΠΡΟΛΗΨΗ ΣΧΗΜΑΤΙΣΜΟΥ ΕΝΑΠΟΘΕΣΕΩΝ ΤΟΥ ΑΝΘΡΑΚΙΚΟΥ ΑΣΒΕΣΤΙΟΥ ΣΕ ΕΝΑΛΛΑΚΤΕΣ ΘΕΡΜΟΤΗΤΑΣ Π. Κλεπετσάνης 1,2, I. Xh. Malollari 3, M. Bakalli 3, E. Shehu 3, Π. Κουτσούκος 1,4 1. ΙΤΕ/ΕΙΧΗΜΥΘ, Τ.Θ. 1414, 26500 ΠΑΤΡΑ
ΠΡΟΛΗΨΗ ΣΧΗΜΑΤΙΣΜΟΥ ΕΝΑΠΟΘΕΣΕΩΝ ΤΟΥ ΑΝΘΡΑΚΙΚΟΥ ΑΣΒΕΣΤΙΟΥ ΣΕ ΕΝΑΛΛΑΚΤΕΣ ΘΕΡΜΟΤΗΤΑΣ Π. Κλεπετσάνης 1,2, I. Xh. Malollari 3, M. Bakalli 3, E. Shehu 3, Π. Κουτσούκος 1,4 1. ΙΤΕ/ΕΙΧΗΜΥΘ, Τ.Θ. 1414, 26500 ΠΑΤΡΑ
ΑΞΙΟΛΟΓΗΣΗ ΑΦΗΓΗΜΑΤΙΚΩΝ ΙΚΑΝΟΤΗΤΩΝ ΜΕΣΩ ΧΟΡΗΓΗΣΗΣ ΤΟΥ ΕΡΓΑΛΕΙΟΥ ΜΑΙΝ ΣΕ ΤΥΠΙΚΩΣ ΑΝΑΠΤΥΣΣΟΜΕΝΑ ΠΑΙΔΙΑ ΣΤΗΝ ΚΥΠΡΟ
 Σχολή Επιστημών Υγείας Πτυχιακή εργασία ΑΞΙΟΛΟΓΗΣΗ ΑΦΗΓΗΜΑΤΙΚΩΝ ΙΚΑΝΟΤΗΤΩΝ ΜΕΣΩ ΧΟΡΗΓΗΣΗΣ ΤΟΥ ΕΡΓΑΛΕΙΟΥ ΜΑΙΝ ΣΕ ΤΥΠΙΚΩΣ ΑΝΑΠΤΥΣΣΟΜΕΝΑ ΠΑΙΔΙΑ ΣΤΗΝ ΚΥΠΡΟ Γεωργίου Μύρια Λεμεσός, Μάιος 2018 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
Σχολή Επιστημών Υγείας Πτυχιακή εργασία ΑΞΙΟΛΟΓΗΣΗ ΑΦΗΓΗΜΑΤΙΚΩΝ ΙΚΑΝΟΤΗΤΩΝ ΜΕΣΩ ΧΟΡΗΓΗΣΗΣ ΤΟΥ ΕΡΓΑΛΕΙΟΥ ΜΑΙΝ ΣΕ ΤΥΠΙΚΩΣ ΑΝΑΠΤΥΣΣΟΜΕΝΑ ΠΑΙΔΙΑ ΣΤΗΝ ΚΥΠΡΟ Γεωργίου Μύρια Λεμεσός, Μάιος 2018 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΣΧΕΔΙΑΣΜΟΣ ΚΑΙ ΕΝΙΣΧΥΣΗ ΤΩΝ ΚΟΜΒΩΝ ΟΠΛΙΣΜΕΝΟΥ ΣΚΥΡΟΔΕΜΑΤΟΣ ΜΕ ΒΑΣΗ ΤΟΥΣ ΕΥΡΩΚΩΔΙΚΕΣ
 Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΣΧΕΔΙΑΣΜΟΣ ΚΑΙ ΕΝΙΣΧΥΣΗ ΤΩΝ ΚΟΜΒΩΝ ΟΠΛΙΣΜΕΝΟΥ ΣΚΥΡΟΔΕΜΑΤΟΣ ΜΕ ΒΑΣΗ ΤΟΥΣ ΕΥΡΩΚΩΔΙΚΕΣ Σωτήρης Παύλου Λεμεσός, Μάιος 2018 i ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΣΧΕΔΙΑΣΜΟΣ ΚΑΙ ΕΝΙΣΧΥΣΗ ΤΩΝ ΚΟΜΒΩΝ ΟΠΛΙΣΜΕΝΟΥ ΣΚΥΡΟΔΕΜΑΤΟΣ ΜΕ ΒΑΣΗ ΤΟΥΣ ΕΥΡΩΚΩΔΙΚΕΣ Σωτήρης Παύλου Λεμεσός, Μάιος 2018 i ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
ΑΝΑΠΤΥΞΗ ΤΟΥ ΠΤΥΧΙΑΚΗ. Λεμεσός
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΤΟ ΚΑΠΝΙΣΜΑ ΚΑΤΑ ΤΗΝ ΕΓΚΥΜΟΣΥΝΗ ΚΑΙ Η ΒΛΑΠΤΙΚΗ ΕΠΙΔΡΑ ΑΣΗ ΤΟΥ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΤΟΥ ΝΕΟΓΝΟΥ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Ονοματεπώνυμο Αγγελική Παπαπαύλου Αριθμός Φοιτητικής
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΤΟ ΚΑΠΝΙΣΜΑ ΚΑΤΑ ΤΗΝ ΕΓΚΥΜΟΣΥΝΗ ΚΑΙ Η ΒΛΑΠΤΙΚΗ ΕΠΙΔΡΑ ΑΣΗ ΤΟΥ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΤΟΥ ΝΕΟΓΝΟΥ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Ονοματεπώνυμο Αγγελική Παπαπαύλου Αριθμός Φοιτητικής
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ.
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ Φίλιππος Λουκά Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΗΣ ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ Φίλιππος Λουκά Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΣΥΓΚΡΙΣΗ ΥΔΡΟΠΟΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΣΕ ΚΑΛΛΙΕΡΓΕΙΑ ΜΑΡΟΥΛΙΟΥ Νικόλας Χαραλάμπους Λεμεσός 2015 ΤΕΧΝΟΛΟΓΙΚΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΣΥΓΚΡΙΣΗ ΥΔΡΟΠΟΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΣΕ ΚΑΛΛΙΕΡΓΕΙΑ ΜΑΡΟΥΛΙΟΥ Νικόλας Χαραλάμπους Λεμεσός 2015 ΤΕΧΝΟΛΟΓΙΚΟ
ΣYΓΓΕΝΕΙΣ ΑΝΑΤΟΜΙΚΕΣ ΑΝΩΜΑΛΙΕΣ ΤΗΣ ΚΑΡΔΙΑΣ
 ΣYΓΓΕΝΕΙΣ ΑΝΑΤΟΜΙΚΕΣ ΑΝΩΜΑΛΙΕΣ ΤΗΣ ΚΑΡΔΙΑΣ Παραμένων αρτηριακός (Βοτάλλειος) πόρος Ο αρτηριακός πόρος, μεταξύ της αορτής και της πνευμονικής αρτηρίας, επιτρέπει στο αίμα να παρακάμπτει τους πνεύμονες κατά
ΣYΓΓΕΝΕΙΣ ΑΝΑΤΟΜΙΚΕΣ ΑΝΩΜΑΛΙΕΣ ΤΗΣ ΚΑΡΔΙΑΣ Παραμένων αρτηριακός (Βοτάλλειος) πόρος Ο αρτηριακός πόρος, μεταξύ της αορτής και της πνευμονικής αρτηρίας, επιτρέπει στο αίμα να παρακάμπτει τους πνεύμονες κατά
ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ. «ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΑΞΙΟΛΟΓΗΣΗ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΝΟΣΟΚΟΜΕΙΑΚΟΥ ΠΡΟΣΩΠΙΚΟΥ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ ΤΜΗΜΑ ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΑΞΙΟΛΟΓΗΣΗ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΝΟΣΟΚΟΜΕΙΑΚΟΥ ΠΡΟΣΩΠΙΚΟΥ Μαστρογιάννη Μαρία Διπλωματική Εργασία υποβληθείσα
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΕΙΡΑΙΩΣ ΤΜΗΜΑ ΟΙΚΟΝΟΜΙΚΗΣ ΕΠΙΣΤΗΜΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΔΙΟΙΚΗΣΗ της ΥΓΕΙΑΣ» ΑΞΙΟΛΟΓΗΣΗ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΝΟΣΟΚΟΜΕΙΑΚΟΥ ΠΡΟΣΩΠΙΚΟΥ Μαστρογιάννη Μαρία Διπλωματική Εργασία υποβληθείσα
ΠΑΡΑΣΚΕΥΗ ΝΑΝΟΣΥΝΘΕΤΩΝ ΒΙΟΔΡΑΣΤΙΚΟΥ ΓΥΑΛΙΟΥ/ΠΟΛΥ(D,L-ΓΑΛΑΚΤΙΚΟΥ ΟΞΕΟΣ) ΚΑΙ IN- VITRO ΜΕΛΕΤΗ ΤΗΣ ΒΙΟΣΥΜΒΑΤΟΤΗΤΑΣ
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ IV: ΣΥΝΘΕΣΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΒΙΟΜΗΧΑΝΙΚΩΝ ΔΙΑΔΙΚΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΠΟΛΥΜΕΡΩΝ Διπλωματική Εργασία ΠΑΡΑΣΚΕΥΗ ΝΑΝΟΣΥΝΘΕΤΩΝ ΒΙΟΔΡΑΣΤΙΚΟΥ ΓΥΑΛΙΟΥ/ΠΟΛΥ(D,L-ΓΑΛΑΚΤΙΚΟΥ
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ IV: ΣΥΝΘΕΣΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΒΙΟΜΗΧΑΝΙΚΩΝ ΔΙΑΔΙΚΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΠΟΛΥΜΕΡΩΝ Διπλωματική Εργασία ΠΑΡΑΣΚΕΥΗ ΝΑΝΟΣΥΝΘΕΤΩΝ ΒΙΟΔΡΑΣΤΙΚΟΥ ΓΥΑΛΙΟΥ/ΠΟΛΥ(D,L-ΓΑΛΑΚΤΙΚΟΥ
ΒΕΛΤΙΩΣΗ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΟΥ ΕΛΕΓΧΟΥ ΠΟΙΟΤΗΤΑΣ ΚΑΙ ΕΦΑΡΜΟΓΗ ΕΡΓΑΛΕΙΩΝ ΔΙΑΣΦΑΛΙΣΗΣ ΠΟΙΟΤΗΤΑΣ ΣΕ ΜΕΤΑΛΛΟΒΙΟΜΗΧΑΝΙΑ
 Σχολή Mηχανικής και Τεχνολογίας Πτυχιακή εργασία ΒΕΛΤΙΩΣΗ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΟΥ ΕΛΕΓΧΟΥ ΠΟΙΟΤΗΤΑΣ ΚΑΙ ΕΦΑΡΜΟΓΗ ΕΡΓΑΛΕΙΩΝ ΔΙΑΣΦΑΛΙΣΗΣ ΠΟΙΟΤΗΤΑΣ ΣΕ ΜΕΤΑΛΛΟΒΙΟΜΗΧΑΝΙΑ Στέλιος Καράσαββας Λεμεσός, Μάιος 2017
Σχολή Mηχανικής και Τεχνολογίας Πτυχιακή εργασία ΒΕΛΤΙΩΣΗ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΟΥ ΕΛΕΓΧΟΥ ΠΟΙΟΤΗΤΑΣ ΚΑΙ ΕΦΑΡΜΟΓΗ ΕΡΓΑΛΕΙΩΝ ΔΙΑΣΦΑΛΙΣΗΣ ΠΟΙΟΤΗΤΑΣ ΣΕ ΜΕΤΑΛΛΟΒΙΟΜΗΧΑΝΙΑ Στέλιος Καράσαββας Λεμεσός, Μάιος 2017
ΜΟΝΤΕΛΟΠΟΙΗΣΗ ΤΩΝ ΦΑΙΝΟΜΕΝΩΝ ΡΟΗΣ, ΜΕΤΑΦΟΡΑΣ ΚΑΙ ΕΛΕΓΧΟΜΕΝΗΣ ΚΑΤΑΒΥΘΙΣΗΣ ΚΑΤΑ ΤΗΝ ΑΝΑΜΕΙΞΗ ΑΛΑΤΟΥΧΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΕ ΔΙΚΤΥΑ ΠΟΡΩΝ ΣΥΝΘΕΤΗΣ ΓΕΩΜΕΤΡΙΑΣ
 10 ο ΠΑΝΕΛΛΗΝΙΟ ΕΠΙΣΤΗΜΟΝΙΚΟ ΣΥΝΕΔΡΙΟ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ, ΠΑΤΡΑ, 4-6 ΙΟΥΝΙΟΥ, 2015. ΜΟΝΤΕΛΟΠΟΙΗΣΗ ΤΩΝ ΦΑΙΝΟΜΕΝΩΝ ΡΟΗΣ, ΜΕΤΑΦΟΡΑΣ ΚΑΙ ΕΛΕΓΧΟΜΕΝΗΣ ΚΑΤΑΒΥΘΙΣΗΣ ΚΑΤΑ ΤΗΝ ΑΝΑΜΕΙΞΗ ΑΛΑΤΟΥΧΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΕ ΔΙΚΤΥΑ
10 ο ΠΑΝΕΛΛΗΝΙΟ ΕΠΙΣΤΗΜΟΝΙΚΟ ΣΥΝΕΔΡΙΟ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ, ΠΑΤΡΑ, 4-6 ΙΟΥΝΙΟΥ, 2015. ΜΟΝΤΕΛΟΠΟΙΗΣΗ ΤΩΝ ΦΑΙΝΟΜΕΝΩΝ ΡΟΗΣ, ΜΕΤΑΦΟΡΑΣ ΚΑΙ ΕΛΕΓΧΟΜΕΝΗΣ ΚΑΤΑΒΥΘΙΣΗΣ ΚΑΤΑ ΤΗΝ ΑΝΑΜΕΙΞΗ ΑΛΑΤΟΥΧΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΕ ΔΙΚΤΥΑ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ. Πτυχιακή εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ Πτυχιακή εργασία ΥΠΟΛΟΓΙΣΤΙΚΗ ΡΕΥΣΤΟΔΥΝΑΜΙΚΗ ΜΕΛΕΤΗ ΤΟΥ ΣΗΜΕΙΟΥ ΠΡΟΣΒΑΣΗΣ ΑΡΤΗΡΙΟΦΛΕΒΙΚΟΥ ΜΟΣΧΕΥΜΑΤΟΣ ΣΕ ΑΙΜΟΚΑΘΑΙΡΟΜΕΝΟΥΣ ΑΣΘΕΝΕΙΣ Παντελάκης
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ Πτυχιακή εργασία ΥΠΟΛΟΓΙΣΤΙΚΗ ΡΕΥΣΤΟΔΥΝΑΜΙΚΗ ΜΕΛΕΤΗ ΤΟΥ ΣΗΜΕΙΟΥ ΠΡΟΣΒΑΣΗΣ ΑΡΤΗΡΙΟΦΛΕΒΙΚΟΥ ΜΟΣΧΕΥΜΑΤΟΣ ΣΕ ΑΙΜΟΚΑΘΑΙΡΟΜΕΝΟΥΣ ΑΣΘΕΝΕΙΣ Παντελάκης
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή διατριβή. Ονοματεπώνυμο: Αργυρώ Ιωάννου. Επιβλέπων καθηγητής: Δρ. Αντρέας Χαραλάμπους
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή διατριβή Διερεύνηση της αποτελεσματικότητας εναλλακτικών και συμπληρωματικών τεχνικών στη βελτίωση της ποιότητας της ζωής σε άτομα με καρκίνο
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή διατριβή Διερεύνηση της αποτελεσματικότητας εναλλακτικών και συμπληρωματικών τεχνικών στη βελτίωση της ποιότητας της ζωής σε άτομα με καρκίνο
ΙΑΤΡΙΚΗ ΑΠΕΙΚΟΝΙΣΗ ΥΠΕΡΗΧΟΓΡΑΦΙΑ
 ΙΑΤΡΙΚΗ ΑΠΕΙΚΟΝΙΣΗ ΥΠΕΡΗΧΟΓΡΑΦΙΑ Κλινικές εφαρμογές 4 Αιμοδυναμική μελέτη Doppler 1. Αγγεία κοιλιάς 2. Περιφερικά αγγεία Κ. Χατζημιχαήλ Υπερηχοτομογραφία Μορφολογική μελέτη Αιμοδυναμική μελέτη Doppler
ΙΑΤΡΙΚΗ ΑΠΕΙΚΟΝΙΣΗ ΥΠΕΡΗΧΟΓΡΑΦΙΑ Κλινικές εφαρμογές 4 Αιμοδυναμική μελέτη Doppler 1. Αγγεία κοιλιάς 2. Περιφερικά αγγεία Κ. Χατζημιχαήλ Υπερηχοτομογραφία Μορφολογική μελέτη Αιμοδυναμική μελέτη Doppler
ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ. Λουκία Βασιλείου
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΠΑΙΔΙΚΗ ΚΑΙ ΕΦΗΒΙΚΗ ΚΑΚΟΠΟΙΗΣΗ: ΕΠΙΠΤΩΣΕΙΣ ΣΤΗΝ ΥΓΕΙΑ Λουκία Βασιλείου 2010646298 Επιβλέπουσα καθηγήτρια: Δρ.
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΠΑΙΔΙΚΗ ΚΑΙ ΕΦΗΒΙΚΗ ΚΑΚΟΠΟΙΗΣΗ: ΕΠΙΠΤΩΣΕΙΣ ΣΤΗΝ ΥΓΕΙΑ Λουκία Βασιλείου 2010646298 Επιβλέπουσα καθηγήτρια: Δρ.
ΣΤΙΓΜΙΑΙΑ ΚΑΤΑΣΚΕΥΗ ΣΤΕΡΕΟΥ ΜΕΙΓΜΑΤΟΣ ΥΛΙΚΟΥ ΜΕΣΑ ΑΠΟ ΕΛΕΓΧΟΜΕΝΗ ΦΥΣΙΚΗ ΔΙΑΔΙΚΑΣΙΑ
 Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΣΤΙΓΜΙΑΙΑ ΚΑΤΑΣΚΕΥΗ ΣΤΕΡΕΟΥ ΜΕΙΓΜΑΤΟΣ ΥΛΙΚΟΥ ΜΕΣΑ ΑΠΟ ΕΛΕΓΧΟΜΕΝΗ ΦΥΣΙΚΗ ΔΙΑΔΙΚΑΣΙΑ Χριστόδουλος Χριστοδούλου Λεμεσός, Μάϊος 2017 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΣΤΙΓΜΙΑΙΑ ΚΑΤΑΣΚΕΥΗ ΣΤΕΡΕΟΥ ΜΕΙΓΜΑΤΟΣ ΥΛΙΚΟΥ ΜΕΣΑ ΑΠΟ ΕΛΕΓΧΟΜΕΝΗ ΦΥΣΙΚΗ ΔΙΑΔΙΚΑΣΙΑ Χριστόδουλος Χριστοδούλου Λεμεσός, Μάϊος 2017 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΠΡΟΣΤΑΣΙΑ ΑΤΜΟΣΦΑΙΡΙΚΗΣ ΔΙΑΒΡΩΣΗΣ ΑΛΟΥΜΙΝΙΟΥ/ΑΝΟΔΙΩΣΗ Al
 Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΠΡΟΣΤΑΣΙΑ ΑΤΜΟΣΦΑΙΡΙΚΗΣ ΔΙΑΒΡΩΣΗΣ ΑΛΟΥΜΙΝΙΟΥ/ΑΝΟΔΙΩΣΗ Al Ανδρέας Παπαχριστοδούλου Λεμεσός, Μάιος 2017 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ
Σχολή Μηχανικής και Τεχνολογίας Πτυχιακή εργασία ΠΡΟΣΤΑΣΙΑ ΑΤΜΟΣΦΑΙΡΙΚΗΣ ΔΙΑΒΡΩΣΗΣ ΑΛΟΥΜΙΝΙΟΥ/ΑΝΟΔΙΩΣΗ Al Ανδρέας Παπαχριστοδούλου Λεμεσός, Μάιος 2017 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΗΣ ΚΑΙ
Γ. Χ. Μπομπότης 1, Ι. Π. Λαζαρίδης 2, Η. Ι. Καπιτσίνης 1, Α. Θ. Παπαδόπουλος 1, Π. Γ. Δοκόπουλος 1, Α. Ι. Καρακάνας 1, Ι.Γ. Στυλιάδης 1 1.
 Γ. Χ. Μπομπότης 1, Ι. Π. Λαζαρίδης 2, Η. Ι. Καπιτσίνης 1, Α. Θ. Παπαδόπουλος 1, Π. Γ. Δοκόπουλος 1, Α. Ι. Καρακάνας 1, Ι.Γ. Στυλιάδης 1 1. Β ΚΑΡΔΙΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ Γ.Ν. «ΠΑΠΑΓΕΩΡΓΙΟΥ» 2. Α Πανεπιστημιακή
Γ. Χ. Μπομπότης 1, Ι. Π. Λαζαρίδης 2, Η. Ι. Καπιτσίνης 1, Α. Θ. Παπαδόπουλος 1, Π. Γ. Δοκόπουλος 1, Α. Ι. Καρακάνας 1, Ι.Γ. Στυλιάδης 1 1. Β ΚΑΡΔΙΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ Γ.Ν. «ΠΑΠΑΓΕΩΡΓΙΟΥ» 2. Α Πανεπιστημιακή
ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ
 ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ Ηλεκτροκαρδιογράφηµα Ι. ΑΡΤΗΡΙΑΚΗ ΠΙΕΣΗ Η πίεση στην αορτή, στην αρτηρία του βραχίονα και σε άλλες µεγάλες αρτηρίες σ' ένα ενήλικο άτοµο µεταβάλλεται από 120 mmhg (συστολική
ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ Ηλεκτροκαρδιογράφηµα Ι. ΑΡΤΗΡΙΑΚΗ ΠΙΕΣΗ Η πίεση στην αορτή, στην αρτηρία του βραχίονα και σε άλλες µεγάλες αρτηρίες σ' ένα ενήλικο άτοµο µεταβάλλεται από 120 mmhg (συστολική
ΜΕΤΑΤΡΟΠΗ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΜΕΘΑΝΙΟ ΜΕ ΤΗ ΧΡΗΣΗ ΑΠΟΒΛΗΤΩΝ ΣΙΔΗΡΟΥ ΚΑΙ ΑΝΑΕΡΟΒΙΑΣ ΛΑΣΠΗΣ
 Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Μεταπτυχιακή διατριβή ΜΕΤΑΤΡΟΠΗ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΜΕΘΑΝΙΟ ΜΕ ΤΗ ΧΡΗΣΗ ΑΠΟΒΛΗΤΩΝ ΣΙΔΗΡΟΥ ΚΑΙ ΑΝΑΕΡΟΒΙΑΣ ΛΑΣΠΗΣ Κρίστια Καρολίνα Μενοικέα
Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Μεταπτυχιακή διατριβή ΜΕΤΑΤΡΟΠΗ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΜΕΘΑΝΙΟ ΜΕ ΤΗ ΧΡΗΣΗ ΑΠΟΒΛΗΤΩΝ ΣΙΔΗΡΟΥ ΚΑΙ ΑΝΑΕΡΟΒΙΑΣ ΛΑΣΠΗΣ Κρίστια Καρολίνα Μενοικέα
Μπούντας Ιωάννης Πανεπιστήμιο Πατρών Τμήμα Χημικών Μηχανικών και ITE/IΕXΜΗ jmpountas@chemeng.upatras.gr
 Ανάκτηση φωσφορικών από αστικά λύματα με τη μορφή MgNH 4 PO 4.6H 2 O (στρουβίτη) Μπούντας Ιωάννης Πανεπιστήμιο Πατρών Τμήμα Χημικών Μηχανικών και ITE/IΕXΜΗ jmpountas@chemeng.upatras.gr Πανεπιστήμιο Πατρών
Ανάκτηση φωσφορικών από αστικά λύματα με τη μορφή MgNH 4 PO 4.6H 2 O (στρουβίτη) Μπούντας Ιωάννης Πανεπιστήμιο Πατρών Τμήμα Χημικών Μηχανικών και ITE/IΕXΜΗ jmpountas@chemeng.upatras.gr Πανεπιστήμιο Πατρών
Η πρόληψη των κατακλίσεων σε βαριά πάσχοντες και η χρήση ειδικών στρωμάτων για την πρόληψη και αντιμετώπιση των κατακλίσεων
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Η πρόληψη των κατακλίσεων σε βαριά πάσχοντες και η χρήση ειδικών στρωμάτων για την πρόληψη και αντιμετώπιση των κατακλίσεων Ονοματεπώνυμο
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Η πρόληψη των κατακλίσεων σε βαριά πάσχοντες και η χρήση ειδικών στρωμάτων για την πρόληψη και αντιμετώπιση των κατακλίσεων Ονοματεπώνυμο
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή εργασία Η ΚΑΤΑΘΛΙΨΗ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 1
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία Η ΚΑΤΑΘΛΙΨΗ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 1 ΑΝΔΡΕΑΣ ΑΝΔΡΕΟΥ Φ.Τ:2008670839 Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία Η ΚΑΤΑΘΛΙΨΗ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 1 ΑΝΔΡΕΑΣ ΑΝΔΡΕΟΥ Φ.Τ:2008670839 Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή Εργασία ΕΠΙΛΟΧΕΙΑ ΚΑΤΑΘΛΙΨΗ: Ο ΡΟΛΟΣ ΤΗΣ ΚΑΤ ΟΙΚΟΝ ΝΟΣΗΛΕΙΑΣ. Φοινίκη Αλεξάνδρου
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία ΕΠΙΛΟΧΕΙΑ ΚΑΤΑΘΛΙΨΗ: Ο ΡΟΛΟΣ ΤΗΣ ΚΑΤ ΟΙΚΟΝ ΝΟΣΗΛΕΙΑΣ Φοινίκη Αλεξάνδρου Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΕΠΙΣΤΗΜΩΝ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία ΕΠΙΛΟΧΕΙΑ ΚΑΤΑΘΛΙΨΗ: Ο ΡΟΛΟΣ ΤΗΣ ΚΑΤ ΟΙΚΟΝ ΝΟΣΗΛΕΙΑΣ Φοινίκη Αλεξάνδρου Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΕΠΙΣΤΗΜΩΝ
Μεταπτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΕΚΛΕΚΤΙΚΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΟΞΕΙΔΩΣΗΣ ΤΟΥ ΜΕΘΑΝΙΟΥ ΠΡΟΣ ΔΙΟΞΕΙΔΙΟ ΤΟΥ ΑΝΘΡΑΚΑ Βασιλική
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΕΚΛΕΚΤΙΚΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΟΞΕΙΔΩΣΗΣ ΤΟΥ ΜΕΘΑΝΙΟΥ ΠΡΟΣ ΔΙΟΞΕΙΔΙΟ ΤΟΥ ΑΝΘΡΑΚΑ Βασιλική
Ο νοσηλευτικός ρόλος στην πρόληψη του μελανώματος
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή διατριβή Ο νοσηλευτικός ρόλος στην πρόληψη του μελανώματος Ονοματεπώνυμο: Αρτέμης Παναγιώτου Επιβλέπων καθηγητής: Δρ. Αντρέας Χαραλάμπους
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή διατριβή Ο νοσηλευτικός ρόλος στην πρόληψη του μελανώματος Ονοματεπώνυμο: Αρτέμης Παναγιώτου Επιβλέπων καθηγητής: Δρ. Αντρέας Χαραλάμπους
ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΛΕΠΤΩΝ ΥΜΕΝΙΩΝ ΥΔΡΟΓΟΝΩΜΕΝΟΥ ΠΥΡΙΤΙΟΥ (Si:H) ΜΕ ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΥΠΕΡΙΩΔΟΥΣ ΟΡΑΤΟΥ (UV/VIS)
 ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΛΕΠΤΩΝ ΥΜΕΝΙΩΝ ΥΔΡΟΓΟΝΩΜΕΝΟΥ ΠΥΡΙΤΙΟΥ (Si:H) ΜΕ ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΥΠΕΡΙΩΔΟΥΣ ΟΡΑΤΟΥ (UV/VIS) Γ. Αλεξίου, Β. Περδικάρη, Π. Δημητρακέλλης, Ε. Φάρσαρη, Α. Καλαμπούνιας, Ε.Αμανατίδης και Δ.Ματαράς
ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΛΕΠΤΩΝ ΥΜΕΝΙΩΝ ΥΔΡΟΓΟΝΩΜΕΝΟΥ ΠΥΡΙΤΙΟΥ (Si:H) ΜΕ ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΥΠΕΡΙΩΔΟΥΣ ΟΡΑΤΟΥ (UV/VIS) Γ. Αλεξίου, Β. Περδικάρη, Π. Δημητρακέλλης, Ε. Φάρσαρη, Α. Καλαμπούνιας, Ε.Αμανατίδης και Δ.Ματαράς
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΕΠΙΔΡΑΣΗ ΥΠΕΡΗΧΩΝ ΣΤΗΝ LISTERIA GRAYI ΣΤΟ ΓΑΛΑ: ΕΠΙΒΙΩΣΗ ΚΑΙ ΦΥΣΙΚΟΧΗΜΙΚΕΣ ΕΠΙΔΡΑΣΕΙΣ. Άρτεμις
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΕΠΙΔΡΑΣΗ ΥΠΕΡΗΧΩΝ ΣΤΗΝ LISTERIA GRAYI ΣΤΟ ΓΑΛΑ: ΕΠΙΒΙΩΣΗ ΚΑΙ ΦΥΣΙΚΟΧΗΜΙΚΕΣ ΕΠΙΔΡΑΣΕΙΣ. Άρτεμις
ΓΕΩΡΓΟΥ ΠΑΝΑΓΙΩΤΑ ΧΑΡΔΑΒΕΛΑ ΜΑΓΔΑΛΗΝΗ
 ΑΝΟΙΚΤΟΣ ΑΡΤΗΡΙΑΚΟΣ ΠΟΡΟΣ ΣΕ ΝΕΟΓΝΑ ΓΕΩΡΓΟΥ ΠΑΝΑΓΙΩΤΑ ΧΑΡΔΑΒΕΛΑ ΜΑΓΔΑΛΗΝΗ Συγγενείς ανωμαλίες της καρδιάς, είναι οι ατέλειες στη δομή της καρδιάς, που είναι παρούσες κατά τη γέννηση. Μια από αυτές είναι
ΑΝΟΙΚΤΟΣ ΑΡΤΗΡΙΑΚΟΣ ΠΟΡΟΣ ΣΕ ΝΕΟΓΝΑ ΓΕΩΡΓΟΥ ΠΑΝΑΓΙΩΤΑ ΧΑΡΔΑΒΕΛΑ ΜΑΓΔΑΛΗΝΗ Συγγενείς ανωμαλίες της καρδιάς, είναι οι ατέλειες στη δομή της καρδιάς, που είναι παρούσες κατά τη γέννηση. Μια από αυτές είναι
ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ
 ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ Η αξιοποίηση της γεωθερμικής ενέργειας συναντά ορισμένα τεχνικά προβλήματα, Τα προβλήματα αυτά είναι: (α) ο σχηματισμός επικαθίσεων (ή καθαλατώσεις
ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ Η αξιοποίηση της γεωθερμικής ενέργειας συναντά ορισμένα τεχνικά προβλήματα, Τα προβλήματα αυτά είναι: (α) ο σχηματισμός επικαθίσεων (ή καθαλατώσεις
Στρογγυλό τραπέζι: βαλβιδοπάθειες Παρουσίαση περιστατικού Πολυβαλβιδοπάθεια. 15 ο Συνέδριο New Trends in Cardiology Θεσσαλονίκη, Απριλίου 2015
 Στρογγυλό τραπέζι: βαλβιδοπάθειες Παρουσίαση περιστατικού Πολυβαλβιδοπάθεια 15 ο Συνέδριο New Trends in Cardiology Θεσσαλονίκη, 17-18 Απριλίου 2015 Νικόλαος Β.Κωνσταντινίδης 1 η Καρδιολογική Κλινική, Πανεπιστημιακό
Στρογγυλό τραπέζι: βαλβιδοπάθειες Παρουσίαση περιστατικού Πολυβαλβιδοπάθεια 15 ο Συνέδριο New Trends in Cardiology Θεσσαλονίκη, 17-18 Απριλίου 2015 Νικόλαος Β.Κωνσταντινίδης 1 η Καρδιολογική Κλινική, Πανεπιστημιακό
Πτυχιακή εργασία Ο ΡΟΛΟΣ ΤΩΝ ΚΟΙΝΟΤΙΚΩΝ ΝΟΣΗΛΕΥΤΩΝ ΣΤΗ ΔΙΔΑΣΚΑΛΙΑ ΤΟΥ ΠΑΙΔΙΟΥ ΜΕ ΧΡΟΝΙΟ ΑΣΘΜΑ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή εργασία Ο ΡΟΛΟΣ ΤΩΝ ΚΟΙΝΟΤΙΚΩΝ ΝΟΣΗΛΕΥΤΩΝ ΣΤΗ ΔΙΔΑΣΚΑΛΙΑ ΤΟΥ ΠΑΙΔΙΟΥ ΜΕ ΧΡΟΝΙΟ ΑΣΘΜΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΚΥΡΙΑΚΟΣ ΛΟΙΖΟΥ ΑΡΙΘΜΟΣ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή εργασία Ο ΡΟΛΟΣ ΤΩΝ ΚΟΙΝΟΤΙΚΩΝ ΝΟΣΗΛΕΥΤΩΝ ΣΤΗ ΔΙΔΑΣΚΑΛΙΑ ΤΟΥ ΠΑΙΔΙΟΥ ΜΕ ΧΡΟΝΙΟ ΑΣΘΜΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΚΥΡΙΑΚΟΣ ΛΟΙΖΟΥ ΑΡΙΘΜΟΣ
ΔΗΜΗΤΡΙΟΣ Γ. ΚΕΤΙΚΟΓΛΟΥ MD PhD FESC ΚΑΡΔΙΟΛΟΓΟΣ ΔΙΔΑΚΤΩΡ Α.Π.Θ. Δ/ΝΤΗΣ ΣΤΕΦΑΝΙΑΙΑΣ ΜΟΝΑΔΑΣ ΚΑΙ ΗΧΩΚΑΡΔΙΟΓΡΑΦΙΑΣ ΙΑΤΡΙΚΟ ΔΙΑΒΑΛΚΑΝΙΚΟ ΚΕΝΤΡΟ
 ΔΗΜΗΤΡΙΟΣ Γ. ΚΕΤΙΚΟΓΛΟΥ MD PhD FESC ΚΑΡΔΙΟΛΟΓΟΣ ΔΙΔΑΚΤΩΡ Α.Π.Θ. Δ/ΝΤΗΣ ΣΤΕΦΑΝΙΑΙΑΣ ΜΟΝΑΔΑΣ ΚΑΙ ΗΧΩΚΑΡΔΙΟΓΡΑΦΙΑΣ ΙΑΤΡΙΚΟ ΔΙΑΒΑΛΚΑΝΙΚΟ ΚΕΝΤΡΟ ΘΕΣΣΑΛΟΝΙΚΗ 2016 DECLARATION OF INTEREST NONE (Not disclosures)
ΔΗΜΗΤΡΙΟΣ Γ. ΚΕΤΙΚΟΓΛΟΥ MD PhD FESC ΚΑΡΔΙΟΛΟΓΟΣ ΔΙΔΑΚΤΩΡ Α.Π.Θ. Δ/ΝΤΗΣ ΣΤΕΦΑΝΙΑΙΑΣ ΜΟΝΑΔΑΣ ΚΑΙ ΗΧΩΚΑΡΔΙΟΓΡΑΦΙΑΣ ΙΑΤΡΙΚΟ ΔΙΑΒΑΛΚΑΝΙΚΟ ΚΕΝΤΡΟ ΘΕΣΣΑΛΟΝΙΚΗ 2016 DECLARATION OF INTEREST NONE (Not disclosures)
ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΜΗΤΡΙΚΟΣ ΘΗΛΑΣΜΟΣ ΚΑΙ ΠΑΙΔΙΚΗ ΠΑΧΥΣΑΡΚΙΑ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΜΗΤΡΙΚΟΣ ΘΗΛΑΣΜΟΣ ΚΑΙ ΠΑΙΔΙΚΗ ΠΑΧΥΣΑΡΚΙΑ Ονοματεπώνυμο: Μιχαέλλα Σάββα Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΜΗΤΡΙΚΟΣ ΘΗΛΑΣΜΟΣ ΚΑΙ ΠΑΙΔΙΚΗ ΠΑΧΥΣΑΡΚΙΑ Ονοματεπώνυμο: Μιχαέλλα Σάββα Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ
1. ΠΡΟΕΛΕΥΣΗ ΚΟΚΚΩΝ ΑΝΘΡΑΚΙΚΟΥ ΑΣΒΕΣΤΙΟΥ 2. ΓΕΩΧΗΜΕΙΑ ΘΑΛΑΣΣΙΟΥ ΝΕΡΟΥ 3. ΚΥΡΙΑ ΑΝΘΡΑΚΙΚΑ ΟΡΥΚΤΑ 4. ΠΡΩΤΟΓΕΝΗΣ ΚΑΘΙΖΗΣΗ 5.
 1. ΠΡΟΕΛΕΥΣΗ ΚΟΚΚΩΝ ΑΝΘΡΑΚΙΚΟΥ ΑΣΒΕΣΤΙΟΥ 2. ΓΕΩΧΗΜΕΙΑ ΘΑΛΑΣΣΙΟΥ ΝΕΡΟΥ 3. ΚΥΡΙΑ ΑΝΘΡΑΚΙΚΑ ΟΡΥΚΤΑ 4. ΠΡΩΤΟΓΕΝΗΣ ΚΑΘΙΖΗΣΗ 5. ΒΙΟΓΕΝΗΣ ΚΑΘΙΖΗΣΗ 1 Σχηματισμός μέσα σε λεκάνες απόθεσης κυρίως στη θάλασσα Θαλάσσια
1. ΠΡΟΕΛΕΥΣΗ ΚΟΚΚΩΝ ΑΝΘΡΑΚΙΚΟΥ ΑΣΒΕΣΤΙΟΥ 2. ΓΕΩΧΗΜΕΙΑ ΘΑΛΑΣΣΙΟΥ ΝΕΡΟΥ 3. ΚΥΡΙΑ ΑΝΘΡΑΚΙΚΑ ΟΡΥΚΤΑ 4. ΠΡΩΤΟΓΕΝΗΣ ΚΑΘΙΖΗΣΗ 5. ΒΙΟΓΕΝΗΣ ΚΑΘΙΖΗΣΗ 1 Σχηματισμός μέσα σε λεκάνες απόθεσης κυρίως στη θάλασσα Θαλάσσια
Πτυχιακή Εργασία Η ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΤΩΝ ΑΣΘΕΝΩΝ ΜΕ ΣΤΗΘΑΓΧΗ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Η ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΤΩΝ ΑΣΘΕΝΩΝ ΜΕ ΣΤΗΘΑΓΧΗ Νικόλας Χριστοδούλου Λευκωσία, 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή Εργασία Η ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΤΩΝ ΑΣΘΕΝΩΝ ΜΕ ΣΤΗΘΑΓΧΗ Νικόλας Χριστοδούλου Λευκωσία, 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ
ΤΑΞΗ: B ΓΥΜΝΑΣΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: ΟΝΟΜΑΤΕΠΩΝΥΜΟ:. ΤΜΗΜΑ: ΑΡ. Να προσέξετε την εμφάνιση του γραπτού σας και να γράψετε με μελάνι μπλε ή μαύρο.
 Β ΠΕΡΙΦΕΡΕΙΑΚΟ ΓΥΜΝΑΣΙΟ ΛΕΥΚΩΣΙΑΣ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2017-2018 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2018 ΒΑΘΜΟΣ:.... /100 ΟΛΟΓΡΑΦΩΣ:... ΥΠΟΓΡ:... ΤΑΞΗ: B ΓΥΜΝΑΣΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 01.06.2018 ΜΑΘΗΜΑ: ΦΥΣΙΚΑ (ΒΙΟΛΟΓΙΑ)
Β ΠΕΡΙΦΕΡΕΙΑΚΟ ΓΥΜΝΑΣΙΟ ΛΕΥΚΩΣΙΑΣ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2017-2018 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2018 ΒΑΘΜΟΣ:.... /100 ΟΛΟΓΡΑΦΩΣ:... ΥΠΟΓΡ:... ΤΑΞΗ: B ΓΥΜΝΑΣΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 01.06.2018 ΜΑΘΗΜΑ: ΦΥΣΙΚΑ (ΒΙΟΛΟΓΙΑ)
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή Διατριβή Η ΣΥΝΕΙΣΦΟΡΑ ΤΟΥ CΗ 4 ΣΤΟ ΦΑΙΝΟΜΕΝΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή Διατριβή Η ΣΥΝΕΙΣΦΟΡΑ ΤΟΥ CΗ 4 ΣΤΟ ΦΑΙΝΟΜΕΝΟ
