Σε ένα διάλυμα η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη
|
|
|
- Χαρικλώ Δραγούμης
- 7 χρόνια πριν
- Προβολές:
Transcript
1 Διαλύματα 1
2 Διαδικασία διάλυσης Σε ένα διάλυμα η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται από μόρια του διαλύτη. 3. Μεταβάλλεται η ενθαλπία (ΔH) με κάθε αλληλεπίδραση διάσπασης ή σχηματισμού 2 Ιονικό στερεό διαλυόμενο στο νερό
3 3
4 Instant hot and cold compress packs CaCl 2 NH 4 NO 3 4
5 Διαδικασία διάλυσης Τα ιόντα περιβάλλονται από διαλύτη (επιδιαλύτωση... Ενυδάτωση) ) Οι διαμοριακές δυνάμεις είναι ιόντος διπόλου
6 Διαλυτότητα 6
7 Διαλυτότητα 7
8 Διαλυτότητα Τα υπέρκορα διαλύματα είναι ασταθή. Η κρυστάλλωση μπορεί συχνά να επαχθεί προσθέτοντας πυρήνα κρυσταλλώσεως ή και με τριβή του περιέκτη 8
9 Παράγοντες που επιδρούν στη διαλυτότητα 9
10 Μοριακά διαλύματα Παράγοντες που επιδρούν στη διαλυτότητα Νερό αιθανόλη Διαμοριακές δυνάμεις = δεσμοί H, διπόλου διπόλου,, διασποράς 10
11 Παράγοντες που επιδρούν στη διαλυτότητα 11
12 Διαλυτότητα αλκοολών στο νερό 12
13 Παράγοντες που επιδρούν στη διαλυτότητα Η βιταμίνη Α είναι λιποδιαλυτή, η βιταμίνη C λιποδιαλυτή 13
14 Διαλύματα αερίων Η διαλυτότητα των αερίων αυξάνει όσο αυξάνει το μέγεθος και το ΑΒ/ΜΒ. Διότι Μεγαλύτερα μόρια έχουν μεγαλύτερες δυνάμεις διασποράς 14
15 Διαλύματα Επίδραση της πίεσης στη διαλυτότητα Ηδιαλυτότηταυγρών υγρών και στερεών δεν αυξάνει σημαντικά με την πίεση. Ηδιαλυτότητααερίου αερίου αυξάνει ανάλογα με την πίεση. Νόμος Henry: S g = kp g S g διαλυτότητα αερίου; k σταθερά Ηenry (για το αέριο στο συγκεκριμένο διαλύτη); P g μερική πίεση αερίου πάνω από το διάλυμα 15
16 Επίδραση θερμοκρασίας στη διαλυτότητα στερεών Εν γένει η διαλυτότητα των στερεών αυξάνει με αύξηση της θερμοκρασίας 16
17 Επίδραση θερμοκρασίας στη διαλυτότητα αερίων Αντίθετα η διαλυτότητα των αερίων μειώνεται με αύξηση της θερμοκρασίας 17
18 Έκφραση περιεκτικότητας διαλυμάτων % κατά βάρος (%κβ, %w/w) : g δ/νης ουσίας σε 100g δ/τος % βάρος προς όγκο (%βο, %w/v) /): g δ/νης ουσίας σε 100mL δ/τος % κατ όγκο (%κο, %v/v) : ml δ/νης ουσίας σε 100mL δ/τος g/l, mg/ml, ppm, ppb, ppt Molarity (M) μοριακότητα: mol δ/νης ουσίας σε 1000mL δ/τος Molality (M) γραμμομοριακότητα: mol δ/νης ουσίας σε 1000g δ/τη 18
19 Γραμμομοριακό κλάσμα 19
20 20
21 Κανόνες αραίωσης και ανάμιξης δ/των Αραίωση: c1v1=c2v2 Aνάμιξη: cv=c 1 v 1 +c 2 v 2 + +c+c n v n 21
22 Αθροιστικές (προσθετικές) ιδιότητες διαλυμάτων Οι Αθροιστικές ιδιότητες επηρεάζονται μόνο από τον αριθμό των σωματιδίων και όχι από την ταυτότητά τους Ισχύουν για αραιά διαλύματα Σ/Υ ή μη πτητικών υγρών σε υγρά Ελάττωση της τάσης ατμών Αύξηση σημείου ζέσεως Μείωση σημείου πήξεως Ωσμωτική πίεση 22
23 Ιδανικά & πραγματικά διαλύματα Ιδανικά διαλύματα: : τα διαλύματα που ακολουθούν επακριβώς τους νόμους και σχέσεις των φυσικών φαινομένων. Κάθε σωματίδιο δεν επηρεάζει τη συμπεριφορά του άλλου Σε μοριακά: ανάλογη χημική δομή Σε ιοντικά: πολύ αραιά (<0,01Μ) Πραγματικά διαλύματα: επηρεάζει το ένα συστατικό τον τρόπο που συμπεριφέρεται το άλλο 23
24 Τάση ατμών Τάση ατμών: η πίεση που ασκείται, υπό ορισμένη θερμοκρασία, από τον ατμό που βρίσκεται σε δυναμική ισορροπία με το υγρό του σε ένα κλειστό σύστημα 24
25 Τάση ατμών νόμος Raoult, δ/τα Υ/Υ 1886 Για την περίπτωση 2 πτητικών υγρών Η τάση ατμών του κάθε υγρού εξαρτάται από τον αριθμό μορίων στο διάλυμα δηλ το Χ Νόμος Raoult των μερικών πιέσεων P A = X A P A X A γραμμομοριακό κλάσμα Α Νόμος Dalton (μερικών πιέσεων) P A τάση ατμών του καθαρού συστατικού Α P= X A P A + X B P B (+.) Το νόμο του Raoult ακολουθούν τα ιδανικά διαλύματα ενώ τα πραγματικά εμφανίζουν αποκλίσεις 25
26 Νόμος Raoult, πτητικά ιδανικά υγρά P 1 = X 1 P 1 P 2 = X 2 P 2 P tot = P 1 +P 2
27 Αποκλίσεις από το νόμο Raoult, πτητικά υγρά Παρατηρούνται στα πραγματικά δ/τα διότι οι δυνάμεις Α Α, Α, Β Β, Β, Α Β δεν είναι όμοιες Θετικές: Οι μερικές πιέσεις μεγαλύτερες των θεωρητικών, δεσμοί Α Β ασθενέστεροι (πιο εύκολη εξάτμιση, ΜeOH eoh H 2 O, αιθανόλη εξάνιο) Αρνητικές: Οι μερικές πιέσεις μικρότερες των θεωρητικών, δεσμοί Α Β ισχυρότεροι (πιο δύσκολη εξάτμιση,, HCOOH HH 2 O) +
28 Αποκλίσεις από το νόμο Raoult, πτητικά υγρά
29 Ελάττωση Τάσης ατμών Έστω η διάλυση μη πτητικών υγρών ή στερεών ενώσεων σε (πτητικό) δ/τη Η μείωση της τάσης ατμών οφείλεται στο γεγονός γ ότι θέσεις στην επιφάνεια του διαλύματος καταλαμβάνονται από μόρια της δ/νης ουσίας (μειώνεται η επιφανειακή τάση του δ/τος)
30 Ελάττωση Τάσης ατμών Κατά τη διάλυση μη πτητικών υγρών ή στερεών ενώσεων: Σε αραιά διαλύματα α α ο νόμος Raoult καθορίζει ότι ΔP P = P o A X B Ρ=Ρ ο Α (1 Χ Β ) 1=solvent
31 Ανύψωση ΣΖ, ταπείνωση ΣΠ T b = K b m T f = K f m Kb, Kf εξαρτώνται από το διαλύτη
32 Ώσμωση Ωσμωτική Πίεση
33 Ωσμωτική Πίεση n =( ( )RT = MRT V
34 Διάλυση Τεχνητός νεφρός A cellophane (polymeric) tube acts as the semipermeable membrane Purifies blood by washing impurities (solutes) into the dialyzing solution.
35 Χαρακτηριστικά προσθετικών ιδιοτήτων Οι Αθροιστικές ιδιότητες εξαρτώνται Τη συγκέντρωση σωματιδίων της δ/νης ουσίας και όχι τη φύση τους Ισχύουν για όλους τους τύπους διαλυμάτων (όχι μόνο τα υδατικά) Για τα μοριακά δ/τα οι τιμές είναι οι προβλεπόμενες από τους ν. Raoult, Van t Hoff Για τα ιονικά είναι πολαπλάσσιες των θεωρητικών Όταν υπάρχει διαμοριακή σύζευξη οι τιμές είναι υποπολλαπλάσσιες Ωσμωμοριακότητα (osmol) osmol = k M 35
Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη
 Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη
 Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
Διαλύματα 1 Διαδικασία διάλυσης Σε ένα δάλ διάλυμα, η διαλυμένη ουσία διασπείρεται ομοιόμορφα σε όλη τη μάζα του διαλύτη 1. Τα μόρια του διαλύτη έλκονται από τα επιφανειακά ιόντα 2. Κάθε ιόν περιβάλλεται
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας
 Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
1 ΦΥΣΙΚΟ ΦΥΣΙΚ ΧΗΜΕΙΑ Ο ΣΥΣΤΗΜΑΤΩΝ
 1 ΦΥΣΙΚΟΧΗΜΕΙΑ ΣΥΣΤΗΜΑΤΩΝ Φυσικοχημεία συστημάτων 2 «Όμοιος Ό αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη είναι δύο ουσίες τόσο μεγαλύτερη είναι η αμοιβαία διαλυτότητά τους. Οι ανόργανες ενώσεις διαλύονται
1 ΦΥΣΙΚΟΧΗΜΕΙΑ ΣΥΣΤΗΜΑΤΩΝ Φυσικοχημεία συστημάτων 2 «Όμοιος Ό αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη είναι δύο ουσίες τόσο μεγαλύτερη είναι η αμοιβαία διαλυτότητά τους. Οι ανόργανες ενώσεις διαλύονται
Ανάλυση Τροφίμων. Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Διαλύματα Τα ομοιογενή μίγματα
Ανάλυση Τροφίμων Ενότητα 6: Διαλύματα & οι ιδιότητές τους Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Διαλύματα Τα ομοιογενή μίγματα
Διάλυμα καλείται κάθε ομογενές σύστημα, το οποίο αποτελείται από δύο ή περισσότερες χημικές ουσίες, και έχει την ίδια σύσταση σε όλη του τη μάζα.
 1. ΔΙΑΛΥΜΑ Διάλυμα καλείται κάθε ομογενές σύστημα, το οποίο αποτελείται από δύο ή περισσότερες χημικές ουσίες, και έχει την ίδια σύσταση σε όλη του τη μάζα. Ετερογενές σύστημα καλείται αυτό, το οποίο αποτελείται
1. ΔΙΑΛΥΜΑ Διάλυμα καλείται κάθε ομογενές σύστημα, το οποίο αποτελείται από δύο ή περισσότερες χημικές ουσίες, και έχει την ίδια σύσταση σε όλη του τη μάζα. Ετερογενές σύστημα καλείται αυτό, το οποίο αποτελείται
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 15: Διαλύματα
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Ποσοτική και Ποιoτική Ανάλυση
 Ποσοτική και Ποιoτική Ανάλυση ιδάσκων: Σπύρος Περγαντής Γραφείο: Α206 Τηλ. 2810 545084 E-mail: spergantis@chemistry.uoc.gr ΙΑΛΥΜΑΤΑ (Γενική Χημεία, Ebbing and Gammon κεφ. 12) Εισαγωγή: Γιατί διαλύματα;
Ποσοτική και Ποιoτική Ανάλυση ιδάσκων: Σπύρος Περγαντής Γραφείο: Α206 Τηλ. 2810 545084 E-mail: spergantis@chemistry.uoc.gr ΙΑΛΥΜΑΤΑ (Γενική Χημεία, Ebbing and Gammon κεφ. 12) Εισαγωγή: Γιατί διαλύματα;
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ
 1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ ΗΛΙΑΣ ΝΟΛΗΣ-ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΘΕΟΔΩΡΟΣ 2012 Διαλύματα Διάλυμα ονομάζεται κάθε ομογενές μείγμα δύο ή περισσοτέρων συστατικών. Κάθε
1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ ΗΛΙΑΣ ΝΟΛΗΣ-ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΘΕΟΔΩΡΟΣ 2012 Διαλύματα Διάλυμα ονομάζεται κάθε ομογενές μείγμα δύο ή περισσοτέρων συστατικών. Κάθε
1. ΔΙΑΜΟΡΙΑΚΕΣ ΔΥΝΑ- ΜΕΙΣ - ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ - ΠΡΟΣΘΕ- ΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ
 27 1. ΔΙΑΜΟΡΙΑΚΕΣ ΔΥΝΑ- ΜΕΙΣ - ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ - ΠΡΟΣΘΕ- ΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 28 29 ΔΙΔΑΚΤΙΚΗ ΩΡΑ: 1 ΔΙΔΑΚΤΙΚΗ ΕΝΟΤΗΤΑ: Διαμοριακές δυνάμεις - Καταστάσεις της ύλης - Προσθετικές ιδιότητες 1.1α Διαμοριακές
27 1. ΔΙΑΜΟΡΙΑΚΕΣ ΔΥΝΑ- ΜΕΙΣ - ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ - ΠΡΟΣΘΕ- ΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 28 29 ΔΙΔΑΚΤΙΚΗ ΩΡΑ: 1 ΔΙΔΑΚΤΙΚΗ ΕΝΟΤΗΤΑ: Διαμοριακές δυνάμεις - Καταστάσεις της ύλης - Προσθετικές ιδιότητες 1.1α Διαμοριακές
ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ
 ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ εσµός Υδρογόνου 1) Τι ονοµάζεται δεσµός υδρογόνου; εσµός ή γέφυρα υδρογόνου : είναι µια ειδική περίπτωση διαµοριακού δεσµού διπόλου-διπόλου,
ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ εσµός Υδρογόνου 1) Τι ονοµάζεται δεσµός υδρογόνου; εσµός ή γέφυρα υδρογόνου : είναι µια ειδική περίπτωση διαµοριακού δεσµού διπόλου-διπόλου,
Διάλυμα, είναι κάθε ομογενές μίγμα δύο ή περισσότερων ουσιών.
 Διάλυμα, είναι κάθε ομογενές μίγμα δύο ή περισσότερων ουσιών. Διαλύτης: Είναι το συστατικό του διαλύματος που έχει την ίδια φυσική κατάσταση με το διάλυμα. Όταν περισσότερα από ένα συστατικά έχουν την
Διάλυμα, είναι κάθε ομογενές μίγμα δύο ή περισσότερων ουσιών. Διαλύτης: Είναι το συστατικό του διαλύματος που έχει την ίδια φυσική κατάσταση με το διάλυμα. Όταν περισσότερα από ένα συστατικά έχουν την
1 η Εργαστηριακή άσκηση. Παρασκευή Αραίωση. διαλύματος. Δρ. Άρης Γιαννακάς - Ε.ΔΙ.Π.
 1 η Εργαστηριακή άσκηση Παρασκευή Αραίωση διαλύματος 1 Θεωρητικό Μέρος Εισαγωγικές έννοιες Όπως είναι γνωστό η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις)
1 η Εργαστηριακή άσκηση Παρασκευή Αραίωση διαλύματος 1 Θεωρητικό Μέρος Εισαγωγικές έννοιες Όπως είναι γνωστό η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις)
ΕΚΦΡΑΣΕΙΣ ΠΕΡΙΕΚΤΙΚΟΤΗΤΑΣ ΚΑΙ ΣΥΓΚΕΝΤΡΩΣΗΣ
 ΕΚΦΡΑΣΕΙΣ ΠΕΡΙΕΚΤΙΚΟΤΗΤΑΣ ΚΑΙ ΣΥΓΚΕΝΤΡΩΣΗΣ Η συγκέντρωση συμβολίζεται γενικά με το σύμβολο C ή γράφοντας τον μοριακό τύπο της διαλυμένης ουσίας ανάμεσα σε αγκύλες, π.χ. [ΝΗ 3 ] ή [Η 2 SO 4 ]. Σε κάθε περίπτωση,
ΕΚΦΡΑΣΕΙΣ ΠΕΡΙΕΚΤΙΚΟΤΗΤΑΣ ΚΑΙ ΣΥΓΚΕΝΤΡΩΣΗΣ Η συγκέντρωση συμβολίζεται γενικά με το σύμβολο C ή γράφοντας τον μοριακό τύπο της διαλυμένης ουσίας ανάμεσα σε αγκύλες, π.χ. [ΝΗ 3 ] ή [Η 2 SO 4 ]. Σε κάθε περίπτωση,
ΦΥΣΙΚΟΧΗΜΕΙΑ. Δημήτριος Τσιπλακίδης e-mail: dtsiplak@chem.auth.gr url: users.auth.gr/~dtsiplak. Φυσικοχημεία συστημάτων
 1 ΦΥΣΙΚΟΧΗΜΕΙΑ Δημήτριος Τσιπλακίδης e-mail: dtsiplak@chem.auth.gr url: users.auth.gr/~dtsiplak Φυσικοχημεία συστημάτων Φυσικοχημεία συστημάτων 2 «Όμοιος αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη
1 ΦΥΣΙΚΟΧΗΜΕΙΑ Δημήτριος Τσιπλακίδης e-mail: dtsiplak@chem.auth.gr url: users.auth.gr/~dtsiplak Φυσικοχημεία συστημάτων Φυσικοχημεία συστημάτων 2 «Όμοιος αρέσει όμοιο» Όσο συγγενέστερες από χημική άποψη
Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ. Χημεία ΒΑΣΙΚΕΣ ΓΝΩΣΕΙΣ ΑΣΠΡΟΠΥΡΓΟΣ
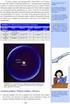 ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία ΒΑΣΙΚΕΣ ΓΝΩΣΕΙΣ ΑΣΠΡΟΠΥΡΓΟΣ 2 Ογκομέτρηση προχοϊδα διάλυμα HCl ΕΔΩ ακριβώς μετράμε τον όγκο ( στην εφαπτομένη της καμπύλης
ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία ΒΑΣΙΚΕΣ ΓΝΩΣΕΙΣ ΑΣΠΡΟΠΥΡΓΟΣ 2 Ογκομέτρηση προχοϊδα διάλυμα HCl ΕΔΩ ακριβώς μετράμε τον όγκο ( στην εφαπτομένη της καμπύλης
Συγκέντρωση διαλύματος
 Συγκέντρωση διαλύματος Συγκέντρωση διαλύματος: η ποσότητα της ουσίας που έχει διαλυθεί σε δεδομένη ποσότητα διαλύτη ή διαλύματος. Αραιό διάλυμα: όταν η συγκέντρωση της διαλυμένης ουσίας είναι χαμηλή Πυκνό
Συγκέντρωση διαλύματος Συγκέντρωση διαλύματος: η ποσότητα της ουσίας που έχει διαλυθεί σε δεδομένη ποσότητα διαλύτη ή διαλύματος. Αραιό διάλυμα: όταν η συγκέντρωση της διαλυμένης ουσίας είναι χαμηλή Πυκνό
ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι
 ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 5 η - Α ΜΕΡΟΣ ΔΙΑΛΥΜΑΤΑ Όνομα καθηγητή: ΕΥΑΓΓΕΛΙΟΥ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Στόχος (1): Κατανόηση των εννοιών:
ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 5 η - Α ΜΕΡΟΣ ΔΙΑΛΥΜΑΤΑ Όνομα καθηγητή: ΕΥΑΓΓΕΛΙΟΥ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Στόχος (1): Κατανόηση των εννοιών:
ΔΙΑΛΥΜΑΤΑ. Χρήστος Παππάς Επίκουρος Καθηγητής
 Χρήστος Παππάς Επίκουρος Καθηγητής 1 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1. Γραμμομοριακή μάζα (γραμμομόριο) (M) Γραμμομόριο (M) = Μ r ή ΜΒ σε g ΠΑΡΑΔΕΙΓΜΑ M r,h2o =18 M H2O =18 g 2. Αριθμός mol ενός χημικού στοιχείου ή μιας
Χρήστος Παππάς Επίκουρος Καθηγητής 1 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1. Γραμμομοριακή μάζα (γραμμομόριο) (M) Γραμμομόριο (M) = Μ r ή ΜΒ σε g ΠΑΡΑΔΕΙΓΜΑ M r,h2o =18 M H2O =18 g 2. Αριθμός mol ενός χημικού στοιχείου ή μιας
ΚΕΦΑΛΑΙΟ 1: ΔΙΑΜΟΡΙΑΚΕΣ ΑΥΝΑΜΕΙΣ-ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΑΗΣ -ΠΡΟΣΘΕΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ
 ΚΕΦΑΛΑΙΟ 1: ΔΙΑΜΟΡΙΑΚΕΣ ΑΥΝΑΜΕΙΣ-ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΑΗΣ -ΠΡΟΣΘΕΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 1-15. βλέπε θεωρία. Ασκήσεις - προβλήματα α. Διαμοριακές δυνάμεις 16. Βλέπε θεωρία για τη συμπλήρωση των κενών. 17. To NaCl
ΚΕΦΑΛΑΙΟ 1: ΔΙΑΜΟΡΙΑΚΕΣ ΑΥΝΑΜΕΙΣ-ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΑΗΣ -ΠΡΟΣΘΕΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 1-15. βλέπε θεωρία. Ασκήσεις - προβλήματα α. Διαμοριακές δυνάμεις 16. Βλέπε θεωρία για τη συμπλήρωση των κενών. 17. To NaCl
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων. Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης
 Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι
 ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 8 η ΑΘΡΟΙΣΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ Όνομα καθηγητή: ΕΥΑΓΓΕΛΙΟΥ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Στόχος (): Κατανόηση των αθροιστικών
ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 8 η ΑΘΡΟΙΣΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ Όνομα καθηγητή: ΕΥΑΓΓΕΛΙΟΥ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Στόχος (): Κατανόηση των αθροιστικών
Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους.
 ΔΙΑΛΥΜΑΤΑ Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους. Διαλύτης: η ουσία που βρίσκεται σε μεγαλύτερη αναλογία
ΔΙΑΛΥΜΑΤΑ Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους. Διαλύτης: η ουσία που βρίσκεται σε μεγαλύτερη αναλογία
2.3 Περιεκτικότητα διαλύματος Εκφράσεις περιεκτικότητας
 1 Η θεωρία του μαθήματος με ερωτήσεις. 2.3 Περιεκτικότητα διαλύματος Εκφράσεις περιεκτικότητας Ερωτήσεις θεωρίας με απάντηση 3-1. Τι ονομάζεται περιεκτικότητα ενός διαλύματος; Είναι μία έκφραση που δείχνει
1 Η θεωρία του μαθήματος με ερωτήσεις. 2.3 Περιεκτικότητα διαλύματος Εκφράσεις περιεκτικότητας Ερωτήσεις θεωρίας με απάντηση 3-1. Τι ονομάζεται περιεκτικότητα ενός διαλύματος; Είναι μία έκφραση που δείχνει
Άσκηση 2η. Παρασκευή Αραίωση διαλύματος
 Άσκηση 2η Παρασκευή Αραίωση διαλύματος 2 Θεωρητικό μέρος Η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις) Τα μίγματα (δύο ή περισσότερες καθαρές ουσίες) Τα μίγματα
Άσκηση 2η Παρασκευή Αραίωση διαλύματος 2 Θεωρητικό μέρος Η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις) Τα μίγματα (δύο ή περισσότερες καθαρές ουσίες) Τα μίγματα
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
ΠΑΡΑΡΤΗΜΑ A > ΛΕΞΙΛΟΓΙΟ OPΩΝ > ΕΥΡΕΤΗΡΙΟ >ΕΥΡΕΤΗΡΙΟΟΝΟΜΑΤΩΝ
 ΠΑΡΑΡΤΗΜΑ A > ΛΕΞΙΛΟΓΙΟ OPΩΝ > ΕΥΡΕΤΗΡΙΟ >ΕΥΡΕΤΗΡΙΟΟΝΟΜΑΤΩΝ A Αμφίδρομη αντίδραση: αυτή που πραγματοποιείται προς τις δύο κατευθύνσεις ταυτόχρονα και καταλήγει σε κατάσταση ισορροπίας. Αναγωγή: η ελάττωση
ΠΑΡΑΡΤΗΜΑ A > ΛΕΞΙΛΟΓΙΟ OPΩΝ > ΕΥΡΕΤΗΡΙΟ >ΕΥΡΕΤΗΡΙΟΟΝΟΜΑΤΩΝ A Αμφίδρομη αντίδραση: αυτή που πραγματοποιείται προς τις δύο κατευθύνσεις ταυτόχρονα και καταλήγει σε κατάσταση ισορροπίας. Αναγωγή: η ελάττωση
Χημεία (Τμήμα Φυσικής) ΔΙΑΛΥΜΑΤΑ
 Χημεία (Τμήμα Φυσικής) ΔΙΑΛΥΜΑΤΑ 3/11/2015 2 μίγματα και διαλύματα μίγματα και διαχωρισμός μιγμάτων διαλύματα ουσίες και μίγματα 3 Ι. μίγματα και διαλύματα Α. μίγματα και διαχωρισμός μιγμάτων 1. τα υλικά
Χημεία (Τμήμα Φυσικής) ΔΙΑΛΥΜΑΤΑ 3/11/2015 2 μίγματα και διαλύματα μίγματα και διαχωρισμός μιγμάτων διαλύματα ουσίες και μίγματα 3 Ι. μίγματα και διαλύματα Α. μίγματα και διαχωρισμός μιγμάτων 1. τα υλικά
Α = Ζ + Ν ΑΤΟΜΟ. ΙΣΟΤΟΠΑ είναι. ΝΕΤΡΟΝΙΑ (n) ΠΥΡΗΝΑΣ
 ΚΕΦ.1: 3. ΔΟΜΗ ΑΤΟΜΟΥ ΑΤΟΜΟ ΠΥΡΗΝΑΣ ΠΡΩΤΟΝΙΑ (p + ) ΝΕΤΡΟΝΙΑ (n) 1.3.1 Να βρείτε τον αριθμό πρωτονίων νετρονίων και ηλεκτρονίων που υπάρχουν στα παρακάτω άτομα ή ιόντα: ΗΛΕΚΤΡΟΝΙΑ (e - ) ΠΡΟΣΟΧΗ 1) Στα
ΚΕΦ.1: 3. ΔΟΜΗ ΑΤΟΜΟΥ ΑΤΟΜΟ ΠΥΡΗΝΑΣ ΠΡΩΤΟΝΙΑ (p + ) ΝΕΤΡΟΝΙΑ (n) 1.3.1 Να βρείτε τον αριθμό πρωτονίων νετρονίων και ηλεκτρονίων που υπάρχουν στα παρακάτω άτομα ή ιόντα: ΗΛΕΚΤΡΟΝΙΑ (e - ) ΠΡΟΣΟΧΗ 1) Στα
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Διαλύματα Παρασκευή Διαλυμάτων
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Διαλύματα Παρασκευή Διαλυμάτων Ιωάννης Πούλιος Ιωάννης Ζιώγας Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Διαλύματα Παρασκευή Διαλυμάτων Ιωάννης Πούλιος Ιωάννης Ζιώγας Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
Τρόποι έκφρασης της συγκέντρωσης
 Τρόποι έκφρασης της συγκέντρωσης Συγκέντρωση διαλύματος: η ποσότητα της ουσίας (g ή moles) που έχει διαλυθεί σε δεδομένη ποσότητα διαλύτη ή διαλύματος (όγκο ή μάζα). Δημιουργούνται έτσι διάφοροι τρόποι
Τρόποι έκφρασης της συγκέντρωσης Συγκέντρωση διαλύματος: η ποσότητα της ουσίας (g ή moles) που έχει διαλυθεί σε δεδομένη ποσότητα διαλύτη ή διαλύματος (όγκο ή μάζα). Δημιουργούνται έτσι διάφοροι τρόποι
w P M = Απόσταξη με υδρατμούς ουσ ίας ουσ ίας ουσ ίας νερου νερου ν έρου
 Απόσταξη με υδρατμούς Η απόσταξη υγρών ουσιών που δεν αναμιγνύονται με το νερό χρησιμοποιείται πολύ συχνά τόσο στο εργαστήριο όσο και στην βιομηχανία για τον διαχωρισμό και καθαρισμό υγρών που έχουν πολύ
Απόσταξη με υδρατμούς Η απόσταξη υγρών ουσιών που δεν αναμιγνύονται με το νερό χρησιμοποιείται πολύ συχνά τόσο στο εργαστήριο όσο και στην βιομηχανία για τον διαχωρισμό και καθαρισμό υγρών που έχουν πολύ
1 o ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ ΚΟΡΔΕΛΙΟΥ ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ, ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 1. ΚΕΦΑΛΑΙΟ 1- ΒΑΣΙΚΑ ΜΕΓΕΘΗ-ΣΩΜΑΤΙΔΙΑ - Τι πρέπει να γνωρίζουμε
 1 o ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ ΚΟΡΔΕΛΙΟΥ ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ, ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 1 ΚΕΦΑΛΑΙΟ 1- ΒΑΣΙΚΑ ΜΕΓΕΘΗ-ΣΩΜΑΤΙΔΙΑ - Τι πρέπει να γνωρίζουμε 1. Βασικά μεγέθη και μονάδες αυτών που θα χρησιμοποιηθούν
1 o ΓΕΛ ΕΛΕΥΘΕΡΙΟΥ ΚΟΡΔΕΛΙΟΥ ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ, ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 1 ΚΕΦΑΛΑΙΟ 1- ΒΑΣΙΚΑ ΜΕΓΕΘΗ-ΣΩΜΑΤΙΔΙΑ - Τι πρέπει να γνωρίζουμε 1. Βασικά μεγέθη και μονάδες αυτών που θα χρησιμοποιηθούν
5. Εξώθερμο φαινόμενο είναι: α. ο βρασμός. β. η τήξη. γ. η εξάτμιση. δ. η εξουδετέρωση.
 ΔΙΑΓΩΝΙΜΑ: Μ Α Θ Η Μ Α : Β ΣΑΞΗ ΛΤΚΕΙΟΤ ΦΗΜΕΙΑ ΚΑΣΕΤΘΤΝΗ Ε Π Ω Ν Τ Μ Ο : < < < < < <
ΔΙΑΓΩΝΙΜΑ: Μ Α Θ Η Μ Α : Β ΣΑΞΗ ΛΤΚΕΙΟΤ ΦΗΜΕΙΑ ΚΑΣΕΤΘΤΝΗ Ε Π Ω Ν Τ Μ Ο : < < < < < <
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ
 ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ ΔΙΑΛΥΜΑΤΑ Διάλυμα ονομάζεται κάθε ομοιογενές σύστημα, αποτελούμενο από δύο ή περισσότερες χημικές ουσίες, το οποίο έχει την ίδια σύσταση σε όλη τη μάζα του. Είναι δυνατό να υπάρχουν
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ ΔΙΑΛΥΜΑΤΑ Διάλυμα ονομάζεται κάθε ομοιογενές σύστημα, αποτελούμενο από δύο ή περισσότερες χημικές ουσίες, το οποίο έχει την ίδια σύσταση σε όλη τη μάζα του. Είναι δυνατό να υπάρχουν
Συγκέντρωση ή μοριακότητα κατά όγκο ή Molarity διαλύματος
 79 Συγκέντρωση ή μοριακότητα κατά όγκο ή Molarity διαλύματος Molarity ( Μ ) ή μοριακότητα κατ όγκο: μας δίνει τα mol της διαλυμένης ουσίας που περιέχονται σε 1000 ml ( = 1 L ) διαλύματος. Π.χ. υδατικό
79 Συγκέντρωση ή μοριακότητα κατά όγκο ή Molarity διαλύματος Molarity ( Μ ) ή μοριακότητα κατ όγκο: μας δίνει τα mol της διαλυμένης ουσίας που περιέχονται σε 1000 ml ( = 1 L ) διαλύματος. Π.χ. υδατικό
Σύντομη περιγραφή του πειράματος
 Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
Χημεία Α Λυκείου. Διαλύματα
 Διαλύματα Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων ουσιών, οι οποίες αποούν τα συστατικά του διαλύματος. Από τα συστατικά αυτά, εκείνο που έχει την ίδια φυσική κατάσταση με αυτή του διαλύματος
Διαλύματα Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων ουσιών, οι οποίες αποούν τα συστατικά του διαλύματος. Από τα συστατικά αυτά, εκείνο που έχει την ίδια φυσική κατάσταση με αυτή του διαλύματος
2. ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΧΟΜΕΝΑ
 2. ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΧΟΜΕΝΑ Τύποι διαλυμάτων Διαλυτότητα και η διαδικασία διάλυσης Επιδράσεις θερμοκρασίας και πίεσης πάνω στη διαλυτότητα Τρόποι έκφρασης της συγκέντρωσης Τάση ατμών διαλύματος Ανύψωση σημείου
2. ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΧΟΜΕΝΑ Τύποι διαλυμάτων Διαλυτότητα και η διαδικασία διάλυσης Επιδράσεις θερμοκρασίας και πίεσης πάνω στη διαλυτότητα Τρόποι έκφρασης της συγκέντρωσης Τάση ατμών διαλύματος Ανύψωση σημείου
Σωματίδιο (σύμβολο) Θέση Σχετικό φορτίο
 XHMEIA-NOTES Μάζα: είναι το μέτρο της αντίστασης που παρουσιάζει ένα σώμα ως προς την μεταβολή της ταχύτητάς του και εκφράζεται το ποσό της ύλης που περιέχεται σε μια ουσία. Όργανο μέτρησης: Ζυγός Όγκος:
XHMEIA-NOTES Μάζα: είναι το μέτρο της αντίστασης που παρουσιάζει ένα σώμα ως προς την μεταβολή της ταχύτητάς του και εκφράζεται το ποσό της ύλης που περιέχεται σε μια ουσία. Όργανο μέτρησης: Ζυγός Όγκος:
Παράγοντες που εξηγούν τη διαλυτότητα. Είδη διαλυμάτων
 Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ
 ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ B ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ 1. Ταξινόμηση
ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ B ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ 1. Ταξινόμηση
IΣΟΡΡΟΠΙΑ ΣΥΣΤΗΜΑΤΩΝ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΜΗ ΗΛΕΚΤΡΟΛΥΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΥΓΡΩΝ
 Ιωάννης Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας, ΑΠΘ IΣΟΡΡΟΠΙΑ ΣΥΣΤΗΜΑΤΩΝ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΜΗ ΗΛΕΚΤΡΟΛΥΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΥΓΡΩΝ ΘΕΣΣΑΛΟΝΙΚΗ 2018 ς Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας,
Ιωάννης Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας, ΑΠΘ IΣΟΡΡΟΠΙΑ ΣΥΣΤΗΜΑΤΩΝ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΜΗ ΗΛΕΚΤΡΟΛΥΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΥΓΡΩΝ ΘΕΣΣΑΛΟΝΙΚΗ 2018 ς Πούλιος Εργαστήριο Φυσικής Χημείας, Τμήμα Χημείας,
ΚΕΦΑΛΑΙΟ 1: Διαμοριακές Δυνάμεις-Καταστάσεις της ύλης-προσθετικές ιδιότητες
 ΚΕΦΑΛΑΙΟ 1: Διαμοριακές Δυνάμεις-Καταστάσεις της ύλης-προσθετικές ιδιότητες 1. Η τάση ατμών ενός υγρού εξαρτάται: i. Από την ποσότητα του υγρού ii. Τη θερμοκρασία iii. Τον όγκο του δοχείου iv. Την εξωτερική
ΚΕΦΑΛΑΙΟ 1: Διαμοριακές Δυνάμεις-Καταστάσεις της ύλης-προσθετικές ιδιότητες 1. Η τάση ατμών ενός υγρού εξαρτάται: i. Από την ποσότητα του υγρού ii. Τη θερμοκρασία iii. Τον όγκο του δοχείου iv. Την εξωτερική
Καταστάσεις της ύλης. αέρια υγρή στερεά
 Καταστάσεις της ύλης αέρια υγρή στερεά Ύλη Καθαρή ουσία Μίγμα Στοιχείο Ένωση Ομογενές Ετερογενές Παράδειγμα: νάτριο, υδρογόνο Παράδειγμα: Αλάτι, νερό Παράδειγμα: αέρας, Αλάτι σε νερό Παράδειγμα: λάδι και
Καταστάσεις της ύλης αέρια υγρή στερεά Ύλη Καθαρή ουσία Μίγμα Στοιχείο Ένωση Ομογενές Ετερογενές Παράδειγμα: νάτριο, υδρογόνο Παράδειγμα: Αλάτι, νερό Παράδειγμα: αέρας, Αλάτι σε νερό Παράδειγμα: λάδι και
Ασκήσεις διαλυμάτων. Επαναληπτικές ασκήσεις Α' Λυκείου 1
 Επαναληπτικές ασκήσεις Α' Λυκείου 1 Ασκήσεις διαλυμάτων. 1. Διαλύουμε πλήρως 20 g σε 20 g H 2 O και προκύπτει διάλυμα Α. Να υπολογιστεί η % w/w περιεκτικότητα του διαλύματος. μάζα Δ/τος = 1 + 2 20 + 20
Επαναληπτικές ασκήσεις Α' Λυκείου 1 Ασκήσεις διαλυμάτων. 1. Διαλύουμε πλήρως 20 g σε 20 g H 2 O και προκύπτει διάλυμα Α. Να υπολογιστεί η % w/w περιεκτικότητα του διαλύματος. μάζα Δ/τος = 1 + 2 20 + 20
Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων
 Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ
 Θέματα Πανελλ. Εξετάσεων Χημείας Προσανατολισμού Β Λυκείου 1 ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1984 2004 (Περιέχει όσα από τα θέματα αναφέρονται στην ύλη της
Θέματα Πανελλ. Εξετάσεων Χημείας Προσανατολισμού Β Λυκείου 1 ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1984 2004 (Περιέχει όσα από τα θέματα αναφέρονται στην ύλη της
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις
 Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση : Προσδιορισμός μοριακής μάζας με ζεσεοσκοπία Αθανάσιος Τσεκούρας Τμήμα Χημείας 1. Θεωρία... 3. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 4 Σελίδα 1. Θεωρία
Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση : Προσδιορισμός μοριακής μάζας με ζεσεοσκοπία Αθανάσιος Τσεκούρας Τμήμα Χημείας 1. Θεωρία... 3. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 4 Σελίδα 1. Θεωρία
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 8 ΥΔΑΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΑΣΘΕΝΩΝ ΗΛΕΚΤΡΟΛΥΤΩΝ
 ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 8 ΥΔΑΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΑΣΘΕΝΩΝ ΗΛΕΚΤΡΟΛΥΤΩΝ 1. Να βρεθεί το ph διαλύματος CH 3 COOH συγκέντρωσης 0,1Μ στους 25 ο C. Δίνεται για το CH 3 COOH στους 25 ο C Κ α =10-5.
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 8 ΥΔΑΤΙΚΑ ΔΙΑΛΥΜΑΤΑ ΑΣΘΕΝΩΝ ΗΛΕΚΤΡΟΛΥΤΩΝ 1. Να βρεθεί το ph διαλύματος CH 3 COOH συγκέντρωσης 0,1Μ στους 25 ο C. Δίνεται για το CH 3 COOH στους 25 ο C Κ α =10-5.
Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ
 Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 pulis@chem.auth.gr phtcatalysisgrup.web.auth.gr Διαλύματα και Συστήματα υγρών Διαμόρφωση μαθήματος Θεωρία/Ασκήσεις
Φυσικοχημεία II, Διαλύματα Ιωάννης Πούλιος, Καθηγητής Εργ. Φυσικοχημείας Α.Π.Θ. Τηλ. 2310-997785 pulis@chem.auth.gr phtcatalysisgrup.web.auth.gr Διαλύματα και Συστήματα υγρών Διαμόρφωση μαθήματος Θεωρία/Ασκήσεις
ΦΥΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι
 ΦΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 6 η - Β ΜΕΡΟΣ ΔΙΑΛΜΑΤΑ Όνομα καθηγητή: ΕΑΓΓΕΛΙΟ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟ ΜΑΘΗΜΑΤΟΣ Στόχος (): Κατανόηση των εννοιών: υγρά διαλύματα,
ΦΣΙΚΟΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ Ι Ενότητα 6 η - Β ΜΕΡΟΣ ΔΙΑΛΜΑΤΑ Όνομα καθηγητή: ΕΑΓΓΕΛΙΟ ΒΑΣΙΛΙΚΗ Τμήμα: Επιστήμης Τροφίμων και Διατροφής του Ανθρώπου ΣΤΟΧΟΙ ΤΟ ΜΑΘΗΜΑΤΟΣ Στόχος (): Κατανόηση των εννοιών: υγρά διαλύματα,
ΔΙΑΜΟΡΙΑΚΕΣ ΔΥΝΑΜΕΙΣ ΔΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ
 ΔΙΑΜΟΡΙΑΚΕΣ ΔΥΝΑΜΕΙΣ ΔΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΔΙΠΟΛΙΚΗ ΡΟΠΗ Α------------Β δ+ δ- μ Εάν µ ΟΛ 0 πολική Εάν µ ΟΛ =0 άπολη ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΔΙΑΤΟΜΙΚΑ ΜΟΡΙΑ Εάν τα άτοµα είναι ίδια
ΔΙΑΜΟΡΙΑΚΕΣ ΔΥΝΑΜΕΙΣ ΔΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΔΙΠΟΛΙΚΗ ΡΟΠΗ Α------------Β δ+ δ- μ Εάν µ ΟΛ 0 πολική Εάν µ ΟΛ =0 άπολη ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΔΙΑΤΟΜΙΚΑ ΜΟΡΙΑ Εάν τα άτοµα είναι ίδια
Για την επίλυση αυτής της άσκησης, αλλά και όλων των παρόμοιων χρησιμοποιούμε ιδιότητες των αναλογιών (χιαστί)
 ΜΕΘΟΔΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΔΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυμάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούμε ή
ΜΕΘΟΔΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΔΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυμάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούμε ή
(Θεωρία-Λυμένες Ασκήσεις) Σπουδές στις Φυσικές Επιστήμες Σχολή Θετικών Επιστημών και Τεχνολογίας
 ΕΙΣΑΓΩΓΗ ΣΤΑ ΔΙΑΛΥΜΑΤΑ (Θεωρία-Λυμένες Ασκήσεις) Εργαστηριακές Ασκήσεις Βιολογίας I Σπουδές στις Φυσικές Επιστήμες Σχολή Θετικών Επιστημών και Τεχνολογίας Παξινού Ευγενία 1o ΜΕΡΟΣ ΘΕΩΡΙΑ Η ύλη μπορεί να
ΕΙΣΑΓΩΓΗ ΣΤΑ ΔΙΑΛΥΜΑΤΑ (Θεωρία-Λυμένες Ασκήσεις) Εργαστηριακές Ασκήσεις Βιολογίας I Σπουδές στις Φυσικές Επιστήμες Σχολή Θετικών Επιστημών και Τεχνολογίας Παξινού Ευγενία 1o ΜΕΡΟΣ ΘΕΩΡΙΑ Η ύλη μπορεί να
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ
 ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2016-2017 ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ 1 ΕΙΣΑΓΩΓΗ ΑΤΟΜΙΚΗ ΘΕΩΡΙΑ Δομικά σωματίδια (άτομα-μόρια-ιόντα) Δομή του ατόμου Ατομικός και μαζικός αριθμός Ισότοπα Ηλεκτρονική
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2016-2017 ΠΕΡΙΓΡΑΜΜΑ ΎΛΗΣ ΓΙΑ ΤΟ ΜΑΘΗΜΑ ΤΗΣ ΧΗΜΕΙΑΣ ΕΝΟΤΗΤEΣ 1 ΕΙΣΑΓΩΓΗ ΑΤΟΜΙΚΗ ΘΕΩΡΙΑ Δομικά σωματίδια (άτομα-μόρια-ιόντα) Δομή του ατόμου Ατομικός και μαζικός αριθμός Ισότοπα Ηλεκτρονική
Τράπεζα Χημεία Α Λυκείου
 Τράπεζα Χημεία Α Λυκείου 1 ο Κεφάλαιο Όλα τα θέματα του 1 ου Κεφαλαίου από τη Τράπεζα Θεμάτων 25 ερωτήσεις Σωστού Λάθους 30 ερωτήσεις ανάπτυξης Επιμέλεια: Γιάννης Καλαμαράς, Διδάκτωρ Χημικός Ερωτήσεις
Τράπεζα Χημεία Α Λυκείου 1 ο Κεφάλαιο Όλα τα θέματα του 1 ου Κεφαλαίου από τη Τράπεζα Θεμάτων 25 ερωτήσεις Σωστού Λάθους 30 ερωτήσεις ανάπτυξης Επιμέλεια: Γιάννης Καλαμαράς, Διδάκτωρ Χημικός Ερωτήσεις
Enrico Fermi, Thermodynamics, 1937
 I. Θερµοδυναµικά συστήµατα Enrico Feri, herodynaics, 97. Ένα σώµα διαστέλλεται από αρχικό όγκο. L σε τελικό όγκο 4. L υπό πίεση.4 at. Να υπολογισθεί το έργο που παράγεται. W - -.4 at 5 a at - (4..) - -
I. Θερµοδυναµικά συστήµατα Enrico Feri, herodynaics, 97. Ένα σώµα διαστέλλεται από αρχικό όγκο. L σε τελικό όγκο 4. L υπό πίεση.4 at. Να υπολογισθεί το έργο που παράγεται. W - -.4 at 5 a at - (4..) - -
Στοιχειομετρικοί Υπολογισμοί στη Χημεία
 Στοιχειομετρικοί Υπολογισμοί στη Χημεία Δομικές μονάδες της ύλης ΑΤΟΜΑ ΜΟΡΙΑ ΣΤΟΙΧΕΙΑ ΕΝΩΣΕΙΣ Αριθμός Avogadro N A = 6,02 10 23 mol -1 Δηλαδή αυτός ο αριθμός παριστάνει την ποσότητα μιας ουσίας που περιέχει
Στοιχειομετρικοί Υπολογισμοί στη Χημεία Δομικές μονάδες της ύλης ΑΤΟΜΑ ΜΟΡΙΑ ΣΤΟΙΧΕΙΑ ΕΝΩΣΕΙΣ Αριθμός Avogadro N A = 6,02 10 23 mol -1 Δηλαδή αυτός ο αριθμός παριστάνει την ποσότητα μιας ουσίας που περιέχει
ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ - ΠΑΡΑΔΕΙΓΜΑ
 ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ - ΠΑΡΑΔΕΙΓΜΑ ΘΕΜΑ 1ο Για τις παρακάτω ερωτήσεις Α1-Α3 να μεταφέρετε στο φύλλο απαντήσεων τον αριθμό της ερώτησης και δίπλα μόνο το γράμμα που αντιστοιχεί στη σωστή απάντηση.
ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ - ΠΑΡΑΔΕΙΓΜΑ ΘΕΜΑ 1ο Για τις παρακάτω ερωτήσεις Α1-Α3 να μεταφέρετε στο φύλλο απαντήσεων τον αριθμό της ερώτησης και δίπλα μόνο το γράμμα που αντιστοιχεί στη σωστή απάντηση.
Κεφάλαιο 5 Διαλύματα
 Κεφάλαιο 5 Διαλύματα Σύνοψη Τα διαλύματα είναι ομογενή μείγματα τα οποία βρίσκουν σημαντικές εφαρμογές σχεδόν σε όλους τους τομείς της ζωής. Κάθε διάλυμα περιέχει μία ή περισσότερες διαλυμένες ουσίες σε
Κεφάλαιο 5 Διαλύματα Σύνοψη Τα διαλύματα είναι ομογενή μείγματα τα οποία βρίσκουν σημαντικές εφαρμογές σχεδόν σε όλους τους τομείς της ζωής. Κάθε διάλυμα περιέχει μία ή περισσότερες διαλυμένες ουσίες σε
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ
 ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
Τύποι Διαρροών. Κίνηση Ρύπου. Ανίχνευση Ρύπου. Ρύπος. εμείς τι παίρνουμε χαμπάρι με χημικές αναλύσεις δειγμάτων νερού;
 Ρύπος υγρός στερεός Υ 1 Υ 2 διαρροή σε διάλυμα διαρροή σε καθαρή φάση πχ οινόπνευμα, βενζίνη διαλυμένος σε οργανική ουσία διαλυμένος σε νερό σαν Υ 2a ή Υ 2b σαν Υ 1 Τύποι Διαρροών μεταφορά διαλυμένης ουσίας
Ρύπος υγρός στερεός Υ 1 Υ 2 διαρροή σε διάλυμα διαρροή σε καθαρή φάση πχ οινόπνευμα, βενζίνη διαλυμένος σε οργανική ουσία διαλυμένος σε νερό σαν Υ 2a ή Υ 2b σαν Υ 1 Τύποι Διαρροών μεταφορά διαλυμένης ουσίας
Κεφάλαιο 12. Διαλύματα
 Κεφάλαιο 12 Διαλύματα 1 Διαλύματα ονομάζονται τα ομογενή συστήματα διασποράς στα οποία η εν διασπορά ουσία έχει διαστάσεις μικρότερες από 10-7 cm. Διαλύματα ονομάζονται και ομογενή μίγματα δύο ή περισσότερων
Κεφάλαιο 12 Διαλύματα 1 Διαλύματα ονομάζονται τα ομογενή συστήματα διασποράς στα οποία η εν διασπορά ουσία έχει διαστάσεις μικρότερες από 10-7 cm. Διαλύματα ονομάζονται και ομογενή μίγματα δύο ή περισσότερων
Γεωργική Χημεία Εργαστηριακές ασκήσεις
 Γεωργική Χημεία Εργαστηριακές ασκήσεις Γεώργιος Παπαδόπουλος, Καθηγητής Τμ. Τεχνολόγων Γεωπόνων Τ.Ε. Άρτα, 2015 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
Γεωργική Χημεία Εργαστηριακές ασκήσεις Γεώργιος Παπαδόπουλος, Καθηγητής Τμ. Τεχνολόγων Γεωπόνων Τ.Ε. Άρτα, 2015 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
Τι ονομάζουμε χημικό στοιχείο; Δώστε ένα παράδειγμα. Ερώτηση θεωρίας. Τι ονομάζουμε χημική ένωση; Δώστε ένα παράδειγμα. Ερώτηση θεωρίας.
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ Β ΓΥΜΝΑΣΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 23-04-2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΜΑΡΙΝΟΣ ΙΩΑΝΝΟΥ ΑΠΑΝΤΗΣΕΙΣ ο ΘΕΜΑ 1 1.1 Τα πρωτόνια που περιέχονται στον πυρήνα του στοιχείου Χ είναι κατά 1 λιγότερα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ Β ΓΥΜΝΑΣΙΟΥ ΗΜΕΡΟΜΗΝΙΑ: 23-04-2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΜΑΡΙΝΟΣ ΙΩΑΝΝΟΥ ΑΠΑΝΤΗΣΕΙΣ ο ΘΕΜΑ 1 1.1 Τα πρωτόνια που περιέχονται στον πυρήνα του στοιχείου Χ είναι κατά 1 λιγότερα
Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου 2000
 Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό νερό διαλύεται
Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό νερό διαλύεται
1 Ο ΚΕΦΑΛΑΙΟ ΕΡΩΤΗΣΕΙΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΜΕ ΑΠΑΝΤΗΣΗ
 1 Ο ΚΕΦΑΛΑΙΟ ΕΡΩΤΗΣΕΙΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΜΕ ΑΠΑΝΤΗΣΗ 1. Το στοιχείο Χ έχει 17 ηλεκτρόνια. Αν στον πυρήνα του περιέχει 3 νετρόνια περισσότερα από τα πρωτόνια, να υπολογισθούν ο ατομικός και ο μαζικός του
1 Ο ΚΕΦΑΛΑΙΟ ΕΡΩΤΗΣΕΙΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΜΕ ΑΠΑΝΤΗΣΗ 1. Το στοιχείο Χ έχει 17 ηλεκτρόνια. Αν στον πυρήνα του περιέχει 3 νετρόνια περισσότερα από τα πρωτόνια, να υπολογισθούν ο ατομικός και ο μαζικός του
Για αραιά διαλύματα : x 1 0 : μ i = μ i 0 RTlnx i χ. όπου μ i φ =μ i 0 χ
 Για ιδανικά διαλύματα : μ i = μ i lnx i x= γ=1 Για αραιά διαλύματα : x 1 : μ i = μ i lnx i χ μ i = μ i φ lnx i όπου μ i φ =μ i χ Χημική Ισορροπία λ Από σελ. 7 Χημική Ισορροπία όταν ν i μ i = (T,P σταθερό)
Για ιδανικά διαλύματα : μ i = μ i lnx i x= γ=1 Για αραιά διαλύματα : x 1 : μ i = μ i lnx i χ μ i = μ i φ lnx i όπου μ i φ =μ i χ Χημική Ισορροπία λ Από σελ. 7 Χημική Ισορροπία όταν ν i μ i = (T,P σταθερό)
ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων)
 ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων) 1. Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές. i. H σχετική ατομική μάζα μετριέται σε γραμμάρια. ii. H σχετική ατομική μάζα είναι
ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων) 1. Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές. i. H σχετική ατομική μάζα μετριέται σε γραμμάρια. ii. H σχετική ατομική μάζα είναι
Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου 2000
 Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου ΕΚΦΩΝΗΕΙ τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό
Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου ΕΚΦΩΝΗΕΙ τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό
ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 2004 ΕΚΦΩΝΗΣΕΙΣ
 ΘΕΜΑ 1ο ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 004 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Στην
ΘΕΜΑ 1ο ΧΗΜΕΙΑ Β ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 004 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Στην
M V n. nm V. M v. M v T P P S V P = = + = σταθερή σε παραγώγιση, τον ορισµό του συντελεστή διαστολής α = 1, κυκλική εναλλαγή 3
 Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος εκεµβρίου 04- (//04. ίνονται οι ακόλουθες πληροφορίες για τον διθειάνθρακα (CS. Γραµµοµοριακή µάζα 76.4 g/mol, κανονικό σηµείο ζέσεως 46 C, κανονικό
Τµήµα Χηµείας Μάθηµα: Φυσικοχηµεία Ι Εξέταση: Περίοδος εκεµβρίου 04- (//04. ίνονται οι ακόλουθες πληροφορίες για τον διθειάνθρακα (CS. Γραµµοµοριακή µάζα 76.4 g/mol, κανονικό σηµείο ζέσεως 46 C, κανονικό
Περιεκτικότητα διαλύματος ονομάζουμε την ποσότητα της διαλυμένης ουσίας που περιέχεται σε ορισμένη μάζα ή όγκο διαλύματος.
 Διαλύματα Περιεκτικότητες 11 Αν ο καθηγητής Χημείας έδινε στους μαθητές του τη δυνατότητα να παρασκευάσουν στο Εργαστήριο Χημείας, ο καθένας χωριστά, ένα υδατικό διάλυμα ζάχαρης, είναι προφανές ότι το
Διαλύματα Περιεκτικότητες 11 Αν ο καθηγητής Χημείας έδινε στους μαθητές του τη δυνατότητα να παρασκευάσουν στο Εργαστήριο Χημείας, ο καθένας χωριστά, ένα υδατικό διάλυμα ζάχαρης, είναι προφανές ότι το
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΧΗΜΕΙΑ Ι Ενότητα 12: Διαλύματα
 ΧΗΜΕΙΑ Ι Ενότητα 12: Διαλύματα Χρυσή Κ. Καραπαναγιώτη Τμήμα Χημείας Ορολογία Ε Δημοτικού, σελ. 23 Μίγματα Διαλύματα Διαλύτης Διαλυμένες ουσίες Ετερογενή Ίζημα Κατηγορίες της ύλης σύμφωνα με τα συστατικά
ΧΗΜΕΙΑ Ι Ενότητα 12: Διαλύματα Χρυσή Κ. Καραπαναγιώτη Τμήμα Χημείας Ορολογία Ε Δημοτικού, σελ. 23 Μίγματα Διαλύματα Διαλύτης Διαλυμένες ουσίες Ετερογενή Ίζημα Κατηγορίες της ύλης σύμφωνα με τα συστατικά
Περιεχόμενα. Κεφάλαιο 1 ΜΕΓΕΘΗ ΚΑΙ ΜΟΝΑΔΕΣ... 9. Κεφάλαιο 2 ΑΤΟΜΙΚΗ ΚΑΙ ΜΟΡΙΑΚΗ ΜΑΖΑ, ΓΡΑΜΜΟΜΟΡΙΑΚΗ ΜΑΖΑ... 25
 Περιεχόμενα Κεφάλαιο 1 ΜΕΓΕΘΗ ΚΑΙ ΜΟΝΑΔΕΣ... 9 Εισαγωγή. Μετρικά συστήματα. Διεθνές Σύστημα Μονάδων. Θερμοκρασία. Άλλες κλίμακες θερμοκρασιών. Ορθή και λανθασμένη χρήση των μονάδων. Μέθοδος του συντελεστή
Περιεχόμενα Κεφάλαιο 1 ΜΕΓΕΘΗ ΚΑΙ ΜΟΝΑΔΕΣ... 9 Εισαγωγή. Μετρικά συστήματα. Διεθνές Σύστημα Μονάδων. Θερμοκρασία. Άλλες κλίμακες θερμοκρασιών. Ορθή και λανθασμένη χρήση των μονάδων. Μέθοδος του συντελεστή
ΑΣΕΠ ΕΚΠΑΙΔΕΥΤΙΚΩΝ 2009. Κλάδος: ΠΕ 04.02 Χημικών ΑΠΑΝΤΗΣΕΙΣ ΕΙΔΙΚΗΣ ΔΙΔΑΚΤΙΚΗΣ
 ΑΣΕΠ ΕΚΠΑΙΔΕΥΤΙΚΩΝ 2009 Κλάδος: ΠΕ 04.02 Χημικών Λίγα λόγια για τα θέματα.. ΑΠΑΝΤΗΣΕΙΣ ΕΙΔΙΚΗΣ ΔΙΔΑΚΤΙΚΗΣ Τα θέματα σε γενικές γραμμές κρίνονται βατά και σχετικά πιο εύκολα από τα θέματα που τέθηκαν στον
ΑΣΕΠ ΕΚΠΑΙΔΕΥΤΙΚΩΝ 2009 Κλάδος: ΠΕ 04.02 Χημικών Λίγα λόγια για τα θέματα.. ΑΠΑΝΤΗΣΕΙΣ ΕΙΔΙΚΗΣ ΔΙΔΑΚΤΙΚΗΣ Τα θέματα σε γενικές γραμμές κρίνονται βατά και σχετικά πιο εύκολα από τα θέματα που τέθηκαν στον
Καταστατική εξίσωση ιδανικών αερίων
 Καταστατική εξίσωση ιδανικών αερίων 21-1. Από τι εξαρτάται η συμπεριφορά των αερίων; Η συμπεριφορά των αερίων είναι περισσότερο απλή και ομοιόμορφη από τη συμπεριφορά των υγρών και των στερεών. Σε αντίθεση
Καταστατική εξίσωση ιδανικών αερίων 21-1. Από τι εξαρτάται η συμπεριφορά των αερίων; Η συμπεριφορά των αερίων είναι περισσότερο απλή και ομοιόμορφη από τη συμπεριφορά των υγρών και των στερεών. Σε αντίθεση
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ
 ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 1. Σε δοχείο σταθερού όγκου και σε σταθερή θερμοκρασία, εισάγονται κάποιες ποσότητες των αερίων Η 2(g) και Ι 2(g) τα οποία αντιδρούν σύμφωνα με
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 1. Σε δοχείο σταθερού όγκου και σε σταθερή θερμοκρασία, εισάγονται κάποιες ποσότητες των αερίων Η 2(g) και Ι 2(g) τα οποία αντιδρούν σύμφωνα με
ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΧΗΜΕΙΑΣ Για τη Β τάξη Λυκείων ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΛΥΣΕΙΣ
 ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΧΗΜΕΙΑΣ 00 Για τη Β τάξη Λυκείων ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΛΥΣΕΙΣ ΘΕΜΑ (Μονάδες 7) -δ, -γ, -α, 4-β 4x= Αύξηση σημείου ζέσεως: H < PH < AsH < NH Χαμηλότερο σ.ζ. έχει το Η διότι το μόριό του είναι
ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΧΗΜΕΙΑΣ 00 Για τη Β τάξη Λυκείων ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΛΥΣΕΙΣ ΘΕΜΑ (Μονάδες 7) -δ, -γ, -α, 4-β 4x= Αύξηση σημείου ζέσεως: H < PH < AsH < NH Χαμηλότερο σ.ζ. έχει το Η διότι το μόριό του είναι
ΟΛΑ ΤΑ ΘΕΜΑΤΑ ΣΤΗ ΔΙΑΛΥΤΟΤΗΤΑ ΑΠΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ
 ΟΛΑ ΤΑ ΘΕΜΑΤΑ ΣΤΗ ΔΙΑΛΥΤΟΤΗΤΑ ΑΠΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ 1. Σε ορισμένη ποσότητα ζεστού νερού διαλύεται μεγαλύτερη ποσότητα ζάχαρης απ ότι σε ίδια ποσότητα κρύου νερού Σωστό ή λάθος; 2. Εξηγήστε τι θα συμβεί,
ΟΛΑ ΤΑ ΘΕΜΑΤΑ ΣΤΗ ΔΙΑΛΥΤΟΤΗΤΑ ΑΠΟ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ 1. Σε ορισμένη ποσότητα ζεστού νερού διαλύεται μεγαλύτερη ποσότητα ζάχαρης απ ότι σε ίδια ποσότητα κρύου νερού Σωστό ή λάθος; 2. Εξηγήστε τι θα συμβεί,
ΚΕΦΑΛΑΙΟ 1o ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ
 ΚΕΦΑΛΑΙΟ 1o ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-50 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Οι δυνάµεις
ΚΕΦΑΛΑΙΟ 1o ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-50 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Οι δυνάµεις
Μοριακός Χαρακτηρισμός Πολυμερών
 Μοριακός Χαρακτηρισμός Πολυμερών Μοριακό Βάρος Πολυμερών Υψηλά όχι ακριβή ΜΒ λόγω τυχαιότητας πολυμερισμού Μίγμα αλυσίδων με διαφορετικό μήκος Μέσο ΜΒ ή κατανομή ΜΒ Βαθμός Πολυμερισμού (DP) = MB πολυμερούς
Μοριακός Χαρακτηρισμός Πολυμερών Μοριακό Βάρος Πολυμερών Υψηλά όχι ακριβή ΜΒ λόγω τυχαιότητας πολυμερισμού Μίγμα αλυσίδων με διαφορετικό μήκος Μέσο ΜΒ ή κατανομή ΜΒ Βαθμός Πολυμερισμού (DP) = MB πολυμερούς
1. Το στοιχείο Χ έχει 17 ηλεκτρόνια. Αν στον πυρήνα του περιέχει 3 νετρόνια περισσότερα από
 Ερωτήσεις Ανάπτυξης 1. Το στοιχείο Χ έχει 17 ηλεκτρόνια. Αν στον πυρήνα του περιέχει 3 νετρόνια περισσότερα από τα πρωτόνια, να υπολογισθούν ο ατομικός και ο μαζικός του στοιχείου Χ 2. Δίνεται 40 Ca. Βρείτε
Ερωτήσεις Ανάπτυξης 1. Το στοιχείο Χ έχει 17 ηλεκτρόνια. Αν στον πυρήνα του περιέχει 3 νετρόνια περισσότερα από τα πρωτόνια, να υπολογισθούν ο ατομικός και ο μαζικός του στοιχείου Χ 2. Δίνεται 40 Ca. Βρείτε
Σημειώσεις Χημείας Α Λυκείου - Κεφάλαιο 1 ο
 ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ ΔΙΑΛΥΜΑΤΩΝ ΔΙΑΛΥΤΟΤΗΤΑ - ΜΕΘΟΔΟΛΟΓΙΑ ΑΣΚΗΣΕΩΝ Γενικά για τα διαλύματα Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων ουσιών, οι οποίες αποτελούν τα συστατικά του διαλύματος.
ΔΙΑΛΥΜΑΤΑ ΠΕΡΙΕΚΤΙΚΟΤΗΤΕΣ ΔΙΑΛΥΜΑΤΩΝ ΔΙΑΛΥΤΟΤΗΤΑ - ΜΕΘΟΔΟΛΟΓΙΑ ΑΣΚΗΣΕΩΝ Γενικά για τα διαλύματα Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων ουσιών, οι οποίες αποτελούν τα συστατικά του διαλύματος.
τα βιβλία των επιτυχιών
 Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
( α πό τράπεζα θεµάτων) ΚΕΦΑΛΑΙΟ 1 : ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ. 1. Να χαρακτηρίσετε τις επόµενες προτάσεις ως σωστές (Σ) ή λανθασµένες (Λ).
 Χηµεία Α Λυκείου Φωτεινή Ζαχαριάδου 1 από 12 ( α πό τράπεζα θεµάτων) ΚΕΦΑΛΑΙΟ 1 : ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1. Να χαρακτηρίσετε τις επόµενες προτάσεις ως σωστές (Σ) ή λανθασµένες (Λ). α) Ένα µείγµα είναι πάντοτε
Χηµεία Α Λυκείου Φωτεινή Ζαχαριάδου 1 από 12 ( α πό τράπεζα θεµάτων) ΚΕΦΑΛΑΙΟ 1 : ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 1. Να χαρακτηρίσετε τις επόµενες προτάσεις ως σωστές (Σ) ή λανθασµένες (Λ). α) Ένα µείγµα είναι πάντοτε
Νίκος Ξεκουκουλωτάκης. Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος. Γραφείο Κ1.122, τηλ.:28210-37796 e-mail:nikosxek@gmail.
 Υδατική Χημεία Νίκος Ξεκουκουλωτάκης Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ1.122, τηλ.:28210-37796 e-mail:nikosxek@gmail.com Σύγγραμμα 2 Άσκηση εμπέδωσης Σε κλειστό δοχείο αναμιγνύονται
Υδατική Χημεία Νίκος Ξεκουκουλωτάκης Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ1.122, τηλ.:28210-37796 e-mail:nikosxek@gmail.com Σύγγραμμα 2 Άσκηση εμπέδωσης Σε κλειστό δοχείο αναμιγνύονται
1. Ο ατμοσφαιρικός αέρας, ως αέριο μίγμα, είναι ομογενές. Άρα, είναι διάλυμα.
 2.8 Διαλύματα Υπόδειξη: Στα αριθμητικά προβλήματα, τα πειραματικά μεγέθη που δίνονται με ένα ή δύο σημαντικά ψηφία θεωρούνται ότι πρακτικά έχουν 3 ή 4 σημαντικά ψηφία. 1. Ο ατμοσφαιρικός αέρας, ως αέριο
2.8 Διαλύματα Υπόδειξη: Στα αριθμητικά προβλήματα, τα πειραματικά μεγέθη που δίνονται με ένα ή δύο σημαντικά ψηφία θεωρούνται ότι πρακτικά έχουν 3 ή 4 σημαντικά ψηφία. 1. Ο ατμοσφαιρικός αέρας, ως αέριο
Διαλυτότητα. Μάθημα 7
 Διαλυτότητα 7.1. SOS: Τι ονομάζουμε διαλυτότητα μιας χημικής ουσίας σε ορισμένο διαλύτη; Διαλυτότητα είναι η μέγιστη ποσότητα της χημικής ουσίας που μπορεί να διαλυθεί σε ορισμένη ποσότητα του διαλύτη,
Διαλυτότητα 7.1. SOS: Τι ονομάζουμε διαλυτότητα μιας χημικής ουσίας σε ορισμένο διαλύτη; Διαλυτότητα είναι η μέγιστη ποσότητα της χημικής ουσίας που μπορεί να διαλυθεί σε ορισμένη ποσότητα του διαλύτη,
ΕΚΦΕ Τρικάλων. Πειραματική Δοκιμασία στη Χημεία. Τοπικός Μαθητικός Διαγωνισμός. Τρίκαλα, Σάββατο, 8 Δεκεμβρίου 2012
 1 Τοπικός Μαθητικός Διαγωνισμός 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2013 11Η ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΕΠΙΣΤΗΜΩΝ EUSO 2013 ΕΚΦΕ Τρικάλων Πειραματική Δοκιμασία στη Χημεία Τοπικός Μαθητικός Διαγωνισμός Τρίκαλα,
1 Τοπικός Μαθητικός Διαγωνισμός 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2013 11Η ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΕΠΙΣΤΗΜΩΝ EUSO 2013 ΕΚΦΕ Τρικάλων Πειραματική Δοκιμασία στη Χημεία Τοπικός Μαθητικός Διαγωνισμός Τρίκαλα,
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου 1999
 Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου 1999 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Αν διαλύσουµε σε νερό κάποια στερεά ουσία µε αµελητέα τάση ατµών, τότε η τάση ατµών του διαλύµατος που προκύπτει, σε σχέση µε την
Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου 1999 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Αν διαλύσουµε σε νερό κάποια στερεά ουσία µε αµελητέα τάση ατµών, τότε η τάση ατµών του διαλύµατος που προκύπτει, σε σχέση µε την
