ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ. ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ
|
|
|
- Ἥβη Γεννάδιος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ 1
2 Δομή των αμινοξέων Τα αμινοξέα περιέχουν στο μόριο τους: Καρβοξύλιο και αμινομάδα. Τα αμινοξέα των πρωτεϊνών είναι α-αμινοξέα. Συνέπειες: Έχουν *C (α-άνθρακας) με υποκαταστάτες: Το καρβοξύλιο, Την αμινομάδα, Ένα άτομο υδρογόνου, Μια πλευρική ομάδα (R) διαφορετική για κάθε αμινοξύ. Ανήκουν στην L-στερεοχημική οικογένεια. 2
3 3
4 Αμινοξέα Στη φύση συναντώνται 700 αμινοξέα, όμως στη σύνθεση των λευκωμάτων συμμετέχουν 20. Τα αμινοξέα χωρίζονται στα άπολα, δηλαδή αυτά που φέρουν μη-φορτισμένες πλευρικές ομάδες (R) και στα πολικά που φέρουν φορτισμένες πλευρικές ομάδες. Επίσης, σε αρωματικά αμινοξέα, δηλαδή μόρια που φέρουν αρωματικούς δακτυλίους. Τα πολικά αμινοξέα, σε φυσιολογικό ph, χωρίζονται σε αυτά που φέρουν καρβοξυλομάδες και σε αυτά που φέρουν αμινομάδες ως πλευρικές ομάδες (αναφέρονται και ως όξινα ή βασικά αμινοξέα). 4
5 Ονοματολογία αμινοξέων Η ισομορφή που συναντάται στα κύτταρα είναι αυτή των L-αμινοξέων 5
6 Δεξιόστροφα (+) και αριστερόστροφα (-) αμινοξέα 6
7 Κατάταξη αμινοξέων Με βάση τη συμπεριφορά τους απέναντι στο νερό: Yδρόφοβα: Αλανίνη, Βαλίνη, Ισολευκίνη, Λευκίνη, Μεθειονίνη, Προλίνη, Τρυπτοφάνη, Φαινυλαλανίνη. Yδρόφιλα: Γλυκίνη, Σερίνη, Θρεονίνη, Ασπαραγγίνη, Κυστείνη, Γλουταμίνη, Τυροσίνη. Όξινα: Ασπαραγγινικό Οξύ, Γλουταμικό Οξύ. Βασικά: Λυσίνη, Αργινίνη, Ιστιδίνη. 7
8 Κατάταξη αμινοξέων Με βάση τα χημικά τους χαρακτηριστικά: Αλειφατικά: Γλυκίνη, Αλανίνη, Βαλίνη, Ισολευκίνη, Λευκίνη (τα τρία τελευταία αμινοξέα διακλαδισμένης αλυσίδας). Αρωματικά: Φαινυλαλανίνη, Τυροσίνη, Τρυπτοφάνη. Θειούχα: Κυστείνη, Μεθειονίνη. Υδρόξυ-αμινοξέα: Σερίνη, Θρεονίνη. Αμίδια οξέων: Ασπαραγγίνη, Γλουταμίνη. Δικαρβονικά οξέα: Ασπαραγγινικό, Γλουταμικό. Βασικά αμινοξέα: Αργινίνη, Ιστιδίνη, Λυσίνη. Ιμινοξέα: Προλίνη. 8
9 Αμινοξέα Αλειφατικά Αμινοξέα Γλυκίνη (Gly,G) Αλανίνη (Ala, A) Βαλίνη (Val, V)* Λευκίνη (Leu, L)* Ισολευκίνη (Ile, I)* Αμινοξέα με υδροξυ- και σουλφο- ομάδες Σερίνη (Ser, S) Κυστεϊνη (Cys, C) Θρεονίνη (Thr, T)* Μεθειονίνη (Met, M)* 9
10 Αμινοξέα Αρωματικά Αμινοξέα Βασικά Αμινοξέα Φαινυλαλανίνη (Phe, P)* Τυροσίνη, (Tyr, Y) Όξινα Αμινοξέα και τα Αμίδιά τους Θρυπτοφάνη (Trp, W)* Ιστιδίνη (His, H) Λυσίνη (Lys, K)* Κυκλικό Αμινοξύ Αργινίνη (Arg, R) Ασπαρτικό οξύ (Asp, D) Γλουταμικό οξύ (Glu, E) Ασπαραγίνη (Asn, N) Γλουταμίνη (Gln, Q) Προλίνη (Pro, P) 10
11 Ασυνήθιστα αμινοξέα Δεν συμμετέχουν στη δομή των πρωτεϊνών: β-αλανίνη (παντοθενικό οξύ), Κιτρουλλίνη (κύκλος της ουρίας), Ορνιθίνη (κύκλος της ουρίας), γ-αμινο-βουτυρικό οξύ (GABA, νευροδιαβιβαστής), D-αλανίνη (κυτταρικό τοίχωμα βακτηρίων), D-σερίνη (κυτταρικό τοίχωμα βακτηρίων). Προϊόντα μετασχηματισμού αμινοξέων: 4-υδροξυ-προλίνη, 5-υδροξυ-λυσίνη, κ.λπ. 11
12 Ασυνήθιστα αμινοξέα 12
13 Συνέπειες της παρουσίας -COOH και -NH2 Σε ουδέτερα διαλύματα έχουν μορφή διπολικού ιόντος, Εμφανίζουν ισοηλεκτρικό σημείο (Ι.Σ.), Έχουν pk στην όξινη και στην αλκαλική περιοχή. Συνέπειες της παρουσίας της πλευρικής ομάδας: Οι τιμές pk διαφορετικές για κάθε αμινοξύ, Διαφορές στις ιονίσιμες ομάδες της πλευρικής ομάδας. 13
14 Οξεοβασικές Ιδιότητες Αμινοξέων (π.χ. ΑLA) Ισοδύναμα ΟΗ - 14
15 Οξεοβασικές Ιδιότητες Αμινοξέων Το σημείο που το φορτίο του αμινοξέος είναι μηδέν (0) ονομάζεται ισοηλεκτρικό σημείο pi pk 1 pk 2 2 Αμινοξύ pk 1 pk 2 pk 3 pi Αλανίνη 2,35 9,69-6,02 Αλανίνη Ασπαρτικό οξύ Ασπαρτικό οξύ 1,8 3,7 9,6 2,8 Λυσίνη Λυσίνη 2,2 9,0 10,5 9,7 15
16 16
17 Χημικές Ιδιότητες Αμινοξέων Αντιδράσεις του α-cooh NaBH 4 R C H 2 OH + H 2 O Αναγωγή NH2CH C 2 H 5 OH R C H NH 2 COOC 2 H 5 + H 2 O Εστεροποίηση R C H NH 2 COOH Αποκαρβοξυλίωση + R C H2 NH 2 CO 2 NaOCl + H 2 O Οξείδωση + + RCHO NH 3 NaCl CO 2 + NaOH R C H NH 2 COONa + H 2 O Αντίδραση παραγωγής γλουταμινικού νατρίου 17
18 Χημικές Ιδιότητες Αμινοξέων Αντιδράσεις της α-νη 2 R COCl Ακυλίωση R C H N H COOH COR' + HCl NO 2 O 2 N F NO 2 Αλκυλίωση O 2 N N H C H R COOH + HF R C H NH 2 COOH HNO 2 R C H + N 2 + H 2 O OHCOOH HCHO R C H N CH 2 + H 2 O COOH 18
19 Χημικές Ιδιότητες Αμινοξέων Αντιδράσεις της α-νη 2 (συνέχεια) Αντιδράσεις Maillard R C H NH 2 COOH + R'-CHO R C H N COOH C H R' + H 2 O Αντίδραση με νινυδρίνη 1. R C H NH 2 COOH O + O + H 2 O O O O CHOH + R-CHO + ΝΗ 3 + CO 2 2. O O ONH 4 O CHOH + O + 2ΝΗ N 3 + 2H 2 O O (Η προλίνη και η υδρόξυ-προλίνη δίνουν κίτρινο παράγωγο) O O O Μπλε χρώμα 19
20 Χημικές Ιδιότητες Αμινοξέων Αντιδράσεις της σουλφυδριλικής ομάδας H 2 HOOC C C SH οξείδωση HOOC C H C H2 H2 NH 2 S S C H2 C H NH 2 COOH NH 2 κυστεΐνη κυστίνη 20
21 Η δημιουργία του πεπτιδικού δεσμού 21
22 22
23 Κατάταξη των Πρωτεϊνών ΠΡΩΤΕΪΝΕΣ Απλές Σύνθετες Σφαιρικές Γλοβουλίνες Αλβουμίνες Γλουτελίνες Προλαμίνες Ινώδεις Κολλαγόνο Ελαστίνη Κερατίνη Γλυκοπρωτεΐνες Λιποπρωτεΐνες Μεταλλοπρωτεΐνες Νουκλεοπρωτεΐνες Φωσφοπρωτεΐνες 23
24 Ταξινόμηση ανάλογα με τις φυσικές ιδιότητες Αλβουμίνες (διαλύονται στο νερό), Γλοβουλίνες (διαλύονται σε αραιά διαλύματα ηλεκτρολυτών), Γλουτελίνες (διαλύονται σε αραιά διαλύματα οξέων-βάσεων), Προλαμίνες (διαλύονται σε αλκοόλη 70-80ο, ζεϊνη, γλοιαδίνη), Σκληροπρωτεΐνες (αδιάλυτες, ελαστίνη, κερατίνη, φιβροϊνη), Ιστόνες (έχουν ισχυρά βασικό χαρακτήρα). 24
25 25
26 Οι συζευγμένες πρωτεΐνες ως προς την προσθετική ομάδα Νουκλεοπρωτεϊνες (νουκλεϊνικά οξέα, συστατικά της χρωματίνης), Χρωμοπρωτεϊνες (έγχρωμη προσθετική ομάδα, αιμοσφαιρίνη), Φωσφορο-πρωτεΐνες (φωσφορικό οξύ, καζεΐνη), Γλυκοπρωτεΐνες (ανοσοσφαιρίνες, βλεννο-πρωτεΐνες, λεκτίνες), Λιποπρωτεΐνες. 26
27 Δομή των Πρωτεϊνών Πρωτοταγής Δομή Αλληλουχία αμινοξέων A A S X D X S L V E V H X X V F I V P P X I L Q A V V S I A 31 T T R X D D X D S A A A S I P M V P G W V L K Q V X G S Q A 61 G S F L A I V M G G G D L E V I L I X L A G Y Q E S S I X A 91 S R S L A A S M X T T A I P S D L W G N X A X S N A A F S S 121 X E F S S X A G S V P L G F T F X E A G A K E X V I K G Q I 151 T X Q A X A F S L A X L X K L I S A M X N A X F P A G D X X 181 X X V A D I X D S H G I L X X V N Y T D A X I K M G I I F G 211 S G V N A A Y W C D S T X I A D A A D A G X X G G A G X M X 241 V C C X Q D S F R K A F P S L P Q I X Y X X T L N X X S P X 271 A X K T F E K N S X A K N X G Q S L R D V L M X Y K X X G Q 301 X H X X X A X D F X A A N V E N S S Y P A K I Q K L P H F D 331 L R X X X D L F X G D Q G I A X K T X M K X V V R R X L F L 361 I A A Y A F R L V V C X I X A I C Q K K G Y S S G H I A A X 391 G S X R D Y S G F S X N S A T X N X N I Y G W P Q S A X X S 421 K P I X I T P A I D G E G A A X X V I X S I A S S Q X X X A 451 X X S A X X A Π.χ. Εξωκινάση 27
28 Πρωτοταγής δομή Είναι η αλληλουχία των αμινοξέων στην πεπτιδική αλυσίδα. Τα αμινοξέα καθορίζουν τη δυνατότητα περιστροφής. Τα αμινοξέα καθορίζονται από τη δομή του αντίστοιχου γονιδίου. Τα στάδια για τον προσδιορισμό πρωτοταγούς δομής είναι: απομόνωση και καθαρισμός της πρωτεΐνης, προσδιορισμός της σύστασης σε αμινοξέα, πολλαπλή ειδική υδρόλυση με διαφορετικό μέσο κάθε φορά, διαχωρισμός των μερικών πεπτιδίων κάθε φορά, προσδιορισμός των ακραίων αμινοξέων στα πεπτίδια, προσδιορισμός της πρωτοταγούς δομής των πεπτιδίων, προσδιορισμός των ακραίων αμινοξέων της πρωτεΐνης. 28
29 Δομή των Πρωτεϊνών Δευτεροταγής - α-έλικα Υδρόφιλα R: προς τα έξω Δεσμοί Η 3,6 αμινοξέα ανά στροφή Υδρόφοβα R: προς τα μέσα 29
30 Δευτεροταγής δομή Αιτιολόγηση της σταθερής δομής στο χώρο. Διαμόρφωση α-έλικας: γεωμετρικά χαρακτηριστικά, σύναψη δεσμών υδρογόνου, παραδείγματα. Διαμόρφωση πτυχωτής επιφάνειας: σύναψη δεσμών υδρογόνου, παράλληλη και αντιπαράλληλη φορά της πεπτιδικής αλυσίδας, παραδείγματα. 30
31 Δομή των Πρωτεινών Δευτεροταγής -β-πτυχωτό φύλλο στροφή αντι-παράλληλο παράλληλο 31
32 Διαφορές ΜΟΡΦΩΝ ΔΕΥΤΕΡΟΤΑΓΟΥΣ ΔΟΜΗΣ α-έλικα Στην α-έλικα η πρωτεΐνη αναδιπλώνεται με τη βοήθεια δεσμών υδρογόνου μεταξύ αμινοξέων της ΙΔΙΑΣ πολυπεπτιδικήςαλυσίδας τα οποία είναι σε κοντινή μεταξύ τους απόσταση. Έτσι η πρωτεΐνη παίρνει ελικοειδή μορφή με 3,6 αμινοξέα για κάθε σπείρα (18 αμινοξέα για κάθε 5 σπείρες). β-πτυχωτή επιφάνεια Στη β-πτυχωτή επιφάνεια η αναδίπλωση γίνεται με την βοήθεια δεσμών υδρογόνου κυρίως μεταξύ ΔΙΑΦΟΡΕΤΙΚΩΝ πολυπεπτιδικών αλυσίδων του ίδιου πρωτεϊνικού μορίου. Έτσι, η πρωτεΐνη αποκτά σχήμα επιφάνειας με πτυχώσεις. 32
33 Δομή των Πρωτεινών Τριτοταγής Τεταρτοταγής 33
34 Τριτοταγής δομή Εκτροπή από την δευτεροταγή δομή: στερεοχημική παρεμπόδιση, η παρουσία της προλίνης. Επιπλέον σταθεροποίηση του πρωτεϊνικού μορίου. Δεσμοί υδρογόνου: περιοχές αποκλεισμού νερού. Ιοντικές επιδράσεις: αφετηρία οι ιονίσιμες ομάδες, η διηλεκτρική σταθερά, η ιδιαιτερότητα του νερού. Υδρόφοβες ή απολικές επιδράσεις: υδρόφοβες ομάδες, παρουσία των υδρόφοβων αμινοξέων, αποφυγή νερού. Δυνάμεις van der Waals: υδρόφοβες ομάδες. Δισουλφιδικές γέφυρες: οξείδωση σουλφυδρυλίων. 34
35 Τεταρτοταγής δομή Αναφέρεται σε πρωτεΐνες με περισσότερες πεπτιδικές αλυσίδες. Χρησιμοποιεί τις σταθεροποιητικές δυνάμεις της τριτοταγούς δομής. Παράδειγμα, η δομή της αιμοσφαιρίνης. 35
36 Κολλαγόνο Ιδιόρρυθμη τριπλή έλικα 36
37 Ισοηλεκτρικό σημείο Περισσότερες όξινες ομάδες χαμηλό Περισσότερες βασικές ομάδες υψηλό Διαλυτότητα ph Άλατα (εναλάτωση, εξαλάτωση) Οργανικοί διαλύτες Θερμοκρασία Υδρόλυση με οξέα, βάσεις ή ένζυμα θερμανση Μετουσίωση Φυσικές ιδιότητες Ζελατινοποίηση Κολλαγόνο Θέρμανση, οξύ ή άλκαλι Προσθήκη ζεστού νερού διόγκωση ζελατίνης Συγκράτηση μεγάλης ποσότητας νερού στο πλέγμα Θέρμανση υδρόλυμα Ψύξη πηκτή 37
38 Μετουσίωση Φυσικές ιδιότητες Φυσικοί παράγοντες φυσική μετουσιωμένη Θερμοκρασία Μηχανική επεξεργασία Πίεση Αφρός 38
39 Η αύξηση της θερμοκρασίας προκαλεί: μείωση της ισχύος των δεσμών υδρογόνου, μείωση της ισχύος των ιοντικών επιδράσεων, μείωση των δυνάμεων van der Waals, ισχυροποίηση των Θέρμανση πρωτεΐνης υδρόφοβων επιδράσεων. 39
40 Υδρόλυση του πεπτιδικού δεσμού με ισχυρά οξέα: συνθήκες (120 οc, για ώρες), Συνέπειες: καταστροφή της τρυπτοφάνης, μερική καταστροφή της σερίνης και θρεονίνης, Φυσική-χημική υδρόλυση υδρόλυση των αμιδίων. 40
41 Η εξειδίκευση των πρωτεολυτικών ενζύμων στην προέλευση του καρβοξυλίου του πεπτιδικού δεσμού: η τρυψίνη στα βασικά αμινοξέα, η χυμοτρυψίνη στα αρωματικά αμινοξέα, η θερμολυσίνη σε λευκίνη, ισολευκίνη, βαλίνη (υδρόφοβα), η καρβοξυπεπτιδάση στο καρβοξυ-τελικό αμινοξύ. Ενζυμική υδρόλυση 41
42 Φυσικές ιδιότητες Μετουσίωση - Χημικοί παράγοντες Οργανικοί διαλύτες Οξέα Βάσεις Απορρυπαντικά RCOO - 42
43 Ανάλυση των πρωτεϊνών Μέθοδος Kjeldahl Αναλύεται το πρωτεινικό άζωτο. Το Ν σε gr πολλαπλασιάζεται με ένα συντελεστή ( 6,25) για τη μετατροπή σε gr πρωτείνης. Φασματοφωτομετρικά Μέτρηση στα 280nm (απορρόφηση τυροσίνης). Αντίδραση της διουρίας (σε αλκαλικό διάλυμα CuSO4). Αντίδραση Lowry (με το αντιδραστήριο Folin-Ciocalteau). 43
44 Βιολογικός ρόλος των πρωτεϊνών 1. Το κύριο συστατικό του μυϊκού ιστού είναι οι πρωτεΐνες. Τα μυοϊνίδια αποτελούνται κυρίως από παχειές ίνες της πρωτεΐνης μυοσίνης και λεπτές ίνες των πρωτεϊνών ακτίνης και τροπομυοσίνης. Η μυϊκή συστολή ρυθμίζεται από τη συγκέντρωση ιόντων Ca+2, τα οποία αντιδρούν με μία άλλη σημαντική πρωτεΐνη του μυϊκού ιστού, την τροπονίνη. Επίσης πρωτεΐνες όπως η ελαστίνη και το κολλαγόνο είναι συστατικά των συνδέσμων των οστών και του συνδετικού ιστού αντίστοιχα. 44
45 Βιολογικός ρόλος των πρωτεϊνών 2. Άλλες πρωτεΐνες έχουν ορμονική δράση. Για παράδειγμα, η ινσουλίνη και η γλυκαγόνη είναι ορμόνες πεπτιδικής φύσεως, που εκκρίνονται από το πάγκρεας και ρυθμίζουν τη συγκέντρωση του σακχάρου στο αίμα. 3. Άλλες πρωτεΐνες έχουν μεταφορικό ρόλο. Για παράδειγμα, η αιμοσφαιρίνη είναι υπεύθυνη για την μεταφορά οξυγόνου στο αίμα, ενώ η μυοσφαιρίνη είναι υπεύθυνη για την πρόσληψη οξυγόνου από τους μυς. 45
46 Βιολογικός ρόλος των πρωτεϊνών 4. Τα διάφορα αντισώματα, με τα οποία ο οργανισμός του ανθρώπου ή των ζώων αμύνεται στην εισβολή ενός ξένου σώματος, είναι πρωτεΐνες που παράγονται από τον ίδιο τον οργανισμό και έχουν δομή τέτοια, που τις καθιστά ειδικές στο να δεσμεύουν και να εξουδετερώνουν το ξένο σώμαεισβολέα, που ονομάζεται γενικά αντιγόνο. Πρόκειται δηλαδή για αμυντικές πρωτεΐνες. 5. Τα διάφορα ένζυμα είναι σώματα με πρωτεϊνική δομή. Για παράδειγμα, το ένζυμο ριβονουκλεάση είναι πρωτεΐνη αποτελούμενη από 124 αμινοξέα. 46
47 Βιολογικός ρόλος των πρωτεϊνών 6. O ρόλος άλλων πρωτεϊνών είναι αποθηκευτικός. Για παράδειγμα, η καζεΐνη -πρωτεΐνη του γάλακτος, έχει ως ρόλο την αποθήκευση ασβεστίου, ενώ η ωαλβουμίνη, που είναι κύριο συστατικό στο ασπράδι του αβγού, είναι πηγή αμινοξέων για το αναπτυσσόμενο έμβρυο. 7. Στη μεμβράνη των κυττάρων υπάρχουν πρωτεΐνες υποδοχείς, ο ρόλος των οποίων είναι να αναγνωρίζουν και να συνδέονται με ουσίες σημαντικές για το μεταβολισμό των κυττάρων. Είναι συνήθως γλυκοπρωτεΐνες. 47
48 Χρησιμότητα των πρωτεϊνών Απαραίτητες στην ανάπτυξη, δομή, διαμόρφωση σώματος, Σύνθεση ιστών αντικατάσταση φθορών, Πρώτη ύλη για πεπτικά υγρά, ορμόνες, πλάσμα, ένζυμα κ.α. Πηγή ενέργειας, Ρυθμιστικές ιδιότητες. 48
49 49
50 Πρωτεΐνες πλάσματος αίματος ΑΛΒΟΥΜΙΝΗ (ΛΕΥΚΩΜΑΤΙΝΗ) 3,5-5 g/dlή g/l Η κύρια πρωτεΐνη πλάσματος 50
51 Ανάλυση των πρωτεϊνών του ορού αίματος, ηλεκτροφορητικά και ποσοτικά Ο ΟΡΟΣ ΛΑΜΒΑΝΕΤΑΙ ΜΕΤΑ ΤΗΝ ΠΗΞΗ ΤΟΥ ΑΙΜΑΤΟΣ, ΑΡΑ ΣΤΙΣ ΠΑΡΑΠΑΝΩ ΤΙΜΕΣ ΔΕΝ ΣΥΜΠΕΡΙΛΑΜΒΑΝΟΝΤΑΙ ΟΙ ΠΡΩΤΕΪΝΕΣ ΤΗΣ ΠΗΞΗΣ (ΙΝΩΔΟΓΟΝΟ Ή ΦΙΜΠΡΙΝΟΓΟΝΟ) 51
52 Ο ρόλος της αλβουμίνης του πλάσματος/ορού 52
53 Εργαστηριακοί δείκτες θρέψης βάσει πρωτεϊνών 53
54 Τρόπος πρόσκτησης των αμινοξέων Ο ανθρώπινος οργανισμός χρειάζεται τα αμινοξέα, για να συνθέσει πρωτεΐνες και πεπτίδια. Πού βρίσκει όμως τα αμινοξέα; Δύο είναι οι τρόποι: α) από τις πρωτεΐνες της τροφής, οι οποίες υδρολύονται απελευθερώνοντας αμινοξέα, β) από άλλες πρώτες ύλες συνθέτοντας τα. Τα αμινοξέα που μπορούν να συντεθούν από τον οργανισμό ονομάζονται μη απαραίτητα, σε αντίθεση με εκείνα που είναι αναγκασμένος να τα προμηθεύεται αποκλειστικά από πρωτεϊνούχα τρόφιμα. Αυτά χαρακτηρίζονται ως απαραίτητα: λυσίνη, λευκίνη, ισολευκίνη, βαλίνη, φαινυλαλανίνη, θρεονίνη, μεθειονίνη και τρυπτοφάνη. 54
55 Τρόπος πρόσκτησης των αμινοξέων Εκτός όμως από τα παραπάνω, τα αμινοξέα ιστιδίνη και αργινίνη αν και μπορούν να συντεθούν από τον ανθρώπινο οργανισμό, παρουσιάζουν πολύ μικρό ρυθμό βιοσύνθεσης για να καλυφθούν οι ανάγκες σε ορισμένες περιπτώσεις. Συγκεκριμένα, σε αναπτυσσόμενους οργανισμούς η ιστιδίνη αποτελεί απαραίτητο αμινοξύ λόγω της αυξημένης ανάγκης του για τη συνεχή δημιουργία νέων ιστών. Για το λόγο αυτό τα δύο αυτά αμινοξέα ονομάζονται ημιαπαραίτητα. 55
πρωτεΐνες πολυμερείς ουσίες δομούν λειτουργούν λευκώματα 1.Απλές πρωτεΐνες 2.Σύνθετες πρωτεΐνες πρωτεΐδια μη πρωτεϊνικό μεταλλοπρωτεΐνες
 ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
Δρ. Ιωάννης Τσαγκατάκης Σύμβουλος Διατροφικής Αγωγής. Οι Πρωτεΐνες. Ένωση Ελλήνων Χημικών Περιφερειακό Τμήμα Κρήτης
 Δρ. Ιωάννης Τσαγκατάκης Σύμβουλος Διατροφικής Αγωγής Οι Πρωτεΐνες Ένωση Ελλήνων Χημικών Περιφερειακό Τμήμα Κρήτης Αμινοξέα, Πεπτίδια, Πρωτεΐνες, Ένζυμα Πεπτιδικός δεσμός Αμινοξέα Πεπτίδια (
Δρ. Ιωάννης Τσαγκατάκης Σύμβουλος Διατροφικής Αγωγής Οι Πρωτεΐνες Ένωση Ελλήνων Χημικών Περιφερειακό Τμήμα Κρήτης Αμινοξέα, Πεπτίδια, Πρωτεΐνες, Ένζυμα Πεπτιδικός δεσμός Αμινοξέα Πεπτίδια (
Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου
 Πρωτεΐνες 1 Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου Οι πρωτεΐνες είναι πολύπλοκα µόρια που περιέχουν 2 Είναι πηγές αµινοξέων (απαραίτητα, µη απαραίτητα)
Πρωτεΐνες 1 Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου Οι πρωτεΐνες είναι πολύπλοκα µόρια που περιέχουν 2 Είναι πηγές αµινοξέων (απαραίτητα, µη απαραίτητα)
MAΘΗΜΑ 4 ο AMINOΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ
 MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
COOH R 2. H α-αμινοξύ 2
 7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
Κεφάλαιο 22 Πρωτεΐνες
 Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων. 1/10/2015 Δ.Δ. Λεωνίδας
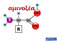 αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
Κεφάλαιο 1. Οι δομικοί λίθοι
 Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν;
 Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
Η πλειοψηφία των αμινοξέων είναι του τύπου :
 ΚΕΦΑΛΑΙΟ 5 Η πλειοψηφία των αμινοξέων είναι του τύπου : H 2 NCHCOOH R O συνδυασμός καρβοξυλίου και αμινομάδας στο μόριό τους έχει ως αποτέλεσμα να συμπεριφέρονται είτε ως οξέα είτε ως βάσεις (αμφολύτες).
ΚΕΦΑΛΑΙΟ 5 Η πλειοψηφία των αμινοξέων είναι του τύπου : H 2 NCHCOOH R O συνδυασμός καρβοξυλίου και αμινομάδας στο μόριό τους έχει ως αποτέλεσμα να συμπεριφέρονται είτε ως οξέα είτε ως βάσεις (αμφολύτες).
ΠΡΩΤΕΪΝΕΣ. Φατούρος Ιωάννης Αναπληρωτής Καθηγητής
 ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
3.1. Γενικά για τις πρωτείνες
 Π ρ ω τ ε ί ν ε ς 3.1. Γενικά για τις πρωτείνες Οι πρωτεΐνες είναι ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Αλλωστε το όνομά τους υποδηλώνει το ρόλο αυτό. Αποτελούν απαραίτητο στοιχείο για κάθε
Π ρ ω τ ε ί ν ε ς 3.1. Γενικά για τις πρωτείνες Οι πρωτεΐνες είναι ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Αλλωστε το όνομά τους υποδηλώνει το ρόλο αυτό. Αποτελούν απαραίτητο στοιχείο για κάθε
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
 1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α
 Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ
 ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α
 Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
 ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
Διαλέξεις Χημείας Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων
 Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ
 ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ Παππάς Χρήστος Επίκουρος καθηγητής ΑΜΙΝΟΞΕΑ Αμινοξέα είναι οργανικά μόρια που διαθέτουν καρβοξύλιο (-α) και αμινομάδα (-ες). Πλευρική αλυσίδα R NH 2 α O α- αμινοξύ OH Είναι
ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ Παππάς Χρήστος Επίκουρος καθηγητής ΑΜΙΝΟΞΕΑ Αμινοξέα είναι οργανικά μόρια που διαθέτουν καρβοξύλιο (-α) και αμινομάδα (-ες). Πλευρική αλυσίδα R NH 2 α O α- αμινοξύ OH Είναι
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ»
 «ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
Αμινοξέα-Πεπτίδια-Πρωτείνες
 Αμινοξέα-Πεπτίδια-Πρωτείνες Αμινοξέα είναι χημικές ενώσεις με τουλάχιστον μία αμινική και μία καρβοξυλική ομάδα. Αμινοξέα των πρωτεϊνών είναι περίπου 20, και έχουν όλα την αμινοομάδα σε α-θέση ως προς
Αμινοξέα-Πεπτίδια-Πρωτείνες Αμινοξέα είναι χημικές ενώσεις με τουλάχιστον μία αμινική και μία καρβοξυλική ομάδα. Αμινοξέα των πρωτεϊνών είναι περίπου 20, και έχουν όλα την αμινοομάδα σε α-θέση ως προς
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ
 ΚΕΦΑΛΑΙΟ 1ο ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ 2010-11 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 1 ο : ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΚΑΙ ΒΙΟΧΗΜΕΙΑ 1. Τι είναι η Βιοχημεία και με ποιες ενώσεις ασχολείται. 2. Πόσα και ποια στοιχεία
ΚΕΦΑΛΑΙΟ 1ο ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ 2010-11 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 1 ο : ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΚΑΙ ΒΙΟΧΗΜΕΙΑ 1. Τι είναι η Βιοχημεία και με ποιες ενώσεις ασχολείται. 2. Πόσα και ποια στοιχεία
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ
 ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
Αμινοξέα-Πεπτίδια-Πρωτείνες
 Αμινοξέα-Πεπτίδια-Πρωτείνες Αμινοξέα είναι χημικές ενώσεις με τουλάχιστον μία αμινική και μία καρβοξυλική ομάδα. Αμινοξέα των πρωτεϊνών είναι περίπου 20, και έχουν όλα την αμινοομάδα σε α- θέση ως προς
Αμινοξέα-Πεπτίδια-Πρωτείνες Αμινοξέα είναι χημικές ενώσεις με τουλάχιστον μία αμινική και μία καρβοξυλική ομάδα. Αμινοξέα των πρωτεϊνών είναι περίπου 20, και έχουν όλα την αμινοομάδα σε α- θέση ως προς
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράμμα που αντιστοιχεί στη σωστή απάντηση:
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
Οργανική Χημεία. Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες
 Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής
 Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών.
 ΑΜΙΝΟΞΕΑ Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών. Ο γενικός μοριακός τύπος ενός α- αμινοξέος παρουσιάζεται στο διπλανό σχήμα και συνίσταται
ΑΜΙΝΟΞΕΑ Τα αμινοξέα αποτελούν τις δομικές μονάδες των πρωτεϊνών και αποτελούν βασικό στοιχείο των οργανισμών. Ο γενικός μοριακός τύπος ενός α- αμινοξέος παρουσιάζεται στο διπλανό σχήμα και συνίσταται
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
Μεταβολισμός πρωτεϊνών και των αμινοξέων
 Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
Μεταβολισμός πρωτεϊνών και των αμινοξέων Πρωτεΐνες Πολυσακχαρίτες Λίπη Γαλακτικό Γλυκόζη Αμινοξέα Πρωτεΐνες οργανισμού Δεξαμενή Αζώτου Πυροστα φυλικό Γλυκονεογένεση Γλυκόλυση Acetyl-CoA 6- φωσφορική Γλυκόζη
β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]
![β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ] β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]](/thumbs/92/111021029.jpg) ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1ο Στις προτάσεις
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1ο Στις προτάσεις
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
Θέµατα ιάλεξης ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ ΠΡΩΤΕΪΝΕΣ. ιαχωρισµός Αµινοξέων
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράμμα που αντιστοιχεί στη σωστή απάντηση:
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
ΒΙΟΛΟΓΙΑ. Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ.
 ΒΙΟΛΟΓΙΑ Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ. Ηλιούπολης Κεφάλαιο 1ο ΒΙΟΛΟΓΙΚΑ ΜΑΚΡΟΜΟΡΙΑ Η ΙΕΡΑΡΧΙΑ ΤΩΝ ΒΙΟΜΟΡΙΩΝ ΠΡΟΔΡΟΜΕΣ
ΒΙΟΛΟΓΙΑ Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ. Ηλιούπολης Κεφάλαιο 1ο ΒΙΟΛΟΓΙΚΑ ΜΑΚΡΟΜΟΡΙΑ Η ΙΕΡΑΡΧΙΑ ΤΩΝ ΒΙΟΜΟΡΙΩΝ ΠΡΟΔΡΟΜΕΣ
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Γ' ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 2006 ΕΚΦΩΝΗΣΕΙΣ
 ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Γ' ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 006 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1 και 1. να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Γ' ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 006 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1 και 1. να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα
ΑΠΑΝΤΗΣΕΙΣ. Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Το συζυγές οξύ της ΝΗ 3 είναι: α. ΝΗ 2 - β.νa
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Το συζυγές οξύ της ΝΗ 3 είναι: α. ΝΗ 2 - β.νa
ΘΕΜΑ 1 ο. 1.2 Όξινο είναι το υδατικό διάλυμα του α. ΝaCl. β. ΝΗ 4 Cl. γ. CH 3 COONa. δ. KOH. Μονάδες 5 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΤΕΛΟΣ 1ΗΣ ΑΠΟ 7 ΣΕΛΙ ΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 30 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 30 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
Celia Koutrafouri Undergraduate Student at Food and Technology Department ΤΜΗΜΑ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ & ΔΙΑΤΡΟΦΗΣ ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ
 Celia Koutrafouri Undergraduate Student at Food and Technology Department ΤΜΗΜΑ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ & ΔΙΑΤΡΟΦΗΣ ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ AΣΚΗΣΗ 4 η : ΠΟΣΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΠΡΩΤΕΙΝΩΝ ΘΕΩΡΙΑ ΕΡΓΑΣΤΗΡΙΟΥ:
Celia Koutrafouri Undergraduate Student at Food and Technology Department ΤΜΗΜΑ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ & ΔΙΑΤΡΟΦΗΣ ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ AΣΚΗΣΗ 4 η : ΠΟΣΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΠΡΩΤΕΙΝΩΝ ΘΕΩΡΙΑ ΕΡΓΑΣΤΗΡΙΟΥ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ. . Σύμφωνα με τη θεωρία Brönsted Lowry συζυγές ζεύγος οξέος βάσης είναι το ζεύγος α.
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΠΑΝΕΛΛΑ ΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΕΣΠΕΡΙΝΟΥ ΕΠΑΛ (ΟΜΑ ΑΣ Β ) ΣΑΒΒΑΤΟ 22 ΜΑΪΟΥ 2010 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΠΑΝΕΛΛΑ ΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΕΣΠΕΡΙΝΟΥ ΕΠΑΛ (ΟΜΑ ΑΣ Β ) ΣΑΒΒΑΤΟ 22 ΜΑΪΟΥ 2010 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
Τάξη. Γνωστικό αντικείµενο: Ειδικοί διδακτικοί στόχοι
 Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Kυτταρική Bιολογία ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ ΔIAΛEΞΗ 3 (7/3/2012) Δρ. Xρήστος Παναγιωτίδης, Τμήμα Φαρμακευτικής Α.Π.Θ.
 Kυτταρική Bιολογία ΔIAΛEΞΗ 3 (7/3/2012) ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ AΣ ΘYMHΘOYME Στην προηγούμενη διάλεξη μιλήσαμε για τη χημική σύσταση των κυττάρων και για τα βιολογικά πολυμερή που αποτελούν
Kυτταρική Bιολογία ΔIAΛEΞΗ 3 (7/3/2012) ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΕΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ AΣ ΘYMHΘOYME Στην προηγούμενη διάλεξη μιλήσαμε για τη χημική σύσταση των κυττάρων και για τα βιολογικά πολυμερή που αποτελούν
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
οµή και Αναδίπλωση πρωτεϊνών
 οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ
 Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
ΘΕΜΑ 1 ο Να γράψετε στο τετράδιό σας τον παρακάτω πίνακα σωστά συμπληρωμένο: Η 2 SO 4 NH 4 HNO 3 H 2 O. Μονάδες 5 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 10 ΙΟΥΝΙΟΥ 2005 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 10 ΙΟΥΝΙΟΥ 2005 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΘΕΜΑ 1 ο. 1.2 To αντιδραστήριο Tollens (αμμωνιακό διάλυμα AgNO 3 ) οξειδώνει την ένωση α. CH 3 CH 2 ΟΗ. β. γ. CH 3 COOH. δ. CH 3 CH=O.
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 1 ΙΟΥΝΙΟΥ 2007 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 1 ΙΟΥΝΙΟΥ 2007 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Ιωάννα Καλλιώρα
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 30 11-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Ιωάννα Καλλιώρα ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ A Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑΣ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 30 11-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Ιωάννα Καλλιώρα ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ A Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες
 Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
ΑΡΧΗ 2ΗΣ ΣΕΛΙ ΑΣ. 1.4. Να συμπληρώσετε στο τετράδιό σας τις παρακάτω χημικές εξισώσεις:
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 30 ΜΑΪΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ ΣΕΛΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 30 ΜΑΪΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ ΣΕΛΙ
β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]
![β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ] β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]](/thumbs/27/10188901.jpg) ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
1.1 Η συζυγής βάση του Η 2 SO 4 είναι α. SO 4 2. β. HSO 4. γ. H 2 SO 3. δ. H 2 S. Μονάδες 5
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 7 ΙΟΥΝΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 7 ΙΟΥΝΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 01/12/2013
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 01/12/2013 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 01/12/2013 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΕΣΠΕΡΙΝΩΝ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΥ ΓΕΝΙΚΥ ΛΥΚΕΙΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΥ 2013 ΕΞΕΤΑΖΜΕΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΧΗΜΕΙΑ ΤΕΧΝΛΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΣ ΤΕΧΝΛΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΛ ΣΕΛΙΔΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΥ ΓΕΝΙΚΥ ΛΥΚΕΙΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΥ 2013 ΕΞΕΤΑΖΜΕΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΧΗΜΕΙΑ ΤΕΧΝΛΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΣ ΤΕΧΝΛΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΛ ΣΕΛΙΔΩΝ:
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ
 ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το
ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το
Μικρά αμινοξέα. Βιοχημεία Ι Β-3
 Βιοχημεία Ι Β-2 Μικρά αμινοξέα Βιοχημεία Ι Β-3 Aλειφατικά αμινοξέα Βιοχημεία Ι Β-4 Ιμινοξύ Βιοχημεία Ι Β-5 Αρωματικά αμινοξέα Βιοχημεία Ι Β-6 Βιοχημεία Ι Β-7 Η Tyr και η Trp απορροφούν στα 280nm-έτσι μετράται
Βιοχημεία Ι Β-2 Μικρά αμινοξέα Βιοχημεία Ι Β-3 Aλειφατικά αμινοξέα Βιοχημεία Ι Β-4 Ιμινοξύ Βιοχημεία Ι Β-5 Αρωματικά αμινοξέα Βιοχημεία Ι Β-6 Βιοχημεία Ι Β-7 Η Tyr και η Trp απορροφούν στα 280nm-έτσι μετράται
ΚΕΦΑΛΑΙΟ 6ο ΑΜΙΝΟΞΕΑ
 138 ΚΕΦΑΛΑΙΟ 6ο ΑΜΙΝΟΞΕΑ 6.1. Τα αμινοξέα Τα αμινοξέα είναι οι ενώσεις που έχουν αμινομάδα ( NH2) και καρβοξυλομάδα ( COOH) στην ίδια ανθρακική αλυσίδα και είναι ενώσεις γενικά διαλυτές στο νερό. Τα α
138 ΚΕΦΑΛΑΙΟ 6ο ΑΜΙΝΟΞΕΑ 6.1. Τα αμινοξέα Τα αμινοξέα είναι οι ενώσεις που έχουν αμινομάδα ( NH2) και καρβοξυλομάδα ( COOH) στην ίδια ανθρακική αλυσίδα και είναι ενώσεις γενικά διαλυτές στο νερό. Τα α
1.2. Να γράψετε στο τετράδιό σας την παρακάτω πρόταση. συμπλήρωσή της. Από τα παρακάτω ζεύγη ουσιών ρυθμιστικό διάλυμα είναι το α. HF / NaF.
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 10 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 10 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε
Αντιδράσεις της α-αμινομάδος
 Αντιδράσεις της α-αμινομάδος Μπορεί να αλκυλιωθεί με οξινα χαλίδια ή ανυδρίτες.η Κατεργασία χρησιμοποιείται για να προστατευθεί η α-αμινομάδα Αντιδρά με την νινυδρίνη.χρησιμοποιείται για ποσοτικό προσδιορισμό
Αντιδράσεις της α-αμινομάδος Μπορεί να αλκυλιωθεί με οξινα χαλίδια ή ανυδρίτες.η Κατεργασία χρησιμοποιείται για να προστατευθεί η α-αμινομάδα Αντιδρά με την νινυδρίνη.χρησιμοποιείται για ποσοτικό προσδιορισμό
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΥ ΓΕΝΙΚΥ ΛΥΚΕΙΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΥ 2013 ΕΞΕΤΑΖΜΕΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΧΗΜΕΙΑ ΤΕΧΝΛΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΣ ΤΕΧΝΛΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΛ ΣΕΛΙΔΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΥ ΓΕΝΙΚΥ ΛΥΚΕΙΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΥ 2013 ΕΞΕΤΑΖΜΕΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΧΗΜΕΙΑ ΤΕΧΝΛΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΣ ΤΕΧΝΛΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΛ ΣΕΛΙΔΩΝ:
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης
 Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 2008 ΕΚΦΩΝΗΣΕΙΣ
 ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 2008 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1 και 1.2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 2008 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1 και 1.2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα
Οργανική χηµεία και βιοχηµεία
 Οργανική χηµεία και βιοχηµεία Ερωτήσεις πολλαπλής επιλογής 1. Στις χηµικές ενώσεις, που αποτελούν το κύτταρο, περιέχονται περίπου a) δέκα χηµικά στοιχεία b) ενενήντα χηµικά στοιχεία c) είκοσι χηµικά στοιχεία
Οργανική χηµεία και βιοχηµεία Ερωτήσεις πολλαπλής επιλογής 1. Στις χηµικές ενώσεις, που αποτελούν το κύτταρο, περιέχονται περίπου a) δέκα χηµικά στοιχεία b) ενενήντα χηµικά στοιχεία c) είκοσι χηµικά στοιχεία
ΑΡΧΗ 2ΗΣ ΣΕΛΙ ΑΣ. 1.4 Να μεταφέρετε στο τετράδιό σας τις παρακάτω χημικές εξισώσεις σωστά συμπληρωμένες: καταλύτες
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 27 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ ΣΕΛΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 27 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ ΣΕΛΙ
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ. Καρβουντζή Ηλιάνα Βιολόγος
 Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
Ν 2. 78% της σύστασης της ατμόσφαιρας
 Αφομοίωση του Ν 2 Ν 2 78% της σύστασης της ατμόσφαιρας 3.8 x 10 15 τόνοι Ν 2 σε ατμόσφαιρα 18 x 10 15 τόνοι Ν 2 σε ιζήματα του φλοιού της γης Κύκλος του Ν 2 Αφομοίωση Ν 2 στα φυτά - Άλατα Βασική πηγή αζώτου
Αφομοίωση του Ν 2 Ν 2 78% της σύστασης της ατμόσφαιρας 3.8 x 10 15 τόνοι Ν 2 σε ατμόσφαιρα 18 x 10 15 τόνοι Ν 2 σε ιζήματα του φλοιού της γης Κύκλος του Ν 2 Αφομοίωση Ν 2 στα φυτά - Άλατα Βασική πηγή αζώτου
ÖÑÏÍÔÉÓÔÇÑÉÁ ÁÑÅÉÔÏËÌÏ ÁÃ. ÄÇÌÇÔÑÉÏÓ - ÄÁÖÍÇ
 ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) Γ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 6 ΜΑΪΟΥ 007 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1. και 1.. να γράψετε στο τετράδιό σας τον αριθµό της
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) Γ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 6 ΜΑΪΟΥ 007 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1. και 1.. να γράψετε στο τετράδιό σας τον αριθµό της
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ
 ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
τα βιβλία των επιτυχιών
 Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 5 ΣΕΛΙΔΕΣ
 Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ
 ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
1.2. Να γράψετε στο τετράδιό σας την παρακάτω πρόταση. Από τα παρακάτω ζεύγη ουσιών ρυθµιστικό διάλυµα είναι το α. HF / NaF.
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 10 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 10 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 5 ΣΕΛΙ ΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ)
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ)
Δομή και λειτουργία πρωτεϊνών. Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο
 Δομή και λειτουργία πρωτεϊνών Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο Πρωτεΐνες Κύριο συστατικό κυττάρου Δομικοί λίθοι αλλά και επιτελεστές λειτουργίας κυττάρου ένζυμα, μεταφορά,
Δομή και λειτουργία πρωτεϊνών Το κύριο δομικό συστατικό των κυττάρων. Το κύριο λειτουργικό μόριο Πρωτεΐνες Κύριο συστατικό κυττάρου Δομικοί λίθοι αλλά και επιτελεστές λειτουργίας κυττάρου ένζυμα, μεταφορά,
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 5 ΣΕΛΙΔΕΣ
 Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
 ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΛΑ Β ) ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από
ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΛΑ Β ) ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ. δ. S 2 Μονάδες 4
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 26 ΜΑΪΟΥ 2007 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 26 ΜΑΪΟΥ 2007 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002
 ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΘΕΜΑ 1 ο ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 1.1 και 1.2 να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΘΕΜΑ 1 ο ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 1.1 και 1.2 να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί
 ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑ Α Β ) ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) Θέμα Α Για τις προτάσεις
ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑ Α Β ) ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) Θέμα Α Για τις προτάσεις
ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ ΜΑΚΡΟΜΟΡΙΑ
 ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ ΜΑΚΡΟΜΟΡΙΑ ΕΙΣΑΓΩΓΗ Oι ζωντανοί οργανισμοί αποτελούνται από ένα ή περισσότερα κύτταρα. Χαρακτηρίζονται αντίστοιχα, μονοκύτταροι (μονοκυτταρικοί) και πολυκύτταροι (πολυκυτταρικοί)
ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ ΜΑΚΡΟΜΟΡΙΑ ΕΙΣΑΓΩΓΗ Oι ζωντανοί οργανισμοί αποτελούνται από ένα ή περισσότερα κύτταρα. Χαρακτηρίζονται αντίστοιχα, μονοκύτταροι (μονοκυτταρικοί) και πολυκύτταροι (πολυκυτταρικοί)
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
συμπεριφέρεται ως α. βάση. β. οξύ. γ. πρωτονιοδότης. δ. αμφολύτης. Μονάδες 5
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 2 ΙΟΥΝΙΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΘΕΜΑ 1 ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 2 ΙΟΥΝΙΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ
ΑΡΧΗ 2ΗΣ ΣΕΛΙ ΑΣ. 1.4 Να μεταφέρετε στο τετράδιό σας τις παρακάτω χημικές εξισώσεις σωστά συμπληρωμένες: καταλύτες
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 27 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ ΣΕΛΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 27 ΜΑΪΟΥ 2008 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΣΥΝΟΛΟ ΣΕΛΙ
Είναι σημαντικές επειδή: Αποτελούν βασικά δοµικά συστατικά του σώµατος Εξυπηρετούν ενεργειακές ανάγκες Ασκούν έλεγχο σε όλες τις βιοχηµικές διεργασίες
 ΕΞΕΤΑΣΤΕΑ ΥΛΗ ΕΝΟΤΗΤΑ 2: Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ, 5 9 (απλή αναφορά) 2.2 ΤΟ ΝΕΡΟ ΚΑΙ Η ΒΙΟΛΟΓΙΚΗ ΤΟΥ ΣΗΜΑΣΙΑ, 9 14 (απλή αναφορά), 2.4 ΟΡΓΑΝΙΚΕΣ ΟΥΣΙΕΣ, σελ. 20 36 Οργανικές Ουσίες
ΕΞΕΤΑΣΤΕΑ ΥΛΗ ΕΝΟΤΗΤΑ 2: Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ, 5 9 (απλή αναφορά) 2.2 ΤΟ ΝΕΡΟ ΚΑΙ Η ΒΙΟΛΟΓΙΚΗ ΤΟΥ ΣΗΜΑΣΙΑ, 9 14 (απλή αναφορά), 2.4 ΟΡΓΑΝΙΚΕΣ ΟΥΣΙΕΣ, σελ. 20 36 Οργανικές Ουσίες
οµικά στοιχεία βιοµορίων
 2-1 Κεφάλαιο 2 οµικά στοιχεία βιοµορίων 2.1. ιαστάσεις των Βιοµορίων Οι διαστάσεις των βιοµορίων κυµαίνονται από µερικά Ångströms (10-10 m) έως µερικές εκατοντάδες Ångströms (10-8 m). (εικόνα 2.1, 2.2)
2-1 Κεφάλαιο 2 οµικά στοιχεία βιοµορίων 2.1. ιαστάσεις των Βιοµορίων Οι διαστάσεις των βιοµορίων κυµαίνονται από µερικά Ångströms (10-10 m) έως µερικές εκατοντάδες Ångströms (10-8 m). (εικόνα 2.1, 2.2)
ΑΡΧΗ 2ΗΣ ΣΕΛΙ ΑΣ - ΕΣΠΕΡΙΝΩΝ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ - ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 30 ΜΑΪΟΥ 2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ)
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ - ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 30 ΜΑΪΟΥ 2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ)
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ & ΠΑΡΑΓΩΓΗΣ) 2010 ΕΚΦΩΝΗΣΕΙΣ
 ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ & ΠΑΡΑΓΩΓΗΣ) 010 ΕΚΦΩΝΗΣΕΙΣ Για τις ηµιτελείς προτάσεις Α1 και Α να γράψετε στο τετράδιό σας τον αριθµό της πρότασης και δίπλα το
ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ & ΠΑΡΑΓΩΓΗΣ) 010 ΕΚΦΩΝΗΣΕΙΣ Για τις ηµιτελείς προτάσεις Α1 και Α να γράψετε στο τετράδιό σας τον αριθµό της πρότασης και δίπλα το
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
