Τεχνολογία Υλικών Οχημάτων ΤΕΥΧΟΣ Ι
|
|
|
- Πολωνα Μοσχοβάκης
- 8 χρόνια πριν
- Προβολές:
Transcript
1 Α.Τ.Ε.Ι ΘΕΣΣΑΛΟΝΙΚΗΣ Σ.Τ.Ε.Φ. Τεχνολογία Υλικών Οχημάτων ΤΕΥΧΟΣ Ι (ΤΜΗΜΑ ΟΧΗΜΑΤΩΝ) Παναγιώτης Ματζινός, Επιστημονικός Συνεργάτης Χημικός Μηχανικός, MPhil, PhD Θεσσαλονίκη 2010
2 ΠΕΡΙΕΧΟΜΕΝΑ 1. ΕΙΣΑΓΩΓΗ 1.1 ΙΣΤΟΡΙΚΗ ΑΝΑΔΡΟΜΗ 1.2 ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΩΝ ΥΛΙΚΩΝ 1.3 ΚΑΤΑΤΑΞΗ ΤΩΝ ΥΛΙΚΩΝ 1.4 ΕΠΙΛΟΓΗ ΥΛΙΚΩΝ 1.5 ΑΝΑΠΤΥΞΗ ΝΕΩΝ ΥΛΙΚΩΝ 1.6 ΥΛΙΚΑ ΟΧΗΜΑΤΩΝ 2. ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ ΚΑΙ ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ 2.1 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 2.2 ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΠΡΟΤΥΠΟ ΤΟΥ RUTHERFORD ΠΡΟΤΥΠΟ ΤΟΥ BOHR ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΙΑΜΟΡΦΩΣΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ 2.3 ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΙΟΝΤΙΚΟΣ Η ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΜΕΤΑΛΛΙΚΟΣ ΔΕΣΜΟΣ ΔΕΥΤΕΡΕΥΟΝΤΕΣ ΔΕΣΜΟΙ Η ΔΕΣΜΟΙ VAN DER WAALS 2.4 ΕΝΕΡΓΕΙΕΣ ΔΕΣΜΩΝ ΚΑΙ ΘΕΡΜΟΚΡΑΣΙΕΣ ΤΗΞΗΣ 2.5 ΕΠΙΔΡΑΣΗ ΤΩΝ ΧΗΜΙΚΩΝ ΔΕΣΜΩΝ ΣΤΙΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΥΛΙΚΩΝ 3. ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΤΩΝ ΣΤΕΡΕΩΝ 3.1 ΓΕΝΙΚΕΣ ΑΡΧΕΣ 3.2 ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΤΩΝ ΜΕΤΑΛΛΩΝ ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΧΩΡΟΚΕΝΤΡΩΜΕΝΟΥ ΚΥΒΙΚΟΥ (BCC) ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΕΔΡΟΚΕΝΤΡΩΜΕΝΟΥ ΚΥΒΙΚΟΥ (FCC) ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΜΕΓΙΣΤΗΣ ΠΥΚΝΟΤΗΤΑΣ ΕΞΑΓΩΝΙΚΟΥ (HCP) 3.3 ΦΑΙΝΟΜΕΝΟ ΑΛΛΟΤΡΟΠΙΑΣ 3.4 ΚΡΥΣΤΑΛΛΙΚΑ ΠΛΕΓΜΑΤΑ ΚΑΙ ΣΥΣΤΗΜΑΤΑ 3.5 ΚΡΥΣΤΑΛΛΙΚΑ ΚΑΙ ΑΜΟΡΦΑ ΥΛΙΚΑ ΚΡΥΣΤΑΛΛΩΣΗ Η ΣΤΕΡΕΟΠΟΙΗΣΗ ΠΟΛΥΚΡΥΣΤΑΛΛΙΚΟΥ ΥΛΙΚΟΥ ΜΟΝΟΚΡΥΣΤΑΛΛΟΙ ΑΝΙΣΟΤΡΟΠΙΑ ΑΜΟΡΦΑ ΥΛΙΚΑ 4. ΑΤΕΛΕΙΕΣ ΤΗΣ ΚΡΥΣΤΑΛΛΙΚΗΣ ΔΟΜΗΣ 4.1 ΕΙΔΗ ΑΤΕΛΕΙΩΝ 4.2 ΣΗΜΕΙΑΚΕΣ ΑΤΕΛΕΙΕΣ ΠΛΕΓΜΑΤΙΚΑ ΚΕΝΑ ΜΗΤΡΙΚΑ ΕΝΘΕΤΑ ΑΤΟΜΑ (ΑΥΤΟΠΑΡΕΜΒΟΛΗ) ΞΕΝΑ ΕΝΘΕΤΑ ΑΤΟΜΑ ΑΤΕΛΕΙΕΣ FRENKEL ΚΑΙ SCOHTTKY 4.3 ΓΡΑΜΜΙΚΕΣ ΑΤΕΛΕΙΕΣ H ΔΙΑΤΑΡΑΧΕΣ ΓΡΑΜΜΙΚΕΣ ΑΤΕΛΕΙΕΣ Η ΔΙΑΤΑΡΑΧΕΣ
3 4.4 ΑΤΕΛΕΙΕΣ ΔΥΟ ΔΙΑΣΤΑΣΕΩΝ Η ΕΠΙΠΕΔΕΣ ΑΤΕΛΕΙΕΣ ΟΡΙΑ ΚΟΚΚΩΝ ΔΙΔΥΜΙΕΣ ΣΦΑΛΜΑΤΑ ΕΠΙΣΤΟΙΒΑΣΗΣ 4.5 ΑΤΕΛΕΙΕΣ ΟΓΚΟΥ 5. ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΘΕΜΟΧΩΡΗΤΙΚΟΤΗΤΑ Η ΕΙΔΙΚΗ ΘΕΡΜΟΤΗΤΑ ΘΕΡΜΙΚΗ ΑΓΩΓΙΜΟΤΗΤΑ ΘΕΡΜΙΚΗ ΔΙΑΣΤΟΛΗ ΗΛΕΚΤΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΗΛΕΚΤΡΙΚΗ ΕΙΔΙΚΗ ΑΝΤΙΣΤΑΣΗ ΚΑΙ ΑΓΩΓΙΜΟΤΗΤΑ ΗΜΙΑΓΩΓΟΙ 5.3 ΜΑΓΝΗΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΕΙΔΗ ΜΑΓΝΗΤΙΣΜΟΥ ΕΙΔΗ ΜΑΓΝΗΤΩΝ ΜΑΓΝΗΤΙΚΑ ΜΕΤΑΛΛΙΚΑ ΥΛΙΚΑ ΜΗΧΑΝΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 6.1 ΓΕΝΙΚΑ 6.2 ΔΟΚΙΜΗ ΕΦΕΛΚΥΣΜΟΥ 6.3 ΔΟΚΙΜΗ ΘΛΙΨΗΣ 6.4 ΔΟΚΙΜΗ ΚΑΜΨΗΣ 6.5 ΔΟΚΙΜΕΣ ΔΙΑΤΜΗΣΗΣ ΚΑΙ ΣΤΡΕΨΗΣ ΔΟΚΙΜΗ ΚΡΟΥΣΗΣ Η ΔΥΣΘΡΑΥΣΤΟΤΗΤΑΣ ΔΟΚΙΜΗ ΣΚΛΗΡΟΤΗΤΑΣ ΔΟΚΙΜΗ ΣΚΛΗΡΟΤΗΤΑΣ BRINELL ΔΟΚΙΜΗ ΣΚΛΗΡΟΤΗΤΑΣ VICKERS ΔΟΚΙΜΗ ΣΚΛΗΡΟΤΗΤΑΣ ROCKWELL ΔΟΚΙΜΕΣ ΜΙΚΡΟΣΚΛΗΡΟΤΗΤΑΣ VICKERS ΚΑΙ KNOOP ΣΥΣΧΕΤΙΣΗ ΣΚΛΗΡΟΤΗΤΑΣ ΚΑΙ ΑΝΤΟΧΗΣ ΕΦΕΛΚΥΣΜΟΥ 6.8 ΔΟΚΙΜΗ ΕΡΠΥΣΜΟΥ 6.9 ΔΟΚΙΜΗ ΚΟΠΩΣΗΣ ΚΥΚΛΙΚΕΣ ΤΑΣΕΙΣ Η ΚΑΜΠΥΛΗ S-N ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΔΙΑΡΚΕΙΑ ΖΩΗΣ ΣΕ ΚΟΠΩΣΗ ΜΗΧΑΝΙΣΜΟΙ ΙΣΧΥΡΟΠΟΙΗΣΗΣ ΜΕΤΑΛΛΙΚΩΝ ΥΛΙΚΩΝ 7.1 ΓΕΝΙΚΑ 7.2 ΣΚΛΗΡΥΝΣΗ ΜΕ ΕΝΔΟΤΡΑΧΥΝΣΗ 7.3 ΙΣΧΥΡΟΠΟΙΗΣΗ ΜΕ ΔΗΜΙΟΥΡΓΙΑ ΣΤΕΡΕΟΥ ΔΙΑΛΥΜΑΤΟΣ 7.4 ΣΚΛΗΡΥΝΣΗ ΜΕ ΚΑΤΑΚΡΗΜΝΙΣΗ ΛΟΓΩ ΓΗΡΑΝΣΗΣ 7.5 ΙΣΧΥΡΟΠΟΙΗΣΗ ΜΕ ΕΛΑΤΤΩΣΗ ΤΟΥ ΜΕΓΕΘΟΥΣ ΤΩΝ ΚΟΚΚΩΝ 8. ΜΟΡΦΟΠΟΙΗΣΗ ΤΩΝ ΜΕΤΑΛΛΩΝ 8.1 ΓΕΝΙΚΑ 8.2 ΜΗΧΑΝΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ ΔΙΑΜΟΡΦΩΣΗΣ ΤΩΝ ΜΕΤΑΛΛΩΝ ΕΛΑΣΗ ΔΙΕΛΑΣΗ ΜΕ ΣΥΜΠΙΕΣΗ (ΕΞΩΘΗΣΗ) ΔΙΕΛΑΣΗ ΜΕ ΕΛΞΗ (ΔΙΕΛΚΥΣΗ)
4 8.2.4 ΣΦΥΡΗΛΑΤΗΣΗ ΚΑΤΕΡΓΑΣΙΕΣ ΔΙΑΜΟΡΦΩΣΗΣ ΕΠΙΠΕΔΟΥ ΕΛΑΣΜΑΤΟΣ 8.3 ΧΥΤΕΥΣΗ ΑΜΜΟΧΥΤΕΥΣΗ ΧΥΤΕΥΣΗ ΕΠΕΝΔΥΣΗΣ ΧΥΤΕΥΣΗ ΣΕ ΜΟΝΙΜΟ ΚΑΛΟΥΠΙ ΥΠΟ ΠΙΕΣΗ ΣΥΝΕΧΗΣ ΧΥΤΕΥΣΗ ΔΟΜΗ ΧΥΤΟΥ 8.4 ΔΙΑΦΟΡΕΣ ΤΕΧΝΙΚΕΣ ΚΟΝΙΟΜΕΤΑΛΛΟΥΡΓΙΑ ΣΥΓΚΟΛΛΗΣΗ
5 ΚΕΦΑΛΑΙΟ 1 ΕΙΣΑΓΩΓΗ 1.1 ΙΣΤΟΡΙΚΗ ΑΝΑΔΡΟΜΗ Η ιστορία του ανθρώπινου πολιτισμού είναι άρρηκτα συνδεδεμένη με τα υλικά που χρησιμοποιεί και μπορεί να κατεργάζεται ο άνθρωπος. Δεν είναι τυχαίο ότι οι πρώτοι πολιτισμοί προσδιορίζονται από τα υλικά που χρησιμοποίησαν οι άνθρωποι για να καλύψουν τις ανάγκες τους. Για παράδειγμα, οι διάφορες εποχές της ανθρωπότητας αποκαλούνται ως η Εποχή του Λίθου, η Εποχή του Xαλκού, η Εποχή του Σιδήρου. Ίσως, η σημερινή εποχή που χαρακτηρίζεται από την αλματώδη ανάπτυξη των ηλεκτρονικών υπολογιστών και των εφαρμογών τους, την ανάπτυξη των οπτικών ινών, χαρακτηριστεί ως η Εποχή του Πυριτίου. Στην αρχαιότητα οι πρώτοι άνθρωποι χρησιμοποιούσαν υλικά που ήταν διαθέσιμα στη φύση, όπως πέτρα, πηλός, ξύλα, δέρματα κλπ. Όμως με την πάροδο του χρόνου ο άνθρωπος άρχισε να επεμβαίνει στα υλικά και να παράγει υλικά με ιδιότητες ανώτερες από αυτές των φυσικών υλικών. Παρήχθησαν κεραμικά και μέταλλα. Ανακαλύφθηκε ότι οι ιδιότητες των υλικών τροποποιούνται με θερμικές κατεργασίες, καθώς και με την προσθήκη άλλων υλικών. Αναπτύχθηκαν οι τεχνικές κατεργασίας των υλικών και ακόμη παρήχθησαν νέα, σύνθετα υλικά από το συνδυασμό δυο ή περισσότερων υλικών με ιδιότητες ανώτερες από αυτές των επιμέρους υλικών. Για παράδειγμα, ο πηλός συνδυάστηκε με άχυρο και η αντοχή των κατασκευών βελτιώθηκε. Έως σχετικά πρόσφατα η χρησιμοποίηση των υλικών ήταν θέμα επιλογής. Για κάποια συγκεκριμένη εφαρμογή επιλεγόταν το πλέον κατάλληλο υλικό από κάποιον ορισμένο αριθμό διαθέσιμων υλικών. Η αλματώδης όμως ανάπτυξη των γνώσεων για την ατομική, κρυσταλλική και μικροδομή των υλικών από τις οποίες εξαρτώνται και μπορούν να διαμορφωθούν οι μακροσκοπικές ιδιότητες των υλικών, οδήγησε τα τελευταία εξήντα χρόνια στην ανάπτυξη δεκάδων χιλιάδων νέων υλικών. Αναπτύχθηκαν νέα μεταλλικά υλικά, πλαστικά, κεραμικά και γυαλιά. Επιπλέον αναπτύχθηκαν οι ίνες, όπως οι υαλοΐνες και τα ανθρακονήματα, που χρησιμοποιούνται για την μηχανική ενίσχυση άλλων υλικών και την παραγωγή μιας νέας κατηγορίας υλικών, των σύνθετων υλικών. 1.2 ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΩΝ ΥΛΙΚΩΝ Επιστήμη είναι η γνώση των υλικών και τεχνολογία η διαδικασία επέμβασης στα υλικά. Η επιστήμη των υλικών περιλαμβάνει την μελέτη της σχέσης ανάμεσα στην δομή των υλικών και τις ιδιότητές τους. Ενώ, η τεχνολογία των υλικών περιλαμβάνει την επέμβαση στη δομή του υλικού, με βάση τη σχέση δομής-ιδιότητας, έτσι ώστε το υλικό να αποκτήσει τις επιθυμητές ιδιότητες για μια συγκεκριμένη εφαρμογή. Με την έννοια δομή ενός υλικού εννοούμε τον τρόπο οργάνωσης των επιμέρους συστατικών του. Συνήθως η δομή ενός υλικού συνδέεται με το μέσο παρατήρησής του και αναφέρεται στη διευθέτηση των δομικών στοιχείων του σε ενότητες ή σύνολα ορισμένης τάξης μεγέθους. Σε υποατομικό επίπεδο, η δομή αφορά την οργάνωση των στοιχειωδών σωματιδίων (πρωτονίων, νετρονίων, ηλεκτρονίων) από τα οποία αποτελείται ένα άτομο π.χ. ηλεκτρονιακή δομή. Σε ατομικό επίπεδο, η δομή αφορά την οργάνωση των ατόμων ή μορίων ενός υλικού π.χ. η κρυσταλλική δομή. Με τον όρο μικροσκοπική δομή ή μικροδομή εννοούμε 4
6 τη δομή που μπορεί να παρατηρηθεί με την βοήθεια διάφορων μικροσκοπίων π.χ. προσδιορισμός των φάσεων σε ένα κράμα, το μέγεθος και ο αριθμός των κόκκων, η ύπαρξη προσμείξεων, ή πόρων. Με τον όρο μακροσκοπική δομή εννοούμε τη δομή που αποκαλύπτεται με την παρατήρηση του υλικού δια γυμνού οφθαλμού π.χ. ύπαρξη πόρων σε ένα χυτό, λόγω αερίων που εγκλωβίστηκαν μέσα στη μάζα του κατά την χύτευσή του, ύπαρξη ρωγμών που σχηματίστηκαν κατά την πλαστική παραμόρφωση ενός μετάλλου. Με την έννοια ιδιότητα ενός υλικού εννοούμε το φυσικό μέγεθος που εκφράζει την απόκριση του υλικού απέναντι σε εξωτερικές επιδράσεις. Για παράδειγμα, όταν σε ένα υλικό εξασκούνται δυνάμεις μεγαλύτερες από ένα χαρακτηριστικό όριο, τότε το υλικό παραμορφώνεται μόνιμα. Όταν η θερμοκρασία μιας μεταλλικής ράβδου αυξάνεται ή μειώνεται τότε το υλικό διαστέλλεται ή συστέλλεται αντίστοιχα. Γενικά, οι ιδιότητες των στερεών υλικών διακρίνονται σε μηχανικές, φυσικές και χημικές. Μηχανικές είναι οι ιδιότητες του υλικού που χαρακτηρίζουν τη συμπεριφορά του κάτω από την επίδραση εξωτερικών δυνάμεων. Χαρακτηριστικές μηχανικές ιδιότητες είναι η αντοχή και το μέτρο ελαστικότητας. Φυσικές είναι οι ιδιότητες του υλικού που χαρακτηρίζουν τη συμπεριφορά του κάτω από την επίδραση παραγόντων που δεν αλλοιώνουν τη χημική του σύσταση. Οι θερμικές, οι ηλεκτρικές, οι μαγνητικές και οι οπτικές ιδιότητες περιλαμβάνονται σε αυτή την κατηγορία. Οι θερμικές ιδιότητες εκφράζουν την συμπεριφορά του υλικού στη θερμότητα, οι ηλεκτρικές ιδιότητες αποτελούν την απόκριση του υλικού στην εφαρμογή ηλεκτρικού πεδίου, οι μαγνητικές ιδιότητες την συμπεριφορά του υλικού στην εφαρμογή μαγνητικού πεδίου και οι οπτικές ιδιότητες την απόκριση του υλικού στη φωτεινή ακτινοβολία. Χημικές είναι οι ιδιότητες του υλικού που χαρακτηρίζουν τη συμπεριφορά του κάτω από την επίδραση παραγόντων που τείνουν να αλλοιώσουν τη χημική του σύσταση. Η διάβρωση των μετάλλων, των κεραμικών καθώς και η υποβάθμιση των πλαστικών οφείλονται στη χημική δραστικότητα των δομικών στοιχείων τους. Οι ιδιότητες των υλικών εξαρτώνται από τη δομή τους, η οποία με τη σειρά της εξαρτάται από την επεξεργασία που έχει υποστεί το υλικό. Για παράδειγμα, η μορφοποίηση των μεταλλικών υλικών με μηχανικές κατεργασίες, συνοδεύεται από την επιμήκυνση των κόκκων του υλικού στην κατεύθυνση της μηχανικής κατεργασίας (π.χ. συρματοποίηση, έλαση, σφυρηλασία, κλπ.). Ο προσανατολισμός αυτός των κόκκων είναι γνωστός ως ιστός και έχει ως άμεση συνέπεια την ανισοτροπία του υλικού. Το υλικό αποκτά μια ινώδη δομή λόγω της πλαστικής ροής του υλικού στη κατεύθυνση της κατεργασίας. Όλες οι ιδιότητες του υλικού π.χ. μηχανικές, θερμικές, ηλεκτρικές είναι διαφορετικές σε κατεύθυνση παράλληλη της ινώδους δομής από ότι σε κατεύθυνση κάθετη σε αυτή. Ένα άλλο στοιχείο που διερευνά η επιστήμη και τεχνολογία των υλικών είναι η απόδοση του υλικού σε συγκεκριμένη εφαρμογή, η οποία είναι συνάρτηση των ιδιοτήτων του. Συνοπτικά ο σχεδιασμός, η παραγωγή και η χρήση των υλικών διέπεται από την παρακάτω σχέση: Επεξεργασία Δομή Ιδιότητες Απόδοση. Στο Σχήμα 1.1 παρουσιάζεται ένας τεντωτήρας που χρησιμοποιείται σε οχήματα κατασκευασμένος από ανθρακούχο χάλυβα με σφυρηλασία. 5
7 Εφαρμογή της σχέσης επεξεργασία δομή ιδιότητες απόδοση έχει ως εξής: 1. Σφυρηλασία. 2. Σχηματισμός ινώδους δομής παράλληλα με τον κύριο άξονα του τεντωτήρα. (εκδήλωση ανισοτροπίας). 3. Η αντοχή σε κρούση είναι μεγαλύτερη σε κατεύθυνση παράλληλη με την ινώδη δομή από ότι σε κάθετη. Για παράδειγμα, η δυσθραυστότητα κατά Charpy είναι 114 N.m (παράλληλα) και 76 N.m (κάθετα), για μείωση της διατομής κατά 48.5% και 37% αντίστοιχα. 4. Ο τεντωτήρας μπορεί με επιτυχία να δεχθεί κρουστικές καταπονήσεις στην κατεύθυνση του κύριου άξονά του. Σχήμα 1.1: Τεντωτήρας, ανθρακούχος χάλυβας, μορφοποίηση με σφυρηλασία (forging). 1.3 ΚΑΤΑΤΑΞΗ ΤΩΝ ΥΛΙΚΩΝ Τα στερεά υλικά συνήθως διακρίνονται σε τρεις βασικές κατηγορίες: τα μέταλλα, τα κεραμικά και τα πολυμερή. Τα περισσότερα υλικά σύμφωνα με τη χημική σύσταση και την ατομική δομή τους κατατάσσονται σε μια από τις παραπάνω κατηγορίες. Εάν τα μέταλλα, τα κεραμικά και τα πολυμερή καταλάμβαναν τις κορυφές ενός τριγώνου, τότε στο κέντρο του τριγώνου θα βρισκόταν μια σημαντική κατηγορία τεχνολογικών υλικών, τα σύνθετα υλικά. Σύνθετα υλικά καλούνται τα υλικά που αποτελούνται από τουλάχιστον δύο υλικά, τα οποία σχηματίζουν ξεχωριστές φάσεις στο τελικό υλικό. Δυο άλλες σημαντικές κατηγορίες εξειδικευμένων υλικών είναι οι ημιαγωγοί και τα βιοϋλικά. Οι ημιαγωγοί χρησιμοποιούνται για τις ασυνήθιστες ηλεκτρικές ιδιότητές τους και τα βιοϋλικά χρησιμοποιούνται στον ανθρώπινο οργανισμό, για την αντικατάσταση κατεστραμμένων τμημάτων. Παρακάτω περιγράφονται συνοπτικά οι διαφορετικές κατηγορίες των υλικών. Μέταλλα Τα μεταλλικά υλικά είναι ανόργανες ουσίες που αποτελούνται από ένα ή περισσότερα μεταλλικά στοιχεία, όπως Fe, Cu, Al, Ni, Zn κλπ. Συνήθως περιέχουν και ανόργανες προσμίξεις C, N, O και S. Πολλές ιδιότητες των μετάλλων οφείλονται στην ηλεκτρονιακή διαμόρφωση των ατόμων τους και στην ιδιαιτερότητα των δεσμών που αναπτύσσονται 6
8 μεταξύ τους, με συνέπεια την ύπαρξη ενός «νέφους» από ελεύθερα ηλεκτρόνια, που δεν είναι συνδεδεμένα με συγκεκριμένα άτομα. Τα μέταλλα είναι καλοί αγωγοί του ηλεκτρισμού και της θερμότητας και είναι αδιαφανή στο ορατό φως. Ακόμη, παρουσιάζουν υψηλή μηχανική αντοχή και πλαστικότητα, γεγονός που επιτρέπει την ευρεία χρήση τους στις κατασκευές. Κεραμικά Τα κεραμικά είναι ενώσεις μεταξύ μετάλλων και αμετάλλων. Η οικογένεια των κεραμικών υλικών περιλαμβάνει τα παραδοσιακά κεραμικά που αποτελούνται από ορυκτές αργίλλους (Al2O3.2SiO2.2H2O), τα προηγμένα κεραμικά αποτελούμενα από οξείδια, καρβίδια και νιτρίδια (Al2O3, SiC, Si3N4), τα γυαλιά (70SiO2.10CaO.15Na2O), τα ορυκτά κεραμικά (γρανίτης: αλουμινοπυριτική σύσταση) και το τσιμέντο (CaO+SiO2+Al2O3). Τα κεραμικά είναι μονωτές του ηλεκτρισμού και της θερμότητας. Λόγω των υψηλότερων σημείων τήξης από τα μέταλλα και τα πλαστικά και την καλή αντιδιαβρωτική τους συμπεριφορά, χρησιμοποιούνται σε εφαρμογές υψηλών θερμοκρασιών. Ως προς τη μηχανική τους συμπεριφορά παρουσιάζουν πολύ υψηλή σκληρότητα, αλλά και ευθραυστότητα (ψαθυρότητα). Πολυμερή Ως πολυμερή θεωρούνται τα πλαστικά και τα ελαστικά υλικά. Είναι φυσικές ή συνθετικές οργανικές χημικές ενώσεις του άνθρακα με το υδρογόνο, το οξυγόνο, το άζωτο και άλλα μη μεταλλικά στοιχεία. Τα πολυμερή (πολύς + μέρος) έχουν μεγάλες μοριακές δομές που χαρακτηρίζονται από επανάληψη μικρών τμημάτων, τα μονομερή. Τα φυσικά πολυμερή περιλαμβάνουν το κέρατο, τη γομμαλάκα, τη γουταπέρκα και το ελαστικό (καουτσούκ). Τα συνθετικά πολυμερή είναι χιλιάδες και χρησιμοποιούνται σε υφάσματα, εξαρτήματα αυτοκινήτων, χρώματα κλπ. Τα πολυμερή έχουν χαμηλή πυκνότητα, καλές μηχανικές ιδιότητες και πολύ συχνά χαμηλό κόστος, με συνέπεια να μπορούν να αντικαταστήσουν τα μεταλλικά υλικά καθώς και το γυαλί σε πολλές εφαρμογές. Σύνθετα υλικά Τα σύνθετα υλικά προκύπτουν από το συνδυασμό δυο ή περισσότερων υλικών με αποτέλεσμα το σχηματισμό ενός νέου υλικού με ιδιότητες, ανώτερες από αυτές των επιμέρους υλικών. Από αυτά το ένα συστατικό συνήθως λειτουργεί ως μέσο ενίσχυσης και προσδίδει υψηλές μηχανικές ιδιότητες στο υλικό. Ένα γνωστό παράδειγμα σύνθετου υλικού είναι το φάιμπεργκλας, στο οποίο ίνες υάλου ενσωματώνονται σε μια πολυμερική μήτρα. Το σύνθετο υλικό αποκτά υψηλή αντοχή από τις υαλοΐνες και ευκαμψία από το πολυμερές. Ένα μεγάλο μέρος της ανάπτυξης νέων υλικών αφορά τα σύνθετα υλικά. Ημιαγωγοί Τα στερεά υλικά με βάση την ευκολία που άγουν το ηλεκτρικό ρεύμα διακρίνονται σε αγωγούς, ημιαγωγούς και μονωτές. Οι ημιαγωγοί είναι υλικά, όπως το πυρίτιο και το γερμάνιο, που επιτρέπουν τη δίοδο του ηλεκτρικού ρεύματος, κάτω από ορισμένες συνθήκες, όπως είναι η αύξηση της θερμοκρασίας ή η πρόσπτωση ακτινοβολίας. Τα τανζίστορ, οι δίοδοι και τα ολοκληρωμένα κυκλώματα (microchips) είναι μερικές διατάξεις ημιαγωγών, η χρήση των οποίων έφερε επανάσταση στο χώρο των ηλεκτρονικών και υπολογιστών. Βιοϋλικά Τα βιοϋλικά χρησιμοποιούνται στον ανθρώπινο οργανισμό για την αντικατάσταση κατεστραμμένων μερών. Τα υλικά αυτά πρέπει να είναι βιοσυμβατά με τον ανθρώπινο οργανισμό, δηλαδή να μην προκαλούν την απόρριψή τους, να μην διαβρώνονται, να μην παράγουν τοξικές ουσίες, κ.λ.π. Τα μέταλλα, τα κεραμικά, τα πολυμερή, τα σύνθετα υλικά 7
9 και οι ημιαγωγοί μπορούν να χρησιμοποιηθούν ως βιοϋλικά. Μια κοινή εφαρμογή τους είναι τα τεχνητά εμφυτεύματα ισχίου από το βιοσυμβατό κράμα τιτανίου Ti-6Al-4V. 1.4 ΕΠΙΛΟΓΗ ΥΛΙΚΩΝ Πολλοί μηχανικοί κάποια στιγμή της απασχόλησής τους σε κλάδους σχετικούς με την επιστήμη και τεχνολογία των υλικών θα αντιμετωπίσουν ένα πρόβλημα μελέτης και σχεδιασμού ενός εξαρτήματος. Για μια συγκεκριμένη εφαρμογή, ο μηχανικός θα πρέπει να επιλέξει το σωστό υλικό ανάμεσα σε ένα μεγάλο αριθμό διαθέσιμων υλικών. Παράμετροι όπως η αντοχή του υλικού, η υποβάθμιση των ιδιοτήτων του στις συνθήκες λειτουργίας (θερμοκρασία, διαβρωτικό περιβάλλον, κ.λ.π.), το κόστος του υλικού, η μέθοδος μορφοποίησής του, η δυνατότητα ανακύκλωσής του, καθώς και άλλοι παράγοντες συνήθως λαμβάνονται υπόψη κατά τη διαδικασία σχεδιασμού του. Παρακάτω αναφέρονται ορισμένοι παράγοντες που λαμβάνονται υπόψη κατά το σχεδιασμό μιας τροχαλίας. Οι τροχαλίες χρησιμοποιούνται για τη μετάδοση ισχύος μέσω ιμάντων, και υπόκεινται σε τάσεις που εξαρτώνται τόσο από τον τρόπο χύτευσης, τις λεπτομέρειες κατασκευής τους (διαιρούμενες ή ενιαίες), όσο και από τις συνθήκες λειτουργίας τους. Υλικά όπως ο χυτοσίδηρος, ο χυτοχάλυβας ή το αλουμίνιο συνήθως χρησιμοποιούνται για την κατασκευή τους. Εάν ο χυτοσίδηρος επιλεχθεί ως υλικό κατασκευής, θα πρέπει στη συνέχεια να γίνει επιλογή του κατάλληλου τύπου χυτοσιδήρου. Ο φαιός χυτοσίδηρος έχει μικρή αντοχή και επιμήκυνση ( MPa, 1%), ενώ ο μαλακτικοποιημένος ( MPa, 10-2%) και ο ελατός ( MPa, 22-2%) έχουν υψηλότερες μηχανικές ιδιότητες. Ο φαιός χυτοσίδηρος χρησιμοποιείται για την κατασκευή π.χ. τροχαλιών για γερανογέφυρες, ενώ ο μαλακτικοποιημένος και ελατός χρησιμοποιούνται για την κατασκευή τροχαλιών οχημάτων. Σε περίπτωση που η τροχαλία υπόκειται σε υψηλές καταπονήσεις, τότε θα μπορούσε να επιλεγεί ως υλικό κατασκευής ο χυτοχάλυβας, που συγκεντρώνει τα πλεονεκτήματα του χάλυβα και ιδιαίτερα την υψηλή αντοχή και συνεκτικότητα του ( MPa, 25-12%). Ωστόσο, η χύτευση του χυτοχάλυβα είναι δυσκολότερη συγκρινόμενη με τη χύτευση του χυτοσιδήρου. Ακόμη σε κάποιες περιπτώσεις θα μπορούσε να χρησιμοποιηθεί κάποιο κράμα αλουμινίου, το οποίο είναι ελαφρύτερο από τους χυτοσιδήρους και τους χυτοχάλυβες, παρουσιάζει καλύτερη αντοχή στη διάβρωση, αλλά έχει το μειονέκτημα του υψηλότερου κόστους. Συνεπώς, η γνώση των ιδιοτήτων των υλικών, των σχέσεων δομής-ιδιότητας, καθώς και των μεθόδων κατεργασίας τους είναι απαραίτητη προϋπόθεση για την επιτυχή επιλογή των υλικών. 1.5 ΑΝΑΠΤΥΞΗ ΝΕΩΝ ΥΛΙΚΩΝ Αναμφισβήτητα η ανάπτυξη όλων των επιστημονικών τομέων είναι στενά συνυφασμένη με την ανάπτυξη νέων, ακόμη πιο προηγμένων και εξειδικευμένων υλικών. Για παράδειγμα, η αξιοποίηση της «πράσινης» ενέργειας, ηλιακής και αιολικής, προϋποθέτει την ύπαρξη πολύπλοκων υλικών. Οι νέες ανεμογεννήτριες παραγωγής ηλεκτρικής ενέργειας είναι αποδοτικότερες, λόγω της μείωσης του βάρους των τουρμπινών τους. Αυτό επιτυγχάνεται με την προσθήκη ελάχιστων ποσοτήτων μιας σπάνιας γαίας, του δυσπροσίου (Pr), που έχει ως αποτέλεσμα τη μείωση του βάρους του ηλεκτρομαγνήτη κατά 90%. Οι συσκευές μαγνητικής εγγραφής εικόνας (βίντεο), οι συσκευές οπτικού δίσκου (CD), οι οθόνες υγρών κρυστάλλων (LCD), οι οθόνες διόδων φωτοεκπομπής (LED), τα laser, 8
10 οι οπτικές ίνες, κ.λ.π. είναι τεχνολογίες που η εξέλιξή τους έγινε δυνατή λόγω της ανάπτυξης κατάλληλων υλικών. Στον τομέα των μεταφορών, στόχος είναι η μείωση του βάρους των μεταφορικών μέσων, αυτοκινήτων, τρένων, πλοίων, αεροπλάνων, κ.λ.π., και συνεπώς μείωσης της κατανάλωσης των καυσίμων. Η ανάπτυξη νέων υλικών με υψηλές μηχανικές ιδιότητες και χαμηλή πυκνότητα είναι απαραίτητη. Η κατασκευή μεγάλων τμημάτων και πρωτευουσών δομών από σύνθετα υλικά, πολυμερικά υλικά ενισχυμένα με ανθρακονήματα, επέτρεψε την αύξηση του μεγέθους των αεροπλάνων και μείωσης του βάρους τους, π.χ. το Airbus A380. Σε κάθε είδους συσκευή, από κινητά τηλέφωνα, φορητούς υπολογιστές μέχρι και φωτογραφικές μηχανές, χρησιμοποιούνται συσσωρευτές ενέργειας. Οι μπαταρίες ιόντων λιθίου αποτελούν την ιδανική λύση, επειδή συσσωρεύουν περισσότερη ενέργεια, αποφορτίζονται αργότερα και είναι ελαφρύτερες από άλλα υλικά. Επιπλέον, η ανάπτυξη υβριδικών και ηλεκτρικών αυτοκινήτων τείνει να καταστήσει το λίθιο πρωταγωνιστή σε αυτό τον τομέα. Οι πηγές προέλευσης, ανανεώσιμες ή μη, η επίδραση στο περιβάλλον, η δυνατότητα ανακύκλωσης, κ.λ.π, είναι ορισμένοι άλλοι παράγοντες που πρέπει να λαμβάνονται υπόψη κατά την ανάπτυξη νέων υλικών. 1.6 ΥΛΙΚΑ ΟΧΗΜΑΤΩΝ Ένα όχημα αποτελείται από ένα πλήθος εξαρτημάτων και κάθε εξάρτημα είναι κατασκευασμένο από κατάλληλα υλικά, έτσι ώστε αυτό να εκτελεί μια συγκεκριμένη αποστολή για μεγάλη χρονική διάρκεια. Όλα τα υλικά, μεταλλικά, κεραμικά, πλαστικά και σύνθετα χρησιμοποιούνται στην κατασκευή των οχημάτων. Για παράδειγμα, μια άτρακτος ενός γραναζοκιβωτίου αποτελείται από βελτιωμένο χάλυβα, που έχει μεγάλη αντοχή. Ο κορμός ενός κινητήρα αποτελείται από χυτοσίδηρο, υλικό που αποσβένει ταλαντώσεις, Ακόμη μορφοποιείται με χύτευση λόγω του δύσκολου σχήματός του. Το κέλυφος (χελώνα) ενός κινητήρα εσωτερικής καύσης μπορεί να κατασκευαστεί από αλουμίνιο, το οποίο συνδυάζει υψηλές μηχανικές ιδιότητες με μικρό βάρος. Η περιέλιξη ενός ηλεκτροκινητήρα αποτελείται από χαλκό, ο οποίος είναι καλός αγωγός του ηλεκτρισμού, ενώ το περίβλημα των καλωδιώσεων από πλαστικό που έχει μονωτικές ιδιότητες. Ένας ιμάντας πρέπει να μεταφέρει υψηλές εφελκυστικές δυνάμεις και για αυτό χρησιμοποιείται κάποιο ελαστικό υλικό ενισχυμένο με χαλύβδινα σύρματα ή νήματα. Παρακάτω παρουσιάζονται παραδείγματα από όλες τις κατηγορίες υλικών που χρησιμοποιούνται στον τομέα των οχημάτων. Μέταλλα Σιδηρούχα μεταλλικά υλικά, όπως οι χάλυβες και οι χυτοσίδηροι, καθώς και μη σιδηρούχα, όπως ο χαλκός, το αλουμίνιο, το μαγνήσιο, κ.λ.π. βρίσκουν εφαρμογή ως υλικά κατασκευής των οχημάτων. Οι χάλυβες έχουν υψηλές μηχανικές ιδιότητες και συνήθως χρησιμοποιούνται για την κατασκευή εξαρτημάτων που παραλαμβάνουν και μεταφέρουν μεγάλες δυνάμεις. Εξαρτήματα μηχανών όπως άτρακτοι, άξονες, και γρανάζια κατασκευάζονται από χάλυβες (Σχήμα 1.2). 9
11 Σχήμα 1.2: Εκκεντροφόρος άξονας κινητήρα εσωτερικής καύσης από χάλυβα. Οι χυτοσίδηροι είναι σιδηρούχα κράματα, τα οποία τήκονται εύκολα και είναι δεκτικά σε χύτευση. Επιπλέον λόγω της μικροδομής τους έχουν την ικανότητα να αποσβένουν ταλαντώσεις. Χρησιμοποιούνται για τη χύτευση εξαρτημάτων με πολύπλοκη γεωμετρία. π.χ. κορμούς κινητήρων, καλύμματα μηχανών, φτερωτών κ.λ.π. (Σχήμα 1.3). Σχήμα 1.3: Φτερωτή αντλίας νερού οχήματος από χυτοσίδηρο. Ο χαλκός, ο ψευδάργυρος, ο κασσίτερος, το χρώμιο, το νικέλιο, ο μόλυβδος, καθώς και άλλα μη σιδηρούχα μέταλλα, βρίσκουν ευρεία εφαρμογή στη μηχανολογία. Ο χαλκός παρουσιάζει εξαιρετική ηλεκτρική αγωγιμότητα και χρησιμοποιείται π.χ. ως σύρμα περιέλιξης στους ηλεκτροκινητήρες (Σχήμα 1.4). Ο ψευδάργυρος, ο κασσίτερος, το χρώμιο, και το νικέλιο παρουσιάζουν υψηλή αντιδιαβρωτική αντοχή και χρησιμοποιούνται π.χ. ως επιμεταλλώσεις για τους χάλυβες. 10
12 Σχήμα 1.4: Περιέλιξη ηλεκτροκινητήρα από χαλκό. Η σημασία του αλουμινίου, του μαγνησίου και του τιτανίου (ελαφρά μέταλλα) είναι ιδιαίτερα σημαντική στην κατασκευαστική βιομηχανία, λόγω της υψηλής τους αντοχής και της μικρής πυκνότητάς τους. Στα Σχήματα 1.5 και 1.6 παρουσιάζονται εξαρτήματα κινητήρων κατασκευασμένα από αλουμίνιο και μαγνήσιο. Σχήμα 1.5: Κέλυφος (χελώνα) κινητήρα εσωτερικής καύσης από αλουμίνιο. 11
13 Σχήμα 1.6: Κάλυμμα κυλινδοκεφαλής πετρελαιοκινητήρα από μαγνήσιο. Κεραμικά Τα κεραμικά, λόγω των υψηλών σημείων τήξης των, χρησιμοποιούνται σε κατασκευές που λειτουργούν σε υψηλές θερμοκρασίες, όπως κινητήρες, εξατμίσεις, μπουζί αυτοκινήτων (Σχήμα 1.7), κ.λ.π. Ακόμη και τα κεραμικά, τα οποία υπάρχουν στη φύση (ορυκτά), όπως ο γρανίτης, χρησιμοποιούνται για ειδικούς σκοπούς π.χ. ως πλάκα ποιοτικού ελέγχου (Σχήμα 1.8) ανταλλακτικών οχημάτων. Σχήμα 1.7: Μόνωση σε μπουζί αυτοκινήτου από κεραμικό (αλουμίνα: Al2O3). 12
14 Σχήμα 1.8: Πλάκα ελέγχου από γρανίτη. Πολυμερή Οι εφαρμογές των πολυμερών στην αυτοκινητοβιομηχανία είναι ποικίλες. Η χρήση τους εκτείνεται από τα ελαστικά των αυτοκινήτων μέχρι την κατασκευή στοιχείων, όπως δακτυλίων στεγανότητας, μεταλλοπλαστικών παρεμβυσμάτων (τσιμούχες), σωλήνων, φτερωτών ανεμιστήρων ψύξης (Σχήμα 1.9), κ.λ.π. Σχήμα 1.9: Φτερωτή ανεμιστήρα ψύξης αυτοκινήτου από πλαστικό. Σύνθετα υλικά Τα σύνθετα υλικά βρίσκουν ολοένα και μεγαλύτερη εφαρμογή στην αυτοκινητοβιομηχανία, τη ναυπηγική και την αεροναυπηγική. Για παράδειγμα, τμήματα αμαξωμάτων, αεροπλάνων και λέμβων κατασκευάζονται από σύνθετα υλικά πολυεστερικής ή εποξειδικής μήτρας ενισχυμένων με υαλονήματα ή ανθρακονήματα. Μια άλλη εφαρμογή των σύνθετων υλικών είναι τα φερμουίτ αυτοκινήτων (Σχήμα 1.10). 13
15 Σχήμα 1.10: Φερμουίτ πέδης από σύνθετο υλικό (πολυμερές, π.χ φαινολική ρητίνη ενισχυμένh με βιομηχανικές ίνες, όπως αραμιδικές, ίνες υάλου, ίνες Kevlar, γραφιτικές, κλπ.). 14
16 ΚΕΦΑΛΑΙΟ 2 ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ ΚΑΙ ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ 2.1 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ Όπως είναι γνωστό η ύλη αποτελείται από βασικές μονάδες που ονομάζονται άτομα (άτμητο=α στερητικό+τέμνω). Η δομή του ατόμου μπορεί να περιγραφεί ικανοποιητικά από την ύπαρξη τριών ειδών μικρότερων σωματιδίων, των πρωτονίων, των ηλεκτρονίων και των νετρονίων. Κάθε άτομο έχει ένα πολύ μικρό πυρήνα αποτελούμενο από πρωτόνια και νετρόνια, ο οποίος περιβάλλεται από ηλεκτρόνια. Σε ένα ηλεκτρικά ουδέτερο άτομο, το αρνητικό φορτίο των ηλεκτρονίων είναι ίσο με το θετικό φορτίο των πρωτονίων. Τo φορτίο των πρωτονίων είναι 1,60 X Cb, ενώ των ηλεκτρονίων είναι ίσο και αντίθετο με αυτό των πρωτονίων. Τα νετρόνια είναι ηλεκτρικά ουδέτερα. Η μάζα όλων των σωματιδίων είναι απειροελάχιστη. Η μάζα των πρωτονίων είναι Χ g, η οποία είναι περίπου ίση με τη μάζα των νετρονίων Χ g, ενώ η μάζα των ηλεκτρονίων είναι περίπου 1840 φορές μικρότερη, Χ g, από τη μάζα των πρωτονίων. Συνεπώς όλη σχεδόν η μάζα του ατόμου βρίσκεται στον πυρήνα. Η διάμετρος του πυρήνα είναι περίπου mm, ενώ η διάμετρος του ατόμου είναι περίπου 10-7 mm. Ο αριθμός των πρωτονίων που περιέχει ο πυρήνας κάθε χημικού στοιχείου είναι καθορισμένος και ονομάζεται ατομικός αριθμός. Σε ένα ηλεκτρικά ουδέτερο άτομο, ο ατομικός αριθμός είναι ίσος με τον αριθμό των ηλεκτρονίων του. Η ατομική μάζα ενός ατόμου μπορεί να θεωρηθεί ως το άθροισμα των μαζών των πρωτονίων και των νετρονίων του. Αν και τα άτομα όλων των στοιχείων έχουν τον ίδιο αριθμό πρωτονίων, ο αριθμός των νετρονίων τους μπορεί να διαφέρει. Άτομα που έχουν διαφορετικό αριθμό νετρονίων και συνεπώς διαφορετική ατομική μάζα ονομάζονται ισότοπα. Τα ισότοπα χαρακτηρίζονται από το μαζικό αριθμό, ο οποίος ισούται με το άθροισμα των πρωτονίων και νετρονίων, π.χ.: 12 C = ισότοπο του άνθρακα με μαζικό αριθμό 12 (6 πρωτόνια+6 νετρόνια) C = ισότοπο του άνθρακα με μαζικό αριθμό 13 (6 πρωτόνια+7 νετρόνια) 14 C = ισότοπο του άνθρακα με μαζικό αριθμό 14 (6 πρωτόνια+8 νετρόνια) 13 Το ατομικό βάρος ενός στοιχείου είναι ο αριθμός που δείχνει πόσες φορές το άτομο του στοιχείου είναι βαρύτερο από το 1/12 του βάρους του κοινότερου και ελαφρύτερου ισοτόπου του άνθρακα 12, 12C (ατομικό βάρος 12C = ). Το 1/12 του βάρους του ισοτόπου του άνθρακα 12, ορίζεται ως μια μονάδα ατομικής μάζας (atomic mass unit, amu). Το ατομικό βάρος ενός στοιχείου είναι ο μέσος όρος των ατομικών βαρών των ισοτόπων του που υπάρχουν στη φύση. Για παράδειγμα, το ατομικό βάρος του άνθρακα είναι Τα άτομα συνδέονται μεταξύ τους και σχηματίζουν μόρια, τα οποία είναι τα μικρότερα σωματίδια μιας χημικής ένωσης ή στοιχείου, που διατηρούν τις ιδιότητες του σώματος. Για παράδειγμα, το μόριο του Cl2 αποτελείται από δυο άτομα χλωρίου, ενώ το μόριο του Η2Ο αποτελείται από δυο άτομα υδρογόνου ενωμένα με ένα άτομο οξυγόνου. Η διάμετρος των μορίων είναι περίπου 10-6 έως 10-5 mm. Το μοριακό βάρος είναι ίσο με το άθροισμα των ατομικών βαρών. Τόσο το ατομικό όσο και το μοριακό βάρος είναι καθαροί αριθμοί. Επειδή όμως στις αντιδράσεις μεταξύ στοιχείων και ενώσεων πρέπει να χρησιμοποιούνται ποσότητες 15
17 μετρήσιμες, για αυτό εισήχθησαν οι όροι γραμμοάτομο και γραμμομόριο, οι οποίοι ταυτίζονται με το ατομικό και μοριακό βάρος αντίστοιχα, αλλά έχουν μονάδες σε γραμμάρια, g/mol. Σε ένα mole μιας ουσίας υπάρχουν NA=6.023x1023 άτομα ή μόρια ή ιόντα, NA = αριθμός Avogadro. Για παράδειγμα, το ατομικό βάρος του χαλκού είναι 63.5 g/mol ή 63.5 amu/άτομο (δηλαδή το άτομο του χαλκού είναι 63.5 φορές βαρύτερο από το 1/12 του βάρους του ισοτόπου του άνθρακα 12). 2.2 ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ Κατά την προσπάθεια περιγραφής της ηλεκτρονιακής δομής των ατόμων προτάθηκαν διάφορα μοντέλα. Ωστόσο, η κατανόηση της συμπεριφοράς των ηλεκτρονίων επιτεύχθηκε με την εισαγωγή εννοιών και αρχών από δύο νέους κλάδους της κλασσικής μηχανικής: της κβαντομηχανικής και της κυματομηχανικής ΠΡΟΤΥΠΟ ΤΟΥ RUTHERFORD Σύμφωνα με τον Ε. Rutherford, το άτομο παρουσιάζεται ως μικρογραφία του πλανητικού συστήματος. Στο κέντρο του υπάρχει ένας θετικός πυρήνας γύρω από τον οποίο κινούνται σε διάφορες κυκλικές τροχιές τα ηλεκτρόνια, όπως οι πλανήτες γύρω από τον ήλιο. Τα ηλεκτρόνια συγκρατούνται στις τροχιές τους λόγω της ισορροπίας της φυγόκεντρης δύναμης και της ηλεκτροστατικής έλξης με τον πυρήνα. Στο συμπέρασμα αυτό κατέληξε μετά από μια σειρά πειραμάτων «βομβαρδισμού» λεπτών φύλλων χρυσού ή αλουμινίου με ακτίνες α (θετικά φορτισμένα σωματίδια που προέρχονταν από ράδιο). Παρατηρήθηκε, ότι ενώ τα περισσότερα σωματίδια διαπερνούσαν τα φύλλα του μετάλλου, χωρίς σημαντική εκτροπή από την ευθύγραμμη πορεία τους, σε σπάνιες περιπτώσεις ορισμένα σωματίδια υφίσταντο πολύ μεγάλη εκτροπή. Η εκτροπή αυτών των σωματιδίων αποδόθηκε στο πλησίασμά τους στους θετικά φορτισμένους πυρήνες, ενώ η σπανιότητα των εκτροπών αποτέλεσε μια ένδειξη του εξαιρετικά μικρού όγκου των πυρήνων ΠΡΟΤΥΠΟ ΤΟΥ BOHR Για πρώτη φορά η κβαντική θεωρία εφαρμόστηκε το 1913 από τον Δανό φυσικό Ν. Bohr, στην προσπάθειά του να εξηγήσει το φάσμα του ατόμου του υδρογόνου. Με βάση τις αρχές της κβαντομηχανικής έγιναν δύο βασικές παραδοχές: 1) τα ηλεκτρόνια των ατόμων κινούνται πάνω σε διακριτές ενεργειακές τροχιές και 2) η ενέργειά τους είναι κβαντισμένη. Αυτό σημαίνει ότι για να μεταπηδήσει ένα ηλεκτρόνιο από μια στάθμη χαμηλότερης ενέργειας σε μια στάθμη υψηλότερης, πρέπει να απορροφήσει ενέργεια. Αντίθετα, όταν μεταπηδήσει από μια στάθμη υψηλότερης ενέργειας σε μια στάθμη χαμηλότερης, εκπέμπει τη διαφορά ενέργειας με τη μορφή ακτινοβολίας ορισμένης συχνότητας, δηλαδή Ε2-Ε1=hν, όπου h = σταθερά του Planck και ν = συχνότητα ακτινοβολίας. Τα ηλεκτρόνια κατά την περιστροφή τους πάνω στις σταθερές ενεργειακές τροχιές δεν εκπέμπουν ακτινοβολία και συνεπώς διατηρούν την ενέργειά τους. Συνέπεια αυτών των αρχών ήταν το ατομικό πρότυπο του Bohr. Στο Σχήμα 2.1 παρουσιάζεται αυτό το πρότυπο. 16
18 Σχήμα 2.1: Σχηματική παράσταση του ατομικού προτύπου του Bohr. Η θεωρία του Bohr αποτέλεσε επίτευγμα για την εποχή του και άνοιξε νέους ορίζοντες. Η κατανομή όμως των ηλεκτρονίων γύρω από τον πυρήνα του ατόμου, κατανοήθηκε περισσότερο με την εφαρμογή των αρχών της κυματομηχανικής, προτείνοντας την παραδοχή ότι το ηλεκτρόνιο δεν συμπεριφέρεται μόνο ως σωματίδιο, αλλά και ως κύμα. Σύμφωνα με αυτή τη θεωρία, το ηλεκτρόνιο δεν αντιμετωπίζεται ως σωματίδιο που κινείται σε κυκλική τροχιά, αλλά πλέον η θέση του περιγράφεται από την πιθανότητα να βρίσκεται σε συγκεκριμένο σημείο γύρω από τον πυρήνα. Έτσι δημιουργείται ένα νέφος του οποίου η πυκνότητα στο χώρο αυξάνεται, όταν αυξάνεται και η πιθανότητα του ηλεκτρονίου να βρεθεί σε αυτό το χώρο. Οι κυκλικές τροχιές του Bohr συμπίπτουν με τις περιοχές υψηλής πυκνότητας του ηλεκτρονιακού νέφους ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ Σύμφωνα με τις αρχές της κυματομηχανικής η κατανομή των ηλεκτρονίων γύρω από τον πυρήνα καθορίζεται από τέσσερις παραμέτρους, που ονομάζονται κβαντικοί αριθμοί. Ο κύριος κβαντικός αριθμός n μπορεί να έχει ακέραιες τιμές 1,2,3,4, και προσδιορίζει τις στιβάδες στις οποίες κατανέμονται τα ηλεκτρόνια. Οι στιβάδες επίσης συμβολίζονται με τα γράμματα K, L, M, N,...και συμπίπτουν με τις ενεργειακές τροχιές του ατομικού πρότυπου του Bohr. Ο κύριος κβαντικός αριθμός προσδιορίζει την απόσταση και συνεπώς τη θέση του ηλεκτρονίου από τον πυρήνα. Το πρότυπο Bohr αρχικά μπορούσε να εξηγήσει το φάσμα του υδρογόνου. Ωστόσο όταν χρησιμοποιήθηκαν φασματοσκόπια με μεγαλύτερη διακριτική ικανότητα φάνηκε ότι κάθε φασματική γραμμή αποτελείται από περισσότερες φασματικές γραμμές. Προκειμένου να υπάρχει αντιστοιχία μεταξύ θεωρίας και πειραματικών δεδομένων έγινε δεκτό ότι οι στιβάδες χωρίζονται σε υποστιβάδες. Οι μεταπτώσεις των ηλεκτρονίων μεταξύ αυτών των υποστιβάδων μπορούσε να εξηγήσει το διαχωρισμό της μιας φασματικής γραμμής σε περισσότερες. Ο αριθμός των υποστιβάδων καθώς και το σχήμα τους προσδιορίζεται από το δευτερεύοντα κβαντικό αριθμό ℓ. Ο δευτερεύων κβαντικός αριθμός μπορεί να παίρνει τις τιμές 0, 1,.( n -1). Για το συμβολισμό των υποστιβάδων χρησιμοποιούνται τα γράμματα s (ℓ=0), p (ℓ=1), d (ℓ=2) και f (ℓ=3). Οι υποστιβάδες έχουν διαφορετικό σχήμα, π.χ. η υποστιβάδα s παρουσιάζει σφαιρική συμμετρία, η p έχει δυο λοβούς (σχήμα οκτώ), κλπ. Το γεγονός ότι παρουσία μαγνητικού πεδίου οι φασματικές γραμμές διασπώνται σε περισσότερες συνιστώσες οδήγησε στην αποδοχή ενός τρίτου κβαντικού αριθμού, του μαγνητικού κβαντικού αριθμού mℓ. Οι τιμές του κυμαίνονται από -ℓ, -(ℓ-1). 0,.+( ℓ+1), +ℓ, δηλαδή 2ℓ+1 τιμές. Συνεπώς σε κάθε υποστιβάδα υπάρχουν 2ℓ+1 ενεργειακές 17
19 καταστάσεις (τροχιακά). Για την υποστιβάδα s υπάρχει μια ενεργειακή κατάσταση, ενώ για τις υποστιβάδες p, d και f υπάρχουν 3, 5 και 7 ενεργειακές καταστάσεις αντίστοιχα. Ο τέταρτος κβαντικός αριθμός, ο μαγνητικός κβαντικός αριθμός του spin, ms, συνδέεται με τη στροφορμή του ηλεκτρονίου λόγω αυτοπεριστροφής και μπορεί να πάρει μόνο δυο τιμές, +1/2 και -1/2. Σύμφωνα με την απαγορευτική αρχή του Pauli, κάθε ενεργειακή κατάσταση μπορεί να πάρει δυο ηλεκτρόνια, τα οποία έχουν αντίθετα σπιν. Συνεπώς, η υποστιβάδα s που έχει μια ενεργειακή κατάσταση μπορεί να έχει το πολύ 2 ηλεκτρόνια, η υποστιβάδα p, η οποία έχει τρεις ενεργειακές καταστάσεις (px, py,pz) μπορεί να έχει 6 ηλεκτρόνια, η υποστιβάδα d η οποία έχει πέντε ενεργειακές καταστάσεις (dxy, dxz, dyz, dx2-y2, dz2), μπορεί να έχει 10 ηλεκτρόνια και η υποστιβάδα f, η οποία έχει επτά ενεργειακές καταστάσεις, μπορεί να πάρει 14 ηλεκτρόνια. Απουσία μαγνητικού πεδίου, οι μαγνητικοί κβαντικοί αριθμοί, mℓ και ms, δεν υφίστανται και οι ενεργειακές καταστάσεις δεν διαφέρουν ενεργειακά, είναι ίδιες. Σε αντίθεση, παρουσία μαγνητικού πεδίου, οι ενεργειακές καταστάσεις αποκτούν ελαφρώς διαφορετικές ενέργειες. Στον Πίνακα 2.1 παρουσιάζονται συγκεντρωτικά οι κύριες στιβάδες, οι υποστιβάδες, οι ενεργειακές τους καταστάσεις καθώς και ο μεγαλύτερος αριθμός ηλεκτρονίων που μπορούν να τοποθετηθούν, για n=1, 2, 3, 4. Πίνακας 2.1: Κατανομή ηλεκτρονίων σύμφωνα με τους τέσσερις κβαντικούς αριθμούς. Στιβάδες, Υποστιβάδες, Ενεργειακές Ηλεκτρόνια Ηλεκτρόνια n ℓ καταστάσεις ανά ανά (τροχιακά) υποστιβάδα στιβάδα K (n=1) s(ℓ=0) L (n=2) s(ℓ=0) p(ℓ=1) 3 (px, py,pz) 6 M(n=3) s(ℓ=0) p(ℓ=1) 3(px, py,pz) 6 d(ℓ=2) 5(dxy, dxz, dyz, dx2-y2, dz2) 10 N(n=4) s(ℓ=0) p(ℓ=1) 3(px, py,pz) 6 d(ℓ=2) 5(dxy, dxz, dyz, dx2-y2, dz2) 10 f(ℓ=3)
20 2.2.4 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΙΑΜΟΡΦΩΣΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ηλεκτρονιακή διαμόρφωση ενός ατόμου περιγράφει τον τρόπο που τα ηλεκτρόνια συμπληρώνουν τα υπάρχοντα τροχιακά. Σε ένα άτομο τα ηλεκτρόνια συμπληρώνουν πρώτα τα τροχιακά με τις χαμηλότερες ενέργειες, έτσι ώστε το άτομο να περικλείει τη μικρότερη εσωτερική ενέργεια και να έχει μεγαλύτερη σταθερότητα. Η ενέργεια των τροχιακών αυξάνεται με αυξανόμενο κβαντικό αριθμό, n. Για παράδειγμα, το τροχιακό 1s έχει μικρότερη ενέργεια από το τροχιακό 2s και αυτό μικρότερη από το τροχιακό 3s. Για τον ίδιο κβαντικό αριθμό, η ενέργεια των υποστιβάδων αυξάνεται με αυξανόμενο τον δευτερεύοντα κβαντικό αριθμό, l. Η υποστιβάδα 3s έχει μικρότερη ενέργεια από την υποστιβάδα 3p και αυτή μικρότερη από την 3d. Τροχιακά γειτονικών στιβάδων μπορεί να επικαλύπτονται με συνέπεια να υπάρχει διαφοροποίηση στην ενέργεια των τροχιακών, π.χ. η ενέργεια του τροχιακού 3d είναι μεγαλύτερη από την ενέργεια του τροχιακού 4s. Για τις σχετικές ενέργειες των τροχιακών ισχύει η παρακάτω σειρά: 1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p<6f<7d Στον Πίνακα 2.2 παρουσιάζονται οι ηλεκτρονιακές διαμορφώσεις των στοιχείων με ατομικό αριθμό από 1 μέχρι 36, για τα στοιχεία υδρογόνο μέχρι κρυπτό. Ο αριθμός των ηλεκτρονίων σε κάθε τροχιακό υποδεικνύεται με ένα εκθέτη. Για παράδειγμα το υδρογόνο έχει ένα ηλεκτρόνιο και η ηλεκτρονιακή του διαμόρφωση είναι 1s1, ενώ ο άνθρακας έχει έξη ηλεκτρόνια και η ηλεκτρονιακή του διαμόρφωση είναι 1s22s22p2. Όλα τα στοιχεία με βάση την διάταξη των ηλεκτρονίων στις στιβάδες των ατόμων τους ταξινομούνται στον περιοδικό πίνακα (Πίνακας 2.3). Τα στοιχεία τοποθετούνται κατά αύξουσα σειρά του ατομικού αριθμού τους σε επτά οριζόντιες γραμμές, που ονομάζονται περίοδοι και δεκαοκτώ κάθετες στήλες, που λέγονται ομάδες. Οι ομάδες αποτελούνται από επτά κύριες, συνοδευόμενες από το γράμμα Α (ΙΑ έως VIIΑ), επτά δευτερεύουσες, συνοδευόμενες από το γράμμα Β (ΙΒ έως VIIΒ), την ομάδα VIIΙ και την ομάδα 0, των ευγενών αερίων. Τα στοιχεία κάθε ομάδας έχουν την ίδια διαμόρφωση ηλεκτρονίων και παρουσιάζουν παρόμοιες φυσικές και χημικές ιδιότητες. Τα στοιχεία που βρίσκονται στην ίδια περίοδο, έχουν τα ηλεκτρόνιά τους κατανεμημένα στον ίδιο αριθμό στιβάδων, και οι ιδιότητές τους μεταβάλλονται βαθμιαία κατά μήκος της κάθε περιόδου. Συγκρίνοντας την ηλεκτρονιακή διαμόρφωση των στοιχείων (Πίνακας 2.2) με τη θέση τους στον περιοδικό πίνακα (Σχήμα 2.3), βλέπουμε ότι ο αριθμός κάθε περιόδου αντιστοιχεί με τον αριθμό των στιβάδων ηλεκτρονίων, ενώ ο αριθμός της ομάδας είναι ίσος με τον αριθμό ηλεκτρονίων της εξώτατης στιβάδας. Τα αέρια ήλιο, νέο, αργό, κρυπτό, ξένο και ραδόνιο (ομάδα 0) δεν έχουν την τάση να σχηματίσουν κανενός είδους ένωση και για αυτό ονομάζονται ευγενή αέρια. Αυτά τα αέρια, εκτός του ηλίου, έχουν στην εξωτερική τους στιβάδα συνολικά 8 ηλεκτρόνια, 2 στην s και 6 στην p υποστιβάδα και πιστεύεται ότι αυτός είναι ο λόγος της σταθερότητάς τους. Το ήλιο έχει δύο ηλεκτρόνια που τοποθετούνται στο τροχιακό 1s. 19
21 Πίνακας 2.2: Ηλεκτρονιακή διαμόρφωση των στοιχείων με ατομικό (υδρογόνο μέχρι κρυπτό). Ατομικός Στοιχείο Ηλεκτρονιακή Αριθμός διαμόρφωση 1s1 1η 1 Υδρογόνο (H) 1s2 Περίοδος 2 Ήλιο (He) 1s22s1 3 Λίθιο (Li) 1s22s2 4 Βηρύλιο (Be) 1s22s22p1 2η 5 Βόριο (B) 1s22s22p2 Περίοδος 6 Άνθρακας (C) 1s22s22p3 7 Άζωτο (N) 1s22s22p4 8 Οξυγόνο (O) 1s22s22p5 9 Φθόριο (F) 1s22s22p6 10 Νέο (Ne) 1s22s22p63s1 11 Νάτριο (Na) 1s22s22p63s2 12 Μαγνήσιο (Mg) 1s22s22p63s23p1 3η 13 Αλουμίνιο (Al) 1s22s22p63s23p2 Περίοδος 14 Πυρίτιο (Si) 1s22s22p63s23p3 15 Φώσφορος (P) 1s22s22p63s23p4 16 Θείο (S) 1s22s22p63s23p6 17 Χλώριο (Cl) 1s22s22p63s23p6 18 Αργό (Ar) 1s22s22p63s23p64s1 19 Κάλιο (Κ) 1s22s22p63s23p64s2 20 Ασβέστιο (Ca) 1s22s22p63s23p63d14s2 21 Σκάνδιο (Sc) 1s22s22p63s23p63d24s2 22 Τιτάνιο (Ti) 1s22s22p63s23p63d34s2 23 Βανάδιο (V) 1s22s22p63s23p63d54s1 24 Χρώμιο Cr) 1s22s22p63s23p63d54s2 4η 25 Μαγγάνιο (Mn) 1s22s22p63s23p63d64s2 Περίοδος 26 Σίδηρος (Fe) 1s22s22p63s23p63d74s2 27 Κοβάλτιο (Co) 1s22s22p63s23p63d84s2 28 Νικέλιο (Ni) 1s22s22p63s23p63d104s1 29 Χαλκός (Cu) 30 Ψευδάργυρος (Zn) 1s22s22p63s23p63d104s2 1s22s22p63s23p63d104s24p1 31 Γάλλιο (Ga) 1s22s22p63s23p63d104s24p2 32 Γερμάνιο (Ge) 1s22s22p63s23p63d104s24p3 33 Αρσενικό (As) 1s22s22p63s23p63d104s24p4 34 Σελήνιο (Se) 1s22s22p63s23p63d104s24p5 35 Βρώμιο (Br) 1s22s22p63s23p63d104s24p6 36 Κρυπτό (Kr) αριθμό 1 μέχρι 36 αμέταλλο αέριο ευγενές αέριο μέταλλο μέταλλο ενδιάμεσο* ενδιάμεσο* αμέταλλο αέριο αμέταλλο αέριο αμέταλλο αέριο ευγενές αέριο μέταλλο μέταλλο μέταλλο ενδιάμεσο* αμέταλλο αμέταλλο αμέταλλο αέριο ευγενές αέριο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο μέταλλο ενδιάμεσο* ενδιάμεσο* ενδιάμεσο* αμέταλλο αέριο ευγενές αέριο * Τα στοιχεία B, C, Si, Ge, As, Se καλούνται ενδιάμεσα, επειδή παρουσιάζουν ιδιότητες μεταξύ των μετάλλων και αμετάλλων. `Όλα τα στοιχεία με βάση την διάταξη των ηλεκτρονίων στις στιβάδες των ατόμων τους ταξινομούνται στον περιοδικό πίνακα (Πίνακας 2.3). Τα στοιχεία τοποθετούνται κατά αύξουσα σειρά του ατομικού αριθμού τους σε επτά οριζόντιες γραμμές, που ονομάζονται περίοδοι και δεκαοκτώ κάθετες στήλες, που λέγονται ομάδες. Οι ομάδες αποτελούνται από επτά κύριες, συνοδευόμενες από το γράμμα Α (ΙΑ έως VIIΑ), επτά δευτερεύουσες, συνοδευόμενες από το γράμμα Β (ΙΒ έως VIIΒ), την ομάδα VIIΙ και την ομάδα 0, των ευγενών αερίων. Τα στοιχεία κάθε ομάδας έχουν την ίδια διαμόρφωση ηλεκτρονίων και 20
22 παρουσιάζουν παρόμοιες φυσικές και χημικές ιδιότητες. Τα στοιχεία που βρίσκονται στην ίδια περίοδο, έχουν τα ηλεκτρόνιά τους κατανεμημένα στον ίδιο αριθμό στιβάδων, και οι ιδιότητές τους μεταβάλλονται βαθμιαία κατά μήκος της κάθε περιόδου. Συγκρίνοντας την ηλεκτρονιακή διαμόρφωση των στοιχείων (Πίνακας 2.2) με τη θέση τους στον περιοδικό πίνακα (Σχήμα 2.2), βλέπουμε ότι ο αριθμός κάθε περιόδου αντιστοιχεί με τον αριθμό των στιβάδων ηλεκτρονίων, ενώ ο αριθμός της ομάδας είναι ίσος με τον αριθμό ηλεκτρονίων της εξώτατης στιβάδας. Τα αέρια ήλιο, νέο, αργό, κρυπτό, ξένο και ραδόνιο (ομάδα 0) δεν έχουν την τάση να σχηματίσουν κανενός είδους ένωση και για αυτό ονομάζονται ευγενή αέρια. Αυτά τα αέρια, εκτός του ηλίου, έχουν στην εξωτερική τους στιβάδα συνολικά 8 ηλεκτρόνια, 2 στην s και 6 στην p υποστιβάδα και πιστεύεται ότι αυτός είναι ο λόγος της σταθερότητάς τους. Το ήλιο έχει δύο ηλεκτρόνια που τοποθετούνται στο τροχιακό 1s. Σχήμα 2.2: Περιοδικός Πίνακας Xημικών Στοιχείων. 2.3 ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ Η πρόσληψη, η αποβολή ή το μοίρασμα των ηλεκτρονίων της εξωτερικής στιβάδας των ατόμων (ηλεκτρόνια σθένους), προκειμένου να αποκτήσουν σταθερή ηλεκτρονιακή διαμόρφωση, όπως εκείνες των ευγενών αερίων, αποτελεί τη βάση σχηματισμού των ατομικών δεσμών. Γενικά οι δεσμοί διακρίνονται σε δυο κατηγορίες στους πρωτεύοντες ή ισχυρούς δεσμούς (χημικοί δεσμοί) και στους δευτερεύοντες ή ασθενείς δεσμούς (φυσικοί δεσμοί). Παρακάτω εξετάζονται τα τρία είδη των κύριων δεσμών, ιοντικός ή ετεροπολικός δεσμός, ομοιοπολικός δεσμός, μεταλλικός δεσμός καθώς και οι δευτερεύοντες δεσμοί. 21
23 2.3.1 ΙΟΝΤΙΚΟΣ Η ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Ιοντικοί δεσμοί σχηματίζονται ανάμεσα στα μέταλλα και στα αμέταλλα. Τα άτομα των μετάλλων τείνουν να δώσουν τα ηλεκτρόνια σθένους και έτσι να γίνουν θετικά ιόντα (ηλεκτροθετικά άτομα), ενώ τα αμέταλλα τείνουν να προσλάβουν ηλεκτρόνια και να γίνουν αρνητικά ιόντα (ηλεκτραρνητικά άτομα). Τα θετικά ιόντα έλκονται με τα αρνητικά ιόντα και σχηματίζεται ο ιοντικός δεσμός. Ο ιοντικός δεσμός είναι μη κατευθυντικός δεσμός και η ισχύς του είναι ίδια σε όλες τις κατευθύνσεις. Όσο πιο μεγάλη είναι η διαφορά ηλεκτραρνητικότητας μεταξύ των ατόμων, τόσο πιο μεγάλη είναι η τάση τους προς σχηματισμό ιοντικού δεσμού. Τα περισσότερο ηλεκτροθετικά στοιχεία είναι τα αλκάλια (Li, Na,, K, κ.λ.π.), ενώ τα περισσότερο ηλεκτραρνητικά στοιχεία είναι το F, O και N. Το μόριο του χλωριούχου νατρίου NaCl αποτελεί κλασσικό παράδειγμα ιοντικού δεσμού. To νάτριο έχει ένα ηλεκτρόνιο στην εξωτερική του στιβάδα, 3s, το οποίο τείνει να το αποβάλλει αποκτώντας τη σταθερή ηλεκτρονιακή διαμόρφωση του ευγενούς αερίου νέου. Τα χλώριο έχει επτά ηλεκτρόνια στην εξωτερική του στιβάδα, 3s23p5 και με την πρόσληψη ενός ηλεκτρονίου αποκτά τη σταθερή διαμόρφωση του ευγενούς αερίου αργού. Στο Σχήμα 2.3 απεικονίζεται ο ιοντικός δεσμός. Σχήμα 2.3: Σχηματική παράσταση του ιοντικού δεσμού. Ο ιοντικός δεσμός είναι ο επικρατέστερος δεσμός στα κεραμικά υλικά. Οι ενέργειες των δεσμών είναι αρκετά υψηλές, γεγονός που οδηγεί σε υψηλά σημεία τήξης. Για παράδειγμα, η ενέργεια δεσμού στο MgO είναι 940 Kcal/mol και το σημείο τήξης 2800 C. Όσο μεγαλύτερο είναι το μέγεθος των ατόμων, τόσο μικρότερη είναι η ενέργεια του δεσμού. Αυτό συμβαίνει γιατί τα ηλεκτρόνια σθένους βρίσκονται πιο μακριά από τον πυρήνα με συνέπεια τη μείωση των ελκτικών δυνάμεων. Στον Πίνακα 2.3 παρουσιάζονται οι ενέργειες δεσμών και τα σημεία τήξεως για μερικές ιοντικές ενώσεις ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Ομοιοπολικός δεσμός σχηματίζεται μεταξύ των ατόμων ως αποτέλεσμα της αμοιβαίας συνεισφοράς ηλεκτρονίων της εξωτερικής τους στιβάδας, έτσι ώστε καθένα από τα άτομα να αποκτήσει σταθερή ηλεκτρονιακή διαμόρφωση. Ο ομοιοπολικός δεσμός αντίθετα με τον ιοντικό είναι κατευθυντικός. Η κατεύθυνσή του είναι μεταξύ των ατόμων που συνεισφέρουν τα ηλεκτρόνια. Όταν ο δεσμός πραγματοποιείται μεταξύ ατόμων διαφορετικής ηλεκτραρνητικότητας, τότε το κοινό ζεύγος ηλεκτρονίων έλκεται περισσότερο από το ηλεκτραρνητικότερο άτομο, 22
24 με συνέπεια την πόλωση του μορίου, όπως στην περίπτωση των ιοντικών δεσμών. Όσο μεγαλύτερη είναι η διαφορά ηλεκτραρνητικότητας τόσο πιο ιοντικός είναι ο δεσμός. Ο ομοιοπολικός δεσμός κυρίως συναντάται στις οργανικές ενώσεις, όπως τα πολυμερή. Επίσης συναντάται σε στερεές ανόργανες ενώσεις όπως το διαμάντι, το πυρίτιο και το γερμάνιο. Παρακάτω παρατίθενται μερικά παραδείγματα ενώσεων ομοιοπολικού δεσμού. Στο μόριο του υδρογόνου, Η2, κάθε άτομο υδρογόνου συνεισφέρει το μοναδικό του ηλεκτρόνιο (1s1) αποκτώντας με αυτό τον τρόπο τη διαμόρφωση του ατόμου του ηλίου. Σχήμα 2.4: Σχηματική παράσταση του ομοιοπολικού δεσμού στο μόριο του μεθανίου (CH4). Στο μόριο του μεθανίου, CH4, ένα άτομο άνθρακα ενώνεται με τέσσερα άτομα υδρογόνου. Κάθε άτομο άνθρακα έχει τέσσερα ηλεκτρόνια στην εξωτερική του στιβάδα (2s22p2), τα οποία μοιράζεται με τα τέσσερα άτομα του υδρογόνου. Έτσι ο άνθρακας έχει τώρα οκτώ ηλεκτρόνια στην εξωτερική του στιβάδα, αποκτώντας τη διαμόρφωση του νέου, ενώ το υδρογόνο δυο ηλεκτρόνια, αποκτώντας τη διαμόρφωση του ηλίου (Σχήμα 2.4). Στο διαμάντι κάθε άτομο άνθρακα συνδέεται με ομοιοπολικούς δεσμούς με τέσσερα άλλα άτομα άνθρακα τα οποία βρίσκονται στις κορυφές ενός κανονικού τετραέδρου. Ο μόλυβδος έχει 82 ηλεκτρόνια και τα 4 ηλεκτρόνια σθένους βρίσκονται μακριά από τον πυρήνα του και συγκρατούνται με ασθενείς δυνάμεις. Οι ομοιοπολικοί δεσμοί που μπορεί να σχηματίσει ο μόλυβδος είναι επίσης πολύ ασθενείς, με συνέπεια ο μόλυβδος να θεωρείται περισσότερο μέταλλο παρά στοιχείο ομοιοπολικού δεσμού. Οι ομοιοπολικοί δεσμοί μπορεί να είναι πολύ ισχυροί ή πολύ ασθενείς. Για παράδειγμα, στο διαμάντι η ενέργεια δεσμού είναι 108 Kcal/mol και το σημείο τήξης 2800 C, ενώ ο κασσίτερος σχηματίζει ασθενείς δεσμούς και έχει χαμηλό σημείο τήξης, 232 C. Στον Πίνακα 2.3 παρουσιάζονται οι ενέργειες δεσμών και τα σημεία τήξεως για μερικές ομοιοπολικές ενώσεις ΜΕΤΑΛΛΙΚΟΣ ΔΕΣΜΟΣ Ο μεταλλικός δεσμός συναντάται στα μέταλλα και στα κράματά τους. Τα ηλεκτρόνια σθένους των μετάλλων, ένα, δυο ή τρία, δεν συγκρατούνται σταθερά από τα άτομα, αλλά σχηματίζουν ένα νέφος ελεύθερων ηλεκτρονίων, τα οποία μπορούν να κινούνται σε όλη τη μάζα του μετάλλου και είναι κοινά για όλα τα θετικά φορτισμένα ιόντα. Μεταξύ των ελεύθερων ηλεκτρονίων και των θετικών ιόντων αναπτύσσονται ελκτικές δυνάμεις. Συνεπώς ο μεταλλικός δεσμός δεν είναι κατευθυντικός (Σχήμα 2.5). 23
25 Σχήμα 2.6: Σχηματική παράσταση του μεταλλικού δεσμού. Οι μεταλλικοί δεσμοί μπορεί να είναι πολύ ισχυροί ή πολύ ασθενείς. Για παράδειγμα, στο βολφράμιο η ενέργεια δεσμού είναι 203 Kcal/mol και το σημείο τήξης 3410 C, ενώ στο κάλιο η ενέργεια δεσμού είναι 21.4 Kcal/mol και το σημείο τήξης 63.5 C. Στον Πίνακα 2.3 παρουσιάζονται οι ενέργειες δεσμών και τα σημεία τήξεως για μερικά μέταλλα ΔΕΥΤΕΡΕΥΟΝΤΕΣ ΔΕΣΜΟΙ Η ΔΕΣΜΟΙ VAN DER WAALS Οι δευτερεύοντες δεσμοί είναι ασθενείς δεσμοί και οφείλονται στην έλξη ηλεκτρικών διπόλων που σχηματίζονται σε άτομα ή μόρια. Τα δίπολα μπορεί να είναι μόνιμα ή επαγόμενα. Έτσι έχουμε δεσμούς που προκύπτουν από την ηλεκτροστατική έλξη μεταξύ επαγόμενων διπόλων, ή μεταξύ επαγόμενων και μόνιμων διπόλων, ή μεταξύ μόνιμων διπόλων. Ο δεσμός υδρογόνου είναι μια περίπτωση δευτερεύοντος δεσμού που οφείλεται στην έλξη μόνιμων διπόλων. Αναπτύσσεται μεταξύ μορίων στα οποία το υδρογόνο είναι συνδεδεμένο με ένα άτομο μεγάλης ηλεκτραρνητικότητας. Τυπικά παραδείγματα αποτελούν τα μόρια του υδροφθορίου, HF, του νερού, H2O και της αμμωνίας, ΝΗ3. Αυτά τα μόρια παρουσιάζουν ισχυρή πόλωση γιατί τα ηλεκτρόνια έλκονται περισσότερο από τα ηλεκτραρνητικά άτομα. Αυτό έχει ως συνέπεια, το άκρο του μορίου, που βρίσκεται το υδρογόνο, να είναι θετικά φορτισμένο, ενώ το άκρο του μορίου που βρίσκεται το ηλεκτραρνητικό άτομο να είναι αρνητικά φορτισμένο. Ο δεσμός υδρογόνου σχηματίζεται από την έλξη μεταξύ του θετικού τμήματος ενός μορίου και του αρνητικού τμήματος ενός γειτονικού μορίου. Στο Σχήμα 2.6 απεικονίζεται ο δεσμός υδρογόνου στο μόριο του νερού. Στη θερμοκρασία περιβάλλοντος, 25 C, το νερό είναι υγρό λόγω του δεσμού υδρογόνου που συγκρατεί τα μόρια του σε αυτή την κατάσταση. Επίσης το υψηλό σημείο βρασμού του νερού, λαμβάνοντας υπόψη το χαμηλό μοριακό του βάρος, δικαιολογείται από την ανάπτυξη του δεσμού υδρογόνου. Σχήμα 2.6: Σχηματική παράσταση του δεσμού υδρογόνου. 24
26 Η υγροποίηση και η στερεοποίηση των ευγενών αερίων καθώς και άλλων ουδέτερων και συμμετρικών μορίων οφείλεται σε δευτερεύοντες δεσμούς (έλξη ανάμεσα σε επαγόμενα δίπολα). Οι ενέργειες των δευτερευόντων δεσμών είναι της τάξης των 2.5 Kcal/mol. Οι δεσμοί υδρογόνου είναι οι πιο ισχυροί δεσμοί αυτού του είδους, με ενέργεια δεσμού της τάξης των 12 Kcal/mol. Στον Πίνακα 2.3 παρουσιάζονται ορισμένα παραδείγματα δευτερευόντων δεσμών. 2.4 ΕΝΕΡΓΕΙΕΣ ΔΕΣΜΩΝ ΚΑΙ ΘΕΡΜΟΚΡΑΣΙΕΣ ΤΗΞΗΣ Στον Πίνακα 2.3 παρουσιάζονται η ενέργεια δεσμού και το σημείο τήξης για ιοντικά, ομοιοπολικά και μεταλλικά υλικά, καθώς και για ενώσεις στις οποίες αναπτύσσονται δευτερεύοντες δεσμοί. Πίνακας 2.3: Ενέργειες ιοντικών, ομοιοπολικών, μεταλλικών και δευτερευόντων δεσμών και σημεία τήξης διάφορων υλικών [1, 2]. Υλικό CaO MgO KCl C(διαμάντι) Si W V Ti Cr Fe Co Ni Cu Al Hg Η2Ο ΝΗ3 Cl2 Ar Ενέργεια Δεσμού, Kcal/mol Ιοντικός δεσμός Ομοιοπολικός δεσμός Μεταλλικός δεσμός Δεσμός υδρογόνου Δεσμός Van der Waals Σημείο Τήξης, C >
27 2.5 ΕΠΙΔΡΑΣΗ ΤΩΝ ΧΗΜΙΚΩΝ ΔΕΣΜΩΝ ΣΤΙΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΥΛΙΚΩΝ Οι ιδιότητες των υλικών, τόσο οι φυσικές όσο και οι μηχανικές, κατά ένα μέρος μπορούν να εξηγηθούν από τον τύπο του δεσμού. Γενικά υψηλή ενέργεια δεσμών συνοδεύεται από υψηλό σημείο τήξης. Σε θερμοκρασία περιβάλλοντος, ουσίες με μεγάλες ενέργειες δεσμών είναι στερεές, με ενδιάμεσες υγρές, ενώ ουσίες με μικρές ενέργειες δεσμών είναι αέριες (Πίνακας 2.3). Τα μέταλλα είναι καλοί αγωγοί του ηλεκτρισμού και της θερμότητας, λόγω των ελεύθερων ηλεκτρονίων που διαθέτουν. Αντίθετα, τα υλικά που έχουν ιοντικό ή ομοιοπολικό δεσμό, στα οποία τα ηλεκτρόνια κατέχουν συγκεκριμένες θέσεις, είναι ηλεκτρικοί και θερμικοί μονωτές. Ιδιότητες των μεταλλικών υλικών, όπως η ολκιμότητα και η πλαστικότητα, αναμφίβολα συνδέονται με τη φύση του μεταλλικού δεσμού. Τα μέταλλα αστοχούν με όλκιμο τρόπο, δηλαδή σπάνε αφού πρώτα υποστούν σημαντική παραμόρφωση. Στα μέταλλα, τα θετικά ιόντα βρίσκονται μέσα σε μια «θάλασσα» ηλεκτρονίων και η σχετική μετατόπισή τους είναι δυνατή επιτρέποντας την πλαστική παραμόρφωσή τους. Αντίθετα, στα ιοντικά και ομοιοπολικά υλικά, όπως τα κεραμικά, οι γωνίες των δεσμών δεν μεταβάλλονται με συνέπεια να μην είναι δυνατή η πλαστική παραμόρφωσή τους. Αυτά τα υλικά είναι ψαθυρά και αστοχούν με θραύση των δεσμών τους. Γενικά πολύ λίγες ενώσεις έχουν αμιγώς ένα τύπο δεσμού. Ένας δεσμός μπορεί να είναι εν μέρει ιοντικός και εν μέρει ομοιοπολικός. Για παράδειγμα, το υψηλό σημείο τήξης, καθώς και το υψηλό μέτρο ελαστικότητας (Ε) ορισμένων ενώσεων, όπως του MgO, Al2O3, κλπ. αποδίδεται στο μικτό ιοντικό-ομοιοπολικό χαρακτήρα των δεσμών τους. Για μια ένωση, στην οποία τα άτομά της συνδέονται με έναν μικτό ομοιοπολικόμεταλλικό δεσμό, η ηλεκτρική και θερμική αγωγιμότητά τους θα εξαρτάται από το ποσοστό του ομοιοπολικού χαρακτήρα του δεσμού. 26
28 ΚΕΦΑΛΑΙΟ 3 ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΤΩΝ ΣΤΕΡΕΩΝ 3.1 ΓΕΝΙΚΕΣ ΑΡΧΕΣ Τα στερεά υλικά με βάση τον τρόπο διευθέτησης των ατόμων τους στο χώρο διακρίνονται σε κρυσταλλικά και άμορφα. Τα κρυσταλλικά υλικά εμφανίζουν κρυσταλλική δομή. Ως κρυσταλλική δομή ορίζεται μια διάταξη ατόμων στο χώρο που παρουσιάζει κανονικότητα στις τρεις διαστάσεις. Όλα τα μέταλλα, πολλά κεραμικά και ορισμένα πλαστικά παρουσιάζουν κρυσταλλική δομή. Στα άμορφα ή μη κρυσταλλικά στερεά απουσιάζει η κρυσταλλική δομή και τα άτομα τοποθετούνται με ακανόνιστο τρόπο ως προς τα γειτονικά τους άτομα. Αρκετές ιδιότητες των υλικών εξαρτώνται από την ύπαρξη ή όχι κρυσταλλικής δομής. Για παράδειγμα, τα άμορφα κεραμικά (π.χ. γυαλιά) και πολυμερή (π.χ plexiglass), είναι συνήθως διαφανή, ενώ τα κρυσταλλικά είναι αδιαφανή ή στην καλύτερη περίπτωση ημιδιαφανή. Σημαντικές ιδιότητες των υλικών εξαρτώνται από τον τύπο της κρυσταλλικής δομής, δηλαδή από τον τρόπο που διευθετούνται τα άτομα, ιόντα ή μόρια στο χώρο. Για παράδειγμα, στο γραφίτη τα άτομα του άνθρακα είναι διατεταγμένα σε παράλληλα επίπεδα, τα οποία συνδέονται μεταξύ τους με ασθενείς δεσμούς, με συνέπεια την εύκολη απόσπαση επιπέδων, γεγονός στο οποίο οφείλονται οι άριστες λιπαντικές ιδιότητες του γραφίτη. Αντίθετα, το διαμάντι εμφανίζει υψηλή σκληρότητα, γεγονός που οφείλεται στην κρυσταλλική δομή του, στην οποία όλα τα άτομα του άνθρακα συνδέονται μεταξύ τους με ισχυρούς ομοιοπολικούς δεσμούς. Οι κρυσταλλικές δομές αποτελούνται από μικρές επαναλαμβανόμενες περιοχές που ονομάζονται μοναδιαίες κυψελίδες (στοιχειώδη κύτταρα). Οι μοναδιαίες κυψελίδες είναι παραλληλεπίπεδα ή πρίσματα αποτελούμενα από ομάδες παράλληλων εδρών. Στο Σχήμα 3.1 παρουσιάζεται μια κρυσταλλική δομή που συναντάται αρκετά συχνά στα μέταλλα. Τα άτομα παριστάνονται ως μικρές σφαίρες, (μοντέλο μικρών σφαιρών) ή θεωρούνται ως σφαίρες με πραγματικές ατομικές διαστάσεις (μοντέλο σκληρών σφαιρών). Σχήμα 3.1: Χωροκεντρωμένη κρυσταλλική δομή α) Μοναδιαία κυψελίδα όπου τα άτομα αναπαριστάνονται ως μικρές σφαίρες β) Μοναδιαία κυψελίδα όπου τα άτομα αναπαριστάνονται ως σφαίρες με πραγματικές ατομικές διαστάσεις. Συχνά οι κρυσταλλικές δομές περιγράφονται χρησιμοποιώντας τον όρο κρυσταλλικό πλέγμα. Ως πλέγμα ορίζεται ένα σύνολο διατεταγμένων σημείων στις τρεις διαστάσεις, όπου τα σημεία ταυτίζονται με τα κέντρα των ατόμων. 27
29 3.2 ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΤΩΝ ΜΕΤΑΛΛΩΝ Τα περισσότερα κοινά μέταλλα κρυσταλλώνονται σε τρία σχετικά απλά και μεγάλης συμμετρίας κρυσταλλικά συστήματα: το χωροκεντρωμένο κυβικό BCC, το εδροκεντρωμένο κυβικό FCC και το μέγιστης πυκνότητας εξαγωνικό HCP ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΧΩΡΟΚΕΝΤΡΩΜΕΝΟΥ ΚΥΒΙΚΟΥ (BCC) Στο χωροκεντρωμένο κυβικό σύστημα (BCC=Body-Centered Cubic) τα άτομα τοποθετούνται στις κορυφές της μοναδιαίας κυβικής κυψελίδας, καθώς και ένα άτομο στο κέντρο του κύβου (Σχήμα 3.1α). Για μια δεδομένη κυψελίδα μόνο το 68% του όγκου της καταλαμβάνεται από άτομα, ενώ το υπόλοιπο 32% παραμένει κενό. Ο καθαρός σίδηρος Fe (α), σε θερμοκρασία μικρότερη από 912 C, κρυσταλλώνεται στη BCC δομή. Στον Πίνακα 3.1 παρουσιάζονται οι ατομικές ακτίνες και οι σταθερές πλέγματος επιλεγμένων μετάλλων που κρυσταλλώνονται σε αυτό το σύστημα. Πίνακας 3.1: Σταθερές πλέγματος και ατομικές ακτίνες για κοινά μέταλλα του χωροκεντωμένου κυβικού BCC. Μέταλλο Σταθερά πλέγματος*, Ατομική ακτίνα, α (nm)** r (nm) Χρώμιο 0,289 0,125 Σίδηρος (α) 0,287 0,124 Μολυβδαίνιο 0,315 0,136 Κάλλιο 0,533 0,231 Νάτριο 0,429 0,186 Ταντάλιο 0,330 0,143 Βολφράμιο 0,316 0,137 Βανάδιο 0,304 0,132 *α: μήκος της πλευράς του κύβου ** 1 nm=10-9 m Å ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΕΔΡΟΚΕΝΤΡΩΜΕΝΟΥ ΚΥΒΙΚΟΥ (FCC) Στο εδροκεντρωμένο κυβικό σύστημα (FCC=Face-Centered Cubic) τα άτομα τοποθετούνται στις κορυφές της μοναδιαίας κυβικής κυψελίδας, καθώς και στο κέντρο της κάθε έδρας του κύβου (Σχήμα 3.2α). Σχήμα 3.2: Εδροκεντρωμένη κρυσταλλική δομή α) Μοναδιαία κυψελίδα όπου τα άτομα αναπαριστάνονται ως μικρές σφαίρες β) Μοναδιαία κυψελίδα όπου τα άτομα αναπαριστάνονται ως σφαίρες με πραγματικές ατομικές διαστάσεις. 28
30 Στο εδροκεντρωμένο κυβικό σύστημα μεγαλύτερο ποσοστό του όγκου μιας κυψελίδας καταλαμβάνεται από άτομα, 74% από ότι στο χωροκεντρωμένο κυβικό, 68%. Η κρυσταλλική δομή του καθαρού σιδήρου από BCC σε θερμοκρασία περιβάλλοντος μετατρέπεται σε FCC στους 912 C. Στον Πίνακα 3.2 παρουσιάζονται οι ατομικές ακτίνες και η σταθερές πλέγματος ορισμένων μετάλλων που κρυσταλλώνονται σε αυτό το σύστημα. Πίνακας 3.2: Σταθερές πλέγματος και ατομικές ακτίνες για κοινά μέταλλα του χωροκεντωμένου κυβικού FCC. Μέταλλο Σταθερά πλέγματος*, Ατομική ακτίνα, α (nm)** r (nm) Αλουμίνιο 0,405 0,143 Χαλκός 0,362 0,128 Χρυσός 0,408 0,144 Μόλυβδος 0,495 0,175 Νικέλιο 0,352 0,125 Πλατίνα 0,393 0,139 Άργυρος 0,409 0,144 *α: μήκος της πλευράς του κύβου ** 1 nm=10-9 m Å ΚΡΥΣΤΑΛΛΙΚΗ ΔΟΜΗ ΜΕΓΙΣΤΗΣ ΠΥΚΝΟΤΗΤΑΣ ΕΞΑΓΩΝΙΚΟΥ (HCP) Στο μέγιστης πυκνότητας εξαγωνικό σύστημα (HCP=Hexagonal Close-Packed) η μοναδιαία κυψελίδα είναι ένα ορθό πρίσμα με εξαγωνική βάση (Σχήμα 3.3α). Τα άτομα τοποθετούνται στις κορυφές και στα κέντρα των εξαγώνων των δυο βάσεων, καθώς και τρία άτομα σε επίπεδο, το οποίο βρίσκεται σε ίση απόσταση μεταξύ των δυο βάσεων. Σχήμα 3.3: Εξαγωνική κρυσταλλική δομή α) Μοναδιαία κυψελίδα όπου τα άτομα αναπαριστάνονται ως μικρές σφαίρες β) Μοναδιαία κυψελίδα όπου τα άτομα αναπαριστάνονται ως σφαίρες με πραγματικές ατομικές διαστάσεις. Στον Πίνακα 3.3 παρουσιάζονται οι ατομικές ακτίνες, οι σταθερές πλέγματος και ο λόγος c/α ορισμένων μετάλλων που κρυσταλλώνονται σε αυτό το σύστημα. 29
31 Πίνακας 3.3: Σταθερές πλέγματος, ατομικές ακτίνες και ο λόγος c/α για κοινά μέταλλα του εξαγωνικού συστήματος HCP [1]. Μέταλλο Σταθερά Σταθερά Ατομική c/a πλέγματος*, πλέγματος**, ακτίνα, α (nm)*** c (nm) r (nm) Κάδμιο 0,2973 0,5618 0,149 1,890 Ψευδάργυρος 0,2665 0,4947 0,133 1,856 Ιδανική δομή, HCP 1,633 Μαγνήσιο 0,3209 0,495 0,175 0,495 Κοβάλτιο 0,2507 0,352 0,125 0,352 Ζιρκόνιο 0,3231 0,5148 0,160 1,593 Τιτάνιο 0,2950 0,4683 0,147 0,587 Βηρύλλιο 0,2286 0,3584 0,113 0,568 *α: μήκος της πλευράς της εξαγωνικής βάσης **c: ύψος του εξαγώνου *** 1 nm=10-9 m Å. 3.3 ΦΑΙΝΟΜΕΝΟ ΑΛΛΟΤΡΟΠΙΑΣ Αλλοτροπία ονομάζεται το φαινόμενο κατά το οποίο μερικά στερεά παρουσιάζουν περισσότερες από μια κρυσταλλικές δομές. Η κρυσταλλική δομή που θα σχηματιστεί εξαρτάται από τις εξωτερικές συνθήκες πίεσης και θερμοκρασίας. Για παράδειγμα, ο άνθρακας συναντάται σε διάφορες κρυσταλλικές δομές, καθώς και σε άμορφη κατάσταση. Σε θερμοκρασία και πίεση περιβάλλοντος βρίσκεται υπό τη μορφή γραφίτη, ενώ σε υψηλές πιέσεις μετατρέπεται σε διαμάντι. Ακόμη, μια άλλη νεώτερη δομή του άνθρακα είναι τα φουλλερένια. Όπως ήδη αναφέρθηκε ο καθαρός σίδηρος σε θερμοκρασίες κάτω των 912 C κρυσταλλώνεται στο χωροκεντρωμένο κυβικό σύστημα BCC, ενώ σε θερμοκρασίες άνω των 912 C κρυσταλλώνεται στο εδροκεντρωμένο κυβικό σύστημα FCC. Η αλλαγή της κρυσταλλικής δομής συνήθως συνεπάγεται μεταβολή σε πλήθος φυσικών ιδιοτήτων των υλικών π.χ. πυκνότητα. 3.4 ΚΡΥΣΤΑΛΛΙΚΑ ΠΛΕΓΜΑΤΑ ΚΑΙ ΣΥΣΤΗΜΑΤΑ Για την περιγραφή των κρυσταλλικών δομών χρησιμοποιείται η έννοια των κρυσταλλικών πλεγμάτων. Ως κρυσταλλικό πλέγμα ορίζεται ένα σύνολο απείρων σημείων στο χώρο, διατεταγμένων κατά τέτοιο τρόπο, ώστε τα γειτονικά σημεία τυχόντος σημείου του πλέγματος να έχουν την ίδια διάταξη κατά μήκος τυχαίας διεύθυνσης (Σχήμα 3.4). Τα σημεία αυτά καλούνται κόμβοι του πλέγματος. Ο Γάλλος φυσικός Bravais (1848) με βάση τον παραπάνω ορισμό έδειξε ότι τα δυνατά είδη πλεγμάτων είναι 14. Στο Σχήμα 3.5 παρουσιάζονται οι μοναδιαίες κυψελίδες αυτών των πλεγμάτων. Τα κρυσταλλικά πλέγματα του Bravais διανέμονται σε επτά κρυσταλλικά συστήματα. Κάθε κρυσταλλικό σύστημα χαρακτηρίζεται από το είδος του γεωμετρικού σχήματος της κυψελίδας, τις σχετικές τιμές των γωνιών α, β και γ και των παραμέτρων a, b και c. Τα επτά κρυσταλλικά συστήματα είναι: το κυβικό, το τετραγωνικό, το ορθορομβικό, το ρομβοεδρικό, το μονοκλινές, το τρικλινές και το εξαγωνικό (Πίνακας 3.4). 30
32 Σχήμα 3.4: Αναπαράσταση κρυσταλλικού πλέγματος σε σύστημα συντεταγμένων x, y και z. Απεικονίζονται τα μοναδιαία διανύσματα a, b και c καθώς και οι γωνίες μεταξύ των διευθύνσεών τους α, β και γ. Σχήμα 3.5: Τα 14 κρυσταλλικά πλέγματα του Bravais. 31
33 Πίνακας 3.4: Παράμετροι πλέγματος των 7 κρυσταλλικών συστημάτων. Κρυσταλλικό σύστημα Γωνίες, α,β,γ Παράμετροι, a,b,c Κυβικό Γεωμετρία μοναδιαίας κυψελίδας Κύβος α=β=γ=90 a=b=c Τετραγωνικό Ορθογ. Πρίσμα α=β=γ=90 a=b c Ορθορομβικό Ορθογ. Πρίσμα α=β=γ=90 ab#c Ρομβοεδρικό Παραλληλεπίπεδο α=β=γ=90 a=b=c Μονικλινές Παραλληλεπίπεδο a b c Τρικλινές Παραλληλεπίπεδο α=γ=90 β 90 α β γ 90 Εξαγωνικό Παραλληλεπίπεδο α=β=90 γ=120 a=b c a b c 3.5 ΚΡΥΣΤΑΛΛΙΚΑ ΚΑΙ ΑΜΟΡΦΑ ΥΛΙΚΑ ΚΡΥΣΤΑΛΛΩΣΗ Η ΣΤΕΡΕΟΠΟΙΗΣΗ ΠΟΛΥΚΡΥΣΤΑΛΛΙΚΟΥ ΥΛΙΚΟΥ Πολυκρυσταλλικά υλικά ονομάζονται τα στερεά που αποτελούνται από ένα σύνολο μικρών κρυστάλλων ή κόκκων. Το υλικό δεν αποτελείται από ένα συνεχές κρυσταλλικό πλέγμα, δηλαδή δεν είναι μονοκρυσταλλικό, αλλά από πολλούς μικρούς κρυστάλλους, που ο καθένας έχει διαφορετικό προσανατολισμό. Παρακάτω παρουσιάζεται συνοπτικά η κρυστάλλωση των μετάλλων, τα οποία αποτελούν τυπικό παράδειγμα πολυκρυσταλλικού υλικού. Τα άτομα των μετάλλων στην υγρή κατάσταση συγκρατούνται με ασθενείς ελκτικές δυνάμεις και διευθετούνται με τυχαίο τρόπο. Όταν όμως ένα μέταλλο ψύχεται από την υγρή στη στερεή κατάσταση, σε ορισμένη θερμοκρασία γνωστή ως θερμοκρασία πήξης συντελείται η στερεοποίησή του. Στη διάρκεια της στερεοποίησης τα άτομα διευθετούνται με συγκεκριμένο τρόπο και το μέταλλο στερεοποιείται ή κρυσταλλώνεται, δηλαδή αποκτά κρυσταλλική δομή. Στο Σχήμα 3.6 απεικονίζονται σχηματικά τα διάφορα στάδια στερεοποίησης ενός μετάλλου. Αρχικά σχηματίζονται μικροσκοπικοί κρύσταλλοι ή πυρήνες σε τυχαίες θέσεις. Στη συνέχεια οι πυρήνες αναπτύσσονται σε κρυστάλλους με τη διαδοχική προσθήκη ατόμων στη δομή τους από το υγρό που τους περιβάλλει. Καθώς οι κρύσταλλοι αναπτύσσονται, παρακείμενοι κρύσταλλοι συναντώνται μεταξύ τους, με αποτέλεσμα η ανάπτυξή τους να παρεμποδίζεται σε ορισμένες κατευθύνσεις, ενώ να συνεχίζεται σε άλλες, μέχρι την στερεοποίηση και της τελευταίας σταγόνας υγρού. Μετά το τέλος της διαδικασίας στερεοποίησης το μέταλλο αποτελείται από κόκκους διαφορετικού μεγέθους και μορφής. Οι κόκκοι έχουν την ίδια κρυσταλλική δομή, αλλά διαφορετικό κρυσταλλογραφικό προσανατολισμό, επειδή οι κόκκοι αναπτύσσονται από πυρήνες τυχαίου προσανατολισμού. Η περιοχή που συναντιούνται γειτονικοί κόκκοι είναι ανομοιογενής, γιατί τα άτομα που βρίσκονται σε αυτή την περιοχή δεν είναι δυνατόν να παρουσιάζουν την ίδια τέλεια γεωμετρική οργάνωση με τα άτομα των κόκκων. Αυτή η περιοχή ονομάζεται όριο κόκκου. 32
34 Σχήμα 3.6: Σχηματική παράσταση της στερεοποίησης ενός μετάλλου. α) Σχηματισμός πυρήνων τυχαίου κρυσταλλογραφικού προσανατολισμού β) Ανάπτυξη των πυρήνων γ) Ολοκλήρωση της στερεοποίησης και σχηματισμός κόκκων ποικίλου μεγέθους και προσανατολισμού δ) Αναπαράσταση μικροσκοπικής δομής. Οι μαύρες γραμμές αντιπροσωπεύουν τα όρια των κόκκων. Στο Σχήμα 3.7 παρουσιάζεται η δομή ενός μετάλλου όπως φαίνεται σε ένα οπτικό μικροσκόπιο. Τα όρια των κόκκων αποκαλύφθηκαν με λείανση και προσβολή με κατάλληλο χημικό αντιδραστήριο. Σχήμα 3.7: Μικροσκοπική δομή μεταλλικού υλικού. Εμφάνιση των ορίων των κόκκων μετά από λείανση και χημική προσβολή. 33
35 3.5.2 ΜΟΝΟΚΡΥΣΤΑΛΛΟΙ Μονοκρύσταλλος ονομάζεται ένα κρυσταλλικό υλικό, στο οποίο το κρυσταλλικό πλέγμα εκτείνεται χωρίς διακοπή σε ολόκληρο το δείγμα. Όλες οι μοναδιαίες κυψελίδες συνδέονται με τον ίδιο τρόπο και δημιουργούν μια τέλεια τρισδιάστατη διάταξη. Εάν τα άκρα του μονοκρυστάλλου αναπτυχθούν χωρίς εξωτερικούς περιορισμούς, τότε ο κρύσταλλος παίρνει γεωμετρικές μορφές με επίπεδες επιφάνειες όπως κάποιοι πολύτιμοι λίθοι. Οι μονοκρύσταλλοι συναντώνται πολύ σπάνια στη φύση, ωστόσο μπορούν να παραχθούν στο εργαστήριο κάτω από ελεγχόμενες συνθήκες. Το γεγονός ότι οι μονοκρύσταλλοι δεν περιέχουν όρια κόκκων, που επηρεάζουν σε μεγάλο βαθμό τις φυσικές και ηλεκτρικές ιδιότητες ενός υλικού, βρίσκουν εφαρμογή σε πολλές σύγχρονες τεχνολογίες, όπως στα ηλεκτρονικά μικροκυκλώματα, στα οπτικά, κλπ.. Για παράδειγμα μονοκρύσταλλοι πυριτίου βρίσκουν εφαρμογή στην κατασκευή ημιαγωγών, μονοκρύσταλλοι σαπφείρου (ζαφείρι, Al2O3) στην κατασκευή οπτικών για laser, μονοκρύσταλλοι χαλκού χρησιμοποιούνται ως ηλεκτρικοί αγωγοί υψηλής απόδοσης, ενώ μονοκρύσταλλοι κατάλληλων κραμάτων για την κατασκευή υλικών υψηλής αντοχής, όπως πτερύγια τουρμπινών ΑΝΙΣΟΤΡΟΠΙΑ Ανισοτροπικά υλικά είναι τα υλικά τα οποία παρουσιάζουν διαφορετικές ιδιότητες σε διαφορετικές κατευθύνσεις, σε αντίθεση με το ισοτροπικά τα οποία εμφανίζουν ομοιογένεια σε όλες τις κατευθύνσεις. Για παράδειγμα οι φυσικές ιδιότητες ενός μονοκρυστάλλου, όπως ο δείκτης διάθλασης, η απορρόφηση, το μέτρο ελαστικότητας και η ηλεκτρική αγωγιμότητα μπορεί να έχουν διαφορετικές τιμές, όταν μετρώνται κατά μήκος διαφορετικών κρυσταλλογραφικών κατευθύνσεων. Πολλά πολυκρυσταλλικά υλικά, παρόλο που αποτελούνται από ανισοτροπικούς κόκκους, συμπεριφέρονται ως ισοτροπικά. Αυτό συμβαίνει γιατί κάθε κόκκος έχει διαφορετικό κρυσταλλογραφικό προσανατολισμό, με αποτέλεσμα την αλληλεξουδετέρωση των επιδράσεών τους. Πολλές φορές όμως, οι κόκκοι ενός πολυκρυσταλλικού υλικού μπορεί να αποκτήσουν έναν επιθυμητό προσανατολισμό, μέσω της επεξεργασίας τους π.χ μικροδομή (υφή) ινών, μικροδομή σφυρήλατων εξαρτημάτων ΑΜΟΡΦΑ ΥΛΙΚΑ Όπως ήδη αναφέρθηκε στα άμορφα ή μη κρυσταλλικά στερεά απουσιάζει η κρυσταλλική δομή και τα άτομα τοποθετούνται με ακανόνιστο τρόπο ως προς τα γειτονικά τους άτομα. Ορισμένα άμορφα υλικά παρουσιάζουν μια μικρής εμβέλειας ατομική τάξη (κανονικότητα), ενώ τα περισσότερα δεν εμφανίζουν καμία τάξη. Ένα τυπικό παράδειγμα άμορφου υλικού είναι τα εμπορικά γυαλιά (κεραμικά, SiO2). Ο μικρός χρόνος στερεοποίησής τους δεν επιτρέπει τη διευθέτηση των ατόμων και τη δημιουργία ατομικής τάξης, με αποτέλεσμα να διατηρούν τη μικροδομή του υγρού. Στο Σχήμα 3.8 παρουσιάζεται η κρυσταλλική και η μη κρυσταλλική δομή του SiO2. 34
36 Σχήμα 3.8: Δισδιάτατες απεικονίσεις της δομής α) του κρυσταλλικού και β) μη κρυσταλλικού διοξειδίου του πυριτίου (SiO2). Τα πολυμερικά υλικά μπορεί να είναι κρυσταλλικά, άμορφα ή να διαθέτουν μικτή δομή, δηλαδή να είναι κατά ένα μέρος κρυσταλλικά και κατά ένα μέρος άμορφα. Είναι σημαντικό να σημειωθεί ότι για την εύρεση της κρυσταλλικής δομής των στερεών καθώς και της απόστασης μεταξύ των κρυσταλλογραφικών επιπέδων χρησιμοποιείται η τεχνική της περίθλασης των ακτίνων X. Σύμφωνα με αυτή την τεχνική όταν μια δέσμη ακτίνων προσπίπτει σε ένα κρυσταλλικό στερεό, τότε μπορεί να υποστεί περίθλαση (ενίσχυση λόγω συμβολής) από σειρά παράλληλων επιπέδων, σύμφωνα με το νόμο του Bragg. Η περιγραφή της τεχνικής παρουσιάζεται σε επόμενο κεφάλαιο. 35
37 ΚΕΦΑΛΑΙΟ 4 ΑΤΕΛΕΙΕΣ ΤΗΣ ΚΡΥΣΤΑΛΛΙΚΗΣ ΔΟΜΗΣ 4.1 ΕΙΔΗ ΑΤΕΛΕΙΩΝ Οι κρύσταλλοι ποτέ δεν είναι τέλειοι. Συνήθως περιέχουν ένα μεγάλο αριθμό ατελειών, που επηρεάζουν πολλές ιδιότητες των υλικών. Είναι αποδεδειγμένο ότι η πραγματική αντοχή των υλικών είναι μικρότερη από τη θεωρητικά υπολογιζόμενη, λόγω της ύπαρξης ατελειών στη δομή τους. Ωστόσο, η επίδραση των ατελειών δεν είναι πάντα αρνητική. Πολύ συχνά η παρουσία τους αυξάνει την αντοχή των υλικών. Για παράδειγμα, η ισχυροποίηση των μετάλλων, μέσω της πλαστικής παραμόρφωσης εν ψυχρώ, εξηγείται από την αύξηση του αριθμού των ατελειών και την αλληλεπίδρασή τους. Επιπλέον, η ηλεκτρική αγωγιμότητα των ημιαγωγών, οι οποίοι χρησιμοποιούνται στους ηλεκτρονικούς υπολογιστές και σε πολλές οικιακές συσκευές, καθορίζεται από ειδικές προσμείξεις (ατέλειες), οι οποίες εισάγονται στους ημιαγωγούς σε απειροελάχιστες συγκεντρώσεις. Άλλες ιδιότητες των υλικών όπως η διάβρωση των μετάλλων, η ταχύτητα διάχυσης των ατόμων στα μεταλλικά κράματα επίσης εξαρτώνται από την παρουσία ατελειών. Οι ατέλειες διακόπτουν την κανονικότητα του κρυσταλλικού πλέγματος και σύμφωνα με τη γεωμετρία και τη μορφή τους διαιρούνται σε τέσσερις κατηγορίες: Ατέλειες μηδενικής διάστασης ή σημειακές ατέλειες Πλεγματικά κενά, ένθετα άτομα παρεμβολής και αντικατάστασης, ατέλειες Frenkel και Schottky. Ατέλειες μίας διάστασης ή γραμμικές ατέλειες (διαταραχές) Διαταραχές ακμής, έλικα και μικτές. Ατέλειες δύο διαστάσεων ή επίπεδες ατέλειες Όρια κόκκων, διδυμίες, σφάλματα επιστοίβασης. Ατέλειες τριών διαστάσεων Πόροι, ρωγμές, ακαθαρσίες (εγκλείσματα), κατακρημνίσματα. 4.2 ΣΗΜΕΙΑΚΕΣ ΑΤΕΛΕΙΕΣ Οι σημειακές ατέλειες δεν εκτείνονται στο χώρο σε οποιαδήποτε κατεύθυνση και το μέγεθός είναι της τάξης των ατομικών διαστάσεων. Σχετίζονται με μια ή δυο ατομικές θέσεις. Διακρίνονται σε πλεγματικά κενά, σε παρουσία μητρικού ατόμου σε μια διαπλεγματική θέση (αυτοπαρεμβολή) ή σε παρουσία ξένου ατόμου σε πλεγματική θέση (αντικατάσταση) ή διαπλεγματική θέση (παρεμβολή). Ακόμη σε ιοντικά στερεά απαντώνται οι ατέλειες Frenkel και Schottky ΠΛΕΓΜΑΤΙΚΑ ΚΕΝΑ Η απλούστερη σημειακή ατέλεια είναι το πλεγματικό κενό, το οποίο δημιουργείται από την έλλειψη ενός ατόμου που κανονικά, σε ένα τέλειο κρύσταλλο, θα έπρεπε να βρίσκεται σε αυτή την θέση (Σχήμα 4.1α). 36
38 Σχήμα 4.1: Σημειακές ατέλειες: α) Πλεγματικό κενό β) Αυτοπαρεμβολή (μητρικό άτομο) γ) Άτομο αντικατάστασης (ξένο άτομο) δ) Άτομο παρεμβολής (ξένο άτομο) ΜΗΤΡΙΚΑ ΕΝΘΕΤΑ ΑΤΟΜΑ (ΑΥΤΟΠΑΡΕΜΒΟΛΗ) Άτομο αυτοπαρεμβολής είναι ένα άτομο της μήτρας το οποίο συνωστίζεται σε μια διαπλεγματική θέση η οποία σε ένα τέλειο κρύσταλλο δεν είναι κατειλημμένη (Σχήμα 4.1β). Οι αυτοπαρεμβολές δημιουργούν μεγάλες παραμορφώσεις στο κρυσταλλικό πλέγμα, επειδή το άτομο βρίσκεται σε μια θέση μικρότερη από το μέγεθός του, με συνέπεια ο σχηματισμός τους να μην είναι πολύ πιθανός. Η συγκέντρωση αυτών των ατελειών παραμένει πάντοτε πολύ χαμηλή ΞΕΝΑ ΕΝΘΕΤΑ ΑΤΟΜΑ Τα υλικά δεν είναι ποτέ καθαρά, στην πραγματικότητα πάντοτε υπάρχουν προσμίξεις. Οι προσμίξεις συχνά εισάγονται στα υλικά για να βελτιώσουν τις ιδιότητές τους. Για παράδειγμα, ο άνθρακας προστίθεται σε μικρά ποσά στο σίδηρο για να παραχθεί ο χάλυβας, ο οποίος είναι ισχυρότερος από το σίδηρο. Προσθήκη βορίου στο πυρίτιο αλλάζει δραστικά τις ηλεκτρικές του ιδιότητες. Όταν η εισαγωγή ατόμων πρόσμιξης σε ένα υλικό δεν έχει ως αποτέλεσμα τη δημιουργία μιας νέας φάσης ή αλλαγή της κρυσταλλικής δομής του, τότε έχουμε το σχηματισμό ενός στερεού διαλύματος. Το στερεά διαλύματα αποτελούνται από το υλικό υποδοχής ή διαλύτη και τις προσμίξεις ή διαλυμένη ουσία. Η δυνατότητα της διάλυσης καλείται διαλυτότητα. Στα στερεά διαλύματα συναντώνται δυο ειδών ατέλειες: οι ατέλειες αντικατάστασης και οι ατέλειες παρεμβολής. Ατέλειες αντικατάστασης έχουμε όταν ξένα άτομα υποκαθιστούν μητρικά άτομα (Σχήμα 4.1γ), ενώ ατέλειες παρεμβολής όταν ξένα άτομα τοποθετούνται σε διαπλεγματικές θέσεις (Σχήμα 4.1δ). Στα στερεά διαλύματα παρεμβολής τα άτομα πρόσμιξης τοποθετούνται στα διάκενα που δημιουργούνται μεταξύ των ατόμων του μητρικού κρυσταλλικού πλέγματος. Για μέταλλα με μεγάλους αριθμούς ατομικής πλήρωσης τα διάκενα είναι σχετικά μικρά. Συνεπώς η διάμετρος των παρεμβαλλόμενων ατόμων πρέπει να αρκετά μικρότερη από την διάμετρο των ατόμων του κρυσταλλικού πλέγματος και της τάξης μεγέθους των διαθέσιμων κενών. Τα συνηθέστερα στοιχεία που σχηματίζουν στερεά διαλύματα παρεμβολής είναι τα C, N, H, O και B. 37
39 Η εισαγωγή άνθρακα στο σίδηρο σχηματίζει στερεό διάλυμα παρεμβολής. Η μέγιστη επιτρεπτή συγκέντρωση του άνθρακα είναι περίπου 2%. Η ατομική ακτίνα του άνθρακα, 0.071nm, είναι πολύ μικρότερη από την ακτίνα του σιδήρου, nm ΑΤΕΛΕΙΕΣ FRENKEL ΚΑΙ SCOHTTKY Στην περίπτωση των ιοντικών στερεών, ο σχηματισμός σημειακών ατελειών θα πρέπει να συνοδεύεται από ηλεκτρική ουδετερότητα, δηλαδή το φορτίο των αρνητικών ιόντων πρέπει να ισούται με το φορτίο των θετικών ιόντων. Όταν ένα πλεγματικό κενό που αντιπροσωπεύει τη θέση ενός κατιόντος συνδέεται με ένα πλεγματικό κενό που αντιπροσωπεύει τη θέση ενός ανιόντος, το ζεύγος των δυο πλεγματικών κενών καλείται ατέλεια Schottky (Σχήμα 4.2). Στην περίπτωση που ένα κατιόν φύγει από την κανονική του θέση και καταλάβει μια γειτονική θέση παρεμβολής, τότε το ζεύγος κατιονικού κενού-κατιόντος σε θέση παρεμβολής καλείται ατέλεια Frenkel (Σχήμα 4.2). Σχήμα 4.2: Ατέλειες Frenkel και Scohttky σε ένα ιοντικό κρυσταλλικό στερεό. Οι μικρές σφαίρες αντιπροσωπεύουν τα κατιόντα και οι μεγάλες σφαίρες τα ανιόντα. 4.3 ΓΡΑΜΜΙΚΕΣ ΑΤΕΛΕΙΕΣ H ΔΙΑΤΑΡΑΧΕΣ ΓΡΑΜΜΙΚΕΣ ΑΤΕΛΕΙΕΣ H ΔΙΑΤΑΡΑΧΕΣ Οι γραμμικές ατέλειες αφορούν τη διατάραξη μερικών ατόμων του κρυσταλλικού πλέγματος κατά μήκος μιας γραμμής. Συνήθως αποκαλούνται διαταραχές. Οι διαταραχές δημιουργούνται κατά τη διάρκεια της στερεοποίησης ή της πλαστικής παραμόρφωσης του υλικού ή λόγω των θερμικών τάσεων που αναπτύσσονται κατά τη γρήγορη ψύξη του υλικού. Υπάρχουν δυο βασικοί τύποι διαταραχών, οι διαταραχές ακμής και οι διαταραχές κοχλία ή ελικοειδείς διαταραχές. Αρκετά κοινές είναι και οι μικτές διαταραχές, οι οποίες συνδυάζουν στοιχεία και από τους δυο τύπους. Στο Σχήμα 4.3 απεικονίζεται μια διαταραχή ακμής, όπου ένα ημιεπίπεδο ατόμων καταλήγει στο μέσο του κρυστάλλου. Τα γειτονικά επίπεδα κατά μήκος του άκρου του πρόσθετου ημιεπιπέδου ατόμων, που συχνά αποκαλείται γραμμή διαταραχής, δεν είναι παράλληλα, αλλά λυγίζουν έτσι ώστε να διατηρηθεί η συνέχεια τους. Πάνω από το άκρο του πρόσθετου ημιεπιπέδου τα επίπεδα βρίσκονται σε κατάσταση συμπίεσης, ενώ κάτω από το άκρο σε κατάσταση εφελκυσμού. Η διαταραχές ακμής σύμφωνα με τη θέση του πρόσθετου ημιεπιπέδου, στο πάνω ή κάτω μέρος του κρυστάλλου, συμβολίζονται με τα σύμβολα και αντίστοιχα. Η γραμμή διαταραχής δημιουργείται από την ολίσθηση ενός τμήματος του υλικού σε σχέση με το άλλο τμήμα. 38
40 Σχήμα 4.3: Σχηματική αναπαράσταση μιας διαταραχής ακμής. Το διάνυσμα Burgers είναι κάθετο με τη γραμμή διαταραχής. Ένας άλλος τύπος διαταραχής, είναι η ελικοειδής διαταραχή που δημιουργείται από την εφαρμογή μιας διατμητικής τάσης σε ένα τμήμα του κρυστάλλου προς τη μία καθώς και την αντίθετη κατεύθυνσή ταυτόχρονα (Σχήμα 4.4). Οφείλει το όνομά της στην ελικοειδή ή κοχλιωτή διαδρομή που σχηματίζεται γύρω από τη γραμμή διαταραχής από τα επίπεδα των ατόμων στον κρύσταλλο. Σχήμα 4.4: Σχηματική αναπαράσταση μιας ελικοειδούς διαταραχής. Το διάνυσμα Burgers είναι παράλληλο με τη γραμμή διαταραχής. Συχνά οι διαταραχές στους κρυστάλλους είναι μικτού τύπου, δηλαδή συνδυάζουν στοιχεία των διαταραχών ακμής και διαταραχών κοχλία (Σχήμα 4.5). 39
41 Σχήμα 4.5: Σχηματική αναπαράσταση μιας μικτής διαταραχής. Στο σημείο Α έχουμε διαταραχή έλικα, στο σημείο Β διαταραχή ακμής και στις ενδιάμεσες περιοχές όπου η γραμμή αναταραχής είναι καμπύλη η διαταραχή έχει χαρακτήρα μικτό. Η διεύθυνση και το μέγεθος των παραμορφώσεων που προκαλούνται στο κρυσταλλικό πλέγμα από την παρουσία των διαταραχών εκφράζεται με το διάνυσμα του Burgers, b. Όπως φαίνεται στα παραπάνω σχήματα για τις διαταραχές τύπου ακμής το διάνυσμα b και η γραμμή διαταραχής είναι κάθετα μεταξύ τους, για τις ελικοειδείς διαταραχές το διάνυσμα b και η γραμμή διαταραχής είναι παράλληλα μεταξύ τους, ενώ για τις μικτές διαταραχές ούτε κάθετα ούτε παράλληλα. Οι διαταραχές μπορούν να κινηθούν εάν τα άτομα από τα γειτονικά πλεγματικά επίπεδα σπάσουν τους δεσμούς τους και σχηματίσουν νέους δεσμούς με τα άτομα του άκρου του πρόσθετου ημιεπιπέδου. Στο Σχήμα 4.6 αναπαρίσταται η κίνηση μιας διαταραχής ακμής διαμέσου ενός κρυστάλλου. Το κατώτερο τμήμα του κρυστάλλου ολισθαίνει κάτω από το ανώτερο τμήμα του, κατά απόσταση b, όταν σε αυτό εφαρμόζεται διατμητική τάση τ. Το επίπεδο πάνω στο οποίο γίνεται η ολίσθηση λέγεται επίπεδο ολίσθησης. Η κίνηση της διαταραχής είναι ανάλογη της κίνησης μιας πτυχής χαλιού, υπό την επίδραση της διατνητικής τάσης τ, κατά μήκος του πατώματος. Η κίνηση της πτυχής είναι πολύ ευκολότερη διαδικασία από την κίνηση ολόκληρου του χαλιού. Σχήμα 4.6: Αναπαράσταση της κίνησης μιας διαταραχής ακμής διαμέσου κρυσταλλικού πλέγματος. 40
42 Η παρουσία διαταραχών σε ένα κρυσταλλικό υλικό, η δυνατότητα κίνησής τους καθώς και η αλληλεπίδρασή τους κάτω από την επίδραση εφαρμοζόμενων τάσεων καθιστούν δυνατή την πλαστική παραμόρφωση των μετάλλων. Η πλαστική παραμόρφωση μέσω της κίνησης των διαταραχών ονομάζεται ολίσθηση. Οι διαταραχές στα κρυσταλλικά υλικά μπορούν να παρατηρηθούν με τεχνικές ηλεκτρονικής μικροσκοπίας (SEM= Scanning Electron Microscopy, TEM= Transmission Electron Microscopy) και μικροσκοπίας σάρωσης ακίδας (SPM=Scanning Probe Microscopy, AFM=Atomic Force Microscopy). 4.4 ΑΤΕΛΕΙΕΣ ΔΥΟ ΔΙΑΣΤΑΣΕΩΝ Ή ΕΠΙΠΕΔΕΣ ΑΤΕΛΕΙΕΣ Οι επίπεδες ατέλειες χωρίζουν περιοχές που έχουν διαφορετικό κρυσταλλογραφικό προσανατολισμό. Διακρίνονται σε όρια κόκκων, διδυμίες και σφάλματα επιστοίβασης ΟΡΙΑ ΚΟΚΚΩΝ Τα όρια κόκκων είναι οι διαχωριστικές επιφάνειες μεταξύ των κόκκων ή κρυστάλλων ενός πολυκρυσταλλικού υλικού. Ένα μέταλλο αποτελείται από πολλούς κρυστάλλους, τοποθετημένους τον ένα δίπλα στον άλλο, έτσι ώστε να σχηματίζεται ένα συνεχές υλικό (Σχήμα 4.7). Κάθε κόκκος έχει διαφορετικό κρυσταλλογραφικό προσανατολισμό και τα άτομα που βρίσκονται στην περιοχή των διαχωριστικών επιφανειών των κόκκων κατέχουν ενδιάμεσες θέσεις μεταξύ των γειτονικών κρυσταλλικών πλεγμάτων. Η σύνδεση αυτών των ατόμων δεν είναι ομαλή (π.χ. οι γωνίες δεσμού είναι μακρύτερες) με συνέπεια να αναπτύσσεται μια διεπιφανειακή ενέργεια, η οποία είναι τόσο μεγαλύτερη όσο μεγαλύτερη είναι η απόκλιση μεταξύ των προσανατολισμών των γειτονικών κόκκων. Σχήμα 4.7: Μικρογραφία κοινού ανθρακούχου χάλυβα (St 50-2), μετά από λείανση και χημική προσβολή (200x). Λόγω της αυξημένης διεπιφανειακής ενέργειας τα όρια των κόκκων είναι πιο ενεργά χημικά από ότι οι κόκκοι, με συνέπεια την επιλεκτική διάβρωσή τους με κατάλληλο χημικό αντιδραστήριο. Ενώ σε άλλες εφαρμογές αυτό το φαινόμενο έχει αρνητικές συνέπειες, στην 41
43 περίπτωση της μεταλλογραφικής προετοιμασίας των μετάλλων για την παρατήρησή τους με μικροσκόπιο, η χημική προσβολή των ορίων των κόκκων είναι απαραίτητη. Ακόμη, η ύπαρξη υψηλότερης διεπιφανειακής ενέργειας εξηγεί φαινόμενα όπως την συγκέντρωση ξένων προσμίξεων (ακαθαρσιών) στα όρια των κόκκων, καθώς και την ευκολότερη διάχυση των ατόμων διαμέσου των ορίων των κόκκων. Επίσης, η διεπιφανειακή ενέργεια στα λεπτόκοκκα υλικά είναι μεγαλύτερη από ότι στα χονδρόκοκκα, λόγω της ύπαρξης μεγαλύτερης διαχωριστικής επιφάνειας. Αυτό έχει ως συνέπεια οι κόκκοι να μεγεθύνονται σε υψηλές θερμοκρασίες προκειμένου να μειωθεί η συνολική διαχωριστική τους επιφάνεια ΔΙΔΥΜΙΕΣ Οι διδυμίες είναι επίπεδες ατέλειες κατά μήκος των οποίων υπάρχει κατοπτρική συμμετρία, δηλαδή ένα μέρος ενός κρυστάλλου αποτελεί το είδωλο του άλλου μέρους ως προ το επίπεδο διδυμίας (Σχήμα 4.9). Σχήμα 4.8: Σχηματική αναπαράσταση διδυμίας. Οι διδυμίες προκαλούνται είτε κατά την θερμική κατεργασία της ανόπτησης (διδυμίες ανόπτησης), είτε κατά την πλαστική παραμόρφωση του υλικού λόγω της εφαρμογής διατμητικών τάσεων (μηχανικές διδυμίες). Στο Σχήμα 4.9 απεικονίζεται η μικροφωτογραφία ενός πολυκρυσταλλικού ορείχαλκου, κράμα Cu-Zn, ο οποίος παρουσιάζει το φαινόμενο της διδυμίας. Οι διδυμίες βρίσκονται υπό τη μορφή ταινιών στο εσωτερικό των κόκκων, έχουν σχετικά ευθείες και παράλληλες πλευρές και διαφορετικό τόνο από τις περιοχές μη διδυμίας των κόκκων. Αυτό οφείλεται στο γεγονός ότι η ανάκλαση του φωτός εξαρτάται από τον κρυσταλλογραφικό προσανατολισμό της κάθε περιοχής του κρυστάλλου. Αν και οι διδυμίες δεν αφορούν μεγάλο μέρος του κρυστάλλου, ωστόσο ο ρόλος τους είναι ιδιαίτερα σημαντικός στη διαδικασία της πλαστικής παραμόρφωσης των μεταλλικών υλικών. Το ποσό της πλαστικής παραμόρφωσης που οφείλεται στις διδυμίες είναι πολύ μικρό συγκρινόμενο με αυτό που παράγεται λόγω ολίσθησης. Όμως οι αλλαγές του προσανατολισμού περιοχών του κρυστάλλου λόγω των διδυμιών, μπορεί να έχει ως αποτέλεσμα τη δημιουργία νέων συστημάτων ολίσθησης, με ευνοϊκή κατεύθυνση ως προς την εφαρμοζόμενη τάση, επιτρέποντας έτσι τη πραγματοποίηση νέας συμπληρωματικής ολίσθησης. 42
44 Σχήμα 4.9: Μικρογραφία κράματος Cu-Zn (ορείχαλκος), μετά από λείανση και χημική προσβολή (100x) ΣΦΑΛΜΑΤΑ ΕΠΙΣΤΟΙΒΑΣΗΣ Τα σφάλματα επιστοίβασης απαντώνται κυρίως στις δομές πυκνής διάταξης. Η εδροκεντρωμένη κυβική κρυσταλλική δομή (FCC) και η εξαγωνική μέγιστης πυκνότητας (HCP), μπορούν να παραχθούν από την επιστοίβαση, με συγκεκριμένη αλληλουχία, ατομικών επιπέδων μέγιστης πυκνότητας. Σφάλματα στην ακολουθία επιστοίβασης των επιπέδων έχει ως αποτέλεσμα το σχηματισμό των σφαλμάτων επιστοίβασης. Τα σφάλματα επιστοίβασης αφορούν ένα ή δυο επίπεδα, π.χ. μια ακολουθία επιστοίβασης ABCABCABC μετατρέπεται σε ABCACABC (λείπει το επίπεδο Β). 4.5 ΑΤΕΛΕΙΕΣ ΟΓΚΟΥ Σε όλα τα στερεά υλικά υπάρχουν ατέλειες όγκου, οι οποίες είναι αρκετά μεγαλύτερες από τις σημειακές, γραμμικές και επίπεδες ατέλειες. Συνήθως δημιουργούνται κατά την παραγωγή ή την κατεργασία του υλικού. Διακρίνονται σε πόρους ή ρωγμές, εγκλείσματα και κατακρημνίσματα. Πόροι ή ρωγμές είναι μικρές περιοχές στις οποίες δεν υπάρχουν άτομα. Επηρεάζουν τις μηχανικές ιδιότητες των υλικών. Ξένα εγκλείσματα είναι οι «ακαθαρσίες» εντός του υλικού. Για παράδειγμα, οξείδια, θειούχες ή πυριτικές ενώσεις αποτελούν συνήθη εγκλείσματα στα μέταλλα. Δημιουργούνται κατά την διαδικασία παραγωγής του μετάλλου σε υγρή κατάσταση. Κατακρημνίσματα, είναι ενώσεις που σχηματίζονται μεταξύ του μητρικού μετάλλου και κραματικών στοιχείων. Το μέγεθός τους είναι μικρό και επηρεάζουν σημαντικά τις μηχανικέ ιδιότητες των μετάλλων. 43
45 ΚΕΦΑΛΑΙΟ 5 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ Σε αυτό το κεφάλαιο παρουσιάζονται οι κυριότερες φυσικές ιδιότητες των υλικών, όπως οι θερμικές, οι ηλεκτρικές και οι μαγνητικές. 5.1 ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΘΕΜΟΧΩΡΗΤΙΚΟΤΗΤΑ Η ΕΙΔΙΚΗ ΘΕΡΜΟΤΗΤΑ Η θερμοχωρητικότητα δείχνει το ποσό της θερμότητας dq που απαιτείται για να προκαλέσει αύξηση της θερμοκρασίας του υλικού κατά dt. Εκφράζεται από το παρακάτω πηλίκο: C= dq dt Συνήθως η θερμοχωρητικότητα εκφράζεται ανά γραμμομόριο υλικού π.χ. J/mol.K ή ανά μονάδα μάζας J/g.K. Όταν εκφράζεται ανά μονάδα μάζας καλείται ειδική θερμότητα και συμβολίζεται με το σύμβολο c. Η θερμοχωρητικότητα μιας ουσίας μπορεί να μετρηθεί με δυο τρόπους: είτε το δείγμα να βρίσκεται υπό σταθερή πίεση, Cp είτε υπό σταθερό όγκο, Cv. Οι τιμές της θερμοχωρητικότητας υπό σταθερή πίεση είναι μεγαλύτερες από τις τιμές υπό σταθερό όγκο. Στην περίπτωση των στερεών η διαφορά είναι πολύ μικρή για θερμοκρασίες περιβάλλοντος καθώς και για χαμηλότερες. Μια κοινή ειδική θερμότητα είναι αυτή του νερού: cp = J/g.K (15 C, 1 atm). Στον Πίνακα 5.1 παρουσιάζονται οι τιμές της ειδικής θερμότητας cp για ορισμένα κοινά μέταλλα, κεραμικά και πολυμερή ΘΕΡΜΙΚΗ ΑΓΩΓΙΜΟΤΗΤΑ Θερμική αγωγιμότητα είναι η ιδιότητα του υλικού που χαρακτηρίζει την ικανότητα του να μεταφέρει θερμότητα. Η θερμότητα πάντοτε μεταφέρεται από την υψηλότερη θερμοκρασία προς την χαμηλότερη. Ορίζεται από την παρακάτω σχέση: q= k dt dx όπου q υποδηλώνει τη ροή θερμότητας, δηλ. το ποσό θερμότητας που διέρχεται διαμέσου του υλικού ανά μονάδα χρόνου και ανά μονάδα επιφάνειας, k είναι η θερμική αγωγιμότητα και dt/dx είναι η θερμοκρασιακή βαθμίδα κατά τη διεύθυνση μεταφοράς της θερμότητας. Η ροή θερμότητας μετρείται σε W/m2 και η θερμική αγωγιμότητα σε W/m.K. Το αρνητικό πρόσημο στην έκφραση υποδηλώνει ότι η θερμότητα μεταφέρεται από το θερμό στο ψυχρό, με φορά αντίθετη από την θερμοκρασιακή βαθμίδα. Στον Πίνακα 4.1 παρουσιάζονται οι τιμές της θερμικής αγωγιμότητας για ορισμένα κοινά μέταλλα, κεραμικά και πολυμερή. Παρατηρείται ότι η θερμική αγωγιμότητα των 44
46 μετάλλων είναι σημαντικά μεγαλύτερη από τη θερμική αγωγιμότητα των κεραμικών και των πολυμερών ΘΕΡΜΙΚΗ ΔΙΑΣΤΟΛΗ Κατά το σχεδιασμό ποικίλων κατασκευών είναι επιβεβλημένο στους μηχανικούς να λαμβάνουν υπόψη τη διαστολή και τη συστολή των υλικών π.χ. κατά το σχεδιασμό καλουπιών για τη χύτευση θερμών υλικών ή σε μηχανολογικές εφαρμογές όπου αναμένονται μεγάλες διαστασιακές μεταβολές λόγω της θερμοκρασίας. Η μεταβολή του μήκους ενός υλικού είναι ανάλογη με τη μεταβολή της θερμοκρασίας και μπορεί να εκφραστεί από την παρακάτω σχέση: al = 1 l l0 T ή L = al T l0 όπου αl είναι ο συντελεστής γραμμικής θερμικής διαστολής, lf και l0 υποδηλώνουν το τελικό και το αρχικό μήκος αντίστοιχα, ενώ Τf και Τ0 την τελική και αρχική θερμοκρασία του υλικού. Ο γραμμικός συντελεστής θερμικής διαστολής έχει μονάδες αντίστροφης θερμοκρασίας (ανά C) και για τα μέταλλα είναι συνήθως της τάξης 10-6/ C. Κατά τη θέρμανση ή ψύξη ενός υλικού υπάρχει μεταβολή όλων των διαστάσεων του υλικού και συνεπώς υπάρχει μεταβολή του όγκου του. Για ισότροπα υλικά ο ογκομετρικός συντελεστής θερμικής διαστολής αv είναι προσεγγιστικά ίσος με 3αl, αv 3 αl. Από ατομική άποψη, η θερμική διαστολή μπορεί να θεωρηθεί ως το αποτέλεσμα της αύξησης της μέσης απόστασης των ατόμων ενός υλικού. Αν τα άτομα θεωρηθούν ως μικροί ταλαντωτές, τότε η διαδοχική αύξηση της θερμοκρασίας αυξάνει το πλάτος των ατομικών δονήσεων με συνέπεια την διαστολή του υλικού. Στον Πίνακα 4.1 παρουσιάζονται οι συντελεστές θερμικής διαστολής για ορισμένα κοινά μέταλλα, κεραμικά και πολυμερή. Παρατηρείται ότι οι συντελεστές γραμμικής διαστολής των μετάλλων κυμαίνονται από περίπου 5x10-6 έως 25x10-6/ C. Ωστόσο έχουν αναπτυχθεί κράματα με πολύ μικρούς συντελεστές γραμμική διαστολής, τα οποία χρησιμοποιούνται σε εφαρμογές όπου απαιτείται μικρή μεταβολή των διαστάσεων σε μια περιοχή θερμοκρασιών. Ένα από αυτά είναι το Invar (64%Fe-36%Ni) με ένα συντελεστή γραμμικής διαστολής περίπου 1.6x10-6/ C. Ακόμη υπάρχει και το Super Invar, το οποίο έχει συντελεστή θερμικής διαστολής περίπου 0.72x106 / C (63%Fe-32%Ni-5Co). Αυτά τα κράματα βρίσκουν εφαρμογή στην αεροναυπηγική, όπου υπάρχουν μεγάλες μεταβολές θερμοκρασίας. Ένα άλλο γνωστό εμπορικό κράμα είναι το Covar (54%Fe-29%Ni-17Co), το οποίο σχεδιάστηκε έτσι ώστε να έχει παρόμοιο συντελεστή θερμικής διαστολής με τη βοριοπυριτική ύαλο (Pyrex). Συνεπώς, σε κατασκευές που περιλαμβάνουν αυτά τα υλικά μειώνεται η πιθανότητα θραύσης, λόγω των θερμικών τάσεων που αναπτύσσονται κάτω από την επίδραση των θερμικών μεταβολών. Ακόμη, η ιδιότητα της διαστολής των υλικών βρίσκει εφαρμογή κατά την προσαρμογή των εξαρτημάτων σε μηχανοκατασκευές. Για παράδειγμα, η τοποθέτηση ενός άξονα μέσα σε ένα δακτύλιο επιτυγχάνεται κατασκευάζοντας την εσωτερική διάμετρο του δακτυλίου ελαφρά μικρότερη από τη διάμετρο του άξονα, θερμαίνοντας το δακτύλιο ώστε να μπορεί να τοποθετηθεί ο άξονας μέσα στο δακτύλιο και μετά επιτρέποντας τη ψύξη του δακτυλίου και συνεπώς τη στερέωσή του λόγω συστολής επάνω στον άξονα. 45
47 Πίνακας 5.1: Θερμικές ιδιότητες ορισμένων μετάλλων, κεραμικών και πολυμερών σε θερμοκρασία περιβάλλοντος. Υλικό Αλουμίνιο Χαλκός Χρυσός Σίδηρος Νικέλιο Άργυρος Βολφράμιο Χάλυβας 1025 Ανοξείδωτος χάλυβας 316 Ορείχαλκος (70Cu-30Zn) Κράμα Kovar (54Fe-29Ni-17Co) Κράμα Invar (64Fe-36Ni) Κράμα Super Invar (63Fe-32Ni-5Co) cp k ( J/Κg.K) (W/m.K) Μέταλλα αl 10-6/ C Κεραμικά Αλουμίνα (Al2O3) Τηγμένη Silica (SiO2) Ύαλος νατρίου-ασβεστίου Βοριοπυριτική ύαλος Πολυμερή Πολυαιθυλένιο (χαμηλής πυκνότητας) Πολυαιθυλένιο (υψηλής πυκνότητας) Πολυπροπυλένιο Πολυτετραφθοροαιθυλένιο (τεφλόν) Πολυμερές Φαινόληςφορμαλδεύδης (βακελίτης) Νάιλον 6,6 Πολυϊσοπρένιο Στον Πίνακα ακόμη παρατηρείται ότι τα κεραμικά έχουν σχετικά μικρούς συντελεστές θερμικής διαστολής, οι οποίοι κυμαίνονται περίπου από 0.5x10-6 έως 15x10-6/ C, ενώ αντίθετα τα πολυμερή παρουσιάζουν σχετικά μεγάλους συντελεστές θερμικής διαστολής, που κυμαίνονται από 50x10-6 έως 400x10-6/ C. 46
48 5.2 ΗΛΕΚΤΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΗΛΕΚΤΡΙΚΗ ΕΙΔΙΚΗ ΑΝΤΙΣΤΑΣΗ ΚΑΙ ΑΓΩΓΙΜΟΤΗΤΑ Όταν μια ηλεκτρική τάση V εφαρμόζεται σε ένα υλικό, τότε ρέει ρεύμα έντασης Ι. Σύμφωνα με το νόμο του OHM, το ρεύμα Ι είναι ανάλογο με την τάση V και εκφράζεται από την παρακάτω σχέση: I= V R όπου R είναι η ηλεκτρική αντίσταση. Οι μονάδες των μεγεθών I, V και R είναι τα amperes, volts και ohms (V/A) αντίστοιχα. Η αντίσταση R εξαρτάται από τη γεωμετρία του υλικού (μήκος l και εμβαδό διατομής A) και την ειδική αντίσταση ρ του υλικού, που είναι ανεξάρτητη από τη γεωμετρία του δοκιμίου. R= ρl RA ή ρ = A l Οι μονάδες του ρ είναι ohm.m (Ω.m). Πολλές φορές για να χαρακτηριστεί η ηλεκτρική αγωγιμότητα ενός υλικού χρησιμοποιείται η ηλεκτρική ειδική αγωγιμότητα, η οποία ορίζεται ως το αντίστροφο της ηλεκτρικής ειδικής αντίστασης: σ = 1 ρ Οι μονάδες του σ είναι (Ω.m)-1. Στον Πίνακα 5.2 παρουσιάζεται η ειδική αγωγιμότητα ορισμένων χαρακτηριστικών μετάλλων σε θερμοκρασία περιβάλλοντος. Πίνακας 5.2: Ηλεκτρική ειδική αγωγιμότητα ορισμένων συνήθων μετάλλων σε και κραμάτων σε θερμοκρασία περιβάλλοντος. Μέταλλο Ηλεκτρική Ειδική Αγωγιμότητα (Ω.m)-1 Άργυρος 6.8 x 107 Χαλκός 6.0 x 107 Χρυσός 4.3 x 107 Αλουμίνιο 3.8 x 107 Σίδηρος 1.0 x 107 Ορείχαλκος (70Cu-30Zn) 1.6 x 107 Λευκόχρυσος 0.94 x 107 Κοινός ανθρακούχος χάλυβας 0.6 x 107 Ανοξείδωτος χάλυβας 0.2 x
49 5.2.2 ΗΜΙΑΓΩΓΟΙ Οι ημιαγωγοί είναι υλικά τα οποία έχουν ηλεκτρική αγωγιμότητα που κυμαίνεται μεταξύ των αγωγών και των μονωτών. Στα μέταλλα, τα οποία είναι καλοί αγωγοί του ηλεκτρισμού, το ρεύμα δημιουργείται από τη ροή των ηλεκτρονίων, ενώ στους ημιαγωγούς από τη ροή των ηλεκτρονίων καθώς και των θετικά φορτισμένων «οπών». Μια οπή δημιουργείται κάθε φορά που ένα ηλεκτρόνιο μετακινείται λόγω προσφοράς ενέργειας, με συνέπεια τη δημιουργία δυο φορέων ηλεκτρικού φορτίου, των ηλεκτρονίων και των θετικά φορτισμένων οπών. Τα τρανζίστορ, τα ολοκληρωμένα κυκλώματα, τα ηλιακά κελιά, οι δίοδοι, περιλαμβανομένων και των διόδων φωτοεκπομπής (LED), είναι μερικές μόνο εφαρμογές των ημιαγωγών. Για παράδειγμα, τα φωτοβολταϊκά πάνελ είναι μεγάλες διατάξεις ημιαγωγών που μετατρέπουν απευθείας την ηλιακή ενέργεια σε ηλεκτρική. Τα υλικά που χρησιμοποιούνται για την κατασκευή των ημιαγωγών είναι συνήθως κρυσταλλικά Ωστόσο, άμορφα υλικά μπορούν επίσης να χρησιμοποιηθούν για την κατασκευή τους. Το πιο κοινό υλικό κατασκευής των ημιαγωγών είναι το πυρίτιο. Ακόμη πολλά άλλα υλικά όπως το γερμάνιο, το αρσενίδιο του γαλλίου, το καρβίδιο του πυριτίου χρησιμοποιούνται για την κατασκευή ημιαγωγών. Οι ημιαγωγοί που η ηλεκτρική τους συμπεριφορά βασίζεται στην ηλεκτρονιακή δομή του καθαρού υλικού κατασκευής τους (χωρίς προσμείξεις) συχνά ονομάζονται ενδογενείς. Όταν όμως τα ηλεκτρικά χαρακτηριστικά των ημιαγωγών οφείλονται στην προσθήκη άλλων στοιχείων, τότε αποκαλούνται εξωγενείς ή ημιαγωγοί προσμείξεων. Σχεδόν όλοι οι εμπορικοί ημιαγωγοί είναι εξωγενείς, γιατί η αγωγιμότητα των ενδογενών ημιαγωγών είναι πολύ μικρή για να χρησιμοποιηθούν σε ηλεκτρικά κυκλώματα. Οι εξωγενείς ημιαγωγοί διακρίνονται σε ημιαγωγούς τύπου-n και τύπου-p. Στους ημιαγωγούς τύπου-n τα άτομα των προσμείξεων δίνουν ηλεκτρόνια στο υλικό υποδοχής, με συνέπεια τη δημιουργία ελεύθερων ηλεκτρονίων και τη θεαματική αύξηση της αγωγιμότητας του υλικού. Τυπικό παράδειγμα είναι η προσθήκη φωσφόρου σε πυρίτιο. Το πυρίτιο έχει τέσσερα ηλεκτρόνια, ενώ ο φωσφόρος πέντε. Συνεπώς δημιουργούνται τέσσερις ομοιοπολικοί δεσμοί μεταξύ των ατόμων του πυριτίου και του φωσφόρου και περισσεύει ένα ηλεκτρόνιο, το οποίο με μικρή προσφορά ενέργειας π.χ. θέρμανση ή ακτινοβολία μετατρέπεται σε ηλεκτρόνιο αγωγιμότητας. Αντίθετα στους ημιαγωγούς τύπου-p τα άτομα προσμείξεων αφαιρούν ηλεκτρόνια από το υλικό υποδοχής. Για παράδειγμα, η προσθήκη σε πυρίτιο ή γερμάνιο τρισθενών στοιχείων όπως του αλουμινίου, βορίου και γαλλίου, έχει ως αποτέλεσμα για κάθε τέσσερις ομοιοπολικούς δεσμούς την έλλειψη ενός ηλεκτρονίου από έναν ομοιοπολικό δεσμό, το οποίο μπορεί να συμπληρωθεί από τη μετακίνηση ενός άλλου ηλεκτρονίου από γειτονικό άτομο του ημιαγωγού, με συνέπεια τη μετακίνηση της κενής θέσης. Αυτή η κενή θέση αποκαλείται οπή. Κάτω από την επίδραση ηλεκτρικού πεδίου τα ηλεκτρόνια και οι οπές μετακινούνται σε αντίθετη κατεύθυνση. Στους ημιαγωγούς τύπου-n, το γράμμα n προέρχεται από τη λέξη negative και υποδηλώνει την ύπαρξη περισσοτέρων ηλεκτρονίων, ενώ στους ημιαγωγούς τύπου-p, το γράμμα p προέρχεται από τη λέξη positive και υποδηλώνει την ύπαρξη περισσοτέρων οπών, που σημαίνει την απουσία ηλεκτρονίων και συνεπώς την ύπαρξη θετικών φορτίων. Η διαδικασία πρόσμειξης ονομάζεται doping (εμπλουτισμός). 48
50 5.3 ΜΑΓΝΗΤΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΒΑΣΙΚΕΣ ΑΡΧΕΣ Μαγνητισμός ονομάζεται το φαινόμενο σύμφωνα με το οποίο ορισμένα υλικά, αποκαλούμενα μαγνήτες, ασκούν ελκτικές ή απωστικές δυνάμεις σε άλλα υλικά. Πολλές σύγχρονες συσκευές όπως οι ηλεκτρικές γεννήτριες, οι μετασχηματιστές, οι ηλεκτρικοί κινητήρες, οι υπολογιστές καθώς και τα συστήματα αναπαραγωγής εικόνας και ήχου στηρίζονται στα μαγνητικά υλικά. Οι μαγνητικές ιδιότητες του ορυκτού μαγνητίτη ήταν γνωστές από την αρχαιότητα. Ο σίδηρος, ορισμένοι χάλυβες, το νικέλιο, το κοβάλτιο καθώς και τα κράματα ή οξείδιά τους παρουσιάζουν μαγνητικές ιδιότητες. Άλλα υλικά όπως ο χαλκός, το αλουμίνιο και τα πλαστικά είναι γνωστά ως μη μαγνητικά υλικά. Τα μαγνητικά πεδία εμφανίζονται ως δίπολα με έναν βόρειο και έναν νότιο πόλο. Οι όροι αυτοί έχουν καθιερωθεί από την εποχή που οι μαγνήτες χρησιμοποιούνταν ως πυξίδες για να δείξουν το βόρειο και το νότιο πόλο της γης. Έχει αποδειχτεί ότι, στα μαγνητικά υλικά υπάρχουν μαγνητικά δίπολα τα οποία κάτω από την επίδραση ενός μαγνητικού πεδίου τείνουν να προσανατολιστούν με αυτό, όπως ακριβώς η πυξίδα ευθυγραμμίζεται με το μαγνητικό πεδίο της γης. Οι μαγνητικές ιδιότητες των υλικών οφείλονται στην κίνηση ηλεκτρικών φορτίων. Μαγνητισμός μπορεί να προκύψει είτε από την κίνηση των ηλεκτρονίων του ηλεκτρικού ρεύματος, που καλείται ηλεκτρομαγνητισμός, είτε από την κίνηση των ηλεκτρονίων σε ατομικό επίπεδο που έχει ως αποτέλεσμα τη δημιουργία μαγνητικών διπόλων. Κάθε ηλεκτρόνιο σε ένα άτομο μπορεί να θεωρηθεί ως ένας μικρός μαγνήτης που έχει δύο μαγνητικές ροπές. Οι μαγνητικές ροπές είναι το αποτέλεσμα των δυο ειδών κινήσεων που εκτελεί ένα ηλεκτρόνιο. Η πρώτη είναι η περιστροφική κίνηση του ηλεκτρονίου γύρω απ' τον πυρήνα του ατόμου, που έχει ως αποτέλεσμα τη δημιουργία μιας περιστροφικής μαγνητικής διπολικής ροπής στην κατεύθυνση του άξονα περιστροφής του πυρήνα. Η δεύτερη πηγή της μαγνητικής ροπής, που είναι πολύ ισχυρότερη, οφείλεται στην περιστροφή του ηλεκτρονίου γύρω από τον εαυτό του και ονομάζεται μαγνητική διπολική ροπή ιδιοπεριστροφής (σπιν). Η συνισταμένη μαγνητική ροπή του ατόμου είναι το διανυσματικό άθροισμα των ξεχωριστών μαγνητικών ροπών όλων των ηλεκτρονίων. Σε κάθε άτομο οι μαγνητικές ροπές ορισμένων ζευγαριών ηλεκτρονίων αλληλοεξουδετερώνονται. Αυτό ισχύει τόσο για τις μαγνητικές ροπές λόγω της περιστροφικής κίνησης, όσο και λόγω της ιδιοπεριστροφής. Συνεπώς, σε άτομα με συμπληρωμένες στιβάδες ή υποστιβάδες, όπου όλα τα ηλεκτρόνια είναι σε ζευγάρια, οι μαγνητικές ροπές αλληλοεξουδετερώνονται και μόνο άτομα με μερικώς γεμάτες στιβάδες έχουν μαγνητική ροπή. Έτσι, υλικά που αποτελούνται από πλήρως συμπληρωμένες ηλεκτρονιακές στιβάδες δεν είναι ικανά να μαγνητιστούν μόνιμα. Για παράδειγμα, στα άτομα του Mg (1s22s22p63s2) και του Ne (1s22s22p6), όλα τα ηλεκτρόνια είναι σε ζεύγη και η συνολική μαγνητική ροπή των ατόμων είναι μηδέν. Αντίθετα, άτομα που έχουν και μονήρη ηλεκτρόνια, όπως το Na (1s22s22p63s1), έχουν μαγνητική ροπή. Συνεπώς οι μαγνητικές ιδιότητες των υλικών καθορίζονται από την εμφάνιση μαγνητικών ροπών, οι οποίες με τη σειρά τους καθορίζονται από τη διάταξη των ηλεκτρονίων στα διάφορα στοιχεία. 49
51 5.3.2 ΕΙΔΗ ΜΑΓΝΗΤΙΣΜΟΥ Ο διαμαγνητισμός, ο παραμαγνητισμός και ο σιδηρομαγνητισμός είναι τα μερικά είδη μαγνητισμού που παρουσιάζουν τα διαφορετικά υλικά. Διαμαγνητισμός Ο διαμαγνητισμός είναι μια ασθενής μορφή μαγνητισμού και είναι το αποτέλεσμα της απόκρισης ορισμένων υλικών στην εφαρμογή ενός εξωτερικού μαγνητικού πεδίου. Διαρκεί μόνο όσο εφαρμόζεται το εξωτερικό μαγνητικό πεδίο. Οφείλεται στην τροποποίηση της τροχιακής κίνησης των ηλεκτρονίων, η οποία γίνεται με τέτοιο τρόπο ώστε οι επαγόμενες ροπές που αναπτύσσονται στο υλικό να αντιτίθενται στο εξωτερικό μαγνητικό πεδίο. Τα διαμαγνητικά υλικά απωθούνται ελαφρά από κάποιο μόνιμο μαγνήτη. Τα διαμαγνητικά υλικά θεωρούνται ως μη μαγνητικά γιατί μαγνητίζονται μόνο παρουσία μαγνητικού πεδίου. Τυπικά διαμαγνητικά υλικά είναι το οξείδιο του αλουμινίου, ο χαλκός, ο χρυσός, το πυρίτιο, ο άργυρος, ο ψευδάργυρος, κ.λ.π Παραμαγνητισμός Σε ορισμένα υλικά η αλληλοεξουδετέρωση των τροχιακών μαγνητικών ροπών καθώς και των ροπών λόγω σπιν δεν είναι πλήρης, με αποτέλεσμα κάθε άτομο να διαθέτει διπολική ροπή. Κάτω από την επίδραση εξωτερικού μαγνητικού πεδίου αυτές οι στοιχειώδεις μαγνητικές ροπές τείνουν να προσανατολιστούν κατά τη διεύθυνση και φορά του πεδίου. Αυτό έχει ως αποτέλεσμα την ενίσχυση του εξωτερικού πεδίου. Τα παραμαγνητικά υλικά έλκονται ελαφρά από κάποιο μόνιμο μαγνήτη. Τα παραμαγνητικά υλικά θεωρούνται ως μη μαγνητικά γιατί μαγνητίζονται μόνο παρουσία μαγνητικού πεδίου. Τυπικά παραμαγνητικά υλικά είναι το αλουμίνιο, το χρώμιο, το μολυβδαίνιο το νάτριο, το τιτάνιο, το ζιρκόνιο, κ.λ.π. Σιδηρομαγνητισμός Ορισμένα μεταλλικά υλικά διαθέτουν μόνιμη μαγνητική ροπή, χωρίς να βρίσκονται κάτω από την επίδραση εξωτερικού μαγνητικού πεδίου, αλλά σε φυσική κατάσταση. Αυτός ο τύπος μαγνητισμού καλείται σιδηρομαγνητισμός και επιδεικνύεται από τα μέταλλα μετάπτωσης όπως ο σίδηρος, το κοβάλτιο, το νικέλιο καθώς και κάποιες από τις σπάνιες γαίες όπως το γαδολίνιο και το δυσπρόσιο. Στα σιδηρομαγνητικά υλικά οι μαγνητικές ροπές προσανατολίζονται αμοιβαία προς κοινή διεύθυνση, ακόμη και απουσία εξωτερικού μαγνητικού πεδίου. Τα σιδηρομαγνητικά υλικά έλκονται έντονα από μαγνήτη. Η αύξηση της θερμοκρασίας έχει ως αποτέλεσμα την αύξηση της κινητικότητας των ατόμων με αποτέλεσμα, όταν η θερμοκρασία φθάσει μια κρίσιμη τιμή Tc (θερμοκρασία Curie), οι μαγνητικές ροπές αποπροσανατολίζονται και παρατηρείται μετάβαση από το σιδηρομαγνητισμό στον παραμαγνητισμό ΕΙΔΗ ΜΑΓΝΗΤΩΝ Ηλεκτρομαγνήτες Ένας ηλεκτρομαγνήτης αποτελείται από ένα κυλινδρικό πηνίο, το οποίο όταν διαρρέεται από ρεύμα λειτουργεί ως μαγνήτης, ενώ όταν σταματά η διέλευση του ρεύματος, τότε σταματά να είναι μαγνήτης. Οι ηλεκτρομαγνήτες χρησιμοποιούνται σε εφαρμογές, στις οποίες είναι απαραίτητο ο μαγνήτης να τίθεται σε λειτουργία με τη βοήθεια διακόπτη, π.χ. οι μεγάλοι γερανοί που χρησιμοποιούνται για την ανύψωση αυτοκινήτων με σκοπό την ανακύκλωση. 50
52 Όταν ρεύμα έντασης Ι, διέρχεται από κυλινδρικό πηνίο ή σωληνοειδές (Σχήμα 5.1α) που αποτελείται από σπείρες Ν και έχει μήκος l, τότε δημιουργείται μαγνητικό πεδίο έντασης Η, που δίνεται από την παρακάτω εξίσωση: H= NI l Οι μονάδες του Η είναι amperes x στροφές/μέτρο ή amperes/μέτρο (A/m). (α) (β) Σχήμα 5.1: Σχηματικό διάγραμμα ενός κυλινδρικού πηνίου (α) με κενό και (β) στερεό υλικό στο εσωτερικό του. Σε ένα στερεό υλικό που βρίσκεται κάτω από την επίδραση εξωτερικού μαγνητικού πεδίου έντασης Η εμφανίζεται μαγνητική επαγωγή ή πυκνότητα μαγνητικής ροής Β (Σχήμα 5.1β). Η μαγνητική επαγωγή αναπαριστά την ένταση του εσωτερικού μαγνητικού πεδίου μέσα στο υλικό, λόγω της διευθέτησης των μαγνητικών ροπών των ατόμων του υλικού παράλληλα με το εξωτερικό πεδίο. Η ένταση του μαγνητικού πεδίου και η μαγνητική επαγωγή συνδέονται με τη σχέση B = µh όπου μ είναι η μαγνητική διαπερατότητα του υλικού. Η διαπερατότητα μετράται σε Tesla (webers/ampere x μέτρο, Wb/A.m). Για το κενό ισχύει η σχέση B0 = µ 0 H όπου μ0 είναι η μαγνητική διαπερατότητα του κενού, 4π10-7 Wb/A.m. Μόνιμοι και προσωρινοί μαγνήτες Οι μόνιμοι μαγνήτες κατασκευάζονται από σιδηρομαγνητικά υλικά, τα οποία εφόσον μαγνητιστούν, συνεχίζουν να διατηρούν τις μαγνητικές τους ιδιότητες και χωρίς την επίδραση εξωτερικού μαγνητικού πεδίου. Αυτά τα υλικά καλούνται σκληρά. Αντίθετα οι προσωρινοί μαγνήτες κατασκευάζονται από σιδηρομαγνητικά υλικά, τα οποία έχουν μαγνητικές ιδιότητες μόνο μέσα σε εξωτερικό μαγνητικό πεδίο. Αυτά τα υλικά καλούνται μαλακά. Τα μαλακά υλικά, όπως π.χ. ο σίδηρος, είναι κατάλληλα για την κατασκευή ηλεκτρομαγνητών. 51
53 5.3.4 ΜΑΓΝΗΤΙΚΑ ΜΕΤΑΛΛΙΚΑ ΥΛΙΚΑ Τα μαγνητικά υλικά σύμφωνα με το πόσο εύκολα μαγνητίζονται και απομαγνητίζονται διακρίνονται, όπως έχει ήδη αναφερθεί, σε σκληρά και μαλακά. Τα πιο κοινά μαλακά μαγνητικά υλικά είναι ο σίδηρος, τα κράματα σιδήρου-πυριτίου και τα κράματα σιδήρου-νικελίου. Χρησιμοποιούνται για την κατασκευή ηλεκτρομαγνητών. Βρίσκουν εφαρμογή σε μετασχηματιστές, γεννήτριες, κινητήρες, δυναμό και σε διακόπτες κυκλωμάτων. Τα πιο κοινά σκληρά μαγνητικά υλικά είναι τα κράματα αλουμινίου-νικελίουκοβαλτίου, κράματα νεοδυμίου-σιδήρου-βορίου, κράματα σιδήρου-χρωμίου-κοβαλτίου και τα κράματα σπανίων γαιών. Χρησιμοποιούνται για την κατασκευή μόνιμων μαγνητών. Ένας τυπικό παράδειγμα είναι οι μικροί μαγνήτες ψυγείου, που χρησιμεύουν για τη συγκράτηση σημειωμάτων στην πόρτα του ψυγείου. Είναι αξιοσημείωτο ότι τα κράματα των σπανίων γαιών έχουν μεγάλο βιομηχανικό ενδιαφέρον λόγω των πολύ καλών μαγνητικών τους ιδιοτήτων. Οι μαγνητικές τους ιδιότητες οφείλονται στα μερικώς ασυμπλήρωτα f τροχιακά (μπορούν να έχουν έως 14 ηλεκτρόνια). Το σπιν αυτών των ηλεκτρονίων μπορεί να αποκτήσει την ίδια φορά, έχοντας ως αποτέλεσμα τη δημιουργία πολύ ισχυρών μαγνητικών πεδίων. Η χρήση τους, σε εφαρμογές όπου το υψηλό κόστος τους δεν αποτελεί εμπόδιο, έχει ως αποτέλεσμα τη μείωση του μεγέθους των μαγνητών. 52
54 ΚΕΦΑΛΑΙΟ 6 ΜΗΧΑΝΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 6.1 ΓΕΝΙΚΑ Πολλά υλικά κατά τη διάρκεια της λειτουργίας τους, υπόκεινται σε δυνάμεις ή φορτία. Συνεπώς, κατά το σχεδιασμό ενός εξαρτήματος ή κατασκευής, είναι απαραίτητο να γνωρίζουμε τις μηχανικές ιδιότητες των χρησιμοποιούμενων υλικών, έτσι ώστε να μην εμφανισθούν μη αποδεκτές παραμορφώσεις ή θραύση. Η εξοικείωση των μηχανικών με τις δοκιμές που χρησιμοποιούνται για τη μέτρηση των διάφορων μηχανικών ιδιοτήτων, καθώς και η κατανόηση των δεδομένων που παράγονται από αυτές τις δοκιμές είναι επιβεβλημένη. Τρείς είναι οι βασικοί τρόποι εφαρμογής ενός φορτίου: ο εφελκυσμός, η θλίψη και η διάτμηση. Η κάμψη παράγει εφελκυστικές και θλιπτικές τάσεις, ενώ η στρέψη είναι παραλλαγή της διάτμησης. Οι κυριότερες μηχανικές δοκιμές που χρησιμοποιούνται για να μετρηθούν οι μηχανικές ιδιότητες των υλικών είναι: η δοκιμή εφελκυσμού, θλίψης, κάμψης, διάτμησης, στρέψης, κρούσης, σκληρότητας, ερπυσμού και κόπωσης. Με τη δοκιμή του υλικού σε εφελκυσμό, θλίψη ή διάτμηση παράγονται πληροφορίες για την ικανότητα του υλικού να παραλάβει στατικά φορτία, ενώ η δοκιμή κρούσης δίνει πληροφορίες σχετικά με τη δυσθραυστότητα του υλικού, δηλαδή την ικανότητα του να απορροφά ενέργεια πριν τη θραύση του. Πρόσθετα, οι δοκιμές σκληρότητας μετρούν την αντίσταση του υλικού στη διείσδυση ενός σώματος. Mε τη δοκιμή ερπυσμού παράγονται πληροφορίες για την αντοχή ενός υλικού σε περιβάλλον υψηλών θερμοκρασιών, ενώ με τη δοκιμή κόπωσης ελέγχεται η αντοχή του υλικού σε εναλλασσόμενες κυκλικές καταπονήσεις. Η διεξαγωγή των μηχανικών δοκιμών καθώς και η ερμηνεία των αποτελεσμάτων τους πρέπει να γίνεται με τον ίδιο τρόπο από όλους. Για το λόγο αυτό, εθνικοί οργανισμοί, όπως ASTM (American Society for Testing and Materials), DIN (Deutsches Institut für Normung), ΕΛΟΤ (Ελληνικός Οργανισμός Τυποποίησης), κλπ. καθώς και διεθνείς οργανισμοί, ISO (International Standardization Organisation), έχουν καθιερώσει πρότυπα σύμφωνα με τα οποία εκτελούνται οι μηχανικές δοκιμές. Τα πρότυπα αφορούν τη γεωμετρία των δοκιμίων, τις συσκευές των δοκιμών, τον τρόπο εκτέλεσής τους (π.χ. ταχύτητα εφαρμογής του φορτίου) καθώς και τον τρόπο παρουσίασης των αποτελεσμάτων. Η συζήτηση που ακολουθεί αφορά κυρίως τη μηχανική συμπεριφορά των μετάλλων. 6.2 ΔΟΚΙΜΗ ΕΦΕΛΚΥΣΜΟΥ Η δοκιμή εφελκυσμού είναι μια από τις πιο συνηθισμένες μηχανικές δοκιμές. Κατά τη δοκιμή αυτή ένα δοκίμιο επιμηκύνεται κάτω από την επίδραση εφελκυστικού φορτίου, με σταθερή ταχύτητα, μέχρι την θραύση του. Στο Σχήμα 6.1 φαίνεται ένα τυπικό δοκίμιο εφελκυσμού. Το δοκίμιο έχει κυλινδρική διατομή. Επίσης υπάρχουν και δοκίμια με ορθογώνια διατομή. Η επιμήκυνση μετράται στο κεντρικό τμήμα του δοκιμίου l0, το οποίο είναι πενταπλάσιο της διαμέτρου d0 (DIN) ή τετραπλάσιο της διαμέτρου (ASTM). Για το λόγο αυτό τα δοκίμια ονομάζονται αναλογικά. 53
55 Σχήμα 6.1: Τυποποιημένο δοκίμιο εφελκυσμού κυκλικής διατομής. Οι μηχανές εφελκυσμού (Σχήμα 6.2) είναι σχεδιασμένες με τέτοιο τρόπο ώστε να επιμηκύνουν το δοκίμιο με σταθερό ρυθμό, ενώ συνεχώς μετρείται η εφαρμοζόμενη δύναμη, με ένα κελίο φόρτισης, καθώς και η επιμήκυνση του δοκιμίου, με ένα επιμηκυνσιόμετρο. Από τις μετρούμενες τιμές της δύναμης εφελκυσμού και επιμήκυνσης σχηματίζεται το λεγόμενο διάγραμμα τάσης-παραμόρφωσης (Σχήμα 6.3). Σχήμα 6.2: Αναπαράσταση δοκιμής εφελκυσμού και συσκευή δοκιμών εφελκυσμού. 54
56 Η μηχανική τάση ορίζεται από την σχέση σ = F A0 όπου F είναι το φορτίο που εφαρμόζεται κάθετα στη διατομή του δοκιμίου, σε newton, N και Α0 το εμβαδό της αρχικής διατομής του δοκιμίου σε mm2. Η τάση μετρείται σε Megapascal, 1 MPa= 106 N/m2 = 1 N/mm2. Η μηχανική παραμόρφωση ορίζεται από τη σχέση ε = l l0 l = l0 l0 όπου l είναι το μήκος του δοκιμίου, μετά την εφαρμογή της δύναμης F και l0 το αρχικό μήκος δοκιμής. Η παραμόρφωση ε είναι καθαρός αριθμός. Μερικές φορές εκφράζεται επί τοις εκατό και σε αυτή την περίπτωση πολλαπλασιάζεται με 100. Στο Σχήμα 6.3 απεικονίζεται το διάγραμμα τάσης-παραμόρφωσης ενός τυπικού μετάλλου. Σχήμα 6.3: α) Διάγραμμα τάσης-παραμόρφωσης τυπικού μετάλλου. β) Σχηματική αναπαράσταση των παραμορφωμένων δοκιμίων μέχρι το σημείο θραύσης κατά τη δοκιμή εφελκυσμού. Αρχικά το υλικό επιμηκύνεται ελαστικά. Αυτό σημαίνει ότι, αν η τάση αφαιρεθεί το δοκίμιο θα επιστρέψει στο μήκος που είχε πριν την εφαρμογή του φορτίου. Η παραμόρφωση είναι αντιστρέψιμη, όχι μόνιμη. Καθώς το φορτίο αυξάνεται, μετά την αρχική ελαστική παραμόρφωση, ξεκινά η πλαστική παραμόρφωση του δοκιμίου. Αυτό σημαίνει ότι, αν η τάση αφαιρεθεί το δοκίμιο δεν θα επιστρέψει στο αρχικό του μήκος, αλλά ότι υπάρχει μόνιμη, μη αντιστρέψιμη παραμόρφωση. Η τάση πάνω από την οποία εμφανίζεται πλαστική παραμόρφωση, καλείται όριο διαρροής, σy. Πέρα από αυτό το σημείο, το οποίο ονομάζεται όριο ελαστικότητας, η επιμήκυνση του δοκιμίου απαιτεί την αύξηση της επιβαλλόμενης τάσης και τότε λέγεται ότι το υλικό εργοσκληρύνεται ή σκληραίνει λόγω της παραμόρφωσης (εργοσκλήρυνση). Η σκλήρυνση του υλικού οφείλεται στην παρεμποδιζόμενη, από άλλες διαταραχές, κίνηση των διαταραχών (φαινόμενο ενδοτράχυνσης). Η τάση φτάνει σε ένα 55
57 μέγιστο, στη μέγιστη αντοχή σε εφελκυσμό, σts. Στο σημείο αυτό το η διατομή αρχίζει να μειώνεται τοπικά και σχηματίζει ένα λαιμό. Από το σημείο αυτό και μετά όλη η παραμόρφωση περιορίζεται σε αυτόν τον λαιμό, η εφαρμοζόμενη τάση μειώνεται και η θραύση συμβαίνει εντός των ορίων του λαιμού. Στην περιοχή ελαστικής παραμόρφωσης, η σχέση ανάμεσα στην τάση και την παραμόρφωση είναι γραμμική για μέταλλα και κεραμικά και ισχύει ο νόμος του Hooke: σ = Eε όπου Ε είναι το μέτρο ελαστικότητας σε εφελκυσμό ή μέτρο του Young. Το μέτρο ελαστικότητας αποτελεί μέτρο της στιβαρότητας ενός υλικού. Μπορεί να θεωρηθεί ως η δυσκαμψία του υλικού ή ως η αντίστασή του στην ελαστική παραμόρφωση. Όσο μεγαλύτερο είναι το μέτρο ελαστικότητας, τόσο πιο δύσκαμπτο είναι το υλικό και συνεπώς για δεδομένη τάση παρουσιάζει μικρότερη ελαστική παραμόρφωση. Επειδή η παραμόρφωση είναι αδιάστατο μέγεθος, το μέτρο ελαστικότητας έχει μονάδες τάσης. Συνήθως εκφράζεται σε GPa=109 Pa. Συνήθως, για τα μεταλλικά υλικά και τα κεραμικά η μέγιστη ελαστική παραμόρφωση είναι μικρότερη από 0.1%. Το καουτσούκ και άλλα ελαστομερή δεν εμφανίζουν γραμμική ελαστική συμπεριφορά. Για αυτά τα υλικά η επί τοις εκατό ελαστική παραμόρφωση μπορεί να είναι μερικές εκατοντάδες. Το μέτρο ελαστικότητας για τα περισσότερα μέταλλα κυμαίνεται από 45 MPa για το μαγνήσιο έως 407 MPa για το βολφράμιο. Όταν η μετάβαση από την ελαστική στην πλαστική συμπεριφορά, είναι σταδιακή, τότε ως σημείο μετάβασης μπορεί να ορισθεί το σημείο απόκλισης της καμπύλης τάσηςπαραμόρφωσης από την γραμμικότητα. Το σημείο αυτό αποκαλείται πολλές φορές όριο αναλογίας. Επειδή σε πολλές περιπτώσεις, όπως π.χ. για τα κράματα του αλουμινίου, το σημείο που αρχίζει το φαινόμενο της διαρροής, δεν μπορεί να οριστεί με ακρίβεια, έχει οριστεί μια σύμβαση σύμφωνα με την οποία φέρεται μια ευθεία παράλληλη με το ελαστικό τμήμα της καμπύλης τάσης-παραμόρφωσης για συγκεκριμένο βαθμό παραμόρφωσης, συνήθως 0.2%. Η τάση που αντιστοιχεί στο σημείο τομής, αυτής της γραμμής και της καμπύλης, ορίζεται ως συμβατικό όριο διαρροής. Συγκεντρωτικά, παρουσιάζονται παρακάτω τα μεγέθη που φαίνονται στο Σχήμα 6.3. σy : όριο διαρροής. Είναι η τάση πάνω από την οποία το υλικό παρουσιάζει πλαστική παραμόρφωση. Ο νόμος του Hooke δεν είναι έγκυρος πέρα από αυτό το σημείο, το οποίο ονομάζεται σημείο διαρροής. σts : μέγιστη αντοχή σε εφελκυσμό. Είναι η μέγιστη τάση στο διάγραμμα τάσηςπαραμόρφωσης, η οποία στη συνέχεια μειώνεται καθώς αρχίζει να εμφανίζεται ο λαιμός, εf : παραμόρφωση θραύσης. Είναι η παραμόρφωση που εμφανίζεται μετά τη θραύση του υλικού. E : το μέτρο ελαστικότητας. Κλίση της ευθείας. Αποτελεί μέτρο της στιβαρότητας ή αλλιώς της δυσκαμψίας του υλικού. Σε χάλυβες με μικρό ποσοστό άνθρακα καθώς και σε άλλα υλικά εμφανίζεται διπλό όριο διαρροής (Σχήμα 6.4). Η πλαστική παραμόρφωση του υλικού αρχίζει σε ένα σημείο που καλείται άνω σημείο διαρροής και αμέσως μετά η τάση πέφτει σε ένα σημείο που αποκαλείται κάτω σημείο διαρροής. 56
58 Σχήμα 6.4: Αντιπροσωπευτικό διάγραμμα τάσης παραμόρφωσης για αρκετούς χάλυβες με εμφάνιση ανώτερου και κατώτερου σημείου διαρροής. Τα μεγέθη της τάσης και της παραμόρφωσης που αναφέρθηκαν προηγουμένως υπολογίστηκαν βάση της αρχικής διατομής και του αρχικού μήκους του δοκιμίου. Τα μεγέθη αυτά καλούνται ονομαστικά. Εάν όμως για τους υπολογισμούς χρησιμοποιηθούν το πραγματικό εμβαδό και η πραγματική παραμόρφωση σε κάθε χρονική στιγμή, τότε υπολογίζονται η πραγματική τάση και παραμόρφωση. Για τις περισσότερες μηχανικές κατασκευές η πιο σημαντική ιδιότητα είναι η αντοχή σε διαρροή και όχι η μέγιστη αντοχή σε εφελκυσμό, επειδή μόλις αυτή η τάση ξεπεραστεί η κατασκευή αρχίζει να παραμορφώνεται πλαστικά πέρα από αποδεκτά όρια. Το μέγεθος της αντοχής διαρροής ενός μετάλλου εκφράζει την αντίσταση του υλικού στην πλαστική παραμόρφωση. Στις περισσότερες κατασκευές μόνο η ελαστική παραμόρφωση είναι αποδεκτή. Εκτός της αντοχής σε διαρροή, άλλες μηχανικές ιδιότητες όπως η ολκιμότητα, η πλαστησιμότητα, η ταχύτητα με την οποία το υλικό εργοσκληρύνεται είναι ιδιαίτερα σημαντικές κατά τις διάφορες διεργασίες μορφοποίησης των μετάλλων, όπως η έλαση, ή ολκή, η τύπωση, η σφυρηλάτηση, κλπ. Ένα υλικό που παρουσιάζει πολύ λίγη ή και μηδενική πλαστική παραμόρφωση πριν την θραύση του καλείται ψαθυρό. Τυπικά ψαθυρά υλικά είναι το γυαλί και τα κεραμικά υλικά. Τα μέταλλα συνήθως παρουσιάζουν πλαστική παραμόρφωση, ενώ τα περισσότερα πολυμερή παρουσιάζουν πολύ μεγαλύτερη πλαστική παραμόρφωση πριν την θραύση τους. Η ολκιμότητα ενός υλικού αποτελεί μέτρο της πλαστικής παραμόρφωσης που υφίσταται ένα υλικό πριν την θραύση του. Η ολκιμότητα είναι έννοια αντίθετη της ψαθυρότητας. Εκφράζεται ποσοτικά είτε ως το επί τοις εκατό ποσοστό μέγιστης επιμήκυνσης, εmax, είτε επί τοις εκατό ποσοστό μείωσης της επιφάνειας. % EL = ε max 100% % AR = ( A0 A f ) / A0 100% όπου Α0 το αρχικό εμβαδό της διατομής και Αf το εμβαδό της διατομής στο σημείο θραύσης. Ανάλογα με το βαθμό πλαστικής παραμόρφωσης που λαμβάνει χώρα πριν την θραύση διακρίνονται δυο βασικά είδη θραύσης: η όλκιμη και η ψαθυρή θραύση. Μακροσκοπική παρατήρηση των επιφανειών θραύσης δίνει πληροφορίες για το είδος 57
59 της θραύσης. Στην περίπτωση της όλκιμης θραύσης υπάρχει στένωση της διατομής του δοκιμίου, λόγω πλαστικής παραμόρφωσης, ενώ στην περίπτωση της ψαθυρής θραύσης, η μείωση της διατομής είναι αμελητέα ή μηδενική. Στο σχήμα 6.5 παρουσιάζονται οι επιφάνειες θραύσης ενός όλκιμου και ενός ψαθυρού υλικού. Σχήμα 6.5: α) Όλκιμη θραύση μαλακού χάλυβα β) ψαθυρή θραύση φαιού (γκρίζου) χυτοσιδήρου. Το εμβαδόν της περιοχής κάτω από την καμπύλη τάσης - παραμόρφωσης αντιπροσωπεύει την ενέργεια ανά μονάδα όγκου που μπορεί να απορροφηθεί από το υλικό πριν σπάσει και αποτελεί ένα μέτρο της δυσθραυστότητας του υλικού. Το εμβαδόν της περιοχής κάτω από την καμπύλη τάσης - παραμόρφωσης στην ελαστική περιοχή αντιπροσωπεύει την ελαστική ενέργεια ανά μονάδα όγκου που αποθηκεύεται στο υλικό και καλείται ελαστικότητα. Στον Πίνακα 6.1 παρουσιάζονται μερικές χαρακτηριστικές μηχανικές ιδιότητες, όπως η αντοχή σε διαρροή, η αντοχή σε εφελκυσμό και η ολκιμότητα διάφορων μετάλλων και κραμάτων. Πίνακας 6.1: Αντοχή διαρροής, μέγιστη αντοχή σε εφελκυσμό και ολκιμότητα, μετρημένα σε θερμοκρασία δωματίου, κοινών μετάλλων και κραμάτων. Υλικό Αντοχή διαρροής, Αντοχή σε εφελκυσμό, Ολκιμότητα, % EL MPa MPa (L0=50mm) Αλουμίνιο Χαλκός Ορείχαλκος (70Cu- 30Zn) Σίδηρος Νικέλιο Χάλυβας (1020) Τιτάνιο Μολυβδαίνιο
60 6.3 ΔΟΚΙΜΗ ΘΛΙΨΗΣ Η δοκιμή θλίψης διεξάγεται με παρόμοιο τρόπο με τη δοκιμή εφελκυσμού, με τη διαφορά ότι η εφαρμοζόμενη δύναμη δεν επιμηκύνει, αλλά μειώνει το μήκος του δοκιμίου στην διεύθυνση της εφαρμογής της (Σχήμα 6.6). Τόσο η τάση, όσο και η παραμόρφωση του δοκιμίου υπολογίζονται με τις ίδιες εξισώσεις, όπως και στη δοκιμή εφελκυσμού. Οι θλιπτικές δυνάμεις λαμβάνονται ως αρνητικές, ενώ η παραμόρφωση είναι επίσης αρνητική, λόγω συστολής του δοκιμίου (l> l0). Τα υλικά γενικά εμφανίζουν υψηλότερη αντοχή στην θλίψη από ότι στον εφελκυσμό. Αυτό οφείλεται στο γεγονός ότι στα υλικά υπάρχουν ρωγμές, πόροι και άλλες ατέλειες, που τείνουν να διαδοθούν κάτω από την επίδραση εφελκυστικών δυνάμεων και να οδηγήσουν σε θραύση το υλικό, πριν την υλοποίηση της θεωρητικά υπολογιζόμενης αντοχή τους. Σχήμα 6.6: Σχηματική αναπαράσταση θλιπτικής παραμόρφωσης. Τα ψαθυρά υλικά αν και έχουν μικρή αντοχή στον εφελκυσμό, τα ίδια υλικά παρουσιάζουν υψηλή αντοχή στη θλίψη. Αυτά τα υλικά χρησιμοποιούνται σε εφαρμογές για την παραλαβή υψηλών συμπιεστικών τάσεων. Δυο τυπικά ψαθυρά υλικά είναι ο γκρίζος χυτοσίδηρος και το τσιμέντο. Μερικά όλκιμα μέταλλα δεν σπάζουν κατά την δοκιμή θλίψης. 6.4 ΔΟΚΙΜΗ ΚΑΜΨΗΣ Στο Σχήμα 6.7 απεικονίζεται η διάταξη για την εκτέλεση της δοκιμής κάμψης τριών σημείων. Ένα φορτίο εφαρμόζεται στο κέντρο του δοκιμίου. Το επάνω τμήμα του δοκιμίου βρίσκεται σε κατάσταση θλίψης, ενώ το κάτω τμήμα σε κατάσταση εφελκυσμού. Οι τάσεις που αναπτύσσονται λαμβάνουν τη μέγιστη τιμή τους στις εξωτερικές επιφάνειες. Η κατανομή τάσεων κατά μήκος της διατομής ακολουθεί το τριγωνικό σχέδιο, λαμβάνοντας την τιμή μηδέν στον ουδέτερο άξονα. Η μέγιστη τάση που αναπτύσσεται σε ένα δοκίμιο τετραγωνικής διατομής δίνεται από τη σχέση: σ max = 3 FL 2 bh 2 όπου F είναι το εφαρμοζόμενο φορτίο στο κέντρο του δοκιμίου, L η απόσταση μεταξύ των σημείων στήριξης, b το πλάτος του δοκιμίου και h το ύψος του δοκιμίου. 59
61 Σχήμα 6.7: Αναπαράσταση δοκιμής κάμψης τριών σημείων και διάταξη δοκιμών κάμψης. 6.5 ΔΟΚΙΜΕΣ ΔΙΑΤΜΗΣΗΣ ΚΑΙ ΣΤΡΕΨΗΣ Διατμητική τάση είναι η τάση που αναπτύσσεται από την ολίσθηση ενός τμήματος του υλικού σε σχέση με το άλλο τμήμα. Προκαλείται όταν ένα ζεύγος αντίθετων δυνάμεων εφαρμόζεται κατά μήκος παράλληλων διευθύνσεων σε ένα υλικό (Σχήμα 6.8α). Η διατμητική τάση τ δίνεται από τη σχέση: τ = F A0 όπου F είναι το φορτίο ή η δύναμη που εφαρμόζεται στην ανώτερη και κατώτερη πλευρά ενός σώματος, εμβαδού Α0. Η παραμόρφωση γ ορίζεται ως η εφαπτομένη της γωνίας θ. γ = tan θ Η διατμητική τάση και παραμόρφωση έχουν τις ίδιες μονάδες όπως και τα αντίστοιχα μεγέθη του εφελκυσμού. Ένα παράδειγμα διάτμησης είναι το ψαλίδισμα των λαμαρινών ή η κοπή ενός χαρτιού με το ψαλίδι. (α) (β) Σχήμα 6.8: Σχηματική αναπαράσταση α) διατμητικής παραμόρφωσης, γ = tan θ στρεπτικής παραμόρφωσης. 60 και β)
62 Η στρέψη είναι μια παραλλαγή της διάτμησης, όπου ένα δοκίμιο υποβάλλεται σε στρέψη όπως φαίνεται στο Σχήμα 6.8β. Η διατμητική τάση τ είναι συνάρτηση της εφαρμοζόμενης ροπής Τ και η παραμόρφωση γ σχετίζεται με τη γωνία στρέψης φ. Στρεπτικές δυνάμεις αναπτύσσονται στους άξονες των μηχανών, στους άξονες μεταφοράς κίνησης καθώς και στα ελικοειδή τρυπάνια. Στο Σχήμα 6.9 απεικονίζεται μια μηχανή δοκιμών στρέψης. Η μια κεφαλή είναι σταθερή, ενώ ή άλλη μπορεί να περιστρέφεται. Με αυτό τον τρόπο παράγεται μια περιστροφική κίνηση γύρω από τον διαμήκη άξονα του ενός άκρου του δοκιμίου ως προς το άλλο. Σχήμα 6.9: α) Μηχανή δοκιμών στρέψης, β) Δοκιμή λάμας σε στρέψη, min ροπή (90 περιστροφή) 95 lbs.in ή 10,81 N.m. Σκληρότητα λάμας HRC (Rockwell C). Στην περιοχή της ελαστικής παραμόρφωσης η διατμητική τάση τ και η παραμόρφωση γ συνδέονται με τη σχέση (νόμος του Hooke): τ = Gγ όπου G είναι το μέτρο διάτμησης. Για τα ισότροπα υλικά, το μέτρο ελαστικότητας Ε και το μέτρο διάτμησης G σχετίζονται μεταξύ τους με τη σχέση: E = 2G (1 + ν ) όπου ν είναι ο λόγος Poisson. Ο λόγος Poisson ορίζεται ως εξής: Όταν ένα δοκίμιο υποβάλλεται σε εφελκυσμό τότε κατά την διεύθυνση της εφαρμοζόμενης τάσης παρατηρείται επιμήκυνση. Αποτέλεσμα της επιμήκυνσης στην αξονική διεύθυνση, είναι η συρρίκνωση στις πλάγιες διευθύνσεις, κάθετα στην εφαρμοζόμενη τάση. Ο λόγος της πλευρικής και αξονικής παραμόρφωσης, υπό την προϋπόθεση ότι οι παραμορφώσεις είναι ελαστικές, ονομάζεται λόγος Poisson και ορίζεται από τη σχέση: ν = ε π λ ευ ρ ικ ή ε α ξ ο ν ικ ή Το αρνητικό πρόσημο τοποθετείται γιατί η αξονική και η πλευρική παραμόρφωση έχουν πάντοτε αντίθετα πρόσημα, έτσι ώστε το ν να είναι πάντοτε θετικό. 61
63 Ο συντελεστής ν παίρνει τιμές από 0.25 έως Για τα περισσότερα μέταλλα η τιμή του κυμαίνεται από 0.25 έως Στον Πίνακα 6.2 παρουσιάζονται τιμές του μέτρου ελαστικότητας, του μέτρου διάτμησης και του λόγου Poisson για μερικά κοινά μέταλλα και κράματα. Πίνακας 6.2: Μέτρο ελαστικότητας, μέτρο διάτμησης και λόγος Poisson, μετρημένα σε θερμοκρασία δωματίου, για κοινά μέταλλα και κράματα. Μέτρο Μέτρο Λόγος Υλικό ελαστικότητας (Ε), Διάτμησης (G), Poisson (ν) GPa GPa Αλουμίνιο Ορείχαλκος Χαλκός Μαγνήσιο Νικέλιο Χάλυβας Τιτάνιο Βολφράμιο ΔΟΚΙΜΗ ΚΡΟΥΣΗΣ Η ΔΥΣΘΡΑΥΣΤΟΤΗΤΑΣ Μια από τις κυριότερες μηχανικές ιδιότητες των υλικών είναι η δυσθραυστότητα, η οποία εκφράζει την ικανότητα του υλικού να απορροφά ενέργεια πριν τη θραύση του. Αποτελεί ένα μέτρο της αντίστασης του υλικού στη διάδοση των ρωγμών. Τα όλκιμα υλικά έχουν υψηλή δυσθραυστότητα, ενώ τα ψαθυρά χαμηλή. Όπως ήδη αναφέρθηκε το εμβαδόν της περιοχής κάτω από την καμπύλη εφελκυσμού αντιπροσωπεύει την ενέργεια ανά μονάδα όγκου που μπορεί να απορροφηθεί από το υλικό πριν σπάσει και αποτελεί ένα μέτρο της δυσθραυστότητάς του. Ωστόσο, στην πράξη διάφορα μέρη μηχανών και κατασκευών υφίστανται σύνθετες δυναμικές φορτίσεις, ενώ η ταχύτητα φόρτισης κατά τη δοκιμή εφελκυσμού είναι μικρή. Έτσι η δυσθραυστότητα των υλικών προσδιορίζεται με τη δοκιμή σε κρούση (στιγμιαία φόρτιση). Κατά τη δοκιμή σε κρούση χρησιμοποιούνται τυποποιημένα δοκίμια τα οποία στη μια πλευρά τους έχουν εγκοπή. Η συγκέντρωση τάσεων στην κορυφή της εγκοπής βοηθάει στη θραύση του υλικού. Υπάρχουν δυο μέθοδοι μέτρησης της δυσθραυστότητας ενός υλικού: η μέθοδος Charpy και η μέθοδος Izod. Η μέθοδος Charpy είναι η συνηθέστερη, ενώ η μέθοδος Izod χρησιμοποιείται για τη μέτρηση της δυσθραυστότητας μη μεταλλικών υλικών, π.χ. πολυμερών. Στο Σχήμα 6.10 απεικονίζεται μια τυπική συσκευή δοκιμής σε κρούση. Το δοκίμιο στερεώνεται σε κατάλληλο υποστήριγμα στη βάση της μηχανής και δέχεται κτύπημα από το αιωρούμενο εκκρεμές, καθώς αυτό περνάει από το χαμηλότερο σημείο της τροχιάς του, πριν συνεχίσει την κίνησή του προς τα πάνω. Η ενέργεια που απορροφάται κατά τη θραύση του δοκιμίου μπορεί να υπολογισθεί από τη μάζα του εκκρεμούς και τη διαφορά ύψους ανάμεσα στην αρχική και τελική θέση της διαδρομής του. 62
64 Σχήμα 6.10: Σχηματική αναπαράσταση συσκευής δοκιμών σε κρούση. Στο Σχήμα 6.11 παρουσιάζεται η γεωμετρία και ο τρόπος στήριξης των δοκιμίων στις δοκιμές Charpy και Izod. (α) (β) Σχήμα 6.11: Γεωμετρία και στήριξη δοκιμίων για τις δοκιμές α) Charpy και β) Izod. Γενικά, σε χαμηλές θερμοκρασίες η θραύση των μετάλλων πραγματοποιείται με ψαθυρό τρόπο και μικρή απορρόφηση ενέργειας, ενώ σε υψηλές με όλκιμο τρόπο και υψηλότερη απορρόφηση ενέργειας. Γι αυτό το λόγο η δοκιμή κρούσης συχνά χρησιμοποιείται για να προσδιοριστεί η θερμοκρασία μετάβασης από την όλκιμη στη ψαθυρή συμπεριφορά ενός μεταλλικού υλικού. Στα μέταλλα που κρυσταλλώνονται στο χωροκεντρωμένο κυβικό σύστημα (BCC), π.χ. οι χάλυβες, η μετάβαση είναι εμφανής, ενώ 63
65 στα μέταλλα που κρυσταλλώνονται στο εδροκεντρωμένο κυβικό σύστημα (FCC), π.χ. τα κράματα αλουμινίου η μετάβαση συμβαίνει βαθμιαία. Η μετάβαση από την όλκιμη στη ψαθυρή συμπεριφορά εξηγείται με βάση τη θεωρία των διαταραχών. Σε υψηλές θερμοκρασίες η κίνηση των διαταραχών είναι δυνατή, επιτρέποντας την πλαστική παραμόρφωση του υλικού, οδηγώντας σε όλκιμη θραύση, ενώ αντίθετα σε χαμηλές θερμοκρασίες κάποια συστήματα ολίσθησης αδρανοποιούνται, οδηγώντας σε ψαθυρή θραύση. Στο Σχήμα 6.12 παρουσιάζεται η επίδραση της περιεκτικότητας σε άνθρακα στις καμπύλες μετάβασης ανοπτημένων χαλύβων. Σχήμα 6.12: Επίδραση της περιεκτικότητας σε άνθρακα στη θερμοκρασία μετάβασης από την όλκιμη στη ψαθυρή συμπεριφορά ανοπτημένων χαλύβων. 6.7 ΔΟΚΙΜΗ ΣΚΛΗΡΟΤΗΤΑΣ Μια ακόμη σημαντική μηχανική ιδιότητα των υλικών είναι η σκληρότητα. Αποτελεί μέτρο της αντίστασης του υλικού στη διείσδυση ενός άλλου σώματος μεγαλύτερης σκληρότητας. Με άλλα λόγια, εκφράζει την αντίσταση του υλικού σε περιορισμένη πλαστική παραμόρφωση, π.χ. μικρό κοίλωμα ή χαραγή. Οι πρώτες μετρήσεις σκληρότητας στηρίχτηκαν σε φυσικά ορυκτά. Ο Mohs πρότεινε μια κλίμακα σκληρότητας, με βάση την ικανότητα ενός υλικού να χαράζει κάποιο άλλο μαλακότερο. Σε αυτή την κλίμακα οι τιμές κυμαίνονται από 1 για τον μαλακό τάλκη έως το 10 για το διαμάντι. Όμως με την πάροδο των χρόνων αναπτύχθηκαν οι σύγχρονες τεχνικές μέτρησης της σκληρότητας. Συνήθως, στις δοκιμές σκληρότητας μια σταθερή δύναμη εφαρμόζεται με ελεγχόμενο ρυθμό σε ένα διεισδυτή, που πιέζεται κάθετα στην επιφάνεια του υλικού. Η επιφάνεια ή το βάθος του προκαλούμενου αποτυπώματος σχετίζεται με έναν αριθμό σκληρότητας. Όσο πιο μαλακό είναι το υλικό τόσο πιο μεγάλο και βαθύ είναι το αποτύπωμα και πιο μικρή είναι η σκληρότητα. Οι δοκιμές σκληρότητας αποτελούν την πιο απλή και οικονομική μέθοδο ποιοτικού ελέγχου των υλικών. Κατά τη δοκιμή δεν υπάρχει θραύση του δοκιμίου, παρά μόνο ένα μικρό αποτύπωμα και πρακτικά η δοκιμή μπορεί να χαρακτηριστεί ως μη καταστρεπτική. Η διεξαγωγή της είναι εύκολη, όπως επίσης εύκολη είναι και η αξιολόγηση των παραγόμενων αποτελεσμάτων. Η δοκιμές σκληρότητας χρησιμοποιούνται ευρέως για τον ποιοτικό έλεγχο ανταλλακτικών, εργαλείων καθώς και προϊόντων που υφίστανται θερμική επεξεργασία. Από τα αποτελέσματα της σκληρότητας μπορεί ακόμη προσεγγιστικά να προσδιοριστεί η αντοχή σε εφελκυσμό του υλικού. Επιπλέον, το ανακάτεμα διαφορετικών υλικών μπορεί να αναγνωριστεί με μετρήσεις σκληρότητας. 64
66 Για τη μέτρηση της σκληρότητας έχουν αναπτυχθεί διάφορες τεχνικές. Διαφοροποιούνται με βάση το υλικό και τη γεωμετρία του διεισδυτή, το φορτίο που εφαρμόζεται καθώς και το γεωμετρικό χαρακτηριστικό του αποτυπώματος που μετρείται. Στον Πίνακα 6.3 παρουσιάζονται τα χαρακτηριστικά των κυριότερων μεθόδων μέτρησης της σκληρότητας: Brinell, Vickers, Rockwell C και B και Knoop. Πίνακας 6.3: Σύγκριση των κυριότερων μεθόδων μέτρησης της σκληρότητας ΔΟΚΙΜΗ ΣΚΛΗΡΟΤΗΤΑΣ BRINELL Στην μέθοδο αυτή ο διεισδυτής είναι σφαίρα από σκληρυμένο χάλυβα ή καρβίδιο του βολφραμίου (WC), με διάμετρο (D) 5 ή 10 mm. Η σφαίρα πιέζεται στην επιφάνεια του υλικού με φορτίο (F) που κυμαίνεται μεταξύ 500 και 3000 Kg. Κατά τη διάρκεια της δοκιμής το φορτίο διατηρείται σταθερό για καθορισμένο χρόνο 10 μέχρι 30 s. Η τιμή της σκληρότητας υπολογίζεται από το πηλίκο της δύναμης F προς την επιφάνεια του αποτυπώματος (Πίνακας 6.3). Η διάμετρος του αποτυπώματος D μετρείται με μικροσκόπιο μικρής μεγεθυντικής ισχύος. Η σκληρότητα κατά Brinell, HB, μετρούμενη σε Kg/mm2, δίνεται από τη σχέση: HB = [ 2F πdd 65 (D 2 d2 )]
67 Στην πράξη η τιμή της σκληρότητας υπολογίζεται από πίνακες χρησιμοποιώντας τη μετρούμενη διάμετρο του αποτυπώματος και το εφαρμοζόμενο φορτίο. Η δοκιμή σκληρότητας Brinell, λόγω του κινδύνου πλαστικής παραμόρφωσης του διεισδυτή, χρησιμοποιείται μόνο για μαλακά και μέτριας σκληρότητας υλικά (HB 450). Επειδή στη μέθοδο Brinell χρησιμοποιούνται μεγάλα φορτία και σφαίρες, η μέθοδος αυτή είναι λιγότερο ευαίσθητη σε επιφανειακές ατέλειες και είναι ιδιαίτερα κατάλληλη για ημιέτοιμα προϊόντα καθώς και για χυτά. Συνήθως χρησιμοποιείται για τη μέτρηση της σκληρότητας υλικών όπως: χάλυβες, γκρίζοι χυτοσίδηροι, μη σιδηρούχα μέταλλα, αλουμίνιο που έχει υποστεί γήρανση και πολύ μαλακά υλικά. Το φορτίο F και η διάμετρος του διεισδυτή D πρέπει να επιλέγεται με τέτοιο τρόπο, έτσι ώστε ο διεισδυτής να μην βυθίζεται μέσα στο υλικό και να σχηματίζεται αποτύπωμα σαφών ορίων. Για την ορθή μέτρηση της σκληρότητας είναι απαραίτητο να ισχύει η σχέση: 0.2D<d<0.7D Μια άλλη απαίτηση της δοκιμής Brinell είναι ο συνδυασμός φορτίου-διαμέτρου διεισδυτή να γίνεται με τέτοιο τρόπο, έτσι ώστε ο λόγος F/D2, να παίρνει ορισμένες τιμές σε ορισμένες περιοχές σκληρότητας. Συνήθως χρησιμοποιούνται σφαίρες διαμέτρων 1, 2,5, 5 και 10 mm και φορτία 50, 125, 250, 500, 1000 και 3000 Kg. Ακόμη μπορεί να χρησιμοποιηθούν μικρότερα φορτία καθώς και σφαίρες μικρότερης διαμέτρου. Για την ορθή μέτρηση της σκληρότητας είναι απαραίτητο να τηρούνται ορισμένες απαιτήσεις σχετικά με το πάχος του δοκιμίου, την απόσταση μεταξύ δυο διαδοχικών αποτυπώσεων καθώς και την απόσταση από τις άκρες του δοκιμίου. Έχει βρεθεί ότι το πάχος του δοκιμίου πρέπει να είναι τουλάχιστον δεκαπλάσιο του βάθους διείσδυσης, ενώ η απόσταση μεταξύ διαδοχικών μετρήσεων ή μεταξύ μέτρησης και άκρων πρέπει να είναι τουλάχιστον τρεις φορές της διαμέτρου του αρχικού αποτυπώματος. Επιπλέον, η ακρίβεια της μεθόδου εξαρτάται από τον σχηματισμό καλού, με σαφή όρια, αποτυπώματος. Αυτό κάνει αναγκαία την ύπαρξη επίπεδης και λείας επιφάνειας ΔΟΚΙΜΗΣΚΛΗΡΟΤΗΤΑΣ VICKERS Στη μέθοδο Vickers, όπως και στη μέθοδο Brinell, η σκληρότητα ενός υλικού μετρείται σύμφωνα με τη σχέση του εφαρμοζόμενου φορτίου και της επιφάνειας του σχηματιζόμενου αποτυπώματος (Πίνακας 6.3). Ο διεισδυτής είναι μια αδαμάντινη πυραμίδα με τετραγωνική βάση και γωνία κορυφής 136. Το προκαλούμενο αποτύπωμα είναι τετράγωνο. Με τη χρήση μικροσκοπικής διάταξης μετρείται το μέσο μήκος των δυο διαγώνιων του αποτυπώματος (d = d1+d2/2). Η σκληρότητα Vickers, HV, μετρούμενη σε Kg/mm2, δίνεται από τη σχέση: HV = 1854 F d2 όπου F είναι το εφαρμοζόμενο φορτίο και d η μέση τιμή των δυο διαγώνιων του αποτυπώματος. Στην πράξη, η τιμή της σκληρότητας, που αντιστοιχεί στη μετρούμενη διαγώνιο του αποτυπώματος, διαβάζεται από τον κατάλληλο πίνακα. Η δοκιμή Vickers μπορεί να χαρακτηριστεί ως η πιο ακριβής μέθοδος μέτρησης της σκληρότητας και πρακτικά μπορεί να χρησιμοποιηθεί για τη μέτρηση της σκληρότητας όλων των υλικών, καθώς επίσης και πολύ λεπτών ή επιφανειακά σκληρυμένων εξαρτημάτων. 66
68 Οι τιμές Brinell καιvickers σχεδόν συμπίπτουν μέχρι την τιμή 400, ωστόσο για μεγαλύτερες τιμές ακριβέστερη είναι η μέθοδος Vickers ΔΟΚΙΜΗ ΣΚΛΗΡΟΤΗΤΑΣ ROCKWELL Στη μέθοδο Rockwell, σε αντίθεση με τη μέθοδο Brinell και Vickers, δεν μετρείται η διάμετρος ή η διαγώνιος του αποτυπώματος, αλλά το βάθος του z (Πίνακας 6.3). Το βάθος z προσδιορίζεται από τη διαφορά των βαθών που προκύπτουν από την εφαρμογή ενός αρχικού φορτίου f, βάθος κοιλότητας h1, και στη συνέχεια ενός μεγαλύτερου φορτίου F, βάθος κοιλότητας h2. Η χρήση προφόρτισης f αυξάνει την ακρίβεια της μεθόδου, γιατί με αυτόν τον τρόπο αποφεύγονται λάθη που οφείλονται σε ανωμαλίες της επιφάνειας του δοκιμίου. Επειδή το αποτέλεσμα της σκληρομέτρησης διαβάζεται στην οθόνη της συσκευής, η δοκιμή Rockwell εκτελείται σχετικά γρήγορα και ενδείκνυται στις περιπτώσεις που απαιτείται μέτρηση μεγάλων ποσοτήτων υλικών. Για μετρήσεις σκληρότητας σκληρυμένων χαλύβδινων ανταλλακτικών, εργαλείων, καθώς και εξαρτημάτων με επιφανειακή σκλήρυνση, ο διεισδυτής είναι κώνος από διαμάντι με γωνία κορυφής 120 και σφαιρικό άκρο διαμέτρου 0.2mm. Για μετρήσεις μαλακών χαλύβων, χυτοσιδήρων, ορείχαλκο, μπρούντζου, κ.λ.π., ο διεισδυτής είναι σφαίρες από σκληρυμένο χάλυβα. Με βάση το μέγεθος της προφόρτισης και της κυρίας φόρτισης η μέθοδος διακρίνεται στη Rockwell και στην επιφανειακή Rockwell. Στη Rockwell η προφόρτιση είναι 10 Kg (98.07 N) και η φόρτιση 60, 100 ή 150 Kg (588.4 Ν, 80,7 ή 1471 Ν). Μια μονάδα σκληρότητας Rockwell αντιστοιχεί σε διείσδυση mm. Στην επιφανειακή Rockwell η προφόρτιση είναι 3 Kg (29.42 N) και η φόρτιση 15, 30 ή 45 Kg (147.1 Ν, ή Ν). Μια μονάδα σκληρότητας επιφανειακής Rockwell αντιστοιχεί σε διείσδυση mm. Η μέθοδος Rockwell διακρίνεται σε διάφορες κλίμακες. Κάθε κλίμακα συμβολίζεται με ένα γράμμα, όπως Β ή C, το οποίο υποδεικνύει τόσο το φορτίο, όσο και τον διεισδυτή που χρησιμοποιείται. Στη επιφανειακή Rockwell οι διάφορες κλίμακες αναγνωρίζονται από τους αριθμούς 15, 30, 45 (φορτίο) ακολουθούμενοι από γράμματα, όπως Ν, Τ, κλπ. ανάλογα με το διεισδυτή. Στους Πίνακες 6.4 και 6.5 παρουσιάζονται μερικές κλίμακες σκληρότητας Rockwell καθώς και της επιφανειακής Rockwell. Πίνακας 6.4: Κλίμακες σκληρότητας Rockwell. Κλίμακα Rockwell B C A D E F G H K Διεισδυτής Μέγιστο φορτίο, Kg 1/16 in σφαίρα 120 διαμάντι 120 διαμάντι 120 διαμάντι 1/8 in σφαίρα 1/16 in σφαίρα 1/16 in σφαίρα 1/8 in σφαίρα 1/8 in σφαίρα Μικρότερο φορτίο, Kg
69 Πίνακας 6.5: Κλίμακες σκληρότητας επιφανειακής Rockwell. Κλίμακα Rockwell 15Ν 30Ν 45Ν 15Τ 30Τ 45Τ Διεισδυτής Μέγιστο φορτίο, Kg 120 διαμάντι 120 διαμάντι 120 διαμάντι 1/16 in σφαίρα 1/16 in σφαίρα 1/16 in σφαίρα Μικρότερο φορτίο, Kg Στο Σχήμα 6.13 παρουσιάζεται μια μηχανή δοκιμής σκληρότητας Rockwell. Σχήμα 6.13: Μηχανή δοκιμής σκληρότητας Rockwell ΔΟΚΙΜΕΣ ΜΙΚΡΟΣΚΛΗΡΟΤΗΤΑΣ VICKERS ΚΑΙ KNOOP Αν το αποτύπωμα της δοκιμής σκληρότητας πρέπει να είναι πολύ μικρό, τότε οι μετρήσεις γίνονται με την εφαρμογή μικρών φορτίων που κυμαίνονται μεταξύ 1 και 1000 gr. Επειδή τα εφαρμοζόμενα φορτία και τα σχηματιζόμενα αποτυπώματα είναι πολύ μικρά, αυτές οι μετρήσεις αποκαλούνται μικροσκληρομετρήσεις. Δυο δοκιμές χρησιμοποιούνται για τη μέτρηση της μικροσκληρότητας: οι Vickers (HV) και Knoop (HK) (Πίνακας 6.3). Και στις δυο τεχνικές ο διεισδυτής είναι μια διαμαντένια πυραμίδα, με διαφορετική όμως βάση: τετραγωνική στην μέθοδο Vickers και ρόμβος στη μέθοδο Knoop. Οι μετρήσεις με την εφαρμογή μικρών δυνάμεων χρησιμοποιούνται για τη μέτρηση της σκληρότητας πολύ λεπτών στιβάδων καθώς και σε έτοιμα αντικείμενα. Ακόμη μπορεί να μελετηθεί η σκληρότητα μιας πολύ μικρής περιοχής του υλικού ή ακόμη η σκληρότητα ενός κόκκου μερικών δεκάδων μικρομέτρων. Η μέτρηση των διαγώνιων του αποτυπώματος γίνεται με τη βοήθεια οπτικού μικροσκοπίου και στη συνέχεια η μέτρηση μετατρέπεται σε αριθμό σκληρότητας. Απαιτείται η ύπαρξη εξαιρετικά λείας επιφάνειας, που επιτυγχάνεται με λείανση και στίλβωση, έτσι ώστε να λαμβάνεται καλά οριζόμενο αποτύπωμα που να μπορεί να μετρηθεί με ακρίβεια. 68
70 6.7.5 ΣΥΣΧΕΤΙΣΗ ΣΚΛΗΡΟΤΗΤΑΣ ΚΑΙ ΑΝΤΟΧΗΣ ΕΦΕΛΚΥΣΜΟΥ Όπως ήδη αναφέρθηκε η δοκιμή σκληρότητας αποτελεί μια προσεγγιστική μέθοδο προσδιορισμού της αντοχής σε εφελκυσμό του υλικού. Σε μια πρώτη προσέγγιση, η σκληρότητα καθώς η αντοχή σε εφελκυσμό αποτελούν μεγέθη ανάλογα, γιατί και οι δύο ιδιότητες αποτελούν ένα μέτρο της αντίστασης του υλικού στην πλαστική παραμόρφωση. Η αντοχή σε εφελκυσμό και η σκληρότητα κατά Brinell συνδέονται με την παρακάτω σχέση: TS ( MPa) = k HB όπου k είναι ένας συντελεστής αναλογίας, που είναι διαφορετικός για κάθε υλικό. Παρακάτω δίνονται οι συντελεστές αναλογίας για ορισμένα κοινά υλικά: Υλικό Ανθρακούχοι χάλυβες Χάλυβες Cr-Ni Χαλκός, μπρούντζος Μπρούντζος, έλαση Μπρούντζος, χύτευση Κράμα Al-Cu-Mg Κράμα Al-Mg Κράμα Mg Αλουμίνιο, χύτευση Συντελεστής αναλογίας Στον Πίνακα 6.6 παρουσιάζονται δεδομένα σκληρότητας και αντοχής σε εφελκυσμό για τους χάλυβες. Επίσης δίνονται δεδομένα μετατροπής για τις δοκιμές σκληρότητας Brinell, Vickers, Rockwell B και C. 69
71 Πίνακας 6.6: Σύγκριση διαφορετικών μεθόδων σκληρότητας για χάλυβες. Brinell Vickers Rockwell σt HB HV B C /16 in N/mm
72 6.8 ΔΟΚΙΜΗ ΕΡΠΥΣΜΟΥ Η αργή και συνεχής παραμόρφωση ενός υλικού κάτω από την επίδραση ακόμη και μιας σταθερής τάσης, καλείται ερπυσμός. Σε θερμοκρασίες μικρότερες από περίπου το 1/3 της απόλυτης θερμοκρασίας τήξης του υλικού, το φαινόμενο του ερπυσμού είναι αμελητέο. Σε υψηλότερες όμως θερμοκρασίες το φαινόμενο του ερπυσμού γίνεται ιδιαίτερα σημαντικό. Για αυτό το λόγο η δοκιμή ερπυσμού θεωρείται δοκιμή υψηλών θερμοκρασιών. Σε πολλά μέταλλα που χρησιμοποιούνται σε εφαρμογές υψηλών θερμοκρασιών, όπως βραστήρες, τουρμπίνες, αντιδραστήρες, κάτω από ορισμένες συνθήκες το φαινόμενο του ερπυσμού μπορεί να εμφανιστεί ακόμη και για τάσεις μικρότερες από το όριο διαρροής τους. Οι λαμπτήρες πυρακτώσεως αποτελούν μια κοινή εφαρμογή, στην οποία εμφανίζεται το φαινόμενο του ερπυσμού. Το βολφράμιο που χρησιμοποιείται ως υλικό κατασκευής το νημάτων των λαμπτήρων έχει απόλυτο σημείο τήξεως, Τ m, 3680Κ. Η συνήθης θερμοκρασία λειτουργίας των λαμπτήρων είναι 2000Κ, η οποία είναι αρκετά υψηλή, με συνέπεια να καίγονται λόγω ερπυσμού. Η παραμόρφωση ενός υλικού κατά τον ερπυσμό είναι συνάρτηση τριών παραγόντων: της τάσης, του χρόνου και της θερμοκρασίας, ε = f (σ, t, T ). Στο Σχήμα 6.14 παρουσιάζεται μια τυπική καμπύλη ερπυσμού, η οποία είναι ένα διάγραμμα της επιμήκυνσης του δοκιμίου εφελκυσμού, σαν συνάρτηση του χρόνου, για μια ορισμένη θερμοκρασία και σταθερό φορτίο ή σταθερή πραγματική τάση. Σχήμα 6.14: Τυπική καμπύλη ερπυσμού για υψηλές θερμοκρασίες και μεγάλους χρόνους. Συνήθως σε μια καμπύλη ερπυσμού διακρίνονται τρία στάδια επιμήκυνσης: του πρωτογενούς, του δευτερογενούς και του τριτογενούς ερπυσμού. Η διεργασία ερπυσμού είναι το αποτέλεσμα της δράσης δυο αντίθετων μηχανισμών: του μηχανισμού της σκλήρυνσης λόγω της μηχανικής παραμόρφωσης ή εργοσκλήρυνσης και του μηχανισμού μείωσης της σκληρότητας μέσω διεργασιών αποκατάστασης. Η μετακίνηση ή αναρρίχηση διαταραχών στα σύνορα των κόκκων, η μετακίνηση οπών, κλπ. αποτελούν τέτοιες διεργασίες αποκατάστασης. Κατά το στάδιο του πρωτογενούς ερπυσμού η ταχύτητα εργοσκλήρυνσης είναι μεγαλύτερη από την ταχύτητα αποκατάστασης και για αυτό το λόγο η ταχύτητα ερπυσμού μειώνεται σε συνάρτηση με το χρόνο. Κατά το στάδιο του δευτερογενούς ερπυσμού η ταχύτητα εργοσκλήρυνσης είναι περίπου ίση με την ταχύτητα αποκατάστασης με συνέπεια η ταχύτητα ερπυσμού να είναι 71
73 περίπου σταθερή. Σε αυτό το στάδιο η κίνηση των διαταραχών αντισταθμίζει το φαινόμενο της σκλήρυνσης και έτσι το υλικό επιμηκύνεται με σταθερή ταχύτητα. Κατά το στάδιο του τριτογενούς ερπυσμού υπάρχει μια επιτάχυνση της παραμόρφωσης του υλικού μέχρις ότου επέλθει η τελική θραύση του. Η διαδοχική άφιξη των μετακινούμενων ή αναρριχούμενων διαταραχών στα περατωτικά όρια των κόκκων, προκαλεί τον σχηματισμό πόρων μεταξύ των κόκκων, με συνέπεια την αναντίστρεπτη ολίσθηση τους, η οποία με τη σειρά της οδηγεί στη θραύση του υλικού. Αύξηση της τάσης ερπυσμού έχει ως αποτέλεσμα την μεταφορά της καμπύλης ερπυσμού σε υψηλότερα επίπεδα (Σχήμα 6.15α), ενώ αύξηση της θερμοκρασίας προκαλεί αύξηση της ταχύτητας ερπυσμού, λόγω της επιτάχυνσης των διεργασιών αποκατάστασης (Σχήμα 6.15β). (α) (β) Σχήμα 6.15: Επίδραση της θερμοκρασίας και της τάσης στην καμπύλη ερπυσμού. 6.9 ΔΟΚΙΜΗ ΚΟΠΩΣΗΣ Κόπωση είναι η προοδευτική τοπική καταστροφή της δομής των υλικών, που εμφανίζεται, όταν αυτά υποβάλλονται σε κυκλικές τάσεις, για μεγάλο χρονικό διάστημα. Κάτω από αυτές τις συνθήκες το υλικό μπορεί να οδηγηθεί σε θραύση για τάσεις πολύ χαμηλότερες από την αντοχή σε εφελκυσμό (σts) ή ακόμη και από την αντοχή σε διαρροή (σy). Τα εξαρτήματα των μηχανών συχνά υφίστανται τέτοιου είδους καταπονήσεις. Αυτό ιδιαίτερα ισχύει για τους κοχλίες, τους άξονες και τις ατράκτους. Η θραύση λόγω κοπώσεως ή δυναμική θραύση αναγνωρίζεται από την τυπική εμφάνιση της επιφάνειας θραύσης του υλικού (Σχήμα 6.16). Αυτή περιλαμβάνει μια πρώτη ρωγμή, μια λεία περιοχή και μια περιοχή που παρουσιάζει πλαστική παραμόρφωση. Η αρχική ρωγμή συνήθως εμφανίζεται στην επιφάνεια του υλικού, σε κάποιο σημείο συγκέντρωσης τάσεων. Στη συνέχεια υπάρχει αργή επέκταση της ρωγμής, που αντιστοιχεί στο σχηματισμό της λείας επιφανείας. Όταν η ρωγμή αποκτήσει ένα κρίσιμο μήκος, η διατομή του υλικού δεν μπορεί να παραλάβει το εφαρμοζόμενο φορτίο, με συνέπεια την γρήγορη διάδοση της ρωγμής και την ξαφνική θραύση του υλικού. Το σχήμα μιας κατασκευής είναι ένας από τους κυριότερους παράγοντες που επηρεάζουν την διάρκεια ζωής της σε κόπωση. Τετράγωνες οπές ή οξείες γωνίες λειτουργούν ως σημεία συγκέντρωσης τάσεων, όπου μπορεί να σχηματιστεί ή πρώτη ρωγμή λόγω κόπωσης. Κυκλικές οπές, ομαλές μεταβολές των διατομών αποτελούν απαραίτητο όρο αύξησης της διάρκειας ζωής μιας κατασκευής. 72
74 Σχήμα 6.16: Επιφάνεια θραύσης περιστρεφόμενου χαλύβδινου άξονα από κόπωση. α) έναρξη ρωγμής (Α) β) λεία επιφάνεια (Β): αργή ανάπτυξη της ρωγμής γ) επιφάνεια με πλαστική παραμόρφωση: ξαφνική θραύση (Β) ΚΥΚΛΙΚΕΣ ΤΑΣΕΙΣ Σε μια δοκιμή κόπωσης η εφαρμοζόμενη τάση μπορεί να είναι αξονική (εφελκυσμός θλίψη), καμπτική ή στρεπτική. Στο Σχήμα 6.17 παρουσιάζονται οι τρεις δυνατοί τύποι κυμαινόμενης τάσης α) αναστρεφόμενη κυκλική τάση, κατά την οποία η μέγιστη εφελκυστική τάση σmax, είναι ίση με τη μέγιστη θλιπτική σmin. β) επαναλαμβανόμενη κυκλική τάση, κατά την οποία η σmax και η σmin δεν είναι ίσες. γ) τυχαίος κύκλος τάσης. Στο Σχήμα 6.17 παρουσιάζονται τα διάφορα χαρακτηριστικά μεγέθη των κυμαινόμενων κύκλων τάσης. Σχήμα 6.17: Τύποι φορτίου (α) αναστρεφόμενη κυκλική τάση, η μέγιστη εφελκυστική τάση σmax, είναι ίση με τη μέγιστη θλιπτική σmin. β) επαναλαμβανόμενη κυκλική τάση, η σmax και η σmin δεν είναι ίσες. γ) τυχαίος κύκλος τάσης. 73
75 Η μέση τάση σm ορίζεται ως η μέση τιμή της μέγιστης και της ελάχιστης τάσης: σ m σ = max +σ 2 min Το εύρος των τάσεων στ ορίζεται ως η διαφορά της μέγιστης και της ελάχιστης τάσης: σ = σ r max σ min Το πλάτος της τάσης σα ορίζεται ως το μισό του εύρους των τάσεων: σ α = σ r 2 = σ max σ 2 min Ο λόγος των τάσεως ορίζεται ως: R= σ σ min max Η ΚΑΜΠΥΛΗ S-N Όπως και με τις άλλες μηχανικές ιδιότητες, τα χαρακτηριστικά της κόπωσης προσδιορίζονται με την εκτέλεση δοκιμών κόπωσης. Στο Σχήμα 6.18 απεικονίζεται μια πειραματική διάταξη για την εκτέλεση μιας τυπικής δοκιμής κόπωσης. Σε αυτή τη δοκιμή το δοκίμιο περιστρέφεται γύρω από τον άξονά του και ταυτόχρονα φορτίζεται με δύναμη P. Το δοκίμιο υποβάλλεται σε περιστροφική κάμψη, δηλαδή φορτίζεται κυκλικά σε καθαρή κάμψη. Με την περιστροφή του δοκιμίου, η επιφάνεια του περνάει διαδοχικά από εφελκυσμό (σt) σε συμπίεση (σc). Σε κάθε στροφή υπάρχει ένας πλήρης κύκλος ημιτονοειδούς φόρτισης. Αυτό επαναλαμβάνεται χιλιάδες φορές το λεπτό, στροφές/min. Σχήμα 6.18: Σχηματική αναπαράσταση δοκιμής κόπωσης με περιστροφική κάμψη. Δοκιμές κόπωσης μπορεί ακόμη να διεξαχθούν με εναλλασσόμενη φόρτιση εφελκυσμού-θλίψης. 74
76 Στα πειράματα κόπωσης προσδιορίζεται ο αριθμός των κύκλων (Ν) που χρειάζονται έως τη θραύση του δοκιμίου, για κάθε τάση (σ). Τα δεδομένα απεικονίζονται σε καμπύλες της μορφής σ=f(logn) (Σχήμα 6.19). Μια τέτοια καμπύλη ονομάζεται καμπύλη S-N (StressNumber of cycles) ή καμπύλη του Wöhler. Ως S λαμβάνονται τα πλάτη της τάσης σα και Nf παριστάνει τον αριθμό των κύκλων που απαιτούνται για τη θραύση του δοκιμίου για δεδομένη τάση. Σχήμα 6.19: Καμπύλη S-N για κραματοχάλυβα 4140 (έπειτα από εξομάλυνση). Στην καμπύλη S-N διακρίνονται τρεις ζώνες: (α) Ζώνη ολιγοκυκλικής κόπωσης, σε αυτή τη ζώνη ο αριθμός των εναλλαγών φορτίου (κύκλων) έως τη θραύση του δοκιμίου είναι σχετικά μικρός, Νf<102. (β) Ζώνη περιορισμένης αντοχής, κατά την οποία ο αριθμός των κύκλων έως τη θραύση του δοκιμίου αυξάνει, καθώς η τάση μειώνεται, 102 <Νf<106. (γ) Ζώνη απεριόριστης αντοχής. Για πολλά υλικά, όπως χάλυβες, κράματα Ti, η καμπύλη από πτωτική γίνεται οριζόντια. Η τάση που αντιστοιχεί σε αυτή το τμήμα της καμπύλης ονομάζεται όριο αντοχής ή όριο κόπωσης. Όταν το δοκίμιο φορτιστεί με τάση μικρότερη από το όριο κόπωσης, τότε ουσιαστικά δεν θα υπάρξει θραύση του υλικού για ένα άπειρο αριθμό κύκλων. Άλλα υλικά, όπως οι ωστενιτικοί χάλυβες, τα περισσότερα μη σιδηρούχα κράματα (αλουμινίου, χαλκού, κλπ.) δεν επιδεικνύουν όριο κόπωσης, δηλαδή η καμπύλη συνεχίζει την πτωτική της πορεία. Για τα υλικά αυτά ορίζεται ένα όριο κόπωσης για δεδομένο αριθμό κύκλων ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΔΙΑΡΚΕΙΑ ΖΩΗΣ ΣΕ ΚΟΠΩΣΗ Η διάρκεια ζωής σε κόπωση ενός υλικού εξαρτάται από μια σειρά παράγοντες. Οι κυριότεροι παράγοντες είναι: το μέσο επίπεδο τάσης, η γεωμετρία της κατασκευής, η ποιότητα της επιφάνειας, ο τύπος του υλικού, οι απομένουσες τάσεις, το μέγεθος και η κατανομή των εσωτερικών ατελειών, το μέγεθος των κόκκων, καθώς και το περιβάλλον. Μέση τάση: Όπως ήδη αναφέρθηκε η καμπύλη S-N εκφράζει την εξάρτηση της διάρκειας ζωής σε κόπωση από το πλάτος της τάσης. Πολλές φορές όμως απαιτείται να ληφθούν υπόψη και άλλα χαρακτηριστικά της τάσης, όπως π.χ. η μέση τάση. Αύξηση της μέσης τάσης οδηγεί σε μείωση της διάρκειας ζωής σε κόπωση. Γεωμετρικός σχεδιασμός: Εγκοπές, γεωμετρικές ασυνέχειες, μη ομαλή μεταβολή της διατομής ενός εξαρτήματος λειτουργούν ως σημεία συγκέντρωσης τάσεων, όπου μπορεί να σχηματιστεί ή πρώτη ρωγμή λόγω κόπωσης. Ακόμη θα πρέπει να λαμβάνεται υπόψη ότι στις συνήθεις συνθήκες φόρτισης, η μέγιστη τάση εμφανίζεται 75
77 στην επιφάνειά ενός εξαρτήματος. Συνεπώς, η διαμόρφωση της επιφάνειας επηρεάζει σε μεγάλο βαθμό την αντοχή σε κόπωση. Ποιότητα επιφάνειας: Η επιφανειακή τραχύτητα, που δημιουργείται λόγω της επεξεργασίας των υλικών στο μηχανουργείο, μπορεί να προκαλέσει συγκέντρωση τάσεων σε μικροσκοπικό επίπεδο, με συνέπεια τη μείωση της αντοχής σε κόπωση. Έχει αποδειχτεί ότι καλύτερο επιφανειακό τελείωμα (φινίρισμα) με λείανση αυξάνει την αντοχή σε κόπωση. Εισαγωγή υπολειπόμενων θλιπτικών τάσεων στην επιφάνεια του υλικού π.χ. με σφαιροβολή επίσης αυξάνει τη διάρκεια ζωής σε κόπωση. Αυτό συμβαίνει γιατί ένα μέρος των εφελκυστικών τάσεων θα ακυρωνόταν από τις υπολειπόμενες θλιπτικές τάσεις. Το ίδιο αποτέλεσμα μπορεί να παραχθεί με ακτίνες laser και υπερήχους. Μια άλλη τεχνική με την οποία βελτιώνεται η επιφανειακή σκληρότητα και η αντοχή σε κόπωση των χαλύβων είναι ο εμποτισμός (case hardening). Δυο βασικές διεργασίες εμποτισμού και είναι η ενανθράκωση και η εναζώτωση. Επιτυγχάνονται με έκθεση του εξαρτήματος σε ανθρακούχα ή αζωτούχα ατμόσφαιρα σε υψηλές θερμοκρασίες. Η αύξηση της αντοχής σε κόπωση οφείλεται τόσο στην δημιουργία ενός περιβλήματος με αυξημένη σκληρότητα, όσο και στην εισαγωγή θλιπτικών τάσεων στην επιφάνεια του εξαρτήματος, που σχηματίζονται κατά την διαδικασία της ενανθράκωσης και εναζώτωσης. Η τεχνική του εμποτισμού χρησιμοποιείται για την επιφανειακή σκλήρυνση των γραναζιών. Τύπος υλικού: η αντοχή σε κόπωση καθώς και η συμπεριφορά των υλικών σε επαναλαμβανόμενες κυκλικές καταπονήσεις εξαρτάται από το είδος του υλικού. Για παράδειγμα, τα σύνθετα υλικά και τα πολυμερή παρουσιάζουν σημαντικές διαφορές από τα μέταλλα. Απομένουσες τάσεις: η κατασκευή των ποικίλων μεταλλικών προϊόντων γίνεται με τη χρήση τεχνικών όπως η συγκόλληση, η κατεργασία με εργαλειομηχανές, η χύτευση καθώς και η διαμόρφωση με διάφορες μηχανικές κατεργασίες (έλαση, σφυρηλάτηση, κλπ.). Η κατεργασία του υλικού συνήθως περιλαμβάνει τη χρήση θερμότητας ή την πρόσδοση μηχανικού έργου ή συχνά το συνδυασμό τους. Αυτό μπορεί να προκαλέσει την ανάπτυξη υψηλών συγκεντρώσεων εφελκυστικών τάσεων, που παραμένουν στο υλικό μετά το τέλος της κατεργασίας. Η παρουσία απομενουσών τάσεων έχει ως συνέπεια τη μείωση της αντοχής σε κόπωση. Μέγεθος και κατανομή εσωτερικών ατελειών: Σφάλματα κατά τη χύτευση, όπως πόροι λόγω παγίδευσης αερίων, εγκλείσματα οξειδίων και σκουριάς, οπές λόγω συστολής μπορεί να μειώσουν σημαντικά την αντοχή των χυτών σε κόπωση. Μέγεθος κόκκου: Για τα περισσότερα μέταλλα η ελάττωση του μεγέθους των κόκκων συνοδεύεται από αύξηση της αντοχής σε κόπωση. Ωστόσο, η επίδραση των επιφανειακών ατελειών είναι πολύ μεγαλύτερη σε λεπτόκκοκα υλικά από ότι σε χονδρόκκοκα. Το περιβάλλον: Η παρουσία χημικά ενεργού, διαβρωτικού περιβάλλοντος ευνοεί την ανάπτυξη και το ρυθμό διάδοσης των ρωγμών. Ως συνέπεια των χημικών αντιδράσεων μεταξύ του περιβάλλοντος και του υλικού μπορεί να σχηματισθούν μικρές οπές, οι οποίες στη συνέχεια λειτουργούν ως συγκεντρωτές τάσεων και συνεπώς ως θέσεις έναρξης ρωγμών. Ο συνδυασμός χημικής προσβολής και κυκλικής τάσης αποκαλείται κόπωση από διάβρωση. Θερμοκρασία: Υψηλές θερμοκρασίες έχουν ως συνέπεια την δημιουργία θερμικών τάσεων λόγω περιορισμού διαστολής/συστολής του υλικού. Γενικά υψηλές θερμοκρασίες μειώνουν την αντοχή σε κόπωση του υλικού. Αυτού του είδους κόπωση αποκαλείται θερμική κόπωση. 76
78 ΚΕΦΑΛΑΙΟ 7 ΜΗΧΑΝΙΣΜΟΙ ΙΣΧΥΡΟΠΟΙΗΣΗΣ ΜΕΤΑΛΛΙΚΩΝ ΥΛΙΚΩΝ 7.1 ΓΕΝΙΚΑ Σχετικά με την σκλήρυνση και την ισχυροποίηση των υλικών έχουν αναπτυχθεί παρά πολλές τεχνικές. Για παράδειγμα, η υψηλή αντοχή του χάλυβα είναι το αποτέλεσμα της εισαγωγής ατόμων άνθρακα στο πλέγμα του σιδήρου (σχηματισμός στερεού διαλύματος παρεμβολής). Ο ορείχαλκος, ο οποίος είναι κράμα χαλκού και ψευδαργύρου, έχει υψηλότερες μηχανικές ιδιότητες από τα επιμέρους συστατικά του, λόγω της αντικατάστασης ατόμων χαλκού από άτομα ψευδαργύρου (σχηματισμός στερεού διαλύματος αντικατάστασης). Ακόμη, η εργοσκλήρυνση, πχ. η σφυρηλασία θερμών εύπλαστων μεταλλικών αντικειμένων στο αμόνι, έχει χρησιμοποιηθεί για αιώνες από τους σιδεράδες, ως τεχνική αύξησης της αντοχής μέσω της εισαγωγής διαταραχών στο υλικό. Το βασικό στοιχείο στο οποίο στηρίζεται η ισχυροποίηση των μεταλλικών υλικών είναι η ύπαρξη διαταραχών στα μεταλλικά υλικά. Ο σχηματισμός, τα είδη (ακμής, έλικα και μικτού τύπου), ο μηχανισμός κίνησή τους (διαδοχικό σπάσιμο και επανασχηματισμός δεσμών) έχουν ήδη αναπτυχθεί προηγουμένως (Κεφ. 4). Η κατανόηση των μηχανισμών ισχυροποίησης προϋποθέτει την πλήρη διαφώτιση της σχέσης μεταξύ της μετακίνησης των υπαρχουσών διαταραχών και της μηχανικής συμπεριφοράς των μετάλλων. Η ικανότητα των μετάλλων να παραμορφώνονται πλαστικά οφείλεται στην δυνατότητα κίνησης των διαταραχών. Η παραμόρφωσή τους οφείλεται στην κίνηση και τον πολλαπλασιασμό ενός μεγάλου αριθμού διαταραχών. Εάν κάποιος θέλει να αυξήσει τις μηχανικές ιδιότητες του υλικού π.χ. αντοχή σε διαρροή και μέγιστη αντοχή σε εφελκυσμό, δεν έχει παρά να εισάγει έναν μηχανισμό παρεμπόδισης της κίνησης των διαταραχών. Αντίθετα, όσο απεριόριστη είναι η κίνηση των διαταραχών, τόσο πιο εύκολα παραμορφώνεται το μέταλλο και τόσο ασθενέστερο και μαλακότερο γίνεται. Συνήθως, η σκλήρυνση και ισχυροποίηση οδηγεί σε μείωση της ολκιμότητας. Υπάρχουν τέσσερις βασικοί μηχανισμοί ισχυροποίησης των μετάλλων: η σκλήρυνση με ενδοτράχυνση. η ισχυροποίηση με δημιουργία στερεού διαλύματος. η σκλήρυνση με κατακρήμνιση λόγω γήρανσης. η σκλήρυνση με ελάττωση του μεγέθους κόκκων. Ωστόσο, είναι αξιοσημείωτο ότι όλες οι τεχνικές ισχυροποίησης στηρίζονται στην εξής απλή αρχή: τον περιορισμό ή παρεμπόδιση της κίνησης και της διάδοσης των διαταραχών. Ένας άλλος σημαντικός μηχανισμός ισχυροποίησης των χαλύβων είναι ο μαρτενσιτικός μετασχηματισμός, ο οποίος θα αναπτυχθεί σε επόμενο κεφάλαιο. 77
79 7.2 ΣΚΛΗΡΥΝΣΗ ΜΕ ΕΝΔΟΤΡΑΧΥΝΣΗ Σκλήρυνση με ενδοτράχυνση καλείται το φαινόμενο κατά το οποίο τα όλκιμα μέταλλα γίνονται σκληρότερα και ισχυρότερα με την εν ψυχρώ κατεργασία τους, δηλαδή όταν παραμορφώνονται πλαστικά σε θερμοκρασίες αρκετά χαμηλότερες του σημείου τήξης τους. Η εν ψυχρώ κατεργασία των μετάλλων είναι διαφορετική από την εν θερμώ, η οποία πραγματοποιείται σε υψηλές θερμοκρασίες και περιλαμβάνει μεγαλύτερες παραμορφώσεις. Μετά την εν ψυχρώ κατεργασία τους τα μέταλλα παρουσιάζουν μεγαλύτερη σκληρότητα, όριο διαρροής και θραύσης, αλλά μικρότερη πλαστικότητα και δυσθραυστότητα. Η σκλήρυνση με ενδοτράχυνση οφείλεται στο γεγονός της αύξησης της πυκνότητας των διαταραχών με την πλαστική παραμόρφωση, εξαιτίας του πολλαπλασιασμού τους. Καθώς η πυκνότητά των διαταραχών αυξάνεται, η μέση απόσταση διαχωρισμού τους μειώνεται και οι διαταραχές αρχίζουν να εμποδίζουν η μια την κίνηση της άλλης, οδηγώντας σε αύξηση των μηχανικών ιδιοτήτων του υλικού. Η σκλήρυνση με ενδοτράχυνση χρησιμοποιείται πολύ συχνά για να αυξήσει τις μηχανικές ιδιότητες των μετάλλων κατά τη διαδικασία παραγωγής τους π.χ με διέλαση. Σε πολλές περιπτώσεις όμως η σκλήρυνση λόγω ενδοτράχυνσης μπορεί να αυξηθεί σε τέτοιο βαθμό, ώστε να απαιτείται ένα ενδιάμεσο βήμα θερμικής επεξεργασίας ανόπτησης, για την εξάλειψη των αποτελεσμάτων της ενδοτράχυνσης, προκειμένου να καταστεί δυνατή η συνέχιση της κατεργασίας. Παρακάτω παρουσιάζονται μερικές πλευρές του φαινομένου της ενδοτράχυνσης. Κατά την ενδοτράχυνση ενός μετάλλου π.χ. με έλαση, οι κόκκοι του υλικού επιμηκύνονται στην διεύθυνση της κατεργασίας, σχηματίζοντας ένα ιστό, με αποτέλεσμα το υλικό να καθίσταται ανισότροπο. Δηλαδή, το υλικό παρουσιάζει διαφορετικές ιδιότητες (μηχανικές, ηλεκτρικές, κλπ.) κατά διεύθυνση κάθετη ή παράλληλη με τη διεύθυνση του ιστού. Η παραμόρφωση των κόκκων συνίσταται στην μετακίνηση ολόκληρων πλεγματικών επιπέδων κατά τη διεύθυνση της κατεργασίας. Παρά την παραμόρφωση, οι κόκκοι διατηρούν συνεχή κρυσταλλική δομή και σταθερό όγκο. Μικροσκοπικά, στους παραμορφωμένους κόκκους υπάρχει αποθηκευμένη δυναμική ενέργεια. Επειδή όμως τα διάφορα τμήματα του υλικού παραμορφώνονται με διαφορετικό τρόπο, όταν αυτά τείνουν να επανέλθουν στο αρχικό τους σχήμα αναπτύσσονται μεταξύ τους εσωτερικές τάσεις. Με βάση τους παραπάνω προβληματισμούς, ως ενδοτράχυνση θα μπορούσε να ορισθεί η εν ψυχρώ πλαστική παραμόρφωση του υλικού, που καθορίζεται από την ανάπτυξη εσωτερικών μηχανικών τάσεων, οφειλομένων στην ανομοιογενή παραμόρφωση των κόκκων και τον σχηματισμό ιστού κατά τη διεύθυνση της κατεργασίας. Ο βαθμός της πλαστικής παραμόρφωσης εκφράζεται ως % ποσοστό της ψυχρής κατεργασίας. Η επί τοις % ψυχρή κατεργασία ορίζεται ως εξής: n= A0 Ad 100 A0 όπου n o συντελεστής ελάττωσης της διατομής Α0 το εμβαδό της διατομής πριν την παραμόρφωση Αd το εμβαδό της διατομής μετά την παραμόρφωση 78
80 Στο σχήμα Σχήμα 7.1 παρουσιάζεται η αύξηση της αντοχής σε διαρροή, η αύξηση της αντοχής σε εφελκυσμό και η μείωση της ολκιμότητας συναρτήσει του % ποσοστού ψυχρής κατεργασίας, για τον χάλυβα 1040, έναν ορείχαλκο και έναν χαλκό. Σχήμα 7.1: (α) Αύξηση του ορίου διαρροής, (β) αύξηση της αντοχής σε εφελκυσμό και (γ) μείωση της ολκιμότητας συναρτήσει της επί τοις % ψυχρής κατεργασίας για το χάλυβα 1040, έναν ορείχαλκο και τον καθαρό χαλκό. Επίσης στον Πίνακα 7.1 παρουσιάζεται η αύξηση της αντοχής σε διαρροή τριών κραμάτων αλουμινίου που συνήθως υφίστανται σκλήρυνση με ενδοτράχυνση. Η ισχυροποίηση λόγω ενδοτράχυνσης προστίθεται στην ισχυροποίηση του υλικού λόγω σχηματισμού στερεού διαλύματος με συνέπεια να παρατηρείται σημαντική αύξηση των μηχανικών του ιδιοτήτων. Πίνακας 7.1: Αύξηση της αντοχής σε διαρροή τριών κραμάτων Al, τα οποία υπέστησαν σκλήρυνση με ενδοτράχυνση. Αντοχή σε διαρροή, σy (MPa) Κράμα Al Ανοπτημένο Ημίσκληρο Σκληρό ΙΣΧΥΡΟΠΟΙΗΣΗ ΜΕ ΔΗΜΙΟΥΡΓΙΑ ΣΤΕΡΕΟΥ ΔΙΑΛΥΜΑΤΟΣ Μια άλλη τεχνική ισχυροποίησης και σκλήρυνσης των μετάλλων είναι η προσθήκη ατόμων ενός άλλου στοιχείου στο καθαρό μέταλλο. Τα στοιχεία πρόσμιξης εισέρχονται σε παραπλεγματικές ή πλεγματικές θέσεις του μητρικού κρυσταλλικού πλέγματος, σχηματίζοντας με αυτό τον τρόπο, ένα στερεό διάλυμα παρεμβολής ή αντικατάστασης, αντίστοιχα. Αυτός ο μηχανισμός καλείται ισχυροποίηση στερεού διαλύματος. Υψηλής καθαρότητας μέταλλα είναι συνήθως μαλακότερα και λιγότερο στιβαρά από τα αντίστοιχα κράματά τους. Αύξηση της συγκέντρωσης του προστιθέμενου στοιχείου, έχει ως αποτέλεσμα την αύξηση του των μηχανικών ιδιοτήτων του υλικού. Ωστόσο υπάρχει ένα ανώτερο όριο για την περιεκτικότητα του στοιχείου πρόσμιξης, έτσι ώστε να αποφευχθεί η δημιουργία δεύτερης φάσης (το στερεό διάλυμα αποτελείται από μια φάση). Στο Σχήμα 7.2 παρουσιάζεται η αύξηση των μηχανικών ιδιοτήτων του χαλκού συναρτήσει του % προστιθέμενου ποσοστού ψευδαργύρου με σκοπό το σχηματισμό ορείχαλκου. 79
81 Σχήμα 7.2: Αύξηση της (α) αντοχής σε εφελκυσμό, (β) σκληρότητας και (γ) της επιμήκυνσης συναρτήσει της περιεκτικότητας σε ψευδάργυρο κραμάτων Cu-Zn (ορείχαλκος). Τα άτομα της πρόσμιξης που υπεισέρχονται στο μητρικό κρυσταλλικό πλέγμα, προκαλούν ένα πεδίο παραμορφώσεων του πλέγματος, το οποίο παρεμποδίζει την κίνηση των διαταραχών, οδηγώντας σε αύξηση της αντοχής σε διαρροή του μετάλλου. Στο Σχήμα 7.3 φαίνονται οι παραμορφώσεις του μητρικού πλέγματος, που προκαλούνται από τη προσθήκη ατόμων αντικατάστασης και παρεμβολής σε πλεγματικές και σε παραπλεγματικές θέσεις, αντίστοιχα. Για παράδειγμα, τα άτομα παρεμβολής θα μπορούσαν να είναι άτομα άνθρακα διαλυμένα σε άτομα σιδήρου. Τα άτομα άνθρακα τοποθετημένα σε παραπλεγματικές θέσεις δημιουργούν παραμορφώσεις του πλέγματος, οι οποίες εμποδίζουν την κίνηση των διαταραχών. (α) (β) Σχήμα 7.3: Σχηματική αναπαράσταση των πλεγματικών παραμορφώσεων που προκαλούνται από την προσθήκη ατόμων (α) αντικατάστασης και (β) παρεμβολής. Όταν υπάρχουν άτομα πρόσμιξης μέσα στο μητρικό κρυσταλλικό πλέγμα, η συνολική παραμόρφωση του πλέγματος αυξάνεται, με συνέπεια η αντίσταση στην ολίσθηση των διαταραχών να είναι μεγαλύτερη. Επομένως, στα κράματα στερεού διαλύματος, είναι αναγκαία η εφαρμογή μιας μεγαλύτερης τάσης, προκειμένου να ξεκινήσει και να συνεχισθεί η πλαστική παραμόρφωση. Οι υπάρχουσες διαταραχές "αγκυρώνονται" από τα άτομα πρόσμιξης και η μετακίνησή τους είναι εξαιρετικά δύσκολη. Συνεπώς, για να ξεκινήσει η διαδικασία της πλαστικής παραμόρφωσης απαιτείται η δημιουργία νέων διαταραχών, γεγονός που επιτυγχάνεται με την εφαρμογή υψηλότερης τάσης. Χαρακτηριστικό παράδειγμα αυτού του μηχανισμού σκλήρυνσης αποτελεί η θραύση σε εφελκυσμό ενός μαλακού χάλυβα (Κεφ. 6). Στην περίπτωση του μαλακού χάλυβα, το διάγραμμα εφελκυσμού παρουσιάζει ένα ανώτερο και ένα κατώτερο όριο διαρροής. Το ανώτερο όριο αντιστοιχεί στην τάση που απαιτείται για την δημιουργία των νέων διαταραχών, μιας και οι υπάρχουσες διαταραχές "αγκυρώνονται" από τα άτομα του άνθρακα, ενώ το κατώτερο όριο στην τάση που απαιτείται για την μετακίνηση των νέων διαταραχών. 80
82 7.4 ΣΚΛΗΡΥΝΣΗ ΜΕ ΚΑΤΑΚΡΗΜΝΙΣΗ ΛΟΓΩ ΓΗΡΑΝΣΗΣ Στα περισσότερα διμερή συστήματα, η αύξηση της συγκέντρωσης του ενός συστατικού πάνω από ορισμένη συγκέντρωση, η οποία δίνεται από το διάγραμμα φάσεων, έχει ως συνέπεια την εμφάνιση μιας δεύτερης φάσης. Ο σχηματισμός μικρών και ομοιόμορφα διασκορπισμένων σωματιδίων μιας δεύτερης φάσης, μέσα στο αρχικό μητρικό κρυσταλλικό πλέγμα, επιτυγχάνεται με κατάλληλες θερμικές κατεργασίες και έχει ως συνέπεια την αύξηση της αντοχής και της σκληρότητας των μεταλλικών κραμάτων. Η διαδικασία καλείται σκλήρυνση με κατακρήμνιση και τα μικρά σωματίδια της δεύτερης φάσης καλούνται κατακρημνίσματα. Ό όρος σκλήρυνση με γήρανση χρησιμοποιείται για να καταδείξει ότι η αντοχή του κράματος αναπτύσσεται με το πέρασμα του χρόνου, καθώς το κράμα "γερνά". Παραδείγματα κραμάτων που υφίστανται σκλήρυνση με κατακρήμνιση είναι: a) b) c) d) Κράματα Al-Cu, Al-Mg-Si και Al-Zn-Mg. Κράματα Cu-Be, Cu-Sn. Κοινοί μαλακοί χάλυβες, χάλυβες Maraging και ανοξείδωτοι χάλυβες. Υπερκράματα νικελίου και υπερκράματα κοβαλτίου. Η σκλήρυνση με κατακρήμνιση οφείλεται στο γεγονός ότι τα σωματίδια/κατακρημνίσματα παρεμποδίζουν την μετακίνηση των διαταραχών με τρόπο ανάλογο των ατόμων πρόσμιξης, στην περίπτωση σχηματισμού στερεού διαλύματος, αν και τα κατακρημνίσματα δεν αποτελούνται απαραίτητα από άτομα ενός στοιχείου. Στον Πίνακα 7.2 παρουσιάζεται η αύξηση της αντοχής σε διαρροή τριών κραμάτων αλουμινίου των σειρών 2000, 6000 και 7000, τα οποία υπέστησαν σκλήρυνση με κατακρήμνιση. Πίνακας 7.2: Αύξηση της αντοχής σε διαρροή κραμάτων Al, τα οποία υπέστησαν σκλήρυνση με κατακρήμνιση. Αντοχή σε διαρροή, σy (MPa) Κράματα Al Τυπική σύσταση Αργή ψύξη Βαφή και γήρανση 2014 Al, 4.4 %Cu, Mg, Si, Mn Al, 1.0 %Mg, Si, Cr Al, 5.6% Zn, Mg, Cu ΙΣΧΥΡΟΠΟΙΗΣΗ ΜΕ ΕΛΑΤΤΩΣΗ ΤΟΥ ΜΕΓΕΘΟΥΣ ΤΩΝ ΚΟΚΚΩΝ Σε ένα πολυκρυσταλλικό μέταλλο το μέγεθος των κόκκων ή η μέση διάμετρος του έχει σημαντική επίδραση στις μηχανικές του ιδιότητες. Επειδή οι κόκκοι έχουν συνήθως διαφορετικούς κρυσταλλογραφικούς προσανατολισμούς, για αυτό και υπάρχει ο σχηματισμός των ορίων μεταξύ των κόκκων. Κατά την διάρκεια της πλαστικής παραμόρφωσης, η κίνηση μιας διαταραχής πρέπει να γίνει διαμέσου των κοινών αυτών ορίων. Τα όρια των κόκκων λειτουργούν ως εμπόδιο στην κίνηση μιας διαταραχής. Ένα υλικό το οποίο έχει μικρούς κόκκους (λεπτόκοκκο) είναι σκληρότερο και ισχυρότερο από ένα υλικό με μεγάλους κόκκους (χονδρόκοκκο), γιατί διαθέτει μεγαλύτερη συνολική επιφάνεια ορίων κόκκων, έτσι ώστε να παρεμποδίζει την κίνηση των διαταραχών. Για πολλά υλικά η αντοχή σε διαρροή σy είναι αντιστρόφως ανάλογη του μεγέθους των κόκκων, σύμφωνα με τη σχέση Hall-Petch. Στο Σχήμα 7.9 παρουσιάζεται η αύξηση της 81
83 αντοχής σε διαρροή σε συνάρτηση με τη μείωση του μεγέθους των κόκκων για ένα κράμα ορείχαλκου. Σχήμα 7.9: Αύξηση της αντοχής σε διαρροή σε συνάρτηση με το μέγεθος των κόκκων για ένα κράμα ορείχαλκου 70 Cu-30 Zn. Η διάμετρος των κόκκων (d) μειώνεται από αριστερά προς δεξιά. Το μέγεθος των κόκκων μπορεί να ρυθμιστεί με διάφορες τεχνικές όπως, με έλεγχο της ταχύτητας στερεοποίησης καθώς και με εδοτράχυνση ακολουθούμενη από θερμική επεξεργασία. Θα πρέπει επίσης να αναφερθεί ότι η μείωση του μεγέθους των κόκκων βελτιώνει όχι μόνο το όριο διαρροής και της αντοχής σε εφελκυσμό πολλών κραμάτων, αλλά επίσης βελτιώνει και την δυσθραυστότητά τους. Το γεγονός ότι η μείωση του μεγέθους των κόκκων έχει ως συνέπεια την αύξηση της αντοχής του υλικού, δεν σημαίνει επίσης ότι το μέγεθος των κόκκων μπορεί να μειώνεται απεριόριστα. Έχει βρεθεί ότι για κόκκους μικρότερους από ~ 10 nm, λαμβάνει χώρα ένα φαινόμενο, γνωστό ως ολίσθηση των ορίων των κόκκων, με αποτέλεσμα τη μείωση της αντοχής του υλικού. Αυτό είναι ιδιαίτερα ενδιαφέρον, γιατί μόνο πρόσφατα έγινε δυνατή η κατασκευή υλικών με μέγεθος κόκκων μικρότερο από 10 nm. 82
84 ΚΕΦΑΛΑΙΟ 8 ΜΟΡΦΟΠΟΙΗΣΗ ΤΩΝ ΜΕΤΑΛΛΩΝ 8.1 ΓΕΝΙΚΑ Για την κατασκευή κάθε προϊόντος απαιτείται η εφαρμογή διάφορων τεχνικών κατεργασίας, προκειμένου το προϊόν να αποκτήσει το επιθυμητό σχήμα και κατάλληλες ιδιότητες. Η χύτευση καθώς και η σφυρηλασία αποτελούν ίσως τις αρχαιότερες τεχνικές κατεργασίας των μετάλλων στην ιστορία του ανθρώπινου είδους. Οι πιο συνήθεις τεχνικές κατεργασίας των μετάλλων είναι: διάφορες μηχανικές κατεργασίες διαμόρφωσης (σφυρηλάτηση, έλαση, διέλαση με έλξη, διέλαση με συμπίεση, κλπ.), η χύτευση, η κονιομεταλλουργία, η συγκόλληση και η κατεργασία με εργαλειομηχανές. Συνήθως δυο ή περισσότερες από τις προηγούμενες μεθόδους εφαρμόζονται για την παραγωγή ενός τελικού προϊόντος. Η επιλογή της κατάλληλης μεθόδου για την μορφοποίηση ενός προϊόντος εξαρτάται από παράγοντες όπως το είδος του μετάλλου, οι ιδιότητές του, το σχήμα και το μέγεθος του αντικειμένου καθώς και το οικονομικό κόστος. Στο Σχήμα 8.1 παρουσιάζονται οι κυριότερες τεχνικές κατεργασίας των μετάλλων. Στη συνέχεια ακολουθεί σύντομη περιγραφή αυτών των τεχνικών, δηλ. των μηχανικών κατεργασιών διαμόρφωσης των μετάλλων, της χύτευσης καθώς και διάφορων άλλων τεχνικών. Σχήμα 8.1: Ταξινόμηση των κυριότερων τεχνικών μορφοποίησης των μετάλλων. 8.2 ΜΗΧΑΝΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ ΔΙΑΜΟΡΦΩΣΗΣ ΤΩΝ ΜΕΤΑΛΛΩΝ Μηχανικές κατεργασίες διαμόρφωσης είναι εκείνες οι μέθοδοι μορφοποίησης των μετάλλων κατά τις οποίες το προϊόν αποκτά την επιθυμητή γεωμετρία με την πρόσδοση μηχανικού έργου. Για παράδειγμα, η σφυρηλάτηση, η έλαση, η διέλαση με συμπίεση (εξώθηση) και η διέλαση με έλξη (διέλκυση) αποτελούν ορισμένες συνήθεις μηχανικές κατεργασίες. Ακόμη η κάμψη, η βαθεία κοίλανση και η έκταση αποτελούν διαδεδομένες μεθόδους διαμόρφωσης επίπεδων ελασμάτων (π.χ. λαμαρινών). Με αυτές τις τεχνικές το σχήμα του μεταλλικού προϊόντος μεταβάλλεται με πλαστική παραμόρφωση. Φυσικά, η πλαστική παραμόρφωση είναι το αποτέλεσμα της επιβολής εξωτερικής δύναμης, υψηλότερης από την αντοχή 83
85 διαρροής του υλικού. Τα περισσότερα μεταλλικά υλικά είναι επιδεκτικά σε αυτές τις τεχνικές, γιατί διαθέτουν κατάλληλη ολκιμότητα, με συνέπεια να μπορούν να παραμορφωθούν πλαστικά χωρίς να υποστούν θραύση ή ρηγμάτωση. Όταν η παραμόρφωση πραγματοποιείται σε θερμοκρασία μεγαλύτερη από την θερμοκρασία ανακρυστάλλωσης, η κατεργασία ονομάζεται θερμηλασία (Ενότητα ), ενώ όταν γίνεται σε θερμοκρασία περιβάλλοντος, εν ψυχρώ, ονομάζεται ψυχρηλασία (Ενότητα 7.2). Στην περίπτωση της θερμηλασίας μπορεί να επιτευχθούν μεγάλες παραμορφώσεις, επειδή το μέταλλο παραμένει μαλακό και όλκιμο. Η ενέργεια που απαιτείται για τη θερμηλασία είναι μικρότερη από την αντίστοιχη της ψυχρηλασίας. Η ψυχρηλασία προκαλεί αύξηση της αντοχής, λόγω ενδοτράχυνσης του μετάλλου, με συνέπεια τη μείωση της ολκιμότητας. Σε πολλές περιπτώσεις απαιτείται η εφαρμογή ενδιάμεσου βήματος θερμικής επεξεργασίας ανόπτησης, έτσι ώστε να καταστεί δυνατή η συνέχιση της κατεργασίας. Ένα από τα πλεονεκτήματα της ψυχρηλασίας είναι η καλύτερη ποιότητα της τελικής επιφάνειας. Σε πολλές περιπτώσεις η μορφοποίηση με θερμηλασία, ακολουθείται από τελικό στάδιο ψυχρηλασίας. Ακόμη, θα πρέπει να σημειωθεί ότι ορισμένες τεχνικές διαμόρφωσης π.χ. η διέλαση με συμπίεση, η διέλαση με έλξη, σε χώρες όπως οι Ηνωμένες Πολιτείες Αμερικής, περιγράφονται με τους όρους εξώθηση (extrusion) και διέλκυση (drawing) ΕΛΑΣΗ Έλαση είναι μια μηχανική κατεργασία διαμόρφωσης των μετάλλων, η οποία συνίσταται στο πέρασμα ενός μετάλλου μεταξύ δυο κυλίνδρων (Σχήμα 8.2). Η μείωση στο πάχος οφείλεται σε θλιπτικές τάσεις που ασκούνται από τους κυλίνδρους. Σχήμα 8.2: Σχηματική αναπαράσταση έλασης (α) με πρωτεύοντα ράουλα και (β) με συνδυασμό πρωτευόντων και δευτερευόντων ραούλων. Η έλαση πραγματοποιείται είτε εν θερμώ είτε εν ψυχρώ. Η θερμή έλαση είναι η πιο διαδεδομένη τεχνική μορφοποίησης, ενώ η ψυχρή έλαση η πιο διαδεδομένη από όλες τις εν ψυχρώ κατεργασίες. Η θερμή έλαση χρησιμοποιείται κυρίως για την παραγωγή ελασμάτων, λωρίδων, φύλλων, δοκών, όπως οι ράγες σιδηροτροχιών τρένων. Το αρχικό υλικό είναι συνήθως ημιτελή προϊόντα χύτευσης, όπως πλάκες, κορμοί ή μπιγιέτες. Εάν αυτά τα προϊόντα προέρχονται από συνεχή διαδικασία χύτευσης τότε τροφοδοτούνται απευθείας σε διατάξεις ελάστρων στην κατάλληλη θερμοκρασία. Για την παραγωγή δοκών σε σχήμα Ι ή ραγών χρησιμοποιούνται κύλινδροι με αυλακώσεις. Η ψυχρή έλαση χρησιμοποιείται για την παραγωγή ελασμάτων, λωρίδων και φύλλων με τελική επιφάνεια υψηλής ποιότητας. 84
86 Στο Σχήμα 8.3 παρουσιάζεται η προοδευτική μείωση του πάχους του αρχικού υλικού για την παραγωγή χαλυβδόφυλλων σε μια τυπική διάταξη έξη συνεχών ελάστρων. Σχήμα 8.3: Σχηματική αναπαράσταση παραγωγής χαλυβδόφυλλων. Στο Σχήμα 8.4 παρουσιάζονται μορφοποιήθηκαν με ψυχρή έλαση. ροδέλες γενικής χρήσης οχημάτων που Σχήμα 8.4: Ροδέλες γενικής χρήσης, ανθρακούχος χάλυβας, ψυχρή έλαση (cold rolled) ΔΙΕΛΑΣΗ ΜΕ ΣΥΜΠΙΕΣΗ (ΕΞΩΘΗΣΗ) Στην διέλαση με συμπίεση (εξώθηση) μια δοκός μετάλλου διέρχεται μέσα από μια μήτρα υπό την πίεση ενός εμβόλου (Σχήμα 8.5α). Αυτό έχει ως συνέπεια την μείωση της διατομής συνοδευόμενη από αύξηση του μήκους. Το πλεονέκτημα της διέλασης με συμπίεση είναι ότι επιτυγχάνονται πολύπλοκες γεωμετρίες διατομής. Η κατεργασία συνήθως πραγματοποιείται εν θερμώ. Προϊόντα όπως ράβδοι και σωλήνες παράγονται με αυτή την τεχνική. 85
87 Σχήμα 8.5: Σχηματική αναπαράσταση διέλασης (α) συμαπαγούς μεταλλικού τεμαχίου και (β) σωλήνα. α: βελόνα ενωμένη με το έμβολο, b: μπιγιέτα, c: μεταλλικός θάλαμος, f: μήτρα, p: έμβολο. Η παραγωγή σωλήνων (χωρίς ραφή) αποτελεί μια από τις σημαντικότερες εφαρμογές αυτής της μεθόδου (Σχήμα 8.5β). Στην περίπτωση αυτή η μπιγιέτα, η οποία είναι προηγουμένως τρυπημένη, διαπερνάται από βελόνα που ενώνεται με το έμβολο. Η βελόνα κατασκευάζεται από κατάλληλο εργαλειοχάλυβα. Στο Σχήμα 8.6 παρουσιάζεται ένας σωλήνας λαδιού οχημάτων χωρίς ραφή, ο οποίος μπορεί να μορφοποιηθεί είτε με θερμή έλαση, είτε με διέλκυση εν ψυχρώ.. Σχήμα 8.6: Σωλήνας λαδιού χωρίς ραφή (seamless), ανθρακούχος χάλυβας, θερμή έλαση (hot rolled) ή διέλκυση εν ψυχρώ (cold-drawn). Επίσης, αυτή η μέθοδος βρίσκει ευρεία εφαρμογή στη διαμόρφωση μη σιδηρούχων μετάλλων, όπως το αλουμίνιο. Στο Σχήμα 8.7 παρουσιάζεται μια μήτρα θερμής διέλασης αλουμινίου (εξώθηση). 86
88 (α) (β) Σχήμα 8.7: Καλούπι θερμής διέλασης αλουμινίου(extrusion) (α) εμπρός πλευρά (β) πίσω πλευρά. ( ΔΙΕΛΑΣΗ ΜΕ ΕΛΞΗ (ΔΙΕΛΚΥΣΗ) Στην διέλαση με έλξη (διέλκυση) το μέταλλο διέρχεται διαδοχικά μέσα από μήτρες, ολοένα και πιο στενές λόγω μιας δύναμης ελκυσμού, που εφαρμόζεται στο μέταλλο από την πλευρά της εξόδου. Το αποτέλεσμα είναι η μείωση της διατομής και αύξηση του μήκους. Με αυτή την μέθοδο συνήθως παράγονται κύλινδροι, σωλήνες και σύρματα. Στο Σχήμα 8.8 απεικονίζεται η κατεργασία συρματοποίησης. Οι μήτρες κατασκευάζονται από κατάλληλους εργαλειοχάλυβες. Σχήμα 8.8: (α) Συρματοποίηση και (β) κάτοψη μήτρας συρματοποίησης. 87
89 Στο Σχήμα 8.9 παρουσιάζεται ένα ελατήριο συμπιέσεως οχημάτων, το οποίο διαμορφώνεται με διέλκυση εν ψυχρώ. Σχήμα 8.9: Ελατήριο συμπιέσεως, διέλκυση εν ψυχρώ (cold drawn) ΣΦΥΡΗΛΑΤΗΣΗ Σφυρηλάτηση είναι η μηχανική κατεργασία μορφοποίησης των μετάλλων με εφαρμογή πίεσης ή διαδοχικών χτυπημάτων (θλιπτική καταπόνηση) (Σχήμα 8.10). Σχήμα 8.10: Διαμόρφωση με σφυρηλασία. Μερικά μέταλλα μπορούν να σφυρηλατηθούν εν ψυχρώ, ωστόσο ο σίδηρος και οι χάλυβες σφυρηλατούνται σχεδόν πάντοτε εν θερμώ. Υπάρχουν δυο τύποι σφυρηλάτησης: ανοιχτής και κλειστής μήτρας. Στην τεχνική κλειστής μήτρας ένα φορτίο εφαρμόζεται στα δυο ή περισσότερα μέρη της μήτρας, η οποία περικλείει πλήρως το μεταλλικό τεμάχιο. Αντιθέτως Στην τεχνική ανοιχτής μήτρας, η μήτρα δεν περικλείει πλήρως το μεταλλικό τεμάχιο. Συνήθως δυο παράλληλα ή ημικυκλικά επίπεδα εφαρμόζονται σε μεγάλα μεταλλικά τεμάχια. Τα σφυρήλατα εξαρτήματα χρειάζονται συνήθως περαιτέρω επεξεργασία για να παραχθεί ένα τελειωμένο προϊόν. 88
90 Τα εξαρτήματα που μορφοποιούνται με σφυρηλάτηση είναι ισχυρότερα από αυτά που μορφοποιούνται με χύτευση ή σε εργαλειομηχανές. Κατά την σφυρηλάτηση, οι κόκκοι του υλικού επιμηκύνονται, ακολουθώντας το σχήμα του μεταλλικού αντικειμένου, με συνέπεια το σχηματισμό συγκεκριμένου ιστού σε όλο το σώμα του αντικειμένου, δίνοντας εξαρτήματα με βελτιωμένες μηχανικές ιδιότητες (Σχήμα 8.11). Ακόμη, η σφυρηλάτηση προκαλεί εκλέπτυνση και ομογενοποίηση της μικροδομής με μηχανικό (καταστροφή της δενδριτικής δομής) καθώς θερμικό (μέσω διάχυσης) τρόπο. Στροφαλοφόροι άξονες αυτοκινήτων, διωστήρες (μπιέλες) και μηχανικά κλειδιά αποτελούν τυπικά προϊόντα αυτής της τεχνικής. Σχήμα 8.11: Τομή σφυρήλατου διωστήρα (μπιέλας), στον οποίο φαίνεται η ροή των κόκκων ΚΑΤΕΡΓΑΣΙΕΣ ΔΙΑΜΟΡΦΩΣΗΣ ΕΠΙΠΕΔΟΥ ΕΛΑΣΜΑΤΟΣ Κάμψη Η διαμόρφωση με κάμψη είναι η πλέον διαδεδομένη μηχανική κατεργασία διαμόρφωσης. Με αυτή επιτυγχάνονται καμπυλότητες σε επίπεδα ελάσματα με την εφαρμογή κάμψης (Σχήμα 8.12). Ενώ στη διαμόρφωση με εφελκυσμό ή θλίψη παραμορφώνεται ολόκληρο το αντικείμενο, στην κάμψη παραμορφώνεται μόνο ένα τμήμα του αντικειμένου, η ζώνη κάμψης. Στην κάμψη ένα μέρος του αντικειμένου υπόκειται σε εφελκυσμό και ένα μέρος σε θλίψη. Η επάνω πλευρά επιμηκύνεται, η κάτω συμπιέζεται, ενώ μεταξύ αυτών βρίσκεται μια αμετάβλητη ουδέτερη ζώνη, η ουδέτερη ίνα. Με την κατεργασία αυτή κατασκευάζονται τοιχώματα δοχείων, τύμπανα και διάφορα άλλα εξαρτήματα. Τα ελάσματα θα πρέπει κατά το δυνατόν να κάμπτονται κάθετα στην διεύθυνση της ελάσεως. Με κάμψη μπορούν επίσης να διαμορφωθούν οι σωλήνες και τα προφίλ. 89
91 Σχήμα 8.12: Διαμόρφωση με κάμψη. Στο Σχήμα 8.13 παρουσιάζεται ένα κλίπ καθίσματος οχημάτων, το οποίο διαμορφώνεται με κάμψη, κάθετα στη διεύθυνση της έλασης. Σχήμα 8.13: Κλιπ καθίσματος, ανθρακούχος χάλυβας, κάμψη. Βαθεία κοίλανση Βαθεία κοίλανση είναι η μηχανική κατεργασία διαμόρφωσης ενός ελάσματος σε κοίλο σώμα (κυάθιο), χωρίς ουσιαστική μεταβολή του πάχους του ελάσματος. Η δύναμη διαμόρφωσης εφαρμόζεται μέσω ενός εμβόλου, το οποίο κατά την κάθοδό του καταπονεί το υλικό σε θλίψη και εφελκυσμό (Σχήμα 8.14). Τα υλικά που προορίζονται για βαθεία κοίλανση πρέπει να έχουν υψηλή ικανότητα επιμήκυνσης. Η κατεργασία γίνεται εν ψυχρώ για επίτευξη ακρίβειας της κατασκευής. 90
92 Σχήμα 8.14: Διαμόρφωση με βαθεία κοίλανση. Στο Σχήμα 8.15 παρουσιάζεται μια πόρτα πλατφόρμας φορτηγού, η οποία κατασκευάστηκε με χρήση κοίλης διαμόρφωσης. Σχήμα 8.15: Πόρτα πλατφόρμας φορτηγού, ανθρακούχος χάλυβας, ψυχρή κοίλη διαμόρφωση και συγκόλληση χαλυβδοελασμάτων. Διαμόρφωση σε έκταση Στην διαμόρφωση με έκταση, ένα λεπτό έλασμα κυκλικής διατομής μορφοποιείται σε κέλυφος. Αυτό επιτυγχάνεται με την εφαρμογή μιας διαξονικής εφελκυστικής τάσης μέσω ενός εμβόλου (Σχήμα 8.16). Σχήμα 8.16: Διαμόρφωση με έκταση. 91
93 8.3 ΧΥΤΕΥΣΗ Η χύτευση είναι μια τεχνική μορφοποίησης των μετάλλων κατά την οποία ένα πλήρως τηγμένο μέταλλο χύνεται στην κοιλότητα ενός καλουπιού (τύπος ή μήτρα) με το επιθυμητό σχήμα. Μετά ακολουθεί η στερεοποίηση του μετάλλου, η οποία συνοδεύεται από κάποιο βαθμό συστολής. Το στερεοποιημένο στερεό είναι γνωστό ως χυτό. Η χύτευση εφαρμόζεται για την κατασκευή αντικειμένων με πολύπλοκη γεωμετρία, που η κατασκευή τους με οποιαδήποτε άλλη μέθοδο θα ήταν δύσκολη ή μη οικονομική. Οι τεχνικές χύτευσης διακρίνονται σε δυο βασικές κατηγορίες: χύτευση σε μη μόνιμο και χύτευση σε μόνιμο καλούπι. Στην χύτευση σε μη μόνιμο καλούπι, τα καλούπια κατασκευάζονται από άμμο, πολυμερές ή γύψο. Ακόμη υπάρχουν τα καλούπια κελύφους και τα καλούπια επένδυσης (τεχνική του απωλεσθέντος κεριού). Τα καλούπια καταστρέφονται κατά την εξαγωγή του χυτού και συνεπώς δεν επαναχρησιμοποιούνται. Στην χύτευση σε μόνιμο καλούπι, τα καλούπια συνήθως κατασκευάζονται από μέταλλο. Οι χυτεύσεις σε μόνιμο καλούπι μπορεί να υποβοηθούν από τη χρήση πίεσης, κενού ή φυγόκεντρης δύναμης. Διακρίνονται τουλάχιστον τέσσερις μέθοδοι: χύτευση σε μόνιμο καλούπι (χαμηλή πίεση), χύτευση σε μόνιμο καλούπι (υπό πίεση), φυγοκεντρική χύτευση και συνεχής χύτευση. Επιπλέον με βάση τον τρόπο τροφοδοσίας του τήγματος διακρίνονται δυο είδη χύτευσης: η εκ των άνω ή κατευθείαν χύτευση και η εν αναρροή ή πηγαία χύτευση. Στην πρώτη περίπτωση, η απόχυση πραγματοποιείται από πάνω και η στερεοποίηση αρχίζει από το κατώτερο τμήμα του καλουπιού, ενώ στη δεύτερη περίπτωση η τροφοδοσία πραγματοποιείται από τη βάση (Σχήμα 8.17). Σχήμα 8.17: Χύτευση με (α) απόχυση εκ των άνω και (β) απόχυση κατ αναρροή. Ακόμη με βάση τον ρυθμό απόχυσης του τήγματος, υπάρχει η διάκριση σε συνεχή χύτευση και σε χύτευση κατά ποσότητες. Παρακάτω περιγράφονται συνοπτικά μερικές από τις πιο κοινές μεθόδους χύτευσης: η αμμοχύτευση, η χύτευση επένδυσης, η χύτευση σε μόνιμο καλούπι (υπό πίεση) και η συνεχής χύτευση ΑΜΜΟΧΥΤΕΥΣΗ Η αμμοχύτευση είναι ίσως η πιο κοινή και απλή μέθοδος χύτευσης, η οποία χρησιμοποιείται για αιώνες. Ως υλικό κατασκευής του καλουπιού χρησιμοποιείται κοινή άμμος. Αρχικά κατασκευάζεται ένα μοντέλο από ξύλο, πλαστικό ή αν η καταπόνηση είναι μεγάλη από μέταλλο (Σχήμα 8.18). 92
94 Σχήμα 8.18: Μεταλλικά μοντέλα. Επίσης, όταν το χυτό έχει κοιλότητες χρησιμοποιούνται πυρήνες (καρδιές) από ειδική άμμο (Σχήμα 8.19). Σχήμα 8.19: Διάφορες καρδιές έτοιμες για χρήση. Το μοντέλο και οι καρδιές είναι συχνά διαιρούμενα. Στη συνέχεια ένα καλούπι που αποτελείται από δυο τμήματα κατασκευάζεται συμπιέζοντας άμμο γύρω από το μοντέλο. Πρώτα πληρώνεται με άμμο η κάτω κάσα που περιέχει το μισό μοντέλο, και μετά πληρώνεται η επάνω κάσα που περιέχει το άλλο μισό μοντέλο. Στη συνέχεια η κάθε κάσα τοποθετείται στη θέση της. Επίσης τοποθετούνται οι κώνοι για το σχηματισμό των ανοιγμάτων τροφοδοσίας, εξαερισμού καθώς και των αποθηκών τροφοδοσίας (προσεπιχωνεύματα). Ακολουθεί η πλήρωση με άμμο. Κατόπιν διαχωρίζεται το καλούπι και αφαιρούνται το μοντέλο, οι κώνοι τροφοδοσίας και εξαερισμού. Στο τέλος τοποθετείται η καρδιά στη θέση της, εφόσον απαιτείται, και ακολουθεί η χύτευση (Σχήματα 8.20 και 8.21). 93
95 Σχήμα 8.20: Αποτυπώματα των μοντέλων στην άμμο. Σχήμα 8.21: Αμμοχύτευση χυτοσιδήρου. Τα κανάλια τροφοδοσίας θα πρέπει να βρίσκονται σε τέτοια θέση ώστε να διευκολύνουν τη ροή του λιωμένου μετάλλου, προκειμένου να ελαχιστοποιούνται τα εσωτερικά ελαττώματα κατά τη χύτευση. Με αμμοχύτευση κατασκευάζονται προϊόντα όπως, κυλινδροκεφαλές κινητήρων αυτοκινήτων, βάσεις βαγονιών, πυροσβεστικοί κρουνοί, καθώς και μεγάλοι σύνδεσμοι σωληνώσεων. 94
96 Στο Σχήμα 8.22 παρουσιάζονται γωνίες νερού οχημάτων, οι οποίες μπορούν να μορφοποιηθούν είτε με αμμοχύτευση, είτε με χύτευση σε μόνιμο καλούπι. Σχήμα 8.22: Γωνίες νερού, χύτευση σε άμμο ή μεταλλικό τύπο (sand casting, permanent casting) ΧΥΤΕΥΣΗ ΕΠΕΝΔΥΣΗΣ Η χύτευση επένδυσης (γνωστή ως χύτευση απωλεσθέντος κεριού), είναι ένα είδος χύτευσης που χρησιμοποιείται εδώ και 5000 χρόνια. Είτε με χρήση κεριού μέλισσας, είτε με χρήση των σημερινών υψηλής τεχνολογίας κεριών, πάντοτε με τη μέθοδο αυτή κατασκευάζονται χυτά με μεγάλη ακρίβεια στις διαστάσεις και υψηλή ποιότητα στην επιφάνεια. Στη μέθοδο επένδυσης το μοντέλο κατασκευάζεται από κερί ή πλαστικό με χαμηλό σημείο τήξης. Γύρω από το μοντέλο χύνεται ένα ρευστό διάλυμα, συνήθως γύψος ή άλλο κεραμικό, το οποίο σχηματίζει μια επένδυση, που αποτελεί το καλούπι του χυτού. Στη συνέχεια το καλούπι θερμαίνεται, έτσι ώστε να λιώσει το μοντέλο αφήνοντας μια κοιλότητα στο επιθυμητό σχήμα. Ένα πλεονέκτημα της μεθόδου αυτής είναι ότι το κερί μπορεί να επαναχρησιμοποιηθεί. Αυτή η τεχνική εφαρμόζεται όταν απαιτείται η αναπαραγωγή πολύπλοκων λεπτομερειών, καμπυλών καθώς και έξοχο φινίρισμα. Αν και γενικά αυτή η μέθοδος χρησιμοποιείται για την χύτευση μικρών αντικειμένων π.χ. στην κοσμηματοποιία και στην οδοντοτεχνική, επίσης χρησιμοποιείται για την παραγωγή ολόκληρων σκελετών πορτών αεροπλάνων. Επιπλέον, τα πτερύγια σε αεροστροβίλους και αεροπροωθούμενες μηχανές είναι χυτά επένδυσης. Στο Σχήμα 8.23 παρουσιάζεται ένα κάλυμμα βαλβίδας, που έχει κατασκευαστεί με τη μέθοδο επένδυσης.. 95
97 Σχήμα 8.23: Κάλυμμα βαλβίδας, χύτευση επένδυσης (investment casting) ΧΥΤΕΥΣΗ ΣΕ ΜΟΝΙΜΟ ΚΑΛΟΥΠΙ ΥΠΟ ΠΙΕΣΗ Στη χύτευση σε μόνιμο καλούπι, το λιωμένο μέταλλο διοχετεύεται στην κοιλότητα του καλουπιού υπό πίεση, η οποία διατηρείται σε όλη την διάρκεια της στερεοποίησης. Το καλούπι κατασκευάζεται από μέταλλο και αποτελείται από δυο τμήματα. Όταν το μέταλλο στερεοποιηθεί τα δυο τμήματα ανοίγουν και εξάγεται το χυτό (Σχήμα 8.24). Σχήμα 8.24: Χύτευση σε μόνιμο καλούπι (υπό πίεση). Τα περισσότερα καλούπια κατασκευάζονται από μη σιδηρούχα μέταλλα, όπως κράματα ψευδαργύρου, χαλκού και αλουμινίου. Σιδηρούχα μέταλλα μπορούν επίσης να χρησιμοποιηθούν για την κατασκευή των καλουπιών. Οι υψηλοί ρυθμοί χύτευσης, καθώς και 96
98 η χρησιμοποίηση του ίδιου καλουπιού για χιλιάδες χυτεύσεις καθιστούν αυτή τη μέθοδο αρκετά οικονομική. Η χύτευση υπό πίεση είναι ιδιαίτερα κατάλληλη για την παραγωγή μικρού και μεσαίου μεγέθους εξαρτημάτων με υψηλή ποιότητα επιφάνειας, αναπαραγωγή λεπτομερειών και διαστασιακή σταθερότητα. Συνήθως η τεχνική προσφέρεται για την χύτευση κραμάτων αλουμινίου, ψευδαργύρου και μαγνησίου, τα οποία έχουν χαμηλό σημείο τήξεως. Στο Σχήμα 8.25 παρουσιάζεται μια τροχαλία οχημάτων, που μορφοποιήθηκε με χύτευση υπό πίεση. Σχήμα 8.25: Τροχαλία, χύτευση υπό πίεση (die casting) ΣΥΝΕΧΗΣ ΧΥΤΕΥΣΗ Στην συνεχή χύτευση το λιωμένο μέταλλο, στο τέλος της διαδικασίας εξαγωγής του από τα ορυκτό, στερεοποιείται στη μορφή ημιτελών προϊόντων, όπως κορμών (blooms), μπιγιετών (billets) ή πλακών (slabs) (βλ. Σχήμα 12.42, Κεφ. 12). Τα τελευταία είναι κατάλληλα ως αρχικό υλικό για επακόλουθες διεργασίες μορφοποίησης (π.χ. έλασης, διέλασης, κλπ.). Πριν την εισαγωγή της συνεχούς χύτευσης, το λιωμένο μέταλλο λάμβανε τη μορφή του, αποκλειστικά, με χύτευση κατά ποσότητες, σε μεγάλα μεταλλικά καλούπια (κοκίλ). Έτσι σχηματιζόταν μεγάλα χυτεύματα, γνωστά ως χελώνες ή πλινθώματα (ingots). Ωστόσο, πριν τη χρήση των χελωνών, κατά κανόνα απαιτείται μια προκαταρκτική διεργασία έλασης για το σχηματισμό κορμών, μπιγιετών ή πλακών, τα οποία στη συνέχεια χρησιμοποιούνται για την παραγωγή τελικών προϊόντων. Με τη συνεχή χύτευση, μπορούν να παραχθούν μικρότερες διατομές, με συνέπεια να μπορεί να παραλειφθεί η προκαταρκτική έλαση, στην οποία υπόκεινται τα πλινθώματα. Η εφαρμογή της συνεχούς χύτευσης επιτρέπει την παραγωγή ημιτελών προϊόντων διαφόρων διατομών με καλύτερη ποιότητα και μικρότερο κόστος παραγωγής. Επιπλέον, η συνεχής χύτευση είναι ιδιαίτερα αυτοματοποιημένη και αποδοτική. Η συνεχής χύτευση χρησιμοποιείται πιο συχνά για τη χύτευση χάλυβα (βάσει ποσοτικών κριτηρίων). Επίσης χρησιμοποιείται για τη χύτευση χαλκού και αλουμινίου. Στη συνεχή χύτευση το λιωμένο μέταλλο εκχύνεται στη χοάνη χύτευσης (Σχήμα 8.26). Στη συνέχεια, μετά την υποβολή του μετάλλου σε επεξεργασίες όπως κραματοποίηση και απαέρωση και αφού φθάσει στη σωστή θερμοκρασία, το τήγμα ρέει σε ένα ή περισσότερα υδρόψυκτα καλούπια από χαλκό (κοκίλ). Στα καλούπια το εξωτερικό στρώμα του μετάλλου 97
99 στερεοποιείται, ενώ το εσωτερικό του είναι ακόμη ρευστό. Η δημιουργούμενη ράβδος, όπως αποκαλείται τώρα, έλκεται συνεχώς προς τα κάτω, έξω από τη βάση του καλουπιού. Στη συνέχεια, η ράβδος υποστηριζόμενη από ράουλα, ψεκάζεται με νερό, με αποτέλεσμα τη στερεοποίηση ολόκληρης της διατομής. Μετά από την έξοδό της από τους χώρους ψεκασμού, η ράβδος περνάει από τα ράουλα έλξης και ευθυγράμμισης. Σε αυτό το σημείο, προκειμένου να αξιοποιηθεί η θερμή κατάσταση της ράβδου, μπορεί να πραγματοποιηθεί θερμή έλαση ή εξώθηση ή άλλη διεργασία μορφοποίησης, έτσι ώστε η ράβδος να αποκτήσει ένα επιθυμητό αρχικό σχήμα. Στο τέλος η ράβδος κόβεται με μηχανικά πριόνια ή φλόγα σε συγκεκριμένα μήκη. Σχήμα 8.26: Σχηματικά αναπαράσταση συνεχούς χύτευσης. 1. Κάδος χύτευσης, 2. Ράβδος διακοπής ροής, 3. Ενδιάμεσο δοχείο, 4. Πυρίμαχος σωλήνας 5. Υδρόψυκτο καλούπι, 6. Ράουλα υποστήριξης, 7. Ζώνη κάμψης, 8. Πυρίμαχος σωλήνας, 9. Στάθμη τήγματος, 10. Μηνίσκος, 11. Μηχανή έλξης και ευθυγράμμισης, 12. Ημιτελής πλάκα. Α. Τήγμα, Β. Στερεοποιημένο μέταλλο, C. Σκουριά, D. Υδρόψυκτο καλούπι από χαλκό, Ε. Πυρίμαχο υλικό. Οι μηχανές συνεχούς χύτευσης είναι σχεδιασμένες για να παράγουν κορμούς, μπιγιέτες ή πλάκες: Οι πλάκες είναι ημιτελή προϊόντα, των οποίων το πλάτος είναι συνήθως πολύ μεγαλύτερο από το πάχος τους. o Οι συνήθεις πλάκες έχουν πλάτος mm, πάχος mm και μήκος έως 12 m. o Υπάρχουν πλάκες με μεγαλύτερο πλάτος, π.χ. 3250x150mm. 98
100 o Υπάρχουν λεπτές πλάκες: 1680x50mm. o Οι τυπικές διαστάσεις ενός κορμού είναι συνήθως μεγαλύτερες από 200x200 mm π.χ. 560x400 mm. Το μήκος των κορμών είναι 4-10 m. Οι μπιγιέτες έχουν διαστάσεις μικρότερες από 200x200mm και μήκος που φθάνει τα 12m. Κολώνες με διαμέτρους 500 ή 140 mm. Δοκοί με διατομή σχήματος Ι, 1048x450 mm ή 438x381 mm. Δοκοί με διαστάσεις κοντά στις πραγματικές: 850x250 mm. Ταινίες: πάχος 2-5 mm και πλάτος mm. Υπάρχουν τρεις τύποι μηχανών συνεχούς χύτευσης: η οριζόντια, η κάθετη και ένας τρίτος τύπος, στον οποίο η ράβδος ακολουθεί καμπύλη πορεία (Σχήμα 8.25). Στο Σχήμα 8.27 παρουσιάζεται μια κάθετη μηχανή συνεχούς χύτευσης αλουμινίου, ενώ στο Σχήμα 8.28 παρουσιάζονται κολώνες και πλάκες πρωτόχυτου αλουμινίου. Χρησιμοποιείται ο όρος πρωτόχυτο για το αλουμίνιο που παράγεται με ηλεκτρόλυση της άνυδρης αλουμίνας, σε αντιδιαστολή με το δευτερόχυτο αλουμίνιο που ανακτάται από ανακύκλωση (ανάτηξη) μεταχειρισμένων προϊόντων. Σχήμα 8.27: Μηχανή συνεχούς χύτευσης αλουμινίου. 99
101 Σχήμα 8.28: Κολώνες και πλάκες πρωτόχυτου αλουμινίου ΔΟΜΗ ΧΥΤΟΥ Η κρυσταλλική δομή των πλινθωμάτων και των περισσότερων χυτών αποτελείται από τρεις δικριτές περιοχές ή ζώνες: τη ψυχρή ζώνη, την κιονική ζώνη και την ισοαξονική ζώνη. Στο Σχήμα 8.29 απεικονίζονται οι τρεις ζώνες. Σχήμα 8.29: Δομή χυτού όπου φαίνονται οι τρεις ζώνες: ψυχρή, κιονική και ισοαξονική ζώνη ( Ψυχρή ζώνη Αποτελείται από μικρούς ισοαξονικούς κόκκους. Κιονική ζώνη Μια ενδιάμεση περιοχή από επιμήκεις κόκκους, παράλληλους προς τη διεύθυνση της ροής της θερμότητας. Είναι ανεπιθύμητοι γιατί έχουν ανισοτροπικές ιδιότητες. Ισοαξονική ζώνη - Μια κεντρική περιοχή από ισοαξονικούς κρυστάλλους. Είναι επιθυμητοί γιατί έχουν ισοτροπικές ιδιότητες. Ο σχηματισμός αυτή της ζώνης ευνοείται από τη χρήση μικρής θερμοκρασίας έκχυσης, προσθήκης συστατικών που ενισχύουν την πυρήνωση. 100
102 8.4 ΔΙΑΦΟΡΕΣ ΤΕΧΝΙΚΕΣ ΚΟΝΙΟΜΕΤΑΛΛΟΥΡΓΙΑ Η κονιομεταλλουργία είναι μια τεχνική μορφοποίησης μεταλλικών αντικειμένων από μεταλλικές σκόνες. Αυτή περιλαμβάνει την ανάμιξη των μεταλλικών σκόνεων, τη συμπίεσή τους και ακολούθως τη θερμική κατεργασία τους (πυροσυσσωμάτωση). Η πυροσυσσωμάτωση (sintering) σε στερεά κατάσταση πραγματοποιείται σε θερμοκρασία χαμηλότερη του σημείου τήξης των συστατικών του μίγματος των σκόνεων, μέχρι που τα σωματίδια να κολλήσουν το ένα με το άλλο. Σε νεότερες τεχνικές τα στάδια της συμπίεσης και της πυροσυσσωμάτωσης πραγματοποιούνται ταυτόχρονα. Αυτή η μέθοδος παραδοσιακά χρησιμοποιήθηκε για την κατασκευή κεραμικών προϊόντων. Σήμερα χρησιμοποιείται όλο και περισσότερο για την παραγωγή ενός σημαντικού αριθμού προϊόντων. Στο Σχήμα 8.30 παρουσιάζεται σχηματικά μια τυπική διαδικασία παραγωγής προϊόντων κονιομεταλλουργίας. Σχήμα 8.30: Σχηματική κονιομεταλλουργίας. αναπαράσταση των σταδίων παραγωγής Η διαδικασία παραγωγής περιλαμβάνει τα παρακάτω στάδια: Ανάμιξη σκόνεων Συμπίεση Πυροσυσσωμάτωση Καλιμπράρισμα 101 αντικειμένων
103 Η παραγωγή των αντικειμένων επιτυγχάνεται με συμπίεση μεταλλικών σκόνεων σε μεγάλης ακρίβειας καλούπια, με ειδικές πρέσσες και μετά με πυροσυσσωμάτωση σε κατάλληλους φούρνους. Τα πυροσυσσωματωμένα αντικείμενα έχουν υψηλή ακρίβεια διαστάσεων και καλή ποιότητα επιφάνειας. Σε περίπτωση όμως που υπάρχουν υψηλές απαιτήσεις για αυτές τις ιδιότητες, τότε ακολουθεί και ένα βήμα καλιμπραρίσματος του αντικειμένου (συμπίεση εκ νέου). Ανάμιξη σκόνεων και συμπίεση Η κοκκομετρία των σκόνεων καθώς και το σχήμα των κόκκων επηρεάζουν σε σημαντικό βαθμό την ποιότητα του τελικού προϊόντος. Οι σκόνες παράγονται με φυσικές ή χημικές μεθόδους. o Φυσικές μέθοδοι Εξαιρετικά λεπτόκοκκες και με ομοιόμορφη δομή σκόνες παρασκευάζονται με εκνέφωση μεταλλικών τηγμάτων, παρουσία αδρανούς αερίου π.χ αργού, αζώτου για την αποφυγή οξείδωσης. Η τεχνική αυτή είναι γνωστή ως ξήρανση δια ψεκασμού (spray drying). o Χημικές μέθοδοι Σκόνες Fe, Cu, Mo και W παρασκευάζονται με αναγωγή των αντίστοιχων οξειδίων, σκόνες Fe, Ni με θερμική διάσπαση ενώσεών τους, σκόνες Fe, Cu και Be με ηλεκτρόλυση, σκόνες Ni και Cu με καταβύθιση από διάλυμα και σκόνη Ti με αναγωγή από τήγμα άλατός του. Σύμφωνα με τις φυσικές ιδιότητες του υπό κατασκευή εξαρτήματος αρκετές σκόνες αναμιγνύονται με ποικίλες αναλογίες. Στη συνέχεια αυτές συμπιέζονται σε πρέσσες με την εφαρμογή μονοαξονικής πίεσης ή πίεσης που εφαρμόζεται από πολλές κατευθύνσεις. Το πορώδες του συμπιέσματος εξαρτάται από την πίεση και την κοκκομετρία των πρώτων υλών. Με εφαρμογή μικρών πιέσεων κατασκευάζονται εξαρτήματα όπως, αντιτριβικοί δακτύλιοι και πορώδη φίλτρα. Αντίθετα υψηλής αντοχής εξαρτήματα κατασκευάζονται με εφαρμογή υψηλών πιέσεων. Πυροσυσσωμάτωση Με την πυροσυσσωμάτωση το συμπίεσμα αποκτά την τελική του αντοχή. Η πυροσυσσωμάτωση είναι μια θερμική κατεργασία κατά την οποία γειτονικά μεταλλικά σωματίδια συνδέονται μεταξύ τους, με αποτέλεσμα την αύξηση των τελικών ιδιοτήτων του υλικού. Μεταξύ των κόκκων δημιουργούνται γέφυρες, με τη μορφή λαιμών, που συνδέουν τους κόκκους μεταξύ τους (Σχήμα 8.31). Άτομα από τους κόκκους μεταφέρονται στην περιοχή του λαιμού, μέσω διάχυσης καθώς και άλλων μηχανισμών μεταφοράς μάζας, με αποτέλεσμα την ανάπτυξή τους. Ταυτόχρονα οι πόροι αρχίζουν να αποκτούν σφαιρική μορφή. Καθώς η μεταφορά μάζας συνεχίζεται το αρχικό συνεχές πλέγμα πόρων δίνει τη θέση του σε μεμονωμένους πόρους, οι οποίοι γίνονται περισσότερο σφαιρικοί και το μέγεθός τους μειώνεται (Σχήμα 8.32). Το τελικό στάδιο της πυροσυσσωμάτωσης είναι η ψύξη του αντικειμένου. 102
104 Σχήμα 8.31: Ηλεκτρονική μικροφωτογραφία των λαιμών που συνδέουν τους κόκκους. Σχήμα 8.32: Σχηματική αναπαράσταση της διαδικασίας πυροσυσσωμάτωσης. Τεχνικές κονιομεταλλουργίας Οι τεχνικές κονιομεταλλουργίας διακρίνονται σε τεχνικές, στις οποίες το στάδιο πυροσυσσωμάτωσης ακολουθεί το στάδιο συμπίεσης και σε τεχνικές, στις οποίες η πυροσυσσωμάτωση πραγματοποιείται ταυτόχρονα με τη συμπίεση. Στην περίπτωση που η μορφοποίηση πραγματοποιείται σε δυο στάδια, όταν εφαρμόζεται μονοαξονική πίεση η τεχνική αποκαλείται απλώς συμπίεση, ενώ όταν εφαρμόζεται πίεση από πολλές διευθύνσεις αποκαλείται ισοστατική συμπίεση. Στην περίπτωση του συνδυασμού των σταδίων της συμπίεσης και πυροσυσσωμάτωσης, οι αντίστοιχες τεχνικές αποκαλούνται συμπίεση εν θερμώ (Hot Pressing) (Σχήμα 8.33) και ισοστατική συμπίεση εν θερμώ (Hot Isostatic Pressure, HIP) (Σχήμα 8.34). 103
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Βασικά σωματίδια της ύλης
 1 Βασικά σωματίδια της ύλης Τα βασικά σωματίδια της ύλης είναι τα άτομα, τα μόρια και τα ιόντα. «Άτομο ονομάζουμε το μικρότερο σωματίδιο της ύλης που μπορεί να πάρει μέρος στο σχηματισμό χημικών ενώσεων».
1 Βασικά σωματίδια της ύλης Τα βασικά σωματίδια της ύλης είναι τα άτομα, τα μόρια και τα ιόντα. «Άτομο ονομάζουμε το μικρότερο σωματίδιο της ύλης που μπορεί να πάρει μέρος στο σχηματισμό χημικών ενώσεων».
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ
 ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 2 Κατηγορίες Υλικών ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Παραδείγματα Το πεντάγωνο των υλικών Κατηγορίες υλικών 1 Ορυκτά Μέταλλα Φυσικές πηγές Υλικάπουβγαίνουναπότηγημεεξόρυξηήσκάψιμοή
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 2 Κατηγορίες Υλικών ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Παραδείγματα Το πεντάγωνο των υλικών Κατηγορίες υλικών 1 Ορυκτά Μέταλλα Φυσικές πηγές Υλικάπουβγαίνουναπότηγημεεξόρυξηήσκάψιμοή
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
ΕΤΥ-349 ΜΗΧΑΝΙΚΕΣ ΚΑΙ ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ
 ΕΤΥ-349 ΜΗΧΑΝΙΚΕΣ ΚΑΙ ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Χειμερινό εξάμηνο ακαδημαϊκού έτους 2017-2018 Τμήμα Επιστήμης και Τεχνολογία Υλικών, Πανεπιστήμιο Κρήτης Διδάσκων: Βασίλης Παλτόγλου email: vaspal@physics.uoc.gr
ΕΤΥ-349 ΜΗΧΑΝΙΚΕΣ ΚΑΙ ΘΕΡΜΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Χειμερινό εξάμηνο ακαδημαϊκού έτους 2017-2018 Τμήμα Επιστήμης και Τεχνολογία Υλικών, Πανεπιστήμιο Κρήτης Διδάσκων: Βασίλης Παλτόγλου email: vaspal@physics.uoc.gr
Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2
 Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
ΔΟΜΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΕΡΑΜΙΚΩΝ. Χ. Κορδούλης
 ΔΟΜΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΕΡΑΜΙΚΩΝ Χ. Κορδούλης ΚΕΡΑΜΙΚΑ ΥΛΙΚΑ Τα κεραμικά υλικά είναι ανόργανα µη μεταλλικά υλικά (ενώσεις μεταλλικών και μη μεταλλικών στοιχείων), τα οποία έχουν υποστεί θερμική κατεργασία
ΔΟΜΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΕΡΑΜΙΚΩΝ Χ. Κορδούλης ΚΕΡΑΜΙΚΑ ΥΛΙΚΑ Τα κεραμικά υλικά είναι ανόργανα µη μεταλλικά υλικά (ενώσεις μεταλλικών και μη μεταλλικών στοιχείων), τα οποία έχουν υποστεί θερμική κατεργασία
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
κυματικής συνάρτησης (Ψ) κυματική συνάρτηση
 Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό
 Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
5. Να βρείτε τον ατομικό αριθμό του 2ου μέλους της ομάδας των αλογόνων και να γράψετε την ηλεκτρονιακή δομή του.
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Θεωρία Μοριακών Τροχιακών (ΜΟ)
 Θεωρία Μοριακών Τροχιακών (ΜΟ) Ετεροπυρηνικά διατομικά μόρια ή ιόντα (πολικοί δεσμοί) Το πιο ηλεκτραρνητικό στοιχείο (με ατομικά τροχιακά χαμηλότερης ενεργειακής στάθμης) συνεισφέρει περισσότερο στο δεσμικό
Θεωρία Μοριακών Τροχιακών (ΜΟ) Ετεροπυρηνικά διατομικά μόρια ή ιόντα (πολικοί δεσμοί) Το πιο ηλεκτραρνητικό στοιχείο (με ατομικά τροχιακά χαμηλότερης ενεργειακής στάθμης) συνεισφέρει περισσότερο στο δεσμικό
Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων
 Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων Κβαντικοί αριθμοί Κύριος κβαντικός αριθμός (n) Αζιμουθιακός κβαντικός αριθμός (l) Μαγνητικός κβαντικός αριθμός (ml) Στροφορμή (Spin) ηλεκτρονίου κβαντικός
Κβαντική θεωρία και ηλεκτρονιακή δομή των ατόμων Κβαντικοί αριθμοί Κύριος κβαντικός αριθμός (n) Αζιμουθιακός κβαντικός αριθμός (l) Μαγνητικός κβαντικός αριθμός (ml) Στροφορμή (Spin) ηλεκτρονίου κβαντικός
Περιοδικό Σύστημα Ιστορική Εξέλιξη
 Περιοδικό Σύστημα Ιστορική Εξέλιξη Newlands (1864): ταξινόμηση στοιχείων κατά αύξουσα ατομική μάζα και σε οκτάβες H Li Be B C N O F Na Mg Al Si P S Cl K Ca Cr Ti Mn Fe Meyer (1865): σχέση ιδιοτήτων και
Περιοδικό Σύστημα Ιστορική Εξέλιξη Newlands (1864): ταξινόμηση στοιχείων κατά αύξουσα ατομική μάζα και σε οκτάβες H Li Be B C N O F Na Mg Al Si P S Cl K Ca Cr Ti Mn Fe Meyer (1865): σχέση ιδιοτήτων και
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων. Περιοδικός πίνακας. Σταυρακαντωνάκης Γιώργος Λύκειο Γαζίου Page 1
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 4 η σειρά διαφανειών Δημήτριος Λαμπάκης Ορισμός και ιδιότητες των μετάλλων Τα χημικά στοιχεία διακρίνονται σε μέταλλα (περίπου 70 τον αριθμό)
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 4 η σειρά διαφανειών Δημήτριος Λαμπάκης Ορισμός και ιδιότητες των μετάλλων Τα χημικά στοιχεία διακρίνονται σε μέταλλα (περίπου 70 τον αριθμό)
Δομή ενεργειακών ζωνών
 Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα
 1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα Θεωρία 3.1. Ποια είναι τα δομικά σωματίδια της ύλης; Τα άτομα, τα μόρια και τα ιόντα. 3.2. SOS Τι ονομάζεται άτομο
1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα Θεωρία 3.1. Ποια είναι τα δομικά σωματίδια της ύλης; Τα άτομα, τα μόρια και τα ιόντα. 3.2. SOS Τι ονομάζεται άτομο
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
ΕΝΟΤΗΤΑ 2η:Ταξινόμηση των στοιχείων-στοιχεία με ιδιαίτερο ενδιαφέρον
 ΕΝΟΤΗΤΑ 2η:Ταξινόμηση των στοιχείων-στοιχεία με ιδιαίτερο ενδιαφέρον 1. ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ανάγκη της ταξινόμησης των στοιχείων Ενώ στην αρχαιότητα ήταν γνωστά γύρω στα 13 περίπου στοιχεία, τον 18o αιώνα
ΕΝΟΤΗΤΑ 2η:Ταξινόμηση των στοιχείων-στοιχεία με ιδιαίτερο ενδιαφέρον 1. ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Η ανάγκη της ταξινόμησης των στοιχείων Ενώ στην αρχαιότητα ήταν γνωστά γύρω στα 13 περίπου στοιχεία, τον 18o αιώνα
ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ. Ενότητα 1: ΑΤΟΜΑ ΚΑΙ ΔΕΣΜΟΙ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 1: ΑΤΟΜΑ ΚΑΙ ΔΕΣΜΟΙ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 1: ΑΤΟΜΑ ΚΑΙ ΔΕΣΜΟΙ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα. Θεωρητικη αναλυση
 ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα Θεωρητικη αναλυση ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ στα στερεα Ομοιοπολικός δεσμός Ιοντικός δεσμός Μεταλλικός δεσμός Δεσμός του υδρογόνου Δεσμός van der Waals ΔΟΜΗ ΑΤΟΜΟΥ Στοιβάδες Χώρος κίνησης των
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα Θεωρητικη αναλυση ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ στα στερεα Ομοιοπολικός δεσμός Ιοντικός δεσμός Μεταλλικός δεσμός Δεσμός του υδρογόνου Δεσμός van der Waals ΔΟΜΗ ΑΤΟΜΟΥ Στοιβάδες Χώρος κίνησης των
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 1 η : Στοιχεία, Ιδιότητες. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
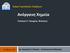 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 1 η : Στοιχεία, Ιδιότητες Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής 2 Οποιοδήποτε αντικείμενο στο περιβάλλον σχηματίζεται από τα μέχρι
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 1 η : Στοιχεία, Ιδιότητες Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής 2 Οποιοδήποτε αντικείμενο στο περιβάλλον σχηματίζεται από τα μέχρι
2.1 Ηλεκτρονική δοµή των ατόµων
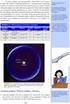 ΕΡΩΤΗΣΕΙΣ ΑΠΑΝΤΗΣΕΙΣ ΑΠΟ ΤΗΝ ΕΞΕΤΑΣΤΕΑ ΥΛΗ ΤΟΥ 2ου ΚΕΦΑΛΑΙΟΥ 2.1 Ηλεκτρονική δοµή των ατόµων ΕΡΩΤΗΣΗ 1 : Πως περιέγραψε ο Bohr την δοµή του ατόµου; ΑΠΑΝΤΗΣΗ : Ο Bohr φαντάστηκε το άτοµο σαν ένα µικροσκοπικό
ΕΡΩΤΗΣΕΙΣ ΑΠΑΝΤΗΣΕΙΣ ΑΠΟ ΤΗΝ ΕΞΕΤΑΣΤΕΑ ΥΛΗ ΤΟΥ 2ου ΚΕΦΑΛΑΙΟΥ 2.1 Ηλεκτρονική δοµή των ατόµων ΕΡΩΤΗΣΗ 1 : Πως περιέγραψε ο Bohr την δοµή του ατόµου; ΑΠΑΝΤΗΣΗ : Ο Bohr φαντάστηκε το άτοµο σαν ένα µικροσκοπικό
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός.
 2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ. Τ μαθητ : Σχολικό Έτος:
 Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής κατάστασης; 3 1.3
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής κατάστασης; 3 1.3
Καταστάσεις της ύλης. Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο.
 Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
Καταστάσεις της ύλης Αέρια: Παντελής απουσία τάξεως. Τα µόρια βρίσκονται σε συνεχή τυχαία κίνηση σε σχεδόν κενό χώρο. Υγρά: Τάξη πολύ µικρού βαθµού και κλίµακας-ελκτικές δυνάµεις-ολίσθηση. Τα µόρια βρίσκονται
Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Εισαγωγή σε προχωρημένες μεθόδους υπολογισμού στην Επιστήμη των Υλικών Χτίζοντας τους κρυστάλλους από άτομα Είδη δεσμών Διδάσκων : Επίκουρη Καθηγήτρια
1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ)
 ΣΧΟΛΗ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΜΠ ΤΕΧΝΙΚΑ ΥΛΙΚΑ 1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ) Ε. Βιντζηλαίου (Συντονιστής), Ε. Βουγιούκας, Ε. Μπαδογιάννης Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΣΧΟΛΗ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΜΠ ΤΕΧΝΙΚΑ ΥΛΙΚΑ 1 η ΕΝΟΤΗΤΑ ΔΟΜΙΚΑ ΥΛΙΚΑ (ΕΙΣΑΓΩΓΗ) Ε. Βιντζηλαίου (Συντονιστής), Ε. Βουγιούκας, Ε. Μπαδογιάννης Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Εργαστήριο Τεχνολογίας Υλικών
 Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 01 Κατηγοριοποιήση υλικών-επίδειξη δοκιμίων Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών
Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 01 Κατηγοριοποιήση υλικών-επίδειξη δοκιμίων Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ. Χημεία της ζωής 1
 ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
ΚΕΦΑΛΑΙΟ 2 Ο H XHΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημεία της ζωής 1 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ Η Βιολογία μπορεί να μελετηθεί μέσα από πολλά και διαφορετικά επίπεδα. Οι βιοχημικοί, για παράδειγμα, ενδιαφέρονται περισσότερο
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1
 ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1 Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΝΙΚΟΛΑΟΣ ΚΟΥΤΡΟΥΜΑΝΗΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 5 Μαρτίου 2015 2 ο Φροντιστήριο 1) Ποια είναι τα ηλεκτρόνια σθένους και ποιός ο ρόλος τους;
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1 Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΝΙΚΟΛΑΟΣ ΚΟΥΤΡΟΥΜΑΝΗΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 5 Μαρτίου 2015 2 ο Φροντιστήριο 1) Ποια είναι τα ηλεκτρόνια σθένους και ποιός ο ρόλος τους;
ηλεκτρονιακές Κατανοµή
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΧΗΜΙΚΟΙ ΕΣΜΟΙ 1. ίνεται ο πίκας: Σύµβολο Στοιχείου Να Ηλεκτρονιακή Κατανοµή X K (2) L(4) Ψ K (2) L(8) M(7) Ζ K (2) L(7) αντιγράψετε τον πίκα Οµάδα Π.Π. στη κόλλα Περίοδος Π.Π. σας τον
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΧΗΜΙΚΟΙ ΕΣΜΟΙ 1. ίνεται ο πίκας: Σύµβολο Στοιχείου Να Ηλεκτρονιακή Κατανοµή X K (2) L(4) Ψ K (2) L(8) M(7) Ζ K (2) L(7) αντιγράψετε τον πίκα Οµάδα Π.Π. στη κόλλα Περίοδος Π.Π. σας τον
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ
 ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ. Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών. Να εξηγούν το σχηματισμό του ιοντικού ομοιοπολικού δεσμού.
 ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
2. ΜΕΤΑΛΛΑ - ΚΡΑΜΑΤΑ. 2.2 Κύριοι χημικοί δεσμοί
 1 2. ΜΕΤΑΛΛΑ - ΚΡΑΜΑΤΑ 2.1 Γενικά Τα μικρότερα σωματίδια της ύλης, που μπορούν να βρεθούν ελεύθερα και να διατηρούν τις ιδιότητες του σώματος στο οποίο ανήκουν, λέγονται μόρια. Τα ελάχιστα σωματίδια της
1 2. ΜΕΤΑΛΛΑ - ΚΡΑΜΑΤΑ 2.1 Γενικά Τα μικρότερα σωματίδια της ύλης, που μπορούν να βρεθούν ελεύθερα και να διατηρούν τις ιδιότητες του σώματος στο οποίο ανήκουν, λέγονται μόρια. Τα ελάχιστα σωματίδια της
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Ερωτήσεις Σωστού Λάθους
 Ερωτήσεις Σωστού Λάθους Να χαρακτηρίσετε τις παρακάτω προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ) και να αιτιολογήσετε την απάντησή σας. 1. Το ιόν του νατρίου, 11 Na +, προκύπτει όταν το άτομο του Na προσλαμβάνει
Ερωτήσεις Σωστού Λάθους Να χαρακτηρίσετε τις παρακάτω προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ) και να αιτιολογήσετε την απάντησή σας. 1. Το ιόν του νατρίου, 11 Na +, προκύπτει όταν το άτομο του Na προσλαμβάνει
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις
 Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις Ακολουθώντας τους κανόνες δόμησης των πολυηλεκτρονιακών ατόμων που αναπτύχθηκαν παραπάνω, θα διαπιστώσουμε ότι σε ορισμένες περιπτώσεις παρατηρούνται αποκλίσεις
Εξαιρέσεις στις ηλεκτρονιακές διαμορφώσεις Ακολουθώντας τους κανόνες δόμησης των πολυηλεκτρονιακών ατόμων που αναπτύχθηκαν παραπάνω, θα διαπιστώσουμε ότι σε ορισμένες περιπτώσεις παρατηρούνται αποκλίσεις
Ατομική Ακτίνα ατομική ακτίνα δραστικού μείωση δραστικό πυρηνικό φορτίο και ο κύριος κβαντικός αριθμός των εξωτ. ηλεκτρονίων
 ATOMIKH AKTINA Ατομική Ακτίνα ορίζεται ως το μισό της απόστασης μεταξύ δύο γειτονικών ατόμων, όπως αυτά διατάσσονται στο κρυσταλλικό πλέγμα του στοιχείου. Η ατομική ακτίνα ενός στοιχείου: Κατά μήκος μιας
ATOMIKH AKTINA Ατομική Ακτίνα ορίζεται ως το μισό της απόστασης μεταξύ δύο γειτονικών ατόμων, όπως αυτά διατάσσονται στο κρυσταλλικό πλέγμα του στοιχείου. Η ατομική ακτίνα ενός στοιχείου: Κατά μήκος μιας
Αριθµόςοξείδωσηςενός ιόντος σε µια ιοντική (ετεροπολική) ένωση είναι το πραγµατικό ηλεκτρικό φορτίο του ιόντος.
 Αριθµόςοξείδωσηςενός ιόντος σε µια ιοντική (ετεροπολική) ένωση είναι το πραγµατικό ηλεκτρικό φορτίο του ιόντος. Αριθµόςοξείδωσηςενός ατόµου σε µια οµοιοπολική ένωση είναι το φαινοµενικό ηλεκτρικό φορτίο
Αριθµόςοξείδωσηςενός ιόντος σε µια ιοντική (ετεροπολική) ένωση είναι το πραγµατικό ηλεκτρικό φορτίο του ιόντος. Αριθµόςοξείδωσηςενός ατόµου σε µια οµοιοπολική ένωση είναι το φαινοµενικό ηλεκτρικό φορτίο
ΤΕΧΝΟΛΟΓΙΑ ΥΛΙΚΩΝ ΜΑΘΗΜΑ 1 Ο ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ. Δρ. M.Χανιάς Αν.Καθηγητής Τμήμα Ηλεκτρολόγων Μηχανικών ΤΕ, ΤΕΙ Ανατολικής Μακεδονίας και Θράκης
 ΤΕΧΝΟΛΟΓΙΑ ΥΛΙΚΩΝ ΜΑΘΗΜΑ 1 Ο ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Δρ. M.Χανιάς Αν.Καθηγητής Τμήμα Ηλεκτρολόγων Μηχανικών ΤΕ, ΤΕΙ Ανατολικής Μακεδονίας και Θράκης ΚΑΒΑΛΑ 018 1 1. ΕΙΣΑΓΩΓΗ ΣΤΑ ΥΛΙΚΑ. ΑΓΩΓΙΜΑ ΥΛΙΚΑ 3. ΗΜΙΑΓΩΓΟΙ
ΤΕΧΝΟΛΟΓΙΑ ΥΛΙΚΩΝ ΜΑΘΗΜΑ 1 Ο ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Δρ. M.Χανιάς Αν.Καθηγητής Τμήμα Ηλεκτρολόγων Μηχανικών ΤΕ, ΤΕΙ Ανατολικής Μακεδονίας και Θράκης ΚΑΒΑΛΑ 018 1 1. ΕΙΣΑΓΩΓΗ ΣΤΑ ΥΛΙΚΑ. ΑΓΩΓΙΜΑ ΥΛΙΚΑ 3. ΗΜΙΑΓΩΓΟΙ
1o Kριτήριο Αξιολόγησης
 1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 11-11-2012
 ΘΕΜΑ Α ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 11-11-2012 Για τις ερωτήσεις Α.1 έως Α.5 να γράψετε το γράμμα που αντιστοιχεί στη σωστή απάντηση δίπλα στον αριθμό της ερώτησης. Α.1 Τα χημικά στοιχεία μιας κύριας ομάδας
ΘΕΜΑ Α ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ 11-11-2012 Για τις ερωτήσεις Α.1 έως Α.5 να γράψετε το γράμμα που αντιστοιχεί στη σωστή απάντηση δίπλα στον αριθμό της ερώτησης. Α.1 Τα χημικά στοιχεία μιας κύριας ομάδας
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ. Τ μαθητ : Σχολικό Έτος: vyridis.weebly.com
 Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: vyridis.weebly.com 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: vyridis.weebly.com 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. Όλα τα Σωστό-Λάθος της τράπεζας θεμάτων για τη Χημεία Α Λυκείου
 Όλα τα Σωστό-Λάθος της τράπεζας θεμάτων για τη Χημεία Α Λυκείου 1. Το ιόν του νατρίου, 11Νa +, προκύπτει όταν το άτομο του Na προσλαμβάνει ένα ηλεκτρόνιο. Λ, όταν αποβάλλει ένα ηλεκτρόνιο 2. Σε 2 mol NH3
Όλα τα Σωστό-Λάθος της τράπεζας θεμάτων για τη Χημεία Α Λυκείου 1. Το ιόν του νατρίου, 11Νa +, προκύπτει όταν το άτομο του Na προσλαμβάνει ένα ηλεκτρόνιο. Λ, όταν αποβάλλει ένα ηλεκτρόνιο 2. Σε 2 mol NH3
Ζαχαριάδου Φωτεινή Σελίδα 1 από 21. Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου
 Ζαχαριάδου Φωτεινή Σελίδα 1 από 21 Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου Θέµατα Σωστού/Λάθους και Πολλαπλής επιλογής Πανελληνίων, ΟΕΦΕ, ΠΜ Χ Το 17Cl σχηµατίζει ενώσεις µε ένα µόνο
Ζαχαριάδου Φωτεινή Σελίδα 1 από 21 Γ Λυκείου Κατεύθυνσης Κεφάλαιο 1: Ηλεκτρονιακή δοµή του ατόµου Θέµατα Σωστού/Λάθους και Πολλαπλής επιλογής Πανελληνίων, ΟΕΦΕ, ΠΜ Χ Το 17Cl σχηµατίζει ενώσεις µε ένα µόνο
ΜΗΧΑΝΙΚΗ ΤΩΝ ΥΛΙΚΩΝ 2016
 ΜΗΧΑΝΙΚΗ ΤΩΝ ΥΛΙΚΩΝ 2016 Κεραμικών και Πολυμερικών Υλικών Κώστας Γαλιώτης, καθηγητής Τμήμα Χημικών Μηχανικών galiotis@chemeng.upatras.gr 1 Εισαγωγή Όπως ήδη είδαμε, η μηχανική συμπεριφορά των υλικών αντανακλά
ΜΗΧΑΝΙΚΗ ΤΩΝ ΥΛΙΚΩΝ 2016 Κεραμικών και Πολυμερικών Υλικών Κώστας Γαλιώτης, καθηγητής Τμήμα Χημικών Μηχανικών galiotis@chemeng.upatras.gr 1 Εισαγωγή Όπως ήδη είδαμε, η μηχανική συμπεριφορά των υλικών αντανακλά
Μεταβολή ορισμένων περιοδικών ιδιοτήτων
 Μεταβολή ορισμένων περιοδικών ιδιοτήτων 1. Ερώτηση: Ποια θεωρούνται θεμελιώδη χαρακτηριστικά του ατόμου και γιατί; Θεμελιώδη χαρακτηριστικά του ατόμου είναι: η ατομική ακτίνα, η ενέργεια ιοντισμού και
Μεταβολή ορισμένων περιοδικών ιδιοτήτων 1. Ερώτηση: Ποια θεωρούνται θεμελιώδη χαρακτηριστικά του ατόμου και γιατί; Θεμελιώδη χαρακτηριστικά του ατόμου είναι: η ατομική ακτίνα, η ενέργεια ιοντισμού και
Μάθημα 23 ο. Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις
 Μάθημα 23 ο Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις Μεταλλικός Δεσμός Μοντέλο θάλασσας ηλεκτρονίων Πυρήνες σε θάλασσα e -. Μεταλλική λάμψη. Ολκιμότητα. Εφαρμογή δύναμης Γενική και
Μάθημα 23 ο Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις Μεταλλικός Δεσμός Μοντέλο θάλασσας ηλεκτρονίων Πυρήνες σε θάλασσα e -. Μεταλλική λάμψη. Ολκιμότητα. Εφαρμογή δύναμης Γενική και
Κατανομή μετάλλων και αμετάλλων στον Π.Π.
 Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
2.3 ΜΕΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΕΤΑΛΛΩΝ. Επιμέλεια παρουσίασης Παναγιώτης Αθανασόπουλος Δρ - Χημικός
 2.3 ΜΕΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΕΤΑΛΛΩΝ Επιμέλεια παρουσίασης Παναγιώτης Αθανασόπουλος Δρ - Χημικός Σκοπός του μαθήματος: Να επισημαίνουμε τη θέση των μετάλλων στον περιοδικό πίνακα των στοιχείων. Να αναφέρουμε
2.3 ΜΕΡΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΕΤΑΛΛΩΝ Επιμέλεια παρουσίασης Παναγιώτης Αθανασόπουλος Δρ - Χημικός Σκοπός του μαθήματος: Να επισημαίνουμε τη θέση των μετάλλων στον περιοδικό πίνακα των στοιχείων. Να αναφέρουμε
Χημεία Γ Λυκείου Θετικής Κατεύθυνσης
 Χημεία Γ Λυκείου Θετικής Κατεύθυνσης Κεφάλαιο 1 Ηλεκτρονιακή δομή των ατόμων 1 Εισαγωγή Δομή του ατόμου Δημόκριτος Αριστοτέλης Dalton Thomson 400 π.χ. 350π.χ. 1808 1897 Απειροελάχιστα τεμάχια ύλης (τα
Χημεία Γ Λυκείου Θετικής Κατεύθυνσης Κεφάλαιο 1 Ηλεκτρονιακή δομή των ατόμων 1 Εισαγωγή Δομή του ατόμου Δημόκριτος Αριστοτέλης Dalton Thomson 400 π.χ. 350π.χ. 1808 1897 Απειροελάχιστα τεμάχια ύλης (τα
Χημεία Α Λυκείου. Ασκήσεις τράπεζας θεμάτων στο 2 ο Κεφάλαιο
 Χημεία Α Λυκείου Ασκήσεις τράπεζας θεμάτων στο 2 ο Κεφάλαιο 1) Θέμα 2530 (Ερώτημα 2.1. ) Δίνονται: υδρογόνο, 1 H, άζωτο, 7 N α) Να γράψετε την κατανομή των ηλεκτρονίων σε στιβάδες για το άτομο του αζώτου.
Χημεία Α Λυκείου Ασκήσεις τράπεζας θεμάτων στο 2 ο Κεφάλαιο 1) Θέμα 2530 (Ερώτημα 2.1. ) Δίνονται: υδρογόνο, 1 H, άζωτο, 7 N α) Να γράψετε την κατανομή των ηλεκτρονίων σε στιβάδες για το άτομο του αζώτου.
1.2. Ο ΣΙΔΗΡΟΣ ΚΑΙ ΤΑ ΚΡΑΜΑΤΑ ΤΟΥ.
 1.2. Ο ΣΙΔΗΡΟΣ ΚΑΙ ΤΑ ΚΡΑΜΑΤΑ ΤΟΥ. Ο σίδηρος πολύ σπάνια χρησιμοποιείται στη χημικά καθαρή του μορφή. Συνήθως είναι αναμεμειγμένος με άλλα στοιχεία, όπως άνθρακα μαγγάνιο, νικέλιο, χρώμιο, πυρίτιο, κ.α.
1.2. Ο ΣΙΔΗΡΟΣ ΚΑΙ ΤΑ ΚΡΑΜΑΤΑ ΤΟΥ. Ο σίδηρος πολύ σπάνια χρησιμοποιείται στη χημικά καθαρή του μορφή. Συνήθως είναι αναμεμειγμένος με άλλα στοιχεία, όπως άνθρακα μαγγάνιο, νικέλιο, χρώμιο, πυρίτιο, κ.α.
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 3 η σειρά διαφανειών Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα διατάσσονται στο χώρο ώστε να σχηματίσουν στερεά? Τύποι Στερεών
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 3 η σειρά διαφανειών Δημήτριος Λαμπάκης Τύποι Στερεών Βασική Ερώτηση: Πως τα άτομα διατάσσονται στο χώρο ώστε να σχηματίσουν στερεά? Τύποι Στερεών
Τίτλος Μαθήματος: Βασικές Έννοιες Φυσικής. Ενότητα: Στερεά. Διδάσκων: Καθηγητής Κ. Κώτσης. Τμήμα: Παιδαγωγικό, Δημοτικής Εκπαίδευσης
 Τίτλος Μαθήματος: Βασικές Έννοιες Φυσικής Ενότητα: Στερεά Διδάσκων: Καθηγητής Κ. Κώτσης Τμήμα: Παιδαγωγικό, Δημοτικής Εκπαίδευσης 7. Στερεά Η επιβεβαίωση ότι τα στερεά σώματα αποτελούνται από μια ιδιαίτερη
Τίτλος Μαθήματος: Βασικές Έννοιες Φυσικής Ενότητα: Στερεά Διδάσκων: Καθηγητής Κ. Κώτσης Τμήμα: Παιδαγωγικό, Δημοτικής Εκπαίδευσης 7. Στερεά Η επιβεβαίωση ότι τα στερεά σώματα αποτελούνται από μια ιδιαίτερη
διατήρησης της μάζας.
 6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
ΑΤΟΜΙΚΑ ΤΟΜΙΚΑ ΠΡΟΤΥΠΑ
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
2.9 Υποατομικά σωματίδια Ιόντα
 1 Ερωτήσεις θεωρίας με απαντήσεις 2.9 Υποατομικά σωματίδια Ιόντα 9-1. Ποια είναι τα «υποατομικά σωματίδια»: 1. Τα πρωτόνια (ρ). Κάθε πρωτόνιο είναι ένα θετικά φορτισμένο σωματίδιο με μία μονάδα θετικού
1 Ερωτήσεις θεωρίας με απαντήσεις 2.9 Υποατομικά σωματίδια Ιόντα 9-1. Ποια είναι τα «υποατομικά σωματίδια»: 1. Τα πρωτόνια (ρ). Κάθε πρωτόνιο είναι ένα θετικά φορτισμένο σωματίδιο με μία μονάδα θετικού
Επιστήμη των Υλικών. Πανεπιστήμιο Ιωαννίνων. Τμήμα Φυσικής
 Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Ατέλειες, διαταραχές και σχέση τους με τις μηχανικές ιδιότητες των στερεών (μεταλλικά στερεά) μικτή διαταραχή διαταραχή κοχλία
Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Ατέλειες, διαταραχές και σχέση τους με τις μηχανικές ιδιότητες των στερεών (μεταλλικά στερεά) μικτή διαταραχή διαταραχή κοχλία
ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ
 ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ 1. ΓΕΝΙΚΑ Από τις καταστάσεις της ύλης τα αέρια και τα υγρά δεν παρουσιάζουν κάποια τυπική διάταξη ατόμων, ενώ από τα στερεά ορισμένα παρουσιάζουν συγκεκριμένη διάταξη ατόμων
ΣΤΟΙΧΕΙΑ ΚΡΥΣΤΑΛΛΟΓΡΑΦΙΑΣ 1. ΓΕΝΙΚΑ Από τις καταστάσεις της ύλης τα αέρια και τα υγρά δεν παρουσιάζουν κάποια τυπική διάταξη ατόμων, ενώ από τα στερεά ορισμένα παρουσιάζουν συγκεκριμένη διάταξη ατόμων
2.2 Κατάταξη των στοιχείων (Περιοδικός Πίνακας) - Χρησιμότητα του Περιοδικού Πίνακα
 2.2 Κατάταξη των στοιχείων (Περιοδικός Πίνακας) - Χρησιμότητα του Περιοδικού Πίνακα Θεωρία 9.1. Τι είναι ο περιοδικός πίνακας; Αποτελεί μία από τις σημαντικότερες ανακαλύψεις στης Χημείας. Πρόκειται για
2.2 Κατάταξη των στοιχείων (Περιοδικός Πίνακας) - Χρησιμότητα του Περιοδικού Πίνακα Θεωρία 9.1. Τι είναι ο περιοδικός πίνακας; Αποτελεί μία από τις σημαντικότερες ανακαλύψεις στης Χημείας. Πρόκειται για
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις
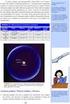 1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
ΝΟΜΟΣ ΤΗΣ ΠΕΡΙΟ ΙΚΟΤΗΤΑΣ : Οι ιδιότητες των χηµικών στοιχείων είναι περιοδική συνάρτηση του ατοµικού τους αριθµού.
 1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
1. Ο ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ Οι άνθρωποι από την φύση τους θέλουν να πετυχαίνουν σπουδαία αποτελέσµατα καταναλώνοντας το λιγότερο δυνατό κόπο και χρόνο. Για το σκοπό αυτό προσπαθούν να οµαδοποιούν τα πράγµατα
Ο Περιοδικός Πίνακας Φυσικές και Χημικές Ιδιότητες των Στοιχείων. Εισαγωγική Χημεία
 Ο Περιοδικός Πίνακας Φυσικές και Χημικές Ιδιότητες των Στοιχείων Εισαγωγική Χημεία 2013-14 1 Δομή του Π.Π. Γραμμές (περίοδοι) σύμφωνα με την σειρά συμπλήρωσης των τροχιακών (1 σειρά ανά κύριο κβαντικό
Ο Περιοδικός Πίνακας Φυσικές και Χημικές Ιδιότητες των Στοιχείων Εισαγωγική Χημεία 2013-14 1 Δομή του Π.Π. Γραμμές (περίοδοι) σύμφωνα με την σειρά συμπλήρωσης των τροχιακών (1 σειρά ανά κύριο κβαντικό
Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Πανεπιστήμιο Δυτικής Αττικής - ΣΑΕΤ
 Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
Γενική και Ανόργανη Χημεία Περιοδικές ιδιότητες των στοιχείων. Σχηματισμός ιόντων. Στ. Μπογιατζής 1 Αναπληρωτής Καθηγητής Τμήμα Συντήρησης Αρχαιοτήτων και Έργων Τέχνης Π Δ Χειμερινό εξάμηνο 2018-2019 Π
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ
 ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου. Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη
 Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος
 2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
Εισαγωγή. 1.1 Ο κόσμος των υλικών
 Εισαγωγή 1 1 Εισαγωγή Βατάλης Αργύρης 1.1 Ο κόσμος των υλικών Tα υλικά αποτελούν μέρος της βάσης όλων των τεχνολογικών εξελίξεων. Όλες οι ανθρώπινες δραστηριότητες και το επίπεδο ζωής επηρεάζονται σε μεγάλο
Εισαγωγή 1 1 Εισαγωγή Βατάλης Αργύρης 1.1 Ο κόσμος των υλικών Tα υλικά αποτελούν μέρος της βάσης όλων των τεχνολογικών εξελίξεων. Όλες οι ανθρώπινες δραστηριότητες και το επίπεδο ζωής επηρεάζονται σε μεγάλο
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα:
 ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΧΑΡΑΛΑΜΠΟΣ ΔΡΙΒΑΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 1 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 1. Τι τάξη μεγέθους είναι οι ενδοατομικές αποστάσεις και ποιες υποδιαιρέσεις του
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΧΑΡΑΛΑΜΠΟΣ ΔΡΙΒΑΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 1 η ΣΕΙΡΑ ΑΣΚΗΣΕΩΝ 1. Τι τάξη μεγέθους είναι οι ενδοατομικές αποστάσεις και ποιες υποδιαιρέσεις του
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
ΗΛΕΚΤΡΟΝΙΚΑ Ι ΚΕΦΑΛΑΙΟ 1 Ο :ΗΜΙΑΓΩΓΟΙ
 ΗΛΕΚΤΡΟΝΙΚΑ Ι ΚΕΦΑΛΑΙΟ 1 Ο :ΗΜΙΑΓΩΓΟΙ 1 1. ΗΛΕΚΤΡΙΚΗ ΔΟΜΗ. ΕΝΔΟΓΕΝΕΙΣ ΗΜΙΑΓΩΓΟΙ Δομή του ατόμου Σήμερα γνωρίζουμε ότι η ύλη αποτελείται από ενώσεις ατόμων, δημιουργώντας τις πολυάριθμες χημικές ενώσεις
ΗΛΕΚΤΡΟΝΙΚΑ Ι ΚΕΦΑΛΑΙΟ 1 Ο :ΗΜΙΑΓΩΓΟΙ 1 1. ΗΛΕΚΤΡΙΚΗ ΔΟΜΗ. ΕΝΔΟΓΕΝΕΙΣ ΗΜΙΑΓΩΓΟΙ Δομή του ατόμου Σήμερα γνωρίζουμε ότι η ύλη αποτελείται από ενώσεις ατόμων, δημιουργώντας τις πολυάριθμες χημικές ενώσεις
ΧΗΜΕΙΑ Β ΓΥΜΝΑΣΙΟΥ ΕΝΟΤΗΤΑ: 1.2
 ΕΝΟΤΗΤΑ: 1.2 Η ύλη συναντάται σε τρεις φυσικές καταστάσεις: Στερεή: έχει καθορισμένη μάζα, σχήμα και όγκο. Υγρή: έχει καθορισμένη μάζα και όγκο, ενώ σχήμα κάθε φορά παίρνει το σχήμα του δοχείου που το
ΕΝΟΤΗΤΑ: 1.2 Η ύλη συναντάται σε τρεις φυσικές καταστάσεις: Στερεή: έχει καθορισμένη μάζα, σχήμα και όγκο. Υγρή: έχει καθορισμένη μάζα και όγκο, ενώ σχήμα κάθε φορά παίρνει το σχήμα του δοχείου που το
Πρωτόνια, νετρόνια και ηλεκτρόνια. πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1
 Πρωτόνια, νετρόνια και ηλεκτρόνια. σχετική μάζα σχετικό φορτίο πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1 Ο πυρήνας βρίσκεται στο κέντρο του ατόμου και περιέχει
Πρωτόνια, νετρόνια και ηλεκτρόνια. σχετική μάζα σχετικό φορτίο πρωτόνιο 1 (1,67X10-24 g) +1 νετρόνιο 1 0 1,6X10-19 Cb ηλεκτρόνιο 1/1836 (9X10-28 g) -1 Ο πυρήνας βρίσκεται στο κέντρο του ατόμου και περιέχει
Μετά το τέλος της μελέτης του 2ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει τα βασικά σημεία του ατομικού προτύπου του Bohr.
 Μετά το τέλος της μελέτης του 2ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει τα βασικά σημεία του ατομικού προτύπου του Bohr. Να κατανέμει σε στιβάδες τα ηλεκτρόνια ατόμων και ιόντων.
Μετά το τέλος της μελέτης του 2ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει τα βασικά σημεία του ατομικού προτύπου του Bohr. Να κατανέμει σε στιβάδες τα ηλεκτρόνια ατόμων και ιόντων.
ΚΑΤΕΡΓΑΣΙΕΣ ΜΟΡΦΟΠΟΙΗΣΗΣ. Δρ. Φ. Σκιττίδης, Δρ. Π. Ψυλλάκη
 ΚΑΤΕΡΓΑΣΙΕΣ ΜΟΡΦΟΠΟΙΗΣΗΣ Δρ. Φ. Σκιττίδης, Δρ. Π. Ψυλλάκη ΔΙΕΡΓΑΣΙΕΣ ΠΑΡΑΓΩΓΗΣ ΠΡΟΪΟΝΤΩΝ Ορυκτά Πρώτες ύλες Κεραμικά Οργανικά υλικά (πετρέλαιο, άνθρακας) Μέταλλα (ελατά και όλκιμα) Μεταλλικός δεσμός Κεραμικά
ΚΑΤΕΡΓΑΣΙΕΣ ΜΟΡΦΟΠΟΙΗΣΗΣ Δρ. Φ. Σκιττίδης, Δρ. Π. Ψυλλάκη ΔΙΕΡΓΑΣΙΕΣ ΠΑΡΑΓΩΓΗΣ ΠΡΟΪΟΝΤΩΝ Ορυκτά Πρώτες ύλες Κεραμικά Οργανικά υλικά (πετρέλαιο, άνθρακας) Μέταλλα (ελατά και όλκιμα) Μεταλλικός δεσμός Κεραμικά
Μάθημα 12. ΓΝΩΡΙΖΟΥΜΕ ΠΕΡΙΣΣΟΤΕΡΟ ΤΑ ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ Έχουν τόσες διαφορές (αλλά και ομοιότητες στις φυσικές και στις χημικές τους ιδιότητες!
 Μάθημα 12 ΓΝΩΡΙΖΟΥΜΕ ΠΕΡΙΣΣΟΤΕΡΟ ΤΑ ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ Έχουν τόσες διαφορές (αλλά και ομοιότητες στις φυσικές και στις χημικές τους ιδιότητες! Τόσο από την εμπειρία μας, όσο και από τα προηγούμενα μαθήματα,
Μάθημα 12 ΓΝΩΡΙΖΟΥΜΕ ΠΕΡΙΣΣΟΤΕΡΟ ΤΑ ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ Έχουν τόσες διαφορές (αλλά και ομοιότητες στις φυσικές και στις χημικές τους ιδιότητες! Τόσο από την εμπειρία μας, όσο και από τα προηγούμενα μαθήματα,
Διάλεξη 7: Μοριακή Δομή
 Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Ονοματεπώνυμο: Χημεία Α Λυκείου Δομή του ατόμου Περιοδικός Πίνακας. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Δομή του ατόμου Περιοδικός Πίνακας Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Δομή του ατόμου Περιοδικός Πίνακας Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες
Επιστήμη των Υλικών. Πανεπιστήμιο Ιωαννίνων. Τμήμα Φυσικής
 Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Σημειακές ατέλειες Στοιχειακά στερεά Ατέλειες των στερεών Αυτοπαρεμβολή σε ενδοπλεγματική θέση Κενή θέση Αριθμός κενών θέσεων Q
Επιστήμη των Υλικών Πανεπιστήμιο Ιωαννίνων Τμήμα Φυσικής 2017 Α. Δούβαλης Σημειακές ατέλειες Στοιχειακά στερεά Ατέλειες των στερεών Αυτοπαρεμβολή σε ενδοπλεγματική θέση Κενή θέση Αριθμός κενών θέσεων Q
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ 1 ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ
 ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
ΚΕΦ.2 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ, ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ
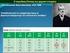 ΚΕΦ.2 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ, ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ Α. ΕΡΩΤΗΣΕΙΣ ΓΝΩΣΗΣ ΤΗΣ ΘΕΩΡΙΑΣ 2.1 Ποιοι κανόνες (3) εφαρμόζονται για την κατανομή των ηλεκτρονίων σε στιβάδες; Ποια ηλεκτρόνια έχουν μεγαλύτερη ενέργεια, αυτά
ΚΕΦ.2 ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ, ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ Α. ΕΡΩΤΗΣΕΙΣ ΓΝΩΣΗΣ ΤΗΣ ΘΕΩΡΙΑΣ 2.1 Ποιοι κανόνες (3) εφαρμόζονται για την κατανομή των ηλεκτρονίων σε στιβάδες; Ποια ηλεκτρόνια έχουν μεγαλύτερη ενέργεια, αυτά
Εργαστήριο Τεχνολογίας Υλικών
 Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 07 Εφελκυσμός Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ Θεόδωρος Λούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών Πάτρα 2011 1 Μηχανικές
Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 07 Εφελκυσμός Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ Θεόδωρος Λούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών Πάτρα 2011 1 Μηχανικές
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ 2 Η ΕΝΟΤΗΤΑ
 ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ 2 Η ΕΝΟΤΗΤΑ Ονοματεπώνυμο: Ημερομηνία: Επιμέλεια θεμάτων: Ειρήνη Χ. Μπαρμπούτη Σελίδα 1 ΕΡΩΤΗΣΗ 1 Για κάθε πρόταση να κυκλώσετε το γράμμα που αντιστοιχεί στη σωστή απάντηση: 1) Στο σύγχρονο
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ 2 Η ΕΝΟΤΗΤΑ Ονοματεπώνυμο: Ημερομηνία: Επιμέλεια θεμάτων: Ειρήνη Χ. Μπαρμπούτη Σελίδα 1 ΕΡΩΤΗΣΗ 1 Για κάθε πρόταση να κυκλώσετε το γράμμα που αντιστοιχεί στη σωστή απάντηση: 1) Στο σύγχρονο
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα 3ο μεροσ. Θεωρητικη αναλυση
 ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα 3ο μεροσ Θεωρητικη αναλυση μεταλλα Έχουν κοινές φυσικές ιδιότητες που αποδεικνύεται πως είναι αλληλένδετες μεταξύ τους: Υψηλή φυσική αντοχή Υψηλή πυκνότητα Υψηλή ηλεκτρική και θερμική
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα 3ο μεροσ Θεωρητικη αναλυση μεταλλα Έχουν κοινές φυσικές ιδιότητες που αποδεικνύεται πως είναι αλληλένδετες μεταξύ τους: Υψηλή φυσική αντοχή Υψηλή πυκνότητα Υψηλή ηλεκτρική και θερμική
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ
 ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ Ενεργειακές Ζώνες και Στατιστική Φορέων Φορτίου Required Text: Microelectronic Devices, Keith Leaver (2 nd Chapter) Εισαγωγή Στο προηγούμενο κεφάλαιο προσεγγίσαμε τους ημιαγωγούς
ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ Ενεργειακές Ζώνες και Στατιστική Φορέων Φορτίου Required Text: Microelectronic Devices, Keith Leaver (2 nd Chapter) Εισαγωγή Στο προηγούμενο κεφάλαιο προσεγγίσαμε τους ημιαγωγούς
1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα. Παράδειγμα 1.4. Παράδειγμα 1.5. Δομικά σωματίδια της ύλης
 Εύχρηστες όμως μονάδες είναι το g/ml (ή g/cm 3 ). Ειδικά στα αέρια, ό- που έχουμε μικρές πυκνότητες, συνήθως χρησιμοποιούμε το g/l. Παράδειγμα 1.4 Το αργίλιο (Al) είναι ένα πολύ εύχρηστο μέταλλο. Ένας
Εύχρηστες όμως μονάδες είναι το g/ml (ή g/cm 3 ). Ειδικά στα αέρια, ό- που έχουμε μικρές πυκνότητες, συνήθως χρησιμοποιούμε το g/l. Παράδειγμα 1.4 Το αργίλιο (Al) είναι ένα πολύ εύχρηστο μέταλλο. Ένας
Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων
 Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων Περιεχόμενα Κεφαλαίου 39 Τα άτομα από την σκοπιά της κβαντικής μηχανικής Το άτομο του Υδρογόνου: Η εξίσωση του Schrödinger και οι κβαντικοί αριθμοί ΟΙ κυματοσυναρτήσεις
Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων Περιεχόμενα Κεφαλαίου 39 Τα άτομα από την σκοπιά της κβαντικής μηχανικής Το άτομο του Υδρογόνου: Η εξίσωση του Schrödinger και οι κβαντικοί αριθμοί ΟΙ κυματοσυναρτήσεις
ΕΠΙΛΟΓΗ ΥΛΙΚΩΝ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΠΡΟΪΟΝΤΩΝ. Οικογενειακά δένδρα: οργάνωση υλικών και διεργασιών
 ΕΠΙΛΟΓΗ ΥΛΙΚΩΝ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΠΡΟΪΟΝΤΩΝ Οικογενειακά δένδρα: οργάνωση υλικών και διεργασιών 1 Επιτυχημένο προϊόν: Αποδίδει καλά. Καλή αξία σε σχέση με το κόστος. Προσφέρει ευχαρίστηση στον χρήστη. ΥΛΙΚΑ
ΕΠΙΛΟΓΗ ΥΛΙΚΩΝ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΠΡΟΪΟΝΤΩΝ Οικογενειακά δένδρα: οργάνωση υλικών και διεργασιών 1 Επιτυχημένο προϊόν: Αποδίδει καλά. Καλή αξία σε σχέση με το κόστος. Προσφέρει ευχαρίστηση στον χρήστη. ΥΛΙΚΑ
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Από πού προέρχεται η θερμότητα που μεταφέρεται από τον αντιστάτη στο περιβάλλον;
 3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό
 Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Θέμα 2. Για καθεμία από τις παρακάτω περιπτώσεις να
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Θέμα 2. Για καθεμία από τις παρακάτω περιπτώσεις να
ΚΕΦΑΛΑΙΟ 2 : ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ - ΕΣΜΟΙ 2.1
 Χηµεία Α Λυκείου Φωτεινή Ζαχαριάδου 1 από 6 ΚΕΦΑΛΑΙΟ 2 : ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ - ΕΣΜΟΙ 2.1 Ατοµικό πρότυπο του Τα ηλεκτρόνια κινούνται σε Στιβάδα ή φλοιός ή Bhr καθορισµένες (επιτρεπτές) τροχιές ενεργειακή
Χηµεία Α Λυκείου Φωτεινή Ζαχαριάδου 1 από 6 ΚΕΦΑΛΑΙΟ 2 : ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ - ΕΣΜΟΙ 2.1 Ατοµικό πρότυπο του Τα ηλεκτρόνια κινούνται σε Στιβάδα ή φλοιός ή Bhr καθορισµένες (επιτρεπτές) τροχιές ενεργειακή
