ΟΙ ΠΕΡΙ ΤΡΟΦΙΜΩΝ (ΕΛΕΓΧΟΣ ΚΑΙ ΠΩΛΗΣΗ) ΝΟΜΟΙ ΤΟΥ 1996 ΕΩΣ (Αρ. 3) ΤΟΥ 2001
|
|
|
- Εφθαλία Λαιμός
- 8 χρόνια πριν
- Προβολές:
Transcript
1 Ε.Ε. Παρ. III(I) 739 Κ.Δ.Π. 115/2002 Αρ. 3583, Αριθμός 115 Οι περί Μεθόδων Ανάλυσης ή Εξέτασης για τον Έλεγχο της Συμμόρφωσης Προσθέτων Τροφίμων με Καθοριζόμενα Κριτήρια Καθαρότητας Κανονισμοί του 2002, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των διατάξεων του άρθρου 29 της περί Τροφίμων (Έλεγχος και Πώληση) νομοθεσίας, αφού κατατέθηκαν στη Βουλή των Αντιπροσώπων και εγκρίθηκαν από αυτή, δημοσιεύονται στην Επίσημη Εφημερίδα της Δημοκρατίας σύμφωνα με το εδάφιο (3) του άρθρου 3 του περί Καταθέσεως στη Βουλή των Αντιπροσώπων των Κανονισμών που Εκδίδονται με Εξουσιοδότηση Νόμου, Νόμου (Ν. 99 του 1989 όπως τροποποιήθηκε από τον 227 του 1990). ΟΙ ΠΕΡΙ ΤΡΟΦΙΜΩΝ (ΕΛΕΓΧΟΣ ΚΑΙ ΠΩΛΗΣΗ) ΝΟΜΟΙ ΤΟΥ 1996 ΕΩΣ (Αρ. 3) ΤΟΥ 2001 Κανονισμοί, δυνάμει του άρθρου 29 Για σκοπούς εναρμόνισης με την πράξη της Ευρωπαϊκής Κοινότητας με τίτλο «Πρώτη Οδηγία της Επιτροπής της 28ης Ιουλίου 1981 περί καθορισμού των κοινοτικών μεθόδων αναλύσεως για τον έλεγχο των κριτηρίων καθαρότητας ορισμένων πρόσθετων υλών που χρησιμοποιούνται στα τρόφιμα (81/712/ ΕΟΚ)» (EEL 257" της , σ.1), Το Υπουργικό Συμβούλιο, ασκώντας τις εξοτισίες που χορηγούνται σ' αυτό από το άρθρο 29 των περί Τροφίμων (Έλεγχος και Πώληση) Νόμων του του 1996 έως εκδίδει τους ακόλουθους Κανονισμούς. ΙΟ^! του 1Έ[ 3 3 ^ = 122(1) του (1) του (1) του (1) του Οι παρόντες Κανονισμοί θα.αναφέρονται ως οι περί Μεθόδων Ανάλυ Συνοπτικός σης ή Εξέτασης, για τον Έλεγχο της Συμμόρφ(οσης Προσθέτων Τροφίμων με τιτλο * Καθοριζόμενα Κριτήρια Καθαρότητας Κανονισμοί του (1) Στους παρόντες Κανονισμούς Ερμηνεία. «πρόσθετο τροφίμων» σημαίνει οποιαδήποτε ουσία, με ή χωρίς θρεπτική αξία, που δεν καταναλώνεται συνήθως μόνη της ως τρόφιμο ούτε χρησιμοποιείται συνήθως ως χαρακτηριστικό συστατικό τροφίμων και της οποίας η σκόπιμη προσθήκη σε τρόφιμο, για τεχνολογικούς σκοπούς, κατά τη μεταποίηση, παρασκευή, συσκευασία, μεταφορά ή αποθήκευση του εν λόγω τροφίμου, έχει ως αποτέλεσμα ή αναμένεται λογικά να έχει ως αποτέλεσμα το να αποτελούν η ίδια ή τα παράγωγα της συστατικό στοιχείο του τροφίμου αυτού, άμεσα ή έμμεσα. (2) Οποιοιδήποτε άλλοι όροι, που περιέχονται στους παρόντες Κανονισμούς και δεν ερμηνεύονται διαφορετικά, έχουν την έννοια που τους αποδίδει ο Νόμος. 3. (1) Σε περίπτωση που εξουσιοδοτημένος λειτουργός υποβάλλει, δυνάμει Ανάλυση του Νόμου, δείγμα ή μέρος δείγματος προσθέτου τροφίμων, το οποίο καθόριζε ^.^ετ ση Γ. ται στο Πρώτο Παράρτημα, σε Κυβερνητικό Χημικό για ανάλυση ή εξέταση, ο εν ή μέρους' αυτ0υ σε λόγω Κυβερνητικός Χημικός ή πρόσωπο υπό τις οδηγίες και την άμεση επίβλεψη του, το συντομότερο δυνατό αναλύει ή, ανάλογα με την περίπτωση, εξετάζει το x^o' 1111 * 0 υποβαλλόμενο δείγμα ή μέρος δείγματος, βάσει των μεθόδων που καθορίζονται, Πρώτο αναφορικά με το εν λόγω πρόσθετο τροφίμων, στο Δεύτερο Παράρτημα, με Παράρτημα, σκοπό τον έλεγχο της συμμόρφωσης του εν λόγω προσθέτου τροφίμων με τα σχε παράοτημα. τικά προς αυτό κριτήρια καθαρότητας τα οποία τυχόν καθορίζονται σε εκάστοτε ισχύοντες Κανονισμούς δυνάμει του Νόμου.
2 Κ.Δ.Π. 115/ Δεύτεοο Παράρτημα. (2) Μετά το πέρας της αναφερόμενης στην παράγραφο (1) ανάλυσης ή εξέτασης, ο Κυβερνητικός Χημικός εκδίδει, και αποστέλλει ή παραδίδει στον εξουσιοδοτημένο λειτουργό, ο οποίος υπέβαλε το δείγμα ή μέρος του δείγματος, πιστοποιητικό ή, ανάλογα με την περίπτωση, εργαστηριακή έκθεση, σύμφωνα με τα διαλαμβανόμενα στις παραγράφους (β) και (δ) του εδαφίου (3) του άρθρου 15 του Νόμου, το οποίο πιστοποιητικό ή έκθεση καταδεικνύει το αποτέλεσμα της διενεργηθείσας ανάλυσης ή εξέτασης, όπως αυτό το αποτέλεσμα εκφράζεται σύμφωνα με τα διαλαμβανόμενα στο Δεύτερο Παράρτημα. (3) Το εδάφιο (4) του άρθρου 15 του Νόμου εφαρμόζεται αναφορικά με κάθε πιστοποιητικό και έκθεση που εκδίδεται δυνάμει, της παραγράφου (2). (4) Κάθε πρόσωπο, υπό την ευθύνη του οποίου Κ\)βερνητικό Χημείο λειτουργεί, λαμβάνει τα δέοντα μέτρα ώστε να διασφαλίζει τη συμμόρφωση κάθε Κυβερνητικού Χημικού, ο οποίος υπηρετεί ή εργάζεται στο εν λόγω Κυβερνητικό Χημείο, με τις παραγράφους (1) και (2).
3 741 Κ.Δ.Π. 115/2002 ΠΡΩΤΟ ΠΑΡΑΡΤΗΜΑ ( Κανονισμός 3(1)) ΠΡΟΣΘΕΤΑ ΤΡΟΦΙΜΩΝ ΤΑ ΟΠΟΙΑ ΚΥΒΕΡΝΗΤΙΚΟΣ ΧΗΜΙΚΟΣ Ή ΠΡΟΣΩΠΟ ΥΠΟ ΤΙΣ ΟΔΗΓΙΕΣ ΚΑΙ ΤΗΝ ΑΜΕΣΗ ΕΠΙΒΑΕΨΗ ΤΟΥ ΑΝΑΔΥΕΙ Ή ΕΞΕΤΑΖΕΙ ΒΑΣΕΙ ΤΩΝ ΜΕΘΟΔΩΝ ΟΙ ΟΠΟΙΕΣ ΚΑΘΟΡΙΖΟΝΤΑΙ, ΑΝΑΦΟΡΙΚΑ ΜΕ ΕΚΑΣΤΟ ΤΕΤΟΙΟ ΠΡΟΣΘΕΤΟ ΤΡΟΦΙΜΩΝ, ΣΤΟ ΔΕΥΤΕΡΟ ΠΑΡΑΡΤΗΜΑ Μέρος 1 Χρωστικές Ουσίες Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρ Λεύτερο τήματος, και η μέθοδος, που καθορίζεται στο Μέρος 2 του Δεύτερου Παραρ j^f" 0," 1^ τήματος, εφαρμόζονται με σκοπό τον προσδιορισμό των ουσιών, που δύνανται να ληφθούν μετά από εκχύλιση με διαιθυλικό αιθέρα, από τις διαλυτές στο νερό οργανοσουλφονικές χρωστικές ουσίες οι οποίες χρησιμοποιούνται εντός ή επί τροφίμου. Μέρος 2 Συντηρητικά 1. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Δεύτερο Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 3 του Δεύτερου ^"on^xa^s Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό του μυρμηκικού οξέος, των μυρμηκικών αλάτων και άλλων οξειδούμενων προσμίξεων, εντός του οξικού οξέος (Ε260), του οξικού καλίου (Ε261), του διοξικού νατρίου (Ε262) και του οξικού ασβεστίου (Ε263). 2. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Δεύτερο Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 4 του Δεύτερου M^" 0 /^^ Παρατήματος, εφαρμόζονται με σκοπό τον προσδιορισμό των μη πτητικών ουσιών εντός του προπιονικού οξέος (Ε280). 3. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Δεύτερο Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 5 του Δευτέρου ^ont^s Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό της απώλειας μάζας κατά την ξήρανση του νιτρώδους νατρίου (Ε250). 4. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Δεύτερο Παραρτήματος, και η μέθοδος που καθορίζεται στο Μέρος 6 του Δεύτερου ^ητκω^ Παραρτήματος, εφαρμόζονται με σκοπό την ανίχνευση του σαλικυλικού οξέως εντός του π υδροξυ βενζοϊκού αιθυλεστέρα (Ε214), του μετά νατρίου παραγώγου του π υδροξυ βενζοϊκού αιθυλεστέρα (Ε215), του π υδροξύβενζοϊκού κ προπυλεστέρα (Ε216), του μετά νατρίου παραγώγου του π υδροξύ βενζοϊκού κ προπυλεστέρα (Ε217), του π υδροξύ βενζοϊκού μεθυλεστέρα (Ε218) και του μετά νατρίου παραγώγου του π υδροξύ βενζοϊκού μεθυλεστέρα(ε219). 5. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Δεύτερο Παραρτήματος, και η μέθοδος που καθορίζεται στο Μέρος 7 του Δεύτερου M"^Y^' 7 Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό του ελεύθερου οξικού οξέος εντός του διοξικού νατρίου (Ε262). 6. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Δεύτερο Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 8 του Δεύτερου M^f^g Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό του οξικού νατρίου (Ε262) εντός του διοξικού νατρίου.
4 Δεύτερο Παράρτημα, Μέρη 1 και 9. Δεύτερο Παράρτημα, Μέρη 1 και 10. Δεύτερο Παράρτημα, Μέρη 1 και 11. Δεύτερο Παράρτημα, Μέρη 1 και 12. Δεύτερο Παράρτημα, Μέρη 1 και 13. Δεύτερο Παράρτημα, Μέρη 1 και 14. Δεύτερο Παράρτημα, Μέρη 1 και 15. Δεύτερο Παράρτημα, Μέρη 1 και 16. Κ.Δ.Π. 115/ Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 9 του Δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό την ανίχνευση των αλδεϋδών εντός τον σοόβικού οξέος (Ε200), των μετά νατρίου, καλίου ή ασβεστίου σορβικών αλάτων (Ε201, Ε202, Ε203) και του προπιονικού οξέος (Ε280). Μέρος 3 Αντιοξειδωτικά 1. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 10 του Δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό του δείκτη των υπεροξειδίων των λεκιθινών (Ε322). 2. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 11 του Δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό της περιεκτικότητας των λεκιθινών (Ε322) σε αδιάλυτες στο τολουόλιο ουσίες. 3. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 12 του Δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό την ανίχνευση των αναγωγικών ουσιών εντός των. γαλακτικών αλάτων νατρίου, καλίου και ασβεστίου (Ε325,Ε326,Ε327). 4. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 13 του Δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό των πτητικών οξέων εντός του ορθοφωσφορικού οξέος (Ε338). 5. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 14 του Δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό την ανίχνευση των νιτρικών αλάτων εντός του ορθοφωσφορικού οξέος (Ε338). 6. Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 15 του Δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό ουσιών που είναι αδιάλυτες στο νερό και εμφανίζονται εντός τ(ον ακόλουθων ορθοφωσφορικών αλάτων: δισόξινο φωσφορικό νάτριο, μονόξινο φωσφορικό νάτριο, φωσφορικό νάτριο, διόξινο φωσφορικό κάλιο, μονόξινο φωσφορικό κάλιο και φωσφορικό κάλιο (E339(i), Ε339(Η), E339(iii), E340(i), E340(ii), E340(iii)). Μέρος 4 Πρόσθετα τροφίμων Οι γενικές διατάξεις, που καθορίζονται στο Μέρος 1 του Δεύτερου Παραρτήματος, και η μέθοδος, που καθορίζεται στο Μέρος 16 του.δεύτερου Παραρτήματος, εφαρμόζονται με σκοπό τον προσδιορισμό του ρη των προσθέτων τροφίμων.
5 743 Κ.Δ.Π. 115/2002 ΔΕΥΤΕΡΟ ΠΑΡΑΡΤΗΜΑ ( Κανονισμός 3(1) και (2), και Πρώτο Παράρτημα) ΜΕΘΟΔΟΙ ΠΟΥ ΕΦΑΡΜΟΖΟΝΤΑΙ ΑΠΟ ΚΥΒΕΡΝΗΤΙΚΟΥ! ΧΗΜΙΚΟΥΣ Ή ΠΡΟΣΩΠΑ ΥΠΟ ΤΙΣ ΟΔΗΓΙΕΣ ΚΑΙ ΤΗΝ ΑΜΕΣΗ ΕΠΙΒΛΕΨΗ ΤΟΥΣ, ΚΑΤΑ ΤΗΝ ΑΝΑΛΥΣΗ Ή ΕΞΕΤΑΣΗ ΔΕΙΓΜΑΤΟΣ Ή ΜΕΡΟΥΣ ΔΕΙΓΜΑΤΟΣ ΠΡΟΣΘΕΤΟΥ ΤΡΟΦΙΜΩΝ Μέρος 1 Γενικές Διατάξεις 1. Ορισμός: Στο παρόν Παράρτημα, «δείγμα» σημαίνει οτιδήποτε υποβάλλεται από εξουσιοδοτημένο λειτουργό σε Κυβερνητικό Χημικό, είτε είναι δείγμα είτε μέρος του δείγματος. 2. Προετοιμασία του δείγματος: 2.1. Γενικά: Η μάζα του εργαστηριακού δείγματος, που προορίζεται για ανάλυση ή εξέταση, πρέπει, υπό κανονικές συνθήκες, να ισούται με 50g, εκτός εάν για κάποιο ειδικό προσδιορισμό, απαιτείται σημαντικότερη ποσότητα. 2.2 Προετοιμασία του δείγματος: Πριν να πραγματοποιηθεί η ανάλυση ή η εξέταση, το δείγμα είναι απαραίτητο να ομογενοποιηθεί Διατήρηση: Το δείγμα πρέπει να ετοιμαστεί βάσει των όσων περιγράφονται πιο πάνω και έπειτα πρέπει να διατηρείται πάντοτε σε ερμητικά κλεισμένο δοχείο, για αποφυγή οποιασδήποτε αλλοίωσης. 3. Αντιδραστήρια: 3.1. Νερό. (α) Κάθε φορά που αναφέρεται η λέξη «νερό», για τα διαλύματα, τις αραιώσεις ή τις εκπλύσεις, πρόκειται πάντα για απεσταγμένο νερό ή για απιονισμένο νερό αντίστοιχης καθαρότητας. (β) Κάθε φορά που αναφέρεται η λέξη «διάλυμα» ή «αραίωση», χωρίς να αναφέρεται αντιδραστήριο, πρόκειται για υδατικό διάλυμα Χημικές ουσίες: Όλες οι χημικές ουσίες πρέπει να είναι αναλυτικής καθαρότητας, εκτός εάν υπάρχουν αντίθετες ενδείξεις. 4. Συσκευές: 4.1. Κατάλογος συσκευών: Ο αναφερόμενος στον κατάλογο των υλικών εξοπλισμός είναι ειδικής χρήσης και έχει ιδιαίτερα χαρακτηριστικά Αναλυτικός ζυγός: Ο όρος «αναλυτικός ζυγός» σημαίνει ζυγό με ευαισθησία που ισούται τουλάχιστο με 0,1 mg. 5. Διατύπωση των αποτελεσμάτων: 5.1. Αποτελέσματα: Τα αποτελέσματα, για τα οποία γίνεται αναφορά στο πιστοποιητικό, ή ανάλογα με την περίπτωση, την εργαστηριακή έκθεση, που αναφέρονται στον Κανονισμό 3(2), είναι η μέση τιμή που υπολογίζεται από δυο τουλάχιστο προσδιορισμούς, που η επαναληπτικότητά τους είναι ικανοποιητική.
6 Κ.Δ.Π. 115/ Υπολογισμός του ποσοστού επί τοις εκατόν: Εκτός από τις περιπτώσεις που ιδιαιτέρως ορίζεται σε οποιοδήποτε των ακόλουθων Μερών, τα αποτελέσματα εκφράζονται σε ποσοστά επί τοις εκατόν (m/m) του αρχικού δείγματος, όπως αυτό υποβλήθηκε στον Κυβερνητικό Χημικό Αριθμός δεκαδικών ψηφίων: Το αποτέλεσμα δεν πρέπει να εκφράζεται με αριθμό που φέρει περισσότερα δεκαδικά ψηφία από όσα επιτρέπει η ακρίβεια της μεθόδου. Μέρος 2 Μέθοδος προσδιορισμού των ουσιών που δύνανται να ληφθούν μετά από εκχύλιση με διαιθυλικό αιθέρα, από τις διαλυτές στο νερό οργανοσουλφονικές χρωστικές ουσίες οι οποίες χρησιμοποιούνται εντός ή επί τροφίμου Η παρούσα μέθοδος επιτρέπει τον προσδιορισμό των ουσιών που δύνανται να ληφθούν μετά από εκχύλιση με διαιθυλικό αιθέρα από τις διαλυτές στο νερό οργανοσουλφονικές χρωστικές ουσίες, οι οποίες έχουν αναμιχθεί με οποιοδήποτε υπόστρωμα. Η μέθοδος που περιγράφεται πιο κάτω, προσδιορίζει την περιεκτικότητα των ουσιοη' που λαμβάνονται μετά από εκχύλιση με διαιθυλικό αιθέρα. Εκχύλιση της χρωστικής ουσίας με διαιθυλικό αιθέρα και ζύγιση του ξηρού υπολείμματος μετά από εξάτμιση του αιθέρα. 4. Αντιδραστήρια: 4.1. Ξηρός διαιθυλικός αιθέρας απαλλαγμένος από υπεροξείδια (η ξήρανση επιτυγχάνεται με χλωριούχο ασβέστιο που πυρώθηκε πρόσφατα). 5. Συσκευές: 5.1. Συσκευή Soxhlet με σφαιρική φιάλη Ξηραντήρας με Silica gel (S1O2) σε άνυδρη κατάσταση ή με άλλο αντίστοιχο υγροσκοπικό μέσο, και εφοδιασμένος με δείκτη υγρασίας Αναλυτικός ζυγός Κλίβανος ρυθμισμένος στους 85 ± 2 C. 6. Εκτέλεση του πειράματος: Επί χάρτινου ηθμού ζυγίζονται 10g χρωστικών ουσιών, με προσέγγιση 10 mg. Ο χάρτινος ηθμός διπλώνεται και εισάγεται εντός χάρτινου κυλίνδρου, ο οποίος σφραγίζεται με βάμβακα που είναι απαλλαγμένος από λιπαρές ουσίες. Η εκχύλιση πραγματοποιείται με διαιθυλικό αιθέρα (βλέπε υποπαράγραφο 4.1) επί 6 ώρες, μέσα σε συσκευή εκχύλισης Soxhlet (βλέπε υποπαράγραφο 5.1). Στη συνέχεια πρέπει να γίνεται εξάτμιση σε όσο το δυνατό χαμηλότερη θερμοκρασία. Η σφαιρική φιάλη της συσκευής Soxhlet, αφού ζυγιστεί κατάλληλα μαζί με το υπόλειμμα τοποθετείται στον κλίβανο (βλέπε υποπαράγραφο 5.4.). Ξηραίνεται στους 85±2 C επί είκοσι λεπτά. Το υπόλειμμα καλύπτεται με ύαλο ωρολογίου και αφήνεται να ψυχθεί σε ξηραντήρα (βλέπε υποπαράγραφο 5.2), και ακολούθως ζυγίζονται η σφαιρική φιάλη και το υπόλειμμα. Η ξήρανση και η ζύγιση επαναλαμβάνονται μέχρι που η διαφορά που θα προκύψει, μεταξύ δύο διαδοχικών ζυγίσεων να είναι μικρότερη από 0,5mg. Όμως, για ορθό υπολογισμό, σε πιθανή περίπτωση αύξησης της μάζας, λαμβάνεται υπόψη ο μικρότερος αριθμός που θα καταγραφεί.
7 745 Κ.Δ.Π. 115/ Διατύπωση των αποτελεσμάτων: Τύπος και τρόπος υπολογισμού: Η περιεκτικότητα σε ουσίες που εκχυλίζονται με αιθέρα υπολογίζεται σε ποσοστά επί τοις εκατόν του δείγματος, με βάση τον εξής τύπο: όπου: mi χ 100 mo ΙΤΙΙ= μάζα, σε γραμμάρια, του υπολείμματος μετά από εξάτμιση, mo= αρχική μάζα, σε γραμμάρια, της ποσότητας του δείγματος που χρησιμοποιήθηκε. 7.2 Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα 20 mg για 100 g δείγματος. Μέρος 3 Μέθοδος προσδιορισμού του μυρμηκικού οξέος, των μυρμηκικών αλάτων και άλλων οξειδούμενων προσμίξεων, εντός του οξικού οξέος (Ε260), του οξικού καλίου (Ε261). του διοξικού νατρίου (Ε262) και του οξικού ασβεστίου (Ε263) Η παρούσα μέθοδος επιτρέπει τον προσδιορισμό του μυρμηκικού οξέος, των μυρμηκικών αλάτων και άλλων οξειδούμενων προσμίξεων, υπολογιζόμενων ως μυρμηκικό οξύ, εντός: Του οξικού οξέος (Ε2ό0). του οξικού καλίου (Ε261), του διοξικού νατρίου (Ε 262). του οξικού ασβεστίου (Ε263). Με τη μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται η περιεκτικότητα σε μυρμηκικό οξύ, σε μυρμηκικά άλατα και σε άλλες οξειδούμενες προσμίξεις του οξικού οξέος (Ε260), του οξικού καλίου (Ε261), του διοξικού νατρίου (Ε262) και του οξικού ασβεστίου (Ε263). Μετά από την κατεργασία του δείγματος, που δόθηκε για ανάλυση ή εξέταση, με περίσσεια υπερμαγγανικού καλίου σε αλκαλικό περιβάλλον, λαμβάνεται διοξείδιο του μαγγανίου. Το τελευταίο καθώς και η περίσσεια του υπερμαγγανικού καλίου ογκομετρούνται με ιωδομετρία, αφού προηγουμένως το διάλυμα καταστεί όξινο. Η συγκέντρωση των οξειδούμενων προσμίξεων εκφράζεται σε μυρμηκικό οξύ. 4. Αντιδραστήρια: 4.1. Ιωδιούχο κάλιο Υπερμαγγανικό κάλιο 0,02 mol/i Ανθρακικό νάτριο (άνυδρο) Θειοθειικό νάτριο 0,1 mol/i Διάλυμα αμύλου (περίπου 1% m/v).
8 Κ.Δ.Π. 115/ Αραιωμένο διάλυμα θειικού οξέος: 90 ml θειικού οξέος (O2o=l,84 g/ml) στο οποίο προστίθεται νερό μέχρι το Συσκευές: 5.1. Ζέον υδρόλουτρο Αναλυτικός ζυγός. 6. Εκτέλεση του πειράματος: Στην περίπτωση που το προς ανάλυση ή εξέταση δείγμα παρουσιάζεται με την μορφή ελεύθερου οξέος, 10g, ζυγιζόμενα με προσέγγιση 10mg, διαλύονται σε 70 ml νερού, όπου προστίθεται διάλυμα, που περιέχει 10g άνυδρου ανθρακικού νατρίου (βλέπε υποπαράγραφο 4.3) διαλυμένοι) σε 30ml νερού. Εάν το δείγμα παρουσιάζεται με τη μορφή άλατος, 10g, ζυγιζόμενα με προσέγγιση 10mg, διαλύονται σε 100ml νερού όπου προστίθεται lg άνυδρου ανθρακικού νατρίου, αναδεύοντας μέχρι πλήρους διάλυσης. Προστίθενται 20ml υπερμαγγανικού καλίου 0,02 mol/1 (βλέπε υποπαράγραφο 4.2) και το όλο διάλυμα θερμαίνεται σε ζέον υδρόλουτρο επί 15 λεπτά. Το διάλυμα αφήνεται να ψυχθεί και στη συνέχεια προστίθενται 50ml αραιού θειικού οξέος (βλέπε υποπαράγραφο 4.6) και 0,5g ιωδιούχου καλίου (βλέπε υποπαράγραφο 4.1). Το μείγμα αναδεύεται μέχρι να διαλυθεί το ίζημα του διοξειδίοΐ' του μαγγανίου. Ογκομετρείται με διάλυμα θειοθειικού νατρίου 0,1 mol/1 (βλέπε υποπαράγραφο 4.4) μέχρι το διάλυμα να αποκτήσει χρώμα ελαφρώς κίτρινο, οπότε προστίθενται μερικές σταγόνες διαλύματος αμύλου (βλέπε υποπαράγραφο 4.5) και συνεχίζεται η ογκομέτρηση μέχρι πλήρους αποχρωματισμού. 7. Διατύπωση των αποτελεσμάτων: 7.1. Τύπος και τρόπος υπολογισμού: Το ποσοστό μυρμηκικού οξέος, μυρμηκικών αλάτων και άλλων οξειδούμενων προσμίξεων υπολογίζεται σε μυρμηκικό οξύ με βάση τον πιο κάτω τύπο: 2,3b (100a V) mo b όπου: a = μοριακότητα του υπερμαγγανικού καλίου, b = μοριακότητα του θειοθειικού νατρίου, mo = αρχική μάζα του δείγματος σε γραμμάρια, V = όγκος σε ml, του θειοθειικού νατρίου (0,1 mol/1) που χρησιμοποιείται για την ογκομέτρηση Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα 5mg για 100g δείγματος. 8. Παρατηρήσεις: 8.1. Σε 10g δείγματος, 11,3ml θποθειικού νατρίου 0,1 moi/l ισοδυναμούν με 0,2% μυρμηκικού οξέος Στην απουσία μυρμηκικών αλάτων, ο όγκος του θειοθειικού νατρίου ανέρχεται σε 20ml, αλλά εάν υπάρχει πάνω από 0,27 % (m/m) μυρμηκικού οξέος, η περίσσεια KMnCk δεν επαρκεί και ο λαμβανόμενος όγκος του θειοθειικού οξέος σταθεροποιείται στα 8ml. Στην περίπτωση αυτή, ο προσδιορισμός πρέπει να επαναληφθεί χρησιμοποιώντας μικρότερη ποσότητα δείγματος.
9 747 Κ.Δ.Π. 115/2002 Μέρος 4 Μέθοδος προσδιορισμού των μη πτητικών ουσιών εντός του προπιονικοΰ οξέος (Ε280) Η παρούσα μέθοδος επιτρέπει τον ποσοτικό προσδιορισμό των μη πτητικών ουσιών εντός του προπιονικοΰ οξέος (Ε280). Με την μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται η περιεκτικότητα του προπιονικοΰ οξέος σε μη πτητικές ουσίες. Το δείγμα εξατμίζεται και ξηραίνεται στους 103±2 C. Το υπόλειμμα προσδιορίζεται σταθμικά. 4. Συσκευές: 4.1 Κάψα από διοξείδιο του πυριτίου ή λευκόχρυσο για 100g δείγματος Ηλεκτρικός κλίβανος, ρυθμισμένος στους 103±2 C Αναλυτικός ζυγός Ζέον υδρόλουτρο Ξηραντήρας με Silica gel (S1O2) σε άνυδρη κατάσταση ή με άλλο αντίστοιχο υγροσκοπικό μέσο και εφοδιασμένος με δείχτη υγρασίας. 5. Εκτέλεση του πειράματος: Ζυγίζονται 100g περίπου προπιονικοΰ οξέος με προσέγγιση 0,lg σε κάψα (βλέπε υποπαράγραφο 4.1) που έχει ξηοανίΐεί καταλλήλως και της οποίας έχει προσδιορισθεί η τάρα. Επί ζέοντος υδρόλουτρου και κάτω από απαγωγέα υφίσταται εξάτμιση. Όταν εξατμιστεί όλο το προπιονικό οξύ, το υπόλειμμα υφίσταται ξήρανση επί μια ώρα εντός κλιβάνου (βλέπε υποπαράγραφο 4.2.) στους 103±2 C. Στη συνέχεια, τοποθετείται σε ξηραντήρα μέχρι να ψυχθεί. Ζυγίζεται. Η όλη διαδικασία επαναλαμβάνεται μέχρι που η διαφορά μεταξύ δύο διαδοχικών ζυγίσεων να μην υπερβαίνει τα 0,5 mg. Όμως, για ορθό υπολογισμό, σε πιθανή περίπτωση αύξησης της μάζας, λαμβάνεται υπόψη ο μικρότερος αριθμός που θα καταγραφεί. 6. Διατύπωση των αποτελεσμάτων: 6.1. Τύπος και τρόπος υπολογισμού: Η επί τοις εκατόν περιεκτικότητα του δείγματος σε μη πτητικές ουσίες υπολογίζεται με βάση τον πιο κάτω τύπο: 100 χ mi mo όπου: mi = μάζα του υπολείμματος της εξατμίσεως, σε γραμμάρια, mo = αρχική μάζα της ποσότητας του δείγματος που χρησιμοποιήθηκε, σε γραμμάρια Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα 5mg για 100g δείγματος.
10 Κ.Δ.Π. 115/ Μέρος 5 Μέθοδος προσδιορισμοί) της απώλειας μάζας κατά την ξήρανση του νιτρώδους νατρίου (Ε250) Η παρούσα μέθοδος επιτρέπει τον προσδιορισμό της απώλειας μάζας κατά την ξήρανση του νιτρώδους νατρίου (Ε250). Με την μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται η περιεκτικότητα σε υγρασία του νιτρώδους νατρίου, η οποία αντιστοιχεί στην απώλεια μάζας του τελευταίου. Προσδιορισμός της απώλειας μετά από θέρμανση στους 103±2 C. 4. Συσκευές: 4.1. Ηλεκτρικός κλίβανος, ρυθμισμένος στους 103±2 C Γυάλινο σκεύος με επίπεδο πυθμένα, διαμέτρου mm και με τοιχώματα ύψους τουλάχιστον 25mm, εφοδιασμένο με καπάκι Ξηραντήρας με Silica gel (S1O2) σε άνυδρη κατάσταση ή με άλλο αντίστοιχο υγροσκοπικό μέσο, και εφοδιασμένος με δείκτη υγρασίας Αναλυτικός ζυγός. 5. Εκτέλεση του πειράματος: Αφαιρείται το καπάκι του γυάλινου σκεύους (βλέπε υποπαράγραφο 4.2.) και αμφότερα σκεύος και καπάκι τοποθετούνται για μια ώρα εντός κλιβάνου (βλέπε υποπαράγραφο 4.1) ρυθμισμένου στους 103±2 C. Το καπάκι τοποθετείται επί του σκεύους και αμφότερα αφήνονται να ψυχθούν μέχρι να φτάσουν σε θερμοκρασία περιβάλλοντος, μέσα σε ξηραντήρα (βλέπε υποπαράγραφο 4.3). Το σκεύος με το καπάκι του (βλέπε υποπαράγραφο 4.2.) ζυγίζονται με προσέγγιση 10mg. Εντός του σκεύους, με το καπάκι του, ζυγίζονται 10g δείγματος με προσέγγιση 1 Omg. Αφού αφαιρεθεί το καπάκι, αμφότερα σκεύος και καπάκι τοποθετούνται επί μία ώρα σε κλίβανο (βλέπε υποπαράγραφο 4.1.) ρυθμισμένο στους 103±2 C. Το καπάκι τοποθετείται επί του σκεύους, που αφήνεται να ψυχθεί μέσα στον ξηραντήρα (βλέπε υποπαράγραφο 4.3), επί μία ώρα μέχρι να φτάσει τη θερμοκρασία περιβάλλοντος. Στη συνέχεια, ζυγίζεται με προσέγγιση 1 Omg. Οι τρεις τελευταίες διαδικασίες (θέρμανση, ψύξη, ζύγιση) επαναλαμβάνονται μέχρι που η διαφορά μάζας μεταξύ δύο διαδοχικών μετρήσεων να μην υπερβαίνει τα 10 mg. Όμως, για ορθό υπολογισμό, σε πιθανή περίπτωση αύξησης της μάζας, λαμβάνεται υπόψη ο μικρότερος αριθμός που θα καταγραφεί. 6. Διατύπωση των αποτελεσμάτων: 6.1. Τύπος και τρόπος υπολογισμού: Η επί τοις εκατόν (m/m) απώλεια μάζας του δείγματος, κατά την ξήρανση, υπολογίζεται με βάση τον πιο κάτω τύπο: 100 χ (rm rm) (im mi) όπου: mi= η μάζα του σκεύους και του καπακιού, σε γραμμάρια, rri2= η μάζα, σε γραμμάρια, του σκεύους μαζί με το δείγμα πριν από την ξήρανση,
11 749 Κ.Δ.Π. 115/2002 ins = η μάζα, σε γραμμάρια, του σκεύους μαζί με το δείγμα, μετά την ξήρανση Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο παράλληλων προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα loomg για 100g δείγματος. Μέρος 6 Μέθοδος ανίχνευσης του σαλικυλικού οξέος εντός του π υδροξύ βενζοϊ'κού αιθυλεστέρα (Ε214), του μετά νατρίου παραγώγου του π υδροξύ βενζοϊκού αιθυλεστέρα (Ε 215), του π υδροξύ βενζοϊκού κ προπυλεστέρα (Ε216), του μετά νατρίου παραγώγου του π υδροξύ βενζοϊκού κ προπυλεστέρα (Ε217), τον π υδροξύ βενζοϊκού μεθυλεστέρα (Ε218) και του μετά νατρίου παραγώγου, του π υδροξύ βενζοϊκού μεθυλεστέρα (Ε219) Η παρούσα μέθοδος επιτρέπει την ανίχνευση του σαλικυλικού οξέος εντός του π υδροξύ βενζοϊκού αιθυλεστέρα (Ε214), του π υδροξύ βενζοϊκού κ προπυλεστέρα (Ε216), του π υδροξύ βενζοϊκού μεθυλεστέρα (Ε218) και των μετά νατρίου παραγώγων αυτών (Ε215, Ε217 και Ε219). Με τη μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται το όριο ανίχνευσης του σαλικυλικού οξέος. Διάλυμα σαλικυλικού οξέος λαμβάνει, παρουσία εναμμωνίου θειικού σιδήρου (III), μωβ χροιά, της οποίας η ένταση συγκρίνεται με εκείνη του διαλύματος αναφοράς. 4. Αντιδραστήρια: 4.1 Διάλυμα 0,2% (m/v) εναμμωνίου θειικού σιδήρου (III): 0,2 g εναμμωνίου θειικού σιδήρου (III) με 12 μόρια κρυσταλλικού νερού διαλύονται σε 50ml νερού. Προστίθενται 10ml νιτρικού οξέος αραιωμένου προς 10% (ν/ν) και στη συνέχεια προστίθεται νερό μέχρι τα 100ml. 4.2 Αιθανόλη, 95% (ν/ν). 4.3 Διάλυμα σαλικυλικού οξέος περιεκτικότητας 0,lg/l Θειικό οξύ 1 mol/1. 5. Συσκευές: 5.1. Σωλήνας Nessler ολικής χωρητικότητας 60 ml περίπου, βαθμολογημένος μέχρι τα 50 ml. 6. Εκτέλεση του πειράματος: 6.1. Δείγματα του π υδροξύ βενζοϊκού αιθυλεστέρα, του π υδροξύβενζοϊκού κ προπυλεστέρα και του π υδροξύ κ βενζοϊκού μεθυλεστέρα ,lg του προς ανάλυση ή εξέταση δείγματος, που ζυγίστηκε με προσέγγιση Img, διαλύεται εντός 10ml αιθανόλης 95% (ν/ν) (βλέπε υποπαράγραφο 4.2.). Το διάλυμα αυτό μεταφέρεται σε βαθμολογημένο σωλήνα Nessler (βλέπε υποπαράγραφο 5.1.) και προστίθεται νερό μέχρι τα 50ml. Μετά από ανατάραξη του μείγματος προστίθεται 1ml διαλύματος εναμμωνίου θειικού σιδήρου (βλέπε υποπαράγραφο 4.1.). Το μείγμα αναταράζεται εκ νέου και αφήνεται να ηρεμήσει για ένα λεπτό.
12 Κ.Δ.Π. 115/ Κατά τον ίδιο τρόπο ετοιμάζεται διάλυμα αναφοράς, όπως περιγράφεται στην υπο υποπαράγραφο , αλλά αντικαθιστώντας το O.lg του δείγματος με 1 ml από το διάλυμα του σαλικυλικού οξέος (βλέπε υποπαράγραφο 4.3) Γίνεται σύγκριση μεταξύ της χροιάς του δοκιμαστικού σωλήνα που περιέχει το υπό ανάλυση ή εξέταση δείγμα και εκείνης του διαλύματος αναφοράς Δείγματα των μετά νατρίου παραγώγων του π υδροξύ βενζοϊκού μεθυλεστέρα, αιθυλεστέρα και κ προπυλεστέρα Επαναλαμβάνεται η διαδικασία που περιγράφεται στην υπουποπαράγραφο , καθιστώντας το διάλυμα όξινο (ρη=5) με προσθήκη θειικού οξέος 1 mol/l (βλέπε υποπαράγραφο 4.4) πριν από την αραίωση μέχρι 50ml Επαναλαμβάνεται η διαδικασία που περιγράςοεται στην υπόυποπαράγραφο Επαναλαμβάνεται η διαδικασία που περιγράφεται στην υπόυποπαράγραφο Διατύπωση των αποτελεσμάτων: 7.1. Ερμηνεία της δοκιμασίας ανίχνευσης: Εάν η μωβ χροιά του δοκιμαστικού σωλήνα, που περιέχει το υπό ανάλυση ή εξέταση δείγμα, είναι πιο έντονη από εκείνη του διαλύματος αναφοράς, το πείραμα θεωρείται ότι έχει θετικά αποτελέσματα και το δείγμα περιέχει πλέον του 0,1 % σαλικυλικού οξέος Ευαισθησία: Το όριο ανίχνευσης που μπορεί να προσδιοριστεί με την παρούσα μέθοδο είναι 30 mg σαλικυλικού οξέος για 100g δείγματος Παρατήρηση: Τα αποτελέσματα δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, πρέπει να είναι ταυτόσημα. Μέρος 7 Μέθοδος προσδιορισμού του ελεύθερου οξικού οξέος εντός του διοξικού νατρίου (Ε262) Η παρούσα μέθοδος επιτρέπει την ανίχνευση οξικού οξέος εντός του διοξικού νατρίου (Ε262). Με τη μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται η περιεκτικότητα σε οξικό οξύ. Εξουδετέρωση του οξικού οξέος με καυστικό νάτριο παρουσία φαινολοφθαλεΐνης. 4. Αντιδραστήρια: 4.1 Διάλυμα l%(m/v) φαινολοφθαλεΐνης με αιθανόλη Καυστικό νάτριο 1 mol/l. 5. Συσκευές: 5.1. Αναλυτικός ζυγός.
13 751 Κ.Δ.Π. 115/ Εκτέλεση του πειράματος: Ζυγίζονται. 3g περίπου του υπό ανάλυση ή εξέταση δείγματος, με προσέγγιση lmg,. και διαλύονται εντός 50 ml νερού. Προστίθενται δύο ως τρεις σταγόνες διαλύματος φαινολοφοαλεΐ'νης (βλέπε υποπαράγραφο 4.1.) και γίνεται ογκομέτρηση με καυστικό νάτριο 1 mol/i (βλέπε υποπαράγραφο 4.2.), μέχρι που η κόκκινη χροιά, η οποία οφείλεται στη μετατροπή της φαινολοφθαλε'ίνης, να διατηρηθεί επί πέντε δευτερόλεπτα. 7. Διατύπωση των αποτελεσμάτων: 7.1.Τύπος και τρόπος υπολογισμού: Η επί τοις εκατόν (m/m) περιεκτικότητα του δείγματος σε οξικό οξύ υπολογίζεται με βάση τον πιο κάτω τύπο: 6,005 χ V χ c mo όπου: V = ο όγκος, σε ml, του διαλύματος καυστικού νατρίου που χρησιμοποιήθηκε για την ογκομέτρηση (βλέπε υποπαράγραφο 4.2.), c = η μοριακότητα του διαλύματος του καυστικού νατρίου, σε mol/1. mo = η αρχική μάζα, σε γραμμάρια, του δείγματος Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο παράλληλων προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα 500 mg για 100 g δείγματος. 8. Παρατήρηση: Απαιτούνται 20ml καυστικού νατρίου 1 mol/1 για την ογκομέτρηση 3g δείγματος που περιέχει 40% οξικό οξύ. Μέρος 8 Μέθοδος προσδιορισμού του οξικού νατρίου εντός του διοξικού νατρίου (Ε262) Η παρούσα μέθοδος επιτρέπει τον προσδιορισμό του οξικού νατρίου και του νερού, εκφραζόμενων ως οξικού νατρίου, εντός του διοξικού νατρίου (Ε262). Ο όρος «περιεκτικότητα σε οξικό νάτριο» σημαίνει την περιεκτικότητα σε οξικό νάτριο και νερό, εκφραζόμενη σε οξικό νάτριο, όπως προσδιορίζεται από την πιο κάτο3 μέθοδο. Κατάλληλη αραίωση του δείγματος με ψυχρό οξικό οξύ και ογκομέτρηση με διάλυμα αναφοράς υπερχλωρικού οξέος παρουσία δείκτη violet cristallise. 4. Αντιδραστήρια: 4.1. Παγόμορφο οξικό οξύ (ρ2ο C=l,049 g/ml για ογκομέτρηση σε μη υδατικό περιβάλλον). 4.2.Violet cristallise CI n υπό τη μορφή διαλύματος με 0,2% (m/v) εντός ψυχρού οξικού οξέος.
14 Κ.Δ.Π. 115/ Φθαλικό κάλιο C8H5KO Ανυδρίτης του οξικού οξέος (CFbCO )2θ Υπερχλωρικό οξύ, 0.1 mol/ι εντός παγόμορφου οξικού οξέος. Το διάλυμα ετοιμάζεται και τιτλοδοτείται ως ακολούθως: Ζυγίζονται Ρ g διαλύματος υπερχλωρικού οξέος εντός βαθμολογημένης σφαιρικής φιάλης των ml εφοδιασμένης με εσμυρισμένο γυάλινο πώμα. Τα Ρ g υπολογίζονται με βάση τον τύπο: 1 004,6 Ρ= m όπου: ΙΤΊ= η συγκέντρωση του υπερχλωρικού οξέος επί τοις εκατόν (m/m), που προσδιορίζεται με ογκομέτρηση (70 72% mm), είναι η πιο κατάλληλη συγκέντρωση. Προστίθενται 100 ml περίπου ψυχρού οξικού οξέος και στη συνέχεια Q g σε μικρές διαδοχικές ποσότητες ανυδρίτου του οξικού οξέος. Το μείγμα αναδεύεται και ψύχεται συνεχώς κατά τη διάρκεια των διεργασιών προσθήκης. Τα Q g δύνανται να υπολογιστούν με βάση τον τύπο: (567 χ Ρ) Q= a όπου: Ρ = η ζυγισμένη ποσότητα σε γραμμάρια του υπερχλωρικού οξέος, a. = η επί τοις εκατόν συγκέντρωση (m/m) του ανυδρίτου του οξικού οξέος. Η σφαιρική φιάλη σφραγίζεται και αφήνεται για 24 ώρες μακριά από το φως. Προστίθεται κατόπιν αρκετό ψυχρό οξικό οξύ για να ληφθεί διάλυμα 1 000ml. Το διάλυμα που παρασκευάζεται με τον τρόπο αυτό είναι σχεδόν άνυδρο. Το διάλυμα ρυθμίζεται με φθαλικό κάλιο κατά τον ακόλουθο τρόπο: Ζυγίζονται περίπου 0,2g φθαλικού καλίου, με προσέγγιση 0,1 mg, που έχουν υποστεί κατάλληλη ξήρανση στους 110 C για δύο ώρες και διαλύονται μέσα σε 25ml ψυχρού οξικού οξέος μέσα σε κωνική φιάλη, θερμαίνοντας σιγά σιγά. Το διάλυμα ψύχεται. Προστίθενται δύο σταγόνες του διαλύματος που περιέχει 0,2 % (m/v) violet cristallise (βλέπε υποπαράγραφο 4.2) εντός ψυχρού οξικού οξέος και ογκομετρείται με διάλυμα υπερχλωρικού οξέος μέχρι που το χρώμα του δείκτη να μετατραπεί σε ανοιχτό πράσινο. Διεξάγεται τακρλή ογκομέτρηση με τον ίδιο όγκο, και το αριθμητικό αποτέλεσμα του τυφλού προσδιορισμού αφαιρείται από εκείνο του αρχικού προσδιορισμού. 20,42mg φθαλικού καλίου αντιστοιχούν σε 1ml υπερχλωρικού οξέος 0,1 mol/1. 5. Συσκευές: 5.1. Αναλυτικός ζυγός: 6. Εκτέλεση του πειράματος: Ζυγίζονται περίπου 0,2 g δείγματος με προσέγγιση 0,5 mg και διαλύονται εντός 50ml ψυχρού οξέος (βλέπε υποπαράγραφο 4.1.). Προστίθενται μερικές σταγόνες του δείκτη violet cristallise (βλέπε υποπαράγραφο 4.2.) και το διάλυμα ογκομετρείται με διάλυμα υπερχλωρικού οξέος 0,1 mol/ι (βλέπε υποπαράγραφο 4.5.) μέχρι που το χρώμα του δείκτη να αλλάξει προς ανοικτό πράσινο.
15 753 Κ.Δ.Π. 115/ Διατύπωση των αποτελεσμάτων: 7.1. Τύπος και τρόπος υπολογισμού: Η επί τοις εκατόν (m/m) περιεκτικότητα του δείγματος σε οξικό νάτριο, όπως ορίζεται στην παράγραφο 2, υπολογίζεται με βάση τον πιο κάτω τύπο: 8,023 χ V χ c mo όπου: V = ο όγκος του υπερχλωρικού οξέος (βλέπε υποπαράγραφο 4.5.) που χρησιμοποιήθηκε για την ογκομέτρηση, c = η μοριακότητα του υπερχλωρικού οξέος (βλέπε υποπαράγραφο 4.5.), mo = η αρχική μάζα του δείγματος σε γραμμάρια Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο προσδιορισμών, πον πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα l,5g για 100g δείγματος. 8. Παρατηρήσεις: Τα αντιδραστήρια που χρησιμοποιούνται στην παρούσα μέθοδο είναι τοξικά και εκρηκτικά. Πρέπει λοιπόν να χρησιμοποιούνται με προσοχή. Μέρος 9 Μέθοδος ανίχνευσης των αλδεϋδών εντός του σορβικού οξέος (Ε200), των μετά νατρίου, καλίου ή ασβεστίου σορβικών αλάτων (Ε201, Ε202, Ε203) και τον προπιονικού οξέος (Ε280) Η παρούσα μέθοδος επιτρέπει την ανίχνευση το^ν αλδεϋδών, εκφραζόμενων σε φορμαλδεΰδη εντός: Του σορβικού οξέος (Ε200), των μετά νατρίου, καλίου ή ασβεστίου σορβικών αλάτων (Ε201, Ε202, Ε203), του προπιονικού οξέος (Ε280). Προσδιορισμός του ορίου ανιχνεύσεως. Η συγκέντρωση των αλδεϋδών, εκφραζόμενη σε φορμαλδεΰδη, λαμβάνεται με τη μέθοδο που περιγράφεται πιο κάτω. Αντίδραση των αλδεϋδών του υπό ανάλυση ή εξέταση διαλύματος με το αντιδραστήριο Schiff και σύγκριση της έντασης της κόκκινης χροιάς διαλύματος φορμαλδεΰδης, διάλυμα αναφοράς, που περιέχει το αντιδραστήριο Schiff. 4. Αντιδραστήρια: 4.1. Διάλυμα αναφοράς που περιέχει 0,01 mg φορμαλδεΰδης ανά ml, που παρασκευάζεται με διάλυση πυκνού διαλύματος φορμαλδεΰδης (400 mg/ml) Αντιδραστήριο Schiff.
16 Κ.Δ.Π. 115/ Εκτέλευη ιου.ιιειράμαχος: 5.1. Ζυγίζεται lg δείγματος με προσέγγιση lmg. Προστίθενται 100 ml νερού. Το διάλυμα αναταράσσεται. Εαν θεωρηθεί αναγκαίο, το διάλυμα διηθείται και προστίθεται σε 1ml του διηθήματος ή του διαλύματος 1 ml αντιδραστηρίου Schiff (βλέπε υποπαράγραφο 4.2.). Ταυτόχρονα, σε 1ml του διαλύματος αναφοράς που περιέχει τη φορμαλδεΰδη (βλέπε υποπαράγραφο 4.1.) προστίθεται 1ml του αντιδραστηρίου Schiff (βλέπε υποπαράγραφο 4.2.) Η χροιά του διαλύματος που περιέχει το υπό ανάλυση ή εξέταση δείγμα συγκρίνεται με εκείνη του διαλύματος αναφοράς. 6. Διατύπωση των αποτελεσμάτων: 6.1.Ερμηνεία της δοκιμασίας ανίχνευσης: Εάν η κόκκινη χροιά του δοκιμαστικού σωλήνα που περιέχει το υπό ανάλυση ή εξέταση δείγμα είναι πιο έντονη από εκείνη του δοκιμαστικού σωλήνα που περιέχει το διάλυμα αναφοράς, η δοκιμασία είναι θετική και το δείγμα περιέχει πλέον του 0,1% αλδεΰδης εκφραζόμενης σε φορμαλδεΰδη Ευαισθησία: Το όριο ανιχνεύσεως, που μπορεί να προσδιοριστεί με τη μέθοδο αυτή, είναι 30mg φορμαλδεΰδης για 100g δείγματος Παρατήρηση: Τα αποτελέσματα δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, πρέπει να είναι ταυτόσημα. Σχήμα. Μέρος 10 Μέθοδος προσδιορισμού του δείκτη υπεροξειδίων των λεκιθινών Η παρούσα μέθοδος επιτρέπει τον προσδιορισμό του δείκτη υπεροξειδίων των λεκιθινών. Με τη μέθοδο που περιγράφεται πιο κάτ(ύ προσδιορίζεται ο δείκτης υπεροξειδίων των λεκιθινών. Οξείδωση του ιωδιούχου καλίου από τα υπεροξείδια των λεκιθινών και ογκομέτρηση του ελευθερούμενου ιωδίου με θειοθειικό νάτριο. 4. Αντιδραστήρια: 4.1. Παγόμορφο οξικό οξύ Χλωροφόρμιο Ιωδιούχο κάλιο Θειοθειϊ'κό νάτριο 0,1 mol/1 ή 0,01 mol/ Διάλυμα αμύλου (περίπου 1% m/v). 5. Συσκευές: 5.1. Αναλυτικός ζυγός Συσκευή (βλέπε Σχήμα παρόντος Μέρους) που αποτελείται από: σφαιρική φιάλη (με σφαιρικό πυθμένα), χωρητικότητος 100 ml, κάθετο ψυκτήρα, γυάλινο σωλήνα μήκους 250mm και εσωτερικής διαμέτρου 22mm, με εσμυρισμένα άκρα,
17 755 Κ.Δ.Ιί. 115/ μικρό ποτήρι ζέσεως, εξωτερικών διαστάσεων: 35 50mm ύψος και 20mm διάμετρος. 6. Εκτέλεση του πειράματος: 6.1. Μέσα σε σφαιρική φιάλη 100ml (βλέπε υπο υποπαράγραφο ) τοποθετούνται 10ml ψυχρού οξικού οξέος (βλέπε υποπαράγραφο 4.1.) και 10ml χλωροφορμίου (βλέπε υποπαράγραφο 4.2.). Τοποθετούνται ο γυάλινος σωλήνας (βλέπε υπο υποπαράγραφο ) και ο κάθετος ψυκτήρας (βλέπε υπό υποπαράγραφο ). Το μείγμα φέρεται βραδέως στο σημείο βρασμού, επί δύο λεπτά, για να απαλλαγεί από τον αέρα που βρίσκεται υπό διάλυση, lg ιωδιούχου καλίου (βλέπε υποπαράγραφο 4.3.) διαλύεται σε 1,3ml νερού και το διάλυμα αυτό προστίθεται στη σφαιρική φιάλη (βλέπε υπο υποπαράγραφο 5.2.1) φροντίζοντας να μη διακοπεί ο βρασμός. Εάν τη στιγμή αυτή εμφανιστεί μια κίτρινη χροιά μέσα στη σφαιρική φιάλη, το πείραμα θεωρείται ότι απέτυχε και πρέπει να επαναληφθεί με αντιδραστήρια που παρασκευάστηκαν πρόσφατα Στη συνέχεια, μετά από δύο λεπτά βρασμού, προστίθεται στη σφαιρική φιάλη (βλέπε υπό υποπαράγραφο ) lg του υπό ανάλυση ή εξέταση δείγματος, ζυγισμένο με προσέγγιση lmg, φροντίζοντας και πάλι να μη διακοπεί ο βρασμός. Για το σκοπό αυτό το δείγμα τίθεται σε μικρό ποτήρι ζέσεως (βλέπε υπουποπαράγραφο ) που εισάγεται εντός της σφαιρικής φιάλης από το γυάλινο σωλήνα (βλέπε υπο υποπαράγραφο ) με τη βοήθεια σύρματος του οποίου το κάτω άκρο προσαρμόζεται στο εν λόγω ποτήρι ζέσεως (βλέπε Σχήμα του παρό Σχήμα, ντος Μέρους). Ο ψυκτήρας μπορεί να απομακρυνθεί όσο διαρκεί η ταχεία αυτή δοκιμασία. Ο βρασμός διατηρείται για τρία τέσσερα ακόμα λεπτά. Στη συνέχεια, παύει η θέρμανση, απομακρύνεται αμέσους ο ψυκτήρας (βλέπε υπο υποπαράγραφο ) και προστίθενται ταχέως 50 ml νερού από το γυάλινο σωλήνα (βλέπε υπο υποπαράγραφο ). Αφαιρείται ο γυάλινος σωλήνας (βλέπε υπο υποπαράγραφο ) και ψύχεται η σφαιρική φιάλη (βλέπε υπο υποπαράγραφο ) κάτω από το τρεχούμενο νερό μέχρι να φτάσει στη θερμοκρασία δωματίου. Ογκομετρείται με Οειοθειικό νάτριο (0,lmol/l ή 0,01mol/l) (βλέπε υποπαράγραφο 4.4.) μέχρι να αποχρωματιστεί το υδάτινο στρώμα. Ακριβώς πριν από το τέλος της όγκο μέτρησης, προστίθεται 1ml διαλύματος αμύλου (βλέπε υποπαράγραφο 4.5.) και η ογκομέτρηση συνεχίζεται μέχρι να εξαφανιστεί η μπλε χροιά. Κατά τη διάρκεια της ογκομέτρησης, η σφαιρική φιάλη (βλέπε υπο υποπαράγραφο ) αναταράζεται καλά ώστε να εξέλθει πλήρους το κοδιο από το μη υδάτινο στρώμα Να εκτελεσθεί τυφλή ογκομέτρηση σύμφωνα με τις υποπαραγράφους 6.1 και Διατύπωση των αποτελεσμάτων: 7.1. Τύπος και τρόπος υπολογισμού: Ο δείκτης υπεροξειδίων του δείγματος, σε χιλιοστοϊσοδύναμα ανά χιλιόγραμμο, υπολογίζεται με βάση τον πιο κάτω τύπο: χ ax (V1 V2) mo όπου: Vi = ο όγκος, σε ml,του διαλύματος του θειοθειικου άλατος που χρησιμοποιήθηκε για την ογκομέτρηση του δείγματος σύμφωνα με την υποπαράγραφο 6.2.,
18 Κ.Δ.ΪΙ. 115/ V2 = όγκος, σε m!, του διαλύματος του θειοθειικού άλατος που χρησιμοποιήθηκε για τον τυφλό προσδιορισμό σύμφωνα με την υποπαράγραφο 6.3, a = η συγκέντρωση του διαλύματος του θειοθειικού νατρίου σε mol/i, mo = η αρχική μάζα του δείγματος σε γραμμάρια Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα 0,5 χιλιοστοϊσοδύναμα ανά χιλιόγραμμο του δείγματος. 8. Παρατηρήσεις: 8.1. Η εκλογή της συγκεντρώσεως του χρησιμοποιούμενου θειοθειικού νατρίου εξαρτάται από το αποσκοπούμενο αποτέλεσμα. Εάν χρησιμοποιηθούν λιγότερα από 0,5m/l διαλύματος θειοθειικού νατρίου 0,1 mol/i, ο προσδιορισμός επαναλαμβάνεται χρησιμοποιώντας διάλυμα θειοθειικού άλατος 0,01 mol/i Η ανάλυση εκτελείται μακριά από το έντονο φως. Συσκευή για τον προσδιορισμό του δείκτη υπεροξειδίων των λεκιθινών: m 'ι */.; is! «.!?.{ /«j yvs ri^ki:, ; Li $ i.ψ* :>> \ Z4<s.\ew*t * ίλ*( ί it* *;! «&:οί. 4;Υ* -.(K-.t&dtit&py jjjbiftt Κώιτκκ; ifttik&kikiv'tij» &&: > *.
19 757 Κ.Δ.Π. 115/2002 Μέρος 11 Μέθοδος προσδιορισμού της περιεκτικότητας των λεκιοινών (Ε322) σε αδιάλυτες στο τολουόλιο ουσίες Η παρούσα μέθοδος επιτρέπει τον προσδιορισμό των ουσιών, που είναι αδιάλυτες στο τολουόλιο, εντός των λεκιθινών (Ε322). Με τη μέθοδο που περιγράφεται πιο κάτω, προσδιορίζεται η περιεκτικότητα σε ουσίες αδιάλυ.τες στο τολουόλιο. Διήθηση των αδιάλυτων στο τολουόλιο προσμίξεων και ξήρανση του υπολείματος. 4. Αντιδραστήρια: 4.1. Τολουόλιο. 5. Συσκευές: 5.1. Ηθμός από φρυγμένο γυαλί G3 των 30 ml ή ισοδύναμου μεγέθους πόρων Θερμοηλεκτρικός κλίβανος, ρυθμισμένος στους 103±2 C Υδρόλουτρο του οποίου η θερμοκρασία δεν υπερβαίνει τους 60 C Ξηραντήρας με Silica gel (SiO>) σε άνυδρη κατάσταση ή με άλλο αντίστοιχο υγροσκοπικό μέσο και εφοδιασμένος με δείκτη υγρασίας Κωνική φιάλη των 500ml Αντλία κενού Αναλυτικός ζυγός. 6. Εκτέλεση του πειράματος: 6.1. Ο ηθμός από φρυγμένο γυαλί των 30ml (βλέπε υποπαράγραφο 5.1.). υφίσταται ξήρανση μέσα στον κλίβανο ρυθμισμένο στους 103±2 C (βλέπε υποπαράγραφο 5.2.). Ο ηθμός αφήνεται να ψυχθεί σε ξηραντήρα (βλέπε υποπαράγραφο 5.4.) και ζυγίζεται Αναδεύεται το δείγμα της λεκιθίνης μετά από θέρμανση σε υδρόλουτρο (βλέπε υποπαράγραφο 5.3.) εφόσον αυτό έχει θεωρηθεί αναγκαίο. Εντός κωνικής φιάλης (βλέπε υποπαράγραφο 5.5.) ζυγίζονται, με προσέγγιση Img, περίπου 10g του δείγματος. Προστίθενται 3 00ml τολουολίου (βλέπε υποπαράγραφο 4.1.) και το μείγμα αναδεύεται μέχρι να διαλυθεί όλη η λεκιθίνη. Το διάλυμα διηθείται μέσω του ηθμού από φρυγμένο γυαλί (βλέπε υποπαράγραφο 5.1.). Με 25ml τολουολίου (βλέπε υποπαράγραφο 4.1.) εκπλύνεται η κωνική φιάλη (βλέπε υποπαράγραφο 5.5.). Τα διαλύματα εκπλύσεως διηθούνται μέσω του ηθμού (βλέπε υποπαράγραφο 5.1.). Η διαδικασία αυτή επαναλαμβάνεται με νέα ποσότητα 25ml τολουολίου (βλέπε υποπαράγραφο 4.1.). Ο ηθμός αφαιρείται και το τολουόλιο απορροφάται από το κενό Ο ηθμός (βλέπε υποπαράγραφο 5.1.) με το υπόλειμμα υφίσταται ξήρανση στους 103±2 C για δύο ώρες στον κλίβανο (βλέπε υποπαράγραφο 5.2.). Ο ηθμός αφήνεται να ψυχθεί στον ξηραντήρα (βλέπε υποπαράγραφο 5.4.) και στη συνέχεια ζυγίζεται Τα διαλαμβανόμενα στην υποπαράγραφο 6.3. επαναλαμβάνονται μέχρι που η διαφορά μεταξύ δύο διαδοχικών ζυγίσεων να μην υπερβαίνει τα 0,5 mg. Όμως, για ορθό υπολογισμό, σε πιθανή περίπτωση αύξησης της μάζας, λαμβάνεται υπόψη ο μικρότερος αριθμός που θα καταγραφεί.
20 Κ.Δ.Π. 115/ Διατύπωση των αποτελεσμάτων: 7.1. Τύπος και τρόπος υπολογισμού: Η περιεκτικότητα σε αδιάλυτες στο τολουόλιο ουσίες υπολογίζεται με βάση τον πιο κάτω τύπο: 100 (ΙΌ2 mi) mo όπου: mi = η μάζα του κενού ηθμού (βλέπε υποπαράγραφο 6.1.) εκφραζόμενη σε γραμμάρια, im = η μάζα του ηθμού μαζί με το υπόλειμμα (βλέπε υποπαράγραφο 6.4.) εκφραζόμενη σε γραμμάρια, mo = η αρχική μάζα του δείγματος εκφραζόμενη σε γραμμάρια Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει τα 30mg για 100g δείγματος. Μέρος 12 Μέθοδος ανίχνευσης των αναγωγικών ουσιών, εντός των γαλακτικών αλατών νατρίου, καλίου και ασβεστίου (Ε325, Ε326, Ε327) Η μέθοδος επιτρέπει τον ποιοτικό προσδιορισμό των αναγωγικών ουσιών: Του γαλακτικού νατρίου (Ε325), του γαλακτικού καλίου (Ε326), του γαλακτικού ασβεστίου (Ε327). Κατά το πείραμα προσδιορισμού του ορίου ανίχνευσης με αναγωγή του αντιδραστηρίου Fehling, το δείγμα αντιδρά με το αντιδραστήριο Fehling υπό τις συνθήκες που περιγράφονται πιο κάτω. Αναγωγή του αντιδραστηρίου Fehling από αναγωγικές ουσίες. Παρόμοιες ουσίες αποτελούνται γενικά από αναγωγικά σάκχαρα. 4. Αντιδραστήρια: 4.1. Αντιδραστήριο Fehling Α (διαλύονται 6,93g ένυδρου θειικού χαλκού (CuS04 5Η2Ο) εντός νερού και προστίθεται νερό μέχρι τα 100ml) Αντιδραστήριο Fehling Β (διαλύονται 34,6g μετά νατρίου και καλίου ένυδρο τρυγικό άλας) (KNaQH^CMFkO) και 10g καυστικού νατρίου μέσα στο νερό και προστίθεται νερό μέχρι τα 100ml. 5. Εκτέλεση του πειράματος: Διαλύεται lg δείγματος, ζυγισμένου με προσέγγιση Img μέσα σε 10ml ζεστού νερού. Προστίθενται 2ml αντιδραστηρίου Fehling Α (βλέπε υποπαράγραφο 4.1.) και 2ml αντιδραστηρίου Fehling Β (βλέπε υποπαράγραφο 4.2.). Παρατηρείται εάν επέρχεται αλλαγή της χροιάς μετά από ζέση του μείγματος επί ενός λεπτού. Η καθίζηση θειικού ασβεστίου, που συμβαίνει μερικές φορές, δεν επηρεάζει τη μέθοδο.
21 759 Κ.Δ.Π. 115/ Διατύπωση των αποτελεσμάτων: 6.1. Ερμηνεία της δοκιμασίας ανίχνευσης: Εάν παρατηρηθεί αλλαγή του χρώματος μετά τη ζέση (βλέπε παράγραφο 5), η δοκιμασία είναι θετική και επομένως υπάρχουν αναγωγικές ουσίες Ευαισθησία: Το όριο ανίχνευσης των αναγωγικών ουσιών είναι 10'Omg γλυκόζης σε 100g δείγματος Παρατηρήσεις: Τα αποτελέσματα δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, πρέπει να είναι ταυτόσημα Εάν το δείγμα περιέχει 2% γλυκόζη, τότε αντιδρά όλο το αντιδραστήριο Fehling. Μέρος 13 Μέθοδος προσδιορισμού των πτητικών οξέων εντός του ορθοφωσφορικού οξέος (Ε338) Η παρούσα μέθοδος επιτρέπει την ανίχνευση των πτητικών οξέίΰν εντός του ορθοφωσφορικού οξέος (Ε338), εκφραζόμενων σε οξικό οξύ. Με τη μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται η περιεκτικότητα σε πτητικά οξέα, εκφραζόμενων σε οξικό οξύ. Διάλυση του δείγματος και απόσταξη του διαλύματος. Ογκομέτρηση του αποστάγματος με διάλυμα καυστικού νατρίου και υπολογισμός της οξύτητας εκφραζόμενης σε οξικό οξύ. 4. Αντιδραστήρια: 4.1. Διάλυμα 1 % (m/v) φαινολοφθαλεΐ'νης σε αιθανόλη Καυστικό νάτριο 0,01 moi/1 5. Συσκευές: 5.1. Σφαιρική φιάλη απόσταξης με ατμοπαγίδα. 6. Εκτέλεση του πειράματος: Ζυγίζονται 60g δείγματος με προσέγγιση 50mg και τοποθετούνται εντός σφαιρικής φιάλης απόσταξης με ατμοπαγίδα (βλέπε υποπαράγραφο 5.1.) όπου προστίθενται 75ml νερού, το οποίο έχει πρόσφατα υποστεί ζέση και στη συνέχεια έχει ψυχθεί, αναδεύεται το διάλυμα και αποστάζονται 50ml από αυτό. Στο απόσταγμα προστίθενται μερικές σταγόνες διαλύματος φαινοφθαλεΐνης (βλέπε υποπαράγραφο 4.1.) και γίνεται ογκομέτρηση με διάλυμα καυστικού νατρίου 0,01 mol/l (βλέπε υποπαράγραφο 4.2.) μέχρι που η πρώτη κόκκινη χροιά διατηρηθεί επί 10 δευτερόλεπτα. 7. Διατύπωση των αποτελεσμάτων: 7.1. Τύπος και τρόπος υπολογισμού: Η περιεκτικότητα σε πτητικά οξέα, εκφραζόμενη σε mg/kg οξέος, υπολογίζεται με βάση τον πιο κάτω τύπο: 600 χ V mo
22 Κ.Δ.Π. 115/ όπου: V = ο όγκος σε ml του διαλύματος καυστικού νατρίου 0,01 mol/ι που χρησιμοποιήθηκε για την εξουδετέρωση, mo = η μάζα σε γραμμάρια του δείγματος του οροοφωσφορικού οξέος Επαναληπτικότητα: Η διαφορά μεταξύ των αποτελεσμάτων δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, δεν πρέπει να υπερβαίνει το 1 mg για 100g δείγματος. Μέρος 14 Μέθοδος ανίχνευσης των νιτρικών αλάτων εντός του οροοφωσφορικού οξέος (Ε338) Η παρούσα μέθοδος επιτρέπει την ανίχνευση των νιτρικών αλάτων εντός του οροοφωσφορικού οξέος (Ε338). Με τη μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται το όριο ανίχνευσης των νιτρικών αλάτων εκφραζόμενων σε νιτρικά άλατα νατρίου. Σε όξινο περιβάλλον, που επιτυγχάνεται με πυκνό διάλυμα θειικού οξέος, προστίθεται στο δείγμα ινδικοκαρμίνιο. Αποχρο)ματισμός με οξείδωση, οφειλόμενη σε οξειδούμενες ουσίες και συγκεκριμένα στα νιτρικά άλατα. 4. Αντιδραστήρια: 4.1. Διάλυμα ινδικοκαρμι.νίου περιεκτικότητας 0,18% (rn/v): διαλύονται 0,18g ινδικού δι Οειικού νατρίου μέσα σε 100ml νερού Διάλυμα 0,05% (m/v) χλωριούχου νατρίου Πυκνό θειικό οξύ ^)2o=l,84g/ml). 5. Εκτέλεση του πειράματος: 2ml του υπό ανάλυση ή εξέταση δείγματος διαλύονται μέσα σε διάλυμα χλωριούχου νατρίου (βλέπε υποπαράγραφο 4.2.) μέχρι να πάρει όγκο 10ml. Προστίθενται 0.1ml διαλύματος ινδικοκαρμινίου (βλέπε υποπαράγραφο 4.1.) και 10ml πυκνού θειικού οξέος (βλέπε υποπαράγραφο 4.3.) στάγδην και με σύγχρονη ψύξη. Να σημειωθεί εάν η μπλε χροιά του διαλύματος διατηρείται επί πέντε λεπτά. 6. Διατύπωση των αποτελεσμάτων: 6.1 Ερμηνεία της δοκιμασίας ανίχνευσης: Εάν η μπλε χροιά εξαφανιστεί εντελώς εντός πέντε λεπτών, το πείραμα είναι θετικό και η περιεκτικότητα σε οξειδούμενες ουσίες, εκφραζόμενες σε νιτρικά άλατα νατρίου, υπερβαίνει τα 5 mg/kg δείγματος Παρατηρήσεις: Να πραγματοποιηθεί μια τυφλή δοκιμασία των αντιδραστηρίων Τα αποτελέσματα των δύο προσδιορισμών, που πραγματοποιούνται ταυτόχρονα ή με μικρή διαφορά χρόνου, στο ίδιο δείγμα, υπό τις ίδιες συνθήκες και από το ίδιο πρόσωπο, πρέπει να είναι ταυτόσημα Το διάλυμα του ινδικοκαρμινίου δεν πρέπει να έχει ετοιμαστεί περισσότερο από 60 ημέρες από την εκτέλεση της παρούσας μεθόδου.
23 761 Κ.Δ.Π." 115/ Το θετικό αποτέλεσμα, σημαίνει ότι. το δείγμα μπορεί να περιέχει νιτρικά άλατα και άλλες οξειδούμενες ουσίες. Το πείραμα πρέπει να επαναληφθεί χρησιμοποιώντας αναγνωρισμένη μέθοδο περί φωσφορικού οξέος για βιομηχανική χρήση (περιλαμβανομένης και της βιομηχανίας τροφίμων) και περί ποσοτικής ανάλυσης του οξειδίου του αζώτου φασματομετρική μέθοδος με ξυλενόλη 3,4. Μέρος 15 Μέθοδος προσδιορισμού αδιάλυτων στο νερό ουσιών που εμφανίζονται εντός των ακόλουθων ορθοφωσφορικών αλάτων: δισόξινο φωσφορικό νάτριο, μονόξινο φωσφορικό νάτριο, φωσφορικό νάτριο, διόξινο φωσφορικό κάλιο, μονόξινο φωσφορικό κάλιο και φωσφορικό κάλιο (E339(i), E339(ii),' E339(iii), E340(i), E340(ii), E340(iii)) Η παρούσα μέθοδος επιτρέπει τον προσδιορισμό των αδιάλυτων στο νερό ουσιών που υπάρχουν στο: Δισόξινο φωσφορικό νάτριο (Ε339 (ϊ)), μονόξινο φωσφορικό νάτριο (Ε 339(ϋ)), φωσφορικό νάτριο (Ε339 (iii)), δισόξινο φοοσφορικό κάλιο (Ε340 (i)), μονόξινο φκοσφορικό κάλιο (Ε340 (ii)), φωσφορικό κάλιο (Ε340 (iii)). Με τη μέθοδο που περιγράφεται πιο κάτω προσδιορίζεται η περιεκτικότητα σε αδιάλυτες στο νερό ουσίες. Διάλυση του δείγματος στο νερό και διήθηση των αδιάλυτων ουσιών. Ξήρανση του υπολείμματος που εκφράζεται σε ουσίες που είναι αδιάλυτες στο νερό. 4. Συσκευές: 4.1. Ηθμός εκ πορώδους πορσελάνης G 3 ή ισοδύναμου μεγέθους πόρων Ξηραντήρας με Silica gel (S1O2), σε άνυδρη κατάσταση ή με άλλο αντίστοιχο υγροσκοπικό μέσο και εφοδιασμένος με δείκτη υγρασίας Ηλεκτρικός κλίβανος, ρυθμισμένος στους 103±2 C Ποτήρι των 400ml από πολυπροπυλένιο Ζέον υδρόλουτρο. 5. Εκτέλεση του πειράματος: Διαλύονται 10g δείγματος φωσφορικού άλατος, ζυγισμένα με προσέγγιση 10mg, εντός 100ml ζεστού νερού σε ποτήρι από πολυπροπυλένιο (βλέπε υποπαράγραφο 4.4) και διατηρείται εντός του ζέοντος υδρύλουτρου (βλέπε υποπαράγραφο 4.5.) επί 15 λεπτά. Το διάλυμα διηθείται μέσω του ηθμού (βλέπε υποπαράγραφο 4.1.) που έχει προηγουμένως υποστε' έκπλυση, ξήρανση και ζύγιση. Το αδιάλυτο υπόλειμα υφίσταται έκλουση με ζεστό νερό και ξηραίνεται εντός του κλιβάνου (βλέπε υποπαράγραφο 4.3.) στους 103±2 C. Μετά από πλήρη ξήρανση, που διαρκεί δύο ώρες, αφήνεται να ψυχθεί εντός του ξηραντήρα και ζυγίζεται. Η ξήρανση θεωρείται πλήρης, όταν η διαφορά μεταξύ δύο διαδοχικο.>ν ζυγίσεων δεν υπερβαίνει τα 0,5mg. Όμως, για ορθό υπολογίσιμο, σε πιθανή περίπτωση αύξησης της μάζας, λαμβάνεται υπόψη ο μ.ικρότερος αριθμός που θα καταγραφεί.
Επίσηµη Εφηµερίδα της Ευρωπαϊκής Ένωσης ΚΑΝΟΝΙΣΜΟΙ
 8.10.2016 L 273/5 ΚΑΝΟΝΙΣΜΟΙ ΕΚΤΕΛΕΣΤΙΚΟΣ ΚΑΝΟΝΙΣΜΟΣ (ΕΕ) 2016/1784 ΤΗΣ ΕΠΙΤΡΟΠΗΣ της 30ής Σεπτεμβρίου 2016 για την τροποποίηση του κανονισμού (ΕΟΚ) αριθ. 2568/91 σχετικά με τον προσδιορισμό των χαρακτηριστικών
8.10.2016 L 273/5 ΚΑΝΟΝΙΣΜΟΙ ΕΚΤΕΛΕΣΤΙΚΟΣ ΚΑΝΟΝΙΣΜΟΣ (ΕΕ) 2016/1784 ΤΗΣ ΕΠΙΤΡΟΠΗΣ της 30ής Σεπτεμβρίου 2016 για την τροποποίηση του κανονισμού (ΕΟΚ) αριθ. 2568/91 σχετικά με τον προσδιορισμό των χαρακτηριστικών
ΕΠΙΣΗΜΗ ΕΦΗΜΕΡΙΔΑ ΤΩΝ ΕΥΡΩΠΑΪΚΩΝ ΚΟΙΝΟΤΗΤΩΝ 373/65 ΟΔΗΓΙΑ ΤΟΥ ΣΥΜΒΟΥΛΙΟΥ
 162 Επίσημη Εφημερίδα των Ευρωπαϊκών Κοινοτήτων 365L0066 9.2.65 ΕΠΙΣΗΜΗ ΕΦΗΜΕΡΙΔΑ ΤΩΝ ΕΥΡΩΠΑΪΚΩΝ ΚΟΙΝΟΤΗΤΩΝ 373/65 ΟΔΗΓΙΑ ΤΟΥ ΣΥΜΒΟΥΛΙΟΥ της 26ης ' Ιανουαρίου 1965 περί θεσπίσεως ειδικών κριτηρίων καθαρότητας
162 Επίσημη Εφημερίδα των Ευρωπαϊκών Κοινοτήτων 365L0066 9.2.65 ΕΠΙΣΗΜΗ ΕΦΗΜΕΡΙΔΑ ΤΩΝ ΕΥΡΩΠΑΪΚΩΝ ΚΟΙΝΟΤΗΤΩΝ 373/65 ΟΔΗΓΙΑ ΤΟΥ ΣΥΜΒΟΥΛΙΟΥ της 26ης ' Ιανουαρίου 1965 περί θεσπίσεως ειδικών κριτηρίων καθαρότητας
Αναλυτική Χημεία Ι (Θ) Ερωτήσεις Πιστοποίησης
 Αναλυτική Χημεία Ι (Θ) Ερωτήσεις Πιστοποίησης Ερώτηση 1η: (Ομάδα 2.3.89) Πότε η φλόγα λέγεται αναγωγική και πότε οξειδωτική; Πολλά χημικά πειράματα για να γίνουν απαιτούν θέρμανση που γίνεται συνήθως με
Αναλυτική Χημεία Ι (Θ) Ερωτήσεις Πιστοποίησης Ερώτηση 1η: (Ομάδα 2.3.89) Πότε η φλόγα λέγεται αναγωγική και πότε οξειδωτική; Πολλά χημικά πειράματα για να γίνουν απαιτούν θέρμανση που γίνεται συνήθως με
1ο και 2ο ΕΚΦΕ Ηρακλείου ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO Σάββατο 3 Δεκεμβρίου 2017
 1ο και 2ο ΕΚΦΕ Ηρακλείου ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2017 Σάββατο 3 Δεκεμβρίου 2017 Διαγωνισμός στη Χημεία (Διάρκεια 1 ώρα) ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΜΑΘΗΤΩΝ 1)... ΣΧΟΛΕΙΟ
1ο και 2ο ΕΚΦΕ Ηρακλείου ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2017 Σάββατο 3 Δεκεμβρίου 2017 Διαγωνισμός στη Χημεία (Διάρκεια 1 ώρα) ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΜΑΘΗΤΩΝ 1)... ΣΧΟΛΕΙΟ
Σημειώσεις για την εργαστηριακή άσκηση ΑΝΑΛΥΣΗ ΟΙΝΟΥ του Εργαστηρίου Ανάλυσης και Τεχνολογίας Τροφίμων Καθηγητής Ιωάννης Ρούσσης.
 Σημειώσεις για την εργαστηριακή άσκηση ΑΝΑΛΥΣΗ ΟΙΝΟΥ του Εργαστηρίου Ανάλυσης και Τεχνολογίας Τροφίμων Καθηγητής Ιωάννης Ρούσσης Προσδιορισμοί Αλκοόλη Ολική οξύτητα Πτητική οξύτητα Ελεύθερος θειώδης ανυδρίτης
Σημειώσεις για την εργαστηριακή άσκηση ΑΝΑΛΥΣΗ ΟΙΝΟΥ του Εργαστηρίου Ανάλυσης και Τεχνολογίας Τροφίμων Καθηγητής Ιωάννης Ρούσσης Προσδιορισμοί Αλκοόλη Ολική οξύτητα Πτητική οξύτητα Ελεύθερος θειώδης ανυδρίτης
Προσδιορισμός της διαλυτότητας στο νερό στερεών ουσιών - Φύλλο εργασίας
 Προσδιορισμός της διαλυτότητας στο νερό στερεών ουσιών - Φύλλο εργασίας Γνωστικό αντικείμενο: Τάξη Διδακτική ενότητα Απαιτούμενος χρόνος Διαλυτότητα ουσιών σε υγρούς διαλύτες B Γυμνασίου Ενότητα 2: ΑΠΟ
Προσδιορισμός της διαλυτότητας στο νερό στερεών ουσιών - Φύλλο εργασίας Γνωστικό αντικείμενο: Τάξη Διδακτική ενότητα Απαιτούμενος χρόνος Διαλυτότητα ουσιών σε υγρούς διαλύτες B Γυμνασίου Ενότητα 2: ΑΠΟ
Πείραμα 4 ο. Προσδιορισμός Οξύτητας Τροφίμων
 Πείραμα 4 ο Προσδιορισμός Οξύτητας Τροφίμων Εισαγωγή Τα οργανικά οξέα που υπάρχουν ως συστατικά σε διάφορα τρόφιμα επηρεάζουν το άρωμα, το χρώμα, τη μικροβιακή σταθερότητα και τη διατήρηση της ποιότητας
Πείραμα 4 ο Προσδιορισμός Οξύτητας Τροφίμων Εισαγωγή Τα οργανικά οξέα που υπάρχουν ως συστατικά σε διάφορα τρόφιμα επηρεάζουν το άρωμα, το χρώμα, τη μικροβιακή σταθερότητα και τη διατήρηση της ποιότητας
ΑΝΑΛΥΣΕΙΣ ΒΑΣΙΚΗΣ ΣΥΣΤΑΣΗΣ ΟΙΝΟΥ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΝΑΛΥΣΕΙΣ ΒΑΣΙΚΗΣ ΣΥΣΤΑΣΗΣ ΟΙΝΟΥ ΚΑΘΗΓΗΤΗΣ ΙΩΑΝΝΗΣ ΡΟΥΣΣΗΣ Ο οίνος είναι αλκοολούχο ποτό που λαμβάνεται με ζύμωση χυμού σταφυλιών (γλεύκος, μούστος) Συστατικά Οίνου
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΝΑΛΥΣΕΙΣ ΒΑΣΙΚΗΣ ΣΥΣΤΑΣΗΣ ΟΙΝΟΥ ΚΑΘΗΓΗΤΗΣ ΙΩΑΝΝΗΣ ΡΟΥΣΣΗΣ Ο οίνος είναι αλκοολούχο ποτό που λαμβάνεται με ζύμωση χυμού σταφυλιών (γλεύκος, μούστος) Συστατικά Οίνου
Ο αλκοολικός τίτλος % vol είναι % v/v. Η αλκοόλη, % vol, μετράται στους 20 o C. Γίνεται διόρθωση της αλκοόλης όταν η θερμοκρασία είναι διαφορετική
 ΟΙΝΟΣ ΑΛΚΟΟΛΗ Με απόσταξη 200 ml οίνου συλλέγονται 133-150 ml αποστάγματος. Για την εξουδετέρωση της οξύτητας του οίνου, για να μη ληφθούν στο απόσταγμα πτητικά οξέα (οξικό, ανθρακικό και θειώδες), στα
ΟΙΝΟΣ ΑΛΚΟΟΛΗ Με απόσταξη 200 ml οίνου συλλέγονται 133-150 ml αποστάγματος. Για την εξουδετέρωση της οξύτητας του οίνου, για να μη ληφθούν στο απόσταγμα πτητικά οξέα (οξικό, ανθρακικό και θειώδες), στα
3016 Οξείδωση του ρικινολεϊκού οξέος ( από το καστορέλαιο) µε KMnO 4 προς αζελαϊκό οξύ
 6 Οξείδωση του ρικινολεϊκού οξέος ( από το καστορέλαιο) µε KMnO 4 προς αζελαϊκό οξύ CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Ταξινόµιση Τύποι
6 Οξείδωση του ρικινολεϊκού οξέος ( από το καστορέλαιο) µε KMnO 4 προς αζελαϊκό οξύ CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Ταξινόµιση Τύποι
ΕΝΟΡΓΑΝΗ ΑΝΑΛΥΣΗ ΕΡΓΑΣΤΗΡΙΟ
 ΕΝΟΡΓΑΝΗ ΑΝΑΛΥΣΗ ΕΡΓΑΣΤΗΡΙΟ ΗΜΕΡΑ: ΤΡΙΤΗ 11-11-2014 ΩΡΑ: 11:00-14:00 OMADA 3 Name: Celia Koutrafouri ΆΣΚΗΣΗ 10 (p.107-114) Εργαστηριακές Σημειώσεις Τίτλος Άσκησης: Φασματοφωτομετρικός Προσδιορισμός Σορβικού
ΕΝΟΡΓΑΝΗ ΑΝΑΛΥΣΗ ΕΡΓΑΣΤΗΡΙΟ ΗΜΕΡΑ: ΤΡΙΤΗ 11-11-2014 ΩΡΑ: 11:00-14:00 OMADA 3 Name: Celia Koutrafouri ΆΣΚΗΣΗ 10 (p.107-114) Εργαστηριακές Σημειώσεις Τίτλος Άσκησης: Φασματοφωτομετρικός Προσδιορισμός Σορβικού
Πείραμα 1 ο. Προσδιορισμός Υγρασίας Τροφίμων
 Πείραμα 1 ο Προσδιορισμός Υγρασίας Τροφίμων Εισαγωγή Η μέτρηση της υγρασίας των τροφίμων είναι ιδιαιτέρως σημαντική για τους παρακάτω λόγους: Απαιτήσεις νομοθεσίας: υπάρχουν θεσμοθετημένα όρια για τη μέγιστη
Πείραμα 1 ο Προσδιορισμός Υγρασίας Τροφίμων Εισαγωγή Η μέτρηση της υγρασίας των τροφίμων είναι ιδιαιτέρως σημαντική για τους παρακάτω λόγους: Απαιτήσεις νομοθεσίας: υπάρχουν θεσμοθετημένα όρια για τη μέγιστη
ΜΕΡΟΣ Α : Ερωτήσεις 1-6 Να απαντήσετε σε όλες τις ερωτήσεις 1-6. Κάθε ορθή απάντηση βαθμολογείται με πέντε (5) μονάδες.
 ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2008-2009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΔΕΙΓΜΑΤΙΚΟ ΕΞΕΤΑΣΤΙΚΟ ΔΟΚΙΜΙΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΤΑΞΗ: Β ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΧΡΟΝΟΣ: 2 ώρες και 30 λεπτά Το εξεταστικό δοκίμιο αποτελείται από
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2008-2009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΔΕΙΓΜΑΤΙΚΟ ΕΞΕΤΑΣΤΙΚΟ ΔΟΚΙΜΙΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΤΑΞΗ: Β ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΧΡΟΝΟΣ: 2 ώρες και 30 λεπτά Το εξεταστικό δοκίμιο αποτελείται από
ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργ. Κέντρου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργ. Κέντρου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ
 ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιμοποιούμενα όργανα Προχοϊδα: Μετράει
ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιμοποιούμενα όργανα Προχοϊδα: Μετράει
Σύντομη περιγραφή του πειράματος. Διδακτικοί στόχοι του πειράματος
 Σύντομη περιγραφή του πειράματος Υπολογισμός της περιεκτικότητας σε οξικό οξύ, του ξυδιού του εμπορίου με τη μέθοδο της ογκομέτρησης που καλείται αλκαλιμετρία. Χρησιμοποιείται δείκτης φαινολοφθαλεΐνης
Σύντομη περιγραφή του πειράματος Υπολογισμός της περιεκτικότητας σε οξικό οξύ, του ξυδιού του εμπορίου με τη μέθοδο της ογκομέτρησης που καλείται αλκαλιμετρία. Χρησιμοποιείται δείκτης φαινολοφθαλεΐνης
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
1004 Νίτρωση του πυριδινο-ν-οξειδίου σε 4-νιτροπυριδινο-Νοξείδιο
 1004 Νίτρωση του πυριδινο-ν-οξειδίου σε 4-νιτροπυριδινο-Νοξείδιο O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Ταξινόµηση Τύποι αντιδράσεων και τάξεις ουσιών Ηλεκτρονιόφιλη
1004 Νίτρωση του πυριδινο-ν-οξειδίου σε 4-νιτροπυριδινο-Νοξείδιο O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Ταξινόµηση Τύποι αντιδράσεων και τάξεις ουσιών Ηλεκτρονιόφιλη
FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4
![FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4 FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4](/thumbs/27/9949444.jpg) ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΤΟΜΕΑΣ ΓΕΝΙΚΗΣ ΚΑΙ ΑΝΟΡΓΑΝΗΣ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΤΟΥ ΜΑΘΗΜΑΤΟΣ «ΧΗΜΕΙΑ» για τους ΦΟΙΤΗΤΕΣ του ΤΜΗΜΑΤΟΣ ΦΥΣΙΚΗΣ Οι διδάσκοντες Αικατερίνη
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΤΟΜΕΑΣ ΓΕΝΙΚΗΣ ΚΑΙ ΑΝΟΡΓΑΝΗΣ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΤΟΥ ΜΑΘΗΜΑΤΟΣ «ΧΗΜΕΙΑ» για τους ΦΟΙΤΗΤΕΣ του ΤΜΗΜΑΤΟΣ ΦΥΣΙΚΗΣ Οι διδάσκοντες Αικατερίνη
ΟΙ ΠΕΡΙ ΤΡΟΦΙΜΩΝ (ΕΛΕΓΧΟΣ ΚΑΙ ΠΩΛΗΣΗ) ΝΟΜΟΙ ΤΟΥ 1996 ΕΩΣ Κανονισμοί δυνάμει του άρθρου 29
 Ε.Ε. Παρ. III(I) 4018 ΚΛ.Π. 477/2004 Αρ. 3852, 30.4.2004 Αριθμός 477 Οι περί Φυσικών Μεταλλικών Νερών (Τροποποιητικοί) Κανονισμοί του 2004, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των διατάξεων
Ε.Ε. Παρ. III(I) 4018 ΚΛ.Π. 477/2004 Αρ. 3852, 30.4.2004 Αριθμός 477 Οι περί Φυσικών Μεταλλικών Νερών (Τροποποιητικοί) Κανονισμοί του 2004, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των διατάξεων
1367 Κ.Δ.Π. 290/2003
 E.E. Παρ. ΙΠ(Ι) Αρ. 3704,11.4.2003 1367 Κ.Δ.Π. 290/2003 Αριθμός 290 ΟΙ ΠΕΡΙ ΤΡΟΦΙΜΩΝ (ΕΛΕΓΧΟΣ ΚΑΙ ΠΩΛΗΣΗ) ΝΟΜΟΙ ΤΟΥ 1996 ΕΩΣ (ΑΡ. 2) ΤΟΥ 2002 Διάταγμα δυνάμει του άρθρου 28 περί Τροποποίησης Παραρτήματος
E.E. Παρ. ΙΠ(Ι) Αρ. 3704,11.4.2003 1367 Κ.Δ.Π. 290/2003 Αριθμός 290 ΟΙ ΠΕΡΙ ΤΡΟΦΙΜΩΝ (ΕΛΕΓΧΟΣ ΚΑΙ ΠΩΛΗΣΗ) ΝΟΜΟΙ ΤΟΥ 1996 ΕΩΣ (ΑΡ. 2) ΤΟΥ 2002 Διάταγμα δυνάμει του άρθρου 28 περί Τροποποίησης Παραρτήματος
ΤΙΤΛΟΔΟΤΗΣΗ ΔΙΑΛΥΜΑΤΟΣ FeSO 4 ΜΕ ΠΡΟΤΥΠΟ ΔΙΑΛΥΜΑ KMnO 4 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΚΑΘΑΡΟΤΗΤΑΣ ΔΕΙΓΜΑΤΟΣ
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ για το EUSO 2017 ΕΚΦΕ ΘΗΡΑΣ ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΤΙΤΛΟΔΟΤΗΣΗ ΔΙΑΛΥΜΑΤΟΣ FeSO 4 ΜΕ ΠΡΟΤΥΠΟ ΔΙΑΛΥΜΑ KMnO 4 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΚΑΘΑΡΟΤΗΤΑΣ ΔΕΙΓΜΑΤΟΣ ΕΙΣΑΓΩΓΗ
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ για το EUSO 2017 ΕΚΦΕ ΘΗΡΑΣ ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΤΙΤΛΟΔΟΤΗΣΗ ΔΙΑΛΥΜΑΤΟΣ FeSO 4 ΜΕ ΠΡΟΤΥΠΟ ΔΙΑΛΥΜΑ KMnO 4 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΚΑΘΑΡΟΤΗΤΑΣ ΔΕΙΓΜΑΤΟΣ ΕΙΣΑΓΩΓΗ
54(1) του (1) του (1) του (1) του (1) του (1) του (1) του (1) του Συνοπτικός τίτλος.
 Ε.Ε. Παρ. III(I) 4872 Κ.Δ.Π. 456/2002 Αρ. 3639, 27.9.2002 Αριθμός 456 Οι περί Εκχυλισμάτων Καφέ και Εκχυλισμάτων Κιχωρίου Κανονισμοί του 2002, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των
Ε.Ε. Παρ. III(I) 4872 Κ.Δ.Π. 456/2002 Αρ. 3639, 27.9.2002 Αριθμός 456 Οι περί Εκχυλισμάτων Καφέ και Εκχυλισμάτων Κιχωρίου Κανονισμοί του 2002, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των
Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Διαλύματα Παρασκευή Διαλυμάτων
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Διαλύματα Παρασκευή Διαλυμάτων Ιωάννης Πούλιος Ιωάννης Ζιώγας Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ Διαλύματα Παρασκευή Διαλυμάτων Ιωάννης Πούλιος Ιωάννης Ζιώγας Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Β ΤΑΞΗΣ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ
 Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργαστηρίου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Β ΤΑΞΗΣ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ
Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργαστηρίου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Β ΤΑΞΗΣ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ
ΓΕΛ ΠΑΡΑΒΟΛΑΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 2013-2014
 ΓΕΛ ΠΑΡΑΒΟΛΑΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 2013-2014 Ερευνητική εργασία: Β2 λυκείου ΘΕΜΑ: ''Η Χημεία είναι χρώματα, αρώματα και γεύσεις'' Ομάδα Δ: Μαριάμ Χριστογιάννη Μαρία Χριστοπούλου Χριστίνα Σταμάτη Βάσω Σιρμιντζέλη
ΓΕΛ ΠΑΡΑΒΟΛΑΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 2013-2014 Ερευνητική εργασία: Β2 λυκείου ΘΕΜΑ: ''Η Χημεία είναι χρώματα, αρώματα και γεύσεις'' Ομάδα Δ: Μαριάμ Χριστογιάννη Μαρία Χριστοπούλου Χριστίνα Σταμάτη Βάσω Σιρμιντζέλη
5007 Αντίδραση φθαλικού ανυδρίτη µε ρεσορκίνη προς φλουρεσκεϊνη
 57 Αντίδραση φθαλικού ανυδρίτη µε ρεσορκίνη προς φλουρεσκεϊνη CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Ταξινόµηση Τύποι αντιδράσεων και τάξεις ουσιών Αντίδραση του καρβονυλίου
57 Αντίδραση φθαλικού ανυδρίτη µε ρεσορκίνη προς φλουρεσκεϊνη CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Ταξινόµηση Τύποι αντιδράσεων και τάξεις ουσιών Αντίδραση του καρβονυλίου
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ
 ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ Ογκομετρική Ανάλυση Ογκομετρική Ανάλυση Ογκομετρική ανάλυση ή ογκομέτρηση ονομάζεται η διαδικασία εύρεσης της συγκέντρωσης ενός διαλύματος υπολογίζοντας τον όγκο διαλύματος γνωστής
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ Ογκομετρική Ανάλυση Ογκομετρική Ανάλυση Ογκομετρική ανάλυση ή ογκομέτρηση ονομάζεται η διαδικασία εύρεσης της συγκέντρωσης ενός διαλύματος υπολογίζοντας τον όγκο διαλύματος γνωστής
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
3033 Σύνθεση του ακετυλενοδικαρβοξυλικού οξέος από το µεσοδιβρωµοηλεκτρικό
 3033 Σύνθεση του ακετυλενοδικαρβοξυλικού οξέος από το µεσοδιβρωµοηλεκτρικό οξύ HOOC H Br Br H COOH KOH HOOC COOH C 4 H 4 Br 2 O 4 C 4 H 2 O 4 (275.9) (56.1) (114.1) Ταξινόµηση Τύποι αντιδράσεων και τάξεις
3033 Σύνθεση του ακετυλενοδικαρβοξυλικού οξέος από το µεσοδιβρωµοηλεκτρικό οξύ HOOC H Br Br H COOH KOH HOOC COOH C 4 H 4 Br 2 O 4 C 4 H 2 O 4 (275.9) (56.1) (114.1) Ταξινόµηση Τύποι αντιδράσεων και τάξεις
ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ
 ΠΑΝΕΚΦE ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΥΠΕΥΘΥΝΩΝ ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΕΝΤΡΩΝ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 16 η Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών EUSO 2018 Τοπικός Διαγωνισμός Καρδίτσας Ε.Κ.Φ.Ε. Καρδίτσας ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ
ΠΑΝΕΚΦE ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΥΠΕΥΘΥΝΩΝ ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΕΝΤΡΩΝ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 16 η Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών EUSO 2018 Τοπικός Διαγωνισμός Καρδίτσας Ε.Κ.Φ.Ε. Καρδίτσας ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
Σύντομη περιγραφή του πειράματος
 Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
Στοιχειμετρικοί υπολογισμοί σε διαλύματα
 Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Για σκοπούς εναρμόνισης με την πράξη της Ευρωπαϊκής. Κοινότητας με τίτλο «Οδηγία 2004/45/ΕΚ της Επιτροπής της 16ης
 Ε.Ε. Παρ. ΠΙ(Ι) 3186 Κ.Λ.Π. 352/2005 Αρ. 4019, 29.7.2005 Αριθμός 352 Οι περί Ποικίλων Ουσιών στα Τρόφιμα (Τροποποιητικοί) Κανονισμοί του 2005, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των
Ε.Ε. Παρ. ΠΙ(Ι) 3186 Κ.Λ.Π. 352/2005 Αρ. 4019, 29.7.2005 Αριθμός 352 Οι περί Ποικίλων Ουσιών στα Τρόφιμα (Τροποποιητικοί) Κανονισμοί του 2005, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των
1. Οι παρόντες Κανονισμοί θα αναφέρονται ως οι περί Σακχάρων Κανονισμοί
 Ε.Ε. Παρ. III(I) 4659 Κ.Δ.Π. 433/2002 Αρ. 3638, 27.9.2002 Αριθμός 433 Οι περί Σακχάρων Κανονισμοί του 2002, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των διατάξεων του άρθρου 29 των περί Τροφίμων
Ε.Ε. Παρ. III(I) 4659 Κ.Δ.Π. 433/2002 Αρ. 3638, 27.9.2002 Αριθμός 433 Οι περί Σακχάρων Κανονισμοί του 2002, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των διατάξεων του άρθρου 29 των περί Τροφίμων
9. Προσδιορισμός της σταθεράς του γινομένου διαλυτότητας του ιωδικού ασβεστίου, Ca(IO 3 ) 2
 9. Προσδιορισμός της σταθεράς του γινομένου διαλυτότητας του ιωδικού ασβεστίου, Ca(IO 3 ) 2 Σκοπός Σκοπός αυτής της εργαστηριακής άσκησης είναι να μάθουμε να προσδιορίζουμε τη γραμμομοριακή διαλυτότητα
9. Προσδιορισμός της σταθεράς του γινομένου διαλυτότητας του ιωδικού ασβεστίου, Ca(IO 3 ) 2 Σκοπός Σκοπός αυτής της εργαστηριακής άσκησης είναι να μάθουμε να προσδιορίζουμε τη γραμμομοριακή διαλυτότητα
(Μη νομοθετικές πράξεις) ΚΑΝΟΝΙΣΜΟΙ
 31.3.2012 Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης L 95/1 II (Μη νομοθετικές πράξεις) ΚΑΝΟΝΙΣΜΟΙ ΚΑΤ ΕΞΟΥΣΙΟΔΟΤΗΣΗ ΚΑΝΟΝΙΣΜΟΣ (ΕΕ) αριθ. 286/2012 ΤΗΣ ΕΠΙΤΡΟΠΗΣ της 27ης Ιανουαρίου 2012 για τροποποίηση με
31.3.2012 Επίσημη Εφημερίδα της Ευρωπαϊκής Ένωσης L 95/1 II (Μη νομοθετικές πράξεις) ΚΑΝΟΝΙΣΜΟΙ ΚΑΤ ΕΞΟΥΣΙΟΔΟΤΗΣΗ ΚΑΝΟΝΙΣΜΟΣ (ΕΕ) αριθ. 286/2012 ΤΗΣ ΕΠΙΤΡΟΠΗΣ της 27ης Ιανουαρίου 2012 για τροποποίηση με
ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO Ε.Κ.Φ.Ε. Νέας Σμύρνης
 ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2015-2016 Ε.Κ.Φ.Ε. Νέας Σμύρνης Εξέταση στη Χημεία ΛΥΚΕΙΟ: Τριμελής ομάδα μαθητών: 1. 2. 3. Αναπληρωματικός: Συνεργάτης Χημικός: Ανδρέας Δαζέας Α Σειρά Θεμάτων (Χημεία)
ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2015-2016 Ε.Κ.Φ.Ε. Νέας Σμύρνης Εξέταση στη Χημεία ΛΥΚΕΙΟ: Τριμελής ομάδα μαθητών: 1. 2. 3. Αναπληρωματικός: Συνεργάτης Χημικός: Ανδρέας Δαζέας Α Σειρά Θεμάτων (Χημεία)
ΟΙ ΠΕΡΙ ΤΡΟΦΙΜΩΝ (ΕΛΕΓΧΟΣ ΚΑΙ ΠΩΛΗΣΗ) ΝΟΜΟΙ ΤΟΥ 1996 ΕΩΣ 2002
 Ε.Ε. Παρ. III(I) 2479 Κ.Δ.Π. 263/2002 Αρ. 3608, 31.5.2002 Αριθμός 263 Οι περί Ερουσικού Οξέος στα Τρόφιμα (Τροποποιητικοί) Κανονισμοί του 2002, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των
Ε.Ε. Παρ. III(I) 2479 Κ.Δ.Π. 263/2002 Αρ. 3608, 31.5.2002 Αριθμός 263 Οι περί Ερουσικού Οξέος στα Τρόφιμα (Τροποποιητικοί) Κανονισμοί του 2002, οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει των
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΟΞΥΤΗΤΑΣ ΣΕ ΚΡΑΣΙ (ΛΕΥΚΟ)
 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΥΠΕΥΘΥΝΩΝ ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΕΝΤΡΩΝ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ - «ΠΑΝΕΚΦE» email:panekfe@yahoo.gr www.ekfe.gr ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2010 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΣΤΗ
ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΥΠΕΥΘΥΝΩΝ ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΕΝΤΡΩΝ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ - «ΠΑΝΕΚΦE» email:panekfe@yahoo.gr www.ekfe.gr ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2010 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΣΤΗ
ΛΥΚΕΙΟ ΣΟΛΕΑΣ Σχολική χρονιά
 ΛΥΚΕΙΟ ΣΟΛΕΑΣ Σχολική χρονιά 008-009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 009 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ (επιλογής) ΤΑΞΗ: Β ΗΜΕΡΟΜΗΝΙΑ: Δευτέρα, 1/6/009 ΧΡΟΝΟΣ:,5 ώρες ΒΑΘΜΟΣ Αριθμητικώς: Ολογράφως: Υπογραφή: Ονοματεπώνυμο:
ΛΥΚΕΙΟ ΣΟΛΕΑΣ Σχολική χρονιά 008-009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 009 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ (επιλογής) ΤΑΞΗ: Β ΗΜΕΡΟΜΗΝΙΑ: Δευτέρα, 1/6/009 ΧΡΟΝΟΣ:,5 ώρες ΒΑΘΜΟΣ Αριθμητικώς: Ολογράφως: Υπογραφή: Ονοματεπώνυμο:
5012 Σύνθεση του ακετυλοσαλικυλικού οξέος (ασπιρίνης) από σαλικυλικό οξύ και οξικό ανυδρίτη
 NP 0 Σύνθεση του ακετυλοσαλικυλικού οξέος (ασπιρίνης) από σαλικυλικό οξύ και οξικό ανυδρίτη CH CH + H H S + CH CH C H 6 C 7 H 6 C 9 H 8 C H (0.) (8.) (98.) (80.) (60.) Ταξινόµηση Τύποι αντιδράσεων και
NP 0 Σύνθεση του ακετυλοσαλικυλικού οξέος (ασπιρίνης) από σαλικυλικό οξύ και οξικό ανυδρίτη CH CH + H H S + CH CH C H 6 C 7 H 6 C 9 H 8 C H (0.) (8.) (98.) (80.) (60.) Ταξινόµηση Τύποι αντιδράσεων και
Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και συνήθως έχει χωρητικότητα από 10 έως 250 ml.
 ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει
ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει
ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ
 ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ Α. ΙΣΟΡΡΟΠΙΑ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΥΔΑΤΙΚO ΔΙΑΛΥΜΑ Λίγα λόγια πριν από το πείραμα. Η σόδα περιέχει διαλυμένο αέριο διοξείδιο του άνθρακα το οποίο προστίθεται κατά την
ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ Α. ΙΣΟΡΡΟΠΙΑ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΥΔΑΤΙΚO ΔΙΑΛΥΜΑ Λίγα λόγια πριν από το πείραμα. Η σόδα περιέχει διαλυμένο αέριο διοξείδιο του άνθρακα το οποίο προστίθεται κατά την
ΣΧΟΛΕΙΟ: ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ - ΙΟΥΝΙΟΥ. ΧΡΟΝΟΣ: 2,5 ώρες ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΧΡΗΣΙΜΑ ΔΕΔΟΜΕΝΑ
 ΣΧΟΛΕΙΟ: ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2014 2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ - ΙΟΥΝΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΗΜΕΡΟΜΗΝΙΑ : ΧΡΟΝΟΣ: 2,5 ώρες ΤΑΞΗ: Β Ενιαίου Λυκείου ΩΡΑ ΕΝΑΡΞΗΣ:. ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Τμήμα: Aρ.:.
ΣΧΟΛΕΙΟ: ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2014 2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ - ΙΟΥΝΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΗΜΕΡΟΜΗΝΙΑ : ΧΡΟΝΟΣ: 2,5 ώρες ΤΑΞΗ: Β Ενιαίου Λυκείου ΩΡΑ ΕΝΑΡΞΗΣ:. ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Τμήμα: Aρ.:.
ΣΧΟΛΕΙΟ: ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ - ΙΟΥΝΙΟΥ. ΧΡΟΝΟΣ: 2,5 ώρες ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΧΡΗΣΙΜΑ ΔΕΔΟΜΕΝΑ
 ΣΧΟΛΕΙΟ: ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2014 2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ - ΙΟΥΝΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΗΜΕΡΟΜΗΝΙΑ : ΧΡΟΝΟΣ: 2,5 ώρες ΤΑΞΗ: Β Ενιαίου Λυκείου ΩΡΑ ΕΝΑΡΞΗΣ:. ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Τμήμα: Aρ.:.
ΣΧΟΛΕΙΟ: ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2014 2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ - ΙΟΥΝΙΟΥ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΚΑΤΕΥΘΥΝΣΗΣ ΗΜΕΡΟΜΗΝΙΑ : ΧΡΟΝΟΣ: 2,5 ώρες ΤΑΞΗ: Β Ενιαίου Λυκείου ΩΡΑ ΕΝΑΡΞΗΣ:. ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Τμήμα: Aρ.:.
4014 ιαχωρισµός των εναντιοµερών (R)- και (S)- 2,2 διυδροξυ-1,1 -διναφθαλινίων ((R)- και (S)-1,1-δι-2- ναφθολών)
 4014 ιαχωρισµός των εναντιοµερών (R)- και (S)- 2,2 διυδροξυ-1,1 -διναφθαλινίων ((R)- και (S)-1,1-δι-2- ναφθολών) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O R-εναντιοµερές S-εναντιοµερές (286.3) (421.0)
4014 ιαχωρισµός των εναντιοµερών (R)- και (S)- 2,2 διυδροξυ-1,1 -διναφθαλινίων ((R)- και (S)-1,1-δι-2- ναφθολών) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O R-εναντιοµερές S-εναντιοµερές (286.3) (421.0)
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΕΛΕΓΧΟΣ ΛΙΠΩΝ & ΕΛΑΙΩΝ. Β/Ο: ΠΟΙΟΤΙΚΟΣ ΕΛΕΓΧΟΣ Β ΠΡΟΟΔΟΣ- 1.ΕΝΟΤΗΤΑ (p.34-44) Α) ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΥΓΡΑΣΙΑΣ ΛΙΠΑΡΩΝ ΥΛΩΝ
 ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΕΛΕΓΧΟΣ ΛΙΠΩΝ & ΕΛΑΙΩΝ Β/Ο: ΠΟΙΟΤΙΚΟΣ ΕΛΕΓΧΟΣ Β ΠΡΟΟΔΟΣ- 1.ΕΝΟΤΗΤΑ (p.34-44) Α) ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΥΓΡΑΣΙΑΣ ΛΙΠΑΡΩΝ ΥΛΩΝ Oι Συνηθισμένες Μέθοδοι Προσδιορισμού Υγρασίας των Λ.Υ, Ταξινομούνται
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΕΛΕΓΧΟΣ ΛΙΠΩΝ & ΕΛΑΙΩΝ Β/Ο: ΠΟΙΟΤΙΚΟΣ ΕΛΕΓΧΟΣ Β ΠΡΟΟΔΟΣ- 1.ΕΝΟΤΗΤΑ (p.34-44) Α) ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΥΓΡΑΣΙΑΣ ΛΙΠΑΡΩΝ ΥΛΩΝ Oι Συνηθισμένες Μέθοδοι Προσδιορισμού Υγρασίας των Λ.Υ, Ταξινομούνται
Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους.
 ΔΙΑΛΥΜΑΤΑ Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους. Διαλύτης: η ουσία που βρίσκεται σε μεγαλύτερη αναλογία
ΔΙΑΛΥΜΑΤΑ Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους. Διαλύτης: η ουσία που βρίσκεται σε μεγαλύτερη αναλογία
Πείραμα 7 ο. Προσδιορισμός βιταμίνης C σε χυμούς φρούτων
 Πείραμα 7 ο Προσδιορισμός βιταμίνης C σε χυμούς φρούτων Εισαγωγή Συντακτικός τύπος βιταμίνης C Η βιταμίνη C είναι παράγωγο εξοζών και γι αυτό μπορεί να ταξινομηθεί στους υδατάνθρακες. Εμφανίζεται σε δύο
Πείραμα 7 ο Προσδιορισμός βιταμίνης C σε χυμούς φρούτων Εισαγωγή Συντακτικός τύπος βιταμίνης C Η βιταμίνη C είναι παράγωγο εξοζών και γι αυτό μπορεί να ταξινομηθεί στους υδατάνθρακες. Εμφανίζεται σε δύο
Ογκομετρήσεις Εξουδετέρωσης
 Άσκηση 5η Ογκομετρήσεις Εξουδετέρωσης Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Ποσοτική Ανάλυση Αναλυτική Χημεία Ποιοτική Ανάλυση Ποσοτική Ανάλυση Ογκομετρική ανάλυση Ποσοτικός προσδιορισμός
Άσκηση 5η Ογκομετρήσεις Εξουδετέρωσης Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Ποσοτική Ανάλυση Αναλυτική Χημεία Ποιοτική Ανάλυση Ποσοτική Ανάλυση Ογκομετρική ανάλυση Ποσοτικός προσδιορισμός
Παρασκευαστικό διαχωρισμό πολλών ουσιών με κατανομή μεταξύ των δύο διαλυτών.
 1. ΕΚΧΥΛΙΣΗ Η εκχύλιση είναι μία από τις πιο συνηθισμένες τεχνικές διαχωρισμού και βασίζεται στην ισορροπία κατανομής μιας ουσίας μεταξύ δύο φάσεων, που αναμιγνύονται ελάχιστα μεταξύ τους. Η ευρύτητα στη
1. ΕΚΧΥΛΙΣΗ Η εκχύλιση είναι μία από τις πιο συνηθισμένες τεχνικές διαχωρισμού και βασίζεται στην ισορροπία κατανομής μιας ουσίας μεταξύ δύο φάσεων, που αναμιγνύονται ελάχιστα μεταξύ τους. Η ευρύτητα στη
ΕΚΦΕ Τρικάλων. Πειραματική Δοκιμασία στη Χημεία. Τοπικός Μαθητικός Διαγωνισμός. Τρίκαλα, Σάββατο, 8 Δεκεμβρίου 2012
 1 Τοπικός Μαθητικός Διαγωνισμός 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2013 11Η ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΕΠΙΣΤΗΜΩΝ EUSO 2013 ΕΚΦΕ Τρικάλων Πειραματική Δοκιμασία στη Χημεία Τοπικός Μαθητικός Διαγωνισμός Τρίκαλα,
1 Τοπικός Μαθητικός Διαγωνισμός 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2013 11Η ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΕΠΙΣΤΗΜΩΝ EUSO 2013 ΕΚΦΕ Τρικάλων Πειραματική Δοκιμασία στη Χημεία Τοπικός Μαθητικός Διαγωνισμός Τρίκαλα,
Σημειώσεις για την εργαστηριακή άσκηση ΑΝΑΛΥΣΗ ΓΑΛΑΚΤΟΣ του Εργαστηρίου Ανάλυσης και Τεχνολογίας Τροφίμων Καθηγητής Ιωάννης Ρούσσης.
 Σημειώσεις για την εργαστηριακή άσκηση ΑΝΑΛΥΣΗ ΓΑΛΑΚΤΟΣ του Εργαστηρίου Ανάλυσης και Τεχνολογίας Τροφίμων Καθηγητής Ιωάννης Ρούσσης Προσδιορισμοί Ειδικό βάρος Οξύτητα Στερεό υπόλειμμα Λακτόζη Έλεγχος παστερίωσης
Σημειώσεις για την εργαστηριακή άσκηση ΑΝΑΛΥΣΗ ΓΑΛΑΚΤΟΣ του Εργαστηρίου Ανάλυσης και Τεχνολογίας Τροφίμων Καθηγητής Ιωάννης Ρούσσης Προσδιορισμοί Ειδικό βάρος Οξύτητα Στερεό υπόλειμμα Λακτόζη Έλεγχος παστερίωσης
Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ
 Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ Ονόματα διαγωνιζομένων: 1) 2) 3) Σχολείο: Όνομα Υπεύθυνου Καθηγητή: 1 η ΠΕΙΡΑΜΑΤΙΚΗ ΔΡΑΣΤΗΡΙΟΤΗΤΑ
Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ Ονόματα διαγωνιζομένων: 1) 2) 3) Σχολείο: Όνομα Υπεύθυνου Καθηγητή: 1 η ΠΕΙΡΑΜΑΤΙΚΗ ΔΡΑΣΤΗΡΙΟΤΗΤΑ
- 87 - ΕΝΟΤΗΤΑ Θ ΣΥΝΘΕΣΗ ΕΣΤΕΡΩΝ
 - 87 - ΕΝΟΤΗΤΑ Θ ΣΥΝΘΕΣΗ ΕΣΤΕΡΩΝ Οι εστέρες είναι μια κατηγορία οργανικών ενώσεων πολύ διαδεδομένη στη φύση, με γενικό τύπο: C R R' Πολλοί πτητικοί εστέρες έχουν έντονη, ευχάριστη οσμή και άρωμα φρούτων.
- 87 - ΕΝΟΤΗΤΑ Θ ΣΥΝΘΕΣΗ ΕΣΤΕΡΩΝ Οι εστέρες είναι μια κατηγορία οργανικών ενώσεων πολύ διαδεδομένη στη φύση, με γενικό τύπο: C R R' Πολλοί πτητικοί εστέρες έχουν έντονη, ευχάριστη οσμή και άρωμα φρούτων.
Ο! ΠΕΡΙ ΤΡΟΦΙΜΩΝ (ΕΛΕΓΧΟΣ ΚΑΙ ΠΩΛΗΣΗ) ΝΟΜΟΙ ΤΟΥ 1996 ΕΩΣ (ΑΡ. 3) ΤΟΥ Κανονισμοί δυνάμει του άρθρου 29
 .Ε. Παρ. ΙΪΙ(Ι) 3964 Κ.Δ.Π. 474/2004 ρ. 3852, 30.4.2004.ριθμός 474 Οι περί Μεθόδων Δειγματοληψίας και Ανάλυσης Τροφίμων για Έλεγχο των Μεγίτων Περιεκτικοτήτων Πατουλίνης στα Τρόφιμα Κανονισμοί του 2004,
.Ε. Παρ. ΙΪΙ(Ι) 3964 Κ.Δ.Π. 474/2004 ρ. 3852, 30.4.2004.ριθμός 474 Οι περί Μεθόδων Δειγματοληψίας και Ανάλυσης Τροφίμων για Έλεγχο των Μεγίτων Περιεκτικοτήτων Πατουλίνης στα Τρόφιμα Κανονισμοί του 2004,
5. Η ισχύς ενός λευκαντικού ρούχων
 5. Η ισχύς ενός λευκαντικού ρούχων Σκοπός Τα λευκαντικά είναι συνήθως υδατικά διαλύματα υποχλωριώδους νατρίου, NaOCl, και κυκλοφορούν με την εμπορική ονομασία «χλωρίνη». Σκοπός αυτού του πειράματος είναι
5. Η ισχύς ενός λευκαντικού ρούχων Σκοπός Τα λευκαντικά είναι συνήθως υδατικά διαλύματα υποχλωριώδους νατρίου, NaOCl, και κυκλοφορούν με την εμπορική ονομασία «χλωρίνη». Σκοπός αυτού του πειράματος είναι
ΤΙΤΛΟΔΟΤΗΣΗ ΟΞΕΩΝ ΚΑΙ ΒΑΣΕΩΝ
 ΤΙΤΛΟΔΟΤΗΣΗ ΟΞΕΩΝ ΚΑΙ ΒΑΣΕΩΝ Σκοπός Εργαστηριακής Άσκησης Η εξοικείωση με τις τεχνικές τιτλοδότησης και η κατανόηση των ογκομετρικών μεθόδων ανάλυσης. Θεωρητικό Μέρος Πάρα πολύ συχνά προκύπτει η ανάγκη
ΤΙΤΛΟΔΟΤΗΣΗ ΟΞΕΩΝ ΚΑΙ ΒΑΣΕΩΝ Σκοπός Εργαστηριακής Άσκησης Η εξοικείωση με τις τεχνικές τιτλοδότησης και η κατανόηση των ογκομετρικών μεθόδων ανάλυσης. Θεωρητικό Μέρος Πάρα πολύ συχνά προκύπτει η ανάγκη
Επιχάλκωση μεταλλικού αντικειμένου και συγκεκριμένα ενός μικρού ελάσματος αλουμινίου με τη μέθοδο της γαλβανοπλαστικής επιμετάλλωσης.
 Σύντομη περιγραφή του πειράματος Επιχάλκωση μεταλλικού αντικειμένου και συγκεκριμένα ενός μικρού ελάσματος αλουμινίου με τη μέθοδο της γαλβανοπλαστικής επιμετάλλωσης. Διδακτικοί στόχοι του πειράματος Στο
Σύντομη περιγραφή του πειράματος Επιχάλκωση μεταλλικού αντικειμένου και συγκεκριμένα ενός μικρού ελάσματος αλουμινίου με τη μέθοδο της γαλβανοπλαστικής επιμετάλλωσης. Διδακτικοί στόχοι του πειράματος Στο
Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ. Χημεία. Εργαστηριακή άσκηση ΑΣΠΡΟΠΥΡΓΟΣ
 ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία Εργαστηριακή άσκηση ΑΣΠΡΟΠΥΡΓΟΣ 2 ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΦΥΛΛΟ ΕΡΓΟΥ 1 ΤΙΤΛΟΣ ΑΣΚΗΣΗΣ Προσδιορισμός περιεκτικότητας άγνωστου
ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία Εργαστηριακή άσκηση ΑΣΠΡΟΠΥΡΓΟΣ 2 ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΦΥΛΛΟ ΕΡΓΟΥ 1 ΤΙΤΛΟΣ ΑΣΚΗΣΗΣ Προσδιορισμός περιεκτικότητας άγνωστου
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:.
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 15 η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2017 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συμμετέχουν: (1) (2) (3) Σέρρες 10/12/2016
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 15 η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2017 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συμμετέχουν: (1) (2) (3) Σέρρες 10/12/2016
Πρόταση Φύλλου Εργασίας για την εργαστηριακή άσκηση «Μελετώντας το περιεχόμενο τού χυμού του πορτοκαλιού»
 Πρόταση Φύλλου Εργασίας για την εργαστηριακή άσκηση «Μελετώντας το περιεχόμενο τού χυμού του πορτοκαλιού» Χαραλαμπάτου Λιάνα, υπεύθυνη Ε.Κ.Φ.Ε. Νίκαιας Αποστολόπουλος Κωνσταντίνος, Σχολικός Σύμβουλος ΠΕ04,
Πρόταση Φύλλου Εργασίας για την εργαστηριακή άσκηση «Μελετώντας το περιεχόμενο τού χυμού του πορτοκαλιού» Χαραλαμπάτου Λιάνα, υπεύθυνη Ε.Κ.Φ.Ε. Νίκαιας Αποστολόπουλος Κωνσταντίνος, Σχολικός Σύμβουλος ΠΕ04,
1 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ A' ΛΥΚΕΙΟΥ
 1 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ A' ΛΥΚΕΙΟΥ "Μελετώντας το περιεχόμενο τού χυμού του πορτοκαλιού" Ομάδα μαθητών: 1. 2. 3. 4. [2] Βασικό ερευνητικό ερώτημα: Ποιες ουσίες περιέχονται στο φρέσκο χυμό πορτοκαλιού;
1 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ A' ΛΥΚΕΙΟΥ "Μελετώντας το περιεχόμενο τού χυμού του πορτοκαλιού" Ομάδα μαθητών: 1. 2. 3. 4. [2] Βασικό ερευνητικό ερώτημα: Ποιες ουσίες περιέχονται στο φρέσκο χυμό πορτοκαλιού;
1. Ταυτοποίηση μιας άγνωστης χημικής ένωσης
 Σκοπός 1. Ταυτοποίηση μιας άγνωστης χημικής ένωσης Σκοπός αυτής της εργαστηριακής άσκησης είναι να μάθετε να δίνετε έμφαση στη σημασία της παρατήρησης κατά την εκτέλεση ενός πειράματος. Παρατήρηση, γενικά,
Σκοπός 1. Ταυτοποίηση μιας άγνωστης χημικής ένωσης Σκοπός αυτής της εργαστηριακής άσκησης είναι να μάθετε να δίνετε έμφαση στη σημασία της παρατήρησης κατά την εκτέλεση ενός πειράματος. Παρατήρηση, γενικά,
5585 ' ' Κ.Δ.Π. 511/2002
 E.E. Παρ. ΙΙΙ(Ι) 5584 Κ.Δ.Π. 511/2002 Αρ. 3647, 25.10.2002 Αριθμός 511 Οι περί Ελέγχου της Ρύπανσης των Νερών (Απόρριψη Υδραργύρου από Τομείς Εκτός του Βιομηχανικού Τομέα της Ηλεκτρόλυσης των Χλωριούχων
E.E. Παρ. ΙΙΙ(Ι) 5584 Κ.Δ.Π. 511/2002 Αρ. 3647, 25.10.2002 Αριθμός 511 Οι περί Ελέγχου της Ρύπανσης των Νερών (Απόρριψη Υδραργύρου από Τομείς Εκτός του Βιομηχανικού Τομέα της Ηλεκτρόλυσης των Χλωριούχων
Το χρώμα του μπλε της θυμόλης σε διαφορετικές τιμές ph
 Ε.Κ.Φ.Ε. Χαλανδρίου 9 ος Εργαστηριακός Διαγωνισμός Φυσικών Επιστημών Γυμνασίων Μέρος 2 ο : Χημεία - Τρίτη 9 Μαΐου Όνομα σχολείου: Ονοματεπώνυμο μαθητών 1.. 2... 3.. Όπως γνωρίζετε, σύμφωνα με τον Arrhenius,
Ε.Κ.Φ.Ε. Χαλανδρίου 9 ος Εργαστηριακός Διαγωνισμός Φυσικών Επιστημών Γυμνασίων Μέρος 2 ο : Χημεία - Τρίτη 9 Μαΐου Όνομα σχολείου: Ονοματεπώνυμο μαθητών 1.. 2... 3.. Όπως γνωρίζετε, σύμφωνα με τον Arrhenius,
Στόχοι της εργαστηριακής άσκησης
 ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2013-2014 Τοπικός διαγωνισμός στη Χημεία Ονόματα των μαθητών της ομάδας: 1) 2) 3) Στόχοι της εργαστηριακής
ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2013-2014 Τοπικός διαγωνισμός στη Χημεία Ονόματα των μαθητών της ομάδας: 1) 2) 3) Στόχοι της εργαστηριακής
Τοπικός Μαθητικός Διαγωνισμός EUSO
 2014 Ε.Κ.Φ.Ε. Καστοριάς Τοπικός Μαθητικός Διαγωνισμός EUSO 2014-2015 ΟΜΑΔΑ : 1] 2] 3] Γενικό Λύκειο Άργους Ορεστικού. 6 - Δεκ. - 1014 Χημεία ΟΔΗΓΙΕΣ ΚΑΝΟΝΕΣ ΑΣΦΑΛΕΙΑΣ Το εργαστήριο είναι χώρος για σοβαρή
2014 Ε.Κ.Φ.Ε. Καστοριάς Τοπικός Μαθητικός Διαγωνισμός EUSO 2014-2015 ΟΜΑΔΑ : 1] 2] 3] Γενικό Λύκειο Άργους Ορεστικού. 6 - Δεκ. - 1014 Χημεία ΟΔΗΓΙΕΣ ΚΑΝΟΝΕΣ ΑΣΦΑΛΕΙΑΣ Το εργαστήριο είναι χώρος για σοβαρή
5004 Ακεταλοποίηση της 3-νιτροβενζαλδεΰδης µε αιθανοδιόλη προς το αντίστοιχο διοξολάνιο καταλυόµενη από οξέα
 5004 Ακεταλοποίηση της 3-νιτροβενζαλδεΰδης µε αιθανοδιόλη προς το αντίστοιχο διοξολάνιο καταλυόµενη από οξέα H O O O + HO 4-τολουολοσουλφονικό οξύ + H 2 O NO 2 HO NO 2 C 7 H 5 NO 3 C 2 H 6 O 2 C 7 H 8
5004 Ακεταλοποίηση της 3-νιτροβενζαλδεΰδης µε αιθανοδιόλη προς το αντίστοιχο διοξολάνιο καταλυόµενη από οξέα H O O O + HO 4-τολουολοσουλφονικό οξύ + H 2 O NO 2 HO NO 2 C 7 H 5 NO 3 C 2 H 6 O 2 C 7 H 8
ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων)
 ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων) 1. Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές. i. H σχετική ατομική μάζα μετριέται σε γραμμάρια. ii. H σχετική ατομική μάζα είναι
ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων) 1. Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές. i. H σχετική ατομική μάζα μετριέται σε γραμμάρια. ii. H σχετική ατομική μάζα είναι
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Σέρρες 05/12/2015
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 14 η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2016 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συμμετέχουν: (1) (2) (3) Σέρρες 05/12/2015
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 14 η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2016 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συμμετέχουν: (1) (2) (3) Σέρρες 05/12/2015
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΧΗΜΕΙΑ. 5 - Δεκεμβρίου Ερρίκος Γιακουμάκης
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΧΗΜΕΙΑ 5 - Δεκεμβρίου - 2015 Ερρίκος Γιακουμάκης 1 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ...... Εισαγωγικό σημείωμα Θεωρία Brőnsted- Lowry
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΧΗΜΕΙΑ 5 - Δεκεμβρίου - 2015 Ερρίκος Γιακουμάκης 1 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ...... Εισαγωγικό σημείωμα Θεωρία Brőnsted- Lowry
5. Η ισχύς ενός λευκαντικού ρούχων
 5. Η ισχύς ενός λευκαντικού ρούχων Σκοπός Τα λευκαντικά είναι συνήθως υδατικά διαλύματα υποχλωριώδους νατρίου, NaOCl, και κυκλοφορούν με την εμπορική ονομασία «χλωρίνη». Σκοπός αυτού του πειράματος είναι
5. Η ισχύς ενός λευκαντικού ρούχων Σκοπός Τα λευκαντικά είναι συνήθως υδατικά διαλύματα υποχλωριώδους νατρίου, NaOCl, και κυκλοφορούν με την εμπορική ονομασία «χλωρίνη». Σκοπός αυτού του πειράματος είναι
4023 Σύνθεση του κυκλοπεντανο-2-καρβοξυλικού αιθυλεστέρα από αδιπικό διαιθυλεστέρα
 NP 4023 Σύνθεση του κυκλοπεντανο-2-καρβοξυλικού αιθυλεστέρα από αδιπικό διαιθυλεστέρα NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Ταξινόµηση Τύποι αντιδράσεων και τάξεις ουσιών
NP 4023 Σύνθεση του κυκλοπεντανο-2-καρβοξυλικού αιθυλεστέρα από αδιπικό διαιθυλεστέρα NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Ταξινόµηση Τύποι αντιδράσεων και τάξεις ουσιών
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:.
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 13 η Ευρωπαϊκή Ολυµπιάδα Επιστηµών EUSO 2015 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συµµετέχουν: (1) (2) (3) Σέρρες 13/12/2014
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 13 η Ευρωπαϊκή Ολυµπιάδα Επιστηµών EUSO 2015 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συµµετέχουν: (1) (2) (3) Σέρρες 13/12/2014
ΛΑΝΙΤΕΙΟ ΓΥΜΝΑΣΙΟ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2014 2015 ΓΡΑΠΤΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ XHMEIAΣ Γ ΓΥΜΝΑΣΙΟΥ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ:. ΑΡ:...
 ΛΑΝΙΤΕΙΟ ΓΥΜΝΑΣΙΟ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2014 2015 ΓΡΑΠΤΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ XHMEIAΣ Γ ΓΥΜΝΑΣΙΟΥ ΗΜΕΡΟΜΗΝΙΑ : 05 /06 /15 ΔΙΑΡΚΕΙΑ : Χημεία Βιολογία 2 ώρες ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ:. ΑΡ:...
ΛΑΝΙΤΕΙΟ ΓΥΜΝΑΣΙΟ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2014 2015 ΓΡΑΠΤΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ XHMEIAΣ Γ ΓΥΜΝΑΣΙΟΥ ΗΜΕΡΟΜΗΝΙΑ : 05 /06 /15 ΔΙΑΡΚΕΙΑ : Χημεία Βιολογία 2 ώρες ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ:. ΑΡ:...
ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΠΕΙΡΑΜΑΤΑ ΧΗΜΕΙΑΣ Β ΓΥΜΝΑΣΙΟΥ
 ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΠΕΙΡΑΜΑΤΑ ΧΗΜΕΙΑΣ Σύμφωνα με την εγκύκλιο του ΥΠΠΕΘ (με Αρ. Πρωτ. 150022/Δ2/15-9-2016) Β ΓΥΜΝΑΣΙΟΥ 1. 1.1 Γνωριμία με το εργαστήριο του Χημικού Από τον εργαστηριακό οδηγό να χρησιμοποιηθούν
ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΠΕΙΡΑΜΑΤΑ ΧΗΜΕΙΑΣ Σύμφωνα με την εγκύκλιο του ΥΠΠΕΘ (με Αρ. Πρωτ. 150022/Δ2/15-9-2016) Β ΓΥΜΝΑΣΙΟΥ 1. 1.1 Γνωριμία με το εργαστήριο του Χημικού Από τον εργαστηριακό οδηγό να χρησιμοποιηθούν
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ. Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και µπορεί να έχει χωρητικότητα από 10 έως 250 ml.
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ-ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και µπορεί να έχει χωρητικότητα από 10 έως 250
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ-ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και µπορεί να έχει χωρητικότητα από 10 έως 250
4006 Σύνθεση του 2-(3-οξοβουτυλο)κυκλοπεντανονο-2- καρβοξυλικού αιθυλεστέρα
 NP 4006 Σύνθεση του 2-(3-οξοβουτυλο)κυκλοπεντανονο-2- καρβοξυλικού αιθυλεστέρα CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Ταξινόµηση Τύποι αντιδράσεων και τάξεις
NP 4006 Σύνθεση του 2-(3-οξοβουτυλο)κυκλοπεντανονο-2- καρβοξυλικού αιθυλεστέρα CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Ταξινόµηση Τύποι αντιδράσεων και τάξεις
ΑΠΑΝΤΗΣΕΙΣ Α ΛΥΚΕΙΟΥ 32 ου ΠΜΔΧ 2018
 ΑΠΑΝΤΗΣΕΙΣ Α ΛΥΚΕΙΟΥ 32 ου ΠΜΔΧ 2018 ΠΟΛΛΑΠΛΕΣ ΕΠΙΛΟΓΕΣ 1 η ΑΣΚΗΣΗ 2 η ΑΣΚΗΣΗ 1. Β 1.1. Β 2.1. Β 2. Δ 1.2. Γ 2.2. Β 3. Γ 1.3. Α 2.3. Β 4. Α 1.4. Α 2.4. Α 5. Α 1.5. Α 6. Δ 1.6. Β 7. Α 1.7. Β 8. Δ 9. Α 10.
ΑΠΑΝΤΗΣΕΙΣ Α ΛΥΚΕΙΟΥ 32 ου ΠΜΔΧ 2018 ΠΟΛΛΑΠΛΕΣ ΕΠΙΛΟΓΕΣ 1 η ΑΣΚΗΣΗ 2 η ΑΣΚΗΣΗ 1. Β 1.1. Β 2.1. Β 2. Δ 1.2. Γ 2.2. Β 3. Γ 1.3. Α 2.3. Β 4. Α 1.4. Α 2.4. Α 5. Α 1.5. Α 6. Δ 1.6. Β 7. Α 1.7. Β 8. Δ 9. Α 10.
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 2 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Β ΛΥΚΕΙΟΥ ΣΧΟΛΕΙΟ Όξινος χαρακτήρας των καρβοξυλικών οξέων. 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Β ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2 3 4 5 Αυτή την εργαστηριακή
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 2 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Β ΛΥΚΕΙΟΥ ΣΧΟΛΕΙΟ Όξινος χαρακτήρας των καρβοξυλικών οξέων. 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Β ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2 3 4 5 Αυτή την εργαστηριακή
ΧΥΜΟΣ - Μέτρηση οξύτητας - Προσδιορισμός σακχάρων. 3 η Εργαστηριακή Άσκηση Εργαστήριο Χημείας & Τεχνολογίας Τροφίμων
 ΧΥΜΟΣ - Μέτρηση οξύτητας - Προσδιορισμός σακχάρων 3 η Εργαστηριακή Άσκηση Εργαστήριο Χημείας & Τεχνολογίας Τροφίμων Παρασκευή χυμού Στύψιμο νωπών φρούτων, όπως: Εσπεριδοειδή Μήλα Σταφύλια Βύσσινα Μίγματα
ΧΥΜΟΣ - Μέτρηση οξύτητας - Προσδιορισμός σακχάρων 3 η Εργαστηριακή Άσκηση Εργαστήριο Χημείας & Τεχνολογίας Τροφίμων Παρασκευή χυμού Στύψιμο νωπών φρούτων, όπως: Εσπεριδοειδή Μήλα Σταφύλια Βύσσινα Μίγματα
ΕΡΓΑΣΙΕΣ ΜΕ ΔΙΑΛΥΜΑΤΑ Γραμμομοριακή συγκέντρωση διαλυμάτων
 ΕΡΓΑΣΙΕΣ ΜΕ ΔΙΑΛΥΜΑΤΑ Γραμμομοριακή συγκέντρωση διαλυμάτων Συγκέντρωση διαλύματος: ποσότητα διαλυμένης ουσίας σε καθορισμένη ποσότητα διαλύματος Αραιό διάλυμα: μικρή συγκέντρωση διαλυμένης ουσίας Πυκνό
ΕΡΓΑΣΙΕΣ ΜΕ ΔΙΑΛΥΜΑΤΑ Γραμμομοριακή συγκέντρωση διαλυμάτων Συγκέντρωση διαλύματος: ποσότητα διαλυμένης ουσίας σε καθορισμένη ποσότητα διαλύματος Αραιό διάλυμα: μικρή συγκέντρωση διαλυμένης ουσίας Πυκνό
ph< 8,2 : άχρωμη ph> 10 : ροζ-κόκκινη
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2016 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΑΝΙΧΝΕΥΣΗ ΟΞΕΟΣ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ 2. ΟΓΚΟΜΕΤΡΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2016 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΑΝΙΧΝΕΥΣΗ ΟΞΕΟΣ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ 2. ΟΓΚΟΜΕΤΡΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ
Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου.
 Σύντομη περιγραφή του πειράματος Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού του πειράματος θα πρέπει ο μαθητής: Να περιγράφει τον τρόπο
Σύντομη περιγραφή του πειράματος Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού του πειράματος θα πρέπει ο μαθητής: Να περιγράφει τον τρόπο
Εισαγωγικό φροντιστήριο
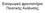 Εισαγωγικό φροντιστήριο Ποιοτικής Ανάλυσης Υπόδειγµα γραφής τετραδίου ΗΜΕΡΟΛΟΓΙΟ ΕΡΓΑΣΤΗΡΙΟΥ ΑΝΑΛΥΤΙΚΗΣ ΧΗΜΕΙΑΣ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Α.Θ.: Α.Μ. : Γενικές οδηγίες για τη γραφή του ηµερολογίου του Εργαστηρίου
Εισαγωγικό φροντιστήριο Ποιοτικής Ανάλυσης Υπόδειγµα γραφής τετραδίου ΗΜΕΡΟΛΟΓΙΟ ΕΡΓΑΣΤΗΡΙΟΥ ΑΝΑΛΥΤΙΚΗΣ ΧΗΜΕΙΑΣ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Α.Θ.: Α.Μ. : Γενικές οδηγίες για τη γραφή του ηµερολογίου του Εργαστηρίου
ΠΑΡΑΡΤΗΜΑΤΑ. της πρότασης ΟΔΗΓΙΑ ΤΟΥ ΕΥΡΩΠΑΪΚΟΥ ΚΟΙΝΟΒΟΥΛΙΟΥ ΚΑΙ ΤΟΥ ΣΥΜΒΟΥΛΙΟΥ
 ΕΥΡΩΠΑΪΚΗ ΕΠΙΤΡΟΠΗ Βρυξέλλες, 20.3.2014 COM(2014) 174 final ANNEXES 1 to 3 ΠΑΡΑΡΤΗΜΑΤΑ της πρότασης ΟΔΗΓΙΑ ΤΟΥ ΕΥΡΩΠΑΪΚΟΥ ΚΟΙΝΟΒΟΥΛΙΟΥ ΚΑΙ ΤΟΥ ΣΥΜΒΟΥΛΙΟΥ για την προσέγγιση των νομοθεσιών των κρατών μελών
ΕΥΡΩΠΑΪΚΗ ΕΠΙΤΡΟΠΗ Βρυξέλλες, 20.3.2014 COM(2014) 174 final ANNEXES 1 to 3 ΠΑΡΑΡΤΗΜΑΤΑ της πρότασης ΟΔΗΓΙΑ ΤΟΥ ΕΥΡΩΠΑΪΚΟΥ ΚΟΙΝΟΒΟΥΛΙΟΥ ΚΑΙ ΤΟΥ ΣΥΜΒΟΥΛΙΟΥ για την προσέγγιση των νομοθεσιών των κρατών μελών
ΠΑΡΑΡΤΗΜΑ ΤΡΙΤΟ ΤΗΣ ΕΠΙΣΗΜΗΣ ΕΦΗΜΕΡΙΔΑΣ ΤΗΣ ΔΗΜΟΚΡΑΤΙΑΣ Αρ της 21ης ΔΕΚΕΜΒΡΙΟΥ 2001 ΔΙΟΙΚΗΤΙΚεΣ ΠΡΑΞΕΙΣ
 / Κ.Α.Π. 476/2001 ΠΑΡΑΡΤΗΜΑ ΤΡΙΤΟ ΤΗΣ ΕΠΙΣΗΜΗΣ ΕΦΗΜΕΡΙΔΑΣ ΤΗΣ ΔΗΜΟΚΡΑΤΙΑΣ Αρ. 3561 της 21ης ΔΕΚΕΜΒΡΙΟΥ 2001 ΔΙΟΙΚΗΤΙΚεΣ ΠΡΑΞΕΙΣ ΜΕΡΟΣ Ι Κανονιστικές Διοικητικές Πράξεις Αριθμός 476 Οι περί Καζεϊνών και
/ Κ.Α.Π. 476/2001 ΠΑΡΑΡΤΗΜΑ ΤΡΙΤΟ ΤΗΣ ΕΠΙΣΗΜΗΣ ΕΦΗΜΕΡΙΔΑΣ ΤΗΣ ΔΗΜΟΚΡΑΤΙΑΣ Αρ. 3561 της 21ης ΔΕΚΕΜΒΡΙΟΥ 2001 ΔΙΟΙΚΗΤΙΚεΣ ΠΡΑΞΕΙΣ ΜΕΡΟΣ Ι Κανονιστικές Διοικητικές Πράξεις Αριθμός 476 Οι περί Καζεϊνών και
Ε.Ε. Παρ. III(I) 5569 Κ.Δ.Π. 509/2002 Αρ. 3647,
 Ε.Ε. Παρ. III(I) 5569 Κ.Δ.Π. 509/2002 Αρ. 3647, 25.10.2002 Αριθμός 509 Οι περί Ελέγχου της Ρύπανσης των Νερών (Απόρριψη Καδμίου) Κανονισμοί του 2002 οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει
Ε.Ε. Παρ. III(I) 5569 Κ.Δ.Π. 509/2002 Αρ. 3647, 25.10.2002 Αριθμός 509 Οι περί Ελέγχου της Ρύπανσης των Νερών (Απόρριψη Καδμίου) Κανονισμοί του 2002 οι οποίοι εκδόθηκαν από το Υπουργικό Συμβούλιο δυνάμει
ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΧΗΜΕΙΑΣ 2011 ΓΙΑ ΤΗ Β ΤΑΞΗ ΛΥΚΕΙΟΥ
 ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΧΗΜΕΙΑΣ 2011 ΓΙΑ ΤΗ Β ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 20 ΜΑΡΤΙΟΥ 2011 ΔΙΑΡΚΕΙΑ: ΤΡΕΙΣ (3) ΩΡΕΣ ΥΠΟ ΤΗΝ ΑΙΓΙΔΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ Να μελετήσετε
ΠΑΓΚΥΠΡΙΑ ΕΝΩΣΗ ΕΠΙΣΤΗΜΟΝΩΝ ΧΗΜΙΚΩΝ ΠΑΓΚΥΠΡΙΑ ΟΛΥΜΠΙΑΔΑ ΧΗΜΕΙΑΣ 2011 ΓΙΑ ΤΗ Β ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΥΡΙΑΚΗ 20 ΜΑΡΤΙΟΥ 2011 ΔΙΑΡΚΕΙΑ: ΤΡΕΙΣ (3) ΩΡΕΣ ΥΠΟ ΤΗΝ ΑΙΓΙΔΑ ΤΟΥ ΥΠΟΥΡΓΕΙΟΥ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ Να μελετήσετε
ΟΙ ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ
 ΟΙ ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Οξειδωτικά στοιχεία: Αυτά που προκαλούν οξείδωση, δηλαδή κερδίζουν ένα ή περισσότερα ηλεκτρόνια, ανάγονται, ο Α. Ο. του στοιχείου μειώνεται. Αναγωγικά στοιχεία: Προκαλούν
ΟΙ ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Οξειδωτικά στοιχεία: Αυτά που προκαλούν οξείδωση, δηλαδή κερδίζουν ένα ή περισσότερα ηλεκτρόνια, ανάγονται, ο Α. Ο. του στοιχείου μειώνεται. Αναγωγικά στοιχεία: Προκαλούν
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ ΧΗΜΕΙΑ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Η σωστή τετράδα κβαντικών αριθμών για το μονήρες
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Η σωστή τετράδα κβαντικών αριθμών για το μονήρες
Παρασκευή αιθανόλης-απόσταξη αλκοολούχου διαλύματος. Τεχνική της απόσταξης
 Παρασκευή αιθανόλης-απόσταξη αλκοολούχου διαλύματος Με τον όρο απόσταξη εννοείται η θέρμανση ενός υγρού μέχρι να εξατμισθεί, η συμπύκνωση των ατμών του με ψύξη και η συλλογή τους σε ένα άλλο δοχείο. Με
Παρασκευή αιθανόλης-απόσταξη αλκοολούχου διαλύματος Με τον όρο απόσταξη εννοείται η θέρμανση ενός υγρού μέχρι να εξατμισθεί, η συμπύκνωση των ατμών του με ψύξη και η συλλογή τους σε ένα άλλο δοχείο. Με
ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Ενότητα : Σύνθεση Διβενζαλακετόνης
 ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Ενότητα : Σύνθεση Διβενζαλακετόνης Διδάσκοντες: Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Μαρία Τσάμη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοπός
ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Ενότητα : Σύνθεση Διβενζαλακετόνης Διδάσκοντες: Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Μαρία Τσάμη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοπός
Πανελλήνιος Μαθητικός Διαγωνισμός για την επιλογή στην 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών - EUSO 2013 Σάββατο 19 Ιανουαρίου 2013 ΧΗΜΕΙΑ
 Πανελλήνιος Μαθητικός Διαγωνισμός για την επιλογή στην 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών - EUSO 2013 Σάββατο 19 Ιανουαρίου 2013 ΧΗΜΕΙΑ Σχολείο: 1) Ονομ/επώνυμα μαθητών: 2)... 3) ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΧΗΜΙΚΗΣ
Πανελλήνιος Μαθητικός Διαγωνισμός για την επιλογή στην 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών - EUSO 2013 Σάββατο 19 Ιανουαρίου 2013 ΧΗΜΕΙΑ Σχολείο: 1) Ονομ/επώνυμα μαθητών: 2)... 3) ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΧΗΜΙΚΗΣ
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα. Χημική Τεχνολογία. Εργαστηριακό Μέρος
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 8.2: Χημικώς Απαιτούμενο Οξυγόνο (Chemical Oxygen Demand, COD) Ευάγγελος Φουντουκίδης
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 8.2: Χημικώς Απαιτούμενο Οξυγόνο (Chemical Oxygen Demand, COD) Ευάγγελος Φουντουκίδης
Όξινη μορφή Ουδέτερη μορφή αλκαλική μορφή ή zwitterion
 11 Απομόνωση της καζεΐνης από το γάλα και ιδιότητές της Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με τις ηλεκτρικές ιδιότητες των πρωτεϊνών και την επίδραση οξέων και
11 Απομόνωση της καζεΐνης από το γάλα και ιδιότητές της Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με τις ηλεκτρικές ιδιότητες των πρωτεϊνών και την επίδραση οξέων και
