ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
|
|
|
- Εκάτη Ελευθερίου
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΕΛΛΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΜΙΟ Παπαφλέσσα και Υψηλάντη, ΠΑΤΡΑ Ονοματεπώνυμο: Α.Μ. Διεύθυνση: Τηλέφωνο / μερομηνία αποστολής: Βαθμολογία θεμάτων Γενικός Βαθμός 3 η ΓΡΑΠΤ ΕΡΓΑΣΙΑ ΣΤ "ΓΕΝΙΚ ΚΑΙ ΑΝΟΡΓΑΝ ΧΜΕΙΑ ΦΥΕ 12" ΑΚΑΔΜΑΪΚΟ ΕΤΟΣ ΔΕΚΑ ΟΔΓΙΕΣ ΓΙΑ ΤΝ ΕΚΠΟΝΣ, ΑΞΙΟΛΟΓΣ ΚΑΙ ΔΙΑΚΙΝΣ ΤΣ 3ης ΓΡΑΠΤΣ ΕΡΓΑΣΙΑΣ 1. Για να εκτελέσετε σωστά την εργασία αυτή, θα πρέπει να έχετε εμπεδώσει την ύλη των Κεφαλαίων 5 και 6. Όλα τα θέματα είναι παρεμφερή των παραδειγμάτων, των ασκήσεων αυτοαξιολόγησης και των επαναληπτικών ασκήσεων των αντίστοιχων ενοτήτων! 2. Για τις απαντήσεις χρησιμοποιήστε τις κόλλες με τα θέματα, όπως σας έχουν σταλεί. Ο κενός χώρος κάτω και πίσω από κάθε θέμα είναι αρκετός για την απάντηση. Μην προσθέσετε σε καμιά περίπτωση δικές σας κόλλες. 3. Γράφετε ευανάγνωστα, καθαρά και κατά το δυνατόν ορθογραφημένα, διατυπώνοντας τις σκέψεις με τρόπο απλό, κατανοητό και συγχρόνως μεστό. 4. Μη γράφετε περισσότερα από αυτά που ζητούνται στο θέμα, αφού τα επιπλέον, αν μεν είναι σωστά δεν λαμβάνονται υπ' όψιν, αν όμως είναι λάθος, επηρεάζουν αρνητικά τη βαθμολογία του θέματος. 5. Όποια δεδομένα χρειάζεστε για τη λύση των ασκήσεων (φυσικές σταθερές, συντελεστές μετατροπής, Περιοδικό Πίνακα κ.λπ.), μπορείτε να τα πάρετε από το βιβλίο σας. 6. Στα αριθμητικά προβλήματα, δώστε προσοχή στα σημαντικά ψηφία, στον εκθετικό συμβολισμό, στο στρογγύλεμα των αριθμητικών αποτελεσμάτων και στη συνέπεια ως προς τις διαστάσεις των μεγεθών (βλ. Παράλληλα Κείμενα στο ξεχωριστό βιβλίο των λύσεων). Εξετάζετε πάντοτε, αν οι διάφορες μονάδες απαιτούν μετατροπή στο σύστημα SI. Ελέγχετε πάντοτε στο τέλος, το πόσο λογικό είναι το αποτέλεσμα στο οποίο καταλήξατε. 7. Σε ερωτήσεις (κυρίως του τύπου Σωστό Λάθος), στις οποίες ζητείται εξήγηση, θα πρέπει αυτή να δίνεται. απλή παραπομπή σε πίνακες ή σχήματα του βιβλίου δεν θεωρείται αιτιολογημένη απάντηση και δεν λαμβάνεται υπ' όψιν. 8. Φωτοτυπήστε την τελειωμένη εργασία σας δύο φορές, κρατήστε ένα αντίγραφο και στείλτε το πρωτότυπο + ένα φωτοαντίγραφο στη διεύθυνση που σας έχει γνωστοποιήσει ο Καθηγητής σας, στην καθορισμένη ημερομηνία (Δευτέρα, 07 / 02 / 2005). Παράταση δίνεται από τον Συντονιστή και μόνο για πολύ σοβαρούς λόγους, οι οποίοι αποδεικνύονται με σχετικά έγγραφα. διορθωμένη εργασία θα σας επιστραφεί γύρω στις 21 / 02 / Όσοι έχετε αντιρρήσεις για τη βαθμολογία σας και απορίες σχετικά με τις απαντήσεις των θεμάτων, θα τις συζητήσουμε τηλεφωνικά, με φαξ, με ή στην επόμενη συνάντησή μας. 10. Προσοχή! Γνωστοποιείτε κάθε φορά στον Καθηγητή σας (τηλεφωνικά, με φαξ ή με ) την παραλαβή εκ μέρους σας τόσο της προς εκτέλεση εργασίας όσο και της διορθωμένης εργασίας. Καλή επιτυχία!
2 1. Προσδιορίστε την τάξη δεσμού και τον αριθμό των ασύζευκτων ηλεκτρονίων για κάθε ένα από τα παρακάτω χημικά είδη: (α) NO + (β) B 2 (γ) CO 2 (δ) Ο 2 (ε) BC. ΑΠΑΝΤΣ άσκηση αυτή είναι εφαρμογή της θεωρίας των Μοριακών Τροχιακών (Molecular Orbitals, ΜΟ) [Ε (2/ )]. Το πρώτο βήμα για την επίλυση της άσκησης είναι ο υπολογισμός του αριθμού των ηλεκτρονίων σθένους που εμφανίζει κάθε χημική οντότητα. Στη συνέχεια, θα πρέπει να κατανεμηθούν τα συνολικά ηλεκτρόνια στο αντίστοιχο διάγραμμα ΜΟ [Σχ 5.18 (2/138) και Σχ 5.19 (2/139)]. τάξη nb n δεσμού (Τ.Δ.) υπολογίζεται από τη σχέση Τ. Δ. = a, όπου n b και n a είναι ο αριθμός των 2 ηλεκτρονίων στα δεσμικά και τα αντιδεσμικά μοριακά τροχιακά, αντιστοίχως (2/132). Τέλος, κάθε ηλεκτρόνιο που είναι μόνο του σε τροχιακό είναι ασύζευκτο ηλεκτρόνιο. ΝΟ BB2 + CO 2 Ο 2 BC 11 e (5 +6) 5 e ( ) 10 e (4 + 6) 14 e ( ) 7 e (3 +4) σ* 2p σ* 2p σ* 2p σ* 2p σ* 2p π* 2p π* 2p π* 2p π* 2p π* 2p σ 2p σ 2p σ 2p π 2p σ 2p π 2p π 2p π 2p π 2p σ 2p σ* 2s σ* 2s σ* 2s σ* 2s σ* 2s σ 2s σ 2s σ 2s σ 2s σ 2s Με βάση τα παραπάνω διαγράμματα ΜΟ των χημικών ειδών προκύπτουν τα ακόλουθα: Χημικό είδος NO + B 2 CO 2 Ο 2 BC Τάξη Δεσμού 2,5 0, ,5 Αριθμός ασύζευκτων ηλεκτρονίων
3 2. (α) Αντιστοιχίστε τα δεδομένα της πρώτης στήλης με αυτά της δεύτερης στήλης. Είναι δυνατές και πολλαπλές αντιστοιχίσεις. Δώστε μια σύντομη εξήγηση. CO sp Τριγωνική πυραμιδική sp 2 BF 3 sp 3 Γραμμικό μόριο Πολικό μόριο ΑΒ 5 sp 3 d Εξαφθορίδιο του θείου sp 3 d 2 (β) Ποια είναι η διαφορά μεταξύ των όρων πολωμένος δεσμός και πολικό μόριο ; Πολωμένος δεσμός Ν 2 ΑΠΑΝΤΣ (α) CO Τριγωνική πυραμιδική BF 3 Γραμμικό μόριο ΑΒ 5 Εξαφθορίδιο του θείου (SF 6 ) Είναι γραμμικό μόριο με τάξη δεσμού 3 (τριπλός δεσμός), όπως και το μόριο Ν 2. O υβριδισμός του C είναι sp ανάλογος με τον υβριδισμό του ατόμου C στο μόριο του ακετυλενίου, HC CH, όπου τα άτομα άνθρακα είναι ενωμένα με τριπλό δεσμό (2/127). Επίσης το μόριο εμφανίζει διπολική ροπή γιατί ο δεσμός C O είναι πολωμένος. Αυτή τη γεωμετρία παρουσιάζουν όλα τα μόρια των οποίων το κεντρικό άτομο εμφανίζει sp 3 υβριδισμό και διαθέτει ένα μονήρες ζεύγος ηλεκτρονίων στο φλοιό σθένους του. παρουσία του μονήρους ζεύγους ηλεκτρονίων κάνει το μόριο πολικό, ανεξάρτητα αν οι δεσμοί του είναι πολωμένοι ή όχι. Οι ενώσεις που παρουσιάζουν αυτή τη γεωμετρία έχουν γενικό τύπο ΑΒ 3 Ε και συνήθως τα άτομα Α και Β διαφέρουν σε ηλεκτραρνητικότητα με αποτέλεσμα οι δεσμοί Α Β να είναι πολωμένοι. Το μόριο αυτό έχει sp 2 υβριδισμό και παρουσιάζει δεσμούς οι οποίοι είναι πολωμένοι, αφού το Β διαφέρει σημαντικά σε ηλεκτραρνητικότητα από το F. Λόγω συμμετρίας, όμως, το μόριο δεν είναι πολικό. Είναι κάθε μόριο που το κεντρικό του άτομο έχει sp υβριδισμό και φυσικά όλα τα διατομικά μόρια όπως το Ν 2. Επίσης, γραμμικό μόριο είναι κάθε μόριο με υβριδισμό sp 3 d αρκεί να έχει δύο δεσμικά και τρία μονήρη ζεύγη ηλεκτρονίων γύρω από το κεντρικό άτομο (π.χ. XeF 2 ). Τα μόρια αυτού του τύπου έχουν υβριδισμό sp 3 d με την προϋπόθεση να μην υπάρχουν μονήρη ζεύγη ηλεκτρονίων γύρω από το κεντρικό τους άτομο. Επίσης, μόρια αυτού του τύπου εμφανίζουν, τις περισσότερες φορές, πολωμένους δεσμούς λόγω της διαφοράς ηλεκτραρνητικότητας μεταξύ των ατόμων Α και Β. ένωση αυτή είναι του γενικού τύπου ΑΒ 6, άρα ο υβριδισμός του S θα είναι sp 3 d 2. Επίσης, επειδή S και F εμφανίζουν διαφορά στην τιμή ηλεκτραρνητικότητας τους, οι δεσμοί είναι πολωμένοι, το μόριο όμως εμφανίζει συνολική διπολική ροπή ίση με μηδέν. Ν 2 sp Πολωμένος δεσμός Πολικό μόριο sp 3 Πολικό μόριο Πολωμένος δεσμός sp 2 Πολωμένος δεσμός sp Ν 2 sp 3 d sp 3 d Πολωμένος δεσμός sp 3 d 2 Πολωμένος δεσμός (β) Πολωμένος δεσμός είναι εκείνος που σχηματίζεται μεταξύ δύο ατόμων που εμφανίζουν διαφορετική τιμή ηλεκτραρνητικότητας. Ο όρος «πολικό μόριο» περιγράφει ένα μόριο, στο οποίο τα κέντρα θετικού και αρνητικού φορτίου δεν συμπίπτουν (2/157). Με άλλα λόγια, πολικό μόριο είναι ένα μόριο στο οποίο το άθροισμα των διπολικών ροπών των επιμέρους δεσμών είναι διάφορο του μηδενός.
4 3. Συμπληρώστε τον πίνακα που ακολουθεί. Στη στήλη Πολικότητα συμπληρώστε ναι, αν η ένωση είναι πολική και όχι, αν δεν είναι πολική. Ένωση Δομή Lewis Γενικός τύπος (ΑΒ n E m ) Γεωμετρία λεκτρονικών ζευγών Μοριακή Γεωμετρία Υβριδισμός κεντρικού ατόμου Πολικότητα (α) SF 2 (β) XeO 4 (γ) BeCl 2 (δ) HCN (ε) AsH 3 (στ) CH 3 Cl (ζ) BrF 3 (η) ΧeF 2 (θ) SeF 4 (ι) TeF 6
5 Ένωση Δομή Lewis Γενικός τύπος (ΑΒ n E m ) Γεωμετρία λεκτρονικών ζευγών Μοριακή Γεωμετρία Υβριδισμός κεντρικού ατόμου Πολικότητα (α) SF 2 F S F ΑΒ 2 E 2 τετραεδρική κεκαμμένη sp 3 ναι (β) XeO 4 Xe Ȯ. Ȯ. O ΑΒ 4 τετραεδρική τετραεδρική sp 3 όχι O (γ) BeCl 2 Cl Be Cl ΑΒ 2 γραμμική γραμμική sp όχι (δ) HCN H C N γραμμική γραμμική sp ναι ΑΒ2 H As H (ε) AsH 3 H H ΑΒ 3 E τετραεδρική τριγωνική πυραμίδα sp 3 ναι (στ) CH 3 Cl H C H ΑΒ 4 τετραεδρική τετραεδρική sp 3 ναι Cl Br (ζ) BrF 3 F F F ΑΒ 3 E 2 τριγωνική διπυραμιδική σχήματος Τ sp 3 d ναι (η) ΧeF 2 F Xe F ΑΒ 2 E 3 τριγωνική διπυραμιδική γραμμική sp 3 d όχι (θ) SeF 4 F F Se Ḟ. ΑΒ 4 E τριγωνική διπυραμιδική παραμορφωμένη τετραεδρική sp 3 d ναι F (ι) TeF 6 Te F F F F F F ΑΒ 6 οκταεδρική οκταεδρική sp 3 d 2 όχι Για να συμπληρώσουμε τον πίνακα, θα πρέπει να ακολουθήσουμε το Πρδ 5.1 και την ΑΑ 5.2 (2/ ). Για κάθε μία από τις παραπάνω ενώσεις σχεδιάζουμε τη δομή Lewis, βρίσκουμε το γενικό τύπο, τον προσανατολισμό των ηλεκτρονικών ζευγών [Πίν 4.4 (2/79)], τη μοριακή γεωμετρία [Πίν 4.5 και 4.6, (2/85 και 2/88)] και, τέλος, τον υβριδισμό του κεντρικού ατόμου [Πίν. 5.1, (2/120)].
6 πολικότητα της ένωσης εκτιμάται με βάση τον κανόνα, ότι ενώσεις του γενικού τύπου ΑΒ n (n = 2 6) είναι μη πολικές, ενώ αυτές με γενικό τύπο ΑΒ n E m είναι πολικές, με εξαίρεση τις περιπτώσεις όπου n = 2, m = 3, και n = 4, m = 2 [Πρδ 6.2, (2/161)]. Τα προηγούμενα βέβαια ισχύουν μόνο για τις περιπτώσεις που το κεντρικό άτομο έχει όμοια περιφερειακά άτομα. Αν τα περιφερειακά άτομα του κεντρικού ατόμου είναι διαφορετικά, τότε η ένωση είναι πολική ακόμα και αν ανήκει σε γενικό τύπο μη πολικών ενώσεων (π.χ. το μόριο HCN).
7 4. Υπολογίστε την πυκνότητα του αερίου HF στους 300 Κ και σε πίεση 1,00 atm. πραγματική τιμή που προσδιορίζεται για την πυκνότητα του HF σε αυτές τις συνθήκες είναι 3,17 g L -1. Συγκρίνετέ την με την τιμή που υπολογίσατε. Γιατί διαφέρουν οι τιμές αυτές; Υπόδειξη: Για να υπολογίστε την πυκνότητα του αερίου HF θα πρέπει να χρησιμοποιήσετε την καταστατική εξίσωση των ιδανικών αερίων P V = n R T, όπου R η παγκόσμια σταθερά των αερίων με τιμή 0,0820 atm L K 1 mol 1. ΑΠΑΝΤΣ Γνωρίζουμε ότι η πυκνότητα ορίζεται ως το πηλίκο της μάζας μιας ουσίας, m, προς τον όγκο, V, που αυτή καταλαμβάνει. Χρησιμοποιώντας την καταστατική εξίσωση των αερίων, μπορούμε να υπολογίσουμε την πυκνότητα του HF. m m P MB P MB P V = n R T PV = RT = d = (1) MB V R T R T H γραμμομοριακή μάζα του HF είναι: (1, ,9984) g mol -1 = 20,0063 g mol -1 Αντικαθιστώντας τις τιμές των μεγεθών στη σχέση (1) προκύπτει: d = 1,00 atm 20,0063 g mol 0,0820 atm L mol -1 K K d = 0,813 g L -1 Όπως μπορούμε να παρατηρήσουμε, η πυκνότητα που υπολογίζεται διαφέρει σημαντικά από την 3,17 πειραματικά προσδιοριζόμενη. Μάλιστα, η πραγματική πυκνότητα είναι = 3,90, δηλαδή περίπου 4 0,813 φορές μεγαλύτερη από την τιμή που υπολογίζουμε. Αν λοιπόν χρησιμοποιήσουμε την προηγούμενη εξίσωση [εξίσωση (1)] για να προσδιορίσουμε τη γραμμομοριακή μάζα του HF θα βρούμε ότι το HF, εμφανίζεται να έχει γραμμομοριακή μάζα ίση με 78,2 g mol 1, περίπου 4 φορές μεγαλύτερη από την πραγματική. Αυτό σημαίνει ότι 4 μόρια HF εμφανίζονται να καταλαμβάνουν το χώρο ενός μοριακού συγκροτήματος. Άρα, ακόμα και στην αέρια φάση τα μόρια του HF αλληλεπιδρούν μεταξύ τους. αλληλεπίδραση γίνεται μέσω δεσμών και οφείλεται στην ισχυρή ηλεκτραρνητικότητα που εμφανίζει το άτομο του φθορίου (F).
8 5. Θεωρήστε το οργανικό μόριο. C A H 3 -C B - C Γ -O Α H Ν A O Β (α) Ποιος είναι ο γεωμετρικός προσανατολισμός των ηλεκτρονικών ζευγών κάθε επισημασμένου ατόμου; C A C B C Γ Ο A.Ο Β.Ν A. (β) Βρείτε τον υβριδισμό κάθε επισημασμένου ατόμου. C A C B C Γ Ο A. Ο Β. Ν A. (γ) Ποιες είναι οι προβλεπόμενες τιμές των γωνιών των δεσμών γύρω από τα επισημασμένα άτομα; C A C B C Γ Ο A. Ν A. (δ) Ποιες από τις προβλεπόμενες τιμές των γωνιών των δεσμών διαφέρουν από τις πραγματικές και γιατί; Υπόδειξη: Για να λύσετε την άσκηση θα πρέπει αρχικά να γράψετε τη δομή Lewis της ένωσης. ΑΠΑΝΤΣ δομή Lewis για την ένωση είναι: C Α C Β C Γ Ο Α Ν Α Ο Β Αντιμετωπίζοντας κάθε επισημασμένο άτομο ως κεντρικό άτομο, γράφουμε το συμβολισμό του κατά VSEPR. Στη συνέχεια, με τη χρήση των πινάκων 4.4 (2/79) και 5.1 (2/120) μπορούμε να προσδιορίσουμε το γεωμετρικό προσανατολισμό των ηλεκτρονικών ζευγών, τον υβριδισμό και τις προβλεπόμενες τιμές των γωνιών για κάθε επισημασμένο άτομο. Ο συμβολισμός κατά VSEPR κάθε επισημασμένου ατόμου είναι: C A : ΑΒ 4 C B : ΑΒ 3 C Γ : ΑΒ 3 Ο A : ΑΒ 2 Ε 2 Ο Β : ΑΒΕ 2 Ν A : ΑΒ 2 Ε (α) C A : τετραεδρικός C B : επίπεδος τριγωνικός C Γ : επίπεδος τριγωνικός Ο A : τετραεδρικός Ο Β : επίπεδος τριγωνικός Ν A : επίπεδος τριγωνικός (β) C A : sp 3 C B : sp 2 C Γ : sp 2 Ο A : sp 3 Ο Β : sp 2 Ν A : sp 2 (γ) C A : 109,5 o C B :120 o C Γ :120 o Ο A : 109,5 o Ν A :120 o
9 (δ) Οι πραγματικές γωνίες διαφοροποιούνται από τις ιδανικές στις περιπτώσεις που έχουμε μονήρη ζεύγη ηλεκτρονίων γύρω από το κεντρικό άτομο. Αυτό συμβαίνει γιατί το μονήρες ζεύγος ηλεκτρονίων δέχεται την επίδραση μόνο ενός πυρήνα με αποτέλεσμα να είναι πιο διάχυτο στο χώρο. Συμπιέζει με αυτόν τον τρόπο τις γωνίες μεταξύ των δεσμικών ζευγών (2/84). Επίσης, οι γωνίες δεσμού επηρεάζονται, σε μικρότερο βαθμό, από τη παρουσία πολλαπλών δεσμών (2/84), καθώς και υποκαταστατών διαφορετικής ηλεκτραρνητικότητας. Για τον υβριδισμό sp 3 οι πραγματικές και οι θεωρητικές τιμές των γωνιών δεσμών συμπίπτουν απόλυτα σε περιπτώσεις μορίων όπως π.χ. CH 4, CCl 4, SiH 4 κλπ, ενώ για τον υβριδισμό sp 2, σε περιπτώσεις μορίων όπως το BF 3. Έτσι, σε όλες τις παραπάνω περιπτώσεις οι πραγματικές τιμές των γωνιών δεσμού διαφέρουν από τις προβλεπόμενες (ιδανικές) βάσει του τύπου υβριδισμού τιμές.
10 6. Στο οργανικό μόριο της προηγούμενης άσκησης βρείτε: (α) Πόσοι σ και πόσοι π δεσμοί υπάρχουν στο μόριο. (β) Περιγράψτε όλους τους δεσμούς του μορίου με τη μέθοδο VB. (Για κάθε δεσμό που υπάρχει στο μόριο, γράψτε ποια τροχιακά επικαλύπτονται για το σχηματισμό του δεσμού. Π.χ. το μεθάνιο, CH 4, έχει 4 σ δεσμούς C H που προκύπτουν με επικάλυψη των sp 3 τροχιακών του C με τα 1s τροχιακά των τεσσάρων. Οι δεσμοί λοιπόν περιγράφονται ως C(sp 3 ) H(1s)). ΑΠΑΝΤΣ C Α C Β C Γ Ο Α Ν Α Ο Β (α) Όπως μπορούμε να δούμε από τη δομή Lewis της ένωσης, στο μόριο υπάρχουν 8 απλοί δεσμοί και 2 διπλοί δεσμοί. Γνωρίζουμε (2/ ) ότι οι απλοί δεσμοί είναι σ δεσμοί, ενώ οι διπλοί δεσμοί αποτελούνται από ένα σ δεσμό και ένα π δεσμό. Άρα, συνολικά υπάρχουν 10 σ δεσμοί και 2 π δεσμοί. (β) Οι σ δεσμοί προκύπτουν όταν η επικάλυψη των τροχιακών γίνεται κατά μήκος του άξονά τους (2/110). Ένας π δεσμός μεταξύ ατόμων της 2 ης Περιόδου προκύπτει όταν δύο p τροχιακά επικαλύπτονται πλευρικά (2/124). Το υδρογόνο χρησιμοποιεί στους δεσμούς του το τροχιακό 1s, ενώ τα υπόλοιπα άτομα (C,N,O) τα υβριδικά τροχιακά που έχουμε προσδιορίσει στη προηγούμενη άσκηση (sp 3 ή sp 2 ). Τέλος, όσα άτομα έχουν υβριδισμό sp 2, έχουν και ένα μη υβριδοποιημένο 2p τροχιακό (2/ ). Τα μη υβριδοποιημένα 2p τροχιακά επικαλύπτονται μεταξύ τους πλευρικά και δημιουργούν τους π δεσμούς. Έτσι, σύμφωνα με τα παραπάνω, η περιγραφή των δεσμών του μορίου παρουσιάζεται στον πίνακα που ακολουθεί. σ δεσμοί π δεσμοί 3 C A H sp 3 1s C A C B sp 3 sp 2 C B C Γ sp 2 sp 2 C B Ν Α sp 2 sp 2 C B Ν Α 2p 2p C Γ Ο Α sp 2 sp 3 C Γ Ο Β sp 2 sp 2 C Γ Ο Β 2p 2p Ν A H sp 2 1s Ο A H sp 3 1s
11 7. Ποια από τα μόρια ΑΧ 2, ΑΧ 3, ΑΧ 4, ΑΧ 5, ΑΧ 6 είναι πιθανό να έχουν κεντρικό άτομο με υβριδισμό sp 3 d; Δώστε ένα παράδειγμα σε κάθε περίπτωση. ΑΠΑΝΤΣ Ένα κεντρικό άτομο για να έχει υβριδισμό sp 3 d θα πρέπει να έχει γεωμετρία ηλεκτρονικών ζευγών τριγωνική διπυραμιδική [Πίν 5.1 (2/120)]. συγκεκριμένη γεωμετρία απαιτεί την ύπαρξη πέντε ζευγών ηλεκτρονίων γύρω από το κεντρικό άτομο. Τα πέντε αυτά ζεύγη μπορεί να είναι δεσμικά ή μονήρη [Πίν 4.4 (2/79) και Πίν 4.6 (2/88)]. Είναι λοιπόν φανερό, ότι όποιο μόριο έχει την μορφή ΑBBnE m όπου n + m = 5, ικανοποιεί την παραπάνω απαίτηση. Το μόνο μόριο, λοιπόν, που σίγουρα δεν μπορεί να έχει γεωμετρία ηλεκτρονικών ζευγών τριγωνική διπυραμιδική είναι το μόριο ΑΧ 6, αφού έχει περισσότερα από 5 ηλεκτρονικά ζεύγη γύρω από το κεντρικό άτομο. Το μόριο ΑΧ 5 δεν θα πρέπει να έχει μονήρη ζεύγη ηλεκτρονίων (π.χ. PCl 5 ), ενώ τα μόρια ΑΧ 2, ΑΧ 3 και ΑΧ 4 θα πρέπει να έχουν 3, 2 και 1 μονήρη ζεύγη ηλεκτρονίων, αντίστοιχα. Για να έχουν λοιπόν τα μόρια ΑΧ 2, ΑΧ 3, ΑΧ 4 και ΑΧ 5 κεντρικό άτομο με γεωμετρία ηλεκτρονικών ζευγών τριγωνική διπυραμιδική, θα πρέπει να είναι της μορφής ΑΒ 2 Ε 3, ΑΒ 3 Ε 2, ΑΒ 4 Ε και ΑΒ 5 Ε 0, αντίστοιχα. Έτσι, π.χ. το μόριο XeF 2 είναι της μορφής ΑΒ 2 Ε 3 (Άσκηση 3η), το μόριο BrF 3 είναι της μορφής ΑΒ 3 Ε 2 (Άσκηση 3ζ), ενώ το μόριο SeF 4 είναι της μορφής ΑΒ 4 Ε (Άσκηση 3θ).
12 8. (Ι) χημική οντότητα e μπορεί να υπάρξει; (ΙΙ) Έχουμε 2 άτομα και 2 άτομα He. Ποια από τις ακόλουθες καταστάσεις είναι ενεργειακά σταθερότερη; (α) He (β) 2 + He 2 (γ) He (δ) 2 + He 2 ΑΠΑΝΤΣ (Ι) Για να μπορεί να υπάρξει η χημική οντότητα e θα πρέπει η τάξη δεσμού της να είναι μεγαλύτερη nb n από το μηδέν. τάξη δεσμού (Τ.Δ.) υπολογίζεται από τη σχέση Τ. Δ. = a, όπου n b και n a είναι ο 2 αριθμός των ηλεκτρονίων στα δεσμικά και τα αντιδεσμικά μοριακά τροχιακά, αντιστοίχως (2/132). Από το διάγραμμα ΜΟ της ένωσης βρίσκουμε ότι η τάξη δεσμού για το μόριο e είναι ίση με 0,5 και άρα, το μόριο αυτό μπορεί να υπάρξει. σ* 1s Άτομο H σ 1s Άτομο He Μόριο He (ΙΙ) απάντηση σε αυτό το ερώτημα προκύπτει από τη σύγκριση των ενεργειακών καταστάσεων που ζητούνται. περίπτωση (α) είναι η αρχική μας κατάσταση. Στην περίπτωση (β) τα δύο άτομα He έχουν σχηματίσει το διατομικό μόριο He 2. Το μόριο όμως αυτό είναι ασταθές (εμφανίζει τάξη δεσμού μηδέν, όπως φαίνεται στο παρακάτω διάγραμμα ΜΟ του He 2 ) και γι αυτό θα προτιμήσει να διασπασθεί στα δύο άτομα He και να γυρίσει στην αρχική κατάσταση [κατάσταση (α)]. περίπτωση (γ) είναι πιο σταθερή από την (α), αφού το μόριο που σχηματίζεται ( 2 ) έχει τάξη δεσμού 1. Αντίθετα, η κατάσταση (δ) μας οδηγεί στη (γ) αφού, όπως δείξαμε στην περίπτωση (β), το μόριο He 2 είναι ασταθές και διασπάται. He 2 H 2 σ* 1s σ* 1s Άτομο He σ 1s Άτομο He Άτομο H σ 1s Άτομο H Μόριο He 2 Μόριο H 2 nb n Τ. Δ. = a = 0 2 nb n Τ. Δ. = a = 1 2 Όπως γίνεται εύκολα αντιληπτό, η πιο σταθερή κατάσταση είναι η κατάσταση (γ).
13 9. (Ι) Συμπληρώστε (χωρίς αιτιολόγηση) τα κενά επιλέγοντας τις κατάλληλες λέξεις από αυτές που δίνονται στον πίνακα. (α) Όταν στο πλέγμα καθαρού γερμανίου εμφυτευτούν άτομα, η αγωγιμότητα του γερμανίου αυξάνεται και ο ημιαγωγός που προκύπτει χαρακτηρίζεται ως (β) Όταν αλληλεπιδρούν υβριδικά τροχιακά για σχηματισμό δεσμού, ο δεσμός που προκύπτει είναι (γ) Όταν συνδυάζονται πλήρη τροχιακά, τότε τα μοριακά τροχιακά που προκύπτουν είναι (δ) Το HCl είναι ένωση πολικότερη από το Ι και γι αυτό οι στο HCl είναι ισχυρότερες. Ταυτόχρονα όμως, το μόριο του HCl είναι πολύ μικρότερο από το μόριο του Ι, με αποτέλεσμα οι στο HCl να είναι πολύ ασθενέστερες. (ε) Όταν το π ηλεκτρονικό νέφος δεν είναι συγκεντρωμένο ανάμεσα σε μεμονωμένα ζεύγη ατόμων, αλλά απλώνεται ομοιόμορφα καλύπτοντας όλα τα άτομα του μορίου, τότε τα π μοριακά τροχιακά καλούνται μοριακά τροχιακά. αντιδεσμικά, απεντοπισμένα, ασβεστίου, ασθενείς, ατομικά, διατομικές αλληλεπιδράσεις, δεσμικά, δυνάμεις London, δυνάμεις διπόλου διπόλου, δυνάμεις διπόλου ιόντος, ενδομοριακές δυνάμεις, εντοπισμένα, θαλλίου, μη δεσμικά, μοριακά, π δεσμός, πυριτίου, σ δεσμός, τύπου n, τύπου p, φωσφόρου (ΙΙ) Συμπληρώστε τα κενά, επιλέγοντας την κατάλληλη λέξη και δικαιολογώντας την επιλογή σας. (α) Τα μόρια CO 2 και SO 2 έχουν γεωμετρία. (όμοια διαφορετική). (β) Το μόριο He 2 δεν μπορεί να υπάρξει στη θεμελιώδη κατάσταση.. να υπάρξει στην πρώτη διεγερμένη κατάσταση. (Μπορεί Δεν μπορεί). (γ) Κάθε μοριακό τροχιακό μπορεί να δεχθεί το πολύ μέχρι ηλεκτρόνια. (δύο τρία). (δ) Για κάποιο συγκεκριμένο δίπολο, οι δυνάμεις κατιόντος διπόλου είναι γενικά σε σύγκριση με τις δυνάμεις ανιόντος διπόλου, όταν το κατιόν και το ανιόν έχουν ίδιο φορτίο, κατά απόλυτη τιμή, και ανήκουν στην ίδια περίοδο του Περιοδικού Πίνακα. (ισχυρότερες ασθενέστερες). (ε) Στην ένωση το σημείο ζέσεως καθορίζεται από την ισχύ των δυνάμεων London. (CH 4 CH 3 OH). ΑΠΑΝΤΣ (Ι) (α) Όταν στο πλέγμα καθαρού γερμανίου εμφυτευτούν άτομα θαλλίου (φωσφόρου), η αγωγιμότητα του γερμανίου αυξάνεται και ο ημιαγωγός που προκύπτει χαρακτηρίζεται ως τύπου p(τύπου n). (β) Όταν αλληλεπιδρούν υβριδικά τροχιακά για σχηματισμό δεσμού, ο δεσμός που προκύπτει είναι σ δεσμός. (γ) Όταν συνδυάζονται πλήρη ατομικά τροχιακά, τότε τα μοριακά τροχιακά που προκύπτουν είναι μη δεσμικά. (δ) Το HCl είναι ένωση πολικότερη από το Ι και γι αυτό οι δυνάμεις διπόλου διπόλου στο HCl είναι ισχυρότερες. Ταυτόχρονα όμως, το μόριο του HCl είναι πολύ μικρότερο από το μόριο του Ι, με αποτέλεσμα οι δυνάμεις London στο HCl να είναι πολύ ασθενέστερες. (ε) Όταν το π ηλεκτρονικό νέφος δεν είναι συγκεντρωμένο ανάμεσα σε μεμονωμένα ζεύγη ατόμων, αλλά απλώνεται ομοιόμορφα καλύπτοντας όλα τα άτομα του μορίου, τότε τα π μοριακά τροχιακά καλούνται απεντοπισμένα μοριακά τροχιακά. (ΙΙ) (α) Τα μόρια CO 2 και SO 2 έχουν διαφορετική γεωμετρία. Αν γράψουμε τις δομές Lewis για τα δύο αυτά μόρια, θα δούμε ότι το CO 2 έχει γενικό τύπο ΑΒ 2 με συνέπεια η γεωμετρία του να είναι γραμμική, ενώ το SO 2 έχει γενικό τύπο ΑΒ 2 Ε και γεωμετρία κεκαμμένη (2/160). (β) Το μόριο He 2 δεν μπορεί να υπάρξει στη θεμελιώδη κατάσταση. Μπορεί να υπάρξει στην πρώτη διεγερμένη κατάσταση.
14 Το μόριο έχει, στη θεμελιώδη κατάσταση, τάξη δεσμού ίση με μηδέν. Αν όμως προσφέρουμε ενέργεια, τότε ένα ηλεκτρόνιο από το σ* 1s μεταπηδά στο μοριακό τροχιακό σ 2s (πρώτη διεγερμένη κατάσταση). μετακίνηση αυτή δημιουργεί ένα χημικό είδος με τάξη δεσμού 1 και μπορεί να υπάρξει. Βέβαια, η κατάσταση αυτή δεν είναι σταθερή, αφού το μόριο θα εκπέμψει την επιπλέον ενέργεια και θα επιστρέψει στη θεμελιώδη κατάσταση (τάξη δεσμού = 0) με αποτέλεσμα να διασπασθεί. σ 2s σ 2s σ* 1s σ* 1s Άτομο He σ 1s Άτομο He Άτομο He σ 1s Άτομο He Μόριο He 2 Διεγερμένο Μόριο He 2 (γ) Κάθε μοριακό τροχιακό μπορεί να δεχθεί το πολύ μέχρι δύο ηλεκτρόνια. Ένα μοριακό τροχιακό μπορεί να δεχτεί μέχρι δύο ηλεκτρόνια με αντίθετο spin. Σε κάθε άλλη περίπτωση, ερχόμαστε σε αντίθεση με την απαγορευτική αρχή του Pauli (2/135 και 1/122). (δ) Για κάποιο συγκεκριμένο δίπολο, οι δυνάμεις κατιόντος διπόλου είναι γενικά ισχυρότερες σε σύγκριση με τις δυνάμεις ανιόντος διπόλου, όταν το κατιόν και το ανιόν έχουν ίδιο φορτίο, κατά απόλυτη τιμή, και ανήκουν στην ίδια περίοδο του Περιοδικού Πίνακα. Αυτό οφείλεται στο γεγονός ότι τα κατιόντα έχουν μικρότερο μέγεθος από τα ανιόντα. Το φορτίο τους λοιπόν είναι πιο εντοπισμένο και γι αυτό αλληλεπιδρούν ισχυρότερα με ένα δίπολο. (ε) Στην ένωση CH 4 το σημείο ζέσεως καθορίζεται από την ισχύ των δυνάμεων London. Το σημείο ζέσεως για ένα συγκεκριμένο μόριο καθορίζεται από την ισχύ των πιο ισχυρών διαμοριακών δυνάμεων που εμφανίζονται σε αυτό. Το CH 4 είναι ένα μη πολικό μόριο. Οι μόνες διαμοριακές δυνάμεις που υπάρχουν είναι οι δυνάμεις London. Αντίθετα, στη CH 3 Ο το σημείο ζέσεως καθορίζεται από τους δεσμούς υδρογόνου, που είναι οι πιο ισχυρές διαμοριακές δυνάμεις που εμφανίζονται στο μόριο.
15 10. Ποια είναι σωστή και ποια λάθος από τις παρακάτω προτάσεις; Σε κάθε περίπτωση να δοθεί μια σύντομη εξήγηση. α/α Πρόταση Σωστό Λάθος 1 Για να σχηματισθεί ο δεσμός στα μέταλλα, τα μισά άτομα του μετάλλου αποβάλλουν ηλεκτρόνια και μετατρέπονται σε κατιόντα, ενώ τα άλλα μισά προσλαμβάνουν ηλεκτρόνια και μετατρέπονται σε ανιόντα. Τα αντιθέτου φορτίου ιόντα συγκρατούνται μέσω ηλεκτροστατικών δυνάμεων. 2 Ο υβριδισμός είναι μια υποθετική διαδικασία και δεν μπορεί να αποδειχθεί ότι λαμβάνει χώρα στην πραγματικότητα. 3 Κατά τη θεωρία VB για να σχηματισθεί ένας ομοιοπολικός δεσμός μεταξύ δύο ατόμων, θα πρέπει να υπάρχει σε κάθε άτομο μονήρες (ασύζευκτο) ηλεκτρόνιο σε αμιγές τροχιακό. 4 Οι σ δεσμοί είναι οι δεσμοί στους οποίους η ηλεκτρονική πυκνότητα είναι συγκεντρωμένη σε δύο χωριστές περιοχές πάνω και κάτω από το διαπυρηνικό άξονα. Όταν γνωρίζουμε τη διπολική ροπή ενός διατομικού μορίου Α Β μπορούμε να 5 προσδιορίσουμε εύκολα τα μερικά φορτία που αυτό εμφανίζει, αρκεί να γνωρίζουμε το μήκος του δεσμού Α Β. 6 Ένας από τους παράγοντες που καθορίζουν την πολικότητα ενός μορίου ΑΧ n (n>2) είναι η 7 γεωμετρία που αυτό εμφανίζει. Τα μόρια CH 3 F και CCl 3 F έχουν παρόμοια γεωμετρία. Οι ηλεκτραρνητικότητες των ατόμων C, Cl και H είναι αντίστοιχα 2,5 3,0 και 2,1. Θεωρώντας ότι η διαφορά ηλεκτραρνητικότητας Δχ για τους δεσμούς C H και C Cl είναι σχεδόν ίση, αναμένεται οι ενώσεις αυτές να εμφανίζουν όμοια διπολική ροπή. 8 Ο όρος δυνάμεις van der Walls περιγράφει μόνο τις διαμοριακές δυνάμεις διπόλου διπόλου. 9 Μολονότι η NH 3 έχει χαμηλότερη μοριακή μάζα από τη PH 3, εντούτοις ζέει σε υψηλότερη θερμοκρασία. 10 Διατομικά μόρια με άρτιο αριθμό ηλεκτρονίων είναι οπωσδήποτε διαμαγνητικά. α/α Πρόταση Σωστό Λάθος 1 Για να σχηματισθεί ο δεσμός στα μέταλλα, τα μισά άτομα του μετάλλου αποβάλλουν ηλεκτρόνια και μετατρέπονται σε κατιόντα, ενώ τα άλλα μισά προσλαμβάνουν ηλεκτρόνια και μετατρέπονται σε ανιόντα. Τα αντιθέτου φορτίου ιόντα συγκρατούνται μέσω ηλεκτροστατικών δυνάμεων. Λάθος. Τα μέταλλα έχουν χαμηλές τιμές ενέργειας ιοντισμού με αποτέλεσμα να έχουν τάση να σχηματίσουν μόνο κατιόντα και όχι ανιόντα (2/146). Στο μεταλλικό δεσμό τα άτομα συγκρατούνται στον κρύσταλλο χάρις στα ηλεκτρόνια σθένους που βρίσκονται σε απεντοπισμένα μοριακά τροχιακά εκτεινόμενα σε ολόκληρο τον κρύσταλλο (2/147). 2 Ο υβριδισμός είναι μια υποθετική διαδικασία και δεν μπορεί να αποδειχθεί ότι λαμβάνει χώρα στην πραγματικότητα. Σωστό. Ο υβριδισμός είναι η μαθηματική ανάμειξη ή γραμμικός συνδυασμός των αμιγών τροχιακών ενός ατόμου, κατά τρόπο ώστε να σχηματίζονται νέα, τελείως ισοδύναμα μεταξύ τους, ατομικά τροχιακά (υβριδικά τροχιακά). Αυτό δεν μπορεί να αποδειχθεί ότι συμβαίνει στην πραγματικότητα [Ε 5.2, (2/112)]. 3 Κατά τη θεωρία VB για να σχηματισθεί ένας ομοιοπολικός δεσμός μεταξύ δύο ατόμων, θα πρέπει να υπάρχει σε κάθε άτομο μονήρες (ασύζευκτο) ηλεκτρόνιο σε αμιγές τροχιακό. Λάθος. Κατά τη θεωρία VB, ομοιοπολικός δεσμός μεταξύ δύο ατόμων Α και Β μπορεί να σχηματιστεί (α) όταν καθένα από τα Α και Β διαθέτει ένα μονήρες ηλεκτρόνιο σε αμιγές ή υβριδοποιημένο τροχιακό και (β) όταν το ένα από τα δύο άτομα διαθέτει μονήρες ζεύγος ηλεκτρονίων σθένους και το άλλο άτομο διαθέτει κενό τροχιακό σθένους κατάλληλης ενέργειας και γεωμετρίας 4 Οι σ δεσμοί είναι οι δεσμοί στους οποίους η ηλεκτρονική πυκνότητα είναι συγκεντρωμένη σε δύο χωριστές περιοχές πάνω και κάτω από το διαπυρηνικό άξονα. Λάθος. πιο πάνω περιγραφή είναι χαρακτηριστική του π δεσμού (2/ , Σχ.5,9-5,10). Στο σ δεσμό η ηλεκτρονική πυκνότητα είναι επί του διαπυρηνικού άξονα.
16 Όταν γνωρίζουμε τη διπολική ροπή ενός διατομικού μορίου Α Β μπορούμε να προσδιορίσουμε εύκολα τα μερικά φορτία που αυτό εμφανίζει, αρκεί να γνωρίζουμε το μήκος του δεσμού Α Β. Σωστό. Το φορτίο (δ) που εμφανίζει κάθε άτομο υπολογίζεται από τη σχέση μ = δ r [Εξ.6.1, (2/157)]. Κοιτάξτε και το Πρδ 6.1 (2/158). Ένας από τους παράγοντες που καθορίζουν την πολικότητα ενός μορίου ΑΧ n (n>2) είναι η γεωμετρία που αυτό εμφανίζει. Σωστό. Οι δύο παράγοντες που καθορίζουν την πολικότητα ενός πολυατομικού μορίου ΑΧ n είναι η διαφορά ηλεκτραρνητικότητας Δχ και η γεωμετρία του μορίου [Πρδ 6.2, ( 2/161)]. Τα μόρια CH 3 F και CCl 3 F έχουν παρόμοια γεωμετρία. Οι ηλεκτραρνητικότητες των ατόμων C, Cl και H είναι αντίστοιχα 2,5 3,0 και 2,1. Θεωρώντας ότι η διαφορά ηλεκτραρνητικότητας Δχ για τους δεσμούς C H και C Cl είναι σχεδόν ίση, αναμένεται οι ενώσεις αυτές να εμφανίζουν όμοια διπολική ροπή. Λάθος. Στους δεσμούς C H και C Cl η διαφορά ηλεκτραρνητικότητας Δχ μπορεί να είναι σχεδόν η ίδια, όμως οι επιμέρους διπολικές ροπές έχουν διαφορετική διεύθυνση, αφού στο δεσμό C H το δ+ εμφανίζεται στο ενώ στο δεσμό C Cl εμφανίζεται στον C. Επίσης, η διπολική ροπή καθορίζεται και από το μήκος του δεσμού που εδώ είναι διαφορετικό. [Ε 6.1, (2/ )]. Ο όρος δυνάμεις van der Walls περιγράφει μόνο τις διαμοριακές δυνάμεις διπόλου διπόλου. Λάθος. Ο όρος δυνάμεις van der Walls περιγράφει όλες τις διαμοριακές δυνάμεις, εκτός από τις δυνάμεις διπόλου ιόντος και το δεσμό υδρογόνου (2/163). Μολονότι η NH 3 έχει χαμηλότερη μοριακή μάζα από τη PH 3, εντούτοις ζέει σε υψηλότερη θερμοκρασία. Σωστό. Αυτό οφείλεται στους δεσμούς υδρογόνου που σχηματίζουν τα μόρια της Ν 3. Διατομικά μόρια με άρτιο αριθμό ηλεκτρονίων είναι οπωσδήποτε διαμαγνητικά. Λάθος. Αυτό δεν συμβαίνει πάντα. Κλασσικό παράδειγμα είναι το μόριο του Ο 2,(με 16 ηλεκτρόνια) το οποίο είναι παραμαγνητικό. [Ε 5.5,(2/134),Σχ 5.16, (2/136) 5.18, (2/138)].
Γεωμετρία Μορίων Θεωρία VSEPR
 Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΕΣΜΟΥ
 ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
Ασκήσεις. Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3
 Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Μάθημα 21 ο. Το σχήμα των μορίων. Θεωρία VSEPR. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μοριακά Πρότυπα (Μοντέλα)
 Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΠΑΡΑΔΕΙΓΜΑ
 ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
Κεφάλαιο 2 Ο Χημικός Δεσμός
 Κεφάλαιο 2 Ο Χημικός Δεσμός Σύνοψη O Χημικός Δεσμός εξηγεί τον τρόπο με τον οποίο δημιουργούνται οι ενώσεις. Υπάρχουν οι ιοντικές ενώσεις στις οποίες ιόντα αντίθετου φορτίου ενώνονται μεταξύ τους προς
Κεφάλαιο 2 Ο Χημικός Δεσμός Σύνοψη O Χημικός Δεσμός εξηγεί τον τρόπο με τον οποίο δημιουργούνται οι ενώσεις. Υπάρχουν οι ιοντικές ενώσεις στις οποίες ιόντα αντίθετου φορτίου ενώνονται μεταξύ τους προς
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, S = 32,066 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Σχετική ισχύς οξέων (ελάττωση από αριστερά προς τα δεξιά):
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, S = 32,066 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Σχετική ισχύς οξέων (ελάττωση από αριστερά προς τα δεξιά):
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ένωση Χ 3 το κεντρικό άτομο Χ φέρει δύο μονήρη ζεύγη ηλεκτρονίων σθένους, ενώ στην ένωση Υ 2 το κεντρικό άτομο Υ φέρει τρία μονήρη ζεύγη ηλεκτρονίων σθένους.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ένωση Χ 3 το κεντρικό άτομο Χ φέρει δύο μονήρη ζεύγη ηλεκτρονίων σθένους, ενώ στην ένωση Υ 2 το κεντρικό άτομο Υ φέρει τρία μονήρη ζεύγη ηλεκτρονίων σθένους.
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού
 7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
Χημικοί Χημικ σμ σμ & Μοριακά Τροχιακά
 Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ο άργυρος εμφανίζεται στη φύση υπό τη μορφή δύο ισοτόπων τα οποία έχουν ατομικές μάζες 106,905 amu και 108,905 amu. (α) Γράψτε το σύμβολο για καθένα ισότοπο του αργύρου
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ο άργυρος εμφανίζεται στη φύση υπό τη μορφή δύο ισοτόπων τα οποία έχουν ατομικές μάζες 106,905 amu και 108,905 amu. (α) Γράψτε το σύμβολο για καθένα ισότοπο του αργύρου
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ. Παππάς Χρήστος Επίκουρος Καθηγητής
 ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Είδη Δεσμών Ιοντικός δεσμός (Ionic bond), σχηματίζεται πάντα μεταξύ ηλεκτροθετικών
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Ι: Ο ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΚΑΙ ΜΙΑ ΠΡΩΤΗ ΠΡΟΣΕΓΓΙΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ ΔΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Είδη Δεσμών Ιοντικός δεσμός (Ionic bond), σχηματίζεται πάντα μεταξύ ηλεκτροθετικών
5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση
 5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι μια πρώτη προσέγγιση των κυματομηχανικών θεωριών του ομοιοπολικού δεσμού και η ανακάλυψη του πώς οι θεωρίες αυτές δημιουργούν
5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι μια πρώτη προσέγγιση των κυματομηχανικών θεωριών του ομοιοπολικού δεσμού και η ανακάλυψη του πώς οι θεωρίες αυτές δημιουργούν
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Στην ετικέτα φιάλης νερού Λουτρακίου (atural Mineral Water) αναγράφεται η τιμή ολικής σκληρότητας 89 αμερικανικοί βαθμοί σκληρότητας. Πόσα ml προτύπου διαλύματος EDTA
Ομοιοπολικός εσμός Θεωρία Lewis
 Ομοιοπολικός εσμός Θεωρία Lewis Oμοιοπολικός δεσμός: αμοιβαία συνεισφορά ηλεκτρονίων σθένους κοινά ζεύγη ηλεκτρονίων δομή ευγενούς αερίου (κανόνας της οκτάδας) Πλεονεκτήματα: η πληρέστερη προ-κβαντική
Ομοιοπολικός εσμός Θεωρία Lewis Oμοιοπολικός δεσμός: αμοιβαία συνεισφορά ηλεκτρονίων σθένους κοινά ζεύγη ηλεκτρονίων δομή ευγενούς αερίου (κανόνας της οκτάδας) Πλεονεκτήματα: η πληρέστερη προ-κβαντική
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Κατατάξετε τα ακόλουθα υδατικά διαλύματα, συγκεντρώσεως 0,10 Μ το καθένα, κατά σειρά αυξανόμενου ph: (α) CaCl (β) NH 3 (γ) KNΟ (δ) HClO 4 (ε) NaOH (στ) CH 3 COOH Υπόδειξη:
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Κατατάξετε τα ακόλουθα υδατικά διαλύματα, συγκεντρώσεως 0,10 Μ το καθένα, κατά σειρά αυξανόμενου ph: (α) CaCl (β) NH 3 (γ) KNΟ (δ) HClO 4 (ε) NaOH (στ) CH 3 COOH Υπόδειξη:
ΧΗΜΕΙΑ» ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ. Διδάσκουσα: ΣΟΥΠΙΩΝΗ Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ)
 ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ ΧΗΜΕΙΑ» Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ) ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ Διδάσκουσα: ΣΟΥΠΙΩΝΗ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΡΙΑ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ ΧΗΜΕΙΑ» Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ) ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ Διδάσκουσα: ΣΟΥΠΙΩΝΗ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΡΙΑ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Χημικοί Χημικ σμ σμ & Μοριακά Τροχιακά
 Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 17 Ιουνίου 2007
 ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 17 Ιουνίου 2007 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 17 Ιουνίου 2007 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Γράφετε ευανάγνωστα και καθαρά! Όλες οι απαντήσεις να είναι επαρκώς αιτιολογημένες!!! Δώστε προσοχή στα σημαντικά ψηφία των αριθμητικών αποτελεσμάτων! Καλή επιτυχία. Δεδομένα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Γράφετε ευανάγνωστα και καθαρά! Όλες οι απαντήσεις να είναι επαρκώς αιτιολογημένες!!! Δώστε προσοχή στα σημαντικά ψηφία των αριθμητικών αποτελεσμάτων! Καλή επιτυχία. Δεδομένα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, Ca = 40,078 amu, N = 14,0067 amu, H = 1,00794 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Γράφετε ευανάγνωστα και
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, Ca = 40,078 amu, N = 14,0067 amu, H = 1,00794 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Γράφετε ευανάγνωστα και
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Θεωρία δεσµού σθένους - Υβριδισµός. Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης. Αντιδράσεις υποκατάστασης Πολυµερισµός
 11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής
Μοριακή Γεωμετρία Πολικότητα των Μορίων. Εισαγωγική Χημεία
 Μοριακή Γεωμετρία Πολικότητα των Μορίων Εισαγωγική Χημεία 2013-14 1 Τα σχήματα των μορίων Οι δομές Lewis δίνουν πληροφορίες για την σύνδεση μεταξύ των ατόμων : Μας πληροφορούν για το ποια άτομα συνδέονται
Μοριακή Γεωμετρία Πολικότητα των Μορίων Εισαγωγική Χημεία 2013-14 1 Τα σχήματα των μορίων Οι δομές Lewis δίνουν πληροφορίες για την σύνδεση μεταξύ των ατόμων : Μας πληροφορούν για το ποια άτομα συνδέονται
Οι δομές, οι οποίες δεν περιέχουν τυπικά φορτία υψηλά (δηλαδή είναι 2) είναι:
 Answers to Homework Set 3 12162016 1. Πριν από μερικά χρόνια δημοσιεύθηκε η σύνθεση του ιόντος 5 +. Ποια είναι η πλέον πιθανή α) γεωμετρία ηλεκτρονικών ζευγών, και β) μοριακή γεωμετρική δομή του ιόντος
Answers to Homework Set 3 12162016 1. Πριν από μερικά χρόνια δημοσιεύθηκε η σύνθεση του ιόντος 5 +. Ποια είναι η πλέον πιθανή α) γεωμετρία ηλεκτρονικών ζευγών, και β) μοριακή γεωμετρική δομή του ιόντος
Θεωρία του δεσμού σθένους
 ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε μια αρκετά απλή θεωρία, τη θεωρία του δεσμού σθένους, με την οποία θα μπορούμε να εξηγούμε με αρκετή επιτυχία τη γεωμετρία των συμπλόκων, καθώς και
ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε μια αρκετά απλή θεωρία, τη θεωρία του δεσμού σθένους, με την οποία θα μπορούμε να εξηγούμε με αρκετή επιτυχία τη γεωμετρία των συμπλόκων, καθώς και
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2005 2006 Ημερομηνία εξετάσεων: 1 Ιουλίου 2006
 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2005 2006 Ημερομηνία εξετάσεων: 1 Ιουλίου 2006 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2005 2006 Ημερομηνία εξετάσεων: 1 Ιουλίου 2006 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή
 Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.
![ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας. ΘΕΜΑ 1. Δίνονται. h = 6,63 10 ΑΠΑΝΤΗΣΗΗ Ε 1. σχέση. οπότε έχουμε: ii) Με βάση ΘΕΜΑ 2. η: [Αr] 3d s ατομική ακτίνα. τις απαντήσεις σας.](/thumbs/102/153828250.jpg) ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ 1 ο Εξάμηνο Χημικων Μηχανικών Εξεταστική Περίοδος Σεπτέμβριος 2019 Διδάσκοντες: Γ. Κακάλη, Κ. Κορδάτος 5/9/20199 ΘΕΜΑ 1 i) Να υπολογιστεί η ενέργεια ιοντισμού 1 mol υδρογόνου με βάση τη
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (10/02/2016)
 ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΑΡΙΘΜΟΣ ΜΗΤΡΩΟΥ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (10/02/2016) ΕΞΑΜΗΝΟ ΣΠΟΥΔΩΝ Οδηγίες εξετάσεως Θέματα 1-8: Σημειώστε Χ στον κύκλο με τη σωστή απάντηση. Θέματα 9 και 10: Αιτιολογείστε λεπτομερώς
ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΑΡΙΘΜΟΣ ΜΗΤΡΩΟΥ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ (10/02/2016) ΕΞΑΜΗΝΟ ΣΠΟΥΔΩΝ Οδηγίες εξετάσεως Θέματα 1-8: Σημειώστε Χ στον κύκλο με τη σωστή απάντηση. Θέματα 9 και 10: Αιτιολογείστε λεπτομερώς
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ταξινομήστε τις παρακάτω ενώσεις κατά σειρά αυξανόμενου όξινου χαρακτήρα: (α) HBr, H Se, H S (β) HBr, HCl, HBr.. Ποιες από τις ακόλουθες προτάσεις είναι σωστές και
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ταξινομήστε τις παρακάτω ενώσεις κατά σειρά αυξανόμενου όξινου χαρακτήρα: (α) HBr, H Se, H S (β) HBr, HCl, HBr.. Ποιες από τις ακόλουθες προτάσεις είναι σωστές και
1. (α) Ποιες είναι οι τιμές των κβαντικών αριθμών για το ηλεκτρόνιο. (β) Ποια ουδέτερα άτομα ή ιόντα μπορεί να έχουν αυτή την ηλεκτρονική διάταξη;
 1 η ΔΟΚΙΜΑΣΙΑ ΠΡΟΟΔΟΥ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ : ΑΡΙΘΜΟΣ ΜΗΤΡΩΟΥ : ΗΜΕΡΟΜΗΝΙΑ : 1. (α) Ποιες είναι οι τιμές των κβαντικών αριθμών για το ηλεκτρόνιο (β) Ποια ουδέτερα άτομα ή ιόντα μπορεί να έχουν
1 η ΔΟΚΙΜΑΣΙΑ ΠΡΟΟΔΟΥ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ : ΑΡΙΘΜΟΣ ΜΗΤΡΩΟΥ : ΗΜΕΡΟΜΗΝΙΑ : 1. (α) Ποιες είναι οι τιμές των κβαντικών αριθμών για το ηλεκτρόνιο (β) Ποια ουδέτερα άτομα ή ιόντα μπορεί να έχουν
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
Μάθημα 22 ο. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 22 ο Θεωρία Δεσμού Σθένους- Υβριδισμός Linus Pauling Έγραψε τη μονογραφία : Nature of the chemical bond Τιμήθηκε για το έργο του με το βραβείο Nobel το 1954 Εισήγαγε την ιδέα του υβριδισμού Υβριδισμένα
Μάθημα 22 ο Θεωρία Δεσμού Σθένους- Υβριδισμός Linus Pauling Έγραψε τη μονογραφία : Nature of the chemical bond Τιμήθηκε για το έργο του με το βραβείο Nobel το 1954 Εισήγαγε την ιδέα του υβριδισμού Υβριδισμένα
ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ
 ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
Ομοιοπολικός Δεσμός. Ασκήσεις
 Ασκήσεις Ομοιοπολικός Δεσμός 1. Δίνεται η οργανική ένωση CH 3 -CH 2 -C CH της οποίας τα άτομα αριθμούνται από 1 έως 4, όπως φαίνεται παραπάνω. Πόσοι και τι είδους σ δεσμοί και π δεσμοί υπάρχουν στην ένωση;
Ασκήσεις Ομοιοπολικός Δεσμός 1. Δίνεται η οργανική ένωση CH 3 -CH 2 -C CH της οποίας τα άτομα αριθμούνται από 1 έως 4, όπως φαίνεται παραπάνω. Πόσοι και τι είδους σ δεσμοί και π δεσμοί υπάρχουν στην ένωση;
6. ιαμοριακές δυνάμεις
 6. ιαμοριακές δυνάμεις ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τα είδη των ελκτικών δυνάμεων που αναπτύσσονται μεταξύ των μορίων των ομοιοπολικών ενώσεων και την επίδραση που ασκούν οι δυνάμεις
6. ιαμοριακές δυνάμεις ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε τα είδη των ελκτικών δυνάμεων που αναπτύσσονται μεταξύ των μορίων των ομοιοπολικών ενώσεων και την επίδραση που ασκούν οι δυνάμεις
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Προβλέψτε ποιες από τις παρακάτω αντιδράσεις έχουν σταθερά ισορροπίας Κ c > 1: (α) NH 2 (aq) + H 2 O(aq) NH 3 (aq) + OH (aq) (β) H 3 PO 4 (aq) + CH 3 COO (aq) H 2
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Προβλέψτε ποιες από τις παρακάτω αντιδράσεις έχουν σταθερά ισορροπίας Κ c > 1: (α) NH 2 (aq) + H 2 O(aq) NH 3 (aq) + OH (aq) (β) H 3 PO 4 (aq) + CH 3 COO (aq) H 2
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται οι ενώσεις: H 2 O 2, I 3, K 2 S, N 2 H 4, Ca 2, CH 2, Ca 3 P 2 Βρείτε τα ιόντα από τα οποία αποτελούνται οι ιοντικές ενώσεις και τοποθετήστε τα κατά σειρά
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται οι ενώσεις: H 2 O 2, I 3, K 2 S, N 2 H 4, Ca 2, CH 2, Ca 3 P 2 Βρείτε τα ιόντα από τα οποία αποτελούνται οι ιοντικές ενώσεις και τοποθετήστε τα κατά σειρά
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Προβλέψτε τον υβριδισμό καθενός ατόμου που συνδέεται με περισσότερα από ένα άλλα άτομα στο ακόλουθο μόριο. Πόσες μοίρες είναι περίπου η γωνία Ο C 1 C 2 ; 2. Σε ποιο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Προβλέψτε τον υβριδισμό καθενός ατόμου που συνδέεται με περισσότερα από ένα άλλα άτομα στο ακόλουθο μόριο. Πόσες μοίρες είναι περίπου η γωνία Ο C 1 C 2 ; 2. Σε ποιο
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ποιο άτομο έχει το ακόλουθο διάγραμμα ηλεκτρονικής δομής; 3d 4s 4p Ar 2. Σε καθεμιά από τις ακόλουθες σφαίρες αντιστοιχείστε τα άτομα των στοιχείων K, Rb, Ca και Br.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ποιο άτομο έχει το ακόλουθο διάγραμμα ηλεκτρονικής δομής; 3d 4s 4p Ar 2. Σε καθεμιά από τις ακόλουθες σφαίρες αντιστοιχείστε τα άτομα των στοιχείων K, Rb, Ca και Br.
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
ΔΟΚΙΜΑΣΙΑ ΠΡΟΟΔΟΥ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΔΟΚΙΜΑΣΙΑ ΠΡΟΟΔΟΥ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ 1. Ο άργυρος έχει δύο φυσικά ισότοπα. Το ένα έχει μάζα 106,91 amu και το άλλο 108,90 amu. Υπολογίστε την κλασματική αφθονία των δύο ισοτόπων. Πώς συμβολίζονται τα δύο
ΔΟΚΙΜΑΣΙΑ ΠΡΟΟΔΟΥ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ 1. Ο άργυρος έχει δύο φυσικά ισότοπα. Το ένα έχει μάζα 106,91 amu και το άλλο 108,90 amu. Υπολογίστε την κλασματική αφθονία των δύο ισοτόπων. Πώς συμβολίζονται τα δύο
) σχηματίζονται : α. Ένας σ και δύο π δεσμοί β. Τρεις σ δεσμοί γ. Ένας π και δύο σ δεσμοί δ. Τρεις π δεσμοί.
 ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Να ερμηνευθούν τα πειραματικά δεδομένα: (α) Η διπολική ροπή του F 2 O είναι κατά πολύ μικρότερη από τη διπολική ροπή του Η 2 Ο, μολονότι οι γωνίες δεσμών στα δύο μόρια
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Να ερμηνευθούν τα πειραματικά δεδομένα: (α) Η διπολική ροπή του F 2 O είναι κατά πολύ μικρότερη από τη διπολική ροπή του Η 2 Ο, μολονότι οι γωνίες δεσμών στα δύο μόρια
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Για να παρασκευάσετε ένα διάλυμα ορισμένου p στο Εργαστήριο χρησιμοποιήσατε το ρυθμιστικό ζεύγος C 3 COOΗ / C 3 COONa 3 2 O. Έστω τώρα ότι θέλετε να παρασκευάσετε,
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Για να παρασκευάσετε ένα διάλυμα ορισμένου p στο Εργαστήριο χρησιμοποιήσατε το ρυθμιστικό ζεύγος C 3 COOΗ / C 3 COONa 3 2 O. Έστω τώρα ότι θέλετε να παρασκευάσετε,
και να υπολογίσετε την ενωτική ενέργεια του κρυσταλλικού πλέγματος του. ίνονται: Ενθαλπία σχηματισμού SrCl 2
 Ποιά από τις ενώσεις NaCl και CaCl 2 είναι περισσότερο ιοντική και γιατί; Να σχεδιαστεί ο κύκλος Born-Haber για την ένωση AlF 3 Να σχεδιάσετε τον κύκλο Born-Haber της ένωσης SrCl 2 και να υπολογίσετε την
Ποιά από τις ενώσεις NaCl και CaCl 2 είναι περισσότερο ιοντική και γιατί; Να σχεδιαστεί ο κύκλος Born-Haber για την ένωση AlF 3 Να σχεδιάσετε τον κύκλο Born-Haber της ένωσης SrCl 2 και να υπολογίσετε την
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Για καθεμιά από τις ακόλουθες ομάδες, τοποθετήστε τα άτομα και / ή τα ιόντα κατά σειρά ελαττούμενου μεγέθους (από το μεγαλύτερο προς το μικρότερο) (α) Cu, Cu +, Cu
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Για καθεμιά από τις ακόλουθες ομάδες, τοποθετήστε τα άτομα και / ή τα ιόντα κατά σειρά ελαττούμενου μεγέθους (από το μεγαλύτερο προς το μικρότερο) (α) Cu, Cu +, Cu
Οργανική Χημεία 24 4
 Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ Ημερομηνία εξετάσεων: 12 Ιουνίου 2005
 ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2004 2005 Ημερομηνία εξετάσεων: 12 Ιουνίου 2005 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2004 2005 Ημερομηνία εξετάσεων: 12 Ιουνίου 2005 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ
 Ακαδημαϊκό έτος 0-3 Στατιστική Θερμοδυναμική ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ Επώνυμο: Όνομα: Προσωπικός Αριθμός: Ημερομηνία: Βαθμολογία θεμάτων 3 4 5 6 7 8 9 0 Γενικός Βαθμός η ΓΡΑΠΤΗ ΕΡΓΑΣΙΑ ΣΤΗ "ΦΥΣΙΚΟΧΗΜΕΙΑ"
Ακαδημαϊκό έτος 0-3 Στατιστική Θερμοδυναμική ΕΛΛΗΝΙΚΟ ΑΝΟΙΚΤΟ ΠΑΝΕΠΙΣΤΗΜΙΟ Επώνυμο: Όνομα: Προσωπικός Αριθμός: Ημερομηνία: Βαθμολογία θεμάτων 3 4 5 6 7 8 9 0 Γενικός Βαθμός η ΓΡΑΠΤΗ ΕΡΓΑΣΙΑ ΣΤΗ "ΦΥΣΙΚΟΧΗΜΕΙΑ"
Ιοντικός Δεσμός Πολωσιμότητα ιόντος Κανόνες Fajans
 Ιοντικός Δεσμός Πολωσιμότητα ιόντος: εκφράζει την παραμόρφωση που υφίσταται το ηλεκτρονιακό νέφος από ένα γειτονικό ιόν αντιθέτου φορτίου. Η ιοντική αυτή παραμόρφωση αυξάνει τον ομοιοπολικό χαρακτήρα του
Ιοντικός Δεσμός Πολωσιμότητα ιόντος: εκφράζει την παραμόρφωση που υφίσταται το ηλεκτρονιακό νέφος από ένα γειτονικό ιόν αντιθέτου φορτίου. Η ιοντική αυτή παραμόρφωση αυξάνει τον ομοιοπολικό χαρακτήρα του
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 7: Μοριακή γεωμετρία. Τόλης Ευάγγελος
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 7: Μοριακή γεωμετρία Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 7: Μοριακή γεωμετρία Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Μάθημα 16 ο. Γραφή Χημικών Τύπων κατά Lewis. Ο Χημικός Δεσμός Τυπικό φορτίο
 Μάθημα 16 ο Γραφή Χημικών Τύπων κατά Lewis. Ο Χημικός Δεσμός Τυπικό φορτίο Δεσμός στο μοριακό υδρογόνο ( 2 ) Το υδρογόνο σχηματίζει έναν ομοιοπολικό δεσμό. Όταν δύο άτομα υδρογόνου συνδέονται μεταξύ τους,
Μάθημα 16 ο Γραφή Χημικών Τύπων κατά Lewis. Ο Χημικός Δεσμός Τυπικό φορτίο Δεσμός στο μοριακό υδρογόνο ( 2 ) Το υδρογόνο σχηματίζει έναν ομοιοπολικό δεσμό. Όταν δύο άτομα υδρογόνου συνδέονται μεταξύ τους,
1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα
 1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα Θεωρία 3.1. Ποια είναι τα δομικά σωματίδια της ύλης; Τα άτομα, τα μόρια και τα ιόντα. 3.2. SOS Τι ονομάζεται άτομο
1.3 Δομικά σωματίδια της ύλης - Δομή ατόμου - Ατομικός αριθμός - Μαζικός αριθμός - Ισότοπα Θεωρία 3.1. Ποια είναι τα δομικά σωματίδια της ύλης; Τα άτομα, τα μόρια και τα ιόντα. 3.2. SOS Τι ονομάζεται άτομο
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Άτομα υδρογόνου απορροφούν ενέργεια και τα ηλεκτρόνιά τους διεγείρονται ανερχόμενα στο ενεργειακό επίπεδο με n = 7. Μερικές από τις ηλεκτρονικές μεταπτώσεις που ακολουθούν
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Άτομα υδρογόνου απορροφούν ενέργεια και τα ηλεκτρόνιά τους διεγείρονται ανερχόμενα στο ενεργειακό επίπεδο με n = 7. Μερικές από τις ηλεκτρονικές μεταπτώσεις που ακολουθούν
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2005 2006 Ημερομηνία εξετάσεων: 10 Ιουνίου 2006
 ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2005 2006 Ημερομηνία εξετάσεων: 10 Ιουνίου 2006 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
ΤΕΛΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2005 2006 Ημερομηνία εξετάσεων: 10 Ιουνίου 2006 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή το
1o Kριτήριο Αξιολόγησης
 1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια.
 ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
ΑΡΧΕΣ ΧΗΜΕΙΑΣ Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές ηλεκτροσυγγένειας. Να εξηγήσετε γιατί το άζωτο έχει σχεδόν μηδενική ηλεκτροσυγγένεια. Και ο άνθρακας και το οξυγόνο έχουν σημαντικές τιμές
ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ
 ΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ Χρήστος Παππάς Επίκουρος Καθηγητής 1 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΠΟΛΙΚΗ ΡΟΠΗ δ+ δ- Α------------Β μ Aν μ ΟΛ 0 πολική Aν μ ΟΛ =0 άπολη 2 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΑΤΟΜΙΚΑ ΜΟΡΙΑ Αν τα άτομα
ΥΝΑΜΕΙΣ ΜΕΤΑΞΥ ΙΟΝΤΩΝ Χρήστος Παππάς Επίκουρος Καθηγητής 1 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΠΟΛΙΚΗ ΡΟΠΗ δ+ δ- Α------------Β μ Aν μ ΟΛ 0 πολική Aν μ ΟΛ =0 άπολη 2 ΠΟΛΙΚΕΣ ΑΠΟΛΕΣ ΕΝΩΣΕΙΣ ΙΑΤΟΜΙΚΑ ΜΟΡΙΑ Αν τα άτομα
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής
 ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
ΘΕΜΑ 1ο: Πολλαπλής Επιλογής (i) Ποιός απλός δεσμός C-C από αυτούς που δείχνονται με βέλος έχει το μικρότερο μήκος? (α) 3C (β) 3C C C (γ) 3C C C 2 (δ) C C C C(ε) 2 C C C C Το (δ) καθώς οι C είναι σε sp-sp
ΘΕΩΡΙΑ ΤΟΥ ΕΣΜΟΥ ΣΘΕΝΟΥΣ
 ΘΕΩΡΙΑ ΤΟΥ ΕΣΜΟΥ ΣΘΕΝΟΥΣ Υβριδισµός Πως σχηµατίζεται το µόριο του CH 4 ; ηλαδή συνοπτικά έχουµε ΘΕΩΡΙΑ ΤΟΥ ΕΣΜΟΥ ΣΘΕΝΟΥΣ Υβριδισµός Πως σχηµατίζεται το µόριο του ΡF 5 ; Το µόριο είναι τριγωνικό διπυραµιδικό
ΘΕΩΡΙΑ ΤΟΥ ΕΣΜΟΥ ΣΘΕΝΟΥΣ Υβριδισµός Πως σχηµατίζεται το µόριο του CH 4 ; ηλαδή συνοπτικά έχουµε ΘΕΩΡΙΑ ΤΟΥ ΕΣΜΟΥ ΣΘΕΝΟΥΣ Υβριδισµός Πως σχηµατίζεται το µόριο του ΡF 5 ; Το µόριο είναι τριγωνικό διπυραµιδικό
Μοριακή δομή Ο2 σύμφωνα με VB διαμαγνητικό
 Μοριακή δομή Ο 2 σύμφωνα με VB? διαμαγνητικό Θεωρία Μοριακών Τροχιακών Μolecular Orbital Theory (MO) Τα μοριακά τροχιακά (molecular orbital) είναι κυματοσυναρτήσεις οι οποίες προκύτπουναπότογραμμικόσυνδυασμότωνκυματοσυναρτήσεωντωναο.
Μοριακή δομή Ο 2 σύμφωνα με VB? διαμαγνητικό Θεωρία Μοριακών Τροχιακών Μolecular Orbital Theory (MO) Τα μοριακά τροχιακά (molecular orbital) είναι κυματοσυναρτήσεις οι οποίες προκύτπουναπότογραμμικόσυνδυασμότωνκυματοσυναρτήσεωντωναο.
Μάθημα 20 ο. Το σχήμα των μορίων
 Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
(Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου )
 Δυνάμεις διπόλου διπόλου (Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου ) Τα πολικά μόρια μπορούν να έλκονται αμοιβαία μέσω δυνάμεων διπόλου διπόλου. Η δύναμη διπόλου
Δυνάμεις διπόλου διπόλου (Από το βιβλίο Γενική Χημεία των Ebbing, D. D., Gammon, S. D., Εκδόσεις Παπασωτηρίου ) Τα πολικά μόρια μπορούν να έλκονται αμοιβαία μέσω δυνάμεων διπόλου διπόλου. Η δύναμη διπόλου
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 14 Ιουλίου 2007
 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 14 Ιουλίου 2007 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ (ΦΥΕ 12) Ονοματεπώνυμο Φοιτητή: Αριθμός Μητρώου: ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2006 2007 Ημερομηνία εξετάσεων: 14 Ιουλίου 2007 ΓΕΝΙΚΕΣ ΟΔΗΓΙΕΣ Διαβάστε με προσοχή
7. Μοριακά πρότυπα και ομοιοπολικός δεσμός
 Σκοπός 7. Μοριακά πρότυπα και ομοιοπολικός δεσμός Σκοπός αυτής της άσκησης είναι να κατανοήσουμε πληρέστερα τις θεωρίες που αναφέρονται στη δημιουργία του ομοιοπολικού δεσμού και στη γεωμετρία των μορίων,
Σκοπός 7. Μοριακά πρότυπα και ομοιοπολικός δεσμός Σκοπός αυτής της άσκησης είναι να κατανοήσουμε πληρέστερα τις θεωρίες που αναφέρονται στη δημιουργία του ομοιοπολικού δεσμού και στη γεωμετρία των μορίων,
5. Να βρείτε τον ατομικό αριθμό του 2ου μέλους της ομάδας των αλογόνων και να γράψετε την ηλεκτρονιακή δομή του.
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
Μια πρόταση παρουσίασης με
 Διαμοριακές δυνάμεις Μια πρόταση παρουσίασης με το PowerPoint Διαμοριακές δυνάμεις Είναι οι ελκτικές δυνάμεις ηλεκτροστατικής φύσης (ασθενέστερες από τις ενδομοριακές) που ασκούνται μεταξύ μορίων (του
Διαμοριακές δυνάμεις Μια πρόταση παρουσίασης με το PowerPoint Διαμοριακές δυνάμεις Είναι οι ελκτικές δυνάμεις ηλεκτροστατικής φύσης (ασθενέστερες από τις ενδομοριακές) που ασκούνται μεταξύ μορίων (του
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Διατάξτε τα τροχιακά 1s, 2s, 2p, 3s, 3p, 3d των ατόμων H και Κ κατά σειρά αυξανόμενης ενέργειας. 2. Ένας όγκος αέρα που συλλέχθηκε στην επιφάνεια της Γης σε 15 o C
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Διατάξτε τα τροχιακά 1s, 2s, 2p, 3s, 3p, 3d των ατόμων H και Κ κατά σειρά αυξανόμενης ενέργειας. 2. Ένας όγκος αέρα που συλλέχθηκε στην επιφάνεια της Γης σε 15 o C
Μοριακά Πρότυπα και Ομοιοπολικός Δεσμός
 Μοριακά Πρότυπα και Ομοιοπολικός Δεσμός ΣΚΟΠΟΣ Σκοπός αυτής της άσκησης είναι να κατανοήσουμε πληρέστερα τις θεωρίες που αναφέρονται στη δημιουργία του ομοιοπολικού δεσμού και στη γεωμετρία των μορίων,
Μοριακά Πρότυπα και Ομοιοπολικός Δεσμός ΣΚΟΠΟΣ Σκοπός αυτής της άσκησης είναι να κατανοήσουμε πληρέστερα τις θεωρίες που αναφέρονται στη δημιουργία του ομοιοπολικού δεσμού και στη γεωμετρία των μορίων,
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται τα ιόντα Mg 2+, 2, F, Na + και Al + και οι τιμές ιοντικών ακτίνων 16 pm, 95 pm, 50 pm, 140 pm και 65 pm. Βρείτε ποια ακτίνα ταιριάζει σε καθένα από τα ιόντα
Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2
 Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται οι αντιδράσεις: (i) KClO 3 KCl + O 2 (ii) H 2 O 2 H 2 O + O 2 (iii) NaNO 3 NaNO 2 + O 2 (iv) KClO 4 KCl + O 2 (α) Ποιες από αυτές τις αντιδράσεις είναι αντιδράσεις
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Δίνονται οι αντιδράσεις: (i) KClO 3 KCl + O 2 (ii) H 2 O 2 H 2 O + O 2 (iii) NaNO 3 NaNO 2 + O 2 (iv) KClO 4 KCl + O 2 (α) Ποιες από αυτές τις αντιδράσεις είναι αντιδράσεις
Κατανομή μετάλλων και αμετάλλων στον Π.Π.
 Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
Κατανομή μετάλλων και αμετάλλων στον Π.Π. Ιδιότητες Μετάλλων και Αμετάλλων ΜΕΤΑΛΛΑ ΑΜΕΤΑΛΛΑ Ιόντα αντιπροσωπευτικών στοιχείων Ιόντα αντιπροσωπευτικών μετάλλων Ιόντα μετάλλων με δομή ευγενούς αερίου (1Α,
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ. ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α A1. Ποιο από τα επόμενα άτομα έχει μεγαλύτερη ατομική ακτίνα; α. 11 Na β. 12 Mg γ. 14 Si δ.
 ΧΜΕΙΑ Α ΛΥΚΕΙΟΥ 2/12/2018 Σταυρούλα Γκιτάκου, Μαρία Ρήγα, Γιάννης Παπαντωνάκης, Γιάννης Τσάφος, Μαρίνος Ιωάννου ΑΠΑΝΤΣΕΙΣ ΘΕΜΑ Α A1. Ποιο από τα επόμενα άτομα έχει μεγαλύτερη ατομική ακτίνα; α. 11 Na β.
ΧΜΕΙΑ Α ΛΥΚΕΙΟΥ 2/12/2018 Σταυρούλα Γκιτάκου, Μαρία Ρήγα, Γιάννης Παπαντωνάκης, Γιάννης Τσάφος, Μαρίνος Ιωάννου ΑΠΑΝΤΣΕΙΣ ΘΕΜΑ Α A1. Ποιο από τα επόμενα άτομα έχει μεγαλύτερη ατομική ακτίνα; α. 11 Na β.
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 4 Καταστάσεις της Ύλης: Αέρια, Υγρά και Στερεά
 Κεφάλαιο 4 Καταστάσεις της Ύλης: Αέρια, Υγρά και Στερεά Σύνοψη Η ύλη χαρακτηρίζεται από μεγάλη ποικιλία φυσικών καταστάσεων όπως αέρια, υγρή, στερεή. Οι διάφορες αυτές φάσεις που μπορεί να έχει μία ουσία
Κεφάλαιο 4 Καταστάσεις της Ύλης: Αέρια, Υγρά και Στερεά Σύνοψη Η ύλη χαρακτηρίζεται από μεγάλη ποικιλία φυσικών καταστάσεων όπως αέρια, υγρή, στερεή. Οι διάφορες αυτές φάσεις που μπορεί να έχει μία ουσία
Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων
 Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων Στις παρακάτω ερωτήσεις επιλέξτε τη σωστή απάντηση. Ο μέγιστος αριθμός ηλεκτρονίων για κάθε στιβάδα προκύπτει με εφαρμογή: α. της αρχής της ελάχιστης ενέργειας
Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων Στις παρακάτω ερωτήσεις επιλέξτε τη σωστή απάντηση. Ο μέγιστος αριθμός ηλεκτρονίων για κάθε στιβάδα προκύπτει με εφαρμογή: α. της αρχής της ελάχιστης ενέργειας
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Γράψτε την τετράδα των κβαντικών αριθμών που χαρακτηρίζει τα ακόλουθα ηλεκτρόνια: (α) Το εξώτατο ηλεκτρόνιο του ατόμου Rb. (β) Το ηλεκτρόνιο που κερδίζει το ιόν S
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Γράψτε την τετράδα των κβαντικών αριθμών που χαρακτηρίζει τα ακόλουθα ηλεκτρόνια: (α) Το εξώτατο ηλεκτρόνιο του ατόμου Rb. (β) Το ηλεκτρόνιο που κερδίζει το ιόν S
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. (α) Σχεδιάστε τη δομή Lewis για το μόριο του φθοριδίου του αντιμονίου(ιιι), SbF 3. (β) Προβλέψτε τη γεωμετρία του μορίου. (γ) Βρείτε τα υβριδικά τροχιακά που χρησιμοποιεί
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. (α) Σχεδιάστε τη δομή Lewis για το μόριο του φθοριδίου του αντιμονίου(ιιι), SbF 3. (β) Προβλέψτε τη γεωμετρία του μορίου. (γ) Βρείτε τα υβριδικά τροχιακά που χρησιμοποιεί
ΥΒΡΙ ΙΣΜΟΣ υβριδισµός
 ΥΒΡΙ ΙΣΜΟΣ Οσχηµατισµός δεσµών µε απλή επικάλυψη ατοµικών τροχιακών, σε πολλές περιπτώσεις, αδυνατεί να ερµηνεύσει τη δοµή των µορίων, όπως π.χ. των οργανικών ενώσεων. Μια προωθηµένη αντίληψη για την ερµηνεία
ΥΒΡΙ ΙΣΜΟΣ Οσχηµατισµός δεσµών µε απλή επικάλυψη ατοµικών τροχιακών, σε πολλές περιπτώσεις, αδυνατεί να ερµηνεύσει τη δοµή των µορίων, όπως π.χ. των οργανικών ενώσεων. Μια προωθηµένη αντίληψη για την ερµηνεία
Οργανική Χημεία. Κεφάλαιο 1: Δομή και δεσμοί
 Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Μοριακή δομή. Απλοϊκή εικόνα του μορίου του νερού. Ηλεκτρονιακοί τύποι κατά Lewis. Δημόκριτος π.χ.
 Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού
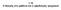 1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Πόσα γραμμάρια NaCl περιέχουν τον ίδιο συνολικό αριθμό ιόντων που περιέχουν 381 g MgCl 2 ; 2. Ταξινομήστε τις ακόλουθες ενώσεις κατά σειρά αυξανόμενου όξινου χαρακτήρα:
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Πόσα γραμμάρια NaCl περιέχουν τον ίδιο συνολικό αριθμό ιόντων που περιέχουν 381 g MgCl 2 ; 2. Ταξινομήστε τις ακόλουθες ενώσεις κατά σειρά αυξανόμενου όξινου χαρακτήρα:
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ένας συμπληρωμένος με ηλεκτρόνια υποφλοιός ατόμου χαρακτηρίζεται από αυξημένη σταθερότητα. (α) Με πόσα ηλεκτρόνια θεωρούνται συμπληρωμένοι οι υποφλοιοί 7s, 6p, 5d,
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1. Ένας συμπληρωμένος με ηλεκτρόνια υποφλοιός ατόμου χαρακτηρίζεται από αυξημένη σταθερότητα. (α) Με πόσα ηλεκτρόνια θεωρούνται συμπληρωμένοι οι υποφλοιοί 7s, 6p, 5d,
ΜΕΡΟΣ Α' (Διάρκεια εξέτασης: 15 min)
 ΣΕΜΦΕ ΕΜΠ Γενική Χημεία Διαγώνισμα 11/02/20 1 ΜΕΡΟΣ Α' (Διάρκεια εξέτασης: 15 min) 1.Σημειώστε τη σωστή ηλεκτρονική διαμόρφωση του 28 Ni +2, [ 18 Ar]=1s 2 2s 2 2p 6 3s 2 3p 6 a. [Ar] 4s 2 3d 6 b. [Ar]
ΣΕΜΦΕ ΕΜΠ Γενική Χημεία Διαγώνισμα 11/02/20 1 ΜΕΡΟΣ Α' (Διάρκεια εξέτασης: 15 min) 1.Σημειώστε τη σωστή ηλεκτρονική διαμόρφωση του 28 Ni +2, [ 18 Ar]=1s 2 2s 2 2p 6 3s 2 3p 6 a. [Ar] 4s 2 3d 6 b. [Ar]
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων. Περιοδικός πίνακας. Σταυρακαντωνάκης Γιώργος Λύκειο Γαζίου Page 1
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
Σχ. 1: Τυπική μορφή μοριακού δυναμικού.
 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-1 Κεφάλαιο 6. Μόρια Εδάφια: 6.a. Μόρια και μοριακοί δεσμοί 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού 6.c. Περιστροφή και ταλάντωση μορίων 6.d. Μοριακά φάσματα 6.a.
ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-1 Κεφάλαιο 6. Μόρια Εδάφια: 6.a. Μόρια και μοριακοί δεσμοί 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού 6.c. Περιστροφή και ταλάντωση μορίων 6.d. Μοριακά φάσματα 6.a.
ΑΤΟΜΙΚΑ ΤΟΜΙΚΑ ΠΡΟΤΥΠΑ
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
Gilbert Newton Lewis, USA, Συμβολή στην ανάπτυξη της θεωρίας του χημικού δεσμού 1
 Χημικοί δεσμοί: Θεωρία Lewis Gilbert Newton Lewis, USA, 1875 1946 Συμβολή στην ανάπτυξη της θεωρίας του χημικού δεσμού 1 Xημικός ς δεσμός Προϋπόθεση για τη δημιουργία χημικού δεσμού: Η διάταξη η οποία
Χημικοί δεσμοί: Θεωρία Lewis Gilbert Newton Lewis, USA, 1875 1946 Συμβολή στην ανάπτυξη της θεωρίας του χημικού δεσμού 1 Xημικός ς δεσμός Προϋπόθεση για τη δημιουργία χημικού δεσμού: Η διάταξη η οποία
