Θεωρία δεσµού σθένους - Υβριδισµός. Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης. Αντιδράσεις υποκατάστασης Πολυµερισµός
|
|
|
- Ἀλαλά Τρικούπη
- 7 χρόνια πριν
- Προβολές:
Transcript
1 11 ο Μάθηµα: Θεωρία δεσµού σθένους - Υβριδισµός 12 ο Μάθηµα: Αντιδράσεις προσθήκης Αντιδράσεις απόσπασης 13 ο Μάθηµα: Αντιδράσεις υποκατάστασης Πολυµερισµός 14 ο Μάθηµα: Αντιδράσεις οξείδωσης - αναγωγής Αντιδράσεις οξέων - βάσεων 15 ο Μάθηµα: Αλογονοφορµική αντίδραση Ταυτοποίηση - ιάκριση
2 Αν ν = 0, ο τύπος C ν Η 2ν+1 µπορεί να συµπεριλάβει και το Η
3 Θεωρία δεσµού σθένους - Υβριδισµός o Θεωρία δεσµού σθένους Υβριδισµός Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Θεωρία δεσµού σθένους: Οι κυριότερες κβαντοµηχανικές θεωρίες περιγραφής του οµοιοπολικού δεσµού είναι: Θεωρία των µοριακών τροχιακών Θεωρία δεσµού σθένους Θεωρία των µοριακών τροχιακών: Τα βασικά σηµεία της θεωρίας των µοριακών τροχιακών είναι: α. Τα µοριακά τροχιακά προκύπτουν µε συνδυασµό ατοµικών τροχιακών. Όσα ατοµικά τροχιακά συνδυάζονται, τόσα µοριακά τροχιακά προκύπτουν. β. Τα µοριακά τροχιακά περιγράφουν τις περιοχές του χώρου σε ένα µόριο, όπου υπάρχει µεγάλη πιθανότητα να βραθεί το κοινό ζεύγος ηλεκτρονίων. Τα µοριακά τροχιακά περιβάλλουν δύο ή περισσότερους πυρήνες, σε αντίθεση µε τα ατοµικά τροχιακά που περιβάλλουν µόνον ένα. γ. Τα µοριακά τροχιακά έχουν ορισµένο σχήµα, µέγεθος και ενεργειακό επίπεδο. δ. Υπάρχουν δύο είδη µοριακών τροχιακών, τα δεσµικά που έχουν χαµηλή ενέργεια και τα αντιδεσµικά που έχουν υψηλή ενέργεια. Με τη θεωρία των µοριακών τροχιακών δεν θα ασχοληθούµε στο συγκεκριµένο βιβλίο. Θεωρία δεσµού σθένους: Τα βασικά σηµεία της θεωρίας δεσµού σθένους είναι: α. Κατά το σχηµατισµό οµοιοπολικού δεσµού ανάµεσα σε δύο άτοµα, γίνεται επικάλυψη ανάµεσα σε τροχιακά της στιβάδας σθένους των δύο ατόµων. β. Αν κάθε τροχιακό που επικαλύπτεται περιέχει ένα µονήρες ηλεκτρόνιο, τότε ηλεκτρόνια µε αντιπαράλληλα spin δηµιουργούν ζεύγη ηλεκτρονίων που ανήκουν και στα δύο άτοµα. Η έλξη του κοινού ζεύγους και από τους δύο πυρήνες οδηγεί στο σχηµατισµό δεσµού µεταξύ των ατόµων. γ. Όσο µεγαλύτερος είναι ο βαθµός επικάλυψης µεταξύ των ατοµικών τροχιακών µε ένα µονήρες ηλεκτρόνιο, τόσο ισχυρότερος είναι ο δεσµός που σχηµατίζεται. Οι δεσµοί που σχηµατίζονται, σύµφωνα µε τη θεωρία δεσµού σθένους, χαρακτηρίζονται ως δεσµοί σ (σίγµα) ή δεσµοί π (πι).
4 258. Τρίτο Κεφάλαιο - 11 ο Μάθηµα εσµοί σ: Οι σ δεσµοί προκύπτουν µε επικαλύψεις s s, s p και p p ατοµικών τροχιακών, κατά τον άξονα που συνδέει τους πυρήνες των δύο ατόµων που συνδέονται. Κατά τη διεύθυνση του άξονα που συνδέει τους πυρήνες των δύο ατόµων εξασφαλίζεται η µεγαλύτερη επικάλυψη. Η ευθεία που ενώνει τους πυρήνες των δύο ατόµων, ονοµάζεται άξονας του δεσµού και συµπίπτει µε τους άξονες συµµετρίας των τροχιακών που επικαλύπτονται. Κατά τη δηµιουργία του σ δεσµού, οι πυρήνες των ατόµων βρίσκονται σε απόσταση τέτοια ώστε η ενέργεια του συστήµατος να είναι ελάχιστη. Η απόσταση αυτή ονοµάζεται µήκος δεσµού. Παράδειγµα: α. Σχηµατισµός σ δεσµού στο µόριο του υδρογόνου (Η 2 ): Η ηλεκτρονιακή δοµή του Η είναι: 1 Η: 1s 1 Στο µόριο του υδρογόνου, ο σ δεσµός δηµιουργείται µε επικάλυψη (s s) των δύο τροχιακών 1s. β. Σχηµατισµός σ δεσµού στο µόριο του υδροχλωρίου (ΗCl): Η ηλεκτρονιακή δοµή του Η είναι: 1 Η: 1s 1 Η ηλεκτρονιακή δοµή του Cl είναι: 17 Cl: 1s 2, 2s 2, 2p 6, 3p 2 x, 3p 2 y, 3p 1 z Στο µόριο του υδρογόνου, ο σ δεσµός δηµιουργείται µε επικάλυψη (s p) µεταξύ του 1s τροχιακού του υδρογόνου και του 3p z τροχιακού του χλωρίου. γ. Σχηµατισµός σ δεσµού στο µόριο του φθορίου (F 2 ): Η ηλεκτρονιακή δοµή του F είναι: 9 F: 1s 2, 2s 2, 2p 2 x, 2p 2 y, 2p 1 z Στο µόριο του φθορίου, ο σ δεσµός δηµιουργείται µε επικάλυψη (p p) µεταξύ των 2p z ατοµικών τροχιακών.
5 Θεωρία δεσµού σθένους - Υβριδισµός 259. Παρατήρηση: Ο σ δεσµός έχει κυλινδρική συµµετρία ως προς τον άξονα του δεσµού και η µέγιστη πυκνότητα του ηλεκτρονιακού νέφους βρίσκεται στο χώρο µεταξύ των δύο πυρήνων. εσµοί π: Οι π δεσµοί προκύπτουν µε πλευρικές επικαλύψεις p p ατοµικών τροχιακών, των οποίων οι άξονες είναι παράλληλοι. Στον π δεσµό, οι άξονες των τροχιακών που επικαλύπτονται, είναι κάθετοι στον άξονα του δεσµού και η πυκνότητα του ηλεκτρονιακού νέφους είναι µέγιστη εκατέρωθεν του άξονα και µηδενική πάνω στον άξονα. Στον π δεσµό η επικάλυψη είναι µικρότερη από ότι στον σ δεσµό, για αυτό ο σ δεσµός είναι ισχυρότερος του π δεσµού. Στα s τροχιακά, είναι αδύνατη η πλευρική επικάλυψη, για αυτό δε συµµετέχουν σε π δεσµούς. π.χ. Το άτοµο του υδρογόνου, που έχει µόνο s τροχιακά, δε σχηµατίζει π δεσµούς. Μεταξύ δύο ατόµων, δηµιουργείται π δεσµός µόνο εφόσον έχει προηγηθεί δηµιουργία σ δεσµού. Παράδειγµα: Ερµηνεία δεσµών στο µόριο του αζώτου (Ν 2 ): Η ηλεκτρονιακή δοµή του Ν είναι: 7 Ν: 1s 2, 2s 2, 2p 1 x, 2p 1 y, 2p 1 z Κάθε άτοµο αζώτου έχει τρία p τροχιακά µε µονήρη ηλεκτρόνια. Κατά τη δηµιουργία του µορίου Ν 2 δηµιουργούνται οι παρακάτω δεσµοί: 1 σ δεσµός µε επικάλυψη (p p) ενός 2p τροχιακού κάθε ατόµου, κατά τον άξονα που συνδέει τους πυρήνες των ατόµων. 2 π δεσµοί µε πλευρική επικάλυψη (p p) µεταξύ των δύο 2p τροχιακών που αποµένουν σε κάθε άτοµο αζώτου. Στο παρακάτω σχήµα φαίνεται η δηµιουργία ενός π δεσµού µε πλευρική επικάλυψη δύο 2p x τροχιακών: Παρατήρηση: α. Ο απλός οµοιοπολικός δεσµός ( ) αποτελείται από ένα σ δεσµό. β. Ο διπλός οµοιοπολικός δεσµός (=) αποτελείται από ένα σ και ένα π δεσµό. γ. Ο τριπλός οµοιοπολικός δεσµός ( ) αποτελείται από ένα σ και δύο π δεσµούς.
6 260. Τρίτο Κεφάλαιο - 11 ο Μάθηµα Υβριδισµός: Η θεωρία του υβριδισµού προτάθηκε από τον Linus Pauling και µε τη βοήθειά της ερµηνεύτικε η δοµή οµοιοπολικών µορίων, που δεν µπορούσε να ερµηνευτεί µε το σχηµατισµό δεσµών µε απλή επικάλυψη ατοµικών τροχιακών. Υβριδισµός είναι ο γραµµικός συνδυασµός (πρόσθεση ή αφαίρεση) ατοµικών τροχιακών που οδηγεί στη δηµιουργία νέων ισότιµων ατοµικών τροχιακών, τα οποία ονοµάζονται υβριδικά τροχιακά. Τα υβριδικά τροχιακά έχουν τις παρακάτω ιδιότητες: α. Είναι αριθµητικά ίσα µε τα ατοµικά τροχιακά που συνδυάζονται για το σχηµατισµό τους. β. ιαφέρουν από τα ατοµικά τροχιακά που συνδυάζονται για το σχηµατισµό τους, ως προς την ενέργεια, τη µορφή και τον προσανατολισµό. γ. Έχουν σχήµα οµοαξονικών αλλά άνισου µεγέθους λοβών. δ. Τα ηλεκτρόνια που υπήρχαν στα ατοµικά τροχιακα που συνδυάζονται για το σχηµατισµό τους, κατανέµονται σε αυτά µε βάση τις αρχές ηλεκτρονιακής δόµησης. Είδη υβριδικών τροχιακών: sp υβριδικά τροχιακά: Τα sp υβριδικά τροχιακά δηµιουργούνται από το γραµµικό συνδιασµό ενός s και ενός p ατοµικού τροχιακού. Τα δύο ισότιµα sp υβριδικά τροχιακά έχουν ευθύγραµµη διάταξη και στο σχηµατισµό τους συνεισφέρουν κατά 50% το τροχιακό s και κατά 50% το τροχιακό p. Η ενέργεια των sp υβριδικών τροχιακών είναι ενδιάµεση της ενέργειας των s και p ατοµικών τροχιακών. sp 2 υβριδικά τροχιακά: Τα sp 2 υβριδικά τροχιακά δηµιουργούνται από το συνδιασµό ενός s και δύο p ατοµικών τροχιακών. Τα τρία ισότιµα sp 2 υβριδικά τροχιακά έχουν επίπεδη τριγωνική διάταξη και η γωνία που σχηµατίζουν µεταξύ τους είναι 120 ο.
7 Θεωρία δεσµού σθένους - Υβριδισµός 261. sp 3 υβριδικά τροχιακά: Τα sp 3 υβριδικά τροχιακά δηµιουργούνται από το συνδιασµό ενός s και τριών p ατοµικών τροχιακών. Τα τέσσερα ισότιµα sp 2 υβριδικά τροχιακά έχουν τετραεδρική διάταξη και η γωνία που σχηµατίζουν µεταξύ τους είναι 109,5 ο. Υβριδισµό δεν έχουµε µόνο µεταξύ s και p ατοµικών τροχιακών. Υπάρχουν περιπτώσεις σχηµατισµού υβριδικών τροχιακών, στις οποίες συµµετέχουν και d ατοµικά τροχιακά. Η µελέτη των περιπτώσεων αυτών δεν γίνεται σε αυτό το βιβλίο. Παρατήρηση: Επειδή ο µεγάλος λοβός των υβριδικών τροχιακών έχει µεγαλύτερο µέγεθος από τους λοβούς των ατοµικών τροχιακών, για αυτό ο βαθµός επικάλυψης των υβριδικών τροχιακών είναι µεγαλύτερος, µε αποτέλεσµα να οδηγεί σε ισχυρότερους δεσµούς.
8 262. Τρίτο Κεφάλαιο - 11 ο Μάθηµα Παράδειγµα: α. Ερµηνεία των δεσµών στο µόριο του ΒeF 2 : Oι ηλεκτρονιακές δοµές των Bε, F στη θεµελιώδη κατάσταση είναι: (Θεµελιώδης κατάσταση) Παρατηρούµε ότι το Βe δεν έχει µονήρη ηλεκτρόνια, συνεπώς δεν θα έπρεπε να σχηµατίζει οµοιοπολικούς δεσµούς. Για να εξηγήσουµε το σχηµατισµό του ΒeF 2 δεχόµαστε ότι ένα από τα δύο ηλεκτρόνια του 2s ατοµικού τροχιακού προωθείται σε τροχιακό 2p και προκύπτει η προωθηµένη κατάσταση του Be: (Προωθηµένη κατάσταση) Με βάση την παραπάνω ηλεκτρονιακή δοµή, στο µόριο του ΒeF 2 οι δύο δεσµοί θα έπρεπε να είναι διαφορετικοί, γιατί ο ένας θα σχηµατιζόταν µε επικάλυψη (s p) και ο άλλος µε επικάλυψη (p p). Πειραµατικά όµως βρέθηκε ότι οι δύο δεσµοί στο BeF 2 είναι ισότιµοι. Αυτό εξηγήται γιατί στο άτοµο του Be τα 2s και 2p τροχιακά συνδυάζονται και δηµιουργούν δύο sp υβριδικά τροχιακά, τα οποία είναι ισότιµα µεταξύ τους και προκύπτει η παρακάτω ηλεκτρονιακή δοµή: (Υβριδισµός sp) Συνεπώς, στο µόριο του ΒeF 2 οι δύο ισότιµοι δεσµοί σχηµατίζονται µε επικάλυψη των sp υβριδικών τροχιακών του Be, µε τα δύο p ατοµικά τροχιακά των ατόµων του F. ηλαδή, έχουµε δύο ισότιµους σ δεσµούς, όπως φαίνεται στο παρακάτω σχήµα: β. Ερµηνεία των δεσµών στο µόριο του ΒF 3 : Oι ηλεκτρονιακές δοµές των B, F στη θεµελιώδη κατάσταση είναι: (Θεµελιώδης κατάσταση) Ένα από τα δύο ηλεκτρόνια του 2s ατοµικού τροχιακού του Β προωθείται σε τροχιακό 2p και προκύπτει η προωθηµένη κατάσταση του B: (Προωθηµένη κατάσταση) Στο άτοµο του B τα 2s και 2p τροχιακά συνδυάζονται και δηµιουργούν τρία sp 2 υβριδικά τροχιακά, τα οποία είναι ισότιµα µεταξύ τους και προκύπτει η παρακάτω ηλεκτρονιακή δοµή: (Υβριδισµός sp 2 ) Συνεπώς, στο µόριο του ΒF 3 υπάρχουν τρεις ισότιµοι σ δεσµοί που σχηµατίζονται µε επικάλυψη των sp 2 υβριδικών τροχιακών του B, µε τα τρία p ατοµικά τροχιακά των ατόµων του F.
9 Θεωρία δεσµού σθένους - Υβριδισµός 263. β. Ερµηνεία των δεσµών στο µόριο του CH 4 : Oι ηλεκτρονιακές δοµές των C, H στη θεµελιώδη κατάσταση είναι: (Θεµελιώδης κατάσταση) Ένα από τα δύο ηλεκτρόνια του 2s ατοµικού τροχιακού του C προωθείται σε τροχιακό 2p και προκύπτει η προωθηµένη κατάσταση του C: (Προωθηµένη κατάσταση) Στο άτοµο του C τα 2s και 2p τροχιακά συνδυάζονται και δηµιουργούν τέσσερα sp 3 υβριδικά τροχιακά, τα οποία είναι ισότιµα µεταξύ τους και προκύπτει η παρακάτω ηλεκτρονιακή δοµή: (Υβριδισµός sp 3 ) Συνεπώς, στο µόριο του CH 4 υπάρχουν τέσσερις ισότιµοι σ δεσµοί που σχηµατίζονται µε επικάλυψη των sp 3 υβριδικών τροχιακών του C, µε τα τέσσερα s ατοµικά τροχιακά των ατόµων του H. εσµοί µεταξύ ατόµων άνθρακα: Μεταξύ δύο ατόµων άνθρακα µπορεί να σχηµατιστεί απλός, διπλός ή τριπλός δεσµός. Ανάλογα µε το είδος του δεσµού που συµµετέχει ο άνθρακας, έχει διαφορετικό υβριδισµό.
10 264. Τρίτο Κεφάλαιο - 11 ο Μάθηµα Απλός δεσµός µεταξύ ατόµων άνθρακα (C C): Tα άτοµα του άνθρακα που συµµετέχουν µόνο σε απλούς δεσµούς, έχουν sp 3 υβριδισµό, για αυτό ο απλός δεσµός µεταξύ ατόµων άνθρακα είναι ένας σ δεσµός του τύπου sp 3 sp 3. Άρα, στα αλκάνια, όλα τα άτοµα του άνθρακα έχουν sp 3 υβριδισµό. Παράδειγµα: Ερµηνεία των δεσµών στο µόριο του αιθανίου (C 2 H 6 ): Oι ηλεκτρονιακές δοµές των C, H στη θεµελιώδη κατάσταση είναι: (Θεµελιώδης κατάσταση) Ένα από τα δύο ηλεκτρόνια του 2s ατοµικού τροχιακού του C προωθείται σε τροχιακό 2p και προκύπτει η προωθηµένη κατάσταση του C: (Προωθηµένη κατάσταση) Στο άτοµο του C τα 2s και 2p τροχιακά συνδυάζονται και δηµιουργούν τέσσερα sp 3 υβριδικά τροχιακά, τα οποία είναι ισότιµα µεταξύ τους και προκύπτει η παρακάτω ηλεκτρονιακή δοµή: (Υβριδισµός sp 3 ) Συνεπώς, στο µόριο του C 2 H 6 υπάρχουν: Έξι σ δεσµοί του τύπου (sp 3 s) µεταξύ ατόµων άνθρακα και υδρογόνου. Ένας σ δεσµός του τύπου (sp 3 sp 3 ) µεταξύ των ατόµων του άνθρακα. ιπλός δεσµός µεταξύ ατόµων άνθρακα (C = C): Tα άτοµα του άνθρακα που συµµετέχουν σε διπλούς δεσµούς, έχουν sp 2 υβριδισµό. Ο διπλός δεσµός µεταξύ ατόµων άνθρακα αποτελείται από ένα σ δεσµό του τύπου sp 2 sp 2 και ένα π δεσµό του τύπου p p. Επειδή ο σ δεσµός είναι ισχυρότερος του π δεσµού, είναι σχετικά εύκολο ο διπλός δεσµός να σπάσει και να γίνει απλός. Άρα, όλα τα άτοµα του άνθρακα που συµµετέχουν σε διπλό δεσµό στο µόριο της οργανικής ένωσης (C = C, C = O) έχουν sp 2 υβριδισµό. Παράδειγµα: Ερµηνεία των δεσµών στο µόριο του αιθενίου (C 2 H 4 ):
11 Θεωρία δεσµού σθένους - Υβριδισµός 265. Oι ηλεκτρονιακές δοµές των C, H στη θεµελιώδη κατάσταση είναι: (Θεµελιώδης κατάσταση) Ένα από τα δύο ηλεκτρόνια του 2s ατοµικού τροχιακού του C προωθείται σε τροχιακό 2p και προκύπτει η προωθηµένη κατάσταση του C: (Προωθηµένη κατάσταση) Στο άτοµο του C το 2s και δύο από τα τρία 2p τροχιακά συνδυάζονται και δηµιουργούν τρία sp 2 υβριδικά τροχιακά, το p ατοµικό τροχιακό που παραµένει είναι προσανατολισµένο κάθετα προς το επίπεδο των υβριδικών τροχιακών. (Υβριδισµός sp 2 ) Συνεπώς, στο µόριο του C 2 H 4 υπάρχουν: Tέσσερις σ δεσµοί του τύπου (sp 2 s) µεταξύ ατόµων άνθρακα και υδρογόνου. Ένας σ δεσµός του τύπου (sp 2 sp 2 ) και ένας π δεσµός του τύπου (p p) µεταξύ των ατόµων του άνθρακα. Οι δύο αυτοί δεσµοί δηµιουργούν τον διπλό δεσµό. Τριπλός δεσµός µεταξύ ατόµων άνθρακα (C C): Tα άτοµα του άνθρακα που συµµετέχουν σε τριπλούς δεσµούς, έχουν sp υβριδισµό. Ο τριπλός δεσµός µεταξύ ατόµων άνθρακα αποτελείται από ένα σ δεσµό του τύπου sp sp και δύο π δεσµούς του τύπου p p. Επειδή ο σ δεσµός είναι ισχυρότερος του π δεσµού, είναι σχετικά εύκολο ο τριπλός δεσµός να σπάσει και να γίνει αρχικά διπλός και στη συνέχεια απλός. Άρα, όλα τα άτοµα του άνθρακα που συµµετέχουν σε τριπλό δεσµό στο µόριο της οργανικής ένωσης (C C, C Ν) έχουν sp υβριδισµό. Παράδειγµα: Ερµηνεία των δεσµών στο µόριο του αιθινίου (C 2 H 2 ): Oι ηλεκτρονιακές δοµές των C, H στη θεµελιώδη κατάσταση είναι: (Θεµελιώδης κατάσταση)
12 266. Τρίτο Κεφάλαιο - 11 ο Μάθηµα Ένα από τα δύο ηλεκτρόνια του 2s ατοµικού τροχιακού του C προωθείται σε τροχιακό 2p και προκύπτει η προωθηµένη κατάσταση του C: (Προωθηµένη κατάσταση) Στο άτοµο του C το 2s και ένα από τα τρία 2p τροχιακά συνδυάζονται και δηµιουργούν τρία sp υβριδικά τροχιακά, τα δύο p ατοµικά τροχιακά που παραµένουνέχουν από ένα µονήρες ηλεκτρόνιο. (Υβριδισµός sp 2 ) Συνεπώς, στο µόριο του C 2 H 2 υπάρχουν: ύο σ δεσµοί του τύπου (sp s) µεταξύ ατόµων άνθρακα και υδρογόνου. Ένας σ δεσµός του τύπου (sp sp) και δύο π δεσµοί του τύπου (p p) µεταξύ των ατόµων του άνθρακα. Οι τρείς αυτοί δεσµοί δηµιουργούν τον τριπλό δεσµό. Παρατήρηση: Η ισχύς των δεσµών µεταξύ ατόµων άνθρακα είναι: C C < C = C < C C Όµως όσο ισχυρότερος είναι ένας δεσµός, τόσο µικρότερο είναι το µήκος του. Παρακάτω φαίνεται ο υβριδισµός των ατόµων του άνθρακα και το µήκος των παραπάνω δεσµών: C C sp pm C = C sp pm C C sp 120 pm
13 Θεωρία δεσµού σθένους - Υβριδισµός 267. Β. ΜΕΘΟ ΟΛΟΓΙΑ ΑΣΚΗΣΕΩΝ Κατηγορία Μέθοδος 1 Ασκήσεις όπου πρέπει να βρούµε το είδος των δεσµών και τον υβριδισµό των ατόµων του άνθρακα, σε ένα µόριο οργανικής ένωσης: Αρχικά γράφουµε το συντακτικό τύπο της οργανικής ένωσης. Για να βρούµε το είδος των δεσµών, εργαζόµαστε µε βάση το γεγονός ότι: α. Ο απλός δεσµός αποτελείται από ένα σ δεσµό. β. Ο διπλός δεσµός αποτελείται από ένα σ και ένα π δεσµό. γ. Ο τριπλός δεσµός αποτελείται από ένα σ και δύο π δεσµούς. Για να βρούµε τον υβριδισµό των ατόµων του C, εργαζόµαστε µε βάση το γεγονός ότι: α. Άτοµο άνθρακα που συµµετέχει µόνο σε απλούς δεσµούς, έχει sp 3 υβριδισµό. β. Άτοµο άνθρακα που συµµετέχει σε διπλό δεσµό, έχει sp 2 υβριδισµό. γ. Άτοµο άνθρακα που συµµετέχει σε τριπλό δεσµό, έχει sp υβριδισµό. Παράδειγµα 1: ίνεται η οργανική ένωση CH 2 =CH-C CH της οποίας τα άτοµα αριθµούνται από 1 έως 4, όπως φαίνεται παραπάνω. α. Πόσοι δεσµοί σ και πόσοι δεσµοί π υπάρχουν στην ένωση; β. Μεταξύ ποιών ατόµων σχηµατίζονται π δεσµοί; γ. Να αναφέρετε τι είδος υβριδικά τροχιακά έχει κάθε άτοµο άνθρακα της ένωσης. (Εξετάσεις 2002) Λύση: Στο µόριο της ένωσης υπάρχουν: Τέσσερις δεσµοί σ µεταξύ ατόµων άνθρακα και υδρογόνου. Τρείς δεσµοί σ µεταξύ των ατόµων του άνθρακα. Ένας δεσµός π µεταξύ των άνθρακα 3 και άνθρακα 4, γιατί συνδέονται µε διπλό δεσµό. ύο δεσµοί π µεταξύ των άνθρακα 1 και άνθρακα 2, γιατί συνδέονται µε τριπλό δεσµό. α. Άρα, στο µόριο της ένωσης υπάρχουν 7 δεσµοί σ και 3 δεσµοί π. β. Οι δεσµοί π σχηµατίζονται µεταξύ των άνθρακα 3 άνθρακα 4 και άνθρακα 1 άνθρακα 2. γ. Ο άνθρακας 1 συµµετέχει σε τριπλό δεσµό, άρα έχει sp υβριδικά τροχιακά. Ο άνθρακας 2 συµµετέχει σε τριπλό δεσµό, άρα έχει sp υβριδικά τροχιακά. Ο άνθρακας 3 συµµετέχει σε διπλό δεσµό, άρα έχει sp 2 υβριδικά τροχιακά. Ο άνθρακας 4 συµµετέχει σε διπλό δεσµό, άρα έχει sp 2 υβριδικά τροχιακά.
14 268. Τρίτο Κεφάλαιο - 11 ο Μάθηµα Γ. ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ Nα περιγράψετε τους δεσµούς στο µόριο CH3 C N. ίνονται οι ατοµικοί αριθµοί: Η = 1, C = 6, N = 7. Λύση: Oι ηλεκτρονιακές δοµές των C, H και Ν, στη θεµελιώδη κατάσταση είναι: Το άτοµο άνθρακα 2 συµµετέχει µόνο σε απλούς δεσµούς, συνεπώς έχει sp 3 υβριδισµό. Οι ηλεκτρονιακές του δοµές στην προωθηµένη κατάσταση και στον υβριδισµό, φαίνονται παρακάτω: (προωθηµένη κατάσταση) (υβριδισµός) Άρα, οι δεσµοί του ατόµου του άνθρακα 2 µε τα άτοµα του υδρογόνου είναι δεσµοί σ της µορφής (sp 3 s). Το άτοµο άνθρακα 1 συµµετέχει σε τριπλό δεσµό, συνεπώς έχει sp υβριδισµό. Οι ηλεκτρονιακές του δοµές στην προωθηµένη κατάσταση και στον υβριδισµό, φαίνονται παρακάτω: (προωθηµένη κατάσταση) (υβριδισµός) Άρα: Ο δεσµός του άνθρακα 1 µε τον άνθρακα 2 είναι δεσµός σ της µορφής (sp sp 3 ). O τριπλός δεσµός µεταξύ του άνθρακα 1 και του αζώτου αποτελείται από ένα δεσµό σ της µορφής (sp p) και δύο δεσµούς π της µορφής (p p) Nα περιγράψετε τους δεσµούς στο µόριο CH C CH. ίνονται οι ατοµικοί αριθµοί: Η = 1, C = 6, O = Λύση: Oι ηλεκτρονιακές δοµές των C, H και O, στη θεµελιώδη κατάσταση είναι: O Τα άτοµα του άνθρακα 1 και 3 συµµετέχουν µόνο σε απλούς δεσµούς, συνεπώς έχουν sp 3 υβριδισµό. Οι ηλεκτρονιακές τους δοµές στην προωθηµένη κατάσταση και στον υβριδισµό, φαίνονται παρακάτω: (προωθηµένη κατάσταση) (υβριδισµός)
15 Θεωρία δεσµού σθένους - Υβριδισµός 269. Άρα, οι δεσµοί των ατόµων του άνθρακα 1 και 3 µε τα άτοµα του υδρογόνου είναι δεσµοί σ της µορφής (sp 3 s). Το άτοµο άνθρακα 2 συµµετέχει σε διπλό δεσµό, συνεπώς έχει sp 2 υβριδισµό. Οι ηλεκτρονιακές του δοµές στην προωθηµένη κατάσταση και στον υβριδισµό, φαίνονται παρακάτω: (προωθηµένη κατάσταση) (υβριδισµός) Άρα: Οι δεσµοί του άνθρακα 2 µε τους άνθρακες 1 και 3, είναι δεσµοί σ της µορφής (sp 2 sp 3 ). O διπλός δεσµός µεταξύ του άνθρακα 2 και του οξυγόνου αποτελείται από ένα δεσµό σ της µορφής (sp 2 p) και ένα δεσµό π της µορφής (p p). 3. Nα περιγράψετε τους δεσµούς στο µόριο ΗCOOH. ίνονται οι ατοµικοί αριθµοί: Η = 1, C = 6, O = 8. Λύση: O συντακτικός τύπος της ένωσης είναι: H C O H O Oι ηλεκτρονιακές δοµές των C, H και O, στη θεµελιώδη κατάσταση είναι: Το άτοµο του άνθρακα συµµετέχει σε διπλό δεσµό, συνεπώς έχει sp 2 υβριδισµό. Οι ηλεκτρονιακές του δοµές στην προωθηµένη κατάσταση και στον υβριδισµό, φαίνονται παρακάτω: (προωθηµένη κατάσταση) (υβριδισµός) Άρα: Ο δεσµός του άνθρακα µε το υδρογόνο είναι δεσµός σ της µορφής (sp 2 s). Ο διπλός δεσµός του άνθρακα µε το οξυγόνο αποτελείται από ένα δεσµό σ της µορφής (sp 2 p) και ένα δεσµό π της µορφής (p p). Ο απλός δεσµός του άνθρακα µε το οξυγόνο είναι δεσµός σ της µορφής (sp 2 p). Ο απλός δεσµός του οξυγόνου µε το υδρογόνο είναι δεσµός σ της µορφής (p s).
16 270. Τρίτο Κεφάλαιο - 11 ο Μάθηµα. ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ Ερωτήσεις Σύντοµης απάντησης: 1. Ποιες είναι οι κυριότερες κβαντοµηχανικές θεωρίες περιγραφής του οµοιοπολικού δεσµού; 2. Να αναφέρετε τα κύρια σηµεία της θεωρίας δεσµού σθένους. 3. Με ποιες επικαλύψεις προκύπτει σ δεσµός; 4. Τι ονοµάζουµε µήκος δεσµού; 5. Με ποιες επικαλύψεις προκύπτει π δεσµός; 6. Γιατί ο δεσµός σ είναι ισχυρότερος του δεσµού π; 7. Που βρίσκεται η µέγιστη ηλεκτρονιακή πυκνότητα σε ένα δεσµό σ και που σε ένα δεσµό π; 8. Τι είναι ο υβριδισµός; 9. Τι σχήµα έχουν τα υβριδικά τροχιακά; 10. Από τον συνδυασµό ποιων ατοµικών τροχιακών δηµιουργούνται τα sp υβριδικά τροχιακά και τί διάταξη έχουν; 11. Από τον συνδυασµό ποιων ατοµικών τροχιακών δηµιουργούνται τα sp 2 υβριδικά τροχιακά και τί διάταξη έχουν; 12. Από τον συνδυασµό ποιων ατοµικών τροχιακών δηµιουργούνται τα sp 3 υβριδικά τροχιακά και τί διάταξη έχουν; 13. Τι είδους υβριδισµό έχει το άτοµο του άνθρακα όταν συµµετέχει: α. Μόνο σε απλούς δεσµούς. β. Σε διπλό δεσµό. γ. Σε τριπλό δεσµο. 14. Τι γνωρίζετε για την ισχύ και το µήκος του απλού, διπλού και τριπλού δεσµού µεταξύ των ατόµων του άνθρακα; 15. Ποια η γωνία µεταξύ των υβριδικών τροχιακών sp, sp 2, sp 3 ενός ατόµου; Συµπλήρωσης κενών: 1. Σύµφωνα µε τη θεωρία δεσµού σθένους, κατά τον σχηµατισµό... δεσµού ανάµεσα σε δύο άτοµα, γίνεται... ανάµεσα σε τροχιακά της στιβάδας σθένους των δύο ατόµων. Όσο µεγαλύτερος είναι ο βαθµός... µεταξύ των ατοµικών τροχιακών, τόσο... είναι ο δεσµός που σχηµατίζεται. Οι δεσµοί που σχηµατίζονται σύµφωνα µε τη θεωρία αυτή χαρακτηρίζονται ως ή Οι σ δεσµοί προκύπτουν µε επικαλύψεις......, και ατοµικών τροχιακών, κατά τον άξονα που συνδέει τους... των δύο ατόµων που συνδέονται. Η ευθεία που ενώνει τους πυρήνες των δύο ατόµων, ονοµάζεται... του δεσµού και συµπίπτει µε τους άξονες... των τροχιακών που επικα-
17 Θεωρία δεσµού σθένους - Υβριδισµός 271. λύπτονται. Κατά τη δηµιουργία του σ δεσµού, οι πυρήνες των ατόµων βρίσκονται σε απόσταση τέτοια ώστε η ενέργεια του συστήµατος να είναι ελάχιστη. Η απόσταση αυτή ονοµάζεται... δεσµού. 3. Οι π δεσµοί προκύπτουν µε... επικαλύψεις p p ατοµικών τροχιακών, των οποίων οι άξονες είναι... Στον π δεσµό, οι άξονες των τροχιακών που επικαλύπτονται, είναι... στον άξονα του δεσµού και η πυκνότητα του ηλεκτρονιακού νέφους είναι... εκατέρωθεν του άξονα και... πάνω στον άξονα. Στον π δεσµό η επικάλυψη είναι µικρότερη από ότι στον σ δεσµό, για αυτό ο σ δεσµός είναι... του π δεσµού. Στα... τροχιακά, είναι αδύνατη η πλευρική επικάλυψη, για αυτό δε συµµετέχουν σε π δεσµούς. 4. Στο µόριο του C 2 H 6 υπάρχουν... σ δεσµοί του τύπου (......) µεταξύ ατόµων άνθρακα και υδρογόνου και ένας... δεσµός του τύπου (......) µεταξύ των ατόµων του άνθρακα. 5. Στο µόριο του C 2 H 4 υπάρχουν... σ δεσµοί του τύπου (......) µεταξύ ατόµων άνθρακα και υδρογόνου, ένας σ δεσµός του τύπου (......) και ένας π δεσµός του τύπου (......) µεταξύ των ατόµων του άνθρακα. Οι δύο αυτοί δεσµοί δηµιουργούν τον... δεσµό. 6. Στο µόριο του C 2 H 2 υπάρχουν... σ δεσµοί του τύπου (......) µεταξύ ατόµων άνθρακα και υδρογόνου, ένας σ δεσµός του τύπου (......) και... π δεσµοί του τύπου (......) µεταξύ των ατόµων του άνθρακα. Οι τρείς αυτοί δεσµοί δηµιουργούν τον... δεσµό. Σωστό - Λάθος: Ποιες από τις παρακάτω προτάσεις είναι σωστές (Σ) και ποιες λάθος (Λ); 1. Ο σ δεσµός σχηµατίζεται µόνο µε επικάλυψη s τροχιακών. ( ) 2. Κατά την επικάλυψη δύο p ατοµικών τροχιακών κατά τον άξονα που συνδέει τους πυρήνες των δύο ατόµων, σχηµατίζεται σ δεσµός. ( ) 3. Ο σ δεσµός έχει κυλινδρική συµµετρία ως προς τον άξονα του δεσµού. ( ) 4. Στο σ δεσµό ο άξονας του δεσµού συµπίπτει µε τους άξονες συµµετρίας των τροχιακών που επικαλύπτονται. ( ) 5. Στον π δεσµό, η πυκνότητα του ηλεκτρονιακού νέφους είναι µέγιστη στο χώρο που βρίσκεται µεταξύ των πυρήνων. ( ) 6. Μήκος δεσµού είναι η απόσταση µεταξύ των πυρήνων όπου έχουµε τη µέγιστη ενέργεια. ( ) 7. Ο π δεσµός είναι ισχυρότερος του σ δεσµού. ( ) 8. Ο µόνος τρόπος σχηµατισµού οµοιοπολικού δεσµού είναι µε επικάλυψη ατο- µικών τροχιακών. ( ) 9. Τα υβριδικά τροχιακά δηµιουργούνται µε γραµµικό συνδυασµό ατοµικών τροχιακών διαφορετικών ατόµων. ( ) 10. Τα υβριδικά τροχιακά έχουν σχήµα οµοαξονικών αλλά άνισου µεγέθους λοβών. ( )
18 272. Τρίτο Κεφάλαιο - 11 ο Μάθηµα 11. Τα υβριδικά τροχιακά είναι αριθµιτικά ίσα µε τα ατοµικά τροχιακά που συνδυάζονται για το σχηµατισµό τους. ( ) 12. Στο µόριο του µεθανίου (CH 4 ): α. Το άτοµο του άνθρακα έχει sp υβριδισµό. ( ) β. Όλοι οι δεσµοί µεταξύ άνθρακα και υδρογόνου είναι ισότιµοι. ( ) γ. Το σχήµα του µορίου είναι τετραεδρικό. ( ) 13. Στο µόριο του φθοριούχου βορίου (ΒF 3 ): α. Το άτοµο του B έχει sp 2 υβριδισµό. ( ) β. Όλοι οι δεσµοί µεταξύ βορίου και φθορίου είναι ισότιµοι. ( ) γ. Οι σ δεσµοί είναι του τύπου (sp 2 p). ( ) 14. Στο µόριο του αιθενίου (C 2 H 4 ): α. Τα άτοµα του C έχουν sp 2 υβριδισµό. ( ) β. Υπάρχουν πέντε σ δεσµοί. ( ) γ. Υπάρχουν δύο π δεσµοί. ( ) 15. Στο µόριο του αιθινίου (C 2 H 2 ): α. Τα άτοµα του C έχουν sp 3 υβριδισµό. ( ) β. Υπάρχουν τρεις σ δεσµοί. ( ) γ. Υπάρχουν δύο π δεσµοί. ( ) δ. Όλα τα άτοµα βρίσκονται στην ίδια ευθεία. ( ) Πολλαπλής επιλογής: 1. Το άτοµο του άνθρακα έχει sp 3 υβριδισµό, στο µόριο του: α. CO 2 β. HCH=O γ. CH 2 Cl 2 δ. C 2 H 4 2. Στο µόριο του CH 2 = CHCH = CH 2 υπάρχουν: α. 11 δεσµοί σ β. 8 δεσµοί σ και 3 δεσµοί π γ. 9 δεσµοί σ και 2 δεσµοί π δ. 7 δεσµοί σ και 4 δεσµοί π 3. Μικρότερη απόσταση µεταξύ των ατόµων του άνθρακα έχουµε στο µόριο του: α. C 2 H 6 β. C 2 H 4 γ. C 2 H 2 4. H γωνία µεταξύ των sp 2 υβριδικών τροχιακών του ατόµου του άνθρακα είναι: α. 90 ο β. 120 ο γ. 150 ο δ. 180 ο 5. Ο σ δεσµός στο µόριο του BeF 2 είναι του τύπου: α. s s β. s p γ. sp p δ. sp 2 p 6. H διάταξη των ατόµων στο µόριο του BF 3 είναι: α. γραµµική β. επίπεδη τριγωνική γ. τετραεδρική
19 Θεωρία δεσµού σθένους - Υβριδισµός Στο µόριο του CH 2 = CHCl υπάρχουν: α. 5 δεσµοί σ και 1 δεσµός π β. 4 δεσµοί σ και 2 δεσµοί π γ. 3 δεσµοί σ και 3 δεσµοί π δ. 6 δεσµοί σ 8. Στο µόριο του CH 2 = CHC CCH 3 υπάρχουν: α. 2 άτοµα C µε sp 2 υβριδισµό, 2 άτοµα C µε sp υβριδισµό και 1 άτοµο C µε sp 3 υβριδισµό. β. 3 άτοµα C µε sp 2 υβριδισµό, 1 άτοµο C µε sp υβριδισµό και 1 άτοµο C µε sp 3 υβριδισµό. γ. 1άτοµο C µε sp 2 υβριδισµό, 1 άτοµο C µε sp υβριδισµό και 3 άτοµα C µε sp 3 υβριδισµό. δ. 1 άτοµο C µε sp 2 υβριδισµό, 2 άτοµα C µε sp υβριδισµό και 2 άτοµα C µε sp 3 υβριδισµό. Αντιστοίχισης: 1. Αντιστοιχίστε τους µοριακούς τύπους στη στήλη Α µε τον αριθµό και τα είδη των δεσµών που αναφέρονται στη στήλη Β: Στήλη Α Στήλη Β 1. Ο 2 2. Ν 2 3. CH 2 FCl 4. HCN 5. C 3 H 4 α. 6 σ δεσµοί, 2 π δεσµοί β. 1 σ δεσµός, 1 π δεσµός γ. 4 σ δεσµοί δ. 1 σ δεσµός, 2 π δεσµοί ε. 2 σ δεσµοί, 2 π δεσµοί 2. Αντιστοιχίστε τους µοριακούς τύπους στη στήλη Α µε το είδος του υβριδισµού του ατό- µου του άνθρακα που αναφέρεται στη στήλη Β: Στήλη Α Στήλη Β 1. C 4 H C 2 H 2 3. CO 2 4. CHCl = CH 2 5. HCH = O α. sp β. sp 2 γ. sp 3 3. Αντιστοιχίστε τα µόρια της στήλης Α µε τη διάταξη των ατόµων που αναφέρονται στη στήλη Β: Στήλη Α Στήλη Β 1. ΒeF 2 2. BF 3 3. CH 4 4. C 2 H 2 α. γραµµική διάταξη β. επίπεδη τριγωνική διάταξη γ. τετραεδρική διάταξη
20 274. Τρίτο Κεφάλαιο - 11 ο Μάθηµα Ασκήσεις - Προβλήµατα 1. Nα περιγράψετε τους δεσµούς στα µόρια: α. C 3 H 8 β. CH 2 = C = CH 2 γ. CH 3 C CH δ. CH CCH = CH 2 ίνονται οι ατοµικοί αριθµοί: Η = 1, C = 6 (Απ. α. 10 δεσµοί σ β. 6 δεσµοί σ, 2 δεσµοί π γ. 6 δεσµοί σ, 2 δεσµοί π δ. 7 δεσµοί σ, 3 δεσµοί π) 2. Nα περιγράψετε τους δεσµούς στα µόρια: α. C 2 H 5 Cl β. CH 3 CH CN γ. CH 3 CH 2 OH δ. CH 3 OCH 3 CH 3 ίνονται οι ατοµικοί αριθµοί: Η = 1, C = 6, O = 8, N = 7, Cl = 17. (Απ. α. 7 δεσµοί σ β. 11 δεσµοί σ, 2 δεσµοί π γ. 8 δεσµοί σ δ. 8 δεσµοί σ) 3. Nα περιγράψετε τους δεσµούς στα µόρια: α. CH 3 COOH β. CH 2 ClCH = O γ. CH 3 CH 2 NH 2 δ. CH 3 COCH 3 ίνονται οι ατοµικοί αριθµοί: Η = 1, C = 6, O = 8, N = 7, Cl = 17. (Απ. α. 7 δεσµοί σ, 1 δεσµός π β. 6 δεσµοί σ, 1 δεσµός π γ. 9 δεσµοί σ δ. 8 δεσµοί σ, 1 δεσµός π) Ε. ΤΟ ΞΕΧΩΡΙΣΤΟ ΘΕΜΑ Τα χηµικά στοιχεία X, Ψ ανήκουν στην δεύτερη περίοδο του περιοδικού πίνακα και έχουν στην εξωτερική τους στιβάδα 6 και 7 ηλεκτρόνια αντίστοιχα. α. Να βρείτε τον ατοµικό αριθµό και την οµάδα στην οποία ανήκουν τα Χ και Ψ. β. Ποιο από τα δύο στοιχεία µπορεί να σχηµατίσει π δεσµούς; γ. Να περιγράψετε τους δεσµούς στο µόριο της οργανικής ένωσης: CH 2 ΨCH = Χ (Aπ. α. Χ: Ζ = 8, 16η οµάδα, Ψ: Ζ = 9, 17η οµάδα β. το Χ δ. 6 δεσµοί σ, 1 δεσµός π)
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός Βύρωνας, 2015 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία. Δ. Παπαδόπουλος, χημικός
 7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
7 ο Κεφάλαιο Οργανική Χημεία Δ. Παπαδόπουλος, χημικός ΓΕΛ Καρέα, 2018 Θεωρίες ερμηνείας του ομοιοπολικού δεσμού με βάση την κβαντική θεωρία. Θεωρία δεσμού σθένους. Θεωρία των μοριακών τροχιακών. Κάθε θεωρία
ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ
 ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
ΕΡΜΗΝΕΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΧΗΜΙΚΩΝ ΕΣΜΩΝ ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΘΕΩΡΙΑ ΜΟΡΙΑΚΩΝ ΤΡΟΧΙΑΚΩΝ ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ 1. Κατά την ανάπτυξη ομοιοπολικού δεσμού ανάμεσα σε δύο άτομα, τροχιακά της στιβάδας σθένους του
ΥΒΡΙ ΙΣΜΟΣ υβριδισµός
 ΥΒΡΙ ΙΣΜΟΣ Οσχηµατισµός δεσµών µε απλή επικάλυψη ατοµικών τροχιακών, σε πολλές περιπτώσεις, αδυνατεί να ερµηνεύσει τη δοµή των µορίων, όπως π.χ. των οργανικών ενώσεων. Μια προωθηµένη αντίληψη για την ερµηνεία
ΥΒΡΙ ΙΣΜΟΣ Οσχηµατισµός δεσµών µε απλή επικάλυψη ατοµικών τροχιακών, σε πολλές περιπτώσεις, αδυνατεί να ερµηνεύσει τη δοµή των µορίων, όπως π.χ. των οργανικών ενώσεων. Μια προωθηµένη αντίληψη για την ερµηνεία
Οργανική Χημεία 24 4
 Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
Οργανική Χημεία 24 4 5. ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Οι κυριότερες από τις διαφορετικές κβαντομηχανικές
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΘΕΩΡΙΑ ΤΟΥ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ - ΥΒΡΙΔΙΣΜΟΣ ΑΠΑΝΤΗΣΕΙΣ ΕΡΩΤΗΣΕΩΝ
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΘΕΩΡΙΑ ΤΟΥ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ - ΥΒΡΙΔΙΣΜΟΣ ΑΠΑΝΤΗΣΕΙΣ ΕΡΩΤΗΣΕΩΝ 7.2 Ποιες από τις προτάσεις είναι σωστές και ποιες λάθος ; α) Λ β) Σ γ) Λ 7.3 Όχι. Θα πρέπει τα ατομικά τροχιακά που θα επικαλυφθούν,
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΘΕΩΡΙΑ ΤΟΥ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ - ΥΒΡΙΔΙΣΜΟΣ ΑΠΑΝΤΗΣΕΙΣ ΕΡΩΤΗΣΕΩΝ 7.2 Ποιες από τις προτάσεις είναι σωστές και ποιες λάθος ; α) Λ β) Σ γ) Λ 7.3 Όχι. Θα πρέπει τα ατομικά τροχιακά που θα επικαλυφθούν,
Γεωμετρία Μορίων Θεωρία VSEPR
 Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Γεωμετρία Μορίων Θεωρία VSEPR Μεθοδολογία για την πρόβλεψη της μοριακής γεωμετρία: Γράφουμε τον ηλεκτρονιακό τύπο κατά Lewis. Μετρούμε το συνολικό
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΕΣΜΟΥ
 ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
ΧΗΜΙΚΟΣ ΕΣΜΟΣ ΙΙ : ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΘΕΩΡΗΣΗ ΤΟΥ ΟΜΟΙΟΠΟΛΙΚΟΥ Ή ΟΜΟΣΘΕΝΟΥΣ ΕΣΜΟΥ Παππάς Χρήστος Επίκουρος Καθηγητής Το μόριο του Η 2 Σύμφωνα με τη θεωρία του Lewis στο μόριο του Η 2 τα άτομα συγκρατούνται
Ομοιοπολικός εσμός Θεωρία Lewis
 Ομοιοπολικός εσμός Θεωρία Lewis Oμοιοπολικός δεσμός: αμοιβαία συνεισφορά ηλεκτρονίων σθένους κοινά ζεύγη ηλεκτρονίων δομή ευγενούς αερίου (κανόνας της οκτάδας) Πλεονεκτήματα: η πληρέστερη προ-κβαντική
Ομοιοπολικός εσμός Θεωρία Lewis Oμοιοπολικός δεσμός: αμοιβαία συνεισφορά ηλεκτρονίων σθένους κοινά ζεύγη ηλεκτρονίων δομή ευγενούς αερίου (κανόνας της οκτάδας) Πλεονεκτήματα: η πληρέστερη προ-κβαντική
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C;
 Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Γιατί ο σχηματισμός του CΗ 4 δεν μπορεί να ερμηνευθεί βάσει της διεγερμένης κατάστασης του ατόμου C; 1. Οι 4 ομοιοπολικοί δεσμοί στο μεθάνιο θα ήταν δύο τύπων: ένας δεσμός από την επικάλυψη του τροχιακού
Ασκήσεις. Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3
 Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
Ασκήσεις Γράψτε μια δομή Lewis για καθένα από τα παρακάτω μόρια και βρείτε τα τυπικά φορτία των ατόμων. (α) CΟ (β) ΗΝO 3 (γ) ClΟ 3 (δ) ΡΟCl 3 Γεωμετρία Μορίων Θεωρία VSEPR Μοριακή γεωμετρία: είναι η διάταξη
ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ (Valence bond theory) Οιβασικές αρχές της θεωρίας δεσµού σθένους είναι:
 ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ (Valence bond theory) Οιβασικές αρχές της θεωρίας δεσµού σθένους είναι: Κατάτην ανάπτυξη οµοιοπολικού δεσµού ανάµεσα σε δύο άτοµα, τροχιακά της στιβάδας σθένους του ενός ατόµου επικαλύπτουν
ΘΕΩΡΙΑ ΕΣΜΟΥ ΣΘΕΝΟΥΣ (Valence bond theory) Οιβασικές αρχές της θεωρίας δεσµού σθένους είναι: Κατάτην ανάπτυξη οµοιοπολικού δεσµού ανάµεσα σε δύο άτοµα, τροχιακά της στιβάδας σθένους του ενός ατόµου επικαλύπτουν
ΘΕΩΡΙΑ ΤΟΥ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΥΒΡΙΔΙΣΜΟΣ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ
 ΘΕΩΡΙΑ ΤΟΥ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΥΒΡΙΔΙΣΜΟΣ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 2000. 1.1 Να βρείτε ποιο από τα ακόλουθα σύνολα δεσμών, αντιστοιχεί στο μόριο του CH 3-C C-CH 3. α. 3σ, 1π β. 8σ, 1π
ΘΕΩΡΙΑ ΤΟΥ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΥΒΡΙΔΙΣΜΟΣ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 2000. 1.1 Να βρείτε ποιο από τα ακόλουθα σύνολα δεσμών, αντιστοιχεί στο μόριο του CH 3-C C-CH 3. α. 3σ, 1π β. 8σ, 1π
Οργανική Χημεία. Κεφάλαιο 1: Δομή και δεσμοί
 Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
Οργανική Χημεία Κεφάλαιο 1: Δομή και δεσμοί 1. Οργανική χημεία Οργανικές ενώσεις μέχριτομισότου1800 αναφέρονταν σε ενώσεις από ζωντανούς οργανισμούς Wöhler το 1828 έδειξε ότι η ουρία, μία οργανική ένωση,
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού
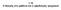 1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
1.15 Ο δεσμός στο μεθάνιο και ο υβριδισμός τροχιακού Η δομή του Μεθανίου τετραεδρική γωνίες δεσμού = 109.5 Μήκη δεσμού = 110 pm αλλά η δομή εμφανίζεται ασυνεπής με την ηλεκτρονική διάταξη του άνθρακα Η
) σχηματίζονται : α. Ένας σ και δύο π δεσμοί β. Τρεις σ δεσμοί γ. Ένας π και δύο σ δεσμοί δ. Τρεις π δεσμοί.
 ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
ΘΕΜΑΤΑ Θγ 1 0 ΚΕΦΑΛΑΙΟ 1.1. Σε ένα πολυηλεκτρονιακό άτομο ο μέγιστος αριθμός ηλεκτρονίων με κβαντικούς αριθμούς n= και m s = -½ είναι : α. οκτώ β. τέσσερα γ. δύο δ. ένα 1.. Από τα επόμενα χημικά στοιχεία
Μάθημα 22 ο. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 22 ο Θεωρία Δεσμού Σθένους- Υβριδισμός Linus Pauling Έγραψε τη μονογραφία : Nature of the chemical bond Τιμήθηκε για το έργο του με το βραβείο Nobel το 1954 Εισήγαγε την ιδέα του υβριδισμού Υβριδισμένα
Μάθημα 22 ο Θεωρία Δεσμού Σθένους- Υβριδισμός Linus Pauling Έγραψε τη μονογραφία : Nature of the chemical bond Τιμήθηκε για το έργο του με το βραβείο Nobel το 1954 Εισήγαγε την ιδέα του υβριδισμού Υβριδισμένα
Μοριακά Πρότυπα (Μοντέλα)
 Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
Μοριακά Πρότυπα (Μοντέλα) ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ 1. ΟΜΕΣ LEWIS - ΤΥΠΙΚΟ ΦΟΡΤΙΟ (ΚΕΦ. 9.6, 9.9) 2. ΜΟΡΙΑΚΗ ΓΕΩΜΕΤΡΙΑ - ΤΟ ΜΟΝΤΕΛΟ VSEPR (ΚΕΦ. 10.1) 3. ΥΒΡΙ ΙΣΜΟΣ ΑΤΟΜΙΚΩΝ ΤΡΟΧΙΑΚΩΝ (ΚΕΦ. 10.3) Αναγραφή τύπων
Μάθημα 21 ο. Το σχήμα των μορίων. Θεωρία VSEPR. Θεωρία Δεσμού Σθένους- Υβριδισμός
 Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
Μάθημα 21 ο Το σχήμα των μορίων Θεωρία VSEPR Θεωρία Δεσμού Σθένους- Υβριδισμός Συμβολισμός A = Κεντρικό άτομο X = Συναρμοτής E = Μονήρες ζεύγος SN: Στερεοχημικός αριθμός Γενική και Ανόργανη Χημεία 2016-17
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ. 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο. Θεωρία δεσμού σθένους (Valence bond theory)
 ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Για την περιγραφή του ομοιοπολικού δεσμού έχουν διατυπωθεί πολλές
ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ 5.1 Δομή οργανικών ενώσεων - διπλός και τριπλός δεσμός - επαγωγικό φαινόμενο Θεωρία δεσμού σθένους (Valence bond theory) Για την περιγραφή του ομοιοπολικού δεσμού έχουν διατυπωθεί πολλές
ΙΟΝΤΙΚΟΣ ΔΕΣΜΟΣ ΠΑΡΑΔΕΙΓΜΑ
 ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
ΧΗΜΙΚΟΣ ΔΕΣΜΟΣ Είδη Δεσµών Ιοντικός Δεσµός (Ionic bond): σχηµατίζεται πάντα µεταξύ ηλεκτροθετικών και ηλεκτραρνητικών στοιχείων και περιλαµβάνει την πλήρη µεταφορά ενός ή περισσοτέρων ηλεκτρονίων από το
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
ΚΕΦΑΛΑΙΟ 1 ο Απαντήσεις των ερωτήσεων από πανελλήνιες 2001 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ. 4. δ. 2.
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις
 Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
Οργανική Χημεία της συντήρησης (ή γενική οργανική χημεία για συντηρητές) Ενότητα 2 - Ο σχηματισμός των δεσμών στις οργανικές χημικές ενώσεις Βιβλίο McMurry: σελ. 3-22 Διδάσκων: Στ. Μπογιατζής Επίκουρος
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 8: Η θεωρία δεσμού σθένους. Τόλης Ευάγγελος
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 8: Η θεωρία δεσμού σθένους Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 8: Η θεωρία δεσμού σθένους Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
 Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
Τί είναι χημικός δεσμός και είδη χημικών δεσμών... Κατανομή εξωτερικών ηλεκτρονίων: ΕΝ την ξεχνάμε ΠΟΤΕ!!! Θυμόμαστε ΠΑΝΤΑ πόσα μονήρη e- και πόσα ζεύγη e- έχουν τα άτομα στην εξωτερική τους στοιβάδα...
ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ
 Αρχές δόµησης πολυηλεκτρονιακών ατόµων 39. 2 o Αρχές δόµησης Πολυηλεκτρονιακών ατόµων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Η συµπλήρωση των τροχιακών ενός ατόµου µε ηλεκτρόνια γίνεται µε βάση την αρχή ηλεκτρονιακής
Αρχές δόµησης πολυηλεκτρονιακών ατόµων 39. 2 o Αρχές δόµησης Πολυηλεκτρονιακών ατόµων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Η συµπλήρωση των τροχιακών ενός ατόµου µε ηλεκτρόνια γίνεται µε βάση την αρχή ηλεκτρονιακής
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
4 o. Ηλεκτρονιακή θεωρία σθένους Ηλεκτρονιακοί τύποι κατά Lewis ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ 87.
 87 4 o Ηλεκτρονιακή θεωρία σθένους Ηλεκτρονιακοί τύποι κατά Lewis Α ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Ηλεκτρονιακή θεωρία σθένους Πρίν τη διατύπωση της κβαντικής θεωρίας και την εισαγωγή της έννοιας του ατοµικού
87 4 o Ηλεκτρονιακή θεωρία σθένους Ηλεκτρονιακοί τύποι κατά Lewis Α ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Ηλεκτρονιακή θεωρία σθένους Πρίν τη διατύπωση της κβαντικής θεωρίας και την εισαγωγή της έννοιας του ατοµικού
Μοριακή δομή Ο2 σύμφωνα με VB διαμαγνητικό
 Μοριακή δομή Ο 2 σύμφωνα με VB? διαμαγνητικό Θεωρία Μοριακών Τροχιακών Μolecular Orbital Theory (MO) Τα μοριακά τροχιακά (molecular orbital) είναι κυματοσυναρτήσεις οι οποίες προκύτπουναπότογραμμικόσυνδυασμότωνκυματοσυναρτήσεωντωναο.
Μοριακή δομή Ο 2 σύμφωνα με VB? διαμαγνητικό Θεωρία Μοριακών Τροχιακών Μolecular Orbital Theory (MO) Τα μοριακά τροχιακά (molecular orbital) είναι κυματοσυναρτήσεις οι οποίες προκύτπουναπότογραμμικόσυνδυασμότωνκυματοσυναρτήσεωντωναο.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση.
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση.
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 9: Υβριδισμός. Τόλης Ευάγγελος
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 9: Υβριδισμός Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 9: Υβριδισμός Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2
 Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ομοιοπολικός Δεσμός. Ασκήσεις
 Ασκήσεις Ομοιοπολικός Δεσμός 1. Δίνεται η οργανική ένωση CH 3 -CH 2 -C CH της οποίας τα άτομα αριθμούνται από 1 έως 4, όπως φαίνεται παραπάνω. Πόσοι και τι είδους σ δεσμοί και π δεσμοί υπάρχουν στην ένωση;
Ασκήσεις Ομοιοπολικός Δεσμός 1. Δίνεται η οργανική ένωση CH 3 -CH 2 -C CH της οποίας τα άτομα αριθμούνται από 1 έως 4, όπως φαίνεται παραπάνω. Πόσοι και τι είδους σ δεσμοί και π δεσμοί υπάρχουν στην ένωση;
Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων
 Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων Στις παρακάτω ερωτήσεις επιλέξτε τη σωστή απάντηση. Ο μέγιστος αριθμός ηλεκτρονίων για κάθε στιβάδα προκύπτει με εφαρμογή: α. της αρχής της ελάχιστης ενέργειας
Ασκήσεις στην ηλεκτρονιακή δόμηση των ατόμων Στις παρακάτω ερωτήσεις επιλέξτε τη σωστή απάντηση. Ο μέγιστος αριθμός ηλεκτρονίων για κάθε στιβάδα προκύπτει με εφαρμογή: α. της αρχής της ελάχιστης ενέργειας
ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 1 ΚΕΦ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ
 ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 1 ΚΕΦ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ Α θεωρία Bohr-σύγχρονη ατομική θεωρία Β περιοδικός πίνακας Γ ηλεκτρονικοί τύποι Δ υβριδικά τροχιακά- μοριακά τροχιακά Α θεωρία Bohr-σύγχρονη ατομική θεωρία Α1. Να
ΘΕΜΑΤΑ ΕΞΕΤΑΣΕΩΝ 1 ΚΕΦ ΧΗΜΕΙΑ Γ ΛΥΚΕΙΟΥ Α θεωρία Bohr-σύγχρονη ατομική θεωρία Β περιοδικός πίνακας Γ ηλεκτρονικοί τύποι Δ υβριδικά τροχιακά- μοριακά τροχιακά Α θεωρία Bohr-σύγχρονη ατομική θεωρία Α1. Να
5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση
 5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι μια πρώτη προσέγγιση των κυματομηχανικών θεωριών του ομοιοπολικού δεσμού και η ανακάλυψη του πώς οι θεωρίες αυτές δημιουργούν
5. Χημικός εσμός ΙI: Κβαντομηχανική Θεώρηση ΣΚΟΠΟΣ Σκοπός αυτού του κεφαλαίου είναι μια πρώτη προσέγγιση των κυματομηχανικών θεωριών του ομοιοπολικού δεσμού και η ανακάλυψη του πώς οι θεωρίες αυτές δημιουργούν
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ 1 ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ
 ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
ΘΕΜΑΤΑ ΑΠΟ ΠΜΔΧ ΣΧΕΤΙΚΑ ΜΕ ΤΟ ΚΕΦΑΛΑΙΟ ΤΗΣ Γ ΛΥΚΕΙΟΥ 27 ος ΠΜΔΧ Γ ΛΥΚΕΙΟΥ 30 03 203. Στοιχείο Μ το οποίο ανήκει στην πρώτη σειρά στοιχείων μετάπτωσης, σχηματίζει ιόν Μ 3+, που έχει 3 ηλεκτρόνια στην υποστιβάδα
Δομή και δεσμικότητα των οργανικών ενώσεων. Αδαμαντοειδή: πενταμαντάνιο
 Δομή και δεσμικότητα των οργανικών ενώσεων Αδαμαντοειδή: πενταμαντάνιο Δομή και δεσμικότητα των οργανικών ενώσεων Σχεδόν οτιδήποτε βλέπετε στην εικόνα αυτή είναι φτιαγμένο από οργανικές χημικές ενώσεις.
Δομή και δεσμικότητα των οργανικών ενώσεων Αδαμαντοειδή: πενταμαντάνιο Δομή και δεσμικότητα των οργανικών ενώσεων Σχεδόν οτιδήποτε βλέπετε στην εικόνα αυτή είναι φτιαγμένο από οργανικές χημικές ενώσεις.
Ανακτήθηκε από την ΕΚΠΑΙΔΕΥΤΙΚΗ ΚΛΙΜΑΚΑ ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 4 ΙΟΥΛΙΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1-1.3
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 4 ΙΟΥΛΙΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1-1.3
ΠΩΣ ΙΑΤΑΣΣΟΝΤΑΙ ΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΙΒΑ Α
 1 ΠΩΣ ΙΑΤΑΣΣΟΝΤΑΙ ΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΙΒΑ Α Πριν προχωρήσουµε στον τρόπο που συνδέονται τα άτοµα σκέψου τα παρακάτω και επιστράτευσε τη φαντασία σου για να µπορέσεις να καταλάβεις καλύτερα πως
1 ΠΩΣ ΙΑΤΑΣΣΟΝΤΑΙ ΤΑ ΗΛΕΚΤΡΟΝΙΑ ΣΤΗΝ ΕΞΩΤΕΡΙΚΗ ΣΤΙΒΑ Α Πριν προχωρήσουµε στον τρόπο που συνδέονται τα άτοµα σκέψου τα παρακάτω και επιστράτευσε τη φαντασία σου για να µπορέσεις να καταλάβεις καλύτερα πως
53 Χρόνια ΦΡΟΝΤΙΣΤΗΡΙΑ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΣΑΒΒΑΪΔΗ-ΜΑΝΩΛΑΡΑΚΗ ΠΑΓΚΡΑΤΙ : Φιλολάου & Εκφαντίδου 26 : Τηλ.: ΔΙΑΓΩΝΙΣΜΑ : Γ ΛΥΚΕΙΟΥ 2013
 53 Χρόνια ΦΡΟΝΤΙΣΤΗΡΙΑ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΣΑΒΒΑΪΔΗ-ΜΑΝΩΛΑΡΑΚΗ ΠΑΓΚΡΑΤΙ : Φιλολάου & Εκφαντίδου 26 : Τηλ.: 2107601470 ΔΙΑΓΩΝΙΣΜΑ : Γ ΛΥΚΕΙΟΥ 2013 Θέμα Α Α1. Ο μέγιστος αριθμός ηλεκτρονίων που χαρακτηρίζονται
53 Χρόνια ΦΡΟΝΤΙΣΤΗΡΙΑ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΣΑΒΒΑΪΔΗ-ΜΑΝΩΛΑΡΑΚΗ ΠΑΓΚΡΑΤΙ : Φιλολάου & Εκφαντίδου 26 : Τηλ.: 2107601470 ΔΙΑΓΩΝΙΣΜΑ : Γ ΛΥΚΕΙΟΥ 2013 Θέμα Α Α1. Ο μέγιστος αριθμός ηλεκτρονίων που χαρακτηρίζονται
5. Να βρείτε τον ατομικό αριθμό του 2ου μέλους της ομάδας των αλογόνων και να γράψετε την ηλεκτρονιακή δομή του.
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. α) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που μπορεί να πάρει κάθε μία από τις στιβάδες: K, L, M, N. β) Ποιος είναι ο μέγιστος αριθμός ηλεκτρονίων που
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ Α Α3. γ Α4. δ. Α5. α
 1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ TETΡΤΗ 8 ΙΟΥΝΙΟΥ 016 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) ΘΕΜΑ Α Α1. γ Α. δ Α. γ Α4. δ Α5. α ΑΠΑΝΤΗΣΕΙΣ
1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ TETΡΤΗ 8 ΙΟΥΝΙΟΥ 016 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) ΘΕΜΑ Α Α1. γ Α. δ Α. γ Α4. δ Α5. α ΑΠΑΝΤΗΣΕΙΣ
Μάθημα 20 ο. Το σχήμα των μορίων
 Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
Μάθημα 20 ο Το σχήμα των μορίων Tα μόρια Μπορεί να είναι μη πολικά έστω και άν οι δεσμοί μεταξύ των ατόμων τους είναι πολωμένοι Δεν είναι επίπεδα (έχουν τρισδιάστατη διάταξη στο χώρο) Γενική και Ανόργανη
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί
 1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
ΑΤΟΜΙΚΑ ΤΟΜΙΚΑ ΠΡΟΤΥΠΑ
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (6): Τροχιακά και υβριδισμός Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΓΕΝΙΚΗ ΚΑΙ ΑΝΟΡΓΑΝΗ ΧΗΜΕΙΑ Ενότητα # (6): Τροχιακά και υβριδισμός Ακρίβος Περικλής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί
 1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
1.12 Ηλεκτρονιακά κύματα και χημικοί δεσμοί Ο Lewis πρότεινε το μοντέλο του κοινού ηλεκτρονιακού ζεύγους των δεσμών το 1916, σχεδόνμιαδεκαετίαπριναπότηθεωρίατουde Broglie τηςδυαδικότηταςκύματος-σωματιδίου.
1.4. «Σωστό» «Λάθος» Μονάδες Στήλης Στήλη ΙΙ Στήλης Ι Στήλης ΙΙ Στήλης ΙΙ Στήλη Ι Στήλη ΙΙ στ. Μονάδες 6
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 26 ΜΑΪΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ : ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Για τις προτάσεις 1.1 έως
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 26 ΜΑΪΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ : ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Για τις προτάσεις 1.1 έως
Χημεία Α Λυκείου. Ασκήσεις τράπεζας θεμάτων στο 2 ο Κεφάλαιο
 Χημεία Α Λυκείου Ασκήσεις τράπεζας θεμάτων στο 2 ο Κεφάλαιο 1) Θέμα 2530 (Ερώτημα 2.1. ) Δίνονται: υδρογόνο, 1 H, άζωτο, 7 N α) Να γράψετε την κατανομή των ηλεκτρονίων σε στιβάδες για το άτομο του αζώτου.
Χημεία Α Λυκείου Ασκήσεις τράπεζας θεμάτων στο 2 ο Κεφάλαιο 1) Θέμα 2530 (Ερώτημα 2.1. ) Δίνονται: υδρογόνο, 1 H, άζωτο, 7 N α) Να γράψετε την κατανομή των ηλεκτρονίων σε στιβάδες για το άτομο του αζώτου.
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός.
 2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό
 Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων. Περιοδικός πίνακας. Σταυρακαντωνάκης Γιώργος Λύκειο Γαζίου Page 1
 Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
Ερωτήσεις στο 2o κεφάλαιο από τράπεζα θεμάτων 1. Για τις ενέργειες ΕL και ΕN των στιβάδων L και N αντίστοιχα, ισχύει ότι ΕL < ΕN ΣΩΣΤΟ, Όσο απομακρυνόμαστε από τον πυρήνα τόσο αυξάνεται η ενεργειακή στάθμη
ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν. 2. Ο µέγιστος αριθµός των ηλεκτρονίων που είναι δυνατόν να υπάρχουν
 ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
ΚΕΦΑΛΑΙΟ 1 ο Ερωτήσεις από πανελλήνιες εξετάσεις από το 2001 ως το 2014 ΘΕΜΑ 1 ο 1. Πόσα ηλεκτρόνια στη θεµελιώδη κατάσταση του στοιχείου 18 Ar έχουν µαγνητικό κβαντικό αριθµό m l = 1 ; α. 6. β. 8. γ.
ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΑΝΤΙΛΗΨΗ ΓΙΑ ΤΟΝ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ - ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΣΥΝΟΠΤΙΚΗ ΘΕΩΡΙΑ
 8Α ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΑΝΤΙΛΗΨΗ ΓΙΑ ΤΟΝ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ - ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΣΥΝΟΠΤΙΚΗ ΘΕΩΡΙΑ Σύνοψη Διατυπώνεται η κβαντική θεωρία Δεσμού Σθένους(VB) που ερμηνεύει τον μοριακό δεσμό. Ορίζονται οι σ (σίγμα)
8Α ΚΒΑΝΤΟΜΗΧΑΝΙΚΗ ΑΝΤΙΛΗΨΗ ΓΙΑ ΤΟΝ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ - ΘΕΩΡΙΑ ΔΕΣΜΟΥ ΣΘΕΝΟΥΣ ΣΥΝΟΠΤΙΚΗ ΘΕΩΡΙΑ Σύνοψη Διατυπώνεται η κβαντική θεωρία Δεσμού Σθένους(VB) που ερμηνεύει τον μοριακό δεσμό. Ορίζονται οι σ (σίγμα)
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις
 1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
1 ο Κεφάλαιο Χημείας Θετικής Κατεύθυνσης Γ Λυκείου 100 Ερωτήσεις τύπου Σωστού Λάθους Στο τέλος οι απαντήσεις 1. Η εξίσωση E = h v μας δίνει την ενέργεια μιας ηλεκτρομαγνητικής ακτινοβολίας 2. H κβαντική
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ
 ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-54 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Η θεωρία των κβάντα:
ΚΕΦΑΛΑΙΟ 1 ΗΛΕΚΤΡΟΝΙΑΚΗ ΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟ ΙΚΟΣ ΠΙΝΑΚΑΣ 1.1 Ερωτήσεις πολλαπλής επιλογής Στις ερωτήσεις 1-54 βάλτε σε ένα κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Η θεωρία των κβάντα:
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό
 Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Θέμα 2. Για καθεμία από τις παρακάτω περιπτώσεις να
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Θέμα 2. Για καθεμία από τις παρακάτω περιπτώσεις να
Διαγώνισμα στην Οργανική.
 Χημεία Γ Λυκείου. Διαγώνισμα στην Οργανική. Θέμα 1 ο.... 1.1. Δεν είναι αλκαλικό το υδατικό διάλυμα της ουσίας: α) CH 3 CH 2 COONa, β)c 6 H 5 OH, γ) CH 3C CNa, δ) CH 3CH 2ONa. Μονάδες 2 1.2. Κατά την αναγωγή
Χημεία Γ Λυκείου. Διαγώνισμα στην Οργανική. Θέμα 1 ο.... 1.1. Δεν είναι αλκαλικό το υδατικό διάλυμα της ουσίας: α) CH 3 CH 2 COONa, β)c 6 H 5 OH, γ) CH 3C CNa, δ) CH 3CH 2ONa. Μονάδες 2 1.2. Κατά την αναγωγή
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1.1. Η μάζα του πρωτονίου
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1.1. Η μάζα του πρωτονίου
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΧΗΜΕΙΑ
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΧΗΜΕΙΑ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΧΗΜΕΙΑ ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 2005 ΕΚΦΩΝΗΣΕΙΣ
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 005 ΘΕΜΑ 1 ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 11-1 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση 11 Ο µέγιστος αριθµός
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 005 ΘΕΜΑ 1 ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 11-1 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση 11 Ο µέγιστος αριθµός
Λύνουµε περισσότερες ασκήσεις
 Χηµεία Γ Λυκείου - Θετικής Κατεύθυνσης Βήµα 3 ο Λύνουµε περισσότερες ασκήσεις 17. Λύνουµε περισσότερες ασκήσεις 1. Ηλεκτρόνιο ατόµου του υδρογόνου που βρίσκεται στη θεµελιώδη κατάσταση απορροφά ένα φωτόνιο
Χηµεία Γ Λυκείου - Θετικής Κατεύθυνσης Βήµα 3 ο Λύνουµε περισσότερες ασκήσεις 17. Λύνουµε περισσότερες ασκήσεις 1. Ηλεκτρόνιο ατόµου του υδρογόνου που βρίσκεται στη θεµελιώδη κατάσταση απορροφά ένα φωτόνιο
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 14 Ιουνίου 2013 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Απαντήσεις Θεμάτων Επαναληπτικών Πανελληνίων Εξετάσεων Ημερησίων Γενικών Λυκείων Περιεχόμενα ΘΕΜΑ Α... 1 Α1. Β... 1 Α2. Γ... 1 Α3. Δ... 1 Α4. Α... 1 Α5. Α....
14 Ιουνίου 2013 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Απαντήσεις Θεμάτων Επαναληπτικών Πανελληνίων Εξετάσεων Ημερησίων Γενικών Λυκείων Περιεχόμενα ΘΕΜΑ Α... 1 Α1. Β... 1 Α2. Γ... 1 Α3. Δ... 1 Α4. Α... 1 Α5. Α....
ΑΠΑΝΣΗΕΙ ΔΙΑΓΩΝΙΜΑΣΟ ΧΗΜΕΙΑ 06 04 2014
 ΑΠΑΝΣΗΕΙ ΔΙΑΓΩΝΙΜΑΣΟ ΧΗΜΕΙΑ 06 04 2014 ΘΕΜΑ 1 Ο 1 (β), 2 (δ), 3 (γ), 4 (δ), 5 α (), β (Λ), γ: i (Λ), ii (), δ (), ε (Λ). ΘΕΜΑ 2 o 1. Α. «Υβριδισμός είναι ο γραμμικός συνδυασμός (πρόσθεση και αφαίρεση)
ΑΠΑΝΣΗΕΙ ΔΙΑΓΩΝΙΜΑΣΟ ΧΗΜΕΙΑ 06 04 2014 ΘΕΜΑ 1 Ο 1 (β), 2 (δ), 3 (γ), 4 (δ), 5 α (), β (Λ), γ: i (Λ), ii (), δ (), ε (Λ). ΘΕΜΑ 2 o 1. Α. «Υβριδισμός είναι ο γραμμικός συνδυασμός (πρόσθεση και αφαίρεση)
Διάλεξη 7: Μοριακή Δομή
 Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Μοριακή δομή. Απλοϊκή εικόνα του μορίου του νερού. Ηλεκτρονιακοί τύποι κατά Lewis. Δημόκριτος π.χ.
 Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
Μοριακή δομή Και καθώς τα άτομα κινούνται στο κενό, συγκρούονται και αλληλοσυμπλέκονται και μερικά αναπηδούν και άλλα ενώνονται και παραμένουν μαζί σύμφωνα με το σχήμα και το μέγεθος και την τάξη τους.
Κεφάλαιο 2 Ο Χημικός Δεσμός
 Κεφάλαιο 2 Ο Χημικός Δεσμός Σύνοψη O Χημικός Δεσμός εξηγεί τον τρόπο με τον οποίο δημιουργούνται οι ενώσεις. Υπάρχουν οι ιοντικές ενώσεις στις οποίες ιόντα αντίθετου φορτίου ενώνονται μεταξύ τους προς
Κεφάλαιο 2 Ο Χημικός Δεσμός Σύνοψη O Χημικός Δεσμός εξηγεί τον τρόπο με τον οποίο δημιουργούνται οι ενώσεις. Υπάρχουν οι ιοντικές ενώσεις στις οποίες ιόντα αντίθετου φορτίου ενώνονται μεταξύ τους προς
Περίληψη 1 ου Κεφαλαίου
 Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
Περίληψη 1 ου Κεφαλαίου Άτοµο: θετικά φορτισµένος πυρήνας περικυκλωµένος από αρνητικά φορτισµένα ηλεκτρόνια Ηλεκτρονική δοµή ατόµου περιγράφεται από κυµατοσυνάρτηση Ηλεκτρόνια καταλαµβάνουν τροχιακά γύρω
1o Kριτήριο Αξιολόγησης
 1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
1o Kριτήριο Αξιολόγησης 11 ΚΒΑΝΤΙΚΟΙ ΑΡΙΘΜΟΙ - ΑΡΧΕΣ ΟΜΗΣΗΣ ΠΟΛΥΗΛΕΚΤΡΟΝΙΑΚΩΝ ΑΤΟΜΩΝ ΖΗΤΗΜΑ 1ο Στις ερωτήσεις 1-4 βάλτε σε κύκλο το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. Κατά τις µεταπτώσεις: L
ΧΗΜΕΙΑ» ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ. Διδάσκουσα: ΣΟΥΠΙΩΝΗ Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ)
 ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ ΧΗΜΕΙΑ» Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ) ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ Διδάσκουσα: ΣΟΥΠΙΩΝΗ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΡΙΑ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΜΑΘΗΜΑ: «ΓΕΝΙΚΗ ΧΗΜΕΙΑ» Α ΕΞΑΜΗΝΟ (ΧΕΙΜΕΡΙΝΟ) ΣΟΥΠΙΩΝΗ ΜΑΓΔΑΛΗΝΗ Διδάσκουσα: ΣΟΥΠΙΩΝΗ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΡΙΑ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6)
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού
 7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
7. Μοριακή Γεωμετρία και Θεωρία του Χημικού Δεσμού ΠΕΡΙΕΧΟΜΕΝΑ Το μοντέλο VSEPR Διπολική ροπή και μοριακή γεωμετρία Θεωρία του δεσμού σθένους Περιγραφή πολλαπλών δεσμών Αρχές της θεωρίας των μοριακών τροχιακών
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
ΤΕΛΟΣ 2ΗΣ ΑΠΟ 5 ΣΕΛΙ ΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 23 ΜΑΪΟΥ 2011 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ Α Για τις ερωτήσεις
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 23 ΜΑΪΟΥ 2011 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ Α Για τις ερωτήσεις
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6)
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 8 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 7: Μοριακή γεωμετρία. Τόλης Ευάγγελος
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 7: Μοριακή γεωμετρία Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 7: Μοριακή γεωμετρία Τόλης Ευάγγελος e-mail: etolis@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Για τις ερωτήσεις 1.1 1.4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στην σωστή απάντηση. 1.1. Τα ατομικά τροχιακά
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Για τις ερωτήσεις 1.1 1.4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στην σωστή απάντηση. 1.1. Τα ατομικά τροχιακά
ΧΗΜΕΙΑ Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 2006 ÈÅÌÅËÉÏ ΕΚΦΩΝΗΣΕΙΣ
 ΘΕΜΑ 1ο ΧΗΜΕΙΑ Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 006 ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1. Ο
ΘΕΜΑ 1ο ΧΗΜΕΙΑ Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 006 ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1. Ο
ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4
 ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4 ΘΕΜΑ Α Α1. Στον σύγχρονο Περιοδικό Πίνακα τα χημικά στοιχεία έχουν ταξινομηθεί: α. κατ αύξοντα ατομικό
ΑΡΧΗ 1 ΗΣ ΣΕΛΙΔΑΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ (ΚΕΦ 2-3 ) ΚΥΡΙΑΚΗ 4 ΔΕΚΕΜΒΡΙΟΥ 2016 ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ 4 ΘΕΜΑ Α Α1. Στον σύγχρονο Περιοδικό Πίνακα τα χημικά στοιχεία έχουν ταξινομηθεί: α. κατ αύξοντα ατομικό
Θεωρία του δεσμού σθένους
 ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε μια αρκετά απλή θεωρία, τη θεωρία του δεσμού σθένους, με την οποία θα μπορούμε να εξηγούμε με αρκετή επιτυχία τη γεωμετρία των συμπλόκων, καθώς και
ΣΚΟΠΟΣ Ο σκοπός αυτού του κεφαλαίου είναι να γνωρίσουμε μια αρκετά απλή θεωρία, τη θεωρία του δεσμού σθένους, με την οποία θα μπορούμε να εξηγούμε με αρκετή επιτυχία τη γεωμετρία των συμπλόκων, καθώς και
Στήλη ΙΙ (κατηγορία οργανικών αντιδράσεων) 1. οξείδωση 2. υποκατάσταση 3. απόσπαση 4. προσθήκη 5. πολυµερισµός Μονάδες 8
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 13 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ : ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Στις ερωτήσεις 1.1 έως
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ʹ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 13 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ : ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ : ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Στις ερωτήσεις 1.1 έως
ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου. Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη
 Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
Υπεύθυνη καθηγήτρια: Ε. Ατσαλάκη ΘΕΜΑΤΑ ΠΑΝΕΛΛΗΝΙΩΝ ΕΞΕΤΑΣΕΩΝ 1 ο ΚΕΦΑΛΑΙΟΥ (2000-2011) Χημεία Γ Λυκείου Α) Να επιλέξετε σε κάθε μία από τις παρακάτω προτάσεις τη σωστή απάντηση: 1. To στοιχείο που περιέχει
ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ (4)
 ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ (4) β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα
ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό ΠΡΟΤΕΙΝΟΜΕΝΕΣ ΑΠΑΝΤΗΣΕΙΣ ΧΗΜΕΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ (4) β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα
Ονοματεπώνυμο: Χημεία Α Λυκείου Δομή του ατόμου Περιοδικός Πίνακας. Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Δομή του ατόμου Περιοδικός Πίνακας Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες
Ονοματεπώνυμο: Μάθημα: Υλη: Επιμέλεια διαγωνίσματος: Αξιολόγηση : Χημεία Α Λυκείου Δομή του ατόμου Περιοδικός Πίνακας Τσικριτζή Αθανασία Θέμα Α 1. Να επιλέξετε τη σωστή απάντηση σε καθεμία από τις επόμενες
Χημικοί Χημικ σμ σμ & Μοριακά Τροχιακά
 Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
Χημικοί δεσμοί & Μοριακά Τροχιακά Χημικός δεσμός είναι η δύναμη που συγκρατεί τα άτομα (ήάλλ άλλες δομικές μονάδες της ύλης, π.χ ιόντα) ) ενωμένα μεταξύ τους. Δημιουργείται, όταν οι δομικές μονάδες της
κυματικής συνάρτησης (Ψ) κυματική συνάρτηση
 Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 2011 ΕΚΦΩΝΗΣΕΙΣ
 ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 2011 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το στοιχείο
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ 2011 ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το στοιχείο
σύμφωνα με τη θεωρία της μεταβατικής κατάστασης. Ισχύει ότι: Α. E 1 ΔH = E 3 Σελίδα 1 από 7 g g g Δ g
 ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 4 ΜΑΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΠΤΑ (7) ΘΕΜΑ Α Στις ερωτήσεις Α.1. έως Α.4. να γράψετε στο τετράδιο
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 4 ΜΑΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΠΤΑ (7) ΘΕΜΑ Α Στις ερωτήσεις Α.1. έως Α.4. να γράψετε στο τετράδιο
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
Διαγώνισμα στη Χημεία Γ Λυκείου.
 Διαγώνισμα στη Χημεία Γ Λυκείου. 1 ο Κεφάλαιο: μέχρι και Ηλ. τύποι Lewis. 5 ο Κεφάλαιο μέχρι πολυμερισμός Θέμα 1 ο.... Σημειώστε τη σωστή απάντηση στις ερωτήσεις 1.1 έως 1.4 1.1. Ο μέγιστος αριθμός ηλεκτρονίων
Διαγώνισμα στη Χημεία Γ Λυκείου. 1 ο Κεφάλαιο: μέχρι και Ηλ. τύποι Lewis. 5 ο Κεφάλαιο μέχρι πολυμερισμός Θέμα 1 ο.... Σημειώστε τη σωστή απάντηση στις ερωτήσεις 1.1 έως 1.4 1.1. Ο μέγιστος αριθμός ηλεκτρονίων
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α. Α1. α. Α2. α. Α3. β. Α4. δ. Α5. α. Σωστό β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β
 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα είναι: και 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1, Z=24 1s
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. α Α2. α Α3. β Α4. δ Α5. α. Σωστό β. Σωστό γ. Λάθος δ. Λάθος ε. Σωστό ΘΕΜΑ Β Β1. i) Οι πιθανές ηλεκτρονιακές διαμορφώσεις θα είναι: και 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1, Z=24 1s
Γενικές εξετάσεις Χημεία Γ λυκείου θετικής κατεύθυνσης
 1 Γενικές εξετάσεις 2005 Χημεία Γ λυκείου θετικής κατεύθυνσης Θέμα 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
1 Γενικές εξετάσεις 2005 Χημεία Γ λυκείου θετικής κατεύθυνσης Θέμα 1 ο Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 9ος
 Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 9ος 22-0231_l_c_chemistry_bm 251-300 28b.indd 1 1/17/17 1:26:15 PM ΣΤΟΙΧΕΙΑ ΑΡΧΙΚΗΣ ΕΚ ΟΣΗΣ Το παρόν βιβλίο περιέχει τα παρακάτω κεφάλαια:
Χημεία γ λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών Tόμος 9ος 22-0231_l_c_chemistry_bm 251-300 28b.indd 1 1/17/17 1:26:15 PM ΣΤΟΙΧΕΙΑ ΑΡΧΙΚΗΣ ΕΚ ΟΣΗΣ Το παρόν βιβλίο περιέχει τα παρακάτω κεφάλαια:
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ
 ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, S = 32,066 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Σχετική ισχύς οξέων (ελάττωση από αριστερά προς τα δεξιά):
ΕΞΕΤΑΣΕΙΣ ΣΤΗ ΓΕΝΙΚΗ ΧΗΜΕΙΑ Δεδομένα: Α.Β.: Ο = 15,9994 amu, S = 32,066 amu Εξίσωση του Bohr για τα επίπεδα ενέργειας του ατόμου Η: E = R H /n 2 Σχετική ισχύς οξέων (ελάττωση από αριστερά προς τα δεξιά):
Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΧΗΜΕΙΑ ΕΚΦΩΝΗΣΕΙΣ ÅÐÉËÏÃÇ
 1 Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΧΗΜΕΙΑ ΘΕΜΑ 1 ο ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1. Οι παρακάτω
1 Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΧΗΜΕΙΑ ΘΕΜΑ 1 ο ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις 1.1-1.4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1. Οι παρακάτω
