Εθνικό και Καποδιστριακό Πανεπιστήμιο Αθηνών ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΛΟΓΙΑΣ ΚΥΤΤΑΡΟΥ & ΒΙΟΦΥΣΙΚΗΣ. Διπλωματική Εργασία
|
|
|
- Διδώ Φιλιππίδης
- 5 χρόνια πριν
- Προβολές:
Transcript
1 Εθνικό και Καποδιστριακό Πανεπιστήμιο Αθηνών ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΛΟΓΙΑΣ ΚΥΤΤΑΡΟΥ & ΒΙΟΦΥΣΙΚΗΣ Διπλωματική Εργασία «Επιπτώσεις των διαφορετικών τεχνικών αιμοκάθαρσης στο αιματολογικό πρότυπο και στα ερυθροκύτταρα ασθενών με χρόνια νεφρική ανεπάρκεια τελικού σταδίου» Δάρλα Ξανθή-Γεωργία ΑΜ: Επιβλέπουσα: Μαριάννα Χ. Αντωνέλου, Επίκουρη Καθηγήτρια ΑΘΗΝΑ 2017
2 ΠΡΟΛΟΓΟΣ Η παρούσα εργασία εκπονήθηκε στον Τομέα Βιολογίας Κυττάρου και Βιοφυσικής του Τμήματος Βιολογίας, του Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών, στο πλαίσιο των προπτυχιακών μου σπουδών. Η εργασία αυτή αποτέλεσε την πρώτη μου επαφή με τον κόσμο της έρευνας και ήταν ένα όμορφο ταξίδι μέσα από το οποίο εμπλούτισα τις γνώσεις μου, αποκομίζοντας παράλληλα όμορφες εμπειρίες. Έτσι λοιπόν, αισθάνομαι την ανάγκη να ευχαριστήσω τους ανθρώπους που βρέθηκαν μαζί μου σε αυτό το ταξίδι και με βοήθησαν στην επιτυχή περάτωσή του. Αρχικά, θα ήθελα να ευχαριστήσω την Επίκουρη Καθηγήτρια κα Αντωνέλου Μαριάννα για την εμπιστοσύνη και την ευκαιρία που μου έδωσε να ασχοληθώ με ένα πολύ ενδιαφέρον και αξιόλογο θέμα. Η καθοδήγηση και οι πολύτιμες συμβουλές της με βοήθησαν καταλυτικά στην ολοκλήρωση της διπλωματικής μου εργασίας. Ευχαριστώ ιδιαίτερα την Καθηγήτρια και Διευθύντρια του Τομέα Βιολογίας Κυττάρου και Βιοφυσικής κα Ισιδώρα Σ. Παπασιδέρη για τη φιλοξενία στον Τομέα και την εξασφάλιση της εύρυθμης λειτουργίας του. Ένα θερμό ευχαριστώ στην Διδάκτορα Γεωργατζάκου Χαρά για τη στενή συνεργασία που είχαμε και την υπομονή που έδειξε προς εμένα σε όλα τα στάδια της εργασίας, από τα πειραματικά μέχρι και την ολοκλήρωση της συγγραφής της. Οι πολύτιμες γνώσεις που μου προσέφερε, καθώς και η δεκτικότητά της να απαντήσει επακριβώς σε όλα τα ερωτήματα και τις απορίες μου, με βοήθησαν στη σε βάθος κατανόηση του θέματος της εργασίας. Επίσης, θα ήθελα να ευχαριστήσω τον μεταδιδακτορικό ερευνητή Δρ Βασίλη Τζούνακα, που σε συνεργασία με την Δρ Γεωργατζάκου Χαρά, μου μετέφεραν τις γνώσεις τους πάνω στο θέμα της εργασίας, με εκπαίδευσαν πάνω στις πειραματικές διαδικασίες που ακολουθήθηκαν, δημιουργώντας παράλληλα ένα ευχάριστο κλίμα στο εργαστήριο. Τέλος, θα ήθελα να ευχαριστήσω την συμφοιτήτρια μου Λουίζα Δολιανίτη για την άψογη συνεργασία κατά τη διεξαγωγή των πειραμάτων και την υποστήριξή της, και να της ευχηθώ καλή συνέχεια στην ακαδημαϊκή της πορεία. ~ 2 ~
3 Περιεχόμενα ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ ΕΙΣΑΓΩΓΗ Το ερυθροκύτταρο Η Αιμοσφαιρίνη Ερυθροκυτταρική μεμβράνη Μεμβρανικά λιπίδια Πρωτεΐνες της ερυθροκυτταρικής μεμβράνης Διαμεμβρανικές Μεμβρανοσυνδεόμενες πρωτεΐνες Σκελετικές Κυτοσολικές πρωτεΐνες Σύμπλοκα της ερυθροκυτταρικής μεμβράνης Γήρανση ερυθροκυττάρων Ερυθρόπτωση Λειτουργία Νεφρών Χρόνια Νεφρική Ανεπάρκεια Αιτιολογία της Χρόνιας Νεφρικής Ανεπάρκειας Εξέλιξη της ΧΝΑ Κλινικά ευρήματα και επιπτώσεις της ΧΝΑ Υποκατάσταση της νεφρικής λειτουργίας Αιμοκάθαρση Αιμοδιαδιήθηση Αιμοκάθαρση vs. Αιμοδιαδιήθηση ΣΚΟΠΟΣ ΤΗΣ ΕΡΓΑΣΙΑΣ ΥΛΙΚΑ - ΜΕΘΟΔΟΙ Υλικά Όργανα-Συσκευές Χρωστικές Αντισώματα Φωτογραφικά Υλικά Αναλώσιμα Μέθοδοι ~ 3 ~
4 3.2.1 Αιματολογικός έλεγχος Λευκαφαίρεση Απομόνωση ερυθροκυτταρικών μεμβρανών (ghosts) Υπολογισμός ολικής πρωτεϊνικής συγκέντρωσης δείγματος Προετοιμασία πρωτεϊνικού δείγματος για ηλεκτροφόρηση SDS-PAGE ηλεκτροφόρηση πρωτεϊνών κατά Laemmli Χρώση ολικών πρωτεϊνών (εκτός γλυκοφορινών) σε πήκτωμα Ανοσοαποτύπωμα (Western blotting) Ποσοτική εκτίμηση των πρωτεϊνών πηκτωμάτων και φιλμ Προετοιμασία για παρατήρηση της μορφολογίας ερυθροκυττάρων με Ηλεκτρονικό Μικροσκόπιο Σάρωσης -(ΗΜΣ) Scanning Electron Microscope (SEM) Μέτρηση Μηχανικής Ευθραυστότητας (Mechanical Fragility-MFΙ) Μέτρηση Ωσμωτικής Ευθραυστότητας (Mean corpuscular fragility-mcf) Μέτρηση αντιοξειδωτικής ικανότητας του πλάσματος (FRAP) Μέτρηση επιπέδων ενδοκυττάριων Ca ΑΠΟΤΕΛΕΣΜΑΤΑ Μέρος Α Μεταβολές στα ερυθροκύτταρα και στο πλάσμα των ασθενών που υποβάλλονται σε αιμοδιαδιήθηση (HDF) σε σύγκριση ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση (HD), πριν από τη διαδικασία της κάθαρσης Μέρος Β Μεταβολές στα ερυθροκύτταρα και στο πλάσμα των ασθενών που υποβάλλονται σε αιμοδιαδιήθηση (HDF) σε σύγκριση ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση (HD), μετά τη διαδικασία της κάθαρσης Συζήτηση- Συμπεράσματα ΠΕΡΙΛΗΨΗ ~ 4 ~
5 ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ AC: Antioxidant Capacity (αντιοξειδωτική ικανότητα) Ca 2+ : ιόντα ασβεστίου Cl - : ιόντα χλωρίου DHA: Dehydroascorbic acid (L-αφυδροασκορβικό οξύ) GFR: Glomerular Filtration Rate (ρυθμός σπειραματικής διήθησης) Glut-1: Glucose transporter 1 (μεταφορέας γλυκόζης-1) GPA: γλυκοφορίνες A GPB: γλυκοφορίνες B GPC: γλυκοφορίνες C GPD: γλυκοφορίνες D GPE: γλυκοφορίνες E Hb: Hemoglobin (αιμοσφαιρίνη) HCO3: διττανθρακικά ιόντα Hct: Hematocrit (αιματοκρίτης) HD: conventional hemodialysis (συμβατική αιμοκάθαρση) HDF: hemodiafiltration (αιμοδιαδιήθηση) ICAM: Intercellular Adhesion Molecules (μόρια ενδοκυτταρικής προσκόλλησης) IgG: Immunoglobulin G (ανοσοσφαιρίνη G) IL-1: Ιντερλευκίνη 1 IL-6: Ιντερλευκίνη 6 MCH: Mean corpuscular hemoglobin (μέση περιεκτικότητα αιμοσφαιρίνης ανά ερυθροκύτταρο) MCHC: Mean corpuscular hemoglobin concentration (μέση συγκέντρωση αιμοσφαιρίνης ερυθροκυττάρων) PS: phisphatidylserine (φωσφατιδυλοσερίνη) RDW: Red cell distribution width (εύρος κατανομής μεγέθους ερυθροκυττάρων) Rh: Rhesus rhepo: recombinant human erythropoietin (ανασυνδυασμένη ανθρώπινη ερυθροποιητίνη) ROS: Reactive Oxygen Species (δραστικές ρίζες οξυγόνου) TAC: Total Antioxidant Capacity (ολική αντιοξειδωτική ικανότητα) TNF-a: Tumor necrosis factor alpha (παράγοντας νέκρωσης όγκων-α) UA: Uric Acid (ουρικό οξύ) URR: Urea reduction ratio ΑΙΚ: Αιμοκάθαρση ΧΝΑ: Χρόνια Νεφρική Ανεπάρκεια ~ 5 ~
6 1.ΕΙΣΑΓΩΓΗ 1.1 Το ερυθροκύτταρο Σε όλα τα σπονδυλωτά το αίμα αποτελείται από έμμορφα στοιχεία στα οποία περιλαμβάνονται τα κύτταρα και το άμορφο συστατικό που ονομάζεται πλάσμα. Τα ερυθροκύτταρα αποτελούν τον πολυπληθέστερο κυτταρικό τύπο του αίματος (~45% του συνολικού όγκου του). Με εξαίρεση τα θηλαστικά, τα ερυθροκύτταρα στα υπόλοιπα σπονδυλωτά, παραμένουν εμπύρηνα καθ όλη τη διάρκεια της ζωής τους. Η κύρια λειτουργία στην οποία εμπλέκονται, είναι η μεταφορά και η ανταλλαγή των αναπνευστικών αερίων (οξυγόνο από τους πνεύμονες στους ιστούς και διοξείδιο του άνθρακα από τους ιστούς στους πνεύμονες). Ωστόσο υπάρχουν και άλλες λειτουργίες που αποδίδονται στα κύτταρα αυτά, όπως η αλληλεπίδρασή τους με το ανοσοποιητικό σύστημα και η ρύθμιση του μεταβολισμού του μονοξειδίου του αζώτου. Το ανθρώπινο σώμα, διαθέτει περίπου 5 λίτρα αίματος τα οποία περιέχουν 4.5 x 10 9 ερυθροκύτταρα/ml. Η διάρκεια ζωής των ερυθροκυττάρων στον άνθρωπο κυμαίνεται γύρω στις 120 ημέρες (Lutz H., 2012). Έχουν χαρακτηριστικό σχήμα αμφίκοιλου δίσκου που τους επιτρέπει να αποκτούν το μέγιστο δυνατό λόγο επιφάνειας/όγκο (140 μm 2 /90fl) και να έχουν μεγάλη ικανότητα παραμόρφωσης. Το χαρακτηριστικό αυτό τους δίνει τη δυνατότητα να αντέχουν τις συνεχείς μηχανικές καταπονήσεις που δέχονται κατά το πέρασμά τους ανάμεσα από τα στενά τριχοειδή αγγεία χωρίς να υφίστανται μη αναστρέψιμες παραμορφώσεις (Μohandas and Gallagher, 2008) (Εικ.1). Εικόνα 1: Φυσιολογικά ερυθροκύτταρα από μικροφωτογραφία ηλεκτρονικού μικροσκοπίου σάρωσης (SEM). Τα ερυθροκύτταρα παράγονται στο μυελό των οστών και ειδικότερα στον ερυθρό μυελό των οστών. Στους ενήλικες βρίσκεται στα οστά του κρανίου, στα οστά της ωμικής ζώνης, στους σπονδύλους, στις πλευρές, στα οστά της λεκάνης και στις άνω επιφύσεις του βραχιονίου και του μηριαίου οστού. Κατά την κυτταρική διαφοροποίηση, τα πρόδρομα ερυθροκύτταρα χάνουν τους πυρήνες και τα οργανίδιά τους και συνθέτουν μεγάλες ποσότητες αιμοσφαιρίνης. Ωστόσο τα νέα ερυθροκύτταρα που εξακολουθούν να βρίσκονται στον μυελό των οστών περιέχουν λίγα ριβοσώματα και ονομάζονται δικτυοερυθροκύτταρα. Αυτά, εισέρχονται στην κυκλοφορία και εντός ~ 6 ~
7 λίγων ημερών χάνουν τα υπολειπόμενα ριβοσώματα και μετατρέπονται σε ώριμα ερυθροκύτταρα (Εικ.2) («Φυσιολογία του ανθρώπου»,8 η έκδοση, Vander,2001). 1.2 Η Αιμοσφαιρίνη Τα ερυθροκύτταρα περιέχουν μεγάλες ποσότητες μιας κυτοσολικής πρωτεΐνης, της αιμοσφαιρίνης. Η αιμοσφαιρίνη περιέχει ένα άτομο σιδήρου (Fe) το οποίο ενώνεται με μόρια οξυγόνου. Εναλλακτικά, αλλά σε μικρότερο βαθμό, η αιμοσφαιρίνη ενώνεται και με διοξείδιο του άνθρακα. («Φυσιολογία του ανθρώπου»,8 η έκδοση, Vander et al.2001). Η αιμοσφαιρίνη είναι ένα τετραμερές μόριο που αποτελείται από δύο ειδών αλυσίδες παρόμοιου μήκους, δύο τύπου α με μήκος 141 αμινοξέα και δύο τύπου β με μήκος 146 αμινοξέα. Οι αλυσίδες αυτές μοιάζουν σε μεγάλο βαθμό και ως προς την πρωτοταγή τους δομή και ως προς την τρισδιάστατη μορφή τους στο χώρο («Ιατρική Γενετική», Thompson & Thompson, 2007). Κάθε μία από τις τέσσερις πολυπεπτιδικές αλυσίδες περιέχει μία ομάδα αίμης, η οποία αποτελείται από ένα πορφυρινικό δακτύλιο με ένα άτομο σιδήρου στο κέντρο. Τα ώριμα ερυθροκύτταρα των θηλαστικών δε μπορούν να συνθέσουν από μόνα τους αιμοσφαιρίνη και γενικότερα νέες πρωτεΐνες καθώς στερούνται πυρήνα και ενδοκυττάριων οργανιδίων. Έτσι, η αιμοσφαιρίνη παράγεται από τους ερυθροβλάστες και τα δικτυοερυθροκύτταρα (προγονικά κύτταρα των ερυθροκυττάρων) στον ερυθρό μυελό των οστών (Nikinmaa M., 1990). Εικόνα 2: Σχηματική αναπαράσταση της αιμοποίησης, δηλαδή των διεργασιών που επιτελούνται με σκοπό τη συνεχή αναπαραγωγή των κυττάρων του αίματος. Όλα τα κύτταρα του αίματος (λευκά αιμοσφαίρια, ερυθρά αιμοσφαίρια, αιμοπετάλια), προέρχονται από τα αρχέγονο πολυδύναμα κύτταρα, τα οποία αυτοανανεώνονται, πολλαπλασιάζονται και διαφοροποιούνται σε προγονικά κύτταρα. Τα προγονικά κύτταρα προορίζονται για συγκεκριμένη κυτταρική σειρά και σε αντίθεση με τα αρχέγονα προγονικά διαθέτουν περιορισμένη πολλαπλασιαστική ικανότητα, δεν ~ 7 ~
8 αυτοανανεώνονται και διαφοροποιούνται με μη αναστρέψιμο τρόπο προς κάποια κυτταρική σειρά (Ανατύπωση από Wikipedia, the free encyclopedia ). Όσον αφορά στο σίδηρο, αυτός συναντάται σε δισθενή (ανηγμένη) ή τρισθενή μορφή (οξειδωμένη). Ωστόσο, το οξυγόνο προσδένεται στην αίμη μόνο όταν ο σίδηρος βρίσκεται στην ανηγμένη του μορφή δημιουργώντας την οξυαιμοσφαιρίνη, δηλαδή τη μορφή της αιμοσφαιρίνης που έχει την ικανότητα αντιστρεπτής οξυγόνωσης. Παρόλα αυτά, ένα μικρό ποσοστό της αιμοσφαιρίνης μετατρέπεται σε μεθαιμοσφαιρίνη η οποία προκύπτει από την αυθόρμητη οξείδωση του σιδήρου στην τρισθενή του μορφή. Το μόριο αυτό δεν είναι ικανό για αντιστρεπτή οξυγόνωση. Για το λόγο αυτό, το ένζυμο αναγωγάση της μεθαιμοσφαιρίνης αναλαμβάνει το ρόλο της διατήρησης του σιδήρου της αίμης στην ανηγμένη του μορφή,ώστε να επιτυγχάνεται η απόδοση του οξυγόνου από τους πνεύμονες στους ιστούς («Ιατρική Γενετική», Thompson & Thompson, 2007). 1.3 Ερυθροκυτταρική μεμβράνη Η ερυθροκυτταρική μεμβράνη, η οποία καταλαμβάνει επιφάνεια 163μm 2 κατά πολύ μεγαλύτερη δηλαδή από την επιφάνεια μιας σφαίρας όγκου ίσου με του ερυθροκυττάρου (85μm 2 ), είναι μία από τις καλύτερα μελετημένες ευκαρυωτικές μεμβράνες, αποτελώντας πρότυπο σύστημα διερεύνησης της οργάνωσης και λειτουργίας των διαφόρων συστατικών μορίων στις βιολογικές μεμβράνες. Το απύρηνο ώριμο ερυθροκύτταρο, του οποίου η διάμετρος κυμαίνεται στα 6-8μm, αποτελείται μόνο από την εξωτερική μεμβράνη, ενώ δεν έχει άλλες μεμβράνες εσωτερικά. Η ευελιξία των ερυθροκυττάρων, η οποία τους επιτρέπει να περνούν μέσα από τριχοειδή μικρότερης διαμέτρου χωρίς να υφίστανται λύση, καθώς και η ικανότητα τους να παραμορφώνονται αντιστρεπτά διατηρώντας τη δομική τους ακεραιότητα, οφείλονται στις ιδιότητες της ερυθροκυτταρικής μεμβράνης και στον κυτταροσκελετό. Η ερυθροκυτταρική μεμβράνη αποτελεί μία πολύπλοκη δομή που περιλαμβάνει πληθώρα συστατικών (Yiqin and Jufan, 2007). Η λιπιδική διπλοστοιβάδα, η οποία χαρακτηρίζει την ερυθροκυτταρική μεμβράνη, αποτελείται από φωσφολιπίδια και χοληστερόλη και αγκυροβολεί σε ένα δυσδιάστατο ελαστικό δίκτυο σκελετικών πρωτεϊνών. Η αγκυροβόληση επιτυγχάνεται μέσω περιοχών αγκυροβόλησης που βρίσκονται πάνω στις κυτταροπλασματικές περιοχές των βυθισμένων στη λιπιδική διπλοστοιβάδα διαμεμβρανικών πρωτεϊνών (Mohandas and Gallagher, 2008). Σχετικά με τη χημική σύσταση της μεμβράνης, αυτή καταλαμβάνεται κατά 52% από πρωτεΐνες, 40% από λιπίδια και 8% από πολυσακχαρίτες. Αξίζει να αναφερθεί πως το 95% των ολικών λιπιδίων της ερυθροκυτταρικής μεμβράνης το αποτελούν η χοληστερόλη και τα φωσφολιπίδια ενώ το υπόλοιπο 5% καταλαμβάνεται από γλυκοσφιγγολιπίδια (Εικ.3). ~ 8 ~
9 Εικόνα 3: Ρευστό μωσαϊκό μοντέλο της μεμβρανικής δομής. Οι γλυκοπρωτεΐνες είναι σημαντικές για την κυτταρική σηματοδότηση, την κυτταρική αναγνώριση και την κυτταρική προσκόλληση στους ιστούς. Τα γλυκολιπίδια βρίσκονται στην εξωτερική πλευρά της μεμβράνης, προσκολλώνται στα φωσφολιπίδια της μεμβράνης και έχουν σημαντικό ρόλο στην κυτταρική σηματοδότηση και αναγνώριση. Η χοληστερόλη περιορίζει την κίνηση των παρακείμενων φωσφολιπιδίων με αποτέλεσμα τη μείωση της ρευστότητας και την αύξηση της σταθερότητας της μεμβράνης. Οι διαμεμβρανικές πρωτεΐνες βρίσκονται μόνιμα συνδεδεμένες στη μεμβράνη ενώ οι περιφερειακές αλληλεπιδρούν με πρωτεΐνες και λιπίδια αλλά δεν εισχωρούν στο λιπιδικό στρώμα και υπερέχουν ποσοτικά. (Ανατύπωση από Cell and Molecular Biology, Gerald Karp, 2008). 1.4 Μεμβρανικά λιπίδια Η λιπιδική διπλοστιβάδα αποτελείται από χοληστερόλη και φωσφολιπίδια σε αναλογικά ίσες ποσότητες. Ενώ η χοληστερόλη κατανέμεται ισομερώς ανάμεσα στα δύο φύλλα, τα φωσφολιπίδια (τα τέσσερα κυρίαρχα), είναι ασυμμετρικά κατανεμημένα στα δύο μισά της λιπιδικής διπλοστιβάδας. Αναλυτικότερα, η φωσφατιδυλοχολίνη και η σφιγγομυελίνη κυριαρχούν στην εξωτερική μονοστιβάδα της μεμβράνης, ενώ το μεγαλύτερο ποσό της φωσφατιδυλοαιθανολαμίνης και όλη η ποσότητα της φωσφατιδυλοσερίνης μαζί με μικροποσότητες φωσφοϊνοσιτιδίων περιορίζονται στην εσωτερική μονοστιβάδα (Εικ.4). Έχουν βρεθεί πολλοί διαφορετικοί τύποι πρωτεϊνών μεταφοράς (εξαρτώμενων ή ανεξάρτητων από ATP) φωσφολιπιδίων που έχουν ως σκοπό τη διατήρηση της φωσφολιπιδικής ασυμμετρίας (Μohandas and Gallagher, 2008). Τα μόρια των φωσφολιπιδίων παρουσιάζουν μικρή τάση να περνούν από τη μία λιπιδική μονοστιβάδα στην άλλη, διαδικασία που ονομάζεται flip-flop. Αυτή η κατακόρυφη ροή, αν πάρει μεγαλύτερες διαστάσεις, απειλεί τη φωσφολιπιδική ασυμμετρία κατά τη διάρκεια ζωής του ερυθροκυττάρου. Προς αποφυγή αυτής της εν δυνάμει καταστροφικής κατάστασης, έχει αναπτυχθεί ένας μηχανισμός ενεργής μεταφοράς των αμινοφωσφολιπιδίων που έχουν περάσει στην εξωτερική μονοστιβάδα πάλι πίσω στην εσωτερική. Μία ATP-εξαρτώμενη πρωτεΐνη, η αμινοφωσφολιπιδική μετατοπάση, είναι το υπεύθυνο ένζυμο για τη διαδικασία αυτή. Η απενεργοποίηση του ενζύμου, είτε λόγω απουσίας ATP είτε από άλλα αίτια όπως πχ. οξείδωση, θα οδηγήσει τελικά σε απώλεια της φωσφολιπιδικής ασυμμετρίας της μεμβράνης. Αυτό θα έχει ως αποτέλεσμα την αναγνώριση των ερυθροκυττάρων ~ 9 ~
10 από τα μακροφάγα και την επικείμενη καταστροφή τους στο σπλήνα (Μohandas and Gallagher, 2008). Εικόνα 4: Η εισαγωγή της χοληστερόλης στη μεμβράνη. Η χοληστερόλη εισέρχεται εντός της μεμβράνης με την πολική υδροξυλική της ομάδα κοντά στις πολικές κεφαλές των φωσφολιπιδίων (Ανατύπωση από The Cell: A Molecular Approach, G.M. Cooper, 2 nd edition, 2000). 1.5 Πρωτεΐνες της ερυθροκυτταρικής μεμβράνης Η ερυθροκυτταρική μεμβράνη αποτελείται από διαμεμβρανικές πρωτεΐνες που διαπερνούν τη λιπιδική διπλοστοιβάδα, μεμβρανοσυνδεόμενες πρωτεΐνες οι οποίες εισχωρούν στη μεμβράνη αλλά δεν τη διαπερνούν και σκελετικές πρωτεΐνες οι οποίες συμμετέχουν στη δημιουργία του κυτταροσκελετού Διαμεμβρανικές Με την τεχνική του ψυκτοτεμαχισμού και της ψυκτοεξάχνωσης, οι διαμεμβρανικές πρωτεΐνες εμφανίζονται στο ηλεκτρονικό μικροσκόπιο ως διαμεμβρανικά σωματίδια με πυκνότητα περίπου 5000 σωματίδια/μm 2. Έχουν βρεθεί περισσότερες από 300 διαμεμβρανικές πρωτεΐνες, η αφθονία των οποίων ποικίλλει από μερικές εκατοντάδες μέχρι ένα εκατομμύριο αντίγραφα ανά ερυθροκύτταρο. Οι πρωτεΐνες αυτές παρουσιάζουν λειτουργική ετερογένεια. Κάποιες από αυτές έχουν ως κύρια λειτουργία τους τη μεταφορά ουσιών, όπως η ζώνη 3 (ανιοντικός ανταλλάκτης), η υδατοπορίνη 1 (μεταφορέας νερού), ο Glut 1 (Glucose transporter 1- μεταφορέας γλυκόζης και αφυδροασκορβικού οξέος), η πρωτεΐνη του αντιγόνου Kidd (μεταφορέας ουρίας), η RhAG (μεταφορέας αερίων, κυρίως διοξειδίου του άνθρακα), η ATPάση Na + -K +, η ATPάση Ca ++, ο συμμεταφορέας Na + -K + -2Cl -, ο συμμεταφορέας Na + -K, ο συμμεταφορέας K + -Cl - και τα κανάλια Gardos. Μεμβρανικές πρωτεΐνες με λειτουργία προσκόλλησης περιλαμβάνουν τις ICAM-4 (Intracellular adhesion molecules), που αλληλεπιδρούν με ιντεγκρίνες, και τις Lu, που προσδένονται σε λαμινίνες (Μohandas and Gallagher, 2008). ~ 10 ~
11 Ζώνη 3 Πρόκειται για μέλος της οικογένειας των ανιονικών ανταλλακτών και αποτελεί την μεγαλύτερη σε αφθονία πρωτεΐνη της ερυθροκυτταρικής μεμβράνης, με 10 6 αντίγραφα ανά κύτταρο. Το μοριακό της βάρος ανέρχεται περίπου στα 100kDa (Bruce L., 2006). Καταλαμβάνει το 25% της επιφάνειας της ερυθροκυτταρικής μεμβράνης περίπου και αναλαμβάνει έναν μεγάλο αριθμό λειτουργιών, την ανταλλαγή ιόντων, τη ρύθμιση του γλυκολυτικού μονοπατιού, τη σταθεροποίηση της μεμβρανικής δομής και τον έλεγχο της μέσης διάρκειας ζωής του ερυθροκυττάρου (Shimo et al., 2015). H Ζώνη 3 επιτελεί σημαντικό ρόλο στην ανταλλαγή αερίων στο ερυθροκύτταρο, καθώς και στη διατήρηση του ενδοκυτταρικού ph. Ο ρόλος της στη διατήρηση της σταθερότητας της μεμβράνης επιτυγχάνεται λόγω του ότι η πρωτεΐνη αυτή λειτουργεί σαν ένα σημείο προσκόλλησης του κυτταροσκελετού στη μεμβράνη διατηρώντας έτσι τις μηχανικές ιδιότητες του ερυθροκυττάρου. Πρόκειται για μια γλυκοζυλιωμένη πρωτεΐνη αποτελούμενη από 911 αμινοξικά κατάλοιπα, η οποία απαρτίζεται από τρεις διακριτές περιοχές στην ερυθροκυτταρική μεμβράνη, η κάθε μία από τις οποίες έχει και διαφορετικό ρόλο. Μία μεγάλη αμινοτελική κυτταροπλασματική περιοχή (αμινοξέα 1-359) που συνδέεται με περιφερειακές πρωτεΐνες και αποτελεί την περιοχή σύνδεσης ανάμεσα στη μεμβράνη και τον υπομεμβρανικό σκελετό του ερυθροκυττάρου. Η περιοχή αυτή συνδέεται με την αγκυρίνη, την πρωτεΐνη 4.1, την πρωτεΐνη 4.2 και την αδουσίνη, ενώ αποτελεί και θέση ανταγωνιστικής δέσμευσης ανάμεσα στην οξυαιμοσφαιρίνη και σε πολλά γλυκολυτικά ένζυμα. Η καρβοξυτελική περιοχή (αμινοξέα ), η οποία αποτελείται από διαμεμβρανικά τμήματα και εκτελεί την ανταλλαγή ιόντων. Τέλος σε μία μικρή κυτταροπλασματική ουρά 33 αμινοξέων του καρβοξυτελικού άκρου βρίσκεται η περιοχή δέσμευσης για την καρβονική ανυδράση ΙΙ. Στα ερυθροκύτταρα, η ζώνη 3 απαντάται κυρίως υπό τη μορφή διμερών (60%) ή τετραμερών (40%). Η σύσταση του διμερούς συμπλόκου, περιλαμβάνει σύνδεση μορίων ζώνης 3 με την πρωτεΐνη 4.1, η οποία με τη σειρά της συνδέεται με άλλες πρωτεΐνες, όπως η αδουσίνη, η GPC (γλυκοφορίνη C) και η πρωτεΐνη p55, δημιουργώντας ένα πολυπρωτεϊνικό σύμπλοκο (Αkker et al., 2010). Στην τετραμερή της μορφή, η ζώνη 3 συνδέεται στην αγκυρίνη και στην πρωτεΐνη 4.2. Η σύνδεση αυτή βοηθά τη ζώνη 3 να προσκολληθεί στη β-σπεκτρίνη (Michaeli and Bennett, 1995). Επιπλέον, το σύμπλεγμα Rh (Rhesus), αποτελούμενο από τα αντιγόνα Rh, τις συνδεμένες με Rh γλυκοπρωτεΐνες RhAG, το μόριο LW (Landsteiner-Wiener), την πρωτεΐνη CD47 (Cluster of Differentiation 47) και τη GPB (γλυκοφορίνη B), συνδέεται επίσης με την ζώνη 3 (Αkker et al., 2010). Αυτή η αλληλεπίδραση με τις πρωτεΐνες του συμπλόκου Rhesus καθώς και με την GPA (γλυκοφορίνη A), έχει σαν αποτέλεσμα τη δημιουργία ενός πολυπρωτεϊνικού συμπλόκου, το οποίο ονομάζεται μακροσύμπλοκο της ζώνης 3 (Bruce L., 2006) (Εικ.5). Η σύνδεση του καρβοξυτελικού άκρου με την καρβονική ανυδράση II είναι απαραίτητη για την ενυδάτωση του διοξειδίου του άνθρακα και τη μεταφορά του από τους ιστούς στους πνεύμονες (Tanner M., 2002). Η αποδοτική μεταφορά τους διοξειδίου του άνθρακα και του οξυγόνου στους πνεύμονες και στους ιστούς οφείλεται στη λειτουργία της ζώνης 3. Στους ιστούς, το διοξείδιο του άνθρακα παραλαμβάνεται από τα ερυθροκύτταρα και μετατρέπεται με τη βοήθεια της καρβονικής ανυδράσης II σε διττανθρακικά ιόντα (HCO - 3 ) και H + -. Το HCO 3 ανταλλάσσεται με το Cl - μέσω της ζώνης 3 και το H + προσδένεται στην αιμοσφαιρίνη διευκολύνοντας με αυτόν τον τρόπο την απελευθέρωσή του οξυγόνου. Έτσι επιτρέπεται η μεταφορά του διοξειδίου του άνθρακα στο πλάσμα υπό μορφή HCO - 3, ενώ προωθείται αποτελεσματικά η απελευθέρωση του οξυγόνου στους ιστούς. Στους πνεύμονες ακολουθείται η αντίστροφη διαδικασία (Bruce L., 2008). ~ 11 ~
12 Τέλος, ένα χαρακτηριστικό της ζώνης 3 είναι η δημιουργία συσσωματωμάτων τα οποία συμμετέχουν στην απομάκρυνση των ερυθροκυττάρων από την κυκλοφορία. Πιο συγκεκριμένα, η συσσωμάτωση της ζώνης 3 υπό συνθήκες στρες, δημιουργεί μία περιοχή υψηλής συγγένειας για την πρόσδεση αυτόλογων αντισωμάτων τα οποία αναγνωρίζονται από τα μακροφάγα και οδηγούν στην ερυθροφαγοκυττάρωση. Παρόλο που η δημιουργία συσσωματωμάτων της ζώνης 3 έχει συσχετισθεί στενά με συγκεκριμένες διαταραχές της ερυθροκυτταρικής μεμβράνης που προκαλούν αιμολυτική αναιμία, δεν έχουν κατανοηθεί πλήρως οι μηχανισμοί δημιουργίας τους (Stefanovic et al., 2012). Εικόνα 5: Σχηματική αναπαράσταση της ανθρώπινης ερυθροκυτταρικής μεμβράνης, της ζώνης 3 και των αλληλεπιδράσεών της (Ανατύπωση από Pediatric Hereditary Elliptocytosis and Related Disorders, Trisha Simone Tavares, 2013). Γλυκοφορίνες Οι γλυκοφορίνες είναι διαμεμβρανικές πρωτεΐνες της ερυθροκυτταρικής μεμβράνης, με το αμινοτελικό τους άκρο να βρίσκεται στην εξωκυττάρια περιοχή και είναι πλούσιες σε σιαλικό οξύ. Οι γλυκοφορίνες που εντοπίζονται στον άνθρωπο ανήκουν στην οικογένεια των σιαλογλυκοπρωτεϊνών, η οποία περιλαμβάνει τις γλυκοφορίνες Α (GPA), τις γλυκοφορίνες Β (GPB), τις γλυκοφορίνες C (GPC), τις γλυκοφορίνες D (GPD) και τις γλυκοφορίνες Ε (GPE) ή διαφορετικά τις α, β, γ,δ γλυκοφορίνες και την GPE. Tο μοριακό βάρος των γλυκοφορινών ποικίλλει από kda. Οι γλυκοφορίνες A, B και Ε φέρουν τα αντιγόνα της ομάδας αίματος MNS, ενώ οι γλυκοφορίνες C και D φέρουν αυτά της ομάδας αίματος Gerbich (Ge) (Yiqin and Junfan, 2007). Oι γλυκοφορίνες A και D είναι οι πιο άθφονες γλυκοπρωτεΐνες στα ερυθροκύτταρα, με την Α να διαθέτει τα περισσότερα αντίγραφα ( ) ανά ερυθροκύτταρο. Oι γλυκοφορίνες αυτές σχηματίζουν ομοδιμερή σύμπλοκα Α 2 και D 2 καθώς και ετεροδιμερή A D (Merry et al., 1986). Η γλυκοφορίνη Α έχει αποτελέσει αντικείμενο μελέτης για πολλά χρόνια καθώς έχει βρεθεί πως παίζει ρόλο στις αλλαγές του σχήματος των ερυθροκυττάρων (Chasis et al., 1985). Η γλυκοφορίνη Β έχει παρόμοια οργάνωση στη μεμβράνη με αυτή της Α αλλά διαθέτει πολύ λιγότερα αντίγραφα (50.000) ανά ερυθροκύτταρο. Σε αντίθεση με τις γλυκοφορίνες Α και D, οι γλυκοφορίνες Β και C συνδέονται με τον ερυθροκυτταρικό σκελετό. Πιο συγκεκριμένα, έχει προταθεί πως η γλυκοφορίνη Β αλληλεπιδρά με την πρωτεΐνη 4.1 (Anstee and Tanner, 1986) ενώ η σύνδεση της γλυκοφορίνης C με την πρωτεΐνη 4.1 αποτελεί σημαντικό συστατικό του μηχανισμού αγκυροβόλησης της λιπιδικής ~ 12 ~
13 διπλοστιβάδας με τον υπομεμβρανικό σκελετό (Reid et al., 1987). Τα ερυθροκύτταρα στα οποία λείπει η GPA ή η GPB ή και οι δύο αυτές γλυκοφορίνες, εμφανίζουν κανονικά το δισκοειδές τους σχήμα, ενώ τα ερυθροκύτταρα με έλλειψη της γλυκοφορίνης C, εμφανίζουν ελλειψοειδές σχήμα καθώς επίσης μειωμένη ικανότητα παραμόρφωσης και μηχανική σταθερότητα (Reid et al., 1990) Μεμβρανοσυνδεόμενες πρωτεΐνες Στοματίνη Η στοματίνη είναι μία μεμβρανοσυνδεόμενη πρωτεΐνη μοριακού βάρους 31kDa. Αποτελείται από 288 αμινοξικά κατάλοιπα από τα οποία τα πρώτα 25 σχηματίζουν το εξωκυτταρικό τμήμα του μορίου που δε φέρει υδατάνθρακες, τα το διαμεμβρανικό τμήμα που περνά στη λιπιδική διπλοστιβάδα, ενώ τα υπόλοιπα κατάλοιπα αποτελούν μία μεγάλη κυτταροπλασματική περιοχή. Ενσωματώνεται στη μεμβράνη ως δομή που θυμίζει φουρκέτα, με την υδρόφοβη αλληλουχία να διεισδύει στο λιπιδικό στρώμα (Desneves et al., 1996). H στοματίνη σχετίζεται με τις λιπιδικές σχεδίες σχηματίζοντας σύμπλοκα λιπιδίων-πρωτεϊνών. Λειτουργεί σαν ικρίωμα ενώ παράλληλα ελέγχει τη δράση διαφόρων πρωτεϊνών, όπως αυτή του μεταφορέα γλυκόζης καθώς και ιονικών καναλιών και ρυθμίζει αντιστρεπτά τη συμμετοχή τους στις λιπιδικές σχεδίες (Salzer et al., 2007) Σκελετικές Ο κυτταροσκελετός είναι ένα νηματοειδές δίκτυο, το οποίο αποτελείται από τρία βασικά συστατικά: την σπεκτρίνη (α και β), τη β-ακτίνη και την πρωτεΐνη 4.1. Ο εύκαμπτος κυτταροσκελετός απαρτίζεται κυρίως από πολυμερή μόρια σπεκτρίνης, τα οποία ενώνονται μέσω της ακτίνης και της πρωτεΐνης 4.1 σε κόμβους που ονομάζονται σύμπλοκα ζεύξης (junctional complexes) (Gov et al., 2009). Eκτός από αυτά, το δυσδιάστατο υπομεμβρανικό σκελετικό δίκτυο που βασίζεται στην σπεκτρίνη, περιλαμβάνει και άλλες πρωτεΐνες, όπως η αδουσίνη, η δεματίνη, η τροπομυοσίνη και η τροπομοντουλίνη, η αγκυρίνη, η πρωτεΐνη p55 και η παλλιδίνη (Mohandas and Gallagher, 2008). Σπεκτρίνη Η σπεκτρίνη, το κύριο συστατικό του υπομεμβρανικού σκελετού, δημιουργεί νημάτια που χαρακτηρίζονται από ευκαμψία και καταλαμβάνει το 20-25% της μάζας των πρωτεϊνών της ερυθροκυτταρικής μεμβράνης. Αποτελείται τις υπομονάδες α και β που είναι διαφορετικές μεταξύ τους και συνδέονται μεταξύ τους με σκοπό τον σχηματισμό ενός ετεροδιμερούς. Τα ετεροδιμερή αυτά συνδέονται μεταξύ τους κεφαλή με κεφαλή προς σχηματισμό τετραμερών (Gov et al., 2009). Οι ποσότητες των υπομονάδων, δηλαδή η α-σπεκτρίνη και η β- σπεκτρίνη είναι ίσες μεταξύ τους, αλλά κωδικοποιούνται από διαφορετικά γονίδια. Κάθε ερυθροκύτταρο περιέχει περίπου αντίγραφα σπεκτρίνης α και β. Το μοριακό βάρος της α- σπεκτρίνης ανέρχεται στα 240kDa, και συνίσταται από 20 επαναλαμβανόμενες δομές μήκους 106 αμινοξέων η κάθε μία και δύο μη ~ 13 ~
14 επαναλαμβανόμενες δομές, ενώ το μοριακό βάρος της β- σπεκτρίνης είναι 220 kda, με 17 επαναλαμβανόμενες δομές μήκους επίσης 106 αμινοξέων καθώς και μία δομή στο αμινοτελικό άκρο που αποτελεί τη θέση δέσμευσης της ακτίνης και μία μικρή περιοχή στο καρβοξυτελικό άκρο, η οποία περιέχει μία ακολουθία που φωσφορυλιώνεται από την κασεΐνη. Οι κύριες λειτουργίες της σπεκτρίνης είναι η διατήρηση του σχήματος του ερυθροκυττάρου, η ρύθμιση της πλευρικής κίνησης των δομικών μεμβρανικών πρωτεϊνών καθώς και η προσφορά μηχανικής υποστήριξης στη λιπιδική διπλοστιβάδα (Yiqin and Junfan, 2007). Οι αλυσίδες της α- και β- σπεκτρίνης συντίθενται σε περίσσεια και τοποθετούνται σε αντιπαράλληλη διάταξη ενώ συνδέονται ομοιοπολικά μεταξύ τους σε πολλά σημεία και στα άκρα τους προς σχηματισμό του ετεροδιμερούς. Η έναρξη της σύνθεσης γίνεται στην περιοχή πυρήνωσης ενώ ο σχηματισμός του ετεροτετραμερούς μήκους 200nm πραγματοποιείται απέναντι από αυτήν, σε δύο ταυτόσημες και αντιπαράλληλα προσανατολισμένες θέσεις, που ονομάζονται περιοχές αυτοσυγκρότησης. Αγκυρίνη Η αγκυρίνη είναι η πρωτεΐνη μέσω της οποίας η σπεκτρίνη προσκολλάται στην ερυθροκυτταρική μεμβράνη. Η αγκυρίνη των ανθρώπινων ερυθροκυττάρων αποτελείται από 1881 αμινοξικά κατάλοιπα, το μοριακό της βάρος ανέρχεται στα 206kDa και περιλαμβάνει τρεις λειτουργικές περιοχές. Το αμινοτελικό της άκρο βάρους 89kDa που περιλαμβάνει τη θέση σύνδεσης για την ζώνη 3, την κεντρική περιοχή των 62kDa, στην οποία εμπεριέχονται οι θέσεις δέσμευσης της β- σπεκτρίνης και των ενδιάμεσων νηματοειδών πρωτεϊνών βιμεντίνη και δεσμίνη, και τέλος το εναπομείναν λειτουργικό καρβοξυτελικό άκρο βάρους 55kDa, που ρυθμίζει την αλληλεπίδραση της αγκυρίνης με την σπεκτρίνη και τη ζώνη 3 (Υiqin and Junfan, 2007). Πρωτεΐνη 4.1 Η πρωτεΐνη 4.1 (και συγκεκριμένα η 4.1R η οποία αποτελεί μέλος της οικογένειας των 4.1 πρωτεϊνών), συνιστά περίπου το 6% της συνολικής ποσότητας των πρωτεϊνών της ερυθροκυτταρικής μεμβράνης και συναντάται σε δύο ισομορφές, την 4.1α και την 4.1b, με μοριακά βάρη 80kDa και 78kDa αντίστοιχα (Υiqin and Junfan, 2007). Κύρια λειτουργία της πρωτεΐνης 4.1R των ερυθροκυττάρων, είναι να συνεισφέρει στην ενίσχυση των μηχανικών ιδιοτήτων της μεμβράνης, προωθώντας την αλληλεπίδραση μεταξύ ακτίνης και σπεκτρίνης. Ακόμα, η παρουσία της κρίνεται απαραίτητη για την σταθερή σύνδεση στον υπομεμβρανικό σκελετό πληθώρας άλλων πρωτεϊνών (Baines et al., 2009). Οι λειτουργικές περιοχές της πρωτεΐνης 4.1R των ερυθροκυττάρων είναι δύο : 1) η περιοχή μοριακού βάρους 10kDa, η οποία αλληλεπιδρά με το αμινοτελικό άκρο της β-σπεκτρίνης προκειμένου να πραγματοποιηθεί η σύνδεση σπεκτρίνης-ακτίνης και 2) το αμινοτελικό της άκρο που προσδένεται στην GPC και στα αρνητικά φορτισμένα λιπίδια στα εσωτερικά φύλλα της λιπιδικής διπλοστιβάδας, κάνοντας έτσι τα απομακρυσμένα άκρα του τετραμερούς της σπεκτρίνης να προσκολληθούν στην ερυθροκυτταρική μεμβράνη (Υiqin and Junfan, 2007). Η πρωτεΐνη 4.1R προσδένεται επίσης στα φωσφολιπίδια φωσφατιδυλοσερίνη (phosphatidylserine-ps) και στην 4,5- διφωσφορική φωσφατιδυλοϊνοσιτόλη (phosphatidylinositol-pip 2 ). Οι διαμεμβρανικές πρωτεΐνες ζώνη 3 και γλυκοφορίνη C συνδέονται επίσης στενά με την πρωτεΐνη 4.1R. Μία περιοχή 30kDa, γνωστή με το όνομα FERM domain (F for protein 4.1, E for ezrin, R for radixin, M for moesin), είναι αυτή που εξασφαλίζει τις ικανότητες πρόσδεσης της πρωτεΐνης 4.1R. Η ~ 14 ~
15 περιοχή αυτή διαθέτει 3 σφαιρικούς λοβούς. Κάθε λοβός περιέχει μία μοναδική περιοχή πρόσδεσης του κατάλληλου συνδέτη: η ζώνη 3 προσδένεται στον λοβό Α (αμινοτελική περιοχή), η γλυκοφορίνη C στον κεντρικό λοβό Β και οι p55 και φωσφατιδυλοσερίνη προσδένονται στον λοβό C (καρβοξυτελική περιοχή). Η PIP 2 προσδένεται ανάμεσα στους λοβούς Α και C. Αδουσίνη Η αδουσίνη είναι ένα ετεροτετραμερές του υπομεμβρανικού σκελετού, που αποτελείται από τις υπομονάδες α και β και επιτελεί σημαντικές και ποικίλες λειτουργίες. Η πρωτεΐνη αυτή δημιουργεί μία γέφυρα η οποία συνδέει το σύμπλοκο σπεκτρίνης- ακτίνης στη ζώνη 3. Η σύνδεση αυτή συνιστά την κυριότερη σύνδεση μεταξύ πρωτεϊνών της ερυθροκυτταρικής μεμβράνης, καθώς αν αυτή διακοπεί, θα προκληθεί μεμβρανική αστάθεια και κυστιδιοποίηση. Επίσης η αδουσίνη λειτουργεί και ως πρωτεΐνη κάλυψης των νηματίων ακτίνης, παρεμποδίζοντας την επιμήκυνσή τους, ενώ προάγει και σταθεροποιεί τη σύνδεση σπεκτρίνης στην ακτίνη. Έτσι, διασφαλίζει πως το σύμπλοκο ακτίνης- σπεκτρίνης παραμένει άθικτο παρά τις μηχανικές παραμορφώσεις που υφίσταται το ερυθροκύτταρο κατά την κυκλοφορία του. Τέλος, η αδουσίνη ανταποκρίνεται στα κρίσιμα ερεθίσματα για τη διατήρηση του συνόλου των ιδιοτήτων του ερυθροκυττάρου, όπως είναι η μεταφορά κατιόντων, η μορφολογία του κυττάρου και η μεμβρανική ικανότητα παραμόρφωσης (Franco and Low, 2010). Όσον αφορά στη δομή της, όπως αναφέρθηκε, αυτή αποτελείται από δύο υπομονάδες, 103kDa και 97kDa αντίστοιχα (Nehls et al., 1991). Kάθε μία από τις υπομονάδες διαθέτει τρεις λειτουργικές περιοχές: την αμινοτελική κεφαλή, την αυχενική περιοχή, η οποία εμπλέκεται στη σύνδεση των μονομερών στα λειτουργικά ετεροδιμερή της πρωτεΐνης και τέλος την ανθεκτική σε πρωτεάσες καρβοξυτελική περιοχή, η οποία και θεωρείται υπεύθυνη για τη σύνδεση σπεκτρίνηςακτίνης (Hughes and Bennett, 1995). Η αδουσίνη εμφανίζεται στην ερυθροκυτταρική μεμβράνη είτε με τη μορφή ετεροδιμερούς, είτε με τη μορφή ετεροτετραμερούς, με την μικρότερη από τις δύο υπομονάδες να προσδένει καλμοντουλίνη με έναν τρόπο εξαρτώμενο από ιόντα Ca 2+ (Palfrey and Waseem, 1985). Τα ετεροδιμερή και ετεροτετραμερή ανέρχονται σε αντίγραφα ανά ερυθροκύτταρο, ενώ οι επιμέρους υπομονάδες κωδικοποιούνται από τρία συνδεμένα γονίδια : το ADD1 (Alpha Adducin) που κωδικοποιεί την περιοχή α, το ADD2 που κωδικοποιεί την β και το ADD3 τη γ. Οι α και γ υπομονάδες βρίσκονται παντού, ενώ η β εκφράζεται μόνο στον εγκέφαλο και στους αιμοποιητικούς ιστούς (Franco and Low, 2010). Ενώ η αδουσίνη προωθεί τη σύνδεση σπεκτρίνης-ακτίνης, η σύνδεση αυτή αναστέλλεται, όταν σε αυτήν προσδένεται η καλμοντουλίνη. Πιο συγκεκριμένα, ενώ αδουσίνη προωθεί την πρόσδεση της σπεκτρίνης στην ακτίνη ανεξάρτητα από την πρωτεΐνη 4.1R,η πρόσδεση της αδουσίνης στην ακτίνη και ικανότητά της να διεγείρει τη σύνδεση της τελευταίας με την σπεκτρίνη εξαρτάται από την καλμοντουλίνη (Palfrey and Waseem, 1985). Παλλιδίνη (Πρωτεΐνη 4.2) Η περιφερειακή πρωτεΐνη 4.2 είναι ένα από τα πιο άφθονα πρωτεϊνικά συστατικά της ερυθροκυτταρικής μεμβράνης. Αντιπροσωπεύει περίπου το 5% της μεμβρανικής πρωτεϊνικής σύστασης με 2,5x10 5 αντίγραφα ανά ερυθροκύτταρο. Υπάρχουν δύο ισομορφές της πρωτεΐνης, μία ~ 15 ~
16 κύρια μοριακού βάρους 72kDa και μία δευτερεύουσα μοριακού βάρους 74kDa. Η πρωτεΐνη 4.2 έχει την ικανότητα να αλληλεπιδρά απευθείας με την εσωτερική στιβάδα της ερυθροκυτταρικής μεμβράνης. Προσδένεται στην αμινοτελική κυτταροπλασματική περιοχή της ζώνης 3, ενώ επίσης αλληλεπιδρά και με την αγκυρίνη. Επίσης, έχει βεθεί πως αλληλεπιδρά με την πρωτεΐνη CD47 (μία πρωτεΐνη του συμπλέγματος Rhesus) βοηθώντας στην αγκυροβόλησή του στον υπομεμβρανικό σκελετό. Η πρωτεΐνη 4.2 διαδραματίζει έναν πολύ σημαντικό ρόλο στη διατήρηση της δομικής ακεραιότητας της ερυθροκυτταρικής μεμβράνης μέσω των αλληλεπιδράσεων της με τον ανιοντικό μεταφορέα Β3 (ζώνη 3) και με άλλα συστατικά του κυτταροσκελετού. Προστατεύει επίσης το ερυθροκύτταρο από φαγοκυττάρωση, μέσω της σύνδεσής της με το μόριο CD47, το οποίο αποτελεί το non-eat me σήμα του κυττάρου (Satchwell et al., 2009). Σε περιπτώσεις έλλειψης της παλλιδίνης, έχει παρατηρηθεί μειωμένη οσμωτική αντίσταση και ήπιας μορφής αιμολυτική αναιμία, με την τελευταία να εμφανίζεται σοβαρότερη σε περιπτώσεις ομοζυγωτίας ως προς την έλλειψη ( Ghanem et al., 1990). Δεματίνη Η δεματίνη είναι μία πρωτεΐνη του κυτταροσκελετού, η οποία προσδένεται πάνω σε μόρια ακτίνης τα οποία και σταθεροποιεί σε νημάτια ορισμένου μήκους (Αzim et al., 1995). Συναντάται στο σύμπλοκο σπεκτρίνης- ακτίνης και η ικανότητά της να πακετάρει την ακτίνη ρυθμίζεται από την φωσφορυλίωσή της από τη camp- εξαρτώμενη πρωτεϊνική κινάση (cyclic Adenosine monophosphate kinase). Η δεματίνη είναι ένα τριμερές μόριο, το οποίο αποτελείται από δύο πολυπεπτίδια 48-kDa το καθένα και από ένα πεπτίδιο με μοριακό βάρος 52-kDa. Στο ερυθροκύτταρο συναντάμε περίπου αντίγραφα του τριμερούς δεματίνης (Khanna et al., 2002). Ένα τριμερές δεματίνης αντιστοιχεί σε ένα ολιγομερές ακτίνης. Παρόλο που η δεματίνη φωσφορυλιώνεται από μία σειρά πρωτεϊνικών κινασών, η φωσφορυλίωση αναστέλλει την ενεργότητα πακεταρίσματος των ινιδίων ακτίνης (Siegel and Branton, 1985). Ωστόσο, η ικανότητά της να προσδένεται στην ακτίνη διατηρείται παρά την φωσφορυλίωση. Πρόσφατα δεδομένα έχουν δείξει πως εξάλειψη μίας συγκεκριμένης περιοχής της δεματίνης οδηγεί σε ήπια σφαιροκυττάρωση συνοδευόμενη από αιμολυτική αναιμία και μειωμένη σταθερότητα της ερυθροκυτταρικής μεμβράνης (Koshino et al., 2012). Ακτίνη- Τροπομυοσίνη- Τροπομοντουλίνη (Ζώνη 5) Η ακτίνη είναι μία σημαντική πρωτεΐνη, απαραίτητη γα τη μυϊκή συστολή και την κυτταρική κίνηση. Κάθε ερυθροκύτταρο περιέχει περίπου μόρια μονομερούς ακτίνης (Gακτίνη), τα οποία πολυμερίζονται ανά μονομερή και σχηματίζουν κοντά νημάτια F-ακτίνης μήκους 30-40nm. Στα ερυθροκύτταρα εμφανίζεται ο β-ισότυπος της ακτίνης (Yiqin and Junfan, 2007). Η ακτίνη εμφανίζεται στο σκελετό με τη μορφή ολιγομερών. Δεδομένου ότι υπάρχουν τετραμερή σπεκτρίνης ανά ερυθροκύτταρο, τελικά αντιστοιχούν 3-4 τετραμερή σπεκτρίνης για κάθε ολιγομερές ακτίνης κατά τον σχηματισμό του σκελετού. Όσον αφορά στην τροπομυοσίνη, η λειτουργία της έγκειται στην ενίσχυση της σταθερότητας της ερυθροκυτταρικής μεμβράνης, πράγμα που το επιτυγχάνει σταθεροποιώντας το σύμπλοκο σπεκτρίνη-ακτίνη-4.1r (An et al., 2007). Η πρωτεΐνη αυτή έχει τη μορφή ράβδου, δημιουργεί διμερή α-έλικας και προσδένεται κατά μήκος των νηματίων ακτίνης σε μυϊκά αλλά και σε μη μυϊκά κύτταρα. Στα ερυθροκύτταρα την συναντάμε σε δύο ισομορφές, με μοριακά βάρη ~ 16 ~
17 27kDa και 29kDa και συνιστά περίπου το 1% των πρωτεϊνών της ερυθροκυτταρικής μεμβράνης με ένα μόριο τροπομυοσίνης να αντιστοιχεί σε 7-8 μονομερή ακτίνης (Fowler and Bennett, 1984). Η τροπομοντουλίνη είναι μία πρωτεΐνη η οποία συνδέεται στην τροπομυοσίνη μπλοκάροντας με αυτόν τον τρόπο την ικανότητα της δεύτερης να συνδέεται στο νημάτιο ακτίνης (Fowler V.M., 1987). Συγκεκριμένα, η τροπομοντουλίνη έχει μοριακό βάρος 40 kda, προσδένεται στο ένα άκρο της τροπομυοσίνης και ανευρίσκεται σε περίπου ισομοριακές ποσότητες με αυτήν στα ερυθροκύτταρα. Εμποδίζει την επιμήκυνση αλλά και τον αποπολυμερισμό των νηματίων ακτίνης in vitro. Καλύπτει δηλαδή τα άκρα τους, περιορίζοντας το μήκος των νηματίων ακτίνης. Η τροπομυοσίνη και η τροπομοντουλίνη λειτουργούν μαζί προκειμένου να σταθεροποιήσουν και να ορίσουν τα μήκη των κοντών νηματίων ακτίνης του υπομεμβρανικού ερυθροκυτταρικού σκελετού (Ursitti and Fowler V, 1994). Πρωτεΐνη p55 Η πρωτεΐνη p55 είναι ένα πολυπεπτίδιο με μοριακό βάρος 55kDa που περιλαμβάνει 466 αμινοξέα. Στο ερυθροκύτταρο συναντάμε αντίγραφα p55 διμερούς μορφής, στο μόριο της οποίας υπάρχει πληθώρα μορίων παλμιτικού οξέως. Η p55 έχει ενεργότητα γουανυλικής κινάσης (Christi et al., 1992). Προσδένεται στην πρωτεΐνη 4.1R και στη γλυκοφορίνη C δημιουργώντας με αυτές ένα τριμερές σύμπλοκο (Alloisio et al., 1993), το οποίο εξασφαλίζει τη διατήρηση της μορφής και των ιδιοτήτων του ερυθροκυττάρου συνδέοντας επίσης το σύμπλοκο σπεκτρίνης ακτίνης με τη λιπιδική διπλοστιβάδα (Κim et al., 1996) Κυτοσολικές πρωτεΐνες Το κυτταροπλασματικό πρωτέωμα του ερυθροκυττάρου αποτελείται σε ποσοστό περίπου 98% από την αιμοσφαιρίνη. Υπεροξειρεδοξίνη-2(Prx-2) Η υπεροξειρεδοξίνη-2 αποτελεί την τρίτη πιο άφθονη πρωτεΐνη στο κυτοσόλιο. Πρόκειται για ένα αντιοξειδωτικό ένζυμο το οποίο αποδομεί τα υπεροξείδια και η καταλυτική του δράση οφείλεται στα ισχυρά συντηρημένα κατάλοιπα κυστεΐνης (Low et al., 2008). Το μοριακό της βάρος έγκειται στα 21.8 kda και στο κυτοσόλιο μπορεί να υφίσταται είτε με τη μορφή διμερών είτε με τη μορφή δεκαμερών. Παρόλο που εντοπίζεται στο κυτοσόλιο, η υπεροξειρεδοξίνη-2 μπορεί να συνδεθεί και στην ερυθροκυτταρική μεμβράνη, όπου εμπλέκεται σε μηχανισμούς άμυνας έναντι της λιπιδικής υπεροξείδωσης. Συγκεκριμένα, σε καταστάσεις υψηλού οξειδωτικού στρες όπου η αιμοσφαιρίνη οξειδώνεται και συνδέεται στη μεμβράνη, παρατηρείται επίσης σύνδεση της υπεροξειρεδοξίνης-2 στη μεμβράνη (Rocha et al., 2005). Επιπλέον, η πρωτεϊνη αυτή δρα και ως μοριακός συνοδός, συμμετέχοντας έτσι στην προστασία άλλων πρωτεϊνών από την αποικοδόμηση (Low et al., 2006). Κλαστερίνη (sclu) Η κλαστερίνη, ή αλλιώς απολιποπρωτεϊνη J, είναι μια ετεροδιμερής γλυκοπρωτεΐνη με συνολικό μοριακό βάρος kda. Μπορεί να εντοπιστεί είτε στην εξωκυττάρια πλευρά της ερυθροκυτταρικής μεμβράνης προερχόμενη από το πλάσμα, είτε στην ενδοκυττάρια πλευρά της ερυθροκυτταρικής μεμβράνης, αλλά επίσης υπάρχει και σε ελεύθερη μορφή στο κυτοσόλιο (Antonelou et al., 2011). ~ 17 ~
18 Όσον αφορά στις λειτουργίες τις, αποτελεί μεταφορέα λιπιδίων καθώς και δείκτη γήρανσης για τα ερυθροκύτταρα. Πιο συγκεκριμένα, η πρωτεΐνη αυτή, προσδένεται σε πρωτεΐνες που έχουν υποστεί βλάβη όπως η ζώνη-3 και η αιμοσφαιρίνη και τις απομακρύνει μέσω κυστιδιοποίησης (Antonelou et al., 2011). Hsp70 (Πρωτεϊνη Θερμικού Σοκ 70-Heat Shock Protein 70) H Hsp70 αποτελεί μία πολύ καλά συντηρημένη πρωτεΐνη που εντάσσεται στην οικογένεια πρωτεϊνών θερμικού σοκ μοριακού βάρους 70 kda. Ανήκει επίσης και στην οικογένεια των πρωτεϊνών μοριακών συνοδών (chaperones) και η έκφρασή της επάγεται από περιβαλλοντικά, φυσικά ή χημικά ερεθίσματα. Εμπλέκεται σε μοριακούς κυτταρικούς μηχανισμούς, όπως η αναδίπλωση των πρωτεϊνών, σε κυτταρικά μονοπάτια, όπως η επιδιόρθωση, η κυτταρική επιβίωση, η θερμοανοχή και η επιδιόρθωση του DNA, καθώς και στην προστασία των οργανισμών από ασθένειες και διάφορες παθολογικές καταστάσεις. Η παρουσία της Hsp70 φαίνεται να προσδίδει ανθεκτικότητα στον προγραμματισμένο κυτταρικό θάνατο μετά από διάφορα εξαρτώμενα ή ανεξάρτητα από κασπάσες ερεθίσματα, όπως ο TNF και το θερμικό ή οξειδωτικό στρες (Lanneau et al., 2008) Σύμπλοκα της ερυθροκυτταρικής μεμβράνης Οι αλληλεπιδράσεις των πρωτεϊνών οδηγούν στη δημιουργία συμπλόκων μεταξύ τους που έχουν ως σκοπό την εξασφάλιση της ακεραιότητας του ερυθροκυττάρου. Ένα από τα πιο σημαντικά σύμπλοκα που σχηματίζονται, είναι το σύμπλοκο της ζώνης 3, το οποίο εμφανίζεται με τη μορφή τετραμερούς και παρέχει τα σημεία αγκυροβόλησης για την αγκυρίνη καθώς και για τις πρωτεΐνες 4.1 και 4.2. Το κυτταροπλασματικό αμινοτελικό άκρο του μονομερούς της ζώνης 3, είναι αυτό που συνδέεται με την αγκυρίνη, η οποία με τη σειρά της συνδέεται στην καρβοξυτελική περιοχή της αλυσίδας της β-σπεκτρίνης. Η πρωτεΐνη 4.2, συνδέεται με την κυτταροπλασματική περιοχή της ζώνης 3, της αγκυρίνης και της πρωτεΐνης 4.1 (Υiqin and Junfan, 2007). Οι πρωτεΐνες του συμπλόκου Rhesus έχουν πολύ σημαντικό βιολογικό ρόλο για το ερυθροκύτταρο, ο οποίος έγκειται στη διατήρηση των μηχανικών ιδιοτήτων του. Οι κυριότερες πρωτεΐνες του συμπλόκου αυτού είναι οι Rh (D και CcEe), RhAG και CD47. Οι Rh/RhAG και CD47 αλληλεπιδρούν με τον σκελετό μέσω της σύνδεσής τους με την αγκυρίνη και την πρωτεΐνη 4.2 (Nicolas et al., 2006). ~ 18 ~
19 Eικόνα 6: Οι αλληλεπιδράσεις και οι συνδέσεις των πρωτεϊνών της ερυθροκυτταρικής μεμβράνης (Ανατύπωση από Patrick G. Gallagher, 2013). Μία από τις σημαντικότερες συνδέσεις, είναι αυτή της σπεκτρίνης στη μεμβράνη, μέσω της πρωτεΐνης 4.1, με τη συμμετοχή νηματίων ακτίνης και άλλων πρωτεϊνών που συνδέονται με την ακτίνη, δημιουργώντας το επονομαζόμενο σύμπλοκο ζεύξης. Παρά τις ασθενείς συνδέσεις της σπεκτρίνης και της 4.1 με την φωσφατιδυλοσερίνη, η οποία βρίσκεται στα εσωτερικό της λιπιδικής διπλοστιβάδας, αυτές οι κατακόρυφες συνδέσεις πρωτεΐνης- πρωτεΐνης και πρωτεΐνης- λιπιδικής διπλοστιβάδας είναι κρίσιμες για τη σταθεροποίηση και τη συγκράτηση της λιπιδικής διπλοστιβάδας στο ερυθροκύτταρο (Υiqin and Junfan, 2007). Οι πρωτεΐνες του υπομεμβρανικού σκελετικού δικτύου συνδέονται μεταξύ τους σχηματίζοντας κυρίως εξαγωνική διάταξη. Τα νημάτια σπεκτρίνης στην τετραμερή τους μορφή είναι τα υπεύθυνα για αυτή τη διάταξη, συνδέοντας τα διπλανά σύμπλοκα ζεύξης μεταξύ τους, τοποθετώντας τα στο κέντρο και στις έξι άκρες του εξαγώνου (Liu et al., 1987). Τα σύμπλοκα που σχηματίζονται με τη βοήθεια της αδουσίνης είναι και αυτά εξίσου σημαντικά για τη διατήρηση της ακεραιότητας της ερυθροκυτταρικής μεμβράνης. Το σύμπλοκο αδουσίνη-ζώνη 3-σπεκτρίνη συνδέει το σύμπλοκο ζεύξης με τη λιπιδική διπλοστιβάδα (Anong et al., 2009) (Εικ.6). Τέλος, ο μεταφορέας γλυκόζης Glut 1, είναι μία διαμεμβρανική πρωτεΐνη, η οποία προσδένεται στη δεματίνη και την αδουσίνη δημιουργώντας έτσι ένα σύμπλοκο, το οποίο βοηθά την αγκυροβόληση του συμπλόκου ζεύξης στη λιπιδική διπλοστιβάδα (Khan et al., 2008). ~ 19 ~
20 1.6 Γήρανση ερυθροκυττάρων Με τον όρο γήρανση, καλούμε το σύνολο των μονοδιάστατων και χρονοεξαρτώμενων μοριακών γεγονότων, τα οποία οδηγούν το κύτταρο σε κυτταρική εκκαθάριση-θάνατο. Παρόλο που τα ερυθροκύτταρα έχουν χρησιμοποιηθεί ως μοντέλο για την μελέτη της διαδικασίας της γήρανσης, τα μόρια που συμμετέχουν σ αυτήν καθώς και τα εμπλεκόμενα σηματοδοτικά μονοπάτια δεν έχουν αποσαφηνιστεί πλήρως. Όλα τα ερυθροκύτταρα, υπό κανονικές συνθήκες στην κυκλοφορία του αίματος, έχουν διάρκεια ζωής περίπου 120 μέρες. Αυτό το αυστηρό χρονοδιάγραμμα ζωής τους προϋποθέτει την ύπαρξη ενός ρυθμιστικού συστήματος μοριακών μηχανισμών, το οποίο επωμίζεται τον έλεγχο της διάρκειας ζωής καθώς και την στοχευόμενη απομάκρυνση των γηρασμένων ερυθροκυττάρων (Antonelou et al., 2010). Η γήρανση των ερυθροκυττάρων επέρχεται κυρίως ως συνέπεια οξειδωτικών βλαβών που υφίστανται τα κύτταρα καθώς επιτελούν τον κυρίαρχο ρόλο τους στη μεταφορά οξυγόνου. Η εκκαθάριση των ερυθροκυττάρων από την κυκλοφορία είναι μείζονος σημασίας για την ομοιόσταση του οργανισμού. Γενικά, η οξειδωτική βλάβη τόσο σε πρωτεΐνες και ένζυμα όσο και σε λιπίδια, οδηγεί σε απώλεια λειτουργικής ικανότητας. Όσον αφορά τα ερυθροκύτταρα των ανώτερων σπονδυλωτών, το γεγονός ότι είναι απύρηνα και συνεπώς δεν μπορούν να επιτελέσουν de novo πρωτεϊνοσύνθεση, τα καθιστά μη-ικανά να αντισταθμίσουν τις απώλειες που έχουν εξαιτίας της οξειδωτικής βλάβης. Αυτή τελικά, επιφέρει την απώλεια της ερυθροκυτταρικής μεμβράνης και των ιόντων και την αύξηση της κυτταρικής πυκνότητας (Lutz Η., 2012). Στις συνεχείς μεταβολικές και φυσικές αλλοιώσεις που βιώνουν τα ερυθροκύτταρα καθώς γερνούν, συγκαταλέγονται, εκτός από την μεμβρανική κυστιδιοποίηση, τροποποιήσεις της αιμοσφαρίνης καθώς και προοδευτική ελάττωση της κυτταρικής ομοιόστασης και των αντιοξειδωτικών αμυντικών αποκρίσεων. Η αύξηση της ερυθροκυτταρικής πυκνότητας, που αναφέρεται παραπάνω, η μη ενζυμική γλυκοζυλίωση της αιμοσφαιρίνης και η απαμίδωση της πρωτεΐνης 4.1b σε 4.1a χρησιμοποιούνται σε ευρεία κλίμακα ως ευαίσθητοι δείκτες ερυθροκυτταρικής γήρανσης. Ακόμα, μια πληθώρα μετα-μεταφραστικών πρωτεϊνικών τροποποιήσεων, συμπεριλαμβανομένων της φωσφορυλίωσης, οξείδωσης και συσσωμάτωσης έχουν ενεργή εμπλοκή στη ρύθμιση της ομοιόστασης και του προσδόκιμου ζωής των ερυθροκυττάρων. Ωστόσο, τα παραπάνω δεν εμφανίζονται σταδιακά στα ερυθροκύτταρα, παρά αποτελούν έναν ξαφνικό, γρήγορα εξελισσόμενο και μη γραμμικό καταρράκτη γεγονότων στο τελικό στάδιο της διαδικασίας της γήρανσης, πιθανόν λίγο πριν την απομάκρυνση των ερυθροκυττάρων από το δικτυοενδοθηλιακό σύστημα. Τελικά, ο φαινότυπος της ερυθροκυτταρικής γήρανσης, μπορεί να συσχετισθεί χωρίς καμία αμφιβολία με μία πτώση της μεταβολικής δραστηριότητας, μία προοδευτική αλλαγή του κυτταρικού σχήματος, μία μεμβρανική αναδιαμόρφωση καθώς επίσης και με οξειδωτική βλάβη, μικροκυστιδιοποίηση και έκθεση επιφανειακών δεικτών απομάκρυνσης. Όλες αυτές οι τροποποιήσεις έχουν ως κοινό παρανομαστή το γεγονός ότι είτε ευθέως είτε έμμεσα, πυροδοτούν την ερυθροφαγοκυττάρωση (Antonelou et al., 2010). Πιο αναλυτικά, τα βασικά χαρακτηριστικά των γηρασμένων ερυθροκυττάρων είναι τα εξής: ~ 20 ~
21 Εικόνα 7 : Η πρωτεόλυση των μορίων της ζώνης-3 των γηρασμένων ερυθροκυττάρων, η πρόσδεση των φυσικών αυτοαντισωμάτων και η αναγνώριση του σήματος προς φαγοκυττάρωση από τα μακροφάγα (Ανατύπωση από Bosman G., 2013). Εξωκυστιδιοποίηση: Όσον αφορά την κυστιδιοποίηση της ερυθροκυτταρικής μεμβράνης που αναφέρθηκε παραπάνω, πρόκειται για μια αυστηρά ρυθμιζόμενη διαδικασία, η συχνότητα εμφάνισης της οποίας σχετίζεται άμεσα με την ηλικία του ερυθροκυττάρου. Εξαρτωμένων των συνθηκών, η διαδικασία αυτή μπορεί να λειτουργεί είτε ενάντια είτε υπέρ των αναπτυσσόμενων ερυθροκυττάρων. Στην πρώτη περίπτωση, η διαδικασία της μικροκυστιδιοποίησης οδηγεί στη μη αντιστρεπτή απώλεια μεμβράνης και αιμοσφαιρίνης, ενώ στην δεύτερη απομακρύνει κατεστραμμένα κυτταρικά συστατικά και σηματοδοτικούς δείκτες εκκαθάρισης. Με την εξωκυττάρωση, δηλαδή την απομάκρυνση μη λειτουργικών πρωτεϊνών και αποπτωτικών δεικτών, τα ερυθροκύτταρα προστατεύονται από πρόωρο θάνατο. Χάρη στους ίδιους δείκτες βέβαια, επιτυγχάνεται και η γρήγορη απομάκρυνση των γηρασμένων ερυθροκυττάρων, όταν είναι απαραίτητη. Η συνεχής απελευθέρωση κυστιδίων, έχει σαν αποτέλεσμα την αλλαγή των χαρακτηριστικών και του περιεχομένου των ερυθροκυττάρων. Ακόμα, η κυτταρική πυκνότητα αυξάνεται προοδευτικά με ταυτόχρονη μείωση της κυτταρικής παραμορφωσιμότητας και της μεμβρανικής ευκαμψίας (Antonelou et al., 2010). Μονοπάτι ζώνης 3: Ένα μονοπάτι που συνδέεται στενά με την απομάκρυνση των γηρασμένων ανθρώπινων ερυθροκυττάρων στο τέλος του προσδόκιμου ζωής τους είναι αυτό της συσσωμάτωσης ή πρωτεόλυσης της ζώνης 3 στη μεμβράνη. H παρουσία των ερυθροκυττάρων στο κυκλοφορικό σύστημα, συνεπάγεται τη συνεχή έκθεσή τους σε οξειδωτικό στρες, το οποίο μπορεί με τη σειρά του να οδηγήσει στην οξείδωση της αιμοσφαιρίνης (Hb) και την μετατροπή της σε μεθαιμοσφαιρίνη (MetHb), ενώ μπορεί επίσης να προκαλέσει οξειδωτική βλάβη στα μεμβρανικά λιπίδια και πρωτεΐνες. Παρόλο που ούτε η υπεροξείδωση της μεμβράνης, ούτε ο σχηματισμός της μεθαιμοσφαρίνης, μπορούν ως μεμονωμένα γεγονότα να προκαλέσουν την δημιουργία συσσωματωμάτων ζώνης 3 στα ανθρώπινα ερυθροκύτταρα, η συνεργιστική τους δράση επιφέρει αυτό το αποτέλεσμα. Αυτή η παράλληλη δράση αποτελεί στην κλίμακα του χρόνου ένα από τα τελευταία γεγονότα που συμβαίνουν κατά τη διάρκεια ζωής των ερυθροκυττάρων. Έτσι, γίνεται εύκολα κατανοητό το γεγονός ότι τα γηρασμένα ερυθροκύτταρα χαρακτηρίζονται από ~ 21 ~
22 συσσωρευμένη οξειδωτική βλάβη στη μεμβράνη τους και από αυξημένη ποσότητα μεθαιμοσφαρίνης σαν αποτέλεσμα της μειωμένης δραστικότητας της αναγωγάσης της μεθαιμοσφαιρίνης (Arashiki et al., 2013). Η αναδιαμόρφωση της ζώνης-3 στη μεμβράνη, η οποία οφείλεται είτε σε πρωτεόλυση των μορίων της πρωτεΐνης είτε σε σύνδεση πολλών μονομερών της, πυροδοτεί την πρόσδεση των φυσικών αυτοαντισωμάτων του ορού IgGs οδηγώντας σε αναγνώριση και φαγοκυττάρωση των ερυθροκυττάρων από τα μακροφάγα (Hans U.Lutz, 2012) (Εικ.7). Διαταραχή της ομοιόστασης του ασβεστίου (Ca 2+ ): Το ιόν Ca 2+ είναι ένα σηματοδοτικό μόριο το οποίο εμπλέκεται στη ρύθμιση του κυτταρικού κύκλου και μεταβολισμού, καθώς και της κυτταρικής δομικής ακεραιότητας, κινητικότητας και κυτταρικού όγκου. Όπως άλλα κύτταρα, έτσι και τα ερυθροκύτταρα βασίζονται σε μονοπάτια σηματοδότησης εξαρτώμενα από το Ca 2+ κατά τη διαφοροποίησή τους από τα πρόδρομα κύτταρα. Τα ενδοκυτταρικά επίπεδα Ca 2+ των κυκλοφορούντων ερυθροκυττάρων ελέγχουν τόσο ρεολογικές και βιοφυσικές ιδιότητες, όπως η μεμβρανική σύσταση και ο κυτταρικός όγκος, όσο φυσιολογικές παραμέτρους, όπως είναι η μεταβολική δραστηριότητα, η οξειδοαναγωγική κατάσταση και η κυτταρική κάθαρση. Η εξαιρετικά χαμηλή διαπερατότητα της ανθρώπινης ερυθροκυτταρικής μεμβράνης στο Ca 2+ και η αντλία ιόντων Ca 2+ διατηρούν τα επίπεδα του ελεύθερου ενδοκυττάριου Ca 2+ μεταξύ 30 και 60 nm, ενώ η ποσότητα του Ca 2+ του πλάσματος κυμαίνεται περίπου στα 1.8 mm. Έτσι, η ενεργοποίηση της πρόσληψης Ca 2+ στα ερυθροκύτταρα, έχει μια εντυπωσιακά μεγάλη επίπτωση σε μια πληθώρα διαδικασιών που συμβαίνουν σε αυτά. Για παράδειγμα, η πρόσληψη Ca 2+ συνδέεται αναπόσπαστα με την ενίσχυση της διαφοροποίησης και του πολλαπλασιασμού των προγονικών ερυθροειδών κυττάρων. Τα επίπεδα Ca 2+ των δικτυοερυθροκυττάρων είναι έτσι υψηλότερα από αυτά των ώριμων ερυθροκυττάρων. Ένας ακόμη ρόλος που αποδίδεται στο ενδοκυττάριο Ca 2+, είναι η εμπλοκή του στην ενίσχυση και προώθηση της ικανότητας των ερυθροκυττάρων για μεταφορά οξυγόνου. Σχετικά με τη σύνδεση μεταξύ επιπέδων ενδοκυττάριου Ca 2+ και αποβολής γηρασμένων ερυθροκυττάρων, είναι σήμερα γνωστό πως τα ενδοκυττάρια επίπεδα Ca 2+ είναι πολύ υψηλότερα στα γηρασμένα ερυθροκύτταρα από ό,τι στα δικτυοερυθροκύτταρα και στα νεαρά ερυθροκύτταρα (Bogdanova et al., 2013). H διατάραξη της ομοιόστασης του Ca 2+ είναι ένα ακόμα μονοπάτι που σχετίζεται με την ερυθροκυτταρική γήρανση, είτε πυροδοτώντας την είτε σαν αποτέλεσμά της. Η ενδοκυττάρια εισροή ασβεστίου σχετίζεται ξεκάθαρα με την οξειδωτική βλάβη, την κυστιδιοποίηση, την αφυδάτωση και την απώλεια της ικανότητας παραμόρφωσης που υπομένουν τα γηρασμένα ερυθροκύτταρα. Υπάρχει όμως και λειτουργική σύνδεση μεταξύ της εισροής ασβεστίου και αποπτωτικών γεγονότων στα ώριμα ερυθροκύτταρα. Συγκεκριμένα, το σύνολο των μονοπατιών που εμπλέκουν το ασβέστιο και λειτουργούν ως απόκριση στα διάφορα είδη στρες στα οποία υπόκειται το ερυθροκύτταρο, ονομάζεται ερυθρόπτωση και ίσως αποτελεί έναν μηχανισμό αποφυγής της αιμόλυσης των ερυθροκυττάρων που έχουν υποστεί βλάβες (Antonelou et al., 2010) (Eικ. 8). Σηματοδότηση μέσω κασπασών Έκθεση φωσφατυδιλοσερίνης: Το γεγονός ότι η in vitro ενεργοποίηση της προκασπάσης-3 σε συνθήκες οξειδωτικού στρες, οδηγεί σε τροποποιήσεις της ζώνης 3, σε έκθεση φωσφατυδιλοσερίνης (PS) και τέλος σε ερυθροφαγοκυττάρωση, έκανε εμφανή έναν πολύ πιθανό ρόλο του μηχανισμού αυτού in vivo στην γήρανση καθώς και στην εκκάθαριση των ερυθροκυττάρων. Αυτό υποδηλώνεται από την ανίχνευση ενεργής κασπάσης-3 και κασπάσης-8 καθώς και από τον σχηματισμό του αποπτωτικού μονοπατιού Fas στις λιπιδικές σχεδίες της μεμβράνης των γηρασμένων ερυθροκυττάρων. Σήμα κατατεθέν των τελευταίων που τα διαχωρίζει από τα νεαρά σε ηλικία ερυθροκύτταρα, αποτελεί το γεγονός ότι παρουσιάζουν μειωμένη ~ 22 ~
23 ενεργότητα αμινοφωσφολιπιδικής τρανσλοκάσης και υψηλά επίπεδα εξωτερίκευσης PS (Εικ.7.). Η ενεργοποίηση της κασπάσης-3 κάτω από συνθήκες οξειδωτικού στρες κατά την πορεία της ερυθροκυτταρικής γήρανσης,επηρεάζει τη μορφή και τη δομή της ζώνης 3, πυροδοτώντας παράλληλα έναν καταρράκτη γεγονότων, οποίος αποφέρει την απομάκρυνση των ερυθροκυττάρων από τον οργανισμό. Έτσι λοιπόν, η διέγερση και ενεργοποίηση των κασπασών σε γηρασμένα ερυθροκύτταρα ή σε ερυθροκύτταρα που έχουν υποστεί βλάβη, θα μπορούσε να επιφέρει την φαγοκυττάρωση τους ούτως ώστε να αποφευχθεί η αιμόλυση. Η υπόθεση ότι η in vivo έκθεση φωσφατιδυλοσερίνης συνεπάγεται το βαθμό της απομάκρυνσης των γηρασμένων και κατεστραμμένων ερυθροκυττάρων, μένει να διαλευκανθεί περαιτέρω καθώς αυτή η έκθεση μπορεί να συγχέεται με τη φωσφατιδυλοσερίνη που εξωτερικεύεται λόγω των στρεσογόνων in vitro κατεργασιών της απομάκρυνσης γηρασμένων ερυθροκυττάρων. Το γεγονός όμως ότι η εξωτερίκευση φωσφατιδυλοσερίνης (PS) έχει ως επίπτωση στη θρομβογένεση, καθιστά πιο πιθανό τον ρόλο και τη συσχέτισή της με την ερυθροκυτταρική γήρανση και την απομάκρυνση από τον οργανισμό φυσιολογικών ή προβληματικών ερυθροκυττάρων κάτω από συγκεκριμένες περιστάσεις, μέσω της ενεργοποίησης διαφορετικών κάθε φορά σηματοδοτικών μονοπατιών (Antonelou et al., 2010). Εκτός από τα χαρακτηριστικά που προαναφέρθηκαν, κεντρικό ρόλο στη στη σηματοδότηση της ερυθροκυτταρικής γήρανσης έχει το οξειδωτικού στρες. Πέραν της επίπτωσής του στην ενεργοποίηση προ-αποπτωτικών συστατικών, το οξειδωτικό στρες επηρεάζει την αιμοσφαιρίνη και τις αλληλεπιδράσεις της με μεμβρανικά συστατικά ενώ ενεργοποιεί και την προκασπάση-3. Συγκεκριμένα, η αιμοσφαιρίνη, υπό οξειδωτικό στρες, πέραν από τη σύνδεσή της σε περιοχές υψηλής συγγένειας πάνω στη ζώνη 3, συμπλοκοποιείται με τη σπεκτρίνη και αυτό αποτελεί έναν από τους πρώτους δείκτες της in vivo διεργασίας της ερυθροκυτταρικής γήρανσης, ο οποίος σχετίζεται στενά με την επερχόμενη ακαμψία του κυττάρου, την μειωμένη ικανότητα παραμόρφωσης, την εχινοκυττάρωση και την ερυθροφαγοκυττάρωση. Αυτό το σύμπλεγμα (αιμοσφαιρίνης-σπεκτρίνης) διαταράσσει την συνοχή του κυτταροσκελετού με την διπλοστιβάδα, επηρεάζει τη φυσιολογική σύνδεση του τετραμερούς της σπεκτρίνης, το κύτταρο οδηγείται σε εξωτερίκευση φωσφατιδυλοσερίνης και τελικά σε αναγνώριση από τα μακροφάγα (Antonelou et al., 2010). ~ 23 ~
24 Εικόνα 8: Σχηματική αναπαράσταση ανίχνευσης της εξωτερίκευσης φωσφατιδυλοσερίνης. Η ανεξίνη V χρησιμοποιείται ευρέως για την ανίχνευση αποπτωτικών κυττάρων. Έχει την ιδιότητα να συνδέεται με την φωσφατιδυλοσερίνη, η οποία μετατοπίζεται στην εξωτερική πλευρά της ερυθροκυτταρικής μεμβράνης, παρουσία Ca 2+ κατά τη διάρκεια της αποπτωτικής διεργασίας (Ανατύπωση από Η αναγνώριση και η απομάκρυνση των γηρασμένων ερυθροκυττάρων τελείται από τα μακροφάγα του δικτυοενδοθηλιακού συστήματος, κυρίως από τα Kuppfer κύτταρα του ήπατος και στον σπλήνα. Ο καταλύτης που επιφέρει τη φαγοκυττάρωση, είναι η συσσώρευση των επονομαζόμενων σημάτων eat me στη μεμβράνη των γηρασμένων ερυθροκυττάρων, όπως είναι η έκθεση της φωσφατιδυλοσερίνης (PS) στην εξωτερική πλευρά της ερυθροκυτταρικής μεμβράνης. Ένας ακόμα πολύ σημαντικός παράγοντας που ρυθμίζει την ερυθροφαγοκυττάρωση, είναι το μόριο CD47. Συγκεκριμένα, η πρωτεΐνη αυτή είναι αναστολέας της ερυθροφαγοκυττάρωσης από τα μακροφάγα, αποτελώντας ένα don t eat me σήμα. Το αν ένα ερυθροκύτταρο θα φαγοκυτταρωθεί από τα μακροφάγα καθορίζεται από την ισορροπία μεταξύ eat me και don t eat me σημάτων στην κυτταρική επιφάνεια. Ακόμα, η σταδιακή μείωσης της έκφρασης του CD47, αποτελεί έναν από τους μηχανισμούς που οδηγούν στην απομάκρυνση των ερυθροκυττάρων κατά τη φυσιολογική διαδικασία της γήρανσης. Η αναστολή της ερυθροφαγοκυττάρωσης χάρη στο CD47 επιτυγχάνεται μέσω της αλληλεπίδρασής του με τον υποδοχέα SIRPα, ο οποίος εκφράζεται στα μακροφάγα. Η CD47-SIRPα αλληλεπίδραση αποτελεί έτσι ένα αρνητικό σήμα έναντι της ερυθροφαγοκυττάρωσης. Παρόλα αυτά, το CD47 μπορεί να συμπεριφερθεί και ως σήμα eat me, γεγονός που του προσδίδει τελικά έναν ακόμα πιο περίπλοκο ρόλο στη ρύθμιση της ερυθροφαγοκυττάρωσης. Συγκεκριμένα, έχει δειχθεί πως ένας μικρός αριθμός γηρασμένων ερυθροκυττάρων προσδένεται και φαγοκυτταρώνεται εν τέλει μέσω CD47-SIRPα αλληλεπιδράσεων. Συμβαίνει δηλαδή μια αλλαγή στη διαμόρφωση της CD47, που μετατρέπει το μόριο από ανασταλτικό, σε σήμα ενεργοποίησης της φαγοκυττάρωσης ύστερα από πρόσδεση της πρωτεΐνης θρομβοσπονδίνης-1 (Burger et al., 2012). Τελικά, φαίνεται πως το CD47 ρυθμίζει την ερυθροφαγοκυττάρωση με θετικό και με αρνητικό τρόπο, παίζοντας έτσι έναν πρωταρχικό ρόλο στον έλεγχο της ανακύκλωσης των ερυθροκυττάρων in vivo (R.van Bruggen., 2013). 1.7 Ερυθρόπτωση Η ερυθρόπτωση (eryptosis) αφορά στον προγραμματισμένο κυτταρικό θάνατο, δηλαδή στην απόπτωση των ερυθροκυττάρων. Με δεδομένο όμως ότι τα ερυθροκύτταρα δε διαθέτουν πυρήνα και μιτοχόνδρια, δεν εμφανίζουν πολλά χαρακτηριστικά στοιχεία της απόπτωσης όπως είναι η μιτοχονδριακή αποπόλωση και η συμπύκνωση χρωματίνης και πυρήνα. Κύρια χαρακτηριστικά της ερυθρόπτωσης αποτελούν η ερυθροκυτταρική συρρίκνωση, η φυσαλιδοποίηση της ερυθροκυτταρικής μεμβράνης, και η αναδιάρθρωση των λιπιδίων της μεμβράνης, που οδηγούν στην έκθεση φωσφατιδυλοσερίνης (PS) στην κυτταρική επιφάνεια. Η φυσιολογική της σημασία έγκειται στην απομάκρυνση των γηρασμένων ερυθροκυττάρων από την κυκλοφορία, στην αποφυγή της αιμόλυσης καθώς και στην αποτροπή της εξάπλωσης παθογόνων μικροοργανισμών. Η ερυθρόπτωση ενεργοποιείται από διάφορα ερεθίσματα, όπως είναι η αύξηση της συγκέντρωσης του κυτοσολικού Ca 2+ μέσω της ενεργοποίησης καναλιών κατιόντων που επιτρέπουν ~ 24 ~
25 τη διέλευση του Ca 2+. Η δραστηριότητα των καναλιών μάλιστα έχει ως συνέπεια την έξοδο H 2 O από το ερυθροκύτταρο και κατά συνέπεια τη συρρίκνωσή του. Μερικά ακόμη ερεθίσματα που οδηγούν σε ερυθρόπτωση περιλαμβάνουν το ωσμωτικό σοκ και το οξειδωτικό στρες, το οποίο ενεργοποιεί τόσο τα διαπερατά σε κατιόντα -άρα και στο Ca 2+ -κανάλια, όσο και τα κανάλια Cl - επιφέροντας έτσι κυτταρική συρρίκνωση (Εικ.9). Ακόμα έχει παρατηρηθεί ότι η εξάντληση των ενεργειακών αποθεμάτων, η υπερθερμία και πλήθος μικρών μορίων πυροδοτούν το μηχανισμό της ερυθρόπτωσης. Από την άλλη πλευρά, η ερυθρόπτωση αναστέλλεται από διάφορες ουσίες συμπεριλαμβανομένων των κατεχολαμινών και του νιτρικού οξέος. Το τελευταίο αποτελεί ισχυρό αναστολέα της ερυθρόπτωσης με το να καθιστά τα ερυθροκύτταρα μερικώς ανθεκτικά απέναντι στα ερυθροαποπτωτική δράση του αυξημένου κυτοσολικού Ca 2+. Επίσης, η ερυθροποιητίνη αναστέλλει τη διαπερατότητα σε Ca 2+ των καναλιών κατιόντων, αποτρέποντας με αυτόν τον τρόπο την ερυθρόπτωση. Η επιταχυνόμενη ερυθρόπτωση μπορεί να αντισταθμιστεί με αυξημένη ερυθροποίηση. Ο μηχανισμός της ερυθρόπτωσης επιταχύνεται σε πολλές ασθένειες, όπως η β-μεσογειακή αναιμία, η κληρονομική σφαιροκυττάρωση, η έλλειψη σιδήρου, η νεφρική ανεπάρκεια κ.α. Εικόνα 9 : Σχηματική αναπαράσταση της εισροής Ca 2+ και της δραστηριότητας των καναλιών Gardos (απεικονίζονται με χρώμα μπλε στην επιφάνεια της ερυθροκυτταρικής μεμβράνης). Τα κανάλια αυτά ενεργοποιούνται από την εισροή Ca 2+ και σαν αποτέλεσμα αποβάλλουν ενδοκυτταρικό K +. Παράλληλα, αποβάλλεται νερό και Cl -. Έτσι το ερυθροκύτταρο συρρικνώνεται και η συγκέντρωση της ενδοκυτταρικής αιμοσφαιρίνης αυξάνεται. Σαν αποτέλεσμα, αποτρέπεται η αιμόλυση και οι τοξικές τις συνέπειες για τον οργανισμό (Ανατύπωση από Brugnara C., 2000). 1.8 Λειτουργία Νεφρών Κύριος ρόλος των νεφρών είναι η απομάκρυνση των άχρηστων ουσιών και της περίσσειας νερού από τον οργανισμό. Κάθε νεφρός αποτελείται από νεφρώνες, ενώ καθένας από τους τελευταίους απαρτίζεται από το σπείραμα και τα ουροφόρα σωληνάρια. Πολύ σημαντικό είναι το γεγονός ότι τα σπειράματα δεν αποβάλλουν εκλεκτικά τις τοξίνες από την πλευρά του αίματος προς αυτή των ούρων, αλλά διηθούν αρχικά έναν μεγάλο όγκο υπερδιηθήματος, το πρόουρο. To υπερδιήθημα αυτό, εκτός από τις τοξίνες, περιέχει και νερό, ηλεκτρολύτες καθώς και όλες τις ~ 25 ~
26 μικρού και μεσαίου μοριακού βάρους ουσίες του αίματος. Ωστόσο, δεν περιέχει πρωτεΐνες και έμορφα συστατικά του αίματος, όπως είναι τα ερυθροκύτταρα, τα λευκοκύτταρα και τα αιμοπετάλια. Καθώς το πρόουρο ρέει κατά μήκος των ουροφόρων σωληναρίων, τα επιθηλιακά κύτταρα επαναρροφούν ενεργητικά το 99% του πρόουρου και έτσι μόνο το 1% αυτού απεκκρίνεται τελικά με τη μορφή ούρων. Για να παραμείνει σταθερό το εσωτερικό περιβάλλον του οργανισμού (ομοιόσταση), τα ούρα αποβάλλουν σε καθημερινή βάση όσο νερό, άλατα, πρωτόνια, ωσμωτικές ουσίες και τοξίνες προσελήφθησαν ή παρήχθησαν κατά τον μεταβολισμό («Εσωτερική Παθολογία», 2010, σ.823). 1.9 Χρόνια Νεφρική Ανεπάρκεια Η Χρόνια Νεφρική Ανεπάρκεια (ΧΝΑ) χαρακτηρίζεται από σταδιακή απώλεια της φυσιολογικής λειτουργίας των νεφρών, ενώ η νεφρική ανεπάρκεια τελικού σταδίου είναι η ολική απώλεια της λειτουργίας των νεφρών και συνεπάγεται την ανάγκη για αιμοκάθαρση (Udden et al., 1984). Πιο συγκεκριμένα, ως Χρόνια Νεφρική Ανεπάρκεια (ΧΝΑ), καλείται η νεφρική νόσος που χαρακτηρίζεται από ρυθμό σπειραματικής διήθησης (glomerular filtration rate, GFR) <60 ml/min για χρονικό διάστημα μεγαλύτερο των τριών μηνών ή από νεφρική βλάβη η οποία διαπιστώνεται με βιοψία νεφρού, ή με παθολογικά ευρήματα στη γενική εξέταση ούρων ή με κάποια απεικονιστική μέθοδο (υπερηχοτομογραφική εξέταση νεφρών, ενδοφλέβιος πυελογραφία, αξονική τομογραφία). Ανεξάρτητα από την αιτία της νεφρικής βλάβης, μόλις ο GFR πέσει κάτω από τα 50 ml/min ακολουθεί μια σταδιακή και μη αναστρέψιμη απώλεια της νεφρικής λειτουργίας η οποία καταλήγει σε τελικού σταδίου ΧΝΑ. Αυτή είναι και η κατάσταση κατά την ο οποία ο ασθενής πρέπει να εισαχθεί σε θεραπεία νεφρικής υποκατάστασης (αιμοκάθαρση, περιτοναϊκή κάθαρση), ή να υποβληθεί σε μεταμόσχευση νεφρού. Η καλύτερη διάγνωση της ΧΝΑ γίνεται βάσει του ρυθμού σπειραματικής διήθησης (GFR), μιας και αυτός αποτελεί τον καλύτερο δείκτη για την εκτίμηση της λειτουργικής μάζας των νεφρών και της ικανότητάς τους να διηθούν το πλάσμα (Πίνακας 1). Ο φυσιολογικός ρυθμός GFR κυμαίνεται ημερησίως περί τα 180L. Επειδή όμως δεν είναι δυνατό να μετρηθεί η σπειραματική διήθηση κάθε νεφρώνα ξεχωριστά και να γνωρίζουμε τον αριθμό των λειτουργούντων νεφρώνων, ο GFR υπολογίζεται έμμεσα από την κάθαρση μιας ουσίας η οποία διέρχεται ελεύθερα από το αίμα στο πρόουρο και δεν επαναρροφάται ούτε απεκκρίνεται από τα ουροφόρα σωληνάρια. Στην κλινική πρακτική, έχει επιλεγεί ο GFR να ταυτίζεται με την κάθαρση της κρεατινίνης. Η κρεατινίνη είναι ένα ενδογενές μικρό μόριο, που παράγεται νυχθημερόν με μη ενζυμικό τρόπο (σταθερό ρυθμό) από την κρεατίνη των μυών, περνά ελεύθερα στο πρόουρο και απεκκρίνεται ελάχιστα από τα ουροφόρα σωληνάρια, ενώ προσδιορίζεται στο εργαστήριο με εύκολο, γρήγορο και φθηνό τρόπο. Βάσει του GFR, οι ασθενείς κατατάσσονται σε ένα από τα πέντε στάδια,τα οποία είναι αντιπροσωπευτικά για τη βαρύτητα της νόσου («Εσωτερική Παθολογία», 2010, σ ) ~ 26 ~
27 Πίνακας 1. Η κατάταξη της ΧΝΑ σε 5 στάδια ανάλογα με τα επίπεδα του δείκτη σπειραματικής διήθησης. Στάδιο GFR(ml/min) Κλινική σημασία 1 >90 Φυσιολογική νεφρική κάθαρση Ήπια νεφρική ανεπάρκεια Μέτρια νεφρική ανεπάρκεια Σοβαρή νεφρική ανεπάρκεια 5 <15 Τελικό στάδιο ΧΝΑ (μεταμόσχευση νεφρού ή αιμοκάθαρση) Αιτιολογία της Χρόνιας Νεφρικής Ανεπάρκειας Μέχρι και πριν από μερικές δεκαετίες, η κύρια αιτία της ΧΝΑ ήταν οι διάφορες μορφές σπειραματονεφρίτιδας. Τελευταία όμως, ιδιαίτερα στις βιομηχανοποιημένες χώρες του Δυτικού Κόσμου, παρατηρείται αλλαγή της επιδημιολογίας της ΧΝΑ, κυρίως λόγω της γήρανσης του πληθυσμού, της παχυσαρκίας και του σακχαρώδους διαβήτη, που έχουν λάβει επιδημιολογικό χαρακτήρα (Πίνακας 2). Το γήρας, όπως είναι αναμενόμενο σχετίζεται με απώλεια λειτουργίας και έκπτωση των οργάνων του οργανισμού, από τα οποία δεν θα μπορούσε να λείπει και ο νεφρός. Ιδιαίτερο ενδιαφέρον αποτελεί η διαπίστωση πως από την ηλικία των 40 ετών και μετά, η νεφρική κάθαρση μειώνεται κατά 1ml/min ανά έτος. Παράλληλα, το 1/3 των διαβητικών ασθενών, θα αναπτύξει διαβητική νεφροπάθεια καταλήγοντας σε ΧΝΑ τελικού σταδίου. Πολύ σημαντικό είναι το γεγονός πως η πλειοψηφία των ασθενών με ΧΝΑ είναι υπερτασικοί, ενώ αντίστροφα η υπέρταση αποτελεί τον κυριότερο παράγοντα επιδείνωσης της νεφρικής λειτουργίας. Ο νεφρός δηλαδή αποτελεί θύμα και θύτη της υπέρτασης. Πολλοί ασθενείς με υπέρταση και νεφροπάθεια χαρακτηρίζονται από το επονομαζόμενο μεταβολικό σύνδρομο και πάσχουν από μια γενικευμένη αρτηριοσκλήρωση, η οποία μπορεί να προσβάλει και τις νεφρικές αρτηρίες («Εσωτερική Παθολογία», 2010, σ.826). ~ 27 ~
28 Πίνακας 2. Οι κυριότεροι αιτιολογικοί παράγοντες σε ασθενείς με ΧΝΑ τελικού σταδίου (Mc Phee et al., 2000). Παράγοντας Ποσοστό % Διαβητική νεφροπάθεια 27,7 Αρτηριακή υπέρταση 24,5 Σπειραματονεφρίτιδα 21,2 Πολυκυστικοί νεφροί 3,9 Άλλα άγνωστα αίτια 22, Εξέλιξη της ΧΝΑ Η μείωση του GFR κάτω από τα 50-60ml/min, η οποία είναι αποτέλεσμα της βλάβης μεγάλου αριθμού νεφρώνων, οδηγεί σε έναν φαύλο κύκλο μεταξύ σπειραματικής «υπέρτασης», υπερδιήθησης/πρωτεϊνουρίας και αυξημένης επαναρρόφησης πρωτεϊνών από τα επιθήλια των ουροφόρων σωληναρίων. Όλα αυτά έχουν σαν αποτέλεσμα τη συνεχή απώλεια της νεφρικής λειτουργίας έως ότου επέλθει ολική απώλεια. Καταλύτη της καταστροφής των σπειραμάτων αποτελεί η ενεργοποίηση του συστήματος Ρενίνης-Αγγειοτασίνης (ΣΡΑ). Πιο συγκεκριμένα, η αύξηση της ενδοσπειραματικής υδροστατικής πίεσης που επιφέρει σπειραματική υπέρταση οφείλεται στο ότι η αγγειοτασίνη II (ενεργό πεπτίδιο του ΣΡΑ), προκαλεί εκλεκτική σύσπαση μόνο του απαγωγού αρτηριολίου του σπειράματος και όχι του προσαγωγού. Σαν επακόλουθο αυτού του γεγονότος, αυξάνεται ο ρυθμός σπειραματικής διήθησης (υπερδιήθηση) και επιδεινώνεται η πρωτεϊνουρία. Μεταξύ των πρωτεϊνών που επαναρροφώνται, συμπεριλαμβάνονται παράγοντες φλεγμονής και αυξητικοί παράγοντες, οι οποίοι καταστρέφουν τα ουροφόρα σωληνάρια και τον περιβάλλων διάμεσο ιστό. Με τη συνέχιση της καταστροφής των νεφρώνων, ο παραπάνω κύκλος επαναλαμβάνεται, η νεφρική κάθαρση μειώνεται ολοένα και περισσότερο, έως ότου ο ασθενής οδηγηθεί σε ΧΝΑ τελικού σταδίου («Εσωτερική Παθολογία», 2010, σ ) Κλινικά ευρήματα και επιπτώσεις της ΧΝΑ Η ΧΝΑ χαρακτηρίζεται από ένα ευρύ φάσμα συμπτωμάτων στα οποία συμπεριλαμβάνονται η ανορεξία, η ναυτία, ατονία, αύξηση καρδιακού-αναπνευστικού ρυθμού, υπέρταση, αναιμία, μελάγχρωση δέρματος, λευκονυχία, περιφερειακή νευροπάθεια, περικαρδίτιδα κ.α. («ΟΥΡΟΛΟΓΙΑ», Δεληβελιώτης Χ., 2009, σ.146). Το σύνολο των συμπτωμάτων από όλα τα συστήματα (καρδιαγγειακό, γαστρεντερολογικό, αιμοποιητικό, ανοσολογικό, νευρολογικό, ενδοκρινολογικό, ~ 28 ~
29 σκελετικό, δέρμα) συνοψίζονται στο λεγόμενο «ουραιμικό σύνδρομο». Η απώλεια των νεφρώνων επηρεάζει τόσο την εξωκρινή λειτουργία (ομοιόσταση ύδατος και ηλεκτρολυτών, αποβολή τοξινών, οξεοβασική ισορροπία), όσο και την ενδοκρινή λειτουργία του νεφρού (παραγωγή ερυθροποιητίνης, ρενίνης, καλσιτριόλης), οδηγώντας στην κατακράτηση των τοξικών παραπροϊόντων του μεταβολισμού. Τα συμπτώματα ωστόσο εμφανίζουν ποικιλομορφία ως προς το είδος και την ένταση από ασθενή σε ασθενή και εξαρτώνται από το είδος της νεφρικής νόσου και από το πόσο γρήγορα αυτή εξελίσσεται προς νεφρική ανεπάρκεια. Μερικές από τις σημαντικότερες διαταραχές που χαρακτηρίζουν την ΧΝΑ, αναλύονται ακολούθως. Διαταραχές στην ομοιόσταση ύδατος-άλατος: Σε αντίθεση με τον φυσιολογικό νεφρό, ο οποίος μπορεί να προσλαμβάνει σε καθημερινή βάση 0,5-12L ύδατος καθώς και αντίστοιχη ποσότητα άλατος από λίγα μέχρι πολλά γραμμάρια, ο πάσχων νεφρός δεν μπορεί να διαχειριστεί τέτοιες ποσότητες με αποτέλεσμα ο νεφροπαθής να υποφέρει είτε από αφυδάτωση, είτε από υπερυδάτωση. Ένα από τα πρώιμα ευρήματα της νεφρικής ανεπάρκειας είναι η μειωμένη ικανότητα συμπύκνωσης των ούρων, ενώ σε προχωρημένο στάδιο, όταν η αποβολή των υγρών είναι μειωμένη, οιδήματα μπορεί να κάνουν την εμφάνισή τους («Εσωτερική Παθολογία», 2010, σ.829). Διαταραχές στην οξεοβασική ισορροπία: Τα 2/3 του φορτίου των πρωτονίων υδρογόνου που πρέπει να αποβληθεί από τα ούρα, αποβάλλεται με τη μορφή αμμωνίου (NH 4+ ). Σε προχωρημένη νεφρική ανεπάρκεια, παρατηρείται αδυναμία σύνθεσης επαρκούς ποσότητας αμμωνίας από το νεφρικό παρέγχυμα και σαν αποτέλεσμα μείωση της αποβολής των πρωτονίων υδρογόνου. Στη ΧΝΑ τελικού σταδίου απαντάται μεταβολική οξέωση (HCO 3 = meq/l), η οποία σε σοβαρές περιπτώσεις οδηγεί σε υπερκαλιαιμία. Η βαριά οξέωση της ΧΝΑ τελικού σταδίου αντιμετωπίζεται μόνο με αιμοκάθαρση. Διαταραχές φωσφόρου-ασβεστίου: Η απώλεια της νεφρικής λειτουργίας οδηγεί σε υπερφωσφαταιμία, λόγω του ότι ο πάσχων νεφρός αδυνατεί να αποβάλλει το προσλαμβανόμενο από την τροφή φώσφορο. Άμεση συνέπεια της υπερφωσφαταιμίας είναι η υπασβεσταιμία και αυτό διότι πάντα το γινόμενο ασβεστίου x φωσφόρου (Ca x P) πρέπει να παραμένει σταθερό. Οι υποδοχείς ασβεστίου στην κυτταρική μεμβράνη των κυττάρων του παραθυρεοειδούς αδένα ανιχνεύουν το χαμηλό ασβέστιο με αποτέλεσμα να εκκρίνεται παραθορμόνη. Παράλληλα όμως υπάρχουν χαμηλά επίπεδα καλσιτριόλης, της οποίας ο ρόλος είναι η καταστολή της έκκρισης παραθορμόνης. Τελικά, τα χαμηλά επίπεδα ασβεστίου σε συνδυασμό με τη μειωμένη παραγωγή καλσιτριόλης, οδηγούν σε υπερτροφία των παραθυρεοειδών αδένων, υπερέκκριση παραθορμόνης και εμφάνιση δευτεροπαθούς υπερπαραθυρεοειδισμού. Διαταραχές καρδιαγγειακού συστήματος: Τα νοσήματα του καρδιαγγειακού συστήματος συνδέονται στενά με τη ΧΝΑ αφού αποτελούν τη συχνότερη αιτία νοσηρότητας και θνησιμότητας στους νεφροπαθείς. Αξίζει να αναφερθεί πως σχεδόν όλοι οι ασθενείς είναι υπερτασικοί και εμφανίζουν σκλήρυνση της αορτής και των μεγάλων ελαστικών αγγείων. Περισσότεροι από τους μισούς εμφανίζουν στεφανιαία νόσο, ενώ το έμφραγμα και το εγκεφαλικό επεισόδιο ευθύνονται για την πλειοψηφία των θανάτων των νεφροπαθών. Διαταραχές του αιμοποιητικού συστήματος: Η κύρια αιματολογική εκδήλωση της ΧΝΑ είναι η αναιμία. Η αναιμία εμφανίζεται κυρίως λόγω ανεπάρκειας σε ερυθροποιητίνη αφού ο πάσχων νεφρός αδυνατεί να παράγει επαρκή ποσότητα ερυθροποιητίνης. Σε αυτή την περίπτωση, η αναιμία μπορεί να αποκατασταθεί μετά από εξωγενή χορήγηση συνθετικής ερυθροποιητίνης. Η καταστολή της ερυθροποίησης στο μυελό των οστών από τις τοξίνες καθώς και η ελάττωση του ~ 29 ~
30 χρόνου ημιζωής των ερυθροκυττάρων στις ημέρες ευθύνονται επίσης για την εμφάνιση της αναιμίας («Εσωτερική Παθολογία», 2010, σ ). Αναιμία μπορεί να προκληθεί ακόμα, λόγω μορφολογικών αλλαγών των ερυθροκυττάρων, ως αποτέλεσμα της μειωμένης ικανότητας παραμόρφωσής τους, η οποία απαιτείται για την μετακίνησή τους μέσω των λεπτών τριχοειδών (Udden et al., 1984). Αντιπροσωπευτικοί παθολογικοί τύποι ερυθροκυττάρων που απαντώνται στη ΧΝΑ είναι τα εχινοκύτταρα, τα στοματοκύτταρα, τα κνιζοκύτταρα, τα σχιστοκύτταρα, τα δακρυοκύτταρα, τα ελλειπτοκύτταρα και τα λεπτοκύτταρα, ενώ παρατηρείται και αυξημένος αριθμός δικτυοερυθροκυττάρων. Τα αιμοπετάλια στη ΧΝΑ υπολειτουργούν, ενώ τα λευκοκύτταρα έχουν μειωμένη ικανότητα φαγοκυττάρωσης και ελαττωμένη παραγωγή ελεύθερων ριζών οξυγόνου. Έτσι, οι νεφροπαθείς εμφανίζουν ελαττωμένη ανοσολογική απόκριση. Μεταβολικές-Νευρολογικές διαταραχές: Η εμφάνιση «ψευτοδιαβήτη» με αυξημένη αντίσταση στη γλυκόζη σε μη διαβητικούς ασθενείς αποτελεί πιθανότητα στη ΧΝΑ, ενώ η πλειοψηφία των ασθενών με ΧΝΑ πάσχει από περιφερική νευροπάθεια, εκδηλώνοντας αδυναμία στα άκρα, απώλεια μυϊκής μάζας και παραισθήσεις («Εσωτερική Παθολογία», 2010, σ ) Υποκατάσταση της νεφρικής λειτουργίας Τιμές GFR μικρότερες από 5-10ml/min είναι ασυμβίβαστες με τη ζωή, γι αυτό και η επιβίωση των ασθενών σε τέτοιες περιπτώσεις είναι δυνατή μόνο με την εφαρμογή μεθόδων υποκατάστασης της νεφρικής λειτουργίας. Στους ασθενείς με ΧΝΑ τελικού σταδίου η νεφρική υποκατάσταση πρέπει να τελείται εφ όρου ζωής, ή μέχρι να υποβληθούν σε μεταμόσχευση νεφρού. Μέσω των μεθόδων αυτών ωστόσο, αναπληρώνεται μόνο η απεκκριτική λειτουργία των νεφρών (απομάκρυνση τοξικών αζωτούχων μεταβολικών ουσιών, κυρίως μικρομοριακών) και αποκαθίστανται οι διαταραχές του εξωκυτταρικού όγκου υγρών, των ηλεκτρολυτών (υπερκαλιαιμία, υπερφωσφαταιμία, υπερμαγνησιαιμία) καθώς και οι διαταραχές της οξεοβασικής ισορροπίας. Αυτές που δεν αναπληρώνονται είναι οι ενδοκρινείς και μεταβολικές νεφρικές λειτουργίες. Παρόλα αυτά, ιδιαίτερα μετά την εξωγενή χορήγηση ουσιών, όπως η ερυθροποιητίνη (ΕPO) και η δραστική μορφή της βιταμίνης D- η ελλιπής παραγωγή των οποίων στη ΧΝΑ τελικού σταδίου οδηγεί σε βαριάς μορφής αναιμία- η ποιότητας ζωής των ασθενών και η αναιμία έχουν βελτιωθεί αισθητά, καθώς επιτυγχάνονται τιμές αιματοκρίτη (Hct) από 35-38%, οι οποίες είναι παραπλήσιες του φυσιολογικού υγιούς πληθυσμού. Στους ασθενείς με ΧΝΑ τελικού σταδίου, ως μέθοδοι υποκατάστασης της νεφρικής λειτουργίας εφαρμόζονται κυρίως η αιμοκάθαρση (συχνότερα χρησιμοποιούμενη μέθοδος) και η περιτοναϊκή κάθαρση, ενώ για κάθε μία από τις δύο έχουν αναπτυχθεί πολλές παραλλαγές που αποσκοπούν κυρίως στη βελτίωση της αποτελεσματικότητάς τους ως προς την κάθαρση των ουραιμικών τοξινών, στη μείωση των επιπλοκών και τελικά στη μείωση της ιδιαίτερα αυξημένης καρδιαγγειακής θνησιμότητας των ασθενών («Εσωτερική Παθολογία», 2010, σ ) Αιμοκάθαρση Αιμοκάθαρση ονομάζουμε τη διαδικασία κατά την οποία το αίμα περνά μέσα από ένα ειδικό φίλτρο ώστε να απομακρυνθούν οι άχρηστες ουσίες και το πλεονάζον νερό, ενώ το καθαρό πλέον αίμα επιστρέφει στο σώμα του ασθενή. ~ 30 ~
31 Πιο συγκεκριμένα, για την εφαρμογή της κλασικής (συμβατικής) αιμοκάθαρσης (conventional hemodialysis, HD), απαιτείται αγγειακή προσπέλαση του ασθενούς. Αυτή επιτυγχάνεται με ειδικές βελόνες που εφαρμόζονται σε δύο διαφορετικά σημεία στο αντιβράχιο. Η μία βελόνα χρησιμοποιείται για την εισαγωγή και προώθηση του αίματος του ασθενούς στο μηχάνημα της κάθαρσης (τεχνητός νεφρός), ενώ η δεύτερη χρησιμοποιείται για την επιστροφή του αίματος στον ασθενή. Το αίμα που κυκλοφορεί στον τεχνητό νεφρό, ανανεώνεται συνεχώς, και για χρονικό διάστημα 4-5 ωρών ανά συνεδρία αιμοκάθαρσης, διέρχεται από το φίλτρο αιμοκάθαρσης πριν επιστρέψει στον ασθενή. Το φίλτρο αιμοκάθαρσης χαρακτηρίζεται από δύο ανεξάρτητα διαμερίσματα, τα οποία διαχωρίζονται μεταξύ τους με ειδική μεμβράνη, τη λεγόμενη μεμβράνη αιμοκάθαρσης. Η μεμβράνη αυτή φέρει μικροσκοπικούς πόρους, ώστε να αποτελεί ένα ανάλογο του σπειραματικού ηθμού του νεφρού. Στο ένα διαμέρισμα του φίλτρου (αυτό που φέρει τριχοειδή μικροσκοπικής διαμέτρου) κυκλοφορεί το αίμα του ασθενούς, ενώ στο άλλο το διάλυμα αιμοκάθαρσης, το οποίο ανανεώνεται συνεχώς με τη βοήθεια ειδικής αντλίας. Το διάλυμα αιμοκάθαρσης είναι ένα ειδικό διάλυμα ηλεκτρολυτών (διττανθρακικών), του οποίου η σύνθεση προσομοιάζει με τη σύνθεση του εξωκυτταρικού υγρού. Χρησιμοποιούνται διαλύματα με διττανθρακικά διότι δε διαταράσσουν την καρδιαγγειακή ισορροπία, διορθώνουν ομαλά το ph και δεν προκαλούν συμπτώματα στο Κεντρικό Νευρικό Σύστημα και το κυκλοφορικό (Jacobs et al., 1996). Το νερό που χρησιμοποιείται για τη σύνθεση του διαλύματος αιμοκάθαρσης, είναι νερό του συστήματος ύδρευσης, το οποίο όμως έχει υποβληθεί σε απιονισμό και αποστείρωση προκειμένου να αποβληθούν άλατα, μικροσωματίδια, ιχνοστοιχεία μικροοργανισμών και άλλα στοιχεία που είναι εν δυνάμει επιβλαβή για τον ασθενή. Η μεμβράνη αιμοκάθαρσης καλύπτει το 90% της επιφάνειας του εξωσωματικού συστήματος. Υπάρχουν διάφορα είδη μεμβρανών. Οι μεμβράνες μπορεί να είναι συμμετρικές ή ασύμμετρες, ομοιογενείς ή ανομοιογενείς, ενώ έχουν τη δυνατότητα διακίνησης ουσιών αντιστρόφως ανάλογη του πάχους. Όσον αφορά τα είδη μεμβρανών, διακρίνονται οι κυτταρινικές (αναγεννημένη κυτταρίνη, οξική κυτταρίνη, τριοξική κυτταρίνη, αιμοφάνη) και τις συνθετικές (πολυακρυλονιτρίλη, πολυαμίδη, πολυκαρβονική πολυσουλφόνη). Προκειμένου η κάθαρση των ουραιμικών ουσιών να είναι αποτελεσματική, η κατεύθυνση της ροής του αίματος και αυτή του διαλύματος εντός του φίλτρου αιμοκάθαρσης είναι αντίθετες μεταξύ τους. Η αρχή στην οποία βασίζεται η απομάκρυνση των τοξινών στην κλασική αιμοκάθαρση είναι η διάχυση η οποία συμβαίνει χάρη στη διαφορά συγκέντρωσης των ουσιών εκατέρωθεν της ημιδιαπερατής μεμβράνης και έγκειται στην παθητική μεταφορά διαλυτών ουσιών (από την υψηλότερη συγκέντρωση στη χαμηλότερη), χωρίς τη μετακίνηση του νερού Επιδράσεις της νόσου και της αιμοκάθαρσης στα ερυθροκύτταρα και το πλάσμα Τα ερυθροκύτταρα των ασθενών με ΧΝΑ έχουν μικρό προσδόκιμο ζωής κι αυτό οφείλεται στο γεγονός ότι τα κύτταρα αυτά υφίστανται οξειδωτικό στρες μέσω της ενεργοποίησης των ουδετερόφιλων που έρχονται σε επαφή με το φίλτρο της αιμοκάθαρσης, μηχανικό στρες λόγω της ροής τους μέσα από τη συσκευή αιμοκάθαρσης αλλά και μεταβολικό στρες εξαιτίας της απώλειας γλυκόζης, η οποία είναι το κύριο υπόστρωμα του ερυθροκυτταρικού μεταβολισμού και μπορεί να οδηγήσει σε μείωση της ικανότητας του συστήματος αντιοξειδωτικής άμυνας των κυττάρων (Stepniewska et al., 2006). Πιο συγκεκριμένα, όσον αφορά στο οξειδωτικό στρες, οι ασθενείς εμφανίζουν πριν την αιμοκάθαρση αυξημένα επίπεδα δραστικών ριζών οξυγόνου (ROS) περίπου κατά 140%, ποσοστό ~ 31 ~
32 που μειώνεται ελάχιστα μόλις ολοκληρωθεί η συνεδρία. Έτσι, η αιμοκάθαρση δεν καταφέρνει να επαναφέρει το οξειδωτικό στρες σε φυσιολογικά επίπεδα, γεγονός που υποδηλώνει πως το οξειδωτικό στρες δεν είναι αποτέλεσμα της αιμοκάθαρσης, αλλά είναι χαρακτηριατικό της ουραιμίας το οποίο αδυνατεί να αντιμετωπιστεί από τη διαδικασία της αιμοκάθαρσης. Επιπλέον, η απώλεια αντιοξειδωτικών ουσιών κατά τη διάρκεια της αιμοκάθαρσης, αποτελεί έναν ακόμη παράγοντα που πυροδοτεί τη συσσώρευση ενδοκυττάριων ROS μετά τη συνεδρία. Όσον αφορά στη μορφολογία των ερυθροκυττάρων, αυτή παρουσιάζει μεγάλη απόκλιση στους ασθενείς σε σχέση με τα υγιή άτομα. Έτσι, σε αιμοκαθαιρόμενους ασθενείς, πριν την αιμοκάθαρση, παρατηρούνται αυξημένα ποσοστά εχινοκυττάρων, στοματοκυττάρων και κνιζοκυττάρων, μορφές κυττάρων δηλαδή με αλλοιωμένο σχήμα σε σχέση με το φυσιολογικό δισκοειδές. Μάλιστα, τα επίπεδα των ROS πριν από την αιμοκάθαρση είναι ανάλογα με το ποσοστό των εχινοκυττάρων, ενώ αντιστρόφως ανάλογα με τα ποσοστά των στοματοκυττάρων και των κνιζοκυττάρων, επομένως η εχινοκυττάρωση μπορεί να θεωρηθεί ως δείκτης αυξημένου οξειδωτικού στρες. Τα στοματοκύτταρα και εχινοκύτταρα αποτελούν αναστρέψιμες μορφές, δηλαδή σε πολύ μεγάλο βαθμό καταφέρνουν να αποκτήσουν φυσιολογικό σχήμα όταν βελτιωθούν οι συνθήκες του περιβάλλοντος. Αν όμως η μορφολογική αλλοίωση έχει προχωρήσει στο στάδιο του σφαιροκυττάρου, τότε η αναστρεψιμότητα καθίσταται αδύνατη. Εκτός από τα σφαιροκύτταρα, στις μη αναστρέψιμες μορφολογικές τροποποιήσεις περιλαμβάνονται τα ελλειπτοκύτταρα, οβαλοκύτταρα, σχιστοκύτταρα, δακρυοκύτταρα και σφαιροεχινοκύτταρα. Ένα άλλο σημαντικό χαρακτηριστικό που παρατηρείται με το πέρας της αιμοκάθαρσης, είναι η βελτίωση της δομικής ακεραιότητας και της ερυθροκυτταρικής μεμβράνης λόγω της απομάκρυνσης των ουραιμικών τοξινών, απομάκρυνση που σχετίζεται επίσης και με τη βελτιωμένη ωσμωτική ευθραυστότητα του ερυθροκυττάρου. Ακόμη, το γεγονός ότι με την αιμοκάθαρση απομακρύνονται από την κυκλοφορία τα καταστραμμένα ερυθροκύτταρα, έχει θετική επίδραση στην μεγαλύτερη και καλύτερη έκφραση κάποιων μεμβρανικών πρωτεϊνών, όπως είναι η σπεκτρίνη, σε ερυθροκύτταρα ασθενών μετά την αιμοκάθαρση (Antonelou et al., 2011) Αιμοδιαδιήθηση Η ανάγκη για ελάττωση της νοσηρότητας και θνησιμότητας των αιμοκαθαιρόμενων ασθενών παράλληλα με την ανάγκη για βελτίωση της ποιότητας ζωής τους, έχουν οδηγήσει στην ανεύρεση βελτιωμένων τεχνικών υποκατάστασης της νεφρικής λειτουργίας, οι οποίες να προσομοιάζουν κατά το μεγαλύτερο δυνατό βαθμό με τη φυσιολογική λειτουργία των νεφρών. Μία τέτοια μέθοδος είναι η αιμοδιαδιήθηση (hemodiafiltration, HDF). Αυτή η τεχνική υποκατάστασης της νεφρικής λειτουργίας συνδυάζει τη διάχυση και τη διήθηση για την απομάκρυνση των τοξινών. Ένα από τα βασικότερα πλεονεκτήματά της έναντι της συμβατικής αιμοκάθαρσης είναι το γεγονός ότι επιτυγχάνει καλύτερη κάθαρση των μεσαίου μοριακού βάρους τοξινών. Για την εφαρμογή της αιμοδιαδιήθησης, απαιτείται η χρησιμοποίηση μεμβρανών υψηλής διαπερατότητας (high-flux), καθώς και ειδικό μηχάνημα τεχνητού νεφρού με δύο αντλίες, αφού λόγω της μεγάλης ποσότητας των υγρών και ηλεκτρολυτών του ορού που απομακρύνονται από τον ασθενή (12-15L) κατά την αιμοδιαδιήθηση, είναι απαραίτητη η μερική αντικατάστασή τους με ειδικό διάλυμα αναπλήρωσης. Χρησιμοποιείται επίσης και διάλυμα αιμοκάθαρσης, το οποίο διέρχεται από το φίλτρο, όπως ακριβώς συμβαίνει και στην κλασική αιμοκάθαρση, ώστε να επιτευχθεί παράλληλα και η κάθαρση των μικρού μοριακού βάρους ουραιμικών τοξινών (Εικ.10). Οι ουραιμικές τοξίνες μπορούν να κατηγοριοποιηθούν ως εξής: τις ελεύθερες υδατοδιαλυτές, μικρού μοριακού βάρους τοξίνες (MB <500 D), όπως είναι η ουρία, τις μεσαίου ~ 32 ~
33 μοριακού βάρους (MB>500 D), όπως η β-2 μικροσφαιρίνη και αυτές που προσδένονται σε πρωτεΐνες (Vanholder et al., 2008). Η συμβατική αιμοκάθαρση επιτυγχάνει την απομάκρυνση μικρού μοριακού βάρους ουσιών (ουρία). Η β-2 μικροσφαιρίνη χρησιμοποιείται στις μελέτες ως δείκτης των ουραιμικών τοξινών μεσαίου μοριακού βάρους προκειμένου να αξιολογηθεί η αποτελεσματικότητα των μεθόδων αιμοκάθαρσης μέσω της απομάκρυνσής της. Με τη χρήση μεθόδων που χαρακτηρίζονται από μεμβράνες υψηλής διαπερατότητας, όπως η HDF, επιτυγχάνεται σημαντική μείωση της β-2 μικροσφαιρίνης στον ορό (Blankestijn et al., 2010). Επομένως, μέθοδοι που χρησιμοποιούν μεμβράνες υψηλής διαπερατότητας επιτυγχάνουν απομάκρυνση ενός ευρύτερου φάσματος ουραιμικών τοξινών, γεγονός που μειώνει τη νοσηρότητα-θνησιμότητα των ασθενών με ΧΝΑ, βελτιώνοντας την ποιότητα και το προσδόκιμο ζωής τους (El-Wakil et al., 2013) Αιμοκάθαρση vs. Αιμοδιαδιήθηση Ένα από τα σημαντικότερα πλεονεκτήματα της αιμοδιαδιήθησης έναντι της κλασικής αιμοκάθαρσης, όπως έχει ήδη αναφερθεί, είναι η καλύτερη κάθαρση ουραιμικών τοξινών μεγαλύτερου μοριακού βάρους που αυτή επιτυγχάνει, σαν αποτέλεσμα του συνδυασμού διάχυσης και διήθησης. Ωστόσο υπάρχουν και άλλα σημεία στα οποία η αιμοδιαδιήθηση υπερτερεί έναντι της συμβατικής αιμοκάθαρσης ως μέθοδος υποκατάστασης της νεφρικής λειτουργίας. Πιο συγκεκριμένα: Αρκετές μελέτες αναφέρουν ότι σε σύγκριση με την συμβατική αιμοκάθαρση, η HDF βελτιώνει την αναιμία των αιμοκαθαιρόμενων νεφροπαθών, αυξάνοντας σημαντικά την αιμοσφαιρίνη (Ηb) και τα επίπεδα του αιματοκρίτη (Hct). Αυτή η επίτευξη υψηλότερων επιπέδων αιματοκρίτη και αιμοσφαιρίνης αποδίδεται στην εξάλειψη ουραιμικών τοξινών μεσαίου μοριακού βάρους, χάρη στη χρήση μεμβρανών υψηλής διαπερατότητας που χρησιμοποιούνται σε αυτή τη μέθοδο. Η συσσώρευση αυτών των ουσιών θεωρείται ότι παρεμποδίζει τη διαδικασία της ερυθροποίησης. Mέσω της HDF επιτυγχάνεται καλύτερη απομάκρυνση αυτών των ουσιών με αποτέλεσμα να επιτυγχάνονται υψηλότερα επίπεδα αιματοκρίτη και αιμοσφαιρίνης αίματος με ταυτόχρονη μείωση των χορηγούμενων δόσεων ερυθροποιητίνης από εκείνη που συνηθίζεται στη συμβατική αιμοκάθαρση. Επιπλέον, η HDF είναι ιδιαίτερα αποτελεσματική όσον αφορά τη μείωση της υπερφωσφαταιμίας, η οποία είναι συνήθης στους νεφροπαθείς και έχει να κάνει με τη μείωση της σύνθεσης καλσιτριόλης (ενεργός μορφή της βιταμίνης D) και τη μειωμένη εντερική απορρόφηση ασβεστίου, προκαλώντας έτσι αυξημένα επίπεδα παραθορμόνης. Η εψιδίνη είναι ένα μόριο που εκκρίνεται από το ήπαρ, αποτελεί κύριο μεσολαβητή της ομοιόστασης τους σιδήρου και αποβάλλεται από τους νεφρούς. Στη ΧΝΑ παρατηρείται αυξημένη έκφραση εψιδίνης, η οποία παρεμποδίζει την εντερική απορρόφηση του σιδήρου και αναστέλλει την απελευθέρωσή του από τις αποθήκες του δικτυοενδοθηλιακού συστήματος και των ηπατοκυττάρων. Σε αντίθεση με την συμβατική αιμοκάθαρση η οποία σε γενικές γραμμές δεν επιτυγχάνει μείωση της εψιδίνης, η HDF καταφέρνει να μειώσει αποτελεσματικά τα επίπεδά της, γεγονός που συνεισφέρει και αυτό με τη σειρά του σε βελτίωση της αναιμίας των ασθενών. Η χρόνια και συστημική φλεγμονή αποτελεί κύρια συνιστώσα της ΧΝΑ και είναι υπεύθυνη σε μεγάλο βαθμό για τη νοσηρότητα και θνησιμότητα των ασθενών, καθώς σε συνδυασμό με το οξειδωτικό στρες οδηγεί σε δυσλειτουργία του ενδοθηλίου, αγγειακές βλάβες και αθηροσκλήρωση, οι οποίες με τη σειρά τους καταλήγουν στην εμφάνιση καρδιαγγειακής νόσου. Κυτταροκίνες που ~ 33 ~
34 εκκρίνονται κατά τη φλεγμονή, όπως είναι οι ιντερλευκίνες IL-1 και IL-6 και ο παράγοντας TNF-α καταστέλλουν τη δραστηριότητα των πρόδρομων κυττάρων στα διαφορετικά στάδια της ερυθροποίησης. Η HDF επιτυγχάνει μία σημαντική μείωση της φλεγμονής χάρη στην αποτελεσματική απομάκρυνση των παραγόντων που προάγουν τη φλεγμονή και των αναστολέων της ερυθροποίησης (Bowry and Gatti, 2011). Μάλιστα, έχει βρεθεί ότι αυξάνονται τα επίπεδα της C- αντιδρώσας πρωτεΐνης και της ιντερλευκίνης IL-6 στους ασθενείς που υπόκεινται σε συμβατική αιμοκάθαρση, ενώ παραμένουν σταθερά σε αυτούς που αιμοκαθαιρούνται μέσω της HDF (Santoro and Mancini, 2014). Η αυξημένη έκθεση της φωσφατιδυλοσερίνης που αποτελεί ένα δείκτη απομάκρυνσης των ερυθροκυττάρων από την κυκλοφορία, σχετίζεται με την παθοφυσιολογία του ουραιμικού συνδρόμου. Σαν συνέπεια, τα ερυθροκύτταρα προσκολλώνται στο ενδοθήλιο των αγγείων, γεγονός που πιθανά παίζει ρόλο στην επιδείνωση των καρδιαγγειακών επιπλοκών που συναντάται στους ασθενείς με ΧΝΑ. Υπάρχουν ορισμένοι ουραιμικοί παράγοντες του πλάσματος με μοριακό βάρος που κυμαίνεται μεταξύ των και Da, οι οποίοι προκαλούν αυξημένη έκθεση PS και δεν είναι ξεκάθαρο εάν και σε τι βαθμό αυτοί απομακρύνονται από την κυκλοφορία με τη διαδικασία της αιμοκάθαρσης. Η HDF σε αυτό το σημείο, έχει αποδειχθεί πιο αποτελεσματική μέθοδος έναντι της αιμοκάθαρσης όσον αφορά την απομάκρυνση των ουραιμικών παραγόντων που προκαλούν έκθεση PS, με αποτέλεσμα να οδηγεί σε μείωση της εξωτερίκευσης PS, γεγονός που οδηγεί σε αύξηση του προσδόκιμου ζωής των ερυθροκυττάρων των ασθενών (Bonomimi et al., 2004). Εικόνα 10: Σχηματική αναπαράσταση βασικών μεθόδων υποκατάστασης της νεφρικής λειτουργίας: αιμοκάθαρση και αιμοδιαδιήθηση. (Ανατύπωση από Ronco, C. In Critical Care Nephrology, 2008). Η ΧΝΑ είναι μια κατάσταση οξειδωτικού στρες, λόγω της έλλειψης ισορροπίας μεταξύ οξειδωτικών και αντιοξειδωτικών ουσιών. Το οξειδωτικό στρες, συνδέεται στενά με πολλές παθολογικές καταστάσεις, όπως είναι η καρκινογένεση, η αθηροσκλήρωση, οι νευροεκφυλιστικές ασθένειες, το σύνδρομο επίκτητης ανοσολογικής ανεπάρκειας και οι μακροπρόθεσμες επιπλοκές του διαβήτη. Κύριες οξειδωτικές ουσίες σε όλα τα βιολογικά συστήματα είναι οι ROS, όπως είναι για ~ 34 ~
35 παράδειγμα το ανιόν σουπεροξειδίου (O - 2 ), το υπεροξείδιο του υδρογόνου (H 2 O 2 ), η ελεύθερη ρίζα υδροξυλίου (OH - ) και το μονήρες οξυγόνο. Οι ασθενείς με ΧΝΑ υφίστανται περαιτέρω οξειδωτικό στρες το οποίο προκαλείται κατά τη διαδικασία της αιμοκάθαρσης ενώ οι δραστικές μορφές οξυγόνου εμπλέκονται στην εμφάνιση διαφόρων επιπλοκών της ασθένειας εξαιτίας της αιμοδιάλυσης, όπως είναι η αμυλοείδωση, η αθηροσκλήρωση και οι καρδιαγγειακές νόσοι γενικότερα. Προκειμένου να ελαχιστοποιηθεί τόσο επιπλέον οξειδωτικό στρες όσο και οι επιπλοκές του που προκαλούνται κατά την αιμοκάθαρση, ακολουθούνται διάφορες στρατηγικές όπως είναι η χρήση βιοσυμβατών μεμβρανών, η χρήση μεμβρανών οι οποίες μπορούν να επιτύχουν την απομάκρυνση φλεγμονωδών μεσολαβητών του πλάσματος, η χρήση υπερ-καθαρού νερού για τα διαλύματα κάθαρσης, η χρήση βιταμινών καθώς και η αλλαγή της συχνότητας των εβδομαδιαίων συνεδριών αιμοκάθαρσης (Torregrosa et al., 2007). Επομένως, η HDF λόγω της καλύτερης ποιότητας μεμβρανών και διαλυμάτων κάθαρσης υπερτερεί έναντι της συμβατικής αιμοκάθαρσης στην αντιμετώπιση του οξειδωτικού στρες. Συνοψίζοντας τα παραπάνω, καταλήγουμε πως η HDF πλεονεκτεί έναντι της συμβατικής αιμοκάθαρσης όσον αφορά τη βελτίωση της αναιμίας των ασθενών με τη σημαντική αύξηση της ερυθροποίησης ταυτόχρονα με μειωμένη εξωγενή χορήγηση ερυθροποιητίνης, με τη βελτίωση του μεταβολισμού του σιδήρου αλλά και των επιπέδων οξειδωτικού στρες. Υπάρχει δηλαδή σημαντική βελτίωση όλων των παραμέτρων που οδηγούν σε αύξηση του προσδόκιμου ζωής των ερυθροκυττάρων (Bowry and Gatti, 2011), παρότι στη βιβλιογραφία αναφέρονται συγκριτικές μελέτες που υποστηρίζουν πως η HDF δεν είναι πλεονεκτικότερη σε σχέση με τη συμβατική αιμοκάθαρση. Η βελτιωμένη ποιότητα ζωής που μπορεί να εξασφαλίζει η HDF έναντι της κλασικής αιμοκάθαρσης στους ασθενείς, έγκειται σε έναν συνδυασμό καλύτερου ελέγχου της αναιμίας, μείωσης των διαταραχών φωσφόρου-ασβεστίου και αποτελεσματικότερης απομάκρυνσης των μεσαίου και μεγαλύτερου μοριακού βάρους ουραιμικών τοξινών. Ακόμα, εξασφαλίζει καλύτερο έλεγχο της υπέρτασης και της αιμοδυναμικής σταθερότητας, ενώ συντονίζει καλύτερα τους μηχανισμούς που εμπλέκονται στη μείωση των φλεγμονωδών αποκρίσεων, του οξειδωτικού στρες και της ενδοθηλιακής δυσλειτουργίας (Bowry and Gatti, 2011). Όλα τα παραπάνω γίνονται καλύτερα αντιληπτά αν λάβουμε υπό όψιν μας τα αποτελέσματα ερευνών που δείχνουν πως οι ασθενείς στους οποίους εφαρμόζεται αιμοδιαδιήθηση παρουσιάζουν μικρότερα ποσοστά θνησιμότητας εξαιτίας καρδιαγγειακών επιπλοκών, της συχνότερης δηλαδή αιτίας θανάτου των νεφροπαθών, σε ποσοστό 33%, καθώς και 55% λιγότερο κίνδυνο θνησιμότητας εξαιτίας λοιμώξεων, μια επίσης συνήθη αιτία νοσηρότητας και θνησιμότητας στους αιμοκαθαιρόμενους ασθενείς (Blankestijn P., 2014). ~ 35 ~
36 2. ΣΚΟΠΟΣ ΤΗΣ ΕΡΓΑΣΙΑΣ Η συγκεκριμένη εργασία είχε ως στόχο τη μελέτη των επιδράσεων δύο διαφορετικών μεθόδων κάθαρσης και συγκεκριμένα της συμβατικής αιμοκάθαρσης (HD) και της αιμοδιαδιήθησης (HDF) στο αιματολογικό πρότυπο και σε χαρακτηριστικά της φυσιολογίας των ερυθροκυττάρων και του πλάσματος ασθενών με χρόνια νεφρική ανεπάρκεια τελικού σταδίου. Για το σκοπό αυτό λήφθηκε αίμα από κλινικά σταθερούς ασθενείς που πάσχουν από Χρόνια Νεφρική Ανεπάρκεια (ΧΝΑ) και οι οποίοι υποβάλλονταν σε συμβατική αιμοκάθαρση και σε αιμοδιαδιήθηση. Και οι δύο ομάδες των αιμοκαθαιρόμενων ασθενών βρίσκονταν υπό θεραπεία με ερυθροποιητίνη (rhepo). Ως μάρτυρες, χρησιμοποιήθηκαν δείγματα αίματος από υγιείς αιμοδότες. Η λήψη αίματος από τους ασθενείς πραγματοποιήθηκε πριν και μετά τη συνεδρία της κάθαρσης. ~ 36 ~
37 3. ΥΛΙΚΑ - ΜΕΘΟΔΟΙ 3.1 Υλικά Αντιδραστήρια APS Αιθανόλη Ακρυλαμίδη Αντιδραστήριο Drapkin s β - μερκαπτοαιθανόλη Βουτανόλη t-bhp (tert-butyl hydroperoxide) Γλουταρική αλδεΰδη Γλυκερόλη Γλυκίνη DMSO (dimethyl sulfoxide) Δις Ακρυλαμίδη Αιθυλενοδιαμινοτετραοξικό Οξύ (EDTA) FeCl 3 Fluo 4-AM Υδροχλωρικό Οξύ (HCl) Hepes Ισοπροπανόλη Κυτταρίνη Μεταλλικά σφαιρίδια (beads) Na 2 HPO 4 2H2O NaH2PO4H2O KH 2 HPO 4 Χλωριούχο Κάλιο (KCl) Χλωριούχο Νάτριο (NaCl) N, N, N, N - Tetramethylethylendiamin (TEMED) Διάλυμα Οξικού Οξέος Τετροξείδιο του Οσμίου (OsO 4 ) PMSF (Phenyl methyl sulfonyl fluoride) Πυροσταφυλικό Nάτριο Θειικό Δωδεκακυλικό Νάτριο (SDS, sodium dodecyl sulfate) Κακοδυλικό Νάτριο (Sodium cacodylate) Σουκρόζη (Sucrose) TPTZ (2,4,6 tripyridyl-s-triazine ) Tris Ουρικάση (Uricase) Χρυσό-Παλλάδιο ~ 37 ~
38 3.1.2 Όργανα-Συσκευές Επιτραπέζια φυγόκεντρος Εppendorf Ηλεκτρονικό Μικροσκόπιο Σάρωσης, Philips SEM 515 Ηλεκτρονικό πεχάμετρο Κλίβανος Rocker, Grant Bio PTR-35 Συσκευή ηλεκτροφόρησης Συσκευή κάλυψης Χρυσού-Παλλαδίου Τransblot SDI Semidry Transfer Gel Φθορισμόμετρο Φωτόμετρο Ψυχόμενη επιτραπέζια φυγόκεντρος Χρωστικές Bradford Βρωμοφαινόλη μπλε Coomassie Brilliant Blue R Αντισώματα anti-aqp 1 anti-glut 1 anti-stomatin anti-cd47 anti-spectrin anti-iggs-hrp HRP-conjugated anti-mouse IgG HRP-conjugated anti-rabbit IgG Φωτογραφικά Υλικά Ακτινογραφικό φιλμ (X-ray film) Εμφανιστής D-19 ECL Western Blotting Detection Reagents Στερεωτής (fixer) ακτινογραφικού φιλμ Αναλώσιμα Διηθητικό χαρτί Whatmann 3MM Eppendorfs των 0.5 ml, 1.5 ml Κυβέτες φασματοφωτομέτρου Νιτροκυτταρίνη 0.45 μm Πιπέτες Σύριγγες ~ 38 ~
39 3.2 Μέθοδοι Αιματολογικός έλεγχος Ο αιματολογικός έλεγχος πραγματοποιήθηκε με τον αυτόματο αναλυτή Sysmex Κ Λευκαφαίρεση Η διαδικασία της λευκαφαίρεσης στοχεύει στην απομάκρυνση όλων των τύπων λευκοκυττάρων και των αιμοπεταλίων. Η μέθοδος αυτή περιλαμβάνει το πέρασμα ολικού αίματος από στήλες που αποτελούνται από μείγμα κυτταρινών (μικροκρυσταλλικής και α-κυτταρίνης), με αποτέλεσμα την απομάκρυνση πάνω από το 99,75% του συνόλου των λευκοκυττάρων και της πλειονότητας των αιμοπεταλίων. Η διαδικασία που ακολουθήθηκε ήταν η εξής: Φυγοκέντρηση δειγμάτων στις 3.000rpm για 10 λεπτά, αφαίρεση υπερκειμένου και αραίωση των πακεταρισμένων ερυθροκυττάρων με διάλυμα PBS 310mOsm. Ανάμειξη κυτταρινών σε ίση αναλογία για τη δημιουργία κολώνων κυτταρίνης. Εμποτισμός των κολώνων με PBS 310mOsm. Προσθήκη δειγμάτων στις στήλες. Συλλογή των ερυθροκυττάρων και διαδοχικές πλύσεις με PBS 310mΟsm σε ψυχόμενη φυγόκεντρο για την απομάκρυνση των κυτταρινών Απομόνωση ερυθροκυτταρικών μεμβρανών (ghosts) Η απομόνωση των ερυθροκυτταρικών μεμβρανών ελευθέρων αιμοσφαιρίνης πραγματοποιείται με τη μέθοδο της υποτονικής αιμόλυσης (Dodge et al. 1963), η οποία βασίζεται στο φαινόμενο της ώσμωσης, ελαφρά τροποποιημένη με την προσθήκη PMSF (Advani R. et al. 1992) για αναστολή της πρωτεόλυσης. Συγκεκριμένα, σε απομονωμένα ερυθροκύτταρα προστίθεται το διάλυμα λύσης (υπότονο). Έτσι, προκαλείται οσμωτική λύση των ερυθροκυττάρων δηλαδή δημιουργία ρηγμάτων στην ερυθροκυτταρική μεμβράνη και απελευθέρωση του κυτοσολίου. Μετά από τις διαδοχικές πλύσεις και φυγοκεντρήσεις οι μεμβράνες παραμένουν ως ίζημα στον πυθμένα των σωλήνων (Dodge J. et al, 1963). Για την επίτευξη καλύτερων αποτελεσμάτων όσον αφορά, αφενός μεν την αποφυγή αλλοιώσεων στα συστατικά της μεμβράνης, αφετέρου δε την απομάκρυνση του μεγαλύτερου δυνατού ποσού της αιμοσφαιρίνης, επιλέγονται κατάλληλες τιμές ιοντικής ισχύος και pη (20mOsm και 8,0 αντίστοιχα). Για την απομόνωση ερυθροκυτταρικών μεμβρανών ελευθέρων αιμοσφαιρίνης (ghosts), χρησιμοποιήθηκε 5ml ολικό αίμα ασθενών σε αντιπηκτικό EDTΑ. Τα στάδια της πειραματικής διαδικασίας είναι τα εξής : 1. Λύση των ερυθροκυττάρων που λήφθηκαν μετά από τη διαδικασία λευκαφαίρεσης με υπότονο διάλυμα φωσφορικών, στο οποίο έχει προστεθεί διάλυμα αναστολέων πρωτεασών (PMSF). Το αιμόλυμα επωάζεται στον πάγο για 45 λεπτά, με ανάδευση ανά 5 λεπτά με ήπιες κινήσεις (διαδικασία κρίσιμη για τις διαμεμβρανικές πρωτεΐνες). ~ 39 ~
40 2. Φυγοκέντρηση λύσης στις rpm για 20 λεπτά (4 o C) και ύστερα απομάκρυνση του υπερκειμένου (περιέχει Ηb) καθώς και του δεύτερου ιζήματος στο οποίο περιέχονται λευκοκύτταρα, άσπαστα ερυθροκύτταρα και πρωτεάσες. 3. Ακολουθούν πλυσίματα με υπότονο διάλυμα φωσφορικών. Η διαδικασία επαναλαμβάνεται όσες φορές χρειαστεί ώστε το ίζημα να αποχρωματιστεί, να απομακρυνθεί δηλαδή όλη η ποσότητα της αιμοσφαιρίνης και να μείνουν αποκλειστικά οι μεμβράνες των ερυθροκυττάρων (ghosts) Υπολογισμός ολικής πρωτεϊνικής συγκέντρωσης δείγματος Αμέσως μετά την απομόνωση των ερυθροκυτταρικών μεμβρανών (ghosts), ακολουθεί η εύρεση της ολικής πρωτεϊνικής συγκέντρωσης των δειγμάτων. Αυτό γίνεται με την μέθοδο Bradford, η οποία βασίζεται στη δέσμευση της χρωστικής Coomasie Brilliant Blue G-250 στις πρωτεΐνες, δημιουργώντας σταθερό σύμπλοκο, το οποίο προκαλεί μετατόπιση του μέγιστου της απορρόφησης της χρωστικής από τα 465 στα 595 nm. Για τον υπολογισμό της συγκέντρωσης των δειγμάτων απαιτείται η δημιουργία πρότυπης καμπύλης αναφοράς, δηλαδή πρωτεΐνης γνωστής συγκέντρωσης, η οποία είναι της μορφής y=αx+β, όπου (y) είναι η απορρόφηση των δειγμάτων σε μήκος κύματος 595 nm, (x) είναι η ποσότητα της πρωτεΐνης του δείγματος σε mg και α, β τα σημεία που τέμνει η ευθεία τους άξονες. Κάθε δείγμα, περιέχει 790λ υπότονου διαλύματος φωσφορικών, 200λ διαλύματος Bradford και 10λ δείγματος ερυθροκυτταρικών μεμβρανών. Μετά την προσθήκη του αντιδραστηρίου Bradford ακολουθεί αναμονή 25min για να σταθεροποιηθεί ο χρωματισμός του δείγματος και φωτομέτρηση στα 595nm. Με τις τιμές των απορροφήσεων (Α 595nm ) και τη χρήση πρότυπης καμπύλης υπολογίζεται η συγκέντρωση κάθε δείγματος σε mg/ml. Το τυφλό που χρησιμοποιήθηκε περιείχε 800λ υπότονου διαλύματος και 200λ διαλύματος Bradford Προετοιμασία πρωτεϊνικού δείγματος για ηλεκτροφόρηση Προκειμένου να ηλεκτροφορηθούν οι απομονωμένες μεμβράνες, είναι απαραίτητη η επεξεργασία τους με ένα διάλυμα χρώσης, το οποίο παρασκευάζεται με την ανάμειξη διαλύματος 20% SDS-10mM EDTA, γλυκερόλης 100%, β-μερκαπτοαιθανόλης και 1% μπλε της βρωμοφαινόλης, σε αναλογία όγκου 10:10:5:1, αντίστοιχα. Για τελικό όγκο βαμμένου δείγματος 100λ, προστίθενται 26 λ του διαλύματος χρώσης σε 74 λ απομονωμένων μεμβρανών. Τα βαμμένα δείγματα, τοποθετούνται σε νερό που βράζει για 3 λεπτά για την ολοκλήρωση της αποδιάταξης των πρωτεϊνών SDS-PAGE ηλεκτροφόρηση πρωτεϊνών κατά Laemmli Η ηλεκτροφόρηση είναι μια μέθοδος κατά την οποία με τη βοήθεια επίδρασης ηλεκτρικού πεδίου, γίνεται διαχωρισμός φορτισμένων μακρομορίων σύμφωνα με το μοριακό τους βάρος, το ισοηλεκτρικό τους σημείο ή το φορτίο τους. Στην εργασία αυτή, πραγματοποιήθηκε η επίπεδη SDS- PAGE ηλεκτροφόρηση ομοιογενούς σύστασης 10%, κατά Laemmli (Laemmli, 1970). Σε αυτή τη μέθοδο χρησιμοποιείται διάλυμα SDS για να καλυφθούν όλες οι πρωτεΐνες με αρνητικό φορτίο, ώστε ο διαχωρισμός τους να γίνει ανάλογα το μοριακό βάρος τους. Αρχικά, παρασκευάζεται το πήκτωμα πακεταρίσματος (stacking gel), το οποίο εξασφαλίζει ότι όλες οι πρωτεΐνες θα ξεκινήσουν από το ίδιο σημείο για το διαχωρισμό τους. Έπειτα γίνεται η παρασκευή του πηκτώματος διαχωρισμού (resolving gel), με σκοπό τον διαχωρισμό των πρωτεϊνών. Τα ~ 40 ~
41 διαλύματα που χρησιμοποιούνται για την παρασκευή αυτών των πηκτωμάτων είναι: διάλυμα ακρυλαμίδης-δις ακρυλαμίδης 30:0.8 w/v, 0.4% SDS σε 1.5 Μ Tris/HCl ph 8.8, 0.4% SDS σε 0.5 M Tris/HCl ph 6.8, 10% APS και TEMED. Στο πήκτωμα διαχωρισμού, εκτός από τη συγκέντρωση της ακρυλαμίδης, η οποία διαφέρει κάθε φορά ανάλογα με το μοριακό βάρος των πρωτεϊνών που θέλουμε να διαχωριστούν, τα υπόλοιπα διαλύματα βρίσκονται σε σταθερή συγκέντρωση. Δηλαδή: 0.375M Tris/HCl ph 8.8, 0.1% SDS, 0.025% APS, 0.083% TEMED. Η συγκέντρωση της ακρυλαμίδης στο πήκτωμα αποτελεί τον καθοριστικό παράγοντα όσον αφορά τη διακριτική του ικανότητα, καθώς μεγάλη συγκέντρωση συνεπάγεται καλύτερη ανάλυση πρωτεϊνών χαμηλού μοριακού βάρους ενώ χαμηλή συγκέντρωση βοηθά στην ανάλυση πρωτεϊνών υψηλού μοριακού βάρους. Το πήκτωμα πακεταρίσματος έχει σταθερή σύσταση ανεξάρτητα από αυτό του διαχωρισμού, δηλαδή: 3.05% ακρυλαμίδη-δις, 0.127Μ Tris/HCl ph 6.8, 0.1% SDS, 0,05% APS, 0.17% TEMED. Μετά τον πολυμερισμό των πηκτωμάτων, τα δείγματα εισάγονται στις ειδικές θέσεις υποδοχείς. Στην πρώτη υποδοχή εισάγονται δείγματα πρωτεϊνών γνωστού μοριακού βάρους, τα οποία χρησιμεύουν ως μάρτυρες. Έπειτα, προστίθεται στη συσκευή το διάλυμα ηλεκτροδίων (Running buffer), το οποίο περιέχει 17.7 mm Tris, 192 mm γλυκίνη και 0.1% SDS ph 8.3 και βοηθά στην επίδραση του ρεύματος πάνω στις πρωτεΐνες. Απαιτείται ιδιαίτερη προσοχή στη ρύθμιση του ph, η οποία δεν πρέπει να γίνεται με υδροχλωρικό οξύ διότι τα ιόντα χλωρίου μειώνουν την αναλυτική ικανότητα της μεθόδου. Η συσκευή ηλεκτροφόρησης κλείνει και τα δύο ηλεκτρόδια συνδέονται με ειδική συσκευή εφαρμογής τάσης. Έτσι, επιτυγχάνεται ο διαχωρισμός των πρωτεϊνών υπό σταθερό ρεύμα I=20 ma, για κάθε πήκτωμα πακεταρίσματος και υπό σταθερό ρεύμα I=35 ma, για κάθε πήκτωμα διαχωρισμού. Η ηλεκτροφόρηση σταματάει όταν η χρωστική μπλε της βρωμοφαινόλης φτάσει σε απόσταση μισό εκατοστό από τη βάση του πηκτώματος διαχωρισμού και είναι εμφανείς όλες οι ζώνες των μαρτύρων μοριακών βαρών Χρώση ολικών πρωτεϊνών (εκτός γλυκοφορινών) σε πήκτωμα Μετά το τέλος της ηλεκτροφόρησης, τα πηκτώματα χρωματίζονται ώστε να γίνονται ορατές οι διαχωρισμένες σε αυτά πρωτεΐνες. Για τη χρώση χρησιμοποιείται η χρωστική Coomassie Blue- R250. Τα στάδια που ακολουθούνται είναι τα εξής: 1. Ολονύκτια επώαση των πηκτωμάτων σε διάλυμα 25% ισοπροπανόλη-10% v/v οξικό οξύ (fixer). 2. Αφαίρεση του διαλύματος fixer (φυλάσσεται για το επόμενο βήμα) και προσθήκη χρωστικής CB- R % w/v σε διάλυμα 10% οξικού οξέος. Επώαση σε κλίβανο στους 60 C για 1 ώρα και 30 λεπτά. 3. Αφαίρεση της χρωστικής και προσθήκη του διαλύματος fixer (που χρησιμοποιήθηκε στο πρώτο στάδιο). Επώαση για 2 ώρες υπό ανάδευση. 4. Αφαίρεση του διαλύματος fixer και προσθήκη διαλύματος 5% v/v ισοπροπανόλης σε 10% v/v οξικό οξύ. Επώαση για δύο ώρες υπό ανάδευση. 5. Αφαίρεση του προηγούμενου διαλύματος και ολονύκτια επώαση σε 10% v/v οξικό οξύ. 6. Σάρωση του πηκτώματος και αποθήκευση της εικόνας, η οποία μπορεί να χρησιμοποιηθεί για ποσοτική εκτίμηση των πρωτεϊνών Ανοσοαποτύπωμα (Western blotting) Η τεχνική του ανοσοαποτυπώματος των πρωτεϊνών είναι μια αναλυτική μέθοδος που περιλαμβάνει τη μεταφορά των πρωτεϊνών, που έχουν διαχωριστεί ηλεκτροφορητικά, από το ~ 41 ~
42 πήκτωμα σε ένα λεπτό και μεμβρανώδες υλικό στήριξης (νιτροκυτταρίνη) καθώς και την ανίχνευσή τους με αντισώματα. Αυτή η διαδικασία είναι χρήσιμη για την ευκολότερη ανίχνευση των πρωτεϊνών από τα αντισώματα καθώς οι πρωτεΐνες προσδένονται επιφανειακά στις μεμβράνες της νιτροκυτταρίνης. Η μεταφορά των πρωτεϊνών γίνεται με τη χρήση της ειδικής συσκευής Transblot- SDI Semidry Transfer Gel. Αρχικά, τοποθετούνται 6 φύλλα χαρτιών Whatmann, διαστάσεων 6x9.3 mm, το ένα πάνω στο άλλο, τα οποία έχουν εμποτιστεί προηγουμένως σε ρυθμιστικό διάλυμα μεταφοράς (Transfer buffer). Μετά από την τοποθέτηση κάθε χαρτιού είναι αναγκαία η απομάκρυνση φυσαλίδων που μπορεί να έχουν εγκλωβιστεί ενδιάμεσα, καθώς τα κενά αέρος που ίσως υπάρχουν θα εμποδίσουν τη μεταφορά των πρωτεϊνών. Στη συνέχεια τοποθετείται η μεμβράνη νιτροκυτταρίνης, διαστάσεων 5.5x8.8 mm, η οποία προηγουμένως έχει εμποτιστεί σε απεσταγμένο νερό. Ακολουθεί η τοποθέτηση του πηκτώματος πάνω στην νιτροκυτταρίνη με το σωστό προσανατολισμό και τέλος τοποθετούνται άλλα 6 φύλλα χαρτιών Whatmann εμποτισμένα σε ρυθμιστικό διάλυμα μεταφοράς. Σε κάθε στάδιο είναι απαραίτητη η αφαίρεση των φυσαλίδων. Η συσκευή κλείνει, ενώνεται με συσκευή εφαρμογής τάσης μέσω ηλεκτροδίων και ακολουθεί η μεταφορά πρωτεϊνών στη νιτροκυτταρίνη για περίπου 1 ώρα και 10 λεπτά σε σταθερή τάση 20 V. Η σύσταση του ρυθμιστικού διαλύματος μεταφοράς είναι: Tris 50mM, Glycine 40mM, SDS 0.04%,Methanol 20% ph8.3. Μετά τη μεταφορά των πρωτεϊνών στο φύλλο νιτροκυτταρίνης ακολουθεί ανίχνευση της πρωτεΐνης που μας ενδιαφέρει με, ειδικά για την πρωτεΐνη, αντισώματα. Αρχικά, γίνεται κάλυψη των μη ειδικών θέσεων πρόσδεσης του αντισώματος με επώαση της μεμβράνης σε άπαχο γάλα (blocking). Ακολουθεί επώαση των μεμβρανών με το πρωτογενές αντίσωμα ειδικό για την πρωτεΐνη. Ακολουθούν ξεπλύματα με διάλυμα PBS-T (Tween 0,1% σε PBS) και επώαση με το δευτερογενές αντίσωμα (αραιωμένο στο διάλυμα blocking), το οποίο είναι συζευγμένο με το ένζυμο υπεροξειδάση (HRP-Horseradish Peroxidase). Στη συνέχεια γίνεται ανίχνευση του σήματος με το σύστημα ECL που βασίζεται στη χημειοφωταύγεια. Συγκεκριμένα, η νιτροκυτταρίνη επωάζεται με το υπόστρωμα του ενζύμου HRP, τη luminol, η οποία οξειδώνεται και διεγείρεται. Επιστρέφοντας στην κατάσταση ηρεμίας παράγει φως το οποίο προσβάλλει φωτοευαίσθητα φιλμ αυτοραδιογραφίας. Η ανίχνευση του σήματος γίνεται σε σκοτεινό θάλαμο, λόγω της φωτοευαισθησίας των φιλμ. Στη συνέχεια γίνεται εμφάνιση των ζωνών με το διάλυμα D19. Το φιλμ ξεπλένεται σε νερό και ακολουθεί στερέωση με το διάλυμα fixer. Μετά το τέλος της ανοσοεντόπισης, είναι δυνατή η επαναχρησιμοποίηση της μεμβράνης νιτροκυτταρίνης, ύστερα από κατάλληλη επεξεργασία, για τον εντοπισμό και άλλων πρωτεϊνών που πιθανόν υπάρχουν στο ίδιο δείγμα. Για την πραγματοποίηση ενός νέου κύκλου ανοσοεντόπισης, είναι αναγκαία η αποκόλληση (stripping) των προηγούμενων ιχνηθετών που τοποθετήθηκαν στη μεμβράνη κατά τον πρώτο κύκλο. Αυτό επιτυγχάνεται με επώαση της μεμβράνης στους 50 C, για 30 λεπτά σε διάλυμα απορρυπαντικού PBS-T που περιέχει μερκαπτοαιθανόλη, σε κατάλληλη ποσότητα ώστε η τελική συγκέντρωσή της να είναι 0.7%. Ακολουθούν ξεπλύματα της μεμβράνης και στέγνωμα, ώστε να είναι έτοιμη για τον επόμενο κύκλο ανοσοεντόπισης Ποσοτική εκτίμηση των πρωτεϊνών πηκτωμάτων και φιλμ Τα πηκτώματα καθώς και τα φιλμ σαρώνονται και πυκνομετρούνται με τη βοήθεια του προγράμματος επεξεργασίας εικόνων GelAnalyserver 1.0. Ο τρόπος με τον οποίο γίνεται εκτίμηση της ποσότητας της κάθε ζώνης περιλαμβάνει τον ορισμό του υποβάθρου και του περιγράμματος της κάθε ζώνης. Συγκεκριμένα, ο χρήστης ορίζει την ~ 42 ~
43 περιοχή του υποβάθρου της ζώνης και στη συνέχεια το περίγραμμα της ζώνης. Μετά την αφαίρεση του υποβάθρου υπολογίζεται το άθροισμα της φωτεινότητας όλων των εικονοστοιχείων (pixels) που περιέχονται στη ζώνη και οι τιμές που προκύπτουν επεξεργάζονται με τη βοήθεια του προγράμματος Excel. Για κάθε δείγμα, υπολογίζεται η τιμή της κάθε πρωτεϊνικής ζώνης και η τιμή του λόγου της κάθε πρωτεΐνης προς το άθροισμα όλων των πρωτεϊνών ή προς μια πρωτεΐνη αναφοράς η οποία εμφανίζει σταθερές τιμές ανάμεσα στα δείγματα Προετοιμασία για παρατήρηση της μορφολογίας ερυθροκυττάρων με Ηλεκτρονικό Μικροσκόπιο Σάρωσης -(ΗΜΣ) Scanning Electron Microscope (SEM) Το Ηλεκτρονικό Μικροσκόπιο Σάρωσης στηρίζεται στην αρχή λειτουργίας ενός καθοδικού σωλήνα, ο οποίος περιέχει πηνία για την απόκλιση δέσμης ηλεκτρονίων. Η δέσμη αυτή, «σαρώνει» την επιφάνεια του παρασκευάσματος. Η αλληλεπίδραση των ηλεκτρονίων με το παρασκεύασμα μπορεί να έχει ως αποτέλεσμα: 1) την ανάκλαση των ηλεκτρονίων (οπισθοσκεδαζόμενα), 2) την έξοδο των ηλεκτρονίων από την επιφάνεια του παρασκευάσματος (δευτερογενή), 3) την απελευθέρωση ηλεκτρομαγνητικής ακτινοβολίας. Ανάλογα τις πληροφορίες που θέλουμε να πάρουμε οι ανιχνευτές χρησιμοποιούν και τα αντίστοιχα ηλεκτρόνια. Για παράδειγμα, για την παρατήρηση της ακρότατης επιφανειακής μορφολογίας, χρησιμοποιούνται μόνο τα δευτερογενή ηλεκτρόνια, ενώ για την παρατήρηση της βαθύτερης μορφολογίας, τα οπισθοσκεδαζόμενα. Στη συγκεκριμένη εργασία έγινε παρατήρηση της επιφανειακής μορφολογίας των ερυθροκυττάρων. Για την παραγωγή των δευτερογενών ηλεκτρονίων από την επιφάνεια του δείγματος πραγματοποιείται κάλυψη με στρώμα Χρυσού-Παλλαδίου (Au-Pd) ώστε το δείγμα να γίνει αγώγιμο. Η διαδικασία που ακολουθήθηκε για την παρατήρηση των δειγμάτων στο ΗΜΣ είναι η εξής: 1. Προσθήκη διαλύματος 2% γλουταρικής αλδεΰδης σε 0,1 mm κακοδυλικό νάτριο, ph 7.4, σε μικροποσότητα αίματος και επώαση για 1 ώρα σε θερμοκρασία δωματίου. 2. Ξέπλυμα με διάλυμα 4% σουκρόζης σε 0.1 mm κακοδυλικό νάτριο ph 7.4, επώαση για 15 λεπτά σε θερμοκρασία 4 C. Η διαδικασία επαναλαμβάνεται δύο φορές. 3. Προσθήκη 1% OsO4 σε 0.1 mm κακοδυλικό νάτριο ph 7.4 και επώαση για μια ώρα στους 4 C. 4. Ξέπλυμα με διάλυμα 4% σουκρόζης σε 0.1 mm κακοδυλικό νάτριο ph 7.4, επώαση για 15 λεπτά σε θερμοκρασία 4 C. Η διαδικασία επαναλαμβάνεται ακόμη μια φορά. 5. Διαδοχική αφυδάτωση σε αιθανόλη συγκεντρώσεων %, επώαση για δεκαπέντε λεπτά σε διάλυμα κάθε συγκέντρωσης. 6. Αραίωση των πακεταρισμένων ερυθροκυττάρων με διάλυμα 100% αιθανόλης σε αναλογία 1:5 ή 1:6 και επίστρωση του δείγματος σε στρογγυλή καλυπτρίδα. 7. Στέγνωμα στον αέρα. 8. Στερέωση της καλυπτρίδας σε stub του ΗΜΣ με ταινία διπλής όψης. 9. Κάλυψη με Χρυσό-Παλλάδιο. 10. Παρατήρηση στο Ηλεκτρονικό Μικροσκόπιο Σάρωσης Μέτρηση Μηχανικής Ευθραυστότητας (Mechanical Fragility-MFΙ) Ο όρος μηχανική ευθραυστότητα αναφέρεται στη ροπή των ερυθροκυττάρων προς αιμόλυση (ρήξη), κάτω από συνθήκες μηχανικής καταπόνησης (stress). Για τη μέτρηση της ~ 43 ~
44 ευαισθησίας των ερυθροκυττάρων στη μηχανική καταπόνηση χρησιμοποιούνται μεταλλικά σφαιρίδια και ειδική συσκευή για την ανάδευση των δειγμάτων. Δημιουργία πακεταρισμένων ερυθροκυττάρων με φυγοκέντρηση και προσθήκη PBS 310mOsm (όπως πάνω) Μέτρηση της ενδοκυττάριας Hb (αιμοσφαιρίνης) κατά Harboe (*) Κάθε δείγμα χωρίζεται στα δύο: ένα non-rocked, το οποίο δεν υποβάλεται σε καταπόνηση και χρησιμοποιείται ως δείγμα-μάρτυρας της αυτοαιμόλυσης του κάθε δείγματος και ένα rocked στο οποίο προστέθηκαν τα σφαιρίδια. Τα δείγματα με τα σφαιρίδια τοποθετείται στο μηχάνημα ανακίνησης για 1 ώρα σε 18rpm (10 )- 17 (5 ). Ακολουθεί φυγοκέντρηση των δειγμάτων στις 2750xg για 15 λεπτά, σε θερμοκρασία 4 C και λήψη του υπερκειμένου. Το υπερκείμενο φυγοκεντρείται στις xg για 20 λεπτά σε θερμοκρασία 4 C. Τέλος, πραγματοποιείται μέτρηση Hb στα υπερκείμενα rocked και non-rocked κατά Harboe. Η μηχανική ευθραυστότητα υπολογίζεται από τον εξής τύπο: MFI= [(PFHb rocked PFHb control )/ (Hb aliquot PFHb control )]x100, PFHb rocked : η μέση συγκέντρωση της αιμοσφαιρίνης στα υπερκείμενα των δειγμάτων με τα σφαιρίδια PFHb control : η μέση συγκέντρωση της αιμοσφαιρίνης στα δείγματα μάρτυρες (non-rocked) Hb aliquot : η μέση συγκέντρωση αιμοσφαιρίνης των δειγμάτων στο 20% του αιματοκρίτη (*) Μέτρηση Hb κατά Harboe για ενδοκυττάρια Hb: Αραίωση του δείγματος 1:10 σε dh 2 O (απεσταγμένο νερό) και ανάδευση. Επώαση για 30 λεπτά, σε RT. Μέτρηση στα 380nm - 415nm - 450nm. (Harm S.K. et al.,2012) Μέτρηση Ωσμωτικής Ευθραυστότητας (Mean corpuscular fragility-mcf) Η Ωσμωτική Ευθραυστότητα αναφέρεται στο βαθμό της αιμόλυσης που συμβαίνει όταν δείγμα ερυθροκυττάρων υποβάλλεται σε ωσμωτικό στρες λόγω της τοποθέτησής του σε υπότονο διάλυμα. Ο βαθμός της αντίστασης των ερυθροκυττάρων στην αιμόλυσή τους σε μια επερχόμενη μείωση ή αύξηση της περιεκτικότητας σε άλας του περιβάλλοντος τους (ωσμωτικές αλλαγές), αποτελεί δείκτη της βιωσιμότητας των ερυθροκυττάρων. Η ωσμωτική ευθραυστότητα επηρεάζεται από ποικίλους παράγοντες, συμπεριλαμβανομένης της μεμβρανικής σύστασης και ακεραιότητας καθώς και της αναλογίας εμβαδού επιφάνειας προς όγκο. Το τεστ μέτρησης της ωσμωτικής ευθραυστότητας είναι σύνηθες και χρησιμοποιείται για τη διάγνωση ασθενειών που σχετίζονται με ανωμαλίες της ερυθροκυτταρικής μεμβράνης. Πειραματική βάση του τεστ αποτελεί το γεγονός ότι η αιμοσφαιρίνη ενός ερυθροκυττάρου που υπόκειται σε ωσμωτικό στρες διαχέεται προκειμένου να ~ 44 ~
45 αποκατασταθεί η ισορροπία μεταξύ του εξωτερικού και του εσωτερικού του κυττάρου, συνήθως χωρίς να επέλθει ρήξη της πλασματικής του μεμβράνης. Σε διαλύματα NaCl διαφορετικών συγκεντρώσεων ( %) προστίθεται ποσότητα ολικού αίματος και ακολουθεί ήπιο vortex. Επώαση για 15 λεπτά σε RT. Φυγοκέντρηση για 5 λεπτά στις 1500 στροφές. Φωτομέτρηση υπερκείμενου στα 540nm. Το πείραμα πραγματοποιήθηκε μετά από επώαση στους 37 0 C για 24 ώρες (μεταβολικό στρες). (Parpart AK., et al., 1947) Μέτρηση αντιοξειδωτικής ικανότητας του πλάσματος (FRAP) Η δοκιμασία FRAP (Ferric Reducing Ability of Plasma), αποτελεί μια απλή διαδικασία για τον προσδιορισμό της αντιοξειδωτικής ικανότητας του πλάσματος in vitro. H μέθοδος αυτή προσδιορίζει την ικανότητα των αντιοξειδωτικών του πλάσματος των ερυθροκυττάρων να ανάγουν το Fe 3+ στο σύμπλοκο σιδηρο-2,4,6, τριπυριδυλ-s-τριαζίνης (Fe 3+ TPTZ) σε Fe 2+ (Fe 2+ TPTZ), σε χαμηλό ph (όξινο περιβάλλον). Πιο συγκεκριμένα, παρουσία του TPTΖ, το σύμπλοκο Fe 3+ -TPTZ ανάγεται σε Fe 2+ -TPTZ εξαιτίας της δράσης των αντιοξειδωτικών, αποκτά μπλε χρώμα και εμφανίζει μέγιστη απορρόφηση στα 593nm. Oι τιμές απορρόφησης αντιστοιχούν σε ιόντα σιδήρου Fe 2+ με τη χρήση κατάλληλης πρότυπης καμπύλης. Η πειραματική διαδικασία που ακολουθήθηκε ήταν η εξής: Φυγοκέντρηση ολικού αίματος στις στροφές για 10 λεπτά και λήψη πλάσματος από το υπερκείμενο. Αραίωση πλάσματος με το αντιδραστήριο FRAP. Επώαση για 4min στους 37 C. Φωτομέτρηση στα 593nm. Το αντιδραστήριο FRAP είναι έτοιμο μετά από ανάμειξη των διαλυμάτων: Οξικό οξύ (300mM, ph 3.6), TPTZ 10mM HCl (40mM) και FeCl3 6H2O 20mM, σε αναλογία 10:1:1 αντίστοιχα. Επιπλέον, προσδιορίστηκε και η αντιοξειδωτική ικανότητα του πλάσματος που οφείλεται είτε αποκλειστικά στο ουρικό οξύ είτε στα υπόλοιπα αντιοξειδωτικά συστατικά του πλάσματος εκτός του ουρικού οξέος. Είναι γνωστό πως το ουρικό οξύ συνεισφέρει σημαντικά στην αντιοξειδωτική ικανότητα του πλάσματος. Προκειμένου να καθοριστεί με μια σχετική ακρίβεια η συμβολή του ουρικού οξέος στην ολική αντιοξειδωτική ικανότητα, προστέθηκε στο δείγμα του πλάσματος ουρικάση. Έτσι, μετρήθηκε η αντιοξειδωτική ικανότητα των υπολοίπων αντιοξειδωτικών συστατικών του πλάσματος εκτός του ουρικού οξέος (uric-acid-independent antioxidant capacity, AC-(UA)), η αντιοξειδωτική ικανότητα του πλάσματος που οφείλεται στο ουρικό οξύ (UA/AC) και η ολική αντιοξειδωτική ικανότητα του πλάσματος (total antioxidant capacity-tac). Η πειραματική διαδικασία που ακολουθήθηκε ήταν η εξής: Φυγοκέντρηση ολικού αίματος Προσθήκη ουρικάσης και επώαση για λεπτά, σε RT. ~ 45 ~
46 Φωτομέτρηση στα 593nm Μέτρηση επιπέδων ενδοκυττάριων Ca 2+ Η μέτρηση των ενδοκυττάριων επιπέδων Ca 2+ βασίζεται στη χρήση του αντιδραστηρίου Fluo 4-AM το οποίο είναι ένα λιπόφιλο, μη φθορίζον συστατικό το οποίο διαπερνά τη πλασματική μεμβράνη, εισέρχεται στο κύτταρο, κόβεται από εστεράσες, αντιδρά με ιόντα ασβεστίου και φθορίζει. Δηλαδή, το ιόν που παράγεται δεσμεύει χηλικά τα ιόντα ασβεστίου. Το σύμπλοκο του Fluo- 4 με τα ιόντα Ca 2+ εκπέμπει φθορισμό, ο οποίος μετράται με το φθορισμόμετρο. Προσθήκη αντιδραστηρίου Fluo 4-ΑΜ (2μM) σε μικροποσότητα ερυθροκυττάρων αραιωμένων σε διάλυμα Ca 2+ - Αφήνεται για 40 λεπτά, στους 37 C, στο σκοτάδι υπό ανάδευση. Φυγοκέντρηση 3.300rpm/20 - Αφαίρεση υπερκείμενου και προσθήκη διαλύματος Ca 2+ - Αφήνεται για 30 λεπτά, σε θερμοκρασία δωματίου, στο σκοτάδι υπό ανάδευση. Φυγοκέντρηση 3.300rpm/20 - Αφαίρεση υπερκείμενου Λύση με 1ml ddh 2 O ~ 46 ~
47 4. ΑΠΟΤΕΛΕΣΜΑΤΑ Μέρος Α Μεταβολές στα ερυθροκύτταρα και στο πλάσμα των ασθενών που υποβάλλονται σε αιμοδιαδιήθηση (HDF) σε σύγκριση ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση (HD), πριν από τη διαδικασία της κάθαρσης. Οι δύο ομάδες ασθενών που μελετήθηκαν υποβάλλονται σε διαφορετικές τεχνικές αιμοκάθαρσης αλλά δεν παρουσιάζουν στατιστικά σημαντικές διαφορές μεταξύ τους στα δημογραφικά στοιχεία, την κλινική κατάσταση, το χρονικό διάστημα της κάθαρσης και σε χαρακτηριστικά της θεραπείας ερυθροποιητίνης. Πιο συγκεκριμένα, οι ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση έχουν μέσο όρο ηλικίας 64±11 έτη, υποβάλλονται στη θεραπεία αιμοκάθαρσης για διάστημα 35±15 μηνών και λαμβάνουν ερυθροποιητίνη 9,100±5,527 IU/εβδομάδα κατά μέσο όρο, ενώ οι ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση κυμαίνονται ηλικιακά στα 72±7 έτη, ακολουθούν τη θεραπεία για διάστημα 40±30 μηνών και λαμβάνουν ερυθροποιητίνη 9,350±4,204 IU/εβδομάδα. Η μελέτη του αιματολογικού προτύπου και των δύο ομάδων ασθενών πριν τη διαδικασία της αιμοκάθαρσης (ΑΙΚ) έδειξε μειωμένα επίπεδα αιμοσφαιρίνης (Hb), αιματοκρίτη (Hct) καθώς και ενδοκυττάριας συγκέντρωσης αιμοσφαιρίνης (MCHC) σε σχέση με τα υγιή άτομα, ταυτόχρονα με αύξηση του δείκτη εύρους μεγέθους των ερυθροκυττάρων (RDW) (Πίνακας 3). Πίνακας 3: Αιματολογικές παράμετροι ασθενών πριν την αιμοκάθαρση (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν σε μέσο όρο ± τυπική απόκλιση. (έντονη γραφή): p<0.05 έναντι υγιών ατόμων, p<0.05 έναντι υγιών ατόμων, (*): p<0.05 HDF έναντι HD. Hb (gr/dl) Hct (%) MCH (pg) MCHC (gr) RDW (%) HDF 11,7±0,3* 36,2±1,0* 32,1±1,6 32,4±1,0* 15,1±0,9* HD 10,9±0,7* 35,9±1,9* 30,8±1,5 30,7±2,4* 16,6±1,3* Υγιείς 15,0±1,4 44,1±4,6 31,4±2,2 33,9±1,3 12,8±0,9 Όσον αφορά στη μελέτη του βιοχημικού προτύπου και οι δύο ομάδες των ασθενών παρουσιάζουν αυξημένα επίπεδα κρεατινίνης και ουρικού οξέος, καθώς οι ασθενείς με ΧΝΑ τελικού σταδίου είναι γνωστό πως χαρακτηρίζονται από συσσώρευση ουραιμικών τοξινών (Πίνακας 4). Ωστόσο, οι ασθενείς που υποβάλλονται σε HDF χαρακτηρίζονται από στατιστικά υψηλότερα επίπεδα κρεατινίνης και ουρικού οξέος σε σχέση με τους ασθενείς που υποβάλλονται σε συμβατική ~ 47 ~
48 ΑΙΚ. Η ολική αντιοξειδωτική ικανότητα του πλάσματος (TAC) καθώς και η αντιοξειδωτική ικανότητα του πλάσματος που οφείλεται στα επίπεδα του ουρικού οξέος (AC/UA) ή στα υπόλοιπα αντιοξειδωτικά συστατικά του πλάσματος (AC-UA), εμφανίζονται αυξημένες και στις δύο ομάδες ασθενών συγκρινόμενες με τους υγιείς (Πίνακας 4). Κατά αντιστοιχία με τα επίπεδα UA διαφέρει και η εξαρτώμενη από UA αντιοξειδωτική ικανότητα του πλάσματος στις δύο ομάδες των ασθενών. Πίνακας 4: Βιοχημικές παράμετροι και χαρακτηριστικά πλάσματος ασθενών πριν την αιμοκάθαρση (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν σε μέσο όρο ± τυπική απόκλιση. (Έντονη γραφή): p<0.05 έναντι υγιών ατόμων, (*): p<0.05 HDF έναντι HD. TAC: ολική αντιοξειδωτική ικανότητα πλάσματος, AC(-UA): αντιοξειδωτική ικανότητα πλάσματος οφειλόμενη σε συστατικά εκτός του ουρικού οξέος, AC/UA: αντιοξειδωτική ικανότητα πλάσματος οφειλόμενη στο ουρικό οξύ. Κρεατινίνη Ουρικό οξύ TAC AC(-UA) AC/UA (mg/dl) (mg/dl) (μμ Fe 2+ ) (μμ Fe 2+ ) (μμ Fe 2+ ) HDF 8,6±1,2* 7,6±2* 1118,5±161,9 449,4±85,4 669,1±103* HD 6,7±2* 5,9±1,2* 1021±198,2 450,4± ,8±107,2* Υγιείς 0.8±0.2 3,7±0,8 695,3±157,1 242,8±45,3 452,5±132,1 Σχετικά με τις ερυθροκυτταρικές παραμέτρους, οι ασθενείς και των δύο ομάδων κυμαίνονται σε φυσιολογικά επίπεδα μηχανικής ευθραυστότητας, ενώ όσον αφορά στην οσμωτική ευθραυστότητα, μόνο οι ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση (HD) εμφανίζουν στατιστικά σημαντική μείωση σε σχέση με τους υγιείς. Τα επίπεδα του ενδοκυττάριου Ca 2+ είναι επίσης φυσιολογικά, αν και οι δύο ομάδες των ασθενών διαφέρουν μεταξύ τους, με τα ερυθροκύτταρα των ασθενών σε HDF να παρουσιάζουν υψηλότερα επίπεδα. Επίσης, οι δύο ομάδες των ασθενών χαρακτηρίζονται από σημαντική αύξηση των μη αναστρέψιμων μορφολογικά τροποποιημένων ερυθροκυττάρων (Εικόνες 11-13), χωρίς όμως στατιστικά σημαντικές διαφορές μεταξύ τους. Ως τέτοια θεωρούνται τα σφαιρο-εχινοκύτταρα, τα σφαιρο-στοματοκύτταρα, τα ελλειπτοκύτταρα, τα δακρυοκύτταρα, τα οβαλοκύτταρα και τα σχιστοκύτταρα. Και οι τρεις ομάδες μελέτης (οι δύο των ασθενών και η ομάδα των υγιών), εμφανίζουν τα ίδια επίπεδα στοματοκυττάρων (Πίνακας 5, Διαγράμματα 1 και 2). Πίνακας 5: Ερυθροκυτταρικές παράμετροι ασθενών πριν τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική ~ 48 ~
49 αιμοκάθαρση). Τα δεδομένα αντιστοιχούν σε μέσο όρο ± τυπική απόκλιση. (έντονη γραφή): p<0.05 έναντι υγιών ατόμων, (*): p<0.05 HDF έναντι HD. ica 2+ : επίπεδα ενδοκυττάριων ιόντων ασβεστίου, MFI: μηχανική ευθραυστότητα, MCF : οσμωτική ευθραυστότητα ύστερα από επώαση στους 37 C για 24 ώρες. ica 2+ Δισκοκύτταρα (%) Μη αναστρέψιμα (%) Αναστρέψιμα (%) Στοματο κύτταρα (%) MFI MCF (% NaCl) HDF 2814±675* 34±7 4±1 61±7 8±2 0,86±0,22 0,55±0,05 HD 2122±782* 32±15 5±3 62±16 7±3 0,88±0,24 0,53±0,05 Υγιείς 2386±425 43±7 3±1 53±6 6±3 0,80±1,19 0,57±0,02 Ερυθροκυτταρικές παράμετροι ica2+ MFI MCF' HDF HD Διάγραμμα 1: Ερυθροκυτταρικές παράμετροι ασθενών, πριν τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν στον μέσο όρο ± την τυπική απόκλιση, μετά από κανονικοποίηση στις τιμές των υγιών ατόμων (100% μαύρη γραμμή). : p<0.05 έναντι υγιών, : p<0.05 μεταξύ HDF και HD. ica 2+ : επίπεδα ενδοκυττάριων ιόντων ασβεστίου, MFI: μηχανική ευθραυστότητα, MCF : οσμωτική ευθραυστότητα ύστερα από επώαση στους 37 C. ~ 49 ~
50 Μορφολογικές τροποποιήσεις ερυθροκυττάρων HDF HD 50 0 Μη αναστρέψιμα Δισκοκύτταρα Αναστρέψιμα Στοματοκύτταρα Διάγραμμα 2: Ερυθροκυτταρικές παράμετροι ασθενών, πριν τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν στον μέσο όρο ± την τυπική απόκλιση, μετά από κανονικοποίηση στις τιμές των υγιών ατόμων (100% μαύρη γραμμή). : p<0.05 έναντι υγιών. Εικόνα 11: Ενδεικτική μικροφωτογραφία ΗΜ Σάρωσης ερυθροκυττάρων υγιούς ατόμου. Ράβδος μεγέθυνσης: 10μm. ~ 50 ~
51 Εικόνα 12: Ενδεικτική μικροφωτογραφία ΗΜ Σάρωσης ερυθροκυττάρων ασθενούς που υποβάλλεται σε αιμοδιαδιήθηση (HDF), πριν από την αιμοκάθαρση. Ράβδος μεγέθυνσης: 10μm. Με κόκκινα βέλη υποδεικνύονται ερυθροκύτταρα μη αναστρέψιμης παραμόρφωσης. Εικόνα 13: Ενδεικτική μικροφωτογραφία ΗΜ Σάρωσης ασθενούς που υποβάλλεται σε συμβατική αιμοκάθαρση (HD), πριν από την αιμοκάθαρση. Ράβδος μεγέθυνσης: 10μm. Με κόκκινα βέλη υποδεικνύονται ερυθροκύτταρα μη αναστρέψιμης παραμόρφωσης. Τέλος, όσον αφορά στην πρωτεϊνική σύσταση της ερυθροκυτταρικής μεμβράνης, οι δύο ομάδες των ασθενών διαφέρουν σε αρκετά συστατικά μεταξύ τους. Πιο συγκεκριμένα, οι ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση παρουσιάζουν έλλειψη στην υδατοπορίνη-1 και αύξηση στα IgGs σε σχέση με τα υγιή άτομα. Αντίστοιχα, η ομάδα των ασθενών που υποβάλλονται σε συμβατική αιμοκάθαρση παρουσιάζει αύξηση στα IgGs και στον μεταφορέα γλυκόζης 1 (Glut-1) και έλλειψη στο μόριο CD47 σε σχέση τόσο με τα υγιή άτομα όσο και με την άλλη ομάδα των ασθενών. (Διάγραμμα 3, Εικόνα 14). ~ 51 ~
52 Πρωτεϊνική σύσταση της ερυθροκυτταρικής μεμβράνης HDF HD 0 Διάγραμμα 3: Πρωτεϊνική σύσταση της ερυθροκυτταρικής μεμβράνης των ασθενών, πριν τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υπόκεινται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν σε μέσο όρο ± τυπική απόκλιση, μετά από κανονικοποίηση στις τιμές των υγιών ατόμων (100% μαύρη γραμμή). : p<0.05 έναντι υγιών, : p<0.05 μεταξύ HDF και HD. ~ 52 ~
53 Εικόνα 14: Ενδεικτικές εικόνες Aνοσοστυπώματος κατά Western πρωτεϊνών της ερυθροκυτταρικής μεμβράνης ασθενών πριν την αιμοκάθαρση και φυσιολογικών ατόμων. ~ 53 ~
54 Μέρος Β Μεταβολές στα ερυθροκύτταρα και στο πλάσμα των ασθενών που υποβάλλονται σε αιμοδιαδιήθηση (HDF) σε σύγκριση ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση (HD), μετά τη διαδικασία της κάθαρσης. Μετά τη διαδικασία της αιμοκάθαρσης, οι δύο ομάδες ασθενών εξακολουθούν να χαρακτηρίζονται από μειωμένα επίπεδα αιμοσφαιρίνης αίματος (Hb) και αιματοκρίτη (Hct) σε σχέση με τους υγιείς. Παρόλα αυτά, η ομάδα των ασθενών που υποβάλλεται σε αιμοδιαδιήθηση παρουσιάζει υψηλότερα επίπεδα αιματοκρίτη και τάση για υψηλότερα επίπεδα αιμοσφαιρίνης, οι τιμές της οποίας δεν παρουσιάζουν ουσιαστικές διαφορές σε σχέση με αυτές των υγιών. Επιπλέον, παρατηρείται βελτίωση της ενδοκυττάριας συγκέντρωσης αιμοσφαιρίνης (MCHC), η οποία βρίσκεται εντός των φυσιολογικών τιμών σε όλους τους ασθενείς, ενώ και οι δύο ομάδες ασθενών εξακολουθούν να έχουν αυξημένο το δείκτη εύρους μεγέθους των ερυθροκυττάρων (RDW) σε σχέση με τα υγιή άτομα (Πίνακας 6). Πίνακας 6: Αιματολογικές παράμετροι ασθενών μετά την αιμοκάθαρση (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν σε μέσο όρο ± τυπική απόκλιση. (έντονη γραφή): p<0.05 έναντι υγιών ατόμων, (*): p<0.05 HDF έναντι HD. Hb (gr/dl) Hct (%) MCH (pg) MCHC (gr) RDW (%) URR HDF 13,2±1,6 38,3±4,3* 31,9±2,0 34,1±1,3 14,1±1,7 77,9±5,8* HD 11,8±1,0 33,2±3,8* 29,6±4,4 33,6±3,7 15,8±2,1 69,2±6,8* Υγιείς 14,0±1,4 44,1±4,6 31,4±2,2 33,9±1,3 12,8±0,9 - Όσον αφορά στην αποδοτικότητα κάθαρσης σε κάθε μέθοδο, παρατηρήθηκε πως η μείωση της ουρίας (URR) είναι μεγαλύτερη στους ασθενείς που ακολουθούν την αιμοδιαδιήθηση (HDF) σαν μέθοδο υποκατάστασης της νεφρικής λειτουργίας έναντι των ασθενών που ακολουθούν την συμβατική αιμοκάθαρση (HD) (Πίνακας 6). Μελετώντας τα χαρακτηριστικά του πλάσματος παρατηρήθηκε πως όλοι οι ασθενείς χαρακτηρίζονται από παθολογικά χαμηλά επίπεδα ολικής αντιοξειδωτικής ικανότητας (TAC). Η μείωση αυτή φαίνεται να οφείλεται κυρίως στη σημαντική μείωση της αντιοξειδωτικής ικανότητας του ουρικού οξέος (AC/UA), καθώς αυτή παρουσιάζεται χαμηλή και στις δύο ομάδες, σε αντίθεση με την αντιοξειδωτική ικανότητα του πλάσματος που οφείλεται σε άλλα συστατικά του πλάσματος ~ 54 ~
55 (AC-(UA)) η οποία δεν παρουσιάζει διαφορά σε καμία ομάδα σε σχέση με τα υγιή άτομα. Μάλιστα, η μεγαλύτερη μείωση της αντιοξειδωτικής ικανότητας του πλάσματος που οφείλεται στο ουρικό οξύ, παρατηρείται στην ομάδα των ασθενών που υποβάλλονται σε αιμοδιαδιήθηση έναντι αυτών που υποβάλλονται σε συμβατική αιμοκάθαρση (Πίνακας 7). Πίνακας 7: Βιοχημικές παράμετροι ασθενών μετά την αιμοκάθαρση (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν σε μέσο όρο ± τυπική απόκλιση. (έντονη γραφή): p<0.05 έναντι υγιών ατόμων, (*): p<0.05 HDF έναντι HD. TAC: ολική αντιοξειδωτική ικανότητα πλάσματος, AC(-UA): αντιοξειδωτική ικανότητα πλάσματος οφειλόμενη σε συστατικά του πλάσματος εκτός του ουρικού οξέος, AC/UA: αντιοξειδωτική ικανότητα πλάσματος οφειλόμενη στο ουρικό οξύ. TAC (μμ Fe 2+ ) AC(-UA) (μμ Fe 2+ ) AC/UA (μμ Fe 2+ ) HDF 398,5±62,5* 249,0±34,2 149,2±44,8* HD 465,4±77,1* 260,6±53,0 198,6±44,8* Υγιείς 695,3±157,1 242,8±45,3 452,5±132,1 Όσον αφορά στις παραμέτρους της φυσιολογίας των ερυθροκυττάρων, μετά τη διαδικασία της αιμοκάθαρσης, διαπιστώθηκε πως ο αριθμός των μη αναστρέψιμων ερυθροκυττάρων και στις δύο ομάδες ασθενών παραμένει υψηλός σε σχέση τα υγιή άτομα. Στους ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση (HDF), παρατηρείται με το πέρας της αιμοκάθαρσης αύξηση του ποσοστού των στοματοκυττάρων σε σχέση με τα υγιή άτομα. Τέλος, οι τιμές της μηχανικής και της οσμωτικής ευθραυστότητας των ασθενών κυμαίνονται στα ίδια επίπεδα με τις αντίστοιχες των υγιών ατόμων (Πίνακας 8, Διαγράμματα 4 και 5). Πίνακας 8: Ερυθροκυτταρικές παράμετροι ασθενών μετά τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν στον μέσο όρο ± την τυπική απόκλιση. (έντονη γραφή): p<0.05 έναντι υγιών ατόμων, (*): p<0.05 HDF έναντι HD. ica 2+ : επίπεδα ενδοκυττάριων ιόντων ασβεστίου, MFI: μηχανική ευθραυστότητα, MCF : οσμωτική ευθραυστότητα ύστερα από επώαση στους 37 C για 24 ώρες. HDF ica 2+ (RFU) Δισκο- Κύτταρα (%) Μη αναστρέψιμα (%) Αναστρέψιμα (%) Στοματοκύτταρα (%) MFI MCF (% NaCl) 2656±608 67±7 5±3 28±8 9±3* 0,73±0,17 0,56±0,06 HD 2291±485 63±11 5±2 32±14 6±2* 0,75±0,15 0,55±0,06 Υγιείς 2386±425 43±7 3±1 54±6 6±3 0,80±0,19 0,57±0,02 ~ 55 ~
56 Ερυθροκυτταρικές παράμετροι (μετά από την αιμοκάθαρση) ica2+ MFI MCF' HDF HD Διάγραμμα 4: Ερυθροκυτταρικές παράμετροι ασθενών, μετά τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν στον μέσο όρο ± την τυπική απόκλιση, μετά από κανονικοποίηση στις τιμές των υγιών ατόμων (100% μαύρη γραμμή). 300 Μορφολογικές τροποποιήσεις ερυθροκυττάρων (μετά από την αιμοκάθαρση) HDF HD 50 0 Μη αναστρέψιμα Δισκοκύτταρα Αναστρέψιμα Στοματοκύτταρα Διάγραμμα 5: Ερυθροκυτταρικές παράμετροι ασθενών, μετά από τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν στον μέσο όρο ± την τυπική απόκλιση, μετά από κανονικοποίηση στις τιμές των υγιών ατόμων (100% μαύρη γραμμή). : p<0.05 μεταξύ HDF και HD. : p<0.05 έναντι υγιών, ~ 56 ~
57 Εικόνα 15: Ενδεικτική φωτομικρογραφία ΗΜ Σάρωσης ερυθροκυττάρων υγιούς ατόμου. Ράβδος μεγέθυνσης: 10μm. Εικόνα 16: Ενδεικτική φωτομικρογραφία ΗΜ Σάρωσης ερυθροκυττάρων ασθενούς που υποβάλλεται σε αιμοδιαδιήθηση (HDF), μετά από τη διαδικασία της αιμοκάθαρσης. Ράβδος μεγέθυνσης: 10μm. Με κόκκινα βέλη υποδεικνύονται ερυθροκύτταρα μη αναστρέψιμης παραμόρφωσης. ~ 57 ~
58 Εικόνα 17: Ενδεικτική φωτομικρογραφία ΗΜ Σάρωσης ασθενούς που υπόκειται σε HD, μετά από την αιμοκάθαρση. Ράβδος μεγέθυνσης: 10μm. Με κόκκινα βέλη υποδεικνύονται ερυθροκύτταρα μη αναστρέψιμης παραμόρφωσης. Όσον αφορά στην πρωτεϊνική σύσταση της ερυθροκυτταρικής μεμβράνης, οι ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση συνεχίζουν να παρουσιάζουν έλλειψη στην υδατοπορίνη-1 και αύξηση στα IgGs σε σχέση με τα υγιή άτομα. Παρατηρείται μάλιστα πως παρουσιάζουν έλλειψη στον μεταφορέα γλυκόζης-1 και στη στοματίνη σε σχέση με τα υγιή άτομα, σε αντίθεση με τα επίπεδα των πρωτεϊνών αυτών πριν από την αιμοκάθαρση, που ήταν φυσιολογικά. Αντίστοιχα, η ομάδα των ασθενών που υποβάλλονται σε συμβατική αιμοκάθαρση εξακολουθεί να παρουσιάζει αύξηση στα IgGs και έλλειψη CD47 αλλά επιπρόσθετα, εμφανίζει και έλλειψη στην υδατοπορίνη-1 και τη στοματίνη σε σχέση με τα υγιή άτομα, κάτι που δεν συνέβαινε πριν την αιμοκάθαρση. Οι δύο ομάδες των ασθενών διαφέρουν μεταξύ τους στα επίπεδα της υδατοπορίνης-1, του μεταφορέα γλυκόζης 1 (Glut-1), του μορίου CD47 και των IgGs (Διάγραμμα 6, Εικόνα 18), καθώς οι ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση παρουσιάζουν μειωμένα επίπεδα υδατοπορίνης-1, μεταφορέα γλυκόζης-1 και IgGs και αυξημένα επίπεδα του μορίου CD47 σε σχέση με τους ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση. ~ 58 ~
59 Πρωτεϊνική σύσταση της ερυθροκυτταρικής μεμβράνης (μετά από την αιμοκάθαρση) HDF HD Διάγραμμα 6: Πρωτεϊνική σύσταση της ερυθροκυτταρικής μεμβράνης των ασθενών, μετά τη διαδικασία της αιμοκάθαρσης (HDF: ασθενείς που υποβάλλονται σε αιμοδιαδιήθηση, HD: ασθενείς που υποβάλλονται σε συμβατική αιμοκάθαρση). Τα δεδομένα αντιστοιχούν σε μέσο όρο ± τυπική απόκλιση, μετά από κανονικοποίηση στις τιμές των υγιών ατόμων (100% μαύρη γραμμή). : p<0.05 έναντι υγιών, : p<0.05 μεταξύ HDF και HD. ~ 59 ~
60 Εικόνα 18: Ενδεικτικές εικόνες Aνοσοστυπώματος κατά Western για πρωτεΐνες της ερυθροκυτταρικής μεμβράνης στους ασθενείς με ΧΝΑ μετά την αιμοκάθαρση σε σχέση με τα υγιή άτομα. ~ 60 ~
Στοιχεία και λειτουργίες του κυτταροσκελετού
 Στοιχεία και λειτουργίες του κυτταροσκελετού ΔΟΜΗ ΤΩΝ ΙΝΙΔΙΩΝ ΑΚΤΙΝΗΣ Ακτίνη: Η μονάδα πολυμερισμού Δομή μονομερούς G- (globular) ακτίνης ATP και ADP μονομερή G-ακτίνης Πολυμερισμός της G-(globular) ακτίνης
Στοιχεία και λειτουργίες του κυτταροσκελετού ΔΟΜΗ ΤΩΝ ΙΝΙΔΙΩΝ ΑΚΤΙΝΗΣ Ακτίνη: Η μονάδα πολυμερισμού Δομή μονομερούς G- (globular) ακτίνης ATP και ADP μονομερή G-ακτίνης Πολυμερισμός της G-(globular) ακτίνης
Kυτταρική Bιολογία ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ ΔIAΛEΞΗ 4 (6/3/2013)
 Kυτταρική Bιολογία ΔIAΛEΞΗ 4 (6/3/2013) ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ Οι λιπιδικές διπλοστιβάδες ως φραγμοί Νερό Υδρόφιλες φωσφολιπιδικές κεφαλές Φωσφολιπιδική μεμβράνη
Kυτταρική Bιολογία ΔIAΛEΞΗ 4 (6/3/2013) ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ Οι λιπιδικές διπλοστιβάδες ως φραγμοί Νερό Υδρόφιλες φωσφολιπιδικές κεφαλές Φωσφολιπιδική μεμβράνη
Kυτταρική Bιολογία ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ ΔIAΛEΞΕΙΣ 4 & 5 (29/2 & 2/3/2016)
 Kυτταρική Bιολογία ΔIAΛEΞΕΙΣ 4 & 5 (29/2 & 2/3/2016) ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ Οι λιπιδικές διπλοστιβάδες λειτουργούν ως φραγμοί Νερό Υδρόφιλες φωσφολιπιδικές κεφαλές
Kυτταρική Bιολογία ΔIAΛEΞΕΙΣ 4 & 5 (29/2 & 2/3/2016) ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ Οι λιπιδικές διπλοστιβάδες λειτουργούν ως φραγμοί Νερό Υδρόφιλες φωσφολιπιδικές κεφαλές
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΛΟΓΙΑΣ ΚΥΤΤΑΡΟΥ ΚΑΙ ΒΙΟΦΥΣΙΚΗΣ. Διπλωματική Εργασία
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΛΟΓΙΑΣ ΚΥΤΤΑΡΟΥ ΚΑΙ ΒΙΟΦΥΣΙΚΗΣ Διπλωματική Εργασία Κυτταροβιολογική προσέγγιση της αναιμίας στη Χρόνια Νεφρική
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΛΟΓΙΑΣ ΚΥΤΤΑΡΟΥ ΚΑΙ ΒΙΟΦΥΣΙΚΗΣ Διπλωματική Εργασία Κυτταροβιολογική προσέγγιση της αναιμίας στη Χρόνια Νεφρική
Κυτταρική Βιολογία. Ενότητα 08 : Βιολογικές μεμβράνες, μεμβρανικά διαμερίσματα, μεταφορά πρωτεϊνών Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 08 : Βιολογικές μεμβράνες, μεμβρανικά διαμερίσματα, μεταφορά πρωτεϊνών Παναγιωτίδης Χρήστος Φαρμακευτικής ΑΠΘ
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 08 : Βιολογικές μεμβράνες, μεμβρανικά διαμερίσματα, μεταφορά πρωτεϊνών Παναγιωτίδης Χρήστος Φαρμακευτικής ΑΠΘ
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης
 Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Kυτταρική Bιολογία ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ ΔIAΛEΞΕΙΣ 4 & 5 (3/3 & 6/3/2017)
 Kυτταρική Bιολογία ΔIAΛEΞΕΙΣ 4 & 5 (3/3 & 6/3/2017) ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ Οι λιπιδικές διπλοστιβάδες λειτουργούν ως φραγμοί Νερό Υδρόφιλες φωσφολιπιδικές κεφαλές
Kυτταρική Bιολογία ΔIAΛEΞΕΙΣ 4 & 5 (3/3 & 6/3/2017) ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ, ΜΕΜΒΡΑΝΙΚΑ ΔΙΑΜΕΡΙΣΜΑΤΑ & ΔΙΑΛΟΓΗ ΠΡΩΤΕΪΝΩΝ Οι λιπιδικές διπλοστιβάδες λειτουργούν ως φραγμοί Νερό Υδρόφιλες φωσφολιπιδικές κεφαλές
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Η ΔΟΜΗ ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ ΚΥΡΙΑΚΗ ΒΑΣΙΛΙΚΟΥ Γ1
 Η ΔΟΜΗ ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ ΚΥΡΙΑΚΗ ΒΑΣΙΛΙΚΟΥ Γ1 ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΣ Τρισδιάστατο δίκτυο που αποτελείται από μικροσωληνίσκους, μικροϊνίδια και ενδιάμεσα ινίδια. Οι νηματοειδείς πρωτεΐνες του
Η ΔΟΜΗ ΚΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ ΚΥΡΙΑΚΗ ΒΑΣΙΛΙΚΟΥ Γ1 ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΣ Τρισδιάστατο δίκτυο που αποτελείται από μικροσωληνίσκους, μικροϊνίδια και ενδιάμεσα ινίδια. Οι νηματοειδείς πρωτεΐνες του
ΜΕΤΑΦΟΡΑ ΑΕΡΙΩΝ ΠΡΟΣ ΚΑΙ ΑΠΟ ΤΟΥΣ ΣΤΟΥΣ ΙΣΤΟΥΣ
 ΜΕΤΑΦΟΡΑ ΑΕΡΙΩΝ ΠΡΟΣ ΚΑΙ ΑΠΟ ΤΟΥΣ ΣΤΟΥΣ ΙΣΤΟΥΣ Μεταφορά οξυγόνου (Ο 2 ) από τον αέρα μέσω κυψελίδων στο αίμα και ιστούς Μεταφορά διοξειδίου άνθρακα (CO 2 ) από ιστούς σε κυψελίδες Οι κλίσεις των μερικών
ΜΕΤΑΦΟΡΑ ΑΕΡΙΩΝ ΠΡΟΣ ΚΑΙ ΑΠΟ ΤΟΥΣ ΣΤΟΥΣ ΙΣΤΟΥΣ Μεταφορά οξυγόνου (Ο 2 ) από τον αέρα μέσω κυψελίδων στο αίμα και ιστούς Μεταφορά διοξειδίου άνθρακα (CO 2 ) από ιστούς σε κυψελίδες Οι κλίσεις των μερικών
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Δομή των μυϊκών κυττάρων.
 Δομή των μυϊκών κυττάρων. Οι μύες αποτελούνται από δεμάτια μεγάλων κυττάρων (που ονομάζονται μυϊκά κύτταρα ή μυϊκές ίνες). Κάθε μυϊκή ίνα περιέχει πολλά μυϊκά ινίδια, δηλαδή δεμάτια ινιδίων ακτίνης και
Δομή των μυϊκών κυττάρων. Οι μύες αποτελούνται από δεμάτια μεγάλων κυττάρων (που ονομάζονται μυϊκά κύτταρα ή μυϊκές ίνες). Κάθε μυϊκή ίνα περιέχει πολλά μυϊκά ινίδια, δηλαδή δεμάτια ινιδίων ακτίνης και
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
Μόρια κυτταρικής πρόσφυσης
 Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
ΒΑΣΙΚΕΣ ΔΟΜΕΣ - ΤΟ ΚΥΤΤΑΡΟ
 ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ I ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιμος Π. Βανδώρος ΒΑΣΙΚΕΣ ΔΟΜΕΣ - ΤΟ ΚΥΤΤΑΡΟ Οι βασικές δομές που εξετάζουμε στην ανατομία μπορούν ιεραρχικά να ταξινομηθούν ως εξής:
ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ I ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιμος Π. Βανδώρος ΒΑΣΙΚΕΣ ΔΟΜΕΣ - ΤΟ ΚΥΤΤΑΡΟ Οι βασικές δομές που εξετάζουμε στην ανατομία μπορούν ιεραρχικά να ταξινομηθούν ως εξής:
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ Η άσκηση, επιφέρει ευεργετικά αποτελέσματα στα διάφορα συστήματα του οργανισμού. Τα αποτελέσματα αυτά ενδέχεται να είναι παροδικά ή μόνιμα ανάλογα
ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ Η άσκηση, επιφέρει ευεργετικά αποτελέσματα στα διάφορα συστήματα του οργανισμού. Τα αποτελέσματα αυτά ενδέχεται να είναι παροδικά ή μόνιμα ανάλογα
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ
 ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2014-2015 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑΤΑ 1.Πώς οι κινητικές παράμετροι Κ m και K cat χρησιμεύουν για να συγκριθεί η ανακύκλωση διαφορετικών
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ»
 «ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01%
 ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ <=> R
 ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ R ΔΕΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ ΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ (Σταθερότητα, χαμηλή συγγένεια για Ο2Εύκαμπτη, υψηλή συγγένεια για Ο2) Λόγο των
ΑΙΜΟΣΦΑΙΡΙΝΗ (ΑΜΦ) ΑΙΜΟΣΦΑΙΡΙΝΗ: Hb, είναι τετραμερής πρωτείνη. ΜΕΤΑΠΤΩΣΗ ΑΠΟ Τ R ΔΕΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ ΟΞΥΑΙΜΟΣΦΑΙΡΙΝΗ (Σταθερότητα, χαμηλή συγγένεια για Ο2Εύκαμπτη, υψηλή συγγένεια για Ο2) Λόγο των
Kυτταρική Bιολογία. Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος ΔIAΛEΞΗ 20 (9/5/2017) Δρ. Xρήστος Παναγιωτίδης, Τμήμα Φαρμακευτικής Α.Π.Θ.
 Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ
 ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-CoA Αναπνευστική Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-CoA Αναπνευστική Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική
Ομαδες μοριων κυτταρικης προσφυσης
 Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ. Πετρολιάγκης Σταμάτης Τμήμα Γ4
 ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Πετρολιάγκης Σταμάτης Τμήμα Γ4 ΕΝΝΟΙΑ ΤΗΣ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Η κυτταρική μεμβράνη ή πλασματική μεμβράνη είναι η εξωτερική μεμβράνη που περιβάλλει το κύτταρο
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Πετρολιάγκης Σταμάτης Τμήμα Γ4 ΕΝΝΟΙΑ ΤΗΣ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Η κυτταρική μεμβράνη ή πλασματική μεμβράνη είναι η εξωτερική μεμβράνη που περιβάλλει το κύτταρο
ΚΕΦΑΛΑΙΟ 11. Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα
 ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι. ΒΙΟΧΗΜΕΙΑ (Lubert Stryer)
 BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 17.1 Η πυροσταφυλική αφυδρογονάση συνδέει τη γλυκόλυση με τον κύκλο του κιτρικού οξέος 17.2 O κύκλος του κιτρικού οξέος οξειδώνει μονάδες δύο ατόμων
BIOΛ154 ΒΙΟΧΗΜΕΙΑ Ι ΒΙΟΧΗΜΕΙΑ (Lubert Stryer) ΠΕΡΙΓΡΑΜΜΑ 17.1 Η πυροσταφυλική αφυδρογονάση συνδέει τη γλυκόλυση με τον κύκλο του κιτρικού οξέος 17.2 O κύκλος του κιτρικού οξέος οξειδώνει μονάδες δύο ατόμων
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
Μεταγωγή σήματος και βιολογικές μεμβράνες
 Μεταγωγή σήματος και βιολογικές μεμβράνες ΜΕΜΒΡΑΝΙΚΕΣ ΠΡΩΤΕΪΝΕΣ ΠΡΩΤΕΪΝΕΣ ΒΙΟΛΟΓΙΚΩΝ ΜΕΜΒΡΑΝΩΝ Ορισμός / Μονάδες Δομές (πρωτοταγής κλπ) Ταξινόμηση με βάση τις λειτουργίες Απεικόνιση - Μοντέλα (συρμάτων
Μεταγωγή σήματος και βιολογικές μεμβράνες ΜΕΜΒΡΑΝΙΚΕΣ ΠΡΩΤΕΪΝΕΣ ΠΡΩΤΕΪΝΕΣ ΒΙΟΛΟΓΙΚΩΝ ΜΕΜΒΡΑΝΩΝ Ορισμός / Μονάδες Δομές (πρωτοταγής κλπ) Ταξινόμηση με βάση τις λειτουργίες Απεικόνιση - Μοντέλα (συρμάτων
Eρυθροκυτταρική μεμβράνη
 Eρυθροκυτταρική μεμβράνη Είναι η καλύτερα μελετημένη βιολογική μεμβράνη Αν και αντιπροσωπεύει μόνο το 1% του βάρους του ερυθρού Σημαντικό ρόλο στη διατήρηση της ακεραιότητας του κυττάρου Αποτελεί άριστο
Eρυθροκυτταρική μεμβράνη Είναι η καλύτερα μελετημένη βιολογική μεμβράνη Αν και αντιπροσωπεύει μόνο το 1% του βάρους του ερυθρού Σημαντικό ρόλο στη διατήρηση της ακεραιότητας του κυττάρου Αποτελεί άριστο
Οξειδωτικό Stress, άσκηση και υπερπροπόνηση
 Οξειδωτικό Stress, άσκηση και υπερπροπόνηση Τζιαμούρτας Ζ. Αθανάσιος Επίκουρος Καθηγητής Βιοχημείας της Άσκησης, ΠΘ Ερευνητής, Ινστιτούτο Σωματικής Απόδοσης και Αποκατάστασης Οξειδωτικό στρες Γενικός όρος
Οξειδωτικό Stress, άσκηση και υπερπροπόνηση Τζιαμούρτας Ζ. Αθανάσιος Επίκουρος Καθηγητής Βιοχημείας της Άσκησης, ΠΘ Ερευνητής, Ινστιτούτο Σωματικής Απόδοσης και Αποκατάστασης Οξειδωτικό στρες Γενικός όρος
Βιοχημεία Τροφίμων Ι. Ενότητα 2 η Κρέας και ψάρι II (μέρος α) Όνομα καθηγητή: Έφη Τσακαλίδου. Τμήμα: Επιστήμης Τροφίμων & Διατροφής του Ανθρώπου
 Βιοχημεία Τροφίμων Ι Ενότητα 2 η Κρέας και ψάρι II (μέρος α) Όνομα καθηγητή: Έφη Τσακαλίδου Τμήμα: Επιστήμης Τροφίμων & Διατροφής του Ανθρώπου Στόχοι ενότητας Κατανόηση της δομής του σαρκομερούς. Κατανόηση
Βιοχημεία Τροφίμων Ι Ενότητα 2 η Κρέας και ψάρι II (μέρος α) Όνομα καθηγητή: Έφη Τσακαλίδου Τμήμα: Επιστήμης Τροφίμων & Διατροφής του Ανθρώπου Στόχοι ενότητας Κατανόηση της δομής του σαρκομερούς. Κατανόηση
Βιολογία Α Λυκείου Κεφ. 3. Κυκλοφορικό Σύστημα. Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα
 Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
8 η Παρουσίαση Εισαγωγή στο Αίμα
 ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
 ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΟΞΕΟΒΑΣΙΚΗ ΙΣΟΡΡΟΠΙΑ ΣΗΜΑΣΙΑ ΟΞΕΟΒΑΣΙΚΗΣ Η ακριβής ρύθμιση των ιόντων υδρογόνου (Η
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΟΞΕΟΒΑΣΙΚΗ ΙΣΟΡΡΟΠΙΑ ΣΗΜΑΣΙΑ ΟΞΕΟΒΑΣΙΚΗΣ Η ακριβής ρύθμιση των ιόντων υδρογόνου (Η
πρωτεΐνες πολυμερείς ουσίες δομούν λειτουργούν λευκώματα 1.Απλές πρωτεΐνες 2.Σύνθετες πρωτεΐνες πρωτεΐδια μη πρωτεϊνικό μεταλλοπρωτεΐνες
 ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Βιολογικές Μεμβράνες και Μεταγωγή Σήματος
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογικές Μεμβράνες και Μεταγωγή Σήματος Πρωτεΐνες Διδάσκουσα: Καθ. Μαρία - Ελένη Ε. Λέκκα Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογικές Μεμβράνες και Μεταγωγή Σήματος Πρωτεΐνες Διδάσκουσα: Καθ. Μαρία - Ελένη Ε. Λέκκα Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Τα ερυθροκύτταρα αποτελούν τα πολυαριθμότερα κύτταρα του περιφερικού
 EΡΥΘΡΟΚΥΤΤΑΡΑ 5 Στο κεφάλαιο αυτό: Ανασκοπείται η λειτουργία του ερυθροκυττάρου και η δομή και λειτουργία της ερυθροκυτταρικής μεμβράνης. Περιγράφονται τα κύτταρα της ερυθροκυτταρικής σειράς. Τονίζονται
EΡΥΘΡΟΚΥΤΤΑΡΑ 5 Στο κεφάλαιο αυτό: Ανασκοπείται η λειτουργία του ερυθροκυττάρου και η δομή και λειτουργία της ερυθροκυτταρικής μεμβράνης. Περιγράφονται τα κύτταρα της ερυθροκυτταρικής σειράς. Τονίζονται
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
 ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΟΞΕΟΒΑΣΙΚΗ ΙΣΟΡΡΟΠΙΑ ΣΗΜΑΣΙΑ ΟΞΕΟΒΑΣΙΚΗΣ Η ακριβής ρύθμιση των ιόντων υδρογόνου (Η
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΟΞΕΟΒΑΣΙΚΗ ΙΣΟΡΡΟΠΙΑ ΣΗΜΑΣΙΑ ΟΞΕΟΒΑΣΙΚΗΣ Η ακριβής ρύθμιση των ιόντων υδρογόνου (Η
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου. Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση:
 KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
Περιήγηση στο εσωτερικό του Κυττάρου. Φώτης Καρβέλης
 Περιήγηση στο εσωτερικό του Κυττάρου Φώτης Καρβέλης Όλα τα κύτταρα οριοθετούνται από την πλασματική μεμβράνη ή το κυτταρικό τοίχωμα που την περιβάλλει. Εσωτερικά της πλασματικής μεμβράνης υπάρχουν τα οργανίδια
Περιήγηση στο εσωτερικό του Κυττάρου Φώτης Καρβέλης Όλα τα κύτταρα οριοθετούνται από την πλασματική μεμβράνη ή το κυτταρικό τοίχωμα που την περιβάλλει. Εσωτερικά της πλασματικής μεμβράνης υπάρχουν τα οργανίδια
Θέματα πριν τις εξετάσεις. Καλό διάβασμα Καλή επιτυχία
 Θέματα πριν τις εξετάσεις Καλό διάβασμα Καλή επιτυχία 2013-2014 Θέματα πολλαπλής επιλογής Μετουσίωση είναι το φαινόμενο α. κατά το οποίο συνδέονται δύο αμινοξέα για τον σχηματισμό μιας πρωτεΐνης β. κατά
Θέματα πριν τις εξετάσεις Καλό διάβασμα Καλή επιτυχία 2013-2014 Θέματα πολλαπλής επιλογής Μετουσίωση είναι το φαινόμενο α. κατά το οποίο συνδέονται δύο αμινοξέα για τον σχηματισμό μιας πρωτεΐνης β. κατά
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ
 ΠΕΡΙΓΡΑΜΜΑ 2.1 ΒΑΣΙΚΑ ΟΡΓΑΝΙΚΑ ΜΟΡΙΑ ΧΡΗΣΙΜΟΠΟΙΟΥΝΤΑΙ ΑΠΌ ΤΟΥΣ ΖΩΝΤΕΣ ΟΡΓΑΝΙΣΜΟΥΣ 2.2 Η ΕΞΕΛΙΞΗ ΧΡΕΙΑΖΕΤΑΙ ΑΝΑΠΑΡΑΓΩΓΗ, ΠΟΙΚΙΛΟΜΟΡΦΙΑ, ΚΑΙ ΕΞΕΛΙΚΤΙΚΗ ΠΙΕΣΗ 2.3 ΕΝΕΡΓΕΙΑΚΟΙ ΜΕΤΑΣΧΗΜΑΤΙΣΜΟΙ ΕΊΝΑΙ ΑΠΑΡΑΙΤΗΤΟΙ
ΠΕΡΙΓΡΑΜΜΑ 2.1 ΒΑΣΙΚΑ ΟΡΓΑΝΙΚΑ ΜΟΡΙΑ ΧΡΗΣΙΜΟΠΟΙΟΥΝΤΑΙ ΑΠΌ ΤΟΥΣ ΖΩΝΤΕΣ ΟΡΓΑΝΙΣΜΟΥΣ 2.2 Η ΕΞΕΛΙΞΗ ΧΡΕΙΑΖΕΤΑΙ ΑΝΑΠΑΡΑΓΩΓΗ, ΠΟΙΚΙΛΟΜΟΡΦΙΑ, ΚΑΙ ΕΞΕΛΙΚΤΙΚΗ ΠΙΕΣΗ 2.3 ΕΝΕΡΓΕΙΑΚΟΙ ΜΕΤΑΣΧΗΜΑΤΙΣΜΟΙ ΕΊΝΑΙ ΑΠΑΡΑΙΤΗΤΟΙ
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Τα χημικά στοιχεία που είναι επικρατέστερα στους οργανισμούς είναι: i..
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΠΡΩΤΕΪΝΕΣ. Φατούρος Ιωάννης Αναπληρωτής Καθηγητής
 ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
Γενική αίµατος. Καταµέτρηση των έµµορφων στοιχείων του αίµατος
 Γενική αίµατος Αθανασία Μουζάκη, Καθηγήτρια Εργαστηριακής Αιµατολογίας-Αιµοδοσίας, Εργαστήριο Αιµατολογίας, Αιµατολογικό Τµήµα, Παθολογική Κλινική, Τµήµα Ιατρικής, Παν/ο Πατρών Γενική αίµατος Καταµέτρηση
Γενική αίµατος Αθανασία Μουζάκη, Καθηγήτρια Εργαστηριακής Αιµατολογίας-Αιµοδοσίας, Εργαστήριο Αιµατολογίας, Αιµατολογικό Τµήµα, Παθολογική Κλινική, Τµήµα Ιατρικής, Παν/ο Πατρών Γενική αίµατος Καταµέτρηση
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ
 ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΙΚΡΟΣΚΟΠΙΚΗ ΠΑΡΑΤΗΡΗΣΗ ΜΟΝΙΜΟΥ ΠΑΡΑΣΚΕΥΑΣΜΑΤΟΣ ΑΙΜΑΤΟΣ (άσκηση 4 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος:
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΙΚΡΟΣΚΟΠΙΚΗ ΠΑΡΑΤΗΡΗΣΗ ΜΟΝΙΜΟΥ ΠΑΡΑΣΚΕΥΑΣΜΑΤΟΣ ΑΙΜΑΤΟΣ (άσκηση 4 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος:
Το φωσφορικό ανιόν δεν ανάγεται µέσα στο φυτό. Παραµένει στην υψηλότερη οξειδωτική µορφή του
 Το φωσφορικό ανιόν δεν ανάγεται µέσα στο φυτό Παραµένει στην υψηλότερη οξειδωτική µορφή του 1)ελεύθερο Pi (inorganic phosphate) 2)προσαρτηµένο ως φωσφορική οµάδα πάνω σε κάποιο µόριο το συµβολίζουµε ως
Το φωσφορικό ανιόν δεν ανάγεται µέσα στο φυτό Παραµένει στην υψηλότερη οξειδωτική µορφή του 1)ελεύθερο Pi (inorganic phosphate) 2)προσαρτηµένο ως φωσφορική οµάδα πάνω σε κάποιο µόριο το συµβολίζουµε ως
ΠΡΟΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΥΔΩΝ ΤΕΦΑΑ/ΔΠΘ ΜΑΘΗΜΑ ΚΑΤΕΥΘΥΝΣΗΣ ΠΡΟΠΟΝΗΤΙΚΗΣ. Φατούρος Γ. Ιωάννης, Επίκουρος Καθηγητής
 ΠΡΟΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΥΔΩΝ ΤΕΦΑΑ/ΔΠΘ ΜΑΘΗΜΑ ΚΑΤΕΥΘΥΝΣΗΣ ΠΡΟΠΟΝΗΤΙΚΗΣ ΒΙΟΧΗΜΕΙΑ ΤΗΣ ΑΣΚΗΣΗΣ Φατούρος Γ. Ιωάννης, Επίκουρος Καθηγητής ΔΙΑΛΕΞΗ 1 - ΓΡΗΓΟΡΗ ΑΝΑΣΚΟΠΗΣΗ ΒΑΣΙΚΩΝ ΓΝΩΣΕΩΝ A. Το Περιβάλλον του
ΠΡΟΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΥΔΩΝ ΤΕΦΑΑ/ΔΠΘ ΜΑΘΗΜΑ ΚΑΤΕΥΘΥΝΣΗΣ ΠΡΟΠΟΝΗΤΙΚΗΣ ΒΙΟΧΗΜΕΙΑ ΤΗΣ ΑΣΚΗΣΗΣ Φατούρος Γ. Ιωάννης, Επίκουρος Καθηγητής ΔΙΑΛΕΞΗ 1 - ΓΡΗΓΟΡΗ ΑΝΑΣΚΟΠΗΣΗ ΒΑΣΙΚΩΝ ΓΝΩΣΕΩΝ A. Το Περιβάλλον του
Σημειώσεις Βιοφυσικής 1
 Σημειώσεις Βιοφυσικής 1 Διαπερατότητα διπλοστιβάδας λιπιδίων Όλα τα ζωντανά κύτταρα θα πρέπει να είναι σε θέση να ανταλλάσσουν υλικά (θρεπτικές ουσίες και παραπροϊόντα) με το εξωτερικό τους περιβάλλον,
Σημειώσεις Βιοφυσικής 1 Διαπερατότητα διπλοστιβάδας λιπιδίων Όλα τα ζωντανά κύτταρα θα πρέπει να είναι σε θέση να ανταλλάσσουν υλικά (θρεπτικές ουσίες και παραπροϊόντα) με το εξωτερικό τους περιβάλλον,
3. Με ποιο άλλο σύστημα είναι συνδεδεμένο το κυκλοφορικό σύστημα;
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ
 ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
ΓΩΝΙΕΣ φ, ψ ΚΑΙ ΕΠΙΤΡΕΠΤΕΣ ΔΙΑΜΟΡΦΩΣΕΙΣ ΤΗΣ ΠΟΛΥΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ φ φ Ccarbonyl n Ccarbonyl n N Cα n Ccarbonyl n-1 Cα n N φ Ccarbonyl n-1 ΜΕΤΡΗΣΗ ΤΗΣ ΓΩΝΙΑΣ ψ φ ψ Ccarbonyl n N (Ca
ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του
 ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του ΤΑ ΜΟΝΟΜΕΡΗ ΣΥΝΔΕΟΝΤΑΙ ΜΕ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ. 1. ΠΡΩΤΕΪΝΕΣ
ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του ΤΑ ΜΟΝΟΜΕΡΗ ΣΥΝΔΕΟΝΤΑΙ ΜΕ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ. 1. ΠΡΩΤΕΪΝΕΣ
Εργασία για το μάθημα της Βιολογίας. Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου
 Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης. Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010
 ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ
 2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
τα βιβλία των επιτυχιών
 Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Η δοµή και η λειτουργία του κυτταροσκελετού: Ο κυτταροσκελετός είναι ένα δίκτυο από ινίδια που εκτείνονται σε όλο το κυτταρόπλασµα και σχηµατίζουν
 Η δοµή και η λειτουργία του κυτταροσκελετού: Ο κυτταροσκελετός είναι ένα δίκτυο από ινίδια που εκτείνονται σε όλο το κυτταρόπλασµα και σχηµατίζουν ένα δυναµικό σκελετό που χρησιµεύει στη στήριξη και την
Η δοµή και η λειτουργία του κυτταροσκελετού: Ο κυτταροσκελετός είναι ένα δίκτυο από ινίδια που εκτείνονται σε όλο το κυτταρόπλασµα και σχηµατίζουν ένα δυναµικό σκελετό που χρησιµεύει στη στήριξη και την
4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ. περιλαμβάνονται ο σπλήνας και ο θύμος αδένας (εικ.4.1). Το λεμφικό σύστημα είναι πολύ σημαντικό γιατί:
 ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΚΕΦΑΛΑΙΟ 2. Η σύσταση των κυττάρων
 ΚΕΦΑΛΑΙΟ 2 Η σύσταση των κυττάρων Τα μόρια των κυττάρων Νερό Υδατάνθρακες Λιπίδια Νουκλεϊκά οξέα Πρωτεΐνες Νερό Νερό: ένα μόριο με πολικότητα 1: 554 million Copyright 2002 Pearson Education, Inc., publishing
ΚΕΦΑΛΑΙΟ 2 Η σύσταση των κυττάρων Τα μόρια των κυττάρων Νερό Υδατάνθρακες Λιπίδια Νουκλεϊκά οξέα Πρωτεΐνες Νερό Νερό: ένα μόριο με πολικότητα 1: 554 million Copyright 2002 Pearson Education, Inc., publishing
IΣTOΛOΓIA. Tα δείγµατα του βιολογικού υλικού λαµβάνονται µε > βελόνες ενδοσκοπικούς σωλήνες εύκαµπτους καθετήρες
 IΣTOΛOΓIA H ιστολογία κλάδος της ιατρικής που µελετά > υφή βιολογικού υλικού και τους τρόπους που τα επιµέρους συστατικά στοιχεία σχετίζονται µεταξύ τους δοµικά & λειτουργικά Tα δείγµατα του βιολογικού
IΣTOΛOΓIA H ιστολογία κλάδος της ιατρικής που µελετά > υφή βιολογικού υλικού και τους τρόπους που τα επιµέρους συστατικά στοιχεία σχετίζονται µεταξύ τους δοµικά & λειτουργικά Tα δείγµατα του βιολογικού
Β. ΚΑΜΙΝΕΛΛΗΣ ΒΙΟΛΟΓΙΑ. Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα).
 ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
ΟΛΛΙΝΤΖΑ ΠΑΝΕΠΙΣΤΗΜΙΑΚΑ ΦΡΟΝΤΙΣΤΗΡΙΑ
 Κ Kάνιγγος ΠΑΝΕΠΙΣΤΗΜΙΑΚΑ ΦΡΟΝΤΙΣΤΗΡΙΑ ΟΛΛΙΝΤΖΑ 10, (5ος όροφ. Τηλ: 210-3300296-7. www.kollintzas.gr 1. Χημική σύσταση του κυττάρου. 2. Δομή και λειτουργία του κυττάρου. 3. Μεταβολισμός: βασικές αρχές,
Κ Kάνιγγος ΠΑΝΕΠΙΣΤΗΜΙΑΚΑ ΦΡΟΝΤΙΣΤΗΡΙΑ ΟΛΛΙΝΤΖΑ 10, (5ος όροφ. Τηλ: 210-3300296-7. www.kollintzas.gr 1. Χημική σύσταση του κυττάρου. 2. Δομή και λειτουργία του κυττάρου. 3. Μεταβολισμός: βασικές αρχές,
Μεταβολισμός του γλυκογόνου. Μεταβολισμός των υδατανθράκων κατά την άσκηση. Από που προέρχεται το μυϊκό και ηπατικό γλυκογόνο;
 Μεταβολισμός των υδατανθράκων κατά την άσκηση Μεταβολισμός του γλυκογόνου Το γλυκογόνο είναι ο αφθονότερος υδατάνθρακας των ζώων Το γλυκογόνο αποθηκεύεται κυρίως στο ήπαρ (3-7% κατά βάρος) και στους μύες
Μεταβολισμός των υδατανθράκων κατά την άσκηση Μεταβολισμός του γλυκογόνου Το γλυκογόνο είναι ο αφθονότερος υδατάνθρακας των ζώων Το γλυκογόνο αποθηκεύεται κυρίως στο ήπαρ (3-7% κατά βάρος) και στους μύες
Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki M.
 10th Panhellenic Conference of Alzheimer's Disease and Related Disorders (PICAD) and 2nd Mediterranean Conference of Neurodegenerative Diseases (MeCOND) Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki
10th Panhellenic Conference of Alzheimer's Disease and Related Disorders (PICAD) and 2nd Mediterranean Conference of Neurodegenerative Diseases (MeCOND) Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki
Κεφ. 12 ΛΙΠΙ ΙΑ ΚΑΙ ΚΥΤΤΑΡΙΚΕΣ ΜΕΜΒΡΑΝΕΣ
 Κεφ. 12 ΛΙΠΙ ΙΑ ΚΑΙ ΚΥΤΤΑΡΙΚΕΣ ΜΕΜΒΡΑΝΕΣ Ποικιλότητα και κοινά χαρακτηριστικά των κυτταρικών µεµβρανών Τα λιπαρά οξέα: βασικά συστατικά των λιπιδίων Mεµβρανικά λιπίδια και είδη τους (3) Σχηµατισµός µεµβρανών
Κεφ. 12 ΛΙΠΙ ΙΑ ΚΑΙ ΚΥΤΤΑΡΙΚΕΣ ΜΕΜΒΡΑΝΕΣ Ποικιλότητα και κοινά χαρακτηριστικά των κυτταρικών µεµβρανών Τα λιπαρά οξέα: βασικά συστατικά των λιπιδίων Mεµβρανικά λιπίδια και είδη τους (3) Σχηµατισµός µεµβρανών
ρευστότητα (εξασφαλίζεται µε τα φωσφολιπίδια)
 Λειτουργίες Πλασµατική µεµβράνη οριοθέτηση του κυττάρου εκλεκτική διαπερατότητα ή ηµιπερατότητα αναγνώριση και υποδοχή µηνυµάτων πρόσληψη και αποβολή ουσιών Πλασµατική µεµβράνη Ιδιότητες σταθερότητα ρευστότητα
Λειτουργίες Πλασµατική µεµβράνη οριοθέτηση του κυττάρου εκλεκτική διαπερατότητα ή ηµιπερατότητα αναγνώριση και υποδοχή µηνυµάτων πρόσληψη και αποβολή ουσιών Πλασµατική µεµβράνη Ιδιότητες σταθερότητα ρευστότητα
Φυσιολογία ΙΙ Ενότητα 2:
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 2: Ορμόνες Ανωγειανάκις Γεώργιος Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 2: Ορμόνες Ανωγειανάκις Γεώργιος Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ. Λειτουργία των νεφρών. Συμπτώματα της χρόνιας νεφρικής ανεπάρκειας
 ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ Η χρόνια νεφρική ανεπάρκεια είναι η προοδευτική, μη αναστρέψιμη μείωση της νεφρικής λειτουργίας, η οποία προκαλείται από βλάβη του νεφρού ποικίλης αιτιολογίας. Η χρόνια νεφρική ανεπάρκεια
ΜΕΤΑΜΟΣΧΕΥΣΗ ΝΕΦΡΟΥ Η χρόνια νεφρική ανεπάρκεια είναι η προοδευτική, μη αναστρέψιμη μείωση της νεφρικής λειτουργίας, η οποία προκαλείται από βλάβη του νεφρού ποικίλης αιτιολογίας. Η χρόνια νεφρική ανεπάρκεια
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ ΚΕΦΑΛΑΙΟ 2 ΚΥΤΤΑΡΟ: Η ΘΕΜΕΛΙΩΔΗΣ ΜΟΝΑΔΑ ΤΗΣ ΖΩΗΣ ΘΕΜΑ Β 1. Η εικόνα απεικονίζει τμήμα μιας δομής του κυττάρου.
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ ΚΕΦΑΛΑΙΟ 2 ΚΥΤΤΑΡΟ: Η ΘΕΜΕΛΙΩΔΗΣ ΜΟΝΑΔΑ ΤΗΣ ΖΩΗΣ ΘΕΜΑ Β 1. Η εικόνα απεικονίζει τμήμα μιας δομής του κυττάρου. I. Πώς ονομάζεται η κυτταρική δομή που απεικονίζεται στην εικόνα; Οι αριθμοί:
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ ΚΕΦΑΛΑΙΟ 2 ΚΥΤΤΑΡΟ: Η ΘΕΜΕΛΙΩΔΗΣ ΜΟΝΑΔΑ ΤΗΣ ΖΩΗΣ ΘΕΜΑ Β 1. Η εικόνα απεικονίζει τμήμα μιας δομής του κυττάρου. I. Πώς ονομάζεται η κυτταρική δομή που απεικονίζεται στην εικόνα; Οι αριθμοί:
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Τμήμα Βιολογίας Τομέας Βιολογίας Κυττάρου & Βιοφυσικής ΜΑΘΗΜΑ: «ΒΙΟΛΟΓΙΑ ΚΥΤΤΑΡΟΥ»
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Τμήμα Βιολογίας Τομέας Βιολογίας Κυττάρου & Βιοφυσικής Εργαστηριακή άσκηση: ΜΑΘΗΜΑ: «ΒΙΟΛΟΓΙΑ ΚΥΤΤΑΡΟΥ» «ΗΛΕΚΤΡΟΦΟΡΗΣΗ ΠΡΩΤΕΪΝΩΝ ΣΕ ΠΗΚΤΩΜΑ ΠΟΛΥΑΚΡΥΛΑΜΙΔΗΣ-
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ Τμήμα Βιολογίας Τομέας Βιολογίας Κυττάρου & Βιοφυσικής Εργαστηριακή άσκηση: ΜΑΘΗΜΑ: «ΒΙΟΛΟΓΙΑ ΚΥΤΤΑΡΟΥ» «ΗΛΕΚΤΡΟΦΟΡΗΣΗ ΠΡΩΤΕΪΝΩΝ ΣΕ ΠΗΚΤΩΜΑ ΠΟΛΥΑΚΡΥΛΑΜΙΔΗΣ-
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ
 ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ: ΜΙΚΡΟΪΝΙΔΙΑ- ΕΝΔΙΑΜΕΣΑ ΙΝΙΔΙΑ- ΜΙΚΡΟΣΩΛΗΝΙΣΚΟΙ Η δοµή και η λειτουργία του κυτταροσκελετού: Ο κυτταροσκελετός είναι ένα δίκτυο από ινίδια που εκτείνονται σε όλο
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΚΥΤΤΑΡΟΣΚΕΛΕΤΟΥ: ΜΙΚΡΟΪΝΙΔΙΑ- ΕΝΔΙΑΜΕΣΑ ΙΝΙΔΙΑ- ΜΙΚΡΟΣΩΛΗΝΙΣΚΟΙ Η δοµή και η λειτουργία του κυτταροσκελετού: Ο κυτταροσκελετός είναι ένα δίκτυο από ινίδια που εκτείνονται σε όλο
Τμήμα Βιολογίας Μάθημα: ΒΙΟΛΟΓΙΑ ΚΥΤΤΑΡΟΥ Γ εξάμηνο 2014-2015 Διαλέξεις κάθε Τρίτη 13-15 μ.μ. και Παρασκευή 11-13
 Τμήμα Βιολογίας Μάθημα: ΒΙΟΛΟΓΙΑ ΚΥΤΤΑΡΟΥ Γ εξάμηνο 2014-2015 Διαλέξεις κάθε Τρίτη 13-15 μ.μ. και Παρασκευή 11-13 Ισιδώρα Παπασιδέρη, Καθηγήτρια...για περισσότερα... http://kyttariki.biol.uoa.gr, ttp://multimedia.biol.uoa.gr
Τμήμα Βιολογίας Μάθημα: ΒΙΟΛΟΓΙΑ ΚΥΤΤΑΡΟΥ Γ εξάμηνο 2014-2015 Διαλέξεις κάθε Τρίτη 13-15 μ.μ. και Παρασκευή 11-13 Ισιδώρα Παπασιδέρη, Καθηγήτρια...για περισσότερα... http://kyttariki.biol.uoa.gr, ttp://multimedia.biol.uoa.gr
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010
 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 Μεγεθυντική ικανότητα και διακριτική ικανότητα ή ανάλυση Μέγιστη ανάλυση
CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 Μεγεθυντική ικανότητα και διακριτική ικανότητα ή ανάλυση Μέγιστη ανάλυση
ΚΕΦΑΛΑΙΟ ΤΡIΤΟ ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ
 ΚΕΦΑΛΑΙΟ ΤΡIΤΟ ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ 2015 2 ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ Λέξεις-κλειδιά Κυτταρική ή πλασματική μεμβράνη... Βασικές ιδιότητες της πλασματικής μεμβράνης... Βασικές λειτουργίες
ΚΕΦΑΛΑΙΟ ΤΡIΤΟ ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ 2015 2 ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ ΒΙΟΛΟΓΙΚΕΣ ΜΕΜΒΡΑΝΕΣ Λέξεις-κλειδιά Κυτταρική ή πλασματική μεμβράνη... Βασικές ιδιότητες της πλασματικής μεμβράνης... Βασικές λειτουργίες
ΠΟΙΑ ΕΙΝΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΡΥΘΜΙΣΤΙΚΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΤΟΝ ΟΡΓΑΝΙΣΜΟ ΚΑΙ ΠΟΙΑ Η ΣΥΜΒΟΛΗ ΤΟΥΣ ΣΤΗ ΡΥΘΜΙΣΗ ΤΗΣ ΟΞΕΟΒΑΣΙΚΗΣ ΙΣΟΡΡΟΠΙΑΣ;
 ΠΟΙΑ ΕΙΝΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΡΥΘΜΙΣΤΙΚΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΤΟΝ ΟΡΓΑΝΙΣΜΟ ΚΑΙ ΠΟΙΑ Η ΣΥΜΒΟΛΗ ΤΟΥΣ ΣΤΗ ΡΥΘΜΙΣΗ ΤΗΣ ΟΞΕΟΒΑΣΙΚΗΣ ΙΣΟΡΡΟΠΙΑΣ; Ελένη Α. Φράγκου Νεφρολόγος ΧΩΡΙΣ ΣΥΓΚΡΟΥΣΗ ΣΥΜΦΕΡΟΝΤΩΝ ΜΕ ΤΟΥΣ ΧΟΡΗΓΟΥΣ
ΠΟΙΑ ΕΙΝΑΙ Η ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΡΥΘΜΙΣΤΙΚΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΤΟΝ ΟΡΓΑΝΙΣΜΟ ΚΑΙ ΠΟΙΑ Η ΣΥΜΒΟΛΗ ΤΟΥΣ ΣΤΗ ΡΥΘΜΙΣΗ ΤΗΣ ΟΞΕΟΒΑΣΙΚΗΣ ΙΣΟΡΡΟΠΙΑΣ; Ελένη Α. Φράγκου Νεφρολόγος ΧΩΡΙΣ ΣΥΓΚΡΟΥΣΗ ΣΥΜΦΕΡΟΝΤΩΝ ΜΕ ΤΟΥΣ ΧΟΡΗΓΟΥΣ
ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ
 1 ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ Οι δύο πολυνουκλεοτιδικές αλυσίδες του DNA αποτελούνται από νουκλεοτίδια τα οποία ενώνονται με φωσφοδιεστερικούς δεσμούς. Πιο συγκεκριμένα
1 ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ Οι δύο πολυνουκλεοτιδικές αλυσίδες του DNA αποτελούνται από νουκλεοτίδια τα οποία ενώνονται με φωσφοδιεστερικούς δεσμούς. Πιο συγκεκριμένα
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
ΑΝΟΣΟΒΙΟΛΟΓΙΑ. Εξεταστική Ιανουαρίου 2010
 Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
ΓENIKA ΣTOIXEIA. Η φυσιολογία του ανθρώπου μελετά τα χαρακτηριστικά και τους λειτουργικούς μηχανισμούς που κάνουν το ανθρώπινο σώμα ζωντανό οργανισμό.
 1 ΓENIKA ΣTOIXEIA Η φυσιολογία του ανθρώπου μελετά τα χαρακτηριστικά και τους λειτουργικούς μηχανισμούς που κάνουν το ανθρώπινο σώμα ζωντανό οργανισμό. ΤΑ ΚΥΤΤΑΡΑ Η βασική ζώσα μονάδα του σώματος είναι
1 ΓENIKA ΣTOIXEIA Η φυσιολογία του ανθρώπου μελετά τα χαρακτηριστικά και τους λειτουργικούς μηχανισμούς που κάνουν το ανθρώπινο σώμα ζωντανό οργανισμό. ΤΑ ΚΥΤΤΑΡΑ Η βασική ζώσα μονάδα του σώματος είναι
Στοιχεία και λειτουργίες του κυτταροσκελετού
 Στοιχεία και λειτουργίες του κυτταροσκελετού ΔΟΜΗ ΤΩΝ ΙΝΙΔΙΩΝ ΑΚΤΙΝΗΣ Ακτίνη: Η μονάδα πολυμερισμού Δομή μονομερούς G- (globular) ακτίνης ATP και ADP μονομερή G-ακτίνης Πολυμερισμός της G-(globular) ακτίνης
Στοιχεία και λειτουργίες του κυτταροσκελετού ΔΟΜΗ ΤΩΝ ΙΝΙΔΙΩΝ ΑΚΤΙΝΗΣ Ακτίνη: Η μονάδα πολυμερισμού Δομή μονομερούς G- (globular) ακτίνης ATP και ADP μονομερή G-ακτίνης Πολυμερισμός της G-(globular) ακτίνης
ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ
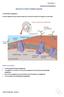 Οι Βιολογικές Μεμβράνες Είναι δυναμικές και όχι στατικές δομές που επιτελούν πολλές λειτουργίες στα κύτταρα. Πρέπει να γνωρίζετε Τη σύσταση βιολογικών μεμβρανών Τι προβλέπει το μοντέλο του ρευστού μωσαϊκού
Οι Βιολογικές Μεμβράνες Είναι δυναμικές και όχι στατικές δομές που επιτελούν πολλές λειτουργίες στα κύτταρα. Πρέπει να γνωρίζετε Τη σύσταση βιολογικών μεμβρανών Τι προβλέπει το μοντέλο του ρευστού μωσαϊκού
1. Εισαγωγή στο Κύτταρο
 1. Εισαγωγή στο Κύτταρο 1.1. Ορισμός του κυττάρου. Το κύτταρο είναι η δομική και λειτουργική μονάδα της ζωής (σχήμα 1). Το κύτταρο αποτελεί τη βάση της δομικής και λειτουργικής οργάνωσης ενός οργανισμού.
1. Εισαγωγή στο Κύτταρο 1.1. Ορισμός του κυττάρου. Το κύτταρο είναι η δομική και λειτουργική μονάδα της ζωής (σχήμα 1). Το κύτταρο αποτελεί τη βάση της δομικής και λειτουργικής οργάνωσης ενός οργανισμού.
Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C.
 Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
ΟΜΑΔΕΣ ΑΙΜΑΤΟΣ ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΓΕΝΕΤΙΚΗΣ. Εργαστηριακό Μάθημα ΙΙ-Εαρινό εξάμηνο
 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΓΕΝΕΤΙΚΗΣ ΟΜΑΔΕΣ ΑΙΜΑΤΟΣ Εργαστηριακό Μάθημα ΙΙ-Εαρινό εξάμηνο 2016-17 Α Έτος Δρ. Χρύσα Μεταλλινού Τι είναι το Αίμα; Το αίμα είναι ένας εξειδικευμένος
ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΓΕΝΕΤΙΚΗΣ ΟΜΑΔΕΣ ΑΙΜΑΤΟΣ Εργαστηριακό Μάθημα ΙΙ-Εαρινό εξάμηνο 2016-17 Α Έτος Δρ. Χρύσα Μεταλλινού Τι είναι το Αίμα; Το αίμα είναι ένας εξειδικευμένος
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών
 Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Δοµή και Λειτουργία της Κυτταρικής Μεµβράνης Ε. Παρασκευά 0
 Δοµή και Λειτουργία της Κυτταρικής Μεµβράνης 12.11.2015 Ε. Παρασκευά 0 Η κυτταρική µεµβράνη Αποµόνωση του κυττάρου από το περιβάλλον Καθορισµός του ως οντότητα Περιβάλλει το κύτταρο Καθορίζει τα όρια του
Δοµή και Λειτουργία της Κυτταρικής Μεµβράνης 12.11.2015 Ε. Παρασκευά 0 Η κυτταρική µεµβράνη Αποµόνωση του κυττάρου από το περιβάλλον Καθορισµός του ως οντότητα Περιβάλλει το κύτταρο Καθορίζει τα όρια του
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ)
 ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» Η κυκλοφορία του αίματος και
ΠΡΟΓΡΑΜΜΑ ΔΙΑ ΒΙΟΥ ΜΑΘΗΣΗΣ ΑΕΙ ΓΙΑ ΤΗΝ ΕΠΙΚΑΙΡΟΠΟΙΗΣΗ ΓΝΩΣΕΩΝ ΑΠΟΦΟΙΤΩΝ ΑΕΙ (ΠΕΓΑ) «Οι σύγχρονες τεχνικές βιο-ανάλυσης στην υγεία, τη γεωργία, το περιβάλλον και τη διατροφή» Η κυκλοφορία του αίματος και
