Κεφάλαιο Σ5. Μόρια και στερεά Τμήμα Μηχανικών Βιοϊατρικής /Πανεπιστήμιο Δυτικής Αττικής
|
|
|
- Άτροπος Γαλάνη
- 6 χρόνια πριν
- Προβολές:
Transcript
1 Κεφάλαιο Σ5 Μόρια και στερεά Τμήμα Μηχανικών Βιοϊατρικής /Πανεπιστήμιο Δυτικής Αττικής
2 Μόρια Τα μόρια είναι συσσωρεύσεις ατόμων. Η διάταξη των ατόμων επηρεάζει τις ιδιότητες του υλικού. Τον 19ο αιώνα μελετήθηκαν και κατανοήθηκαν πλήρως τα αέρια. Η πιο τυχαία διάταξη ατόμων που υπάρχει στη φύση είναι αυτή των αερίων. Τα στερεά μπορεί να είναι κρυσταλλικά ή άμορφα. Στα κρυσταλλικά στερεά, τα άτομα σχηματίζουν κανονικές διατάξεις. Στα άμορφα στερεά, τα άτομα δεν σχηματίζουν κανονικές διατάξεις. Κατά τη διάρκεια του 20ου αιώνα σημείωσε πρόοδο και η μελέτη των υγρών. Εισαγωγή
3 Μοριακοί δεσμοί Εισαγωγή Οι μηχανισμοί σχηματισμού δεσμών στα μόρια βασίζονται ουσιαστικά στις ηλεκτρικές δυνάμεις. Οι δυνάμεις αυτές περιγράφονται από μια συνάρτηση δυναμικής ενέργειας. Κάθε σταθερό μόριο αναμένεται να έχει τέτοια διάταξη ώστε η συνάρτηση της δυναμικής του ενέργειας να έχει ελάχιστη τιμή. Ενότητα Σ5.1
4 Χαρακτηριστικά των μοριακών δεσμών Σε πολύ μικρές αποστάσεις, η δύναμη που αναπτύσσεται μεταξύ των ατόμων είναι απωστική. Αυτή η άπωση οφείλεται κατά ένα μέρος στις ηλεκτροστατικές δυνάμεις, αλλά είναι και απόρροια της απαγορευτικής αρχής. Λόγω της απαγορευτικής αρχής, κάποια ηλεκτρόνια που βρίσκονται σε αλληλεπικαλυπτόμενες στιβάδες αναγκάζονται να μεταπέσουν σε καταστάσεις υψηλότερης ενέργειας. Η ενέργεια ολόκληρου του συστήματος αυξάνεται όπως ακριβώς θα αυξανόταν αν υπήρχε απωστική δύναμη μεταξύ των ατόμων. Σε μεγαλύτερες αποστάσεις η δύναμη που αναπτύσσεται μεταξύ των ατόμων είναι ελκτική. Ενότητα Σ5.1
5 Συνάρτηση δυναμικής ενέργειας Η δυναμική ενέργεια ενός συστήματος δύο ατόμων δίνεται από τη σχέση: Ur A r B r () n m Όπου: r είναι η απόσταση μεταξύ των πυρήνων των δύο ατόμων. m και n είναι μικροί ακέραιοι αριθμοί. A είναι μια παράμετρος που αντιστοιχεί στην ελκτική δύναμη. B είναι μια παράμετρος που αντιστοιχεί στην απωστική δύναμη. Ενότητα Σ5.1
6 Συνάρτηση δυναμικής ενέργειας Γράφημα Όταν η απόσταση μεταξύ των δύο ατόμων είναι μεγάλη, η κλίση της καμπύλης είναι θετική. Η συνισταμένη δύναμη είναι ελκτική. Στην απόσταση ισορροπίας, οι ελκτικές και απωστικές δυνάμεις αλληλοεξουδετερώνονται. Στο συγκεκριμένο σημείο, το δυναμικό (ισούται αριθμητικά με τη δυναμική ενέργεια ανά μονάδα μάζας για σωματίδιο χωρίς διαστάσεις) έχει ελάχιστη τιμή. Η κλίση της καμπύλης είναι μηδενική. Ενότητα Σ5.1
7 Μοριακοί δεσμοί Είδη Στα απλουστευμένα μοντέλα των μοριακών δεσμών περιλαμβάνονται: οι ιοντικοί (ετεροπολικοί) δεσμοί, οι ομοιοπολικοί δεσμοί, οι δεσμοί van der Waals, οι δεσμοί υδρογόνου. Ενότητα Σ5.1
8 Ιοντικοί (ετεροπολικοί) δεσμοί Όταν δύο άτομα συνδυάζονται μέσω της μεταφοράς ενός ή περισσότερων ηλεκτρονίων από την εξωτερική στιβάδα του ενός ατόμου σε αυτήν του άλλου, τότε σχηματίζεται ιοντικός ή ετεροπολικός δεσμός. Οι ιοντικοί δεσμοί οφείλονται στην ελκτική δύναμη Coulomb που αναπτύσσεται μεταξύ αντίθετα φορτισμένων ιόντων. Όταν το ηλεκτρόνιο μεταπίπτει από την κατάσταση E = 0 στην κατάσταση αρνητικής ενέργειας, τότε εκλύεται ενέργεια. Αυτή η ενέργεια ονομάζεται ηλεκτρονική συγγένεια ή ηλεκτροσυγγένεια του ατόμου. Η ενέργεια που απαιτείται για τη διάσπαση του μοριακού δεσμού και τον σχηματισμό ουδέτερων ατόμων ονομάζεται ενέργεια διαχωρισμού ή ενέργεια διάστασης. Ενότητα
9 Παράδειγμα ιοντικού δεσμού: NaCl Στο γράφημα παρουσιάζεται η συνολική ενέργεια του μορίου του NaCl συναρτήσει της απόστασης μεταξύ των πυρήνων. Η ελάχιστη τιμή της συνολικής ενέργειας παρατηρείται στην απόσταση ισορροπίας. Ενότητα Σ5.1
10 Ιοντικοί δεσμοί (τελική διαφάνεια) Η ενέργεια του μορίου είναι μικρότερη από εκείνη του συστήματος των δύο ουδέτερων ατόμων. Ο σχηματισμός του μορίου αντιπροσωπεύει μια ενεργειακά ευνοϊκή κατάσταση. Το σύστημα των δύο ατόμων μπορεί να μειώσει τη συνολική του ενέργεια εκλύοντας ενέργεια και σχηματίζοντας ένα μόριο. Ενότητα Σ5.1
11 Ομοιοπολικοί δεσμοί Μεταξύ δύο ατόμων σχηματίζεται ομοιοπολικός δεσμός όταν τα δύο άτομα μοιράζονται ηλεκτρόνια τα οποία έχουν προέλθει είτε από το ένα άτομο είτε και από τα δύο άτομα. Μπορούμε να περιγράψουμε τον ομοιοπολικό δεσμό χρησιμοποιώντας ατομικές κυματοσυναρτήσεις. Παράδειγμα ομοιοπολικού δεσμού αποτελεί το μόριο του H 2 που σχηματίζεται από δύο άτομα υδρογόνου. Ενότητα Σ5.1
12 Κυματοσυνάρτηση Άτομα σε μεγάλη απόσταση μεταξύ τους Κάθε άτομο έχει κυματοσυνάρτηση: 1 ψ r e rao 1s () 3 παo Όταν τα δύο άτομα βρίσκονται σε μεγάλη απόσταση μεταξύ τους, τότε οι αντίστοιχες κυματοσυναρτήσεις επικαλύπτονται ελάχιστα. Ενότητα Σ5.1
13 Κυματοσυνάρτηση Σχηματισμός μορίου Υποθέτουμε ότι τα δύο άτομα έρχονται κοντά το ένα στο άλλο. Οι κυματοσυναρτήσεις τους αλληλοεπικαλύπτονται και σχηματίζουν τη σύνθετη κυματοσυνάρτηση που παρουσιάζεται στην εικόνα. Το πλάτος πιθανότητας είναι μεγαλύτερο στην περιοχή μεταξύ των ατόμων απ ό,τι εκατέρωθεν της περιοχής συνένωσής τους. Ενότητα Σ5.1
14 Ομοιοπολικοί δεσμοί (τελική διαφάνεια) Τα ηλεκτρόνια των ατόμων είναι πιθανότερο να βρίσκονται στην περιοχή μεταξύ των ατόμων παρά στις εξωτερικές περιοχές του συστήματος. Μπορούμε να μοντελοποιήσουμε αυτή την περίπτωση θεωρώντας ότι υπάρχει ένα σταθερό αρνητικό φορτίο μεταξύ των ατόμων, το οποίο ασκεί ελκτική δύναμη Coulomb και στους δύο πυρήνες. Έτσι, μεταξύ των ατόμων αναπτύσσεται μια ελκτική δύναμη, η οποία έχει ως αποτέλεσμα τον σχηματισμό του ομοιοπολικού δεσμού. Ενότητα Σ5.1
15 Δεσμοί Van der Waals Δύο ουδέτερα μόρια έλκονται μεταξύ τους με ασθενείς ηλεκτροστατικές δυνάμεις, τις δυνάμεις van der Waals. Άτομα που δεν σχηματίζουν ιοντικούς ή ομοιοπολικούς δεσμούς έλκονται μεταξύ τους με δυνάμεις van der Waals. Οι δυνάμεις van der Waals αναπτύσσονται επειδή το ηλεκτρικό φορτίο είναι κατανεμημένο στο μόριο και τα κέντρα του θετικού και του αρνητικού φορτίου του βρίσκονται σε διαφορετικές θέσεις μέσα σε αυτό. Λόγω αυτής της κατανομής του φορτίου, το μόριο συμπεριφέρεται ως ηλεκτρικό δίπολο. Λόγω των διπολικών ηλεκτρικών πεδίων, δύο μόρια μπορούν να αλληλεπιδρούν σαν να ασκείται μια ελκτική δύναμη μεταξύ τους. Υπενθυμίζουμε ότι αυτό το φαινόμενο συμβαίνει παρά το γεγονός ότι τα μόρια είναι ηλεκτρικά ουδέτερα. Ενότητα Σ5.1
16 Είδη δυνάμεων Van der Waals Δύναμη διπόλου-διπόλου Πρόκειται για μια αλληλεπίδραση μεταξύ δύο μορίων, καθένα από τα οποία έχει μια μόνιμη ηλεκτρική διπολική ροπή. Δύναμη διπόλου από πόλωση Παρατηρείται όταν ένα πολικό μόριο, το οποίο έχει μόνιμη ηλεκτρική διπολική ροπή, πολώνει ένα μη πολικό μόριο, επάγοντας σε αυτό διπολική ροπή. Δύναμη διασποράς Πρόκειται για μια ελκτική δύναμη που αναπτύσσεται μεταξύ δύο μη πολικών μορίων. Η αλληλεπίδραση συμβαίνει επειδή, παρά το γεγονός ότι η μέση διπολική ροπή είναι μηδενική στα μη πολικά μόρια, η μέση τιμή του τετραγώνου της διπολικής ροπής δεν είναι μηδενική λόγω των διακυμάνσεων του φορτίου. Δύο μη πολικά μόρια, που βρίσκονται κοντά το ένα στο άλλο, τείνουν να έχουν διπολικές ροπές που είναι συσχετισμένες χρονικά. Λόγω αυτής της κατάστασης αναπτύσσεται μεταξύ τους μια ελκτική δύναμη van der Ενότητα Σ5.1 Waals.
17 Δεσμοί υδρογόνου Ένα άτομο υδρογόνου που αποτελεί μέρος ενός μορίου, εκτός από ομοιοπολικό δεσμό, μπορεί να σχηματίσει και έναν άλλο τύπο δεσμού μεταξύ μορίων, τον δεσμό υδρογόνου. Θα δούμε ως παράδειγμα το μόριο του νερού (H 2 O). Στο μόριο υπάρχουν δύο ομοιοπολικοί δεσμοί. Τα ηλεκτρόνια των ατόμων του υδρογόνου είναι πιθανότερο να βρίσκονται πιο κοντά στο άτομο του οξυγόνου παρά στα άτομα του υδρογόνου. Στις θέσεις των ατόμων υδρογόνου υπάρχουν στην ουσία «εκτεθειμένα» πρωτόνια. Το αρνητικό άκρο του άλλου μορίου έχει τη δυνατότητα να πλησιάσει κοντά στο πρωτόνιο ώστε να δημιουργηθεί ένας δεσμός. Αυτός ο δεσμός είναι αρκετά ισχυρός για τον σχηματισμό στερεής κρυσταλλικής δομής. Ενότητα Σ5.1
18 Δεσμοί υδρογόνου (συνέχεια) Συγκρινόμενος με άλλους χημικούς δεσμούς, ο δεσμός υδρογόνου είναι αρκετά ασθενής. Αποτελεί σημαντικό μηχανισμό σύνδεσης των βιολογικών μορίων και των πολυμερών. Παράδειγμα αποτελεί το μόριο του DNA. Ενότητα Σ5.1
19 Οι ενεργειακές καταστάσεις των μορίων Η ενέργεια ενός μορίου (αν θεωρήσουμε ένα μεμονωμένο μόριο αερίου) διακρίνεται σε τέσσερις κατηγορίες: Ηλεκτρονική ενέργεια Οφείλεται στις αλληλεπιδράσεις μεταξύ των ηλεκτρονίων και των πυρήνων των ατόμων που αποτελούν το μόριο. Ενέργεια λόγω μεταφορικής κίνησης Οφείλεται στην κίνηση του κέντρου μάζας του μορίου στον χώρο. Ενέργεια περιστροφής Οφείλεται στην περιστροφή του μορίου γύρω από το κέντρο μάζας του. Ενέργεια ταλάντωσης Οφείλεται στην ταλάντωση των ατόμων που αποτελούν το μόριο. Η ολική ενέργεια του μορίου είναι το άθροισμα των παραπάνω τιμών ενέργειας: E = E ηλ. + E μετ. + E περ. + E ταλ. Ενότητα Σ5.2
20 Τα φάσματα των μορίων Η ενέργεια λόγω μεταφορικής κίνησης δεν σχετίζεται με την εσωτερική δομή των μορίων και επομένως δεν λαμβάνεται υπόψη στην ερμηνεία των μοριακών φασμάτων. Αναλύοντας τις κβαντισμένες καταστάσεις των ενεργειών περιστροφής και ταλάντωσης του μορίου, μπορούμε να πάρουμε σημαντικές πληροφορίες για ένα μόριο. Ενότητα Σ5.2
21 Περιστροφική κίνηση των μορίων Θα εξετάσουμε το διατομικό μόριο, αλλά μπορούμε να επεκτείνουμε την ίδια μεθοδολογία και στην περίπτωση πολυατομικών μορίων. Ένα διατομικό μόριο ευθυγραμμισμένο με τον άξονα y έχει μόνο δύο βαθμούς ελευθερίας για την περιστροφική κίνηση. Δηλαδή εκείνους που αντιστοιχούν στην περιστροφή γύρω από τους άξονες x και z. Ενότητα Σ5.2
22 Περιστροφική κίνηση των μορίων Ενέργεια Η ενέργεια περιστροφής δίνεται από τη σχέση: E περ. 1 2 I ω 2 Όπου I είναι η ροπή αδράνειας του μορίου. I m mm 1 2 r 2 μr 2 m 1 2 µ είναι η ανηγμένη μάζα του μορίου. Ενότητα Σ5.2
23 Περιστροφική κίνηση των μορίων Στροφορμή Σύμφωνα με την κλασική θεωρία της φυσικής, η στροφορμή του μορίου μπορεί να πάρει οποιαδήποτε τιμή που δίνει η σχέση: L = Iω Σύμφωνα με την κβαντική μηχανική, η στροφορμή περιορίζεται στις τιμές: L J J 1 J 0, 1, 2, Όπου J είναι ένας ακέραιος αριθμός, που ονομάζεται κβαντικός αριθμός περιστροφής. Ενότητα Σ5.2
24 Κινητική ενέργεια περιστροφής του μορίου Επιτρεπτές στάθμες Οι επιτρεπτές τιμές της κινητικής ενέργειας περιστροφής είναι: 2 Eπερ. EJ J J 1 2 I J 0 1 2,,, Η κινητική ενέργεια περιστροφής του μορίου είναι κβαντισμένη και εξαρτάται από τη ροπή αδράνειάς του. Όσο αυξάνεται ο κβαντικός αριθμός J, τόσο αυξάνονται και οι αποστάσεις μεταξύ των ενεργειακών καταστάσεων. Ενότητα Σ5.2
25 Επιτρεπτές στάθμες (συνέχεια) Στα περισσότερα μόρια, η μετάπτωση από μια στάθμη ενέργειας περιστροφής σε μια γειτονική της έχει ως αποτέλεσμα την εκπομπή ή απορρόφηση ακτινοβολίας στο εύρος συχνοτήτων των μικροκυμάτων. Οι επιτρεπτές μεταπτώσεις δίνονται από τη συνθήκη: Eφωτονίου Eπερ. J I 2 h J J 1, 2, 3, 2 4π I 2 Όπου J είναι ο κβαντικός αριθμός περιστροφής της υψηλότερης ενεργειακής κατάστασης. Ενότητα Σ5.2
26 Ταλάντωση των μορίων Μπορούμε να θεωρήσουμε τα μόρια ως ελαστικές δομές, στις οποίες τα άτομα συνδέονται μεταξύ τους με «ελατήρια». Έτσι μπορούμε να μοντελοποιήσουμε το μόριο ως απλό αρμονικό ταλαντωτή. Με την προϋπόθεση ότι τα άτομα του μορίου δεν απέχουν πολύ από τις θέσεις ισορροπίας τους. Ενότητα Σ5.2
27 Ταλάντωση των μορίων Δυναμική ενέργεια Στην εικόνα παρουσιάζεται το γράφημα της συνάρτησης δυναμικής ενέργειας. Όπου r o είναι η απόσταση ισορροπίας μεταξύ των δύο ατόμων. Για αποστάσεις κοντά στην r 0, το σχήμα της καμπύλης δυναμικής ενέργειας προσεγγίζει αυτό της παραβολής. Ενότητα Σ5.2
28 Ενέργεια ταλάντωσης Η κλασική μηχανική δίνει τη συχνότητα ταλάντωσης του απλού αρμονικού ταλαντωτή. Σύμφωνα με την κβαντομηχανική, κάθε μόριο ταλαντώνεται σε κβαντισμένες καταστάσεις. Η ταλαντωτική κίνηση και η κβαντισμένη ενέργεια ταλάντωσης του μορίου μπορούν να μεταβληθούν αν το μόριο προσλάβει κατάλληλη ποσότητα ενέργειας, ικανή να προκαλέσει τη μετάπτωσή του από μια κβαντισμένη κατάσταση ταλάντωσης σε μια άλλη. Οι επιτρεπτές τιμές της ενέργειας ταλάντωσης είναι: 1 Eταλ. v hƒ v 0, 1, 2, 2 Όπου v είναι ένας ακέραιος αριθμός που ονομάζεται κβαντικός αριθμός ταλάντωσης. Όταν v = 0, τότε η ενέργεια θεμελιώδους κατάστασης του μορίου ισούται με ½hƒ. Το μόριο ταλαντώνεται ακόμα και Ενότητα αν δεν Σ5.2 είναι διεγερμένο.
29 Ενέργεια ταλάντωσης (τελική διαφάνεια) Οι επιτρεπτές τιμές της ενέργειας ταλάντωσης δίνονται από τη σχέση: E v ταλ. v 0, 1, 2, Ο κανόνας επιλογής για τις επιτρεπτές μεταπτώσεις είναι: Δv = ±1. 1 h 2 2π Η ενέργεια ενός απορροφώμενου φωτονίου δίνεται από τη σχέση: E φωτονίου = ΔE ταλ. = hƒ. k μ Ενότητα Σ5.2
30 Τα φάσματα των μορίων Γενικά, κάθε μόριο ταλαντώνεται και περιστρέφεται ταυτοχρόνως. Σε μια αρχική προσέγγιση, οι κινήσεις αυτές είναι ανεξάρτητες μεταξύ τους. Η συνολική ενέργεια του μορίου ισούται με το άθροισμα των ενεργειών των δύο επιμέρους κινήσεων: 2 1 E v hƒ J J 1 2 2I Ενότητα Σ5.2
31 Το διάγραμμα ενεργειακών σταθμών του μορίου Σε κάθε επιτρεπτή τιμή του κβαντικού αριθμού ταλάντωσης v αντιστοιχεί ένα πλήρες σύνολο σταθμών περιστροφής με αριθμούς J = 0, 1, 2, Η ενεργειακή απόσταση μεταξύ διαδοχικών σταθμών περιστροφής είναι πολύ μικρότερη από την απόσταση μεταξύ διαδοχικών σταθμών ταλάντωσης. Στις συνήθεις θερμοκρασίες, τα περισσότερα μόρια βρίσκονται στην κατάσταση ταλάντωσης v = 0. Ενότητα Σ5.2
32 Μοριακό φάσμα απορρόφησης Το μοριακό φάσμα απορρόφησης αποτελείται από δύο ομάδες γραμμών: Μία ομάδα που βρίσκεται δεξιά από το μέσο του φάσματος και ικανοποιεί τους κανόνες επιλογής ΔJ = +1 και Δv = +1. Μία ομάδα που βρίσκεται αριστερά από το μέσο του φάσματος και ικανοποιεί τους κανόνες επιλογής ΔJ = 1 και Δv = +1. Η διαφορά συχνότητας μεταξύ των διαδοχικών γραμμών ισούται με την ποσότητα h/2πi. Ενότητα Σ5.2
33 Το μοριακό φάσμα απορρόφησης του μορίου HCl Το γράφημα που προκύπτει από τα πειραματικά αποτελέσματα συμφωνεί με το γράφημα που προβλέπει η θεωρία. Ωστόσο, παρατηρούμε μία ιδιομορφία: κάθε γραμμή είναι διπλή. Στο δείγμα υπήρχαν δύο ισότοπα του χλωρίου. Επειδή τα ισότοπα έχουν διαφορετικές μάζες, τα δύο μόρια του HCl έχουν διαφορετικές τιμές I. Ενότητα Σ5.2
34
35 Ένταση των φασματικών γραμμών Η ένταση καθορίζεται από το γινόμενο δύο συναρτήσεων του J. Η πρώτη συνάρτηση είναι το πλήθος των διαθέσιμων καταστάσεων για μια δεδομένη τιμή του J. Υπάρχουν 2J + 1 διαθέσιμες καταστάσεις. Η δεύτερη συνάρτηση είναι ο συντελεστής Boltzmann. 2 J J n n e o ( 1)/(2 I k T ) B Πολλαπλασιάζοντας τους δύο παράγοντες, παίρνουμε: 2 J( J 1)/(2 I kbt ) I 2J 1 e Ο παράγοντας 2J + 1 είναι αύξουσα συνάρτηση του J. Ο εκθετικός παράγοντας είναι φθίνουσα συνάρτηση του J. Από το γινόμενο των δύο παραγόντων προκύπτει μια συμπεριφορά που προσεγγίζει πολύ την περιβάλλουσα των φασματικών γραμμών. Ενότητα Σ5.2
36 Φασματοσκοπία απορρόφησης Οι μεταβάσεις από μια ενεργειακή κατάσταση (ενός μορίου) σε μια άλλη ανώτερης ενέργειας απαιτούν την απορρόφηση ενέργειας. Οι μεταβάσεις που αφορούν στις ενεργειακές καταστάσεις των ηλεκτρονίων απαιτούν ενέργειες φωτονίων στην περιοχή του υπεριώδους ή των ακτίνων Χ. Οι μεταβάσεις των ενεργειακών καταστάσεων δόνησης (ταλάντωσης) απαιτούν ενέργειες φωτονίων στην περιοχή του υπερύθρου κλπ
37 Φασματοσκοπία Υπερύθρου-IR Η Φασματοσκοπία υπερύθρου IR (Infrared Spectroscopy) παρέχει πληροφορίες για μοριακές ταλαντώσεις βασίζεται στο δεδομένο ότι το φως που απαιτείται να απορροφηθεί για να διεγείρει ενεργειακές στάθμες ταλάντωσης βρίσκεται στη φασματική περιοχή του υπερύθρου Η περιοχή του ηλεκτρομαγνητικού φάσματος που αντιστοιχεί στο υπέρυθρο εκτείνεται από τα 0,7 μm έως 300 μm. Τα πειραματικά φάσματα εκφράζονται ως συνάρτηση του κυματάριθμου (αντίστροφο μήκος κύματος) σε cm -1
38 Οι δεσμοί στα στερεά Στα στερεά σχηματίζονται οι εξής τύποι δεσμών: ιοντικοί (ετεροπολικοί) δεσμοί, ομοιοπολικοί δεσμοί. μεταλλικοί δεσμοί. Ενότητα Σ5.3
39 Ιοντικοί δεσμοί στα στερεά Τα ιόντα αλληλεπιδρούν μεταξύ τους κυρίως μέσω της δύναμης Coulomb. Πολλοί κρύσταλλοι σχηματίζονται με ιοντικούς δεσμούς. Μεταξύ γειτονικών ατόμων συμβαίνουν πολλές αλληλεπιδράσεις. Αποτέλεσμα όλων αυτών των αλληλεπιδράσεων είναι μια συνολική αρνητική ηλεκτρική δυναμική ενέργεια, η οποία δίνεται από τη σχέση: e Uελκτική αke r 2 Όπου α είναι ένας αδιάστατος αριθμός, ο οποίος ονομάζεται σταθερά Madelung. Η τιμή της σταθεράς α εξαρτάται αποκλειστικά από την κρυσταλλική δομή κάθε στερεού.
40 Παράδειγμα ιοντικού δεσμού: Ο κρύσταλλος του NaCl Στην εικόνα (α) παρουσιάζεται η κρυσταλλική δομή. Κάθε θετικό ιόν νατρίου περιστοιχίζεται από έξι αρνητικά ιόντα χλωρίου (εικ. β). Κάθε ιόν χλωρίου περιστοιχίζεται από έξι ιόντα νατρίου (εικ. γ). Για την κρυσταλλική δομή του NaCl, α = Ενότητα Σ5.3
41 Η συνολική ενέργεια ενός κρυσταλλικού στερεού Όταν τα ιόντα που απαρτίζουν έναν κρύσταλλο πλησιάσουν το ένα στο άλλο, τότε αναπτύσσεται απωστική δύναμη μεταξύ τους. Ο όρος B/r m της δυναμικής ενέργειας (βλέπε επόμενη διαφάνεια) αντιστοιχεί σε αυτήν ακριβώς την απωστική δύναμη. Η απωστική δύναμη είναι απόρροια των ηλεκτροστατικών δυνάμεων και της απαγορευτικής αρχής. Ενότητα Σ5.3
42 Η συνολική ενέργεια ενός κρυσταλλικού στερεού (συνέχεια) Η συνολική δυναμική ενέργεια του κρυστάλλου είναι: 2 e B U αk r r συν. e m Η δυναμική ενέργεια παίρνει την ελάχιστη τιμή της, U συν, στην απόσταση ισορροπίας r = r o. Αυτή η ελάχιστη ενέργεια, U o, ονομάζεται ενέργεια ιοντικής συνοχής του στερεού. Η απόλυτη τιμή της αντιπροσωπεύει την ενέργεια που απαιτείται για τον διαχωρισμό του στερεού σε μεμονωμένα θετικά και αρνητικά ιόντα. Ενότητα Σ5.3
43 Ιδιότητες των ιοντικών κρυστάλλων Οι ιοντικοί κρύσταλλοι είναι σχετικά σταθεροί και σκληροί. Είναι κακοί αγωγοί του ηλεκτρισμού. Δεν έχουν ελεύθερα ηλεκτρόνια. Κάθε ηλεκτρόνιο του στερεού είναι ισχυρά δεσμευμένο σε κάποιο ιόν. Έχουν υψηλό σημείο τήξης. Είναι διαφανείς (επιτρέπουν τη διέλευση της ορατής ακτινοβολίας), αλλά απορροφούν σε μεγάλο βαθμό την υπέρυθρη ακτινοβολία. Τα ηλεκτρόνια είναι τόσο ισχυρά δεσμευμένα στις στιβάδες που σχηματίζουν, ώστε η ορατή ακτινοβολία δεν έχει αρκετή ενέργεια για να προκαλέσει τη μετάπτωση των ηλεκτρονίων στην επόμενη επιτρεπτή στιβάδα. Η υπέρυθρη ακτινοβολία απορροφάται σε πολύ μεγάλο βαθμό, επειδή τα ιόντα έχουν ιδιοσυχνότητες ταλάντωσης που ανήκουν στην υπέρυθρη περιοχή χαμηλής ενέργειας του φάσματος. Ενότητα Σ5.3
44 Ιδιότητες στερεών με ομοιοπολικούς δεσμούς Ιδιότητες: Συνήθως είναι πολύ σκληρά. Λόγω των υψηλών τιμών ενέργειας ατομικής συνοχής (η ενέργεια σύνδεσης σε σχέση με την ενέργεια των ουδέτερων ατόμων). Υψηλές τιμές ενέργειας σύνδεσης. Υψηλό σημείο τήξης. Καλοί μονωτές του ηλεκτρισμού. Ενότητα Σ5.3
45 Ενέργειες ατομικής συνοχής ορισμένων ομοιοπολικών στερεών Ενότητα Σ5.3
46 Παράδειγμα ομοιοπολικού στερεού Διαμάντι Κάθε άτομο άνθρακα στον κρύσταλλο του διαμαντιού συνδέεται με ομοιοπολικό δεσμό με τέσσερα άλλα άτομα άνθρακα. Έτσι σχηματίζεται μια τετραεδρική δομή. Ενότητα Σ5.3
47 Δεύτερο παράδειγμα με άνθρακα Το μόριο buckminsterfullerene Ο άνθρακας σχηματίζει πολλούς διαφορετικούς τύπους δομών. Η μεγάλη κοίλη δομή της εικόνας είναι το μόριο buckminsterfullerene. Ενότητα Σ5.3
48 Μεταλλικά στερεά Γενικά, οι μεταλλικοί δεσμοί είναι ασθενέστεροι από τους ιοντικούς και τους ομοιοπολικούς δεσμούς. Τα εξωτερικά ηλεκτρόνια των ατόμων ενός μετάλλου κινούνται σχετικά ελεύθερα στο υλικό. Το πλήθος αυτών των ελεύθερα κινούμενων ηλεκτρονίων είναι μεγάλο. Ενότητα Σ5.3
49 Μεταλλικά στερεά (συνέχεια) Η μεταλλική δομή μπορεί να εκληφθεί ως μια «θάλασσα» ή ένα «αέριο» από σχεδόν ελεύθερα ηλεκτρόνια, τα οποία περιβάλλουν ένα πλέγμα θετικών ιόντων. Ο μηχανισμός σχηματισμού δεσμών στα μέταλλα είναι η ελκτική δύναμη μεταξύ του συνόλου των θετικών ιόντων και του «αερίου» των ηλεκτρονίων. Ενότητα Σ5.3
50 Ιδιότητες των μεταλλικών στερεών Το φως αλληλεπιδρά έντονα με τα ελεύθερα ηλεκτρόνια των μετάλλων. Το ορατό φως απορροφάται και επανεκπέμπεται πολύ κοντά στην επιφάνεια των μετάλλων. Αυτό εξηγεί τη λάμψη των μεταλλικών επιφανειών. Υψηλή ηλεκτρική αγωγιμότητα Ο μεταλλικός δεσμός κατευθύνεται προς κάθε δυνατή διεύθυνση. Αυτό επιτρέπει σε πολλούς διαφορετικούς τύπους ατόμων μετάλλων να διασκορπίζονται μέσα σε άλλα μέταλλα σε διάφορες αναλογίες. Με αυτόν τον τρόπο, μπορούμε να παράγουμε στερεά διαλύματα, ή κράματα, σχεδιασμένα να έχουν συγκεκριμένες ιδιότητες. Τα μέταλλα κάμπτονται όταν υφίστανται μηχανική τάση. Επειδή οι δεσμοί στα μέταλλα σχηματίζονται μεταξύ όλων των ηλεκτρονίων και όλων των θετικών ιόντων. Ενότητα Σ5.3
51 Η θεωρία των ελεύθερων ηλεκτρονίων των μετάλλων Η κβαντική θεωρία των ελεύθερων ηλεκτρονίων ηλεκτρικής αγωγιμότητας των μετάλλων λαμβάνει υπόψη την κυματική φύση των ηλεκτρονίων. Σε αυτό το μοντέλο, τα ηλεκτρόνια της εξωτερικής στιβάδας κινούνται ελεύθερα στο μέταλλο, αλλά είναι εγκλωβισμένα στο τριδιάστατο κουτί που σχηματίζουν οι επιφάνειες του μετάλλου. Επομένως, κάθε ηλεκτρόνιο παριστάνεται ως σωματίδιο σε κουτί. Ενότητα Σ5.4
52 Συνάρτηση κατανομής Fermi-Dirac Εφαρμόζοντας τις αρχές της στατιστικής φυσικής σε ένα σύνολο σωματιδίων, μπορούμε να συσχετίσουμε ιδιότητες μικροσκοπικής κλίμακας με χαρακτηριστικά που εμφανίζονται σε μακροσκοπική κλίμακα. Στην περίπτωση των ηλεκτρονίων, σύμφωνα με την κβαντική στατιστική, κάθε κατάσταση του συστήματος μπορεί να καταλαμβάνεται μόνο από δύο ηλεκτρόνια. Η πιθανότητα κάποιο ηλεκτρόνιο ενός στερεού να βρίσκεται σε μια ορισμένη ενεργειακή κατάσταση με ενέργεια E είναι: ƒ( E) 1 ( E EF ) kbt e 1 ƒ(e) είναι η συνάρτηση κατανομής Fermi-Dirac. E F είναι η ενέργεια Fermi. Ενότητα Σ5.4
53 Η συνάρτηση κατανομής Fermi-Dirac για T = 0 Για T = 0, όλες οι καταστάσεις με ενέργεια μικρότερη της ενέργειας Fermi είναι κατειλημμένες. Όλες οι καταστάσεις με ενέργεια μεγαλύτερη της ενέργειας Fermi είναι κενές. Ενότητα Σ5.4
54 Η συνάρτηση κατανομής Fermi-Dirac για T > 0 Καθώς αυξάνεται η θερμοκρασία, T, η κατανομή γίνεται λίγο πιο ομαλή. Λόγω της θερμικής διέγερσης: Σε καταστάσεις με ενέργεια παραπλήσια της E F αλλά μικρότερη από αυτήν, ο πληθυσμός μειώνεται. Σε καταστάσεις με ενέργεια παραπλήσια της E F αλλά μεγαλύτερη από αυτήν, ο πληθυσμός αυξάνεται. Η ενέργεια Fermi, E F, εξαρτάται και από τη θερμοκρασία, αλλά αυτή η εξάρτηση είναι ασθενής στα μέταλλα. Ενότητα Σ5.4
55 Ηλεκτρόνιο ως σωματίδιο σε τρισδιάστατο κουτί
56 Το ηλεκτρόνιο ως σωματίδιο σε τριδιάστατο κουτί Οι ενεργειακές στάθμες των ηλεκτρονίων είναι πολύ κοντά η μία στην άλλη. Η συνάρτηση πυκνότητας καταστάσεων δίνει το πλήθος των επιτρεπτών καταστάσεων ανά μονάδα όγκου, οι οποίες έχουν τιμές ενέργειας μεταξύ E και E + de: 8 2πm h 32 e 12 g( E) de E de 3 Ενότητα Σ5.4
57 Πυκνότητα ηλεκτρονίων και ενέργεια Fermi
58 Συνάρτηση κατανομής ηλεκτρονίων ως προς την ενέργεια
59 Η ενέργεια Fermi σε θερμοκρασία T = 0 K Η ενέργεια Fermi στους T = 0 K είναι: E F (0) 2 h 3ne 2m 8π e 23 Οι τιμές της ενέργειας Fermi των μετάλλων είναι της τάξης των μερικών ev. Η μέση τιμή της ενέργειας ενός ελεύθερου ηλεκτρονίου σε ένα μέταλλο στους 0 K είναι: E μέση = (3/5) E F. Ενότητα Σ5.4
60 Tιμές της ενέργειας Fermi για μερικά μέταλλα Ενότητα Σ5.4
61 Μέταλλα Σύνοψη Μπορούμε να θεωρούμε τα μέταλλα ως συστήματα με έναν πολύ μεγάλο αριθμό διαθέσιμων ενεργειακών σταθμών για τα ελεύθερα ηλεκτρόνια. Αυτά τα ηλεκτρόνια συμπληρώνουν τις στάθμες όπως ορίζει η απαγορευτική αρχή του Pauli. Ξεκινώντας από την κατάσταση E = 0 και καταλήγοντας στην E F. Σε θερμοκρασία T = 0 K, όλες οι στάθμες με ενέργεια μικρότερη από την ενέργεια Fermi είναι συμπληρωμένες και όλες οι στάθμες με ενέργεια μεγαλύτερη από την ενέργεια Fermi είναι κενές. Στους 300 K, ένα μικρό ποσοστό των ελεύθερων ηλεκτρονίων είναι διεγερμένα σε ενέργεια μεγαλύτερη από την ενέργεια Fermi. Ενότητα Σ5.4
62 Κυματοσυναρτήσεις στερεών Για να είναι το μοντέλο που περιγράφει τα μέταλλα πιο πλήρες, πρέπει να λάβουμε υπόψη τη συνεισφορά των γονικών ατόμων που σχηματίζουν τον κρύσταλλο. Για ένα άτομο με ατομικό αριθμό Z, το οποίο έχει ένα ηλεκτρόνιο στην υποστιβάδα s έξω από μια συμπληρωμένη στιβάδα, είναι αποδεκτές οι ακόλουθες δύο κυματοσυναρτήσεις: Zr nαo ψ ( r ) Aƒ( r ) e ψ ( r ) Aƒ( r ) e s A είναι η σταθερά κανονικοποίησης. Zr nα ƒ(r) είναι μια συνάρτηση της μεταβλητής r, η οποία μεταβάλλεται με το n. Είτε επιλέξουμε τη μία, είτε την άλλη κυματοσυνάρτηση, θα καταλήξουμε στην ίδια τιμή ψ ², οπότε οι δύο επιλογές είναι ισοδύναμες. Ωστόσο, όταν ενώνονται δύο άτομα, προκύπτει μια διαφοροποίηση. s o Ενότητα Σ5.5
63 Συνδυασμός κυματοσυναρτήσεων Οι κυματοσυναρτήσεις μπορούν να συνδυαστούν όπως παρουσιάζεται στην εικόνα. Ο συνδυασμός Ψ s + (r) + Ψ s + (r) είναι ισοδύναμος με τον συνδυασμό Ψ s (r) + Ψ s (r). Αυτοί οι δύο πιθανοί συνδυασμοί κυματοσυναρτήσεων αντιστοιχούν σε δύο πιθανές καταστάσεις του συστήματος των δύο ατόμων. Ενότητα Σ5.5
64
65 Διαχωρισμός των καταστάσεων σε στάθμες (1) Λόγω των δύο τρόπων συνδυασμού των κυματοσυναρτήσεων, οι καταστάσεις χωρίζονται σε δύο ενεργειακές στάθμες. Η διαφορά ενέργειας είναι σχετικά μικρή, γι αυτό και οι δύο καταστάσεις είναι αρκετά κοντά η μία στην άλλη σε ενεργειακή κλίμακα. Για μεγάλες τιμές της απόστασης r, τα ηλεκτρονικά νέφη δεν παρουσιάζουν αλληλοεπικαλύψεις και δεν γίνεται διαχωρισμός της ενεργειακής στάθμης. Ενότητα Σ5.5
66 Διαχωρισμός των καταστάσεων σε στάθμες (2) Όσο αυξάνεται ο αριθμός των ατόμων, τόσο αυξάνεται ο αριθμός των πιθανών συνδυασμών των κυματοσυναρτήσεων. Κάθε συνδυασμός αντιστοιχεί σε διαφορετική ενεργειακή στάθμη. Ενότητα Σ5.5
67 Διαχωρισμός των καταστάσεων σε στάθμες (τελική διαφάνεια) Αν επεκτείνουμε τον συλλογισμό μας στο μεγάλο πλήθος ατόμων των στερεών, τότε παίρνουμε έναν μεγάλο αριθμό διαφορετικών ενεργειακών σταθμών. Αυτές οι στάθμες βρίσκονται τόσο κοντά η μία στην άλλη ώστε να μπορούμε να τις θεωρήσουμε ως μια συνεχή ζώνη. Ενότητα Σ5.5
68 Οι ενεργειακές ζώνες ενός κρυστάλλου Γενικά, ένα κρυσταλλικό στερεό έχει μεγάλο αριθμό επιτρεπτών ενεργειακών ζωνών. Οι λευκές περιοχές του σχήματος είναι ενεργειακά χάσματα, τα οποία αντιστοιχούν σε απαγορευμένες ενέργειες. Κάποιες ζώνες αλληλοεπικαλύπτονται. Σε αυτό το παράδειγμα του νατρίου, οι συμπληρωμένες ζώνες παρουσιάζονται με μπλε χρώμα, ενώ οι κενές ζώνες με κίτρινο χρώμα. Η θεωρία των ζωνών μας επιτρέπει να δημιουργήσουμε απλά μοντέλα ώστε να κατανοήσουμε τη συμπεριφορά υλικών που είναι αγωγοί ή μονωτές του ηλεκτρισμού, καθώς και των ημιαγώγιμων υλικών. Ενότητα Σ5.5
69 Ηλεκτρική αγωγιμότητα Κατηγορίες υλικών Οι καλοί αγωγοί του ηλεκτρισμού έχουν μεγάλη αριθμητική πυκνότητα ελεύθερων φορέων φορτίου. Στους μονωτές η αντίστοιχη αριθμητική πυκνότητα είναι σχεδόν μηδενική. Οι ημιαγωγοί είναι υλικά με αριθμητικές πυκνότητες φορτίου που βρίσκονται μεταξύ εκείνων των μονωτών και των αγωγών. Μπορούμε να μελετήσουμε τους μηχανισμούς αγωγιμότητας σε καθεμιά από αυτές τις τρεις κατηγορίες υλικών, χρησιμοποιώντας ένα μοντέλο βασισμένο στη θεωρία των ενεργειακών ζωνών. Ενότητα Σ5.6
70 Μέταλλα Για να είναι ένα υλικό καλός αγωγός του ηλεκτρισμού, οι φορείς φορτίου που υπάρχουν σε αυτό πρέπει να έχουν τη δυνατότητα να κινούνται ελεύθερα υπό την επίδραση ενός ηλεκτρικού πεδίου. Θα εξετάσουμε ως φορείς φορτίου τα ηλεκτρόνια ενός μετάλλου. Η κίνηση των ηλεκτρονίων υπό την επίδραση ενός ηλεκτρικού πεδίου αντιπροσωπεύει αύξηση της ενέργειας του συστήματος. Όταν εφαρμόζεται ηλεκτρικό πεδίο σε έναν αγωγό, τα ηλεκτρόνια πρέπει να μεταπέσουν σε μια ανώτερη διαθέσιμη ενεργειακή κατάσταση. Ενότητα Σ5.6
71 Μέταλλα Ενεργειακές ζώνες Σε θερμοκρασία T = 0 K, η ενέργεια Fermi, E F, βρίσκεται στο μέσο της ζώνης. Όλες οι στάθμες με ενέργεια μικρότερη από την ενέργεια E F είναι συμπληρωμένες, ενώ όλες οι στάθμες με ενέργεια μεγαλύτερη από την ενέργεια E F είναι κενές. Αν εφαρμοστεί στο μέταλλο μια διαφορά δυναμικού, τότε τα ηλεκτρόνια με ενέργειες κοντά στην ενέργεια E F χρειάζονται λίγη μόνο επιπλέον ενέργεια από το εφαρμοζόμενο ηλεκτρικό πεδίο προκειμένου να φτάσουν σε γειτονικές, κενές καταστάσεις, με ενέργεια μεγαλύτερη από την ενέργεια Fermi. Ενότητα Σ5.6
72 Τα μέταλλα ως καλοί αγωγοί Όταν σε ένα μέταλλο εφαρμόζεται ακόμα και ένα ασθενές ηλεκτρικό πεδίο, τα ηλεκτρόνιά του κινούνται ελεύθερα, επειδή κοντά στις κατειλημμένες ενεργειακές στάθμες υπάρχουν διαθέσιμες πολλές άλλες κενές στάθμες. Αυτό δείχνει ότι τα μέταλλα αποτελούν εξαιρετικούς αγωγούς του ηλεκτρισμού. Ενότητα Σ5.6
73 Μονωτές Δεν υπάρχουν ενεργειακά κοντινές διαθέσιμες καταστάσεις, στις οποίες να μπορούν να «προβιβαστούν» ηλεκτρόνια με την επιπλέον κινητική ενέργεια που σχετίζεται με την κίνηση στο υλικό υπό την επίδραση ηλεκτρικού πεδίου. Παρότι οι μονωτές διαθέτουν πολλές μη κατειλημμένες καταστάσεις στη ζώνη αγωγιμότητάς τους, μεσολαβεί μεγάλο ενεργειακό χάσμα μεταξύ αυτών των καταστάσεων και των συμπληρωμένων καταστάσεων. Τις υψηλότερες καταστάσεις καταλαμβάνουν λίγα μόνο ηλεκτρόνια, γι αυτό και συνολικά η ηλεκτρική αγωγιμότητα των μονωτών είναι πολύ μικρή. Ενότητα Σ5.6
74 Μονωτές Ενεργειακές ζώνες Σε θερμοκρασία T = 0, η ζώνη σθένους είναι συμπληρωμένη και η ζώνη αγωγιμότητας είναι κενή. Η ενέργεια Fermi βρίσκεται κάπου μέσα σε αυτό το ενεργειακό χάσμα. Σε θερμοκρασία περιβάλλοντος, πολύ λίγα ηλεκτρόνια διεγείρονται θερμικά ώστε να μεταπέσουν στη ζώνη αγωγιμότητας. Ενότητα Σ5.6
75 Ημιαγωγοί Οι ημιαγωγοί έχουν παρόμοια δομή ζωνών με τους μονωτές, αλλά το ενεργειακό χάσμα είναι πολύ μικρότερο. Στον πίνακα αναφέρονται οι τιμές του ενεργειακού χάσματος για ορισμένα χαρακτηριστικά υλικά. Ενότητα Σ5.6
76 Ημιαγωγοί Ενεργειακές ζώνες Αρκετά ηλεκτρόνια διεγείρονται θερμικά και μεταπίπτουν από τη ζώνη σθένους στη ζώνη αγωγιμότητας. Αρκεί μια μικρή διαφορά δυναμικού για να αυξηθεί η ενέργεια των ηλεκτρονίων και να ανέβουν στη ζώνη αγωγιμότητας. Ενότητα Σ5.6
77 Ημιαγωγοί Κίνηση των φορτίων Στους ημιαγωγούς, οι φορείς φορτίου μπορεί να είναι θετικοί, αρνητικοί ή και τα δύο. Όταν ένα ηλεκτρόνιο μεταπίπτει από τη ζώνη σθένους στη ζώνη αγωγιμότητας, αφήνει μια κενή θέση, μια οπή. Ενότητα Σ5.6
78 Ημιαγωγοί Κίνηση των φορτίων (συνέχεια) Οι οπές παίζουν τον ρόλο των φορέων φορτίου. Σε μια οπή μπορεί να μεταφερθεί ένα ελεύθερο ηλεκτρόνιο. Στη θέση που εγκαταλείπει, δημιουργείται μια νέα οπή. Επομένως, μπορούμε να θεωρήσουμε το τελικό αποτέλεσμα ως κίνηση της οπής στο υλικό, σε κατεύθυνση αντίθετη της κίνησης των ηλεκτρονίων. Η οπή συμπεριφέρεται σαν να ήταν σωματίδιο με θετικό φορτίο +e. Ενότητα Σ5.6
79 Ενδογενείς ημιαγωγοί Ένας αμιγής κρύσταλλος ημιαγωγού που αποτελείται από ένα μόνο χημικό στοιχείο ή μία χημική ένωση ονομάζεται ενδογενής ημιαγωγός. Το πλήθος των ηλεκτρονίων αγωγιμότητας είναι ίσο με το πλήθος των οπών. Αυτοί οι συνδυασμοί φορτίων ονομάζονται ζεύγη ηλεκτρονίων-οπών. Ενότητα Σ5.6
80 Εμπλουτισμένοι ημιαγωγοί Στους ημιαγωγούς μπορούν να προστεθούν προσμίξεις. Αυτή η διαδικασία ονομάζεται εμπλουτισμός. Ο εμπλουτισμός τροποποιεί τη δομή των ζωνών του ημιαγωγού, τροποποιεί την ειδική αντίσταση, μπορεί να χρησιμοποιηθεί για να ρυθμίσει την αγωγιμότητα του ημιαγωγού. Ενότητα Σ5.6
81 Ημιαγωγοί τύπου n Το άτομο του υλικού πρόσμιξης μπορεί να προσθέσει ένα ηλεκτρόνιο στη δομή του ημιαγωγού. Γι αυτόν τον λόγο, το άτομο του υλικού πρόσμιξης αναφέρεται ως άτομο-δότης. Οι ημιαγωγοί που είναι εμπλουτισμένοι με άτομα-δότες ονομάζονται ημιαγωγοί τύπου n. Ενότητα Σ5.6
82 Ημιαγωγοί τύπου n Ενεργειακές στάθμες Η ενεργειακή στάθμη του ηλεκτρονίου του ατόμου-δότη απέχει ελάχιστα από το κάτω όριο της ζώνης αγωγιμότητας. Γι αυτόν τον λόγο, το ηλεκτρόνιο χρειάζεται ελάχιστη θερμική διέγερση προκειμένου να μετακινηθεί στη ζώνη αγωγιμότητας. Ενότητα Σ5.6
83 Ημιαγωγοί τύπου p Το άτομο του υλικού πρόσμιξης μπορεί να προσθέσει μια οπή στη δομή του ημιαγωγού. Δηλαδή δημιουργείται έλλειμμα ηλεκτρονίων. Γι αυτόν τον λόγο, το άτομο του υλικού πρόσμιξης αναφέρεται ως άτομολήπτης. Οι ημιαγωγοί που είναι εμπλουτισμένοι με άτομα-λήπτες ονομάζονται ημιαγωγοί τύπου p. Ενότητα Σ5.6
84 Ημιαγωγοί τύπου p Ενεργειακές στάθμες Η ενεργειακή στάθμη της οπής απέχει ελάχιστα από το επάνω όριο της ζώνης σθένους. Με την προσθήκη ενός μικρού ποσού ενέργειας, ένα ηλεκτρόνιο από τη ζώνη σθένους μπορεί να καταλάβει την οπή. Έτσι δημιουργείται μια οπή στη ζώνη σθένους. Αν εφαρμοστεί ηλεκτρικό πεδίο, η οπή μπορεί να φέρει ρεύμα. Ενότητα Σ5.6
85 Εξωγενείς ημιαγωγοί Όταν η αγωγιμότητα ενός ημιαγωγού είναι αποτέλεσμα της πρόσμιξης ατόμων-δοτών ή ατόμων-ληπτών, τότε το υλικό λέγεται εξωγενής ημιαγωγός. Η αριθμητική πυκνότητα των προσμίξεων στους εξωγενείς ημιαγωγούς κυμαίνεται από έως cm 3. Η συνηθισμένη πυκνότητα ηλεκτρονίων σε έναν ημιαγωγό είναι περίπου cm 3. Ενότητα Σ5.6
86 Συσκευές ημιαγωγών Πολλές ηλεκτρονικές συσκευές βασίζονται στους ημιαγωγούς. Σε αυτές περιλαμβάνονται: η δίοδος ημιαγωγού, οι δίοδοι φωτοεκπομπής και φωτοαπορρόφησης, τα τρανζίστορ, τα ολοκληρωμένα κυκλώματα. Ενότητα Σ5.7
87 Δίοδος ημιαγωγού (1) Όταν ενώνεται ένας ημιαγωγός τύπου p με έναν ημιαγωγό τύπου n, τότε σχηματίζεται μια επαφή p-n. Η δίοδος ημιαγωγού είναι μια συσκευή που βασίζεται σε μία μόνο επαφή p- n. Ο ρόλος μιας διόδου είναι να επιτρέπει τη διέλευση του ρεύματος μόνο προς μία κατεύθυνση. Ενότητα Σ5.7
88 Δίοδος ημιαγωγού (2) Η επαφή p-n αποτελείται από τρεις ξεχωριστές περιοχές: την περιοχή p, την περιοχή n, και την περιοχή απογύμνωσης. Η περιοχή απογύμνωσης δημιουργείται από τη διάχυση των ηλεκτρονίων προκειμένου να συμπληρώσουν τις οπές. Μπορούμε να θεωρήσουμε ότι οι οπές που συμπληρώνονται διαχέονται στην περιοχή n. Ενότητα Σ5.7
89 Δίοδος ημιαγωγού (τελική διαφάνεια) Επειδή οι δύο πλευρές φέρουν ηλεκτρικό φορτίο, στην περιοχή απογύμνωσης υπάρχει ένα εσωτερικό ηλεκτρικό πεδίο. Αυτό το εσωτερικό ηλεκτρικό πεδίο δημιουργεί μια εσωτερική διαφορά δυναμικού που αποτρέπει την περαιτέρω διάχυση οπών και ηλεκτρονίων, και επομένως εξασφαλίζει την απουσία ρεύματος στην επαφή όταν δεν εφαρμόζεται κάποια εξωτερική διαφορά δυναμικού. Ενότητα Σ5.7
90 Δίοδος ημιαγωγού Πόλωση Μια δίοδος είναι ορθά πολωμένη όταν η πλευρά p είναι συνδεδεμένη με τον θετικό πόλο της μπαταρίας. Έτσι μειώνεται η εσωτερική διαφορά δυναμικού, με αποτέλεσμα να δημιουργηθεί ρεύμα το οποίο αυξάνεται εκθετικά με την τάση. Μια δίοδος είναι αντίστροφα πολωμένη όταν η πλευρά n είναι συνδεδεμένη με τον θετικό πόλο της μπαταρίας. Έτσι αυξάνεται η εσωτερική διαφορά δυναμικού, με αποτέλεσμα να δημιουργηθεί ένα ασθενές ρεύμα αντίθετης φοράς, το οποίο φτάνει γρήγορα σε μια τιμή κορεσμού. Σε μια ιδανική δίοδο, η τάση και το ρεύμα συνδέονται με τη σχέση: I I e o e V k T B 1 Ενότητα Σ5.7
91 Δίοδος ημιαγωγού Πόλωση και χαρακτηριστική καμπύλη I- V Ενότητα Σ5.7
92 Δίοδοι φωτοεκπομπής και φωτοαπορρόφησης Οι μηχανισμοί εκπομπής και απορρόφησης φωτός στους ημιαγωγούς μοιάζουν με εκείνους στα άτομα των αερίων, αλλά στη μελέτη των ημιαγωγών βασιζόμαστε στην έννοια των ενεργειακών ζωνών. Ένα ηλεκτρόνιο που έχει μεταπέσει στη ζώνη αγωγιμότητας λόγω ηλεκτρικής διέγερσης μπορεί εύκολα να ανασυνδυαστεί με μια οπή της ζώνης σθένους, εκπέμπτοντας ταυτόχρονα ένα φωτόνιο. Ένα ηλεκτρόνιο στη ζώνη σθένους μπορεί να απορροφήσει ένα εισερχόμενο φωτόνιο και να προβιβαστεί στη ζώνη αγωγιμότητας, αφήνοντας πίσω του μια οπή. Ενότητα Σ5.7
93
94 Τρανζίστορ Το τρανζίστορ επαφής αποτελείται από δύο επαφές p-n. Μια στενή περιοχή τύπου n μεταξύ δύο περιοχών τύπου p ή μια στενή περιοχή τύπου p μεταξύ δύο περιοχών τύπου n. Το τρανζίστορ μπορεί να χρησιμοποιηθεί ως ενισχυτής διακόπτης Ενότητα Σ5.7
95 Ολοκληρωμένα κυκλώματα Το ολοκληρωμένο κύκλωμα είναι ένα σύνολο διασυνδεδεμένων τρανζίστορ, διόδων, αντιστατών, και πυκνωτών που έχουν ενσωματωθεί σε ένα μόνο τεμάχιο πυριτίου, το οποίο ονομάζεται τσιπ. Τα ολοκληρωμένα κυκλώματα Έδωσαν λύση στο πρόβλημα της διασύνδεσης του μεγάλου πλήθους εξαρτημάτων των σύγχρονων ηλεκτρονικών συσκευών. Διαθέτουν τα πλεονεκτήματα του εξαιρετικά μικρού μεγέθους και της ταχείας απόκρισης. Ενότητα Σ5.7
96 Υπεραγωγοί Οι υπεραγωγοί είναι μια κατηγορία μετάλλων και ενώσεων των οποίων η αντίσταση μειώνεται στο μηδέν όταν η θερμοκρασία τους πέσει κάτω από μια ορισμένη τιμή T c. Η θερμοκρασία T c ονομάζεται κρίσιμη θερμοκρασία. Σε θερμοκρασίες μεγαλύτερες της T c, το γράφημα μοιάζει με εκείνο ενός απλού μετάλλου, αλλά στη θερμοκρασία T c μηδενίζεται απότομα. Ενότητα Η5.5
97 Υπεραγωγοί (συνέχεια) Η τιμή της κρίσιμης θερμοκρασίας T c εξαρτάται από: τη χημική σύσταση την πίεση τη μοριακή δομή Από τη στιγμή που δημιουργηθεί ρεύμα σε έναν υπεραγωγό, τότε το ρεύμα αυτό παραμένει χωρίς να απαιτείται η εφαρμογή εξωτερικής τάσης. Επειδή R = 0. Ενότητα Η5.5
98 Εφαρμογές των υπεραγωγών Μια σημαντική εφαρμογή των υπεραγωγών είναι ο υπεραγώγιμος μαγνήτης. Το μέτρο του μαγνητικού πεδίου ενός υπεραγώγιμου μαγνήτη είναι περίπου δεκαπλάσιο από εκείνο που παράγει ένας απλός ηλεκτρομαγνήτης. Οι υπεραγώγιμοι μαγνήτες έχουν προταθεί ως μέσα αποθήκευσης ενέργειας. Χρησιμοποιούνται σε ιατρικούς μαγνητικούς τομογράφους. Ενότητα Η5.5
99 Το φαινόμενο Meissner Ορισμένοι τύποι υπεραγωγών παρουσιάζουν επίσης τέλειες διαμαγνητικές ιδιότητες όταν βρίσκονται σε κατάσταση υπεραγωγιμότητας. Αυτό ονομάζεται φαινόμενο Meissner. Αν ένας μόνιμος μαγνήτης βρεθεί κοντά σε κάποιον υπεραγωγό, τότε ο μαγνήτης και ο υπεραγωγός απωθούνται. Ενότητα Η8.6
100 Υπεραγωγιμότητα Ένας υπεραγωγός αποβάλλει τα μαγνητικά πεδία σχηματίζοντας επιφανειακά ρεύματα. Στην επιφάνεια του υπεραγωγού επάγονται ρεύματα, τα οποία παράγουν ένα μαγνητικό πεδίο που εξουδετερώνει πλήρως στο εσωτερικό του υπεραγωγού το εξωτερικά εφαρμοζόμενο πεδίο. Τα επιφανειακά ρεύματα εξαφανίζονται όταν παύει να εφαρμόζεται το εξωτερικό μαγνητικό πεδίο. Ενότητα Σ5.8
101
102 Υπεραγωγιμότητα και ζεύγη Cooper Όταν δύο ηλεκτρόνια αλληλεπιδρούν μέσω παραμορφώσεων του ιοντικού πλέγματος, με τρόπο που να αναπτύσσεται μεταξύ τους μια συνισταμένη ελκτική δύναμη, τότε σχηματίζεται το λεγόμενο ζεύγος Cooper. Τα ζεύγη Cooper συμπεριφέρονται ως μποζόνια και δεν υπακούουν στην απαγορευτική αρχή. Τα μποζόνια είναι σωματίδια με ακέραιο σπιν. Όλα τα ζεύγη Cooper ενός μετάλλου περιγράφονται από μία και μοναδική κυματοσυνάρτηση. Υπό την επίδραση ενός εφαρμοζόμενου ηλεκτρικού πεδίου, τα ζεύγη Cooper δέχονται μια ηλεκτρική δύναμη και κινούνται μέσα στο μέταλλο. Τα ζεύγη Cooper κινούνται ελεύθερα. Βρίσκονται στη χαμηλότερη δυνατή ενεργειακή κατάσταση. Δεν υπάρχουν άλλες διαθέσιμες ενεργειακές καταστάσεις επάνω από την ενεργειακή στάθμη των ζευγών Cooper λόγω του ενεργειακού χάσματος. Ενότητα Σ5.8
103 Υπεραγωγιμότητα Κρίσιμη θερμοκρασία Κρίσιμη θερμοκρασία ονομάζεται η θερμοκρασία στην οποία η ηλεκτρική αντίσταση ενός υλικού πρακτικά μηδενίζεται. Ανακαλύφθηκε μια οικογένεια ενώσεων που παρουσιάζουν υπεραγώγιμη συμπεριφορά σε «υψηλές» θερμοκρασίες. Ανακαλύφθηκαν το Έχουν αναφερθεί ισχυρές ενδείξεις υπεραγωγιμότητας στους 30 K. Έχουν ανακαλυφθεί υλικά αποτελούμενα από οξείδια στοιχείων, στα οποία έχει αναφερθεί υπεραγωγιμότητα στους 150 K. Το 2006, επιστήμονες παρατήρησαν το φαινόμενο της υπεραγωγιμότητας σε υλικά που έχουν ως βάση τον σίδηρο. Η υψηλότερη κρίσιμη θερμοκρασία που έχει αναφερθεί μέχρι τώρα σε υλικά με βάση τον σίδηρο είναι οι 55 K. Προς το παρόν δεν υπάρχει αντίστοιχη ευρέως αποδεκτή θεωρία, η οποία να εξηγεί την υπεραγωγιμότητα σε υψηλές θερμοκρασίες. Ενότητα Σ5.8
104 Υπεραγώγιμοι μαγνήτες σε συστήματα Απεικόνισης Μαγνητικού Συντονισμού-MRI
Κεφάλαια (από το βιβλίο Serway-Jewett) και αναρτημένες παρουσιάσεις
 Ύλη μαθήματος «Σύγχρονη Φυσική» Κεφάλαια (από το βιβλίο Serway-Jewett) και αναρτημένες παρουσιάσεις Σ2-Σελίδες: 673-705, (όλο το κεφάλαιο από το βιβλίο) και η παρουσίαση Σ2 που έχει αναρτηθεί στο e-class
Ύλη μαθήματος «Σύγχρονη Φυσική» Κεφάλαια (από το βιβλίο Serway-Jewett) και αναρτημένες παρουσιάσεις Σ2-Σελίδες: 673-705, (όλο το κεφάλαιο από το βιβλίο) και η παρουσίαση Σ2 που έχει αναρτηθεί στο e-class
ηλεκτρικό ρεύμα ampere
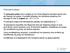 Ηλεκτρικό ρεύμα Το ηλεκτρικό ρεύμα είναι ο ρυθμός με τον οποίο διέρχεται ηλεκτρικό φορτίο από μια περιοχή του χώρου. Η μονάδα μέτρησης του ηλεκτρικού ρεύματος στο σύστημα SI είναι το ampere (A). 1 A =
Ηλεκτρικό ρεύμα Το ηλεκτρικό ρεύμα είναι ο ρυθμός με τον οποίο διέρχεται ηλεκτρικό φορτίο από μια περιοχή του χώρου. Η μονάδα μέτρησης του ηλεκτρικού ρεύματος στο σύστημα SI είναι το ampere (A). 1 A =
Διάλεξη 7: Μοριακή Δομή
 Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια Γιατί; Διότι η ολική ενέργεια ενός ευσταθούς μορίου είναι μικρότερη από την ολική ενέργεια των μεμονωμένων ατόμων που αποτελούν
7.a. Οι δεσμοί στα στερεά
 ΤΕΤΥ Σύγχρονη Φυσική Κεφ. 7-1 Κεφάλαιο 7. Στερεά Εδάφια: 7.a. Οι δεσμοί στα στερεά 7.b. Η θεωρία των ενεργειακών ζωνών 7.c. Νόθευση ημιαγωγών και εφαρμογές 7.d. Υπεραγωγοί 7.a. Οι δεσμοί στα στερεά Με
ΤΕΤΥ Σύγχρονη Φυσική Κεφ. 7-1 Κεφάλαιο 7. Στερεά Εδάφια: 7.a. Οι δεσμοί στα στερεά 7.b. Η θεωρία των ενεργειακών ζωνών 7.c. Νόθευση ημιαγωγών και εφαρμογές 7.d. Υπεραγωγοί 7.a. Οι δεσμοί στα στερεά Με
Δομή ενεργειακών ζωνών
 Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
Ατομικό πρότυπο του Bohr Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Βασικές αρχές του προτύπου Bohr Θετικά φορτισμένος
ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ
 Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Τμήμα Τεχνολόγων Περιβάλλοντος Κατεύθυνσης Συντήρησης Πολιτισμικής Κληρονομιάς ΤΕΧΝΟΛΟΓΙΑ & ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 3 η Ενότητα ΔΕΣΜΟΙ Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια
Υλικά Ηλεκτρονικής & Διατάξεις
 Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Τμήμα Ηλεκτρονικών Μηχανικών Υλικά Ηλεκτρονικής & Διατάξεις 2 η σειρά διαφανειών Δημήτριος Λαμπάκης ΜΟΡΙΑΚΗ ΔΟΜΗ Μεμονωμένα άτομα: Μόνο τα ευγενή αέρια Μόρια: Τα υπόλοιπα άτομα σχηματίζουν μόρια, γιατί
Σχ. 1: Τυπική μορφή μοριακού δυναμικού.
 ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-1 Κεφάλαιο 6. Μόρια Εδάφια: 6.a. Μόρια και μοριακοί δεσμοί 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού 6.c. Περιστροφή και ταλάντωση μορίων 6.d. Μοριακά φάσματα 6.a.
ΤΕΤΥ - Σύγχρονη Φυσική Κεφ. 6-1 Κεφάλαιο 6. Μόρια Εδάφια: 6.a. Μόρια και μοριακοί δεσμοί 6.b. Κβαντομηχανική περιγραφή του χημικού δεσμού 6.c. Περιστροφή και ταλάντωση μορίων 6.d. Μοριακά φάσματα 6.a.
ηλεκτρικό ρεύµα ampere
 Ηλεκτρικό ρεύµα Το ηλεκτρικό ρεύµα είναι ο ρυθµός µε τον οποίο διέρχεται ηλεκτρικό φορτίο από µια περιοχή του χώρου. Η µονάδα µέτρησης του ηλεκτρικού ρεύµατος στο σύστηµα SI είναι το ampere (A). 1 A =
Ηλεκτρικό ρεύµα Το ηλεκτρικό ρεύµα είναι ο ρυθµός µε τον οποίο διέρχεται ηλεκτρικό φορτίο από µια περιοχή του χώρου. Η µονάδα µέτρησης του ηλεκτρικού ρεύµατος στο σύστηµα SI είναι το ampere (A). 1 A =
ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ
 ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ Ενεργειακές Ζώνες και Στατιστική Φορέων Φορτίου Required Text: Microelectronic Devices, Keith Leaver (2 nd Chapter) Εισαγωγή Στο προηγούμενο κεφάλαιο προσεγγίσαμε τους ημιαγωγούς
ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ Ενεργειακές Ζώνες και Στατιστική Φορέων Φορτίου Required Text: Microelectronic Devices, Keith Leaver (2 nd Chapter) Εισαγωγή Στο προηγούμενο κεφάλαιο προσεγγίσαμε τους ημιαγωγούς
ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ
 ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ Ενεργειακές Ζώνες και Στατιστική Φορέων Φορτίου Required Text: Microelectronic Devices, Keith Leaver (2 nd Chapter) Εισαγωγή Στο προηγούμενο κεφάλαιο προσεγγίσαμε τους ημιαγωγούς
ΑΡΧΕΣ ΗΛΕΚΤΡΟΝΙΚΩΝ ΣΤΟΙΧΕΙΩΝ Ενεργειακές Ζώνες και Στατιστική Φορέων Φορτίου Required Text: Microelectronic Devices, Keith Leaver (2 nd Chapter) Εισαγωγή Στο προηγούμενο κεφάλαιο προσεγγίσαμε τους ημιαγωγούς
1.1 Ηλεκτρονικές ιδιότητες των στερεών. Μονωτές και αγωγοί
 1. Εισαγωγή 1.1 Ηλεκτρονικές ιδιότητες των στερεών. Μονωτές και αγωγοί Από την Ατομική Φυσική είναι γνωστό ότι οι επιτρεπόμενες ενεργειακές τιμές των ηλεκτρονίων είναι κβαντισμένες, όπως στο σχήμα 1. Σε
1. Εισαγωγή 1.1 Ηλεκτρονικές ιδιότητες των στερεών. Μονωτές και αγωγοί Από την Ατομική Φυσική είναι γνωστό ότι οι επιτρεπόμενες ενεργειακές τιμές των ηλεκτρονίων είναι κβαντισμένες, όπως στο σχήμα 1. Σε
ΤΕΧΝΟΛΟΓΙΑ ΥΛΙΚΩΝ ΜΑΘΗΜΑ 1 Ο ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ. Δρ. M.Χανιάς Αν.Καθηγητής Τμήμα Ηλεκτρολόγων Μηχανικών ΤΕ, ΤΕΙ Ανατολικής Μακεδονίας και Θράκης
 ΤΕΧΝΟΛΟΓΙΑ ΥΛΙΚΩΝ ΜΑΘΗΜΑ 1 Ο ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Δρ. M.Χανιάς Αν.Καθηγητής Τμήμα Ηλεκτρολόγων Μηχανικών ΤΕ, ΤΕΙ Ανατολικής Μακεδονίας και Θράκης ΚΑΒΑΛΑ 018 1 1. ΕΙΣΑΓΩΓΗ ΣΤΑ ΥΛΙΚΑ. ΑΓΩΓΙΜΑ ΥΛΙΚΑ 3. ΗΜΙΑΓΩΓΟΙ
ΤΕΧΝΟΛΟΓΙΑ ΥΛΙΚΩΝ ΜΑΘΗΜΑ 1 Ο ΙΔΙΟΤΗΤΕΣ ΥΛΙΚΩΝ Δρ. M.Χανιάς Αν.Καθηγητής Τμήμα Ηλεκτρολόγων Μηχανικών ΤΕ, ΤΕΙ Ανατολικής Μακεδονίας και Θράκης ΚΑΒΑΛΑ 018 1 1. ΕΙΣΑΓΩΓΗ ΣΤΑ ΥΛΙΚΑ. ΑΓΩΓΙΜΑ ΥΛΙΚΑ 3. ΗΜΙΑΓΩΓΟΙ
Μοριακή Φασματοσκοπία I. Παραδόσεις μαθήματος Θ. Λαζαρίδης
 Μοριακή Φασματοσκοπία I Παραδόσεις μαθήματος Θ. Λαζαρίδης 2 Τι μελετά η μοριακή φασματοσκοπία; Η μοριακή φασματοσκοπία μελετά την αλληλεπίδραση των μορίων με την ηλεκτρομαγνητική ακτινοβολία Από τη μελέτη
Μοριακή Φασματοσκοπία I Παραδόσεις μαθήματος Θ. Λαζαρίδης 2 Τι μελετά η μοριακή φασματοσκοπία; Η μοριακή φασματοσκοπία μελετά την αλληλεπίδραση των μορίων με την ηλεκτρομαγνητική ακτινοβολία Από τη μελέτη
κυματικής συνάρτησης (Ψ) κυματική συνάρτηση
 Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
Στην κβαντομηχανική ο χώρος μέσα στον οποίο κινείται το ηλεκτρόνιο γύρω από τον πυρήνα παύει να περιγράφεται από μια απλή τροχιά, χαρακτηριστικό του μοντέλου του Bohr, αλλά περιγράφεται ο χώρος μέσα στον
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ Ένα σημαντικό αποτέλεσμα της κβαντομηχανικής θεωρίας είναι ότι τα μόρια, όχι μόνο βρίσκονται σε διακριτές ενεργειακές
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες ΕΦΑΡΜΟΓΗ ΣΤΑ ΦΑΣΜΑΤΑ Ένα σημαντικό αποτέλεσμα της κβαντομηχανικής θεωρίας είναι ότι τα μόρια, όχι μόνο βρίσκονται σε διακριτές ενεργειακές
Οι ηµιαγωγοι αποτελουν την πλεον χρησιµη κατηγορια υλικων απο ολα τα στερεα για εφαρµογες στα ηλεκτρονικα.
 Οι ηµιαγωγοι αποτελουν την πλεον χρησιµη κατηγορια υλικων απο ολα τα στερεα για εφαρµογες στα ηλεκτρονικα. Οι ηµιαγωγοι εχουν ηλεκτρικη ειδικη αντισταση (ή ηλεκτρικη αγωγιµοτητα) που κυµαινεται µεταξυ
Οι ηµιαγωγοι αποτελουν την πλεον χρησιµη κατηγορια υλικων απο ολα τα στερεα για εφαρµογες στα ηλεκτρονικα. Οι ηµιαγωγοι εχουν ηλεκτρικη ειδικη αντισταση (ή ηλεκτρικη αγωγιµοτητα) που κυµαινεται µεταξυ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Σύγxρονη Φυσική II. Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική II Μοριακή Δομή Ι Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που
 ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
Ξεκινώντας από την εξίσωση Poisson για το δυναμικό V στο στατικό ηλεκτρικό πεδίο:
 1 2. Διοδος p-n 2.1 Επαφή p-n Στο σχήμα 2.1 εικονίζονται δύο μέρη ενός ημιαγωγού με διαφορετικού τύπου αγωγιμότητες. Αριστερά ο ημιαγωγός είναι p-τύπου και δεξια n-τύπου. Και τα δύο μέρη είναι ηλεκτρικά
1 2. Διοδος p-n 2.1 Επαφή p-n Στο σχήμα 2.1 εικονίζονται δύο μέρη ενός ημιαγωγού με διαφορετικού τύπου αγωγιμότητες. Αριστερά ο ημιαγωγός είναι p-τύπου και δεξια n-τύπου. Και τα δύο μέρη είναι ηλεκτρικά
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Αγωγιμότητα στα μέταλλα
 Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Μάθημα 23 ο. Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις
 Μάθημα 23 ο Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις Μεταλλικός Δεσμός Μοντέλο θάλασσας ηλεκτρονίων Πυρήνες σε θάλασσα e -. Μεταλλική λάμψη. Ολκιμότητα. Εφαρμογή δύναμης Γενική και
Μάθημα 23 ο Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις Μεταλλικός Δεσμός Μοντέλο θάλασσας ηλεκτρονίων Πυρήνες σε θάλασσα e -. Μεταλλική λάμψη. Ολκιμότητα. Εφαρμογή δύναμης Γενική και
Ασκήσεις Φασµατοσκοπίας
 Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
αγωγοί ηµιαγωγοί µονωτές Σχήµα 1
 Η2 Μελέτη ηµιαγωγών 1. Σκοπός Στην περιοχή της επαφής δυο ηµιαγωγών τύπου p και n δηµιουργούνται ορισµένα φαινόµενα τα οποία είναι υπεύθυνα για τη συµπεριφορά της επαφής pn ή κρυσταλλοδιόδου, όπως ονοµάζεται,
Η2 Μελέτη ηµιαγωγών 1. Σκοπός Στην περιοχή της επαφής δυο ηµιαγωγών τύπου p και n δηµιουργούνται ορισµένα φαινόµενα τα οποία είναι υπεύθυνα για τη συµπεριφορά της επαφής pn ή κρυσταλλοδιόδου, όπως ονοµάζεται,
( J) e 2 ( ) ( ) x e +, (9-14) = (9-16) ω e xe v. De = (9-18) , (9-19)
 Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
Ασκήσεις Φασµατοσκοπίας Η φασµατική περιοχή στην οποία βρίσκεται µια φωτεινή ακτινοβολία χαρακτηρίζεται από την συχνότητα ν (Hz) µε την οποία ταλαντώνεται το ηλεκτρικό και το µαγνητικό πεδίο του φωτός.
ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ. Εργαστήριο Φυσικής IΙ. Μελέτη της απόδοσης φωτοβολταϊκού στοιχείου με χρήση υπολογιστή. 1. Σκοπός. 2. Σύντομο θεωρητικό μέρος
 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ 1. Σκοπός Το φωτοβολταϊκό στοιχείο είναι μία διάταξη ημιαγωγών η οποία μετατρέπει την φωτεινή ενέργεια που προσπίπτει σε αυτήν σε ηλεκτρική.. Όταν αυτή φωτιστεί με φωτόνια κατάλληλης συχνότητας
ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ 1. Σκοπός Το φωτοβολταϊκό στοιχείο είναι μία διάταξη ημιαγωγών η οποία μετατρέπει την φωτεινή ενέργεια που προσπίπτει σε αυτήν σε ηλεκτρική.. Όταν αυτή φωτιστεί με φωτόνια κατάλληλης συχνότητας
PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που
 ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
ΑΤΟΜΙΚΗ ΦΥΣΙΚΗ PLANCK 1900 Προκειμένου να εξηγήσει την ακτινοβολία του μέλανος σώματος αναγκάστηκε να υποθέσει ότι η ακτινοβολία εκπέμπεται σε κβάντα ενέργειας που είναι ανάλογα με τη συχνότητα (f). PLANCK
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Αγωγιμότητα στα μέταλλα
 Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
ΗΛΕΚΤΡΟΝΙΚΑ Ι ΚΕΦΑΛΑΙΟ 1 Ο :ΗΜΙΑΓΩΓΟΙ
 ΗΛΕΚΤΡΟΝΙΚΑ Ι ΚΕΦΑΛΑΙΟ 1 Ο :ΗΜΙΑΓΩΓΟΙ 1 1. ΗΛΕΚΤΡΙΚΗ ΔΟΜΗ. ΕΝΔΟΓΕΝΕΙΣ ΗΜΙΑΓΩΓΟΙ Δομή του ατόμου Σήμερα γνωρίζουμε ότι η ύλη αποτελείται από ενώσεις ατόμων, δημιουργώντας τις πολυάριθμες χημικές ενώσεις
ΗΛΕΚΤΡΟΝΙΚΑ Ι ΚΕΦΑΛΑΙΟ 1 Ο :ΗΜΙΑΓΩΓΟΙ 1 1. ΗΛΕΚΤΡΙΚΗ ΔΟΜΗ. ΕΝΔΟΓΕΝΕΙΣ ΗΜΙΑΓΩΓΟΙ Δομή του ατόμου Σήμερα γνωρίζουμε ότι η ύλη αποτελείται από ενώσεις ατόμων, δημιουργώντας τις πολυάριθμες χημικές ενώσεις
Βρέντζου Τίνα Φυσικός Μεταπτυχιακός τίτλος: «Σπουδές στην εκπαίδευση» ΜEd Email : stvrentzou@gmail.com
 1 2.4 Παράγοντες από τους οποίους εξαρτάται η αντίσταση ενός αγωγού Λέξεις κλειδιά: ειδική αντίσταση, μικροσκοπική ερμηνεία, μεταβλητός αντισ ροοστάτης, ποτενσιόμετρο 2.4 Παράγοντες που επηρεάζουν την
1 2.4 Παράγοντες από τους οποίους εξαρτάται η αντίσταση ενός αγωγού Λέξεις κλειδιά: ειδική αντίσταση, μικροσκοπική ερμηνεία, μεταβλητός αντισ ροοστάτης, ποτενσιόμετρο 2.4 Παράγοντες που επηρεάζουν την
Κεφάλαιο Η5. Ρεύμα και αντίσταση
 Κεφάλαιο Η5 Ρεύμα και αντίσταση Ηλεκτρικό ρεύμα Το ηλεκτρικό ρεύμα εμπλέκεται στις πρισσότερες πρακτικές εφαρμογές του ηλεκτρισμού. Τα ηλεκτρικά φορτία κινούνται σε κάποια περιοχή του χώρου. Σε αυτό το
Κεφάλαιο Η5 Ρεύμα και αντίσταση Ηλεκτρικό ρεύμα Το ηλεκτρικό ρεύμα εμπλέκεται στις πρισσότερες πρακτικές εφαρμογές του ηλεκτρισμού. Τα ηλεκτρικά φορτία κινούνται σε κάποια περιοχή του χώρου. Σε αυτό το
ΦΑΣΜΑΤΑ ΕΚΠΟΜΠΗΣ ΑΠΟΡΡΟΦΗΣΗΣ
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα 3ο μεροσ. Θεωρητικη αναλυση
 ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα 3ο μεροσ Θεωρητικη αναλυση μεταλλα Έχουν κοινές φυσικές ιδιότητες που αποδεικνύεται πως είναι αλληλένδετες μεταξύ τους: Υψηλή φυσική αντοχή Υψηλή πυκνότητα Υψηλή ηλεκτρική και θερμική
ΗΛΕΚΤΡΟΤΕΧΝΙΚΑ Υλικα 3ο μεροσ Θεωρητικη αναλυση μεταλλα Έχουν κοινές φυσικές ιδιότητες που αποδεικνύεται πως είναι αλληλένδετες μεταξύ τους: Υψηλή φυσική αντοχή Υψηλή πυκνότητα Υψηλή ηλεκτρική και θερμική
Κεφάλαιο 1 Χημικός δεσμός
 Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Κεφάλαιο 1 Χημικός δεσμός 1.1 Άτομα, Ηλεκτρόνια, και Τροχιακά Τα άτομα αποτελούνται από + Πρωτόνια φορτισμένα θετικά μάζα = 1.6726 X 10-27 kg Νετρόνια ουδέτερα μάζα = 1.6750 X 10-27 kg Ηλεκτρόνια φορτισμένα
Διατάξεις ημιαγωγών. Δίοδος, δίοδος εκπομπής φωτός (LED) Τρανζίστορ. Ολοκληρωμένο κύκλωμα
 Δίοδος, δίοδος εκπομπής φωτός (LED) Διατάξεις ημιαγωγών p n Άνοδος Κάθοδος Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Άνοδος Κάθοδος dpapageo@cc.uoi.gr http://pc64.materials.uoi.gr/dpapageo
Δίοδος, δίοδος εκπομπής φωτός (LED) Διατάξεις ημιαγωγών p n Άνοδος Κάθοδος Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Άνοδος Κάθοδος dpapageo@cc.uoi.gr http://pc64.materials.uoi.gr/dpapageo
ΑΝΑΛΟΓΙΚΑ ΗΛΕΚΤΡΟΝΙΚΑ
 ΑΝΑΛΟΓΙΚΑ ΗΛΕΚΤΡΟΝΙΚΑ ΚΕΦΑΛΑΙΟ 2ο ΗΜΙΑΓΩΓΟΙ Αγωγοί, Μονωτές, Ημιαγωγοί Κατηγοριοποίηση υλικών βάσει των ηλεκτρικών τους ιδιοτήτων: Αγωγοί (αφήνουν το ρεύμα να περάσει) Μονωτές (δεν αφήνουν το ρεύμα να
ΑΝΑΛΟΓΙΚΑ ΗΛΕΚΤΡΟΝΙΚΑ ΚΕΦΑΛΑΙΟ 2ο ΗΜΙΑΓΩΓΟΙ Αγωγοί, Μονωτές, Ημιαγωγοί Κατηγοριοποίηση υλικών βάσει των ηλεκτρικών τους ιδιοτήτων: Αγωγοί (αφήνουν το ρεύμα να περάσει) Μονωτές (δεν αφήνουν το ρεύμα να
Οργανική Χημεία. Κεφάλαια 12 &13: Φασματοσκοπία μαζών και υπερύθρου
 Οργανική Χημεία Κεφάλαια 12 &13: Φασματοσκοπία μαζών και υπερύθρου 1. Γενικά Δυνατότητα προσδιορισμού δομών με σαφήνεια χρησιμοποιώντας τεχνικές φασματοσκοπίας Φασματοσκοπία μαζών Μέγεθος, μοριακός τύπος
Οργανική Χημεία Κεφάλαια 12 &13: Φασματοσκοπία μαζών και υπερύθρου 1. Γενικά Δυνατότητα προσδιορισμού δομών με σαφήνεια χρησιμοποιώντας τεχνικές φασματοσκοπίας Φασματοσκοπία μαζών Μέγεθος, μοριακός τύπος
Δρ. Ιωάννης Καλαμαράς, Διδάκτωρ Χημικός. Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό
 Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
Όλα τα Θέματα της Τράπεζας στη Χημεία που σχετίζονται με το Χημικό Δεσμό Θέμα 1. Να αναφέρετε δυο διαφορές μεταξύ ομοιοπολικών και ιοντικών ενώσεων. Στις ιοντικές ενώσεις οι δομικές μονάδες είναι τα ιόντα,
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1
 ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1 Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΝΙΚΟΛΑΟΣ ΚΟΥΤΡΟΥΜΑΝΗΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 5 Μαρτίου 2015 2 ο Φροντιστήριο 1) Ποια είναι τα ηλεκτρόνια σθένους και ποιός ο ρόλος τους;
ΕΠΙΣΤΗΜΗ ΤΩΝ ΥΛΙΚΩΝ 1 Ενότητα: ΦΡΟΝΤΙΣΤΗΡΙΟ Επιμέλεια: ΝΙΚΟΛΑΟΣ ΚΟΥΤΡΟΥΜΑΝΗΣ Τμήμα: ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΤΡΑΣ 5 Μαρτίου 2015 2 ο Φροντιστήριο 1) Ποια είναι τα ηλεκτρόνια σθένους και ποιός ο ρόλος τους;
1. Να χαρακτηρίσετε τις παρακάτω προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ):
 1. Να χαρακτηρίσετε τις παρακάτω προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ): 1) Ηλεκτρισμένα ονομάζουμε τα σώματα τα οποία, αφού τα τρίψουμε έχουν την ιδιότητα να έλκουν μικρά αντικείμενα. 2) Οι ηλεκτρικές
1. Να χαρακτηρίσετε τις παρακάτω προτάσεις ως σωστές (Σ) ή λανθασμένες (Λ): 1) Ηλεκτρισμένα ονομάζουμε τα σώματα τα οποία, αφού τα τρίψουμε έχουν την ιδιότητα να έλκουν μικρά αντικείμενα. 2) Οι ηλεκτρικές
Κεφάλαιο 37 Αρχική Κβαντική Θεωρία και Μοντέλα για το Άτομο. Copyright 2009 Pearson Education, Inc.
 Κεφάλαιο 37 Αρχική Κβαντική Θεωρία και Μοντέλα για το Άτομο Περιεχόμενα Κεφαλαίου 37 Η κβαντική υπόθεση του Planck, Ακτινοβολία του μέλανος (μαύρου) σώματος Θεωρία των φωτονίων για το φως και το Φωτοηλεκτρικό
Κεφάλαιο 37 Αρχική Κβαντική Θεωρία και Μοντέλα για το Άτομο Περιεχόμενα Κεφαλαίου 37 Η κβαντική υπόθεση του Planck, Ακτινοβολία του μέλανος (μαύρου) σώματος Θεωρία των φωτονίων για το φως και το Φωτοηλεκτρικό
Επαφές μετάλλου ημιαγωγού
 Δίοδος Schottky Επαφές μετάλλου ημιαγωγού Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Τι είναι Ημιαγωγός Κατασκευάζεται με εξάχνωση μετάλλου το οποίο μεταφέρεται στην επιφάνεια
Δίοδος Schottky Επαφές μετάλλου ημιαγωγού Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων Τι είναι Ημιαγωγός Κατασκευάζεται με εξάχνωση μετάλλου το οποίο μεταφέρεται στην επιφάνεια
1η ΠΑΡΟΥΣΙΑΣΗ. Ηλεκτρικά πεδία
 1η ΠΑΡΟΥΣΙΑΣΗ Ηλεκτρικά πεδία Ηλεκτρισμός και μαγνητισμός Κλάδος της Φυσικής που μελετάει τα ηλεκτρικά και τα μαγνητικά φαινόμενα. (Σχεδόν) όλα τα φαινομενα που αντιλαμβανόμαστε με τις αισθήσεις μας οφείλονται
1η ΠΑΡΟΥΣΙΑΣΗ Ηλεκτρικά πεδία Ηλεκτρισμός και μαγνητισμός Κλάδος της Φυσικής που μελετάει τα ηλεκτρικά και τα μαγνητικά φαινόμενα. (Σχεδόν) όλα τα φαινομενα που αντιλαμβανόμαστε με τις αισθήσεις μας οφείλονται
ΠΡΟΤΥΠΟ ΛΥΚΕΙΟ ΕΥΑΓΓΕΛΙΚΗΣ ΣΧΟΛΗΣ ΣΜΥΡΝΗΣ
 ΠΡΟΤΥΠΟ ΛΥΚΕΙΟ ΕΥΑΓΓΕΛΙΚΗΣ ΣΧΟΛΗΣ ΣΜΥΡΝΗΣ ΕΠΙΛΟΓΗ ΘΕΜΑΤΩΝ ΑΠΟ ΤΗΝ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ «Β ΘΕΜΑΤΑ ΑΤΟΜΙΚΑ ΜΟΝΤΕΛΑ» ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Β ΛΥΚΕΙΟΥ Χ. Δ. ΦΑΝΙΔΗΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 0-05 ΘΕΜΑ B Σχέσεις μεταξύ κινητικής,
ΠΡΟΤΥΠΟ ΛΥΚΕΙΟ ΕΥΑΓΓΕΛΙΚΗΣ ΣΧΟΛΗΣ ΣΜΥΡΝΗΣ ΕΠΙΛΟΓΗ ΘΕΜΑΤΩΝ ΑΠΟ ΤΗΝ ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ «Β ΘΕΜΑΤΑ ΑΤΟΜΙΚΑ ΜΟΝΤΕΛΑ» ΦΥΣΙΚΗ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Β ΛΥΚΕΙΟΥ Χ. Δ. ΦΑΝΙΔΗΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 0-05 ΘΕΜΑ B Σχέσεις μεταξύ κινητικής,
Διατομικά μόρια- Περιστροφική ενέργεια δονητικά - περιστροφικά φάσματα
 Διατομικά μόρια- Περιστροφική ενέργεια δονητικά - περιστροφικά φάσματα Πολυατομικά μόρια περιστροφική ενέργεια περιστροφικά φάσματα Σκέδαση φασματοσκοπία n συνεισφορά του πυρηνικού σπιν Δονητικά περιστροφικά
Διατομικά μόρια- Περιστροφική ενέργεια δονητικά - περιστροφικά φάσματα Πολυατομικά μόρια περιστροφική ενέργεια περιστροφικά φάσματα Σκέδαση φασματοσκοπία n συνεισφορά του πυρηνικού σπιν Δονητικά περιστροφικά
1η ΠΑΡΟΥΣΙΑΣΗ. Ηλεκτρικά φορτία, ηλεκτρικές δυνάμεις και πεδία
 1η ΠΑΡΟΥΣΙΑΣΗ Ηλεκτρικά φορτία, ηλεκτρικές δυνάμεις και πεδία Ηλεκτρισμός και μαγνητισμός Κλάδος της Φυσικής που μελετάει τα ηλεκτρικά και τα μαγνητικά φαινόμενα. (Σχεδόν) όλα τα φαινομενα που αντιλαμβανόμαστε
1η ΠΑΡΟΥΣΙΑΣΗ Ηλεκτρικά φορτία, ηλεκτρικές δυνάμεις και πεδία Ηλεκτρισμός και μαγνητισμός Κλάδος της Φυσικής που μελετάει τα ηλεκτρικά και τα μαγνητικά φαινόμενα. (Σχεδόν) όλα τα φαινομενα που αντιλαμβανόμαστε
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος
 2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
Από πού προέρχεται η θερμότητα που μεταφέρεται από τον αντιστάτη στο περιβάλλον;
 3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
ΑΝΑΛΟΓΙΚΑ ΗΛΕΚΤΡΟΝΙΚΑ
 ΑΝΑΛΟΓΙΚΑ ΗΛΕΚΤΡΟΝΙΚΑ Διάλεξη 1: Ημιαγωγοί Δίοδος pn Δρ. Δ. ΛΑΜΠΑΚΗΣ 1 Ταλαντωτές. Πολυδονητές. Γεννήτριες συναρτήσεων. PLL. Πολλαπλασιαστές. Κυκλώματα μετατροπής και επεξεργασίας σημάτων. Εφαρμογές με
ΑΝΑΛΟΓΙΚΑ ΗΛΕΚΤΡΟΝΙΚΑ Διάλεξη 1: Ημιαγωγοί Δίοδος pn Δρ. Δ. ΛΑΜΠΑΚΗΣ 1 Ταλαντωτές. Πολυδονητές. Γεννήτριες συναρτήσεων. PLL. Πολλαπλασιαστές. Κυκλώματα μετατροπής και επεξεργασίας σημάτων. Εφαρμογές με
ΚΕΦΑΛΑΙΟ Το ηλεκτρικό φορτίο στο εσωτερικό του ατόμου 1. Από τι σωματίδια αποτελούνται τα άτομα σύμφωνα με τις απόψεις των Rutherford και Bohr;
 ΚΕΦΑΛΑΙΟ 1 1.1 Γνωριμία με τη ηλεκτρική δύναμη. 1. Ποιες δυνάμεις λέγονται ηλεκτρικές; Λέμε τις δυνάμεις που ασκούνται μεταξύ σωμάτων που έχουμε τρίψει προηγουμένως δηλαδή σωμάτων ηλεκτρισμένων. 2. Τι
ΚΕΦΑΛΑΙΟ 1 1.1 Γνωριμία με τη ηλεκτρική δύναμη. 1. Ποιες δυνάμεις λέγονται ηλεκτρικές; Λέμε τις δυνάμεις που ασκούνται μεταξύ σωμάτων που έχουμε τρίψει προηγουμένως δηλαδή σωμάτων ηλεκτρισμένων. 2. Τι
Ανάστροφη πόλωση της επαφής p n
 Ανάστροφη πόλωση της επαφής p n Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Επαφή p n Ανάστροφη πόλωση Πολώνουμε
Ανάστροφη πόλωση της επαφής p n Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Επαφή p n Ανάστροφη πόλωση Πολώνουμε
Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR
 Φασματοσκοπία Ερμηνεία & εφαρμογές : Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR Ποια φαινόμενα παράγουν τα
Φασματοσκοπία Ερμηνεία & εφαρμογές : Φασματοσκοπίας UV/ορατού Φασματοσκοπίας υπερύθρου Φασματοσκοπίας άπω υπερύθρου / μικροκυμάτων Φασματοσκοπίας φθορισμού Φασματοσκοπίας NMR Ποια φαινόμενα παράγουν τα
Τμήμα Φυσικής Πανεπιστημίου Κύπρου Χειμερινό Εξάμηνο 2016/2017 ΦΥΣ102 Φυσική για Χημικούς Διδάσκων: Μάριος Κώστα
 Τμήμα Φυσικής Πανεπιστημίου Κύπρου Χειμερινό Εξάμηνο 2016/2017 ΦΥΣ102 Φυσική για Χημικούς Διδάσκων: Μάριος Κώστα ΔΙΑΛΕΞΗ 11 Εισαγωγή στην Ηλεκτροδυναμική Ηλεκτρικό φορτίο Ηλεκτρικό πεδίο ΦΥΣ102 1 Στατικός
Τμήμα Φυσικής Πανεπιστημίου Κύπρου Χειμερινό Εξάμηνο 2016/2017 ΦΥΣ102 Φυσική για Χημικούς Διδάσκων: Μάριος Κώστα ΔΙΑΛΕΞΗ 11 Εισαγωγή στην Ηλεκτροδυναμική Ηλεκτρικό φορτίο Ηλεκτρικό πεδίο ΦΥΣ102 1 Στατικός
ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ Περιεχόμενα 1. Όρια καταστατικής εξίσωσης ιδανικού αερίου 2. Αποκλίσεις των Ιδιοτήτων των πραγματικών αερίων από τους Νόμους
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΠΡΑΓΜΑΤΙΚΑ ΑΕΡΙΑ ΘΕΩΡΙΑ Περιεχόμενα 1. Όρια καταστατικής εξίσωσης ιδανικού αερίου 2. Αποκλίσεις των Ιδιοτήτων των πραγματικών αερίων από τους Νόμους
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Ανάστροφη πόλωση της επαφής p n
 Ανάστροφη πόλωση της επαφής p n Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Επαφή p n Ανάστροφη πόλωση Πολώνουμε
Ανάστροφη πόλωση της επαφής p n Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Επαφή p n Ανάστροφη πόλωση Πολώνουμε
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ. Σύγxρονη Φυσική II. Μοριακή Δομή ΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική Μοριακή Δομή ΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Ceative Coons. Για
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Σύγxρονη Φυσική Μοριακή Δομή ΙΙ Διδάσκων : Επίκ. Καθ. Μ. Μπενής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Ceative Coons. Για
είναι τα μήκη κύματος του φωτός αυτού στα δύο υλικά αντίστοιχα, τότε: γ. 1 Β) Να δικαιολογήσετε την επιλογή σας.
 Β.1 Μονοχρωματικό φως, που διαδίδεται στον αέρα, εισέρχεται ταυτόχρονα σε δύο οπτικά υλικά του ίδιου πάχους d κάθετα στην επιφάνειά τους, όπως φαίνεται στο σχήμα. Οι χρόνοι διάδοσης του φωτός στα δύο υλικά
Β.1 Μονοχρωματικό φως, που διαδίδεται στον αέρα, εισέρχεται ταυτόχρονα σε δύο οπτικά υλικά του ίδιου πάχους d κάθετα στην επιφάνειά τους, όπως φαίνεται στο σχήμα. Οι χρόνοι διάδοσης του φωτός στα δύο υλικά
ΑΤΟΜΙΚΑ ΤΟΜΙΚΑ ΠΡΟΤΥΠΑ
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Thomson (σταφιδόψωμο) Rutherford (πλανητικό μοντέλο) Bohr (επιτρεπόμενες τροχιές ενεργειακές στάθμες) Κβαντομηχανική β ή (τροχιακό) ρχ 24/9/2008 1 ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ Bohr 1η Συνθήκη (Μηχανική
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ
 ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
ΥΛΙΚΑ ΠΑΡΟΝ ΚΑΙ ΜΕΛΛΟΝ Ι 4 Δεσμοί ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ μεταξύ ατόμων γίνονται με τα ηλεκτρόνια σθένους κατά τέτοιο τρόπο ώστε να ελαττώνεται η συνολική ενέργεια του
ΝΑΝΟΥΛΙΚΑ ΚΑΙ ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΣΤΕΛΛΑ ΚΕΝΝΟΥ ΚΑΘΗΓΗΤΡΙΑ
 ΣΤΕΛΛΑ ΚΕΝΝΟΥ ΚΑΘΗΓΗΤΡΙΑ 1 Ιδιότητες εξαρτώμενες από το μέγεθος Στην νανοκλίμακα, οι ιδιότητες εξαρτώνται δραματικά από το μέγεθος Για παράδειγμα, ΙΔΙΟΤΗΤΕΣ ΝΑΝΟΥΛΙΚΩΝ (1) Θερμικές ιδιότητες θερμοκρασία
ΣΤΕΛΛΑ ΚΕΝΝΟΥ ΚΑΘΗΓΗΤΡΙΑ 1 Ιδιότητες εξαρτώμενες από το μέγεθος Στην νανοκλίμακα, οι ιδιότητες εξαρτώνται δραματικά από το μέγεθος Για παράδειγμα, ΙΔΙΟΤΗΤΕΣ ΝΑΝΟΥΛΙΚΩΝ (1) Θερμικές ιδιότητες θερμοκρασία
Η επαφή p n. Η επαφή p n. Υπενθύμιση: Ημιαγωγός τύπου n. Υπενθύμιση: Ημιαγωγός τύπου p
 Η επαφή p n Τι είναι Που χρησιμεύει Η επαφή p n p n Η διάταξη που αποτελείται από μία επαφή p n ονομάζεται δίοδος. Άνοδος Κάθοδος Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων
Η επαφή p n Τι είναι Που χρησιμεύει Η επαφή p n p n Η διάταξη που αποτελείται από μία επαφή p n ονομάζεται δίοδος. Άνοδος Κάθοδος Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων
ΦΩΤΟΒΟΛΤΑΪΚΑ. Γ. Λευθεριώτης Αναπλ. Καθηγητής Γ. Συρροκώστας Μεταδιδακτορικός Ερευνητής
 ΦΩΤΟΒΟΛΤΑΪΚΑ Γ. Λευθεριώτης Αναπλ. Καθηγητής Γ. Συρροκώστας Μεταδιδακτορικός Ερευνητής Αγωγοί- μονωτές- ημιαγωγοί Μέταλλα: Μία ζώνη μερικώς γεμάτη ή μία ζώνη επικαλύπτει την άλλη Τα ηλεκτρόνια μπορούν
ΦΩΤΟΒΟΛΤΑΪΚΑ Γ. Λευθεριώτης Αναπλ. Καθηγητής Γ. Συρροκώστας Μεταδιδακτορικός Ερευνητής Αγωγοί- μονωτές- ημιαγωγοί Μέταλλα: Μία ζώνη μερικώς γεμάτη ή μία ζώνη επικαλύπτει την άλλη Τα ηλεκτρόνια μπορούν
Spin του πυρήνα Μαγνητική διπολική ροπή Ηλεκτρική τετραπολική ροπή. Τάσος Λιόλιος Μάθημα Πυρηνικής Φυσικής
 Spin του πυρήνα Μαγνητική διπολική ροπή Ηλεκτρική τετραπολική ροπή Τάσος Λιόλιος Μάθημα Πυρηνικής Φυσικής Εξάρτηση του πυρηνικού δυναμικού από άλλους παράγοντες (πλην της απόστασης) Η συνάρτηση του δυναμικού
Spin του πυρήνα Μαγνητική διπολική ροπή Ηλεκτρική τετραπολική ροπή Τάσος Λιόλιος Μάθημα Πυρηνικής Φυσικής Εξάρτηση του πυρηνικού δυναμικού από άλλους παράγοντες (πλην της απόστασης) Η συνάρτηση του δυναμικού
Προβλήματα Κεφαλαίου 2
 Άνοιξη 2019 14/3/2019 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 23,24 και 25 * να παραδοθούν μέχρι τις 22/3/2019 Οι λύσεις των προβλημάτων 27 και 28 * να παραδοθούν μέχρι τις 28/3/2019 1. Θεωρείστε
Άνοιξη 2019 14/3/2019 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 23,24 και 25 * να παραδοθούν μέχρι τις 22/3/2019 Οι λύσεις των προβλημάτων 27 και 28 * να παραδοθούν μέχρι τις 28/3/2019 1. Θεωρείστε
ΚΕΦΑΛΑΙΟ 2: Ηλεκτρικό Ρεύμα Μέρος 1 ο
 ΚΕΦΑΛΑΙΟ 2: Ηλεκτρικό Ρεύμα Μέρος 1 ο Βασίλης Γαργανουράκης Φυσική ήγ Γυμνασίου Εισαγωγή Στο προηγούμενο κεφάλαιο μελετήσαμε τις αλληλεπιδράσεις των στατικών (ακίνητων) ηλεκτρικών φορτίων. Σε αυτό το κεφάλαιο
ΚΕΦΑΛΑΙΟ 2: Ηλεκτρικό Ρεύμα Μέρος 1 ο Βασίλης Γαργανουράκης Φυσική ήγ Γυμνασίου Εισαγωγή Στο προηγούμενο κεφάλαιο μελετήσαμε τις αλληλεπιδράσεις των στατικών (ακίνητων) ηλεκτρικών φορτίων. Σε αυτό το κεφάλαιο
Χημεία Γ Λυκείου Θετικής Κατεύθυνσης
 Χημεία Γ Λυκείου Θετικής Κατεύθυνσης Κεφάλαιο 1 Ηλεκτρονιακή δομή των ατόμων 1 Εισαγωγή Δομή του ατόμου Δημόκριτος Αριστοτέλης Dalton Thomson 400 π.χ. 350π.χ. 1808 1897 Απειροελάχιστα τεμάχια ύλης (τα
Χημεία Γ Λυκείου Θετικής Κατεύθυνσης Κεφάλαιο 1 Ηλεκτρονιακή δομή των ατόμων 1 Εισαγωγή Δομή του ατόμου Δημόκριτος Αριστοτέλης Dalton Thomson 400 π.χ. 350π.χ. 1808 1897 Απειροελάχιστα τεμάχια ύλης (τα
Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2
 Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ερωτήσεις Ανάπτυξης 1. Δίνεται ότι: 40 20 Ca. Να μεταφέρετε στην κόλλα σας συμπληρωμένο τον παρακάτω πίνακα που αναφέρεται στο άτομο του ασβεστίου: ΣΤΙΒΑΔΕΣ νετρόνια K L M N Ca 2 2. Tι είδους δεσμός αναπτύσσεται
Ημιαγωγοί. Ημιαγωγοί. Ενδογενείς εξωγενείς ημιαγωγοί. Ενδογενείς ημιαγωγοί Πυρίτιο. Δομή ενεργειακών ζωνών
 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Δομή ενεργειακών ζωνών Δεν υπάρχουν διαθέσιμες θέσεις Κενή ζώνη αγωγιμότητας
Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo Δομή ενεργειακών ζωνών Δεν υπάρχουν διαθέσιμες θέσεις Κενή ζώνη αγωγιμότητας
ΦΥΣΙΚΗ Γ ΓΥΜΝΑΣΙΟΥ 2.1 ΤΟ ΗΛΕΚΤΡΙΚΟ ΡΕΥΜΑ
 ΦΥΣΙΚΗ Γ ΓΥΜΝΑΣΙΟΥ 2Η ΕΝΟΤΗΤΑ ΗΛΕΚΤΡΙΚΟ ΡΕΥΜΑ 2.1 ΤΟ ΗΛΕΚΤΡΙΚΟ ΡΕΥΜΑ Τι είναι ; Ηλεκτρικό ρεύμα ονομάζεται η προσανατολισμένη κίνηση των ηλεκτρονίων ή γενικότερα των φορτισμένων σωματιδίων Που μπορεί να
ΦΥΣΙΚΗ Γ ΓΥΜΝΑΣΙΟΥ 2Η ΕΝΟΤΗΤΑ ΗΛΕΚΤΡΙΚΟ ΡΕΥΜΑ 2.1 ΤΟ ΗΛΕΚΤΡΙΚΟ ΡΕΥΜΑ Τι είναι ; Ηλεκτρικό ρεύμα ονομάζεται η προσανατολισμένη κίνηση των ηλεκτρονίων ή γενικότερα των φορτισμένων σωματιδίων Που μπορεί να
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ. Θέμα B
 ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Θέμα B _70 Β. Το ηλεκτρόνιο ενός ατόμου υδρογόνου που βρίσκεται στη τρίτη διεγερμένη ενεργειακή κατάσταση (n = ), αποδιεγείρεται εκπέμποντας φωτόνιο ενέργειας Ε.Κατά τη συγκεκριμένη αποδιέγερση
ΑΤΟΜΙΚΑ ΠΡΟΤΥΠΑ Θέμα B _70 Β. Το ηλεκτρόνιο ενός ατόμου υδρογόνου που βρίσκεται στη τρίτη διεγερμένη ενεργειακή κατάσταση (n = ), αποδιεγείρεται εκπέμποντας φωτόνιο ενέργειας Ε.Κατά τη συγκεκριμένη αποδιέγερση
Λύση 10) Λύση 11) Λύση
 1)Το ηλεκτρόνιο στο άτομο του υδρογόνου, έχει κινητική ενέργεια Κ, ηλεκτρική δυναμική ενέργεια U και ολική ενέργεια Ε. Να επιλέξετε τη σωστή πρόταση. Η ορθή σχέση μεταξύ της κινητικής και της ολικής του
1)Το ηλεκτρόνιο στο άτομο του υδρογόνου, έχει κινητική ενέργεια Κ, ηλεκτρική δυναμική ενέργεια U και ολική ενέργεια Ε. Να επιλέξετε τη σωστή πρόταση. Η ορθή σχέση μεταξύ της κινητικής και της ολικής του
ΦΩΤΟΒΟΛΤΑΪΚΑ. Γ. Λευθεριώτης Αναπλ. Καθηγητής Γ. Συρροκώστας Μεταδιδακτορικός Ερευνητής
 ΦΩΤΟΒΟΛΤΑΪΚΑ Γ. Λευθεριώτης Αναπλ. Καθηγητής Γ. Συρροκώστας Μεταδιδακτορικός Ερευνητής Αγωγοί- μονωτές- ημιαγωγοί Μέταλλα: Μία ζώνη μερικώς γεμάτη ή μία ζώνη επικαλύπτει την άλλη Τα ηλεκτρόνια μπορούν
ΦΩΤΟΒΟΛΤΑΪΚΑ Γ. Λευθεριώτης Αναπλ. Καθηγητής Γ. Συρροκώστας Μεταδιδακτορικός Ερευνητής Αγωγοί- μονωτές- ημιαγωγοί Μέταλλα: Μία ζώνη μερικώς γεμάτη ή μία ζώνη επικαλύπτει την άλλη Τα ηλεκτρόνια μπορούν
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 5 η : Ομοιοπολικοί δεσμοί & μοριακή δομή Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ο Ομοιοπολικός Δεσμός 2 Ο δεσμός Η Η στο μόριο Η
Ο Πυρήνας του Ατόμου
 1 Σκοποί: Ο Πυρήνας του Ατόμου 15/06/12 I. Να δώσει μία εισαγωγική περιγραφή του πυρήνα του ατόμου, και της ενέργειας που μπορεί να έχει ένα σωματίδιο για να παραμείνει δέσμιο μέσα στον πυρήνα. II. III.
1 Σκοποί: Ο Πυρήνας του Ατόμου 15/06/12 I. Να δώσει μία εισαγωγική περιγραφή του πυρήνα του ατόμου, και της ενέργειας που μπορεί να έχει ένα σωματίδιο για να παραμείνει δέσμιο μέσα στον πυρήνα. II. III.
Κεφάλαιο 9. Ιοντικός και Ομοιοπολικός Δεσμός
 Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
Κεφάλαιο 9 Ιοντικός και Ομοιοπολικός Δεσμός Ηλεκτρόνια σθένους είναι τα ηλεκτρόνια της εξώτατης στοιβάδας ενός ατόμου. Είναι τα ηλεκτρόνια τα οποία συμμετέχουν στους χημικούς δεσμούς. Ομάδα Δομή e - #
ΟΡΟΣΗΜΟ ΘΕΜΑ Δ. Δίνονται: η ταχύτητα του φωτός στο κενό c 0 = 3 10, η σταθερά του Planck J s και για το φορτίο του ηλεκτρονίου 1,6 10 C.
 Σε μια διάταξη παραγωγής ακτίνων X, η ηλεκτρική τάση που εφαρμόζεται μεταξύ της ανόδου και της καθόδου είναι V = 25 kv. Τα ηλεκτρόνια ξεκινούν από την κάθοδο με μηδενική ταχύτητα, επιταχύνονται και προσπίπτουν
Σε μια διάταξη παραγωγής ακτίνων X, η ηλεκτρική τάση που εφαρμόζεται μεταξύ της ανόδου και της καθόδου είναι V = 25 kv. Τα ηλεκτρόνια ξεκινούν από την κάθοδο με μηδενική ταχύτητα, επιταχύνονται και προσπίπτουν
1ο Επαναληπτικό Διαγώνισμα Φυσικής Γενικής Παιδείας Β τάξης Λυκείου.
 ο Επαναληπτικό Διαγώνισμα Φυσικής Γενικής Παιδείας Β τάξης Λυκείου Θέμα Α: (Για τις ερωτήσεις Α έως και Α να γράψετε στο τετράδιό σας τον αριθμό της πρότασης και δίπλα το γράμμα που αντιστοιχεί στη σωστή
ο Επαναληπτικό Διαγώνισμα Φυσικής Γενικής Παιδείας Β τάξης Λυκείου Θέμα Α: (Για τις ερωτήσεις Α έως και Α να γράψετε στο τετράδιό σας τον αριθμό της πρότασης και δίπλα το γράμμα που αντιστοιχεί στη σωστή
Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων
 Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων Περιεχόμενα Κεφαλαίου 39 Τα άτομα από την σκοπιά της κβαντικής μηχανικής Το άτομο του Υδρογόνου: Η εξίσωση του Schrödinger και οι κβαντικοί αριθμοί ΟΙ κυματοσυναρτήσεις
Κεφάλαιο 39 Κβαντική Μηχανική Ατόμων Περιεχόμενα Κεφαλαίου 39 Τα άτομα από την σκοπιά της κβαντικής μηχανικής Το άτομο του Υδρογόνου: Η εξίσωση του Schrödinger και οι κβαντικοί αριθμοί ΟΙ κυματοσυναρτήσεις
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ A ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 14 12-2014 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Μαρίνος Ιωάννου, Σταυρούλα Γκιτάκου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α.1 έως Α.4 να γράψετε στην κόλλα σας το
Τίτλος Μαθήματος: Βασικές Έννοιες Φυσικής. Ενότητα: Στερεά. Διδάσκων: Καθηγητής Κ. Κώτσης. Τμήμα: Παιδαγωγικό, Δημοτικής Εκπαίδευσης
 Τίτλος Μαθήματος: Βασικές Έννοιες Φυσικής Ενότητα: Στερεά Διδάσκων: Καθηγητής Κ. Κώτσης Τμήμα: Παιδαγωγικό, Δημοτικής Εκπαίδευσης 7. Στερεά Η επιβεβαίωση ότι τα στερεά σώματα αποτελούνται από μια ιδιαίτερη
Τίτλος Μαθήματος: Βασικές Έννοιες Φυσικής Ενότητα: Στερεά Διδάσκων: Καθηγητής Κ. Κώτσης Τμήμα: Παιδαγωγικό, Δημοτικής Εκπαίδευσης 7. Στερεά Η επιβεβαίωση ότι τα στερεά σώματα αποτελούνται από μια ιδιαίτερη
Προβλήματα Κεφαλαίου 2
 Άνοιξη 2017 8/3/2017 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 23,24 και 25 * να παραδοθούν μέχρι τις 17/3/2017 Οι λύσεις των προβλημάτων 26 και 27 * να παραδοθούν μέχρι τις 24/3/2017 1. Θεωρείστε
Άνοιξη 2017 8/3/2017 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 23,24 και 25 * να παραδοθούν μέχρι τις 17/3/2017 Οι λύσεις των προβλημάτων 26 και 27 * να παραδοθούν μέχρι τις 24/3/2017 1. Θεωρείστε
ΠΥΡΗΝΙΚΟΣ ΜΑΓΝΗΤΙΚΟΣ ΣΥΝΤΟΝΙΣΜΟΣ ΚΑΙ ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ. Του Αλέκου Χαραλαμπόπουλου ΕΙΣΑΓΩΓΗ
 ΠΥΡΗΝΙΚΟΣ ΜΑΓΝΗΤΙΚΟΣ ΣΥΝΤΟΝΙΣΜΟΣ ΚΑΙ ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ Του Αλέκου Χαραλαμπόπουλου ΕΙΣΑΓΩΓΗ Ένα επαναλαμβανόμενο περιοδικά φαινόμενο, έχει μία συχνότητα επανάληψης μέσα στο χρόνο και μία περίοδο. Επειδή κάθε
ΠΥΡΗΝΙΚΟΣ ΜΑΓΝΗΤΙΚΟΣ ΣΥΝΤΟΝΙΣΜΟΣ ΚΑΙ ΔΟΜΗ ΤΟΥ ΑΤΟΜΟΥ Του Αλέκου Χαραλαμπόπουλου ΕΙΣΑΓΩΓΗ Ένα επαναλαμβανόμενο περιοδικά φαινόμενο, έχει μία συχνότητα επανάληψης μέσα στο χρόνο και μία περίοδο. Επειδή κάθε
ΦΥΣΙΚΗ Γ ΓΥΜΝΑΣΙΟΥ. Ηλεκτρισμένα σώματα. πως διαπιστώνουμε ότι ένα σώμα είναι ηλεκτρισμένο ; Ηλεκτρικό φορτίο
 ΦΥΣΙΚΗ Γ ΓΥΜΝΑΣΙΟΥ 1 Η ΕΝΟΤΗΤΑ ΗΛΕΚΤΡΙΣΜΟΣ ΚΕΦΑΛΑΙΟ 1 Ο Ηλεκτρική δύναμη και φορτίο Ηλεκτρισμένα σώματα 1.1 Ποια είναι ; Σώματα (πλαστικό, γυαλί, ήλεκτρο) που έχουν την ιδιότητα να ασκούν δύναμη σε ελαφρά
ΦΥΣΙΚΗ Γ ΓΥΜΝΑΣΙΟΥ 1 Η ΕΝΟΤΗΤΑ ΗΛΕΚΤΡΙΣΜΟΣ ΚΕΦΑΛΑΙΟ 1 Ο Ηλεκτρική δύναμη και φορτίο Ηλεκτρισμένα σώματα 1.1 Ποια είναι ; Σώματα (πλαστικό, γυαλί, ήλεκτρο) που έχουν την ιδιότητα να ασκούν δύναμη σε ελαφρά
ΗΜΙΑΓΩΓΟΙ. Σπύρος Νικολαΐδης Καθηγητής Τομέας Ηλεκτρονικής & ΗΥ Τμήμα Φυσικής
 ΗΜΙΑΓΩΓΟΙ Σπύρος Νικολαΐδης Καθηγητής Τομέας Ηλεκτρονικής & ΗΥ Τμήμα Φυσικής Ηλεκτρονικοί φλοιοί των ατόμων Σθένος και ομοιοπολικοί δεσμοί Η πρώτη ύλη με την οποία κατασκευάζονται τα περισσότερα ηλεκτρονικά
ΗΜΙΑΓΩΓΟΙ Σπύρος Νικολαΐδης Καθηγητής Τομέας Ηλεκτρονικής & ΗΥ Τμήμα Φυσικής Ηλεκτρονικοί φλοιοί των ατόμων Σθένος και ομοιοπολικοί δεσμοί Η πρώτη ύλη με την οποία κατασκευάζονται τα περισσότερα ηλεκτρονικά
ΔΟΜΗ ΑΤΟΜΩΝ ΚΑΙ ΜΟΡΙΩΝ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ ΤΟΥ BOHR
 ΔΟΜΗ ΑΤΟΜΩΝ ΚΑΙ ΜΟΡΙΩΝ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ ΤΟΥ BOHR Μοντέλο του Bohr : Άτομο ηλιακό σύστημα. Βασικά σημεία της θεωρίας του Bohr : 1 η συνθήκη ( μηχανική συνθήκη ) Τα ηλεκτρόνια κινούνται
ΔΟΜΗ ΑΤΟΜΩΝ ΚΑΙ ΜΟΡΙΩΝ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ ΑΤΟΜΙΚΟ ΠΡΟΤΥΠΟ ΤΟΥ BOHR Μοντέλο του Bohr : Άτομο ηλιακό σύστημα. Βασικά σημεία της θεωρίας του Bohr : 1 η συνθήκη ( μηχανική συνθήκη ) Τα ηλεκτρόνια κινούνται
Η ΕΝΕΡΓΕΙΑ ΤΟΥ ΑΤΟΜΟΥ ΤΟΥ ΥΔΡΟΓΟΝΟΥ
 Η ΕΝΕΡΓΕΙΑ ΤΟΥ ΑΤΟΜΟΥ ΤΟΥ ΥΔΡΟΓΟΝΟΥ ΑΣΚΗΣΗ 1 Άτομα αερίου υδρογόνου που βρίσκονται στη θεμελιώδη κατάσταση (n = 1), διεγείρονται με κρούση από δέσμη ηλεκτρονίων που έχουν επιταχυνθεί από διαφορά δυναμικού
Η ΕΝΕΡΓΕΙΑ ΤΟΥ ΑΤΟΜΟΥ ΤΟΥ ΥΔΡΟΓΟΝΟΥ ΑΣΚΗΣΗ 1 Άτομα αερίου υδρογόνου που βρίσκονται στη θεμελιώδη κατάσταση (n = 1), διεγείρονται με κρούση από δέσμη ηλεκτρονίων που έχουν επιταχυνθεί από διαφορά δυναμικού
Μοντέρνα Φυσική. Κβαντική Θεωρία. Ατομική Φυσική. Μοριακή Φυσική. Πυρηνική Φυσική. Φασματοσκοπία
 Μοντέρνα Φυσική Κβαντική Θεωρία Ατομική Φυσική Μοριακή Φυσική Πυρηνική Φυσική Φασματοσκοπία ΚΒΑΝΤΙΚΗ ΘΕΩΡΙΑ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης:
Μοντέρνα Φυσική Κβαντική Θεωρία Ατομική Φυσική Μοριακή Φυσική Πυρηνική Φυσική Φασματοσκοπία ΚΒΑΝΤΙΚΗ ΘΕΩΡΙΑ Φωτόνια: ενέργεια E = hf = hc/λ (όπου h = σταθερά Planck) Κυματική φύση των σωματιδίων της ύλης:
Βασικές αρχές της Φασµατοσκοπίας NMR
 Βασικές αρχές της Φασµατοσκοπίας NMR Φώτης Νταής Καθηγητής Πανεπιστηµίου Κρήτης, Τµήµα Χηµείας Φασµατοσκοπία NMR Ο Πυρηνικός µαγνητικός Συντονισµός (NMR) είναι ένα φαινόµενο που συµβαίνει όταν πυρήνες
Βασικές αρχές της Φασµατοσκοπίας NMR Φώτης Νταής Καθηγητής Πανεπιστηµίου Κρήτης, Τµήµα Χηµείας Φασµατοσκοπία NMR Ο Πυρηνικός µαγνητικός Συντονισµός (NMR) είναι ένα φαινόµενο που συµβαίνει όταν πυρήνες
ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ ΙΙ - Ενότητα 6
 Κβαντική Μηχανική ΙΙ Ακ. Ετος 2013-14, Α. Λαχανάς 1/ 25 ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ ΙΙ - Ενότητα 6 Α. Λαχανάς ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ, Τµήµα Φυσικής Τοµέας Πυρηνικής Φυσικής & Στοιχειωδών Σωµατιδίων Ακαδηµαικό έτος
Κβαντική Μηχανική ΙΙ Ακ. Ετος 2013-14, Α. Λαχανάς 1/ 25 ΚΒΑΝΤΙΚΗ ΜΗΧΑΝΙΚΗ ΙΙ - Ενότητα 6 Α. Λαχανάς ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ, Τµήµα Φυσικής Τοµέας Πυρηνικής Φυσικής & Στοιχειωδών Σωµατιδίων Ακαδηµαικό έτος
Ηλεκτρονική Φυσική (Εργαστήριο) ρ. Κ. Ι. ηµητρίου ΙΟ ΟΙ
 Ηλεκτρονική Φυσική (Εργαστήριο) ρ. Κ. Ι. ηµητρίου ΙΟ ΟΙ Για να κατανοήσουµε τη λειτουργία και το ρόλο των διόδων µέσα σε ένα κύκλωµα, θα πρέπει πρώτα να µελετήσουµε τους ηµιαγωγούς, υλικά που περιέχουν
Ηλεκτρονική Φυσική (Εργαστήριο) ρ. Κ. Ι. ηµητρίου ΙΟ ΟΙ Για να κατανοήσουµε τη λειτουργία και το ρόλο των διόδων µέσα σε ένα κύκλωµα, θα πρέπει πρώτα να µελετήσουµε τους ηµιαγωγούς, υλικά που περιέχουν
ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ
 ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Απεικόνιση ηλεκτρονίων ατόμων σιδήρου ως κύματα, διατεταγμένων κυκλικά σε χάλκινη επιφάνεια, με την τεχνική μικροσκοπικής σάρωσης σήραγγας. Δημήτρης
ΗΛΕΚΤΡΟΝΙΑΚΗ ΔΟΜΗ ΤΩΝ ΑΤΟΜΩΝ ΚΑΙ ΠΕΡΙΟΔΙΚΟΣ ΠΙΝΑΚΑΣ Απεικόνιση ηλεκτρονίων ατόμων σιδήρου ως κύματα, διατεταγμένων κυκλικά σε χάλκινη επιφάνεια, με την τεχνική μικροσκοπικής σάρωσης σήραγγας. Δημήτρης
ΠΑΡΑΓΩΓΗ ΜΙΚΡΟΚΥΜAΤΩΝ ΜΕ ΔΙΟΔΟ GUNN
 ΠΑΡΑΓΩΓΗ ΜΙΚΡΟΚΥΜAΤΩΝ ΜΕ ΔΙΟΔΟ GUNN Το φαινόμενο Gunn, ή το φαινόμενο των μεταφερόμενων ηλεκτρονίων, που ανακαλύφθηκε από τον Gunn το 1963 δηλώνει ότι όταν μια μικρή τάση DC εφαρμόζεται κατά μήκος του
ΠΑΡΑΓΩΓΗ ΜΙΚΡΟΚΥΜAΤΩΝ ΜΕ ΔΙΟΔΟ GUNN Το φαινόμενο Gunn, ή το φαινόμενο των μεταφερόμενων ηλεκτρονίων, που ανακαλύφθηκε από τον Gunn το 1963 δηλώνει ότι όταν μια μικρή τάση DC εφαρμόζεται κατά μήκος του
Προβλήματα Κεφαλαίου 2
 Άνοιξη 2018 8/3/2018 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 23,24 και 25 * να παραδοθούν μέχρι τις 22/3/2018 Οι λύσεις των προβλημάτων 26 και 27 * να παραδοθούν μέχρι τις 29/3/2018 1. Θεωρείστε
Άνοιξη 2018 8/3/2018 Προβλήματα Κεφαλαίου 2 Οι λύσεις των προβλημάτων 23,24 και 25 * να παραδοθούν μέχρι τις 22/3/2018 Οι λύσεις των προβλημάτων 26 και 27 * να παραδοθούν μέχρι τις 29/3/2018 1. Θεωρείστε
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός.
 2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
2.3 Είδη χημικών δεσμών: Ιοντικός ομοιοπολικός δοτικός ομοιοπολικός δεσμός. 11.1. Ποια είδη χημικών δεσμών γνωρίζετε; Υπάρχουν δύο βασικά είδη χημικών δεσμών: ο ιοντικός ή ετεροπολικός δεσμός και ο ομοιοπολικός
γ ρ α π τ ή ε ξ έ τ α σ η σ τ ο μ ά θ η μ α Φ Υ Σ Ι Κ Η Γ Ε Ν Ι Κ Η Σ Π Α Ι Δ Ε Ι Α Σ B Λ Υ Κ Ε Ι Ο Υ
 η εξεταστική περίοδος από 9//5 έως 9//5 γ ρ α π τ ή ε ξ έ τ α σ η σ τ ο μ ά θ η μ α Φ Υ Σ Ι Κ Η Γ Ε Ν Ι Κ Η Σ Π Α Ι Δ Ε Ι Α Σ B Λ Υ Κ Ε Ι Ο Υ Τάξη: Β Λυκείου Τμήμα: Βαθμός: Ονοματεπώνυμο: Καθηγητής: Θ
η εξεταστική περίοδος από 9//5 έως 9//5 γ ρ α π τ ή ε ξ έ τ α σ η σ τ ο μ ά θ η μ α Φ Υ Σ Ι Κ Η Γ Ε Ν Ι Κ Η Σ Π Α Ι Δ Ε Ι Α Σ B Λ Υ Κ Ε Ι Ο Υ Τάξη: Β Λυκείου Τμήμα: Βαθμός: Ονοματεπώνυμο: Καθηγητής: Θ
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
