[prnrnpiikoi ηηιοι. Wo. Hs S. SOe. C O O O i -Hs Ή3Ρ. (S-Hs. C0H12 Ο ό Λ ( 9 3. C-f-/
|
|
|
- Δευκαλίων Σπυρόπουλος
- 9 χρόνια πριν
- Προβολές:
Transcript
1 ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ H s S O 4 I V Hs S [prnrnpiikoi ηηιοι 0 f Wo. C0H12 Ο ό Ή3Ρ λ SOe Λ ( H a C = ^ - H z C-f-/ (S-Hs C O O O i -Hs ΟΡΓΑΝΙΣΜΟΣ ΕΚΔΟΣΕΩΝ ΔΙΔΑΚΤΙΚΩΝ ΒΙΒΑΙΩΝ ΑΘΗΝΑ
2 ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ Στέλιος Λιοδάκης Δημήτρης Γάκης εργαστηριακός οδηγός χημείας α Γενικού Λυκείου ΟΕΔΒ ΑΘΗΝΑ
3 Επιστημονικός υπεύθυνος- Διεύθυνση Ομάδων Εργασίας: ΣΤΕΛΙΟΣ ΛΙΟΔΑΚΗΣ Ομάδα συγγραφής ΣΤΕΛΙΟΣ. ΛΙΟΔΑΚΗΣ, Δρ. Χημικός, Επίκουρος Καθηγητής ΕΜΠ ΔΗΜΗΤΡΗΣ. ΤΑΚΗΣ, Δρ. Χημικός Μηχανικός, Λέκτορας ΕΜΠ Ομάδα Τεχνικής Υποστήριξης: ΣΤΑΘΗΣ ΣΙΑΝΟΣ Χημικός Μηχανικός Ε.Μ.Π. ΑΝΝΑ Γ ΑΚΗ, φοιτήτρια στη σχολή Χημικών Μηχανικών ΕΜΠ ΗΡΑΚΛΗΣ ΑΓΙΟΒΛΑΣΙΤΗΣ, φοιτητής στη σχολή Χημικών Μηχανκών ΕΜΠ ΒΛΑΣΗΣ ΠΑΠΑΝΙΚΟΛΑΟΥ, φοιτητής στη σχολή Ηλεκτρολόγων Μηαχανικών ΕΜΠ Υπεύθυνος στο Πλαίσιο του Παιδαγωγικού Ινστιτούτου: Αντώνιος Σ. Μπομπέτσης, Χημικός, M.ed, Ph.D, Σύμβουλος Π.I. Βασιλική N. Περάκη, Δρ. Βιολογίας, Μόνιμη Πάρεδρος του ILI.
4 ΟΔΗΓΙΕΣ ΓΙΑ TH ΧΡΗΣΗ ΕΡΓΑΣΤΗΡΙΑΚΟΥ ΟΔΗΓΟΥ ΓΙΑ ΤΗΝ ΕΚΤΕΛΕΣΗ ΤΩΝ ΠΕΙΡΑΜΑΤΩΝ O εργαστηριακός οδηγός περιλαμβάνει αναλυτικές οδηγίες για τη σωστή και ασφαλή εκτέλεση των πειραμάτων που αναφέρονται. Όμως κάθε πείραμα είναι αποτυχημένο, αν απλώς είναι μια πίστη ακολουθία κάποιων «συνταγών». Χρειάζεται ενεργός συμμετοχή του μαθητή και αυτή πετυχαίνεται μόνον αν αυτός προηγουμένως έχει μελετήσει και κατανοήσει σαφώς τα πάντα γύρω από αυτό. Για να τονισθεί αυτή η ανάγκη στο τετράδιο εργαστηριακών ασκήσεων υπάρχει μια μικρή καινοτομία με παράθεση προκαταρκτικών ερωτήσεων. Πριν λοιπόν μπει κανείς στην εκτέλεση του πειράματος είναι απαραίτητο να μπορεί να εξετάζεται και να απαντά στις ερωτήσεις αυτές. Κατά τα άλλα η δομή του οδηγού είναι λίγο πολύ κλασική. Περιλαμβάνει: 1 ΣΚΟΠΟΣ ΤΟΥ ΠElPAIMΑΤΟΣ Εδώ αναφέρονται οι επιδιωκόμενοι στόχοι, δηλαδή τι αναμένεται να κατέχει ο μαθητής μετά την επιτυχή εκτέλεση του πειράματος. Αυτό δε τόσο σε επίπεδο θεωρίας, όσο και απόκτηση δεξιοτήτων. 2 ΘΕΩΡΗΤΙΚΟ ΥΠΟΒΑΘΡΟ Εδώ αναφέρονται συνοπτικά ορισμένα θέματα θεωρίας τα οποία κατά κανόνα υπάρχουν και στο βιβλίο θεωρίας. Πολλές φορές όμως αναφέρονται επιπλέον θέματα, αν οι ανάγκες και οι σκοποί του πειράματος το απαιτούν. 3 ΑΠΑΙΤΟΥΜΕΝΑ ΟΡΓΑΝΑ, ΣΥΣΚΕΥΕΣ, ΑΝΤΙΔΡΑΣΤΗΡΙΑ ΚΑΙ ΥΛΙΚΑ Εδώ έχουν ταξινομηθεί τα όργανα, οι συσκευές, τα αντιδραστήρια και τα γενικότερα υλικά τα οποία χρειάζονται για τη
5 διεξαγωγή του πειράματος. Πριν την έναρξη πρέπει να γίνεται έλεγχος για το αν αυτά υπάρχουν και αν είναι σωστά τοποθετημένα ή συναρμολογημένα. H καθαριότητα, η τάξη και η πειθαρχία είναι βασικά χαρακτηριστικά κάθε εργαστηριακής δουλειάς. 4 ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ Εδώ περιγράφονται, το δυνατόν λεπτομερειακά, τα βήματα που πρέπει να ακολουθηθούν για την εκτέλεση του πειράματος. Τα βήματα να ακολουθούνται όχι «ρομποτικά», αλλά συνειδητά. Και με πολλά «γιατί». Είναι φανερό ότι πριν κανείς ξεκινήσει το πείραμα οφείλει με προσοχή να μελετήσει τη διαδικασία και να την κατανοήσει πλήρως. Κλείνοντας την μικρή αυτή εισαγωγή πρέπει να τονίσουμε και κάτι εξίσου σημαντικό. To εργαστήριο διδάσκει πολλά πράγματα τα οποία πιθανόν κανείς να τα λησμονήσει. Όμως του δίνει την δυνατότητα να «μάθει τον τρόπο δουλειάς» γενικότερα. Οργάνωση, τάξη και πειθαρχία είναι οι μεγαλύτερο στόχοι που κρύβονται πίσω από τους επιμέρους. «μου το είπαν... το ακουσα το διάβασα... το έμαθα το έκανα... το κατάλαβα»
6 ΠΕΡΙΕΧΟΜΕΝΑ ΕΡΓΑΣΤΗΡΙΑΚΟΎ ΟΑΗΓΟΥ A ' AYKEIOY I ΕΙΣΑΓΩΓΙΚΕΣ ΓΝΩΣΕΙΣ 1.1 Οδηγίες - Κανόνες Ασφάλειας Εργαστηρίου 1.2 Βασικά Όργανα Εργαστηρίου 1.3 Βασικές Εργαστηριακές τεχνικές 1.4 Σφάλματα κατά τις μετρήσεις 1.5 Σημαντικά ψηφία Ασκήσεις ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΕΡΓΑΣΤΗΡΙΑΚΕΣΑΣΚΗΣΕΙΣ ΑΣΚΗΣΕΙΣ 1. Χημικά φαινόμενα 1. Παράγοντες Χημικά φαινόμενα 2. που επηρεάζουν την ταχύτητα 2. Παράγοντες που επηρεάζουν την ταχύτητα διάλυσης διάλυσης 3. Πυροχημική ανίχνευση μετάλλων 3. Χημικές Πυροχημική ανίχνευση 4. αντιδράσεις καιμετάλλων ποιοτική ανάλυση ιόντων 4. Ηλεκτρική αγωγιμότητα διαλυμάτων ηλεκτρολυτών 5. Παρασκευή διαλύματος ορισμένης συγκέντρωσης5. Εύρεση ρη διαλυμάτων με χρήση δεικτών Αραίωση διαλυμάτων 6. Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων 6. Υπολογισμός Θερμότητας Αντίδρασης 7. Παρασκευή διαλύματος ορισμένης συγκέντρωσης7. Ανίχνευση Υδατανθράκων Αραίωση διαλυμάτων 8. Παρασκευή Σαπουνιού ΠΑΡΑΡΤΗΜΑΤΑ
7 1 Εισαγωγικές γνώσεις
8 EfflAME NA ΠΡΟΣΕΞΟΥΜΕ, AΑΛΑ ΟΧΙ ΚΑΙ ΕΤΣΙ!!!!!
9 Εργαστηριακός Οδηγός 1.1 Οδηγίες-κανόνες ασφάλειας εργαστηρίου 1. Μη ξεχνάτε ότι το εργαστήριο είναι χώρος για σοβαρή εργασία. 2. Να έρχεστε πάντα προετοιμασμένοι για το πείραμα που θα εκτελέσετε. 3. Ποτέ μη αυτοσχεδιάζετε, να κάνετε μόνο όσα δίνονται στις οδηγίες. 4. Av πεταχτεί πάνω σας οξύ ή κάποιο καυστικό αντιδραστήριο, ξεπλυθείτε αμέσως με άφθονο νερό. 5. Μη πιάνετε τα αντιδραστήρια με τα χέρια σας. 6. Πριν γίνει χρήση ενός αντιδραστηρίου, διαβάσετε προσεκτικά την ετικέτα. Ποτέ μη κάνετε χρήση ενός αντιδραστηρίου, από φιάλη που δεν έχει ετικέτα. 7. H μετάγγιση καυστικών και τοξικών υγρών με σιφώνιο δεν γίνεται με αναρρόφηση με το στόμα αλλά με πουάρ. 8. Κατά τις αραιώσεις των πυκνών οξέων, ιδιαίτερα του H2SO4, ποτέ δεν προστίθεται το νερό στο οξύ αλλά το οξύ προστίθεται σιγά-σιγά στο νερό. 9. Να ενημερωθείτε για τη θέση / λειτουργία των πυροσβεστήρων. 10. Να ενημερωθείτε για το κουτί πρώτων βοηθειών και τη χρησιμότητα του. 11. Πριν την αποχώρηση σας από το εργαστηριακό χώρο πρέπει να γίνεται σχολαστικός έλεγχος στους διακόπτες παροχής ηλεκτρικού ρεύματος, υγραερίου και νερού.
10 Εργαστηριακός Οδηγός T T H i H I W M TIffHiIf h i III 11 ΙΛΖΦΑ^Κιά^, (με βάση τα συνηθέστερα ατυχήματα) ΠΡΟΣΟΧΗ ΣΤΑ MAT1IA Φοράτε προστατευτικά γυαλιά. Μη θερμαίνετε το δοκιμαστικό σωλήνα στο πυθμένα του, αλλά λίγο παρακάτω από την επιφάνεια του υγρού, ανακινώντας συγχρόνως τον σωιλήνα. Έτσι αποφεύγουμε τον απότομο βρασμό με εκτίναξη του περιεχομένου του. Όχι στους φακούς επαφής, αυτοί μπορούν να παγιδεύσουν στα μάτια σας επικίνδυνα αντιδραστήρια. r Μη ξεχνάτε ότι το θερμό γυαλί δεν ξεχωρίζει από το κρύο. V Αυτό συμβαίνει συνήθως από σπασμένα γυαλιά. Γι' αυτό να χρησιμοποιείται πανί όταν πιέζετε γυάλινους σωλήνες π.χ. όταν περνάτε θερμόμετρο από την τρύπα φελλού. Επίσης η μεταφορά σπασμένων γυαλιών να γίνεται με πανί.
11 5 Εργαστηριακός Οδηγός Σύμβολα επικινδυνότητας χημικών ουσιών Τοξικό Επιβλαβές / εοεθιστικό Διαβρωτικό ΨΨ Εύφλεκτο Εκρηκτικό Ραδιενεργό Τα σύμβολα επικίνδυνων ουσιών αποτελούν ένα τρόπο επισήμανσης τους, ώστε να πάρουμε τα κατάλληλα μέτρα προφύλαξης, όταν χρειαστεί να κάνουμε χρήση τους. Έτσι αποφεύγουμε τυχόν ατυχήματα. Για κάθε ενδεχόμενο καλό είναι να θυμάστε: Πρώτες βοήθειες: 166 Πυροσβεστική υπηρεσία: 199 Τηλεφωνικό κέντρο δηλητηριάσεων:
12 6 1.2 Εργαστήρι. υηγός Βασικά όργανα εργαστηρίου Όργανα Μέτρησης Όγκου Υγρών ml ti < 100 Λ* U H 16 ι? M A I mim Ν nil 2 * 20 Προχοΐδα Σιφώνιο Ογκομετρικός κύλινδρος Ογκομετρική φιάλη 1.Προχοΐδα: όργανο για την ακριβή μέτρηση όγκων υγρών, χρησιμοποιείται κυρίως για την ποσοτική ανάλυση (ογκομετρήσεις). 2.Σιφώνιο εκροής για την ακριβή μέτρηση και μεταφορά ενός σταθερού όγκου υγρού. 3.Ογκομετρικός κύλινδρος: μετραται ο όγκος ενός υγρού με σχετικά μικρή ακρίβεια. 4. Ογκομετρική φιάλη: για τη μέτρηση ορισμένου όγκου υγρού και ιδιαίτερα για την παρασκευή διαλυμάτων ορισμένης συγκέντρωσης.
13 7 Εργαστηριακός Οδηγός Όργανα Μέτρησης Μάζας (Ζυγοί) ' * 1. Εργαστηριακός ζυγός δύο δίσκων. Στον ένα δίσκο βάζουμε την ουσία που θέλουμε να ζυγίσουμε και στον άλλο τα σταθμά. 2. Εργαστηριακός ζυγός ενός δίσκου με βερνιέρο. 3. Σύγχρονοι ηλεκτρονικοί ζυγοί ακριβείας.
14 8 Εργαστηριακός Οδηγός Μερικά Από Τα Πιο Συνηθισμένα Όργανα Χημείας 1. Ογκομετρικός κύλινδρος των 100 ml 2.Χωνί διηθήσεως. 3. Ογκομετρική φιάλη των 250 ml. 4. χωνευτήριο πορσελάνης. 5. Κωνική φιάλη (Erlenmeyer) των 250 ml. 6. Ογκομετρική φιάλη των 100 ml. 7. Δοκιμαστικός σωλήνας. 8. Κωνική φιάλη (Erlenmeyer) των 100 ml. 9. Ποτήρι ζέσεως των 500 ml. 10.Θερμόμετρο. 11. Πορτοκάλι για να γίνει η σύγκριση μεγέθους γάνων. 12. Ογκομετρικός κύλινδρος των 10 ml. TOJV χημικών ορ-
15 Εργαστηριακός Οδηγός Χρήση Σιφωνίου Εκροής re- rf* Παρατηρήσεις α) Με το σιφώνιο μεταφέρεται με μεγάλη ακρίβεια ένας ορισμένος όγκος υγρού από ένα δοχείο σε κάποιο άλλο. H αναρρόφηση από το δοχείο στο σιφώνιο γίνεται με το στόμα, αν το υγρό δεν είναι τοξικό ή καυστικό. Σ' αντίθετη περίπτωση, η αναρρόφηση του υγρού γίνεται με τη βοήθεια ελαστικής σφαίρας (πουάρ), όπως φαίνεται στο σχήμα. β) H τελευταία σταγόνα που μένει στην άκρη του σιφωνίου έχει υπολογιστεί κατά τη βαθμονόμηση του σιφωνίου και γι' αυτό δεν πρέπει να αποφυσάται.
16 10 Εργαστηριακός Οδηγός Συνήθη Σιδερένια Σκεύη ,, ^8«ίΜ»ί8 Μεταλλικό στήριγμα Rf?
17 11 Εργαστηριακός Οδηγός 1.3 Βασικές Εργαστηριακές Τεχνικές Διήθηση H διήθηση είναι η πιο συνηθισμένη μέθοδος διαχωρισμού στερεού από υγρό. Βασίζεται στην αδυναμία του στερεού να περάσει λόγω μεγέθους μέσα από τους πόρους του ηθμού (φίλτρο). Έτσι το στερεό συγκρατείται στο ηθμό (ίζημα), ενώ το υγρό διαπερνά τον ηθμό (διήθημα). Υπάρχουν διάφορα είδη ηθμών τα οποία έχουν διαφορετική διάμετρο πόρων, ώστε να χρησιμοποιούνται για ανάλογα ιζήματα O ηθμός πριν την τοποθέτηση του στο χωνί διπλώνεται, όπως φαίνεται στο παρακάτω σχήμα: «S. ' I 11.- Τ M M r mmm MB ta ΣΧΗΜΑ 1.1 Πως διπλώνεται ο ηθμός. Αμέσως μετά την τοποθέτηση του ηθμού στο χωνί αυτός διαβρέχεται με λίγο απιονισμένο νερό ή λίγο από το υπερκείμενο υγρό του μείγματος που πρόκειται να διηθήσουμε. Ακολουθεί η διήθηση, όπως φαίνεται στο παρακάτω σχήμα.
18 12 Εργαστηριακός Οδηγός ΣΧΗΜΑ 1.2 Διάταξη διήθησης και στη λεπτομέρεια η αρχή λειτουργία διήθησης. Να σημειωθεί ότι αν το χωνί έχει μακρύ στέλεχος εκροής και μικρή διάμετρο, τότε λόγω των τριχοειδών φαινομένων η διήθηση γίνεται γρηγορότερα (χωνί ταχείας διηθήσεως). To ίζημα που λαμβάνεται εκπλένεται για να απαλλαγεί από το τυχόν προσμίξεις που περιέχει με κατάλληλο υγρό έκπλυσης. Έτσι παίρνουμε καθαρό ίζημα. To ίζημα στη συνέχεια τοποθετείται σε ύαλο ωρολογίου και τοποθετείται στο πυριατήριο προς ξήρανση. To πυριατήριο είναι ηλεκτρική συσκευή θέρμανσης με μεταλλικά ράφια στα οποία τοποθετούνται τα προς ξήρανση υλικά. Στην περίπτωση που αποτυγχάνει η μέθοδος της διήθησης να διαχωρίσει το στερεό, π.χ. το ίζημα διαπερνά τους πόρους του ηθμού, η εναλλακτική λύση είναι η φυγοκέντρηση. To διάλυμα τοποθετείται στους σωλήνες φυγοκέντρισης και περιστρέφεται με μεγάλη ταχύτητα σε κατάλληλη συσκευή. Στην περίπτωση αυτή το ίζημα κολλάει στον πυθμένα του σωλήνα και διαχωρίζεσαι από το υπερκείμενο υγρό με απόχυση.
19 13 Εργαστηριακός Οδηγός Χωνί διήθημα Λ ε π τ ο μ έ ρ ε ι ε ς α π ό τη διαδικασία της δ ι ή θ9ηση ησης
20 14 Εργαστηριακός Οδηγός Απόσταξη H απόσταξη είναι μέθοδος διαχωρισμού ή καθαρισμού ενός ομογενούς μίγματος (διαλύματος), λόγω της διαφοράς στα σημεία βρασμού μεταξύ των διαχωριζομένων συστατικών. H διάταξη μιας απλής απόσταξης δίνεται στο παρακατω σχήμα. H διαδικασία της απόσταξης με λίγα λόγια είναι η εξής: Βάζουμε το υγρό που θέλουμε να αποστάξουμε στον κλασματι)ρα, που είναι μια σφαιρική φιάλη μ' ένα πλάγιο σωλήνα (περίπου μέχρι τη μέση). Τοποθετούμε το θερμόμετρο στο στόμιο του κλασματήρα σε τέτοιο ύψος, ώστε το άκρο του θερμομέτρου να βρίσκεται στο ύψος του πλάγιου σωλήνα του. Στη συνέχεια θερμαίνουμε το υγρό, οπότε αρχίζει ο βρασμός του. Οι παραγόμενοι ατμοί περνούν στο ψυκτήρα, που ένας σωλήνα με διπλά τοιχώματα από όπου περνά το υγρό ψύξεως (συνήθως νερό). Εκεί οι ατμοί του αποσταζόμενου υγρού συμπυκνώνονται και στη συνέχεια συλλέγονται στο υποδοχέα σταγόνα - σταγόνα. Αυτό είναι το απόσταγμα, ενώ το υγρό που παρέμεινε στο κλασματήρα αποτελεί το υπόλειμμα της απόσταξης. Να σημειωθεί ότι για να αποφύγουμε απότομο βρασμό και εκτινάξεις σταγονιδίων από τον κλασματήρα, προσθέτουμε γυάλινα σφαιρίδια ή κομμάτια πορσελάνης στο υγρό που αποστάζουμε κατά την έναρξη της απόσταξης (πυρήνες βρασμού). H απόσταξη μπορεί να χρησιμοποιηθεί για την παρασκευή αποσταγμένου νερού ή την απόσταξη κρασιού για την παρασκευή κονιάκ κλπ. H απόσταξή που περιγράψαμε είναι η απλή απόσταξη. Πέραν αυτής υπάρχουν πολλά είδη απόσταξης, πχ απόσταξη υπό κενό, με υδρατμούς, κλασματική κλπ. To τελευταίο είδος περιλαμβάνει πολλές διαδοχικές απλές αποστάξεις δηλαδή, το απόσταγμα αποστάζεται ξανά και το νέο απόσταγμα ξανά κοκ. H κλασματική απόσταξη βρίσκει εφαρμογή στη διύλιση του πετρελαίου.
21 15 D D I= D δ W =L IO W O «Εργαστηριακός Οδηγός
22 16 Εργαστηριακός Οδηγός Εξάτμιση H εξάτμιση αποσκοπεί στην μερική ή ολική απομάκρυνση του διαλύτη (νερό) από το διάλυμα. Κατά την εξάτμιση ελαττώνεται ο όγκος του διαλύματος, οπότε συμπυκνώνεται το διάλυμα. Av συνεχιστεί η εξάτμιση, τότε απομακρύνεται εντελώς το διαλυτικό μέσο και το διαλυμένο σώμα παραμένει σε στερεή κατάσταση. To στερεό αυτό σώμα λέγεται στερεό υπόλειμμα και η διαδικασία καλείται εξάτμιση μέχρι ξηρού. H εξάτμιση γίνεται συνήθως σε κάψες πορσελάνης σε ειδικές συσκευές, όπως είναι τα ατμόλουτρα ή αμμόλουτρα. Τα ατμόλουτρα είναι μεταλλικά δοχεία που περιέχουν νερό, το οποίο θερμαίνεται συνήθως ηλεκτρικά. Οι παραγόμενοι ατμοί υδρατμοί θερμαίνουν το διάλυμα που πρόκειται να εξατμίσουμε. Ανάλογα τα αμμόλουτρα είναι δοχεία που περιέχουν άμμο που θερμαίνεται ομοιόμορφα. Στην επιφάνεια της άμμου τοποθετείται η κάψα με το προς εξάτμιση διάλυμα. στερεό υπόλειμμα ατμός διάλυμα Λ π ΣΧΗΜΑ 1.4 Διάταξη εξάτμισης στερεό υπόλειμμα
23 17 Εργαστηριακός Οδηγός Κ ά ψ α γυάλινη Πλέγμα αμιάντου Λύχνος Bunsen Τρίποδας στήριξης Λεπτομέρειες στη δ ι ά τ α ξ η ε ξ ά τ μ ι σ η ς
24 18 Εργαστηριακός Οδηγός θέρμανση - Πύρωση H θέρμανση αποτελεί μια από τις βασικές διεργασίες στο χημικό εργαστήριο. Αυτό συμβαίνει επειδή πολλές χημικές αντιδράσεις γίνονται σε υψηλές μόνο θερμοκρασίες. Επίσης, πολλές φυσικές διεργασίες, όπως η απόσταξη, η εξάτμιση κλπ, απαιτούν θέρμανση. Συνηθίζουμε να λέμε θέρμανση, όταν η αύξηση της θερμοκρασίας φτάνει τους 500 0C και πύρωση, όταν ξεπερνά τους 500 0C. Οι πιο συνηθισμένοι τύποι καυστήρων που χρησιμοποιούνται στο εργαστήριο είναι ο λύχνος Bunsen και Teclu που εικονίζονται στο παρακάτω σχήμα. ΣΧΗΜΑ 1.5 Από αριστερά π ρ ο ς τα δεξιά λύχνος Bunsen 1 λύχνος Teclu, καυστήρας τύπου Bunsen με ενσωματωμένη φιάλη υγραερίου.
25 19 Εργαστηριακός Οδηγός Με τους λύχνους μπορούν να επιτύχουμε πολύ υψηλές θερμοκρασίες. H θερμοκρασία της φλόγας εξαρτάται από το ύψος αυτής, το είδος του καυσίμου, την αναλογία καυσίμου - αέρα και τον τύπο του λύχνου. 1500uC 1600uC Ανάμιξη καυσίμου αέρα 300 0C Ρύθμιση αέρα Εισαγωγή καυσίμου ΣΧΗΜΑ 1.6 H θερμοκρασία π ο υ αναπτύσσεται συσχετίζεται με το ύψος της φλόγας.
26 20 Εργαστηριακός Οδηγός Λλλα βοηθητικά όργανα πύρωσης είναι τα τρίγωνα πορσελάνης, τα χωνευτήρια, τα πλέγματα αμιάντου, οι τρίποδες πυρώσεως κλπ. Στο παρακάτω σχήμα εικονίζεται διάταξη πύρωσης σε χωνευτήριο με τη βοήθεια λύχνου. M' αυτό τον τρόπο μπορούμε να πετύχουμε τη σύντηξη (λιώσιμο) στερεών σωμάτων υψηλού σημείου τήξης. Να σημειωθεί ότι το ίδιο αποτέλεσμα μπορεί να επιτευχθεί και με ηλεκτρική θέρμανση ( ηλεκτρικοί κάμινοι). ΣΧΗΜΑ 1.7 Σύντηξη με π ύ ρ ω σ η με λύχνο Bunsen.
27 Εργαστηριακός Οδηγός To παρακάτω -σχήμα απεικονίζει διάταξη θέρμανσης ουσίας σε δοκιμαστικό σωλήνα. To συνηθισμένο όμως γυαλί αντέχει μέχρι C, γι' αυτό συνήθως μεταξύ φλόγας και γυαλιού παρεμβάλλεται ειδικό πλέγμα. Γυαλί από Pyrex αντέχει μέχρι τους C, ενώ τα πυρίμαχα πχ. το χωνευτήριο πορσελάνης έχει θερμική αντοχή που ξεπερνά τους C. σφικτήρας y στήριγμα Αοκιμ αστικό σωλήνας Λύχνος Bunsen ΣΧΗΜΑ 1.8 Διάταξη θέρμανσης.
28 22 Εργαστηριακός Οδηγός Κατά τη θέρμανση αντιδραστηρίων με δοκιμαστικούς σωλήνες πρέπει να είμαστε ιδιαίτερα προσεκτικοί για να αποφύγουμε ατυχήματα από την εκτίναξη σταγονιδίων από το σωλήνα. Ποτέ δε στρέφουμε το στόμιο του σωλήνα στο πρόσωπο μας ή στο πρόσωπο άλλου. To καλύτερο που μπορούμε να κάνουμε κατά τη διάρκεια μιας θερμικής διεργασίας είναι να προστατεύσουμε τα μάτια μας, φορώντας προστατευτικά γυαλιά. 1
29 23 Εργαστηριακός Οδηγός 1.4 Σφάλματα κατά τις μετρήσεις To σφάλμα (E) σε μια μέτρηση αναφέρεται στην αριθμητική διαφορά ανάμεσα στην πειραματική τιμή (χ) και την πραγματική τιμή C"), δηλαδή E = χ-μ. Τα σφάλματα διακρίνονται σε συστηματικά, π.χ. σφάλματα λόγω του τύπου του ζυγού που χρησιμοποιούμε και σε τυχαία, π.χ. αν ξεχάσουμε να καθαρίσουμε το ζυγό πριν τη μέτρηση. Ακρίβεια είναι ο βαθμός συμφωνίας ανάμεσα ση/ν πειραματική και πραγματική τιμή. Προφανώς όσο μικρότερο είναι το σφάλμα, τόσο μεγαλύτερη είναι η ακρίβεια. Μπορούμε να κάνουμε έλεγχο της ακρίβειας μιας μέτρησης χρησιμοποιώντας πρότυπο δείγμα, δηλαδή ουσία της οποίας το προσδιοριζόμενο μέγεθος είναι εκ των προτέρων γνωστό. Λναπαραγωγιμότητα ή επανα/,ηπτικότητα εκφράζει τι] συμφωνία που δείχνουν οι πειραματικές τιμές μεταξύ τους. H ακρίβεια και η αναπαραγωγιμότητα δεν πρέπει να συγχέονται. Καλή ακρίβεια δε σημαίνει κατ' ανάγκη και καλή αναπαραγωγιμότητα και το αντίστροφο, όπως φαίνεται στο παρακατω σχήμα. ΣΧΗΜΑ 1.9 α) μικρή ακρίβεια και αναπαραγωγιμότητα β) μικρή ακρίβεια με μεγάλη αναπαραγωγιμότητα γ) μεγάλη ακρίβεια και αναπαραγωγιμότητα.
30 24 Εργαστηριακός Οδηγός 1.5 Σημαντικά ψηφία Όλα τα ψηφία ενός αριθμού θεωρούνται βέβαια εκτός από το τελευταίο που θεωρείται αβέβαιο. Ta βέβαια ψηφία μαζί με το αβέβαιο δίνουν τον αριθμό των σημαντικών ψηφίων Για παράδειγμα σε 9,12 g έχουμε 3 σημαντικά ψηφία, ενώ σε 11,245 g έχουμε 5 σημαντικά ψηφία. Γενικά, θα πρέπει να γνωρίζουμε: 1) τα μηδενικά που βρίσκονται ανάμεσα σε άλλα ψηφία θεωρούνται σημαντικά π.χ. ο αριθμός 55,002 έχει 5 σημαντικά ψηφία. 2) τα μηδενικά που βρίσκονται στην αρχή ενός αριθμού δεν είναι σημαντικά π.χ. ο αριθμός 0,0021 έχει 2 σημαντικά ψηφία. 3) τα μηδενικά που βρίσκονται δεξιά της υποδιαστολής είναι σημαντικά π.χ. ο αριθμός 0,6021 έχει 4 σημαντικά ψηφία. 4) τα μηδενικά στο τέλος ενός αριθμού που δεν έχει υποδιαστολή μπορεί να είναι σημαντικά ή όχι, π.χ. ο αριθμός 150 έχει δύο ή τρία σημαντικά ψηφία, ενώ ο αριθμός 1400 έχει δύο ή τρία ή τέσσερα σημαντικά ψηφία. H εκθετική μορφή ενός αριθμού είναι : A x 10 μ Οπου, A είναι ένας δεκαδικός αριθμός με ένα μη μηδενικό ψηφίο πριν την υποδιαστολή και μ ακέραιος αριθμός. Για παράδειγμα ο αριθμός 500 με ακρίβεια δύο σημαντικών ψηφίοjv γράφεται 5,0 χ IO2. Επίσης, η ταχύτητα του φωτός με ακρίβεια τριών δεκαδικών ψηφίων γράφεται 3,00 x IO8 m s 1. Αριθμητικές πράξεις και σημαντικά ψηφία 1) Στον πολλαπλασιασμό και τη διαίρεση το τελικό αποτέλεσμα έχει τα σημαντικά ψηφία του μικρότερου σε ακρίβεια (σημαντικά ψηφία) αριθμού. π.χ. 26,19 (4σψ) x 11,12(4<τψ) χ 1,00(3σψ) = 291,23^28=291(3σψ). 2) Στην πρόσθεση και αφαίρεση το τελικό αποτέλεσμα έχει τόσα δεκαδικά ψηφία, όσα ο αριθμός με τα λιγότερα δεκαδικά ψηφία, π.χ. 26,2 (ΐδψ) + 11,21 (2δψ) + 0,005(3δψ) = 37,4jo=37,4(1 δψ).
31 25 Εργαστηριακός Οδηγός -τρογγυλοποίηση αριθμητικών αποτελεσμάτων Av για τη στρογγυλοποίηση ενός αριθμητικού αποτελέσματος πρέπει να απορριφθεί ένα ψηφίο, έστω το χ, τότε ακολουθείται ο εξής κανόνας: 1) αν χ είναι μικρότερο του 5, τότε το ψηφίο που προηγείται του χ παραμένει αμετάβλητο. Π.χ. η στρογγυλοποίηση του αριθμού 7,248 σε δύο σημαντικά ψηφία είναι 7,2. 2) αν χ είναι μεγαλύτερο ή ίσο του 5, τότε το ψηφίο που προηγείται του χ μεγαλώνει κατά μία μονάδα. Π.χ. η στρογγυλοποίηση του αριθμού 4,945 σε τρία σημαντικά ψηφία είναι 4,95. Ασκήσεις 1. Να γραφούν σε εκθετική μορφή οι παρακάτω αριθμοί: α) β) 425,6 γ) 0,00256 δ) ε) 0, Πόσα είναι τα σημαντικά ψηφία στους παρακάτω αριθμούς; α) 0,00123 β) 7,310 γ) 322 δ) 2,574 x IO"3 ε) 2.00 χ IO"5. 3.Να γίνουν οι παρακάτω υπολογισμοί και να εκφραστούν τα αποτελέσματα σε εκθετική μορφή με βάση τον κατάλληλο αριθμό σημαντικών ψηφίων: α) , ,0223 β) 217,843/0,025 γ)18,55-0,02-1,001 δ) (2,7χ103) χ (3,005x10"2).
32 2 Εργαστηριακές ασκήσεις A' Λυκείου
33 % αντίδραση ανθρακικού ί.ίσβεστίου? με οιαζ-υμα
34 29 Πείραμα Πείραμα 1 ΧΗΜΙΚΑ ΦΑΙΝΌΜΕΝΑ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς: 1. Να εξηγείς ότι σε ένα χημικό φαινόμενο παρατηρούνται αλλαγές που εκδηλώνονται πολλές φορές με δημιουργία ιζημάτων, αλλαγές χρώματος, έκλυση αερίου και μεταβολή στη θερμοκρασία. 2. Να αναγνωρίζεις ότι ένα χημικό φαινόμενο μπορεί να παρασταθεί με μία χημική εξίσωση η οποία δίνει ποιοτικές και ποσοτικές πληροφορίες για το φαινόμενο. ΕΙΣΑΓΩΓΗ ΣΤΟ ΘΕΜΑ Κάθε χημικό φαινόμενο είναι και μια μεταβολή, ριζική θα έλεγε κανείς, των σωμάτων που συμμετέχουν. Αυτά είναι τα λεγόμενα αντιδρώντα σώματα. H αλλαγή αυτή μπορεί να γίνει άμεσα αντιληπτή κυρίως αν συνοδεύεται από : ίζημα, χρώμα, αέριο ή αλλαγή στη θερμοκρασία. Στις περισσότερες των περιπτώσεων η μεταβολή που γίνεται δεν αντιστρέφεται, τουλάχιστον με απλό τρόπο. Πάρτε για παράδειγμα την οξείδωση του σιδήρου (ένα μέταλλο στερεό, συνεκτικό) η οποία θα δώσει οξείδιο του σιδήρου, Fe2O3 (μια καφεκόκκινη σκόνη): 4 Fe + 3 Ο2» 2Fe Για να ξαναπάρει κανείς το Fe πρέπει να καταφύγει σε άλλη αντίδραση π.χ. θέρμανση του οξειδίου με C : 2 Fe2O3 +3 C > 4 Fe +3 CO2 Για μια μεγάλη κατηγορία αντιδράσεων, γνωστή ως καύση, κύριο χαρακτηριστικό είναι η έκλυση ποσοτήτων θερμότητας προς
35 30 Πείραμα 1 το περιβάλλον, πράγμα το οποίο ανεβάζει τη θερμοκρασία του τελευταίου. Αυτές είναι οι εξώθερμες αντιδράσεις. Π.χ C + O2 > CO2 + Q (Q = θερμότητα) Av σ' ένα διάλυμα CuSO4 το οποίο έχει χρώμα μπλε εμβαπτιστεί ένα σιδερένιο καρφί, τότε το μεν καρφί θα καλυφθεί από μία στρώση ερυθρωπού χαλκού, το δε διάλυμα θα χάνει προοδευτικά το χρώμα του. H μεταβολή αυτή παριστάνεται με την αντίδραση: Fe + CuSO4 > FeSO4 + Cu Av σε διάλυμα σόδας, NaHCO3, ρίξει κανείς σταγόνες από λεμόνι θα παρατηρηθεί ένας αφρισμός, λόγω έκλυσης ενός αερίου που είναι το CO2: NaHCO3 + οξύ -> + CO2T Χημικά φαινόμενα γίνονται διαρκώς γύρω μας, μέσα μας, παντού. Από την «τρύπα του όζοντος» μέχρι τις ηφαιστειακές εκρήξεις, από το μάσημα μιας σοκολάτας ως το μεταβολισμό της, από την εξόρυξη ενός ασβεστόλιθου μέχρι την παραγωγή τσιμέντου ή γυαλιού, τα πάντα γίνονται, καλύπτονται, με και από χημικές αντιδράσεις. Στο πείραμα που ακολουθεί θα παρακολουθήσετε την πορεία ενός κομματιού χαλκού, Cu. Αυτό θα υποστεί ένα σύνολο μεταβολών, αντιδράσεων, οι οποίες μάλιστα θα φαίνονται και με απλή παρατήρηση. ΟΡΓΑΝΑ ΚΑΙ ΧΗΜΙΚΕΣ ΟΥΣΙΕΣ Για την εκτέλεση του πειράματος θ' απαιτηθούν: 1. 6 μεγάλοι δοκιμαστικοί σωλήνες. 2. Έλασμα από καθαρό χαλκό. 3. Διάλυμα HNO3 ( 1:2 ή 1 ml πυκνό και 2 ml νερό). 4. Διάλυμα NaOH 1 Μ. 5. Ογκομετρικός κύλινδρος των 10 ml. 6. Ένα μεγάλο σιδερένιο καρφί.
36 31 Πείραμα 1 ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ Από το έλασμα του χαλκού κόβονταν δύο κομμάτια βάρους περίπου 0,2 g το καθένα και ρίπτονται σε δύο σωλήνες (ένα στον καθένα). Σε κάθε σωλήνα προστίθενται από 5 ml από το αραιωμένο διάλυμα του ΗΝΟ3. Σημειώστε τις μεταβολές στο χρώμα του διαλύματος. Ti γίνεται με το κομμάτι του Cu; Στον ένα από τους δύο σωλήνες προσθέστε 5 ml από το διάλυμα του NaOH. Σημειώστε το χρώμα του ιζήματος που καταβυθίζεται και τη τυχόν αλλαγή στο χρώμα του διαλύματος. Στον άλλο εμβαπτίστε το σιδερένιο καρφί το οποίο έχετε προηγουμένως ζυγίσει. Περιμένετε 5 min και μετά ανασύρετε το καρφί. Ti παρατηρείτε; To καρφί στη συνέχεια ξεπλένεται με νερό, προσεκτικά, ξηραίνεται με μαλακό χαρτί και ζυγίζεται. Σημειώστε τη νέα μάζα. Στη συνέχεια, να χύσετε το υπερκείμενο διάλυμα στο σωλήνα με το ίζημα και να μεταφέρετε το ίζημα στην κάψα Να θερμάνετε την κάψα στη φλόγα του λύχνου και να σημειώσετε την αλλαγή στο χρώμα του στερεού. Σ Χ Η Μ Α 1.1 Επίδραση NaOH και καταβύ.2 θιση Cu + υ π ό μορφή Cu(OH) 2.
37 Πείραμα 1 32 ΣΧΗΜΑ 1.2 Διάλυση Cu σε πυκνό ΗΝΟ3 με έκλυση ατμών NO2, fx#-**, (,' ^ ','4^, ν ****** ΣΧΗΜΑ 1.3 Επίδραση Fe σε διάλυμα ιόντων Cu +. To μεταλλικό καρφί επικαλύπτεται με μεταλλικό Cu.
38 33 Πείραμα 2 Πείραμα 2 ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ SiM ¾. ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι αποτέλεσμα «ανταγωνισμού» δυνάμεων μεταξύ μορίων (ή ιόντων) διαλυμένης ουσίας - διαλύτη και διαλυμένης ουσίας - διαλυμένης ουσίας. 2,Να ορίζεις την ταχύτητα διάλυσης και να αναλύεις τους παράγοντες που μπορούν να επηρεάζουν την ταχύτητα, με την οποία ένα στερεό διαλύεται σε ένα διαλύτη. ΕΙΣΑΓΩΓΗ ΣΤΟ ΘΕΜΑ Για να μπορέσει κανείς να μελετήσει τους παράγοντες που επηρεάζουν την ταχύτητα διόύ.υσης ενός στερεού σε ένα διαλύτη, π.χ. στο νερό, πρέπει να καταλάβει πρώτα από όλα δύο πράγματα. To ένα είναι ο μηχανισμός ή τα «βήματα» με τα οποία γίνεται αυτή η διάλυση. To άλλο είναι να ορίσει την ταχύτητα της διάλυσης, καθώς και τον τρόπο με τον οποίο αυτή θα μετρηθεί. Ωστόσο, θα πρέπει να τονίσουμε ότι οι δομικές μονάδες ενός κρυσταλλικού στερεοί) (μόρια ή ιόντα ), συγκρατούνται στις θέσεις τους με δυνάμεις είτε χημικού δεσμού είτε δια-μοριακές. Όταν εισαχθεί ο κρύσταλλος στο διαλύτη (συνήθως νερό) τα μόρια ή ιόντα του αρχικά περιβάλλονται από τα μόρια του διαλύτη. Αυτό γίνεται μια και αναπτύσσεται μια νέα δύναμη μεταξύ μορίων διαλύτη και δομικών μονάδων του στερεού. Υπάρχουν δηλαδή συνολικά τρεις δυνάμεις. H μία αναπτύσσεται μεταξύ των δομικών μονάδων του στερεού, η άλλη μεταξύ των μορίων του δια-
39 34 Πείραμα 2 λύτη και η τρίτη μεταξύ των μορίων του διαλύτη και των δομικών μονάδων του στερεού. Ανάλογα τώρα με την ένταση των δυνάμεων αυτών - η οποία εξαρτάται από τη φύση του στερεού και του διαλύτη - και από τις συνθήκες διάλυσης (π.χ. θερμοκρασία), είναι δυνατόν οι δυνάμεις μεταξύ μορίων διαλύτη και δομικών μονάδων του στερεού να υπερισχύσουν των δύο άλλων. Τότε το μόριο ή ιόν περιβάλλεται από κάποια μόρια διαλύτη, δηλαδή διαλύεται. Άρα για δεδομένα στερεό και διαλύτη, οι παράγοντες που επηρεάζουν τη διάλυση, θα είναι εκείνοι οι οποίοι θα μεταβάλλουν την ένταση των δυνάμεων μεταξύ των μορίων του διαλύτη, καθώς και μεταξύ των δομικών μονάδων του στερεού. Τέτοιοι παράγοντες είναι: α. H θερμοκρασία. H αύξηση της θερμοκρασίας του διαλύματος κάνει τα μόρια του διαλύτη, αλλά και του στερεού, πιο ευκίνητα, β. H ανάδευση του διαλύματος, η οποία έχει μικρότερο, αλλά ανάλογο αποτέλεσμα, με τη θερμοκρασία. H ανάδευση επιπλέον, ομογενοποιεί το διάλυμα, αραιώνοντάς το κυρίως γύρω από τον κρύσταλλο. γ. H επιφάνεια επαφής στερεού. Προφανώς, όσο μεγαλύτερος είναι ο αριθμός των δομικών μονάδων του στερεού, οι οποίοι έρχονται σε επαφή με το διαλύτη, τόσο ταχύτερη είναι η διάλυση. O αριθμός αυτός εξαρτάται από την επιφάνεια του στερεού σε επαφή με το διαλύτη. Όσο πιο λεπτόκοκκο είναι το στερεό, τόσο μεγαλύτερη επιφάνεια παρουσιάζει στο διαλύτη και τόσο γρηγορότερη είναι η διάλυση. Όσον αφορά την ταχύτητα της διάλυσης, αυτή μπορεί να οριστεί σαν η ποσότητα της ουσίας, η οποία διαλύεται στη μονάδα του χρόνου σε ορισμένο ποσό διαλύτη, κάτω από ορισμένες συνθήκες. Για ευδιόλυτα σώματα ορίζεται συνήθως σε g ανά 100 ml διαλύτη στην μονάδα του χρόνου (π.χ. 5 ). H μέτρησή της ταχύτητας μπορεί να βασιστεί στην εξάτμιση μέχρι ξηρού του διαλύματος και ζύγιση του στερεού υπολείμματος. Στο πείραμα που ακολουθεί θα μελετηθεί η επίδραση των παρακάτω παραγόντων στη ταχύτητα διάλυσης της ζάχαρης: θερμοκρασία, ανάδευση και μέγεθος κόκκων.
40 35 Πείραμα 2 ΟΡΓΑΝΑ ΚΑΙ ΧΗΜΙΚΕΣ ΟΥΣΙΕΣ Πα την εκτέλεση του πειράματος απαιτούνται: 1. Δύο ποτήρια ζέσεως των 250 ml. 2. Διάταξη διήθησης με χωνί, στήριγμα, δακτύλιο στήριξης, ηθμούς, υάλινα ραβδιά. 3. Κάψα πορσελάνης με 12 cm διάμετρο και μία ύαλος ωρολογίου αντίστοιχη. 4. Λύχνο και πλέγμα. 5. Μικρό γουδί από πορσελάνη. 6. Θερμόμετρο. 7. Ποτήρι ζέσεως των 400 ml σαν υδρόλουτρο. 8. Ογκομετρικός κύλινδρος των 10 ml. 9. Χρονόμετρο. 10. Ζάχαρη σε κύβους και μικροκρυσταλλική. ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ α. μελέτη της επίδρασης της θερμοκρασίας 1. Σε ποτήρι ζέσειος τ(ον 100 ml φέρονται 50 ml απιονισμένο νερό και μετριέται η θερμοκρασία του (~ 20 0C). Ζυγίζονται τώρα 20 g ζάχαρης και ρίχνονται στο ποτήρι, ενώ ταυτόχρονα με την ρίψη αρχίζει η μέτρηση του χρόνου. Χωρίς καμία άλλη επέμβαση, μετά την πάροδο 5 min,διηθείται το διάλυμα και συλλέγεται στην κάψα, η οποία προηγουμένως έχει ζυγιστεί με ακρίβεια. To διάλυμα τώρα καλύπτεται με την ύαλο ωρολογίου και εξατμίζεται μέχρι ξηρού, προσεκτικά με μικρή φλόγα. Μετά την ψύξη της, ζυγίζεται η κάψα και σημειώνεται η ποσότητα του στερεού εκ διαφοράς. 2. Σε ποτήρι ζέσεως τοον 400 ml προστίθεται ποσότητα νερού βρύσης και θερμαίνεται με μικρή φλόγα, ώστε η θερμοκρασία να φτάσει τους ~ 60 C. Μετριέται τότε ακριβέστερα η θερμοκρασία και συντηρείται με τη μικρή φλόγα. Επαναλαμβάνουμε τη
41 36 Πείραμα 2 διαδικασία που περιγράφτηκε στο 1 και προσδιορίζουμε την ποσότητα της ζάχαρης η οποία διαλύεται σε 5 min στους =60 C. β. μελέτη της επίδρασης της ανάδευσης Επαναλαμβάνεται η ίδια με την αρχική διαδικασία (θερμοκρασία σταθερή και ίση με του περιβάλλοντος), μόνο που κατά την διάρκεια των 5 min το μίγμα αναδεύεται σταθερά με την υάλινη ράβδο. Σημειώνεται η ποσότητα της ζάχαρης που διαλύεται. γ. μελέτη της κοκκομετρίας Θα επαναληφθεί η ίδια διαδικασία μόνο που η αρχική ποσότητα της ζάχαρης είναι σε μορφή κύβων ακμής = Icm. Av υπάρχει ευχέρεια χρόνου μπορεί σε άλλη μέτρηση να χρησιμοποιηθεί ζάχαρη η οποία προηγουμένα>ς έχει λειοτριβηθεί στο γουδί, ώστε να γίνει αναφής σκόνη (άχνη). Και στις δύο περιπτώσεις σημειώνεται η ποσότητα της ζάχαρης η οποία διαλύθηκε στα 5 αυτά λεπτά της ώρας.
42 37 Πείραμα 3 Πείραμα 3 ΠΥΡΟΧΗΜΙΚΗ ΑΝΙΧΝΕΥΣΗ ΜΕΤΑΛΛΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το χρώμα μιας φλόγας αλλάζει ανάλογα με την παρουσία διαφόρου αλάτων. 2. Να ορίζεις το φάσμα εκπομπής διαφόρων στοιχείων και τη χρήση του σα «δακτυλικό αποτύπωμα» στην ανίχνευση των στοιχείων. 3. Να αναγνωρίζεις ότι ο πυροχημικός έλεγχος είναι μια μέθοδος ποιοτικής ανάλυσης. ΕΙΣΑΓΩΓΗ ΣΤΟ ΘΕΜΑ Θέρμανση μιας ουσίας ουσιαστικά σημαίνει προσφορά ενέργειας σ' αυτή. Ενέργεια η οποία αυξάνει όσο αυξάνει η θερμοκρασία. Τα αποτελέσματα της θέρμανσης αυτής ποικίλλουν ανάλογα με το είδος της ουσίας η οποία θερμαίνεται. Ένα από τα φαινόμενα που περιμένουμε είναι η διάσπαση της ουσίας στα στοιχεία που την αποτελούν και η απελευθέρωση τους σε μορφή ατόμων ή ιόντων. Αυτό συνήθους γίνεται αφού προηγουμένως η ένιυση περάσει τα στάδια της τήξης και της εξαέρωσης. Στη συνέχεια και εφόσον η πηγή ενέργειας είναι ικανή, γίνεται διέγερση ατόμων που εκδηλώνεται με άλματα ηλεκτρονίων σε στιβάδες μεγαλύτερης ενέργειας. H φάση αυτή κρατά κλάσματα του δευτερολέπτου. Τα ηλεκτρόνια που επιστρέφουν στην αρχική τους ενεργειακή στάθμη εκπέμπουν την επιπλέον ενέργεια με μορφή ηλεκτρομαγνητικής ακτινοβολίας. Μέρος της ακτινοβολίας αυτής ανήκει στην περιοχή του ορατού φωτός με αποτέλεσμα, στην προκειμένη περίπτωση, τον χραιματισμό της φλόγας.
43 38 Πείραμα 3 Εκείνα τα στοιχεία τα οποία διεγείρονται ευκολότερα είναι τα μέταλλα και μάλιστα τα ελαφρά, όπως τα αλκάλια και οι αλκαλικές γαίες. Επειδή δε η ηλεκτρονιακή δομή καθενός από αυτά είναι μοναδική, αναμένεται και ο χρωματισμός της φλόγας να ταυτοποιεί το διεγειρόμενο στοιχείο. Πρέπει να τονισθεί ότι το χρώμα της φλόγας οφείλεται αποκλειστικά στο μεταλλικό ιόν. To ανιόν δηλαδή, με το οποίο είναι συνδεδεμένο το μεταλλικό ιόν στη στερεά κατάσταση, δεν επηρεάζει το χρίομα της φλόγας. Παρακάτω δίνεται πίνακας με τα χαρακτηριστικά χρώματα ορισμένων στοιχείων που μπορούν ν' ανιχνευθούν πυροχημικά. ΠΙΝΑΚΑΣ 3.1: Πυροχημική ανίχνευση μερικών ιόνιων. ΙΟΝ Λίθιο, Li+ Νάτριο, Na+ Κάλιο, K+ Ασβέστιο, Ca2+ Βάριο, Ba2+ Στρόντιο, Sr2+ Χαλκός, Cu2+ ΧΡΩΜΑ ΦΑΟΓΑΣ κόκκινο έντονο κίτρινο ιώδες κεραμιδί πρασινοκίτρινο βυσσινί γαλαζοπράσινο ΟΡΓ ΑΝΑ ΚΑΙ ΧΗΜΙΚΕΣ ΟΥΣΙΕΣ Για την εκτέλεση του πειράματος απαιτούνται: 1. Ένα σύρμα από λευκόχρυσο ή από χρωμονικελίνη. 2. Μία ύαλος ωρολογίου. 3. Πυκνό διάλυμα HCl. 4. Μία σειρά από στερεά άλατα τα οποία θα εξεταστούν Na2CO3, NaCl, NaNO35Li2CO3,CaCl2, BaCl2, Sr(NO3)2, CuSO4. 5. To "άγνωστο" δείγμα το οποίο μπορεί να είναι αλάτι του εμπορίου κατά προτίμηση ιωδιομένο.
44 ΣΧΗΜΑ 3.1 Παραδείγματα ττυροχημικής ανίχνευσης σε αλκάλια ( π ά ν ω σειρά) και αλκαλικές γαίες (κάτω σειρά).
45 40 Πείραμα 3 ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ Καθαρίζεται αρχικά το σύρμα λευκοχρύσου ή χρωμονικελίνης βουτώντας το σε πυκνό HCl, μικρή ποσότητα του οποίου έχει τοποθετηθεί σε ύαλο ωρολογίου. H διαδικασία αυτή του καθαρισμού επαναλαμβάνεται μετά από κάθε δοκιμασία. H ποσότητα του HCl θα πρέπει να ανανεώνεται μετά από κάθε εμβάπτιση, ώστε να μη μολύνεται το σύρμα Φέρεται τώρα η άκρη του καθαρού σύρματος στη φλόγα και πυρώνεται. H πυρακτωμένη άκρη τώρα βυθίζεται στο στερεό υπό εξέταση δείγμα και φέρεται πάλι στη φλόγα. Σημειώνεται το χρώμα της. Στην πρώτη αυτή φάση επιβεβαιώνει κανείς τη σχέση φύσεως ιόντος και χρώματος φλόγας, όπως προκύπτει από τον παραπάνω πίνακα. Επαναλαμβάνεται η διαδικασία και με το άγνιοστο δείγμα, οπότε από το χρώμα της φλόγας γίνεται μία ποιοτική εκτίμηση της σύστασής του. χρώμα φλόγας γυάλινο ραβδί σύρμα Pt Λύχνος Bunsen ΣΧΗΜΑ 3.2 Διάταξη για την πυροχημική ανίχνευση μετάλλων
46 52 Πείραμα 6 Πείραμα 64 ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΚΑΙ ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΙΟΝΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : Ι.Να αναγνωρίζεις τις μεταθετικές χημικές αντιδράσεις ή α\τιόράσεις διπλής αλτικατάστασης. Ιδιαίτερα αυτές με συνένωση ιόντων προς δημιουργία ιζήματος. 2.Να αναγνωρίζεις ότι οι αντιδράσεις αυτές γίνονται μέσα σε υδατικά διαλύματα και κυρίως, ότι το ίζημα σε πολλές περιπτώσεις επιτρέπει την ταυτοποίηση ενός αντιδρώντος σώματος ή καλύτερα ιόντος. 3.Να αναλύεις ποιοτικά ορισμένα ιόντα. ΕΙΣΑΓΩΓΗ ΣΤΟ ΘΕΜΑ Όπως είναι ήδη γνωστό, τα χημικά στοιχεία συνδυάζονται και σχηματίζουν τις χημικές ενώσεις. Για παράδειγμα συναντά κανείς το θείο ελεύθερο, σαν ένα κίτρινο στερεό, αλλά και σε ενώσεις του, όπως είναι το H2S, H2SO4, CaSO4, κλπ. Σε κάθε μάλιστα ένωση εμφανίζει και άλλες ιδιότητες, διαφορετικές από εκείνες του ελεύθερου στοιχείου. Αυτό κάνει την αναζήτηση των στοιχείων από τα οποία αποτελείται μία ένωση - ποιοτική ανάλυση - όχι ιδιαίτερα εύκολη υπόθεση. Για τις ενώσεις εκείνες που διαλυόμενες στο νερό διίστανται σε ιόντα, δηλαδή τους ηλεκτρολύτες (οξέα, βάσεις και άλατα) ο «παραδοσιακός» τρόπος ταυτοποίησης των ιόντων είναι κυρίως οι μεταθετικές αντιδράσεις. Απ' αυτές, επιλέγουμε εκείνες που οδηγούν σε ιζήματα με χαρακτηριστικές ιδιότητες. Στις ιδιότητες αυτές περιλαμβάνονται το χρώμα του ιζήματος, η διαλυτότητά του -όχι βέβαια στο νερό, αλλά σε οξέα ή βάσεις ή άλλους διαλύτες και σε δεύτερη μοίρα πιο εξειδικευμένες ιδιότητες. Τέλος,
47 53 Πείραμα 6 θα πρέπει να διευκρινίσουμε ότι οι αντιδράσεις αυτές είναι χαρακτηριστικές των ιόντων και όχι των ενώσεων που τα περιέχουν. H ένωση της οποίας το διάλυμα χρησιμοποιείται για τον προσδιορισμό ενός ιόντος ονομάζεται αντιδραστήριο. Av για παράδειγμα σε τρία διαλύματα που περιέχουν αντίστοιχα NaCl, CaCl2 και HCl προστεθούν σταγόνες από διάλυμα AgNO3 (αντιδραστήριο των χλωροίόντων), τότε η «καθαρή» αντίδραση που λαμβάνει χώρα είναι : Cl" + Ag+ > AgCI I ( ιοντική μορφή) και όχι η (για το πρώτο από τα διαλύματα) NaCl + AgNO3 -^NaNO 3 + AgCI i (μοριακή μορφή) η οποία είναι κατάλληλη για στοιχειομετρικούς υπολογισμούς. O παραγόμενος χλωριούχος άργυρος είναι ένα λευκό ίζημα αδιάλυτο σε οξέα, αλλά διαλυτό σε αραιή NH3. Επιπλέον, το ίζημα αυτό είναι φωτοπαθές και αν εκτεθεί σε ηλιακό φως μαυρίζει. Av αναζητήσει κανείς άλλα χλωριούχα ιζήματα, θα βρει τα PbCl2 και Hg2Cl2 τα οποία όμως δεν διαλύονται στην NH3 ούτε είναι φωτοπαθή. Γι'αυτό και διακρίνονται από το AgCl. Συνεπώς, η παραπάνω αντίδραση μπορεί να αποτελέσει τη βάση για την ταυτοποίηση των ιόντων Ag+. Με ανάλογο τρόπο, μπορούν να ανιχνευτούν Χ" ( ιόντα αλογόνων)" με προσθήκη Ag+. O σχηματιζόμενος λευκός AgCl, θα πρέπει να διαφοροποιηθεί από τον λευκοκίτρινο και διαλυτό στην πυκνή NH3, AgBr, καθώς και από τον κίτρινο και αδιάλυτο και στην πυκνή NH3, AgI. H αναζήτηση τέτοιων αντιδράσεων και ιδιοτήτων οδήγησε τελικά σε ταξινόμηση των κατιόντων και των ανιόντων σε αναλυτικές ομάδες και σε μία πορεία ανάλυσης η οποία είναι η, υγροχημική, ποιοτική ανάλυση. H εξέλιξη έφερε την ενόργανη ποιοτική ανάλυση, όπου με τη βοήθεια οργάνων γίνεται ανάλυση πολύπλοκων δειγμάτων ταχύτατα, ακριβέστατα και αν χρειαστεί εξ αποστάσεως- θυμηθείτε τον path finder της τελευταίας αποστολής στον πλανήτη Αρη-, Στο πείραμα που ακολουθεί, θα δοθούν οι αντιδράσεις ταυτοποίησης μερικών από τα συνήθη ιόντα, τα οποία συναντά κανείς
48 54 Πείραμα 6 συχνά, ακόμα και στις ετικέτες των εμφιαλωμένων νερών. Αυτά είναι τα Cl" και τα SO42", από τα ανιόντα και τα Fe3+ και Al3+, από τα κατιόντα. ΟΡΓΑΝΑ ΚΑΙ ΧΗΜΙΚΕΣ ΟΥΣΙΕΣ Για την εκτέλεση του πειράματος αυτού θα χρειαστούν: δοκιμαστικοί σωλήνες με το στήριγμά τους. 2. Σταγονόμετρο. 3. Διαλύματα = 100 ppm από: NaCl, A I C I 3, Na2SO4, FeCl3,* AgNO3. Αντί διαλυμάτων είναι δυνατόν να χρησιμοποιηθούν στερεά. Από αυτά απαιτείται ελάχιστη ποσότητα στην άκρη της σπαθίδας και διάλυση τους σε 5-10 ml νερό. 4. H2SO4 0,01 Μ, HCl 0,01 Μ, Ba(NO3)2 0,01 Μ, πυκνό HNO3, διάλυμα NH3 1 Μ, διάλυμα NaOH 1 Μ. 5. Σιφώνιο των 5 ml βαθμολογημένο. 6. Χαλύβδινη σπαθίδα. To διάλυμα του FeCl3 να οξινίζεται με 2-3 σταγόνες πυκνού HCl. ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ α. ανίχνευση χλωριόντων Σε τρεις δοκιμαστικούς σωλήνες εισάγονται από 5 ml των διαλυμάτων NaCl, AlCl3 και HCl. Σε καθένα τώρα από τους τρεις δοκιμαστικούς σωλήνες, προστίθενται με το σταγονόμετρο δύο σταγόνες από το διάλυμα του AgNO3. Στον πρώτο από τους δοκιμαστικούς σωλήνες, προστίθενται σταγόνες από πυκνό HNO3. Στο δεύτερο προστίθεται 1 ml από το διάλυμα NH3 1 M και αναταράσσεται ο σωλήνας. Ti παρατηρείτε; Στον τρίτο σωλήνα χύνουμε το υπερκείμενο διάλυμα και εκθέτουμε το ίζημα στο άμεσο ηλιακό φως. Σημειώστε τυχόν αλλαγή στο χρώμα του ιζήματος.
49 55 Πείραμα 6 ΣΧΗΜΑ 6.1 Ανίχνευση Cl", Br, Γ με αντιδραστήριο Ag+, π ρ ο ς σχηματισμό αντίστοιχα λευκού ι ζ ή μ α τ ο ς ^ ΰ Ι ) διαλυτού σε αραιή ΝΗ3, κίτρινου ιζήματος (AgBr) διαλυτού σε πυκνή ΝΗ3 και κίτρινου ιζήματος (AgI) αδιάλυτου σε πυκνή NH 3 //. ανίχνευση θειικών Σε δύο δοκιμαστικούς σωλήνες προστίθενται 10 ml διαλύματος Na2SO4 και H2SO4. αντίστοιχα. Στη συνέχεια προστίθενται σε κάθε σωλήνα από δύο σταγόνες διαλύματος Ba(NOj)2. το οποίο είναι το αντιδραστήριο των SO4".Ti παρατηρείτε; Αποβάλουμε τώρα το υπερκείμενο διάλυμα από τους σωλήνες και προστίθεται στο μεν ένα διάλυμα HCl και στο άλλο διάλυμα NH1. Υπάρχει καμιά μεταβολή;
50 56 Πείραμα 6 ΣΧΗΜΑ 6. 2 Ανίχνευση SO4 2" με αντιδραστήριο Ba 2+, π ρ ο ς σχηματισμό λευκού ιζήματος BaSC>4. γ. ανίχνευση ιόντων Αργιλίου, AI3+ Σε τρεις δοκιμαστικούς σωλήνες προστίθενται από 10 ml του διαλύματος του AlCl3. Στη συνέχεια προστίθενται από δύο σταγόνες από το διάλυμα του NaOH. Ti παρατηρείτε; Στον ένα τώρα από τους σωλήνες προστίθεται περίσσεια από το αντιδραστήριο, το διάλυμα του NaOH και το μίγμα αναταράσσεται. Σημειώστε όποια αλλαγή. Στον δεύτερο προστίθενται σταγόνες από το διάλυμα του HCl και το μίγμα αναταράσσεται. Σημειώνεται η τυχόν μεταβολή. Στον τρίτο προστίθενται σταγόνες από το διάλυμα της NH3 και μετά την ανατάραξη, σημειώνεται η τυχόν μεταβολή.
51 57 Πείραμα 6 SO ^ Um HYDI -JXHJE NaOH ΣΧΗΜΑ 6. 3 Ανίχνευση ΑΙ3+"με αντιδραστήριο OH, π ρ ο ς σχηματισμό λευκού ιζήματος AI(OH)3. To σχηματιζόμενο ίζημα διαλύεται τόσο σε διάλυμα HCI όσο και σε διάλυμα NaOH. Δηλαδή, το AI(OH)3 έχει επαμφοτερίζοντα χαρακτήρα (αντιδρά τόσο με οξέα όσο και με βάσεις). <5. ανίχνευση ιόντων Fe3+ Σε δύο δοκιμαστικούς σωλήνες προστίθενται από 10 ml του διαλύματος του FeCb. Στην συνέχεια προστίθενται από δύο σταγόνες από το διάλυμα του NaOH. Αναταράσσονται οι σωλήνες και σημειώνεται η μεταβολή. Στον ένα τώρα από τους σωλήνες προστίθεται περίσσεια από το αντιδραστήριο, ενώ στον άλλο περίσσεια από το διάλυμα του HCl. Σημειώστε τις μεταβολές.
52 58 Πείραμα 6 ΣΧΗΜΑ 6. 5 Ανίχνευση Ρβ3+"με αντιδραστήριο OH', π ρ ο ς σχηματισμό ιζήματος Fe(OH) 3. To σχηματιζόμενο ίζημα διαλύεται σε διάλυμα HCI.
53 59 Πείραμα 7 Πείραμα 75 ΠΑΡΑΣΚΕΥΗ ΔΙΑΛΥΜΑΤΟΣ ΟΡΙΣΜΕΝΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ-ΑΡΑΙΩΣΗ ΔΙΑΛΥΜΑΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : Ι.Να εφαρμόζεις το ζυγό. 2. Να μετράς τον όγκο ενός υγρού. 3.Να παρασκευάζεις διαλύματα ορισμένης συγκέντρωσης. ΕΙΣΑΓΩΓΗ ΣΤΟ ΘΕΜΑ Αιά/Μμα είναι το ομογενές μίγμα δύο ή περισσοτέρων συστατικών. Αιαλΐ)της είναι το συστατικό που βρίσκεται συνήθως στη μεγαλύτερη αναλογία στο διάλυμα και που διατηρεί τη φυσική του κατάσταση μετά την ανάμιξη. Διαλυμένη ουσία είναι το συστατικό που βρίσκεται σε μικρότερη αναλογία στο διάλυμα. Από τα διαλύματα τα πιο σημαντικά είναι τα υδατικά. To νερό έχει την ικανότητα να διαλύει τόσο τις ομοιοπολικές ενώσεις π.χ. ζάχαpi(ci2h22oii), όσο και τις ετεροπολικές π.χ. NaCl. H διάλυση επιτυγχάνεται με την εφυδάτωση μορίων ή ιόντων, όπως φαίνεται στο παρακάτω σχήμα. M1 αυτό τον τρόπο σχηματίζονται τα μοριακά και τα ιοντικά διαλύματα, αντίστοιχα. ΣΧΗΜΑ 7.1 To νερό διαλύει τις ομοιοπολικές και ετεροπολικές ενώσεις.
54 60 Πείραμα 7 H παρασκευή διαλύματος ορισμένης συγκέντρωσης, γίνεται με διάλυση προζυγισμένης ποσότητας στερεού σε ορισμένο όγκο απιονισμένου νερού. H διαδικασία που ακολουθούμε για την παρασκευή ενός διαλύματος, περιλαμβάνει τα εξής στάδια, όπως φαίνεται στο σχήμα 7.2 : α) ποσότητα του στερεού προστίθεται στην ογκομετρική φιάλη, κατόπιν προστίθεται απιονισμένο νερό με τη βοήθεια του υδροβολέα. β) το στερεό διαλύεται με προσεκτική ανακίνηση της ογκομετρικής φιάλης, γ) όταν το στερεό έχει πλήρως διαλυθεί προσθέτουμε νερό μέχρι τη χαραγή. Με βάση τον όγκο του διαλύματος και την ποσότητα του στερεού μπορούμε να υπολογίσουμε τη μοριακή κατ'όγκο συγκέντρωση (Molarity) του διαλύματος. Να σημειωθεί ότι η θερμοκρασία παίζει ιδιαίτερο ρόλο στην παρασκευή ενός διαλύματος, γιατί η θερμοκρασία επηρεάζει τον όγκο του διαλύματος. Γι' αυτό τα διαλύματα ορισμένης συγκέντρωσης αναφέρονται σε ορισμένη θερμοκρασία, που συνήθως είναι η θερμοκρασία δωματίου. ί - ΣΧΗΜΑ 7.2 Παρασκευή διαλύματος. S
55 61 Πείραμα 7 H αραίωση ενός διαζώματος π.χ. σε δεκαπλάσιο όγκο, οδηγεί σε υποδεκαπλασιασμό της μοριακής συγκέντρωσης του διαλύματος, σύμφωνα με τη σχέση: MiVi=M 2 V 2 Όπου Mi και M2 η μοριακή κατ'όγκο συγκέντρωση του διαλύματος πριν και μετά την αραίωση, ενώ Vi και V2 ο όγκος του διαλύματος πριν και μετά την αραίωση H διαδικασία που ακολουθούμε για την αραίωση ενός διαλύματος περιλαμβάνει τα εξής στάδια, όπως φαίνεται στο σχήμα 7.2 : α) παίρνουμε 100 ml του προς αραίωση διαλύματος σε ογκομετρική φιάλη β) την ποσότητα αυτή μεταφέρουμε σε ογκομετρική φιάλη του 1 L γ) κατόπιν προστίθεται απιονισμένο νερό με τη βοήθεια του υδροβολέα. Αραίωση διαλύματος.
56 62 Πείραμα 7 ΟΡΓΑΝΑ ΚΑΙ ΧΗΜΙΚΕΣ ΟΥΣΙΕΣ Για το πείραμα αυτό θα χρειαστείτε: 1. Αναλυτικό ζυγό. 2. Ογκομετρικές φιάλες των 100 ml και 1 L. 3. Υδροβολέα. 4. Ύαλο ωρολογίου. 5. CuSO4-SH2O περίπου 5 g. ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ ΜΕΡΟΣ 1: Παρασκευή Διαλύματος CuSO 4 0,1 M Ζυγίζουμε την ύαλο ωρολογίου και στη συνέχεια προσθέτουμε με τη σπάτουλα 2,50 g CUSO45H2O. Την ποσότητα αυτή, μεταφέρουμε σε ογκομετρική φιάλη των 100 ml και τη διαλύουμε προσθέτοντας μικρή ποσότητα απιονισμένου νερού (πωματίζουμε τη φιάλη και ανακινούμε προσεκτικά). Μετά την πλήρη διάλυση συνεχίζουμε την προσθήκη νερού, μέχρις ότου ο όγκος του διαλύματος να γίνειΐ 00 ml, δηλαδή μέχρι το διάλυμα να φθάσει τη χαραγή (πρέπει η εφαπτομένη της κορυφής του υγρού μηνίσκου να περνά από τη χαραγή). Με ανάλογο τρόπο να παρασκευαστεί διάλυμα 0,05 M CuSC>4 ΜΕΡΟΣ 2: Αραίωση Διαλύματος Παίρνουμε τα 100 ml του διαλύματος CuSO4 0,1 Μ, που έχουμε παρασκευάσει και τα μεταφέρουμε προσεκτικά σε ογκομετρική φιάλη του 1 L Στη συνέχεια προστίθεται απιονισμένο νερό με τη βοήθεια του υδροβολέα, μέχρι το διάλυμα να φθάσει τη χαραγή. M' αυτό τον τρόπο δεκαπλασιάζεται ο όγκος του διαλύματος και συνεπώς, με βάση τη σχέση MiVi=M 2 V 2, η μοριακή κατ'όγκο συγκέντρωση του διαλύματος υποδεκαπλασιάζεται. Με αντίστοιχο τρόπο να παρασκευαστεί διάλυμα 0,005 Μ.
57 33 Πείραμα 1 Πείραμα 16 ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΑΝΤΙΔΡΑΣΗΣ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς: 1. Να μετράς τη θερμότητα μιας αντίδρασης. 2. Να αναγνωρίζεις την έννοια της περίσσειας των αντιδρώντων. 3. Να αναγνωρίζεις ότι απαιτείται ενέργεια για το σπάσιμο δεσμών, ενώ ελευθερώνεται κατά το σχηματισμό τους. 4. Να διατυπώνεις και να εφαρμόζεις το νόμο του Hess. ΕΙΣΑΓΩΓΗ ΣΤΟ ΘΕΜΑ Οι χημικές αντιδράσεις συνήθως συνοδεύονται από ενεργειακές μεταβολές. Όταν τα προϊόντα έχουν μικρότερο ενεργειακό περιεχόμενο (ενθαλπία) από τα αντιδρώντα, τότε ενέργεια ελευθερώνεται και η θερμοκρασία του μέσου που γίνεται η αντίδραση (συνήθως το νερό ή γενικότερα το περιβάλλον) αυξάνεται. Τότε ΔΗ <0 και η αντίδραση είναι εξώθερμη. Το αντίστροφο συμβαίνει όταν \Η > 0, δηλαδή τότε έχουμε ψύξη του μέσου και η αντίδραση είναι ενδόθερμη. Ενέργεια απαιτείται για τη διάσπαση δεσμών, ενώ ενέργεια ελευθερώνεται κατά το σχηματισμό δεσμών από ελεύθερα άτομα. Η ενεργειακή αυτή διαφορά καθορίζει το ενθόθερμο ή το εξώθερμο της αντίδρασης. Όταν μια ένωση διαλύεται στο νερό απαιτείται ενέργεια για να σπάσει ο κρύσταλλος (ενωτική ενέργεια κρυστάλλου), ενώ ελευθερώνεται ενέργεια κατά το σχηματισμό δεσμών μεταξύ ιόντων και μορίων νερού (ενέργεια εφυδάτωσης). Η ενεργειακή αυτή διαφορά καθόριζα και πάλι το ενδόθερμο ή εξώθερμο της αντίδρασης. Η μέτρηση της θερμότητας μιας αντίδρασης επιτυγχάνεται με μια συσκευή που λέγεται θερμιδόμετρο.
58 34 Πείραμα 1 Τα θερμιδόμετρα είναι όργανα υψηλής ακρίβειας. Για χαμηλότερες απαιτήσεις μπορούν να χρησιμοποιηθούν τα θερμιδόμετρα τύπου πλαστικού κυπέλλου (coffee-cup). Ο υπολογισμός της θερμότητας αντίδρασης γίνεται με βάση τη σχέση: q= m cat Όπου, m c : η θερμοχωρητικότητα της ουσίας (π.χ. νερό), εκφρασμένη συνήθως σε J grad ' η calgrad 1 c : η ειδική θερμοχωρητικότητα της ουσίας (π.χ. νερό) εκφρασμένη συνήθως σε J g"1 grad"1 ή calg 'grad"1. AT: η μεταβολή της θερμοκρασίας σε C ή Κ. W W «ΛΜΚΚ ^ κακύ/μ avotikflffc uo*u/rim>uai«$ liaotxxrottr&vau βδμ&ί (οντιδρβστήραξ) tfiwipo*avtiyhit/] ΣΧΗΜΑ 1. 1 Θερμιδόμετρο βόμβας.
59 35 Πείραμα 1 Να σημειωθεί ότι σε πολλές αντιδράσεις, όπως αυτές που γίνονται υπό μορφή διαλυμάτων, η πίεση παραμένει σχεδόν σταθερή και ΔΗ = qp Θερμόμετρο Γυάλινος αναδευτήρας Καπάκι από φελλό Δυό πλαστικά ποτήρια μεγάλης σκληρότητας ΣΧΗΜΑ 1.2 Θερμιδόμετρο τύπου πλαστικού κυπέλλου (coffee-cup). Η αντίδραση γίνεται σε υδατικά διαλύματα υπό σταθερή πίεση.
60 36 Πείραμα 1 ΟΡΓΑΝΑ ΚΑΙ ΧΗΜΙΚΕΣ ΟΥΣΙΕΣ Για το πείραμα αυτό θα χρειαστείτε : 1. Κωνική φιάλη των 250 ml (Erlenmeyer). Αυτή θα παίξει το ρόλο τόσο του θερμιδόμετρου, όσο και του αντιδραστήρα. Να έχετε υπ' όψη σας ότι χρειάζονται 1,0 cal για να αλλάξει η θερμοκρασία 1 g νερού κατά 1 C και 0,2 cal για να αλλάξει η θερμοκρασία 1 g γυαλιού κατά 1 C. Γ ια μεγαλύτερη ακρίβεια μπορεί να χρησιμοποιηθεί πλαστικό κύπελλο (θερμιδόμετρο τύπου coffee-cup, όπως φαίνεται στο προηγούμενο σχήμα). 2. Θερμόμετρο με υποδιαιρέσεις 0,1 "C. 3. Ογκομετρικό κύλινδρο ( mL). 4. Γυάλινο ραβδί ανάδευσης. 5. Ζυγό με ακρίβεια δύο δεκαδικών ψηφίων. 6. Περίπου 2 g στερεού NaOH ml διαλύματος NaOH 0,50 Μ ml διαλύματος HC10,50 Μ. ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ Στο πείραμα που ακολουθεί θα μετρηθούν και θα συγκριθούν μεταξύ τους οι θερμότητες τριών αντιδράσεων: Γ' αντίδραση: NaOH(s) > Na+(aq) + OH'(aq) + x, cal ΔΗ\ = - Χι cal 2η αντίδραση: NaOH(s) + WC\(aq)»Na+(o<7)+ OH (aq) + H 2 0 +x2 cal ΔΗ2 = - X2 cal 3η αντίδραση: NaOHfa^J + HC\(aq) >N&+(aq) + OHY aq) + H 2 0 +x2cal ΔΗ2 =- X2 cal
61 37 Πείραμα 1 Υπολογισμός της 1ης θερμότητας αντίδρασης 1. Ζυγίζουμε την κωννκή φνάλη των 250 ml, αφού προηγουμένως την έχουμε καθαρίσει και στεγνώσει καλά. 2. Προσθέτουμε 200 ml νερού δικτύου ύδρευσης και ανακατεύουμε καλά με το θερμόμετρο, μέχρι περίπου να φθάσει τη θερμοκρασία δωματίου. Στη συνέχεια καταγράφουμε τη θερμοκρασία αυτή. 3. Ζυγίζουμε περίπου 2 g NaOH με ακρίβεια 0,01 g. Η ζύγιση θα πρέπει να γίνει όσο το δυνατό γρηγορότερα, γιατί το NaOH(s) έχει τη ιδιότητα να απορροφά CO2 από τον ατμοσφαιρικό αέρα. 4. Προσθέτουμε την ποσότητα αυτή του NaOH στην κωνική φιάλη των 250 ml με το νερό και διαλύουμε το στερεό με τη βοήθεια της γυάλινης ράβδου ανάδευσης. Με τη βοήθεια του θερμόμετρου, διαβάζουμε τη θερμοκρασία του διαλύματος και καταγράφουμε τη μέγιστη τιμή. Πλένουμε καλά την κωνική φιάλη, χωρίς να είναι απαραίτητο να τη ξηράνουμε και συνεχίζουμε με το επόμενο πείραμα. Υπολογισμός της 2ης θερμότητας αντίδρασης (ΑΗ2): Επαναλαμβάνουμε τα βήματα 2, 3 και 4, πλην όμως στη θέση του νερού χρησιμοποιούμε διάλυμα όγκου 200 ml HC1 0,50 Μ. Αφού τελειώσει το πείραμα πλένουμε καλά την κωνική φιάλη, χωρίς να είναι απαραίτητη η ξήρανσή της και συνεχίζουμε με το επόμενο πείραμα. Υπολογισμός της 3ης θερμότητας αντίδρασης (Λ//?): Προσθέτουμε στην κωνική φιάλη 100 ml HC1 0,50Μ, αφήνουμε αυτό να αποκτήσει περίπου τη θερμοκρασία δωματίου και στη συνέχεια καταγράφουμε τη θερμοκρασία του. Κατόπιν προσθέτουμε 100 ml. NaOH 0,50Μ (αφού προηγουμένως αφήσουμε να αποκτήσει τη θερμοκρασία δωματίου και καταγράψουμε τη θερμοκρασία του). Το τελικό διάλυμα αναδεύεται καλά και καταγράφεται η μέγιστη θερμοκρασία του.
62 49 Πείραμα 5 Πείραμα 57 ΑΝΙΧΝΕΥΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να χρησιμοποιείς τα αντιδραστήρια του Fehling και του Tollens, για την ανίχνευση των υδατανθράκων και συγκεκριμένα όσων εξ αυτών είναι αναγόμενα σάκχαρα. Εξέλιξη του πρώτου αντιδραστηρίου είναι το αντιδραστήριο Benedickt. ΕΙΣΑΓΩΓΗ ΣΤΟ ΘΕΜΑ Από χημική σκοπιά οι υδατάνθρακες ή σάκχαρα είναι πολυυδροξυαλδεΰδες ή πολυυδροξυκετόνες. Φέροντες λοιπόν δυο χαρακτηριστικές ομάδες, -ΟΗ και -CH=0 ή >C=0, θα έχουν και τις αντίστοιχες αυτών ιδιότητες. Μια από τις πιο χαρακτηριστικές είναι και ο αναγωγικός ή μη χαρακτήρας των σακχάρων οφειλόμενος κατά κύριο λόγο στην -CHO. Αυτό άλλωστε αποτελεί και μία βάση διάκρισης των σακχάρων σε αναγόμενα και μη. Επίσης, διακρίνονται σε μόνο ή πολυσακχαρίτες, σε σακχαροειδείς και μη, σε αλδόζες και κετόζες. Η ανίχνευση των υδατανθράκων στηρίζεται στον έντονο αναγωγικό τους χαρακτήρα, για όσους βέβαια από αυτούς ανήκουν στα αναγόμενα ζάχαρα. Αυτός οφείλεται κυρίως στην -CHO. Οι κυριότεροι από τους υδατάνθρακες που ανάγονται, είναι η γλυκόζη και η μαλτόζη. Αντίθετα, το καλαμοζάχαρο (κοινή ζάχαρη) δεν οξειδώνεται άμεσα. Το οξειδιοτικό το οποίο θα χρησιμοποιηθεί θα πρέπει να είναι ήπιο, ώστε εκλεκτικά να οξειδώνει την αλδεϋδομάδα και όχι τα αλκοολικά υδροξύλια τα οποία υπάρχουν άφθονα στο μόριο. Επίσης, πρέπει η αντίδραση να έχει ένα άμεσο οπτικό αποτέλεσμα,
63 50 Πείραμα 5 όπως π.χ. δημιουργία χαρακτηριστικού ιζήματος ή αλλαγή χρώματος. Τα δύο πιο κλασικά οξειδωτικά τα οποία ^ησιμοποιούνται στην περιοχή αυτή, είναι τα ιόντα Ag+ και Cu +, σε κατάλληλες και αυστηρά ορισμένες συνθήκες. Το πρώτο με τη μορφή αμμινοσυμπλόκου, Ag(NH3)2+ είναι το αντιδραστήριο του Tollens Αυτό αναφέρεται ως αμμωνιακό διάλυμα AgNOj και ήδη χρησιμοποιήθηκε στην ανίχνευση των αλδεϋδών με προϊόν Ag (κάτοπτρο αργύρου). Η αντίδραση για την αλδεϋδομάδα είναι: RCHO + 2 Ag(NH3) Η' -> 2Agi + RCOO" + 4NH3 + 2H20 To δεύτερο που είναι και το πλέον χρησιμοποιούμενο είναι τυ αντιδραστήριο του Fehling. Αυτό περιέχει το Cu2+ με μορφή τρυγικού συμπλόκου και η αντίδραση της οξειδοαναγωγής γίνεται σε αλκαλικό περιβάλλον. Παράγεται ένα ερυθρό ίζημα από Cu20 το οποίο αποτελεί τη θετική ένδειξη της δοκιμασίας (test). Η αντίδραση είναι (πάλι για την αλδεϋδομάδα): RCHO +2Cu(Tpuy. 2 ") 2 +50Η" ->Cu204- +RCOO +4τρυγ.2+3Η20 Οπου το ιόν τρυγ.2" είναι το "OOCCHOHCHOHCOO. Εξέλιξη του αντιδραστηρίου του Fehling, το οποίο παρασκευάζεται λίγο πριν την αντίδραση από την ανάμειξη δύο διαλυμάτων, είναι το διάλυμα του Benedict. Αυτό είναι ένα διάλυμα το οποίο περιέχει ιόντα Cu2+ συμπλοκοποιημένα με κιτρικά, αντί τρυγικά, ιόντα. Η στοιχειομετρία της αντίδρασης και το ερυθρό ίζημα του Cu 2 0 είναι τα ίδια. Στο πείραμα που ακολουθεί, γίνονται και οι δύο δοκιμασίες με τα ανάγοντα απλά σάκχαρα, γλυκόζη και φρουκτόζη, καθώς και με τη μη ανάγουσα κοινή ζάχαρη. ΟΡΓΑΝΑ ΚΑΙ ΧΗΜΙΚΕΣ ΟΥΣΙΕΣ Για την εκτέλεση του πειράματος θ' απαιτηθούν: δοκιμαστικοί σωλήνες των 20 ml. 2. Στήριγμα δοκιμαστικών σωλήνων. 3. Ξύλινη λαβίδα.
ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΚΑΙ ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΙΟΝΤΩΝ
 52 Πείραμα 36 ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΚΑΙ ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΙΟΝΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : Ι.Να αναγνωρίζεις τις μεταθετικές χημικές αντιδράσεις ή α\τιόράσεις διπλής αλτικατάστασης.
52 Πείραμα 36 ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ ΚΑΙ ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΙΟΝΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : Ι.Να αναγνωρίζεις τις μεταθετικές χημικές αντιδράσεις ή α\τιόράσεις διπλής αλτικατάστασης.
ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΑΝΤΙΔΡΑΣΗΣ
 33 Πείραμα 1 Πείραμα 1 ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΑΝΤΙΔΡΑΣΗΣ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς: 1. Να μετράς τη θερμότητα μιας αντίδρασης. 2. Να αναγνωρίζεις την έννοια της περίσσειας
33 Πείραμα 1 Πείραμα 1 ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΑΝΤΙΔΡΑΣΗΣ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς: 1. Να μετράς τη θερμότητα μιας αντίδρασης. 2. Να αναγνωρίζεις την έννοια της περίσσειας
EfflAME NA ΠΡΟΣΕΞΟΥΜΕ, AΑΛΑ ΟΧΙ ΚΑΙ ΕΤΣΙ!!!!!
 1 Εισαγωγικές γνώσεις EfflAME NA ΠΡΟΣΕΞΟΥΜΕ, AΑΛΑ ΟΧΙ ΚΑΙ ΕΤΣΙ!!!!! Εργαστηριακός Οδηγός 1.1 Οδηγίες-κανόνες ασφάλειας εργαστηρίου 1. Μη ξεχνάτε ότι το εργαστήριο είναι χώρος για σοβαρή εργασία. 2. Να
1 Εισαγωγικές γνώσεις EfflAME NA ΠΡΟΣΕΞΟΥΜΕ, AΑΛΑ ΟΧΙ ΚΑΙ ΕΤΣΙ!!!!! Εργαστηριακός Οδηγός 1.1 Οδηγίες-κανόνες ασφάλειας εργαστηρίου 1. Μη ξεχνάτε ότι το εργαστήριο είναι χώρος για σοβαρή εργασία. 2. Να
Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
Εργαστηριακή άσκηση 3: ΧΗΜΙΚΕΣ ΑΝΤΙ ΡΑΣΕΙΣ ΚΑΙ ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΙΟΝΤΩΝ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 3: ΧΗΜΙΚΕΣ ΑΝΤΙ ΡΑΣΕΙΣ ΚΑΙ ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΙΟΝΤΩΝ Οι στόχοι αυτής της εργαστηριακής άσκησης είναι οι µαθητές: Να χρησιµοποιούν τις φυσικές και χηµικές ιδιότητες
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 3: ΧΗΜΙΚΕΣ ΑΝΤΙ ΡΑΣΕΙΣ ΚΑΙ ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΙΟΝΤΩΝ Οι στόχοι αυτής της εργαστηριακής άσκησης είναι οι µαθητές: Να χρησιµοποιούν τις φυσικές και χηµικές ιδιότητες
Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων.
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Α ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2 3 4 5 Ορίστε
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Χημικές αντιδράσεις και ποιοτική ανάλυση ιόντων. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Α ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2 3 4 5 Ορίστε
Σύντομη περιγραφή του πειράματος. Διδακτικοί στόχοι του πειράματος
 Σύντομη περιγραφή του πειράματος Μεταθετικές αντιδράσεις διπλής αντικατάστασης οι οποίες οδηγούν σε σχηματισμό ιζήματος. Το ίζημα σε πολλές περιπτώσεις επιτρέπει την ταυτοποίηση ενός αντιδρώντος σώματος
Σύντομη περιγραφή του πειράματος Μεταθετικές αντιδράσεις διπλής αντικατάστασης οι οποίες οδηγούν σε σχηματισμό ιζήματος. Το ίζημα σε πολλές περιπτώσεις επιτρέπει την ταυτοποίηση ενός αντιδρώντος σώματος
ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΑΝΙΧΝΕΥΣΗ ΑΛΔΕΫΔΩΝ
 36 Πείραμα 2 Πείραμα 2 ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΑΝΙΧΝΕΥΣΗ ΑΛΔΕΫΔΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να κάνεις χρήση των ήπιων οξειδωτικών, όπως του CuO, για την παρασκευή αλδεϋδών απο
36 Πείραμα 2 Πείραμα 2 ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΑΝΙΧΝΕΥΣΗ ΑΛΔΕΫΔΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να κάνεις χρήση των ήπιων οξειδωτικών, όπως του CuO, για την παρασκευή αλδεϋδών απο
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
Οξείδωση της αιθανόλης
 1 Εργαστηριακή Διδασκαλία των Φυσικών εργασιών στα Γενικά Λύκεια Περίοδος 2006 2007 Χημεία Γενικής Παιδείας Β Λυκείου Ενδεικτική προσέγγιση της εργαστηριακή δραστηριότητας : Οξείδωση της αιθανόλης Από
1 Εργαστηριακή Διδασκαλία των Φυσικών εργασιών στα Γενικά Λύκεια Περίοδος 2006 2007 Χημεία Γενικής Παιδείας Β Λυκείου Ενδεικτική προσέγγιση της εργαστηριακή δραστηριότητας : Οξείδωση της αιθανόλης Από
Σύντομη περιγραφή του πειράματος
 Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ-ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ
 ΕΚΦΕ ΝΕΑΣ ΙΩΝΙΑΣ ΕΚΦΕ ΧΑΛΑΝΔΡΙΟΥ ΘΕΜΑΤΑ ΧΗΜΕΙΙΑΣ ΤΟΠΙΙΚΟΥ ΔΙΙΑΓΩΝΙΙΣΜΟΥ EUSO 2012 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ-ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ Αποφασίσατε να δουλέψετε στο πλαίσιο της Ερευνητικής Εργασίας το θέμα που προτάθηκε
ΕΚΦΕ ΝΕΑΣ ΙΩΝΙΑΣ ΕΚΦΕ ΧΑΛΑΝΔΡΙΟΥ ΘΕΜΑΤΑ ΧΗΜΕΙΙΑΣ ΤΟΠΙΙΚΟΥ ΔΙΙΑΓΩΝΙΙΣΜΟΥ EUSO 2012 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ-ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ Αποφασίσατε να δουλέψετε στο πλαίσιο της Ερευνητικής Εργασίας το θέμα που προτάθηκε
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:.
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 13 η Ευρωπαϊκή Ολυµπιάδα Επιστηµών EUSO 2015 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συµµετέχουν: (1) (2) (3) Σέρρες 13/12/2014
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 13 η Ευρωπαϊκή Ολυµπιάδα Επιστηµών EUSO 2015 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συµµετέχουν: (1) (2) (3) Σέρρες 13/12/2014
1ο και 2ο ΕΚΦΕ Ηρακλείου ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO Σάββατο 3 Δεκεμβρίου 2017
 1ο και 2ο ΕΚΦΕ Ηρακλείου ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2017 Σάββατο 3 Δεκεμβρίου 2017 Διαγωνισμός στη Χημεία (Διάρκεια 1 ώρα) ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΜΑΘΗΤΩΝ 1)... ΣΧΟΛΕΙΟ
1ο και 2ο ΕΚΦΕ Ηρακλείου ΤΟΠΙΚΟΣ ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2017 Σάββατο 3 Δεκεμβρίου 2017 Διαγωνισμός στη Χημεία (Διάρκεια 1 ώρα) ΟΝΟΜΑΤΕΠΩΝΥΜΟ ΜΑΘΗΤΩΝ 1)... ΣΧΟΛΕΙΟ
Eργαστηριακές ασκήσεις Χημείας Λυκείου
 Eργαστηριακές ασκήσεις Χημείας Λυκείου Γκιγκούδη Αναστασία Χημικός MEd Ημερήσια διάταξη Α Τάξη: Παράγοντες που επηρεάζουν την ταχύτητα διάλυσης Εργαστηριακός οδηγός-εναλλακτικό Πυροχημική ανίχνευση μετάλλων
Eργαστηριακές ασκήσεις Χημείας Λυκείου Γκιγκούδη Αναστασία Χημικός MEd Ημερήσια διάταξη Α Τάξη: Παράγοντες που επηρεάζουν την ταχύτητα διάλυσης Εργαστηριακός οδηγός-εναλλακτικό Πυροχημική ανίχνευση μετάλλων
Τοπικός Μαθητικός Διαγωνισμός EUSO
 2014 Ε.Κ.Φ.Ε. Καστοριάς Τοπικός Μαθητικός Διαγωνισμός EUSO 2014-2015 ΟΜΑΔΑ : 1] 2] 3] Γενικό Λύκειο Άργους Ορεστικού. 6 - Δεκ. - 1014 Χημεία ΟΔΗΓΙΕΣ ΚΑΝΟΝΕΣ ΑΣΦΑΛΕΙΑΣ Το εργαστήριο είναι χώρος για σοβαρή
2014 Ε.Κ.Φ.Ε. Καστοριάς Τοπικός Μαθητικός Διαγωνισμός EUSO 2014-2015 ΟΜΑΔΑ : 1] 2] 3] Γενικό Λύκειο Άργους Ορεστικού. 6 - Δεκ. - 1014 Χημεία ΟΔΗΓΙΕΣ ΚΑΝΟΝΕΣ ΑΣΦΑΛΕΙΑΣ Το εργαστήριο είναι χώρος για σοβαρή
Μg + 2 HCL MgCl 2 +H 2
 Εργαστηριακή άσκηση 3: Επεξήγηση πειραμάτων: αντίδραση/παρατήρηση: Μέταλλο + νερό Υδροξείδιο του μετάλλου + υδρογόνο Νa + H 2 0 NaOH + ½ H 2 To Na (Νάτριο) είναι αργυρόχρωμο μέταλλο, μαλακό, κόβεται με
Εργαστηριακή άσκηση 3: Επεξήγηση πειραμάτων: αντίδραση/παρατήρηση: Μέταλλο + νερό Υδροξείδιο του μετάλλου + υδρογόνο Νa + H 2 0 NaOH + ½ H 2 To Na (Νάτριο) είναι αργυρόχρωμο μέταλλο, μαλακό, κόβεται με
ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ
 J ο ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ ϊ ΙΖ& Μ iillsllis I 1 C - f y ΟΡΓΑΝΙΣΜΟΣ ΕΚΔΟΣΕΩΝ ΔΙΔΑΚΤΙΚΩΝ ΒΙΒΛΙΩΝ ΑΘΗΝΑ ΥΠΟΥΡΓΕΙΟ ΕΟΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ
J ο ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ ϊ ΙΖ& Μ iillsllis I 1 C - f y ΟΡΓΑΝΙΣΜΟΣ ΕΚΔΟΣΕΩΝ ΔΙΔΑΚΤΙΚΩΝ ΒΙΒΛΙΩΝ ΑΘΗΝΑ ΥΠΟΥΡΓΕΙΟ ΕΟΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ
ΕΚΦΕ Τρικάλων. Πειραματική Δοκιμασία στη Χημεία. Τοπικός Μαθητικός Διαγωνισμός. Τρίκαλα, Σάββατο, 8 Δεκεμβρίου 2012
 1 Τοπικός Μαθητικός Διαγωνισμός 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2013 11Η ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΕΠΙΣΤΗΜΩΝ EUSO 2013 ΕΚΦΕ Τρικάλων Πειραματική Δοκιμασία στη Χημεία Τοπικός Μαθητικός Διαγωνισμός Τρίκαλα,
1 Τοπικός Μαθητικός Διαγωνισμός 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2013 11Η ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΕΠΙΣΤΗΜΩΝ EUSO 2013 ΕΚΦΕ Τρικάλων Πειραματική Δοκιμασία στη Χημεία Τοπικός Μαθητικός Διαγωνισμός Τρίκαλα,
FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4
![FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4 FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4](/thumbs/27/9949444.jpg) ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΤΟΜΕΑΣ ΓΕΝΙΚΗΣ ΚΑΙ ΑΝΟΡΓΑΝΗΣ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΤΟΥ ΜΑΘΗΜΑΤΟΣ «ΧΗΜΕΙΑ» για τους ΦΟΙΤΗΤΕΣ του ΤΜΗΜΑΤΟΣ ΦΥΣΙΚΗΣ Οι διδάσκοντες Αικατερίνη
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΤΟΜΕΑΣ ΓΕΝΙΚΗΣ ΚΑΙ ΑΝΟΡΓΑΝΗΣ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΤΟΥ ΜΑΘΗΜΑΤΟΣ «ΧΗΜΕΙΑ» για τους ΦΟΙΤΗΤΕΣ του ΤΜΗΜΑΤΟΣ ΦΥΣΙΚΗΣ Οι διδάσκοντες Αικατερίνη
Σύντομη περιγραφή του πειράματος. Διδακτικοί στόχοι του πειράματος
 Σύντομη περιγραφή του πειράματος Παρασκευή μίγματος σιδήρου θείου και στη συνέχεια παρασκευή της χημικής ένωσης θειούχου σιδήρου από τα στοιχεία της, με σκοπό να διαπιστώσουμε τις διαφορές μεταξύ μίγματος
Σύντομη περιγραφή του πειράματος Παρασκευή μίγματος σιδήρου θείου και στη συνέχεια παρασκευή της χημικής ένωσης θειούχου σιδήρου από τα στοιχεία της, με σκοπό να διαπιστώσουμε τις διαφορές μεταξύ μίγματος
ph< 8,2 : άχρωμη ph> 10 : ροζ-κόκκινη
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2016 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΑΝΙΧΝΕΥΣΗ ΟΞΕΟΣ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ 2. ΟΓΚΟΜΕΤΡΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2016 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΑΝΙΧΝΕΥΣΗ ΟΞΕΟΣ ΚΑΙ ΠΟΙΟΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ 2. ΟΓΚΟΜΕΤΡΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ
ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ
 ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ Α. ΙΣΟΡΡΟΠΙΑ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΥΔΑΤΙΚO ΔΙΑΛΥΜΑ Λίγα λόγια πριν από το πείραμα. Η σόδα περιέχει διαλυμένο αέριο διοξείδιο του άνθρακα το οποίο προστίθεται κατά την
ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ Α. ΙΣΟΡΡΟΠΙΑ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΥΔΑΤΙΚO ΔΙΑΛΥΜΑ Λίγα λόγια πριν από το πείραμα. Η σόδα περιέχει διαλυμένο αέριο διοξείδιο του άνθρακα το οποίο προστίθεται κατά την
1. Ταυτοποίηση μιας άγνωστης χημικής ένωσης
 Σκοπός 1. Ταυτοποίηση μιας άγνωστης χημικής ένωσης Σκοπός αυτής της εργαστηριακής άσκησης είναι να μάθετε να δίνετε έμφαση στη σημασία της παρατήρησης κατά την εκτέλεση ενός πειράματος. Παρατήρηση, γενικά,
Σκοπός 1. Ταυτοποίηση μιας άγνωστης χημικής ένωσης Σκοπός αυτής της εργαστηριακής άσκησης είναι να μάθετε να δίνετε έμφαση στη σημασία της παρατήρησης κατά την εκτέλεση ενός πειράματος. Παρατήρηση, γενικά,
ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Β ΤΑΞΗΣ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ
 Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργαστηρίου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Β ΤΑΞΗΣ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ
Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργαστηρίου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Β ΤΑΞΗΣ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ
ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργ. Κέντρου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
Εργαστηριακό Κέντρο Φυσικών Επιστηµών Aγίων Αναργύρων Υπεύθυνος Εργ. Κέντρου : Χαρακόπουλος Καλλίνικος Επιµέλεια Παρουσίαση : Καραγιάννης Πέτρος ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΜΑΘΗΤΗ Παράγοντες που επηρεάζουν την θέση της χημικής ισορροπίας 4 η εργαστηριακή άσκηση
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΜΑΘΗΤΗ 4 η εργαστηριακή άσκηση Διδακτικοί στόχοι 1. Να διαπιστώσεις την επίδραση της μεταβολής της συγκέντρωσης και της θερμοκρασίας στη θέση της χημικής ισορροπίας. 2. Να εξηγείς τη μετατόπιση
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΜΑΘΗΤΗ 4 η εργαστηριακή άσκηση Διδακτικοί στόχοι 1. Να διαπιστώσεις την επίδραση της μεταβολής της συγκέντρωσης και της θερμοκρασίας στη θέση της χημικής ισορροπίας. 2. Να εξηγείς τη μετατόπιση
Ε.Κ.Φ.Ε ΑΓΙΩΝ ΑΝΑΡΓΥΡΩΝ
 2015 2016 Ε.Κ.Φ.Ε ΑΓΙΩΝ ΑΝΑΡΓΥΡΩΝ ΦΥΛΛΑ ΕΡΓΑΣΙΑΣ Αρχή του Le Chatelier Όταν μεταβάλλουμε ένα από τους συντελεστές ισορροπίας (συγκέντρωση, πίεση, θερμοκρασία) η θέση της ισορροπίας μετατοπίζεται προς εκείνη
2015 2016 Ε.Κ.Φ.Ε ΑΓΙΩΝ ΑΝΑΡΓΥΡΩΝ ΦΥΛΛΑ ΕΡΓΑΣΙΑΣ Αρχή του Le Chatelier Όταν μεταβάλλουμε ένα από τους συντελεστές ισορροπίας (συγκέντρωση, πίεση, θερμοκρασία) η θέση της ισορροπίας μετατοπίζεται προς εκείνη
Τοπικός διαγωνισμός EUSO2018
 ΕΚΦΕ Νέας Ιωνίας ΕΚΦΕ Χαλανδρίου Τοπικός διαγωνισμός EUSO2018 Πειραματική δοκιμασία Χημείας Υδατικά διαλύματα 9 Δεκεμβρίου 2017 ΣΧΟΛΙΚΗ ΜΟΝΑΔΑ: ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1) 2). 3).. Aριθμός ομάδας Α. Ανίχνευση αγνώστων
ΕΚΦΕ Νέας Ιωνίας ΕΚΦΕ Χαλανδρίου Τοπικός διαγωνισμός EUSO2018 Πειραματική δοκιμασία Χημείας Υδατικά διαλύματα 9 Δεκεμβρίου 2017 ΣΧΟΛΙΚΗ ΜΟΝΑΔΑ: ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1) 2). 3).. Aριθμός ομάδας Α. Ανίχνευση αγνώστων
Σύντομη περιγραφή του πειράματος. Διδακτικοί στόχοι του πειράματος
 Σύντομη περιγραφή του πειράματος Α. Διάσπαση του ανθρακικού χαλκού με θέρμανση, (σε χαμηλότερη θερμοκρασία από ότι η διάσπαση του ανθρακικού ασβεστίου), προς οξείδιο του χαλκού και διοξείδιο του άνθρακα.
Σύντομη περιγραφή του πειράματος Α. Διάσπαση του ανθρακικού χαλκού με θέρμανση, (σε χαμηλότερη θερμοκρασία από ότι η διάσπαση του ανθρακικού ασβεστίου), προς οξείδιο του χαλκού και διοξείδιο του άνθρακα.
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΛΙΜΟΥ
 1 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2015 ΧΗΜΕΙΑ 6 - Δεκεμβρίου - 2014 Ερρίκος Γιακουμάκης Χημικός 2 1 η ΔΡΑΣΤΗΡΙΟΤΗΤΑ Ανίχνευση κατιόντων ή ανιόντων που υπάρχουν σε
1 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2015 ΧΗΜΕΙΑ 6 - Δεκεμβρίου - 2014 Ερρίκος Γιακουμάκης Χημικός 2 1 η ΔΡΑΣΤΗΡΙΟΤΗΤΑ Ανίχνευση κατιόντων ή ανιόντων που υπάρχουν σε
Δύο εναλλακτικές εργαστηριακές ασκήσεις Χημείας της Α Λυκείου ή πώς να κάνουμε τη ζωή μας πιο εύκολη στο εργαστήριο
 Δύο εναλλακτικές εργαστηριακές ασκήσεις Χημείας της Α Λυκείου ή πώς να κάνουμε τη ζωή μας πιο εύκολη στο εργαστήριο Αναστασία Γκιγκούδη Η διδακτική αξία της εργαστηριακής άσκησης στα μαθήματα Φυσικών Επιστημών
Δύο εναλλακτικές εργαστηριακές ασκήσεις Χημείας της Α Λυκείου ή πώς να κάνουμε τη ζωή μας πιο εύκολη στο εργαστήριο Αναστασία Γκιγκούδη Η διδακτική αξία της εργαστηριακής άσκησης στα μαθήματα Φυσικών Επιστημών
[prnrnpiikoi ηηιοι. Hs S. SO e. COOOi -Hs Ή3Ρ. (S-Hs. f Wo. 0H12 Ο ό. C-f-/ ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ
 H s S O 4 I V ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ [prnrnpiikoi ηηιοι Hs S 0 f Wo. 0H12 Ο ό Ή3Ρ SO e λ Λ ( 9 3 - H a C = ^ - H z C-f-/ (S-Hs ΟΡΓΑΝΙΣΜΟΣ ΕΚΔΟΣΕΩΝ ΔΙΔΑΚΤΙΚΩΝ
H s S O 4 I V ΥΠΟΥΡΓΕΙΟ ΕΘΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΑΙ ΘΡΗΣΚΕΥΜΑΤΩΝ ΠΑΙΔΑΓΩΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ [prnrnpiikoi ηηιοι Hs S 0 f Wo. 0H12 Ο ό Ή3Ρ SO e λ Λ ( 9 3 - H a C = ^ - H z C-f-/ (S-Hs ΟΡΓΑΝΙΣΜΟΣ ΕΚΔΟΣΕΩΝ ΔΙΔΑΚΤΙΚΩΝ
Υπολογισμός θερμότητας αντίδρασης
 1 Εργαστηριακή Διδασκαλία των Φυσικών εργασιών στα Γενικά Λύκεια Περίοδος 2006 2007 Χημεία Κατεύθυνσης Β Λυκείου Ενδεικτική προσέγγιση της εργαστηριακή δραστηριότητας : Υπολογισμός θερμότητας αντίδρασης
1 Εργαστηριακή Διδασκαλία των Φυσικών εργασιών στα Γενικά Λύκεια Περίοδος 2006 2007 Χημεία Κατεύθυνσης Β Λυκείου Ενδεικτική προσέγγιση της εργαστηριακή δραστηριότητας : Υπολογισμός θερμότητας αντίδρασης
Εισαγωγικό φροντιστήριο
 Εισαγωγικό φροντιστήριο Ποιοτικής Ανάλυσης Υπόδειγµα γραφής τετραδίου ΗΜΕΡΟΛΟΓΙΟ ΕΡΓΑΣΤΗΡΙΟΥ ΑΝΑΛΥΤΙΚΗΣ ΧΗΜΕΙΑΣ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Α.Θ.: Α.Μ. : Γενικές οδηγίες για τη γραφή του ηµερολογίου του Εργαστηρίου
Εισαγωγικό φροντιστήριο Ποιοτικής Ανάλυσης Υπόδειγµα γραφής τετραδίου ΗΜΕΡΟΛΟΓΙΟ ΕΡΓΑΣΤΗΡΙΟΥ ΑΝΑΛΥΤΙΚΗΣ ΧΗΜΕΙΑΣ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Α.Θ.: Α.Μ. : Γενικές οδηγίες για τη γραφή του ηµερολογίου του Εργαστηρίου
23 Ιανουαρίου 2016 ΛΥΚΕΙΟ:... ΟΜΑΔΑ ΜΑΘΗΤΩΝ: ΜΟΝΑΔΕΣ:
 ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΒΟΡΕΙΑΣ ΕΛΛΑΔΑΣ ΧΗΜΕΙΑ 23 Ιανουαρίου 2016 ΛΥΚΕΙΟ:..... ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1.. 2..... 3..... ΜΟΝΑΔΕΣ: Στοιχεία από τη θεωρία: Α. Τα οξέα, οι βάσεις και τα άλατα ανήκουν στην κατηγορία
ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΒΟΡΕΙΑΣ ΕΛΛΑΔΑΣ ΧΗΜΕΙΑ 23 Ιανουαρίου 2016 ΛΥΚΕΙΟ:..... ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1.. 2..... 3..... ΜΟΝΑΔΕΣ: Στοιχεία από τη θεωρία: Α. Τα οξέα, οι βάσεις και τα άλατα ανήκουν στην κατηγορία
ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ ΣΤΕΡΕΗΣ ΟΥΣΙΑΣ ΣΤΟ ΝΕΡΟ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ
 ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ ΣΤΕΡΕΗΣ ΟΥΣΙΑΣ ΣΤΟ ΝΕΡΟ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΕΙΣΑΓΩΓΗ ΚΑΙ ΣΤΟΧΟΙ Σε αυτή την εργαστηριακή άσκηση θα ορίσουμε την ταχύτητα διάλυσης μιας στερεής ουσίας στο νερό και θα
ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ ΣΤΕΡΕΗΣ ΟΥΣΙΑΣ ΣΤΟ ΝΕΡΟ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΕΙΣΑΓΩΓΗ ΚΑΙ ΣΤΟΧΟΙ Σε αυτή την εργαστηριακή άσκηση θα ορίσουμε την ταχύτητα διάλυσης μιας στερεής ουσίας στο νερό και θα
ΑΣΚΗΣΕΙΣ ΓΕΝΙΚΗΣ ΧΗΜΕΙΑΣ (2 η Εργαστηριακή Ημέρα) ΘΕΜΑ : ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ
 ΑΣΚΗΣΕΙΣ ΓΕΝΙΚΗΣ ΧΗΜΕΙΑΣ (2 η Εργαστηριακή Ημέρα) ΘΕΜΑ : ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΑΣΚΗΣΗ 5η: Ανάλυση Α αναλυτικής ομάδας κατιόντων (Ag +, Hg 2, Pb ) ΣΚΟΠΟΣ: Μελέτη εργαστηριακών μεθόδων για την ταυτοποίηση (αναγνώριση)
ΑΣΚΗΣΕΙΣ ΓΕΝΙΚΗΣ ΧΗΜΕΙΑΣ (2 η Εργαστηριακή Ημέρα) ΘΕΜΑ : ΠΟΙΟΤΙΚΗ ΑΝΑΛΥΣΗ ΑΣΚΗΣΗ 5η: Ανάλυση Α αναλυτικής ομάδας κατιόντων (Ag +, Hg 2, Pb ) ΣΚΟΠΟΣ: Μελέτη εργαστηριακών μεθόδων για την ταυτοποίηση (αναγνώριση)
Επιχάλκωση μεταλλικού αντικειμένου και συγκεκριμένα ενός μικρού ελάσματος αλουμινίου με τη μέθοδο της γαλβανοπλαστικής επιμετάλλωσης.
 Σύντομη περιγραφή του πειράματος Επιχάλκωση μεταλλικού αντικειμένου και συγκεκριμένα ενός μικρού ελάσματος αλουμινίου με τη μέθοδο της γαλβανοπλαστικής επιμετάλλωσης. Διδακτικοί στόχοι του πειράματος Στο
Σύντομη περιγραφή του πειράματος Επιχάλκωση μεταλλικού αντικειμένου και συγκεκριμένα ενός μικρού ελάσματος αλουμινίου με τη μέθοδο της γαλβανοπλαστικής επιμετάλλωσης. Διδακτικοί στόχοι του πειράματος Στο
Στόχοι της εργαστηριακής άσκησης
 ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2013-2014 Τοπικός διαγωνισμός στη Χημεία Ονόματα των μαθητών της ομάδας: 1) 2) 3) Στόχοι της εργαστηριακής
ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2013-2014 Τοπικός διαγωνισμός στη Χημεία Ονόματα των μαθητών της ομάδας: 1) 2) 3) Στόχοι της εργαστηριακής
Διάσπαση του ανθρακικού ασβεστίου με θέρμανση σε υψηλή θερμοκρασία προς οξείδιο του ασβεστίου και διοξείδιο του άνθρακα.
 Σύντομη περιγραφή του πειράματος Διάσπαση του ανθρακικού ασβεστίου με θέρμανση σε υψηλή θερμοκρασία προς οξείδιο του ασβεστίου και διοξείδιο του άνθρακα. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού
Σύντομη περιγραφή του πειράματος Διάσπαση του ανθρακικού ασβεστίου με θέρμανση σε υψηλή θερμοκρασία προς οξείδιο του ασβεστίου και διοξείδιο του άνθρακα. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΧΗΜΕΙΑ. 5 - Δεκεμβρίου Ερρίκος Γιακουμάκης
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΧΗΜΕΙΑ 5 - Δεκεμβρίου - 2015 Ερρίκος Γιακουμάκης 1 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ...... Εισαγωγικό σημείωμα Θεωρία Brőnsted- Lowry
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΧΗΜΕΙΑ 5 - Δεκεμβρίου - 2015 Ερρίκος Γιακουμάκης 1 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ...... Εισαγωγικό σημείωμα Θεωρία Brőnsted- Lowry
Χημικές αντιδράσεις Χημική εξίσωση ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ
 Χημικές αντιδράσεις Χημική εξίσωση Χημεία Β Γυμνασίου Προσδοκώμενα μαθησιακά αποτελέσματα Μετά την εργαστηριακή άσκηση οι μαθητές να μπορούν: Να αναφέρουν παραδείγματα χημικών αντιδράσεων και να διακρίνουν
Χημικές αντιδράσεις Χημική εξίσωση Χημεία Β Γυμνασίου Προσδοκώμενα μαθησιακά αποτελέσματα Μετά την εργαστηριακή άσκηση οι μαθητές να μπορούν: Να αναφέρουν παραδείγματα χημικών αντιδράσεων και να διακρίνουν
Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ. Χημεία. Εργαστηριακή άσκηση ΑΣΠΡΟΠΥΡΓΟΣ
 ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία Εργαστηριακή άσκηση ΑΣΠΡΟΠΥΡΓΟΣ 2 ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΦΥΛΛΟ ΕΡΓΟΥ 1 ΤΙΤΛΟΣ ΑΣΚΗΣΗΣ Προσδιορισμός περιεκτικότητας άγνωστου
ΑΕΝ / ΑΣΠΡΟΠΥΡΓΟΥ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ Καθηγητής : ΓΕΩΡΓΙΟΣ ΔΑΝΙΗΛ ΠΛΑΪΝΑΚΗΣ Χημεία Εργαστηριακή άσκηση ΑΣΠΡΟΠΥΡΓΟΣ 2 ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΦΥΛΛΟ ΕΡΓΟΥ 1 ΤΙΤΛΟΣ ΑΣΚΗΣΗΣ Προσδιορισμός περιεκτικότητας άγνωστου
2 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ A ΛΥΚΕΙΟΥ
 2 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ A ΛΥΚΕΙΟΥ "Πυροχημική ανίχνευση μεταλλοϊόντων" Απαιτούμενα Όργανα Ράβδος χρωμονικελίνης (ή μαγνησίας ή λευκοχρύσου) λύχνος Bunsen ύαλος ωρολογίου ποτήρι ζέσεως υδροβολέας
2 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ A ΛΥΚΕΙΟΥ "Πυροχημική ανίχνευση μεταλλοϊόντων" Απαιτούμενα Όργανα Ράβδος χρωμονικελίνης (ή μαγνησίας ή λευκοχρύσου) λύχνος Bunsen ύαλος ωρολογίου ποτήρι ζέσεως υδροβολέας
ΔΙΑΧΩΡΙΣΜΟΣ ΜΙΓΜΑΤΩΝ (4 η εργαστηριακή άσκηση Β Γυμνασίου)
 2 ο ΕΚΦΕ ΗΡΑΚΛΕΙΟΥ Επιμέλεια: Ορφανάκη Πόπη Χημικός Φωτογραφίες: Κωτίτσας Αριστοτέλης Βιολόγος ΔΙΑΧΩΡΙΣΜΟΣ ΜΙΓΜΑΤΩΝ (4 η εργαστηριακή άσκηση Β Γυμνασίου) 1. Διαχωρισμός μίγματος με διήθηση Με τη μέθοδο
2 ο ΕΚΦΕ ΗΡΑΚΛΕΙΟΥ Επιμέλεια: Ορφανάκη Πόπη Χημικός Φωτογραφίες: Κωτίτσας Αριστοτέλης Βιολόγος ΔΙΑΧΩΡΙΣΜΟΣ ΜΙΓΜΑΤΩΝ (4 η εργαστηριακή άσκηση Β Γυμνασίου) 1. Διαχωρισμός μίγματος με διήθηση Με τη μέθοδο
-Η συγκράτηση νερού από διάφορα υλικά, ουσίες και ενώσεις είναι ένα θέμα με μεγάλο τεχνολογικό ενδιαφέρον. Και αυτό γιατί το αν υπάρχει ή όχι υγρασία
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2017 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΤΑΥΤΟΠΟΙΗΣΗ 7 ΛΕΥΚΩΝ ΣΤΕΡΕΩΝ 2. ΠΕΙΡΑΜΑΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΝΕΡΩΝ ΚΡΥΣΤΑΛΛΩΣΗΣ
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΣΥΡΟΥ για το EUSO 2017 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 1. ΤΑΥΤΟΠΟΙΗΣΗ 7 ΛΕΥΚΩΝ ΣΤΕΡΕΩΝ 2. ΠΕΙΡΑΜΑΤΙΚΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΝΕΡΩΝ ΚΡΥΣΤΑΛΛΩΣΗΣ
ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ: ΠΑΡΑΣΚΕΥΗ ΣΑΠΟΥΝΙΟΥ. Η εργαστηριακή αυτή άσκηση πραγματοποιήθηκε στο ΕΚΦΕ Ιωαννίνων
 ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ: ΠΑΡΑΣΚΕΥΗ ΣΑΠΟΥΝΙΟΥ Η εργαστηριακή αυτή άσκηση πραγματοποιήθηκε στο ΕΚΦΕ Ιωαννίνων 1/3/2013 και 6/3/2013 Μάντζιου Μαρία χημικός ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς:
ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ: ΠΑΡΑΣΚΕΥΗ ΣΑΠΟΥΝΙΟΥ Η εργαστηριακή αυτή άσκηση πραγματοποιήθηκε στο ΕΚΦΕ Ιωαννίνων 1/3/2013 και 6/3/2013 Μάντζιου Μαρία χημικός ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς:
CH 3 CHO + Cu + H 2 O Το οξείδιο του χαλκού μπορεί να σχηματιστεί κατά την πύρωση του χαλκού. CuO. Cu O 2
 Οξείδωση της αιανόλης Ανίχνευση αλδεΰδης ΟΔΗΓΙΕΣ ΚΗΘΗΓΗΤΗ Διδακτικοί στόχοι 1. Να γνωστοποιηούν τα ήπια αλλά και τα πιο δραστικά οξειδωτικά αντιδραστήρια. 2. Να συνδυαστεί η οξείδωση/ανίχνευση της αιανόλης
Οξείδωση της αιανόλης Ανίχνευση αλδεΰδης ΟΔΗΓΙΕΣ ΚΗΘΗΓΗΤΗ Διδακτικοί στόχοι 1. Να γνωστοποιηούν τα ήπια αλλά και τα πιο δραστικά οξειδωτικά αντιδραστήρια. 2. Να συνδυαστεί η οξείδωση/ανίχνευση της αιανόλης
Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ
 Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ Ονόματα διαγωνιζομένων: 1) 2) 3) Σχολείο: Όνομα Υπεύθυνου Καθηγητή: 1 η ΠΕΙΡΑΜΑΤΙΚΗ ΔΡΑΣΤΗΡΙΟΤΗΤΑ
Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ Ονόματα διαγωνιζομένων: 1) 2) 3) Σχολείο: Όνομα Υπεύθυνου Καθηγητή: 1 η ΠΕΙΡΑΜΑΤΙΚΗ ΔΡΑΣΤΗΡΙΟΤΗΤΑ
ΓΕΛ ΠΑΡΑΒΟΛΑΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 2013-2014
 ΓΕΛ ΠΑΡΑΒΟΛΑΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 2013-2014 Ερευνητική εργασία: Β2 λυκείου ΘΕΜΑ: ''Η Χημεία είναι χρώματα, αρώματα και γεύσεις'' Ομάδα Δ: Μαριάμ Χριστογιάννη Μαρία Χριστοπούλου Χριστίνα Σταμάτη Βάσω Σιρμιντζέλη
ΓΕΛ ΠΑΡΑΒΟΛΑΣ ΣΧΟΛΙΚΟ ΕΤΟΣ 2013-2014 Ερευνητική εργασία: Β2 λυκείου ΘΕΜΑ: ''Η Χημεία είναι χρώματα, αρώματα και γεύσεις'' Ομάδα Δ: Μαριάμ Χριστογιάννη Μαρία Χριστοπούλου Χριστίνα Σταμάτη Βάσω Σιρμιντζέλη
ΙΑΝΟΥΑΡΙΟΣ 2012 Πειράματα Χημείας
 http://ekfe.chi.sch.gr 5 η - 6 η Συνάντηση ΙΑΝΟΥΑΡΙΟΣ 2012 Πειράματα Χημείας Aντικατάσταση χαλκού από σίδηρο Επίδραση της θερμοκρασίας στη χημική ισορροπία Επίδραση της συγκέντρωσης στη χημική ισορροπία
http://ekfe.chi.sch.gr 5 η - 6 η Συνάντηση ΙΑΝΟΥΑΡΙΟΣ 2012 Πειράματα Χημείας Aντικατάσταση χαλκού από σίδηρο Επίδραση της θερμοκρασίας στη χημική ισορροπία Επίδραση της συγκέντρωσης στη χημική ισορροπία
ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΑΝΤΙΔΡΑΣΗΣ ΕΞΟΥΔΕΤΕΡΩΣΗΣ ΜΕ ΤΗ ΧΡΗΣΗ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ ΣΥΓΧΡΟΝΙΚΗΣ ΛΗΨΗΣ ΚΑΙ ΑΠΕΙΚΟΝΙΣΗΣ MultiLog
 ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΑΝΤΙΔΡΑΣΗΣ ΕΞΟΥΔΕΤΕΡΩΣΗΣ ΜΕ ΤΗ ΧΡΗΣΗ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ ΣΥΓΧΡΟΝΙΚΗΣ ΛΗΨΗΣ ΚΑΙ ΑΠΕΙΚΟΝΙΣΗΣ MultiLog Αντωνίου Κωνσταντίνος ΠΕ04-02 (χημικός) ΓΕ.Λ Ζωσιμαίας Σχολής Ιωαννίνων. Το MultiLog
ΥΠΟΛΟΓΙΣΜΟΣ ΘΕΡΜΟΤΗΤΑΣ ΑΝΤΙΔΡΑΣΗΣ ΕΞΟΥΔΕΤΕΡΩΣΗΣ ΜΕ ΤΗ ΧΡΗΣΗ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ ΣΥΓΧΡΟΝΙΚΗΣ ΛΗΨΗΣ ΚΑΙ ΑΠΕΙΚΟΝΙΣΗΣ MultiLog Αντωνίου Κωνσταντίνος ΠΕ04-02 (χημικός) ΓΕ.Λ Ζωσιμαίας Σχολής Ιωαννίνων. Το MultiLog
Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2014 Τοπικός διαγωνισμός στη Χημεία
 ΕΚΦΕ ΝΕΑΣ ΙΩΝΙΑΣ - ΧΑΛΑΝΔΡΙΟΥ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2014 Τοπικός διαγωνισμός στη Χημεία ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Β' ΑΘΗΝΑΣ ΠΑΡΑΣΚΕΥΗ ΔΙΑΛΥΜΑΤΟΣ ΟΞΕΟΣ ΗΑ ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ
ΕΚΦΕ ΝΕΑΣ ΙΩΝΙΑΣ - ΧΑΛΑΝΔΡΙΟΥ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2014 Τοπικός διαγωνισμός στη Χημεία ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Β' ΑΘΗΝΑΣ ΠΑΡΑΣΚΕΥΗ ΔΙΑΛΥΜΑΤΟΣ ΟΞΕΟΣ ΗΑ ΠΕΙΡΑΜΑΤΙΚΗ ΔΙΑΔΙΚΑΣΙΑ
Εισαγωγή στο Εργαστήριο
 Εισαγωγή στο Εργαστήριο ΒΑΣΙΚΟΙ ΚΑΝΟΝΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΦΑΛΕΙΑΣ Οι κανόνες εργαστηριακής άσκησης αποβλέπουν στη σωστή λειτουργία του εργαστηρίου και κυρίως εξασφαλίζουν την ασφάλεια των εργαζομένων σε
Εισαγωγή στο Εργαστήριο ΒΑΣΙΚΟΙ ΚΑΝΟΝΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΦΑΛΕΙΑΣ Οι κανόνες εργαστηριακής άσκησης αποβλέπουν στη σωστή λειτουργία του εργαστηρίου και κυρίως εξασφαλίζουν την ασφάλεια των εργαζομένων σε
Ποιοτική ανάλυση ιόντων 1 ο Πείραμα
 Εισαγωγή Ποιοτική ανάλυση ιόντων 1 ο Πείραμα Η ρύπανση του υδροφόρου ορίζοντα και των εδαφών από βιομηχανικά απόβλητα είναι ένα από τα καίρια περιβαλλοντικά προβλήματα της εποχής μας. Ειδικά η απόρριψη
Εισαγωγή Ποιοτική ανάλυση ιόντων 1 ο Πείραμα Η ρύπανση του υδροφόρου ορίζοντα και των εδαφών από βιομηχανικά απόβλητα είναι ένα από τα καίρια περιβαλλοντικά προβλήματα της εποχής μας. Ειδικά η απόρριψη
ΜΕΡΟΣ Α : Ερωτήσεις 1-6 Να απαντήσετε σε όλες τις ερωτήσεις 1-6. Κάθε ορθή απάντηση βαθμολογείται με πέντε (5) μονάδες.
 ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2008-2009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΔΕΙΓΜΑΤΙΚΟ ΕΞΕΤΑΣΤΙΚΟ ΔΟΚΙΜΙΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΤΑΞΗ: Β ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΧΡΟΝΟΣ: 2 ώρες και 30 λεπτά Το εξεταστικό δοκίμιο αποτελείται από
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2008-2009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΔΕΙΓΜΑΤΙΚΟ ΕΞΕΤΑΣΤΙΚΟ ΔΟΚΙΜΙΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΤΑΞΗ: Β ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΧΡΟΝΟΣ: 2 ώρες και 30 λεπτά Το εξεταστικό δοκίμιο αποτελείται από
ΧΗΜΙΚΕ ΑΝΣΙΔΡΑΕΙ ΚΑΙ ΠΟΙΟΣΙΚΗ ΑΝΑΛΤΗ ΙΟΝΣΩΝ
 ΕΡΓΑΣΗΡΙΑΚΗ ΑΚΗΗ 6 ΧΗΜΙΚΕ ΑΝΣΙΔΡΑΕΙ ΚΑΙ ΠΟΙΟΣΙΚΗ ΑΝΑΛΤΗ ΙΟΝΣΩΝ α. ανίχνευση ιόντων χλωρίου Cl Δοκιμαστικοί σωλήνες ( ) διάλυμα υδροχλωρίου HCl 0,01Μ Σταγονόμετρα χλωριούχο νάτριο NaCl, χλωριούχου αργιλίου
ΕΡΓΑΣΗΡΙΑΚΗ ΑΚΗΗ 6 ΧΗΜΙΚΕ ΑΝΣΙΔΡΑΕΙ ΚΑΙ ΠΟΙΟΣΙΚΗ ΑΝΑΛΤΗ ΙΟΝΣΩΝ α. ανίχνευση ιόντων χλωρίου Cl Δοκιμαστικοί σωλήνες ( ) διάλυμα υδροχλωρίου HCl 0,01Μ Σταγονόμετρα χλωριούχο νάτριο NaCl, χλωριούχου αργιλίου
Εργαστηριακή άσκηση 4: ΠΑΡΑΣΚΕΥΗ ΙΑΛΥΜΑΤΟΣ ΟΡΙΣΜΕΝΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ - ΑΡΑΙΩΣΗ ΙΑΛΥΜΑΤΩΝ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ Εργαστηριακή άσκηση 4: ΠΑΡΑΣΚΕΥΗ ΙΑΛΥΜΑΤΟΣ ΟΡΙΣΜΕΝΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ - ΑΡΑΙΩΣΗ ΙΑΛΥΜΑΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράµατος αυτού θα πρέπει να µπορείς : 1. Να εφαρµόζεις το ζυγό. 2. Να µετράς
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ Εργαστηριακή άσκηση 4: ΠΑΡΑΣΚΕΥΗ ΙΑΛΥΜΑΤΟΣ ΟΡΙΣΜΕΝΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ - ΑΡΑΙΩΣΗ ΙΑΛΥΜΑΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράµατος αυτού θα πρέπει να µπορείς : 1. Να εφαρµόζεις το ζυγό. 2. Να µετράς
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ. ΚΕΦ.3.1: ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ (α)
 ΚΕΦ.3.1: ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ (α ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ είναι οι μεταβολές κατά τις οποίες από κάποια αρχικά σώματα (αντιδρώντα παράγονται νέα σώματα (προϊόντα. CO 2 O γλυκόζη (Φωτοσύνθεση Σάκχαρα αλκοόλη
ΚΕΦ.3.1: ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ (α ΧΗΜΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ είναι οι μεταβολές κατά τις οποίες από κάποια αρχικά σώματα (αντιδρώντα παράγονται νέα σώματα (προϊόντα. CO 2 O γλυκόζη (Φωτοσύνθεση Σάκχαρα αλκοόλη
Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2014 Τοπικός διαγωνισμός στη Χημεία Ονοματεπώνυμο μαθητών. Το σενάριο
 ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Β' ΑΘΗΝΑΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2014 Τοπικός διαγωνισμός στη Χημεία 07-12-2013 α. β. γ. Ονοματεπώνυμο μαθητών Σχολείο Το σενάριο Δυο μαθητές βγαίνοντας
ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Β' ΑΘΗΝΑΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2014 Τοπικός διαγωνισμός στη Χημεία 07-12-2013 α. β. γ. Ονοματεπώνυμο μαθητών Σχολείο Το σενάριο Δυο μαθητές βγαίνοντας
Το εξεταστικό δοκίμιο αποτελείται από οκτώ (8) σελίδες
 Το εξεταστικό δοκίμιο αποτελείται από οκτώ (8) σελίδες Ερωτήσεις 1-25: Για κάθε μια από τις ερωτήσεις που ακολουθούν δίνονται πέντε πιθανές απαντήσεις. Να επιλέξετε την ορθή απάντηση. Για κάθε ερώτηση
Το εξεταστικό δοκίμιο αποτελείται από οκτώ (8) σελίδες Ερωτήσεις 1-25: Για κάθε μια από τις ερωτήσεις που ακολουθούν δίνονται πέντε πιθανές απαντήσεις. Να επιλέξετε την ορθή απάντηση. Για κάθε ερώτηση
Περιγραφή Βασικού Εργαστηριακού Εξοπλισμού
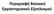 Περιγραφή Βασικού Εργαστηριακού Εξοπλισμού Ζυγοί Αναλυτικός Ζυγός με ακρίβεια 0,0001 g δηλ. 0,1 mg. Είναι απλός και ακριβής. Η ζύγιση γίνεται αφού κλείσουμε τις συρόμενες θύρες του. Ηλεκτρονικός Ζυγός
Περιγραφή Βασικού Εργαστηριακού Εξοπλισμού Ζυγοί Αναλυτικός Ζυγός με ακρίβεια 0,0001 g δηλ. 0,1 mg. Είναι απλός και ακριβής. Η ζύγιση γίνεται αφού κλείσουμε τις συρόμενες θύρες του. Ηλεκτρονικός Ζυγός
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΟΞΥΤΗΤΑΣ ΣΕ ΚΡΑΣΙ (ΛΕΥΚΟ)
 ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΥΠΕΥΘΥΝΩΝ ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΕΝΤΡΩΝ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ - «ΠΑΝΕΚΦE» email:panekfe@yahoo.gr www.ekfe.gr ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2010 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΣΤΗ
ΠΑΝΕΛΛΗΝΙΑ ΕΝΩΣΗ ΥΠΕΥΘΥΝΩΝ ΕΡΓΑΣΤΗΡΙΑΚΩΝ ΚΕΝΤΡΩΝ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ - «ΠΑΝΕΚΦE» email:panekfe@yahoo.gr www.ekfe.gr ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2010 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΣΤΗ
ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΟΞΕΙΔΩΣΗ ΑΙΘΑΝΟΛΗΣ (Πείραμα 1 εργαστηριακού οδηγού-β Λυκείου Γενικής Παιδείας)
 2o ΕΚΦΕ ΗΡΑΚΛΕΙΟΥ Επιμέλεια: Ορφανάκη Πόπη - Χημικός Φωτογραφίες: Κωτίτσας Αριστοτέλης - Βιολόγος ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΟΞΕΙΔΩΣΗ ΑΙΘΑΝΟΛΗΣ (Πείραμα 1 εργαστηριακού οδηγού-β Λυκείου Γενικής Παιδείας) ΠΑΡΑΣΚΕΥΗ
2o ΕΚΦΕ ΗΡΑΚΛΕΙΟΥ Επιμέλεια: Ορφανάκη Πόπη - Χημικός Φωτογραφίες: Κωτίτσας Αριστοτέλης - Βιολόγος ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΟΞΕΙΔΩΣΗ ΑΙΘΑΝΟΛΗΣ (Πείραμα 1 εργαστηριακού οδηγού-β Λυκείου Γενικής Παιδείας) ΠΑΡΑΣΚΕΥΗ
3. Όταν χλωριούχο νάτριο πυρωθεί στο λύχνο Bunsen, η φλόγα θα πάρει χρώμα: Α. Κόκκινο Β. Κίτρινο Γ. Μπλε Δ. Πράσινο Ε. Ιώδες
 Το εξεταστικό δοκίμιο αποτελείται από οκτώ (8) σελίδες Ερωτήσεις 1-22: Για κάθε μια από τις ερωτήσεις που ακολουθούν δίνονται πέντε πιθανές απαντήσεις. Να επιλέξετε την ορθή απάντηση. Για κάθε ερώτηση
Το εξεταστικό δοκίμιο αποτελείται από οκτώ (8) σελίδες Ερωτήσεις 1-22: Για κάθε μια από τις ερωτήσεις που ακολουθούν δίνονται πέντε πιθανές απαντήσεις. Να επιλέξετε την ορθή απάντηση. Για κάθε ερώτηση
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΠΡΑΚΤΙΚΗ ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ
 17η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2019 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΑΜΠΕΛΟΚΗΠΩΝ ΗΛΙΟΥΠΟΛΗΣ ΝΕΑΣ ΦΙΛΑΔΕΛΦΕΙΑΣ - ΟΜΟΝΟΙΑΣ ΠΡΑΚΤΙΚΗ ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ ΣΧΟΛΕΙΟ: ΟΝΟΜΑΤΑ ΔΙΑΓΩΝΙΖΟΜΕΝΩΝ ΜΑΘΗΤΩΝ: 1) 2) 3) ΥΠΕΥΘΥΝΟΣ
17η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2019 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΑΜΠΕΛΟΚΗΠΩΝ ΗΛΙΟΥΠΟΛΗΣ ΝΕΑΣ ΦΙΛΑΔΕΛΦΕΙΑΣ - ΟΜΟΝΟΙΑΣ ΠΡΑΚΤΙΚΗ ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ ΣΧΟΛΕΙΟ: ΟΝΟΜΑΤΑ ΔΙΑΓΩΝΙΖΟΜΕΝΩΝ ΜΑΘΗΤΩΝ: 1) 2) 3) ΥΠΕΥΘΥΝΟΣ
Γεωργική Χημεία Εργαστηριακές ασκήσεις
 Γεωργική Χημεία Εργαστηριακές ασκήσεις Γεώργιος Παπαδόπουλος, Καθηγητής Τμ. Τεχνολόγων Γεωπόνων Τ.Ε. Άρτα, 2015 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
Γεωργική Χημεία Εργαστηριακές ασκήσεις Γεώργιος Παπαδόπουλος, Καθηγητής Τμ. Τεχνολόγων Γεωπόνων Τ.Ε. Άρτα, 2015 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ
 ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ ΚΑΝΟΝΕΣ ΕΡΓΑΣΤΗΡΙΟΥ ΟΡΓΑΝΑ ΕΡΓΑΣΤΗΡΙΟΥ ΧΗΜΕΙΑΣ ΚΑΝΟΝΕΣ ΕΡΓΑΣΤΗΡΙΟΥ Σήματα που υποδηλώνουν τον βαθμό επικινδυνότητας των χημικών ουσιών εκρηκτικό πολύ εύφλεκτο (F) τοξικό (Τ)
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ ΚΑΝΟΝΕΣ ΕΡΓΑΣΤΗΡΙΟΥ ΟΡΓΑΝΑ ΕΡΓΑΣΤΗΡΙΟΥ ΧΗΜΕΙΑΣ ΚΑΝΟΝΕΣ ΕΡΓΑΣΤΗΡΙΟΥ Σήματα που υποδηλώνουν τον βαθμό επικινδυνότητας των χημικών ουσιών εκρηκτικό πολύ εύφλεκτο (F) τοξικό (Τ)
Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου.
 Σύντομη περιγραφή του πειράματος Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού του πειράματος θα πρέπει ο μαθητής: Να περιγράφει τον τρόπο
Σύντομη περιγραφή του πειράματος Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού του πειράματος θα πρέπει ο μαθητής: Να περιγράφει τον τρόπο
Άσκηση 3η. Μέθοδοι Διαχωρισμού. Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας
 Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
(είναι οι αντιδράσεις στις οποίες δεν μεταβάλλεται ο αριθμός οξείδωσης σε κανένα από τα στοιχεία που συμμετέχουν)
 Κατηγορίες Χημικών Αντιδράσεων Μεταθετικές Αντιδράσεις (είναι οι αντιδράσεις στις οποίες δεν μεταβάλλεται ο αριθμός οξείδωσης σε κανένα από τα στοιχεία που συμμετέχουν) l Αντιδράσεις εξουδετέρωσης Χαρακτηρίζονται
Κατηγορίες Χημικών Αντιδράσεων Μεταθετικές Αντιδράσεις (είναι οι αντιδράσεις στις οποίες δεν μεταβάλλεται ο αριθμός οξείδωσης σε κανένα από τα στοιχεία που συμμετέχουν) l Αντιδράσεις εξουδετέρωσης Χαρακτηρίζονται
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 12 η Ευρωπαϊκή Ολυµπιάδα Επιστηµών EUSO 2014 ΧΗΜΕΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 12 η Ευρωπαϊκή Ολυµπιάδα Επιστηµών EUSO 2014 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συµµετέχουν: (1) (2) (3) Σέρρες 07/12/2013
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΣΕΡΡΩΝ 12 η Ευρωπαϊκή Ολυµπιάδα Επιστηµών EUSO 2014 ΤΟΠΙΚΟΣ ΜΑΘΗΤΙΚΟΣ ΙΑΓΩΝΙΣΜΟΣ ΠΕΙΡΑΜΑΤΩΝ ΧΗΜΕΙΑΣ ΣΧΟΛΕΙΟ:. Μαθητές/τριες που συµµετέχουν: (1) (2) (3) Σέρρες 07/12/2013
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ
 ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ B ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ 1. Ταξινόμηση
ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ B ΤΑΞΗ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ 1. Ταξινόμηση
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΠΡΑΚΤΙΚΗ ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ
 16η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2018 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΑΜΠΕΛΟΚΗΠΩΝ ΗΛΙΟΥΠΟΛΗΣ ΝΕΑΣ ΦΙΛΑΔΕΛΦΕΙΑΣ - ΟΜΟΝΟΙΑΣ ΠΡΑΚΤΙΚΗ ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ ΣΧΟΛΕΙΟ: ΟΝΟΜΑΤΑ ΔΙΑΓΩΝΙΖΟΜΕΝΩΝ ΜΑΘΗΤΩΝ: 1) 2) 3) ΥΠΕΥΘΥΝΟΣ
16η Ευρωπαϊκή Ολυμπιάδα Επιστημών EUSO 2018 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΚΦΕ ΑΜΠΕΛΟΚΗΠΩΝ ΗΛΙΟΥΠΟΛΗΣ ΝΕΑΣ ΦΙΛΑΔΕΛΦΕΙΑΣ - ΟΜΟΝΟΙΑΣ ΠΡΑΚΤΙΚΗ ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ ΣΧΟΛΕΙΟ: ΟΝΟΜΑΤΑ ΔΙΑΓΩΝΙΖΟΜΕΝΩΝ ΜΑΘΗΤΩΝ: 1) 2) 3) ΥΠΕΥΘΥΝΟΣ
Άσκηση 7η. Χημική Ισορροπία. Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών
 Άσκηση 7η Χημική Ισορροπία Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Η έννοια της Χημικής Ισορροπίας Υπάρχουν χηµικές αντιδράσεις που εξελίσσονται προς µία µόνο μόνο κατεύθυνση, όπως π.χ. η σύνθεση
Άσκηση 7η Χημική Ισορροπία Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Η έννοια της Χημικής Ισορροπίας Υπάρχουν χηµικές αντιδράσεις που εξελίσσονται προς µία µόνο μόνο κατεύθυνση, όπως π.χ. η σύνθεση
ΓΕΝΙΚΟΙ ΚΑΝΟΝΕΣ ΑΣΦΑΛΕΙΑΣ ΓΙΑ ΤΟ ΧΗΜΙΚΟ ΕΡΓΑΣΤΗΡΙΟ
 ΓΕΝΙΚΟΙ ΚΑΝΟΝΕΣ ΑΣΦΑΛΕΙΑΣ ΓΙΑ ΤΟ ΧΗΜΙΚΟ ΕΡΓΑΣΤΗΡΙΟ Πυρίμαχα γάντια Μπορώ να τρώω το σάντουιτς και να πίνω το αναψυκτικό ή τον καφέ μου μέσα στο εργαστήριο; ΟΧΙ! Μέσα στο εργαστήριο δεν τρώμε και δεν
ΓΕΝΙΚΟΙ ΚΑΝΟΝΕΣ ΑΣΦΑΛΕΙΑΣ ΓΙΑ ΤΟ ΧΗΜΙΚΟ ΕΡΓΑΣΤΗΡΙΟ Πυρίμαχα γάντια Μπορώ να τρώω το σάντουιτς και να πίνω το αναψυκτικό ή τον καφέ μου μέσα στο εργαστήριο; ΟΧΙ! Μέσα στο εργαστήριο δεν τρώμε και δεν
ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ
 ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ 05 ΔΕΚΕΜΒΡΙΟΥ 2015 (Διάρκεια εξέτασης 60 min) ΘΕΜΑ: Σειρά δραστικότητας μετάλλων ΣΧΟΛΙΚΗ ΜΟΝΑΔΑ:. ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1).. 2)... 3).. ΒΑΘΜΟΛΟΓΙΑ ΘΕΩΡΗΤΙΚΟ
ΠΡΟΚΡΙΜΑΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2016 ΕΞΕΤΑΣΗ ΣΤΗ ΧΗΜΕΙΑ 05 ΔΕΚΕΜΒΡΙΟΥ 2015 (Διάρκεια εξέτασης 60 min) ΘΕΜΑ: Σειρά δραστικότητας μετάλλων ΣΧΟΛΙΚΗ ΜΟΝΑΔΑ:. ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1).. 2)... 3).. ΒΑΘΜΟΛΟΓΙΑ ΘΕΩΡΗΤΙΚΟ
Τάξη B Εργαστηριακές ασκήσεις χημείας στις ιδιότητες των διαλυμάτων
 Τάξη B Εργαστηριακές ασκήσεις χημείας στις ιδιότητες των διαλυμάτων Β.Βελεχέρης ΕΚΦΕ Δωδεκανήσου Γυμνάσιο Ιαλυσού ΣΤΑΔΙΟ Ι Εισαγωγή - Υπολογισμοί Τάξη Β Εργαστηριακές ασκήσεις χημείας στα διαλύματα Οι
Τάξη B Εργαστηριακές ασκήσεις χημείας στις ιδιότητες των διαλυμάτων Β.Βελεχέρης ΕΚΦΕ Δωδεκανήσου Γυμνάσιο Ιαλυσού ΣΤΑΔΙΟ Ι Εισαγωγή - Υπολογισμοί Τάξη Β Εργαστηριακές ασκήσεις χημείας στα διαλύματα Οι
14 η ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΕΚΦΕ ΧΑΛΑΝΔΡΙΟΥ και ΝΕΑΣ ΙΩΝΙΑΣ Τοπικός διαγωνισμός στη XHMEIA 05 Δεκεμβρίου 2015
 14 η ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΕΚΦΕ ΧΑΛΑΝΔΡΙΟΥ και ΝΕΑΣ ΙΩΝΙΑΣ Τοπικός διαγωνισμός στη XHMEIA 05 Δεκεμβρίου 2015 Μαθητές Σχολείο 1. 2. 3. ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΑΡΑΙΩΣΗ ΔΙΑΛΥΜΑΤΩΝ ΗΛΕΚΤΡΙΚΗ ΑΓΩΓΙΜΟΤΗΤΑ ΔΙΑΛΥΜΑΤΩΝ
14 η ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΕΚΦΕ ΧΑΛΑΝΔΡΙΟΥ και ΝΕΑΣ ΙΩΝΙΑΣ Τοπικός διαγωνισμός στη XHMEIA 05 Δεκεμβρίου 2015 Μαθητές Σχολείο 1. 2. 3. ΠΑΡΑΣΚΕΥΗ ΚΑΙ ΑΡΑΙΩΣΗ ΔΙΑΛΥΜΑΤΩΝ ΗΛΕΚΤΡΙΚΗ ΑΓΩΓΙΜΟΤΗΤΑ ΔΙΑΛΥΜΑΤΩΝ
1. Παρατήρηση βρασμού του νερού μέσω των αισθητήρων.
 Εισηγητές, οι συνεργάτες του ΕΚΦΕ : Γαβρίλης Ηλίας, Χημικός Βράκα Ελένη, Φυσικός Α. ΠΕΙΡΑΜΑΤΑ ΕΠΙΔΕΙΞΗΣ 1. Παρατήρηση βρασμού του νερού μέσω των αισθητήρων. 2. Σύσταση του ατμοσφαιρικού αέρα Σκοπός Να
Εισηγητές, οι συνεργάτες του ΕΚΦΕ : Γαβρίλης Ηλίας, Χημικός Βράκα Ελένη, Φυσικός Α. ΠΕΙΡΑΜΑΤΑ ΕΠΙΔΕΙΞΗΣ 1. Παρατήρηση βρασμού του νερού μέσω των αισθητήρων. 2. Σύσταση του ατμοσφαιρικού αέρα Σκοπός Να
Άσκηση 3η. Μέθοδοι Διαχωρισμού. Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας
 Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
+ ή ΟΗ OH ( 1 ) ( 2 ) ( 1 ) ( 2 )
 ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ 5 ΕΥΡΕΣΗ pη ΔΙΑΛΥΜΑΤΩΝ ΜΕ ΧΡΗΣΗ ΔΕΙΚΤΩΝ Στόχοι Οι μαθητές: Να κατανοήσουν το τι εκφράζει το pη ενός διαλύματος. Να προσδιορίζουν το pη ενός διαλύματος με τη χρήση διαλυμάτων δεικτών
ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ 5 ΕΥΡΕΣΗ pη ΔΙΑΛΥΜΑΤΩΝ ΜΕ ΧΡΗΣΗ ΔΕΙΚΤΩΝ Στόχοι Οι μαθητές: Να κατανοήσουν το τι εκφράζει το pη ενός διαλύματος. Να προσδιορίζουν το pη ενός διαλύματος με τη χρήση διαλυμάτων δεικτών
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ. 9 - Δεκεμβρίου
 1 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ 9 - Δεκεμβρίου - 2017 2 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ..... 1 η Δραστηριότητα Παρασκευή δυο υδατικών διαλυμάτων ΝaCl με
1 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ 9 - Δεκεμβρίου - 2017 2 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ..... 1 η Δραστηριότητα Παρασκευή δυο υδατικών διαλυμάτων ΝaCl με
Παρασκευαστικό διαχωρισμό πολλών ουσιών με κατανομή μεταξύ των δύο διαλυτών.
 1. ΕΚΧΥΛΙΣΗ Η εκχύλιση είναι μία από τις πιο συνηθισμένες τεχνικές διαχωρισμού και βασίζεται στην ισορροπία κατανομής μιας ουσίας μεταξύ δύο φάσεων, που αναμιγνύονται ελάχιστα μεταξύ τους. Η ευρύτητα στη
1. ΕΚΧΥΛΙΣΗ Η εκχύλιση είναι μία από τις πιο συνηθισμένες τεχνικές διαχωρισμού και βασίζεται στην ισορροπία κατανομής μιας ουσίας μεταξύ δύο φάσεων, που αναμιγνύονται ελάχιστα μεταξύ τους. Η ευρύτητα στη
Το χρώμα του μπλε της θυμόλης σε διαφορετικές τιμές ph
 Ε.Κ.Φ.Ε. Χαλανδρίου 9 ος Εργαστηριακός Διαγωνισμός Φυσικών Επιστημών Γυμνασίων Μέρος 2 ο : Χημεία - Τρίτη 9 Μαΐου Όνομα σχολείου: Ονοματεπώνυμο μαθητών 1.. 2... 3.. Όπως γνωρίζετε, σύμφωνα με τον Arrhenius,
Ε.Κ.Φ.Ε. Χαλανδρίου 9 ος Εργαστηριακός Διαγωνισμός Φυσικών Επιστημών Γυμνασίων Μέρος 2 ο : Χημεία - Τρίτη 9 Μαΐου Όνομα σχολείου: Ονοματεπώνυμο μαθητών 1.. 2... 3.. Όπως γνωρίζετε, σύμφωνα με τον Arrhenius,
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
Α + Β - + Γ + Δ - Α + Δ - + Γ + Β - Στις αντιδράσεις αυτές οι Α.Ο όλων των στοιχείων παραμένουν σταθεροί.
 1. Στόχοι του μαθήματος 4 o Μάθημα : Μεταθετικές αντιδράσεις Οι μαθητές να γνωρίσουν: i) ποιες είναι οι σπουδαιότερες κατηγορίες των μεταθετικών αντιδράσεων. ii) τις μορφές των αντιδράσεων διπλής αντικατάστασης
1. Στόχοι του μαθήματος 4 o Μάθημα : Μεταθετικές αντιδράσεις Οι μαθητές να γνωρίσουν: i) ποιες είναι οι σπουδαιότερες κατηγορίες των μεταθετικών αντιδράσεων. ii) τις μορφές των αντιδράσεων διπλής αντικατάστασης
ΘΕΜΑΤΑ ΧΗΜΕΙΑΣ ΤΟΠΙΚΟΥ ΙΑΓΩΝΙΣΜΟΥ EUSO 2009
 ΘΕΜΑΤΑ ΧΗΜΕΙΑΣ ΤΟΠΙΚΟΥ ΙΑΓΩΝΙΣΜΟΥ EUSO 2009 ΘΕΜΑΤΑ Α. Αραίωση ιαλύµατος ΗCl 1M. Παρασκευή 100mL διαλύµατος HCl 0.8Μ. Β. Θερµότητα Αντίδρασης. Υπολογισµός της θερµότητας αντίδρασης στην εξουδετέρωση του
ΘΕΜΑΤΑ ΧΗΜΕΙΑΣ ΤΟΠΙΚΟΥ ΙΑΓΩΝΙΣΜΟΥ EUSO 2009 ΘΕΜΑΤΑ Α. Αραίωση ιαλύµατος ΗCl 1M. Παρασκευή 100mL διαλύµατος HCl 0.8Μ. Β. Θερµότητα Αντίδρασης. Υπολογισµός της θερµότητας αντίδρασης στην εξουδετέρωση του
Κεφάλαιο 3 Χημικές Αντιδράσεις
 Κεφάλαιο 3 Χημικές Αντιδράσεις Οι χημικές αντιδράσεις μπορούν να ταξινομηθούν σε δύο μεγάλες κατηγορίες, τις οξειδοαναγωγικές και τις μεταθετικές. Α. ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Στις αντιδράσεις αυτές
Κεφάλαιο 3 Χημικές Αντιδράσεις Οι χημικές αντιδράσεις μπορούν να ταξινομηθούν σε δύο μεγάλες κατηγορίες, τις οξειδοαναγωγικές και τις μεταθετικές. Α. ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΑΝΤΙΔΡΑΣΕΙΣ Στις αντιδράσεις αυτές
ΤΙΤΛΟΣ ΑΣΚΗΣΗΣ : Παρασκευή και ιδιότητες ρυθμιστικών διαλυμάτων Τάξη : Γ Λυκείου, Χημεία κατ/νσης
 ΕΚΦΕ Α & Β ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ ΤΙΤΛΟΣ ΑΣΚΗΣΗΣ : Παρασκευή και ιδιότητες ρυθμιστικών διαλυμάτων Τάξη : Γ Λυκείου, Χημεία κατ/νσης ΔΙΔΑΚΤΙΚΟΙ ΣΤΟΧΟΙ Να παρασκευάσουν ρυθμιστικό διάλυμα με ορισμένη τιμή pη.
ΕΚΦΕ Α & Β ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ ΤΙΤΛΟΣ ΑΣΚΗΣΗΣ : Παρασκευή και ιδιότητες ρυθμιστικών διαλυμάτων Τάξη : Γ Λυκείου, Χημεία κατ/νσης ΔΙΔΑΚΤΙΚΟΙ ΣΤΟΧΟΙ Να παρασκευάσουν ρυθμιστικό διάλυμα με ορισμένη τιμή pη.
ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
 Επιμέλεια: Νίκος Δάκος ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έω ς και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
Επιμέλεια: Νίκος Δάκος ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έω ς και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2014 ΧHMEIA. 7 Δεκεμβρίου 2013 ΛΥΚΕΙΟ :... ΟΜΑΔΑ ΜΑΘΗΤΩΝ: ΜΟΝΑΔΕΣ:
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2014 ΧHMEIA 7 Δεκεμβρίου 2013 ΛΥΚΕΙΟ :.... ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1.. 2.. 3.. ΜΟΝΑΔΕΣ: 1 η δραστηριότητα Οι σκόνες μιλούνε. Στη δραστηριότητα αυτή θα ταυτοποιήσετε καθεμία από τις πέντε
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2014 ΧHMEIA 7 Δεκεμβρίου 2013 ΛΥΚΕΙΟ :.... ΟΜΑΔΑ ΜΑΘΗΤΩΝ: 1.. 2.. 3.. ΜΟΝΑΔΕΣ: 1 η δραστηριότητα Οι σκόνες μιλούνε. Στη δραστηριότητα αυτή θα ταυτοποιήσετε καθεμία από τις πέντε
3.5 Αντιδράσεις οξειδοαναγωγής
 3.5 Αντιδράσεις οξειδοαναγωγής Αντίδραση σιδήρου με Cu 2+ (aq) Αριστερά: Ένα σιδερένιο καρφί και ένα διάλυμα θειικού χαλκού(ιι), το οποίο έχει χρώμα μπλε. Κέντρο: Ο Fe αντιδρά με Cu 2+ (aq) παρέχοντας
3.5 Αντιδράσεις οξειδοαναγωγής Αντίδραση σιδήρου με Cu 2+ (aq) Αριστερά: Ένα σιδερένιο καρφί και ένα διάλυμα θειικού χαλκού(ιι), το οποίο έχει χρώμα μπλε. Κέντρο: Ο Fe αντιδρά με Cu 2+ (aq) παρέχοντας
ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ SiM ¾
 33 Πείραμα 2 Πείραμα 12 ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ SiM ¾. ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι αποτέλεσμα
33 Πείραμα 2 Πείραμα 12 ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ SiM ¾. ΣΤΟΧΟΙ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι αποτέλεσμα
ΤΙΤΛΟΔΟΤΗΣΗ ΔΙΑΛΥΜΑΤΟΣ FeSO 4 ΜΕ ΠΡΟΤΥΠΟ ΔΙΑΛΥΜΑ KMnO 4 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΚΑΘΑΡΟΤΗΤΑΣ ΔΕΙΓΜΑΤΟΣ
 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ για το EUSO 2017 ΕΚΦΕ ΘΗΡΑΣ ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΤΙΤΛΟΔΟΤΗΣΗ ΔΙΑΛΥΜΑΤΟΣ FeSO 4 ΜΕ ΠΡΟΤΥΠΟ ΔΙΑΛΥΜΑ KMnO 4 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΚΑΘΑΡΟΤΗΤΑΣ ΔΕΙΓΜΑΤΟΣ ΕΙΣΑΓΩΓΗ
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ για το EUSO 2017 ΕΚΦΕ ΘΗΡΑΣ ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ - ΧΗΜΕΙΑ Μαθητές: Σχολείο 1. 2. 3. ΤΙΤΛΟΔΟΤΗΣΗ ΔΙΑΛΥΜΑΤΟΣ FeSO 4 ΜΕ ΠΡΟΤΥΠΟ ΔΙΑΛΥΜΑ KMnO 4 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΚΑΘΑΡΟΤΗΤΑΣ ΔΕΙΓΜΑΤΟΣ ΕΙΣΑΓΩΓΗ
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 3 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Γ ΛΥΚΕΙΟΥ Υπολογισμός της περιεκτικότητας του ξιδιού σε οξικό οξύ με την κλασική μέθοδο. ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ Γ θετ ΗΜΕΡΟΜΗΝΙΑ
