ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΜΕΑΣ ΥΓΕΙΑΣ ΠΑΙ ΙΟΥ ΝΕΟΓΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ Γ.Ν
|
|
|
- Κασσάνδρα Γαλάνη
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΜΕΑΣ ΥΓΕΙΑΣ ΠΑΙ ΙΟΥ ΝΕΟΓΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ Γ.Ν. ΠΑΠΑΓΕΩΡΓΙΟΥ ΙΕΥΘΥΝΤΗΣ: ΚΑΘΗΓΗΤΗΣ ΝΙΚΟΛΑΟΣ ΝΙΚΟΛΑΪ ΗΣ ΠΑΝΕΠΙΣΤΗΜΙΑΚΟ ΕΤΟΣ Αρ. ιατριβής 2780 «ΜΕΛΕΤΗ ΤΩΝ ΚΥΤΤΑΡΟΠΛΑΣΜΑΤΙΚΩΝ ΜΕΤΑΤΡΟΠΕΩΝ ΣΗΜΑΤΟΣ ΚΑΙ ΜΕΤΑΓΡΑΦΙΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΗ ΝΕΟΓΝΙΚΗ ΛΟΙΜΩΞΗ» ΜΑΡΙΑ ΛΙΘΟΞΟΠΟΥΛΟΥ ΠΑΙ ΙΑΤΡΟΣ - ΕΠΙΜΕΛΗΤΡΙΑ ΝΕΟΓΝΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΑΠΘ Γ.Ν. ΠΑΠΑΓΕΩΡΓΙΟΥ Ι ΑΚΤΟΡΙΚΗ ΙΑΤΡΙΒΗ ΥΠΟΒΛΗΘΗΚΕ ΣΤΗΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΥ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΘΕΣΣΑΛΟΝΙΚΗ 2012
2
3 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΜΕΑΣ ΥΓΕΙΑΣ ΠΑΙ ΙΟΥ ΝΕΟΓΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ Γ.Ν. ΠΑΠΑΓΕΩΡΓΙΟΥ ΙΕΥΘΥΝΤΗΣ: ΚΑΘΗΓΗΤΗΣ ΝΙΚΟΛΑΟΣ ΝΙΚΟΛΑΪ ΗΣ ΠΑΝΕΠΙΣΤΗΜΙΑΚΟ ΕΤΟΣ Αρ. ιατριβής 2780 «ΜΕΛΕΤΗ ΤΩΝ ΚΥΤΤΑΡΟΠΛΑΣΜΑΤΙΚΩΝ ΜΕΤΑΤΡΟΠΕΩΝ ΣΗΜΑΤΟΣ ΚΑΙ ΜΕΤΑΓΡΑΦΙΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΗ ΝΕΟΓΝΙΚΗ ΛΟΙΜΩΞΗ» ΜΑΡΙΑ ΛΙΘΟΞΟΠΟΥΛΟΥ ΠΑΙ ΙΑΤΡΟΣ - ΕΠΙΜΕΛΗΤΡΙΑ ΝΕΟΓΝΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΑΠΘ Γ.Ν. ΠΑΠΑΓΕΩΡΓΙΟΥ Ι ΑΚΤΟΡΙΚΗ ΙΑΤΡΙΒΗ ΥΠΟΒΛΗΘΗΚΕ ΣΤΗΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΥ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΘΕΣΣΑΛΟΝΙΚΗ
4 Η ΤΡΙΜΕΛΗΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗ ΕΠΙΤΡΟΠΗ ΝΙΚΟΛΑΪ ΗΣ ΝΙΚΟΛΑΟΣ, ΚΑΘΗΓΗΤΗΣ-ΕΠΙΒΛΕΠΩΝ ΧΑΤΖΗΣΤΥΛΙΑΝΟΥ ΜΑΡΙΑ, ΚΑΘΗΓΗΤΡΙΑ ΣΑΜΑΡΑΣ ΚΩΝΣΤΑΝΤΙΝΟΣ, ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ Η ΕΠΤΑΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ ΝΙΚΟΛΑΪ ΗΣ ΝΙΚΟΛΑΟΣ, ΚΑΘΗΓΗΤΗΣ ΧΑΤΖΗΣΤΥΛΙΑΝΟΥ ΜΑΡΙΑ, ΚΑΘΗΓΗΤΡΙΑ ΣΑΜΑΡΑΣ ΚΩΝΣΤΑΝΤΙΝΟΣ, ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΚΥΡΙΑΖΗΣ ΓΕΩΡΓΙΟΣ, ΚΑΘΗΓΗΤΗΣ ΑΝΙΗΛΙ ΗΣ ΜΙΧΑΗΛ, ΚΑΘΗΓΗΤΗΣ ΛΑΜΠΡΟΠΟΥΛΟΣ ΑΛΕΞΑΝ ΡΟΣ, ΑΝΑΠΛΗΡΩΤΗΣ ΚΑΘΗΓΗΤΗΣ ΤΣΑΚΑΛΙ ΗΣ ΧΡΗΣΤΟΣ, ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ «Η έγκριση της διδακτορικής διατριβής από την Ιατρική Σχολή του Αριστοτελείου Πανεπιστηµίου Θεσσαλονίκης δεν υποδηλώνει αποδοχή των γνωµών του συγγραφέα». (Νόµος 5343/32,άρθρ και ν. 1268/82,άρθρ
5 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΡΟΕ ΡΟΣ ΤΗΣ ΣΧΟΛΗΣ ΒΑΣΙΛΕΙΟΣ ΤΑΡΛΑΤΖΗΣ ΚΑΘΗΓΗΤΗΣ ΜΑΙΕΥΤΙΚΗΣ ΓΥΝΑΙΚΟΛΟΓΙΑΣ ΚΑΙ ΑΝΘΡΩΠΙΝΗΣ ΑΝΑΠΑΡΑΓΩΓΗΣ 5
6
7 Στο σύζυγό µου Θωµά Πατσανά και στα παιδιά µου ηµήτρη και Στυλιανό Στους γονείς µου 7
8 ΠΕΡΙΕΧΟΜΕΝΑ ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ 11 ΠΡΟΛΟΓΟΣ 13 ΓΕΝΙΚΟ ΜΕΡΟΣ 17 1o ΚΕΦΑΛΑΙΟ: ΝΕΟΓΝΙΚΗ ΛΟΙΜΩΞΗ Ορισµός Συχνότητα Τρόποι µετάδοσης των λοιµώξεων Προδιαθεσικοί παράγοντες ή παράγοντες κινδύνου Νεογνική σηψαιµία Παθογένεια Κλινική εικόνα ιάγνωση 27 Εργαστηριακή διάγνωση νεογνικής σηψαιµίας- πρώιµοι διαγνωστικοί δείκτες λοίµωξης 27 8
9 1.8. Θεραπεία 2o ΚΕΦΑΛΑΙΟ: ΑΜΥΝΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΟΥ ΝΕΟΓΝΟΥ 2.1. ΜΗ ΕΙ ΙΚΗ Ή ΦΥΣΙΚΗ ΑΝΟΣΙΑ Επιφανειακοί επιθηλιακοί φραγµοί Επιφανειακοί επιθηλιακοί φραγµοί στα νεογνά Το σύστηµα του συµπληρώµατος Το συµπλήρωµα στα νεογνά Το σύστηµα φαγοκυττάρωσης (πολυµορφοπύρηνα - µονοπύρηνα) 52 Α. Τα ουδετερόφιλα στην εµβρυϊκή και νεογνική περίοδο 52 Β. Τα µονοκύτταρα στα νεογνά Μόρια προσκόλλησης ΝΚ κύτταρα Κυτταροκίνες 61 Οι κυτταροκίνες στη νεογνική λοίµωξη-σηψαιµία Αισθητηριακά συστήµατα STATs (Κυτταροπλασµατικοί µετατροπείς σήµατος και µεταγραφικοί παράγοντες) ΕΙ ΙΚΗ ΑΝΟΣΙΑ Κυτταρική ανοσία Τ λεµφοκύτταρα στα νεογνά Χυµική ανοσία Β λεµφοκύτταρα στα νεογνά 68 3o ΚΕΦΑΛΑΙΟ: STATs Γενικά 71 9
10 3.2. Ο ρόλος των STATs στη σηψαιµία Ο ρόλος των STATs στη φλεγµονή και στα φλεγµονώδη νοσήµατα STAT1 και STAT STAT STAT 4 και STAT STAT o ΚΕΦΑΛΑΙΟ: ΚΥΤΤΑΡΟΜΕΤΡΙΑ ΡΟΗΣ 85 ΕΙ ΙΚΟ ΜΕΡΟΣ 89 ΑΣΘΕΝΕΙΣ ΜΕΘΟ ΟΙ 91 ΣΤΑΤΙΣΤΙΚΗ ΑΝΑΛΥΣΗ 95 ΑΠΟΤΕΛΕΣΜΑΤΑ 97 ΣΥΖΗΤΗΣΗ 169 ΠΕΡΙΛΗΨΗ 189 SUMMARY 193 ΒΙΒΛΙΟΓΡΑΦΙΑ 197 ΕΙΚΟΝΕΣ
11 ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ IUGR ενδοµήτρια καθυστέρηση ανάπτυξης GBS Group B Streptococcus ΠΡΕΥ παρατεταµένη ρήξη των υµένων HSV Herpes Simplex Virus CMV Cytomegalovirus HBV Hepatitis B Virus ΝΕΚ Νεκρωτική Εντεροκολίτιδα VLBW πολύ χαµηλού βάρους γέννησης ΣΑ Σύνδροµο αναπνευστικής δυσχέρειας Κ ιάρκεια κύησης HK ηλικία κύησης ΒΓ Βάρος Γέννησης ΝΟ µονοξείδιο του αζώτου CRP C-reactive protein PCT προκαλσιτονίνη IL-1,6,8, ιντερλευκίνη 1,6,8 LPS λιποπολυσακχαρίδη TNF-a Tumor necrosis Factor α RANTES regulated upon activation normal Τcell expressed and secreted ΝΚ natural killer -κύτταρα φυσικοί φονείς CD64 αντιγόνο επιφανείας 64 CONS coagulase negative staphylococcus -αρνητικό στην πηκτάση σταφυλόκοκκο IVIG ενδοφλέβιας γ-σφαιρίνης RCTs τυχαιοποιηµένες ελεγχόµενες µελέτες G-CSF παράγοντας διέγερσης σχηµατισµού αποικιών των κοκκιοκυττάρων APC activated protein C-ενεργοποιηµένης πρωτεΐνης C LTB4 λευκοτριένη Β4 FcγR υποδοχέας του Fc τµήµατος των IgG ΙCAM-1 Intracellular adhesion molecule (ενδοκυττάριο µόριο προσκόλλησης) IFN-γ Ιντερφερόνη-γ TLR Toll like Receptors ΙΤΑΜ τυροσινικοί ανοσο-υποδοχείς STAT signal transducer and activator of transcription SOCS suppressor of cytokine signaling Th Τ λεµφοκύτταρα βοηθητικά TcLs επαγωγικά κυτταροτοξικά 11
12 TsLs κατασταλτικά ΚΡ κυτταροµετρία ροής ISGF interferon stimulated gene factor ISRE interferon stimulated response element 12
13 ΠΡΟΛΟΓΟΣ Η συχνότητα της νεογνικής λοίµωξης-σηψαιµίας αυξάνεται ευθέως ανάλογα προς το ποσοστό της επιβίωσης πιο ανώριµων νεογνών και τους προδιαθεσικούς παράγοντες εκδήλωσης λοίµωξης-σηψαιµίας κατά την περιγεννητική περίοδο.(1) Η διάγνωση των λοιµώξεων, όµως, κυρίως των πρόωρων αλλά και των τελειόµηνων νεογνών, είναι δύσκολη εξαιτίας της άτυπης κλινικής εικόνας και της έλλειψης εξειδικευµένων εργαστηριακών εξετάσεων για την ταυτοποίηση της λοίµωξης.(2) Είναι γνωστό βέβαια ότι η έγκαιρη διάγνωση και έγκαιρη θεραπευτική αντιµετώπιση των νεογνικών λοιµώξεων µειώνει τη θνησιµότητα, η οποία παραµένει ακόµη αυξηµένη.(3) Η µεγάλη συχνότητα των λοιµώξεων σε αυτή την ηλικία καθώς και η δυσκολία κλινικής και εργαστηριακής διάγνωσης έστρεψε τους ερευνητές στην αναζήτηση κλινικών σηµείων και εργαστηριακών δεικτών. Οι δείκτες αυτοί θα πρέπει να πληρούν ορισµένα βασικά χαρακτηριστικά, όπως µεγάλη ευαισθησία, ειδικότητα και επαναληψιµότητα, εύκολο προσδιορισµό, να µη χρειάζονται ιδιαίτερο εργαστηριακό εξοπλισµό και να είναι χαµηλού κόστους. Με αυτό το στόχο σχεδιάστηκε η παρούσα µελέτη. Οι προδιαθεσικοί παράγοντες εκδήλωσης λοίµωξης κατά την περιγεννητική περίοδο είναι αρκετοί. Σε αυτούς συγκαταλέγονται η προγεννητική χορήγηση στεροειδών στην µητέρα, η χοριοαµνιονίτιδα της µητέρας, η ΡΕΥ, ο τρόπος τοκετού, το Apgar score, ο µηχανικός αερισµός και οι χειρισµοί κατά τη νοσηλεία. (4-6) Η στατιστική ανάλυση των παραπάνω προδιαθεσικών παραγόντων για την ανεύρεση του σχετικού κινδύνου (Relative Risk) εκδήλωσης λοίµωξης-σηψαιµίας υποδεικνύει ότι ένας παράγοντας ή συνδυασµός περισσοτέρων δε µεταβάλλει σηµαντικά το σχετικό κίνδυνο λοίµωξης. Για παράδειγµα, οι κεντρικοί καθετήρες ή ο µηχανικός αερισµός µόνοι τους ή σε συνδυασµό µε άλλους προδιαθεσικούς παράγοντες έχουν τον ίδιο σχεδόν σχετικό κίνδυνο Μια πιθανή ερµηνεία αυτού είναι η αυτοαναίρεση του ενός από τον άλλο παράγοντα κινδύνου. Όταν, λοιπόν, συνυπάρχουν περισσότεροι από τρεις παράγοντες δεν αυξάνεται η πληροφορία, διότι υπάρχει «η υπερπληροφόρηση» µε το συνδυασµό πολλών παραγόντων συγχρόνως. Πρόωρα νεογνά υψηλού κινδύνου για την εκδήλωση λοίµωξης- σηψαιµίας είναι τα πολύ ανώριµα νεογνά, τα νεογνά µε ΣΑ, µε ενδοµήτρια δυστροφία, άπνοια, ανοικτό αρτηριακό πόρο, περιγεννητική ασφυξία, εγκεφαλική αιµορραγία, σύνδροµα διαφυγής αέρα και πνευµονική υπέρταση.(7,8) Οι παθολογικές καταστάσεις που ευνοούν την εκδήλωση λοίµωξης σηψαιµίας στα τελειόµηνα νεογνά είναι η άπνοια, η περιγεννητική ασφυξία, η παροδική ταχύπνοια, τα σύνδροµα διαφυγής και η παραµένουσα πνευµονική υπέρταση. Οι αιµατολογικοί και βιοχηµικοί δείκτες που χρησιµοποιήσαµε για τη διάγνωση της σηψαιµίας ήταν η λευκοπενία, η ουδετεροπενία, η θροµβοπενία, η µεταβολική και γαλακτική οξέωση και οι διαταραχές της οµοιόστασης της γλυκόζης. Οι δείκτες αυτοί µεµονωµένοι 13
14 παρουσιάζουν µικρή ευαισθησία και ειδικότητα για τη διάγνωση της µικροβιακής σηψαιµίας. Ο συνδυασµός των περισσότερων δεικτών, αριθµός λευκών, σχέση αώρων προς ολικά ουδετερόφιλα, CRP, PCT) αυξάνει τη διαγνωστική αξία.(2, 9-11) Οι µέχρι τώρα γνωστοί δείκτες λοίµωξης, όπως ο αριθµός των λευκών, η CRP και η PCT δεν έχουν την ίδια ευαισθησία και ειδικότητα στα νεογνά, ιδιαίτερα τις πρώτες ηµέρες της ζωής τους, όπως στους ενήλικες. Οι πρωτεΐνες STAT είναι µεταγραφικοί παράγοντες, οι οποίοι συνδέονται σε φωσφορυλιωµένες τυροσίνες στην κυτταροπλασµατική πλευρά του υποδοχέα gp130 και διµερίζονται µετά από φωσφορυλίωση σε τυροσινικά υπολείµµατα από τις Jak κινάσες. Μετά από το διµερισµό, οι STATs µεταφέρονται στον πυρήνα, όπου και ενεργοποιούν γονίδιαστόχους. Οι STATs πρωτεΐνες συµµετέχουν τόσο στην ειδική όσο και στη µη ειδική ανοσία έναντι λοιµογόνων και άλλων παραγόντων µέσω της παραγωγής των αντίστοιχων κυτταροκινών.(12) Η παρούσα µελέτη υποδεικνύει ότι οι STATs διαδραµατίζουν σηµαντικό ρόλο σε συνδυασµένα µηνύµατα ενεργοποίησης, που προέρχονται από µικροβιακά προϊόντα έτσι, τα επίπεδα της ενδοκυττάριας έκφρασης των STATs στα πολυµορφοπύρηνα στα µονοκύτταρα των πρόωρων και τελειοµήνων νεογνών µε λοίµωξη. Σκοπός της εργασίας ήταν η µελέτη της έκφρασης των STAT πρωτεϊνών σε κυτταρικούς πληθυσµούς κατά την νεογνική λοίµωξη και ο προσδιορισµός ποιας από αυτές αποτελεί πρώιµο εργαστηριακό δείκτη για την ανίχνευση της νεογνικής σηψαιµίας. Η µελέτη χωρίστηκε στα εξής µέρη: 1. Πρόλογος 2. Γενικό µέρος. Περιλαµβάνει 4 κεφάλαια. Στο πρώτο, γίνεται ανασκόπηση των νεότερων δεδοµένων για τους τρόπους µετάδοσης των λοιµώξεων, τους προδιαθεσικούς παράγοντες, την παθογένεια της νεογνικής σηψαιµίας, τους εργαστηριακούς διαγνωστικούς δείκτες για την νεογνική σηψαιµία. Στο δεύτερο κεφάλαιο γίνεται αναφορά στους αµυντικούς µηχανισµούς του νεογνού, της µη ειδικής και ειδικής ανοσίας. Στο τρίτο κεφάλαιο γίνεται ανασκόπηση των νεότερων δεδοµένων για τους κυτταροπλασµατικούς µετατροπείς σήµατος και τους µεταγραφικούς παράγοντες και το ρόλο τους στη λοίµωξη. Στο τέταρτο κεφάλαιο γίνεται αναφορά στη µέθοδο της κυτταροµετρίας ροής που εφαρµόστηκε. 3. Ασθενείς και µέθοδοι. Περιγράφονται οι οµάδες των νεογνών που µελετήθηκαν, η κλινική και εργαστηριακή παρακολούθηση καθώς και οι µέθοδοι των εργαστηριακών παραµέτρων. Επίσης περιγράφονται οι µέθοδοι που χρησιµοποιήθηκαν για τη στατιστική ανάλυση των αποτελεσµάτων. 4. Αποτελέσµατα. Αναλύονται τα ευρήµατα της µελέτης και εκτίθενται σε πίνακες και γραφήµατα. 14
15 5. Συζήτηση. Σχολιάζονται τα αποτελέσµατα και συσχετίζονται µε τα βιβλιογραφικά δεδοµένα 6. Περίληψη και συµπεράσµατα στην Ελληνική και Αγγλική γλώσσα 7. Βιβλιογραφία Η εργασία αυτή εκπονήθηκε στη Β Πανεπιστηµιακή Νεογνολογική Κλινική του Α.Π.Θ. Γ. Ν. Παπαγεωργίου. Η κυτταροµετρία ροής έγινε στο Ανοσολογικό Εργαστήριο της Β Παιδιατρικής Κλινικής του Α.Π.Θ. Νοσοκοµείου ΑΧΕΠΑ. Από τη θέση αυτή θα ήθελα να ευχαριστήσω θερµά τον Καθηγητή Νεογνολογίας και ιευθυντή της Β Πανεπιστηµιακής Νεογνολογικής Κλινικής κ. Νικόλαο Νικολαΐδη, πρώτο επιβλέποντα της τριµελούς συµβουλευτικής επιτροπής για τη βοήθεια, το συνεχές ενδιαφέρον και την ηθική υποστήριξη που µου έδειξε όλο αυτό το χρονικό διάστηµα. Επιθυµώ να τον ευχαριστήσω θερµά γιατί είναι αυτός που δόµησε τις προϋποθέσεις για την εκπόνηση της διατριβής και υπήρξε ο στενότερος καθοδηγητής. Επιπλέον τον ευχαριστώ για τις διορθώσεις, τις υποδείξεις, την κριτική και την καθοριστική καθοδήγηση, δίχως τις οποίες θα ήταν αδύνατη η συγγραφή. Παράλληλα, αισθάνοµαι την ανάγκη να ευχαριστήσω ιδιαίτερα την κ. Μαρία Χατζηστυλιανού, Καθηγήτρια Παιδιατρικής- Ανοσολογίας, υπεύθυνη του Εργαστηρίου Κλινικής Ανοσολογίας της Β Παιδιατρικής Κλινικής, δεύτερο µέλος της τριµελούς συµβουλευτικής επιτροπής, για το ενδιαφέρον και τη βοήθεια που µου προσέφερε κατά το χρονικό διάστηµα της µελέτης. Η συνεχής επίβλεψή της, η συνεργασία µαζί της και η επιστηµονική της καθοδήγηση ήταν σηµαντικές για την οργάνωση της µελέτης καθώς και οι εποικοδοµητικές υποδείξεις της κατά τη διάρκεια της συγγραφής της διατριβής. Ήταν, επίσης, ουσιαστική και πολύτιµη η βοήθειά της στην πειραµατική διαδικασία της µελέτης και στην αξιολόγηση των αποτελεσµάτων. Ευχαριστώ, επίσης, τον κ. Κωνσταντίνο Σαµαρά, Επίκουρο Καθηγητή Παιδιατρικής, τρίτο µέλος της τριµελούς συµβουλευτικής επιτροπής για την επιστηµονική βοήθεια και συµπαράσταση που µου προσέφερε στη διάρκεια της µελέτης. Οφείλω επίσης να ευχαριστήσω τα µέλη της επταµελούς εξεταστικής επιτροπής τον κ. Γεώργιο Κυριαζή, Καθηγητή Βιοπαθολογίας του Α.Π.Θ., τον κ. Μιχαήλ ανιηλίδη Καθηγητή Παθολογίας- Ανοσολογίας του Α.Π.Θ., τον κ. Αλέξανδρο Λαµπρόπουλο, Αναπληρωτή Καθηγητή Γενετικής του Α.Π.Θ., και τον κ. Χρήστο Τσακαλίδη, Επίκουρο Καθηγητή Νεογνολογίας του Α.Π.Θ. Εκφράζω ιδιαίτερες ευχαριστίες για τις εποικοδοµητικές υποδείξεις τους, για τις εύστοχες παρατηρήσεις και τις ουσιαστικές διορθώσεις τους. Θερµά ευχαριστώ την κ. Χριστίνα Αναγνωστοπούλου Επίκουρη Καθηγήτρια στον Τοµέα Μετεωρολογίας και Κλιµατολογίας του Α.Π.Θ. για τις πολύτιµες συµβουλές της στη στατιστική επεξεργασία των αποτελεσµάτων. 15
16 Οφείλω να ευχαριστήσω ιδιαίτερα τους βιολόγους κ. Στυλιανή Παππά και κ. ηµήτριο Μπουγιουκλή για τη βοήθεια που ακούραστα µου προσέφεραν στο εργαστηριακό µέρος της µελέτης. Τέλος, οφείλω να ευχαριστήσω την κ. Ελένη Γιαννατσούλια, φιλόλογο, για την πολύτιµη βοήθειά της στη συγγραφή της διατριβής. Επίσης, ευχαριστώ τους γιατρούς και το νοσηλευτικό προσωπικό της Β Νεογνολογικής Πανεπιστηµιακής Κλινικής για την κατανόηση και συµπαράσταση που µου έδειξαν. 16
17 1ο ΚΕΦΑΛΑΙΟ ΝΕΟΓΝΙΚΗ ΛΟΙΜΩΞΗ Η συχνότητα των µικροβιακών λοιµώξεων είναι πολύ υψηλή στη νεογνική ηλικία, καθώς κυµαίνεται από 1 µέχρι 5/1000 γεννήσεις ζώντων νεογνών, ενώ είναι ακόµη µεγαλύτερη στα πρόωρα και ανέρχεται σε 1 /250 γεννήσεις.(13,14) Η νεογνική λοίµωξη εκδηλώνεται µε διάφορες µορφές, όπως: α. επιφανειακή λοίµωξη δέρµατος και βλεννογόνων, β. νεογνική σηψαιµία, γ. εστιακές εντοπίσεις σε διάφορα όργανα (πνεύµονες, κεντρικό νευρικό σύστηµα, γαστρεντερικό σύστηµα, οστά-αρθρώσεις κ.ά.) και δ. λοιµώξεις που µεταδίδονται περιγεννητικά και µπορούν να εκδηλωθούν µήνες ή και χρόνια µετά τη γέννηση (ηπατίτιδες Β, C, µεγαλοκυτταροϊός).(15-17) Οι λοιµώξεις αποτελούν σηµαντική αιτία νεογνικής νοσηρότητας, θνητότητας και θνησιµότητας, ιδιαίτερα στα πρόωρα νεογνά. Η θνητότητα κυµαίνεται από 5% µέχρι 10% και έχει αυξηθεί πλασµατικά τα τελευταία χρόνια, καθώς επιζούν όλο και µικρότερου βάρους αλλά και πιο ανώριµα νεογνά, τα οποία νοσηλεύονται σε εντατικές µονάδες νεογνών.(14) Ακόµη υψηλότερη καταγράφεται η θνητότητα λόγω σηψαιµίας, που ανέρχεται στο 15-20% ιδιαίτερα στα πρόωρα νεογνά, παρά τις ραγδαίες εξελίξεις στην εντατική νοσηλεία νεογνών και τη χρήση νέων ισχυρών αντιµικροβιακών φαρµάκων και βιολογικών παραγόντων. (15,18,19) Τις τελευταίες δεκαετίες δεν έχει παρατηρηθεί µείωση της συχνότητας της θνητότητας γεγονός που οφείλεται στο ότι όλο και περισσότερα νεογνά εξαιρετικά χαµηλού βάρους νοσηλεύονται και επιβιώνουν Τρόποι µετάδοσης λοιµώξεων Το έµβρυο, κατά την ενδοµήτρια ζωή του, είναι αρκετά προστατευµένο από τη µικροβιακή χλωρίδα του γεννητικού συστήµατος της µητέρας. Προστατεύεται µε τις χοριακές µεµβράνες, τον πλακούντα και τους αντιµικροβιακούς παράγοντες του αµνιακού υγρού. Παρά τη σχετική προστασία, όµως, πολλοί είναι οι τρόποι προσβολής του από λοιµογόνους παράγοντες, µε τελικό αποτέλεσµα την εκδήλωση λοίµωξης. Οι µικροοργανισµοί του κόλπου προκαλούν φλεγµονή των εµβρυϊκών µεµβρανών, του οµφαλίου λώρου και του πλακούντα, γι αυτό και 1-4% των εµβρύων αυτών σε περίπτωση τοκετού αναπτύσσουν συστηµατική λοίµωξη.(20,21) Οι µικροοργανισµοί που αποµονώνονται από το µολυσµένο αµνιακό υγρό είναι αναερόβια µικρόβια, GBS, E. Coli, mycoplasma hominis και ureoplasma urealiticum.(22,23) Η µετάδοση των λοιµωδών παραγόντων γίνεται διαµνιακά, κυρίως όταν υπάρχει ρήξη των χοριακών µεµβρανών πέραν του 24/ώρου, µε εισρόφηση µολυσµένου αµνιακού υγρού από το έµβρυο ή το νεογνό κατά τον τοκετό, γεγονός που µπορεί να οδηγήσει στον πρόωρο τοκετό ή τον ενδοµήτριο θάνατο ή τη γέννηση νεογνού µε σήψη. Στις πιο πολλές περιπτώσεις το νεογνό αποικίζεται µε τη 17
18 χλωρίδα του γεννητικού σωλήνα, µε τη δίοδο µέσω αυτού, κατά τη διαδικασία του τοκετού. ιαπλακουντιακά µεταδίδονται κυρίως οι συγγενείς λοιµώξεις. Επίσης, οι µαιευτικές επιπλοκές κατά τον τοκετό αυξάνουν τον κίνδυνο περιγεννητικών λοιµώξεων.(24) Τέτοιες είναι ο πρόωρος τοκετός, η παρατεταµένη ρήξη των υµένων (ΠΡΕΥ), η υψηλή εµβρυουλκία και η χοριοαµνιονίτιδα της µητέρας. Τέλος, µαιευτικές µέθοδοι όπως η αµνιοπαρακέντηση, η περίδεση του τραχήλου της µήτρας, η διατραχηλική λήψη εµβρυϊκών λαχνών και η παρακέντηση του οµφαλίου λώρου για λήψη αίµατος, διευκολύνουν τη δίοδο µικροβίων από το δέρµα και ευνοούν την ανάπτυξη χοριοαµνιονίτιδας και λοίµωξης του εµβρύου. Η νεογνική λοίµωξη διακρίνεται σε πρώιµη και όψιµη. Η πρώιµη νεογνική λοίµωξη µεταδίδεται κυρίως µέσω του αµνιακού υγρού µε κάθετη µετάδοση και µέσω της αποικισµένης γεννητικής οδού. Η όψιµη νεογνική λοίµωξη διακρίνεται σε αυτή που µεταδίδεται κάθετα περιγεννητικά, αλλά και οριζόντια από το περιβάλλον όπου διαβιοί το νεογνό. Η οριζόντια µετάδοση της λοίµωξης συντελείται είτε δια µέσου των χεριών του προσωπικού που εργάζεται σε τµήµατα νοσηλείας νεογνών είτε λόγω των επεµβατικών υποστηρικτικών τεχνικών, όπως είναι η χρήση οργάνων, τραχειοσωλήνων, στοµατογαστρικών καθετήρων σίτισης, οµφαλικών καθετήρων, ουροκαθετήρων, ενδοφλέβιων καθετήρων, παροχετεύσεων, υπερθερµιδικών εγχύσεων και υποστηρικτικού µηχανικού αερισµού.(25) Η νεογνική λοίµωξη έχει ορισµένα χαρακτηριστικά ανάλογα µε το χρόνο εµφάνισης. Ο παρακάτω πίνακας δίνει µε συντοµία στοιχεία για τις τρεις περιόδους των νεογνικών λοιµώξεων. Πίνακας 1.1. Χαρακτηριστικά της νεογνικής λοίµωξης ανάλογα µε το χρόνο εµφάνισής της. Πρώιµη (<7 ηµέρες) Όψιµη ( 7 µέρες έως 3 µήνες) Πολύ όψιµη (>3 µήνες) Μαιευτικές επιπλοκές Συχνά παρούσες Συνήθως απούσες Ποικίλλουν Μετάδοση Κάθετη. Από το γεννητικό Συνήθως από το Κάθετη ή από το περιβάλλον σύστηµα της µητέρας περιβάλλον Κλινικές Κεραυνοβόλος έναρξη, Λανθάνουσα ή οξεία, εστιακή εκδηλώσεις συµµετέχουν οι πνεύµονες λοίµωξη, συχνά µηνιγγίτιδα Λανθάνουσα Θνητότητα 5%-20% 5% Χαµηλή Hyde et al, (τροποποιηµένο) 18
19 1.3. Προδιαθεσικοί παράγοντες κινδύνου ιάφοροι περιγεννητικοί παράγοντες συνδέονται µε αυξηµένο κίνδυνο σηψαιµίας κατά τη νεογνική περίοδο. Από αυτούς, άλλοι συνδέονται µε περιγεννητικές λοιµώξεις (χοριοαµνιονίτιδα, ουρολοίµωξη µητέρας) και άλλοι µε επίκτητες ενδονοσοκοµειακές λοιµώξεις (προωρότητα, χαµηλό βάρος γέννησης, θεραπευτικοί χειρισµοί στην εντατική µονάδα νοσηλείας). Προδιαθεσικοί παράγοντες για την εµφάνιση νεογνικών λοιµώξεων είναι: Από τη µητέρα: Η ουρολοίµωξη, ο αποικισµός του κόλπου από µικρόβια [Group Β Streptococcus (GBS), mycopasma hominis, χλαµύδια, µύκητες (επίπτωση 6,3%) (26)] οι ιογενείς λοιµώξεις και ο πυρετός της µητέρας κατά την περιγεννητική περίοδο ως κύριο κλινικό εύρηµα στη χοριοαµνιονίτιδα µε ευαισθησία %.(21,27) Η συνύπαρξη κάποιων παραγόντων, όπως η παρατεταµένη ρήξη θυλακίου, µε πυρετό και προωρότητα, πολλαπλασιάζουν τον κίνδυνο εµφάνισης της λοίµωξης. Η ασυµπτωµατική βακτηριουρία συσχετίζεται µε πρόωρο τοκετό και ο αποικισµός του κόλπου µε µυκόπλασµα συνδέεται µε χαµηλού βάρους γέννησης νεογνά.(20) Το χαµηλό κοινωνικό-οικονοµικό επίπεδο της οικογένειας, η κακή υγιεινή και διατροφή της µητέρας, η µητέρα από τη µαύρη φυλή και η µητέρα µε νόσηµα σεξουαλικώς µεταδιδόµενο είναι παράγοντες που αυξάνουν τη συχνότητα των λοιµώξεων.(28) Από το νεογνό: Η προωρότητα αυξάνει τον κίνδυνο περιγεννητικής λοίµωξης 4-11 φορές, όπως και το χαµηλό βάρος γέννησης, γι αυτό όσο µικρότερο είναι το νεογνό τόσο ελλοχεύει µεγαλύτερος κίνδυνος εκδήλωσης σηψαιµίας.(29) Για τη λοίµωξη µε GBS αναφέρονται ποσοστά 5.99/1000, 2.51/1000 και 0.89/1000 νεογνά µε βάρος γέννησης µικρότερο των 1500γρ., γρ. και πάνω από 2500 γρ. αντίστοιχα.(14,30) Σε άλλη µελέτη αναφέρεται ότι η συχνότητα πρώιµης λοίµωξης από GBS παραµένει σταθερή την τελευταία 20ετία και µικρότερη των 0,4/1000 περιπτώσεις ζώντων νεογνών.(31) Επίσης, πολλαπλασιασµός των µικροοργανισµών στο ανώτερο αναπνευστικό, ουροποιητικό ή στο γαστρεντερικό µπορεί να οδηγήσει σε µικροβιαιµία ή σηψαιµία, ενώ παράλληλα θα ενεργοποιήσει τους αµυντικούς µηχανισµούς. υστυχώς, το ανώριµο ανοσολογικό σύστηµα του πρόωρου νεογνού προδιαθέτει σε γενίκευση της λοίµωξης. Η φλεγµονώδης απάντηση εξαρτάται από την ηλικία κύησης, τη λοιµογόνο δράση του µικροβίου, τον αριθµό των παθογόνων µικροβίων στο αίµα, τη διατροφική και ανοσιακή κατάσταση του ξενιστή, το χρόνο και το είδος της θεραπευτικής παρέµβασης. Το άρρεν φύλο, ο τραυµατικός τοκετός (κεφαλαιµάτωµα), η υποξία του νεογνού και το χαµηλό Apgar (<6 στο 5 λεπτό) είναι άλλοι επιβαρυντικοί παράγοντες, που προδιαθέτουν σε λοίµωξη. (25,32) Στα πολύ χαµηλού βάρους πρόωρα νεογνά η όψιµη σηψαιµία συνδέεται µε παρατεταµένη µηχανική υποστήριξη, (33) λόγω βρογχοπνευµονικής δυσπλασίας ή συνδέεται µε ανοικτό αρτηριακό πόρο, σοβαρή ενδοκοιλιακή αιµορραγία και νεκρωτική εντεροκολίτιδα. (34,35) 19
20 Περιγεννητικό περιβάλλον: Η πρόωρη ρήξη των εµβρυϊκών υµένων για περισσότερο από 24 ώρες συνδυάζεται µε κίνδυνο εµφάνισης λοίµωξης 1%, η χοριοαµνιονίτιδα αυξάνει τη συχνότητα σε 3-5%, ενώ το εµπύρετο και η σηψαιµία της µητέρας αυξάνουν επιπλέον το σχετικό κίνδυνο. Ο κίνδυνος τετραπλασιάζεται, αν η ρήξη εµβρυϊκών υµένων επιπλακεί µε χοριαµνιονίτιδα (21). Η προωρότητα και το χαµηλό βάρος γέννησης, επειδή συνδέονται µε νοσηλεία σε εντατική µονάδα νεογνών, κατά συνέπεια αύξηση των παρεµβάσεων, αυξάνουν τον κίνδυνο περαιτέρω. Η αναλογία νοσηλευτριών-νεογνών, οι τραυµατικοί χειρισµοί, η ενδοτραχειακή διασωλήνωση, η τοποθέτηση ενδαγγειακών καθετήρων και η παρεντερική χορήγηση υγρών, είναι άλλοι συνήθεις παράγοντες που πρέπει να λαµβάνονται υπόψη για εκδήλωση λοίµωξης. (36,37) Άλλοι παράγοντες: Η σίτιση µε γάλα τροποποιηµένο αντί του µητρικού αποτελεί έναν επιπλέον κίνδυνο εµφάνισης λοιµώξεων, καθότι απουσιάζουν τα προστατευτικά συστατικά του µητρικού γάλακτος, όπως οι ανοσοσφαιρίνες, τα µακροφάγα και τα λεµφοκύτταρα, που παρέχουν γενική ή τοπική προστασία από λοιµώξεις. Οι πηγές παθογόνων µικροοργανισµών µπορεί να προέρχονται: α) από το γεννητικό σωλήνα: GΒS, E. coli, στρεπτόκοκκοι (Viridans, Group D, pneumoniococcus) σταφυλόκοκκος aureus, πρωτέας, λιστέρια µονοκυτογόνος, αιµόφιλος influenza, είδη εντεροκόκκου, µυκόπλασµα hominis, ουρεόπλασµα urealiticum και parvum, ιοί (ερυθράς, HSV, CMV, HBV), τοξόπλασµα, β) από το περιβάλλον και το προσωπικό των µονάδων εντατικής νεογνών: gram-αρνητικοί βάκιλοι, ψευδοµονάδα, κλεµπσιέλλα, enterobacter, serratia, πρωτέας, είδη στρεπτοκόκκου, σταφυλόκοκκοι (Coagulase-negative Staphylococcus, Αureus, Εpidermitis), εντερόκοκκος, είδη Candida, ιοί (Respiratory Syncytial Virus, coxsackie, echo, αδενοϊοί, ροταϊοί).(14,27) Στην Ελλάδα, αν και οι Gram αρνητικοί µικροοργανισµοί (Escherichia coli, κλεµπσιέλλα) αποτελούν τα συχνότερα µικρόβια της πρώιµης νεογνικής σηψαιµίας, εντούτοις παρατηρείται αύξηση στη συχνότητα αποµόνωσης του GBS. (38,39) 1.4. Νεογνική σηψαιµία Νεογνική σηψαιµία είναι κάθε συστηµατική λοίµωξη κατά τη διάρκεια του πρώτου µήνα ζωής που τεκµηριώνεται µε θετική καλλιέργεια αίµατος, (40,41) είναι συχνή τις πρώτες µέρες και αποτελεί σηµαντική απειλή για τη ζωή των νεογνών, ειδικά των προώρων. Στις βιοµηχανικές χώρες η επίπτωσή της στα τελειόµηνα νεογνά µε κανονικό βάρος γέννησης για την ηλικία κύησης είναι 0,1%, αυξάνεται στο 10% σε νεογνά µε βάρος γέννησης γρ., στο 35% σε νεογνά κάτω των 1000 γρ και στο 50% σε µικρότερα των 750 γρ. (42,43) Περισσότερα των 25% των νεογνών µε σηψαιµία αναπτύσσουν και µηνιγγίτιδα, γεγονός που επιδεινώνει την πρόγνωση και καθιστά δυσκολότερη τη θεραπεία. (25) Η νεογνική σηψαιµία αποτελεί ένα από τα σηµαντικότερα προβλήµατα της νεογνικής 20
21 περιόδου και σχετίζεται µε υψηλή νοσηρότητα και θνητότητα, ιδιαίτερα στα πρόωρα νεογνά. (14,18,19) Ανάλογα µε τη χρονική εµφάνιση των σηµείων και συµπτωµάτων της νόσου διακρίνεται σε πρώιµη νεογνική σηψαιµία, σε όψιµη και σε πολύ όψιµη. Η πρώιµη εµφανίζεται στις 72 πρώτες ώρες ζωής, (17,44) η όψιµη από τις 72 ώρες έως και την 90ή µέρα, η δε πολύ όψιµη µετά την 90ή µέρα ζωής. Η συνολική θνητότητα της πρώιµης είναι 15-40% (για την πρώιµη σηψαιµία από GBS είναι 2-30%) και της όψιµης 10-20% (για την όψιµη σηψαιµία από GBS είναι 2-6%). (4,45) Συχνότερα τα µικρόβια εισέρχονται στο νεογνό κατά τη διάρκεια του τοκετού. Η όψιµη και η πολύ όψιµη σηψαιµία οφείλεται σε µικρόβια αποικισµού µέσα στις µονάδες εντατικής θεραπείας νεογνών (στο 40% των περιπτώσεων). Από τα Gram αρνητικά το E. coli είναι το πιο σηµαντικό παθογόνο και ακολουθούν είδη της κλεµπσιέλλας, του Enterobacter, του Citrobacter, της Serratia και της ψευδοµονάδας. Οι σταφυλόκοκκοι (θετικοί και αρνητικοί στην πηκτάση) είναι συχνοί στα νεογνά µε µακροχρόνια νοσηλεία και σε τοποθετηµένους κεντρικούς φλεβικούς καθετήρες (17,46). Πρώιµη σηψαιµία Η πρώιµη σηψαιµία εµφανίζεται τις πρώτες 3 µέρες της ζωής του νεογνού. Είναι νόσος πολυσυστηµατική, εκδηλώνεται µε εικόνα shock ή σοβαρής αναπνευστικής ανεπάρκειας. Τα νεογνά είναι συνήθως πρόωρα ή χαµηλού βάρους γέννησης µε ιστορικό µαιευτικών επιπλοκών, όπως η πρόωρη ρήξη εµβρυϊκών υµένων και η χοριοαµνιονίτιδα. Η συχνότητά της είναι περίπου 2/1000 γεννήσεις νεογνών. (18,23) Στα πρόωρα και στα χαµηλού βάρους νεογνά η συχνότητα είναι 2-5% και η θνητότητα κυµαίνεται 5-20%. (22,29) Το συχνότερα ενοχοποιούµενο µικρόβιο είναι ο GBS περίπου στο 50% (ορότυποι Ia, Ib, II, III και V), ένα µικρόβιο αποικισµού του κόλπου των γυναικών, σύνηθες στις ΗΠΑ, όπου ανέρχεται στο 20% των περιπτώσεων. Η µόλυνση του αµνιακού υγρού και η κατάποση µολυσµένων υγρών κατά τη δίοδο µέσω του κόλπου είναι η κύρια αιτία µετάδοσης. Το µικρόβιο αυτό προκαλεί πρώιµη σηψαιµία αλλά και όψιµη νόσο µε συνοδό µηνιγγίτιδα σε ποσοστό 6.3%. (47) Άλλο µικρόβιο είναι το E. coli, το οποίο µπορεί να προκαλέσει πρώιµη σηψαιµία σε ποσοστό 20% και αποικισµό 12,6%. Ενοχοποιούνται ιδιαιτέρως τα στελέχη µε Κ1 πολυσακχαριδικό αντιγόνο. Η λιστέρια µονοκυτογόνος ευθύνεται, επίσης, για την πρώιµη νεογνική σηψαιµία (0,5%) αλλά και για την όψιµη νόσο µε εµφάνιση και µηνιγγίτιδας. Άλλοι µικροοργανισµοί είναι οι gram θετικοί, όπως ο σταφυλόκοκκος aureus (17,3%), o αρνητικός και θετικός στην πηκτάση σταφυλόκοκκος (17%), και τύποι στρεπτοκόκκου (3-8%) (Viridans, Group D, pneumoniococcus), o αιµόφιλος influenza (0,1%), η κλεµπσιέλλα (26,4%), η ψευδοµονάδα (5,9%), είδη Enterobacter (3,6-7%) ο πρωτέας, το ουρεόπλασµα urealiticum και αναερόβια 21
22 (3%), παρβοϊοί, άλλοι ιοί (HSV, CMV), καθώς και το τοξόπλασµα (4,32,46). Επίσης η προφυλακτική χορήγηση αντιβιοτικών µπορεί να δηµιουργήσει ανθεκτικά εντεροβακτηριοειδή, τα οποία θα προκαλέσουν σηψαιµία στο νεογνό. (44) Συνοψίζοντας, οι παράγοντες κινδύνου για την εκδήλωση και την ανάπτυξη της πρώιµης νεογνικής σηψαιµίας µπορεί να προέρχονται από τη µητέρα ή το νεογνό. Στους παράγοντες που προέρχονται από τη µητέρα περιλαµβάνονται, όπως και γενικότερα αναφέρθηκε, ο αποικισµός του κόλπου, η λοίµωξη της µητέρας κατά την περιγεννητική περίοδο (ουρολοίµωξη, χοριοαµνιονίτιδα, ενδοµητρίτιδα) καθώς και η ρήξη των εµβρυϊκών υµένων για περισσότερο από 24 ώρες.(20) Οι παράγοντες αυτοί ευθύνονται για την αύξηση του κινδύνου της σηψαιµίας στα πρόωρα νεογνά, που ανέρχεται στο 15%, ενώ στα τελειόµηνα είναι χαµηλότερος. Στους παράγοντες που προέρχονται από το νεογνό ανήκει η προωρότητα και το χαµηλό βάρος γέννησης, καθότι η ίδια η περιγεννητική λοίµωξη αποτελεί σηµαντικό παράγοντα έναρξης πρόωρου τοκετού. (22,27,29) Όψιµη σηψαιµία Η όψιµη και η πολύ όψιµη σηψαιµία οφείλονται στους ίδιους µικροοργανισµούς που προκαλούν την πρώιµη ή σε µικρόβια αποικισµού µέσα στις µονάδες εντατικής θεραπείας νεογνών (στο 40% των περιπτώσεων). Από τα Gram αρνητικά, το E. coli είναι το πιο σηµαντικό παθογόνο και ακολουθούν είδη της κλεµπσιέλλας, του Enterobacter, του Citrobacter, της Serratia, της ψευδοµονάδας και, τύποι Candida. Οι σταφυλόκοκκοι (θετικοί και αρνητικοί στην πηκτάση) είναι συχνοί σε µακρόχρονες νοσηλείες και σε τοποθετηµένους κεντρικούς φλεβικούς καθετήρες. (46,48) Η σηψαιµία αυτή εµφανίζεται συνήθως αργά και αµβληχρά ή µε εστιακή λοίµωξη και συχνά µηνιγγίτιδα. ιακρίνεται σε ενδονοσοκοµειακή όψιµη σηψαιµία και σε όψιµη σηψαιµία των νεογνών που έχουν εξέλθει από το µαιευτήριο και βρίσκονται στο σπίτι. ιαφέρουν ως προς τους µικροοργανισµούς που τις προκαλούν. Στα νεογνά που δεν νοσηλεύονται, η όψιµη νεογνική σηψαιµία οφείλεται στο GBS, στη λιστέρια και στο E. coli. Η συχνότητα της όψιµης νεογνικής σηψαιµίας είναι /1000 ζώντα νεογνά (4,18), για το GBS (0,4/1000) (49,50), ενώ εκείνη της ενδονοσοκοµειακής όψιµης σηψαιµίας είναι αντιστρόφως ανάλογη της ηλικίας κύησης και του βάρους γέννησης. Στα µεγάλα πρόωρα νεογνά υπολογίζονται 0.76 επεισόδια/1000 ηµέρες νοσηλείας. Στα πολύ χαµηλού βάρους γέννησης (VLBW) το ποσοστό κυµαίνεται µεταξύ 20-25% (58% σε Κ:22 και 20% στις 28 εβδοµάδες), το 11% των νεογνών αναπτύσσουν ΝΕΚ (22,51), ενώ, και σύµφωνα µε πρόσφατη πολυκεντρική µελέτη, περίπου το 21% των VLBW έχουν τουλάχιστον ένα επεισόδιο όψιµης σηψαιµίας. (35) Η εµφάνισή της σχετίζεται µε την παρουσία επιπλοκών της προωρότητας, όπως το ΣΑ και η ανάγκη εφαρµογής µηχανικού αερισµού, η εγκεφαλική αιµορραγία, η παραµονή του ανοικτού αρτηριακού πόρου και η βρογχοπνευµονική 22
23 δυσπλασία. (51,52) Στα τµήµατα νοσηλείας Ι και ΙΙ επιπέδων η συχνότητα σηψαιµίας είναι 1%. Η παρατεταµένη νοσηλεία και η χρήση παρεµβατικών µεθόδων θεραπείας αποτελούν επιβαρυντικούς παράγοντες για την εµφάνιση της σηψαιµίας. Κατά την παραµονή σε µονάδες εντατικής νοσηλείας το δέρµα και οι βλεννογόνοι αποικίζονται µε µικροοργανισµούς της χλωρίδας της κάθε µονάδας και µε όλους τους άλλους επιβαρυντικούς παράγοντες που ευθύνονται για την όψιµη νεογνική σηψαιµία. (35,53) Το 6,2% των µεγάλων πρόωρων νεογνών ( Κ:34-36) µεταξύ της 4ης και της 120ης µέρας ζωής έχει ένα τουλάχιστον επεισόδιο µε θετική καλλιέργεια. (4) Η πολύ όψιµη σηψαιµία εκδηλώνεται συνήθως µετά τον 3ο µήνα ζωής και αφορά πρόωρα πολύ χαµηλού βάρους γέννησης, που νοσηλεύονται σε εντατική νεογνών. Οφείλεται σε µικροοργανισµούς όπως η Candida, οι σταφυλόκοκκοι (coagulase-negative, CONS) και methicillin-resistant S aureus (MRSA), οι vancomycin-resistant enterocococcus faecium (VREF), και οι πολυανθεκτικοί (multidrug-resistsant [MDR] gram negatives). Αίτια είναι η µακρά νοσηλεία στην εντατική νεογνών αλλά και η χρήση ενδαγγειακών καθετήρων, η χορήγηση παρεντερικής διατροφής, η καθυστέρηση σίτισης καθώς και η χορήγηση στεροειδών. (35,37,54) Οι παθογόνοι παράγοντες που σχετίζονται µε τη νεογνική σήψη ποικίλλουν. Στη δυτική Ευρώπη είναι ίδιοι µε εκείνους στις ΗΠΑ, στις χώρες της Λατινικής Αµερικής οι εντεροβάκιλοι είναι οι πιο συχνοί, ενώ οι GBS σπάνιοι.(4,55) Η συνολική αναλογία των Gram αρνητικών και θετικών µικροοργανισµών είναι 2:1 στα παγκόσµια δεδοµένα. Στις αφρικανικές χώρες η αναλογία είναι 1:1 µε µεγαλύτερη συχνότητα του S. Aureus και GBS.(44) Οι Gram αρνητικοί µικροοργανισµοί αναπτύσσουν αντίσταση, µέσω µηχανισµών µεταλλάξεων, κυρίως µε την απενεργοποίηση ενζύµων, όπως οι ευρέος φάσµατος β λακταµάσες, που αναπτύσσουν αντίσταση στα αντιβιοτικά, π.χ. κεφαλοσπορίνες 3ης γενιάς.(56) Τα τελευταία χρόνια ευρωπαϊκές µελέτες σε ενήλικες νοσηλευόµενους σε ΜΕΘ δείχνουν σηµαντική και αυξανόµενη αντίσταση των µικροβίων στα αντιβιοτικά.(57,58) Επιπλέον, τα πλασµίδια είναι υπεύθυνα για τη µεταφορά των γονιδίων που αυξάνουν την αντίσταση σε αντιβιοτικά, όπως στις αµινογλυκοσίδες, και οδηγούν σε συνολική πολλαπλή αντίσταση σε πολλά άλλα αντιβιοτικά. Η ευαισθησία είναι περιορισµένη σε καρβαπενέµες και τιγεκυκλίνη.(59) Μερικά gram αρνητικά µικρόβια είναι ευαίσθητα µόνο σε τιγεκυκλίνη ή/και πολυµυξίνη B. (60-63) Η αντιβιοτική θεραπεία είναι απαραίτητη και πρέπει να είναι επιθετική, ώστε να επιτυγχάνεται µικροβιοκτόνος συγκέντρωση στο αίµα ή ΕΝΥ, ούρα κ.τ.λ. Η ποικιλία των παθογόνων µικροβίων που ενοχοποιούνται στη νεογνική σηψαιµία, απαιτεί αντιβιοτική κάλυψη αρχικά σε όλο το φάσµα των µικροβίων Gram θετικών και αρνητικών και, στη συνέχεια, κάλυψη που στοχεύει στο παθογόνο µικρόβιο της καλλιέργειας. (63,64) 23
24 1.5. Παθογένεια Η παθογένεια της σηψαιµίας είναι πολύπλοκη, γι αυτό και για την ανάπτυξή της απαιτείται σειρά παθοφυσιολογικών αλλαγών µε τη συµµετοχή παραγόντων της ειδικής και µη ανοσίας. Η σηψαιµία προκαλείται από την είσοδο διαφόρων παθογόνων µικροοργανισµών στον ξενιστή, οι οποίοι κατά την είσοδό τους στην κυκλοφορία αντιµετωπίζονται αρχικά από ανοσολογικούς παράγοντες της µη ειδικής ανοσίας, όπως το δέρµα, οι βλεννογόνοι, το συµπλήρωµα, τα ουδετερόφιλα, τα µακροφάγα κ.ά. Οι µικροοργανισµοί φαγοκυτταρώνονται από τα ουδετερόφιλα και τα µακροφάγα. Κατά τη φαγοκυττάρωση, τα ενεργοποιηµένα φαγοκύτταρα απελευθερώνουν ένζυµα, τοξικά προϊόντα οξυγόνου, τον παράγοντα ενεργοποίησης των αιµοπεταλίων και προϊόντα του αραχιδονικού οξέος. (48,65-67) Για τη φαγοκυττάρωση το συµπλήρωµα διαδραµατίζει σηµαντικό ρόλο και συγκεκριµένα, κατά την ενεργοποίηση της κλασσικής και εναλλακτικής οδού, απελευθερώνονται διάφορα κλάσµατα και παράγοντες, όπως το C3a, C5a και το C3b. Τα προϊόντα αυτά έχουν ισχυρή χηµειοτακτική δράση στα ουδετερόφιλα, προάγουν την οψωνινοποίηση (C3b) και την απελευθέρωση αγγειοδιασταλτικών ουσιών, µε αύξηση της διαπερατότητας των τριχοειδών. Ανάλογα µε το είδος των µικροοργανισµών που αποδοµούνται, απελευθερώνονται διάφορες ουσίες, όπως από την αποδόµηση των Gram αρνητικών µικροβίων απελευθερώνεται η ενδοτοξίνη τους, ενώ από τα Gram θετικά µικρόβια οι εξωτοξίνες τους. Οι ουσίες αυτές ενεργοποιούν τα µακροφάγα, τα οποία και παράγουν φλεγµονώδεις κυτταροκίνες.(1,68-70) Η ιντερλευκίνη-1 (IL-1) και ο παράγοντας νέκρωσης του όγκου (TNF) αποτελούν τις αρχικές κυτταροκίνες, οι οποίες µε τη σειρά τους προκαλούν την απελευθέρωση και άλλων διαβιβαστών (IL-6, IL-8) από πληθώρα κυττάρων και από την ενεργοποίηση της ειδικής ανοσίας (68,71-73). Οι προφλεγµονώδεις κυτταροκίνες, και σε µικρότερο βαθµό ή ίδια η ενδοτοξίνη, ενεργοποιούν ποικίλα ενζυµικά και κυτταρικά συστήµατα. (65,66,74,75) Στη µη ειδική ανοσιακή απάντηση, το ενεργοποιηµένο ενδοθήλιο των αγγείων διαδραµατίζει κυρίαρχο ρόλο στην παθογένεια της σηψαιµίας, µε την ενεργοποίηση των µορίων προσκόλλησης των ενδοθηλιακών κυττάρων και των λευκοκυττάρων, καθώς και µε την παραγωγή µονοξειδίου του αζώτου (ΝΟ). Αυτό προκαλεί αγγειοδιαστολή, ασκώντας τη δράση του στις παρακείµενες λείες µυϊκές ίνες, µε αποτέλεσµα τα λευκοκύτταρα να πλησιάζουν το αντιγόνο-στόχο. Άλλες αγγειοδραστικές ουσίες που προέρχονται από τα ενδοθηλιακά κύτταρα είναι ο παράγοντας ενεργοποίησης των αιµοπεταλίων (PAF), η θροµβοξάνη (TBX), τα λευκοτριένια, το ΝΟ, η ισταµίνη, η βραδυκινίνη και οι προσταγλανδίνες. (76-78) Στους ενήλικες η σηπτική καταπληξία χαρακτηρίζεται από ελάττωση των συστηµατικών 24
25 αγγειακών αντιστάσεων, αντίθετα στα παιδιά είναι πιο συχνή η ελάττωση της καρδιακής παροχής και η αύξηση των αντιστάσεων. Στα νεογνά, όµως, απαντάται παθολογική περιφερική αγγειορρύθµιση µε ή χωρίς καρδιακή δυσλειτουργία και ίσως ταχυκαρδία, φτωχή περιφερική κυκλοφορία και φυσιολογική αρτηριακή πίεση (υψηλές συστηµατικές αγγειακές αντιστάσεις). Παρουσιάζουν, επίσης, υπόταση µε ικανοποιητική περιφερική κυκλοφορία (θερµό shock, αγγειοδιαστολή) ή ανεπαρκή περιφερική κυκλοφορία (ψυχρό shock, ψυχρή φάση της καταπληξίας, αγγειοσύσπαση). (79,80) Η φλεγµονώδης απάντηση µπορεί να οδηγήσει σε ιστικές βλάβες µέσω του ενεργοποιηµένου ή κατεστραµµένου ενδοθηλίου και σε προθροµβωτική κατάσταση, µε αποτέλεσµα περιοχικά µικροέµφρακτα και διάχυτη ενδαγγειακή πήξη. Στη συνέχεια, η ελαττωµένη µικροκυκλοφορία, σε συνδυασµό µε τη διάχυτη ενδαγγειακή πήξη ( ΕΠ) οδηγεί σε βλάβες στους νεφρούς, το ήπαρ, το έντερο και στο ΚΝΣ. Η ελαττωµένη παροχή οξυγόνου στους ιστούς και η µιτοχονδριακή δυσλειτουργία οδηγούν στην εµφάνιση του συνδρόµου πολυοργανικής ανεπάρκειας. (81) Αν αποτύχει η φαγοκυττάρωση του µικροοργανισµού, τότε αρχίζει η ειδική ανοσιακή απάντηση. Τα αντιγονοπαρουσιαστικά (APC) κύτταρα, αφού τροποποιήσουν τον µικροοργανισµό, τον προβάλλουν στην κυτταρική τους µεµβράνη υπό µορφή αντιγόνου. Στη συνέχεια, ακολουθεί η παρουσίασή τους στα Τ βοηθητικά (Τh) και Β λεµφοκύτταρα. Η IL-1 που απελευθερώνεται από τα µακροφάγα, διεγείρει τα Τh κύτταρα για την παραγωγή και απελευθέρωση IL-2, η οποία ενεργοποιεί και προσελκύει στον τόπο της φλεγµονής άλλα αποµακρυσµένα Τh κύτταρα και, επιπλέον, προκαλεί τη διαφοροποίηση των Β λεµφοκυττάρων σε πλασµατοκύτταρα ικανά να παράγουν αντισώµατα. Οι ανοσοσφαιρίνες που παράγονται, αρχικά, είναι του τύπου IgM και πιθανόν IgΑ, ανάλογα µε το είδος του µικροοργανισµού και ακολουθεί η παραγωγή των IgG. Τα αντισώµατα συνδέονται µε τους µικροοργανισµούς, υποβοηθώντας τη φαγοκυττάρωση, ενώ το σύµπλεγµα αντιγόνου αντισώµατος ενεργοποιεί την κλασσική οδό του συµπληρώµατος, οδηγώντας σε βακτηριόλυση.(81) Αποτέλεσµα της απελευθέρωσης των διαφόρων µεσολαβητικών ουσιών κατά την ανοσιακή απάντηση είναι: α. η εµφάνιση των γενικών συµπτωµάτων της λοίµωξης (πυρετός, άρνηση λήψης τροφής), β. η αύξηση της διαπερατότητας των τριχοειδών και γ. η εµφάνιση αιµοδυναµικών (καταστολή του µυοκαρδίου, αγγειοσύσπαση ή αγγειοπαράλυση) και αιµατολογικών διαταραχών (λευκοκυττάρωση, λευκοπενία, διάχυτη ενδαγγειακή πήξη). Έτσι, η ανεπάρκεια στο επίπεδο της µικροκυκλοφορίας συµβάλλει συχνά στην εµφάνιση πολυοργανικής ανεπάρκειας, συνήθως µε κακή έκβαση. (3,81-84) 25
26 1.6. Κλινική εικόνα Τα συµπτώµατα και τα σηµεία είναι µη ειδικά- π.χ. η θερµοκρασία µπορεί να είναι υψηλή εντός φυσιολογικών ορίων ή χαµηλή (85), µερικά νεογνά εµφανίζουν κυάνωση ή άπνοια, νωθρότητα, υποτονία, ενώ συνήθεις είναι οι διαταραχές περιφερικής αιµάτωσης και σίτισης. Το σηπτικό νεογνό µπορεί να εκδηλώσει νευρολογικές διαταραχές, σπασµούς, προπέτεια πηγής ή µηνιγγίτιδα και συµπτώµατα από το γαστρεντερικό, όπως ηπατοµεγαλία, κοιλιακή διάταση, έµετος, εισρόφηση γαστρικού περιεχοµένου, αίµα στις κενώσεις και ίκτερο. (25-32) Οι εστιακές λοιµώξεις µπορεί να προηγούνται ή να συνοδεύουν τη σηψαιµία, όπως συµβαίνει µε την κυτταρίτιδα, το µολυσµατικό κηρίο, το απόστηµα του δέρµατος ή των βλεννογόνων, την οµφαλίτιδα, την επιπεφυκίτιδα, τη µέση ωτίτιδα και οστεοµυελίτιδα. (14,86) Νεογνική σηψαιµία και κλινικά κριτήρια εν υπάρχει οµοφωνία ως προς τον ορισµό της πιθανής νεογνικής σηψαιµίας. Έχει Κλινικά κριτήρια Υποθερµία ή πυρετός ή αστάθεια θερµοκρασίας Ελάττωση διούρησης ή υπόταση ή διαταραχή της περιφερικής κυκλοφορίας, µαρµαροειδές δέρµα Άπνοια ή αυξηµένη ανάγκη για οξυγόνο ή αύξηση των αναγκών στον αναπνευστήρα Βραδυκαρδία ή ταχυκαρδία ή αστάθεια καρδιακού ρυθµού υσανοχή στη σίτιση ή διάταση κοιλίας Λήθαργος ή υποτονία ή ευερεθιστότητα Πετέχειες δέρµατος βλεννογόνων ή σκλήρηµα Εργαστηριακά κριτήρια Λευκά <4000 ή > x 10 9 cells/l Ανώριµα/ολικά ουδετερόφιλα (I/T) >0.2 Αιµοπετάλια <100,000 x 10 9 /L C-reactive protein (CRP) >15 mg/l ή προκαλσιτονίνη 2 ng/ml υσανοχή γλυκόζης µε χορηγούµενη γλυκόζη (8-15g/kg/d) Γλυκόζη >180mg/dl ή υπογλυκαιµία <40mg/dl Οξέωση (base excess (BE) > -10 mmol/l ή γαλακτικό (lactate) >2 mmol/l 26
27 προταθεί η παρουσία ενός κλινικού σηµείου µε παράλληλη αύξηση της CRP σε επίπεδα άνω του 10mg/L, χωρίς όµως και αυτά να είναι επαρκή για τη διάγνωση της πρώιµης νεογνικής κλινικής σήψης. (2,10) Νεότερες, ωστόσο, µελέτες προτείνουν ότι, για να οριστεί η πιθανή νεογνική σηψαιµία, απαιτούνται τουλάχιστον δύο κλινικά κριτήρια και δύο εργαστηριακοί δείκτες. (80) Επιβεβαιωµένη σηψαιµία ορίζεται η ανεύρεση θετικής καλλιέργειας αίµατος µαζί µε ένα από τα κλινικά ή εργαστηριακά κριτήρια. Στα νεογνά τα µεγαλύτερα των 44 εβδοµάδων (διορθωµένη ηλικία), η κλινική σηψαιµία ορίζεται σύµφωνα µε τα κριτήρια του Goldstein (67), δηλαδή τουλάχιστον 2 από τα προηγούµενα κριτήρια, το ένα εκ των οποίων να είναι ο πυρετός ή η αστάθεια στη θερµοκρασία (θερµοκρασία> 38.5 C ή < 36 C) ιάγνωση εν υπάρχει εργαστηριακή εξέταση που να πιστοποιεί ή να αποκλείει τη µικροβιακή λοίµωξη µε 100% βεβαιότητα. (87) Ο ιδανικός εργαστηριακός δείκτης (ideal biomarker) θα πρέπει να έχει καθορισµένη κατώτερη τιµή (cut-off value), η ευαισθησία του (sensitivity) και η αρνητική προγνωστική αξία του (negative predictive value ) να πλησιάζει το 100%, ενώ συγχρόνως να έχει υψηλή ειδικότητα (specificity) και θετική προγνωστική αξία (positive predictive value) >85%. Θα πρέπει, επίσης, να ανιχνεύει τη λοίµωξη νωρίς, να µπορεί να χρησιµοποιηθεί για παρακολούθηση πολλών συνεχόµενων τιµών (επαναληψιµότητα), να είναι εύκολος στη µέτρησή του, να χρειάζεται µικρή ποσότητα αίµατος, να ανευρίσκεται εύκολα στα εργαστήρια και να είναι χαµηλού κόστους. (35) Τα συµπτώµατα και τα σηµεία είναι µη ειδικά και µπορεί να εµφανίζονται και σε µη λοιµώδη αίτια. Η σηψαιµία µε ή χωρίς πνευµονία εµφανίζεται ως σύνδροµο αναπνευστικής δυσχέρειας ή ως παροδική ταχύπνοια. Η ενδοκοιλιακή αιµορραγία και οι διαταραχές µεταβολισµού έχουν σηµεία και συµπτώµατα παρόµοια µε της σηψαιµίας. Επίσης, η νεκρωτική εντεροκολίτιδα, η διάτρηση του εντέρου και ο ειλεός µπορεί να παρουσιαστούν µε τον ίδιο τρόπο. Η έγκαιρη διάγνωση της σηψαιµίας είναι απαραίτητη. Η καθυστέρηση στη διάγνωση έχει ως αποτέλεσµα την αύξηση της θνητότητας, ενώ η πρώιµη έναρξη θεραπείας, βάσει γενικών συµπτωµάτων, µπορεί να οδηγήσει σε άσκοπη θεραπεία, αν δεν αποδειχθεί σηψαιµία, και σε απώλεια χρόνου, µε τον αποπροσανατολισµό της κλινικής σκέψης από το πραγµατικό παθολογικό αίτιο. Συνοψίζοντας, πρέπει να επισηµανθεί ότι η διάγνωση στηρίζεται στην κλινική εικόνα, το ιστορικό και τον εργαστηριακό έλεγχο. Οι εργαστηριακές εξετάσεις αξιολογούνται σε 27
28 συνδυασµό µε τη συµπτωµατολογία και την παρουσία επιβαρυντικών παραγόντων. (88) Καλλιέργειες Απαραίτητη, όπως προαναφέρθηκε, για τη διάγνωση της σηψαιµίας είναι η θετική καλλιέργεια, µε την αποµόνωση του µικροοργανισµού ή των µυκήτων από το αίµα. Αίµα, ούρα και ΕΝΥ ελέγχονται σε νεογνά ύποπτα σήψης. Η επαναληπτική καλλιέργεια αίµατος επαυξάνει την πιθανότητα διάγνωσης. Η ανάπτυξη των µικροβίων εξαρτάται από διαφόρους παράγοντες, όπως το είδος των µικροβίων, τη µικροβιαιµία, τη χορήγηση αντιµικροβιακών πριν από την καλλιέργεια, τις συνθήκες και τη µέθοδο των καλλιεργειών καθώς και την επαρκή ποσότητα αίµατος που τέθηκε για καλλιέργεια στη φιάλη. Κάθε αρνητική καλλιέργεια αίµατος δεν είναι απαλλαγµένη από λάθος, µπορεί να είναι ψευδώς αρνητική, όπως αποδεικνύεται από µεταθανάτιες καλλιέργειες, εξαιτίας των απαραίτητων παραπάνω προϋποθέσεων. (15,41,89) Η καλλιέργεια ούρων που λαµβάνεται µε καθετήρα ή υπερηβικά αξιολογείται για το θετικό αποτέλεσµα, ακόµη και αν η καλλιέργεια αίµατος είναι αρνητική.(90) Επίσης, η καλλιέργεια και η κυτταροχηµική ΕΝΥ πιστοποιούν ή αποκλείουν µηνιγγίτιδα, η οποία συνυπάρχει στο 10-13% πρώιµης νεογνικής σηψαιµίας (2) και συχνότερα στην όψιµη (25% στην όψιµη σηψαιµία από GBS).(91) Σε ποσοστό 15-50% οι αιµοκαλλιέργειες είναι αρνητικές στη µηνιγγίτιδα της πρώιµης όσο και της όψιµης λοίµωξης. (2,92,93) Καλλιέργειες ακόµη συλλέγονται από τραχειοβρογχικές εκκρίσεις στα διασωληνωµένα νεογνά, η αξιοπιστία τους, όµως, είναι πολύ µικρή. Σε περιτονίτιδα, πλευρίτιδα και αρθρίτιδα λαµβάνεται φλεγµονώδες υγρό συλλογών (πυώδες ή ορώδες). Κόπρανα ή υλικό από εντεροστοµία είναι απαραίτητα και βοηθούν στην ενοχοποίηση ενός µικροβιακού παράγοντα.(2) Ανίχνευση αντιγόνων µε ανοσολογική µέθοδο Με την ανοσολογική µέθοδο ανιχνεύεται το κυτταρικό τοίχωµα των βακτηρίων και άλλων αντιγόνων σε βιολογικά υγρά (αίµα, ούρα, ΕΝΥ). Η µέθοδος προσφέρει µεγάλη βοήθεια στη διάγνωση, ώστε, ακόµη και αν οι καλλιέργειες δεν αναπτύξουν µικρόβια, να µπορεί να δοθεί κατεύθυνση στη θεραπεία, όπως σε περίπτωση λήψης αντιβιοτικών από τη µητέρα (αρνητική καλλιέργεια στο νεογνό).(94) Υπάρχει η µέθοδος µε συγκόλληση σωµατιδίων latex (latex agglutination test) καθώς και η ανοσοηλεκτροφόρηση αντίθετης φάσης (countercurrent immunoelectrophoresis-cie). (95) Η εκτίµηση του αποτελέσµατος απαιτεί προσοχή, διότι οι µέθοδοι έχουν χαµηλή ευαισθησία και εξειδίκευση. (96,97) 28
29 Αριθµός λευκοκυττάρων Ο ολικός αριθµός των λευκοκυττάρων είναι περιορισµένης αξίας. Είναι δείκτης µη ειδικός (specificity 45-90%) και µε µικρή ευαισθησία (sensitivity 31-68%) τις πρώτες ώρες ζωής. (2) Λευκοκυττάρωση ορίζεται η αύξηση του αριθµού των λευκοκυττάρων πάνω από /mm 3 και λευκοπενία η ελάττωση κάτω από 5.000/mm 3. (98) Ο αριθµός των ολικών λευκών αιµοσφαίριων εξαρτάται από την ηλικία του νεογνού, εάν το δείγµα είναι αρτηριακό ή φλεβικό και από την κατάσταση του νεογνού κατά την αιµοληψία, αν δηλαδή το νεογνό κλαίει ή είναι ήρεµο. Η τιµή δεν είναι στατική και υπάρχει διαφορά µεταξύ των ατόµων. Ο απόλυτος αριθµός των ουδετεροφίλων, ο αριθµός των αώρων ουδετεροφίλων και η σχέση αώρων προς ολικά αποτελούν καλύτερο διαγνωστικό εργαστηριακό δείκτη. Ωστόσο, ο λόγος ανώριµα προς ολικά διαφέρει σηµαντικά µεταξύ διαφόρων παρατηρητών. Οι κατώτερες τιµές για τα ουδετερόφιλα είναι 1.800/ mm 3 κατά τη γέννηση, αυξάνουν σε 7200/ mm 3 τις πρώτες 12 ώρες και ελαττώνονται στα 1.800/ mm 3 µετά την 3η µέρα ζωής. Ουδετεροπενία ονοµάζεται η πτώση του ΑΑΟ κάτω από 1.800/ mm 3. Η παρουσία ουδετεροπενίας στη σηψαιµία είναι δυσµενές προγνωστικό σηµείο (2). Ουδετεροφιλία ορίζεται η αύξηση πάνω από / mm 3 τις πρώτες 12 ώρες και πάνω από 7.200/mm 3 µετά τις 60 ώρες ζωής. Οι Mouzinho και συν. καθόρισαν διαφορετικές τιµές για πολύ χαµηλού βάρους νεογνά (ΒΓ µικρότερο των 1500γρ και ΗΚ < 30 εβδ.). (99) Πολλά µη λοιµώδη αίτια εκφράζονται µε ουδετεροπενία ή/και ουδετεροφιλία. (88,100) Πολλά νεογνά εµφανίζουν σηψαιµία µε φυσιολογικό αριθµό ουδετεροφίλων. Οι Manroe και συν (1979), (101) παρατήρησαν ότι το ποσοστό των νεογνών µε λοίµωξη που είχαν φυσιολογικές τιµές ουδετεροφίλων ήταν µόλις 1.6%. Αριθµός και σχέση αώρων προς ολικό αριθµό ουδετεροφίλων Ο αριθµός άωρων ουδετεροφίλων (µυελοκύτταρα, µεταµυελοκύτταρα, ραβδοπύρηνα) στα φυσιολογικά νεογνά είναι µικρότερος από 1.100/mm 3 και 800/mm 3 στις 0 και 60 ώρες αντίστοιχα και η σχέση αώρων/ολικά ουδετεροφίλα µικρότερη από 0.16 και 0.12 στα αντίστοιχα διαστήµατα. (99,101) Αναλογία αώρων προς ολικά ουδετερόφιλα µεγαλύτερη από 0.2 θεωρείται ένδειξη λοίµωξης.(102) Αυξηµένος αριθµός αώρων ουδετεροφίλων και σχέση αώρων/ολικά ουδετερόφιλα παρατηρούνται στην περιγεννητική ασφυξία και σε νεογνά µητέρων µε υπέρταση της κύησης και, κατά συνέπεια, δεν αποτελούν παθογνωµονικό εύρηµα. Μορφολογικές αλλοιώσεις των ουδετεροφίλων, όπως τα σωµατίδια Döhle, και η τοξική κοκκίωση που παρατηρούνται στη σηψαιµία ανευρίσκονται και σε άλλες καταστάσεις, όπως στην υπέρταση της µητέρας και την αιµόλυση από ΑΒΟ ασυµβατότητα. (88,101) 29
30 Αριθµός αιµοπεταλίων Στη νεογνική ηλικία ως θροµβοπενία ορίζεται η ελάττωση του αριθµού αιµοπεταλίων κάτω των /mm 3 (ή /mm 3 ) και παρατηρείται συχνά στη νεογνική σηψαιµία.(103,104) Παρότι στη βαριά νεογνική σηψαιµία υπάρχει συχνά λευκοπενία, ουδετεροπενία και θροµβοπενία, το 20% των νεογνών µε σηψαιµία δεν παρουσιάζει αυτές τις αιµατολογικές διαταραχές. (92,105,106) Πρωτεΐνες οξείας φάσης- Υποδοχείς αναγνώρισης προτύπων H φλεγµονώδης αντίδραση µπορεί να οφείλεται σε λοίµωξη, τραύµα ή άλλης αιτίας ιστική καταστροφή. Στη φλεγµονώδη αντίδραση παράγονται από το ήπαρ πρωτεΐνες οξείας φάσης, όπως CRP, αµυλοειδές Α (SSA) ινωδογόνο, C3 του συµπληρώµατος, όξινη α1- γλυκοπρωτεΐνη, α1-αντιθρυψίνη, το σύµπλεγµα ελαστάσης, ο αναστολέας της α1 πρωτεϊνάσης (Ια1-ΡΙ, inter-α-inhibitor proteins), η απτοσφαιρίνη, η λακτοφερρίνη, η νεοπτερίνη, καθώς και πρωτεΐνες όπως η Lipopolysaccharide Binding Protein (LBP) και τµήµατα των κλασµάτων του συµπληρώµατος (C5a, C5L2) (35). Πρωτεΐνη οξείας φάσης χαρακτηρίζεται η πρωτεΐνη που η συγκέντρωσή της στο πλάσµα αυξάνεται (θετική πρωτεΐνη οξείας φάσης) ή ελαττώνεται (αρνητική πρωτεΐνη οξείας φάσης) κατά τουλάχιστον 25% στη διάρκεια της φλεγµονώδους αντίδρασης. Οι πρωτεΐνες οξείας φάσης έχουν διαφορετικό χρόνο παραγωγής κατά τη φλεγµονώδη αντίδραση και διαφορετικό χρόνο ηµίσειας ζωής. Οι µέθοδοι ανίχνευσης των πρωτεϊνών οξείας φάσης είναι ταχείες, αυτόµατες και ποσοτικοποιηµένες. (53, 107,108) 1. C-αντιδρώσα πρωτεΐνη Η C-αντιδρώσα πρωτεΐνη (CRP) είναι ένας από τους κυριότερους υποδοχείς αναγνώρισης προτύπων (PRR), ανιχνεύεται στο αίµα και τα επίπεδά της αυξάνουν σε διάφορες παθολογικές καταστάσεις, όπως στη φλεγµονώδη αντίδραση, στα αυτοάνοσα, στα νεοπλασµατικά, σε καρδιαγγειακά νοσήµατα, σε τραύµατα κ.α. Είναι µη ειδική πρωτεΐνη φλεγµονώδους αντίδρασης, η οποία ανακαλύφθηκε το 1930 από τους Tillett και Franci. Ονοµάσθηκε έτσι, διότι προσδιορίστηκε στον ορό ασθενών µε οξεία πνευµονία και είχε την ιδιότητα σχηµατισµού ιζήµατος παρουσία του C πολυσακχαρίτη της µεµβράνης του Streptococcus Pneumoniae και των ιόντων ασβεστίου (109). Το γονίδιο της CRP βρίσκεται στο χρωµόσωµα 1q Η πρωτεΐνη αυτή αποτελείται από πέντε όµοιες πολυπεπτιδικές µονάδες και σχηµατίζει µία πενταµερή κυκλική δοµή. Παράγεται στο ήπαρ και απελευθερώνεται από τα λιποκύτταρα κατόπιν προκλήσεως από τις φλεγµονώδεις κυτταροκίνες. Η πρωτεΐνη αυτή αποτελείται από πέντε όµοιες πολυπεπτιδικές µονάδες και σχηµατίζει µία πενταµερή κυκλική δοµή. Παράγεται στο ήπαρ και απελευθερώνεται από τα λιποκύτταρα κατόπιν προκλήσεως από τις 30
31 φλεγµονώδεις κυτταροκίνες. Ανήκει στους διαλυτούς υποδοχείς PRRs (υποδοχείς αναγνώρισης προτύπων) όπως είναι οι κολλεκτίνες (λεκτίνη και µαννόζη) και οι πενταξίνες (η CRP, το αµυλοειδές Ρ του ορού (SAP), η πρωτεΐνη LBP, ο διαλυτός υποδοχέας scd14 και ο παράγοντας 3 του συµπληρώµατος (C3). (111) Ως διαλυτός υποδοχέας αναγνώρισης προτύπων, εκτός από την αναγνώριση, η δράση της περιλαµβάνει την επαγωγή προφλεγµονωδών κυτταροκινών, ενώ εµπλέκεται στην οψωνοποίηση, στην ενεργοποίηση του συµπληρώµατος, στη στρατολογηση και στην προσκόλληση λευκοκυττάρων και στην απόπτωση. Η CRP απελευθερώνεται συνήθως εντός έξι ωρών από το ερέθισµα και επανέρχεται στα φυσιολογικά επίπεδα εντός τεσσάρων ηµερών από τη διακοπή του. Έχει ιδιότητες οψωνίνης και φαίνεται πως προστατεύει τον οργανισµό, αρχικά, από κάθε βλαπτικό παράγοντα. Παρουσία ασβεστίου, συνδέεται ειδικά µε τη φωσφορυλχολίνη, κάτι που της δίνει την ιδιότητα να ενεργοποιεί την κλασσική οδό του συµπληρώµατος και να αυξάνει τη φαγοκυττάρωση. Συνδέεται µόνο µε µεµβράνες κυττάρων που έχουν υποστεί βλάβη. Τέλος, ενεργοποιεί τους φυσικούς φονείς (Natural Killers, ΝΚ) και µπορεί να συνδεθεί µε το Fc τµήµα της ανοσοσφαιρίνης. Υπάρχει µικρή ποσότητα CRP που διέρχεται από τον πλακούντα στο έµβρυο -µητρικής προέλευσης CRP, ενώ οι συγκεντρώσεις της δεν επηρεάζονται από την ηλικία κύησης. Φυσιολογικές συγκεντρώσεις σε νεογνά είναι 1mg/dL ή λιγότερο. Ο χρόνος ηµίσειας ζωής είναι 19 ώρες. Η αύξηση της τιµής της παρατηρείται 6-18 ώρες µετά την έναρξη της φλεγµονώδους διαδικασίας, φθάνοντας το µέγιστο της τιµής της σε 8-60 ώρες, ενώ στη νεογνική σηψαιµία η µέγιστη αύξησή της παρατηρείται στις ώρες. ( ) Αύξηση της τιµής της CRP στην έναρξη βακτηριακής λοίµωξης παρατηρείται στο 50-90% των περιπτώσεων, ενώ σε λοίµωξη από GBS δεν παρατηρείται αύξηση κατά τις πρώτες 12 ώρες της ζωής του νεογνού. Η αποκατάσταση της τιµής της CRP σε φυσιολογικά επίπεδα έχει αξία για την εκτίµηση της πορείας της λοίµωξης, δίχως να αποτελεί καθοριστικό κριτήριο διακοπής της αντιµικροβιακής θεραπείας. (113) Η CRP ως δείκτης σηψαιµίας έχει αυξηµένη ευαισθησία αλλά χαµηλή ειδικότητα και χρησιµοποιείται µόνο σε συνδυασµό µε άλλους δείκτες, µεγαλύτερης ειδικότητας στη νεογνική σηψαιµία. (88) Έτσι, η λευκοπενία σε συνδυασµό µε την αυξηµένη τιµή της CRP αποτελούν σηµαντικούς δείκτες πιθανής σηψαιµίας κατά τις πρώτες τρεις ηµέρες ζωής.(88,100) Ο προσδιορισµός, επίσης, της CRP µπορεί να είναι ποιοτικός και ποσοτικός. Ο ποσοτικός προσδιορισµός των επιπέδων της σε τακτά χρονικά διαστήµατα, ανά ώρες, κατά τη διάρκεια µιας λοίµωξης ή σηψαιµίας αποτελεί σηµαντικό δείκτη πορείας της νόσου και ανταπόκρισης στη θεραπεία.(114) Η πτωτική πορεία, τέλος, των τιµών της CRP σηµαίνει βελτίωση της νόσου και ανταπόκριση στη θεραπεία, ενώ η ανοδική πορεία υποδηλώνει επιδείνωση της νόσου και ανάγκη αλλαγής θεραπείας. 31
32 2. Ταχύτητα Καθίζησης Ερυθρών (ΤΚΕ) Η ΤΚΕ ή µικρο-τκε δεν είναι άµεσος δείκτης πρωτεϊνών οξείας φάσης, αλλά αντανακλά τις µεταβολές που συµβαίνουν σε αρκετές πρωτεΐνες οξείας φάσης του ορού. Η µικρο-τκε σπάνια προσδιορίζεται στα νεογνά, λόγω της περιορισµένης αξίας, εφόσον και µη φλεγµονώδεις παράγοντες, όπως είναι η αναιµία, µπορεί να την επηρεάσουν. Οι τιµές της µικρο-τκε µεταβάλλονται ανάλογα µε την τιµή του αιµατοκρίτη, όχι όµως µε το βάρος γέννησης ή την ηλικία κύησης. Αυξάνεται, επίσης, σε επιφανειακές λοιµώξεις και σε µη λοιµώδεις διαδικασίες, όπως η ασφυξία, η εισρόφηση µηκωνίου και η αναπνευστική δυσχέρεια. Πολύ αυξηµένες τιµές της ανευρίσκονται σε αιµόλυση µε Coombs θετική και σε υπερχολερυθριναιµία, ενώ ανευρίσκεται ψευδώς αρνητική σε διάχυτη ενδαγγειακή πήξη, λόγω κατανάλωσης του ινωδογόνου.(32, 115,116) Η τιµή της αυξάνεται αργά και επανέρχεται ηµέρες µετά την αντιµετώπιση της λοίµωξης, λόγω του µεγάλου χρόνου ηµίσειας ζωής. Συνήθως σε βακτηριακές λοιµώξεις είναι αυξηµένη, όµως είναι συχνά φυσιολογική στην έναρξη της λοίµωξης. (116) 3. Ινωδογόνο του πλάσµατος Το ινωδογόνο είναι πρωτεΐνη οξείας φάσης, υψηλού µοριακού βάρους αποτελούµενο από δύο αντίγραφα τριών διαφορετικών αλύσεων (117) και εµφανίζεται ετερογενές ανάλογα µε το βαθµό φωσφορυλίωσής του. Η βιοσύνθεσή του προάγεται από ειδικούς µεσολαβητές, όπως η IL-6. Η αύξηση του ινωδογόνου µπορεί να ενεργοποιήσει τα αιµοπετάλια, την πήξη και να µεταβάλει τη γλοιότητα του αίµατος, µε τελικό αποτέλεσµα τη δηµιουργία του θρόµβου. (118) Το ινωδογόνο του πλάσµατος αυξάνεται σε περίπτωση λοίµωξης, αν και σε µερικές περιπτώσεις µπορεί να είναι χαµηλή η τιµή του ακόµη και σε σηψαιµία. Παθολογικές τιµές παρατηρούνται σε διάχυτη ενδαγγειακή πήξη, αφαιµαξοµετάγγιση και στο σύνδροµο αναπνευστικής δυσχέρειας. Η µέτρηση του ινωδογόνου στην αρχή µιας λοίµωξης δεν θεωρείται αξιόπιστος δείκτης, λόγω της ποικιλίας τιµών σε νεογνό µε λοίµωξη ή σε υγιές.(119) 4. Ινωδεσµίνη του πλάσµατος Η ινωδεσµίνη είναι πολυλειτουργική, υψηλού µοριακού βάρους γλυκοπρωτεΐνη, η οποία παράγεται στο ήπαρ και τα ενδοθηλιακά κύτταρα. Ανευρίσκεται στο πλάσµα, σε αρκετά βιολογικά υγρά και σε κυτταρικές επιφάνειες. Συµµετέχει στην αιµόσταση, στην ακεραιότητα των αγγείων και στην επούλωση των τραυµάτων. Είναι βασική γλυκοπρωτεΐνη στην εµβρυογένεση, τη µετανάστευση καθώς και στον πολλαπλασιασµό και τη διαφοροποίηση των κυττάρων. Βοηθά στην ανοσολογική απάντηση µέσω των µακροφάγων, της φαγοκυττάρωσης των ουδετεροφίλων και δρα ως µη ειδική οψωνίνη για το δικτυοενδοθηλιακό σύστηµα. Η συγκέντρωσή της ποικίλλει ανάλογα µε την ηλικία. Σε υγιή 32
33 νεογνά τα επίπεδά της είναι περίπου τα µισά και στα πρόωρα νεογνά το ένα τρίτο των επιπέδων των ενηλίκων.(120) Μετά τη γέννηση η συγκέντρωση σταδιακά αυξάνεται και φτάνει στην τιµή των ενηλίκων κατά το 2ο µήνα ζωής. Φαίνεται ότι ελαττώνεται στα νεογνά µε λοίµωξη, ασφυξία, σύνδροµο αναπνευστικής δυσχέρειας και στη βρογχοπνευµονική δυσπλασία.(121,122) Θεωρείται, τέλος, πρώιµος δείκτης συστηµατικής λοίµωξης. (32,123) 5. Προκαλσιτονίνη Κατά καιρούς αναζητήθηκαν πολλοί δείκτες φλεγµονής για την έγκαιρη διάγνωση και αντιµετώπιση των λοιµώξεων. Οι δείκτες αυτοί, όπως προαναφέρθηκε, πρέπει να προσδιορίζονται εύκολα, γρήγορα, χωρίς µεγάλο κόστος, µε µεγάλη ευαισθησία και ειδικότητα κατά την εξέλιξη της φλεγµονώδους αντίδρασης. Ένας τέτοιος δείκτης είναι και η προκαλσιτονίνη (PCT). Είναι µία πρωτεΐνη µε αλληλουχία αµινοξέων ίδια µε αυτή της προορµόνης, µε µοριακό βάρος 13kD (124), η οποία παράγεται στο ήπαρ. (125) Σε in vitro µελέτες, οι βακτηριακές ενδοτοξίνες (LPS) και οι φλεγµονώδεις κυτταροκίνες, TNF-a, IL-6, IL-1b, IL-6, µπορούν να προκαλέσουν φορές αύξηση του mrna της PCT σε µονοκύτταρα περιφερικού αίµατος, ενώ καµία αύξηση δεν προκαλείται από την IL-10.( ) Ιn vivo, όµως, η πιθανότητα η PCT να παράγεται µε τη δράση προφλεγµονωδών µεσολαβητών δεν έχει ακόµα διευκρινιστεί. Σηµαντική αύξηση της PCT παρατηρήθηκε σε ασθενείς που υποβάλλονται σε ανοσοθεραπεία µε TNF-a και IL-6.(130,131) Σε φυσιολογικές συνθήκες, η ορµονικά ενεργός καλσιτονίνη παράγεται και εκκρίνεται από τα κύτταρα C του θυρεοειδούς αδένα, µετά από πρωτεολυτική διάσπαση της προορµόνης προκαλσιτονίνης. Ο τόπος παραγωγής της PCT κατά τη λοίµωξη δεν έχει καθοριστεί πλήρως, ενώ µελέτες πιθανολογούν την παραγωγή της σε σηµεία εκτός του θυρεοειδή, όπως είναι τα µακροφάγα, τα µονοκύτταρα και τα νευροενδοκρινικά κύτταρα των πνευµόνων. (132) Η παραγωγή της είναι ταχεία και τα επίπεδά της αυξάνονται 2-6 ώρες µετά το ερέθισµα λοιµογόνου παράγοντα. Μετά την αρχική άνοδο, η πτώση των τιµών της PCT εξαρτάται από την εκ νέου παραγωγή της. Σε ασθενείς µε σηπτικό shock τα επίπεδα στο πλάσµα παραµένουν υψηλά, λόγω της συνεχιζόµενης παραγωγής της. Πτώση κατά 30% ή και περισσότερο στις τιµές της PCT ανά 24ωρο συνδυάζεται µε έλεγχο της λοίµωξης. Σε ασθενείς που αναρρώνουν από σηπτικό shock, η πτώση των επιπέδων PCT στο πλάσµα κατά 50% των αρχικών συγκεντρώσεων παρατηρήθηκε µετά από 2,4 ηµέρες, ενώ παρέµειναν αυξηµένα για 27 ηµέρες σε ασθενείς που κατέληξαν. (9,133) Οι ιδιότητες αυτές της PCT την καθιστούν χρήσιµο δείκτη παρακολούθησης της πορείας των λοιµώξεων. Η οδός απέκκρισης της PCT δεν έχει ακόµα βρεθεί, πιθανότατα αποδοµείται µε πρωτεόλυση. Η νεφρική κάθαρσή της υπολογίζεται <1ml/min, η λειτουργικότητα των νεφρών δεν επηρεάζει το ρυθµό αποδόµησης και τα επίπεδά της στο πλάσµα, διότι η νεφρική 33
34 απέκκρισή της είναι προσδιορίσιµη. Η PCT, εποµένως, µπορεί να χρησιµοποιηθεί διαγνωστικά στους ασθενείς µε σοβαρή νεφρική δυσλειτουργία και βακτηριακή λοίµωξη.(124) Οι φυσιολογικές τιµές της PCT στον ορό είναι <0,1ng/ml. Όταν αυτές κυµαίνονται µεταξύ 0,1-2ng/ml θεωρούνται ελαφρώς αυξηµένες, µεταξύ 2-5ng/ml µετρίως αυξηµένες και >5ng/ml υψηλές. Στα νεογνά τα επίπεδα της PCT αυξάνονται τις πρώτες µέρες της ζωής µέχρι τα 5ng/ml, χωρίς να συνυπάρχει λοίµωξη και υποχωρούν στις τιµές του ενηλίκου µετά την τρίτη ηµέρα.(2,11,122) Η παραγωγή της PCT και η αύξηση των επιπέδων της στον ορό σχετίζονται µε την αιτία και την έκταση της λοίµωξης. Οι κύριοι παράγοντες διέγερσης της παραγωγής της είναι η έκθεση σε ενδοτοξίνες βακτηρίων (λιποπολυσακχαρίτες), σε εξωτοξίνες καθώς και σε ορισµένες κυτταροκίνες. Η παραγωγή της εµφανίζεται µόνο σε βακτηριακές και µυκητιασικές συστηµατικές οξείες λοιµώξεις.( ) Εντοπισµένες λοιµώξεις γενικά δεν προκαλούν σηµαντική αύξηση της PCT στο πλάσµα (138). Οι µέχρι τώρα εφαρµογές της PCT είναι ποικίλες και αφορούν τη διάγνωση λοιµωδών νοσηµάτων, την παρακολούθηση της πορείας και την απάντηση στη θεραπεία µιας λοίµωξης. Η µέτρηση της PCT, µετά την τρίτη ηµέρα ζωής, σε νεογνά είναι πολύ χρήσιµη για πιθανότητα σήψης.( ) Στην ηλικία αυτή οι ασθενείς δεν παρουσιάζουν πολλές φορές ειδικά συµπτώµατα και η κλινική διάγνωση πρέπει να τεκµηριωθεί εργαστηριακά. Σηµαντικό κλινικό πρόβληµα αποτελεί η αναγκαιότητα ταχείας διερεύνησης µιας λοίµωξης, δηλαδή αν πρόκειται για µικροβιακή ή ιογενή. Για το λόγο αυτό διάφορες παράµετροι (αιµατολογικές, βιοχηµικές, ανοσολογικές), που συµµετέχουν στη λοίµωξη, µελετήθηκαν προκειµένου να αποτελέσουν δείκτες έγκαιρης διάγνωσης βακτηριακών λοιµώξεων και διάκρισής τους από τις ιογενείς. Οι παράµετροι αυτές έχουν αρκετά πλεονεκτήµατα αλλά και µειονεκτήµατα, όσον αφορά την ταχύτητα προσδιορισµού τους, την ευαισθησία, την ειδικότητα, την επαναληψιµότητα και το κόστος προσδιορισµού. Τα τελευταία χρόνια προσδιορίζεται η PCT σε ολοένα και περισσότερες λοιµώξεις και θεωρείται χρήσιµη παράµετρος στη διάκριση αυτή. Στις ιογενείς λοιµώξεις, σε αντίθεση µε τις βακτηριακές, παρατηρείται µικρή ή καµία αύξηση των συγκεντρώσεών της. Στη µικροβιακή µηνιγγίτιδα, σε αντίθεση µε την ιογενή, παρατηρείται σηµαντική αύξηση των συγκεντρώσεών της και αυτό την καθιστά διαγνωστικό δείκτη διάκρισής τους. ( ) 6. Κυτταροκίνες και χηµειοκίνες Οι πρωτεΐνες οξείας φάσης προκαλούν έκκριση προφλεγµονωδών κυτταροκινών, όπως της ΙL-1β, IL-6, IL-8, του διαλυτού υποδοχέα της IL-2, sil2r (soluble IL-2 receptor) και του TNF-α. Οι παράγοντες αυτοί αποτελούν πρώιµους δείκτες µικροβιακής λοίµωξης. Η ευαισθησία και η ειδικότητα κυµαίνονται µεταξύ 74 και 94% (149). Οι κυτταροκίνες, όπως η προφλεγµονώδης IL-6, η αντιφλεγµονώδης IL-10, οι χηµειοκίνες IL-8, η πρωτεΐνη IP-10 34
35 (10kDa interferon-γ inducible protein), τα κύτταρα RANTES (regulated upon activation normal Τcell expressed and secreted) και ο διαλυτός ενεργοποιητής του υποδοχέα που εκφράζεται στα µυελοειδή κύτταρα [serum soluble triggering receptor expressed on myeloid cells (strem)-1] έχουν χρησιµοποιηθεί ως δείκτες υποψίας όψιµης νεογνικής σηψαιµίας.(11,150,151) Η IL-6, που ενεργοποιεί την παραγωγή της CRP από το ήπαρ, προηγείται της αύξησής της. Η IL-6 και ο ανταγωνιστής του υποδοχέα της IL-1 (IL-1 receptor antagonist, IL-1ra) είναι δυνατόν να βοηθήσουν στη διάγνωση της σηψαιµίας δύο µέρες πριν από την έναρξη των κλινικών συµπτωµάτων.(152) Ο συνδυασµός των IL-6 και IL- 8 αποτελεί καλό διαγνωστικό δείκτη. Άλλες χηµειοκίνες, όπως ο TNF-α, το monokine induced by interferon-γ, η πρωτεΐνη MCP-1 (monocyte chemoattractant protein) και το ογκογονίδιο (growth-related oncogene-α) αυξάνουν τη συγκέντρωσή τους στη διάρκεια της λοίµωξης και της ΝΕΚ. ( ) Οι αντιφλεγµονώδεις κυτταροκίνες, όπως η IL-10 και ο παράγοντας transforming growth factor β είναι σηµαντικοί για την πρόγνωση της σηψαιµίας. Αυξηµένος λόγος IL-10/TNF-α σχετίζεται µε σοβαρή όψιµη σηψαιµία. (35) Ένας αλγόριθµος µε µετρήσεις των IL-10, IL-6, RANTES προβλέπει την ανάπτυξη διάχυτης ενδαγγειακής πήξης σε σοβαρές σηψαιµίες. Αποτελεί συγχρόνως διαγνωστικό εργαλείο πρόγνωσης και θεραπευτικής αντιµετώπισης σοβαρών καταστάσεων µε υψηλή θνησιµότητα.(153) Το υψηλό κόστος, η δύσκολη µεθοδολογία, η ελαττωµένη χρήση των δοκιµασιών από τα κλινικά εργαστήρια δεν επέτρεψε να αξιοποιηθούν οι κυτταροκίνες ως διαγνωστικές εξετάσεις ρουτίνας. 7. Συνδυασµοί µεθόδων Τα επίπεδα των κυτταροκινών, όπως της IL-8, και του διαλυτού υποδοχέα sil2r, σε συνδυασµό µε τα επίπεδα της CRP βελτιώνουν την ευαισθησία στο 85% και την ειδικότητα στο 97% για τη σηψαιµία. (149) Αντίστοιχα κι άλλοι ερευνητές έχουν µελετήσει συνδυασµούς µεθόδων καθώς επίσης την ευαισθησία και την ειδικότητά τους.(2,155) 8. Αντιγόνα επιφανείας κυττάρων Η κυτταροµετρία ροής διευκολύνει τη µέτρηση των κυκλοφορούντων φλεγµονωδών κυττάρων, όπως των ουδετεροφίλων, των λεµφοκυττάρων, των µονοκυττάρων και των φυσικών φονέων κυττάρων (ΝΚ, natural killer). Ειδικά αντιγόνα της επιφανείας των κυττάρων εκφράζονται υπέρµετρα, όταν τα κύτταρα-στόχοι ενεργοποιούνται από τα µικροβιακά προϊόντα και τις βακτηριακές τοξίνες. Πολλά τέτοια µόρια και ο ρόλος τους στη λοίµωξη έχουν µελετηθεί, µε σηµαντικότερα το CD64 των ουδετεροφίλων και το CD11b των ουδετεροφίλων και µονοκυττάρων. (156) Αυτά ανιχνεύονται µε τον κυτταροµετρητή ροής, είναι αυξηµένα στη σηψαιµία, στη µυκηθαιµία αλλά και στην ΝΕΚ. Το CD64 των ουδετεροφίλων ανιχνεύεται αυξηµένο σε ΝΕΚ, σε διάτρηση κοίλου σπλάχνου και στην 35
36 περιτονίτιδα. (35) To CD11b των ουδετεροφίλων και των µονοκυττάρων είναι δείκτης πρώιµης νεογνικής σηψαιµίας. Η διαγνωστική του αξία είναι µεγάλη, καθότι ανιχνεύεται 3 µέρες, πριν ακόµη εκδηλωθούν κλινικά συµπτώµατα. (157) Αύξηση του αντιγόνου αυτού παρατηρείται και στο σύνδροµο αναπνευστικής δυσχέρειας.(35) Άλλα αντιγόνα επιφανείας που έχουν µελετηθεί σε λοιµώξεις, είναι το CD69 στα NK κύτταρα, το CD25 και το CD45RO στα λεµφοκύτταρα. Επίσης, µελετήθηκαν το CD19, το CD33, το CD66b (που θεωρείται δείκτης µεγάλης διαγνωστικής αξίας) και τα CD64 και CD11b. (156,158) Μοριακές µέθοδοι ανίχνευσης σηψαιµίας Οι µέθοδοι αυτές βασίζονται στη στοχευµένη ενίσχυση ενός βιολογικού υλικού π.χ. ολικό αίµα, µε ή χωρίς εµπλουτισµό µε θρεπτικό υλικό, και στην ανίχνευση του rdna ή rrna (ριβοσωµικό DNA ή RNA) µε PCR (polymerase chain reaction) τεχνική. (159) Υπάρχουν µοριακές µέθοδοι που ανιχνεύουν ενισχυµένο σήµα από ακολουθίες πυρηνικού οξέος [Nucleic Acid Sequence-Based Amplification (NASBA)] ή µε τεχνική ενισχυµένου φθορισµού (FISH). Άλλες σύγχρονες τεχνικές ανιχνεύουν βακτήρια από τις θετικές καλλιέργειες. Τέτοια τεχνική είναι η φασµατοσκοπική [matrix-assisted laser desorption ionization time-of-flight mass spectrometry (MALDI-TOF MS)].( ) Οι νέες τεχνικές ανίχνευσης της πρώιµης νεογνικής σηψαιµίας ή της χοριοαµνιονίτιδας βασίζονται στη µελέτη των λειτουργικών πρωτεϊνών που εκφράζονται κατά τη διάρκεια µιας λοίµωξης, τα Proteomics. (163) Μοιάζουν µε τα Genomics µόνο που τα τελευταία βασίζονται στο DNA ή στο mrna. Είναι βελτιωµένες τεχνικές ηλεκτροφόρησης και χρωµατογραφίας και ανιχνεύουν βιολογικούς δείκτες-biomarkers (defensin-1 και 2, των S100A12, S100A8). Η ανίχνευση τέτοιων δεικτών βαθµολογείται µε έναν αύξοντα αριθµό και το Score που προκύπτει, ενισχύει τη διάγνωση της πρώιµης νεογνικής σηψαιµίας. Με την ανίχνευση των ανοσολογικών αυτών διαταραχών συσχετίστηκε η ενδοµήτρια χρόνια φλεγµονώδης διαδικασία, η οποία προκαλεί βλάβες στο έµβρυο µε απώτερες συνέπειες (163). O ρόλος των ενδοκυττάριων πρωτεϊνών DAMPs (Damage Associated Molecular pattern Proteins) είναι να ενεργοποιούν σηµατοδοτικά µονοπάτια και µεµβρανικούς υποδοχείς, για να ξεκινήσει η κυτταρική βλάβη. Η συµµετοχή κι άλλων µορίων, όπως της πρωτεΐνης HMGB1 (highmobility group box protein-1), που απελευθερώνεται από τα σωµατικά κύτταρα, και του υποδοχέα RAGE (receptor of advanced glycation end products) καταδεικνύει γιατί η συστηµατική φλεγµονή και η γενικευµένη ενδοθηλιακή βλάβη προκαλεί κλινική εικόνα βαριάς σηψαιµίας πολύ πριν από την ανίχνευση των µικροβιακών αντιγόνων. ( ) Οι τεχνικές της φασµατοµετρίας που βασίζονται στα Proteomics, όπως η mass spectrometry-based proteomic profiling και η surface enhanced laser desorption/ionization, ανιχνεύουν πρωτεΐνες-βιολογικούς δείκτες για τη διάγνωση της όψιµης νεογνικής σηψαιµίας 36
37 και της νεκρωτικής εντεροκολίτιδας στα πρόωρα νεογνά. Αποτελούν, ακόµη, νέο χρήσιµο δείκτη για την έγκαιρη αφαίρεση της αντιβιοτικής αγωγής στις αµφίβολες και ύποπτες περιπτώσεις. Επιπλέον, βοηθούν τον νεογνολόγο για την πρώιµη έναρξη της θεραπείας, όταν υπάρχει σηψαιµία, υποβοηθώντας τη διάγνωση µίας ύποπτης κλινικής εικόνας. (35) 1.8. Θεραπεία Η εµπειρική αντιµικροβιακή θεραπεία αρχίζει µε την κλινική υπόνοια λοίµωξης, αµέσως µετά τη λήψη καλλιεργειών. Συχνά τα συµπτώµατα είναι υποκλινικά, µη ειδικά. Γι αυτό και η επιλογή της εµπειρικής θεραπείας βασίζεται στο χρόνο έναρξης της λοίµωξης (πρώιµη ή όψιµη, ενδονοσοκοµειακή ή πολύ όψιµη νεογνική λοίµωξη στο σπίτι), στα συνήθη µικρόβια, στην κλινική πορεία που παρουσιάζει ο κάθε µικροοργανισµός, στη χλωρίδα της κλινικής, στην περιοχή που προσβάλλεται και στη διεισδυτικότητα του αντιβιοτικού.(58) Μη βακτηριακές λοιµώξεις λαµβάνουν την κατάλληλη αντιϊκή ή αντιµυκητιασική θεραπεία. Στην έναρξη µίας πρώιµης λοίµωξης στις ΗΠΑ, η αντιµικροβιακή θεραπεία περιλαµβάνει φάσµα για την καταπολέµηση µικροβίων όπως GBS, λιστέριας µονοκυτογόνου, E.Coli και άλλων gram αρνητικών εντερικών βακτηρίων. Ο συνδυασµός της αµπικιλλίνης και µίας αµινογλυκοσίδης είναι συνήθης. Η επιλογή της αµινογλυκοσίδης γίνεται για τα µικρόβια της κοινότητας και συνήθως προτιµάται η γενταµυκίνη. Αν θεωρείται πιθανή η µηνιγγίτιδα, προστίθεται κεφαλοσπορίνη τρίτης γενιάς, όπως η κεφοταξίµη, που περνά τον αιµατοεγκεφαλικό φραγµό. (167) Η ενδονοσοκοµειακή όψιµη σηψαιµία µπορεί να προκληθεί από τον CONS, από είδη εντεροκόκκου, από gram αρνητικούς εντεροβάκιλλους και µύκητες. Οι παράγοντες κινδύνου συνδέονται µε τις ενδονοσοκοµειακές παρεµβάσεις, τη χρήση καθετήρων, παροχετεύσεων και νοσηλευτικών ή ιατρικών χειρισµών. Πάντα λαµβάνεται υπόψη η ενδονοσοκοµειακή µικροβιακή χλωρίδα για την επιλογή του κατάλληλου αντιβιοτικού. Οι σταφυλόκοκκοι που παράγουν πενικιλλινάση είναι ανθεκτικοί στην πενικιλλίνη και την αµπικιλλίνη. Η επιλογή γίνεται µεταξύ µίας κεφαλοσπορίνης τρίτης γενιάς ή της βανκοµυκίνης ή µίας πενικιλλίνης ανθεκτικής στην πενικιλλινάση, όπως η ναφκιλλίνη ή η µεθικιλλίνη. Η βανκοµυκίνη είναι κατάλληλη για όλα τα είδη του σταφυλοκόκκου και τους εντεροκόκκους, ενώ η πενικιλλίνη, η ανθεκτική στην πενικιλλινάση, είναι κατάλληλη για στρεπτοκόκκους και µία µεθικιλλίνη για τους CONS και S. Aureus. (168) Η κεφοταξίµη ή η κεφτριαξόνη είναι αποτελεσµατικές εναντίον του GBS, του πνευµονιόκοκκου, του εντερόκοκκου, της λιστέριας, των gram αρνητικών εντεροβακίλλων, όπως της ψευδοµονάδας, του εντεροβακτηριδίου, της σερράτιας και του κιτροβακτηριδίου. Η κεφταζιδίµη ή η αµινογλυκοσίδη ή ο συνδυασµός τους καλύπτουν την ψευδοµονάδα. Άλλοι συνδυασµοί αντιµικροβιακών µπορεί να είναι κατάλληλοι για ενδονοσοκοµειακές σηψαιµίες. Ωστόσο, ο κίνδυνος έναντι του οφέλους πρέπει να υπολογίζεται, όταν χρησιµοποιείται κεφαλοσπορίνη τρίτης γενιάς. Η αύξηση των 37
38 ανθεκτικών στελεχών και ο αποικισµός του γαστρεντερικού µε µύκητες είναι παράγοντες που οι νεογνικές µονάδες αντιµετωπίζουν συχνά. Η κεφτριαξόνη µετατοπίζει τη χολερυθρίνη από τη λευκωµατίνη, λόγω της υψηλής δυνατότητάς της να συνδέεται µε πρωτεΐνες και θεωρητικά προκαλεί υπερχολερυθριναιµία. Παρόλα αυτά, οι κεφαλοσπορίνες δεν έχουν δοσοεξαρτώµενη τοξικότητα, όπως οι αµινογλυκοσίδες και η χλωραµφαινικόλη, και δεν απαιτείται προσδιορισµός των επιπέδων τους στο πλάσµα. Η εµπειρική θεραπεία ενδέχεται να τροποποιηθεί, όταν υπάρχει το αποτέλεσµα της καλλιέργειας και το αντιβιόγραµµα ή το επιβάλλει η πορεία της νόσου. (169) Η δόση και η συχνότητα χορήγησης ποικίλλουν ανάλογα µε την ηλικία κύησης, το βάρος γέννησης, την ηπατική και τη νεφρική λειτουργία. Η διάρκεια της θεραπείας εξαρτάται από το είδος της λοίµωξης. Υποστηρικτική θεραπεία Εκτός της αντιµικροβιακής θεραπείας, η υποστηρικτική θεραπεία είναι επίσης απαραίτητη. Η υποστήριξη µε τον αναπνευστήρα µπορεί να είναι αναγκαία, ιδιαίτερα σε νεογνά µε κεραυνοβόλο σηψαιµία πρώιµης έναρξης. Είναι, επίσης, αναγκαία η ενδοφλέβια χορήγηση υγρών, η παρεντερική διατροφή, η συνεχής καταγραφή των ζωτικών σηµείων καθώς και ο έλεγχος των ηλεκτρολυτών, της γλυκόζης και των βιοχηµικών δεικτών, ώστε να επιτυγχάνεται η διόρθωση των µεταβολικών διαταραχών. Το σηπτικό shock απαιτεί υποστήριξη της κυκλοφορίας µε ογκωτικά διαλύµατα και ινότροπα. (3,171) Αντιµετωπίζονται, επίσης, οι σπασµοί και οι επιπλοκές του ΚΝΣ, ενώ σε περίπτωση µηνιγγίτιδας χορηγούνται κατάλληλα αντιβιοτικά, αποκαθίστανται οι µεταβολικές διαταραχές και, τέλος, παρέχεται συµπτωµατική αντιεπιληπτική αγωγή. Σε περίπτωση διάχυτης ενδαγγειακής πήξης χορηγείται πρόσφατο κατεψυγµένο πλάσµα, βιταµίνη Κ, συµπυκνωµένα ερυθρά και αιµοπετάλια, για την αντιµετώπιση της αναιµίας και θροµβοπενίας αντίστοιχα.(171) Ανοσοθεραπεία- Ανοσοπαρέµβαση Το ανοσιακό σύστηµα του νεογνού υπολείπεται γενικότερα και όχι µόνο στο επίπεδο της χηµειοταξίας των ουδετεροφίλων έναντι παθογόνων µικροοργανισµών, στην παραγωγή προφλεγµονωδών κυτταροκινών, µέσω των Τ-λεµφοκυττάρων, και στη λειτουργική δράση του συµπληρώµατος. Στα πρόωρα νεογνά είναι ακόµη πιο αποδυναµωµένη η ανοσία λόγω της υπογαµµασφαιριναιµίας, καθότι η µεταφορά των IgG µητρικών αντισωµάτων γίνεται την 32η-34η εµβρυϊκή εβδοµάδα. Ακόµη και τα τελειόµηνα νεογνά έχουν έλλειψη αντισωµάτων εναντίον κάποιων αντιγόνων, όπως των GBS, E. Coli. Ο αυξηµένος κίνδυνος βακτηριακής λοίµωξης, εξαιτίας της υπογαµµασφαιριναιµίας, οδήγησε στη χορήγηση ενδοφλέβιας γ- σφαιρίνης για την πρόληψη και θεραπεία των λοιµώξεων. Υπάρχουν µελέτες που 38
39 αξιολόγησαν την αποτελεσµατικότητα της IVIG στη θεραπεία των νεογνών, τα οποία βρίσκονται σε λοίµωξη.(172) Η γ-σφαιρίνη συνδέεται µε την επιφάνεια των κυτταρικών υποδοχέων, προάγει την οψωνική δράση, ενεργοποιεί το συµπλήρωµα, προάγει την κυτταροτοξικότητα που είναι εξαρτώµενη από τα αντισώµατα και βελτιώνει τη λειτουργία των ουδετεροφίλων. Επιπλέον, ρυθµίζει τον καταρράκτη των κυτταροκινών, καταστέλλει το σύστηµα της IL-1, παγιδεύει τους υποδοχείς Fc των φαγοκυττάρων και ρυθµίζει την έκφρασή τους. Σε τυχαιοποιηµένες µελέτες παρατηρήθηκε στατιστικά σηµαντική ελάττωση της θνητότητας στην οµάδα χορήγησης ανοσοσφαιρίνης έναντι των placebo.( ) Η πολυκλωνική γ-σφαιρίνη (polyclonal IVIG) για θεραπευτικούς ή προφυλακτικούς λόγους µελετάται σε τυχαιοποιηµένες ελεγχόµενες µελέτες (RCTs). Σε σύνολο 4986 νεογνών, από µεταναλύσεις φαίνεται ότι υπάρχει 3% ελάττωση της επίπτωσης της σηψαιµίας, αλλά δεν παρατηρείται διαφορά στη θνητότητα.(29,175,177) Άλλοι µελετώµενοι παράγοντες είναι ανθρώπινα µονοκλωνικά αντισώµατα και υπεράνοση γ-σφαιρίνη για συγκεκριµένο αντιγόνο, όπως του σταφυλοκόκκου (δύο µελέτες µε INH A-21 και µία µελέτη µε Altastaph που περιελάµβαναν σύνολο νεογνών) για πρόληψη και θεραπεία της νεογνικής σηψαιµίας. Τα αποτελέσµατα δεν δείχνουν διαφορές ως προς τη θνητότητα.(1,178,179) Η αντισταφυλοκοκκική γ-σφαιρίνη, προφυλακτικά σε πολύ µικρά για την ηλικία κύησης νεογνά, είναι µία πρόσφατη προσέγγιση αντιµετώπισης των αυξανοµένων λοιµώξεων εντός των µονάδων εντατικής νεογνών.(174,180) Στη νεογνική σηψαιµία είναι γνωστό ότι τα επίπεδα του παράγοντα G-CSF και της IL-6 είναι αυξηµένα, ενώ τα ουδετερόφιλα εµφανίζουν ελαττωµένη δραστηριότητα της αναπνευστικής έκρηξης ή της έκκρισης των β2 ιντεγκρινών. Στην πορεία της σηψαιµίας παρατηρείται πτώση των επιπέδων του παράγοντα G-CSF και της IL-6, ενώ σταδιακά βελτιώνεται η δραστηριότητα της αναπνευστικής έκρηξης και της έκκρισης των β2 ιντεγκρινών.(174,181) Η χορήγηση ανασυνδυασµένου G-CSF προκαλεί αύξηση των ουδετεροφίλων, της δραστηριότητας της αναπνευστικής έκρηξης και της έκφρασης στα ουδετερόφιλα των CD11c. Σε συστηµατικές µεταναλύσεις φαίνεται ότι δεν υπάρχει στατιστικά σηµαντική διαφορά στη θνητότητα και στην επίπτωση της σηψαιµίας, τόσο στη θεραπευτική όσο και στην προφυλακτική χορήγηση. (174, ,189) Η χορήγηση ενεργοποιηµένης πρωτεΐνης C (activated protein C,-APC) προάγει την ινωδόλυση και έχει αντιφλεγµονώδη δράση παρεµποδίζοντας την παραγωγή του TNF (tumor necrosis factor). Ωστόσο, σε µεταναλύσεις (188) και σε τυχαιοποιηµένες ελεγχόµενες µελέτες (RCT) σε ενήλικες µε χορήγηση ανασυνδυασµένης APC τα αποτελέσµατα είναι αµφιλεγόµενα. (174) Από µελέτες της pentoxifylline, αναστολέα της φωσφοδιεστεράσης, προκύπτει ότι αυτή καταστέλλει τον TNF-α ενεργοποιώντας την αδενυλ-κυκλάση και αυξάνοντας τη 39
40 συγκέντρωση του c-amp. Πιο συγκεκριµένα, σε δύο τυχαιοποιηµένες ελεγχόµενες µελέτες (RCTs) που διενεργήθηκαν σε ενήλικες και νεογνά, φαίνεται ότι η pentoxifylline µειώνει τη βλάβη του πνεύµονα και τη σοβαρότητα της ΝΕΚ και βελτιώνει τη λειτουργία των ενδοθηλιακών κυττάρων, ελαττώνοντας την παρατεταµένη διαταραχή στη διαδικασία της πήξης. (189,190) Η ελάττωση του οξειδωτικού stress µε selenium, συστατικό της υπεροξειδάσης της γλουταθειόνης και µε melatonin που δεσµεύει τις ελεύθερες ρίζες, δεν δίνουν σαφή συµπεράσµατα για την αποτελεσµατικότητά τους, όπως καταγράφεται σε RCTs και ανασκοπικές µελέτες-cochrane reviews. (191,192) Επίσης, η γλουταµίνη, η λακτοφερρίνη, τα προβιοτικά και τα πρεβιοτικά καθώς και το µητρικό γάλα αποτελούν νέες θεραπευτικές προσεγγίσεις, µε αµφιλεγόµενη, όµως, αποτελεσµατικότητα.(193,194) Νέες θεραπευτικές προσεγγίσεις δοκιµάζονται στον τοµέα της ανοσολογίας, όπως τα αντιµικροβιακά πεπτίδια και οι πρωτεΐνες (ΑΑΡs), όπως και µία ανασυνδυασµένη πρωτεΐνη, η rbpi21, µε δυνατότητα να εξουδετερώνει την ενδοτοξίνη, να ελαττώνει τις φλεγµονώδεις κυτταροκίνες και να βελτιώνει την κάθαρση των βακτηρίων. (195) Στην έναρξη της θεραπείας µε πρωτεΐνη ΙL-37 σε πειραµατόζωα ελαττώνεται η φλεγµονώδης αντίδραση και αντίστοιχα η θνητότητα. (196) Θεραπεία σε ενήλικες µε χορήγηση αντιφλεγµονωδών κυτταροκινών στη διάρκεια της σηψαιµίας έχουν αµφισβητούµενα αποτελέσµατα. (29) Κλινική και εργαστηριακή βελτίωση-κριτήρια H ανταπόκριση στη θεραπεία καθορίζεται µε τη θετική τροποποίηση της κλινικής εικόνας και των εργαστηριακών ευρηµάτων της σηψαιµίας µερικές ώρες µετά την έναρξη θεραπείας και καθορίζεται σύµφωνα µε τα παρακάτω κλινικά ή/και τα εργαστηριακά στοιχεία βελτίωσης. 40
41 Η βελτίωση ορίζεται από τον κλινικό ιατρό που ελέγχει αν ισχύουν τα ακόλουθα κριτήρια: Θερµοκρασία Χωρίς πυρετό (>38 ο C) ή υποθερµία σε θερµικά ουδέτερο περιβάλλον Αναπνευστικά σηµεία Λιγότερες ή καθόλου άπνοιες το τελευταίο 24ωρο Αν υποστηρίζεται µε n-cpap: αφαίρεσή του ή ελάττωση του FiO 2 Αν υποστηρίζεται µε µηχανικό αερισµό, ελαττώνονται οι παράµετροι του αναπνευστήρα ή χορηγείται n-cpap Αιµοδυναµικά Χωρίς αγγειοδραστικά φάρµακα -χωρίς αστάθεια στον καρδιακό ρυθµό (ταχυκαρδία, βραδυκαρδία) (καρδιακός ρυθµός στη 10η-90η εκ. θέση) Ελάττωση των αγγειοδραστικών φαρµάκων Χωρίς ολιγουρία. Χωρίς µαρµαροειδές δέρµα, φυσιολογικός χρόνος τριχοειδικής επαναπλήρωσης Καλύτερη ανοχή σίτισης-η σίτιση από το στόµα συνεχίζεται χωρίς πρόβληµα Σε συµπτώµατα από την κοιλιά παρατηρείται βελτίωση Νευρολογικά βελτίωση αυτόµατης κινητικότητας χωρίς ευερεθιστότητα έρµα χωρίς πετέχειες ή άλλα εξανθήµατα Εργαστηριακά Λευκά: x 10 9 cells/l Ανώριµα /ολικά (Ι/Τ):<0,2 Αιµοπετάλια:> x 10 9 /L C-Reactive Protein (ελάττωση κατά 30% από προηγούµενη τιµή) PCT προκαλσιτονίνη: <2 ng/ml Γλυκόζη αίµατος: <180 mg/dl και >40 mg/dl µε χορήγηση (8-15 g/kg/η) Οξέωση (BE): >-10 mmol/l ή γαλακτικό <2 mmol/l Goldstein et al,
42
43 2o ΚΕΦΑΛΑΙΟ ΑΜΥΝΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΟΥ ΝΕΟΓΝΟΥ Η ανοσία αποτελεί το αµυντικό σύστηµα του ανθρώπου µε οργάνωση και λειτουργία πολύπλοκη, που περιλαµβάνει συλλογή κυττάρων, ιστών και µορίων, τα οποία µε τη συντονισµένη αντίδρασή τους εναντίον των λοιµογόνων παραγόντων συνιστούν την ανοσιακή απάντηση. Βασικό χαρακτηριστικό του φυσιολογικού ανοσιακού συστήµατος είναι η αναγνώριση και διάκριση των δικών του στοιχείων από τα ξένα, µε σκοπό να ανέχεται τα ίδια/δικά του και να επιτίθεται και να απορρίπτει τα µη ίδια/ξένα, ώστε να προστατεύει την ακεραιότητα του οργανισµού. Η ανοσιακή απάντηση περιλαµβάνει σειρά γεγονότων, στα οποία συµµετέχουν πολλοί τύποι κυττάρων και διακρίνεται α) στη φυσική ή µη ειδική ανοσία και β) στην επίκτητη ή ειδική ανοσία.(197) Τα νεογνά αµέσως µετά τον τοκετό διαθέτουν τους απαραίτητους αµυντικούς µηχανισµούς για να αντιµετωπίσουν την επίθεση των «ξένων» αντιγόνων. Η λειτουργία, όµως, ορισµένων τµηµάτων του αµυντικού συστήµατος υπολείπεται, ιδιαίτερα στα πρόωρα νεογνά, µε αποτέλεσµα να είναι ιδιαίτερα ευάλωτα στις µικροβιακές λοιµώξεις. (Πίνακας 1.2) 2.1. MH EI ΙΚΗ Ή ΦΥΣΙΚΗ ΑΝΟΣΙΑ Η µη ειδική ανοσία περιλαµβάνει αντιδράσεις ενεργοποίησης σειράς χηµικών και κυτταρικών παραγόντων. Οι αντιδράσεις αυτές είναι επαγόµενες αλλά µη ειδικές και προϋποθέτουν µηχανισµούς αναγνώρισης που βασίζονται σε υποδοχείς µε περιορισµένη ποικιλία, οι οποίοι οδηγούν στην ίδια απάντηση για όλους τους παθογόνους µικροοργανισµούς. Η ανοσία, η οποία προκαλείται δεν διαρκεί γι αυτό και δεν δηµιουργείται ανοσολογική µνήµη. (199) Επιφανειακοί επιθηλιακοί φραγµοί Ο ανθρώπινος οργανισµός προκειµένου να προστατευτεί από διάφορους µικροοργανισµούς του εξωτερικού περιβάλλοντος ανέπτυξε ένα πολύπλοκο σύστηµα αµυντικών µηχανισµών. Η πρώτη γραµµή άµυνας του οργανισµού είναι οι φυσικοί ανατοµικοί φραγµοί (δέρµα και βλεννογόνοι) που δρουν µηχανικά, εµποδίζοντας τη διείσδυση των διαφόρων λοιµογόνων παραγόντων. Αυτό κυρίως επιτυγχάνεται από τα επιθήλια και τις συνδέσεις των κυττάρων τους, που καθίστανται ισχυρές µέσω κυτταρικών συνάψεων. (200) 43
44 ΠΙΝΑΚΑΣ 1.2. Ανοσολογική απάντηση σε νεογνική σηψαιµία Ανοσολογι κός παράγοντας Λειτουργία Νεογνική ηλικία Κλινική σηµασία Ελαττωµένη παραγωγή Ελαττωµένο Χηµειοτακτισµός χηµειοτακτικών παραγόντων, Συµπλήρωµα συµπλήρωµα ειδικά σε οψωνινοποίηση ελαττωµένη οψωνινοποίηση των πρόωρα νεογνά βακτηρίων Αντίσωµα Οψωνινοποίηση ενεργοποίηση του συµπληρώµατος Η συγκέντρωση της IgG στα πρόωρα Έλλειψη αντισωµάτων εναντίον νεογνά ελαττωµένη. ειδικών παθογόνων µικροβίων, Στα τελειόµηνα νεογνά αυξηµένος κίνδυνος λοιµώξεων και υψηλότερη από αυτή αποικισµού των βλεννογόνων µε των ενηλίκων. δυνητικά παθογόνα µικρόβια IgA απούσα από τις εκκρίσεις Ελαττωµένη Ουδετερόφιλα Χηµειοταξία µετανάστευση, ελαττωµένη σύνδεση σε χηµειοτακτικούς Ελαττωµένη φλεγµονώδης απάντηση, δυσκολία περιορισµού της λοίµωξης (επέκταση λοίµωξης) παράγοντες Φαγοκυττάρωση Φυσιολογική µε ικανοποιητική ποσότητα οψωνίνης Μικροβιοκτονία Φυσιολογική σε υγιή νεογνά, ελαττωµένη σε stress Μονοκύτταρα Χηµειοταξία Ελαττωµένη Ελαττωµένη φλεγµονώδης απάντηση Φαγοκυττάρωση Αµφιλεγόµενη Ακαθόριστη Μικροβιοκτονία Αµφιλεγόµενη Ακαθόριστη Τροποποιηµένο από Polin et al, Neonatal sepsis, Adv Pediatr Infect Dis 7:25, O βλεννογόνος του γαστρεντερικού βοµβαρδίζεται από τα µικρόβια και τις πρωτεΐνες των τροφών, ενώ ο αναπνευστικός βλεννογόνος βρίσκεται σε διαρκή απειλή, λόγω της µεταφοράς µικροοργανισµών µε τον εισπνεόµενο αέρα. Αυτοί οι δύο βλεννογόνοι αποτελούν µία 44
45 τεράστια επιφάνεια ανταλλαγής ουσιών µε το εξωτερικό περιβάλλον, το οποίο βρίσκεται συγχρόνως σε κατάσταση διαρκούς προσβολής. (201) Στο βλεννογόνο του γαστρεντερικού συστήµατος η συνοχή των επιθηλιακών κυττάρων είναι εξαιρετικά ισχυρή και επιτυγχάνεται µε τη σύγκλιση των πλάγιων επιφανειών και την ύπαρξη πολυάριθµων δεσµοσωµάτων, ώστε να παρακωλύεται η δίοδος µορίων µεταξύ των κυττάρων. Άλλα µηχανικά µέσα που ενισχύουν τη λειτουργία του βλεννογόνου ως φυσικού φραγµού είναι: η κίνηση των κροσσών στο επιθήλιο του αναπνευστικού συστήµατος, η ροή των υγρών στο ουροποιητικό, η ροή αέρα στους αεραγωγούς, οι εκκρίσεις και η κινητικότητα του εντέρου, που προκαλούν µηχανική αποµάκρυνση. Οι επιθηλιακές επιφάνειες δεν είναι απλώς ένας φυσικός µηχανικός φραγµός αλλά ένας δυναµικός χηµικός φραγµός. Έτσι, το όξινο ph του στοµάχου και τα πεπτικά ένζυµα δηµιουργούν ένα σηµαντικό φραγµό στη λοίµωξη. Επίσης, µία άλλη λειτουργία των επιθηλίων είναι αυτή του µικροβιακού φραγµού. Η φυσιολογική χλωρίδα (αποικισµός των επιθηλίων από µη πυογόνους µικροοργανισµούς) παρέχει προστασία, διότι ανταγωνίζεται τα παθογόνα µικρόβια, µε τον περιορισµό της διάθεσης των θρεπτικών συστατικών και την κατάληψη των θέσεων προσκόλλησής τους στο επιθήλιο, ενώ συγχρόνως παράγει µικροβιακές ουσίες που εµποδίζουν τον αποικισµό άλλων βακτηριδίων. Όταν τα µη παθογόνα µικρόβια της χλωρίδας καταστρέφονται, όπως αυτό µπορεί να συµβεί µετά τη χορήγηση των αντιβιοτικών, συχνά τη θέση τους καταλαµβάνουν παθογόνοι µικροοργανισµοί που προκαλούν λοιµώξεις. Επιφανειακοί επιθηλιακοί φραγµοί στα νεογνά Στα νεογνά οι µηχανισµοί αυτοί είναι ανώριµοι και ανεπαρκείς. Η ανεπαρκής ανάπτυξη του δέρµατος, ιδιαίτερα των πρόωρων νεογνών, οδηγεί στην αυξηµένη διαπερατότητά του, λόγω της ελαττωµένης παραγωγής ελεύθερων λιπαρών οξέων και του αλκαλικού ph. Τα πρόωρα νεογνά παρουσιάζουν ανεπαρκή επιθηλιοποίηση του δέρµατος, γι αυτό και η διαπερατότητά του είναι αυξηµένη. Η συχνή λύση της ακεραιότητας της επιφάνειας του δέρµατος µε φλεβοκεντήσεις διευκολύνει τη διείσδυση των µικροοργανισµών. Η ανωριµότητα του ανοσολογικού και του γαστρεντερικού συστήµατος προδιαθέτει σε λοιµώξεις του γαστρεντερικού, προκαλεί νεκρωτική εντεροκολίτιδα και οδηγεί σε σηψαιµία.. Η φυσιολογική µικροβιακή χλωρίδα αποτελεί έναν ακόµη προστατευτικό φραγµό µαζί µε την ακεραιότητα του δέρµατος και των βλεννογόνων. Η χρήση, ωστόσο, των αντιµικροβιακών φαρµάκων οδηγεί σε διαταραχή της χλωρίδας και υπερανάπτυξη των παθογόνων. Οι βλάβες του αναπνευστικού επιθηλίου µετά από µηχανικό αερισµό και χορήγηση οξυγόνου προδιαθέτουν σε βακτηριακές λοιµώξεις, πνευµονίες και σηψαιµίες. Όταν 45
46 βλάπτεται η ακεραιότητα των επιθηλιακών βλεννογόνιων φραγµών του αναπνευστικού, τότε η αποικισµένη γεννητική οδός µπορεί να µεταδώσει τον στρεπτόκοκκο group B (GBS) µε ακόλουθη πνευµονική λοίµωξη ή γενικευµένη σηψαιµία. Οι προσκολλητίνες είναι µόρια της επιφανείας των µικροβίων, τα οποία διευκολύνουν τη σύνδεση µε τον ξενιστή. Το λιποτοιχοεικό οξύ και οι πρωτεΐνες επιφανείας βοηθούν τον GBS να προσβάλλει το αναπνευστικό επιθήλιο. Η µεγαλύτερη προσκολλητική ικανότητα του GBS τύπου ΙΙΙ στο αναπνευστικό επιθήλιο ευκολύνει τον αποικισµό του και την πρώιµη νεογνική σηψαιµία. (3) Ωστόσο, δεν είναι απαραίτητο να υπάρχει διαταραχή επιθηλιακής δοµής για το συγκεκριµένο µικρόβιο, το οποίο µπορεί να προσβάλει και να καταλάβει ακόµη και ανέπαφα επιθηλιακά κύτταρα µέσω της ακτίνης, όπως αποδεικνύεται πειραµατικά σε καλλιέργειες κυττάρων αναπνευστικού επιθηλίου. (202) Οι κροσσοί του ανώτερου και κατώτερου αναπνευστικού βλεννογόνου βοηθούν στην αποµάκρυνση κάθε παθογόνου µικροοργανισµού. Ανωµαλίες, όπως αυτές στο σύνδροµο Kartagener, επισηµαίνουν το σηµαντικό ρόλο τους. Νεογνά µε χρόνια πνευµονοπάθεια και βρογχεκτασία παρουσιάζουν διαταραχή του τύπου αυτού των κροσσών. Οι ασθενείς, επίσης, µε τραχειοτοµή και παρατεταµένη διασωλήνωση έχουν επηρεασµένη την ακεραιότητα του βλεννογόνιου επιθηλίου. Η βλέννη αποτελεί µία ακόµη ασπίδα προστασίας στο ανοσιακό σύστηµα. Οι γλυκοπρωτεΐνες βλέννης (mucin) αυξάνουν το ιξώδες και προστατεύουν τον βλεννογόνο. To αναπνευστικό επιθήλιο περιέχει βλέννη µε αντιµικροβιακούς παράγοντες, όπως λυσοζύµη, β- defensins 1-3, LL-37, BPI, λακτοφερρίνη, ενεργό οξυγόνο και άζωτο.(28) Επίσης, περιλαµβάνονται στο ανοσιακό σύστηµα των πνευµόνων µακροφάγα, ουδετερόφιλα, µαστοκύτταρα και κύτταρα φυσικοί φονείς (ΝΚ-κύτταρα). Στην κυστική ίνωση η περιεκτικότητα της αναπνευστικής βλέννας σε ΝaCl είναι πολύ σηµαντική, καθώς µειώνεται η αντιµικροβιακή ικανότητα των επιθηλίων, µε αποτέλεσµα τις συχνές και χρόνιες λοιµώξεις. Η διαπλακουντιακή µεταφορά ανοσοσφαιρινών και ορµονών βοηθούν στην ωρίµανση του εντερικού ανοσιακού συστήµατος. Η αδυναµία παραγωγής IgA τις πρώτες µέρες ζωής καθιστά το επιθήλιο του γαστρεντερικού και του αναπνευστικού ευάλωτο στους λοιµογόνους παράγοντες. (203) Οι ανοσοσφαιρίνες και ιδιαίτερα η IgA του µητρικού γάλακτος προάγουν την ανοσία του εντερικού βλεννογόνου. Η προωρότητα, η µη χορήγηση µητρικού γάλακτος και η παράλληλη χορήγηση αντιµικροβιακών φαρµάκων για την αντιµετώπιση συστηµατικής λοίµωξης, µεταβάλλουν τη χλωρίδα του εντέρου, προκαλούν τοπική φλεγµονή και, στη συνέχεια, διεισδυτική λοίµωξη. (204) Τα πρόωρα νεογνά, ως γνωστό, έχουν λιγότερα κύτταρα του Paneth, µε αποτέλεσµα τα πεπτίδια που παράγονται από αυτά, να είναι ελαττωµένα και εποµένως να παρέχουν λιγότερη αντιµικροβιακή προστασία. (28) 46
47 Το σύστηµα του συµπληρώµατος Το συµπλήρωµα είναι το πολυπλοκότερο από τα λεγόµενα συστήµατα πρωτεασών ή συστήµατα ενεργοποίησης (πήξη, ινωδόλυση, συστήµατα κινίνης - καλλικρεΐνης, σύστηµα ρενίνης - αγγειοτενσίνης κ.λπ.), τα οποία, σε στενή συνεργασία και αλληλεξάρτηση µεταξύ τους, συµβάλλουν καθοριστικά στη διατήρηση της οµοιόστασης του οργανισµού. Το σύστηµα του συµπληρώµατος περιλαµβάνει ένα σύνολο διαλυτών και µεµβρανικών πρωτεϊνών, οι οποίες ανάλογα µε τη λειτουργία τους και τη βιολογική αποστολή τους διακρίνονται σε διαλυτές πρωτεΐνες και µεµβρανικές πρωτεΐνες. (205,206) Το σύστηµα του συµπληρώµατος ακολουθεί δύο διαφορετικές οδούς ενεργοποίησης, γνωστές ως η κλασσική και η εναλλακτική οδός. (207,207) Τελευταία, αναγνωρίστηκε και µία επιπλέον οδός, της λεκτίνης, που στη βιβλιογραφία αναγνωρίζεται ως «οδός της µαννόζης» η οποία ενεργοποιείται από τη µαννόζη του τοιχώµατος των µικροβίων και ακολουθεί τα στάδια της ενεργοποίησης της κλασσικής οδού.(209) Η εναλλακτική οδός θεωρείται ότι είναι πιο παλιά και ότι αποτελεί τµήµα της φυσικής ανοσίας, ενώ η κλασσική οδός εµπλέκεται αργότερα µε στόχο την ολοκλήρωση της ειδικής ανοσιακής απάντησης που ξεκινά από το αντίσωµα.(199) Οι περισσότερες πρωτεΐνες και των δύο οδών βρίσκονται σε αδρανή µορφή και ενεργοποιούνται από τα στοιχεία που συµµετέχουν σε προηγούµενα στάδια ενεργοποίησης. Αντίθετα, µερικές πρωτεΐνες όπως ο παράγοντας D, βρίσκονται εξ αρχής σε φάση ενζυµικής δραστηριοποίησης περιµένοντας να δηµιουργηθεί το κατάλληλο υπόστρωµα για να εκδηλώσουν τη δράση τους (208). Και οι δύο οδοί συγκλίνουν προς την C3 πρωτεΐνη που αποτελεί σηµαντικό σηµείο ελέγχου µε τελικό σκοπό το σχηµατισµό της C3 κονβερτάσης. Αυτή είναι µία πρωτεΐνη που συµµετέχει σηµαντικά στην ενεργοποίηση του συµπληρώµατος. (210) Η κλασσική οδός ενεργοποιείται από το σύµπλεγµα αντιγόνου - αντισώµατος παρουσία ιόντων ασβεστίου. Βέβαια, βασικός ρόλος της είναι η αποµάκρυνση των ανοσοσυµπλεγµάτων από την κυκλοφορία. Σε περίπτωση ανεπάρκειας κάποιας πρωτεΐνης αυτής της οδού, µία από τις κύριες επιπτώσεις είναι η ανάπτυξη νόσων που οφείλονται σε καθήλωση ανοσοσυµπλεγµάτων σε ιστούς. (210) Η εναλλακτική οδός αποτελώντας τµήµα της φυσικής ανοσίας µε συµµετοχή στην πρώτη γραµµή άµυνας του οργανισµού ακόµα και χωρίς την παρουσία αντισωµάτων µε ειδικότητα προς το αντιγόνο, έχει τη δυνατότητα της αυτοενεργοποίησης, εάν δηµιουργηθούν οι κατάλληλες συνθήκες. Έτσι, η οδός, ξεκινώντας από τη C3 πρωτεΐνη θα οδηγηθεί στη σύνθεση του κλάσµατος C5 που αποτελεί το σηµείο σύγκλισης και των δύο οδών ενεργοποίησης. Μετά τη δηµιουργία του C3b σχηµατίζεται η κονβερτάση του C5, η οποία προκαλεί διάσπαση του τελευταίου στα τµήµατα C5a, έναν ισχυρό χηµειοτακτικό και ενεργοποιητικό παράγοντα, και το C5b, το οποίο αποτελεί την αφετηρία σχηµατισµού του τελικού συµπλόκου. Έτσι, µετά τη διάσπαση του C5, οι δύο οδοί οδηγούνται στην «τελική 47
48 οδό» που συνιστά τη διαδοχική σύνδεση των παραγόντων C6, C7, C8 και C9 µε την µεµβράνη του ενεργοποιητή. Με αυτόν τον τρόπο σχηµατίζεται ένα πολυµοριακό λιποδιαλυτό σύµπλεγµα, το σύµπλεγµα προσβολής της µεµβράνης (membrane attact complex, MAC). (211) Το σύµπλοκο C5b,6,7, που δηµιουργείται, συνδέεται µε τη µεµβράνη του κυττάρου, ενώ η συνένωση του C8 σ αυτό έχει ως αποτέλεσµα τη βαθύτερη διείσδυση στη λιποειδική στιβάδα, χωρίς όµως να κατορθώνει την πλήρη καταστροφή της κυτταρικής µεµβράνης. Η σύνδεση τελικά του C9 ενεργοποιεί τη δηµιουργία διαµεµβρανικής οπής, η οποία θα οδηγήσει στην καταστροφή του κυττάρου µέσω ωσµωτικής λύσης. (202) Οι κυριότερες βιολογικές δράσεις της ενεργοποίησης του συµπληρώµατος µπορούν να συνοψιστούν στα ακόλουθα (205) 1. συµµετοχή στη διαδικασία της φλεγµονής µε χηµειοτακτική δράση και ενεργοποίηση των λεµφοκυττάρων 2. κυτταρόλυση 3. οψωνινοποίηση και φαγοκυττάρωση και 4. δηµιουργία ανοσοσυµπλεγµάτων. Η σύνθεση του συµπληρώµατος στο έµβρυο. Πολλές είναι οι µελέτες που προσεγγίζουν τη σύνθεση των συστατικών του συµπληρώµατος και ερευνούν το συµπλήρωµα των ενηλίκων, ενώ υπάρχουν στοιχεία για την ποσοτική και ποιοτική διαφοροποίηση από την εµβρυϊκή ηλικία. ( ) Με ραδιοανοσολογική µέθοδο διερευνήθηκε η σύνθεση του C1q στον εµβρυϊκό σπλήνα τη 14η εβδοµάδα. (217,218) Η σύνθεση των C4, C2, C3, η δραστηριότητα και ο ρόλος τους στη δηµιουργία αντισωµάτων διερευνήθηκε την 8η-14η εβδοµάδα, ενώ το ήπαρ θεωρείται το υπεύθυνο όργανο γι αυτή τη λειτουργία. (218) Η σύνθεση του C5 από το ήπαρ και τους πνεύµονες αρχίζει κατά την 8η-9η εβδοµάδα. Το εµβρυϊκό ήπαρ ηλικίας 11 εβδοµάδων παράγει ενεργό αναστολέα της C1 εστεράσης σε ιστικές καλλιέργειες. Το C3 και ο παράγων Β των µονοκυττάρων του οµφαλίου είναι ίδια µε του ενηλίκου, η δε ικανότητα παραγωγής τους σε ερέθισµα, όπως σε λιποπολυσακχαρίδη (LPS), είναι ελλιπής. (219) Μελέτες έχουν δείξει ότι η παραγωγή συστατικών του συµπληρώµατος γίνεται στην εµβρυϊκή ζωή, καθότι βρέθηκε στο αίµα του οµφαλίου λώρου νεογνού C2, ενώ η µητέρα του είχε ανεπάρκεια του C2. (220) Συµπερασµατικά, µπορεί να υπάρχουν δεδοµένα που υποδεικνύουν τη σύνθεση των πρωτεϊνών του συµπληρώµατος στο έµβρυο από τις πρώτες εβδοµάδες ζωής, ενώ συγχρόνως υποδεικνύουν τη διαπλακουντιακή µεταφορά. (211) 48
49 Το συµπλήρωµα στα νεογνά Τα νεογνά έχουν χαµηλά επίπεδα των περισσότερων κλασµάτων του συµπληρώµατος. Αρκετές είναι οι µελέτες που έχουν ασχοληθεί µε το αντικείµενο αυτό. ( ) Οι έγκυες γυναίκες έχουν ελαφρώς αυξηµένα επίπεδα κάποιων κλασµάτων του συµπληρώµατος σε σύγκριση µε αυτά των µη εγκύων (224). Τα επίπεδα του συµπληρώµατος φυσιολογικών τελειόµηνων νεογνών συγκρινόµενα µε εκείνα των µητέρων τους είναι χαµηλότερα (215,216,225,226). Τα κλάσµατα του συµπληρώµατος στο νεογνό προέρχονται από δική τους παραγωγή, καθότι τα µητρικά δεν διέρχονται τον πλακούντα. Σε τελειόµηνα νεογνά η δραστηριότητα του συµπληρώµατος είναι περίπου 50% σε σύγκριση µε των µητέρων τους. Το C3 στα τελειόµηνα είναι 40-60% των επιπέδων των µητέρων αλλά 60-70% των άλλων ενηλίκων. Τα επίπεδα των C3 και C4 στα νεογέννητα είναι 30-50% των τιµών του ενηλίκου και είναι αντιστρόφως ανάλογα της ηλικίας κύησης (120). Αν και τα επίπεδα των κλασµάτων του συµπληρώµατος είτε της κλασσικής είτε της εναλλακτικής οδού στα τελειόµηνα ανέρχονται στο 50% των τιµών του ενηλίκου, τα επίπεδα των C8 και C9 είναι χαµηλότερα, στο 28-10% των τιµών των µητέρων. H κλασσική οδός ανεπαρκεί λιγότερο της εναλλακτικής (227), δεν απαιτεί αντισώµατα για να ενεργοποιηθεί και διαδραµατίζει σηµαντικό ρόλο στην ανοσία, ειδικά στα πρόωρα, που δεν έχουν υψηλά επίπεδα ανοσοσφαιρινών. Μελετήθηκαν τα επίπεδα των πρωτεϊνών του συµπληρώµατος στα έµβρυα και τα πρόωρα νεογνά, όπου τα κλάσµατα C4, C3, C7, C9, οι παράγοντες Β, Ρ και ο αναστολέας της εστεράσης C1 ανιχνεύονται στον ορό των εµβρύων στο τέλος του πρώτου και στην αρχή του δευτέρου τριµήνου (215,216,228,229). Σ αυτή την περίπτωση παρατηρείται τάση αύξησης των επιπέδων των ανωτέρω κλασµάτων του συµπληρώµατος µε την αύξηση της ηλικίας (224). Σποραδικά, όµως, συµβαίνει ακόµη και τελειόµηνα να εµφανίζουν χαµηλότερα επίπεδα C3 και παράγοντα Β από πρόωρα των 30 εβδοµάδων (222). Η καθυστέρηση ενδοµήτριας ανάπτυξης δεν επηρεάζει τα επίπεδα των C3, C4 και του παράγοντα Β, τα οποία φαίνεται ότι εξαρτώνται κυρίως από την ηλικία κύησης και όχι από το βάρος γέννησης (231). 49
50 ΠΙΝΑΚΑΣ 2.2. Ποσοστό (%) των συστατικών του συµπληρώµατος νεογνών σε σχέση µε τα επίπεδα των τιµών των ενηλίκων Συστατικά συµπληρώµατος Τελειόµηνα νεογνά Πρόωρα νεογνά CH AP C1q C C C C5 75 C6 47 C7 67 C9 14 B P H 61 ic3b 55 Remington JS et al, editors: Infectious diseases of the fetus and newborn infant, 3rd ed, Philadelphia, 1990, Saunders, p 25.(232) Oι λειτουργίες του συµπληρώµατος στα νεογνά Η υπολειπόµενη οψωνική δραστηριότητα και η χηµειοταξία των νεογνών οφείλεται στην ανεπάρκεια των κλασµάτων του συµπληρώµατος. Η οψωνική δραστηριότητα σε τελειόµηνα νεογνά έναντι της Ε.Coli ανευρίσκεται ελαττωµένη σύµφωνα µε κάποιους ερευνητές (233) ή φυσιολογική κατ άλλους. (234,235) Ως προς τον σταφυλόκοκκο η οψωνική δραστηριότητα είναι φυσιολογική στα τελειόµηνα, ενώ στα πρόωρα υπάρχουν µελέτες που υποδεικνύουν ότι είναι ελαττωµένη και αυξάνεται ανάλογα µε την ηλικία κύησης. (120,211) Μολονότι τα επίπεδα συµπληρώµατος σε πρόωρα νεογνά είναι χαµηλά, εν τούτοις µπορούν να παράγουν ικανοποιητικά ποσά ενεργοποιηµένων κλασµάτων του συµπληρώµατος, στην έναρξη µιας λοίµωξης. (236) Οι διαταραχές στην άµυνα του νεογνού, όµως, δεν σχετίζονται µόνο µε τα χαµηλά επίπεδα του συµπληρώµατος. Η χηµειοτακτική δραστηριότητα στα τελειόµηνα είναι ελαττωµένη µετά την ενεργοποίηση από ένα µικρόβιο.(237) εν είναι, ωστόσο, δυνατό να φανεί η ελαττωµένη δραστηριότητα τόσο της οψωνικής όσο και της χηµειοτακτικής δραστηριότητας στον ορό του νεογνού, µε µέτρηση των πρωτεϊνών του συµπληρώµατος, διότι η ελάττωση οφείλεται και σε άλλους παράγοντες, 50
51 όπως είναι οι χυµικοί, που συµµετέχουν σε αυτές τις λειτουργίες. Ένας τέτοιος παράγοντας είναι τα χαµηλά επίπεδα της IgM ανοσοσφαιρίνης που έχει το νεογνό, λόγω της ελαττωµένης ενδοµήτριας σύνθεσης και της µη διαπλακουντιακής µεταφοράς. (223) Έτσι, σε λοίµωξη ενός νεογνού από gram αρνητικά µικρόβια, η ελαττωµένη οψωνική δραστηριότητα οφείλεται, αφενός µεν στην ανεπαρκή παραγωγή των IgM αντισωµάτων και αφετέρου στη µη ενεργοποίηση της κλασσικής οδού του συµπληρώµατος -αδυναµία παραγωγής του κλάσµατος C3b, λόγω των χαµηλών επιπέδων της IgM ανοσοσφαιρίνης. (238) Οι µελέτες του συµπληρώµατος στα νεογνά κατέληξαν σε αποτελέσµατα που µερικές φορές είναι αντικρουόµενα. Έτσι, υπάρχει µελέτη η οποία υποδεικνύει ότι υπολείπεται η ικανότητα διαφόρων βακτηριδίων να ενεργοποιήσουν το C3 µέσω της εναλλακτικής και κλασσικής οδού του συµπληρώµατος (211), ενώ άλλη µελέτη υποδεικνύει διαταραχή της δοµής των πρωτεϊνών του συµπληρώµατος, όπως του C3, που συµβάλλει στη δυσλειτουργία του συµπληρώµατος. (239) Μία άλλη µελέτη υποδεικνύει ελαττωµένη την οψωνική δραστηριότητα νεογνών, λόγω ανεπάρκειας του συµπληρώµατος, σε λοίµωξη από το στρεπτόκοκκο 1a της οµάδας B, που ενεργοποιεί την κλασσική οδό χωρίς τη συµµετοχή αντισωµάτων. (240) Συµπερασµατικά, διαπιστώθηκε ότι ένα µέρος της ελαττωµένης οψωνικής και χηµειοτακτικής δραστηριότητας στα νεογνά οφείλεται και στην ανεπάρκεια του συµπληρώµατος. Ο ρόλος του συµπληρώµατος στη νεογνική άµυνα Γενετικά καθορισµένη ανεπάρκεια των κλασµάτων του συµπληρώµατος ανευρίσκεται σε ανθρώπους µε αυξηµένη τάση λοιµώξεων. Το συµπλήρωµα συµµετέχει στην άµυνα εναντίον βακτηρίων (241), ιών (237) και µυκήτων. (242) Συµµετέχει, ακόµη, σε λοιµώξεις εντοπισµένες, όπως πνευµονία, µηνιγγίτιδα, αλλά και γενικευµένες, όπως η σηψαιµία. Τα νεογνά, κυρίως τα πρόωρα, έχουν χαµηλά επίπεδα των περισσότερων κλασµάτων της κλασσικής και της εναλλακτικής οδού του συµπληρώµατος, αν και η κλασσική οδός ανεπαρκεί σε µικρότερο βαθµό σε σύγκριση µε την εναλλακτική οδό. (227) Η εναλλακτική οδός, επειδή δε χρειάζεται την παρουσία αντισωµάτων για να ενεργοποιηθεί, διαδραµατίζει σηµαντικό ρόλο στη µη ειδική ανοσία, ειδικά στα πρόωρα που έχουν χαµηλά επίπεδα ανοσοσφαιρινών. Τα κλάσµατα του συµπληρώµατος στο νεογέννητο προέρχονται από ενδογενή παραγωγή, επειδή δε διέρχονται τον πλακούντα. Η συγκέντρωση των κλασµάτων του συµπληρώµατος της εναλλακτικής οδού σε τελειόµηνα είναι ίση µε αυτή των ενηλίκων. Έτσι, χαµηλά επίπεδα ολικού αιµολυτικού συµπληρώµατος σχετίζονται µε φτωχή έκβαση και µεγαλύτερη θνητότητα στα σηψαιµικά νεογνά (243), ενώ µελέτη αποδεικνύει ότι, όταν χορηγείται το κλάσµα C9 σε νεογνό, η βακτηριοστατική ικανότητα του νεογνού εναντίον στελεχών του Ε. Coli γίνεται φυσιολογική. (229) 51
52 Συµπερασµατικά, η προδιάθεση των νεογνών στη λοίµωξη οφείλεται κατά ένα µεγάλο µέρος σε ανεπάρκειες του συµπληρώµατος στα νεογνά, λόγω της γενετικά προκαθορισµένης ανεπάρκειας των κλασµάτων του συµπληρώµατος Το σύστηµα φαγοκυττάρωσης (πολυµορφοπύρηνα - µονοκύτταρα) Πολυµορφοπύρηνα Τα ουδετερόφιλα κοκκιοκύτταρα, τα οποία ονοµάζονται και πολυµορφοπύρηνα λόγω του πολυλοβώδους πυρήνα τους, παράγονται στο µυελό των οστών, στη διάρκεια της αιµοποίησης, από το πολυδύναµο αρχέγονο κύτταρο (stem cell), µε µία διαδικασία που διαρκεί ηµέρες. (244) Στη συνέχεια, απελευθερώνονται στην κυκλοφορία, όπου παραµένουν για 7-10 ώρες πριν µεταναστεύσουν στους ιστούς, όπου έχουν µικρή διάρκεια ζωής. Ως απάντηση σε πολλούς τύπους λοίµωξης, ο µυελός των οστών απελευθερώνει µεγαλύτερο αριθµό ουδετεροφίλων προς την κυκλοφορία, µε αποτέλεσµα την αύξηση του αριθµού των κυκλοφορούντων ουδετεροφίλων (λευκοκυττάρωση), γεγονός που αποτελεί κλινική ένδειξη λοίµωξης. (245) Στη διάρκεια της οξείας φλεγµονής, η αύξηση του αριθµού των ουδετεροφίλων στο περιφερικό αίµα οφείλεται όχι µόνο στην αυξηµένη απελευθέρωσή τους από το µυελό των οστών αλλά και σε κινητοποίηση των περιθωριοποιηµένων ουδετεροφίλων (marginating pool). Από το µυελό εξέρχονται ώριµα ουδετερόφιλα και η έξοδός τους καθορίζεται από την πλαστικότητα που διαθέτουν, ώστε να µπορούν να περάσουν τα µεσοθηλιακά διαστήµατα των µυελικών φλεβοκόλπων. Όταν, όµως, η φλεγµονή εξελιχθεί, είναι δυνατή η απελευθέρωση από το µυελό πιο άωρων µορφών ουδετεροφίλων, µία κατάσταση που µοιάζει µε οξεία µυελογενή λευχαιµία και γι αυτό ονοµάζεται λευχαιµοειδής αντίδραση. Μονοκύτταρα Το σύστηµα των µονοκυττάρων φαγοκυττάρων (ΜΦ) αποτελείται από κύτταρα διάσπαρτα κατανεµηµένα σε όλο το σώµα και περιλαµβάνει τόσο τα µονοκύτταραυ του περιφερικού αίµατος όσο και τα µακροφάγα που βρίσκονται σε διάφορους ιστούς. (246) Τα µονοκύτταρα του αίµατος προέρχονται από πρόδροµες µορφές του µυελού των οστών και, αφού παραµείνουν στο αίµα αρκετές µέρες, διαφοροποιούνται και, εν συνεχεία, µεταναστεύουν στους ιστούς ως µακροφάγα. Τα µακροφάγα του λιπώδους ιστού παράγουν προφλεγµονώδεις κυτταροκίνες όπως ο TNF- α και η IL-6. (247,248) Έτσι, τα µονοκύτταρα συνθέτουν και εκκρίνουν µεγάλο αριθµό προϊόντων που συµµετέχουν στη διαδικασία της 52
53 φλεγµονής. Τα προϊόντα αυτά περιλαµβάνουν πολυπεπτιδικές ορµόνες, συστατικά του συµπληρώµατος, κυτταροκίνες, παράγοντες συγκόλλησης, ένζυµα, πρωτεΐνες της εξωκυττάριας ουσίας και βιοδραστικά ολιγοπεπτίδια και λιπίδια. Κύρια προϊόντα, όπως είναι τα πολυπεπτίδια, η IL-1, η IFN-α και ο παράγοντας νέκρωσης του όγκου α (TNF- α) συντίθενται σε παρόµοιες συγκεντρώσεις από τα µονοκύτταρα των νεογνών και των ενηλίκων. (246) Εκτός των ανωτέρω, άλλα µόρια όπως IFNγ, IL-8, IL-10 και G-CSF, πρωτεΐνες του εξωκυττάριου υλικού, όπως η φιµπρονεκτίνη και τα βιοδραστικά λιπίδια (π.χ. τα λευκοτριένια Β4), συντίθενται σε µειωµένες συγκεντρώσεις από τα νεογνικά µονοκύτταρα. Τα φαγοκύτταρα έχουν την ικανότητα να καταστρέφουν το µεγαλύτερο ποσοστό των µικροοργανισµών που εισέρχονται στο κυτταρόπλασµά τους, τους εγκλωβίζουν στα ενδοκυτταροπλασµατικά κενοτόπια (intracytoplasmic vacuoles) και τους θανατώνουν µε τη δράση οργανικών και ανόργανων ουσιών. (249) Στα εξ επαγγέλµατος φαγοκύτταρα (professional phagocytes), για τα οποία η φαγοκυττάρωση είναι η κύρια λειτουργία τους, ανήκουν το σύστηµα των µονοκυττάρων µακροφάγων, τα κοκκιοκύτταρα, ιδίως τα ουδετερόφιλα και σε µικρότερο βαθµό τα ηωσινόφιλα.(250) Τα φαγοκύτταρα παράγουν αρκετούς µεσολαβητές και πρωτεΐνες που συνεισφέρουν στην καταστροφή των µικροβίων. Οι συνδέτες περιλαµβάνουν συστατικά που προέρχονται από το µονοπάτι του αραχιδονικού οξέος, όπως τα λευκοτριένια Β4, ενώ οι πρωτεΐνες περιλαµβάνουν τη λυσοζύµη, τη λακτοφερρίνη, την τρανσφερρίνη καθώς και αντιµικροβιακά πεπτίδια, όπως οι ντιφενσίνες (defensins). (44) Τα φαγοκύτταρα έχουν περιγραφεί στο λεκιθικό σάκο, τον πνεύµονα και το ήπαρ, πολύ πριν εγκαθιδρυθεί η ανάπτυξη των µονοκυττάρων από το µυελό των οστών. (251) Τα εµβρυϊκά φαγοκύτταρα του ήπατος και του πνεύµονα έχουν την ικανότητα να πολλαπλασιάζονται µόνα τους. Τα φαγοκύτταρα τοποθετούνται στα κολπώδη τριχοειδή αγγεία του σπλήνα, του ήπατος και των λεµφαδένων. Η στρατηγική αυτή τοποθέτησή τους επιτρέπει την άµυνα του ξενιστή ενάντια στα παθογόνα ακριβώς κάτω από τους επιθηλιακούς φραγµούς του δέρµατος, του γαστρεντερικού και αναπνευστικού συστήµατος και στις θέσεις διήθησης του αίµατος. (252) Κύρια λειτουργία των ΜΦ είναι η φαγοκυττάρωση (αποτελούν το δεύτερο µεγάλο φαγοκυτταρικό πληθυσµό µετά τα ουδετερόφιλα πολυµορφοπύρηνα), όµως παράλληλα δρουν ως ρυθµιστικά κύτταρα στην έκφραση και πρόκληση της χυµικής και κυτταρικής ανοσίας παρουσιάζοντας το αντιγόνο στα Τ λεµφοκύτταρα (αντιγονοπαρουσιαστικό κύτταρο) και εκκρίνοντας κυτταροκίνες, οι οποίες συµµετέχουν ποικιλοτρόπως στην ανοσιακή απάντηση. (13) Οι µεσολαβητές που προέρχονται από τα µακροφάγα ξεκινούν τη φλεγµονώδη αντίδραση και επιστρατεύουν τα ουδετερόφιλα. Πρόκειται για τις κυτταροκίνες TNF-α, IL-1, IL-12, 53
54 IFNγ, GM-CSF, G-CSF, τις χηµειοκίνες, τα χηµειοτακτικά πεπτίδια, τις φλεγµονώδεις πρωτεΐνες των µακροφάγων κ.ά.. (80) Τέλος, τα µακροφάγα, όπως και τα ουδετερόφιλα, παράγουν µεταβολίτες του οξυγόνου (αναπνευστική έκρηξη) και διαθέτουν διάφορα ένζυµα απαραίτητα για την ενδοκυττάρια καταστροφή παθογόνων µικροοργανισµών. (253) Α. Τα ουδετερόφιλα στην εµβρυϊκή και νεογνική περίοδο 1. H ανάπτυξη των κυττάρων του αίµατος στο έµβρυο Στο έµβρυο, ανευρίσκονται κοκκιοκύτταρα στο ήπαρ από τις πρώτες εβδοµάδες της κύησης, ο αριθµός των οποίων αυξάνεται µετά τη 15η εβδοµάδα. Ο µυελός των οστών αποικίζεται µε προδροµικά κύτταρα περίπου τη 15η-16η εβδοµάδα της κύησης. Ώριµα ουδετερόφιλα δεν ανευρίσκονται στο εµβρυϊκό ήπαρ και στο µυελό των οστών έως τη 12η 16η εβδοµάδα κύησης. (254) Εµβρυοσκοπικές µελέτες έδειξαν ότι πολύ λίγα κοκκιοκύτταρα κυκλοφορούν στο αίµα του εµβρύου στα αρχικά στάδια της κύησης (<1000/mm3). (210) Tα ραβδοπύρηνα και τα ώριµα ουδετερόφιλα εµφανίζονται µόλις την 9η µε 10η εβδοµάδα της κύησης. (13) Με την πρόοδο της κύησης αυξάνεται ο ολικός αριθµός των λευκών, αλλά ο αριθµός των ουδετεροφίλων παραµένει χαµηλός και τα λεµφοκύταρα αποτελούν τον κυριότερο πληθυσµό των λευκοκυττάρων. Οι χαµηλές τιµές των λευκοκυττάρων συνοδεύονται από υψηλές συγκεντρώσεις προδροµικών κυττάρων στο εµβρυϊκό αίµα. Πιθανή εξήγηση για το φαινόµενο αυτό είναι ότι τα προδροµικά κύτταρα µεταναστεύουν από το ένα αιµοποιητικό όργανο (ήπαρ) στο άλλο (µυελός των οστών), µε αποτέλεσµα υψηλές συγκεντρώσεις, χωρίς όµως αυξηµένο συνολικό αριθµό ουδετεροφίλων. (199,255) 2. Κινητική των ουδετεροφίλων των νεογνών Οι πληροφορίες µας σχετικά µε την κινητική των ουδετεροφίλων και την ποσοτική ανεπάρκεια της µυελοποίησης στα νεογνά προέρχονται από πειραµατικές µελέτες σε αρουραίους. Οι µελέτες αυτές αποδεικνύουν ότι οι νεογέννητοι αρουραίοι έχουν µικρότερη δεξαµενή πολλαπλασιασµού ουδετεροφίλων στο µυελό των οστών (Colony Forming Units- Granulocyte Macrophage, CFU-GM) συγκριτικά µε τους ενηλίκους, ενώ ο δείκτης πολλαπλασιασµού των CFU-GM είναι αυξηµένος (75% έναντι 25%). (13) Επιπλέον, οι µυελικές δεξαµενές των ουδετεροφίλων είναι ελαττωµένες (75% έναντι 100%), µε αποτέλεσµα τα νεογνά να αδυνατούν να ανταποκριθούν µε λευκοκυττάρωση σε περίπτωση λοίµωξης, λόγω χαµηλών αποθεµάτων ουδετεροφίλων και ανεπαρκούς παραγωγής νέων. (256,257) 54
55 3. Αριθµός των ουδετεροφίλων του περιφερικού αίµατος και διαταραχές τους στα νεογνά. Στα πρόωρα αλλά και στα τελειόµηνα, ο ολικός αριθµός των λευκοκυττάρων αυξάνεται τις πρώτες 12 ώρες µετά τη γέννηση, ακολουθεί βαθµιαία πτώση και σταθεροποίηση την 4η ηµέρα ζωής. Ο λευκοκυτταρικός τύπος είναι πολυµορφοπυρηνικός τις τρεις πρώτες ηµέρες ζωής και γίνεται λεµφοκυτταρικός µετά την 3η έως την 7η ηµέρα. (101,258) Ο αριθµός των λευκών αιµοσφαιρίων είναι µικρότερος στα πρόωρα νεογνά από ό,τι στα τελειόµηνα. Τις τρεις πρώτες µέρες της ζωής, µορφολογικά υπάρχει στροφή προς τα αριστερά και µάλιστα είναι δυνατή η παρουσία προµυελοκυττάρων και µυελοκυττάρων στο περιφερικό αίµα. Μετά την 3η ηµέρα της ζωής η παρουσία των ραβδοπύρηνων είναι ενδεικτική λοίµωξης (255). Η λευκοκυττάρωση των πρώτων ηµερών αποδίδεται στα αυξηµένα επίπεδα του G- CSF. Στα φυσιολογικά νεογνά και ιδίως στα πρόωρα παρατηρούνται υψηλότερα επίπεδα G- CSF, αν και δεν βρέθηκε συσχέτιση µεταξύ του αριθµού των ουδετεροφίλων και των επιπέδων του G-CSF στο πλάσµα των νεογνών. (259) ιάφορες καταστάσεις στην περιγεννητική περίοδο, όπως είναι η ασφυξία, η εγκεφαλική αιµορραγία, οι σπασµοί, το σύνδροµο εισρόφησης µηκωνίου, ο πνευµοθώρακας, ο εργώδης τοκετός, η αιµολυτική νόσος του νεογνού καθώς και η υπέρταση ή ο πυρετός της µητέρας, επιδρούν στην κινητική των ουδετεροφίλων, προκαλώντας αύξηση ή ελάττωσή τους. (101) Η συχνότερη διαταραχή του αριθµού των ουδετεροφίλων στα νεογνά και κυρίως στα πρόωρα είναι η ουδετεροπενία. (260) Η συχνότερη αιτία της διαταραχής αυτής είναι οι λοιµώξεις, αλλά για την εµφάνισή της ενοχοποιούνται περισσότεροι του ενός µηχανισµοί: 1) Ελαττωµένες αποθήκες προδροµικών κυττάρων, που λειτουργούν στο µέγιστο βαθµό. 2) ιαταραχή στην έκφραση του γονιδίου του υπεύθυνου για την παραγωγή διαφόρων αιµοποιητικών παραγόντων. Επίσης, βρέθηκε ότι σε καταστάσεις αυξηµένων αναγκών τα φαγοκύτταρα των νεογνών παράγουν µικρότερο ποσοστό GM-CSF και G-CSF. (261) Η θνησιµότητα των νεογνών µε ουδετεροπενία είναι µεγάλη ανεξαρτήτως αιτιολογίας και είναι υψηλότερη σε απόλυτο αριθµό ουδετεροφίλων µικρότερο των 500/mm 3.(13) υσµενές προγνωστικό στοιχείο είναι ο συνδυασµός ουδετεροπενίας και αυξηµένης σχέσης αώρων/ολικά ουδετερόφιλα. 4. ιαταραχές της λειτουργικότητας των ουδετεροφίλων των νεογνών. Η λειτουργικότητα των ουδετεροφίλων έχει µελετηθεί και έχουν περιγραφεί ποικίλες διαταραχές τους, ιδιαίτερα σε πρόωρα και σε νεογνά µε stress (λοίµωξη, ΣΑ, περιγεννητική ασφυξία κ.ά.). Στη συνέχεια, θα περιγραφούν οι διαταραχές αυτές, οι οποίες αυξάνουν την ευαισθησία των νεογνών στις µικροβιακές λοιµώξεις. (13) Αυτές είναι οι εξής: Ι. Προσκόλληση 55
56 ιαταραχή στην ικανότητα των ουδετεροφίλων να προσκολλώνται στα ενδοθηλιακά κύτταρα, µπορεί να προκύψει, κατ αρχάς, από ανεπάρκεια της έκφρασης της L-σελεκτίνης και των β 2 ιντεγκρινών στην επιφάνειά τους, εφόσον στα ουδετερόφιλα φυσιολογικών τελειόµηνων νεογνών έχει βρεθεί ελαττωµένη έκφραση της L-σελεκτίνης. (262) Αντίθετα, στα φυσιολογικά πρόωρα τα επίπεδά της βρέθηκαν υψηλότερα απ ό,τι στα φυσιολογικά τελειόµηνα. (263) Τέλος, διαταραχές στην αλληλεπίδραση της Ρ και Ε- σελεκτίνης µε τους αντι-υποδοχείς τους στην επιφάνεια των λευκοκυττάρων εµπλέκονται στην ανεπαρκή προσκόλληση των ουδετερόφιλων των νεογνών στο ενδοθήλιο. (210) ΙΙ. Χηµειοταξία Τα ουδετερόφιλα στα νεογνά παρουσιάζουν διαταραχές της κινητικότητας, οι οποίες σχετίζονται µε ανωµαλία της δοµής και της λειτουργικότητάς τους. Η ακτίνη είναι ένας σηµαντικός παράγοντας που ρυθµίζει την αλλαγή του σχήµατος και την κινητική συµπεριφορά των ουδετεροφίλων. Γι αυτό, η ελαττωµένη συγκέντρωση και ο πολυµερισµός της F-ακτίνης στα νεογνά ενοχοποιούνται για τις διαταραχές της χηµειοταξίας. (264) Επίσης, η σύσπαση των µικροϊνιδίων του κυτταροσκελετού των ουδετεροφίλων εξαρτάται από τα ενεργειακά αποθέµατα του ΑΤΡ καθώς και από την ενδοκυττάρια συγκέντρωση του ασβεστίου. Στα ουδετερόφιλα των νεογνών, η διαταραχή στη χηµειοταξία αποδίδεται στην αδυναµία τους να αυξήσουν επαρκώς το ενδοκυττάριο ασβέστιο µετά από χηµειοτακτικό ερεθισµό, άποψη µη αποδεκτή από όλους τους ερευνητές, καθώς και στα χαµηλά αποθέµατα σε ΑΤΡ. (265) Στη διαταραχή της χηµειοταξίας συµβάλλει, επίσης, η ανεπαρκής παραγωγή και παρουσία χηµειοτακτικών παραγόντων στον ορό των νεογνών. Η LTB4 παράγεται από τα ουδετερόφιλα και δρα ως χηµειοτακτικός παράγοντας, διεγείροντας τη λειτουργία τους. Η απελευθέρωση της LTB4 είναι ελαττωµένη (266), ενώ η χηµειοτακτική απάντηση των ουδετεροφίλων στη LTB4 in vitro είναι χαµηλότερη στα υγιή τελειόµηνα νεογνά απ ό,τι στους ενηλίκους. (267) Ακόµη, τα µόρια προσκόλλησης παίζουν σηµαντικό ρόλο στη µετανάστευση των ουδετεροφίλων. Στα πρόωρα και στα τελειόµηνα νεογνά, η χηµειοταξία µετά από διέγερση καθώς και η έκφραση των MAC-1 (CR3) στην επιφάνεια των ουδετερόφιλων των νεογνών είναι ελαττωµένη σε σχέση µε τους ενηλίκους. (268) Στη διαταραχή της χηµειοταξίας συντελεί, τέλος η ανεπαρκής έκφραση και άλλων µορίων προσκόλλησης που συµβάλλουν στην κινητικότητά τους. (210) ΙΙΙ. Oψωνινοποίηση και φαγοκυττάρωση ιαπιστώθηκε ότι τα ουδετερόφιλα στα φυσιολογικά τελειόµηνα αλλά και στα νεογνά µε stress φαγοκυτταρώνουν φυσιολογικά οψωνινοποιηµένους στρεπτόκοκκους και Candida Albicans, ενώ στα πρόωρα παρατηρήθηκε σηµαντική ελάττωση της φαγοκυττάρωσης της Candida, µε φυσιολογική όµως φαγοκυτταρική ικανότητα για τα µικρόβια (S. Aureus). (269) 56
57 Για την οψωνινοποίηση και την φαγοκυττάρωση είναι απαραίτητοι οι υποδοχείς του συµπληρώµατος CR1 και CR3 (CD11b) στην επιφάνεια των ουδετεροφίλων. Οι απόψεις για την έκφραση των υποδοχέων του συµπληρώµατος και την ικανότητα των ουδετεροφίλων να αυξάνουν την έκφρασή τους είναι αντικρουόµενες σχετικά µε τα τελειόµηνα και τα πρόωρα.(223) Επιπλέον, η ελαττωµένη έκφραση των FcγR υποδοχέων, οι οποίοι συµµετέχουν στη φαγοκυττάρωση, συµβάλλει στην ελαττωµένη µικροβιοκτόνο ικανότητα των νεογνικών ουδετεροφίλων στα πρόωρα. (270) Η χαµηλή φαγοκυττάρωση, κυρίως στα πρόωρα, αποδίδεται επίσης και στην ανεπάρκεια του νεογνικού ορού σε οψωνίνες. Γενικά, η φαγοκυττάρωση είναι φυσιολογική στα φυσιολογικά τελειόµηνα και ελαττωµένη στα πρόωρα νεογνά. (271) ΙV. Eνδοκυττάρια µικροβιοκτονία Περιλαµβάνει την αναπνευστική έκρηξη των ουδετεροφίλων και την αποκοκκίωση από τα λυσοσσωµατικά ένζυµά τους. α. Οξειδωτικός µηχανισµός Ο οξειδωτικός µηχανισµός (αναπνευστική έκρηξη) έχει µελετηθεί µε διάφορες µεθόδους και τα αποτελέσµατα είναι αντιφατικά. Στο υγιές τελειόµηνο νεογνό, ο οξειδωτικός µηχανισµός αναφέρεται παρόµοιος µε εκείνον των ενηλίκων (272), ελαττωµένος (273) ή αυξηµένος. (274) Στο φυσιολογικό πρόωρο νεογνό, βρέθηκε ότι η αναπνευστική έκρηξη των ουδετεροφίλων υπολείπεται αυτής των τελειοµήνων (275), που είναι παρόµοια µε των ενηλίκων. (275) Φαίνεται ότι ο πληθυσµός των ουδετεροφίλων των νεογνών είναι ετερογενής και ότι µόνο µικρό ποσοστό κυττάρων έχει ικανοποιητικά ανεπτυγµένους οξειδωτικούς µηχανισµούς, δηλαδή το σύστηµα της οξειδάσης του NADP. (276) Επιπλέον, ο οξειδωτικός µηχανισµός των ουδετεροφίλων επηρεάζεται από τη λοίµωξη, χωρίς όµως να έχει διευκρινιστεί πλήρως αυτή η επίδραση. Ο Glesser και συν (1996) διαπίστωσαν αύξηση της αναπνευστικής έκρηξης σε νεογνά µε αύξηση της PCR, γεγονός που αποδόθηκε στα αυξηµένα επίπεδα διαφόρων κυτταροκινών (ΤΝF, IL-1β, G-CSF), οι οποίες παράγονται από τη λοίµωξη(277). Σε µελέτη, όµως, της Drossοu και συν (1997) η αναπνευστική έκρηξη διαπιστώθηκε ότι ελαττώνεται ακόµη περισσότερο στα πρόωρα και τα τελειόµηνα νεογνά µε σηψαιµία. (278) β. Αποκοκκίωση Στα νεογνά, η ενδοκυττάρια µικροβιοκτονία µε µηχανισµούς ανεξάρτητους του οξυγόνου (αν και ένζυµα που περιέχονται στα κοκκία, όπως η µυελοϋπεροξειδάση, συµµετέχουν στην αναπνευστική έκρηξη) πιθανόν είναι ελαττωµένηαυτό αποδίδεται στη χαµηλή συγκέντρωση των διαφόρων παραγόντων στα κοκκία των λυσσοσωµατίων που οδηγεί σε διαταραχές αποκοκκίωσης. (279) Οι Ambruso και συν (1979) απέδειξαν διαταραχή στην αποκοκκίωση, η 57
58 οποία εκτιµήθηκε µε την εξωκυττάρωση της µυελοϋπεροξειδάσης και της λυσοζύµης από ουδετερόφιλα τελειόµηνων νεογνών µετά από διέγερση, αλλά και ελαττωµένη συγκέντρωση λυσοζύµης και λακτοφερίνης στα ειδικά κοκκία των νεογνικών ουδετεροφίλων. (280, 281) Παρόµοια, οι Βektas και συν (1990) (269) βρήκαν ότι η εξωκυττάρωση της ελαστάσης και της λακτοφερίνης είναι ελαττωµένη στα φυσιολογικά πρόωρα νεογνά. Νεότερη µελέτη έδειξε ότι τα ουδετερόφιλα των τελειόµηνων νεογνών διαθέτουν το είδος των κοκκίων που υπάρχουν στα ουδετερόφιλα των ενηλίκων και ότι είναι ικανά να κινητοποιούν και να απελευθερώνουν διάφορα λυσσοσωµατικά ένζυµα, παρότι παρουσιάζουν δοµικές διαφορές. (282) Β. Τα µονοκύτταρα στα νεογνά Τα µονοκύτταρα και τα φαγοκύτταρα διαδραµατίζουν σηµαντικό ρόλο στην άµυνα του εµβρύου και του νεογνού συµβάλλοντας στη θανάτωση ενδοκυττάριων µικροοργανισµών (Listeria Monocytogenes) καθώς και στην εξουδετέρωση ιών, όπως ο ιός του έρπητα. (283) Η µελέτη των µονοκυττάρων φαγοκυττάρων κατά τη νεογνική περίοδο είναι περιορισµένη λόγω του ελάχιστου αριθµού διαθέσιµων δειγµάτων πληθυσµών µακροφάγων. Η ανάλυση παρασκευασµάτων µυελού των οστών από πρόωρα και τελειόµηνα βρέφη έδειξε ότι δεν υπάρχουν σηµαντικές διαφορές στις µετρήσεις µονοπύρηνων φαγοκυττάρων του µυελού. (199) Υπάρχει µία σχετική µονοκυττάρωση κατά τη διάρκεια της νεογνικής περιόδου και ο αριθµός των µονοκυττάρων στο περιφερικό αίµα είναι υψηλότερος κατά τις πρώτες 24 ώρες της ζωής και µειώνεται κατά τη διάρκεια του πρώτου µήνα. Η ολική συγκέντρωση κυττάρων του µυελού των οστών είναι κατά µέσο όρο 1,36 Χ κύτταρα/l την 1η και φθίνει στα 3,5 Χ κύτταρα/l την 9η ηµέρα της ζωής. (44) Στη νεογνική ηλικία, το µονοκυτταρικό φαγοκυτταρικό σύστηµα είναι αρκετά ανεπτυγµένο. (284) Η χηµειοταξία των νεογνικών µονοκυττάρων είναι ελαττωµένη, (285) ενώ η φαγοκυττάρωση, η αναπνευστική έκρηξη και η ενδοκυττάρια µικροβιοκτονία στα τελειόµηνα νεογνά είναι παρόµοια µε αυτή των ενηλίκων, παρά τη µειωµένη έκφραση διαφόρων επιφανειακών µορίων προσκόλλησης. (286) Η µετανάστευση των µονοκυττάρων φαγοκυττάρων έχει µελετηθεί σε αίµα οµφαλίου λώρου και σε περιφερικό αίµα νεογνών, σε σύγκριση µε τα µονοκύτταρα περιφερικού αίµατος ενηλίκων. Στις περισσότερες αναφορές η τυχαία κίνηση των µονοκυττάρων στο αίµα οµφαλίου λώρου φαίνεται να είναι ισοδύναµη µε αυτή των ενηλίκων. Αντίθετα, αρκετοί ερευνητές έχουν αναφέρει µειωµένη κατευθυνόµενη κίνηση των µονοκυττάρων που αποµονώθηκαν από αίµα οµφαλίου λώρου και αίµα νεογνών σε σύγκριση µε των ενηλίκων.(283,287,288) Οι ιδιότητες προσκόλλησης των εµβρυϊκών και νεογέννητων µονοκυττάρων έχουν µελετηθεί σε ελάχιστο βαθµό. Αρκετοί ερευνητές έχουν αναφέρει ανεπάρκεια προσκόλλησης των νεογνικών ουδετεροφίλων σε ενδοθηλιακά κύτταρα ως αποτέλεσµα της µειωµένης 58
59 έκφρασης ιντεγκρινών και L-σελεκτίνης καθώς και του ισχυρού κυτταροσκελετού που εµποδίζει την ανακατανοµή των προσκολληµένων περιοχών. (199,283,289) Οι αναφορές διαφέρουν όσον αφορά τη συστατική και διεγερµένη έκφραση της ΙCAM-1 στα νεογνικά ουδετερόφιλα. Επιπλέον, µελέτες έδειξαν ότι τα ουδετερόφιλα των νεογνών αποτυγχάνουν στη θετική ρύθµιση της επιφανειακής έκφρασης της ΙCAM-1 σε αντίθεση µε το βαθµό που το κάνουν τα ουδετερόφιλα ενηλίκων ως απόκριση σε χηµειοτακτικά ερεθίσµατα. (290) Η παραγωγή της IFN-γ και η απάντηση των µονοκυττάρων φαγοκυττάρων στην εξωγενή χορήγηση IFN-γ είναι, ωστόσο, ελαττωµένη. Ο τρόπος µε τον οποίο τα νεογνικά φαγοκύτταρα των ιστών θανατώνουν µικρόβια, παράσιτα και ιούς καθώς και ο τρόπος µε τον οποίο αυτά ενεργοποιούν ή συνεργάζονται µε κυτταροκίνες δεν έχει ακόµη διευκρινισθεί.(210) Γενικά, η αντιµικροβιακή ικανότητα των νεογνικών φαγοκυττάρων είναι ικανοποιητική, ενώ υπολείπεται η ικανότητα ενδοκυττάριας καταστροφής των ιών. (246,291) Μόρια προσκόλλησης Το σύνολο των υποδοχέων που µεσολαβούν στην προσκόλληση των κυττάρων µε άλλα κύτταρα ή µε τη θεµέλια ουσία αποκαλούνται µε το γενικό όρο µόρια προσκόλλησης. Αυτά είναι εξειδικευµένοι διαµεµβρανικοί υποδοχείς που αναγνωρίζουν είτε ανάλογους άλλους υποδοχείς είτε απλούστερα µόρια στην επιφάνεια των κυττάρων και της θεµέλιας ουσίας. Είναι, µε άλλα λόγια, µία ετερογενής οµάδα πρωτεϊνών της κυτταρικής µεµβράνης που έχουν ως κύρια λειτουργία την προσκόλληση, την επικοινωνία, τη συνεργασία και τη µετακίνηση των κυττάρων. (13) Οι αλληλεπιδράσεις των κυττάρων µεταξύ τους αλλά και µε τη θεµέλια ουσία µέσω των µορίων προσκόλλησης είναι καθοριστικές για την ανάπτυξη, την οργάνωση και τη λειτουργία των ιστών του οργανισµού. Ποικίλες φυσιολογικές λειτουργίες αλλά και παθολογικές καταστάσεις, όπως η φλεγµονή και η µετάσταση των νεοπλασµατικών κυττάρων επιτελούνται µέσω αυτών των µορίων. (199) Ανάλογα µε τη δοµή τους κατατάσσονται σε πέντε οικογένειες, ενώ υπάρχουν κάποια µόρια που παραµένουν αταξινόµητα. Οι οικογένειες που έχουν περιγραφεί είναι: α) οι κατχερίνες (Ε-κατχερίνη, Ν-κατχερίνη), β) η υπεροικογένεια των ανοσοσφαιρινικών υποδοχέων (ICAM-1, ICAM-2, ICAM-3, VCAM-1), γ) οι ιντεγκρίνες (LFA-1, Mac1, VLA- 4, VLA-5), δ) οι σελεκτίνες (P-selectin, L-selectin, E-selectin), ε) οι σιαλοβλεννίνες (MadCAM-1, GlyCAM-1) και στ) τα αταξινόµητα (CD44). (292) O ρόλος των µορίων προσκόλλησης στις αλληλεπιδράσεις των λευκοκυττάρων µε το ενδοθήλιο πραγµατοποιείται στα παρακάτω στάδια: 1) ενεργοποίηση του ενδοθηλίου, 2) αρχική προσκόλληση ή κύλισµα των λευκοκυττάρων στο ενδοθήλιο, 3) ενεργοποίηση των λευκοκυττάρων, 4) ισχυρή προσκόλληση των λευκοκυττάρων στο ενδοθήλιο και 5) διαπίδυση λευκών. (292) 59
60 Μία άλλη άποψη της αλληλεπίδρασης των λευκοκυττάρων και του ενδοθηλίου είναι η κυκλοφορία και ο εποικισµός των λεµφοκυττάρων που συγκεντρώνει τα λεµφοκύτταρα στις περιοχές µε τη µεγαλύτερη προσκολλητικότητα. Επίσης, τα λευκοκύτταρα παρουσιάζουν τη χηµειοταξία, ιδιότητα που τα συγκεντρώνει στην περιοχή µεγαλύτερης συγκέντρωσης χηµειοτακτικών ουσιών. (199) ΝΚ κύτταρα (κύτταρα φυσικοί φονείς) Τα κύτταρα φυσικοί φονείς παίρνουν µέρος και στα δύο σκέλη της ανοσιακής απάντησης του οργανισµού, της µη ειδικής και της ειδικής ανοσίας. Αποτελούν µία ιδιαίτερη κατηγορία µη-τ, µη-β λεµφοκυττάρων, που ανευρίσκονται σε ποσοστό 10% στο περιφερικό αίµα και εµφανίζουν µορφολογία µεγάλων κοκκιωδών λεµφοκυττάρων. Παράγονται στο µυελό των οστών και προέρχονται από πρόδροµα µυελικά κύτταρα. (210,293) Κύρια λειτουργία τους αποτελεί η καταστροφή ορισµένων µεταλλαγµένων κυττάρων και αυτών που έχουν προσβληθεί από ιό. (294) Έχουν την ικανότητα να προκαλούν λύση σε κύτταρα-στόχους χωρίς προηγούµενη ευαισθητοποίηση ή περιορισµό από το Μείζον Σύµπλεγµα Ιστοσυµβατότητας (MHC). (77) Aυτό το επιτυγχάνουν µε δύο τρόπους: α) Καταστρέφουν τα κύτταρα στα οποία έχουν επικαθήσει αντισώµατα (IgG), µέσω των FcγRIII (CD16) υποδοχέων τους, µε την ιδιότητα αυτή τη γνωστή ως κυτταροτοξικότητα που εξαρτάται από τα αντισώµατα β) Καταστρέφουν κύτταρα τα οποία δεν έχουν στην επιφάνειά τους µόρια MHC-Ι, όπως είναι τα κύτταρα που έχουν προσβληθεί από ορισµένους ιούς. (295) Τα κύτταρα φονείς µετά την ενεργοποίησή τους απελευθερώνουν διάφορες κυτταροκίνες (INF-γ, IL-1, GM-CSF), οι οποίες παίζουν σηµαντικό ρόλο στην αιµοποίηση και την ανοσιακή απάντηση (253) και καθοδηγούν τα βοηθητικά Τ-λεµφοκύτταρα (κυτταρική ανοσία). (296) Γενικά, ο ρόλος των ανασταλτικών ΝΚ υποδοχέων φαίνεται να σχετίζεται µε την προστασία των «ίδιων» κυττάρων από λύση των ΝΚ, τη ρύθµιση της ανοσιακής απάντησης, την προστασία του εµβρύου από τη µητρική λυτική δραστικότητα καθώς και την αλλοαναγνώριση στις µεταµοσχεύσεις αιµοποιητικών οργάνων. (13) Τα ΝΚ κύτταρα στη νεογνική περίοδο έχουν το 30%-80% της δράσης των ενηλίκων. Μετά από ενεργοποίηση µε IL-2, IL-12, IL-15 in vitro διορθώνεται η κυτταρολυτική δραστηριότητα των ΝΚ κυττάρων των νεογνών. 60
61 Κυτταροκίνες Η οικογένεια των κυτταροκινών αποτελείται κυρίως από µικρές υδατοδιαλυτές πρωτεΐνες και γλυκοπρωτεΐνες µε χαµηλό µοριακό βάρος (8-30 kda). Αυτά τα χηµικά µόρια είναι παρόµοια µε τις ορµόνες και τους νευροδιαβιβαστές και χρησιµοποιούνται για να επιτρέψουν στα κύτταρα του ανοσολογικού συστήµατος να επικοινωνούν µεταξύ τους. Ενώ οι ορµόνες απελευθερώνονται από τα συγκεκριµένα όργανα στο αίµα και οι νευροδιαβιβαστές απελευθερώνονται από τα νεύρα, οι κυτταροκίνες απελευθερώνονται από πολλούς τύπους κυττάρων. Ο όρος κυτταροκίνες καλύπτει τις κυτταροκίνες που εκκρίνονται από τα λεµφοκύτταρα, όπως οι ιντερφερόνες, παράγοντας νέκρωσης όγκων, οι ιντερλευκίνες που εκκρίνονται από ειδικά λευκοκύτταρα καθώς και οι χηµειοκίνες, µόρια χαµηλού µοριακού βάρους που συµµετέχουν στον χηµειοτακτισµό και επηρεάζουν τη συµπεριφορά άλλων λευκοκυττάρων.(248) Η κύρια πηγή παραγωγής τους είναι τα µονοπύρηνα-φαγοκύτταρα και τα Τ-λεµφοκύτταρα. (297) Οι κυτταροκίνες, λόγω του κεντρικού ρόλου τους στο ανοσολογικό σύστηµα, διαδραµατίζουν σηµαντικό ρόλο στην οξεία και χρόνια φλεγµονή, εφόσον συµµετέχουν ως διαµεσολαβητές στη διαδικασία της πληροφόρησης παρακείµενων ιστών για την έναρξη λοίµωξης ή ιστικής βλάβης. (298) Ειδικότερα, η ανοσιακή απάντηση στη λοίµωξη εξαρτάται από την ανοσιακή κατάσταση του ξενιστή καθώς και από παράγοντες που έχουν σχέση µε το είδος του παθογόνου (βακτήριο, ιός, παράσιτο, µύκητας), την πύλη εισόδου (βλεννογόνοι, παρεντερική οδός), τη φλεγµονώδη αντίδραση που προκαλείται (τοπική, γενικευµένη) και τη θέση πολλαπλασιασµού του (εξωκυττάρια, ενδοκυττάρια). (299) Κυτταροκίνες που συµµετέχουν στη φλεγµονώδη διαδικασία επηρεάζουν την οµοιόσταση του σιδήρου, την παραγωγή της αιµοσφαιρίνης και την απάντηση του µυελού στη δράση της ερυθροποιητίνης.(300) Η σύνδεση της κυτταροκίνης µε τον ειδικό υποδοχέα στην επιφάνεια του λευκοκυττάρου σηµατοδοτεί ενδοκυττάρια µηνύµατα προς το εσωτερικό του, µέσω ενδιάµεσων πρωτεϊνικών µορίων (JAKs/ STATs µορίων), µε σκοπό την ενεργοποίηση µεταγραφικών παραγόντων στον πυρήνα µέσω βιοχηµικών αλλαγών που προκαλούν την έκφραση ενός γονιδίου. (301) Παράγεται mrna που µεταφέρει το µήνυµα εκτός του πυρήνα, µε αποτέλεσµα τη σύνθεση της αντίστοιχης κυτταροκίνης, τη µεταφορά της µέσω του ενδοπλασµατικού δικτύου στο σύστηµα Golgi και, στη συνέχεια, την απέκκρισή της από το κύτταρο για να δράσει στο κύτταρο- στόχο. (302) Οι κυτταροκίνες λόγω του πρωτεϊνικού τους µορίου δεν µπορούν να διαπεράσουν την κυτταρική µεµβράνη, ώστε να επιφέρουν τη δράση τους. Συνδέονται γι αυτό το λόγο µε τους υποδοχείς. Οι υποδοχείς των κυτταροκινών µπορεί να βρίσκονται είτε στην επιφάνεια του 61
62 ίδιου του κυττάρου που παράγει την κυτταροκίνη (αυτοκρινής δράση) είτε στην επιφάνεια ενός παρακείµενου κυττάρου (παρακρινής δράση κυτταροκίνης) είτε τέλος το κύτταροστόχος να βρίσκεται αποµακρυσµένο και η κυτταροκίνη να µεταφέρεται µέχρι εκεί µε την κυκλοφορία (ενδoκρινής δράση κυτταροκίνης). Οι κυτταροκίνες δρουν µεταξύ τους σε ένα πολύπλοκο δίκτυο. Προωθούν ή αναστέλλουν την παραγωγή άλλων κυτταροκινών είτε απευθείας είτε µέσω κυττάρων που απαντούν µε αυτό τον τρόπο στο ερέθισµα. Μία κυτταροκίνη µπορεί να προκαλεί τη σύνθεση και την έκκριση από το κύτταρο µιας άλλης κυτταροκίνης, οι υποδοχείς της οποίας µπορεί να υπάρχουν ήδη στην επιφάνεια του κυττάρου ή να παράγονται και αυτοί από το έναυσµα της πρώτης κυτταροκίνης. Οι υποδοχείς των κυτταροκινών είναι δυνατόν να αποκοπούν µε πρωτεολυτικό µηχανισµό από το κύτταρο και να κυκλοφορούν στην περιφέρεια µε τη µορφή διαλυτών υποδοχέων. Οι κυτταροκίνες στη νεογνική λοίµωξη-σηψαιµία H παραγωγή και οι µεταβολές των κυκλοφορούντων προφλεγµονωδών κυτταροκινών σε σχέση µε την εξέλιξη και έκβαση της λοίµωξης έχει µεγάλη σηµασία στη λοίµωξη και κατ επέκταση στην εµφάνιση της νεογνικής σηψαιµίας. Οι µελέτες σχετικά µε την παραγωγή των κυτταροκινών από τα νεογνικά µακροφάγα είναι αντικρουόµενες Υπάρχουν µελέτες που δείχνουν ελαττωµένη παραγωγή του TNF-α µετά από διέγερση στα τελειόµηνα νεογνά. Άλλες αναφέρουν ότι νεογνικά µακροφάγα είναι ικανά να παράγουν προφλεγµονώδεις και αντιφλεγµονώδεις κυτταροκίνες. (111, ) Αντικρουόµενα είναι, επίσης, τα αποτελέσµατα των κλινικών µελετών, σχετικά µε τα επίπεδα των κυτταροκινών στη νεογνική σηψαιµία. Όσον αφορά τα επίπεδα της ΙL-1β στη νεογνική σηψαιµία δεν υπάρχει οµοφωνία. Oρισµένες µελέτες υποδεικνύουν ότι είναι µετρίως αυξηµένα (304) ενώ άλλες ελαττωµένα. (303) Αυξηµένα επίπεδα της ΙL-6 βρέθηκαν σε νεογνά µε βέβαιη ή πιθανή σηψαιµία. (304) Οι διαφορές µεταξύ των µελετών οφείλονται στις µεθόδους που χρησιµοποιήθηκαν, αλλά και στο χρόνο που έγινε η αιµοληψία από την έναρξη της σηψαιµίας. (28) Οι διαφορετικοί χρόνοι στην απελευθέρωση και την κινητική των κυτταροκινών αυτών µπορούν να εξηγήσουν τα ευρήµατα. Λόγω της µεγάλης θνητότητας και νοσηρότητας κατά τη νεογνική σηψαιµία, αρκετές µελέτες υποδεικνύουν ότι ο προσδιορισµός των επιπέδων των κυτταροκινών βοήθησε στην πρώιµη και ταχεία διάγνωσή της. Σύµφωνα µε αυτές τις µελέτες στα νεογνά µε σηψαιµία τα επίπεδα των προφλεγµονωδών κυτταροκινών, κυρίως του TNF α της ΙL-6 και σε µικρότερο βαθµό της ΙL-1β, αυξάνουν ταχέως και φθάνουν στη µέγιστη τιµή τους το πρώτο 24ωρο από την έναρξη της λοίµωξης, ενώ ελαττώνονται προοδευτικά µε το χρόνο και την ανταπόκριση της λοίµωξης στη θεραπευτική αγωγή. (111,305) 62
63 Αισθητηριακά συστήµατα Το ανοσολογικό σύστηµα διαθέτει αισθητηριακά συστήµατα ανίχνευσης µικροοργανισµών, τους πρωτεϊνικούς υποδοχείς αναγνώρισης (pattern recognition, PRRs). Τα συστήµατα αυτά απαντούν στα σήµατα που στέλνουν συστατικά της κυτταρικής µεµβράνης του µικροβίου, είτε µε άµεση µικροβιοκτονία είτε ενεργοποιώντας άλλα συστήµατα της άµυνας του οργανισµού. (306) Σ αυτά ανήκει η οικογένεια των Toll-υποδοχέων (TLRs), µία οικογένεια που εξελικτικά διατηρείται από τη Drosophila µέχρι τον άνθρωπο. Οι TLRs υποδοχείς πήραν το όνοµα Toll από υποδοχέα της κυτταρικής µεµβράνης στη Drosophila, που έχει κυτταροπλασµατική περιοχή οµόλογη µε τον πρωτεϊνικό υποδοχέα της IL-1. ( ) Στα θηλαστικά υπάρχουν τουλάχιστον 10 TLR υποδοχείς, που αντιπροσωπεύουν τις τύπου Ι διαµεµβρανικές πρωτεΐνες, οι οποίες εκφράζονται σε τρεις περιοχές, την εξωκυττάρια, τη διαµεµβρανική και την ενδοκυττάρια περιοχή. Οι TRL1, TLR2, TLR4, TLR5 και TLR11 εκφράζονται στην κυτταρική µεµβράνη, ενώ οι TLR3, TLR7, TLR8 και TLR9 ενδοκυττάρια (µε έκφραση στα ενδοσωµάτια, στα λυσσοσωµάτια και στο ενδοπλασµατικό δίκτυο). Η δοµή τους δείχνει ότι αποτελούνται από οµοδιµερή ή ετεροδιµερή συµπλέγµατα (παράδειγµα οι TLR1/TLR2, TLR2/TLR6). (306) Τα δοµικά αυτά µόρια έχουν περιοχές που αναγνωρίζονται από πολλά παθογόνα µικρόβια, ιούς, µύκητες και παράσιτα. Οι λιποπολυσακχαρίτες (LPS), συστατικό της κυτταρικής µεµβράνης των Gram (-) µικροβίων, ενεργοποιούν και συνδέονται µε τον TLR4, όπως επίσης και η βακτηριακή ενδοτοξίνη. To CD14 συσχετίζεται µε την αναγνώριση των λιποπολυσακχαριδών, άρα CD14 και TLR4 συσχετίζονται. (310) Η ΜD2 µοριακή πρωτεΐνη σχετίζεται µε τον εξωκυττάριο TLR4 και αυξάνει τη σύνδεση µε τις LPS. (311) O ΤLR2 αναγνωρίζει συστατικά λιποπρωτεϊνών από Gram (-) µικρόβια, µυκοβακτήρια και σπειροχαίτες, πεπτιδογλυκάνες και λιποτοιχοεικό οξύ και από Gram (+) µικρόβια. (312) Άλλα µέρη των µικροβίων που ενεργοποιούν τους υποδοχείς αυτούς είναι η φραγγελίνη (313) και ειδικές ακολουθίες νουκλεοτιδίων που κωδικοποιούν το DNA του βακτηριδίου. (314) Η επίκτητη ανοσία που αντιµετωπίζει µικροβιακούς παράγοντες παράγει αντισώµατα από Β- κύτταρα µέσω παραγωγής των Τ-killer ή Τ-helper, T-λεµφοκυττάρων µε ανοσολογική µνήµη, ενώ η πρώιµη ανοσία µε τα µακροφάγα και τα δενδριτικά κυττάρα (DCs) έχει κεντρικό ρόλο στην παραγωγή προφλεγµονωδών κυτταροκινών και την παραγωγή του µονοξειδίου του αζώτου (ΝΟ). Πρόσφατες µελέτες έδειξαν ότι οι TLRs διαδραµατίζουν σηµαντικό ρόλο στην πρώιµη ανοσιακή απάντηση και οδηγούν όχι µόνο στην αποµάκρυνση (clearance) του παθογόνου αλλά και στην εγκατάσταση επίκτητης ανοσίας µε άµεση ανίχνευση των µορίων των µικροβίων. H οδός των TLRs υποδοχέων που είναι υπεύθυνοι για την ενεργοποίηση των κυττάρων και τη µετατροπή σηµατοδότησης, αποτελεί µηχανισµό για τη σύνδεση της πρωτογενούς µε την επίκτητη ανοσία. (315) 63
64 Οι TLRs ενεργοποιούν τα αντιγονοπαρουσιαστικά κύτταρα. Έτσι, υποστηρίζουν την κυτταρική διαφοροποίηση σε TH1 κύτταρα. Επίσης, διαµορφώνουν την TH1/ΤΗ2 ισορροπία σε πολλά νοσήµατα, όπως ο καρκίνος, η αλλεργία και η αυτοανοσία. Επίσης, οι TLRs είναι αντιπρόσωποι των διαµεµβρανικών σηµατοδοτών των PRRs. H ενδοκυττάρια περιοχή που εµπεριέχει τον Toll/IL-1 υποδοχέα και τoν υποδοχέα της IL-1 είναι βασική για µετατροπή σηµάτων. Οι περιοχές των πυρηνικών συνδέσεων Nucleotidebinding oligomerization domain (NOD) έχουν κυτταροπλασµατικoύς υποδοχείς αναγνώρισης PRRs. (316) Οι NOD έχουν, επίσης, µία περιοχή ενεργοποίησης κασπάσης (CARD), η οποία κινητοποιεί σηµατοδοτικά µονοπάτια για ενεργοποίηση του ΝF- κβ ή των mitogen-activated protein kinases (ΜΑΡΚs). (317) Όταν ένα σύµπλεγµα ενεργοποιεί έναν toll-like υποδοχέα στέλνεται ένα µήνυµα στον πυρήνα του ξενιστή-κυττάρου, παρέχοντας το έναυσµα στο κύτταρο αυτό να τροποποιήσει την έκφραση ορισµένων γονιδίων. (318) Μετά την ενεργοποίηση των TLRs, το σήµα µεταδίδεται στον πυρήνα, όπου µεταγραφικοί παράγοντες ρυθµίζουν την έκφραση των γονιδίων που είναι υπεύθυνα για την παραγωγή αντιµικροβιακών πεπτιδίων (defensins), αντιϊκών παραγόντων (τύπου I interferons), την έκκριση προφλεγµονωδών κυτταροκινών, και διαφόρων συµπαραγόντων, ενώ προάγει την ωρίµανση των δενδριτικών κυττάρων. (201) Όταν ενεργοποιούνται οι TLRs υποδοχείς, ενεργοποιούν έναν καταρράκτη σηµάτων, στον οποίο συµµετέχουν και άλλα µόρια που χρησιµοποιούν τον υποδοχέα της IL-1. Ενεργοποιηµένα µακροφάγα συνθέτουν και εκκρίνουν σειρά προφλεγµονωδών κυτταροκινών, χηµειοκίνες και µεσολαβητές. Μερικές από αυτές τις κυτταροκίνες ενεργοποιούν ουδετερόφιλα για να εκκρίνουν πρωτεάσες και ελεύθερες ρίζες, που έχουν τη δυνατότητα να καταστρέψουν το ενδοθήλιο και να προάγουν την τριχοειδική διαφυγή (leak). Η ρύθµιση των µορίων προσκόλλησης για τα ουδετερόφιλα τους επιτρέπει να συνδέονται σε υποδοχείς των ενδοθηλιακών κυττάρων και να µεταναστεύουν σε φλεγµονώδεις περιοχές. Ο προφλεγµονώδης καταρράκτης διακόπτεται από ρυθµιστικούς µηχανισµούς. ιαταραχές σ αυτά τα πρώιµα αισθητηριακά συστήµατα µπορεί να προκαλέσουν υπερβολική φλεγµονώδη απάντηση. Οι πολυµορφισµοί των TLR έδειξαν ότι αυτοί σχετίζονται συνήθως µε φλεγµονώδεις διαταραχές. Η σηµατοδότησή τους προκαλεί παθογένεση σε χρόνια και φλεγµονώδη νοσήµατα. (319) Μία βασική λειτουργία σηµατοδότησης µέσω τυροσινικών ανοσο-υποδοχέων ΙΤΑΜ είναι να ρυθµίζουν τη σηµατοδότηση ετερόλογων υποδοχέων. Είναι οι µηχανισµοί µέσω των οποίων γίνεται η ρύθµιση από τους ΙΤΑΜ για τον συντονισµό των TLRs, των υποδοχέων της οικογένειας TNF και των υποδοχέων κυτταροκινών που χρησιµοποιούν τις JAK-STAT οδούς σηµατοδότησης. Σηµαντική είναι η βιολογική σηµασία της οργάνωσης και του συντονισµού µεταξύ τους. Οι υποδοχείς ΙΤΑΜ είτε διευρύνουν είτε περιορίζουν τη σηµατοδότηση των άλλων υποδοχέων. Οι TLR και οι κυτταροκίνες, αντίθετα, ρυθµίζουν τη σηµατοδότηση των 64
65 ΙΤΑΜ µε την ενεργοποίηση των β2 ιντεγκρινών που συνδέονται µε τους ΙΤΑΜ συνδέσµους DAP12 (DNAX activation protein 12) και FcRγ (Fc receptor). (320) Οι ΙΤΑΜ υποδοχείς και οι υποδοχείς IFN διευρύνουν τη δράση του παράγοντα µεταγραφής της STAT1 και την έκφραση των γονιδίων φλεγµονής. (321) Τα µακροφάγα ρυθµίζονται από JAK-STAT οδούς, από υποδοχείς αναγνώρισης µικροβίων, όπως TLRs και από ΙΤΑΜ υποδοχείς. Η δράση τους, τα ποιοτικά τους χαρακτηριστικά καθορίζονται από τις προηγούµενες σχέσεις. Οι ΙΤΑΜ είτε δρουν συνεργικά µε τους TLRs είτε αυξάνουν τη σηµατοδότηση της IFN και τη λειτουργικότητα του ενεργοποιητή του υποδοχέα του NF-κΒ. Εκτεταµένη δράση ΙΤΑΜ εµποδίζει τη JAK-STAT σηµατοδότηση. Η µη ένταση και η διαρκής σηµατοδότηση των ΙΤΑΜ καθορίζει αν οι υποδοχείς διευρύνουν τους TLRs και την ανταπόκριση των JAK-STATs. Η IFNγ συνεργάζεται µε TLRs αναστολείς την TLR-ανάδραση µε µεσολαβητές την IL-10 και τη STAT3. (322) Η IL-6 µέσω σηµατοδότησης της STAT3 είναι βασικός ρυθµιστής της LPS προφλεγµονώδους απάντησης µέσω cross-talk ρύθµισης του TLR4/Mal σηµατοδοτικού µονοπατιού και συµµετέχει στην επικοινωνία cross-talk ανάµεσα σε JAK/STAT και TLR οδούς ως µηχανισµός που ρυθµίζει τη σοβαρότητα της φλεγµονώδους απάντησης του ξενιστή. (323) STATs (Κυτταροπλασµατικοί µετατροπείς σήµατος και µεταγραφικοί παράγοντες) Οι ενεργοποιητές µεταγραφικών σηµάτων (signal transducers and activators of transcription -STAT) αποτελούν µία οικογένεια µε επτά µέλη (STAT1, STAT2, STAT3, STAT4, STAT5α, STAT5β, STAT6), η οποία σηµειώνει σηµαντικές βιολογικές δράσεις και συµµετέχει σε λειτουργικές ρυθµίσεις των κυττάρων που αφορούν τον τοµέα της ανοσολογίας της λοίµωξης. ( ) Η ενεργοποίηση των STATs ξεκινάει άµεσα µετά την ανοσολογική αντίδραση εναντίον των µικροβίων. Σηµαντική είναι η δράση τους που γίνεται κατανοητή, όταν υπάρχει ανεπάρκεια ή έλλειµµα των STATs. Οι STATs διαδραµατίζουν διπλό ρόλο ως µεσολαβητές στην ανοσιακή απάντηση, αφού λειτουργούν ως ανοσοκατασταλτικές ουσίες και έχουν συγχρόνως αντιφλεγµονώδη δράση. (329) 2.2. ΕΙ ΙΚΗ ΑΝΟΣΙΑ Οι ειδικoi ανοσιακοί µηχανισµοί (χυµική και κυτταρική ανοσία) χαρακτηρίζονται από την ανοσολογική µνήµη που προϋποθέτει αναγκαστικά προηγούµενο αντιγονικό ερεθισµό, και ενεργοποιούνται, όταν η φυσική ανοσία είναι ανεπαρκής. Στην ειδική ανοσία το αντιγόνο προκαλεί σειρά αντιδράσεων, µε αποτέλεσµα την παραγωγή ευαισθητοποιηµένων κυττάρων και αντισωµάτων. Μ αυτό τον τρόπο προκύπτει ανοσία µακράς διάρκειας. 65
66 Τα κύρια χαρακτηριστικά που τη διαφοροποιούν από τη φυσική ανοσία είναι: (330) 1. Η διάκριση του «ίδιου/εαυτού» από το «µη ίδιου/µη εαυτού» αντιγόνο. Η διάκριση αυτή επιτυγχάνεται µε ειδικούς υποδοχείς επιφανείας των λεµφοκυττάρων. Κυρίαρχο ρόλο στη διαδικασία αυτή κατέχουν τα µόρια του Μείζονος Συστήµατος Ιστοσυµβατότητας. 2. Η ανοσιακή µνήµη, η ιδιότητα δηλαδή να ανακαλεί και να αξιοποιεί προηγούµενες επαφές µε ξένα µόρια αλλά και να αντιδρά µε εξειδικευµένη, ταχύτερη και µαζικότερη ανοσιακή απάντηση. 3. Η ποικιλοµορφία 4. Η αντιγονική εξειδίκευση, η ικανότητα να διακρίνει µεταξύ των πολυάριθµων µορίων, τα οποία παρουσιάζονται στο ανοσιακό σύστηµα και να απαντά µόνο σε ορισµένα, χωρίς να διαµορφώνεται µία τυχαία µη διαφοροποιηµένη απάντηση. Η ειδική ανοσία διακρίνεται σε τρεις φάσεις. Οι πολυάριθµες λειτουργίες και φαινόµενα κατά την ειδική ανοσία αλληλοεπικαλύπτονται µεταξύ τους, χωρίς συχνά να είναι δυνατός ο χρονικός διαχωρισµός των φάσεων αυτών. α. Η επαγωγική ή φάση αναγνώρισης, κατά τη διάρκεια της οποίας πραγµατοποιείται η παραλαβή, η επεξεργασία και η παρουσίαση του αντιγόνου από τα αντιγονοπαρουσιαστικά κύτταρα στα Τ και Β λεµφοκύτταρα. Η επεξεργασία του αντιγόνου είναι δυνατό να πραγµατοποιηθεί µέσα από δύο οδούς: 1) Την ενδογενή, οπότε η παρουσίαση θα γίνει στα Τ- κυτταροτοξικά λεµφοκύτταρα µε τη βοήθεια µορίων MHC τάξης Ι. 2) Την εξωγενή, οπότε η παρουσίαση θα γίνει στα Τ-βοηθητικά µε µόρια MHC τάξης IΙ. β. Η κεντρική φάση ή φάση πολλαπλασιασµού και διαφοροποίησης, κατά τη διάρκεια της οποίας επιτελείται πολλαπλασιασµός και διαφοροποίηση των κυττάρων της ειδικής ανοσίας στο πλαίσιο πολυάριθµων και σύνθετων διακυτταρικών διεργασιών. Αποτέλεσµα της αντιγονικής διέγερσης είναι η διαφοροποίηση των περισσότερων Τ και Β λεµφοκυττάρων σε εκτελεστικά κύτταρα, ενώ µικρό ποσοστό από αυτά διαµορφώνεται σε κύτταρα µνήµης. Βασική προϋπόθεση για την έναρξη πολλαπλασιασµού και διαφοροποίησης των Τ αλλά και Β λεµφοκυττάρων αποτελεί η έκκριση κυτταροκινών και ιδιαίτερα της ιντερλευκίνης-1 (IL-1) από το αντιγονοπαρουσιαστικό κύτταρο, το οποίο έχει ήδη παραλάβει το αντιγόνο. γ. Η δραστική ή εκτελεστική φάση, η οποία αποσκοπεί στην καταστροφή του εισβολέα ή του ξένου κυττάρου και είναι δυνατό να πραγµατοποιηθεί µε τρεις διαφορετικούς µηχανισµούς: 1) µε ειδικά αντισώµατα, τα οποία συντίθενται από τα ώριµα Β λεµφοκύτταρα, 2) µε αντισωµατο-εξαρτώµενη κυτταροτοξικότητα και 3) µε ενεργοποιηµένα µακροφάγα ή Τ κυτταροτοξικά λεµφοκύτταρα ή κύτταρα φυσικούς φονείς (331). Η ειδική ανοσία διακρίνεται στην κυτταρική και τη χυµική ανοσία Κυτταρική ανοσία Η κυτταρική ανοσία αφορά τις αντιδράσεις αντιγονοπαρουσιαστικού κυττάρου ή 66
67 αντιγόνου-τ λεµφοκυττάρου (βοηθητικού και κατασταλτικού), µε αποτέλεσµα την ενεργοποίηση των Τ λεµφοκυττάρων και τη σύνθεση κυτταροκινών για την εντατικοποίηση της ανοσιακής απάντησης. Τα Τ λεµφοκύτταρα είναι µονοπύρηνα λευκά αιµοσφαίρια προερχόµενα από τα προγονικά κύτταρα του µυελού των οστών, έχουν υποστεί ωρίµανση και διαφοροποίηση στο θύµο αδένα και, στη συνέχεια, µεταναστεύουν στους περιφερικούς λεµφικούς ιστούς και στη δεξαµενή του περιφερικού αίµατος. Λειτουργικά τα Τ λεµφοκύτταρα διακρίνονται σε βοηθητικά (Th), επαγωγικά, κυτταροτοξικά (TcLs) και κατασταλτικά (TsLs). Tα Th κύτταρα συνεργάζονται και βοηθούν στην ενεργοποίηση και τον πολλαπλασιασµό των Β λεµφοκυττάρων καθώς και στη διαφοροποίησή τους προς πλασµατοκύτταρα που εκκρίνουν ανοσοσφαιρίνες. Το ιδιαίτερο χαρακτηριστικό της ειδικής ανοσίας είναι η µνήµη, δηλαδή η ικανότητα των Β και Τ λεµφοκυττάρων να ανακαλούν την αντίδραση εναντίον κάποιου αντιγόνου. Τα Τ λεµφοκύτταρα αναγνωρίζουν µέσω ειδικών υποδοχέων τα αντιγόνα, τα οποία προηγουµένως έχουν υποστεί επεξεργασία και έχουν παρουσιαστεί στην επιφάνεια των αντιγονοπαρουσιαστικών κυττάρων συνδεδεµένα µε µόρια MHC τάξης I και ΙΙ. Μετά την αναγνώριση του αντιγόνου, τα Τ κύτταρα µετατρέπονται είτε σε µνηµονικά κύτταρα (CD4 + ) είτε σε κύτταρα που ασκούν συγκεκριµένες λειτουργίες, όπως η καταστροφή µολυσµένων κυττάρων (CD8 + κυτταροτοξικά), η υποβοήθηση (CD4 + Τ βοηθητικά) των Β λεµφοκυττάρων για την παραγωγή ανοσοσφαιρινών και η ενεργοποίηση διαφόρων υποπληθυσµών λεµφοκυττάρων και µακροφάγων (CD4 + Τ inducer). Τα Τ κύτταρα είναι, επίσης, υπεύθυνα για την αντίδραση υπερευαισθησίας επιβραδυνόµενου τύπου (Β). (253) Μετά το τέλος της ανοσιακής απάντησης τα περισσότερα ειδικά για το αντιγόνο CD4 + και CD8 + Τ κύτταρα πεθαίνουν. Επιβιώνουν λίγα και διαφοροποιούνται σε µνηµονικά κύτταρα, που σε µία νέα συνάντηση µε το αντιγόνο επανενεργοποιούνται εύκολα, και παράγουν επιταχυνόµενη και αυξηµένη ανοσιακή απάντηση. Τα µνηµονικά αυτά κύτταρα είναι στην ουσία τα πιο κατάλληλα λεµφοκύτταρα που παρέχουν τη βάση για εφ όρου ζωής ανοσία σε ορισµένες λοιµώξεις και τα θεµέλια για την ανάπτυξη εµβολίων. (199) Τα Τ λεµφοκύτταρα στα νεογνά Ο απόλυτος αριθµός λεµφοκυττάρων είναι αυξηµένος στη γέννηση. Σύµφωνα µε τους Puri και Reen (1985) ο αριθµός αυτός παραµένει σταθερός σ όλη την νεογνική περίοδο µε αύξηση, όµως, της ποσοστιαίας αναλογίας των Τ κυτάρων, ενώ οι Erkeller-Yuskel και συν (1992) αναφέρουν ότι µε την πάροδο του χρόνου ελαττώνεται ο απόλυτος αριθµός των λεµφοκυττάρων, των Τ και Β κυττάρων καθώς και των κυττάρων-φονέων. (332, 333) Στη γέννηση, τα νεογνικά Τ λεµφοκύτταρα εµφανίζουν ανώριµους φαινοτύπους, τα CD3+Τ λεµφοκύτταρα είναι λιγότερα σε σύγκριση µε αυτά των ενηλίκων και τα περισσότερα 67
68 CD4+ Τ κύτταρα εκφράζουν τον δείκτη CD45RA+, που χαρακτηρίζει τα παρθένα, µη αντιγονικά ερεθισµένα Τ κύτταρα. (334) Η ικανότητα παραγωγής κυτταροκινών από τα νεογνικά Τ λεµφοκύτταρα δεν είναι διευκρινισµένη. Ορισµένοι συγγραφείς αναφέρουν ανεπάρκεια, κυρίως της IL-4 και της IL-5 (283), ενώ άλλοι επισηµαίνουν µεγαλύτερη παραγωγή της IL-4. (335) Αντικρουόµενες είναι οι απόψεις και για την παραγωγή της IFN-γ. (335) Αυξηµένος είναι και ο αριθµός των κυττάρων-φονέων κατά τη γέννηση, υπολείπονται όµως λειτουργικά (333), γεγονός που διαµορφώνει πληµµελή αντιµετώπιση ιογενών λοιµώξεων και ιδιαίτερα της ερπητικής Χυµική ανοσία Η χυµική ανοσία αφορά αντιδράσεις αντιγόνου και Β λεµφοκυττάρου, µε αποτέλεσµα τον πολλαπλασιασµό και διαφοροποίηση των Β λεµφοκυττάρων σε αντιγονοπαραγωγά πλασµατοκύτταρα, και περιλαµβάνει τον προστατευτικό µηχανισµό µε την παραγωγή αντισωµάτων εναντίον ειδικών αντιγόνων. Η IgG ανοσοσφαιρίνη αποτελεί την κυριότερη ανοσοσφαιρίνη του ορού και του διάµεσου ιστού και ασκεί προστατευτική επίδραση εναντίον των µικροβίων, των τοξινών τους και των ιών, λόγω της σηµασίας της στη φαγοκυττάρωση (δράση οψωνίνης). Η ανοσοσφαιρίνη G ανιχνεύεται µε τέσσερεις µορφές, τις υποτάξεις IgG1, IgG2, IgG3, IgG4 οι οποίες στον ενήλικο αποτελούν το 70-75% του συνόλου των ανοσοσφαιρινών. Η IgG1 αποτελεί ισχυρό ενεργοποιητή του συµπληρώµατος µετά τη σύνδεσή της µε το αντιγόνο, η δράση της IgG2 είναι περιορισµένη, η IgG3 κυρίως (µαζί µε την IgG1) περνά τον πλακούντα και προσφέρει ανοσία για τους πρώτους 3-6 µήνες ζωής και η IgG4 δεν ενεργοποιεί το συµπλήρωµα. Η ΙgM υπάρχει στον ορό σαν πενταµερές και προστατεύει κυρίως από τα µικρόβια που κυκλοφορούν στο αίµα, γιατί στο διάµεσο ιστό βρίσκεται σε µικρές ποσότητες. Η ΙgM ενεργοποιεί µόνο την κλασσική οδό του συµπληρώµατος και την εναπόθεση κλασµάτων του (C3b) και του λυτικού συµπλέγµατος στα µικρόβια (έµµεση προαγωγή της φαγοκυττάρωσης). εν έχουν, προς το παρόν, αναγνωριστεί στα φαγοκύτταρα υποδοχείς για την ΙgM που να βοηθούν στη φαγοκυττάρωση. Η ανοσοσφαιρίνη Α ασκεί την προστατευτική της δράση στους βλεννογόνους αποτρέποντας τη σύνδεση των µικροβίων. (209) Β λεµφοκύτταρα στα νεογνά Η παραγωγή ανοσοσφαιρινών υπολείπεται ποσοτικά και ποιοτικά στη νεογνική ηλικία, παρότι αυτές απαντούν στον αντιγονικό ερεθισµό. Σχετικά µε την παραγωγή τους, κυριαρχεί η IgM, ενώ η παραγωγή των ανοσοσφαιρινών IgG και IgA είναι µικρότερη και πολύ αργή. Οι διαφορές στην ικανότητα παραγωγής των ανοσοσφαιρινών δεν οφείλονται στην απουσία ικανών Β κυττάρων, αλλά στην έλλειψη αντιγονικών ερεθισµών στην ενδοµήτρια ζωή, στον 68
69 αυξηµένο αριθµό κατασταλτικών κυττάρων στην ηλικία αυτή και στην ανεπαρκή παραγωγή κυτταροκινών. (336) Η εµβρυϊκή και η νεογνική IgG είναι κυρίως µητρικής προέλευσης, καθώς η ενδοµήτρια σύνθεση από το έµβρυο είναι µικρή. Η δίοδος µητρικών IgG αντισωµάτων στο έµβρυο επιτελείται κυρίως µετά την 32η 34η βδοµάδα κύησης. Η δίοδος των µητρικών IgG από τον πλακούντα επιτυγχάνεται λόγω της ύπαρξης υποδοχέων για το Fc κλάσµα της στα τροφοβλαστικά κύτταρα. (337) Η σειρά προτίµησης κατά την ενεργό µεταφορά των υποτάξεων της IgG είναι IgG1, IgG3, IgG2 και IgG4. (120) Γίνεται φανερό, λοιπόν, ότι το είδος των αντισωµάτων του νεογνού εξαρτάται από τη µητέρα και ότι υπάρχουν ποσοτικές και ποιοτικές διαφορές στις ανοσοσφαιρίνες του κάθε νεογνού, ανεξάρτητα από τη διάρκεια κύησης. Στα τελειόµηνα, τα επίπεδα της IgG στο αίµα του οµφάλιου λώρου κατά τη γέννηση είναι παρόµοια ή υψηλότερα των επιπέδων της µητέρας και κυµαίνονται µεταξύ 750 και 1200 mg/dl. (337) Επειδή, όµως, η διέλευση των IgG αντισωµάτων επιτελείται κυρίως µετά την 32η εβδοµάδα κύησης, τα πρόωρα νεογνά έχουν χαµηλότερα επίπεδα IgG και είναι πιο ευάλωτα σε λοιµώξεις. Τα επίπεδα της IgG νεογνών µε ηλικία κύησης 32 εβδοµάδες κυµαίνονται µεταξύ 400 και 500 mg/dl, ελαττώνονται ακόµη περισσότερο κατά την νεογνική και την πρώτη βρεφική ηλικία, φτάνοντας στα χαµηλότερα επίπεδα σε ηλικία 4-6 µηνών µετά τη γέννηση, ενώ τα πρόωρα νεογνά παρουσιάζουν ακόµη µεγαλύτερη πτώση των επιπέδων της. (265) Τα επίπεδα της ολικής IgG και των υποτάξεών της αυξάνονται και φτάνουν τα επίπεδα των ενηλίκων σε ηλικία >7 ετών. (338) Η IgM δεν διέρχεται τον πλακούντα και τα επίπεδα στη γέννηση είναι περίπου το 10% των επιπέδων του ενηλίκου. Επίπεδα IgM >20 mg/dl στη γέννηση είναι ενδεικτικά συγγενούς λοίµωξης. (265) Με την ενεργοποίηση του συµπληρώµατος, τα IgM αντισώµατα προκαλούν µετάθεση του C3b στις επιφάνειες των κυττάρων των µικροβίων και διευκολύνουν τη φαγοκύττωση. (210) Ακόµη, η IgA του ορού δεν διέρχεται τον πλακούντα και στα τελειόµηνα αντιπροσωπεύει το 1% των επιπέδων του ενηλίκου. Η εκκριτική ανοσοσφαιρίνη Α απουσιάζει από τις εκκρίσεις των νεογνών και προσλαµβάνεται µε το πύαρ και το µητρικό γάλα. (338) Γι αυτό, ο πρόωρος τοκετός προκαλεί στο νεογνό ποσοτική αλλά και ποιοτική ανεπάρκεια σε προστατευτικά αντισώµατα και το καθιστά ευάλωτο σε µικροβιακούς κυρίως παράγοντες. 69
70
71 3o ΚΕΦΑΛΑΙΟ ΚΥΤΤΑΡΟΠΛΑΣΜΑΤΙΚΟΙ ΜΕΤΑΤΡΟΠΕΙΣ ΣΗΜΑΤΟΣ ΚΑΙ ΕΝΕΡΓΟΠΟΙΗΤΕΣ ΜΕΤΑΓΡΑΦΗΣ (Signal Transducers and Activators of Transcription, STATs) 3.1. Γενικά Οι Jak-STAT οδοί ανακαλύφθηκαν µέσω της µελέτης της ιντερφερόνης και της µετατροπής του σήµατος ενδοκυττάρια. Οι STATs πρωτεΐνες είναι επτά, οι 1, 2, 3, 4, 5α, 5β, και 6 και είναι γνωστές ως µεταγραφικοί παράγοντες και σηµατοδότες για τις κυτταροκίνες. Έχουν µοριακό βάρος 750 και 950 kda. Προέρχονται από κοινό προγονικό γονίδιο και µοιράζονται τις ίδιες λειτουργικές περιοχές. Ένας µεγάλος αριθµός κυτταροκινών, ορµονών και παραγόντων ανάπτυξης-αύξησης ενεργοποιούν τις Jak-STATs. Κάθε µέλος της οικογενείας αυτής ενεργοποιείται από συγκεκριµένες κυτταροκίνες. Οι Jak κινάσες είναι µία µοναδική τάξη τυροσινικών κινασών που έχουν σχέση µε τους υποδοχείς των κυτταροκινών. Οι κυτταροκίνες οργανώνονται σε οµοδιµερείς ή ετεροδιµερείς υποδοχείς, µε τους οποίους συνδέονται οι Jaks πρωτεΐνες. Πάνω στον επίτοπο σύνδεσης ενεργοποιούν τους µετατροπείς σήµατος και τους ενεργοποιητές µεταγραφής (STATs) µέσω φωσφορυλίωσης της τυροσίνης. Οι ενεργοποιηµένες STATs διαµορφώνονται σε διµερή συµπλέγµατα, µεταβαίνουν στον πυρήνα και συνδέονται σε ειδικά σηµεία απάντησης στους προωθητές των γονιδίων-στόχων, που µεταγραφόµενοι ενεργοποιούν τα γονίδια. (339) Η δράση των STATs γίνεται µε φωσφωρυλίωση της τυροσίνης κατά τη διάρκεια της πρόδροµης αντιµικροβιακής ανοσολογικής απάντησης, όπου σήµατα προκαλούµενα από υποδοχείς, ενεργοποιούν την έκφραση των γονιδίων των κυτταροκινών. Έτσι, ουσίες που λειτουργούν ως σύνδεσµοι µεταξύ των υποδοχέων των κυτταροκινών τάξης Ι και ΙΙ είναι ενεργοποιητές των JAK-STATs. Οι σηµατοδότες που προέρχονται από έλικες RNA µετά από τη σύνδεση µε το ιϊκό RNA ή από TRIF µονοπάτι µε σηµατοδότες των TLR3 και TLR4, θα ενεργοποιήσουν τη µεταγραφή των τύπου Ι γονιδίων INF (IFN-I). Αυτοί θα σηµατοδοτήσουν τους υποδοχείς ΙFN-I προκαλώντας τη φωσφορυλίωση των STAT1 και STAT2. (340) Άλλα µονοπάτια των TLRs, των IL-6 και IL-10 γονιδίων ενεργοποιούν τη STAT3. ( ) Μερικές STATs φωσφορυλιώνουν τη σερίνη στο C-τελικό άκρο τους, ο φωσφόρος, στη συνέχεια, αλλάζει τη δράση της µεταγραφής, ενώ µεταλλάξεις του συγκεκριµένου άκρου της STAT1 και της STAT 4 µειώνουν την ανοσολογική δράση. (344) Έχουν µελετηθεί οι θετικές και αρνητικές ρυθµίσεις των JΑΚ-STATs. (345) Σε µία θετική ανατροφοδοτική οδό, οι ιντερφερόνες µεταγραφικά ενεργοποιούν τα γονίδια για τα συστατικά του γονιδιακού παράγοντα 3 (interferon stimulated gene factor3, ISGF3).(346,347) Ένας αριθµός κυτταροκινών που ενεργοποιεί το µονοπάτι των JΑΚ-STATs, λειτουργεί µε 71
72 ρύθµιση µέσω των SOCS-JAΚs-SSIs, οι οποίοι αποτελούν τους αναστολείς των STATs. Οι κατασταλτικές πρωτεΐνες που σηµατοδοτούν τις κυτταροκίνες (SOCS) είναι κυτταροπλασµατικές πρωτεΐνες, οι οποίες έχουν αρνητική ανατροφοδότηση µε το σύστηµα των JAK/STATs. (348) Πειραµατικά µοντέλα µε καταστροφή γονιδίων για κάποιες JΑΚ-STATs στον ποντικό έχουν αποκαλύψει µία σειρά από βιολογικές ιδιότητες. Όταν στο πειραµατόζωο έχει αποκλειστεί η STAT1, διαταράσσεται η σηµατοδότηση της ιντερφερόνης (349), όταν έχει αποκλειστεί η STAT4, διαταράσσεται η σηµατοδότηση της IL12 και όταν έχει αποκλειστεί η STAT5a, τότε διαταράσσεται η σηµατοδότηση της προλακτίνης. (350) Επίσης, όταν αποκλειστεί η STAT5b, δεν γίνεται η σηµατοδότηση της αυξητικής ορµόνης, ενώ µε τον αποκλεισµό της STAT6 διαταράσσεται η σηµατοδότηση της IL-4 και της IL-13. (351) Ανεπάρκεια στην JΑΚ-STAT οδό και απορρύθµιση της διαδικασίας προκαλεί ανοσολογικού τύπου διαταραχές και παθολογικές καταστάσεις, όπως αλλεργίες, αυτοάνοσα νοσήµατα, λεµφώµατα και ανοσοανεπάρκειες Ο ρόλος των STATs στη σηψαιµία Στη µη ειδική ανοσία (innate immunity) τα λευκοκύτταρα, όπως ουδετερόφιλα, καθώς και τα µακροφάγα αναγνωρίζουν και απαντούν στα παθογόνα µε ειδικό τρόπο. Η ενεργοποίηση των λευκοκυττάρων είναι απαραίτητη και καθορίζεται από σειρά χηµικών µεσολαβητών και κυτταροκινών. (301) Οι κυτταροκίνες διακρίνονται σε δύο τύπους: Οι τύπου Ι είναι βασικές για την τοπική άµυνα, ενώ οι τύπου ΙΙ έχουν προστατευτικό ρόλο, γι αυτό και η αντιφλεγµονώδης απάντηση απευθύνεται σε όλο τον οργανισµό. Οι κυτταροκίνες δρουν µέσω JAK/STATs οδών. Οι STATs 1/3/4/6 είναι µεταγραφικοί παράγοντες για τη σηµατοδότηση των IFN-γ, IL-10, IL-12, IL-13 αντιστοίχως. Κατά τη διάρκεια της σηψαιµίας οι STATs έχουν σηµαντικό ρόλο µέσω της ρύθµισης της πρώιµης ανοσίας. (352) Οι κυτταροκίνες που ενεργοποιούνται από STATs παράγονται από ενεργοποιηµένα λεµφοκύτταρα κατά την ανοσολογική απάντηση για την καταστολή της σηψαιµίας. Επίσης, ακολουθούν την έκθεση σε παραγόµενες κυτταροκίνες κατά την αντιγονοπαρουσίαση ή κατά την πρώιµη φάση ενεργοποίησης Τ- κυττάρων. Οι STATs ενεργοποιούν τα Τ-κύτταρα και παίρνουν µέρος στη διαφοροποίησή τους σε υποοµάδες, καθεµία από τις οποίες παράγει χαρακτηριστικού τύπου STAT ενεργοποιηµένες κυτταροκίνες. Για παράδειγµα, η ΙFN-γ παράγεται από TH1, η IL-4 και η IL-10 παράγονται από TH2 και η TR1 από Τ-κύτταρα. Κατά κανόνα µία κυτταροκίνη θα ενεργοποιήσει την ίδια STAT σε διαφορετικά κύτταρα, µε εξαίρεση την IFN-I, στην οποία οι STAT 1 και STAT2 µπορούν να ενεργοποιήσουν τη STAT4 σε ΤH1 και NK κύτταρα µε φωσφορυλίωση τυροσίνης. (352) Αυτή η µετατροπή των STATs έχει µεγάλη σηµασία για τον ανοσολογικό ρόλο τους εναντίον παθογόνων µικροβίων. Ο ρόλος, όµως, της κάθε STAT στη σηψαιµία δεν έχει πλήρως διευκρινισθεί, διότι η καθεµία 72
73 έχει άλλα λειτουργικά καθήκοντα Ο ρόλος των STATs στη φλεγµονή και στα φλεγµονώδη νοσήµατα Η ανοσολογική απάντηση ρυθµίζεται από τη δράση των προφλεγµονωδών και αντιφλεγµονωδών κυτταροκινών. Η Jak-STAT οδός είναι η µεγαλύτερη οδός για τη σηµατοδότηση κυτταροκινών, την έκφραση γονιδίων, την παραγωγή και τη διαφοροποίηση των ανοσοκυττάρων. Αρκετά µέλη των πρωτεϊνών Jak-STATs και ειδικά η STAT1, η STAT2, η STAT3, η STAT4, και η STAT6 δρουν ως µεταγραφικοί παράγοντες στη ρύθµιση των προ- και αντι-φλεγµονωδών απαντήσεων. (301) H αντιφλεγµονώδης δράση των κυτταροκινών δρα και σε ισχαιµία ή νέκρωση του νευρικού συστήµατος (ισχαιµικό εγκεφαλικό έµφρακτο). Προφλεγµονώδη µόρια συµµετέχουν στη διαδικασία µέσω νευρογλοιακών κυττάρων µε διήθηση από λευκοκύτταρα του τραυµατισµένου ιστού. Οι κυτταροκίνες είναι οι µεσολαβητές της φλεγµονώδους απάντησης, εφόσον προφλεγµονώδεις και αντιφλεγµονώδεις κυτταροκίνες απελευθερώνονται στους ισχαιµικούς νευρικούς ιστούς. Αντιφλεγµονώδεις, όπως η IL-10, προάγουν την κυτταρική επιβίωση, ενώ οι προφλεγµονώδεις κυτταροκίνες, όπως ο TNF-α, προάγουν τον κυτταρικό θάνατο. Ωστόσο, αν η λειτουργία της κυτταροκίνης είναι ωφέλιµη ή όχι, εξαρτάται από τη συγκέντρωσή της, τη χρονική στιγµή που δρα και το δίκτυο των ενδοκυττάριων σηµάτων που ενεργοποιούνται. Ρυθµιστής της λειτουργίας αυτής είναι το σύστηµα των Jak- STATs οδών που προκαλεί µεταβολές των µεταγραφών των γονιδίων. Οι µεταβολές µπορεί να είναι σχετικές µε τον κυτταρικό θάνατο ή την επιβίωση µέσω των πρωτεϊνών που συµµετέχουν. Η ενεργοποίησή της STAT1 είναι σχετική µε τον κυτταρικό θάνατο, ενώ η STAT3 σχετίζεται µε την επιβίωση. (353,354) Η ενεργοποίηση της κάθε STAT επιτυγχάνεται µέσω ρυθµιστών των Jak-STATs. Εκτός των τοπικών αντιδράσεων λόγω ισχαιµίας, οι κυτταροκίνες δρουν και στην κυκλοφορία, όπου η ανισορροπία της αντιφλεγµονώδους και προφλεγµονώδους δραστηριότητας µπορεί να ελαττώσει την ανοσολογική απάντηση. Ενδεικτικά, ένα αποφρακτικό εγκεφαλικό επεισόδιο µπορεί να λειτουργήσει ως έναρξη ανοσοκατασταλτικής κατάστασης και έτσι να αυξηθεί ο κίνδυνος λοίµωξης. Οι STAT4 και STAT6 είναι µεταγραφικοί παράγοντες που οδηγούν στην ανοσολογική απάντηση τύπου Ι και ΙΙ αντίστοιχα. Ειδικότερα, ο ρόλος τους σε ανοσολογική απάντηση για την αντιµετώπιση της σηψαιµίας-περιτονίτιδας µελετήθηκε σε ποντίκια. ιαπιστώθηκε ότι η έλλειψη των συγκεκριµένων STATs εµποδίζει το θάνατο του πειραµατόζωου, ενώ δεν συµβαίνει το ίδιο στο ποντίκι που τις διαθέτει. (355) Στη βακτηριαιµία η ποσότητα των βακτηρίων είναι µικρότερη στο πειραµατόζωο µε έλλειψη της STAT6, γεγονός που συσχετίστηκε µε την αύξηση της IL-12 στο περιτοναϊκό υγρό, του ΤΝF-α και των χηµειοκινών που προέρχονται από τα µακροφάγα (MIP-2, KC). (327) Η νεφρική βλάβη στο πειραµατόζωο µε έλλειψη της STAT4 συσχετίστηκε µε ελαττωµένα νεφρικά επίπεδα των 73
74 MIP-2 και KC χωρίς µεταβολή των επιπέδων της IL-10, IL-13. Το πειραµατόζωο αυτό ήταν ανθεκτικό στην περιτονίτιδα πετυχαίνοντας τη βακτηριδιακή κάθαρση του τοπικού οργάνου και αποτρέποντας την καταστροφή του, µε την αρωγή των συγκεκριµένων κυτταροκινών. Όλα αυτά αποδεικνύουν την καταλυτική δράση της ανοσολογικής απάντησης τύπου Ι και ΙΙ µέσω STATs για την προστασία του οργανισµού κατά τη διάρκεια της σήψης. (356) Το ανοσιακό σύστηµα µε τη µη ειδική ανοσία, που περιλαµβάνει τα ουδετερόφιλα λευκοκύτταρα και µακροφάγα, αναγνωρίζει και απαντά στα παθογόνα µε µη ειδικό τρόπο. Η ενεργοποίηση και δράση των λευκοκυττάρων είναι σηµαντική και εξαρτάται από χυµικούς µεσολαβητές αλλά και από τις κυτταροκίνες. Συγκεκριµένα, οι κυτταροκίνες τύπου Ι είναι σηµαντικές για την τοπική ανοσιακή απάντηση, ενώ οι τύπου ΙΙ λειτουργούν προστατευτικά κατά τη φλεγµονώδη αντίδραση του οργανισµού. Οι λειτουργίες αυτές καθορίζονται από το σύστηµα των JAK/STATs οδών.(354,357) Οι τύπου Ι κυτταροκίνες, (ΤΗ1) Τ-helper, είναι προφλεγµονώδεις και περιλαµβάνουν την IFN-γ και την IL-2. Οι τύπου ΙΙ περιλαµβάνουν τις IL-4, IL-10 και IL-13, είναι αντιφλεγµονώδεις και απαντούν µε τη χυµική ανοσία σε περιπτώσεις σοβαρών λοιµώξεων. Μεταξύ των δυο οµάδων ΤΗ1 και ΤΗ2 κυτταροκινών υπάρχει ανταγωνιστική και ρυθµιστική δράση η οποία είναι απαραίτητη για την ανοσολογική απάντηση στη σηψαιµία. Αν, όµως, οι αντιφλεγµονώδεις κυτταροκίνες υπερισχύσουν έναντι των προφλεγµονωδών, µπορεί να δηµιουργηθεί µεγάλη ιστική βλάβη και καταστροφή οργάνων. Για παράδειγµα, ασθενείς που παρουσιάζουν σηψαιµία βαριάς µορφής απαντούν κυρίως µε κυτταροκίνες ΤΗ2, γεγονός που συσχετίζεται µε κακή έκβαση της νόσου λόγω ανοσοκαταστολής. Έχει αποδειχθεί ότι στο σύστηµα ρύθµισης των µηχανισµών για εξισορρόπηση των ΤΗ1 και ΤΗ2 κυτταροκινών σε περιπτώσεις σήψης και σηπτικού shock, συµµετέχουν οι πρωτεΐνες STATs και άλλα ρυθµιστικά συστήµατα, όπως είναι η πρωτεΐνη p38 mitogen-activated protein kinase. (358) Μόλις το µικρόβιο εισβάλλει στο σηµείο εισόδου, το ανοσιακό σύστηµα αναλαµβάνει δράση, κατ αρχάς, µε διήθηση λευκοκυττάρων και ενεργοποίηση των αµυντικών κυττάρων του ξενιστή εναντίον της λοίµωξης, ενώ, στη συνέχεια, τα λευκοκύτταρα καταστέλλουν τα παθογόνα. Η φλεγµονή αυτή είναι επωφελής για την αντιµετώπιση της λοίµωξης. Μπορεί, όµως, να αποβεί επιβλαβής, επειδή ως παρατεταµένη απάντηση είναι πιθανόν να προκαλέσει βλάβη ιστών και νέκρωση οργάνων. Γι αυτό είναι απαραίτητη η ισορροπηµένη ανοσοκατασταλτική απάντηση των κυτταροκινών εναντίον της λοίµωξης και της ανεξέλεγκτης συστηµατικής φλεγµονώδους αντίδρασης. Οι κυτταροκίνες µέσω των JAK/STATs οδών αξιοποιούν ένα σύνολο σηµατοδοτών που παράγουν ανοσολογικά αποτελέσµατα. (302) Το πόσο σηµαντικές είναι αυτές οι οδοί και η απρόσκοπτη λειτουργία τους διαπιστώνεται από την περίπτωση βλάβης των STATs σε γονιδιακό επίπεδο. (359) Η σήψη και το σηπτικό shock είναι σύνδροµο φλεγµονώδους διαδικασίας και σε κυτταρικό επίπεδο. Η σήψη αρχικά ξεκινά από τοπική λοίµωξη των πνευµόνων, του 74
75 ουροποιητικού και της κοιλιάς. (328) Η απάντηση του ξενιστή εναντίον των µικροβίων απαιτεί την ενεργοποίηση και τη δράση των λευκοκυττάρων στο σηµείο εισόδου, ώστε να ακολουθήσει η φαγοκυττάρωση και η µικροβιοκτονία. Αν ο ξενιστής αποτύχει να περιορίσει τη λοίµωξη σε τοπικό επίπεδο και επεκταθεί αυτή στην κυκλοφορία, τα υποπροϊόντα που έχουν παραχθεί, συνιστούν ερέθισµα για προϊούσα φλεγµονή και οδηγούν στη δηµιουργία µεσολαβητών κυτταροκινών, κάτι που µπορεί να αποβεί επικίνδυνο και θανατηφόρο. Χαρακτηριστικό παράδειγµα είναι η συστηµατική απάντηση του συνδρόµου (SIRS) και της ανεπάρκειας πολλαπλών οργάνων (MOF). Παρά τη ραγδαία εξέλιξη των αντιβιοτικών και της τεχνολογίας του µηχανικού αερισµού καθώς και των µονάδων εντατικής νοσηλείας, η σήψη και το σηπτικό shock είναι καταστάσεις σοβαρές και απειλητικές για τη ζωή του νεογνού, όπως φαίνεται από την παθοφυσιολογία της σήψης σε µοριακό επίπεδο καθώς και τα πειραµατικά µοντέλα της. (360) Σε περίπτωση βακτηριακής λοίµωξης, η τύπου Ι απάντηση των κυτταροκινών που επιτελείται µε έκκριση IFNγ και TNFα, είναι απαραίτητη στον ξενιστή για την άµυνά του. Πρόσφατες µελέτες δείχνουν ότι τα πειραµατόζωα που παράγουν IL-12 καταστρέφουν µέσω της παραγόµενης IFN-γ τις συγκεντρώσεις των βακτηρίων στο περιτόναιο. (361) Η IFN-γ είναι προφλεγµονώδης κυτταροκίνη, αυξάνεται σε ΤΗ1 απάντηση και ενεργοποιεί µακροφάγα που ενισχύουν την απάντηση των αντιµικροβιακών µεσολαβητών, όπως είναι το µονοξείδιο του αζώτου (NO) και ο TNF-α. To πειραµατόζωο, αντίθετα, µε έλλειµµα IL-12 δεν µπορεί να παράγει αρκετή IFN-γ, γι αυτό και δεν έχει επαρκή ΤΗ1 διαφοροποίηση.(362) Αυτό έχει ως αποτέλεσµα περιορισµένη καταστροφή βακτηρίων συγκριτικά µε οµάδα πειραµατόζωων ελέγχου. Ωστόσο, σε πειραµατικά µοντέλα µε σηψαιµία από ενδοτοξίνη διαπιστώθηκε ότι τα αντισώµατα της IL-12 λειτουργούν προστατευτικά. (363) Κατά την έναρξη της νόσου, όταν προκαλείται µικροβιακή λοίµωξη από τοπική φλεγµονή, οι φλεγµονώδεις µεσολαβητές ενεργοποιούν λευκοκύτταρα πολύ σηµαντικά για την πορεία της σήψης και προκαλούν τύπου ΙΙ απάντηση των κυτταροκινών. Συγκεκριµένα, διαπιστώθηκε σε σχετική µελέτη ότι η IL-13 δεν ανιχνεύεται στο περιτόναιο, αλλά βρίσκεται σε όργανα και ιστούς και σηµατοδοτεί την έναρξη της διαδικασίας της ανεπάρκειας πολλαπλών οργάνων κατά τη διάρκεια της σήψης. (325,364) Μία άλλη σηµαντική κυτταροκίνη, που αυξάνει την ΤΗ2 διαφοροποίηση προάγοντας τη χυµική ανοσία, η IL-4, καταγράφεται υψηλή σε περίπτωση σοβαρού τραύµατος καθώς και κατά την εξέλιξη της σηψαιµίας, ωστόσο παρουσιάζεται ελαττωµένη σε ενδονοσοκοµειακή πνευµονία. Χορήγηση αντισωµάτων της IL-4 καταστέλλει την ΤΗ1 παραγωγή κυτταροκίνης στα κύτταρα του ποντικού µε CLP και σχετίζεται µε ελαττωµένη φωσφορυλίωση της STAT6.(365) Σε σηψαιµία από Staphylococcus aureus λόγω έλλειψης της IL-4 παρουσιάζονται διαφοροποιηµένα ποσοστά στην επιβίωση του οργανισµού. (366) Αντίθετα, η θεραπεία µε IL-4 βρέθηκε ότι µειώνει την προοπτική επιβίωσης σε σηψαιµία από 75
76 Pseudomonas aeruginosa, ενώ την ενισχύει, όταν χορηγείται 24 ώρες πριν από την έναρξη της λοίµωξης. (367) Η IL-10 είναι αντιφλεγµονώδης µε ρόλο προστατευτικό µαζί µε άλλες αντιφλεγµονώδεις κυτταροκίνες, όµως αύξησή της σε σηψαιµία προοιωνίζεται κακή έκβαση. Αυτό επιβεβαιώθηκε κατά τη χορήγηση ΙL-10 σε ποντίκι, στο οποίο παρατηρήθηκε στη συνέχεια µείωση της φλεγµονώδους απάντησης (12). Είναι, επίσης, σηµαντική η ύπαρξή της στην αποκατάσταση εγκαυµάτων. Αύξηση, τέλος, στα ποσοστά επιβίωσης παρατηρείται σε χορήγηση anti-il-10 για την αντιµετώπιση πνευµονικής λοίµωξης από κλεµπσιέλλα πνευµονίας. (368) Όλα αυτά ενισχύουν την υπόθεση ότι η ισορροπία µεταξύ του τύπου Ι και ΙΙ απάντησης είναι καθοριστική για την καταστολή της σήψης. Οι STATs 1,3,4,6 προκαλούν την απάντηση των αντίστοιχων κυτταροκινών δηλαδή της IFN-γ, της IL-10, της IL-12 και της IL-13. (301) Μελέτες που χρησιµοποιούν πειραµατόζωα µε γονιδιακούς στόχους αναλύουν τις λειτουργίες των STATs. Ειδικότερα, η STAT3 είναι µεταγραφικός παράγοντας που µεσολαβεί για την έκκριση της IL-10, που είναι αντιφλεγµονώδης κυτταροκίνη. (339) Η ανεπάρκεια της STAT3 στα µακροφάγα και τα ουδετερόφιλα δεν δίνει την ανοσολογική απάντηση µε παραγωγή της IL-10, ενώ συνθέτει TNF-α µετά από ενεργοποίηση µε IL-10. Πειραµατόζωα µε απενεργοποίηση της STAT3 είναι εξαιρετικά ευάλωτα σε ενδοτοξιναιµία και παρουσιάζουν αύξηση των IL-1β, IFN-γ και του TNF-α. (369) Επίσης, παρατηρείται αύξηση και στα επίπεδα της IL-12, της IL-6 και του αµυλοειδούς Α του ορού ενώ διαπιστώνεται ελάττωση των τιµών της αλβουµίνης. Επιπλέον, η εµφάνιση ηπατικής και νεφρικής βλάβης επιδεινώνει περαιτέρω την εικόνα της σηψαιµίας. Η έλλειψη, εποµένως, της STAT3 στα µακροφάγα και τα ουδετερόφιλα αυξάνει τη θνητότητα. Σε πειραµατικές µελέτες η έλλειψη IL-12 εκφράζεται µε διαταραχή στη διαφοροποίηση της TΗ1 και παραγωγή IFN-γ. Η IL-12 αυξάνει την IFN-γ σε κυτταρικό επίπεδο και οι φυσικοί φονείς (ΝΚ) χάνουν την κυτταροτοξική δράση τους εφόσον απουσιάζει η STAT4. Επιπλέον, διαπιστώθηκε αντοχή στην ΤΗ1 χρόνια νόσο, όπως είναι το πνευµονικό κοκκίωµα ή η αυτοάνοση εγκεφαλοµυελίτιδα, κάτι που σηµαίνει ότι η STAT4 παρεµβαίνει καθοριστικά στην ΤΗ1 απάντηση. Ενδεικτικά, στη σηπτική περιτονίτιδα η IL-12 αποµακρύνει τα µικρόβια µέσω παραγωγής IFN-γ. Αντίθετα, το πειραµατόζωο µε έλλειψη STAT4 είναι ανθεκτικό στην περιτονίτιδα και δεν παρουσιάζει αυξηµένα ποσοστά θνητότητας. Η τοπική αντίδραση της φλεγµονής, όµως, είναι ίδια στο ποντίκι µε έλλειψη STAT4 όπως και στο φυσιολογικό (Wild T). Στο πειραµατόζωο αυτό παρατηρείται αύξηση της µυελοϋπεροξιδάσης (MPO) της IL-10 και της IL-13 (325), ενώ τα επίπεδα των πρωτεϊνών φλεγµονής των µακροφάγων (ΜΙΡ)-2, και των KC, CXC χηµειοκινών, που ενεργοποιούν και έλκουν ουδετερόφιλα, εµφανίζονται χαµηλά στο ήπαρ του. (327) Αυτά τα αποτελέσµατα δείχνουν ότι οι κυτταροκίνες κατά τη διάρκεια της σήψης έχουν αντιφλεγµονώδη δράση, ώστε να αποκαθίσταται σταδιακά η βλάβη 76
77 των οργάνων, άρα να επιτυγχάνεται και η επιβίωση του ποντικού µε έλλειψη STAT4. Από την άλλη, ο Lentsch και συν (327) σε έρευνες που διενήργησαν σε ποντίκια µε ενδοτοξιναιµία και έλλειψη STAT4, απέδειξαν ότι ενισχύεται η ευαισθησία στη σήψη εξαιτίας αύξησης της IL-12. (327) H STAT6 συµβάλλει στη διαφοροποίηση των CD4+ T κυττάρων σε TΗ2 ανοσία και ενεργοποιεί την IL-4 και την IL-13, οι οποίες είναι αντιφλεγµονώδεις κυτταροκίνες όπως και ο TNF-α που δρα κατευναστικά στην ενδοτοξιναιµία. (370) Η λειτουργικότητα των µακροφάγων σε απάντηση στην IL-13 είναι ελαττωµένη σε STAT6-/- mice, που γίνεται έτσι ευάλωτο στη θανατηφόρο τοξιναιµία, επειδή παράγονται προφλεγµονώδεις κυτταροκίνες, οι οποίες καταστρέφουν βασικά όργανα. Μπορεί, όµως, να γίνει ανθεκτικό, όπως φάνηκε στην περιτονίτιδα, εξαιτίας αλλαγής στις κυτταροκίνες µε την αύξηση του τύπου Ι, έτσι ώστε να επιτευχθεί ισορροπία των τύπου Ι και ΙΙ ανοσολογικής απάντησης. Η ισορροπία µεταξύ των ΤΗ1 και ΤΗ2 κυτταροκινών είναι αναγκαία στην απάντηση του ξενιστή κατά τη διάρκεια της λοίµωξης. Πολλά πειραµατικά πρωτόκολλα για τη σήψη µε πειραµατόζωα-προϊόντα γενετικής µηχανικής έχουν διαµορφωθεί για να αναδείξουν το ρόλο των JΑΚs και STATs και την απάντησή τους στη λοίµωξη σε συνδυασµό µε τη ρύθµιση της ισορροπίας των ΤΗ1/ΤΗ2. (302) Τα πρωτόκολλα που χρησιµοποιήθηκαν ήταν της πολυµικροβιακής περιτονίτιδας µε ενδοπεριτοναϊκή έγχυση παθογόνων, ενδοτοξινών ή λιποπολυσακχαριδασών και της πνευµονίας από κλεµπσιέλλα πνευµονίας. ύο σηµαντικά µονοπάτια που παρατηρούνται κατά τη σήψη είναι αυτά των STAT4 και STAT6, λόγω της δράσης τους στη διαφοροποίηση των ΤΗ-κυττάρων. Τα πειραµατόζωα που δεν διαθέτουν τις STAT4 και STAT6, διαπιστώθηκε ότι έχουν καλύτερη κλινική εικόνα και περισσότερες πιθανότητες επιβίωσης µετά από περιτονίτιδα. Τα επίπεδα βακτηρίων σε αυτά τα πειραµατόζωα µε έλλειψη STAT6 είναι λιγότερα από ό,τι σε µη τροποποιηµένα ποντίκια, λόγω της αυξηµένης τιµής της IL-12 από τα ενεργοποιηµένα λεµφοκύτταρα. Ωστόσο, τα πειραµατόζωα µε έλλειψη STAT4 έχουν καλύτερες προοπτικές επιβίωσης µετά από περιτονίτιδα παρά τα υψηλότερα επίπεδα βακτηρίων. Το πλεονέκτηµα γι αυτού του είδους την επιβίωση προέρχεται από τις αυξηµένες τιµές της IL-12 στον περιτοναϊκό χώρο και στον ορό, οι οποίες εµποδίζουν την προφλεγµονώδη απάντηση. (327) Το πειραµατόζωο µε έλλειψη STAT4, η οποία είναι βασική για την ΤΗ1 απάντηση, παρουσιάζει αύξηση των ηπατικών IL-10 και IL-13, εικόνα που συνδέεται µε ηπατική βλάβη µετά από περιτονίτιδα. Αυτή η έλλειψη STAT4 συσχετίζεται, επίσης, σύµφωνα µε τον Matsukawa και συν µε ανεπάρκεια πολλαπλών οργάνων. Η έλλειψη της STAT6, που είναι απαραίτητη για την TH2 διαφοροποίηση και ενεργοποιεί την IL-4, µπορεί να επιτευχθεί µε την ΤΗ1 κυτταροκινική δράση της IFN-γ. Μία άλλη µελέτη αποκαλύπτει το ρόλο των STAT4 και STAT6 στην αντιµετώπιση της λοίµωξης µε ενδοκυττάρια παθογόνα όπως Toxoplasma gondii και Trypanosoma cruzi. (371) Οι ασθενείς µε ανεπάρκεια STAT4 έχουν 77
78 την τάση να αναπτύσσουν άτυπες µυκοβακτηριδιακές λοιµώξεις και σταφυλοκοκκικές λοιµώξεις. H STAT6 αλλά όχι η STAT4 είναι καθοριστικής σηµασίας στην ΤΗ1 και ΤΗ2 απάντηση των χηµειοκινών, οι οποίες κατά τη σήψη ρυθµίζουν αποκλειστικά την κατανοµή των λευκοκυττάρων στα σηµεία της λοίµωξης. ιαφορετικές χηµειοκίνες, εξάλλου, ρυθµίζουν τον τρόπο κατανοµής και το είδος των λευκοκυττάρων. Φαίνεται, λοιπόν, ότι τα ΤΗ2 κύτταρα παράγουν χηµειοκίνες για να ελκύσουν ΤΗ2 λεµφοκύτταρα και όχι ΤΗ1 λεµφοκύτταρα. (302) Οι SOCS πρωτεΐνες συµµετέχουν σε πολλά αυτοάνοσα και φλεγµονώδη νοσήµατα. Το SOCS1-/- mice είναι ευαίσθητο στο shock από LPS, λόγω αύξησης του TNF-α στον ορό.(369) Γι αυτό το λόγο η ισορροπία µεταξύ των STATs/SOCSs είναι αναγκαία. Σηµαντικός είναι ο έλεγχος των κυτταροκινών σε βιολογικούς παράγοντες που σχετίζονται µε την αιµοποίηση, την ανοσιακή λειτουργία, την αύξηση των κυττάρων, τη διαφοροποίηση και την αντι-αποπτωτική σηµατοδότηση. Στη λειτουργία αυτή συµµετέχουν οι Janus kinases και οι STATs. ( ) Οι µελέτες σε γονίδια πειραµατόζωων επιβεβαιώνουν το σηµαντικό ρόλο των οδών JAK/STATs στην απάντηση για παραγωγή κυτταροκινών. (345) Στα θηλαστικά υπάρχουν 4 JΑΚs (JΑΚ 1,2,3 και Tyk2) (372). Σε περίπτωση έλλειψης των JΑΚ1 και Tyk2 σε κύτταρα δεν υπάρχει απάντηση στην IFNα/β, ενώ σε απουσία JΑΚ1,2 δεν υπάρχει απάντηση στην IFN-γ. Η σχέση µεταξύ των υποδοχέων των κυτταροκινών και των JAKs καταγράφηκε µε την ερυθροποιητίνη και τον υποδοχέα της αυξητικής ορµόνης. Οι ιντερφερόνες καθώς και οι κυτταροκίνες ενεργοποιούνται µέσω των JΑΚ/ STATs µε ετεροδιµερισµό και οµοδιµερισµό των υποδοχέων των κυτταροκινών (372) STAT1 και STAT2 Οι STAT1 και STAT2 είναι πρωταρχικοί µεσολαβητές απάντησης των ξενιστών στις IFN και τις κυτταροκίνες µετά τη λοίµωξη σε όλες τις κατηγορίες των παθογόνων µικροβίων. Η STAT1 διαµορφώνει τµήµα από τα σπουδαιότερα µονοπάτια σηµατοδότησης για την IFN-γ, η οποία είναι αναγκαία για την ενεργοποίηση των µακροφάγων και των µονοκυττάρων. Η STAT1 συµµετέχει, επίσης, στην αποστολή µηνυµάτων ενεργοποίησης που προέρχονται από µικροβιακά προϊόντα, όπως το LPS, ώστε να κινητοποιήσουν τα µακροφάγα. Αυτό επιτυγχάνεται µε αλλαγή στη φωσφορυλίωση. Η STAT2 ενεργοποιείται σε απάντηση των IFN τύπου Ι και ΙΙΙ (IFN-Ι και IFN-III), ενώ η STAT1 καθορίζει την απάντηση στις IFN-I, IFN-γ και IFN-ΙΙΙ. (353,354,375) H IFN-γ και η τύπου ΙΙ IFN παράγονται από ανοσοκύτταρα, όπως από ενεργοποιηµένο TΗ1 ή CD8+ Τ λεµφοκύτταρα και ΝΚ κύτταρα. Η σηµασία τους για την ενεργοποίηση των µακροφάγων και την προστατευτική ανοσία σε ενδοκυττάρια βακτηρίδια, όπως η Listeria, τα Mycobacteria, η Salmonella και τα Chlamydia, είναι αποδεδειγµένη. (376,377) Όταν η IFN-γ δρα αντιµικροβιακά, η STAT1 είναι απαραίτητη. Επίσης η παραγωγή της IFN-γ ελέγχεται 78
79 από τη STAT4, η οποία είναι µέλος οικογένειας των STATs που ενεργοποιείται από IFN-Ι ή από IL-12. Αντίθετα µε την IFN-γ, όλα τα κύτταρα του σώµατος παράγουν IFN-Ι, µία οικογένεια κυτταροκινών µε είκοσι µέλη. (347) Ωστόσο, η IFN-Ι, η STAT1 και η STAT2 είναι σηµαντικές όχι µόνο για την ανοσία έναντι των ιών αλλά και άλλων παθογόνων.(378,379) Μέσω της σηµατοδότησης των κινασών της σερίνης θρεονίνης (TBK1, IKKE, IRAK4, IKKα) και άµεσα ή έµµεσα φωσφορυλιώνουν µέλη της IFN (IRF3 και IRF7). (340,343,379,380) Φωσφορυλιώνουν επίσης, την IFN-III που η δράση της είναι όµοια µε την IFN-I, µέσω STAT1 και STAT2. (381) Οι υποδοχείς IFN κατηγοριοποιούνται σε δύο οµάδες, την IFNAR1 και την IFNAR2, οι οποίες συνδέονται µε TYK2 και JAK1 τυροσινικές κινάσες για υποδοχείς της IFN-I και IFNGR1 και IFNGR 2 µε JAK1 και JAK2 τυροσινικές κινάσες για υποδοχείς της IFN-γ. Όταν συνδέονται οι IFN µε τους υποδοχείς τους, ενεργοποιούν φωσφορυλιώσεις των JAKs και διαµορφώνουν περιοχές για STAT1 και STAT2, οι οποίες σχετίζονται µε µία πρωτεΐνηρυθµιστή της IFN factor 9 (IRF-9) που προσαρµόζει τον µεταγραφικό γονιδιακό παράγοντα (ISGF-3). (375) Οι STAT1 και STAT2, στη συνέχεια, φωσφορυλιώνονται και κατασκευάζουν ετεροδιµερή και οµοδιµερή συµπλέγµατα. Συνήθως οι IFN-I εξασφαλίζουν την ανοσία σε ιούς. (382) Πολλά γονίδια-στόχοι µε ISGF3 περιοχές σύνδεσης εµφανίζουν αντιϊκή δράση. Επίσης, η IFN-γ είναι ενεργοποιητής µακροφάγων σε απάντηση εναντίον ενδοκυττάριων µικροβίων. Συγκεκριµένα, αναφέρονται περισσότερα από 1000 γονίδια για τη δράση των ΙFN-I και IFN-γ. Επιπλέον, µία οµάδα IFN γονιδιακών στόχων, µελών της γουανιδίνης 5 (GTPase) περιλαµβάνουν γονίδια που κωδικοποιούν Μx πρωτεΐνες των p65 GBP (Guanylate binding proteins) και των p47 GTPase. Η ανθρώπινη ΜxΑ αφορά πολλούς ιούς µεταξύ των οποίων είναι και ο ιός της ηπατίτιδας B. (344,383,384) Οι ιοί έχουν τη δυνατότητα να αναστέλλουν την παραγωγή και τη δράση της IFN-I. Αυτό συµβαίνει γιατί ελαττώνεται η παραγωγή των PAMPS (pathogen- associated molecular pattern) και παρεµποδίζεται η δηµιουργία του PRPs (HCV), ενώ παράγονται ρυθµιστές των IFN (HSV). Τελικά, η εξουδετέρωση των IFN και η αποδόµηση των STATs περιορίζουν τα ένζυµα µε αντιϊκή δράση (ελάττωση της δραστικότητας της RNase-L από HIV). (385,386) Η δράση των STATs αναστέλλεται, επίσης, από ενδοκυττάρια µικρόβια, όπως Salmonella, Mycobacterium, Listeria, Toxoplasma. Ένας επιπλέον αντιµικροβιακός µηχανισµός είναι η δηµιουργία του ΝΟ και των Ο2- ριζών. Η IFN και η STAT1 προάγουν τη σύνθεση και αυξάνουν τη συνθετάση του ΝΟ (inos, inducible Nitric Oxide Synthase) και την οξειδάση του NADPH. Η NADPH ή φαγοκυτταρική οξειδάση (PHOX, phagocyte NADPH oxidase) καταλύει την αντίδραση Ο2- οξυγονοριζών του ROS µε αντιµικροβιακή ιδιότητα. Η φαγοκυττάρωση των µικροβίων µέσω IFN-γ /STAT1 αυξάνει τη δράση της ΡΗΟΧ, επειδή ενεργοποιεί την έκφραση δύο 79
80 υποοµάδων ενζύµων (gp91phox,p67phox). (387,388) Επίσης, η inos καταλύει βιοχηµικές αντιδράσεις και καταστέλλει µικροβιακούς παράγοντες µέσω δράσης DNA. Ο προαγωγέας της inos αφορά περιοχές για ΝF-κΒ και ΑΡ-1 και STAT1 διµερή (GAF). Έχει αποδειχθεί ότι το πειραµατόζωο µε έλλειψη της inos είναι ευάλωτο σε παθογόνα. H έλλειψη STAT1 και STAT2 σε λοιµώξεις Το πειραµατόζωο µε έλλειψη STAT1 µελετάται την τελευταία δεκαετία. Τα κύτταρά του δεν απαντούν σε IFN-α/β/γ και δεν προάγουν τα ISG, όπως αυξητικούς παράγοντες, IL-6, IL-10, GH, IRF, GBP, inos, MHC II. Πεθαίνει συνήθως από ευκαιριακά παθογόνα. Είναι εκατό φορές πιο ευάλωτο σε Infuenza virus και σε ενδοκυττάρια παθογόνα, όπως η Listeria. Η έλλειψη της STAT1 στους ανθρώπους επιβεβαιώνει τη µεγάλη αξία της για την πρώιµη ανοσία στα ενδοκυττάρια παθογόνα. Αναφέρονται δύο περιπτώσεις βρεφών που σε οµόζυγη έλλειψη µε µετάλλαξη της STAT1 παρουσίασαν λοίµωξη από µυκοβακτηρίδιο και κατέληξαν από ιογενή λοίµωξη. (349) Άλλοι ασθενείς µε ετερόζυγη µετάλλαξη εµφάνιζαν φυσιολογική ISGF3, ενώ δεν παρουσίαζαν ευαισθησία σε ιογενείς λοιµώξεις. (389) H STAT1 µεσολαβεί για την παραγωγή της IFNγ, η οποία µε τη σειρά της ενεργοποιεί τα µακροφάγα, σκοτώνοντας βακτήρια και προστατεύοντας το πειραµατόζωο από θανατηφόρο λοίµωξη λόγω της Listeria. Οι µελέτες σε ποντικό µε έλλειψη γονιδίου, το οποίο προκαλεί ανεπάρκεια της IFNγ, δείχνουν ότι το πειραµατόζωο δεν διαθέτει επαρκή άµυνα εναντίον της σαλµονέλλας typhimurium. (390) Η STAT1, λοιπόν, φαίνεται ότι έχει καθοριστική σηµασία για την καταπολέµηση των ενδοκυττάριων παθογόνων. Επιπλέον, η STAT1 προάγει τη συστηµατική φλεγµονή µετά από χορήγηση LPS. (344,391) Ωστόσο, στο πολυµικροβιακό µοντέλο η ενδογενής IFNγ παρόλο που η ίδια εξουδετερώνεται, τελικά µειώνεται η θνητότητα η οποία συσχετίζεται µε ελάττωση του HMGB1-high mobility group box-1 (µεσολαβητής ενδοτοξίνης). (392) Η IFNγ, επειδή προέρχεται από τη STAT1, η οποία ενεργοποιείται στο ήπαρ, το νεφρό και το λεπτό έντερο, αποβαίνει καθοριστικός παράγοντας στην περίπτωση της καταπληξίας και της ενδοτοξιναιµίας. (391) Η λειτουργία της STAT1 έχει βαρύνουσα σηµασία όχι µόνο στην πρώιµη ανοσία αλλά και στην επίκτητη. Το πειραµατόζωο µε ανεπάρκεια στη STAT1 και ανεπάρκεια συγχρόνως σε IFN-I παρουσιάζει παθολογική προφλεγµονώδη απάντηση µε ΤΗ2 στη λοίµωξη µε Influenza. (393) Τα λεµφοκύτταρα του πειραµατόζωου εµφανίζονται αυξηµένα µετά από ενεργοποίηση µε ΤCR και παρουσιάζουν ελαττωµένη απόπτωση εξαιτίας των χαµηλών επιπέδων στις κασπάσες 1 και 11, αποτέλεσµα που κατά ένα µέρος του οφείλεται σε IFN-γ και IFN-Ι. (390) Κάποιοι ερευνητές έχουν δείξει ότι η ενεργοποίηση της IFN-γ αυξάνει την πληθώρα των CD8+ Τ κυττάρων κατά την ιογενή λοίµωξη. (394) Μετά από λοίµωξη µε τον ιό Lymphocytic Choriomeningitis, τα CD8+ Τ κύτταρα αυξάνονται και συγχρόνως η ικανότητα των κυττάρων µνήµης εξαρτάται από τη σηµατοδότηση που αφορά την IFN-I(394) 80
81 Η µελέτη του ιού της ευλογιάς αποδεικνύει τη σηµασία της STAT1 για την παραγωγή ειδικών CD8+ Τ κυττάρων και την ανοσολογική µνήµη για τα κύτταρα αυτά. (395) Επίσης, ο σηµαντικός ρόλος των δενδριτικών κυττάρων για την παραγωγή STAT1 και ΤΗ1 εντοπίστηκε στο ενδοκυττάριο παράσιτο Leishmania major. (396) Η απουσία της STAT2 δηµιουργεί πλήρη απώλεια προστασίας µέσω RNA. (397) Μελέτες έχουν δείξει ότι η STAT2 ενεργοποιείται άµεσα από την IFN-γ. (398) Ο ρόλος της είναι αντιϊκός στην πρώιµη ανοσία STAT3 Η παραγωγή της STAT3 προκαλείται µε ενεργοποίηση υποδοχέων κυτταροκινών. Η σηµατοδότηση της IL-6 είναι σηµαντική για την ανοσία µέσω υποδοχέων gp130 (IL-6, IL-11, IL-27 και IL-31)(323,399) IL-21, (400) IL-22, IL-10, αλλά και αιµοποιητικών κυτταροκινών όπως ο G-CSF. (401) Η STAT3 βελτιώνει τις πιθανότητες επιβίωσης, ενώ η ελλιπής δραστηριότητα της IL-6, µέσω STAT3 σηµατοδότησης συµβάλλει σε αυξηµένη θνητότητα. Η δυνατότητα του οργανισµού να παράγει επαρκείς ποσότητες της IL-6 κατά τη σήψη είναι σηµαντική, γι αυτό και οι τιµές της είναι δείκτης του σηπτικού µοντέλου στους ασθενείς. Επιπλέον, η STAT3 ενεργοποιεί κυτταροκίνες που σηµειώνουν αντιµικροβιακή δραστηριότητα. Συµµετέχει στη διαφοροποίηση µέσω της IL-6, της IL-23 και των ΤΗ-17 κυττάρων, τα οποία παράγουν IL-17 και IL-22. (339,374) Η παρουσία των ΤΗ-17 κυττάρων στα ουδετερόφιλα εξασφαλίζει την άµυνα εναντίον εξωκυττάριων µικροβίων, όπως η κλεµπσιέλλα πνευµονίας. (402) Γι αυτό το λόγο η STAT3 εµφανίζει προφλεγµονώδη και βακτηριοστατική δραστηριότητα µέσω των ΤΗ-17 και της µεσολάβησης της IL-22. Ακόµη, η αντιφλεγµονώδης δράση της STAT3 στα µυελοειδή κύτταρα επιβεβαιώθηκε από το πειραµατόζωο µε ελεγχόµενη κολίτιδα. (328,403) Η αντιφλεγµονώδης και ανοσοκατασταλτική δράση της διαπιστώθηκε, επίσης, από την επιρροή της στη σηµατοδότηση της IL-10. Πιο συγκεκριµένα, η κατασταλτική δράση της STAT3 στο σηπτικό shock, το οποίο προκλήθηκε από LPS, και στη δηµιουργία χρόνιας εντεροκολίτιδας οφείλεται στην ελλιπή απάντηση των µυελοειδών κυττάρων στην IL-10. Με τον ίδιο τρόπο, µε µεσολάβηση δηλαδή της STAT3 και της IL-10, υποτροπίασε η φυµατιώδης λοίµωξη σε πειραµατόζωο. (368) Η λειτουργία της STAT3 µελετήθηκε επίσης στη λοίµωξη µε τοξόπλασµα σε κυτταροκαλλιέργεια µακροφάγων. (404) Οι STAT3α και STAT3β συµµετέχουν στην αντιµετώπιση της φλεγµονής και της λοίµωξης µέσω του µεταγραφικού ελέγχου που διενεργούν στην έκφραση των γονιδίων οξείας φάσης στο ήπαρ. Κατά τη διάρκεια της σήψης τα ηπατοκύτταρα γίνονται ευάλωτα στην IL-6 ελαττώνοντας, κατά συνέπεια, τη φωσφορυλίωση της STAT3. Οι STAT3α και STAT3β ενεργοποιούν, επίσης, την οικογένεια της κυτταροκίνης IL-6 στο σηπτικό shock που προκαλείται από τη LPS. Η STAT3β βελτιώνει την ανάρρωση, ενώ η STAT3α καταστέλλει 81
82 τη δράση της LPS. (405,406) H STAT3 ρυθµίζει την προ-φλεγµονώδη και αντιφλεγµονώδη λειτουργία των ίδιων κυττάρων χωρίς να είναι γνωστό γιατί συµβαίνει αυτό. Ένας σηµαντικός παράγοντας για την ανασταλτική βιοανάδραση της STAT3 είναι η σηµατοδότηση µέσω της SOCS3. Τo γονίδιό της κατευθύνεται προς τη STAT3 και αναστέλλει τους υποδοχείς της IL-6. Αντίθετα, οι υποδοχείς της IL-10 δεν καταστέλλονται από την SOCS3. Επίσης, η αναστολή του υποδοχέα του G-CSF από την SOCS3 είναι πιθανή και διαπιστώνεται από την αύξηση της πολυµοφροπυρήνωσης που παρατηρείται µε την απουσία της STAT3. (401) 3.6. STAT4 και STAT6 Οι STAT4 και STAT6 είναι ανοσολογικά ανταγωνιστές, επειδή η καθεµιά υποστηρίζει το ρόλο της στην τύπου Ι και ΙΙ ανοσολογική απάντηση. Αυτό είναι αποτέλεσµα της λειτουργίας των οδών της IL-12 και IL-4/13. Στο πειραµατόζωο αποδείχθηκε ότι η STAT4 είναι απαραίτητη για την ανάπτυξη της ΤΗ1 καθώς και για την παραγωγή IFN-γ και ΝΚ κυττάρων, ενώ η STAT6 µεσολαβεί για την ΤΗ2 διαφοροποίηση και τη σύνθεση των κυτταροκινών IL- 4, IL-5 και IL-13. (407,408) Η STAT4 δηµιουργεί ανοσία σε παθογόνα, όπως ενδοκυττάρια µικρόβια, ιούς, βακτηρίδια και πρωτόζωα. Η STAT4, που είναι απαραίτητη για την παραγωγή της IFN-γ ως απάντηση για τη σηµατοδότηση του υποδοχέα της IL-12, συνεπάγεται ανοσία σε όλα τα παθογόνα που χρειάζονται IFN-γ/STAT1. (355,409,410) Η STAT6 προάγει µηχανισµούς µέσω αντισωµάτων που προέρχονται από IL-4. Ο συνδυασµός IL-4/IL-13/STAT6 αφορά σε χυµική ανοσία για τις έλµινθες, όπως τα νηµατοειδή του γαστρεντερικού. (411) Επίσης, η STAT6 βοηθά τα µαστοκύτταρα και τις λείες µυϊκές ίνες για την καταστροφή της trichinella spiralis στο γαστρεντερικό. (412,413) Η ανεπάρκεια της STAT4 και STAΤ6 προωθεί τη διαφοροποίηση των ΤΗ σε ΤΗ1 και ΤΗ2 αντιστοίχως. Η σηµασία των STAT4 και STAT6 για την τύπου Ι και τύπου ΙΙ ανοσιακή απάντηση στη λοίµωξη φάνηκε κυρίως από την έρευνα σε πειραµατόζωα και λιγότερο από µελέτες σε ανθρώπους. (371) Αναφέρεται ότι µία πυρηνική βλάβη που παρατηρήθηκε στη µετάθεση του γονιδίου της STAT4 για την παραγωγή της IL-12, δηµιουργεί σε ασθενή επαναλαµβανόµενες µυκοβακτηριδιακές λοιµώξεις. (414) Ακόµη, βρέθηκε ότι οι πολυµορφισµοί του γονιδίου της STAT6 σχετίζονται µε αυξηµένη αντίσταση σε λοιµώξεις µε νηµατοειδή, ενώ στους ίδιους απλοτύπους (Haplotypes) βρέθηκε αυξηµένη IgE και τάση αλλεργίας. (415,416) Εκτός από τη ΤΗ διαφοροποίηση, η STAT4 και η STAT6 παράγουν αντίθετα αποτελέσµατα στη φλεγµονώδη απάντηση που συνοδεύει τη λοίµωξη. Ο συνδυασµός IL-12 /STAT4 εµφανίζει θετική συσχέτιση µε τη λοίµωξη, ενώ ο συνδυασµός IL-4/IL-13/ STAT6 82
83 αρνητική. Ειδικότερα, η συσχέτιση αυτή για την IL-12 προκύπτει µέσω της παραγωγής IFNγ και σηµατοδότησης p38mapk και άλλων µηχανισµών. (365) Επίσης, η αντιφλεγµονώδης δραστηριότητα του συνδυασµού IL-4/IL-13/STAT6 προκύπτει από τον υποστηρικτικό ρόλο του στην ανάπτυξη της IL-10 και του TGF-β που παράγει ΤΗ2 κύτταρα. Η STAT6 φάνηκε να περιορίζει τη ζωή των Τ κυττάρων. (417) Μία σηµαντική λειτουργία της IL-4 για την ανοσοκαταστολή και την αντιφλεγµονώδη δραστηριότητα είναι να ενεργοποιεί τα µακροφάγα. Τα Μ2 µακροφάγα αυξάνονται µε τη χορήγηση IL-4 και έχουν φαινότυπο διαφορετικό από τα κλασικά Μ1 µακροφάγα µετά από ενεργοποίησή τους µε µικρόβια. (418) Τα ενεργοποιηµένα µακροφάγα συµµετέχουν στην άµυνα στα νηµατοειδή. (419) Επίσης, τα µακροφάγα παράγουν µέσω STAT6, την arginase, ένζυµο που προάγει την προφλεγµονώδη και µικροβιοκτόνο δράση του µονοξειδίου του αζώτου. Επιπλέον, προφλεγµονώδη και αντιφλεγµονώδη δράση εµφανίζουν τα πειραµατόζωα µε ανεπάρκεια στις STAT4 και STAT6 και αυξηµένη αντίσταση στη σηπτική περιτονίτιδα. (325) Αυτό ερµηνεύεται από την αυξηµένη τοπικά καταπολέµηση των βακτηριδίων σε έλλειψη της STAT6, και ελάττωση της συστηµατικής φλεγµονής σε STAT4 ανεπάρκεια. Όταν χορηγήθηκε LPS σε οµάδες πειραµατόζωων µε ανεπάρκεια STAT6 διαπιστώθηκε αύξηση των περιπτώσεων shock από ενδοτοξίνη, λόγω ελλείµµατος στην αντιφλεγµονώδη δράση. Αντίστοιχα, όταν χορηγήθηκε LPS σε πειραµατόζωα µε απουσία STAT4, επιβεβαιώθηκε ότι η έλλειψή της ενισχύει την ευαισθησία στο σηπτικό shock, λόγω των αυξηµένων επιπέδων IL-12. (420,327) Η αναλογία των STAT4/STAT1 στα ΤΗ1 και ΝΚ κύτταρα δείχνει τη σχέση τους µε τον υποδοχέα της IFN-I και, κατά συνέπεια, την επιλογή της ενεργοποίησης από την IFN-I της µίας ή της άλλης STAΤ. Ακόµα, µελέτες του ιού Lymphotropic Choriomengitis virus απέδειξαν ότι η ΙFN-I προκαλεί µία τροποποιηµένη δράση για έκκριση της STAT4 στην πρώιµη ανοσολογική απάντηση και της STAT1 στα όψιµα στάδια. (421) H STAT1 δεν µπορεί να υποκαταστήσει τη STAT4 στη ρύθµιση της µεταγραφής της IFN-γ, αλλά η ενεργοποίησή της περιορίζει την υπερβολική παραγωγή της IFN-γ κατά τη διάρκεια της ιογενούς λοίµωξης STAT5 ύο ισοµορφές (isoforms) της STAT5, οι STAT5a και STAT5b, παράγονται από γονίδια που βρίσκονται σε συνάφεια µεταξύ τους. Η STAT5 συµµετέχει στην αιµοποίηση, στη λειτουργία της υπόφυσης, στην αύξηση του σώµατος, στη µεταβολική διαδικασία και στην οµοιόσταση. (326) Η STAT5 ενεργοποιείται από τους υποδοχείς αιµοποίησης (EpoR), τους υποδοχείς των β και γ αλύσεων και τους υποδοχείς των GM-CSF, IL-2, IL-3 και IL-7. Η αλλοίωση των γονιδίων που είναι υπεύθυνα για την παραγωγή των STAT5, προκαλεί σοβαρές βλάβες στο αιµοποιητικό. Πιο συγκεκριµένα, η απουσία της STAT5 επιφέρει 83
84 ανεπάρκεια στην ερυθρά, τη µυελοειδή και τη λεµφοειδή σειρά (422, 423), συµβάλλει στην επέκταση των Τ κυττάρων κατά την ανοσιακή απάντηση (350), την παραγωγή της IL-4 από ΤΗ κύτταρα και ηωσινόφιλα, και ενεργοποιεί τα µαστοκύτταρα από IgE. (424) Επιπλέον, ο GM-CSF και ο µεταγραφικός παράγοντας της STAT5, καθορίζουν τη δράση των προγονικών δενδριτικών κυττάρων. Πιο συγκεκριµένα, ο µεταγραφικός παράγοντας της STAT5 καταστέλλει το γονίδιο του IRF8, που απαιτείται για τη διαφοροποίηση των δενδριτικών κυττάρων (DC). Ο σηµαντικός ρόλος της IL-2 στη γένεση των ρυθµιστικών κυττάρων φαίνεται από την απουσία της STAT5 που οδηγεί τελικά σε ανεπάρκεια των Τ κυττάρων και απώλεια της ανοσίας. (425,426) Επίσης, ασθενείς µε ανεπάρκεια STAT5b παρουσιάζουν ανοσολογικά προβλήµατα και µικρό σωµατικό ανάστηµα. (326) Γενικά, η λειτουργία της STAT5 στη λοίµωξη φάνηκε σε πειραµατόζωα, τα οποία λόγω της έλλειψής της παρουσίασαν αυξηµένη θνητότητα. Από έρευνες που διενεργήθηκαν στη Drosophila διαπιστώθηκε ότι η ανοσία της στα βακτηριακά παθογόνα και τους µύκητες, οφείλεται στη δράση των Toll-υποδοχέων που είναι εξειδικευµένοι στην καταπολέµηση των Gram+ βακτηρίων και µυκήτων, καθώς και στη δράση των Imd- υποδοχέων που είναι ειδικοί για τα Gram- βακτήρια. Συµπερασµατικά, αποδείχθηκε ότι οι JAK-STAT οδοί ενεργοποιούνται σε λοιµώξεις από ιούς. (357) 84
85 4o ΚΕΦΑΛΑΙΟ ΚΥΤΤΑΡΟΜΕΤΡΙΑ ΡΟΗΣ Η κυτταροµετρία ροής (ΚΡ) [Flow Cytometry, FC] αποτελεί µία πολυπαραµετρική µέθοδο µε µεγάλη δυναµική σε εύρος εφαρµογών και σε επίπεδο ποιότητας των εφαρµογών της. Αρχικά, σχεδιάστηκε για να βελτιώσει τη µορφολογική ανάλυση των κυττάρων από το µικροσκόπιο και για το διαχωρισµό τους. Εδώ και δεκαετίες έχει αναγνωριστεί η σηµασία της από πολλούς επιστήµονες διαφόρων ειδικοτήτων σε κλινικό και σε ερευνητικό επίπεδο. Τόσο ο όγκος και η ποιότητα των δηµοσιεύσεων για τις εφαρµογές και τα επιτεύγµατα της κυτταροµετρίας όσο και η συνεχής αύξηση των διαγνωστικών εφαρµογών της σε παγκόσµιο επίπεδο επιβεβαιώνουν την αποτελεσµατικότητα της µεθόδου και ενθαρρύνουν τη χρήση της σε πολλά επιστηµονικά πεδία. Οι εφαρµογές της κυτταροµετρίας ροής είναι ποικίλες µε πρωτεύοντα ρόλο αρχικά στην Αιµατολογία και, στη συνέχεια, στην Ανοσολογία, τη Λοιµωξιολογία, την Ογκολογία, την Ουρολογία, τη Μαιευτική και τη Γυναικολογία, ενώ τα τελευταία χρόνια θεωρείται πολύτιµη η συµµετοχή της µεθόδου αυτής στον τοµέα των Μεταµοσχεύσεων. ( ) Επιπλέον, η Παθολογία και η Παιδιατρική συχνά χρησιµοποιούν την ανοσολογική διαγνωστική της αξία στην καθηµερινή κλινική πράξη, ενώ η Παθολογοανατοµία και η Κυτταρολογία την εφαρµόζουν στη διαφοροδιάγνωση πολλών νοσηµάτων. (430,431) Άλλες ειδικότητες που µπορούν πλέον να αξιοποιήσουν τις δυνατότητες της κυτταροµετρίας ροής είναι η Πνευµονολογία για τη µελέτη του βρογχοκυψελιδικού εκπλύµατος, η Νευρολογία για το εγκεφαλονωτιαίο υγρό και η Οφθαλµολογία για τη µελέτη του υαλοειδούς και του υδατοειδούς υγρού. (432) Εκτός από τη διάγνωση, την πρόγνωση και την πρόληψη, η κυτταροµετρία ροής χρησιµοποιείται και στην έρευνα τόσο σε επίπεδο φαινοτύπου όσο και λειτουργίας κυττάρων, µικροοργανισµών, οργανιδίων κυττάρων και άλλων σωµατιδίων µε τη µορφή εναιωρήµατος. Συγκεκριµένα, η κυτταροµετρία ροής αποτελεί µία αυτοµατοποιηµένη µέθοδο ανάλυσης των φυσικοχηµικών χαρακτηριστικών κυττάρων και σωµατιδίων που βρίσκονται σε µορφή εναιωρήµατος, µε βάση τη σκέδαση και το φθορισµό. Επιπλέον, ο κυτταροδιαχωριστής ροής επιτρέπει την αποµόνωση κυττάρων, µε µερική µόνο απώλεια της βιωσιµότητάς τους, και την κάθαρση των σωµατιδίων χωρίς καταστροφή της δοµής τους. Οι εφαρµογές της κυτταροµετρίας ροής δεν περιορίζονται στο γνωστό προσδιορισµό των CD4+ λεµφοκυττάρων, αλλά επεκτείνονται και στη διάγνωση των αιµατολογικών κακοηθειών, γι αυτό και συντέλεσαν στην περαιτέρω ανάπτυξη της της τεχνολογίας αυτής. (433) Συνεπώς, η κυτταροµετρία ροής αποτελεί µία ταχεία και δυναµική τεχνική συνδυασµένης πολυπαραµετρικής ανάλυσης µεµονωµένων κυττάρων σε εναιώρηµα, ιδιαίτερα σηµαντική 85
86 όµως και για την µελέτη των STATs, όπως θα φανεί και από την ανάλυση σε επόµενο κεφάλαιο. (335,434) Προκειµένου να αποκτηθεί η πλέον λεπτοµερής πληροφορία από µεµονωµένα κύτταρα είναι αναγκαία η εκπλήρωση των παρακάτω παραµέτρων: Ποσοτικοποίηση όσο το δυνατόν περισσοτέρων κυτταρικών συστατικών σε επίπεδο µεµονωµένων κυττάρων Ποσοτική δοµική ανάλυση των κυτταρικών συστατικών και των αλληλεξαρτήσεών τους Ποσοτικοποίηση των κυτταρικών λειτουργιών Ποσοτικοποίηση των κυτταρικών αλληλεπιδράσεων Πρωτόκολλα προτύπωσης Ειδικότερα, η κυτταροµετρία ροής παρέχει τη δυνατότητα ποιοτικής και ποσοτικής εκτίµησης της έκφρασης των αντιγόνων σε κάθε κυτταρικό πληθυσµό. (436) Γι αυτό η ανάλυση µεγάλου αριθµού κυττάρων δίνει µοτίβα (patterns) της έκφρασης των αντιγόνων στον πληθυσµό των λευχαιµικών κυττάρων. Έτσι, ο κυτταρικός πληθυσµός µπορεί να ταυτοποιηθεί µέσω της συχνότητας εµφάνισής του (του ποσοστού) και µέσω µοτίβου έκφρασης των αντιγόνων στη φυσιολογική ωρίµανση. Η ποσοτική ανάλυση της έκφρασης των αντιγόνων είναι πολύ χρήσιµη για τη διάκριση µεταξύ φυσιολογικών και λευχαιµικών κυττάρων καθώς και για την ταυτοποίηση διαφορετικών υποτύπων της AL µε παρόµοιο γενετικό background. Η έκφραση των αντιγόνων, σε αντίθεση µε τις συνήθως χρησιµοποιούµενες cut-off τιµές για τα θετικά κύτταρα, πρέπει να υπολογίζεται µε τη µέση ένταση φθορισµού. Επίσης, για τον καθορισµό των µοτίβων έκφρασης των αντιγόνων η µέθοδος απαιτεί λεπτοµερή γνώση τους στα φυσιολογικά στάδια ωρίµανσης και στις διαταραχές του ανοσοφαινότυπου, οι οποίες είναι κοινές µορφές νεοπλασίας. Επιπλέον, η µέθοδος αυτή συµβάλλει στην ανάλυση κυττάρων που υπάρχουν σε πολύ µικρά ποσοστά στα βιολογικά υγρά, τη γνωστή µε τον όρο «ανάλυση σπάνιων δεδοµένωνκυττάρων» (Rare Event Analysis). Η ανάλυση αυτή προϋποθέτει τη χρήση πολλαπλών φθορισµών, τη µέτρηση µεγάλου αριθµού κυττάρων και µερικές φορές την εφαρµογή συγκεκριµένου λογισµικού προγράµµατος, προκειµένου να εξασφαλισθεί η στατιστική σηµασία των αποτελεσµάτων. Παραδείγµατος χάριν, εάν θέλουµε να προσδιορίσουµε κύτταρα που υπάρχουν σε ποσοστό 0,01%, πρέπει να µετρήσουµε 100 τέτοια κύτταρα, άρα συνολικά 1*106 κύτταρα, για να έχει στατιστική σηµασία το αποτέλεσµα. (437) Στη διεθνή βιβλιογραφία απαντώνται οι όροι κυτταροµετρία ποσοτικoύ φθορισµού (Quantitative Fluorescence Cytometry) και ποσοτική κυτταροµετρία ροής (Quantitative Flow Cytometry) που συµβολίζονται µε τα αρχικά QFCM (το Μ της σύντµησης τονίζει τον παράγοντα -metry στον όρο Cyto-metry)). Αν και οι δύο όροι αφορούν την ίδια εφαρµογή ή 86
87 οµάδα εφαρµογών της κυτταροµετρίας ροής, δόκιµος είναι ο πρώτος, διότι η ποσοτικοποίηση, όπως θα αναλύσουµε παρακάτω, αφορά το φθορισµό και όχι την κυτταροµετρία. Ως κυτταροµετρία ποσοτικoύ φθορισµού ορίζεται η βαθµονοµηµένη µέτρηση της έντασης του φθορισµού µέσω σηµασµένων σωµατιδίων (κυττάρων ή µικροσφαιριδίων), µε σκοπό να προσδιορισθεί ο πραγµατικός αριθµός φθοριζόντων συνδετών (φθοριζουσών ουσιών ή µορίων πρωτεϊνών-φθοριζουσών ουσιών), που συνδέονται µε κάθε σωµατίδιο. Έτσι, µετά την κλασσική κυτταροµετρία ροής, η οποία λόγω του ποιοτικού της χαρακτήρα, αναγνωρίζει κύτταρα θετικά ή αρνητικά σε κάποιο αντιγόνο και παρέχει τη δυνατότητα µέτρησης του απόλυτου αριθµού κυτταρικών υποπληθυσµών µε τη χρήση σφαιριδίων δεδοµένης συγκέντρωσης, η QFCM επιτυγχάνει την ποσοτική εκτίµηση του αριθµού των µορίων ενός συγκεκριµένου αντιγόνου ανά κύτταρο. Αντικαθίστανται πλέον οι υποκειµενικοί χαρακτηρισµοί του φθορισµού ως ασθενούς ή έντονου από συγκεκριµένους αντικειµενικούς αριθµούς, ανεξάρτητους από το χειριστή. Ο γνώστης της πρακτικής εφαρµογής της QFCM αντιλαµβάνεται το ζήτηµα στην ουσία του καθώς και τη συνολική λειτουργία του κυτταροµετρητή ροής, διότι κατανοεί τη συµπεριφορά της λογαριθµικής ενίσχυσης και τις αρχές της ηλεκτρονικής απόσβεσης (compensation), ενώ συγχρόνως αποκτά λειτουργική γνώση των µονάδων φθορισµού, της χρήσης κλιµάκων και της καµπύλης βαθµονόµησης και διαθέτει επιπλέον σαφή εκτίµηση τυποποιηµένων γραφικών παραστάσεων. Για να είναι αξιόπιστα τα αποτελέσµατα αυτά, απαιτείται η σωστή χρήση των δειγµάτων αναφοράς καθώς και των βιολογικών δειγµάτων ελέγχου, στα οποία θα αναφερθούµε παρακάτω. Οι κλινικές εφαρµογές της ποσοτικής κυτταροµετρίας είναι πολλές. Αυτή έχει χρησιµοποιηθεί στη µελέτη των διεργασιών της ενεργοποίησης ουδετεροφίλων και υποδοχέων του συµπληρώµατος, στον προσδιορισµό δεικτών κυτταρικής ενεργοποίησης, ωρίµανσης και διαφοροποίησης (CD38, CD25, HLA-DR, CD71, του HLA-DR σε µονοκύτταρα και του CD62 σε αιµοπετάλια) και στην προγεννητική διάγνωση. Ακόµα, έχει εφαρµοστεί στην κατανόηση της διαδικασίας διαφοροποίησης και ωρίµανσης των αρχέγονων αιµοποιητικών κυττάρων, στην ανάλυση σπανίων δεδοµένων (rare events analysis), στις µεταµοσχεύσεις, στην ορολογική διασταύρωση (cross-match) µε κυτταροµετρία ροής καθώς και στην προσπάθεια προτύπωσης µεταξύ εργαστηρίων που αποσκοπούν σε µακροχρόνιες, πολυεθνικές και πολυκεντρικές µελέτες. ( ) Επίσης, η κυτταροµετρία ροής παρέχει τη δυνατότητα του ποσοτικού προσδιορισµού όλων των πρωτεϊνών ανά κύτταρο, οι οποίες συµµετέχουν στη διαδικασία της απόπτωσης, εάν υπάρχουν τα απαραίτητα αντισώµατα. Η έκφρασή τους µπορεί να συσχετισθεί µε άλλες παραµέτρους, όπως άλλες πρωτεΐνες, ενδοκυττάριο Ca, DNA κ.α. Έχουν ανιχνευθεί πρωτεΐνες της πλασµατικής µεµβράνης σηµαντικές για την επαγωγή απόπτωσης, µέσω της 87
88 επώασης κυττάρων µε τα αντίστοιχα συνδεδεµένα µε FITC µονοκλωνικά αντισώµατα (FAS, TNFR). Με κυτταροµετρία ροής έχουν, ακόµα, προσδιορισθεί ενδοκυττάρια οι πρωτεΐνες bcl-2, bax, c-myc, p53 και η φωσφοτυροσίνη. Στο αρχικό στάδιο της κυτταροµετρίας ροής το δείγµα επωάζεται µε συγκεκριµένα µονοκλωνικά αντισώµατα, τα οποία είναι συνδεδεµένα µε τις κατάλληλες φθορίζουσες ουσίες. Σε περίπτωση που θέλουµε να µελετήσουµε ενδοκυττάρια αντιγόνα, το δείγµα επιδέχεται επιπλέον επεξεργασία, ώστε να είναι διαπερατή η κυτταρική µεµβράνη. Στη συνέχεια, το δείγµα αιµολύεται και είναι έτοιµο για ανάλυση στον κυτταροµετρητή ροής. Ένα πολύ σηµαντικό στάδιο ανάλυσης οποιουδήποτε δείγµατος στον κυτταροµετρητή είναι ο ορισµός του αρνητικού φθορισµού στο συγκεκριµένο πληθυσµό µε τη χρήση του ισοτυπικού control. Τα ισοτυπικά control είναι µονοκλωνικά αντισώµατα κυρίως IgG τάξης (IgG1, IgG2, IgG2a, IgG2b). Ανάλογα µε την τάξη στην οποία ανήκουν τα κυρίως µονοκλωνικά που θα µελετήσουµε, χρησιµοποιούµε και τα αντίστοιχα ισοτυπικά control. Ο αρνητικός φθορισµός είναι ένα είδος cut off για την κυτταροµετρία. Ορίζουµε τα όρια πάνω από τα οποία το αποτέλεσµά µας θα είναι θετικό. Είναι µία αναγκαία συνθήκη λόγω της ύπαρξης αυτοφθορισµού από τα ίδια τα κύτταρα, της πιθανής µη ειδικής σύνδεσης καθώς και της ύπαρξης νεκρών κυττάρων. Όλοι οι παραπάνω παράγοντες θα πρέπει να αποκλειστούν, έτσι ώστε να είναι αληθής και ακριβής η µέτρηση του ποσοστού των κυττάρων που συνδέονται µε το αντίστοιχο µονοκλωνικό αντίσωµα, το οποίο έχει χρησιµοποιηθεί. (444) Μετά τον αποκλεισµό του αρνητικού ποσοστού η ανάλυση και αξιολόγηση των αποτελεσµάτων γίνεται κυρίως µε τη χρήση των ιστογραµµάτων και των στικτογραµµάτων για καθεµία παράµετρο ή συνδυασµό περισσοτέρων της µίας. Η κυτταροµετρία ροής, λοιπόν, αποτελεί µία ιδιαίτερα ευαίσθητη και αυτοµατοποιηµένη µεθοδολογία ανάλυσης πολλαπλών παραµέτρων. Παρόλα αυτά, η αξιολόγηση των αποτελεσµάτων απαιτεί την άρτια και εµπεριστατωµένη γνώση του αντικειµένου, καθώς η ανάλυση των ζητούµενων στοιχείων βασίζεται σε µεγάλο βαθµό στις επιστηµονικές και τεχνικές γνώσεις του χειριστή και αναλυτή ενός κυτταρόµετρου. εδοµένης αυτής της ιδιαιτερότητας η κυτταροµετρία ροής, αν και αυτοµατοποιηµένη, παρουσιάζει µεγάλο βαθµό υποκειµενικότητας, αφού η χρήση του κυτταροµετρητή ροή αξιοποιείται από πολλούς αναλυτές στο σύγχρονο εργαστήριο. Οι εφαρµογές, λοιπόν, της κυτταροµετρίας είναι πολλές, αυξάνονται συνεχώς όσο εξελίσσονται οι τοµείς της µοριακής βιολογίας, της βιοχηµείας, της φυσικής και της ηλεκτρονικής τεχνολογίας, η παρουσία όµως ενός καταρτισµένου επιστήµονα θα παραµένει αναπόσπαστο κοµµάτι ενός έγκυρου αποτελέσµατος από έναν κυτταροµετρητή ροής. 88
89 ΕΙ ΙΚΟ ΜΕΡΟΣ 89
90
91 Σκοπός Σκοπός της εργασίας ήταν η µελέτη της έκφρασης των STAT πρωτεϊνών σε κυτταρικούς πληθυσµούς κατά την νεογνική λοίµωξη και ο προσδιορισµός ποιας από αυτές αποτελεί πρώιµο εργαστηριακό δείκτη για την ανίχνευση της νεογνικής σηψαιµίας. Ασθενείς και Μέθοδοι Μελετήθηκαν συνολικά 101 νεογνά, 79 πρόωρα (36 αγόρια, 38 κορίτσια) και 27 τελειόµηνα (18 αγόρια, 9 κορίτσια) που νοσηλεύθηκαν στη Β Νεογνολογική Κλινική ΜΕΝΝ του Α.Π.Θ. στο Γενικό Νοσοκοµείο Παπαγεωργίου κατά τη χρονική περίοδο Τα νεογνά ταξινοµήθηκαν σε δύο οµάδες την οµάδα Α και την οµάδα Β. οµάδα Α, «οµάδα λοίµωξης» περιελάµβανε 56 νεογνά που παρουσίασαν κλινικά και εργαστηριακά ευρήµατα συµβατά µε λοίµωξη. Τα νεογνά της οµάδας Α ανάλογα µε την επιβεβαιωµένη ή µη λοίµωξη διακρίθηκαν σε 2 υποοµάδες την Α1 (39 νεογνά µε επιβεβαιωµένη σηψαιµία και θετική καλλιέργεια αίµατος) και την Α2 (17 νεογνά µε πιθανή σηψαιµία που παρουσιάζει δυο κλινικά χαρακτηριστικά και δυο εργαστηριακούς δείκτες λοίµωξης αλλά αρνητική καλλιέργεια αίµατος). Η οµάδα Β (οµάδα ελέγχου) περιελάµβανε 45 νεογνά χωρίς εικόνα λοίµωξης που δεν παρουσίασαν εργαστηριακούς δείκτες λοίµωξης. Ως υποοµάδα σηψαιµίας (Α1) ορίστηκε η οµάδα που παρουσίασε θετική καλλιέργεια αίµατος. Ως φυσιολογικά τελειόµηνα νεογνά ορίστηκαν τα κανονικά για την ηλικία κύησης νεογνά µε ηλικία κύησης µεγαλύτερη από 38 συµπληρωµένες εβδοµάδες από την ηµεροµηνία έναρξης της τελευταίας έµµηνης ρύσης που γεννήθηκαν µετά από φυσιολογική κύηση, µε κολπικό τοκετό ή καισαρική τοµή, µε ελεύθερο περιγεννητικό ιστορικό. Ως φυσιολογικά πρόωρα νεογνά ορίστηκαν τα νεογνά µε ηλικία κύησης µικρότερη ή ίση µε 38 συµπληρωµένες εβδοµάδες από την ηµεροµηνία έναρξης της τελευταίας έµµηνης ρύσης. Ως πιθανή σηψαιµία ορίστηκε η ύπαρξη κλινικών ενδείξεων λοίµωξης (κακή κυκλοφορία, νωθρότητα, άπνοιες, σπασµοί, διάταση κοιλίας, γαστρικό υπόλειµµα, διαταραχές της θερµοκρασίας, παρουσία αναπνευστικής δυσχέρειας ή επίταση της ήδη υπάρχουσας, αιµορραγική διάθεση, ηπατοµεγαλία ή και σπληνοµεγαλία), µε δύο τουλάχιστον από τις παρακάτω εργαστηριακές ενδείξεις λοίµωξης: µεταβολική οξέωση (έλλειµα βάσεως>10meq/l), λευκοπενία(<4000/mm3), ουδετεροπενία (ΑΑΟ<1800/mm3), θροµβοπενία (αιµοπετάλια<100000/mm3), αυξηµένη CRP>15mg/L, PCT>2ng/mL). Ως επιβεβαιωµένη σηψαιµία ορίστηκε η ανεύρεση θετικής καλλιέργειας αίµατος. Ως σύνδροµο αναπνευστικής δυσχέρειας (ΣΑ ) ορίστηκε η παρουσία, κυρίως σε πρόωρα νεογνά, αναπνευστικής δυσχέρειας µε ταχύπνοια, γογγυσµό, εισολκές µεσοπλεύριων 91
92 ή/και κυάνωση, που εκδηλώθηκε τις πρώτες ώρες µετά τη γέννηση, συνοδεύεται ακτινογραφικά από την παρουσία διάσπαρτων δικτυοκοκκωδών σκιάσεων µε αεροβρογχόγραµµα ως πλήρη αδιαφάνεια των πνευµόνων και η οποία δε µπορεί να αποδοθεί σε άλλα αίτια (περιγεννητική λοίµωξη-πνευµονία). Ως περιγεννητική ασφυξία ορίστηκε σύµφωνα µε τα 4 κριτήρια που έχουν θεσπίσει η Αµερικανική Παιδιατρική Εταιρεία και το Αµερικανικό Κολλέγιο των Μαιευτήρων και Γυναικολόγων για τη διάγνωσή της. Τα κριτήρια αυτά είναι: 1) Μεταβολική ή µικτή οξέωση (ph<7) στο αίµα της οµφαλικής αρτηρίας. 2) Χαµηλό Apgar score (0-3) για περισσότερο από 5 λεπτά. 3) Κλινικά σηµεία νεογνικής εγκεφαλοπάθεια (σπασµοί, υποτονία, κώµα). 4) Ενδείξεις δυσλειτουργίας πολλών οργάνων στην αµέσως ακόλουθη νεογνική περίοδο. Από τη µελέτη αποκλείσθηκαν τα νεογνά που είχαν µείζονες ανωµαλίες κατασκευής, συγγενή καρδιοπάθεια, σοβαρή εγκεφαλική ανατοµική ανωµαλία. Σε όλα τα νεογνά λήφθηκε η συγκατάθεση γονέων για τη συµµετοχή του νεογνού στη µελέτη. Βάση του ερευνητικού πρωτοκόλλου που έχουµε υποβάλει, για κάθε νεογνό της µελέτης συµπληρωνόταν ειδικό έντυπο στο οποίο εκτός των δηµογραφικών στοιχείων του καταγράφονταν και στοιχεία που αφορούσαν τη διάγνωση του αρχικού τους νοσήµατος για το οποίο νοσηλεύονταν και της τρέχουσας λοίµωξης. Σε όλα τα νεογνά ελήφθη λεπτοµερές οικογενειακό, µαιευτικό, περιγεννητικό και νεογνικό ιστορικό. Το περιγεννητικό ιστορικό περιλάµβανε το ιστορικό της µητέρας, τη θεραπεία µε τοκόλυση ή και στεροειδή προγεννητικά, το χρόνο ρήξης των εµβρυικών υµένων, την παρουσία χοριοαµνιονίτιδας, την ηλικία κύησης, το βάρος γέννησης, τον τρόπο τοκετού, το Apgar score και τις πιθανές µαιευτικές επιπλοκές. Το νεογνικό ιστορικό περιλάµβανε, πριν την έναρξη της λοίµωξης, τα νεογνικά προβλήµατα, την τοποθέτηση ενδοαγγειακών ή άλλων καθετήρων, την εφαρµογή µηχανικού αερισµού, τη χορήγηση επιφανειοδραστικού παράγοντα τις θεραπευτικές παρεµβάσεις που έγιναν στο νεογνό. Καταγράφηκε επίσης η φυσική εξέταση και οι παράµετροι αύξησης και των βασικών λειτουργιών (θερµοκρασία, αριθµός αναπνοών, σφύξεων, αρτηριακή πίεση, ρυθµός διούρησης) Κατά την υποψία της λοίµωξης, στην έναρξή της και πριν από την είσοδο στη µελέτη έγινε κλινική και εργαστηριακή εκτίµηση του νεογνού. Συγκεκριµένα έγινε λεπτοµερής κλινική εξέταση, καταγράφηκαν οι βασικές ζωτικές λειτουργίες και ακολουθούθησε ειδικός εργαστηριακός έλεγχος λοιµώξεων που περιελάµβανε καλλιέργεια αίµατος, πλήρη αιµατολογικό έλεγχος λοίµωξης, µέτρηση της CRP και PCT, έλεγχο των δεικτών ηπατικής και νεφρικής λειτουργίας, ηλεκτρολύτες και οξεοβασική ισορροπία. 92
93 Τα στοιχεία που αφορούσαν τη λοίµωξη ήταν ευρήµατα από την κατά συστήµατα κλινική εξέταση και διάφορες εργαστηριακές εξετάσεις σχετικές µε την τεκµηρίωση της λοίµωξης. Από τα νεογνά της µελέτης εκτός από τον εργαστηριακό έλεγχο του πρωτοκόλλου λαµβάνονταν καλλιέργειες αίµατος από περιφερική φλέβα ή/και από κεντρικό φλεβικό ή αρτηριακό καθετήρα, καλλιέργειες άλλων βιολογικών υγρών του σώµατος και εγένοντο οι απαραίτητες απεικονιστικές µέθοδοι για τη διάγνωση της λοίµωξης, πριν την έναρξη της αντιµικροβιακής θεραπείας και στη συνέχεια µέχρι τη συλλογή των εργαστηριακών αποτελεσµάτων άρχιζε η χορήγηση εµπειρικού αντιµικροβιακού θεραπευτικού σχήµατος. Η παρακολούθηση των νεογνών περιλάµβανε καθηµερινή φυσική εξέταση, καταγραφή των ιατρικών θεραπευτικών χειρισµών και διενέργεια εργαστηριακών εξετάσεων. Μέθοδοι: Η πρώτη αιµοληψία των ασθενών των οµάδων γινόταν αµέσως µετά την υπόνοια της κλινικής σηµειολογίας της λοίµωξης και πριν ακόµη αρχίσει η αντιµικροβιακή θεραπευτική αγωγή. Περιελάµβανε αιµοληψία για την αιµοκαλλιέργεια, αιµατολογικούς, βιοχηµικούς, και ανοσοβιολογικούς προσδιορισµούς στις ακόλουθες χρονικές στιγµές την 1η µέρα, την 3η µέρα και τη 10η µέρα λοίµωξης. Προσδιορίζονταν ο αριθµός και ο τύπος των λευκών αιµοσφαιρίων, ο αριθµός των αιµοπεταλίων, η αιµοσφαιρίνη και ο αιµατοκρίτης, εγένετο πλήρης βιοχηµικός έλεγχος και προσδιορισµός οξεοβασικής ισορροπίας, γαλακτικού οξέος, CRP και PCT. Λαµβάνονταν καλλιέργειες αίµατος από περιφερική φλέβα ή περιφερική αρτηρία, αλλά και από κεντρικούς αρτηριακούς καθετήρες. Επίσης λαµβάνονταν καλλιέργειες ούρων και άλλων βιολογικών υγρών και γίνονταν οι απαραίτητες απεικονιστικές µέθοδοι για την εντόπιση της εστίας της λοίµωξης (ακτινολογικές µέθοδοι, υπερηχογραφήµατα). Ο προσδιορισµός της CRP στον ορό, έγινε µε τη µέθοδο της νεφελοµετρίας. Ο προσδιορισµός της PCT στον ορό έγινε µε χηµειοφωταύγεια (LUMItest-PCT, B.R.A.H.M.S Diagnostica GmbH Berlin) η οποία είναι ποσοτικό προσδιορισµός. Προσδιορισµός µε κυτταροµετρία ροής της ενδοκυττάριας έκφρασης των STAT1, STAT3, STAT4, STAT5 και STAT6 σε δείγµατα ολικού αίµατος µε EDTA: ΕΙ ΙΚΕΣ ΜΕΘΟ ΟΙ Ο προσδιορισµού της ενδοκυττάριας έκφρασης των STAT έγινε µε κυτταροµετρία ροής α) Κυτταροµετρία ροής: Από κάθε νεογνό της µελέτης τις χρονικές περιόδους που καθόριζε το πρωτόκολλο ελαµβάνοντο 4 ml ολικό αίµα µε EDTA. ιεχωρίζοντο σε 5 σωληνάρια που το κάθε ένα περιελάµβανε 500 µl και ένα σωληνάριο µε 500 µl που δεν θα επωασθεί. Στο κάθε σωληνάριο προσετίθεντο οι ενεργοποιητές όπως φαίνονται στον Πίνακα ανάλογα µε την STAT που θέλαµε να προσδιορίσουµε. 93
94 Συγκεκριµένα για την ενεργοποίηση προσθέτουµε για τη STAT1 τον ενεργοποιητή Recombinant Human IFN-γ τη STAT3 τον ενεργοποιητή Recombinant Human IL-6 τη STAT4 τον ενεργοποιητή Recombinant Human IFN-a τη STAT5 τον ενεργοποιητή Recombinant Human IL-2 τη STAT6 τον ενεργοποιητή Recombinant Human IL-4 Οι ενεργοποιητές προέρχονται από την R&D systems Οι STATs προέρχονται από την BD, Biosiences Μετά από επώαση του αίµατος µε τους ενεργοποιητές για 20min στους 37 ο C, µοιράζουµε ανά 100 µl το αίµα στα σωληνάκια και σε κάθε σωληνάκι προσθέτουµε 20µl CD45PC5. Κατόπιν ανάλογα ποια κύτταρα θέλουµε να προσδιορίσουµε προσθέτουµε 20µl µονοκλωνικού mouse anti-human CD4 ή mouse anti-human CD8 ή mouse anti-human CD14 και επωάζουµε σε θερµοκρασία δωµατίου για 20min. Ακολουθεί προσθήκη κυτταρολυτικού υγρού, επώαση και φυγοκέντρηση για 5min σε 2000 στροφές, και αφαιρούµε το υπερκείµενο. Προσθέτουµε 250µl από το Fixation Cytofix/cytoperm και µετά την ανάδευση ακολουθεί επώαση για 10min στο ψυγείο. Ακολουθούν δύο πλύσεις µε 1ml Perm/wash. Κατόπιν προσθέτουµε 20µl STAT επωάζουµε περίπου για 1 ώρα στο ψυγείο Πλένουµε µία φορά µε 1ml Perm/wash και αφαιρούµε το υπερκείµενο. Τέλος προσθέτουµε 500µl PBS για την ανασύσταση. Την ίδια διαδικασία ακολουθήσαµε και για τα µη ενεργοποιηµένα κύτταρα. Ο προσδιορισµός της έκφρασης των STATs γίνεται µε ανάλυση τριπλού ανοσοφθορισµού τουλάχιστον. Όλες οι STATs (STAT1, STAT3, STAT4, STAT5 και STAT6) πρωτεΐνες προσδιορίστηκαν στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4+, CD8+ Τ λεµφοκύτταρα, στα πολυµορφοπύρηνα και στα µονοκύτταρα. 94
95 ΣΤΑΤΙΣΤΙΚΗ ΑΝΑΛΥΣΗ Η στατιστική επεξεργασία των δεδοµένων απαρτίζεται από δύο µέρη: Στο πρώτο µέρος έγινε η περιγραφική στατιστική ανάλυση όλων των δεδοµένων υπολογίζοντας τις µέσες τιµές, το τυπικό σφάλµα της µέσης τιµής, τη µεγαλύτερη και µικρότερη τιµή των παραµέτρων. Για την σύγκριση των συχνοτήτων µεταξύ των διαφορετικών οµάδων (Α1p, A2p, A1t, και Bt) χρησιµοποιήθηκε το Χ 2 κριτήριο σε επίπεδο σηµαντικότητας 95% (αποδεκτές τιµές όταν p<0,05). Για την σύγκριση των µέσων τιµών µεταξύ των διαφορετικών οµάδων (Α1p, A2p, A1t, και Bt) χρησιµοποιήθηκε το t- testκριτήριο σε επίπεδο σηµαντικότητας 95% (αποδεκτές τιµές όταν p<0,05). Στη συνέχεια, στο δεύτερο µέρος, υπολογίστηκαν δύo δείκτες της στατιστικής επιδηµιολογίας, ο σχετικός κίνδυνος (RR) και ο λόγος πιθανοτήτων (OR) που δίνεται από τις σχέσεις: pexp osed RR = (1) p non exp osed OR non exp osed ( 1 pexp osed) ( 1 p ) pexp osed = (2) p non exp osed Ο σχετικός κίνδυνος (RR) εκφράζει τη πιθανότητα εµφάνισης µίας νόσου στην εκτεθειµένη οµάδα σε σχέση µε την οµάδα ελέγχου (τη µη εκτεθειµένη οµάδα). Ενώ, ο λόγος των πιθανοτήτων (OR) είναι ο λόγος των αποδόσεων του συµβάντος σε µία οµάδα µε τις πιθανότητες να συµβεί σε µια άλλη οµάδα. Οι παραπάνω δύο δείκτες εφαρµόστηκαν για ένα πλήθος συνδυασµών έξι παραγόντων. Ειδικότερα, ο αριθµός όλων των συνδυασµών των n ανά r συµβολίζεται µε P n,r. Έχουµε: P n,r =n(n-1) (n-r+1) Για παράδειγµα στη περίπτωση που υπολογίζονται ο σχετικός κίνδυνος (RR) και ο λόγος πιθανοτήτων (OR) για 6 παράγοντες ανά 2 συνδυασµούς, όλοι οι πιθανοί συνδυασµοί είναι P 6,2 =6 5=30 Μία άλλη πολύ γνωστή τεχνική στη στατιστική ιατρική είναι η χρήση της ευαισθησίας και της ειδικότητας των δοκιµών. Η Receiver Operating Characteristic (ROC) καµπύλη είναι η γραφική αναπαράσταση του ποσοστού των αληθώς θετικών δοκιµών (ευαισθησίας) σε σχέση µε ψευδώς θετικών δοκιµών (1- ειδικότητα). 95
96 Η αξιολόγηση µίας κλινικής δοκιµής µπορεί να γίνει µε τη χρήση των ROC καµπύλων και ειδικότερα αξιολογώντας τη περιοχή που βρίσκεται κάτω από την καµπύλη. Όταν η περιοχή αυτή είναι ίση µε το 1 τότε η κλινική δοκιµή παρουσιάζει ακρίβεια 100% και τόσο η ευαισθησία όσο και η ειδικότητα είναι ίσες µε 1 και δεν υπάρχουν λάθος θετικές ή αρνητικές µετρήσεις. ύο η περισσότερες δοκιµές µπορούν να συγκριθούν στατιστικά µεταξύ τους συγκρίνοντας τις περιοχές κάτω από τη καµπύλη. Τέλος, για να ολοκληρωθεί η µελέτη της ευαισθησίας και της ειδικότητας των δοκιµών χρησιµοποιήθηκε ο Youden δείκτης. Ο Youden δείκτης µπορεί να προσδιορίσει το βέλτιστο κρίσιµο σηµείο (όριο-threshold) των δοκιµών, ειδικότερα είναι µία συνάρτηση της ευαισθησίας και της ειδικότητας (445). J=maximum{sensitivity( c)+specificity( c)-1} Για κάθε c σηµείο της ROC καµπύλης Η τιµή του δείκτη κυµαίνεται από 0 έως 1, τιµές κοντά στο 1 υποδηλώνει µεγάλη αποτελεσµατικότητα της δοκιµής, ενώ τιµές κοντά στο 0 δηλώνει ότι η δοκιµή έχει περιορισµένη αποτελεσµατικότητα. Η στατιστική ανάλυση έγινε µε τη χρήση του στατιστικού πακέτου SPSS Statistics Software Package version 18 (SPSS Inc, Chicago, USA). Σκοπός της επεξεργασίας να µελετηθεί αν υπάρχουν στατιστικά σηµαντικές διαφορές στην έκφραση των STAT1, STAT3, STAT4, STAT5, STAT6 στα Τ λεµφοκύτταρα, στα πολυµορφοπύρηνα και στα µονοκύτταρα, τόσο στις οµάδες µεταξύ νεογνών που βρίσκονται σε λοίµωξη µε σύγκριση αυτών της οµάδας ελέγχου, αλλά και των 3 χρονικών στιγµών για την κάθε οµάδα των νεογνών µε λοίµωξη, ξεχωριστά. Οι πίνακες και τα σχήµατα έγιναν στο πρόγραµµα WORD, EXCEL, (WINDOWS XP) 96
97 ΑΠΟΤΕΛΕΣΜΑΤΑ Κλινικά στοιχεία των οµάδων των νεογνών που µελετήθηκαν Συνολικά µελετήθηκαν 101 νεογνά, τα οποία κατατάχθηκαν σε δύο οµάδες. Οµάδα Α: Νεογνά µε λοίµωξη-σηψαιµία: Μελετήθηκαν 56 πρόωρα και τελειόµηνα νεογνά και διακρίθηκαν στην υποοµάδα Α1 (επιβεβαιωµένη λοίµωξη) (n=39) και την Α2 (πιθανή λοίµωξη) (n=17). Στην οµάδα Α1 τα 34 νεογνά ήταν πρόωρα (A1 p ) και τα 5 νεογνά ήταν τελειόµηνα (A1 t ). Στην οµάδα Α2 τα 17 νεογνά ήταν πρόωρα (A2 p ). Οµάδα Β (οµάδα ελέγχου): Μελετήθηκαν 45 νεογνά χωρίς λοίµωξη, εκ των οποίων τα 23 νεογνά ήταν πρόωρα (B p ) και τα 22 τελειόµηνα (B t ). Στον πίνακα 1 φαίνονται το βάρος γέννησης (ΒΓ), η διάρκεια κύησης, το φύλο και η αναλογία αγοριών-κοριτσιών όλων των οµάδων (A1 p, A2 p, B p ) για τα πρόωρα και για τα τελειόµηνα (A1 t και B t ). Η µέση τιµή του βάρους και το τυπικό σφάλµα των νεογνών για κάθε οµάδα είναι: για την Α1 Ρ =1296,47±76,5, την Α2 Ρ =1438,23 ±132,7, την Β Ρ =1844,78 ±150,0, την A1 t =2788±157,8, την B t = 3202,72±106,7. Αντίστοιχα, η µέση διάρκεια κύησης σε εβδοµάδες για κάθε οµάδα είναι: για την Α1 Ρ =29,9±3,4, την Α2 Ρ =30,7 ±4,7, την Β Ρ =33,2 ±4,2, την A1 t =38±0,2, την B t = 39,0±1,26. Οι οµάδες των πρόωρων και τελειόµηνων νεογνών µε λοίµωξη που πήραν µέρος στη µελέτη ήταν συγκρίσιµες µε τις αντίστοιχες οµάδες ελέγχου αναφορικά µε την ηλικία κύησης και το βάρος γέννησης. Στατιστικά το δείγµα θεωρήθηκε επαρκές για στατιστική ανάλυση. ΠΙΝΑΚΑΣ 1. Νεογνικά χαρακτηριστικά των νεογνών της οµάδας Α1, A2 και Β Α1 Ρ Α2 Ρ B p A1 t B t ΑΡΙΘΜΟΣ ΒΓ(γρ.)(mean+SΕ, εύρος) Κ (εβδ.) 1296,47±76,5 1438,23 ±132,7 1844,78 ±150,0 2788±157,8 3202,72±106,7 (mean+se, εύρος) 29,9±3,4 30,7 ±4,7 33,2 ±4,2 38±0,2 39,0±1,26 Αγόρια n% 18 (52,9) 9(52,9) 9(39,1) 3(60,0) 15(68,2) Κορίτσια n% 16(47,1) 8(47,1) 14(60,9) 2(40,0) 7(31,8) 97
98 Στον πίνακα 2 φαίνονται τα περιγεννητικά χαρακτηριστικά των νεογνών των οµάδων Α1, Α2 και Β. Ακόµη, φαίνεται ο τρόπος διεκπεραίωσης του τοκετού (φυσιολογικός κολπικός τοκετός ή καισαρική τοµή). ΠΙΝΑΚΑΣ 2. Περιγεννητικά και νεογνικά χαρακτηριστικά των νεογνών και ο τρόπος διεκπεραίωσης του τοκετού των οµάδων Α1, Α2 και Β στα πρόωρα και τελειόµηνα Α1 Ρ A2-P B p A1 t B t Αριθµός νεογνών Στεροειδή προγεννητικά [n, (%)] 29 (85) 14(82) 18(78) 1(20) 0 ΡΕΥ>24ώρες [n,(%)] 6(17,6) 5(29) 2(8,7) 0 0 Κολπικός τοκετός[n, (%)] 1(2,9) 1(5,9) 3(23) 1(20) 6(27,2) Καισαρική τοµή[n, (%)] 33(97) 16(94) 20(87) 4(80) 16(72,7) Apgar1 o λεπτό 8[n,(%)] 13(38) 10(58,8) 18(78,2) 4(80) 15(68,2) ιασωλήνωση[n, (%)] 21(61,7) 13(76,5) 2(8,7) 3(60) 1(4,5) ιάρκεια νοσηλείας -ηµέρες ΜΕΑΝ ( ± Stdev) 50,0 (30,6) 40,6(23,4) 35,9(32,5) 19,8(36,2) 5,6(3,4) ΕΚΒΑΣΗ-ΘΑΝΑΤΟΣ[n, (%)] 6(17,6) 3(17,6) 0 1(20) 0 Στον πίνακα 2 φαίνεται ότι το 85% της οµάδας Α1 Ρ και το 82% της Α2 Ρ έλαβαν προγεννητικά στεροειδή, επίσης το 84,3% των νεογνών που παρουσίασε λοίµωξη (δηλαδή στο σύνολο των Α1 Ρ και Α2 Ρ οµάδων) και δεν διαφέρει σε ποσοστιαία αναλογία µε το ποσοστό των προώρων της οµάδας ελέγχου (78%). Το 21,5% των πρόωρων νεογνών που παρουσίασε λοίµωξη (οµάδες Α1 Ρ + Α2 Ρ ) είχε και πρόωρη ρήξη των εµβρυϊκών υµένων, ενώ το ποσοστό µε ΡΕΥ στην οµάδα B p ήταν µόνο 8,7%. Το µεγαλύτερο ποσοστό των πρόωρων νεογνών γεννήθηκε µε καισαρική τοµή (93,2%) και µόνο 6,7% των νεογνών γεννήθηκε µε κολπικό τοκετό. Το 45% των πρόωρων νεογνών που ανήκαν στην οµάδα λοιµώξεων (Α1 Ρ + Α2 Ρ ) είχαν Apgar score 8, ενώ το ποσοστό ήταν µεγαλύτερο 78,2% στην οµάδα B p. Σε ποσοστό 66,6% των νεογνών των οµάδων Α1 Ρ + Α2 Ρ στα πρόωρα χρειάστηκαν µηχανικό αερισµό και διασωλήνωση τις πρώτες ηµέρες ζωής, ενώ στην οµάδα B p το ποσοστό ήταν µόλις 8,7%. Η µέση διάρκεια νοσηλείας σε ηµέρες ήταν 50±30,6 και 40,6±23,4 για τις οµάδες Α1 Ρ και Α2 Ρ αντιστοίχως. Παρόµοια ήταν η µέση διάρκεια νοσηλείας για την οµάδα B p των προώρων (35,9±32,5 ηµέρες). Για τα τελειόµηνα µε λοίµωξη η µέση διάρκεια νοσηλείας ήταν 19,8±36,2 ηµέρες, ενώ για την οµάδα B t τελειόµηνων ήταν 5,6±3,4 ηµέρες. Ο θάνατος ήταν η έκβαση για το 17,6% των πρόωρων νεογνών µε λοίµωξη και αντίστοιχα στο 20% των τελειόµηνων νεογνών. 98
99 Στους πίνακες 3 και 4 αναφέρονται αντίστοιχα τα προβλήµατα κατά τη νοσηλεία των πρόωρων και τελειόµηνων πριν από την εκδήλωση της σηψαιµίας καθώς και τα κλινικά και εργαστηριακά ευρήµατα κατά την έναρξη της λοίµωξης. ΠΙΝΑΚΑΣ 3. Προβλήµατα των πρόωρων και τελειοµήνων πριν από την εκδήλωση της σηψαιµίας Α1 Ρ Α2 Ρ B p A1 t B t Αριθµός ασθενών (%) ΣΑ 25(73,5) 14(82,3) 4(17,4) 2(40) 0 Παροδική ταχύπνοια 0 0 4(17,4) 2(40) 5(22,7) Σύνδροµο διαφυγής 2(5,8) 0 1(4,3) 2(40) 2(9) Ανοικτός αρτ πόρος 11(32,3) 6(35,3) 2(8,6) 0 0 ΠΠΥΝ 1(2,9) 1(5,8) 0 1(20) 0 Περιγεννητικη ασφυξία 6(17,6) 3(17,6) 3(13) 1(20) 3(13,6) ιάταση πλαγίων/ PVL 3(8,8) 1(5,8) IVH III-IVέµφρακτο 3(8,8) 1(5,8) IURG 12(35,3) 2(11,7) 3(13) 0 1(4,5) ΑΠΝΟΙΑ 28(82,3) 16(94,1) 7(30,4) 3(60) 0 IVH εγκεφαλική αιµορραγία, ΠΠΥΝ παραµένουσα πνευµονική υπέρταση, IUGR ενδοµήτρια δυστροφία, ΑΑΠ ανοικτός αρτηριακός πόρος,,σα σύνδροµο αναπνευστικής δυσχέρειας Στα πρόωρα της µελέτης τα πιο συχνά προβλήµατα είναι οι άπνοιες (για την οµάδα Α1 Ρ 82,3% και Α2 Ρ 94,1%) και το ΣΑ (Α1 Ρ 73,5% και Α2 Ρ 82,3%) πριν από την έναρξη της λοίµωξης και ακολουθεί η ενδοµήτρια δυστροφία (IUGR) (Α1 Ρ 35,3% και Α2 Ρ 11,7%), η παραµονή ανοικτού αρτηριακού πόρου, η περιγεννητική ασφυξία και το παθολογικό υπερηχογράφηµα εγκεφάλου (διάταση πλαγίων κοιλιών, περικοιλιακή λευκοµαλάκυνση PVL και η σοβαρού βαθµού εγκεφαλική αιµορραγία (IVH III και IV) και το περικοιλιακό έµφρακτο). Άλλα προβλήµατα που παρουσιάστηκαν κατά τη νοσηλεία των πρόωρων νεογνών ήταν η παροδική ταχύπνοια, τα σύνδροµα διαφυγής και η παραµένουσα πνευµονική υπέρταση. Η συχνότητα των προβληµάτων, όπως η άπνοια και το ΣΑ, είναι µεγαλύτερη στις οµάδες Α1 Ρ και Α2 Ρ από ό,τι στην οµάδα B p, χωρίς όµως η διαφορά να είναι στατιστικά σηµαντική (p>0.05). Τα συχνότερα προβλήµατα των τελειόµηνων νεογνών πριν από την εκδήλωση της σηψαιµίας είναι οι άπνοιες (60%), τα αναπνευστικά προβλήµατα µε τις επιπλοκές τους (σύνδροµα διαφυγής, ΠΠΥΝ) και η περιγεννητική ασφυξία. Τα νεογνά που παρουσίασαν ΣΑ ήταν µόνο δύο, το ένα ήταν νεογνό διαβητικής µητέρας και το άλλο νεογνό µε περιγεννητική ασφυξία. Η σύγκριση των αποτελεσµάτων µεταξύ πρόωρων και τελειόµηνων νεογνών γενικά, έδειξε ότι οι συχνότητες των προβληµάτων δεν διαφέρουν σηµαντικά (p>0.05) για όλες τις περιπτώσεις. Ειδικότερα, θα µπορούσε να ειπωθεί ότι η περιγεννητική ασφυξία και η ενδοµήτρια δυστροφία είναι τα προβλήµατα που εµφανίζουν διαφορές στο όριο της 99
100 σηµαντικότητας µεταξύ της οµάδας ελέγχου B p και των οµάδων λοίµωξης Α1 Ρ και Α2 Ρ των προώρων (p= και p=0. 054, αντίστοιχα) Αν και η συχνότητα της ΠΠΥΝ ήταν συχνότερη στα τελειόµηνα νεογνά επιπλέκει συχνά το ΣΑ των προώρων, αν δεν γίνεται συστηµατικά διαγνωστικό υπερηχογράφηµα καρδιάς. ΠΙΝΑΚΑΣ 4. Κλινικά ευρήµατα κατά την έναρξη της λοίµωξης Α1 Ρ Α2 Ρ B p Α1 t B t Αριθµός ασθενών (%) Πυρετός >37,5 14(41,2) 10(58,8) 3(13) 4(80) 0 ιαταρ. περιφ. κυκλοφορίας, 25(73,5) 13(76,4) 1(4,3) 3(60) 0 ιατ. καρδιακού ρυθµού 26(76,4) 15(88,2) 4(17,4) 4(80) 0 Λοιµ. αναπνευστικού 1(2,9) 1(5,8) 0 1(20) 0 Πνευµ. αιµορραγία 2(5,88) 1(5,8) Ηπατοµεγαλία 19(55,8) 11(64,7) 0 3(60) 0 Κοιλιακή διάταση, γαστρικά υπόλοιπα 32(94,1) 15(88,2) 5(21,7) 4(80) 2(9) ΝΕΚ 8(23,5) 3(17,6) 0 1(20) 0 Καταπληξία 4(11,7) 0 0 1(20) 0 Μηνιγγίτιδα* 3(8,8) 2(11,7) 0 2(40) 0 *Το ποσοστό αναφέρεται στα 23/56 νεογνά στα οποία έγινε Ο.Ν.Π. Στον πίνακα 4 αναφέρονται οι κλινικές εκδηλώσεις των νεογνών µε σηψαιµία και πιθανή λοίµωξη. Συχνότερες κλινικές εκδηλώσεις είναι η κακή περιφερική κυκλοφορία (73,5% και 76,4% αντίστοιχα), οι διαταραχές καρδιακού ρυθµού(76,4% και 88,2% αντίστοιχα), η κοιλιακή διάταση και τα γαστρικά υπόλοιπα(94,1% και 88,2% αντίστοιχα). Λιγότερο συχνά ευρήµατα είναι η ηπατοµεγαλία και ο πυρετός. Η συχνότητα µε την οποίαα παρουσιάζουν τις κλινικές εκδηλώσεις τα πρόωρα είναι παρόµοια µε αυτή των τελειόµηνων. Ειδικότερα, ο πυρετός ήταν συχνότερος στα τελειόµηνα (80%) από ό,τι στα πρόωρα (41,2%), οι διαφορές των συχνοτήτων όµως είναι στατιστικά µη σηµαντικές (p=0.483). Η κοιλιακή διάταση είναι η κλινική εκδήλωση που εµφανίζει τις σηµαντικότερες διαφορές ανάµεσα στα πρόωρα και τελειόµηνα νεογνά, µε την Α2 Ρ οµάδα νεογνών να διαφέρει σηµαντικά από την αντίστοιχη οµάδα ελέγχου B p (p=0.03). Επίσης, οι συχνότερες επιπλοκές στα πρόωρα ήταν η ΝΕΚ (23,5%) και η µηνιγγίτιδα (8,8%), ενώ η πνευµονική αιµορραγία (5,88%) και η λοίµωξη αναπνευστικού (2,9%) ακολουθούσαν. Η οσφυονωτιαία παρακέντηση δεν έγινε στα πρόωρα νεογνά που η κλινική τους εικόνα ήταν βαριά και µεγάλος ο κίνδυνος της δηµιουργίας ή της επέκτασης της ενδοκοιλιακής αιµορραγίας λόγω αιµοδυναµικής αστάθειας, διαταραχών πήξης ή θροµβοπενίας. Καταγράφηκαν, επίσης, το επίπεδο συνείδησης, η εµφάνιση σπασµών, ο µυϊκός τόνος, η αυτόµατη ενεργητικότητα, η ανάγκη για υποστήριξη της αναπνευστικής λειτουργίας από µηχανικό αερισµό. 100
101 ΠΙΝΑΚΑΣ 5. Εργαστηριακά ευρήµατα κατά την έναρξη της λοίµωξης Οµάδα Α1 Ρ Οµάδα Α2 Ρ Οµάδα B p Σύνολο P Οµάδα A1 t Οµάδα B t T Σύνολο N (%) CRP >15 mg/l 21 (61,7) 14(82,3) 3(13) 38(51,3) 3(60) 4(18,2) 7(26) PCT 2 ng/ml 27 (79,4) 12(70,6) 2(8,7) 41(55,4) 5(100) 4(18,2) 9(33,3) Λευκοκυττάρωση 14 (41,2) 6(35,3) 8(34,8) 28(37,8) 4(80) 4(18,2) 8(29,6) Λευκοπενία 6 (17,6) 4(23,5) 12(52,2) 22(29,7) 1(20) 2(9,1) 3(11,1) Ουδετεροφιλία 15(44,1) 5(29,4) 10(43,5) 30(40,5) 4(80) 4(18,2) 8(29,6) Ουδετεροπενία 4(11,7) 2(11,7) 3(13) 9(12,2) Θροµβοκυττάρωση 3(8,8) 0 0 3(4) 1(20) 0 1(3,7) Θροµβοπενία 17(50) 7(41,2) 0 24(32,4) 4(80) 0 4(14,8) Υπεργλυκαιµία 11(32,3) 4(23,5) 0 15(20,2) Μετ. οξέωση 15(44,1) 6(35,3) 0 21(28,4) 4(80) 0 4(14,8) Γαλακτικό >2 mmol/l οξύ 22(64,7) 10(58,8) 0 32(43,2) 5(100) 0 5(18,5) Η C-αντιδρώσα πρωτεΐνη (CRP) και η προκαλσιτονίνη (PCT) είναι οι δύο κύριοι δείκτες λοίµωξης που καταγράφηκαν κατά την έναρξη, τη διάρκεια και την αποδροµή της λοίµωξης. Μελετήθηκαν τόσο στις οµάδες Α1 Ρ και Α2 Ρ αλλά και στην οµάδα B p. Θετικός δείκτης θεωρήθηκε η τιµή CRP>15mg/L. Η τιµή της κατά την έναρξη της λοίµωξης ήταν αυξηµένη µε στατιστικά σηµαντική διαφορά τόσο µεταξύ των οµάδων Α1 Ρ και B p (p=0,012) όσο και µεταξύ των οµάδων Α2 Ρ και B p (p=0,0017). επίσης, η διαφορά είναι στατιστικά σηµαντική και µεταξύ των οµάδων Α1 Ρ + Α2 Ρ σε σχέση µε τα νεογνά της οµάδας B p (p=0,001). Παθολογική τιµή PCT ορίστηκε η τιµή >2ng/mL. Η τιµή της PCT κατά την έναρξη της λοίµωξης ήταν αυξηµένη µε στατιστικά σηµαντική διαφορά τόσο στην οµάδα Α1 Ρ σε σχέση µε την οµάδα B p (p=0,007) όσο και στην οµάδα Α2 Ρ µε την B p (p=0,0013). Ακόµη, στατιστικά σηµαντική ήταν η διαφορά µεταξύ του συνόλου των λοιµώξεων Α1 Ρ + Α2 Ρ σε σχέση µε τα νεογνά της οµάδας B p (p=0,0009). Από τους αιµατολογικούς δείκτες που επηρεάζονται σε λοίµωξη, η θροµβοπενία ήταν συχνότερη στα τελειόµηνα (80%) συγκριτικά µε τα πρόωρα (47%). Από τους βιοχηµικούς δείκτες η παρουσία µεταβολικής οξέωσης (έλλειµµα βάσεων >10mEq/L) και η υπεργλυκαιµία (γλυκόζη αίµατος >180 mg/dl) ήταν στα πρόωρα νεογνά Α1 Ρ και Α2 Ρ 41,2% 101
102 και 29,4% αντίστοιχα. Στα τελειόµηνα η παρουσία µεταβολικής οξέωσης εµφανίζεται σε ποσοστό 80% των σηψαιµικών νεογνών. ΠΙΝΑΚΑΣ 6. Το είδος των µικροοργανισµών που αναπτύχθηκαν στην καλλιέργεια αίµατος στα νεογνά µε σηψαιµία Α1 Ρ A1 t σύνολο Μικροοργανισµοί n (%) n (%) n (%) Staphylococcus epidermidis 13 (38,2) 1 (20) 14 (35,98) Staphylococcus hominis 1(2,9) 1(2,5) Staphylococcus haemolyticus, 1(2,9) 1(2,5) Staphylococcus. auricularis 1(2,9) 1(2,5) Streptococcus agalactiae (GBS) 1(2,9) 1(2,5) Enterobacter cloace 2 (5,88) 2 (5) E.coli 3 (60) 3 (7,5) Enterobacter aerogenes 5 (14,7) 1 (20) 6 (15,38) Acinetobacter baumani 3 (8,8) 3 (7,5) Pseudomonas aeruginosa 1(2,9) 1(2,5) Klebsiella pneumoniae 2 (5,88) 2 (5,1) Candida parapsilosis 2 (5,88) 2 (5,1) Candida tropicalis 1 (2,9) 1 (2,5) Candida albicans 1 (2,9) 1 (2,5) Σύνολο Οι µικροοργανισµοί που αποµονώθηκαν από τις καλλιέργειες αίµατος των πρόωρων νεογνών είναι στελέχη enterobacter (20,6%), acinetobacter (8,8%), κλεµπσιέλλας (5,9%), ψευδοµονάδας (2,9%), σταφυλοκόκκου (47%), στρεπτοκόκκου (2,9%) και στελέχη κάντιντα (11,7%). Οι Gram+ µικροοργανισµοί αποτελούν το 50% των σηψαιµιών των πρόωρων. Οι Gram- αποτελούν το 38,2% των σηψαιµιών και οι µύκητες το 11,7%. Οι µικροοργανισµοί που αποµονώθηκαν από τις καλλιέργειες αίµατος των τελειόµηνων νεογνών είναι κολοβακτηρίδιο (60%), εντεροβακτηριδίο (20%) δηλαδή στο σύνολο οι Gram- µικροοργανισµοί φτάνουν το 80% και οι Gram+ (σταφυλόκοκκος) το 20% των σηψαιµιών των τελειόµηνων. Οι κυριότεροι προδιαθεσικοί παράγοντες για σηψαιµία φαίνονται στον πίνακα 7. Η συχνότητα των προδιαθεσικών παραγόντων δεν διαφέρει σηµαντικά µεταξύ των προόωρων και των τελειόµηνων νεογνών µε σηψαιµία (διαφορά µη σηµαντική στατιστικά, p>0,05 ). 102
103 Ο σχετικός κίνδυνος (Relative Risk) εµφάνισης της λοίµωξης κυµαίνεται από 1 έως 1,5 (Odds Ratio: 1,8-7,3), όταν υπάρχει ένας παράγοντας κινδύνου. Πιο συγκεκριµένα, αυξηµένος είναι ο κίνδυνος, όταν υπάρχουν διαταραχές σίτισης (δυσανοχή στην εντερική σίτιση και µετεωρισµός), και όταν τοποθετείται θωρακική παροχέτευση. Ο σχετικός κίνδυνος (RR) εµφάνισης της λοίµωξης είναι από 1,09 έως 1,62 (OR 1,38-7,32), όταν υπάρχουν 2 παράγοντες µαζί και ειδικότερα, όταν συνυπάρχουν οι διαταραχές στη σίτιση και η τοποθέτηση της θωρακικής παροχέτευσης. Ο σχετικός κίνδυνος εµφάνισης της λοίµωξης είναι 1,08 έως 1,44 (OR 2,1-6,5), όταν υπάρχουν τρεις παράγοντες και συγκεκριµένα οι διαταραχές στη σίτιση, η τοποθέτηση της θωρακικής παροχέτευσης και η παρατεταµένη ρήξη των εµβρυϊκών υµένων. Ο σχετικός κίνδυνος εµφάνισης της λοίµωξης είναι λίγο µικρότερος, όταν υπάρχουν τέσσερις παράγοντες και συγκεκριµένα οι διαταραχές στη σίτιση και η τοποθέτηση της θωρακικής παροχέτευσης, η παρατεταµένη ρήξη των εµβρυϊκών υµένων και η χορήγηση παρεντερικής διατροφής [RR: 1,09 έως 1,27 (OR 2,2-4,4)]. Ο σχετικός κίνδυνος εµφάνισης της λοίµωξης είναι 1,12 έως 1,2 (OR 2,4-3,6), όταν υπάρχουν πέντε παράγοντες, οι ίδιοι που αναφέρθηκαν παραπάνω σε συνδυασµό µε τη χρήση του µηχανικού αερισµού. Εδώ σηµειώνουµε ότι ο µηχανικός αερισµός µειώνει το σχετικό κίνδυνο και παρόλο που υπάρχουν και άλλοι παράγοντες που µπορεί να επιδεινώσουν τη λοίµωξη, φαίνεται ότι ο µηχανικός αερισµός σταθεροποιεί την κατάσταση του νεογνού, άρα µειώνει το σχετικό κίνδυνο. Στις ηµέρες µηχανικού αερισµού υπολογίζονται συνολικά όχι µόνο οι πρώτες, που το νεογνό χρειάζεται για τη σταθεροποίηση του αναπνευστικού του προβλήµατος, αλλά συνολικά και οι ηµέρες που απαιτείται µηχανικός αερισµός λόγω υποξαιµικών επεισοδίων και απνοιών. Ο σχετικός κίνδυνος εµφάνισης της λοίµωξης είναι 1,15 (OR 2,89), όταν υπάρχουν και οι έξι παράγοντες, δηλαδή όλοι οι παραπάνω παράγοντες σε συνδυασµό µε τη χρήση κεντρικών καθετήρων (οµφαλικών αγγείων ή κεντρικών φλεβικών καθετήρων). Είναι φανερό ότι η χρήση κεντρικών καθετήρων µειώνει τον κίνδυνο λοίµωξης και ελαττώνει το σχετικό κίνδυνο, ακόµη και όταν συνυπάρχουν άλλοι παράγοντες, όπως παρεντερική χορήγηση διατροφής, µηχανικός αερισµός, θεραπευτικές παρεµβάσεις, όπως θωρακική παροχέτευση, διαταραχές και δυσανοχή στην εντερική σίτιση. 103
104 ΠΙΝΑΚΑΣ 7. Προδιαθεσικοί παράγοντες για σηψαιµία στις οµάδες σηψαιµικών νεογνών παράγοντες Α1 Ρ Α2 Ρ B p A1 t B t n (%) n (%) n (%) n (%) n (%) ΡΕΥ 6 (17,6) 5(29,4) 2 (8,7) 0 0 Κεντρικοί καθετήρες (ΟΑ, ΟΦ, picc line, Hickmann) Ο.Π.. Μ.Α. (ηµέρες συνολικά) Θωρακική παροχέτευση ιαταραχές σίτισης 27 (79,4) 10 (58,8) 9 (39,1) 3 (60) 2(9) 32 (94,1) 17 (100) 20(86,9) 5 (100) 4(18,2) 25 (73,5) 13 (76,4) 7 (30,4) 3 (60) 1(4,5) 2 (5,88) 0 1(4,3) 2 (40) 2(9) 30 (88,2) 14 (82,3) 4(17,4) 3 (60) 2(9) ΡΕΥ= ρήξη εµβρυϊκών υµένων για περισσότερο από 24 ώρες Ο.Π..= ολική παρεντερική διατροφή Μ.Α. =µηχανικός αερισµός Ο.Α.= οµφαλική αρτηρία Ο.Φ.= οµφαλική φλέβα ΠΙΝΑΚΑΣ 8. Οµαδοποίηση της ηλικίας των νεογνών κατά την έναρξη της σηψαιµίας Οµάδα Α1 Ρ n(%) Α2 Ρ n(%) Α1 Ρ + Α2 Ρ n(%) A1 t n(%) Αριθµός νεογνών: Πρώιµη σηψαιµία ( 3η ηµέρα) 1 (2,9) 3 (17,6) 5 (9,8) 1 (20) Όψιµη σηψαιµία (3η-28η ηµέρα) 28 (82,3) 12 (70,5) 35(68,6) 4 (80) Πολύ όψιµη σηψαιµία (>28η ηµέρα) 5 (14,7) 2 (11,7) 7(13,7) 0 Πρώιµη νεογνική λοίµωξη παρουσίασε το 2,9% και το 17,6% των πρόωρων της οµάδας Α1 Ρ και Α2 Ρ αντίστοιχα. Το µεγαλύτερο ποσοστό των πρόωρων νεογνών εµφάνισε όψιµη σηψαιµία και συγκεκριµένα για την οµάδα Α1 Ρ το 82,3% για την οµάδα Α2 Ρ το 70% και συνολικά τις οµάδες Α1 Ρ + Α2 Ρ το 68,6%. Πρώιµη σηψαιµία είχε µόνο το 9,8% των πρόωρων νεογνών. Πολύ όψιµη σηψαιµία παρουσίασε το 13,7% (14,7% και 11,7% για την οµάδα Α1 Ρ και Α2 Ρ αντίστοιχα). Ανάλογα είναι τα ευρήµατα και για την οµάδα των τελειόµηνων νεογνών, όπου το 80% των νεογνών εµφάνισε όψιµη σηψαιµία. 104
105 ΠΙΝΑΚΑΣ 9. Εµφάνιση της σηψαιµίας σύµφωνα µε τη διάρκεια κύησης ιάρκεια κύησης >38 Αριθµός νεογνών n(%) n(%) n(%) n(%) n(%) Α1: επιβεβαιωµένη λοίµωξη 3(75) 15(48,4) 14(45,2) 2(25) 5(18,5) Α2: πιθανή λοίµωξη 0(0) 7(22,6) 7(22,6) 3(37,5) 0 Β: οµάδα ελέγχου 1(25) 9(29) 10(32,2) 3(37,5) 22(81,5) Σύνολο 4(100) 31(100) 31(100) 8(100) 27(100) Στον πίνακα 9 εµφανίζονται οι οµάδες των νεογνών ανάλογα µε τη διάρκεια κύησης και την προωρότητά τους. Έτσι, στα νεογνά από εβδοµάδες κύησης έχουµε εµφάνιση σηψαιµίας σε ποσοστό 85,3%(15+14/34) και 82,4% (7+7/17) αντίστοιχα για την οµάδα Α1 Ρ και Α2 Ρ. Παρατηρούµε ότι για ηλικίες κύησης 26 εβδοµάδες έχουµε µόνο 8,8%(3/34) σηψαιµία στο σύνολο των σηψαιµικών νεογνών και για τις ηλικίες από 35 εβδοµάδες και άνω το ποσοστό είναι 5,9% (2/34) και 17,6% (3/34) για Α1 Ρ και Α2 Ρ αντίστοιχα. Στο συνολικό αριθµό των πρόωρων µε ηλικίες κύησης 26, το 75% των νεογνών παρουσίασε σηψαιµία, στις ηλικίες εβδοµάδες το 70,9% παρουσίασε σηψαιµία, στις ηλικίες εβδοµάδες κύησης το 67,7%, στις ηλικίες εβδοµάδες κύησης το 62,5%, ενώ για τις ηλικίες >38 εβδοµάδες κύησης (τελειόµηνα) µόνο το 18,5% παρουσίασε σηψαιµία. 105
106 Αποτελέσµατα των µετρήσεων για τα CD3, CD4, CD8 Τα λεµφοκύτταρα και των STATs σε ενεργοποιηµένα και µη ενεργοποιηµένα κύτταρα. Πίνακας 1. Σύγκριση των τιµών των ενεργοποιηµένων CD3 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες CD3 A1 p A2 p A p B p A1 t B t t1 mean±se 44.01± ± ± ± ± ± (max-min) t2 mean±se 50.69± ± ± ±6.39 (max-min) t3 mean±se 50.04± ± ± ±6.62 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0,05 Πίνακας 2. Σύγκριση των τιµών των µη ενεργοποιηµένων CD3 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες CD3 A1 p A2 p A p B p A1 t B t t1 mean±se 42.61± ± ± ± ± ±2.53 (max-min) t2 mean±se 52.79± ± ± ±9.57 (max-min) t3 mean±se 48.87± ± ± ±6.44 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0,05 Στους πίνακες 1 και 2 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή στα ενεργοποιηµένα και µη ενεργοποιηµένα CD3 σε όλες τις οµάδες και η σύγκριση των τιµών των CD3(α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των ενεργοποιηµένων CD3 στην οµάδα Αp µεταξύ των t1 και t2 χρονικών στιγµών καθώς και 106
107 µεταξύ των t2 και t3 χρονικών στιγµών στην ίδια οµάδα ήταν στατιστικά σηµαντική (p=0,02 και p=0,04 αντίστοιχα). Επίσης η διαφορά των τιµών των µη ενεργοποιηµένων CD3 στην οµάδα Α1p µεταξύ των t1 και t2 χρονικών στιγµών ήταν στατιστικά σηµαντική (p=0,01) Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp στα ενεργοποιηµένα (p=0.00, p=0.00, p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.00, p=0.00 και p= 0.03 αντίστοιχα) Ενεργοποιηµένα CD3 Μη ενεργοποιηµένα CD3 CD A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mea Mea Mea Extr A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 20 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 3. Σύγκριση των τιµών των ενεργοποιηµένων CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες t 1 t 2 t 3 CD4 A1 p A2 p A p B p A1 t B t mean±se 29.07± ± ± ± ± ±1.91 (max-min) mean±se 35.89± ± ± ±5.08 (max-min) mean±se 37.07± ± ± ±7.88 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
108 Πίνακας 4. Σύγκριση των τιµών των µη ενεργοποιηµένων CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες t 1 t 2 t 3 CD4 A1 p A2 p A p B p A1 t B t mean±se 30.37± ± ± ± ± ±1.85 (max-min) mean±se 37.69± ± ± ±6.70 (max-min) mean±se 37.00± ± ± ±7.96 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 3 και 4 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4 σε όλες τις οµάδες και η σύγκριση των τιµών των CD4 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των ενεργοποιηµένων CD4 στην οµάδα Αp µεταξύ των t1 και t2 χρονικών στιγµών καθώς και µεταξύ των t1 και t3 χρονικών στιγµών στην ίδια οµάδα ήταν στατιστικά σηµαντική (p=0,01 και p=0,01 αντίστοιχα). Επίσης η διαφορά των τιµών των ενεργοποιηµένων CD4 της οµάδος Α1p είναι στατιστικά σηµαντική για τη σύγκριση µεταξύ των t1 και t3 (p=0,02). Επίσης η διαφορά των τιµών των µη ενεργοποιηµένων CD4 στην οµάδα Α1p µεταξύ των t1 και t2 χρονικών στιγµών και t1 και t3 ήταν στατιστικά σηµαντική (p=0,04 και p=0,04 αντίστοιχα). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp στα ενεργοποιηµένα (p=0.00, p=0.00, p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.00, p=0.00 και p= 0.03 αντίστοιχα) 108
109 Ενεργοποιηµένα CD4 Μη ενεργοποιηµένα CD4 CD A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 10 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 5. Σύγκριση των τιµών των ενεργοποιηµένων CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες CD8 A1 p A2 p A p B p A1 t B t t1 mean±se 17.70± ± ± ± ± ±1.18 (max-min) t2 mean±se 17.46± ± ± ±3.70 (max-min) t3 mean±se 15.73± ± ± ±3.60 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 6. Σύγκριση των τιµών των µη ενεργοποιηµένων CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες CD8 A1 p A2 p A p B p A1 t B t t1 mean±se 14.41± ± ± ± ± ±1.03 (max-min) t2 mean±se 17.84± ± ± ±5.01 (max-min) t3 mean±se 13.84± ± ± ±3.16 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
110 Στους πίνακες 5 και 6 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8 σε όλες τις οµάδες και η σύγκριση των τιµών των CD8 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των µη ενεργοποιηµένων CD8 είναι στατιστικά σηµαντική (p=0,05) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα A1p. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Ap σε χρόνο t1 µε την οµάδα Βp στα µη ενεργοποιηµένα (p=0.05). Ενεργοποιηµένο CD8 Μη ενεργοποιηµένα CD8 CD A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±S Mean±S Extreme -10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 4 2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 7. Σύγκριση των τιµών έκφρασης της STAT1 στα ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 I A1 p A2 p A p B p A1 t B t t1 mean±se 8.18± ± ± ± ± ±1.25 (max-min) t2 mean±se 9.31± ± ± ±3.51 (max-min) t3 mean±se 7.53± ± ± ±3.28 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
111 Πίνακας 8. Σύγκριση των τιµών έκφρασης της STAT1 στα µη ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 I A1 p A2 p A p B p A1 t B t t1 mean±se 6.23± ± ± ± ± ±0.90 (max-min) t2 mean±se 5.21± ± ± ±3.14 (max-min) t3 mean±se 2.66± ± ± ±1.30 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 7 και 8 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT1 στα ενεργοποιηµένα και µη ενεργοποιηµένα πολυµορφοπύρηνα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT1 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η.διαφορά των τιµών των STAT1 στα ενεργοποιηµένα πολυµορφοπύρηνα στην οµάδα Α1p µεταξύ των t2 και t3 χρονικών στιγµών καθώς και µεταξύ των t1 και t2 χρονικών στιγµών στην οµάδα Α2p ήταν στατιστικά σηµαντική (p=0,05 και p=0,03 αντίστοιχα). Επίσης η.διαφορά των τιµών των µη ενεργοποιηµένων πολυµορφοπυρήνων στην οµάδα Α1p µεταξύ των t1 και t2 χρονικών στιγµών ήταν στατιστικά σηµαντική (p=0,01) Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp στα ενεργοποιηµένα (p=0.00, p=0.00 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.01 και p= 0.03 αντίστοιχα) 111
112 Ενεργοποιηµένα STAT1 I Μη ενερργοποιηµένα STAT1 Ι STAT1 I A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -2-4 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 9. Σύγκριση των τιµών έκφρασης της STAT1 στα ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 J A1 p A2 p A p B p A1 t B t t1 mean±se 6,74±1,24 6,29±1,14 6,72±1, ± ± ±0.90 (maxmin) 36,00-0,20 13,00-0,08 36,00-0, t2 mean±se 8,82±1,11 6,93±2,04 8,10±1, ±1.61 (maxmin) 32,00-0,11 32,00-0,65 32,00-0, t3 mean±se 9,63±2,20 9,78±3,11 10,13±2, ±2.63 (maxmin) 48,80-0,33 21,30-0,53 48,80-0, P0 0,31 0,27 0, P1 0,11 0,39 0, P2 0,13 0,16 0, P3 0,37 0,23 0, *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 10. Σύγκριση των τιµών έκφρασης της STAT1 στα µη ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 J A1 p A2 p A p B p A1 t B t t1 mean±se 4.64± ± ± ± ± ±0.74 (max-min) t2 mean±se 6.16± ± ± ±0.98 (max-min) t3 mean±se 2.62± ± ± ±1.57 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) 112
113 *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 9 και 10 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT1 στα ενεργοποιηµένα και µη ενεργοποιηµένα µονοκύτταρα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT1 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η.διαφορά των τιµών των STAT1 στα µη ενεργοποιηµένα µονοκύτταρα στην οµάδα Α1p µεταξύ των t2 και t3 χρονικών στιγµών ήταν στατιστικά σηµαντική (p=0,05). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.01) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.00 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT1 J Μη ενερργοποιηµένα STAT1 J STAT1 J A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-5 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 11. Σύγκριση των τιµών έκφρασης της STAT1 στα ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 D A1 p A2 p A p B p A1 t B t t1 mean±se 5.59± ± ± ± ± ±0.39 (max-min) t2 mean±se 7.34± ± ± ±2.28 (max-min) t3 mean±se 4.46± ± ± ±2.89 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
114 Πίνακας 12. Σύγκριση των τιµών έκφρασης της STAT1 στα µη ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 D A1 p A2 p A p B p A1 t B t t1 mean±se 3.35± ± ± ± ± ±0.2 6 (max-min) t2 mean±se 4.47± ± ± ±2.42 (max-min) t3 mean±se 1.78± ± ± ±1.77 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 11 και 12 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT1 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT1 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η.διαφορά των τιµών των STAT1 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4 στην οµάδα Α1p µεταξύ των t2 και t3 χρονικών στιγµών στην ίδια οµάδα ήταν στατιστικά σηµαντική (p=0,02 και p=0,05 αντίστοιχα). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp στα ενεργοποιηµένα (p=0.00, p=0.00, p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.00 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT1 D Μη ενεργοποιηµένα STAT1 D STAT1 D A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-5 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes 114
115 Πίνακας 13. Σύγκριση των τιµών έκφρασης της STAT1 στα ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 E A1 p A2 p A p B p A1 t B t t1 mean±se 21.24± ± ± ± ± ± (max-min) t2 mean±se 23.52± ± ± ± (max-min) t3 mean±se 15.63± ± ± ± (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 14. Σύγκριση των τιµών έκφρασης της STAT1 στα µη ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT1 E A1 p A2 p A p B p A1 t B t t1 mean±se 19.41± ± ± ± ± ±3.28 (maxmin) t2 mean±se 22.29± ± ± ±7.16 (maxmin) t3 mean±se 15.32± ± ± ± (maxmin) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Σ Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 13 και 14 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT1 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT1 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη 115
116 διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η.διαφορά των τιµών των STAT1 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8 στην οµάδα Α1p µεταξύ των t2 και t3 χρονικών στιγµών είναι στατιστικά σηµαντική (p=0,02 και p=0,05 αντίστοιχα). Επίσης η.διαφορά των τιµών των STAT1 των ενεργοποιηµένων CD8 στην οµάδα Αp µεταξύ των t2 και t3 χρονικών στιγµών ήταν στατιστικά σηµαντική (p=0,03). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.00, p=0.02 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.03, p=0.02 και p= 0.00 αντίστοιχα). Ενεργοποιηµένα STAT1 E Μη ενερργοποιηµένα STAT1 Ε 70 STAT1 E A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 15. Σύγκριση των τιµών έκφρασης της STAT3 στα ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 I A1 p A2 p A p B p A1 t B t t1 mean±se 11.71± ± ± ± ± ±2.21 (max-min) t2 mean±se 14.12± ± ± ±7.02 (max-min) t3 mean±se 10.03± ± ± ±5.78 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
117 Πίνακας 16. Σύγκριση των τιµών έκφρασης της STAT3 στα µη ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 I A1 p A2 p A p B p A1 t B t t1 mean±se 11.41± ± ± ± ± ±2.14 (max-min) t2 mean±se 10.84± ± ± ±4.40 (max-min) t3 mean±se 6.38± ± ± ±3.54 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 15 και 16 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή STAT3 στα ενεργοποιηµένα και µη ενεργοποιηµένα πολυµορφοπύρηνα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT3 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η.διαφορά των τιµών των STAT3 στα µη ενεργοποιηµένα πολυµορφοπύρηνα στην οµάδα Α1p µεταξύ των t2 και t3 χρονικών στιγµών ήταν στατιστικά σηµαντική (p=0,05). Επίσης η.διαφορά των τιµών των STAT3 στα ενεργοποιηµένα πολυµορφοπύρηνα στην οµάδα Αp µεταξύ των t2 και t3 χρονικών στιγµών ήταν στατιστικά σηµαντική (p=0,03). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.00, p=0.00, p=0.00 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp στα µη ενεργοποιηµένα (p=0.00 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT3 I Μη ενερργοποιηµένα STAT3 I STAT3 I A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes 117
118 Πίνακας 17. Σύγκριση των τιµών έκφρασης της STAT3 στα ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 J A1 p A2 p A p B p A1 t B t t1 mean±se 10.67± ± ± ± ± ±2.31 (max-min) t2 mean±se 15.11± ± ± ±3.98 (max-min) t3 mean±se 15.09± ± ± ±5.09 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 18. Σύγκριση των τιµών έκφρασης της STAT3 στα µη ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 J A1 p A2 p A p B p A1 t B t t1 mean±se 11.23± ± ± ± ± ±2.14 (max-min) t2 mean±se 12.11± ± ± ±1.89 (max-min) t3 mean±se 11.43± ± ± ±3.35 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 17 και 18 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή STAT3 στα ενεργοποιηµένα και µη ενεργοποιηµένα µονοκύτταρα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT3 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η.διαφορά των τιµών των STAT3 στα µη ενεργοποιηµένα µονοκύτταρα στην οµάδα Α1p µεταξύ των t2 και t3 χρονικών στιγµών ήταν στατιστικά σηµαντική 118
119 (p=0,05). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.00) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.00 και p= 0.05 αντίστοιχα) Ενεργοποιηµένα STAT3 J Μη ενερργοποιηµένα STAT3 J STAT3 J A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 19. Σύγκριση των τιµών έκφρασης της STAT3 στα ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 D A1 p A2 p A p B p A1 t B t t1 mean±se 12.99± ± ± ± ± ±4.71 (max-min) t2 mean±se 16.88± ± ± ±6.11 (max-min) t3 mean±se 15.36± ± ± ±12.51 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 20. Σύγκριση των τιµών έκφρασης της STAT3 στα µη ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 D A1 p A2 p A p B p A1 t B t t1 mean±se 11.60± ± ± ± ± ±3.19 (max-min) t2 mean±se 13.33± ± ± ±3.42 (max-min) t3 mean±se 12.77± ± ± ±6.31 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β 119
120 *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 19 και 20 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT3 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT3 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT3 στα µη ενεργοποιηµένα CD4 είναι στατιστικά σηµαντική (p=0.05) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα A1p. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.01, p=0.03, p=0.04 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.02 και p= 0.05 αντίστοιχα) Ενεργοποιηµένα STAT3 D Μη ενερργοποιηµένα STAT3 D STAT3 D A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 21. Σύγκριση των τιµών έκφρασης της STAT3 στα ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 E A1 p A2 p A p B p A1 t B t t1 mean±se 43.42± ± ± ± ± ±9.87 (max-min) t2 mean±se 44.17± ± ± ±12.53 (max-min) t3 mean±se 40.51± ± ± ± (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β 120
121 *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 22. Σύγκριση των τιµών έκφρασης της STAT3 στα µη ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT3 E A1 p A2 p A p B p A1 t B t t1 mean±se 42.69± ± ± ± ± ± (max-min) t2 mean±se 41.27± ± ± ±10.12 (max-min) t3 mean±se 34.81± ± ± ±15.19 (max-min) P0 0, P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 21 και 22 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή STAT3 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT3 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η.διαφορά των τιµών των STAT3 στα µη ενεργοποιηµένα CD8 στην οµάδα Α1p µεταξύ των t2 και t3 χρονικών στιγµών ήταν στατιστικά σηµαντική (p=0,05). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.00, p=0.01, p=0.00 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp στα µη ενεργοποιηµένα (p=0.00 και p= 0.00 αντίστοιχα). Ενεργοποιηµένα STAT3 E Μη ενερργοποιηµένα STAT3 Ε STAT3 E A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-20 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-20 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes 121
122 Πίνακας 23. Σύγκριση των τιµών έκφρασης της STAT4 στα ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4 I A1 p A2 p A p B p A1 t B t t1 mean±se 6.94± ± ± ± ± ±1.27 (max-min) t2 mean±se 8.18± ± ± ±0.86 (max-min) t3 mean±se 9.50± ± ± ±1.14 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 24. Σύγκριση των τιµών έκφρασης της STAT4 στα µη ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4 I A1 p A2 p A p B p A1 t B t t1 mean±se 7.25± ± ± ± ± ±0.75 (max-min) t2 mean±se 7.28± ± ± ±1.38 (max-min) t3 mean±se 4.87± ± ± ±4.53 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 23 και 24 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT4 στα ενεργοποιηµένα και µη ενεργοποιηµένα πολυµορφοπύρηνα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT4 στα πολυµορφοπύρηνα (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT4 στα µη ενεργοποιηµένα στα 122
123 πολυµορφοπύρηνα είναι στατιστικά σηµαντική (p=0,05) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα A1p, η διαφορά των τιµών των STAT4 στα ενεργοποιηµένα πολυµορφοπύρηνα είναι στατιστικά σηµαντική (p<0,001) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα A1t και τέλος η διαφορά των τιµών των STAT4 στα ενεργοποιηµένα πολυµορφοπύρηνα είναι στατιστικά σηµαντική (p=0,01) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα A1t. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.00) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.04, p=0.01 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT4 I Μη ενερργοποιηµένα STAT4 I STAT4 I A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 25. Σύγκριση των τιµών έκφρασης της STAT4 στα ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4 J A1 p A2 p A p B p A1 t B t t1 mean±se 2.77± ± ± ± ± ±0.6 5 (max-min) t2 mean±se 4.86± ± ± ±0.15 (max-min) t3 mean±se 7.01± ± ± ±1.23 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
124 Πίνακας 26. Σύγκριση των τιµών έκφρασης της STAT4 στα µη ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4J A1 p A2 p A p B p A1 t B t t1 mean±se 2.80± ± ± ± ± ±0.48 (max-min) t2 mean±se 5.39± ± ± ±0.27 (max-min) t3 mean±se 3.74± ± ± ±2.34 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 25 και 26 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT4 στα ενεργοποιηµένα και µη ενεργοποιηµένα µονοκύτταρα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT4 στα µονοπύρηνα (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT4 στα µη ενεργοποιηµένα στα µονοκύτταρα είναι στατιστικά σηµαντική (p=0,03) µεταξύ των t1 και t2 χρονικών στιγµών για την οµάδα A1p, η διαφορά των τιµών των STAT4 στα ενεργοποιηµένα µονοπύρηνα είναι στατιστικά σηµαντική (p<0,03) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα A1p και τέλος η διαφορά των τιµών των STAT4 στα ενεργοποιηµένα µονοκύτταρα είναι στατιστικά σηµαντική (p=0,02) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα Ap.. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.00) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00) Ενεργοποιηµένα STAT4 J Μη ενερργοποιηµένα STAT4 J STAT4 J A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes 124
125 Πίνακας 27. Σύγκριση των τιµών έκφρασης της STAT4 στα ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4 D A1 p A2 p A p B p A1 t B t t1 mean±se 3.49± ± ± ± ± ±1.04 (max-min) t2 mean±se 4.60± ± ± ±0.40 (max-min) t3 mean±se 4.76± ± ± ±0.88 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 28. Σύγκριση των τιµών έκφρασης της STAT4 στα µη ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4 D A1 p A2 p A p B p A1 t B t t1 mean±se 3.47± ± ± ± ± ±0.71 (max-min) t2 mean±se 5.25± ± ± ±1.19 (max-min) t3 mean±se 3.02± ± ± ±3.05 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 27 και 28 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή STAT4 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT4 (α)µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT4 στα µη ενεργοποιηµένα CD4 είναι στατιστικά σηµαντική (p=0,04) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα A1p, η διαφορά των τιµών των STAT4 στα µη ενεργοποιηµένα CD4 είναι στατιστικά σηµαντική (p=0,03) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα A2p και τέλος η διαφορά των τιµών των STAT4 στα µη 125
126 ενεργοποιηµένα CD4 είναι στατιστικά σηµαντική (p=0,03) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα Ap. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.01) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A2p και Ap µε την οµάδα Βp στα µη ενεργοποιηµένα (p=0.03 και p= 0.01 αντίστοιχα) Ενεργοποιηµένα STAT4 D Μη ενερργοποιηµένα STAT4 D STAT4 D A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-5 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 29. Σύγκριση των τιµών έκφρασης της STAT4 στα ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4 E A1 p A2 p A p B p A1 t B t t1 mean±se 16.24± ± ± ± ± ±1.80 (max-min) t2 mean±se 18.93± ± ± ±6.44 (max-min) t3 mean±se 13.42± ± ± ±3.48 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 30. Σύγκριση των τιµών έκφρασης της STAT4 στα µη ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT4 Ε A1 p A2 p A p B p A1 t B t t1 mean±se 15.36± ± ± ± ± ±1.73 (max-min) t2 mean±se 18.88± ± ± ±7.39 (max-min) t3 mean±se 12.71± ± ± ±3.71 (max-min) P P P P
127 *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 29 και 30 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT4 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT4 στα CD8 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT4 στα µη ενεργοποιηµένα CD8 είναι στατιστικά σηµαντική (p=0,04) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα A1p, η διαφορά των τιµών των STAT4 στα µη ενεργοποιηµένα CD8 είναι στατιστικά σηµαντική (p=0,03) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα A2p και τέλος η διαφορά των τιµών των STAT4 στα µη ενεργοποιηµένα CD8 είναι στατιστικά σηµαντική (p=0,03) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα Ap. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p= 0.04) Ενεργοποιηµένα STAT4 E Μη ενερργοποιηµένα STAT4 Ε STAT4 E A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 31. Σύγκριση των τιµών έκφρασης της STAT5 στα ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5 I A1 p A2 p A p B p A1 t B t t1 mean±se 5.23± ± ± ± ± ±1.05 (max-min) t2 mean±se 4.76± ± ± ±1.10 (max-min) t3 mean±se 4.91± ± ± ±1.37 (max-min) P P P P
128 *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 32. Σύγκριση των τιµών έκφρασης της STAT5 στα µη ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5 I A1 p A2 p A p B p A1 t B t t1 mean±se 5.08± ± ± ± ± ±0.8 (max-min) t2 mean±se 4.25± ± ± ±0.76 (max-min) t3 mean±se 5.29± ± ± ±1.22 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT5 στα ενεργοποιηµένα και µη ενεργοποιηµένα πολυµορφοπύρηνα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT5 στα πολυµορφοπύρηνα (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT5 στα ενεργοποιηµένα πολυµορφοπύρηνα είναι στατιστικά σηµαντική (p=0,04) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα Α1t, η διαφορά των τιµών των STAT5 στα µη ενεργοποιηµένα πολυµορφοπύρηνα είναι στατιστικά σηµαντική (p=0,04) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα A1t.. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.02 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.02, p=0.00 και p= 0.00 αντίστοιχα) 128
129 Ενεργοποιηµένα STAT5 I Μη ενερργοποιηµένα STAT5 I STAT5 I A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 33. Σύγκριση των τιµών έκφρασης της STAT5 στα ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5 J A1 p A2 p A p B p A1 t B t t1 mean±se 2.96± ± ± ± ± ±0.67 (max-min) t2 mean±se 3.07± ± ± ±0.27 (max-min) t3 mean±se 3.21± ± ± ±0.44 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 34. Σύγκριση των τιµών έκφρασης της STAT5 στα µη ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5 J A1 p A2 p A p B p A1 t B t t1 mean±se 2.93± ± ± ± ± ±0.38 (max-min) t2 mean±se 3.10± ± ± ±0.26 (max-min) t3 mean±se 2.31± ± ± ±0.47 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
130 Στους πίνακες 33 και 34 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT5 στα ενεργοποιηµένα και µη ενεργοποιηµένα µονοκύτταρα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT5 στα µονοκύτταρα (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT5 στα ενεργοποιηµένα και στα µη ενεργοποιηµένα στα µονοκύτταρα δεν είναι στατιστικά σηµαντική µεταξύ των χρονικών στιγµών για την οµάδα A1p, Ap και Α1t..Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.03, p=0.02 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT5 J Μη ενερργοποιηµένα STAT5 J STAT5 J A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -1-2 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 35. Σύγκριση των τιµών έκφρασης της STAT5 στα ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5 D A1 p A2 p A p B p A1 t B t t1 mean±se 2.34± ± ± ± ± ±0.59 (max-min) t2 mean±se 3.01± ± ± ±0.27 (max-min) t3 mean±se 2.39± ± ± ±0.43 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
131 Πίνακας 36. Σύγκριση των τιµών έκφρασης της STAT5 στα µη ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5D A1 p A2 p A p B p A1 t B t t1 mean±se 2.02± ± ± ± ± ±0.53 (max-min) t2 mean±se 2.79± ± ± ±0.29 (max-min) t3 mean±se 2.59± ± ± ±0.49 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 35 και 36 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT5 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT5 στα CD4 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT5 στα ενεργοποιηµένα CD4 δεν είναι στατιστικά σηµαντική για τη σύγκριση µεταξύ των χρονικών στιγµών των Α1p στα ενεργοποιηµένα και µη ενεργοποιηµένα. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα ( p=0.04 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.03, p=0.02 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT5 D Μη ενερργοποιηµένα STAT5 D STAT5 D A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -20 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-1 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes 131
132 Πίνακας 37. Σύγκριση των τιµών έκφρασης της STAT5 στα ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5 E A1 p A2 p A p B p A1 t B t t1 mean±se 15.87± ± ± ± ± ±2.99 (max-min) t2 mean±se 17.67± ± ± ±2.58 (max-min) t3 mean±se 10.79± ± ± ±4.32 (max-min) P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 38. Σύγκριση των τιµών έκφρασης της STAT5 στα µη ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT5E A1 p A2 p A p B p A1 t B t t1 mean±se 13.96± ± ± ± ± ±2.51 (max-min) t2 mean±se 17.39± ± ± ±3.80 (max-min) t3 mean±se 14.22± ± ± ±3.35 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 37 και 38 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT5 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT5 στα CD8 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT5 στα ενεργοποιηµένα CD8 είναι στατιστικά σηµαντική (p=0,03) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα A1p, η διαφορά των τιµών των STAT5 στα ενεργοποιηµένα CD8 είναι στατιστικά σηµαντική (p=0,05) µεταξύ των t2 και t3 χρονικών στιγµών για την οµάδα Ap. Παρατηρήθηκε στατιστικά σηµαντική διαφορά 132
133 στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.03, p=0.02 και p=0.04 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p= 0.05) Ενεργοποιηµένα STAT5 E Μη ενερργοποιηµένα STAT5 Ε STAT5 E A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±S Mean±S Extreme 0-10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 Πίνακας 39. Σύγκριση των τιµών έκφρασης της STAT6 στα ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes STAT6 I A1 p A2 p A p B p A1 t B t T1 mean±se 17.83± ± ± ± ± ±4.36 (max-min) T2 mean±se 17.25± ± ± ±7.70 (max-min) T3 mean±se 17.53± ± ± ±8.27 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 40. Σύγκριση των τιµών έκφρασης της STAT6 στα µη ενεργοποιηµένα πολυµορφοπύρηνα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT6 I A1 p A2 p A p B p A1 t B t t1 mean±se 13.60± ± ± ± ± ±3.43 (max-min) t2 mean±se 13.84± ± ± ±7.62 (max-min) t3 mean±se 11.65± ± ± ±5.60 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β 133
134 *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 39 και 40 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT6 στα ενεργοποιηµένα και µη ενεργοποιηµένα πολυµορφοπύρηνα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT6 στα πολυµορφοπύρηνα (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT6 στα µη ενεργοποιηµένα πολυµορφοπύρηνα είναι στατιστικά σηµαντική (p=0,05) µεταξύ των t1 και t3 χρονικών στιγµών για την οµάδα Α1t. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp και Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.04, p=0.02, p=0.00 και p=0.04 αντίστοιχα) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.02, p=0.01 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT6I Μη ενεργοποιηµένα STAT6 I STAT6 I A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 41. Σύγκριση των τιµών έκφρασης της STAT6 στα ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT6 J A1 p A2 p A p B p A1 t B t t1 mean±se 12.51± ± ± ± ± ±4.70 (max-min) t2 mean±se 16.59± ± ± ±4.48 (max-min) t3 mean±se 18.75± ± ± ±5.45 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<
135 Πίνακας 42. Σύγκριση των τιµών έκφρασης της STAT6 στα µη ενεργοποιηµένα µονοκύτταρα κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT6 J A1 p A2 p A p B p A1 t B t t1 mean±se 8.51± ± ± ± ± ±3.39 (max-min) t2 mean±se 11.61± ± ± ±3.58 (max-min) t3 mean±se 9.13± ± ± ±4.07 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 41 και 42 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT6 στα ενεργοποιηµένα και µη ενεργοποιηµένα µονοκύτταρα σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT6 στα µονοκύτταρα (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών έκφρασης της STAT6 στα ενεργοποιηµένα µονοκύτταρα στην οµάδα A1p και Ap µεταξύ των t1 και t3 χρονικών στιγµών βρίσκεται στο όριο της σηµαντικότητας (p=0,06 και p=0,06 αντίστοιχα). Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A2p σε χρόνο t1 µε την οµάδα Βp στα ενεργοποιηµένα (p=0.04) και στατιστικά σηµαντική διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.00, p=0.00 και p= 0.00 αντίστοιχα. Ενεργοποιηµένα STAT6 J Μη ενεργοποιηµένα STAT6 J STAT6 J A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 Πίνακας 43. Σύγκριση των τιµών έκφρασης της STAT6 στα ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-5 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes 135
136 STAT6 D A1 p A2 p A p B p A1 t B t t1 mean±se 11.74± ± ± ± ± ±4.38 (max-min) t2 mean±se 13.45± ± ± ±4.30 (max-min) t3 mean±se 11.52± ± ± ±7.88 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 44. Σύγκριση των τιµών έκφρασης της STAT6 στα µη ενεργοποιηµένα CD4 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT6 D A1 p A2 p A p B p A1 t B t t1 mean±se 8.27± ± ± ± ± ±2.90 (max-min) t2 mean±se 10.04± ± ± ±4.76 (max-min) t3 mean±se 7.75± ± ± ±3.95 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 43 και 44 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT6 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT6 στα CD4 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT6 στα ενεργοποιηµένα CD4 δεν είναι στατιστικά σηµαντική για τη σύγκριση µεταξύ των χρονικών στιγµών των Α1p, A2p, Ap, και A1t στα ενεργοποιηµένα και µη ενεργοποιηµένα CD4. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας A1p, A2p και Ap σε χρόνο t1 µε την οµάδα Βp στα ενεργοποιηµένα (p=0.03, p=0.02 και p=0.00 αντίστοιχα) και στατιστικά σηµαντική 136
137 διαφορά στη σύγκριση σε χρόνο t1 µεταξύ της οµάδας A1p και Ap µε την οµάδα Βp και Α1t µε την οµάδα Bt στα µη ενεργοποιηµένα (p=0.02, p=0.00 και p= 0.00 αντίστοιχα) Ενεργοποιηµένα STAT6 D Μη ενεργοποιηµένα STAT6 D STAT6 D A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes -10 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes Πίνακας 45. Σύγκριση των τιµών έκφρασης της STAT6 στα ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT6 E A1 p A2 p A p B p A1 t B t t1 mean±se 26.68± ± ± ± ± ±7.65 (max-min) t2 mean±se 33.11± ± ± ±6.59 (max-min) t3 mean±se 27.92± ± ± ±16.05 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Πίνακας 46. Σύγκριση των τιµών έκφρασης της STAT6 στα µη ενεργοποιηµένα CD8 κατά την έναρξη της λοίµωξης (t1) κατά την διάρκεια της λοίµωξης (t2) και κατά την αποδροµή της λοίµωξης (t3) σε όλες τις οµάδες STAT6 E A1 p A2 p A p B p A1 t B t t1 mean±se 19.24± ± ± ± ± ±6.0- (max-min) ± t2 mean±se 24.43± ± ± ±3.15 (-ax-min) t3 mean±±e 19.16± ± ± ±7.39 (max-min) P P P P *p0: σύγκριση µεταξύ της κάθε οµάδας σε χρόνο t1 µε την οµάδα Β *p1: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2) *p2: σύγκριση µεταξύ έναρξης της λοίµωξης (t1) και την αποδροµή της λοίµωξης (t3) 137
138 *p3: σύγκριση µεταξύ της χρονικής στιγµής (t2) και (t3) Οι διαφορές είναι στατιστικά σηµαντικές όταν p<0.05 Στους πίνακες 45 και 46 φαίνονται η µέση τιµή, το τυπικό σφάλµα, η µέγιστη και ελάχιστη τιµή της STAT6 στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8 σε όλες τις οµάδες και η σύγκριση των τιµών έκφρασης της STAT6 στα CD8 (α) µεταξύ έναρξης της λοίµωξης (t1) και κατά τη διάρκεια της λοίµωξης (t2), (β) µεταξύ της έναρξης της λοίµωξης (t1) και της αποδροµής της λοίµωξης (t3) και (γ) µεταξύ της χρονικής στιγµής (t2) και (t3). Παρατηρούµε ότι η διαφορά των τιµών των STAT6 στα ενεργοποιηµένα CD8 δεν είναι στατιστικά σηµαντική για τη σύγκριση µεταξύ των χρονικών στιγµών των Α1p, A2p, Ap, και A1t στα ενεργοποιηµένα και µη ενεργοποιηµένα CD8. Παρατηρήθηκε στατιστικά σηµαντική διαφορά στη σύγκριση µεταξύ της οµάδας Α1t µε την οµάδα Bt στα ενεργοποιηµένα (p=0.05). Ενεργοποιηµένα STAT6 E Μη ενεργοποιηµένα STAT6 E STAT6 E A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-10 A1p-t1 A2p-t1 A1p-t2 A2p-t2 A1p-t3 A2p-t3 Mean Mean±SE Mean±SD Extremes 0-10 A1t-t1-energ A1t-t2-energ A1t-t3-energ Bt-energ A1t-t1-no energ A1t-t2-no energ A1t-t3-no energ Bt-no energ Mean Mean±SE Mean±SD Extremes ROC καµπύλες Οι ROC καµπύλες που δηµιουργήθηκαν έγιναν σε µετρήσεις που αφορούν ασθενείς µε λοίµωξη (οµάδα Α1 ή Α2) και τους υγιείς µάρτυρες (οµάδα Β). Από την ανάλυση των ROC καµπύλων µπορεί να ελαχιστοποιηθούν τα ψευδώς θετικά και ψευδώς αρνητικά αποτελέσµατα, συµπέρασµα που ταυτίζεται µε τη µεγιστοποίηση της ευαισθησίας και της ειδικότητας. Η σύγκριση των διαφορετικών δοκιµών µπορεί να γίνει µε τη σύγκριση των περιοχών κάτω από τη καµπύλη (area under curve AUC). Η µεγαλύτερη τιµή υποδεικνύει και τη δοκιµή µε τα καλύτερα αποτελέσµατα. 138
139 Σχήµα 1., 2. και 3. Σχήµα 1. Test Result Variable(s) Asymptotic Area Std. Error a Sig. b CD3%,811,057,000 CD3+CD4+%,810,060,000 CD3+CD8+%,550,080,528 Σχήµα 2. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CD3%,767,081,006 CD3+CD4+%,812,081,001 CD3+CD8+%,384,111,232 Σχήµα 3. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CD3%,682,159,212 CD3+CD4+%,759,116,075 CD3+CD8+%,536,179,803 Στο σχήµα 1 φαίνονται οι ROC καµπύλες για τα CD3, CD4 και CD8. Οι περιοχές κάτω από τη καµπύλη για τα CD3 και CD4 είναι και 0.810, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για το CD8 είναι 0.550, τιµή αρκετά µικρή που φανερώνει ότι η χρήση του CD8 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των CD3 και CD4 είναι συγκρίσιµα, το CD3 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από το CD4, ενώ και τα δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για το CD3 βρέθηκε ευαισθησία 87%, και 66% ειδικότητα, για το CD4+ ευαισθησία 96% και 70% ειδικότητα, και για το CD8+ ευαισθησία 96% και ειδικότητα 40%. Στο σχήµα 2 φαίνονται οι ROC καµπύλες για τα CD3, CD4 και CD8. Οι περιοχές κάτω από τη καµπύλη για τα CD3 και CD4 είναι και 0.812, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για το CD8 είναι 0.384, τιµή αρκετά µικρή που φανερώνει ότι η χρήση του CD8 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των CD3 και CD4 είναι συγκρίσιµα, το CD3 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από το CD4, ενώ και τα δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index 139
140 προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για το CD3 βρέθηκε ευαισθησία 83%, και 60% ειδικότητα, για το CD4+ ευαισθησία 78% και 80% ειδικότητα, και για το CD8+ ευαισθησία 91% και ειδικότητα 30%. Στο σχήµα 3 φαίνονται οι ROC καµπύλες για τα CD3, CD4 και CD8. Οι περιοχές κάτω από τη καµπύλη για τα CD3 και CD4 είναι και 0.759, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για το CD8 είναι 0.536, τιµή αρκετά µικρή που φανερώνει ότι η χρήση του CD8 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των CD3 και CD4 είναι συγκρίσιµα, το CD3 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από το CD4, ενώ και τα δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτές της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για το CD3 βρέθηκε ευαισθησία 96%, και 60% ειδικότητα, για το CD4+ ευαισθησία 68% και 80% ειδικότητα, και για το CD8+ ευαισθησία 95% και ειδικότητα 40%. Σχήµα 4.,5. και 6 Test Result Variable(s) Area Std. Errora STAT1 D,663,077 STAT3 D,676,082 STAT4 D,527,091 STAT5 D,521,083 STAT6 D,595,084 Test Result Variable(s) Area Std. Error a STAT1 D,711,096 STAT3 D,719,093 STAT4 D,531,105 STAT5 D,514,107 STAT6 D,658,
141 Σχήµα 6. Test Result Variable(s) Area Std. Error a STAT1 D,738,174 STAT3 D,892,103 STAT4 D,831,120 STAT5 D,754,113 STAT6 D,554,135 Στο σχήµα 4 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για STAT1και STAT3 είναι και 0.676, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,527, 0,521, 0,595 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1και STAT3 είναι συγκρίσιµα, τη STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ενώ και οι δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 72% και ειδικότητα 56%, για τη STAT3 βρέθηκε ευαισθησία 69% και ειδικότητα 75%, για τη STAT4 βρέθηκε ευαισθησία 60% και ειδικότητα 56%, για τη STAT5 βρέθηκε ευαισθησία 41% και ειδικότητα 87% και για τη STAT6 βρέθηκε ευαισθησία 75% και ειδικότητα 50%. Στο σχήµα 5 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για STAT1και STAT3 είναι και 0.719, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,531, 0,514, 0,658 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1και STAT3 είναι συγκρίσιµα, τη STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ενώ και οι δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 56% και ειδικότητα 87%, για τη STAT3 βρέθηκε ευαισθησία 69% και ειδικότητα 75%, για τη STAT4 βρέθηκε ευαισθησία 31% και ειδικότητα 87%, για τη STAT5 βρέθηκε ευαισθησία 44% και ειδικότητα 80% και για τη STAT6 βρέθηκε ευαισθησία 38% και ειδικότητα 100%. Στο σχήµα 6 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη 141
142 καµπύλη για STAT1, STAT3, STAT4 και STAT5 είναι 0.738, 0.892, 0,831 και αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τη STAT6. είναι 0,554, τιµή αρκετά µικρή που φανερώνει ότι η χρήση της STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1, STAT3, STAT4 και STAT5 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ή τη STAT4, και STAT5 ενώ και οι 4 φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτές της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 77% και ειδικότητα 45%, για τη STAT3 βρέθηκε ευαισθησία 100% και ειδικότητα 80%, για τη STAT4 βρέθηκε ευαισθησία 100% και ειδικότητα 60%, για τη STAT5 βρέθηκε ευαισθησία 62% και ειδικότητα 100% και για τη STAT6 βρέθηκε ευαισθησία 54% και ειδικότητα 80%. Σχήµα 7.,8. και 9 Σχήµα 7. Test Result Variable(s) Area Std. Error a STAT1E,631,083 STAT3E,713,078 STAT4E,626,090 STAT5E,645,086 STAT6E,600,087 Σχήµα 8. Test Result Variable(s) Area Std. Error a STAT1E,652,098 STAT3E,777,082 STAT4E,582,106 STAT5E,645,101 STAT6E,666,
143 Σχήµα 9. Test Result Variable(s) Area Std. Error a STAT1E,800,113 STAT3E,769,121 STAT4E,600,168 STAT5E,631,152 STAT6E,723,134 Στο σχήµα 7 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,631, 0,626, 0,645, αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATς, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 63% και ειδικότητα 70%, για τη STAT3 βρέθηκε ευαισθησία 84% και ειδικότητα 56%, για τη STAT4 βρέθηκε ευαισθησία 84% και ειδικότητα 50%, για τη STAT5 βρέθηκε ευαισθησία 81% και ειδικότητα 50% και για τη STAT6 βρέθηκε ευαισθησία 50% και ειδικότητα 75%. Στο σχήµα 8 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,652, 0,582, 0,645, αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATς, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 94% και ειδικότητα 40%, για τη STAT3 βρέθηκε ευαισθησία 75% και ειδικότητα 76%, για τη STAT4 βρέθηκε ευαισθησία 81% και ειδικότητα 50%, για τη STAT5 βρέθηκε ευαισθησία 88% και ειδικότητα 50% και για τη STAT6 βρέθηκε ευαισθησία 94% και ειδικότητα 40%. 143
144 Στο σχήµα 9 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για STAT1και STAT3 είναι και 0.769, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,600, 0,631, 0,723 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1και STAT3 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ενώ και οι δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτές της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 54% και ειδικότητα 100%, για τη STAT3 βρέθηκε ευαισθησία 62% και ειδικότητα 100%, για τη STAT4 βρέθηκε ευαισθησία 100% και ειδικότητα 40%, για τη STAT5 βρέθηκε ευαισθησία 77% και ειδικότητα 60% και για τη STAT6 βρέθηκε ευαισθησία 54% και ειδικότητα 100%. Σχήµα 10. Test Result Variable(s) Area Std. Error a STAT1I,680,077 STAT3I,732,076 STAT4I,496,089 STAT5I,535,086 STAT6I,604,084 Σχήµα 11. Test Result Variable(s) Area Std. Error a STAT1I,846,078 STAT3I,779,089 STAT4I,504,106 STAT5I,594,104 STAT6I,700,
145 Σχήµα 12. Test Result Variable(s) Area Std. Error a STAT1I,792,152 STAT3I,923,078 STAT4I,954,047 STAT5I,800,110 STAT6I,662,134 Στο σχήµα 10 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,680, 0,496, 0,535, αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATς, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 66% και ειδικότητα 75%, για τη STAT3 βρέθηκε ευαισθησία 75% και ειδικότητα 75%, για τη STAT4 βρέθηκε ευαισθησία 38% και ειδικότητα 75%, για τη STAT5 βρέθηκε ευαισθησία 31% και ειδικότητα 94% και για τη STAT6 βρέθηκε ευαισθησία 75% και ειδικότητα 56%. Στο σχήµα 11 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για STAT1και STAT3 είναι και 0.779, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,504, 0,594, 0,700 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1και STAT3 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ενώ και οι δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 80% και ειδικότητα 98%, για τη STAT3 βρέθηκε ευαισθησία 80% και ειδικότητα 75%, για τη STAT4 βρέθηκε ευαισθησία 33% και ειδικότητα 80%, για τη STAT5 βρέθηκε ευαισθησία 60% και ειδικότητα 62% και για τη STAT6 βρέθηκε ευαισθησία 60% και ειδικότητα 80%. 145
146 Στο σχήµα 12 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για STAT1, STAT3, STAT4 και STAT5 είναι 0.792,0.923, και αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τη STAT6. είναι 0,662, τιµή αρκετά µικρή που φανερώνει ότι η χρήση της STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1, STAT3, STAT4 και STAT5 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, STAT4 και STAT5 ενώ και οι 4 φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτούς της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 100% και ειδικότητα 60%, για τη STAT3 βρέθηκε ευαισθησία 100% και ειδικότητα 80%, για τη STAT4 βρέθηκε ευαισθησία 85% και ειδικότητα 100%, για τη STAT5 βρέθηκε ευαισθησία 54% και ειδικότητα 100% και για τη STAT6 βρέθηκε ευαισθησία 46% και ειδικότητα 100% Σχήµα 13. Test Result Variable(s) Area Std. Error a STAT1J,602,098 STAT3J,629,091 STAT4J,423,096 STAT5J,528,086 STAT6J,587,088 Σχήµα 14. Test Result Variable(s) Area Std. Error a STAT1J,617,107 STAT3J,660,102 STAT4J,429,105 STAT5J,544,109 STAT6J,675,
147 Σχήµα 15. Test Result Variable(s) Area Std. Error a STAT1J,862,096 STAT3J,969,038 STAT4J,954,050 STAT5J,631,144 STAT6J,623,142 Στο σχήµα 13 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα µονοκύτταρα. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,602, 0,423, 0,528, αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATς, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 78% και ειδικότητα 62%, για τη STAT3 βρέθηκε ευαισθησία 66% και ειδικότητα 70%, για τη STAT4 βρέθηκε ευαισθησία 97% και ειδικότητα 20%, για τη STAT5 βρέθηκε ευαισθησία 50% και ειδικότητα 70% και για τη STAT6 βρέθηκε ευαισθησία 78% και ειδικότητα 50%. Στο σχήµα 14 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα µονοκύτταρα. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 και STAT6 είναι και αντιστοίχως. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4 και STAT5 είναι 0,617, 0,429, 0,544 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4 και STAT5 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT6 και STAT3 είναι συγκρίσιµα, η STAT6 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ενώ και οι δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 80% και ειδικότητα 64%, για τη STAT3 βρέθηκε ευαισθησία 73% και ειδικότητα70%, για τη STAT4 βρέθηκε ευαισθησία 73% και ειδικότητα40%, για τη STAT5 βρέθηκε ευαισθησία 60% και ειδικότητα 62% και για τη STAT6 ευαισθησία 73% και ειδικότητα75%. Στο σχήµα 15 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα ενεργοποιηµένα µονοκύτταρα. Οι 147
148 περιοχές κάτω από τη καµπύλη για STAT1, STAT3 και STAT4 είναι 0,862, 0,969 και 0,954 αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τη STAT5 και STAT6. είναι 0,631, και τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1, STAT3, και STAT4 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3 και STAT4 ενώ και οι 3 φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτούς της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 62% και ειδικότητα 100%, για τη STAT3 βρέθηκε ευαισθησία 85% και ειδικότητα 100%, για τη STAT4 βρέθηκε ευαισθησία 92% και ειδικότητα 100%, για τη STAT5 βρέθηκε ευαισθησία 31% και ειδικότητα 100% και για τη STAT6 βρέθηκε ευαισθησία 54% και ειδικότητα 80%. Σχήµα 16. Test Result Variable(s) Asymptotic Sig. b Std. Area Error a CD3%,861,051,000 CD3+CD4+%,823,057,000 CD3+CD8+%,679,073,025 Σχήµα 17. Test Result Variable(s) Asymptotic Area Std. Error a Sig. b CD3%,820,070,001 CD3+CD4+%,842,068,000 CD3+CD8+%,422,114,
149 Σχήµα 18. Test Result Variable(s) Std. Area Error a CD3%,800,123,039 CD3+CD4+%,800,121,039 CD3+CD8+%,668,141,248 Asymptotic Sig. b Στο σχήµα 16 φαίνονται οι ROC καµπύλες για τα µη ενεργοποιηµένα CD3, CD4 και CD8. Οι περιοχές κάτω από τη καµπύλη για τα CD3 και CD4 είναι και 0.823, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για το CD8 είναι 0.679, τιµή αρκετά µικρή που φανερώνει ότι η χρήση του CD8 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των CD3 και CD4 είναι συγκρίσιµα, το CD3 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από το CD4, ενώ και τα δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για το CD3 βρέθηκε ευαισθησία 96% και ειδικότητα70%, για το CD4+ ευαισθησία 91% και ειδικότητα70% και για το CD8+ ευαισθησία 83% και ειδικότητα50%. Στο σχήµα17 φαίνονται οι ROC καµπύλες για τα µη ενεργοποιηµένα CD3, CD4 και CD8. Οι περιοχές κάτω από τη καµπύλη για τα CD3 και CD4 είναι και 0.841, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για το CD8 είναι 0.422, τιµή αρκετά µικρή που φανερώνει ότι η χρήση του CD8 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των CD3 και CD4 είναι συγκρίσιµα, το CD3 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από το CD4, ενώ και τα δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για το CD3 βρέθηκε ευαισθησία 74% και ειδικότητα 80%, για το CD4+ ευαισθησία 91% και ειδικότητα 73%και για το CD8+ ευαισθησία 96% και ειδικότητα 33%. Στο σχήµα 18 φαίνονται οι ROC καµπύλες για τα µη ενεργοποιηµένα CD3, CD4 και CD8. Οι περιοχές κάτω από τη καµπύλη για τα CD3 και CD4 είναι και 0.800, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για το CD8 είναι 0.668, τιµή αρκετά µικρή που φανερώνει ότι η χρήση του CD8 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των CD3 και CD4 είναι συγκρίσιµα, το CD3 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από το CD4, ενώ και τα δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτές της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για το CD3 βρέθηκε ευαισθησία 149
150 77% και ειδικότητα80% για το CD4+ ευαισθησία 86% και ειδικότητα80% και για το CD8+ ευαισθησία 91% και ειδικότητα 40%. Σχήµα 19. Test Result Asymptotic Variable(s) Area Std. Error a Sig. b STAT1 D,717,073,015 STAT3 D,742,077,007 STAT4 D,629,086,149 STAT5 D,548,085,592 STAT6 D,623,083,168 Σχήµα 20. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b STAT1 D,695,101,060 STAT3 D,809,078,003 STAT4 D,670,096,101 STAT5 D,563,104,546 STAT6 D,674,098,094 Σχήµα 21. Asymptotic Test Result Variable(s) Area Std. Error a Sig. b STAT1 D,969,038,003 STAT3 D,862,105,021 STAT4 D,754,162,104 STAT5 D,708,124,183 STAT6 D,615,135,460 Στο σχήµα 19 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα µη ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για STAT1και STAT3 είναι και 0.742, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,629, 0,548, 0,623 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1και STAT3 είναι συγκρίσιµα, τη STAT1 δεν µπορεί να θεωρηθεί σηµαντικά 150
151 καλύτερος διαχωριστικός παράγοντας από τη STAT3, ενώ και οι δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτές της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 60% και ειδικότητα 94%, για τη STAT3 βρέθηκε ευαισθησία 81% και ειδικότητα 62%, για τη STAT4 βρέθηκε ευαισθησία 56% και ειδικότητα75%, για τη STAT5 βρέθηκε ευαισθησία 31% και ειδικότητα 94%και για τη STAT6 72% και ειδικότητα 62%. Στο σχήµα 20 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα µη ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,695, 0,670, 0,563, αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATs, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 63% και ειδικότητα94%, για τη STAT3 βρέθηκε ευαισθησία 94% και ειδικότητα62%, για τη STAT4 βρέθηκε ευαισθησία 50% και ειδικότητα80%, για τη STAT5 βρέθηκε ευαισθησία 50% και ειδικότητα75% και για τη STAT6 75% και ειδικότητα64%. Στο σχήµα 21 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα µη ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για STAT1, STAT3, STAT4 και STAT5 είναι 0,969, 0,862, 0,754, 0,708 αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τη STAT6. είναι 0,615, τιµή αρκετά µικρή που φανερώνει ότι η χρήση της STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1, STAT3, STAT4 και STAT5 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ή τη STAT4, και STAT5 ενώ και οι 4 φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτές της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 85% και ειδικότητα 100%, για τη STAT3 βρέθηκε ευαισθησία 92% και ειδικότητα 80%, για τη STAT4 βρέθηκε ευαισθησία 85% και ειδικότητα 80%, για τη STAT5 βρέθηκε ευαισθησία 70% και ειδικότητα 100% και για τη STAT6 39% και ειδικότητα 100%. 151
152 Σχήµα 22. Test Result Variable(s) Area Std. Error a Sig. b Asymptotic STAT1E,681,084,043 STAT3E,742,076,007 STAT4E,645,092,106 STAT5E,631,091,143 STAT6E,600,093,265 Σχήµα 23. Test Result Variable(s) Area Std. Error a Sig. b Asymptotic STAT1E,648,100,152 STAT3E,803,079,003 STAT4E,637,104,187 STAT5E,625,103,228 STAT6E,635,102,194 Σχήµα 24. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b STAT1E,823,116,038 STAT3E,754,120,104 STAT4E,569,147,657 STAT5E,615,163,460 STAT6E,662,151,301 Στο σχήµα 23 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα µη ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,681, 0,646, 0,631 και 0,600.αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός 152
153 παράγοντας από τις υπόλοιπες STATs ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 75% και ειδικότητα 56%, για τη STAT3 βρέθηκε ευαισθησία 72% και ειδικότητα 70%, για τη STAT4 βρέθηκε ευαισθησία 72% και ειδικότητα 62%, για τη STAT5 βρέθηκε ευαισθησία 63% και ειδικότητα 70% και για τη STAT6 91% και ειδικότητα 37%. Στο σχήµα 24 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα µη ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,648, 0,637, 0,625 και 0,636.αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATs ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτούς της οµάδας Βp. Μετά την χρήση του Youden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 100% και ειδικότητα 37% για τη STAT3 βρέθηκε ευαισθησία 75% και ειδικότητα 80%, για τη STAT4 βρέθηκε ευαισθησία 81% και ειδικότητα 62%, για τη STAT5 βρέθηκε ευαισθησία 69% και ειδικότητα 70% και για τη STAT6 94% και ειδικότητα 44%. Στο σχήµα 25 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα µη ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για STAT1και STAT3 είναι και 0.754, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,569, 0,615, 0,662 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1και STAT3 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, ενώ και οι δύο φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτές της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 100% και ειδικότητα 60%, για τη STAT3 βρέθηκε ευαισθησία 61% και ειδικότητα100%, για τη STAT4 βρέθηκε ευαισθησία 31% και ειδικότητα 100%, για τη STAT5 βρέθηκε ευαισθησία 100% και ειδικότητα40% και για τη STAT6 100% και ειδικότητα 40%. 153
154 Σχήµα 25. Test Result Variable(s) Area Std. Error a Sig. b Asymptotic STAT1I,637,081,126 STAT3I,780,071,002 STAT4I,572,086,418 STAT5I,561,087,498 STAT6I,609,088,221 Σχήµα 26. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b STAT1I,688,100,075 STAT3I,846,070,001 STAT4I,588,104,406 STAT5I,656,099,138 STAT6I,675,101,097 Σχήµα 27. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b STAT1I,954,050,004 STAT3I,877,095,016 STAT4I,938,062,005 STAT5I,785,113,068 STAT6I,631,133,402 Στο σχήµα 25 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα µη ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0.637, 0,572, 0,561 και 0,609αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος 154
155 διαχωριστικός παράγοντας από τις υπόλοιπες STATs, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 50% και ειδικότητα 88%, για τη STAT3 βρέθηκε ευαισθησία 84% και ειδικότητα 62%, για τη STAT4 βρέθηκε ευαισθησία 28% και ειδικότητα 94%, για τη STAT5 βρέθηκε ευαισθησία 28% και ειδικότητα 100%και για τη STAT6 78% και ειδικότητα 56%. Στο σχήµα 26 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα µη ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6 είναι 0.688, 0,588, 0,656 και 0,675 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATs, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 47% και ειδικότητα 100%, για τη STAT3 βρέθηκε ευαισθησία 73% και ειδικότητα 88%, για τη STAT4 βρέθηκε ευαισθησία 100% και ειδικότητα 25%, για τη STAT5 βρέθηκε ευαισθησία 33% και ειδικότητα 100% και για τη STAT6 73% και ειδικότητα 70%. Στο σχήµα 27 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα µη ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για STAT1, STAT3, STAT4 και STAT5 είναι 0,954, 0,877, 0,938, 0,785 αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τη STAT6. είναι 0,632, τιµή αρκετά µικρή που φανερώνει ότι η χρήση της STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1, STAT3, STAT4 και STAT5 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3, STAT4 και STAT5 ενώ και οι 4 φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτούς της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 92% και ειδικότητα 100%, για τη STAT3 βρέθηκε ευαισθησία 85% και ειδικότητα80%, για τη STAT4 βρέθηκε ευαισθησία 92% και ειδικότητα100%, για τη STAT5 βρέθηκε ευαισθησία 85% και ειδικότητα 80% και για τη STAT6 46% και ειδικότητα 100%. 155
156 Σχήµα 28. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b STAT1J,672,080,054 STAT3J,723,080,013 STAT4J,517,102,853 STAT5J,637,086,126 STAT6J,659,084,075 Σχήµα 29. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b STAT1J,613,102,286 STAT3J,769,088,011 STAT4J,519,110,859 STAT5J,608,104,304 STAT6J,698,102,060 Σχήµα 30. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b STAT1J,938,056,005 STAT3J,862,096,021 STAT4J,923,074,007 STAT5J,631,139,402 STAT6J,685,135,237 Στο σχήµα 28 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα µη ενεργοποιηµένα µονοκύτταρα. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι 0,723. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,672, 0,517, 0,637 και 0,659 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος 156
157 διαχωριστικός παράγοντας από τις υπόλοιπες STATs, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α1p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 66% και ειδικότητα 75%, για τη STAT3 βρέθηκε ευαισθησία 63% και ειδικότητα80%, για τη STAT4 βρέθηκε ευαισθησία 97% και ειδικότητα33%, για τη STAT5 βρέθηκε ευαισθησία 87% και ειδικότητα 37%και για τη STAT6 72% και ειδικότητα70%. Στο σχήµα 29 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα µη ενεργοποιηµένα µονοκύτταρα. Οι περιοχές κάτω από τη καµπύλη για τη STAT3 είναι 0,769. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0,613, 0,519, 0,608 και 0,698. αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα της STAT3 είναι συγκρίσιµα, και µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τις υπόλοιπες STATs, ενώ φαίνεται να διαχωρίζει σηµαντικά τους ασθενείς της οµάδας Α2p µε αυτούς της οµάδας Βp. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 73% και ειδικότητα 50%, για τη STAT3 βρέθηκε ευαισθησία 80% και ειδικότητα 75%, για τη STAT4 βρέθηκε ευαισθησία 93% και ειδικότητα 37%, για τη STAT5 βρέθηκε ευαισθησία 53% και ειδικότητα 75%και για τη STAT6 67% και ειδικότητα 80%. Στο σχήµα 30 φαίνονται οι ROC καµπύλες για τις τιµές των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1t στα µη ενεργοποιηµένα µονοκύτταρα. Οι περιοχές κάτω από τη καµπύλη για STAT1, STAT3 και STAT4 είναι 0,938, 0,862, 0,924αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τη STAT5 και STAT6. είναι 0,631 και 0,685τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Τα αποτελέσµατα των STAT1, STAT3, και STAT4 είναι συγκρίσιµα, η STAT1 δεν µπορεί να θεωρηθεί σηµαντικά καλύτερος διαχωριστικός παράγοντας από τη STAT3 και STAT4 ενώ και οι 3 φαίνεται να διαχωρίζουν σηµαντικά τους ασθενείς της οµάδας Α1t µε αυτούς της οµάδας Βt. Μετά την χρήση τουyouden index προσδιορίστηκε η cut off τιµή ώστε να ανευρεθεί το ποσοστό ευαισθησίας και ειδικότητας για την τιµή. Έτσι για τη STAT1 βρέθηκε ευαισθησία 85% και ειδικότητα 100%, για τη STAT3 βρέθηκε ευαισθησία 85% και ειδικότητα 80%, για τη STAT4 βρέθηκε ευαισθησία 92% και ειδικότητα 100%, για τη STAT5 βρέθηκε ευαισθησία 38% και ειδικότητα 100% και για τη STAT6 46% και ειδικότητα 100%. 157
158 Τα αποτελέσµατα σε συνοπτικό πίνακα. Α1-p Α1-p Α1-p Α2-p Α2-p Α2-p Α1-t Α1-t Α1-t cut off Sensitivity 1 - Specificity cut off Sensitivity 1 - Specificity cut off Sensitivity 1 - Specificity CD3 47,000,957,313 62,400,739,200 57,90,773,200 CD4 37,60,913,313 37,150,913,267 39,00,864,200 CD8 13,150,826,531 11,50,957,667 7,900,909,600 STAT1D 2,0700,594,063 1,9450,625,063 1,8250,846,000 STAT3D 1,5400,813,375 1,5050,938,375 3,7300,923,200 STAT4D 3,2400,563,250 3,8600,500,188 2,7150,846,200 STAT5D 2,6650,313,063 1,6650,500,250,7450,692,000 STAT6D 3,2650,719,375 3,3700,750,375 8,8250,385,000 STAT1E 9,5300,750,438 5,9800 1,000,625 4,8900 1,000,400 STAT3E 19,4000,719,313 30,1500,750,188 45,2000,615,000 STAT4E 7,8200,719,375 7,5150,813,375 12,0500,308,000 STAT5E 8,7050,625,313 8,8150,688,313 1,9250 1,000,600 STAT6E 2,3700,906,625 4,7700,938,563,8450 1,000,600 STAT1I 2,4950,500,125 5,5750,467,000 1,2750,923,000 STAT3I 1,4050,844,375 3,9750,733,125 2,7650,846,200 STAT4I 9,8350,281,063 1,2300 1,000,750 4,5100,923,000 STAT5I 5,8350,281,000 5,7950,333,000,3850,846,200 STAT6I 1,8200,781,438 6,4400,733,313 14,1750,462,000 STAT1J 1,9900,656,250 1,1200,733,500 2,6350,846,000 STAT3J 6,3000,625,188 4,2800,800,250 6,7300,846,200 STAT4J,2000,969,688,5100,933,625 1,5200,923,000 STAT5J,2300,875,625,6600,533,250 1,0600,385,000 STAT6J 2,6000,719,313 6,9650,667,188 8,3400,462,000 ROC καµπύλες των STATs, CRP και PCT Οι ROC καµπύλες για STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στα ενεργοποιηµένα CD4, CD8, πολυµορφοπύρηνα και µονοκύτταρα µαζί µε τις τιµές των CRP και PCT κατά την πρώτη µέρα λοίµωξης. 158
159 Σχήµα 21. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,863,059,000 PCT,958,031,000 STAT1 D,673,077,054 STAT3 D,692,082,033 STAT4 D,526,091,770 STAT5 D,537,084,678 STAT6 D,614,084,205 Σχήµα 22. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,863,059,000 PCT,958,031,000 STAT1E,649,083,097 STAT3E,736,077,009 STAT4E,644,091,108 STAT5E,665,086,066 STAT6E,613,088,209 Στο σχήµα 21 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT1και STAT3 είναι 0,863, 0,958, και 0.692, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,526, 0,537, 0,614 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Στο σχήµα 22 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT1STAT3 και STAT5 είναι 0,863, 0,958, 0.649, και αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4 και STAT6. είναι 0,644 και 0,613 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα 159
160 Σχήµα 23. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,863,059,000 PCT,958,031,000 STAT1I,696,077,029 STAT3I,748,076,006 STAT4I,494,089,946 STAT5I,552,087,559 STAT6I,624,085,167 Σχήµα 24. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,863,059,000 PCT,958,031,000 STAT1J,595,099,291 STAT3J,635,091,133 STAT4J,412,097,329 STAT5J,537,087,678 STAT6J,600,089,266 Στο σχήµα 23 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT1και STAT3 είναι 0,863, 0,958, και 0.748, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,494, 0,552, 0,624 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα Στο σχήµα 24 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα ενεργοποιηµένα µονοκύτταρα. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT και STAT3 είναι 0,863, 0,958 και 0.635, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4, STAT5 και STAT6. είναι 0.595, 0,412, 0,537, 0,600 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα 160
161 Σχήµα 25. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,938,061,000 PCT,955,045,000 STAT1 D,728,103,034 STAT3 D,719,099,042 STAT4 D,482,110,868 STAT5 D,467,112,755 STAT6 D,665,106,124 Σχήµα 26. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,938,061,000 PCT,955,045,000 STAT1E,629,103,228 STAT3E,781,084,009 STAT4E,545,111,678 STAT5E,621,105,262 STAT6E,701,095,061 Στο σχήµα 25 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT1και STAT3 είναι 0,938, 0,955, και 0.719, αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,482, 0,467, 0,665 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. Στο σχήµα 26 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα CD8. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT3 είναι 0,938, 0,955, και αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1,STAT4, STAT5 και STAT6. είναι 0,629, 0.545, 621 και 0,701 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT1, STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα 161
162 Σχήµα 27. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,938,061,000 PCT,955,045,000 STAT1I,835,083,002 STAT3I,772,092,011 STAT4I,478,108,835 STAT5I,569,107,519 STAT6I,679,102,096 Σχήµα 28. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,938,061,000 PCT,955,045,000 STAT1J,616,108,280 STAT3J,658,104,140 STAT4J,424,106,480 STAT5J,529,112,787 STAT6J,661,105,135 Στο σχήµα 27.φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα πολυµορφοπύρηνα. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT1και STAT3 είναι 0,938, 0,955, και αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,478, 0,569, 0,679 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα Στο σχήµα 28 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α2p στα ενεργοποιηµένα µονοκύτταρα. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT3 και STAT6 είναι 0,938, 0,955, και αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT1, STAT4 και STAT5 είναι 0.616, 0,424 και 0,529 αντίστοιχα, τιµές αρκετά µικρές που 162
163 φανερώνουν ότι η χρήση των STAT1, STAT4 και STAT5 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα Οι ROC καµπύλες για την έκφραση των STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στα µη ενεργοποιηµένα CD4, CD8, πολυµορφοπύρηνα και µονοκύτταρα µαζί µε τις τιµές των CRP και PCT κατά την πρώτη µέρα λοίµωξης. Σχήµα 29. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,889,054,000 PCT,958,031,000 STAT1 D,736,072,009 STAT3 D,756,076,004 STAT4 D,635,085,133 STAT5 D,564,086,479 STAT6 D,643,083,111 Σχήµα 30. Test Result Variable(s) Area Std. Error a Asymptotic Sig. b CRP,889,054,000 PCT,958,031,000 STAT1E,684,084,040 STAT3E,746,075,006 STAT4E,643,092,111 STAT5E,629,091,151 STAT6E,599,093,271 Στο σχήµα 29 φαίνονται οι ROC καµπύλες για τις τιµές των CRP, PCT, STAT1, STAT3, STAT4, STAT5 και STAT6 την 1 η µέρα στην οµάδα Α1p στα µη ενεργοποιηµένα CD4. Οι περιοχές κάτω από τη καµπύλη για CRP, PCT, STAT1και STAT3 είναι 0,889, 0,958, και αντίστοιχα. Αντίθετα, η περιοχή κάτω από τη καµπύλη για τις STAT4, STAT5 και STAT6. είναι 0,634, 0,564, 0,643 αντίστοιχα, τιµές αρκετά µικρές που φανερώνουν ότι η χρήση των STAT4, STAT5 και STAT6 δεν µπορεί να δώσει ικανοποιητικά διαγνωστικά αποτελέσµατα. 163
Φλεγμονή. Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ
 Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
ΛΟΙΜΩΞΗ ΕΓΚΥΟΥ ΚΑΙ ΝΕΟΓΝΟΥ ΑΠΟ ΣΤΡΕΠΤΟΚΟΚΚΟ ΟΜΑΔΑΣ Β. Σταυρούλα Γαβρίλη, MD, PhD Παιδίατρος-Νεογνολόγος
 ΛΟΙΜΩΞΗ ΕΓΚΥΟΥ ΚΑΙ ΝΕΟΓΝΟΥ ΑΠΟ ΣΤΡΕΠΤΟΚΟΚΚΟ ΟΜΑΔΑΣ Β Σταυρούλα Γαβρίλη, MD, PhD Παιδίατρος-Νεογνολόγος ΕΠΙΔΗΜΙΟΛΟΓΙΑ - O β-αιμολυτικός στρεπτόκοκκος της ομάδας Β (group B Streptococcus, GBS ή Streptococcus
ΛΟΙΜΩΞΗ ΕΓΚΥΟΥ ΚΑΙ ΝΕΟΓΝΟΥ ΑΠΟ ΣΤΡΕΠΤΟΚΟΚΚΟ ΟΜΑΔΑΣ Β Σταυρούλα Γαβρίλη, MD, PhD Παιδίατρος-Νεογνολόγος ΕΠΙΔΗΜΙΟΛΟΓΙΑ - O β-αιμολυτικός στρεπτόκοκκος της ομάδας Β (group B Streptococcus, GBS ή Streptococcus
ΛΟΙΜΩΞΕΙΣ ΤΗΣ ΕΓΚΥΟΥ, ΤΟΥ ΕΜΒΡΥΟΥ ΚΑΙ ΤΟΥ ΝΕΟΓΝΟΥ
 ΛΟΙΜΩΞΕΙΣ ΤΗΣ ΕΓΚΥΟΥ, ΤΟΥ ΕΜΒΡΥΟΥ ΚΑΙ ΤΟΥ ΝΕΟΓΝΟΥ ISBN 960-7081-87-0 ΠΕΡΙΕΧΟΜΕΝΑ Εισαγωγή... 1 1. Αντίδραση της εγκύου, του εμβρύου και του νεογνού στη λοίμωξη... 5 Εισαγωγή... 5 Επίδραση της λοίμωξης
ΛΟΙΜΩΞΕΙΣ ΤΗΣ ΕΓΚΥΟΥ, ΤΟΥ ΕΜΒΡΥΟΥ ΚΑΙ ΤΟΥ ΝΕΟΓΝΟΥ ISBN 960-7081-87-0 ΠΕΡΙΕΧΟΜΕΝΑ Εισαγωγή... 1 1. Αντίδραση της εγκύου, του εμβρύου και του νεογνού στη λοίμωξη... 5 Εισαγωγή... 5 Επίδραση της λοίμωξης
να ταράξουν την λειτουργία των ιστών και των οργάνων του; α. τη θέση τους στο ανθρώπινο σώμα β. την γενικευμένη ή εξειδικευμένη δράση
 Ερωτήσεις κατανόησης της θεωρίας του 1 ο κεφαλαίου (συνέχεια) 1. Από τι εξαρτάται η επιβίωση του ανθρώπου και ποιοι εξωτερικοί παράγοντες θα μπορούσαν να ταράξουν την λειτουργία των ιστών και των οργάνων
Ερωτήσεις κατανόησης της θεωρίας του 1 ο κεφαλαίου (συνέχεια) 1. Από τι εξαρτάται η επιβίωση του ανθρώπου και ποιοι εξωτερικοί παράγοντες θα μπορούσαν να ταράξουν την λειτουργία των ιστών και των οργάνων
ΜΙΚΡΟΒΙΟΛΟΓΙΚΟ ΤΜΗΜΑ Π.Γ.Ν.Θ.ΑΧΕΠΑ ΙΑΤΡΟΣ ΒΙΟΠΑΘΟΛΟΓΟΣ ΑΡΤΕΜΙΣ ΚΟΛΥΝΟΥ
 ΜΙΚΡΟΒΙΟΛΟΓΙΚΟ ΤΜΗΜΑ Π.Γ.Ν.Θ.ΑΧΕΠΑ ΙΑΤΡΟΣ ΒΙΟΠΑΘΟΛΟΓΟΣ ΑΡΤΕΜΙΣ ΚΟΛΥΝΟΥ Τα λεμφοκύτταρα προέρχονται από την λεμφική σειρά, ενώ τα μονοπύρηνα, τα πολυμορφοπύρηνα λευκοκύτταρα (κοκκιοκύτταρα) και τα βασεόφιλα
ΜΙΚΡΟΒΙΟΛΟΓΙΚΟ ΤΜΗΜΑ Π.Γ.Ν.Θ.ΑΧΕΠΑ ΙΑΤΡΟΣ ΒΙΟΠΑΘΟΛΟΓΟΣ ΑΡΤΕΜΙΣ ΚΟΛΥΝΟΥ Τα λεμφοκύτταρα προέρχονται από την λεμφική σειρά, ενώ τα μονοπύρηνα, τα πολυμορφοπύρηνα λευκοκύτταρα (κοκκιοκύτταρα) και τα βασεόφιλα
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ. Εργαστήριο Γενετικής, ΓΠΑ
 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
13. ΝΕΟΓΝΙΚΕΣ ΛΟΙΜΩΞΕΙΣ
 Νεογνικές Λοιµώξεις 13 13. ΝΕΟΓΝΙΚΕΣ ΛΟΙΜΩΞΕΙΣ Η συχνότητα των νεογνικών λοιµώξεων έχει αυξηθεί τις τελευταίες δεκαετίες καθώς επιζούν όλο και µικρότερα και πιο ανώριµα νεογνά, που χρειάζονται εντατική
Νεογνικές Λοιµώξεις 13 13. ΝΕΟΓΝΙΚΕΣ ΛΟΙΜΩΞΕΙΣ Η συχνότητα των νεογνικών λοιµώξεων έχει αυξηθεί τις τελευταίες δεκαετίες καθώς επιζούν όλο και µικρότερα και πιο ανώριµα νεογνά, που χρειάζονται εντατική
Νεογνικές και παιδιατρικές μεταγγίσεις. Ελισάβετ Γεωργίου Αιματολόγος, Επίμ. Β Αιματολογικό Τμήμα Γ. Ν. Παπαγεωργίου
 Νεογνικές και παιδιατρικές μεταγγίσεις Ελισάβετ Γεωργίου Αιματολόγος, Επίμ. Β Αιματολογικό Τμήμα Γ. Ν. Παπαγεωργίου Μεταγγίσεις σε νεογνά και παιδιά Μεταγγίσεις στον νεογνικό πληθυσμό Μεταγγίσεις στον
Νεογνικές και παιδιατρικές μεταγγίσεις Ελισάβετ Γεωργίου Αιματολόγος, Επίμ. Β Αιματολογικό Τμήμα Γ. Ν. Παπαγεωργίου Μεταγγίσεις σε νεογνά και παιδιά Μεταγγίσεις στον νεογνικό πληθυσμό Μεταγγίσεις στον
Μικροοργανισμοί. Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς
 Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
ΦΡΟΝΤΙΣΤΗΡΙΑ ΜΗΤΑΛΑΣ ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ
 ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΚΕΦΑΛΑΙΟ 1.3 : ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ ΘΕΜΑ 1 Χαρακτηρίστε τις προτάσεις ως σωστές ή λανθασµένες. 1. Οι βλεννογόνοι
ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΚΕΦΑΛΑΙΟ 1.3 : ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ ΘΕΜΑ 1 Χαρακτηρίστε τις προτάσεις ως σωστές ή λανθασµένες. 1. Οι βλεννογόνοι
Νικόλαος Δ. Βραχνής. και Εμβρυομητρικής. Αρεταίειο Νοσοκομείο
 Υπερηχογραφικά καθοδηγούμενος επεμβατικός έλεγχος στη Μαιευτική Νικόλαος Δ. Βραχνής Επίκουρος Καθηγητής Μαιευτικής Γυναικολογίας και Εμβρυομητρικής Ιατρικής Σχολής Πανεπιστημίου Αθηνών Αρεταίειο Νοσοκομείο
Υπερηχογραφικά καθοδηγούμενος επεμβατικός έλεγχος στη Μαιευτική Νικόλαος Δ. Βραχνής Επίκουρος Καθηγητής Μαιευτικής Γυναικολογίας και Εμβρυομητρικής Ιατρικής Σχολής Πανεπιστημίου Αθηνών Αρεταίειο Νοσοκομείο
ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS
 ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS ΑΜΕΣΗ COOMBS Θεμελιώδες γνώρισμα του κάθε οργανισμού είναι ότι αναγνωρίζει τα κύτταρα των άλλων οργανισμών ως ξένα Αντιδρά με σκοπό την καταστροφή ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ
ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS ΑΜΕΣΗ COOMBS Θεμελιώδες γνώρισμα του κάθε οργανισμού είναι ότι αναγνωρίζει τα κύτταρα των άλλων οργανισμών ως ξένα Αντιδρά με σκοπό την καταστροφή ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ Η πρώτη γραπτή αναφορά στο φαινόμενο της ανοσίας μπορεί να αναζητηθεί στον Θουκυδίδη, τον μεγάλο ιστορικό του Πελοποννησιακού Πολέμου Ανάπτυξη και επιβίωση o
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ Η πρώτη γραπτή αναφορά στο φαινόμενο της ανοσίας μπορεί να αναζητηθεί στον Θουκυδίδη, τον μεγάλο ιστορικό του Πελοποννησιακού Πολέμου Ανάπτυξη και επιβίωση o
Χρόνια φλεγμονή. Βαλεντίνη Τζιούφα-Ασημακοπούλου. Νοέμβριος 2018
 Χρόνια φλεγμονή Βαλεντίνη Τζιούφα-Ασημακοπούλου Νοέμβριος 2018 Οξεία φλεγμονή Ταχεία εισβολή και λύση Εξιδρωματικά στοιχεία Πολυμορφοπύρηνα Χρόνια φλεγμονή Ύπουλη εισβολήπαρατεταμένη πορείαβραδεία λύση
Χρόνια φλεγμονή Βαλεντίνη Τζιούφα-Ασημακοπούλου Νοέμβριος 2018 Οξεία φλεγμονή Ταχεία εισβολή και λύση Εξιδρωματικά στοιχεία Πολυμορφοπύρηνα Χρόνια φλεγμονή Ύπουλη εισβολήπαρατεταμένη πορείαβραδεία λύση
Μοριακή κυτταρική βιοχημεία Ανοσοποιητικό σύστημα
 Μοριακή κυτταρική βιοχημεία Ανοσοποιητικό σύστημα κωδικός μαθήματος: ETY-335 Χειμερινό εξάμηνο 2014 / 2015 Μαρία Χατζηνικολαΐδου mchatzin@materials.uoc.gr Έμφυτο και προσαρμοστικό ανοσοποιητικό σύστημα
Μοριακή κυτταρική βιοχημεία Ανοσοποιητικό σύστημα κωδικός μαθήματος: ETY-335 Χειμερινό εξάμηνο 2014 / 2015 Μαρία Χατζηνικολαΐδου mchatzin@materials.uoc.gr Έμφυτο και προσαρμοστικό ανοσοποιητικό σύστημα
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ
 ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ Συγκρίνατε την πρωτογενή µε τη δευτερογενή ανοσοβιολογική απόκριση και απεικονίστε αυτές στο ίδιο διάγραµµα αξόνων. Πρωτογενή ανοσοβιολογική απόκριση ονοµάζουµε την απόκριση του
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ Συγκρίνατε την πρωτογενή µε τη δευτερογενή ανοσοβιολογική απόκριση και απεικονίστε αυτές στο ίδιο διάγραµµα αξόνων. Πρωτογενή ανοσοβιολογική απόκριση ονοµάζουµε την απόκριση του
Πνευμονική Εμβολή. Έλενα Σολωμού Αιματολόγος Επίκουρη Καθηγήτρια Παθολογίας-Αιματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών
 Πνευμονική Εμβολή Έλενα Σολωμού Αιματολόγος Επίκουρη Καθηγήτρια Παθολογίας-Αιματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών Πήξη αίματος Αιμόσταση: διακοπή της απώλειας αίματος Μηχανισμοί αιμόστασης : Αγγειοσύσπαση
Πνευμονική Εμβολή Έλενα Σολωμού Αιματολόγος Επίκουρη Καθηγήτρια Παθολογίας-Αιματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών Πήξη αίματος Αιμόσταση: διακοπή της απώλειας αίματος Μηχανισμοί αιμόστασης : Αγγειοσύσπαση
ΦΡΟΝΤΙΣΤΗΡΙΑ ΠΡΟΟΠΤΙΚΗ
 Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Κεφάλαιο 4 ο ΑΙΜΑ ΜΑΡΙΑ ΣΗΦΑΚΗ ΣΤΟΙΧΕΙΑ ΑΝΑΤΟΜΙΑΣ - ΦΥΣΙΟΛΟΓΙΑΣ ΙΙ 1
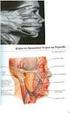 Κεφάλαιο 4 ο ΑΙΜΑ ΜΑΡΙΑ ΣΗΦΑΚΗ ΣΤΟΙΧΕΙΑ ΑΝΑΤΟΜΙΑΣ - ΦΥΣΙΟΛΟΓΙΑΣ ΙΙ 1 Το αίμα Έχει όγκο περίπου 5 λίτρα Αποτελείται από Πλάσμα (55%) Είναι νερό και διαλυμένες ουσίες Πρωτεΐνες Ορμόνες Άλατα Άλλες θρεπτικές
Κεφάλαιο 4 ο ΑΙΜΑ ΜΑΡΙΑ ΣΗΦΑΚΗ ΣΤΟΙΧΕΙΑ ΑΝΑΤΟΜΙΑΣ - ΦΥΣΙΟΛΟΓΙΑΣ ΙΙ 1 Το αίμα Έχει όγκο περίπου 5 λίτρα Αποτελείται από Πλάσμα (55%) Είναι νερό και διαλυμένες ουσίες Πρωτεΐνες Ορμόνες Άλατα Άλλες θρεπτικές
Κεφάλαιο 4ο Αίµα. στην άµυνα του οργανισµού (µε τα λευκά αιµοσφαίρια και τα αντισώµατα) και. Τεχνητή. Φυσική
 Κεφάλαιο 4ο Αίµα 4.1 Γενικά Το αίµα έχει όγκο περίπου 5 λίτρα. Αποτελείται από το πλάσµα (55%), το οποίο είναι νερό και µέσα του βίσκονται διαλυµένες πρωτεϊνες, ορµόνες, άλατα και άλλες θρεπτικές ουσίες
Κεφάλαιο 4ο Αίµα 4.1 Γενικά Το αίµα έχει όγκο περίπου 5 λίτρα. Αποτελείται από το πλάσµα (55%), το οποίο είναι νερό και µέσα του βίσκονται διαλυµένες πρωτεϊνες, ορµόνες, άλατα και άλλες θρεπτικές ουσίες
ΟΞΕΙΑ ΚΥΚΛΟΦΟΡΙΚΗ ΑΝΕΠΑΡΚΕΙΑ
 SHOCK ΟΞΕΙΑ ΚΥΚΛΟΦΟΡΙΚΗ ΑΝΕΠΑΡΚΕΙΑ ΕΙΔΟΣ SHOCK ανάλογα με το αίτιο Εκτεταμένη ισχαιμία Πιθανή πτώση ΑΠ Πιθανώς ωχρά κρύα άκρα (ισχαιμία αγγειοσύσπαση) Πιθανώς ιδρώτες ταχυκαρδία (υπερέκκριση αδρεναλίνης)
SHOCK ΟΞΕΙΑ ΚΥΚΛΟΦΟΡΙΚΗ ΑΝΕΠΑΡΚΕΙΑ ΕΙΔΟΣ SHOCK ανάλογα με το αίτιο Εκτεταμένη ισχαιμία Πιθανή πτώση ΑΠ Πιθανώς ωχρά κρύα άκρα (ισχαιμία αγγειοσύσπαση) Πιθανώς ιδρώτες ταχυκαρδία (υπερέκκριση αδρεναλίνης)
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς. Οι φάσεις των Τ κυτταρικών απαντήσεων
 ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
μαθητικό φροντιστήριο
 σύγχρονο Φάσμα group προπαρασκευή για μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990 50.20.990 Πρωτεσιλάου
σύγχρονο Φάσμα group προπαρασκευή για μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 50.51.557 50.56.296 25ης Μαρτίου 74 ΠΛ.ΠΕΤΡΟΥΠΟΛΗΣ 50.50.658 50.60.845 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 50.27.990 50.20.990 Πρωτεσιλάου
ΓΕΩΡΓΟΥ ΠΑΝΑΓΙΩΤΑ ΧΑΡΔΑΒΕΛΑ ΜΑΓΔΑΛΗΝΗ
 ΑΝΟΙΚΤΟΣ ΑΡΤΗΡΙΑΚΟΣ ΠΟΡΟΣ ΣΕ ΝΕΟΓΝΑ ΓΕΩΡΓΟΥ ΠΑΝΑΓΙΩΤΑ ΧΑΡΔΑΒΕΛΑ ΜΑΓΔΑΛΗΝΗ Συγγενείς ανωμαλίες της καρδιάς, είναι οι ατέλειες στη δομή της καρδιάς, που είναι παρούσες κατά τη γέννηση. Μια από αυτές είναι
ΑΝΟΙΚΤΟΣ ΑΡΤΗΡΙΑΚΟΣ ΠΟΡΟΣ ΣΕ ΝΕΟΓΝΑ ΓΕΩΡΓΟΥ ΠΑΝΑΓΙΩΤΑ ΧΑΡΔΑΒΕΛΑ ΜΑΓΔΑΛΗΝΗ Συγγενείς ανωμαλίες της καρδιάς, είναι οι ατέλειες στη δομή της καρδιάς, που είναι παρούσες κατά τη γέννηση. Μια από αυτές είναι
Κύηση Υψηλού Κινδύνου Δεδομένα ΜΕΝΝ ΡΕΑ
 Κύηση Υψηλού Κινδύνου Δεδομένα ΜΕΝΝ ΡΕΑ 2011-2017 Αντωνία Χαρίτου Συντονίστρια-Διευθύντρια ΜΕΝΝ ΡΕΑ Αντιπρόεδρος ΕΕΠΙ Γενικός Γραμματέας ΕΝΕ 30ο Συνέδριο ΕΕΚΠΠΥ- Τήνος 1 Κύηση Υψηλού Κινδύνου Κύηση στην
Κύηση Υψηλού Κινδύνου Δεδομένα ΜΕΝΝ ΡΕΑ 2011-2017 Αντωνία Χαρίτου Συντονίστρια-Διευθύντρια ΜΕΝΝ ΡΕΑ Αντιπρόεδρος ΕΕΠΙ Γενικός Γραμματέας ΕΝΕ 30ο Συνέδριο ΕΕΚΠΠΥ- Τήνος 1 Κύηση Υψηλού Κινδύνου Κύηση στην
ΛΟΙΜΩΞΕΙΣ ΑΠΌ ΕΝΔΑΓΓΕΙΑΚΟΥΣ ΚΑΘΕΤΗΡΕΣ
 ΛΟΙΜΩΞΕΙΣ ΑΠΌ ΕΝΔΑΓΓΕΙΑΚΟΥΣ ΚΑΘΕΤΗΡΕΣ ΕΜΜΑΝΟΥΗΛΙΔΗΣ ΙΩΑΝΝΗΣ ΧΕΙΡΟΥΡΓΟΣ & ΕΝΤΑΤΙΚΟΛΟΓΟΣ ΑΝΑΠΛ. ΔΙΕΥΘΥΝΤΗΣ ΧΕΙΡΟΥΡΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΓΕΝΙΚΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΛΑΜΙΑΣ ΛΑΜΙΑ ΟΚΤΩΒΡΙΟΣ 2005 Η σύγχρονη ιατρική και βιοτεχνολογία
ΛΟΙΜΩΞΕΙΣ ΑΠΌ ΕΝΔΑΓΓΕΙΑΚΟΥΣ ΚΑΘΕΤΗΡΕΣ ΕΜΜΑΝΟΥΗΛΙΔΗΣ ΙΩΑΝΝΗΣ ΧΕΙΡΟΥΡΓΟΣ & ΕΝΤΑΤΙΚΟΛΟΓΟΣ ΑΝΑΠΛ. ΔΙΕΥΘΥΝΤΗΣ ΧΕΙΡΟΥΡΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΓΕΝΙΚΟΥ ΝΟΣΟΚΟΜΕΙΟΥ ΛΑΜΙΑΣ ΛΑΜΙΑ ΟΚΤΩΒΡΙΟΣ 2005 Η σύγχρονη ιατρική και βιοτεχνολογία
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ
 23-10-11 ΘΕΡΙΝΑ ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν κυτταρικό
23-10-11 ΘΕΡΙΝΑ ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν κυτταρικό
Κύηση και συγγενείς καρδιοπάθειες. Στέλλα Μπρίλη Α! Καρδιολογική Κλινική Πανεπιστηµίου Αθηνών
 Κύηση και συγγενείς καρδιοπάθειες Στέλλα Μπρίλη Α! Καρδιολογική Κλινική Πανεπιστηµίου Αθηνών Αιµοδυναµικές αλλαγές κατά την εγκυµοσύνη Όγκος αίµατος 30-50% Μέγιστο 20-24 εβδ Όγκος παλµού Καρδιακή Συχνότητα
Κύηση και συγγενείς καρδιοπάθειες Στέλλα Μπρίλη Α! Καρδιολογική Κλινική Πανεπιστηµίου Αθηνών Αιµοδυναµικές αλλαγές κατά την εγκυµοσύνη Όγκος αίµατος 30-50% Μέγιστο 20-24 εβδ Όγκος παλµού Καρδιακή Συχνότητα
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων
 Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Σεξουαλικά µεταδιδόµενα νοσήµατα και AIDS στους εφήβους. Χαράλαµπος Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ
 Σεξουαλικά µεταδιδόµενα νοσήµατα και AIDS στους εφήβους Χαράλαµπος Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ Εφηβική ηλικία και σεξουαλικά µεταδιδόµενα νοσήµατα (STDs) Έναρξη σεξουαλικής ζωής Έλλειψη προφυλάξεων
Σεξουαλικά µεταδιδόµενα νοσήµατα και AIDS στους εφήβους Χαράλαµπος Ανταχόπουλος 3 η Παιδιατρική Κλινική ΑΠΘ Εφηβική ηλικία και σεξουαλικά µεταδιδόµενα νοσήµατα (STDs) Έναρξη σεξουαλικής ζωής Έλλειψη προφυλάξεων
Ποιες είναι οι προϋποθέσεις που πρέπει να τηρούνται για την αποφυγή µετάδοσης ασθενειών που οφείλονται σε παθογόνους µικροοργανισµούς;
 ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Ποιες είναι οι προϋποθέσεις που πρέπει να τηρούνται για την αποφυγή µετάδοσης ασθενειών που οφείλονται σε παθογόνους µικροοργανισµούς; ΘΕΜΑ Β ίνεται το παρακάτω
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Ποιες είναι οι προϋποθέσεις που πρέπει να τηρούνται για την αποφυγή µετάδοσης ασθενειών που οφείλονται σε παθογόνους µικροοργανισµούς; ΘΕΜΑ Β ίνεται το παρακάτω
Aποµυελινωτικά νοσήµατα Γεώργιος Καρκαβέλας Καθηγητής Παθολογικής
 Aποµυελινωτικά νοσήµατα Γεώργιος Καρκαβέλας Καθηγητής Παθολογικής Ανατοµικής ΑΠΘ ΑΠΟΜΥΕΛΙΝΩΣΗ καταστροφή µυελίνης αποκλείονται παθολογικές καταστάσεις από αποτυχία σχηµατισµού µυελίνης (δυσµυελίνωση) ή
Aποµυελινωτικά νοσήµατα Γεώργιος Καρκαβέλας Καθηγητής Παθολογικής Ανατοµικής ΑΠΘ ΑΠΟΜΥΕΛΙΝΩΣΗ καταστροφή µυελίνης αποκλείονται παθολογικές καταστάσεις από αποτυχία σχηµατισµού µυελίνης (δυσµυελίνωση) ή
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ
 23 10 2011 ΘΕΡΙΝΑ ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν
23 10 2011 ΘΕΡΙΝΑ ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ 1 Ο Α. Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Όλα τα βακτήρια: Α. διαθέτουν
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ. ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera
 Α1. 1. β Βιολογία ΘΕΜΑ Α γενιικής παιιδείίας 2. γ 3. γ 4. γ 5. δ Α2. ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera Ηπατίτιδα C + Candida albicans
Α1. 1. β Βιολογία ΘΕΜΑ Α γενιικής παιιδείίας 2. γ 3. γ 4. γ 5. δ Α2. ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera Ηπατίτιδα C + Candida albicans
Ιοί & HPV. Ευστάθιος Α. Ράλλης. Επικ. Καθηγητής Δερματολογίας - Αφροδισιολογίας
 Ιοί & HPV Ευστάθιος Α. Ράλλης Επικ. Καθηγητής Δερματολογίας - Αφροδισιολογίας Περί ΙΩΝ Ορισμός Οι ιοί είναι ατελείς, λοιμώδεις οργανισμοί μικρότεροι σε μέγεθος από τα μικρόβια και ορατοί μόνο με το ηλεκτρονικό
Ιοί & HPV Ευστάθιος Α. Ράλλης Επικ. Καθηγητής Δερματολογίας - Αφροδισιολογίας Περί ΙΩΝ Ορισμός Οι ιοί είναι ατελείς, λοιμώδεις οργανισμοί μικρότεροι σε μέγεθος από τα μικρόβια και ορατοί μόνο με το ηλεκτρονικό
8 η Παρουσίαση Εισαγωγή στο Αίμα
 ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ
 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ Εργαστηριακή αξιολόγηση της αξιοπιστίας του strep testστη διάγνωση και τον καθορισμό της κατάλληλης αντιβιοτικής αγωγής σε ασθενείς με οξεία πυώδη αμυγδαλίτιδα
ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ Εργαστηριακή αξιολόγηση της αξιοπιστίας του strep testστη διάγνωση και τον καθορισμό της κατάλληλης αντιβιοτικής αγωγής σε ασθενείς με οξεία πυώδη αμυγδαλίτιδα
Θέµατα Πανελληνίων Βιολογίας Γ.Π Άµυνα - Ανοσία
 2012 Α2. Τα φαγοκύτταρα παράγονται α. στο νωτιαίο µυελό β. στο θύµο αδένα γ. στους λεµφαδένες δ. στον ερυθρό µυελό των οστών. Α3. Το συµπλήρωµα και η προπερδίνη συµβάλλουν στην καταπολέµηση α. των ιών
2012 Α2. Τα φαγοκύτταρα παράγονται α. στο νωτιαίο µυελό β. στο θύµο αδένα γ. στους λεµφαδένες δ. στον ερυθρό µυελό των οστών. Α3. Το συµπλήρωµα και η προπερδίνη συµβάλλουν στην καταπολέµηση α. των ιών
ΕΡΩΤΗΣΕΙΣ 1 ου ΚΕΦΑΛΑΙΟΥ
 ΕΡΩΤΗΣΕΙΣ 1 ου ΚΕΦΑΛΑΙΟΥ Επιλέξτε τη σωστή απάντηση: Το τρυπανόσωμα προκαλεί α. δυσεντερία β. ελονοσία γ. ασθένεια του ύπνου δ. χολέρα Τα ενδοσπόρια σχηματίζονται από β. φυτά γ. ιούς δ. πρωτόζωα Η σύφιλη
ΕΡΩΤΗΣΕΙΣ 1 ου ΚΕΦΑΛΑΙΟΥ Επιλέξτε τη σωστή απάντηση: Το τρυπανόσωμα προκαλεί α. δυσεντερία β. ελονοσία γ. ασθένεια του ύπνου δ. χολέρα Τα ενδοσπόρια σχηματίζονται από β. φυτά γ. ιούς δ. πρωτόζωα Η σύφιλη
Δεκαπεντάλεπτη προετοιμασία του φοιτητή για το μάθημα των ουρολοιμώξεων.
 Δεκαπεντάλεπτη προετοιμασία του φοιτητή για το μάθημα των ουρολοιμώξεων. Τι είναι ουρολοίμωξη; Σαν ουρολοίμωξη χαρακτηρίζουμε την βακτηριδιακή λοίμωξη κυρίως οποιοδήποτε σημείου του ουροποιητικού συστήματος.
Δεκαπεντάλεπτη προετοιμασία του φοιτητή για το μάθημα των ουρολοιμώξεων. Τι είναι ουρολοίμωξη; Σαν ουρολοίμωξη χαρακτηρίζουμε την βακτηριδιακή λοίμωξη κυρίως οποιοδήποτε σημείου του ουροποιητικού συστήματος.
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών
 Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Ο ρόλος της ενεργοποίησης των φαγοκυττάρων
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Ο ρόλος της ενεργοποίησης των φαγοκυττάρων
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις μεμβράνες 2. Φυσιολογικοί φραγμοί
2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις μεμβράνες 2. Φυσιολογικοί φραγμοί
ΟΥΡΟΛΟΙΜΩΞΕΙΣ ΤΟΥ ΣΚΥΛΟΥ & ΤΗΣ ΓΑΤΑΣ Λ.Β.Α. 1
 ΟΥΡΟΛΟΙΜΩΞΕΙΣ ΤΟΥ ΣΚΥΛΟΥ & ΤΗΣ ΓΑΤΑΣ Λ.Β.Α. 1 ΕΠΙΔΗΜΙΟΛΟΓΙΚΑ ΔΕΔΟΜΕΝΑ Συχνότητα: Σκύλος >> γάτα Συχνότητα: Θηλυκά >> αρσενικά Εντόπιση: ουροδόχος κύστη, ουρήθρα Αιτιολογία: βακτήρια>μυκοπλάσματα, χλαμύδιες,
ΟΥΡΟΛΟΙΜΩΞΕΙΣ ΤΟΥ ΣΚΥΛΟΥ & ΤΗΣ ΓΑΤΑΣ Λ.Β.Α. 1 ΕΠΙΔΗΜΙΟΛΟΓΙΚΑ ΔΕΔΟΜΕΝΑ Συχνότητα: Σκύλος >> γάτα Συχνότητα: Θηλυκά >> αρσενικά Εντόπιση: ουροδόχος κύστη, ουρήθρα Αιτιολογία: βακτήρια>μυκοπλάσματα, χλαμύδιες,
Κεφ. 8. ραστικοί µηχανισµοί της χυµικής ανοσίας: Η εξάλειψη των εξωκυττάριων µικροοργανισµών και τοξινών
 Κεφ. 8. ραστικοί µηχανισµοί της χυµικής ανοσίας: Η εξάλειψη των εξωκυττάριων µικροοργανισµών και τοξινών Οι ιδιότητες των αντισωµάτων που καθορίζουν τις δραστικές τους λειτουργίες Οι δραστικές λειτουργίες
Κεφ. 8. ραστικοί µηχανισµοί της χυµικής ανοσίας: Η εξάλειψη των εξωκυττάριων µικροοργανισµών και τοξινών Οι ιδιότητες των αντισωµάτων που καθορίζουν τις δραστικές τους λειτουργίες Οι δραστικές λειτουργίες
4. Η κίρρωση του ήπατος προκαλείται εξαιτίας της αποθήκευσης στα ηπατικά κύτταρα: Πρωτεϊνών Υδατανθράκων Λιπών Αλκοόλ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
όλοι αναπνευστική οδός στομάχι στόμα
 κεράτινη στιβάδα περιέχει σμήγμα λιπαρά οξέα Μηχανισμοί που παρεμποδίζουν την είσοδο Δέρμα περιέχει ιδρώτας φυσιολογική μικροχλωρίδα λυσοζύμη γαλακτικό οξύ μικροοργανισμών Βλεννογόνοι όλοι αναπνευστική
κεράτινη στιβάδα περιέχει σμήγμα λιπαρά οξέα Μηχανισμοί που παρεμποδίζουν την είσοδο Δέρμα περιέχει ιδρώτας φυσιολογική μικροχλωρίδα λυσοζύμη γαλακτικό οξύ μικροοργανισμών Βλεννογόνοι όλοι αναπνευστική
ΜΕΤΑΔΟΣΗ ΚΑΙ ΑΝΤΙΜΕΤΩΠΙΣΗ ΠΑΘΟΓΟΝΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ
 ΜΕΤΑΔΟΣΗ ΚΑΙ ΑΝΤΙΜΕΤΩΠΙΣΗ ΠΑΘΟΓΟΝΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΜΟΛΥΝΣΗ : Η είσοδος ενός παθογόνου μικροοργανισμού στον οργανισμό του ανθρώπου. ΛΟΙΜΩΞΗ : Η εγκατάσταση και ο πολλαπλασιασμός του παθογόνου μικροοργανισμού
ΜΕΤΑΔΟΣΗ ΚΑΙ ΑΝΤΙΜΕΤΩΠΙΣΗ ΠΑΘΟΓΟΝΩΝ ΜΙΚΡΟΟΡΓΑΝΙΣΜΩΝ ΜΟΛΥΝΣΗ : Η είσοδος ενός παθογόνου μικροοργανισμού στον οργανισμό του ανθρώπου. ΛΟΙΜΩΞΗ : Η εγκατάσταση και ο πολλαπλασιασμός του παθογόνου μικροοργανισμού
Η ΕΠΙΔΡΑΣΗ ΤΟΥ ΚΑΠΝΙΣΜΑΤΟΣ
 Η ΕΠΙΔΡΑΣΗ ΤΟΥ ΚΑΠΝΙΣΜΑΤΟΣ ΣΤΗΝ ΚΥΗΣΗ ΚΑΙ ΣΤΟ ΝΕΟΓΝΟ 7ο ΕΤΗΣΙΟ ΣΥΝΕΔΡΙΟ ΑΘΗΡΟΣΚΛΗΡΩΣΗΣ Δρ. Μαρία Τζητηρίδου- Χατζοπούλου Παιδίατρος Νεογνολόγος-Αναπτυξιολόγος Διδάκτωρ Ιατρικής Σχολής ΑΠΘ ΕΙΣΑΓΩΓΗ Π.Ο.Υ
Η ΕΠΙΔΡΑΣΗ ΤΟΥ ΚΑΠΝΙΣΜΑΤΟΣ ΣΤΗΝ ΚΥΗΣΗ ΚΑΙ ΣΤΟ ΝΕΟΓΝΟ 7ο ΕΤΗΣΙΟ ΣΥΝΕΔΡΙΟ ΑΘΗΡΟΣΚΛΗΡΩΣΗΣ Δρ. Μαρία Τζητηρίδου- Χατζοπούλου Παιδίατρος Νεογνολόγος-Αναπτυξιολόγος Διδάκτωρ Ιατρικής Σχολής ΑΠΘ ΕΙΣΑΓΩΓΗ Π.Ο.Υ
2. Τα πρωτόζωα α. δεν έχουν πυρήνα. β. είναι μονοκύτταροι ευκαρυωτικοί οργανισμοί. γ. είναι πολυκύτταρα παράσιτα. δ. είναι αυτότροφοι οργανισμοί.
 1 ΘΕΜΑΤΑ κεφ 1. Α. Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή στη φράση η οποία συμπληρώνει σωστά την ημιτελή πρόταση.
1 ΘΕΜΑΤΑ κεφ 1. Α. Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ημιτελείς προτάσεις και δίπλα το γράμμα που αντιστοιχεί στη λέξη ή στη φράση η οποία συμπληρώνει σωστά την ημιτελή πρόταση.
Φυσική Ανοσία. Ανοσολογικοί µηχανισµοί. Κυτταροκίνες
 Ανοσολογικοί µηχανισµοί Ειδικοί ανοσολογικοί µηχανισµοί (επίκτητη ανοσία) εξαρτώνται από την ειδική αναγνώριση από τα λεµφοκύτταρα της ξένης ουσίας ή κυττάρου Φυσική Ανοσία Μηχανισµοί φυσικής (µη ειδικής)
Ανοσολογικοί µηχανισµοί Ειδικοί ανοσολογικοί µηχανισµοί (επίκτητη ανοσία) εξαρτώνται από την ειδική αναγνώριση από τα λεµφοκύτταρα της ξένης ουσίας ή κυττάρου Φυσική Ανοσία Μηχανισµοί φυσικής (µη ειδικής)
Το γόνατο ως στόχος ρευματικών νοσημάτων
 Το γόνατο ως στόχος ρευματικών νοσημάτων Χ. Μ. ΜουτσόπουΛος Αντεπιστέλλον μέλος της Ακαδημίας Αθηνών, Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών α ρευματικά νοσήματα είναι ασθένειες που προσβάλλουν
Το γόνατο ως στόχος ρευματικών νοσημάτων Χ. Μ. ΜουτσόπουΛος Αντεπιστέλλον μέλος της Ακαδημίας Αθηνών, Καθηγητής Ιατρικής Σχολής Πανεπιστημίου Αθηνών α ρευματικά νοσήματα είναι ασθένειες που προσβάλλουν
Παθογένεια της έξαρσης της Χ.Α.Π
 α ρ χ ή π ρ ο η γ ο ύ µ ε ν ο ε π ό µ ε ν ο Παθογένεια της έξαρσης της Χ.Α.Π Νίκος Τζανάκης, Πνευµονολόγος Επίκουρος Καθηγητής Πανεπιστήµιο Κρήτης ΧΑΠ -παρόξυνση Ορισµός! Ορισµός δύσκολος και σχετικά ανακριβής!
α ρ χ ή π ρ ο η γ ο ύ µ ε ν ο ε π ό µ ε ν ο Παθογένεια της έξαρσης της Χ.Α.Π Νίκος Τζανάκης, Πνευµονολόγος Επίκουρος Καθηγητής Πανεπιστήµιο Κρήτης ΧΑΠ -παρόξυνση Ορισµός! Ορισµός δύσκολος και σχετικά ανακριβής!
Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C.
 Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 5 ΣΕΛΙΔΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΣΑΒΒΑΤΟ 26 ΟΚΤΩΒΡΙΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΠΕΝΤΕ (5) Θέμα Α Μονάδες 25 Α1.
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΑΠΑΝΤΗΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β ) ΣΑΒΒΑΤΟ 26 ΟΚΤΩΒΡΙΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΠΕΝΤΕ (5) Θέμα Α Μονάδες 25 Α1.
3. Με ποιο άλλο σύστημα είναι συνδεδεμένο το κυκλοφορικό σύστημα;
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
ΝΟΣΗΛΕΥΤΙΚΗ ΦΡΟΝΤΙΔΑ ΤΟΥ ΔΙΑΒΗΤΙΚΟΥ ΑΣΘΕΝΗ ΣΤΗ ΣΤΕΦΑΝΙΑΙΑ ΜΟΝΑΔΑ ΚΑΙ ΣΤΗ ΜΕΘ
 ΝΟΣΗΛΕΥΤΙΚΗ ΦΡΟΝΤΙΔΑ ΤΟΥ ΔΙΑΒΗΤΙΚΟΥ ΑΣΘΕΝΗ ΣΤΗ ΣΤΕΦΑΝΙΑΙΑ ΜΟΝΑΔΑ ΚΑΙ ΣΤΗ ΜΕΘ Χ Ο Ν Δ Ρ Ο Μ Α Τ Ι Δ Ο Υ Μ Α Ρ Ι Α Ν Ο Σ Η Λ Ε Υ Τ Ρ Ι Α T E, M S C, Μ Ε Θ Α, Π Γ Ν Α Χ Ε Π Α ΕΙΣΑΓΩΓΙΚΑ.. Όπως είναι ευρέως
ΝΟΣΗΛΕΥΤΙΚΗ ΦΡΟΝΤΙΔΑ ΤΟΥ ΔΙΑΒΗΤΙΚΟΥ ΑΣΘΕΝΗ ΣΤΗ ΣΤΕΦΑΝΙΑΙΑ ΜΟΝΑΔΑ ΚΑΙ ΣΤΗ ΜΕΘ Χ Ο Ν Δ Ρ Ο Μ Α Τ Ι Δ Ο Υ Μ Α Ρ Ι Α Ν Ο Σ Η Λ Ε Υ Τ Ρ Ι Α T E, M S C, Μ Ε Θ Α, Π Γ Ν Α Χ Ε Π Α ΕΙΣΑΓΩΓΙΚΑ.. Όπως είναι ευρέως
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
 ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΤΟ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΕ ΚΑΤΑΣΤΑΣΕΙΣ STRESS ΦΥΣΙΟΛΟΓΙΑ ΜΕΓΑΛΟΥ ΥΨΟΜΕΤΡΟΥ Η ατμοσφαιρική
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΤΟ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΕ ΚΑΤΑΣΤΑΣΕΙΣ STRESS ΦΥΣΙΟΛΟΓΙΑ ΜΕΓΑΛΟΥ ΥΨΟΜΕΤΡΟΥ Η ατμοσφαιρική
- Θεωρία- Δρ. ΠέτρουΚαρκαλούσου
 - Θεωρία- Έκδοση2008 Πρόλογος Αγαπητοίσπουδαστέςοισημειώσειςπουκρατάτεσταχέριασαςέχουνσκοπόνασας εισαγάγουνστιςβασικέςγνώσειςμιαςαπότιςσημαντικότερεςβιοιατρικέςεπιστήμες, της ανοσολογίας. Η ανοσολογίαείναιμιασχετικάνέαεπιστήμηηοποίαεμφανίστηκεστοτέλοςτου
- Θεωρία- Έκδοση2008 Πρόλογος Αγαπητοίσπουδαστέςοισημειώσειςπουκρατάτεσταχέριασαςέχουνσκοπόνασας εισαγάγουνστιςβασικέςγνώσειςμιαςαπότιςσημαντικότερεςβιοιατρικέςεπιστήμες, της ανοσολογίας. Η ανοσολογίαείναιμιασχετικάνέαεπιστήμηηοποίαεμφανίστηκεστοτέλοςτου
-Αναστολή της οργανικής σύνδεσης του ιωδίου που προσλαμβάνεται από το θυρεοειδή αδένα -Ανοσοκατασταλτική δράση με αποτέλεσμα τη μείωση της παραγωγής
 Άννα Ναξάκη Επιμελήτρια Α Γ Παθολογική Κλινική ΠΑΡΑΓΩΓΑ ΘΕΙΟΥΡΙΑΣ(ΠΡΟΠΥΛΟ ΚΑΙ ΜΕΘΥΛΟΘΕΙΟΥΡΑΚΙΛΗ) ΠΑΡΑΓΩΓΑ ΙΜΙΔΑΖΟΛΗΣ(ΚΑΡΒΙΜΑΖΟΛΗ ΚΑΙ ΘΕΙΑΜΑΖΟΛΗ) -Αναστολή της οργανικής σύνδεσης του ιωδίου που προσλαμβάνεται
Άννα Ναξάκη Επιμελήτρια Α Γ Παθολογική Κλινική ΠΑΡΑΓΩΓΑ ΘΕΙΟΥΡΙΑΣ(ΠΡΟΠΥΛΟ ΚΑΙ ΜΕΘΥΛΟΘΕΙΟΥΡΑΚΙΛΗ) ΠΑΡΑΓΩΓΑ ΙΜΙΔΑΖΟΛΗΣ(ΚΑΡΒΙΜΑΖΟΛΗ ΚΑΙ ΘΕΙΑΜΑΖΟΛΗ) -Αναστολή της οργανικής σύνδεσης του ιωδίου που προσλαμβάνεται
Βιολογία γενικής παιδείας τάξη Γ
 Βιολογία γενικής παιδείας τάξη Γ Παραδόσεις του μαθήματος Επιμέλεια: Γιάννης Αργύρης Βιολόγος M.Sc. Καθηγητής 3 ου Γεν. Λυκ. Ηλιούπολης Κεφάλαιο 1ο Άνθρωπος και υγεία 2. Μηχανισμοί Άμυνας του Ανθρώπινου
Βιολογία γενικής παιδείας τάξη Γ Παραδόσεις του μαθήματος Επιμέλεια: Γιάννης Αργύρης Βιολόγος M.Sc. Καθηγητής 3 ου Γεν. Λυκ. Ηλιούπολης Κεφάλαιο 1ο Άνθρωπος και υγεία 2. Μηχανισμοί Άμυνας του Ανθρώπινου
6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών
 6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών Οι δύο τύποι της κυτταρικής ανοσίας Η µετανάστευση των δραστικών Τ κυττάρων στις εστίες της λοίµωξης (εντόπιση
6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών Οι δύο τύποι της κυτταρικής ανοσίας Η µετανάστευση των δραστικών Τ κυττάρων στις εστίες της λοίµωξης (εντόπιση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ / Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 15/11/2015 ΘΕΜΑ Α Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: Α1. Η φαγοκυττάρωση
ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ
 ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ Ερωτήσεις πολλαπλής επιλογής: επιλέξτε το γράμμα που αντιστοιχεί στη σωστή συνέχεια της πρότασης. 1. Δυσμενές χημικό περιβάλλον στην επιδερμίδα προκαλείται από:
ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ Ερωτήσεις πολλαπλής επιλογής: επιλέξτε το γράμμα που αντιστοιχεί στη σωστή συνέχεια της πρότασης. 1. Δυσμενές χημικό περιβάλλον στην επιδερμίδα προκαλείται από:
OMA Α ΜΕΛΕΤΗΣ ΤΗΣ ΣΗΨΗΣ (HELLENIC SEPSIS STUDY GROUP) Επικ. Καθηγητής Παθολογίας Παθολογική Κλινική, Σχολή Πανεπιστηµίου Αθηνών.
 OMA Α ΜΕΛΕΤΗΣ ΤΗΣ ΣΗΨΗΣ (HELLENIC SEPSIS STUDY GROUP) Ευάγγελος Ι. Γιαµαρέλλος-Μπουρµπούλης Ιατρική Σχολή Επικ. Καθηγητής Παθολογίας Παθολογική Κλινική, Σχολή Πανεπιστηµίου Αθηνών ΣΚΟΠΟΣ ΤΗΣ ΟΜΑ ΑΣ Καταγραφή
OMA Α ΜΕΛΕΤΗΣ ΤΗΣ ΣΗΨΗΣ (HELLENIC SEPSIS STUDY GROUP) Ευάγγελος Ι. Γιαµαρέλλος-Μπουρµπούλης Ιατρική Σχολή Επικ. Καθηγητής Παθολογίας Παθολογική Κλινική, Σχολή Πανεπιστηµίου Αθηνών ΣΚΟΠΟΣ ΤΗΣ ΟΜΑ ΑΣ Καταγραφή
ΘΕΜΑ 1 Ο ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Οι αποικοδομητές είναι:
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΘΕΡΙΝΑ ΗΜΕΡΟΜΗΝΙΑ: 10/11/2013 ΘΕΜΑ 1 Ο Να επιλέξετε την φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Οι αποικοδομητές είναι:
4. ΟΙ ΑΣΘΕΝΕΙΕΣ ΚΑΙ ΟΙ ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΣΧΕΤΙΖΟΝΤΑΙ ΜΕ ΤΗΝ ΕΜΦΑΝΙΣΗ ΤΟΥΣ
 4.1 Ομοιόσταση 4.2 Ασθένειες 4. ΟΙ ΑΣΘΕΝΕΙΕΣ ΚΑΙ ΟΙ ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΣΧΕΤΙΖΟΝΤΑΙ ΜΕ ΤΗΝ ΕΜΦΑΝΙΣΗ ΤΟΥΣ 4.3 Αμυντικοί μηχανισμοί του ανθρώπινου οργανισμού 4.4 Τρόποι ζωής και ασθένειες Μάρθα Καρβουνίδου ΠΕ1404
4.1 Ομοιόσταση 4.2 Ασθένειες 4. ΟΙ ΑΣΘΕΝΕΙΕΣ ΚΑΙ ΟΙ ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΣΧΕΤΙΖΟΝΤΑΙ ΜΕ ΤΗΝ ΕΜΦΑΝΙΣΗ ΤΟΥΣ 4.3 Αμυντικοί μηχανισμοί του ανθρώπινου οργανισμού 4.4 Τρόποι ζωής και ασθένειες Μάρθα Καρβουνίδου ΠΕ1404
προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι.
 σύγχρονο Φάσµα & Group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 210 50 51 557 210 50 56 296 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 210 50 20 990 210 50 27 990 25ης Μαρτίου 74 ΠΕΤΡΟΥΠΟΛΗ
σύγχρονο Φάσµα & Group προπαρασκευή για Α.Ε.Ι. & Τ.Ε.Ι. μαθητικό φροντιστήριο Γραβιάς 85 ΚΗΠΟΥΠΟΛΗ 210 50 51 557 210 50 56 296 25ης Μαρτίου 111 ΠΕΤΡΟΥΠΟΛΗ 210 50 20 990 210 50 27 990 25ης Μαρτίου 74 ΠΕΤΡΟΥΠΟΛΗ
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ 1 ου ΚΕΦΑΛΑΙΟΥ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ
 ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ 1 ου ΚΕΦΑΛΑΙΟΥ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο A. Ερωτήσεις πολλαπλής επιλογής 1. β 2. γ 3. β 4. γ 5. δ B. Ερωτήσεις σωστού - λάθους 1. Σωστό 2. Σωστό 3. Λάθος 4. Λάθος 5.
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ ΔΙΑΓΩΝΙΣΜΑ 1 ου ΚΕΦΑΛΑΙΟΥ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο A. Ερωτήσεις πολλαπλής επιλογής 1. β 2. γ 3. β 4. γ 5. δ B. Ερωτήσεις σωστού - λάθους 1. Σωστό 2. Σωστό 3. Λάθος 4. Λάθος 5.
ΑΛΛΕΡΓΙΑ: Ο ΑΟΡΑΤΟΣ ΕΧΘΡΟΣ ΠΩΣ ΓΙΝΕΤΑΙ ΚΑΠΟΙΟΣ ΑΛΛΕΡΓΙΚΟΣ;
 ΑΛΛΕΡΓΙΑ: Ο ΑΟΡΑΤΟΣ ΕΧΘΡΟΣ ΠΩΣ ΓΙΝΕΤΑΙ ΚΑΠΟΙΟΣ ΑΛΛΕΡΓΙΚΟΣ; Αλλεργία, όπως ορίζει και η λέξη, σημαίνει άλλο έργο. Είναι η μη αναμενόμενη αντίδραση του ανοσιακού συστήματος του οργανισμού εναντίον ακίνδυνων
ΑΛΛΕΡΓΙΑ: Ο ΑΟΡΑΤΟΣ ΕΧΘΡΟΣ ΠΩΣ ΓΙΝΕΤΑΙ ΚΑΠΟΙΟΣ ΑΛΛΕΡΓΙΚΟΣ; Αλλεργία, όπως ορίζει και η λέξη, σημαίνει άλλο έργο. Είναι η μη αναμενόμενη αντίδραση του ανοσιακού συστήματος του οργανισμού εναντίον ακίνδυνων
ΑΠΟΚΌΛΛΗΣΗ ΠΛΑΚΟΎΝΤΑ
 ΑΠΟΚΌΛΛΗΣΗ ΠΛΑΚΟΎΝΤΑ Παθοφυσιολογία, Διάγνωση και Αντιμετώπιση Alexander Kofinas, MD Director Kofinas Perinatal Associate Professor Clinical Obstetrics and Gynecology Cornell University, College of Medicine
ΑΠΟΚΌΛΛΗΣΗ ΠΛΑΚΟΎΝΤΑ Παθοφυσιολογία, Διάγνωση και Αντιμετώπιση Alexander Kofinas, MD Director Kofinas Perinatal Associate Professor Clinical Obstetrics and Gynecology Cornell University, College of Medicine
ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ. Εισαγωγή στην αιματολογία
 ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ Εισαγωγή στην αιματολογία Αιματολογία Κλινική και εργαστηριακή Διαγνωστική και θεραπευτική Αυτόνομη και συνεργατική Αίμα-Λειτουργίες Μεταφορά οξυγόνου Απομάκρυνση
ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ Εισαγωγή στην αιματολογία Αιματολογία Κλινική και εργαστηριακή Διαγνωστική και θεραπευτική Αυτόνομη και συνεργατική Αίμα-Λειτουργίες Μεταφορά οξυγόνου Απομάκρυνση
ΜΕΤΑΒΟΛΙΚΗ ΦΑΣΗ ΤΗΣ ΑΝΑΚΟΠΗΣ
 Από την καρδιοπνευμονική στην καρδιοεγκεφαλική αναζωογόνηση ΤΗΣ ΑΝΑΚΟΠΗΣ Μαρία Ι. Σεφέρου Ειδικευόμενη Καρδιολογίας Σισμανόγλειο Γ.Ν.Α. ΑΝΑΚΟΠΗ Ηλεκτρική Φάση Κυκλοφορική Φάση Μεταβολική Φάση ΕΛΛΗΝΙΚΗ
Από την καρδιοπνευμονική στην καρδιοεγκεφαλική αναζωογόνηση ΤΗΣ ΑΝΑΚΟΠΗΣ Μαρία Ι. Σεφέρου Ειδικευόμενη Καρδιολογίας Σισμανόγλειο Γ.Ν.Α. ΑΝΑΚΟΠΗ Ηλεκτρική Φάση Κυκλοφορική Φάση Μεταβολική Φάση ΕΛΛΗΝΙΚΗ
ταχύτητα καθίζησης ερυθρών (ΤΚΕ)
 ταχύτητα καθίζησης ερυθρών (ΤΚΕ) ταχύτητα καθίζησης ερυθρών (ΤΚΕ) {Erythrocyte Sedimentation Rate (ESR)} η ταχύτητα με την οποία καθιζάνουν τα ερυθρά αιμοσφαίρια μέσα στον εξεταστικό σωλήνα του μεγαλύτερου
ταχύτητα καθίζησης ερυθρών (ΤΚΕ) ταχύτητα καθίζησης ερυθρών (ΤΚΕ) {Erythrocyte Sedimentation Rate (ESR)} η ταχύτητα με την οποία καθιζάνουν τα ερυθρά αιμοσφαίρια μέσα στον εξεταστικό σωλήνα του μεγαλύτερου
Παγκόσμια κατανομή οροομάδων
 Η βακτηριακή μηνιγγίτιδα προκαλείται στις περισσότερες περιπτώσεις από τα βακτήρια Haemophilus influenzae, Streptococcus pneumoniae, group B Streptococcus, Listeria monocytogenes, και Neisseria meningitidis.
Η βακτηριακή μηνιγγίτιδα προκαλείται στις περισσότερες περιπτώσεις από τα βακτήρια Haemophilus influenzae, Streptococcus pneumoniae, group B Streptococcus, Listeria monocytogenes, και Neisseria meningitidis.
10 ο Πανελλήνιο Συνέδριο Ιατρικής Βιοπαθολογίας. Μαρία Εξηντάρη Εργαστήριο Μικροβιολογίας, Ιατρικό Τμήμα ΑΠΘ
 10 ο Πανελλήνιο Συνέδριο Ιατρικής Βιοπαθολογίας Μαρία Εξηντάρη Εργαστήριο Μικροβιολογίας, Ιατρικό Τμήμα ΑΠΘ Παγκόσμιος Οργανισμός Υγείας, Οκτ. 2017 : Υπέρβαρος (overweight) ή παχύσαρκος (obese): Ατομο
10 ο Πανελλήνιο Συνέδριο Ιατρικής Βιοπαθολογίας Μαρία Εξηντάρη Εργαστήριο Μικροβιολογίας, Ιατρικό Τμήμα ΑΠΘ Παγκόσμιος Οργανισμός Υγείας, Οκτ. 2017 : Υπέρβαρος (overweight) ή παχύσαρκος (obese): Ατομο
Νεογνικές και παιδιατρικές μεταγγίσεις
 Νεογνικές και παιδιατρικές μεταγγίσεις Ελισάβετ Γεωργίου Αιματολόγος Αιματολογικό Τμήμα Γ. Ν. Παπαγεωργίου Ακαδημία Αιμοδοσίας, Ιούνιος 2014 Μεταγγίσεις σε νεογνά και παιδιά Μεταγγίσεις στον νεογνικό πληθυσμό
Νεογνικές και παιδιατρικές μεταγγίσεις Ελισάβετ Γεωργίου Αιματολόγος Αιματολογικό Τμήμα Γ. Ν. Παπαγεωργίου Ακαδημία Αιμοδοσίας, Ιούνιος 2014 Μεταγγίσεις σε νεογνά και παιδιά Μεταγγίσεις στον νεογνικό πληθυσμό
Γράφει: Μιλτιάδης Μαρκάτος, Πνευμονολόγος
 Γράφει: Μιλτιάδης Μαρκάτος, Πνευμονολόγος Πάνω από ένα αιώνα πριν, ο J. Hutchinson, ένας χειρουργός-δερματολόγος, αναγνώρισε την πρώτη περίπτωση σαρκοείδωσης, στο Λονδίνο. Στα χρόνια πριν και μετά την
Γράφει: Μιλτιάδης Μαρκάτος, Πνευμονολόγος Πάνω από ένα αιώνα πριν, ο J. Hutchinson, ένας χειρουργός-δερματολόγος, αναγνώρισε την πρώτη περίπτωση σαρκοείδωσης, στο Λονδίνο. Στα χρόνια πριν και μετά την
Νεότερες παρεµβάσεις στην πρόληψη και θεραπεία του διαβητικού ποδιού
 Στρογγυλό τραπέζι Νεότερες παρεµβάσεις στην πρόληψη και θεραπεία του διαβητικού ποδιού Συντονιστής: Η. Ν. Μυγδάλης Β Παθολογική Κλινική και ιαβητολογικό Κέντρο, Γενικό Νοσοκοµείο ΝΙΜΤΣ, Αθήνα Οι διαταραχές
Στρογγυλό τραπέζι Νεότερες παρεµβάσεις στην πρόληψη και θεραπεία του διαβητικού ποδιού Συντονιστής: Η. Ν. Μυγδάλης Β Παθολογική Κλινική και ιαβητολογικό Κέντρο, Γενικό Νοσοκοµείο ΝΙΜΤΣ, Αθήνα Οι διαταραχές
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
Όταν χρειάζεται ρύθμιση της ποσότητας των χορηγούμενων υγρών του ασθενή. Όταν θέλουμε να προλάβουμε την υπερφόρτωση του κυκλοφορικού συστήματος
 Ερωτήσεις Αξιολόγησης Εργαστηριακού Μαθήματος Θέμα: «Κεντρική Φλεβική Πίεση» 1. Τι είναι η Κεντρική Φλεβική Πίεση (ΚΦΠ); Είναι η υδροστατική πίεση των μεγάλων φλεβών που είναι πλησιέστερα στην καρδιά,
Ερωτήσεις Αξιολόγησης Εργαστηριακού Μαθήματος Θέμα: «Κεντρική Φλεβική Πίεση» 1. Τι είναι η Κεντρική Φλεβική Πίεση (ΚΦΠ); Είναι η υδροστατική πίεση των μεγάλων φλεβών που είναι πλησιέστερα στην καρδιά,
Το συχνότερο χρόνιο νόσημα της παιδικής ηλικίας.
 ΤΟ ΠΑΙΔΙΚΟ ΑΣΘΜΑ Το συχνότερο χρόνιο νόσημα της παιδικής ηλικίας. Αν από το τρέξιμο, τη γυμναστική ή άλλη εργασία, δυσκολεύεται η αναπνοή, αυτό λέγεται άσθμα. Αρεταίος Καππαδόκης, 100 μχ Οι γυναίκες ήταν
ΤΟ ΠΑΙΔΙΚΟ ΑΣΘΜΑ Το συχνότερο χρόνιο νόσημα της παιδικής ηλικίας. Αν από το τρέξιμο, τη γυμναστική ή άλλη εργασία, δυσκολεύεται η αναπνοή, αυτό λέγεται άσθμα. Αρεταίος Καππαδόκης, 100 μχ Οι γυναίκες ήταν
Μήπως έχω Σκληρόδερµα;
 Μήπως έχω Σκληρόδερµα; Για να πληροφορηθώ µýëïò ôçò Σπάνιος ναι... Μόνος όχι Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών σπανίων παθήσεων
Μήπως έχω Σκληρόδερµα; Για να πληροφορηθώ µýëïò ôçò Σπάνιος ναι... Μόνος όχι Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών σπανίων παθήσεων
ΠΝΕΥΜΟΝΙΚΗ ΥΠΕΡΤΑΣΗ ΣΕ. Παρουσίαση περιστατικού. ΑΜΕΘ Γ.Ν.Θ. «Γ. Παπανικολάου»
 ΠΝΕΥΜΟΝΙΚΗ ΥΠΕΡΤΑΣΗ ΣΕ ARDS - ΑΝΤΙΜΕΤΩΠΙΣΗ ΜΕ ΝΟ Παρουσίαση περιστατικού ΑΜΕΘ Γ.Ν.Θ. «Γ. Παπανικολάου» Παρουσίαση περιστατικού Από τον απεικονιστικό έλεγχο διαπιστώθηκαν: κατάγµατα λεκάνης και δεξιού άνω
ΠΝΕΥΜΟΝΙΚΗ ΥΠΕΡΤΑΣΗ ΣΕ ARDS - ΑΝΤΙΜΕΤΩΠΙΣΗ ΜΕ ΝΟ Παρουσίαση περιστατικού ΑΜΕΘ Γ.Ν.Θ. «Γ. Παπανικολάου» Παρουσίαση περιστατικού Από τον απεικονιστικό έλεγχο διαπιστώθηκαν: κατάγµατα λεκάνης και δεξιού άνω
ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1(ΥΓΕΙΑ-ΑΝΘΡΩΠΟΣ)
 ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1(ΥΓΕΙΑ-ΑΝΘΡΩΠΟΣ) Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση ή στη φράση που συμπληρώνει σωστά την πρόταση: 1. Οι ιοί αποτελούνται
ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΤΜΗΜΑ: ΒΙΟΛΟΓΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΚΕΦΑΛΑΙΟ 1(ΥΓΕΙΑ-ΑΝΘΡΩΠΟΣ) Να βάλετε σε κύκλο το γράμμα που αντιστοιχεί στη σωστή απάντηση ή στη φράση που συμπληρώνει σωστά την πρόταση: 1. Οι ιοί αποτελούνται
Ορθολογική χρήση κοινών εργαστηριακών παραμέτρων στην παιδιατρική πράξη: ASTO
 Ορθολογική χρήση κοινών εργαστηριακών παραμέτρων στην παιδιατρική πράξη: ASTO Πολυξένη Πρατσίδου-Γκέρτση Πανεπιστημιακός Υπότροφος ΑΠΘ στην Παιδιατρική Ρευματολογία Α Παιδιατρική Κλινική ΑΠΘ Περίγραμμα
Ορθολογική χρήση κοινών εργαστηριακών παραμέτρων στην παιδιατρική πράξη: ASTO Πολυξένη Πρατσίδου-Γκέρτση Πανεπιστημιακός Υπότροφος ΑΠΘ στην Παιδιατρική Ρευματολογία Α Παιδιατρική Κλινική ΑΠΘ Περίγραμμα
OMA Α ΜΕΛΕΤΗΣ ΤΗΣ ΣΗΨΗΣ (HELLENIC SEPSIS STUDY GROUP)
 OMA Α ΜΕΛΕΤΗΣ ΤΗΣ ΣΗΨΗΣ (HELLENIC SEPSIS STUDY GROUP) ΕΛΛΗΝΙΚΗ ΟΜΑ Α ΓΙΑ ΤΗ 09-05-2006 ΜΕΛΕΤΗ ΤΗΣ ΣΗΨΗΣ Παθολογική, ΑΤΤΙΚΟΝ Β Προπ. Παθολογική, ΑΤΤΙΚΟΝ Β ΜΕΘ ΑΤΤΙΚΟΝ ΜΕΘ «Ευγενιδείο» ΜΕΘ «Μεταξά» ΜΕΘ «Κοργιαλένειο-Μπενάκειο»
OMA Α ΜΕΛΕΤΗΣ ΤΗΣ ΣΗΨΗΣ (HELLENIC SEPSIS STUDY GROUP) ΕΛΛΗΝΙΚΗ ΟΜΑ Α ΓΙΑ ΤΗ 09-05-2006 ΜΕΛΕΤΗ ΤΗΣ ΣΗΨΗΣ Παθολογική, ΑΤΤΙΚΟΝ Β Προπ. Παθολογική, ΑΤΤΙΚΟΝ Β ΜΕΘ ΑΤΤΙΚΟΝ ΜΕΘ «Ευγενιδείο» ΜΕΘ «Μεταξά» ΜΕΘ «Κοργιαλένειο-Μπενάκειο»
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών
 Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Διερεύνηση των μηχανισμών δυσλειτουργίας
Περιγραφή Χρηματοδοτούμενων Ερευνητικών Έργων 1η Προκήρυξη Ερευνητικών Έργων ΕΛ.ΙΔ.Ε.Κ. για την ενίσχυση Μεταδιδακτόρων Ερευνητών/Τριών Τίτλος Ερευνητικού Έργου «Διερεύνηση των μηχανισμών δυσλειτουργίας
Εισαγωγή στην Ανοσολογία
 Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
Κλινικές Εκδηλώσεις Ύποπτες για Πρωτοπαθή Ανοσοανεπάρκεια
 6ο Συμπόσιο Πρωτοπαθείς Ανοσοανεπάρκειες Παιδιατρική Ανοσολογία Κλινικές Εκδηλώσεις Ύποπτες για Πρωτοπαθή Ανοσοανεπάρκεια Αλεξάνδρα Σολδάτου Επίκουρη Καθηγήτρια Παιδιατρικής B Παιδιατρική Κλινική Ε.Κ.Π.Α.
6ο Συμπόσιο Πρωτοπαθείς Ανοσοανεπάρκειες Παιδιατρική Ανοσολογία Κλινικές Εκδηλώσεις Ύποπτες για Πρωτοπαθή Ανοσοανεπάρκεια Αλεξάνδρα Σολδάτου Επίκουρη Καθηγήτρια Παιδιατρικής B Παιδιατρική Κλινική Ε.Κ.Π.Α.
ΑΝΟΣΟΛΟΓΙΑ ΘΕΩΡΙΑ 1 Ο ΜΑΘΗΜΑ
 ΑΝΟΣΟΛΟΓΙΑ ΘΕΩΡΙΑ 1 Ο ΜΑΘΗΜΑ ΑΝΟΣΙΑ Η ανοσία (α- στερητικό + νόσος) είναι η ικανότητα ενός οργανισμού να αμύνεται ενάντια σε κάποιον εξωτερικό βλαπτικό παράγοντα και να μην υφίσταται τις συνέπειές του.
ΑΝΟΣΟΛΟΓΙΑ ΘΕΩΡΙΑ 1 Ο ΜΑΘΗΜΑ ΑΝΟΣΙΑ Η ανοσία (α- στερητικό + νόσος) είναι η ικανότητα ενός οργανισμού να αμύνεται ενάντια σε κάποιον εξωτερικό βλαπτικό παράγοντα και να μην υφίσταται τις συνέπειές του.
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ 1 ο ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ
 ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ 1 ο ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο Α. Ερωτήσεις πολλαπλής επιλογής 1. γ 2. α 3. β 4. δ 5. δ Β. Ερωτήσεις σωστού - λάθους 1. Σωστό 2. Λάθος 3. Λάθος 4. Λάθος 5. Σωστό ΘΕΜΑ
ΑΠΑΝΤΗΣΕΙΣ ΣΤΟ 1 ο ΔΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ ΘΕΜΑ 1 ο Α. Ερωτήσεις πολλαπλής επιλογής 1. γ 2. α 3. β 4. δ 5. δ Β. Ερωτήσεις σωστού - λάθους 1. Σωστό 2. Λάθος 3. Λάθος 4. Λάθος 5. Σωστό ΘΕΜΑ
Συσχέτιση Περιοδοντικών Λοιμώξεων με Συστηματικά Νοσήματα
 Συσχέτιση Περιοδοντικών Λοιμώξεων με Συστηματικά Νοσήματα Πέτρος Δ. Δαμουλής, D.M.D., D.M.Sc. Περιοδοντολόγος Επισκέπτης Καθηγητής Πανεπιστημίου Tufts, ΗΠΑ Η Περιοδοντική Νόσος είναι μία Λοίμωξη που προκαλείται
Συσχέτιση Περιοδοντικών Λοιμώξεων με Συστηματικά Νοσήματα Πέτρος Δ. Δαμουλής, D.M.D., D.M.Sc. Περιοδοντολόγος Επισκέπτης Καθηγητής Πανεπιστημίου Tufts, ΗΠΑ Η Περιοδοντική Νόσος είναι μία Λοίμωξη που προκαλείται
ΜΕΣΗ ΩΤΙΤΙΣ ΤΙ ΕΙΝΑΙ Η ΜΕΣΗ ΩΤΙΤΙΣ
 ΜΕΣΗ ΩΤΙΤΙΣ Η συχνότερη αιτία επίσκεψης των παιδιών στον ιατρό είναι η μέση ωτίτις. Περίπου το 1/3 των παιδιών ηλικίας από 1-5 ετών, παρουσιάζουν παραπάνω από τρεις προσβολές μέσης ωτίτιδας το χρόνο. Αποτελεί
ΜΕΣΗ ΩΤΙΤΙΣ Η συχνότερη αιτία επίσκεψης των παιδιών στον ιατρό είναι η μέση ωτίτις. Περίπου το 1/3 των παιδιών ηλικίας από 1-5 ετών, παρουσιάζουν παραπάνω από τρεις προσβολές μέσης ωτίτιδας το χρόνο. Αποτελεί
Σάββατο 15/11/2014, ώρα 14.30 15.30
 Σάββατο 15/11/2014, ώρα 14.30 15.30 ΝΟΣΗΛΕΙΑ ΑΣΘΕΝΩΝ ΜΕ ΠΝΕΥΜΟΝΙΑ ΣΧΕΤΙΖΌΜΕΝΗ ΜΕ ΑΝΑΠΝΕΥΣΤΗΡΑ ΣΕ ΜΕΘ. ΕΠΙΔΡΑΣΗ ΠΑΡΑΓΟΝΤΩΝ ΣΧΕΤΙΖΟΜΕΝΩΝ ΜΕ ΤΗΝ ΤΟΠΟΘΕΤΗΣΗ ΚΕΝΤΡΙΚΟΥ ΦΛΕΒΙΚΟΥ ΚΑΘΕΤΗΡΑ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΛΟΙΜΩΞΗΣ
Σάββατο 15/11/2014, ώρα 14.30 15.30 ΝΟΣΗΛΕΙΑ ΑΣΘΕΝΩΝ ΜΕ ΠΝΕΥΜΟΝΙΑ ΣΧΕΤΙΖΌΜΕΝΗ ΜΕ ΑΝΑΠΝΕΥΣΤΗΡΑ ΣΕ ΜΕΘ. ΕΠΙΔΡΑΣΗ ΠΑΡΑΓΟΝΤΩΝ ΣΧΕΤΙΖΟΜΕΝΩΝ ΜΕ ΤΗΝ ΤΟΠΟΘΕΤΗΣΗ ΚΕΝΤΡΙΚΟΥ ΦΛΕΒΙΚΟΥ ΚΑΘΕΤΗΡΑ ΣΤΗΝ ΑΝΑΠΤΥΞΗ ΛΟΙΜΩΞΗΣ
Γνωριμία με τα αυτοάνοσα ρευματικά νοσήματα
 Γνωριμία με τα αυτοάνοσα ρευματικά νοσήματα Αντώνης Φανουριάκης Μονάδα Ρευματολογίας και Κλινικής Ανοσολογίας Δ Πανεπιστημιακή Παθολογική Κλινική Πανεπιστημιακό Γενικό Νοσοκομείο «Αττικόν» Αθήνα, 01/02/2016
Γνωριμία με τα αυτοάνοσα ρευματικά νοσήματα Αντώνης Φανουριάκης Μονάδα Ρευματολογίας και Κλινικής Ανοσολογίας Δ Πανεπιστημιακή Παθολογική Κλινική Πανεπιστημιακό Γενικό Νοσοκομείο «Αττικόν» Αθήνα, 01/02/2016
Σαλπιγκτής Ιωάννης Ειδικός Παθολόγος Επιμελητής Κλινική SOS Ιατρών ΕΥΡΩΚΛΙΝΙΚΗ ΑΘΗΝΩΝ
 Σαλπιγκτής Ιωάννης Ειδικός Παθολόγος Επιμελητής Κλινική SOS Ιατρών ΕΥΡΩΚΛΙΝΙΚΗ ΑΘΗΝΩΝ CRP (C- reactive protein) Προκαλσιτονίνη (PCT) Αντιθρομβίνη ΙΙΙ Κυτταροκίνες Η CRP είναι πρωτεΐνη (β-σφαιρίνη) που
Σαλπιγκτής Ιωάννης Ειδικός Παθολόγος Επιμελητής Κλινική SOS Ιατρών ΕΥΡΩΚΛΙΝΙΚΗ ΑΘΗΝΩΝ CRP (C- reactive protein) Προκαλσιτονίνη (PCT) Αντιθρομβίνη ΙΙΙ Κυτταροκίνες Η CRP είναι πρωτεΐνη (β-σφαιρίνη) που
Γράφει: Ελένη Αναστασίου, Υπεύθυνη Διαβητολογικού Κέντρου Κύησης του Α' Ενδοκρινολογικού Τμήματος» του Νοσοκομείου «Αλεξάνδρα»
 Γράφει: Ελένη Αναστασίου, Υπεύθυνη Διαβητολογικού Κέντρου Κύησης του Α' Ενδοκρινολογικού Τμήματος» του Νοσοκομείου «Αλεξάνδρα» Παρακάτω θα αναφερθούμε χωριστά στις επιπτώσεις και την αντιμετώπιση (α) του
Γράφει: Ελένη Αναστασίου, Υπεύθυνη Διαβητολογικού Κέντρου Κύησης του Α' Ενδοκρινολογικού Τμήματος» του Νοσοκομείου «Αλεξάνδρα» Παρακάτω θα αναφερθούμε χωριστά στις επιπτώσεις και την αντιμετώπιση (α) του
ΣΥΝΔΡΟΜΟ ΕΠΙΚΤΗΤΗΣ ΑΝΟΣΟΒΙΟΛΟΓΙΚΗΣ ΑΝΕΠΑΡΚΕΙΑΣ (AIDS)
 ΣΥΝΔΡΟΜΟ ΕΠΙΚΤΗΤΗΣ ΑΝΟΣΟΒΙΟΛΟΓΙΚΗΣ ΑΝΕΠΑΡΚΕΙΑΣ (AIDS) Στα τέλη της δεκαετίας του 1970 εμφανίστηκε μία από τις σοβαρότερες ασθένειες ανεπάρκειας του ανοσοβιολογικού συστήματος Ανοσοβιολογική ανεπάρκεια
ΣΥΝΔΡΟΜΟ ΕΠΙΚΤΗΤΗΣ ΑΝΟΣΟΒΙΟΛΟΓΙΚΗΣ ΑΝΕΠΑΡΚΕΙΑΣ (AIDS) Στα τέλη της δεκαετίας του 1970 εμφανίστηκε μία από τις σοβαρότερες ασθένειες ανεπάρκειας του ανοσοβιολογικού συστήματος Ανοσοβιολογική ανεπάρκεια
