Σύνθεση Βιοαποκοδομήσιμων Νανοσωματιδίων για μεταφορά φαρμάκων
|
|
|
- ῾Ερμιόνη Καλλιγάς
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ Εργαστήριο Λεπτών Υμενίων - Νανοσυστημάτων & Νανομετρολογίας (LTFN) Διατμηματικό Πρόγραμμα Μεταπτυχιακών Σπουδών Νανοεπιστήμες & Νανοτεχνολογίες Σύνθεση Βιοαποκοδομήσιμων Νανοσωματιδίων για μεταφορά φαρμάκων Ρεπανάς Αλέξανδρος Φαρμακοποιός Επιβλέπων Καθηγητής: Στέργιος Λογοθετίδης Θεσσαλονίκη, Μάρτιος 2013
2 Ε Υ Χ Α Ρ Ι Σ Τ Ι Ε Σ Η συγκεκριμένη Διπλωματική Εργασία εκπονήθηκε στο Εργαστήριο Λεπτών Υμενίων-Νανοσυστημάτων & Νανομετρολογίας (LTFN) του τμήματος Φυσικής του Αριστοτελείου Πανεπιστημίου Θεσσαλονίκης σε συνεργασία με τον Τομέα Φαρμακευτικής Τεχνολογίας του τμήματος Φαρμακευτικής του Αριστοτελείου Πανεπιστημίου Θεσσαλονίκης. Η πρώτη μου επαφή με το Διατμηματικό Μεταπτυχιακό Πρόγραμμα σπουδών με θέμα «Νανοεπιστήμες & Νανοτεχνολογίες» συνέβη κατά τη διάρκεια της Διεθνούς Έκθεσης Θεσσαλονίκης το Σεπτέμβριο του 2010, όπου τυχαία βρέθηκα στο περίπτερο που φιλοξενούσε τα εκθέματα του Εργαστηρίου Λεπτών Υμενίων Νανοσυστημάτων & Νανομετρολογίας (LTFN). Οι δραστηριότητες του προγράμματος μου κινητοποίησαν το ενδιαφέρον μιας και είχα μόλις πάρει το πτυχίο μου από το τμήμα Φαρμακευτικής (Ιούλιος 2010) και έψαχνα για κάποιο μεταπτυχιακό πρόγραμμα ώστε να συνεχίσω τις σπουδές μου. Η έννοια της Νανοτεχνολογίας καθώς και η εφαρμογή των τεχνικών και μεθόδων που βασίζονται σε αυτή δε μου ήταν άγνωστες καθώς σε θεωρητικό επίπεδο είχα διαβάσει ήδη αρκετά, ειδικά πάνω στον τομέα της ανάπτυξης νέων συστημάτων μεταφοράς φαρμάκων και της μηχανικής ιστών. Αυτό που δεν γνώριζα ήταν η πρακτική εφαρμογή αυτών των αρχών καθώς και η λειτουργία των διατάξεων που χρησιμοποιούνται σε εφαρμογές Νανοτεχνολογίας καθώς οι περισσότερες δεν ήταν διαθέσιμες στο τμήμα Φαρμακευτικής του Αριστοτελείου Πανεπιστημίου Θεσσαλονίκης. Για μένα βεβαίως η απόφαση να συνεχίσω της σπουδές μου πρώτα σε μεταπτυχιακό επίπεδο και ύστερα σε διδακτορικό και μετά-διδακτορικό επίπεδο ήταν ειλημμένη αρκετά χρόνια πίσω. Ήδη από την άνοιξη του 2008 είχα ξεκινήσει τα πρώτα μου βήματα στον ερευνητικό κόσμο μέσω του τομέα Φαρμακευτικής Χημείας του τμήματος Φαρμακευτικής του Αριστοτελείου Πανεπιστημίου Θεσσαλονίκης, όντας επιστημονικός συνεργάτης της Καθηγήτριας κ. Χατζηπαύλου-Λίτινα Δήμητρας και μέλος της εργαστηριακής της ομάδας. Σε αυτό το σημείο θα ήθελα να ευχαριστήσω ιδιαίτερα την κ. Χατζηπαύλου, για την ευκαιρία που μου έδωσε τότε αλλά και την εμπιστοσύνη που μου έδειξε καθ' όλη τη διάρκεια της συνεργασίας μας, που συνεχίζει να υφίσταται ακόμη και σήμερα, έχοντας δώσει καρπούς σε επίπεδο επιστημονικών ανακοινώσεων σε αριθμό συνεδρίων αλλά και πολύ πρόσφατα και σε μια δημοσίευση μιας ανασκόπησης στον τομέα της Ιατρικής/Φαρμακευτικής Χημείας σε έγκυρο επιστημονικό περιοδικό. Εκτός από αυτό θα ήθελα να την ευχαριστήσω ακόμα, για 2
3 την παρότρυνσή της να ακολουθήσω το Διατμηματικό Πρόγραμμα Μεταπτυχιακών Σπουδών (Ν&Ν) που θα ήθελα να τονίσω πως ήταν καταλυτική στην απόφαση μου. Τέλος θα ήθελα να την ευχαριστήσω για όλη την ψυχολογική και υλική υποστήριξη και καθοδήγηση που μου παρείχε όχι μόνο κατά τη διάρκεια του Μεταπτυχιακού αλλά και πιο πριν, και να τονίσω πως πάντα τη θεωρούσα και τη θεωρώ την Επιστημονική μου Μητέρα εάν ένας τέτοιος όρος μπορεί να θεωρηθεί δόκιμος. Θα ήθελα επίσης να ευχαριστήσω τα μέλη της τριμελούς εξεταστικής επιτροπής, τον καθηγητή κ. Λογοθετίδη Στέργιο, την Επίκουρη Καθηγήτρια κ. Γιώτη Μαρία και τη Μεταδιδακτορική Ερευνήτρια κ. Καραγκιοζάκη Βαρβάρα, που συνέβαλλαν στην εκπόνηση αυτού του εγχειρήματος. Όσον αφορά το σκέλος της διπλωματικής εργασίας, αρχικά θα ήθελα να ευχαριστήσω τον τότε επί πτυχίο φοιτητή Βαβουλίδη Ελευθέριο, ο οποίος ήταν αυτός που με εισήγαγε και μου έδειξε διάφορες τεχνικές που χρησιμοποιούνται στο εργαστήριο του LTFN και μου παρείχε σημαντικές συμβουλές κατά τη διάρκεια των σπουδών μου από την οπτική του φοιτητή. Από το διδακτικό και ερευνητικό προσωπικό θα ήθελα να ευχαριστήσω ιδιαίτερα την μεταδιδακτορική ερευνήτρια Παρασκευή Καβατζικίδου για την καθοδήγηση και τη βοήθεια που μου παρείχε κατά τη συνολική διάρκεια των σπουδών μου καθώς και τη βοήθεια που μου παρείχε όταν χρειάστηκε κατά την εκπόνηση της διπλωματικής μου. Στη συνέχεια θα ήθελα να ευχαριστήσω τους μεταδιδακτορικούς ερευνητές Λασκαράκη Αργύρη και Κασσαβέτη Σπύρο. Ήταν δυο ακόμα άτομα που με ώθησαν μέσω των διαλέξεων τους και της δουλειάς τους στο εργαστήριο να επεκτείνω το πεδίο των γνώσεων πέραν του κλασσικού Βιολογικού προσανατολισμού, κάτι που με βοήθησε πολύ. Τέλος θα ήθελα να ευχαριστήσω θερμά τον υποψήφιο διδάκτορα Καραγιαννίδη Παναγιώτη για τη θεωρητική και πρακτική βοήθεια που παρείχε στην κατανόηση των αρχών λειτουργίας του Μικροσκοπίου Ατομικών Δυνάμεων (AFM) καθώς και στην εκτέλεση μετρήσεων, και επεξεργασία εικόνων στο AFM για την εκπόνηση της διπλωματικής μου εργασίας. Από τον τομέα Φυσικής στερεάς κατάστασης θα ήθελα να ευχαριστήσω την Επίκουρη Καθηγήτρια κ. Παυλίδου Ελένη για τη συμβολή της στις μετρήσεις Σαρωτικής Μικροσκοπίας Ηλεκτρονίων (SEM) για την εκπόνηση της διπλωματικής μου εργασίας. Ακόμη θα ήθελα να ευχαριστήσω και όλα τα μέλη του Εργαστηρίου LTFN για την άψογη συνεργασία μας καθώς και για το θερμό κλίμα που υπήρχε ώστε η ερευνητική εργασία να γίνεται σε ευχάριστο και ήσυχο περιβάλλον. 3
4 Από τον τομέα Γενετικής, Εξέλιξης και Μοριακής Βιολογίας του τμήματος Βιολογίας του Αριστοτελείου Πανεπιστημίου Θεσσαλονίκης θα ήθελα να ευχαριστήσω ιδιαίτερα τον Λέκτορα κ. Καππά Ηλία για την υποστήριξη και καθοδήγησή του προς το πρόσωπό μου. Ακόμα θα ήθελα να ευχαριστήσω τον Καθηγητή κ. Αρσενάκη Μηνά για την προσφορά του στο να βοηθήσει στην εκπόνηση της διπλωματικής μου εργασίας στο κομμάτι του διαχωρισμού των Νανοσωματιδίων. Από τον τομέα Φαρμακευτικής Τεχνολογίας του τμήματος Φαρμακευτικής θα ήθελα να εκφράσω τις ιδιαίτερες ευχαριστίες μου στον Επίκουρο Καθηγητή, κ. Φατούρο Δημήτριο. Ο κύριος Φατούρος διετέλεσε βασικός παράγοντας και κινητήριος μοχλός του συνολικού εγχειρήματος της εκπόνησης της διπλωματικής μου εργασίας μιας και όχι μόνο παρείχε όλο τον εξοπλισμό του εργαστηρίου του καθώς και κάποια αναλώσιμα πέραν των πιο βασικών που προήλθαν από το LTFN, αλλά επίσης συνετέλεσε βασικός παράγοντας στη χάραξη της στρατηγικής εκπόνησης της διπλωματικής εργασίας, του πλάνου εφαρμογής της, και της εκμάθησης από εμένα διατάξεων και μεθόδων απαραίτητων για την εκπόνηση της διπλωματικής εργασίας. Επιπρόσθετα θα ήθελα να τον ευχαριστήσω τόσο για την ψυχολογική όσο και την υλική υποστήριξή του, για την καθοδήγησή του και την συμβολή του στην εξήγηση των αποτελεσμάτων. Τέλος θα ήθελα να τον ευχαριστήσω για την άψογη συνεργασία που είχαμε καθ' όλη τη διάρκεια της εκπόνησης της διπλωματικής εργασίας, παρά το πολύ επιβαρυμένο πρόγραμμά του και για τη συνολική συμβολή του. Σε αυτό το σημείο θα ήθελα να ευχαριστήσω ιδιαίτερα τη μεταδιδακτορική ερευνήτρια, Ιατρό-Καρδιολόγο, κ. Καραγκιοζάκη Βαρβάρα. Η κ. Καραγκιοζάκη αποτέλεσε την προσωπική μου Σύμβουλο (Project Advisor), συνδετικό κρίκο όλων των παραπάνω μελών, οργανώνοντας ουσιαστικά και καθοδηγώντας με ασφαλώς στην επίτευξη της εκπόνησης αυτής της διπλωματικής εργασίας. Θεωρώ ότι η συμβολή της όχι μόνο στη διπλωματική εργασία αυτή καθ αυτή αλλά και στην εξέλιξή μου στα πλαίσια του μεταπτυχιακού προγράμματος σπουδών ήταν καταλυτική. Την ευχαριστώ ιδιαίτερα για τη καθοδήγηση και τη βοήθεια που προσέφερε σε κρίσιμες στιγμές για την εκπόνηση της εργασίας καθώς και για τον οργανωτικό της ρόλο αλλά και την άψογη συνεργασία και συνεννόηση που είχαμε, αλλά και την προσωπική της συμβολή στη διευθέτηση θεμάτων, στον κατάλληλο χρόνο. Θα ήθελα ακόμα να την ευχαριστήσω για την άψογη και φιλική αντιμετώπισή της προς το πρόσωπό μου και για τα ερεθίσματα που μετέδωσε μέσω των διαλέξεών της στα πλαίσια του μαθήματος του 2 ου εξαμήνου Εμβιομηχανική που με οδήγησαν στο να στραφώ στο εργαστήριο του LTFN και στον κ. Λογοθετίδη για την ανάθεση θέματος διπλωματικής εργασίας. 4
5 Τέλος, θα ήθελα να εκφράσω τις θερμές μου ευχαριστίες στον Καθηγητή του τμήματος Φυσικής, Διευθυντή του εργαστηρίου LTFN, Διευθυντή του Διατμηματικού Προγράμματος Μεταπτυχιακών Σπουδών Νανοεπιστήμες & Νανοτεχνολογίες, και επιβλέποντα Καθηγητή μου κ. Λογοθετίδη Στέργιο για την εμπιστοσύνη που μου έδειξε για την ανάθεση του θέματος και την πολύτιμη συμβολή του στην καθοδήγηση μου τόσο σε επίπεδο των διαλέξεων που παρέδωσε κατά τη διάρκεια των μαθημάτων όσο και σε επίπεδο διπλωματικής εργασίας. Η συμβουλευτική του παρέμβαση αλλά και η προσέγγισή του όχι μόνο ερευνητικά αλλά και σε επίπεδο διαχείρισης της έρευνας και γεφύρωσης της έρευνας στο εργαστήριο με την εφαρμογή στη βιομηχανία/αγορά μπορώ μετά βεβαιότητας να πω ότι υπήρξαν μεγάλο σχολείο για μένα και με βοήθησαν ιδιαίτερα στο να ανεβάσω το επίπεδο του τρόπου σκέψης μου και της δουλειάς μου ώστε να αντεπεξέλθω στις απαιτήσεις του προγράμματος. Κατανοώ τώρα ότι αυτό είναι κάτι που θα με βοηθήσει ιδιαίτερα μακροπρόθεσμα τόσο στην ύπαρξη μου στον ακαδημαϊκό χώρο όσο και στην ευρύτερη επιστημονική κοινότητα και τον ευχαριστώ ιδιαίτερα γι αυτό. Η δουλειά του και το έργο του όχι μόνο όσον αφορά το N&Ν αλλά και γενικότερα έπαιξε επίσης πολύ σημαντικό έργο στο να επιλέξω αυτό το πρόγραμμα εξ αρχής και εύχομαι και ελπίζω ότι παρά τις οικονομικές δυσκολίες που αντιμετωπίζει γενικότερα η Ελληνική κοινωνία και ειδικότερα το Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης να συνεχίσει αυτό το έργο και να επεκτείνεται όλο και περισσότερο. Το ελληνικό Πανεπιστήμιο έχει ανάγκη τέτοιες προσπάθειες πολύ περισσότερο στην σημερινή δυσχερή συγκυρία. Κλείνοντας το κομμάτι των Ευχαριστιών θα ήθελα να εκφράσω την αγάπη μου προς την οικογένειά μου για την ψυχολογική και οικονομική στήριξη που μου παρείχαν καθ όλη τη διάρκεια της ζωής μου και πιο συγκεκριμένα των σπουδών μου, καθώς και προς τους στενούς μου φίλους που υπήρξαν συνοδοιπόροι της ζωής μου και κατά τη διάρκεια των σπουδών μου. 5
6 Π Ε Ρ Ι Ε Χ Ο Μ Ε Ν Α Περιεχόμενα.6 Περίληψη ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Α. ΚΕΦΑΛΑΙΟ 1. Νανοτεχνολογία και Εφαρμογές στην Ιατρική Νανοτεχνολογία και Νανοεπιστήμη στην Ιατρική Τα νανοσωματίδια ως βασική ιδέα για συστήματα μεταφοράς φαρμάκων Συνθετικοί πολυμερικοί φορείς Νανοτεχνολογία βασισμένη στο PLGA Κριτήρια επιλογής PLGA Καρδιαγγειακές Παθήσεις Μοριακοί και κυτταρικοί μηχανισμοί των αγγειακών ασθενειών Νανοσωματίδια και αγγειακές παθήσεις Εφαρμογές και προκλήσεις στις αγγειακές παθήσεις Άλλες εφαρμογές των Νανοσωματιδίων από PLGA ΚΕΦΑΛΑΙΟ 2. Τεχνικές Σύνθεσης Νανοσωματιδίων Nanoprecipitation Εισαγωγή Γενική Περιγραφή της Μεθόδου Ιστορία της τεχνικής Θεωρητικό υπόβαθρο, το φαινόμενο ούζο, και παράμετροι επεξεργασίας Πλεονεκτήματα και περιορισμοί της τεχνικής του nanoprecipitation
7 Σωματίδια PLA, PLGA και PCL Σύνοψη της τεχνικής του Nanoprecipitation...42 ΚΕΦΑΛΑΙΟ 3. Τεχνική Μέτρησης Μεγέθους και ζ-δυναμικού Νανοσωματιδίων ζ-δυναμικό Ηλεκτροφόρηση Υπολογισμός του δυναμικού ζήτα Nano Zetasizer Λειτουργία Μετρήσεις Μεγέθους και ζ-δυναμικού Δυναμική Σκέδαση Φωτός(DLS)...49 ΚΕΦΑΛΑΙΟ 4. Τεχνικές Απεικόνισης Μικροσκοπία Σάρωσης Ηλεκτρονίων (SEM) Αρχές λειτουργίας και δυνατότητες Διαδικασία σάρωσης και σχηματισμός εικόνας Βιολογικά δείγματα Ανίχνευση δευτερογενών ηλεκτρονίων Ανίχνευση των οπισθοσκεδαζόμενων ηλεκτρονίων Ανάλυση του SEM Μικροσκοπία Ατομικών Δυνάμεων (AFM) Βασικές αρχές Τρόποι απεικόνισης Contact mode Non-Contact Mode Tapping Mode Βιολογικές εφαρμογές
8 Υψηλής ευκρίνειας απεικόνιση βιολογικών δειγμάτων Πλεονεκτήματα και μειονεκτήματα...61 ΚΕΦΑΛΑΙΟ 5. Άλλες τεχνικές Φασματοσκοπία Υπεριώδους-Ορατού Αρχή της απορρόφησης υπεριώδους-ορατού Εφαρμογές Νόμος Beer-Lambert Φασματοφωτόμετρο Υπεριώδους-ορατού Διάγραμμα μονής δέσμης UV / Vis φασματοφωτομέτρου Θολερότητα και πειράματα θολερότητας Spincoating Αρχή Λειτουργίας Εφαρμογές της τεχνικής...69 ΚΕΦΑΛΑΙΟ 6. Κινητική Μελέτη Απελευθέρωσης Κινητική Απελευθέρωσης Φαρμάκων, Μοντέλα και Θεωρίες Βασικές αρχές της κινητικής της αποδέσμευσης φαρμάκου Noyes-Whitney Θεωρία Φιλμ Nernst & Brunner Μοντελοποίηση κινητικής απελευθέρωσης Μοντέλα εξαρτώμενα από τις μεθόδους που ακολουθούνται Μοντέλο μηδενικής τάξης Μοντέλα κινητικής πρώτης τάξης Μοντέλο Higuchi Μοντέλο Korsmeyer-Πέππας...75 ΚΕΦΑΛΑΙΟ 7. Αντιδραστήρια και Φάρμακο που χρησιμοποιούνται Διπυριδαμόλη
9 Μηχανισμός δράσης και φαρμακευτικά αποτελέσματα Ιατρικές χρήσεις Υπερβολική δόση Bovine serum albumin (BSA), αλβουμίνη από βοοειδή Ιδιότητες Εφαρμογές Πολυαιθυλενογλυκόλη (PEG) Ιδιότητες Ιατρικές χρήσεις Νέες κλινικές χρήσεις Βιολογικές χρήσεις Phosphate buffered saline (PBS) Εφαρμογές Προετοιμασία...83 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Β. ΚΕΦΑΛΑΙΟ 8. Σύνθεση και διαχωρισμός Νανοσωματιδίων Υλικά που χρησιμοποιήθηκαν για τη σύνθεση και μελέτη των Νανοσωματιδίων Πειραματική διαδικασία για τον σχηματισμό των Νανοσωματιδίων Πειραματική διαδικασία για το διαχωρισμό των Νανοσωματιδίων Συμπεράσματα...91 ΚΕΦΑΛΑΙΟ 9. Μετρήσεις μεγέθους και ζ-δυναμικού των Νανοσωματιδίων Μετρήσεις μεγέθους Μετρήσεις ζ-δυναμικού
10 9.3. Μετρήσεις μετά την επεξεργασία με PEG και Αλβουμίνη Συμπεράσματα ΚΕΦΑΛΑΙΟ 10. Χρήση Φασματοσκοπίας UV-Vis για μελέτες σταθερότητας και θολερότητας Νανοσωματιδίων Πειράματα Σταθερότητας και θολερότητας Πειράματα Σταθερότητας συναρτήσει του χρόνου Πειράματα Θολερότητας συναρτήσει του χρόνου Συμπεράσματα ΚΕΦΑΛΑΙΟ 11. Χρήση Φασματοσκοπίας UV-Vis για μελέτες εγκλωβισμού Φαρμάκου από τα πολυμερικά Νανοσωματίδια Καμπύλες Αναφοράς διπυριδαμόλης Επιλογή Χλωροφορμίου ως διαλύτη Πειραματική διαδικασία Συμπεράσματα ΚΕΦΑΛΑΙΟ 12. Χρήση Φασματοσκοπίας UV-Vis για μελέτες απελευθέρωσης Φαρμάκου από τα πολυμερικά Νανοσωματίδια Καμπύλες Αναφοράς διπυριδαμόλης Πειραματική διαδικασία Γραφικές παραστάσεις συναρτήσει του χρόνου Αποσαφήνιση κινητικού μοντέλου κατά την απελευθέρωση Συμπεράσματα ΚΕΦΑΛΑΙΟ 13. Χρήση της Μικροσκοπίας Σάρωσης Ηλεκτρονίων Προετοιμασία δείγματος Εικόνες από SEM Συμπεράσματα ΚΕΦΑΛΑΙΟ 14. Χρήση της Μικροσκοπίας Ατομικών Δυνάμεων Προετοιμασία δείγματος
11 14.2. Περιγραφή και ανάλυση εικόνων Συμπεράσματα ΚΕΦΑΛΑΙΟ 15. Γενικά συμπεράσματα - Προτάσεις για μελλοντική έρευνα Γενικά Συμπεράσματα Προτάσεις για μελλοντική έρευνα ΥΠΟΜΝΗΜΑ ΒΙΒΛΙΟΓΡΑΦΙΑ Δημοσιεύσεις και ανακοινώσεις σχετικές με την εργασία
12 ΠΕΡΙΛΗΨΗ Τελευταία, ποικιλία πολυμερών έχουν χρησιμοποιηθεί στον τομέα της Νανοϊατρικής, και της φαρμακευτικής βιομηχανίας. Μερικά βιοαποικοδομήσιμα πολυμερή είναι σε θέση να σχηματίσουν νανοσωματίδια που μπορεί να μπορεί να μεταφέρουν διάφορα φάρμακα, και ως εκ τούτου, μπορούν να χρησιμοποιηθούν ως φορείς ή συστήματα χορήγησης φαρμάκων. Ενδιαφέρον παρουσιάζουν τα πολυμερικά νανοσωματίδια που βαθμιαία αποικοδομούνται εντός του οργανισμού απελευθερώνοντας συγκεκριμένη ποσότητα του φαρμάκου με ελεγχόμενο τρόπο και έτσι μπορούν να χρησιμοποιηθούν σε καρδιαγγειακές εφαρμογές, σε stents και σε ιατρικά εμφυτεύματα, προκειμένου να αναστείλουν την θρόμβωση και να αποκαταστήσει τη φυσική επούλωση των ιστών γρηγορότερα, ελαχιστοποιώντας πιθανές επιβλαβείς αντιδράσεις, όπως είναι η φλεγμονή, η οποία προκαλείται από το ανοσοποιητικό σύστημα. Χρησιμοποιήθηκε μια πειραματική διαδικασία για να συντεθούν βιοαποικοδομήσιμα πολυμερικά νανοσωματίδια φορτωμένα με Διπυριδαμόλη, με την τεχνική του nanopercipitation. Πιο συγκεκριμένα, χρησιμοποιούνται πολύ-(dl-γαλακτικό-συν-γλυκολίκό οξύ PLGA) με διαφορετικές αναλογίες γαλακτικού/γλυκολικού (65:35 και 75:25) τα οποία είναι επικαλυμμένα με πολυαιθυλενογλυκόλη (PEG) και αλβουμίνη βόειου ορού (BSA), για το σχηματισμό νανοσωματιδίων σε ένα διάλυμα τα οποία στη συνέχεια διαχωρίζονται από το ελεύθερο φάρμακο με επανειλημμένες διαδικασίες φυγοκέντρισης. Μετρώνται οι τιμές του ζ- δυναμικού και το μέσο μέγεθος των νανοσωματιδίων. Τα μορφολογικά χαρακτηριστικά των νανοσωματιδίων μελετώνται μέσω της Ηλεκτρονικής Μικροσκοπίας Σάρωσης (SEM) και της Μικροσκοπία Ατομικών Δυνάμεων (AFM). Το μέσο μέγεθος και οι τιμές ζ-δυναμικού των νανοσωματιδίων σχετίζονται με την ύπαρξη του φαρμάκου. Πειράματα σταθερότητας και θολερότητας έδειξαν ότι οι διασπορές των νανοσωματιδίων είναι σταθερά συναρτήσει του χρόνου, αποφεύγοντας τον σχηματισμό συσσωματωμάτων. Τα πειράματα απελευθέρωσης φαρμάκου αποκάλυψαν ένα διφασικό κινητικό μοντέλο συναρτήσει του χρόνου παρατήρησης. Οι εικόνες από το SEM και το AFM επαληθεύουν τα αποτελέσματα από το Zetasizer. Τέλος, η επιλογή ενός από τους τύπους του πολυμερούς (65:35 ή 75:25) δεν είναι σημαντικός παράγοντας. 12
13 13 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Α.
14 ΚΕΦΑΛΑΙΟ 1. Νανοτεχνολογία και Εφαρμογές στην Ιατρική Νανοτεχνολογία και Νανοεπιστήμη στην Ιατρική Η Νανοτεχνολογία ή Νανοεπιστήμη, είναι ένα διεπιστημονικό πεδίο όπου οι θετικές και βιολογικές επιστήμες και η τεχνολογία συναντώνται με σκοπό τη δημιουργία, την κατανόηση και τη χρήση ατομικών και μοριακών δομών ( nm) και την κατασκευή συσκευών ή υλικών που εντάσσονται στο εύρος της νανοκλίμακας [1]. Η Νανοτεχνολογία εφαρμόζει τις αργές της μηχανικής, της ηλεκτρονικής, της φυσικής και της επιστήμης υλικών για να δημιουργήσει και να χειριστεί δομές σε μοριακό ή μm επίπεδο [2]. Έχει ήδη επηρεάσει και προωθήσει την ανάπτυξη πρότυπων προϊόντων στην βιομηχανία. Πολλά υλικά που χαρακτηρίζονται από τη νανοδομή τους, όπως τα νανοσωματίδια (NPs), οι νανοαισθητήρες, οι νανο-ίνες, νανοκαλώδια κ.α. έχουν αναπτυχθεί και μελετούνται εκτενώς. Αυτά τα υλικά είναι συνήθως τρισδιάστατα, και μικρότερα των 100 nm. Παρόλα αυτά, πολλά σημαντικά νάνο-υλικά έχουν μία ή περισσότερες διαστάσεις που ξεπερνούν τα 100nm, όπως για παράδειγμα οι νανοσωλήνες που έχουν συνήθως μήκος μεγαλύτερο από 500nm όταν η διάμετρος τους μπορεί να είναι της τάξεως των 1-5nm. Τα περισσότερα νάνο-υλικά μπορούν να κατηγοριοποιηθούν σε 4 τύπους/ομάδες: υλικά βασισμένα στον άνθρακα, υλικά βασισμένα σε μέταλλα, πολυμερικά υλικά και δενδριμερή και τέλος σύνθετα υλικά. Οι μοναδικές ιδιότητες που έχουν αυτά τα νάνο-υλικά εξαιτίας των διατάσεων τους που βρίσκονται στην περιοχή της νανοκλίμακας, είναι ιδιαιτέρως ελκυστικά για εμπορικές, ιατρικές, στρατιωτικές και περιβαλλοντικές εφαρμογές. Οι ηλεκτρικές, καταλυτικές, μαγνητικές, μηχανικές, θερμικές και απεικονιστικές ιδιότητες αυτών των υλικών διαφέρουν από τις ιδιότητες που κατέχουν τα bulk ανάλογά τους. Η έρευνα και ανάπτυξη αυτών των υλικών οδήγησε στην ευρεία χρήση των εφαρμογών τους για την ανάπτυξη νέων τομέων έρευνας όπως η νάνο-ιατρική, η νανοβιολογία, η νανοβιοτεχνολογία, η νανοθεραπευτική και νανοχειρουργική, η νανοτοξικολογία και φυσικά η νανομηχανική. (Πίνακας 1) Η νανοβιοτεχνολογία είναι ένας κλάδος της Νανοτεχνολογίας με βιολογικές και βιοχημικές εφαρμογές και χρήσεις. Η νανοβιοτεχνολογία μελετά τα υπάρχοντα στοιχεία της φύσης έτσι ώστε να μπορέσει να δημιουργήσει νέες συσκευές και εφαρμογές που πολλές φορές μιμούνται την ίδια τη φύση. Η εφαρμογή της της Νανοτεχνολογίας στη Βιολογία οδηγεί στην Νανοβιολογία. Η νανομηχανική είναι ένας κλάδος της νανοεπιστήμης που μελετά τις στοιχειώδεις μηχανικές ιδιότητες (ελαστικές, θερμικές, κινητικές) φυσικών συστημάτων στη νανοκλίμακα. Η νάνο-ιατρική είναι η πιο σημαντική εφαρμογή της νανοτεχνολογίας στον ιατρικό κλάδο. Η εφαρμογή των αρχών της νανοτεχνολογίας για τη 14
15 θεραπεία ασθενειών, τη διάγνωση, την απεικόνιση και τον έλεγχο των βιολογικών συστημάτων αναγνωρίζεται πλέον ως Νανοϊατρική στις Ηνωμένες Πολιτείες της Αμερικής. Η έρευνα στην εκλεκτική και στοχευμένη μεταφορά και απελευθέρωση φαρμακευτικών, διαγνωστικών και θεραπευτικών παραγόντων είναι στην πρώτη γραμμή από τα διάφορα προγράμματα της νάνο-ιατρικής. [3,4] Έχουν σχεδιαστεί νανοσυστήματα με διαφορετικές συνθέσεις των διαφόρων μερών τους που έχουν μοναδικές φυσικές και βιολογικές ιδιότητες ανάλογα με τις αναλογίες των συστατικών, και μπορούν να χρησιμοποιηθούν για να ξεπεράσουν τους περιορισμούς και τα εμπόδια που συναντούν οι κλασσικές μέθοδοι μοριακής απεικόνισης ή μεταφοράς φαρμάκων/γονιδίων [1,5]. Η ιατρική χρήση των βιοϋλικών συμπεριλαμβάνει συστήματα μεταφοράς φαρμάκων, νέες θεραπείες και in vivo απεικόνιση [6-10]. Νανο-ηλεκτρικές διεπιφάνειες και άλλοι αισθητήρες που βασίζονται στην νάνο-ηλεκτρονική είναι ένα άλλο πολύ σημαντικό πεδίο έρευνας. Μέχρι σήμερα, έχουν γίνει πάρα πολύ σημαντικές προσπάθειες και έχουν δαπανηθεί πολλά κεφάλαια για την ανάπτυξη μεταφοράς φαρμάκων μέσω της χρήσης της νανοτεχνολογίας μιας και προσφέρει τη δυνατότητα μεταφοράς μικρού μοριακού βάρους νανοσωματιδίων εγκλωβισμένα σε νανοσωματίδια, καθώς και μακρομόρια, πρωτεΐνες, πεπτίδια, γονίδια και άλλα μόρια βιολογικού ενδιαφέροντος με τοπική ή εκλεκτική απελευθέρωση στο σημείο/ιστό που μας ενδιαφέρει [11]. Υπάρχουν πάρα πολλά σημαντικά άρθρα και ανασκοπήσεις για την εφαρμογή της νανοτεχνολογίας στη μοριακή απεικόνιση και τη θεραπεία παθήσεων του καρδιαγγειακού συστήματος [6-10], καθώς και για απεικόνιση και θεραπεία νεοπλασμάτων με λειτουργικά νανοσωματίδια [1,12]. Τα αναβολικά που χρησιμοποιούνται για τη μεταφορά φαρμάκων πρέπει να έχουν ορισμένες προδιαγραφές, όπως βιοσυμβατότητα, ικανότητα εγκλωβισμού του φαρμάκου, ικανοποιητικά κινητικά χαρακτηριστικά βιοαποικοδόμησης και μηχανικές ιδιότητες. Ακόμα πρέπει να έχουν εύκολο χειρισμό και να συντίθενται με απλές διαδικασίες και σε χαμηλό κόστος. [5,6] Τα τελευταία χρόνια συνθετικά βιοαποικοδομήσιμα πολυμερή έχουν χρησιμοποιηθεί σε μεγάλο πλήθος εφαρμογών για να δημιουργηθούν μοριακοί παράγοντες απεικόνισης και φορείς θεραπευτικών ουσιών φαρμάκων και γονιδίων εξαιτίας της βιοσυμβατότητας και της βιοαποικοδομησιμότητας τους. [14] Τα πολυμερή μπορεί να είναι γραμμικά, διακλαδισμένα ή σφαιρικά και το μέγεθός τους μπορεί να ελεγχθεί. Polyamides, poly(amino acids), poly(alkyl-α-cyano acrylates), polyesters, poly orthoesters, polyurethanes και polyacrylamides έχουν χρησιμοποιηθεί για να αναπτυχθούν συστήματα μεταφοράς φαρμάκων [15,16]. Μεταξύ αυτών, οι θερμοπλαστικοί αλειφατικοί πολυεστέρες, όπως το πολυγαλακτικό οξύ, πολύ γλυκολικό οξύ και ιδιαίτερα το συμπολυμερές πολύ (γαλακτικό- 15
16 συν-γλυκολικό οξύ) (PLGA), έχουν μια μακρά ιστορία χρήσης ως βιοϋλικά εξαιτίας της εξαιρετικής βιοσυμβατότητας και βίοαποικοδομησιμότητας που παρουσιάζουν, αρχής γενομένης από τη δεκαετία του 1970 με βιοδιασπώμενα ράμματα [10,17]. Επιπλέον, έχουν εγκριθεί από το FDA των ΗΠΑ για εφαρμογές μεταφοράς φαρμάκων Τα νανοσωματίδια ως βασική ιδέα για συστήματα μεταφοράς φαρμάκων Τα νανοσωματίδια είναι σωματίδια με εύρος διαμέτρου από 1nm ως 100nm αν και συνήθως το μέγεθός τους μπορεί να καλύψει όλη τη νανοκλίμακα. Το ιδανικό μέγεθος για ένα σύστημα μεταφοράς φαρμάκων κυμαίνεται από 10 έως 100nm [5]. Μπορούν να κατανεμηθούν σε διάφορες κατηγορίες, ανάλογα με τις φυσικοχημικές τους ιδιότητες (ph ευαίσθητα, μαγνητικά, stealth νανοσωματίδια), το σχήμα τους (νανοσφαίρες, νανοσωλήνες, δενδριμερή κλπ), και τα υλικά που έχουν χρησιμοποιηθεί για τη σύνθεσή τους (φυσικά, συνθετικά, υβριδικά, νανοσωματίδια χρυσού κλπ) [6]. Το μικρό τους μέγεθος τους προσδίδει αρκετές ενδιαφέρουσες φυσικές, οπτικές χημικές και μηχανικές ιδιότητες οι οποίες διαφέρουν αρκετά έως πολύ από αυτές που παρουσιάζουν τα υλικά από τα οποία είναι φτιαγμένα στην μακροσκοπική κλίμακα. Ένα παράδειγμα για ένα τέτοιο χαρακτηριστικό είναι η ικανότητα που έχουν να διασχίζουν ελεύθερα το σώμα και να μπορούν να επιδεικνύουν εκλεκτική στόχευση σε κάποια περιοχή, αποφεύγοντας παράλληλα να αναγνωριστούν ως εισβολείςαντιγόνα από το ανοσοποιητικό σύστημα. Ένα άλλο χαρακτηριστικό παράδειγμα είναι ότι μπορούν να επηρεάζουν και να αλληλεπιδρούν τη φυσιολογία κυττάρων και ιστών με το να υπόκεινται χημική επιφανειακή τροποποίηση. Τα συστήματα μεταφοράς φαρμάκων έχουν την ικανότητα της ασφαλούς μεταφοράς μιας φαρμακευτικής ουσίας συνδυάζοντας νάνο-υλικά με βίο-ενεργά μόρια ή φάρμακα, τα οποία σε διαφορετική περίπτωση θα είχαν ανεπαρκή ή μη επιθυμητά φαρμακοκινητικά χαρακτηριστικά ή θα ήταν τοξικά για τα υγιή ζωντανά κύτταρα. Τέτοιου είδους τεχνικές μπορούν να χρησιμοποιηθούν με σκοπό να υπάρχει ακριβής έλεγχος των διαφόρων παραμέτρων της δράσης ενός φαρμάκου, όπως είναι η φαρμακοκινητική, η βιοδιαθεσιμότητα, η στοχευμένη μεταφορά του φαρμάκου, η μη ειδική τοξικότητα και η βιοσυμβατότητα. Τα συστήματα μεταφοράς φαρμάκων επιδεικνύουν αρκετά πλεονεκτήματα σε σχέση με τις κλασσικές θεραπευτικές προσεγγίσεις διαφόρων ασθενειών και έχουν αρχίσει να εφαρμόζονται όλο και περισσότερο ειδικά ακολουθώντας πολυδύναμες (multimodal) προσεγγίσεις [7]. 16
17 Ένα αποδοτικό σύστημα μεταφοράς φαρμάκων χρειάζεται ιδανικά να συντεθεί με τέτοιο τρόπο ώστε να είναι σε θέση να μιμείται ένα in vivo φυσιολογικό ανάλογο και παράλληλα να μπορεί να χρησιμοποιηθεί για τοπική ή συστηματική χορήγηση. Σε αυτή την περίπτωση, αναλόγως με τη συγκεκριμένη εφαρμογή για την οποία προορίζονται, μπορούν να πραγματοποιηθούν περαιτέρω τροποποιήσεις όσον αφορά την υδροφιλικότητα ή λιποφιλικότητα, τη συνάφεια με το φάρμακο, τη βιοδιαθεσιμότητα, τη βιοσυμβατότητα και το μέγεθος [8] Συνθετικοί πολυμερικοί φορείς Τα πολυμερικά συστήματα μεταφοράς φαρμάκων περιέχουν ένα εύρος μακρομοριακών δομών που κυμαίνονται από πολυμερικά μικκύλια μέχρι σύνθετα συστήματα είτε με φαρμακομόρια είτε με πρωτεΐνες [23]. Μέχρι σήμερα έχει χρησιμοποιηθεί μεγάλο εύρος πολυμερών και συνδυασμών πολυμερών μέχρι και το στάδιο των κλινικών δοκιμών, κάποια από τα οποία είναι και τα παρακάτω: πολυαιθυλενογλυκόλη, πολυβινυλοπυρρολιδόνη, πολύ-l-λυσίνη, πολύ-l-γλουταμικό οξύ, πολυασπαρταμίδες και δεξτράνες [24]. Το κυριότερο πλεονέκτημα αυτών των συστημάτων είναι η διαφορετικότητα και η ποικιλία των σχημάτων τα οποία μπορούν να επιτευχθούν. Διάφορες μορφές σχέδια έχουν δημιουργηθεί, τα οποία κυμαίνονται από απλά γραμμικά και διακλαδισμένα σχέδια μέχρι σχέδια που έχουν το σχήμα άστρου [8,23]. Είναι πολύ σημαντικό να τονιστεί ότι οι πολυμερικές αρχιτεκτονικές δομές παίζουν σημαντικό ρόλο στην αποδοτικότητα αυτών των δομών ως συστήματα μεταφοράς φαρμάκων. Σε περίπτωση που συμβούν μικρές αλλαγές στη δομή μπορούν να επάγουν αλλαγές στην διαλυτότητα, στην ικανότητα πρόσληψης φαρμάκου και στη βιοαποικοδόμηση [8]. Στις ίδιες γραμμές κυμαίνονται τα όσα ισχύουν και για τη μορφολογία, μιας και η αναλογία του μονομερούς και η τοπολογία του σε ένα συν-πολυμερές αλλάζουν τις φυσικές ιδιότητες [25]. Το φάρμακο μπορεί να ενσωματωθεί φυσικά στη μήτρα ή την εξωτερική επιφάνεια του πολυμερούς, ή μπορεί να συνδεθεί με το πολυμερές με ομοιοπολικούς δεσμούς είτε μόνο του είτε με ενδιάμεσο φορέα [26]. Ένα πολύ χαρακτηριστικό πλεονέκτημα που εμφανίζουν αυτά τα συστήματα μεταφοράς φαρμάκων σε σχέση με αυτά από μικροσωματίδια (1-10μm) είναι ότι, εξαιτίας του μεγέθους τους που βρίσκεται στη νανοκλίμακα, τα φάρμακα που ενσωματώνουν μπορούν να μεταφερθούν πολύ πιο αποδοτικά και στοχευμένα. Έχει παρατηρηθεί ότι νανοσωματίδια από PLGA (poly-lacticco-glycolic acid) (50:50) μεγέθους 100 nm εμφάνισαν πολύ καλύτερες αποδόσεις εγκλωβισμού σε σχέση με μεγαλύτερα σωματίδια ίδιου μεγέθους [27]. 17
18 Μια στρατηγική που ακολουθείται ευρέος για να βελτιώσει την μεταφορά των νανοσωματιδίων, μέθοδος που χρησιμοποιείται ευρέως και στη μεταφορά λιποσωμάτων, είναι ή χρήση PEG(πολυαιθυλενογλύκόλη) (PEGylation). Αυτό γίνεται γιατί από τη στιγμή που τα νανοσωματίδια υπόκεινται σε αλληλεπιδράσεις και με το φάρμακο και με το εξωτερικό τους περιβάλλον, η μέθοδος του PEGylation μπορεί να μειώσει το φαινόμενο opsonization effect και τον εγκλωβισμό από τα μακροφάγα [28]. Η επικάλυψη με PEG, δεν χρησιμοποιείται μόνο για να εξασθενίσει την ενεργοποίηση του ανοσοποιητικού συστήματος του ξενιστή, αλλά ακόμα, μπορεί να βελτιώσει τα φαρμακοκινητικά χαρακτηριστικά των νανοσωματιδίων [29]. Για παράδειγμα, πολυμερικά μικκύλια επικαλυμμένα με PEG έχουν αποδειχτεί ότι παρουσίαζαν αυξημένη κατακράτηση από αθηρωματικές πλάκες [30], κάτι που επαληθεύτηκε και με τη χρήση μαγνητική τομογραφίας (MRI) [31] Νανοτεχνολογία βασισμένη στο PLGA Το πολύ (γαλακτικό-συν-γλυκολικό οξύ) PLGA είναι ένα συμπολυμερές που συντίθεται μέσω τυχαίων συμπολυμερισμών με άνοιγμα του δακτυλίου των δύο διαφορετικών μονομερών,τα οποία είναι τα κυκλικά διμερή (1,4-διοξανο-2,5-διόνη) του γλυκολικού οξέος και γαλακτικού οξέος (Εικόνα 1). Οι πιο κοινοί καταλύτες που χρησιμοποιούνται στην παρασκευή αυτού του συμπολυμερούς περιλαμβάνουν τον κασσίτερος (ΙΙ) 2-αιθυλεξανοϊκό, κασσίτερος (II) με αλκοξείδια ή ισοπροποξειδικό αλουμίνιο. Κατά τη διάρκεια του πολυμερισμού, οι διαδοχικές μονομερείς μονάδες (από γλυκολικό ή γαλακτικό οξύ) συνδέονται μεταξύ τους σε PLGA με εστερικούς δεσμούς, αποδίδοντας έτσι ένα γραμμικό, άμορφο προϊόν αλειφατικού πολυεστέρα [18]. Οι μορφές του PLGA συνήθως προσδιορίζονται από την αναλογία των μονομερών που χρησιμοποιούνται (πχ., PLGA 50:50), το οποίο τυγχάνει να είναι και το πιο συχνά χρησιμοποιούμενες στις νανοτεχνολογικές εφαρμογές, και προσδιορίζει ένα συμπολυμερές του οποίου η σύνθεση είναι 50% γαλακτικό οξύ και 50% γλυκολικό οξύ. Διαφορετικά φυσικά χαρακτηριστικά των PLGA NPs που συντίθενται (μέγεθος, κατανομή μεγέθους, μορφολογία και ζ-δυναμικό) μπορούν να επιτευχθούν με έλεγχο των παραμέτρων που χρησιμοποιούνται, ειδικά για την μέθοδο σύνθεσης. Οι μέθοδοι παρασκευής και οι ιδιότητες των PLGA NPs έχουν μελετηθεί εκτεταμένα [18]. Η συνηθέστερα χρησιμοποιούμενη μέθοδος για τον σχηματισμό των PLGA NPs είναι η μονού-ή διπλούγαλακτώματος-εξάτμιση του διαλύτη(single/double emulsion solvent evaporation). H μονού γαλακτώματος διεργασία χρησιμοποιεί έλαιο-σε-νερό (o/w) γαλακτωματοποίηση, ενώ η 18
19 διπλού γαλακτώματος διαδικασία είναι μια νερό-σε-έλαιο-σε-νερό (w / o / w) μέθοδος. Η ν / ε / ν μέθοδος είναι η καταλληλότερη για εγκλεισμό υδατο-διαλυτών φαρμάκων, όπως πεπτίδια, πρωτεΐνες και εμβόλια, ενώ η o / w μέθοδος είναι ιδανική για αδιάλυτα στο νερό φάρμακα, όπως στεροειδή κ.α. [16]. Σε ορισμένες περιπτώσεις έχουν αξιοποιηθεί στερεού / ελαίου / ύδατος (s / o / w) τεχνικές με PLGA μικροσφαίρες, ειδικά για μια υψηλότερο ποσοστό εγκλωβισμού φαρμάκου μεγάλων υδατο-διαλυτών πεπτιδίων, όπως η ινσουλίνη. Εν συντομία, για την o / w μέθοδο,το PLGA διαλύεται πρώτα σε έναν πτητικό οργανικό διαλύτη (πχ., διχλωρομεθάνιο ή ακετόνη). Το φάρμακο προστίθεται στη συνέχεια στο διάλυμα του πολυμερούς για να παραχθεί ένα διάλυμα ή μια διασπορά των σωματιδίων του φαρμάκου. Αυτό το πολυμερές-διαλύτης-φάρμακο διάλυμα / διασπορά στη συνέχεια γαλακτωματοποιείται με ανάδευση υπό κατάλληλες συνθήκες σε έναν μεγαλύτερο όγκο νερού υπό την παρουσία ενός γαλακτωματοποιητή όπως πολύ (βινυλική αλκοόλη) (PVA), για να παραχθεί ένα ε/υ γαλάκτωμα. Το PVA χρησιμοποιείται για τη σταθεροποίηση του γαλακτώματος, διότι σχηματίζει σωματίδια σχετικά μικρού μεγέθους με ομοιόμορφη κατανομή μεγέθους [19]. Το επόμενο βήμα είναι η απομάκρυνση του διαλύτη είτε με εξάτμιση ή εκχύλιση ώστε να σκληρύνουν τα σταγονίδια ελαίου, και οι στερεές νανοσφαίρες λαμβάνονται και στη συνέχεια πλένονται και συλλέγονται με διήθηση, κοσκίνισμα ή φυγοκέντριση. Αυτά στη συνέχεια ξηραίνονται κάτω από κατάλληλες συνθήκες ή λυοφιλοποιούνται για να δώσουν το τελικό ελεύθερης ροής ενέσιμο προϊόν [16,20-23]. Αυτή η μέθοδος έχει χρησιμοποιηθεί για την παραγωγή PLGA NPs 100 nm σε μέγεθος. Τα PLGA NPs είναι κολλοειδή συστήματα που τυπικά κυμαίνονται από 10 έως 1000 nm σε διάμετρο, με τον θεραπευτικό παράγοντα είτε εγκλωβισμένο στο εσωτερικό ή προσροφημένο ή χημικά συζευγμένο επί της πολυμερικής επιφάνειας [15]. Ο λόγος για τον οποίο τα PLGA NPs είναι βιοδιασπώμενα στο σώμα είναι επειδή υφίστανται υδρόλυση των εστερικών δεσμών τους υπό την παρουσία νερού με αποτέλεσμα να παράγουν τα αρχικά μονομερή, γαλακτικό οξύ και γλυκολικό οξύ, τα οποία είναι παραπροϊόντα διαφόρων μεταβολικών οδών στο σώμα υπό κανονικές φυσιολογικές συνθήκες [26]. Ο ρυθμός αποικοδόμησης των PLGA πολυμερών σχετίζεται με την αναλογία των μονομερών που χρησιμοποιούνται στην παραγωγή. Το πολυμερές που περιέχει μία αναλογία 50:50 γαλακτικού και γλυκολικού οξέος υδρολύεται πολύ ταχύτερα από ότι εκείνα που περιέχουν υψηλότερες αναλογίες του ενός εκ των δύο μονομερών [16,27]. Τα προϊόντα αποικοδόμησης μεταβολίζονται εύκολα στο σώμα μέσω του κύκλου του Krebs και αποβάλλονται [28]. Έτσι, υπάρχει μια πολύ ελάχιστη συστηματική τοξικότητα που σχετίζεται με τη χρήση PLGA για τη μεταφορά φαρμάκων ή βιοϋλικών εφαρμογών. Οι in vivo και in 19
20 vitro μελέτες για δοκιμή της τοξικότητας και βιοσυμβατότητας απέδειξαν ότι τα PLGA νανοϋλικά εμφανίζουν ικανοποιητική βιοσυμβατότητα και απουσία σημαντικής τοξικότητας [26]. Η in νίνο μελέτες έγιναν κυρίως σε εφαρμογές αρθρικού χόνδρου και μηνίσκου, και σε ένα σημαντικό αριθμό άλλων μελετών που διεξάγονται in situ σε μυς ή άλλους μαλακούς ιστούς. Όλα τα αποτελέσματα φαίνεται να υποστηρίζουν την in vivo χρήση του PLGA, αν σε και ορισμένες περιπτώσεις έχουν αναφερθεί φλεγμονώδεις αντιδράσεις [26]. Οι μελέτες βιοκατανομής των PLGA NPς δείχνουν ενισχυμένη ικανότητα μεταφοράς και αποδέσμευσης διαγνωστικών ή θεραπευτικών παραγόντων λόγω της αυξημένης διαπερατότητας και του φαινομένου της συγκράτησης. Για παράδειγμα, όταν το πράσινο ινδοκυανίνης μεταφέρεται μέσω NPs σε υγιή ποντίκια χρησιμοποιώντας μια φθορομετρική μέθοδο ποσοτικού προσδιορισμού, τα νανοσωματίδια οδήγησαν σε υψηλότερη απόθεση του πρασίνου της ινδοκυανίνης σε όργανα (από δύο έως οκτώ φορές) καθώς και στο αίμα (πέντε έως δέκα-φορές) σε σύγκριση με το διάλυμα όπου το φάρμακο υπάρχει ελεύθερο, υποδεικνύοντας τις τεράστιες δυνατότητες των PLGA NPs ως ένα σύστημα μεταφοράς για το πράσινο της ινδοκυανίνης και τη χρήση του στη διάγνωση όγκων και φωτοδυναμική θεραπεία [29]. Αυτό το φαινόμενο ενισχύεται όταν τα ΝΡs είναι επικαλυμμένα με μια πολύ (αιθυλενογλυκόλη / οξείδιο) επιφανειακή τροποποίηση [30,31]. Επικάλυψη της επιφάνειας των νανοσωματιδίων με ένα υδρόφιλο πολυμερές, όπως η πολύ-(αιθυλενογλυκόλη) (PEG), έχει αποδειχθεί ότι προσδίδουν ιδιοτήτων μακράς διάρκειας στην κυκλοφορία του αίματος για τα νανοσωματίδια από πολύ-(γαλακτικό οξύ) PLA, PLGA, πολυκαπρολακτόνη (PCL) και πολυφωσφαζένιο. Η παρουσία των υδρόφιλων πολυμερικών αλυσίδων στην επιφάνεια των νανοσωματιδίων θεωρείται ότι τα σταθεροποιήσει στερικά ενάντια σε οψωνοποίηση και φαγοκυττάρωση [30]. Η μεταφορά φαρμάκων (drug delivery) είναι η μέθοδος ή διαδικασία της χορηγήσεως μίας φαρμακευτικής ένωσης ώστε να επιτευχθεί ένα θεραπευτικό αποτέλεσμα σε ανθρώπους ή ζώα [5]. Θεραπευτικές αγωγές με παράγοντες όπως πεπτίδια, πρωτεΐνες, αντισώματα, εμβόλια και γονίδια, δεν μπορούν να μεταφερθούν χρησιμοποιώντας συμβατικές μεθόδους μεταφοράς επειδή μπορεί να είναι ευαίσθητα σε ενζυματική αποικοδόμηση ή δεν μπορούν να απορροφηθούν στην συστηματική κυκλοφορία αρκετά αποτελεσματικά, λόγω του μοριακού μεγέθους τους και του φορτίου τους, για να είναι θεραπευτικά αποτελεσματικά. Συνεπώς, πολλές προσπάθειες έχουν επικεντρωθεί στην στοχευμένη αποδέσμευση και μεταφορά, όπου το φάρμακο είναι ενεργό μόνο στην περιοχή-στόχο του σώματος, όπως σε καρκινικούς ιστούς, και σε συστήματα παρατεταμένης απελευθερώσεως στα οποία το φάρμακο απελευθερώνεται κατά τη διάρκεια συγκεκριμένης χρονικής περιόδου με ελεγχόμενο τρόπο. 20
21 1.3. Κριτήρια επιλογής PLGA Το πόλυ-(γαλακτικό-συν-γλυκολικό οξύ) είναι ένα πολυμερές που εγκρίθηκε από τον FDA για εφαρμογές μεταφοράς φαρμάκων εξαιτίας των ακόλουθων ιδιοτήτων που εμφανίζει: βιοαποδομησιμότητα, βιοσυμβατότητα, κατάλληλη και τροποποιήσιμη κινητική βιοαποικοδόμησης και μηχανικές ιδιότητες καθώς και ευκολία επεξεργασίας [16]. Έχει χρησιμοποιηθεί ευρέως για τη δημιουργία διαφόρων βιοαποικοδομήσιμων φορέων, όπως μικροσωματίδια, NPs, εμφυτεύματα και διάφορες διατάξεις, καθώς και in situσχηματιζόμενους φορείς. Βιοδιασπώμενα NPs από PLGA έχουν διερευνηθεί για παρατεταμένη και στοχευμένη / εντοπισμένη χορήγηση διαφόρων παραγόντων, συμπεριλαμβανομένων φαρμάκων, πρωτεϊνών και πεπτιδίων, και πρόσφατα πλασμιδιακού DNA [15,23,32-35]. Λόγω του μεγέθους τους, τα συστήματα απελευθέρωσης από NPs έχουν σημαντικά πλεονεκτήματα για εφαρμογές μεταφοράς φαρμάκων. Τα νανοσωματίδια μπορούν να διεισδύσουν βαθιά μέσα στους ιστούς μέσω πόρων, (πχ., στο ήπαρ) και, γενικά, εισέρχονται στα κύτταρα σε μεγάλες αποδόσεις [36]. Αυτό επιτρέπει την αποτελεσματική παροχή θεραπευτικών παραγόντων σε θέσεις στόχους (κάποιο ιστό ή όργανο) στο σώμα. Τα NPs έχουν επίσης το πλεονέκτημα της διατήρησης της απελευθέρωσης του έγκλειστου θεραπευτικού παράγοντα σε περίοδο από μερικές ημέρες έως μερικές εβδομάδες σε σύγκριση με τα φυσικά πολυμερή τα οποία έχουν μία σχετικά μικρή διάρκεια απελευθέρωσης του φαρμάκου [15]. Το PLGA εμφανίζεται ως μια συχνή επιλογή για την παραγωγή ποικιλίας των βιοϊατρικών συσκευών, όπως είναι τα μοσχεύματα, τα ράμματα, εμφυτεύματα και προσθετικές συσκευές [16]. Για παράδειγμα, μία εμπορικά διαθέσιμη συσκευή παροχής φαρμάκου χρησιμοποιώντας PLGA είναι Lupron (Depot ) για τη θεραπεία του καρκίνου του προστάτη σε προχωρημένο στάδιο. Έτσι, τα νανοσωματίδια από PLGA εμφανίζουν σημαντική δυναμική για ποικίλες εφαρμογές και χρησιμοποιούνται σε έρευνες εκτενώς Καρδιαγγειακές Παθήσεις Οι Καρδιαγγειακές παθήσεις (CVD) είναι η κύρια αιτία θανάτου κάθε χρόνο από το 1900 και ύστερα στις ΗΠΑ και εξακολουθεί να είναι η πιο συχνή αιτία θανάτου στις ΗΠΑ. Περισσότερο από το 50% αυτών των θανάτων προκαλούνται από στεφανιαία νόσο, σύμφωνα με τα πιο πρόσφατα στοιχεία από την American Heart Association and Stroke Statistics με βάση έρευνα που διεξήχθη το Αποτελεσματικές θεραπείες των καρδιαγγειακών παθήσεων περιλαμβάνουν προληπτικές αλλαγές στον τρόπο ζωής, φαρμακευτική αγωγή και 21
22 χειρουργικές επεμβάσεις [17,37,38]. Οι ραγδαία εξελισσόμενες καινοτόμες εφαρμογές και η ανάπτυξη της νανοτεχνολογίας έχουν ανοίξει νέους δρόμους για τη διαχείριση των CVDs. Αρκετές εξαιρετικές ανασκοπήσεις έχουν γραφεί και συνοψίζουν την υπάρχουσα βιβλιογραφία σχετικά με την εφαρμογή της νανοτεχνολογίας στην διαγνωστική και θεραπευτική των καρδιαγγειακών παθήσεων [6,8,9]. Θεραπευτικές εφαρμογές των νανοϋλικών στον καρδιαγγειακό τομέα της ιατρικής περιλαμβάνουν καρδιαγγειακές συσκευές για χορήγηση φαρμάκων και βιοδραστικών μορίων, ή νέες τεχνολογίες για τη μείωση της συσσώρευσης χοληστερόλης και για την διάλυση των θρόμβων [39]. Η τοποθέτηση stent είναι σήμερα η κύρια παρέμβαση για καρδιαγγειακές αποφρακτικές νόσους, ωστόσο, μπορεί να οδηγήσει σε σε επαναστένωση [40-42]. Έχουν υπάρξει κάποια ενθαρρυντικά αποτελέσματα σε πρώιμες κλινικές δοκιμές με stents που απελευθερώνουν φάρμακα (Drug Eluting Stents) όπως αντι-πολλαπλασιαστικούς (antiproliferative drugs) παράγοντες. Stents από νανοσωματίδια PLGA μπορούν να μεταφέρουν αποτελεσματικά γονίδια ή φάρμακα στα τοιχώματα των αγγείων. Ελεγχόμενη απελευθέρωση του DNA από αγγειακά stents διερευνήθηκε σε μία σειρά μελετών με τη χρήση πράσινης πρωτεΐνης φθορισμού για πλασμιδιακό DNA που ενσωματώνεται σε ένα PLGA γαλάκτωμα πάνω σε stent από ανοξείδωτο χάλυβα [43]. Η μελέτη έδειξε ότι η φθορίζουσα πρωτεΐνη εκφράζεται αποτελεσματικά σε κυτταροκαλλιέργειες αγγειακών SMCs, καθώς και σε στεφανιαίες αρτηρίες χοίρου. Μια άλλη μελέτη έδειξε οτι η ελεγχόμενη απελευθέρωση από stent ενδοαγγειακά αγγειοστατίνης περιορίζει την εξέλιξη πλάκας και την επαναστένωση πάνω στο στεντ, στην οποία φορτώθηκαν σε DES, ελεγχόμενης απελευθέρωσης βιοδιασπώμενα μικροσφαιρίδια που μετέφεραν αγγειοστατίνη (PLGAπολυαιθυλενογλυκόλη), και αποδεσμεύτηκαν και αναπτύχθηκαν στην αορτή κουνελιών [65]. Έχει υπάρξει επίσης αναφορά ότι στεντ για τη μεταφορά τυρφοστίνης AGL-2043 από μια επικάλυψη PLGA μειώνει την υπερπλασία εσωτερικά του stent σε στεφανιαίες αρτηρίες κατά 50% μετά από 28 ημέρες [44]. Ο πολλαπλασιασμός των αγγειακών SMCs παίζει σημαντικό ρόλο στην αθηροσκλήρωση, επαναστένωση και φλεβικής νόσου που παρατηρείται μετά από επέμβαση bypass. Ένας μεγάλος αριθμός των φαρμάκων έχουν αποδειχθεί ότι παράγουν αντιπολλαπλασιαστικά αποτελέσματα επί SMCs (Anti-proliferative drugs). Επειδή η στένωση είναι μια σημαντική βλάβη που συνήθως εμφανίζεται στην αναστόμωση του μοσχεύματος, η τοπική παροχή φαρμάκων στην θέση στόχο είναι μια καλύτερη στρατηγική για την επίτευξη επαρκούς θεραπευτικής συγκεντρώσεις, ελαχιστοποιώντας ταυτόχρονα τις συστηματικές παρενέργειες. Εκτός από τα επικαλυμμένα stents, πολλά τοπικά συστήματα χορήγησης 22
23 φαρμάκων, συμπεριλαμβανομένων διαφόρων καθετήρων μπαλονιού διάχυσης και υδρολογίες επικαλυμμένων καθετήρων μπαλονιού, έχουν αναπτυχθεί για τη θεραπεία των καρδιαγγειακών παθήσεων και έχουν επιφέρει σημαντικά αποτελέσματα σε ζωικά μοντέλα. Ωστόσο, καμία ιδανική θεραπεία για την επαναστένωση και τη νόσο μοσχεύματος παράκαμψης έχει επιτευχθεί σε κλινικό επίπεδο. Τα μεγάλα μειονεκτήματα αυτών των μεθόδων είναι η χαμηλή πρόσληψη των φαρμάκων που μεταφέρονται από τον ιστό και η ταχεία έκλυση των φαρμάκων με την ροή αίματος [45-47]. Για την αποφυγή αυτών των μειονεκτημάτων, συστήματα μεταφοράς και απελευθέρωσης φαρμάκου τοπικά που αποτελούνται από NPs έχουν μελετηθεί, παρουσιάζοντας ελπιδοφόρα αποτελέσματα. Για παράδειγμα, έχει αναφερθεί ότι η ηπαρίνη που απελευθερώνεται από μικροσφαίρες PLGA μείωσε αποτελεσματικά πολλαπλασιασμό ανθρώπινων SMC [45]. Επίσης έχει αναφερθεί η ανάπτυξη φορέα πακλιταξέλης, ενός ανταγωνιστικού παράγοντα μικροσωληνίσκων, σε βιοαποικοδομήσιμο πολύ-(οξείδιο του αιθυλενίου)-πολύ-(λακτίδιο / γλυκολίδιο) νανοσφαιρίδιο ως ένα σύστημα παρατεταμένης απελευθέρωσης φαρμάκου για να μελετηθούν οι επιπτώσεις της επί των αγγειακών SMCs σε κυτταροκαλλιέργεια [48]. Βρέθηκε ότι τα φορτωμένα πακλιταξέλη νανοσφαιρίδια, που παρασκευάστηκαν από μέθοδο emulsificationdiffusion, εμφάνισαν ένα προφίλ παρατεταμένης απελευθέρωσης σε διάστημα 4 εβδομάδων. Άλλη επιστημονική ομάδα έχει αναπτύξει ένα συνδυασμό PLGA μικροσφαιριδίων με Regel, ένα ενέσιμο συμπολυμερές, ως ένα σύστημα παρατεταμένης απελευθέρωσης για περιαγγειακή χορήγηση ενός αντιπολλαπλασιαστικού φαρμάκου, τη διπυριδαμόλη. Ενσωμάτωση της διπυριδαμόλης εντός των μικροσφαιριδίων PLGA μείωσε το αρχικό φαινόμενο burst και επιμήκυνε την απελευθέρωση, με την κινητική απελευθερώσεως να εξαρτάται από το μοριακό βάρος του PLGA [49] Η παρατεταμένη απελευθέρωση φαρμάκου ή γονιδιακού παράγοντα και κυτταρική απορρόφησή του από in vitro μελέτες υποδηλώνουν ότι οι PLGA μικροσφαίρες θα μπορούσαν να χρησιμοποιηθούν για εγκλεισμό αντιπολλαπλασιαστικών παραγόντων και μπορούν να παρέχει μια νέα προσέγγιση για την τοπική χορήγηση φαρμάκου μετά από PTCA και, και έτσι να οδηγήσουν στην πρόληψη της επαναστένωσης ή της νόσου μετά από επέμβαση bypass. Έχει αναφερθεί ότι φορτωμένα NPs PLGA με πακλιταξέλη τροποποιημένα με βρωμιούχου διδωδεκυλδιμεθυλαμμώνιο ήταν ένα αποτελεσματικό μέσο αναστολής της πολλαπλασιαστικής απόκρισης προς αγγειακό τραυματισμό σε ένα μοντέλο αρτηριακού τραυματισμού σε κουνέλι [50]. Μια άλλη μελέτη των NPs για τοπική χορήγηση της πακλιταξέλης για τη θεραπεία επαναστένωσης έδειξε επίσης την αντι-επαναστενωτική δράση των φορτωμένων με πακλιταξέλη NPs in vivo. Τα φορτωμένα με paclitaxel NPs, που 23
24 αποτελούνται από πολύ-(βινυλική αλκοόλη)-graft-plga (PVA-g-PLGA) με διαφορετικά PLGA όσον αφορά το μήκος της αλυσίδας, καθώς και απλά PLGA NPs, χορηγήθηκαν τοπικά στο τοίχωμα του μπαλονιού που ακουμπά με τις τραυματισμένες λαγόνιες αρτηρίες του κουνελιού χρησιμοποιώντας ένα πορώδη καθετήρα μπαλονιού [51] Μοριακοί και κυτταρικοί μηχανισμοί των αγγειακών ασθενειών Οι αγγειακές ασθένειες εμπεριέχουν όλων των ειδών τις καταστάσεις οι οποίες επηρεάζουν το κυκλοφορικό σύστημα, όπως για παράδειγμα η αρτηριοσκλήρωση (σκλήρυνση των αρτηριών) η αθηροσκλήρωση (η αρτηριακή σκλήρυνση που σχετίζεται με τις αθηρωματικές πλάκες), η στένωση λόγω θρομβοεμβολισμού και η ισχαιμία στην αορτή, την καρωτίδα, την ρινική και άλλες περιφερειακές αρτηρίες. Ακόμα παθήσεις όπως τα ανευρύσματα, θρόμβοι αίματος στις φλέβες, ανωμαλίες στη διαδικασία της φυσιολογικής αιμόστασης, (αιμοπετάλια, παράγοντας von Willebrand) κ.α. Πολλές από αυτές τις παθήσεις εμφανίζουν χώρο-χρονικά επικαλυπτόμενα φαινόμενα που συμβαίνουν σε κυτταρικό και μοριακό επίπεδο. Η αθηροσκλήρωση συχνά χρησιμοποιείται σαν μοντέλο για να μελετηθούν και περιγραφούν κάποια από αυτά τα φαινόμενα αυτά καθώς και για να αναπτυχθούν στρατηγικές αντιμετώπισης από τη νάνο-ιατρική με σκοπό την στοχευμένη θεραπεία. Ένας από τους λόγους για τους οποίους χρησιμοποιείται σαν μοντέλο η συγκεκριμένη πάθηση είναι διότι είναι από τις πιο διαδεδομένες αγγειακές παθήσεις. Μετέπειτα επιπλοκές αυτής της πάθησης συχνά οδηγούν σε θρόμβωση και στένωση των αιμοφόρων αγγείων, στις οποίες εμπλέκονται κυρίως οι ίδιες μοριακές και κυτταρικές διαδικασίες οι οποίες συμβαίνουν σε κάθε επεισόδιο σχηματισμού θρόμβου ή πήξης του αίματος. Έτσι χρησιμοποιείται η αθηροσκλήρωση για να δημιουργηθεί ένα έγκυρο και λογικό μοντέλο περιγραφής των κυτταρικών και μοριακών διαδικασιών που λαμβάνουν χώρα στις αγγειακές παθήσεις οι οποίες αποτελούν τους πιο κοινούς στόχους της νάνο-ιατρικής. Η αθηροσκλήρωση είναι μια φλεγμονώδης πάθηση των αρτηριών, στην οποία 3 από τα αρχικά στάδια συχνά περιλαμβάνουν κατάτμηση και οξείδωση των λιπιδικών μορίων (στο αίμα) μέσα στα όρια του υποενδοθηλιακού χιτώνα και παθολογικό τραύμα/ενεργοποίηση/αποσταθεροποίηση των ενδοθηλιακών κυττάρων (EC) αφήνοντας εκτεθειμένο το ενδοθηλιακό τοίχωμα στην ροή του αίματος. Ενδοθηλιακός τραυματισμός μπορεί επίσης να προκληθεί από κακή διατροφή, το κάπνισμα η από κάποιο ξαφνικό σοκ στο τοίχωμα. Στο τραυματισμένο, φλεγμονώδες απορυθμισμένο ενδοθήλιο, διαμοριακά 24
25 συσσωματώματα όπως τα σωματίδια Wiebel-Palade (τα οποία αποθηκεύουν vwf και P- σελεκτίνη) ενώνονται με την κυτταρική μεμβράνη και μετέπειτα εκθέτουν vwf και P- σελεκτίνη στην επιφάνεια των ενδοθηλιακών κυττάρων. Ο vwf και η P-σελεκτίνη μπορούν να προάγουν την προσέλκυση και την σύνδεση των αιμοπεταλίων στο αγγειακό τραύμα μέσω της αλληλεπίδρασης με την ιντεγκρίνη GPIb/IX/V και τoν P-selectin γλυκοπρωτεϊνικό προσδέτη 1 (PSGL-1), αντίστοιχα, που βρίσκονται στην επιφάνεια των αιμοπεταλίων. Η P- selectin καθώς και άλλες σελεκτίνες επίσης διευκολύνουν την προσκόλληση κυττάρων που σχετίζονται με τη φλεγμονή όπως οι λευκοκύτες στη σημείο του τραυματισμού. Το προθρομβικό περιβάλλον επίσης παράγει αγωνιστές όπως η θρομβίνη, το ADP και τον παράγοντα ενεργοποίησης των αιμοπεταλίων (PAF), οι οποίοι πυροδοτούν περαιτέρω ενεργοποίηση των αιμοπεταλίων και του ενδοθηλίου. Αυτές οι διαδικασίες ενεργοποίησης οδηγούν στην έκφραση/απορύθμιση της ιντεγκρίνης αιιβ33 στα αιμοπετάλια και του αvβ3 στα ενδοθηλιακά κύτταρα. Τα ενεργοποιημένα αιμοπετάλια επίσης εκφράζουν την P-selectin μέσω των κυτοπλασμικών κοκκίων αποθήκευσης που έχουν και ονομάζονται a-granules. Η ιντεγκρίνη αιιbβ3 υιοθετεί μια διαμόρφωση ειδική για την πρόσδεση με κάποιο ligand (προσδέτη) ακολουθώντας την ενεργοποίηση των αιμοπεταλίων και προσδένεται με τον φυσικό της προσδέτη, το ινωδογόνο (Fg) μέσω μοριακών αλληλεπιδράσεων ανάμεσα στα πεπτίδια Αργινίνη-Γλυκίνη-Ασπαρτικό οξύ (RGD) και Αλανίνη-Γλυκίνη-Ασπαρτικό οξύ και τα τελικά άκρα του ινωδογόνου. Αυτή η αλληλεπίδραση ινωδογόνου-αιιbβ3 ιντεγκρίνης είναι ο κύριος μηχανισμός γεφύρωσης μεταξύ των αιμοπεταλίων, ο οποίος οδηγεί τελικά στον σχηματισμό θρόμβου. Η ιντεγκρίνη αvβ3, που είναι ένας υποδοχέας fibronectin/vitronectin, βοηθά στην διαμόρφωση της περιοχής σύνδεσης του εξωτερικού πλέγματος των ενδοθηλιακών κυττάρων και στην εστιακή προσκόλληση των ενδοθηλιακών κυττάρων. Έχει την ικανότητα να αλληλεπιδρά σταυρωτά με αιμοπεταλιακή αιιbβ3 μέσω γεφύρωσης με τις πεπτιδικές ακολουθίες RGD και το ινωδογόνο και αυτό έχει ως επακόλουθο την περαιτέρω προαγωγή ενός ασφαλούς προσαρτήματος ενεργοποιημένων αιμοπεταλίων στο σημείο του αγγειακού τραύματος. Αν θέλουμε να συνοψίσουμε όλες τις διαδικασίες που συμβαίνουν κατά τη διάρκεια της φλεγμονής και ακολουθούν την ενεργοποίηση των αιμοπεταλίων και των ενδοθηλιακών κυττάρων και τις μετέπειτα αλληλεπιδράσεις μεταξύ αιμοπεταλίων ενδοθηλιακών κυττάρων και λευκοκυττάρων, αυτές θα ήταν οι ακόλουθες: (α) Υποενδοθηλιακή διείσδυση στον εσωτερικό χιτώνα των κυττάρων και μεταμόρφωση των λευκοκυττάρων από μονοκύτταρα σε μακροφάγα. 25
26 (β) Έκκριση χημειοκινών και κυτοκινών από τα ενδοθηλιακά κύτταρα, αιμοπετάλια, και μακροφάγα για την προαγωγή της διείσδυσης στο εσωτερικό των λείων μυικών ινών (SMCs) από τα εξωτερικά στρώματα του αρτηριακού τοιχώματος. (γ) Τα μακροφάγα ωθούν τα λιπίδια στο μεταβολισμό για να σχηματίσουν αφρώδη κύτταρα (foam cells) και αυτό οδηγεί στην δημιουργία και την ανάπτυξη λιπιδικών ραβδώσεων (fatty streaks) και δημιουργία και εξέλιξη πλάκας στον χιτώνα. (δ) Έκκριση μεταλοπρωτεϊνασών (MMPs) από των πυρήνα των μακροφάγων και των αιμοπεταλίων που οδηγούν στην αποικοδόμηση του κολλαγόνου στο ενδοθηλιακό πλέγμα (ECM). (ε) Σύνθεση κολλαγόνου από τα λεία μυικά κύτταρα που δρα ως αντίβαρο της αποικοδόμησης του ενδοθηλιακού πλέγματος από της μεταλλοπρωτεινάσες. Σε αυτήν την περίπτωση αν ο ρυθμός παραγωγής κολλαγόνου ξεπερνά τον ρυθμό αποικοδόμησης του πλέγματος, αυτό μπορεί να οδηγήσει σε σταθεροποίηση της πλάκας ή παθολογική σκλήρυνση των αρτηριών (θετική αναδόμηση). (στ) Σταδιακή ανάπτυξη λιπιδικού νεκρωτικού πυρήνα που σχηματίζεται από λιπίδια πλούσια σε αφρώδη κύτταρα (foam cells) και ινώδους κολλαγονικού καλύμματος που σχηματίζεται από την αποικοδόμηση του πλεγμάτων των ενδοθηλιακών κυττάρων και τον ανασχηματισμό που προκαλείται από την δραστηριότητα των μακροφάγων και των λείων μυικών κυττάρων. Αν ο ρυθμός αποικοδόμησης του πλέγματος (MMP δράση) ξεπερνά την παραγωγή κολλαγόνου (SMCs δράση), το αποτέλεσμα είναι η σταδιακή αποικοδόμηση και η λέπτυνση του ινώδους καλύμματος της πλάκας. Σε προχωρημένες αθηροσκληρωτικές βλάβες, η δραστηριότητα των μεταλλοπρωτεϊνασών αυξάνεται και ιντερφερόνη γ (INF-γ) που παράγεται από Τ- λεμφοκύτταρα μειώνει την παραγωγή του κολλαγόνου, κάτι που οδηγεί στην λέπτυνση του ινώδους καλύμματος της πλάκας, μια κατάσταση που συνήθως ορίζεται ως ευάλωτες ή υψηλού κινδύνου αθηρωματικές πλάκες. Είναι σύνηθες φαινόμενο εξαιτίας άγχους και αιμοδυναμικών αλλαγών να δημιουργούνται ρήξεις σε τέτοιες υψηλού κινδύνου πλάκες προκαλώντας αιμορραγίες στην πλάκα και έκθεση του νεκρωτικού λιπιδικού πυρήνα και ιστικού παράγοντα στην κυκλοφορία του αίματος. Αυτό οδηγεί στην συγκέντρωση και ενεργοποίηση περισσότερων αιμοπεταλίων καθώς και πυροδότηση περαιτέρω πήξης του αίματος. Η συσσωμάτωση των αιμοπεταλίων μέσω του ινοδωγόνου και η πήξη που λαμβάνει χώρα λόγω της δράσης της θρομβίνης και του σχηματισμού ινικής κορυφώνονται σε θρόμβους αίματος στο αγγειακό τραύμα ή στο σημείο δημιουργίας ρήξης στην πλάκα. Τέτοια επεισόδια θρομβώσεων μπορούν να οδηγήσουν σε εμφρακτικά επεισόδια, και να 26
27 προκαλέσουν μείωση της ορθόδρομης ροής του αίματος, στένωση, ισχαιμία και σοβαρή ιστική νοσηρότητα και θνησιμότητα. Πρέπει να σημειωθεί εδώ ότι η δημιουργία θρόμβου είναι μια φυσιολογική διαδικασία, ένας φυσικός επουλωτικός μηχανισμός στην φυσιολογική αιμόσταση, κατάσταση στην οποία, μετά την δημιουργία θρόμβου και την επούλωση, λαμβάνει χώρα μηχανισμός αποικοδόμησης του θρόμβου και αποκαθίσταται η ομαλή ιστική δομή και λειτουργία. Παρόλα αυτά στις περιπτώσεις των αγγειακών ασθενειών, οι διαδικασίες που εμπεριέχουν τη δημιουργία θρόμβων γίνονται ανεξέλεγκτες, κάτι που οδηγεί τελικά σε αγγειακά εμφράγματα. Η Εικόνα 2 δείχνει με ένα απλό σχηματικό τρόπο των μηχανισμών τέτοιων διαδικασιών που συμβαίνουν στις αγγειακές παθήσεις. Lusis Libby et al Νανοσωματίδια και αγγειακές παθήσεις Έχοντας τώρα περιγράψει τους κυριότερους μηχανισμούς και διαδικασίες που λαμβάνουν χώρα σε αθηροσκληρωτικές, θρομβωτικές και στενωτικές αγγειακές παθολογικές καταστάσεις, μπορούμε να δούμε πως η χρήση νανοσωματιδίων έχει αποδειχτεί ευεργετική. Στρατηγικές θεραπευτικές, διαγνωστικές ή και τα δύο βασισμένες στη χρήση νανοσωματιδίων, έχουν χρησιμοποιηθεί σε τραυματισμό ενδοθηλίου, υπερδραστηριότητα αιμοπεταλίων, για διαδικασίες που επάγονται από τα μκροφάγα, για αναδόμηση του πλέγματα των ενδοθηλίων, παράγοντες συσσωμάτωσης και απορύθμιση μεταβολικών διεργασιών ως παράγοντες που στοχεύουν ειδικά συγκεκριμένες παθήσεις. Αυτοί οι στόχοι μπορούν να παρουσιαστούν σε διαφορετικά ποσοτικά επίπεδα ανάλογα με το στάδιο που λαμβάνει χώρα κάθε φορά κατά την εξέλιξη των αγγειακών παθήσεων γι αυτό και είναι πολύ σημαντικό οι στρατηγικές θεραπείας και διάγνωσης που εφαρμόζονται να είναι συσχετισμένες με την εκάστοτε φάση της διαδικασίας και να είναι εφαρμόσιμες σε μοριακό και κυτταρικό επίπεδο. Επιπρόσθετα, σε κλινικό στάδιο, είναι πολύ σημαντικό να μπορεί να πραγματοποιηθεί άμεση αφαίρεση εμφρακτικών θρόμβων καθώς και άμεση αποκατάσταση τις ροής του αίματος, διαδικασίες κρίσιμες για τη διατήρηση της λειτουργίας των ιστών και την υγεία του ασθενούς. Σε αυτό το πλαίσιο, οι πιο σημαντικές στρατηγικές είναι η αγγειοπλαστική (με η χωρίς τη χρήση Stents), η ενδο-αρτηριακή τομή (endarterectomy) και η μέθοδος bypass, οι οποίες συνήθως οδηγούν σε φλεγμονή και θρομβωτικά επεισόδια (επαναστένωση ή απόρριψη του εμφυτεύματος) που σχετίζονται με τη μέθοδο που ακολουθείται ή τα εμφυτεύματα που χρησιμοποιούνται. Σε τέτοιες περιπτώσεις εμπλέκονται πολλά από τα ίδια μοριακά/κυτταρικά συστατικά που σχετίζονται με τις αγγειακές παθήσεις (τραυματισμός ενδοθηλίου, ενεργοποιημένα αιμοπετάλια, μακροφάγα, κυτοκίνες κλπ). Γι 27
28 αυτό το λόγο, στρατηγικές που έχουν μοριακούς ή κυτταρικούς στόχους από την οπτική της νάνο-ιατρικής δεν χρησιμοποιούνται μόνο για τη θεραπεία τέτοιων αγγειακών παθήσεων αλλά μπορούν να χρησιμοποιηθούν και σαν εναλλακτικές προσεγγίσεις για να θεραπεύσουν ή να προλάβουν παρενέργειες ή επιπλοκές που συνήθως εμφανίζονται λόγω των μεθόδων και υλικών-συσκευών που χρησιμοποιούνται. Ένα πολύ καλό παράδειγμα είναι η ενδοφλέβια χορήγηση αντιθρομβωτικών φαρμάκων όπως η ηπαρίνη, για την άμεση διάλυση θρόμβων και απόφραξη αιμοφόρων αγγείων. Όταν η τελευταία χορηγείται ενδοφλεβίως ή από τη στοματική οδό, παρουσιάζει σοβαρές παρενέργειες όπως συστηματική διαταραχή της αιμόστασης και αιμορραγία. Ινοδωλιτικά φάρμακα όπως διάφορες κινάσες (πχ. Στρεπτοκινάση) και ο ενεργοποιητής/επαγωγέας του ιστικού πλασμινογόνου (tpa), όταν χορηγούνται ενδοφλέβια ή ενδοαρτηριακά, υπόκεινται σε γρήγορη και εκτεταμένη απενεργοποίηση από το πλάσμα του αίματος και αποτυγχάνουν στο να φτάσουν τα επιθυμητά θεραπευτικά επίπεδα για εύλογα χρονικά διαστήματα στο σημείο όπου υπάρχει ο θρόμβος εξαιτίας της συνεχούς συστηματικής κυκλοφορίας και του αιμοδυναμικού περιβάλλοντος. Η συστηματική κατανομή αυτών των φαρμάκων επίσης οδηγεί σε ανεπιθύμητες ενέργειες όπως προβλήματα πήξης του αίματος. Για να μπορέσει να επιλυθεί αυτό το ζήτημα, έχουν γίνει πολύ σημαντικές ερευνητικές προσπάθειες και η έρευνα έχει μετατοπιστεί προς την κατεύθυνση της τοπικής και στοχευμένης μεταφοράς φαρμάκων με στόχος την βελτίωση του δείκτη και του χρόνου παραμονής του φαρμάκου στο σημείο ενδιαφέροντος για ένα συνολικά καλύτερο φαρμακολογικό αποτέλεσμα. Προς αυτήν την κατεύθυνση, έχει σημειωθεί σημαντική έρευνα σε σχέση με την δημιουργία συσκευών που θα εμφυτεύονται όντας φορτωμένες με την κατάλληλη ποσότητα φαρμάκου/ων όπως εξωχιτώνια εμφυτεύματα παρατεταμένης αποδέσμευσης φαρμάκου, καθετήρες τοπικής έγχυσης μέθοδοι παρατεταμένης αποδέσμευσης με επικαλύψεις (coating) και ενδοπρόσθετα με δυνατότητα απελευθέρωσης φαρμάκου (DES, Drug Eluting Stents) [52-54]. Μια εναλλακτική στρατηγική για αποδέσμευση φαρμάκων σε εξακριβωμένο σημείοστόχο είναι η χρήση διαφόρων θεραπευτικών και διαγνωστικών παραγόντων, που έχουν υποστεί σύζευξη με προσδέτες και αντισώματα τα οποία στοχεύουν και προσδένονται εκλεκτικά σε κυτταρικούς/μοριακούς στόχους σχετιζόμενους με τις αγγειακές παθήσεις [55]. Άλλη μια προσέγγιση είναι η εφαρμογή τεχνικών γενετικής μηχανικής για την Παρασκευή φαρμάκων τα οποία έχουν ενισχυμένη συγγένεια με μόρια που σχετίζονται με σημεία στα οποία εντοπίζονται θρόμβοι σε σχέση με τα ίδια μόρια που συναντώνται στην συστηματική κυκλοφορία, και που η αλληλεπίδραση με αυτά οδηγεί σε ανεπιθύμητες 28
29 ενέργειες/παρενέργειες. Ένα πολύ χαρακτηριστικό παράδειγμα είναι μια ανασυνδιασμένη μορφή του tpa η οποία παρουσιάζει μεγαλύτερη συγγένεια για την ινική που σχετίζεται με κάποιο θρόμβο από την ινική που θα συναντούσε φυσιολογικά κατά την συστηματική κυκλοφορία. Αυτού του είδους οι στρατηγικές έχουν αποδειχτεί στην πράξη πιο αποτελεσματικές με βελτιωμένο θεραπευτικό εύρος σε σχέση με τις κλασσικές φαρμακευτικές αγωγές. Παρόλα αυτά όμως σε πολλές περιπτώσεις δεν έχει ακόμα βελτιστοποιηθεί η συγκράτηση της απαραίτητης συγκέντρωσης του φαρμάκου για το επιθυμητό χρονικό διάστημα ώστε να μιλάμε για σταθερή απόδοση κατά τη διάρκεια του χρόνου. Μια προσέγγιση ώστε να επιτευχθεί η μέγιστη θεραπευτική συγκέντρωση με το βέλτιστο θεραπευτικό αποτέλεσμα είναι με τη χρήση νανοσωματιδίων είναι ή εφαρμογή τεχνικών εμβιομηχανικής για να επιτευχθούν οι παρακάτω στόχοι: (α) Διατήρηση της σταθερής κυκλοφορίας στο αίμα και αύξηση του χρόνου ημιζωής του εγκλωβισμένου στα νανοσωματίδια φαρμάκου. (β) Στόχευση/σύνδεση με συγκεκριμένα συστατικά που εμφανίζονται ή υπερεκφράζονται κατά την ανάπτυξη των αγγειακών παθήσεων με τη βοήθεια συγκεκριμένων βιομοριακών αλληλεπιδράσεων. Σε αυτή την περίπτωση ο στόχος είναι είτε η διατήρηση της σταθερότητας κάτω από ένα αιμοδυναμικό περιβάλλον ροής αίματος (πχ. πάνω στα ενδοθηλιακά κύτταρα ή σε διάφορες πρωτεΐνες υπό-ενδοθηλιακά), ή η εκλεκτική απορρόφηση ή αλληλεπίδραση με μηχανισμούς που σχετίζονται με τις αγγειακές παθήσεις (πχ. τα μακροφάγα). (γ) Η εκλεκτική μεταφορά και απελευθέρωση της εγκλωβισμένης ουσίας/φαρμάκου με τρόπο ελεγχόμενο και επαγώμενο από κάποιο ερέθισμα που θα καθορίζει και την κινητική απελευθέρωσης. (δ) Χρήση βιοδιασπώμενων ή βιοαπορροφήσημων φορέων από το σώμα σε συγκεκριμένο χρονικό περιθώριο που θα εγγυάται την ασφάλεια χορήγησης και χρήσης. Γι αυτό το σκοπό έχουν δημοσιευτεί πάρα πολλά άρθρα και ανασκοπήσεις σε σχέση με διαφόρων ειδών νανοσωματίδια και έχει μελετηθεί η μεταφορά και απελευθέρωση θεραπευτικών και διαγνωστικών παραγόντων μέσω αυτών, για την αντιμετώπιση αγγειακών παθήσεων [55-60] Εφαρμογές και προκλήσεις στις αγγειακές παθήσεις 29 Η έλευση της Νανοτεχνολογίας και η εξέλιξή της τα τελευταία χρόνια έχει επιφέρει επαναστατικές και ρηξικέλευθες αλλαγές στις στρατηγικές που χρησιμοποιούνται για τη
30 διάγνωση και θεραπεία πλήθους ασθενειών, συμπεριλαμβανομένων και των αγγειακών παθήσεων. Η Νάνο-ιατρική προσέγγιση κατασκευής βιοσυμβατών ( και σε πολλές περιπτώσεις βιοαποικοδομήσιμων) νανοσωματιδίων, εγκλωβίζοντας το φάρμακο ή τον απεικονιστικό/διαγνωστικό παράγοντα μέσα στο σωματίδιο, και τροποποιώντας τις επιφανειακές ιδιότητες του σωματιδίου με επικαλύψεις που οδηγούν σε in vivo δομική σταθερότητα αλλά και μεγαλύτερη συγγένεια και εξειδίκευση προς τα μόρια/προσδέτες στόχους. Παράλληλα οδηγεί σε έλεγχο του απαιτούμενου χρόνου παραμονής του παράγοντα στο σημείο-στόχο (πχ. με τη χρήση PEG). Μπορεί να γίνει περαιτέρω τροποποίηση της επιφάνειας των σωματιδίων με προσδέτες για εκλεκτική στόχευση κυτταρικών ή μοριακών στοιχείων που σχετίζονται με τις παθήσεις. Κάτι τέτοιο έχει μελετηθεί εκτενώς με τη χρήση ποικιλίας σωματιδίων, επικαλύψεων με ενθαρρυντικά αποτελέσματα. Επιπλέον τροποποιήσεις ή βελτιώσεις προς αυτήν την κατεύθυνση στοχεύουν κυρίως στο να καλυτερεύσουν το ίδιο το σχέδιο των νανοσωματιδίων, ή να εμπερικλείουν και θεραπευτικούς και διαγνωστικούς και απεικονιστικούς παράγοντες σε ένα νανοσωματίδιο (Multi-modal/multi-functional nanoparticles) ώστε να υπάρχει η δυνατότητα για ταυτόχρονη διάγνωση και θεραπεία, ή για θεραπεία απευθείας οδηγούμενη μέσω ζωντανής απεικόνισης, ή αξιολόγηση της θεραπείας μέσω απεικόνισης ανίχνευσης μετά το στάδιο της αντιμετώπισης. Τέτοιου είδους προσεγγίσεις θα συμβάλουν σημαντικά προς την κατεύθυνση της εξατομικευμένης θεραπείας μέσω του πυλώνα της Νανοτεχνολογίας. Κρίσιμα δομικά και λειτουργικά χαρακτηριστικά των νανοσωματιδίων καθώς και η χώρο/χρονική συμπεριφορά των στόχων τους στα αγγεία είναι πολύ σημαντικά στοιχεία όταν σχεδιάζεται η θεραπευτική προσέγγιση που θα ακολουθηθεί καθώς κι η στρατηγική σύνθεσής τους και η κλινική εφαρμογή. Στην περίπτωση των σωματιδιακών δομών, η σύσταση, ή η δομή και η λειτουργική ευελιξία δεν πρέπει να θεωρούνται πιο σημαντικά χαρακτηριστικά από την ευκολία μεθόδου και χειρισμού, την ικανότητα και ασφάλεια αποθήκευσης, της ικανότητα scale-up της διαδικασίας, και τέλος, το κόστος παραγωγής και την ποιότητα του προϊόντος. Σε διαφορετική περίπτωση είναι πιθανό μια εφαρμογή που στο εργαστήριο και σε μικρή κλίμακα να έχει θεαματικά αποτελέσματα in vitro και in vivo άλλα όταν περάσει στην παραγωγή να μην μπορεί να εφαρμοστεί σε μεγάλη κλίμακα, να συναντήσει εμπόδια και να είναι πολύ απαιτητική για την εφαρμογή της, να έχει μεγάλο κόστος και τελικά να απορριφτεί, μην έχοντας τη δυνατότητα να φτάσει ποτέ σε κλινική χρήση και στους ασθενείς. Από την άλλη πλευρά, η έμφαση μόνο στο να είναι η εφαρμογή αποδεκτή και αποδοτική για την φαρμακευτική βιομηχανία δεν πρέπει να οδηγήσει το προϊόν στο να γίνει λειτουργικά υποδεέστερο. Λεπτομερής ανάλυση και βελτιστοποίηση των παραμέτρων 30
31 σχεδιασμού, και των λειτουργικών ιδιοτήτων καθώς και πως αυτές μεταφράζονται κατά τη χορήγηση στον στόχο πρέπει να είναι ένα από τα κύρια μελήματα κατά τον αρχικό σχεδιασμό των στρατηγικών θεραπείας και διάγνωσης που εφαρμόζει η Νάνο-ιατρική. Ανάμεσα στις διάφορες νανοδομές, οι πιο απλές για μεταφορά θεραπευτικών παραγόντων είναι τα λιποσώματα, τα μικκύλια και οι πολυμερικές δομές, μιας και είναι πιο απλά στην σύνθεσή τους αφού μπορούν να δημιουργηθούν μόνα τους (self-assemply) είτε λόγω διαχωρισμού φάσεων όπως στο nano-precipitation. Από την άλλη, τέτοιες απλοϊκές δομές μπορούν να παρέχουν μόνο περιορισμένες επιλογές για τον εγκλωβισμό φαρμάκων, επιφανειακή τροποποίηση. Όσον αφορά τις πολυμερικές δομές, είναι ιδιαιτέρως σημαντικό να δοθεί σημασία στη φύση του πολυμερούς, τη συγκέντρωση καθώς και το αν παίζουν ρόλο και ποιος είναι αυτός, τυχόν σταθεροποιητικές ουσίες που χρησιμοποιούνται για να κρατούν σταθερές τις πολυμερικές δομές σε υδατικό περιβάλλον. Πολλές φορές τέτοιες ουσίες επηρεάζουν σε πολύ μεγάλο βαθμό την σταθερότητα και την κατανομή του μεγέθους των πολυμερικών σωματιδίων. Ακόμα, όπως είναι αναμενόμενο, τέτοιες ουσίες πρέπει να μην επιφέρουν αρνητικές βιολογικές αντιδράσεις. Στην περίπτωση των μοριακών ή κυτταρικών στόχων, είναι πάρα πολύ σημαντικό να αντιληφθεί κανείς ότι η ταυτοποίηση των στόχων όχι μόνο στατικά αλλά και σε μια χώροχρονική βάση όπου αυτά εμφανίζονται στις αγγειακές παθήσεις είναι απαραίτητη. Παρόλα αυτά, ακόμα και αυτή σε ορισμένες περιπτώσεις κρίνεται ανεπαρκής αν δεν βρίσκονται σε ανιχνεύσιμες ποσότητες. Στόχοι που εκφράζονται σε μικρό ή οριακά ανιχνεύσιμο βαθμό μπορούν να φανούν χρήσιμοι σε εφαρμογές υψηλής ευαισθησίας για μοριακή απεικόνιση, όπως για παράδειγμα, για ραδιοεπισήμανση, όπου χρειάζεται μια ελάχιστη ποσότητα στα όρια του ανιχνεύσιμο για να μπορέσει να δώσει σήμα. Από την άλλη οι ίδιοι στόχοι μπορεί να αποδειχθούν μη εκλεκτικοί να μην πετυχαίνουν επιθυμητές συγκεντρώσεις για εκλεκτική αποδέσμευση φαρμάκου ή απεικόνιση μέσω μαγνητικής τομογραφίας όταν είναι απαραίτητη η υψηλή συγκέντρωση των στόχων για να ανιχνευτεί σήμα in vivo. Μια άλλη παράμετρος που επίσης πρέπει να ληφθεί υπόψη είναι το που βρίσκεται ο στόχος όπου επιθυμούμε να γίνει η εκλεκτική μεταφορά και αποδέσμευση του φαρμάκου. Υπάρχουν σημαντικές διαφορές στον όλο σχεδιασμό και στη στρατηγική που ακολουθείται όταν για παράδειγμα τα νανοσωματίδια προορίζονται για την αντιμετώπιση κάποια μορφής καρκίνου και διαφορετική για την αντιμετώπιση αγγειακών παθήσεων. Στην δεύτερη περίπτωση πρέπει κανείς να λάβει υπόψη ότι, τα νανοσωματίδια ή γενικά ο φορέας που θα επιλεγεί υπόκεινται σε διάφορες δυνάμεις ευρισκόμενος σε ένα αιμοδυναμικό περιβάλλον κατά την κυκλοφορία του αίματος και για να μπορεί να είναι εκλεκτικός ως προς την περιοχή 31
32 που είναι επιθυμητό να δράσει αλλά και για εύλογο χρονικό διάστημα, πρέπει να έχει γίνει η κατάλληλη προεργασία και μελέτη κατά την επιλογή του, σύνθεση και τροποποίηση του ώστε να έχει τη βέλτιστη και αναμενόμενη συμπεριφορά σε ένα περιβάλλον δυναμικής ροής αίματος. Σε αντίθετη περίπτωση, η μεταφορά φαρμάκων μέσω σωματιδίων είναι πιθανό να υποστεί τους ίδιους περιορισμούς όπως το φαινόμενο του rapid wash-out ή της πρώτης διάβασης από το ήπαρ που οδηγεί σε εκτεταμένο μεταβολισμό του φαρμάκου, με τα συμβατικά συστήματα μεταφοράς φαρμάκων. Η σταθερότητα όσο αναφορά την σύνδεσή με τους στόχους είναι πάρα πολύ σημαντικός παράγοντας για την εξασφάλιση του βέλτιστου χρόνου παραμονής, άρα και της επιθυμητής απελευθέρωσης του φαρμάκου στο σημείο ενδιαφέροντος από τα νανοσωματίδια που επιτελούν το ρόλο των φορέων του φαρμάκου. Κάτι τέτοιο προϋποθέτει την μελέτη και τον υπολογισμό όλων των παραμέτρων που σχετίζονται με τους μοριακούς/κυτταρικούς στόχους και ποσοτικά αλλά και ποιοτικά. Σε περίπτωση που είναι αυξημένη η επιφάνεια για αλληλεπιδράσεις με προσδέτες ή υποδοχείς χρησιμοποιώντας ανισοτροπικές γεωμετρίες ή επιτρέποντας την ταυτόχρονη συγγένεια προς πολλαπλά υποστρώματα τα νανοσωματίδια μπορούν να αποκτήσουν πολύ-λειτουργικές ιδιότητες. Εκτός από τις παραμέτρους που αφορούν το σχεδιασμό και τη σύνθεση των σωματιδίων και των πιθανών στόχων τους, πρέπει να δοθεί ιδιαίτερη σημασία και στις φαρμακοκινητικές ιδιότητες καθώς και στον μηχανισμό απελευθέρωσης του φαρμάκου καθώς και στο επακόλουθο θεραπευτικό αποτέλεσμα. Για παράδειγμα τα λιποσώματα είναι γνωστά για την ευελιξία τους σε σχέση με την ικανότητα εγκλωβισμού και υδροφοβικών (σε λιποσωμική μεμβράνη) και υδροφιλικών (σε λιποσωμικό πυρήνα) φαρμάκων, αλλά υπολογισμοί βασισμένοι σε γεωμετρικές παραμέτρους δείχνουν ότι η πραγματική τάξη μεγέθους για έναν τέτοιο εγκλωβισμό είναι πολύ μικρή. Γι αυτό το λόγο είναι πολύ σημαντικό να μπορεί να αναλυθεί εάν η ποσότητα του φαρμάκου που μπορεί να μεταφερθεί μέσω ενός λιποσωμικού φορέα ή γενικά είναι αρκετή ώστε να παρατηρείται θεραπευτικό αποτέλεσμα. Ακόμα μια παράμετρος προς αποσαφήνιση είναι ο καθορισμός του εύρους των αληθινών συγκεντρώσεων όταν σε έναν φορέα υπάρχουν περισσότερα του ενός φάρμακα ή άλλα μόρια, για παράδειγμα για ανίχνευση και αν η παρουσία του ενός επηρεάζει το άλλο και πως. Παραδείγματος χάρη στις εφαρμογές όπου υπάρχει και διαγνωστικός και θεραπευτικός παράγοντας στον ίδιο φορέα είναι πολύ σημαντικό να καθοριστεί το εύρος των απαιτούμενων ή αποδεχτών συγκεντρώσεων και για τα δύο, πολύ περισσότερο μάλιστα αν οι συγκεντρώσεις των ουσιών που εγκλωβίζονται στο νανοσωματίδιο επηρεάζουν το μέγεθος και το σχήμα του 32
33 φορέα. Η στρατηγική σχεδιασμού και βελτίωσης της τεχνικής σύνθεσης ενός φορέα στον οποίο ο θεραπευτικός παράγοντας θα είναι στον πυρήνα του σωματιδίου και ο διαγνωστικός παράγοντας στην επιφάνεια είναι εντελώς διαφορετική από κάποια στην οποία και οι δύο παράγοντες είναι στον πυρήνα ή στην εξωτερική επιφάνεια των σωματιδίων. Γι αυτό το λόγο μαζί με τα δομικά και λειτουργικά χαρακτηριστικά των νανοσωματιδίων που λαμβάνονται υπόψη για την εφαρμογή σε στόχους στη θεραπεία των αγγειακών παθήσεων είναι επίσης σημαντικός ο καθορισμός της θέσης, της ικανότητας εγκλωβισμού και της χωρητικότητας των διαφόρων φορέων. Ιδιαίτερη προσοχή θα πρέπει επίσης να δοθεί το μηχανισμό της απελευθέρωσης και της δράσεως του φαρμάκου. Για παράδειγμα, για μία μέθοδο απεικόνισης, ενδοπλακική ή ενδοκυτταρική πρόσληψη του φορέα με τα φορτωμένα ΝΡs μπορεί από μόνα τους να είναι επαρκής για να παρέχει εκλεκτικότητα και ενίσχυσης της αντίθεσης του διαγνωστικού σήματος, αλλά για ένα ινωδολυτικό παράγοντα, το φάρμακο πρέπει να απελευθερώνεται εξωκυτταρικά με ταχύ ρυθμό για γρήγορη επιλεκτική αποικοδόμηση ινώδους και διάλυσης θρόμβου. Ως εκ τούτου, εάν ένα ινωδολυτικό φορτωμένο με φάρμακο ΝΡ υφίσταται ενδοκυττάρωση κάπως ενώ αλληλεπιδρά και να συνδέεται με ειδικά κύτταρα για αγγειακή νόσο, ή, εάν το φάρμακο παραμένει συνδεδεμένο / συζευγμένο με τον φορέα και δεν έχει απελευθερωθεί στη θέση-στόχο για θεραπευτική δράση, το πραγματικό θεραπευτικό όφελος αυτών των νανοδομών μπορεί να μειωθεί. Η τοξικότητα των διαφόρων νανοδομών είναι επίσης ένας σημαντικός παράγοντας στον καθορισμό της μεταφοράς της εφαρμογής από το εργαστήριο στην κλινική πράξη. Επειδή οι περισσότερες από τις αναφερθείσες εφαρμογές των NPs στον κόσμο του φαρμάκου είναι αρκετά πρόσφατες, η in vivo κατανομή και το προφίλ τοξικότητας είναι ακόμα μόνο εν μέρει κατανοητά επί του παρόντος, ειδικά όσον αφορά την περίπτωση των μηχανισμών που λαμβάνουν χώρα. Είναι πολύ συχνό φαινόμενο να οι επιστήμονες να έρχονται αντιμέτωποι με αντικρουόμενες απόψεις σχετικά με την in vitro ή in vivo τοξικότητα του ίδιου ή παρόμοιου φορέα. Για παράδειγμα, αν και οι Κβαντικές τελείες (QD) έχουν επιδείξει εξαιρετικές τροποποιήσιμες οπτικές ιδιότητες για διαγνωστικούς σκοπούς και μοριακή απεικόνιση, αλλά και τη δυναμική για εφαρμογές που βασίζονται πάνω σε φωτοευαίσθητες ιδιότητες, τα προφίλ τοξικότητας και η κατανομή των QD είναι ακόμα ένα θέμα συζήτησης. Η μεταβλητότητα και οι αντικρουόμενες πληροφορίες αλλά και εξηγήσεις για τους μηχανισμούς δράσης όσον αφορά την in vivo συμπεριφορά των διαφόρων NPs πρέπει να επιλυθεί οριστικά ώστε να μπορέσουν να εγκαθιδρυθούν ως υποσχόμενη επιλογή για κλινικές εφαρμογές. 33
34 1.5. Άλλες εφαρμογές των Νανοσωματιδίων από PLGA Το πολύ-(γαλακτικό-συν-γλυκολικό οξύ), έχει διερευνηθεί για την παροχή φαρμάκων για φαρμακευτικές και βιοϊατρικές εφαρμογές για μία ποικιλία άλλων ασθενειών, όπως ο διαβήτης, ο πόνος, η αρθρίτιδα, νόσοι του εντέρου και απεικόνισης του εγκεφάλου, λόγω της βιοαποικοδόμησης και της βιοκατανομής του, όπως περιγράφηκε προηγουμένως. Πολλές μελέτες επικεντρώθηκαν στη χρήση των PLGA NPs για μεταφορά και απελευθέρωση φαρμάκου εκλεκτικά για ασθένειες στα μοντέλα πειραματόζωων με στοματική χορήγηση ή έγχυση. Μια τέτοια στρατηγική της τοπικής παροχής φαρμάκου θα είναι μια σημαντική βελτίωση σε σχέση με τις υπάρχουσες συσκευές παροχής για αυτές τις ασθένειες. Ο διαβήτης αναπτύσσεται λόγω μειωμένης ή σχεδόν μηδαμινής παραγωγής ινσουλίνης. Μελέτες διερεύνησαν την παρασκευή PLGA NPs και PLGA-ΗΡ55 NPs σαν δυνητικούς φορείς φαρμάκου για στοματική χορήγηση ινσουλίνης με μια τροποποιημένη emulsification diffusion μέθοδο διάχυσης σε ύδωρ. Τα φυσικοχημικά χαρακτηριστικά τους, η απελευθέρωση του φαρμάκου in vitro και τα αποτελέσματα σε διαβητικούς αρουραίους αξιολογήθηκαν [61,62]. Η σταθερότητα της ινσουλίνης κατά τη διάρκεια του μικροεγκλωβισμού και η επακόλουθη απελευθέρωση είναι απαραίτητη για τη διατήρηση της βιολογικής δραστικότητας. Μία νέα s / o / w άνυδρη μέθοδο ενθυλάκωσης αναπτύχθηκε με ένα συνδυασμό σταθεροποιητών για την διατήρηση της ακεραιότητας της ινσουλίνης κατά τη διάρκεια της συνθέσεως και της απελευθέρωσης [63]. Η λιποδιαλυτότητα της ινσουλίνης είναι μια άλλη παράμετρος κατά την προετοιμασία των φορτωμένα με ινσουλίνη PLGA νανοσωματιδίων. Έχει παρασκευαστεί ινσουλίνη με σύμπλοκο φωσφολιπιδίου φορτωμένα σε NPs με μια νέα αντίστροφη μικυλλίου-μέθοδο εξάτμισης διαλύτη, όπου χρησιμοποιήθηκε φωσφατιδυλοχολίνη σόγιας για να βελτιώσει την λιποδιαλυτότητα της ινσουλίνης [64]. Αρκετές μελέτες οδηγούν στο συμπέρασμα ότι οι τροποποιημένα νανοσωματίδια από PLGA, με ανάμιξη με άλλα πολυμερή, έδειξαν βελτιωμένα ή ενισχυμένα χαρακτηριστικά και επιθυμητές φυσιολογικές ιδιότητες. Για παράδειγμα, μία απλή και ευέλικτη πλατφόρμα παροχής πεπτιδίων και πρωτεϊνών βασίζεται σε φυσικά διασταυρωμένες υδρογέλες PVA που περιέχουν PLGA NPs φορτωμένα με ινσουλίνη. Όταν τα PLGA NPs φορτωμένα με ινσουλίνη χορηγήθηκαν ενδοπεριτοναϊκά ως εφάπαξ δόση (20 U / kg) προς σε διαβητικών με στρεπτοζοτοκίνη επαγόμενα ποντίκια, τα επίπεδα γλυκόζης στο αίμα αυτών των ποντικών μειώθηκαν και το αποτέλεσμα διατηρήθηκε πάνω από 24 ώρες. In vitro μελέτες προτείνουν ότι τα PLGA NPs παγιδευμένα εντός των PVA υδρο-πηκτών έδειξαν καταλληλότερη κινητική ελεγχόμενης απελευθέρωσης για παράδοση πρωτεΐνης και προκάλεσαν μια μείωση 34
35 τόσο του ρυθμού απελευθέρωσης, όσο και του συνολικού ποσού της ινσουλίνης που απελευθερώνεται [62]. Τα πολύ-(γαλακτικό-συν-γλυκολικό οξύ) NPs είναι από τα πιο καινοτόμα σε μηεπεμβατικές προσεγγίσεις για την παράδοση φαρμάκων στο ΚΝΣ. Τροποποιημένα PLGA νανοσωματίδια μπορούν να διασχίσουν τον φραγμό αίματος-εγκεφάλου και να μεταφέρουν τα φάρμακα που ασκούν την φαρμακολογική τους δράση στο ΚΝΣ [65-67]. Σε μία από τις πρόσφατες μελέτες σε ζώα, PLGA αναμείχθηκαν με το πεπτίδιο g7 (g7-nps) φορτώθηκαν με λοπεραμίδη και με μια φθορίζουσα χρωστική, Ροδαμίνη-123 [65]. Τα αποτελέσματα έδειξαν ότι η g7-nps είναι σε θέση να διασχίσει το αιματοεγκεφαλικό φραγμό, εξασφαλίζοντας μια παρατεταμένη απελευθέρωση του ενσωματωμένου φαρμάκου, και ότι τα νανοσωματίδια είναι σε θέση να φθάσουν όλες τις περιοχές του εγκεφάλου που εξετάστηκαν. Η ικανότητα να εισέρχονται στο ΚΝΣ φαίνεται να συνδέεται με την αλληλουχία του πεπτιδικών αλληλουχιών που υπάρχουν στην επιφάνειά τους. Σε μια άλλη μελέτη, η ροδαμίνη-123 είχε μόνο ενθυλακωθεί σε PLGA NPs για να εξετάσει την βιοκατανομή των φαρμάκων που μεταφέρονται στις εντοπισμένες σαν στόχους τοποθεσίες στον κοχλία, το ήπαρ και τους νεφρούς των χοίρων [68]. Η παροχή φαρμάκου στον κοχλία είναι δύσκολη λόγω της περιορισμένης ροής αίματος προς τον κοχλία και τον αιματοεγκεφαλικό φραγμό στον λαβύρινθο, ο οποίος περιορίζει τη μεταφορά των μορίων από το αίμα προς τον κοχλία. Τα NPs με ροδαμίνη, χορηγούμενα με ενδοφλέβια ένεση εντοπίστηκαν στον κοχλία μετά από συστηματική ή τοπική εφαρμογή, γεγονός που υποδηλώνει ότι τα PLGA NPs έχουν πιθανή χρήση στη χορήγηση φαρμάκων στον κοχλία. Η μεταφορά των PLGA NPs διαμέσου της μεμβράνης στρογγυλού-παραθύρου στο περιλέμφιο δείχνει την αποτελεσματικότητα της ενθυλάκωσης φαρμάκων σε PLGA NPs ως μια στρατηγική για παρατεταμένη και εκλεκτική χορήγηση φαρμάκων στον κοχλία [68]. Τα PLGA NPs χρησιμοποιούνται επίσης ως φορείς φαρμάκων για την θεραπευτική αγωγή των ασθενειών φλεγμονής, όπως η αρθρίτιδα και η νόσος του εντέρου, στα μοντέλα πειραματόζωων. Σε αρκετές άλλες μελέτες χρησιμοποιούνται PLGA NPs για να μεταφέρουν την βιταμίνη Ε ή αντιοξειδωτικά ένζυμα, όπως η υπερ-οξείδιο δισμουτάση και το συνένζυμο Q10, στις επιθυμητές θέσεις [69-71]. Τα PLGA NPs έχουν μεγάλες περιοχές επιφάνειας και λειτουργικές ομάδες για σύζευξη με πολλαπλούς διαγνωστικούς (πχ., οπτικούς, ραδιοϊσοτοπικούς ή μαγνητικούς) παράγοντες. Σωματίδια PLGA εμφυτεύθηκαν σε ασθενείς με καρκίνο για την έγκαιρη ανίχνευση του καρκίνου. Νανοτεχνολογκές εφαρμογές του PLGA έχει χρησιμοποιηθεί ευρέως στη διάγνωση και θεραπεία του καρκίνου. 35
36 ΚΕΦΑΛΑΙΟ 2. Τεχνικές Σύνθεσης Νανοσωματιδίων Nanoprecipitation Εισαγωγή Η μετατροπή των υλικών σε νανοσωματιδιακά συστήματα είναι εξίσου σημαντική όσο και η σύνθεση λειτουργικών πολυμερών σε ατομική κλίμακα. Για παράδειγμα, τα πολυμερή μπορούν να παρασκευαστούν απ 'ευθείας στη νανοκλίμακα όπως συνήθως εφαρμόζεται σε διαδικασίες πολυμερισμού γαλακτωμάτων [72]. Ωστόσο, ο καθαρισμός των νανοσφαιρών από τα μονομερή, τα ολιγομερή, και τα υπολείμματα αντιδραστηρίων όπως εκκινητές, και τασιενεργές ουσίες είναι ένα δύσκολο έργο, και το ίδιο ισχύει και τον έλεγχο των μοριακών ιδιοτήτων των πολυμερών. Μια εναλλακτική προσέγγιση για το σχηματισμό των νανοσωματιδίων είναι η αυτό-συναρμολόγηση (self-assembly) των πολυμερών υλικών σε αντικείμενα στη νανοκλίμακα. Ένα τυπικό παράδειγμα είναι η διάλυση των αμφίφιλων μπλοκ- συμπολυμερών σε ένα μπλοκ-εκλεκτικό διαλύτη με επακόλουθη σταθεροποίηση των μυκκιλιακών συστημάτων με ομοιοπολικές αλληλεπιδράσεις [73]. Η ύπαρξη μεγάλης ποικιλίας στα συμπολυμερή επιτρέπει τον έλεγχο του μεγέθους, του σχήματος, τη λειτουργία στόχευσης και την ικανότητα καψυλιώσεως των πολυμερικών μυκκιλίων,νανοσωματιδίων κλπ. Εφαρμόζοντας την τεχνική της εξάτμισης του διαλύτη του γαλακτώματος, το παρασκεύασμα δεν περιορίζεται μόνο σε αμφίφιλα πολυμερή, αλλά μπορεί επίσης να αποτελείται από εντελώς υδρόφοβα πολυμερή [74]. Ωστόσο, τα γαλακτώματα αυτά πρέπει να ομογενοποιούνται συνεχώς, κάτι το οποίο είναι μόνον εφικτό με τη χρήση τασιενεργών ουσιών και συσκευών με υψηλές απαιτήσεις ενέργειας όπως συσκευές υπερήχων ή ομογενοποιητες. Ως εκ τούτου, η τεχνική του nanoprecipitation αντιπροσωπεύει μια πιο εύκολη, λιγότερο απαιτητική, με κατανάλωση λιγότερης ενέργειας, καθώς και ευρέως εφαρμόσιμη τεχνική χωρίς πρόσθετα για την παρασκευή νανοσωματιδίων και με καλά καθορισμένες ιδιότητες. Ο σχηματισμός βασίζεται στην διεπιφανειακή εναπόθεση λόγω της μετατόπισης μιας διαλυτής ουσίας έναντι μιας μη-διαλυτής [75]. Δύο διαφορετικές τεχνικές παρασκευής νανοσωματιδίων μπορούν να εφαρμοστούν για τον σχηματισμό των νανοσωματιδίων από πολυμερή μέσω nanoprecipitation, είτε με την τεχνική της διάλυσης είτε με την τεχνική της εξάτμισης Εικόνα 3. Βασικές προϋποθέσεις είναι η αναμιξιμότητα των διαλυτών και η ύπαρξη αραιών πολυμερικών διαλυμάτων. Αν και είναι μια εύκολη και επαναλήψιμη τεχνική, η εφαρμογή 36
37 του nanoprecipitation έχει περιοριστεί μέχρι τώρα στην παρασκευή νανοσωματιδίων από PLA και PLGA για μελέτες εγκλωβισμού φαρμάκων [76]. Μόνο πολύ λίγες μελέτες περιγράφουν το σχηματισμό πολυμερικών νανοσωματιδίων μέσω της τεχνικής του nanoprecipitation από άλλα πολυμερή όπως προϊόντα πολυσακχαριτών [77] Γενική Περιγραφή της Μεθόδου Η τεχνική του Nanoprecipitation είναι μία εύκολη, ήπια, και χαμηλής ενέργειας διεργασία για την παρασκευή πολυμερικών νανοσωματίδίων. Επί του παρόντος, όπως αναφέρθηκε ήδη η κύρια εστίαση της έρευνας βασισμένη στα πολυμερή για την εφαρμογή του nanoprecipitation καθορίζεται με πολύ (γαλακτικό οξύ) (PLA) και τα συμπολυμερή αυτού, πολύ (γαλακτικό-συν-γλυκολικό οξύ) (PLGA). Επιπλέον, σε συνδυασμό με υψηλής απόδοσης συσκευές όπως μικρορευστομηχανικών, ρομπότ σιφωνισμού, εκτυπωτές inkjet, και αυτοματοποιημένων αναλυτικών οργάνων, οι ικανότητες του nanoprecipitation μπορούν να διευρυνθούν με παρά πολύ σημαντικές επιπτώσεις για νέες εφαρμογές. Είναι γνωστό ότι τα νανοσωματίδια μπορούν να κατέχουν εξαιρετικά, συχνά τροποποιήσιμα χαρακτηριστικά, πολύ διαφορετικά από το ίδιο υλικό όταν βρίσκεται σε bulk μορφή [72-77]. Ως εκ τούτου, υπάρχει μια τεράστια ζήτηση αυτή τη στιγμή στην ερευνητική και βιομηχανική κοινότητα για tailormade λειτουργικά συστήματα νανοσωματιδίων. Ουσιαστικά, οι διάφορες τεχνικές παρασκευής νανοσωματιδίων μπορούν να ταξινομηθούν σε δύο γενικές κατηγορίες. Η πρώτη κατηγορία περιλαμβάνει την in situ σύνθεση των νανοσωματιδίων, ξεκινώντας από τη διάλυση μικρών πρόδρομων ουσιών σε επίπεδο μορίου (πχ. προετοιμασία νανοσωματιδίων χρυσού, τεχνικές πολυμερισμού γαλακτώματος). Στη δεύτερη κατηγορία, η διαμόρφωση του bulk υλικού σε νανοδομές (πχ. nanoprecipitation, γαλάκτωμα / διαλύτη τεχνική διάχυσης, ξήρανση με ψεκασμό, εξαλάτωση, διεργασίες άλεση) αποδίδει νανοσωματίδια που βασίζονται σε ενώσεις χαμηλής ή υψηλής μοριακής μάζας. Σε αυτό το πλαίσιο, τα πολυμερικά νανοσωματίδια αντιπροσωπεύουν μια κατηγορία, ιδιαίτερα πλούσια σε ευκαιρίες για τη ρύθμιση και τον έλεγχο των αποτελεσμάτων των υλικών των νανοσωματιδίων, δεδομένου ότι μπορούν να υποβάλλονται σε επεξεργασία ώστε να μεταβάλλεται η λειτουργικότητα καθώς και τα χαρακτηριστικά τους, και μπορούν συνεπώς να καλύπτουν ένα ευρύ φάσμα εφαρμογών. Μια λεπτομερής επισκόπηση σχετικά με τις μεθόδους που είναι διαθέσιμες για την παρασκευή πολυμερικών νανοσωματιδίων είναι παρέχονται από τους Lassalle και Ferreira για το παράδειγμα του πολύ 37
38 (γαλακτικού οξύ) (PLA), που είναι ένα καθιερωμένο πολυμερές για συστήματα μεταφοράς φαρμάκου [75]. Ο όρος nanoprecipitation αναφέρεται σε μια αρκετά απλή μέθοδο επεξεργασίας για την παρασκευή πολυμερικών νανοσωματιδίων. Γενικώς, η μέθοδος περιγράφει την καταβύθιση ενός διαλυμένου υλικό ως σωματίδιο που μπορεί να ενταχθεί στη νανοκλίμακα μετά την έκθεση σε μια μη-διαλύτη ουσία που είναι αναμίξιμη με το διαλύτη. Αυτό έρχεται σε αντίθεση με την τεχνική διάχυσης γαλάκτωμα / διαλύτη που χρησιμοποιεί μερικώς αναμίξιμος solvents [76]. Αν και η ονοματολογία που αποδίδεται στην τεχνική εξακολουθεί να είναι ένα σχετικά πρόσφατο φαινόμενο, η εφαρμογή της τεχνικής του nanoprecipitation ως τεχνική επεξεργασία πολυμερών έχει πολύ μεγαλύτερη ιστορία Ιστορία της τεχνικής Στην πραγματικότητα, η χρησιμότητα της τεχνικής του nanoprecipitation αναγνωρίστηκε πολύ νωρίτερα από ότι η έννοια της Νανοτεχνολογίας [77]. Σε γενικές γραμμές, η εφαρμογή της τεχνικής του nanoprecipitation μπορεί να διαιρεθεί σε δύο ευρείες κατηγορίες: (α) εφαρμογές όπου η τεχνική του nanoprecipitation χρησιμοποιείται ως τεχνική σχηματισμού για την παρασκευή πολυσύνθετων, προστιθέμενης αξίας διασπορών σαν το επιθυμητό τελικό προϊόν, και (β) εφαρμογές όπου η τεχνική του nanoprecipitation χρησιμοποιείται ως ενδιάμεσο στάδιο της επεξεργασίας των πολυμερών. Ήδη από έναν αιώνα πριν, η ιδιότητα της τεχνικής nanoprecipitation να μπορεί να τροποποιηθεί και να έρθει στα μέτρα της εκάστοτε εφαρμογής είχε αρχίσει να αποκαλύπτεται, με βάση τα φυσικά πολυμερή. Η δημιουργικότητα αυτών των πρώιμων ερευνητών που ασχολήθηκαν με την τεχνική nanoprecipitation σε πολυμερή αντικατοπτρίζεται στο ευρύ πεδίο της επιστήμη υλικών που απευθύνεται στις ευρεσιτεχνίες του χρόνου. Σε μία από τις πρώτες εφαρμογές στον τομέα της υγείας, κολλοειδή από φυσικό καουτσούκ προτάθηκαν ως αντίδοτο στην δηλητηρίαση από στρυχνίνη (τουλάχιστον όπως αποδεικνύεται σε βατράχια) [78]. Στην πρόσφατη βιβλιογραφία, η πλειονότητα των αναφερόμενων πολυμερικών συστημάτων που σχηματίζουν νανοσωματίδια μέσω του nanoprecipitation βασίζεται σε συμπολυμερή, δεδομένου ότι αυτά τα συστήματα συνήθως κατέχουν αμφίφιλο χαρακτήρα και σχηματίζουν μία δομή πυρήνα-κελύφους λόγω της συμπεριφοράς τους που παρομοιάζεται με αυτή των μυκκιλίων. Το μέγεθος και η μορφολογία των νανοσωματιδίων μπορεί να ελέγχεται με ρύθμιση των μηκών μπλοκ-συμπολυμερών. 38
39 Διάφορα συστήματα περιέχουν υδρόφοβες μονάδες πολυμερούς και πολύ- (Αιθυλενογλυκόλη) PEG ως υδρόφιλο τμήμα, που οδηγεί σε δι-, τρι-, ή υψηλότερα συμπολυμερικά polyblock. Η μεταφορά με αμφιφιλικούς φορείς έχει ήδη εφαρμοστεί με επιτυχία για την μεταφορά υδρόφοβων φαρμάκων όπως η δοξορουβικίνη, η κλομαζεπάμη, και και η ανδριαμυκίνη, ή με ενσωμάτωση πρωτεϊνών με φαρμακευτικό χαρακτήρα. Αποδοτικά συστήματα μεταφοράς γονιδίων, με βάση πχ. πολύ (αιθυλένιο ιμίνες), διαιθυλαμινο αιθυλ (DΕΑΕ) δεξτράνη, ή πολύ (λυσίνη), έχουν ήδη αναπτυχθεί και είναι υπό εξέταση για in vivo μελέτες [79]. Σε αντίθεση με αυτό, πολυμερικά συστήματα που δεν έχουν την κλασική αμφιφιλική μορφή αλλά έχουν ουδέτερο φορτίο μπορεί επίσης να υποβληθούν σε επεξεργασία για την παραγωγή νανοσωματιδίων μέσω nanoprecipitation. Το πια σημαντικά παραδείγματα είναι το PLA και το πολύ (γαλακτικό-συν-γλυκολικό οξύ) (PLGA) που χρησιμοποιούνται ως βιοσυμβατά υλικά ως φορείς μεταφοράς φαρμάκου [80]. Η πολύ (3-καπρολακτόνη) (PCL), είναι επίσης γνωστή ως εναλλακτικός βιοσυμβατός και βιοδιασπώμενος πολυεστέρας είναι με τη μορφή νανοσωματιδίων με τη μέθοδο του nanoprecipitation ενσωματώνοντας αποτελεσματικά λιπόφιλα μόρια που σχετίζονται με καλλυντικά, φάρμακα, ή παράσιτα Θεωρητικό υπόβαθρο, το φαινόμενο ούζο, και παράμετροι επεξεργασίας Ο σχηματισμός νανοσωματιδίων μέσω της τεχνικής του nanoprecipitation υποτίθεται ότι συμβαίνει λόγω της πυρήνωσης των μικρών συσσωματωμάτων μακρομορίων ακολουθούμενη από συσσωμάτωση αυτών των πυρήνων. Η συσσωμάτωση σταματά μόλις επιτευχθεί κολλοειδή σταθερότητα. Μια θεωρία που περιγράφει την πυρήνωση σε υπέρκορα διαλύματα είναι σε νανοδιασπορές προτείνεται από τον Lamer [81]. Το προκύπτον μέγεθος στο τέλος της συσσωμάτωσης συσχετίζεται έντονα με τη συγκέντρωση του πολυμερούς και, κατά συνέπεια, το ιξώδες του διαλύματος [82]. Το ιξώδες θα πρέπει να είναι επαρκώς χαμηλό για να καταστείλει την εμπλοκή μεταξύ των πολυμερικών αλυσίδων, φαινόμενο το οποίο, όταν υπάρξει, είναι επαρκές για να αποτύχει η δημιουργία των νανοσωματιδίων [83]. Εξάλλου, ο χαρακτήρας του πολυμερούς είναι υπεύθυνος για την πρόληψη της ανάπτυξης των νανοσωματιδίων, διαφορετικά, πρέπει να χρησιμοποιούνται σταθεροποιητικοί παράγοντες [82]. Καθώς η συνολική ποσότητα του πολυμερούς διανέμεται ομοιογενώς σε όλο το διάλυμα κατά τη διάρκεια της τεχνικής του nanoprecipitation, το προτιμώμενο σχήμα των σωματιδίων είναι μια σφαίρα. Η συγκέντρωση, όπου το διάλυμα πολυμερούς είναι αρκετά αραιωμένο για να είναι μετασταθές με αποτέλεσμα την πυρηνοποίηση των 39
40 πολυμερών, είναι η λεγόμενη περιοχή ούζο. Αυτό το φαινόμενο πήρε το όνομά του από το ελληνικό απεριτίφ που γίνεται θολό μετά από αυθόρμητη γαλακτωματοποίηση του ύδατος και της ανιθόλης [83]. Εκτός του nanoprecipitation, από άποψη χημείας πολυμερών, μια τέτοια αυθόρμητη γαλακτωματοποίηση μπορεί επίσης να χρησιμοποιηθεί για τεχνικές πολυμερισμού για να σχηματίσει πολυμερή nanoparticles [84], ή για τη δημιουργία ολιγομερών για μετασυμπύκνωση εντός νανοκαψούλων [83]. Σε όλες τις περιπτώσεις, η υδρόφοβη ουσία γίνεται σημαντικά υπέρκορη κατά την προσθήκη μιας υδρόφιλης ουσίας, που έχει σαν αποτέλεσμα τον σχηματισμό μικρών συσσωματωμάτων ή σταγονιδίων. Αυτή η έννοια δεν περιορίζεται σε πολυμερή, αλλά μπορεί επίσης να χρησιμοποιηθεί για τη παρασκευή των ουσιών όπως β-καροτένιο ή ελαίων [85]. Λόγω του γεγονότος ότι ο συντελεστής διάχυσης των διαλυτών πρέπει να είναι επαρκής για να επάγεται αυθόρμητη γαλακτωματοποίηση, και έτσι πυρήνωση, οι διηλεκτρικές σταθερές των διαλυτών επίσης εμπλέκονται στην εύρεση των βέλτιστων συνθηκών επεξεργασίας για νανοσωματίδια ομοιόμορφου μεγέθους [86]. Ως ένα τυπικό παράδειγμα, το αποτέλεσμα του τύπου διαλύτη / μη-διαλύτη μπορεί να περιγραφεί για PLA / PLGA. Ένα γενικό συμπέρασμα είναι ότι οι διαλύτες με μικρότερη διηλεκτρική σταθερά οδηγούν σε μεγαλύτερα σωματίδια. Ωστόσο, ο συνδυασμός του διαλύτη / μη-διαλύτη φαίνεται να έχει μια ακόμη μεγαλύτερη επιρροή στον ρυθμόν διάχυσης και, έτσι, στο μέγεθος των σωματιδίων. Η συγγένεια των διαλυμένων προς τις μη διαλυμένες ουσίες είναι σημαντική και μπορεί να περιγραφεί με την παράμετρο αλληλεπίδρασης, c [86]. Η αλληλεπίδραση μεταξύ του διαλύτη και του ίδιου του πολυμερούς χρειάζεται επίσης να ληφθεί υπόψη. Προβάλλεται ο ισχυρισμός ότι υψηλός βαθμός συγγένειας μεταξύ του διαλύτη και των πολυμερών οδηγεί σε υψηλότερη συγκέντρωση του διαλύτη που παραμένει στην υπέρκορη περιοχή του πολυμερούς. Η κίνηση του διαλύτη στο μη-διαλυτό μέρος παρεμποδίζεται, με αποτέλεσμα τα μικρότερα μεγέθη σωματιδίων. Σε γενικές γραμμές, πολικοί διαλύτες δείχνουν αυτή τη συμπεριφορά, και ως εκ τούτου, είναι πολλά υποσχόμενοι διαλύτες για εφαρμογές όπως η nanoencapsulation πεπτιδίων ή πρωτεϊνών. Επιπλέον, το DMSO είναι ο διαλύτης επιλογής από την άποψη της σταθερότητας και διαλυτότητα για πρωτεΐνες. Από τη σκοπιά της επεξεργασίας, υπάρχουν βασικά δύο διαφορετικές διαδρομές για την παρασκευή πολυμερικών νανοσωματιδίων μέσω nanoprecipitation, και αυτές είναι η διάλυση και η τεχνική ενστάλαξης, όπως απεικονίζεται στην Εικόνα 3. Η χρήση μιας μεμβράνης διαπίδυσης δίνει το πλεονέκτημα της εξασφάλισης μία πλήρους ανταλλαγή του διαλυτού πολυμερούς κατά του μη-διαλυτού μέρους, όπου η επιλογή του διαλύτη περιορίζεται μόνο από τα χαρακτηριστικά της μεμβράνης και, φυσικά, την αναμιξιμότητα με τον μη-διαλυτό μέρος. Ωστόσο, αυτή η διεργασία είναι συγκριτικά 40
41 χρονοβόρα και δεν μπορεί να χρησιμοποιηθεί για λιγότερο σταθερά συστήματα σωματιδίων. Η στάγδην προσθήκη του διαλύματος πολυμερούς συνήθως εφαρμόζεται κατά τη χρήση συγκριτικά πτητικών διαλυτών, που επιτρέπουν την εύκολη εξάτμιση (επίσης σε υψηλότερες θερμοκρασίες) που οδηγεί σε καθαρές διασπορές νανοσωματιδίων. Η πορεία της παρασκευής, δηλ. ο τρόπο διάχυσης, επηρεάζει έντονα το μέγεθος των νανοσωματιδίων [87]. Σε γενικές γραμμές για όλες τις τεχνικές, η επιλογή του διαλυτού και μη διαλυτού μέρους, η ποιότητα των διαλυτών (pη, συγκεντρώσεις άλατος), [88] και η συγκέντρωση του πολυμερούς έχουν σημαντικό αντίκτυπο για τις προκύπτουσες διασπορές σωματιδίων Πλεονεκτήματα και περιορισμοί της τεχνικής του nanoprecipitation Λόγω του γεγονότος ότι δεν είναι απαραίτητη παροχή ενέργειας από το περιβάλλον για το σχηματισμό των νανοσωματιδίων (πχ. δεν απαιτείται υψηλή διατμιτική ομογενοποίηση, άλεση, ή κατεργασία με υπερήχους), η μέθοδος του nanoprecipitation μπορεί να θεωρηθεί ως μια ήπια και ευαίσθητη διαδικασία, με περιορισμένες απαιτήσεις εξοπλισμού και χαμηλό ενεργειακό κόστος. Σε αντίθεση με την τεχνική γαλακτώματος / διαλύτη διάχυσης, δεν είναι απαραίτητο να χρησιμοποιηθούν τασενεργές ουσίες που θα μπορούσαν να επηρεάσουν τα χαρακτηριστικά επιφάνειας ή να προκαλέσουν τοξικές επιδράσεις. Επιπλέον, μια ευρεία ποικιλία από διαλύτες, όπως το DMSO ή ακετόνη, μπορούν να χρησιμοποιηθούν. Η χρήση ήδη προετοιμασμένων πολυμερών εξασφαλίζει την ποιότητα των νανοσφαιρών χωρίς κάποια υπολειμματικά μονομερή που μπορεί να περιέχονται χρησιμοποιώντας τεχνικές πολυμερισμού γαλακτώματος. Το μέγεθος και το σχήμα των σωματιδίων μπορεί να είναι δύσκολα προβλεπόμενο αλλά είναι συγκριτικά εύκολο να επηρεάσει το σχηματισμό του σωματιδίου αλλάζοντας τη συγκέντρωση, και την τεχνική προετοιμασίας. Σε αντίθεση με την τεχνική emulsion/solvent diffusion, η οποία συνήθως περιλαμβάνει τη χρήση λίαν πτητικών οργανικών διαλυτών όπως διχλωρομεθάνιο ή εξάνιο, στην τεχνική του nanoprecipitation μπορεί επίσης να χρησιμοποιηθούν μη πτητικοί διαλύτες, δηλ. διαλύτες οι οποίοι δεν είναι εύκολα εξατμιζόμενοι μόνον από ανάδευση ή εξάτμιση που υποβοηθάται από ήπια θέρμανση, όπως το DMSO, η διμεθυλοακετόνη (DMA), η 2-πυρρολιδόνη, κ.α.. Σε τέτοιες περιπτώσεις, οι διαλύτες πρέπει να απομακρυνθούν προσεκτικά. Προβλήματα μπορεί να προκύψουν εάν ουσίες που διαθέτουν παρόμοια πολικότητα όπως τα πολυμερή πρέπει να είναι ενσωματωμένες μέσα στα νανοσωματίδια. Σε γενικές γραμμές, τα υδατοδιαλυτά φάρμακα συνήθως δεν ενσωματώνονται επαρκώς εντός της πολυμερικής μήτρας, ωστόσο, υπάρχουν επίσης ορισμένες προσπάθειες να παγιδευθούν 41
42 υδρόφιλα φάρμακα αποτελεσματικά σε νανοσωματίδια με τροποποίηση των τιμών του ph (πχ. για την ενθυλάκωση υδροχλωρικής προκαΐνης) [89] ή επιλέγοντας τον κατάλληλο τύπο του διαλύτη(πχ., πολικούς διαλύτες και για την ενθυλάκωση πρωτεϊνών) [90] Σωματίδια PLA, PLGA και PCL Παρόλο που αρχικά επινοήθηκε για να χρησιμοποιηθεί μια ευρεία ποικιλία πολυμερών, η τεχνική του nanoprecipitation είναι μέχρι τώρα εφαρμόσιμη κυρίως για τους βιοαποικοδομήσιμους πολυεστέρες PLA, PLGA, PCL σε εφαρμογές μεταφοράς φαρμάκων και σε βιομηχανικές εφαρμογές. Πολλά σχόλια που δημοσιεύθηκαν τα τελευταία χρόνια αποδεικνύουν το τεράστιο δυναμικό των πολυεστέρων απελευθέρωσης γονιδίου [75, 91,92]. Θα μπορούσε να δειχθεί ότι ΡΙΑ / PLGA σωματίδια in vitro και in vivo μπορούν να διαφύγουν από τα ενδο-λυσοσωματικά διαμερίσματα κατά την κυτταρική πρόσληψη στο κυτοσόλιο, ενώ παράλληλα απελευθερώνουν τους θεραπευτικούς παράγοντες. Διάφορες υδρόφοβα καθώς υδρόφιλα φάρμακα μπορούν να ενθυλακώνονται αποτελεσματικά μέσα στην πολυμερική μήτρα των νανοσωματιδίων που απελευθερώνουν το ωφέλιμο φορτίο τους βραδέως κατά τη διάρκεια του χρόνου [93]. Η κινητική απελευθέρωσης εξαρτάται έντονα από το ίδιο το φάρμακο και τις παραμέτρους επεξεργασίας. Με αυτό τον τρόπο, υδρόφοβα φάρμακα, όπως η κλοναζεπάμη, η πακλιταξέλη, η κυκλοσπορίνη Α, η ινδομεθακίνη, το βαλπροϊκό οξύ, η κετοπροφένη, η διγιτοξίνη, η ρισπεριδόνη,η αμοξιφαίνη, και άλλοι υδρόφιλοι παράγοντες, π.χ. ινσουλίνη, βανκομυκίνη, φαινοβαρβιτάλη, πεπτίδια ή πρωτεΐνες μπορούν να εγκλωβιστούν στα πολυμερικά νανοσωματίδια [94,95]. Η μέθοδος του nanoprecipitation εμφανίζει επίσης πλεονεκτήματα για την ακινητοποίηση πρωτεϊνών με προσρόφηση επί των επιφανειών των σωματιδίων, δεδομένου ότι δεν χρησιμοποιούνται επιφανειοδραστικές ουσίες που διαφορετικά μπορεί να επηρεάσουν ή να αναστέλλουν την προσρόφηση [96]. Δενδριτικά κύτταρα φορτωμένα με HIV-1 p24 πρωτεΐνες που έχουν προσροφηθεί σε PLA νανοσωματίδια φαίνεται να επάγουν μια ενισχυμένη κυτταρική ανοσοαπόκριση έναντι του HIV-1 μετά από εμβολιασμό [97] Σύνοψη της τεχνικής του Nanoprecipitation Η τεχνική του nanoprecipitation παρέχει μια εύκολη, ήπια, και χαμηλής κατανάλωσης ενέργειας μέθοδο για την παρασκευή πολυμερικών εναιωρημάτων νανοσωματιδίων. Μπορούν να ελεγχθούν οι παράμετροι που επηρεάζουν το σχηματισμό των σωματιδίων 42
43 καθώς και τα πλεονεκτήματα, αλλά και μειονεκτήματα σε σχέση με άλλες μεθόδους για την παρασκευή πολυμερικών νανοσωματιδίων. Εν τούτοις, μέχρι τώρα η κύρια χρήση της τεχνικής βασίζεται στη δημιουργία σωματιδίων από PLA και PLGA με στόχο την έρευνα για ποικίλες εφαρμογές. Η γνώση σχετικά με την αυτο-συναρμολόγηση των άλλων συνθετικών πολυμερών απαιτεί μια διευκρίνιση για να επιτραπεί να γίνει το nanoprecipitation μία εύκολη τεχνική για ένα ευρύ φάσμα πολυμερών. Υπάρχει πλέον μια γενική εικόνα σχετικά με το είδος των εναλλακτικών πολυμερών που μπορούν να σχηματίσουν νανοσωματίδια μέσω nanoprecipitation προκειμένου να επεκταθεί η τεχνική σε ευρύτερο πεδίο με τη χρήση και διαφορετικών πολυμερών. Φαίνεται ότι σχεδόν κάθε υδρόφοβο πολυμερές μπορεί να είναι σε θέση να καθιζάνει στη νανοκλίμακα εάν εφαρμοστούν οι κατάλληλες συνθήκες. Επιπλέον, υπάρχουν πλέον μέθοδοι που μπορούν να μετατρέψουν την απλή ενστάλαξη ή τη διαδικασίας διάλυσης μέσω μεμβράνης σε βιομηχανικά πιο εφαρμόσιμες συσκευές δοκιμών με στόχο την επίτευξη της επαναληψιμότητας της συνθέσεως των νανοσωματιδίων με χρήση microfluidic συσκευών. 43
44 ΚΕΦΑΛΑΙΟ 3. Τεχνική Μέτρησης Μεγέθους και ζ-δυναμικού Νανοσωματιδίων ζ-δυναμικό Το ζ-δυναμικό είναι ένας επιστημονικός όρος για το ηλεκτροκινητικό δυναμικό [98] σε κολλοειδή συστήματα. Στην βιβλιογραφία που αναφέρεται στην χημεία κολλοειδών συστημάτων, συνήθως συμβολίζεται χρησιμοποιώντας το ελληνικό γράμμα ζήτα. Από θεωρητική άποψη, το δυναμικό ζήτα είναι ηλεκτρικό δυναμικό στην διεπιφανειακό διπλό στρώμα (DL) στην θέση του επιπέδου ολίσθησης έναντι ενός σημείου στο bulk ρευστό μακριά από τη διεπιφάνεια μορίου-υγρού. Με άλλα λόγια, το δυναμικό ζήτα είναι η διαφορά δυναμικού μεταξύ του μέσου διασποράς και του σταθερού στρώματος του ρευστού που συνδέεται/έρχεται σε επαφή με το διασπειρώμενο σωματίδιο. Μια τιμή γύρω στα 25 mv (με θετικό ή αρνητικό πρόσημο), μπορεί να ληφθεί ως μια αυθαίρετη τιμή που χωρίζει τις χαμηλού φορτίου επιφάνειες από τις υψηλού-φορτίου επιφάνειες. Η σημασία του δυναμικού ζήτα είναι ότι η τιμή του μπορεί να σχετίζεται με τη σταθερότητα των κολλοειδών διασπορών. Το δυναμικό ζήτα δείχνει το βαθμό της απώθησης μεταξύ γειτονικών, παρομοίως φορτισμένων σωματιδίων σε μία διασπορά. Για μόρια και τα σωματίδια τα οποία είναι αρκετά μικρά, ένα υψηλό δυναμικό ζήτα θα προσδώσει σταθερότητα, δηλαδή, το διάλυμα ή διασπορά θα αντιστέκονται στη δημιουργία συσσωματωμάτων. Όταν το δυναμικό είναι χαμηλό, η έλξη υπερβαίνει την άπωση και η διασπορά θα αρχίσει να εμφανίζει φαινόμενα κροκίδωσης και συσσωματωμάτων. Έτσι, τα κολλοειδή με υψηλό δυναμικό ζήτα (αρνητικό ή θετικό) είναι ηλεκτρικά σταθεροποιημένα ενώ τα κολλοειδή με χαμηλά δυναμικά ζήτα τείνουν να πήζουν ή να κροκιδώνονται όπως περιγράφεται στον παρακάτω πίνακα [99,100]. Το δυναμικό ζήτα χρησιμοποιείται ευρέως για την ποσοτικοποίηση του μεγέθους του ηλεκτρικού φορτίου στη διπλή στιβάδα στη διεπιφάνεια. Ωστόσο, το δυναμικό ζήτα είναι συχνά η μόνη διαθέσιμη διαδρομή για το χαρακτηρισμό των ιδιοτήτων διπλής-στρώσης. Το ζήτα δυναμικό δεν πρέπει να συγχέεται με το δυναμικό του ηλεκτροδίου ή το ηλεκτροχημικό δυναμικό (επειδή οι ηλεκτροχημικές αντιδράσεις γενικώς δεν εμπλέκονται στην ανάπτυξη του δυναμικού ζήτα). 44
45 Zeta potential [mv] Stability behavior of the colloid from 0 to ±5, Rapid coagulation or flocculation from ±10 to ±30 Incipient instability from ±30 to ±40 Moderate stability from ±40 to ±60 Good stability more than ±61 Excellent stability Πίνακας 2 Συσχέτιση ζ-δυναμικού με τη σταθερότητα μιας διασπορά Μέτρηση του δυναμικού ζήτα Το ζήτα δυναμικό δεν είναι άμεσα μετρήσιμο αλλά μπορεί να υπολογιστεί χρησιμοποιώντας θεωρητικά μοντέλα και να προσδιοριστεί πειραματικά υπολογίζοντας την ηλεκτροφορητική κινητικότητα ή τη δυναμική ηλεκτροφορητική κινητικότητα. Τα ηλεκτροκινητικά και ηλεκτροακουστικά φαινόμενα είναι οι συνήθεις πηγές των δεδομένων για τον υπολογισμό του δυναμικού ζήτα. Ηλεκτροκινητικά φαινόμενα Η ηλεκτροφόρηση χρησιμοποιείται για την εκτίμηση του ζήτα δυναμικού των σωματιδίων, ενώ ο λόγος δυναμικό/ ρεύμα χρησιμοποιείται για πορώδη σώματα και επίπεδες επιφάνειες. Στην πράξη, το δυναμικό ζήτα της διασποράς μετράται με την εφαρμογή ενός ηλεκτρικού πεδίου κατά μήκος της διασποράς. Σωματίδια εντός της διασποράς με ένα δυναμικό ζήτα θα μεταναστεύσουν προς το ηλεκτρόδιο αντίθετου φορτίου με μία ταχύτητα ανάλογη με το μέγεθος του δυναμικού ζήτα. Η ταχύτητα αυτή μετράται χρησιμοποιώντας την τεχνική της Laser Doppler Anemometer. Η μετατόπιση συχνότητας ή μετατόπισης φάσης μίας προσπίπτουσας δέσμης λέιζερ που προκαλούνται από αυτά κινούμενα σωματίδια μετράται ως η κινητικότητα των σωματιδίων, καθώς και η κινητικότητα αυτή μετατρέπεται στο δυναμικό ζήτα εισάγοντας το ιξώδες διασποράς και τη διηλεκτρική διαπερατότητα, καθώς και με την εφαρμογή των θεωριών Smoluchowski [101]. 45
46 Ηλεκτροφόρηση Η ηλεκτροφορητική ταχύτητα είναι ανάλογη προς την ηλεκτροφορητική κινητικότητα, η οποία είναι η μετρήσιμη παράμετρος. Υπάρχουν διάφορες θεωρίες που συνδέουν την ηλεκτροφορητική κινητικότητα με δυναμικό ζήτα. Από άποψη οργανοληπτική, υπάρχουν δύο διαφορετικές πειραματικές τεχνικές: μικροηλεκτροφόρηση. Έχει το πλεονέκτημα του να αποδίδει μία εικόνα των κινούμενων σωματιδίων. Από την άλλη πλευρά, περιπλέκεται από φαινόμενα ηλεκτροωσμώσεως στα τοιχώματα της κυψελίδας του δείγματος. Ηλεκτροφορητική σκέδαση φωτός (Light Scattering). Βασίζεται σε δυναμική σκέδαση φωτός (Dynamic Light Scattering). Επιτρέπει τη μέτρηση σε μία ανοικτή κυψελίδα που εξαλείφει το πρόβλημα της ηλεκτρο-οσμωτικής ροής όπως στην προηγούμενη περίπτωση. Μπορεί να χρησιμοποιηθεί για να χαρακτηρίσει πολύ μικρά σωματίδια, αλλά πληρώνοντας το τίμημα του να χάνει την ικανότητα για την εμφάνιση εικόνων των κινούμενων σωματιδίων. Και οι δύο αυτές τεχνικές μέτρησης μπορεί να απαιτούν αραίωση του δείγματος. Μερικές φορές αυτή η αραίωση μπορεί να επηρεάσει τις ιδιότητες του δείγματος και να αλλάξει το ζήτα δυναμικό. Υπάρχει μόνο μία περίπτωση που να δικαιολογεί αυτή την αραίωση η χρήση υπερκείμενου εξισσοροποιητή. Στην περίπτωση αυτή, η διεπιφανειακή ισορροπία μεταξύ της επιφάνειας των σωματιδίων και του υγρού θα διατηρηθεί και το ζήτα δυναμικό θα είναι η ίδιο για όλα τα κλάσματα όγκου των σωματιδίων στο αιώρημα. Όταν το αραιωτικό είναι γνωστό, πρόσθετο αραιωτικό μπορεί να παρασκευαστεί. Εάν το αραιωτικό μέσο είναι άγνωστο, το υπερκείμενο ισορροπίας μπορεί να ληφθεί εύκολα με φυγοκέντριση Υπολογισμός του δυναμικού ζήτα Η πιο γνωστή και ευρέως χρησιμοποιούμενη θεωρία για τον υπολογισμό του δυναμικού ζήτα από πειραματικά δεδομένα αναπτύχθηκε από τον Marian Smoluchowski το 1903 [102]. Αυτή η θεωρία αναπτύχθηκε αρχικά για την ηλεκτροφόρηση. Ωστόσο, μια επέκταση στην ηλεκτροακουστική είναι τώρα επίσης διαθέσιμη [103]. Η θεωρία του 46
47 Smoluchowski είναι ισχυρή, διότι είναι έγκυρη για διασκορπισμένα σωματίδια κάθε σχήματος και για κάθε συγκέντρωση. Ωστόσο, έχει τους περιορισμούς της: Λεπτομερής θεωρητική ανάλυση απέδειξε ότι η θεωρία του Smoluchowski ισχύει μόνο για ένα επαρκώς λεπτή διπλό στρώμα, όταν το μήκος Debye, 1 / κ, είναι πολύ μικρότερο από την ακτίνα α των σωματιδίων: Το μοντέλο του "διπλού λεπτού στρώματος" προσφέρει τεράστιες απλουστεύσεις όχι μόνο για τη θεωρία της ηλεκτροφόρηση, αλλά και για πολλές άλλες ηλεκτροκινητικές και ηλεκτροακουστικές θεωρίες. Αυτό το μοντέλο είναι έγκυρο για τα περισσότερα υδατικά συστήματα επειδή το μήκος Debye είναι τυπικά μόνο μερικά νανόμετρα στο νερό. Το μοντέλο δεν ισχύει μόνο για νανο-κολλοειδή σε ένα διάλυμα με ιονική ισχύ που προσεγγίζει εκείνη του καθαρού νερού. Η θεωρία του Smoluchowski παραμελεί την συμβολή της επιφανειακής αγωγιμότητας. Αυτό εκφράζεται σε σύγχρονες θεωρίες ως όρος Dukhin: Η ανάπτυξη της ηλεκτροφοριτικής και ηλεκτροακουστικής θεωρίας με ένα ευρύτερο φάσμα ισχύος ήταν ένας στόχος πολλών μελετών κατά τη διάρκεια του 20ου αιώνα. Υπάρχουν αρκετές θεωρίες ανάλυσης που ενσωματώνουν την επιφανειακή αγωγιμότητα και εξαλείφουν τον περιορισμό του μικρού αριθμού Dukhin τόσο για τις ηλεκτροκινητικές όσο και για τις ηλεκτροακουστικές εφαρμογές Nano Zetasizer Λειτουργία Το φάσμα των οργάνων που περιέχει το Zetasizer Nano δίνει τη δυνατότητα να μπορούν να μετρηθούν τρεις χαρακτηριστικές ιδιότητες των σωματιδίων ή μορίων σε ένα υγρό μέσο. Αυτές οι τρεις θεμελιώδεις παράμετροι είναι το μέγεθος των σωματιδίων, το ζ- δυναμικό και το μοριακό βάρος. Με τη χρήση της μοναδικής τεχνολογίας που παρέχεται στο πλαίσιο του συστήματος Zetasizer αυτές οι παράμετροι μπορούν να μετρηθούν σε ένα ευρύ φάσμα συγκεντρώσεων. Το σύστημα Zetasizer επιτρέπει επίσης τον προσδιορισμό του σημείου τήξεως πρωτεΐνης. Η σειρά Zetasizer διαθέτει προ-ευθυγραμμισμένα οπτικά 47
48 συστήματα και προγραμματιζόμενο μετρητή θέσης συν τον ακριβή έλεγχο της θερμοκρασίας που απαιτούνται για να είναι οι μετρήσεις ακριβείς, και επαναλαμβανόμενες. Επιπλέον στην εγκατάσταση περιλαμβάνονται όργανα για μετρήσεις άλλων βασικών παραμέτρων όπως το pη και η συγκέντρωση. Η σειρά Zetasizer έχει σχεδιαστεί με γνώμονα την απλότητα, έτσι ώστε ένα ελάχιστο ποσό της αλληλεπίδρασης των χρηστών με το λογισμικό να είναι απαραίτητο για την επίτευξη εξαιρετικών αποτελεσμάτων. Η χρήση των τυποποιημένων διαδικασιών λειτουργίας (SOP) και αυτοματοποιεί τη διαδικασία, χωρίς απαραίτητα συνεχή επίβλεψη. Το μέγεθος των σωματιδίων που μετράται σε ένα μέσο DLS είναι η διάμετρος της σφαίρας που διαχέεται με την ίδια ταχύτητα όπως το σωματίδιο που μετράται. Το σύστημα Zetasizer καθορίζει το μέγεθος καταρχάς με μέτρηση της Brownian κίνηση των σωματιδίων σε ένα δείγμα με τη χρήση Δυναμικής Σκέδασης Φωτός (DLS) και στη συνέχεια, αποδίδει ένα μέγεθος από αυτό χρησιμοποιώντας καθιερωμένες θεωρίες. Η Brownian κίνηση ορίζεται ως: "Η τυχαία κίνηση των σωματιδίων σε ένα υγρό που οφείλεται στο βομβαρδισμό από τα μόρια που τους περιβάλλουν. " Τα σωματίδια σε ένα υγρό εκτελούν περίπου τυχαία κίνηση και η ταχύτητα κυκλοφορίας τους χρησιμοποιείται για τον προσδιορισμό του μεγέθους των σωματιδίων. Είναι γνωστό ότι τα μικρά σωματίδια κινούνται γρήγορα σε ένα υγρό και τα μεγάλα σωματίδια κινούνται πιο αργά. Η κίνηση αυτή εκτελείται όλη την ώρα, οπότε αν πάρουμε δύο «εικόνες» από το δείγμα που χωρίζονται από ένα σύντομο χρονικό διάστημα, όπως πχ 100 μsec, μπορούμε να δούμε πόσο το σωματίδιο έχει μετακινηθεί και ως εκ τούτου να καταλάβουμε το πόσο μεγάλο είναι. Εάν υπήρξε μια ελάχιστη κίνηση και οι θέσεις των σωματιδίων είναι πολύ παρόμοιες, τότε τα σωματίδια στο δείγμα θα είναι μεγάλα. Παρομοίως εάν υπήρξε έντονη κινητικότητα και οι θέσεις των σωματιδίων είναι αρκετά διαφορετικές, τότε τα σωματίδια στο δείγμα είναι μικρά. Χρησιμοποιώντας αυτή τη γνώση και τη σχέση μεταξύ της ταχύτητας διάδοσης και του μεγέθους, το τελευταίο μπορεί να προσδιοριστεί. Η παραπάνω θεωρία είναι μία πολύ απλουστευτική εξήγηση Μετρήσεις Μεγέθους και ζ-δυναμικού Μετρήσεις Μεγέθους Εισάγεται η κυψελίδα, το πρόγραμμα αρχίζει να εκτελείται και η συλλογή δεδομένων ξεκινά. Ο μετρητής προόδου δείχνει την πρόοδο της μέτρησης, ενώ δείχνουν παράλληλα 48
49 εμφανίζεται και ο αριθμός των μετρήσεων που έχουν προεπιλεγεί από το χρήστη (Συνήθως τα τρεξίματα είναι από 3 έως 5). Στο τέλος της συλλογής δεδομένων, η ποιότητα των δεδομένων του κάθε «RUN» αξιολογείται με τα run που περιέχουν τα φτωχότερα δεδομένα να απορρίπτονται, ενώ τα υπόλοιπα run αναλύονται και χρησιμοποιούνται στον τελικό υπολογισμό της μέτρησης. Μέτρηση ζ-δυναμικού Η κυψελίδα εισάγεται στη διάταξη και εκτελείται έναρξη του προγράμματος από τον ηλεκτρονικό υπολογιστή. Η κυψελίδα ελέγχεται πρώτα για να προσδιορίσει ο τύπος που έχει τοποθετηθεί, και ότι συμφωνεί με την επιλογή της SOP. Κάθε πλήρης μέτρηση διαιρείται σε έναν αριθμό εκτελέσεων RUNs. Όλες οι ατομικές εκτελέσεις μέτρησης συσσωρεύονται μαζί και κατόπιν αθροίζονται για να δώσoυν ένα τελικό αποτέλεσμα Zeta Δυναμική Σκέδαση Φωτός(DLS) Η σειρά Zetasizer Nano πραγματοποιεί μετρήσεις μεγέθους χρησιμοποιώντας μια διαδικασία που ονομάζεται Δυναμική Σκέδαση Φωτός (DLS). Η Δυναμική Σκέδαση Φωτός (επίσης γνωστή ως PCS - Photon Correlation Spectroscopy) μετρά την κίνηση Brown και τη συσχετίζει με το μέγεθος των σωματιδίων. Αυτό επιτυγχάνεται με το φωτισμό των σωματιδίων με ένα λέιζερ και με ανάλυση των διακυμάνσεων της έντασης του σκεδαζόμενου φωτός. Στην πράξη, τα σωματίδια που αιωρούνται σε ένα υγρό δεν είναι ποτέ στάσιμα. Τα σωματίδια κινούνται συνεχώς λόγω της κίνηση Brown. Ένα σημαντικό χαρακτηριστικό της κίνησης Brown των DLS είναι ότι τα μικρά σωματίδια κινούνται γρήγορα και μεγάλα σωματίδια κινούνται πιο αργά. Η σχέση μεταξύ του μεγέθους του σωματιδίου και της ταχύτητα του λόγω της κίνησης Brown ορίζεται η Stokes-Einstein εξίσωση. Το Zetasizer Nano σύστημα μετρά το ποσοστό της διακύμανσης της έντασης και στη συνέχεια χρησιμοποιεί αυτό για να υπολογισθεί το μέγεθος των σωματιδίων. 49
50 ΚΕΦΑΛΑΙΟ 4. Τεχνικές Απεικόνισης Μικροσκοπία Σάρωσης Ηλεκτρονίων (SEM) Ένα μικροσκόπιο σάρωσης ηλεκτρονίων (SEM) είναι ένας τύπος ηλεκτρονικού μικροσκοπίου που παράγει εικόνες ενός δείγματος σκανάροντας το με μία εστιασμένη δέσμη ηλεκτρονίων. Αυτά τα ηλεκτρόνια αλληλεπιδρούν με τα ηλεκτρόνια στο δείγμα, παράγοντας διάφορα σήματα που μπορούν να ανιχνευτούν και που περιέχουν πληροφορίες σχετικά με την επιφανειακή τοπογραφία και τη σύνθεση του δείγματος. Η δέσμη ηλεκτρονίων σαρώνονται γενικά με βάση ένα πρότυπο σαρώσεως raster, και η θέση της δέσμης συνδυάζεται με το ανιχνευόμενο σήμα για να παραχθεί μια εικόνα. Το SEM μπορεί να επιτύχει ανάλυση καλύτερη από 1 νανόμετρο. Η πρώτη εικόνα SEM λήφθηκε από τον Knoll Max, ο οποίος το 1935 έλαβε την εικόνα από πυριτίου-χάλυβα. Περαιτέρω πρωτοποριακό έργο για τις φυσικές αρχές της μικροσκοπίας SEM και τις αλληλεπιδράσεις μεταξύ δέσμης και δείγματος έγιναν από τον Manfred von Ardenne το 1937, ο οποίος κατοχύρωσε ένα βρετανικό δίπλωμα ευρεσιτεχνίας, αλλά ποτέ δεν έκανε ένα πρακτικό εργαλείο. Το SEM αναπτύχθηκε περαιτέρω από τον καθηγητή Sir Charles Oatley και το μεταπτυχιακό φοιτητή του Gary Stewart και κυκλοφόρησε για πρώτη φορά στην αγορά το 1965 από την εταιρία Cambridge Scientific Instrument Company με το όνομα Stereoscan [104,108] Αρχές λειτουργίας και δυνατότητες Οι τύποι των σημάτων που παράγονται από το SEM περιλαμβάνουν δευτερογενή ηλεκτρόνια, οπισθοσκεδαζόμενα ηλεκτρόνια (BSE), χαρακτηριστικές ακτίνες Χ, φως (cathodoluminescence), ηλεκτρικό ρεύμα από το δείγμα και εκπεμπόμενα ηλεκτρόνια. Ανιχνευτές δευτερευόντων ηλεκτρονίων είναι κοινοί σε όλα τα SEM, αλλά είναι αρκετά σπάνιο για ένα μοναδικό μηχάνημα να έχει ανιχνευτές για όλα τα πιθανά σήματα. Το σήμα είναι αποτέλεσμα αλληλεπιδράσεων ανάμεσα στη δέσμη ηλεκτρονίων και στα άτομα στην επιφάνεια ή κοντά στην επιφάνεια του δείγματος. Στην πιο κοινή ή τυπική λειτουργία ανίχνευσης, δηλαδή την απεικόνιση δευτερευόντων ηλεκτρονίων ή SEI, το SEM μπορεί να παράγει πολύ υψηλής ανάλυσης εικόνες της επιφάνειας του δείγματος, αποκαλύπτοντας λεπτομέρειες μικρότερες από 1 nm σε μέγεθος. Λόγω της πολύ στενής δέσμης ηλεκτρονίων, 50
51 τα μικρογραφήματα SEM έχουν ένα μεγάλο βάθος πεδίου αποδίδοντας μια χαρακτηριστική τρισδιάστατη εμφάνιση, ικανότητα πολύ χρήσιμη για την κατανόηση της επιφανειακής δομής του δείγματος. Ένα ευρύ φάσμα μεγεθύνσεων είναι δυνατό, από περίπου 10 φορές (περίπου ισοδύναμο με εκείνο ενός ισχυρού φακού χειρός) μέχρι και περισσότερο από φορές, περίπου δηλαδή 250 φορές το όριο μεγέθυνσης των καλύτερων μικροσκοπίων. Τα οπισθοσκεδαζόμενα ηλεκτρόνια (BSE) είναι η δέσμη ηλεκτρονίων που αντανακλάται από το δείγμα, με ελαστική σκέδαση. Τα BSE χρησιμοποιούνται συχνά σε μια ανάλυση SEM μαζί με τα φάσματα που δημιουργούνται από τις χαρακτηριστικές ακτίνες-χ, διότι η ένταση του σήματος των BSE είναι στενά συνδεδεμένη με τον ατομικό αριθμό (Ζ) του δείγματος. Οι εικόνες BSE μπορούν να παρέχουν πληροφορίες σχετικά με την κατανομή των διαφορετικών στοιχείων στο δείγμα. Για τον ίδιο λόγο, η απεικόνιση των BSE μπορεί να δώσει εικόνες κολλοειδών συστημάτων με επιχρυσωμένα αντισώματα μαρκαρίσματος των 5 ή 10 nm σε διάμετρο, κάτι το οποίο διαφορετικά θα ήταν δύσκολο ή αδύνατο να ανιχνευθεί στις εικόνες δευτερευόντων ηλεκτρονίων σε βιολογικά δείγματα. Χαρακτηριστικές ακτίνες Χ εκπέμπονται όταν η δέσμη ηλεκτρονίων αφαιρεί ένα ηλεκτρόνιο εσωτερικής στοιβάδας από το δείγμα, προκαλώντας ένα υψηλότερης ενέργειας ηλεκτρόνιο για να γεμίσει την κενή θέση στην εσωτερική στοιβάδα και προκαλώντας έτσι την απελευθέρωση ενέργειας. Αυτές οι χαρακτηριστικές ακτίνες Χ χρησιμοποιούνται για την αναγνώριση της σύνθεσης και να μετρηθεί η αναλογία των στοιχείων στο δείγμα Διαδικασία σάρωσης και σχηματισμός εικόνας Σε μία τυπική διαδικασία σάρωσης SEM, μια δέσμη ηλεκτρονίων εκπέμπεται από ένα πυροβόλο ηλεκτρονίων εφοδιασμένο με μία κάθοδο από νήμα βολφραμίου. Το βολφράμιο χρησιμοποιείται συνήθως σε θερμιονικά όπλα ηλεκτρονίων επειδή έχει το υψηλότερο σημείο τήξεως και τη χαμηλότερη πίεση ατμών σε σύγκριση με τα υπόλοιπα μέταλλα, επιτρέποντας το έτσι να μπορεί να θερμαίνεται για την εκπομπή των ηλεκτρονίων. Επίσης είναι μέταλλο επιλογής λόγω του χαμηλού κόστους του. Η δέσμη ηλεκτρονίων, η οποία τυπικά έχει μια ενέργεια που κυμαίνεται από 0,2 kev έως 40 kev, εστιάζεται από έναν ή δύο φακούς σε ένα σημείο περίπου 0,4 nm έως 5 nm σε διάμετρο. Η δέσμη περνά μέσα από ζεύγη πηνίων σάρωσης ή ζεύγη των πλακών εκτροπής στην στήλη ηλεκτρονίων, τυπικά στον τελικό φακό, ο οποίος εκτρέπει τη δέσμη στους άξονες χ και γ, έτσι ώστε να γίνει σάρωση σε ράστερ σε μια ορθογώνια περιοχή της επιφάνειας του δείγματος. Όταν η πρωτογενής δέσμη ηλεκτρονίων αλληλεπιδρά με το δείγμα, τα ηλεκτρόνια 51
52 χάνουν την ενέργεια τους με επαναλαμβανόμενες τυχαίες σκεδάσεις και απορρόφηση εντός ενός σταγονοειδούς σχήματος όγκου του δείγματος που είναι γνωστός ως ο όγκος αλληλεπίδρασης, ο οποίος εκτείνεται από λιγότερο από 100 nm έως περίπου 5μm στην επιφάνεια. Το μέγεθος του όγκου αλληλεπίδρασης εξαρτάται από την ενέργεια των ηλεκτρονίων κατά την προσγείωση στην επιφάνεια, τον ατομικό αριθμό του δείγματος και την πυκνότητα του δείγματος. Η ανταλλαγή ενέργειας μεταξύ της δέσμης ηλεκτρονίων και του δείγματος οδηγεί στην αντανάκλαση των υψηλής ενέργειας ηλεκτρονίων με ελαστική σκέδαση, την εκπομπή των δευτερογενών ηλεκτρονίων από ανελαστική σκέδαση και την εκπομπή ηλεκτρομαγνητικής ακτινοβολίας, καθένα από τα οποία μπορεί να ανιχνευθεί από εξειδικευμένους ανιχνευτές. Το ρεύμα της δέσμης που απορροφάται από το δείγμα μπορεί επίσης να ανιχνευθεί και να χρησιμοποιηθεί. Ενισχυτές ηλεκτρονίων διαφόρων τύπων χρησιμοποιούνται για την ενίσχυση των σημάτων, τα οποία εμφανίζονται ως διακυμάνσεις φωτεινότητας σε μια οθόνη υπολογιστή (ή, σε παλαιότερα μοντέλα, σε ένα σωλήνα καθοδικών ακτίνων). Κάθε pixel της εικόνας του υπολογιστή είναι συγχρονισμένο με τη θέση της δέσμης επί του δείγματος στο μικροσκόπιο, και η προκύπτουσα εικόνα είναι συνεπώς ένας χάρτης κατανομής της έντασης του σήματος που εκπέμπεται από την περιοχή σάρωσης του δείγματος. Σε παλαιότερες μικροσκόπια η εικόνα μπορεί να ληφθεί με φωτογραφία από ένα υψηλής ευκρίνειας καθοδικό σωλήνα, αλλά σε σύγχρονα μηχανήματα η εικόνα αποθηκεύεται στον σκληρό δίσκο του ηλεκτρονικού υπολογιστή Βιολογικά δείγματα Για το SEM, ένα δείγμα απαιτείται κανονικά να είναι εντελώς στεγνό, δεδομένου ότι ο θάλαμος που τοποθετείται το δείγμα είναι σε υψηλό κενό. Σκληρά, ξηρά υλικά όπως ξύλο, οστά, φτερά, αποξηραμένα έντομα, ή κοχύλια μπορεί να εξεταστούν με μικρή περαιτέρω επεξεργασία, αλλά ζωντανά κύτταρα και ολόκληροι ιστοί, μαλακοί ιστοί από οργανισμούς κ.α. συνήθως απαιτούν χημική στερέωση για τη διατήρηση και σταθεροποίηση της δομή τους. Η στερέωση πραγματοποιείται συνήθως με επώαση σε ένα διάλυμα ενός ρυθμισμένου μονιμοποιητικού χημικού, όπως γλουταραλδεϋδη, ενίοτε σε συνδυασμό με φορμαλδεΰδη και άλλα στερεωτικά, και προαιρετικά ακολουθούμενη από μεταμονιμοποίηση με τετροξείδιο του οσμίου. [105] Ο σταθερός ιστός στη συνέχεια αφυδατώνεται. Επειδή ξήρανση στον αέρα προκαλεί κατάρρευση και συρρίκνωση, αυτό επιτυγχάνεται συνήθως με αντικατάσταση του νερού στα κύτταρα με οργανικούς διαλύτες όπως αιθανόλη ή ακετόνη, και την 52
53 αντικατάσταση αυτών των διαλυτών με την σειρά τους με ένα μεταβατικό ρευστό όπως υγρό διοξείδιο του άνθρακα με ξήρανση κρίσιμου σημείου. Το διοξείδιο του άνθρακα τελικά απομακρύνεται, ενώ βρίσκεται σε υπερκρίσιμη κατάσταση, έτσι ώστε να μην είναι παρούσα διεπιφάνεια αερίου-υγρού εντός του δείγματος κατά τη διάρκεια της ξηράνσεως. Το ξηρό δείγμα είναι συνήθως προσαρμοσμένο σε ένα στέλεχος χρησιμοποιώντας ένα συγκολλητικό όπως η εποξική ρητίνη ή ηλεκτρικά αγώγιμη διπλής όψης κολλητική ταινία, και επιμεταλλωμένο με χρυσό ή κράμα χρυσού / παλλαδίου πριν την εξέταση στο μικροσκόπιο Ανίχνευση δευτερογενών ηλεκτρονίων Ο πιο συνηθισμένος τρόπος απεικόνισης συλλέγει χαμηλής ενέργειας (<50 ev) δευτερογενή ηλεκτρόνια που εκτινάσσονται από τα k-τροχιακά των ατόμων του δείγματος με ανελαστική σκέδαση λόγω αλληλεπιδράσεων με τη δέσμη ηλεκτρονίων. Λόγω της χαμηλής ενέργειας τους, αυτά τα ηλεκτρόνια προέρχονται από θέσεις λίγα νανόμετρα από την επιφάνεια του δείγματος [106]. Τα ηλεκτρόνια ανιχνεύεται με έναν ανιχνευτή Everhart- Thornley, [107], ο οποίος είναι ένας τύπος συστήματος σπινθηριστή-φωτοπολλαπλασιαστή. Τα δευτερεύοντα ηλεκτρόνια συγκεντρώνονται αρχικά με την προσέλκυση τους προς ένα ηλεκτρικά φορτισμένο πλέγμα περίπου +400 V, και στη συνέχεια επιταχύνονται περαιτέρω προς την κατεύθυνση ενός σπινθηριστή θετικά φορτισμένου σε περίπου V. Τα δευτερεύοντα ηλεκτρόνια επιταχυνόμενα είναι τώρα αρκετά ενεργητικός ώστε να προκαλέσουν στον σπινθηριστή την εκπομπή λάμψεων φωτός (cathodoluminescence), οι οποίες οδηγούνται σε ένα φωτοπολλαπλασιαστή εκτός της στήλης του SEM μέσω ενός σωλήνα φωτός και ένα παράθυρο στο τοίχωμα του θαλάμου του δείγματος. Το ενισχυμένο ηλεκτρικό σήμα εξόδου από τον φωτοπολλαπλασιαστή εμφανίζεται ως μια δισδιάστατη κατανομή έντασης που μπορεί να απεικονισθεί και να φωτογραφηθεί σε μία αναλογική οθόνη βίντεο, ή να υποβληθεί σε μετατροπή από αναλογικό προς ψηφιακό σήμα και να απεικονισθεί και αποθηκεύονται ως ψηφιακή εικόνα. Η φωτεινότητα του σήματος εξαρτάται από τον αριθμό των δευτερογενών ηλεκτρονίων που φθάνουν στον ανιχνευτή. Εάν η δέσμη εισέρχεται στην επιφάνεια του δείγματος κάθετα προς την επιφάνεια, τότε η περιοχή είναι ενεργοποιημένη ομοιόμορφα γύρω από τον άξονα της δέσμης και ένας ορισμένος αριθμός ηλεκτρονίων "διαφεύγουν" μέσα από το δείγμα. Καθώς η γωνία πρόσπτωσης αυξάνεται, η απόσταση "διαφυγή" της μιας πλευράς της δέσμης θα μειωθεί, και περισσότερα δευτερεύοντα ηλεκτρόνια θα εκπέμπονται. Έτσι απότομες επιφάνειες και ακμές τείνουν να είναι πιο φωτεινές από επίπεδες επιφάνειες, γεγονός που οδηγεί σε εικόνες με μια καλά καθορισμένη, 53
54 τρισδιάστατη εμφάνιση. Χρησιμοποιώντας το σήμα από τα δευτερογενή ηλεκτρόνια, ανάλυση εικόνας μικρότερη από 0,5 nm είναι δυνατή Ανίχνευση των οπισθοσκεδαζόμενων ηλεκτρονίων Τα οπισθοσκεδαζόμενα ηλεκτρόνια (BSΕ) αποτελούνται από ηλεκτρόνια υψηλής ενέργειας που προέρχονται από την δέσμη ηλεκτρονίων, που αντανακλάται ή οπισθοσκεδάζεται από τον όγκο αλληλεπίδρασης του δείγματος από ελαστική σκέδαση λόγω των αλληλεπιδράσεων με τα άτομα του δείγματος. Δεδομένου ότι τα βαριά στοιχεία (με υψηλό ατομικό αριθμό) οπισθοσκεδάζουν ηλεκτρόνια πιο έντονα από ό, τι τα ελαφριά στοιχεία (χαμηλός ατομικός αριθμός), και έτσι εμφανίζονται φωτεινότερα στην εικόνα, τα BSE χρησιμοποιούνται για την ανίχνευση της αντίθεσης μεταξύ των περιοχών με διαφορετική χημική σύνθεση [106]. Ο Everhart Thornley ανιχνευτής, ο οποίος είναι συνήθως τοποθετημένος στη μια πλευρά του δείγματος, είναι αναποτελεσματικός για την ανίχνευση των οπισθοσκεδαζόμενων ηλεκτρονίων επειδή λίγες τέτοια ηλεκτρόνια εκπέμπονται υπό γωνία που φτάνει στον ανιχνευτή, και επειδή το θετικά φορτισμένο πλέγμα ανιχνεύσεως έχει μικρή ικανότητα να προσελκύει τα υψηλότερα ενεργειακά BSE ηλεκτρόνια. Ανιχνευτές οπισθοσκεδαζόμενων ηλεκτρονίων είναι τοποθετημένοι πάνω από το δείγμα σε διάταξη τύπου «ντόνατ», ομοκεντρικά με την δέσμη ηλεκτρονίων, μεγιστοποιώντας τη γωνία συλλογής. Οι ανιχνευτές BSE είναι συνήθως είτε τύπου σπινθηριστή ή ημιαγωγών. Όταν όλα τα τμήματα του ανιχνευτή χρησιμοποιούνται για τη συλλογή των ηλεκτρόνια συμμετρικά γύρω από τη δέσμη, παράγεται αντίθεση που σχετίζεται με τον ατομικό αριθμό. Ωστόσο, ισχυρή τοπογραφική αντίθεση παράγεται με τη συλλογή των οπισθοσκεδαζόμενων ηλεκτρονίων από μια πλευρά πάνω από το δείγμα χρησιμοποιώντας μία ασύμμετρη, κατευθυντική διάταξη ανιχνευτή BSE. Η προκύπτουσα αντίθεση εμφανίζεται ως φθορισμός της τοπογραφίας από εκείνη την πλευρά Ανάλυση του SEM Η χωρική ανάλυση του SEM εξαρτάται από το μέγεθος της κηλίδας των ηλεκτρονίων, η οποία με τη σειρά της εξαρτάται τόσο από το μήκος κύματος των ηλεκτρονίων όσο και από το ηλεκτρονικό-οπτικό σύστημα που παράγει τη δέσμη σάρωσης. Η ανάλυση περιορίζεται επίσης από το μέγεθος του όγκου αλληλεπίδρασης, ή την έκταση στην οποία το υλικό αλληλεπιδρά με την δέσμη των ηλεκτρονίων. Το μέγεθος της κηλίδας και ο όγκος 54
55 αλληλεπίδρασης είναι και τα δύο μεγάλα σε σύγκριση με τις αποστάσεις μεταξύ των ατόμων, με αποτέλεσμα η ανάλυση του SEM να μην είναι αρκετά υψηλή ώστε να δώσει εικόνα για μεμονωμένα άτομα, όπως είναι δυνατόν στο βραχύτερου μήκους κύματος (δηλαδή σε υψηλότερη ενέργεια) ηλεκτρονικό μικροσκόπιο (ΤΕΜ). Το SEM έχει πλεονεκτήματα, όμως, όπως είναι η ικανότητα να απεικονίζει μια συγκριτικά μεγάλη περιοχή του δείγματος. Έχει επίσης την ικανότητα να απεικονίζει bulk υλικά (όχι μόνο λεπτά υμένια). Ακόμα υπάρχει ποικιλία των αναλυτικών μέσων που διατίθενται για τη μέτρηση της σύνθεση και των ιδιοτήτων στο δείγμα. Ανάλογα με το όργανο, η ανάλυση μπορεί να είναι της τάξεως κάπου μεταξύ λιγότερο από 1 nm και 20 nm Μικροσκοπία Ατομικών Δυνάμεων (AFM) Η Μικροσκοπία ατομικών δυνάμεων (AFM) ή σαρωτική μικροσκοπία δυνάμεων (SFM) είναι μια πολύ υψηλής ανάλυσης μικροσκοπία σάρωσης με τη χρήση ανιχνευτή, με αποδεδειγμένη ανάλυση της τάξης των κλασμάτων του ενός νανομέτρου, πάνω από 1000 φορές καλύτερα από το οπτικό όριο διάθλασης. Ο πρόδρομος του AFM, το σαρωτικό μικροσκόπιο σήραγγας (STM), αναπτύχθηκε από τους Gerd Binnig και Heinrich Rohrer στις αρχές της δεκαετίας του 1980 στην IBM στη Ζυρίχη, μια εξέλιξη που τους χάρισε το βραβείο Νόμπελ Φυσικής το Οι Binnig, Quate και Gerber εφηύραν το πρώτο μικροσκόπιο ατομικών δυνάμεων το Το πρώτο εμπορικά διαθέσιμο ατομικό μικροσκόπιο εισήχθη το Το AFM είναι ένα από τα κύρια εργαλεία για την απεικόνιση, τη μέτρηση και το χειρισμό ύλης στην περιοχή της νανοκλίμακας. Οι πληροφορίες συγκεντρώνονται από την "αίσθηση" της επιφάνειας με ένα μηχανικό ανιχνευτή. Πιεζοηλεκτρικά στοιχεία που διευκολύνουν μικρές αλλά και ακριβείς κινήσεις με ηλεκτρονική εντολή επιτρέπουν την σάρωση με μεγάλη ακρίβεια. Σε μερικές παραλλαγές, ηλεκτρικά δυναμικά μπορούν επίσης να σαρωθούν με τη χρήση αγώγιμων ανιχνευτών (cantilevers) Βασικές αρχές Το AFM αποτελείται από έναν ανιχνευτή (cantilever) με ένα αιχμηρό tip (probe) στο άκρο του, ο οποίος χρησιμοποιείται για τη σάρωση της επιφάνειας του δείγματος. Το cantilever είναι τυπικά από πυρίτιο ή νιτρίδιο του πυριτίου με ακτίνα καμπυλότητας της κορυφής της τάξης των νανομέτρων. Όταν το tip φέρεται πολύ κοντά στην επιφάνεια του δείγματος, οι δυνάμεις μεταξύ του tip και του δείγματος οδηγούν σε εκτροπή του cantilever 55
56 σύμφωνα με το νόμο του Hooke. Ανάλογα με την περίσταση, οι δυνάμεις που μετρούνται με το AFM περιλαμβάνουν μηχανικές δυνάμεις επαφής, δυνάμεις van der Waals, τριχοειδείς δυνάμεις, χημικούς δεσμούς, ηλεκτροστατικές δυνάμεις, μαγνητικές δυνάμεις, δυνάμεις επιδιαλύτωσης, κλπ. Μαζί με τη μέτρηση της δύναμης, και άλλες ιδιότητες μπορούν ταυτόχρονα να μετρηθούν μέσω της χρήσης εξειδικευμένων τύπων ανιχνευτή (θερμική μικροσκοπία σάρωσης). Τυπικά, η εκτροπή μετράται χρησιμοποιώντας μία κηλίδα λέιζερ που ανακλάται από την επιφάνεια της κορυφής του cantilever σε μια σειρά φωτοδιόδων. Αυτά τα cantilever κατασκευάζονται με πιεζοηλεκτρικά στοιχεία που δρουν ως μανόμετρα τάσεως. Εάν το tip εκτελούσε σάρωση σε σταθερό ύψος, θα υπήρχε ο κίνδυνος να συγκρουστεί με την επιφάνεια, προκαλώντας ζημιές. Ως εκ τούτου, στις περισσότερες περιπτώσεις, ένας μηχανισμός ανάδρασης χρησιμοποιείται για να προσαρμόσει απόσταση μεταξύ tip και δείγματος για να διατηρηθεί μία σταθερή δύναμη μεταξύ του tip και του δείγματος. Παραδοσιακά, το δείγμα τοποθετείται σε έναν πιεζοηλεκτρικό σωλήνα, που μπορεί να κινεί το δείγμα στην κατεύθυνση ζ για τη διατήρηση μιας σταθερής δύναμης, και στις χ και γ διευθύνσεις για τη σάρωση του δείγματος. Εναλλακτικά, μια διαμόρφωση τριπόδου των τριών πιεζοηλεκτρικών κρυστάλλων μπορούν να χρησιμοποιηθούν, με καθένα από αυτούς υπεύθυνο για τη σάρωση στις χ, y και z κατευθύνσεις. Αυτό εξαλείφει μερικά από τα παραμορφωτικά σφάλματα που παρατηρούνται με τη χρήση ενός σωλήνα σάρωσης. Σε νεώτερα σχέδια, η κορυφή τοποθετείται σε ένα κατακόρυφο πιεζοηλεκτρικό σαρωτή ενώ το δείγμα σαρώνεται στις χ και ψ διευθύνσεις χρησιμοποιώντας ένα άλλο πιεζοηλεκτρικό μπλοκ. Ο προκύπτον χάρτης της περιοχής z = f (x, y) αντιπροσωπεύει την τοπογραφία του δείγματος. Το AFM μπορεί να λειτουργεί με έναν αριθμό τρόπων, ανάλογα με την εφαρμογή. Σε γενικές γραμμές, οι πιθανές λειτουργίες απεικόνισης διακρίνονται σε στατικές (contact mode) μεθόδους και μια ποικιλία δυναμικών (non-contact, tapping mode), όπου το cantilever πάλλεται Τρόποι απεικόνισης Οι πρωτογενείς τρόποι λειτουργίας για ένα AFM είναι στατική λειτουργία και δυναμική λειτουργία. Σε στατική κατάσταση λειτουργίας, το cantilever σέρνεται σε όλη την επιφάνεια του δείγματος και τα περιγράμματα της επιφάνειας μετρούνται απευθείας χρησιμοποιώντας την εκτροπή του cantilever. Στη δυναμική λειτουργία, το cantilever ταλαντώνεται εξωτερικά στην ή κοντά στην θεμελιώδη συχνότητα συντονισμού του ή στην αρμονική. Το πλάτος της ταλάντωσης, η φάση και η συχνότητα συντονισμού είναι 56
57 τροποποιημένα από δυνάμεις αλληλεπίδρασης μεταξύ tip και δείγματος. Αυτές οι αλλαγές στην ταλάντωση σε σχέση με την εξωτερική ταλάντωση αναφοράς παρέχουν πληροφορίες σχετικά με τα χαρακτηριστικά του δείγματος Contact mode Στο στατικό τρόπο λειτουργίας, η παραμόρφωση του στατικού tip χρησιμοποιείται ως σήμα ανάδρασης. Επειδή η μέτρηση του στατικού σήματος είναι επιρρεπής σε θόρυβο και μετατόπισης, οι χαμηλής ακαμψίας ανιχνευτές χρησιμοποιούνται για να ενισχύσουν το σήμα εκτροπής. Ωστόσο, κοντά στην επιφάνεια του δείγματος, οι ελκτικές δυνάμεις μπορεί να είναι αρκετά ισχυρές, προκαλώντας το tip για να εισέλθει στην επιφάνεια. Έτσι η στατική λειτουργία AFM σχεδόν πάντα γίνεται σε επαφή, όπου η συνολική δύναμη είναι απωθητική. Κατά συνέπεια, αυτή η τεχνική ονομάζεται συνήθως "λειτουργία επαφής". Στη λειτουργία επαφής, η δύναμη μεταξύ του άκρου και της επιφάνειας διατηρείται σταθερή κατά τη σάρωση με τη διατήρηση μιας σταθερής εκτροπής Non-Contact Mode Στη λειτουργία αυτή, το άκρο του ανιχνευτή δεν έρχεται σε επαφή με την επιφάνεια του δείγματος. Ο ανιχνευτής αντί αυτού ταλαντώνεται σε συχνότητα λίγο πάνω από τη συχνότητα συντονισμού του, όπου το εύρος της ταλάντωσης είναι συνήθως μερικά νανόμετρα (<10 nm). Οι δυνάμεις van der Waals, οι οποίες είναι ισχυρότερες από 1 nm έως 10 nm πάνω από την επιφάνεια, ή οποιαδήποτε άλλη μεγάλη δύναμη το φάσμα της οποίας εκτείνεται πάνω από την επιφάνεια δρα για να μειώσει την συχνότητα συντονισμού του ανιχνευτή. Αυτή η μείωση στην συχνότητα συντονισμού σε συνδυασμό με το σύστημα βρόχου ανάδρασης διατηρεί σταθερό το πλάτος ταλάντωσης ή τη συχνότητα με την προσαρμογή της μέσης απόστασης tip δείγματος. Η μέτρηση της απόστασης tip δείγματος σε κάθε (x, y) σημείο δεδομένων επιτρέπει στο λογισμικό σάρωσης να κατασκευάσει μια τοπογραφική εικόνα της επιφάνειας του δείγματος. Η λειτουργία non-contact AFM δεν υποφέρει από τις επιπτώσεις αποδόμησης του tip ή του δείγματος που παρατηρείται μερικές φορές μετά τη λήψη πολλών σαρώσεων με τη λειτουργία επαφής στο AFM. Το γεγονός αυτό καθιστά τη λειτουργία μη επαφής AFM προτιμότερη να χρησιμοποιηθεί για τη μέτρηση μαλακών δειγμάτων. Στην περίπτωση των άκαμπτων δειγμάτων, οι επαφής και μη-επαφής εικόνες μπορεί να φανούν το ίδιο. Ωστόσο, 57
58 εάν μερικές μονοστοιβάδες προσροφημένου ρευστού κείτονται επί της επιφανείας ενός άκαμπτου δείγματος, οι εικόνες μπορεί να φαίνονται εντελώς διαφορετικές. Μια AFM λειτουργία σε λειτουργία επαφής θα διεισδύσει στο υγρό στρώμα για την εικόνα της υποκείμενης επιφάνειας, ενώ σε κατάσταση μη-επαφής θα κυμαίνεται πάνω από το προσροφημένο στρώμα υγρού δίνοντας εικόνα τόσο για το υγρό όσο και για την επιφάνεια. Σχέδια για τη δυναμική λειτουργία περιλαμβάνουν διαμόρφωση συχνότητας και πιο συχνά διαμόρφωση πλάτους (amplitude modulation). Στην διαμόρφωση συχνότητας, αλλαγές στη συχνότητα ταλάντωσης παρέχουν πληροφορίες σχετικά με τις αλληλεπιδράσεις tipδείγματος. Η συχνότητα μπορεί να μετρηθεί με πολύ μεγάλη ευαισθησία και, συνεπώς, ο τρόπος διαμόρφωσης της συχνότητας επιτρέπει τη χρήση πολύ δύσκαμπτων cantilever [109]. Στην διαμόρφωση πλάτους, αλλαγές στο πλάτος ταλάντωσης ή τη φάση παρέχουν το σήμα ανάδρασης για την απεικόνιση. Στην διαμόρφωση πλάτους, οι μεταβολές στη φάση της ταλάντωσης μπορεί να χρησιμοποιηθούν για τη διάκριση μεταξύ των διαφόρων τύπων των υλικών επί της επιφανείας. Η διαμόρφωση εύρους μπορεί να λειτουργήσει είτε σε λειτουργία μη-επαφής ή στο καθεστώς διακοπτόμενης επαφής. Σε δυναμική λειτουργία επαφής, ο ανιχνευτής ταλαντώνεται έτσι ώστε η απόσταση διαχωρισμού μεταξύ του άκρου του και της επιφάνειας του δείγματος να μπορεί να διαμορφωθεί Tapping Mode Μονές αλυσίδες πολυμερών (0,4 nm πάχους) έχουν καταγραφεί σε λειτουργία tapping σε υδατικό μέσο με διαφορετικό ph [110]. Σε συνθήκες περιβάλλοντος, τα περισσότερα δείγματα αναπτύσσουν ένα υγρό στρώμα μηνίσκου. Εξαιτίας αυτού του γεγονότος, πρέπει να διατηρείται η άκρη του ανιχνευτή αρκετά κοντά στο δείγμα ώστε μια μικρή εμβέλεια δυνάμεων να καταστεί ανιχνεύσιμη ενώ παράλληλα εμποδίζεται το άκρο από το να κολλήσει στην επιφάνεια και αυτό παρουσιάζει ένα σημαντικό πρόβλημα για δυναμική λειτουργία μη επαφής σε συνθήκες περιβάλλοντος. Η δυναμική λειτουργία επαφής (επίσης ονομάζεται intermittent contact ή λειτουργία tapping) αναπτύχθηκε για να παρακαμφθεί αυτό το πρόβλημα [111]. Σε λειτουργία tapping, που ονομάζεται επίσης "AC Mode" ή "διακοπτόμενη λειτουργία επαφής", το cantilever οδηγείται να ταλαντεύονται πάνω-κάτω γύρω από τη συχνότητα συντονισμού του από ένα μικρό πιεζοηλεκτρικό στοιχείο συναρμολογημένο στην άκρη του tip παρόμοια με τη λειτουργία μη-επαφής. Ωστόσο, το πλάτος αυτής της ταλάντωσης είναι μεγαλύτερο από 10 nm, συνήθως από 100 έως 200 nm. Η αλληλεπίδραση των δυνάμεων που επενεργούν επί του ανιχνευτή όταν η κορυφή έρχεται κοντά στην 58
59 επιφάνεια, δυνάμεις Van der Waals, διπόλου-διπόλου, ηλεκτροστατικές δυνάμεις, κλπ. προκαλούν το πλάτος αυτής της ταλάντωσης να μειώνεται καθώς το άκρο πλησιάζει στο δείγμα. Μια tapping εικόνα AFM επομένως παράγεται με απεικόνιση των δυνάμεων που αλληλεπιδρούν μεταξύ της άκρης του ανιχνευτή και της επιφάνειας του δείγματος [112]. Αυτή η μέθοδος " tapping " μειώνει τη ζημία που γίνεται στην επιφάνεια και στο άκρο σε σύγκριση με αυτή που γίνεται σε κατάσταση επαφής. Η tapping λειτουργία είναι αρκετά ήπια ακόμα και για την οπτικοποίηση των υποστηριζόμενων λιπιδικών διπλοστιβάδων ή προσροφημένων μεμονωμένων μορίων πολυμερούς σε υγρό μέσο. Με τις κατάλληλες παραμέτρους σάρωσης, η διαμόρφωση των μεμονωμένων μορίων μπορεί να παραμείνει αμετάβλητη για ώρες [110] Βιολογικές εφαρμογές Η φασματοσκοπία δυνάμεων χρησιμοποιείται στη βιοφυσική για να μετρήσει τις δυνάμεις αλληλεπίδρασης μεταξύ μιας πρωτεΐνης και του συνδέτη [113], και για τη μέτρηση των μηχανικών ιδιοτήτων του ζωντανών υλικών (όπως ιστών ή κυττάρων) [114]. Όσον αφορά τη μικροσκοπίες σάρωσης, το AFM χρησιμοποιείται συχνά με επιτυχία σε ένα ευρύ φάσμα επιστημονικών κλάδων, όπως η βιολογία, η φυσική στερεάς κατάστασης, η επιστήμη των υλικών. Το AFM έχει εξελιχθεί σε μία μέθοδο απεικόνισης που αποδίδει δομικές λεπτομέρειες των βιολογικών δειγμάτων όπως πρωτεΐνες, νουκλεϊνικά οξέα, μεμβράνες, και κύτταρα στο φυσικό τους περιβάλλον [ ]. Το AFM είναι μια μοναδική τεχνική μια λογική αναλογία σήματος προς θόρυβο υπό φυσιολογικές συνθήκες. Ως αποτέλεσμα των συνεχών εξελίξεων στην προετοιμασία του δείγματος, τις τεχνικές απεικόνισης, καθώς και οργάνων, το AFM είναι τώρα μια τεχνική που συμπληρώνει την κρυσταλλογραφία ακτίνων-χ και την ηλεκτρονική μικροσκοπία (ΕΜ), για τον προσδιορισμό πρωτεϊνικών δομών, για παράδειγμα. Η ΕΜ συμπληρώνει τις προηγούμενες επιτρέποντας την οπτικοποίηση βιολογικών δειγμάτων σε ρυθμιστικά διαλύματα που διατηρούν φυσική δομή τους επί μακρές χρονικές περιόδους. Το AFM δεν βασίζεται σε μέσους όρους συμμετρίας και κρυστάλλωσης, ως εκ τούτου αποκαλύπτει ελαττώματα και δομικές ανωμαλίες που δεν παρατηρείται με τις κλασσικές μετρήσεις [119]. Σε αντίθεση με την ηλεκτρονική μικροσκοπία, το AFM αποδίδει τρισδιάστατους χάρτες με μια εξαιρετικά καλή κάθετη ανάλυση (λιγότερο από ένα νανόμετρο). Επιπλέον όσον αφορά την απεικόνιση υψηλής ανάλυσης πρωτεϊνών, νουκλεοτιδίων, μεμβρανών, και 59
60 ζωντανών κυττάρων [115], η μέτρηση των μηχανικών δυνάμεων στο μοριακό επίπεδο παρέχει λεπτομερείς γνώσεις για τη λειτουργία και τη δομή των βιομοριακών συυστημάτων [118]. Δια-και ενδομοριακές αλληλεπιδράσεις μπορούν να μελετηθούν άμεσα στο μοριακό επίπεδο. Σε άλλη περίπτωση, καθορίζονται οι δυνάμεις που εξασκούνται επί ενός συμπλόκου υποδοχέα-συνδέτη και η διαδικασία αποσύνδεσης μπορεί να παρακολουθείται με την πάροδο του χρόνου. Με τα δεδομένα που λαμβάνονται από μετρήσεις δυνάμεων, οι μοριακές αλληλεπιδράσεις μπορεί να αναλυθούν από την άποψη των κινητικών σταθερών ρυθμού. Σε σύγκριση με το σύνολο των συμβατικών μεθόδων, τα πειράματα ενός μόνο μορίου (single mollecule experiments) προσφέρουν αρκετά πλεονεκτήματα. Πρώτον, με τη διεξαγωγή πολλών διαδοχικών μετρήσεων, η κατανομή των μοριακών ιδιοτήτων ανομοιογενών συστημάτων μπορεί να προσδιοριστεί. Δεύτερον, τροχιές ένας μόνο μορίου, δεδομένου ότι είναι άμεσα συνδεδεμένα με τις διακυμάνσεις του συστήματος, παρέχουν δυναμικές και στατιστικές πληροφορίες που είναι συχνά κρυμμένες σε σύνολο μέσων όρων των αποτελεσμάτων. Τέλος, είναι δυνατόν να παρακολουθηθούν σπάνια κατοικημένες μεταβατικές καταστάσεις σε πραγματικό χρόνο, οι οποίες είναι δύσκολο ή αδύνατο να συλληφθούν χρησιμοποιώντας συμβατικές μεθόδους [120, 121] Υψηλής ευκρίνειας απεικόνιση βιολογικών δειγμάτων Η κατανόηση του πώς τα συγκροτήματα των βιομορίων συναρμολογούνται υπό φυσιολογικές συνθήκες είναι θεμελιώδους σημασίας για τη διαλεύκανση της λειτουργίας τους. Συνεπώς, σημαντική προσοχή έχει δοθεί στην υψηλής ανάλυσης τοπογραφική απεικόνιση των μεμονωμένων βιολογικών μορίων και των συμπλοκών τους. Το AFM λειτουργεί με σάρωση ένας αιχμηρού ανιχνευτή πάνω σε μία επιφάνεια, ρυθμίζοντας τη δύναμη που εφαρμόζεται στο δείγμα σε όσο το δυνατόν ελάχιστες τιμές που να εμποδίζουν τη μετατόπιση ή καταστροφή των ασθενώς προσκολλημένων βιομοριακών συμπλόκων [122,123] Εικόνα 4. Τα προβλήματα που προκύπτουν από δυσμενείς αλληλεπιδράσεις μεταξύ ανιχνευτή και επιφάνειας σε λειτουργία επαφής AFM, ειδικά από τις πλευρικές δυνάμεις, σε μεγάλο βαθμό έχουν ξεπεραστεί με την ανάπτυξη των δυναμικών μεθόδων μικροσκοπίας δύναμης (DFM), που χρησιμοποιούνται κυρίως για τη διερεύνηση των μαλακών βιολογικών μεμβρανών και υπερμοριακών συμπλόκων [124,125]. Με την αξιοποίηση της απευθείας διέγερσης του ανιχνευτή σε μαγνητική ac λειτουργία AFM (όπου η ταλάντωση του άκρου επιτυγχάνεται από ένα εξωτερικό μαγνητικό πεδίο), οι πλευρικές δυνάμεις μπορούν να ελαχιστοποιηθούν και η ταλάντωση του tip να ελέγχεται σωστά [125,126]. Οι Möller et 60
61 al.[127] έχουν πρόσφατα αποδείξει ότι το DFM επιτρέπει ακόμη και την απεικόνιση της πρωτεΐνης σε σκληρές επιφάνειες με παρόμοια ανάλυση με τη λειτουργία επαφής στο AFM. Απαραίτητη προϋπόθεση για τη λήψη εικόνων υψηλής ποιότητας από AFM των βιολογικών δειγμάτων είναι η σφιχτή ακινητοποίηση σε μια επίπεδη υποστήριξη. Η απλούστερη και πιο κοινή τεχνική ακινητοποίησης είναι φυσική προσρόφηση από το διάλυμα. Η μίκα, είναι η συχνότερα χρησιμοποιούμενη υποστήριξη για βιολογικές εφαρμογές, και είναι ένα στρωματοποιημένο μεταλλικό στοιχείο που μπορεί να διασπάται εύκολα, οδηγώντας σε καθαρές, ατομικές επίπεδες επιφάνειες. Επειδή η επιφάνεια της μίκα είναι αρνητικά φορτισμένη σε ουδέτερο pη, απλή προσρόφηση των θετικά φορτισμένων δειγμάτων είναι επαρκής για την σταθερή ακινητοποίηση. Ακόμη και τα αρνητικά φορτισμένα μόρια (π.χ. DNA) μπορούν να προσροφώνται φυσικά επί των επιφανειών μίκα όταν πολυσθενή κατιόντα (όπως Νί2+, Mg2 +, Zn2+) είναι παρόντα σε ρυθμιστικά διαλύματα [128] Πλεονεκτήματα και μειονεκτήματα Ακριβώς όπως και κάθε άλλο εργαλείο, η χρησιμότητα ενός AFM έχει περιορισμούς. Κατά τον προσδιορισμό εάν ή όχι η ανάλυση ενός δείγματος με ένα AFM είναι κατάλληλη, υπάρχουν διάφορα πλεονεκτήματα και μειονεκτήματα που θα πρέπει να ληφθούν υπόψη. Πλεονεκτήματα Το AFM έχει αρκετά πλεονεκτήματα σε σχέση με το ηλεκτρονικό μικροσκόπιο σάρωσης (SEM). Σε αντίθεση με το ηλεκτρονικό μικροσκόπιο το οποία παρέχει μία δύο διαστάσεων προεξοχή ή μια δισδιάστατη εικόνα ενός δείγματος, το AFM παρέχει ένα τρισδιάστατο προφίλ επιφανείας. Επιπλέον, τα δείγματα από το AFM δεν απαιτούν καμία ειδική επεξεργασία (όπως μέταλλου / άνθρακα επικαλύψεις) που θα αλλάξει μη αντιστρεπτά ή θα βλάψει το δείγμα, και δεν έχουν artifacts λόγω φόρτισης στην τελική εικόνα. Ενώ ένα ηλεκτρονικό μικροσκόπιο χρειάζεται ένα ακριβό περιβάλλον κενού για τη σωστή λειτουργία, οι περισσότεροι τρόποι λειτουργίας AFM μπορεί να εφαρμοστούν πολύ καλά στον ατμοσφαιρικό αέρα ή ακόμη και σε ένα υγρό περιβάλλον. Αυτό καθιστά δυνατή τη μελέτη βιολογικών μακρομορίων και ακόμη ζωντανών οργανισμών. Ακόμα, το AFM μπορεί να παρέχει υψηλότερη ανάλυση από ότι το SEM. Έχει αποδειχθεί ότι μπορεί να δώσει πραγματική ατομική ανάλυση σε υπέρ-υψηλού κενού (UHV) και, πιο πρόσφατα, σε υγρά περιβάλλοντα. Η υψηλή ανάλυση που επιτυγχάνεται στο AFM είναι συγκρίσιμη σε ανάλυση μικροσκοπίου σάρωσης σήραγγας και ηλεκτρονικού μικροσκοπίου. 61
62 Μειονεκτήματα Ένα μειονέκτημα του AFM σε σύγκριση με το μικροσκόπιο σάρωσης ηλεκτρονίων (SEM) είναι το μέγεθος εικόνας μονής σάρωσης. Σε ένα πέρασμα, το SEM μπορεί να απεικονίσει μια περιοχή της τάξης των τετραγωνικών χιλιοστών με ένα βάθος πεδίου της τάξεως των χιλιοστών, ενώ το AFM μπορεί να δώσει μόνο εικόνα σε ένα μέγιστο ύψος της τάξης των μm και μια μέγιστη επιφάνεια σαρώσεως περίπου μικρόμετρα. Μία μέθοδος βελτίωσης του μεγέθους της σαρωμένης περιοχής για το AFM είναι με τη χρήση παράλληλων ανιχνευτών με ένα τρόπο παρόμοιο με εκείνο της πολλαπλής αποθήκευσης δεδομένων. Η ταχύτητα σάρωσης του AFM είναι επίσης ένας περιορισμός. Παραδοσιακά, μια διάταξη AFM δεν μπορεί να σαρώσει τις εικόνες τόσο γρήγορα όσο μια διάταξη SEM. Απαιτεί αρκετά λεπτά για μία τυπική σάρωση, ενώ ένα SEM είναι ικανό να σαρώσει σε σχεδόν πραγματικό χρόνο, αν και σε σχετικά χαμηλή ποιότητα. Ο σχετικά αργός ρυθμός σάρωσης κατά τη διάρκεια της AFM απεικόνισης συχνά οδηγεί σε θερμική μετατόπιση στην εικόνα [130,131,132] κάνοντας το AFM λιγότερο κατάλληλο για ακριβή μέτρηση των αποστάσεων μεταξύ τοπογραφικών χαρακτηριστικών της εικόνας. Ωστόσο, αρκετά σχέδια ταχείας δράσης [133,134] προτάθηκαν για την αύξηση της παραγωγικότητας του μικροσκοπίου σάρωσης όπως αυτό που ονομάζεται VideoAFM (οι λογικής ποιότητας εικόνες που λαμβάνονται με VideoAFM είναι γρηγορότερα από το μέσο όρο στο SEM). Για να εξαλειφθούν οι στρεβλώσεις που προκαλούνται στην εικόνα από τη θερμική μετατόπιση, διάφορες μέθοδοι έχουν εισαχθεί [123,131,132]. Οι εικόνες από AFM μπορούν επίσης να επηρεαστούν από μηγραμμικότητα, φαινόμενο υστερήσεως, και ερπυσμό του πιεζοηλεκτρικού υλικού και διαμάχη μεταξύ των x, y, z αξόνων που μπορεί να απαιτούν βελτίωση του λογισμικού και ειδικά φίλτρα. Τέτοιο φιλτράρισμα θα μπορούσε να «ισιώσει» τα πραγματικά τοπογραφικά χαρακτηριστικά. Ωστόσο, νεότερες διατάξεις AFM χρησιμοποιούν λογισμικό διορθώσεως πραγματικού χρόνου ή κλειστού βρόχου σαρωτές που εξαλείφουν πρακτικά τα προβλήματα αυτά. Όπως και με οποιαδήποτε άλλη τεχνική απεικόνισης, υπάρχει η δυνατότητα ύπαρξης επαναλαμβανόμενων μοτίβων στην εικόνα (artifacts), γεγονός το οποίο μπορεί να προκληθεί από μια ακατάλληλη άκρη, ένα φτωχό περιβάλλον λειτουργίας, ή ακόμα και από το ίδιο το δείγμα. Αυτά τα είδωλα μερικές φορές είναι αναπόφευκτα, ωστόσο, η εμφάνιση και η επίδρασή τους στα αποτελέσματα μπορεί να μειωθεί με διάφορες μεθόδους. Τα artifacts που προκύπτουν από ένα πολύ χοντρό άκρο μπορούν να προκληθούν για παράδειγμα με ακατάλληλο χειρισμό ή με de facto συγκρούσεις με το δείγμα, είτε με σάρωση πολύ γρήγορα ή λόγω τραχείας επιφάνειας του δείγματος που προκαλεί τη φθορά του tip. 62
63 ΚΕΦΑΛΑΙΟ 5. Άλλες τεχνικές Φασματοσκοπία Υπεριώδους-Ορατού Η φασματοσκοπία ή φασματοφωτομετρία Υπεριώδους-ορατού (UV-Vis) αναφέρεται σε φασματοσκοπία απορρόφησης ή φασματοσκοπία ανάκλασης στην φασματική περιοχή από το υπεριώδες ως και το ορατό. Αυτό σημαίνει ότι χρησιμοποιεί το φως που κυμαίνεται στην περιοχή του ορατού και γειτονικά (εγγύς UV και εγγύς υπέρυθρο (NIR)). Η απορρόφηση ή ανάκλαση του φωτός στην ορατή περιοχή επηρεάζει άμεσα το αντιληπτό χρώμα των εμπλεκόμενων χημικών. Σε αυτή την περιοχή του ηλεκτρομαγνητικού φάσματος, τα μόρια υποβάλλονται σε ηλεκτρονικές μεταπτώσεις. Η τεχνική αυτή είναι συμπληρωματική της φασματοσκοπίας φθορισμού, η οποία ασχολείται με ότι έχει να κάνει με τις μεταβάσεις από τη διεγερμένη κατάσταση στην βασική κατάσταση, ενώ η φασματοσκοπία απορρόφηση μέτρα μεταβάσεις από την βασική στην διεγερμένη κατάσταση [133] Αρχή της απορρόφησης υπεριώδους-ορατού Μόρια που περιέχουν π-ηλεκτρόνια ή n-ηλεκτρόνια μπορούν να απορροφήσουν την ενέργεια με τη μορφή υπεριώδους ή ορατού φωτός για να διεγείρουν τα ηλεκτρόνια σε υψηλότερα αντί-δεσμικά μοριακά τροχιακά [134]. Όσο πιο εύκολα διεγείρονται τα ηλεκτρόνια (δηλαδή όσο μικρότερο ενεργειακό χάσμα υπάρχει μεταξύ της ΗΟΜΟ και LUMO ), τόσο μεγαλύτερο είναι το μήκος κύματος του φωτός που μπορεί να απορροφηθεί Εφαρμογές Η φασματοσκοπία UV / Vis χρησιμοποιείται συνήθως στην αναλυτική χημεία για τον ποσοτικό προσδιορισμό των διαφόρων αναλυτών, όπως ιόντα μετάλλων μεταπτώσεως, οργανικών ενώσεων, και των βιολογικών μακρομορίων. Η φασματοσκοπική ανάλυση συνήθως πραγματοποιείται σε διαλύματα αλλά στερεά και αέρια μπορεί επίσης να μελετηθούν. Τα διαλύματα ιόντων των μετάλλων μεταπτώσεως μπορούν να είναι χρωματισμένα (απορροφούν το ορατό φως) επειδή δ ηλεκτρόνια εντός των ατόμων των μετάλλων μπορούν να διεγερθούν από μια κατάσταση σε μια άλλη. Το χρώμα των διαλυμάτων ιόντων μετάλλων 63
64 επηρεάζεται έντονα από την παρουσία άλλων ειδών, όπως ορισμένα ανιόντα ή συνδέτες. Οι οργανικές ενώσεις, ιδιαίτερα εκείνες με υψηλό βαθμό σύζευξης όπως πχ DNA, RNA, πρωτεΐνες, απορροφούν επίσης φως στην ορατή ή UV περιοχή του ηλεκτρομαγνητικού φάσματος. Οι διαλύτες για τους προσδιορισμούς αυτούς είναι συχνά νερό (ή PBS) για τις υδατοδιαλυτές ενώσεις, ή αιθανόλη (ή χλωροφόρμιο) για τις ενώσεις διαλυτές σε οργανικούς διαλύτες. Οι οργανικοί διαλύτες μπορούν να έχουν σημαντική απορρόφηση στο UV, και δεν είναι όλοι οι διαλύτες κατάλληλοι για χρήση σε UV φασματοσκοπία. Η αιθανόλη έχει ασθενή απορρόφηση στα περισσότερα μήκη κύματος. Η πολικότητα του διαλύτης και το pη μπορεί να επηρεάσουν το φάσμα απορρόφησης μιας οργανικής ένωσης. Ο νόμος των Beer-Lambert ορίζει ότι η απορρόφηση ενός διαλύματος είναι ευθέως ανάλογη προς τη συγκέντρωση των σωματιδίων απορροφήσεως στο διάλυμα και το μήκος διαδρομής μέσα στο όργανο μέτρησης [135]. Έτσι, για ένα σταθερό μήκος διαδρομής, η φασματοσκοπία UV / Vis μπορεί να χρησιμοποιηθεί για τον προσδιορισμό της συγκέντρωσης του απορροφητή σε ένα διάλυμα. Είναι πολύ σημαντικό να γνωρίζει κάποιος το πόσο γρήγορα μεταβάλλεται η απορρόφηση με τη συγκέντρωση. Αυτό μπορεί να ληφθεί από αναφορές (πίνακες των συντελεστών μοριακής αποσβέσεως), ή ακριβέστερα, να προσδιοριστεί από μια καμπύλη βαθμονόμησης η αναφοράς. Ένα φασματοφωτόμετρο UV / Vis μπορεί να χρησιμοποιηθεί ως ανιχνευτής για ανάλυση HPLC. Για ακριβή αποτελέσματα, η αντίδραση του μέσου με τον αναλυτή στο άγνωστο δείγμα θα πρέπει να συγκριθεί με την απόκριση σε ένα πρότυπο(τυφλό δείγμα). Αυτή η διαδικασία είναι παρόμοια με τη χρήση των καμπυλών βαθμονόμησης ή αναφοράς. Η απόκριση (το ύψος της κορυφής) για μία συγκεκριμένη συγκέντρωση είναι γνωστή ως ο συντελεστή απόκρισης (response factor). Τα μήκη κύματος των κορυφών απορρόφησης μπορεί να συσχετιστούν με τους τύπους των δεσμών σε ένα δεδομένο μόριο και είναι πολύτιμα για τον προσδιορισμό των λειτουργικών ομάδων που υπάρχουν σε ένα μόριο. Οι κανόνες Woodward-Fieser, για παράδειγμα, είναι ένα σύνολο από εμπειρικές παρατηρήσεις που χρησιμοποιούνται για την πρόβλεψη του λmax, του μήκους κύματος της πιο έντονης UV / Vis απορρόφησης, για συζευγμένες οργανικές ενώσεις όπως τα διένια και οι κετόνες. Το φάσμα από μόνο του δεν είναι, ωστόσο, μια ειδική δοκιμή για οποιοδήποτε δεδομένο δείγμα. Η φύση του διαλύτη, το pη του διαλύματος, η θερμοκρασία, οι συγκεντρώσεις των ηλεκτρολυτών, και η παρουσία άλλων ουσιών μπορούν να επηρεάσουν το φάσμα απορρόφησης. Πειραματικές παραλλαγές όπως το πλάτος της σχισμής του φασματοφωτομέτρου θα μεταβάλλει επίσης το φάσμα. Για 64
65 να χρησιμοποιηθεί η UV / Vis φασματοσκοπία για ανάλυση, αυτές οι μεταβλητές πρέπει να ελέγχονται ή να λαμβάνονται υπόψη για τον προσδιορισμό των ουσιών που υπάρχουν [136] Νόμος Beer-Lambert Η μέθοδος χρησιμοποιείται πιο συχνά για ποσοτικούς προσδιορισμούς των συγκεντρώσεων των μορίων που απορροφούν σε ένα διάλυμα, χρησιμοποιώντας το νόμο των Beer-Lambert: Α = log 10 (Ιο / I) = ε*c*l όπου Α είναι η μετρoύμενη απορρόφηση, Ιο είναι η ένταση του προσπίπτοντος φωτός σε ένα δεδομένο μήκος κύματος, Ι είναι η ένταση του φωτός που εξέρχεται, L το μήκος διαδρομής μέσω του δείγματος, και c η συγκέντρωση των σωματιδίων απορροφήσεως. Για κάθε είδος και μήκος κύματος, το ε είναι μια σταθερά γνωστή ως μοριακή απορροφητικότητα ή συντελεστής απόσβεσης. Η σταθερά αυτή είναι μια θεμελιώδης μοριακή ιδιότητα σε ένα δεδομένο διαλύτη, σε μια συγκεκριμένη θερμοκρασία και πίεση, και έχει μονάδες 1 / Μ * cm. Η απορρόφηση και η απόσβεση ε μερικές φορές ορίζονται με βάση τον φυσικό λογάριθμο e αντί του δεκαδικού λογαρίθμου. Ο νόμος Beer-Lambert είναι χρήσιμος για τον χαρακτηρισμό πολλών ενώσεων Φασματοφωτόμετρο Υπεριώδους-ορατού Το μέσο που χρησιμοποιείται στην φασματοσκοπία υπεριώδους-ορατού ονομάζεται φασματοφωτόμετρο UV / Vis. Μετρά την ένταση του φωτός που διέρχεται μέσω ενός δείγματος (Ι), και τη συγκρίνει με την ένταση του φωτός όταν αυτό περνά μέσω του δείγματος (Ιο). Η αναλογία Ι / Ιο καλείται διαπερατότητα, και συνήθως εκφράζεται ως εκατοστιαίο ποσοστό (% Τ). Η απορρόφηση, Α, βασίζεται στην διαπερατότητα: Τα βασικά μέρη ενός φασματοφωτομέτρου είναι μία πηγή φωτός, μία βάση για το δείγμα, ένα πλέγμα περίθλασης σε έναν μονοχρωμάτορα ή ένα πρίσμα για να διαχωριστούν τα διαφορετικά μήκη κύματος του φωτός, και ένας ανιχνευτής. Η πηγή ακτινοβολίας αποτελείται συχνά από ένα νήμα βολφραμίου ( nm), ένα λαμπτήρα τόξου από δευτέριο, που είναι συνεχής πάνω από την υπεριώδη περιοχή ( nm), έναν Xenon λαμπτήρα τόξου, ο οποίος είναι συνεχής από 160-2,000 nm, ή πιο πρόσφατα, δίοδοι 65
66 εκπομπής φωτός (LED) [137] για τα ορατά μήκη κύματος. Ο ανιχνευτής είναι τυπικά ένας σωλήνας φωτοπολλαπλασιαστής, μία φωτοδίοδος, μία σειρά φωτοδιόδων ή μια chargecoupled device (CCD). Οι ανιχνευτές μιας φωτοδιόδου και οι σωλήνες/φωτοπολλαπλασιαστές χρησιμοποιούνται για τη σάρωση με μονοχρωμάτορες, οι οποία φιλτράρουν το φως, έτσι ώστε μόνο φως ενός ενιαίου μήκους κύματος να φθάνει στον ανιχνευτή σε ένα χρόνο Διάγραμμα μονής δέσμης UV / Vis φασματοφωτομέτρου Ένα φασματοφωτόμετρο μπορεί να είναι είτε μονής δέσμης ή διπλής δέσμης. Σε ένα μονής δέσμης φασματοφωτόμετρο, όλο το φως περνά μέσα από την κυψελίδα του δείγματος. Η Ιο πρέπει να μετράται με την αφαίρεση του δείγματος. Αυτός ήταν ο πρώτος σχεδιασμός και χρησιμοποιείται ακόμα ευρέος στους τομείς της διδασκαλίας και σε βιομηχανικά εργαστήρια. Σε ένα όργανο διπλής δέσμης, το φως χωρίζεται σε δύο δέσμες πριν φτάσει στο δείγμα. Η μία δέσμη χρησιμοποιείται ως αναφορά, ενώ η άλλη δέσμη περνά μέσα από το δείγμα. Η ένταση της δέσμης αναφοράς λαμβάνεται ως μετάδοση 100% (ή 0 Απορρόφηση), και η μέτρηση που εμφανίζεται είναι η αναλογία των δύο εντάσεων δέσμης. Ορισμένα φασματοφωτόμετρα διπλής δέσμης μέσα έχουν δύο ανιχνευτές (φωτοδίοδοι), και το δείγμα και η δέσμη αναφοράς μετρώνται την ίδια χρονική στιγμή. Τα δείγματα για φασματοφωτομετρία UV / Vis είναι πιο συχνά υγρά, αν και απορρόφηση αερίων και στερεών δειγμάτων, μπορεί επίσης να μετρηθεί. Τα δείγματα τοποθετούνται τυπικά σε μια διαφανή κυψελίδα. Οι κυψελίδες έχουν τυπικά ορθογωνική μορφή, συνήθως με ένα εσωτερικό πλάτος 1 cm. (Αυτό το πλάτος γίνεται το μήκος της διαδρομής, το L, στο νόμο των Beer-Lambert.) Δοκιμαστικοί σωλήνες μπορούν επίσης να χρησιμοποιηθούν ως κυψελίδες σε ορισμένα μέσα. Ο τύπος του δοχείου που χρησιμοποιείται για το δείγμα πρέπει να επιτρέπει στην ακτινοβολία να περάσει πάνω από την φασματική περιοχή ενδιαφέροντος. Οι πιο ευρέως χρησιμοποιούμενες κυψελίδες είναι κατασκευασμένες από υψηλής ποιότητας τηγμένο διοξείδιο του πυριτίου ή από γυαλί χαλαζία, διότι αυτά είναι διαφανή σε όλη την υν, ορατή και εγγύς υπέρυθρη περιοχή. Γυάλινες και πλαστικές κυψελίδες είναι επίσης ευρέως χρησιμοποιούμενες, μολονότι το γυαλί και τα περισσότερα πλαστικά απορροφούν στο UV, κάτι το οποίο περιορίζει την χρησιμότητα τους σε μήκη κύματος στο ορατό [138]. 66
67 Θολερότητα και πειράματα θολερότητας Turbidity είναι η θολότητα ή θολερότητα ενός ρευστού που προκαλείται από μεμονωμένα σωματίδια (αιωρούμενα στερεά) που είναι γενικά αόρατα με γυμνό μάτι, και το φαινόμενο πολλές φορές μοιάζει με την εικόνα του καπνού στον αέρα [139]. Είναι μια ένδειξη για τη σταθερότητα μιας διασποράς και για την ύπαρξη ή μη συσσωματωμάτων (aggregates). Τα υγρά μπορούν να περιέχουν αιωρούμενη στερεά ύλη που αποτελείται από σωματίδια πολλών διαφορετικών μεγεθών. Ενώ μερικά από τα αιωρούμενα υλικά είναι αρκετά μεγάλα και αρκετά βαριά ώστε να καθιζάνουν γρήγορα στον πυθμένα του δοχείου, όταν ένα υγρό δείγμα αφήνεται σε ηρεμία, πολύ μικρά σωματίδια καθιζάνουν μόνον πολύ αργά ή καθόλου εάν το δείγμα αναδεύεται τακτικά ή τα σωματίδια είναι κολλοειδή. Αυτά τα μικρά στερεά σωματίδια προκαλούν την εμφάνιση θολερότητας στο υγρό. Όσον αφορά την μέτρηση της θολερότητας σε διαλύματα διασπορές νανοσωματιδίων, έχουν καθιερωθεί κάποια πρωτόκολλα/πειράματα για τη μέτρηση της θολερότητας συναρτήσει του χρόνου με τη χρήση διαλυμάτων αλάτων όπως το χλωριούχο ασβέστιο (CaCl 2 ) συγκεκριμένες συγκεντρώσεις. Τα δείγματα μετρώνται με τη χρήση φωτόμετρου UV, και το μήκος κύματος στο οποίο γίνεται η μέτρηση της απορρόφησης εξαρτάται από τα υλικά των σωματιδίων (πολυμερικά, ανόργανα κλπ) Spincoating Η τεχνική δημιουργίας υμενίων που αναμφισβήτητα είναι η πιο σημαντική για την ανάπτυξη των πολυμερικών ηλιακών κυττάρων, και σημαντικών εφαρμογών στον τομέα της βιολογίας και της ιατρικής μέχρι αυτή την ημέρα είναι η τεχνική του spincoating. Η τεχνική αυτή έχει υποβληθεί σε πολυάριθμες θεμελιώδεις μελέτες και η χρήση της και το πεδίο εφαρμογής της έχει αναθεωρηθεί πρόσφατα [140]. Παρά την πολυπλοκότητα του σχηματισμού του φιλμ, η τεχνική επιτρέπει με υψηλή επαναληψιμότητα τον σχηματισμό μεμβρανών και έχει διάφορα πλεονεκτήματα έναντι των άλλων τεχνικών επικάλυψης κατά τη διάρκεια της ξήρανσης η οποία επιτρέπει τον σχηματισμό υψηλής ομοιογένειας φιλμ σε μια μεγάλη περιοχή (η διάμετρος του υποστρώματος μπορεί να είναι υψηλή ως 30 εκατοστά). Η τεχνική χρησιμοποιείται στη βιομηχανία μικροηλεκτρονικής κατά την εφαρμογή πολυμερών σε πυρίτιο και εμπλέκεται σε κρίσιμα στάδια κατά τη διάρκεια της παραγωγής ψηφιακών δίσκων πολλαπλών χρήσεων (DVD) και ψηφιακών δίσκων (CD). 67
68 Αρχή Λειτουργίας Η τυπική λειτουργία spincoating περιλαμβάνει εφαρμογή ενός υγρού σε ένα υπόστρωμα που ακολουθείται από την επιτάχυνση του υποστρώματος σε μία επιλεγμένη ταχύτητα περιστροφής (Εικόνα 5). Εναλλακτικά το υγρό διάλυμα μπορεί να εφαρμοστεί ενώ το υπόστρωμα γυρνά. Η γωνιακή ταχύτητα του υποστρώματος με τα διάλυμα υπερκείμενων οδηγεί στην εκτόξευση του μεγαλύτερου μέρους του εφαρμοζόμενου υγρού και άρα σε μεγάλα ποσοστά απωλειών, και τελικά μόνο ένα λεπτό φιλμ αφήνεται επί του υποστρώματος. Η τοπογραφία πάχους, η μορφολογία και η επιφάνεια του τελικού φιλμ που λαμβάνεται από ένα συγκεκριμένο υλικό σε ένα δεδομένο διαλύτη σε μία δεδομένη συγκέντρωση είναι ιδιαίτερα αναπαραγωγίσιμη. Θα πρέπει να αναφερθεί ότι υπάρχει η πιθανότητα περιορισμού στην παρατήρηση της προκύπτουσας τοπογραφίας πάχους, μορφολογίας και της επιφάνειας και ότι η παρασκευή ενός φιλμ σύμφωνα με διαφορετικές προδιαγραφές μπορεί να προσφέρει μια σημαντική πρόκληση αν και τυπικά μόνο ένα εύρος εφαρμογών είναι προσβάσιμο (μόνο ένα εύρος από πάχη μπορούν να ληφθούν). Αυτές οι τρεις ιδιότητες είναι γνωστό ότι εξαρτώνται σε μεγάλο βαθμό από την ταχύτητα περιστροφής, το ιξώδες, την πτητικότητα, τη διαχυτότητα, το μοριακό βάρος και τη συγκέντρωση των διαλυμένων ουσιών. Εξαρτώνται σχετικά λίγο από την ποσότητα του διαλύματος που εναποτίθενται, το ρυθμός εναπόθεσης και το χρόνο λειτουργίας του οργάνου. Το πάχος της μεμβράνης, d, που λαμβάνεται κατά τη διάρκεια ενός πειράματος spincoating μπορεί να εκφραστεί από την εμπειρική σχέση d = kω α, όπου ω είναι η γωνιακή ταχύτητα και, k και α είναι εμπειρικές σταθερές που σχετίζονται με τις φυσικές ιδιότητες του διαλύτη, της διαλυμένης ουσίας και του υποστρώματος. Τυπικά, το α έχει τιμή περίπου -0.5 και η σταθερά k περιέχει πολλές παραμέτρους, όπως το αρχικό ιξώδες του διαλύματος. Μια προσεκτική εξέταση για το θέμα αυτό μπορούν να βρεθεί στη βιβλιογραφία [140]. Το μεγαλύτερο μέρος του διαλύματος που εφαρμόζεται κατά τη διάρκεια της διαδικασίας του spincoating εκτοξεύεται αλλά επειδή απαιτείται ένας πολύ μικρός όγκος για την ολοκλήρωση της λειτουργίας αυτό δεν είναι κρίσιμο (πεπειραμένοι επιστήμονες μπορούν επιτυχώς να κάνουν spincoating χρησιμοποιώντας 0,1 ml). Όταν ένα διάλυμα εναποτίθεται και το μεγαλύτερο μέρος της περίσσειας του διαλύματος έχει εκτιναχθεί κατά την περιστροφή, το ακατέργαστο υγρό φιλμ υπόκειται σε διάφορες αλλαγές, οι οποίες περιλαμβάνουν εξάτμιση του διαλύτη, αλλαγές στο ιξώδες, την ακτινική ροή του διαλύματος, τη μοριακή οργάνωση στις στερεού-υγρού και αέρος-υγρού διεπιφάνειες, τον μοριακό προσανατολισμό ως αποτέλεσμα της διάτμησης πεδίου, τον 68
69 σχηματισμός συσσωματωμάτων, τον διαχωρισμό φάσεων των μιγμάτων, τη διάχυση των μορίων στο υμένιο, κλπ Εφαρμογές της τεχνικής Οι περισσότερες από τις μελέτες του σχηματισμού φιλμ χρησιμοποιώντας την τεχνική του spincoating έχουν επικεντρωθεί στο πάχος της μεμβράνης και είναι γενικά αποδεκτό ότι το πάχος εξαρτάται από την ταχύτητα περιστροφής και το ιξώδες του διαλύματος [141]. Η τελευταία ιδιότητα εξαρτάται από την συγκέντρωση της διαλυμένης ουσίας και το μοριακό βάρος της διαλυμένης ουσίας, εάν το υμένιο είναι πολυμερικό. Εκτός από το πάχος της μεμβράνης που είναι σημαντικό, επίσης και η ομοιογένεια και η συγκέντρωση είναι σημαντική. Περαιτέρω, η μορφολογία της μεμβράνης έχει μελετηθεί για μίγματα πολυμερών και συμπολυμερών κατά συστάδες και αυτό είναι σημαντικό στα πλαίσια των πολυμερικών φωτοβολταϊκών καθώς η σωστή μορφολογία στη νανοκλίμακα μπορεί να βελτιώσει σημαντικά την απόδοση της συσκευής, όπως μπορεί και η επιφανειακή τοπογραφία. Το γεγονός ότι οι ιδιότητες της διεπιφάνειας είναι υπό κάποιο βαθμό ελεγχόμενες και ότι η τεχνική επιτρέπει τον επαναλήψιμο χαρακτήρα στο σχηματισμό ενός φιλμ με σταθερό πάχος, μορφολογία και τοπογραφία επιφάνειας είναι πιθανότατα ο λόγος που αυτή η τεχνική είναι τόσο επιτυχής. 69
70 ΚΕΦΑΛΑΙΟ 6. Κινητική Μελέτη Απελευθέρωσης Κινητική Απελευθέρωσης Φαρμάκων, Μοντέλα και Θεωρίες Τα τελευταία χρόνια, έχει συντελεστεί σημαντική πρόοδος στον τομέα της μεταφοράς και απελευθέρωσης φαρμακευτικών μορίων με την ανάπτυξη μορφών δοσολογίας ελεγχόμενης αποδέσμευσης. Υπάρχει μεγάλη ποικιλία συνθέσεων που διατίθενται για από του στόματος ελεγχόμενη απελευθέρωση φαρμάκου, όπως επίσης και μεγάλη ποικιλία φυσικών ιδιοτήτων που επηρεάζουν την απελευθέρωση φαρμάκου από αυτά τα σκευάσματα. Τα διάφορα μοτίβα απελευθέρωσης μπορούν να διαιρεθούν σε εκείνα που οδηγούν στην απελευθέρωση του φαρμάκου με έναν αργό ρυθμό μηδενικής ή πρώτης τάξης και σε εκείνα που αποδίδουν μία αρχική ταχεία δόση, που ακολουθείται από βραδεία, μηδενικής ή πρώτης τάξεως παρατεταμένη απελευθέρωση του συστατικού [142]. Ο σκοπός των συστημάτων ελεγχόμενης αποδέσμευσης είναι να διατηρηθεί η συγκέντρωση του φαρμάκου στο αίμα ή στους ιστούς-στόχους σε μία επιθυμητή τιμή όσο το δυνατόν περισσότερο [143]. Με άλλα λόγια, να είναι σε θέση να ασκήσουν έλεγχο επί του ρυθμού απελευθέρωσης του φαρμάκου καθ όλη τη διάρκεια της φαρμακευτικής αγωγής [144]. Για το σκοπό αυτό σε γενικές γραμμές, τα συστήματα ελεγχόμενης αποδέσμευσης αρχικά απελευθερώνουν μέρος της δόσης που περιέχεται στο σύστημα προκειμένου να επιτύχουν ταχέως την αποτελεσματική θεραπευτική συγκέντρωση του φαρμάκου (ED 50 ). Στη συνέχεια, η κινητική απελευθέρωσης του φαρμάκου ακολουθεί μια καλά καθορισμένη συμπεριφορά με σκοπό την παροχή της δόσης συντήρησης (Css) που επιτρέπει την επίτευξη της επιθυμητής συγκέντρωσης του φαρμάκου στον στόχο για διάστημα που έχει καθοριστεί σημαντικό και απαραίτητο για την επίτευξη του φαρμακολογικού αποτελέσματος. Τα σκευάσματα ελεγχόμενης αποδέσμευσης που έχουν μελετηθεί μέχρι σήμερα παρέχουν ένα ευρύ και ευέλικτο εύρος εφαρμογών στο πεδίο των ιατρικών επιστημών, και αποτελούν χρήσιμα εργαλεία για την εκμετάλλευση της σύγχρονης έννοιας της θεραπευτικής αγωγής της οποίας στόχος είναι να αυξηθεί η αποτελεσματικότητα του φαρμάκου και η συμμόρφωση του ασθενούς στη φαρμακευτική αγωγή, για να μειωθεί η συχνότητας χορήγησης και οι ανεπιθύμητες ενέργειες που συνδέονται με τη δοσολογία. Για τη δημιουργία συστημάτων ελεγχόμενης αποδέσμευσης φέρνουν ερευνητές από το χώρο των θετικών επιστημών και φαρμακοποιοί, μπορούν να συνεργαστούν με κοινό στόχο την επίτευξη όλο και πιο αποτελεσματικών προϊόντων. Για το σκοπό αυτό, η χρήση των μαθηματικών μοντέλων αποδεικνύεται να είναι πολύ χρήσιμη ως μια προσέγγιση που δίνει τη 70
71 δυνατότητα της πρόβλεψης της κινητικής απελευθέρωσης πριν τα συστήματα απελευθέρωσης μπορέσουν να κατανοηθούν πλήρως. Τις περισσότερες φορές, επιτρέπουν τη μέτρηση ορισμένων σημαντικών φυσικών παραμέτρων, όπως είναι ο συντελεστής διάχυσης του φαρμάκου και να καταλήγουν σε κάποιο μοντέλο το οποίο να ταιριάζει σε πειραματικά δεδομένα απελευθέρωσης. Έτσι, η μαθηματική μοντελοποίηση, η ανάπτυξη της οποίας απαιτεί την κατανόηση όλων των φαινομένων που επηρεάζουν την κινητική απελευθέρωσης των φαρμάκων [145], έχει πολύ σημαντική αξία στη βελτιστοποίηση της εφαρμογής των συστημάτων ελεγχόμενης αποδέσμευσης. Τα μοντέλα αυτά μπορούν να θεωρηθούν απλά ως μια μαθηματική μεταφορά ορισμένων πτυχών της πραγματικότητας που, στην περίπτωση της ελεγχόμενης αποδέσμευσης φαρμάκων, ταυτίζονται με το σύνολο των φαινομένων που διέπουν τις κινητικές απελευθέρωσης [ ]. Γι 'αυτό το λόγο, η μαθηματική μοντελοποίηση χρησιμοποιείται ευρέως σε διάφορους κλάδους, όπως η γενετική, η ιατρική, η ψυχολογία, η βιολογία, η οικονομία και προφανώς η μηχανική και η τεχνολογία Βασικές αρχές της κινητικής της αποδέσμευσης φαρμάκου Noyes-Whitney Η θεμελιώδης αρχή για την αξιολόγηση της κινητικής της απελευθέρωσης του φαρμάκου προσφέρθηκε από τους Noyes και Whitney το 1897 ως η εξίσωση (1): dm/dt = KS (Cs -Ct) (1) όπου το Μ, είναι η μάζα που μεταφέρεται ως προς το χρόνο t, με διάλυση από το στερεό σωματίδιο μιας στιγμιαίας επιφάνειας S, υπό την επίδραση της επικρατούσας κατευθυντήριας δύναμης συγκέντρωσης (Cs - Ct), όπου Ct είναι η συγκέντρωση σε χρόνο t και Cs είναι η διαλυτότητα ισορροπίας (equilibrium solubility) της διαλυμένης ουσίας σε πειραματική θερμοκρασία. Ο ρυθμός της διάλυσης dm / dt είναι η ποσότητα που διαλύεται ανά μονάδα επιφανείας και ανά μονάδα χρόνου και για τα περισσότερα στερεά μπορούν να εκφράζονται σε μονάδες g*cm -2 *s -1. Όταν η Ct είναι μικρότερη από το 15% διαλυτότητας κορεσμού Cs, η Ct έχει αμελητέα επίδραση στο ρυθμό διάλυσης του στερεού. Υπό αυτές τις συνθήκες, η διάλυση του στερεού θεωρείται ότι συμβαίνει υπό συνθήκες «νεροχύτη». Σε γενικές γραμμές, το εμβαδόν επιφανείας, S δεν είναι σταθερό παρά μόνο όταν η ποσότητα του υπάρχοντος υλικού υπερβαίνει την διαλυτότητα κορεσμού, ή στην αρχή, όταν μόνο μικρές ποσότητες του φαρμάκου έχουν διαλυθεί. 71
72 6.3. Θεωρία Φιλμ Nernst & Brunner Οι Brunner και Nernst [151,152] χρησιμοποίησαν το νόμο διάχυσης του Fick για τη δημιουργία μιας σχέσης μεταξύ της σταθεράς στην εξίσωση (1) και του συντελεστή διάχυσης της διαλυμένης ουσίας, καταλήγοντας στην εξίσωση: K=DS/hγ (2) όπου D είναι ο συντελεστής διάχυσης, το S είναι η περιοχή της επιφανείας ή περιοχή διαλύσεως της στοιβάδας διάχυσης, γ είναι ο όγκος του διαλύματος και το h είναι το πάχος του στρώματος διαχύσεως. Οι θεωρίες των Nernst και Brunner υιοθετούν την υπόθεση ότι η διαδικασία στην επιφάνεια προχωρεί πολύ γρηγορότερα από τη διαδικασία μεταφοράς και ότι μια γραμμική βαθμίδωση συγκέντρωσης περιορίζεται στο στρώμα του διαλύματος που περιβάλλει τη στερεά επιφάνεια. Η ιδανική κατάσταση δεν μπορεί ποτέ να επιτευχθεί όσο η πραγματική επιφάνεια αλλάζει μόνιμα με την εξέλιξη των διαδικασιών κατά τη διάρκεια της διάλυσης στον προσδιορισμό της απελευθέρωσης του φαρμάκου. Στην εξίσωση Noyes- Whitney, η διαδικασία διάλυσης αντιστοιχεί σε μια αντίδραση πρώτης τάξης Μοντελοποίηση κινητικής απελευθέρωσης Υπάρχουν διάφορα κινητικά μοντέλα, τα οποία περιγράφουν τη συνολική απελευθέρωση του φαρμάκου από τις διάφορες μορφές δοσολογίας. Επειδή η ύπαρξη ποιοτικών και ποσοτικών μεταβολών σε ένα σκεύασμα μπορεί να μεταβάλει την απελευθέρωση του φαρμάκου και την in vivo απόδοση, η εφαρμογή εργαλείων που διευκολύνουν την ανάπτυξη του προϊόντος μειώνοντας την αναγκαιότητα βιο-μελετών είναι πάντα επιθυμητή και χρήσιμη για την καλύτερη αξιολόγηση και αξιοποίηση των δεδομένων που προκύπτουν. Από την άποψη αυτή, η χρήση in vitro δεδομένων διαλυτοποίησης φαρμάκου για να προβλεφθεί in vivo συμπεριφορά μπορεί να θεωρηθεί ως μια ορθολογική στρατηγική για την ανάπτυξη σκευασμάτων ελεγχόμενης απελευθέρωσης [ ]. Οι μέθοδοι προσέγγισης για τη διερεύνηση της κινητικής απελευθέρωσης του φαρμάκου από το σκεύασμα ελεγχόμενης απελευθέρωσης μπορούν να ταξινομηθούν σε τρεις κατηγορίες: Στατιστικές μέθοδοι (διερευνητική μέθοδος ανάλυσης δεδομένων, σχεδιασμός επαναλαμβανόμενων μετρήσεων, πολυπαραγοντική προσέγγιση [MANOVA: πολυμεταβλητή ανάλυση διακύμανσης] [153, 154]. Μοντέλα εξαρτώμενα από τις μεθόδους (μηδενικής τάξης, πρώτης τάξης, Higuchi, Korsmeyer-Πέππας, Baker-Lonsdale, Weibull, κλπ.) [155, 156]. 72
73 Μοντέλα ανεξάρτητα από τις μεθόδους [παράγοντα διαφοράς (f1), παράγοντα ομοιότητας (f2) ( )] Μοντέλα εξαρτώμενα από τις μεθόδους που ακολουθούνται Τα μοντέλα που εξαρτώνται από τις μεθόδους βασίζονται σε διαφορετικές μαθηματικές συναρτήσεις, οι οποίες περιγράφουν το προφίλ διάλυσης. Όταν μία κατάλληλη λειτουργία έχει επιλεγεί, τα προφίλ διάλυσης αξιολογούνται ανάλογα με τις παραμέτρους του μοντέλου από όπου προέρχονται. Προκειμένου να προσδιοριστεί το κατάλληλο κινητικό μοντέλο απελευθέρωσης φαρμάκου που περιγράφει το προφίλ διάλυσης, χρησιμοποιούνται πολλές φορές μη-γραμμικά μοντέλα. Σε μη-γραμμική ανάλυση παλινδρόμησης οι μέθοδοι Quasi-Newton και Simplex ελαχιστοποιούν τα ελάχιστα τετράγωνα [155,156]. Στις προσεγγίσεις που εξαρτώνται από τις μεθόδους περιλαμβάνονται τα μοντέλα μηδενικής τάξης, πρώτης τάξης, Higuchi, Korsmeyer-Πέππας, Baker-Lonsdale και μοντέλα παλινδρόμησης [160, 161] Μοντέλο μηδενικής τάξης Η διαλυτοποίηση του φαρμάκου από μορφές δοσολογίας που δεν αποσυσσωματώνονται και απελευθερώνουν το φάρμακο αργά μπορεί να αποτυπωθεί με την εξίσωση: Q t -Q 0 = K 0 t (I) ή αλλιώς: Qt =Q 0 +K 0 t όπου Qt είναι η ποσότητα του φαρμάκου που διαλύθηκε σε χρόνο t, Q 0 είναι η αρχική ποσότητα του φαρμάκου στο διάλυμα (τις περισσότερες φορές, Q 0 = 0) και το Κ 0 είναι η σταθερά απελευθέρωση μηδενικής τάξεως που εκφράζεται σε μονάδες συγκέντρωσης / χρόνου. Για να μελετηθεί η κινητική απελευθέρωσης, τα δεδομένα που λαμβάνονται από in vitro μελέτες απελευθέρωσης φαρμάκου επεξεργάζονται ως αθροιστική ποσότητα του φαρμάκου που απελευθερώνεται συναρτήσει του χρόνου [162, 163]. Αυτή η σχέση μπορεί να χρησιμοποιηθεί για να περιγράψει την διάλυση του φαρμάκου διαφόρων τύπων τροποποιημένης απελευθέρωσης φαρμακευτικών δοσολογικών μορφών, όπως στην περίπτωση ορισμένων διαδερμικών συστημάτων, δισκίων με χαμηλή διαλυτότητας φάρμακα σε επικαλυμμένα μορφές, οσμωτικά συστήματα, κλπ.[164,165]. 73
74 Μοντέλα κινητικής πρώτης τάξης Αυτό το μοντέλο έχει χρησιμοποιηθεί επίσης για να περιγράψει την απορρόφηση και / ή την απέκκριση ορισμένων φαρμάκων, αν και είναι δύσκολο να συλληφθεί αυτός ο μηχανισμός σε θεωρητική βάση. Η αποδέσμευση του φαρμάκου που ακολουθεί κινητική πρώτης τάξεως μπορεί να εκφραστεί από την εξίσωση: dc/dt=-kc (II) όπου Κ είναι η σταθερά πρώτης τάξης εκφρασμένη σε μονάδες χρόνου -1. Η εξίσωση (II) μπορεί να εκφρασθεί ως: log C = log C 0 - Kt / 2,303 όπου C 0 είναι η αρχική συγκέντρωση του φαρμάκου, K είναι η σταθερά ταχύτητας πρώτης τάξεως, και t είναι ο χρόνος [165]. Τα δεδομένα που λαμβάνονται απεικονίζονται ως λογαριθμικό αθροιστικό ποσοστό του φαρμάκου που απομένει συναρτήσει του χρόνου το οποίο δίνει μία ευθεία γραμμή με κλίση - K/ Αυτή η σχέση μπορεί να χρησιμοποιηθεί για να περιγράψει την διάλυση του φαρμάκου σε φαρμακευτικές μορφές όπως αυτές που περιέχουν υδατο-διαλυτά φάρμακα σε πορώδεις μήτρες [166,167] Μοντέλο Higuchi 74 Το πρώτο παράδειγμα ενός μαθηματικού μοντέλου που αποσκοπεί στο να περιγράψει την απελευθέρωση του φαρμάκου από ένα σύστημα μήτρας προτάθηκε από τον Higuchi το 1961 [168]. Αρχικά σχεδιάστηκε για επίπεδα συστήματα, στη συνέχεια όμως επεκτάθηκε σε διάφορα γεωμετρικά και πορώδη συστήματα [169]. Αυτό το μοντέλο βασίζεται στις υποθέσεις ότι (α) η αρχική συγκέντρωση του φαρμάκου στην μήτρα είναι πολύ υψηλότερη από την διαλυτότητα του φαρμάκου, (β) η διάχυση του φαρμάκου λαμβάνει χώρα μόνο σε μία διάσταση, (γ) τα σωματίδια του φαρμάκου είναι πολύ μικρότερα από το πάχος του συστήματος, (δ) η διόγκωση και η διάλυση της μήτρας είναι αμελητέα, (ε) η διάχυση του φαρμάκου είναι σταθερή. Επομένως το μοντέλο εκφράζεται με την εξίσωση: (III) όπου Q είναι η ποσότητα του φαρμάκου που αποδεσμεύεται σε χρόνο t ανά μονάδα εμβαδού Α, C είναι η αρχική συγκέντρωση φαρμάκου, Cs είναι η διαλυτότητα του φαρμάκου στη μήτρα και D είναι η ικανότητα διάχυσης των μορίων του φαρμάκου (συντελεστής διάχυσης), στην ουσία της μήτρας. Αυτή η σχέση μπορεί να χρησιμοποιηθεί για να περιγράψει την διάλυση του φαρμάκου από διάφορους τύπους μορφών τροποποιημένης απελευθέρωσης
75 φαρμάκων, όπως στην περίπτωση ορισμένων διαδερμικών συστημάτων και δισκίων μήτρας με υδατοδιαλυτά φάρμακα [ ] Μοντέλο Korsmeyer-Πέππας Αυτό το μοντέλο αποδίδει μια απλή σχέση που περιγράφεται την απελευθέρωση του φαρμάκου από ένα πολυμερές σύστημα [152]. Για να περιγραφεί ο μηχανισμός της απελευθέρωσης του φαρμάκου, το πρώτο 60% των δεδομένων απελευθέρωσης του φαρμάκου τοποθετείται στο Korsmeyern-Peppas μοντέλο [171]. Mt / M = K t n. (IV) όπου Mt / M είναι το κλάσμα του φαρμάκου που απελευθερώνεται κατά το χρόνο t, k είναι η σταθερά ρυθμού απελευθέρωσης και n είναι ο εκθέτης απελευθέρωσης. Η τιμή n χρησιμοποιείται για να χαρακτηρίσει διαφορετική απελευθέρωση για κυλινδρικού σχήματος μήτρες. Στο μοντέλο αυτό, η τιμή του n χαρακτηρίζει τον μηχανισμό απελευθέρωσης του φαρμάκου, όπως περιγράφεται στον Πίνακα 3. Για την περίπτωση των κυλινδρικών δισκίων, 0,45 n αντιστοιχεί σε ένα μηχανισμό διάχυσης Fickian, 0,45 <n <0,89 σε μη-fickian μεταφορά, n = 0,89 για την υπόθεση ΙΙ (relaxational) μεταφορά, και n> 0,89 σε περίπτωση μεταφοράς σούπερ ΙΙ [172,173]. Για να μάθουμε τον εκθέτη n του το τμήματος της καμπύλης αποδέσμευσης, πρέπει να χρησιμοποιείται μόνο το κομμάτι όπου Mt / M <0,6. Για να μελετηθεί η κινητική απελευθέρωσης, τα δεδομένα που λαμβάνονται από in vitro μελέτες απελευθέρωσης φαρμάκου αποδίδονται ως λογαριθμική συσσωρευτική ποσοστιαία απελευθέρωση φαρμάκου συναρτήσει του χρόνου καταγραφής. Πίνακας 3 75
76 ΚΕΦΑΛΑΙΟ 7. Σημαντικά Αντιδραστήρια και Φάρμακα που χρησιμοπούνται Διπυριδαμόλη Η Διπυριδαμόλη (Εικόνα 6) (εμπορικές ονομασίες Persantine, Antistenocardin) είναι ένα φάρμακο που αναστέλλει το σχηματισμό θρόμβου [174] σε χρόνια χορήγηση, και προκαλεί αγγειοδιαστολή όταν δοθεί σε υψηλές δόσεις επί σύντομο χρονικό διάστημα. Dipyridamole Ονομασία κατά IUPAC 2,2',2'',2'''-(4,8-di(piperidin-1-yl)pyrimido[5,4-d]pyrimidine-2,6 diyl)bis(azanetriyl)tetraethanol Κλινικά δεδομένα Trade name: Persantine Routes PO, IV Φαρμακοκινητικά δεδομένα Protein binding 99% Metabolism Hepatic Χημικά δεδομένα Formula C24H40N8O4 Mol. mass g/mol Μηχανισμός δράσης και φαρμακευτικά αποτελέσματα Δρα ως αναστολέας της συνθάσης της TXA2, επομένως επάγει τη μείωση των επιπέδων της ΤΧΑ2 και συνεπώς σταματά τα αποτελέσματα της ΤΧΑ2 (συσσωμάτωση αιμοπεταλίων, βρογχοσυστολή και αγγειοσυστολή). Αναστέλλει την κυτταρική επαναπρόσληψη της αδενοσίνης σε αιμοπετάλια, ερυθρά αιμοσφαίρια και ενδοθηλιακά κύτταρα, γεγονός που οδηγεί σε αυξημένη εξωκυτταρική συγκέντρωση της αδενοσίνης. 76
77 Επίσης, αναστέλλει το ένζυμο απαμινάση της αδενοσίνης, η οποία κανονικά διασπά την αδενοσίνη σε ινοσίνη. Αυτή η αναστολή οδηγεί σε περαιτέρω αύξηση των επιπέδων της εξωκυττάριας αδενοσίνης. Η διπυριδαμόλη αναστέλλει επίσης τις φωσφοδιεστεράσες, ένζυμα που κανονικά διασπούν το camp (αυξάνοντας τα κυτταρικά επίπεδα camp και εμποδίζοντας την απόκριση των αιμοπεταλίων στο ADP) και / ή το cgmp (με αποτέλεσμα πρόσθετο πλεονέκτημα όταν χορηγείται μαζί με νιτρικό οξείδιο [ΝΟ] ή στατίνες) Ιατρικές χρήσεις Η διπυριδαμόλη έχει αποδειχθεί ότι μειώνει την πνευμονική υπέρταση, χωρίς σημαντική πτώση της συστηματικής αρτηριακής πίεσης Αναστέλλει το σχηματισμό των προφλεγμονωδών κυτοκινών (MCP-1, ΜΜΡ-9) in vitro και οδηγεί στη μείωση της hscrp σε ασθενείς. Αναστέλλει τον πολλαπλασιασμό των λείων μυϊκών κυττάρων in vivo και έχει δειχθεί ότι αποτρέπει την AV-shunt ανεπάρκεια σε ασθενείς σε αιμοκάθαρση. Επίσης αυξάνει την απελευθέρωση του ί-ρα από εγκέφαλικά μικροαγγειακά ενδοθηλιακά κύτταρα. Οδηγεί σε μία αύξηση του 13 - ΗODE και μείωση της 12-ΗΕΤΕ στην υποενδοθηλιακή μήτρα (SEM) και οδηγεί μειωμένη θρομβογονικότητα του SEM. Έχει αποδειχθεί να επάγει την αύξηση της αιμάτωσης του μυοκαρδίου και τη λειτουργία της αριστερής κοιλίας σε ασθενείς με ισχαιμική μυοκαρδιοπάθεια. Ακόμα, οδηγεί σε μείωση του αριθμού των υποδοχέων της θρομβίνης και PECAM-1 επί των αιμοπεταλίων σε ασθενείς με εγκεφαλικό. Το camp μειώνει τη συσσωμάτωση των αιμοπεταλίων και επίσης προκαλεί χαλάρωση των λείων μυικών ινών. Χρόνια θεραπεία δεν επέδειξε σημαντική πτώση της συστηματικής αρτηριακής πίεσης. Αναστέλλει την αντιγραφή του RNA του mengovirus [175]. Μπορεί να χρησιμοποιηθεί για δοκιμή στρες του μυοκαρδίου ως εναλλακτική λύση Υπερβολική δόση Υπερδοσολογία από διπυριδαμόλη μπορεί να αντιμετωπιστεί με αμινοφυλλίνη [176] που αντιστρέφει τα αιμοδυναμικά αποτελέσματα της (αγγειοδιαστολή). Συμπτωματική θεραπεία συνιστάται, ενδεχομένως να περιλαμβάνει ένα αγγειοσυσπαστικό φάρμακο. Η πλύση στομάχου θα πρέπει να εξεταστεί σαν λύση στην περίπτωση υπερδοσολογίας. Η 77
78 χορήγηση παραγώγων ξανθίνης (π.χ., αμινοφυλλίνη) μπορεί να αναστρέψει τα αιμοδυναμικά αποτελέσματα της υπερδοσολογίας από διπυριδαμόλη και αποτελεί επιλογή άμεσης αντιμετώπισης στην περίπτωση αυτή. Δεδομένου ότι η διπυριδαμόλη είναι ιδιαίτερα συνδεδεμένη με τις πρωτεΐνες του αίματος, η αιμοκάθαρση δεν είναι πιθανό να είναι επωφελής Bovine serum albumin (BSA), αλβουμίνη από βοοειδή Η αλβουμίνη βόειου ορού (επίσης γνωστή ως BSA ή «Κλάσμα V") είναι μια πρωτεΐνη του ορού του αίματος που προέρχεται από αγελάδες. Χρησιμοποιείται συχνά ως πρότυπο για μοντέλα συγκέντρωσης πρωτεΐνης. Το ψευδώνυμο "Κλάσμα V" έχει καθιερωθεί εξαιτίας του γεγονότος ότι η αλβουμίνη είναι το πέμπτο κλάσμα της αρχικής μεθοδολογίας καθαρισμού Edwin Cohn που έκανε χρήση των χαρακτηριστικών της διαφορικής διαλυτότητας των πρωτεϊνών του πλάσματος. Με τον έλεγχο της συγκέντρωσης του διαλύτη, του pη, των επιπέδων άλατος, και της θερμοκρασίας, ο Cohn ήταν σε θέση να τραβήξει έξω διαδοχικά "κλάσματα" του πλάσματος του αίματος. Η διαδικασία εμφανίστηκε για πρώτη φορά στο εμπόριο με ανθρώπινη αλβουμίνη για ιατρική χρήση και αργότερα υιοθετήθηκε για την παραγωγή της BSA Ιδιότητες Η πρόδρομη πρωτεΐνη πλήρους μήκους BSA αριθμεί 607 αμινοξέα σε μήκος. Ένα Ν- τελικό 18-αμινοξέων πεπτίδιο που λειτουργεί σαν σήμα αποκόπτεται από την πρόδρομη πρωτεΐνη μετά την έκκριση, συνεπώς το αρχικό προϊόν πρωτεΐνης περιέχει 589 υπολείμματα αμινοξέων. Επιπλέον 4 αμινοξέα αποκόπτονται για να δώσουν την ώριμη BSA πρωτεΐνη που περιέχει 583 αμινοξέα [177] Εφαρμογές Η BSA έχει πολυάριθμες βιοχημικές εφαρμογές συμπεριλαμβανομένων των τεχνικών ELISA (Enzyme-Linked Immunosorbent Assay), ανοσοκηλιδώσεων, και ανοσοϊστοχημείας. Επίσης, χρησιμοποιείται ως ένα θρεπτικό συστατικό σε κυτταρικές και μικροβιακές καλλιέργειες. Στην διαδικασίες πέψης περιορισμού, η αλβουμίνη χρησιμοποιείται για να 78
79 σταθεροποιήσει κάποια ένζυμα κατά την πέψη του DNA και για να εμποδίσει την προσκόλληση του ενζύμου σε σωλήνες αντίδρασης, απολήξεις, και άλλους φορείς [178]. Η πρωτεΐνη αυτή δεν επηρεάζει άλλα ένζυμα που δεν τη χρειάζονται για σταθεροποίηση. Η BSA επίσης συνήθως χρησιμοποιείται για τον προσδιορισμό της ποσότητας των άλλων πρωτεϊνών, συγκρίνοντας μία άγνωστη ποσότητα της πρωτεΐνης με γνωστές ποσότητες της BSA (δοκιμασία Bradford). Η BSA χρησιμοποιείται λόγω της σταθερότητας της να αυξάνει το σήμα σε ανιχνεύσεις, επειδή δεν προκαλεί αλλαγές σε πολλές βιοχημικές αντιδράσεις, και το χαμηλό κόστος της, δεδομένου ότι μεγάλες ποσότητες μπορεί εύκολα να καθαριστούν από το αίμα βοοειδών, ένα υποπροϊόν της βιομηχανίας βοοειδών Πολυαιθυλενογλυκόλη (PEG) Ονομασία κατά IUPAC: πολύ(αιθύλενο οξείδιο) Μοριακός τύπος: C2nH4n+2On+1, Μοριακή μάζα: ποικίλει Η πολυαιθύλενο γλυκόλη (PEG) είναι μία ένωση πολυαιθέρα με πολλές εφαρμογές από τη βιομηχανία ως και την ιατρική. Η δομή του PEG είναι: HO-CH2-(CH2-O-CH2-)n-CH2-OH. Το PEG είναι επίσης γνωστό ως οξείδιο του πολυαιθυλενίου (ΡΕΟ) ή πολυοξυαιθυλένιο (ΡΟΕ), ανάλογα με το μοριακό βάρος του. Και τα τρία παρακάτω ονόματα, PEG, ΡΕΟ, ή ΡΟΕ αναφέρονται σε ένα ολιγομερές ή πολυμερές του οξειδίου του αιθυλενίου. Τα τρία ονόματα είναι χημικώς συνώνυμα, αλλά ιστορικά η ονομασία PEG έχει την τάση να αναφέρεται σε ολιγομερή και πολυμερή με μία μοριακή μάζα κάτω των g / mol, η ονομασία ΡΕΟ για πολυμερή με μοριακό βάρος πάνω από g / mol, και η ΡΟΕ σε πολυμερή οποιασδήποτε μοριακής μάζας [179] Ιδιότητες Τα PEG και ΡΕΟ είναι υγρά ή χαμηλού σημείου τήξεως στερεά, ανάλογα με τα μοριακά βάρη τους. Οι PEGs παρασκευάζονται με πολυμερισμό αιθυλενοξειδίου και είναι εμπορικά διαθέσιμα σε ένα ευρύ φάσμα μοριακών βαρών από 300 g / mol έως g / mol. Ενώ ΡΕΟ και ΡΟΕ με διαφορετικά μοριακά βάρη βρίσκουν χρήση σε διάφορες εφαρμογές, και έχουν διαφορετικές φυσικές ιδιότητες (π.χ. ιξώδες) λόγω των επιπτώσεων του μήκους αλυσίδας, οι χημικές τους ιδιότητες είναι σχεδόν ταυτόσημες. Διαφορετικές μορφές του PEG είναι επίσης διαθέσιμες, ανάλογα με τον εκκινητή που χρησιμοποιείται για τη διαδικασία πολυμερισμού - ο πιο κοινός εκκινητής είναι ένα ο ΡΕΟ μεθυλαιθέρας, ή 79
80 μεθοξυπολυ (αιθυλενογλυκόλη), με τη συντομογραφία mpeg. Κατώτερο-μοριακού βάρους PEGs είναι επίσης διαθέσιμα ως καθαρότερα ολιγομερή, που αναφέρονται ως μονοδιασπειρόμενα, ομοιόμορφα, ή διακριτά. PEG πολύ υψηλής καθαρότητας έχει πρόσφατα αποδειχθεί ότι είναι κρυσταλλικό, επιτρέποντας τον προσδιορισμό της κρυσταλλικής δομής του με περίθλαση ακτίνων Χ [180]. Από τη στιγμή που ο καθαρισμός και ο διαχωρισμός των καθαρών ολιγομερών είναι δύσκολος, η εμπορική τιμή αυτού του τύπου ποιότητας είναι συχνά φορές μεγαλύτερη από εκείνη της πολυδιασποράς PEG. Το PEG είναι επίσης διαθέσιμο με διαφορετικά σχήματα. Διακλαδισμένες PEG έχουν τρία έως δέκα αλυσίδες PEG προερχόμενες από μια κεντρική ομάδα/πυρήνα. PEGs με σχήμα αστεριού έχουν 10 με 100 αλυσίδες PEG που προέρχονται από έναν κεντρικό πυρήνα. Συνδυασμένες ΡΕΟs έχουν πολλαπλές αλυσίδες PEG που συνήθως έχουν ενσωματωθεί σε ένα σκελετό πολυμερούς. Οι αριθμοί που συχνά περιλαμβάνονται στις ονομασίες των PEGs υποδεικνύουν το μέσο μοριακό τους βάρος (πχ PEG με n = 9 θα έχουν ένα μέσο μοριακό βάρος περίπου 400 daltons, και θα επισημαίνονται PEG 400. Τα περισσότερα PEGs περιλαμβάνουν μόρια με μία κατανομή μοριακών βαρών (δηλαδή είναι πολυδιασποράς). Η κατανομή του μεγέθους μπορεί να χαρακτηρίζεται στατιστικά με το μέσο μοριακό βάρος του (Μw) και τη μέση τιμή των τιμών που παίρνει το μέσο μοριακό βάρος (Μn), η αναλογία των οποίων καλείται δείκτης πολυδιασποράς (Mw / Mn). Οι τιμές των Mw και Μn μπορούν να μετρηθούν με φασματοσκοπία μάζας. Η μέθοδος του PEGylation είναι η πράξη της ομοιοπολική σύζευξη μιας δομής PEG σε ένα άλλο μεγαλύτερο μόριο, για παράδειγμα, μία θεραπευτική πρωτεΐνη, η οποία στη συνέχεια αναφέρεται ως PEGylated πρωτεΐνη. PEGylated ιντερφερόνες άλφα-2α ή-2b χρησιμοποιούνται ευρέως ως ενέσιμες θεραπείες για μόλυνση από ηπατίτιδα C. Η PEG είναι διαλυτή στο νερό, μεθανόλη, βενζόλιο, και διχλωρομεθάνιο, και είναι αδιάλυτη σε διαιθυλαιθέρα και εξάνιο. Μπορεί να συνδεθεί με υδρόφοβα μόρια για την παραγωγή μη-ιονικά επιφανειοδραστικά ουσιών Ιατρικές χρήσεις Το PEG αποτελεί τη βάση ενός αριθμού υπακτικών φαρμάκων (πχ, προϊόντα που περιέχουν macrogol, όπως Movicol και πολυαιθυλενογλυκόλη 3350, ή SoftLax, MiraLAX, ή GlycoLax). Η πολυαιθυλενογλυκόλη με την προσθήκη ηλεκτρολυτών χρησιμοποιείται για την προετοιμασία του εντέρου πριν από την επέμβαση ή κολονοσκόπηση. Στις Ηνωμένες 80
81 Πολιτείες, τα MiraLAX και Dulcolax πωλούνται χωρίς συνταγή για τη βραχυπρόθεσμη ανακούφιση της χρόνιας δυσκοιλιότητας, αν και υπάρχει πλέον αυξανόμενη πεποίθηση στην ιατρική κοινότητα ότι αυτά τα φάρμακα μπορούν να ληφθούν επ 'αόριστον για τη θεραπεία της χρόνιας δυσκοιλιότητας. Το Miralax είναι σήμερα εγκεκριμένο από τον FDA για ενήλικες για χορήγηση περιόδου 7 ημερών, και δεν έχει εγκριθεί για παιδιά [181]. Όταν είναι συνδεδεμένη με διάφορα φάρμακα πρωτεϊνών, η πολυαιθυλενογλυκόλη επιβραδύνει την κάθαρση της μεταφερόμενης πρωτεΐνης από το αίμα. Αυτό οδηγεί σε μακράς-δράσης φαρμακευτικό αποτέλεσμα και μειώνει την τοξικότητα, και επιτρέπει μεγαλύτερα διαστήματα μεταξύ δόσεων. Παραδείγματα περιλαμβάνουν την PEGιντερφερόνη άλφα, η οποία χρησιμοποιείται για τη θεραπεία της ηπατίτιδας C, και το pegfilgrastim (Neulasta), το οποίο χρησιμοποιείται για τη θεραπεία της ουδετεροπενίας. Έχει αποδειχθεί ότι η πολυαιθυλενογλυκόλη μπορεί να βελτιώσει την επούλωση τραυματισμών της σπονδυλικής στήλης σε σκύλους [182]. Το PEG επίσης συνήθως χρησιμοποιείται για τη σύντηξη Β-κυττάρων με κύτταρα μυελώματος για την παραγωγή μονοκλωνικών αντισωμάτων. Το PEG χρησιμοποιείται ως έκδοχο σε πολλά φαρμακευτικά προϊόντα. Οι χαμηλότερου μοριακού βάρους παραλλαγές που χρησιμοποιούνται ως διαλύτες σε από του στόματος υγρά και μαλακές κάψουλες, ενώ οι στερεές παραλλαγές του χρησιμοποιούνται ως βάσεις αλοιφής, συνδετικά δισκίων, επικαλύψεις φιλμ, και λιπαντικά [183]. Το PEG χρησιμοποιείται επίσης ως λιπαντικό σε οφθαλμικές σταγόνες Νέες κλινικές χρήσεις Το PEG, όταν επισημαίνεται με μόριο που φθορίζει στο εγγύς υπέρυθρο, έχει χρησιμοποιηθεί σε προκλινικές δοκιμές ως απεικονιστικός παράγοντας για αγγειακή, λεμφική, και γενικά όγκου απεικόνιση εκμεταλλευόμενος το φαινόμενο της ενισχυμένης διαπερατότητας και το φαινόμενο συγκράτησης (EPR) που παρατηρείται στους όγκους [184]. Υψηλού μοριακού βάρους ΡΕΟ (πχ PEG 8000) έχει μελετηθεί ως προληπτικός παράγων εναντίον καρκίνου του παχέος εντέρου σε ζωικά μοντέλα [185]. Το PEG δείχνει να είναι ο πιο αποτελεσματικός γνωστός παράγοντας για την καταστολή της χημικής καρκινογένεσης σε αρουραίους. Εφαρμογές πρόληψης του καρκίνου σε ανθρώπους, ωστόσο, δεν έχουν ακόμη δοκιμαστεί σε κλινικές δοκιμές [186]. Η ένεση του PEG 2000 στην κυκλοφορία του αίματος σε ινδικά χοιρίδια μετά από τραυματισμό του νωτιαίου μυελού οδηγεί σε ταχεία ανάκτηση μέσω μοριακής επισκευή των νευρικών μεμβρανών [187]. Η αποτελεσματικότητα αυτής της 81
82 θεραπείας για την πρόληψη της παραπληγίας σε ανθρώπους μετά από ένα ατύχημα δεν είναι ακόμη γνωστή. Έρευνα γίνεται για τη χρήση του PEG να συγκαλύψει αντιγόνα στα ερυθρά κύτταρα του αίματος. Διάφορα ερευνητικά ινστιτούτα έχουν αναφέρει ότι η χρήση PEG μπορεί συγκαλύψει αντιγόνα χωρίς να καταστραφεί η λειτουργία και το σχήμα του κυττάρου. Έρευνα γίνεται επίσης για τη χρήση του PEG στο πεδίο της γονιδιακής θεραπείας Βιολογικές χρήσεις Το PEG χρησιμοποιείται συνήθως ως ένα μέσο καταβύθισης για απομόνωση πλασμιδιακού DNA και κρυστάλλωση πρωτεϊνών. Περίθλαση ακτίνων Χ των κρυστάλλων της πρωτεΐνης μπορεί να αποκαλύψει την ατομική δομή των πρωτεϊνών. Τμήματα πολυμερούς που προέρχονται από πολυόλες PEG προσδίδουν ευελιξία για πολυουρεθάνες για εφαρμογές όπως ελαστομερικές ίνες (spandex) και μαξιλάρια αφρού. Το PEG χρησιμοποιείται επίσης για την επαγωγή πλήρους σύντηξης (ανάμειξη των δύο εσωτερικών και εξωτερικών φυλλαδίων) σε λιποσώματα που ανασυντίθενται in vitro. Φορείς γονιδιακής θεραπείας (όπως ιοί) μπορεί να επικαλυφθούν με ΡΕΟ για να προστατευτούν από απενεργοποίηση από το ανοσοποιητικό σύστημα και να τους αποτρέψουν από το να στοχεύσουν όργανα όπου μπορούν να έχουν μια τοξική επίδραση [188]. Το μέγεθος της PEG πολυμερικής αλυσίδας έχει δειχθεί να είναι σημαντικό, με τα μεγαλύτερα πολυμερή να επιτυγχάνουν την καλύτερη ανοσολογική προστασία. Σε τράπεζες αίματος, το PEG χρησιμοποιείται ως ένα δυναμικοποιητής (potentiator) για να ενισχυθεί η ανίχνευση των αντιγόνων και των αντισωμάτων [189]. Κατά την εργασία με φαινόλη σε εργαστηριακή κλίμακα, το PEG 300 μπορεί να χρησιμοποιηθεί σε εγκαύματα στο δέρμα από φαινόλη για την απενεργοποίηση τυχόν υπολειμματικής φαινόλης στο σημείο του εγκαύματος Phosphate buffered saline (PBS) Το φωσφορικό ρυθμιστικό αλατούχο διάλυμα (PBS συντομογραφία) είναι ένα ρυθμιστικό διάλυμα που χρησιμοποιείται συνήθως στη βιολογική έρευνα. Είναι ένα διάλυμα άλατος με βάση το νερό που περιέχει χλωριούχο νάτριο, φωσφορικό νάτριο, και, σε ορισμένες διαμορφώσεις, χλωριούχο κάλιο και φωσφορικό κάλιο. Οι φωσφορικές ομάδες του ρυθμιστικού διαλύματος βοηθούν να διατηρηθεί ένα σταθερό pη. Οι συγκεντρώσεις ιόντων και η ωσμωτικότητα του διαλύματος αντιστοιχούν συνήθως εκείνες του ανθρώπινου σώματος (ισοτονικό). 82
83 Εφαρμογές Το PBS έχει πολλές χρήσεις, επειδή είναι ισοτονικό και μη-τοξικό για τα κύτταρα. Αυτές οι χρήσεις περιλαμβάνουν αραίωση ουσιών και χρήση σε περιέκτες έκπλυσης κυττάρου. PBS με ΕDΤΑ χρησιμοποιούνται επίσης για να απεμπλέξουν συσσωμάτωμα κυττάρων. Δισθενή μέταλλα όπως ο ψευδάργυρος, ωστόσο, δεν μπορούν να προστεθούν σε τέτοιο διάλυμα καθώς αυτό θα οδηγήσει σε καταβύθιση Προετοιμασία Υπάρχουν πολλοί διαφορετικοί τρόποι για την παρασκευή PBS. Ορισμένα σκευάσματα δεν περιέχουν κάλιο, ενώ άλλα περιέχουν ασβέστιο ή μαγνήσιο [190]. Γενικά, ένα διάλυμα PBS περιέχει τα ακόλουθα συστατικά.: Salt Concentration Concentration ( ) (mmol/l) (g/l) NaCl KCl Na 2 HPO 4.2 H 2 O KH 2 PO ph Ο απλούστερος τρόπος για την παρασκευή ενός διαλύματος PBS είναι να χρησιμοποιηθούν ρυθμιστικά δισκία PBS. Αυτές δημιουργούνται για να δώσουν ένα έτοιμο προς χρήση διάλυμα PBS κατά την διάλυση σε καθορισμένη ποσότητα αποσταγμένου νερού. Αυτά είναι διαθέσιμα στις τυποποιημένους όγκους:. 100, 200, 500 και 1000 ml [190]. Εάν τέτοιου τύπου διάλυμα χρησιμοποιηθεί σε καλλιέργεια κυττάρου, το διάλυμα μπορεί να διανεμηθεί σε κλάσματα και να αποστειρώνεται σε αυτόκαυστο (20 λεπτά, 121 C, υγρός κύκλος). Η αποστείρωση μπορεί να μην είναι απαραίτητη ανάλογα με τη χρήση του. Το PBS μπορεί να φυλαχτεί σε θερμοκρασία δωματίου, αλλά μπορεί να χρειάζεται να διατηρηθεί σε κατάσταση ψύξης για την πρόληψη της βακτηριακής ανάπτυξης εάν το διάλυμα δεν είναι στείρο και διατηρείται για μεγάλες χρονικές περιόδους. Ωστόσο, συμπυκνωμένα διαλύματα μπορεί να καθιζάνουν, όταν ψυχθούν και πρέπει να διατηρούνται σε θερμοκρασία δωματίου μέχρι το ίζημα να επαναδιαλυτοποιηθεί τελείως πριν τη χρήση. 83
84 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Β. 84
85 ΚΕΦΑΛΑΙΟ 8. Σύνθεση και διαχωρισμός Νανοσωματιδίων Υλικά που χρησιμοποιήθηκαν για τη σύνθεση και μελέτη των Νανοσωματιδίων. Τα υλικά που χρησιμοποιήθηκαν κατά τις πειραματικές διαδικασίες είναι τα εξής: Poly(D,L-lactide-co-glycolide) lactide:glycolide (65:35), Mw 40,000-75,000, -Sigma Aldrich (PLGA) Poly(D,L-lactide-co-glycolide) lactide:glycolide (75:25), Mw 66, ,000,-Sigma Aldrich (PLGA) BSA (Αλβουμίνη) -Sigma Aldrich PEG 2000 (Πολυαιθυλενογλυκόλη) -Sigma Aldrich Dipyridamole (Διπυριδαμόλη) -Sigma Aldrich Ακετόνη 99.9% -Sigma Aldrich H 2 O (Απιονισμένο Νερό) Παρήχθηκε στο εργαστήριο CHCl 3 (Χλωροφόρμιο) -Sigma Aldrich PBS (ph 7.4) Παρήχθηκε στο εργαστήριο CaCl 2 (Χλωριούχο Ασβέστιο) -Sigma Aldrich Ο εργαστηριακός εξοπλισμός που χρησιμοποιήθηκε είναι ο εξής: Μαγνητικός Αναδευτήρας με ρύθμιση ταχύτητας ανάδευσης σε rpm. Επιστημονικός Ζυγός ακριβείας. Σφαιρική Φιάλη των 100ml. Πλαστική Σύριγγα των 10ml με βελόνα διαμέτρου 0.8mm. Συσκευή Υπερήχων για τη διάλυση των πολυμερών στην οργανική φάση Zetasizer Malvern 3600 AFM (Atomic Force Microscope) NT-MDT Solver P47H Pro SEM (Scanning Electron Microscope) JEOL JSM 6390 UV Spectrometer DSC-50 (SHIMADZU) Rotary Evaporator Φυγόκεντρος Eppendorf Μαγνήτες Πιπέτες (1000μl, 200μl,20μl) Σπάτουλες, Τσιμπίδες 85
86 8.2. Πειραματική διαδικασία για τον σχηματισμό των Νανοσωματιδίων Αρχικά πρέπει να ξεκαθαριστεί ότι επειδή χρησιμοποιήθηκαν 2 τύποι πολυμερούς PLGA με διαφορετικές αναλογίες σε λακτικό και γλυκολικό οξύ, όλα τα πειράματα πραγματοποιήθηκαν και με τους δύο τύπους πολυμερών ώστε να μπορέσει να γίνει μια συγκριτική μελέτη μεταξύ των δύο και να εξαχθούν συμπεράσματα όσον αφορά εάν η επιλογή πολυμερούς επηρεάζει τη συμπεριφορά των νανοσωματιδίων. Εξαρχής αναμένεται να μην υπάρχει εμφανής διαφορά μεταξύ των δύο τύπων καθώς έχουν παρόμοιες αναλογίες λακτικού και γλυκολικού οξέως (65/35 72/25). Οι δύο τύποι πολυμερών αγοράστηκαν από την εταιρία Sigma Aldrich σε πλαστικούς περιέκτες του ενός γραμμαρίου και διατηρήθηκαν στην κατάψυξη σύμφωνα με τις οδηγίες καθ όλη τη διάρκεια των πειραμάτων. Κατά τις διαδικασίες που απαιτούσαν την έξοδό τους από την κατάψυξη έγινε προσπάθεια να παραμένουν εκτός κατάψυξης κατά το ελάχιστο δυνατό διάστημα έτσι ώστε να μην αλλοιωθεί η σύστασή τους. Οι πειραματικές διαδικασίες που ακολουθήθηκαν είναι ίδιες για τους δύο τύπους του πολυμερούς και γι αυτόν τον λόγο από τουδε και στο εξής θα περιγράφεται κάθε διαδικασία για το ένα πολυμερές, εννοώντας ότι ακολουθήθηκε ακριβώς η ίδια και για τον άλλον τύπο. Πριν από κάθε πειραματική διαδικασία όλα τα σκεύη που πρέπει να χρησιμοποιηθούν υφίστανται προσεκτικό καθαρισμό είτε με διαδοχικές πλύσεις με νερό βρύσης και έπειτα με απιονισμένο νερό είτε με αιθανόλη και μετέπειτα μεταφέρονται σε κλίβανο για θέρμανση και στέγνωση στους o C για 15 λεπτά. Το πολυμερές απομακρύνεται από το ψυγείο και ζυγίζεται μια αρχική ποσότητα, συνήθως ένα ή δύο κομμάτια, μιας και βρίσκεται σε μορφή μικρών ορθογωνικών κομματιών μεγέθους περίπου δύο χιλιοστών ακμής. Η μάζα των κομματιών κυμαίνεται από 7 ως 25 mg και εξαρτάται κάθε φορά από το μέγεθος του κομματιού. Είναι πολύ σημαντικό να τονιστεί εδώ ότι εξαιτίας του κόστους του PLGA όλες οι διαδικασίες πραγματοποιήθηκαν με τη φιλοσοφία του scale-down, δηλαδή με άλλα λόγια έχοντας πάντα υπόψη τη χρήση της ελάχιστης ποσότητας πολυμερούς σε σχέση με την αναγκαία ποσότητα για την εκάστοτε πειραματική διαδικασία. Για την παραγωγή των νανοσωματιδίων επιλέχθηκε η τεχνική του nanoprecipitation όπως αυτό έχει ήδη περιγραφεί στο κεφάλαιο 3 ως μια απλή χαμηλού κόστους και υψηλής απόδοσης τεχνική που συνήθως δεν απαιτεί χρήση σταθεροποιητικών ουσιών και έχει χρησιμοποιηθεί παρουσιάζοντας πολύ καλά αποτελέσματα. 86
87 Για την παρασκευή των νανοσωματιδίων χρησιμοποιήθηκε η φόρμουλα που παρουσιάζεται από τον Fejien et al [191], η οποία είναι δοκιμασμένη και οδηγεί στη δημιουργία νανοσωματιδίων με μικρό μέγεθος, ικανοποιητικό για τις εφαρμογές για τις οποίες προορίζονται τα νανοσωματίδια που θέλουμε να φτιάξουμε, δηλαδή για καρδιαγγειακές εφαρμογές. Σύμφωνα με αυτή τη φόρμουλα η συγκέντρωση του πολυμερούς στην οργανική φάση, που κατα τη διάρκεια των πειραμάτων ήταν η ακετόνη, που είναι και εγκεκριμένη για χρήση σε ιατρικές εφαρμογές από τον FDA, βρίσκεται σε συγκέντρωση 10mg/ml. Αυτή η συγκέντρωση παρέμεινε καθ όλη τη διάρκεια των πειραμάτων σταθερή ώστε να είναι συγκρίσιμα τα αποτελέσματα. Στην οργανική φάση εκτός από το πολυμερές διαλύεται και το φάρμακο, δηλαδή η δυπιριδαμόλη, καθώς είναι λιπόφιλο και πρακτικά αδιάλυτο στο νερό. Για τον καθορισμό της συγκέντρωσης της διπυριδαμόλης στην οργανική φάση, παράμετρος πάρα πολύ σημαντική για τη συμπεριφορά των νανοσωματιδίων και ιδιαίτερα για το ποσοστό εγκλωβισμού και τη μετέπειτα απελευθέρωση του φαρμάκου από τα νανοσωματίδια έγιναν πειράματα διαλυτότητας της διπυριδαμόλης σε ακετόνη σε διάφορες συγκεντρώσεις. Αποδείχθηκε ότι συγκέντρωση πάνω από 1mg/ml διπυριδαμόλης σε ακετόνη οδηγούσε σε σχηματισμό διασποράς και καθίζηση ιζήματος διπυριδαμόλης που κατέστη αδύνατο να επαναδιαλυτοποιηθεί ακόμα και μετά από μαγνητική ανατάραξη υπό θέρμανση και διάλυση σε υδατόλουτρο υπερήχων μετά από 30 λεπτά. Γι αυτό το λόγο αποφασίστηκε να χρησιμοποιηθεί η συγκέντρωση 1mg/ml διπυριδαμόλης σε ακετόνη ως η πρότυπη συγκέντρωση αλλά παράλληλα διερευνήθηκε και αν η συγκέντρωση της διπυριδαμόλης επηρεάζει το σχηματισμό των νανοσωματιδίων, το τελικό μέγεθός τους και το δυναμικό ζήτα όπως θα αναλυθεί σε επόμενο κεφάλαιο. Η αναλογία οργανικής- υδατικής φάσης σύμφωνα με την ίδια φόρμουλα καθορίστηκε στο 1/3, δηλαδή για κάθε 1ml ακετόνης χρησιμοποιήθηκαν 3ml απιονισμένου νερού είτε PBS. Από αυτή την αναλογία συμπεραίνει κανείς ότι η διασπορά που θα σχηματιστεί αρχικά κατά την ανάμειξη των φάσεων μπορεί να χαρακτηριστεί σαν μια διασπορά όπου η συνεχής φάση είναι το ύδωρ και η διασπειρώμενη φάση είναι η οργανική. Η αλβουμίνη και η πολυαιθυλενογλυκόλη είναι αμφότερες υδατοδιαλυτές οπότε προστίθενται στην υδατική φάση. Συνήθως στη βιβλιογραφία η αλβουμίνη προστίθεται μετά τη φάση του διαχωρισμού των νανοσωματιδίων από τα ελεύθερα συστατικά κατά την επαναδιαλυτοποίηση των νανοσωματιδίων. Εδώ παρ όλα αυτά η προσθήκη της γίνεται στο αρχικό στάδιο αμέσως μετά την προσθήκη της πολυαιθυλενογλυκόλης χάριν απλούστευσης 87
88 της διαδικασίας αλλά εξαιτίας και των προβλημάτων που αντιμετωπίσαμε κατά το διαχωρισμό και θα αναλυθούν σε επόμενο κεφάλαιο. Οι συγκεντρώσεις της αλβουμίνης και της πολυαιθυλενογλυκόλης στην υδατική φάση αλλά και η μεταξύ τους αναλογίας είναι επίσης μέρος αυτής της φόρμουλας και ορίζεται ώς εξής: Η αναλογία μεταξύ αλβουμίνης και πολυαιθυλενογλυκόλης είναι 1/5 και η συγκέντρωση της πολυαιθυλενογλυκόλης στην υδατική φάση είναι 10mg/ml. Αφού λοιπόν ζυγιστεί με ακρίβεια η μάζα του πολυμερούς και με βάση τη φόρμουλα γίνουν οι υπολογισμοί για τις ανάλογες μάζες και όγκους των άλλων συστατικών τοποθετείται η υδατική φάση σε υάλινο περιέκτη (συνήθως υάλινο μπουκάλι χωρητικότητας ml), και με τη χρήση μαγνήτη μήκους 1cm ο περιέκτης τοποθετείται σε μαγνητικό αναδευτήρα με ταχύτητα λειτουργίας 250 rpm. Η επιρροή της ταχύτητας λειτουργίας του μαγνητικού αναδευτήρα μελετήθηκε σε εύρος λειτουργίας από 100rpm έως 400rpm. Αποδείχθηκε ότι το εύρος λειτουργίας μεταξύ 200 και 300 rpm είναι το πιο ιδανικό καθώς κάτω από 200 rpm η υδατική φάση αναδεύεται σχετικά αργά και κατά την προσθήκη της οργανικής φάσης με ενστάλαξη στάγδην οδηγούσε στη δημιουργία ενός επιφανειακού φιλμ από συσσωματώματα πολυμερούς που δύσκολα μετέπειτα επαναδιαλυτοποιούταν. Πάνω από 300 rpm η ανάδευση οδηγούσε στην εκτίναξη κατά την ενστάλαξη μέρους της οργανικής φάσης στα τοιχώματα του περιέκτη και απώλεια κάποιου μέρους της οργανικής φάσης που έμενε εκεί. Οπότε αποφασίστηκε να χρησιμοποιείται μια μέση ταχύτητα ανάμεσα στις 200 και 300 rpm, ήτοι 250 rpm για όλα τα πειράματα. Ταχύτητα αναδευτήρα rpm Αποτέλεσμα Έντονος σχηματισμός φιλμ Σχηματισμός φιλμ Φυσιολογική ανάδευση Φυσιολογική ανάδευση Φυσιολογική ανάδευση Απώλειες στα τοιχώματα Έντονες απώλειες στα τοιχώματα Πίνακας 4 Μετά την ανάδευση της υδατικής φάσης για 5 λεπτά προστίθεται η πολυαιθυλενογλυκόλη υπό ανάδευση. Αφού είναι εμφανής με γυμνό μάτι η πλήρης διάλυση της στην υδατική φάση, διαδικασία που δεν διαρκεί πάνω από 2 λεπτά, προστίθεται και η αλβουμίνη υπό ανάδευση. 88
89 Παράλληλα η οργανική φάση, δηλαδή η ακετόνη, προστίθεται σε διαφορετικό περιέκτη, συνήθως υάλινο περιέκτη χωρητικότητας 25 ml. Στην οργανική φάση προστίθεται η διπυριδαμόλη και αναδεύεται ήπια για 30 δευτερόλεπτα ώστε να διαλυθεί πλήρως. Μετέπειτα προστίθεται το πολυμερές και ο περιέκτης μεταφέρεται σε λουτρό υπερήχων για διάλυση. Συνήθως η διαδικασία διαρκεί από 2 έως 5 λεπτά, αναλόγως με τη μάζα του πολυμερούς. Για μάζα πολυμερούς 20 mg (που ήταν και το πιο σύνηθες) η διαδικασία διαρκεί 5 λεπτά μέχρι την πλήρη διάλυση του PLGA στο ακετονικό διάλυμα της διπυριδαμόλης. Αξίζει να σημειωθεί ότι ο τύπος 65/35 του πολυμερούς διαλύεται πάντα στο μισό χρόνο από ότι ο τύπος 75/25. Τώρα που και η οργανική φάση είναι έτοιμη, μεταφέρεται σε πλαστική σύριγγα μίας χρήσης των 10ml. Ακολουθεί η ενστάλαξη της οργανικής φάσης στην αναδευόμενη υδατική στάγδην. Σε αυτό το σημείο της διαδικασίας υπάρχουν δύο παράμετροι που πρέπει να μελετηθούν. Ο πρώτος είναι η απόσταση που θα έχει η άκρη της βελόνας της σύριγγας από την επιφάνεια της αναδευώμενης υδατικής φάσης και ο δεύτερος είναι ο ρυθμός ενστάλαξης. Η βελόνα τοποθετείται κεντρικά του περιέκτη και παρατηρήθηκε η ενστάλαξη σε διάφορες αποστάσεις. Απόσταση 1cm από την επιφάνεια της αναδευόμενης υδατικής φάσης φαίνεται να είναι ιδανική αφού σε μικρότερη απόσταση υπάρχει πάντα ο κίνδυνος να ακουμπήσει η άκρης της βελόνας με την επιφάνεια και να μεταφερθεί μέσω τριχοειδών φαινομένων υδατική φάση μέσα στον περιέκτη της οργανικής. Σε απόσταση μεγαλύτερη από 2 cm παρατηρήθηκαν σε ορισμένες περιπτώσεις κάποιες απώλειες οργανικής φάσης στα τοιχώματα λόγω δημιουργίας αναταράξεων στην επιφάνεια της υδατικής. Τελικώς αποφασίστηκε να χρησιμοποιείται σε όλα τα πειράματα η απόσταση του 1 cm μεταξύ της άκρης της βελόνας και της επιφάνειας του δείγματος. Ο δεύτερος παράγοντας, δηλαδή αυτός του ρυθμού ενστάλαξης ήταν και ο πιο κρίσιμος να ελεγχθεί καθώς απουσία κάποιας συσκευής ελεγχόμενης ροής ή κάποια διάταξης παρόμοιας με τις διατάξεις ελεγχόμενης έγχυσης ουσιών σε ασθενείς έκανε κάτι τέτοιο αδύνατο. Παρ όλα αυτά ελέγχθηκε εάν ο ρυθμός ή ακόμα και ο τρόπος της ενστάλαξης έχει κάποια εμφανή αποτελέσματα κατά την ανάμειξη των δυο φάσεων. Ο ρυθμός ενστάλαξης δε φαίνεται να επηρεάζει τη διαδικασία είτε όταν έχουμε 1 σταγόνα ανά δευτερόλεπτο ή σχεδόν συνεχόμενη ροή. Επίσης δοκιμάστηκε να γίνει εφάπαξ ενστάλαξη όλης της οργανικής φάσης. Ακόμα και σε αυτή την περίπτωση δεν φάνηκε να υπάρχει κάποια διαφορά εκτός ελαχίστων περιπτώσεων όπου λόγω της ταχύτητας με την οποία εκτοξεύεται η οργανική φάση μέσα στην υδατική δημιουργεί έντονη ανατάραξη στην επιφάνεια και εγκλωβισμό φυσαλίδων αέρα. Αυτό οδηγεί παροδικά, στον σχηματισμό ενός επιφανειακού φιλμ, το οποίο όμως κατά 89
90 τη συνέχεια διαλύεται πάντα λόγω της ανάδευσης. Τελικώς αποφασίστηκε ένας ρυθμός ροής μεταξύ 2 και 5 σταγόνων ανά δευτερόλεπτο για την ενστάλαξη. Το δείγμα αφού ολοκληρωθεί η ενστάλαξη αφήνεται προς ανάδευση για 30 λεπτά και μετέπειτα μεταφέρεται αυτούσιο σε σφαιρική φιάλη των 100 ml, και τοποθετείται σε συσκευή rotary evaporator για την επιτάχυνση της εξάτμισης του διαλύτη και τη δημιουργία των νανοσωματιδίων. Αυτή η διάταξη επιλέχτηκε για την επιτάχυνση της διαδικασίας της εξάτμισης της ακετόνης μιας και διαφορετικά ανάλογα πάντα και με τον όγκο της οργανικής φάσης η διαδικασία θα διαρκούσε πολύ περισσότερο. Η θερμοκρασία λειτουργίας της διάταξης ρυθμίστηκε στους 40 o C, και η ταχύτητα περιστροφής της σφαιρικής φιάλης στη μια στροφή ανά δευτερόλεπτο. Είναι πολύ κρίσιμο να διατηρηθεί η θερμοκρασία σε αυτά τα επίπεδα και οπωσδήποτε να μην ξεπεράσει τους 45 o C, θερμοκρασία στην οποία το PLGA παρουσιάζει glass transition, άρα αλλά ζουν οι ιδιότητες με αποτέλεσμα να αλλάζει ολόκληρο το δείγμα και να δημιουργείται συνεχές φιλμ. Οπότε είναι πολύ σημαντικό να παρακολουθείται η θερμοκρασία μέσω του ενσωματωμένου θερμομέτρου που είχε η διάταξη ώστε να μην ξεπεράσει τους 45 βαθμούς. Πτώση της θερμοκρασίας κάτω από τους 40 βαθμούς δε δημιουργεί κάποιο πρόβλημα απλώς επιβραδύνει τη διαδικασία. Ο απαιτούμενος χρόνος για την εξάτμιση της ακετόνης εξαρτάται από τον όγκο της οργανικής φάσης και τη θερμοκρασία κυρίως. Για τις πειραματικές συνθήκες που επικρατούσαν κατά τη διάρκεια των πειραμάτων αυτός κυμαίνεται μεταξύ 15 έως 30 λεπτών. Ακολούθως η διασπορά των νανοσωματιδίων που έχει σχηματιστεί μεταφέρεται σε περιέκτη Eppendorf και αφήνεται στο ψυγείο για να ηρεμήσει για 10 λεπτά και ακολουθεί ο διαχωρισμός Πειραματική διαδικασία για το διαχωρισμό των Νανοσωματιδίων Αρχικά για τη διαδικασία του διαχωρισμού θα πρέπει να τονιστεί ότι σύμφωνα με τη βιβλιογραφία για το διαχωρισμό σωματιδίων μεγέθους μικρότερου των νανομέτρων χρησιμοποιείται υπερφυγόκεντρος. Εμείς δεν είχαμε αυτή τη δυνατότητα μιας και αφενός μεν ούτε το τμήμα Φυσικής ούτε το τμήμα Φαρμακευτικής διαθέτουν αυτή τη διάταξη. Βρέθηκε υπερφυγόκεντρος στο τμήμα Βιολογίας, στον τομέα Μοριακής Βιολογίας, Γενετικής και Εξέλιξης αλλά αφενός μεν το μηχάνημα δεν είχε χρησιμοποιηθεί πρόσφατα και αφετέρου για τα συγκεκριμένα πειράματα χρειαζόταν να αγοραστούν ειδικές κυψελίδες που ήταν ιδιαίτερα ακριβές. Γι αυτό το λόγο αποφασίσαμε να χρησιμοποιήσουμε απλή φυγόκεντρο και με παραμετροποίηση, κάνοντας επαναλαμβανόμενες φυγοκεντρίσεις και επαναδιαλυτοποιήσεις 90
91 να προσεγγίσουμε το επιθυμητό αποτέλεσμα. Γνωρίζουμε εξαρχής ότι πλήρης διαχωρισμός δε μπορεί κατά αυτόν τον τρόπο να επιτευχθεί αλλά και με βάση κάποια αποτελέσματα που θα συζητηθούν σε επόμενα κεφάλαια πιστεύουμε ότι προσεγγίσαμε πάρα πολύ τον στόχο του τέλειου διαχωρισμού. Έχοντας λοιπόν υπόψιν αυτή την αδυναμία της μεθόδου, τα δείγματα αφού ηρεμήσουν για 10 λεπτά στο ψυγείο μεταφέρονται σε φυγόκεντρο που υποδέχεται πλαστικούς περιέκτες Eppendorf και τοποθετούνται πάντα σε δυάδες αντιδιαμετρικά με τέτοιο τρόπο ώστε να εξασφαλιστεί η σωστή λειτουργία της συσκευής. Η διαδικασία της φυγοκέντρισης πραγματοποιείται σε ταχύτητα rpm, που είναι και το όριο του οργάνου και για 30 λεπτά. Ακολούθως οι περιέκτες συλλέγονται από το όργανο, το υπερκείμενο απομακρύνεται, γίνεται επαναδιαλυτοποίηση στην ίδια υδατική φάση που χρησιμοποιήθηκε και κατά το σχηματισμό των νανοσωματιδίων και η φυγοκέντριση επαναλαμβάνεται άλλες 3 φορές για τον καλύτερο διαχωρισμό των νανοσωματιδίων. Μετά και από την τελευταία φυγοκέντριση απομακρύνεται το υπερκείμενο υγρό και συλλέγονται τα νανοσωματίδια έιτε σε στερεή κατάσταση είτε επαναδιαλυτοποιούνται αναλόγως το πείραμα ή τη διαδικασία που ακολουθεί Συμπεράσματα Η επιλογή του πολυμερούς βασίστηκε στο γεγονός ότι χρειαζόμαστε ένα πολυμερές που να παρουσιάζει κατάλληλες ιδιότητες όπως βιοσυμβατότητα και βιοαποικοδομησιμότητα και να είναι εγκεκριμένο για ιατρικές χρήσεις. Πράγματι το PLGA παρουσιάζει όλα τα απαραίτητα χαρακτηριστικά για αυτές τις εφαρμογές και έχει μελετηθεί εκτενώς σαν φορέας μεταφοράς φαρμάκων, ελεγχόμενης και παρατεταμένης αποδέσμευσης. Για το σχηματισμό νανοσωματιδίων ως φορέων για τη μεταφορά φαρμάκων χρησιμοποιήθηκαν 2 τύποι του συμπολυμερούς PLGA, που διαφέρουν κατά λίγο στην αναλογία του λακτικού και του γλυκολικού οξέως. Κατά τη διάρκεια της σύνθεσης και του διαχωρισμού δεν παρατηρήθηκε καμία εμφανής διαφορά μεταξύ των δύο τύπων, κάτι αναμενόμενο καθώς δε διαφέρουν ιδιαίτερα στις αναλογίες των πολυμερών στο συμπολυμερές. Παρ όλα αυτά αποφασίστηκε να συνεχιστεί η χρήση και των 2 τύπων ώστε να διευκρινιστεί αν παρουσιάζουν κάποια διαφορά σε περαιτέρω πειράματα. Η μέθοδος που επιλέχτηκε είναι αυτή του Nanoprecipitation. Οι λόγοι γι αυτή την επιλογή είναι αφενός μεν η απλότητα της μεθόδου και αφετέρου η μη ύπαρξη ανάγκης χρήσης σταθεροποιητικών ουσιών, όπως στην τεχνική emulsion-difussion όπως συζητήθηκε στο κεφάλαιο Ακόμα ένας πολύ σημαντικός λόγος που έκανε την τελευταία μη ιδανική 91
92 για αυτή την εργασία είναι το γεγονός ότι οι υπάρχουσες συσκευές ομογενοποίησης που είχαμε στη διάθεσή μας απαιτούσαν scale up τις μεθόδου σε όγκους και μάζες που για τα δεδομένα της χρηματικής αξίας του PLGA κρίνονται απαγορευτικές. Οπότε η τεχνική του Nanoprecipitation κρίνεται η καταλληλότερη για αυτές τις συνθήκες. Για να πραγματοποιηθεί η παραπάνω τεχνική αφού έχει επιλεγεί το πολυμερές, πρέπει να επιλεχθεί από τι θα αποτελείται η υδατική και η οργανική φάση. Για την οργανική επιλέχτηκε η ακετόνη, μιας και είναι εγκεκριμένη για τέτοιες εφαρμογές, είναι φθηνή και είναι γνωστά τα χαρακτηριστικά της. Άλλοι διαλύτες που αναφέρονται στη βιβλιογραφία όπως το ακετονιτρίλιο απορρίφθηκαν σε αρχικά πειράματα διότι σχημάτιζαν πολυδιασπορές με συσσωματώματα εξ αρχής. Για την υδατική φάση μια πολύ λογική επιλογή είναι το ύδωρ. Μιας και στο πλαίσιο των πειραμάτων αυτής της εργασίας δεν απαιτούνται ιδιαίτερες συνθήκες αποστείρωσης μιας και δεν έχουμε να κάνουμε με κάποια πειράματα in vitro και in vivo η επιλογή του απιονισμένου νερού προκρίθηκε έναντι αυτής του απεσταγμένου, για οικονομικούς κυρίως λόγους. Η επιλογή νερού βρύσης κρίνεται ανεπαρκής γιατί αφενός μεν πρέπει να γίνει ανάλυση των αλάτων καθώς και όλων των άλλων διαλυμένων ουσιών, και θα πρέπει να μελετηθεί και πως αυτά επηρεάζουν την όλη διαδικασία, και αφ ετέρου, η σύσταση αυτών των συστατικών τείνει να μην είναι σταθερή στο νερό του δικτύου. Οπότε η επιλογή του απιονισμένου νερού (διαδικασία που επιτελείται στο εργαστήριο της Φαρμακευτικής Τεχνολογίας) κρίθηκε η καταλληλότερη ή εναλλακτικά χρήση ρυθμιστικού διαλύματος PBS. Η επιλογή του φαρμάκου καθώς και τα φυσικοχημικά χαρακτηριστικά αυτού είναι πολύ σημαντική παράμετρος μιας και καθορίζει και τις επιλογές των υπόλοιπων στοιχείων. Στην περίπτωσή μας η διπυριδαμόλη είναι πρακτικά αδιάλυτη στο νερό οπότε διαλύεται στη οργανική φάση, δηλαδή στην ακετόνη μαζί με το πολυμερές. Αν είχαμε να κάνουμε με κάποιο υδρόφιλο φάρμακο που έπρεπε να διαλυθεί στην υδατική φάση η όλη διαδικασία θα σχεδιαζόταν διαφορετικά. Τέλος οι επιλογή τόσο της αλβουμίνης αλλά και της πολυαιθυλενογλυκόλης για να προσδώσουν στα νανοσωματίδια συγκεκριμένα χαρακτηριστικά που παρουσιάστηκαν πιο πάνω στα αντίστοιχα κεφάλαια αλλά θα συζητηθούν και αργότερα, έγινε με βάση τη βιβλιογραφία [191]. Κατά το στάδιο της σύνθεσης ελέγχθηκαν αρκετοί παράγοντες που επηρεάζουν τη σύνθεση, κάποιοι από αυτούς διατηρήθηκαν σταθεροί ενώ άλλοι μελετήθηκαν σε σχέση με την επιρροή τους στο στάδιο του σχηματισμού και παρουσιάστηκαν είτε σε αυτό το κεφάλαιο είτε θα παρουσιαστούν σε επόμενα κεφάλαιο. 92
93 Καταφέραμε με όλες αυτές τις μελέτες να καταλήξουμε σε ένα σετ παραμέτρων που διατηρούνται σταθερές κατά τη σύνθεση των νανοσωματιδίων και οδηγούν σε επαναλαμβανόμενα αποτελέσματα, άρα η προσέγγισή μας όσον αφορά αυτή τη μέθοδο μπορεί να κριθεί επαναλήψιμη, αποτελεσματική και όσο πιο απλή γίνεται έτσι ώστε να μπορεί να μεταφερθεί και σε μεγαλύτερη κλίμακα παραγωγής με scale up. Τέλος επιτελέστηκε κατά τέτοιον τρόπο ώστε να διατηρηθεί το κόστος χαμηλά αλλά παράλληλα να μη γίνει κάποια παραχώρηση στην ποιότητα των αποτελεσμάτων όσο αυτό κατέστη δυνατό υπό τις υπάρχουσες οικονομικές συνθήκες. Όπως θα φανεί και στα επόμενα κεφάλαια είχαμε πολύ ικανοποιητικά αποτελέσματα όσον αφορά τη σύνθεση των νανοσωματιδίων, τα χαρακτηριστικά τους και τη σταθερότητά τους στο χρόνο. Για το κομμάτι του διαχωρισμού κρατάμε πάντα το γεγονός ότι ελλείψει υπερφυγοκέντρου αυτός δεν είναι τέλειος, αλλά μετά από εκτεταμένες προσπάθειες φτάσαμε στο σημείο με τη διαδικασία που ακολουθούμε να προσεγγίζουμε το επιθυμητό αποτέλεσμα πάρα πολύ. 93
94 ΚΕΦΑΛΑΙΟ 9. Μετρήσεις μεγέθους και ζ-δυναμικού των Νανοσωματιδίων Μετρήσεις μεγέθους Αρχικά αξίζει να σημειωθεί ότι έγιναν πολλά προκαταρκτικά πειράματα για να καταλήξουμε σε ένα σταθερό σετ παραμέτρων και να υπάρχει μεγαλύτερη άνεση και εμπειρία κατά τη εκτέλεση των μετρήσεων για πιο αξιόπιστα αποτελέσματα. Τα αποτελέσματα αυτών των πειραμάτων δεν παρουσιάζονται στα πλαίσια αυτής της εργασίας μιας και αποτέλεσαν κυρίως πρακτική άσκηση και προσαρμογή με τις συνθήκες του εργαστηρίου. Για τη μέτρηση του μεγέθους αλλά και του ζ-δυναμικού των νανοσωματιδίων χρησιμοποιήθηκε η διάταξη Zetasizer 3600 από τη Malvern, όργανο που παρουσιάστηκε εκτενώς στο κεφάλαιο 3. Οι μετρήσεις των δειγμάτων γίνονται αμέσως μετά το τέλος τη σύνθεσης των νανοσωματιδίων, παίρνοντας ένα μέρος του δείγματος, συνήθως μl, μεταφέροντας το στη ειδική κυψελίδα που παρουσιάστηκε στο κεφάλαιο 3, και εκτελώντας τις μετρήσεις πάντα εις τριπλούν σε θερμοκρασία 25 o C. Για όλες τις μετρήσεις χρησιμοποιήθηκαν προ εγκατεστημένα πρωτόκολλα στο λογισμικό του προγράμματος κατάλληλα για τη μελέτη νανοσωματιδίων από πολυμερή. Αρχικά μετρήθηκε το μέγεθος των απλών νανοσωματιδίων από PLGA, απουσία φαρμάκου αλλά και των άλλων στοιχείων όπως αλβουμίνη και πολυαιθυλενογλυκόλη. Φυσικά όπως έχει αναφερθεί και παραπάνω οι μετρήσεις πάντα γίνονται σε δείγματα και από τα δύο πολυμερή και αυτό το πείραμα αποτελεί μια πρώτη ένδειξη για το αν υπάρχουν διαφοροποιήσεις μεταξύ των 2 τύπων του πολυμερούς. Ακολουθήθηκε η διαδικασία σύνθεσης όπως περιγράφηκε και στο προηγούμενο κεφάλαιο και πάρθηκαν δείγματα και από τους δύο τύπους πολυμερούς. Το αποτέλεσμα ήταν και στις 2 περιπτώσεις νανοσωματίδια μεγέθους γύρω στα 160 με 170 νανόμετρα, με πολύ καλές κατανομές χωρίς την ύπαρξη συσσωματωμάτων. Εικόνες 8 & 9. Το επόμενο βήμα ήταν να μελετήσουμε εάν η συγκέντρωση της διπυριδαμόλης στον υδατικό φορέα επηρεάζει το μέγεθος αλλά και το ζ-δυναμικό των νανοσωματιδίων. Γι αυτό το σκοπό πραγματοποιήθηκαν συγκριτικές μελέτες χρησιμοποιώντας διαφορετικές συγκεντρώσεις διπυριδαμόλης, ξεκινώντας από άδεια νανοσωματίδια με 0μg/ml ή όπως θα αναφέρεται από τούδε και στο εξής 0ppm (1μg/ml=1ppm), μέχρι τη μέγιστη εφικτή συγκέντρωση που επιτυγχάνεται στην ακετόνη, 1000ppm (Διαγράμματα 1α,β & 2). 94
95 Εικόνα 8, PLGA 75/25 Απουσία Φαρμάκου Εικόνα 9, PLGA 65/35 Απουσία Φαρμάκου 95
96 Διάγραμμα 1α, PLGA 65/35 Διάγραμμα 1β, PLGA 75/25 96
97 Διάγραμμα 2. Συγκριτικό διάγραμμα μετάξυ PLGA6535 και PLGA7525 για μέγεθος. Από ότι φαίνεται από τα παραπάνω διαγράμματα και οι 2 τύποι πολυμερών παρουσιάζουν το ίδιο προφίλ με τη συγκέντρωση της διπυριδαμόλης να μην επηρεάζει αισθητά το μέγεθος των νανοσωματιδίων όσο αυτή αυξάνεται. Αντιθέτως παρατηρείται μείωση του μεγέθους των νανοσωματιδίων γενικά παρουσία διπυριδαμόλης σε σχέση με τα άδεια νανοσωματίδια. Από διαμέτρους λοιπόν γύρω στα 160 με 170 νανόμετρα, παρουσία διπυριδαμόλης το μέγεθος μειώνεται, και κυμαίνεται γύρω στα 150 νανόμετρα. Βέβαια, και αυτό είναι κάτι που πρέπει να σημειωθεί όπως είναι εμφανές, και ιδιαίτερα από το διάγραμμα του τύπου 75/25 υπάρχει μια σημαντική τυπική απόκλιση, που εμφανίζεται στα αποτελέσματα και στατιστικά δεν πρέπει να αγνοηθεί. Με άλλα λόγια αν μελετήσει κάποιο πιο λεπτομερώς τα διαγράμματα θα καταλάβει ότι, λαμβάνοντας υπόψιν και την τυπική απόκλιση, δε μπορούμε να πούμε ότι η συγκέντρωση της διπυριδαμόλης επηρεάζει τόσο πολύ τη διάμετρο των σωματιδίων της, αλλά παρουσία διπυριδαμόλης στο ακετονικό διάλυμα, ωθεί το τελευταίο στο να έχει ίσως ελάχιστα διαφορετικά φυσικοχημικά χαρακτηριστικά και άρα να οδηγεί στο σχηματισμό νανοσωματιδίων με ελάχιστα μικρότερο μέγεθος. Παρ όλα αυτά, μελετώντας και πάλι τις κατανομές των μεγεθών των νανοσωματιδίων βλέπουμε ότι σε κάθε περίπτωση είναι πολύ καλές, με πολύ ικανοποιητικούς δείκτες πολυδιασποράς (PDI) και χωρίς να εμφανίζονται σωματίδια μεγαλύτερου μεγέθους και συσσωματώματα. Αυτό φαίνεται καλύτερα και στις παρακάτω εικόνες. 97
98 Εικόνα 10, PLGA 75/25, Συγκέντρωση Διπυριδαμόλης 250ppm Εικόνα 11, PLGA 75/25, Συγκέντρωση Διπυριδαμόλης 500ppm 98
99 Εικόνα 12, PLGA 75/25, Συγκέντρωση Διπυριδαμόλης 1000ppm Εικόνα 13, PLGA 65/35, Συγκέντρωση Διπυριδαμόλης 250ppm 99
100 Εικόνα 14, PLGA 65/35, Συγκέντρωση Διπυριδαμόλης 500ppm Εικόνα 15, PLGA 65/35, Συγκέντρωση Διπυριδαμόλης 1000ppm 100
101 9.2. Μετρήσεις ζ-δυναμικού Αρχικά όπως και με τις μετρήσεις για το μέγεθος των σωματιδίων, διερευνήθηκε το αν οι δυο τύποι του πολυμερούς παρουσιάζουν διαφορετικό προφίλ ως αναφορά το δυναμικό ζήτα. Σύμφωνα και με τις Εικόνες 8 & 9 φτάνουμε στο συμπέρασμα ότι δεν υπάρχει ουσιαστική διαφορά ανάμεσα στους 2 τύπους όσον αφορά τα άδεια νανοσωματίδια απουσία φαρμάκου αλλά το ίδιο ισχύει και για τις διάφορες συγκεντρώσεις διπυριδαμόλης όπως φαίνεται και στα διαγράμματα 1 & 2. Το δυναμικό ζήτα είναι μια σημαντική παράμετρος και όπως ήδη έχει παρουσιαστεί στο κεφάλαιο 3.1. αποτελεί ένα μέτρο για το πόσο σταθερή είναι μια διασπορά μέσα σε ένα μέσο. Σύμφωνα με τον Πίνακα 2 η περιοχή τιμών για το ζ- δυναμικό ανάμεσα σε -10 και -30 mv υποδεικνύει μια ελάχιστη κατάσταση σταθερότητας. Αυτό το μέγεθος εξαρτάται πάντα βέβαια και από το μέσο διασποράς. Κρατάμε αυτήν την παρατήρηση γιατί θα μας απασχολήσει σε επόμενο κεφάλαιο. Μετά το πέρας των πρώτων πειραμάτων εκτελούνται πειράματα για τον καθορισμό της επίδρασης της συγκέντρωσης της διπυριδαμόλης στα νανοσωματίδια όπως ακριβώς έγινε και με τη μέτρηση του μεγέθους. Εικόνα 16, PLGA 75/25 Απουσία Φαρμάκου 101
102 Εικόνα 17, PLGA 65/35 Απουσία Φαρμάκου Διάγραμμα 3α, PLGA 65/35 102
103 Διάγραμμα 3β, PLGA 75/25 Διάγραμμα 4, Συγκριτικό διάγραμμα μετάξυ PLGA6535 και PLGA7525 για ζ-δυναμικό. 103 Αρχικά το πρώτο που πρέπει να προσέξουμε είναι ότι σε κάθε περίπτωση είτε τα σωματίδια είναι άδεια είτε περιέχουν κάποια ποσότητα διπυριδαμόλης, οι τιμές του ζ-
104 δυναμικού κυμαίνονται από -12mV έως -16mV. Αυτή η περιοχή βρίσκεται μέσα στο εύρος της περιοχής που εκφράζει μια αμφίβολη σταθερότητα, και πιθανή δημιουργία συσσωματωμάτων και ιζημάτων κατά την πάροδο του χρόνου. Κατά τα άλλα φαίνεται πως παρουσία φαρμάκου υπάρχει μια μικρή μεταβολή του ζ-δυναμικού προς μικρότερες τιμές και αυτό πιστεύουμε ότι οφείλεται στο ότι ένα διάλυμα ακετόνης χωρίς και με διαλυμένη μέσα ποσότητα διπυριδαμόλης έχει κάποιες, ίσως ελάχιστες, αλλά σίγουρα υπαρκτές διαφορές όσον αφορά τις φυσικοχημικές ιδιότητες. Έτσι αυτό επηρεάζει το ζ-δυναμικό, έστω και ελάχιστα. Η διαφορά όμως που παρατηρείται δεν μπορεί να θεωρηθεί ικανή να επάγει σημαντικές τροποποιήσεις στη συμπεριφορά των νανοσωματιδίων. Τέλος για ακόμη μια φορά θα τονίσουμε ότι τα πολυμερή εμφανίζουν παρόμοιο προφίλ χωρίς διαφοροποιήσεις μεταξύ τους Μετρήσεις μετά την επεξεργασία με PEG και Αλβουμίνη Αφού ολοκληρώθηκαν οι αρχικές μετρήσεις μεγέθους και ζ-δυναμικού το επόμενο βήμα ήταν να μελετηθεί το εάν και πόσο επηρεάζει η παρουσία της πολυαιθυλενογλυκόλης και της αλβουμίνης τις παραπάνω παραμέτρους και γενικά το σχηματισμό των νανοσωματιδίων, δηλαδή αν έχουμε κάποια συσσωματώματα ή κάποια πολυδιασπορά. Πραγματοποιήθηκαν λοιπόν μετρήσεις πάνω στους 2 τύπους του πολυμερούς και τα αποτελέσματα συγκρίθηκαν με αυτά των νανοσωματιδίων χωρίς πολυαιθυλενογλυκόλη και αλβουμίνη. Οι μετρήσεις του μεγέθους δεν έδειξαν σημαντική διαφοροποίηση και παράλληλα δεν εμφανίστηκαν ούτε συσσωματώματα ούτε πολλαπλές κορυφές στη διασπορά των τιμών, γεγονός πολύ ενθαρρυντικό για τη συνέχεια. Διαγράμματα 5, 6, 7 & 8 Αξίζει να σημειωθεί πως βάσει των προηγούμενων μετρήσεων χρησιμοποιείται πλέον η συγκέντρωση των 1000ppm δυπιριδαμόλης σε όλα τα δείγματα για τις μετρήσεις από εδώ και στο εξής μιας και αυτή η συγκέντρωση είναι η μέγιστη δυνατή που μπορούμε να επιτύχουμε. Όσον αφορά όμως τις μετρήσεις του δυναμικού ζ, βλέπουμε ότι όταν έγινε σύνθεση των νανοσωματιδίων μόνο με πολυαιθυλενογλυκόλη, η τιμή του ζ-δυναμικού εμφάνισε μια αύξηση, έστω και μικρή. Αυτό πιθανότατα οφείλεται στο γεγονός ότι η συγκέντρωση της πολυαιθυλενογλυκόλης στον υδατικό φορέα είναι της ίδιας τάξης μεγέθους με αυτή του PLGA στον οργανικό και επομένως είναι αναμενόμενο να επηρεάζει η ύπαρξή της στη διασπορά των ναοσωματιδίων. Αφετέρου είναι μια ένδειξη τάσης της διασποράς προς 104
105 μεγαλύτερες τιμές ζ-δυναμικού που μπορεί να αναδεικνύουν μια μικρότερη σταθερότητα και τάση προς συσσωμάτωση, αν και η τελευταία δεν παρατηρήθηκε. Είναι πολύ ενδιαφέρον, διότι η χρήση πολυαιθυλενογλυκόλης συχνά συνδέεται με μια τάση προς δημιουργία συσσωματωμάτων κατά τη διάρκεια της αποικοδόμησης της πολυαιθυλενογλυκόλης με το χρόνο. Δεδομένου ότι στη διασπορά υπάρχει και ελεύθερη πολυαιθυλενογλυκόλη που δε ενσωματώθηκε στα νανοσωματίδια, είναι πιθανόν αυτή η τάση προς μια πιο ασταθή κατάσταση να οφείλεται σε αυτό το φαινόμενο. Ακόμα πιο ενδιαφέρουσα είναι η παρατήρηση ότι η προσθήκη της αλβουμίνης οδήγησε στην επαναφορά των τιμών του δυναμικού ζ στις τιμές των νανοσωματιδίων πριν από την επεξεργασία με πολυαιθυλενογλυκόλη, ακόμα και σε μικρότερες τιμές, ως μια ένδειξη σταθεροποίησης της διασποράς. Ακόμα αποτρέπει την αλληλεπίδραση με άλλους παράγοντες του αίματος κατά τη χορήγηση. Από την άλλη η πολυαιθυλενογλυκόλη προσδίδει στα νανοσωματίδια ιδιότητες που τους επιτρέπουν να μην μεταβολίζονται γρήγορα κατά το πέρασμά τους από το ήπαρ αλλά και κατά τη διάρκεια δράσης τους στα σημεία για τα οποία προορίζονται στο καρδιαγγειακό σύστημα. Αλλά εδώ η αλβουμίνη φαίνεται να λειτουργεί και σαν αντισταθμιστικός παράγοντας στην τάση που δημιουργείται από την πολυαιθυλενογλυκόλη προς μεγαλύτερες τιμές ζ-δυναμικού. Οπότε λαμβάνοντας υπόψιν ότι θα τις χρησιμοποιήσουμε αμφότερες για τα πειράματα μελέτης των νανοσωματιδίων μπορούμε να πούμε ότι η αθροιστική επιρροή και των δύο στο μέγεθος και το ζ-δυναμικό δεν είναι σημαντική. Διάγραμμα 5, PLGA 75/25 Μέγεθος παρουσία PEG & BSA 105
106 Διάγραμμα 6, PLGA 65/35 Μέγεθος παρουσία PEG & BSA Διάγραμμα 7, PLGA 75/25 ζ-δυναμικό παρουσία PEG & BSA. 106
107 Διάγραμμα 8, PLGA 65/35 ζ-δυναμικό παρουσία PEG & BSA Συμπεράσματα Σε αυτό το κεφάλαιο περιγράφηκαν με λεπτομέρειες όλα τα πειράματα που έγιναν για τη μελέτη του μεγέθους των σωματιδίων και του ζ-δυναμικού διερευνώντας διάφορους παράγοντες που πιθανότατα μπορούν να επηρεάσουν τη συμπεριφορά των νανοσωματιδίων. Προσπαθήσαμε να καταλήξουμε σε κάποια βασικά συμπεράσματα για το τι επηρεάζει αυτές τις δύο παραμέτρους αναφορά πάντα με τις διαδικασίες που ακολουθούνται και τα αντιδραστήρια και υλικά που χρησιμοποιούνται. Η πρώτη γενική παρατήρηση έχει να κάνει με τους 2 τύπους του πολυμερούς, και όπως φαίνεται και από τα αποτελέσματα δεν υπάρχει κάποια εμφανής διαφορά ανάμεσα στα δύο. Η επόμενη παρατήρηση έχει να κάνει γενικά με το εύρος των τιμών που παίρνει το μέγεθος. Αυτό κυμαίνεται κυρίως μεταξύ 145 και 165 νανόμετρα με κάποιες πιο ακραίες τιμές είτε γύρω στα 135 είτε στα 175 νανόμετρα να έχουν παρατηρηθεί. Παρ όλα αυτά, και αυτό είναι πάρα πολύ σημαντικό, σε καμία από τις μετρήσεις δεν παρουσιάστηκαν συσσωματώματα ή πολυδιασπορές. Από τα διαγράμματα είναι εμφανές ότι σε αρκετές περιπτώσεις η τυπική απόκλιση μεταξύ των διαφόρων δειγμάτων για μια μέτρηση δεν ήταν μικρή, γεγονός που αναδεικνύει ότι υπάρχουν και άλλοι παράγοντες που είτε δεν μπορούν να 107
108 ελεγχθούν απευθείας, όπως η θερμοκρασία ή σχετική υγρασία, είτε δεν εξετάστηκαν στα πλαίσια της παρούσας εργασίας, και μπορεί να επηρεάζουν τη διαδικασία παραγωγής των νανοσωματιδίων οδηγώντας μερικές φορές σε μεγάλες τυπικές αποκλίσεις. Παρ όλα αυτά, θα πρέπει να τονιστεί για ακόμα μια φορά ότι η διαδικασία κρίθηκε αξιόπιστη και επαναλήψιμη όσον αφορά τη δημιουργία διασποράς νανοσωματιδίων χωρίς συσσωματώματα και με ευνοϊκά χαρακτηριστικά. Όσον αφορά τις τιμές που παίρνει το ζ-δυναμικό, αυτές κυμαίνονται μεταξύ -12mV και -19mV, τιμές οριακές για να χαρακτηριστεί η διασπορά ως επαρκώς σταθερή. Η ποιότητα του απιονισμένου ύδατος που χρησιμοποιήθηκε στο εργαστήριο δεν μπορεί να ελεγχθεί άμεσα και σίγουρα είναι ένας από τους παράγοντες που δεν μπορούν να ελεγχθούν σε αυτά τα πλαίσια με ευκολία. Υπάρχει η πιθανότητα οι τυπικές αποκλίσεις που παρουσιάστηκαν στις μετρήσεις και των δυο ιδιοτήτων να οφείλονται και σε αυτό. Κανονικά το ph του απιονισμένου ύδατος πρέπει να είναι 7 ή να πλησιάζει το 7 αλλά απιονισμένο ύδωρ αρκετών ημερών ή μολυσμένο απιονισμένο ύδωρ από άλατα, υπολείμματα των περιεκτών κ.α. μπορεί να έχει διαφορετικό ph. Συνήθως απιονισμένο ύδωρ αρκετών ημερών έχει ελαφρώς όξινο ph στην περιοχή του 6 με 7 εξαιτίας της διάλυσης του διοξειδίου του άνθρακα από την ατμόσφαιρα, τον σχηματισμό ανθρακικού οξέος και την υδρόλυση του σε κατιόντα υδρογόνου και ανθρακικά ανιόντα. Η συνδυασμένη χρήση πολυαιθυλενογλυκόλης και αλβουμίνης φαίνεται να μην οδηγεί σε θεαματικές αλλαγές ούτε στο μέγεθος των σωματιδίων ούτε στο ζ-δυναμικό. Η χρήση μόνο της πολυαιθυλενογλυκόλης φάνηκε να επηρέασε ελάχιστα το ζ-δυναμικό δείχνοντας μια τάση προς μειωμένη σταθερότητα της διασποράς και πιθανό μελλοντικό συσσωματωμάτων αλλά αυτό είναι αναμενόμενο από τη βιβλιογραφία με τη χρήση της πολυαιθυλενογλυκόλης, κυρίως κατά την αποικοδόμηση της. Η ταυτόχρονη χρήση όμως αλβουμίνης φαίνεται να αντισταθμίζει την επιρροή της πολυαιθυλενογλυκόλης. Η συγκέντρωση της διπυριδαμόλης στην οργανική φάση δεν φαίνεται να παιζει ρόλο ούτε στο μέγεθος ούτε στο ζ-δυναμικό αλλά η παρουσία φαρμάκου στην οργανική φάση σαν σύνολο οδηγεί σε ελαφρώς μικρότερα μεγέθη και τιμές ζ-δυναμικού από ότι απουσία του, και αυτό πιστεύουμε ότι οφείλεται στην σχετική αλλαγή των συνθηκών που επικρατούν στην οργανική φάση με την προσθήκη του φαρμάκου. 108
109 ΚΕΦΑΛΑΙΟ 10. Χρήση Φασματοσκοπίας UV-Vis για μελέτες σταθερότητας και θολερότητας Νανοσωματιδίων Πειράματα Σταθερότητας και θολερότητας Η παρουσία υδροφιλικής επικάλυψης που προσφέρει η πολυαιθυλενογλυκόλη στα νανοσωματίδια, θεωρείται ότι σταθεροποιεί στερικά τα τελευταία έναντι οψονισμού και φαγοκύττωσης [21, Αυγουστάκης et al.]. Η κολλοειδική σταθερότητα των νανοσωματιδίων μπορεί να εκτιμηθεί από την αντίστασή τους σε συσσωμάτωση νανοσωματιδίων που επάγεται από ηλεκτρολύτες, στην περίπτωσή μας από διάλυμα χλωριούχου ασβεστίου CaCl 2, κατά τη διατήρησή τους σε σύντομο χρονικό διάστημα υπό καθορισμένες συνθήκες. Συνήθως για αυτές τις παρατηρήσεις χρησιμοποιούνται διάφορα διαλύματα ηλεκτρολυτών για να μελετηθεί η αντίσταση της διασποράς σε συσσωμάτωση συναρτήσει διαφόρων συγκεντρώσεων. Στα πλαίσια αυτής της μελέτης όμως εξαιτίας του κόστους του πολυμερούς επικεντρωθήκαμε σε μια μέση συγκέντρωση του χλωριούχου ασβεστίου και μελετήσαμε τα προφίλ σταθερότητας αλλά και θολερότητας σε σχέση με το χρόνο στους 37 o C, διατηρώντας τα δείγματα σε υδατόλουτρο Πειράματα Σταθερότητας συναρτήσει του χρόνου Για τα πειράματα σταθερότητας, οι διασπορές των νανοσωματιδίων αραιώθηκαν με διάλυμα χλωριούχου ασβεστίου ώστε στον τελικό όγκο του διαλύματος η συγκέντρωση του χλωριούχου ασβεστίου να είναι πάντα 1.8mM ενώ υπήρχε πάντα για κάθε δείγμα και ένα αντίστοιχο τυφλό δείγμα με ίδιο τελικό όγκο αλλά απουσία χλωριούχου ασβεστίου για συγκριτικές μελέτες. Τα δείγματα φυλάχτηκαν σε υδατόλουτρο στους 37 o C, και μετρήθηκαν σε τακτικά χρονικά διαστήματα όσον αφορά το μέγεθος των σωματιδίων αλλά και το δυναμικό ζ ώστε να δούμε πως επηρεάζονται κατά το πέρας του χρόνου. Για τα πειράματα χρησιμοποιήθηκαν διασπορές νανοσωματιδίων και από τα δύο πολυμερή, είτε παρουσία είτε απουσία φαρμάκου και τα χρονικά διαστήματα κατά τα οποία λαμβάνονται οι μετρήσεις είναι, 0, 3, 24, 48 ώρες. Μετά το πέρας των μετρήσεων τα αποτελέσματα συλλέχθηκαν για δημιουργήθηκαν τα παρακάτω συγκεντρωτικά διαγράμματα. 109
110 Διάγραμμα 9, PLGA 75/25 απουσία φαρμάκου Διαγραμμα 10, PLGA 75/25 παρουσία φαρμάκου 110
111 Διαγραμμα 11, PLGA 65/35 απουσία φαρμάκου Διάγραμμα 12, PLGA 65/35 παρουσία φαρμάκου Όπως παρατηρούμε από τα παραπάνω διαγράμματα μεγέθους των σωματιδίων, το τελευταίο παραμένει μέσα στα πλαίσια που ήδη συζητήθηκαν στο προηγούμενο κεφάλαιο. 111
112 Υπάρχουν κάποιες διαφοροποιήσεις αλλά δε φαίνεται να αλλάζει κάτι δραματικά. Το πιο σημαντικό που πρέπει να κρατήσει κάποιος από εδώ είναι ότι οι τυπικές αποκλίσεις είναι στατιστικά καλύτερες από προηγούμενες μετρήσεις και αυτό δίνει μεγαλύτερη αξιοπιστία σε αυτές τις μετρήσεις. Το ακόμα πιο σημαντικό είναι όπως διαπιστώνεται και από τις επόμενες εικόνες, οι κατανομές του μεγέθους είναι πολύ καλές, δεν παρουσιάζονται συσσωματώματα και ούτε πολυδιασπορές. Εικόνα 18, PLGA 65/35 παρουσία φαρμάκου, 24 ώρες Εικόνα 19, PLGA 65/35 παρουσία φαρμάκου, 48 ώρες 112
113 Διάγραμμα 13, PLGA 65/35 απουσία φαρμάκου Διάγραμμα 14, PLGA 65/35 παρρουσία φαρμάκου 113
114 Διάγραμμα 15, PLGA 75/25 απουσία φαρμάκου Διάγραμμα 16, PLGA 75/25 παρουσία φαρμάκου Όπως είναι φανερό από τα διαγράμματα, στην περίπτωση του ζ-δυναμικού, παρατηρείται μεγάλη διαφορά ανάμεσα στα control δείγματα απουσία ηλεκτρολύτη και στα δείγματα με χλωριούχο ασβέστιο. Αυτό είναι φυσικά αναμενόμενο καθώς ο φορέας είναι διαφορετικός και έτσι επηρεάζεται το δυναμικό ζ. Αυτό που είναι επίσης αναμενόμενο είναι ότι παρουσία χλωριούχο ασβεστίου τα δείγματα είναι πιο επιρρεπή σε συσσωματώματα και 114
115 παρουσιάζουν μεγαλύτερες τιμές δυναμικού ζ. Για ακόμα μια φορά οι δύο τύποι του πολυμερούς δεν δείχνουν σημαντική διαφοροποίηση στα προφίλ. Αυτό που είναι πολύ ενδιαφέρον είναι ότι εάν και τα δείγματα όπου υπάρχει χλωριούχο ασβέστιο παρουσιάζουν ένα σταθερό εύρος τιμών καθ όλη τη χρονική διάρκεια των μετρήσεων, τα τυφλά δείγματα σχεδόν στο σύνολό τους, έδειξαν μια σημαντική αλλαγή, κυρίως προς μεγαλύτερες τιμές ζ- δυναμικού, άρα και μια τάση προς αποσταθεροποίηση και πιθανή δημιουργία συσσωματωμάτων, αν και κάτι τέτοιο δεν παρατηρήθηκε Πειράματα Θολερότητας συναρτήσει του χρόνου Στην ίδια φιλοσοφία με τα προηγούμενα πειράματα σταθερότητας εκτελούνται και τα πειράματα θολερότητας, σε μήκος κύματος 594nm με τη χρήση φασματοφωτομέτρου. Αυτό είναι το μήκος κύματος που χρησιμοποιείται στη βιβλιογραφία για τον προσδιορισμό της θολερότητας σε διασπορές νανοσωματιδίων που περιέχουν PLGA και PEG [21]. Για τα πειράματα αυτά χρησιμοποιήθηκαν και πάλι τα ίδια δείγματα με πριν και οι μελέτες έγιναν παράλληλα. Η θολερότητα υπολογίζεται ως σχετικό μέγεθος (%) της απορρόφησης στα 594 nm για κάθε χρονικό διάστημα σε σχέση με την αρχική. Τα πειράματα θολερότητας εκτός του ότι είναι χρήσιμα ως ένδειξη για την τάση των διασπορών να σχηματίζουν συσσωματώματα, μπορούν να δώσουν πληροφορίες για το αν υπάρχει διαχωρισμός φάσεων των συστατικών. Διάγραμμα 17, PLGA 65/35 απουσία φαρμάκου 115
116 Διάγραμμα 18, PLGA 65/35 παρουσία φαρμάκου Διάγραμμα 19, PLGA 75/25 απουσία φαρμάκου 116
117 Διάγραμμα 20, PLGA 75/25 παρουσία φαρμάκου Τα διαγράμματα παραπάνω δε δείχνουν κάποια ένδειξη σχηματισμού συσσωματωμάτων ή διαχωρισμού φάσεων. Η αύξηση της σχετικής θολερότητας είναι φυσιολογική και οφείλεται στη φυσιολογική αποικοδόμηση των πολυμερών κατά το πέρας του χρόνου Συμπεράσματα Σε αυτό το κεφάλαιο παρουσιάστηκαν τα πειράματα σταθερότητας και θολερότητας που πραγματοποιήθηκαν συναρτήσει του χρόνου για να μελετηθεί η η κολλοειδική σταθερότητα των νανοσωματιδίων. Παρατηρήθηκε ότι συναρτήσει του χρόνου το μέσο μέγεθος των σωματιδίων δεν υφίσταται κάποια σημαντική αλλαγή και το εύρος των τιμών κυμαίνεται στα πλαίσια των προηγούμενων μετρήσεων. Πολύ πιο σημαντική ήταν η παρατήρηση πως δεν υπήρξαν συσσωματώματα που να παρατηρηθούν σαν πολλαπλές κορυφές στην κατανομή του μεγέθους των σωματιδίων ακόμα και μετά από 48 ώρες. Δεν υπήρξε ουσιαστική διαφοροποίηση παρουσία και απουσία χλωριούχου νατρίου, ενώ οι διαφορές ανάμεσα στα άδεια και τα γεμάτα με φάρμακο νανοσωματίδια ήταν οι αναμενόμενες με βάση τα προηγούμενα πειράματα 117
118 Στις μετρήσεις δυναμικού ζήτα, παρατηρήθηκε διαφορά ανάμεσα στα δείγματα όπου περιείχαν χλωριούχο ασβέστιο και σε αυτά που απουσίαζε το τελευταίο, με το εύρος των τιμών σε κάθε περίπτωση να παραμένει σταθερό, εκτός από από τα τυφλά δείγματα όπου μετά από 24 ώρες παρατηρήθηκε διαφοροποίηση και αύξηση των τιμών του δυναμικού που πιστεύουμε ότι κυρίως οφείλεται στην φυσιολογική απελευθέρωση της πολυαιθυλενογλυκόλης και των άλλων συστατικών στο διάλυμα, και έτσι την τάση προς σχηματισμό συσσωματωμάτων που όπως έχουμε πει είναι αναμενόμενη κατά την απελευθέρωση της πολυαιθυλενογλυκόλης, αλλά και στην αλλαγή των συνθηκών που επικρατούν μέσα στο διάλυμα επηρεάζοντας το δυναμικό ζήτα. Κάτι τέτοιο δεν ήταν εμφανές στα διαλύματα με χλωριούχο ασβέστιο και πιστεύουμε ότι αυτό οφείλεται στην παρουσία του άλατος που κάνει το διάλυμα πιο ανθεκτικό σε μικρο αλλαγές. Γενικά αυτή η παρατηρούμενη μειωμένη σταθερότητα στα νανοσωματιδια παρουσία PEG γενικότερα, και ειδικότερα στην περίπτωση παρουσία χλωριούχου ασβεστίου μπορεί να οφείλεται στην κινητικότητα των αλυσίδων τους η οποία επάγει τη συσσωμάτωση κατά την παρουσία Ca 2+ ή κατά τον χρόνο επώασης. Κατά τις πρώτες μέρες τα νανοσωματίδια με υψηλό ποσοστό PEG υφίστανται σημαντική αποικοδόμηση όταν βρίσκονται υπό επώαση στους 37 [Αυγουστάκης et al. 2002], παρουσιάζοντας και μειωμένη σταθερότητα. o C 118
119 ΚΕΦΑΛΑΙΟ 11. Χρήση Φασματοσκοπίας UV-Vis για μελέτες εγκλωβισμού Φαρμάκου από τα πολυμερικά Νανοσωματίδια Καμπύλες Αναφοράς διπυριδαμόλης Για τον προσδιορισμό του ποσοστού εγκλωβισμού του φαρμάκου στα νανοσωματίδια, χρησιμοποιείται η φασματοσκοπία ορατού υπεριώδους. Συγκεκριμένα πρέπει να δημιουργηθεί μια πρότυπη καμπύλα αναφοράς με βάση μέτρηση της απορρόφησης διαλυμάτων γνωστής συγκέντρωσης. Με τη βοήθεια αυτής της καμπύλης αναφοράς μπορεί να βρεθεί η συγκέντρωση οποιουδήποτε από τα διαλύματα των νανοσωματιδίων ως προς τη δυπιριδαμόλη, και από εκεί να υπολογιστεί η ποσότητα της διπυριδαμόλης που τελικά εγκλωβίστηκε στα νανοσωματίδια. Σε αυτό το σημείο υπάρχει όμως ένα πρόβλημα. Για να μελετήσουμε το ποσοστό εγκλωβισμού της διπυριδαμόλης στα νανοσωματίδια, αφού αρχικά γίνει η σύνθεση των νανοσωματιδίων όπως αυτή περιγράφηκε σε προηγούμενο κεφάλαιο, και μετέπειτα ο διαχωρισμός, τα νανοσωματίδια κανονικά θα επαναδιαλυτοποιούνταν σε ακετόνη, θα έσπαζαν όπως αναφέρεται στην εργαστηριακή γλώσσα και θα μετρούνταν η συγκέντρωσή τους στα ακετονικά διαλύματα με τη χρήση φωτομέτρου. Όμως δυστυχώς η ακετόνη παρουσιάζει αρκετά προβλήματα κατά τη μέτρηση διαλυμάτων στο φασματοφωτόμετρο και γενικά τείνει να αποφεύγεται. Γι αυτό το λόγω έπρεπε να βρεθεί ένας άλλος οργανικός διαλύτης, στον οποίο το PLGA αλλά και η διπυριδαμόλη να διαλύονται με ευκολία, αλλά και να μπορεί να χρησιμοποιηθεί για τις μετρήσεις στο φασματοφωτόμετρο. Αυτός ο διαλύτης δεν είναι άλλος από το χλωροφόρμιο Επιλογή Χλωροφορμίου ως διαλύτη Το χλωροφόρμο είναι ένας οργανικός διαλύτης που μπορεί να χρησιμοποιηθεί σε αυτήν την περίπτωση και έτσι δημιουργήθηκαν πρότυπα διαλύματα και μετρήθηκαν οι απορροφήσεις τους στο φασματοφωτόμετρο αφού πρώτα χρησιμοποιήθηκε αυτό με τη μικρότερη συγκέντρωση από αυτά για να εξαχθεί το φάσα απορρόφησης και να οριστεί το μήκος κύματος που θα χρησιμοποιηθεί για τις μετρήσεις. Το τελευταίο βρίσκεται στα 285nm. Αφού έγιναν οι μετρήσεις, συλλέχθηκαν και οδήγησαν στη δημιουργία της παρακάτω 119
120 πρότυπης καμπύλης από την οποία μπορεί να χρησιμοποιηθεί η μαθηματική εξίσωση που την εκφράζει για να βρεθεί η συγκέντρωση οποιουδήποτε διαλύματος σε διπυριδαμόλη. Εικόνα 20, Πρότυπη καμπύλη αναφοράς διπυριδαμόλης. Πίνακας 5, Πρότυπα διαλύματα διπυριδαμόλης σε χλωροφόρμιο. ppm(μg/ml) ABS WaveLength 20 0, , , ,
121 11.3. Πειραματική διαδικασία Μετά την επιτυχή δημιουργία της καμπύλης αναφοράς, δείγματα και από τους δυο τύπους πολυμερών, επαναδιαλυτοποιήθηκαν σε γνωστούς όγκους χλωροφορμίου, με τη βοήθεια και της συσκευής υπερήχων. Οι διαδικασία δεν κράτησε πάνω από 5 λεπτά καθώς το χλωροφόρμιο είναι άριστος διαλύτης για αυτήν την περίπτωση όπως είπαμε και παραπάνω. Τα δείγματα μετρήθηκαν και με βάση την παραπάνω εξίσωση και αφού ο όγκος του διαλύματος του χλωροφορμίου ήταν γνωστός, βρέθηκε η ποσότητα της δυπιριδαμόλης σε κάθε περίπτωση. Γνωρίζοντας την ποσότητα της διπυριδαμόλης που αρχικά διαλύθηκε στην ακετόνη για τη σύνθεση των νανοσωματιδίων μπορούμε να υπολογίζουμε το ποσοστό επί τις εκατό της αρχικής ποσότητας. Τα αποτελέσματα φαίνονται στον παρακάτω πίνακα. Μάλιστα εδώ παρουσιάζονται και τα αποτελέσματα από τα αντίστοιχα πειράματα εγκλωβισμού που έγιναν σε ορισμένα δείγματα από τα οποία χρησιμοποιήθηκαν για τα πειράματα απελευθέρωσης όπως θα δούμε και σε επόμενο κεφάλαιο, και αυτό έγινε με προσωπική πρωτοβουλία για να εξασφαλιστεί ένα δείγμα γραφής της επαναληψιμότητας των μετρήσεων. Πίνακες 6 & 7, Ποσοστά επι της αρχικής ποσότητας διπυριδαμόλης στα νανοσωματίδια Παρατηρούμε ότι υπάρχει μια σχετική επαναληψιμότητα σε σχέση με τα πειράματα που έγιναν στα πλαίσια της μελέτης του εγκλωβισμού και με αυτά που έγιναν για τη μελέτη της απελευθέρωσης. Υπάρχει μια διαφορά όμως για πρώτη φορά ανάμεσα στους δύο τύπους του πολυμερούς, με το 65:35 να εμφανίζει μεγαλύτερα ποσοστά. Γενικά τα ποσοστά μπορούν και στις δύο περιπτώσεις να θεωρηθούν σχετικά μικρά, και είναι μια παράμετρος που πρέπει μελλοντικά να διερευνηθεί το πώς και αν μπορεί να βελτιωθεί ο εγκλωβισμός, αλλά ήταν αναμενόμενο με βάση τη βιβλιογραφία [191] Συμπεράσματα 121 Για να μελετηθεί ο εγκλωβισμός της διπυριδαμόλης στα νανοσωματίδια αλλά και να χρησιμοποιηθούν αυτές οι πληροφορίες για τα πειράματα απελευθέρωσης χρειάστηκε να
122 χρησιμοποιηθεί το χλωροφόρμιο ως διαλύτης. Έγινε η πρότυπη καμπύλη αναφοράς χρησιμοποιώντας πρότυπα διαλύματα και μετρήθηκαν διάφορα δείγματα για εξαχθεί ο μέσος όρος του ποσοστού επί της αρχικής ποσότητας της διπυριδαμόλης που υπάρχει στα νανοσωματίδια. Τα αποτελέσματα όπως αναμενόταν έδειξαν σχετικά χαμηλά ποσοστά εγκλωβισμού αλλά αυτό ήταν κάτι αναμενόμενο με βάση τη βιβλιογραφία και εξαρτάται άμεσα από τη μέθοδο που χρησιμοποιείται για την παρασκευή των νανοσωματιδίων. Είναι ένας τομέας που σίγουρα ενδέχεται βελτιώσει και θα συζητηθεί περαιτέρω το πώς προτείνουμε να γίνει αυτό στο κεφάλαιο της μελλοντικής έρευνας. Το πιο σημαντικό στοιχείο παρ όλα αυτά που προέκυψε από αυτή τη μελέτη ήταν ότι για πρώτη φορά στα πειράματα μέχρι τώρα υπήρξε μια διαφοροποίηση, μικρή αλλά σημαντική, ανάμεσα στους δύο τύπους του πολυμερούς, με τον τύπο 65/35 να εμφανίζει ελαφρώς καλύτερα ποσοστά. Ο λόγος για τον οποίο προτείνουμε ότι συμβαίνει αυτό βρίσκεται σε μια λεπτομέρεια που τονίστηκε στο κεφάλαιο της σύνθεσης και συγκεκριμένα κατά τη διάλυση του πολυμερούς στο ακετονικό διάλυμα που περιείχε το φάρμακο. Εκεί, όπως τονίζω στο αντίστοιχο κεφάλαιο, ο τύπος 65/35 διαλυόταν σε κάθε περίπτωση, τουλάχιστον αναφορικά με την απλή παρατήρηση με γυμνό μάτι, πάντα γρηγορότερα, ίσως στο 70% του χρόνου σε σχέση με τον άλλο τύπο. Έτσι αφού τα δείγματα και από του δύο τύπους του πολυμερούς έμεναν στους υπερήχους τον ίδιο χρόνο για λόγους συγκρισιμότητας της μεθόδου, πιστεύουμε ότι τα διαλύματα με το 65/35 τύπο είχαν περισσότερο χρόνο στη διάθεση τους για καλύτερη ανάμειξη των συστατικών, άρα και εγκλωβισμό περισσότερης διπυριδαμόλης αρχικά. Σίγουρα δεν είναι κάποια υπόθεση που μπορεί με ευκολία να αποδειχτεί αλλά φαίνεται λογική πάραυτα. 122
123 ΚΕΦΑΛΑΙΟ 12. Χρήση Φασματοσκοπίας UV-Vis για μελέτες απελευθέρωσης Φαρμάκου από τα πολυμερικά Νανοσωματίδια Καμπύλες Αναφοράς διπυριδαμόλης Για τη μελέτη της απελευθέρωσης της διπυριδαμόλης από τα νανοσωματίδια θα πρέπει και πάλι να δημιουργηθεί μια πρότυπη καμπύλη αναφοράς, αυτή τη φορά χρησιμοποιώντας πρότυπα διαλύματα διπυριδαμόλης σε PBS. Σε αυτήν την περίπτωση υπάρχει θέμα με τη διαλυτότητα της διπυρυδαμόλης στο PBS μιας και η τελευταία δεν είναι υπό φυσιολογικές συνθήκες ιδιαίτερα υδατοδιαλυτή. Με τη χρήση όμως της συσκευής των υπερήχων καταφέραμε να παρασκευάσουμε τα πρότυπα διαλύματα και αφού πρώτα πήραμε το φάσμα της διπυριδαμόλης από το φασματοφωτόμετρο, ύστερα μετρήσαμε τις απορροφήσεις των πρότυπων διαλυμάτων στα 291 nm. Πίνακας 8, Πρότυπα διαλύματα διπυριδαμόλης σε PBS (ph=7.4) Με τη βοήθεια των πρότυπων διαλυμάτων δημιουργήθηκε η πρότυπη καμπύλη αναφοράς με βάση της οποία μετρώντας την απορρόφηση των δειγμάτων για τα πειράματα απελευθέρωσης και γνωρίζοντας τον όγκο κάθε φορά μπορούμε να υπολογίζουμε την ποσότητα που έχει απελευθερωθεί συναρτήσει του χρόνου. (Διάγραμμα 21 ) Πειραματική διαδικασία Για τα πειράματα απελευθέρωσης προετοιμάστηκαν δείγματα και από τους δύο τύπους του πολυμερούς. Επειδή γι αυτά τα πειράματα θα χρειαστούν 3 δείγματα για τον κάθε τύπο αλλά και 1 για το πείραμα εγκλωβισμού έτσι ώστε να γνωρίζουμε την αρχική ποσότητα δυπιριδαμόλης που υπάρχει σε κάθε ένα από τα δείγματα τα αρχικά δείγματα από τον κάθε τύπο ήταν μεγαλύτερα σε όγκο από τα συνηθισμένα αλλά ακολουθώντας πάντα την 123
124 ίδια συνταγή. Αυτά μετά τη σύνθεσή τους διαχωρίστηκαν σε ίσους όγκους, (4 δείγματα για το κάθε τύπο πολυμερούς), με τα 3 από το καθένα να επαναδιαλυτοποιούνται σε PBS και να τοποθετούνται σε υδατόλουτρο στους 37 o C για τις μετρήσεις απελευθέρωσης και το άλλο να διαλύεται σε καθορισμένο όγκο χλωροφορμίου για μέτρηση της ποσότητας της διπυριδαμόλης στο φασματοφωτόμετρο. Όπως έχει ήδη αναφερθεί στο Κεφάλαιο τα ποσοστά απελευθέρωσης για τους δύο τύπους είναι τα ακόλουθα. Διάγραμμα 21, Πρότυπη καμπύλη αναφοράς διπυριδαμόλης σε PBS (ph=7.4) Πίνακες 9 & 10, Ποσοστά επι της αρχικής ποσότητας διπυριδαμόλης στα νανοσωματίδια 124 Για τα δείγματα που θα χρησιμοποιηθούν για τις μελέτες της απελευθέρωσης της διπυριδαμόλης θεωρούμε ότι έχουν την ίδια ποσότητα διπυριδαμόλης με το αδερφό τους
125 δείγμα που μετρήθηκε για την ποσότητα διπυριδαμόλης που εγκλωβίστηκε, μιας και ο αρχικός όγκος του μητρικού δείγματος διαιρέθηκε σε 4 ίδια δείγματα. Η ποσότητα της διπυριδαμόλης που βρέθηκε στα δείγματα από τους τύπους 65/35 και 75/25 είναι αντίστοιχα 80.41μg, 52.48μg με αρχική θεωρητική ποσότητα διπυριδαμόλης που είναι και στις δύο περιπτώσεις 500μg. Από αυτά άλλωστε προκύπτουν και τα ποσοστά εγκλωβισμού που αναφέραμε και παραπάνω. Είναι πολύ σημαντικό να αναφερθεί εδώ ότι τόσο για τα πειράματα εγκλωβισμού στο σύνολό τους όσο και για τα πειράματα απελευθέρωσης, στο στάδιο του διαχωρισμού των νανοσωματιδίων από τα ελεύθερα συστατικά μέσα στο δείγμα πραγματοποιήθηκαν 4 επαναλαμβανόμενες φυγοκεντρίσεις στις rpm για 30 λεπτά η κάθε μία, ώστε να εξασφαλιστεί με τέτοιο τρόπο ο μέγιστος δυνατός διαχωρισμός. Σε κάθε περίπτωση τα υπερκείμενα μετρήθηκαν στο φασματοφωτόμετρο. Μετά την τέταρτη φυγοκέντριση η απορρόφηση στο φασματοφωτόμετρο ήταν σχεδόν μηδενική και αυτό μας οδηγεί στο συμπέρασμα ότι έχει επιτευχθεί πάρα πολύ καλός διαχωρισμός. Τα δείγματα αφού επαναδιαλυτοποιήθηκαν σε καθορισμένο όγκο PBS τοποθετήθηκαν στο υδατόλουτρο στους 37 o C και ξεκίνησαν οι μετρήσεις απελευθέρωσης φαρμάκου. Αμέσως μετά την τοποθέτηση των δειγμάτων, που βρίσκονται μέσα σε υάλινους κλειστούς περιέκτες χωρητικότητας 50 ml στο υδατόλουτρο πάρθηκαν τα πρώτα δείγματα. Σε κάθε μέτρηση λαμβάνεται από το αρχικό δείγμα 1ml και τοποθετείται σε περιέκτη eppendorf. Ακολούθως οι περιέκτες αυτοί μεταφέρονται στη συσκευή φυγοκέντρισης για να διαχωριστεί το φάρμακο που απελευθερώθηκε από αυτό που παραμένει εγκλωβισμένο στα νανοσωματίδια. Ύστερα από αυτό τα υπερκείμενα μετρώνται στο φασματοφωτόμετρο στο κατάλληλο μήκος κύματος όπως αυτό περιγράφηκε προηγουμένως και γνωρίζοντας τους όγκους και κάνοντας τις κατάλληλες αναγωγές και μετατροπές βρίσκουμε την ποσότητα του φαρμάκου που έχει απελευθερωθεί αυτή τη στιγμή. Για κάθε μελλοντική μέτρηση προστίθενται πάντα και οι προηγούμενες για να έχουμε αθροιστική μέτρηση της ποσότητας του φαρμάκου που έχει απελευθερωθεί μέχρι ένα συγκεκριμένο χρονικό σημείο κάθε φορά και υπολογίζεται το ποσοστό επί της αρχικής θεωρητικής ποσότητας που υπολογίστηκε από το 4 ο δείγμα που πάρθηκε από το αρχικό μεγάλο δείγμα. Οι ποσότητες του φαρμάκου που υπολογίστηκαν για τα δείγματα και για τους δύο τύπους του πολυμερούς παρουσιάζονται στους Πίνακες συναρτήσει με το χρόνο 125
126 Πίνακας 11, Απελευθέρωση διπυριδαμόλης από PLGA 65/35 0min 30min 60min 120min 180min 24h 48h 72h 6535I 6,27 26,32 34,31 40,92 46,69 78,34 89,22 98,60 % 6535II 6,83 27,93 36,42 41,61 46,05 80,20 90,69 98,27 % 6535III 7,94 29,04 35,53 40,72 47,83 81,14 91,63 98,13 % Mean 7,01 27,76 35,42 41,08 46,86 79,89 90,52 98,33 % Values STD 0, , , , , , , ,24253 Πίνακας 12, Απελευθέρωση διπυριδαμόλης από PLGA 75/25 0min 30min 60min 120min 180min 24h 48h 72h 7525I 8,76 22,50 32,45 43,30 46,02 79,19 89,91 99,31 % 7525II 7,91 20,84 29,26 40,83 46,95 78,21 90,72 99,56 % 7525III 10,46 24,20 28,79 42,53 44,57 77,11 90,21 99,61 % Mean 9,04 22,51 30,17 42,22 45,85 78,17 90,28 99,49 % Values STD 1, , , ,2626 1, , , ,16102 Όπως θα φανεί καλύτερα και από τις καμπύλες κινητικής απελευθέρωσης οι δύο τύποι του πολυμερούς παρουσιάζουν μια μικρή διαφορά μόνο στο αρχικό στάδιο της απελευθέρωσης όπου παρατηρείται το burst effect και μέχρι να ομαλοποιηθεί η απελευθέρωση, δηλαδή κυρίως κατά τις 2 πρώτες ώρες. Αυτό οφείλεται στη διαφορά στις αναλογίες των συν-πολυμερών στους δύο τύπους και στο ρυθμό αποικοδόμησης του καθενός. Στον τύπο 65/35 φαίνεται το φαινόμενο burst effect να είναι πιο έντονο, και έτσι να απελευθερώνεται ελαφρώς περισσότερη ποσότητα φαρμάκου σε σχέση με τον άλλο τύπο. Όμως το γενικό προφίλ της απελευθέρωσης και για τους 2 τύπους φαίνεται ίδιο Γραφικές παραστάσεις συναρτήσει του χρόνου Στα επόμενα διαγράμματα φαίνονται οι καμπύλες απελευθέρωσης για τους δύο τύπους του πολυμερούς συναρτήσει του χρόνου. Στον άξονα των Ψ αναπαρίσταται το 126
127 ποσοστό επί της αρχικής ποσότητας της διπυριδαμόλης που έχει απελευθερωθεί σε κάθε χρονική στιγμή ενώ στον άξονα των Χ αναπαρίσταται ο χρόνος σε min. Διάγραμμα 22, Καμπύλες απελευθέρωσης διπυριδαμόλης από NPs PLGA 65/35 (Experimental Data) 127
128 Διάγραμμα 23, Καμπύλες απελευθέρωσης διπυριδαμόλης από NPs PLGA (Experimental Data & logarithm fitting) Αποσαφήνιση κινητικού μοντέλου κατά την απελευθέρωση Η διάχυση είναι ο κύριος μηχανισμός για την απελευθέρωση φαρμάκου από τις περισσότερες πολυμερικές μήτρες και το PLGA δεν αποτελεί εξαίρεση. Η διάχυση των μορίων μπορεί να περιγραφεί από τους Νόμους του Fick. Ο πρώτος Νόμος περιγράφει διάχυση σταθερής κατάστασης και αξιώνει ότι η ροή των διαχεόμενων μορίων είναι ευθέως ανάλογη με τον λόγο των συγκεντρώσεων μεταξύ δυο περιοχών με διαφορετική συγκέντρωση ως προς τα μόρια και συμβαίνει πάντα από την περιοχή με τη μεγαλύτερη συγκέντρωση προς την περιοχή με τη μικρότερη συγκέντρωση σύμφωνα με τον επόμενο μαθηματικό τύπο: 128
129 J = -D(dc/dx) όπου το J περιγράφει τη ροή της διάχυσης των μορίων και οι μονάδες μέτρησής του είναι (mol/m 2 s). Το D είναι μια σταθερά γνωστή ως συντελεστής διάχυσης και οι μονάδες μέτρησής του είναι (m 2 /s). Το αρνητικό πρόσημο του συντελεστή διάχυσης υποδεικνύει την κατεύθυνση της ροής της διάχυσης από υψηλότερη σε χαμηλότερη συγκέντρωση συναρτήσει του λόγου των συγκεντρώσεων dc/dx. Ο δεύτερος νόμος του Fick για τη διάχυση περιγράφει μια μη σταθερή κατάσταση διάχυσης, παραδείγματος χάρη διάχυση που προκαλεί την αλλαγή της συγκέντρωσης συναρτήσει του χρόνου, και μπορεί να περιγραφεί με τον ακόλουθο μαθηματικό τύπο: (Dc/dt) = D (d 2 c/dx 2 ) Χρησιμοποιώντας τους Νόμους του Fick για τη διάχυση μπορεί κάποιος να περιγράψει τη μεταφορά ουσιών από νανοσωματίδια πολυμερών. Τέλειες συνθήκες διαβροχής διατηρούνται στο μέσο απελευθέρωσης και έτσι το φάρμακο που απελευθερώνεται από τα νανοσωματίδια δημιουργία ένα δυναμικό ροής προς το μέσο και ο λόγος των συγκεντρώσεων του φαρμάκου στο μέσο και στα νανοσωματίδια οδηγεί στη διάχυση των μορίων του φαρμάκου. Αν και ο λόγος των συγκεντρώσεων είναι η δύναμη που ωθεί τη διάχυση των μορίων, ο ρυθμός της διάχυσης επηρεάζεται ακόμα και από άλλους παράγοντες όπως το μέγεθος των μορίων που απελευθερώνονται, τη διαπερατότητα της πολυμερικής μήτρας από τα μόρια, την προσρόφηση νερού και την ενυδάτωση της επιφάνειας των σωματιδίων. Και αυτοί οι παράγοντες επηρεάζονται επιπλέον από τον ρυθμό αποικοδόμησης του πολυμερούς. Οπότε σε αρκετές περιπτώσεις και άλλοι παράγοντες εκτός από το λόγο των συγκεντρώσεων γίνονται ο περιοριστικός παράγοντας που καθορίζει την κινητική απελευθέρωσης των μορίων του φαρμάκου. Η απελευθέρωση των μορίων του φαρμάκου μέσω της διάχυσης από τα νανοσωματίδια μπορεί να κατηγοριοποιηθεί σε δύο τύπους: 1) διάχυση μέσω της πολυμερικής μήτρας (Τύπος διάχυσης 1) και 2) διάχυση διαμέσου ενός φραγμού όπως η πολυμερική μήτρα (Τύπος διάχυσης 2). Για τον πρώτο τύπο διάχυσης, ο ρυθμός απελευθέρωσης περιορίζεται από τη διαχυτότητα των μορίων, ενώ για τον δεύτερο τύπο διάχυσης, η διαπερατότητα της πολυμερικής μήτρας είναι ο περιοριστικός παράγοντας. Είναι σημαντικό λοιπόν να μπορέσουμε να προσδιορίσουμε τον τύπο της διάχυσης η οποία καθορίζει την απελευθέρωση του φαρμάκου. Ο πρώτος τύπος διάχυσης οδηγεί σε ένα τυπικό προφίλ απελευθέρωσης το οποίο δείχνει ένα αρχικό υψηλό ρυθμό απελευθέρωσης, ο οποίος σταδιακά μειώνεται όσο η συγκέντρωση της ουσίας μέσα στα νανοσωματίδια μειώνεται. Στην περίπτωση του δεύτερου τύπου διάχυσης, η διάχυση διαμέσου ενός στρώματος που 129
130 αποτελεί φραγμό είναι πολύ χαμηλότερη από ότι ο ρυθμός με τον οποίο απομακρύνονται τα μόρια από την πολυμερική μήτρα προς τον μέσο και έχουμε ένα σχεδόν γραμμικό κινητικό προφίλ εξαιτίας ενός σταθερού λόγου συγκεντρώσεων μεταξύ του φραγμού και της μήτρας, και του φραγμού και του μέσου που περιβάλει τα νανοσωματίδια. Με το χρόνο, η αποικοδόμηση του πολυμερούς μπορεί να επηρεάσει τη γραμμικότητα της κινητικής. Από τα διαγράμματα φαίνεται πως έχουμε να κάνουμε με τον πρώτο τύπο διάχυσης. Για την κινητική απελευθέρωσης από νανοσωματίδια PLGA ή PLGA/PEG έχει περιγραφεί στη βιβλιογραφία ένα τρισφασικό προφίλ [ ]. Στην πρώτη φάση παρατηρείται το φαινόμενο burst effect το οποίο οφείλεται στην απελευθέρωση του φαρμάκου που βρίσκεται κοντά στην επιφάνεια των νανοσωματιδίων. Η δεύτερη φάση χαρακτηρίζεται από σχετικά χαμηλή απελευθέρωση εξαιτίας διάχυσης του φαρμάκου από την πολυμερική μήτρα. Στην τρίτη φάση παρατηρείται αυξημένη απελευθέρωση φαρμάκου λόγω αυξημένη αποικοδόμησης του πολυμερούς, που οδηγεί στην αυξημένη διαπερατότητα του φαρμάκου από την πολυμερική μήτρα. Η απελευθέρωση της διπυριδαμόλης από τα νανοσωματίδια φαίνεται στα Διαγράμματα Σύμφωνα με αυτά που έχουν συζητηθεί έως τώρα μπορούμε να διακρίνουμε το πρώτο στάδιο, όπου έχουμε αυξημένη απελευθέρωση φαρμάκου καθώς και το δεύτερο στάδιο όπου έχουμε σταθερή απελευθέρωση του φαρμάκου λόγω διάχυσης από την πολυμερική μήτρα. Δεν μπορούμε να πούμε όμως ότι φαίνεται ξεκάθαρα και η τρίτη φάση, δηλαδή αυτής της αυξημένης απελευθέρωσης λόγω αποικοδόμησης της πολυμερικής μήτρας. Και αυτό δε θα ήταν δυνατό σε αυτό το διάστημα καθώς ο χρόνος αποικοδόμησης του PLGA είναι μεγαλύτερος από το διάστημα στο οποίο έγιναν οι μετρήσεις. Αυτό πιστεύουμε ότι είναι το τελικό αποτέλεσμα όλων των επιλογών κατά τη διάρκεια της προετοιμασίας των νανοσωματιδίων, που οδηγούν στην απελευθέρωση σχεδόν ολόκληρης της ποσότητας της διπυριδαμόλης από τα νανοσωματίδια προτού ξεκινήσει να λαμβάνει χώρα ο μηχανισμό της αποικοδόμησης του πολυμερούς σε τέτοιο βαθμό που να επηρεάζει την κινητική. Η αρχική έντονη απελευθέρωση του φαρμάκου κατά την πρώτη φάση εξηγείται στη βιβλιογραφία από την ύπαρξη πόρων στα νανοσωματίδια. [195,196]. Η παρουσία πόρων αυξάνει τη συνολική επιφάνεια η οποία είναι διαθέσιμη για διάχυση του φαρμάκου από την πολυμερική μήτρα, οδηγώντας σε ένα σχετικά υψηλό ρυθμό απελευθέρωσης του φαρμάκου σε αυτή τη φάση. Η παρουσία πόρων μπορεί να εξηγήσει την υψηλή διαπερατότητα του φαρμάκου από την πολυμερική μήτρα και έτσι και τον χρόνο που χρειάζεται το φάρμακο για να απελευθερωθεί σχεδόν πλήρως από τα νανοσωματίδια. Κατά τη διάρκεια της σύνθεσης των ναοσωματιδίων μπορεί λόγω κάποιου στιγμιαίου διαχωρισμού φάσεων να 130
131 δημιουργηθούν περιοχές με υψηλή σύσταση πολυμερούς και περιοχές με χαμηλή σύσταση πολυμερούς, φαινόμενο το οποίο μπορεί να οδηγήσει στο σχηματισμό πόρων. Το αν συμβαίνει κάτι τέτοιο δεν μπορεί να αποδειχτεί από τα δεδομένα που παρουσιάζονται σε αυτή την εργασία και από τις μελέτες που πραγματοποιήθηκαν. Ένας λόγος για τον οποίο δεν μπορέσαμε να παρατηρήσουμε πόρους κατά τη διάρκεια των μετρήσεων στο SEM και το AFM μπορεί να είναι και το γεγονός ότι αυτοί καταρρέουν κατά την απομάκρυνση του υδατικού φορέα και την ξήρανση για να μπορέσουν να μελετηθούν στα αντίστοιχα μικροσκόπια με βάση την προετοιμασία. Ο χρόνος για την απελευθέρωση όλης της ποσότητας του φαρμάκου επηρεάζεται φυσικά και από την παρουσία της αλβουμίνης. Αρχικά όπως βλέπουμε στα διαγράμματα παρατηρείται το burst effect το οποίο δεν είναι τόσο έντονο και σε αυτό συντελεί η αλβουμίνη. Στη φάση που ακολουθεί η απελευθέρωση του φαρμάκου τείνει με το χρόνο να γίνει γραμμική μέχρι και το χρονικό διάστημα των 3 ημερών όπου παρατηρείται σχεδόν πλήρης απελευθέρωση του φαρμάκου Συμπεράσματα Οι κλασσικές εξισώσεις που περιγράφουν τη διάχυση ενός φαρμάκου από σφαιρική μήτρα όπως η εξίσωση Korsmeyer-Peppas δύναται να εφαρμοστούν για να περιγράψουν το μοντέλο της απελευθέρωσης της διπυριδαμόλης από αυτά τα νανοσωματίδια λαμβάνοντας υπόψη όμως ορισμένες σοβαρές παραδοχές. Πρώτα απ όλα υπάρχει απώλεια μάζας εξαιτίας της κατάρρευσης των εστερικών δεσμών που υφίστανται μεταξύ του PLGA και του PEG [199]. Αυτό οδηγεί σε αυξημένη υδροφιλικότητα της πολυμερικής μήτρας με το χρόνο. Αφού το μέγεθος των σωματιδίων μένει σταθερό με το χρόνο όπως έδειξαν τα πειράματα σταθερότητας, αυτό σημαίνει ότι το πορώδες της πολυμερικής μήτρας αυξάνεται με το χρόνο, οδηγώντας σε αυξημένη διάχυση του φαρμάκου από την τελευταία. Δεύτερον, η κατανομή του μεγέθους των νανοσωματιδίων παίζει ρόλο στην απελευθέρωση του φαρμάκου. Τα μικρότερα σωματίδια απελευθερώνουν το φάρμακο με υψηλότερο ρυθμό από ότι τα μεγαλύτερα σωματίδια, εξαιτίας του μεγαλύτερο λόγου επιφάνειας προς όγκο. Η χρήση της αλβουμίνης μπορεί να επηρεάσει με διάφορους τρόπους τα χαρακτηριστικά της κινητικής απελευθέρωσης και να παίξει σημαντικό ρόλο. Η πρωτεΐνη μπορεί να προσροφηθεί στη επιφάνεια και να σχηματίσει μια επικάλυψη που θα μειώνει τη διάχυση του φαρμάκου από την πολυμερική μήτρα. Αυτό θα προσπαθήσουμε να προσδιορίσουμε αν υφίσταται με τη χρήση του μικροσκόπιο ατομικών δυνάμεων σε επόμενο 131
132 κεφάλαιο. Η πρωτεΐνη μπορεί επίσης να αναμιγνύεται με τα υπόλοιπα συστατικά στα νανοσωματίδια και να αλληλεπιδρά με το φάρμακο το PLGA ή το PEG, μειώνοντας το πορώδες, το οποίο οδηγεί σε μικρότερο συντελεστή διάχυσης του φαρμάκου. Μια πολύ πιθανή εξήγηση για την επιρροή της αλβουμίνης στην απελευθέρωση της διπυριδαμόλης είναι ότι τα μόρια της αλβουμίνης διεισδύουν ή μπλοκάρουν τους πόρους των νανοσωματιδίων, και έτσι μειώνουν τη διάχυση του φαρμάκου μέσα από τους πόρους [196]. Εξαιτίας της παρουσίας της αλβουμίνης, το ιξώδες της υδατικής φάσης στους πόρους αυξάνεται με αποτέλεσμα τη μείωση της διάχυσης μέσω αυτών [200]. Ως λογικό επακόλουθο, ο ρυθμός απελευθέρωσης του φαρμάκου μειώνεται. Πίνακας 13α Πίνακας 13β Για την καλύτερη κατανόηση των αποτελεσμάτων έγινε απόπειρα μαθηματικής μοντελοποίησης χρησιμοποιώντας την εξίσωση που αναφέρεται στον παραπάνω πίνακα. Οι παράμετροι a και n αποκτήθηκαν από τη δημιουργία γραφικής παράστασης ln(mt/m ) συναρτήσει του χρόνου ln(t) και μετά από απόπειρα fitting των δεδομένων σε ευθεία γραμμή, όπου ft=mt/m [201]. Η παράμετρος n αποκτήθηκε από την κλίση της καμπύλης ενώ η παράμετρος a αποκτήθηκε για ln(t)=0. 132
133 ln(mt/m ) Πίνακας 13γ Mt/M = at n <=> ln(y) = ln(at n ) <=> <=> Όπου Mt/M = y <=> ln(y) = ln(a) + ln(t n ) <=> <=> ln(y) = ln(a) + nln(t) <=> <=> y = c + nt Όπου c=ln(a) Διάγραμμα 24 Mathematical Fitting πειραματικών δεδομένων από τον τύπο 7525 στο μοντέλο Korsmeyer-Peppas 5 PLGA 7525 y = 0,36x + 1,74 R² = 0, Experimental Theoritical Γραμμική (Experimental) ln(t) Πίνακας 14, Δεδομένα που προκύπτουν από τη μοντελοποίηση PLGA7525 a c=ln(a) n Τάση Fitting δεδομένων y = c + nt 5,697 0,36 Fickian diffusion Γραμμική Εξίσωση γραμμ. τάσης 133
134 ln(mt/m ) Διάγραμμα 25 Mathematical Fitting πειραματικών δεδομένων από τον τύπο 6535 στο μοντέλο Korsmeyer-Peppas 5 PLGA 6535 y = 0,3678x + 1,7127 R² = 0, Experimental Theoritical Γραμμική (Experimental) ln(t) Πίνακας 15, Δεδομένα που προκύπτουν από τη μοντελοποίηση PLGA6535 a c=ln(a) n Τάση Fitting δεδομένων y = c + nt 5,54 0,367 Fickian diffusion Γραμμική Εξίσωση γραμμ. τάσης Και για τους δύο τύπους του πολυμερούς η παράμετρος n που σύμφωνα με το μοντέλο καθορίζει το μηχανισμό μεταφοράς του φαρμάκου κυμαίνεται από 0,36 ως 0,367. Αυτό σημαίνει ότι η διάχυση είναι ο καθοριστικός παράγοντας στην απελευθέρωση του φαρμάκου από τα πολυμερικά νανοσωματίδια και άρα επαληθεύται το αρχικό συμπέρασμα στο οποίο είχαμε καταλήξει. Οι εξισώσεις που προκύπτουν και από τους δύο τύπους είναι στατιστικά σημαντικές μια και ο συντελεστής R 2 που αντικατοπτρίζει το πόσο το μοντέλο ανταποκρίνεται στα πειραματικά δεδομένα κυμαίνεται από 0,867 εως 0,936 και κρίνεται ικανοποιητικός. 134
135 ΚΕΦΑΛΑΙΟ 13. Χρήση της Μικροσκοπίας Σάρωσης Ηλεκτρονίων για την απεικόνιση των Νανοσωματιδίων Προετοιμασία δέιγματος Για να μετρηθεί το μέγεθος και η μορφολογία των νανοσωματιδίων στη στερεά κατάσταση, τα δείγματα αναλύθηκαν με τη χρήση της μικροσκοπίας σάρωσης ηλεκτρονίων. Τα δείγματα προετοιμάστηκαν ενσταλάζοντας μια διασπορά νανοσωματιδίων, όχι περισσότερο από 500 μl, πάνω σε υποστρώματα από πυρίτιο που είχαν προηγουμένως καθαριστεί με ισοπροπανόλη (10 λεπτά, 2 φορές) και ακετόνη (10 λεπτά, 2 φορές) με επαναλαμβανόμενες πλύσεις, και είχαν στεγνώσει με τη χρήση πεπιεσμένου αζώτου. Τα δείγματα αφέθηκαν σε ηρεμία μέχρις εξάτμισης του υδατικού φορέα για ένα 24ωρο και ύστερα το τοποθετήθηκαν πάνω σε μεταλλικές τράπεζες και υφιστάθηκαν διαδικασία απανθράκωσης για την εξέταση τους αργότερα στο μικροσκόπιο ηλεκτρονίων. Οι αναλύσεις πραγματοποιήθηκαν σε 1 KV με μεγεθύνσεις από 2000 ως 15000Χ. Σε όσες περιπτώσεις κατέστη δυνατό μετρήθηκαν κάποια νανοσωματίδια και για να εξακριβωθεί το μέσο μέγεθός τους η τυπική απόκλιση Εικόνες από SEM Για τις εικόνες στο SEM χρησιμοποιήθηκαν δείγματα και από τους δύο τύπους του πολυμερούς, είτε άδεια είτε με φάρμακο και απουσία και παρουσία πολυαιθυλενογλυκόλης και αλβουμίνης. Παράλληλα για τα ίδια δείγματα πραγματοποιήθηκαν και μετρήσεις μεγέθους στο και παρουσιάζονται οι κατανομές των μεγεθών σε κάθε περίπτωση για άμεση σύγκριση των μετρήσεων. Από τις εικόνες του SEM μπορέσαμε και πήραμε τις παρακάτω τιμές για το μέσο μέγεθος των σωματιδίων. 135
136 Πίνακας 16, μέσω μέγεθος σωματιδίων από εικόνες SEM Δείγμα Μέσο Μέγεθος nm Τυπική Απόκλιση PLGA 65:35 EMPTY 153, , PLGA 75:25 EMPTY 157, , PLGA 65:35 BSA PEG EMPTY 155, , PLGA 75:25 BSA PEG EMPTY 157, , PLGA 65:35 BSA PEG 1000ppm dipyridamole 154, , PLGA 75:25 BSA PEG 1000ppm dipyridamole 162, , Εικόνα 21, PLGA 65:35 απουσία φαρμάκου 136
137 Εικόνα 22, PLGA 75:25 απουσία φαρμάκου 137
138 Εικόνα 23, PLGA 65:35 παρουσία φαρμάκου 138
139 Εικόνα 24, PLGA 75:25 παρουσία φαρμάκου 139
140 Εικόνα 25, PLGA 65:35 παρουσία φαρμάκου, PEG,BSA 140
141 Εικόνα 26, PLGA 75:25 παρουσία φαρμάκου, PEG,BSA 141
142 13.3. Συμπεράσματα Για να μελετήσουμε το σχήμα και και μέγεθος των νανοσωματιδίων χρησιμοποιήσαμε τη μικροσκοπία σάρωσης ηλεκτρονίων. Παράλληλα κάναμε μετρήσεις μεγέθους των νανοσωματιδίων χρησιμοποιώντας το Zetasizer όπως και σε προηγούμενα κεφάλαια. Από τις εικόνες είναι εμφανές ότι το σχήμα των νανοσωματιδίων είναι σφαιρικό ή περίπου σφαιρικό και το μέγεθος κυμαίνεται στο εύρος που μελετήθηκε και προηγουμένως χωρίς μεγάλες διακυμάνσεις. Για τη μέτρηση του μέσου μεγέθους των νανοσωματιδίων μετρήθηκαν στις περισσότερες περιπτώσεις 20 νανοσωματίδια ή περισσότερα όπου αυτό κατέστη δυνατό. Σε μια περίπτωση εμφανίστηκαν κάποια συσσωματώματα αλλά αυτό είναι φυσιολογικό εξαιτίας των διαδικασιών που ακολουθούνται μέχρι τα δείγματα να είναι έτοιμα για τις μετρήσεις στο SEM. Είναι φυσιολογικό ότι με την εξάτμιση του υγρού φορέα τα νανοσωματίδια που βρίσκονται σε κοντινές αποστάσεις τείνουν να έρχονται πιο κοντά και έτσι δημιουργούνται κάποια συσσωματώματα σε ποσοστό όμως που δεν ξεπέρασε κατά πολύ το 1%. Για ακόμα μια φορά παρατηρούμε ότι δεν παρουσιάζονται μεγάλες διαφοροποιήσεις μεταξύ των δύο τύπων των πολυμερών, και ακόμα ότι δεν παρουσιάζονται μορφολογικές αλλαγές κατά την επεξεργασία με πολυαιθυλενογλυκόλη και αλβουμίνη. Δυστυχώς οι εικόνες δεν είναι τόσο καλές ώστε να εξαχθούν περαιτέρω συμπεράσματα για μορφολογικά χαρακτηριστικά, αλλά ήταν ότι καλύτερο μπορούσε να γίνει δεδομένου ότι γενικά οι διασπορές νανοσωματιδίων σε τέτοια κλίμακα είναι πάντα απαιτητικές στην επεξεργασία για να δώσουν καλές εικόνες στο SEM. Γι αυτό το λόγο αποφασίσαμε να χρησιμοποιήσουμε και το μικροσκόπιο ατομικών δυνάμεων για να μπορέσουμε να πάρουμε καλύτερες εικόνες. Τα αποτελέσματα αναλύονται στο επόμενο κεφάλαιο. 142
143 ΚΕΦΑΛΑΙΟ 14. Χρήση της Μικροσκοπίας Ατομικών Δυνάμεων (AFM) Προετοιμασία δείγματος Όπως αναφέρθηκε και στο προηγούμενο κεφάλαιο, για την καλύτερη κατανόηση των μορφολογικών ιδιοτήτων των σωματιδίων χρησιμοποιήθηκε η μικροσκοπία ατομικών δυνάμεων μιας και προσφέρει πολύ καλή ευαισθησία και μεγέθυνση ώστε να μπορέσουν να εξαχθούν κάποια περαιτέρω συμπεράσματα για τα νανοσωματίδια από αυτά που εμφανίστηκαν κατά την ανάλυση των εικόνων στο μικροσκόπιο σάρωσης ηλεκτρονίων. Για την προετοιμασία των δειγμάτων πρέπει να ακολουθηθεί ένα πρωτόκολλο κατάλληλο για την ακινητοποίηση των νανοσωματιδίων σε έναν φορέα, που και σε αυτήν την περίπτωση, όπως και κατά την προετοιμασία των δειγμάτων για το SEM, ήταν κομμάτια από πυρίτιο, σχήματος τετραπλεύρου, με εμβαδόν περίπου 1cm 2, τα οποία προηγουμένως είχαν καθαριστεί ακολουθώντας την ίδια διαδικασία όπως περιγράφηκε στο κεφάλαιο Παρ όλα αυτά έπρεπε πρώτα να επιλεγεί η μέθοδος με την οποία θα τοποθετούνταν τα δείγματα από τα νανοσωματίδια πάνω στα υποστρώματα από πυρίτιο. Επιλέξαμε να χρησιμοποιήσουμε την τεχνική του spincoating, με παραμέτρους παρόμοιες με αυτές που ακολουθούνται κατά τη χρήση της τεχνικής για τη δημιουργία λεπτών υμενίων PLGA για τις μελέτες που πραγματοποιούνται στο εργαστήριο. Ο τρόπος λειτουργίας που χρησιμοποιήθηκε ήταν το tapping mode, μιας και είναι κατάλληλο για τη μελέτη βιολογικών δειγμάτων. Spincoating Για την προετοιμασία των δειγμάτων λαμβάνουμε 3μl από τα δείγματα των νανοσωματιδίων και αραιώνονται μέχρι 200μl με απιονισμένο ύδωρ. Τα δείγματα μεταφέρονται μέσα στο glove-box όπου επικρατούν συνθήκες κενού και όπου βρίσκεται η συσκευή του spincoating. Χρησιμοποιείται λειτουργία κατά την οποία το δείγμα θα περιστραφεί υπό κενό πρώτα στις 800rpm για 6 δευτερόλεπτα και μετά στις 2000rpm για 30 δευτερόλεπτα. Μετά το τέλος της διαδικασίας τα δείγματα συλλέγονται, τοποθετούνται σε ένα πλαστικό πετρί, και αφήνονται προς εξάτμιση του διαλύτη για 24 ώρες σε θερμοκρασία δωματίου. Η μελέτη των δειγμάτων στο ατομικό μικροσκόπιο πραγματοποιείται την επόμενη μέρα. 143
144 14.2. Περιγραφή και ανάλυση εικόνων Για τις εικόνες του AFM πάρθηκαν δείγματα από διασπορά νανοσωματιδίων, παρουσία διπυριδαμόλης σε συγκέντρωση 1000ppm, αλβουμίνης και πολυαιθυλενογλυκόλης. Εικόνες 27 Τοπογραφία (αριστερά), Εικόνα 28 Φάση (δεξιά), 10*10μm επιφάνειας Στις εικόνες φαίνονται καθαρά τα νανοσωματίδια καθώς και κάποια συσσωματώματα σωματιδίων που δημιουργήθηκαν λόγω των τεχνικών και κατά την εξάτμιση του υγρού μέσου πάνω στο πυρίτιο. Από τις εικόνες φάσης παρατηρούμε διαφορετική αλλαγή φάσης στο εξωτερικό και το εσωτερικό του σωματιδίου κάτι που αποδεικνύει όπως αναμενόταν με βάση την τεχνική που χρησιμοποιήθηκε και αναλύθηκε σε προηγούμενο κεφάλαιο την συσσώρευση της διπυριδαμόλης και του PLGA στο εσωτερικό και του PEG και της αλβουμίνης στον εξωτερικό φλοιό. Το σχήμα ως αναμενόταν είναι σφαιρικό ή σχεδόν σφαιρικό και η διάμετρος των σωματιδίων είναι αυτή που αναμένεται και από τα αποτελέσματα του zetasizer και από τις εικόνες SEM. Υπάρχει φυσικά μια κατανομή μεγέθους των σωματιδίων αλλά αυτή είναι φυσιολογική και έχει δειχθεί και στις μετρήσεις στο Zetasizer ότι είναι πολύ ικανοποιητική με μικρό δείκτη πολυδιασποράς. 144
145 Εικόνα 29 Τοπογραφία (αριστερά), Εικόνα 30 Φάση (δεξιά), 5*5 μm επιφάνειας Εδώ έχουμε την ίδια εικόνα σε μεγαλύτερη μεγέθυνση. Φαίνονται χαρακτηριστικά ότι τα περισσότερα νανοσωματίδια είναι στην περιοχή μεγεθών που έχουμε ήδη επισημάνει, κάτι τέτοιο φαίνεται καλύτερα παρακάτω σε μια καλύτερη μεγέθυνση. Υπάρχουν ακόμα μεγαλύτερα νανοσωματίδια όπως αυτό που βρίσκεται στο κέντρο της εικόνας αλλά και ένα συσσωμάτωμα δυο μικρότερων σωματιδίων επάνω, κεντρικά, στο οποίο όμως είναι εμφανείς οι δύο πυρήνες των νανοσωματιδίων και το εξωτερικό του περίβλημα από την εικόνα φάσης. Επίσης στην ίδια εικόνα στο κέντρο αριστερά μπορούμε να διακρίνουμε ένα μεγαλύτερο νανοσωματίδιο το οποίο, με βάση την εικόνα τοπογραφίας αριστερά, φαίνεται να είναι συσσωμάτωμα δυο μικρότερων νανοσωματιδίων. Σε αυτή την περίπτωση όμως όπως υποδηλώνει η εικόνα φάσης, οι δύο πυρήνες έχουν ενωθεί ενώ το ίδιο συμβαίνει και με τα εξωτερικά περιβλήματα. Αυτή η διαδικασία οδηγεί σε ένα σχήμα με πυρήνα σφαιρικό αλλά εξωτερικό περίβλημα που προσεγγίζει ένα πιο ωοειδές σχήμα. Επίσης πολύ ενδιαφέρον είναι το γεγονός ότι παρατηρούμε και κάποια μικρότερα νανοσωματίδια τα οποία δεν έχουν τόσο έντονο περίβλημα. Πιστεύουμε ότι αυτά είναι νανοσωματίδια τα οποία κατά τη διάρκεια της σύνθεσης και του σχηματισμού τους, δεν περιέλαβαν μεγάλη ποσότητα πολυαιθυλενογλυκόλης ή και σχεδόν καθόλου και γι αυτό δείχνουν να διαφοροποιούνται από τα υπόλοιπα και να μην εμφανίζουν τόσο έντονες διαφορές όσον αφορά τον εσωτερικό πυρήνα και το εξωτερικό περίβλημα. 145
146 Εικόνα 31α τομή (αριστερά), Εικόνα 31β (δεξιά) Φάση, 5*5μm επιφάνειας Για να μπορέσουμε να μελετήσουμε περαιτέρω τη μορφολογία των νανοσωματιδίων πήραμε εικόνες σε ακόμα μεγαλύτερες μεγεθύνσεις καθώς και κάποιες τομές. Εικόνα 32α τομή (αριστερά), Εικόνα 32β (δεξιά) Φάση, 1*1μm επιφάνειας Από αυτή την εικόνα φαίνεται ότι το μέγεθος του εσωτερικού πυρήνα, αν θεωρήσουμε ότι το συγκεκριμένο σωματίδιο έχει διάμετρο περίπου 250 nm, είναι περίπου 200nm, άρα, καλύπτει το 80% περίπου της επιφάνειας του, με το υπόλοιπο 20% να αποτελεί τον εξωτερικό φλοιό που αποτελείται κυρίως από πολυαιθυλενογλυκόλη και αλβουμίνη. Στη συγκεκριμένη περίπτωση το πάχος του εξωτερικού φλοιού είναι 20 nm, και θα ήταν πολύ ενδιαφέρον για μελλοντική έρευνα να καθοριστεί πως και εάν αυτό επηρεάζει την κινητική απελευθέρωσης 146
147 του φαρμάκου, και πως σχετίζεται με τη τεχνική σύνθεσης των νανοσωματιδίων. Στα πλαίσια αυτής της μελέτης, κάτι τέτοιο δεν συνέβη. Εικόνα 33α τομή (αριστερά), Εικόνα 32β (δεξιά) Φάση, 2*2μm επιφάνειας Εδώ έχουμε μια τομή από ένα σωματιδίου μεγέθους περίπου 160 nm. Βλέπουμε ότι και πάλι ο εξωτερικός φλοιός που αποτελείται κυρίως από πολυαιθυλενογλυκόλη έχει πάχος περίπου 20 nm ενώ ο πυρήνας αποτελεί περίπου το 75% της διαμέτρου του σωματιδίου. Έχει πολύ ενδιαφέρον να παρατηρήσουμε ότι στο συγκεκριμένο σωματίδιο η εξωτερική επίστρωση με πολυαιθυλενογλυκόλη παρουσιάζει έντονη ανομοιομορφία και προσδίδει στο νανοσωματίδιο ένα σχήμα πιο ωοειδές. Αυτό με τη σειρά του αναμένουμε να επηρεάζει και την κινητική απελευθέρωσης από το εσωτερικό, μιας και από τα σημεία που η επίστρωση είναι μικρότερη θα είναι πιο γρήγορη απελευθέρωση του φαρμάκου. Περισσότερες λεπτομέρειες για την απελευθέρωση της διπυριδαμόλης δίνονται στο αντίστοιχο κεφάλαιο Συμπεράσματα Σε αυτό το κεφάλαιο παρουσιάστηκαν και αναλύθηκαν οι εικόνες που λάβαμε από το μικροσκόπιο ατομικών δυνάμεων για τον προσδιορισμό της μορφολογίας και του μεγέθους των νανοσωματιδίων, μιας και οι εικόνες από το SEM δεν μας έδωσαν αρκετές πληροφορίες. Αρχικά είδαμε ότι τα νανοσωματίδια παρουσιάζονται έχοντα σχήμα σχετικά σφαιρικό ή ορισμένες φορές με μια τάση προς ωοειδές, κυρίως εξαιτίας της ανομοιόμορφης επίστρωσης με πολυαιθυλενογλυκόλη που έχουν. Είδαμε ξεκάθαρα στις εικόνες φάσης τον διαχωρισμό των υδρόφοβων συστατικών, δηλαδή του PLGA και της διπυριδαμόλης που 147
148 βρίσκονται στον πυρήνα, με τα υδρόφιλα PEG και αλβουμίνη που αποτελούν τον εξωτερικό φλοιό. Δυστυχώς δεν έχουμε αρκετές εικόνες με τομές ώστε να μπορέσουμε να υποστηρίξουμε με στατιστική ακρίβεια αυτές τις παρατηρήσεις μιας και έγιναν σε μεμονωμένα σωματίδια, εντούτοις, είναι πολύ σημαντικές. Στις εικόνες είδαμε επίσης ορισμένα νανοσωματίδια να δημιουργούν συσσωματώματα είτε διατηρώντας τους αρχικούς τους πυρήνες είτε όχι. Ο πυρήνας φαίνεται να κατέχει γύρω στο 70-80% του συνολικού όγκου αν και κάτι τέτοιο δεν μπορεί να υποστηριχτεί στην παρούσα εργασία στατιστικά, οπότε το κρατάμε απλώς ως μια μεμονωμένη παρατήρηση. Άλλο σημαντικό στοιχείο είναι πως η επίστρωση με πολυαιθυλενογλυκόλη δεν είναι ούτε ομοιόμορφη σε αρκετές περιπτώσεις, ούτε και ποσοτικά παρόμοια σε διάφορα σωματίδια. Αυτό αφενός τα κάνει να ξεχωρίζουν στις εικόνες φάσης σε αυτά που η αντίθεση μεταξύ πυρήνα και εξωτερικού φλοιού είναι πιο έντονη και σε αυτά που δεν είναι εύκολα ορατός ο εξωτερικός φλοιός. Κάτι τέτοιο σίγουρα επηρεάζει την κατανομή του μεγέθους των σωματιδίων. Γνωρίζοντας ήδη και από τις προηγούμενες εικόνες από το SEM και από τα πειράματα στο Zetasizer ότι δεν παρατηρείται διαφορά ανάμεσα στους δύο τύπους του πολυμερούς όσον αφορά το μέγεθος ή το σχήμα, στα πλαίσια αυτής της μελέτης παρουσιάζονται εικόνες μόνο από τον ένα τύπο. Μέσα στα πλαίσια της μελλοντικής έρευνας θα υπάρξουν και εικόνες από το άλλο πολυμερές, χωρίς όμως να αναμένονται διαφορές. Τέλος η ποιότητα των εικόνων έδειξε ότι η τεχνική του spincoating μπορεί να χρησιμοποιηθεί για τη μελέτη νανοσωματιδίων πάνω σε υποστρώματα από πυρίτιο χωρίς τη χρήση ειδικών ενδιάμεσων υποστρωμάτων όπως η mica. 148
149 ΚΕΦΑΛΑΙΟ 15. Γενικά συμπεράσματα - Προτάσεις για έρευνα. μελλοντική Γενικά Συμπεράσματα Στα πλαίσια αυτής της διπλωματικής εργασίας, έγινε σύνθεση νανοσωματιδίων από 2 διαφορετικούς τύπους του πολυμερούς PLGA, που διαφέρουν μεταξύ τους στην αναλογία των δύο συν-πολυμερών που το αποτελούν. Το συγκεκριμένο πολυμερές επιλέχτηκε λόγω των δύο κύριων χαρακτηριστικών του που είναι σημαντικά για ιατρικές εφαρμογές και αυτές είναι η βιοσυμβατότητα και η βιοαποικοδομησιμότητα. Η επιλογή του φαρμάκου ήταν φυσικά καθοριστική και για τη μέθοδο που έπρεπε να ακολουθηθεί. Παράλληλα η ίδια η επιλογή του φαρμάκου καθορίζεται από την τελική εφαρμογή που προορίζεται όλη η ερευνητική αυτή δουλεία και αυτή είναι η ελεγχόμενη αποδέσμευση φαρμάκου σε καρδιαγγειακές εφαρμογές. Γι αυτό το λόγο το φάρμακο που επιλέχτηκε ήταν η διπυριδαμόλη, καθώς η τελευταία εμφανίζει αντιθρομβωτική δράση αλλά ακόμα και άλλες ενέργειες που αναλύθηκαν στα κεφάλαια και Η διπυριδαμόλη είναι μια φαρμακευτική ένωση που παρουσιάζει προβληματική διάλυση σε υδατικούς διαλύτες γι αυτό και χρησιμοποιούνται οργανικοί διαλύτες όπως το χλωροφόρμιο, η ακετόνη, η αιθανόλη, το ακετονιτρίλιο κ.α. για τη διάλυση της. Αυτός είναι και ο πρώτος παράγοντας που πρέπει να λάβουμε υπόψιν για την επιλογή της μεθόδου σύνθεσης των νανοσωματιδίων μιας και αφού και το PLGA θα διαλυθεί σε οργανικό διαλύτη θα πρέπει να βρεθεί ένας κοινός που να παρουσιάζει και τα κατάλληλα χαρακτηριστικά όπως έγκριση για ιατρικές εφαρμογές κλπ. Η ακετόνη ήταν αυτή που επιλέχτηκε γιατί ταίριαζαν τα χαρακτηριστικά της με αυτά που ζητούσαμε, είναι φθηνή και χρησιμοποιείται γενικά σε αναμείξεις οργανικών με υδατικές φάσεις για γαλακτώματα ή διασπορές κ.α. Όσον αφορά τη μέθοδο παρασκευής των νανοσωματιδίων, σχετικά με τον εργαστηριακό εξοπλισμό, την υπάρχουσα βιβλιογραφία, αλλά και την επιθυμία για μια τεχνική απλή, φθηνή αλλά παράλληλα αποτελεσματική είχαμε τις εξής δύο επιλογές. Η πρώτη ήταν η μέθοδος emulsion/solvent diffusion και η δεύτερη η τεχνική του nanoprecipitation. Η πρώτη απορρίφθηκε λόγω ανάγκης χρήσης πτητικών ουσιών και σταθεροποιητών και κυρίως λόγω του υπάρχοντος εργαστηριακού εξοπλισμού που θα απαιτούσε scale up της μεθόδου, κάτι που λόγω του κόστους του πολυμερούς δεν ήταν επιθυμητό. Αντιθέτως το nanoprecipitation είναι μια απλή τεχνική που δε χρειάζεται εξτρά 149
150 προσθετικές ουσίες και μπορεί να γίνει και με πολύ μικρές ποσότητες των διαφόρων αντιδραστηρίων. Έχει αποδειχθεί δε ότι με βάση τη βιβλιογραφία έδωσε σημαντικά αποτελέσματα στον τομέα της σύνθεσης νανοσωματιδίων και έχει χρησιμοποιηθεί ευρέως. Το επόμενο βήμα ήταν η επιλογή κάποιων ακόμα στοιχείων που θα έδιναν στα νανοσωματίδια κάποια εξτρά επιθυμητά χαρακτηριστικά. Γι, αυτό το σκοπό επιλέχτηκαν η πολυαιθυλενογλυκόλη και η αλβουμίνη. Η πρώτη χρησιμοποιείται με κύριο σκοπό να προσδώσει στα νανοσωματίδια stealth ιδιότητες ενώ η αλβουμίνη για να προσδώσει χαρακτηριστικά ελεγχόμενες αποδέσμευσης του φαρμάκου. Η επεξεργασία με αυτές τις δύο ουσίες είχε βέβαια και άλλα αποτελέσματα που αναλύθηκαν στα αντίστοιχα κεφάλαια. Και οι δύο ουσίες είναι υδατοδιαλυτές και κατά την διαδικασία σύνθεσης βρίσκονται στην υδατική φάση. Η τελευταία ήταν για τα πειράματά μας το απιονισμένο νερό είτε ρυθμιστικό διάλειμα PBS ph 7.4. Κατά τη σύνθεση των νανοσωματιδίων ελέγχθηκαν κάποιες βασικοί παράμετροι που είχαν να κάνουν με την τεχνική μετά από κάποια αρχικά πειράματα καθιερώθηκε ένα είδος πρωτόσκολου με βάση το οποίο έγινε η σύνθεση όλων των νανοσωματιδιακών διασπορών ώστε να είναι συγκρίσιμα τα αποτελέσματα. Είναι πολύ σημαντικό να αναφερθεί εδώ πως δύο σημαντικοί παράγοντες όπως είναι οι θερμοκρασία και η σχετική υγρασία δεν κατέστη δυνατόν να ελεγχθούν οπότε είναι δύο μεταβλητές που άλλαζαν κατά το πέρας των πειραμάτων με όποια επίδραση μπορεί να έχουν στα αποτελέσματα. Θεωρούμε παρ αυτά ότι η συμβολή τους δεν είναι τόσο σημαντική καθώς δεν φαίνεται να απασχολεί ιδιαίτερα με βάση πάντα τη βιβλιογραφία. Είναι όμως σημαντικό να μπορούν να παρακολουθούνται τουλάχιστον. Ελέγχθηκε η μέγιστη αρχική συγκέντρωση του φαρμάκου που μπορεί να επιτευχθεί και αυτή καθορίζεται κυρίως από τη διαλυτότητα της διπυριδαμόλης στην ακετόνη. Επίσης καθιερώθηκε μια φόρμουλα με βάση τη βιβλιογραφία, σύμφωνα με την οποία καθορίζονται όλες οι ποσότητες των αντιδραστηρίων που έχουν καθορισμένη σχέση μεταξύ αλλήλων και όλα καθορίζονται από τη ζύγιση και άρα την αρχική μάζα του πολυμερούς. Αυτό γιατί για να είναι μια μέθοδος εφαρμόσιμη και να μπορεί να μεταφερθεί από εργαστηριακή σε μεγαλύτερη κλίμακα θα πρέπει πάντα να λαμβάνεται υπόψιν και να μεγιστοποιείται το ισοζύγιο απόδοση τιμής/αποτελεσματικότητα. Πραγματοποιήθηκαν μετρήσεις μεγέθους και ζ-δυναμικού συναρτήσει του χρόνου, της συγκέντρωσης της διπυριδαμόλης, παρουσίας και απουσίας πολυαιθυλενογλυκόλης και αλβουμίνης, παρουσίας διαλύματος άλατος καθώς και μελέτες για την ύπαρξη θολερότητας που υποδεικνύει τάση προς συσσωμάτωση. 150
151 Είναι επιθυμητή η μη ύπαρξη συσσωμάτωσης σε όσο το δυνατόν μεγαλύτερο χρόνο ώστε να μην είναι απαραίτητη η χρήση σταθεροποιητών ουσιών που αυξάνουν όμως την πολυπλοκότητα του συστήματος και μπορεί να έχουν κάποιες ανεπιθύμητες επιδράσεις. Ακόμα είναι σημαντικό οι διασπορές των νανοσωματιδίων να είναι σταθερές άλλα και να επηρεάζουν το επιθυμητό μέγεθος για την αντίστοιχη εφαρμογή. Όλα τα παραπάνω ήταν ζητούμενα που έπρεπε να μελετηθούν και να βελτιστοποιηθούν όπου κατέστη δυνατόν. Οι μελέτες αναφορικά με το δυναμικό και το μέγεθος δεν έδειξαν διαφοροποίηση σε σχέση με τη χρήση του πολυμερούς, παρουσίασαν μιας τάση προς μικρότερα μεγέθη παρουσία φαρμάκου ανεξαρτήτου συγκέντρωσης και επίσης δεν έδειξαν διαφοροποίηση κατά τη συνδυασμένη χρήση πολυαιθυλενογλυκόλης και αλβουμίνης. Όσον αφορά το μέγεθος συγκεκριμένα, κυμαίνεται σε ένα εύρος θα λέγαμε από 140 έως 170 nm (±5nm) που είναι γενικά ικανοποιητικό για τέτοιου είδους εφαρμογές και σύμφωνα με προσωπική εκτίμηση ενδέχεται τροποποίηση με παραμετροποίηση που θα αναφερθεί πιο κάτω. Το μέγεθος δεν εμφάνισε διαφορά συναρτήσει του χρόνου και αυτό είναι πολύ σημαντικό για τη σταθερότητα των διασπορών. Μια παράμετρος που σε αυτό το σημείο πρέπει να αναφερθεί και πιστεύουμε ότι είναι σημαντική είναι ο χρόνος που χρειάζεται για να εξατμιστεί ο διαλύτης και αυτό με τη σειρά του επηρεάζεται από τη θερμοκρασία και τη σχετική υγρασία που επικρατεί στον εργαστηριακό χώρο. Παρατηρήσαμε παραδείγματος χάριν ότι κατά τους καλοκαιρινούς μήνες η διαδικασία αυτή επιταχυνόταν αρκετά, γεγονός που αποτελεί ακόμα μια μεταβλητή παράμετρο που εμπλέκεται στην όλη διαδικασία και πιθανότατα πρέπει να λαμβάνεται υπόψιν για την επαναληψιμότητα της μεθόδου. Τα πειράματα σταθερότητας και θολερότητας έδωσαν ικανοποιητικά αποτελέσματα και επιβεβαίωσαν για ακόμα μια φορά ότι οι διασπορές μας ήταν ικανοποιητικά σταθερές ακόμα και παρουσία διαλύματος άλατος σε συνάρτηση με το χρόνο. Θα επαναλάβω εδώ ότι ο τύπος του πολυμερούς δεν φαίνεται με βάση τα αποτελέσματα να παίζει σημαντικό ρόλο. Έγιναν λοιπόν οι μετρήσεις για να χαρακτηριστούν τα νανοσωματίδια ως προς το μέγεθός τους, το σχήμα τους και το δυναμικό ζήτα που εμφανίζουν σε ένα υγρό φορέα. Πραγματοποιήθηκαν πειράματα μελέτης του εγκλωβισμού, της απελευθέρωσης του φαρμάκου και έγινε απεικόνιση των σωματιδίων με τη χρήση της Μικροσκοπίας Σάρωσης Ηλεκτρονίων και της Μικροσκοπίας Ατομικών δυνάμεων. Για τα πειράματα εγκλωβισμού και απελευθέρωσης καθώς και για τα πειράματα θολερότητας που αναφέρθηκαν παραπάνω χρησιμοποιήθηκε η φασματοσκοπία υπεριώδους 151
152 ορατού. Στα πειράματα εγκλωβισμού διαπιστώσαμε ίσως για πρώτη φορά μια διαφοροποίηση ανάμεσα στους δύο τύπους του πολυμερούς με το 6535 να εμφανίζει ελαφρώς μεγαλύτερο ποσοστό εγκλωβισμού 16.61% έναντι 11.15% για το 75/25. Θεωρούμε ως πιο πιθανή εξήγηση γι αυτή τη διαφοροποίηση την πιο εύκολη και σε λιγότερο χρόνο διάλυση του πρώτου τύπου στο ακετονικό διάλυμα της διπυριδαμόλης που οδηγεί σε καλύτερη ανάμειξη και εγκλωβισμό περισσότερης ποσότητας διπυριδαμόλης. Στα πειράματα απελευθέρωσης παρατηρήθηκε παρόμοιο προφίλ και για τους δύο τύπους, και αυτό χαρακτηρίζεται από ένα αναμενόμενο αρχικό burst effect όπου απελευθερώνεται μια σημαντική ποσότητα του φαρμάκου που είναι πιο κοντά στην επιφάνεια και λόγω κάποιων defects στη δομή του νανοσωματιδίων που επιτρέπουν την άμεση απελευθέρωση. Μετά από αυτό ακολούθησε ένα στάδιο στο οποίο η απελευθέρωση ήταν πιο ομαλή και ελεγχόμενη κυρίως από τη διαπερατότητα των φαρμακευτικών μορίων από τους πόρους της πολυμερικής μήτρας προς το εξωτερικό και σίγουρα επηρεάζεται από την παρουσία της πολυαιθυλενογλυκόλης και της αλβουμίνης στο εξωτερικό. Ακόμα η αποικοδόμηση του PLGA του PEG και η απελευθέρωση της αλβουμίνης παίζουν σημαντικό ρόλο στην κινητική απελευθέρωσης. Αυτό που μπορούμε να πούμε είναι ότι το κινητικό προφίλ καθορίζεται από διάχυση μέσω των πόρων της μήτρας. Η απελευθέρωση σχεδόν της συνολικής ποσότητας του εγκλωβισμένου φαρμάκου συμβαίνει σε χρόνο τέτοιο που η αποικοδόμηση του πολυμερούς δεν έχει αρχίσει ακόμα να είναι σημαντικό παράγοντας και γι αυτό δεν παρατηρήθηκε ένα τελικό στάδιο στο κινητικό προφίλ όπου εμφανίζεται ένα νέο burst effect λόγω της αποικοδόμηση της πολυμερικής μήτρας. Κάτι τέτοιο έχει παρατηρηθεί στη βιβλιογραφία αλλά σε αυτή την περίπτωση δεν συμβαίνει λόγου του χρόνου στον οποίο ολοκληρώνεται η απελευθέρωση του φαρμάκου. Έγινε προσπάθεια μαθηματικού fitting των αποτελεσμάτων με τη χρήση του μοντέλου Korsmeyer-Peppas. Από τις εξισώσεις που λήφθηκαν και από τους δυο τύπους υπολογίστηκε η παράμετρος n που δίνει πληροφορίες για το μηχανισμό που καθορίζει τη μεταφορά του φαρμάκου από την πολυμερική μήτρα στο περιβάλλον. Ο συντελεστής ήταν και στις δυο περιπτώσης μικρότερος του 0,5 και αυτό σύμφωνα με το μοντέλο επαληθεύει το συμπέρασμα στο οποίο είχαμε καταλήξει, ότι δηλαδή η διάχυση κατα Fick είναι αυτή που καθορίζει την απελευθέρωση του φαρμάκου. Τα πειράματα που έγιναν στο SEM και AFM αποκάλυψαν πολύ σημαντικές πληροφορίες κυρίως για το σχήμα αλλά και για την τοπογραφία των νανοσωματιδίων. Δυστυχώς δεν ήταν δυνατόν να παρατηρηθούν οι τυχόν υπάρχοντες πόροι και αυτό όπως αναφέρεται και στη βιβλιογραφία πιθανότατα οφείλεται στις διαδικασίες που ακολουθούνται κατά την επεξεργασία των δειγμάτων για την απεικόνιση. Παρόλα αυτά κυρίως το AFM μας 152
153 έδωσε σημαντικές πληροφορίες για το σχήμα των νανοσωματιδίων που είναι γενικά σφαιρικό ή σχεδόν σφαιρικό ορισμένες φορές κυρίως λόγω της εξωτερικής επιφάνειας που αποτελείται από πολυαιθυλενογλυκόλη και αλβουμίνη και δημιουργεί ένα στρώμα που σε κάποια νανοσωματίδια μετρήθηκε περίπου στα 20nm, το οποίο όμως δεν είναι απόλυτα ομοιόμορφο γύρω από τα νανοσωματίδια Προτάσεις για μελλοντική έρευνα Σε αυτό το σημείο θα ήθελα να τονίσω πως με βάση τη συνολική μελέτη που έγινε για την εκπόνηση αυτής της εργασίας προκύπτουν οι εξής τομείς βελτίωσης και περαιτέρω μελέτης. Ένα πρώτο σημείο είναι η βελτιστοποίηση της ίδιας της τεχνικής του nanoprecipitation ίσως με κάποια τεχνική όπως αυτή που αναφέρθηκε στο κεφάλαιο Κάτι τέτοιο θα οδηγούσε στην αυτοματοποίηση αυτού του σταδίου πράγμα σημαντικό. Στο ίδιο πλαίσιο ένας άλλος παράγοντας που μπορεί να μελετηθεί και ίσως να επηρεάζει το μέγεθος των νανοσωματιδίων είναι η διάμετρος της βελόνας που χρησιμοποιείται για την έγχυση. Όσον αφορά τις παραμέτρους που αφορούν τις αναλογίες των συστατικών θα ήταν πολύ ενδιαφέρον να φανεί πως και εάν επηρεάζει η συγκέντρωση της πολυαιθυλενογλυκόλης και της αλβουμίνης στα χαρακτηριστικά ή ακόμα και να ερευνηθεί η χρήση ενός άλλου οργανικού διαλύτη. Μια πολύ σημαντική παράμετρος είναι το στάδιο του διαχωρισμού. Κρίνω σκόπιμο να μπορέσουν να γίνουν πειράματα με χρήση υπερφυγοκέντρου και να συγκριθούν τα αποτελέσματα. Πολύ ενδιαφέρον θα ήταν να μελετηθούν τα νανοσωματίδια για τη σταθερότητά τους και σε άλλες συνθήκες, πχ υπό την παρουσία αλάτων και συναρτήσει της θερμοκρασίας. Θα πρέπει να δοθεί έμφαση στο ποσοστό εγκλωβισμού του φαρμάκου και πως μπορεί αυτός να βελτιωθεί μέσω της διαδικασίας. Εδώ μπορεί κανείς να συμβουλευτεί τη βιβλιογραφία για τυχόν χρήση κάποιας εξτρά ουσίας που να έχει βελτιωμένες αποδόσεις. Άλλο ένα κομμάτι που είναι σημαντικό κατά την προσωπική μου άποψη είναι οι μελέτες απελευθέρωσης να γίνονται σε δυναμικό περιβάλλον δηλαδή σε κάποιο υδατόλουτρο που να έχει μια σχετική κίνηση, για να εξομοιώνονται καλύτερα οι συνθήκες in vivo στην κυκλοφορία του αίματος. Τέλος μπορεί να μελετηθεί ένα σύστημα διπλής απελευθέρωσης φαρμάκων, ίσως κάποιου άλλου φαρμάκου που θα δρα συνεργιστικά η θα έχει κάποια άλλη δράση που να στοχεύουν σε καρδιαγγειακές εφαρμογές. 153
154 ΥΠΟΜΝΗΜΑ Πίνακας 1 Εικόνα1, χημικός τύπος PLGA 154
155 Εικόνα 2, Μοριακοί Μηχανισμοί που λαμβάνουν χώρα σε αγγειακές παθήσεις. 155
156 Εικόνα 3, Τεχνική Nanoprecipitation, A)Διάλυση, Β)Ενστάλαξη-Εξάτμιση Εικόνα 4, Principles of AFM. (a) A sample is probed by an ultrasharp stylus mounted on a cantilever, which scans over the surface. A reflected laser beam reports deflections of the cantilever to a split photodiode. Photoelectric circuitry then converts the deflections into height information recorded as a digital image. (b) Sketch of a ligand tethered to an AFM tip and probing receptors embedded in a cell membrane. 156
157 Εικόνα 5, Τεχνική Spincoating Εικόνα 6, Διπυριδαμόλη Εικόνα 7, Rotary Evaporator 157
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 12 ο Κυτταρική Βιολογία (νανομετρικό μέγεθος) - Βιοδείκτες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ)
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 12 ο Κυτταρική Βιολογία (νανομετρικό μέγεθος) - Βιοδείκτες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ)
Συνδέοντας τη Νανοτεχνολογία με τα Βιολογικά Συστήματα
 Συνδέοντας τη Νανοτεχνολογία με τα Βιολογικά Συστήματα Η νανοβιοτεχνολογία είναι ένας ραγδαία αναπτυσσόμενος κλάδος της σύγχρονης νανοεπιστήμης και νανοτεχνολογίας στον οποίον εφαρμόζονται τα εργαλεία
Συνδέοντας τη Νανοτεχνολογία με τα Βιολογικά Συστήματα Η νανοβιοτεχνολογία είναι ένας ραγδαία αναπτυσσόμενος κλάδος της σύγχρονης νανοεπιστήμης και νανοτεχνολογίας στον οποίον εφαρμόζονται τα εργαλεία
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 15 ο Νανοσωματίδια για γονιδιακή μεταφορά Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας,
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 15 ο Νανοσωματίδια για γονιδιακή μεταφορά Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας,
Ανδρέας-Παναγιώτης Θεοδώρου Μαρία-Ιωάννα Μαλλιαρουδάκη Κωνσταντίνος Καλογερόπουλος Ιάκωβος Παπαϊωάννου Πελαγία Λυδία Πετροπούλου
 Ανδρέας-Παναγιώτης Θεοδώρου Μαρία-Ιωάννα Μαλλιαρουδάκη Κωνσταντίνος Καλογερόπουλος Ιάκωβος Παπαϊωάννου Πελαγία Λυδία Πετροπούλου «CELL NANOHEALERS: ΝΑΝΟΘΕΡΑΠΕΥΤΕΣ ΚΥΤΤΑΡΩΝ ΣΕ ΔΡΑΣΗ!» Ανδρέας-Παναγιώτης
Ανδρέας-Παναγιώτης Θεοδώρου Μαρία-Ιωάννα Μαλλιαρουδάκη Κωνσταντίνος Καλογερόπουλος Ιάκωβος Παπαϊωάννου Πελαγία Λυδία Πετροπούλου «CELL NANOHEALERS: ΝΑΝΟΘΕΡΑΠΕΥΤΕΣ ΚΥΤΤΑΡΩΝ ΣΕ ΔΡΑΣΗ!» Ανδρέας-Παναγιώτης
ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ
 ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ ΧΡΙΣΤΙΝΑ ΚΑΛΟΓΕΡΟΠΟΥΛΟΥ ΑΘΗΝΑ 2010 1 ΣΚΟΠΟΣ Η ανάλυση και μελέτη της μοριακής δομής των καρωτίδων αρτηριών με υπέρυθρη φασματοσκοπία. Η εξαγωγή συμπερασμάτων
ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ ΧΡΙΣΤΙΝΑ ΚΑΛΟΓΕΡΟΠΟΥΛΟΥ ΑΘΗΝΑ 2010 1 ΣΚΟΠΟΣ Η ανάλυση και μελέτη της μοριακής δομής των καρωτίδων αρτηριών με υπέρυθρη φασματοσκοπία. Η εξαγωγή συμπερασμάτων
ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΠΛΗΡΟΦΟΡΙΚΗ Τα τελευταία χρόνια τα οργανικά ηλεκτρονικά (ΟΗ) αποτελούν έναν από τους πιο ραγδαία αναπτυσσόμενους
 ΤΙ ΑΚΡΙΒΩΣ ΕΊΝΑΙ Η ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΚΑΙ Η ΝΑΝΟΕΠΙΣΤΗΜΕΣ Ως Νανοτεχνολογία ορίζεται η επιστήμη, η μηχανική και η τεχνολογία στην νανοκλίμακα, δηλαδή στην κλίμακα διαστάσεων από 1 έως 100nm. Με άλλα λόγια
ΤΙ ΑΚΡΙΒΩΣ ΕΊΝΑΙ Η ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΚΑΙ Η ΝΑΝΟΕΠΙΣΤΗΜΕΣ Ως Νανοτεχνολογία ορίζεται η επιστήμη, η μηχανική και η τεχνολογία στην νανοκλίμακα, δηλαδή στην κλίμακα διαστάσεων από 1 έως 100nm. Με άλλα λόγια
Φλεγμονή. Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ
 Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΘΗΝΑΣ ΓΙΑΓΚΙΝΗ ΧΗΜΙΚΟΥ Μελέτη των ιστολογικών και βιοχημικών αλλοιώσεων
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΘΗΝΑΣ ΓΙΑΓΚΙΝΗ ΧΗΜΙΚΟΥ Μελέτη των ιστολογικών και βιοχημικών αλλοιώσεων
Εργασία βιολογίας Μ. Παναγιώτα A 1 5 ο ΓΕΛ Χαλανδρίου 2013-14. Αγγειοπλαστική Bypass
 Εργασία βιολογίας Μ. Παναγιώτα A 1 5 ο ΓΕΛ Χαλανδρίου 2013-14 Αγγειοπλαστική Bypass Η αντιμετώπιση των καρδιαγγειακών νόσων περιλαμβάνει: φαρμακευτική αγωγή συστάσεις για αλλαγές στον τρόπο ζωής και τις
Εργασία βιολογίας Μ. Παναγιώτα A 1 5 ο ΓΕΛ Χαλανδρίου 2013-14 Αγγειοπλαστική Bypass Η αντιμετώπιση των καρδιαγγειακών νόσων περιλαμβάνει: φαρμακευτική αγωγή συστάσεις για αλλαγές στον τρόπο ζωής και τις
Νανο-τεχνολογία. Νανο-Επιστήμη. Προσέγγιση από κάτω προς τα πάνω
 Νανο-τεχνολογία Ο σχεδιασμός, ο χαρακτηρισμός, η παραγωγή και η εφαρμογή των δομών, συσκευών και συστημάτων, ελέγχοντας τη μορφή και το μέγεθος σε κλίμακα νανόμετρου Νανο-Επιστήμη Η μελέτη των φαινομένων
Νανο-τεχνολογία Ο σχεδιασμός, ο χαρακτηρισμός, η παραγωγή και η εφαρμογή των δομών, συσκευών και συστημάτων, ελέγχοντας τη μορφή και το μέγεθος σε κλίμακα νανόμετρου Νανο-Επιστήμη Η μελέτη των φαινομένων
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 11 ο Νανοτεχνολογία εφαρμογές Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 11 ο Νανοτεχνολογία εφαρμογές Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ
ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ. 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε.
 ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε. Αμανατίδης ΤΡΙΤΗ 24/10/2017 ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Κατηγορίες
ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε. Αμανατίδης ΤΡΙΤΗ 24/10/2017 ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Κατηγορίες
ΒΙΟΛΟΓΙΑ: Η επιστήμη της ζωής
 Τμήμα Βιολογικών Επιστημών http://www.ucy.ac.cy/goto/biosci/el-gr/home.aspx ΒΙΟΛΟΓΙΑ: Η επιστήμη της ζωής Μελετά ό,τι έχει σχέση με τους ζωντανούς οργανισμούς στον πλανήτη μας, από το μικροσκοπικό επίπεδο
Τμήμα Βιολογικών Επιστημών http://www.ucy.ac.cy/goto/biosci/el-gr/home.aspx ΒΙΟΛΟΓΙΑ: Η επιστήμη της ζωής Μελετά ό,τι έχει σχέση με τους ζωντανούς οργανισμούς στον πλανήτη μας, από το μικροσκοπικό επίπεδο
τα Λεπτά Υμένια στις Νανοδομές και στις Νανο- & Mεγάλης κλίμακας κατασκευές.
 Από τα Λεπτά Υμένια στις Νανοδομές και στις Νανο- & Mεγάλης κλίμακας κατασκευές. Η εξέλιξη της επιστημονικής έρευνας, πέρα της ικανοποίησης της έμφυτης ανάγκης του ανθρώπου για γνώση, είχε και ως παράλληλο
Από τα Λεπτά Υμένια στις Νανοδομές και στις Νανο- & Mεγάλης κλίμακας κατασκευές. Η εξέλιξη της επιστημονικής έρευνας, πέρα της ικανοποίησης της έμφυτης ανάγκης του ανθρώπου για γνώση, είχε και ως παράλληλο
8 η Παρουσίαση Εισαγωγή στο Αίμα
 ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
Γεώργιος Τρανταλής. Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική
 Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Η αορτική
Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Η αορτική
Ο ΡΟΛΟΣ ΤΟΥ ΠΥΡΙΤΙΟΥ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΠΥΡΙΤΙΟ ΚΑΙ ΙΑΤΡΙΚΗ ΓΕΝΙΚΑ Το πυρίτιο (Silicium) είναι το χημικό στοιχείο με χημικό σύμβολο Si, ατομικό αριθμό 14 και ατομική μάζα 28,0855 amu Είναι ένα μεταλλοειδές που ανήκει στην ομάδα 14 του περιοδικού
ΠΥΡΙΤΙΟ ΚΑΙ ΙΑΤΡΙΚΗ ΓΕΝΙΚΑ Το πυρίτιο (Silicium) είναι το χημικό στοιχείο με χημικό σύμβολο Si, ατομικό αριθμό 14 και ατομική μάζα 28,0855 amu Είναι ένα μεταλλοειδές που ανήκει στην ομάδα 14 του περιοδικού
ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΣΤΗΝ ΚΑΘΗΜΕΡΙΝΗ ΖΩΗ
 ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΣΤΗΝ ΚΑΘΗΜΕΡΙΝΗ ΖΩΗ Επιβλέπων καθηγητής: Μαρράς Σωτήρης Τάξη: Α Λυκείου Έτος: 2013-2014 Περίγραμμα παρουσίασης Οι βασικές αρχές της νανοτεχνολογίας Η νανοτεχνολογία στην ιατρική Επίδραση
ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΣΤΗΝ ΚΑΘΗΜΕΡΙΝΗ ΖΩΗ Επιβλέπων καθηγητής: Μαρράς Σωτήρης Τάξη: Α Λυκείου Έτος: 2013-2014 Περίγραμμα παρουσίασης Οι βασικές αρχές της νανοτεχνολογίας Η νανοτεχνολογία στην ιατρική Επίδραση
3. Με ποιο άλλο σύστημα είναι συνδεδεμένο το κυκλοφορικό σύστημα;
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 3 ο ΚΕΦΑΛΑΙΟ «ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ» ΕΙΣΑΓΩΓΗ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος του κυκλοφορικού συστήματος;...... 2. Το κυκλοφορικό σύστημα αποτελείται από: i 3.
Φαρμακευτικές Σπουδές στο Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης
 Φαρμακευτικές Σπουδές στο Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Χρήστος Παναγιωτίδης, Ph.D Αναπλ. Καθηγητής Κυτταρικής/Μοριακής Βιολογίας Τμήμα Φαρμακευτικής, Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Email:
Φαρμακευτικές Σπουδές στο Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Χρήστος Παναγιωτίδης, Ph.D Αναπλ. Καθηγητής Κυτταρικής/Μοριακής Βιολογίας Τμήμα Φαρμακευτικής, Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης Email:
Εφαρμοσμένη Διατροφική Ιατρική
 Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
Μεταπτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΕΚΛΕΚΤΙΚΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΟΞΕΙΔΩΣΗΣ ΤΟΥ ΜΕΘΑΝΙΟΥ ΠΡΟΣ ΔΙΟΞΕΙΔΙΟ ΤΟΥ ΑΝΘΡΑΚΑ Βασιλική
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΕΚΛΕΚΤΙΚΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΟΞΕΙΔΩΣΗΣ ΤΟΥ ΜΕΘΑΝΙΟΥ ΠΡΟΣ ΔΙΟΞΕΙΔΙΟ ΤΟΥ ΑΝΘΡΑΚΑ Βασιλική
Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C.
 Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Εφαρμογές Νανοτεχνολογίας στην Ιατρική
 Μελέτη Εφαρμογές Νανοτεχνολογίας στην Ιατρική Mια Υπόσχεση για το Μέλλον* Δ.Κ. Η εφαρμογή της νανοτεχνολογίας στη ιατρική έχει οδηγήσει στην ανάπτυξη μίας νέας γενιάς διαγνωστικών εργαλείων τα οποία παρέχουν
Μελέτη Εφαρμογές Νανοτεχνολογίας στην Ιατρική Mια Υπόσχεση για το Μέλλον* Δ.Κ. Η εφαρμογή της νανοτεχνολογίας στη ιατρική έχει οδηγήσει στην ανάπτυξη μίας νέας γενιάς διαγνωστικών εργαλείων τα οποία παρέχουν
ΚΥΚΛΟΦΟΡΙΚΕΣ ΔΙΑΤΑΡΑΧΕΣ
 ΚΥΚΛΟΦΟΡΙΚΕΣ ΔΙΑΤΑΡΑΧΕΣ ΑΡΤΗΡΙΟΣΚΛΗΡΥΝΣΗ ΑΘΗΡΟΣΚΛΗΡΩΣΗ Κολέτσα Τριανταφυλλιά Eπικ. Καθηγήτρια Παθολογικής Ανατομικής ΑΠΘ Aρτηριοσκλήρωση * Αρτηριδιοσκλήρωση (Υπερτασική) * Τύπου Mockemberg
ΚΥΚΛΟΦΟΡΙΚΕΣ ΔΙΑΤΑΡΑΧΕΣ ΑΡΤΗΡΙΟΣΚΛΗΡΥΝΣΗ ΑΘΗΡΟΣΚΛΗΡΩΣΗ Κολέτσα Τριανταφυλλιά Eπικ. Καθηγήτρια Παθολογικής Ανατομικής ΑΠΘ Aρτηριοσκλήρωση * Αρτηριδιοσκλήρωση (Υπερτασική) * Τύπου Mockemberg
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες
 Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3], Δ. Καραμήτσος[1]
![Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3], Δ. Καραμήτσος[1] Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3], Δ. Καραμήτσος[1]](/thumbs/20/414553.jpg) Ολόγοςλεπτίνης/αδιπονεκτίνης ως ανεξάρτητος προγνωστικός παράγοντας 10ετούς καρδιαγγειακού κινδύνου σε ινσουλινοθεραπευόμενους ασθενείς με διαβήτη τύπου 2 Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1],
Ολόγοςλεπτίνης/αδιπονεκτίνης ως ανεξάρτητος προγνωστικός παράγοντας 10ετούς καρδιαγγειακού κινδύνου σε ινσουλινοθεραπευόμενους ασθενείς με διαβήτη τύπου 2 Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1],
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΤΩΝ ΟΞΕΙΔΙΩΝ ΤΟΥ ΑΖΩΤΟΥ (NO X
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΤΩΝ ΟΞΕΙΔΙΩΝ ΤΟΥ ΑΖΩΤΟΥ (NO X
Tμήμα Α1 Επιβλέπων καθηγητής: Σ. Μαρράς
 Tμήμα Α1 Επιβλέπων καθηγητής: Σ. Μαρράς -Πλαστικά/πολυμερή (πλεονεκτήματα μειονεκτήματα) -Βιοαποικοδομήσιμα πολυμερη (πλεονεκτήματα μειονεκτήματα) -Βιοαποικοδομήσιμα πολυμερή ως υλικά συσκευασίας -Ιατρικές
Tμήμα Α1 Επιβλέπων καθηγητής: Σ. Μαρράς -Πλαστικά/πολυμερή (πλεονεκτήματα μειονεκτήματα) -Βιοαποικοδομήσιμα πολυμερη (πλεονεκτήματα μειονεκτήματα) -Βιοαποικοδομήσιμα πολυμερή ως υλικά συσκευασίας -Ιατρικές
Κυκλοφορικό Σύστηµα. Σοφία Χαβάκη. Λέκτορας
 Κυκλοφορικό Σύστηµα Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας Εβρυολογίας, Ιατρική Σχολή, ΕΚΠΑ Κυκλοφορικό Σύστηµα Αιµοφόροκυκλοφορικό σύστηµα Λεµφoφόροκυκλοφορικό σύστηµα Αιµοφόρο Κυκλοφορικό Σύστηµα
Κυκλοφορικό Σύστηµα Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας Εβρυολογίας, Ιατρική Σχολή, ΕΚΠΑ Κυκλοφορικό Σύστηµα Αιµοφόροκυκλοφορικό σύστηµα Λεµφoφόροκυκλοφορικό σύστηµα Αιµοφόρο Κυκλοφορικό Σύστηµα
IΣTOΛOΓIA. Tα δείγµατα του βιολογικού υλικού λαµβάνονται µε > βελόνες ενδοσκοπικούς σωλήνες εύκαµπτους καθετήρες
 IΣTOΛOΓIA H ιστολογία κλάδος της ιατρικής που µελετά > υφή βιολογικού υλικού και τους τρόπους που τα επιµέρους συστατικά στοιχεία σχετίζονται µεταξύ τους δοµικά & λειτουργικά Tα δείγµατα του βιολογικού
IΣTOΛOΓIA H ιστολογία κλάδος της ιατρικής που µελετά > υφή βιολογικού υλικού και τους τρόπους που τα επιµέρους συστατικά στοιχεία σχετίζονται µεταξύ τους δοµικά & λειτουργικά Tα δείγµατα του βιολογικού
ΑΣΚΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΕΙΣΑΓΩΓΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΑΠΟ ΤΟ 2003-2013
 ΑΣΚΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΕΙΣΑΓΩΓΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΑΠΟ ΤΟ 2003-2013 ΧΡΙΣΤΙΝΑ ΠΕΡΔΙΟΥ ΒΙΟΛΟΓΟΣ (MSc) 1 ΠΕΡΙΕΧΟΜΕΝΑ ΕΝΟΤΗΤΑ ΣΕΛΙΔΑ Ενότητα 2 : Χημεία της ζωής 4 Ενότητα 3: Ενέργεια και οργανισμοί 13 Ενότητα 4: κυτταρική
ΑΣΚΗΣΕΙΣ ΒΙΟΛΟΓΙΑΣ ΕΙΣΑΓΩΓΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΑΠΟ ΤΟ 2003-2013 ΧΡΙΣΤΙΝΑ ΠΕΡΔΙΟΥ ΒΙΟΛΟΓΟΣ (MSc) 1 ΠΕΡΙΕΧΟΜΕΝΑ ΕΝΟΤΗΤΑ ΣΕΛΙΔΑ Ενότητα 2 : Χημεία της ζωής 4 Ενότητα 3: Ενέργεια και οργανισμοί 13 Ενότητα 4: κυτταρική
ΤΕΧΝΟΛΟΓΙΑ ΜΗ ΚΑΤΑΣΤΡΟΦΙΚΟΥ ΕΛΕΓΧΟΥ 4 ο ΜΑΘΗΜΑ ΘΕΩΡΙΑ 2017
 ΤΕΧΝΟΛΟΓΙΑ ΜΗ ΚΑΤΑΣΤΡΟΦΙΚΟΥ ΕΛΕΓΧΟΥ 4 ο ΜΑΘΗΜΑ ΘΕΩΡΙΑ 2017 Εξοπλισμός και Υλικά Σε ένα σιδηρομαγνητικό υλικό, το μαγνητικό πεδίο που επάγεται πρέπει να βρίσκει την ασυνέχεια υπό γωνία 90 ο ή 45 ο μοίρες.
ΤΕΧΝΟΛΟΓΙΑ ΜΗ ΚΑΤΑΣΤΡΟΦΙΚΟΥ ΕΛΕΓΧΟΥ 4 ο ΜΑΘΗΜΑ ΘΕΩΡΙΑ 2017 Εξοπλισμός και Υλικά Σε ένα σιδηρομαγνητικό υλικό, το μαγνητικό πεδίο που επάγεται πρέπει να βρίσκει την ασυνέχεια υπό γωνία 90 ο ή 45 ο μοίρες.
ΕΛΛΗΝΙΚΗ ΑΓΓΕΙΟΧΕΙΡΟΥΡΓΙΚΗ ΕΤΑΙΡΕΙΑ ΕΝΗΜΕΡΩΤΙΚΟ ΦΥΛΛΑΔΙΟ ΑΝΕΥΡΥΣΜΑ ΤΗΣ ΚΟΙΛΙΑΚΗΣ ΑΟΡΤΗΣ
 ΑΝΕΥΡΥΣΜΑ ΚΟΙΛΙΑΚΗΣ ΑΟΡΤΗΣ Κάθε χρόνο περίπου 200.000 νέοι ασθενείς διαγιγνώσκονται με Ανεύρυσμα Κοιλιακής Αορτής. Είναι γνωστό επίσης, ότι η ρήξη του Ανευρύσματος Κοιλιακής Αορτής οδηγεί σε ποσοστό τουλάχιστον
ΑΝΕΥΡΥΣΜΑ ΚΟΙΛΙΑΚΗΣ ΑΟΡΤΗΣ Κάθε χρόνο περίπου 200.000 νέοι ασθενείς διαγιγνώσκονται με Ανεύρυσμα Κοιλιακής Αορτής. Είναι γνωστό επίσης, ότι η ρήξη του Ανευρύσματος Κοιλιακής Αορτής οδηγεί σε ποσοστό τουλάχιστον
Εργασία στο μάθημα της βιολογίας υπεύθυνη καθηγήτρια : Ζαρφτσιάν Μαρία Ελένη
 Εργασία στο μάθημα της βιολογίας υπεύθυνη καθηγήτρια : Ζαρφτσιάν Μαρία Ελένη Εισαγωγή: Το κυκλοφορικό είναι από τα πιο σημαντικά αλλά και από τα πιο ευαίσθητα συστήματα του οργανισμού μας. Τα προβλήματα
Εργασία στο μάθημα της βιολογίας υπεύθυνη καθηγήτρια : Ζαρφτσιάν Μαρία Ελένη Εισαγωγή: Το κυκλοφορικό είναι από τα πιο σημαντικά αλλά και από τα πιο ευαίσθητα συστήματα του οργανισμού μας. Τα προβλήματα
ΕΠΙΤΥΧΗΣ ΧΡΗΣΗ ΤΟΥ ΚΑΘΕΤΗΡΑ GUIDELINERΓΙΑ ΤΗΝ ΠΡΟΩΘΗΣΗ ΕΝΔΟΣΤΕΦΑΝΙΑΙΩΝ ΠΡΟΘΕΣΕΩΝ ΜΕ ΤΗΝ ΤΕΧΝΙΚΗ MOTHER AND CHILD : ΠΡΩΙΜΗ ΚΛΙΝΙΚΗ ΕΜΠΕΙΡΙΑ
 ΕΠΙΤΥΧΗΣ ΧΡΗΣΗ ΤΟΥ ΚΑΘΕΤΗΡΑ GUIDELINERΓΙΑ ΤΗΝ ΠΡΟΩΘΗΣΗ ΕΝΔΟΣΤΕΦΑΝΙΑΙΩΝ ΠΡΟΘΕΣΕΩΝ ΜΕ ΤΗΝ ΤΕΧΝΙΚΗ MOTHER AND CHILD : ΠΡΩΙΜΗ ΚΛΙΝΙΚΗ ΕΜΠΕΙΡΙΑ Σκοπός Σκοπός της εργασίας είναι η αξιολόγηση του καθετήρα GuideLiner
ΕΠΙΤΥΧΗΣ ΧΡΗΣΗ ΤΟΥ ΚΑΘΕΤΗΡΑ GUIDELINERΓΙΑ ΤΗΝ ΠΡΟΩΘΗΣΗ ΕΝΔΟΣΤΕΦΑΝΙΑΙΩΝ ΠΡΟΘΕΣΕΩΝ ΜΕ ΤΗΝ ΤΕΧΝΙΚΗ MOTHER AND CHILD : ΠΡΩΙΜΗ ΚΛΙΝΙΚΗ ΕΜΠΕΙΡΙΑ Σκοπός Σκοπός της εργασίας είναι η αξιολόγηση του καθετήρα GuideLiner
Βιοϊατρική τεχνολογία
 Τμήμα Μηχανικών Πληροφορικής & Τηλεπικοινωνιών Βιοϊατρική τεχνολογία Ενότητα 1: Εισαγωγή στη Βιοϊατρική Τεχνολογία Αν. καθηγητής Αγγελίδης Παντελής e-mail: paggelidis@uowm.gr ΕΕΔΙΠ Μπέλλου Σοφία e-mail:
Τμήμα Μηχανικών Πληροφορικής & Τηλεπικοινωνιών Βιοϊατρική τεχνολογία Ενότητα 1: Εισαγωγή στη Βιοϊατρική Τεχνολογία Αν. καθηγητής Αγγελίδης Παντελής e-mail: paggelidis@uowm.gr ΕΕΔΙΠ Μπέλλου Σοφία e-mail:
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ. ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
AIΜΟΣΤΑΣΗ Τι είναι η αιμόσταση? Ποια είναι τα κύρια στάδια?
 AIΜΟΣΤΑΣΗ Τι είναι η αιμόσταση? Ποια είναι τα κύρια στάδια? Aιμόσταση=πρόληψη απώλειας αίματος Aιμόσταση=πρόληψη απώλειας Tο αίμα: αίματος Πρέπει να είναι υγρό Δεν έρχεται σε επαφή με αρνητικά φορτισμένες
AIΜΟΣΤΑΣΗ Τι είναι η αιμόσταση? Ποια είναι τα κύρια στάδια? Aιμόσταση=πρόληψη απώλειας αίματος Aιμόσταση=πρόληψη απώλειας Tο αίμα: αίματος Πρέπει να είναι υγρό Δεν έρχεται σε επαφή με αρνητικά φορτισμένες
ΠΑΖΑΪΥΟΥ-ΠΑΝΑΓΙΩΤΟΥ Κ.
 Γιατί μας απασχολεί Ο σακχαρώδης διαβήτης τύπου 1 και 2 συνοδεύονται από μικρο και μακροαγγειακές επιπλοκές Σημαντικότερη αιτία νοσηρότητας και θνητότητας του διαβητικού πληθυσμού Ο κίνδυνος για καρδιαγγειακή
Γιατί μας απασχολεί Ο σακχαρώδης διαβήτης τύπου 1 και 2 συνοδεύονται από μικρο και μακροαγγειακές επιπλοκές Σημαντικότερη αιτία νοσηρότητας και θνητότητας του διαβητικού πληθυσμού Ο κίνδυνος για καρδιαγγειακή
Διδάσκων: Καθ. Αλέξανδρος Ρήγας Εξάμηνο: 9 ο
 Δημοκρίτειο Πανεπιστήμιο Θράκης Τμήμα Ηλεκτρολόγων Μηχανικών & Μηχανικών Υπολογιστών Τομέας Τηλεπικοινωνιών και Διαστημικής Εργαστήριο Ηλεκτρομαγνητικής Θεωρίας Διδάσκων: Καθ. Αλέξανδρος Ρήγας Εξάμηνο:
Δημοκρίτειο Πανεπιστήμιο Θράκης Τμήμα Ηλεκτρολόγων Μηχανικών & Μηχανικών Υπολογιστών Τομέας Τηλεπικοινωνιών και Διαστημικής Εργαστήριο Ηλεκτρομαγνητικής Θεωρίας Διδάσκων: Καθ. Αλέξανδρος Ρήγας Εξάμηνο:
No conflict of interest
 Άλφα 2B - αδρενεργικοί υποδοχείς στα αιμοπετάλια ασθενών με στεφανιαία νόσο: Η επίδραση της αναστολής τους στη συγκόλληση των αιμοπεταλίων Μ.Τουλουπάκη, Μ.Ε. Μαρκέτου, Γ. Κοχιαδάκης, Ν.Ε.Ανδρουλάκης, Κ.Ρούφας,
Άλφα 2B - αδρενεργικοί υποδοχείς στα αιμοπετάλια ασθενών με στεφανιαία νόσο: Η επίδραση της αναστολής τους στη συγκόλληση των αιμοπεταλίων Μ.Τουλουπάκη, Μ.Ε. Μαρκέτου, Γ. Κοχιαδάκης, Ν.Ε.Ανδρουλάκης, Κ.Ρούφας,
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ
 ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Δελτίο μαθήματος (Syllabus): ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Κωδικός μαθήματος: 79 Κύκλος/Επίπεδο σπουδών: Εξάμηνο σπουδών: Προπτυχιακό 8 ο Εξάμηνο Τύπος μαθήματος Υποβάθρου / Γενικών Γνώσεων
ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Δελτίο μαθήματος (Syllabus): ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Κωδικός μαθήματος: 79 Κύκλος/Επίπεδο σπουδών: Εξάμηνο σπουδών: Προπτυχιακό 8 ο Εξάμηνο Τύπος μαθήματος Υποβάθρου / Γενικών Γνώσεων
Αιωρήματα & Γαλακτώματα
 Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2015-16 Μάθημα 9ο 5 May 2017 Αιωρήματα Γαλακτώματα 1 Στρατηγική δοσολογίας (Για άλατα μετάλλων τα οποία υδρολύονται ) Περιοχές δραστικότητας: Περιοχή 1:
Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2015-16 Μάθημα 9ο 5 May 2017 Αιωρήματα Γαλακτώματα 1 Στρατηγική δοσολογίας (Για άλατα μετάλλων τα οποία υδρολύονται ) Περιοχές δραστικότητας: Περιοχή 1:
Νανοτεχνολογία ΧΑΡΙΣ ΑΣΗΜΑΚΟΠΟΥΛΟΣ ΕΦΑΡΜΟΓΕΣ ΠΛΗΡΟΦΟΡΙΚΗΣ 2013 14
 Νανοτεχνολογία 1.Ορισμός της Νανοτεχνολογίας 2.Πότε έκανε την εμφάνιση της; 3.Τα επιτευγματά της 4.Σε τι ωφελει την ανθρωπότητα 5.Που τη συναντάμε στη φύση 6.Κριτικές 7.Τι περιμένουμε απο την εξέλιξη της
Νανοτεχνολογία 1.Ορισμός της Νανοτεχνολογίας 2.Πότε έκανε την εμφάνιση της; 3.Τα επιτευγματά της 4.Σε τι ωφελει την ανθρωπότητα 5.Που τη συναντάμε στη φύση 6.Κριτικές 7.Τι περιμένουμε απο την εξέλιξη της
ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ
 2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης. Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010
 ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
Μάθημα «Εισαγωγή στις Βιοϊατρικές Επιστήμες»
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΔΥΤΙΚΗΣ ΑΤΤΙΚΗΣ Τμήμα Βιοϊατρικών Επιστήμων Εαρινό εξάμηνο 2018-19 Μάθημα «Εισαγωγή στις Βιοϊατρικές Επιστήμες» Παράδοση 13/05/2019 Διδάσκουσα: Κατερίνα Βλαντώνη, Συμβασιούχος Διδάσκουσα ΕΣΠΑ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΔΥΤΙΚΗΣ ΑΤΤΙΚΗΣ Τμήμα Βιοϊατρικών Επιστήμων Εαρινό εξάμηνο 2018-19 Μάθημα «Εισαγωγή στις Βιοϊατρικές Επιστήμες» Παράδοση 13/05/2019 Διδάσκουσα: Κατερίνα Βλαντώνη, Συμβασιούχος Διδάσκουσα ΕΣΠΑ
Φαρμακοκινητική. Χρυσάνθη Σαρδέλη
 Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
ΥΝΑΜΙΚΟ ΕΓΧΡΩΜΟ TRIPLEX ΤΩΝ ΑΓΓΕΙΩΝ ΤΟΥ ΠΕΟΥΣ
 ηµήτρης Γ. Χατζηχρήστου Καθηγητής Ουρολογίας Ανδρολογίας Αριστοτελείου Πανεπιστηµίου Θεσσαλονίκης 01 ΥΝΑΜΙΚΟ ΕΓΧΡΩΜΟ TRIPLEX ΤΩΝ ΑΓΓΕΙΩΝ ΤΟΥ ΠΕΟΥΣ Ποια είναι τα αγγειακά προβλήµατα της στύσης; Τα αγγειακά
ηµήτρης Γ. Χατζηχρήστου Καθηγητής Ουρολογίας Ανδρολογίας Αριστοτελείου Πανεπιστηµίου Θεσσαλονίκης 01 ΥΝΑΜΙΚΟ ΕΓΧΡΩΜΟ TRIPLEX ΤΩΝ ΑΓΓΕΙΩΝ ΤΟΥ ΠΕΟΥΣ Ποια είναι τα αγγειακά προβλήµατα της στύσης; Τα αγγειακά
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 14 ο Νανοαισθητήρες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ Πανεπιστημίου
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 14 ο Νανοαισθητήρες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ Πανεπιστημίου
Autonomous movement of platinum-loaded stomatocytes
 Autonomous movement of platinum-loaded stomatocytes Daniela A. Wilson, Roeland J. M. Nolte and Jan C. M. van Hest, NATURE CHEMISTRY, advance paper ΓΙΩΡΓΟΣ ΦΡΑΓΚΙΑΔΑΚΗΣ 364 ΣΤΟΧΟΣ Στη φύση υπάρχει μια συνεχής
Autonomous movement of platinum-loaded stomatocytes Daniela A. Wilson, Roeland J. M. Nolte and Jan C. M. van Hest, NATURE CHEMISTRY, advance paper ΓΙΩΡΓΟΣ ΦΡΑΓΚΙΑΔΑΚΗΣ 364 ΣΤΟΧΟΣ Στη φύση υπάρχει μια συνεχής
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Οι σπουδές στο Τμήμα Φαρμακευτικής του Α.Π.Θ.
 Οι σπουδές στο Τμήμα Φαρμακευτικής του Α.Π.Θ. Δ. ΧΑΤΖΗΠΑΥΛΟΥ-ΛΙΤΙΝΑ, Ph.D Kαθηγήτρια Φαρμακευτικής Χημείας, Τμήμα Φαρμακευτικής, Α.Π.Θ. e-mail: hadjipav@pharm.auth.gr Σύμφωνα με τονπαγκόσμιο Οργανισμό
Οι σπουδές στο Τμήμα Φαρμακευτικής του Α.Π.Θ. Δ. ΧΑΤΖΗΠΑΥΛΟΥ-ΛΙΤΙΝΑ, Ph.D Kαθηγήτρια Φαρμακευτικής Χημείας, Τμήμα Φαρμακευτικής, Α.Π.Θ. e-mail: hadjipav@pharm.auth.gr Σύμφωνα με τονπαγκόσμιο Οργανισμό
ΕΝΑΝΤΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΜΕ ΚΟΙΝΑ ΦΑΡΜΑΚΑ Η ΜΕ ΝΑΝΟΦΑΡΜΑΚΑ?
 Η ΕΝ ΑΘΗΝΑΙΣ ΦΙΛΕΚΠΑΙΔΕΥΤΙΚΗ ΕΤΑΙΡΕΙΑ ΕΝΑΝΤΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΜΕ ΚΟΙΝΑ ΦΑΡΜΑΚΑ Η ΜΕ ΝΑΝΟΦΑΡΜΑΚΑ? Ευδοκία Κολιάκου Χριστίνα Κοτίνου Κωνσταντίνα Σκλιάμη Αγλαΐα Σφακάκη Χαρούλα Σφέτσα Υπεύθυνες καθηγήτριες:
Η ΕΝ ΑΘΗΝΑΙΣ ΦΙΛΕΚΠΑΙΔΕΥΤΙΚΗ ΕΤΑΙΡΕΙΑ ΕΝΑΝΤΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΜΕ ΚΟΙΝΑ ΦΑΡΜΑΚΑ Η ΜΕ ΝΑΝΟΦΑΡΜΑΚΑ? Ευδοκία Κολιάκου Χριστίνα Κοτίνου Κωνσταντίνα Σκλιάμη Αγλαΐα Σφακάκη Χαρούλα Σφέτσα Υπεύθυνες καθηγήτριες:
ΚΥΤΟΚΙΝΕΣ, ΜΥΟΚΙΝΕΣ ΚΑΙ ΑΣΚΗΣΗ Χαρά Κ. Δελή, PhD
 Σχολή Επιστήμης Φυσικής Αγωγής και Αθλητισμού Πανεπιστήμιο Θεσσαλίας ΚΥΤΟΚΙΝΕΣ, ΜΥΟΚΙΝΕΣ ΚΑΙ ΑΣΚΗΣΗ Χαρά Κ. Δελή, PhD Εργαστήριο Φυσιολογίας, Βιοχημείας και Διατροφής της Άσκησης Σχολή Επιστήμης Φυσικής
Σχολή Επιστήμης Φυσικής Αγωγής και Αθλητισμού Πανεπιστήμιο Θεσσαλίας ΚΥΤΟΚΙΝΕΣ, ΜΥΟΚΙΝΕΣ ΚΑΙ ΑΣΚΗΣΗ Χαρά Κ. Δελή, PhD Εργαστήριο Φυσιολογίας, Βιοχημείας και Διατροφής της Άσκησης Σχολή Επιστήμης Φυσικής
Πνευμονική Εμβολή. Έλενα Σολωμού Αιματολόγος Επίκουρη Καθηγήτρια Παθολογίας-Αιματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών
 Πνευμονική Εμβολή Έλενα Σολωμού Αιματολόγος Επίκουρη Καθηγήτρια Παθολογίας-Αιματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών Πήξη αίματος Αιμόσταση: διακοπή της απώλειας αίματος Μηχανισμοί αιμόστασης : Αγγειοσύσπαση
Πνευμονική Εμβολή Έλενα Σολωμού Αιματολόγος Επίκουρη Καθηγήτρια Παθολογίας-Αιματολογίας Ιατρική Σχολή Πανεπιστημίου Πατρών Πήξη αίματος Αιμόσταση: διακοπή της απώλειας αίματος Μηχανισμοί αιμόστασης : Αγγειοσύσπαση
Μεταπτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΑΡΤΕΜΙΣΙΝΙΝΗΣ ΜΕ ΑΙΜΙΝΗ ΚΑΙ ΑΙΜΑΤΙΝΗ ΜΕΣΩ ΦΑΣΜΑΤΟΣΚΟΠΙΑΣ ΥΠΕΡΥΘΡΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΑΡΤΕΜΙΣΙΝΙΝΗΣ ΜΕ ΑΙΜΙΝΗ ΚΑΙ ΑΙΜΑΤΙΝΗ ΜΕΣΩ ΦΑΣΜΑΤΟΣΚΟΠΙΑΣ ΥΠΕΡΥΘΡΟΥ
Εφαρμοσμένη Διατροφική Ιατρική
 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Σημείωση: Το κείμενο αποτελεί απόσπασμα του κεφαλαίου «Χοληστερίνη και φλεγμονή». Έχει αναπαραχθεί λόγω των πολύτιμων πληροφοριών
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Σημείωση: Το κείμενο αποτελεί απόσπασμα του κεφαλαίου «Χοληστερίνη και φλεγμονή». Έχει αναπαραχθεί λόγω των πολύτιμων πληροφοριών
Σήμερα η hyaluronan αναφέρεται ως υαλουρονικό οξύ.
 Μαρία Καρδάση Το 1934 ο Κάρλ Μάγιερ απομόνωσε από το υαλώδες υγρό του βόειου οφθαλμού μια άγνωστη μέχρι τότε μη θεϊκή γλυκοζαμινογλυκάνη και την ονόμασε hyaluronan. Σήμερα η hyaluronan αναφέρεται ως υαλουρονικό
Μαρία Καρδάση Το 1934 ο Κάρλ Μάγιερ απομόνωσε από το υαλώδες υγρό του βόειου οφθαλμού μια άγνωστη μέχρι τότε μη θεϊκή γλυκοζαμινογλυκάνη και την ονόμασε hyaluronan. Σήμερα η hyaluronan αναφέρεται ως υαλουρονικό
Επιτροπάκη Ειρήνη. Xianghui Xu,Hui Yuan,Jing Chang,Bin He and Zhongwei Gu. Angew.Chem.Int.Ed. 2012,51,1-5
 Επιτροπάκη Ειρήνη ΑΜ:429 Xianghui Xu,Hui Yuan,Jing Chang,Bin He and Zhongwei Gu Angew.Chem.Int.Ed. 2012,51,1-5 Κατασκευή υπερμοριακών δομών με μεταφορικές λειτουργίες για χρήση σε ιατρικές εφαρμογές σε
Επιτροπάκη Ειρήνη ΑΜ:429 Xianghui Xu,Hui Yuan,Jing Chang,Bin He and Zhongwei Gu Angew.Chem.Int.Ed. 2012,51,1-5 Κατασκευή υπερμοριακών δομών με μεταφορικές λειτουργίες για χρήση σε ιατρικές εφαρμογές σε
Κυκλοφορικό σύστημα. Από μαθητές και μαθήτριες του Στ 1
 Κυκλοφορικό σύστημα Από μαθητές και μαθήτριες του Στ 1 Η καρδία Χτύπα 2 δισεκατομμύρια φορές σε όλη μας τη ζωή. Βρίσκεται στο θώρακα, κέντρο προς αριστερά. Έχει το μέγεθος μιας γροθιάς. Αλεξάνδρα, Αναστασία,
Κυκλοφορικό σύστημα Από μαθητές και μαθήτριες του Στ 1 Η καρδία Χτύπα 2 δισεκατομμύρια φορές σε όλη μας τη ζωή. Βρίσκεται στο θώρακα, κέντρο προς αριστερά. Έχει το μέγεθος μιας γροθιάς. Αλεξάνδρα, Αναστασία,
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
Φαρμακολογία Τμήμα Ιατρικής Α.Π.Θ.
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΧΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Α.Π.Θ. Ενότητα 3: Φαρμακοδυναμική Μαρία Μυρωνίδου-Τζουβελέκη Α.Π.Θ. Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΧΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Α.Π.Θ. Ενότητα 3: Φαρμακοδυναμική Μαρία Μυρωνίδου-Τζουβελέκη Α.Π.Θ. Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΛΙΠΗ. ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΛΙΠΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Τα λίπη αποτελούν μια συμπυκνωμένη πηγή ενέργειας Ενεργούν σαν διαλύτες
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΛΙΠΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Τα λίπη αποτελούν μια συμπυκνωμένη πηγή ενέργειας Ενεργούν σαν διαλύτες
ΚΕΦΑΛΑΙΟ 8 ο...2 I. Εφαρµογές της βιοτεχνολογίας στην ιατρική...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 ΝΑ ΣΥΜΠΛΗΡΩΣΕΤΕ ΤΑ ΚΕΝΑ ΜΕ ΤΗΝ ΚΑΤΑΛΛΗΛΗ ΛΕΞΗ...
 ΚΕΦΑΛΑΙΟ 8 ο ΚΕΦΑΛΑΙΟ 8 ο...2 I. Εφαρµογές της βιοτεχνολογίας στην ιατρική...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 ΝΑ ΣΥΜΠΛΗΡΩΣΕΤΕ ΤΑ ΚΕΝΑ ΜΕ ΤΗΝ ΚΑΤΑΛΛΗΛΗ ΛΕΞΗ...10 1 ΚΕΦΑΛΑΙΟ 8 ο I. Εφαρµογές της βιοτεχνολογίας
ΚΕΦΑΛΑΙΟ 8 ο ΚΕΦΑΛΑΙΟ 8 ο...2 I. Εφαρµογές της βιοτεχνολογίας στην ιατρική...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 ΝΑ ΣΥΜΠΛΗΡΩΣΕΤΕ ΤΑ ΚΕΝΑ ΜΕ ΤΗΝ ΚΑΤΑΛΛΗΛΗ ΛΕΞΗ...10 1 ΚΕΦΑΛΑΙΟ 8 ο I. Εφαρµογές της βιοτεχνολογίας
ΕΝΗΜΕΡΩΣΗ ΓΙΑ ΤΙΣ ΕΜΒΑΘΥΝΣΕΙΣ
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Επιτροπή Σπουδών ΕΝΗΜΕΡΩΣΗ ΓΙΑ ΤΙΣ ΕΜΒΑΘΥΝΣΕΙΣ ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2010-2011 ΟΙ ΕΜΒΑΘΥΝΣΕΙΣ ΣΤΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ ΧΜ ΕΜΠ Η Σχολή Χημικών Μηχανικών του Ε.Μ.Π.
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Επιτροπή Σπουδών ΕΝΗΜΕΡΩΣΗ ΓΙΑ ΤΙΣ ΕΜΒΑΘΥΝΣΕΙΣ ΑΚΑΔΗΜΑΪΚΟ ΕΤΟΣ 2010-2011 ΟΙ ΕΜΒΑΘΥΝΣΕΙΣ ΣΤΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ ΧΜ ΕΜΠ Η Σχολή Χημικών Μηχανικών του Ε.Μ.Π.
Λόγοι έκδοσης γνώμης για τον χαρακτηρισμό φαρμακευτικού προϊόντος ως ορφανού
 Παράρτημα 1 Λόγοι έκδοσης γνώμης για τον χαρακτηρισμό φαρμακευτικού προϊόντος ως ορφανού Η Επιτροπή Ορφανών Φαρμάκων (COMP), έχοντας εξετάσει την αίτηση, κατέληξε στα ακόλουθα: Σύμφωνα με το άρθρο 3 παράγραφος
Παράρτημα 1 Λόγοι έκδοσης γνώμης για τον χαρακτηρισμό φαρμακευτικού προϊόντος ως ορφανού Η Επιτροπή Ορφανών Φαρμάκων (COMP), έχοντας εξετάσει την αίτηση, κατέληξε στα ακόλουθα: Σύμφωνα με το άρθρο 3 παράγραφος
ΣΤΕΡΕΕΣ ΜΟΡΦΕΣ ΧΟΡΗΓΗΣΗΣ ΑΙΘΕΡΙΩΝ ΕΛΑΙΩΝ
 ΣΤΕΡΕΕΣ ΜΟΡΦΕΣ ΧΟΡΗΓΗΣΗΣ ΑΙΘΕΡΙΩΝ ΕΛΑΙΩΝ http://www.ypaithros.gr/kalliergeia-me-prooptikh-h-riganh/ http://www.bostanistas.gr/?i=bostanistas.el.article&id=3551 http://www.ethnos.gr/ epaggelmatikes_eukairies/arthro/
ΣΤΕΡΕΕΣ ΜΟΡΦΕΣ ΧΟΡΗΓΗΣΗΣ ΑΙΘΕΡΙΩΝ ΕΛΑΙΩΝ http://www.ypaithros.gr/kalliergeia-me-prooptikh-h-riganh/ http://www.bostanistas.gr/?i=bostanistas.el.article&id=3551 http://www.ethnos.gr/ epaggelmatikes_eukairies/arthro/
Μπαλόνια που εκλύουν φάρμακο. Αθανάσιος Αγγελής Ά Πανεπιστημιακή Καρδιολογική Κλινική Ιπποκράτειο ΓΝΑ
 Μπαλόνια που εκλύουν φάρμακο Αθανάσιος Αγγελής Ά Πανεπιστημιακή Καρδιολογική Κλινική Ιπποκράτειο ΓΝΑ Αγγειοπλαστική στεφανιαίων αγγείων - 1 1977 1.Balloon (PTCA) Andreas Gruntzig performs the first PTCA
Μπαλόνια που εκλύουν φάρμακο Αθανάσιος Αγγελής Ά Πανεπιστημιακή Καρδιολογική Κλινική Ιπποκράτειο ΓΝΑ Αγγειοπλαστική στεφανιαίων αγγείων - 1 1977 1.Balloon (PTCA) Andreas Gruntzig performs the first PTCA
Είναι σχεδόν βέβαιο, είτε να γνωρίζετε κάποιον που πάσχει από μια τέτοια ασθένεια είτε να έχετε μια εσείς οι ίδιοι.
 Γράφει: Δημήτρης Τσουκαλάς, Ιατρός Φυσικής Υγείας Τα αυτοάνοσα νοσήματα είναι ασθένειες που προκύπτουν γιατί το σώμα μας επιτίθεται και καταστρέφει τα δικά του κύτταρα και όργανα. Γνωρίζετε ότι ένας στους
Γράφει: Δημήτρης Τσουκαλάς, Ιατρός Φυσικής Υγείας Τα αυτοάνοσα νοσήματα είναι ασθένειες που προκύπτουν γιατί το σώμα μας επιτίθεται και καταστρέφει τα δικά του κύτταρα και όργανα. Γνωρίζετε ότι ένας στους
Βιολογικές δοκιμές σε Βιοϋλικά
 Βιολογικές δοκιμές σε Βιοϋλικά Γενικές έννοιες (κυτο)τοξικότητας In vitro αποτίμηση ιστών Δοκιμές (assays) Μορφολογία κυττάρων α) Μέθοδος άμεσης επαφής (direct contact) Ζωντανά-νεκρά κύτταρα (βαφή με αιματοξυλίνη
Βιολογικές δοκιμές σε Βιοϋλικά Γενικές έννοιες (κυτο)τοξικότητας In vitro αποτίμηση ιστών Δοκιμές (assays) Μορφολογία κυττάρων α) Μέθοδος άμεσης επαφής (direct contact) Ζωντανά-νεκρά κύτταρα (βαφή με αιματοξυλίνη
Το σύστημα τελομερών/τελομεράσης στις χρόνιες φλεγμονώδεις διαταραχές
 Το σύστημα τελομερών/τελομεράσης στις χρόνιες φλεγμονώδεις διαταραχές Βιβλιογραφική Ανασκόπηση Κορδίνας Βασίλειος Μοριακός Βιολόγος και Γενετιστής Ειδικευόμενος Παθολόγος Γενικό Νοσοκομείο Νίκαιας-Πειραιά
Το σύστημα τελομερών/τελομεράσης στις χρόνιες φλεγμονώδεις διαταραχές Βιβλιογραφική Ανασκόπηση Κορδίνας Βασίλειος Μοριακός Βιολόγος και Γενετιστής Ειδικευόμενος Παθολόγος Γενικό Νοσοκομείο Νίκαιας-Πειραιά
ΑΜΥΛΟ Ζελατινοποίηση αμύλου. Άσκηση 4 η Εργαστήριο Χημείας και Τεχνολογίας Τροφίμων
 ΑΜΥΛΟ Ζελατινοποίηση αμύλου Άσκηση 4 η Εργαστήριο Χημείας και Τεχνολογίας Τροφίμων Θεωρητικό μέρος Υδατάνθρακες Άμυλο Ζελατινοποίηση αμύλου Υδατάνθρακες Αποτελούνται από: Άνθρακα (C) Οξυγόνο (O) Υδρογόνο
ΑΜΥΛΟ Ζελατινοποίηση αμύλου Άσκηση 4 η Εργαστήριο Χημείας και Τεχνολογίας Τροφίμων Θεωρητικό μέρος Υδατάνθρακες Άμυλο Ζελατινοποίηση αμύλου Υδατάνθρακες Αποτελούνται από: Άνθρακα (C) Οξυγόνο (O) Υδρογόνο
Η Τεχνολογία στην Ιατρική
 Εκπαιδευτήριο TO ΠΑΓΚΡΗΤΙΟΝ Σχολικό Έτος 2007-2008 Συνθετικές εργασίες στο μάθημα Πληροφορική Τεχνολογία της Β Γυμνασίου: Όψεις της Τεχνολογίας Θέμα: Η Τεχνολογία στην Ιατρική Τμήμα: ΗΥ: Ομάδα: Β2 pc27
Εκπαιδευτήριο TO ΠΑΓΚΡΗΤΙΟΝ Σχολικό Έτος 2007-2008 Συνθετικές εργασίες στο μάθημα Πληροφορική Τεχνολογία της Β Γυμνασίου: Όψεις της Τεχνολογίας Θέμα: Η Τεχνολογία στην Ιατρική Τμήμα: ΗΥ: Ομάδα: Β2 pc27
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
 ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΤΟ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΕ ΚΑΤΑΣΤΑΣΕΙΣ STRESS ΦΥΣΙΟΛΟΓΙΑ ΜΕΓΑΛΟΥ ΥΨΟΜΕΤΡΟΥ Η ατμοσφαιρική
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΤΟ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΕ ΚΑΤΑΣΤΑΣΕΙΣ STRESS ΦΥΣΙΟΛΟΓΙΑ ΜΕΓΑΛΟΥ ΥΨΟΜΕΤΡΟΥ Η ατμοσφαιρική
Το πιο μικρό και συμπαγές LASER μεγάλης ισχύος για την φυσικοθεραπεία και την φυσική αποκατάσταση
 Το πιο μικρό και συμπαγές LASER μεγάλης ισχύος για την φυσικοθεραπεία και την φυσική αποκατάσταση Χημικοί Μηχανισμοί Παραγωγή εξ επαγωγής, φωτο-χημικών φαινομένων φωτο-ευαισθητοποίησης και φωτο-απομάκρυνσης.
Το πιο μικρό και συμπαγές LASER μεγάλης ισχύος για την φυσικοθεραπεία και την φυσική αποκατάσταση Χημικοί Μηχανισμοί Παραγωγή εξ επαγωγής, φωτο-χημικών φαινομένων φωτο-ευαισθητοποίησης και φωτο-απομάκρυνσης.
Ανευρύσματα Εγκεφάλου
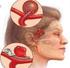 Ανευρύσματα Εγκεφάλου Το εγκεφαλικό ανεύρυσμα είναι μια παθολογική διάταση σε ένα μέρος του τοιχώματος ενός αγγείου του εγκεφάλου που οφείλεται σε ένα έλλειμμα του μέσου χιτώνα του τοιχώματος του αγγείου.
Ανευρύσματα Εγκεφάλου Το εγκεφαλικό ανεύρυσμα είναι μια παθολογική διάταση σε ένα μέρος του τοιχώματος ενός αγγείου του εγκεφάλου που οφείλεται σε ένα έλλειμμα του μέσου χιτώνα του τοιχώματος του αγγείου.
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
314 ΒΙΟΧΗΜΕΙΑ ΤΗΣ ΑΣΚΗΣΗ ΜΥΪΚΗ ΥΠΕΡΤΡΟΦΙΑ. ΦΑΤΟΥΡΟΣ Γ. ΙΩΑΝΝΗΣ, Ph.D. Επίκουρος Καθηγητής Τ.Ε.Φ.Α.Α. Δ.Π.Θ.
 314 ΒΙΟΧΗΜΕΙΑ ΤΗΣ ΑΣΚΗΣΗ ΜΥΪΚΗ ΥΠΕΡΤΡΟΦΙΑ ΦΑΤΟΥΡΟΣ Γ. ΙΩΑΝΝΗΣ, Ph.D. Επίκουρος Καθηγητής Τ.Ε.Φ.Α.Α. Δ.Π.Θ. ΜΗΧΑΝΙΣΜΟΙ ΜΥΪΚΗΣ ΥΠΕΡΤΡΟΦΙΑΣ ΠΡΟΣΩΡΙΝΗ ΥΠΕΡΤΡΟΦΙΑ ΧΡΟΝΙΑ Ή ΜΟΝΙΜΗ ΥΠΕΡΤΡΟΦΙΑ ΥΠΕΡΤΡΟΦΙΑ ΜΥΪΚΩΝ
314 ΒΙΟΧΗΜΕΙΑ ΤΗΣ ΑΣΚΗΣΗ ΜΥΪΚΗ ΥΠΕΡΤΡΟΦΙΑ ΦΑΤΟΥΡΟΣ Γ. ΙΩΑΝΝΗΣ, Ph.D. Επίκουρος Καθηγητής Τ.Ε.Φ.Α.Α. Δ.Π.Θ. ΜΗΧΑΝΙΣΜΟΙ ΜΥΪΚΗΣ ΥΠΕΡΤΡΟΦΙΑΣ ΠΡΟΣΩΡΙΝΗ ΥΠΕΡΤΡΟΦΙΑ ΧΡΟΝΙΑ Ή ΜΟΝΙΜΗ ΥΠΕΡΤΡΟΦΙΑ ΥΠΕΡΤΡΟΦΙΑ ΜΥΪΚΩΝ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΣΤΥΤΙΚΗ ΔΥΣΛΕΙΤΟΥΡΓΙΑ.
 ΣΤΥΤΙΚΗ ΔΥΣΛΕΙΤΟΥΡΓΙΑ. Η στυτική δυσλειτουργία είναι ένα από τα συχνότερα νοσήματα των ανδρών στην σημερινή εποχή.σε νεαρότερες ηλικίες το 30% οφείλεται σε οργανικές αιτίες και το 70 % σε ψυχολογικά αίτια
ΣΤΥΤΙΚΗ ΔΥΣΛΕΙΤΟΥΡΓΙΑ. Η στυτική δυσλειτουργία είναι ένα από τα συχνότερα νοσήματα των ανδρών στην σημερινή εποχή.σε νεαρότερες ηλικίες το 30% οφείλεται σε οργανικές αιτίες και το 70 % σε ψυχολογικά αίτια
ΠΕΡΙΓΡΑΜΜΑ ΜΑΘΗΜΑΤΟΣ
 ΠΕΡΙΓΡΑΜΜΑ ΜΑΘΗΜΑΤΟΣ (1) ΓΕΝΙΚΑ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΕΠΙΣΤΗΜΗΣ ΥΛΙΚΩΝ ΕΠΙΠΕΔΟ ΣΠΟΥΔΩΝ Προπτυχιακό ΚΩΔΙΚΟΣ ΜΑΘΗΜΑΤΟΣ ΕΤΥ 704 ΕΞΑΜΗΝΟ ΣΠΟΥΔΩΝ 7 ο ΤΙΤΛΟΣ ΜΑΘΗΜΑΤΟΣ ΣΥΝΘΕΤΑ ΥΛΙΚΑ ΑΥΤΟΤΕΛΕΙΣ
ΠΕΡΙΓΡΑΜΜΑ ΜΑΘΗΜΑΤΟΣ (1) ΓΕΝΙΚΑ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΕΠΙΣΤΗΜΗΣ ΥΛΙΚΩΝ ΕΠΙΠΕΔΟ ΣΠΟΥΔΩΝ Προπτυχιακό ΚΩΔΙΚΟΣ ΜΑΘΗΜΑΤΟΣ ΕΤΥ 704 ΕΞΑΜΗΝΟ ΣΠΟΥΔΩΝ 7 ο ΤΙΤΛΟΣ ΜΑΘΗΜΑΤΟΣ ΣΥΝΘΕΤΑ ΥΛΙΚΑ ΑΥΤΟΤΕΛΕΙΣ
Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής
 1 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής Μικροσκοπικοί οργανισμοί που ρυθμίζουν τη λειτουργία του ανθρώπινου σώματος σε
1 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής Μικροσκοπικοί οργανισμοί που ρυθμίζουν τη λειτουργία του ανθρώπινου σώματος σε
ΥΓΕΙΑ ΔΙΑΤΗΡΗΣΗ ΤΗΣ ΖΩΗΣ
 ΕΠΙΣΤΗΜΕΣ ΤΗΣ ΖΩΗΣ Βιοποικιλότητα Περιβάλλον ΥΓΕΙΑ Άνθρωπος ΔΙΑΤΗΡΗΣΗ ΤΗΣ ΖΩΗΣ ΤΟ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΣΤΟ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ Υπόγειο (Μουσείο οργάνων, Θαλ. Πειραματόζωα) Ισόγειο (Αιθ. Διδασκαλίας-Βιβλιοθήκη)
ΕΠΙΣΤΗΜΕΣ ΤΗΣ ΖΩΗΣ Βιοποικιλότητα Περιβάλλον ΥΓΕΙΑ Άνθρωπος ΔΙΑΤΗΡΗΣΗ ΤΗΣ ΖΩΗΣ ΤΟ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΣΤΟ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ Υπόγειο (Μουσείο οργάνων, Θαλ. Πειραματόζωα) Ισόγειο (Αιθ. Διδασκαλίας-Βιβλιοθήκη)
Βιολογία Α Λυκείου Κεφ. 3. Κυκλοφορικό Σύστημα. Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα
 Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
4. Η κίρρωση του ήπατος προκαλείται εξαιτίας της αποθήκευσης στα ηπατικά κύτταρα: Πρωτεϊνών Υδατανθράκων Λιπών Αλκοόλ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
4. Η κίρρωση του ήπατος προκαλείται εξαιτίας της αποθήκευσης στα ηπατικά κύτταρα: Πρωτεϊνών Υδατανθράκων Λιπών Αλκοόλ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
ΜΑΘΗΜΑ / ΤΑΞΗ : ΒΙΟΛΟΓΙΑ ΓΠ Γ ΛΥΚΕΙΟΥ (ΘΕΡΙΝΑ) ΗΜΕΡΟΜΗΝΙΑ: 22/10/2017 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΛΑΖΑΡΑΚΗ ΝΟΤΑ ΘΕΜΑ Α Να επιλέξετε τη φράση που συμπληρώνει ορθά κάθε μία από τις ακόλουθες προτάσεις: 1. Το
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ
 ΠΕΡΙΓΡΑΜΜΑ 2.1 ΒΑΣΙΚΑ ΟΡΓΑΝΙΚΑ ΜΟΡΙΑ ΧΡΗΣΙΜΟΠΟΙΟΥΝΤΑΙ ΑΠΌ ΤΟΥΣ ΖΩΝΤΕΣ ΟΡΓΑΝΙΣΜΟΥΣ 2.2 Η ΕΞΕΛΙΞΗ ΧΡΕΙΑΖΕΤΑΙ ΑΝΑΠΑΡΑΓΩΓΗ, ΠΟΙΚΙΛΟΜΟΡΦΙΑ, ΚΑΙ ΕΞΕΛΙΚΤΙΚΗ ΠΙΕΣΗ 2.3 ΕΝΕΡΓΕΙΑΚΟΙ ΜΕΤΑΣΧΗΜΑΤΙΣΜΟΙ ΕΊΝΑΙ ΑΠΑΡΑΙΤΗΤΟΙ
ΠΕΡΙΓΡΑΜΜΑ 2.1 ΒΑΣΙΚΑ ΟΡΓΑΝΙΚΑ ΜΟΡΙΑ ΧΡΗΣΙΜΟΠΟΙΟΥΝΤΑΙ ΑΠΌ ΤΟΥΣ ΖΩΝΤΕΣ ΟΡΓΑΝΙΣΜΟΥΣ 2.2 Η ΕΞΕΛΙΞΗ ΧΡΕΙΑΖΕΤΑΙ ΑΝΑΠΑΡΑΓΩΓΗ, ΠΟΙΚΙΛΟΜΟΡΦΙΑ, ΚΑΙ ΕΞΕΛΙΚΤΙΚΗ ΠΙΕΣΗ 2.3 ΕΝΕΡΓΕΙΑΚΟΙ ΜΕΤΑΣΧΗΜΑΤΙΣΜΟΙ ΕΊΝΑΙ ΑΠΑΡΑΙΤΗΤΟΙ
ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ. Σχηµατική απεικόνιση της µεγάλης και της µικρής κυκλοφορίας
 ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
Γεώργιος Τρανταλής. Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική
 Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Εισαγωγή. Εμβρυολογία. Ανατομία Απεικονιστικός έλεγχος. Παράδοξη εμβολή και Ανοικτό ωοειδές τρήμα. Ανοικτό
Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Εισαγωγή. Εμβρυολογία. Ανατομία Απεικονιστικός έλεγχος. Παράδοξη εμβολή και Ανοικτό ωοειδές τρήμα. Ανοικτό
ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΓΓΕΛΙΚΗΣ ΠΑΠΑΒΑΣΙΛΕΙΟΥ
 ~ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΓΓΕΛΙΚΗΣ ΠΑΠΑΒΑΣΙΛΕΙΟΥ ~ ΠΕΡΙΛΗΨΗ H παρούσα Διδακτορική Διατριβή περιλαμβάνει συστηματική μελέτη για την ανάπτυξη τριοδικού καταλυτικού μετατροπέα (TWC) που να επιδεικνύει
~ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΓΓΕΛΙΚΗΣ ΠΑΠΑΒΑΣΙΛΕΙΟΥ ~ ΠΕΡΙΛΗΨΗ H παρούσα Διδακτορική Διατριβή περιλαμβάνει συστηματική μελέτη για την ανάπτυξη τριοδικού καταλυτικού μετατροπέα (TWC) που να επιδεικνύει
3 η Ημερίδα του Δ.Π.Μ.Σ. «Ιατρική Χημεία»
 3 η Ημερίδα του Δ.Π.Μ.Σ. «Ιατρική Χημεία» Πέμπτη, 15 Φεβρουαρίου, 2018 Συνεδριακό κέντρο «Κάρολος Παπούλιας» Πανεπιστημίου Ιωαννίνων Υπό την Αιγίδα της Περιφέρειας Ηπείρου Επιστημονικό πρόγραμμα 11.00-11.45
3 η Ημερίδα του Δ.Π.Μ.Σ. «Ιατρική Χημεία» Πέμπτη, 15 Φεβρουαρίου, 2018 Συνεδριακό κέντρο «Κάρολος Παπούλιας» Πανεπιστημίου Ιωαννίνων Υπό την Αιγίδα της Περιφέρειας Ηπείρου Επιστημονικό πρόγραμμα 11.00-11.45
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά
 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
Αποφρακτική αρτηριακή νόσος που εντοπίζεται στον καρωτιδικό διχασμό ή στην αρχική μοίρα της έσω καρωτίδας και χαρακτηρίζεται από το σχηματισμό
 Αποφρακτική αρτηριακή νόσος που εντοπίζεται στον καρωτιδικό διχασμό ή στην αρχική μοίρα της έσω καρωτίδας και χαρακτηρίζεται από το σχηματισμό αθηρωματικής πλάκας που προκαλεί στένωση του αγγειακού αυλού,
Αποφρακτική αρτηριακή νόσος που εντοπίζεται στον καρωτιδικό διχασμό ή στην αρχική μοίρα της έσω καρωτίδας και χαρακτηρίζεται από το σχηματισμό αθηρωματικής πλάκας που προκαλεί στένωση του αγγειακού αυλού,
Τα χημικά στοιχεία που είναι επικρατέστερα στους οργανισμούς είναι: i..
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
