Α. Παπαδοπούλου, E. Ρίζος, Α. Αγγελή Τµήµα Χηµικών Μηχανικών, Αριστοτέλειο Πανεπιστήµιο, Θεσσαλονίκη
|
|
|
- Νάρκισσος Σκλαβούνος
- 8 χρόνια πριν
- Προβολές:
Transcript
1 AΠΟΙΚΟ ΟΜΗΜΕΝΟ ΚΟΛΛΑΓΟΝΟ ΩΣ ΕΝΕΣΙΜΟ ΝΑΝΟ-ΥΛΙΚΟ ΣΤΗΝ ΒΙΟΪΑΤΡΙΚΗ ΜΗΧΑΝΙΚΗ: ΜΕΛΕΤΗ ΤΗΣ ΦΥΣΙΚΗΣ ΣΥΜΠΕΡΙΦΟΡΑΣ ΚΑΙ ΡΕΟΛΟΓΙΚΩΝ Ι ΙΟΤΗΤΩΝ ΖΕΛΑΤΙΝΗΣ ΤΥΠΟΥ Β ΣΕ ΦΥΣΙΟΛΟΓΙΚΕΣ ΣΥΝΘΗΚΕΣ ΚΑΙ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΟΣΤΕΟΑΡΘΡΙΤΙ Α Α. Παπαδοπούλου, E. Ρίζος, Α. Αγγελή Τµήµα Χηµικών Μηχανικών, Αριστοτέλειο Πανεπιστήµιο, Θεσσαλονίκη ΠΕΡΙΛΗΨΗ Η παρούσα εργασία αναφέρεται στη µελέτη της φυσικής συµπεριφοράς και των ρεολογικών ιδιοτήτων ζελατίνης τύπου Β υπό διάφορους συνδυασµούς συνθηκών, αρχικά σε υδατικά διαλύµατα, µεταβάλλοντας τη συγκέντρωση της πρωτεΐνης, το ph και την περιεκτικότητα του διαλύµατος σε NaCl. Πρωτίστως όµως επικεντρώνεται στη µελέτη των µηχανικών ιδιοτήτων του συγκεκριµένου τύπου ζελατίνης υπό φυσιολογικές συνθήκες διαλύµατος (DMEM) και θερµοκρασίας (~37 o C) καθώς και στις πιθανές εφαρµογές του στη θεραπεία της οστεοαρθρίτιδας, η οποία έγκειται στη διόρθωση της σύστασης του αρθρικού υγρού / επιφάνειας χόνδρου. Από πειραµατικά δεδοµένα που αφορούν κυρίως οπτικές παρατηρήσεις προκύπτουν ορισµένα συµπεράσµατα, όπως η ιδιαίτερη ευαισθησία του βιοϋλικού σε µικροβιακή επιµόλυνση, για αυτό και κρίνεται απαραίτητη η προσθήκη µικρής ποσότητας αζιδίου του νατρίου (NaN 3, ~0.1% wt) ως βιοκτόνο. Επιπλέον, σε ακραίες τιµές ph παρατηρείται αυξηµένη αποικοδόµηση της ζελατίνης και µείωση της ικανότητας της να σχηµατίσει gel. Από την άλλη, η προσθήκη ορισµένης ποσότητας χλωριούχου νατρίου (NaCl) δε φαίνεται να επιδρά σηµαντικά στις διαµοριακές αλληλεπιδράσεις µεταξύ αλυσίδων ζελατίνης παρά µόνο σε εξαιρετικά όξινες συνθήκες. ιαπιστώνεται ακόµη, ότι πιθανόν η σταθερή δοµή τριπλής έλικας του συγκεκριµένου υλικού αποσταθεροποιείται σε φυσιολογικές συνθήκες, δηλαδή στους 37 o C, προκαλώντας κατάρρευση του gel. ΕΙΣΑΓΩΓΗ Το κολλαγόνο αποτελεί ένα από τα κυριότερα βιοπολυµερή του ανθρώπινου οργανισµού, απαρτίζοντας το 70% της πρωτεΐνης που συνθέτει δέρµα, τένοντες, κόκκαλα. Οποιαδήποτε µορφή κολλαγόνου εκτός του φυσικού του περιβάλλοντος αναφέρεται ως ζελατίνη ή αποικοδοµηµένο κολλαγόνο, καθώς προκύπτει από τη µερική υδρόλυση του φυσικού κολλαγόνου και δεν απαντάται η ίδια στη φύση. Η ζελατίνη κυρίως προέρχεται από δέρµα και κόκκαλα θηλαστικών (χοιροειδή, βοοειδή), ενώ πρόσφατα άρχισε να αποµονώνεται και ένα διαφορετικό είδος ζελατίνης από δέρµα ψαριών [1]. Ανάλογα µε τις συνθήκες αποµόνωσης και την προέλευση η ζελατίνη διακρίνεται σε τρεις κατηγορίες: ζελατίνη τύπου Α, ζελατίνη τύπου Β και ζελατίνη από ψάρι. Στη συγκεκριµένη περίπτωση µελετάται η ζελατίνη τύπου Β µε bloom number ~225 g. Η ζελατίνη τύπου Β αποµονώνεται κυρίως από δέρµα και κόκκαλα βοοειδών υπό αλκαλικές συνθήκες. Η εν λόγω διεργασία προσδίδει στη ζελατίνη ισοηλεκτρικό σηµείο περίπου ίσο µε 5 (± 0.3) [2]. Ο όρος bloom number εκφράζει την ικανότητα της πρωτεΐνης να σχηµατίζει σταθερό gel όταν βρίσκεται διαλυµένη σε κάποιο µέσο και µετράται σε γραµµάρια. Η ελάχιστη συγκέντρωση που απαιτείται ώστε να σχηµατιστεί gel έχει βρεθεί ίση µε 0.5% wt. Επιπλέον, οι στερεοί κόκκοι ζελατίνης όταν τοποθετηθούν για αρκετές ώρες σε κρύο νερό (4 o C) έχουν την ικανότητα να διογκώνονται απορροφώντας νερό. Το στάδιο της διόγκωσης της ζελατίνης παίζει µεγάλο ρόλο, ιδιαίτερα στην περίπτωση υψηλών συγκεντρώσεων ζελατίνης, καθώς επιτρέπει τη διάλυση µε ήπια θερµική επεξεργασία στους 40 o C [1]. Οι παράγοντες που επηρεάζουν το σχηµατισµό της έλικας στο µόριο της ζελατίνης, όταν βρίσκεται διαλυµένη σε κάποιο διαλύτη είναι: συγκέντρωση της ζελατίνης, αύξηση της οποίας οδηγεί και σε αύξηση της ικανότητας σχηµατισµού σταθερού gel. Το ποσοστό ανάκτησης της τριπλής έλικας στη ζελατίνη συγκριτικά µε το µητρικό µόριο κολλαγόνου έχει αποδειχθεί ότι εξαρτάται επίσης από το ρυθµό και τη θερµοκρασία όπου λαµβάνει χώρα η ανάπτυξη των δεσµών υδρογόνου για το σχηµατισµό της τελικής δοµής έλικας της πρωτεΐνης. Πιο συγκεκριµένα, σε υψηλότερες θερµοκρασίες (>20 o C) ο σχηµατισµός της τριπλής έλικας πραγµατοποιείται µε πιο αργό ρυθµό µε αποτέλεσµα την ανάκτηση δοµών µε ιδιότητες όµοιες µε του φυσικού µορίου του κολλαγόνου συγκριτικά µε την ωρίµανση του gel σε χαµηλότερες θερµοκρασίες [3] µοριακό βάρος: υψηλά µοριακά βάρη ευνοούν το σχηµατισµό σταθερής έλικας κατά τη διαµόρφωση της πρωτεΐνης στο χώρο [1] πηγή προέλευσης της ζελατίνης, η οποία καθορίζει και τα ποσοστά αµινοξέων στο µόριο της εκάστοτε ζελατίνης. Ειδικότερα τα αµινοξέα προλίνη και υδροξυπρολίνη σταθεροποιούν το µόριο της ζελατίνης για το σχηµατισµό gel. Στη προερχόµενη από θηλαστικά ζελατίνη το ποσοστό των δύο κύριων αµινοξέων αποτελεί το 25% wt [1] ph: σε σχετικά υψηλές συγκεντρώσεις η επίδραση του ph στην περιοχή δε επηρεάζει σηµαντικά το σχηµατισµό gel [1]
2 ιονική ισχύς: προσθήκη NaCl έως 0.10 Μ δεν παίζει σπουδαίο ρόλο στο σχηµατισµό γέλης [1]. Αντιθέτως, υψηλές συγκεντρώσεις άλατος φαίνεται να επιδρούν αρνητικά στη σταθεροποίηση της ζελατίνης και την ανάπτυξη της τρισδιάστατης δοµής [1,4] Η ζελατίνη ανήκει στην κατηγορία των πρωτεϊνών που σχηµατίζουν φυσικά gel. Φυσικά χαρακτηρίζονται εκείνα τα gel στα οποία η διεργασία µετατροπής µεταξύ των δύο καταστάσεων, της στερεής (gel) και της υγρής (διάλυµα) είναι αντιστρεπτή και πραγµατοποιείται µε µείωση ή αύξηση της θερµοκρασίας αντίστοιχα. Η µελέτη των µηχανικών ιδιοτήτων του συγκεκριµένου πολυµερούς παρουσιάζει ιδιαίτερο ενδιαφέρον καθώς επιτρέπει τη συλλογή αξιόπιστων πληροφοριών σχετικά µε το σηµείο τήξης και την ιξωδοελαστικότητα του υλικού, δηλαδή την ικανότητα να αντιστέκεται στην παραµόρφωση, κάτω από την άσκηση δύναµης συναρτήσει της θερµοκρασίας. Πιο συγκεκριµένα, κατά τη ρεολογική ανάλυση ενδιαφέρουν κυρίως δύο συντελεστές: ο συντελεστής αποθήκευσης ή δυναµική ακαµψία, G (Pa), ο οποίος εκφράζει την ικανότητα του υλικού να αποθηκεύει ενέργεια την οποία και απελευθερώνει κατά την παραµόρφωση, και ο συντελεστής απώλειας, G (Pa), ο οποίος εκφράζει την ικανότητα του υλικού να χάνει ενέργεια υπό µορφή θερµότητας κατά τη διάρκεια της ασκούµενης παραµόρφωσης. Οι δύο συντελεστές συνδέονται µεταξύ τους µε έναν συντελεστή απόσβεσης που δίνεται από τη σχέση (1) [5]: G '' tanδ = (1) G ' Το σηµείο τήξης της ζελατίνης ισούται µε τη θερµοκρασία όπου η τιµή του συντελεστή απόσβεσης τείνει στο 1, δηλαδή ισχύει η σχέση: G = G. Μέρος της διάταξης που χρησιµοποιείται για τη µέτρηση των µηχανικών ιδιοτήτων απεικονίζεται στο Σχήµα 1. Επιπροσθέτως, η εν λόγω εργασία διεξάγεται προκειµένου να µελετηθεί η εφαρµογή της ζελατίνης στο σχηµατισµό βιοσυµβατών υλικών για τη θεραπεία της οστεοαρθρίτιδας και ειδικότερα την αποκατάσταση της σύστασης του αρθρικού υγρού / επιφάνειας του χόνδρου. Άρθρωση ονοµάζεται κάθε σηµείο όπου δύο ή περισσότερα οστά έρχονται σε επαφή επιτρέποντας την ελεύθερη αλλά και εντός ορίων κίνησή τους. Η εξωτερική επιφάνεια των οστών καλύπτεται από ένα σκληρό αλλά και ολισθηρό στρώµα ιστό, το χόνδρο, ο οποίος απορροφά τυχόν κραδασµούς και επιτρέπει την οµοιόµορφη κατανοµή του φορτίου στην άρθρωση. Η οστεοαρθρίτιδα αποτελεί εκφυλιστική ασθένεια που προσβάλει τις αρθρώσεις. Στην περίπτωση της οστεοαρθρίτιδας η επιφάνεια του χόνδρου γίνεται τραχεία και φθείρεται µε αποτέλεσµα οι δύο επιφάνειες των οστών να έρχονται σε άµεση επαφή κατά την κίνηση. Ο οργανισµός προσπαθώντας να αποκαταστήσει τη φυσιολογική λειτουργία του χόνδρου ενεργοποιεί την παραγωγή µεγαλύτερων ποσοτήτων αρθρικού υγρού µε αποτέλεσµα να προκαλείται οίδηµα στην περιοχή που πάσχει από οστεοαρθρίτιδα. Στις µέρες µας η αύξηση του ορίου ηλικίας έχει οδηγήσει και σε εξαιρετικά αυξηµένα ποσοστά ατόµων που πάσχουν από τη συγκεκριµένη ασθένεια. Από την άλλη µεριά, δυστυχώς, τα µέχρι στιγµής χρησιµοποιούµενα φάρµακα επικεντρώνονται στην ανακούφιση του πόνου και την προσωρινή µόνο αποκατάσταση της φυσιολογικής λειτουργίας της άρθρωσης [6]. Για αυτό το λόγο κρίνεται επιτακτική η ανάγκη ανάπτυξης προηγµένων ενέσιµων υλικών που θα στοχεύουν στη θεραπεία της πάθησης χωρίς τη µεσολάβηση επεµβατικών µεθόδων και την αποφυγή της ταλαιπωρίας των ασθενών από µια µετεγχειρητική περίοδο. Τα βασικά στάδια του πειραµατικού µέρους που ακολουθεί η παρούσα εργασία είναι: παρασκευή υδατικών διαλυµάτων ζελατίνης σε τρεις διαφορετικές συγκεντρώσεις πρωτεΐνης, περιοχή ph µεταξύ 2.0 και 10.0 και προσθήκη NaCl µε βάση τις περιεκτικότητες άλατος που συναντώνται σε φυσιολογικές συνθήκες παρασκευή δείγµατος ζελατίνης πολύ υψηλής συγκέντρωσης σε DMEM, το οποίο είναι πλούσιο σε ανόργανα άλατα, αµινοξέα και βιταµίνες προσοµοιάζοντας σε µεγάλο βαθµό τις ιδιότητες των φυσιολογικών υγρών στο σώµα συλλογή οπτικών παρατηρήσεων όσον αφορά τη συµπεριφορά των υλικών που παρασκευάστηκαν σε δύο θερµοκρασίες (25 o C και 37 o C) µέτρηση των µηχανικών ιδιοτήτων της ζελατίνης σε ρεόµετρο
3 Σχήµα 1: Πειραµατική διάταξη µέτρησης µηχανικών ιδιοτήτων (προσαρµοσµένο από [5]) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ Για τη διεξαγωγή των πειραµάτων χρησιµοποιήθηκαν τα εξής αντιδραστήρια: Ζελατίνη τύπου Β (~225g Bloom number, Sigma Aldrich Co. LLC., USA), Αζίδιο του Νατρίου (NaN 3, Sigma Aldrich Co. LLC., USA), Απεσταγµένο νερό, Χλωριούχο Νάτριο (NaCl), Πυκνό διάλυµα υδροχλωρικού οξέος (HCl, 37% w/w, ChemLab, Belgium, Europe), Υδροξείδιο του Νατρίου (NaOH, ChemLab, Belgium, Europe), ιάλυµα αιθανόλης (Καθαρότητα 99.8%, Sigma Aldrich Co. LLC., USA), DMEM (Dulbecco s Modified Eagle Medium, Sigma Aldrich Co. LLC., USA), Ρυθµιστικά διαλύµατα ph 4.0, 7.0 και 10.0 (20 o C) (Fluka Analytical, Sigma Aldrich Co. LLC., USA). Επιπλέον, για τη διάλυση της ζελατίνης χρησιµοποιήθηκε θερµαντική πλάκα µε µαγνητική ανάδευση (Snijders 34532, Gemini BV, Netherlands, Europe), για τη µέτρηση του ph πεχάµετρο της Metrohm 744 (Switzerland, Europe), ενώ η µέτρηση των µηχανικών ιδιοτήτων έγινε µε ρεόµετρο AR-G2 (TA Instruments, USA). Το πρώτο πειραµατικό µέρος περιελάµβανε την παρασκευή δειγµάτων ζελατίνης σε συγκεντρώσεις 0.1, 2.0 και 5.0% wt σε υδατικό µέσο. Αρχικά έγινε σχολαστικός καθαρισµός των σκευών που επρόκειτο να χρησιµοποιηθούν µε απορρυπαντικό, απεσταγµένο νερό και τέλος, µε αιθανόλη, προκειµένου να περιοριστεί η πιθανότητα βακτηριακής επιµόλυνσης των δειγµάτων. Έπειτα προετοιµάστηκαν υδατικά διαλύµατα συγκεκριµένου ph µε την προσθήκη αραιών διαλυµάτων HCl ή NaOH αντίστοιχα. Ακολούθησε υπολογισµός και ζύγιση των κατάλληλων ποσοτήτων ζελατίνης και υδατικού διαλύµατος καθορισµένου ph ( ). Τα δείγµατα παρέµειναν 1 2 µέρες στο ψυγείο (4 o C) ώστε η ζελατίνη να διογκωθεί σε µεγαλύτερους κόκκους µε την απορρόφηση νερού και να διευκολυνθεί η διάλυσή της στο υδατικό µέσο. Η διάλυση της ζελατίνης πραγµατοποιήθηκε µε ήπια θέρµανση (έως 52 o C) και µαγνητική ανάδευση µε κυλινδρικό µαγνήτη (12*4.5 mm). Το φιαλίδιο σταθεροποιούνταν σε ποτήρι ζέσεως µε νερό και σε κάποιο ύψος από τον πυθµένα του ποτηριού ώστε να µην έρχεται σε άµεση επαφή µε τη θερµαντική πλάκα. Παράλληλα, καθ όλη τη διάρκεια της διάλυσης της ζελατίνης παρακολουθούνταν η θερµοκρασία του νερού, όπου ήταν τοποθετηµένο το φιαλίδιο, µε θερµόµετρο, και ρυθµιζόταν µε το διακόπτη ώστε να αποφευχθούν µεγάλες διακυµάνσεις. Η συγκεκριµένη πειραµατική διάταξη διάλυσης της ζελατίνης φαίνεται στο Σχήµα 2. Ο απαιτούµενος χρόνος για την πλήρη διάλυση της πρωτεΐνης εξαρτάται, όπως αναµένεται, από τη συγκέντρωση της τελευταίας. Για αυτό το λόγο για συγκεντρώσεις 2.0 και 5.0 % wt απαιτούνταν περίπου 2 ώρες ενώ για τη µικρότερη συγκέντρωση 30 λεπτά ήταν αρκετά. Στη συνέχεια, γινόταν µέτρηση και ρύθµιση του ph στην επιθυµητή περιοχή µε την προσθήκη αραιών διαλυµάτων HCl ή/και NaOH 0.4 Μ, 0.2 Μ και 0.1 Μ. Με βάση την προστιθέµενη ποσότητα οξέος ή βάσης υπολογιζόταν η τελική συγκέντρωση της ζελατίνης στο δείγµα. Τέλος, αφού τα δείγµατα παρέµειναν περίπου 1 µέρα σε θερµοκρασία δωµατίου (~20 o C), τοποθετούνταν στο ψυγείο για την αποφυγή ανάπτυξης µικροβίων, το σχηµατισµό πιο σταθερού gel και την αποκατάσταση ισορροπίας στο σύστηµα της πρωτεΐνης. Σε αυτό το σηµείο πρέπει να επισηµανθεί ότι τα δείγµατα µε ph µεγαλύτερο του 6.0 (6.0, 8.0, 10.0) περιείχαν NaN 3 σε περιεκτικότητα 0.1% wt ως συντηρητικό και βιοκτόνο. Σε χαµηλότερες τιµές ph (2.0, 4.0) η χρήση του συγκεκριµένου δηλητηρίου θεωρήθηκε µη ασφαλής λόγω πιθανότητας έκλυσης επικίνδυνων αερίων. Το δεύτερο µέρος αποσκοπούσε στη συλλογή οπτικών παρατηρήσεων σχετικά µε την επίδραση της ιονικής ισχύος στη ζελατίνη. Επιλέχτηκαν τρεις συγκεντρώσεις άλατος (NaCl), 0.30 Μ, 0.15 Μ και 0.05 Μ. Αρχικά παρασκευάστηκαν δύο υδατικά διαλύµατα 0.3 Μ NaCl µε και χωρίς NaN 3, ενώ οι µικρότερες συγκεντρώσεις άλατος προέκυψαν µε διαδοχικές αραιώσεις του αρχικού διαλύµατος. Η µεσαία περιεκτικότητα (0.15 Μ) αποτελεί τη φυσιολογική περιεκτικότητα NaCl της εξωκυττάριας µήτρας στα περισσότερα είδη κυττάρων. Η µεγαλύτερη συγκέντρωση (0.30 Μ) απαντάται µόνο σε ειδικές περιπτώσεις, όπως στη σπονδυλική στήλη, ενώ η µικρότερη συγκέντρωση σε NaCl παρατίθεται συγκριτικά. Επιπλέον, οι συγκεντρώσεις ζελατίνης ήταν 0.5, 2.0, 5.0 % wt, καθώς συγκέντρωση ζελατίνης 0.1% wt στάθηκε αδύνατο να σχηµατίσει gel ακόµα και µετά το πέρας δύο µηνών στους 4 o C. Η πειραµατική διαδικασία που ακολουθήθηκε ήταν παρόµοια µε του πρώτου πειραµατικού µέρους. ιαφορές σηµειώθηκαν στη θέρµανση κατά τη διάλυση της ζελατίνης, όπου γινόταν σε χαµηλότερες θερµοκρασίες (έως 42 o C). Επιπλέον, στην περίπτωση των δειγµάτων µε 0.05 Μ NaCl η τοποθέτηση στο ψυγείο γινόταν την ίδια µέρα µε τη διάλυση της ζελατίνης αφού πρώτα παρέµεναν λίγη ώρα σε
4 θερµοκρασία δωµατίου. Η παραπάνω αλλαγή κρίθηκε σκόπιµη λόγω της µικρής περιεκτικότητας NaN 3 (~0.02% wt) στα συγκεκριµένα δείγµατα. Επιπροσθέτως, παρασκευάσθηκε µε τον ίδιο τρόπο δείγµα ζελατίνης πολύ υψηλής συγκέντρωσης (25.0 % wt) µε διαλύτη DMEM προκειµένου να συλλεχθούν ορισµένες αρχικές πληροφορίες σχετικά µε τη συµπεριφορά του βιοϋλικού σε φυσιολογικές συνθήκες διαλύµατος και θερµοκρασίας (ph 7.1 και Τ 37 o C). Το συγκεκριµένο δείγµα παρουσίασε ιδιαίτερη δυσκολία κατά τη διάλυση της ζελατίνης καθώς απαιτήθηκαν περισσότερες από 15 ώρες και θερµοκρασίες έως και 65 o C. Σχήµα 2: Πειραµατική διάταξη διάλυσης της ζελατίνης Σχήµα 3: είγµα ζελατίνης 2% wt πριν και µετά τη ρύθµιση του ύψους της γεωµετρίας Στο σηµείο αυτό επισηµαίνεται ότι για τη µέτρηση και ρύθµιση του ph, το πεχάµετρο θα έπρεπε πρώτα να βαθµονοµηθεί στην αντίστοιχη περιοχή, δηλαδή σε ph: για την όξινη περιοχή ενώ σε ph: για τη βασική περιοχή. Για τη βαθµονόµηση του πεχαµέτρου χρησιµοποιούνταν πρότυπα ρυθµιστικά διαλύµατα. Προκειµένου να διαπιστωθεί η συµπεριφορά της ζελατίνης σε διάφορες συνθήκες ph και ιονικής ισχύος σε θερµοκρασία δωµατίου (~25 o C) και σε φυσιολογική θερµοκρασία (~37 o C), τα δείγµατα µε συγκέντρωση ζελατίνης 5.0% wt, µετά την παραµονή τους για αρκετό καιρό σε περίπου 4 o C, τοποθετήθηκαν σε υδατόλουτρο πρώτα στους 25 o C, όπου και παρέµειναν για 30 λεπτά. Έπειτα την συλλογή οπτικών παρατηρήσεων τα δείγµατα τοποθετήθηκαν και πάλι στο υδατόλουτρο στους 37 o C για 30 λεπτά ενώ τέλος, έγιναν και πάλι κάποιες οπτικές παρατηρήσεις. Τέλος, πραγµατοποιήθηκαν ορισµένες µετρήσεις (Temperature ramp step) ρεολογικών ιδιοτήτων σε ρεόµετρο (AR G2, TA Instruments). Πιο συγκεκριµένα µελετήθηκαν τα µέτρα αποθήκευσης (G, Pa) και απώλειας (G, Pa) συναρτήσει αυξανόµενης της θερµοκρασίας από τους 5 o C στους 40 o C µε ρυθµό 1 o C/min καθώς και ο συντελεστής απόσβεσης (tanδ). Οι µετρήσεις ελήφθησαν υπό σταθερή συχνότητα (0.1 Hz) και ένταση ασκούµενης δύναµης από τη γεωµετρία 3%. Η γεωµετρία που χρησιµοποιήθηκε ήταν η 25 mm steel plate , Sand-blasted St-steel parallel plate. Στην πλάκα του ρεοµέτρου, της οποίας η θερµοκρασία είχε ήδη ρυθµιστεί στους 5 o C, τοποθετήθηκαν δύο λεπτά κοµµάτια γέλης από δείγµα 2.0% wt ζελατίνης µε ph=7.86 (33 o C), 0.1% NaN 3 και χωρίς την προσθήκη NaCl. Το κενό µεταξύ πλάκας και γεωµετρίας ρυθµίστηκε προσεκτικά στα 215 µm, το οποίο έδωσε όγκο δείγµατος περίπου 0.11 ml. Πριν την έναρξη της µέτρησης το δείγµα έµεινε για 10 λεπτά σε ηρεµία µεταξύ της γεωµετρίας και της πλάκας του ρεοµέτρου στους 5 o C. Στο Σχήµα 3 απεικονίζεται η πλάκα του ρεοµέτρου µε το δείγµα πριν και µετά τη ρύθµιση του ύψους της γεωµετρίας. ΑΠΟΤΕΛΕΣΜΑΤΑ ΚΑΙ ΣΥΖΉΤΗΣΗ Το ισοηλεκτρικό σηµείο της ζελατίνης τύπου Β, όπως έχει ήδη αναφερθεί, είναι κοντά σε ph=5.0. Μετά τη διάλυση της ζελατίνης παρατηρούνταν έντονη τάση να οδηγήσει το ph του διαλύµατος όσο πιο κοντά γίνεται στο ισοηλεκτρικό της σηµείο, γεγονός που εξηγείται και από την εγγενή ανάγκη ενός συστήµατος να επέλθει σε θερµοδυναµική ισορροπία. Η επίδραση στο ph του αρχικού διαλύµατος γίνεται εντονότερη αυξανόµενης της συγκέντρωσης της ζελατίνης. Επιπλέον, όσο µεγαλύτερη η συγκέντρωση της πρωτεΐνης τόσο δυσκολότερη καθίσταται η ρύθµιση του ph στην επιθυµητή τιµή, απαιτώντας προσθήκη µεγαλύτερων ποσοτήτων οξέος ή βάσης. Η προσθήκη διαλυµάτων οξέος ή βάσης επέφερε αλλαγές και στην τελική συγκέντρωση ζελατίνης, για αυτό και κατά την παρασκευή των δειγµάτων υπολογίζονταν υψηλότερες συγκεντρώσεις 5%-10% από την επιθυµητή τιµή ανάλογα µε τη συγκέντρωση και την επιθυµητή τελική τιµή στο ph. Για παράδειγµα, αν οι επιθυµητές τελικές τιµές συγκέντρωσης της ζελατίνης και ph ήταν 5.0% wt και 10.0% wt αντίστοιχα, η αρχική συγκέντρωση ζελατίνης έφτανε τα 5.5% wt.
5 Επιπλέον, παρατηρήθηκε έντονο το πρόβληµα της εξάτµισης κατά τη ρύθµιση του ph ειδικότερα στα δείγµατα µικρότερης συγκέντρωσης της ζελατίνης (0.1 και 0.5% wt), λόγω, πιθανώς, των λιγότερων αλληλεπιδράσεων που αναπτύσσονται µεταξύ ζελατίνης και νερού. Η συγκεκριµένη παρατήρηση προέκυψε µέσω ζύγισης της µάζας του διαλύµατος πριν και µετά τη ρύθµιση του ph στην εκάστοτε τιµή. Από οπτικές παρατηρήσεις των δειγµάτων προέκυψε ότι για όλες τις τιµές ph και ιονικής ισχύος, η κατάρρευση του gel έχει ήδη ξεκινήσει από τους 25 o C, ενώ στους 37 o C όλα τα δείγµατα είχαν µετατραπεί σε νευτωνικά ρευστά. Ειδικότερα στις εξαιρετικά όξινες συνθήκες (ph 2.0) παρατηρήθηκε αυξηµένη ευαισθησία και κατά συνέπεια, κατάρρευση του gel του υλικού ακόµα και στη θερµοκρασία δωµατίου. Ιδιαίτερο ενδιαφέρον παρουσιάζει το δείγµα υψηλότερης συγκέντρωσης (25.0% wt ζελατίνη) το οποίο, ενώ παρέµεινε στερεό και αµετάβλητο στους 25 o C, στους 37 o C µετατράπηκε σε ρευστό εξαιρετικά υψηλού ιξώδους. Επιπροσθέτως, η προσθήκη άλατος στα υδατικά διαλύµατα ζελατίνης δε φάνηκε στις περισσότερες περιπτώσεις να βοηθά το σχηµατισµό σταθερότερου gel. Πιο συγκεκριµένα, σε τιµές ph 2.0 χωρίς την προσθήκη άλατος ο σχηµατισµός gel σε δείγµατα 5.0% wt ζελατίνη παρατηρήθηκε ότι απαιτεί τουλάχιστον 2 µέρες σε θερµοκρασία ~20 o C, ενώ µε την προσθήκη άλατος ο αντίστοιχος χρόνος περιορίστηκε σε λίγες µόνο ώρες. Αντίθετη επίδραση της ιονικής ισχύος παρατηρήθηκε σε δείγµατα µε συγκέντρωση ζελατίνης 0.5% wt και ph 8.0, όπου η προσθήκη άλατος φάνηκε να προκαλεί αποσταθεροποίηση του υλικού και αδυναµία στο σχηµατισµό gel. Το τελευταίο συµφωνεί µε τη βιβλιογραφία, όπου αναφέρεται πως η προσθήκη NaCl σε υδατικά διαλύµατα ζελατίνης εµποδίζει την ανάπτυξη δεσµών υδρογόνου και µειώνει την ικανότητα της πρωτεΐνης να σχηµατίσει σταθερή γέλη. Στο σηµείο αυτό παρατίθενται τα αποτελέσµατα µέτρησης µηχανικών ιδιοτήτων (G, G, tanδ) συναρτήσει της θερµοκρασίας, όπως ελήφθησαν από το ρεόµετρο. Στο Σχήµα 4 φαίνονται οι καµπύλες του µέτρου αποθήκευσης (G ) και απώλειας (G ) καθώς και ο λόγος αυτών των δύο µέτρων, ο οποίος εκφράζει το συντελεστή απόσβεσης (tanδ). Αν και η µέτρηση πραγµατοποιήθηκε σε εύρος θερµοκρασίας 5 o C 40 o C στο Σχήµα 4 παρατίθενται θερµοκρασίες µέχρι και ~32 o C οπότε και έχει καταρρεύσει πλήρως το υλικό. Σε υψηλότερες θερµοκρασίες, όπου το υλικό έχει πλέον µετατραπεί σε νευτωνικό ρευστό, χάνεται η στενή επαφή µεταξύ γεωµετρίας και δείγµατος µε αποτέλεσµα την ύπαρξη αυξηµένου θορύβου και τη λήψη τιµών µε υψηλό σφάλµα. Σύµφωνα µε το Σχήµα 4 οι συντελεστές G και G εµφανίζουν πλατό µέχρι τη θερµοκρασία των 22 o C που σηµαίνει ότι το υλικό µέχρι αυτή τη θερµοκρασία έχει την ικανότητα να διατηρεί πλήρως την ακαµψία του και τις ιδιότητες του gel. Μετά το πέρας των 22 o C παρατηρείται σταδιακή µείωση των δύο µέτρων όπως και η τάση τους να αποκτήσουν την ίδια τιµή. Η µείωση αντιστοιχεί στη σταδιακή κατάρρευση του υλικού και τη µετατροπή του σε νευτωνικό υγρό. Το σηµείο όπου το G εξισώνεται µε το G, ή, µε άλλα λόγια όπου το tanδ τείνει να πάρει την τιµή 1, χαρακτηρίζεται ως το σηµείο τήξης της ζελατίνης. Στη συγκεκριµένη περίπτωση το σηµείο τήξης προκύπτει ίσο µε 30.2 o C σε τιµές G =7.02 Pa, G =7.58 Pa και tanδ= G, G (Pa) tanδ 0,1 G' (Pa) G'' (Pa) tan(delta) 1 0, Temperature ( o C) Σχήµα 4: Μέτρηση των συντελεστών G, G και tanδ συναρτήσει της θερµοκρασίας για δείγµα 2.0% wt ζελατίνης και ph=7.86 (33 o C)
6 ΣΥΜΠΕΡΑΣΜΑΤΑ Η ζελατίνη, ή αλλιώς αποικοδοµηµένο κολλαγόνο, αποτελεί ένα ιδιαίτερα ευαίσθητο υλικό σε µεταβολές της θερµοκρασίας και του ph. Σε εξαιρετικά όξινες συνθήκες και πολύ υψηλές θερµοκρασίες παρατηρείται αυξηµένη αποικοδόµηση του υλικού µέσω της καταστροφής της δοµής τριπλής έλικας της πρωτεΐνης. Επιπλέον, ιδιαίτερη ευαισθησία εµφανίζει η ζελατίνη και στη µικροβιακή επιµόλυνση. Για αυτό και η προσθήκη NaN 3 κρίνεται απαραίτητη προκειµένου να επιµηκυνθεί ο χρόνος ζωής των δειγµάτων, ο οποίος χωρίς την ύπαρξη του βιοκτόνου κυµαίνεται µεταξύ ηµερών ακόµα και σε σχετικά χαµηλή θερµοκρασία ~ 4 o C, που αντιστοιχεί σε τυπική θερµοκρασία ψυγείου. Η µικροβιακή επιµόλυνση παρατηρείται ότι ευνοείται και από την ύπαρξη άλατος (NaCl) στα διαλύµατα ζελατίνης, ειδικότερα για συγκεντρώσεις NaCl 0.30Μ και 0.15Μ, καθώς τα βακτήρια αισθάνονται πως βρίσκονται στο φυσικό τους περιβάλλον. Η ικανότητα των διαλυµάτων ζελατίνης να σχηµατίσουν γέλη όπως και η θερµοκρασία όπου συµβαίνει αυξάνονται αυξανόµενης της συγκέντρωσης της ζελατίνης, ενώ παράλληλα µειώνεται ο χρόνος που απαιτείται. Όµως πιθανόν η σταθερή δοµή του συγκεκριµένου βιοϋλικού να αποσταθεροποιείται σε φυσιολογικές συνθήκες θερµοκρασίας, δηλαδή στους 37 o C ακόµα και σε πολύ υψηλές συγκεντρώσεις πρωτεΐνης, 25.0% wt, καθώς κατά τη διάρκεια των πειραµάτων δεν παρατηρήθηκε κάποιος συνδυασµός συνθηκών που να ευνοεί το σχηµατισµό σταθερού gel σε αυτή τη θερµοκρασία. Στο σηµείο αυτό αξίζει να σηµειωθεί ότι αν και η φυσιολογική θερµοκρασία του χόνδρου είναι 33 o C, τα διάφορα πειράµατα διεξάγονται στους 37 o C, καθώς αποτελεί την τυπική θερµοκρασία που αποκτά η άρθρωση κατά την κίνηση ή τη µηχανική καταπόνηση. Σηµειώνεται µάλιστα ότι 40 λεπτά περπάτηµα αρκούν ώστε να προκαλέσει άνοδο της θερµοκρασίας κατά 4 o C (33 o C 37 o C) [7]. Τέλος, επισηµαίνεται ότι η ζελατίνη αποτελεί ένα πλήρως βιοσυµβατό πολυµερές µε αποτέλεσµα την ευρεία χρήση του σε πληθώρα εφαρµογών από τη βιοµηχανία τροφίµων έως τη βιοϊατρική µηχανική. ΒΙΒΛΙΟΓΡΑΦΙΑ [1]. Djabourov, M., Nishinary, K. and Ross-Murphy, S.B., Physical Gels from Biological and Synthetic Polymers. Cambridge: Cambridge University Press. [2]. Gelatin Manufacturers Institute of America (GMIA), Gelatin Handbook. [3]. Djabourov, M. and Papon, P., Influence of thermal treatments on the structure and stability of gelatin gels. Polymer, 24(5), p [4]. Haug, I.J., Draget, K.I and Smidsrød, O., Physical and rheological properties of fish gelatin compared to mammalian gelatin. Food Hydrocolloids, 18, p [5]. Somwangthanaroj, A., Rheology and Polymer Characterization, [pdf]. Available at: < [Accessed 10 March 2015]. [6]. Osteoarthritis (OA), Arthritis Research UK. [online] Available at: < [Accessed 20 November 2014]. [7]. Abdel-Sayed, P., Vogel, A., Moghadam, M.N. and Pioletti, D.P., Cartilage self-heating contributes to chondrogenic expression. European Cells and Materials, 26, p
Στοιχειμετρικοί υπολογισμοί σε διαλύματα
 Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Θρεπτικές ύλες Τρόφιµα - Τροφή
 ΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ 1 Θρεπτικές ύλες Τι καλούµε θρεπτικές ύλες; Ποιες είναι; Τρόφιµα Τι καλούµε τρόφιµο; Χηµεία Τροφίµων Θρεπτικές ύλες Τρόφιµα - Τροφή Προϋπόθεση για να χαρακτηριστεί ένα προϊόν τρόφιµο; 2
ΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ 1 Θρεπτικές ύλες Τι καλούµε θρεπτικές ύλες; Ποιες είναι; Τρόφιµα Τι καλούµε τρόφιµο; Χηµεία Τροφίµων Θρεπτικές ύλες Τρόφιµα - Τροφή Προϋπόθεση για να χαρακτηριστεί ένα προϊόν τρόφιµο; 2
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
ΑΜΥΛΟ Ζελατινοποίηση αμύλου. Άσκηση 4 η Εργαστήριο Χημείας και Τεχνολογίας Τροφίμων
 ΑΜΥΛΟ Ζελατινοποίηση αμύλου Άσκηση 4 η Εργαστήριο Χημείας και Τεχνολογίας Τροφίμων Θεωρητικό μέρος Υδατάνθρακες Άμυλο Ζελατινοποίηση αμύλου Υδατάνθρακες Αποτελούνται από: Άνθρακα (C) Οξυγόνο (O) Υδρογόνο
ΑΜΥΛΟ Ζελατινοποίηση αμύλου Άσκηση 4 η Εργαστήριο Χημείας και Τεχνολογίας Τροφίμων Θεωρητικό μέρος Υδατάνθρακες Άμυλο Ζελατινοποίηση αμύλου Υδατάνθρακες Αποτελούνται από: Άνθρακα (C) Οξυγόνο (O) Υδρογόνο
Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και συνήθως έχει χωρητικότητα από 10 έως 250 ml.
 ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει
ΠΑΝΕΛΛΗΝΙΟΣ ΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑ ΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ
 Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4
![FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4 FeCl 3(aq) + 6NH 4 SCN (aq) (NH 4 ) 3 [Fe(SCN) 6 ] (aq) +3NH 4 Cl (aq) (1) ή FeCl 4](/thumbs/27/9949444.jpg) ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΤΟΜΕΑΣ ΓΕΝΙΚΗΣ ΚΑΙ ΑΝΟΡΓΑΝΗΣ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΤΟΥ ΜΑΘΗΜΑΤΟΣ «ΧΗΜΕΙΑ» για τους ΦΟΙΤΗΤΕΣ του ΤΜΗΜΑΤΟΣ ΦΥΣΙΚΗΣ Οι διδάσκοντες Αικατερίνη
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΤΟΜΕΑΣ ΓΕΝΙΚΗΣ ΚΑΙ ΑΝΟΡΓΑΝΗΣ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ ΤΟΥ ΜΑΘΗΜΑΤΟΣ «ΧΗΜΕΙΑ» για τους ΦΟΙΤΗΤΕΣ του ΤΜΗΜΑΤΟΣ ΦΥΣΙΚΗΣ Οι διδάσκοντες Αικατερίνη
ΘΕΜΑΤΑ ΧΗΜΕΙΑΣ ΤΟΠΙΚΟΥ ΙΑΓΩΝΙΣΜΟΥ EUSO 2009
 ΘΕΜΑΤΑ ΧΗΜΕΙΑΣ ΤΟΠΙΚΟΥ ΙΑΓΩΝΙΣΜΟΥ EUSO 2009 ΘΕΜΑΤΑ Α. Αραίωση ιαλύµατος ΗCl 1M. Παρασκευή 100mL διαλύµατος HCl 0.8Μ. Β. Θερµότητα Αντίδρασης. Υπολογισµός της θερµότητας αντίδρασης στην εξουδετέρωση του
ΘΕΜΑΤΑ ΧΗΜΕΙΑΣ ΤΟΠΙΚΟΥ ΙΑΓΩΝΙΣΜΟΥ EUSO 2009 ΘΕΜΑΤΑ Α. Αραίωση ιαλύµατος ΗCl 1M. Παρασκευή 100mL διαλύµατος HCl 0.8Μ. Β. Θερµότητα Αντίδρασης. Υπολογισµός της θερµότητας αντίδρασης στην εξουδετέρωση του
Σύντομη περιγραφή του πειράματος
 Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
Σύντομη περιγραφή του πειράματος Παρασκευή διαλυμάτων ορισμένης περιεκτικότητας και συγκέντρωσης, καθώς επίσης και παρασκευή διαλυμάτων συγκεκριμένης συγκέντρωσης από διαλύματα μεγαλύτερης συγκέντρωσης
ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ
 ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ εσµός Υδρογόνου 1) Τι ονοµάζεται δεσµός υδρογόνου; εσµός ή γέφυρα υδρογόνου : είναι µια ειδική περίπτωση διαµοριακού δεσµού διπόλου-διπόλου,
ΙΑΜΟΡΙΑΚΕΣ ΥΝΑΜΕΙΣ ΚΑΤΑΣΤΑΣΕΙΣ ΤΗΣ ΥΛΗΣ ΠΡΟΣΘΕΤΙΚΕΣ Ι ΙΟΤΗΤΕΣ εσµός Υδρογόνου 1) Τι ονοµάζεται δεσµός υδρογόνου; εσµός ή γέφυρα υδρογόνου : είναι µια ειδική περίπτωση διαµοριακού δεσµού διπόλου-διπόλου,
Για την επίλυση αυτής της άσκησης, αλλά και όλων των παρόμοιων χρησιμοποιούμε ιδιότητες των αναλογιών (χιαστί)
 ΜΕΘΟΔΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΔΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυμάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούμε ή
ΜΕΘΟΔΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΔΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυμάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούμε ή
Πείραμα 2 Αν αντίθετα, στο δοχείο εισαχθούν 20 mol ΗΙ στους 440 ºC, τότε το ΗΙ διασπάται σύμφωνα με τη χημική εξίσωση: 2ΗΙ(g) H 2 (g) + I 2 (g)
 Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
[ ] [ ] CH3COO [ ] CH COOH. Cοξ. Cαλ
![[ ] [ ] CH3COO [ ] CH COOH. Cοξ. Cαλ [ ] [ ] CH3COO [ ] CH COOH. Cοξ. Cαλ](/thumbs/60/45209718.jpg) Πριν από κάθε απάντηση, προηγείται η καλή ανάγνωση και η προσπάθεια κατανόησης της ερώτησης. Η κάθε απάντηση πρέπει να σχετίζεται µε την ακριβή διατύπωση της ερώτησης και όχι µε την γενική της ιδέα. Κάθε
Πριν από κάθε απάντηση, προηγείται η καλή ανάγνωση και η προσπάθεια κατανόησης της ερώτησης. Η κάθε απάντηση πρέπει να σχετίζεται µε την ακριβή διατύπωση της ερώτησης και όχι µε την γενική της ιδέα. Κάθε
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική)
 ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική) ενέργεια που έχει ένα σώμα. Συμβολίζεται
ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική) ενέργεια που έχει ένα σώμα. Συμβολίζεται
ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ
 ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιμοποιούμενα όργανα Προχοϊδα: Μετράει
ΠΑΝΕΛΛΗΝΙΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΕΥΡΩΠΑΪΚΗΣ ΟΛΥΜΠΙΑΔΑΣ ΕΠΙΣΤΗΜΩΝ - EUSO 2009 ΑΞΙΟΛΟΓΗΣΗ ΜΑΘΗΤΩΝ ΧΗΜΕΙΑ 1. 2. 3. Μαθητές: Σχολείο ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ - ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιμοποιούμενα όργανα Προχοϊδα: Μετράει
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΑΠΟΜΟΝΩΣΗ ΝΟΥΚΛΕΪΚΩΝ ΟΞΕΩΝ (DNA ΚΑΙ RNA AΠΟ ΦΥΤΙΚΑ ΚΥΤΤΑΡΑ) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΑΠΟΜΟΝΩΣΗ ΝΟΥΚΛΕΪΚΩΝ ΟΞΕΩΝ (DNA ΚΑΙ RNA AΠΟ ΦΥΤΙΚΑ ΚΥΤΤΑΡΑ) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
Άσκηση 3η. Μέθοδοι Διαχωρισμού. Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας
 Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
Γεωργική Χημεία Εργαστηριακές ασκήσεις
 Γεωργική Χημεία Εργαστηριακές ασκήσεις Γεώργιος Παπαδόπουλος, Καθηγητής Τμ. Τεχνολόγων Γεωπόνων Τ.Ε. Άρτα, 2015 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
Γεωργική Χημεία Εργαστηριακές ασκήσεις Γεώργιος Παπαδόπουλος, Καθηγητής Τμ. Τεχνολόγων Γεωπόνων Τ.Ε. Άρτα, 2015 Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
Άσκηση 7η. Χημική Ισορροπία. Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών
 Άσκηση 7η Χημική Ισορροπία Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Η έννοια της Χημικής Ισορροπίας Υπάρχουν χηµικές αντιδράσεις που εξελίσσονται προς µία µόνο μόνο κατεύθυνση, όπως π.χ. η σύνθεση
Άσκηση 7η Χημική Ισορροπία Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Η έννοια της Χημικής Ισορροπίας Υπάρχουν χηµικές αντιδράσεις που εξελίσσονται προς µία µόνο μόνο κατεύθυνση, όπως π.χ. η σύνθεση
ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ ΣΤΕΡΕΗΣ ΟΥΣΙΑΣ ΣΤΟ ΝΕΡΟ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ
 ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ ΣΤΕΡΕΗΣ ΟΥΣΙΑΣ ΣΤΟ ΝΕΡΟ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΕΙΣΑΓΩΓΗ ΚΑΙ ΣΤΟΧΟΙ Σε αυτή την εργαστηριακή άσκηση θα ορίσουμε την ταχύτητα διάλυσης μιας στερεής ουσίας στο νερό και θα
ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ ΣΤΕΡΕΗΣ ΟΥΣΙΑΣ ΣΤΟ ΝΕΡΟ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΕΙΣΑΓΩΓΗ ΚΑΙ ΣΤΟΧΟΙ Σε αυτή την εργαστηριακή άσκηση θα ορίσουμε την ταχύτητα διάλυσης μιας στερεής ουσίας στο νερό και θα
ΕΠΕΞΕΡΓΑΣΙΑ ΤΡΟΦΙΜΩΝ
 ΕΠΕΞΕΡΓΑΣΙΑ ΤΡΟΦΙΜΩΝ Συμπύκνωση Τι είναι η συμπύκνωση Είναι η διαδικασία με την οποία απομακρύνουμε μέρος της υγρασίας του τροφίμου, αφήνοντας όμως αρκετή ώστε αυτό να παραμένει ρευστό (> 20-30%). Εφαρμόζεται
ΕΠΕΞΕΡΓΑΣΙΑ ΤΡΟΦΙΜΩΝ Συμπύκνωση Τι είναι η συμπύκνωση Είναι η διαδικασία με την οποία απομακρύνουμε μέρος της υγρασίας του τροφίμου, αφήνοντας όμως αρκετή ώστε αυτό να παραμένει ρευστό (> 20-30%). Εφαρμόζεται
Μέτρηση ph διαλυμάτων καθημερινή χρήσης με την βοήθεια δεικτών και πεχαμετρικού χαρτιού. Μεταβολή του χρώματος των δεικτών
 Μέτρηση ph διαλυμάτων καθημερινή χρήσης με την βοήθεια δεικτών και πεχαμετρικού χαρτιού Η τιμή του ph ενός διαλύματος εξαρτάται από την συγκέντρωση των υδρογονοκατιόντων του [Η+]. Ορίζεται σαν τον αρνητικό
Μέτρηση ph διαλυμάτων καθημερινή χρήσης με την βοήθεια δεικτών και πεχαμετρικού χαρτιού Η τιμή του ph ενός διαλύματος εξαρτάται από την συγκέντρωση των υδρογονοκατιόντων του [Η+]. Ορίζεται σαν τον αρνητικό
Εργαστηριακή άσκηση 4: ΠΑΡΑΣΚΕΥΗ ΙΑΛΥΜΑΤΟΣ ΟΡΙΣΜΕΝΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ - ΑΡΑΙΩΣΗ ΙΑΛΥΜΑΤΩΝ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ Εργαστηριακή άσκηση 4: ΠΑΡΑΣΚΕΥΗ ΙΑΛΥΜΑΤΟΣ ΟΡΙΣΜΕΝΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ - ΑΡΑΙΩΣΗ ΙΑΛΥΜΑΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράµατος αυτού θα πρέπει να µπορείς : 1. Να εφαρµόζεις το ζυγό. 2. Να µετράς
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ Εργαστηριακή άσκηση 4: ΠΑΡΑΣΚΕΥΗ ΙΑΛΥΜΑΤΟΣ ΟΡΙΣΜΕΝΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ - ΑΡΑΙΩΣΗ ΙΑΛΥΜΑΤΩΝ ΣΤΟΧΟΙ Στο τέλος του πειράµατος αυτού θα πρέπει να µπορείς : 1. Να εφαρµόζεις το ζυγό. 2. Να µετράς
Προσδιορισµός βιταµίνης C σε χυµούς φρούτων και λαχανικών και µελέτη διάφορων παραγόντων που επιδρούν στη ποσότητα της
 ΕΚΦΕ Εύβοιας Προσδιορισµός βιταµίνης C σε χυµούς φρούτων και λαχανικών και µελέτη διάφορων παραγόντων που επιδρούν στη ποσότητα της Απαραίτητα όργανα Προχοϊδα Σιφώνι Κωνική φιάλη Απαραίτητα υλικά 10 ml
ΕΚΦΕ Εύβοιας Προσδιορισµός βιταµίνης C σε χυµούς φρούτων και λαχανικών και µελέτη διάφορων παραγόντων που επιδρούν στη ποσότητα της Απαραίτητα όργανα Προχοϊδα Σιφώνι Κωνική φιάλη Απαραίτητα υλικά 10 ml
Αρχές Επεξεργασίας Τροφίμων
 Αρχές Επεξεργασίας Τροφίμων Κατάψυξη τροφίμων Κατάψυξη Απομάκρυνση θερμότητας από ένα προϊόν με αποτέλεσμα την μείωση της θερμοκρασίας του κάτω από το σημείο πήξης. Ως μέθοδος συντήρησης βασίζεται: Στην
Αρχές Επεξεργασίας Τροφίμων Κατάψυξη τροφίμων Κατάψυξη Απομάκρυνση θερμότητας από ένα προϊόν με αποτέλεσμα την μείωση της θερμοκρασίας του κάτω από το σημείο πήξης. Ως μέθοδος συντήρησης βασίζεται: Στην
1 η Εργαστηριακή άσκηση. Παρασκευή Αραίωση. διαλύματος. Δρ. Άρης Γιαννακάς - Ε.ΔΙ.Π.
 1 η Εργαστηριακή άσκηση Παρασκευή Αραίωση διαλύματος 1 Θεωρητικό Μέρος Εισαγωγικές έννοιες Όπως είναι γνωστό η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις)
1 η Εργαστηριακή άσκηση Παρασκευή Αραίωση διαλύματος 1 Θεωρητικό Μέρος Εισαγωγικές έννοιες Όπως είναι γνωστό η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις)
Από πού προέρχεται η θερμότητα που μεταφέρεται από τον αντιστάτη στο περιβάλλον;
 3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
ΤΡΟΦΟΓΝΩΣΙΑ. Υπεύθυνος Καθηγητής: Παπαμιχάλης Αναστάσιος
 ΤΡΟΦΟΓΝΩΣΙΑ Υπεύθυνος Καθηγητής: Παπαμιχάλης Αναστάσιος ΚΑΤΗΓΟΡΙΕΣ ΘΡΕΠΤΙΚΩΝ ΥΛΩΝ Υδατάνθρακες Λίπη Πρωτεΐνες Νερό Ανόργανα συστατικά Βιταμίνες Υπευθ. Καθηγητής: Παπαμιχάλης Αναστάσιος ΥΔΑΤΑΝΘΡΑΚΕΣ Οι
ΤΡΟΦΟΓΝΩΣΙΑ Υπεύθυνος Καθηγητής: Παπαμιχάλης Αναστάσιος ΚΑΤΗΓΟΡΙΕΣ ΘΡΕΠΤΙΚΩΝ ΥΛΩΝ Υδατάνθρακες Λίπη Πρωτεΐνες Νερό Ανόργανα συστατικά Βιταμίνες Υπευθ. Καθηγητής: Παπαμιχάλης Αναστάσιος ΥΔΑΤΑΝΘΡΑΚΕΣ Οι
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα. Χημική Τεχνολογία. Εργαστηριακό Μέρος
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 6: Διαλυμένο Οξυγόνο Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 6: Διαλυμένο Οξυγόνο Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ. Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια.
 ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]
![β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ] β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]](/thumbs/27/10188901.jpg) ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους.
 ΔΙΑΛΥΜΑΤΑ Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους. Διαλύτης: η ουσία που βρίσκεται σε μεγαλύτερη αναλογία
ΔΙΑΛΥΜΑΤΑ Ομογενή μίγματα χημικών ουσιών τα οποία έχουν την ίδια χημική σύσταση και τις ίδιες ιδιότητες (χημικές και φυσικές) σε οποιοδήποτε σημείο τους. Διαλύτης: η ουσία που βρίσκεται σε μεγαλύτερη αναλογία
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΠΕΧΑΜΕΤΡΙΑ
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΠΕΧΑΜΕΤΡΙΑ Ιωάννης Πούλιος Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124 ΘΕΣΣΑΛΟΝΙΚΗ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΠΕΧΑΜΕΤΡΙΑ Ιωάννης Πούλιος Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124 ΘΕΣΣΑΛΟΝΙΚΗ
Πανελλήνιος Μαθητικός Διαγωνισμός για την επιλογή στην 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών - EUSO 2013 Σάββατο 19 Ιανουαρίου 2013 ΧΗΜΕΙΑ
 Πανελλήνιος Μαθητικός Διαγωνισμός για την επιλογή στην 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών - EUSO 2013 Σάββατο 19 Ιανουαρίου 2013 ΧΗΜΕΙΑ Σχολείο: 1) Ονομ/επώνυμα μαθητών: 2)... 3) ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΧΗΜΙΚΗΣ
Πανελλήνιος Μαθητικός Διαγωνισμός για την επιλογή στην 11η Ευρωπαϊκή Ολυμπιάδα Επιστημών - EUSO 2013 Σάββατο 19 Ιανουαρίου 2013 ΧΗΜΕΙΑ Σχολείο: 1) Ονομ/επώνυμα μαθητών: 2)... 3) ΚΙΝΗΤΙΚΗ ΜΕΛΕΤΗ ΧΗΜΙΚΗΣ
Συγκέντρωση διαλύματος
 Συγκέντρωση διαλύματος 22-1. SOS Ερώτηση: τι ονομάζουμε μοριακότητα κατ όγκο ή Molarity (Μολάριτι); Η μοριακότητα κατ' όγκο ή συγκέντρωση ή Molarity, εκφράζει τα mol διαλυμένης ουσίας που περιέχονται σε
Συγκέντρωση διαλύματος 22-1. SOS Ερώτηση: τι ονομάζουμε μοριακότητα κατ όγκο ή Molarity (Μολάριτι); Η μοριακότητα κατ' όγκο ή συγκέντρωση ή Molarity, εκφράζει τα mol διαλυμένης ουσίας που περιέχονται σε
Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
ΘΕΡΜΟΧΗΜΕΙΑ. Είδη ενέργειας ΘΕΡΜΟΔΥΝΑΜΙΚΟΙ ΟΡΙΣΜΟΙ
 ΘΕΡΜΟΧΗΜΕΙΑ Όλες οι χημικές αντιδράσεις περιλαμβάνουν έκλυση ή απορρόφηση ενέργειας υπό μορφή θερμότητας. Η γνώση του ποσού θερμότητας που συνδέεται με μια χημική αντίδραση έχει και πρακτική και θεωρητική
ΘΕΡΜΟΧΗΜΕΙΑ Όλες οι χημικές αντιδράσεις περιλαμβάνουν έκλυση ή απορρόφηση ενέργειας υπό μορφή θερμότητας. Η γνώση του ποσού θερμότητας που συνδέεται με μια χημική αντίδραση έχει και πρακτική και θεωρητική
Άσκηση 3η. Μέθοδοι Διαχωρισμού. Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας
 Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ
 ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
ΦΑΙΝΟΜΕΝΑ ΠΡΟΣΡΟΦΗΣΕΩΣ ΠΡΟΣΡΟΦΗΣΗ ΟΥΣΙΑΣ ΑΠΟ ΔΙΑΛΥΜΑΤΑ Έννοιες που πρέπει να γνωρίζετε Ισορροπία φάσεων, εξίσωση Clauiu-Clapeyron Θέμα ασκήσεως Προσρόφηση ουσίας από αραιά διαλύματα. Προσδιορισμός ισόθερμων
Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου.
 Σύντομη περιγραφή του πειράματος Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού του πειράματος θα πρέπει ο μαθητής: Να περιγράφει τον τρόπο
Σύντομη περιγραφή του πειράματος Παρασκευή σαπουνιού από ελαιόλαδο και υδροξείδιο του νατρίου. Διδακτικοί στόχοι του πειράματος Στο τέλος αυτού του πειράματος θα πρέπει ο μαθητής: Να περιγράφει τον τρόπο
ΗΛΕΚΤΡΟΧΗΜΙΚΕΣ ΜΕΘΟ ΟΙ ΑΝΑΛΥΣΗΣ - ΠΟΤΕΝΣΙΟΜΕΤΡΙΑ
 ΗΛΕΚΤΡΟΧΗΜΙΚΕΣ ΜΕΘΟ ΟΙ ΑΝΑΛΥΣΗΣ - ΠΟΤΕΝΣΙΟΜΕΤΡΙΑ Αρχές Ποτενσιοµετρικής Τιτλοδότησης Η ποτενσιοµετρία περιλαµβάνει τη µέτρηση της ηλεκτρεγερτικής δύναµης (Η.Ε..) µεταξύ δύο ηλεκτροδίων, του ενδεικτικού
ΗΛΕΚΤΡΟΧΗΜΙΚΕΣ ΜΕΘΟ ΟΙ ΑΝΑΛΥΣΗΣ - ΠΟΤΕΝΣΙΟΜΕΤΡΙΑ Αρχές Ποτενσιοµετρικής Τιτλοδότησης Η ποτενσιοµετρία περιλαµβάνει τη µέτρηση της ηλεκτρεγερτικής δύναµης (Η.Ε..) µεταξύ δύο ηλεκτροδίων, του ενδεικτικού
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2013
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 14 Απριλίου 01 ιάρκεια Εξέτασης: ώρες ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθµό
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Κυριακή 14 Απριλίου 01 ιάρκεια Εξέτασης: ώρες ΕΚΦΩΝΗΣΕΙΣ Για τις ερωτήσεις Α1 έως και Α4 να γράψετε στο τετράδιό σας τον αριθµό
3. Όταν χλωριούχο νάτριο πυρωθεί στο λύχνο Bunsen, η φλόγα θα πάρει χρώμα: Α. Κόκκινο Β. Κίτρινο Γ. Μπλε Δ. Πράσινο Ε. Ιώδες
 Το εξεταστικό δοκίμιο αποτελείται από οκτώ (8) σελίδες Ερωτήσεις 1-22: Για κάθε μια από τις ερωτήσεις που ακολουθούν δίνονται πέντε πιθανές απαντήσεις. Να επιλέξετε την ορθή απάντηση. Για κάθε ερώτηση
Το εξεταστικό δοκίμιο αποτελείται από οκτώ (8) σελίδες Ερωτήσεις 1-22: Για κάθε μια από τις ερωτήσεις που ακολουθούν δίνονται πέντε πιθανές απαντήσεις. Να επιλέξετε την ορθή απάντηση. Για κάθε ερώτηση
ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ. + SO 4 Βάσεις είναι οι ενώσεις που όταν διαλύονται σε νερό δίνουν ανιόντα υδροξειδίου (ΟΗ - ). NaOH Na
 ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ ΙΔΙΟΤΗΤΕΣ ΟΞΕΩΝ Αλλάζουν το χρώμα των δεικτών. Αντιδρούν με μέταλλα και παράγουν αέριο υδρογόνο (δες απλή αντικατάσταση) Αντιδρούν με ανθρακικά άλατα και παράγουν αέριο CO2. Έχουν όξινη
ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ ΙΔΙΟΤΗΤΕΣ ΟΞΕΩΝ Αλλάζουν το χρώμα των δεικτών. Αντιδρούν με μέταλλα και παράγουν αέριο υδρογόνο (δες απλή αντικατάσταση) Αντιδρούν με ανθρακικά άλατα και παράγουν αέριο CO2. Έχουν όξινη
Άσκηση 2η. Παρασκευή Αραίωση διαλύματος
 Άσκηση 2η Παρασκευή Αραίωση διαλύματος 2 Θεωρητικό μέρος Η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις) Τα μίγματα (δύο ή περισσότερες καθαρές ουσίες) Τα μίγματα
Άσκηση 2η Παρασκευή Αραίωση διαλύματος 2 Θεωρητικό μέρος Η ύλη διαχωρίζεται σε δύο βασικές κατηγορίες: Τις καθαρές ουσίες (στοιχεία, χημικές ενώσεις) Τα μίγματα (δύο ή περισσότερες καθαρές ουσίες) Τα μίγματα
Σύντομη περιγραφή του πειράματος
 Σύντομη περιγραφή του πειράματος Παρασκευή νάυλον 6-10 από το διχλωρίδιο του δεκανοδιικού οξέος και την εξαμεθυλενοδιαμίνη. Σύγκριση του νάυλον με φυσικές υφάνσιμες ίνες όπως το μαλλί και το βαμβάκι. Διδακτικοί
Σύντομη περιγραφή του πειράματος Παρασκευή νάυλον 6-10 από το διχλωρίδιο του δεκανοδιικού οξέος και την εξαμεθυλενοδιαμίνη. Σύγκριση του νάυλον με φυσικές υφάνσιμες ίνες όπως το μαλλί και το βαμβάκι. Διδακτικοί
ΤΙΤΛΟΔΟΤΗΣΗ ΟΞΕΩΝ ΚΑΙ ΒΑΣΕΩΝ
 ΤΙΤΛΟΔΟΤΗΣΗ ΟΞΕΩΝ ΚΑΙ ΒΑΣΕΩΝ Σκοπός Εργαστηριακής Άσκησης Η εξοικείωση με τις τεχνικές τιτλοδότησης και η κατανόηση των ογκομετρικών μεθόδων ανάλυσης. Θεωρητικό Μέρος Πάρα πολύ συχνά προκύπτει η ανάγκη
ΤΙΤΛΟΔΟΤΗΣΗ ΟΞΕΩΝ ΚΑΙ ΒΑΣΕΩΝ Σκοπός Εργαστηριακής Άσκησης Η εξοικείωση με τις τεχνικές τιτλοδότησης και η κατανόηση των ογκομετρικών μεθόδων ανάλυσης. Θεωρητικό Μέρος Πάρα πολύ συχνά προκύπτει η ανάγκη
Διάλυμα καλείται κάθε ομογενές σύστημα, το οποίο αποτελείται από δύο ή περισσότερες χημικές ουσίες, και έχει την ίδια σύσταση σε όλη του τη μάζα.
 1. ΔΙΑΛΥΜΑ Διάλυμα καλείται κάθε ομογενές σύστημα, το οποίο αποτελείται από δύο ή περισσότερες χημικές ουσίες, και έχει την ίδια σύσταση σε όλη του τη μάζα. Ετερογενές σύστημα καλείται αυτό, το οποίο αποτελείται
1. ΔΙΑΛΥΜΑ Διάλυμα καλείται κάθε ομογενές σύστημα, το οποίο αποτελείται από δύο ή περισσότερες χημικές ουσίες, και έχει την ίδια σύσταση σε όλη του τη μάζα. Ετερογενές σύστημα καλείται αυτό, το οποίο αποτελείται
Συζητείστε και περιγράψτε την πορεία ενός πειράµατος για να ελέγξετε αν οι προβλέψεις σας είναι σωστές:
 Η Εξουδετέρωση: 1 ο φύλλο εργασίας Όνοµα:..Τµήµα.. Στόχοι: Να διαπιστώνετε τον όξινο ή βασικό χαρακτήρα ενός διαλύµατος κατά την ανάµιξη δ/τος οξέος µε δ/µα βάσης χρησιµοποιώντας δείκτη και πεχάµετρο.
Η Εξουδετέρωση: 1 ο φύλλο εργασίας Όνοµα:..Τµήµα.. Στόχοι: Να διαπιστώνετε τον όξινο ή βασικό χαρακτήρα ενός διαλύµατος κατά την ανάµιξη δ/τος οξέος µε δ/µα βάσης χρησιµοποιώντας δείκτη και πεχάµετρο.
ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΤΡΙΤΗ 1 ΙΟΥΝΙΟΥ 2004
 ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Γ ΤΑΞΗΣ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΤΡΙΤΗ 1 ΙΟΥΝΙΟΥ 2004 ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1 και 1.2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Γ ΤΑΞΗΣ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΤΡΙΤΗ 1 ΙΟΥΝΙΟΥ 2004 ΘΕΜΑ 1ο Για τις ερωτήσεις 1.1 και 1.2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
1.Εισαγωγή. 2.Επιλεκτικά ηλεκτρόδια ιόντων(εηι)
 ΑΜΕΣΗ ΜΕΤΡΗΣΗ ΙΟΝΤΩΝ Κ + ΣΤΟ ΠΟΣΙΜΟ ΝΕΡΟ ΜΕ ΕΠΙΛΕΚΤΙΚΟ ΗΛΕΚΤΡΟΔΙΟ 1.Εισαγωγή Χημικοί αισθητήρες είναι όργανα τα οποία μπορούν να παρακολουθούν την ενεργότητα φορτισμένων ή μη ουσιών σε υγρή ή αέρια φάση.
ΑΜΕΣΗ ΜΕΤΡΗΣΗ ΙΟΝΤΩΝ Κ + ΣΤΟ ΠΟΣΙΜΟ ΝΕΡΟ ΜΕ ΕΠΙΛΕΚΤΙΚΟ ΗΛΕΚΤΡΟΔΙΟ 1.Εισαγωγή Χημικοί αισθητήρες είναι όργανα τα οποία μπορούν να παρακολουθούν την ενεργότητα φορτισμένων ή μη ουσιών σε υγρή ή αέρια φάση.
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ. 9 - Δεκεμβρίου
 1 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ 9 - Δεκεμβρίου - 2017 2 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ..... 1 η Δραστηριότητα Παρασκευή δυο υδατικών διαλυμάτων ΝaCl με
1 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ 9 - Δεκεμβρίου - 2017 2 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ..... 1 η Δραστηριότητα Παρασκευή δυο υδατικών διαλυμάτων ΝaCl με
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 2002
 ΘΕΜΑ 1 ο ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 00 Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Ισχυρότερες
ΘΕΜΑ 1 ο ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ 00 Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Ισχυρότερες
Ανθεκτικότητα Υλικών και Περιβάλλον
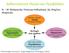 Ανθεκτικότητα Υλικών και Περιβάλλον Ν. Μ. Μπάρκουλα, Επίκουρη Καθηγήτρια, Δρ. Μηχ/γος Μηχανικός 1 Τι είναι: Περίγραμμα Μαθήματος Επιλογής Μάθημα Επιλογής στο 9ο Εξάμηνο του ΤΜΕΥ Με τι ασχολείται: Με την
Ανθεκτικότητα Υλικών και Περιβάλλον Ν. Μ. Μπάρκουλα, Επίκουρη Καθηγήτρια, Δρ. Μηχ/γος Μηχανικός 1 Τι είναι: Περίγραμμα Μαθήματος Επιλογής Μάθημα Επιλογής στο 9ο Εξάμηνο του ΤΜΕΥ Με τι ασχολείται: Με την
Όγδοη Διάλεξη Οξέα - Βάσεις - Άλατα
 Όγδοη Διάλεξη Οξέα - Βάσεις - Άλατα Οξέα Είναι οι χημικές ενώσεις οι οποίες όταν διαλυθούν στο νερό, ελευθερώνουν κατιόντα υδρογόνου (Η + ) Ιδιότητες Οξέων 1. Έχουν όξινη γεύση. 2. Επιδρούν με τον ίδιο
Όγδοη Διάλεξη Οξέα - Βάσεις - Άλατα Οξέα Είναι οι χημικές ενώσεις οι οποίες όταν διαλυθούν στο νερό, ελευθερώνουν κατιόντα υδρογόνου (Η + ) Ιδιότητες Οξέων 1. Έχουν όξινη γεύση. 2. Επιδρούν με τον ίδιο
ΑΠΑΝΤΗΣΕΙΣ. Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Το συζυγές οξύ της ΝΗ 3 είναι: α. ΝΗ 2 - β.νa
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Το συζυγές οξύ της ΝΗ 3 είναι: α. ΝΗ 2 - β.νa
ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Β ΛΥΚΕΙΟΥ 2002
 ΘΕΜΑ 1ο ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Β ΛΥΚΕΙΟΥ 00 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Ισχυρότερες
ΘΕΜΑ 1ο ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ Β ΛΥΚΕΙΟΥ 00 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις 1.1-1.4, να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1.1 Ισχυρότερες
Στόχοι της εργαστηριακής άσκησης
 ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2013-2014 Τοπικός διαγωνισμός στη Χημεία Ονόματα των μαθητών της ομάδας: 1) 2) 3) Στόχοι της εργαστηριακής
ΕΡΓΑΣΤΗΡΙΑΚΑ ΚΕΝΤΡΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΑΝΑΤΟΛΙΚΗΣ ΑΤΤΙΚΗΣ Ευρωπαϊκή Ολυμπιάδα Φυσικών Επιστημών 2013-2014 Τοπικός διαγωνισμός στη Χημεία Ονόματα των μαθητών της ομάδας: 1) 2) 3) Στόχοι της εργαστηριακής
β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]
![β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ] β. [Η 3 Ο + ] > 10-7 Μ γ. [ΟΗ _ ] < [Η 3 Ο + ]](/thumbs/92/111021029.jpg) ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1ο Στις προτάσεις
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 6 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1ο Στις προτάσεις
1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ
 1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ ΗΛΙΑΣ ΝΟΛΗΣ-ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΘΕΟΔΩΡΟΣ 2012 Διαλύματα Διάλυμα ονομάζεται κάθε ομογενές μείγμα δύο ή περισσοτέρων συστατικών. Κάθε
1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ ΗΛΙΑΣ ΝΟΛΗΣ-ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΘΕΟΔΩΡΟΣ 2012 Διαλύματα Διάλυμα ονομάζεται κάθε ομογενές μείγμα δύο ή περισσοτέρων συστατικών. Κάθε
Άσκηση 1 : Μικροβιακή κινητική (Τρόποι μέτρησης βιοκαταλυτών)
 ΤΜΗΜΑ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Καθηγητής Βασίλης Σπηλιώτης Εργαστήριο Βιομηχανικής Μικροβιολογίας Άσκηση : Μικροβιακή κινητική (Τρόποι μέτρησης βιοκαταλυτών) Σκοπός Άσκησης Σκοπός της άσκησης αυτής, είναι
ΤΜΗΜΑ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Καθηγητής Βασίλης Σπηλιώτης Εργαστήριο Βιομηχανικής Μικροβιολογίας Άσκηση : Μικροβιακή κινητική (Τρόποι μέτρησης βιοκαταλυτών) Σκοπός Άσκησης Σκοπός της άσκησης αυτής, είναι
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 04 Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 3 Απριλίου 04 ιάρκεια Εξέτασης: 3 ώρες ΑΠΑΝΤΗΣΕΙΣ Ε_3.ΧλΘ(α) Α. γ Α. γ Α3. δ Α4. β Α5. α) Πρόκειται
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 04 Β ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 3 Απριλίου 04 ιάρκεια Εξέτασης: 3 ώρες ΑΠΑΝΤΗΣΕΙΣ Ε_3.ΧλΘ(α) Α. γ Α. γ Α3. δ Α4. β Α5. α) Πρόκειται
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας
 Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
Προσδιορισμός της Γραμμομοριακής Μάζας ουσίας με την μέθοδο της Κρυοσκοπίας ΙΣΟΡΡΟΠΙΑΙ ΙΔΑΝΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΜΕΘ ΕΤΕΡΑΣ ΦΑΣΕΩΣ ΕΚ ΚΑΘΑΡΟΥ ΔΙΑΛΥΤΟΥ Προσδιορισμός μοριακού βάρους κρυοσκοπικώς Γραμμομοριακή
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
ΘΕΡΜΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ
 ΘΕΡΜΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ ΓENIKA Θερµική κατεργασία είναι σύνολο διεργασιών που περιλαµβάνει τη θέρµανση και ψύξη µεταλλικού προϊόντος σε στερεά κατάσταση και σε καθορισµένες θερµοκρασιακές και χρονικές συνθήκες.
ΘΕΡΜΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ ΓENIKA Θερµική κατεργασία είναι σύνολο διεργασιών που περιλαµβάνει τη θέρµανση και ψύξη µεταλλικού προϊόντος σε στερεά κατάσταση και σε καθορισµένες θερµοκρασιακές και χρονικές συνθήκες.
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Πεχαμετρία Προσδιορισμός των σταθερών διάστασης μονοπρωτικών και πολυπρωτικών οξέων από μετρήσεις ph
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Πεχαμετρία Προσδιορισμός των σταθερών διάστασης μονοπρωτικών και πολυπρωτικών οξέων από μετρήσεις ph Ιωάννης Πούλιος ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Πεχαμετρία Προσδιορισμός των σταθερών διάστασης μονοπρωτικών και πολυπρωτικών οξέων από μετρήσεις ph Ιωάννης Πούλιος ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 15: Διαλύματα
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ÔÏÕËÁ ÓÁÑÑÇ ÊÏÌÏÔÇÍÇ
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗ (1ος Κύκλος) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 16 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗ (1ος Κύκλος) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 16 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε
Έλεγχοι. Τη συγκέντρωση του φαρμάκου σε δείγμα ιστού ή βιολογικού υγρού
 Έλεγχοι Τη συγκέντρωση του φαρμάκου σε δείγμα ιστού ή βιολογικού υγρού Το ρυθμό απελευθέρωσης του φαρμάκου από το σκεύασμα Έλεγχο ταυτότητας και καθαρότητας της πρώτης ύλης και των εκδόχων( βάση προδιαγραφών)
Έλεγχοι Τη συγκέντρωση του φαρμάκου σε δείγμα ιστού ή βιολογικού υγρού Το ρυθμό απελευθέρωσης του φαρμάκου από το σκεύασμα Έλεγχο ταυτότητας και καθαρότητας της πρώτης ύλης και των εκδόχων( βάση προδιαγραφών)
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ. Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και µπορεί να έχει χωρητικότητα από 10 έως 250 ml.
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ-ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και µπορεί να έχει χωρητικότητα από 10 έως 250
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ-ΠΡΟΑΠΑΙΤΟΥΜΕΝΕΣ ΓΝΩΣΕΙΣ 1. Χρησιµοποιούµενα όργανα Προχοϊδα: Μετράει τον όγκο ενός υγρού (ή διαλύµατος) µε ακρίβεια 0,1 ml και µπορεί να έχει χωρητικότητα από 10 έως 250
2). i = n i - n i - n i (2) 9-2
 ΕΠΙΦΑΝΕΙΑΚΗ ΤΑΣΗ ΙΑΛΥΜΑΤΩΝ Έννοιες που πρέπει να γνωρίζετε: Εξίσωση Gbbs-Duhem, χηµικό δυναµικό συστατικού διαλύµατος Θέµα ασκήσεως: Μελέτη της εξάρτησης της επιφανειακής τάσης διαλυµάτων από την συγκέντρωση,
ΕΠΙΦΑΝΕΙΑΚΗ ΤΑΣΗ ΙΑΛΥΜΑΤΩΝ Έννοιες που πρέπει να γνωρίζετε: Εξίσωση Gbbs-Duhem, χηµικό δυναµικό συστατικού διαλύµατος Θέµα ασκήσεως: Μελέτη της εξάρτησης της επιφανειακής τάσης διαλυµάτων από την συγκέντρωση,
Βασικές Διεργασίες Μηχανικής Τροφίμων
 Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
Βασικές Διεργασίες Μηχανικής Τροφίμων Ενότητα 8: Εκχύλιση, 1ΔΩ Τμήμα: Επιστήμης Τροφίμων και Διατροφής Του Ανθρώπου Σταύρος Π. Γιαννιώτης, Καθηγητής Μηχανικής Τροφίμων Μαθησιακοί Στόχοι Τύποι εκχύλισης
ΜΕΡΟΣ Α : Ερωτήσεις 1-6 Να απαντήσετε σε όλες τις ερωτήσεις 1-6. Κάθε ορθή απάντηση βαθμολογείται με πέντε (5) μονάδες.
 ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2008-2009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΔΕΙΓΜΑΤΙΚΟ ΕΞΕΤΑΣΤΙΚΟ ΔΟΚΙΜΙΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΤΑΞΗ: Β ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΧΡΟΝΟΣ: 2 ώρες και 30 λεπτά Το εξεταστικό δοκίμιο αποτελείται από
ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2008-2009 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΔΕΙΓΜΑΤΙΚΟ ΕΞΕΤΑΣΤΙΚΟ ΔΟΚΙΜΙΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΤΑΞΗ: Β ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΚΑΤΕΥΘΥΝΣΗΣ ΧΡΟΝΟΣ: 2 ώρες και 30 λεπτά Το εξεταστικό δοκίμιο αποτελείται από
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ
 Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
Μηχανική και Ανάπτυξη Διεργασιών 7ο Εξάμηνο, Σχολή Χημικών Μηχανικών ΕΜΠ ΥΓΡΗ ΕΚΧΥΛΙΣΗ Η υγρή εκχύλιση βρίσκει εφαρμογή όταν. Η σχετική πτητικότητα των συστατικών του αρχικού διαλύματος είναι κοντά στη
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Β ΤΑΞΗ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 25 ΜΑΪΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1 ο Στις ερωτήσεις 1.1-1.4, να γράψετε στο
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Β ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΣΑΒΒΑΤΟ 25 ΜΑΪΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΕΞΙ (6) ΘΕΜΑ 1 ο Στις ερωτήσεις 1.1-1.4, να γράψετε στο
ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ
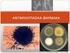 ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ Προσοµοίωση Είναι γνωστό ότι η εξάσκηση των φοιτητών σε επίπεδο εργαστηριακών ασκήσεων, µε χρήση των κατάλληλων πειραµατοζώων, οργάνων και αναλωσίµων
ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ Προσοµοίωση Είναι γνωστό ότι η εξάσκηση των φοιτητών σε επίπεδο εργαστηριακών ασκήσεων, µε χρήση των κατάλληλων πειραµατοζώων, οργάνων και αναλωσίµων
Παράγοντες που εξηγούν τη διαλυτότητα. Είδη διαλυμάτων
 Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
19ο Μάθημα ΔΙΑΛΥΜΑΤΑ
 19ο Μάθημα ΔΙΑΛΥΜΑΤΑ Μια σπουδαία ικανότητα του νερού, η διαλυτική Ξέρουμε ότι το νερό κάνει έναν κύκλο στη φύση. Εξατμίζεται, γίνεται σύννεφο και πέφτει στη γη ως βροχή. Ένα μεγάλο μέρος από το βρόχινο
19ο Μάθημα ΔΙΑΛΥΜΑΤΑ Μια σπουδαία ικανότητα του νερού, η διαλυτική Ξέρουμε ότι το νερό κάνει έναν κύκλο στη φύση. Εξατμίζεται, γίνεται σύννεφο και πέφτει στη γη ως βροχή. Ένα μεγάλο μέρος από το βρόχινο
ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ
 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ ΘΕΜΑ Α Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το ιόν 56 Fe +2 περιέχει:
ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ ΘΕΜΑ Α Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το ιόν 56 Fe +2 περιέχει:
ΝΕΟ ΥΒΡΙΔΙΚΟ ΒΙΟΫΛΙΚΟ ΒΙΟΠΟΛΥΜΕΡΩΝ ΕΝΙΣΧΥΜΕΝΩΝ ΜΕ ΝΑΝΟΣΩΜΑΤΙΔΙΑ ΑΡΓΥΡΟΥ ΚΑΙ Η ΧΡΗΣΗ ΤΟΥ ΣΤΗΝ ΒΙΟΪΑΤΡΙΚΗ ΜΗΧΑΝΙΚΗ
 ο ΠΑΝΕΛΛΗΝΙΟ ΕΠΙΣΤΗΜΟΝΙΚΟ ΣΥΝΕΔΡΙΟ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ, ΠΑΤΡΑ, 4-6 ΙΟΥΝΙΟΥ, 5. ΝΕΟ ΥΒΡΙΔΙΚΟ ΒΙΟΫΛΙΚΟ ΒΙΟΠΟΛΥΜΕΡΩΝ ΕΝΙΣΧΥΜΕΝΩΝ ΜΕ ΝΑΝΟΣΩΜΑΤΙΔΙΑ ΑΡΓΥΡΟΥ ΚΑΙ Η ΧΡΗΣΗ ΤΟΥ ΣΤΗΝ ΒΙΟΪΑΤΡΙΚΗ ΜΗΧΑΝΙΚΗ Σπαθής Ά.,
ο ΠΑΝΕΛΛΗΝΙΟ ΕΠΙΣΤΗΜΟΝΙΚΟ ΣΥΝΕΔΡΙΟ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ, ΠΑΤΡΑ, 4-6 ΙΟΥΝΙΟΥ, 5. ΝΕΟ ΥΒΡΙΔΙΚΟ ΒΙΟΫΛΙΚΟ ΒΙΟΠΟΛΥΜΕΡΩΝ ΕΝΙΣΧΥΜΕΝΩΝ ΜΕ ΝΑΝΟΣΩΜΑΤΙΔΙΑ ΑΡΓΥΡΟΥ ΚΑΙ Η ΧΡΗΣΗ ΤΟΥ ΣΤΗΝ ΒΙΟΪΑΤΡΙΚΗ ΜΗΧΑΝΙΚΗ Σπαθής Ά.,
2.3 Περιεκτικότητα διαλύματος Εκφράσεις περιεκτικότητας
 1 Η θεωρία του μαθήματος με ερωτήσεις. 2.3 Περιεκτικότητα διαλύματος Εκφράσεις περιεκτικότητας Ερωτήσεις θεωρίας με απάντηση 3-1. Τι ονομάζεται περιεκτικότητα ενός διαλύματος; Είναι μία έκφραση που δείχνει
1 Η θεωρία του μαθήματος με ερωτήσεις. 2.3 Περιεκτικότητα διαλύματος Εκφράσεις περιεκτικότητας Ερωτήσεις θεωρίας με απάντηση 3-1. Τι ονομάζεται περιεκτικότητα ενός διαλύματος; Είναι μία έκφραση που δείχνει
Βαθμός ιοντισμού. Για ισχυρούς ηλεκτρολύτες ισχύει α = 1. Για ασθενής ηλεκτρολύτες ισχύει 0 < α < 1.
 Βαθμός ιοντισμού Ο ιοντισμός μιας ομοιοπολικής ένωσης στο νερό μπορεί να είναι πλήρης ή μερικώς. Ένα μέτρο έκφρασης της ισχύος των ηλεκτρολυτών, κάτω από ορισμένες συνθήκες είναι ο βαθμός ιοντισμού (α).
Βαθμός ιοντισμού Ο ιοντισμός μιας ομοιοπολικής ένωσης στο νερό μπορεί να είναι πλήρης ή μερικώς. Ένα μέτρο έκφρασης της ισχύος των ηλεκτρολυτών, κάτω από ορισμένες συνθήκες είναι ο βαθμός ιοντισμού (α).
ΕΚΦΩΝΗΣΕΙΣ. Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση.
 1 ΘΕΜΑ 1 Ο ΕΚΦΩΝΗΣΕΙΣ A ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1) Το άτοµο του καλίου (Κ) έχει µαζικό
1 ΘΕΜΑ 1 Ο ΕΚΦΩΝΗΣΕΙΣ A ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1) Το άτοµο του καλίου (Κ) έχει µαζικό
1.2. Να γράψετε στο τετράδιό σας την παρακάτω πρόταση. Από τα παρακάτω ζεύγη ουσιών ρυθµιστικό διάλυµα είναι το α. HF / NaF.
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 10 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΕΥΤΕΡΑ 10 ΙΟΥΝΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ
ΜΕΘΟ ΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΙΑΛΥΜΑΤΑ
 ΜΕΘΟ ΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυµάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούµε ή να
ΜΕΘΟ ΟΛΟΓΙΑ ΓΙΑ ΤΗΝ ΕΠΙΛΥΣΗ ΑΣΚΗΣΕΩΝ ΠΟΥ ΑΦΟΡΟΥΝ ΙΑΛΥΜΑΤΑ Οι ασκήσεις διαλυµάτων που αφορούν τις περιεκτικότητες % w/w, % w/v και % v/v χωρίζονται σε 3 κατηγορίες: α) Ασκήσεις όπου πρέπει να βρούµε ή να
ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική)
 ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική) ενέργεια που έχει ένα σώμα. Συμβολίζεται
ΘΕΡΜΙΔΟΜΕΤΡΙΑ ΘΕΡΜΟΤΗΤΑ Πρόκειται για τρόπο μεταφοράς ενέργειας από ένα σώμα σε ένα άλλο λόγω διαφοράς θερμοκρασίας. Είναι διαφορετική από την εσωτερική (θερμική) ενέργεια που έχει ένα σώμα. Συμβολίζεται
ΑΣΚΗΣΗ 4η. Προσδιορίζεται ως η ικανότητα εξουδετέρωσης βάσεων
 ΑΣΚΗΣΗ 4η Οξύτητα (Acidity) Θεωρητικό υπόβαθρο Προσδιορίζεται ως η ικανότητα εξουδετέρωσης βάσεων Εκφράζει την ποσοτική ικανότητα του νερού στην εξουδετέρωση ισχυρής βάσεως µέχρι επιθυµητής τιµής ph Οφείλεται
ΑΣΚΗΣΗ 4η Οξύτητα (Acidity) Θεωρητικό υπόβαθρο Προσδιορίζεται ως η ικανότητα εξουδετέρωσης βάσεων Εκφράζει την ποσοτική ικανότητα του νερού στην εξουδετέρωση ισχυρής βάσεως µέχρι επιθυµητής τιµής ph Οφείλεται
AΝΑΛΟΓΙΑ ΜΑΖΩΝ ΣΤΟΧΕΙΩΝ ΧΗΜΙΚΗΣ ΕΝΩΣΗΣ
 2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
2 ο Γυμνάσιο Καματερού 1 ΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΗΣ ΥΛΗΣ 1. Πόσα γραμμάρια είναι: ι) 0,2 kg, ii) 5,1 kg, iii) 150 mg, iv) 45 mg, v) 0,1 t, vi) 1,2 t; 2. Πόσα λίτρα είναι: i) 0,02 m 3, ii) 15 m 3, iii) 12cm
Γ' ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΕΚΦΩΝΗΣΕΙΣ
 Γ' ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ ο ΕΚΦΩΝΗΣΕΙΣ.. Υδατικό διάλυµα οξέος ΗΑ συγκέντρωσης 0, Μ έχει pη = στους 5 C, Αν το διάλυµα ΗΑ αραιωθεί σε δεκαπλάσιο όγκο το pη του θα είναι
Γ' ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ ο ΕΚΦΩΝΗΣΕΙΣ.. Υδατικό διάλυµα οξέος ΗΑ συγκέντρωσης 0, Μ έχει pη = στους 5 C, Αν το διάλυµα ΗΑ αραιωθεί σε δεκαπλάσιο όγκο το pη του θα είναι
6η Εργαστηριακή Άσκηση Μέτρηση διηλεκτρικής σταθεράς σε κύκλωµα RLC
 6η Εργαστηριακή Άσκηση Μέτρηση διηλεκτρικής σταθεράς σε κύκλωµα RLC Θεωρητικό µέρος Αν µεταξύ δύο αρχικά αφόρτιστων αγωγών εφαρµοστεί µία συνεχής διαφορά δυναµικού ή τάση V, τότε στις επιφάνειές τους θα
6η Εργαστηριακή Άσκηση Μέτρηση διηλεκτρικής σταθεράς σε κύκλωµα RLC Θεωρητικό µέρος Αν µεταξύ δύο αρχικά αφόρτιστων αγωγών εφαρµοστεί µία συνεχής διαφορά δυναµικού ή τάση V, τότε στις επιφάνειές τους θα
Απομόνωση ανθρώπινου DNA γονιδιώματος & ποιοτικός και ποσοτικός προσδιορισμός
 Απομόνωση ανθρώπινου DNA γονιδιώματος & ποιοτικός και ποσοτικός προσδιορισμός Ευαγγελία - Ειρήνη Τσερμπίνι 1. Σκοπός Σκοπός της παρούσας άσκησης είναι η απομόνωση ανθρώπινου DNA γονιδιώματος από δείγμα
Απομόνωση ανθρώπινου DNA γονιδιώματος & ποιοτικός και ποσοτικός προσδιορισμός Ευαγγελία - Ειρήνη Τσερμπίνι 1. Σκοπός Σκοπός της παρούσας άσκησης είναι η απομόνωση ανθρώπινου DNA γονιδιώματος από δείγμα
Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ
 Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ Ονόματα διαγωνιζομένων: 1) 2) 3) Σχολείο: Όνομα Υπεύθυνου Καθηγητή: 1 η ΠΕΙΡΑΜΑΤΙΚΗ ΔΡΑΣΤΗΡΙΟΤΗΤΑ
Ε.Κ.Φ.Ε. ΔΙ.Δ.Ε Α ΑΘΗΝΑΣ ΕΥΡΩΠΑΪΚΗ ΟΛΥΜΠΙΑΔΑ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ 2016 ΠΡΟΚΑΤΑΡΚΤΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ ΣΤΗ ΧΗΜΕΙΑ Ονόματα διαγωνιζομένων: 1) 2) 3) Σχολείο: Όνομα Υπεύθυνου Καθηγητή: 1 η ΠΕΙΡΑΜΑΤΙΚΗ ΔΡΑΣΤΗΡΙΟΤΗΤΑ
