ΑΝΔΡΕΑΣ Χ. ΣΕΡΓΙΔΗΣ Φαρμακοποιός
|
|
|
- Μύρων Δελή
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΤΕΧΝΟΛΟΓΙΑΣ Μεταπτυχιακή Διατριβή Μελέτη των παραμέτρων της σύνθεσης υβριδικών κολλοειδών νανοκρυστάλλων με υπερπαραμαγνητικές ιδιότητες για την ανάπτυξη πολυλειτουργικών Συστημάτων Ελεγχόμενης Χορήγησης αντικαρκινικών ουσιών Για την απόκτηση του Μεταπτυχιακού Διπλώματος Ειδίκευσης στην κατεύθυνση «Βιομηχανική Φαρμακευτική - Φαρμακευτική Ανάλυση» ΑΝΔΡΕΑΣ Χ. ΣΕΡΓΙΔΗΣ Φαρμακοποιός Επιβέπων Καθηγητής: Δρ. Κωνσταντίνος Αυγουστάκης Σε συνεργασία με: Δρ. Αριστείδη Μπακανδρίτσο Πάτρα, Δεκέμβιος 2014
2
3 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΤΕΧΝΟΛΟΓΙΑΣ Μεταπτυχιακή Διατριβή Μελέτη των παραμέτρων της σύνθεσης υβριδικών κολλοειδών νανοκρυστάλλων με υπερπαραμαγνητικές ιδιότητες για την ανάπτυξη πολυλειτουργικών Συστημάτων Ελεγχόμενης Χορήγησης αντικαρκινικών ουσιών Για την απόκτηση του Μεταπτυχιακού Διπλώματος Ειδίκευσης στην κατεύθυνση «Βιομηχανική Φαρμακευτική - Φαρμακευτική Ανάλυση» ΑΝΔΡΕΑΣ Χ. ΣΕΡΓΙΔΗΣ Α.Μ:452 Φαρμακοποιός Επιβέπων Καθηγητής: Δρ. Κωνσταντίνος Αυγουστάκης Σε συνεργασία με: Δρ. Αριστείδη Μπακανδρίτσος ΤΡΙΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ Δρ. Κωνσταντίνος Αυγουστάκης Αναπληρωτής Καθηγητής Τμήματος Φαρμακευτικής Δρ. Παύλος Κλεπετσάνης Επίκουρος Καθηγητής Τμήματος Φαρμακευτικής Δρ. Αριστείδης Μπακανδρίτσος Λέκτορας Τμήματος Επιστήμης Υλικών
4
5 Σε όσους έκαναν την επιλογή τους... Εικόνα εξωφύλλου: Nanolipogels: Yale Experts Create Novel Cancer Drug Delivery System.
6
7 Πρόλογος Η παρούσα μεταπτυχιακή διατριβή εκπονήθηκε στο Εργαστήριο Φαρμακευτικής Τεχνολογίας, του Τμήματος Φαρμακευτικής του Πανεπιστημίου Πατρών, σε συνεργασία με το Τμήμα Επιστήμης Υλικών του Πανεπιστημίου Πατρών, στα πλαίσια του Μεταπτυχιακού Προγράμματος Ειδίκευσης του Τμήματος Φαρμακευτικής, στην κατεύθυνση «Βιομηχανική Φαρμακευτική - Φαρμακευτική Ανάλυση» κατά το χρονικό διάστημα Οκτωβρίου Δεκεμβρίου Φτάνοντας στο τέλος δύο χρόνων εντατικής δουλειάς, αισθάνομαι την ανάγκη να ευχαριστήσω ιδιαίτερα ορισμένους ανθρώπους που συνέβαλαν στην επιτυχή διεκπεραίωση της παρούσας εργασίας, τόσο σε επιστημονικό όσο και σε ψυχολογικό επίπεδο. Θα ήθελα να εκφράσω τις θερμές μου ευχαριστίες προς τον επιβλέποντα καθηγήτη μου κ. Κωνσταντίνο Αυγουστάκη, Αναπληρωτή Καθηγητή Φαρμακευτικής Τεχνολογίας του Τμήματος Φαρμακευτικής, για την εξαρχής εμπιστοσύνη που έδειξε στο πρόσωπό μου, την ευκαιρία που μου έδωσε να συμμετάσχω στην ερευνητική του ομάδα, καθώς και για την πολύτιμη καθοδήγησή του. Ένα μεγάλο ευχαριστώ οφείλω στο συνεπιβλέποντα καθηγητή μου κ. Αριστείδη Μπακανδρίτσο, Λέκτορα του Τμήματος Επιστήμης Υλικών, για τη συνεχή καθοδήγηση, το χρόνο που μου διέθεσε και τις γνώσεις που μου μετέφερε σε ερευνητικό, συγγραφικό και ηθικό επίπεδο, καθ όλη τη διάρκεια εκπόνησης της παρούσας εργασίας. Η έρευνα αποτελεί ένα αναπόσπαστο κομμάτι των στόχων μου και ξεκίνησε με τις σωστότερες βάσεις, χάρις στον άνθρωπο αυτόν. Θα ήθελα επίσης να ευχαριστήσω τον κ. Παύλο Κλεπετσάνη, Επίκουρο Καθηγητή του Τμήματος Φαρμακευτικής, για τις χρήσιμες υποδείξεις του. Ιδιαιτέρως ευχαριστώ το μεταδιδάκτορα ερευνητή κ. Ιωάννη Σαρηγιάννη, για τις πολύτιμες συμβουλές του και κυρίως για την εκμάθηση της HPLC. Τις θερμές ευχαριστίες μου θα ήθελα να εκφράσω προς τη μεταδιδάκτορα ερευνήτρια και φίλη μου κ. Σταματία Ροκίδη, για την επιστημονική και ψυχολογική στήριξη που μου παρείχε. I
8 Επιπλέον, θα ήταν παράλειψη μου αν δεν ευχαριστούσα όλα τα παιδιά του εργαστηρίου Φαρμακευτικής Τεχνολογίας και του Τμήματος Επιστήμης Υλικών, και κυρίως τον υποψήφιο διδάκτορα Νικόλαο Παπαϊωάννου και τους μεταπτυχιακούς φοιτητές Αργύρη Κολοκυθά, Ηλία Ρουσάλη, Αθανάσιο Σκανδάλη, Κωνσταντίνο Κολοβό, Γιάννη Μποχωρίδη και Ιωάννα Κοντοπούλου, για το εξαιρετικό κλίμα συνεργασίας και την ευχάριστη ατμόσφαιρα στο εργαστήριο. Θα ήθελα να ευχαριστήσω ιδιαίτερα τους γονείς μου Χρήστο και Άννα και τα αδέρφια μου Ευσεβεία και Μάριο, για την καθολική στήριξη προς το πρόσωπο μου όλα αυτά τα χρόνια. Τέλος, η παρούσα μεταπτυχιακή διατριβή είναι εξαιρετικά αφιερωμένη στην κ. Άντρια Ιωάννου, έναν υπέροχο άνθρωπο στον οποίο οφείλω πολλά. II
9 Περιεχόμενα Πρόλογος... I Περίληψη... VII Abstract... IX Πίνακας Συντομογραφιών... XI Κεφάλαιο 1: Εισαγωγή Νανοτεχνολογία και Νανοεπιστήμες Theranostics Συστήματα Ελεγχόμενης Χορήγησης Φαρμάκων (Drug Delivery Systems, DDS) Ταξινόμηση DDS Παθητική και Ενεργητική στόχευση DDS στην κλινική πράξη Νανοφορείς Φυσικοχημικοί περιορισμοί DDS Κολλοειδή Διάκριση Κολλοειδών Κολλοειδής σταθερότητα Υπερπαραμαγνητικά νανοσωματίδια οξειδίου του σιδήρου (Superparamagnetic Iron Oxide Nanoparticles, SPIONs) Μαγνητίτης και Μαγκεμίτης Μαγνητισμός Τύποι Μαγνητισμού Μαγνητικές νανοδομές και Υπερπαραμαγνητισμός Απόκριση σε εξωτερικά μαγνητικά πεδία Μεθόδοι σύνθεσης SPIONs Επιφανειακή τροποποίηση SPIONs Άμεση επιφανειακή τροποποίηση Έμμεση επιφανειακή τροποποίηση Εφαρμογές SPIONs III
10 Μαγνητική τομογραφία πυρηνικού συντονισμού (Magnetic Resonance Imaging, MRI) Μαγνητική στόχευση φαρμάκων (Magnetic Drug Targeting, MDT) Μαγνητική Υπερθερμία ή Υπερθερμία Μαγνητικών Ρευστών (Magnetic Fluid Hyperthermia, MFH) Πακλιταξέλη (Paclitaxel, PTX) PTX-Mag-PLA-PEG νανοφορείς Στόχος μεταπτυχιακής διατριβής Κεφάλαιο 2: Τεχνικές Χαρακτηρισμού Ηλεκτρονική Μικροσκοπία Διέλευσης (Transmission Electron Microscopy, TEM) Θερμοσταθμική Ανάλυση (Thermogravimetric Analysis, TGA) Δυναμική Σκέδαση Φωτός (Dynamic Light Scattering, DLS) Φασματοφωτομετρία Υπεριώδους-Ορατού (UV-VIS) Μαγνητοφόρηση Υγρή Χρωματογραφία Υψηλής Απόδοσης (High Performance Liquid Chromatography, HPLC) Κεφάλαιο 3: Πειραματικό Μέρος Αντιδραστήρια Χρησιμοποιούμενα Όργανα και Τεχνικές Σύνθεση και χαρακτηρισμός υδρόφοβων SPIONs Συνθέσεις SPIONs με ακετυλακετονικό τρισθενές σίδηρο [Fe(acac) 3 ] ως πρόδρομη ένωση Συνθέσεις SPIONs με υδρόξυ-οξείδιο του τρισθενούς σιδήρου [FeΟ(ΟΗ)] ως πρόδρομη ένωση Συνθέσεις SPIONs με ελαϊκό σίδηρο [Fe(Olate) 3 -ex] ως πρόδρομη ένωση Συνθέσεις SPIONs με ελαϊκό σίδηρο [Fe(Olate) 3 -prc] ως πρόδρομη ένωση Απομόνωση και προσδιορισμός καθαρότητας των συντεθέντων SPIONs Φασματοφωτομετρικός προσδιορισμός ιόντων σιδήρου Χαρακτηρισμός SPIONs με Ηλεκτρονική Μικροσκοπία Διέλευσης (Transmission Electron Microscopy, TEM) IV
11 3.4 Μελέτη των παραμέτρων της σύνθεσης πολυμερικών και υπερπαραμαγνητικών πολυμερικών μικκυλίων Χαρακτηρισμός πολυμερικών και υπερπαραμαγνητικών πολυμερικών μικκυλίων Μελέτη των παραμέτρων της φόρτωσης και αποδέσμευσης Πακλιταξέλης (PTX), ενκαψυλιωμένης σε πολυμερικά και υπερπαραμαγνητικά πολυμερικά μικκύλια Φόρτωση PTX σε PLA-PEG και Mag-PLA-PEG μικκύλια Προσδιορισμός φόρτωσης (Loading) και ενκαψυλίωσης (Encapsulation) της PTX σε PLA-PEG και Mag-PLA-PEG μικκύλια Προσδιορισμός στερεής μάζας PTX-Mag-PLA-PEG νανοφορέων μέσω TGA Προσδιορισμός PTX με υγρή χρωματογραφία υψηλής απόδοσης (High Performance Liquid Chromatography, HPLC) Μελέτη μαγνητικών ιδιοτήτων των PTX-Mag-PLA-PEG νανοφορέων με την τεχνική της μαγνητοφόρησης Μελέτη αποδέσμευσης (Release) PTX απο PLA-PEG και Mag-PLA-PEG μικκύλια Κεφάλαιο 4: Ανάλυση αποτελεσμάτων - Συζήτηση Χαρακτηρισμός συντεθέντων SPIONs Συνθέσεις SPIONs με Fe(acac) 3 ως πρόδρομη ένωση Συνθέσεις SPIONs με FeO(OH) ως πρόδρομη ένωση Συνθέσεις SPIONs με [Fe(Olate) 3 -ex] ως πρόδρομη ένωση Συνθέσεις SPIONs με [Fe(Olate) 3 -prc] ως πρόδρομη ένωση Μελέτη των παραμέτρων της σύνθεσης πολυμερικών και υπερπαραμαγνητικών πολυμερικών μικκυλίων Μελέτη των παραμέτρων της φόρτωσης PTX και SPIONs σε PLA-PEG μικκύλια Μελέτη της μαγνητικής συμπεριφοράς των PTX-Mag-PLA-PEG νανοφορέων Μελέτη των παραμέτρων της αποδέσμευσης PTX απο PTX- και PTX-Magνανοφορείς V
12 Κεφάλαιο 5: Συμπεράσματα Μελλοντική εργασία Συμπεράσματα Μελλοντική εργασία Κεφάλαιο 6: Βιβλιογραφία VI
13 Περίληψη Η Πακλιταξέλη (PTX) αποτελεί ένα ευρέως διαδεδομένο αντινεοπλασματικό φάρμακο και ενδείκνυται σε μεταστατικό καρκίνο του μαστού, καρκίνο ωοθηκών, μη μικροκυτταρικό καρκίνο του πνεύμονα και σε σάρκωμα Kaposi ασθενών με AIDS. Παρ όλα αυτά, η σημαντική τοξικότητα που εμφανίζει (μυελοκαταστολή, νευροτοξικότητα, αντιδράσεις υπερευαισθησίας), υπογραμμίζει την αναγκαιότητα για μορφοποίησή της σε Συστήματα Ελεγχόμενης Χορήγησης Φαρμάκων (DDS), με σκοπό τη μείωση των ανεπιθύμητων ενεργειών και την αύξηση της βιοδιαθεσιμότητας του φαρμάκου. Τα πολυμερικά μικκύλια έχουν μελετεθεί εκτενώς τα τελευταία χρόνια ως Συστήματα Ελεγχόμενης Χορήγησης Φαρμάκων. Η ενσωμάτωση υπερπαραμαγνητικών νανοκρυσταλλιτών οξειδίου του σιδήρου (SPIONs) στον πυρήνα των PTX-μικκυλίων, παρέχει τη δυνατότητα μαγνητικής στόχευσης του φαρμάκου στην επιθυμητή περιοχή δράσης, καθώς και τη θεραπεία του καρκίνου μέσω επαγωγής μαγνητικής υπερθερμίας, με την εφαρμογή εναλλασσόμενου μαγνητικού πεδίου. Επιπλεόν, η χρήση των SPIONs ως σκιαγραφικά μέσα (Τ 2 -contrast enhancement) στη μαγνητική τομογραφία πυρηνικού συντονισμού (MRI), εξασφαλίζει το πλεονέκτημα ταυτόχρονης διάγνωσης και θεραπείας (Theranostics), αποκαλύπτοντας την πολυλειτουργικότητα των συστημάτων αυτών. Οι συγκεκριμένοι νανοφορείς, έχοντας μικρό μέγεθος ( nm), θεωρούνται κατάλληλοι για να αποφύγουν την οψωνινοποίηση απο τις λιποπρωτεϊνες του αίματος, την επίθεση απο τα φαγοκύτταρα του Δικτυοενδοθηλιακού συστήματος (RES) καθώς και την ταχεία νεφρική κάθαρση, με αποτέλεσμα την παρατεταμένη κυκλοφορία τους στο αίμα (stealth systems) και την εκλεκτική πρόσληψη τους απο τους συμπαγείς καρκινικούς όγκους, μέσω του φαινομένου της ενισχυμένης διαπερατότητας και κατακράτησης (EPR effect). Οι ιδιότητες αυτές, καθιστούν τα συγκεκριμένα συστήματα πολύτιμα εργαλεία στον τομέα της νανοϊατρικής. Η παρούσα μεταπτυχιακή διατριβή πραγματεύεται τη σύνθεση υδρόφοβων SPIONs μέσω της τεχνικής της θερμικής αποικοδόμησης. Μελετήθηκαν οι συνθετικές παράμετροι (πρόδρομη ένωση, ποσότητα ελαϊκού οξέος, θερμοκρασία και διάρκεια αντίδρασης, ρυθμός αύξησης της θερμοκρασίας κ.α) που επηρεάζουν το μέγεθος, το σχήμα και τη διασπορά του μεγέθους των σχηματιζομένων νανοκρυσταλλιτών (5-13nm, σ: 10-20%), καθώς διαδραματίζουν σημαντικό ρόλο στη μαγνητική συμπεριφορά των υβριδικών νανονοφορέων. Στη συνέχεια, πραγματοποιήθηκε σύνθεση υβριδικών νανοφορέων με εγκλωβισμό των SPIONs σε VII
14 πολυμερικά μικκύλια. Η παρασκευή των υπερπαραμαγνητικών μικκυλίων επιτελέστηκε με την τεχνικη solvent diffusion and evaporation (nanoprecipitation), με χρήση του αμφίφιλου συμπολυμερούς πολυ(γαλακτικό οξύ)-πολυ(αιθυλενογλυκόλη) (PLA-PEG). Στον υδρόφοβο πυρήνα των μικκυλίων (PLA) δεσμεύονται υδρόφοβες ενώσεις (PTX, SPIONs), ενώ το υδρόφιλο κέλυφος (PEG) προσδίδει κολλοειδή σταθερότητα σε υδατικά μέσα (δομή πυρήνακελύφους). Διερευνήθηκαν διάφορες συνθετικές παράμετροι (μοριακό βάρος συμπολυμερούς, ποσότητα SPIONs, ρυθμός προσθήκης οργανικής φάσης κ.α) και προσδιορίστηκαν οι βέλτιστες συνθήκες για την παρασκευή υπερπαραμαγνητικών μικκυλίων μεγέθους <200nm, με αξιοσημείωτη κολλοειδή σταθερότητα (μέχρι και έξι μήνες), σε συνθήκες παρόμοιες με αυτές του ανθρώπινου πλάσματος (ph: 7.4, ιοντική ισχύς: 0.15Μ). Στο επόμενο στάδιο της παρούσας εργασίας, μελετήθηκαν οι παράγοντες που επηρεάζουν τη φόρτωση-ενκαψυλίωση της PTX και των SPIONs στα πολυμερικά μικκύλια (ποσότητα PTX, ποσότητα και μέγεθος SPIONs, μοριακό βάρος PLA-PEG, ρυθμός προσθήκης οργανικής φάσης κ.α), σε φυσιολογικές συνθήκες (ph:7.4, ιοντική ισχύς: 0.15Μ). Αναπτύχθηκε πρωτόκολλο μέσω του οποίου έγινε κατορθωτός ο διαχωρισμός των μαγνητικών νανοφορέων απο τους μη μαγνητικούς, καθώς και ο υπολογισμός της φόρτωσηςενκαψυλίωσης PTX και SPIONs ξεχωριστά, τόσο στους μαγνητικούς και μη μαγνητικούς νανοφορείς, όσο και στο μέιγμα αυτών. Οι συγκεκριμένοι νανοφορείς χαρακτηρίζονται απο εξαιρετικά υψηλή απόδοση ενκαψυλίωσης φαρμάκου (93 %wt.) και φόρτωση φαρμάκου που ανέρχεται στο 4.8 %wt. Oι αμιγώς μαγνητικοί νανοφορείς επιδεικνύουν υψηλή απόδοση ενκαψυλίωσης νανοκρυσταλλιτών (70 %wt.), ενώ η φόρτωση σε φάρμακο και SPIONs ανέρχεται σε 5.2 και 20 %wt. αντίστοιχα. Σε αμφότερες τις περιπτώσεις οι νανοφορείς, μεγέθους (υδροδυναμική διάμετρος) 170nm, χαρακτηρίζονται απο ικανοποιητική μαγνητική συμπεριφορά. Εξετάστηκε η επίδραση του μεγέθους των νανοκρυσταλλιτών στη μαγνητική συμπεριφορά των νανοφορέων. Οι αμιγώς μαγνητικοί νανοφορείς με μεγαλύτερο μέγεθος SPIONs παρουσιάζουν καλύτερη μαγνητική συμπεριφορά. Τέλος, πραγματοποιήθηκαν μελέτες αποδέσμευσης του φαρμάκου σε PBS (0.14Μ, ph:7.4) στους 37 o C και διερευνήθηκε η επίδραση της εφαρμογής εναλλασσόμενου μαγνητικού πεδίου στην αποδέσμευση της PTX απο τους μαγνητικούς νανοφορείς (Triggered Drug Release). Σε κάθε περίπτωση, παρατηρήθηκε ελεγχόμενη αποδέσμευση του φαρμάκου για 24 ώρες, σε συνθήκες που προσομοιάζουν με αυτές του πλάσματος. Ο φυσικοχημικός χαρακτηρισμός των νανοφορέων πραγματοποιήθηκε με HPLC, DLS, TGA, TEM και μαγνητοφόρηση. VIII
15 Abstract Paclitaxel (PTX) is one of the most successful anticancer drugs against a broad range of solid tumors, such as metastatic breast cancer, ovarian cancer, non-small-cell lung cancer and AIDS-related Kaposi sarcoma. However, the serious systematic side effects of PTX (myelosuppression, neurotoxicity, hypersensitivity) underline the need for formulation of PTX in Drug Delivery Systems (DDS), in order to reduce the side effects and increase the bioavailability of the drug. Among DDS, polymeric micelles have drawn much attention due to their great flexibility in tuning drug solubility, micelle size, targeted drug delivery and stability. Incorporation of Superparamagnetic Iron Oxide Nanocrystals (SPIONs) inside the core of drug-loaded polymeric micelles, imparts to the final Drug Delivery System the prospect of physical (magnetic) targeting, intrinsic therapeutic function (hyperthermia-based cancer therapy under alternating external magnetic field), T 2 -based contrast enhancement in magnetic resonance imaging (MRI) and remotely triggered drug release. These core-shell polymeric micelles having small size ( nm), are considered appropriate for avoiding both opsonization, macrophages attack by ReticuloEndothelial System (RES) and rapid renal clearance, thus allowing micelles to be taken up preferably by solid tumors through Enhanced Permeability and Retention (EPR) effect. Therefore, such nanoassemblies encode high potential in nanomedicine, due to their dual nature (Therapeutic+Diagnostic = Theranostics). In particular, we have studied the synthesis of organophilic SPIONs through thermal decomposition. The synthetic parameters (precursor, precursor:oleic acid ratio, reaction temperature and duration, heat rate, etc.) affecting the size, shape and size distribution of the nanocrystals have also been examined thoroughly, since they play a key-role concerning the magnetic behavior of the final hybrid. Nanosized SPIONs with narrow size distribution were synthesized (5-13nm, σ: 10-20%). The preparation of poly(lactic acid)- block-poly(ethyleneglycol) (PLA-PEG) micelles encapsulating hydrophobic SPIONs, by varying the molecular weight of the polymers, the amount of SPIONs and the addition rate during micelle assembly, has also been investigated. The core-shell superparamagnetic micelles were prepared through solvent diffusion and evaporation technique (nanoprecipitation). PTX and SPIONs are being incorporated into the micelle s hydrophobic core (PLA) through hydrophobic interactions, whereas the hydrophilic shell (PEG) stabilizes IX
16 the micelles in aqueous dispersions, optimizing their colloidal stability and providing prolonged circulating time. The optimum parameters were determined, conferring to the micelles (Hydrodynamic Diameter < 200nm) high colloidal stability (up to six months) at biorelevant conditions (ph:7.4, ionic strenght: 0.15M). The next phase of the present master thesis focused on studying the factors (amount of PTX and SPIONs, molecular weight of PLA-PEG, addition rate, etc.) affecting the Loading of PTX and SPIONs into the polymeric micelles and how they can be fine-tuned towards high drug loading, while retaining their size at a scale where long circulation would not be precluded. Through protocol establishment, we have managed to separate the magnetic and non magnetic micelles, and to determine individually the loading of PTX and SPIONs for magnetic, non magnetic micelles, as well as for the mixture of them. The micelles mixture exhibits very high Drug Encapsulation Efficiency (93 %wt.) and 4.8 %wt. Drug Loading (D.L). Magnetic nanocarriers display high Magnetic Encapsulation Efficiency (70 %wt.), with D.L and Magnetic Loading of 5.2 and 20 %wt. respectively, In both cases, micelles demonstrate adequate magnetic behavior and small sizes (hydrodynamic diameter: 170nm), under conditions which simulate with human plasma (ph:7.4, ionic strenght: 0.15M). The effect of SPIONs size on the magnetic behavior of hybrid colloids, was also examined. Magnetic nanocarriers encapsulating SPIONs of greater size exhibit better magnetic behavior. Finally, we have conducted Drug release studies in PBS (0.14M, ph:7.4) at 37 o C. The effect of SPIONs presence on the release profile of PTX, including triggered drug-release by application of AC magnetic field, has also been investigated. PTX-magnetic micelles exhibit Controlled Drug release for 24 hours. Several techniques have been used for the characterization of such nanoassemblies, like: HPLC, DLS, TGA, TEM, XRD, Magnetophoresis and Triggered Drug release by application of AC magnetic field. X
17 Πίνακας Συντομογραφιών DDS: Drug Delivery Systems, Συστήματα Eλεγχόμενης Χορήγησης Φαρμάκων. SPIONs: SuperParamagnetic Iron Oxide Nanocrystals, Υπερπαραμαγνητικοί Νανοκρυσταλλίτες Οξειδίου του Σιδήρου. PTX: Paclitaxel, Πακλιταξέλη. PLA-PEG: poly(lactide)-block-poly(ethyleneglycol), πολυ(γαλακτικό οξύ)-blockπολυ(αιθελενογλυκόλη) EPR: Enhanced Permeabilty and Retention effect, φαινόμενο Ενισχυμένης Διαπερατότητας και Κατακράτησης. MRI: Magnetic Resonance Imaging, Απεικόνιση Μαγνητικού συντονισμού. MFH: Magnetic Fluid Hyperthermia, Υπερθερμία Μαγνητικών Ρευστών. AMF: Alternating Magnetic Field, Εναλλασσόμενο Μαγνητικό Πεδίο. MDT: Magnetic Drug Targeting, Μαγνητική Στόχευση Φαρμάκων. TEM: Transmission Electrion Microscopy, Ηλεκτρονική Μικροσκοπία Διέλευσης. TGA: ThermoGravimetric Analysis, Θερμοσταθμική Ανάλυση. DLS: Dynamic Light Scattering, Δυναμική Σκέδαση Φωτός. HPLC: High Performance Liquid Chromatography, Υγρή Χρωματογραφία Υψηλής Απόδοσης. D.L: Drug Loading, Φόρτωση Φαρμάκου. D.E.E: Drug Encapsulation Efficiency, Απόδοση Ενκαψυλίωσης Φαρμάκου. M.L: Magnetic Loading, Μαγνητική Φόρτωση. M.E.E: Magnetic Encapsulation Efficiency, Απόδοση Μαγνητικής Ενκαψυλίωσης. M.F.E: Micelles Formation Efficiency, Απόδοση Σχηματισμού Μικκυλίων. D h : Hydrodynamic Diameter, Υδροδυναμική Διάμετρος. XI
18 XII
19 Κεφάλαιο 1 Εισαγωγή 1
20 1.1 Νανοτεχνολογία και Νανοεπιστήμες Η νανοτεχνολογία και οι νανοεπιστήμες αφορούν τη μελέτη, το δομικό σχεδιασμό, παραγωγή και χειρισμό της ύλης σε διαστάσεις νανομέτρων (10-9 nm) [ 1 ]. Τέτοια νανοσυστήματα συχνά βασίζονται στα νανοσωματίδια. Ο όρος νανοσωματίδια (Nanoparticles, NPs) αναφέρεται σε σωματίδια των οποίων τουλάχιστον η μία εκ των διαστάσεων τους είναι μεταξύ 1 και 100nm. Ο λόγος για τον οποίο υπάρχει έντονο επιστημονικό ενδιαφέρον για τα νανοσυστήματα έγκειται στο γεγονός ότι σε αυτά τα μεγέθη τα υλικά παρουσιάζουν ιδιότητες οι οποίες είναι διαφορετικές από αυτές των αντίστοιχων μακροσκοπικών υλικών. Οι δυο βασικότεροι λόγοι για αυτή την αλλαγή είναι αφενός μεν η αύξηση της επιφάνειας σε σχέση με τον συνολικό όγκο και αφετέρου η επικράτηση των κβαντικών φαινομένων με αποτέλεσμα να αλλάζουν σημαντικά οι οπτικές, ηλεκτρικές, φυσικοχημικές και μαγνητικές ιδιότητες του υλικού [2]. Είναι γνωστό πως η επιφάνεια ενός υλικού καθορίζει σε πολύ μεγάλο βαθμό τις αλληλεπιδράσεις με το περιβάλλον και μπορεί να μεταβάλλει αυτήν την αλληλεπίδραση, πολλές φορές, κατά τρόπο ευνοϊκό 1. Εικόνα 1.1: Εφαρμογές των νανοσωματιδίων στη νανοτεχνολογία [ 3 ]. 1 Εικόνα κεφαλαίου: A. Ito, M. Shinkai, H. Honda and T. Kobayashi, Medical Application of Functionalized Magnetic Nanoparticles, Journal of Bioscience and Bioengineering 2005, 100,
21 Το πεδίο των εφαρμογών ποικίλει από τα ηλεκτρονικά μέχρι την οπτική, την κατάλυση χημικών αντιδράσεων και φυσικά τη φαρμακευτική και την ιατρική (Εικόνα 1.1) [3]. Οι νανοεπιστήμες αφορούν λοιπόν ένα πολύ ευρύ αντικείμενο και ως εκ τούτου, ο χαρακτήρας αυτού του κλάδου είναι άκρως διεπιστημονικός. Είναι συχνές οι αναφορές στον επαναστατικό χαρακτήρα της νανοτεχνολογίας, δηλαδή στις δυνατότητες που διαφαίνονται για την ανάπτυξη υλικών με νέες ιδιότητες, βελτιστοποιημένων μεθοδολογιών και νέων εφαρμογών. Τα μικρότερα, ελαφρύτερα, ταχύτερα και αποδοτικότερα υλικά και συστήματα που προσφέρει η νανοτεχνολογία είναι δυνατόν να δώσουν λύσεις σε πολλά τρέχοντα ζητήματα. Η εφαρμογή της νανοτεχνολογίας στον τομέα της ιατρικής έχει δημιουργήσει ένα νέο επιστημονικό πεδίο που συχνά αναφέρεται με τον όρο νανοϊατρική ή βιοϊατρική νανοτεχνολογία. Ο κλάδος της νανοϊατρικής υπόσχεται να ανοίξει νέους δρόμους στη διάγνωση, πρόληψη, αλλά και θεραπεία ασθενειών που μέχρι σήμερα παραμένουν ανίατες [4]. Συνεχώς αναπτύσσονται νέας σύστασης και δομής νανοσωματίδια με στόχο την απεικόνιση και τη θεραπεία του καρκίνου. Η εφαρμογή της νανοτεχνολογίας για την ανάπτυξη μεθόδων και τρόπων με σκοπό τη στοχευμένη μεταφορά αντικαρκινικών φαρμάκων και τη μείωση των ανεπιθύμητων ενεργειών τους μελετάται εκτενώς την τελευταία δεκαετία [ 5, 6, 7 ]. Σημαντικό ερευνητικό ενδιαφέρον συγκεντρώνει η ανάπτυξη συστημάτων για ταυτόχρονη μεταφορά δραστικών ουσιών και απεικόνιση των καρκινικών περιοχών. Αυτή η νέα κατηγορία νανοσυστημάτων ονομάζεται Theranostics [8, 9, 10]. Τέλος, τα κολλοειδή υβριδικά νανοσωματίδια είναι μία κατηγορία υλικών η οποία μελετάται έντονα τα τελευταία χρόνια προς αυτήν την κατεύθυνση [11]. 1.2 Theranostics Ο όρος theranostics εμφανίστηκε για πρώτη φορά στην βιβλιογραφία το 2000 [12] και επινοήθηκε για να περιγράψει φάρμακα ή μεθόδους τα οποία μπορούν να χρησιμοποιηθούν για ταυτόχρονη διάγνωση και θεραπεία. Ένα απλός ορισμός του όρου theranostics που περιγράφηκε από την S. Warner είναι diagnostics plus therapy [ 13 ]. Η εφαρμογή της νανοτεχνολογίας στην ιατρική έχει βοηθήσει στην γεφύρωση του χάσματος μεταξύ διάγνωσης και θεραπείας. Παράγοντες βασισμένοι σε νανοσωματίδια για την απεικόνιση [14, 15, 16] και την θεραπεία [17, 18] έχουν διερευνηθεί ξεχωριστά και έχουν εξελιχθεί σε βαθμό όπου 3
22 είναι πλέον δυνατή η δημιουργία theranostics βασισμένων σε νανοσωματίδια τα οποία είναι ικανά να επιτελέσουν και τις δύο αυτές λειτουργίες [19, 20, 21]. Εικόνα 1.2: Τα συστήματα Theranostics συνδυάζουν ένας πλήθος λειτουργιών με σκοπό την ταυτόχρονη διάγνωση και θεραπεία [ 22]. 1.3 Συστήματα Ελεγχόμενης Χορήγησης Φαρμάκων (Drug Delivery Systems, DDS) DDS είναι τα συστήματα χορήγησης φαρμάκων με τα οποία επιτυγχάνεται έλεγχος του χρόνου (Controlled Release) ή/και του τόπου διάθεσης του φαρμάκου (Targeted Drug Delivery) [23, 24]. Με τη χορήγηση τέτοιων συστημάτων δεν επιδιώκεται μόνο παράταση του χρόνου αποδέσμευσης του φαρμάκου αλλά ταυτόχρονα επιδιώκεται και η αποδέσμευση του με σταθερό ρυθμό για συγκεκριμένη χρονική περίοδο, σε αντιδιαστολή με τις παλαιότερης τεχνολογίας φαρμακευτικές μορφές βραδείας αποδέσμευσης (Sustained or prolonged or retarted Release) όπου είχαμε απλά επιβράδυνση της αποδέσμευσης του φαρμάκου απο την φαρμακομορφή (Εικόνα 1.4). Η κατασκευή των DDS προϋποθέτει την ενσωμάτωση της φαρμακευτικής ουσίας σε ένα μη τοξικό, βιοσυμβατό ή/και βιοαποικοδομήσιμο νανοφορέα, ο οποίος θα χαρακτηρίζεται απο παρατεταμένη παραμονή στη γενική κυκλοφορία (stealth system) ή/και την ικανότητα να δεσμεύεται εκλεκτικά απο το όργανο-στόχο με σκοπό την αποκλειστική αποδέσμευση του φαρμάκου στην πάσχουσα περιοχή (Drug Targeting), 4
23 μειώνοντας έτσι τις ανεπιθύμητες ενέργειες απο τη δράση του φαρμάκου σε άλλα όργανα (Εικόνα 1.3). Γίνεται λοιπόν αντιληπτό πως τα φυσικοχημικά χαρακτηριστικά του νανοφορέα καθορίζουν σε μεγάλο βαθμό το φαρμακοκινητικό προφίλ. Εικόνα 1.3: Εξειδικευμένο DDS για διάγνωση και θεραπεία (Theranostics). Στο νανονοφορέα (2) ενσωματώνεται εκτος του φαρμάκου (6) και φθορίζουσα ομάδα (3) για απεικόνιση. Επιπλέον, το συγκεκριμένο σύστημα διαθέτει ομάδα στόχευσης (4) για εκλεκτική σύνδεση με την περιοχή-στόχο (Targeted Drug Delivery) καθώς και μαγνητικό υλικό για μαγνητική στόχευση. Με την ενσωμάτωση βιοαποκρινόμενων στοιχείων (5), η αποδέσμευση του φαρμάκου ρυθμίζεται απο βιολογικά ερεθίσματα [ 25]. Με τη χορήγηση των συμβατικών μορφών συχνά χορηγούνται δόσεις υψηλότερες των απαιτούμενων ώστε να επιτευχθεί και να διατηρηθεί επί μακρόν η απαιτούμενη θεραπευτική συγκέντρωση του φαρμάκου στα σημεία δράσης του. Όμως, οι υψηλές χορηγούμενες δόσεις δυνατόν να προκαλέσουν ανεπιθύμητες ενέργειες ή τοξικά φαινόμενα. Αντίθετα, με τη χορήγηση DDS αποφεύγεται το παραπάνω φαινόμενο και συνεπώς ελαχιστοποιούνται οι ανεπιθύμητες ενέργειες. Επιπλέον αυξάνεται η βιοδιαθεσιμότητα δεδομένου ότι οι συγκεντρώσεις του φαρμάκου διατηρούνται σταθερές στο αίμα και μέσα στα θεραπευτικά όρια, εν αντιθέσει με τις συμβατικές μορφές που εμφανίζουν ανεπιθύμητη αυξομείωση των επιπέδων του φαρμάκου στο αίμα. Με τις συμβατικές μορφές μόνο η δόση και η συχνότητα χορήγησης μπορούν να καθοριστούν, ενώ το ποσό του φαρμάκου που διατίθεται στο στόχο και ο χρόνος διάθεσής του δεν μπορούν να καθοριστούν ανεξάρτητα. Στον αντίποδα, με την ελεγχόμενη χορήγηση είναι δυνατόν να καθοριστούν τόσο το ποσό του φαρμάκου που διατίθεται στο πάσχον όργανο/ιστό καθώς και ο χρόνος διάθεσης του στην επιθυμητή περιοχή. Ένα άλλο πρόβλημα που δύναται να υπερκεραστεί με τη χορήγηση μορφών ελεγχόμενης χορήγησης είναι η αποφυγή χορήγησης αλλεπάλληλων δόσεων σε σύντομα χρονικά διαστήματα, φαινόμενο που εμφανίζεται σε φάρμακα με μικρό χρόνο ημιζωής (<3-4h). Τέλος, θα πρέπει να σημειωθεί ότι η μορφοποίηση σε DDS φαρμακευτικών 5
24 ουσιών με μεγάλο χρόνο ημιζωής (>12h) είναι ανούσια καθώς οι ουσίες αυτές εμφανίζουν εκ φύσεως παρατεταμένη αποδέσμευση, εκτός αν η χορήγηση τέτοιων συστημάτων παρέχει ορισμένα άλλα πλεονεκτήματα [26]. Συνοψίζοντας, τα κυριότερα πλεονεκτήματα των DDS είναι τα ακόλουθα: Αύξηση της διάρκειας δράσης του φαρμάκου και καλύτερη συμμόρφωση του ασθενούς διότι αποφεύγονται οι συχνές λήψεις π.χ. νυκτερινές δόσεις. Χορήγηση μικρότερης ποσότητας φαρμάκου που έχει σαν αποτέλεσμα την ελαχιστοποίηση των ανεπιθύμητων ενεργειών. Το γεγονός αυτό είναι ιδιαίτερα σημαντικό στις χρόνιες παθήσεις καθώς αποφεύγεται η συσσώρευση του φαρμάκου στον οργανισμό. Βελτίωση της αποτελεσματικότητας της θεραπείας αφού αποφεύγεται η αυξομείωση των επιπέδων φαρμάκου στο αίμα, με αποτέλεσμα την ομοιόμορφη φαρμακολογική δράση. Αύξηση της βιοδιαθεσιμότητας αρκετών φαρμακευτικών ουσιών. Αποφυγή ερεθισμού του γαστρεντερικού συστήματος. Αύξηση της δραστικότητας φαρμάκων με μικρό χρόνο ημιζωής. Αλλαγή των επιφανειακών ιδιοτήτων μιας ουσίας. Βελτίωση των ιδιοτήτων ροής. Αύξηση της σταθερότητας διαφόρων ουσιών. Ωστόσο πρέπει να σημειωθούν και τα μειονεκτήματα των Συστημάτων Ελεγχόμενης Χορήγησης φαρμάκων: Απαιτείται μεγαλύτερος χρόνος για την επίτευξη θεραπευτικών συγκεντρώσεων και παρουσιάζεται μειωμένη βιοδιαθεσιμότητα σε ορισμένα προϊόντα (per os σκευάσματα) Η καθυστερημένη αποδέσμευση μπορεί να επιβραδύνει το θεραπευτικό αποτέλεσμα και να επιμηκύνει τη διάρκεια τυχόν ανεπιθύμητων ενεργειών. Ύπαρξη παραπροϊόντων από τη χημική αποικοδόμηση τέτοιων συστημάτων. Πιθανή απόρριψη της φαρμακευτικής ουσίας από το νανοφορέα (απότομο άδειασμα). Υψηλό κόστος σε σχέση με τα παραδοσιακά σκευάσματα. Πιθανή τοξικότητα και μη βιοσυμβατότητα του νανοφορέα. 6
25 Εικόνα 1.4: Διάγραμμα μεταβολής της συγκεέντρωσης του φαρμάκου στο πλάσμά του αίματος συναρτήσει του χρόνου για τις συμβατικές μορφές χορήγησης, τις μορφές βραδείας αποδέσμευσης (sustained release) και για τα συστήματα ελεγχόμενης χορήγησης (controlled release) [27] Ταξινόμηση DDS Τα Συστήματα Ελεγχόμενης Χορήγησης, ανάλογα με την οδό χορήγησης, διακρίνονται σε: 1) Συστήματα χορηγούμενα από το στόμα (per os), 2) Παρεντερικά συστήματα (κυρίως I.V), 3) Διαδερμικά συστήματα, 4) Συστήματα χορηγούμενα δια των βλεννογόνων (στόματος-ορθού-κόλπου-οφθαλμού) και 5) Εμφυτεύματα. Με βάση τον τύπο του σκευάσματος, τα DDS ταξινομούνται στις παρακάτω κατηγορίες: 1) Συστήματα δεξαμενής (reservoir systems), 2) Συστήματα μήτρας (matrix systems) και 3) Συστήματα ωσμωτικής άντλησης. Επίσης με βάση το μηχανισμό που ελέγχει την ταχύτητα αποδέσμευσης του φαρμάκου, ταξινομούνται σε: 1) Συστήματα ελεγχόμενα από τη διάχυση μέσω του νανοφορέα 2) Συστήματα ελεγχόμενα από τη διαβρωση, τη διάλυση ή κάποια χημική αντίδραση (διάσπαση), 3) Συστήματα ελεγχόμενα από την ωσμωτική πίεση και 4) Συστήματα ελεγχόμενα από την ταχύτητα διόγκωσης του νανοφορέα [28]. Για τους σκοπούς της παρούσας εργασίας δεν θα γίνει περαιτέρω ανάλυση των πιο πάνω κατηγοριών. Αρκετές μορφές DDS κυκλοφορούν σήμερα στην αγορά. Το progestasert είναι ενα ενδομήτριο αντισυλληπτικό εμφύτευμα σχήματος Τ (3.2 x 3.6cm), το οποίο παρέχει με σταθερό ρυθμό 65μg προγεστερόνης ημερησίως για ένα χρόνο. Κρυσταλλική προγεστερόνη διασπείρεται σε έλαιο σιλικόνης και στη συνέχεια ενσωματώνεται σε μη πορώδη μεμβράνη απο αιθυλένο-βινυλοξικό συμπολυμερές, εξασφαλίζοντας έτσι ελεγχόμενη αποδέσμευση για 7
26 μεγάλο χρονικό διάστημα. Τα προϊόντα Mirena και Skyla είναι παρόμοιας τεχνολογίας εμφυτεύματα αντισυλληπτικής δράσης για 5 και 3 χρόνια αντίστοιχα. Στην κατηγορία των υποδόριων αντισυλληπτικών εμφυτευμάτων ανήκουν τα Implanon, Norplant I και Norplant II. Παραδείγματα διαδερμικών DDS αποτελούν τα Transderm-Scop (αποδέσμευση σκοπολαμίνης για 3 μέρες για πρόληψη και θεραπεία της ταξιδιωτικής ναυτίας-κινήτωσης), Deponit, Nitrodisc, Nitrodur ( σκευάσματα νιτρογλυκερίνης για αντιστηθαγχική θεραπεία, μία φορα ημερησίως), Catapress-TTS ( κλονιδίνη, μια φορά την εβδομάδα για θεραπεία της υπέρτασης), Estraderm (οιστραδιόλη για την αντιμετώπιση προβλημάτων της εμμηνόπαυσης) και Duragesic (φαιντανύλιο για αντιμετώπιση του πόνου στους καρκινοπαθείς). Τέλος, το ενδοφθαλμικό σύστημα ελεγχόμενης αποδέσμευσης πιλοκαρπίνης (Alza Ocusert ) (13.4 x 5.7mm) χρησιμοποιείται για τη μείωση της ενδοφθάλμιας πίεσης και τη θεραπεία του γλαυκώματος, αποδεσμεύοντας τη δραστική ουσία με σταθερό ρυθμό (20 ή 40μg/h) για 7 μέρες. 8
27 Ανάλογα με την πολυπλοκότητα που παρουσιάζουν στην τεχνολογία τους, τα Συστήματα Ελεγχόμενης Χορήγησης, όπως παρουσιάζεται και στην Εικόνα 1.5, διακρίνονται στις εξής κατηγορίες [29] : Α. Συστήματα προκαθορισμένου ρυθμού αποδέσμευσης (rate-preprogrammed systems). Β. Συστήματα ενεργοποιούμενης αποδέσμευσης (activation - modulated systems). Γ. Συστήματα στα οποία η αποδέσμευση ελέγχεται από μηχανισμό ανάδρασης (feedback regulated systems). Δ. Συστήματα στόχευσης ή εξειδικευμένης εντόπισης (Drug Targeting Systems) Εικόνα 1.5: Κατηγορίες Συστημάτων Ελεγχόμενης Χορήγησης (DDS) [30]. Α. Στα συστήματα προκαθορισμένου ρυθμού η απελευθέρωση της δραστικής ουσίας έχει προκαθοριστεί ώστε να γίνεται με συγκεκριμένο ρυθμό. Αυτό επιτυγχάνεται με τον κατάλληλο σχεδιασμό του συστήματος, κατά τον οποίο ο ρυθμός αποδέσμευσης της εγκλωβισμένης ουσίας ελέγχεται από τη διάχυση της τελευταίας ή τη διείσδυση του διαλύτη (μέσο εμβάπτισης). Τα ελεγχόμενα μέσω διάχυσης συστήματα διακρίνονται σε συστήματα δεξαμενής (reservoir systems), στα οποία ο φραγμός είναι μια πολυμερική μεμβράνη που 9
28 περιβάλλει το σύστημα και τα συστήματα τύπου μήτρας (matrix systems), όπου το φάρμακο βρίσκεται διαλυμένο ή διεσπαρμένο εντός πολυμερικής ή κηρώδους μήτρας [31]. Α Β Εικόνα 1.6: Συστήματα Δεξαμενής (Α) και Συστήματα Μήτρας (Β) [32]. Στα συστήματα δεξαμενής, ο πυρήνας που περιέχει το ενεργό συστατικό μπορεί να είναι σε στερεή ή υγρή μορφή και η μεμβράνη χαρακτηρίζεται από καθόλου έως και υψηλό πορώδες. Εάν η ποσότητα της δραστικής ουσίας στον πυρήνα διατηρείται σε επίπεδα κορεσμού τότε η μεταφορά της κατά μήκος της μεμβράνης θα είναι συνεχής, αφού και η κινητήριος δύναμη θα παραμένει σταθερή. Μια τέτοια σταθερή (ή zero order) αποδέσμευση θα απαιτούσε το ενεργό συστατικό να παραμείνει σε στερεή μορφή ή τουλάχιστον σε μορφή εναιωρήματος. Η κορεσμένη κατάσταση θα ήταν δύσκολο να διατηρηθεί για ουσίες που παρουσιάζουν υψηλή υδατοδιαλυτότητα. Ακόμη και όταν πληρούνται όλες οι προϋποθέσεις ώστε η αποδέσμευση να είναι συνεχής, ο ρυθμός αποδέσμευσης ποτέ δεν παραμένει σταθερός στο αρχικό και τελικό στάδιο της αποδέσμευσης του φαρμάκου. Όταν το σύστημα τοποθετηθεί σε ένα μέσο εμβάπτισης απαιτείται ένα χρονικό διάστημα μέχρι να επέλθει μια σταθερή κατάσταση και μπορεί να παρατηρηθεί ένας χρόνος καθυστέρησης (Lag time) ή αντίθετα μια ξαφνική απελευθέρωση σημαντικής ποσότητας της δραστικής ουσίας (απότομο άδειασμα, Burst effect). Από την άλλη, στα συστήματα μήτρας ο ρυθμός αποδέσμευσης μειώνεται με το πέρας του χρόνου ως αποτέλεσμα της αύξησης της απόστασης διάχυσης που απαιτείται να διασχίσουν τα μόρια της δραστικής ουσίας από τον πυρήνα προς την επιφάνεια του πλέγματος. Η 10
29 συγκέντρωση του δραστικού συστατικού που αποδεσμεύεται σε δεδομένο χρόνο είναι συνήθως ανάλογη της τετραγωνικής ρίζας του χρόνου που έχει παρέλθει. Επιπλέον, εκτός από τη διάχυση από το πολυμερικό δίκτυο, τα μόρια της εγκλωβισμένης ουσίας μπορούν να βρουν διέξοδο μέσω των καναλιών που σχηματίζονται από τη διαλυτοποίηση και απομάκρυνση της ποσότητας της δραστικής ουσίας που έχει ήδη αποδεσμευτεί. Μάλιστα στην περίπτωση μακρομορίων που λόγω του όγκου τους έχουν περιορισμένη διαπερατότητα από το πολυμερές πλέγμα, η αποδέσμευσή τους επιτυγχάνεται σχεδόν αποκλειστικά μέσω αυτών των πόρων. Η κινητική αποδέσμευσης των παραπάνω ελεγχόμενων μέσω διάχυσης συστημάτων εξαρτάται σε σημαντικό βαθμό από τις φυσικοχημικές ιδιότητες του δραστικού συστατικού που μεταφέρουν. Επιπλέον, εκτός από το βαθμό πλήρωσης του συστήματος σε δραστικό συστατικό, το μέγεθος των σωματιδίων του τελευταίου, η διαλυτότητα του συστατικού αυτού στην πολυμερική μήτρα και η ικανότητα διάχυσής του σε αυτή αποτελούν επίσης σημαντικούς παράγοντες. Τέλος, το σχήμα του πολυμερικού συστήματος φαίνεται πως έχει μεγάλο αντίκτυπο στην ταχύτητα απελευθέρωσης της δραστικής ουσίας, καθώς καθορίζει το μέγεθος της ελεύθερης επιφάνειας που προσφέρεται για διάχυση και το μήκος της διαδρομής που ακολουθεί η διάχυση των μορίων προς της επιφάνεια [33]. Οι δύο παραπάνω μορφές DDS είναι οι απλούστερες μορφές που συναντώνται και πολλά συστήματα αυτού του τύπου χρησιμοποιούνται σήμερα στη θεραπευτική. 11
30 Β. Στην επόμενη κατηγορία Συστημάτων Ελεγχόμενης Χορήγησης ανήκουν τα πιο εξελιγμένα συστήματα ενεργοποιούμενης αποδέσμευσης. Σε αυτήν την κατηγορία η αποδέσμευση του ενεργού συστατικού ενεργοποιείται από την παρέμβαση φυσικών, χημικών και βιοχημικών διαδικασιών ή με την επίδραση εξωτερικώς παρεχόμενης ενέργειας (Εικόνα 1.7). Φυσικές μεθόδοι Χημικές μεθόδοι Βιοχημικές μεθόδοι Εικόνα 1.7: Στα Συστήματα Ενεργοποιούμενης Αποδέσμευσης η αποδέσμευση της δραστικής ουσίας ενεργοποιείται απο φυσικά, χημικά ή βιοχημικά ερεθίσματα [29]. Τα συστήματα όπου η αποδέσμευση του φαρμάκου ελέγχεται από την ωσμωτική πίεση είναι συστήματα φαρμάκου τα οποία περικλείονται από ημιπερατές μεμβράνες με ελεγχόμενη διαπερατότητα νερού. Επομένως πραγματοποιείται αποδέσμευση του φαρμάκου με σταθερό ρυθμό η οποία ελέγχεται από την κλίση της ωσμωτικής πίεσης. Αντίστοιχα, τα συστήματα που η αποδέσμευση του φαρμάκου ενεργοποιείται από την υδροδυναμική πίεση είναι συστήματα στα οποία το φάρμακο τοποθετείται σε μία δεξαμενή, η οποία περικλείεται από ένα διογκούμενο πολυμερικό στρώμα. Όταν αυτό το στρώμα απορροφά υγρό από το γαστρεντερικό σωλήνα, διογκώνεται ασκώντας υδροδυναμική πίεση στη δεξαμενή, ρυθμίζοντας με αυτόν τον τρόπο την αποδέσμευση του φαρμάκου (Εικόνα 1.8). Όμοια υπάρχουν συστήματα φαρμάκου τα οποία περικλείονται από ειδικό υγρό το οποίο στη θερμοκρασία του σώματος εξατμίζεται δημιουργώντας τάση ατμών, η οποία με τη σειρά της αποτελεί την κινητήριο δύναμη για την αποδέσμευση του φαρμάκου. Στις φυσικές μεθόδους υπάγονται συστήματα ενεργοποιούμενης αποδέσμευσης στα οποία εκτός του φαρμάκου ενσωματώνονται επιπλέον και μαγνητικά σωματίδια στη 12
31 πολυμερική μήτρα. Με την εφαρμογή εξωτερικού μαγνητικού πεδίου αυξάνεται ο ρυθμός αποδέσμευσης των μορίων του φαρμάκου (Οι εφαρμογές τέτοιων συστημάτων αναλύονται στη συνέχεια του κεφαλαίου). Στα συστήματα όπου η ενεργοποίηση επιτυγχάνεται μέσω της ιοντοφόρεσης, εφαρμόζεται ηλεκτρικό πεδίο το οποίο διευκολύνει τη διάχυση των φορτισμένων μορίων του φαρμάκου κατά μήκος των βιολογικών μεμβρανών. Αναφέρεται ότι η εφαρμογή υπερήχων αυξάνει την απελευθέρωση ινσουλίνης από συμπολυμερές αιθυλενίου/οξικού βινυλεστέρα. Τέλος, υπάρχουν συστήματα όπου η αποδέσμευση του φαρμάκου ελέγχεται απο την ενυδάτωση της πολυμερικής μήτρας στην οποία έχει διασπαρεί το φάρμακο. Α Β Εικόνα 1.8: DDS όπου η αποδέσμευση ενεργοποιείται απο την ωσμωτική πίεση (Α) και απο τη διόγκωση του πολυμερούς (Β) [31, 32]. Στους χημικούς τρόπους ενεργοποίησης της αποδέσμευσης περιλαμβάνονται η υδρόλυση, η οποία προκαλεί τη σταδιακή in vivo διάσπαση του φραγμού (μήτρας ή δεξαμενής) ο οποίος περιορίζει την αποδέσμευση του φαρμάκου, καθώς επίσης και η phεξαρτώμενη υδρόλυση, η οποία οδηγεί στην εκλεκτική διάλυση του φραγμού όταν βρίσκεται σε περιβάλλον με συγκεκριμένο ph, και η οποία βρίσκει ευρεία εφαρμογή στην παρασκευή εντεροδιαλυτών μορφών. Αναφέρεται ότι η αποδέσμευση καφεΐνης από συμπολυμερή μεθακρυλικού μεθυλεστέρα και μεθακρυλικού Ν,Ν-διμεθυλαμινοαιθυλεστέρα είναι αμελητέα σε ουδέτερο ph, αλλά είναι σημαντική σε όξινο περιβάλλον. Παράδειγμα DDS όπου η αποδέσμευση ενεργοποιείται απο την υδρόλυση αποτελεί το εμφύτευμα γκοζερελίνης (Zoladex ), ένος αντικαρκινικού πεπτιδίου, βασισμένο σε συμπολυμερές γαλακτικούγλυκολικού οξέος. Το συμπολυμερές υδρολύεται βαθμιαία in vivo προκαλώντας το σχηματισμό μικροπόρων απο τους οποίους αποδεσμεύεται το φάρμακο. 13
32 Τέλος, στις βιοχημικές μεθόδους συναντάται η ελεγχόμενη αποδέσμευση του φαρμάκου η οποία ενεργοποιείται από ενζυμική υδρόλυση βιοπολυμερούς το οποίο είναι συνδεδεμένο με το φάρμακο. Η υδρόλυση επιτυγχάνεται από συγκεκριμένo ένζυμο στον ιστό στόχο. Γ. Τα συστήματα στα οποία η αποδέσμευση ελέγχεται από μηχανισμό ανάδρασης αποτελούν την τρίτη γενιά Συστημάτων Ελεγχόμενης Χορήγησης δραστικών ουσιών, στην οποία η αποδέσμευση του φαρμάκου ρυθμίζεται από ένα βιοχημικά ανταποκρινόμενο αισθητήρα, ο οποίος ενσωματώνεται στο νανοφορέα. Ο αισθητήρας αυτός συνήθως ανιχνεύει μια βιολογική ουσία μέσα στο σώμα, η οποία δρα ως ενεργοποιητής για το σύστημα. Ανάλογα με τη συγκέντρωση αυτής της ουσίας, ο μηχανισμός ανάδρασης του συστήματος ρυθμίζει κατάλληλα και το ρυθμό αποδέσμευσης του εγκλωβισμένου συστατικού. Τα συστήματα αυτής της κατηγορίας διακρίνονται στα: Ρυθμιζόμενα συστήματα μέσω βιοδιάσπασης (bioerosion-regulated). Βιο-αποκρινόμενα (bioresponsive) συστήματα. Αυτό-ρυθμιζόμενα (self-regulated) συστήματα. Το αυτορυθμιζόμενο σύστημα χορήγησης ινσουλίνης αποτελεί ένα παράδειγμα της τελευταίας κατηγορίας (Εικόνα 1.9). Εικόνα 1.9: Αυτορυθμιζόμενο σύστημα χορήγησης ινσουλίνης. Δ. Τα συστήματα στόχευσης αποσκοπούν στη μεταφορά και αποδέσμευση της δραστικής ουσίας στην επιθυμητή θέση δράσης. Ως εκ τούτου, η ανάπτυξη τέτοιων συστημάτων έχει ως αποτέλεσμα τη βελτίωση της θεραπευτικής αποτελεσματικότητας των δραστικών ουσιών και τη συμμόρφωση των ασθενών. Παράλληλα συντελεί στη μείωση της εμφάνισης ανεπιθύμητων ενεργειών αφού ο στόχος αυτών των συστημάτων είναι η καταστροφή των κυττάρων που βρίσκονται στον ιστό-στόχο χωρίς να προκαλούν βλάβες στα υγιή κύτταρα. 14
33 Τα συστήματα στόχευσης περιλαμβάνουν τα εξής μέρη: 1. Τη δραστική ουσία που είναι κυρίως ισχυρά φάρμακα με αυξημένη τοξικότητα, όπως τα αντικαρκινικά. 2. Μία μη - ανοσολογική βιοδιασπώμενη πολυμερική αλυσίδα στην οποία έχει προσδεθεί μια κατευθυντήρια ομάδα (targeting moiety), η οποία κατευθύνει το σύστημα στο στόχο. 3. Ένας διαλυτοποιητής (solubiliser) ο οποίος θα ενισχύσει τη διαλυτότητα του συστήματος στα βιολογικά υγρά. 4. Επιπρόσθετα, υπάρχει ένας βραχίονας (spacer) που φέρει χημικούς δεσμούς, με τους οποίους συνδέονται τα μόρια του φαρμάκου και μπορούν να διασπαστούν μόνο από ένζυμα τα οποία βρίσκονται στα κύτταρα στόχους (Εικόνα 1.10) [34]. Εικόνα 1.10: Ιδανικό Σύστημα Ελεγχόμενης Χορήγησης και στόχευσης φαρμακευτικών ουσιών, σύμφωνα με τον Ringsdorf (1978) Παθητική και Ενεργητική στόχευση Η εκλεκτική διάθεση του συστήματος στον ιστό-στόχο συμβαίνει είτε παθητικά (passive targeting) είτε ενεργητικά (active targeting). I) Η παθητική στόχευση βασίζεται στη διαφορετική μορφολογία των αγγείων μεταξύ του υγιούς ιστού και του ιστού-στόχου. Ένα παράδειγμα στο όποιο εκμεταλλευόμαστε τη 15
34 παθητική στόχευση είναι στην περίπτωση καρκινικών όγκων, με σκοπό την εκλεκτική συσσώρευση των νανοφορέων στην περιοχή του όγκου. Πιο συγκεκριμένα, οι περισσότεροι συμπαγείς όγκοι, εμφανίζουν ιδιαίτερα παθοφυσιολογικά χαρακτηριστικά που δεν παρατηρούνται στους φυσιολογικούς ιστούς, όπως εκτεταμένη αγγειογένεση προκειμένου να καλυφθούν οι συνεχώς αυξανόμενες ανάγκες του όγκου σε οξυγόνο και θρεπτικά συστατικά. Αυτή όμως η υπερ-αγγείωση που δημιουργείται έχει δομικές ατέλειες, με διεσταλμένα, ακανόνιστα ή διαπερατά αιμοφόρα αγγεία καθώς και κακή λεμφική παροχεύτευση. Επιπλέον, τα ενδοθηλιακά κύτταρα των κυτταρικών τοιχωμάτων συχνά παρουσιάζουν μεγάλα κενά. Έτσι, αυτή η ελαττωματική αρχιτεκτονική των αιμοφόρων αγγείων του όγκου, σε συνδυασμό με τον ευρύ αυλό τους, έχει σαν αποτέλεσμα την εκτεταμένη διαρροή συστατικών του πλάσματος του αίματος μέσα στον όγκο. Ταυτόχρονα, η κακή λεμφική παροχέτευση του όγκου, οδηγεί στην κατακράτηση αυτών των συστατικών (μακρομόρια, νανοσωματίδια, λιπιδικά νανοσωματίδια) εντός του όγκου. Αυτή η ιδιαιτερότητα των καρκινικών όγκων ονομάζεται φαινόμενο ενισχυμένης διαπερατότητας και κατακράτησης (Enhanced Permeability and Retention effect, EPR) [35, 36, 37]. Μέσω αυτού του μηχανισμού λοιπόν, οι νανοφορείς μπορούν, όπως τα συστατικά του πλάσματος, να συγκεντρωθούν στον καρκινικό ιστό (Εικόνα 1.11). Σημαντική προϋπόθεση για την ικανοποιητική συγκέντρωση των νανοφορέων στο στόχο μέσω του EPR είναι η παρατεταμένη κυκλοφορία τους στο αίμα (stealth system), ώστε σταδιακά να επιτευχθεί αυξημένη εντόπισή τους μέσω της διάχυσης από τα υψηλής διαπερατότητας αιμοφόρα αγγεία του όγκου. Με βάση αυτό το φαινόμενο έχουν γίνει πολλές προσπάθειες στοχευμένης μεταφοράς και αποδέσμευσης φαρμάκων στην περιοχή του όγκου [37, 38]. Έτσι είναι δυνατό να επιτευχθούν τοπικές συγκεντρώσεις φαρμάκων έως και φορές μεγαλύτερες στην περιοχή του όγκου συγκριτικά με τους φυσιολογικούς ιστούς, σε διάστημα 1-2 ημερών. Μελέτες έχουν δείξει ότι το φαινόμενο EPR δεν είναι εφαρμόσιμο σε χαμηλού μοριακού βάρους φάρμακα εξαιτίας της γρήγορης διάχυσης τους στην κυκλοφορία του αίματος, ακολουθούμενη από νεφρική κάθαρση [37]. Τονίζεται ότι το μέγεθος πόρων των τριχοειδών των περισσότερων συμπαγών όγκων κυμαίνεται απο nm, μέγεθος αρκετά μεγαλύτερο απο το αντίστοιχο στους υγιείς ιστούς (10nm). Αποτελέσματα ερευνών με λιποσώματα διαφορετικών μέσων μεγεθών, δείχνουν ότι το όριο μεγέθους των νανοφορέων που 16
35 διεισδύουν στους όγκους είναι περίπου 400nm, ενώ άλλες έρευνες δείχνουν ότι σωματίδια με διαμέτρους μικρότερες των 200 nm είναι πιο αποτελεσματικά [39, 40]. Παρόλο όμως που η παθητική στόχευση αποτελεί τη βάση για την κλινική θεραπεία, ταυτόχρονα παρουσιάζει αρκετούς περιορισμούς. Η στόχευση των κυττάρων μέσα σ έναν όγκο δεν είναι πάντα εφικτή εξαιτίας της μη αποτελεσματικής διάχυσης μερικών φαρμάκων και της τυχαίας φύσης αυτής της προσέγγισης. Αυτός ο περιορισμός βέβαια είναι κοινός με τη συμβατική θεραπεία. Επιπλέον η παθητική στόχευση περιορίζεται απο το γεγονός ότι δεν παρουσιάζουν όλοι οι όγκοι το φαινόμενο EPR, και επειδή η διαπερατότητα των αιμοφόρων αγγείων δεν είναι η ίδια σε όλη την έκταση του όγκου. II) Η ενεργητική στόχευση βασίζεται στη μοριακή τροποποίηση της επιφάνειας των νανοφορέων. Συνήθως μέσω χημικών μεθόδων, επιτυγχάνεται η σύνδεση τους με ποικιλία παραγόντων στόχευσης, οι οποίοι αναγνωρίζονται και συνδέονται εκλεκτικά με συγκεκριμένους υποδοχείς ή αντιγόνα της επιφάνειας των κυττάρων-στόχων. Αυτοί οι παράγοντες στόχευσης συνήθως είναι πρωτεΐνες (κυρίως αντισώματα και τα κλάσματα τους), κλάσματα νουκλεϊκών οξέων (aptamers), ή άλλοι συνδέτες υποδοχέων (πεπτίδια, βιταμίνες, υδατάνθρακες, κ.α.). Γενικά, όταν χρησιμοποιείται ένας παράγοντας στόχευσης για την πρόσδεση του νανοφορέα σε καρκινικά κύτταρα, είναι αναγκαίο ο συνδέτης να προσδένεται με υψηλή εκλεκτικότητα στα μόρια που εκφράζονται στην επιφάνεια των κυττάρων. Επίσης, για τη βελτιστοποίηση της εκλεκτικότητας, κρίνεται σκόπιμο το μόριο στο οποίο θα προσδεθεί ο συνδέτης να είναι υπερ-εκφρασμένο στην επιφάνεια του κυττάρου στόχου, συγκριτικά με τα φυσιολογικά κύτταρα [39, 41]. Μόλις οι νανοφορείς αναγνωριστούν και προσδεθούν στην επιφάνεια των κύτταρων στόχων (μέσω αλληλεπιδράσης συνδέτη-υποδοχέα), τότε ανάλογα με τον συνδέτη τον οποίο φέρουν, είτε θα πραγματοποιηθεί ενδοκυττάρωση του νανοφορέα, είτε θα παραμείνει προσκολλημένος στην επιφάνεια του κυττάρου. Η πρώτη περίπτωση κρίνεται αναγκαία όταν χρειάζεται να γίνει η αποδέσμευση του φαρμάκου εντός του κυττάρου. Ενώ αντίθετα, η δεύτερη περίπτωση πλεονεκτεί σε συμπαγείς όγκους, στους οποίους η αποδέσμευση του φαρμάκου στην επιφάνεια μπορεί να σκοτώσει και τα γειτονικά καρκινικά κύτταρα, τα οποία μπορεί να μην εκφράζουν τον υποδοχέα με τον οποίο θα μπορούσε να προσδεθεί ο νανοφορέας. Οι Kim et al. έδειξαν ότι οι στοχευμένοι με φολικό οξύ πολυμερικοί νανοφορείς παρουσίασαν πάνω από 6.7 φορές μεγαλύτερη κυτταρική πρόσληψη από τους μη στοχευμένους [ 42 ]. Μια άλλη μελέτη αναφέρει πως η αύξηση της πυκνότητας του 17
36 προσδέτη στόχευσης στην επιφάνεια των νανοφορέων (0-10%), οδηγεί σε μεγαλύτερη ενδοκυτταρική πρόσληψη κατά επτά φορές [43]. Τα μειονεκτήματα της ενεργητικής στόχευσης αφορούν α) την εύρεση μη ανοσολογικών και εξαιρετικά εξειδικευμένων παραγόντων στόχευσης, η οποία προϋποθέτει τη μοριακή ανάλυση του πάσχοντα ιστού β) το ιδιαίτερα υψηλό κόστος τέτοιων συστημάτων και γ) την πιθανή επαγωγή ανοσολογικών αποκρίσεων από τους παράγοντες στόχευσης. Διαπιστώθηκε πως όταν οι νανοφορείς εκφράζουν στην επιφάνεια τους μόρια κατάλληλα για στόχευση, τότε μειώνεται ο χρόνος κυκλοφορίας τους στο αίμα, λόγω της αναγνώρισης και της επακόλουθης απόρριψής τους απο το ανοσοποιητικό σύστημα. Αυτό έχει ως αποτέλεσμα οι νανοφορείς να μην προλαβαίνουν να συγκεντρωθούν και να αποδεσμεύσουν το φάρμακο εκλεκτικά [ 44, 45 ]. Η σημασία του γεγονότος αυτού γίνεται περισσότερο αντιληπτή λαμβάνοντας υπόψη πως η διαδικασία της ενεργητικής στόχευσης προϋποθέτει την παραμονή των νανοφορέων για ικανό χρονικό διάστημα στη κυκλοφορία του αίματος, έτσι ώστε να εξασφαλιστεί η μεταφορά τους μέσω του φαινομένου EPR στους συμπαγείς όγκους. Στην Εικόνα 1.11 παρουσιάζονται οι διαδικασίες της παθητικής και ενεργητικής στόχευσης. Εικόνα 1.11: Σχηματική αναπαράσταση του μηχανισμού παθητικής στόχευσης (μέσω του φαινομένου EPR) και της ενεργητικής στόχευσης μέσω της πρόσδεσης συνδετών στην επιφάνεια των νανοφορέων [ 39]. 18
37 1.3.3 DDS στην κλινική πράξη Η έρευνα γύρω απο τα DDS εξελίσσεται με ραγδαίους ρυθμούς τα τελευταία χρόνια (Εικόνα 1.12). Μετά απο τις πρώτες εγκρίσεις κυκλοφορίας τέτοιων συστημάτων στις αρχές της δεκαετίας του 1990, σήμερα δεκάδες Συστήματα Ελεγχόμενης Χορήγησης βρίσκουν εφαρμογή στη θεραπεία αρκετών παθήσεων. Μερικά παραδείγματα DDS που έλαβαν έγκριση και χρησιμοποιούνται σήμερα στην κλινική πράξη παρουσιάζονται στον Πίνακα 1.1 και στον Πίνακα 1.2, ενώ αρκετά συστήματα βρίσκονται σε στάδιο κλινικών μελετών (Πίνακας 1.3). Εικόνα 1.12: Χρονοδιάγραμμα έγκρισης DDS [46]. Πίνακας 1.1: Παραδείγματα DDS που χρησιμοποιούνται σήμερα στη θεραπευτική [47]. 19
38 Πίνακας 1.2: Παραδείγματα DDS που χρησιμοποιούνται σήμερα στη θεραπευτική (συνέχεια) [46]. Πίνακας 1.3: Παραδείγματα DDS, για χορήγηση αντικαρκινικών φαρμάκων, που βρίσκονται σε κλινικές μελέτες [47]. 20
39 Η ενεργητική στόχευση καρκινικών κυττάρων με χρήση μονόκλονων αντισωμάτων (mab) ως παράγοντα στόχευσης, περιγράφηκε απο τον Milstein το 1981 [48]. Τις τελευταίες δύο δεκαετίες έχει μελετηθεί η στόχευση καρκινικών ιστών με 17 διαφορετικά mabs, εγκεκριμένα απο τον Αμερικάνικο οργανισμό τροφίμων και φαρμάκων (FDA). Το αντίσωμα rituximab (Rituxan ) εγκρίθηκε το 1997 για θεραπεία ασθένων με λέμφωμα non-hodgkin, ένα τύπο καρκίνου που προσβάλλει τα λεμφοκύτταρα. Ένα χρόνο αργότερα, το Trastuzumab (Herceptin ), ένα αντί-her2 mab το οποίο προσδένεται στους υποδοχείς ErbB2, εγκρίθηκε για θεραπεία του καρκίνου του μαστού. Το 2004 εγκρίθηκε για θεραπεία του καρκίνου του παχέος εντέρου ο πρώτος αναστολέας αγγειογένεσης, Bevacizumab (Avastin ) [39]. Το Bevacizumab συνδέεται με τον αυξητικό παράγοντα του αγγειακού ενδοθηλίου VEGF και ως εκ τούτου αναστέλλει τη σύνδεση του VEGF με τους υποδοχείς του (VEGFR1, VEGFR2), στην επιφάνεια των ενδοθηλιακών κυττάρων. Η εξουδετέρωση του VEGF μειώνει την αγγειογένεση των καρκινικών όγκων, αναστέλλοντας την ανάπτυξή τους [49]. Σήμερα, πάνω απο 200 DDS τροποποιημένα με αντισώματα βρίσκονται σε πρικλινικές και κλινικές μελέτες. Στον Πίνακα 1.4 παρουσιάζονται μερικά DDS για στόχευση καρκινικών όγκων με χρήση αντισωμάτων. Πίνακας 1.4: Παραδείγματα DDS για στόχευση καρκινικών ιστών με χρήση αντισωμάτων [50]. 21
40 1.4 Νανοφορείς Οι νανοφορείς είναι υπερμοριακά συστήματα (ειδικά σχεδιασμένα νανοσωματίδια) με τη χρήση των οποίων μπορεί να γίνει στόχευση καρκινικών όγκων, μεταφορά θεραπευτικών ενώσεων, γονιδίων, ή σκιαγραφικών παραγόντων. Το μέγεθος τους είναι συγκρίσιμο με αυτό των αντισωμάτων (15-30nm), ιών (20-500nm), υποδοχέων στην επιφάνεια της πλασματικής μεμβράνης, γονιδίων (2nm πλάτος, nm μήκος), πρωτεϊνών (5-50nm) και άλλων βιομορίων. Αυτά τα συστήματα μπορούν να μεταφέρουν μόρια φαρμάκου μέσω της σύνδεσης ή απορρόφησης του φαρμάκου στην επιφάνεια τους, μέσω της ενκαψυλίωσης της δραστικής ουσίας μέσα σε λιπίδια/πολυμερή ή και μέσω της διάλυσης των μορίων του φαρμάκου σε μήτρα. Αποτέλεσμα των παραπάνω σχηματισμών είναι η προστασία του φαρμάκου από το περιβάλλον και η αντικατάσταση των μη επιθυμητών βιοφαρμακευτικών ιδιοτήτων του με τις επιθυμητές ιδιότητες των νανοσωματιδίων [51]. Οι νανοφορείς ανάλογα με τη σύσταση τους διακρίνονται σε: i) Οργανικούς νανοφορείς, η σύνθεση των οποίων πραγματοποιείται εξ ολοκλήρου από οργανικά μόρια. Παραδείγματα τέτοιων νανοφορέων είναι τα λιποσώματα, τα μικκύλια, τα δενδριμερή, οι νανοσφαίρες, οι νανοκάψουλες, οι νανοσωλήνες άνθρακα και τα πολυμερικά νανοσωματίδια (συζευγμένα με φάρμακο πολυμερή) (Εικόνα 1.13) [52]. ii) Υβριδικούς νανοφορείς, οι οποίοι απαρτίζονται από οργανικά και ανόργανα τμήματα. Ο πιο χαρακτηριστικός τύπος υβριδικού νανοφορέα που χρησιμοποιείται σε βιοϊατρικές εφαρμόγες είναι μορφής πυρήνα-κελύφους (core-shell), όπου ο ανόργανος πυρήνας επικαλύπτεται με έναν πολυμερικό φλοιό ώστε να καταστεί βιοσυμβατός και βιολογικά ενεργός καθώς και για να ενισχυθεί η σταθερότητα του συστήματος. Οι σημαντικότεροι τύποι υβριδικών νανοφορέων είναι τα νανοσωματίδια χρυσού, οι κβαντικές τελείες, τα μαγνητικά νανοσωματίδια οξειδίων του σιδήρου και άλλων μετάλλων, μαγνητικά λιποσώματα καθώς και νανοσωματίδια πυριτίας (silica) (Εικόνα 1.14). 22
41 Εικόνα 1.13: Οι κυριότεροι οργανικοί νανοφορείς [53]. Εικόνα 1.14: Παράδειγμα μαγνητικού υβριδικού νανοφορέα. Τα βιομόρια τοποθετούνται σε περίπτωση που επιδιώκεται ενεργητική στόχευση [29, 54]. 23
42 Α. Λιποσώματα Τα λιποσώματα είναι μικρά, τεχνητά λιπιδικά κυστίδια τα οποία συναρμολογούνται αυθόρμητα από αμφίφιλα λιπίδια (φώσφο- και σφίγγο-λιπίδια) και στερόλη, κυρίως χοληστερόλη. Αποτελούνται από μία σφαιρική δομή διπλοστοιβάδας που περιβάλλει έναν υδατικό πυρήνα. Το μέγεθος τους κυμαίνεται από 50nm εώς 5μm. Βρίσκονται στο επίκεντρο του ερευνητικού ενδιαφέροντος ως φορείς φαρμάκων και βιολογικά δραστικών ουσιών, εξαιτίας της βιοσυμβατότητας και βιοαποικοδομησιμότητας τους καθώς και της ικανότητας τους να παγιδεύουν υδρόφιλα και υδρόφοβα φάρμακα (βλ. Πίνακες 1.1-4). Επιπλέον, υπάρχει δυνατότητα ρύθμισης των ιδιοτήτων τους όπως το μέγέθος και το επιφανειακό φορτίο τους, με την προσθήκη ποικίλων παραγόντων στη λιπιδική μεμβράνη. Τα τροποποιημένα λιποσώματα σε νανοκλίμακα έχει βρεθεί ότι εμφανίζουν εξαιρετικό φαρμακοκινητικό προφίλ κατά τη μεταφορά DNA, sirna, πρωτεϊνών και χημειοθεραπευτικών ουσιών. Ωστόσο, τα λιποσώματα παρουσιάζουν κάποια μειονεκτήματα όπως χαμηλή σταθερότητα, μειωμένη αποτελεσματικότητα ενκαψυλίωσης φαρμάκου και γρήγορη αρχική αποδέσμευση του φαρμάκου. Γίνονται προσπάθειες για εξάλειψη των παραπάνω προβλημάτων όπως για παράδειγμα την προσθήκη αλυσίδων πολυαιθυλενογλυκόλης (PEG), η οποία δημιουργεί ένα προστατευτικό στρώμα στην επιφάνεια των λιποσωμάτων με στόχο την αύξηση του χρόνου παραμονής τους στην κυκλοφορία του αίματος [51]. Ανάλογα με το μέγεθός τους και τον αριθμό των διπλοστοιβάδων τους, τα λιποσώματα μπορούν να ταξινομηθούν σε τρεις κατηγορίες: 1) πολυστοιβαδιακά κυστίδια (ΜultiLamellar Vesicle, MLV), 2) μεγάλα μονοστοιβαδιακά κυστίδια (Large Unilamellar Vesicle, LUV) και μικρά μονοστοιβαδιακά κυστίδια (Small Unilamellar Vesicle, SUV). Το μέγεθος τους κυμαίνεται γενικά από 25nm εως 2.5μm και αποτελεί κρίσιμο παράγοντα όσον αφορά το χρόνο ημιζωής τους στο κυκλοφορικό σύστημα και την έκταση του εγκλεισμού δραστικών ουσιών σε αυτά (Εικόνα 1.15). Τα λιποσώματα λόγω του αμφίφιλου χαρακτήρα τους μπορούν να χρησιμοποιηθούν τόσο ως φορείς λιπόφιλων όσο και υδρόφιλων ουσιών. Ανάλογα με τη διαλυτότητα και τα χαρακτηριστικά κατανομής της προς εγκλωβισμό ουσίας, εντοπίζονται σε διαφορετικά σημεία του κυστιδίου των λιποσωμάτων και έχουν διαφορετική παγίδευση και ιδιότητες απεδέσμευσης. Οι ισχυρά λιπόφιλες ουσίες παγιδεύονται σχεδόν αποκλειστικά 24
43 στη λιπιδική διπλοστοιβάδα, ενώ οι υδρόφιλες ουσίες εγκλωβίζονται στον εσωτερικό υδατικό πυρήνα των λιποσωμάτων. Εικόνα 1.15: Διάκριση Λιποσωμάτων ανάλογα με το μέγεθος τους [55]. Β. Πολυμερικά μικκύλια Τα πολυμερικά μικκύλια σχηματίζονται αυθόρμητα όταν αμφίφιλα συμπολυμερή βρεθούν σε υδατικό περιβάλλον, σχηματίζοντας δομή πυρήνα κελύφους. Ο πυρήνας των μικκυλίων είναι υδρόφοβος και εκεί εγκλωβίζονται υδρόφοβα μόρια ή νανοσωματίδια με απλή ενκαψυλίωση ή με ομοιοπολική σύνδεση. Ο πυρήνας περιβάλλεται από υδρόφιλο πολυμερές (συνήθως PEG) το οποίο με τη σειρά του προσδίδει στα μικκύλια μεγάλη σταθερότητα σε υδατικά μέσα. Πιο συγκεκριμένα, το πολυμερές παρατείνει την κυκλοφορία των μικυλλίων στο αίμα εμποδίζοντας τη φαγοκυττάρωση τους και ταυτόχρονα αυξάνει τη συσσώρευση τους στον ιστό-στόχο. Πολυλειτουργικά πολυμερικά μικκύλια που περιέχουν προσδέτες στόχευσης, θεραπευτικούς παράγοντες και παράγοντες απεικόνισης αναπτύσσονται με έντονους ρυθμούς [50, 56] (βλ. Πίνακες 1.1-4). Γ. Δενδριμερή Ένα δενδριμερές είναι ένα συνθετικό πολυμερικό μακρομόριο με διαστάσεις νανομέτρων, που αποτελείται από πολλαπλά, ιδιαίτερα διακλαδισμένα μονομερή που «αναδύονται» ακτινωτά από τον κεντρικό πυρήνα (η δομή τους ομοιάζει με αυτή των δέντρων). Η χημική τους σύσταση και το μοριακό τους βάρος μπορούν να ρυθμιστούν με μεγάλη ακρίβεια σε αντίθεση με τα γραμμικά πολυμερή. Επιπρόσθετα, εμφανίζουν μεγάλη ομοιομορφία με πολύ μικρή διασπορά μεγέθους, το οποίο δεν ξεπερνά τα 10nm. Στις ιδιότητες τους, που τα κατατάσσουν σε Συστήματα Ελεγχόμενης Χορήγησης Φαρμάκων, είναι η υδατοδιαλυτότητα που εμφανίζουν, η βιοσυμβατότητα και η γρήγορη απομάκρυνση τους από την κυκλοφορία του αίματος μέσω των νεφρών εξαιτίας του μικρού τους μεγέθους, ελαχιστοποιώντας την ανάγκη για βιοδιάσπαση. Αν και το μικρό 25
44 τους μέγεθος δεν επιτρέπει υψηλό ποσοστό εγκλεισμού των φαρμάκων, η αύξηση της επιφάνειας λόγω της ύπαρξης των διακλαδώσεων προκαλεί την αύξηση του ποσοστού της φόρτωσης των φαρμάκων στην εξωτερική επιφάνεια των δενδριμερών, μέσω ομοιοπολικής σύνδεσης ή ηλεκτροστατικών αλληλεπιδράσεων. Ωστόσο, η τοξικότητα και η αντιγονικότητα που εμφανίζουν τα δενδριμερή, αποτελούν βασικό πρόβλημα για τη χρησιμοποίηση τους στην εκλεκτική στόχευση των φαρμάκων in vivo [29, 51]. Δ. Συζευγμένα με φάρμακο πολυμερή (Polymer-Drug conjugate) Ένα άλλο είδος νανοσωματιδίων μεταφοράς φαρμάκων, τα συζευγμένα με φάρμακο πολυμερή, έχουν μελετηθεί εκτενώς τα τελευταία χρόνια [41]. Η σύζευξη του φαρμάκου με το πολυμερές όχι μόνο παρατείνει τον in vivo χρόνο κυκλοφορίας από μερικά λεπτά εώς αρκετές ώρες, αλλά επίσης μειώνει την κυτταρική πρόσληψη κατά μήκος της ενδοκυτταρικής πορείας. Αυτά τα χαρακτηριστικά βοηθούν την παθητική μεταφορά των φαρμάκων σε ιστούς με διαπερατά αιμοφόρα αγγεία, όπως είναι για παράδειγμα των συμπαγών όγκων. Οι μεγάλες προκλήσεις των περισσότερων συζευγμένων με φάρμακο πολυμερών περιλαμβάνουν την τοξικότητα, την ανοσογονικότητα, τη μη ειδική βιοκατανομή, την in vivo αστάθεια, τη χαμηλή ικανότητα μεταφοράς φαρμάκου, την ταχεία αποδέσμευση του φαρμάκου καθώς επίσης και προκλήσεις που σχετίζονται με τη σύνθεση τους. Η εισαγωγή του PEG στη κλινική χρήση στις αρχές του 1990, προκάλεσε κατακόρυφη αύξηση της εμφάνισης συζευγμάτων PEG-φαρμάκου στην αγορά (Πίνακας 1.1). Η σύξευξη με PEG ενισχύει τη σταθερότητα και τη διαλυτότητα του φαρμάκου στο πλάσμα, μειώνοντας παράλληλα την ανοσογονικότητα του φαρμάκου. Εκτός από το PEG, άλλα πολυμερή όπως το πολυγλουταμινικό οξύ (PGA), Ν-(2-υδροξυπρόπυλο) μεθυλακρυλαμίδιο (HPMA), πολύ-γαλακτικό οξύ (PLA), πολύ-γλυκολικό οξύ (PLGA) και τα αλγινικά έχουν μελετηθεί ως πολυμερικοί φορείς μεταφοράς φαρμάκων [55]. Ε. Νανοσφαίρες Τα νανοσωματίδια αυτά είναι σφαιρικές δομές που αποτελούνται από ένα σύστημα μήτρας, στην οποία το φάρμακο κατανέμεται κατά τον εγκλωβισμό, τη σύνδεση, ή την ενκαψυλίωση του. Η επιφάνεια της σφαίρας μπορεί να τροποποιηθεί με την προσθήκη πολυμερών και βιολογικών υλικών, ενώ μπορούν να συνδεθούν αντισώματα για ενεργητική στόχευση [57]. 26
45 ΣΤ. Νανοκάψουλες Οι νανοφορείς αυτοί είναι κυστικά συστήματα με μια κεντρική κοιλότητα ή πυρήνα στον οποίο εγκλείεται το φάρμακο. Ο πυρήνας περιβάλλεται από μια εξωτερική πολυμερική μεμβράνη, στην επιφάνεια της οποίας μπορούν να προσδεθούν ομάδες στόχευσης ή αντισώματα. Το υλικό του πυρήνα μπορεί να είναι στερεό, υγρό ή αέριο, ενώ το περιβάλλον του πυρήνα μπορεί να είναι υδατικό ή λιπαρό [57]. Σε αυτή την κατηγορία κατατάσσονται τα αυτογαλακτοποιούμενα και τα αυτομικρογαλακτοποιούμενα Συστήματα Ελεγχόμενης Χορήγησης (SEDDS και SMEDDS αντίστοιχα). Η. Νανοσωλήνες Άνθρακα Οι νανοσωλήνες άνθρακα (carbon nanotubes ή buckytubes) είναι κύλινδροι άνθρακα, που αποτελούνται από δακτύλιους βενζολίου και έχουν χρησιμοποιηθεί στον τομέα της βιολογίας ως αισθητήρες για την ανίχνευση του DNA και πρωτεϊνών, ως διαγνωστικές συσκευές για τη διάκριση των διαφορετικών πρωτεϊνών από δείγματα ορού, και ως φορείς πρωτεϊνών [58]. Οι νανοσωλήνες άνθρακα είναι ελάχιστα διαλυτοί σε πολλούς διαλύτες, δημιουργώντας κάποιους προβληματισμούς όσον αφορά την τοξικότητας τους. Ωστόσο, η χημική τροποποίησή τους μπορεί να τους καταστήσει υδατοδιαλυτούς και ικανούς να συνδεθούν με μια ποικιλία μορίων όπως πεπτίδια, πρωτεΐνες, νουκλεϊκά οξέα, και θεραπευτικούς παράγοντες [ 59 ]. Αντιμυκητιασικοί παράγοντες (αμφοτερικίνη Β) και αντικαρκινικά φάρμακα (μεθοτρεξάτη) έχουν συνδεθεί ομοιοπολικά με νανοσωλήνες άνθρακα, ενώ μια in vitro μελέτη αναφέρει πως τα φάρμακα που δεσμεύτηκαν σε νανοσωλήνες άνθρακα έδειξαν να εσωτερικεύονται πιο αποτελεσματικά εντός των κυττάρων σε σύγκριση με τα ελεύθερα φάρμακα και να έχουν ισχυρή αντιμυκητιασική δράση [60, 61]. Οι πολλαπλές ομοιοπολικές τροποποιήσεις στο πλευρικό τοίχωμα ή στις άκρες των νανοσωλήνων άνθρακα, τους επιτρέπει να μεταφέρουν πολλά μόρια ταυτόχρονα, στρατηγική η οποία παρέχει ένα θεμελιώδες πλεονέκτημα στη θεραπεία του καρκίνου [55]. Παρ όλα αυτά, το μέγεθος (μερικα μm σε μήκος) και κυρίως η υψηλή τοξικότητας τους είναι απαγορευτικοί παράγοντες για χρήση αυτών των δομών σε DDS. Παρόμοιες δομές είναι τα φουλερένια (fullerene ή buckyballs), τα οποία έχουν σφαιρική ή ελλειψοειδή διαμόρφωση αντί κυλινδρική (Εικόνα 1.16). 27
46 Εικόνα 1.16: Δομή Φουλερενίου [62]. 1.5 Φυσικοχημικοί περιορισμοί DDS Όπως λέχθηκε πιο πάνω, οι ιδιότητες του νανοφορέα διαδραματίζουν καθοριστικό ρόλο όσον αφορά την in vivo συμπεριφορά (βιοκατανομή, φαρμακοκινητικό προφίλ) του DDS. Οι νανοφορείς θα πρέπει να είναι βιοσυμβατοί ή/και βιοαποικοδομήσιμοι, έτσι ώστε να μην εγείρουν προβλήματα ανοσογονικότητας. Επιπλέον θα πρεπεί να είναι είτε υδατοδιαλυτοί είτε υδρόφιλοι (κολλοειδείς διασπορές) και να χαρακτηρίζονται απο μεγάλο χρόνο παραμονής στην κυκλοφορία του αίματος, έτσι ώστε να παρέχεται ικανό χρονικό διάστημα για ελεγχόμενη αποδέσμευση του φαρμάκου. Πλήν του ελεγχόμενου ρυθμού αποδέσμευσης, τα DDS θα πρέπει να εντοπίζονται εκλεκτικά στο όργανο-στόχο, ελαχιστοποιώντας έτσι τις ανεπιθύμητες ενέργειες απο τη δράση του φαρμάκου στα υγιή όργανα-ιστούς. Τέλος, όπου απαιτείται, θα πρέπει να παρουσιάζουν υψηλή ενδοκυτταρική πρόσληψη [39]. Οι κυριότεροι περιορισμοί για την ενδοφλέβια (IV) χορήγηση των DDS είναι οι ακόλουθοι [17, 25, 63, 64] : Α. Μέγεθος Το μέγεθος των νανοφορέων αποτελεί καθοριστικό παράγοντα όσον αφορά το χρόνο ημιζωής τέτοιων συστημάτων. Η μικρότερη διάμετρος των τριχοειδών αγγείων του ανθρώπινου οργανισμού είναι 4μm. Έτσι, η χορήγηση νανοσωματίδιων μεγαλύτερου μεγέθους οδηγεί σε πνευμονική εμβολή και θάνατο. Υπο φυσιολογικές συνθήκες, νανοσωματίδια με μέγεθος (διάμετρο) πέραν των 10nm δεν μπορούν να διαπεράσουν το αγγειακό ενδοθήλιο. Σε παθολογικές καταστάσεις όμως (φλεγμονή, συμπαγείς καρκινικοί όγκοι), το μέγεθος πόρων των τριχοειδών αγγείων της πάσχουσας περιοχής αυξάνεται σημαντικά, επιτρέποντας τη διαπέραση νανοσωματιδίων μεγέθους μέχρι και 780nm. Η ενδοφλέβια έγχυση ουσιών με μέγεθος μεγαλύτερο των 200nm, οδηγεί σε ταχεία απομάκρυνση τους απο την κυκλοφορία του αίματος λόγω αναγνώρισής τους απο τα 28
47 φαγοκύτταρα του δικτυοενδοθηλιακού συστήματος (RES: συκώτι, σπλήνα, μυελός των οστών και λεμφαδένες). Έτσι, 15 λεπτά μετά την έγχυση, τα νανοσωματίδια εντοπίζονται κυρίως στο συκώτι και στο σπλήνα. Στον αντίποδα, νανοσωματίδια μικρότερα των 5nm παρουσιάζουν επίσης μικρούς χρόνους ημιζωής, λόγω ταχείας αποβολής τους μέσω νεφρικής κάθαρσης. Γίνεται λοιπόν αντιληπτό πως το μέγεθος των νανοφορέων, για παρατετάμενη κυκλοφορία τους στο αίμα, θα πρέπει να κυμαίνεται απο 5-200nm (σε αυστηρότερα πλαίσια: nm). Το επιθυμητό μέγεθος των νανοφορέων εξαρτάται απο τη φυσιολογία του οργάνου-στόχου, π.χ για παθήσεις του κεντρικού νευρικού συστήματος οι νανοφορείς δεν θα πρέπει να ξεπερνούν τα 50nm, λόγω της ιδιαίτερης δομής του αιματεγκεφαλικού φραγμού (BBB). Το μέγεθος των νανοφορέων δεν επηρεάζει μόνο την βιοκατανομή τους, αλλά και την ικανότητα αποδέσμευσης του φαρμάκου. Μικρότερα σωματίδια έχουν μεγαλύτερη επιφάνεια, και ως εκ τούτου το μεγαλύτερο μέρος του φαρμάκου θα είναι συνδεδεμένο στην επιφάνεια των σωματιδίων (ή κοντά σε αυτήν), οδηγώντας έτσι σε ταχεία αποδέσμευση του φαρμάκου. Ενώ, τα μεγαλύτερα σωματίδια έχουν μεγάλους πυρήνες που επιτρέπουν μεγαλύτερη ενκαψυλίωση του φαρμάκου αλλά και πιο αργή αρχική αποδέσμευση, εξαιτίας της μεγαλύτερης απόστασης που πρέπει να διανύσει το φάρμακο για να διέλθει εκτός του νανοφορέα [65]. Μικρότερα σωματίδια έχουν επίσης μεγαλύτερο κίνδυνο συσσωμάτωσης κατά τη διάρκεια της αποθήκευσης και της μεταφοράς τους. Αποτελεί πρόκληση ο σχηματισμός νανοσωματιδίων με το μικρότερο δυνατό μέγεθος, αλλά με τη μέγιστη σταθερότητα. Β. Επιφανειακό φορτίο και υδροφοβικότητα Γενικά, απαιτούνται υψηλές τιμές ζ-δυναμικού (±40mV) για να αποφευχθεί η συσσωμάτωση των νανοφορέων in vivo, που θα οδηγούσε σε απειλητικά για τη ζωή φαινόμενα (σχηματισμός θρόμβων). Απο την άλλη πλευρά, το υψηλό επιφανειακό φορτίο (θετικό ή αρνητικό) οδήγει σε φαγοκυττάρωση μεγαλύτερης έκτασης, που έχει ως επακόλουθο τη μέιωση του χρόνου παραμονής των νανοφορέων στη γενική κυκλοφορία. Νανοφορείς αρνητικά φορτισμένοι παρουσιάζουν μικρότερη κυτταρική πρόσληψη, λόγω ηλεκτροστατικής άπωσης απο τις αρνητικά φορτισμένες κυτταρικές μεμβράνες του οργανισμού. Αντιθέτως, το θετικό επιφανειακό φορτίο προάγει την μη ειδική προσκόλληση των νανοφορέων στις βιολογικές μεμβράνες (π.χ DNA) μέσω ηλεκτροστατικής έλξης, γεγονός που εξηγεί τη μεγαλύτερη τοξικότητα των κατιονικών νανοσωματιδίων σε σχέση με 29
48 τα ανιονικά. Γενικά, όσο πιο έντονα κατιονικός είναι ο νανοφορέας τόσο πιο τοξικός είναι για τον οργανισμό [66]. Μετά απο I.V χορήγηση, πρωτεϊνες του αίματος (IgG, Cb3) προσκολλώνται στην επιφάνεια των νανοσωματιδίων. Το αποτέλεσμα αυτής της σύνδεσης είναι η αναγνώριση των νανοφορέων απο τα φαγοκύτταρα του RES και η ταχύτατη απομάκρυνση τους απο την κυκλοφορία του αίματος. Η διαδικασία αυτή ονομάζεται οψωνινοποίηση και οι πρωτεϊνες που μεσολαβούν ονομάζονται οψωνίνες (Είκονα 1.17). Όσο μεγαλύτερο το μέγεθος, το φορτίο και η υδροφοβικότητα των νανοφορέων, τόσο μεγαλύτερη η έκταση της οψωνινοποίησης. Έτσι, για να εξασφαλιστεί μεγαλός χρόνος παραμονής των συστημάτων αυτών στην κυκοφορία του αίματος (stealth systems) θα πρέπει να έχουν μικρό μέγεθος (<200nm), ουδέτερο επιφανειακό φορτίο (ή το μικρότερο δυνατόν, κατ απόλυτη τιμή, για να μην συσσωματώνονται) καθώς και υψηλή υδροφιλικότητα. Η ελάττωση της έκτασης της οψωνινοποίησης των νανοφορέων μπορεί να επιτευχθεί μέσω επιφανειακής τροποποίησής τους με υδρόφιλα πολυμερή, όπως το PEG, η δεξτράνη το πολυαιθελενοξείδιο (PEO) κ.α., τα οποία παρέχουν ένα δυναμικό «νέφος» υδρόφιλων και ουδέτερων αλυσίδων στην επιφάνεια των νανοφορέων, το οποίο απωθεί τις πρωτεΐνες του πλάσματος και εμποδίζει την γρήγορη απομάκρυνση τους από το κυκλοφορικό σύστημα. Εικόνα 1.17: Διαδικασία οψωνινοποίησης [67]. Γ. Σχήμα Μια μελέτη αναφέρει πως οι νανοφορείς με ανισοτροπική δομή επιδεικνύουν μεγαλύτερη ικανότητας αποφυγής της απομάκρυνσης τους απο την κυκλοφορία του αίματος [64, 68]. Οι Geng et al. αναφέρουν ότι αυξηση του λόγου μήκος:πλάτος των νανοφορέων οδηγεί σε αύξηση του χρόνου παραμονής τους στη γενική κυκλοφορία [69]. 30
49 1.6 Κολλοειδή Τα κολλοειδή είναι μία διασπορά σωματιδίων μίας ουσίας (διεσπαρμένη φάση) στη μάζα μίας άλλης ουσίας ή διαλύματος (μέσο διασποράς ή συνεχής φάση). Όλοι οι νανοφορείς είναι κολλοειδή συστήματα. Ένα τυπικό παράδειγμα κολλοειδούς είναι η ομίχλη, η οποία συνίσταται από πολύ μικρά σταγονίδια νερού (διεσπαρμένη φάση) μέσα σε αέρα (μέσο διασποράς). Τα κολλοειδή χαρακτηρίζονται σύμφωνα με την κατάσταση της διεσπαρμένης φάσης και του μέσου διασποράς σε στερεά, υγρά και αέρια [21]. Ένα κολλοειδές διάλυμα διαφέρει από ένα πραγματικό διάλυμα λόγω του μεγαλύτερου μεγέθους των σωματιδίων της διασπαρμένης φάσης (1-1000nm και <1nm για τα κολλοειδή και τα διαλύματα αντίστοιχα), παρ όλα αυτά είναι πολύ μικρά για μακροσκοπική παρατήρηση. Το μέγεθος των κολλοειδών σωματιδίων εμπίπτει σε τέτοια κλίμακα μεγέθους, ώστε να υπόκεινται σε κίνηση Brown (αναλύεται παρακάτω). Ένα κολλοειδές διάλυμα μακροσκοπικά εμφανίζεται να είναι ομογενές επειδή τα διεσπαρμένα σωματίδια είναι πολύ μικρά, όμως και αρκετά μεγάλα σε σχέση με τα (μακρο)μοριακά διαλύματα.. Όταν μάλιστα το μέγεθος τους εμπίπτει στην κλίμακα του μήκους κύματος του ορατού φωτός, τότε προκαλούν σκέδαση του φωτός. Το φαινόμενο αυτό είναι γνωστό ως φαινόμενο Tyndall, και έχει ως αποτέλεσμα το κολλοειδές να εμφανίζεται θολό [70]. Εξαιτίας του μεγέθους τους, ο λόγος της επιφάνειας προς τον όγκο είναι πολύ μεγάλος και συνεπώς πολλά άτομα βρίσκονται στη διεπιφάνεια ανάμεσα στη μια και στην άλλη φάση (π.χ. στερεή-υγρή σε μια διασπορά στερεών κολλοειδών σωματιδίων σε διαλύτη). Έτσι, τα επιφανειακά φαινόμενα και οι αλληλεπιδράσεις με το περιβάλλον παίζουν σημαντικό ρόλο στη συμπεριφορά των κολλοειδών συστημάτων [71]. Κολλοειδή συστήματα αποτελούμενα από σωματίδια χρυσού ήταν ήδη γνωστά πολλούς αιώνες πριν, ενώ η φύση τους αναγνωρίστηκε το 1774 από τους Juncher και Macquer, ως σωματίδια χρυσού σε κατάσταση λεπτού διαμερισμού μέσα σε ένα ρευστό. Το 1861 σηματοδοτεί τη χρονολογία έναρξης μιας συστηματικής έρευνας των κολλοειδών συστημάτων από τον Thomas Graham. Ο Graham έκανε τη διάκριση μεταξύ δυο ειδών αιωρημάτων: αιωρήματα στα οποία τα διεσπαρμένα είδη μπορούν να διαχέονται μέσω μεμβράνης και αιωρήματα στα οποία δεν παρατηρούνταν διάχυση μέσω μεμβράνης. Ο Graham έδωσε στο τελευταίο είδος αιωρημάτων την ονομασία «κολλοειδή». Τα 31
50 κολλοειδή δεν διαχέονται μέσω μεμβράνης, πολύ απλά επειδή τα διασπαρμένα σωματίδια είναι μεγαλύτερα από τους πόρους της μεμβράνης [11, 72]. Κίνηση Brown (Brownian motion) Τα διεσπαρμένα σωματίδια ενός κολλοειδούς βρίσκονται σε συνεχή κίνηση προς τις τρεις διευθύνσεις του χώρου και σε περιστροφή, λόγω των συγκρούσεών τους με τα μόρια του διαλύτη. Η κίνηση αυτή είναι άτακτη και χαρακτηρίζεται ως κίνηση Brown. Ο Einstein μελέτησε πρώτος την κίνηση κολλοειδών σωματιδίων χρησιμοποιώντας τη θεωρία των πιθανοτήτων. Κατέληξε στο συμπέρασμα ότι η μέση τιμή του τετραγώνου της μετατόπισης του σωματιδίου που πραγματοποιεί κίνηση Brown είναι συνάρτηση του χρόνου t, της θερμοκρασίας T, της ακτίνας του σωματιδίου r και του ιξώδους του μέσου n, βάση της Εξίσωσης 1.1 [73] : dx 2 = 2t RT N 1 6πnr (Εξίσωση 1.1) όπου, R η σταθερά των αερίων (8.31 J/mol K), Ν ο αριθμός Avogadro (6, mol -1 ) και π η μαθηματική σταθερά (3,14159). Η κίνηση Brown των σωματιδίων έχει ως συνέπεια τη διάχυσή τους προς περιοχές του μέσου με μικρότερη συγκέντρωση σωματιδίων. Η ποσότητα α (σε mol) των σωματιδίων που διαχέονται στη μονάδα του χρόνου ανά μονάδα επιφανείας (mol s -1 m -2 ) δίνεται από το νόμο του Fick (Εξίσωση 1.2): α = D dc dx (Εξίσωση 1.2) όπου, D ο συντελεστής διάχυσης των σωματιδίων στο μέσο και dc/dx η βαθμίδα της συγκέντρωσης των σωματιδίων στη διεύθυνση x. Συνδυάζοντας τις δύο παραπάνω σχέσεις ο Einstein υπολόγισε τη σταθερά διάχυσης D των κολλοειδών σωματιδίων συναρτήσει της θερμοκρασίας Τ του κολλοειδούς, της ακτίνας του σωματιδίου r και του ιξώδους του μέσου n (Εξίσωση 1.3): D = dx2 2t = KT 6πnr (Εξίσωση 1.3) όπου, Κ η σταθερά του Boltzmann ( J K -1 ), D ο συντελεστής διάχυσης, r η υδροδυναμική ακτίνα, T η απόλυτη θερμοκρασία και n το ιξώδες. 32
51 Η εξίσωση αυτή χρησιμοποιείται ευρέως για την εκτίμηση των διαστάσεων κολλοειδών σωματιδίων με την τεχνική της δυναμικής σκέδασης φωτός, η οποία αναφέρεται σε επόμενο κεφάλαιο. Το άνω και κάτω όριο για το μέγεθος ενός σωματιδίου ώστε να χαρακτηριστεί ως κολλοειδές δεν είναι αυστηρά καθορισμένα. Το ελάχιστο μέγεθος ενός κολλοειδούς καθορίζεται από την απαίτηση ότι η δομή του διαλύτη σε μοριακή κλίμακα είναι τέτοια ώστε, η αλληλεπίδραση του κολλοειδούς σωματιδίου με τα μόρια του διαλύτη να περιγράφεται με ένα στατιστικό τρόπο. Με άλλα λόγια, θεωρείται ότι πολλά μόρια διαλύτη αλληλεπιδρούν ταυτόχρονα με την επιφάνεια ενός και μόνο κολλοειδούς σωματιδίου. Η αλληλεπίδραση του κολλοειδούς σωματιδίου με τα μόρια του διαλύτη μπορεί τότε να περιγραφεί με τις μακροσκοπικές εξισώσεις κίνησης των ρευστών. Έτσι, η κίνηση Brown χαρακτηρίζεται από τις μακροσκοπικές ιδιότητες του διαλύτη (όπως είναι το ιξώδες και η θερμοκρασία). Τα παραπάνω ικανοποιούνται όταν το μέγεθος του κολλοειδούς σωματιδίου είναι τουλάχιστον περίπου δέκα φορές η γραμμική διάσταση ενός μορίου διαλύτη. Επομένως, το ελάχιστο μέγεθος ενός σωματιδίου Brown είναι 1nm. Το μέγιστο μέγεθος ενός κολλοειδούς σωματιδίου καθορίζεται από την απαίτηση να συμπεριφέρεται ως ένα μεγάλο μόριο, γεγονός που συνεπάγεται ότι αυτό υπόκειται σε έντονη θερμική κίνηση (κίνηση Brown). Η θερμική κίνηση έχει νόημα μόνο όταν οι θερμικές μετατοπίσεις αποτελούν ένα μετρήσιμο κλάσμα της γραμμικής διάστασης του σωματιδίου, κατά τη διάρκεια των τυπικών πειραματικών χρόνων. Για παράδειγμα, ένα μεγάλο σώμα, όπως ένα τούβλο στο νερό (πριν να βυθιστεί στον πυθμένα του δοχείου) εμφανίζει και αυτό θερμική κίνηση, ωστόσο οι μετατοπίσεις σε σχέση με το μέγεθός του σε μια τυπική πειραματική χρονική κλίμακα είναι εξαιρετικά μικρές. Σε ένα τέτοιο σύστημα η θερμική κίνηση δεν έχει νόημα. Από τη στιγμή που η θερμική κίνηση είναι σημαντική σε διαδικασίες που περιγράφουν αιωρήματα μεγάλων αντικειμένων, τα αντικείμενα αυτά χαρακτηρίζονται ως κολλοειδή ή σωματίδια Brown. Η παραδοχή αυτή περιορίζει το μέγεθος των κολλοειδών σωματιδίων σε 10μm [11, 71]. 33
52 1.6.1 Διάκριση Κολλοειδών Τα κολλοειδή, στα οποία το μέσο διασποράς είναι νερό, μπορούν να διακριθούν σε δύο κατηγορίες: τα υδρόφιλα και τα υδρόφοβα κολλοειδή. α) Υδρόφιλο κολλοειδές, είναι ένα κολλοειδές στο οποίο υπάρχει μία ισχυρή έλξη μεταξύ διεσπαρμένης φάσης και μέσου διασποράς (νερού). Αυτού του τύπου τα κολλοειδή εμφανίζουν σταθερότητα διότι έλκουν τα μόρια του νερού μέσα στο διάλυμα (ενυδατώνονται). Τυπικά παραδείγματα υδρόφιλων κολλοειδών είναι τα τασιενεργά μόρια (π.χ. τα σαπούνια), οι πολυσακχαρίτες (π.χ. το άμυλο) και οι πρωτεΐνες (π.χ. ο ορός του αίματος, το γάλα). β) Υδρόφοβο κολλοειδές, είναι ένα κολλοειδές στο οποίο υπάρχει έλλειψη έλξεων μεταξύ διεσπαρμένης φάσης και μέσου διασποράς (νερού). Τα υδρόφοβα κολλοειδή δεν έχουν συγγένεια με το νερό και η σταθερότητα τους, δηλαδή η παραμονή τους εν αιωρήσει, εξαρτάται απο το μοριακό, οργανικό ή ιοντικό στρώμα που τα περιβάλλει. Έτσι, αν δοθεί επαρκής χρόνος, η διεσπαρμένη φάση συσσωματώνεται σε μεγαλύτερα σωματίδια Κολλοειδής σταθερότητα Σύμφωνα με τις βασικές αρχές της θερμοδυναμικής, οι μεταβολές σε ένα θερμοδυναμικό σύστημα συμβαίνουν στην κατεύθυνση ελαττώσεως της ελεύθερης ενέργειας. Γενικώς, τα κολλοειδή συστήματα είναι ασταθή θερμοδυναμικά λόγω της μεγάλης επιφάνειας που εμφανίζουν στη διαχωριστική επιφάνεια του συνεχούς από το ασυνεχές μέσο. Λόγω αυτής της μεγάλης επιφάνειας, η θερμοδυναμική ισορροπία επιτάσσει μείωση της ελεύθερης επιφανειακής ενέργειας. Η σταθερότητα των κολλοειδών καθορίζεται από τις αλληλεπιδράσεις των σωματιδίων μεταξύ τους. Δύο είναι οι βασικοί τύποι αυτών των αλληλεπιδράσεων, οι απωστικές (αλληλεπίδραση ηλεκτρικών διπλοστοιβάδων) και οι ελκτικές (δυνάμεις Van der Waals). Όταν υπερισχύουν οι ελκτικές δυνάμεις, τα σωματίδια θα συσσωματωθούν και τελικά το κολλοειδές θα καθιζάνει. Αντιθέτως, όταν υπερισχύουν οι απωστικές δυνάμεις, το σύστημα θα βρίσκεται σε μία σταθερή κατάσταση και θα διατηρήσει τον κολλοειδή του χαρακτήρα, το οποίο είναι και το επιθυμητό αποτέλεσμα. 34
53 Δυνάμεις Van der Waals Οι δυνάμεις αυτές είναι η κύρια αιτία συσσωμάτωσης στα κολλοειδή συστήματα. Υπάρχουν ακόμα και αν τα άτομα ή τα μόρια είναι ηλεκτρικά ουδέτερα. Οι δυνάμεις Van der Waals οφείλονται σε αλληλεπιδράσεις μεταξύ μόνιμων διπόλων (δυνάμεις διπόλου-διπόλου), μεταξύ μόνιμων και επαγόμενων διπόλων (διπόλου-επαγόμενου διπόλου) και μεταξύ επαγόμενων διπόλων (επαγόμενου διπόλου-επαγόμενου διπόλου). Με εξαίρεση τα έντονα πολικά μόρια, η κυριότερη συνεισφορά στις δυνάμεις van der Waals είναι αυτή που προέρχεται από τις δυνάμεις μεταξύ επαγόμενων διπόλων (δυνάμεις London). Οι δυνάμεις αυτές είναι σχετικά μικρής εμβέλειας και μπορούν να επικαλυφθούν από τις μεγαλύτερης εμβέλειας απωστικές δυνάμεις. Για να αποφευχθεί η συσσωμάτωση θα πρέπει να υπερνικήθουν οι ελκτικές δυνάμεις, μέσω σταθεροποίησης των κολλοειδών. Αυτό επιτυγχάνεται είτε με σταθεροποίηση μέσω ηλεκτροστατικών απώσεων (αλληλεπίδραση ηλεκτρικών διπλοστοιβάδων) είτε μέσω στερικών αλληλεπιδράσεων. A. Ηλεκτροστατική σταθεροποίηση Οι περισσότερες ουσίες αποκτούν ένα επιφανειακό ηλεκτρικό φορτίο όταν έρχονται σε επαφή με ένα πολικό μέσο (π.χ νερό). Έτσι, όταν σωματίδια διασπείρονται σε ένα υδατικό σύστημα εμφανίζουν ένα επιφανειακό φορτίο εξαιτίας του ιονισμού των επιφανειακών χημικών ομάδων τους ή προσρόφησης φορτισμένων μορίων ή ιόντων. Η ανάπτυξη τέτοιων φορτίων έχει σαν αποτέλεσμα τη μεταβολή της συγκέντρωσης των ιόντων του διαλύματος κοντά στην επιφάνεια των σωματιδίων, δημιουργώντας ένα στρώμα (αποτελούμενο απο δύο μέρη) γύρω από αυτά με διαφορετική κατανομή ιόντων από αυτή του κυρίου όγκου του διαλύματος. Το εσωτερικό μέρος ονομάζεται στρώμα Stern (Stern layer) και αποτελείται από ιόντα τα οποία είναι ισχυρά συνδεδεμένα με τα σωματίδια, λόγω των ετερόνυμων φορτίων τους. Το εξωτερικό μέρος δημιουργείται από διάχυση ασθενέστερα συνδεδεμένων ιόντων του διαλύματος. Στο διάχυτο στρώμα υπάρχει ένα νοητό όριο μέσα στο οποίο ιόντα και μόρια διαλύτη αλληλεπιδρούν αρκετά ισχυρά με τη φορτισμένη επιφάνεια του σωματιδίου, σχηματίζοντας μια σταθερή οντότητα με το σωματίδιο. Το όριο αυτό ονομάζεται επίπεδο ολίσθησης (slipping plane). Το ηλεκτρικό δυναμικό το οποίο υπάρχει στο εξωτερικό μέρος αυτού του ορίου (επίπεδο ολίσθησης) ονομάζεται ζ-δυναμικό (ζ-potential) [74] και αποτελεί ένδειξη του επιφανειακού φορτίου των σωματιδίων (Εικόνα 1.18). Για αυτό το λόγο απαντάται και με τον όρο φαινόμενο επιφανειακό φορτίο. 35
54 Οι ηλεκτροστατικές απωστικές δυνάμεις είναι αποτέλεσμα της αλληλοδιείσδυσης των στρωμάτων διάχυσης των ηλεκτρικών διπλοστοιβάδων του κάθε φορτισμένου σωματιδίου. Το μέγεθος του ζ-δυναμικού δίνει μια ένδειξη της δυναμικής σταθερότητας του κολλοειδούς συστήματος. Αν τα σωματίδια στο διάλυμα εχουν μεγαλή τιμή ζ-δυναμικού, κατ απόλυτη τιμή, θα επικρατούσε η τάση να απομακρυνθούν το ένα από το άλλο και έτσι δεν θα δημιουργείτο το κολλοειδές. Ωστόσο, αν τα σωματίδια έχουν τιμή ζ-δυναμικού κοντά στο μηδέν, τότε δεν υπάρχει καμία δύναμη να τα αποτρέψει από το να έρθουν κοντά και να συσσωματωθούν, λόγω των ελκτικών δυνάμεων Van der Waals. Για το λόγο αυτό, σωματίδια με ζ-δυναμικό μεγαλύτερο από ±40mV θεωρούνται θερμοδυναμικώς σταθερά. Εικόνα 1.18: Σχηματική απεικόνιση της διασποράς των ιόντων του διαλύματος γύρω από ένα φορτισμένο σωματίδιο, και προσδιορισμός του ζ-δυναμικού [75]. Β. Στερική Σταθεροποίηση Η στερική σταθεροποίηση επιτυγχάνεται μέσω πολυμερικής επικάλυψης της επιφάνειας των σωματιδίων. Όταν δύο τέτοιες επιφάνειες προσεγγίσουν η μία την άλλη, θα δεχθούν μία δύναμη καθώς τα εξωτερικά τους τμήματα αρχίσουν να διαπλέκονται. Αυτή η αλληλεπίδραση συνήθως οδηγεί σε απωστικές δυνάμεις επειδή η συμπίεση των πολυμερικών αλυσίδων των δύο επιφανειών δεν ευνοείται εντροπικά (Εικόνα 1.19) [76]. Η στερική άπωση είναι δύσκολο να προβλεφθεί και να ποσοτικοποιηθεί, ενώ έχει περιγραφεί θεωρητικά για τα πολυμερή. Οι δυνάμεις που εμπλέκονται σε αυτές τις αλληλεπιδράσεις εξαρτώνται i) από την ποσοτική κάλυψη των επιφανειών με πολυμερές, ii) αν το πολυμερές είναι ελεύθερο μέσα στο διάλυμα ή χημειοροφημένο στην επιφάνεια των σωματιδίων και iii) από τη φύση του 36
55 μέσου διασποράς, το οποίο καθορίζει τη διαμόρφωση των πολυμερικών αλυσίδων (έκταση ή συστολή). Εικόνα 1.19: Ηλεκτροστατική και στερική σταθεροποίηση των σωματιδίων [77]. Γ. Θεωρία DLVO (Derjaguin-Landau-Verwey-Overbeek) Η σταθερότητα του κολλοειδούς εξαρτάται από την ισορροπία μεταξύ ελκτικών και απωστικών αλληλεπιδράσεων. Ένα κολλοειδές αιώρημα παραμένει σταθερό όταν οι απωστικές ηλεκτροστατικές δυνάμεις (V R ) υπερισχύουν των ελκτικών (V A ), με αποτέλεσμα τα σωματίδια να παραμένουν εν αιωρήσει και να μην μπορούν να έλθουν σε επαφή μεταξύ τους για να συσσωματωθούν (Εικόνα 1.20). Εικόνα 1.20: Σχηματική απεικόνιση των διασωματιδιακών δυνάμεων. Η σταθερότητα των κολλοειδών είναι το αποτέλεσμα της επικράτησης των απωστικών δυνάμεων, ενώ υπερίσχυση των ελκτικών δυνάμεων οδηγεί σε συσσωμάτωση. Η θεωρία DLVO αφορά το συνολικό δυναμικό των αλληλεπιδράσεων (Εικόνα 1.21), το οποίο είναι το άθροισμα των απωστικών (Coulomb) και ελκτικών (Van der Waals) δυνάμεων [78]. Η επίδραση των ελκτικών δυνάμεων Van der Waals θα είναι κυρίαρχη στις μικρές και στις μεγάλες διασωματιδιακές αποστάσεις, ενώ στις ενδιάμεσες αποστάσεις θα 37
56 επικρατεί η ηλεκτροστατική άπωση των διπλοστοιβάδων (δυνάμεις Coulomb). Στη δεύτερη περίπτωση δημιουργείται ένα ενεργειακό φράγμα (Vmax) όπου, όταν τα σωματίδια πλησιάσουν αρκετά και εάν η κινητική τους ενέργεια μετά απο κάποια σύγκρουση είναι μικρότερη απο αυτό, δεν είναι σε θέση να το περάσουν και το σύστημα δεν συσσωματώνεται (Εικόνα 1.21). Γι αυτό, τα κολλοειδή αυτά χαρακτηρίζονται ως κινητικώς σταθερά. Εικόνα 1.21: Συνολικό δυναμικό ηλεκτρικά φορτισμένων σωματιδίων συναρτήσει της μεταξύ τους απόστασης. coagulation Εικόνα 1.22: Το δυναμικό DLVO. Στην κάμπυλη του δυναμικού DLVO (Εικόνα 1.22) υπάρχει και ένα δεύτερο ελάχιστο (σε μεγαλύτερες διασωματιδιακές αποστάσεις), στο οποίο μπορεί να υπάρξει μία σχετικά αδύναμη συσσωμάτωση των κολλοειδών σωματιδίων η οποία όμως είναι αντιστρέψιμη, σε αντίθεση με τη συσσωμάτωση των σωματιδίων στο πρώτο ελάχιστο η οποία είναι μη αναστρέψιμη (μικρές διασωματιδιακές αποστάσεις). 38
57 Τα κολλοειδή που έχουν σταθεροποιηθεί μέσω επιφανειακού φορτίου (ηλεκτροστατική σταθεροποίηση) είναι πολύ ευαίσθητα στην παρουσία ηλεκτρολυτών. Αύξηση της συγκέντρωσης ηλεκτρολυτών εντός του διαλύματος έχει σαν αποτέλεσμα τη συμπίεση της ηλεκτρικής διπλοστοιβάδας, που έχει ως επακόλουθο τη μείωση ή και την εξαφάνιση του ενεργειακού φράγματος (Vmax). Εν τη απουσία του ενεργειακού φράγματος, η συνολική αλληλεπίδραση μεταξύ των σωματιδίων θα είναι καθαρά ελκτική και έτσι η σταθερότητα του κολλοειδούς θα καταρρεύσει με επακόλουθη συσσωμάτωση (Εικόνα 1.23). Εικόνα 1.23: Η προοδευτική αύξηση της συγκέντρωσης των ηλεκτρολυτών οδηγεί σε μείωση ή και εξαφάνιση του ενεργειακού φράγματος, που έχει ως αποτέλεσμα τη συσσωμάτωση του συστήματος. 39
58 1.7 Υπερπαραμαγνητικά νανοσωματίδια οξειδίου του σιδήρου (Superparamagnetic Iron Oxide Nanoparticles, SPIONs) Τα νανοσωματίδια ή νανοκρυσταλλίτες οξειδίου του σιδήρου βρίσκονται τα τελευταία χρόνια στο επίκεντρο του ερευνητικού ενδιαφέροντος. Η βιοσυμβατότητα και η ελάχιστη τοξικότητα που παρουσιάζουν σε συνδυασμό με την υπερπαραμαγνητική τους φύση λόγω του μεγέθους τους (<20nm), είναι αξιόλογες ιδιότητες που εκμεταλλευόμαστε σε βιοϊατρικές εφαρμογές όπως: απεικόνιση μαγνητικού συντονισμού (MRI), μαγνητική στόχευση φαρμάκων και θεραπεία του καρκίνου μέσω επαγώμενης μαγνητικής υπερθερμίας. Ο μαγνητίτης (Fe 3 O 4 ) και ο μαγκεμίτης (γ-fe 2 O 3 ) είναι τα κυρίοτερα οξείδια του σιδήρου, ενώ ο αιματίτης (α-fe 2 O 3 ) και ο βουστίτης (FeO) δεν αποτελούν αντικείμενο κλινικής μελέτης λόγω των ασθενών μαγνητικών ιδιοτήτων τους Μαγνητίτης και Μαγκεμίτης Ο μαγνητίτης (Fe 3 O 4 ) είναι ορυκτό του σιδήρου και είναι το πιο μαγνητικό ορυκτό που υπάρχει στη γη. Είναι σιδηρομαγνητικός σε θερμοκρασία περιβάλλοντος και έχει θερμοκρασία Curie 805ºΚ (η θερμοκρασία αλλαγής από τη σιδηρομαγνητική συμπεριφορά στην παραμαγνητική). Η ιδιότητα που έχει ο μαγνητίτης να έλκει μικρά κομμάτια σιδήρου έκανε τον άνθρωπο από την αρχαιότητα να ανακαλύψει την έννοια του μαγνητισμού. Ο μαγνητίτης ανήκει σε μια σημαντική κατηγορία μεταλλικών οξειδίων, που ονομάζονται φερρίτες. Το σημαντικότερο δομικό χαρακτηριστικό του μαγνητίτη είναι ότι διαθέτει ιόντα σιδήρου σε δισθενή και τρισθενή οξειδωτική βαθμίδα, με αποτέλεσμα να μπορεί να λειτουργήσει και ως οξειδωτικό και ως αναγωγικό μέσο. Κρυσταλλώνεται σε ολοεδρία κατά το κυβικό σύστημα, έχει χρώμα σκούρο καφέ έως μαύρο και μεταλλική λάμψη. Βρίσκεται σε κοκκώδη και φλοιώδη συσσωματώματα υπό μορφή κόκκων με το όνομα «μαγνητίτης άμμος» [79]. Το ορυκτό αυτό περιέχει περίπου 72.4%wt. σίδηρο και 27.6%wt. οξυγόνο και έχει δομή αντίστροφου σπινελίου, ενώ χημικά αναφέρεται ως επιτεταρτοξείδιο του σιδήρου. Το σπινέλιο είναι μια κατηγορία μεικτών μεταλλικών οξειδίων με χημικό τύπο ΑΒ 2 Ο 4. Συνήθως το Α είναι δισθενές άτομο, ατομικής ακτίνας pm (Mg, Fe, Mn, Zn, Cu) και 40
59 καταλαμβάνει θέσεις τετραεδρικής και οκταεδρικής συμμετρίας μέσα στον κρύσταλλο, ενώ το Β είναι τρισθενές άτομο ακτίνας 75-90pm (Ti, Fe, Al, Co) και καταλαμβάνει οκταεδρικές θέσεις. Ένα χαρακτηριστικό παράδειγμα σπινελίου είναι το ορυκτό οξείδιο μαγνησίου και αργιλίου, MgAl 2 O 4. Τα αντίστροφα σπινέλια έχουν τα Β άτομα στις τετραεδρικές θέσεις ενώ τα Α και Β στις οκταεδρικές (Εικόνα 1.24). Το αντίστροφο αυτό μοντέλο προτάθηκε για τον μαγνητίτη έτσι ώστε να εξηγηθεί η γρήγορη διαπίδυση (hoping) και συνεχής ανταλλαγή ηλεκτρονίων μεταξύ των Fe 2+ και Fe 3+ στις οκταεδρικές θέσεις. Γι αυτό το λόγο, η ακριβής χημική δομή του είναι [Fe 3+ (Fe 3+ Fe 2+ )O 4 ]. Εικόνα 1.24: Δομή του μαγνητίτη (α) Πολυεδρικό μοντέλο με εναλλασσόμενα οκταεδρικά και τετραεδρικά επίπεδα. (β) Μοντέλο σφαιρών με σκιαγραφημένη τη μοναδιαία κυψελίδα. (γ) Μοντέλο σφαιρών όπου απεικονίζονται τρείς οκτάεδρικες και δύο τετράεδρικές θέσεις [79]. Ο μαγκεμίτης (γ-fe 2 O 3 ) είναι μέλος της οικογένειας των οξειδίων. Έχει παρόμοια δομή με αυτή του μαγνητίτη, αλλά μόνο τα 5/6 των συνολικών τετραεδρικών και οκταεδρικών θέσεων καταλαμβάνονται από άτομα σιδήρου. Αποτελείται περίπου από 69.9%wt. σίδηρο και 30.1%wt. οξυγόνο [79]. Σε θερμοκρασία δωματίου, ο μαγνητίτης οξειδώνεται σε μαγκεμίτη με αργό ρυθμό, οδηγώντας σε ασθενέστερο μαγνητισμό. Ο μηχανισμός οξείδωσης είναι αρκετά περίπλοκος. H βασική διαφορά του με τον μαγνητίτη, είναι ότι όλα τα κατιόντα σιδήρου του μαγκεμίτη βρίσκονται στην τρισθενή κατάσταση (Fe 3+ ) [80]. Οι ιδιότητες του μαγνητίτη και του μαγκεμίτη παρουσιάζονται παρακάτω στον Πίνακα 1.5 [81]. 41
60 Πίνακας 1.5: Φυσικές και μαγνητικές ιδιότητες των κυριοτέρων οξειδίων του σιδήρου Μαγνητισμός Ο μαγνητισμός είναι το φαινόμενο κατά το οποίο, υλικά και κινούμενα φορτισμένα σωματίδια ασκούν ελκτικές και απωστικές δυνάμεις, καθώς και ροπές, σε άλλα υλικά ή φορτισμένα σωματίδια. Ένα άτομο χαρακτηρίζεται ως μαγνητικό, όταν έχει μη μηδενική μαγνητική ροπή. Μερικά γνωστά υλικά που διαθέτουν εύκολα ανιχνεύσιμες μαγνητικές ιδιότητες (ονομάζονται μαγνήτες) είναι το νικέλιο, ο σίδηρος, το κοβάλτιο, το γαδολίνιο και τα κράματά τους. Όλα τα υλικά επηρεάζονται, σε μεγαλύτερο ή μικρότερο βαθμό, από την παρουσία ενός μαγνητικού πεδίου. Η ύπαρξη μαγνητικών φαινομένων αποδίδεται στην τροχιακή κίνηση και στο spin των ηλεκτρονίων [82]. Κάθε ηλεκτρόνιο έχει δύο μαγνητικές ροπές οφειλόμενες στις δύο περιστροφικές κινήσεις του: γύρω από τον πυρήνα του ατόμου, αλλά και γύρω από τον άξονά τους (spin). Μαγνητική ροπή ονομάζεται το διανυσματικό μέγεθος της έντασης του μαγνητικού πεδίου που δημιουργεί η κίνηση του ηλεκτρονίου. Στα διάφορα άτομα, η συνισταμένη μαγνητική ροπή των ηλεκτρονίων μπορεί να είναι μηδενική ή και διάφορη του μηδενός. Όπως είναι γνωστό από την ενεργειακή κατανομή των ηλεκτρονίων στα άτομα, σε κάθε τροχιακό συγκεκριμένου ενεργειακού επιπέδου υπάρχουν το πολύ δύο ηλεκτρόνια με αντίθετους κβαντικούς αριθμούς του spin, δηλαδή δύο ηλεκτρόνια τα οποία περιστρέφονται με αντίθετη φορά γύρω από τον άξονά τους. Επομένως, τα ηλεκτρόνια 42
61 αυτά θα έχουν αντίθετες μαγνητικές ροπές, και όταν τα τροχιακά είναι πλήρη η συνολική μαγνητική ροπή στο άτομο θα είναι ίση με μηδέν. Στην περίπτωση τώρα που ο αριθμός των ηλεκτρονίων σε ένα άτομο είναι μονός, θα περιμέναμε με βάση τα παραπάνω το άτομο να έχει μαγνητική ροπή διάφορη του μηδενός, λόγω του μονήρους ασύζευκτου ηλεκτρονίου. Όμως, επειδή στα περισσότερα άτομα των στοιχείων, το μονήρες ηλεκτρόνιο είναι ηλεκτρόνιο της εξωτερικής ενεργειακής στάθμης (ηλεκτρόνιο σθένους), παρατηρείται αλληλεπίδραση των ηλεκτρονίων σθένους των διαφορετικών ατόμων, τα οποία συνδέονται μεταξύ τους και σχηματίζουν χημικούς δεσμούς, με αποτέλεσμα οι μαγνητικές τους ροπές να αλληλοεξουδετερώνονται και έτσι να μην παρουσιάζεται μαγνητική ροπή στα υλικά αυτά. Ωστόσο ορισμένα στοιχεία έχουν εσωτερικά ενεργειακά επίπεδα ασυμπλήρωτα. Συγκεκριμένα τα μεταβατικά στοιχεία παρουσιάζουν μερικώς συμπληρωμένα τα 3d τροχιακά τους ενώ διαθέτουν ηλεκτρόνια και στη τέταρτη κύρια ενεργειακή στάθμη. Για παράδειγμα ο χαλκός και το χρώμιο έχουν από ένα ασύζευκτο ηλεκτρόνιο σθένους στο 4s τροχιακό τους, του οποίου η μαγνητική ροπή εξουδετερώνεται από τα ηλεκτρόνια σθένους των άλλων ατόμων. Επίσης, ο χαλκός έχει συμπληρωμένα και τα πέντε 3d τροχιακά του και επομένως δεν εμφανίζει μόνιμη διπολική ροπή. Στοιχεία όπως ο σίδηρος έχουν στα 3d τροχιακά τους ασύζευκτα ηλεκτρόνια με παράλληλα spin και επομένως τα άτομα αυτά παρουσιάζουν μόνιμη μαγνητική ροπή, έντασης ανάλογης του αριθμού των ασύζευκτων ηλεκτρονίων, και συμπεριφέρονται σαν μαγνητικά δίπολα [29]. Όταν μαγνητικό πεδίο (Η) εφαρμόζεται σε υλικό, η απόκριση του υλικού ονομάζεται μαγνητική επαγωγή (Β). Η σχέση μεταξύ Η και Β είναι ιδιότητα του ίδιου του υλικού. Σε μερικά υλικά (όπως και στο κενό) το Β είναι γραμμικά ανάλογο του Η, αλλά εν γένει η σχέση τους είναι αρκετά πιο πολύπλοκη. Η σχέση (Εξίσωση 1.4) που συνδέει αυτές τις δύο ποσότητες σε μονάδες SI είναι : B = μ 0 (H + M) (Εξίσωση 1.4) όπου μ 0 είναι η μαγνητική διαπερατότητα του κενού και Μ είναι η μαγνήτιση του μέσου. Το πεδίο ενός υλικού παρουσία εξωτερικού μαγνητικού πεδίου ονομάζεται μαγνήτιση Μ και ορίζεται ως η μαγνητική ροπή (m) ανά μονάδα όγκου (V) (Εξίσωση 1.5). Μ = m V (Εξίσωση 1.5) 43
62 H Μ είναι ιδιότητα του υλικού και εξαρτάται τόσο από τις επιμέρους μαγνητικές ροπές των ιόντων, ατόμων ή μορίων, όσο και από τον τρόπο που οι ροπές αυτές αλληλεπιδρούν μεταξύ τους. Όλα τα υλικά είναι μαγνητικά ως ένα βαθμό. Η απόκρισή τους εξαρτάται από την ατομική τους δομή, τη θερμοκρασία και το πεδίο. Παρουσία μαγνητικού πεδίου, οι μαγνητικές ροπές των ατόμων τείνουν να διευθετηθούν παράλληλα με αυτό, όμως η τάση αυτή αντισταθμίζεται από τις θερμικές τους κινήσεις [21]. Ο βαθμός απόκρισης ενός υλικού σε ένα εφαρμοζόμενο πεδίο ποσοτικοποιείται μέσω της μαγνητικής επιδεκτικότητας (χ) και καθορίζεται από την Εξίσωση 1.6 (νόμος Curie-Weiss). χ = Μ Η (Εξίσωση 1.6) Οι μετασχηματισμοί των εξισώσεων και οι μονάδες δίνονται στους πίνακες που ακολουθούν (Πίνακες 1.6-7) [μ ο =4π 10 7 V s/(a m)]. Πίνακας 1.6: Μετασχηματισμοί εξισώσεων [82]. Πίνακας 1.7: Μετασχηματισμοί μονάδων [82] Τύποι Μαγνητισμού Όταν ένα μαγνητικό υλικό τοποθετηθεί εντός μαγνητικού πεδίου, μπορεί να παρατηρηθεί αύξηση ή μείωση της πυκνότητας των δυναμικών γραμμών που το διαπερνούν. Γενικά, η πυκνότητα της ροής εντός ενός υλικού είναι διαφορετική απ ότι έξω απ αυτό. Τα μαγνητικά υλικά μπορούν να ενταχθούν σε κατηγορίες ανάλογα με τη διαφορά ανάμεσα στην εξωτερική και εσωτερική μαγνητική ροή (Εικόνα 1.25). Αν η πυκνότητα μέσα στο υλικό είναι μικρότερη απ ότι έξω από το υλικό, τότε το υλικό αυτό ονομάζεται διαμαγνητικό. Τα υλικά αυτά έχουν την τάση να αποκλείουν το μαγνητικό πεδίο από το εσωτερικό τους. Αν η πυκνότητα στο εσωτερικό είναι μεγαλύτερη από ότι στο εξωτερικό, 44
63 τότε το υλικό είναι είτε παραμαγνητικό είτε σιδηρομαγνητικό. Το πρόθεμα αναφέρεται στην φύση των αλληλεπιδράσεων της σύζευξης μεταξύ των ηλεκτρονίων μέσα στο υλικό. Εικόνα 1.25: Διαφοροποιήσεις στην πυκνότητα των δυναμικών γραμμών εντός του υλικού ανάλογα με το είδος του [83]. Συναντώνται οι παρακάτω τύποι μαγνητισμού ανάλογα με τη συμπεριφορά των υλικών στην επίδραση εξωτερικού μαγνητικού πεδίου [21, 29] : Α. Ο διαμαγνητισμός είναι μια πολύ ασθενής μορφή μαγνητισμού, η οποία δεν είναι μόνιμη και διαρκεί μόνο όσο εφαρμόζεται ένα εξωτερικό μαγνητικό πεδίο. Στα διαμαγνητικά υλικά, χωρίς την παρουσία κάποιου εξωτερικού μαγνητικού πεδίου, σε κάθε άτομο, οι ροπές λόγω των ηλεκτρονιακών spin είναι αντίρροπες μεταξύ τους όπως επίσης και οι μαγνητικές ροπές λόγω της τροχιακής κίνησης των ηλεκτρονίων, με αποτέλεσμα, μακροσκοπικά, η ολική μαγνητική ροπή να είναι μηδενική. Υπό την επίδραση ενός εξωτερικού μαγνητικού πεδίου τα τροχιακά των ηλεκτρονίων των ατόμων τροποποιούνται, διότι σύμφωνα με το νόμο του Laplace ένα ηλεκτρικό φορτίο όταν κινείται εντός ενός μαγνητικού πεδίου αποκλίνει από την πορεία του. Aυτή η τροποποίηση των τροχιακών και επομένως των μαγνητικών ροπών των ατόμων, οδηγεί στο σχηματισμό μικρών μαγνητικών διπόλων μέσα στα άτομα που αντιτίθενται στο εξωτερικό πεδίο, με συνέπεια ένα αρνητικό μαγνητικό αποτέλεσμα. Αυτό έχει σαν συνέπεια την άπωση των διαμαγνητικών υλικών από κάποιο μόνιμο μαγνήτη. Τα υλικά αυτά παρουσιάζουν πολύ μικρή μαγνήτιση Μ, αρνητικές τιμές επιδεκτικότητας χ = και πολύ 45
64 μικρές σχετικές διαπερατότητες, λίγο μικρότερες από τη μονάδα. Παράδειγμα διαμαγνητικών υλικών είναι ο χαλκός, ο άργυρος, ο χρυσός, το διαμάντι και το βισμούθιο. Β. Στα παραμαγνητικά υλικά οι μαγνητικές ροπές που σχετίζονται με τα ηλεκτρόνια και τα spin τους μέσα σ ένα άτομο δεν αλληλοαναιρούνται απουσία εξωτερικού μαγνητικού πεδίου. Συνεπώς, κάθε άτομο έχει μια μικρή μαγνητική ροπή η διεύθυνση της οποίας όμως είναι τυχαία, γι αυτό και η ολική μαγνητική ροπή μιας μεγάλης περιοχής δείγματος, όπως και η ολική μαγνήτιση Μ, είναι μηδενικές απουσία εξωτερικού μαγνητικού πεδίου. Όταν εφαρμοστεί εξωτερικό πεδίο τότε τα μαγνητικά δίπολα προσανατολίζονται ελαφρώς κατά τη διεύθυνση του μαγνητικού πεδίου και δίνουν μία μη μηδενική μαγνήτιση Μ παράλληλη προς αυτό. Τα παραμαγνητικά υλικά έλκονται ελαφρά από ένα μόνιμο μαγνήτη. Όπως ο διαμαγνητισμός, έτσι και ο παραμαγνητισμός είναι ένα αντιστρεπτό φαινόμενο. Στα παραμαγνητικά υλικά, οι μαγνητικές επιδεκτικότητες έχουν μικρές θετικές τιμές χ= και οι σχετικές διαπερατότητες είναι λίγο μεγαλύτερες από τη μονάδα. Παράδειγμα παραμαγνητικών υλικών είναι το αλουμίνιο, το μαγγάνιο και ο λευκόχρυσος. Γ. Σε αντίθεση με τα παραμαγνητικά και τα διαμαγνητικά υλικά, κατά το σιδηρομαγνητισμό στα σιδηρομαγνητικά υλικά, τα άτομα απουσία εξωτερικού μαγνητικού πεδίου, παρουσιάζουν πολύ ισχυρές μαγνητικές ροπές που οφείλονται στα ασύζευκτα ηλεκτρονιακά spin στα 3d τροχιακά. Αυτές οι μαγνητικές ροπές συσχετίζονται και δημιουργούν περιοχές μαγνητικών περιοχών ή περιοχών Weiss, διαφόρων μεγεθών και σχημάτων, από ομόρροπα spin. Οι διαστάσεις των περιοχών αυτών εξαρτώνται από την προηγούμενη μαγνητική κατάσταση του υλικού και τη φύση του και ποικίλουν από 1 μm μέχρι και μερικά χιλιοστά. Τα όρια ανάμεσα στις μαγνητικές περιοχές ονομάζονται τοιχώματα Bloch (Εικόνα 1.26). Εκεί, η διεύθυνση των μαγνητικών ροπών αλλάζει συνεχώς και σταδιακά. Εικόνα 1.26: Τοίχωμα Bloch ανάμεσα σε δυο μαγνητικές περιοχές Weiss [84]. 46
65 Σε μακροσκοπική κλίμακα όμως η ολική μαγνήτιση Μ απουσία εξωτερικού μαγνητικού πεδίου είναι μηδέν, διότι οι περιοχές είναι τυχαία προσανατολισμένες και οι μαγνητικές ροπές των διαφόρων ατόμων αλληλοαναιρούνται. Όταν εφαρμοστεί εξωτερικό μαγνητικό πεδίο η συνολική μαγνήτιση είναι μεγάλη δίνοντας πολύ μεγάλες επιδεκτικότητες χ= Στη συνέχεια, όταν το εξωτερικό μαγνητικό πεδίο απομακρυνθεί, οι μαγνητικές ροπές των διαφόρων ατόμων διατηρούν τον προηγούμενο προσανατολισμό τους και παραμένει μια ολική μόνιμη μαγνήτιση Μ. Βλέπουμε λοιπόν ότι η μαγνήτιση ενός σιδηρομαγνητικού υλικού είναι διαφορετική σε μακροσκοπική κλίμακα μετά την απομάκρυνση ενός εξωτερικού πεδίου, δηλαδή η μαγνητική του κατάσταση εξαρτάται από την προηγούμενή του κατάσταση. Έτσι, η εξάρτηση της μαγνήτισης Μ από το εφαρμοζόμενο μαγνητικό πεδίο δεν είναι γραμμική αλλά σχηματίζει ένα βρόγχο υστέρησης (Εικόνα 1.28). Επιπλέον, οι τιμές της επιδεκτικότητας και της διαπερατότητας δεν είναι σταθερές αλλά μεταβάλλονται. Παράδειγμα σιδηρομαγνητικών υλικών είναι ο σίδηρος, το κοβάλτιο και το νικέλιο. Δ. Κατά τον αντισιδηρομαγνητισμό, στα υλικά παρουσία μαγνητικού πεδίου παρατηρείται αντιπαράλληλος προσανατολισμός των μαγνητικών ατομικών ροπών με αποτέλεσμα το μηδενισμό της εσωτερικής τους μαγνητικής ροπής. Τέτοια συμπεριφορά παρουσιάζουν τα μεταβατικά στοιχεία Cr και Mn όπως και ενώσεις των μεταβατικών στοιχείων με αμέταλλα, όπως MnO, NiO και MnS. Η διαφορά μεταξύ σιδηρομαγνητισμού και αντισιδηρομαγνητισμού βρίσκεται στις αλληλεπιδράσεις μεταξύ των μαγνητικών ροπών γειτονικών ατόμων, δηλαδή εάν αυτές ενισχύονται ή αντιτίθενται η μία στην άλλη αντίστοιχα (Εικόνα 1.27). Ε. Στο σιδηριμαγνητισμό, τα ιόντα από τα οποία αποτελούνται τα υλικά παρουσιάζουν διαφορετικές μαγνητικές ροπές, οι οποίες υπό την επίδραση ενός εξωτερικού μαγνητικού πεδίου προσανατολίζονται αντιπαράλληλα, δηλαδή κάποια ιόντα προσανατολίζουν τις μαγνητικές τους ροπές παράλληλα προς το πεδίο και κάποια άλλα αντίθετα. Επειδή όμως οι μαγνητικές ροπές των διαφορετικών ιόντων είναι διαφορετικού μεγέθους, προκύπτει τελικά μια συνισταμένη μαγνητική ροπή διάφορη του μηδενός, η οποία προκαλεί ενίσχυση του μαγνητικού πεδίου. Όταν το υλικό αυτό βρίσκεται μέσα σε μαγνητικό πεδίο, παρουσιάζει μεγάλες τιμές διαπερατότητας, όχι όμως τόσο μεγάλες όσο των σιδηρομαγνητών. Τα κυριώτερα σιδηριμαγνητικά υλικά είναι οι φερρίτες, οι οποίοι είναι μικτά οξείδια του σιδήρου με άλλα μέταλλα. Oι φερρίτες έχουν και αυτοί μαγνητικές περιοχές και βρόγχους υστέρησης όπως τα σιδηρομαγνητικά υλικά. 47
66 Εικόνα 1.27: Ευθυγράμμιση μεμονομένων ατομικών μαγνητικών ροπών για τους διάφορους τύπους μαγνητισμού [81]. 48
67 1.7.3 Μαγνητικές νανοδομές και Υπερπαραμαγνητισμός Ο νανομαγνητισμός αποτελεί εξέλιξη του βασικού μαγνητισμού, εστιάζοντας στα σύγχρονα νανομαγνητικά υλικά και στα σχετικά με τις διαστάσεις τους φαινόμενα, όπως είναι ο υπερπαραμαγνητισμός, η σύζευξη ανταλλαγής και τα φαινόμενα υβριδισμού που οδηγούν σε εμφάνιση μαγνητικής ροπής σε μη μαγνητικά υλικά. Ο υπερπαραμαγνητισμός είναι μία μοναδική ιδιότητα που εμφανίζουν οι νανοδομές που είναι κατασκευασμένες από σιδηρομαγνητικό ή σιδηριμαγνητικό υλικό και βρίσκονται κάτω από ένα ορισμένο μέγεθος (10-20nm). Ειδικά για την περίπτωση των οξειδίων του σιδήρου, το μέγεθος αυτό παίρνει τιμές <20nm. Η ονομασία αυτή έχει δοθεί επειδή τα σωματίδια δείχνουν συμπεριφορά παρόμοια με αυτή των παραμαγνητικών υλικών, αλλά με πολύ μεγαλύτερες μαγνητικές ροπές. Έτσι, σε μεγέθη μικρότερα απο ~20nm τα νανοσωματίδια αυτά εμφανίζουν υπερπαραμαγνητική συμπεριφορά, ενώ σε μεγέθη >20nm εμφανίζουν σιδηρο- ή σιδηριμαγνητική συμπεριφορά. Σε ενδιάμεσες περιπτώσεις, η αυξηση του μεγέθους των νανοκρυσταλλίτων οδηγεί σε αύξηση των μαγνητικών ιδιοτήτων τους (αύξηση της μαγνήτισης κόρου) (Εικόνα 1.28). Εικόνα 1.28: Αριστερά: Καμπύλες υστέρησης (Μαγνήτιση Vs Ένταση μαγνητικού πεδίου) για τα σιδηρο-, δια-, παρα- και υπερ-παραμαγνητικά υλικά. Τα σιδηρομαγνητικά υλικά παρουσιάζουν βρόγχο υστέρησης, λόγω παραμένουσας μαγνήτισης μετά την απομάκρυνση του μαγνητικού πεδίου. Τα υπερπαραμαγνητικά υλικά εμφανίζουν υψηλότερη μαγνητική ροπή (Μαγνήτιση) σε σχέση με τα παραμαγνητικά, ενω η μαγνητική ροπή είναι μηδενική μετά την απομάκρυνση του μαγνητικού πεδίου (απουσία βρόγχου υστέρησης και παραμένουσας μαγνήτισης) [17]. Δεξιά: Εξάρτηση της μαγνήτισης κόρου απο το μέγεθος των νανοκρυσταλλιτών [85] Απόκριση σε εξωτερικά μαγνητικά πεδία Σημαντικό ρόλο στις εφαρμογές των μαγνητικών νανοκολλοειδών διαδραματίζει η μαγνητική τους ροπή. Τα μαγνητικά νανοκολλοειδή που παρασκευάζονται, έχουν συνήθως μεγέθη της τάξης των 5-20 nm. Σε αυτά τα μεγέθη, ένα σημαντικό μέρος των ατόμων 49
68 βρίσκεται στην επιφάνεια των σωματιδίων (υψηλός λόγος επιφάνειας:όγκο). Τα spin όμως αυτών των ατόμων, τείνουν να δυσκολεύονται να ευθυγραμμιστούν με το εξωτερικό μαγνητικό πεδίο, παρουσιάζοντας έτσι μία ελαφριά απόκλιση, σε αντίθεση με τα spin των εσωτερικών ατόμων. Έτσι, στην επιφάνεια του νανοσωματιδίου δημιουργείται ένα στρώμα μη-ευθυγραμμισμένων spin, που έχει σαν αποτέλεσμα τη μείωση της συνολικής μαγνήτισης του νανοσωματιδίου (Εικόνα 1.29). Εικόνα 1.29: Σχηματική απεικόνιση της διαφορετικής ευθυγράμμισης των επιφανειακών spin στα νανοσωματίδια [85]. Το γεγονός αυτό, δυσχεραίνει τον έλεγχο της κίνησής τους στον οργανισμό με τη χρήση μαγνητικών πεδίων. Επομένως, περιορίζει και τη χρήση τους σε εφαρμογές μαγνητικής στόχευσης ιστών. Ένας τρόπος για να αυξηθεί η μαγνητική ροπή των σωματιδίων, είναι να αυξηθεί αρκετά το μέγεθός τους. Κάτι τέτοιο όμως, θα σήμαινε τη μετάβαση των SPIONs από την υπερπαραμαγνητική στη σιδηρομαγνητική κατάσταση (κρίσιμη διάμετρος ~20nm για Fe 3 O 4 ), με αποτέλεσμα τα νανοσωματίδια να μην διασπείρονται πλέον αποτελεσματικά. Μία στρατηγική για την αντιμετώπιση αυτού του εμποδίου, είναι η σύνθεση κολλοειδών πλειάδων (colloidal clusters) μαγνητικών νανοκρυσταλλιτών (Εικόνα 1.30). Με αυτόν τον τρόπο, εξασφαλίζεται το πλεονέκτημα της αύξησης της μαγνητικής ροπής ανά κολλοειδές σωματίδιο (δηλαδή του όγκου μαγνητικού υλικού ανά κολλοειδές σωματίδιο), με ταυτόχρονη διατήρηση των υπερπαραμαγνητικών χαρακτηριστικών. Η σημασία της αύξησης του όγκου του μαγνητικού υλικού ανά κολλοειδές σωματίδιο, γίνεται καλύτερα αντιληπτή, αν ληφθεί υπόψη πως η απόκριση ενός μαγνητικού σωματιδίου σε βαθμίδα μαγνητικού πεδίου περιγράφεται από την παρακάτω εξίσωση [86]. (Εξίσωση 1.7) 50
69 όπου F η μαγνητική δύναμη που ασκείται στο μαγνητικό υλικό, Vt ο συνολικός όγκος του μαγνητικού υλικού που υπάρχει σε κάθε κολλοειδές σωματίδιο, B η μαγνητική επαγωγή και Ms η μαγνήτιση κόρου. Οπότε, η παράμετρος που καθορίζει το πως αποκρίνεται το κολλοειδές σωματίδιο είναι το ποσό του μαγνητικού υλικού που συμμετέχει σε κάθε πλειάδα, ο όρος Vt δηλαδή της Εξίσωσης 1.7. Εικόνα 1.30: Αριστερά: Μεμονωμένα μαγνητικά κολλοειδή. Δεξιά: Κολλοειδής πλειάδα μαγνητικών νανοκρυσταλλιτών [21] Μεθόδοι σύνθεσης SPIONs Τις τελευταίες δεκαετίες έχει αναπτυχθεί ένα πλήθος μεθόδων για την παρασκευή νανοσωματιδίων οξειδίων του σιδήρου. Οι μέθοδοι αυτές μπορούν να είναι φυσικές, όπως η μηχανική λειοτρίβιση, οι συνηθέστερες όμως είναι οι χημικές συνθετικές μέθοδοι, που περιλαμβάνουν αντιδράσεις υδρόλυσης και θερμόλυσης πρόδρομων ενώσεων [ 87, 88 ]. Αρκετές παραλλαγές των μεθόδων αυτών αποτελούν η υδρόλυση με χρήση υπερήχων [89], μικροκυμάτων, sol-gel, μικρογαλακτώματος και συγκαταβύθισης. Επίσης, απατώνται η μέθοδος αέριας φάσης [90] και η μέθοδος στερεής φάσης [91, 92]. Ιδανικά, οι συνθετικές μέθοδοι θα πρέπει να είναι σε θέση να παράγουν νανοσωματίδια με όσο το δυνατόν καλύτερο έλεγχο του μεγέθους των σχηματιζομένων νανοκρυσταλλιτών. Επιπλέον, θα πρέπει να εξασφαλίζουν σύνθεση νανοσωματιδίων με στενό εύρος κατανομής μεγέθους και υψηλή κρυσταλλικότητα της επιθυμητής κρυσταλλικής δομής. Χρήσιμη είναι επίσης η ικανότητα παραγωγής νανοκρυσταλλιτών σε μεγάλη κλίμακα. Σήμερα, οι μέθοδοι της υγρής χημικής σύνθεσης είναι οι πιο διαδεδομένες στην παραγωγή κολλοειδών νανοσωματιδίων, καθώς δίνουν το πλεονέκτημα της ελεγχόμενης κρυστάλλωσης των μοριακών πρόδρομων μεταλλικών ενώσεων παρουσία οργανικών 51
70 επιφανειακών τροποποιητών, οι οποίοι είναι απαραίτητοι για τον περιορισμό των διαστάσεων σε νανοκλίμακα, την εξασφάλιση της κολλοειδούς σταθερότητας των νανοκρυσταλλιτών και την παροχή χημικών ομάδων για περαιτέρω επιφανειακή τροποποίηση [21]. Η κατηγορία της υγρής χημικής σύνθεσης μπορεί να χωριστεί σε δύο υποκατηγορίες: στις υδρολυτικές και στις θερμολυτικές μεθόδους. Οι υδρολυτικές οδοί, βασίζονται κυρίως στην υδρόλυση δισθενών και τρισθενών ιόντων σιδήρου, ενώ οι θερμολυτικές τεχνικές στηρίζονται στη θερμόλυση-αποικοδόμηση οργανομεταλλικών ενώσεων του σιδήρου [87]. Οι κυριότερες τεχνικές σύνθεσεις SPIONs περιγράφονται πιο κάτω: Α. Αλκαλική καταβύθιση Η μέθοδος της αλκαλικής καταβύθισης αποτελεί μία από τις παλαιότερες τεχνικές. Πραγματοποιείται με την προσεκτική ρύθμιση του ph ενός διαλύματος δισθενούς σιδήρου με αποτέλεσμα τη δημιουργία ενός πλέγματος μαγνητικών οξειδίων σιδήρου μέσω της αρχικής παραγωγής Fe(OH) 2 και αντιδράσεων αφυδάτωσης, συμπύκνωσης και οξείδωσης (Aντιδράσεις 1.1-2). Αυτή η τεχνική είναι απλή και δεν απαιτεί συγκεκριμένο εργαστηριακό εξοπλισμό. Fe OH + xh 2 O Fe II (OH) 2 (H 2 O) x (Αντίδραση 1.1) 2Fe II αφυδάτωση, συμπύκνωση (OH) 2 (H 2 O) x + O 2 Fe III 2 O 3 + (x + 1)H 2 O + 2OH (Αντίδραση 1.2) Β. Αλκαλική συγκαταβύθιση (Coprecipitation) Με αυτή τη μέθοδο, υδατικά διαλύματα σιδηρούχων (Fe 2+ ) και σιδηρικών (Fe 3+ ) ιόντων σιδήρου, παρουσία περίσσειας υδροξυλίων (αλκαλικό περιβάλλον), οδηγούν ταχύτατα στην παρασκευή νανοσωματιδίων μαγνητίτη [93], σύμφωνα με την Αντίδραση 1.3: Fe 2 + 2Fe 3 + 8OH Fe 3 O 4 + 4H 2 O (Αντίδραση 1.3) Κατα τη σύνθεση SPIONs με την τεχνική της συγκαταβύθισης, το ph και η ιοντική ισχύς του διαλύματος αποτελούν καθοριστικούς παράγοντες για τον έλεγχο του μεγέθους των παραγόμενων νανοκρυσταλλιτών. Το μέγεθος μειώνεται όσο το ph και η ιονική ισχύς στο διάλυμα αυξάνονται, δεδομένου ότι και οι δύο παράμετροι καθορίζουν τη χημική σύσταση 52
71 της επιφάνειας των αναπτυσσόμενων νανοσωματιδίων, και συνεπώς το ηλεκτροστατικό φορτίο της επιφάνειας τους (Εικόνα 1.31) [92, 94]. Εικόνα 1.31: Εξάρτηση της διαμέτρου των μαγνητικών νανοσωματιδίων απο το ph και την ιοντική ισχύ, κατά την τεχνική της συγκαταβύθισης [92]. Τα παραγόμενα SPIONs έχουν μικρότερο μέγεθος σε σχέση με αυτά που πρόκυπτουν με την τεχνική της αλκαλικής καταβύθισης [95, 96]. Σε αυτό το σημείο θα πρέπει να σημειωθεί ότι είναι απαραίτητη η αποφυγή της οξείδωσης των Fe 2+ για τη δημιουργία μαγνητίτη. Αμφότερες οι προαναφερθείσες τεχνικές είναι απλές, γρήγορες και μη τοξικές αφου δεν χρησιμοποιούνται οργανικοί διαλύτες. Σχεδόν κατ αποκλειστικότητα, όλα τα SPIONs που εγκρίθηκαν για κλινικές και προκλινικές εφαρμογές έχουν συντεθεί με τις πιο πάνω μεθόδους. Παρ όλα αυτά, οι σχηματιζόμενοι νανοκρυσταλλίτες έχουν συνήθως μεγάλο μέγεθος και μεγάλο εύρος κατανομής μεγέθους, ενώ σε μερικές περιπτώσεις παρουσιάζουν και χαμηλή κρυσταλλικότητα. Γ. Θερμική αποικοδόμηση (Thermal Decomposition) Σύμφωνα με τη μέθοδο αυτή, ο σχηματισμός των νανοκρυσταλλιτών πραγματοποιείται με θερμική αποικοδόμηση οργανομεταλλικών ενώσεων του σιδήρου, σε οργανικούς διαλύτες υψηλού σημείου ζέσεως ( ο C ). Το μέγεθος των σχηματιζομένων SPIONs κυμαίνεται απο 3 εώς 20nm. Οι συνηθέστερα χρησιμοποιούμενες πρόδρομες ενώσεις ειναι ο ακετυλακετονικός σίδηρος [Fe(acac) 3 ], ο πεντακαρβονυλικός σίδηρος [Fe(CO) 5 ] και το σύμπλοκο του ελαϊκου σιδήρου [Fe(Olate) 3 ]. 53
72 Με τη συγκεκριμένη μέθοδο, συντείθενται νανοκρυσταλλίτες με πολύ στενό εύρος κατανομής μεγέθους, ενώ εξασφαλίζεται πολύ καλός έλεγχος του μεγέθους των SPIONs ανάλογα με τις συνθετικές παραμέτρους [87, 92]. Επιπλέον, η παρουσία επιφανειοδραστικού παράγοντα (π.χ ελαϊκό οξύ), κατα την τεχνική της θερμικής αποικοδόμησης, οδηγεί στο σχηματισμό νανοκρυσταλλιτών με αυξημένη κολλοειδή σταθερότητα. Η ανάπτυξη του πλέγματος των SPIONs πιστεύεται ότι λαμβάνει χώρα μέσω δημιουργίας και ανασυνδυασμού ριζών των ενδιάμεσων προϊόντων της αντίδρασης [ 97 ]. Τα δομικά χαρακτηριστικά των παραγόμενων νανοσωματιδίων εξαρτώνται από τις συνθετικές παραμέτρους, όπως η θερμοκρασία σύνθεσης και ο ρυθμός αύξησής της, η αναλογία πρόδρομης ένωσης και ελαϊκού οξέος, η φύση του διαλύτη και των προδρόμων ενώσεων. Η θερμική αποικοδόμηση συγκαταλέγεται στις καλύτερες μεθόδους για σύνθεση υδρόφοβων SPIONs με αυξημένη κολλοειδή σταθερότητα, ενώ υπάρχει δυνατότητα για παραγωγή σε μεγάλη κλίμακα. Τα μειονεκτήματα της συγκεκριμένης μεθόδου αφορούν τη δυσκολία πλήρους απομάκρυνσης των οργανικών διαλυτών και την επακόλουθη in vivo τοξικότητα. Επίσης, η θερμική αποικοδόμηση είναι σχετικά χρονοβόρα τεχνική και απαιτεί υψηλές θερμοκρασίες (>250 ο C) για την παραγωγή των SPIONs. Δ. Μικρογαλακτώματα (Microemulsions) Ο σχηματισμός μικρογαλακτωμάτων (ανάστροφων μικκυλίων) αποτελεί ένα μηχανισμό σύνθεσης μαγνητικών νανοσωματιδίων ο οποίος εμφανίζει αρκετά πλεονεκτήματα [98]. Τα κανονικά μικκύλια σχηματίζονται σε υδατικό μέσο ενώ τα ανάστροφα σε ελαιώδες μέσο. Το κέντρο των ανάστροφων μικκυλίων είναι υδρόφιλο και μπορούν να αποθηκευτούν εκεί τα ανόργανα συστατικά του μείγματος της αντίδρασης. Για τη σύνθεση των μαγνητικών οξειδίων του σιδήρου ανόργανες πρόδρομες ουσίες, όπως ο χλωριούχος σίδηρος, διαλύονται σε υδατικό μέσο και προστίθενται σε ελαιώδες μείγμα, το οποίο περιέχει επιφανειοδραστικές ουσίες. Οι χημικές αντιδράσεις για την παρασκευή των νανοκρυσταλλιτών λαμβάνουν χώρα στο εσωτερικό των μικκυλίων, με αποτέλεσμα να εμποδίζεται ο σχηματισμός συσσωματωμάτων και να υπάρχει μικρή διασπορά μεγέθους των νανοσωματιδίων. Επιπρόσθετα, η μέθοδος αυτή εξασφαλίζει καλό έλεγχο του μεγέθους των SPIONs. Μειονεκτήματα της μεθόδου αποτελούν οι διαδικασίες καθαρισμού που απαιτούνται για την απομάκρυνση των επιφανειοδραστικών ουσιών, καθώς και η χαμηλή απόδοση σχηματισμού νανοσωματιδίων, η οποία περιορίζεται από τη φύση της μεθόδου. 54
73 Παρακάτω στον Πίνακα 1.8, παρουσιάζονται οι τεχνικές σύνθεσης SPIONs με τα κυριότερα πλεονεκτήματα και μειονεκτήματά τους, καθώς και τα μεγέθη των νανοκρυσταλλιτών που προκύπτουν απο κάθε τεχνική. Πίνακας 1.8: Μεθόδοι σύνθεσης SPIONs [99]. 55
74 Πίνακας 1.8 (συνέχεια) 56
75 1.7.6 Επιφανειακή τροποποίηση SPIONs Ένα σημαντικό στάδιο για την παρασκευή και χρήση των μαγνητικών νανοσωματιδίων αποτελεί η χημική τροποποίηση της επιφάνειας τους, με στόχο να καταστούν λειτουργικά, ανάλογα με την εφαρμογή για την οποία προορίζονται.. Η κατάλληλη επιφανειακή τροποποίηση έχει ως αποτέλεσμα την αύξηση της βιοσυμβατότητας των SPIONs, την ενίσχυση της κολλοειδούς τους σταθερότητας σε φυσιολογικές συνθήκες (ph, ιοντική ισχύς), την ικανότητα εκλεκτικής προσκόλλησης σε συγκεκριμένες ουσίες-στόχους, τη δυνατότητα να αποφεύγουν βιολογικές διαδικασίες (φαγοκυττάρωση, οψωνινοποίηση) και να μεταφέρουν φαρμακευτικές ενώσεις. Η παρουσία κατάλληλων τερματικών χημικών ομάδων στην επιφάνεια των SPIONs, επιτρέπει την παραπέρα ανάπτυξη και τροποποίηση των υβριδικών κολλοειδών, ανάλογα με την επιθυμητή κάθε φορά εφαρμογή. Στην ιδανική περίπτωση, ένα υβριδικό κολλοειδές για να δράσει επιτυχώς ως νανοφορέας, πρέπει να έχει τέτοια αρχιτεκτονική ώστε να προσδίδει στο σύστημα πολυλειτουργικότητα. Η επιφανειακή τροποποίηση δύναται να πραγματοποιηθεί είτε κατά τη διάρκεια της σύνθεσης των νανοκρυσταλλιτών, με παρουσία κατάλληλων μονομερών ή πολυμερών [100, 101], είτε μετά το πέρας της σύνθεσης. Η τροποποίηση της επιφάνειας των SPIONs μπορεί να γίνει άμεσα ή έμμεσα [21] Άμεση επιφανειακή τροποποίηση Η άμεση τροποποίηση περιλαμβάνει τη φυσική η χημική σύνδεση μορίων και πολυμερών στην επιφάνεια των μαγνητικών νανοσωματιδίων [19, 102, 103]. Χαρακτηριστικά παραδείγματα πολυμερικών επιφανειακών τροποποιητών αποτελούν η πολυαιθυλενογλυκόλη (PEG), η δεξτράνη, η χιτοζάνη, τα αλγινικά και η πολυβινυλική αλκοόλη (PVA). Επίσης, μεταξύ άλλων, χρησιμοποιούνται τα πολυμερή: πολυακριλικό οξύ (PAA), πολυγαλακτικό οξύ (PLA), συμπολυμερές γαλακτικού-γλυκολικού οξέος (PLGA) και πολυαιθυλενιμίνη (PEI) [101, 104]. Η PEG είναι το ευρύτερα χρησιμοποιούμενο πολυμερές, για το σκοπό αυτό, λόγω των αξιόλογων ιδιοτήτων της. Πρόκειται για ενα βιοσυμβατό και μη τοξικό πολυμερές, ενώ δεν επάγει ανοσοαποκρίσεις όσο άλλα πολυμερή. Λόγω του υδρόφιλου και μη ιοντικού χαρακτήρα της, προσδίδει μεγάλη κολλοειδή σταθερότητα, ενώ παρουσιάζει μικρότερη επιδεκτικότα για οψωνινοποίηση λόγω στερικής άπωσης με τα βιολογικά (μακρο)μόρια, με 57
76 αποτέλεσμα την εξασφάλιση παρατεταμένου χρόνου κυκλοφορίας στο αίμα. Το γεγονός αυτό είναι ιδιαίτερα σημαντικό τόσο για τη παθητική αλλά και την ενεργητική στόχευση [64]. Η πρόσδεση των τροποποιητών στην επιφάνεια των νανοσωματιδίων επιτυγχάνεται μέσω ομοιοπολικής ή ηλεκτροστατικής σύνδεσης. Σε άλλες περιπτώσεις, η πρόσδεση γίνεται μέσω χημικών ομάδων, οι οποίες αναπτύσσουν δεσμούς υδρογόνου με τις επιφάνειες των μαγνητικών νανοσωματιδίων, όπως απεικονίζεται παρακάτω στην Εικόνα 1.32 [105]. Εικόνα 1.32: Διαδικάσια πρόσδεσης mpeg στην επιφάνεια των μαγνητικών νανοσωματιδίων μέσω δεσμών υδρογόνου. α) δομή μορίου mpeg, β) ένωση mpeg με TsT, γ) αντίδραση β με ντοπαμίνη, δ) μαγνητικό νανοσωματίδιο επικαλυμμένο με mpeg [105] Έμμεση επιφανειακή τροποποίηση (εγκλωβισμός σε κοίλες δομές) Η έμμεση τροποποίηση αφορά την ενκαψυλίωση των νανοσωματιδίων μέσα σε κατάλληλες διατάξεις όπως π.χ. τα λιποσώματα και τα μικκύλια [106]. Ο εγκλωβισμός των μαγνητικών νανοσωματιδίων σε λιποσώματα, μικκύλια και τεχνητά καψίδια πολυηλεκτρολυτών αποτελεί μια ελπιδοφόρα προσέγγιση που μπορεί να λειτουργήσει ως εφαλτήριο για τη χρήση των SPIONs σε βιοϊατρικές εφαρμογές. Ένα παράδειγμα αυτής της προσέγγισης αποτελεί η μελέτη των J. Gao et al., οι οποίοι εγκλώβισαν επιτυχώς υδρόφοβα υπερπαραμαγνητικά νανοσωματίδια οξειδίου του σιδήρου (διαμέτρου 8nm) σε πολυμερικά μικκύλια (PLA-b-PEG), μαζί με το αντικαρκινικό φάρμακο Δοξορουβικίνη, όπως φαίνεται στην Εικόνα 1.33 [56]. 58
77 Εικόνα 1.33: Σχηματική απεικόνιση έμμεσης επιφανειακής τροποποίησης μαγνητικών νανοσωματιδίων, μέσω εγκλωβισμού τους σε πολυμερικά μικκύλια [56] Εφαρμογές SPIONs Τα μαγνητικά νανοσωματίδια έχουν, όπως έχει προαναφερθεί, ιδιότητες οι οποίες τα καθιστούν πολύτιμα εργαλεία στον τομέα της βιοϊατρικής. Αρχικά, έχουν ρυθμιζόμενο μέγεθος που κυμαίνεται από λίγα εως δεκάδες nm, δηλαδή μέγεθος συγκρινόμενο με εκείνο του κυττάρου, του ιού ή ενός γονιδίου. Η κύρια όμως ιδιότητα των μαγνητικών νανοκρυσταλλιτών, η οποία τους καθιστά πολύτιμο εργαλείο για χρήση στις βιοϊατρικές εφαρμογές, είναι ο μαγνητισμός. Χαρακτηριστικό παράδειγμα αποτελεί η συνδυαστική τεχνική διάγνωσης-θεραπείας (Theranostics) του καρκίνου με τη χρήση SPIONs. Η διάγνωση επιτυγχάνεται με τη τεχνική της μαγνητικής τομογραφίας πυρηνικού συντονισμού (Magnetic Resonance Imaging, MRI) και η θεραπεία μέσω επαγόμενης υπερθερμίας, ως αποτέλεσμα της έκθεσης σε εναλλασσόμενο μαγνητικό πεδίο (μαγνητική υπερθερμία). Μια τρίτη σπουδαία εφαρμογή αφορά τη δυνατοτήτα in vivo κατεύθυνσης των SPIONs στην επιθύμητη περιοχή-στόχο με τη χρήση εξωτερικού μαγνήτη (μαγνητική στόχευση), με σκοπό είτε την πρόκληση μαγνητικής υπερθερμίας είτε τη στοχευμένη μεταφορά φαρμακευτικών ουσιών στην πάσχουσα περιοχή. Τέλος, τα μαγνητικά νανοσωματίδια χρησιμοποιούνται και σε in vitro εφαρμογές οπώς: ο μαγνητικός διαχωρισμός κυττάρων, η επισήμανση και απομόνωση DNA/RNA, η ανίχνευση και απομόνωση μικροοργανισμών κ.α (Εικόνα 1.34) [63, 107, 108]. 59
78 Εικόνα 1.34: Εφαρμογές SPIONs [109] Μαγνητική τομογραφία πυρηνικού συντονισμού (Magnetic Resonance Imaging, MRI) H μαγνητική τομογραφία πυρηνικού συντονισμού βασίζεται στην ανίχνευση των διεργασιών χαλάρωσης των πυρηνικών spin των ατόμων υδρογόνου (δηλ. του νερού) που υπάρχουν στους μαλακούς ιστούς του σώματος (μύες, τένοντες, νεύρα, λίπος), μέσω της εφαρμογής μαγνητικού πεδίου. Αύτο έχει ως αποτέλεσμα την παραγωγή μίας εικόνας αντίθεσης φωτεινών και σκοτεινών περιοχών (contrast). Με τον όρο χαλάρωση εννοείται η επαναφορά των πυρηνικών spin απο τη διεγερμένη κατάσταση, ως αποτέλεμα της εφαρμογής μαγνητικού πεδίου, στην κατάσταση ισορροπίας. Διακρίνονται δύο είδη χαλάρωσης ανάλογα με τον προσανατολισμό των μαγνητικών ροπών στο εξωτερικό μαγνητικό πεδίο: η διαμήκης χαλάρωση (Longitudinal relaxation, T 1 ) και η εγκάρσια χαλάρωση (Transverse relaxation, T 2 ). Γενικά, επιδιώκεται η μείωση των χρόνων χαλάρωσης με σκόπο τη λήψη εικόνων με μεγαλύτερη ευκρίνεια, λόγω υψηλότερου contrast. Τα υπερπαραμαγνητικά νανοσωματίδια μπορούν να χρησιμοποιηθούν σαν σκιαγραφικά μέσα (contrast agents), μειώνοντας το χρόνο Τ 1 και κυρίως το χρόνο Τ 2 των μορίων του νερού, με αποτέλεσμα τη σημαντική βελτίωση της ευαισθησίας της μεθόδου [ 110, 111 ]. Ο χρόνος 60
79 χαλάρωσης Τ 2 των μαγνητικών νανοσωματιδίων καθορίζεται από τη μαγνητική τους ροπή και τις ιδιότητες του μέσου που έχει χρησιμοποιηθεί σαν επιφανειακός τροποποιητής [112]. Γενικά οι μαγνητικοί νανοφορείς με υψηλή τιμή μαγνήτισης κόρου, μεγάλη διάμετρο νανοκρυσταλλιτών και λεπτό πολυμερικό φλοιό παρουσιάζουν υψηλότερους χρόνους χαλάρωσης T 2. Ειδικότερα τα SPIONs μεγάλου μεγέθους και υψηλής μαγνήτισης μπορούν να εμφανίσουν έως και δύο τάξεις μεγέθους υψηλότερους χρόνους χαλάρωσης T 2, συγκρινόμενα με τα πρώτης γενιάς κλινικώς εγκεκριμένα SPIONs. Παράλληλα, μέσω της κατάλληλης τροποποίησης των νανοφορέων με φθορίζοντα μόρια μπορεί να γίνει συνδυασμός διαφορετικών μεθόδων απεικόνισης, ενώ η αύξηση της τοπικής τους συγκέντρωσης στην επιθυμητή περιοχή μπορεί να αξιοποιηθεί για επαγωγή μαγνητικής υπερθερμίας (Εικόνα 1.35). Εικόνα 1.35: Διαφορετικές προσεγγίσεις στην ανάπτυξη συστημάτων theranostics [113]. Βέβαια θα μπορούσε κάλλιστα να χρησιμοποιηθεί και ο σίδηρος σαν σκιαγραφικό μέσο, καθώς η μαγνήτιση κόρου του είναι περίπου διπλάσια από το ισχυρότερο οξείδιό του, στοιχείο σημαντικό αν αναλογιστούμε πως στην μαγνητική τομογραφία χρησιμοποιούνται ισχυρά μαγνητικά πεδία και τα υπερπαραμαγνητικά σωματίδια μαγνητίζονται στον κόρο. Παρ όλα αυτά ο σίδηρος παρουσιάζει το μειονέκτημα ότι οξειδώνεται εύκολα, έτσι η χρήση του θα ήταν εφικτή μόνο αν επικαλυπτόταν με ένα υλικό που θα απέτρεπε την οξείδωσή του. Στον Πίνακα 1.9 παρουσιάζονται μερικά παραδείγματα εμπορικά διαθέσιμων σκιαγραφικών μέσων για MRI, με βάση το παραμαγνητικό γαδολίνιο (Gd), τα SPIONs και τα USPIONs (Ultrasmall Superparamagnetic Iron Oxide Nanocrystalls). Στις περισσότερες περιπτώσεις, τα 61
80 SPIONs επικαλύπτονται με παράγωγα δεξτράνης (πολυσαγχαρίτης αποτελούμενος απο μονομερή γλυκόζης), αυξάνοντας τη βιοσυμβατότητα και την ενδοκυτταρική πρόσληψή τους. Πίνακας 1.9: Παραδείγματα εμπορικά διαθέσιμων σκιαγραφικών μέσων για MRI [114] Μαγνητική στόχευση φαρμάκων (Magnetic Drug Targeting, MDT) Η προσέγγιση της μαγνητικής στόχευσης προσφέρει μία επιπλέον φυσική οδό στη θεραπεία του καρκίνου, κάνοντας χρήση Συστημάτων Ελεγχόμενης Χορήγησης Φαρμάκων βασισμένα σε μαγνητικά νανοσωματίδια (MagDDS) [21]. Η βασική αρχή της MDT είναι η ενσώματωση μίας φαρμακευτικής ένωσης σε έναν μαγνητικό νανοφορέα (MagDDS), η ενδοφλέβια χορήγηση του και εν συνεχεία η ακινητοποίηση του με τη χρήση ενός ισχυρού μαγνητικού πεδίου (σταθερός μαγνήτης) στην περιοχή-στόχο (Εικόνα 1.35). Ακολούθως, το φάρμακο μπορεί να αποδεσμευτεί είτε μέσω ενζυμικών διαδικασιών είτε μέσω φυσικοχημικών αλλαγών (ph, θερμοκρασία) που λαμβάνουν χώρα στην πάσχουσα περιοχή. Η εν λόγω μέθοδος μπορεί να αυξήσει την τοπική συγκέντρωση του φαρμάκου στην επιθυμητή περιοχή κατά αρκετές τάξεις μεγέθους, μειώνοντας έτσι την απαιτούμενη δόση χορήγησης και τις επακόλουθες ανεπιθύμητες ενέργειες από τη δράση των χημειοθεραπευτικών παραγόντων σε υγιής ιστούς. Μελέτες έχουν αναδείξει την 62
81 αποτελεσματικότητα αυτής της μεθόδου σε in vivo εφαρμογές [115, 116]. Χαρακτηριστικό παράδειγμα είναι η μελέτη των C. Alexiou et al., όπου μετά από ενδοαρτηριακή χορήγηση SPIONs συζευγμένων με το αντινεοπλασματικό φάρμακο Μιτοξανδρόνη (MTO) και εφαρμογή εξωτερικού μαγνητικού πεδίου στην περιοχή του όγκου, παρατήρησαν εξαπλάσια ποσότητα ΜΤΟ στην περιοχή του όγκου σε σχέση με άλλους ιστούς. Ο ex vivo χαρακτηρισμός δειγμάτων ιστού που ακολούθησε επιβεβαίωσε το γεγονός αυτό [115]. Εικόνα 1.35: Σχηματική απεικόνιση της τεχνικής της μαγνητικής στόχευσης φαρμάκων σε καρκινικούς ιστούς [34]. Η αποτελεσματικότητα της παραπάνω θεραπείας εξαρτάται από ορισμένες παραμέτρους όπως τη βαθμίδα του μαγνητικού πεδίου, τη συγκέντρωση και τις ιδιότητες των μαγνητικών νανοσωματιδίων. Επιπλέον, η αιματική ροή στον πάσχοντα ιστό, η πορεία έγχυσης του συστήματος και ο χρόνος κυκλοφορίας των νανοφορέων στο αίμα διαδραματίζουν πολύ σημαντικό ρόλο στην επίτευξη της θεραπείας. Τέλος, πρέπει να ληφθεί υπόψη και το βαθος του ιστού τον οποίο στοχεύουμε. Με τους μαγνήτες Nd-Fe-B επιτυχάνεται βάθος στόχευσης μέχρι και 10-15cm. Έχει παρατηρηθεί ότι μεγαλύτερα νανοσωματίδια (1μm) αντιτίθενται περισσότερο στην κυκλοφορία του αίματος, κυρίως στις μεγαλύτερες φλέβες και αρτηρίες. Πρόσφατες μελέτες έχουν δείξει ότι για την MDT στον ιστό-στόχο, η ένταση του μαγνητικού πεδίου πρέπει να είναι της τάξης των 0,2Τ. Η στόχευση των φαρμάκων είναι πιο αποτελεσματική σε περιοχές με χαμηλή αιματική ροή και ειδικότερα αν η θέση στόχος είναι κοντά στο μαγνήτη [29, 117, 118]. 63
82 Μαγνητική Υπερθερμία ή Υπερθερμία Μαγνητικών Ρευστών (Magnetic Fluid Hyperthermia, MFH) Η μαγνητική υπερθερμία αποτέλει την πιο ελπιδοφόρα εφαρμογή για τη θεραπεία του καρκίνου. Θεωρείται ως η καλύτερη εναλλακτική αντικαρκινική θεραπεία της χημειοθεραπείας και της ακτινοβολίας, αφού στερείται πολλών παρενεργειών. H αρχή της MFH στηρίζεται στην εφαρμογή εναλλασσόμενων μαγνητικών πεδίων (AMF) στην περιοχή του καρκινικού όγκου, που έχει ως αποτέλεσμα την αύξηση της θερμοκρασίας των μαγνητικών νανοσωματιδίων, λόγω φαινομένων υστέρησης και χαλάρωσης των μαγνητικών διπολικών ροπών τους (φαινόμενο Neel και Brown). Η εγγενής αυτή ιδιότητα των μαγνητικών νανοσωματιδίων μπορεί να χρησιμοποιηθεί σε εφαρμογές μαγνητικής υπερθερμίας για την αποτελεσματικότερη αντιμετώπιση του καρκίνου [21]. Οι πειραματικές έρευνες για τη χρήση μαγνητικών υλικών προς επίτευξη υπερθερμίας χρονολογούνται το 1957, όταν ο Gilchrist και οι συνεργάτες του προκάλεσαν υπερθερμία σε μία πληθώρα ιστών-δειγμάτων με νανοσωματίδια μαγκεμίτη διαμέτρου nm, τα οποία εξέθεσαν σε μαγνητικό πεδίο συχνότητας 1.2MHz. Εικόνα 1.36: Η αρχή της MFH. Η τοπική αύξηση της θερμοκρασίας (41-46 ο C) μπορεί να κάνει τα καρκινικά κύτταρα πιο ευαίσθητα στη δράση των χημειοθεραπευτικών παραγόντων ή να προκαλέσει ακόμα και την απόπτωσή τους [119]. Επιπλέον, μελέτες αναφέρουν ότι οι υποξικές περιοχές των καρκινικών όγκων παρουσιάζουν μεγαλύτερη αντίσταση στην ακτινοβολία, όμως είναι πολύ πιο ευαίσθητες στην αύξηση της θερμοκρασίας [120]. Σε αυτές τις θερμοκρασίες επιτυγχάνεται θανάτωση των καρκινικών κυττάρων ενώ η ζημιά που προκαλείται στα υγιή κύτταρα είναι αναστρέψιμη [63]. Επομένως, ο συνδυασμός των παραδοσιακών μεθόδων με την εφαρμογή υπερθερμίας δύναται να βελτιώσει την αποτελεσματικότητα της αντικαρκινικής θεραπείας. 64
83 Τονίζεται ότι, η θερμοκρασία κατα την εφαρμογή AMF δεν πρέπει να ξεπεράσει σε καμία περίπτωση τους 56 ο C. Στη θεμοκρασία αυτή επέρχεται κυτταρική νέκρωση του ιστού (Thermoablation). Σε ένα πρόσφατο παράδειγμα, οι Κ. Hayashi et al. χρησιμοποιώντας μαγνητικά νανοσωματίδια συζευγμένα με το χημειοθεραπευτικό παράγοντα δοξορουβικίνη (DOX), μέσω ενός θερμο-αποκρινόμενου πολυμερούς, πέτυχαν σχεδόν πλήρη υποχώρηση του καρκινικού όγκου σε ποντίκια, μέσω του συνδυασμού υπερθερμίας και εκλεκτικής αποδέσμευσης του φαρμάκου απο την επαγόμενη αύξηση της θερμοκρασίας [121]. Επιπλέον, η εφαρμογή AMF δεν οδηγεί μόνο σε MFH αλλά και σε ραγδαία αύξηση της αποδέσμευσης του φαρμάκου, όταν αυτό ενσωματώνεται σε μαγνητικό νανοφορέα κατάλληλης συγκέντρωσης. Στην Εικόνα 1.37 αποτυπώνεται η σταδιακή υποχώρηση του όγκου μετά την εφαρμογή AMF. Γ Δ Chemotherapy MFH without Chemotherapy Chemotherapy + MFH Εικόνα 1.37: (Α,Γ) Φωτογραφίες και θερμική εικόνα κατά την εφαρμογή AMF για 20min. (Β) Μέση θερμοκρασία που αναπτύσσεται στην περιοχή του όγκου κατά την εφαρμογή AMF μετά τη χορήγηση DOX+SPIONs (κόκκινη καμπύλη), SPIONs (μπλέ καμπύλη) και DOX χωρίς SPIONs (γκρίζα καμπύλη). (Δ) Φωτογραφίες μετά απο χημειοθεραπεία, μαγνητική υπερθερμία χωρίς τη χρήση αντικαρκινικού φαρμάκου, μαγνητική υπερθερμία με χρήση αντικαρκινικού φαρμάκου. Οι φωτογραφίες λήφθηκαν μετά απο 45 μέρες θεραπείας [121]. 65
84 Σε αυτό το σημείο πρέπει να υπογραμμιστεί ότι η επίτευξη μαγνητικής υπερθερμίας εξάρταται απο την ένταση του μαγνητικού πεδίου, τη διάρκεια εφαρμογής, το μέγεθος και τη συγκέντρωση των SPIONs στην περιοχή-στόχο. Η συχνότητα του μαγνητικού πεδίου για βιοϊατρικές εφαρμογές δεν πρέπει να ξεπερνά τα KHz, ενώ η διάρκεια εφαρμογής δεν πρέπει να είναι μεγαλύτερη απο 30 λεπτά. Συνοψίζοντας, η ενσωμάτωση των SPIONs σε Συστήματα Ελεγχόμενης Χορήγησης Φαρμάκων εξασφαλίζει αξιοσημείωτα πλεονεκτήματα. Η δυνατότητα της εκλεκτικής στόχευσης φαρμακευτικών ουσιών καθώς και της επαγόμενης υπερθερμίας μέσω εφαρμογής AMF, αποτελούν πολύ ελπιδοφόρες προσεγγίσεις για την αποτελεσματικότερη θεραπεία του καρκίνου. Συν τοις άλλοις, η χρήση των SPIONs ως σκιαγραφικά μέσα στο MRI υπογραμμίζει τη διττή φύση των συστημάτων αυτών (διάγνωση και θεραπεία). 66
85 1.8 Πακλιταξέλη (Paclitaxel, PTX) Η πακλιταξέλη, που είναι καλύτερα γνωστή ως ταξόλη, είναι το πρώτο μέλος της οικογένειας των ταξανών που χρησιμοποιήθηκε στη χημειοθεραπεία του καρκίνου (Εικόνα 1.38). Ανακαλύφθηκε το 1967 ως εκχύλισμα του φλοιού του ελάτου της Βορείου Αμερικής, Taxus brevifolia. Η ολική σύνθεσής της πραγματοποιήθηκε για πρώτη φόρα το 1994 απο τις ερευνητικές ομάδες των R.A. Holton και K.C. Nicolaou. Λόγω της εξαιρετικά χαμηλής υδατοδιαλυτότητάς της, η εταιρεία Bristol-Myers Squibb διέλυσε την PTX σε μείγμα αιθανόλης και πολυαιθόξυ-καστορέλαιου (Cremophor EL). Με αυτή τη μορφή κυκλοφορεί στο εμπορίο με την ονομασία Taxol. Η PTX ενδείκνυται κυρίως σε καρκίνο του πνεύμονα, του μαστού και σε σάρκωμα Kaposi ασθενών με AIDS, ενώ θεωρείται θεραπεία πρώτης γραμμής για καρκίνο των ωοθηκών. Επίσης ενδείκνυται σε καρκίνο της ουροδόχου κύστης, σε καρκίνο κεφάλης και τραχήλου και σε κακοήθες μελάνωμα, ενώ σε συνδυασμό με τη σισπλατίνη χορηγείται σε ασθενής με μη μικροκυτταρικό καρκίνο του πνεύμονα. Εικόνα 1.38: Δομή PTX [122]. Μηχανισμός δράσης: Η PTX είναι ένας μιτωτικός αναστολέας και δρά στη φάση G 2 /M του κυτταρικού κύκλου, αναστέλλοντας τον αποπολυμερισμό των διμερών της τουμπουλίνης των μικροσωληνίσκων. Συνδέεται αναστρέψιμα με την υπομονάδα της τουμπουλίνης-β και προάγει τον πολυμερισμό και τη σταθεροποίηση της. Έτσι, μετατοπίζει την ισορροπία πολυμερισμού-αποπολυμερισμού προς όφελος του σχηματισμού μικροσωληνίσκων. Οι υπέρμετρα σταθεροί μικροσωληνίσκοι που σχηματίζονται παρουσία της PTX είναι δυσλειτουργικοί και δεν επιτρέπουν το διαχωρισμό των χρωματοσωμάτων, γεγονός που αναστέλλει την κυτταρική διαίρεση με επακόλουθο θάνατο του κυττάρου (Εικόνα 1.39). 67
86 Εικόνα 1.39: Μηχανισμός δράσης PTX [123, 124]. Φαρμακοκινητική: Το φάρμακο χορηγείται με ενδοφλέβια έγχυση mg/m 2 για τρείς ώρες, κάθε τρείς εβδομάδες. Δεν απορροφάται απο το στόμα (βιοδιαθεσιμότητα: 6.5%), συνδέεται ισχυρά με τις πρωτεϊνες του πλάσματος (89-98%), παρουσιάζει μεγάλο όγκο κατανομής ( L/m 2 ) και δεν διαπερνά τον αιματεγκεφαλικό φραγμό. Μεταβολίζεται στο ήπαρ απο το σύστημα του κυτοχρώματος P450 (CYPA34, CYP2C8) σε 6αυδροξυπακλιταξέλη (κύριως μεταβολίτης), απεκκρίνεται στη χολή και αποβάλεται με τα κόπρανα και σε μικρότερο βαθμό απο τους νεφρούς. Η κατανομή της εξαρτάται απο τη δόση και τη διάρκεια έγχυσης (t 1/2 =27h). Ανεπιθύμητες ενέργειες: Σοβαρή ουδετεροπενία, αναιμία, περιφερική νευροπάθεια, αλωπεκία, μυαλγία, αρθραλγία, θρομβοπενία και λιγότερο συχνά εμετοί και διάρροια. Εμφανίζονται σοβαρές αντιδράσεις υπερευαισθησίας (με δύσπνοια, κνίδωση και υπόταση) κυρίως λόγω του Cremophor EL, γι αυτό το λόγο οι ασθενείς που πρόκειται να λάβουν PTX προθεραπεύονται με κορτικοστεροειδή (δεξαμεθαζόνη) και με αντιισταμινικά H 1 και H 2 (διφαινυδραμίνη και ρανιτιδίνη αντίστοιχα) [124, 125, 126]. Το Abraxane της εταιρείας Abraxis BioScience εγκρίθηκε για κυκλοφορία το Πρόκειται για ένα Σύστημα Ελεγχόμενης Χορήγησης PTX ενσωματωμένης σε νανοσωματίδια αλβουμίνης (nab-paclitaxel) (Εικόνα 1.40). Με τη χρήση του Abraxane 68
87 μειώθηκαν οι ανεπιθύμητες ενέργειες του Taxol, κυρίως οι αντίδρασεις υπερευαισθησίας λόγω του Cremophor EL, ακόμα και σε χορήγηση 50% υψηλότερης δόσης. Το Abraxane ενδείκνυται ως μονοθεραπεία σε ασθενείς με προχωρημένο και μεταστατικό καρκίνο του μαστού, στους οποίους η θεραπεία πρώτης γραμμής με ανθρακυκλίνες απέτυχε. Επίσης, χορηγείται σε συνδυασμό με την καρβοπλατίνη σε προχωρημένο μη μικροκυτταρικό καρκίνο του πνεύμονα, καθώς και σε συνδυασμό με την γεμσιταβίνη ως θεραπεία πρώτης γραμμής σε ασθενείς με μεταστατικό αδενοκαρκίνωμα του παγκρέατος [46, 127, 128]. Εικόνα 1.40: Abraxane: Eνσωμάτωση PTX σε νανοσωματίδια αλβουμίνης [129]. 69
88 1.9 PTX-Mag-PLA-PEG νανοφορείς Η ενκαψυλίωση SPIONs (Mag) και του αντινεοπλασματικού φαρμάκου Πακλιταξέλη (PTX) σε πολυμερικά μικκύλια, συνδυάζει τα πλεονεκτήματα της Ελεγχόμενης Χορήγησης του φαρμάκου (DDS), καθώς και τη δυνατότητα μαγνητικής στόχευσης και επαγωγής μαγνητικής υπερθερμίας για τη θεραπεία καρκινικών όγκων. Τα πολυμερικά μικκύλια έχουν μελετηθεί εκτενώς τα τελευταία χρόνια ως φορείς ελεγχόμενης αποδέσμευσης φαρμάκων. Συντίθενται αυθόρμητα με την προσθήκη αμφίφιλων συμπολυμερών (PLA-b-PEG) σε υδατικό περιβάλλον, σχηματίζοντας δομή πυρήνακελύφους (core-shell). Στον υδρόφοβο πυρήνα των μικκυλίων (PLA) ενκαψυλιώνονται η PTX και τα SPIONs, ενώ το υδρόφιλο περίβλημα (PEG) εξασφαλίζει μεγάλη κολλοειδή σταθερότητα σε υδατικά μέσα (Εικόνα 1.41). Το PLA [πολυ(γαλακτικό οξύ)] είναι ενα βιοαποικοδομήσιμο πολυμερές ενώ η PEG [πολυ(αιθυλενογκυκόλη)] είναι ένα υδρόφιλο, μη ιοντικό και βιοσυμβατό πολυμερές. Όπως αναλύθηκε και πιο πάνω ( ), η PEG προσδίδει στους νανοφορείς μεγάλους χρόνους παραμονής στην κυκλοφορία του αίματος (stealth systems), λόγω μείωσης της έκτασης της οψωνινοποίησης και της αναγνώρισης απο το Δικτυοενδοθηλιακό σύστημα (RES), μέσω στερικής άπωσης. Το μοριακό βάρος των πολυμερικών αλυσίδων του PLA και της PEG αποτελεί παράγοντα υψίστης σημασίας όσον αφορά τις φυσικοχημικές ιδιότητες του νανοφορέα και την αποτελεσματικότητα φόρτωσηςενκαψυλίωσης της PTX και των SPIONs. PTX Υδρόφιλο περίβλημα (PEG) Υδρόφοβος πυρήνας (PLA) SPIONs Εικόνα 1.41: Σχηματική απεικόνιση PTX-Mag-PLA-PEG μικκυλίων [130]. 70
89 1.10 Στόχος μεταπτυχιακής διατριβής Η παρούσα εργασία πραγματεύεται: i) τη μελέτη των παραμέτρων της σύνθεσης υδρόφοβων SPIONs μέσω της τεχνικής της θερμικής αποικοδόμησης, με σκοπό την παρασκευή νανοκρυσταλλιτών μεγέθους 15-18nm με στενό εύρος κατανομής μεγέθους. ii) τη σύνθεση υπερπαραμαγνητικών μικκυλίων απο συμπολυμερή PLA-b-PEG και τη μελέτη των συνθετικών παραμέτρων που επηρεάζουν το μέγεθος των σχηματιζομένων μικκυλίων, καθώς και την ικανότητα ενκαψυλίωσης SPIONs (Mag). iii) τη διερεύνηση των παραμέτρων της φόρτωσης-ενκαψυλίωσης PTX και SPIONs στα πολυμερικά μικκύλια, τη μαγνητική συμπεριφορά τους, καθώς και μελέτη της αποδέσμευσης του φαρμάκου απο PTX-PLA-PEG και PTX-Μag-PLA-PEG νανοφορείς με και χωρίς την εφαρμογή εναλλασσόμενου μαγνητικού πεδίου. 71
90 72
91 Κεφάλαιο 2 Τεχνικές Χαρακτηρισμού 73
92 2.1 Ηλεκτρονική Μικροσκοπία Διέλευσης (Transmission Electron Microscopy, TEM) Η ηλεκτρονική μικροσκοπία διέλευσης είναι μια σημαντική τεχνική χαρακτηρισμού μιας και μπορεί να φτάσει σε διακριτική ικανότητα περίπου τα nm, εκμεταλλευόμενη την κυματική φύση των ηλεκτρονίων 2. Κατά την τεχνική αυτή, μια δέσμη ηλεκτρονίων διέρχεται από το δείγμα και η προβολή της δέσμης αυτής αντιστοιχεί στο είδωλο του δείγματος. Η πηγή ηλεκτρονίων συνίσταται από νήμα βολφραμίου, το οποίο καθώς διατρέχεται από ηλεκτρικό ρεύμα εκπέμπει ηλεκτρόνια (θερμιονική εκπομπή). Μεταξύ του νήματος, που αποτελεί την κάθοδο, και της ανόδου, εφαρμόζεται διαφορά δυναμικού, της τάξης των kV, η οποία επιταχύνει τα ηλεκτρόνια. Η πορεία και η κλίση των τροχιών των ηλεκτρονίων ρυθμίζεται από τους ηλεκτρομαγνητικούς φακούς (συμπυκνωτές φακοί), στους οποίους αλλάζοντας την ένταση του ηλεκτρικού ρεύματος που τους διαπερνά, μεταβάλλεται η ένταση του μαγνητικού πεδίου, και επομένως η δέσμη των ηλεκτρονίων μπορεί να εστιαστεί στο δείγμα. Αφού η δέσμη ηλεκτρονίων διέλθει του δείγματος, στη συνέχεια διέρχεται απο μία σειρά αντικειμενικών φακών με στόχο τη συγκέντρωση της δέσμης στην οθόνη παρατήρησης. (Εικόνα 2.1). Όπως στην περίθλαση ακτίνων Χ, έτσι και στην ηλεκτρονική μικροσκοπία τα ηλεκτρόνια περιθλώνται από τα κρυσταλλογραφικά επίπεδα του κρυστάλλου έτσι ώστε να ισχύει ο νόμος του Bragg (2d sinθ = nλ). Το δείγμα τοποθετείται σε ένα πολύ λεπτό grid (διάμετρος: 3mm, μέγεθος πόρων: 100μm max) συνήθως απο χαλκό και στη συνέχεια εισάγεται σε ειδική υποδοχή του οργάνου. Το υπο προσδιορισμό δείγμα θα πρέπει να είναι πολύ λεπτό έτσι ώστε τα ηλεκτρόνια να το διαπερνούν, με συνέπεια να λαμβάνει χώρα ελαστική ή και καθόλου σκέδαση των ηλεκτρονίων (σε αντίθεση με τα ηλεκτρονικά μικροσκόπια σάρωσης όπου τα ηλεκτρόνια σταματούν μέσα στο δείγμα). Η συγκεκρίμενη τεχνική απαιτεί το δείγμα να βρίσκεται υπο υψηλό κενό (τουλάχιστο 10-4 Torr), έτσι ώστε να αποφεύγονται οι σκεδάσεις ηλεκτρονίων από μόρια του αέρα. Η εικόνα που λαμβάνεται σχηματίζεται πάνω σε οθόνη επικαλυμμένη με φθορίζουσα ουσία. Η οθόνη αυτή διεγείρεται από τα ηλεκτρόνια που πέφτουν επάνω της, αφού πρώτα έχουν διαπεράσει το δείγμα. Στα σημεία εκείνα όπου το δείγμα δεν είναι διαπερατό από τα ηλεκτρόνια δημιουργούνται σκοτεινές περιοχές, ενώ αντίθετα τα διαπερατά σημεία εμφανίζονται ως φωτεινές περιοχές. Επίσης, υπάρχει η δυνατότητα λήψης εικόνας 2 Εικόνα Κεφαλαίου: 74
93 μέσω ηλεκτρονικού υπολογιστή σε ψηφιακή μορφή, χάρη στη διάταξη με μικροκάμερες που υπάρχει ενσωματωμένη στο σύστημα [131]. Εικόνα 2.1: Σχηματική απεικόνιση της αρχής λειτουργίας του TEM. Ο τρόπος με τον οποίο λειτουργεί το ηλεκτρονικό μικροσκόπιο διέλευσης θέτει πολλούς περιορισμούς ως προς τη φύση των δειγμάτων που μπορούν να μελετηθούν. Κάποιες από τις ιδιότητες που θα πρέπει να έχει ένα δείγμα ώστε να μπορεί να παρατηρηθεί με ΤΕΜ είναι οι ακόλουθες: να μην είναι πτητικό, να αντέχει σε υψηλό κενό, να είναι σταθερό στο βομβαρδισμό ηλεκτρονίων και να είναι αρκετά λεπτό για να μπορούν να το διαπερνούν τα ηλεκτρόνια. Τέλος, το TEM θεωρείται καταστρεπτική τεχνική για το δείγμα λόγω της δυσκολίας ανάκτησης του δείγματος. 75
94 2.2 Θερμοσταθμική Ανάλυση (Thermogravimetric Analysis, TGA) Η θερμοσταθμική ανάλυση αποτελεί μία τεχνική χαρακτηρισμού υλικών αλλά και ποσοτικής ανάλυσης. Βασίζεται στην απώλεια μάζας μίας ουσίας, η οποία μετράται ως συνάρτηση της θερμοκρασίας, καθώς η ουσία υποβάλλεται σε προγραμματισμένη μεταβολή της θερμοκρασίας, συνήθως με σταθερό ρυθμό. Η ατμόσφαιρα διαδραματίζει σημαντικό ρόλο στα πειράματα θερμοσταθμικής ανάλυσης και μπορεί να είναι οξειδωτική (συνθετικός αέρας), αδρανής (Ν 2 ) ή δραστική (reactive). Επιπλέον, σημαντική παράμετρος είναι και ο ρυθμός αύξησης της θερμοκρασίας (συνήθως 10 o C/min). Το δείγμα τοποθετείται σε ειδική υποδοχή του οργάνου (pan) και στη συνέχεια εισάγεται σε κλίβανο, ο οποίος παρέχει τη δυνατότητα ελεγχόμενης αύξησης της θερμοκρασίας μέχρι και 1000 o C. Για το λόγο αυτό, το pan είναι κατασκευασμένο απο αδρανές υλικό, ανθεκτικό σε τέτοιες θερμοκρασίες. (π.χ λευκόχρυσος). Η ποσότητα του δείγματος που μπορεί να αναλυθεί είναι μικρή (<10mg στερεής ουσίας) για να αποφευχθούν σφάλματα λόγω θερμικών συνιστωσών. Ο μικροζυγός ακριβείας του οργάνου έχει ευαισθησία της τάξης του μg, ενώ η θερμοκρασία του δείγματος μετράται και καταγράφεται με ακρίβεια μέσω θερμοζεύγους. Εικόνα 2.2: (α) Όργανο TGA Q-50 (TA Instruments) (β) ο κλίβανος της διάταξης [132]. Η θερμοσταθμική ανάλυση εφαρμόζεται στην παρακολούθηση φαινομένων αποικοδόμησης και οξείδωσης, που έχουν σαν συνέπεια μεταβολές στη μάζα του δείγματος συναρτήσει της θερμοκρασίας. Επίσης, χρησιμοποιείται σε περιπτώσεις εξάχνωσης, εξάτμισης και εκροής αερίων συστατικών από τα δείγματα. Ενδεικτικά αναφέρεται ότι μελετάται η θερμική αποικοδόμηση των πολυμερών και ο μηχανισμός γήρανσής τους, ενώ μέσω της μεθόδου είναι επιπλέον δυνατή η ταυτοποίηση πολυμερών και ο προσδιορισμός προσμίξεων σε αυτά. 76
95 Το διάγραμμα της μάζας ή του ποσοστού της μάζας ως συνάρτηση του χρόνου ή/και της θερμοκρασίας ονομάζεται θερμογράφημα ή καμπύλη θερμικής διάσπασης. Μία εναλλακτική και συμπληρωματική παρουσίαση είναι η χρήση της πρώτης παραγώγου της καμπύλης TGA σε συνάρτηση με τη θερμοκρασία ή το χρόνο. Η συγκεκριμένη παραλαγή επιτρέπει τη μελέτη του ρυθμού μεταβολής της μάζα του δείγμτος, λύνοντας προβλήματα υπερκαλυπτόμενων θερμικών αντιδράσεων, και είναι γνωστή ως διαφορική θερμοσταθμική καμπύλη (Differential ThermoGravimetric curve, DTG) [133]. 77
96 2.3 Δυναμική Σκέδαση Φωτός (Dynamic Light Scattering, DLS) Μια από τις πιο δημοφιλείς τεχνικές για τη μέτρηση του μεγέθους κολλοειδών νανοσωματιδίων είναι η δυναμική σκέδαση φωτός, γνωστή και ως φασματοσκοπία συσχέτισης φωτονίων (photon correlation spectroscopy), καθώς δύναται να μετρήσει το μέγεθος σωματιδίων σε διασπορά, ταχύτατα και απαιτώντας ελάχιστη προετοιμασία του δείγματος (Εικόνα 2.3). Η τεχνική DLS ανιχνεύει τη συχνότητα ταλάντωσης (τρεμοπαίγματος) του μοτίβου που καταγράφεται στον ανιχνευτή από τη σκέδαση του φωτός απο τα σωματίδια. Η ενισχυτική και καταστρεπτική συμβολή του φωτός από τη σκέδαση, είναι υπεύθυνη για την εμφάνιση φωτεινών και σκοτεινών περιοχών σε αυτό το μοτίβο (Εικόνα 2.4). Η συχνότητα αυτή είναι ανάλογη της θερμικής κίνησης Brown των σωματιδίων, η οποία με τη σειρά της εξαρτάται από το μέγεθος των σωματιδίων (όσο μικρότερα τα σωματίδια τόσο μεγαλύτερη είναι η κίνηση Brown) και από το ιξώδες του διαλύτη. Το ιξώδες ενός υγρού σχετίζεται άμεσα με τη θερμοκρασία του, άρα για να μετρηθεί η κινητικότητα των σωματιδίων μέσα σε ένα διάλυμα είναι απαραίτητο οι μετρήσεις να διεξάγονται κάτω από μια γνωστή και σταθερή θερμοκρασία [134]. Εικόνα 2.3: Όργανο DLS (Nano Zeta Sizer/Malvern) [135]. Η ανάλυση της χρονικής εξάρτησης της διακύμανσης/συσχέτισης του μοτίβου τρεμοπαίγματος μπορεί επομένως να αποδώσει το συντελεστή διάχυσης των σωματιδίων (D), μέσω του οποίου χρησιμοποιώντας την εξίσωση Stokes-Einstein (Eξισώση 1.3, D = 78 kt 6πηr ), και γνωρίζοντας το ιξώδες του μέσου (n), μπορεί να υπολογιστεί η υδροδυναμική διάμετρος (D h ) των σωματιδίων [όπου k: η σταθερά Boltzmann, T: η απόλυτη θερμοκρασία, και r: η
97 υδροδυναμική ακτίνα του σωματιδίου (r = 0.5D h )]. Η διάμετρος που υπολογίζεται μέσω της τεχνικής DLS ονομάζεται υδροδυναμική διάμετρος και είναι η διάμετρος μιας ιδεατής σφαίρας που έχει τον ίδιο συντελεστή διάχυσης με το σωματίδιο. Εικόνα 2.4: α) Σχηματική αναπαράσταση ενός μοτίβου τρεμοπαίγματος, β) Το παρατηρηθέν σήμα εξαρτάται από την συμβολή των φάσεων του σκεδαζόμενου φωτός που προσπίπτει στον ανιχνευτή. β 1 ) δύο ακτίνες συμβάλουν και ακυρώνονται μεταξύ τους με συνέπεια να ανιχνεύεται μειωμένη ένταση (σκοτεινή περιοχή). β 2 ) δύο ακτίνες συμβάλουν ενισχυτικά με συνέπεια να ανιχνεύεται αυξημένη ένταση (φωτεινή περιοχή) [134]. Μέσω της τεχνικής DLS μπορεί να γίνει επιλογή μεταξύ τριών διαφορετικών κατανομών υδροδυναμικής διαμέτρου, με βάση την ένταση της σκεδαζόμενης ακτινοβολίας, τον όγκο και τον αριθμό των σωματιδίων. Ένας απλός τρόπος περιγραφής των διαφορών μεταξύ των κατανομών αυτών, είναι να θεωρήσουμε δύο ίσους πληθυσμούς σφαιρικών σωματιδίων διαμέτρου 5 και 50nm. Εάν γίνει απεικόνιση της κατανομής του αριθμού των σωματιδίων, το προκύπτον διάγραμμα θα αποτελείται από 2 κορυφές (στα 5 και 50nm) σε αναλογία 1:1. Όταν η κατανομή αριθμού σωματιδίων μετατραπεί σε κατανομή όγκου σωματιδίων, τότε η αναλογία των δύο κορυφών θα αλλάξει σε 1:1000, καθώς ο όγκος είναι ανάλογος της τρίτης δύναμης της ακτίνας (r 3 ). Εάν στη συνέχεια η κατανομή αυτή μετατραπεί σε κατανομή έντασης σκεδαζόμενου φωτός, ο λόγος της έντασης των δύο κορυφών θα είναι 1: , αφού η ένταση, σύμφωνα με την προσέγγιση Rayleigh είναι ανάλογη της έκτης δύναμης της ακτίνας των σωματιδίων (r 6 ) (Εικόνα 2.5). Οι κατανομές με βάση τον όγκο είναι χρήσιμες σε περιπτώσεις όπου τα διαγράμματα κατανομής με βάση την ένταση, παρουσίαζουν περισσότερες απο μία κορυφές ή ασσύμετρη κορυφή (tailing). Συνήθως όμως, προσδιορίζουμε την D h με βάση την ένταση. 79
98 Εικόνα 2.5: Κατανομή μεγέθους των σωματίδιων με βάση τον αριθμό (number), τον όγκο (volume) και την ένταση της σκεδαζόμενης ακτινοβολίας (intensity) κολλοειδούς διασποράς ίσου πληθυσμού σωματιδίων διαμέτρου 5 και 50nm [134]. Μία τυπική διάταξη DLS αποτελείται από έξι κύρια τμήματα α) Την πηγή φωτός (Laser He- Ne, λ=633nm), η δέσμη της οποίας θα περάσει μέσα από το δείγμα, β) φίλτρα (φακούς) για ρύθμιση της έντασης της ακτινοβολίας γ) την κυψελίδα με το δείγμα και δ) τον ανιχνευτή ο οποίος μετρά η σκεδαζόμενη ακτινοβολία. Επίσης, ε) μία ψηφιακή πλατφόρμα επεξεργασίας του σήματος της έντασης της σκεδαζόμενης ακτινοβολίας (correlator) και τέλος, η πληροφορία αυτή περνά σε ένα ηλεκτρονικό υπολογιστή (στ), όπου με κατάλληλο λογισμικό αναλύονται τα δεδομένα και δίνονται πληροφορίες για το μέγεθος των σωματιδίων (Εικόνα 2.6). Εικόνα 2.6: Σχηματική απεικόνιση της διάταξης DLS 80
99 Τα νεοτέρα συστήματα DLS ανιχνέουν τη σκεδαζόμενη ακτινοβολία σε γωνία 173 ο (Backscattering detection), σε αντίθεση με τα παλαιότερης τεχνολογίας συστήματα, στα οποία η ανίχνευση συντελείται στις 90 ο. Η τεχνολογία αυτή ονομάζεται Non-Invasive Backscatter (NIBS) επειδή το οπτικό σύστημα δεν είναι σε επαφή με το δείγμα (noninvasive). Τα πλεονεκτήματα της NIBS είναι τα εξής: 1. Αύξηση της ευαισθησίας της μεθόδου. 2. Ο όγκος του δείγματος που επεξεργάζεται είναι δέκα φορές μεγαλύτερος από των κοινών συστημάτων των 90 ο. 3. Υπάρχει δυνατότητα μέτρησης μεγάλου φάσματος συγκεντρώσεων του δείγματος. 4. Η ακτίνα laser δεν χρειάζεται να διαπεράσει όλο το δείγμα, εξαλείφοντας το φαινόμενο της πολλαπλής σκέδασης, ενώ είναι δυνατή η μέτρηση πιο πυκνών δειγμάτων. 5. Η ανίχνευση της σκέδασης στις 173 ο μειώνει την επίδραση της παρουσίας σκόνης στα δείγματα, αφού τα μεγαλύτερα σωματίδια (σκόνη) σκεδάζουν περισσότερο φως στην αντίθετη κατεύθυνση. 81
100 2.4 Φασματοφωτομετρία Υπεριώδους-Ορατού (UV- VIS) Η φασματοφωτομετρία απορρόφησης αποτελεί μια από τις πιο χρήσιμες τεχνικές στη χημική ανάλυση. Πολλές χημικές ουσίες απορροφούν ηλεκτρομαγνητική ακτινοβολία, ιδιαίτερα στην υπεριώδη περιοχή του φάσματος, και με τη χρησιμοποίηση του κατάλληλου οργάνου και τεχνικής είναι δυνατή η ταυτοποίηση και ο ποσοτικός προσδιορισμός τους. Το τμήμα του μορίου που είναι υπεύθυνο για την απορρόφηση ηλεκτρομαγνητικής ακτινοβολίας καλείται χρωμοφόρο. Η φασματοφωτομετρία υπεριώδους-ορατού (~ nm) χρησιμοποιείται ευρέως για τον ποσοτικό προσδιορισμό ουσιών. Όταν μονοχρωματική ακτινοβολία διέρχεται από ένα διάλυμα το οποίο περιέχει μια ουσία που απορροφά σε αυτά τα μήκη κύματος, η ισχύς της ακτινοβολίας ελαττώνεται προοδευτικά κατά μήκος της διαδρομής. Η ελάττωση της ισχύος της ακτινοβολίας εξαρτάται από τη συγκέντρωση της ουσίας και από την απόσταση που διένυσε η δέσμη μέσα στο διάλυμα. Οι σχέσεις αυτές εκφράζονται με το νόμο των Lambert-Beer και διατυπώνεται ως εξής: A= log(p 0 /P) = - logt = αbc g/l = εbc mol/l (Εξίσωση 2.1) Όπου, Α η απορρόφηση, Ρ 0 η ισχύς της προσπίπτουσας ακτινοβολίας, Ρ η ισχύς της ακτινοβολίας μετά τη διέλευσή της από το διάλυμα, Τ η διαπερατότητα, α μια σταθερά αναλογίας που ονομάζεται απορροφητικότητα, b το μήκος της διαδρομής που διανύθηκε από την ακτινοβολία μέσα στο διάλυμα, ε μια σταθερά αναλογίας που ονομάζεται μοριακή απορροφητικότητα και c η συγκέντρωση της ουσίας στο διάλυμα. Ο νόμος των Lambert-Beer προϋποθέτει ότι: α) Ο μόνος μηχανισμός αλληλεπίδρασης ηλεκτρομαγνητικής ακτινοβολίας και διαλυμένης ουσίας είναι η απορρόφηση. β) Η προσπίπτουσα ακτινοβολία είναι μονοχρωματική. γ) H απορρόφηση γίνεται σε ένα όγκο διαλύματος ομοιόμορφης διατομής. δ) Τα σωματίδια που απορροφούν δρουν ανεξάρτητα το ένα από το άλλο και άσχετα από τον αριθμό και το είδος τους. Οι βασικές δομικές μονάδες ενός φασματοφωτομέτρου είναι: 1) μια πηγή ακτινοβολίας σταθερής ισχύος, 2) ένας μονοχρωμάτορας για την απομόνωση της επιθυμητής ακτινοβολίας, 82
101 3) μία κυψελίδα για την τοποθέτηση του δείγματος, 4) ένας ανιχνευτής ακτινοβολίας που μετατρέπει το οπτικό σήμα σε ηλεκτρικό και 5) ένα σύστημα μετρήσεως που περιλαμβάνει ενισχυτή του σήματος και όργανο αναγνώσεως. Στην υπεριώδη περιοχή ( nm) χρησιμοποιείται λυχνία εκκενώσεως δευτερίου (D 2 ), ενώ στην ορατή ( nm) λυχνία πυρακτώσεως βολφραμίου (W). Η ακτινοβολία που εκπέμπεται από την πηγή κατευθύνεται μέσω κατόπτρων στο μονοχρωμάτορα, όπου ένα φράγμα περιθλάσεως μπλοκάρει τα μήκη κύματος που δεν είναι επιθυμητά, επιτρέποντας τη διέλευση μόνο της προεπιλεγμένης μονοχρωματικής ακτινοβολίας. Στη συνέχεια, η δέσμη διχάζεται σε δύο τμήματα, το ένα τμήμα διέρχεται απο την κυψελίδα που περιέχει το δέιγμα, ένω το άλλο απο την κυψελίδα που περιέχει το διάλυμα αναφοράς. Οι κυψελίδες είναι κατασκευασμένες από χαλαζία για μετρήσεις στην περιοχή του υπεριώδους ή από γυαλί και πλαστικό για μετρήσεις στο ορατό, έχουν πάχος συνήθως 1cm (οπτική διαδρομή). Μετά τη διέλευσή τους από τις κυψελίδες, οι δέσμες κατευθύνονται προς τους αντίστοιχους ανιχνευτές (φωτοδίοδοι πυριτίου) για τη μετατροπή του οπτικού σήματος σε ηλεκτρικό και την ενίσχυσή του (Εικόνα 2.7). Η διάταξη που περιγράφηκε πιο πάνω αφορά τα φασματοφωτόμετρα διπλής δέσμης. Υπάρχουν επίσης τα φασματοφωτόμετρα μονής δέσμης, στα οποία δεν υπαρχεί υποδοχή για διάλυμα αναφοράς, η δέσμη δεν χωρίζεται και περνά μόνο απο την κυψελίδα που περιέχει το δείγμα [21133]. Είκονα 2.7: Διάταξη Φασματοφωτομέτρου διπλής δέσμης [136]. 83
102 Για να ισχύει ο νόμος Lambert-Beer θα πρέπει τα υπο ανάλυση διαλύματα να είναι αραιά. Σε πυκνά διαλύματα (>0.01Μ) παρατηρούνται αποκλίσεις απο τη γραμμική σχέση μεταξύ απορρόφησης και συγκέντρωσης, και ως εκ τούτου οι μετρήσεις σε τέτοιες περιπτώσεις είναι αναξιόπιστες. Η φασματοφωτομετρία υπεριώδους-ορατού είναι μια απλή, ευαίσθητη και ταχύτατη τεχνική που χρησιμοποιείται τόσο στον ποιοτικό όσο και στον ποσοτικό προσδιορισμό ουσιών. Βασικό μειονέκτηματα της αφορά την έλλειψη εκλεκτικότητας, αφου πολλές ουσίες απορροφούν στα αυτά τα μήκη κύματος, με αποτέλεσμα τον εξαιρετικά δυσκόλο προσδιορισμό μείγματος ουσιών που απορροφούν σε παραπλήσια μήκη κύματος. 84
103 2.5 Μαγνητοφόρηση Η κατευθυνόμενη κίνηση των μαγνητικών σωματιδίων λόγω της δράσης ενός μαγνητικού πεδίου καλείται μαγνητοφόρηση, και έχει βρει τις πρώτες της εφαρμογές σε διάφορους τομείς κατά τη διάρκεια της δεκαετίας του 1970 και του Ένας απλός μαγνήτης στην περιοχή δοκιμαστικού σωλήνα που περιέχει παραμαγνητικά σωματίδια, παράγει βαθμίδα μαγνητικού πεδίου της τάξης του 1T/m, το οποίο αρκεί για να παρατηρηθεί εύκολα η κίνηση της διασποράς των σωματιδίων. Φυσικά, αυτή η απλή διαδικασία μαγνητοφόρησης μπορεί να βελτιωθεί κατά πολύ. Η γενική ιδέα είναι βασισμένη στην παρατήρηση ότι οι ταχύτητες των μαγνητικών σωματιδίων είναι ανάλογες προς τη βαθμίδα του μαγνητικού πεδίου. Η κίνηση των σωματιδίων κατά τη διάρκεια της μαγνητοφόρησης έχει μια σύνθετη, συλλογική συμπεριφορά, όπως επιβεβαιώνεται από άμεσες παρατηρήσεις με τη βοήθεια μικροσκοπίου στην εργασία. [137]. Η ταχύτητα ενός σωματιδίου v c, σε ένα εξωτερικό μαγνητικό πεδίο είναι συνάρτηση της κινητικότητας m του σωματιδίου και της τοπικής ισχύος της δύναμης S m : Η τοπική ισχύς της δύναμης ορίζεται ως: v c = m S m (Εξίσωση 2.2) S m = B2 2μ 0 (Εξίσωση 2.3) Όπου B είναι η ένταση του μαγνητικού πεδίου και μ 0 η μαγνητική επιδεκτικότητα στο κενό [138]. Η μαγνητοφόρηση είναι μια αναστρέψιμη διαδικασία, καθώς όταν γίνει άρση του μαγνητικού πεδίου, η αρχική διασπορά ανακτάται με απλή ανακίνηση του δείγματος. Ο διαχωρισμός εξαρτάται σε μεγάλο βαθμό από τις απαιτήσεις του πειράματος και του περιβάλλοντος (υγρό, εναιωρήματα, αίμα) στο οποίο λαμβάνει χώρα [139]. Η πρόοδος της διαδικασίας διαχωρισμού μπορεί να παρακολουθείται ποσοτικά με μέτρηση της έντασης του φωτός που απορροφάται από το δείγμα. Όπως είναι γνωστό η μαγνήτιση ανά μονάδα όγκου ή μάζας ( M s = M net ) εξαρτάται από την διάμετρο των νανοκρυσταλλιτών και βέβαια από το υλικό [96]. Οπότε, δείγματα μαγνητικών κολλοειδών τα οποία αποτελούνται από νανοκρυσταλλίτες με παρόμοια διάμετρο και ανεξάρτητα από την εσωτερική τους οργάνωση (αν αποτελούνται δηλαδή από έναν ή 85
104 περισσότερους πυρήνες) αναμένεται να έχουν και παρόμοια M s (Εικόνα 2.8a). Όταν όμως εξετάζονται μαγνητικά κολλοειδή εντός βαθμίδων μαγνητικών πεδίων, η κίνηση τους περιγράφεται από την Εξίσωση 2.4: F = (V t M s )B (Εξίσωση 2.4) Όπου, F η μαγνητική δύναμη που ασκείται στο μαγνητικό υλικό, Vt ο συνολικός όγκος του μαγνητικού υλικού που υπάρχει σε κάθε σωματίδιο (κολλοειδές), B η μαγνητική επαγωγή και Ms η μαγνήτιση κόρου. Από τα παραπάνω συνάγεται ότι η απόκριση των μαγνητικών κολλοειδών κατά την αλληλεπίδρασή τους με βαθμίδες μαγνητικών πεδίων, εξαρτάται και από τον όγκο του μαγνητικού υλικού Vt που συμμετέχει σε κάθε κολλοειδές (Εικόνα 2.8b) [21]. Εικόνα 2.8: (a) Μαγνητικοί νανοκρυσταλλίτες ανεξάρτητοι μεταξύ τους και οργανωμένοι σε πλειάδα. (b) Δύναμη που δέχονται οι νανοκρυσταλλίτες σε βαθμίδα μαγνητικού πεδίου αναλόγως της οργάνωσής τους. 86
105 2.6 Υγρή Χρωματογραφία Υψηλής Απόδοσης (High Performance Liquid Chromatography, HPLC) Η αρχή της υγρής χρωματογραφίας στηρίζεται στη διαφορετική κατανομή των συστατικών ενός μείγματος μεταξύ δύο φάσεων, μιας σταθερής (stationary phase) και μιας κινητής (mobile phase). Η κινητή φάση μετακινεί τα συστατικά του μείγματος επί της σταθερής φάσης με διαφορετική ταχύτητα. Μια ουσία, η οποία συγκρατείται ισχυρότερα από τη σταθερή φάση, μετακινείται με μικρότερη ταχύτητα από κάποια άλλη, η οποία συγκρατείται λιγότερο ισχυρά. Ο διαχωρισµός ενός µείγµατος στα συστατικά του βασίζεται στους διαφορετικούς χρόνους ανάσχεσης (t R ) κάθε συστατικού µέσα στη στήλη. Με την ανάπτυξη της υγρής χρωματογραφίας υψηλής απόδοσης, οι χρόνοι διαχωρισμού μειώθηκαν σημαντικά. Κατά την τεχνική αυτή το υλικό πλήρωσης της στήλης (σταθερή φάση) είναι λεπτότατου διαμερισμού (σωματίδια πολύ μικρής διαμέτρου) και έχει υψηλή σφαιρική κανονικότητα, έτσι ώστε να επιτυγχάνονται μεγάλου βαθμού ομοιομορφία και πυκνότητα πλήρωσης. Η υψηλή πυκνότητα πληρώσεως όμως με αυτά τα πολύ μικρά σωματίδια, μειώνει την ταχύτητα ροής της κινητής φάσης μέσα από τη στήλη (μεγάλη αντίσταση μεταφοράς) και για να επιτευχθεί μία λογική ταχύτητα ροής απαιτείται η εφαρμογή υψηλής πίεσης στην κινητή φάση. Συνήθως, η πίεση που αναπτύσσεται στην HPLC κυμαίνεται απο psi. Αν η στατική φάση είναι πιο πολική από την κινητή, αυτό το είδος της χρωµατογραφίας κατονομής ονοµάζεται χρωµατογραφία κανονικής φάσης (normal phase chromatography, NP-HPLC). Αντίθετα, αν η κινητή φάση είναι πιο πολική από τη στατική, τότε η χρωµατογραφία κατανοµής ονοµάζεται χρωµατογραφία αντίστροφης φάσης (reverse phase chromatography, RP-HPLC). Κατά την NP-HPLC ο χρόνος έκλουσης (t R ) των συστατικών μπορεί να μεταβληθεί μεταβάλλοντας την πολικότητα του διαλύτη έκλουσης. Κατά την RP-HPLC η ισχύς έκλουσης αυξάνει με την παράλληλη μείωση της πολικότητας του διαλύτη, διότι έτσι ελαττώνεται η συγκράτηση μιας ουσίας στη στατική φάση. Στην περίπτωση ουσιών που μπορούν να υποστούν ιονισμό, μια αλλαγή στο ph μπορεί να επηρεάσει τη συγκράτηση και την εκλεκτικότητά τους. Η οφθαλµοφανής υπεροχή της HPLC ως προς την κλασική υγροχρωµατογραφία στήλης (µέσω βαρύτητας) έγκειται στο γεγονός ότι τα δείγµατα µπορούν να διαχωριστούν πολύ ταχύτερα. Επίσης µη πτητικά δείγµατα ή δείγµατα που αποσυντίθενται εύκολα θερµικά και δεν µπορούν να αναλυθούν µε την αεριοχρωµατογραφία (GC), µπορούν να διαχωριστούν µε HPLC γρήγορα και αποτελεσµατικά. 87
106 Τα βασικά τμήματα μιας συσκευής HPLC είναι: 1) σύστημα παροχής κινητής φάσης, 2) σύστημα εισαγωγής δείγματος (injector), 3) στήλη, 4) ανιχνευτής και 5) καταγραφέας (Εικόνα 2.9). Εικόνα 2.9: Σχηματική απεικόνιση της διάταξης της HPLC [140]. Το σύστημα παροχής κινητής φάσης (μείγμα διαλυτών) αποτελείται από μία αντλία υψηλής πιέσης και ένα σύστημα για τη βαθμιαία αλλαγή της σύστασης της κινητής φάσης. Όταν η κινητή φάση έχει σταθερή σύσταση έχουμε ισοκρατική έκλουση (isocratic elution), ενώ όταν μεταβάλλεται βαθμιαία έχουμε βαθμιδωτή έκλουση (gradient elution). Για την επίτευξη της βαθμιδωτής έκλουσης, απαιτείται μια μονάδα προγραμματισμού και ελέγχου του συστήματος παροχής. Οι χρησιμοποιούμενοι διαλύτες πρέπει να είναι διαφορετικής πολικότητας (πλήρως αναμίξιμοι), ή διαλύματα διαφορετικού ph, ή διαφορετικής ιοντικής ισχύος ή συγκεντρώσεως κάποιου άλατος, ανάλογα με το είδος του επιδιωκόμενου μηχανισμού διαχωρισμού. Επίσης, θα πρέπει να είναι υψηλής καθαρότητας και πριν τη χρήση τους διηθούνται από ειδικά φίλτρα υπό κενό και απαερώνονται. Οι συνηθέστερα χρησιμοποιούμενοι διαλύτες είναι το νερό, το ακετονιτρίλιο, η μεθανόλη, το οξικό οξύ και ρυθμιστικά διαλύματα. Οι στήλες της HPLC είναι ευθύγραμμοι σωλήνες από χάλυβα, οι οποίες αγοράζονται έτοιμες από τις διάφορες παρασκευάστριες εταιρείες. Εξαιτίας των υψηλών πιέσεων που ασκούνται (μέχρι και 4000psi) τα κλασσικά υλικά πληρώσεως των στηλών, όπως Sephadex και Sepharose, δεν μπορούν να χρησιμοποιηθούν. Έτσι στην HPLC χρησιμοποιούνται συνήθως πολυμερή διοξειδίου του πυριτίου (silica) ή αλουμίνας (alumina). Κατά την RP-HPLC χρησιμοποιούνται υλικά πληρώσεως (κυρίως μικροπορώδη 88
107 σωματίδια πηκτής διοξειδίου του πυριτίου) με χημικά συνδεδεμένες στατικές φάσεις (chemically bonded stationary phases). Τα σωματίδια αυτά είναι συνήθως διαμέτρου 5-10μm με πόρους 20nm και διαθέτουν μεγάλη επιφάνεια επαφής στην οποία συνδέονται ομοιοπολικά οι στατικές φάσεις (αλκυλομάδες και άλλες δραστικές ομάδες). Στατικές φάσεις αλκυλομάδων με αλυσίδες C 8 Η 17 (octyl) και C 18 Η 37 (octadecyl) δεσμευμένες στη silica είναι ευρέως διαδεδομένες και βρίσκουν εφαρμογές σε διαχωρισμούς αμινοξέων, πεπτιδίων, πρωτεϊνών, βιταμινών, λιπών, στεροειδών, αντιβιοτικών, νουκλεοτιδίων, σακχάρων κ.ά. Οι χρησιμοποιούμενοι ανιχνευτές πρέπει να έχουν υψηλή ευαισθησία ικανοποιητικού κατώτατου ορίου ανίχνευσης (LOD), χαμηλά επίπεδα θορύβου, να μην επηρεάζονται από μεταβολές της θερμοκρασίας και της ταχύτητας ροής των διαλυτών έκλουσης κ.ά.. Οι πιο συχνά χρησιμοποιούμενοι ανιχνευτές είναι οι διαφορικοί ανιχνευτές δείκτη διάθλασης, οι ανιχνευτές υπεριώδους-ορατού, οι ανιχνευτές υπεριώδους-ορατού με συστοιχίες φωτοδιόδων (PhotoDiode Array, PDA) οι ανιχνευτές φθορισμού, οι ανιχνευτές υπερύθρου, οι ηλεκτροχημικοί ανιχνευτές και οι φασματογράφοι μάζας. H συνδυασμένη τεχνική υγρής χρωματογραφίας-φασματομετρίας μάζας (LC-MS) χαρακτηρίζεται από εξαιρετική ευαισθησία, εκλεκτικότητα και αξιοπιστία. Η τεχνική LC-MS χρησιμοποιείται για την ταυτοποίηση ουσιών σε πολύπλοκα βιολογικά δείγματα. Σε ένα καλό χρωματογραφικό σύστημα αναλύσης πρέπει να επιτυγχάνεται διαφορετική ταχύτητα μετακινήσεως των ζωνών των συστατικών, λόγω του διαφορετικού βαθμού συγκρατήσεως τους στη στατική φάση. Γενικά, ο διαχωρισμός μιας συγκεκριμένης ουσίας εξαρτάται από το μοριακό βάρος, τη διαλυτότητα και τη χημική της δομή. Τα κριτήρια για την επιλογή του κατάλληλου συστήματος διαλυτών (κινητή φάση) για έκλουση εξαρτώνται από τις φυσικοχημικές ιδιότητες του δείγματος και της εκλουστικής ικανότητας του συστήματος διαλυτών [141]. Εν κατακλείδι, με την επιλογή καταλλήλης κινητής φάσης, συστήματος έκλουσης (ισοκρατικό ή βαθμιδωτό, ταχύτητα ροής κινητής φάσης), στήλης (διαστάσεις, μέγεθος σωματιδίων) και ανιχνευτή, η HPLC παρέχει τη δυνατότητα προσδιορισμού των επιμέρους συστατικών ενος μείγματος, τόσο ποιοτικά όσο και ποσοτικά, με εξαιρετική ακρίβεια και ευαισθησία (Εικόνα 2.10). Ο χρόνος ανάλυσης, που σε κάποιες περιπιπτώσεις είναι μεγάλος, καθώς και το κόστος των διαλυτών, αποτελούν μειονεκτήματα της συγκεκριμένης τεχνικής. 89
108 Εικόνα 2.10: Χρωματογράφημα HPLC. Ταυτόχρονος προσδιορισμός των δραστικών συστατικών του αναλγητικού φαρμακευτικού σκευάσματος Excedrin [142]. 90
109 Κεφάλαιο 3 Πειραματικό μέρος 91
110 Το πειραματικό μέρος της παρούσας μεταπτυχιακής διατριβής εκπονήθηκε σε τρία στάδια: 1. Σύνθεση, απομόνωση και χαρακτηρισμός υπερπαραμαγνητικών νανοκρυσταλλιτών οξειδίου του σιδήρου (Superparamagnetic Iron Oxide Nanocrystals, SPIONs) (μαγνητίτη Fe 3 O 4, μαγκεμίτη γ-fe 2 O 3 ). 2. Μελέτη των παραμέτρων της σύνθεσης πολυμερικών και υπερπαραμαγνητικών πολυμερικών μικκυλίων Μελέτη των παραμέτρων της φόρτωσης και αποδέσμευσης Πακλιταξέλης (PTX), εγκλωβισμένης σε πολυμερικά και υπερπαραμαγνητικά πολυμερικά μικκύλια. 3.1 Αντιδραστήρια Παρακάτω αναγράφονται τα χημικά αντιδραστήρια που χρησιμοποιήθηκαν σε όλα τα στάδια της πειραματικής διαδικασίας, καθώς και η εταιρεία προμήθειάς τους : Ακετυλακετονικός σίδηρος (ΙΙΙ) [Fe(acac) 3 ], Acros Organics. Ελαϊκό οξύ [CH 3 (CH 2 ) 7 CH=CH(CH 2 ) 7 COOH] tech.grade: 90%, Alfa Aesar. 1-Δεκαοκτένιο [CH 3 (CH 2 ) 15 CH=CH 2 ] tech.grade: 90%, Alfa Aesar. Εξαένυδρος τριχλωριούχος σίδηρος (FeCl 3 6H 2 O), Panreac. Ελαϊκό νάτριο [CH 3 (CH 2 ) 7 CH=CH(CH 2 ) 7 COOΝa] tech.grade 82%,Sigma Aldrich. 9- Δεκαοκτενυλαμίνη [CH 3 (CH 2 ) 7 CH=CH(CH 2 ) 7 CH 2 NH 2 ] tech.grade 70%, Fluka. Διφαινυλαιθέρας [(C 6 H 5 ) 2 O], Merck. Διβενζυλαιθέρας [(C 6 H 5 CH 2 ) 2 O], Acros Organics. Τριαιθυλενογλυκόλη (C 6 H ), Merck. Άνυδρο Θειικό Νατριο (Na 2 SO 4 ), Sigma Aldrich. Πόλυ(γαλακτικό οξύ)-b-πόλυ(αιθυλενογλυκόλη) [PLA(2kDa)-b-PEG(5kDa)], Advanced Polymer Materials inc. Πόλυ(γαλακτικό οξύ)-b-πόλυ(αιθυλενογλυκόλη) [PLA(5kDa)-b-PEG(5kDa)], Advanced Polymer Materials inc. Πόλυ(γαλακτικό οξύ)-b-πόλυ(αιθυλενογλυκόλη) [PLA(10kDa)-b-PEG(5kDa)], Advanced Polymer Materials inc. Πακλιταξέλη (Paclitaxel, PTX), Alfa Aesar. Εξάνιο [CH 3 (CH 2 ) 4 CH 3 ], Sigma Aldrich. Αιθανόλη (CH 3 CH 2 OH, EtOH), Sigma Aldrich. 3 Εικόνα Κεφαλαίου: 92
111 Απόλυτη αιθανόλη, Panreac. Ακετόνη (CH 3 CΟCH 3 ), Fischer chemicals. Απόλυτη ακετόνη, Honeywell. Μεθανόλη (CH 3 OH, MeOH), Sigma Aldrich. Διχλωρομεθάνιο (DCM) (CH 2 Cl 2 ), Honeywell. Τετραϋδροφουράνιο (THF) (C 4 H 8 O), Merck. Υδατικό Διάλυμα 1,10-φαινανθρολίνης (C 12 H 8 N 2 ) 0.005M, Alfa Aesar. Υδατικό Διάλυμα υδροχλωρικής υδροξυλαμίνης (NH 2 OH HCl) 1.44M, Alfa Aesar. Υδατικό Διάλυμα οξικού νατρίου (CH 3 COONa) 2Μ, Panreac. Aκετονιτρίλιο (CH 3 CN) tech.grade 99.9%, Sigma Aldrich. Τριφθοροξικό οξύ (TFA) (CF 3 COOH), Alfa Aesar. Υδροχλωρικό οξύ (HCl) 11.9M (37%wt.), Carlo Erba Υδατικό διάλυμα αμμωνίας (NH 4 OH ή ΝΗ 3 ) 15.8M (30%wt.), Carlo Ebra. Υδατικό διάλυμα υροξειδίου του νατρίου ΝaOH 0.01Μ, Sigma Aldrich. Μεμβράνες κυτταρίνης (dialysis tubing) (MWCO:14KDa), Sigma Aldrich. Παρασκευή ρυθμιστικού διαλύματος φωσφορικών (Phosphate buffered saline, PBS 0.14M, ph:7.4) : 7.6g NaCl + 0,99g Na 2 HPO 4 + 0,41g NaH 2 PO 4 x H 2 O σε d.h 2 O με τελικό όγκο 1000ml. Απεσταγμένο νερό (d.h 2 O) αγωγιμότητας 0,7μS / cm. Υπερκάθαρο νερό αγωγιμότητας 0.05μS / cm, για HPLC. 3.2 Χρησιμοποιούμενα Όργανα και Τεχνικές Κάτωθι αναγράφονται τα όργανα, οι μικροσυσκευές και οι τεχνικές που χρησιμοποιήθηκαν σε όλα τα στάδια της πειραματικής διαδικασίας: Ηλεκτρονικός ζυγός ακριβείας (ABJ 220-4M, Kern & Sohn GmbH) Θερμαντικός μανδύας, WiseTherm HM-C10D. Μαγνητικός αναδευτήρας, WiseStir MSH-20D. Η Φυγοκέντρηση των SPIONs πραγματοποιήθηκε σε φυγόκεντρο της εταιρείας Kendro-Megafuge 1.0R - Heraeus (2100g max). Η Φυγοκέντρηση των πολυμερικών μικκυλίων πραγματοποιήθηκε σε φυγόκεντρο της εταιρείας Hettich-Mikro 220 ( x 1000 g max) To Λουτρό Υπερήχων που χρησιμοποιήθηκε είναι το S15H Elmasonic. 93
112 ph-μέτρο, Consort C931. Υδατόλουτρο ρυθμιζόμενης θερμοκρασίας, Bioline Scientific 5020SWB. Περιστροφικός εξατμιστήρας υπο κενό (rotary evaporator), IKA- Werke RV05-ST. Λυοφιλοποιητής, Telstar Cryodos. Κλίβανος, Binder. Ξηραντήρας. Οι μικροσυσκευές που χρησιμοποιήθηκαν κατα τη διαδικασία της σύνθεσης των μαγνητικών νανοσωματιδίων είναι: τρίλαιμη σφαιρική φιάλη των 100 ml, ψυκτήρας, θερμόμετρο (300 ο C) για παρακολούθηση της θερμοκρασίας, οβάλ μαγνήτης (μήκους 2.5cm) για ανάδευση καθώς και μαγνήτης Nd-Fe-B (διαστάσεις: διάμετρος = 20mm, πάχος = 10mm) για χειρισμό των μαγνητικών νανοσωματιδίων κατα τη διάρκεια των πλύσεων. Φασματοφωτόμετρο UV-VIS, Hitachi Digilab U Ηλεκτρονική Μικροσκοπία Διέλευσης (Transmission Electron Microscopy, ΤΕΜ). Υγρή Χρωματογραφία Υψηλής Απόδοσης (High Performance Liquid Chromatography, HPLC). Η τεχνική της θερμοσταθμικής ανάλυσης (Thermogravimetric Analysis, TGA) πραγματοποιήθηκε με τη χρήση του οργάνου Q500 της TA Instruments. Η τεχνική της Δυναμικής Σκέδασης Φωτός (Dynamic Light Scattering, DLS) πραγματοποιήθηκε με τη χρήση του οργάνου της εταιρείας Malvern (Nano Zeta Sizer). Η τεχνική της μαγνητοφόρησης πραγματοποιήθηκε με τη χρήση του φασματοφωτόμετρου Hitachi Digilab U Οι μετρήσεις ζ-δυναμικού πραγματοποιήθηκαν με τη χρήση του οργάνου της εταιρείας Malvern (Nano Zeta Sizer). Η τεχνική της αποδέσμευσης φαρμάκου απο μαγνητικά κολλοειδή με την εφαρμογή εναλλασσόμενου μαγνητικού πεδίου, πραγματοποιήθηκε με τη χρήση της διάταξης magnetherm της εταιρείας nanotherics. 94
113 3.3 Σύνθεση και χαρακτηρισμός υδρόφοβων SPIONs Οι βασικές παραμέτροι που ελέχθησαν κατα τη σύνθεση των μαγνητικών νανοσωματιδίων περιλαμβάνουν την επίδραση της πρόδρομης ουσίας, της θερμοκρασίας αντίδρασης (σημείο ζέσεως διαλύτη), της διάρκειας της σύνθεσης καθώς και της μοριακής αναλογίας πρόδρομης ουσίας ελαϊκού οξέος (oleic acid, O.A), όσον αφορά τη μορφολογία, το μέγεθος και τη διασπορά του μεγέθους των νανοκρυσταλλιτών. Όλες οι συνθέσεις πραγματοποιήθηκαν με τη μέθοδο της θερμικής αποικοδόμησης (thermal decomposition) χρησιμοποιώντας το ελαϊκό οξύ ως σταθεροποιητή επιφανειοδραστική ουσία (coating). Στην Εικόνα 3.1 παρουσιάζεται η πειραματική διάταξη που χρησιμοποιήθηκε κατα τη διάρκεια των συνθέσεων. Εικόνα 3.1. Πειραματική διάταξη που χρησιμοποιήθηκε κατά τη σύνθεση των μαγνητικών νανοσωματιδίων.ορισμένες συνθέσεις πραγματοποιήθηκαν υπο ροή αζώτου όπως απεικονίζεται στη διάταξη (Βλ και Πίνακας 3.3) Συνθέσεις SPIONs με ακετυλακετονικό τρισθενές σίδηρο [Fe(acac) 3 ] ως πρόδρομη ένωση [143] Η πειραματική πορεία που ακολουθήθηκε ήταν η εξής: Ποσότητες Fe(acac) 3 (Εικόνα 3.2) και Ο.Α αναμιγνύονται με διαλύτη συγκεκριμένου όγκου σε τρίλαιμη σφαιρική φυάλη (100ml). Σε κάποιες συνθέσεις προστέθηκε και 9-Δεκαοκτενυλαμίνη (oleylamine, OAm). Οι επιμέρους ποσότητες που χρησιμοποιήθηκαν παρουσιάζονται πιο κάτω στον Πινακα 3.1 Το μείγμα ομογενοποιείται, με έντονη μαγνητική ανάδευση (600 rpm), για είκοσι λεπτά σε 95
114 θερμοκρασία περιβάλλοντος. Ακολούθως, η τρίλαιμη φυάλη τοποθετείται εντός του θερμαντικού μανδύα, όπου και θα λάβει χώρα η θέρμανση. Το μείγμα, αρχικά θερμαίνεται υπο ανάδευση στους 100 ο C, με ρυθμό 18 ο C/λεπτό. Στα στόμια της τρίλαιμης φυάλης τοποθετούνται ο θερμοαισθητήρας του θερμαντικού μανδύα, ένα θερμόμετρο υδραργύρου (300 ο C) για διπλό έλεγχο της θερμοκρασίας, ενώ στο κεντρικό στόμιο εφαρμόζεται ένας Εικόνα 3.2. Fe(acac) 3 κάθετος ψυκτήρας όταν η θερμοκρασία ξεπεράσει τους 150 ο C. Στη συνέχεια, η ταχύτητα ανάδευσης μειώνεται (230 rpm) και το μείγμα θερμαίνεται (καφε-κόκκινο διάλυμα) πρώτα στους 200 ο C με ρυθμό 20 ο C/λεπτό και στη συνέχεια στους 250 ο C με ρυθμό 15 ο C/λεπτό. Το διάλυμα καθίσταται μαύρο όταν η θερμοκρασία υπερβεί τους 220 ο C. Έπειτα, η θερμοκρασία αυξάνεται μέχρι το σημείο ζέσεως (σ.ζ) του διαλύτη με ρυθμό 10 ο C/λεπτό [στην περιπτώση που χρησιμοποιείται ο διφαινυλαιθέρας (σ.ζ: 258 ο C) ως διαλύτης, η τελική θερμοκρασία είναι 250 ο C]. Η θέρμανση συνεχίζεται για μία εώς εικοσιδύο ώρες ( η διάρκεια της αντίδρασης διαφέρει ανάλογα με τη σύνθεση Πίνακας 3.1) απο τη στιγμή που η θερμοκρασία φτάνει στο σ.ζ του διαλύτη και το μείγμα αρχίζει να βράζει. Σε κάποιες συνθέσεις πραγματοποιήθηκε δειγματοληψία σε ενδιάμεσα χρονικά σημεία. Τέλος, το τελικό προϊόν αφήνεται να ψυχθεί σε θερμοκρασία περιβάλλοντος. Στην Εικόνα 3.3 [ 144] φαίνεται η μαγνητική απόκριση των SPIONs. SPIONs Magnet Εικόνα 3.3 : Μαγνητική απόκριση SPIONs. 96
115 Πίνακας 3.1. Σύνοψη Συνθέσεων με Fe(acac) 3 Κωδική Ονομασία Πρόδρομη ένωση Αντιδραστήρια 1 2 Αναλογία Fe(acac) 3 /Ο.Α Διαλύτης (σ.ζ) Διάρκεια Σύνθεσης Μέγεθος (nm) (ΤΕΜ) MagAcac Fe(acac) mmol 0.20g Ο.Α 1mmol 0.28g OAm 2.1mmol 0.57g 0.56 Διφαινυλαιθέρας (258 ο C) 10ml 22h 1h: 5.4 ± 1.4 2h: 5.8 ± 1.4 4h: 7.7 ± h: 7.2 ± h: 7.6 ± 2.4 MagAcac_4 Fe(acac) 3 1.7mmol 0.60g Ο.Α 3mmol 0.85g OAm 6.4mmol 1.7g 0.56 Διφαινυλαιθέρας (258 ο C) 30ml 4h 4h: 9.7 ± 2.2 MagAcac_6 Fe(acac) 3 1.7mmol 0.60g Ο.Α 6mmol 1.7g Διφαινυλαιθέρας (258 ο C) 30ml 4h 4h: 5.8 ± 1.0 MagAcac_285 Fe(acac) 3 1.1mmol 0.40g Ο.Α 4mmol 1.1g OAm 4mmol 1.1g 0.28 Τριαιθυλένογλυκόλη (285 ο C) 20ml 4h 4h: 7.7 ± 1.2 MagAcac_298 Fe(acac) 3 1.7mmol 0.60g Ο.Α 3mmol 0.85g OAm 6.4mmol 1.7g 0.56 Διβενζυλαιθέρας (298 ο C) 30ml 22h 4h: 8.2 ± h: 10.4 ± 2.6 MagAcac_317 Fe(acac) 3 1.7mmol 0.60g O.A 3mmol 0.85g OAm 6.4mmol 1.7g Δεκαοκτένιο (317 ο C) 30ml 4h 1h: 8.8 ± 1.5 4h: 8.7 ± 1.5 MagAcac_1.3 Fe(acac) 3 2mmol 0.71g O.A 6mmol 1.7g Δεκαοκτένιο (317 ο C) 17.5ml 1h 1h: 8.1 ± 2.3 MagAcac_1.2 Fe(acac) 3 2mmol 0.71g O.A 4mmol 1.1g Δεκαοκτένιο 1h: 9.4 ± 1.7 (317 ο 2h C) 17.5ml 2h: 9.1 ± 1.7 MagAcac_1.1 Fe(acac) 3 2mmol 0.71g O.A 2mmol 0.57g Δεκαοκτένιο (317 ο C) 17.5ml 1h 30min:7.6± 1.6 1h: 8.0 ±
116 3.3.2 Συνθέσεις SPIONs με υδρόξυ-οξείδιο του τρισθενούς σιδήρου [FeΟ(ΟΗ)] ως πρόδρομη ένωση [145] Σύνθεση FeΟ(ΟΗ): 10.0g (37.0mmol) εξαένυδρου τριχλωριούχου σιδήρου (FeCl 3 6H 2 O) αναμιγνύονται με 20ml d.h 2 O, σε falcon (50ml), προς σχηματισμό καφέ-κίτρινου διαλύματος. Ακολούθως, η προσθήκη 10ml π.νη 3 (15.8Μ) οδηγεί στον σχηματισμό FeΟ(ΟΗ) (Εικόνα 3.4) υπο μορφή καφέ-κόκκινου ιζήματος,. Το προϊόν υπόκειται σε φυγοκέντρηση για δέκα λεπτά στα 2100g (4000rpm) (Kendro-Megafuge 1.0R - Heraeus) και το υπερκείμενο απορρίπτεται. Το ίζημα εκπλένεται τρεις φορές με 20ml EtOH. Κάθε φορά, μετά τη προσθήκη ΕtOH και ομογενοποίηση του ιζήματος, ακολουθεί φυγοκέντρηση για δέκα λεπτά στα 2100g και το υπερκέιμενο απορρίπτεται. Τέλος το προϊόν εκπλένεται δύο φορές με απόλυτη ακετόνη προς απομάκρυνση της υγρασίας, με τη διαδικασία που περιγράφηκε πιο πάνω, και το ίζημα τοποθετείται στον ξηραντήρα για ξήρανση [4.2g (47.2mmol) FeO(OH)]. Σύνθεση SPIONs: Η πειραματική πορεία που ακολουθήθηκε ήταν η εξής: 0.62g (7.0mmol) FeΟ(ΟΗ) και ποσότητα Ο.Α αναμιγνύονται με 17.5ml 1-Δεκαοκτένιο σε τρίλαιμη σφαιρική φυάλη (100ml). Οι ποσότητες του Ο.Α που χρησιμοποιήθηκαν παρουσιάζονται πιο κάτω στον Πινακα 3.2. Το μείγμα ομογενοποιείται, με έντονη μαγνητική ανάδευση (600 rpm), για είκοσι λεπτά σε θερμοκρασία περιβάλλοντος. Ακολούθως, η τρίλαιμη φυάλη τοποθετείται εντός του θερμαντικού μανδύα, όπου και θα λάβει χώρα η θέρμανση. Το μείγμα, αρχικά θερμαίνεται υπο ανάδευση στους 100 ο C, με ρυθμό 18 ο C/λεπτό. Στα στόμια της τρίλαιμης φυάλης τοποθετούνται ο θερμοαισθητήρας του θερμαντικού μανδύα, ένα θερμόμετρο υδραργύρου (300 ο C) για διπλό έλεγχο της θερμοκρασίας, ενώ στο κεντρικό στόμιο εφαρμόζεται ένας κάθετος ψυκτήρας όταν η θερμοκρασία ξεπεράσει τους 150 ο C. Στη συνέχεια, η ταχύτητα ανάδευσης μειώνεται (150 rpm) και το μείγμα θερμαίνεται (καφεκόκκινο διάλυμα) σταδιακά, πρώτα στους 150 ο C με ρυθμό 20 ο C/λεπτό, μετά στους 200 ο C με ρυθμό 15 ο C/λεπτό και στη συνέχεια στους 250 ο C με ρυθμό 15 ο C/λεπτό. Έπειτα, η θερμοκρασία αυξάνεται μέχρι τους 317 ο C με ρυθμό 10 ο C/λεπτό. Το διάλυμα καθίσταται μαύρο όταν η θερμοκρασία υπερβεί τους 280 ο C, σύμφωνα με την ακόλουθη αντίδραση: 98
117 Η θέρμανση συνεχίζεται για μισή ώρα απο τη στιγμή που η θερμοκρασία φτάνει στο σ.ζ του διαλύτη (317 ο C) και το μείγμα αρχίζει να βράζει. Τέλος, το τελικό προϊόν αφήνεται να ψυχθεί σε θερμοκρασία περιβάλλοντος. Πίνακας 3.2. Σύνοψη Συνθέσεων με FeΟ(ΟΗ) Κωδική Ονομασία Πρόδρομη ένωση Αντιδραστήριο Αναλογία FeΟ(ΟΗ)/Ο.Α Διαλύτης Διάρκεια Σύνθεσης Μέγεθος (nm) (ΤΕΜ) MagOOH_1.1 FeO(OH) 7mmol 0.62g O.Α 7mmol 1.98g 1 1-Δεκαοκτένιο 17.5ml 30 min 34.0 ± 11.5 MagOOH_1.2 FeO(OH) 7mmol 0.62g O.Α 14mmol 3.96g Δεκαοκτένιο 17.5ml 30 min 34.9 ± 9.4 MagOOH_1.3 FeO(OH) 7mmol 0.62g O.Α 21mmol 5.96g Δεκαοκτένιο 17.5ml 30 min 35.1 ± 13.0 MagOOH_1.6 FeO(OH) 7mmol 0.62g O.Α 42mmol 11.9g Δεκαοκτένιο 17.5ml 30 min Ελάχιστη μαγνητική απόκριση Συνθέσεις SPIONs με ελαϊκό σίδηρο [Fe(Olate) 3 -ex]* [146, 147] ως πρόδρομη ένωση Η πειραματική πορεία που ακολουθήθηκε για την υφιστάμενη συνθετική κατηγορία αποτυπώνεται στην Εικόνα 3.5. Εικόνα 3.5: Σχηματική απεικόνιση συνθέσεων με Fe(Olate) 3 [146]. 99
118 *Η Παρασκευή του συμπλόκου πραγματοποιήθηκε με τη μέθοδο της εκχύλισης (extraction). Σύνθεση Fe(Olate) 3 -ex.: Σε τρίλαιμη σφαιρική φυάλη (250ml) μεταφέρονται 8.1g (30.0mmol) FeCl 3 6H 2 O και 27.4g (90.0mmol) ελαϊκό νάτριο (sodium Olate). Ακολούθως, 60ml absolute EtOH και 45ml d.h 2 O εισάγονται στη φυάλη και το μέιγμα ομογενοποιείται με μαγητική ανάδευση (150rpm) για δέκα λεπτά. Η προσθήκη 105ml εξανίου οδηγέι στον σχηματισμό δύο φάσεων: την υδατική (κάτω) φάση και την οργανική (άνω) φάση. Η τρίλαιμη φυάλη βρίσκεται εντός ελαιόλουτρου, και φέρει στο κεντρικό στόμιο ένα κάθετο ψυκτήρα, καθώς επίσης ένα θερμόμετρο και ένα πώμα στα πλαϊνά στόμια. Η θερμοκρασία στο ελαιόλουτρο ελέγχεται με τον θερμοαισθητήρα της θερμαινόμενης πλάκας. Η αύξηση της θέρμοκρασίας γίνεται με άλματα των 10 ο C μέχρι τους 70 ο C (σύμφωνα με την ένδειξη στο ελαιόλουτρο), όπου το μείγμα αρχίζει να βράζει (σ.ζ εξανίου: 68 ο C). Ο μέσος ρυθμός αύξησης της θερμοκρασίας υπολογίζεται σε 1 ο C/λεπτό και το μείγμα αφήνεται να βράσει για τέσσερις ώρες, υπο συνεχή ανάδευση (150rpm). Κάτα τη διάρκεια της σύνθεσης, η πορτοκαλόχρωμη υδατική φάση αποχρωματίζεται ενώ η οργανική φάση, στην οποία σχηματίστηκε το Fe(Olate) 3, καθίσταται ερυθρόμαυρη (Εικόνα 3.6). Το μείγμα αφήνεται να ψυχθεί σε θερμοκρασία περιβάλλοντος και ακολούθως μεταφέρεται σε διαχωριστική χοάνη. Η υδατική (κάτω) φάση απορρίπτεται, ενώ η οργανική φάση εκπλένεται τρεις φορές με 50ml d.h 2 O. Την προσθήκη d.h 2 O ακολουθεί η ήπια ανακίνηση της διαχωριστικής χοάνης, άφεση σε ηρεμία για δέκα λεπτά και απόρριψη της κάτω φάσης. Έπειτα η οργανική φάση μεταφέρεται σε κωνική φυάλη και προστίθεται 0.5g άνυδρο θεϊικό νάτριο για απομάκρυνση της υγρασιας. Το προϊόν διηθείται με απλό ηθμό και συλλέγεται το διήθημα. Ακολουθεί εξάτμιση του εξανίου με χρήση του περιστροφικού εξατμιστήρα υπό κενό (rotary evaporator). Το προκύπτων κηρώδες προϊόν μεταφέρεται στον ξηραντήρα για αποθήκευση [23.32g (25.9mmol) Fe(Olate) 3 ]. Εικόνα 3.6: Σχηματισμός Fe(Olate) 3 [148]. 100
119 Σύνθεση SPIONs: Μετά τη σύνθεση και απομόνωση του Fe(Olate) 3, πραγματοποιήθηκε μια σειρά συνθέσεων μαγνητικών νανοσωματιδίων, που στόχο είχε τη διερεύνηση της επίδρασης της μοριακης αναλογίας Fe(Olate) 3 /Ο.Α και του ρυθμού θέρμανσης, στο μέγεθος των σχηματιζομένων νανοκρυσταλλιτών. Η πειραματική πορεία που ακολουθήθηκε είναι η εξής: Ποσότητες Fe(Olate) 3 και Ο.Α αναμιγνύονται με 1-Δεκαοκτένιο συγκεκριμένου όγκου σε τρίλαιμη σφαιρική φυάλη (100ml). Οι επιμέρους ποσότητες που χρησιμοποιήθηκαν παρουσιάζονται πιο κάτω στον Πινακα 3.3. Το μείγμα ομογενοποιείται, με έντονη μαγνητική ανάδευση (500 rpm), για μία ώρα σε θερμοκρασία περιβάλλοντος. Ακολούθως, η τρίλαιμη φυάλη τοποθετείται εντός του θερμαντικού μανδύα, όπου και θα λάβει χώρα η θέρμανση. Στα στόμια της τρίλαιμης φυάλης τοποθετούνται ο θερμοαισθητήρας του θερμαντικού μανδύα, ένα θερμόμετρο υδραργύρου (300 ο C) για διπλό έλεγχο της θερμοκρασίας, ενώ στο κεντρικό στόμιο εφαρμόζεται ένας κάθετος ψυκτήρας. Σε ορισμένες συνθέσεις εφαρμόζεται ροή αζώτου (1 φυσαλίδα/sec) απο το πάνω μέρος του ψυκτήρα (Πίνακας 3.3 και Εικόνα 3.1). Το μείγμα, αρχικά θερμαίνεται υπο ανάδευση στους 100 ο C, με ρυθμό 10 ο C/λεπτό, και παραμένει για τριάντα λεπτά στην ίδια θερμοκρασία. Στη συνέχεια, η ταχύτητα ανάδευσης μειώνεται (350rpm) και το μείγμα (καφε-κόκκινο διάλυμα) θερμαίνεται μέχρι τους 317 ο C (σ.ζ 1-Δεκαοκτενίου) με μέσο ρυθμό θέρμανσης 3-15 ο C/λεπτό. Το διάλυμα καθίσταται μαύρο όταν η θερμοκρασία υπερβεί τους 220 ο C. Η θέρμανση συνεχίζεται για μία ώρα απο τη στιγμή που η θερμοκρασία φτάνει στο σ.ζ του διαλύτη και το μείγμα αρχίζει να βράζει. Σε κάποιες συνθέσεις πραγματοποιήθηκε δειγματοληψία σε ενδιάμεσα χρονικά σημεία. Τέλος, το τελικό προϊόν αφήνεται να ψυχθεί σε θερμοκρασία περιβάλλοντος. 101
120 Πίνακας 3.3: Σύνοψη συνθέσεων με Fe(Olate) 3 -ex. Κωδική Ονομασία Πρόδρομη ένωση Αντιδραστήριο Αναλογία Fe(Οlate) 3 /Ο.Α Διαλύτης Διάρκεια Σύνθεσης- Ρυθμός θέρμανσης Μέγεθος (nm) (ΤΕΜ) Mag_I.O.C_2.1 Fe(Οlate) 3 4.0mmol 3.6g O.A 2.0mmol 0.56g 2 1-Δεκαοκτένιο 25ml 1h (με N 2 ) 5 o C/min 30min: 7.9 ± 1.0 1h: 8.1 ± 1.1 Mag_I.O.C_3.2 Fe(Οlate) 3 3.0mmol 2.7g O.A 2.0mmol 0.56g Δεκαοκτένιο 25ml 30 min (χωρίς N 2 ) 15 o C/min 30min: 12.7 ± 3.7 Mag_I.O.C_1.1 Fe(Οlate) 3 4.0mmol 3.6g O.Α 4.0mmol 1.1g 1 1-Δεκαοκτένιο 25ml 1h (με N 2 ) 3.5 o C/min 1h: 7.2 ± 0.8 Mag_I.O.C_4.0 Fe(Οlate) 3 4.0mmol 3.6g Χωρίς O.A Δεκαοκτένιο 25ml 1h (με N 2 ) 4 o C/min 1h: 7.3 ± 0.8 Mag_I.O.C_1.3 Fe(Οate) 3 4.0mmol 3.6g O.Α 12.0mmol 3.4g Δεκαοκτένιο 40ml 1h (χωρίς N 2 ) 7 o C/min 1h: 10.1 ± Συνθέσεις SPIONs με ελαϊκό σίδηρο [Fe(Olate) 3 -prc]* ως πρόδρομη ένωση *Η Παρασκευή του συμπλόκου πραγματοποιήθηκε με τη μέθοδο της καταβύθισης (precipitation). Σύνθεση Fe(Olate) 3 -prc.: 10.0g (37.0mmol) FeCl 3 6H 2 O και 52.3g (185mmol) O.A αναμιγνύονται, υπό ανάδευση, με 20ml μεθανόλη (MeOH) προς σχηματισμό καφέ-κίτρινου διαλύματος. Ακολούθως το μείγμα μοιράζεται σε τέσσερα falcons και προστείθεται 10ml π.νη 3 (15.8Μ) στο καθένα. Η αύξηση τoυ ph οδηγεί στο σχηματισμό ελαϊκού νατρίου, το οποίο συμπλέκεται με τα ιόντα Fe 3+ προς σχηματισμό Fe(Olate) 3, υπο μορφή καφέ-κόκκινου ιζήματος (Εικόνα 3.6). Το προϊόν υπόκειται σε φυγοκέντρηση για δέκα λεπτά στα 2100g (4000rpm) (Kendro-Megafuge 1.0R - Heraeus) και το υπερκείμενο απορρίπτεται. Το ίζημα εκπλένεται τρεις φορές με 20ml EtOH. Κάθε φορά, μετά τη προσθήκη ΕtOH και ομογενοποίηση του ιζήματος, ακολουθεί φυγοκέντρηση για δέκα λεπτά στα 2100g και το υπερκέιμενο απορρίπτεται. Τέλος το προϊόν εκπλένεται δύο φορές με απόλυτη ακετόνη προς 102
121 απομάκρυνση της υγρασίας, με τη διαδικασία που περιγράφηκε πιο πάνω, και το ίζημα τοποθετείται στον ξηραντήρα για ξήρανση [6.3g (7.0mmol) Fe(Olate) 3 ]. Σύνθεση SPIONs: Μετά τη σύνθεση και απομόνωση του Fe(Olate) 3, πραγματοποιήθηκε μια σειρά συνθέσεων μαγνητικών νανοσωματιδίων, που στόχο είχε τη διερεύνηση της επίδρασης της μοριακης αναλογιας Fe(Olate) 3 /Ο.Α και της διάρκειας σύνθεσης, στο μέγεθος των σχηματιζομένων νανοκρυσταλλιτών. Η πειραματική πορεία (Εικόνα 3.5) που ακολουθήθηκε είναι η εξής: Ποσότητες Fe(Olate) 3 και Ο.Α αναμιγνύονται με 1-Δεκαοκτένιο συγκεκριμένου όγκου σε τρίλαιμη σφαιρική φυάλη (100ml). Οι επιμέρους ποσότητες που χρησιμοποιήθηκαν παρουσιάζονται πιο κάτω στον Πινακα 3.4. Το μείγμα ομογενοποιείται, με έντονη μαγνητική ανάδευση (600rpm), για είκοσι λεπτά σε θερμοκρασία περιβάλλοντος. Ακολούθως, η τρίλαιμη φυάλη τοποθετείται εντός του θερμαντικού μανδύα, όπου και θα λάβει χώρα η θέρμανση. Το μείγμα, αρχικά θερμαίνεται υπο ανάδευση στους 100 ο C, με ρυθμό 18 ο C/λεπτό. Στα στόμια της τρίλαιμης φυάλης τοποθετούνται ο θερμοαισθητήρας του θερμαντικού μανδύα, ένα θερμόμετρο υδραργύρου (300 ο C) για διπλό έλεγχο της θερμοκρασίας, ενώ στο κεντρικό στόμιο εφαρμόζεται ένας κάθετος ψυκτήρας όταν η θερμοκρασία ξεπεράσει τους 150 ο C. Στη συνέχεια, η ταχύτητα ανάδευσης μειώνεται (200rpm) και το μείγμα θερμαίνεται (καφε-κόκκινο διάλυμα) στους 150 ο C, με ρυθμό 20 ο C/λεπτό, όπου και παραμένει για μισή ώρα. Ακολούθως, η θερμοκρασία αυξάνεται στους 200 ο C με ρυθμό 15 ο C/λεπτό, μετά στους 250 ο C με ρυθμό 15 ο C/λεπτό και στη συνέχεια στους 317 ο C με ρυθμό 10 ο C/λεπτό. Το διάλυμα καθίσταται μαύρο όταν η θερμοκρασία υπερβεί τους 280 ο C. Η θέρμανση συνεχίζεται για μισή ώρα απο τη στιγμή που η θερμοκρασία φτάνει στο σ.ζ του διαλύτη (317 ο C) και το μείγμα αρχίζει να βράζει. Σε μία σύνθεση πραγματοποιήθηκε δειγματοληψία σε ενδιάμεσα χρονικά σημεία. Τέλος, το τελικό προϊόν αφήνεται να ψυχθεί σε θερμοκρασία περιβάλλοντος. 103
122 Πίνακας 3.4: Σύνοψη συνθέσεων με Fe(Olate) 3 -prc. Κωδική Ονομασία Πρόδρομη ένωση Αντιδραστήριο Αναλογία Fe(Οlate) 3 /Ο.Α Διαλύτης Διάρκεια Σύνθεσης Μέγεθος (nm) (ΤΕΜ) MagOlate_1.0 Fe(Olate) 3 2.0mmol 1.8g Χωρίς Ο.Α Δεκαοκτένιο 17.5ml 30 min Μεγάλη μαγνητική απόκριση (SPIONs > 20nm) MagOlate_1.3 Fe(Olate) 3 2.0mmol 1.8g O.A 6.0mmol 1.7g Δεκαοκτένιο 17.5ml 30 min 30 min: 14.0 ± 7.3 MagOlate_1.6 Fe(Olate) mmol 0.77g O.A 5.1mmol 1.4g Δεκαοκτένιο 7.5ml 30 min 2 min: 8.4 ± min: 8.1 ± min: 10.9 ± Απομόνωση και προσδιορισμός καθαρότητας των συντεθέντων SPIONs Οι μαγνητικοί νανοκρυσταλλίτες μετά τη σύνθεση τους υποβάλλονται σε διαδοχικές πλύσεις, με σκοπό την απομάκρυνση των παραπροϊόντων της σύνθεσης. Ο καθαρισμός των SPIONs πραγματοποιήθηκε με την τεχνική της κλασματικής καταβύθισης, με χρήση μείγματος DCM-Ακετόνης, σε αναλογία που διαφέρει σε κάθε πλύση ανάλογα με βαθμό καθαρότητας των νανοκρυσταλλιτών. Γενικά, κατά τη διαδικασία των πλύσεων, επιδιώκουμε την καταβύθιση των SPIONs και τον καθαρισμό τους απο τα παραπροϊόντα της σύνθεσης (συμπεριλαμβανομένου του διαλύτη και της ποσότητας Ο.Α που δεν αντέδρασε), τα οποία παραμένουν εν διαλύσει στο υπερκείμενο μετά απο φυγοκέντρηση. Η ακετόνη, ως πολικό μόριο, προάγει την καταβύθιση των υδρόφοβων SPIONs, ενώ το DCM, ως άπολο μόριο, συντελεί στον καθαρισμό των νανοκρυσταλλιτών απο λιπόφιλες ενώσεις. Η τακτική που ακολουθήθηκε ήταν η προοδευτική αύξηση του λόγου DCM/Ακετόνης, απο πλύση σε πλύση, σε αναλογία τέτοια ώστε να εξασφαλίζεται επαρκής καταβύθιση των SPIONs αλλά και ικανοποιητικός καθαρισμός τους (χρώμα υπερκειμένου). Όσο πιο σκούρο το χρώμα του υπερκειμένου, τόσο καλύτερος ο καθαρισμός του δείγματος αλλά και μεγαλύτερος ο κίνδυνος απώλειας ποσότητας νανοκρυσταλλιτών στην υπερκείμενη φάση. Υπερκείμενο ανοικτού καφέ χρωματισμού θεωρείται ικανοποιητικός οπτικός δείκτης, όσον αφορά την επιλογή της αναλογίας DCM:Ακετόνης. Μετά απο κάθε πλύση, ο βαθμός καθαρότητας των νανοκρυσταλλιτών προσδιορίζεται με την τεχνική της θερμοσταθμικής ανάλυσης (ThermoGravimetric Analysis, TGA). Ο αριθμός των πλύσεων καθορίζεται απο το βαθμό καθαρότητας. Καθαρότητα SPIONs 70%wt. θεωρείται αρκούντως ικανοποιητική. 104
123 Επι του πρακτέου, η γενική πειραματική πορεία που ακολουθήθηκε ήταν η εξής: Το προϊόν κάθε σύνθεσης μοιράζεται ισόποσα σε γυάλινα φιαλίδια (15ml), έτσι ώστε το καθένα να περίεχει 3-4ml προϊόντος. Στη συνέχεια, προστείθεται 1ml DCM και τα φιαλίδια τοποθετούνται σε λουτρό υπερήχων (Elmasonic S15H) μέχρι παρατήρησης ομοιογενούς διασποράς. Έπειτα, προστείθεται σταδιακά ακετόνη, σε μικρές ποσότητες (0.5ml) υπο ανακίνηση, μέχρι να παρατηρηθεί θόλωμα ή/και άρση της ομοιογένειας του δείγματος. Ακολουθεί φυγοκέντρηση (Kendro-Megafuge 1.0R - Heraeus) των δειγμάτων για μισή ώρα στα 2100g. Τα υπερκείμενα απορρίπτονται με απόχυση, τοποθετώντας μόνιμους μαγνήτες χειρός Nd-Fe-B στη βάση των φιαλιδίων. Τα ιζήματα επαναδιασπείρονται σε 1ml DCM με υπερήχους, και συλλέγονται όλα μαζί σε ένα φιαλίδιο. Η περίσσεια του DCM απομακρύνεται με εξάτμιση, μέχρι παραμονής 2-3ml. Εν συνεχεία, ακολουθείται ακριβώς η ίδια διαδικασία που περιγράφεται πιο πάνω (δηλ. Προσθήκη ακετόνης μέχρι θολώματος, φυγοκέντρηση και απόρριψη του υπερκειμένου). Μετά το πέρας της δεύτερης πλύσης, το ίζημα ομογενοποιείται σε 2ml DCM με υπερήχους και προσδιορίζεται η καθαρότητα των νανοκρυσταλλιτών με TGA. Όπως λέχθηκε πιο πάνω, αν ο βαθμός καθαρότητας είναι μικρότερος του 70%wt., τότε συνεχίζουμε σε επόμενες πλύσεις με αυξημένο κάθε φορά το λόγο DCM/Ακετόνης, εως ότου εξασφαλιστεί ο συγκεκριμένος βαθμός καθαρότητας. Προσδιορισμός βαθμού καθαρότητας των SPIONs με TGA: Οι μετρήσεις TGA πραγματοποιήθηκαν με τη χρήση του οργάνου Q500 της TA Instruments, υπό ροή (60 ml/min) συνθετικού αέρα (sample gas). Αρχικά ένας μικρός όγκος (50μl) του υπο προσδιορισμό δείγματος τοποθετείται σε ειδικό δειγματοφορέα, και στη συνέχεια εισάγεται μέσα στο φούρνο του οργάνου. H θερμοκρασία αυξάνεται σταδιακά με ρυθμό 10 ο C/min, πρώτα στους 33 ο C (εξάτμιση DCM), μετά στους 50 ο C (εξάτμιση υπολειμμάτων ακετόνης), έπειτα στους 120 ο C (απομάκρυνση υγρασίας) και τέλος στους 700 ο C. Σε κάθε στάδιο η θερμοκρασία κρατείται σταθερή (ισόθερμη) για δέκα λεπτά, προτού μεταβεί σε επόμενο στάδιο υψηλότερης θερμοκρασίας, κ.ο.κ. Όπως φαίνεται πιο κάτω στο Σχήμα 3.1 (τυπικό διάγραμμα TGA), σε θερμοκρασίες ο C παρατηρείται μείωση της μάζας του δείγματος που οφείλεται στην καύση των οργανικών μορίων. Έτσι η μάζα του δείγματος σε θερμοκρασίες μεγαλύτερες των 400 ο C αντιστοιχεί στη μάζα των νανοκρυσταλλιτών, οι οποίοι δεν καίγονται σε τέτοιες θερμοκρασίες. Ο Βαθμός καθαρότητας (%wt.) αντιστοιχεί στη μάζα (%) του δείγματος σε θερμοκρασίες άνω των 400 ο C, θεωρώντας ως 100% τη μάζα του δείγματος στους 120 ο C. 105
124 Mass(%) Mass Loss Temperature ( O C) Σχήμα 3.1: Διάγραμμα TGA για τη σύνθεση MagAcac_4, μετά απο τρείς πλύσεις. Βαθμός καθαρότητας: 85%wt Φασματοφωτομετρικός προσδιορισμός ιόντων σιδήρου Μετά τo πέρας των πλύσεων πραγματοποιείται προσδιορισμός της συγκέντρωσης των SPIONs, αφού πρώτα αραιωθούν με DCM (τελικός όγκος 10ml). Στην αρχή, οι μαγνητικοί νανοκρυσταλλίτες (γ-fe 2 O 3, Fe 3 O 4 ) διαλύονται σε ιόντα σιδήρου με την προσθήκη π.hcl. Ακολούθως, τα ιόντα Fe 3+ ανάγονται σε ιόντα Fe 2+ με προσθήκη υδροχλωρικής υδροξυλαμίνης (NH 2 OH HCl) και προσδιορίζονται φασματοφωτομετρικά (Hitachi Digilab U-2800) μέσω σύμπλεξης τους με την 1,10-Φαινανθρολίνη (phen), σύμφωνα με τις αντιδράσεις [149] : 4Fe NH 2 OH 4Fe 2+ + N 2 O + 4H + + H 2 O και Το σύμπλοκο που σχηματίζεται [Tris(1,10-phenanthroline)iron(II)], έχει πορτοκαλο-κόκκινο χρώμα και εμφανίζει μέγιστη απορρόφηση στα 510nm. Συγκεκριμένα, 100μl του υπο προσδιορισμό δείγματος διαλύονται σε διπλάσιο όγκο π.hcl (11.9Μ). Μετά απο παραμονή για είκοσι λεπτά σε κλίβανο στους 37 ο C, το διάλυμα καθίσταται κίτρινο και αραιώνεται με d.h 2 O σε ογκομετρική φυάλη μέχρι τα 10ml. Ακολούθως, 3ml του πιο πάνω διαλύματος μεταφέρονται σε ογκομετρική φυάλη (10ml) και 106
125 510nm (A.U) αναμειγνύονται με 100μl NH 2 OH HCl (aq) (1.4M), 1ml phen (aq) (0.005M) και 1.5ml CH 3 COONa (aq) (2M) (ρύθμιση ph). Στη συνέχεια, το προκύπτων πορτοκαλο-κόκκινο διάλυμα αραιώνεται με d.h 2 O μέχρι τα 10ml και αφήνεται για δέκα λεπτά σε σκοτεινό σημείο, ούτως ώστε να ολοκληρωθεί η αντίδραση. Έπειτα, 3ml του διαλύματος αυτού μεταφέρονται σε κυψελίδα και μετράται η απορρόφηση του δείγματος στα 510nm. Τέλος, η συγκέντρωση των SPIONs υπολογίζεται μέσω πρότυπης καμπύλης (Σχήμα 3.2) που έχει κατασκευαστεί προηγουμένως, με χρήση άνυδρου FeCl 2 ως πρότυπο διάλυμα. Με βάση τα ιόντα Fe 2+, η συγκέντρωση των διαλυμάτων εκφράζεται (μετά απο κατάλληλη μετατροπή) ως %w/v Fe 2 O y = x R² = Fe(II) Concentration (μg/ml) Σχήμα 3.2: Πρότυπη καμπύλη για προσδιορισμό Fe(II) μέσω σύμπλεξης με 1,10-Φαινανθρολίνη Χαρακτηρισμός SPIONs με Ηλεκτρονική Μικροσκοπία Διέλευσης (Transmission Electron Microscopy, TEM) Η μελέτη της μορφολόγιας και ο προσδιορισμός του μεγέθους των νανοκρυσταλλιτών πραγματοποιήθηκε με TEM. Μια σταγόνα αραιώμενου κολλοειδούς δείγματος (0.01% w/v Fe 2 O 3 ) τοποθετείται σε δειγματοφορέα χαλκού επικαλυμμένο με υμένιο άνθρακα (formvar). Τα μικρογραφήματα ΤΕΜ (Εικόνα 3.7) λήφθηκαν με τη χρήση του ηλεκτρονικού μικροσκοπίου διέλευσης της εταιρείας JEOL, μοντέλο JEM-2100, χρησιμοποιώντας δυναμικό επιτάχυνσης 200kV. 107
126 Εικόνα 3.7: Παρατήρηση SPIONs μέσω ΤΕΜ 3.4 Μελέτη των παραμέτρων της σύνθεσης πολυμερικών και υπερπαραμαγνητικών πολυμερικών μικκυλίων Τα πολυμερικά μικύλλια (νανοφορείς) σχηματίζονται αυθόρμητα όταν αμφίφιλα επιφανειοδραστικά ή (μακρο)μόρια, βρεθούν σε υδατικό περιβάλλον σχηματίζοντας δομή πυρήνα κελύφους (Εικόνα 3.8 [150] ). Ο πυρήνας του μικυλλίου είναι υδρόφοβος (PLA) και εκεί εγκλωβίζονται 20nm υδρόφοβα μόρια ή νανοσωματίδια (π.χ. PTX, SPIONs). Ο πυρήνας περιβάλλεται από υδρόφιλο πολυμερές (PEG) το οποίο με τη σειρά του προσδίδει στο μικύλλιο μεγάλη σταθερότητα σε υδατικά μέσα. Εικόνα 3.8: Δομή πυρήνα-κελύφους πολυμερικών μικκυλίων (PLA-PEG) και εγκλωβισμός υδρόφοβων SPIONs. Η παρασκευή των μικκυλίων πραγματοποιήθηκε με τη χρήση του αμφίφιλου συμπολυμερούς πόλυ(γαλακτικό οξύ)-b-πόλυ(αιθυλενογλυκόλη) [PLA-PEG], με την τεχνική: solvent diffusion and evaporation (nanoprecipitation) [ 151 ] (Εικόνα 3.9 [ 152 ] ). Μελετήθηκαν τρία συμπολυμερή PLA-PEG, διαφορετικού μοριακού βάρους, ήτοι: PLA(2kDa)-PEG(5kDa), PLA(5kDa)-PEG(5kDa), PLA(10kDa)-PEG(5kDa) (Εικόνα 3.10). Κατα την παρασκευή των 108
127 υπερπαραμαγνητικών μικκυλίων (μαγνητικοί νανοφορείς), χρησιμοποιήθηκε διάλυμα SPIONs σε DCM, με μεγέθος νανοκρυσταλλιτών 10nm (σύνθεση MagAcac_4), βαθμό καθαρότητας 85%wt και συγκέντρωση 0.41%w/v. Εικόνα 3.9: Σχηματική απεικόνιση σύνθεσης μικκυλίων μέσω της τεχνικής: solvent diffusion and evaporation (nanoprecipitation) Η γενική πειραματική διαδικασία που ακολουθήθηκε είναι η εξής: (Ι) Για τα μη μαγνητικά μικκύλια: 5mg PLA-PEG τοποθετούνται σε eppendorf και διαλύονται σε 140μl THF (οργανική φάση), με τη βοήθεια υπερήχων (Elmasonic S15H). Στη συνέχεια η οργανική φάση προστείθεται με συγκεκριμένο ρυθμό, σε 700μl PBS (0.14M, ph:7.4) (υδατική φάση). H υδατική φάση βρίσκεται σε γυάλινο φιαλίδιο (2ml) και η προσθήκη της μιας φάσης στην άλλη πραγματοποιείται σε λουτρό υπερήχων στους 0 ο C (παγόλουτρο). Ακολουθεί εξάτμιση του THF σε κλίβανο στους 37 ο C (Binder) για 15 ώρες και ρύθμιση του ph στο 7.4 με διάλυμα NaOH (0.01M). (ΙΙ) Για τα μαγνητικά μικκύλια: 5mg PLA-PEG τοποθετούνται σε eppendorf και διαλύονται σε 80μl THF, με τη βοήθεια υπερήχων. Σε ένα άλλο eppendorf μεταφέρεται διάλυμα SPIONs (σε DCM) τέτοιου όγκου, που να περιέχει την επιθυμητή στερεή μάζα νανοκρυσταλλιτών. Το διάλυμα αυτό τοποθετείται σε κλίβανο στους 37 ο C προς εξάτμιση του DCM, μέχρι σχηματισμού πάστας, και στη συνέχεια το στερεό υπόλειμμα επαναδιασπείρεται σε 60μl THF. Το διάλυμα του συμπολυμερούς και το διάλυμα των SPIONs ομογενοποιούνται σε ένα eppendorf (140μl οργανική φάση). Έπειτα ακολουθεί η προσθήκη της οργανικής φάσης στην υδατική, εξάτμιση του THF και ρύθμιση του ph με ακριβώς την ίδια διαδικασία που περιγράφηκε πιο πάνω για τα μη μαγνητικά μικκύλια. Μελετήθηκε η σταθερότητα των μαγνητικών μικκυλίων σε συνάρτηση με το χρόνο, καθώς και η επίδραση διάφορων συνθετικών παραμέτρων (μοριακό βάρος συμπολυμερούς, ph, 109
128 ποσότητα SPIONs, ρυθμός προσθήκης οργανικής φάσης, αναλογία οργανικής/υδατικής φάσης, κ.α) στο μέγεθος των σχηματιζομένων μικκυλίων. Οι παραμέτροι αυτοί καθώς και τα αποτελέσματα αναλύονται διεξοδικά στο επόμενο κεφάλαιο. Εικόνα 3.10: Δομή συμπολυμερούς PLA-PEG, όπου n: το μοριακό βάρος των αλυσίδων PLA και m: το μοριακό βάρος των αλυσίδων PEG Χαρακτηρισμός πολυμερικών και υπερπαραμαγνητικών πολυμερικών μικκυλίων Το κριτήριο αξιολόγησης των παρασκευασθέντων νανοφορέων ήταν η υδροδυναμική τους διάμετρος (Hydrodynamic diameter, D h ). H D h των μικκυλίων προσδιορίστηκε, στις περισσότερες περιπτώσεις, στο υπερκείμενο των δειγμάτων μετά απο φυκοκέντρηση (Hettich-Mikro 220) για δέκα λεπτά στα 380g (2krpm). Ο προσδιορισμός της D h πραγματοποιήθηκε με την τεχνική της Δυναμικής Σκέδασης Φωτός (Dynamic Light Scattering, DLS), σε σύστημα της εταιρείας Malvern (Nano Zeta Sizer) εφοδιασμένο με λέιζερ He-Ne 4mW, μήκους κύματος λ=633nm. Το όργανο χρησιμοποιεί μία φωτοδίοδο ως ανιχνευτή και η σκεδαζόμενη ακτινοβολία μετριέται σε γωνία 173 ο. Οι αναφερόμενες τιμές D h είναι ο μέσος όρος τριών μετρήσεων, κάθε μία από τις οποίες είναι το αποτέλεσμα δώδεκα διαγραμμάτων αυτοσυσχέτισης και προσαρμογών. Η μορφολογία των μαγνητικών νανοφορέων εξετάζεται μέσω TEM ( 3.3.7), στο υπερκείμενο των δειγμάτων μετά απο φυκοκέντρηση για δέκα λεπτά στα 380g. Πιο κάτω, στην Είκονα 3.11 παρουσιάζεται ενα τυπικό μικρογράφημα ΤΕΜ μαγνητικών μικκυλίων. Φαίνονται ξεκάθαρα μεμονωμένοι σφαιρικοί σχηματισμοί (μικκύλια), με τον καθένα να περιβάλλει ένα πλήθος SPIONs. (Δομή πυρήνα-κελύφους) 110
129 100nm Εικόνα 3.11: Μικρογράφημα ΤΕΜ μαγνητικών μικκυλίων, δομής πυρήνα-κελύφους. 3.5 Μελέτη των παραμέτρων της φόρτωσης και αποδέσμευσης Πακλιταξέλης (PTX), ενκαψυλιωμένης σε πολυμερικά και υπερπαραμαγνητικά πολυμερικά μικκύλια Στο τρίτο και τελευταίο κομμάτι της παρούσας διατριβής μελετήθηκε η φόρτωση του αντικαρκινικού φαρμάκου Πακλιταξέλη (Paclitaxel, PTX), σε PLA-PEG και υπερπαραμαγνητικά PLA-PEG (Mag-PLA-PEG) μικκύλια (νανοφορείς). Αφού διερευνήθηκε μια σειρά παραμέτρων που επηρεάζουν τη φόρτωση της PTX, ακολούθως μελετήθηκε η αποδέσμευση του φαρμάκου απο τους νανοφορείς Φόρτωση PTX σε PLA-PEG και Mag-PLA-PEG μικκύλια Η διαδικασία της φόρτωσης του φαρμάκου στους φαρμακοφορείς είναι παρόμοια με αυτήν που περιγράφεται πιο πάνω για τα πολυμερικά και υπερπαραμαγνητικά πολυμερικά μικκύλια ( 3.4). Μελετήθηκε η φόρτωση της PTX σε τρία συμπολυμερή PLA-PEG διαφορετικού μοριακού βάρους, ήτοι PLA(2kDa)-PEG(5kDa), PLA(5kDa)-PEG(5kDa) και PLA(10kDa)- PEG(5kDa). Χρησιμοποιήθηκαν διαλύματα SPIONs σε DCM, i) με μεγέθος νανοκρυσταλλιτών 10nm (σύνθεση MagAcac_4), βαθμό καθαρότητας 85%wt και συγκέντρωση 0.41%w/v και ii) με μεγέθος νανοκρυσταλλιτών 13nm (σύνθεση Mag_Ι.Ο.C_3.2), βαθμό καθαρότητας 70%wt και συγκέντρωση 0.31%w/v. Τα μικκύλια παρασκευάστηκαν μέσω της τεχνικής solvent diffusion and evaporation (nanoprecipitation). 111
130 Η γενική πειραματική διαδικασία που ακολουθήθηκε είναι η εξής: (Ι) Για τα μη μαγνητικά μικκύλια (PTX-PLA-PEG): 5mg PLA-PEG και ποσότητα PTX τοποθετούνται σε γυάλινο φιαλίδιο (2ml) και διαλύονται σε 140μl THF (οργανική φάση), με τη βοήθεια υπερήχων. Στη συνέχεια η οργανική φάση προστείθεται με συγκεκριμένο ρυθμό (30 ή 240μl/min), σε 700μl PBS (0.14M, ph:7.4) (υδατική φάση). H υδατική φάση βρίσκεται σε γυάλινο φιαλίδιο (2ml) και η προσθήκη της μιας φάσης στην άλλη πραγματοποιείται σε λουτρό υπερήχων στους 0 ο C (παγόλουτρο). Ακολουθεί εξάτμιση του THF σε κλίβανο στους 37 ο C για 15 ώρες και ρύθμιση του ph στο 7.4 με διάλυμα NaOH (0.01M). (ΙΙ) Για τα μαγνητικά μικκύλια (PTX-Mag-PLA-PEG): 5mg PLA-PEG και ποσότητα PTX τοποθετούνται σε γυάλινο φιαλίδιο (2ml) και αναμειγνύονται με διάλυμα SPIONs (σε DCM) τέτοιου όγκου, που να περιέχει την επιθυμητή στερεή μάζα νανοκρυσταλλιτών. Το διάλυμα αυτό τοποθετείται σε κλίβανο στους 37 ο C προς εξάτμιση του DCM, μέχρι σχηματισμού πάστας, και στη συνέχεια το στερεό υπόλειμμα επαναδιασπείρεται σε 140μl THF (οργανική φάση). Έπειτα ακολουθεί η προσθήκη της οργανικής φάσης στην υδατική, εξάτμιση του THF και ρύθμιση του ph με ακριβώς την ίδια διαδικασία που περιγράφηκε πιο πάνω για τα μη μαγνητικά μικκύλια (Εικόνα 3.12). Σε όλες τις συνθέσεις που πραγματοποιήθηκαν διατηρήθηκε σταθερή η ποσότητα του συμπολυμερούς (5mg) ενώ μελετήθηκε η επίδραση διάφορων συνθετικών παραμέτρων (μοριακό βάρος συμπολυμερούς, ποσότητα PTX, ποσότητα και μέγεθος SPIONs, ρυθμός προσθήκης οργανικής φάσης, κ.α) στη φόρτωση και ενκαψυλίωση της PTX, αλλά και των SPIONs, στα σχηματιζόμενα μικκύλια. Οι παραμέτροι αυτοί καθώς και τα αποτελέσματα αναλύονται διεξοδικά στο επόμενο κεφάλαιο. PTX Εικόνα 3.12: Σχηματική απεικόνιση σύνθεσης PTX-Mag-PLA-PEG μικκυλίων 112
131 3.5.2 Προσδιορισμός φόρτωσης (Loading) και ενκαψυλίωσης (Encapsulation) της PTX σε PLA-PEG και Mag-PLA-PEG μικκύλια Η πειραματική διαδικασία για τον προσδιορισμό της φόρτωσης-ενκαψυλίωσης PTX και SPIONs στα PTX-Mag-PLA-PEG μικκύλια παρουσιάζεται σχηματικά στην Εικόνα Εικόνα 3.13: Σχηματική αναπαράσταση της διαδικασίας προσδιορισμού της φόρτωσης και ενκαψυλίωσης PTX και SPIONs στα PTX-Mag-PLA-PEG μικκύλια Θα πρέπει να υπογραμμιστεί πως με την παραπάνω διαδικασία, έγινε κατορθωτός ο διαχωρισμός των μαγνητικών (D:PTX-Mag-PLA-PEG) μικκυλίων απο τα μη μαγνητικά (C:PTX-PLA-PEG/S), καθώς και ο υπολογισμός της φόρτωσης-ενκαψυλίωσης PTX και 113
132 SPIONs ξεχωριστά, τόσο στα μαγνητικά και μη μαγνητικά μικκύλια, όσο και στο μέιγμα αυτών. Συγκεκριμένα, μέσω της οδού Α1 προσδιορίζεται η φόρτωση στο μείγμα 4 μαγνητικών και μη μαγνητικών μικκυλίων (Α: PTX-Mag-PLA-PEG + PTX-PLA-PEG), και μέσω της οδού Α2 προσδιορίζεται ξεχωριστά η φόρτωση για τα μη μαγνητικά (C) και τα μαγνητικά μικκύλια (D). Στο μεγαλύτερο μέρος της παρούσας διατριβής χρησιμοποίηθηκε μόνο η οδός Α2, χωρίς προσδιοσμό των μη μαγνητικών μικκυλίων (C), με σκοπό τη διερεύνηση των παραμέτρων της φόρτωσης μόνο για τα μαγνητικά μικκύλια (D). Σημειώνεται ότι τα μη μαγνητικά μικκύλια που προκύπτουν απο τον πιο πάνω διαχωρισμό, για σκοπούς καλύτερης διατύπωσης, θα αναφέρονται με την ακρωνυμία PTX-PLA-PEG/S. Σε κάθε παρτίδα, o προσδιορισμός της φόρτωσης γίνεται εις τριπλούν (triplicate). Πιο αναλυτικά, η πειραματική διαδικασία που έλαβε χώρα για τον προσδιορισμό της φόρτωσης και ενκαψυλίωσης PTX και SPIONs στα PTX-PLA-PEG και PTX-Mag-PLA-PEG μικκύλια, είναι η ακόλουθη: (Ι) PTX-Mag-PLA-PEG μικκύλια (Εικόνα 3.13): Μετά τη σύνθεση των μικκυλίων, εξάτμιση του THF, ρύθμιση του ph:7.4 ( 3.5.1), κάθε δείγμα μεταφέρεται σε eppendorf με τη βοήθεια 0.2ml PBS. Ακολουθεί φυγοκέντρηση για δέκα λεπτά στα 380g, έτσι ώστε να καταβυθιστούν τα μεγάλα μικκύλια καθώς και οι ποσότητες PTX και SPIONs που δεν ενκαψυλιώθηκαν στα μικκύλια (Β). Τα υπερκείμενα διαλύματα (μέιγμα μαγνητικών και μη μαγνητικών μικκυλίων-α) συλλέγονται όλα μαζί και υπολογίζεται η μάζα ανα δείγμα: Σε ένα απο αυτά τα δείγματα (A) προσδιορίζεται το μέγεθος (D h ) μέσω DLS ( 3.4.1) (οδός Α1) Τρία δείγματα Α τοποθετούνται σε τρία eppendorfs και λυοφιλοποιούνται (Telstar Cryodos) για 24 ώρες. Στη συνέχεια πραγματοποιούνται δύο πλύσεις με 0.5ml ακετονιτρίλιο (ΑcΝ), φυγοκέντρηση για μισή ώρα στα 30kg (Hettich-Mikro 220) και απόρριψη του ιζήματος. Το ΑcΝ προκαλεί διάνοιξη των μικκυλίων (με σύγχρονη εφαρμογή υπερήχων) και αποδέσμευση της PTX, όποτε στο υπερκείμενο παραμένουν εν διαλύσει η PTX και το PLA-PEG, ενώ καταβυθίζονται τα SPIONs και τα άλατα από το PBS. Τα υπερκείμενα διαλύματα ομογενοποιούνται, 0.2ml χρησιμοποιούνται για προσδιορισμό της στερεής μαζας (PTX+PLA-PEG) μέσω TGA (T=120 ο C), ενώ 2x1ml χρησιμοποιούνται για προσδιορισμό της PTX μέσω HPLC. 4 Μείγμα διότι κατά τη μικκυλιοποίηση, παρουσία SPIONs, παράγονται και μικκύλια τα οποία δεν περιέχουν καθόλου SPIONs. 114
133 Έτσι με αφαίρεση βρίσκουμε και τη μάζα του πολυμερούς. Πρέπει να τονιστεί οι προσδιορισμοί σε αυτό το σημείο αφορούν το μείγμα μαγνητικών και μη μαγνητικών μικκυλίων που συνυπάρχουν στο δείγμα Α. (οδός Α2) Τρία δείγματα Α τοποθετούνται σε τρία eppendorfs και φυγοκεντρούνται για 45 λεπτά στα 30kg. Με αυτό το τρόπο επιτυγχάνεται ο διαχωρισμός των μη μαγνητικών μικκυλίων (C: PTX-PLA-PEG/S), τα οποία βρίσκονται στο υπερκείμενο, απο τα μαγνητικα μικκύλια (D: PTX-Mag-PLA-PEG), τα οποία καθιζάνουν. i) Τα C διαλύματα ομογενοποιούνται και προσδιορίζεται η στερεή μαζά και η PTX, μέσω TGA και HPLC αντίστοιχα, όπως περιγράφηκε πιο πάνω. ii) Όσον αφορά τα δείγματα D, εκπλένονται δύο φόρες με 1ml d.h 2 O προς απομάκρυνση του PBS, το οποίο παρεμποδίζει τον προσδιορισμό της μάζας. Σε δείγμα D προστίθεται νερό, διασπείρεται με υπερήχους και φυγοκεντρείται για 30 λεπτά στα 30kg. Το υπερκείμενο απορίπτεται. Τα στερεά υπολείμματα (απαλλαγμένα πλέον από άλατα του PBS) λυοφιλοποιούνται για 24 ώρες και στη συνέχεια επαναδιασπείρεται το καθένα σε 0.3ml ΑcΝ με τη βοήθεια υπερήχων. Απο κάθε eppendorf, 0.2ml χρησιμοποιούνται για προσδιορισμό της στερεής μάζας (PTX+SPIONs+PLA-PEG) (T=120 o C) και της μάζας των SPIONs (T>400 o C), μέσω TGA. Τα εναπομείναντα 0.1ml ομογενοποιούνται με 0.45ml ΑcΝ και το δείγμα φυγοκεντρείται για 30 λεπτά στα 30kg, με επακόλουθη συλλογή του υπερκειμένου. Το ίζημα εκπλένεται ακόμη μια φορά με 0.45ml ΑcΝ, οπως περιγράφηκε πιο πάνω, και απορρίπτεται. Τα συλλεχθέντα υπερκείμενα διαλύματα (1ml ανά δείγμα) περίεχουν το φάρμακο που ενκαψυλιώθηκε μόνο στα μαγνητικά μικκύλια (D), και το οποίο προσδιορίζεται με HPLC. Τέλος, γνωρίζοντας την ενκαψυλιωμένη μάζα της PTX και τη μάζα των SPIONs T>400 O C), υπολογίζουμε τη μάζα του πολυμερούς, αφαιρόντας τις ποσότητες αυτές απο τη στερεή μάζα του δείγματος T=120 O C). Θα πρέπει να ειπωθεί ότι, η μάζα των SPIONs στα D δείγματα, ισούται με την μάζα αυτών στα δείγματα Α, αφού οπώς φαίνεται και στην Εικόνα 3.13 μετά τη φυγοκέντρηση των δειγμάτων Α (οδός Α2), το υπερκείμενο (C) είναι διάφανο (απουσία SPIONs). Το ίδιο διαπιστώθηκε και με έλεγχο παρουσίας ιόντων σιδήρου με τη μέθοδο της φαινανθρολίνης. Γεγονός που καταδεικνύει την αποκλειστική παρουσία των SPIONs στα δείγματα D. 115
134 (ΙΙ) PTX-PLA-PEG μικκύλια: Η διαδικασία προσδιορισμού της φόρτωσης PTX στα, εξαρχής, μη μαγνητικά μικκύλια (PTX-PLA-PEG) είναι πολύ απλούστερη σε σχέση με αυτήν που περιγράφεται πιο πάνω για τα μαγνητικά μικκύλια. Η διαδικασία που ακολουθείται είναι ίδια με αυτή που παρουσιάζεται στην Εικόνα 3.13, μέσω της οδού Α1. Η οδός Α2 δεν έχει λόγο εφαρμογής στον προσδιορισμό των PTX-PLA-PEG μικκυλίων, λόγω μη συνύπαρξης μαγνητικών μικκυλίων. Έτσι, όπως και στα μαγνητικά μικκύλια, μετά τη σύνθεση των μη μαγνητικών μικκυλίων, εξάτμιση του THF, ρύθμιση του ph:7.4 ( 3.5.1), κάθε δείγμα μεταφέρεται σε eppendorf με τη βοήθεια 0.2ml PBS. Ακολουθεί φυγοκέντρηση για δέκα λεπτά στα 380g, έτσι ώστε να καταβυθιστούν τα μεγάλα μικκύλια καθώς και η ποσότητα της PTX που δεν ενκαψυλιώθηκε στα μικκύλια. Τα υπερκείμενα διαλύματα συλλέγονται όλα μαζί και υπολογίζεται η μάζα ανα δείγμα. Με την τεχνική DLS προσδιορίζεται η D h των PTX-PLA-PEG μικκυλίων. Τρία απο τα παραπάνω υπερκείμενα δείγματα τοποθετούνται σε τρία eppendorfs και λυοφιλοποιούνται για 24 ώρες. Στη συνέχεια πραγματοποιούνται δύο πλύσεις με 0.5ml ΑcΝ, φυγοκέντρηση για μισή ώρα στα 30kg και απόρριψη του ιζήματος (άλατα από το PBS). Τα υπερκείμενα διαλύματα ομογενοποιούνται, 0.2ml χρησιμοποιούνται για προσδιορισμό της στερεής μαζας (PTX+PLA-PEG) μέσω TGA (T=120 ο C), ενώ 2x1ml χρησιμοποιούνται για προσδιορισμό της PTX μέσω HPLC. Η μάζα του πολυμερούς υπολογίζεται αφαιρόντας τη μάζα της PTX απο τη στερεή μάζα του δείγματος T=120 o C). Αφού λοιπόν προσδιοριστούν οι επιμέρους μάζες των PTX, PLA-PEG και SPIONs, υπολογίζεται η φόρτωση φαρμάκου (Drug Loading, D.L) και η απόδοση ενκαψυλίωσης φαρμάκου (Drug Encapsulation Efficiency, D.E.E) για τα PTX-PLA-PEG και PTX-Mag- PLA-PEG μικκύλια. Επιπρόσθετα, για τα PTX-Mag-PLA-PEG μικκύλια, υπολογίζεται επίσης η μαγνητική φόρτωση (Magnetic Loading, M.L) και η απόδοση μαγνητικής ενκαψυλίωσης (Magnetic Encapsulation Efficiency, M.E.E). Οι ορισμοί αυτοί, περιγράφονται με τις Εξισώσεις D. L (%wt) = Mαζα ενκαψυλιωμενης PTX (μg) x 100 Ενκαψυλιωμενης μαζας (PTX + PLA PEG + SPIONs) (μg) (Εξίσωση 3.1) D. E. E (%wt) = Mαζα ενκαψυλιωμενης PTX (μg) Μαζα PTX που χρησιμοποιηθηκε (μg) x 100 (Εξίσωση 3.2) 5 Για τον προσδιορισμό των PTX-PLA-PEG μικκυλίων, στην Εξίσωση 3.1 η μάζα των SPIONs είναι μηδενική. 116
135 Μ. L (%wt) = Mαζα ενκαψυλιωμενων SPIONs (μg) x 100 Ενκαψυλιωμενης μαζας (PTX + PLA PEG + SPIONs) (μg) (Εξίσωση 3.3) M. E. E (%wt) = Mαζα ενκαψυλιωμενων SPIONs (μg) Μαζα SPIONs που χρησιμοποιηθηκε (μg) x 100 (Εξίσωση 3.4) Τέλος, η απόδοση σχηματισμού μικκυλίων (Micelles Formation Efficiency, M.F.E), η απόδοση της διεργασίας δηλαδή, υπολογίζεται σύμφωνα με την Εξίσωση 3.5: Μυκκυλιοποιημένη μάζα PLA PEG (μg) M. F. E (%wt) = Μαζα PLA PEG που χρησιμοποιηθηκε (μg) x 100 (Εξίσωση 3.5) Προσδιορισμός στερεής μάζας PTX-Mag-PLA-PEG νανοφορέων μέσω TGA Όπως φαίνεται πιο πάνω στις Εξισώσεις 3.1 και 3.3, για να υπολογιστεί η φόρτωση του φαρμάκου και των SPIONs, χρειάζεται να γνωρίζουμε τη στερεή μάζα του φορτωμένου με φάρμακο νανοφορέα, ήτοι PTX+PLA-PEG και PTX+PLA-PEG+SPIONs, για τα μη μαγνητικά και τα μαγνητικα μικκύλια αντίστοιχα. Ο προσδιορισμός αυτός επιτελείται με TGA, υπό ροή (60 ml/min) συνθετικού αέρα (sample gas), σε 0.2ml δείγματος. H θερμοκρασία αυξάνεται με ρυθμό 10 ο C/min μέχρι τους 120 ο C, όπου και κρατείται σταθερή (ισόθερμη) για μισή ώρα. Σε αυτό το σημείο, ο διαλύτης (ΑcΝ, σ.ζ:82 ο C) και η υγρασία εξατμίζονται. Η προκύπτουσα στερεή μάζα αντιστοιχεί στο άθροισμα των μαζών PTX+PLA- PEG (Σχήμα 3.3) και PTX+PLA-PEG+SPIONs (Σχήμα 3.4) για τα μη μαγνητικα και τα μαγνητικά μικκύλια αντίστοιχα. Όσον αφορά τα μαγνητικά μικκύλια θα πρέπει να προσδιοριστεί και η μάζα των SPIONs, η οποία είναι απαραίτητη για τον υπολογισμό των Εξισώσεων 3.1, 3.3 και 3.4. Σε αυτή την περίπτωση, μετά την ισόθερμη στους 120 ο C για μισή ώρα, ακολουθεί αύξηση της θερμοκρασίας στους 700 ο C (ρυθμός: 10 ο C/min), όπου και κρατείται σταθερή για δέκα λεπτά. Όπως φαίνεται πιο κάτω στο Σχήμα 3.4, σε θερμοκρασίες ο C παρατηρείται μείωση της μάζας του δείγματος που οφείλεται στην καύση των οργανικών μορίων (PTX και PLA- PEG). Έτσι η μάζα του δείγματος σε θερμοκρασίες μεγαλύτερες των 400 ο C αντιστοιχεί στη μάζα των SPIONs, τα οποία δεν καίγονται σε τέτοιες θερμοκρασίες. Αργότερα, αφού 117
136 προσδιοριστεί και η μάζα της PTX με HPLC, είναι εφικτός ο υπολογισμός και της μάζας του PLA-PEG με απλή αφαίρεση. Σχήμα 3.3: Προσδιορισμός στερεής μάζας για τα PTX-PLA-PEG μικκύλια, μέσω TGA. Σχήμα 3.4: Προσδιορισμός στερεής μάζας και μάζας SPIONs για τα PTX-Mag-PLA-PEG TGA Προσδιορισμός PTX με υγρή χρωματογραφία υψηλής απόδοσης (High Performance Liquid Chromatography, HPLC) Ο προσδιορισμός του ενκαψυλιωμένου φαρμάκου πραγματοποιείται με HPLC αντίστροφης φάσης (reverse phase) (μοντέλο: Waters 2695 με ανιχνευτή Waters 996 Photodiode Array). Η κινητή φάση αποτελείται απο ΑcΝ(0.1%TFA) H 2 O(0.1%TFA) και εφαρμόζεται βαθμιδωτό σύστημα έκλουσης (gradient elution), με ταχυτήτα ροής 0.7ml/min (Πίνακας 3.5). Η αναλυτική στήλη που χρησιμοποιείται είναι η C 18 Aeris Wideboard (Phenomenex) μήκους 150mm, με εσωτερική διάμετρο 4.6mm και μέγεθος σωματιδίων 3.6μm. Ο ενιόμενος όγκος είναι 20μl, η ανίχνευση του φαρμάκου πραγματοποιείται σε λ=227nm και η διάρκεια ανάλυσης κάθε δείγματος ανέρχεται στα 20min. Σε κάθε προσδιορισμό χρησιμοποιούνται τρία ίδια δείγματα του 1ml και το κάθε δέιγμα ενίεται εις τριπλούν. Πίνακας 3.5: Χρησιμοποιούμενο σύστημα βαθμιδωτής έκλουσης Χρόνος (min) Ροή (ml/min) % H 2 O (0.1%TFA) % ΑcN (0.1%TFA)
137 PTX Concentration (ppm) PTX Concentration (ppm) Η ταυτοποίηση (ποιοτικός προσδιορισμός) της PTX επιτελείται με σύγκριση του χρόνου ανάσχεσης (retention time, t R ) της κορυφής του αγνώστου δείγματος, με το t R της κορυφής πρότυπου διαλύματος PTX. Για τις παρούσες χρωματογραφικές συνθήκες, t R = 7.5min. Ο ποσοτικός προσδιορισμός του φαρμάκου πραγματοποιείται με καμπύλες αναφοράς (εμβαδό κορυφής συναρτήσει της συγκέντρωσης PTX) που έχουν κατασκευαστεί προηγουμένως, με πρότυπα διαλύματα PTX σε ΑcΝ, συγκέντρωσης 1 εώς 300ppm. Κατασκευάστηκαν τρείς καμπύλες αναφοράς (1-20ppm, 1-100ppm και ppm) και ανάλογα με το εμβαδό κορυφής (Area Under the Curve, AUC) του υπό προσδιορισμό δείγματος, χρησιμοποιείται η καταλληλότερη καμπύλη. Με στατιστική επεξεργασία (95% διάστημα εμπιστοσύνης), εκτιμήθηκε το όριο ανίχνευσης (Limit of Detection, LOD) και το όριο ποσοτικοποιήσης (Limit of Quantification, LOQ) (Σχήματα 3.5-7) y = x R² = LOD: 0.33ppm LOQ: 1.1ppm x Mean AUC (μv*sec) Σχήμα 3.5: Καμπύλη αναφοράς για συγκεντρώσεις 1-20ppm y = x R² = Millions Mean AUC (μv*sec) Σχήμα 3.6: Καμπύλη αναφοράς για συγκεντρώσεις 1-100ppm. 119
138 y = x R² = Mean AUC (μv*sec) Millions Σχήμα 3.7: Καμπύλη αναφοράς για συγκεντρώσεις ppm. Στο Σχήμα 3.8 παρουσιάζεται ενα τυπικό διάγραμμα HPLC για τον προσδιορισμό της PTX, σύμφωνα με τις χρωματογραφικές συνθήκες που αναφέρθηκαν πιο πάνω. Absorbance (A.U) PTX Cocentration (ppm) Time (min) Σχήμα 3.8: Χρωματογράφημα HPLC δείγματος 10ppm PTX. t R =7.5min. 120
139 3.5.3 Μελέτη μαγνητικών ιδιοτήτων των PTX-Mag-PLA- PEG νανοφορέων με την τεχνική της μαγνητοφόρησης Οι μετρήσεις μαγνητοφόρησης πραγματοποιήθηκαν με τη χρήση του φασματοφωτόμετρου Hitachi Digilab U-2800, με τη σύγχρονη εφαρμογή μαγνητικού πεδίου απο μαγνήτη χειρός Nd-Fe-B (διάμετρος = 20mm, πάχος = 10mm), ο οποίος τοποθετείται ακριβώς δίπλα στην κυψελίδα που περιείχε το προς μέτρηση δείγμα. Οι μετρήσεις πραγματοποιήθηκαν σε υδατικά (PBS) κολλοειδή διαλύματα μαγνητικών νανοφορέων, συγκέντρωσης %w/v σε Fe 2 O 3. Το μήκος κύματος της φωτονικής δέσμης του οργάνου ρυθμίστηκε στα 450nm και καταγράφηκε η απορρόφηση για 7000sec (~2 ώρες), λαμβάνοντας μετρήσεις κάθε 100sec Μελέτη αποδέσμευσης (Release) PTX απο PLA-PEG και Mag-PLA-PEG μικκύλια Εικόνα 3.14: Σχηματική αναπαράσταση της διαδικασίας προσδιορισμού της αποδέσμευσης PTX απο PTX-Mag- PLA-PEG μικκύλια. 121
140 Η διαδικασία προσδιορισμού της αποδέσμευσης (Drug release) PTX από τα μαγνητικά μικκύλια (PTX-Mag-PLA-PEG) αναπαριστάται πιο πάνω στην Εικόνα Όπως και κατα τον προσδιορισμό της φόρτωσης ( 3.5.2), πραγματοποιήθηκαν μελέτες αποδέσμευσης τόσο στο μείγμα μαγνητικών και μη μαγνητικών μικκυλίων (Α) (οδός Α1), όσο και στα αμιγώς μαγνητικά μικκύλια (D), τα οποία προέκυψαν απο το διαχωρισμό του μείγματος αυτών, μέσω της οδού Α2. Σε αμφότερες τις περιπτώσεις διενεργήθηκαν μελέτες αποδέσμευσης του φαρμάκου, με και χωρίς την εφαρμογή εναλλασσόμενου μαγνητικού πεδίου, triggered release και release αντίστοιχα. Η εφαρμογή εναλλασσόμενου μαγνητικού πεδίου (f=113.4khz, B=25mT, I=13.4A, V=28.8V) πραγματοποιήθηκε με τη χρήση της διάταξης magnetherm της εταιρείας nanotherics. Αναλυτικότερα, η πειραματική διαδικασία που ακολουθήθηκε είναι η κάτωθι: (I) Για τους PTX-Mag-PLA-PEG νανοφορείς (Εικόνα 3.14): Μετά τη σύνθεση των μικκυλίων, εξάτμιση του THF, ρύθμιση του ph:7.4 ( 3.5.1), κάθε δείγμα μεταφέρεται σε eppendorf με τη βοήθεια 0.2ml PBS. Ακολουθεί φυγοκέντρηση για δέκα λεπτά στα 380g, έτσι ώστε να καταβυθιστούν τα μεγάλα μικκύλια καθώς και οι ποσότητες PTX και SPIONs που δεν ενκαψυλιώθηκαν στα μικκύλια (Β). Τα υπερκείμενα διαλύματα (μείγμα μαγνητικών και μη μαγνητικών μικκυλίων-α) συλλέγονται όλα μαζί και υπολογίζεται η μάζα ανα δείγμα: Επτά δείγματα Α (~7ml) τοποθετούνται σε μεμβράνη διαπίδυσης, για προσδιορισμό της αποδέσμευσης του φαρμάκου, χωρίς την εφαρμογή εναλλασσόμενου μαγνητικού πεδίου (release). (οδός Α1) Επτά δείγματα Α (~7ml) τοποθετούνται σε μεμβράνη διαπίδυσης, για προσδιορισμό της αποδέσμευσης του φαρμάκου, με εφαρμογή εναλλασσόμενου μαγνητικού πεδίου (triggered release). (οδός Α1) Σαράντα δείγματα Α τοποθετούνται σε eppendorfs και φυγοκεντρούνται για 45min στα 30kg. Έτσι επιτυγχάνεται ο διαχωρισμός των αμιγώς μαγνητικών μικκυλίων (D: PTX-Mag-PLA-PEG) απο τα μη μαγνητικά μικκύλια (C: PTX-PLA-PEG/S) (οδός Α2). Τα υπερκείμενα (C) απορρίπτονται, ενώ τα ιζήματα (D) επαναδιασπείρονται σε 0.2ml PBS με τη βοήθεια υπερήχων. α) Είκοσι απο αυτά τα δείγματα (~ 4ml) τοποθετούνται σε μεμβράνη διαπίδυσης για προσδιορισμό της αποδέσμευσης του φαρμάκου απο τα αμιγώς μαγνητικά μικκύλια, χωρίς εφαρμογή εναλλασσόμενου μαγνητικού πεδίου (release). 122
141 β) Τα υπόλοιπα είκοσι δείγματα (~ 4ml) τοποθετούνται σε μεμβράνη διαπίδυσης για προσδιορισμό της αποδέσμευσης του φαρμάκου απο τα αμιγώς μαγνητικά μικκύλια, με εφαρμογή εναλλασσόμενου μαγνητικού πεδίου (triggered release). (IΙ) Για τους PTX-PLA-PEG νανοφορείς:. Η διαδικασία που ακολουθείται είναι ίδια με αυτή που παρουσιάζεται στην Εικόνα 3.14, μέσω της οδού Α1. Σε αυτή την περιπτώση, η μελέτη της αποδέσμευσης με εφαρμογή μαγνητικού πεδίου δεν έχει κανένα νόημα, λόγω μη χρησιμοποίησης μαγνητικού υλικού. Έτσι λοιπόν, όπως και στα μαγνητικά μικκύλια, μετά τη σύνθεση των μη μαγνητικών μικκυλίων, εξάτμιση του THF, ρύθμιση του ph:7.4 ( 3.5.1), κάθε δείγμα μεταφέρεται σε eppendorf με τη βοήθεια 0.2ml PBS. Ακολουθεί φυγοκέντρηση για δέκα λεπτά στα 380g, έτσι ώστε να καταβυθιστούν τα μεγάλα μικκύλια καθώς και η ποσότητα της PTX που δεν ενκαψυλιώθηκε στα μικκύλια. Τα υπερκείμενα διαλύματα συλλέγονται όλα μαζί και υπολογίζεται η μάζα ανα δείγμα. Τέλος, επτά δείγματα (~7ml) τοποθετούνται σε μεμβράνη διαπίδυσης για προσδιορισμό της αποδέσμευσης της PTX απο τα PTX-PLA-PEG μικκύλια. Tο μέσο αποδέσμευσης (release medium), σε κάθε περίπτωση, είναι 20ml PBS (0.14M, ph:7.4). Οι μεμβράνες διαπίδυσης (Dialysis bag) που χρησιμοποιήθηκαν είναι της εταιρείας Sigma Aldrich, με μοριακό βάρος αποκλεισμού (MWCO) τα 14kDa. Στην Εικόνα 3.15 [153], παρουσιάζεται η αποδέσμευση της PTX απο τα μικκύλια και η διάχυσή της στο μέσο αποδέσμευσης μέχρις ότου εξισορρόπηθουν οι συγκεντρώσεις εκατέρωθεν της μεμβράνης (κατάσταση ισορροπίας). Μελέτηθηκε η αποδέσμευση του φαρμάκου για 24 ώρες σε θερμοκρασία 37 ο C, ενώ τα δείγματα βρίσκονταν υπό συνεχή ανακίνηση, με χρήση υδατόλουτρου ρυθμιζόμενης θερμοκρασίας (Bioline Scientific 5020SWB). Πραγματοποιήθηκαν δειγματοληψίες όγκου 1ml, μετά απο 2,4,8,14 και 24 ώρες. Μετά απο κάθε δειγματοληψία προστείθεται 1ml PBS, έτσι ώστε ο όγκος του μέσου αποδέσμευσης να παραμένει σταθερός καθ όλη τη διάρκεια της διαδικασίας. Η εφαρμογή εναλλασσόμενου μαγνητικού πεδίου στα ανάλογα δείγματα, έλαβε χώρα μία ώρα πριν απο κάθε δειγματοληψία και είχε διάρκεια 30 λεπτά. 123
142 Dialysis bag A. Beginning B. Equilibrium Εικόνα 3.15: Αποδέσμευση PTX απο τα μικκύλια και διάχυσης της διαμέσου της μεμβράνης, μέχρι να επέλθει κατάσταση ισορροπίας. Μετά τη δειγματοληψία τα δείγματα λυοφιλοποιούνται και εκπλένονται δύο φορές με 0.5ml AcΝ, με τη βοήθεια υπερήχων. Ακολουθεί φυγοκέντρηση για 30 λεπτά στα 30kg και απόρριψη του ιζήματος (PBS), μετά απο κάθε πλύση. H PTX, που βρίσκεται διαλυμένη στο υπερκέιμενο, προσδιορίζεται ποσοτικά με HPLC, όπως περιγράφηκε πιο πάνω ( ). Το αθροιστικό ποσοστό αποδέσμευσης του φαρμάκου (Cumulative Release) υπολογίζεται από την παρακάτω σχέση, όπου ι: οι χρονικές στιγμές δειγματοληψίας, Vrm: ο συνολικός όγκος του μέσου αποδέσμευσης (εντός και εκτός της μεμράνης) (ml) και N: ο αριθμός των δειγμάτων που χρησιμοποιήθηκαν. Cumulative Release (%wt) ti = t i=1 (μg PTX που απόδεσμεύθηκαν x Vrm) i μg PTX που έχουν ενκαψυλιωθεί x N (Eξίσωση 3.6) 124
143 Intensity (%) Κεφάλαιο 4 Ανάλυση αποτελεσμάτων - Συζήτηση D h (nm) 125
144 4.1 Χαρακτηρισμός συντεθέντων SPIONs Η σύνθεση των υδρόφοβων SPIONs πραγματοποιήθηκε με τη μέθοδο της θερμικής αποικοδόμησης (Thermal Decomposition). Οι σχηματιζόμενοι νανοκρυσταλλίτες απαρτίζονται κυρίως απο μαγνητίτη (Fe 3 O 4 ) και μαγκεμίτη (γ-fe 2 O 3 ), υπο τη μορφή (Fe 3 O 4 ) χ (Fe 2 O 3 ) 1-χ. Tο χ κυμαίνεται απο και εξαρτάται απο το μέγεθος των νανοκρυσταλλιτών. Για SPIONs μεγέθους 5,12,22nm το χ λαμβάνει τιμές 0.2,0.7,1 αντίστοιχα. Έτσι, όσο αυξάνεται το μέγεθος των SPIONs αυξάνεται το ποσοστό Fe 3 O 4 σε βάρος του γ-fe 2 O 3, και αντίθετα [146]. Επιπλέον, όσο αυξάνεται η θερμοκρασία της αντίδρασης ο μαγνητίτης οξειδώνεται προοδευτικά σε μαγκεμίτη [154]. Στη παρούσα διατριβή μελετήθηκε μια σειρά παραμέτρων με σκοπό τη σύνθεση νανοκρυσταλλιτών διαμέτρου 15-18nm με στενό εύρος κατανομής μεγέθους. Το μέγεθος αυτό εξασφαλίζει τις βέλτιστες μαγνητικές ιδιότητες, δεδομένου ότι η αύξηση του μεγέθους των SPIONs οδηγεί σε αύξηση της Μαγνήτισης κόρου (Ms) [155, 156]. Νανοκρυσταλλίτες με μέγεθος πέραν των 20nm παύουν να συμπεριφέρονται υπερπαραμαγνητικά, αλλά αποκτούν μόνιμη μαγνήτιση (Σιδηρομαγνητισμός ή/και Σιδηριμαγνητισμός). Οι κυριότερες παραμέτροι που μελετήθηκαν αφορούν την επίδραση της πρόδρομης ένωσης, της μοριακής αναλογίας πρόδρομης ένωσης/ελαϊκού οξέος (Ο.Α), της θερμοκρασίας (σ.ζ διαλύτη) καθώς και της διάρκειας σύνθεσης, όσον αφορά τη μορφολογία, το μέγεθος και τη διασπορά του μεγέθους των σχηματιζομένων νανοκρυσταλλιτών. Η ανάλυση των αποτελεσμάτων που θα ακολουθήσει, ταξινομείται με βάση την πρόδρομη ένωση που χρησιμοποιήθηκε. Το μέγεθος των SPIONs που παρουσιάζεται στους επόμενους πίνακες, αφορά τη διάμετρο των νανοκρυσταλλιτών η οποία μετρήθηκε απο μικρογραφήματα TEM, μέσω του λογισμικού Image-pro plus. Η αναγραφόμενη τιμή αποτελεί το μέσο όρο τουλάχιστο 200 σωματιδίων Συνθέσεις SPIONs με Fe(acac) 3 ως πρόδρομη ένωση Οι συνθέσεις που πραγματοποιήθηκαν χρησιμοποιώντας Fe(acac) 3 ως πρόδρομη ένωση, συνοψίζονται παρακάτω στον Πίνακα 4.1. Η προσθήκη Ολεϋλαμίνης (ΟΑm) σε ορισμένες συνθέσεις αποσκοπεί στη μερική αναγωγή των Fe 3+ σε Fe 2+, τα οποία συνυπάρχουν κατα τη σύνθεση των νανοκρυσταλλιτών. Σε κάθε περίπτωση όμως, η παρουσία της δεν κρίνεται απαραίτητη στο σχηματισμό των SPIONs, αν και συμβάλει στον καλύτερο καθαρισμό τους. 126
145 Πίνακας 4.1: Σύνοψη Συνθέσεων με Fe(acac) 3 Κωδική Πρόδρομη Ονομασία ένωση Αντιδραστήρια 1 2 Αναλογία Fe(acac) 3 /Ο.Α Διαλύτης (σ.ζ) Διάρκεια Σύνθεσης Μέγεθος (nm) (ΤΕΜ) MagAcac Fe(acac) mmol 0,20g Ο.Α 1mmol 0.28g OAm 2.1mmol 0.57g 0.56 Διφαινυλαιθέρας (258 ο C) 10ml 22h 1h: 5.4 ± 1.4 2h: 5.8 ± 1.4 4h: 7.7 ± h: 7.2 ± h: 7.6 ± 2.4 MagAcac_4 Fe(acac) 3 1.7mmol 0.60g Ο.Α 3mmol 0.85g OAm 6.4mmol 1.7g 0.56 Διφαινυλαιθέρας (258 ο C) 30ml 4h 4h: 9.7 ± 2.2 MagAcac_6 Fe(acac) 3 1.7mmol 0.60g Ο.Α 6mmol 1.7g Διφαινυλαιθέρας (258 ο C) 30ml 4h 4h: 5.8 ± 1.0 MagAcac_285 Fe(acac) 3 1.1mmol 0.40g Ο.Α 4mmol 1.1g OAm 4mmol 1.1g 0.28 Τριαιθυλένογλυκόλη (285 ο C) 20ml 4h 4h: 7.7 ± 1.2 MagAcac_298 Fe(acac) 3 1.7mmol 0.60g Ο.Α 3mmol 0.85g OAm 6.4mmol 1.7g 0.56 Διβενζυλαιθέρας (298 ο C) 30ml 22h 4h: 8.2 ± h: 10.4 ± 2.6 MagAcac_317 Fe(acac) 3 1.7mmol 0.60g O.A 3mmol 0.85g OAm 6.4mmol 1.7g Δεκαοκτένιο (317 ο C) 30ml 4h 1h: 8.8 ± 1.5 4h: 8.7 ± 1.5 MagAcac_1.3 Fe(acac) 3 2mmol 0.71g O.A 6mmol 1.70g Δεκαοκτένιο (317 ο C) 17.5ml 1h 1h: 8.1 ± 2.3 MagAcac_1.2 Fe(acac) 3 2mmol 0.71g O.A 4mmol 1.1g Δεκαοκτένιο 1h: 9.4 ± 1.7 (317 ο 2h C) 17.5ml 2h: 9.1 ± 1.7 MagAcac_1.1 Fe(acac) 3 2mmol 0.71g O.A 2mmol 0.57g Δεκαοκτένιο (317 ο C) 17.5ml 1h 30min:7.6± 1.6 1h: 8.0 ±
146 Επίδραση αναλογίας Fe(acac) 3 /O.A: Στις συνθέσεις MagAcac_1.1, MagAcac_1.2 και MagAcac_1.3 μελετήθηκε η επίδραση της αναλογίας πρόδρομης ένωσης/ο.α, στο μέγεθος των σχηματιζομένων νανοκρυσταλλιτών, διατηρώντας σταθερές τις υπόλοιπες παραμέτρους. Οι μεγαλύτεροι νανοκρυσταλλίτες (9.4nm) προέκυψαν σε αναλογία 0.5 (MagAcac_1.2). Η αναλογία αυτή φαίνεται να είναι η βέλτιστη για τη συγκεκριμένη πρόδρομη ένωση. Τα μεγέθη αυτά καθαυτά καθώς και η επίδραση της αναλογίας πρόδρομης ένωσης/ο.α στο μέγεθος των SPIONs, δεν επιβεβαιώνουν τη βιβλιογραφία. Στη βιβλιογραφία αναφέρεται επανειλημμένα πως η αύξηση του Ο.Α, δηλαδή μείωση του λόγου πρόδρομης ένωσης/ο.α, οδηγεί στο σχηματισμό μεγαλύτερων νανοκρυσταλλιτών. Με αύξηση του Ο.Α μειώνεται η δραστικότητα των μονομερών με αποτέλεσμα τη μείωση των σχηματιζόμενων πυρήνων κρυστάλλωσης, που έχει σαν αποτέλεσμα το σχηματισμό μεγαλύτερων νανοκρυσταλλιτών [145, 146, 155, 157]. Σύμφωνα με τη συγκεκριμένη θεωρία θα περιμέναμε η σύνθεση MagAcac_1.3 (8.1nm) να οδηγήσει στο σχηματισμό μεγαλύτερων SPIONs σε σχέση με τις συνθέσεις MagAcac_1.1 (8nm) και MagAcac_1.2 (9.4nm), γεγονός το οποίο δεν επαναληθεύεται πειραματικά. Επίδραση θερμοκρασίας αντίδρασης: Η σύνθεση των SPIONs με τη μέθοδο της Θερμικής αποικοδόμησης επιτελείται στο σημείο ζέσεως (σ.ζ) του διαλύτη. Οπότε η επιλογή του διαλύτη καθορίζει τη θερμοκρασία αντίδρασης. Σύμφωνα με βιβλιογραφικά δεδομένα, η αύξηση του σ.ζ του διαλύτη οδηγεί στο σχηματισμό μεγαλύτερων νανοκρυσταλλιτών [154, 155, 157, 158]. Οι συνθέσεις MagAcac_4 (4h:9.7nm), MagAcac_298 (4h:8.2nm) και MagAcac_317 (4h:8.7nm) πραγματοποιήθηκαν σε διφαινυλαιθέρα (σ.ζ: 258 ο C), διβενζυλαιθέρα (σ.ζ: 298 ο C) και 1-Δεκαοκτένιο (σ.ζ: 317 ο C) αντίστοιχα. Συγκρίνοντας το μέγεθος των SPIONs στις τέσσερις ώρες για τις προαναφερθείσες συνθέσεις, όχι μόνο δεν παρατηρήθηκε αύξηση του μεγέθους με αύξηση του σ.ζ του διαλύτη αλλά οι μεγαλυτέροι νανοκρυσταλλίτες προέκυψαν απο τη σύνθεση με το χαμηλότερο σ.ζ διαλύτη (MagAcac_4). Επίδραση διάρκειας σύνθεσης: Όσον αφορά την επίδραση της διάρκειας της σύνθεσης στο μέγεθος των σωματιδίων, παρατηρώντας την τελευταία στήλη του Πινακα 4.1, δεν μπορούν να εξαχθούν ασφαλή συμπεράσματα. Σε κάποιες συνθέσεις φαίνεται πως με την αύξηση του χρόνου σύνθεσης, αυξάνεται το μέγεθος των νανοκρυσταλλιτών. Στη σύνθεση MagAcac παρατηρείται αύξηση του μεγέθους των SPIONs κατα 33% απο τη 2 η μέχρι την 4 η ώρα, ενώ απο την 4 η μέχρι την 22 η ώρα το μέγεθος παραμένει αμετάβλητο. Κατά τη σύνθεση 128
147 Frequency Frequency MagAcac_298 η αύξηση του μεγέθους των νανοκρυσταλλιτών (κατα 27%) συντελείται σε μεγαλύτερους χρόνους, μεταξύ της 4 ης και της 22 ης ώρας. Σε όλες τις λοιπές συνθέσεις, η διάρκεια αντίδρασης δεν διαδραματίζει καθοριστικό ρόλο στο μέγεθος των παραγόμενων SPIONs, αν και αρκετές πηγές αναφέρουν αύξηση του μεγέθους των σωματιδίων με αύξηση του χρόνου αντίδρασης [157, 158]. Αυτό που μπορεί να ειπωθεί με σιγουριά είναι πως η αύξηση του χρόνου αντίδρασης δεν προκαλεί μείωση του μεγέθους των νανοκρυσταλλιτών. Μορφολογία: Οι συνθέσεις που πραγματοποιήθηκαν με τη συγκεκριμένη πρόδρομη ένωση οδήγησαν στο σχηματισμό σφαιρικών νανοκρυσταλλιτών μεγέθους 6-10nm, με εύρος κατανομής μεγέθους σ 15-20%. Κάτωθι στην Εικόνα 4.1 παρουσιάζονται τυπικά μικρογραφήματα TEM καθώς και τα αντίστοιχα ιστογράμματα κατανομής μεγέθους. Α Diameter (nm) Β Γ Δ Diameter (nm) Εικόνα 4.1. Α,Δ: Μικρογραφήματα ΤΕΜ απο τις συνθέσεις MagAcac_4 (9.7 ± 2.2nm) MagAcac_298 (4H: 8.8 ± 1.8nm) αντίστοιχα. Ράβδος=20nm. Β,Γ: Ιστογράμματα κατανομής μεγέθους για τις συνθέσεις MagAcac_4 και MagAcac_298 (4H) αντίστοιχα. 129
148 4.1.2 Συνθέσεις SPIONs με FeO(OH) ως πρόδρομη ένωση Κατα τη σύνθεση SPIONs με πρόδρομη ένωση το FeO(OH) σχηματίζεται in situ Iron Olate Complex [Fe-Olate ή Fe(Olate) 3 ] στους 150 ο C, το οποίο αποικοδομείται σε θερμοκρασίες υψηλότερες των 280 o C προς σχηματισμό μαγνητικών νανοκρυσταλλιτών, σύμφωνα με την αντίδραση [145145] : Επομένως διαλύτες με σημείο ζέσεως μικρότερο των 280 o C θεωρούνται ακατάλληλοι για τη συγκεκριμένη πειραματική πορεία. Όπως παρουσιάζεται παρακάτω στον Πινακα 4.2, η παρούσα συνθετική σειρά πραγματεύεται τη μελέτη επίδρασης της αναλογίας πρόδρομης ένωσης/ο.α στο μέγεθος των σχηματιζομένων νανοκρυσταλλιτών. Πίνακας 4.2. Σύνοψη Συνθέσεων με FeΟ(ΟΗ) Κωδική Ονομασία Πρόδρομη ένωση Αντιδραστήριο Αναλογία FeΟ(ΟΗ)/Ο.Α Διαλύτης Διάρκεια Σύνθεσης Μέγεθος (nm) (ΤΕΜ) MagOOH_1.1 FeO(OH) 7mmol 0.62g O.Α 7mmol 1.98g 1 1-Δεκαοκτένιο 17.5ml 30 min 34.0 ± 11.5 MagOOH_1.2 FeO(OH) 7mmol 0.62g O.Α 14mmol 3.96g Δεκαοκτένιο 17.5ml 30 min 34.9 ± 9.4 MagOOH_1.3 FeO(OH) 7mmol 0.62g O.Α 21mmol 5.94g Δεκαοκτένιο 17.5ml 30 min 35.1 ± 13.0 MagOOH_1.6 FeO(OH) 7mmol 0.62g O.Α 42mmol 11.9g Δεκαοκτένιο 17.5ml 30 min Ελάχιστη μαγνητική απόκριση Οι συνθέσεις που πραγματοποιήθηκαν με πρόδρομη ένωση το FeO(OH) κρίνονται ακατάλληλες για περαιτέρω μελέτη. Οι προκύπτοντες νανοκρυσταλλίτες είναι μεγάλοι σε διάμετρο, χωρίς ουσιαστική επίδραση της αναλογίας FeO(OH)/O.A στο μέγεθος των νανοκρυσταλλιτών. Εντούτοις, παρατηρείται μια μείωση της διασποράς του μεγέθους σε αναλογία 0.5 (MagOOH_1.2). Η σύνθεση MagOOH_1.6 χρήζει περαιτέρω σχολιασμού, αφού παρατηρήθηκε οτι η υπέρμετρη ποσότητα O.A οδήγησε στο σχηματισμό 130
149 Frequency νανοκρυσταλλιτών με ελάχιστη μαγνητική απόκριση. Όπως λέχθηκε πιο πάνω, σύμφωνα με βιβλιογραφικές αναφορές η αύξηση του Ο.Α οδηγεί σε σχηματισμό μεγαλύτερων SPIONs, όμως με αυξηση της αναλογίας πρόδρομης ένωσης:ο.α πέραν του 1:5 παρεμποδίζεται ο σχηματισμός μαγνητικών σωματιδίων (hindered nucleation) [155]. Μάλιστα, οι Lin Song Li et al. αναφέρουν πως σε αναλογίες μεγαλύτερες του 1:4 η κυρίαρχη φάση οξειδίων του σιδήρου είναι ο βουστίτης (FeO), ενώ παραγκωνίζεται ο σχηματισμός Fe 3 O 4 και γ-fe 2 O [145] 3. Μορφολογία: Η σύνθεση SPIONs με την υφιστάμενη πρόδρομη ένωση οδήγησε στο σχηματισμό νανοκρυσταλλιτών μεγάλου μεγέθους (35nm) με μεγάλο εύρος κατανομής (σ>30%), όπως αποτυπώνεται στην Εικάνα 4.2, A Diameter (nm) B Εικόνα 4.2. Α: Μικρογράφημα ΤΕΜ απο τη σύνθεση MagOOH_1.2 (34.9 ± 9.4nm) Ράβδος=50nm. Β: Ιστόγραμμα κατανομής μεγέθους για τη σύνθεση MagOOH_ Συνθέσεις SPIONs με [Fe(Olate) 3 -ex]* ως πρόδρομη ένωση * Η παρασκευή του συμπλόκου πραγματοποιήθηκε με εκχύλιση (extraction). Το σύμπλοκο του ελαϊκού σιδήρου απαρτίζεται απο ενα άτομο Fe 3+ και τρία μόρια ελαϊκού ανιόντος, τα οποία συνδέονται μεταξύ τους ηλεκτροστατικά. Σε θερμοκρασία ο C το ένα μόριο ελαϊκού ανιόντος αποχωρίζεται απο το σύμπλοκο, ενώ τα υπόλοιπα δύο σε θερμοκρασία ~300 ο C. Ο σχηματισμός (nucleation) των νανοκρυσταλλιτών επιτελείται ταχύτατα στους ο C, ενώ η αύξηση του μεγεθούς (growth) αρχίζει στα αμέσως επόμενα λεπτά και ολοκληρώνεται εντός λεπτών [97]. Η συγκεκριμένη πρόδρομη ένωση φέρεται να είναι η καλύτερη για παραγωγή σωματιδίων μεγάλου μεγέθους με στενό 131
150 εύρος κατανομής, αφού έχει τη μεγαλύτερη θερμοκρασία αποικοδόμησης συγκριτικά με άλλες ενώσεις [Fe(acac) 3 : o C, Fe(CO) 5 : 100 o C] [155]. Τα αποτελέσματα που προέκυψαν απο τις συνθέσεις με Fe(Olate) 3 -ex παρουσιάζονται στον Πίνακα 4.3. Η κυρίοτερη παράμετρος που διερευνήθηκε ήταν και πάλι η επίδραση της αναλογίας πρόδρομης ένωσης/ο.α, καθώς επισημαίνεται κατα κόρον στη βιβλιογραφία ως ο κυρίαρχος παράγοντας ελέγχου του μεγέθους των σωματιδίων [145, 146, 155, 157]. Η ροή αζώτου σε ορισμένες συνθέσεις εφαρμόστηκε για πρόληψη της οξείδωσης των νανοκρυσταλλιτών, αλλά δεν κρίνεται απαραίτητη ούτε συμβάλει στο μέγεθος των SPIONs. Η διάρκεια της σύνθεσης δεν φαίνεται να διαδραματίζει ουσιαστικό ρόλο στην αύξηση του μεγέθους των σωματιδίων, μεταξύ ώρας (Mag_I.O.C_2.1). Πίνακας 4.3: Σύνοψη συνθέσεων με Fe(Olate) 3 -ex. Κωδική Ονομασία Πρόδρομη ένωση Αντιδραστήριο Αναλογία Fe(Οlate) 3 /Ο.Α Διαλύτης Διάρκεια Σύνθεσης- Ρυθμός θέρμανσης Μέγεθος (nm) (ΤΕΜ) Mag_I.O.C_2.1 Fe(Οlate) 3 4.0mmol 3.6g O.A 2.0mmol 0.56g 2 1-Δεκαοκτένιο 25ml 1h (με ροή N 2 ) 5 o C/min 30min: 7.9 ± 1.0 1h: 8.1 ± 1.1 Mag_I.O.C_3.2 Fe(Οlate) 3 3.0mmol 2.7g O.A 2.0mmol 0.56g Δεκαοκτένιο 25ml 30 min (χωρίς ροή N 2 ) 15 o C/min 30min: 12.7 ± 3.7 Mag_I.O.C_1.1 Fe(Οlate) 3 4.0mmol 3.6g O.Α 4.0mmol 1.1g 1 1-Δεκαοκτένιο 25ml 1h (με ροή N 2 ) 3.5 o C/min 1h: 7.2 ± 0.8 Mag_I.O.C_4.0 Fe(Οlate) 3 4.0mmol 3.6g Χωρίς O.A Δεκαοκτένιο 25ml 1h (με ροή N 2 ) 4 o C/min 1h: 7.3 ± 0.8 Mag_I.O.C_1.3 Fe(Οate) 3 4.0mmol 3.6g O.Α 12.0mmol 3.4g Δεκαοκτένιο 40ml 1h (χωρίς ροή N 2 ) 7 o C/min 1h: 10.1 ± 1.2 Συγκρίνοντας τις συνθέσεις Mag_I.O.C_2.1, Mag_I.O.C_3.2 και Mag_I.O.C_1.1 θα περιμέναμε η σύνθεση Mag_I.O.C_1.1 να οδηγήσει στο σχηματισμό των μεγαλύτερων νανοκρυσταλλιτών, λόγω μεγαλύτερης ποσότητας Ο.Α. Εντούτοις, αυτό παρατηρείται για τη σύνθεση Mag_I.O.C_3.2. Το γεγονός αυτό δεν αποδίδεται τόσο στην αναλογία πρόδρομης 132
151 ένωσης/ο.α όσο στο ρυθμό θέρμανσης. Μια ενδιαφέρουσα λοιπόν παράμετρος που προκύπτει απο τον πιο πάνω πίνακα είναι η επίδραση του ρυθμού θέρμανσης στο μέγεθος των παραγόμενων SPIONs. Παρατηρήθηκε πως η αύξηση του ρυθμού θέρμανσης οδηγεί στο [ 159 σχηματισμό μεγαλύτερων νανοκρυσταλλιτών ]. Τονίζεται ότι με τη σύνθεση Mag_I.O.C_3.2 παρήχθησαν τα μεγαλύτερα σωματίδια, όμως ο αυξήμενος ρυθμός θέρμανσης που εφαρμόστηκε στη συγκεκριμένη σύνθεση, οδήγησε και σε αύξηση της διασποράς του μεγέθους των SPIONs. Συγκρίνοντας τώρα τις συνθέσεις Mag_I.O.C_1.1 και Mag_I.O.C_1.3, το μεγαλύτερο μέγεθος νανοκρυσταλλιτών που προέκυψε απο τη δεύτερη σύνθεση μπορεί να οφείλεται στην τριπλάσια ποσότητα Ο.Α που χρησιμοποιήθηκε αλλά κυρίως στο διπλάσιο ρυθμό θέρμανσης. Επιπρόσθετα, ένας τρίτος παράγοντας που συνηγορεί στην αύξηση του μεγέθους είναι ο όγκος του διαλύτη. Η αύξηση του όγκου του διαλύτη μειώνει τη συγκέντρωση των δραστικών ειδών που σχηματίζουν τους πυρήνες κρυστάλλωσης και άρα οδηγεί στη μείωση του αριθμού τους, η οποία με τη σειρά της οδηγεί σε αύξηση του μεγέθους των νανοκρυσταλλιτών. Υπογραμμίζεται ότι τα μεγέθη που παρουσιάζονται σε βιβλιογραφικές αναφορές για τις αντίστοιχες συνθέσεις, πλην της Mag_I.O.C_3.2, είναι κατά 20-50% μεγαλύτερα [146, 147, 160]. Μορφολογία: Οι νανοκρυσταλλίτες που συντέθηκαν με Fe(Olate) 3 -ex έχουν σχήμα κυρίως σφαιρικό ενώ σε μεγαλύτερους χρόνους αντίδρασης παρατηρούνται και κυβικοί σχηματισμοί, όπως αποκαλύπτεται πιο κάτω στην Εικόνα 4.3. Οι συνθέσεις αυτές οδήγησαν στο σχηματισμό SPIONs μεγέθους 8-13nm με στενό εύρος κατανομής σ 10-13%, στην πλειοψηφία των περιπτώσεων. Αξίζει να σημειωθεί ότι τα σωματίδια που προέκυψαν απο τη συγκεκριμένη πρόδρομη ένωση, παρουσιάζουν τη μικρότερη διασπορά μεγέθους και την πιο ομοιόμορφη δομή σε σχέση με τις υπόλοιπες συνθέσεις. Μοναδικό αρνητικό σημείο της υφιστάμενης συνθετικής πορείας είναι η χρονοβόρα παρασκευή της πρόδρομης ένωσης. 133
152 Frequency Frequency Α Β Γ Diameter (nm) Δ Diameter (nm) Εικόνα 4.3. Α,Δ: Μικρογραφήματα ΤΕΜ απο τις συνθέσεις Mag_I.O.C_3.2 (12.7 ± 3.7nm) Mag_I.O.C_1.3 (10.1 ± 1.2nm) αντίστοιχα. Ράβδος=20nm. Β,Γ: Ιστογράμματα κατανομής μεγέθους για τις συνθέσεις Mag_I.O.C_3.2 και Mag_I.O.C_1.3 αντίστοιχα Συνθέσεις SPIONs με [Fe(Olate) 3 -prc]* ως πρόδρομη ένωση *Η παρασκευή του συμπλόκου πραγματοποιήθηκε με καταβύθιση (precipitation). Η τελευταία πρόδρομη ένωση που μελετήθηκε ήταν και πάλι το σύμπλοκο του ελαϊκού σιδήρου. Η διαφορά του συμπλόκου αυτου με το προηγούμενο έγκειται στο διαφορετικό τρόπο παρασκευής του, μολονότι έχουν την ίδια χημική δομή. Τα αποτελέσματα παρουσιάζονται παρακάτω στον Πίνακα
153 Πίνακας 4.4: Σύνοψη συνθέσεων με Fe(Olate) 3 -prc. Κωδική Ονομασία Πρόδρομη ένωση Αντιδραστήριο Αναλογία Fe(Οlate) 3 /Ο.Α Διαλύτης Διάρκεια Σύνθεσης Μέγεθος (nm) (ΤΕΜ) MagOlate_1.0 Fe(Olate) 3 2.0mmol 1.8g Χωρίς Ο.Α Δεκαοκτένιο 17.5ml 30 min Μεγάλη μαγνητική απόκριση (SPIONs > 20nm) MagOlate_1.3 Fe(Olate) 3 2.0mmol 1.8g O.A 6.0mmol 1.7g Δεκαοκτένιο 17.5ml 30 min 30 min: 14.0 ± 7.3 MagOlate_1.6 Fe(Olate) mmol 0.77g O.A 5.1mmol 1.4g Δεκαοκτένιο 7.5ml 30 min 2 min: 8.4 ± min: 8.1 ± min: 10.9 ± 3.4 Στην παρούσα συνθετική σειρά παρατηρήθηκε πως η αύξηση του Ο.Α όχι μόνο δεν οδήγει σε αύξηση του μεγέθους των σχηματιζομένων νανοκρυσταλλιτών, αλλά σε προοδευτική μείωσή του. Όταν δεν χρησιμοποιείται καθόλου Ο.Α τα παραγόμενα σωματίδια χαρακτηρίζονται απο μεγάλη μαγνητική απόκριση, γεγονός που οφείλεται στο μεγάλο τους μέγεθος (MagOlate_1.0). Κατά τη σύνθεση MagOlate_1.3 προέκυψαν νανοκρυσταλλίτες ικανοποιητικού μέσου μεγέθους, αλλά η μεγάλη διασπορά του μεγέθους (σ 50%), περιορίζει την περαιτέρω χρήση τους. Όσον αφορά τη σύνθεση MagOlate_1.6, προκύπτουν ενδιαφέροντα στοιχεία για την κινητική της ανάπτυξης των SPIONs. Οι Τ.Ηyeon et al αναφέρουν πως η κύρια αύξηση του μεγέθους των νανοκρυσταλλιτών συντελείται στα πρώτα λεπτά της αντίδρασης [155]. Η συγκεκριμένη θεωρία φαίνεται να επαληθεύεται αφού παρατηρήθηκε αύξηση του μεγέθους των σωματιδίων κατα 35% μεταξύ 10 και 30 λεπτών, ενώ στην πλειοψηφία των προηγούμενων συνθέσεων η αύξηση του μεγεθούς πέρα των 30 λεπτών ήταν πρακτικά ελάχιστη εώς ανύπαρκτη. Μορφολογία: Τα μικρογραφήματα ΤΕΜ στην Εικόνα 4.4 αποκαλύπτουν τη γεωμετρία και το μέγεθος των νανοκρυσταλλιτών που παρήχθησαν κατα τη διάρκεια της σύνθεσης MagOlate_1.6. Στα 10 λεπτά παρατηρούνται σφαιρικοί σχηματισμοί με μέσο μέγεθος 8.1nm και εύρος κατανομής μεγέθους σ 25%, ενώ στα 30 λεπτά τα σωματίδια διατάσσονται είτε σφαιρικά είτε τριγωνικά και έχουν μέσο μέγεθος 10.9nm με εύρος κατανομής μεγέθους σ 30%. 135
154 Frequency Frequency Α Β Diameter (nm) Γ Δ Diameter (nm) Εικόνα 4.4. Α,Δ: Μικρογραφήματα ΤΕΜ απο τις συνθέσεις MagOlate_1.6 στα 10min (8.1 ± 2nm) και MagOlate_1.6 στα 30min (10.9 ± 3.4nm) αντίστοιχα. Ράβδος=20nm. Β,Γ: Ιστογράμματα κατανομής μεγέθους για τις συνθέσεις MagOlate_1.6 στα 10min και MagOlate_1.6 στα 30min αντίστοιχα. 4.2 Μελέτη των παραμέτρων της σύνθεσης πολυμερικών και υπερπαραμαγνητικών πολυμερικών μικκυλίων Η παρασκευή των πολυμερικών (PLA-PEG) και των υπερπαραμαγνητικών πολυμερικών μικκυλίων (Mag-PLA-PEG) πραγματοποιήθηκε με την τεχνική: solvent diffusion and evaporation (nanoprecipitation) [151]. Μελετήθηκαν τρία συμπολυμερή PLA-PEG, διαφορετικού μοριακού βάρους, ήτοι: PLA(2kDa)-PEG(5kDa), PLA(5kDa)-PEG(5kDa) και PLA(10kDa)-PEG(5kDa). Για την παρασκευή των Mag-PLA-PEG μικκυλίων (μαγνητικοί νανοφορείς), χρησιμοποιήθηκαν νανοκρυσταλλίτες μεγέθους 10nm (σύνθεση MagAcac_4). Το κριτήριο αξιολόγησης των παρασκευασθέντων νανοφορέων ήταν η υδροδυναμική τους 136
155 Intensity (%) διάμετρος (Hydrodynamic diameter, D h ). Μελετήθηκε μια σειρά συνθετικών παραμέτρων καθώς και η επίδραση αυτών στην D h των σχηματιζομένων μικκυλίων. Επίδραση ph: To ph της υδατικής φάσης (d.h 2 O) διαδραματίζει σημαντικό ρόλο στο μέγεθος των παραγόμενων μικκυλίων. Μάλιστα, η ρύθμιση του ph πριν (μπλέ γραμμή) ή μετά (κόκκινη γραμμή) την προσθήκη της οργανικής φάσης στην υδατική επηρεάζει σημαντικά την D h των μικκυλίων, όπως φαίνεται στο Σχήμα 4.1. Η μαύρη γραμμή αντιπροσωπεύει το σχηματισμό μικκυλίων χωρίς ρύθμιση του ph (τελικό ph:3.3). Για τη ρύθμιση του ph χρησιμοποιήθηκε διάλυμα ΝaOH 0.01M, ενώ στην περιπτώση που η υδατική φάση συνίσταται απο PBS (ph:7.4) δεν απαιτείται προ-ρύθμιση του ph (πράσινη γραμμή). Σχήμα 4.1: Διαγράμματα DLS. Εξάρτηση της D h των PLA-PEG μικκυλίων απο το ph. Για τα διαγράμματα DLS που παρουσιάζονται στο Σχήμα 4.1, χρησιμοποήθηκε το συμπολυμερές PLA(10kDa)-PEG(5kDa), παρ όλα αυτά τα αποτελέσματα είναι παρόμοια και για τα άλλα δύο συμπολυμερή. Παρατηρήθηκε ραγδαία αύξηση της D h αλλά και της διασποράς του μεγέθους των μικκυλίων με ρύθμιση του ph σε φυσιολογικές τιμές. Η ρύθμιση του ph πριν την ανάμειξη των δύο φάσεων οδήγει στο σχηματισμό μικκυλίων σημαντικά μικρότερου μεγέθους (D h = 177±13nm), σε σχέση με αυτά που προκύπτουν απο τη μετά-ρύθμιση του ph (D h = 269±23nm). Η χρήση PBS (0.14Μ, ph:7.4) πλεονεκτεί έναντι του d.h 2 O αφού εξασφαλίζει τη συνθέση μικκυλίων σε συνθήκες παρόμοιες (ph, ιοντική ισχύ) με αυτές που επικρατούν στο πλάσμα αίματος, έστω και αν τα προκύπτοντα μεγέθη είναι λίγο μεγαλύτερα (D h = 196±30nm) ph: 3.3 no adjustment, Dh= 49±1nm ph: 7.4 post-adjustment (NaOH), Dh= 269±23nm ph: 7.4 pre-adjustment (NaOH), Dh= 177±13nm ph: 7.4 pre-adjustment (PBS), Dh= 196±30nm D h (nm) 137
156 Intensity (%) Intensity (%) Επίδραση του τρόπου ανάμειξης της υδατικής με την οργανικής φάση: Ο σχηματισμός των μικκυλίων συντελείται κατά την προσθήκη της μιας φάσης μέσα στην άλλη. Η ανάμείξη των δύο φάσεων μπορεί να πραγματοποιηθεί είτε με την προσθήκη της οργανικής φάσης στην υδατική (TW), είτε με την προσθήκη της υδατικής φάσης στην οργανική (WT). Όπως φαίνεται στο Σχήμα 4.2, στην περίπτωση που το ph δεν έχει ρυθμιστεί (ph:3.3), το μέγεθος των μικκυλίων δεν επηρεάζεται απο τον τρόπο ανάμειξης των δύο φάσεων. Αντιθέτως, όταν το ph ρυθμιστεί σε φυσιολογικές τιμές, η προσθήκη TW οδηγεί στο σχηματισμό μικκυλίων με υποδιπλάσια D h σε σχέση με την WT προσθήκη. Επιπρόσθετα, η WT προσθήκη αυξάνει σε μεγάλο βαθμό τη διασπόρα του μεγέθους των σχηματιζομένων μικκυλίων A TW Micelles, Dh= 49±1nm WT Micelles, Dh= 51±1nm D h (nm) ph: Σχήμα 4.2: Διαγράμματα DLS. Εξάρτηση της D h των PLA-PEG μικκυλίων απο τη φάση προσθήκης. Α. σε ph:3.3 και Β. σε ph:7.4. TW: Προσθήκη οργανικής φάσης στην υδατική, WT: Προσθήκη υδατικής φάσης στην οργανική. Τα αποτελέσματα αφορούν το συμπολυμερές PLA(10kDa)-PEG(5kDa) TW Micelles, Dh= 269±23nm WT Micelles, Dh= 540±130nm ph:7.4 D h (nm) B Επίδραση ποσότητας SPIONs: Διερευνήθηκε η εξάρτηση της D h των Mag-PLA- PEG μικκυλίων σε σχέση με την ποσότητα των SPIONs που χρησιμοποιήθηκε. Παρατηρήθηκε ότι η αύξηση της μάζας των νανοκρυσταλλιτών οδηγεί σε αύξηση του μεγέθους των μαγνητικών νανοφορέων, ανεξάρτητα απο το μοριακό βάρος του συμπολυμερούς (Πίνακα 4.5 και Σχήμα 4.3). Υπογραμμίζεται ότι τα συντεθέντα Μag-PLA- PEG μικκύλια παρουσιάζουν ικανοποιητικό μέγεθος στην πλειοψηφία τους (D h < 200nm) και μίκρη διασπορά μεγέθους (pdi < 0.25). Η σύνθεση των μικκυλίων πραγματοποιήθηκε με προσθήκη της οργανικής φάσης στην υδατική (PBS, ph:7.4) με ρυθμό: 30μl/min, ενώ η D h προσδιορίστηκε μετά απο φυγοκέντρηση για 10 λεπτά στα 380g (2krpm). 138
157 Πίνακας 4.5: Εξάρτηση της D h των μικκυλίων απο την ποσότητα των SPIONs. *Μικκύλια Mag(X)- PLA(Y)-PEG(Z) **Mάζα SPIONs (mg) Μάζα συμπολυμερούς (mg) D h (nm) PolyDispersity Index (PDI) PLA(2)-PEG(5) ± Mag(0.25)- PLA(2)-PEG(5) ± Mag(0.5)- PLA(2)-PEG(5) ± PLA(5)-PEG(5) ± Mag(0.25)- PLA(5)-PEG(5) ± Mag(0.5)- PLA(5)-PEG(5) ± PLA(10)-PEG(5) ± Mag(0.25)- PLA(10)-PEG(5) ± Mag(0.5)- PLA(10)-PEG(5) ± Mag(1)- PLA(10)-PEG(5) ± * Οι αριθμοί στην παρένθεση αντιπροσωπεύουν την μάζα των SPIONs (X) σε mg και το μοριακό βάρος των πολυμερικών αλυσίδων σε kda (Y,Z). ** Μέθεθος SPIONs=10nm. 139
158 Intensity (%) Intensity (%) Intensity (%) Intensity (%) A Mag(0.25)-PLA(2)-PEG(5), Dh= 137±1nm Mag(0.5)-PLA(2)-PEG(5), Dh= 178±2nm Γ D h (nm) Mag(0.25)-PLA(10)-PEG(5), Dh= 134±2nm Mag(0.5)-PLA(10)-PEG(5), Dh= 174±1nm Mag(1)-PLA(10)-PEG(5), Dh= 208±2nm D h (nm) Β Mag(0.25)-PLA(5)-PEG(5), Dh= 123±1nm Mag(0.5)-PLA(5)-PEG(5), Dh= 143±1nm D h (nm) Mag(0.5)-PLA(2)-PEG(5), Dh= 178±2nm Mag(0.5)-PLA(5)-PEG(5), Dh= 143±1nm Mag(0.5)-PLA(10)-PEG(5), Dh= 174±1nm Δ D h (nm) Σχήμα 4.3: Διαγράμματα DLS. Εξάτρτηση D h των Mag-PLA-PEG μικκυλίων απο την ποσότητα των SPIONs, για τα συμπολυμερή PLA(2kDa)-PEG(5kDa), PLA(5kDa)-PEG(5kDa) και PLA(10kDa)-PEG(5kDa) (Α, B και Γ αντίστοιχα). Δ. Εξάρτηση της D h των Mag-PLA-PEG μικκυλίων απο το μοριακό βάρος του συμπολυμερούς για μάζα SPIONs=0.5mg. Επίδραση όγκου οργανικής φάσης: Εξετάστηκε κατά πόσο ο όγκος της οργανικής φάσης (THF) επηρεάζει το μέγεθος των Mag-PLA-PEG μικκυλίων, διατηρώντας σταθερό τον όγκο της υδατικής φάσης (700μl PBS). Διαπιστώθηκε ότι η αύξηση του όγκου αυτού απο 140μl σε 280μl οδηγεί στην αύξηση της D h των μαγνητικών νανοφορέων, όπως παρουσιάζεται στο Σχήμα 4.4. H μείωση του THF σε όγκο <140μl δεν ενδείκνυται γιατί μειώνεται δραστικά η διαλυτότητα του συμπολυμερούς. Σημειώνεται ότι στην πλειοψηφία των μελετών, η σύνθεση των Mag-PLA-PEG μικκυλίων πραγματοποιήθηκε με προσθήκη της οργανικής φάσης [5mg PLA(10kDa)-PEG(5kDa) και 0.5mg SPIONs (10nm) σε 140μl THF] σε 700μl PBS (0.14M, ph:7.4), με ρυθμό 30μl/min. Ο προσδιορισμός της D h επιτελείται στο υπερκείμενο διάλυμα μετά απο φυγοκέντρηση για
159 Intensity (%) Intensity (%) λεπτά στα 380g (2krpm). Έτσι, απο εδώ και πέρα, όπου δεν αναφέρεται κάτι διαφορετικό, θεωρείται οτι ισχύουν οι συγκεκριμένες συνθήκες V organic phase = 140ul, Dh= 174±1nm V organic phase = 280ul, Dh= 202±0.7nm D h (nm) Σχήμα 4.4: Διάγραμμα DLS. Επίδραση όγκου οργανικής φάσης στο μέγεθος των Mag(0.5)-PLA(10)-PEG(5) μικκυλίων. Επίδραση όγκου υδατικής φάσης: Στο Σχήμα 4.5 παρουσιάζεται η επίδραση του όγκου της υδατικής φάσης στο μέγεθος των μαγνητικών νανοφορέων. Στη συγκεκρίμενη μελέτη εξετάστηκε η σύνθεση Mag-PLA-PEG μικκυλίων σε 0.35, 0.7 και 1.4ml PBS αντίστοιχα, ενώ διατηρήθηκε σταθερός ο όγκος της οργανικής φάσης (0.14ml). Διαπιστώθηκε ότι η βέλτιστη αναλογία οργανικής : υδατικής φάσης, που επάγει στο σχηματισμό μικκυλίων με το μικρότερο μέγεθος, είναι 0.14 : 0.7ml. Όταν ο όγκος της υδατικής φάσης είναι μικρότερος ή μεγαλύτερος απο 0.7ml, παρατηρείται αύξηση τόσο της D h όσο και της διασποράς του μεγέθους των σχηματιζομένων μικκυλίων V aqueous phase = 0.35ml, Dh= 211±2nm V aqueous phase = 0.7ml, Dh= 174±1nm V aqueous phase = 1.4ml, Dh= 251±2nm D h (nm) Σχήμα 4.5: Διάγραμμα DLS. Επίδραση όγκου υδατικής φάσης στο μέγεθος των Mag(0.5)-PLA(10)-PEG(5) μικκυλίων. 141
160 Intensity (%) Επίδραση ποσότητας PLA-PEG: Η συνθεση των μαγνητικών νανοφορέων πραγματοποιήθηκε με χρήση 5mg PLA-PEG. Μελετήθηκε η επίδραση της ποσοτήτας του συμπολυμερούς στο μέγεθος των Mag-PLA-PEG μικκυλίων, χρησιμοποιώντας 10mg PLA(10kDa)-PEG(5kDa) αντί 5mg. Όπως προκύπτει απο το Σχήμα 4.6, η χρήση μεγαλύτερης μάζας συμπολυμερούς οδηγεί σε αύξηση της D h. Επιπρόσθετα, η κορυφή που παρατηρείται σε μέγεθος < 100nm αποδίδεται στο σχηματισμό σημαντικής ποσότητας μημαγνητικών μικκυλίων, λόγω της περίσσειας του PLA-PEG σε σχέση με τη μάζα των SPIONs mg PLA(10kDa)-PEG(5kDa), Dh= 174±1nm 10mg PLA(10kDa)-PEG(5kDa), Dh= 244±4nm D h (nm) Σχήμα 4.6: Διάγραμμα DLS. Επίδραση ποσότητας PLA-PEG στο μέγεθος των Mag(0.5)-PLA(10)-PEG(5) μικκυλίων. Επίδραση τεχνικής εξάτμισης THF: Μια ενδιαφέρουσα παράμετρος που μελετήθηκε αφορά τον τρόπο εξάτμισης του THF. Μετά την ανάμειξη των δύο φάσεων και τον επακόλουθο σχηματισμό των μικκυλίων, επιτελείται εξάτμίση του THF με θέρμανση στους 37 ο C για 15 ώρες. Ωστόσο, εξετάστηκε επίσης η εξάτμιση του THF i) με ροή αζώτου για μία ώρα και ii) με έντονη ανάδευση (800rpm) για 24 ώρες. Στην πρώτη περίπτωση, ο μεγάλος όγκος ιζήματος αποδίδεται σε συσσωμάτωση των μικκυλίων (Εικόνα 4.5 Β). Όσον αφορά την εξάτμιση με ανάδευση (Εικόνα 4.5 Γ), το υπερκείμενο διάλυμα είναι πολύ αραιό, γεγονός που αποδίδεται σε χαμηλή απόδοση μαγνητικής ενκαψυλίωσης (Μ.Ε.Ε). Αντιθέτως, η εξάτμιση του THF με θέρμανση οδηγεί στο σχηματισμό Mag-PLA-PEG μικκυλίων με υψηλή Μ.Ε.Ε (σκούρος χρωματισμός του υπερκειμένου), ενώ δεν παρατηρείται συσσωμάτωση (Εικόνα 4.5 Α). 142
161 A Β Γ Εικόνα 4.5: Mag(0.5)-PLA(10)-PEG(5) μικκύλια. Εξάτμιση THF Α. με θέρμανση, Β. με ροή Ν 2 και Γ. με έντονη ανάδευση. Οι εικόνες λήφθηκαν μετά απο φυγοκέντρηση για 10 λεπτά στα 380g. Επίδραση ρυθμού προσθήκης της οργανικής φάσης: Ο ρυθμός προσθήκης της οργανικής φάσης στην υδατική διαδραματίζει εξαιρετικά σημαντικό ρόλο στο μέγεθος των μαγνητικών νανοφορέων αλλά κυρίως στην απόδοση της μαγνητικής ενκαψυλίωσης (Μ.Ε.Ε). Στον Πίνακα 4.6 παρουσιάζεται η εξάρτηση της D h των μικκυλίων απο το ρυθμό προσθήκης της οργανικής φάσης για τα τρία συμπολυμερή. Η αύξηση του ρυθμού προσθήκης οδηγεί σε μείωση του μεγέθους των Mag(0.5)-PLA(2)-PEG(5) και Mag(0.5)- PLA(10)-PEG(5) μικκυλίων, και σε αύξηση του μεγέθους των Mag(0.5)-PLA(5)-PEG(5) μικκυλίων. Με τον όρο απευθείας προσθήκη (Direct Addition) περιγράφεται η ακαριαία προσθήκη της οργανικής φάσης στην υδατική εντός 3-5 δευτερερολέπτων. Οι Εικόνες 4.6-8, αποκαλύπτουν την επίδραση του ρυθμού προσθήκης στην M.E.E. Όταν η προσθήκη της οργανικής φάσης επιτελείται ταχέως (240μl/min), τα σχηματισθέντα μικκύλια παρουσιάζουν την υψηλότερη Μ.Ε.Ε (εντονότερος χρωματισμός υπερκειμένου) σε σχέση με την αργή (30μl/min) ή την ακαριαία προσθήκη (απευθείας προσθήκη). Το φαινόμενο αυτό διαπιστώθηκε και για τα τρία συμπολυμερή, με τα Mag(0.5)-PLA(2)-PEG(5) μικκύλια να παρουσιάζουν τη μικρότερη Μ.Ε.Ε συγκριτικά με τα άλλα δύο. Πίνακας 4.6: Εξάρτηση της D h των μικκυλίων απο το ρυθμό προσθήκης της οργανικής φάσης. Ρυθμός προσθήκης (μl/min) Mag(0.5)- PLA(2)-PEG(5) D h (nm) Μag(0.5)- PLA(5)-PEG(5) Mag(0.5)- PLA(10)- PEG(5) ± ± ± ± ± ± 2 Απευθείας Προσθήκη 135 ± ± ± 2 143
162 Intensity (%) Intensity (%) Intensity (%) A Addition rate: 30ul/min, Dh= 178±2nm Addition rate: 240ul/min, Dh= 145±1nm Direct Addition, Dh= 135±1nm Mag(0.5)-PLA(2)-PEG(5) D h (nm) Εικόνα 4.6: Α. Διάγραμμα DLS. Επίδραση ρυθμού προσθήκης της οργανικής φάσης στο μέγεθος των Mag(0.5)-PLA(2)-PEG(5) μικκυλίων. Β, Γ, Δ: Σχηματισμός μικκυλίων με ρυθμό προσθήκης 30, 240 μl/min και με απευθείας προσθήκη αντίστοιχα. Οι εικόνες λήφθηκαν μετά απο φυγοκέντρηση για 10 λεπτά 80g A Addition rate: 30ul/min, Dh= 143±1nm Addition rate: 240ul/min, Dh= 148±1nm Direct Addition, Dh= 163±2nm Mag(0.5)-PLA(5)-PEG(5) D h (nm) Εικόνα 4.7: Α. Διάγραμμα DLS. Επίδραση ρυθμού προσθήκης της οργανικής φάσης στο μέγεθος των Mag(0.5)-PLA(5)-PEG(5) μικκυλίων. Β, Γ, Δ: Σχηματισμός μικκυλίων με ρυθμό προσθήκης 30, 240 μl/min και με απευθείας προσθήκη αντίστοιχα. Οι εικόνες λήφθηκαν μετά απο φυγοκέντρηση για 10 λεπτά στα 380g Addition rate: 30ul/min, Dh= 174±1nm Β Addition rate: 240ul/min, Dh= 169±2nm 16 Direct Addition, Dh= 144±2nm 14 Mag(0.5)-PLA(10)-PEG(5) A D h (nm) Εικόνα 4.8: Α. Διάγραμμα DLS. Επίδραση ρυθμού προσθήκης της οργανικής φάσης στο μέγεθος των Mag(0.5)-PLA(10)-PEG(5) μικκυλίων. Β, Γ, Δ: Σχηματισμός μικκυλίων με ρυθμό προσθήκης 30, 240 μl/min και με απευθείας προσθήκη αντίστοιχα. Οι εικόνες λήφθηκαν μετά απο φυγοκέντρηση για 10 λεπτά στα 380g. 144 Γ Γ Γ Β Β Δ Δ Δ
163 D h (nm) Κολλοειδής σταθερότητα Mag-PLA-PEG μικκυλίων: Οι μαγνητικοί νανοφορείς εμφανίζουν αξιοσημείωτη κολλοειδή σταθερότητα για χρονικό διάστημα τουλάχιστον έξι μηνών, σε συνθήκες παρόμοιες (PBS: 0.14M, ph:7.4, ιοντική ισχύ: 0.15Μ) με το πλάσμα αίματος. Το γεγονός αυτό σε συνδυασμό με το μικρό μέγεθος των μαγνητικών νανοφορέων (<200nm), υπογραμμίζουν την καταλληλότητα των συγκεκριμένων δομών για βιοϊατρικές εφαρμογές (MRI, μαγνητική υπερθερμία και Συστήματα Ελεγχόμενης Χορήγησης Φαρμάκων). Στο Σχήμα 4.7 παρουσιάζεται η σταθερότητα των Mag-PLA-PEG μικκυλίων για τα συμπολυμερή PLA-PEG διαφορετικού μοριακού βάρους που μελετήθηκαν Mag(0.5)-PLA(2)-PEG(5) Mag(0.5)-PLA(5)-PEG(5) Mag(0.5)-PLA(10)-PEG(5) Time (months) Σχήμα 4.7: Κολλοειδής σταθερότητα Mag-PLA-PEG μικκυλίων σε PBS, συναρτήσει του χρόνου ( n=3). Μορφολογία : Η μορφολογία των μαγνητικών νανοφορέων εξετάζεται μέσω TEM. Πιο κάτω, στην Είκονα 4.9 παρουσιάζεται ενα τυπικό μικρογράφημα ΤΕΜ των μαγνητικών μικκυλίων. Φαίνονται ξεκάθαρα μεμονωμένοι σφαιρικοί σχηματισμοί (μικκύλια), με τον καθένα να περιβάλλει ένα πλήθος SPIONs (Δομή πυρήνα-κελύφους). Η λήψη των μικρογραφημάτων πραγματοποιήθηκε στο υπερκείμενο των δειγμάτων μετά απο φυκοκέντρηση για δέκα λεπτά στα 380g. 145
164 Εικόνα 4.9: Μικρογραφήματα ΤΕΜ Α. Mag(0.5)-PLA(2)-PEG(5) και Β. Mag(0.5)-PLA(10)-PEG(5) μικκυλίων. Ράβδος = 100nm. 146
165 4.3 Μελέτη των παραμέτρων της φόρτωσης PTX και SPIONs σε PLA-PEG μικκύλια Η πειραματική διαδικασία για προσδιορισμό της φόρτωσης (Loading) PTX και SPIONs στα PTX-Mag-PLA-PEG μικκύλια αναλύθηκε λεπτομερώς στο Κεφάλαιο 3 ( 3.5.2). Στο μεγαλύτερο μέρος της παρούσας διατριβής χρησιμοποίηθηκε μόνο η οδός Α2, χωρίς προσδιορισμό των μη μαγνητικών μικκυλίων (C), με σκοπό τη διερεύνηση των παραμέτρων της φόρτωσης μόνο για τα μαγνητικά μικκύλια (D). Στις περισσότερες περιπτώσεις χρησιμοποιήθηκαν νανοκρυσταλλίτες μεγέθους 10nm, η σύνθεση των PTX-Mag-PLA-PEG μικκυλίων επιτελείται με προσθήκη της οργανικής φάσης (PTX + PLA-PEG + SPIONs σε 140μl THF) στην υδατική (700μl PBS) με ρυθμό 240μl/min, και ο προσδιορισμός της φόρτωσης πραγματοποιήθηκε μεσω της οδού Α2. Σε όλες τις συνθέσεις που πραγματοποιήθηκαν διατηρήθηκε σταθερή η ποσότητα του συμπολυμερούς (5mg) ενώ μελετήθηκε η επίδραση διάφορων συνθετικών παραμέτρων (μοριακό βάρος συμπολυμερούς, ποσότητα PTX, ποσότητα και μέγεθος SPIONs, ρυθμός προσθήκης οργανικής φάσης, κ.α) στη φόρτωση της PTX, αλλά και των SPIONs, στα σχηματιζόμενα μικκύλια. Οι παράμετροι αυτοί αναλύονται παρακάτω: Επίδραση ρυθμού προσθήκης της οργανικής φάσης: Όπως λέχθηκε πιο πάνω για τα Mag-PLA-PEG μικκύλια, η ταχεία προσθήκη (240μl/min) της οργανικής φάσης στην υδατική επάγει το σχηματισμό μικκυλίων με υψηλότερη Μ.Ε.Ε σε σχέση με την αργή προσθήκη (30μl/min). Το γεγονός αυτό επιβεβαιώνεται και για τους PTX-Mag-PLA-PEG νανοφορείς, όπως φαίνεται στον Πίνακα 4.7 και την Εικόνα Συν τοις άλλοις, η ταχεία προσθήκη της οργανικής φάσης οδηγεί αφενός στο σχηματισμό μικκυλίων με σημαντικά μικρότερο μέγεθος και αφετέρου σε αύξηση της μαγνητικής φόρτωσης (M.L). Η ταχύτητα της ανάμειξης (ρυθμός προσθήκης) έχει και σε αυτήν την περίπτωση την ίδια επίδραση στο μέγεθος, όπως και στην περίπτωση μελέτης των μικκυλίων χωρίς φάρμακο. Στην παρούσα περίπτωση η επίδραση αυτή είναι ακόμα ποιο έντονη, δηλαδή η διαφορά της D h είναι σημαντικά μεγαλύτερη. Το πλεονέκτημα για τους σχηματιζόμενους με αργή προσθήκη νανοφορείς, είναι η υψηλότερη φόρτωση φαρμάκου (D.L) που παρουσιάζουν. Παρ όλα αυτά το μέγεθος τους ειναι απαγορευτικό για βιοϊατρικές εφαρμογές. Στον παρακάτω πίνακα φαίνεται πως ενώ το προϊόν με ρυθμό προσθήκης 30μl/min έχει υπερδιπλάσιο D.L σε σχέση με αυτό που παρασκευάσθηκε με 240μl/min, το D.E.E είναι ίδιο και για τα δύο. Αυτό οφείλεται στη διαφορετική απόδοση της διαδικασίας παρασκευής των μικκυλίων (M.F.E). 147
166 Δηλαδή στη δεύτερη περίπτωση έχει μικκυλιοποιηθεί περισσότερο πολυμερές, το οποίο συνολικά έχει εγκλωβίσει την ίδια ποσότητα φαρμάκου, οπότε η ίδια μάζα φαρμάκου κατανέμεται σε περισσότερα μικκύλια. Έτσι λοιπόν, κατά τον προσδιόρισμο της φόρτωσης φαρμακού και νανοκρυσταλλιτών, η μάζα του μικκυλιοποιημένου PLA-PEG (δηλ. η απόδοση της διεργασίας) συμβάλλει καθοριστικά στον υπολογισμό των D.L και Μ.L. Έτσι, η δραστική μείωση της μάζας αυτής οδηγεί σε αύξηση των D.L και M.L, αν οι ενκαψυλιωμένες μάζες PTX και SPIONs δεν μεταβληθούν ιδιαίτερα. Πίνακας 4.7: Επίδραση ρυθμού προσθήκης της οργανικής φάσης στο σχηματισμό των PTX-Mag-PLA-PEG μικκυλίων. *Μικκύλια PTX(X)- Mag(Y)- PLA(Z 1 )- PEG(Z 2 ) Μάζα PTX (mg) Mάζα SPIONs (mg) D.L (%wt) D.E.E (%wt) M.L (%wt) M.E.E (%wt) M.F.E (%wt) D h (nm) PTX(0.5)- Mag(0.5)- PLA(10)- PEG(5) Ρυθμός προσθήκης: 30μl/min ±1 (**D.Lmax: 69±7) 1.5±0.2 21±4 (**M.Lmax: 73±5) 12±2 3.9± ±19 PTX(0.5)- Mag(0.5)- PLA(10)- PEG(5) Ρυθμός προσθήκης: 240μl/min ±0.2 (**D.Lmax: 51±4) 1.5±0.2 33±3 (**M.Lmax: 60±5) 32±4 6.7± ±1 * Οι αριθμοί στην παρένθεση αντιπροσωπεύουν τη μάζα της PTX και των SPIONs (X, Υ) σε mg και το μοριακό βάρος των πολυμερικών αλυσίδων σε kda (Ζ 1, Z 2 ). **Με τους όρους D.Lmax και M.Lmax χαρακτηρίζεται η θεωρητική μέγιστη φόρτωση που μπορεί να επιτευχθεί. D.Lmax: Υπολογίζεται με βάση την ενκαψυλιωμένη μάζα των SPIONs και τη μικκυλιοποιημένη μάζα του PLA-PEG, θεωρώντας ότι έχει εγκαψυλιωθεί όλη η αρχική ποσότητα PTX. Μ.Lmax: Υπολογίζεται με βάση την ενκαψυλιωμένη μάζα της PTX και τη μικκυλιοποιημένη μάζα του PLA-PEG, θεωρώντας ότι έχει εγκαψυλιωθεί όλη η αρχική ποσότητα SPIONs. 148
167 Intensity (%) Addition rate: 30ul/min, Dh= 350±19nm Addition rate: 240ul/min, Dh= 162±1nm PTX(0.5)-Mag(0.5)-PLA(10)-PEG(5) Α Β Γ D h (nm) Εικόνα 4.10: Α. Διάγραμμα DLS. Επίδραση ρυθμού προσθήκης της οργανικής φάσης στο μέγεθος των PTX(0.5)- Mag(0.5)-PLA(10)-PEG(5) μικκυλίων. Β, Γ: Σχηματισμός μικκυλίων με ρυθμό προσθήκης 30 και 240 μl/min αντίστοιχα. Οι εικόνες λήφθηκαν μετά απο φυγοκέντρηση για 10 λεπτά στα 380g. Επίδραση μοριακού βάρους του PLA-PEG : Μία ενδιαφέρουσα παράμετρος που διερευνήθηκε αφορά την επίδραση του μοριακού βάρους (Mw) των πολυμερικών αλυσίδων του PLA-PEG, στη φόρτωση και ενκαψυλίωση του φαρμάκου και των SPIONs. Η απόδοση ενκαψυλίωσης του φαρμάκου (D.E.E) δεν φαίνεται να επηρεάζεται απο το είδος του συμπολυμερούς, όπως παρουσιάζεται στον Πίνακα 4.8. Αντιθέτως, φαίνεται πως όσο αυξάνει το Mw της συστάδας PLA τόσο αυξάνει το Μ.Ε.Ε.. O εντονότερος χρωματισμός των υπερκειμένων στην Εικόνα 4.11 δείχνει και μακροσκοπικά τη διαπίστωση αυτή. Πινακας 4.8: Επίδραση M w PLA-PEG στη φόρτωση και ενκαψυλίωση PTX και SPIONs. Μικκύλια PTX(X)- Mag(Y)- PLA(Z 1 )- PEG(Z 2 ) Μάζα PTX (mg) Mάζα SPIONs (mg) D.L (%wt) D.E.E (%wt) M.L (%wt) M.E.E (%wt) M.F.E (%wt) D h (nm) PTX(0.5)- Mag(0.5)- PLA(2)-PEG(5) ± 0.5 D.Lmax: 73 ± ± ± 5 M.Lmax: 84 ± 1 21 ± ± ± 1 PTX(0.5)- Mag(0.5)- PLA(5)-PEG(5) ± 0.1 D.Lmax: 54 ± ± ±1 M.Lmax: 63 ± 2 28 ± ± ± 1 PTX(0.5)- Mag(0.5)- PLA(10)-PEG(5) ± 0.2 D.Lmax: 51 ± ± ± 3 M.Lmax: 60 ± 5 32 ± ± ± 1 149
168 Intensity (%) Οι PTX(0.5)-Mag(0.5)-PLA(2)-PEG(5) νανοφορείς παρουσιάζουν αρκετά υψηλότερες τιμές D.L και M.L σε σχέση με τους άλλους δύο. Εντούτοις, οι τιμές αυτές δεν οφείλονται στην αύξηση της ενκαψυλιωμένης μάζας PTX και SPIONs, αλλά στη μικρότερη μικκυλιοποιημένη μάζα του συγκεκριμένου συμπολυμερούς. Ενδεικτικά αναφέρεται ότι για τους νανοφορείς PTX(0.5)-Mag(0.5)-PLA(5)-PEG(5), η μέση εγκαψυλιωμένη μάζα PTX, SPIONs και PLA-PEG είναι 8.3, 140 και 281μg αντίστοιχα, για τους PTX(0.5)-Mag(0.5)- PLA(10)-PEG(5) είναι 7.0, 158 και 332μg αντίστοιχα, ενώ για τους νανοφορείς PTX(0.5)- Mag(0.5)-PLA(2)-PEG(5) 7.8, 101 και 80μg αντίστοιχα. Γίνεται λοιπόν αντιληπτό πως το συμπολυμερές PLA(2)-PEG(5) εμφανίζει τη χαμηλότερη απόδοση σχηματισμού μαγνητικών μικκυλίων (1.6%wt), αφού παρέχει τη μικρότερη πολυμερική μάζα προς σχηματισμό μικκυλίων. Παρ όλα αυτά, το προιόν με το πολυμερές PLA(2)-PEG(5) παρουσιάζει ιδιαίτερο ενδιαφέρον εφόσον μπορεί να μεταφέρει περισσότερο φάρμακο στο στόχο, αλλά, και εξαιτίας του μεγαλύτερου M.L, να έχει καλύτερες μαγνητικές ιδιότητες Α PTX(0.5)-Mag(0.5)-PLA(2)-PEG(5), Dh= 141±1nm PTX(0.5)-Mag(0.5)-PLA(5)-PEG(5), Dh= 143±1nm PTX(0.5)-Mag(0.5)-PLA(10)-PEG(5), Dh= 162±1nm Β Γ Δ D h (nm) Εικόνα 4.11: Α. Διάγραμμα DLS. Επίδραση Mw PLA-PEG στο μέγεθος των PTX(0.5)-Mag(0.5)-PLA-PEG μικκυλίων. Β, Γ, Δ: Εικόνες PTX(0.5)-Mag(0.5)-PLA(2)-PEG(5), PTX(0.5)-Mag(0.5)-PLA(5)-PEG(5) και PTX(0.5)-Mag(0.5)-PLA(10)-PEG(5) μικκυλίων αντίστοιχα, μετά απο φυγοκέντρηση για 10 λεπτά στα 380g. Επίδραση αναλογίας PTX:SPIONs : Η φόρτωση και η ενκαψυλίωση PTX και SPIONs εξαρτώνται σε μεγάλο βαθμό απο τις χρησιμοποιούμενες ποσότητες αυτών, καθώς και απο τη σχετική τους αναλογία. Όπως παρουσιάζεται στον Πίνακα 4.9, η μείωση της μάζας του φαρμάκου απο 0.5 σε 0.25mg [PTX(0.25)-Mag(0.5)-PLA(10)-PEG(5)] συμβάλλει στην αύξηση της απόδοσης ενκαψυλίωσης τόσο της PTX (D.E.E) αλλά κυρίως των SPIONs (M.E.E), διατηρώντας σταθερές τις μάζες του συμπολυμερούς (5mg) και των νανοκρυσταλλιτών (0.5mg). Όσον αφορά τη φόρτωση του φαρμάκου και των SPIONs (D.L 150
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 12 ο Κυτταρική Βιολογία (νανομετρικό μέγεθος) - Βιοδείκτες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ)
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 12 ο Κυτταρική Βιολογία (νανομετρικό μέγεθος) - Βιοδείκτες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ)
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 15 ο Νανοσωματίδια για γονιδιακή μεταφορά Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας,
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 15 ο Νανοσωματίδια για γονιδιακή μεταφορά Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας,
ΕΞΕΛΙΞΕΙΣ ΣΤΑ ΣΥΣΤΗΜΑΤΑ ΕΛΕΓΧΟΜΕΝΗΣ ΧΟΡΗΓΗΣΗΣ ΦΑΡΜΑΚΩΝ
 UNIVERSITY OF PATRAS ΕΞΕΛΙΞΕΙΣ ΣΤΑ ΣΥΣΤΗΜΑΤΑ ΕΛΕΓΧΟΜΕΝΗΣ ΧΟΡΗΓΗΣΗΣ ΦΑΡΜΑΚΩΝ ΚΩΝΣΤΑΝΤΙΝΟΣ ΑΥΓΟΥΣΤΑΚΗΣ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ UNIVERSITY OF PATRAS ΣΥΜΒΑΤΙΚΗ ΧΟΡΗΓΗΣΗ Το φάρμακο κατανέμεται
UNIVERSITY OF PATRAS ΕΞΕΛΙΞΕΙΣ ΣΤΑ ΣΥΣΤΗΜΑΤΑ ΕΛΕΓΧΟΜΕΝΗΣ ΧΟΡΗΓΗΣΗΣ ΦΑΡΜΑΚΩΝ ΚΩΝΣΤΑΝΤΙΝΟΣ ΑΥΓΟΥΣΤΑΚΗΣ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ UNIVERSITY OF PATRAS ΣΥΜΒΑΤΙΚΗ ΧΟΡΗΓΗΣΗ Το φάρμακο κατανέμεται
Ανδρέας-Παναγιώτης Θεοδώρου Μαρία-Ιωάννα Μαλλιαρουδάκη Κωνσταντίνος Καλογερόπουλος Ιάκωβος Παπαϊωάννου Πελαγία Λυδία Πετροπούλου
 Ανδρέας-Παναγιώτης Θεοδώρου Μαρία-Ιωάννα Μαλλιαρουδάκη Κωνσταντίνος Καλογερόπουλος Ιάκωβος Παπαϊωάννου Πελαγία Λυδία Πετροπούλου «CELL NANOHEALERS: ΝΑΝΟΘΕΡΑΠΕΥΤΕΣ ΚΥΤΤΑΡΩΝ ΣΕ ΔΡΑΣΗ!» Ανδρέας-Παναγιώτης
Ανδρέας-Παναγιώτης Θεοδώρου Μαρία-Ιωάννα Μαλλιαρουδάκη Κωνσταντίνος Καλογερόπουλος Ιάκωβος Παπαϊωάννου Πελαγία Λυδία Πετροπούλου «CELL NANOHEALERS: ΝΑΝΟΘΕΡΑΠΕΥΤΕΣ ΚΥΤΤΑΡΩΝ ΣΕ ΔΡΑΣΗ!» Ανδρέας-Παναγιώτης
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C.
 Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Ανάπτυξη πολυλειτουργικών νανοκαψακίων φορτωμένα με αντικαρκινικά φάρμακα για τη στοχευμένη φαρμακοθεραπεία καρκινικών όγκων
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΤΕΧΝΟΛΟΓΙΑΣ Ανάπτυξη πολυλειτουργικών νανοκαψακίων φορτωμένα με αντικαρκινικά φάρμακα για τη στοχευμένη φαρμακοθεραπεία
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΤΕΧΝΟΛΟΓΙΑΣ Ανάπτυξη πολυλειτουργικών νανοκαψακίων φορτωμένα με αντικαρκινικά φάρμακα για τη στοχευμένη φαρμακοθεραπεία
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 11 ο Νανοτεχνολογία εφαρμογές Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 11 ο Νανοτεχνολογία εφαρμογές Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ
Συνδέοντας τη Νανοτεχνολογία με τα Βιολογικά Συστήματα
 Συνδέοντας τη Νανοτεχνολογία με τα Βιολογικά Συστήματα Η νανοβιοτεχνολογία είναι ένας ραγδαία αναπτυσσόμενος κλάδος της σύγχρονης νανοεπιστήμης και νανοτεχνολογίας στον οποίον εφαρμόζονται τα εργαλεία
Συνδέοντας τη Νανοτεχνολογία με τα Βιολογικά Συστήματα Η νανοβιοτεχνολογία είναι ένας ραγδαία αναπτυσσόμενος κλάδος της σύγχρονης νανοεπιστήμης και νανοτεχνολογίας στον οποίον εφαρμόζονται τα εργαλεία
ΕΝΑΝΤΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΜΕ ΚΟΙΝΑ ΦΑΡΜΑΚΑ Η ΜΕ ΝΑΝΟΦΑΡΜΑΚΑ?
 Η ΕΝ ΑΘΗΝΑΙΣ ΦΙΛΕΚΠΑΙΔΕΥΤΙΚΗ ΕΤΑΙΡΕΙΑ ΕΝΑΝΤΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΜΕ ΚΟΙΝΑ ΦΑΡΜΑΚΑ Η ΜΕ ΝΑΝΟΦΑΡΜΑΚΑ? Ευδοκία Κολιάκου Χριστίνα Κοτίνου Κωνσταντίνα Σκλιάμη Αγλαΐα Σφακάκη Χαρούλα Σφέτσα Υπεύθυνες καθηγήτριες:
Η ΕΝ ΑΘΗΝΑΙΣ ΦΙΛΕΚΠΑΙΔΕΥΤΙΚΗ ΕΤΑΙΡΕΙΑ ΕΝΑΝΤΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΜΕ ΚΟΙΝΑ ΦΑΡΜΑΚΑ Η ΜΕ ΝΑΝΟΦΑΡΜΑΚΑ? Ευδοκία Κολιάκου Χριστίνα Κοτίνου Κωνσταντίνα Σκλιάμη Αγλαΐα Σφακάκη Χαρούλα Σφέτσα Υπεύθυνες καθηγήτριες:
Υβριδικά μαγνητικά νανοσωματίδια για τη στοχευμένη χορήγηση σισπλατίνης σε καρκινικούς όγκους
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΤΕΧΝΟΛΟΓΙΑΣ Υβριδικά μαγνητικά νανοσωματίδια για τη στοχευμένη χορήγηση σισπλατίνης σε καρκινικούς όγκους ΜΕΤΑΠΤΥΧΙΑΚΟ ΔΙΠΛΩΜΑ ΕΙΔΙΚΕΥΣΗΣ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΤΕΧΝΟΛΟΓΙΑΣ Υβριδικά μαγνητικά νανοσωματίδια για τη στοχευμένη χορήγηση σισπλατίνης σε καρκινικούς όγκους ΜΕΤΑΠΤΥΧΙΑΚΟ ΔΙΠΛΩΜΑ ΕΙΔΙΚΕΥΣΗΣ
ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΠΡΟΣΛΗΨΗ ΚΑΙ ΜΕΤΑΦΟΡΑ ΤΟΥ ΝΕΡΟΥ ΣΤΑ ΦΥΤΑ
 ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΠΡΟΣΛΗΨΗ ΚΑΙ ΜΕΤΑΦΟΡΑ ΤΟΥ ΝΕΡΟΥ ΣΤΑ ΦΥΤΑ Θερινό εξάμηνο 2011 Ο ρόλος του νερού στο φυτό Βασικότερο συστατικό των ιστών
ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΠΡΟΣΛΗΨΗ ΚΑΙ ΜΕΤΑΦΟΡΑ ΤΟΥ ΝΕΡΟΥ ΣΤΑ ΦΥΤΑ Θερινό εξάμηνο 2011 Ο ρόλος του νερού στο φυτό Βασικότερο συστατικό των ιστών
ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ
 ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ Προσοµοίωση Είναι γνωστό ότι η εξάσκηση των φοιτητών σε επίπεδο εργαστηριακών ασκήσεων, µε χρήση των κατάλληλων πειραµατοζώων, οργάνων και αναλωσίµων
ΜΗΧΑΝΙΣΜΟΙ ΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΦΟΡΑΣ ΚΥΤΤΑΡΙΚΗ ΔΙΑΠΕΡΑΤΟΤΗΤΑ Προσοµοίωση Είναι γνωστό ότι η εξάσκηση των φοιτητών σε επίπεδο εργαστηριακών ασκήσεων, µε χρήση των κατάλληλων πειραµατοζώων, οργάνων και αναλωσίµων
Φαρμακοκινητική. Χρυσάνθη Σαρδέλη
 Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
Πεπτικός σωλήνας Κύρια λειτουργία του είναι η εξασφάλιση του διαρκούς ανεφοδιασμού του οργανισμού με νερό, ηλεκτρολύτες και θρεπτικά συστατικά.
 Πεπτικός σωλήνας Κύρια λειτουργία του είναι η εξασφάλιση του διαρκούς ανεφοδιασμού του οργανισμού με νερό, ηλεκτρολύτες και θρεπτικά συστατικά. Στον πεπτικό σωλήνα πραγματοποιείται ο τεμαχισμός της τροφής
Πεπτικός σωλήνας Κύρια λειτουργία του είναι η εξασφάλιση του διαρκούς ανεφοδιασμού του οργανισμού με νερό, ηλεκτρολύτες και θρεπτικά συστατικά. Στον πεπτικό σωλήνα πραγματοποιείται ο τεμαχισμός της τροφής
ΒΙΟΧΗΜΕΙΑ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ. Στοιχείο O C H N Ca P K S Na Mg περιεκτικότητα % ,5 1 0,35 0,25 0,15 0,05
 ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Η κίνηση του νερού εντός των φυτών (Soil-Plant-Atmosphere Continuum) Δημήτρης Κύρκας
 Η κίνηση του νερού εντός των φυτών (Soil-Plant-Atmosphere Continuum) Δημήτρης Κύρκας Η Σεκόγια (Sequoia) «Redwood» είναι το ψηλότερο δέντρο στο κόσμο και βρίσκεται στην Καλιφόρνια των ΗΠΑ 130 μέτρα ύψος
Η κίνηση του νερού εντός των φυτών (Soil-Plant-Atmosphere Continuum) Δημήτρης Κύρκας Η Σεκόγια (Sequoia) «Redwood» είναι το ψηλότερο δέντρο στο κόσμο και βρίσκεται στην Καλιφόρνια των ΗΠΑ 130 μέτρα ύψος
Ανθεκτικότητα Υλικών και Περιβάλλον
 Ανθεκτικότητα Υλικών και Περιβάλλον Ν. Μ. Μπάρκουλα, Επίκουρη Καθηγήτρια, Δρ. Μηχ/γος Μηχανικός 1 Τι είναι: Περίγραμμα Μαθήματος Επιλογής Μάθημα Επιλογής στο 9ο Εξάμηνο του ΤΜΕΥ Με τι ασχολείται: Με την
Ανθεκτικότητα Υλικών και Περιβάλλον Ν. Μ. Μπάρκουλα, Επίκουρη Καθηγήτρια, Δρ. Μηχ/γος Μηχανικός 1 Τι είναι: Περίγραμμα Μαθήματος Επιλογής Μάθημα Επιλογής στο 9ο Εξάμηνο του ΤΜΕΥ Με τι ασχολείται: Με την
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες
 Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Πηγή: ΑΠΟΛΥΜΑΝΣΗ ΤΟΥ ΠΟΣΙΜΟΥ ΝΕΡΟΥ : ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΤΟΥ ΧΛΩΡΙΟΥ, ΘΕΟΔΩΡΑΤΟΥ ΑΓΓΕΛΙΚΗ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ, ΜΥΤΙΛΗΝΗ 2005
 Πηγή: ΑΠΟΛΥΜΑΝΣΗ ΤΟΥ ΠΟΣΙΜΟΥ ΝΕΡΟΥ : ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΤΟΥ ΧΛΩΡΙΟΥ, ΘΕΟΔΩΡΑΤΟΥ ΑΓΓΕΛΙΚΗ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ, ΜΥΤΙΛΗΝΗ 2005 ΠΡΟΧΩΡΗΜΕΝΕΣ ΤΕΧΝΙΚΕΣ ΟΞΕΙΔΩΣΗΣ 1 ΕΙΣΑΓΩΓΗ Οι προχωρημένες τεχνικές
Πηγή: ΑΠΟΛΥΜΑΝΣΗ ΤΟΥ ΠΟΣΙΜΟΥ ΝΕΡΟΥ : ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΝΑΛΛΑΚΤΙΚΕΣ ΤΟΥ ΧΛΩΡΙΟΥ, ΘΕΟΔΩΡΑΤΟΥ ΑΓΓΕΛΙΚΗ, ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΙΓΑΙΟΥ, ΜΥΤΙΛΗΝΗ 2005 ΠΡΟΧΩΡΗΜΕΝΕΣ ΤΕΧΝΙΚΕΣ ΟΞΕΙΔΩΣΗΣ 1 ΕΙΣΑΓΩΓΗ Οι προχωρημένες τεχνικές
Πολυλειτουργικά νανοκαψάκια για την στοχευμένη χορήγηση ιξαμπεπιλόνης: Σύνθεση και in vitro μελέτες
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Εργαστήριο Φαρμακευτικής Τεχνολογίας Πολυλειτουργικά νανοκαψάκια για την στοχευμένη χορήγηση ιξαμπεπιλόνης: Σύνθεση και in vitro μελέτες ΚΟΥΤΣΟΣΠΥΡΟΥ ΝΕΦΕΛΗ του
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Εργαστήριο Φαρμακευτικής Τεχνολογίας Πολυλειτουργικά νανοκαψάκια για την στοχευμένη χορήγηση ιξαμπεπιλόνης: Σύνθεση και in vitro μελέτες ΚΟΥΤΣΟΣΠΥΡΟΥ ΝΕΦΕΛΗ του
Το πιο μικρό και συμπαγές LASER μεγάλης ισχύος για την φυσικοθεραπεία και την φυσική αποκατάσταση
 Το πιο μικρό και συμπαγές LASER μεγάλης ισχύος για την φυσικοθεραπεία και την φυσική αποκατάσταση Χημικοί Μηχανισμοί Παραγωγή εξ επαγωγής, φωτο-χημικών φαινομένων φωτο-ευαισθητοποίησης και φωτο-απομάκρυνσης.
Το πιο μικρό και συμπαγές LASER μεγάλης ισχύος για την φυσικοθεραπεία και την φυσική αποκατάσταση Χημικοί Μηχανισμοί Παραγωγή εξ επαγωγής, φωτο-χημικών φαινομένων φωτο-ευαισθητοποίησης και φωτο-απομάκρυνσης.
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
Εφαρμοσμένη Διατροφική Ιατρική
 Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
ΦΡΟΝΤΙΣΤΗΡΙΑ ΠΡΟΟΠΤΙΚΗ
 Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ
 2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΠΛΗΡΟΦΟΡΙΚΗ Τα τελευταία χρόνια τα οργανικά ηλεκτρονικά (ΟΗ) αποτελούν έναν από τους πιο ραγδαία αναπτυσσόμενους
 ΤΙ ΑΚΡΙΒΩΣ ΕΊΝΑΙ Η ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΚΑΙ Η ΝΑΝΟΕΠΙΣΤΗΜΕΣ Ως Νανοτεχνολογία ορίζεται η επιστήμη, η μηχανική και η τεχνολογία στην νανοκλίμακα, δηλαδή στην κλίμακα διαστάσεων από 1 έως 100nm. Με άλλα λόγια
ΤΙ ΑΚΡΙΒΩΣ ΕΊΝΑΙ Η ΝΑΝΟΤΕΧΝΟΛΟΓΙΑ ΚΑΙ Η ΝΑΝΟΕΠΙΣΤΗΜΕΣ Ως Νανοτεχνολογία ορίζεται η επιστήμη, η μηχανική και η τεχνολογία στην νανοκλίμακα, δηλαδή στην κλίμακα διαστάσεων από 1 έως 100nm. Με άλλα λόγια
ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ. 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε.
 ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε. Αμανατίδης ΤΡΙΤΗ 24/10/2017 ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Κατηγορίες
ΒΙΟΫΛΙΚΑ ΤΑΞΙΝΟΜΗΣΗ ΥΛΙΚΩΝ ΜΕ ΕΦΑΡΜΟΓΕΣ ΣΤΗΝ ΙΑΤΡΙΚΗ 3o Μάθημα 9 ο Εξάμηνο σπουδών Μάθημα Επιλογής Διδάσκων: Αν. Καθηγητής Ε. Αμανατίδης ΤΡΙΤΗ 24/10/2017 ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ Κατηγορίες
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ
 ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ Η αξιοποίηση της γεωθερμικής ενέργειας συναντά ορισμένα τεχνικά προβλήματα, Τα προβλήματα αυτά είναι: (α) ο σχηματισμός επικαθίσεων (ή καθαλατώσεις
ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ Η αξιοποίηση της γεωθερμικής ενέργειας συναντά ορισμένα τεχνικά προβλήματα, Τα προβλήματα αυτά είναι: (α) ο σχηματισμός επικαθίσεων (ή καθαλατώσεις
ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ
 ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Δελτίο μαθήματος (Syllabus): ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Κωδικός μαθήματος: 79 Κύκλος/Επίπεδο σπουδών: Εξάμηνο σπουδών: Προπτυχιακό 8 ο Εξάμηνο Τύπος μαθήματος Υποβάθρου / Γενικών Γνώσεων
ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Δελτίο μαθήματος (Syllabus): ΚΛΙΝΙΚΗ ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Κωδικός μαθήματος: 79 Κύκλος/Επίπεδο σπουδών: Εξάμηνο σπουδών: Προπτυχιακό 8 ο Εξάμηνο Τύπος μαθήματος Υποβάθρου / Γενικών Γνώσεων
ΧΡΩΜΑΤΟΓΡΑΦΙΚΕΣ ΜΕΘΟΔΟΙ ΔΙΑΧΩΡΙΣΜΟΥ. ΑΝΝΑ-ΜΑΡΙΑ ΨΑΡΡΑ Τμήμα Βιοχημείας κ Βιοτεχνολογίας
 ΧΡΩΜΑΤΟΓΡΑΦΙΚΕΣ ΜΕΘΟΔΟΙ ΔΙΑΧΩΡΙΣΜΟΥ ΑΝΝΑ-ΜΑΡΙΑ ΨΑΡΡΑ Τμήμα Βιοχημείας κ Βιοτεχνολογίας ΑΝΝΑ-ΜΑΡΙΑ ΨΑΡΡΑ 1 ΣΥΣΤΗΜΑ ΧΡΩΜΑΤΟΓΡΑΦΙΑΣ Αντλία Στήλη Υγρό Έκλουσης Συλλέκτης κλασμάτων ΧΡΩΜΑΤΟΓΡΑΦΙΚΕΣ ΜΕΘΟΔΟΙ ΔΙΑΧΩΡΙΣΜΟΥ
ΧΡΩΜΑΤΟΓΡΑΦΙΚΕΣ ΜΕΘΟΔΟΙ ΔΙΑΧΩΡΙΣΜΟΥ ΑΝΝΑ-ΜΑΡΙΑ ΨΑΡΡΑ Τμήμα Βιοχημείας κ Βιοτεχνολογίας ΑΝΝΑ-ΜΑΡΙΑ ΨΑΡΡΑ 1 ΣΥΣΤΗΜΑ ΧΡΩΜΑΤΟΓΡΑΦΙΑΣ Αντλία Στήλη Υγρό Έκλουσης Συλλέκτης κλασμάτων ΧΡΩΜΑΤΟΓΡΑΦΙΚΕΣ ΜΕΘΟΔΟΙ ΔΙΑΧΩΡΙΣΜΟΥ
Νανοτεχνολογία ΧΑΡΙΣ ΑΣΗΜΑΚΟΠΟΥΛΟΣ ΕΦΑΡΜΟΓΕΣ ΠΛΗΡΟΦΟΡΙΚΗΣ 2013 14
 Νανοτεχνολογία 1.Ορισμός της Νανοτεχνολογίας 2.Πότε έκανε την εμφάνιση της; 3.Τα επιτευγματά της 4.Σε τι ωφελει την ανθρωπότητα 5.Που τη συναντάμε στη φύση 6.Κριτικές 7.Τι περιμένουμε απο την εξέλιξη της
Νανοτεχνολογία 1.Ορισμός της Νανοτεχνολογίας 2.Πότε έκανε την εμφάνιση της; 3.Τα επιτευγματά της 4.Σε τι ωφελει την ανθρωπότητα 5.Που τη συναντάμε στη φύση 6.Κριτικές 7.Τι περιμένουμε απο την εξέλιξη της
Πτυχιακή εργασία. Ελένη Κυριάκου
 Σχολή Γεωπονικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία Βιοδιάσπαση Ιοντικών Υγρών σε Διαφορετικές Θερμοκρασίες από τον Sphingomonas sp. VITPTHJ Ελένη Κυριάκου Λεμεσός, Μάιος 2017 ΤΕΧΝΟΛΟΓΙΚΟ
Σχολή Γεωπονικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία Βιοδιάσπαση Ιοντικών Υγρών σε Διαφορετικές Θερμοκρασίες από τον Sphingomonas sp. VITPTHJ Ελένη Κυριάκου Λεμεσός, Μάιος 2017 ΤΕΧΝΟΛΟΓΙΚΟ
ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΔΟΜΗ ΚΑΙ ΒΛΑΣΤΗΣΗ ΤΩΝ ΣΠΕΡΜΑΤΩΝ
 ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΔΟΜΗ ΚΑΙ ΒΛΑΣΤΗΣΗ ΤΩΝ ΣΠΕΡΜΑΤΩΝ Θερινό εξάμηνο 2011 ΣΠΕΡΜΑΤΟΦΥΤΑ Τα πιο διαδεδομένα είδη της γήινης βλάστησης βάση διατροφής
ΔΠΘ - Τμήμα Δασολογίας & Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων ΦΥΣΙΟΛΟΓΙΑ ΦΥΤΩΝ ΔΟΜΗ ΚΑΙ ΒΛΑΣΤΗΣΗ ΤΩΝ ΣΠΕΡΜΑΤΩΝ Θερινό εξάμηνο 2011 ΣΠΕΡΜΑΤΟΦΥΤΑ Τα πιο διαδεδομένα είδη της γήινης βλάστησης βάση διατροφής
Β. ΚΑΜΙΝΕΛΛΗΣ ΒΙΟΛΟΓΙΑ. Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα).
 ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
ΒΙΟΛΟΓΙΑ Είναι η επιστήμη που μελετά τους ζωντανούς οργανισμούς. (Αποτελούνται από ένα ή περισσότερα κύτταρα). Είδη οργανισμών Υπάρχουν δύο είδη οργανισμών: 1. Οι μονοκύτταροι, που ονομάζονται μικροοργανισμοί
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Αιωρήματα & Γαλακτώματα
 Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2014-15 Μάθημα 2ο 25 February 2015 Αιωρήματα Γαλακτώματα 1 Παρασκευή αιωρημάτων Οι μέθοδοι παρασκευής αιωρημάτων κατατάσσονται σε δύο μεγάλες κατηγορίες
Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2014-15 Μάθημα 2ο 25 February 2015 Αιωρήματα Γαλακτώματα 1 Παρασκευή αιωρημάτων Οι μέθοδοι παρασκευής αιωρημάτων κατατάσσονται σε δύο μεγάλες κατηγορίες
Τα χημικά στοιχεία που είναι επικρατέστερα στους οργανισμούς είναι: i..
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΚΑΤΑΛΥΤΙΚΗΣ ΑΝΑΓΩΓΗΣ ΝΙΤΡΙΚΩΝ ΚΑΙ ΝΙΤΡΩΔΩΝ ΙΟΝΤΩΝ ΣΕ ΝΕΡΟ ΜΕ ΧΡΗΣΗ ΥΔΡΟΓΟΝΟΥ
Εφαρμογές αρχών φαρμακολογίας
 Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1)Πώς το φαινόμενο Bohr επηρεάζει την πρόσδεση οξυγόνου στην αιμοσφαιρίνη; Που συνδέονται τα ιόντα
ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS
 ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS ΑΜΕΣΗ COOMBS Θεμελιώδες γνώρισμα του κάθε οργανισμού είναι ότι αναγνωρίζει τα κύτταρα των άλλων οργανισμών ως ξένα Αντιδρά με σκοπό την καταστροφή ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ
ΚΕΦΑΛΑΙΟ 5 ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ ΑΜΕΣΗ COOMBS ΑΜΕΣΗ COOMBS Θεμελιώδες γνώρισμα του κάθε οργανισμού είναι ότι αναγνωρίζει τα κύτταρα των άλλων οργανισμών ως ξένα Αντιδρά με σκοπό την καταστροφή ΑΝΟΣΟΑΙΜΑΤΟΛΟΓΙΑ
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 14 ο Νανοαισθητήρες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ Πανεπιστημίου
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 14 ο Νανοαισθητήρες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ) Απόφοιτος Βιολογίας, ΑΠΘ Διδάκτωρ Πανεπιστημίου
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΒΙΟΛΟΓΙΑ Β ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ
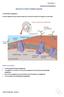 Οι Βιολογικές Μεμβράνες Είναι δυναμικές και όχι στατικές δομές που επιτελούν πολλές λειτουργίες στα κύτταρα. Πρέπει να γνωρίζετε Τη σύσταση βιολογικών μεμβρανών Τι προβλέπει το μοντέλο του ρευστού μωσαϊκού
Οι Βιολογικές Μεμβράνες Είναι δυναμικές και όχι στατικές δομές που επιτελούν πολλές λειτουργίες στα κύτταρα. Πρέπει να γνωρίζετε Τη σύσταση βιολογικών μεμβρανών Τι προβλέπει το μοντέλο του ρευστού μωσαϊκού
(dietary fiber, nonnutritive fiber)
 KΥΤΤΑΡΙΝΗ - ΦΥΤΙΚΕΣ ΙΝΕΣ Στα τρόφιμα, παράλληλα με τους υδατάνθρακες που πέπτονται στον ανθρώπινο οργανισμό (δηλαδή που υδρολύονται, απορροφώνται και μεταβολίζονται κατά τα γνωστά), υπάρχουν και υδατάνθρακες
KΥΤΤΑΡΙΝΗ - ΦΥΤΙΚΕΣ ΙΝΕΣ Στα τρόφιμα, παράλληλα με τους υδατάνθρακες που πέπτονται στον ανθρώπινο οργανισμό (δηλαδή που υδρολύονται, απορροφώνται και μεταβολίζονται κατά τα γνωστά), υπάρχουν και υδατάνθρακες
ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ ΠΡΟΪΟΝ
 Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ
Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Μεταπτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΑΡΤΕΜΙΣΙΝΙΝΗΣ ΜΕ ΑΙΜΙΝΗ ΚΑΙ ΑΙΜΑΤΙΝΗ ΜΕΣΩ ΦΑΣΜΑΤΟΣΚΟΠΙΑΣ ΥΠΕΡΥΘΡΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Μεταπτυχιακή διατριβή ΜΕΛΕΤΗ ΤΗΣ ΑΝΤΙΔΡΑΣΗΣ ΑΡΤΕΜΙΣΙΝΙΝΗΣ ΜΕ ΑΙΜΙΝΗ ΚΑΙ ΑΙΜΑΤΙΝΗ ΜΕΣΩ ΦΑΣΜΑΤΟΣΚΟΠΙΑΣ ΥΠΕΡΥΘΡΟΥ
πρωτεΐνες πολυμερείς ουσίες δομούν λειτουργούν λευκώματα 1.Απλές πρωτεΐνες 2.Σύνθετες πρωτεΐνες πρωτεΐδια μη πρωτεϊνικό μεταλλοπρωτεΐνες
 ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
Νανο-τεχνολογία. Νανο-Επιστήμη. Προσέγγιση από κάτω προς τα πάνω
 Νανο-τεχνολογία Ο σχεδιασμός, ο χαρακτηρισμός, η παραγωγή και η εφαρμογή των δομών, συσκευών και συστημάτων, ελέγχοντας τη μορφή και το μέγεθος σε κλίμακα νανόμετρου Νανο-Επιστήμη Η μελέτη των φαινομένων
Νανο-τεχνολογία Ο σχεδιασμός, ο χαρακτηρισμός, η παραγωγή και η εφαρμογή των δομών, συσκευών και συστημάτων, ελέγχοντας τη μορφή και το μέγεθος σε κλίμακα νανόμετρου Νανο-Επιστήμη Η μελέτη των φαινομένων
ΚΕΦΑΛΑΙΟ 8 ο...2 I. Εφαρµογές της βιοτεχνολογίας στην ιατρική...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 ΝΑ ΣΥΜΠΛΗΡΩΣΕΤΕ ΤΑ ΚΕΝΑ ΜΕ ΤΗΝ ΚΑΤΑΛΛΗΛΗ ΛΕΞΗ...
 ΚΕΦΑΛΑΙΟ 8 ο ΚΕΦΑΛΑΙΟ 8 ο...2 I. Εφαρµογές της βιοτεχνολογίας στην ιατρική...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 ΝΑ ΣΥΜΠΛΗΡΩΣΕΤΕ ΤΑ ΚΕΝΑ ΜΕ ΤΗΝ ΚΑΤΑΛΛΗΛΗ ΛΕΞΗ...10 1 ΚΕΦΑΛΑΙΟ 8 ο I. Εφαρµογές της βιοτεχνολογίας
ΚΕΦΑΛΑΙΟ 8 ο ΚΕΦΑΛΑΙΟ 8 ο...2 I. Εφαρµογές της βιοτεχνολογίας στην ιατρική...2 ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ...7 ΝΑ ΣΥΜΠΛΗΡΩΣΕΤΕ ΤΑ ΚΕΝΑ ΜΕ ΤΗΝ ΚΑΤΑΛΛΗΛΗ ΛΕΞΗ...10 1 ΚΕΦΑΛΑΙΟ 8 ο I. Εφαρµογές της βιοτεχνολογίας
Φλεγμονή. Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ
 Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
Νανοσωματίδια χρυσού για την στοχευμένη χορήγηση πακλιταξέλης σε καρκινικούς όγκους
 Πανεπιστήμιο Πατρών Τμήματα Χημείας, Ιατρικής και Φαρμακευτικής ΔΙΑΤΜΗΜΑΤΙΚΟ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «Ιατρική Χημεία: Σχεδιασμός και Ανάπτυξη Φαρμακευτικών Προϊόντων» ΜΕΤΑΠΤΥΧΙΑΚΗ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ
Πανεπιστήμιο Πατρών Τμήματα Χημείας, Ιατρικής και Φαρμακευτικής ΔΙΑΤΜΗΜΑΤΙΚΟ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «Ιατρική Χημεία: Σχεδιασμός και Ανάπτυξη Φαρμακευτικών Προϊόντων» ΜΕΤΑΠΤΥΧΙΑΚΗ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΣΥΜΒΟΛΗ ΤΟΥ ΤΕΧΝΗΤΟΥ ΘΗΛΑΣΜΟΥ ΣΤΗ ΔΙΑΤΡΟΦΗ ΤΩΝ ΑΜΝΩΝ ΦΥΛΗΣ ΧΙΟΥ ΓΙΑΝΝΟΣ ΜΑΚΡΗΣ Λεμεσός 2014 ii
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΣΥΜΒΟΛΗ ΤΟΥ ΤΕΧΝΗΤΟΥ ΘΗΛΑΣΜΟΥ ΣΤΗ ΔΙΑΤΡΟΦΗ ΤΩΝ ΑΜΝΩΝ ΦΥΛΗΣ ΧΙΟΥ ΓΙΑΝΝΟΣ ΜΑΚΡΗΣ Λεμεσός 2014 ii
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά
 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
Επιτροπάκη Ειρήνη. Xianghui Xu,Hui Yuan,Jing Chang,Bin He and Zhongwei Gu. Angew.Chem.Int.Ed. 2012,51,1-5
 Επιτροπάκη Ειρήνη ΑΜ:429 Xianghui Xu,Hui Yuan,Jing Chang,Bin He and Zhongwei Gu Angew.Chem.Int.Ed. 2012,51,1-5 Κατασκευή υπερμοριακών δομών με μεταφορικές λειτουργίες για χρήση σε ιατρικές εφαρμογές σε
Επιτροπάκη Ειρήνη ΑΜ:429 Xianghui Xu,Hui Yuan,Jing Chang,Bin He and Zhongwei Gu Angew.Chem.Int.Ed. 2012,51,1-5 Κατασκευή υπερμοριακών δομών με μεταφορικές λειτουργίες για χρήση σε ιατρικές εφαρμογές σε
ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΚΠΑ ΑΚ. ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ
 ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΚΠΑ ΑΚ. ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ 1. Να αναφερθούν οι μηχανισμοί αναφοράς μικρών μορίων από το εξωκυττάριο περιβάλλον στο εσωτερικό του κυττάρου. 2. Ποιος
ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΦΑΡΜΑΚΕΥΤΙΚΗΣ ΕΚΠΑ ΑΚ. ΕΤΟΥΣ 2015-2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ 1. Να αναφερθούν οι μηχανισμοί αναφοράς μικρών μορίων από το εξωκυττάριο περιβάλλον στο εσωτερικό του κυττάρου. 2. Ποιος
Προεκλαμψία. Έγκαιρη εκτίμηση κινδύνου στις 11 13+6 εβδομάδες
 Προεκλαμψία Έγκαιρη εκτίμηση κινδύνου στις 11 13+6 εβδομάδες Ο έλεγχος για προεκλαμψία μεταξύ των εβδομάδων 11 έως 13+6 μπορεί να εντοπίσει κυήσεις υψηλού κινδύνου, επιτρέποντας τη θεραπεία με α σπιρίνη
Προεκλαμψία Έγκαιρη εκτίμηση κινδύνου στις 11 13+6 εβδομάδες Ο έλεγχος για προεκλαμψία μεταξύ των εβδομάδων 11 έως 13+6 μπορεί να εντοπίσει κυήσεις υψηλού κινδύνου, επιτρέποντας τη θεραπεία με α σπιρίνη
Εργασία για το μάθημα της Βιολογίας. Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου
 Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
Εργασία για το μάθημα της Βιολογίας Περίληψη πάνω στο κεφάλαιο 3 του σχολικού βιβλίου Στο 3 ο κεφάλαιο του βιβλίου η συγγραφική ομάδα πραγματεύεται την ενέργεια και την σχέση που έχει αυτή με τους οργανισμούς
Ραδιοεπισηµασµένα Πεπτίδια στην Ογκολογία
 Ραδιοεπισηµασµένα Πεπτίδια στην Ογκολογία Θεοδοσία Μάϊνα Berthold ock Εργαστήριο Ραδιοφαρµάκων Ινστιτούτο Ραδιοϊσοτόπων - Ραδιοδιαγνωστικών Προϊόντων, ΕΚΕΦΕ «ηµόκριτος», Αθήνα Στόχευση µε ραδιοπεπτίδια
Ραδιοεπισηµασµένα Πεπτίδια στην Ογκολογία Θεοδοσία Μάϊνα Berthold ock Εργαστήριο Ραδιοφαρµάκων Ινστιτούτο Ραδιοϊσοτόπων - Ραδιοδιαγνωστικών Προϊόντων, ΕΚΕΦΕ «ηµόκριτος», Αθήνα Στόχευση µε ραδιοπεπτίδια
ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ ΙΟΥΝΙΟΥ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ ΜΑΘΗΜΑ : ΒΙΟΛΟΓΙΑ ΤΑΞΗ: Β ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ:
 ΛΥΚΕΙΟ ΑΡΑΔΙΠΠΟΥ «ΤΑΣΟΣ ΜΗΤΣΟΠΟΥΛΟΣ» ΕΠΩΝΥΜΟ:... ΟΝΟΜΑ:.. ΒΑΘΜΟΣ:... ΟΛΟΓΡΑΦΩΣ: TMHMA: ΑΡΙΘΜΟΣ:.... ΥΠΟΓΡΑΦΗ:.... ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ ΙΟΥΝΙΟΥ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2017-2018 ΜΑΘΗΜΑ : ΒΙΟΛΟΓΙΑ
ΛΥΚΕΙΟ ΑΡΑΔΙΠΠΟΥ «ΤΑΣΟΣ ΜΗΤΣΟΠΟΥΛΟΣ» ΕΠΩΝΥΜΟ:... ΟΝΟΜΑ:.. ΒΑΘΜΟΣ:... ΟΛΟΓΡΑΦΩΣ: TMHMA: ΑΡΙΘΜΟΣ:.... ΥΠΟΓΡΑΦΗ:.... ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΜΑΪΟΥ ΙΟΥΝΙΟΥ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2017-2018 ΜΑΘΗΜΑ : ΒΙΟΛΟΓΙΑ
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ
 ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ. Πετρολιάγκης Σταμάτης Τμήμα Γ4
 ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Πετρολιάγκης Σταμάτης Τμήμα Γ4 ΕΝΝΟΙΑ ΤΗΣ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Η κυτταρική μεμβράνη ή πλασματική μεμβράνη είναι η εξωτερική μεμβράνη που περιβάλλει το κύτταρο
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Πετρολιάγκης Σταμάτης Τμήμα Γ4 ΕΝΝΟΙΑ ΤΗΣ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Η κυτταρική μεμβράνη ή πλασματική μεμβράνη είναι η εξωτερική μεμβράνη που περιβάλλει το κύτταρο
Οι περισσότεροι μονοτοιχωματικοί νανοσωλήνες έχουν διάμετρο περί του 1 νανομέτρου (υπενθυμίζεται ότι 1nm = 10 Å).
 1 2 Οι περισσότεροι μονοτοιχωματικοί νανοσωλήνες έχουν διάμετρο περί του 1 νανομέτρου (υπενθυμίζεται ότι 1nm = 10 Å). Οι πολυτοιχωματικοί νανοσωλήνες άνθρακα αποτελούνται από δύο ή περισσότερους ομοαξονικούς
1 2 Οι περισσότεροι μονοτοιχωματικοί νανοσωλήνες έχουν διάμετρο περί του 1 νανομέτρου (υπενθυμίζεται ότι 1nm = 10 Å). Οι πολυτοιχωματικοί νανοσωλήνες άνθρακα αποτελούνται από δύο ή περισσότερους ομοαξονικούς
Λόγοι έκδοσης γνώμης για τον χαρακτηρισμό φαρμακευτικού προϊόντος ως ορφανού
 Παράρτημα 1 Λόγοι έκδοσης γνώμης για τον χαρακτηρισμό φαρμακευτικού προϊόντος ως ορφανού Η Επιτροπή Ορφανών Φαρμάκων (COMP), έχοντας εξετάσει την αίτηση, κατέληξε στα ακόλουθα: Σύμφωνα με το άρθρο 3 παράγραφος
Παράρτημα 1 Λόγοι έκδοσης γνώμης για τον χαρακτηρισμό φαρμακευτικού προϊόντος ως ορφανού Η Επιτροπή Ορφανών Φαρμάκων (COMP), έχοντας εξετάσει την αίτηση, κατέληξε στα ακόλουθα: Σύμφωνα με το άρθρο 3 παράγραφος
Αιωρήματα & Γαλακτώματα
 Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2015-16 Μάθημα 9ο 5 May 2017 Αιωρήματα Γαλακτώματα 1 Στρατηγική δοσολογίας (Για άλατα μετάλλων τα οποία υδρολύονται ) Περιοχές δραστικότητας: Περιοχή 1:
Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2015-16 Μάθημα 9ο 5 May 2017 Αιωρήματα Γαλακτώματα 1 Στρατηγική δοσολογίας (Για άλατα μετάλλων τα οποία υδρολύονται ) Περιοχές δραστικότητας: Περιοχή 1:
ΑΝΑΠΤΥΞΗ ΠΡΟΧΩΡΗΜΕΝΩΝ ΟΞΕΙΔΩΤΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΓΙΑ ΤΗΝ ΑΠΟΜΑΚΡΥΝΣΗ ΟΡΓΑΝΙΚΩΝ ΤΟΞΙΚΩΝ 0ΥΣΙΩΝ ΣΕ ΥΔΑΤΙΚΑ ΣΥΣΤΗΜΑΤΑ ΑΛΕΞΡΙΑ Ε.
 ΑΝΑΠΤΥΞΗ ΠΡΟΧΩΡΗΜΕΝΩΝ ΟΞΕΙΔΩΤΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΓΙΑ ΤΗΝ ΑΠΟΜΑΚΡΥΝΣΗ ΟΡΓΑΝΙΚΩΝ ΤΟΞΙΚΩΝ 0ΥΣΙΩΝ ΣΕ ΥΔΑΤΙΚΑ ΣΥΣΤΗΜΑΤΑ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΑΛΕΞΡΙΑ Ε. ΒΥΜΙΩΤΗ ΠΕΡΙΛΗΨΗ Σκοπός της παρούσας διατριβής είναι η μελέτη
ΑΝΑΠΤΥΞΗ ΠΡΟΧΩΡΗΜΕΝΩΝ ΟΞΕΙΔΩΤΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΓΙΑ ΤΗΝ ΑΠΟΜΑΚΡΥΝΣΗ ΟΡΓΑΝΙΚΩΝ ΤΟΞΙΚΩΝ 0ΥΣΙΩΝ ΣΕ ΥΔΑΤΙΚΑ ΣΥΣΤΗΜΑΤΑ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΑΛΕΞΡΙΑ Ε. ΒΥΜΙΩΤΗ ΠΕΡΙΛΗΨΗ Σκοπός της παρούσας διατριβής είναι η μελέτη
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου. Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση:
 KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
ΘΕΡΜΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ
 ΘΕΡΜΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ ΓENIKA Θερµική κατεργασία είναι σύνολο διεργασιών που περιλαµβάνει τη θέρµανση και ψύξη µεταλλικού προϊόντος σε στερεά κατάσταση και σε καθορισµένες θερµοκρασιακές και χρονικές συνθήκες.
ΘΕΡΜΙΚΕΣ ΚΑΤΕΡΓΑΣΙΕΣ ΓENIKA Θερµική κατεργασία είναι σύνολο διεργασιών που περιλαµβάνει τη θέρµανση και ψύξη µεταλλικού προϊόντος σε στερεά κατάσταση και σε καθορισµένες θερµοκρασιακές και χρονικές συνθήκες.
ΜΟΡΦΟΠΟΙΗΣΗ ΜΕ ΤΕΧΝΙΚΕΣ ΚΟΝΙΟΜΕΤΑΛΛΟΥΡΓΙΑΣ
 ΜΟΡΦΟΠΟΙΗΣΗ ΜΕ ΤΕΧΝΙΚΕΣ ΚΟΝΙΟΜΕΤΑΛΛΟΥΡΓΙΑΣ Η πρώτη ύλη με τη μορφή σωματιδίων (κόνεως) μορφοποιείται μέσα σε καλούπια, με μηχανισμό που οδηγεί σε δομική διασύνδεση των σωματιδίων με πρόσδοση θερμότητας.
ΜΟΡΦΟΠΟΙΗΣΗ ΜΕ ΤΕΧΝΙΚΕΣ ΚΟΝΙΟΜΕΤΑΛΛΟΥΡΓΙΑΣ Η πρώτη ύλη με τη μορφή σωματιδίων (κόνεως) μορφοποιείται μέσα σε καλούπια, με μηχανισμό που οδηγεί σε δομική διασύνδεση των σωματιδίων με πρόσδοση θερμότητας.
IΣTOΛOΓIA. Tα δείγµατα του βιολογικού υλικού λαµβάνονται µε > βελόνες ενδοσκοπικούς σωλήνες εύκαµπτους καθετήρες
 IΣTOΛOΓIA H ιστολογία κλάδος της ιατρικής που µελετά > υφή βιολογικού υλικού και τους τρόπους που τα επιµέρους συστατικά στοιχεία σχετίζονται µεταξύ τους δοµικά & λειτουργικά Tα δείγµατα του βιολογικού
IΣTOΛOΓIA H ιστολογία κλάδος της ιατρικής που µελετά > υφή βιολογικού υλικού και τους τρόπους που τα επιµέρους συστατικά στοιχεία σχετίζονται µεταξύ τους δοµικά & λειτουργικά Tα δείγµατα του βιολογικού
ΜΕΘΟΔΟΙ ΑΠΟΛΥΜΑΝΣΗΣ ΑΝΑΚΥΚΛΟΥΜΕΝΟΥ ΘΡΕΠΤΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΑΠΟΡΡΟΗΣ
 ΜΕΘΟΔΟΙ ΑΠΟΛΥΜΑΝΣΗΣ ΑΝΑΚΥΚΛΟΥΜΕΝΟΥ ΘΡΕΠΤΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΑΠΟΡΡΟΗΣ Σχηματική απεικόνιση κλειστού συστήματος Παστερίωση μέσω θέρμανσης Πλεονεκτήματα Πολύ αποτελεσματικό έναντι όλων των παθογόνων. Σχετικά
ΜΕΘΟΔΟΙ ΑΠΟΛΥΜΑΝΣΗΣ ΑΝΑΚΥΚΛΟΥΜΕΝΟΥ ΘΡΕΠΤΙΚΟΥ ΔΙΑΛΥΜΑΤΟΣ ΑΠΟΡΡΟΗΣ Σχηματική απεικόνιση κλειστού συστήματος Παστερίωση μέσω θέρμανσης Πλεονεκτήματα Πολύ αποτελεσματικό έναντι όλων των παθογόνων. Σχετικά
Κολοκυθάς Ντούκας Αργύρης Α.Μ. 63
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΤΩΝ ΥΛΙΚΩΝ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ ΜΕΤΑΠΤΥΧΙΑΚΗΣ ΕΙΔΙΚΕΥΣΗΣ Μελέτη των Αλληλεπιδράσεων και των Ιδιοτήτων Μαγνητικών Νανοκρυσταλλιτών Πυκνής Διάταξης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΤΩΝ ΥΛΙΚΩΝ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ ΜΕΤΑΠΤΥΧΙΑΚΗΣ ΕΙΔΙΚΕΥΣΗΣ Μελέτη των Αλληλεπιδράσεων και των Ιδιοτήτων Μαγνητικών Νανοκρυσταλλιτών Πυκνής Διάταξης
TERMS USED IN STANDARDIZAfiON OF CHEMICAL FOOD ANALYSIS SUMMARY
 ΑΠΟΔΟΣΗ ΞΕΝΟΓΛΩΣΣΩΝ ΟΡΩΝ ΚΑΤΑ ΤΗΝ ΤΥΠΟΠΟΙΗΣΗ ΤΗΣ ΟΡΟΛΟΓΙΑΣ ΧΗΜΙΚΩΝ ΑΝΑΛΥΣΕΩΝ ΤΡΟΦΙΜΩΝ Τεχνική Επιτροπή ΕΛΟΤ 85 "Τρόφιμα", Κ. Τζιά, I. Σαριδάκης ΠΕΡΙΛΗΨΗ Το αντικείμενο της εργασίας είναι η απόδοση των
ΑΠΟΔΟΣΗ ΞΕΝΟΓΛΩΣΣΩΝ ΟΡΩΝ ΚΑΤΑ ΤΗΝ ΤΥΠΟΠΟΙΗΣΗ ΤΗΣ ΟΡΟΛΟΓΙΑΣ ΧΗΜΙΚΩΝ ΑΝΑΛΥΣΕΩΝ ΤΡΟΦΙΜΩΝ Τεχνική Επιτροπή ΕΛΟΤ 85 "Τρόφιμα", Κ. Τζιά, I. Σαριδάκης ΠΕΡΙΛΗΨΗ Το αντικείμενο της εργασίας είναι η απόδοση των
ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ - ΜΕΡΟΣ Α. Ο ηλεκτρονικός υπολογιστής του οργανισμού μας
 ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ - ΜΕΡΟΣ Α Ο ηλεκτρονικός υπολογιστής του οργανισμού μας Ρόλος του νευρικού συστήματος Το νευρικό σύστημα (Ν.Σ.) ελέγχει, ρυθμίζει και συντονίζει όλες τις λειτουργίες του οργανισμού ανάλογα
ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ - ΜΕΡΟΣ Α Ο ηλεκτρονικός υπολογιστής του οργανισμού μας Ρόλος του νευρικού συστήματος Το νευρικό σύστημα (Ν.Σ.) ελέγχει, ρυθμίζει και συντονίζει όλες τις λειτουργίες του οργανισμού ανάλογα
3.2 ΕΝΖΥΜΑ ΒΙΟΛΟΓΙΚΟΙ ΚΑΤΑΛΥΤΕΣ
 ΠΕΡΙΛΗΨΗ ΣΤΟ 3 Ο ΚΕΦΑΛΑΙΟ: ΜΕΤΑΒΟΛΙΣΜΟΣ ΚΥΡΙΑΚΟΣ Γ. Β1 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί
ΠΕΡΙΛΗΨΗ ΣΤΟ 3 Ο ΚΕΦΑΛΑΙΟ: ΜΕΤΑΒΟΛΙΣΜΟΣ ΚΥΡΙΑΚΟΣ Γ. Β1 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί
να ταράξουν την λειτουργία των ιστών και των οργάνων του; α. τη θέση τους στο ανθρώπινο σώμα β. την γενικευμένη ή εξειδικευμένη δράση
 Ερωτήσεις κατανόησης της θεωρίας του 1 ο κεφαλαίου (συνέχεια) 1. Από τι εξαρτάται η επιβίωση του ανθρώπου και ποιοι εξωτερικοί παράγοντες θα μπορούσαν να ταράξουν την λειτουργία των ιστών και των οργάνων
Ερωτήσεις κατανόησης της θεωρίας του 1 ο κεφαλαίου (συνέχεια) 1. Από τι εξαρτάται η επιβίωση του ανθρώπου και ποιοι εξωτερικοί παράγοντες θα μπορούσαν να ταράξουν την λειτουργία των ιστών και των οργάνων
διατήρησης της μάζας.
 6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ ΦΑΡΜΑΚΟΔΥΝΑΜΙΚΗ
 αλληλεπιδράσεις μεταξύ χημικών ουσιών και ζώντων οργανισμών) ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Διακίνηση του φαρμάκου στον οργανισμό ΦΑΡΜΑΚΟΔΥΝΑΜΙΚΗ Μηχανισμό δράσης Βιοχημικές δράσεις Φυσιολογικές δράσεις η φυσιολογική
αλληλεπιδράσεις μεταξύ χημικών ουσιών και ζώντων οργανισμών) ΦΑΡΜΑΚΟΚΙΝΗΤΙΚΗ Διακίνηση του φαρμάκου στον οργανισμό ΦΑΡΜΑΚΟΔΥΝΑΜΙΚΗ Μηχανισμό δράσης Βιοχημικές δράσεις Φυσιολογικές δράσεις η φυσιολογική
Η Φυσική των ζωντανών Οργανισμών (10 μονάδες)
 Η Φυσική των ζωντανών Οργανισμών (10 μονάδες) Δεδομένα: Κανονική Ατμοσφαιρική Πίεση, P 0 = 1.013 10 5 Pa = 760 mmhg Μέρος A. Η φυσική του κυκλοφορικού συστήματος. (4.5 μονάδες) Q3-1 Στο Μέρος αυτό θα μελετήσετε
Η Φυσική των ζωντανών Οργανισμών (10 μονάδες) Δεδομένα: Κανονική Ατμοσφαιρική Πίεση, P 0 = 1.013 10 5 Pa = 760 mmhg Μέρος A. Η φυσική του κυκλοφορικού συστήματος. (4.5 μονάδες) Q3-1 Στο Μέρος αυτό θα μελετήσετε
Autonomous movement of platinum-loaded stomatocytes
 Autonomous movement of platinum-loaded stomatocytes Daniela A. Wilson, Roeland J. M. Nolte and Jan C. M. van Hest, NATURE CHEMISTRY, advance paper ΓΙΩΡΓΟΣ ΦΡΑΓΚΙΑΔΑΚΗΣ 364 ΣΤΟΧΟΣ Στη φύση υπάρχει μια συνεχής
Autonomous movement of platinum-loaded stomatocytes Daniela A. Wilson, Roeland J. M. Nolte and Jan C. M. van Hest, NATURE CHEMISTRY, advance paper ΓΙΩΡΓΟΣ ΦΡΑΓΚΙΑΔΑΚΗΣ 364 ΣΤΟΧΟΣ Στη φύση υπάρχει μια συνεχής
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 10 η : Χημική κινητική. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 10 η : Χημική κινητική Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ταχύτητες Αντίδρασης 2 Ως ταχύτητα αντίδρασης ορίζεται είτε η αύξηση
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 10 η : Χημική κινητική Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ταχύτητες Αντίδρασης 2 Ως ταχύτητα αντίδρασης ορίζεται είτε η αύξηση
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β
 ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ Η άσκηση, επιφέρει ευεργετικά αποτελέσματα στα διάφορα συστήματα του οργανισμού. Τα αποτελέσματα αυτά ενδέχεται να είναι παροδικά ή μόνιμα ανάλογα
ΠΩΣ ΕΠΙΔΡΑ Η ΑΣΚΗΣΗ ΣΤΑ ΔΙΑΦΟΡΑ ΣΥΣΤΗΜΑΤΑ ΤΟΥ ΟΡΓΑΝΙΣΜΟΥ Η άσκηση, επιφέρει ευεργετικά αποτελέσματα στα διάφορα συστήματα του οργανισμού. Τα αποτελέσματα αυτά ενδέχεται να είναι παροδικά ή μόνιμα ανάλογα
O Νοσηλευτής στο νεφρολογικό τμήμα
 O Νοσηλευτής στο νεφρολογικό τμήμα ΚΟΙΝΟΒΙΑΡΧΟΥ ΕΥΓΕΝΙΑ ΜSc, Ειδική νοσηλεύτρια Ψυχικής Υγείας Α/α Προϊσταμένη Νεφρολογικού Τμήματος, Γ.Ν.Θ. ΠΑΠΑΓΕΩΡΓΙΟΥ Νεφρολογικό τμήμα και μέθοδοι αιμαφαίρεσης 16/10/2018
O Νοσηλευτής στο νεφρολογικό τμήμα ΚΟΙΝΟΒΙΑΡΧΟΥ ΕΥΓΕΝΙΑ ΜSc, Ειδική νοσηλεύτρια Ψυχικής Υγείας Α/α Προϊσταμένη Νεφρολογικού Τμήματος, Γ.Ν.Θ. ΠΑΠΑΓΕΩΡΓΙΟΥ Νεφρολογικό τμήμα και μέθοδοι αιμαφαίρεσης 16/10/2018
3 η Ημερίδα του Δ.Π.Μ.Σ. «Ιατρική Χημεία»
 3 η Ημερίδα του Δ.Π.Μ.Σ. «Ιατρική Χημεία» Πέμπτη, 15 Φεβρουαρίου, 2018 Συνεδριακό κέντρο «Κάρολος Παπούλιας» Πανεπιστημίου Ιωαννίνων Υπό την Αιγίδα της Περιφέρειας Ηπείρου Επιστημονικό πρόγραμμα 11.00-11.45
3 η Ημερίδα του Δ.Π.Μ.Σ. «Ιατρική Χημεία» Πέμπτη, 15 Φεβρουαρίου, 2018 Συνεδριακό κέντρο «Κάρολος Παπούλιας» Πανεπιστημίου Ιωαννίνων Υπό την Αιγίδα της Περιφέρειας Ηπείρου Επιστημονικό πρόγραμμα 11.00-11.45
Βιοϋλικά. Ενότητα 8: Ιδιότητες Βιοϋλικών Δοκιμές Βιοσυμβατότητας. Ελευθέριος Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών
 Βιοϋλικά Ενότητα 8: Ιδιότητες Βιοϋλικών Δοκιμές Βιοσυμβατότητας Ελευθέριος Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περιεχόμενα ενότητας Νανοσωματίδια Ορισμός Μέθοδοι παρασκευής Ιδιαιτερότητες
Βιοϋλικά Ενότητα 8: Ιδιότητες Βιοϋλικών Δοκιμές Βιοσυμβατότητας Ελευθέριος Αμανατίδης Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Περιεχόμενα ενότητας Νανοσωματίδια Ορισμός Μέθοδοι παρασκευής Ιδιαιτερότητες
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η ΣΥΓΚΕΝΤΡΩΣΗ ΤΩΝ ΒΑΡΕΩΝ ΜΕΤΑΛΛΩΝ ΣΤΟ ΕΔΑΦΟΣ ΚΑΙ ΜΕΘΟΔΟΙ ΠΡΟΣΔΙΟΡΙΣΜΟΥ ΤΟΥΣ Μιχαήλ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΕΠΙΣΤΗΜΗΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η ΣΥΓΚΕΝΤΡΩΣΗ ΤΩΝ ΒΑΡΕΩΝ ΜΕΤΑΛΛΩΝ ΣΤΟ ΕΔΑΦΟΣ ΚΑΙ ΜΕΘΟΔΟΙ ΠΡΟΣΔΙΟΡΙΣΜΟΥ ΤΟΥΣ Μιχαήλ
Από πού προέρχεται η θερμότητα που μεταφέρεται από τον αντιστάτη στο περιβάλλον;
 3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής
 1 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής Μικροσκοπικοί οργανισμοί που ρυθμίζουν τη λειτουργία του ανθρώπινου σώματος σε
1 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Κεφάλαιο 7 - Ένζυμα, οι μηχανισμοί της ζωής Μικροσκοπικοί οργανισμοί που ρυθμίζουν τη λειτουργία του ανθρώπινου σώματος σε
Μικροενθυλάκωση βιοδραστικών ουσιών. Ειρήνη Στρατή
 Μικροενθυλάκωση βιοδραστικών ουσιών Ειρήνη Στρατή Μικροενθυλάκωση (microencapsulation) Τεχνική κατά την οποία μια ουσία ή μίγμα ουσιών, περιβάλλεται από ένα άλλο υλικό, το οποίο ονομάζεται μέσο εγκλεισμού,
Μικροενθυλάκωση βιοδραστικών ουσιών Ειρήνη Στρατή Μικροενθυλάκωση (microencapsulation) Τεχνική κατά την οποία μια ουσία ή μίγμα ουσιών, περιβάλλεται από ένα άλλο υλικό, το οποίο ονομάζεται μέσο εγκλεισμού,
Οδοντικά Εμφυτεύματα
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Οδοντικά Εμφυτεύματα Ενότητα 4: Mικροδιεργασίες Επούλωσης Γεώργιος Μακρής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Οδοντικά Εμφυτεύματα Ενότητα 4: Mικροδιεργασίες Επούλωσης Γεώργιος Μακρής Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Πτυχιακή διατριβή. Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN) στην ατμόσφαιρα
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN)
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN)
Το BCS επιδιώκει την ταξινόμηση των δραστικών συστατικών με βάση. τη διαπερατότητα τους διαμέσου της μεμβράνης του ΓΕ σωλήνα.
 ΕΘΝΙΚΟΣ ΟΡΓΑΝΙΣΜΟΣ ΦΑΡΜΑΚΩΝ Η νέα κατευθυντήρια οδηγία που αφορά σε μελέτες βιοϊσοδυναμίας: Νομικό πλαίσιο Ευρωπαϊκή πραγματικότητα Εξελίξεις BCS B ASED BIOWAIVER Λήδα Καλαντζή, Φαρμακοποιός MSc. PhD ΥΠΟΥΡΓΕΙΟ
ΕΘΝΙΚΟΣ ΟΡΓΑΝΙΣΜΟΣ ΦΑΡΜΑΚΩΝ Η νέα κατευθυντήρια οδηγία που αφορά σε μελέτες βιοϊσοδυναμίας: Νομικό πλαίσιο Ευρωπαϊκή πραγματικότητα Εξελίξεις BCS B ASED BIOWAIVER Λήδα Καλαντζή, Φαρμακοποιός MSc. PhD ΥΠΟΥΡΓΕΙΟ
Διδάσκων: Καθ. Αλέξανδρος Ρήγας Εξάμηνο: 9 ο
 Δημοκρίτειο Πανεπιστήμιο Θράκης Τμήμα Ηλεκτρολόγων Μηχανικών & Μηχανικών Υπολογιστών Τομέας Τηλεπικοινωνιών και Διαστημικής Εργαστήριο Ηλεκτρομαγνητικής Θεωρίας Διδάσκων: Καθ. Αλέξανδρος Ρήγας Εξάμηνο:
Δημοκρίτειο Πανεπιστήμιο Θράκης Τμήμα Ηλεκτρολόγων Μηχανικών & Μηχανικών Υπολογιστών Τομέας Τηλεπικοινωνιών και Διαστημικής Εργαστήριο Ηλεκτρομαγνητικής Θεωρίας Διδάσκων: Καθ. Αλέξανδρος Ρήγας Εξάμηνο:
Ο ΡΟΛΟΣ ΤΟΥ ΝΟΣΗΛΕΥΤΗ ΣΤΗ ΜΕΙΩΣΗ ΤΩΝ ΕΠΑΝΕΙΣΑΓΩΓΩΝ ΣΤΗΝ ΚΑΡΔΙΑΚΗ ΑΝΕΠΑΡΚΕΙΑ
 Ο ΡΟΛΟΣ ΤΟΥ ΝΟΣΗΛΕΥΤΗ ΣΤΗ ΜΕΙΩΣΗ ΤΩΝ ΕΠΑΝΕΙΣΑΓΩΓΩΝ ΣΤΗΝ ΚΑΡΔΙΑΚΗ ΑΝΕΠΑΡΚΕΙΑ Η Καρδιακή Ανεπάρκεια(ΚΑ) είναι ένα πολύπλοκο, προοδευτικά εξελισσόμενο σύνδρομο κλινικών, αιμοδυναμικών και νευροορμονικών διαταραχών
Ο ΡΟΛΟΣ ΤΟΥ ΝΟΣΗΛΕΥΤΗ ΣΤΗ ΜΕΙΩΣΗ ΤΩΝ ΕΠΑΝΕΙΣΑΓΩΓΩΝ ΣΤΗΝ ΚΑΡΔΙΑΚΗ ΑΝΕΠΑΡΚΕΙΑ Η Καρδιακή Ανεπάρκεια(ΚΑ) είναι ένα πολύπλοκο, προοδευτικά εξελισσόμενο σύνδρομο κλινικών, αιμοδυναμικών και νευροορμονικών διαταραχών
Αποστείρωση και στειρότητα φαρμακευτικών προϊόντων
 Αποστείρωση και στειρότητα φαρμακευτικών προϊόντων Ιωάννης Τσαγκατάκης, Ph.D. Η αποστείρωση είναι μια διαδικασία κατά την οποία επιτυγχάνεται ο θάνατος ολόκληρου του μικροβιακού φορτίου που πιθανόν να
Αποστείρωση και στειρότητα φαρμακευτικών προϊόντων Ιωάννης Τσαγκατάκης, Ph.D. Η αποστείρωση είναι μια διαδικασία κατά την οποία επιτυγχάνεται ο θάνατος ολόκληρου του μικροβιακού φορτίου που πιθανόν να
