ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΗΝ ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ
|
|
|
- Πάρις Μπλέτσας
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΗΝ ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΠΟΛΥΜΕΡΩΝ "ΦΥΣΙΚΑ ΠΗΚΤΩΜΑΤΑ ΣΥΜΠΟΛΥΜΕΡΩΝ ΚΑΤΑ ΣΥΣΤΑΔΕΣ ΠΟΛΥΣΤΥΡΟΛΙΟΥ (PS)/ ΠΟΛΥΑΙΘΥΛΕΝΟΞΕΙΔΙΟΥ (PEO) ΣΕ ΙΟΝΙΚΑ ΥΓΡΑ" ΜΕΤΑΠΤΥΧΙΑΚΟ ΔΙΠΛΩΜΑ ΣΤΗΝ ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΩΝ ΠΟΛΥΜΕΡΩΝ ΤΗΣ ΓΚΕΡΜΠΟΥΡΑ ΣΑΝΔΡΑΣ ΕΠΙΒΛΕΠΩΝ: ΤΣΙΤΣΙΛΙΑΝΗΣ ΚΩΝΣΤΑΝΤΙΝΟΣ Καθηγητής Τμήματος Χημικών Μηχανικών Πανεπιστημίου Πατρών ΠΑΤΡΑ 2012
2 ΠΡΟΛΟΓΟΣ Η παρούσα μεταπτυχιακή εργασία εκπονήθηκε στο εργαστήριο Μακρομοριακής Μηχανικής του τμήματος Χημικών Μηχανικών του Πανεπιστημίου Πατρών, στα πλαίσια του Διατμηματικού Προγράμματος Μεταπτυχιακών Σπουδών στην "Επιστήμη και Τεχνολογία Πολυμερών". Ευχαριστώ θερμά τον επιβλέποντα Καθηγητή του Τμήματος Χημικών Μηχανικών κ. Κ. Τσιτσιλιάνη για την καθοδήγηση και τις συμβουλές που μου προσέφερε καθ όλη τη διάρκεια της ολοκλήρωσης της εργασίας. Ευχαριστώ ιδιαίτερα την μεταδιδάκτορα Ζαχαρούλα Ιατρίδη για την υποστήριξη και τις συμβουλές της κατά την διεξαγωγή των πειραμάτων, αλλά και την πολύτιμη βοήθειά της στην διαμόρφωση της παρούσας εργασίας. Επίσης, θα ήθελα να πω ένα μεγάλο ευχαριστώ στην υποψήφια διδάκτορα Maria-Teodora Popescu για τις συμβουλές της, τις συζητήσεις μας και τη συμπαραστασή της που μου παρείχε σε όλη τη διάρκεια αυτής της προσπάθειας. Θα ήταν παράλειψη να μην ευχαριστήσω και τους υπόλοιπους συναδέλφους στο εργαστήριο για την συμπαράσταση και το ευχάριστο κλίμα που δημιούργησαν. Τέλος, θέλω να ευχαριστήσω ιδιαίτερα την οικογένειά μου για την ηθική και ψυχολογική υποστήριξη που μου παρείχε.
3 ΠΕΡΙΕΧΟΜΕΝΑ ΠΕΡΙΛΗΨΗ...I ABSTRACT.II ΕΙΣΑΓΩΓΗ... 1 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ Η ΜΙΚΡΟΔΟΜΗ ΤΩΝ ΠΟΛΥΜΕΡΩΝ-ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ ΚΑΤΑΣΥΣΤΑΔΕΣ ΣΥΜΠΟΛΥΜΕΡΗ (BLOCΚ COPOLYMERS) ΠΗΚΤΩΜΑΤΑ ΔΙΑΔΙΚΑΣΙΑ ΔΗΜΙΟΥΡΓΙΑΣ ΠΗΚΤΩΜΑΤΟΣ ΙΟΝΤΙΚΑ ΥΓΡΑ-"ΠΡΑΣΙΝΟΙ ΔΙΑΛΥΤΕΣ" ΔΙΣΥΣΤΑΔΙΚΑ ΣΥΜΠΟΛΥΜΕΡΗ ΔΙΑΛΥΜΑΤΑ ΣΕ ΙΟΝΤΙΚΑ ΥΓΡΑ ΤΡΙΣΥΣΤΑΔΙΚΑ ΣΥΜΠΟΛΥΜΕΡΗ (ΑΒΑ) ΣΕ ΙΟΝΤΙΚΟ ΔΙΑΛΥΤΗ ΒΙΒΛΙΟΓΡΑΦΙΑ 31 ΚΕΦΑΛΑΙΟ ΧΡΩΜΑΤΟΦΡΑΓΙΑ ΑΠΟΚΛΕΙΣΜΟΥ ΜΕΓΕΘΩΝ (SEC) ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΠΥΡΗΝΙΚΟΥ ΜΑΓΝΗΤΙΚΟΥ ΣΥΝΤΟΝΙΣΜΟΥ (NUCLEAR MAGNETIC RESONANCE SPECTROSOPY, NMR) ΔΥΝΑΜΙΚΗ ΣΚΕΔΑΣΗ ΦΩΤΟΣ (DYNAMIC LIGHT SCATTERING) AMVn MICROVISCOMETER ΡΕΟΛΟΓΙΑ Εισαγωγή Ιξώδες και Ιξωδοελαστική Συμπεριφορά Γραμμική Ιξωδοελαστικότητα Μοντέλο Maxwell Μοντέλο Voight (Kelvin) Γενικό Γραμμικό Ιξωδοελαστικό Μοντέλο Ρεολογικά Πειράματα Στην Γραμμική Ιξωδοελαστικότητα Ερπυσμός (Creep) Δυναμική Φόρτιση (Sinuisoidal Oscillations) Τύποι Ρεομέτρων Ρεόμετρο Ελέγχου Τάσης (Stress Control Rheometer) Γεωμετρία Κώνου-Πλάκας (Cone-Plate Geometry)... 53
4 2.7 ΒΙΒΛΙΟΓΡΑΦΙΑ ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΕΙΣΑΓΩΓΗ ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΤΟΥ PEO-PS-PEO ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΠΥΡΗΝΙΚΟΥ ΜΑΓΝΗΤΙΚΟΥ ΣΥΝΤΟΝΙΣΜΟΥ (NMR) ΥΛΙΚΑ ΠΑΡΑΣΚΕΥΗ ΔΕΙΓΜΑΤΩΝ ΜΕΛΕΤΗ ΑΡΑΙΩΝ ΔΙΑΛΥΜΑΤΩΝ PEO-PS-PEO ΔΥΝΑΜΙΚΗ ΣΚΕΔΑΣΗ ΦΩΤΟΣ (DLS) ΥΠΟΛΟΓΙΣΜΟΣ ΤΗΣ ΚΡΙΣΙΜΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ ΕΠΙΚΑΛΥΨΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PEO-PS-PEO/[BMIM][PF 6 ] ΜΕΛΕΤΗ ΠΥΚΝΩΝ ΔΙΑΛΥΜΑΤΩΝ PEO-PS-PEO ΕΙΣΑΓΩΓΗ ΡΕΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΣΤΑΘΕΡΗΣ ΚΑΤΑΣΤΑΣΗΣ (Steady-State) ΠΕΙΡΑΜΑ ΕΡΠΥΣΜΟΥ (Creep) ΕΞΑΡΤΗΣΗ ΤΟΥ ΣΧΕΤΙΚΟΥ ΙΞΩΔΟΥΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PEO-PS- PEO/[BMIM][PF6] ΑΠΟ ΤΗ ΣΥΓΚΕΝΤΡΩΣΗ ΠΕΙΡΑΜΑΤΑ ΔΥΝΑΜΙΚΩΝ ΜΕΤΡΗΣΕΩΝ ΔΥΝΑΜΙΚΟ ΠΕΙΡΑΜΑ ΣΑΡΩΣΗΣ ΤΑΣΕΩΝ (Dynamic Stress Sweep Test) ΔΥΝΑΜΙΚΟ ΠΕΙΡΑΜΑ ΣΑΡΩΣΗΣ ΣΥΧΝΟΤΗΤΩΝ (Dynamic Frequency Sweep Test) ΜΕΤΑΒΟΛΗ ΤΟΥ ΜΕΤΡΟΥ ΑΠΟΘΗΚΕΥΣΗΣ ΚΑΙ ΤΟΥ ΧΡΟΝΟΥ ΧΑΛΑΡΩΣΗΣ ΜΕ ΤΗ ΣΥΓΚΕΝΤΡΩΣΗ ΤΟΥ ΠΟΛΥΜΕΡΟΥΣ ΕΠΙΔΡΑΣΗ ΘΕΡΜΟΚΡΑΣΙΑΣ ΣΥΜΠΕΡΑΣΜΑΤΑ ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟ ΕΙΣΑΓΩΓΗ ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΤΟΥ PS 10 PEO ΧΡΩΜΑΤΟΓΡΑΦΙΑ ΑΠΟΚΛΕΙΣΜΟΥ ΜΕΓΕΘΩΝ (SEC) ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΠΥΡΗΝΙΚΟΥ ΜΑΓΝΗΤΙΚΟΥ ΣΥΝΤΟΝΙΣΜΟΥ (NMR) ΥΛΙΚΑ ΠΑΡΑΣΚΕΥΗ ΔΕΙΓΜΑΤΩΝ ΜΕΛΕΤΗ ΑΡΑΙΩΝ ΔΙΑΛΥΜΑΤΩΝ PS 10 PEO
5 4.4.1 ΔΥΝΑΜΙΚΗ ΣΚΕΔΑΣΗ ΦΩΤΟΣ (DLS) ΥΠΟΛΟΓΙΣΜΟΣ ΤΗΣ ΚΡΙΣΙΜΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ ΕΠΙΚΑΛΥΨΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PS 10 PEO 10 /[BMIM][PF 6 ] ΜΕΛΕΤΗ ΠΥΚΝΩΝ ΔΙΑΛΥΜΑΤΩ PS 10 PEO ΕΙΣΑΓΩΓΗ ΡΕΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΣΤΑΘΕΡΗΣ ΚΑΤΑΣΤΑΣΗΣ (Steady-State) ΕΞΑΡΤΗΣΗ ΤΟΥ ΣΧΕΤΙΚΟΥ ΙΞΩΔΟΥΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PS 10 PEO 10 /[BMIM][PF 6 ] ΑΠΟ ΤΗ ΣΥΓΚΕΝΤΡΩΣΗ ΠΕΙΡΑΜΑΤΑ ΔΥΝΑΜΙΚΩΝ ΜΕΤΡΗΣΕΩΝ ΔΥΝΑΜΙΚΟ ΠΕΙΡΑΜΑ ΣΑΡΩΣΗΣ ΤΑΣΕΩΝ (Dynamic Stress Sweep Test) ΔΥΝΑΜΙΚΟ ΠΕΙΡΑΜΑ ΣΑΡΩΣΗΣ ΣΥΧΝΟΤΗΤΩΝ (Dynamic Frequency Sweep Test) ΣΥΜΠΕΡΑΣΜΑΤΑ ΒΙΒΛΙΟΓΡΑΦΙΑ ΚΕΦΑΛΑΙΟ ΓΕΝΙΚΑ ΣΥΜΠΕΡΑΣΜΑΤΑ
6 ΠΕΡΙΛΗΨΗ Στην παρούσα εργασία μελετήθηκαν φυσικά πηκτώματα κατά συστάδων συμπολυμερών σε ιοντικό υγρό. Τα συμπολυμερή που μελετήθηκαν ήταν το τρισυσταδικό συμπολυμερές πολυ(αιθυλενοξείδιο)-πολυ(στυρόλιο)- πολυ(αιθυλενοξείδιο) (PEO-PS-PEO) και το αστεροειδές συμπολυμερές πολυ(στυρόλιο)-πολυ(αιθυλενοξείδιο) (PS 10 PEO 10 ) στο ιοντικό υγρό εξαφθοροφωσφορούχο 1-βουτυλο-3-μεθυλιμιδαζόλιο [BMIM][PF 6 ], το οποίο είναι "καλός" διαλύτης για το PEO και "κακός" διαλύτης για το PS. Αρχικά πραγματοποιήθηκε μοριακός χαρακτηρισμός των συμπολυμερών PEO- PS-PEO και PS 10 PEO 10 μέσω των τεχνικών χρωματογραφίας αποκλεισμού μεγεθών (SEC) και της φασματοσκοπίας πυρηνικού μαγνητικού συντονισμού ( 1 H-NMR). Στη συνέχεια πραγματοποιήθηκε η μελέτη των συμπολυμερών σε αραιά διαλύματα μέσω των τεχνικών της δυναμικής σκέδασης φωτός (DLS) και της ιξωδομετρίας. Παρατηρήθηκε πως τα συμπολυμερή PEO-PS-PEO και PS 10 PEO 10 δημιουργούν πολυμοριακά και μονομοριακά "μαλακά" νανοσωματίδια μικκυλιακού τύπου, αντίστοιχα. Από τη DLS προσδιορίστηκε η υδροδυναμική ακτίνα, R h, των σωματιδίων. Μέσω της τεχνικής της ιξωδομετρίας AMVn υπολογίστηκε η κρίσιμη συγκέντρωση επικάλυψης, c*, στην οποία τα σωματίδια αρχίζουν να εφάπτονται μεταξύ τους. Σε υψηλές συγκεντρώσεις των πολυμερών παρατηρείται η δημιουργία φυσικών πηκτωμάτων λόγω της πλήρωσης του όγκου του διαλύματος από τα σωματίδια. Μέσω ρεολογικών μελετών προσδιορίστηκε η κρίσιμη συγκέντρωση σχηματισμού πηκτώματος, c gel. Παρατηρήθηκε μεγάλη εξάρτηση του σχετικού ιξώδους από τη συγκέντρωση του συμπολυμερούς καθώς και η αύξηση της ισχύος (μέτρου αποθήκευσης) και του χρόνου χαλάρωσης των φυσικών πηκτωμάτων με την αύξηση της συγκέντρωσης. Τέλος, πραγματοποιήθηκε σύγκριση μεταξύ των συστημάτων PEO-PS- PEO/[BMIM][PF 6 ] και PS 10 PEO 10 /[BMIM][PF 6 ]. Διαπιστώθηκε πως το PS 10 PEO 10 παρουσιάζει μεγαλύτερη c gel από το PEO-PS-PEO λόγω της μικρότερης πυκνότητας των αλυσίδων στην κορώνα του αστεροειδούς από αυτή του τρισυσταδικού με αποτέλεσμα τα σωματίδια του αστεροειδούς να διεισδύουν πολύ περισσότερο μεταξύ τους για να επιτευχθεί το φαινόμενο του συνωστισμού. I
7 II
8 ABSTRACT In the present study the properties of physical gels formed by block copolymers in an ionic liquid were studied. The triblock poly(ethylene oxide)-poly(styrene)-poly(ethylene oxide) (PEO-PS-PEO) and the star polystyrene-polyethylene (PS 10 PEO 10 ) copolymers were studied in 1-butyl-3-methylimadazolium hexafluapophoshate, [BMIM][PF 6 ], which is a good solvent for the PEO blocks and bad solvent for the PS blocks. Initially, the copolymers were characterized by size exclusion chromatography (SEC) and neutron magnetic resonance ( 1 H-NMR). At a next step the study of the polymers in dilute solutions was followed by dynamic light scattering (DLS) and AMVn viscometry. It was found that PEO-PS-PEO and PS 10 PEO 10 self assemble into multimolecular and monomolecular, micellar type soft nanoparticles, respectively. The size of the particles was calculated by DLS. From the AMVn viscometry, the critical overlap concentration at which the formed nanoparticles start adhering to each other, c*, was calculated. At high polymer concentrations, the formation of gels was observed which was due to the jamming of the particles in the total volume of the solution. Through rheological studies, the critical gelation concentration, c gel, was determined. Above c gel a dramatic viscosity rise was observed. At the same time, the storage modulus G o and the relaxation time τ R of the system increased also with increasing concentration. Finally, the comparison between the PEO-PS-PEO/[BMIM][PF 6 ] and PS 10 PEO 10 /[BMIM][PF 6 ] systems was discussed. It was concluded that the PS 10 PEO 10 copolymer exhibits a higher value of c gel than that of PEO-PS-PEO copolymer due to the lower density of the chains in the corona of the star nanoparticles. II
9 ΕΙΣΑΓΩΓΗ Τα ιοντικά υγρά (ionic liquids, ILS) ή "πράσινοι διαλύτες" έχουν προσελκύσει σημαντικό ερευνητικό ενδιαφέρον τα τελευταία χρόνια. Τα ιοντικά υγρά αποτελούνται από ένα μεγάλο οργανικό κατιόν και ένα ανόργανο ανιόν. Λόγω της μη κρυσταλλικής δομής τους είναι υγρά άλατα ακόμα και στη θερμοκρασία περιβάλλοντος (RTILs) και εμφανίζουν χαμηλά σημεία τήξης. Η καλή θερμική σταθερότητα που παρουσιάζουν επιτρέπει την πραγματοποίηση πειραμάτων και χρήσεων σε υψηλές θερμοκρασίες, καθώς η χρήση άλλων διαλυτών όπως πτητικά υγρά και νερό είναι δυσχερής. Επιπλέον, η καλή χημική σταθερότητα που επιτρέπει την αποθήκευση για μεγάλα χρονικά διαστήματα και η υψηλή αγωγιμότητα είναι μερικές σημαντικές ιδιότητες που εμφανίζουν τα ιοντικά υγρά. Οι προαναφερόμενες ιδιότητες καθιστούν τα ιοντικά υγρά κατάλληλους διαλύτες για την αναμιξή τους με πολυμερή, με σκόπο το σχηματισμό φυσικών πηκτωμάτων. Από προηγουμένες μελέτες που πραγματοποιήθηκαν σε διαλύματα πολυμερών σε ιοντικά υγρά, παρατηρήθηκε η δημιουργία φυσικών πηκτωμάτων (gels) από διασυνδεμένα συμπολυμερή. Μάλιστα, ενδιαφέρον παρουσιάζουν τα θερμοευαίσθητα πολυμερικά συστήματα καθώς διαλύματα συμπολυμερών σε ιοντικά υγρά αποκρίνονται στις μεταβολές της θερμοκρασίας και γι αυτό κατατάσσονται στην κατηγορία των αποκρίσιμων συμπολυμερών με πιθανές εφαρμογές στα τρανζίστορ λεπτών οργανικών υμενίων. Με αφορμή τα πλεονεκτήματα που παρουσιάζουν τα ιοντικά υγρά, στην παρούσα εργασία πραγματοποιήθηκε μελέτη διαλυμάτων του τρισυσταδικού συμπολυμερούς πολύ(αιθυλενοξείδιο)-πολύ(στυρόλιο)-πολύ(αιθυλενοξείδιο) (PEO- PS-PEO) και του αστεροειδούς συμπολυμερούς πολύ(στυρόλιο)- πολύ(αιθυλενοξείδιο) (PS 10 PEO 10 ) στο ιοντικό υγρό [BMIM][PF 6 ]. Παρατηρήθηκε πως τα παραπάνω συμπολυμερή σχηματίζουν φυσικά πηκτώματα (gels). Το διαφορετικό αυτών των συστημάτων σε σχέση με τα gels που έχουν μελετηθεί στη βιβλιογραφία είναι ότι στην περίπτωσή μας ο σχηματισμός πηκτώματος οφείλεται στο φαινόμενο του συνωστισμού (jamming). Σε αντίθεση με τις προηγούμενες μελέτες που έχουν πραγματοποιηθεί σε τρισυσταδικά συμπολυμερή όπου η κεντρική συστάδα είναι διαλυτή και οι ακραίες συστάδες είναι αδιάλυτες, με αποτέλεσμα να έχουμε διαμοριακή φυσική διασύνδεση και δημιουργία δικτύου, στην παρούσα εργασία το τρισυσταδικό συμπολυμερές αποτελείται από κεντρική συστάδα (PS) 1
10 αδιάλυτη στο ιοντικό υγρό [BMIM][PF 6 ] και ακραίες διαλυτές συστάδες (PEO). Κατά συνέπεια τόσο το τρισυσταδικό PEO-PS-PEO όσο και το αστεροειδές PS 10 PEO 10 δεν δημιουργούν δομή δικτύου αλλά μη διασυνδέσιμα σφαιρικά σωματίδια τα οποία σε υψηλή συγκέντρωση ακινητοποιούνται λόγω συμφόρησης (gel). 2
11
12 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ Η ΜΙΚΡΟΔΟΜΗ ΤΩΝ ΠΟΛΥΜΕΡΩΝ ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ Πολυμερή τα οποία αποτελούνται από δυο διαφορετικά είδη μονομερών ονομάζονται συμπολυμερή, ενώ αυτά που αποτελούνται από τρία διαφορετικά είδη μονομερών ονομάζονται τριπολυμερή. Όταν τα διαφορετικά είδη επαναλαμβανόμενων μονάδων εντοπίζονται σε διακριτές συστάδες (blocks) κατά μήκος της πολυμερικής αλυσίδας το συμπολυμερές ή το τριπολυμερές ονομάζεται δισυσταδικό συμπολυμερές (diblock copolymer) ή τρισυσταδικό συμπολυμερές (triblock terpolymer), αντίστοιχα. Στην περίπτωση όπου οι δομικές μονάδες του πολυμερούς είναι τυχαία κατανεμημένες κατά μήκος της αλυσίδας, το πολυμερές λέγεται τυχαίο ή στατιστικό (random ή statistical). Στην εικόνα 1.1 αναπαρίστανται σχηματικά ένα δισυσταδικό και ένα στατιστικό συμπολυμερές. Οι διαφορετικές δομικές μονάδες εμφανίζονται με διαφορετικό χρώμα. Η διασύνδεση με ομοιοπολικό δεσμό γραμμικών πολυμερικών αλυσίδων στο ένα τους άκρο έχει σαν αποτέλεσμα το σχηματισμό αστεροειδών πολυμερών. Όταν όλα τα μπράτσα του αστεροειδούς πολυμερούς είναι όμοια (είτε ομοπολυμερή είτε συμπολυμερή) τότε το πολυμερές ονομάζεται ομοκλαδικό (homoarm) 1 αστεροειδές πολυμερές, ενώ όταν είναι διαφορετικά, ονομάζεται ετεροκλαδικό (heteroarm) 2 αστεροειδές πολυμερές. Οι δύο αυτές κατηγορίες αστεροειδών πολυμερών φαίνονται στην εικόνα 1.2. Εικόνα 1.1: Σχηματική αναπαράσταση ενός δισυσταδικού (a) και ενός στατιστικού (b) συμπολυμερούς. 3
13 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.2. Οι δύο τύποι αστεροειδών πολυμερών: (a) ομοκλαδικό δισυσταδικό αστεροειδές συμπολυμερές και (b) ετεροκλαδικό δισυσταδικό αστεροειδές συμπολυμερές. Τα διαφορετικά χρώματα αντιπροσωπεύουν διαφορετικές συστάδες. Όταν οι πολυμερικές αλυσίδες διασυνδέονται και στα δύο άκρα τους σχηματίζονται τρισδιάστατες δομές, που ονομάζονται πολυμερικά δίκτυα. Τα πολυμερικά δίκτυα μπορούν να διακριθούν σε δύο μεγάλες κατηγορίες αναφορικά με την κατανομή των σταυροδεσμών κατά μήκος των αλυσίδων: τα δίκτυα τυχαίας διασύνδεσης και τα πρότυπα δίκτυα. Τα δίκτυα τυχαίας διασύνδεσης είναι τα δίκτυα, στα οποία οι σταυροδεσμοί είναι τυχαία κατανεμημένοι εντός του δικτύου και αυτό έχει ως αποτέλεσμα το μήκος των αλυσίδων μεταξύ των σταυροδεσμών (ελαστικές αλυσίδες) να διαφέρει και μάλιστα να εμφανίζει πλατιά κατανομή. Αντίθετα στα πρότυπα δίκτυα οι σταυροδεσμοί είναι τοποθετημένοι σε ίσες αποστάσεις, οδηγώντας σε ελαστικές αλυσίδες με στενή κατανομή ως προς το μέγεθός τους 3 (εικόνα 1.3). Εικόνα 1.3. Σχηματική αναπαράσταση ενός (α) τυχαία διασυνδεδεμένου και (b) ενός προτύπου πολυμερικού δικτύου. 4
14 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Άλλη μια διάκριση για τα πολυμερικά δίκτυα είναι ως προς το είδος των σταυροδεσμών. Οι σταυροδεσμοί μπορεί να είναι είτε χημικοί (ομοιοπολικοί δεσμοί μεταξύ διαφορετικών αλυσίδων), είτε φυσικοί, οι οποίοι είναι αντιστρεπτοί και μπορούν να επανασχηματιστούν υπο κατάλληλες συνθήκες. Οι χημικοί σταυροδεσμοί προκύπτουν κατά την διαδικασία του πολυμερισμού π.χ με την προσθήκη ενός διακόρεστου μονομερούς EGDMA (αιθυλενογλυκολδιμεθακρυλεστέρας) ή ύπαρξη θειούχων δεσμών μεταξύ των πολυμερικών αλυσίδων στα ελαστικά των αυτοκινήτων (βουλκανισμός). Αντίθετα, οι φυσικοί σταυροδεσμοί σχηματίζονται λόγω υδρόφοβων αλληλεπιδράσεων, ηλεκτροστατικών αλληλεπιδράσεων ή δυνάμεων Van der Waals. 1.2 ΚΑΤΑ ΣΥΣΤΑΔΕΣ ΣΥΜΠΟΛΥΜΕΡΗ (BLOCK COPOLYMERS) Τα τελευταία χρόνια, τα κατά συστάδες συμπολυμερή έχουν αποκτήσει μεγάλο ενδιαφέρον, λόγω της ποικιλίας και των δυνατοτήτων που προσφέρουν στο σχεδιασμό μακρομορίων. Οι ερευνητές για να μπορούν να έχουν τον έλεγχο των μακρομοριακών χαρακτηριστικών τους όπως το μέγεθος των συστάδων, την αρχικτεκτονική τους, τη μοριακή πολυδιασπορά, ανέπτυξαν ειδικές διαδικασίες σύνθεσης γνωστές ως "ζωντανός πολυμερισμός" (living polymerization). Μέσω αυτών των μεθόδων μπορεί να δημιουργηθεί μεγάλη ποικιλία αρχιτεκτονικών. Τα συσταδικά συμπολυμερή, όσον αφορά στην αρχιτεκτονική τους, μπορούν να διαχωριστούν σε δυο μεγάλες κατηγορίες. Την γραμμική αρχιτεκτονική όπου όλες οι συστάδες είναι διατεταγμένες κατά μήκος μιας μακρομοριακής αλυσίδας, όπως γραμμικά δισυσταδικά (ΑΒ) και τρισυσταδικά τύπου ΑΒΑ ή ABC καθώς και την μηγραμμική αρχιτεκτονική όπου οι συστάδες συνδέονται με μη-γραμμικό τρόπο σχηματίζοντας έτσι μια ποικιλία σχημάτων, όπως αστεροειδή δισυσταδικά (ΑΒ) n. 1.3 ΠΗΚΤΩΜΑΤΑ Τα πηκτώματα χρησιμοποιούνται ευρέως στη βιομηχανία αλλά και σε μεγάλη συχνότητα σε καθημερινές χρήσεις. 5
15 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Ο καθορισμός των ιδιοτήτων και της μορφολογίας των πηκτωμάτων αποτελεί ενεργό τομέα της έρευνας και αντικείμενο διαφορετικών επιστημών. Η μεγάλη ποικιλία στη μορφολογία και στις ιδιότητες καθιστούν δύσκολο να κατασταλλάξει κάποιος σε ένα σαφή ορισμό για τα πηκτώματα 4. Ένας ευρέως αποδεκτός καθορισμός ενός πηκτώματος είναι ο εξής: πήκτωμα είναι ένα τρισδιάστατο δίκτυο που αποτελείται από βασικές δομικές μονάδες οι οποίες συνδέονται με κάποιο τρόπο και έχουν τη δυνατότητα να διογκώνονται από μια καθορισμένη ποσότητα διαλύτη. Τα πηκτώματα χωρίζονται σε δυο κυρίες κατηγρίες: τα χημικά και φυσικά πηκτώματα. Τα χημικά πηκτωμάτα είναι διασυνδεμένα με ομοιοπολικούς δεσμούς. Οι ομοιοπολικοί δεσμοί είναι πολύ ισχυροί έτσι ώστε να έχουν μεγάλη αντοχή στη θέρμανση. Παρασκευάζονται συνήθως με διασύνδεση των γραμμικών πολυμερών υψηλού μοριακού βάρους ή με πολυσυμπύκνωση ολιγομερών με τη χρήση ομάδων διασύνδεσης. Στα φυσικά πηκτώματα, η διασύνδεση μεταξύ των αλυσίδων επιτυγχάνεται κατευθείαν με φυσικές αλληλεπιδράσεις (δεσμούς υδρογόνου, υδρόφοβες αλληλεπιδράσεις). Παρουσιάζουν αρκετά κοινά χαρακτηριστικά με τα χημικά πηκτώματα, όμως λόγω της πιο ασθενούς διασύνδεσης που έχουν οι κόμβοι στο πολυμερικό δίκτυο παρουσιάζουν και σημαντικές διαφορές. Για παράδειγμα, τα φυσικά πηκτωμάτα σχηματίζουν πιο αραιά πολυμερικά διαλύματα με την προσθήκη διαλύτη, ενώ τα χημικά πηκτωμάτα διογκώνονται με την προσθήκη διαλύτη. Μια ακόμη σημαντική ιδιότητα των φυσικών πηκτωμάτων είναι η θερμοαντιστρεπτότητα. Μια πολύ σημαντική κατηγορία συνθετικών πολυμερών που ανήκει στα φυσικά πηκτώματα είναι τα συμπολυμερή Α-Β-Α ή Β-Α-Β. Στην περίπτωση, αυτή η συστάδα Α είναι διαλυτή ενώ η Β αδιάλυτη και κάτω από αυτές τις συνθήκες είναι δυνατόν να δημιουργηθούν αλληλεπιδράσεις τύπου Β-Β μεταξύ συστάδων με αποτέλεσμα την ανάπτυξη φυσικών δεσμών. 6
16 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΔΙΑΔΙΚΑΣΙΑ ΔΗΜΙΟΥΡΓΙΑΣ ΠΗΚΤΩΜΑΤΟΣ Κατά την διάρκεια της διαδικασίας σχηματισμού πηκτώματος, οι γραμμικές πολυμερικές αλυσίδες διασυνδέονται είτε με τον εαυτό τους σχηματίζοντας ενδομοριακές διασυνδέσεις είτε με άλλες αλυσίδες για να δημιουργήσουν διακλαδισμένες αλυσίδες. Το μέγεθος των διακλαδισμένων αλυσίδων αυξάνεται συνεχώς όσο περισσότερες πολυμερικές αλυσίδες διασυνδέονται. Το μέσο μοριακό βάρος κατά μάζα αυξάνεται, σχηματίζοντας ένα δίκτυο το οποίο εκτείνεται σε ολόκληρο το σύστημα. Το κρίσιμο σημείο κατά το οποίο διακλαδισμένες αλυσίδες διασυνδέονται μεταξύ τους με αποτέλεσμα το σχηματισμό δικτύου απείρου μάζας, καλείται σημείο δημιουργίας πηκτώματος (gel point). Πολλά φυσικά μεγέθη παρουσιάζουν χαρακτηριστικές αποκλίσεις στο σημείο δημιουργίας πηκτώματος. Για παράδειγμα, το ιξώδες όπως και ο χρόνος χαλάρωσης αυξάνονται απότομα. 1.4 ΙΟΝΤΙΚΑ ΥΓΡΑ-"ΠΡΑΣΙΝΟΙ ΔΙΑΛΥΤΕΣ" Στη σύγχρονη εποχή η χρήση διαλυτών στην παρασκευή συγκολλητικών ουσιών, στις βαφές, σε επικαλύψεις, στη φαρμακευτική, σε εργαστηριακές συνθέσεις και σε πολλές ακόμη εφαρμογές έχει αλλάξει ριζικά τον τρόπο ζωής. Παρά όμως την ευρεία εφαρμογή τους, οι διαλύτες συνδέονται με θέματα οικονομικά, περιβαλλοντικά, υγιεινής και ασφάλειας, αφού είναι μέρος του προβλήματος της εκπομπής πτητικών οργανικών ενώσεων (VOCs). Η βλαβερή τους επίπτωση οφείλεται στην ικανότητα των περισσότερων από αυτούς να εκπέμπουν ατμούς και να εξατμίζονται ακόμα και σε θερμοκρασία δωματίου ενώ κάποιοι αναδύουν ισχυρή μυρωδιά, με αποτέλεσμα τη μόλυνση του περιβάλλοντος 5. Είναι ευνόητο λοιπόν ότι η εξεύρεση εναλλακτικών λύσεων για περιορισμό ή αντικατάσταση της χρήσης αυτών των διαλυτών, όχι μόνο θα δώσει μια οικολογικά αποδεκτή λύση αλλά θα ανακουφίσει και την βιομηχανία διαλυτών από σημαντικά έξοδα. Η ανάγκη για ''πράσινη'' χημεία, δηλαδή βιομηχανική παραγωγή χημικών προϊόντων χρησιμοποιώντας φιλικές προς το περιβάλλον μεθόδους, έχει ωθήσει μεγάλο μέρος της έρευνας προς τα ιοντικά υγρά (ionic liquids, ILS) 6. Τα ιοντικά 7
17 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 υγρά είναι υγρά άλατα σε μια περιοχή θερμοκρασιών από C έως C, ενώ τα συνηθισμένα άλατα είναι υγρά μόνο στη θερμοκρασία τήξεώς τους, που είναι αρκετά υψηλή (πχ, NaCl σ.τ C) 7. Για τις περισσότερες εφαρμογές χρησιμοποιούνται ιοντικά υγρά στην περιοχή θερμοκρασίων από C έως C, ενώ μεγαλύτερο ενδιαφέρον παρουσιάζουν τα ιοντικά υγρά που είναι υγρά κοντά στη θερμοκρασία περιβάλλοντος (RTILs). Τα περισσότερα από αυτά είναι διαυγείς ουσίες με κανονική συμπεριφορά που μοιάζουν και ρέουν όπως το νερό 2,8. Αντίθετα από τα συνηθισμένα άλατα, τα ιοντικά υγρά περιέχουν ένα μεγάλο οργανικό κατιόν και ένα συνήθως ανόργανο ανιόν, ενώ σε σπάνιες περιπτώσεις το μικρό ανιόν είναι επίσης οργανικό (εικόνα 1.4). Τα περισσότερα κοινά κατιόντα είναι βασισμένα στα παράγωγα ιμιδαζολίου (imidazolium), πυριδινινίου (pyridinium), πυρρολιδινίου (pyrrolidinium), αμμωνίου (ammonium) και φωσφωνίου (phosphonium). Τα ανιόντα - - αποτελούνται είτε από πολυπυρηνικά ιόντα, όπως Al Cl, Al3 Cl, είτε μονοπυρηνικά ιόντα, όπως BF, PF6, SbF6, ZnCl3, CuCl2. 4 Η τελική δομή που προκύπτει είναι μη κρυσταλλική, με αποτέλεσμα να μην επιτρέπουν πυκνό «πακετάρισμα» ανιόντων-κατιόντων. Η αδυναμία σχηματισμού κανονικών κρυστάλλων λόγω ασυμμετρίας των ιόντων αποτελεί την αιτία εμφάνισης χαμηλών σημείων τήξης. Οι θερμοκρασίες μετάβασης των ιοντικών υγρών από την στερεή στην υγρή κατάσταση μπορούν να κυμαίνονται κοντά στη θερμοκρασία δωματίου ή να είναι ιδιαίτερα χαμηλές, ακόμη και ίσες με C. Το σημείο τήξης των ιοντικών υγρών εξαρτάται κυρίως από το μέγεθος των ιόντων που τα αποτελούν 9. Εικόνα 1.4: Απεικόνιση ιοντικών υγρών (ILs) που αποτελούνται από οργανικά κατιόντα, βασισμένα σε παράγωγα ιμιδαζολίου ([bmim] (a) και [emim] (b)) και διαφόρων τύπων ανιόντων. 8
18 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Τα ιοντικά υγρά συχνά ονομάζονται και ''πράσινοι διαλύτες'' εξαιτίας της αμελητέας τάσης ατμών και λόγω της καλής χημικής/θερμικής σταθερότητας 10. Επίσης, παρουσιάζουν υψηλή αγωγιμότητα, δεν καίγονται και έχουν ευρύ ηλεκτροχημικό παράθυρο 11,12,13. Η υψηλή τους θερμική σταθερότητα επιτρέπει τη χρήση τους για την πραγματοποίηση αντιδράσεων σε υψηλές θερμοκρασίες, καθώς και η υψηλή χημική σταθερότητα επιτρέπει την αποθήκευσή τους για μεγάλα χρονικά διαστήματα. Οι προαναφερόμενες ιδιότητες, καθιστούν τα ιοντικά υγρά κατάλληλους διαλύτες για την αναμιξή τους με πολυμερή, με σκοπό το σχηματισμό φυσικών πηκτωμάτων, αντικαθιστώντας τη χρήση κοινών διαλυτών. Σε σύγκριση με την παραδοσιακή διάλυση των πολυμερών σε κοινούς διαλύτες, για την δημιουργία των πολυμερικών διαλυμάτων σε ιοντικά υγρά απαιτείται λιγότερη ποσότητα πολυμερούς και τα πολυμερικά διαλύματα παρουσιάζουν υψηλότερη αγωγιμότητα 14. Με επιλογή του κατάλληλου διαλύτη και του κατάλληλου πολυμερούς, μπορούν να παρασκευασθούν πολυμερικά διαλύματα τα όποια βρίσκουν πληθώρα εφαρμογών, συμπεριλαμβανομένων των μπαταρίων λιθίου, χημικών αισθητήρων, τρανζίστορ λεπτών οργανικών υμενίων, ηλεκτρομηχανικών εφαρμογών και φωτοβολταϊκών διατάξεων 15,16,17,18,19. Σ αντίθεση με τη συμβατική παρασκευή πολυμερικών διαλυμάτων σε οργανικούς διαλύτες, η δημιουργία φυσικών πηκτωμάτων σε ιοντικά υγρά δεν παρουσίαζε το ίδιο ενδιαφέρον. Όμως, τα τελευταία χρόνια η επιστημονική κοινότητα εχει στρέψει την προσοχή της προς τα ιοντικά υγρά, όπως ο Watanabe και οι συνεργάτες του, όπου παρασκεύασαν με επιτυχία πολυμερικά διαλύματα βασισμένα σε άλατα ιμιδαζολίων και πυριδινίων 14. Κατά κόρον, χρησιμοποιούνται αμφίφιλα συμπολυμερή. Το χαρακτηριστικό αυτών των συμπολυμερών είναι ότι όταν διαλυθούν σε εκλεκτικό διαλύτη (ο διαλύτης είναι «καλός» για την μια συστάδα του συμπολυμερούς (λυόφιλο) και «κακός» για την άλλη συστάδα (λυόφοβο)) έχουν την τάση να αυτό-οργανώνονται σε δομές πού ονομάζονται μικκύλια (micelles) 6,20. Τα μικκύλια αποτελούνται από τον πυρήνα (περιέχει το αδιάλυτο τμήμα του συμπολυμερούς) και την κορώνα (περιέχει το διαλυτό τμήμα του συμπολυμερούς). 9
19 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Στην συνέχεια θα γίνει παράθεση πειραματικών και θεωρητικών μελετών που έχουν πραγματοποιηθεί τα τελευταία χρόνια, για τη δομή και τις ιδιότητες δισυστατικών και τρισυσταδικών συμπολυμερών σε ιοντικά υγρά. 1.5 ΔΙΣΥΣΤΑΔΙΚΑ ΣΥΜΠΟΛΥΜΕΡΗ ΔΙΑΛΥΜΑΤΑ ΣΕ ΙΟΝΤΙΚΑ ΥΓΡΑ Μια κατηγορία συμπολυμερών που έχει μελετηθεί σε ιοντικά υγρά και παρουσιάζει ενδιαφέρον είναι τα δισυσταδικά συμπολυμερή, τύπου AB. Χαρακτηριστικό γνώρισμα των δισυσταδικών συμπολυμερών είναι η εκλεκτικότητα της μια συστάδας του συμπολυμερούς στο ιοντικό υγρό, η οποία οδηγεί στην αυτόοργανώση σε μικκύλια. Μελετήθηκε πρόσφατα το σύστημα του δισυστατικού συμπολυμερούς πολυ(1,2 βουταδιενιο)-πολυ(αιθυλενοξείδιο), PB-PEO, στο ιοντικό υγρό εξαφθοροφωσφορούχο 1-βουτυλο-3-μεθυλιμιδαζόλιο (1-butyl-3-methylimadazolium hexafluapophoshate), [BMIM][PF 6 ], το οποίο είναι «καλός» διαλύτης για το PEO και είναι το λιγότερο ευαίσθητο στην υγρασία από τα άλλα ιοντικά υγρά ιμιδαζολίου 21. Η αυτό-οργάνωση των συσταδικών συμπολυμερών σε οργανωμένες δομές, συνήθως μικκύλια, σε εκλεκτικό διαλύτη, είναι ήδη τεκμηριωμένη. Οι συνηθισμένες μορφολογίες είναι σφαιρικές, κυλινδρικές (wormlike) ή κυστοειδή μικκύλια 22. Μέσω της ηλεκτρονικής μικροσκοπίας διαπερατότητας (cryo-tem) μελετήθηκε η δομή του συστήματος και παρατηρήθηκε η δημιουργία μικκυλίων στο ιοντικό υγρό [BMIM][PF 6 ], όπως είχε παρατηρηθεί αντίστοιχα στο νερό και σε άλλους οργανικούς διαλύτες. Οι διαφορετικές μορφολογίες των αυτοσυναρμολογούμενων δομών προκύπτουν από την μεταβολή του ποσοστού του PEO (f PEO ) από 0.64 εως 0.25 στο σύστημα PB-PEO/[BMIM][PF 6 ] συγκέντρωσης 1wt%. Ειδικότερα, μειώνοντας το ποσοστό του PEO, παρατηρείται μετατροπή των σφαιρικών σε κυστοειδή μικκύλια, μειώνοντας την διεπιφανειακή καμπυλότητα μεταξύ πυρήνα και κορώνας (εικόνες 1.5 και 1.6). 10
20 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.5: Εικόνες Cryo-Tem των διαλυμάτων PB- PEO/[BMIM][PF 6 ] συγκέντρωσης 1wt%: (Α) PB-PEO(9-20) με f PEO =0.64; (Β) PB-PEO(9-10) με f PEO = Απεικονίζονται οι ανοιχτόχρωμοι πυρήνες μικκυλίων του PB 22. Εικόνα 1.6: Εικόνες Cryo-Tem PB-PEO/[BMIM][PF 6 ] συγκεντρώσης 1wt% με f PEO =0.38. Παρατηρείται η συνύπαρξη σφαιρικών και κυστοειδών μικκυλίων 22. Από μετρήσεις δυναμικής σκέδασης φωτός, DLS, προέκυψαν πληροφορίες σχετικά με τη δομή των αυτοσυναρμολογούμενων δομών, όπως ο υπολογισμός της υδροδυναμικής ακτίνας, R h, και της διασποράς του μεγέθους των μικκυλίων, μ 2 /Γ 2. Οι μετρήσεις για τα δισυσταδικά συμπολυμερή PB-PEO/[BMIM][PF 6 ] πραγματοποιήθηκαν στο θερμοκρασιακό εύρος C και παρατηρήθηκε ότι το μέγεθος των μικκυλίων είναι ανεξάρτητο από την θερμοκρασία. Επιπροσθέτως, τα μεγέθη που μετρήθηκαν δεν παρουσίασαν αισθητές μεταβολές στο συγκεκριμένο 11
21 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 θερμοκρασιακό εύρος. Έτσι, προέκυψε το συμπέρασμα ότι η συμπεριφορά του συστήματος παραμένει αμετάβλητη στο συγκεκριμένο θερμοκρασιακό εύρος. Στη συνέχεια, μελετήθηκε το ίδιο δισυσταδικό συμπολυμερές, PB-PEO, στα ιοντικά υγρά δισ(τριφθορομεθύλσουλφονύλ)ιμιδιούχο 1-αίθυλο-3-μεθυλιμιδαζόλιο, [EMIΜ][TFSI], και [BMIM][PF 6 ] 23. Μέσω σκέδασης ακτίνων-χ σε μικρές γωνίες, SAXS, διερευνήθηκε η λυοτροπική φάση του δισυσταδικού συμπολυμερούς και παρατηρήθηκε πως η μεταβολή του ποσοστού του PEO οδηγεί στην μετατροπή της δομής των μικκυλίων από σφαιρική σε κυστοειδή, τόσο στο ιοντικό υγρό [BMIM][PF 6 ], όπως εχει προαναφερθεί 19, όσο και στο [EMIΜ][TFSI]. Επιπροσθέτως, μέσω των εικόνων cryo-tem και από τα μήκη των δομών των μικκυλίων που μετρήθηκαν μέσω SAXS επιβεβαιώθηκε πως το [BMIM][PF 6 ] είναι πιο εκλεκτικός διαλύτης από το [EMIΜ][TFSI], καθώς η διεπιφανειακή καμπυλότητα πυρήνα-κορώνας των μικκυλίων είναι χαμηλότερη στο [BMIM][PF 6 ]. Πρόσφατα, μελετήθηκε η συμπεριφορά και η αρχιτεκτονική του δισυσταδικού συμπολυμερούς πολυ(στυρόλιο)-πολυ(μεθακρυλικός μεθυλεστέρας), PS-PMMA, στο ιοντικό υγρό [BMIM][PF 6 ] 24. Συγκρίνοντας τη συμπεριφορά του PMMA σ ένα κοινό διαλύτη και στο συγκεκριμένο ιοντικό υγρό, διαπιστώθηκε πως το [BMIM][PF 6 ] είναι καλός διαλύτης για το PMMA. Μέσω των cryo-tem και DLS μελετήθηκε η δομή του συστήματος. Παρατηρήθηκε πως το δισυσταδικό συμπολυμερές αυτοοργανώνεται σε μικκύλια και μεταβάλλοντας το ποσοστό του PMMA στο σύστημα, η σφαιρική δομή των μικκυλίων μετατρέπεται σε κυστοειδή. Συγκεκριμένα, καθώς μειώνεται το ποσοστό του PMMA, αυξάνεται το ποσοστό του PS, δηλαδή το μέγεθος των αλυσίδων του PS και το οποίο οδηγεί στην αύξηση της υδροδυναμικής ακτίνας. Το ενδιαφέρον για τα ιοντικά διαλύματα συμπολυμερών ωθήσε τους Lodge et. al. 25 να μελετήσουν τη συμπεριφορά του συμπολυμερούς PB-PEO σε μίγμα ιοντικού υγρού και νερού. Το πολυμερές ακολούθησε κυκλική μετάβαση μεταξύ ιοντικού υγρού και νερού ανάλογα με τη θερμοκρασία, χωρίς να παρατηρείται διάσπαση της δομής των μικκυλίων. Το [BMIM][PF 6 ] και το νερό, είναι καλοί διαλύτες για το PEO ενώ το PB δημιουργεί τον πυρήνα του μικκυλίου. Ετσι, αφού αρχικά διαλύθηκε το συμπολυμερές στο ιοντικό υγρό, προσθέθηκε συγκεκριμένη ποσότητα νερού με 12
22 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 αποτέλεσμα να παρατηρηθεί διαχωρισμός φάσεων καθώς τα δυο είδη διαλυτών δεν είναι αναμίξιμα. Από μετρήσεις με Cryo-Tem που πραγματοποιήθηκαν για το σύστημα, παρατηρήθηκε ότι σε θερμοκρασία περιβάλλοντος τα μικκύλια βρίσκονται στην υδατική φάση και καθώς αυξάνεται η θερμοκρασία τα μικκύλια εισέρχονται πλέον στην άλλη φάση και παραμένουν εκεί έως τους 90 0 C (εικόνα 1.7). Στη συνέχεια, καθώς μειώνεται η θερμοκρασία, τα μικκύλια επιστρέφουν στην υδατική φάση, διαγράφοντας έτσι μια κυκλική διαδρομή. Εικόνα 1.7: Σχηματική απεικόνιση της κυκλικής μετάβασης των μικκυλίων του συμπολυμερούς PB-PEO σε μίγμα ιοντικού υγρού [BMIM][PF 6 ] και νερού σε διαφορετικές θερμοκρασίες 25. Επιπλέον, το σύστημα μελετήθηκε με πειράματα DLS στις θερμοκρασίες 25 0 C και 90 0 C για τον υπολογισμό της υδροδυναμικής ακτίνας. Παρατηρήθηκε πως η υδροδυναμική ακτίνα, R h, μειώνεται από 61 σε 57 nm καθώς η θερμοκρασία αυξάνεται από τους 25 0 C στους 90 0 C. Η παρατήρηση αυτή είναι σύμφωνη με την συμπεριφορά φάσεως χαμηλότερης κρίσιμης θερμοκρασίας διαλύσεως (LCST) που παρουσιάζει το PEO στο νερό και τη διάσπαση των δεσμών υδρογόνου του νερού καθώς αυξάνεται η θερμοκρασία 26,27. Λόγω της αύξησης της θερμοκρασίας, το νερό δεν είναι πλέον καλός διαλύτης για το PEO με αποτέλεσμα την μείωση του μεγέθους 13
23 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 της κορώνας των μικκυλίων, ενώ η συμπεριφορά του δισυσταδικού συμπολυμερούς PB-PEO στο [BMIM][PF 6 ] δεν επηρεάζεται από την επιβολή της θερμοκρασίας 19. Επεκτείνοντας την παραπάνω έρευνα, το ενδιαφέρον στράφηκε στη δημιουργία πολυμερικών κυστιδίων (polymersomes) του PB-PEO σε νερό και στο ιοντικό υγρό, [EMIM][TFSI], το όποιο περιέχεται στο εσωτερικό των κυστιδίων 28. Το νερό και το ιοντικό υγρό [EMIM][TFSI] δεν είναι αναμίξιμα αλλά παρόλα αυτά, και οι δυο είναι καλοί διαλύτες του PEO. Έτσι παρατηρείται η δημιουργία κυστιδίων (vesicles) όπου τα άκρα του PEO σχηματίζουν τις εσωτερικές και εξωτερικές κορώνες των κυστιδίων και η μεμβράνη των κυστιδίων σχηματίζεται από τις συστάδες του PB. Το δισυσταδικό συμπολυμερές PB-PEO υψηλής συγκέντρωσης, σχηματίζει σταθερά κυστίδια τα οποία έχουν την ικανότητα να μεταναστεύουν μεταφέροντας στο εσωτερικό τους άθικτο το ιοντικό υγρό κατά μήκος της διεπιφάνειας νερό/[emim][tfsi], οδηγώντας σε σταθεροποιημένες διπλοστοιβάδες μικρογαλακτωμάτων ιοντικού υγρού σε νερό. Στη συνέχεια, μελετήθηκαν διαλύματα του ίδιου συμπολυμερούς, PB-PEO στο ιονικό υγρό [EMI][TFSI] όπου η μέθοδος παρασκευής διαλυμάτων πραγματοποιήθηκε ακολουθώντας δυο διαφορετικές μεθόδους 29. Στην πρώτη μέθοδο, τα διαλύματα παρασκευάστηκαν από την απευθείας διάλυση του δισυσταδικού συμπολυμερούς στο ιοντικό υγρό (direct dissolution, (DD)) ενώ στην δεύτερη μέθοδο έγινε χρήση ένος συνδιαλύτη για την αρχική διάλυση του συμπολυμερούς και ύστερα προσθέθηκε το ιοντικό υγρό (cosolvent-aided dissolution, (CS)). Από μετρήσεις με DLS που πραγματοποιήθηκαν, παρατηρήθηκε ότι μέσω της μεθόδου DD σχηματίζονται μικκύλια μεγάλου μεγέθους και μεγάλης πολυδιασποράς, με μέση υδροδυναμική ακτίνα, <R h >, να παρουσιάζει μια σταθερή τιμή μεγέθους γύρω στα 29nm. Οι εικόνες Cryo-Tem επιβεβαίωσαν ύστερα από αύξηση της θερμοκρασίας στους C τη σφαιρική δομή των μικκυλίων, που είχαν δημιουργηθεί μέσω της μεθόδου DD. Επιπροσθέτως. κρίνεται σκόπιμο νʾαναφερθεί, ότι το μέγεθος των μικκυλίων παραμένει αμετάβλητο με την μεταβολή θερμοκρασίας και συγκεκριμένα στο θερμοκρασιακό εύρος C. Μέσω της μεθόδου CS παρατηρήθηκε η δημιουργία σφαιρικών μικκυλίων μικρότερου μεγέθους με τη μέση υδροδυναμική ακτίνα, <R h >, να κυμαίνεται γύρω στα 15nm και να παραμένει 14
24 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 αμετάβλητη κατά την επιβολή θερμοκρασίας. Αξιοσημείωτο είναι πως τα μικκύλια από την μέθοδο CS έχουν το μισό μέγεθος από τα μικκύλια που σχηματίστηκαν με τη μεθόδο DD. Επίσης, είναι σημαντικό νʾαναφερθεί ότι τα μικκύλια που προκύπτουν από την CS μέθοδο, χρησιμοποιώντας ως συνδιαλύτη είτε διχλωρομεθάνιο (CH 2 Cl 2 ) είτε τετραυδροφουράνιο (THF), παρουσιάζουν ίδιο μέγεθος. Έτσι, αποδεικνύεται, πως η επιλογή διαλύτη για τη διάλυση του PEO, δεν επηρεάζει την μορφολογία και το μέγεθος των μικκυλίων 30. Στη συνέχεια, μελετώντας την κινητικότητα των μικκυλίων, προτάθηκε ότι η χαλάρωση των μικκυλίων μέσω διάσπασης/ένωσης είναι δυνατή να παρατηρηθεί μόνο σε μικκύλια που παρασκεάστηκαν με την μέθοδο DD. Τέλος, παρατηρήθηκε πως είτε επιλέγοντας άλλο διαλύτη είτε αντικαθιστώντας το πολυμερές PB με PS, τ αποτελέσματα που προέκυψαν ήταν ανάλογα με αυτά που αναφέρθηκαν προηγουμένως και για τις δυο διαφορετικές μεθόδους. Η μελέτη της θερμοευαισθησίας δισυσταδικών συμπολυμερών, πραγματοποιήθηκε από τους Lodge et al. 31. Τα δισυσταδικά συμπολυμερή (PBnMA(11)-b-PNIPAm) και (PBnMA(22)-b-P(NIPAm-r-ΑΑm)), όπου BnMA, NIPAm και AAm είναι βενζυλικός μεθυλεστέρας, Ν-ισοπροπυλακρυλαμίδιο και ακρυλαμίδιο αντίστοιχα, αυτο-οργανώνονται σε μικκύλια στo μίγμα ιοντικών υγρών [ΕΜΙM][TFSI]/[BMIM][PF 6 ]. Το ενδιαφέρον είναι ότι το PNIPAm ενώ παρουσιάζει κατώτερη κρίσιμη θερμοκρασία διάλυσης (LCST) σε υδατικά διαλύματα 32, σε ιοντικά υγρά παρουσιάζει ανώτερη κρίσιμη θερμοκρασία διάλυσης (UCST) 33 και το PBnMA εμφανίζει κατώτερη κρίσιμη θερμοκρσία διάλυσης (LCST). Σε χαμηλές θερμοκρασίες τα συμπολυμερή αυτο-οργανώνονται σε μικκύλια, όπου ο πυρήνας σχηματίζεται από το PNIPAm, ενώ πάνω από τη κατώτερη κρίσιμη θερμοκρασία διάλυσης (LCST) του PBnMA, ο πυρήνας των μικκυλίων σχηματίζεται από το PBnMA. Σε ενδιάμεσες θερμοκρασίες, παρατηρείται η ύπαρξη μονομερών αλυσίδων (εικόνα 1.8). Από μετρήσεις DLS που πραγματοποιήθηκαν στο σύστημα, παρατηρείται η θερμοκρασιακή εξάρτηση του PBnMA(11)-b-PNIPAm συγκέντρωσης 1wt% στο μίγμα ιοντικών υγρών [ΕΜΙΜ][TFSI]/[BMIM][PF 6 ]. 15
25 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.8: Απεικόνιση θερμοευαίσθητου συμπολυμερούς σε ιοντικό υγρό. Η κόκκινη και μπλέ συστάδα αναφέρονται στο πολυμερες με UCST και LCST, αντίστοιχα. Οι εικόνες αναφέρονται στο PBnMA(22)-b-P(NIPAm-r-AAm) συγκέντρωσης 1wt% στο ιοντικό υγρό [EMIM][TFSI] σε χαμηλή, ενδιάμεση και υψηλή θερμοκρασία, αντίστοιχα 31. Σε θερμοκρασία ~30 0 C, κοντά στη UCST του PNIPAm, και πάνω από τους C, στη LCST του PBnMA, σχηματίζονται μικκύλια, όπως υποδεικνύουν οι υψηλές κορυφές της κανονικοποιημένης έντασης σκέδασης συναρτήσει της θερμοκρασίας (σχήμα 1.9a). Επίσης, παρατηρείται και η θερμοκρασιακή εξάρτηση της υδροδυναμικής ακτίνας, R h, όπου οι δύο κορυφές αντιστοιχούν στη δημιουργία μικκυλίων (σχήμα 1.9b). Τα μικκύλια σε υψηλές θερμοκρασίες, όπου ο πυρήνας σχηματίζεται από το PBnMA και η κορώνα από το PNIPAm, έχουν μεγαλύτερο μέγεθος σε σχέση με τις χαμηλές θερμοκρασίες, όπου το PNIPAm σχηματίζει το πυρήνα. Περαιτέρω αύξηση της θερμοκρασίας πάνω από τους C οδηγεί στην υποβάθμιση τους πολυμερούς. Αυτό, ίσως οφείλεται στο ανιόν [PF 6 ] του ιοντικού υγρού [BMIM][PF 6 ] το οποίο προκαλεί την παραγωγή όξινων προϊόντων HF 34 και οδηγεί στην αποσύνθεση του πολυμερούς. Σε θερμοκρασίες κάτω από τους C αντίθετα δεν παρατηρείται αποσύνθεση του πολυμερούς. 16
26 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.9: (a) Κανονικοποιημένη ένταση σκέδασης συναρτήσει της θερμοκρασίας, του PBnMA(11)-b-PNIPAm σε μίγμα ιοντικών υγρών και σε γωνία 90 ο. Οι τιμές των κανονικοποιημένων εντάσεων είναι διαιρεμένες με τη τιμή της έντασης στους 50 ο C. (b) Θερμοκρασιακή εξάρτηση της υδροδυναμικής ακτίνας του συστήματος PBnMA(11)-b-PNIPAm σε μίγμα ιοντικών υγρών 1:1 [EMIM][TFSI]/[BMIM][PF 6 ] 31. Εν συνεχεία, το ενδιαφέρον για τα θερμο-ευαίσθητα συμπολυμερή οδήγησε στη μελέτη του συστήματος του δισυσταδικού συμπολυμερούς PEO-PNIPAm στα ιοντικά υγρά [EMIM][BF 4 ], [BMIM][BF 4 ] και σε μίγματα αυτών (όπου [EMIM][BF 4 ]: τετραφθοροβοριούχο 1-αίθυλο-3-μεθυλιμιδαζόλιο και [BMIM][BF 4 ]: τετραφθοροβοριούχο 1-βουτυλο-3-μεθυλιμιδαλόλιο) 35. Στα ιοντικά υγρά, το PEO παρουσιάζει LCST και το PNIPAm UCST. Βασιζομένοι σ αυτές τις ιδιότητες παρασκεύασαν θερμο-ευαίσθητα δισυσταδικά συμπολυμερή PEO-PNIPAm. Όπως παρατηρείται στην εικόνα 1.10, σε χαμηλές θερμοκρασίες το PNIPAm σχηματίζει το πυρήνα του μικκυλίου ενώ το PEO την κορώνα. Σε υψηλές θερμοκρασίες, το PEO αποτελεί τον πυρήνα και το PNIPAm την κορώνα του μικκυλίου ενώ, σε ενδιαμέσες θερμοκρασίες προκύπτει διάλυση των συμπολυμερών ή δημιουργία συσσωματομάτων. 17
27 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.10: Σχηματική απεικόνιση δύο τύπων θερμοευαίσθητων συμπολυμερών PEO-PNIPAm σε μίγμα ιοντικών υγρών. Η κόκκινη και μπλε συστάδα αντιπροσωπεύουν το PEO και το PNIPAm, αντίστοιχα. (α) LCMT>UCMT: μικκύλιο-μονομερές-αντίστροφο μικκύλιο. (β) UCMT>LCMT: μικκύλιοσυσσωματώματα συμπολυμερών- αντίστροφο μικκύλιο 35. Μετρήσεις DLS πραγματοποιήθηκαν στο σύστημα PEO-PNIPAm συγκέντρωσης 1%wt στο ιοντικό υγρό [BMIM][BF 4 ] και στο μίγμα ιοντικών υγρών [EMIM][BF 4 ]/[BMIM][BF 4 ]. Στην περίπτωση όπου LCΜT>UCΜT (όπου LCΜT: χαμηλότερη κρίσιμη θερμοκρασία μικκυλοποίησης, UCΜT: ανώτερη κρίσιμη θερμοκρασία μικκυλοποίησης), στο σύστημα PEO-PNIPAm 1wt% στο ιοντικό υγρό [BMIM][BF 4 ] εμφανίζεται η δημιουργία μικκυλίων σε χαμηλές και υψηλές θερμοκρασίες, όπως αποδεικνύεται από τις υψηλές κορυφές της έντασης σκέδασης και της υδροδυναμικής ακτίνας, R h, ενώ σε ενδιάμεσες θερμοκρασίες παρατηρείται διάλυση των αλυσίδων (σχήμα 1.11a και σχήμα 1.12a). Από τα αποτελέσματα της έντασης σκέδασης και της υδροδυναμικής ακτίνας, είναι εμφανείς οι δυο θερμοκρασίες μετάβασης, ~60 ο C (UCΜT) και ~207 ο C (LCΜT). Για το σύστημα PEO-PNIPAm συγκέντρωσης 1wt% στα μείγματα ιοντικών υγρών 85/15 [EMIM][BF 4 ]/[BMIM][BF 4 ] και 70/30 [EMIM][BF 4 ]/[BMIM][BF 4 ] αντίστοιχα, δύο θερμοκρασίες μεταβάσης είναι εμφανείς, υποδεικνύοντας τη μεταβάση μικκυλίων σε μονομερή (unimers) και τελικά σε αντίστροφα μικκύλια. Οι UCMT και LCMT του συστήματος συμπολυμερούς/ιοντικών υγρών αυξάνονται και μειώνονται αντίστοιχα, 18
28 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 καθώς το ποσοστό του [EMIM][BF 4 ] αυξάνεται. Έτσι, μεταβάλλοντας το ποσοστό του ιοντικού υγρού στο σύστημα, ρυθμίζονται οι τιμές των UCMT και LCMT. Εικόνα 1.11: Θερμοκρασιακή εξάρτηση της έντασης σκέδασης για το PEO-PNIPAm συγκέντρωσης 1wt% στο (a) [BMIM][BF 4 ], (b) 85/15 μίγμα [BMIM][BF 4 ]/ [EMIM][BF 4 ], (c) 70/30 μίγμα [BMIM][BF 4 ]/ [EMIM][BF 4 ] 35. Εικόνα 1.12: Θερμοκρασιακή εξάρτηση της υδροδυναμικής ακτίνας R h του PEO-PNIPAm συγκέντρωσης 1wt% στο (a) [BMIM][BF 4 ], (b) 85/15 μίγμα [BMIM][BF 4 ]/ [EMIM][BF 4 ], (c) 70/30 μίγμα [BMIM][BF 4 ]/ [EMIM][BF 4 ] 35. Ομοίως, και στην περίπτωση LCΜT<UCΜT, στο σύστημα PEO-PNIPAm συγκέντρωσης 1wt% στο ιοντικό υγρό [BMIM][BF 4 ] και στο μίγμα ιοντικών υγρών [EMIM][BF 4 ]/[BMIM][BF 4 ], δημιουργούνται μικκύλια όπου το PNIPAm και το PEO σχηματίζουν τον πυρήνα των μικκυλίων σε χαμηλές και υψηλές θερμοκρασίες, αντίστοιχα. Αντίθετα, σε ενδιάμεσες θερμοκρασίες ( ο C), συμβαίνει διάλυση του συμπολυμερούς, το οποίο είναι εμφανές από τη δημιουργία θολώματος (cloudy) στο διάλυμα, το οποίο υποδεικνύει ότι η LCΜT είναι μικρότερη από τη UCΜT 19
29 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 (εικόνα 1.13). Η περαιτέρω αύξηση της θερμοκρασίας, οδηγεί σε δημιουργία συσσωματωμάτων λόγω των διασκορπισμένων μικκυλίων. Εικόνα 1.13: Δημιουργία μικκυλίων στο σύστημα PEO- PNIPAm συγκέντρωσης 1wt% σε μίγμα 50/50 ιοντικών υγρών [EMIM][BF 4 ]/[BMIM][BF 4 ]: (a) θερμοκρασιακή εξάρτηση της υδροδυναμικής ακτίνας (R h ) από πειράματα DLS 35. Εν συνεχεία, μελετήθηκε η λυοτροπική και θερμοτροπική συμπεριφορά του συμπολυμερούς πολυ(στυρόλιο)-b-πολυ(2-βινυλπυριδίνη), S2VP, στο ιοντικό υγρό δι(τριφθοροσουλφονοαμιδιούχο) δισ(τριφθορομεθύλσουλφονύλ)ιμιδιούχο ιμιδαζόλιο, [Im][TFSI], μέσω SAXS και οπτικής μικροσκοπίας 36. Διαπιστώθηκε μέσω των προαναφερόμενων τεχνικών χαρακτηρισμού, ότι το ιοντικό υγρό [Im][TFSI] είναι εκλεκτικός διαλύτης για το πολυμερές P2VP. Μέσω της σκέδασης ακτίνων-χ, παρατηρήθηκε η ύπαρξη φυλλωτής (lamellar) και κυλινδρικής δομής, καθώς επίσης και φάσεις αταξίας. Οι θερμικές ιδιότητες του συστήματος S2VP/[Im][TFSI] παρουσιάζουν σημαντικό ενδιαφέρον. Τα διαλύματα υψηλής συγκέντρωσης παρουσιάζουν αύξηση της θερμοκρασίας υαλώδους μετάπτωσης, T g, του συμπολυμερούς S2VP και κατά συνέπεια το ιοντικό υγρό συμπεριφέρεται ως άλας. Σε ενδιάμεσες θερμοκρασίες, παρατηρείται μείωση της T g και το ιοντικό υγρό συμπεριφέρεται ως "πλαστικοποιητής" (plasticizer). 20
30 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΤΡΙΣΥΣΤΑΔΙΚΑ ΣΥΜΠΟΛΥΜΕΡΗ (ΑΒΑ) ΣΕ ΙΟΝΤΙΚΟ ΔΙΑΛΥΤΗ Τα τρισυσταδικά συμπολυμερή είναι σημαντικά πολυμερικά υλικά, καθώς παρουσιάζουν ενδιαφέρουσα αρχιτεκτονική, δίνοντας μια ποικιλία σε νανοδομές με την επιλογή των κατάλληλων μονομερών τμημάτων. Το ενδιαφέρον της επιστημονικής κοινότητας έχει στράφει σε πειραματικές και θεωρητικές μελετές που αφορούν στον έλεγχο των φυσικών ιδιοτήτων, στην ρεολογική συμπεριφορά των υλικών κ.α.. Η παρασκευή τρισυσταδικών συμπολυμερικών διαλυμάτων σε ιονικά υγρά (ionic liquids), κερδίζει συνεχώς έδαφος τα τελευταία χρόνια. Η επιλογή του κατάλληλου διαλύτη είναι καθοριστική. Τα ιοντικά υγρά, που ανήκουν στην οικογένεια των ιμιδαζολίων όπως το [BMIM][PF 6 ], παρουσιάζουν χαμηλή τάση ατμών και υψηλή αγωγιμότητα και γι αυτό χρησιμοποιούνται κατά κόρον για την παρασκευή πολυμερικών διαλυμάτων 37. Στη συνέχεια γίνεται παράθεση ερευνών που έχουν πραγματοποιηθεί για τα τρισυσταδικά συμπολυμερικά διαλύματα σε ιοντικά υγρά. Οι Lodge et. al. 38 μελέτησαν το σύστημα τρισυσταδικού συμπολυμερούς PS-PEO- PS στο ιοντικό υγρό [BMIM][PF 6 ] που είναι "καλός" διαλύτης για το PEO 19. Φαινόμενα διασύνδεσης και δημιουργία φυσικών πηκτωμάτων (gels) εμφανίζονται στο διάλυμα με συγκέντρωση πολυμερούς ~5wt%. Η τιμή της συγκέντρωσης του πολυμερούς που σχηματίζονται τα gels είναι πολύ χαμηλότερη σε σύγκριση με αυτή στα διαλύματα πολυμερών σε κοινούς διαλύτες. Σε κοινούς διαλύτες, η συγκέντρωση των περισσότερων πολυμερικών πηκτωμάτων κυμαίνεται γύρω στα 10-30wt%. Η διαπίστωση αυτή ώθει στην αντικατάσταση των κοινών διαλυτών από τα ιονικά υγρά, καθώς απαιτείται λιγότερη ποσότητα πολυμερούς για την δημιουργία gels και η αγωγιμότητά τους είναι συγκρίσιμη ή και υψηλότερη από τους συμβατικούς πολυηλεκτρολύτες σε κοινούς οργανικούς διαλύτες. Από ρεολογικές μετρήσεις που πραγματοποιήθηκαν, παρατηρήθηκε ότι το σύστημα PS-PEO-PS/[BMIM][PF 6 ] σε συγκέντρωση πολυμερούς 10%wt, παραμένει θερμικά σταθερό σε θερμοκρασία C και παρουσιάζει καλή μηχανική αντοχή (εικόνα 1.14). Τα δυναμικά μέτρα, G' και G", συναρτήσει της συχνότητας, ω, μετρήθηκαν για τα gels στο θερμοκρασιακό εύρος C. Ελαστική συμπεριφορά παρατηρείται κάτω από 10 rad/s, καθώς το G'> G". Σε υψηλότερες συχνότητες και τα δυο δυναμικά μέτρα αυξάνονται, πιθανόν 21
31 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 λόγω της χαλάρωσης του δικτύου (των συστάδων PEO). Έπισης, σε χαμηλές θερμοκρασίες ( C), το μέτρο αποθήκευσης G' είναι ανεξάρτητο από την θερμοκρασία, ενώ σε υψηλότερες θερμοκρασίες η τιμή του G' αυξάνεται. Γύρω στους C, παρατηρείται η ύπαρξη δυο πλατώ του G': το ένα πλατώ σε χαμηλές συχνότητες, G'=1600 Pa και το άλλο σε υψηλές συχνότητες, G'=2500 Pa.. Εικόνα 1.14: Μέτρο αποθήκευσης (G') και μέτρο απωλειών (G") συναρτήσει της συχνότητας για το σύστημα PS-PEO- PS/[BMIM][PF 6 ] 10wt% σε θερμοκρασιακό εύρος C 38. Ενδιαφέρον θα παρουσίαζε η μέλετη του ίδιου τρισυσταδικού συμπολυμερούς σε άλλο ιοντικό υγρό. Μια τέτοια προσπάθεια έγινε από τους Lodge et al 39 οι οποίοι μελέτησαν την ιξωδοελαστική συμπεριφορά και υπολόγισαν την αγωγιμότητα των 22
32 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 φυσικών πηκτωμάτων του συστήματος PS-PEO-PS/[EMIΜ][TFSΙ] σε συγκεντρώσεις πολυμερούς από 10-50wt% και σε θερμοκρασιακό εύρος C. Καταρχάς, μελετήθηκε η δομική διευθέτηση του τρισυσταδικού συμπολυμερούς μέσω της τεχνικής SAXS. Το τρισυσταδικό συμπολυμερές καθώς διαλύεται στο ιοντικό υγρό δημιούργει μικκύλια όπου το PS είναι το δυσδιάλυτο τμήμα του συμπολυμερούς και σχηματίζει τον πυρήνα και το PEO το οποίο αποτελεί το ευδιάλυτο τμήμα, δημιουργεί την κορώνα του μικκυλίου (εικόνα 1.15). Εικόνα 1.15: Σχηματική αναπαράσταση ενός gel του τρισυσταδικού συμπολυμερούς PS-PEO-PS σε ιοντικό υγρό 39. Στα πηκτώματα PS-PEO-PS/[EMIΜ][TFSΙ] συγκεντρώσεων από 10-50wt%, πραγματοποιήθηκαν πειράματα μέτρησης των δυναμικών μέτρων G' και G" συναρτήσει της συχνότητας, ω, σε εύρος θερμοκρασιών C. Για συγκέντρωση 10wt% σε υψηλές θερμοκρασίες, το σύστημα PS-PEO-PS/[EMIΜ][TFSΙ] "τήκεται" καθώς οι αλυσίδες του PS αποσυνδέονται στους 54 0 C και ο χρόνος χαλάρωσης του συστήματος συναρτήσει της θερμοκρασίας είναι κατά 4 τάξεις μεγέθους μεγαλύτερος σε σύγκριση με τον χρόνο χαλάρωσης του στερεού πολυστυρενίου στις ίδιες συνθήκες. Aυτό αποδίδεται στη θερμοδυναμική ποινή του συστήματος καθώς οι ακραίες συστάδες PS "εξωθούνται" από τη μήτρα του PEO/[EMIM][TFSΙ]. Για διαλύματα υψηλότερης συγκέντρωσης, 20-50wt%, το σύστημα PS-PEO- PS/[EMIΜ][TFSΙ] δεν "τήκεται" σε υψηλές θερμοκρασίες αλλά αντιθέτως παρατηρείται η ύπαρξη δυο πλατώ του μέτρου αποθηκευσης, G', σε χαμηλές και υψηλές συχνότητες αντίστοιχα. Το ενδιαφέρον για θερμο-ευαίσθητα πολυμερικά συστημάτα, οδήγησε σε περαιτέρω έρευνα και παρασκευή τρισυσταδικών πολυμερικών διαλυμάτων 23
33 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 διαφορετικής σύστασης σε ιοντικά υγρά που υπο την επίδραση της θερμοκρασίας σχηματίζουν θερμοαποκρινόμενα πηκτώματα (thermoreversible ion gels). Έτσι, πραγματοποιήθηκαν ρεολογικές μελέτες στο τρισυσταδικό σύστημα συμπολυμερούς PNIPAm-PEO-PNIPAm/[EMIΜ][TFSI] συγκέντρωσης 10wt%, που αποτελείται από θερμο-ευαίσθητες συστάδες PNIPAm 40. Πειράματα εξάρτησης των δυναμικών μέτρων G' και G'' από τη συχνότητα, ω, πραγματοποιήθηκαν για το σύστημα σε θερμοκρασιακό εύρος C. Όπως φαίνεται και στην εικόνα 1.16, σε θερμοκρασία ~50 0 C το σύστημα PNIPAm-PEO-PNIPAm/[EMIΜ][TFSI] συμπεριφέρεται ως υγρό. Το μέτρο αποθήκευσης, G', είναι μικρότερο από το μέτρο απωλείων, G'', και τα δυο δυναμικά μέτρα παρουσιάζουν διαφορετική εξάρτηση από τη συχνότητα: G'~ω 2 και G''~ω, τυπική συμπεριφορά παχύρρευστου υγρού 41. Στους 5 0 C, το σύστημα είναι ένα διαφανές gel. Το μέτρο αποθήκευσης, G', είναι μεγαλύτερο από το μέτρο απωλείων, G'', και τα δυο δυναμικά μέτρα είναι σχέδον ανεξάρτητα από την συχνότητα, ω - χαρακτηριστική συμπεριφορά μαλακού στερεού (solid like). Στις ενδιάμεσες θερμοκρασίες, δηλαδή ~20 0 C, παρατηρείται η μετάβαση από υγρό σε μαλακό στερεό και εντοπίζεται το σημείο δημιουργίας πηκτώματος (gel point) 42. Στην εικόνα 1.17 που ακολουθεί, είναι πιο εμφανής η θερμοκρασία μεταβάσης από μαλακό στερεό σε υγρό, η οποία εντοπίζεται γυρώ στους 17 0 C. Εικόνα 1.16: Τα μέτρα αποθήκευσης, G', και απωλείων, G", του συστήματος PNIPAm-PEO- PNIPAm/[EMIM][TFSI] συναρτήσει της συχνότητας, ω, σε τρεις διαφορετικές θερμοκρασίες
34 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.17: Εξάρτηση του μέτρου αποθήκευσης, G', και μέτρου απωλείων, G", σαν συνάρτηση της θερμοκρασίας για το gel PNIPAm-PEO-PNIPAm/[EMIM][TFSI] σε συχνότητα, ω=0.1 rad/s και τάση, γ=5%. Οι φωτογραφίες αντιστοιχούν στο σύστημα σε αντίστοιχες θερμοκρασίες 40. Στην συνέχεια, η ίδια ερευνητική ομάδα επιχείρησε να ρυθμίσει την κρίσιμη θερμοκρασία δημιουργίας πηκτώματος, T gel (gelation temperature), κοντά στη θερμοκρασία δωματίου 43. Ο σκόπος αυτής της προσπάθειας ήταν να βρούν εφαρμογή τα συγκεκριμένα gels σε διάφορες συσκευές, όπως πχ στα τρανζίστορ. Η ρύθμιση της Τ gel μπορεί να επιτευχθεί με την προσθήκη δυσδιάλυτων μονομερών σε ιοντικά υγρά, όπως έχει αναφερθεί σε κάποια συστήματα πολυμερούς/ιονικού υγρού 44. Ετσι, με την προσθήκη συστάδων PS στο τρισυσταδικό συμπολυμερές PNIPAm-PEO- PNIPAm (NON) προέκυψε το πεντασυσταδικό συμπολυμερές PNIPAm-PS-PEO-PS- PNIPAm (NSOSN), όπου επετεύχθει η ρύθμιση της θερμοκρασίας μετάβασης T gel στο θερμοκρασιακό εύρος C. Όπως παρατηρείται, με την προσθήκη του PS, το πεντασυσταδικό συμπολυμερές παρουσιάζει υψηλότερη θερμοκρασία μεταβάσης σε σχέση με το τρισυσταδικό συμπολυμερές (εικόνα 1.18). Επίσης, είναι αξιόλογο να επισημάνουμε πως η θερμοκρασία μεταβάσης του πεντασυσταδικού συμπολυμερούς (NSOSN-1) συγκέντρωσης 5wt% είναι μόνο κατά 3 0 C μικρότερη από τη θερμοκρασία μετάβασης του ίδιου συμπολυμερούς συγκέντρωσης 10wt%. 25
35 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.18: Τα δυναμικά μέτρα G' και G", συναρτήσει της θερμοκρασίας για το gel NSOSN-1, σε συγκεντρώσεις 5%wt και 10%wt 44. Έκτος, από την προσθήκη PS, οι Lodge et al. παρατήρησαν ότι και με τη μεταβολή του μοριακού βάρους PS και συγκεκριμένα με την αύξηση του μοριακού βάρους, αυξάνεται και η T gel. Στην εικόνα 1.19 που ακολουθεί, παρατηρείται η εξάρτηση των δυναμικών μέτρων G' και G" από την θερμοκρασία για 3 δείγματα (NON, NSOSN-1, NSOSN-2) ίδιας συγκέντρωσης, 10%wt. Το PEO και το PNIPAm έχουν το ίδιο μοριακό βάρος και στα 3 δείγματα, ενώ μεταβάλλεται το μοριακό βάρος του λυόφοβου PS. Στο gel NSOSN-2, το PS έχει μεγαλύτερο μοριακό βάρος από το gel NSOSN-1 (NSOSN-1: MB 3300 Da, NSOSN-2: MB 3800 Da). Είναι εμφανές από το παρακάτω σχήμα ότι με την προσθήκη συστάδων PS στο σύστημα NON, η T gel αυξάνεται κατά 20 0 C στο gel NSOSN-1 και με αύξηση του μοριακού βάρους του PS, η T gel αυξάνεται επιπρόσθετα κατά 10 0 C για το σύστημα NSOSN-2. Επιπλέον, μελετήθηκε η δομική διαμόρφωση του τρισυσταδικού και πεντασυσταδικού συμπολυμερούς μέσω της δυναμικής σκέδασης φώτος (DLS) στο θερμοκρασιακό εύρος C. Η σχηματική απεικόνιση (εικόνα 1.20) δείχνει ότι στην περίπτωση του τρισυσταδικού συμπολυμερούς NON, καθώς αυξάνεται η θερμοκρασία, το συμπολυμερές "τήκεται" λόγω της αποσύνδεσης του πυρήνα που συγκροτείται από το λυόφοβο PNIPAm και η δημιουργία μικκυλίων δεν 26
36 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 παρατηρείται πλεον. Ο μηχανισμός αυτός αποσύνδεσης έχει παρατηρηθεί σε "θερμοπλαστικά ελαστομερή" συστήματα 45. Για το πεντασυσταδικό συμπολυμερές NSOSN αντίθετα, κάτω από την T gel παρατηρείται η δημιουργία μικκυλίων (πυρήνας-φλοιός-κορώνα) όπου το PNIPAm σχηματίζει το πυρήνα, το PS τον φλοιό και τέλος το PEO δημιουργεί την κορώνα του μικκυλίου. Καθώς αυξάνεται η θερμοκρασία, παρατηρείται η θερμοδυναμική διάσπαση των συσσωματωμάτων του PNIPAm και πλέον το PS σχηματίζει το πυρήνα του μικκυλίου. Εικόνα 1.19: Θερμοκρασιακή εξάρτηση των δυναμικών μέτρων G' και G" για τα 3 δείγματα NON, NSOSN-1, NSOSN-2, συγκέντρωσης 10wt% 44. Εικόνα 1.20: Σχηματική απεικόνιση της θερμο-αποκρινόμενης συμπεριφοράς των gels NON και NSOSN
37 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Σε άλλη μελέτη εξερευνήθηκαν οι ιξωδοελαστικές και ηλεκτρικές ιδιότητες δυο τρισυσταδικών συμπολυμερών διαφορετικής σύστασης, του PS-PEO-PS και του PS- PMMA-PS στο ιοντικό υγρό [EMIM][TFSI] 46. Το PS σχηματίζει τον πυρήνα του μικκυλίου καθώς το ιοντικό υγρό είναι "κακός" διαλύτης, ενώ το PEO και το PMMA διαλύονται στο [EMIM][TFSI]. Οι ιδιότητες των gels PS-PEO-PS και PS-PMMA-PS συγκέντρωσης 10-50wt% εξετάστηκαν στο θερμοκρασιακό εύρος C και C, αντίστοιχα. Σύμφωνα με τις ρεολογικές μελέτες (εικόνα 1.21), για το PS- PEO-PS συγκέντρωσης 10%wt το μέτρο αποθήκευσης, G', συναρτήσει της συχνότητας, ω, στο θερμοκρασιακό εύρος C και σε ω=10rad/s παρουσιάζει πλατώ, το οποίο δείχνει πως το δίκτυο του συστήματος είναι αμετάβλητο. Για θερμοκρασία πάνω από C, διακρίνονται δυο πλατώ του G'. Η ίδια συμπεριφορά είχε παρατηρηθεί και για το σύστημα PS-PEO-PS/[EMIM][TFSI] σε προηγουμένη μέλετη 37. Εικόνα 1.21: Δυναμικά μέτρα G' και G" συναρτήσει της συχνότητας, ω, του PS-PMMA-PS/[EMIM][TFSI] συγκέντρωσης 10wt% για (α) αργός ρυθμός χαλάρωσης (b) γρήγορος ρυθμός χαλάρωσης. Συγκρίνοντας τα δυο συστήματα των τρισυσταδικών συμπολυμερών, το PS- PMMA-PS/[EMIM][TFSI] και το PS-PEO-PS/[EMIM][TFSI] και έχοντας την ίδια συγκέντρωση και ίδιο αριθμό συστάδων πολυμερούς, οι Lodge et al. συμπέραναν ότι 28
38 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 το τρισυσταδικό συμπολυμερές PS-PEO-PS παρουσιάζει μεγαλύτερη αγωγιμότητα και μέτρο αποθήκευσης από το PS-PMMA-PS. Πρόσφατα, οι Watanabe et al. 47 χρησιμοποιώντας το τρισυσταδικό συμπολυμερές, PS-PMMA-PS μελέτησαν τις ρεολογικές ιδιότητες στο ιοντικό υγρό [EMIM][TFSΙ]. Καταρχάς, μελέτησαν τη δομή του τρισυσταδικού συστήματος μέσω της AFM. Το PS καθώς είναι δυσδιάλυτο στο ιοντικό υγρό [EMIM][TFSΙ] δημιουργεί σφαιρικές δομές ενώ το PMMA που είναι συμβατό με το [EMIM][TFSΙ] διαλύεται δημιουργώντας μια ομοιόμορφη επιφάνεια. Έτσι, στο τρισυσταδικό συμπολυμερές PS-PMMA-PS/[EMIM][TFSΙ] συγκέντρωσης 30wt% παρατηρείται διαχωρισμός φάσεων (εικόνα 1.22). Οι φωτεινές περιοχές αντιστοιχούν στο PMMA που έχει διαλυθεί πλήρως ενώ οι σφαιρικές σκούρες περιοχές στο PS. Εικόνα 1.22: Εικόνα AFM του gel PS-PMMA-PS-48 συγκέντρωσης 30wt%
39 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 Εικόνα 1.23: (α) Θερμοκρασιακή εξάρτηση του G' και G" των gels PS-PMMA-PS- 48 (10%wt) και PS-PMMA-PS-18 (10wt%) σε συχνότηα ω=1rad/s. (β) Δυναμικά μέτρα (G' και G") συναρτήσει της παραμόρφωσης για τα PS-PMMA-PS-18 και PS- PMMA-PS-48 συγκέντρωσης 15wt% σε θερμοκρασία 25 0 C και συχνότητα ω=1 Hz 47. Μέσω των ρεολογικών μελετών που πραγματοποιήθηκαν για το σύστημα PS- PMMA-PS/[EMIΜ][TFSΙ], οι Watanabe et al. συμπέραναν ότι μεταβάλλοντας το ποσοστό του πολυστυρενίου (f PS ) στο σύστημα, επηρεάζονται οι ιξωδοελαστικές ιδιότητες του gel. Όπως παρατηρούμε και στην εικόνα 1.23α, για το gel PS-PMMA- PS-18 με ποσοστό PS μικρότερο από του gel PS-PMMA-PS-48 σε ίδια συγκέντρωση (10wt%), τα δυναμικά μέτρα G' και G" και η θερμοκρασία μετάβασης (T gel ) παρουσιάζουν μικρότερες τιμές σε σύγκριση με το PS-PMMA-PS-48. Η διαφορά που παρατηρείται στην T gel για τα δυο τρισυσταδικά συστήματα, εμφανίζεται λόγω της ασυμβατότητας του PS με το ιοντικό υγρό και επηρεάζεται σε μεγάλο βαθμό από το ποσοστό πολυστυρενίου. Επιπροσθέτως, οι πειραματικές μετρήσεις του μέτρου αποθήκευσης και του μέτρου απωλειών συναρτήσει της παραμόρφωσης, δείχνουν ότι κατά της εφαρμογή υψηλών τάσεων το φυσικό δίκτυο διασπάται (εικόνα 1.23β). Η συμπεριφορά αυτή παρατηρείται πιθανότατα λόγω του ότι οι αλυσίδες του PS αποσυνδέονται με αποτέλεσμα να αποκτούν κινητικότητα. Έπισης, ο λογος tanδ (= G'/G") είναι μεγαλύτερος για το PS-PMMA-PS-18 σε σύγκριση με το PS-PMMA- PS-48, το οποίο μας οδηγεί στο συμπέρασμα ότι ο αριθμός των αναδιπλούμενων αλυσίδων είναι μεγαλύτερος στο gel PS-PMMA-PS
40 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΒΙΒΛΙΟΓΡΑΦΙΑ 1 Heise A.; Hedrick J. L.; Frank C. W.; Miller A. D., J. Am. Chem. Soc., 1999, 121, Hadjichristidis N.; Pitsikalis M.; Pispas S.; Iatrou H., Chem. Rev., 2001, 101, Triftaridou A. I.; Hadjiyannakou S. C.; Vamvakaki M.; Patrickios C. S., Macromolecules, 2002, 35, Flory, P. J., J. Phys. Chem. 1942, 46, Anastas PT. Benign by design chemistry. In: Benign by Design: Alternative Synthetic Design for Pollution Prevention, ACS Symposium Series 577 (Anastas PT, Farris CA, eds.) Washington: American Chemical Society pp 1-21, Darrell D.Ebbing, Steven D.Gammon General Chemistry 9th Edition Houghton Mifflin Co (2008) pg 7 Winterton N. J. Am. Chem., 2006, 16, "Εναλλακτικοί διαλύτες, ιοντικοί διαλύτες", Α.Ι. Μαρούλης, Κ. Χατζηαντωνίου, Τσιτσιριδάκη Αγγελική, Πρακτικά 2ου Πανελλήνιου Συμποσίου <<Πράσινη Χημεία και Βιώσιμη Ανάπτυξη>>, Πάτρα "Βιομετασχηματισμοί φυσικών αντιοξειδωτικών σε ιοντικά υγρά", Κατσούρα Μαρία, Πανεπιστήμιο Ιωαννίνων, Lee, H. N.; Bai, Z.; Newell, N.; Lodge, T. P. Macromolecules 2010, 43, Ueki T.; Watanabe M.; Lodge, T. P. Macromolecules 2009, 42, He Y.; Boswell P.G.; Bϋhlmann P.; Lodge, T. P. J. Phys.Chem. B 2007, 111, Ueki T.; Watanabe M. Macromolecules 2008, 41, M. A. B. H. Susan, T. Kaneko, A. Noda and M. Watanabe, J. Am. Chem. Soc., 2005, 127, Shobukawa, H.; Tokuda, H.; Tabata, S.; Watanabe, M. Electrochim. Acta 2004, 50, Boswell, P. G.; Lugert, E. C.; Rabaj, J.; Amin, E. A.; Bühlmann, P. J. Am. Chem. Soc. 2005, 127,
41 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 17 Lee, J.; Panzer, M. J.; He, Y.; Lodge, T. P.; Frisbie, C. D. J. Am. Chem. Soc. 2007, 129, Fukushim, T.; Kosaka, A.; Yamamoto, Y.; Aimiya, T.; Notazawa, S.; Takigawa, T.; Inabe, T.; Aida, T. Small 2006, 2, Kawano, R.; Matsui, H.; Matsyama, C.; Sato, A.; Susan, M. A. B. H.; Tanabe, N.; Watanabe, M. J. Photochem. Photobiol., A 2004, 164, (a) He, Y.; Li, Z.; Simone, P.; Lodge, T. P. J. Am. Chem. Soc. 2006, 128, (b) Simone, P.; Lodge, T. P. Macromol. Chem. Phys. 2007, 208, He Y.; Li Z.; Simone P.; Lodge P. T. J. Am. Chem. Soc. 2006, 128, Zhang, L. F.; Eisenberg, A. Science 1995, 268, Simone M. P.; Lodge P. T. Macromolecules 2008, 41, Simone M. P.; Lodge P. T. Macromolecular Chem. Phys. 2007, 208, He Y.; Lodge P. T.; J. Am. Chem. Soc. 2006, 128, Dormidontova, E. E. Macromolecules 2004, 37, Smith, G. D.; Bedrov, D. J. Phys. Chem. B 2003, 107, Bai Z.; Lodge P. T.; J. Am. Chem. Soc. 2010, 132, Meli L.; Santiago M. J.; Lodge P. T. Macromolecules, 2010, 43, pp Moldovan, P. L.; Strazielle, C. Macromol. Chem. 1970, 140, Ueki T.; Watanabe M.; Lodge P. T. Macromolecules 2009,42, Schild, H. G. Prog. Polym. Sci. 1992, 17, Ueki, T.; Watanabe, M. Chem. Lett. 2006, 35, (a) Najdanovic-Visak, V.; Esperanca, J. M. S. S.; Rebelo, L. P. N.; Ponte, M. N.; Guedes, H. J. R.; Seddon, K. R.; Szydlowski, J. Phys. Chem. 2002, 4, (b) Swatloski, R. P.; Holbrey, J. D.; Rogers, R. D. Green Chem. 2003, 4, Lee H-N.; Bai Z.; Newell N.; Lodge P. T. Macromolecules 2010, 43, Virgili M. J.; Hexemer A.; Pople A. J.; Balsara P. N.; Segalman A. R. Macromolecules 2009, 42, Bonhote, P.; Dias, A. P.; Papagergiou, N.; Kalyanasundaram, K.; Gratzel, M. Inorg. Chem. 1996, 35, He Y.; Boswell P. G.; Bühlmann P.; Lodge P. T.; J. Phys. Chem. B. 2007, 111,
42 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 1 39 Zhang S.; Lee H. K.; Sun J.; Frisbie D. C.; Lodge P. T.; Macromoleculus, 2011, 44(22) pp He Y.; Lodge P. T.; Chem. Commun., 2007, R. G. Larson, The Structure and Rheology of Complex Fluids, Oxford University Press, New York, H. H. Winter and F. Chambon, J. Rheol., 1986, 30, 367; F. Chambon, Z. S. Petrovic, W. J. MacKnight and H. H. Winter, Macromoleculus, 1986, 19, He Y.; Lodge P. T.; Macromolecules, 2008, 41, T. Ueki and M. Watanabe, Langmuir, 2007, 23, 988; Y. G. Takei, T. Aoki, K. Sanui, N. Ogata, T. Okano and Y. Sakurai, Bioconjugate Chem. 1993, 4, Drzal, P. L.; Shull, K. R. Macromolecules 2003, 36, Zhang S.; Lee H. K.; Frisbie D. C.; Lodge P. T. Macromolecules 2011, 44, Imaizumi S.; Kokubo H.; Watanabe M.; Macromolecules 2012, 45,
43 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 ΜΕΘΟΔΟΙ ΧΑΡΑΚΤΗΡΙΣΜΟΥ ΠΟΛΥΜΕΡΩΝ 2.1 ΧΡΩΜΑΤΟΓΡΑΦΙΑ ΑΠΟΚΛΕΙΣΜΟΥ ΜΕΓΕΘΩΝ (SEC) Μια από τις σημαντικότερες μεθόδους καθορισμού του μοριακού βάρους και της κατανομής μοριακών βαρών των πολυμερών είναι η χρωματογραφία αποκλεισμού μεγεθών (Size Exclusion Chromatography, SEC) η οποία αναφέρεται συχνά στη βιβλιογραφία και ως χρωματογραφία διείσδυσης (Gel Permeation Chromatography, GPC). Είναι ένα είδος υγρής χρωματογραφίας (Liquid Chromatography) και μια από τις πιο χρήσιμες αναλυτικές μεθόδους στη βιομηχανία των πλαστικών. Η χρωματογραφία SEC λειτουργεί και ως μέθοδος ελέγχου πολυμερών, μιας και μας βοηθάει να βελτιώσουμε την μορφή του πολυμερούς με μεθόδους κλασματοποίησης και να επιτύχουμε το σταδιακό καθαρισμό του από προσμίξεις. Ο προσδιορισμός της κατανομής του μοριακού βάρους μέσω της SEC είναι πολύ σημαντικός μιας και αυτή είναι υπεύθυνη για τις ιδιότητες που χαρακτηρίζουν ένα πολυμερές, όπως η σκληρότητα, η ελαστική αντοχή, η ευθραυστότητα και το ιξώδες πολυμερικού μίγματος. Κατά τη διάρκεια της χρωματογραφίας GPC, τα μακρομόρια διαχωρίζονται σύμφωνα με τον υδροδυναμικό τους όγκο, δηλαδή σύμφωνα με την έκταση που καταλαμβάνει το μόριο τους μέσα στο συγκεκριμένο διαλύτη. Η διαδικασία βασίζεται στο γεγονός ότι ένα αραιό πολυμερικό διάλυμα, το οποίο μπορεί να περίεχει μια πλατειά κατανομή ΜΒ πολυμερικών αλυσίδων, ολιγομερών ή ακόμα και μονομερών, τα οποία δεν πολυμερίστηκαν, αφήνεται να περάσει μέσα από μια στήλη η οποία έχει πληρωθεί με στερεά πορώδη σωματίδια πολύς μικρής διαμέτρου 1. Η αρχή της μεθόδου βασίζεται στο γεγονός ότι τα μικρά μόρια μπορούν να διεισδύσουν βαθύτερα μέσα στους πόρους του πληρωτικού υλικού της στήλης με αποτέλεσμα να καθυστερήσουν να εξέλθουν της στήλης, ενώ τα μεγάλα μόρια, επειδή δεν μπορούν να εισχωρήσουν μέσα στους μικρότερους πόρους, εκλούονται πρώτα 2. Ο τρόπος με 34
44 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 τον οποίο διαχωρίζονται τα μόρια αναλόγως του μεγέθους τους φαίνεται στην εικόνα 2.1. Εικόνα 2.1: Σχηματική αναπαράσταση του διαχωρισμού ενός αραιού πολυμερικού διαλύματος με χρήση της χρωματογραφίας GPC. Όταν τα μόρια εξέλθουν από την στήλη κατευθύνονται στον αναλυτή, οπου μετρά τη συγκέντρωση του πολυμερούς σαν συνάρτηση του χρόνου ή του όγκου έκλουσης (V e ) που δίνεται από τις παρακάτω εξισώσεις 3. Για πολύ μεγάλα μόρια, τα οποία αδυνατούν να εισέλθουν στο εσωτερικό του υλικού της σήλης, ο όγκος έκλουσης δίνεται από την εξισώση 2.1: V e V o (2.1) όπου V o είναι ο αποκλειόμενος όγκος, ο οποίος είναι ο συνολικός όγκος των διάκενων μεταξύ των σφαιρικών σωματιδίων. Ενώ, για μικρότερα μόρια που εισχωρούν στους πόρους του πληρωτικού υλικού ισχύει η εξίσωση 2.2: V V K V e o GPC i (2.2) όπου V i είναι ο συνολικός όγκος των πόρων και k GPC είναι ο συντελεστής κατανομής του δείγματος μεταξύ του εσωτερικού και εξωτερικού των πόρων (δηλαδή του όγκου των διάκενων μεταξύ των σωματιδίων), ο οποίος επηρεάζεται από τη φύση του πολυμερούς, τη θερμοκρασία, τον διαλύτη και εξαρτάται από το μέγεθος των σωματιδίων. Είναι προφανές ότι για μεγάλα μόρια k GPC =0 οπότε προκύπτει η εξίσωση 2.1, ενώ για μικρά μόρια k GPC =1. Οι πιο κοινοί ανιχνευτές που χρησιμοποιούνται στη GPC είναι το διαφορικό διαθλασίμετρο (Differential Refractometer, DRI) και/ή ο ανιχνευτής υπεριώδους- 35
45 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 ορατού (UV-Vis) 4. Ο πρώτος ανιχνευτής κατάγραφει τη διαφορά του δείκτη διάθλασης μεταξύ του καθαρού διαλύτη και του πολυμερικού διαλύματος, που εξέρχεται από την στήλη. Για να χρησιμοποιηθεί ανιχνευτής UV-Vis, θα πρέπει το πολυμερές να φέρει τουλάχιστον μια επαναλαμβανόμενη μονάδα, η οποία να είναι ενεργή στο UV. Έτσι, το φασματοφωτόμετρο ρυθμίζεται στο κατάλληλο μήκος κύματος ώστε το λαμβανόμενο σήμα να βελτιστοποιείται. Η χρωματογραφία GPC είναι μια σχετική μέθοδος προσδιορισμού ΜΒ επειδή απαιτεί βαθμονόμηση για μετατροπή της κατανομής όγκων έκλουσης σε κατανομή ΜΒ 4 (εικόνα 2.2). Εικόνα 2.2: Κατανομή του κλάσματος μάζας των μορίων του πολυμερικού δείγματος ως προς τον όγκο ή το χρόνο έκλουσης. Η βαθμονόμηση γίνεται με πρότυπα, μονοδιάσπαρτα πολυμερή, των οποίων τα ΜΒ είναι γνωστά, καθώς έχουν χαρακτηριστεί με απόλυτες μεθόδους, όπως η στατική σκέδαση φωτός. Έτσι, γίνεται γνωστός ο χρόνος κατακράτησης στη στήλη μορίων συγκεκριμένου ΜΒ και με βάση αυτά μπορούν να μετατραπούν οι χρόνοι κατακράτησης αγνώστων δειγμάτων σε ισοδύναμα ΜΒ, με την προϋπόθεση ότι οι συνθήκες διεξαγωγής της βαθμονόμησης και ανάλυσης ενός αγνώστου ΜΒ δείγματος παραμένουν οι ίδιες (π.χ. η πίεση, η στήλη) 4. Τα πιο συνηθισμένα πρότυπα είναι του πολυστυρενίου, πολύ(μεθακρυλικού μεθυλεστέρα) και του πολυαιθυλενοξειδίου. Έτσι, με τη χρήση πρότυπων δειγμάτων γίνεται η βαθμονόμηση με βάση τον υδροδυναμικό όγκο του πολυμερούς στο διαλύτη. 36
46 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 Με την μέθοδο αυτή, μπορούν να υπολογισθούν το μέσο κατά αριθμό ΜΒ, M n,και το μέσο κατά βάρος ΜΒ, βαρών 2, I. Το όπου M n υπολογίζεται μέσω της σχέσης: M N i είναι ο αριθμός των μορίων με μοριακή μάζα M w, καθώς επίσης και η πολυδιασπορά μοριακών NM i i i n nim i i Ni i (2.3) M i και n i είναι το αριθμητικό κλάσμα αυτών των μορίων ( n N / N ). Το M w λαμβάνεται από την εξίσωση: M i i i i N M W M 2 i i i i i i w wi M i i NiM i Wi i i (2.4) όπου W i είναι η μάζα των μορίων με μοριακή μάζα και κλάσμα μάζας αυτών των μορίων ( w W / W ). Τέλος η I υπολογίζεται ως: i i i i M I M w n (2.5) Η Ι μπορεί να πάρει τιμές από 1 μέχρι. Εάν M / M =1 τότε όλα τα μόρια του πολυμερούς έχουν ακριβώς το ίδιο ΜΒ και το πολυμερές λέγεται ότι είναι μονοδιάσπαρτο. w n 2.2 ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΠΥΡΗΝΙΚΟΥ ΜΑΓΝΗΤΙΚΟΥ ΣΥΝΤΟΝΙΣΜΟΥ (NUCLEAR MAGNETIC RESONANCE SPECTROSCOPY, NMR) Η φασματοσκοπία πυρηνικού μαγνητικού συντονισμού (nuclear magnetic resonance, NMR) βασίζεται στη μέτρηση της απορρόφησης ηλεκτρομαγνητικής ακτινοβολίας στην περιοχή των ραδιοσυχνοτήτων και αποτελεί βασική μέθοδο για τον προσδιορισμό της δομής χημικών ουσίων 5, στην παρούσα εργασία χρησιμοποιήθηκε για τον υπολογισμό της σύστασης των συμπολυμερών. Στην διαδικασία της απορρόφησης μετέχουν οι πυρήνες των ατόμων και όχι τα ηλεκτρόνια. Οι πυρήνες των ατόμων παρουσία ισχυρού μαγνητικού πεδίου, μπορούν να καταλάβουν στάθμες διαφορετικής δυναμικής ενέργειας και η ανίχνευση του ελάχιστου ποσού ενέργειας 37
47 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 που απορροφάται ή εκπέμπεται, καθώς ο πυρήνας μεταβαίνει από μια ενεργειακή στάθμη σ άλλη, γίνεται με το πυρηνικό μαγνητικό συντονισμό 6. Οι πυρήνες των ατόμων, όπως τα ηλεκτρόνια, αυτοπεριστρέφονται (spin) 7,8. Πυρήνες με άρτιο αριθμό πρωτονίων και νετρονίων (π.χ 6 O, 12 C) δεν αυτοπεριστρέφονται, δηλαδή έχουν ιδιοστροφορμή I=0, οποτε δεν εκδηλώνουν μαγνητικές ιδιότητες, με αποτέλεσμα να μην μπορούν ν ανιχνευθούν με χρήση NMR. Ενώ, οι πυρήνες που έχουν περιττό ατομικό ή μαζικό αριθμό (π.χ 19 F, 13 C, 1 H) είναι μαγνητικά ενεργοί 9. Η αυτό-στροφορμή των πυρήνων που έχουν περιττό μαζικό αριθμό δημιουργεί μια μαγνητική ροπη ίση με : h I (2.6) 2 όπου γ είναι η πυρηνική μαγνητική σταθερά του στοιχείου, I είναι ο κβαντικός αριθμός πυρηνικής στροφορμής που παίρνει ημιακέραιες τιμές και h είναι η σταθερά Plank. Αν ένα πρωτόνιο βρεθεί μέσα σε ένα εξωτερικό μαγνητικό πεδίο, έντασης Β ο, η μαγνητική του ροπή μπορεί να είναι είτε αντίθετη με αυτή του εξωτερικού πεδίου (υψηλής ενέργειας) είτε παράλληλη προς το εφαρμοζόμενο πεδίο (χαμηλής ενέργειας) 10. Η ενεργειακή διαφορά μεταξύ των δύο αυτών καταστάσεων είναι: και επειδή h 0 2 h, η συχνότητα στην οποία ένας πυρήνας συντονίζεται, είναι: (2.7) 0 2 (2.8) Δηλαδή η συχνότητα συντονισμού εξαρτάται από τη μαγνητική σταθερά του στοιχείου, άρα από τη φύση του στοιχείου. Όταν το άτομο βρεθεί εντός του μαγνητικού πεδίου τα ηλεκτρόνιά του εκτελούν εξαναγκασμένη κίνηση γύρω από τον πυρήνα η οποία δημιουργεί ένα επαγόμενο μαγνητικό πεδίο που αντιτίθεται στο εξωτερικό και προασπίζει (προστατεύει) τον πυρήνα. Η αποτελεσματική ένταση πεδίου στον πυρήνα διαφέρει από το Β ο κατά το επαγόμενο πεδίο: eff. Bo, όπου σ είναι η αδιάστατη σταθερά θωράκισης. 38
48 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 Τότε η συχνότητα συντονισμού γίνεται: (1 ) (2.9) 2 Τα βασικά τμήματα ενός φασματομέτρου NMR φαίνονται στην εικόνα 2.3. Το δείγμα, που βρίσκεται μέσα σε φιαλίδιο μικρής διαμέτρου, τοποθετείται σε ειδικό γυάλινο υποδοχέα που περιστρέφεται από αεροτουρμπίνα για να επιτυγχάνεται η ισοκατανομή του μαγνητικού πεδίου προς όλες τις διευθύνσεις του. Περιβάλλεται από πηνίο που συνδέεται με δέκτη ραδιοσυχνοτήτων, ενώ ένα δεύτερο πηνίο εκπέμπει ενέργεια προς αυτό σε διεύθυνση κάθετη προς το μαγνητικό πεδίο και συνδέεται με ταλαντωτή ραδιοσυχνοτήτων. Τα δύο πηνία είναι κάθετα μεταξύ τους και προς την διεύθυνση του μαγνητικού πεδίου. Εικόνα 2.3: Σχηματικό διάγραμμα φασματογράφου NMR. 2.3 ΔΥΝΑΜΙΚΗ ΣΚΕΔΑΣΗ ΦΩΤΟΣ (DYNAMIC LIGHT SCATTERING, DLS) Η τεχνική της δυναμικής σκέδασης του φωτός θεωρείται μια από τις σημαντικότερες πειραματικές τεχνικές για τον χαρακτηρισμό των πολυμερών σε αραιά διαλύματα, διότι επιτρέπει τον προσδιορισμό του συντελεστή διάχυσης (μεταφοράς και περιστροφής), αλλά και του μεγέθους, του σχήματος των σωματιδίων, των χρόνων χαλάρωσης και της πολυδιασποράς του συστήματος. Αν στον όγκο σκέδασης υπάρχουν πολλοί σκεδαστές, το σκεδαζόμενο πεδίο έχει κατανομή Gauss (εικόνα 2.4) και η κανονικοποιημένη συνάρτηση αυτοσυσχέτισης 39
49 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 της σκεδαζόμενης έντασης, g (2) (t), σχετίζεται με την κανονικοποιημένη συνάρτηση αυτοσυσχέτησης του πεδίου, g (1) (t) με την ακόλουθη σχέση του Sieggert 11 : (2) (1) g t g t ( ) 1 ( ) 2 (2.10) Για αραιά διαλύματα μονοδιάσπαρτων σφαιρικών σωματιδίων, καθώς και για μη σφαιρικά σωματίδια, τα οποία είναι μικρά σε σχέση με το αντίστροφο του ανύσματος σκέδασης, q, η συνάρτηση αυτοσυσχέτησης γίνεται: g t t (1) ( ) exp (2.11) Σημειώνουμε ότι Γ = Dq 2, όπου q είναι το διάνυσμα σκέδασης, οριζόμενο από την 4 n εξίσωση q sin και D είναι ο μεταφορικός συντελεστής διάχυσης των 2 σωματιδίων και σχετίζεται με την υδροδυναμική τους ακτίνα (R h ) μέσω της εξίσωσης των Stokes-Einstein: kb T D 6 R (2.12) όπου Κ Β, Τ και η αναπαριστούν τη σταθερά Boltzmann, την απόλυτη θερμοκρασία και το ιξώδες του διαλύτη, αντίστοιχα. Για σφαιρικά σωματίδια η υδροδυναμική ακτίνα (R h ) ισοδυναμεί με τη γεωμετρική ακτίνα R. Η μέθοδος DLS μπορεί να χρησιμοποιηθεί για τον υπολογισμό της υδροδυναμικής ακτίνας R h των μακρομορίων στο διάλυμα. Στη δυναμική σκέδαση φωτός γίνεται χρήση μονοχρωματικής ακτινοβολίας και μετράται, υπό συγκεκριμένη γωνία, η χρονική διακύμανση της έντασης της σκεδαζόμενης ακτινοβολίας υπό γωνία θ 12. Η χρονική αυτή διακύμανση οφείλεται στο γεγονός ότι η ένταση του σκεδαζόμενου φωτός στον ανιχνευτή είναι αποτέλεσμα τη συμβολής της ακτινοβολίας, που προέρχεται από τα διάφορα σωματίδια, τα οποία κινούνται άτακτα λόγω θερμικής κίνησης 13. Καθώς τα σωματίδια κινούνται από ή προς τον ανιχνευτή προκύπτει μια διεύρυνση των συχνοτήτων λόγω του φαινομένου Doppler (εικόνα 2.4) 4. Το ημιεύρος της διεύρυνσης κορυφής στο μέσο ύψος της Δω 1/ 2 σχετίζεται με το συντελεστή διάχυσης D ενός σφαιρικού σωματιδίου σύμφωνα με την εξίσωση 2.13: h 2 4 1/2 D c sin 2 (2.13) όπου ω ο η συχνότητα της προσπίπτουσας ακτινοβολίας. 40
50 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 Εικόνα 2.4: Φαινόμενο διεύρυνσης συχνοτήτων Doppler. 2.4 AMVn MICROVISCOMETER Το ιξωδόμετρο AMVn χρησιμοποιείται για τη μέτρηση του ιξώδους αραίων διαλυμάτων. Η αρχή λειτουργίας του ιξωδόμετρου βασίζεται στο Νόμο του Stokes για τη ροή του υγρού γύρω από μια σφαίρα, σύµφωνα µε τον οποίο, για σχετικά µικρές ταχύτητες, η δύναµη της τριβής F v που δυσχεραίνει την κίνηση του σώµατος, είναι ανάλογη ενός συντελεστή µορφής του σώµατος K (για σφαίρα Κ=6πr), της ταχύτητας κίνησης v και του συντελεστή εσωτερικής τριβής η του υγρού (εικόνα 2.5). Ο Νόμος Stokes εκφράζεται από τη παρακάτω εξίσωση: Fv 6 rv (2.14) Εικόνα 2.5: Σχηματική απεικόνιση του Νόμος Stokes. 41
51 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 Το δείγμα τοποθετείται σε ένα γυάλινο τριχοειδή σωλήνα, όπου το ιξώδες του δείγματος υπολογίζεται από το χρόνο ροής της σφαίρας μέσα στο σωλήνα. Ο χρόνος ροής υπολογίζεται από δυο επαγωγικούς αισθήτηρες. Για κάθε γωνία, ο μετρούμενος χρόνος ροής μπορεί να εκφραστεί μέσω του δυναμικού ιξώδους (μονάδες mpa.s), σε γνωστή πυκνότητα του υγρού. Στην εικόνα 2.6 απεικόνιζεται ένα σύγχρονο AMVn ιξωδόμετρο. Εικόνα 2.6: Απεικόνιση του AMVn ιξωδόμετρου. 2.5 ΡΕΟΛΟΓΙΑ Εισαγωγή Με τον όρο ρεολογία αναφερόμαστε στην επιστήμη που μελετά την παραμόρφωση και την ροή ενός υλικού υπο την επίδραση εξωτερικής δύναμης. Ο ορισμός αυτός καθιερώθηκε από τον Bingham και έγινε δεκτός από τους ρεολόγους το Τις τελευταίες δεκαετίες του 16ου αιώνα, ο Robert Hooke πρότεινε τη κλασσική θεωρία της ελαστικότητας όπου σύμφωνα μ αυτήν "η δύναμη που ασκείται σ ένα ελατήριο είναι ανάλογη με την παραμόρφωση που λαμβάνει χώρα σ αυτό", δηλαδή αν διπλασιάστει η δύναμη τοτε διπλασιάζεται και η παραμόρφωση: G (2.15) όπου G είναι η σταθερά του ελατηρίου και γ είναι η παραμόρφωση. 42
52 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 Την ίδια δεκαετία, ο Isaac Newton δίνοντας έμφαση στα ρευστά, πρότεινε μια υπόθεση σύμφωνα με την οποία: "η αντίσταση που εμφανίζεται από την έλλειψη ολισθηρότητας στη κίνηση της πλάκας είναι ανάλογη με την ταχύτητα με την οποία τα μέρη του υγρού διαχωρίζονται το ένα με το άλλο" και σχετίζεται με την απλή διατμητική ροή, όπως δείχνει και η εικόνα 2.7. Εικόνα 2.7: Σχηματική απεικόνηση της διατμητικής ροής ενός ρευστού μεταξύ δυο παράλληλων πλακών. Η "έλλειψη ολισθηρότητας" σήμερα είναι το ιξώδες, το όποιο είναι συνώνυμο με την εσωτερική τριβή και είναι μέτρο αντίστασης στη ροή. Η τάση σ (σ=δύναμη/ μονάδα επιφάνειας) είναι ανάλογη με το ρυθμό διάτμησης U/d δηλαδή, διπλασιάζοντας τη δύναμη διπλασιάζεται και ο τελεστής της ταχύτητας. Η σταθερά αναλογίας η είναι το ιξώδες: U d (2.16) Οι δυο ακραίες αυτές θεωρίες του Hooke και του Newton δεν ίσχυαν πλήρως για τα υλικά, τα οποία παρουσιάζαν συμπεριφορά στερεού (solid-like) ή συμπεριφορά υγρού (liquid-like), με αποτέλεσμα την εισαγωγή της έννοιας της ιξωδοελαστικότητας για να περιγράψει τέτοιες συμπεριφορές. Με την εμφάνιση των πλαστικών ινών, των συνθετικών λιπαντικών, των αυτοκόλλητων ταινιών και της μοντέρνας ιατρικής έρευνας, δόθηκε ακόμη περισσότερη ώθηση στη ρεολογία. Στην επιστήμη της ρεολογίας δεν ύπαρχει διαχωρισμός των εννοιών του ιξώδους και της ελαστικότητας, καθώς ένα υλικό μπορεί να έχει τη μια από τις δυο ή και τις δυο συμπεριφορές ταυτόχρονα. Αν σ ένα υπό εξέταση υλικό εφαρμόσουμε ένα ευρύ φάσμα τάσεων ή ένα ευρύ φάσμα χρόνου ή συχνοτήτων, τότε θα μπορέσουμε να 43
53 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 παρατηρήσουμε συμπεριφορά υγρών από στερεά σώματα ή υγρά σώματα να παρουσιάζουν συμπεριφορά ενός στερεού. Η βασική ιδέα στη ρεολογία είναι ότι τα πάντα ρέουν ανάλογα με την κλίμακα του χρόνου, όπου καθορίζεται από τον αδιάστατο αριθμό Deborah του εκάστοτε υλικού. Ο αριθμός Deborah ορίζεται ως εξής: D (2.17) e T όπου Τ είναι ο χρόνος μέσα στον οποίο παρατηρείται η παραμόρφωση στο υλικό και τ είναι ένας χαρακτηριστικός χρόνος του υλικού. Υψηλός αριθμός Deborah αντιστοιχεί σε στερεό σώμα, ενώ χαμηλός αριθμός Deborah αντιστοιχεί σε υγρό Ιξώδες και ιξωδοελαστική συμπεριφορά Στην έννοια του ιξώδους όπου αναφέρθηκε και προηγουμένως, η διατμητική τάση σ σχετίζεται με την παράγωγο της ταχύτητας ή με τον ρυθμό διάτμησης γ με την σχέση: (2.18) όπου η είναι το ιξώδες και έχει μονάδες Pa.s (S.I). Για τα νευτωνικά ρευστά το ιξώδες, η, έχει σταθερή τιμή σε δεδομένες συνθήκες πίεσης και θερμοκρασίας, δηλαδή είναι ανεξάρτητο του ρυθμού διάτμησης γ. Ενώ, στα μη νευτώνεια ρευστά το ιξώδες είναι μια συνάρτηση του ρυθμού διάτμησης και συμβολίζεται ως η(γ) και πολλές φορές αναφέρεται και ως διατμητικό ιξώδες. Τα νευτώνεια ρευστά έχουν τα εξής χαρακτηριστικά όταν τα μελετάμε υπό σταθερές συνθήκες πίεσης και θερμοκρασίας: 1. Το ιξώδες δεν μεταβάλλεται με το ρυθμό διάτμησης. 2. Σε απλή διατμητική ροή, μόνο η διατμητική τάση, σ, υπάρχει, ενώ οι υπόλοιπες είναι μηδέν. 3. Τα ιξώδη, τα οποία μετρήθηκαν με διαφορετικό είδος παραμόρφωσης, είναι πάντα ανάλογα μεταξύ τους. Για παράδειγμα, το ιξώδες που μετρήθηκε σε μια μονοαξονική εκτατική ροή είναι πάντα τρείς φορές μεγαλύτερο από την τιμή ιξώδους που μετρήθηκε με απλή διατμητική ροή. 4. Το ιξώδες είναι σταθερό με το χρόνο διάτμησης και όταν μηδενιστεί η τάση, η διάτμηση σταματάει αμέσως. 44
54 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 Τα τήγματα και διαλύματα των πολυμερών, τα οποία δεν έχουν συμπεριφορά νευτωνικών ρευστών, παρουσιάζουν περίεργη ρεολογική συμπεριφορά: 1. Ελάττωση του ιξώδους σε διατμητική ροή (shear thinning). To αξιοπερίεργο αυτό φαινόμενο οφείλεται στην ιδιότητα που έχουν τα διαλύματα πολυμερών να παρουσιάζουν ελάττωση του ιξώδους όταν υποβάλλονται σε ροή που τους επιβάλλει διατμητική παραμόρφωση. 2. Αύξηση του ιξώδους με αύξηση της διατμητικής παραμόρφωσης (shear thickening). Σε ορισμένα πολυμερή παρουσιάζεται το ακριβώς αντίθετο φαινόμενο μ αυτό που παρουσιάσθηκε προηγουμένως. 3. Αναρρίχηση σε περιστρεφόμενη ράβδο "Weissenberg effect". Σε μια ράβδο, η οποία περιστρέφεται μέσα σ ένα διάλυμα μη νευτωνικού ρευστού, παρατηρείται το υγρό ν αναρριχάται επάνω στην περιστρεφέμενη ράβδο. Αυτό οφείλεται στο ότι εμφανίζεται μια κάθετη ιξώδης τάση,που έχει ως αποτέλεσμα την αναρρίχηση του διαλύματος στην ράβδο, κ.α Γραμμική ιξωδοελαστικότητα Η γραμμική σχέση μεταξύ της επιβαλλόμενης τάσης και της προκαλούμενης παραμόρφωσης, εκφράζεται με την έννοια της γραμμμικής ιξωδοελαστικότητας του υλικού: f() t (2.19) Για παραμορφώσεις μεγαλύτερες από 1%, η πλειοψηφία των υπό μελέτη υλικών εμφανίζει μη γραμμική ιξωδοελαστικότητα. f(, t) (2.20) Όπως αναφέραμε, ο όρος ιξωδοελαστικός σημαίνει ταυτόχρονη ύπαρξη ελαστικών και ιξωδών ιδιοτήτων ενός υλικού και σημαντικό ρόλο παίζει ο αριθμός Deborah για το χαρακτηρισμό του υλικού ως ελαστικό στερεό ή ως ιξώδες υγρό. Για τη μελέτη της ιξωδοελαστικότητας, προτάθηκαν διάφορα μοντέλα τα οποία συνδιάζουν αποσβεστήρες και ελατήρια σε διάφορους συνδυασμούς. Το ελατήριο αντιστοιχεί στο τέλειο ελαστικό όπως το περιέγραψε ο Hooke και ο αποσβεστήρας είναι το μηχανικό ανάλογο ενός Νευτώνειου ρευστού, τα μοντέλα αυτά είναι του Maxwell και του Kelvin. 45
55 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ Μοντέλο Maxwell Το μοντέλο Maxwell αποτελείται από ένα ελατήριο και έναν αποσβεστήρα συνδεδεμένα εν σειρά, όπως φαίνεται στη παρακάτω εικόνα 3.8. Εικόνα 2.8: Μηχανικό ανάλογο του ιξωδοελαστικού μοντέλου Maxwell. Η καταστατική εξίσωση του μοντέλου είναι: d 1 d (2.21) dt G0 dt όπου γ είναι η παραμόρφωση, G 0 είναι το μέτρο ελαστικότητας, σ είναι η τάση και η το ιξώδες Μοντέλο Voigt (Kelvin) Το μοντέλο Kelvin αποτελείται από ένα ελατήριο και έναν αποσβεστήρα συνδεδεμένα παράλληλα, όπως φαίνεται στην εικόνα 2.9. Εικόνα 2.9: Μηχανικό ανάλογο του ιξωδοελαστικού μοντέλου Voigt. Η καταστατική εξίσωση του μοντέλου είναι: G 0 (2.22) 46
56 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ Γενικό Γραμμικό Ιξωδοελαστικό Μοντέλο Τα μοντέλα που ανάφεραμε πιο πάνω δεν είναι επαρκή για την μελέτη ενός πραγματικού υλικού, γι αυτό είναι αναγκαία η εύρεση άλλων μοντέλων. Από την μελέτη σύγχρονων θεωριών ιξεδοελαστικότητας, προέκυψε η εξής γενική εξίσωση για τη γραμμική ιξωδοελαστικότητα: 2 m (1 (2.23) 1 a2... a 2 ) ( m ) m t t t t t όπου n=m ή n=m-1. Η τάση και η παραμόρφωση μπορεί να είναι συνάρτηση του χρόνου (σχέση 2.20). Η συνολική παραμόρφωση η οποία προκύπτει από την μεταβαλλόμενη με το χρόνο τάση καθώς ασκείται σ ένα πραγματικό υλικό, είναι άθροισμα των παραμορώσεων, που οφείλονται στην κάθε τάση ξεχωριστά. Αυτό πηγάζει από την αρχή της επαλληλίας του Boltzmann, η οποία στηρίζεται σε δυο βασικές υποθέσεις: 1. Η ενδοτικότητα του ερπυσμού είναι ανεξάρτητη από την τάση. 2. Ο ερπυσμός που οφείλεται σε μια συγκεκριμένη τάση, είναι ανεξάρτητος από τον ερπυσμό που οφείλεται σε τυχόν προηγούμενες τάσεις. Σ αυτή την περίπτωση, η παραμόρφωση συναρτήσει του χρόνου δίνεται από την εξίσωση: ( t) J( t ) (2.24) Με την παραπάνω θεωρία, οι επιστήμονες έχουν τη δυνατότητα να προβλέπουν τον ερπυσμό ή την χαλάρωση τάσης σε μια πολύπλοκη ιστορία παραμόρφωσης του δοκιμίου Ρεολογικά Πειράματα στη Γραμμική Ιξωδοελαστική Περιοχή Διαφορετικές πειραματικές μέθοδοι για τη μέτρηση ρεολογικών ιδιοτήτων χρησιμοποιούνται για πιο αξιόπιστα αποτελέσματα. Οι πιο συνηθισμένες τεχνικές είναι ο ερπυσμός (creep), η χαλάρωση τάσης (stress relaxation) και η δυναμική φόρτιση (sinusoidal oscillations). Οι τεχνικές αυτές, μπορούν να συσχετιστούν μεταξύ τους στη γραμμικη ιξωδοελαστική περιοχή μέσω κάποιων εξισώσεων. Τα πειράματα στην γραμμική ιξωδοελαστική περιοχή περιορίζονται σε καταστάσεις μονοαξονικής φόρτισης. Στην συνέχεια θ αναφερθούμε στις έννοιες της δυναμικής φόρτισης και του έρπυσμου. 47
57 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ Ερπυσμός (Creep) Κατά την διάρκεια του πειραμάτος εφαρμόζουμε στιγμιαία τάση από 0 σε σ ο και καταγράφουμε την παραμόρφωση συναρτήσει του χρόνου. Στην παρακάτω εικόνα παρουσιάζεται μια χαρακτηριστική καμπύλη από πείραμα ερπυσμού. Εικόνα 2.10: Διάγραμμα τάσης και παραμόρφωσης συνάρτησει του χρόνου κατά τον ερπυσμό. Ακολούθουν τα διάφορα μοντέλα για τον ερπυσμό: Μοντέλο Maxwell: Η παραμόρφωση κατά τον ερπυσμό σύμφωνα με το μοντέλο Maxwell δίνεται από την σχέση: 1 () t t (2.25) G 0 Ενώ η ένδοση δίνεται από την σχέση: () t G t Jt () (2.26) G Μοντέλο Voigt(Kelvin): Παρακάτω δίνονται οι σχέσεις για την παραμόρφωση και την ένδοση αντίστοιχα. G ( t) 1 exp t (2.27) G n ( t) 1 G J( t) 1 exp t G (2.28) Γενικό γραμμικό ιξωδοελαστικό μοντέλο: Στο πείραμα του ερπυσμού η παραμόρφωση γ(t) δίνεται από την σχέση: ( t) J( s) ( t s) ds 0 (2.29) όπου J(s) είναι το μέτρο ένδοσης σε ερπυσμό (creep compliance) και s=t-t' είναι χρόνος από τη στιγμή που εφαρμόστηκε η τάση. 48
58 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 Η σχέση που συνδέει το J(t) με το G(t) είναι η εξής: t t G( t s) J ( s) ds 0 (2.30) Τα δεδομένα στο πείραμα ερπυσμού συνήθως εκφράζονται βάσει του μέτρου ένδοσης σε ερπυσμό J(t) για μικρή και σταθερή εφαρμοζόμενη τάση σ 0 σε χρόνο t=0. Έτσι, το J(t) δίνεται από την σχέση: () t Jt () 0 (2.31) Σε πολύ μεγάλους χρόνους η καμπύλη ερπυσμού προσεγγίζει μια ευθεία γραμμή, που αντιστοιχεί σε σταθερό ρυθμό παραμόρφωσης: 0 t J () t Je όπου η ο είναι το ιξώδες σε μηδενικό ρυθμό διάτμησης και στην περιοχή του πλατώ Δυναμική Φόρτιση (Sinuisoidal Oscillations) (2.32) 0 J e είναι το μέτρο ένδοσης Με τον όρο δυναμική συμπεριφορά ενός υλικού ονομάζουμε την μηχανική απόκριση του υλικού όταν αυτό υπόκειται σε ταχεία εναλλαγή φορτίων ή παραμορφώσεων 14. Σε αυτή την μηχανική δοκιμή, το δοκίμιο επιβάλλεται σε μια περιοδικά μεταβαλλόμενη (π.χ ημιτονοειδώς) τάση ή παραμόρφωση και μελετάται η απόκριση του υλικού. Στην γραμμική ιξωδοελαστική περιοχή, τόσο η επιβαλλόμενη τάση (ή παραμόρφωση), όσο και η αποκρινόμενη παραμόρφωση (ή τάση) θα μεταβάλλεται ημιτονοειδώς, αλλά θα είναι εκτός φάσης. Έτσι, αν επιβάλλουμε μια παραμόρφωση: 0 isin t (2.33) τοτε η τάση-απόκριση του υλικού θα είναι: sin( t ) (2.34) όπου ω είναι η γωνιακή συχνότητα και δ είναι η διαφορά φάσης μεταξύ της τάσης και της παραμόρφωσης. Η τελευταία εξίσωση μπορεί να γραφεί ως εξής: ( cos ) sin t ( sin ) cos t (2.35) 49
59 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 όποτε παρατηρείται ότι η τάση εκφράζεται από δυο συνιστώσες, η μια μέτρου cos, σε φάση με την παραμόρφωση και η άλλη μέτρου sin, με διαφορά φάσης 90 ο με την παραμόρφωση. Έτσι, η σχέση που συνδέει την τάση με την παραμόρφωση κατά την ταλάντωση του δοκιμίου, γράφεται εξ ορισμού ως εξής: [ G 'sin t G ''cos t (2.36) o ] Οι δυο παραπάνω σχέσεις υποδεικνύουν ότι τα μέτρα G' και G" θα μπορούσαν να αναπαρασταθούν μιγαδικά (εικόνα 2.11) ως εξής: στο υλικό μας αποδίδουμε ένα μιγαδικό μέτρο G*, του οποίου η σχέση με τα μέτρα G' και G" βρίσκεται αν θέσουμε: όποτε προκύπτει η σχέση, exp( i t) και exp[ i( t )] (2.37) G* exp( i ) (cos isin ) G' ig '' (2.38) Εικόνα 2.11: Η γεωμετρική παράσταση του μιγαδικού μέτρου διάτμησης. Το πραγματικό μέρος του G* είναι το G', το οποίο είναι σε φάση με την παραμόρφωση και συχνά αναφέρεται ως μέτρο αποθήκευσης (storage modulus). Το μέτρο αποθήκευσης G', εκφράζει το ποσό της ελαστικής ενέργειας που αποθηκεύεται στο υλικό κατά την διάρκεια μιας περιόδου. Η αποθηκευμένη ελαστική ενέργεια επανακτάται μετά την αφαίρεση του φορτίου, όπως αντίστοιχα συμβαίνει σ ένα ελατήριο. Το φανταστικό μέρος του G* είναι το G", το οποίο είναι 90 εκτός φάσης με την επιβαλλόμενη παραμόρφωση και συχνά αναφέρεται ως μέτρο απωλειών (loss modulus). Το μέτρο απωλειών G", εκφράζει το ποσό ενέργειας που δεν επανακτάται. Γι αυτό και το μέτρο απωλείων, αποτελεί γενικότερα μέτρο της απόσβεσης του συστήματος. Σε ένα ιξωδοελαστικό υλικό από το οποίο περιμένουμε τόσο ελαστική 50
60 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 2 όσο και ιξώδη συμπεριφορά μπορούμε να θεωρήσουμε ότι το μέτρο G αντιπροσωπεύει το ελαστικό μέρος του υλικού ενώ το G αντιπροσωπεύει το ιξώδες μέρος του. Υπάρχει και ένα τρίτο δυναμικό χαρακτηριστικό το οποίο συσχετίζει τις δυο προαναφερθείσες ποσότητες. Το χαρακτηριστικό αυτό είναι η ποσότητα tanδ (damping) που ορίζεται ως ο λόγος του μέτρου απωλειών G" προς το μέτρο αποθήκευσης G': G '' tan (2.39) G ' Η ποσότητα tanδ είναι γνωστή και ως συντελεστής απωλειών (loss factor). Η εξάρτηση των G' και G από την συχνότητα (σχήμα 2.12) παρέχει σημαντικές πληροφορίες σχετικά με την μικροδομή του υλικού. Εικόνα 2.12: Εξάρτηση του μέτρου αποθήκευσης, G', και του μέτρου απωλειών, G, από την συχνότητα για ελαστικά και πολυμερικά διαλύματα. Στο παραπάνω σχήμα παρατηρείται ότι για ελαστικά gels, το μέτρο αποθήκευσης και μέτρο απωλειών είναι ανεξάρτητα από την συχνότητα. Ενώ για πολυμερικά διαλύματα, το G' και το G δεν είναι ανεξάρτητα από τη συχνότητα. Για ιξωδοελαστικά υλικά, η επικάλυψη του G από το G' σε συγκεκριμένη συχνότητα, παρέχει πληροφορίες σχετικά με το χρόνο χαλάρωσης του συστήματος. Για υψηλές συχνότητες, όπου τα G' και G εμφανίζουν πλατώ, μας δίνουν πληροφορίες σχετικά με την ισχύ των δεσμών που σχηματίζονται στο υλικό. 51
61 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ Τύποι Ρεομέτρων Υπάρχει μεγάλη ποικιλία συσκευών μέτρησης ρεολογικών ιδιοτήτων, η οποία δεν κρίνεται σκόπιμο να αναφερθεί στην παρούσα εργασία. Οι πιο διαδεδομένοι τύποι ρεομέτρων είναι το stress control rheometer (με έλεγχο της τάσης) και το strain control rheometer (με έλεγχο της παραμόρφωσης), στο οποίο δεν θα γίνει εκτενής αναφορά Ρεόμετρο ελέγχου τάσης (stress control rheometer) Σε αυτόν τον τύπο ρεομέτρου (εικόνα 2.13), η δύναμη που οδηγεί στην παραμόρφωση του δείγματος προέρχεται από μια καθορισμένη ροπή. Η ροπή αυτή συνδέεται με την εφαρμοζόμενη τάση πάνω στο δείγμα μέσω της σχέσης: (2.40) όπου, σ είναι η τάση, Κ τ είναι σταθερά που εξαρτάται απ την γεωμετρία του οργάνου και Μ η ροπή. Το υπο δοκιμήν δείγμα, ασκεί μια συγκεκριμένη αντίσταση στην περιστροφή που επιβάλλεται, εξαρτώμενη από το ιξώδες. Η μέτρηση της παραμόρφωσης γίνεται με βάση τη γωνιακή ταχύτητα η οποία καταγράφεται από έναν οπτικό αισθητήρα στη συσκευή. Η θερμότητα ελέγχεται από ένα σύστημα Peltier. Εικόνα 2.13: Σχηματική απεικόνιση του ρεομέτρου ελέγχου τάσης. 52
62 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ Γεωμετρία κώνου-πλάκας (cone-plate geometry) Για το ρεόμετρο ελέγχου τάσης χρησιμοποιούνται διάφορες γεωμετρίες ανάλογα με το δείγμα που θέλουμε να μελετήσουμε. Η γεωμετρία κώνου-πλάκας (εικόνα 2.14) είναι μια από τις πιο χρησιμοποιούμενες γεωμετρίες, καθώς είναι χρήσιμη για τη μέτρηση ιξώδους διαφόρων υλικών. Το δείγμα τοποθετείται στο χώρο μεταξύ της πλάκας και του δίσκου και ο κώνος περιστρέφεται σε σχέση με το δίσκο. Το ενδιαφέρον αυτής της γεωμετρίας έγκειται στο ότι ο ρυθμός διάτμησης και η διατμητική τάση είναι ανεξάρτητες απ τη θέση και μπορούν εύκολα να υπολογιστούν. Επιπλέον, ο ρυθμός διάτμησης σ ολη την επιφάνεια διατηρείται σταθέρος. Λόγω της γωνίας β του κώνου, ο λόγος της αντίστοιχης ακτίνας προς το κενό της πλάκας (plate gap), tanβ=h/r, είναι σταθερός για κάθε σημείο στην επιφάνεια του κώνου και ως εκ τουτο το tanβ μπορεί πάντα να ισούται με το β (σε ακτίνια). Άρα ο ρυθμός διάτμησης διατηρείται σταθερός ως εξής: (2.41) Η γωνίας κώνου πρέπει να είναι μικρή, δηλ. tanβ=β, ώστε να αποτρέπεται η τριβή του κώνου στην πλάκα. Όσο μικρότερη είναι η γωνία, τόσο υψηλότερος ρυθμός διάτμησης είναι εφικτός. Παρόλα αυτά, η γεωμετρία κώνου-πλάκας έχει ένα βασικό μειονέκτημα. Ρευστά όπως το νερό, είναι δύσκολο να σταθεροποιηθούν στη πλάκα λόγω του μικρού τους ιξώδους. Εικόνα 2.14: Γεωμετρία κώνου-πλάκας. 53
63 ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΒΙΒΛΙΟΓΡΑΦΙΑ 1 Cowie J. M. G., Polymers: Chemistry & Physics of Modern, 2 nd ed., Stanley Thornes Ltd: UK, 1998, Chap. 9, Gedde U. W., Polymer Physics, Chapman and Hall: UK, 1995, Chap. 1, Hiemenz P., Polymer Chemistry: The Basic Concepts, Marcel Dekker, New York, 1984, Chap. 1, Παναγιώτου Κ., Επιστήμη και Τεχνολογία Πολυμερών, 2 η Θεσσαλονική, 2000, Κεφ. 8, σελ εκδ. Πήγασος: 5 Skoog, D. A.; Holler, F. J.; Nieman, T. A., Αρχές Ενόργανης Ανάλυσης, 5 η εκδ., Μετάφραση: Καραγιάννης Μ. Ι.; Ευσταθίου Η. Κ.; Χανιωτάκης Ν.; Εκδόσεις Κωσταράκης, Αθήνα, 2002, Κεφ. 19, Grubisic, Z.; Rempp. P.; Benoit, H. J., Polymer Science B, 1967, 5, Pecsok, R. L.; Sheilds L. D.; Cairns T.; McWilliam I. G., Σύγχρονες Μέθοδοι στη Χημική Ανάλυση, 2 η εκδ., Μετάφραση: Βολιώτης Σ., Εκδόσεις Πνευματικός, Αθήνα, 1980, Κεφ. 15, Morrison, R. T.; Boyd, R. N., Οργανική Χημεία, Ελληνική Απόδοση: Σακαρέλλος, Κ.; Πηλίδης, Γ.; Γεροθανάσης, Ι., 1991, Εκδόσεις Πανεπιστημίου Ιωαννίνων. 9 Pecsok, R. L.; Sheilds L. D.; Cairns T.; McWilliam I. G., Σύγχρονες Μέθοδοι στη Χημική Ανάλυση, 2η εκδ., Μετάφραση: Βολιώτης Σ., Εκδόσεις Πνευματικός Γ. Α. 10 Bekturov, E. A.; Kudaibergenov S. E.; Klamzamulina R. E.; Frolora V. A.; Nurgalieva D. E.; Schulz R. C.; Zöller J., Macromol. Chem. Rapid Commun. 1992, 13, Hwang, J.S.; Yang, Z. P.; Dai, S. B.; Tyan, S. L.; Kuo, M. T.; Lin, C. L., Chinese Journal of Physics, 1998, 36, Cummins, H. Z.; Pike, E. R., Photon Correlation Spectroscopy and Velocimetry, Plenum Press: New York, Pecora, R., Dynamic Light Scattering. Applications of Photon Correlation Spectroscopy, Plenum Press: New York, 1985, Chap. 1-5, p Κυριαζής Α., Μεταπτυχιακή εργασία: "ΦΑΙΝΟΜΕΝΑ ΣΥΜΦΟΡΗΣΗΣ ΚΑΙ ΡΕΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΠΟΛΥΗΛΕΚΤΡΟΛΥΤΩΝ ΑΣΤΕΡΟΕΙΔΟΥΣ ΣΧΗΜΑΤΟΣ ΣΕ ΥΔΑΤΙΚΑ ΜΕΣΑ", Πανεπιστήμιο Πατρών, Τμήμα Χημικών Μηχανικών, Πάτρα
64
65 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΚΑΙ ΡΕΟΛΟΓΙΚΗ ΜΕΛΕΤΗ ΤΟΥ ΤΡΙΣΥΣΤΑΔΙΚΟΥ ΣΥΜΠΟΛΥΜΕΡΟΥΣ PΕΟ-PS-PEO 3.1 ΕΙΣΑΓΩΓΗ Η μελέτη τρισυσταδικών συμπολυμερικών διαλυμάτων σε ιονικά υγρά (ionic liquids) κερδίζει συνεχώς έδαφος τα τελευταία χρόνια. Οι έρευνες έχουν επικεντρωθεί σε διαλύματα τρισυσταδικών συμπολυμερών τύπου ΑΒΑ, όπου η Α συστάδα είναι αδιάλυτη και η συστάδα Β είναι διαλυτή. Συμπολυμερή τέτοιου είδους δημιουργούν φυσικές διασυνδέσεις (cross links) σχηματίζοντας δίκτυο 1,2. Η αυτοοργάνωση των συμπολυμερών σε διαλύματα εκλεκτικών διαλυτών ("καλοί" διαλύτες για τη μια συστάδα και "κακοί" για την άλλη) οδηγεί στο σχηματισμό διαφόρων νανοδομών. Στο παρόν κεφάλαιο παρουσιάζεται το τρισυσταδικό συμπολυμερές ΒΑΒ, όπου η κεντρική συστάδα (PS) είναι αδιάλυτη στο ιοντικό υγρό [BMIM][PF 6 ] και συνδέεται στα δύο άκρα με δυο διαλυτές συστάδες (PEO). Σκοπός της εργασίας είναι η μελέτη του τρισυσταδικού συμπολυμερούς σε αραιά και πυκνά διαλύματα [BMIM][PF 6 ]. 3.2 ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΤΟΥ PEO-PS-PEO Ο χαρακτηρισμός των μοριακών χαρακτηριστικών του συμπολυμερούς έγινε μέσω της φασματοσκοπίας πυρηνικού μαγνητικού συντονισμού (NMR). Το συμπολυμερές PEO-PS-PEO είχε παρασκευασθεί στο εργαστήριο του τμήματος. 55
66 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΠΥΡΗΝΙΚΟΥ ΜΑΓΝΗΤΙΚΟΥ ΣΥΝΤΟΝΙΣΜΟΥ (NMR) Η φασματοσκοπία πυρηνικού μαγνητικού συντονισμού χρησιμοποιήθηκε για τον υπολογισμό της εκατοστιαίας κατά βάρος σύστασης των μονομερών του συμπολυμερούς. Τα φάσματα έληφθησαν σε φασματόμετρο Brucker Avance DPX (400ΜΗz). Για την λήψη των φασμάτων 1 H-NMR χρησιμοποιήθηκε δευτεριωμένο χλωροφόρμιο, CDCl 3. Το φάσμα 1 H-NMR του PEO-PS-PEO φαίνεται στο σχήμα 3.1. Σχήμα 3.1: Χαρακτηριστικό φάσμα συμπολυμερούς PEO-PS-PEO σε CDCl 3. 1 Η-NMR του τρισυσταδικού Η ισχυρή κορυφή σε χημική μετατόπιση ~7.3 ppm, που παρατηρείται στο φάσμα, αντιστοιχεί στο διαλύτη (CDCl 3 ). Η ομάδα κορυφών με χημική μετατόπιση από 6.5 ppm μέχρι 7.2 ppm αντιστοιχεί στα πέντε πρωτόνια του αρωματικού δακτυλίου του PS (c). Επίσης, η ομάδα κορυφών με χημική μετατόπιση από τα 3.4 ppm μέχρι τα 4.5 ppm, αντιστοιχεί στα πρωτόνια των ομάδων CH2 (d) και 56
67 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 CH 2 (e) του PEO ενώ, η κορυφή που εμφανίζεται στην περιοχή από 1.2 ppm μέχρι 2 ppm αναφέρεται στα πρώτονια των βινυλικών ομάδων CH2 (a) και CH (b) του PS. Από την ολοκλήρωση των κορυφών του φάσματος 1 H-NMR προκύπτει η % κατά βάρος σύσταση των μονομερών στην ένωση. Τα μοριακά χαρακτηριστικά του τρισυσταδικού συμπολυμερούς PEO-PS-PEO που προκύπτουν από μετρήσεις στατικής σκέδασης φωτός και φασματοσκοπίας 1 Η- NMR παρατίθενται στον πίνακα 3.1. Πίνακας 3.1: Μοριακά χαρακτηριστικά του PEO-PS-PEO. PS PEO POLYMER M w a M w(ps) block wt% b DP PS M w(peo) block wt% b DP PEO block PEO-PS-PEO α Μέσω στατικής σκέδασης φωτός (SLS) b Μέσω της ανάλυσης φάσματος 1 H-NMR DP: Βαθμός πολυμερισμού 3.3 ΥΛΙΚΑ Τα υλικά που χρησιμοποιήθηκαν για την παρασκευή διαλυμάτων του συμπολυμερούς στο ιοντικό υγρό είναι τα ακόλουθα: το τρισυσταδικό συμπολυμερές PEO-PS-PEO και το ιονικό υγρό, εξαφθοροφωσφορούχο 1-βούτυλο-3- μέθυλιμιδαζόλιο (1-butyl-3-methylimadazolium hexafluapophoshate), [BMIM][PF 6 ] (Alfa Aesar). Τέλος, χρησιμοποιήθηκε ο συνδιαλύτης (co-solvent) διχλωρομεθάνιο (dichloromethane), CH 2 Cl ΠΑΡΑΣΚΕΥΗ ΔΕΙΓΜΑΤΩΝ Για την παρασκευή πολυμερικών διαλυμάτων ακολουθήθηκε καθορισμένη διαδικασία. Aρχικά, αφού ζυγίστηκαν οι απαιτούμενες ποσότητες πολυμερούς, προστέθηκε συνδιαλύτης CΗ 2 Cl 2 1mL. Υστερα υπό ανάδευση προστέθηκε το ιονικό 57
68 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 υγρό [BMIM][PF 6 ] και για την πλήρη ομογενοποίηση των διαλυμάτων με πολύ υψηλό ιξώδες πραγματοποιήθηκαν φυγογκεντρήσεις σε μηχανή φυγοκέντρησης Sigma 2K15 με περιστροφή 5000στροφές/min για 15min. Στη συνέχεια, τα δείγματα τοποθετήθηκαν σε φούρνο σε θερμοκρασία C για την εξάτμιση του συνδιαλύτη για κάποιες μέρες και μετέπειτα στο φούρνο υπό κενό σε θερμοκρασία έως 70 0 C για την πλήρη εξάτμιση του συνδιαλύτη και την απομάκρυνση υγρασίας μέχρι την επίτευξη σταθερού βάρους. Παρασκευάσθηκαν δείγματα διαφόρων συγκεντρώσεων: 9, 12.5, 13.5, 15.9, 17, 20, 24.8 wt% καθώς και διαλύματα με συγκεντρώσεις 10, 11wt% και 7.1, 6, 5.2, 4, 3 wt%, που προέκυψαν από αραίωση των μητρικών διαλυμάτων 12.5, 13.5 και 9wt% σε [BMIM][PF 6 ], αντίστοιχα. 3.4 ΜΕΛΕΤΗ ΑΡΑΙΩΝ ΔΙΑΛΥΜΑΤΩΝ PEO-PS-PEO ΔΥΝΑΜΙΚΗ ΣΚΕΔΑΣΗ ΦΩΤΟΣ (DLS) Πειράματα DLS πραγματοποιήθηκαν στους 25ºC για γωνίες 40 ο -100 ο, ανά 10 ο, σε διάλυμα πολυμερούς 0.8wt% που προέκυψε έπειτα από αραίωση του διαλύματος 3wt% σε [BMIM][PF 6 ]. Πριν από την πραγματοποίηση του πειράματος, το διάλυμα φιλτραρίστηκε με φίλτρο 0.45μm, προκειμένου να απομακρυνθεί η σκόνη και αφέθηκε να ισορροπήσει για 24 ώρες. Η τεχνική DLS χρησιμοποιήθηκε για τον υπολογισμό της υδροδυναμικής ακτίνας, R h, των μικκυλίων. Η πειραματική διάταξη περιλαμβάνει μια πηγή μονοχρωματικού φωτός He-Ne (laser) μήκους κυμάτος 632,8 nm και διάφορα οπτικά εξαρτήματα για την ρύθμιση της ευθυγράμμισης της ακτίνας του laser. Η ανάλυση της συνάρτησης αυτοσυσχέτισης (g 1 (t)) πραγματοποιήθηκε με βάση τη μέθοδο CONTIN (σχήμα 3.2). Με βάση την ανάλυση αυτή ελήφθησαν τα διαγράμματα που παρουσιάζουν την κατανομή των χρόνων χαλάρωσης. Ενδεικτικά, στο σχήμα 3.3 παρουσιάζεται η συνάρτηση αυτοσυσχέτισης μαζί με την κατανομή του χρόνου χαλάρωσης για το διάλυμα PEO-PS-PEO/[BMIM][PF 6 ] συγκέντρωσης 0.8wt% σε γωνία 90º στους 25ºC. 58
69 g 1 (t) L -1 (t) g 1 (t) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 1,0 0,8 0,6 Angle 40 o Angle 50 o Angle 60 o Angle 70 o Angle 80 o Angle 90 o Angle 100 o 0,4 0,2 0, Time (ms) Σχήμα 3.2: Χρονική εξάρτηση της συνάρτησης αυτοσυσχέτισης (g 1 (t)) του συμπολυμερούς PEO-PS-PEO σε γωνίες 40 ο έως 100 ο και θερμοκρασία 25 ο C. 0,8 θ=90 o 0,6 0,4 0,2 0, Time (ms) Σχήμα 3.3: Χρονική εξάρτηση της συνάρτησης αυτοσυσχέτισης (g 1 (t)) μαζί με την κατανομή του χρόνου χαλάρωσης του διαλύματος συμπολυμερούς PEO-PS-PEO σε γωνία 90 ο και θερμοκρασία 25 ο C. Διαγράμματα κατανομής των διαμέτρων των μικκυλίων του τρισυσταδικού συμπολυμερούς PEO-PS-PEO σε [BMIM][PF 6 ] για γωνίες 40 ο -100 ο στους 25 o C. 59
70 Γ (s -1 ) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 Από το μέγιστο της κατανομής των χρόνων χαλάρωσης λαμβάνεται ένας μέσος χρόνος, απ όπου προκύπτει το μέγεθος των μικκυλίων μέσω του συντελεστή διάχυσης (μέσω της CONTIN ανάλυσης). Ο συντελεστής διάχυσης των μικκυλίων προσδιορίστηκε από την κλίση της ευθείας της γραφικής παράστασης του αντιστρόφου χρόνου χαλάρωσης συναρτήσει του τετραγώνου του ανύσματος της σκέδασης, q 2. Η γραφική παράσταση 2 1/ R f( q ) φαίνεται στο παρακάτω σχήμα 3.4. Παρατηρούμε πως ο αντίστροφος χρόνος χαλάρωσης μεταβάλλεται γραμμικά με το q 2. Από την κλίση της ευθείας προκύπτει ο συντελεστής διάχυσης Do m s και με τη χρήση τη εξίσωσης Stokes Einstein: R h kb T 6 D υπολογίζεται η υδροδυναμική ακτίνα των μικκυλίων: R h = 45nm. Επίσης, στο ένθετο παρουσιάζεται ο συντέλεστης διάχυσης Do 2 / q συναρτήσει του q 2. Το γεγονός πως το D o παραμένει σταθερό σε όλες τις γωνίες σκέδασης δείχνει τη σφαρική δομή των μικκυλίων. o 20 5,0x q 2 (s -1 ) 10 1x x x x x10 14 q 2 (m -2 ) x x x x x10 14 q 2 (m -2 ) Σχήμα 3.4: Εξάρτηση του αντιστρόφου χρόνου χαλάρωσης των μικκυλίων, Γ από το τετράγωνο του ανύσματος της γωνίας σκέδασης, q 2. Στο ένθετο παρουσιάζεται ο συντέλεστης διάχυσης D o συναρτήσει του q 2. Το πείραμα πραγματοποιήθηκε σε διάλυμα συγκέντρωσης 0.8wt%, για γωνίες από 40º έως 100º στους 25ºC. 60
71 Intensity Weighted Distribution ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 Στο σχήμα 3.5 παρουσιάζεται η κατανομή του πληθυσμού των μικκυλίων με βάση την διάμετρό τους σε γωνία 90º όπου παρατηρείται μονομοριακή κατανομή των μικκυλίων. Η συμπεριφορά αυτή είναι χαρακτηριστική για όλες τις γωνίες μέτρησης. 100 θ=90 ο diameter (nm) Σχήμα 3.5: Διάγραμμα κατανομής της διαμέτρου των μικκυλίων του τρισυσταδικού συμπολυμερούς PEO-PS-PEO σε [BMIM][PF 6 ] για γωνία 90 ο στους 25 o C ΥΠΟΛΟΓΙΣΜΟΣ ΤΗΣ ΚΡΙΣΙΜΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ ΕΠΙΚΑΛΥΨΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PEO-PS-PEO/[BMIM][PF 6 ] Μέσω του ιξωδόμετρου AMVn υπολογίστηκε η κρίσιμη συγκέντρωση επικάλυψης (overlap concentration), c*, αραιών διαλυμάτων πολυμερούς. Παρασκευάστηκαν διαλύματα του συμπολυμερούς PEO-PS-PEO συγκέντρωσης 0.4, 0.6 και 1wt% από αραίωση του διαλύματος πολυμερούς 3wt% σε [BMIM][PF 6 ]. Για την αξιοπιστία των μετρήσεων ακολουθήθηκε πρωτόκολλο κατά την προετοιμασία των διαλυμάτων: Εφόσον παρασκευάστηκαν τα διαλύματα συγκεκριμένων συγκεντρώσεων, για την πλήρη ομογενοποίηση ακολούθησε ανάδευση και στη συνέχεια τα δείγματα τοποθετήθηκαν σε φούρνο υπό κενό σε θερμορκασία έως 75 0 C, χρονικής διάρκειας 5-6 ωρών για την απομάκρυνση υγρασίας. Κατά την διάρκεια του πειράματος, το κάθε δείγμα τοποθετήθηκε σε γυάλινο τριχοειδή σωλήνα με διάμετρο σφαίρας 3mm, προσεκτικά για την αποφυγή δημιουργίας φυσαλίδων. Η θερμοκρασία του πειράματος ήταν 25 ο C. Από το χρόνο ροής της σφαίρας μέσα στη στηλή, 61
72 n sp /c ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 υπολογίστηκε το δυναμικό ιξώδες του δείγματος. Στη συνέχεια, από τη σχέση n/ n 1, προσδιορίστηκε το ειδικό ιξώδες. Στο σχήμα 3.6 παραθέτουμε την sp o καμπύλη του ανηγμένου ιξώδους nsp / c συναρτήσει της συγκέντρωσης, c. Το εσωτερικό ιξώδες, [η], ορίζεται από την τεταγμένη επί την άρχη για c 0. Η κρίσιμη συγκέντρωση c* προσδιορίζεται από την σχέση c* 1/[ n] = 4 wt%. 0,30 0,25 PEO-PS-PEO copolymer Fitting linear [n]= c*=4 wt% 0,20 0,15 0,10 0,0 0,5 1,0 1,5 concentration (wt%) Σχήμα 3.6: Καμπύλη εξάρτησης του nsp / c από την συγκέντρωση για διαλύματα του συμπολυμερούς PEO-PS-PEO σε [BMIM][PF 6 ] (οι μπλε γραμμες αντιστοιχούν στο σφάλμα των μετρήσεων). 3.5 ΜΕΛΕΤΗ ΠΥΚΝΩΝ ΔΙΑΛΥΜΑΤΩΝ PEO-PS-PEO ΕΙΣΑΓΩΓΗ Στη συνέχεια πραγματοποιήθηκαν πειράματα σε πυκνά διαλύματα, με σκόπο την μελέτη της ρεολογικής συμπεριφοράς του τρισυσταδικού συμπολυμερούς. Οι μετρήσεις του συστήματος PΕΟ-PS-PEO/[BMIM][PF 6 ] πραγματοποιήθηκαν στην γραμμική και μη γραμμική ιξωδοελαστική περιοχή. Στην παρούσα εργασία διεξήχθηκαν μετρήσεις δυναμικής και σταθερής διατμητικής ροής (oscillatory και steady state shear flow), καθώς και πειράματα ερπυσμού (creep tests), με σκοπό τη διερεύνηση των ιξωδοελαστικών ιδιοτήτων των πηκτωμάτων. Οι πειραματικές μετρήσεις πραγματοποιήθηκαν σε ρεόμετρο ελεγχόμενης τάσης (Stress Control Rheometer) της Rheometric Scientific, μοντέλο SR-200, το οποίο ήταν εφοδιασμένο με γεωμετρία κώνου διαμέτρου 20mm, γωνία κώνου και 62
73 viscosity (Pa.s) viscosity (Pa.s) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 truncation 11 μm (πριν από κάθε πείραμα, η διάταξη απαιτούσε 5 λεπτά ώστε να επιτευχθεί βαθμονόμηση). Σε όλη τη διάρκεια των πειραμάτων η θερμοκρασία ήταν καθορισμένη στους 25 0 C με τη βοήθεια ενός θερμοστάτη ΡΕΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΣΤΑΘΕΡΗΣ ΚΑΤΑΣΤΑΣΗΣ (Steady-State) Η μη γραμμική ιξωδοελαστική συμπεριφορά του τρισυσταδικού συμπολυμερούς PEO-PS-PEO στο ιοντικό υγρό [BMIM][PF 6 ], μελετήθηκε υποβάλλοντας τα δείγματα σε σταθερή διατμητική ροή. Άρχικα παραθέτουμε τα αποτέλεσματα ενός ολοκληρωμένου πειράματος σε συγκέντρωση 9wt%, ενώ ακολουθούν συγκριτικές καμπύλες σε όλη την κλίμακα των συγκεντρώσεων που μελέτηθηκαν ( ) 9wt% increasing stress 9wt% decreasing stress (b) 9wt% increasing shear rate 9wt% decreasing shear rate PEO-PS-PEO shear stress (Pa) 10-1 PEO-PS-PEO shear rate (s -1 ) Σχήμα 3.7: Χαρακτηριστικές καμπύλες ιξώδους-διατμητικής τάσης (a) και ιξώδους-ρυθμού διάτμησης (b), με αυξανόμενα και μειούμενα τάση και ρυθμό διάτμησης για το διάλυμα 9wt% PEO-PS-PEO σε [BMIM][PF 6 ]. Από το σχήμα 3.7 (α&b) διαπιστώνεται ότι το τρισυσταδικό συμπολυμερές συγκέντρωσης 9wt% παρουσιάζει δύο χαρακτηριστικές περιοχές μεταβολής. Στην πρώτη περιοχή, για τιμές της επιβαλλόμενης τάσης σ<5pa ή του ρυθμού διάτμησης <10-1 s -1, η τιμή του ιξώδους, η, παραμένει σταθερή σχηματίζοντας ένα νευτωνικό πλατώ. Στην δεύτερη περιοχή, για τιμές της επιβαλλόμενης τάσης σ>5pa ή του ρυθμού διάτμησης >10-1 s -1, το συμπολυμερές παρουσιάζει την κλασική 63
74 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 συμπεριφορά των πολυμερικών διαλυμάτων, δηλαδή εμφανίζεται συμπεριφορά ρεολέπτυσης (μειώση του ιξώδους με αύξηση της επιβαλλόμενης τάσης ή ρυθμού διάτμησης), όπου λόγω της υψηλής διατμητικής τάσης ή του υψηλού ρυθμού διάτμησης το ιξώδες του συστήματος μειώνεται. Επιπροσθέτως, η αντίστροφη πειραματική διαδικασία με την οποία η επιβαλλόμενη τάση ή αντίστοιχα ο ρυθμός διάτμησης σταδιακά μειώνονται, είναι απόλυτα αντιστρεπτή καθώς δεν παρουσιάζει διαφορές από την προηγούμενη συμπεριφορά. Το ρεολογικό προφίλ των διαλυμάτων σε διαφορετικές συγκεντρώσεις, παρουσιάζεται στο διάγραμμα που δείχνει τη μεταβολή του ιξώδους η συναρτήσει της επιβαλλόμενης τάσης (σχήμα 3.8). Παρουσιάζονται τα ιξώδη διαλυμάτων συγκέντρωσης από 3wt% έως 11wt%. Για διαλύματα υψηλότερης συγκέντρωσης από 11wt%, η περιοχή του πλατώ δεν μπορούσε επακριβώς να προσδιοριστεί και γι αυτό το λόγο διεξήχθησαν πειράματα ερπυσμού, τα οποία παρουσιάζονται στην παράγραφο % wt % wt 5.2% wt 6% wt % wt 9% wt 10% wt % wt (Pa.s) shear stress (Pa) Σχήμα 3.8: Μεταβολή του ιξώδους των διαλυμάτων του τρισυσταδικού συμπολυμερούς PEO-PS-PEO στο ιοντικό υγρό [BMIM][PF 6 ] συναρτήσει της διατμητικής τάσης σε διάφορες συγκεντρώσεις. Από το προφίλ του ιξώδους διαπιστώνεται ότι η αύξηση της συγκέντρωσης οδηγεί στην αύξηση της τιμής του ιξώδους. Παρατηρούμε πως για αραιά διαλύματα η εξάρτηση του ιξώδους μοιάζει με εκείνη των Νευτώνειων ρευστών, καθώς 64
75 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 παρουσιάζουν νευτωνικό πλατώ. Με αύξηση της συγκέντρωσης, το ιξώδες αυξάνεται σημαντικά λόγω του ολοένα αυξανόμενου συνωστισμού των μικκυλίων και για τιμές της επιβαλλόμενης τάσης σ<10pa, το φυσικό πηκτώμα που σχηματίζεται παραμένει αμετάβλητο. Αξίζει να σημειώσουμε ότι παρατηρούνται και φαινόμενα ρεολέπτυσης (shear thinning). Τα μικκύλια, λόγω της παραμόρφωσης που υφίστανται, αποκτούν κινητικότητα και το σύστημα αρχίζει να ρέει. Στον πίνακα 3.2 που ακολουθεί παρουσιάζονται οι τιμές του ιξώδους μηδενικής διάτμησης (zero shear viscosity) στις αντίστοιχες συγκεντρώσεις πολυμερούς, οι οποίες προκύπτουν από το σχήμα 3.8 για μηδενικές τιμές της διατμητικής τάσης. Πίνακας 3.2: Τιμές η ο για διάφορες συγκεντρώσεις του PEO-PS-PEO. c (wt%) η ο (Pa.s) 11 3* ΠΕΙΡΑΜΑ ΕΡΠΥΣΜΟΥ (Creep) Τα πειράματα ερπυσμού πραγματοποιήθηκαν με την επιβολή χαμηλών διατμητικών τάσεων για διαλύματα συγκέντρωσης 10 έως 24.8wt% του τρισυσταδικού συμπολυμερούς PEO-PS-PEO. Τα δεδομένα σε πείραμα ερπυσμού εκφράζονται βάσει του μέτρου ένδοσης J(t), όπου για μεγάλους χρόνους η καμπύλη ερπυσμού προσεγγίζει μια ευθεία γραμμή που αντιστοιχεί σε σταθερό ρυθμό t παραμόρφωσης: J () t Jo. Από την παραπάνω σχέση υπολογίζεται το ιξώδες η ο o σε μηδενικούς ρυθμούς διάτμησης, το μέτρο ένδοσης J ο στην περιοχή του πλατώ, το οποίο αντιστοιχεί στο αντίστροφο του μέτρου αποθήκευσης J 1/ G και ο χρόνος χαλάρωσης n / G. Στο σχήμα 3.9 παρουσιάζεται το μέτρο ένδοσης συναρτήσει R o o του χρόνου των διαλυμάτων του συμπολυμερούς στο ιοντικό υγρό. 65 o o
76 J(t) (Pa -1 ) J(t) (Pa -1 ) J(t) (Pa -1 ) J(t) (Pa -1 ) J(t) (Pa -1 ) J(t) (Pa -1 ) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 2,5 2,0 1,5 10wt% PEO-PS-PEO Linear Fitting stress=2 Pa o =559 Pa.s G o =97 Pa R =6 s 0,030 0,025 0,020 0,015 1,0 0,5 0, Time (s) 0,010 0,005 11wt% PEO-PS-PEO Linear Fitting stress=1 Pa o =2.6*10 4 Pa.s G o =141 Pa R =184 s 0, Time (s) 0,006 0,006 0,005 0,005 0,004 0,004 0,003 0,002 0, wt% PEO-PS-PEO Linear Fitting stress=10 Pa o =2.5*10 5 Pa.s G o =409 Pa R =611 s 0, ,003 0,002 0, wt% PEO-PS-PEO Linear Fitting stress=10 Pa o =2.6*10 5 Pa.s G o =385 Pa R =675 s 0, ,006 0,005 0, wt% PEO-PS-PEO Linear Fitting stress=10 Pa o =1.6*10 6 Pa.s G o =441 Pa R =3628 s Time (s) 0,006 0,005 0,004 17wt% PEO-PS-PEO Linear Fitting stress=10 Pa o =2.8*10 6 Pa.s G o =901 Pa R =3108 s Time(s) 0,003 0,003 0,002 0,002 0,001 0,001 0, Time (s) 0, Time (s) 66
77 J(t) (Pa -1 ) J(t)(1/Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 0,006 0,005 0,004 20wt% PEO-PS-PEO Linear Fitting stress=10 Pa o =2.5*10 6 Pa.s G o =1263 Pa R =1979 s 0,006 0,005 0, wt% PEO-PS-PEO Linear Fitting stress=10 Pa o =7.6*10 6 Pa.s G o =2917 Pa R =2605 s 0,003 0,003 0,002 0,002 0,001 0,001 0, Time (s) 0, Time (s) Σχήμα 3.9: Μέτρο ένδοσης J(t) συναρτήσει του χρόνου για διαλύματα του συμπολυμερούς PEO-PS-PEO σε ιοντικό υγρό [BMIM][PF 6 ] διαφόρων συγκεντρώσεων και σε θερμοκρασία 25 ο C. Από το πείραμα ερπυσμού παρατηρείται η εξάρτηση του μέτρου ένδοσης από τη συγκέντρωση του συμπολυμερούς. Για διάλυμα συγκέντρωσης 10wt%, η ενδοτικότητα παρουσιάζει γραμμική μεταβολή συναρτήσει του χρόνου, το οποίο είναι χαρακτηριστική συμπεριφορά ιξώδους υγρού. Καθώς αυξάνεται η συγκέντρωση, τα διαλύματα του τρισυσταδικού συμπολυμερούς παρουσιάζουν ιξωδοελαστική συμπεριφορά. Το πήκτωμα σε ακόμα υψηλότερες συγκεντρώσεις c>17wt%, προσεγγίζει τη συμπεριφορά του τέλειου ελαστικού ΕΞΑΡΤΗΣΗ ΤΟΥ ΣΧΕΤΙΚΟΥ ΙΞΩΔΟΥΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PEO- PS-PEO/[BMIM][PF 6 ] ΑΠΟ ΤΗ ΣΥΓΚΕΝΤΡΩΣΗ Στο σχήμα 3.10 παραθέτουμε την καμπύλη εξάρτησης του σχετικού ιξώδους (ιξώδες μηδενικής διάτμησης ως προς το ιξώδες του ιοντικού υγρού, n / n ) rel o IL συναρτήσει της συγκέντρωσης. Η μεταβολή του σχετικού ιξώδους εμφανίζει τέσσερις διακριτές περιοχές, ανάλογα με την εξάρτηση του σχετικού ιξώδους από τη συγκέντρωση. Για μικρές συγκεντρώσεις (c<c*), το σχετικό ιξώδες παίρνει τιμές παραπλήσιες του ιοντικού υγρού ([BMIM][PF 6 ]: η=0.270 Pa.s) με παρατηρούμενη μικρή αύξηση με αύξηση της 67
78 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 συγκέντρωσης, 1.5 nrel ~ c που οφείλεται στην αύξηση του αριθμού των μικκυλίων (εικόνα 3.1a). Σε αυτή την περιοχή, το διάλυμα του πολυμερούς είναι αραιό και κυριαρχούν απωστικές δυνάμεις μεταξύ των αλυσίδων του PEO. Καθώς αυξάνεται η συγκέντρωση (c>c*), τα μικκύλα πλησιάζουν μεταξύ τους με αποτέλεσμα να αυξάνεται η δυσκολία κίνησής τους και τελικά να παρατηρείται αύξηση του σχετικού ιξώδους με αύξηση της συγκέντρωσης (εικόνα 3.1b). Μάλιστα, πρέπει να σημείωθει πως το σχετικό ιξώδες αυξάνεται έντονα με τη συγκέντρωση συμφώνα με τη σχέση rel 5 ~ c. Σε αυτή την περιοχή συγκεντρώσεων, οι δυνάμεις άπωσης μεταξύ των αλυσίδων PEO καταργούνται και τα μικκύλια αρχίζουν να αλληλοεμπλέκονται μεταξύ τους λόγω συνωστισμού. Σε ακόμα μεγαλύτερες συγκεντρώσεις, το σχετικό ιξώδες αυξάνεται δραματικά έως και πέντε τάξεις μεγέθους, σύμφωνα με τη σχέση rel ~ c 22. Στο σημείο όπου το σχετικό ιξώδες αυξάνει με τη συγκέντρωση κατά εκθέτη με τιμή 22 χαρακτηρίζεται ως η κρίσιμη συγκέντρωση δημιουργίας πηκτώματος c gel (9wt%). Αυτή η συγκέντρωση είναι χαρακτηριστική της μετάβασης του υπό μελέτη συστήματος από διάλυμα (sol) όπου το σύστημα ρέει σε πήκτωμα (gel) όπου το σύστημα δεν ρέει, όπως θα δούμε στις δυναμικές μετρήσεις που ακολουθούν καθώς και στην εικόνα steady state creep n~c n rel SOL n~c 22 GEL 10 2 n~c n~c 1.5 c*=4wt% concentration (wt%) c gel =9wt% 30 Σχήμα 3.10: Εξάρτηση του σχετικού ιξώδους για πολύ χαμηλές τιμές του ρυθμού διάτμησης, για το σύστημα PEO-PS-PEO /[BMIM][PF 6 ]. Τα σύμβολα με μαύρο χρώμα είναι από πειράματα steady state και με πράσινο χρώμα από creep. 68
79 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 Σε c>c gel, οι αλυσίδες διεισδύουν μεταξύ τους και τα μικκύλια σχετικά ακινητοποιούνται λόγω συμφόρησης (jamming) 3 και τελικά το σύστημα να μην ρέει (εικόνα 3.1c). Με περαιτέρω αύξηση της συγκέντρωσης, το σχετικό ιξώδες αυξάνεται πλέον ελαφρά ακολουθώντας τη σχέση 3 nrel ~ c. Εικόνα 3.1: Απεικόνιση δημιουργίας φυσικού πηκτώματος του PEO-PS-PEO σε [BMIM][PF 6 ]. Στην εικόνα 3.2, παρουσιάζονται οι φωτογραφίες των διαλυμάτων του συμπολυμερούς σε ιοντικό υγρό. Διαλύματα συγκέντρωσης από 5-9wt%, συμπεριφέρονται ως ιξωδοελαστικά υγρά που ρέουν. Η μεταβάση υγρού-στερεού (sol-gel) πραγματοποιείται σε συγκέντρωση >9wt%, όπου τα διαλύματα που προκύπτουν συμπεριφέρονται ως ισχυρά gels (free standing gels). Εικόνα 3.2: Ψηφιακή απεικόνιση της μετάβασης sol-gel PEO-PS-PEO σε [BMIM][PF 6 ]. 69
80 G',G'' (Pa) G',G'' (Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΠΕΙΡΑΜΑΤΑ ΔΥΝΑΜΙΚΩΝ ΜΕΤΡΗΣΕΩΝ Ολοκληρώνοντας τη ρεολογική μελέτη του τρισυσταδικού συμπολυμερούς PEO- PS-PEO, πραγματοποιήθηκαν πειράματα δυναμικών μετρήσεων (oscillatory shear measurements) για συγκεντρώσεις μεγαλύτερες του 9wt%, σε κατάσταση πηκτώματος: 1) Σάρωσης τάσεων (Dynamic Stress Sweep Test) υπό σταθερή συχνότητα (f=1hz), κατά τα οποία προσδιορίζονται τα δυναμικά μέτρα αποθήκευσης, G', και απωλειών, G", σαν συνάρτηση της εκατοστιαίας παραμόρφωσης. 2) Σάρωσης συχνοτήτων στη γραμμική ιξωδοελαστική περιοχή (Dynamic Frequency Sweep Test), με την επιβολή ημιτονοειδούς παραμόρφωσης σταθερού πλάτους για ένα καθορισμένο εύρος συχνοτήτων, f= Hz, όπου προσδιορίζονται τα δυναμικά μέτρα G' και G" σαν συνάρτηση της συχνότητας ΔΥΝΑΜΙΚΟ ΠΕΙΡΑΜΑ ΣΑΡΩΣΗΣ ΤΑΣΕΩΝ (Dynamic Stress Sweep Test) Από το πείραμα σάρωσης τάσεων υπό σταθερή συχνότητα f =1Hz, λαμβάνονται τα διαγράμματα του μέτρου αποθήκευσης G' και μέτρου απωλειών G" σα συνάρτηση της εκατοστιαίας παραμόρφωσης (σχήμα 3.11) G' G'' 9wt% PEO-PS-PEO G' G'' 12.5wt% PEO-PS-PEO 10 3 Frequency 1Hz strain (%) strain(%) 70
81 G',G'' (Pa) G',G'' (Pa) G',G'' (Pa) G', G'' (Pa) G',G'' (Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ G' G'' 13.5wt% PEO-PS-PEO Frequency 1Hz G' G'' 15.9wt% PEO-PS-PEO 10 3 Frequency 1Hz strain (%) strain (%) 10 4 G' G'' 17wt% PEO-PS-PEO Frequency 1Hz G' G'' 20wt% PEO-PS-PEO Frequency 1Hz strain (%) strain (%) G' G'' 24.8wt% PEO-PS-PEO Frequency 1Hz strain (%) Σχήμα 3.11: Μέτρα αποθήκευσης και απωλειών σαν συνάρτηση της %παραμόρφωσης διαφόρων συγκεντρώσεων για το σύστημα PEO-PS- PEO/[BMIM][PF 6 ]. 71
82 G',G'' (Pa) G',G'' (Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 Δύο είναι οι κύριες διαπιστώσεις που αφορούν στη ρεολογική συμπεριφορά του τρισυσταδικού συμπολυμερούς που προκύπτουν από το σχήμα Πρώτον, είναι εμφανής η εξάρτηση των δυναμικών μέτρων από τη συγκέντρωση, καθώς η αύξηση της συγκέντρωσης οδηγεί σε αύξηση των τιμών των δυναμικών μέτρων. Για μικρές παραμορφώσεις, κάτω από την κρίσιμη τιμή παραμόρφωσης c 10%, τα δυναμικά μέτρα εμφανίζουν μια χαρακτηριστική περιοχή πλατώ. Για διαλύματα του συμπολυμερούς συγκέντρωσης πάνω από την c gel =9wt% το μέτρο αποθήκευσης, G', παρουσίαζει υψηλότερες τιμές από το μέτρο απωλείων, G". Η δεύτερη διαπίστωση αφορά στην περιοχή πάνω από την c 10%, όπου το μέτρο αποθήκευσης μειώνεται αποτομά σε υψηλές παραμορφώσεις και μας οδηγεί στο συμπεράσμα ότι υπερισχύει η ιξώδης συμπεριφορά και τα διαλύματα αρχίζουν να ρέουν (liquid-like behavior). Έτσι, η γραμμική ιξωδοελαστική περιοχή ορίζεται στην περιοχή για 10% ΔΥΝΑΜΙΚΟ ΠΕΙΡΑΜΑ ΣΑΡΩΣΗΣ ΣΥΧΝΟΤΗΤΩΝ (Dynamic Frequency Sweep Test) Το πείραμα της δυναμικής σάρωσης συχνοτήτων πραγματοποιήθηκε σε 2%, το οποίο δίνει την δυνατότητα απόκτησης πληροφοριών που αφορούν την ιξωδοελαστική συμπεριφορά του φυσικού πηκτωμάτος, χωρίς να καταστρέφεται η δομή του. Τα αποτελέσματα από την διεξαγωγή του πειράματος παρουσιάζονται στο σχήμα G' G'' 9wt% PEO-PS-PEO strain=2% 10 4 G' G'' 10wt% PEO-PS-PEO 10 3 strain=2% Frequency (Hz) Frequency (Hz) 72
83 G', G'' (Pa) G', G'' (Pa) G',G'' (Pa) G',G'' (Pa) G',G'' (Pa) G',G'' (Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ G' G'' 11wt% PEO-PS-PEO strain=2% 10 0 G' G'' 12.5wt% PEO-PS-PEO strain=2% Frequency (Hz) Frequency (Hz) G' G'' 13.5wt% PEO-PS-PEO strain=2% Frequency (Hz) G' G'' 15.9wt% PEO-PS-PEO strain=2% Frequency (Hz) G' G'' 17wt% PEO-PS-PEO strain=2% Frequency (Hz) G' G'' 20wt% PEO-PS-PEO strain=2% Frequency (Hz) 73
84 G', G'' (Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ G' G'' 24.8wt% PEO-PS-PEO strain=2% Frequency (Hz) Σχήμα 3.12: Μέτρα αποθήκευσης και απωλειών σαν συνάρτηση της συχνότητας για το σύστημα PEO-PS-PEO/[BMIM][PF 6 ] διαφόρων συγκεντρώσεων σε 2%. Από το σχήμα 3.12, παρατηρείται η εξάρτηση των δύο δυναμικών μέτρων από τη συγκέντρωση. Το μέτρο αποθήκευσης παρουσιάζει υψηλότερες τιμές για συγκεντρώσεις πάνω από 10wt% έναντι του μέτρου απωλειών, το οποίο αποδεικνύει την δημιουργία του φυσικού πηκτώματος. Στο σχήμα 3.13 παρουσιάζεται συγκεντρωτικά η εξάρτηση του μέτρου αποθήκευσης συναρτήσει της συχνότητας για διαλύματα διαφόρων συγκεντρώσεων. Επιπλέον, το γεγονός ότι σε όλη την περιοχή των συχνοτήτων για μικρές παραμορφώσεις τα μέτρα εμφανίζουν μικρή εξάρτηση από τη συχνότητα για συγκεντρώσεις μεγαλύτερες από 10wt%, επιβεβαιώνει ότι το φυσικό πήκτωμα προσεγγίζει τη συμπεριφορά τέλειου ελαστικού. Μια σημαντική διαπίστωση από το παραπάνω σχήμα αναφέρεται στην εξάρτηση των μέτρων από τη συχνότητα. Συγκρίνοντας τα αποτελέσματα των μετρήσεων με το θεωρητικό μηχανικό φάσμα 4 (σχήμα 3.14), παρατηρούμε πως για μικρές συχνότητες (terminal zone), τα μέτρα εξαρτώνται από τη συχνότητα ως 2 ' & G'' περιοχή είναι χαρακτηριστική της ιξωδοελαστικής συμπεριφοράς και παρατηρείται μόνο σε συγκέντρωση 9wt%, το οποίο καταδυκνύει την συμπεριφορά ενός ιξωδούς υγρού. Για συγκεντρώσεις πάνω από 11wt%, το μέτρο αποθήκευσης παρουσιάζει πλατώ και το μέτρο απωλειών εμφανίζει ελάχιστο. Η συμπεριφορά αυτή αναφέρεται σύμφωνα με το θεωρητικό μηχανικό φάσμα σε υψηλές συχνότητες, ενώ στο σύστημα μας εμφανίζεται και στις χαμηλές συχνότητες. Η μη εμφάνιση της terminal zone στο εύρος συχνοτήτων που είχε οριστεί, υποδηλώνει ότι η εμφάνισή της πραγματοποιείται σε πολύ πιο χαμηλές συχνότητες και ότι η τιμή του χρόνου χαλάρωσης τους 74 G. Η
85 G' (Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 συστήματος είναι πολύ μεγάλη. Ακόμα, σε πιο υψηλές συχνότητες παρατηρείται η περιοχή transition zone, καθώς το μέτρο απωλειών εμφανίζει υψηλότερη τιμή από το μέτρο αποθήκευσης. Αξιοσημειώτη είναι η συμπεριφορά του διαλυμάτος συγκέντρωσης 10wt%, όπου εμφανίζονται και οι τρεις περιοχές terminal, plateau και transition zone του θεωρητικού φασμάτος c=10wt% c=11wt% c=12.5wt% c=13.5wt% c=15.9wt% c=17wt% c=20wt% c=24.8wt% Frequency (Hz) Σχήμα 3.13: Μεταβολή του μέτρου αποθήκευσης των διαλυμάτων του τρισυσταδικού συμπολυμερούς PEO-PS-PEO στο ιοντικό υγρό [BMIM][PF 6 ] συναρτήσει της συχνότητας σε διάφορες συγκεντρώσεις. Σχήμα 3.14: Θεωρητικό διάγραμμα εξάρτησης των G' και G" από την συχνότητα 5. 75
86 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΜΕΤΑΒΟΛΗ ΤΟΥ ΜΕΤΡΟΥ ΑΠΟΘΗΚΕΥΣΗΣ ΚΑΙ ΤΟΥ ΧΡΟΝΟΥ ΧΑΛΑΡΩΣΗΣ ΜΕ ΤΗ ΣΥΓΚΕΝΤΡΩΣΗ ΤΟΥ ΠΟΛΥΜΕΡΟΥΣ Με βάση τα αποτέλεσματα που προέκυψαν από το πείραμα ερπυσμού και τις δυναμικές μετρήσεις, παρουσιάζεται η μεταβολή του μέτρου αποθήκευσης και του χρόνου χαλάρωσης συναρτήσει της συγκέντρωσης. Από το πείραμα ερπυσμού το μέτρο αποθήκευσης στην περιοχή πλατώ, G o, υπολογίζεται από τη σχέση J 1/ G και ο χρόνος χαλάρωσης n / G. Από τις δυναμικές μετρήσεις το G o R o o προσδιορίστηκε σε συχνότητα f=1ηz και ο τ R υπολογίστηκε από το αντίστροφο της συχνότητας στο σημείο τομής των G' και G". Στον πινάκα 3.3, παρουσίαζονται οι τιμές του μέτρου αποθήκευσης και του χρόνου χαλάρωσης όπως υπολογίσθηκαν από μετρήσεις ερπυσμού και δυναμικές μετρήσεις. o o Πίνακας 3.3: Τιμές των G ο και τ R. Μετρήσεις ερπυσμού Δυναμικές μετρήσεις c (wt%) G ο (Pa) τ R (s) G ο (Pa) τ R (s)
87 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ creep oscillation 10 3 R (sec) G o (Pa) creep oscillation 10 3 SOL GEL concentration (wt%) Σχήμα 3.15: Μέτρο αποθήκευσης στην περιοχή πλατώ, G o, συναρτήσει της συγκέντρωσης για το σύστημα PEO-PS-PEO σε [BMIM][PF 6 ]. Τα μαύρα σύμβολα αντιστοιχούν σε μετρήσεις ερπυσμού ενώ τα κόκκινα σύμβολα σε δυναμικές μετρήσεις SOL GEL concentration (wt%) Σχήμα 3.16: Χρόνος χαλάρωσης, τ R, συναρτήσει της συγκέντρωσης για το σύστημα PEO-PS-PEO σε [BMIM][PF 6 ]. Τα μαύρα σύμβολα αντιστοιχούν σε μετρήσεις ερπυσμού ενώ τα κόκκινα σύμβολα σε δυναμικές μετρήσεις. Στο σχήμα 3.15, παρουσιάζεται η εξάρτηση του μέτρου αποθήκευσης στην περιοχή πλατώ, G o, από την συγκέντρωση. Το G o εκφράζει την ισχύ του φυσικού πηκτώματος, όπου η αύξηση της συγκέντρωσης οδηγεί και στην αύξηση του μέτρου 77
88 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 αποθήκευσης G o. Επιπροσθέτως, στο σχήμα 3.16 παρουσιάζεται ο χρόνος χαλάρωσης συναρτήσει της συγκέντρωσης. Ο χρόνος χαλάρωσης έχει σχέση με το χρόνο που απαιτείται ώστε τα μικκύλια να κινηθούν κατά ένα μήκος ίσο με το μέγεθος τους. Για συγκεντρώσεις μεγαλύτερες από τη c gel (9wt%), δηλαδή στη περιοχή μετάβασης solgel ο χρόνος χαλάρωσης, τ R, εμφανίζει δραματική αύξηση η οποία σχετίζεται με την δραματική μειώση της κινητικότητας των μικκυλίων. Αποτέλεσμα της αύξησης του τ R είναι η δραματική αύξηση του σχετικού ιξώδους, όπως παρατήρηθηκε στο σχήμα 3.10 για c>c gel (n rel ~c 22 ). Σε υψηλότερες συγκεντρώσεις (c>13.5wt%), ο τ R παρουσιάζει πλατώ λόγω του κόρεσμου του φαινόμενου συμφόρησης (jamming effect) όπου λόγω των μεγάλων χρονών χαλάρωσης τα μικκύλια σχεδόν ακινητοποιούνται. 3.6 ΕΠΙΔΡΑΣΗ ΤΗΣ ΘΕΡΜΟΚΡΑΣΙΑΣ Σε επόμενο στάδιο πραγματοποιήθηκε διερεύνιση της επίδρασης της θερμοκρασίας στις ιδιότητες των δυναμικών ρεολογικών μέτρων. Συγκεκριμένα, μελετήθηκε η εξάρτηση των δυναμικών μέτρων αποθήκευσης G' και απωλειών G" του συστήματος 20wt% PEO-PS-PEO/[BMIM][PF 6 ] από τη θερμοκρασία (σχήμα 3.17). Στο σχήμα 3.17 παρατηρείται πως σε όλο το μελετώμενο θερμοκρασιακό εύρος, το μέτρο αποθήκευσης G' είναι πάντα υψηλότερο του μέτρου απωλειών G" κατά ~1 τάξη μεγέθους, συμπεριφορά που υποδεικνύει πως το υπό μελέτη σύστημα είναι ένα ισχυρό gel και συμφωνεί με τα αποτελέσματα από το πείραμα σάρωσης τάσεων υπό σταθερή συχνότητα f =1Hz (σχήμα 3.11). Αξιοσημείωτο είναι το γεγονός πως και τα δυο δυναμικά μέτρα παραμένουν σταθερά, ανεξαρτήτου μεταβολής της θερμoκρασίας. Επίσης είναι σημαντικό να σημειωθεί πως η διαδικασία θέρμανσης σχεδόν συμπίπτει με τη διαδικασία ψύξης, πράγμα που υποδηλώνει πως το gel που έχει σχηματιστεί παραμένει σταθερό. Σε αντίστοιχη μελέτη που έχει πραγματοποιηθεί για ένα πολυμερές που φέρει τις ίδιες συστάδες PS και PEO αλλά διαφορετικής αρχιτεκτονικής όπου το ΡΕΟ αποτελεί την κεντρική συστάδα με τις συστάδες PS να βρίσκονται στα άκρα του πολυμερούς, PS-PEO-PS, βρέθηκε πως τα μέτρα G' και G" εξαρτώνται σημαντικά από τη θερμοκρασία 5. Το σύστημα PS-PEO-PS/[ΕMIM][TFSI] εμφανίζει μετάβαση από gel σε διάλυμα (gel-sol transition) σε θερμοκρασία T gel =70 o C (σχήμα 3.18). Η σταθερότητα των μέτρων G' και G" που παρουσιάζει το σύστημα PEO-PS- 78
89 G', G'' (Pa) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 PEO/[BMIM][PF 6 ] σε θερμοκρασίες μέχρι 150 o C ενισχύει την καινοτομία του. Η διαφορά μεταξύ των δυο συστημάτων έγκειται στο γεγονός πως το PS-PEO- PS/[ΕMIM][TFSI] σχηματίζει ένα δίκτυο το οποίο σε υψηλές θερμοκρασίες (Τ>70 o C) μετατρέπεται από gel σε διάλυμα λόγω της ευκολίας εξόδου των συστάδων του PS από τις φυσικές διασυνδέσεις του δικτύου. Αντίθετα, στο PEO-PS- PEO/[BMIM][PF 6 ] σύστημα όπου το gel σχηματίζεται εξαιτίας του φαινομένου της συμφόρησης (jamming), η δομή του gel δεν επηρεάζεται από την αύξηση της θερμοκρασίας G' heating G' cooling G'' heating G'' cooling Temperature ( o C) Σχήμα 3.17 : Μέτρα αποθήκευσης και απωλειών σαν συνάρτηση της θερμοκρασίας σε ένα κύκλο θέρμανσης-ψύξης για το σύστημα 20wt% PEO-PS-PEO/[BMIM][PF 6 ]. Οι μετρήσεις πραγματοποιήθηκαν σε παραμόρφωση γ=1 % και συχνότητα f=0.1hz με ρυθμό θέρμανσης-ψύξης 5 ο C/min. 79
90 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 Σχήμα 3.18 : Μέτρα αποθήκευσης και απωλειών σαν συνάρτηση της θερμοκρασίας σε ένα κύκλο θέρμανσης-ψύξης για το σύστημα 10wt% PS-PEO-PS/[BMIM][PF 6 ]. Οι μετρήσεις πραγματοποιήθηκαν σε παραμόρφωση γ=2 % και συχνότητα ω=0.1rad/s με ρυθμό θέρμανσης-ψύξης 1 ο C/min ΣΥΜΠΕΡΑΣΜΑΤΑ Στο παρόν κεφάλαιο μελετήθηκε η συμπεριφορά του τρισυσταδικού συμπολυμερούς PEO-PS-PEO στο ιοντικό υγρό [BMIM][PF 6 ]. Η μελέτη πραγματοποιήθηκε σε αραιά διαλύματα μέσω των τεχνικών δυναμικής σκέδασης φωτός (DLS) και της ιξωδομετρίας AMVn, ενώ για πυκνά διαλύματα πραγματοποιήθηκαν ρεολογικές μετρήσεις. Από την τεχνική DLS υπολογίστηκε η υδροδυναμική ακτίνα των μικκυλίων του τρισυσταδικού συμπολυμερούς, R h ~45nm, και προέκυψε η σφαιρική δομή των μικκυλίων που πιθανόν έχουν μεγάλο βαθμό συσσωμάτωσης, N agg, όποτε το κάθε μικκύλιο έχει πυκνή και συμπαγή δομή. Επίσης, μέσω της τεχνικής της ιξωδομετρίας AMVn, η τιμή της κρίσιμης συγκέντρωσης επικάλυψης βρέθηκε να είναι c*=4wt%. Μέσω της ρεολογικής μελέτης που πραγματοποιήθηκε, προσδιορίστηκε η κρίσιμη συγκέντρωση πηκτώματος, c gel =9wt%. Από την μεταβολή του σχετικού ιξώδους, n rel, συναρτήσει της συγκέντρωσης, παρατηρήθηκε η εξάρτηση τους σχετικού ιξώδους από τη συγκέντρωση. Σε c>c*, το n rel αυξάνεται απότομα με τη συγκέντρωση λόγω του ότι τα μικκύλα πλησιάζουν μεταξύ τους με αποτέλεσμα να αυξάνεται η δυσκολία 80
91 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 3 κίνησής τους. Σε αυτή την περιοχή συγκεντρώσεων, οι δυνάμεις άπωσης μεταξύ των αλυσίδων PEO καταργούνται και τα μικκύλια αρχίζουν να αλληλοεμπλέκονται μεταξύ τους. Με περαιτέρω αύξηση της συγκέντρωσης, το σχετικό ιξώδες αυξάνεται δραματικά έως και έξι τάξεις μεγέθους, σύμφωνα με τη σχέση rel ~ c 22. Στην c gel =9wt% παρατηρείται η μετάβαση sol-gel. Σε c>c gel, τα μικκύλια αρχίζουν να αλληλοδιασυνδέονται μεταξύ τους με αποτέλεσμα η κίνηση των μικκυλίων να δυσκολεύει όλο και περισσότερο και τελικά να παρατηρείται συμφόρηση (jamming) και το σύστημα να μην ρέει. Επιπροσθέτως, παρατηρήθηκε η μεταβολή του μέτρου αποθήκευσης, G o, και του χρόνου χαλάρωσης, τ R, με τη συγκέντρωση. Το G o που εκφράζει την ισχύ του φυσικού πηκτώματος, αυξάνεται με την αύξηση της συγκέντρωσης. Για συγκεντρώσεις μεγαλύτερες από τη c gel (9wt%), ο τ R εμφανίζει δραματική αύξηση η οποία σχετίζεται με την δραματική μειώση της κινητικότητας των μικκυλίων. Σε υψηλότερες συγκεντρώσεις, ο τ R παρουσιάζει πλατώ λόγω του κόρεσμου του φαινόμενου συμφόρησης (jamming effect). Το gel που σχηματίζει το σύστημα 20wt% PEO-PS-PEO/[BMIM][PF 6 ] παραμένει σταθερό σε ένα μεγάλο θερμοκρασιακό εύρος 20 o C<T<150 o C, γεγονός που υποδηλώνει πως το σύστημά μας μπορεί να χρησιμοποιηθεί σε εφαρμογές που απαιτούν υψηλές θερμοκρασίες. 3.8 ΒΙΒΛΙΟΓΡΑΦΙΑ 1 He Y.; Boswell P. G.; Bühlmann P.; Lodge P. T. J. Phys. Chem. B. 2007, 111, Zhang S.; Lee H. K.; Sun J.; Frisbie D. C.; Lodge P. T. Macromoleculus, 2011, 44(22) pp Liu A.J.; Nagel S.R, Nature, 1998, 396, Groot R.D.; Agterof W.G.M. Macromolecules, 1995, 28, He Y.; Lodge T. P. Macromolecules, 2008, 41,
92 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΚΑΙ ΡΕΟΛΟΓΙΚΗ ΜΕΛΕΤΗ ΤΟΥ ΕΤΕΡΟΚΛΑΔΙΚΟΥ ΑΣΤΕΡΟΕΙΔΟΥΣ ΣΥΜΠΟΛΥΜΕΡΟΥΣ PS 10 PEO ΕΙΣΑΓΩΓΗ Τα αστεροειδή πολυμερή παρουσιάζουν σημαντικό ενδιαφέρον, καθώς χρησιμοποιούνται σε διάφορες βιομηχανικές εφαρμογές. Επίσης, από πειραματικής απόψεως, η σύνθεση αστεροειδών με μικρή διασπορά και με δυνατότητα επιλογής του πλήθους των κλάδων είναι πρόκληση. Πολλές μελέτες έχουν πραγματοποιηθεί σχετικά με τις ιδιότητες των αστεροειδών συμπολυμερών σε διάλυμα. Λόγω της ιδιαίτερης αρχιτεκτονικής τους, τα αστεροειδή συμπολυμερή, όταν διαλύονται σε ένα εκλεκτικό διαλύτη, αυτοοργανώνονται σχηματίζοντας σωματίδια που μιμούνται τη δομή μικκυλίων. Μάλιστα τα σωματίδια αυτά χαρακτηρίζονται από πολύ μικρούς ή και μηδενικούς αριθμούς συσσωμάτωσης, σε αντίθεση με τα γραμμικά συμπολυμερή που παρουσιάζουν μεγάλους αριθμούς συσσωμάτωσης. Στο κεφάλαιο αυτό μελετάμε τις ιδιότητες των διαλυμάτων του ετεροκλαδικού αστεροειδούς συμπολυμερούς, A n B n, που αποτελείται από συστάδες πολυστυρολίου (PS) και συστάδες πολυαιθυλενοξειδίου (PEO), στο ιοντικό υγρό εξαφθοροφωσφορούχο 1-βούτυλο-3-μέθυλιμιδαζόλιο (1-butyl-3-methylimadozolium hexafluapophoshate), [BMIM][PF 6 ], το οποίο είναι «καλός» διαλύτης για το πολυαιθυλενοξείδιο (PEO) 1. Θα εστιάσουμε κυρίως στη μελέτη των ρεολογικών ιδιοτήτων των διαλυμάτων του αστεροειδούς συμπολυμερούς στο [BMIM][PF 6 ]. 4.2 ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΤΟΥ PS 10 PEO 10 Ο χαρακτηρισμός του ετεροκλαδικού αστεροειδούς συμπολυμερούς PS 10 PEO 10, που είχε παρασκευασθεί στο εργαστήριο αποσκοπεί στον ακριβή προσδιορισμό των μοριακών χαρακτηριστικών. Για να επιτευχθεί αυτό χρησιμοποιήθηκαν οι εξής 82
93 arbitrary units ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 βασικές τεχνικές: χρωματογραφία αποκλεισμού μεγεθών (SEC), στατική σκέδαση φωτός και φασματοσκοπία πυρηνικού μαγνητικού συντονισμού (NMR) ΧΡΩΜΑΤΟΓΡΑΦΙΑ ΑΠΟΚΛΕΙΣΜΟΥ ΜΕΓΕΘΩΝ (SEC) Ο προσδιορισμός του μοριακού βάρους και της πολυδιασποράς του συμπολυμερούς PS 10 PEO 10 πραγματοποιήθηκε με την συγκεκριμένη τεχνική. Χρησιμοποιήθηκε ένας Polymer Lab χρωματογράφος αποτελούμενος από δύο Plgel 5 μm στήλες, ένα διαφορικό διαθλασίμετρο ως ανιχνευτή (RI) καθώς και ένα UV/VIS ανιχνευτή (254 nm). Η κινητή φάση ήταν τετραϋδροφουράνιο (THF) και η ταχύτητα ροής 0.5mL/min. Το σύστημα βαθμονομήθηκε με πρότυπα δείγματα πολυστυρολίου (PS) με μοριακά βάρη MW: Da. Για την πραγματοποίηση του πειράματος, παρασκευάσθηκε δείγμα συγκεκριμένης συγκέντρωσης: (0.2μg PS 10 PEO 10 σε 2mL THF). Το δείγμα έμεινε υπό ανάδευση για 24 ώρες και πριν την έναρξη του πειράματος, το δείγμα φιλτραρίστηκε με φίλτρο PTFE 0.45μm για την απομάκρυνση τυχόν σκόνης. Το χαρακτηριστικό χρωματογράφημα του συμπολυμερούς PS 10 PEO 10 σα συνάρτηση του όγκου έκλουσης φαίνεται στο σχήμα 4.1 που ακολουθεί. Όπως αναμένεται, στο χρωματογράφημα του PS 10 PEO 10 εμφανίζεται μια σχετικά στενή κορυφή που δείχνει στενή κατανομή μοριακών βαρών PS 10 PEO Elution Volume (ml) Σχήμα 4.1: Χρωματογράφημα (SEC) του συμπολυμερούς PS 10 PEO
94 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΦΑΣΜΑΤΟΣΚΟΠΙΑ ΠΥΡΗΝΙΚΟΥ ΜΑΓΝΗΤΙΚΟΥ ΣΥΝΤΟΝΙΣΜΟΥ ( 1 Η-NMR) Η φασματοσκοπία πυρηνικού μαγνητικού συντονισμού τύπου 1 H-NMR χρησιμοποιήθηκε για τον υπολογισμό της σύστασης του συμπολυμερούς PS 10 PEO 10, με την βοήθεια φασματογράφου τύπου Brucker Avance DPX με συχνότητα 400ΜΗz. Ως διαλύτης χρησιμοποιήθηκε το δευτεριωμένο χλωροφόρμιο, CDCl 3. Το φάσμα 1 H- NMR του PS 10 PEO 10 φαίνεται στο σχήμα 4.2. Οι κορυφές του φάσματος που παίρνουμε από τον καταγραφέα αντιστοιχούν σε πρωτόνια (H). Η ισχυρή κορυφή με χημική μετατόπιση περίπου στα 7.3 ppm αντιστοιχεί στο διαλύτη (CDCl 3 ). Η ομάδα κορυφών με χημική μετατόπιση από 6.3 ppm μέχρι 7.2 ppm, αντιστοιχεί στα πέντε πρωτόνια του αρωματικού δακτυλίου. Επίσης, η ομάδα κορυφών με χημική μετατόπιση από τα 3.4 ppm μέχρι τα 3.9 ppm αντιστοιχεί στα πρωτόνια των ομάδων CH 2 (d) και CH2 του PEO (e) ενώ, η κορυφή που εμφανίζεται στην περιοχή από 1.2 ppm μέχρι 2 ppm ανιστοιχεί στα πρωτόνια των βινυλικών ομάδων CH 2 (a) και CH του PS (b). Από την ολοκλήρωση των κορυφών 1 H-NMR προκύπτει η εκατοστιαία κατά βάρος σύσταση των μονομερών στην ένωση. Σχήμα 4.2: Χαρακτηριστικό φάσμα 1 H-NMR του συμπολυμερούς PS 10 PEO 10 σε CDCl 3. 84
95 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 Τα μοριακά χαρακτηριστικά του ετεροκλαδικού αστεροειδούς συμπολυμερούς PS 10 PEO 10 παρατίθενται στον πίνακα 4.1. Πίνακας 4.1:Μοριακά χαρακτηριστικά του PS 10 PEO 10. PS PEO POLYMER M w α I b M wpsn b M w(arm) b wt% c DP M w(arm) d wt% c DP PS 10 PE a Μέσω στατικής σκέδασης φωτός (SLS) b Από μέτρηση SEC c Μέσω της ανάλυσης φασμάτος 1 Η-NMR d Από υπολογισμούς: Mw arm Mw Mw, PS star number of arms DP: βαθμός πολυμερισμού I M M w n : πολυδιασπορά 4.3 ΥΛΙΚΑ Στην παρούσα εργασία τα υλικά που χρησιμοποιήθηκαν είναι τα ακόλουθα: Το ετεροκλαδικό (heteroarm) αστεροειδές συμπολυμερές τύπου Α n Β n που φέρει 10 κλάδους PS και 10 κλάδους PEO, PS 10 PEO 10, το οποίο είχε παρασκευασθεί στο εργαστήριο. Το ιονικό υγρό, εξαφθοροφωσφορούχο 1-βούτυλο-3-μέθυλιμιδαζόλιο (1-butyl-3-methylimadazolium hexafluapophoshate), [BMIM][PF 6 ] (Alfa Aesar) και τέλος ο συνδιαλύτης (co-solvent) διχλωρομεθάνιο (dichloromethane), CH 2 Cl ΠΑΡΑΣΚΕΥΗ ΔΕΙΓΜΑΤΩΝ Για την παρασκευή πολυμερικών διαλυμάτων ακολουθήθηκε καθορισμένη διαδικασία. Άρχικα αφού ζυγίστηκαν οι απαιτούμενες ποσότητες πολυμερούς, προστέθηκε σ αυτές συνδιαλύτης CΗ 2 Cl 2 1mL. Υστερα από ανάδευση προστέθηκε το ιονικό ύγρο, [BMIM][PF 6 ], και για την πλήρη ομογενοποίηση πραγματοποιήθηκε φυγογκέντρηση των δειγμάτων με υψηλό ιξώδες σε μηχάνημα φυγοκέντρησης Sigma 85
96 m (g) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 2K15 με περιστροφή 5000στροφές/min για 15min. Στη συνέχεια, τα δείγματα τοποθετήθηκαν σε φούρνο σε θερμοκρασία C για την εξάτμιση του συνδιαλύτη για κάποιες μέρες και μετέπειτα στο φούρνο ύπο κένο σε θερμοκρασία εως 70 0 C, για την πλήρη εξάτμιση του συνδιαλύτη και την αποφυγή υγρασίας. Πρέπει να σημειωθεί πως κατά την παρασκευή των δειγμάτων ήταν αρκετός ο απαιτούμενος χρόνος για την εξάτμιση του συνδιαλύτη. Τα διαλύματα υψηλής συγκέντρωσης συγκεκριμένα, χρειάστηκαν σχέδον 5 ημέρες παραμονής στο φούρνο. Στο σχήμα 4.3 παρουσιάζεται ο χρόνος που χρειάστηκαν διαλύματα διαφορετικής συγκέντρωσης για την πλήρη εξάτμιση του συνδιαλύτη. Παρασκευάσθηκαν δείγματα του ετεροκλαδικού αστεροειδούς συμπολυμερούς PS 10 PEO 10 διαφόρων συγκεντρώσεων: 9.6, 13.1, 13.5, 14.2, 14.5, 15.2, 16.7, 18 wt%. Oι συγκεντρώσεις 10.5, 11.4, 12.2, 12.4 wt% προέκυψαν από ανάμειξη μητρικών διαλυμάτων wt% 13.5wt% 18wt% time (hours) Σχήμα 4.3: Μεταβολή της μάζας διαλυμάτων PS 10 PEO 10 διαφορετικών συγκεντρώσεων συναρτήσει του χρόνου που απαιτείται για την πλήρη εξάτμιση του συνδιαλύτη, CΗ 2 Cl 2. 86
97 g 1 (t) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΜΕΛΕΤΗ ΑΡΑΙΩΝ ΔΙΑΛΥΜΑΤΩΝ PS 10 PEO ΔΥΝΑΜΙΚΗ ΣΚΕΔΑΣΗ ΦΩΤΟΣ (DLS) Πειράματα DLS πραγματοποιήθηκαν στους 25ºC, σε διάλυμα PS 10 PEO wt% που προέκυψε έπειτα από αραίωση του διαλύματος 9.6 wt% σε [BMIM][PF 6 ]. Πριν από την πραγματοποίηση του πειράματος, το διάλυμα φιλτραρίστηκε για την απομάκρυνση της σκόνης και σωματιδίων που εμποδίζουν την αξιοπιστία της μέτρησης, με φίλτρο 0.45μm και αφέθηκε να ισορροπήσει για 24 ώρες. Η δυναμική σκέδαση του φωτός για αραιά διαλύματα χρησιμοποιήθηκε για τον προσδιορισμό του μεγέθους των διασπαρμένων σωματιδίων του αστεροειδούς PS 10 PEO 10 στο ιοντικό υγρό [BMIM][PF 6 ] (υδροδυναμική ακτίνα, R h ). Η πειραματική διάταξη περιγράφηκε στο προηγούμενο κεφάλαιο (παράγραφος 3.4.1). Η ανάλυση της συνάρτησης αυτοσυσχέτισης (g 1 (t)) πραγματοποιήθηκε με βάση τη μέθοδο CONTIN (σχήμα 4.4). Με βάση την ανάλυση αυτή ελήφθησαν τα διαγράμματα που παρουσιάζουν την κατανομή των χρόνων χαλάρωσης και από το μέγιστο της κατανομής λαμβάνεται ένας μέσος χρόνος απ όπου προκύπτει το μέγεθος των μικκυλίων μέσω του συντελεστή διάχυσης. Στο σχήμα 4.5 παρατίθεται η συνάρτηση αυτοσυσχέτισης μαζί με την κατανομή του χρόνου χαλάρωσης για 0.2wt% διάλυμα PS 10 PEO 10 /[BMIM][PF 6 ] σε γωνία 90º στους 25ºC. 1,0 0,8 Angle=40 o Angle=50 o Angle=60 o Angle=70 o Angle=80 o Angle=90 o 0,6 0,4 0,2 0, Time (ms) Σχήμα 4.4: Χρονική εξάρτηση της συνάρτησης αυτοσυσχέτισης (g 1 (t)) των διαλυμάτων PS 10 PEO 10 /[BMIM][PF 6 ] σε γωνίες 40 ο έως 90 ο και θερμοκρασία 25 ο C. 87
98 g 1 (t) L -1 (t) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 1,0 0,8 Angle=90 o 0,6 0,4 0,2 0, Time (ms) Σχήμα 4.5: Χρονική εξάρτηση της συνάρτησης αυτοσυσχέτισης (g 1 (t)) μαζί με την κατανομή του χρόνου χαλάρωσης του διαλύματος PS 10 PEO 10 /[BMIM][PF 6 ] σε γωνία 90 ο και θερμοκρασία 25 ο C. Ο συντελεστής διάχυσης των συσσωματωμάτων προσδιορίστηκε από την κλίση της ευθείας της γραφικής παράστασης του αντίστροφου χρόνου χαλάρωσης συναρτήσει του τετραγώνου του ανύσματος της σκέδασης. Η γραφική παράσταση 1 2 f( q ) φαίνεται στο παρακάτω σχήμα 4.6. Από την κλίση της ευθείας προκύπτει ο συντελεστής διάχυσης Stokes Einstein: R H Do m s και με τη χρήση της εξίσωσης kb T υπολογίζεται η υδροδυναμική ακτίνα των 6 D o συσσωματωμάτων: R h =23.5 nm. Επίσης, στο ένθετο παρουσιάζεται ο συντέλεστης διάχυσης Do 2 / q συναρτήσει του q 2, που έχει σταθερές τιμές ανεξαρτήτου γωνιών, γεγονός που αποδεικνύει τη σφαιρική δομή των μικκυλίων. Στο σχήμα 4.7 παρουσιάζεται ενδεικτικά η κατανομή μεγέθους του πληθυσμού των σωματιδίων του αστεροειδούς συμπολυμερούς. Για όλες τις γωνίες παρατηρήθηκε μονομοριακή κατανομή των σχηματιζόμενων σωματιδίων. 88
99 Γ (s -1 ) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ,0x10-13 Intensity Weighted Distribution 20 q 2 (s -1 ) 8,0x ,0x ,0x ,0x x x x x x10 14 q 2 (m -2 ) x x x x x10 14 q 2 (m -2 ) Σχήμα 4.6: Εξάρτηση του αντίστροφου χρόνου χαλάρωσης, Γ, από το τετράγωνο του ανύσματος της γωνίας σκέδασης, q 2. Στο ένθετο παρουσιάζεται ο συντέλεστης διάχυσης συναρτήσει του q 2. Το πείραμα πραγματοποιήθηκε σε διάλυμα PS 10 PEO 10 /[BMIM][PF 6 ] συγκέντρωσης 0.2wt%, για γωνίες από 40º έως 90º στους 25ºC θ=90 ο diameter (nm) Σχήμα 4.7: Διάγραμμα κατανομής της διαμέτρου των σωματιδίων του συμπολυμερούς PS 10 PEO 10 σε [BMIM][PF 6 ] για γωνία 90 ο στους 25 o C. 89
100 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΥΠΟΛΟΓΙΣΜΟΣ ΤΗΣ ΚΡΙΣΙΜΗΣ ΣΥΓΚΕΝΤΡΩΣΗΣ ΕΠΙΚΑΛΥΨΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PS 10 PEO 10 /[BMIM][PF 6 ] H κρίσιμη συγκέντρωση επικάλυψης (overlap concentration), c*, αραιών διαλυμάτων υπολογίστηκε μέσω της τεχνικής της ιξωδομετρίας AMVn. Παρασκευάστηκαν διαλύματα του αστεροειδούς συμπολυμερούς PS 10 PEO 10 συγκέντρωσης 0.1, 0.15, 0.4 και 0.5wt% από αραίωση του μητρικού διαλύματος 9.6wt% σε [BMIM][PF 6 ]. Για την αξιοπιστία των μετρήσεων ακολουθήθηκε πρωτόκολλο κατά την προετοιμασία των διαλυμάτων: Αρχικά παρασκευάστηκαν τα διαλύματα συγκεκριμένων συγκεντρώσεων, για την πλήρη ομογενοποίηση των οποίων ακολούθησε ανάδευση και στη συνέχεια τα δείγματα τοποθετήθηκαν σε φούρνο υπό κενό σε θερμορκασία έως 75 0 C για διάστημα 5-6 ωρών για την απομάκρυνση υγρασίας. Κατά την διάρκεια του πειράματος, το κάθε δείγμα τοποθετήθηκε σε γυάλινο τριχοειδή σωλήνα με διάμετρο σφαίρας 3mm, προσεκτικά, για την αποφυγή δημιουργίας φυσαλίδων. Η θερμοκρασία του πειράματος ήταν 25 ο C. Από το χρόνο ροής της σφαίρας μέσα στο σωλήνα, υπολογίστηκε το δυναμικό ιξώδες του δείγματος. Στη συνέχεια, από τη σχέση n/ n 1, προσδιορίστηκε το ειδικό ιξώδες. Από την καμπύλη του sp o ανηγμένου ιξώδους nsp / c συναρτήσει της συγκέντρωσης, c, υπολογίστηκε το εσωτερικό ιξώδες, [η], όπου ορίζεται από την τεταγμένη επί την άρχη για c 0 (σχήμα 4.8). Η κρίσιμη συγκέντρωση επικάλυψης δίνεται από την σχέση c* 1/[ n] = 3.6wt%. 0,4 0,3 PS 10 PEO 10 copolymer Fitting linear [n]= c*=3.6 wt% 0,2 sp /c 0,1 0,0 0,0 0,1 0,2 0,3 0,4 0,5 0,6 concentration (wt%) Σχήμα 4.8: Καμπύλη εξάρτησης του nsp / c από την συγκέντρωση για διαλύματα του συμπολυμερούς PS 10 PEO 10 σε [BMIM][PF 6 ] (οι μπλε γραμμές αντιστοιχούν στο σφάλμα των μετρήσεων). 90
101 viscosity (Pa.s) viscosity (Pa.s) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ ΜΕΛΕΤΗ ΠΥΚΝΩΝ ΔΙΑΛΥΜΑΤΩΝ PS 10 PEO ΕΙΣΑΓΩΓΗ Μέχρι τώρα μελετήσαμε τη συμπεριφορά του ετεροκλαδικού συμπολυμερούς σε αραιά διαλύματα. Στην συνέχεια ακολουθεί η μελέτη του συστήματος PS 10 PEO 10 /[BMIM][PF 6 ] σε πυκνά διαλύματα μέσω ρεολογικών πειραμάτων ΡΕΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΣΤΑΘΕΡΗΣ ΚΑΤΑΣΤΑΣΗΣ (Steady-State) Η μη γραμμική ρεολογική συμπεριφορά των διαλυμάτων του ετεροκλαδικού αστεροειδούς συμπολυμερούς PS 10 PEO 10 διαφόρων συγκεντρώσεων, από συγκέντρωση 9.6wt% όπου το σύστημα συμπεριφέρεται ως νευτώνειο υγρό μέχρι πηκτώματα υψηλού ιξώδους 18wt%, μελετήθηκε υποβάλλοντας τα δείγματα σε σταθερή διατμητική ροή (steady state shear flow). Αρχικά παραθέτουμε τα αποτελέσματα ενός ολοκληρωμένου πειράματος σε συγκέντρωση 13.5wt%, ενώ ακολουθούν συγκριτικές καμπύλες σε όλη την κλίμακα των συγκεντρώσεων που μελετήθηκαν (a) 13.5% wt increasing stress 13.5% wt decreasing stress 10 5 (b) 13.5% wt increasing rate 13.5% wt decreasing rate PS 10 PEO shear stress (Pa) PS 10 PEO shear rate (s -1 ) Σχήμα 4.9: Χαρακτηριστικές καμπύλες ιξώδους-διατμητικής τάσης (a) και ιξώδους-ρυθμού διάτμησης (b), με αυξανόμενα και μειούμενα τάση και ρυθμό διάτμησης για το 13.5wt% PS 10 PEO 10 σε [BMIM][PF 6 ]. Από την καμπύλη του ιξώδους συναρτήσει της διατμητικής τάσης ή του ρυθμού διάτμησης (σχήμα 4.9 (a)&(b) ), μπορούμε να διακρίνουμε κάποιες χαρακτηριστικές περιοχές μεταβολής. Στην πρώτη περιοχή, σ<100pa, το σύστημα δεν επηρεάζεται 91
102 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 από την επιβαλλόμενη τάση και η τιμή του ιξώδους παραμένει σταθερή σχηματίζοντας ένα νευτωνικό πλατώ. Η τιμή του ιξώδους σε αυτή την περιοχή είναι περίπου 2 τάξεις μεγέθους μεγαλύτερη από το ιξώδες του μέσου ([BMIM][PF 6 ] : η=0.270 Pas). Στην δεύτερη περιοχή, σ>100pa, παρατηρείται μια συνεχής μειώση του ιξώδους με αύξηση της επιβαλλόμενης διατμητικής τάσης ή αντίστοιχα του ρυθμού διάτμησης. Παρατηρούνται δηλαδή φαινόμενα ρεολέπτυνσης (shear thinning), όπου λόγω υψηλής διατμητικής τάσης ή ρυθμού διάτμησης το ιξώδες του συστήματος μειώνεται. Η αντίστροφη πειραματική διαδικασία, σύμφωνα με την οποία η επιβαλλόμενη τάση ή αντίστοιχα ο ρυθμός διάτμησης σταδιακά μειώνονται, είναι απόλυτα αντιστρεπτή καθώς δεν παρουσιάζει διαφορές από την προηγούμενη συμπεριφορά και οι καμπύλες συμπίπτουν. Το προφίλ του ιξώδους, όπως αυτό μετρήθηκε σε σειρά διαλυμάτων διαφόρων συγκεντρώσεων σα συνάρτηση της διατμητικής τάσης φαίνεται στο σχήμα Παρατηρούμε πως όσο αυξάνεται η συγκέντρωση, τόσο αυξάνεται και η τιμή του ιξώδους, η, λόγω του αυξανόμενου συνωστισμού των διασπαρμένων αστεροειδών σωματιδίων. Η εξάρτηση του ιξώδους για σ<100pa μοιάζει με εκείνη των Νευτώνειων ρευστών, καθώς εμφανίζουν πλατώ, απ όπου προσδιορίζεται η τιμή του ιξώδους μηδενικής διάτμησης, η ο. Για σ>100pa, παρατηρούνται φαινόμενα ρεολέπτυσης που υποδεικνύουν την διάσπαση του πηκτώματος. Το διάλυμα πολυμερούς συγκέντρωσης 16.7wt% παρουσιάζει σημαντική διαφοροποίηση σε σχέση με τις προηγούμενες συγκεντρώσεις καθώς εμφανίζει αρχικά αύξηση του ιξώδους (ρεοπάχυνση, shear thickening) την οποία διαδέχεται ισχυρή ρεολέπτυνση. Στον πίνακα 4.2 που ακολουθεί παρουσιάζονται οι τιμές του ιξώδους μηδενικής διάτμησης (zero shear viscosity) στις αντίστοιχες συγκεντρώσεις πολυμερούς, οι οποίες προκύπτουν από το σχήμα 4.10 για πολύ χαμηλές τιμές της διατμητικής τάσης. 92
103 viscosity (Pa.s) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 c=9.6wt% c=10.5wt% 10 6 c=11.4wt% c=12.2wt% 10 5 c=12.4wt% c=13.1wt% c=13.5wt% 10 4 c=14.2wt% c=14.5wt% c=15.2wt% 10 3 c=16.7wt% shear stress Σχήμα 4.10: Μεταβολή του ιξώδους του συμπολυμερούς PS 10 PEO 10 συναρτήσει της διάτμητικης τάσης για διάφορες συγκεντρώσεις σε θερμοκρασία 25 ο C. Πίνακας 4.2: Τιμές η ο για διάφορες συγκεντρώσεις του PS 10 PEO 10. c (wt%) η ο (Pa.s) Επειδή η περιοχή του πλατώ δεν μπορούσε επακριβώς να προσδιοριστεί, διεξήχθηκε πείραμα ερπυσμού για το διάλυμα συγκέντρωσης 18wt%. Τα αποτελέσματα του πειράματος ερπυσμού περιγράφονται από την καμπύλη ενδοτικότητας, J(t) (σχήμα 4.11). Η ενδοτικότητα (compliance) για μεγάλους 93
104 J (Pa -1 ) ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 t χρόνους δίνεται από την σχέση: J () t Jo. Από την παραπάνω σχέση υπολογίζεται το μηδενικό ιξώδες, η ο, σε μηδενικούς ρυθμούς διάτμησης το μέτρο ένδοσης J ο στην περιοχή του πλατώ, το οποίο αντιστοιχεί στο αντίστροφο του μέτρου αποθήκευσης στην περιοχή πλατώ ( Jo 1/ Go ) και ο χρόνος χαλάρωσης n / G. Το διάλυμα συγκέντρωσης 18wt%, παρουσιάζει ιξωδοελαστική R o o συμπεριφορά. 0,015 0,010 18wt% PS 10 PEO 10 Linear fitting stress=10 Pa o = 2.1*10 5 Pa.s G o = 226 Pa 0,005 0, Time (s) Σχήμα 4.11: Καμπύλη ενδοτικότητας ερπυσμού για το σύστημα PS 10 PEO 10 /[BMIM][PF 6 ] συγκέντρωσης 18wt% ΕΞΑΡΤΗΣΗ ΤΟΥ ΣΧΕΤΙΚΟΥ ΙΞΩΔΟΥΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ PS 10 PEO 10 /[BMIM][PF 6 ] ΑΠΟ ΤΗ ΣΥΓΚΕΝΤΡΩΣΗ Στο σχήμα 4.12 παραθέτουμε την καμπύλη εξάρτησης του σχετικού ιξώδους ( n / n ) του συμπολυμερούς από τη συγκέντρωση. Η μεταβολή του σχετικού rel o IL ιξώδους από την συγκέντρωση χαρακτηρίζεται από δύο διακριτές περιοχές. Σε συγκεντρώσεις c<c gel, όπου c gel (12.6wt%) είναι η χαρακτηριστική συγκέντρωση μετάβασης sol-gel, το σχετικό ιξώδες αυξάνεται έως και δύο τάξεις μεγέθους σε σχέση με το ιξώδες του ιοντικού υγρού ([BMIM][PF 6 ]: η=0.270 Pa.s), γεγονός που οφείλεται στην αύξηση του αριθμού των αστεροειδών σωματιδίων (εικόνα 4.1b). Σε c>c gel, το σχετικό ιξώδες αυξάνεται δραματικά έως και 5 τάξεις μεγέθους, ακολουθώντας τη σχέση nrel ~ 21 c. Στην περιοχή αυτή καταργούνται οι δυνάμεις 94
105 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 άπωσης μεταξύ των αλυσίδων PEO και τα σχηματιζόμενα σωματίδια αλληλοεμπλέκονται μεταξύ τους με αποτέλεσμα να αυξάνεται η δυσκολία κίνησής τους. Με περαιτέρω αύξηση της συγκέντρωσης, τα αστεροειδή σωματίδια λόγω της στένης επαφής πακτώνονται με αποτέλεσμα να παρατηρείται συμφόρηση (jamming) και τελικά το σύστημα να μην ρέει (εικόνα 4.1c) steady state creep n~c 21 n rel 10 3 SOL GEL 10 2 c gel =12.6% c*=3.6% concentration (wt%) 50 Σχήμα 4.12: Εξάρτηση του σχετικού ιξώδους συναρτήσει της συγκέντρωσης για πολύ χαμηλές τιμές της διατμητικής τάσης, για το σύστημα PS 10 PEO 10 /[BMIM][PF 6 ]. Τα σύμβολα με μαύρο χρώμα είναι από πειράματα steady state και με πράσινο χρώμα από creep. Στην εικόνα 4.2, παρουσιάζονται οι φωτογραφίες των διαλυμάτων του συμπολυμερούς σε ιοντικό υγρό. Για συγκεντρώσεις c<13.1wt%, παρατηρείται η τυπική συμπεριφορά ιξώδους υγρού (liquidlike behavior) και τα διαλύματα ρέουν. Αντίθετα σε υψηλότερες συγκεντρώσεις c>13.1wt%, τα διαλύματα συμπεριφέρονται ως gel (solidlike behavior) καθώς δεν ρέουν μετά την αναστροφή των δοκιμαστικών σωλήνων. 95
106 ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ ΚΕΦΑΛΑΙΟ 4 Εικόνα 4.1: Απεικόνιση δημιουργίας φυσικού πηκτώματος του PS 10 PEO 10 σε [BMIM][PF 6 ]. Εικόνα 4.2: Ψηφιακή απεικόνιση της μετάβασης sol-gel PS 10 PEO 10 [BMIM][PF 6 ]. σε 96
ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ. Ενότητα 8: ΠΟΛΥΜΕΡΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 8: ΠΟΛΥΜΕΡΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ ΗΛΕΚΤΡΟΛΟΓΙΚΑ ΥΛΙΚΑ Ενότητα 8: ΠΟΛΥΜΕΡΗ ΛΙΤΣΑΡΔΑΚΗΣ ΓΕΩΡΓΙΟΣ ΤΗΜΜΥ Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ
 ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΜΟΝΤΕΛΑ ΜΕΜΒΡΑΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ 1. Μονοστιβάδες 2. Διπλοστιβάδες 3. Λιποσώματα 1.1 ΜΟΝΟΣΤΙΒΑΔΕΣ Σχηματίζονται από μη-πολικά μόρια στη μεσόφαση αέρα/νερού Συσκευή
ΟΡΓΑΝΩΣΗ ΛΙΠΙΔΙΩΝ ΣΕ ΥΔΑΤΙΚΟ ΠΕΡΙΒΑΛΛΟΝ ΜΟΝΤΕΛΑ ΜΕΜΒΡΑΝΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ 1. Μονοστιβάδες 2. Διπλοστιβάδες 3. Λιποσώματα 1.1 ΜΟΝΟΣΤΙΒΑΔΕΣ Σχηματίζονται από μη-πολικά μόρια στη μεσόφαση αέρα/νερού Συσκευή
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 8 η : Υγρά, Στερεά & Αλλαγή Φάσεων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Πολικοί Ομοιοπολικοί Δεσμοί & Διπολικές Ροπές 2 Όπως έχει
ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ. Ενότητα : Εισαγωγικές έννοιες. Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής
 ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Εισαγωγικές έννοιες Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ https://www.youtube.com/watch?v=unsngvsvdk 2 Επιστήμη
ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Εισαγωγικές έννοιες Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ https://www.youtube.com/watch?v=unsngvsvdk 2 Επιστήμη
EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ρεολογία πολυμερών
 EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ρεολογία πολυμερών Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών 1 Σκοπός Η εξάσκηση των φοιτητών με την ρεολογία
EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ρεολογία πολυμερών Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών 1 Σκοπός Η εξάσκηση των φοιτητών με την ρεολογία
EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Διαφορική Ανιχνευτική Θερμιδομετρία (DSC)
 EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Διαφορική Ανιχνευτική Θερμιδομετρία (DSC) Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών 1 Σκοπός Η εξοικείωση
EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Διαφορική Ανιχνευτική Θερμιδομετρία (DSC) Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών 1 Σκοπός Η εξοικείωση
ΑΠΟΚΡΗΣΙΜΑ ΦΥΣΙΚΑ ΥΔΡΟΠΗΚΤΩΜΑΤΑ ΤΕΛΕΧΗΛΙΚΟΥ ΠΟΛΥΑΜΦΟΛΥΤΗ PMMA-b-P(DEA-CO-MAA)-b-PMMA
 ΑΠΟΚΡΗΣΙΜΑ ΦΥΣΙΚΑ ΥΔΡΟΠΗΚΤΩΜΑΤΑ ΤΕΛΕΧΗΛΙΚΟΥ ΠΟΛΥΑΜΦΟΛΥΤΗ PMMA-b-P(DEA-CO-MAA)-b-PMMA Ι. Μπεσίρη, 1 Γ. Γκοτζαμάνης, 1 Κ. Τσιτσιλιάνης 1, * 1 Τμήμα Χημικών Μηχανικών, Πανεπιστήμιο Πατρών, Τ.Κ. 26504, Ρίο,
ΑΠΟΚΡΗΣΙΜΑ ΦΥΣΙΚΑ ΥΔΡΟΠΗΚΤΩΜΑΤΑ ΤΕΛΕΧΗΛΙΚΟΥ ΠΟΛΥΑΜΦΟΛΥΤΗ PMMA-b-P(DEA-CO-MAA)-b-PMMA Ι. Μπεσίρη, 1 Γ. Γκοτζαμάνης, 1 Κ. Τσιτσιλιάνης 1, * 1 Τμήμα Χημικών Μηχανικών, Πανεπιστήμιο Πατρών, Τ.Κ. 26504, Ρίο,
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «ΧΗΜΕΙΑΣ» ΕΙΔΙΚΕΥΣΗ «ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ ΚΑΙ ΕΦΑΡΜΟΓΕΣ ΤΗΣ» ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ ΔΙΠΛΩΜΑΤΟΣ
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «ΧΗΜΕΙΑΣ» ΕΙΔΙΚΕΥΣΗ «ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ ΚΑΙ ΕΦΑΡΜΟΓΕΣ ΤΗΣ» ΕΡΕΥΝΗΤΙΚΗ ΕΡΓΑΣΙΑ ΔΙΠΛΩΜΑΤΟΣ
Κεφάλαιο 2 Χημικοί Δεσμοί
 Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Κεφάλαιο 2 Χημικοί Δεσμοί Σύνοψη Παρουσιάζονται οι χημικοί δεσμοί, ιοντικός, μοριακός, ατομικός, μεταλλικός. Οι ιδιότητες των υλικών τόσο οι φυσικές όσο και οι χημικές εξαρτώνται από το είδος ή τα είδη
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Βιολογικές Μεμβράνες και Μεταγωγή Σήματος
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογικές Μεμβράνες και Μεταγωγή Σήματος Πολυμορφισμός Διδάσκουσα: Καθ. Μαρία - Ελένη Ε. Λέκκα Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογικές Μεμβράνες και Μεταγωγή Σήματος Πολυμορφισμός Διδάσκουσα: Καθ. Μαρία - Ελένη Ε. Λέκκα Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε
τραχύτητα των σωματιδίων δεν είχε μέχρι τώρα μελετηθεί σε σημαντικό βαθμό στη βιβλιογραφία. Η παρούσα μελέτη περιλαμβάνει μετρήσεις μορφολογίας,
 Περίληψη Αντικείμενο της παρούσας διδακτορικής διατριβής, υπό τον τίτλο Διεπιφανειακές αλληλεπιδράσεις και μοριακή δυναμική σε οργανικά-ανόργανα νανοσύνθετα πολυμερικά υλικά, είναι η συστηματική μελέτη
Περίληψη Αντικείμενο της παρούσας διδακτορικής διατριβής, υπό τον τίτλο Διεπιφανειακές αλληλεπιδράσεις και μοριακή δυναμική σε οργανικά-ανόργανα νανοσύνθετα πολυμερικά υλικά, είναι η συστηματική μελέτη
ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ισορροπίες φάσεων, διαλυτότητα
 ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ισορροπίες φάσεων, διαλυτότητα Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών IΣΟΡΡΟΠΙΕΣ ΦΑΣΕΩΝ. ΔΙΑΛΥΤΟΤΗΤΑ Τα διαλύματα των μακρομορίων
ΕΠΙΣΤΗΜΗ ΠΟΛΥΜΕΡΩΝ Ενότητα : Ισορροπίες φάσεων, διαλυτότητα Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών IΣΟΡΡΟΠΙΕΣ ΦΑΣΕΩΝ. ΔΙΑΛΥΤΟΤΗΤΑ Τα διαλύματα των μακρομορίων
Σχήμα 1: Εφαρμογές υπερδιακλαδισμένων πολυμερών.
 Τίτλος διατριβής : «Θερμοδυναμική μελέτη διαλυμάτων υπερδιακλαδισμένων πολυμερών» Υποψήφιος Διδάκτορας : Δρίτσας Γεώργιος Περίληψη Διατριβής Τα μακρομόρια δενδριτικής μορφής όπως τα υπερδιακλαδισμένα πολυμερή
Τίτλος διατριβής : «Θερμοδυναμική μελέτη διαλυμάτων υπερδιακλαδισμένων πολυμερών» Υποψήφιος Διδάκτορας : Δρίτσας Γεώργιος Περίληψη Διατριβής Τα μακρομόρια δενδριτικής μορφής όπως τα υπερδιακλαδισμένα πολυμερή
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ
 ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
ΟΡΥΚΤΟΛΟΓΙΑ ΤΟΜΕΑΣ ΓΕΩΛΟΓΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ - ΜΕΤΑΛΛΟΥΡΓΩΝ ΜΑΘΗΜΑ 2. ΟΡΥΚΤΑ - ΠΕΤΡΩΜΑΤΑ Μαρία Περράκη, Επίκουρη Καθηγήτρια ΑΔΕΙΑ ΧΡΗΣΗΣ Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 4 η : Ιοντικοί Δεσμοί Χημεία Κύριων Ομάδων Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Δόμηση Ηλεκτρονίων στα Ιόντα 2 Για τα στοιχεία
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΦΑΡΜΑΚΕΥΤΙΚΗΣ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΟΧΗΜΕΙΑΣ Γραφείο 211 Επίκουρος Καθηγητής: Δ. Τσιπλακίδης Τηλ.: 2310 997766 e mail: dtsiplak@chem.auth.gr url:
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΟΧΗΜΕΙΑΣ Γραφείο 211 Επίκουρος Καθηγητής: Δ. Τσιπλακίδης Τηλ.: 2310 997766 e mail: dtsiplak@chem.auth.gr url:
Παράγοντες που εξηγούν τη διαλυτότητα. Είδη διαλυμάτων
 Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Παράγοντες που εξηγούν τη διαλυτότητα 1. Η φυσική τάση των ουσιών να αναμιγνύονται μεταξύ τους. 2. Οι σχετικές ελκτικές δυνάμεις μεταξύ των χημικών οντοτήτων του διαλύματος Είδη διαλυμάτων Στα διαλύματα
Osmotic effects of hard spheres on star polymer glasses Οσμωτικές επιδράσεις σκληρών σφαιρών σε υάλους ατεροειδών πολυμερών
 Osmotic effects of hard spheres on star polymer glasses Οσμωτικές επιδράσεις σκληρών σφαιρών σε υάλους ατεροειδών πολυμερών Τελική έκθεση προόδου Επιστημονικός Υπεύθυνος: Δ. Βλασσόπουλος Συνεργάτες: D.
Osmotic effects of hard spheres on star polymer glasses Οσμωτικές επιδράσεις σκληρών σφαιρών σε υάλους ατεροειδών πολυμερών Τελική έκθεση προόδου Επιστημονικός Υπεύθυνος: Δ. Βλασσόπουλος Συνεργάτες: D.
ΠΥΚΝΟΤΗΤΑ ΠΟΛΥΜΕΡΙΚΗΣ ΑΛΥΣΙΔΑΣ
 ΠΥΚΝΟΤΗΤΑ ΠΟΛΥΜΕΡΙΚΗΣ ΑΛΥΣΙΔΑΣ Ποιά είναι η πυκνότητα μίας πολυμερικής αλυσίδας με μοριακό βάρος Μ και Ν μονομέρη; (η συγκέντρωση δηλαδή των μονομερών μέσα στον όγκο που καταλαμβάνει η αλυσίδα). Μέγεθος
ΠΥΚΝΟΤΗΤΑ ΠΟΛΥΜΕΡΙΚΗΣ ΑΛΥΣΙΔΑΣ Ποιά είναι η πυκνότητα μίας πολυμερικής αλυσίδας με μοριακό βάρος Μ και Ν μονομέρη; (η συγκέντρωση δηλαδή των μονομερών μέσα στον όγκο που καταλαμβάνει η αλυσίδα). Μέγεθος
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ. Τ μαθητ : Σχολικό Έτος:
 Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής κατάστασης; 3 1.3
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής κατάστασης; 3 1.3
Autonomous movement of platinum-loaded stomatocytes
 Autonomous movement of platinum-loaded stomatocytes Daniela A. Wilson, Roeland J. M. Nolte and Jan C. M. van Hest, NATURE CHEMISTRY, advance paper ΓΙΩΡΓΟΣ ΦΡΑΓΚΙΑΔΑΚΗΣ 364 ΣΤΟΧΟΣ Στη φύση υπάρχει μια συνεχής
Autonomous movement of platinum-loaded stomatocytes Daniela A. Wilson, Roeland J. M. Nolte and Jan C. M. van Hest, NATURE CHEMISTRY, advance paper ΓΙΩΡΓΟΣ ΦΡΑΓΚΙΑΔΑΚΗΣ 364 ΣΤΟΧΟΣ Στη φύση υπάρχει μια συνεχής
Αντιδράσεις Πολυμερών
 Αντιδράσεις Πολυμερών Αντιδράσεις Μετατροπής Πολυμερών Αντιδράσεις που αφορούν την κυρία αλυσίδα Αντιδράσεις που αφορούν πλευρικές ομάδες R Αντιδράσεις τελικής ομάδας X R X Y Αντιδράσεις Κύριας Αλυσίδας
Αντιδράσεις Πολυμερών Αντιδράσεις Μετατροπής Πολυμερών Αντιδράσεις που αφορούν την κυρία αλυσίδα Αντιδράσεις που αφορούν πλευρικές ομάδες R Αντιδράσεις τελικής ομάδας X R X Y Αντιδράσεις Κύριας Αλυσίδας
Άσκηση 3η. Μέθοδοι Διαχωρισμού. Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας
 Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
7. ΧΗΜΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΠΟΛΥΜΕΡΩΝ
 7-1 7. ΧΗΜΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΠΟΛΥΜΕΡΩΝ 7.1. ΙΑΛΥΤΟΤΗΤΑ ΤΩΝ ΠΟΛΥΜΕΡΩΝ ιάφοροι διαλύτες µπορούν να επιφέρουν φυσικές αλλαγές όταν επιδρούν σε διάφορα πολυµερή. Αυτές οι αλλαγές είναι το αποτέλεσµα της αντίδρασης
7-1 7. ΧΗΜΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΠΟΛΥΜΕΡΩΝ 7.1. ΙΑΛΥΤΟΤΗΤΑ ΤΩΝ ΠΟΛΥΜΕΡΩΝ ιάφοροι διαλύτες µπορούν να επιφέρουν φυσικές αλλαγές όταν επιδρούν σε διάφορα πολυµερή. Αυτές οι αλλαγές είναι το αποτέλεσµα της αντίδρασης
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
Πείραμα 2 Αν αντίθετα, στο δοχείο εισαχθούν 20 mol ΗΙ στους 440 ºC, τότε το ΗΙ διασπάται σύμφωνα με τη χημική εξίσωση: 2ΗΙ(g) H 2 (g) + I 2 (g)
 Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Εργαστήριο Τεχνολογίας Υλικών
 Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 01 Κατηγοριοποιήση υλικών-επίδειξη δοκιμίων Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών
Εργαστήριο Τεχνολογίας Υλικών Εργαστηριακή Άσκηση 01 Κατηγοριοποιήση υλικών-επίδειξη δοκιμίων Διδάσκοντες: Δρ Γεώργιος Ι. Γιαννόπουλος Δρ Θεώνη Ασημακοπούλου Δρ ΘεόδωροςΛούτας Τμήμα Μηχανολογίας ΑΤΕΙ Πατρών
ΜΗΧΑΝΙΚΗ ΤΩΝ ΥΛΙΚΩΝ 2016
 ΜΗΧΑΝΙΚΗ ΤΩΝ ΥΛΙΚΩΝ 2016 Κεραμικών και Πολυμερικών Υλικών Κώστας Γαλιώτης, καθηγητής Τμήμα Χημικών Μηχανικών galiotis@chemeng.upatras.gr 1 Εισαγωγή Όπως ήδη είδαμε, η μηχανική συμπεριφορά των υλικών αντανακλά
ΜΗΧΑΝΙΚΗ ΤΩΝ ΥΛΙΚΩΝ 2016 Κεραμικών και Πολυμερικών Υλικών Κώστας Γαλιώτης, καθηγητής Τμήμα Χημικών Μηχανικών galiotis@chemeng.upatras.gr 1 Εισαγωγή Όπως ήδη είδαμε, η μηχανική συμπεριφορά των υλικών αντανακλά
ΑΡΙΣΤΕΙΑ Ι. ΕΡΓΟ: Λειτουργικές Αυτo-οργανούμενες Νανοδομές από Συμπολυμερή κατά Συστάδες και Πρωτεΐνες (NANOMACRO) 1129 ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ ΕΕ2
 ΑΡΙΣΤΕΙΑ Ι ΕΡΓΟ: Λειτουργικές Αυτo-οργανούμενες Νανοδομές από Συμπολυμερή κατά Συστάδες και Πρωτεΐνες (NANOMACRO) 1129 ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ ΕΕ2 ΠΑΡΑΔΟΤΕΟ 2.1:Έκθεση αποτελεσμάτων σύνθεσης και χαρακτηρισμού
ΑΡΙΣΤΕΙΑ Ι ΕΡΓΟ: Λειτουργικές Αυτo-οργανούμενες Νανοδομές από Συμπολυμερή κατά Συστάδες και Πρωτεΐνες (NANOMACRO) 1129 ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ ΕΕ2 ΠΑΡΑΔΟΤΕΟ 2.1:Έκθεση αποτελεσμάτων σύνθεσης και χαρακτηρισμού
ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΗΝ ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΩΝ ΠΟΛΥΜΕΡΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ
 ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΗΝ ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΩΝ ΠΟΛΥΜΕΡΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Υπό του ΓΚΟΤΖΑΜΑΝΗ ΓΕΩΡΓΙΟΥ του ΘΕΜΙΣΤΟΚΛΗ Για την Απόκτηση του Tίτλου του
ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΗΝ ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΩΝ ΠΟΛΥΜΕΡΩΝ ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Υπό του ΓΚΟΤΖΑΜΑΝΗ ΓΕΩΡΓΙΟΥ του ΘΕΜΙΣΤΟΚΛΗ Για την Απόκτηση του Tίτλου του
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ ΙΟΝΤΙΚΟΣ Ή ΕΤΕΡΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ
 ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
ΙΟΝΤΙΚΟΣ ΚΑΙ ΟΜΟΙΟΠΟΛΙΚΟΣ ΔΕΣΜΟΣ Το είδος του χημικού δεσμού που θα προκύψει κατά την ένωση δύο ατόμων εξαρτάται από την σχετική ένταση των ελκτικών δυνάμεων που ασκούν οι πυρήνες των δύο ατόμων στα ηλεκτρόνια
κρυστάλλου απείρου μεγέθους.
 Κρυστάλλωση Πολυμερών Θερμοδυναμική της κρυστάλλωσης πολυμερών Θερμοκρασία ρασία τήξης πολυμερών Μεταβολή ειδικού όγκου ως προς τη θερμοκρασία σε γραμμικό πολυαιθυλένιο:., ακλασματοποίητο πολυμερές, ο,
Κρυστάλλωση Πολυμερών Θερμοδυναμική της κρυστάλλωσης πολυμερών Θερμοκρασία ρασία τήξης πολυμερών Μεταβολή ειδικού όγκου ως προς τη θερμοκρασία σε γραμμικό πολυαιθυλένιο:., ακλασματοποίητο πολυμερές, ο,
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ. Τ μαθητ : Σχολικό Έτος: vyridis.weebly.com
 Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: vyridis.weebly.com 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής
Χημεία Β Γυμνασίου ΦΥΛΛΑΔΙΟ ΑΣΚΗΣΕΩΝ Τ μαθητ : Σχολικό Έτος: vyridis.weebly.com 1 1.2 Καταστάσεις των υλικών 1. Συμπληρώστε το παρακάτω σχεδιάγραμμα 2. Πώς ονομάζονται οι παρακάτω μετατροπές της φυσικής
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 9 η : Διαλύματα & οι ιδιότητές τους Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Διαλύματα 2 Τα ομοιογενή μίγματα μπορούν να ταξινομηθούν
Ανόργανη Χημεία. Τμήμα Τεχνολογίας Τροφίμων. Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 12 η : Υδατική ισορροπία Οξέα & βάσεις Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση: Η Θεωρία Brønsted - Lowry 2 Σύμφωνα
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις
 Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
Μεταλλικός δεσμός - Κρυσταλλικές δομές Ασκήσεις Ποια από τις ακόλουθες προτάσεις ισχύει για τους μεταλλικούς δεσμούς; α) Οι μεταλλικοί δεσμοί σχηματίζονται αποκλειστικά μεταξύ ατόμων του ίδιου είδους μετάλλου.
ΤΕΛΙΚΗ ΕΚΘΕΣΗ ΤΟΥ ΕΡΓΟΥ: «Μέτρηση Ηλεκτρικών Χαρακτηριστικών Πολυουρεθανικών και Εποδειδικών Ρητινών»
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΤΩΝ ΥΛΙΚΩΝ ΤΕΛΙΚΗ ΕΚΘΕΣΗ ΤΟΥ ΕΡΓΟΥ: «Μέτρηση Ηλεκτρικών Χαρακτηριστικών Πολυουρεθανικών και Εποδειδικών Ρητινών» Στα πλαίσια της σύμβασης ανάθεσης
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΤΩΝ ΥΛΙΚΩΝ ΤΕΛΙΚΗ ΕΚΘΕΣΗ ΤΟΥ ΕΡΓΟΥ: «Μέτρηση Ηλεκτρικών Χαρακτηριστικών Πολυουρεθανικών και Εποδειδικών Ρητινών» Στα πλαίσια της σύμβασης ανάθεσης
Συντάκτης: Τζαμτζής Αθανάσιος Σελίδα 1
 ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
ΒΑΘΜΟΛΟΓΙΑ ΟΜΑΔΑΣ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ 4 η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ Παρασκευή διαλύματος ορισμένης συγκέντρωσης Αραίωση διαλυμάτων ΣΧΟΛΕΙΟ 1 ο ΓΕΛ ΑΜΠΕΛΟΚΗΠΩΝ ΤΜΗΜΑ ΗΜΕΡΟΜΗΝΙΑ ΟΜΑΔΑ ΜΑΘΗΤΩΝ 1 2
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις
 Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση 4: Μερικός γραμμομοριακός όγκος Αθανάσιος Τσεκούρας Τμήμα Χημείας . Θεωρία... 3. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 5 4. Τελικά αποτελέσματα... 7 Σελίδα
Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση 4: Μερικός γραμμομοριακός όγκος Αθανάσιος Τσεκούρας Τμήμα Χημείας . Θεωρία... 3. Μετρήσεις... 4 3. Επεξεργασία Μετρήσεων... 5 4. Τελικά αποτελέσματα... 7 Σελίδα
Πολυμερισμός Προσθήκης
 Είδη Πολυμερισμού 1 Πολυμερισμός Προσθήκης Ελευθέρων Ριζών: Ενεργό Κέντρο ελεύθερη Ρίζα. Ανιοντικός Ενεργό Κέντρο Ανιόν - X + Κατιοντικός Ενεργό κέντρο κατιόν + Y - 2 Ιοντικοί Πολυμερισμοί Ανιοντικός Πολυμερισμός
Είδη Πολυμερισμού 1 Πολυμερισμός Προσθήκης Ελευθέρων Ριζών: Ενεργό Κέντρο ελεύθερη Ρίζα. Ανιοντικός Ενεργό Κέντρο Ανιόν - X + Κατιοντικός Ενεργό κέντρο κατιόν + Y - 2 Ιοντικοί Πολυμερισμοί Ανιοντικός Πολυμερισμός
Άσκηση 3η. Μέθοδοι Διαχωρισμού. Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας
 Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
Άσκηση 3η Μέθοδοι Διαχωρισμού 1 2 Θεωρητικό μέρος Χρήση των μεταβολών των φάσεων στην ανάλυση Οι ουσίες λειώνουν και βράζουν σε ορισμένες θερμοκρασίες, αλλάζοντας έτσι μορφή από στερεή σε υγρή ή από υγρή
3.2 ΧΗΜΙΚΑ ΑΠΟΤΕΛΕΣΜΑΤΑ ΤΟΥ ΗΛΕΚΤΡΙΚΟΥ ΡΕΥΜΑΤΟΣ
 Βρέντζου Τίνα Φυσικός Μεταπτυχιακός τίτλος: «Σπουδές στην εκπαίδευση» ΜEd Email : stvrentzou@gmail.com 3.2 ΧΗΜΙΚΑ ΑΠΟΤΕΛΕΣΜΑΤΑ ΤΟΥ ΗΛΕΚΤΡΙΚΟΥ ΡΕΥΜΑΤΟΣ 1 Λέξεις κλειδιά: Ηλεκτρολυτικά διαλύματα, ηλεκτρόλυση,
Βρέντζου Τίνα Φυσικός Μεταπτυχιακός τίτλος: «Σπουδές στην εκπαίδευση» ΜEd Email : stvrentzou@gmail.com 3.2 ΧΗΜΙΚΑ ΑΠΟΤΕΛΕΣΜΑΤΑ ΤΟΥ ΗΛΕΚΤΡΙΚΟΥ ΡΕΥΜΑΤΟΣ 1 Λέξεις κλειδιά: Ηλεκτρολυτικά διαλύματα, ηλεκτρόλυση,
ΦΑΣΜΑΤΑ ΕΚΠΟΜΠΗΣ ΑΠΟΡΡΟΦΗΣΗΣ
 ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
ΚΒΑΝΤΙΚΗ ΦΥΣΙΚΗ: Τα άτομα έχουν διακριτές ενεργειακές στάθμες Τα άτομα και μόρια, βρίσκονται σε διακριτές ενεργειακές στάθμες και Υφίστανται μεταβάσεις μεταξύ αυτών των ενεργειακών σταθμών όταν αλληλεπιδρούν
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος
 2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
2η Εργαστηριακή Άσκηση Εξάρτηση της ηλεκτρικής αντίστασης από τη θερμοκρασία Θεωρητικό μέρος Όπως είναι γνωστό από την καθημερινή εμπειρία τα περισσότερα σώματα που χρησιμοποιούνται στις ηλεκτρικές ηλεκτρονικές
Η πυκνότητα του νερού σε θερμοκρασία 4 C και ατμοσφαιρική πίεση (1 atm) είναι ίση με 1g/mL.
 Πυκνότητα Πυκνότητα ορίζεται το φυσικό μέγεθος που δίνεται από το πηλίκο της μάζας του σώματος προς τον αντίστοιχο όγκο που καταλαμβάνει σε σταθερές συνθήκες πίεσης (όταν πρόκειται για αέριο). Ο Συμβολισμός,
Πυκνότητα Πυκνότητα ορίζεται το φυσικό μέγεθος που δίνεται από το πηλίκο της μάζας του σώματος προς τον αντίστοιχο όγκο που καταλαμβάνει σε σταθερές συνθήκες πίεσης (όταν πρόκειται για αέριο). Ο Συμβολισμός,
ΔΟΜΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΕΡΑΜΙΚΩΝ. Χ. Κορδούλης
 ΔΟΜΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΕΡΑΜΙΚΩΝ Χ. Κορδούλης ΚΕΡΑΜΙΚΑ ΥΛΙΚΑ Τα κεραμικά υλικά είναι ανόργανα µη μεταλλικά υλικά (ενώσεις μεταλλικών και μη μεταλλικών στοιχείων), τα οποία έχουν υποστεί θερμική κατεργασία
ΔΟΜΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΚΕΡΑΜΙΚΩΝ Χ. Κορδούλης ΚΕΡΑΜΙΚΑ ΥΛΙΚΑ Τα κεραμικά υλικά είναι ανόργανα µη μεταλλικά υλικά (ενώσεις μεταλλικών και μη μεταλλικών στοιχείων), τα οποία έχουν υποστεί θερμική κατεργασία
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ. Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών. Να εξηγούν το σχηματισμό του ιοντικού ομοιοπολικού δεσμού.
 ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
ΧΗΜΙΚΟΙ ΔΕΣΜΟΙ ΣΤΟΧΟΙ ΜΑΘΗΜΑΤΟΣ Στο τέλος αυτής της διδακτικής ενότητας οι μαθητές θα πρέπει να μπορούν: Να δίδουν τον ορισμό του χημικού δεσμού. Να γνωρίζουν τα είδη των δεσμών Να εξηγούν το σχηματισμό
Οι ουσίες μικρού μοριακού βάρους μπορούν να βρεθούν στη συμπυκνωμένη φάση σε δύο πιθανές καταστάσεις: α) τη στερεά, όπου παρατηρείται οργάνωση σε
 Άμορφα Πολυμερή Θερμοκρασία Υαλώδους Μετάπτωσης Κινητικότητα πολυμερικών αλυσίδων Οι ουσίες μικρού μοριακού βάρους μπορούν να βρεθούν στη συμπυκνωμένη φάση σε δύο πιθανές καταστάσεις: α) τη στερεά, όπου
Άμορφα Πολυμερή Θερμοκρασία Υαλώδους Μετάπτωσης Κινητικότητα πολυμερικών αλυσίδων Οι ουσίες μικρού μοριακού βάρους μπορούν να βρεθούν στη συμπυκνωμένη φάση σε δύο πιθανές καταστάσεις: α) τη στερεά, όπου
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ
 ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ ph (πε-χα) Έχει διαπιστωθεί ότι το εντελώς καθαρό νερό παρουσιάζει μια πολύ μικρή αγωγιμότητα (δηλ. παρουσία διαλυμένων ιόντων), η οποία αποδείχτηκε ότι οφείλεται στον ιοντισμό
ΓΕΩΡΓΙΚΗ ΧΗΜΕΙΑ ΕΡΓΑΣΤΗΡΙΟ ph (πε-χα) Έχει διαπιστωθεί ότι το εντελώς καθαρό νερό παρουσιάζει μια πολύ μικρή αγωγιμότητα (δηλ. παρουσία διαλυμένων ιόντων), η οποία αποδείχτηκε ότι οφείλεται στον ιοντισμό
ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ
 ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ Α. ΙΣΟΡΡΟΠΙΑ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΥΔΑΤΙΚO ΔΙΑΛΥΜΑ Λίγα λόγια πριν από το πείραμα. Η σόδα περιέχει διαλυμένο αέριο διοξείδιο του άνθρακα το οποίο προστίθεται κατά την
ΙΣΟΡΡΟΠΙΕΣ ΜΕ ΑΝΘΡΑΚΙΚΑ ΙΟΝΤΑ Α. ΙΣΟΡΡΟΠΙΑ ΔΙΟΞΕΙΔΙΟΥ ΤΟΥ ΑΝΘΡΑΚΑ ΣΕ ΥΔΑΤΙΚO ΔΙΑΛΥΜΑ Λίγα λόγια πριν από το πείραμα. Η σόδα περιέχει διαλυμένο αέριο διοξείδιο του άνθρακα το οποίο προστίθεται κατά την
Αυτοοργάνωση Πολυμερών: Πολυηλεκτρολύτες και Σύμπλοκά τους με Πρωτεΐνες
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Αυτοοργάνωση Πολυμερών: Πολυηλεκτρολύτες και Σύμπλοκά τους με Πρωτεΐνες ΜΑΡΙΑ ΚΑΡΑΓΙΑΝΝΗ ΦΥΣΙΚΟΣ
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Αυτοοργάνωση Πολυμερών: Πολυηλεκτρολύτες και Σύμπλοκά τους με Πρωτεΐνες ΜΑΡΙΑ ΚΑΡΑΓΙΑΝΝΗ ΦΥΣΙΚΟΣ
ΔΙΔΑΚΤΕΑ ΥΛΗ ΧΗΜΕΙΑΣ Β ΓΥΜΝΑΣΙΟΥ 2015-16
 ΔΙΔΑΚΤΕΑ ΥΛΗ ΧΗΜΕΙΑΣ Β ΓΥΜΝΑΣΙΟΥ 205-6 ΔΕΙΚΤΕΣ ΕΠΙΤΥΧΙΑΣ Οι μαθητές και οι μαθήτριες θα πρέπει να είναι σε θέση: ΔΕΙΚΤΕΣ ΕΠΑΡΚΕΙΑΣ Διδ. περ. Σύνολο διδ.περ.. Η συμβολή της Χημείας στην εξέλιξη του πολιτισμού
ΔΙΔΑΚΤΕΑ ΥΛΗ ΧΗΜΕΙΑΣ Β ΓΥΜΝΑΣΙΟΥ 205-6 ΔΕΙΚΤΕΣ ΕΠΙΤΥΧΙΑΣ Οι μαθητές και οι μαθήτριες θα πρέπει να είναι σε θέση: ΔΕΙΚΤΕΣ ΕΠΑΡΚΕΙΑΣ Διδ. περ. Σύνολο διδ.περ.. Η συμβολή της Χημείας στην εξέλιξη του πολιτισμού
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις. Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι
 Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
ΓΥΜΝΑΣΙΟ ΑΓΛΑΝΤΖΙΑΣ Σχολική Χρονιά ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΤΑΞΗ Β. Ονοματεπώνυμο μαθητή/τριας:...
 ΓΥΜΝΑΣΙΟ ΑΓΛΑΝΤΖΙΑΣ Σχολική Χρονιά 2014-2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΤΑΞΗ Β Ονοματεπώνυμο μαθητή/τριας:... Τμήμα:... :... Βαθμός/Ολογράφως:... Χρόνος: 2 ώρες Φυσική
ΓΥΜΝΑΣΙΟ ΑΓΛΑΝΤΖΙΑΣ Σχολική Χρονιά 2014-2015 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ: ΧΗΜΕΙΑ - ΤΑΞΗ Β Ονοματεπώνυμο μαθητή/τριας:... Τμήμα:... :... Βαθμός/Ολογράφως:... Χρόνος: 2 ώρες Φυσική
ΠΕΙΡΑΜΑ FRANK-HERTZ ΜΕΤΡΗΣΗ ΤΗΣ ΕΝΕΡΓΕΙΑΣ ΔΙΕΓΕΡΣΗΣ ΕΝΟΣ ΑΤΟΜΟΥ
 ΠΕΙΡΑΜΑ FRANK-HERTZ ΜΕΤΡΗΣΗ ΤΗΣ ΕΝΕΡΓΕΙΑΣ ΔΙΕΓΕΡΣΗΣ ΕΝΟΣ ΑΤΟΜΟΥ Η απορρόφηση ενέργειας από τα άτομα γίνεται ασυνεχώς και σε καθορισμένες ποσότητες. Λαμβάνοντας ένα άτομο ορισμένα ποσά ενέργειας κάποιο
ΠΕΙΡΑΜΑ FRANK-HERTZ ΜΕΤΡΗΣΗ ΤΗΣ ΕΝΕΡΓΕΙΑΣ ΔΙΕΓΕΡΣΗΣ ΕΝΟΣ ΑΤΟΜΟΥ Η απορρόφηση ενέργειας από τα άτομα γίνεται ασυνεχώς και σε καθορισμένες ποσότητες. Λαμβάνοντας ένα άτομο ορισμένα ποσά ενέργειας κάποιο
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων
 Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
Φυσικοχημεία II, Διαλύματα Απλά διαγράμματα τάσης ατμών-σύστασηςιδανικών διαλυματων o P = N P P = A A A N P o B B B PA + PB = P ολ Τ=const P = Ν ολ P + N P o o A A B B Ν Α + Ν =1 o o o P = P + A N ( ολ
EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Χρωματογραφία πηκτώματος(gpc)
 EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Χρωματογραφία πηκτώματος(gpc) Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών 1 Σκοπός Η εξοικείωση των φοιτητών
EΡΓΑΣΤΗΡΙΟ ΠΟΛΥΜΕΡΩΝ Ενότητα : Χρωματογραφία πηκτώματος(gpc) Διδάσκων : Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών 1 Σκοπός Η εξοικείωση των φοιτητών
ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΠΑΤΡΩΝ ΤΜΗΜΑ ΜΗΧΑΝΟΛΟΓΩΝ ΚΑΙ ΑΕΡΟΝΑΥΠΗΓΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓΑΣΤΗΡΙΟ ΜΗΧΑΝΙΚΗΣ ΤΩΝ ΡΕΥΣΤΩΝ ΚΑΙ ΕΦΑΡΜΟΓΩΝ ΑΥΤΗΣ
 ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΠΑΤΡΩΝ ΤΜΗΜΑ ΜΗΧΑΝΟΛΟΓΩΝ ΚΑΙ ΑΕΡΟΝΑΥΠΗΓΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓΑΣΤΗΡΙΟ ΜΗΧΑΝΙΚΗΣ ΤΩΝ ΡΕΥΣΤΩΝ ΚΑΙ ΕΦΑΡΜΟΓΩΝ ΑΥΤΗΣ Διευθυντής: Διονύσιος-Ελευθ. Π. Μάργαρης, Αναπλ. Καθηγητής ΕΡΓΑΣΤΗΡΙΑΚΗ
ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΠΑΤΡΩΝ ΤΜΗΜΑ ΜΗΧΑΝΟΛΟΓΩΝ ΚΑΙ ΑΕΡΟΝΑΥΠΗΓΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓΑΣΤΗΡΙΟ ΜΗΧΑΝΙΚΗΣ ΤΩΝ ΡΕΥΣΤΩΝ ΚΑΙ ΕΦΑΡΜΟΓΩΝ ΑΥΤΗΣ Διευθυντής: Διονύσιος-Ελευθ. Π. Μάργαρης, Αναπλ. Καθηγητής ΕΡΓΑΣΤΗΡΙΑΚΗ
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ
 ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
ΤΕΣΤ 30 ΕΡΩΤΗΣΕΩΝ ΓΝΩΣΤΙΚΟΥ ΧΗΜΕΙΑΣ ο αριθμός Avogadro, N A, L = 6,022 10 23 mol -1 η σταθερά Faraday, F = 96 487 C mol -1 σταθερά αερίων R = 8,314 510 (70) J K -1 mol -1 = 0,082 L atm mol -1 K -1 μοριακός
ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Ενότητα : Σύνθεση Ακετανιλιδίου
 ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Ενότητα : Σύνθεση Ακετανιλιδίου Διδάσκοντες: Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Μαρία Τσάμη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοπός Η
ΕΡΓΑΣΤΗΡΙΟ ΟΡΓΑΝΙΚΗΣ ΧΗΜΕΙΑΣ Ενότητα : Σύνθεση Ακετανιλιδίου Διδάσκοντες: Κων/νος Τσιτσιλιάνης, Καθηγητής Ουρανία Κούλη, Ε.ΔΙ.Π. Μαρία Τσάμη, Ε.ΔΙ.Π. Πολυτεχνική Σχολή Τμήμα Χημικών Μηχανικών Σκοπός Η
Ιοντική ισορροπία Προσδιορισμός του ph υδατικών διαλυμάτων οξέων βάσεων και αλάτων
 Άσκηση 8η Ιοντική ισορροπία Προσδιορισμός του ph υδατικών διαλυμάτων οξέων βάσεων και αλάτων Πανεπιστήμιο Πατρών - Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας - Ακαδ. έτος 2016-17 Διάσταση 2 ετεροπολικών
Άσκηση 8η Ιοντική ισορροπία Προσδιορισμός του ph υδατικών διαλυμάτων οξέων βάσεων και αλάτων Πανεπιστήμιο Πατρών - Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας - Ακαδ. έτος 2016-17 Διάσταση 2 ετεροπολικών
διατήρησης της μάζας.
 6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
6. Ατομική φύση της ύλης Ο πρώτος που ισχυρίστηκε ότι η ύλη αποτελείται από δομικά στοιχεία ήταν ο αρχαίος Έλληνας φιλόσοφος Δημόκριτος. Το πείραμα μετά από 2400 χρόνια ήρθε και επιβεβαίωσε την άποψη αυτή,
Μάθημα 23 ο. Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις
 Μάθημα 23 ο Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις Μεταλλικός Δεσμός Μοντέλο θάλασσας ηλεκτρονίων Πυρήνες σε θάλασσα e -. Μεταλλική λάμψη. Ολκιμότητα. Εφαρμογή δύναμης Γενική και
Μάθημα 23 ο Μεταλλικός Δεσμός Θεωρία Ζωνών- Ημιαγωγοί Διαμοριακές Δυνάμεις Μεταλλικός Δεσμός Μοντέλο θάλασσας ηλεκτρονίων Πυρήνες σε θάλασσα e -. Μεταλλική λάμψη. Ολκιμότητα. Εφαρμογή δύναμης Γενική και
Τελική γραπτή εξέταση «Επιστήμη και Τεχνολογία Υλικών ΙΙ»-Ιούνιος 2016
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Δοκίμιο από PMMA (Poly Methyl MethAcrylate)
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ ΘΕΜΑ 1 ο (25 Μονάδες) (Καθ. Β.Ζασπάλης) Δοκίμιο από PMMA (Poly Methyl MethAcrylate)
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΑΜΥΛΟ ΚΑΙ ΑΡΤΟΣΚΕΥΑΣΜΑΤΑ
 ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΑΜΥΛΟ ΚΑΙ ΑΡΤΟΣΚΕΥΑΣΜΑΤΑ Βιοσύνθεση και χημική δομή Είναι ένας από τους σπουδαιότερους φυσικούς υδατάνθρακες. Δομείται στα πλαστίδια των φυτικών κυττάρων που ονομάζονται
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΑΜΥΛΟ ΚΑΙ ΑΡΤΟΣΚΕΥΑΣΜΑΤΑ Βιοσύνθεση και χημική δομή Είναι ένας από τους σπουδαιότερους φυσικούς υδατάνθρακες. Δομείται στα πλαστίδια των φυτικών κυττάρων που ονομάζονται
[ ] [ ] CH3COO [ ] CH COOH. Cοξ. Cαλ
![[ ] [ ] CH3COO [ ] CH COOH. Cοξ. Cαλ [ ] [ ] CH3COO [ ] CH COOH. Cοξ. Cαλ](/thumbs/60/45209718.jpg) Πριν από κάθε απάντηση, προηγείται η καλή ανάγνωση και η προσπάθεια κατανόησης της ερώτησης. Η κάθε απάντηση πρέπει να σχετίζεται µε την ακριβή διατύπωση της ερώτησης και όχι µε την γενική της ιδέα. Κάθε
Πριν από κάθε απάντηση, προηγείται η καλή ανάγνωση και η προσπάθεια κατανόησης της ερώτησης. Η κάθε απάντηση πρέπει να σχετίζεται µε την ακριβή διατύπωση της ερώτησης και όχι µε την γενική της ιδέα. Κάθε
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ
 ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (3) ΣΧΗΜΑΤΙΣΜΟΣ ΙΖΗΜΑΤΩΝ. ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (3) ΣΧΗΜΑΤΙΣΜΟΣ ΙΖΗΜΑΤΩΝ ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΠΟΙΗΣΗ ΙΖΗΜΑΤΟΣ (1) I.P = [M α+ ] m [X β- ] x < K sp (M m X x ) 1. Σχηµατισµός
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (3) ΣΧΗΜΑΤΙΣΜΟΣ ΙΖΗΜΑΤΩΝ ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΠΟΙΗΣΗ ΙΖΗΜΑΤΟΣ (1) I.P = [M α+ ] m [X β- ] x < K sp (M m X x ) 1. Σχηµατισµός
Ανάλυση Τροφίμων. Ενότητα 10: Εφαρμογές υδατική ισορροπίας Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 10: Εφαρμογές υδατική ισορροπίας Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Αντιδράσεις Εξουδετέρωσης
Ανάλυση Τροφίμων Ενότητα 10: Εφαρμογές υδατική ισορροπίας Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Αντιδράσεις Εξουδετέρωσης
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 10 η : Χημική κινητική. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
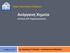 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 10 η : Χημική κινητική Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ταχύτητες Αντίδρασης 2 Ως ταχύτητα αντίδρασης ορίζεται είτε η αύξηση
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 10 η : Χημική κινητική Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Ταχύτητες Αντίδρασης 2 Ως ταχύτητα αντίδρασης ορίζεται είτε η αύξηση
Εθνικόν και Καποδιστριακόν Πανεπιστήμιον Αθηνών ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Τομέας Φαρμακευτικής Χημείας. Ιωάννης Ντότσικας. Επικ.
 Εθνικόν και Καποδιστριακόν Πανεπιστήμιον Αθηνών ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Τομέας Φαρμακευτικής Χημείας Ιωάννης Ντότσικας Επικ. Καθηγητής 1 Οι κυκλοδεξτρίνες (Cyclodextrins, CDs) είναι κυκλικοί ολιγοσακχαρίτες
Εθνικόν και Καποδιστριακόν Πανεπιστήμιον Αθηνών ΤΜΗΜΑ ΦΑΡΜΑΚΕΥΤΙΚΗΣ Τομέας Φαρμακευτικής Χημείας Ιωάννης Ντότσικας Επικ. Καθηγητής 1 Οι κυκλοδεξτρίνες (Cyclodextrins, CDs) είναι κυκλικοί ολιγοσακχαρίτες
Αιωρήματα & Γαλακτώματα
 Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2014-15 Μάθημα 2ο 25 February 2015 Αιωρήματα Γαλακτώματα 1 Παρασκευή αιωρημάτων Οι μέθοδοι παρασκευής αιωρημάτων κατατάσσονται σε δύο μεγάλες κατηγορίες
Αιωρήματα & Γαλακτώματα Εαρινό εξάμηνο Ακ. Έτους 2014-15 Μάθημα 2ο 25 February 2015 Αιωρήματα Γαλακτώματα 1 Παρασκευή αιωρημάτων Οι μέθοδοι παρασκευής αιωρημάτων κατατάσσονται σε δύο μεγάλες κατηγορίες
ΓΥΜΝΑΣΙΟ ΑΓΙΑΣ ΦΥΛΑΞΕΩΣ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2012-2013 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ ΣΤΗ ΧΗΜΕΙΑ ΤΑΞΗ :Β ΗΜΕΡΟΜΗΝΙΑ : 07/06/13 ΒΑΘΜΟΣ:...
 ΓΥΜΝΑΣΙΟ ΑΓΙΑΣ ΦΥΛΑΞΕΩΣ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2012-2013 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ ΣΤΗ ΧΗΜΕΙΑ ΤΑΞΗ :Β ΗΜΕΡΟΜΗΝΙΑ : 07/06/13 ΒΑΘΜΟΣ:... ΟΝΟΜΑΤΕΠΩΝΥΜΟ :...ΤΜΗΜΑ :...Αρ:... Βαθμολογία εξεταστικού δοκιμίου
ΓΥΜΝΑΣΙΟ ΑΓΙΑΣ ΦΥΛΑΞΕΩΣ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ: 2012-2013 ΓΡΑΠΤΕΣ ΠΡΟΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ ΣΤΗ ΧΗΜΕΙΑ ΤΑΞΗ :Β ΗΜΕΡΟΜΗΝΙΑ : 07/06/13 ΒΑΘΜΟΣ:... ΟΝΟΜΑΤΕΠΩΝΥΜΟ :...ΤΜΗΜΑ :...Αρ:... Βαθμολογία εξεταστικού δοκιμίου
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Γραπτό τεστ (συν-)αξιολόγησης στο μάθημα: «ΔΙΑΓΝΩΣΤΙΚΕΣ ΜΕΘΟΔΟΙ ΣΤΗ ΜΕΛΕΤΗ
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ-ΤΟΜΕΑΣ ΤΕΧΝΟΛΟΓΙΩΝ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Γραπτό τεστ (συν-)αξιολόγησης στο μάθημα: «ΔΙΑΓΝΩΣΤΙΚΕΣ ΜΕΘΟΔΟΙ ΣΤΗ ΜΕΛΕΤΗ
Μοριακός Χαρακτηρισμός Πολυμερών
 Μοριακός Χαρακτηρισμός Πολυμερών Μοριακό Βάρος Πολυμερών Υψηλά όχι ακριβή ΜΒ λόγω τυχαιότητας πολυμερισμού Μίγμα αλυσίδων με διαφορετικό μήκος Μέσο ΜΒ ή κατανομή ΜΒ Βαθμός Πολυμερισμού (DP) = MB πολυμερούς
Μοριακός Χαρακτηρισμός Πολυμερών Μοριακό Βάρος Πολυμερών Υψηλά όχι ακριβή ΜΒ λόγω τυχαιότητας πολυμερισμού Μίγμα αλυσίδων με διαφορετικό μήκος Μέσο ΜΒ ή κατανομή ΜΒ Βαθμός Πολυμερισμού (DP) = MB πολυμερούς
ΑΝΑΠΤΥΞΗ ΚΑΙ ΕΦΑΡΜΟΓΗ ΚΙΝΗΤΙΚΩΝ ΜΕΘΟΔΩΝ ΕΚΤΙΜΗΣΗΣ ΤΗΣ ΠΟΙΟΤΗΤΑΣ ΤΩΝ ΤΡΟΦΙΜΩΝ
 ΠΕΡΙΛΗΨΕΙΣ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ της Χαρίκλειας Βαϊκούση, Γεωπόνου με τίτλο: ΑΝΑΠΤΥΞΗ ΚΑΙ ΕΦΑΡΜΟΓΗ ΚΙΝΗΤΙΚΩΝ ΜΕΘΟΔΩΝ ΕΚΤΙΜΗΣΗΣ ΤΗΣ ΠΟΙΟΤΗΤΑΣ ΤΩΝ ΤΡΟΦΙΜΩΝ ΣΥΝΤΟΜΗ ΠΕΡΙΛΗΨΗ Αντικείμενο της μελέτης αποτέλεσε
ΠΕΡΙΛΗΨΕΙΣ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ της Χαρίκλειας Βαϊκούση, Γεωπόνου με τίτλο: ΑΝΑΠΤΥΞΗ ΚΑΙ ΕΦΑΡΜΟΓΗ ΚΙΝΗΤΙΚΩΝ ΜΕΘΟΔΩΝ ΕΚΤΙΜΗΣΗΣ ΤΗΣ ΠΟΙΟΤΗΤΑΣ ΤΩΝ ΤΡΟΦΙΜΩΝ ΣΥΝΤΟΜΗ ΠΕΡΙΛΗΨΗ Αντικείμενο της μελέτης αποτέλεσε
Η Φυσική των ζωντανών Οργανισμών (10 μονάδες)
 Η Φυσική των ζωντανών Οργανισμών (10 μονάδες) Δεδομένα: Κανονική Ατμοσφαιρική Πίεση, P 0 = 1.013 10 5 Pa = 760 mmhg Μέρος A. Η φυσική του κυκλοφορικού συστήματος. (4.5 μονάδες) Q3-1 Στο Μέρος αυτό θα μελετήσετε
Η Φυσική των ζωντανών Οργανισμών (10 μονάδες) Δεδομένα: Κανονική Ατμοσφαιρική Πίεση, P 0 = 1.013 10 5 Pa = 760 mmhg Μέρος A. Η φυσική του κυκλοφορικού συστήματος. (4.5 μονάδες) Q3-1 Στο Μέρος αυτό θα μελετήσετε
ΕΦΕΛΚΥΣΜΟΣ ΚΡΑΜΑΤΩΝ ΜΕ ΜΝΗΜΗΣ ΣΧΗΜΑΤΟΣ
 ΕΦΕΛΚΥΣΜΟΣ ΚΡΑΜΑΤΩΝ ΜΕ ΜΝΗΜΗΣ ΣΧΗΜΑΤΟΣ Το φαινόµενο της µνήµης σχήµατος συνδέεται µε τη δυνατότητα συγκεκριµένων υλικών να «θυµούνται» το αρχικό τους σχήµα ακόµα και µετά από εκτεταµένες παραµορφώσεις
ΕΦΕΛΚΥΣΜΟΣ ΚΡΑΜΑΤΩΝ ΜΕ ΜΝΗΜΗΣ ΣΧΗΜΑΤΟΣ Το φαινόµενο της µνήµης σχήµατος συνδέεται µε τη δυνατότητα συγκεκριµένων υλικών να «θυµούνται» το αρχικό τους σχήµα ακόµα και µετά από εκτεταµένες παραµορφώσεις
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου /3
 Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
Θεωρητική Εξέταση. Τρίτη, 15 Ιουλίου 2014 1/3 Πρόβλημα 2. Καταστατική Εξίσωση Van der Waals (11 ) Σε ένα πολύ γνωστό μοντέλο του ιδανικού αερίου, του οποίου η καταστατική εξίσωση περιγράφεται από το νόμο
Ανθεκτικότητα Υλικών και Περιβάλλον
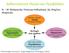 Ανθεκτικότητα Υλικών και Περιβάλλον Ν. Μ. Μπάρκουλα, Επίκουρη Καθηγήτρια, Δρ. Μηχ/γος Μηχανικός 1 Τι είναι: Περίγραμμα Μαθήματος Επιλογής Μάθημα Επιλογής στο 9ο Εξάμηνο του ΤΜΕΥ Με τι ασχολείται: Με την
Ανθεκτικότητα Υλικών και Περιβάλλον Ν. Μ. Μπάρκουλα, Επίκουρη Καθηγήτρια, Δρ. Μηχ/γος Μηχανικός 1 Τι είναι: Περίγραμμα Μαθήματος Επιλογής Μάθημα Επιλογής στο 9ο Εξάμηνο του ΤΜΕΥ Με τι ασχολείται: Με την
ΟΞΕΑ ΒΑΣΕΙΣ ΚΑΙ ΙΟΝΤΙΚΗ ΙΣΟΡΡΟΠΙΑ
 ΟΞΕΑ ΒΑΣΕΙΣ ΚΑΙ ΙΟΝΤΙΚΗ ΙΣΟΡΡΟΠΙΑ Οι ορτανσίες σε όξινα εδάφη έχουν μπλε άνθη, σε βασικά ροζ και σε ουδέτερα μοβ. Δημήτρης Παπαδόπουλος, χημικός Βύρωνας, 2015 Ιοντικά υδατικά διαλύματα Ιοντικές ενώσεις.
ΟΞΕΑ ΒΑΣΕΙΣ ΚΑΙ ΙΟΝΤΙΚΗ ΙΣΟΡΡΟΠΙΑ Οι ορτανσίες σε όξινα εδάφη έχουν μπλε άνθη, σε βασικά ροζ και σε ουδέτερα μοβ. Δημήτρης Παπαδόπουλος, χημικός Βύρωνας, 2015 Ιοντικά υδατικά διαλύματα Ιοντικές ενώσεις.
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΠΕΧΑΜΕΤΡΙΑ
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΠΕΧΑΜΕΤΡΙΑ Ιωάννης Πούλιος Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124 ΘΕΣΣΑΛΟΝΙΚΗ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑΤΟΣ ΒΙΟΛΟΓΙΑΣ ΠΕΧΑΜΕΤΡΙΑ Ιωάννης Πούλιος Αθανάσιος Κούρας Ευαγγελία Μανώλη ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ 54124 ΘΕΣΣΑΛΟΝΙΚΗ
1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ
 1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ ΗΛΙΑΣ ΝΟΛΗΣ-ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΘΕΟΔΩΡΟΣ 2012 Διαλύματα Διάλυμα ονομάζεται κάθε ομογενές μείγμα δύο ή περισσοτέρων συστατικών. Κάθε
1 Η ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΤΜΗΜΑ ΔΙΑΤΡΟΦΗΣ ΚΑΙ ΔΙΑΙΤΟΛΟΓΙΑΣ ΚΑΡΔΙΤΣΑ ΔΙΑΛΥΜΑΤΑ ΗΛΙΑΣ ΝΟΛΗΣ-ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΘΕΟΔΩΡΟΣ 2012 Διαλύματα Διάλυμα ονομάζεται κάθε ομογενές μείγμα δύο ή περισσοτέρων συστατικών. Κάθε
Άσκηση 5η. Οξέα Βάσεις - Προσδιορισμός του ph διαλυμάτων. Πανεπιστήμιο Πατρών - Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας - Ακαδ.
 Άσκηση 5η Οξέα Βάσεις - Προσδιορισμός του ph διαλυμάτων Πανεπιστήμιο Πατρών - Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας - Ακαδ. έτος 2016-17 Ιοντικά διαλύματα- 2 Διάσταση Οι ιοντικές ενώσεις γενικώς διαλύονται
Άσκηση 5η Οξέα Βάσεις - Προσδιορισμός του ph διαλυμάτων Πανεπιστήμιο Πατρών - Τμήμα ΔΕΑΠΤ - Εργαστήριο Γενικής Χημείας - Ακαδ. έτος 2016-17 Ιοντικά διαλύματα- 2 Διάσταση Οι ιοντικές ενώσεις γενικώς διαλύονται
Σύνθετα Υλικά: Χαρακτηρισμός και Ιδιότητες
 Σύνθετα Υλικά: Χαρακτηρισμός και Ιδιότητες Εργαστηριακή Άσκηση 3: Μηχανικός Χαρακτηρισμός της Διεπιφάνειας Ίνας- Μήτρας Χρήση Ακουστικής Εκπομπής και Μικροσκοπίας Διδάσκοντες: Α. Παϊπέτης, Αν. Καθηγητής,
Σύνθετα Υλικά: Χαρακτηρισμός και Ιδιότητες Εργαστηριακή Άσκηση 3: Μηχανικός Χαρακτηρισμός της Διεπιφάνειας Ίνας- Μήτρας Χρήση Ακουστικής Εκπομπής και Μικροσκοπίας Διδάσκοντες: Α. Παϊπέτης, Αν. Καθηγητής,
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΙΙ ΤΜΗΜΑΤΟΣ ΧΗΜΕΙΑΣ Ιωάννης Πούλιος ΔΥΑΔΙΚΑ ΣΥΣΤΗΜΑΤΑ ΜΕΛΕΤΗ ΤΩΝ ΔΙΑΓΡΑΜΜΑΤΩΝ ΤΟΥ ΣΗΜΕΙΟΥ ΖΕΣΗΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ ΧΗΜΕΙΑΣ ΤΜΗΜΑ ΧΗΜΕΙΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ
Κεφάλαιο 9 - Mοριακές διαμορφώσεις πολυμερών
 Κεφάλαιο 9 - Mοριακές διαμορφώσεις πολυμερών Πώς εκτείνεται στο χώρο μια μακρομοριακή αλυσίδα; Στόχοι του κεφαλαίου Μοριακή διαμόρφωση των μακρομορίων στο χώρο. Υπολογισμός της απόστασης από άκρο-σε-άκρο
Κεφάλαιο 9 - Mοριακές διαμορφώσεις πολυμερών Πώς εκτείνεται στο χώρο μια μακρομοριακή αλυσίδα; Στόχοι του κεφαλαίου Μοριακή διαμόρφωση των μακρομορίων στο χώρο. Υπολογισμός της απόστασης από άκρο-σε-άκρο
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια
 πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
πρωτεϊνες νουκλεϊκά οξέα Βιολογικά Μακρομόρια υδατάνθρακες λιπίδια Περιγραφή μαθήματος Επανάληψη σημαντικών εννοιών από την Οργανική Χημεία Χημική σύσταση των κυττάρων Μονοσακχαρίτες Αμινοξέα Νουκλεοτίδια
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΘΕΜΑ Α ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ & Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 3 ΙΟΥΛΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΘΕΜΑ Α ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ & Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 3 ΙΟΥΛΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
Μέθοδοι Πολυμερισμού
 Μέθοδοι Πολυμερισμού 1 Μέθοδοι Πολυμερισμού Προσθήκης Συμπύκνωσης Μέθοδοι Πολυμερισμού Αλυσιδωτός Προσθήκης Σταδιακός Συμπύκνωσης Αλυσιδωτοί Πολυμερισμοί Πολυμερισμός Ελευθέρων ριζών: Ενεργό Κέντρο ελεύθερη
Μέθοδοι Πολυμερισμού 1 Μέθοδοι Πολυμερισμού Προσθήκης Συμπύκνωσης Μέθοδοι Πολυμερισμού Αλυσιδωτός Προσθήκης Σταδιακός Συμπύκνωσης Αλυσιδωτοί Πολυμερισμοί Πολυμερισμός Ελευθέρων ριζών: Ενεργό Κέντρο ελεύθερη
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις
 Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση 7: Κατανομή ουσίας μεταξύ δύο διαλυτών και προσδιορισμός σταθεράς ισορροπίας αντιδράσεως Βασιλική Χαβρεδάκη Τμήμα Χημείας 1. Θεωρία... 3. Μετρήσεις... 5 3. Επεξεργασία
Φυσικοχημεία Εργαστηριακές Ασκήσεις Άσκηση 7: Κατανομή ουσίας μεταξύ δύο διαλυτών και προσδιορισμός σταθεράς ισορροπίας αντιδράσεως Βασιλική Χαβρεδάκη Τμήμα Χημείας 1. Θεωρία... 3. Μετρήσεις... 5 3. Επεξεργασία
Ανάλυση Τροφίμων. Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ. Τμήμα Τεχνολογίας Τροφίμων. Ακαδημαϊκό Έτος
 Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
Ανάλυση Τροφίμων Ενότητα 9: Υδατική ισορροπία Οξέα και βάσεις Τμήμα Τεχνολογίας Τροφίμων Τ.Ε.Ι. ΘΕΣΣΑΛΙΑΣ Ακαδημαϊκό Έτος 2018-2019 Δημήτρης Π. Μακρής PhD DIC Αναπληρωτής Καθηγητής Οι Έννοιες Οξύ Βάση:
27 1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ
 1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 27 28 29 ΔΙΔΑΚΤΙΚΗ ΩΡΑ: 1 ΔΙΔΑΚΤΙΚΗ ΕΝΟΤΗΤΑ: 1.1 Με τι ασχολείται η Χημεία - Ποια είναι η σημασία της Χημείας στη ζωή μας 1.2 Γνωρίσματα της ύλης (μάζα, όγκος, πυκνότητα) - Μετρήσεις
1. ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ 27 28 29 ΔΙΔΑΚΤΙΚΗ ΩΡΑ: 1 ΔΙΔΑΚΤΙΚΗ ΕΝΟΤΗΤΑ: 1.1 Με τι ασχολείται η Χημεία - Ποια είναι η σημασία της Χημείας στη ζωή μας 1.2 Γνωρίσματα της ύλης (μάζα, όγκος, πυκνότητα) - Μετρήσεις
ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ. Διερεύνηση της συσχέτισης μεταξύ των βασικών ηλεκτρικών και γεωμετρικών παραμέτρων μονωτήρων μέσης τάσης. Απταλίδης Θεόφιλος
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΗΛΕΚΤΡΟΛΟΓΩΝ ΜΗΧΑΝΙΚΩΝ & ΜΗΧΑΝΙΚΩΝ ΥΠΟΛΟΓΙΣΤΩΝ ΤΟΜΕΑΣ ΗΛΕΚΤΡΙΚΗΣ ΕΝΕΡΓΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΥΨΗΛΩΝ ΤΑΣΕΩΝ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ Διερεύνηση της συσχέτισης
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΠΟΛΥΤΕΧΝΙΚΗ ΣΧΟΛΗ ΤΜΗΜΑ ΗΛΕΚΤΡΟΛΟΓΩΝ ΜΗΧΑΝΙΚΩΝ & ΜΗΧΑΝΙΚΩΝ ΥΠΟΛΟΓΙΣΤΩΝ ΤΟΜΕΑΣ ΗΛΕΚΤΡΙΚΗΣ ΕΝΕΡΓΕΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΥΨΗΛΩΝ ΤΑΣΕΩΝ ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ Διερεύνηση της συσχέτισης
Ασκήσεις Ακ. Έτους 2014 15 (επιλύθηκαν συζητήθηκαν κατά τη διδασκαλία) Όπου χρειάζεται ο Αριθμός Avogadro λαμβάνεται 0.6023 1024
 Ασκήσεις Ακ. Έτους 014 15 (επιλύθηκαν συζητήθηκαν κατά τη διδασκαλία) Όπου χρειάζεται ο Αριθμός Avoadro λαμβάνεται 0.603 10 4 και τα ατομικά βάρη θεωρείται ότι ταυτίζονται με τον μαζικό αριθμό σε 1. Το
Ασκήσεις Ακ. Έτους 014 15 (επιλύθηκαν συζητήθηκαν κατά τη διδασκαλία) Όπου χρειάζεται ο Αριθμός Avoadro λαμβάνεται 0.603 10 4 και τα ατομικά βάρη θεωρείται ότι ταυτίζονται με τον μαζικό αριθμό σε 1. Το
ΣΥΝΘΕΣΗ, ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΚΑΙ ΜΕΛΕΤΗ ΙΔΙΟΤΗΤΩΝ ΚΑΙΝΟΤΟΜΩΝ ΝΑΝΟΣΥΝΘΕΤΩΝ ΥΛΙΚΩΝ ΕΠΟΞΕΙΔΙΚΩΝ ΡΗΤΙΝΩΝ ΑΡΓΙΛΩΝ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΕΠΙΣΤΗΜΗΣ ΥΛΙΚΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΣΥΝΘΕΣΗ, ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΚΑΙ ΜΕΛΕΤΗ ΙΔΙΟΤΗΤΩΝ ΚΑΙΝΟΤΟΜΩΝ ΝΑΝΟΣΥΝΘΕΤΩΝ ΥΛΙΚΩΝ ΕΠΟΞΕΙΔΙΚΩΝ ΡΗΤΙΝΩΝ ΑΡΓΙΛΩΝ ΠΑΝΑΓΙΩΤΗΣ Ι. ΞΥΔΑΣ ΙΩΑΝΝΙΝΑ,
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΕΠΙΣΤΗΜΗΣ ΥΛΙΚΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΣΥΝΘΕΣΗ, ΧΑΡΑΚΤΗΡΙΣΜΟΣ ΚΑΙ ΜΕΛΕΤΗ ΙΔΙΟΤΗΤΩΝ ΚΑΙΝΟΤΟΜΩΝ ΝΑΝΟΣΥΝΘΕΤΩΝ ΥΛΙΚΩΝ ΕΠΟΞΕΙΔΙΚΩΝ ΡΗΤΙΝΩΝ ΑΡΓΙΛΩΝ ΠΑΝΑΓΙΩΤΗΣ Ι. ΞΥΔΑΣ ΙΩΑΝΝΙΝΑ,
19ο Μάθημα ΔΙΑΛΥΜΑΤΑ
 19ο Μάθημα ΔΙΑΛΥΜΑΤΑ Μια σπουδαία ικανότητα του νερού, η διαλυτική Ξέρουμε ότι το νερό κάνει έναν κύκλο στη φύση. Εξατμίζεται, γίνεται σύννεφο και πέφτει στη γη ως βροχή. Ένα μεγάλο μέρος από το βρόχινο
19ο Μάθημα ΔΙΑΛΥΜΑΤΑ Μια σπουδαία ικανότητα του νερού, η διαλυτική Ξέρουμε ότι το νερό κάνει έναν κύκλο στη φύση. Εξατμίζεται, γίνεται σύννεφο και πέφτει στη γη ως βροχή. Ένα μεγάλο μέρος από το βρόχινο
