ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ. «Μελέτη της αλληλεπίδρασης των σηματοδοτικών μονοπατιών RANK- RANKL και EGFR-EGF στην κυτταρική σειρά μαστού SKBR3»
|
|
|
- Αἴαξ Παππάς
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ Πρόγραμμα Μεταπτυχιακών Σπουδών Εφαρμογές στις Βασικές Ιατρικές Επιστήμες «Μοριακή Βιολογία και Κυτταρογενετική» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ «Μελέτη της αλληλεπίδρασης των σηματοδοτικών μονοπατιών RANK- RANKL και EGFR-EGF στην κυτταρική σειρά μαστού SKBR3» Πλακούλα Εύα Βιολόγος Επιβλέπων Καθηγητής: Ιωάννης Ζαρκάδης ΠΑΤΡΑ 2016
2 1
3 ΠΡΟΛΟΓΟΣ Η παρούσα διπλωματική εργασία εκπονήθηκε στο Εργαστήριο Γενικής Βιολογίας της Ιατρικής Σχολής του Πανεπιστημίου Πατρών, στα πλαίσια του μεταπτυχιακού προγράμματος Εφαρμογές στις Βασικές Ιατρικές Επιστήμες, με κατεύθυνση: Μοριακή Βιολογία- Κυτταρογενετική, υπό την επίβλεψη του Καθηγητή Ι.Κ. Ζαρκάδη, κατά τα έτη Σε αυτό το σημείο θα ήθελα να εκφράσω τις ειλικρινείς μου ευχαριστίες στον επιβλέποντα μου Καθηγητή Ιωάννη Ζαρκάδη, καθώς με ιδιαίτερη προθυμία δέχθηκε να αναλάβει την επίβλεψη της εκπόνησης της διπλωματικής μου εργασίας. Παράλληλα σημαντική υπήρξε η στήριξη του ως προς τα μετέπειτα βήματα των σπουδών μου αφού δεν αρνήθηκε ποτέ να βοηθήσει σε κάθε νέα μου προσπάθεια. Ταυτόχρονα θα ήθελα να ευχαριστήσω τον Καθηγητή Χαράλαμπο Καλόφωνο για την ενεργή συνεπίβλεψη της διπλωματικής μου εργασίας και για την εμπιστοσύνη που μου έδειξε να εργαστώ στο Εργαστήριο Κλινικής και Μοριακής Ογκολογίας όπου διεξήχθη μεγάλο μέρος των πειραμάτων. Επίσης θα ήθελα να ευχαριστήσω την Καθηγήτρια Ζωή Λυγερού η οποία δέχθηκε να γίνει μέλος της τριμελούς επιτροπής, συμβάλλοντας έτσι ενεργά στη βελτίωση της. Τέλος θα ήθελα να ευχαριστήσω τους ερευνητές Χαρούλα Σιρινιάν και Αναστάσιο Παπαναστασίου καθώς υπήρξαν πάντα διαθέσιμοι να ακούσουν αλλά και να λύσουν προβλήματα που συνάντησα σχετικά με την έρευνα και όχι μόνο. Ένα μεγάλο ευχαριστώ σε όλους τους ερευνητές και φοιτητές του εργαστηρίου για τη συμπαράσταση και την εκτίμηση που έδειξαν στο πρόσωπο μου και ειδικότερα στον Κωνσταντίνο Σιατή και στην Άντζελα Λαμπροπούλου καθώς εκτός από συνεργάτες μου υπήρξαν και συνεχίζουν να είναι φίλοι. 2
4 ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ... 2 ΕΙΣΑΓΩΓΗ... 5 ΜΑΣΤΟΣ ΑΝΑΤΟΜΙΑ ΙΣΤΟΛΟΓΙΑ ΦΥΣΙΟΛΟΓΙΚΗ ΑΝΑΠΤΥΞΗ ΜΑΣΤΟΥ ΑΝΑΠΤΥΞΗ ΕΠΙΘΗΛΙΑΚΩΝ ΝΕΟΠΛΑΣΙΩΝ ΤΟΥ ΜΑΣΤΟΥ... 9 ΑΞΟΝΑΣ RANK-RANKL Σηματοδοτικά μονοπάτια Φυσιολογική λειτουργία RANK/RANKL RANK/RANKL και καρκίνος Άξονας EGFR-EGF Σηματοδοτικά μονοπάτια Φυσιολογική λειτουργία EGFR-EGF EGFR-EGF και καρκίνος Υποδοχείς RANK EGFR και θεραπεία Αναστολείς του μονοπατιού RANK-RANKL Αναστολείς του μονοπατιού EGFR-EGF ΣΚΟΠΟΣ ΥΛΙΚΑ ΚΑΙ ΜΕΘΟΔΟΙ ΚΥΤΤΑΡΑ ΚΑΙ ΚΥΤΤΑΡΟΚΑΛΛΙΕΡΓΕΙΕΣ ΒΑΚΤΗΡΙΑ ΚΑΙ ΒΑΚΤΗΡΙΑΚΕΣ ΚΑΛΛΙΕΡΓΕΙΕΣ ΚΑΛΛΙΕΡΓΕΙΑ ΒΑΚΤΗΡΙΩΝ ΣΕ ΑΓΑΡ ΠΑΡΑΣΚΕΥΗ ΥΓΡΗΣ ΒΑΚΤΗΡΙΑΚΗΣ ΚΑΛΛΙΕΡΓΕΙΑΣ ΑΝΑΛΥΣΗ ΠΡΩΤΕΊΝΩΝ ΠΑΡΑΣΚΕΥΗ ΟΛΙΚΟΥ ΠΡΩΤΕΪΝΙΚΟΥ ΕΚΧΥΛΙΣΜΑΤΟΣ ΑΠΟ ΚΥΤΤΑΡΙΚΕΣ ΣΕΙΡΕΣ ΠΟΣΟΤΙΚΟΠΟΪΗΣΗ ΠΡΩΤΕΊΝΩΝ ΗΛΕΚΤΡΟΦΟΡΗΣΗ SDS-PAGE ΠΡΩΤΕΪΝΩΝ ΑΝΟΣΟΑΠΟΤΥΠΩΣΗ ΚΑΤΑ WESTERN ΑΝΟΣΟΦΘΟΡΙΣΜΟΣ ΑΝΑΛΥΣΗ ΝΟΥΚΛΕΙΪΚΏΝ ΟΞΕΩΝ ΑΠΟΜΟΝΩΣΗ ΝΟΥΚΛΕΙΚΩΝ ΟΞΕΩΝ (RNA) ΣΥΝΘΕΣΗ ΣΥΜΠΛΗΡΩΜΑΤΙΚΟΥ DNA (cdna)
5 3. ΑΛΥΣΙΔΩΤΗ ΑΝΤΙΔΡΑΣΗ ΠΟΛΥΜΕΡΑΣΗΣ (PCR) Real-Time PCR (RT-PCR) ΠΟΣΟΤΙΚΟΠΟΙΗΣΗ ΝΟΥΚΛΕΙΚΩΝ ΟΞΕΩΝ ΗΛΕΚΤΡΟΦΟΡΗΣΗ ΝΟΥΚΛΕΙΚΩΝ ΟΞΕΩΝ ΣΕ ΠΗΚΤΩΜΑ ΑΓΑΡΟΖΗΣ ΑΠΟΤΕΛΕΣΜΑΤΑ Προσδιορισμός των ενδογενών επιπέδων mrna των RANK και EGFR σε καρκινικές σειρές μαστού και σε δείγματα ασθενών με καρκίνο μαστού Ταυτοποίηση του μορίου RANK ως επαγωγέα της έκφρασης του EGFR Έλεγχος της ικανότητας του RANK να ελέγχει την έκφραση του EGFR σε πρωτεϊνικό επίπεδο στην κυτταρική σειρά καρκίνου μαστού SKBR Έλεγχος της επίδρασης της έκφρασης του RANK στο σηματοδοτικό μονοπάτι EGFR-EGF στα κύτταρα και SKBR Έλεγχος της επίδρασης της έκφρασης του RANK στην ικανότητα πολλαπλασιασμού των SKBR3 κυττάρων ΣΥΖΗΤΗΣΗ Επαγωγή της έκφρασης του EGFR από το RANK Επαγωγή του σηματοδοτικού μονοπατιού του EGFR από το RANK Αυξημένη πολλαπλασιαστική ικανότητα των SKBR3-RANK-stable κυττάρων σε συνθήκες αποστέρησης θρεπτικού ή/και παρουσία EGF Η χρήση του αναστολέα Erlotinib δεν επηρεάζει σημαντικά την ικανότητα πολλαπλασιασμού των κυττάρων SKBR3-RANK-stable ΠΕΡΙΛΗΨΗ ABSTRACT ΒΙΒΛΙΟΓΡΑΦΙΑ
6 ΕΙΣΑΓΩΓΗ 5
7 ΜΑΣΤΟΣ 1.ΑΝΑΤΟΜΙΑ Οι μαζικοί αδένες αποτελούν βασικό χαρακτηριστικό όλων των θηλαστικών. Οι μαστοί εμβρυολογικά εμφανίζονται και στα δύο φύλα, ωστόσο ωριμάζουν μόνο στα θηλυκά από την περίοδο της εφηβείας και μετά. Αποτελούν δυναμικά όργανα καθώς η μορφολογία τους μεταβάλλεται ανάλογα με την ηλικία της γυναίκας, τον έμμηνο κύκλο, αλλά και την αναπαραγωγική της κατάσταση. Οι μαστικοί αδένες διατηρούνται ανενεργοί, ενώ η τελική τους μορφολογία διαμορφώνεται κατά τη διάρκεια της εγκυμοσύνης. Οι μαστοί αποτελούν διαφοροποιημένους αποκρινείς ιδρωτοποιούς αδένες που προέρχονται από την επιδερμίδα και βρίσκονται στον υποδόριο ιστό. O μαστός αποτελείται από τρεις κύριες δομές: το δέρμα, το υποδόριο λίπος και τον μαζικό αδένα. Ο μαζικός αδένας συνίσταται από δύο διακριτά στοιχεία, το στρώμα και το παρέγχυμα. Ο μαστός συνίσταται από επιμέρους τμήματα, τους λοβούς, οι οποίοι διαχωρίζονται από ινώδεις ζώνες συνδετικού ιστού, ενώ περιβάλλεται από περιτονίες. Η σύνδεση μεταξύ των περιτονιών και των ινωδών δεσμών συνδετικού ιστού, σχηματίζουν τους συνδέσμους του Cooper, οι οποίοι δρουν υποστηρικτικά για το μαστό. Η αιματική παροχή στο μαστό πραγματοποιείται από αρτηρίες που προέρχονται από τα θωρακικά τόξα των μασχαλιαίων αρτηριών, την εσωτερική θωρακική αρτηρία καθώς και τις πρόσθιες μεσοπλεύριες αρτηρίες. Η κατανομή των φλεβών ακολουθεί αυτή των αρτηριών και γίνεται μέσω των έσω μαστικών, των μεσοπλεύριων και των μασχαλιαίων φλεβών. Τα λεμφικά τριχοειδή βρίσκονται κατανεμημένα στο συνδετικό ιστό γύρω από τις κυψελίδες και ενώνονται σε μεγαλύτερα λεμφαγγεία τα οποία αποστραγγίζουν στους μασχαλιαίους, υπερκλείδιους, ή παράπλευρους λεμφαδένες. Οι μασχαλιαίοι λεμφαδένες χαρακτηρίζονται με βάση τη θέση τους ως προς τον ελάσσονα θωρακικό μύ σε τρεις ομάδες Ι, ΙΙ και ΙΙΙ. Η παροχέτευση της λέμφου γίνεται από τους λεμφαδένες του επιπέδου Ι, σε αυτούς τους επιπέδου ΙΙ και έπειτα ΙΙΙ με τη σειρά [1]. 6
8 2.ΙΣΤΟΛΟΓΙΑ Ένας ανενεργός μαζικός αδένας είναι δυνατό να αποτελείται από 15 έως 20 λοβούς (lobes), ενώ κάθε λοβός διακρίνεται σε επιμέρους λοβία (lobules) που κυμαίνονται μεταξύ 20 και 40 σε αριθμό. Οι λοβοί κατανέμονται ακτινικά από τη θηλή προς το εσωτερικό του μαστού. Μεταξύ των λοβών βρίσκεται πυκνός συνδετικός και λιπώδης ιστός, καθένας από τους λοβούς αποστραγγίζει σε ένα γαλακτοφόρο πόρο (lactiferous duct), οι οποίοι στη συνέχεια μετασχηματίζονται στους γαλακτοφόρους κόλπους και είναι ιδιαιτέρως διατεταμένοι. Οι γαλακτοφόροι πόροι κάθε λοβού καταλήγουν στη θηλή, η οποία εμφανίζει στόμια απ όπου εξέρχεται το γάλα. Εικόνα 1: Σχηματική αναπαράσταση του μαστού κατά τη γαλουχία. Ο μαστός αποτελείται από τους τελικούς πόρους οι οποίοι εκτείνονται ανάμεσα στο συνδετικό και το λιπώδη ιστό. (Gray, H., Gray's Anatomy 35 ed, ed. R.a.P.L. Williams1973, Endiburgh: Churchill Livingstone: W. B. Saunders Company.) 7
9 Το 1959 η ομάδα της Parks et al,. ήταν η πρώτη που περιέγραψε τη μικροανατομία του μαστού [2]. Όπως ήδη αναφέρθηκε κάθε λοβός αποτελείται από επιμέρους λοβία, τα οποία φέρουν γαλακτοφόρους πόρους, οι κλάδοι των οποίων αποστραγγίζουν σε τελικούς πόρους. Κάθε τελικός πόρος σχηματίζει μια δομή αποτελούμενη από 10 έως 100 κυψελίδες, δίνοντας την όψη σταφυλλιού, που ονομάζεται τελική προλοβιακή μονάδα (terminal duct lobular unit) που αποτελεί τη βασική λειτουργική και δομική μονάδα του μαστού. Η τελική προλοβιακή μονάδα αποτελείται από: τα τελικά σωληνάρια (terminal ductules) τα οποία κατά την περίοδο της εγκυμοσύνης διαφοροποιούνται σε εκκριτικές κυψελίδες που παράγουν γάλα υπό την ορμονική επίδραση, τους ενδολοβιακούς συλλεκτικούς πόρους που μεταφέρουν τις κυψελιδικές εκκρίσεις στο γαλακτοφόρο πόρο και το ενδολοβιακό στρώμα που περιβάλλει τα τελικά σωληνάρια και τις κυψελίδες. Τα λοβία υπακούουν σε ορμονικό έλεγχο κυρίως οιστρογόνων και προγεστερόνης, λόγω των οιστρογονικών και προγεστερονικών υποδοχέων που φέρουν στην επιφάνεια των κυττάρων τους. Έτσι ανάλογα με το στάδιο του έμμηνου κύκλου, η δομή τους διαφοροποιείται και επανέρχεται στην αρχική της κατάσταση προς το τέλος αυτού, όπου τα επίπεδα των ορμονών μειώνονται. Τα επιθηλιακά κύτταρα των πόρων ανάλογα με τη θέση τους εμφανίζουν και διαφορετική μορφολογία. Κοντά στην εκβολή των πόρων το επιθήλιο χαρακτηρίζεται ως πολύστιβο πλακώδες, πιο εσωτερικά κοντά στους γαλακτοφόρους κόλπους ως κυβοειδές διπλόστιβο, ενώ στην υπόλοιπη περιοχή ως κυβοειδές μονόστιβο. Ανάμεσα στα κύτταρα του επιθηλίου και της βασικής μεμβράνης βρίσκονται μυοεπιθηλιακά κύτταρα τοποθετημένα μεταξύ αυλού και στρώματος κι έτσι διατηρούν την πολικότητα εντός του μαστικού ιστού [1]. 3.ΦΥΣΙΟΛΟΓΙΚΗ ΑΝΑΠΤΥΞΗ ΜΑΣΤΟΥ Η διαδικασία ανάπτυξης των μαστών ξεκινά ήδη από την τέταρτη εβδομάδα της κύησης με το σχηματισμό μιας αρχέγονης μαζικής ακρολοφίας και η διαφοροποίηση του ιστού συνεχίζεται μέχρι την ολοκλήρωση της κύησης. Το αποτέλεσμα είναι η μεγέθυνση του μαστικού αδένα και η ανάπτυξη του συμπλέγματος θηλήςπεριθηλαίας άλου. 8
10 Υπό την επίδραση ορμονών κατά τη διάρκεια της εφηβείας ξεκινά και η ανάπτυξη του μαστικού αδένα. Συγκεκριμένα οι τελικές προλοβιακές μονάδες διαφοροποιούνται και ενεργοποιούνται. Για την ανάπτυξη των πόρων του μαστού απαραίτητα είναι τα οιστρογόνα, ενώ για την ανάπτυξη των λοβών και τη διαφοροποίηση του επιθηλίου, υπεύθυνη είναι η προγεστερόνη. Η έκκριση των ορμονών αυτών ρυθμίζεται από την ωχρινοποιητική ορμόνη, τη θυλακιοτρόπο ορμόνη και την εκλυτική ορμόνη της γοναδοτροπίνης. Από κει κι έπειτα σε κάθε έμμηνο κύκλο συμβαίνουν μικρότερες αλλαγές οι οποίες προετοιμάζουν τον μαστό για την περίοδο της γαλουχίας. Κατά τη διάρκεια της εγκυμοσύνης ο πλακούντας και οι ωοθήκες εκκρίνουν ακόμα μεγαλύτερη ποσότητα οιστρογόνων και προγεστερόνης που οδηγούν σε αλλαγές στο μαστικό ιστό. Οι πόροι και οι λοβοί πολλαπλασιάζονται και το μέγεθος του μαστού αυξάνεται. Στο τέλος της κύησης τα ορμονικά επίπεδα μειώνονται, το μαστικό επιθήλιο ατροφεί και ο μαστός επανέρχεται στο φυσιολογικό του μέγεθος. Αντίθετα στην διάρκεια της εμμηνόπαυσης που η έκκριση των ορμονών από τις ωοθήκες μειώνεται οι πόροι του μαστού εκφυλίζονται, ο ινώδης συνδετικός ιστός αυξάνει σε πυκνότητα και o μαστικός αντικαθίσταται από το λιπώδη ιστό [1]. 4.ΑΝΑΠΤΥΞΗ ΕΠΙΘΗΛΙΑΚΩΝ ΝΕΟΠΛΑΣΙΩΝ ΤΟΥ ΜΑΣΤΟΥ Επιδημιολογία και παράγοντες κινδύνου Ο καρκίνος του μαστού αποτελεί τον πιο συχνό καρκίνο στις γυναίκες παγκοσμίως, καθώς αποτελεί το 23% των νέων περιστατικών ετησίως. Ταυτόχρονα αποτελεί τη συχνότερη αιτία θανάτου μεταξύ των γυναικών σε σχέση με οποιαδήποτε άλλη μορφή νεοπλασίας με τα ποσοστά να αγγίζουν το 14% για το Η συχνότητα εμφάνισης αυτής της μορφής καρκίνου παρουσιάζει σημαντικές διακυμάνσεις γεωγραφικά καθώς τα μισά περίπου περιστατικά εμφάνισης της νόσου και το 60% των θανάτων εμφανίζονται στις αναπτυσσόμενες χώρες. Οι παράγοντες που συντελούν σε αυτή τη διαφοροποίηση είναι κυρίως ορμονικοί αλλά και η ικανότητα ή όχι πρώιμης διάγνωσης της νόσου [3]. Παρότι τα χορηγούμενα είδη θεραπειών (χημειοθεραπεία, ορμονοθεραπεία, ανοσοθεραπεία) έχουν περιορίσει σε κάποιο βαθμό την επανεμφάνιση της νόσου, ένα μεγάλο ποσοστό των ασθενών θα υποτροπιάσει και τελικά θα καταλήξει από την 9
11 ασθένεια. Συγκεκριμένα ασθενείς οι οποίοι διαγιγνώσκονται άμεσα και βρίσκονται στο στάδιο 0 ή 1 έχουν 100% πιθανότητα πενταετούς επιβίωσης, ενώ το ποσοστό μειώνεται κατακόρυφα στο 15% για γυναίκες οι οποίες έχουν εμφανίσει μετάσταση σε κάποιο άλλο ιστό (Cancer Research UK). Για το λόγο αυτό γίνονται σημαντικές προσπάθειες στον τομέα της έρευνας ώστε να εντοπιστούν μόρια-δείκτες τα οποία θα μπορέσουν να χρησιμοποιηθούν για την καλύτερη αντιμετώπιση των ασθενών και στη βέλτιστη περίπτωση να εφαρμοσθεί η εξατομικευμένη θεραπεία, η οποία αφενός δε θα βλάπτει τον ασθενή και αφετέρου θα ξεπερνά την αντίσταση στην αγωγή που εμφανίζεται σε ορισμένους. Πολυάριθμες μελέτες επικεντρώνονται στην αναγνώριση παραγόντων οι οποίοι πιθανώς αυξάνουν τον κίνδυνο εμφάνισης της νόσου. Στους παράγοντες αυτούς ανήκει η ηλικία, αυξανομένης της οποίας τα ποσοστά νεοπλασιών είναι συχνότερα, καθώς και η ηλικία της πρώτης έμμηνου ρύσεως αλλά και εμμηνόπαυσης. Κυρίαρχο αίτιο στον καρκίνο του μαστού αποτελούν οι περιβαλλοντικοί παράγοντες όπως οι συνθήκες διαβίωσης και η διατροφή, ενώ σημαντική φαίνεται να είναι και η γενετική προδιάθεση. Ετσι πολυάριθμές μελέτες σήμερα έχουν επικεντρωθεί στην ταυτοποίηση του γενετικού προφίλ γυναικών με επιβαρυμένο ιστορικό, ώστε να προληφθεί η εμφάνιση της ασθένειας, παραδείγματος χάριν πραγματοποιώντας μαστεκτομή. Στον πίνακα που ακολουθεί παρουσιάζονται οι παράγοντες κινδύνου ανάλογα με την βαρύτητα τους όπως δημοσιεύτηκε από τους Hong et al., το 2009 [4]. 10
12 Παράγοντες κινδύνου ανάπτυξης καρκίνου του μαστού 1. Μεγάλη αύξηση κινδύνου Μεταλλάξεις στα γονίδια BRCA1,2 και Li Fraumeni Αυξανόμενη ηλικία Δυτικός τρόπος ζωής Συγγενείς 1 ου βαθμού με ιστορικό καρκίνου μαστού ή ωοθηκών Καλοήθης όγκος μαστού με άτυπη υπερπλασία Έκθεση σε ιονίζουσα ακτινοβολία 2. Μέτρια αύξηση του κινδύνου Προηγούμενη διάγνωση καρκίνου μαστού Πρώιμη έναρξη εμμήνου ρύσεως Όψιμη εμμηνόπαυση Ατοκία ή πρώτη κύηση σε μεγάλη ηλικία Υψηλό οικονομικό-κοινωνικό επίπεδο Κατανάλωση αλκοόλ Παχυσαρκία μετά την εμμηνόπαυση Μη-ευνοϊκή μαστογραφική απεικόνιση παρεγχύματος Σάρκωμα μαλακών μορίων στα τέκνα Προηγούμενη διάγνωση καρκίνου ωοθηκών, παχέος εντέρου και ενδομητρίου 3. Μικρή αύξηση κινδύνου Καλοήθης όγκος μαστού χωρίς ατυπία Χρήση από του στόματος αντισυλληπτικών για πάνω από 10 έτη Ορμονική υποκατάσταση στην εμμηνόπαυση 4. Αμφισβητούμενη αύξηση Διακοπή κύησης Ψυχοσωματικοί παράμετροι Διατροφή δυτικού τύπου Επιπλεγμένο ινοαδένωμα 5. Μείωση του κινδύνου Πλήρης κύηση πριν τα 20 έτη της μητέρας Πολυάριθμες κυήσεις Αφαίρεση ωοθηκών πριν τα 45 έτη Τακτική άσκηση Θηλασμός Πίνακας 1: Παράγοντες κινδύνου ανάπτυξης καρκίνου μαστού (Waun Ki Hong, R.C.B.J., Holland-Frei Cancer Medicine, ed. H. Frei.) Καρκινογένεση και εξέλιξη του όγκου Για την μετάβαση από ένα φυσιολογικά αναπτυσσόμενο ιστό σε ένα καρκινικό είναι απαραίτητες πολυάριθμες αλλαγές γενετικές ή επιγενετικές πολλαπλών σταδίων. 11
13 Όπως περιγράφεται από τους Hannahan και Weinberg η διαδικασία μετάπτωσης ενός κυττάρου σε καρκινικό οφείλεται στην απόκτηση έξι νέων βιολογικών χαρακτηριστικών [5]. Στους νέους αυτούς χαρακτήρες εντάσσονται η αυτάρκεια σημάτων πολλαπλασιασμού, ενώ ταυτόχρονα απαλείφονται τα ανασταλτικά σήματα, η απόπτωση περιορίζεται και διατηρείται μια αέναη ικανότητα πολλαπλασιασμού στα κύτταρα. Ταυτόχρονα επάγεται η αγγειογένεση και η ικανότητα των κυττάρων να διηθούν νέους ιστούς και να μεθίστανται. Οι απαραίτητες γενετικές αλλαγές για τις ανωτέρω διαδικασίες είναι δυνατό να συμβαίνουν σε οποιαδήποτε θέση στο γονιδίωμα, αλλά συνήθως αφορούν σε αποσιώπηση ογκοκατασταλτικών γονιδίων ή ενεργοποίηση ογκογονιδίων, οπότε αναπτύσσεται γονιδιωματική αστάθεια και τελικά το κύτταρο οδηγείται σε κακοήθη εξαλλαγή. Σε πολυάριθμους όγκους μαστού έχουν βρεθεί να υπερεκφράζονται τα γονίδια Myc, Notch και Wnt τα οποία ελέγχουν σημαντικά στάδια του πολλαπλασιασμού και της ανάπτυξης των κυττάρων φυσιολογικά και η απορρύθμιση τους εμπλέκεται στην ανάπτυξη νεοπλασιών. Ογκογονίδιο Myc: Η πρωτεΐνη Myc εμπλέκεται ενεργά στην εμφάνιση και ανάπτυξη του καρκίνου του μαστού, καθότι αποτελεί σημαντικό ρυθμιστή του κυτταρικού πολλαπλασιασμού μέσα από τον έλεγχο του κυτταρικού κύκλου. Το Myc ελέγχει την μετάβαση από τη φάση G1 στην S μέσω ενεργοποίησης της κυκλίνης Ε/Cdk2 και καταστολής του αναστολέα κυκλινο-εξαρτώμενης κινάσης p21 Cip1 και προάγει τον κυτταρικό κύκλο μέσω ενεργοποίησης της κυκλίνης D1. Ακόμα διευκολύνει τον κυτταρικό πολλαπλασιασμό μέσω καταστολής του ογκοκατασταλτικού γονιδίου p27 Kip1 cdk και επάγει την επιθηλιο-μεσεγχυματική μετάβαση μέσω ενός μεταμεταφραστικού μηχανισμού καταστολής της πρωτεΐνης Ε-cadherin. Ο ρόλος του Myc στον καρκίνο του μαστού παρουσιάζεται συνοπτικά στην εικόνα που ακολουθεί [6]. 12
14 Εικόνα 2: O ρυθμιστικός ρόλος της πρωτεΐνης myc στον καρκίνο του μαστού. Τα μόρια BRCA1 και TGF-β που μπορούν να καταστείλουν την έκφραση του Myc, εμφανίζονται μεταλλαγμένα στον καρκίνο του μαστού. Η συνεχής ενεργοποίηση των Ras, Wnt, Notch, ER-α και EGFR/HER2 επηρεάζει θετικά και σταθεροποιεί την έκφραση του μορίου στα κύτταρα του όγκου.( Xu, J., Y. Chen, and O.I. Olopade, MYC and Breast Cancer. Genes Cancer, : ) Σηματοδοτικό μονοπάτι Wnt/β-κατενίνη: Οι πρωτεΐνες Wnt είναι εκκρινόμενα μόρια, ενώ η β-κατενίνη εντοπίζεται ως δομικό στοιχείο των διακυτταρικών συνδέσεων στην κυτταροπλασματική μεμβράνη, ή ως ρυθμιστής της μεταγραφής στον πυρήνα. Η πρωτεϊνη Wnt αλληλεπιδρά με τις πρωτεΐνες Frizzled και LPR,στην επιφάνεια του κυττάρου κι έτσι προστατεύει τη β-κατενίνη από αποδόμηση στο κυτταρόπλασμα. Με τον τρόπο αυτό περισσότερα μόρια β-κατενίνης θα εισέλθουν στον πυρήνα και θα συμμετάσχουν στη μεταγραφή γονιδίων. Ορισμένα από τα γονίδια τα οποία βρίσκονται υπό τον έλεγχο του διπτύχου Wnt/β-κατενίνη αποτελούν τα ογκογονίδια κυκλίνη D1 και c-myc, υπογραμμίζοντας έτσι το ρόλο του μονοπατιού στον καρκίνο του μαστού[7]. 13
15 Εικόνα 3: Σχηματική απεικόνιση του σηματοδοτικού μονοπατιού Wnt/β-κατενίνης και των παραγόντων που εμπλέκονται. Ο Wnt προσδένεται στις Frizzled και LPR πρωτεΐνες. Ο υποδοχέας αλληλεπιδρά με τους παράγοντες Dishevelled, APC, Axin, GSK3β και β- κατενίνη. Το σύμπλοκο αυτό ευθύνεται για την αποδόμηση της β-κατενίνης, γεγονός το οποίο αναστέλλεται παρουσία του Wnt. Έτσι η β-κατενίνη συσσωρεύεται στο κυτταρόπλασμα και εισέρχεται στον πυρήνα όπου ελέγχει τη μεταγραφή γονιδίων.( Howe, L.R. and A.M. Brown, Wnt signaling and breast cancer. Cancer Biol Ther, : ) Σηματοδοτικό μονοπάτι Notch: Η ενεργοποίηση του μονοπατιού ξεκινά από την αλληλεπίδραση του Notch με τους προσδέτες Delta-like και Jagged, οι οποίοι εκφράζονται από γειτονικά κύτταρα. Έτσι ξεκινά η πρωτεολυτική αποδόμηση του υποδοχέα και απελευθέρωση του ενδοκυττάριου τμήματος του Notch (NICD), επιτρέποντας την είσοδο του στον πυρήνα. Στον πυρήνα το NICD αλληλεπιδρά με τους παράγοντες RBP-jκ/CBF1 και Mastermind και ενεργοποιεί τη μεταγραφή γονιδίων στόχων [8]. Στα γονίδια στόχους του Notch είναι μεταξύ άλλων ο ΝF-κB, η κυκλίνη D1 και το c-myc [9]. 14
16 Εικόνα 4: Σχηματική απεικόνιση των βασικών στοιχείων του σηματοδοτικού μονοπατιού Notch. Με την πρόσδεση του προσδέτη στον υποδοχέα Notch ξεκινά η πρωτεόλυση του Το ενδοκυττάριο τμήμα του υποδοχέα (NICD) απελευθερώνεται και μετατοπίζεται στον πυρήνα όπου σχηματίζει ένα σύμπλοκο ενεργοποίησης της μεταγραφής σε συνδυασμό με τις πρωτεΐνες CoA και CSL, επάγοντας έτσι τη μεταγραφή των γονιδίων στόχων (Guo, S., M. Liu, and R.R. Gonzalez-Perez, Role of Notch and its oncogenic signaling crosstalk in breast cancer. Biochim Biophys Acta, : ) Στην ανάπτυξη καρκίνου του μαστού συμμετέχουν και οι υποδοχείς ορμονών προγεστερόνης και οιστρογόνων. Όπως ήδη αναφέρθηκε ο ρόλος των ορμονών αυτών και των υποδοχέων τους είναι απαραίτητος για να αναπτυχθεί πλήρως ο μαστός, ωστόσο η απορρύθμιση της λειτουργίας τους εμπλέκεται στην καρκινογένεση. Φυσιολογικά οι υποδοχείς ER και PR απουσία ορμονών βρίσκονται συνδεδεμένοι με πρωτεΐνες heatshock και παραμένουν ανενεργοί. Ωστόσο η παρουσία οιστρογόνων και προγεστερόνης αντίστοιχα, τους απελευθερώνει και επιτρέπει τη πρόσδεση τους σε ειδικές θέσεις του DNA, αλληλεπιδρώντας με μεταγραφικούς παράγοντες (NF-κΒ, STAT3 κ.α.) επάγοντας μεταγραφικές αλλαγές στα γονίδια στόχους [10]. Σημαντικά ογκογονίδια όπως είναι η κυκλίνη D1 και το Myc ρυθμίζονται θετικά από τους δύο υποδοχείς, προβάλλοντας έτσι το ρόλο των ER, PR στην εμφάνιση καρκίνου του μαστού [11]. 15
17 Εικόνα 5: Τα σηματοδοτικά μονοπάτια των ERα και PR επάγουν τη μεταγραφή.( Tanos, T., et al., ER and PR signaling nodes during mammary gland development. Breast Cancer Res, :. 210.) Ο υποδοχέας HER2 αποτελεί ακόμα ένα σημαντικό μόριο στη νόσο του καρκίνου του μαστού και βρίσκεται να υπερεκφράζεται σχεδόν σε όλα τα DCIS υψηλής κακοήθειας, στο 20-30% των διηθητικών πορογενών καρκινωμάτων και σε ένα μικρότερο ποσοστό διηθητικών καρκινωμάτων λοβού. Σε καρκινώματα χαμηλής κακοήθειας και σωληνώδη καρκινώματα η έκφραση του υποδοχέα είναι μηδενική [12] [13]. Φυσιολογικά η έκφραση του είναι απαραίτητη για το σχηματισμό των λοβών στο μαστό ωστόσο από πειράματα που έγιναν σε ζώα φαίνεται ότι όταν υπερεκφράζεται λόγω της μιτογόνου δράσης είναι ικανός να οδηγήσει στο σχηματισμό όγκου [14]. 16
18 Εικόνα 6: Το σηματοδοτικό μονοπάτι του HER2. Η ενεργοποίηση του οδηγεί σε κυτταρικό πολλαπλασιασμό και επιβίωση. (Morris, S.R. and L.A. Carey, Trastuzumab and beyond: New possibilities for the treatment of HER2-positive breast cancer. Oncology (Williston Park), : ; discussion , ) Ταξινόμηση του καρκίνου του μαστού Ο καρκίνος του μαστού παρουσιάζει μεγάλη ετερογένεια τόσο σε μοριακό, ιστοπαθολογικό αλλά και κλινικό επίπεδο. Η ετερογένεια σε μοριακό επίπεδο έγινε περισσότερο κατανοητή και εμφανής μετά από την ανάλυση ολόκληρου του γονιδιώματος (Whole Genome Analysis) ως προς την έκφραση του mrna μέσω της οποίας έγινε μια αδρή κατάταξη των όγκων σε 5 ομάδες (Luminal A, Luminal B, Όγκοι που υπρεκφράζουν HER-2, Basal-like και Normal-like). Καθεμία ομάδα παρουσιάζει συγκεκριμένο μοριακό φαινότυπο και κλινική πορεία [15]. Στη ρουτίνα παρόμοια κατηγοριοποίηση γίνεται με τη χρήση ανοσοϊστοχημικών δεικτών, λιγότερων σε αριθμό σε σχέση με την μοριακή προσέγγιση. Και σε αυτή την περίπτωση προκύπτουν 5 ομάδες με βάση την έκφραση των υποδοχέων 17
19 προγεστερόνης (PR), οιστρογόνων (ER), HER2, EGFR και της κερατίνης 5/6 (CK5/6) [16]. ER και/ήpr Υπερέκφραση EGFR και/ήck5/6 HER2 ΤύποςLuminal ή + A Τύπος Luminal ή + B Τύπος HER ή+ Τύπος Basallike ΤύποςNormallike Πίνακας 2: Χαρακτηριστικά των τύπων καρκίνου μαστού με βάση την μοριακή ταξινόμηση. (Subik, K., et al., The Expression Patterns of ER, PR, HER2, CK5/6, EGFR, Ki-67 and AR by Immunohistochemical Analysis in Breast Cancer Cell Lines. Breast Cancer (Auckl), : ) ΑΞΟΝΑΣ RANK-RANKL Ο υποδοχέας RANK (Receptor Activator of NFκΒ) γνωστός και ως ODFR (Osteoclast Differentiation Factor Receptor) και TRANCER (TNF-Related Activation-Induced Cytokine Receptor) ανήκει στην οικογένεια των υποδοχέων TNFR (Tumor Necrosis Factor Receptor) και ταυτοποιήθηκε για πρώτη φορά από τους Anderson et al., το 1997, όταν η ερευνητική ομάδα μελετούσε την ανοσοαπόκριση των δενδριτικών κυττάρων παρουσία των παραγόντων TNF. Ανακάλυψαν έτσι ένα νέο μόριο το οποίο παρουσίαζε 40% ομολογία με τον παράγοντα CD40 που αποτελεί επίσης μέλος της ίδιας οικογένειας. Από τις αρχικές ενδείξεις της ερευνητικής ομάδας, στις δράσεις του RANK αποδόθηκε η ρύθμιση της ανοσοαπόκρισης μέσω ελέγχου του πολλαπλασιασμού, της διαφοροποίησης, της φλεγμονής και του κυτταρικού θανάτου [17]. Ο RANK αποτελεί μια διαμεμβρανική πρωτεΐνη τύπου Ι καθηλωμένη στη μεμβράνη, το αμινοτελικό άκρο της οποίας βρίσκεται εκτεθειμένο στην εξωτερική επιφάνεια του κυττάρου και το καρβοξυτελικό άκρο της προεξέχει στο κυτταρόπλασμα. Ο υποδοχέας εντοπίζεται τόσο στην κυτταροπλασματική μεμβράνη όσο και στη μεμβράνη των μιτοχονδρίων [18]. Αποτελείται από 616 αμινοξέα εκ των οποίων τα 18
20 184 αντιστοιχούν στο εξωκυττάριο τμήμα του και τα 383 στο ενδοκυττάριο. Η πρώιμη πρωτεΐνη φέρει ένα σηματοδοτικό πεπτίδιο που εκτείνεται έως το 29 ο αμινοξύ. Η εξωκυττάρια περιοχή φέρει 4 επαναλαμβανόμενα TNFR μοτίβα πλούσια σε κυστεΐνη CRD (Cystein Rich Domain), ακολουθεί το διαμεμβρανικό τμήμα και μια μακρά κυτταροπλασματική [17]. Ο RANK κωδικοποιείται από το γονίδιο TNFRSF11A (Tumor Necrosis Factor Receptor SuperFamily 11A), βρίσκεται στη θέση q22.1 του χρωμοσώματος 18, έχει μέγεθος ζεύγη βάσεων μεταξύ των οποίων εντοπίζονται 10 εξώνια, για τα οποία είναι γνωστή η πρωτεϊνική αλληλουχία που κωδικοποιούν. Τέλος το ώριμο μετάγραφο του γονιδίου TNFRSF11A έχει βρεθεί ότι υπόκειται σε εναλλακτικό μάτισμα το οποίο οδηγεί στη μεταγραφή ισομόρφων του υποδοχέα RANK [19]. Ο προσδέτης του RANK αναγνωρίσθηκε το 1997, είναι μια κυτταροκίνη της οικογένειας TNF που αρχικά ονομάστηκε TRANCE (TNF-Related Activation- Induced Cytokine) και το γονίδιο TRANCE που το κωδικοποιεί βρίσκεται στο χρωμόσωμα 13q14 [20]. O TRANCE ή RANKL αποτελεί μια διαμεμβρανική πρωτεΐνη τύπου ΙΙ 316 αμινοξέων, η οποία συναντάται τόσο καθηλωμένη στη μεμβράνη του κυττάρου, όσο και σε διαλυτή μορφή [21]. Στο σηματοδοτικό μονοπάτι RANK-RANKL συμμετέχει και ο παράγοντας OPG (Osteoprotogerin) ή OCIF (Osteoclastogenesis Inhibitory Factor), ο οποίος ανήκει στην οικογένεια. Η πρωτεΐνη OPG δρα ανασταλτικά στην ενεργοποίηση του υποδοχέα RANK καθώς αλληλεπιδρά άμεσα με τον συνδέτη RANKL, χωρίς όμως να έχει την ικανότητα να επάγει την ενεργοποίηση του NF-κΒ και γι αυτό χαρακτηρίζεται ως ψεύδο-υποδοχέας [22]. Η μεταγωγή σήματος από το RANK ξεκινά από την πρόσδεση του RANKL, γεγονός το οποίο οδηγεί στον τριμερισμό του υποδοχέα και στη δημιουργία ενός λειτουργικού συμπλόκου [23]. Ο RANK, όπως και πολλά άλλα μέλη της οικογένειας των υποδοχέων TNF, δεν παρουσιάζει δράση κινάσης. Για το λόγο αυτό στρατολογεί συγκεκριμένα μόρια TRAF (TNF Receptor Associated Factors), για να μεταβιβάσουν το σήμα μετά τη σύνδεση με τον προσδέτη [24]. Μέσω των μορίων αυτών γίνεται ενεργοποίηση των μονοπατιών NF-κΒ, JNK (TRAF2, TRAF5, TRAF6) και p38 (TRAF2). Στην εικόνα που ακολουθεί συνοψίζονται τα σηματοδοτικά μονοπάτια που επάγονται μετά την αλληλεπίδραση RANK-RANKL. 19
21 Εικόνα 7: Σχηματική αναπαράσταση των RANK-RANKL επαγόμενων σηματοδοτικών μονοπατιών. Ο RANKL είτε καθηλωμένος στην κυτταρική μεμβράνη είτε στη διαλυτή του μορφή, προσδένεται και ενεργοποιεί τον υποδοχέα. Η διέγερση του RANK επάγει τα μονοπάτια των NF-κΒ, ΜΑΡΚ και φωσφατιδυλινοσιτόλης, μέσω των μορίων TRAFs και Gab2. Η ενεργοποίηση των NF-κΒ-Rel μπορεί να προκύψει μέσω της κανονικής οδού ΤΑΚ1-ΙΚΚβ ή μέσω του μη-κανονικού μονοπατιού ΝΙΚ-ΙΚΚα, οδηγώντας σε μεταγραφική ρύθμιση των γονιδίων στόχων που φέρουν θέσεις δέσμευσης ΝF-κΒ στον υποκινητή του γονιδίου τους. Τα μέλη της οικογένειας των ΜΑΡΚ ελέγχουν τις ΑΡ1 πρωτεΐνες (JUN, FOS, FRA), οι οποίες ρυθμίζουν την έκφραση σημαντικών παρόντων για την κυτταρική διαφοροποίηση. Το μονοπάτι της φωσφατιδυλινοσιτόλης ρυθμίζεται από τη συγχρονισμένη δράση μιας πληθώρας λιπιδικών κινασών και φωσφατασών, οδηγώντας στην ενεργοποίηση των Akt και PKC. (Wada, T., et al., RANKL-RANK signaling in osteoclastogenesis and bone disease. Trends Mol Med, : ) 20
22 Σηματοδοτικά μονοπάτια NF-κΒ: Η διέγερση του υποδοχέα RANK οδηγεί σε άμεση και έντονη επαγωγή του NF-κΒ. Η μεταγωγή σημάτων διέγερσης από τον RANK στον NF-κΒ πραγματοποιείται μέσω μορίων TRAFs τα οποία προσδένονται στο καρβοξυτελικό άκρο του υποδοχέα. Ο παράγοντας NF-κΒ αποτελεί ένα σύμπλοκο μεταξύ των πρωτεϊνών RelA ή RelB και p50 ή p52 και στην ανενεργή του κατάσταση παραμένει στο κυτταρόπλασμα σε σύνδεση με την πρωτεΐνη IκΒα. Μετά την πρόσδεση του RANKL όμως στον RANK ξεκινά ένας σηματοδοτικός καταρράκτης ο οποίος οδηγεί σε φωσφορυλίωση της ΙκΒα από την ΙΚΚ, ουβικουτινυλίωση και αποδέσμευση αυτής από τον NF-κB. Έτσι ο ενεργοποιημένος παράγοντας εισέρχεται στον πυρήνα, προσδένεται σε ειδικές νουκλεοτιδικές αλληλουχίες και επάγει τη μεταγραφή γονιδίων που ελέγχουν τον κυτταρικό πολλαπλασιασμό και την επιβίωση [25]. ΜΑΡΚ: Τα μέλη της οικογένειας των πρωτεϊνικών κινασών που ενεργοποιούνται από μιτογόνο (ΜΑΡΚ, Mitogen Activated Protein Kinase) αποτελούνται από τις p38- MAPK (α, β, γ και δ), τις c-jun Ν-τελικές κινάσες 1, 2 και 3 (JNK, c-jun N-terminal Kinase), τις εξωκυττάριες ρυθμιζόμενες από σηματοδότηση κινάσες 1 και 2 (ERK, Extracellular Signal-Regulated Kinases) καθώς και τις ERK5, ERK7, ERK8. Η ενεργοποίηση τους από το δίπτυχο RANK-RANKL πραγματοποιείται μέσω φωσφορυλίωσης σε κατάλοιπα σερίνης-θρεονίνης από μια ΜΕΚ κινάση, η οποία με τη σειρά της έχει ενεργοποιηθεί από τη Raf-1. Η επαγωγή του μονοπατιού ΜΑΡΚ οδηγεί σε αύξηση της κυτταρικής επιβίωσης [26]. Src: Πριν την ταυτοποίηση του RANK ήταν γνωστό ότι στοχευμένη αναστολή του c- src πρώτο-ογκογονιδίου οδηγεί σε οστεοπέτρωση στα ποντίκια. Αργότερα βρέθηκε ότι ο παράγοντας c-src είναι απαραίτητος για την επαγόμενη από RANK ενεργοποίηση του μονοπατιού της αντί-αποπτωτικής πρωτεΐνης Akt/PKB. Τα μόρια c-src και TRAF6 αλληλεπιδρούν μεταξύ τους και με τον υποδοχέα. Μεταβολισμός φωσφατιδυλινοσιτόλης: Σημαντικό ρόλο στην ικανότητα σηματοδότησης του υποδοχέα RANK παίζει ο μεταβολισμός των λιπιδίων ινοσιτόλης. Η ενεργοποίηση της Akt από τoν Src απαιτεί την κινάση ΡΙ3Κ η οποία οδηγεί στο σχηματισμό των μορίων PtdIns(3,4,5)P3 και PDK1. Συγκεκριμένα 21
23 αναστολή της PI3K οδηγεί σε ανώμαλη οστική αποδόμηση από τους οστεοκλάστες, υπογραμμίζοντας το ρόλο του μορίου στη σηματοδοτική ικανότητα του υποδοχέα. Akt/PI3K: Το μονοπάτι Akt/PI3K ρυθμίζει τον κυτταρικό θάνατο, μέσω μεταφοράς αντί-αποπτωτικών σημάτων από πληθώρα διεγερτικών μορίων, όπως είναι αυξητικοί παράγοντες, κυτοκίνες και η αλληλεπίδραση κυττάρων-μήτρας. Η κινάση της 3- φωσφατιδυλινοσιτόλης οδηγεί στην παραγωγή D3-φωσφορυλιωμένων φωσφοϊνοσιτιδίων, τα οποία στρατολογούν την Akt στην πλασματική μεμβράνη, όπου μεταφέρεται και η κινάση PDK-1, η οποία την ενεργοποιεί. Η πρόσδεση της Akt στη μεμβράνη γίνεται μέσω της περιοχής ομολογίας πλεκστρίνης. Η θέση αυτή είναι υπέυθυνη για αλλαγές που συμβαίνουν στο μόριο της PDK-1, οι οποίες της δίνουν τη δυνατότητα να φωσφορυλιώσει την Akt στη θέση Thr308 [27]. Φυσιολογική λειτουργία RANK/RANKL Ρύθμιση της ομοιόστασης του οστού: Για τη διατήρηση της ομοιόστασης του οστού σημαντική είναι η ισορροπία μεταξύ δύο κυτταρικών ομάδων, των οστεοβλαστών που συνθέτουν νέο οστό και των οστεοκλαστών που το αποδομούν. Οι οστεοβλάστες φαίνεται να συμβάλλουν στην ωρίμανση των οστεοκλαστών από την πρώιμη μορφή τους, όπως παρατήρησαν το 1999 μέσω της έκκρισης του RANKL [18]. Το πρόσδεμα συνδέεται με τον RANK υποδοχέα που βρίσκεται στην επιφάνεια των οστεοκλαστών, έπειτα από κυτταρική επαφή. Η σύνδεση RANK-RANKL οδηγεί ένα σηματοδοτικό καταρράκτη όπου ενεργοποιούνται οι παράγοντες NF-κΒ και JNK. Παρουσία του παράγοντα MCSF οι πρώιμοι οστεοκλάστες είναι δυνατόν να πάρουν την ώριμη μορφή τους η οποία τους επιτρέπει να προχωρήσουν στην έκκριση οστεολυτικών ενζύμων και τελικά στην αποδόμηση του οστού. Ρύθμιση της ανοσολογικής απόκρισης μέσω των δενδριτικών κυττάρων: Τα δενδριτικά κύτταρα παραμένουν ανενεργά έως ότου δεχθούν κάποιο φλεγμονώδες ερέθισμα οπότε μεταφέρονται στους λεμφαδένες, όπου ενεργοποιούν τα Τ λεμφοκύτταρα.. Ο ρόλος της έκφρασης του RANK στα δενδριτικά κύτταρα έγκειται κυρίως στη διατήρηση του πληθυσμού και της επιβίωσης τους, καθώς έχουν πολύ μικρό χρόνο ζωής. Η έκφραση του υποδοχέα επάγεται στα δενδριτικά κύτταρα κατά τη διάρκεια της ωρίμανσης τους και υπό την επίδραση του RANKL οδηγεί σε έκκριση προφλεγμονωδών κυτοκινών, συντελώντας έτσι στην επιβίωση τους. 22
24 Ταυτόχρονα επάγεται η έκφραση της αντί-αποπτωτικής πρωτεΐνης Βcl-xL μέσω των p50 και c-rel παραγόντων του NF-κB, οδηγώντας στο ίδιο αποτέλεσμα. Ακόμα η σύνδεση του RANKL στον υποδοχέα ενεργοποιεί το μονοπάτι της αντί-αποπτωτικής κινάσης σερίνης/θρεονίνης Akt/PKB μέσω στρατολόγησης των ΡΙ3-Κ και Cb1-b από την TRAF6 και RANKL, αντίστοιχα [28]. Ρύθμιση της θερμοκρασίας του σώματος: Ο ρόλος του RANK στον εγκέφαλο ανακαλύφθηκε μόλις το 2009, όταν οι Penninger et al., εισήγαγαν εξωγενώς RANKL στον εγκέφαλο αρουραίων και παρατήρησαν αύξηση της θερμοκρασίας του σώματος και την εμφάνιση πυρετού. Βρέθηκε ότι ο RANKL ενεργοποιεί περιοχές του εγκεφάλου οι οποίες συμμετέχουν στη θερμορύθμιση και επάγουν την εμφάνιση πυρετού μέσω του μονοπατιού COX2-PGE2/EP3R. Στο ίδιο συμπέρασμα σχετικά με τον έλεγχο της θερμοκρασίας του σώματος, οδηγούν και δεδομένα από δύο ασθενείς νεαρής ηλικίας οι οποίοι δεν εμφάνισαν πυρετό ενώ έπασχαν από πνευμονία και ταυτόχρονα έφεραν μεταλλάξεις στο γονίδιο TNFRSF11A (οστεοπέτρωση βαριάς μορφής) [29]. Ρύθμιση της φυσιολογικής ανάπτυξης του μαστού: Από μελέτες που πραγματοποιήθηκαν σε ποντίκια με ανεπάρκεια έκφρασης RANKL, βρέθηκε ότι ενώ τα θηλυκά μπορούσαν να ωριμάσουν σεξουαλικά και να δώσουν απογόνους, τα μικρά τους πέθαιναν. Στην περίπτωση όμως που τα νεογνά δίνονταν σε φυσιολογικές μητέρες για να τα θηλάσουν κατάφερναν να επιβιώσουν. Η παρατήρηση αυτή οδήγησε στο συμπέρασμα ότι η απουσία έκφρασης RANKL δεν επιτρέπει την φυσιολογική ανάπτυξη των μαστών στα θηλυκά κατά την εγκυμοσύνη, κι έτσι ο λόγος που τα νεογνά πέθαιναν ήταν η έλλειψη τροφής [30]. Σε φυσιολογικά ποντίκια ο υποδοχέας RANK εκφράζεται συνεχώς σε όλο τον μαστικό αδένα. Αντίθετα έκφραση του RANKL είναι ορμονο-επαγόμενη στο μαστικό επιθήλιο, σε επίπεδα που ανιχνεύονται την 12,5 ημέρα εγκυμοσύνης και φτάνουν στο μέγιστο κατά την πρώτη ημέρα του θηλασμού. Πειράματα σε RANKL knockout ποντίκια, στα οποία έγινε τοπική χορήγηση RANKL στους μαστικούς αδένες πριν την περίοδο της εγκυμοσύνης, οδήγησαν στη φυσιολογική ανάπτυξη του μαστού, γεγονός που υποδεικνύει ότι ο προσδέτης RANKL δεν είναι απαραίτητος για την πρώιμη ανάπτυξη των μαστών αλλά για την ανάπτυξη κατά την εγκυμοσύνη. Αυτή η 23
25 ανάπτυξη του μαστικού επιθηλίου από το μονοπάτι RANK-RANKLείναι αποτέλεσμα αναστολής της απόπτωσης μέσω ενεργοποίησης του μονοπατιού Akt/PKB [30]. RANK/RANKL και καρκίνος Το γεγονός ότι το μονοπάτι RANK/RANKL ελέγχει τον πολλαπλασιασμό και τη διαφοροποίηση των κυττάρων του μαστικού επιθηλίου, οδήγησε στην υπόθεση ότι πιθανώς εμπλέκεται και στην ανάπτυξη καρκίνου του μαστού. Για να διερευνηθεί αυτή η θεωρία, χρησιμοποιήθηκαν πειραματόζωα στα οποία προκλήθηκαν τεχνητά όγκοι με τη χρήση ορμονών. Στα ζώα αυτά είχε προηγηθεί απαλοιφή του γονιδίου του RANK στα κύτταρα του μαστικού επιθηλίου. Όταν χορηγήθηκε το συνθετικό ανάλογο προγεστερόνης ΜΡΑ παράλληλα με τον παράγοντα DMBA που καταστρέφει το DNA, τα ζώα στα οποία το γονίδιο του RANK είχε απαλειφτεί καθυστέρησαν την ανάπτυξη όγκων στο μαστό σε σχέση με την ομάδα ελέγχου. Το ΜΡΑ δρα αυξάνοντας έως και 3000 φορές τα μόρια RANKL στο μαστικό επιθήλιο, ενισχύοντας έτσι και τη σηματοδοτική ικανότητα του μονοπατιού RANK-RANKL και τελικά οδηγεί σε αυξημένο κυτταρικό πολλαπλασιασμό. Μία ακόμη παρατήρηση που ενισχύει την υπόθεση συμμετοχής του RANKL στο σχηματισμό κακοηθειών αποτελεί η ανοχή στον κυτταρικό θάνατο από γ-ακτινοβολία στα κύτταρα τα οποία υπερέκφραζαν RANKL. Η ιδιότητα αυτή αποτελεί χαρακτηριστικό των κακοηθών όγκων [31]. Σε επόμενη μελέτη προκλήθηκε εξωγενώς η υπερέκφραση του RANK στο μαστικό αδένα, γεγονός που ευαισθητοποίησε τα κύτταρα αυτά σε καρκίνους μαστού επαγόμενους από ΜΡΑ/DMBA ακόμα στα ίδια πειραματόζωα προκλήθηκαν όγκοι στους μαστούς έπειτα από εγκυμοσύνη, οι οποίοι περιορίζονταν σε ένα ποσοστό 90% έπειτα από αποκλεισμό του RANKL. Οι δύο αυτές μελέτες απέδειξαν ότι το ζεύγος RANK/RANKL ελέγχει την ορμονο-εξαρτώμενη εμφάνιση καρκίνου μαστού [32]. Ο υποδοχέας RANK με τον προσδέτη του συμμετέχουν επίσης στην μετάσταση του καρκίνου του μαστού. Οι πρώτες παρατηρήσεις έγιναν από τους Jones et al., οι οποίοι διέγειραν καρκινικές σειρές μαστού με μόρια RANKL και παρατήρησαν ότι η ικανότητα μετάστασης αυξάνεται ανάλογα με την συγκέντρωση του προσδέτη [33]. Η ίδια παρατήρηση δεν επιβεβαιώθηκε σε καρκινικές σειρές οι οποίες δεν εκφράζουν τον υποδοχέα RANK. Ακόμα όταν οι κυτταρικές σειρές καρκίνου μαστού καλλιεργήθηκαν παρουσία RANKL παρατηρήθηκε ισχυρός πολυμερισμός ακτίνης, ο 24
26 οποίος μπορούσε να ανασταλεί με την προσθήκη OPG. Ο πολυμερισμός αυτός αποτελεί εναρκτήριο γεγονός στη διαδικασία της μετάστασης των κυττάρων. Το 2006 οι Penninger et al., απέδειξαν ότι ο RANKL πυροδοτεί την οστική μετάσταση των ανθρώπινων επιθηλιακών κυττάρων και των κυττάρων μελανώματος που εκφράζουν RANK [33]. Ο λόγος που υπάρχει προτίμηση από ορισμένους όγκους να δίνουν μεταστάσεις στα οστά πιθανότατα οφείλεται στο περιβάλλον που δημιουργεί η αποσύνθεση του οστού, καθώς παρέχει τα απαραίτητα θρεπτικά συστατικά στα καρκινικά κύτταρα. Ταυτόχρονα τα ίδια τα κύτταρα του όγκου εκκρίνουν μόρια όπως ο παράγοντας PTHrP, τα οποία περεταίρω οδηγούν σε αποδόμηση του οστού και τη συνεπακόλουθη αύξηση του όγκου. Ακόμη ο καρκίνος του μαστού φαίνεται να δίνει μεταστάσεις με βάση χημειοτακτικά μόρια τα οποία εκφράζονται στον ιστό-στόχο. Συγκεκριμένα τα επιθηλιακά κύτταρα του καρκίνου του μαστού εκκρίνουν τον υποδοχέα χυμοκινών CXCR4, ο προσδέτης του οποίου (SDF-1α) εντοπίζεται σε ιστούς όπου συνήθως εμφανίζεται η μετάσταση. Ωστόσο αναστολή των χημοκινών περιορίζει μερικώς τη μετάσταση στους ασθενείς και για το λόγο αυτό ενισχύεται η υπόθεση ότι εμπλέκονται κι άλλοι παράγοντες. Ο RANKL λοιπόν, εκφράζεται σε πολύ μεγάλο βαθμό στο περιβάλλον των οστών, ενώ παράλληλα αυξημένη έκφραση του υποδοχέα του εντοπίζεται σε επιθηλιακούς όγκους και στο μελάνωμα, δικαιολογώντας έτσι την προτίμηση που δείχνουν. Μάλιστα η χορήγηση αντί-rankl θεραπείας και η εν δυνάμει αναστολή του μονοπατιού RANK-RANKL σε ασθενείς με καρκίνο μαστού και προστάτη που εξέφραζαν RANK φάνηκε αρκετά επωφελής καθώς μείωνε σε σημαντικό βαθμό την ικανότητα μετανάστευσης των καρκινικών κυττάρων [33]. Άξονας EGFR-EGF Ο EGFR (Epidermal Growth Factor Receptor) ανήκει στην υπεροικογένεια των υποδοχέων με δράση κινάσης τυροσίνης HER (Human Epidermal Growth Factor Receptor) ή ErbΒ, μαζί με τους ErbB2 (HER2/Neu), ErbB3 (HER3) και ErbB4 (HER4). Η ταυτοποίηση του υποδοχέα έγινε το 1980 από τους Shimizu et al., κατά τη διάρκεια της μελέτης του μορίου-προσδέτη EGF σε υβρίδια κυττάρων ανθρώπουποντικού. Οι ερευνητές παρατήρησαν ότι η ικανότητα των κυττάρων αυτών να δεσμεύσουν EGF στην επιφάνεια τους εξαρτιόταν από την παρουσία μιας πρωτεΐνης, ο γονιδιακός τόπος της οποίας βρισκόταν στο χρωμόσωμα 7p11.2. Περαιτέρω 25
27 ανάλυση του μορίου αποκάλυψε ότι πρόκειται για μια διαμεμβρανική γλυκοπρωτεΐνη που λειτουργεί ως υποδοχέας για τον EGF, εξ ου και το όνομα που έλαβε [34]. Ο EGFR αποτελεί μια μεγαλομοριακή διαμεμβρανική γλυκοπρωτεΐνη μοριακού βάρους 170kDa. Το πρωτεϊνικό μόριο του υποδοχέα αποτελείται από ένα εξωκυττάριο αμινοτελικό άκρο πλούσιο σε κυστεΐνη, το οποίο φέρει τη θέση δέσμευσης του προσδέτη και ένα βραχίονα διμερισμού, μια υδρόφοβη διαμεμβρανική περιοχή και μια ενδοκυττάρια, ιδιαιτέρως συντηρημένη κυτταροπλασματική καρβοξυτελική περιοχή με θέση κινάσης τυροσίνης με πολλαπλές θέσεις φωσφορυλίωσης. Ενώ το ενδοκυττάριο τμήμα του υποδοχέα παρουσιάζει υψηλή συντήρηση, η εξωκυττάρια περιοχή του φέρει πολυμορφική δομή, επιτρέποντας έτσι την αλληλεπίδραση με πολυάριθμα προσδέματα [35]. Το εξωκυττάριο τμήμα διακρίνεται σε τέσσερεις περιοχές Ι, ΙΙ, ΙΙΙ και ΙV και μπορεί να λαμβάνει κλειστή ή ανοιχτή διαμόρφωση. Στην κλειστή διαμόρφωση υπάρχει αλληλεπίδραση μεταξύ ΙΙ και ΙV, ώστε οι I και ΙΙΙ να μην αλληλεπιδρούν και ο υποδοχέας είναι ανενεργός. Στην ανοιχτή διαμόρφωση οι ΙΙ και IV απομακρύνονται, οι Ι και ΙΙΙ εκθέτουν τη θέση δέσμευσης προσδέματος και αλληλεπιδρούν με το εν λόγω πρόσδεμα, οπότε ο υποδοχέας θεωρείται ενεργός [36]. O EGFR μπορεί να επάγει την κυτταρική σηματοδότηση είτε μόνος του, μέσω ομοδιμερισμού είτε μέσω ετεροδιμερισμού συνεργαζόμενος με άλλα μέλη της ίδιας οικογένειας. Συγκεκριμένα προσδέματα επάγουν είτε τον ομοδιμερισμό είτε τον ετεροδιμερισμό. Για παράδειγμα ο EGF επάγει τον ετεροδιμερισμό του EGFR με τον HER2, HER3 και HER4. Ο EGFR κωδικοποιείται από το γονίδιο ERBB1 το οποίο βρίσκεται στο χρωμόσωμα 7, έχει μέγεθος περίπου ζεύγη βάσεων και αποτελείται από 28 εξώνια. Ο χαρακτηρισμός των εξωνίων του υποδοχέα αποκάλυψε ότι το εξώνιο 1 κωδικοποιεί την 5 UTR αλληλουχία, το σηματοδοτικό πεπτίδιο καθώς και τα 5 πρώτα αμινοξέα του ώριμου EGFR υποδοχέα. Η εξωκυττάρια αλληλουχία κωδικοποιείται από τα εξώνια 2-16, ενώ οι δύο πλούσιες σε κυστεΐνη περιοχές κωδικοποιούνται από τα εξώνια 5-7 και 13-16, αντίστοιχα. Η διαμεμβρανική περιοχή κωδικοποιείται από το εξώνιο 17, η περιοχή κινάσης τυροσίνης από τα εξώνια 18-24, ενώ το καρβοξυτελικό άκρο από τα εξώνια [37]. 26
28 Τα προσδέματα που αναγνωρίζονται ειδικά από τον EGFR ορίζονται ως EGF αγωνιστές και ενεργοποιούν τον υποδοχέα. Υπάρχουν τουλάχιστον 7 διαφορετικοί EGF αγωνιστές, οι οποίοι ονομάζονται EGF, TGFα (Transforming Growth Factor α), αμφιρεγκουλίνη (AR), βήτασελουλίνη (ΒΤC), επιγένη (ΕΡΝ), επιρεγκουλίνη (EPR) και heparin binding EGF-like growth factor (HB-EGF) [36]. Οι EGF αγωνιστές αρχικά συντίθενται ως τύπου Ι διαμεμβρανικές πρωτεΐνες, που συνιστώνται από ένα αμινοτελικό άκρο, ένα EGF μοτίβο, ένα μικρό παραμεμβρανικό στέλεχος, μια υδρόφοβη διαμεμβρανική περιοχή και ένα καρβοξυτελικό άκρο. Ακολουθεί πρωτεολυτική διεργασία μέσω της οποίας αποκόπτονται από τη μεμβράνη και απελευθερώνονται στο κυτταρόπλασμα ως διαλυτοί παράγοντες. Η διάσπαση και απελευθέρωση των EGFR προσδεμάτων πραγματοποιείται από τις ADAM πρωτεΐνες, οι οποίες αποτελούν μεταλλοπρωτεϊνάσες καθηλωμένες στη μεμβράνη [38]. Η πρόσδεση του EGF αγωνιστή στον EGFR οδηγεί στο σχηματισμό ενός ασύμμετρου διμερούς συμπλόκου με δράση κινάσης τυροσίνης [39]. Τα ενεργά διμερή υπόκεινται σε αυτοφωσφορυλίωση των καταλοίπων τυροσίνης στην κυτταροπλασματική ουρά του υποδοχέα. Η κινάση EGFR καταλύει τη μεταφορά του γ-φωσφορικού του δεσμευμένου ΑΤΡ, στα κατάλοιπα τυροσίνης εξωγενών υποστρωμάτων. Ως αποτέλεσμα στρατολογούνται πρωτεΐνες που προσδένονται στις φωσφοτυροσίνες και ενεργοποιούν σηματοδοτικούς καταρράκτες, όπως είναι αυτός των ΜΑΡ κινασών, το μονοπάτι της 3-φωσφοϊνοσιτιδική κινάση (ΡΙ3Κ) που στρατολογεί το σύμπλοκο Akt/PKB στην πλασματική μεμβράνη και το μονοπάτι της φωσφολιπάσης Cγ, που αλληλεπιδρά άμεσα με τον EGFR και οδηγεί στην ενεργοποίηση της πρωτεϊνικής κινάσης C (PKC) [40]. Σηματοδοτικά μονοπάτια ΜΑΡΚ: Η ενεργοποίηση του EGFR οδηγεί σε αυτοφωσφορυλίωση της περιοχής κινάσης, καθιστώντας δυνατή την πρόσδεση του Grb2 στο μόριο του υποδοχέα [41]. Έπειτα στον Grb2 προσδένεται το μόριο Sos, το οποίο αλληλεπιδρά με την πρωτεΐνη Ras, η οποία βρίσκεται καθηλωμένη στη μεμβράνη. Η αλληλεπίδραση Sos-Ras οδηγεί στην ανταλλαγή GDP για GTP και τελικά στην ενεργοποίηση του Ras. Ο ενεργοποιημένος Ras οδηγεί με τη σειρά του σε ενεργοποίηση της κινάσης σερίνης/θρεονίνης Raf-1, οδηγώντας σε φωσφορυλίωση, ενεργοποίηση και πυρηνική μετατόπιση των Erk-1και Erk-2, οι οποίες καταλύουν τη φωσφορυλίωση πυρηνικών 27
29 παραγόντων. Η επαγωγή των ΜΑΡ κινασών παρέχει την ίδια στιγμή αρνητική ανατροφοδότηση στο μονοπάτι, διότι η φωσφορυλίωση τους οδηγεί σε αποδέσμευση του Sos από το σύμπλοκο [42]. Οι ενεργοποιημένες ΜΑΡΚ εισέρχονται στον πυρήνα, όπου φωσφορυλιώνουν πληθώρα μεταγραφικών παραγόντων, οι οποίοι εμπλέκονται στον κυτταρικό πολλαπλασιασμό. ΡΙ3-Κ/ΑΚΤ: Η διέγερση ενός κυττάρου με EGF προκαλεί στον μεταβολισμό των φωσφολιπιδίων του και οδηγεί σε αλλαγές της φωσφατιδυλινοσιτόλης καθώς και παραγωγική φωσφατιδικού (ΡΑ) και αραχιδονικού οξέος (ΑΑ) [43]. Από τα ένζυμα που συμμετέχουν στις διαδικασίες αυτές, τουλάχιστον τρία βρίσκονται υπό τον άμεσο έλεγχο του EGFR, μεταξύ των οποίων η φωσφολιπάση C-γ (PLCγ), η 3-κινάση της φωσφατιδυλινοσιτόλης (ΡΙ3-Κ) και η φωσφολιπάση D (PLD) [44]. Οι κινάσες ΡΙ3Κ ελέγχουν σημαντικές κυτταρικές λειτουργίες όπως είναι ο πολλαπλασιασμός, η επιβίωση, η προσκόλληση και η μετανάστευση. Η ΡΙ3Κ είναι ένα διμερές ένζυμο που αποτελείται από μια ρυθμιστική υπομονάδα p85, και μια καταλυτική υπομονάδα p110. Συγκεκριμένα η κινάση ΡΙ3Κ Ιa οδηγεί στη δημιουργία του δευτερογενούς μηνύματος ΡΙΡ3, το οποίο προσδένεται στην κινάση σερίνης/θρεονίνης Akt (PKB) και την μεταφέρει στην πλασματική μεμβράνη [45]. Η Akt εκεί φωσφορυλιώνεται, ενεργοποιείται και ελέγχει τον κυτταρικό πολλαπλασιασμό και την επιβίωση μέσω της ΡΙ3Κ, συμμετέχοντας έτσι στην αντι-αποπτωτική δράση του EGFR [46]. JAK/STAT: Η σηματοδότηση μέσω του EGFR ξεκινά με την πρόσδεση των JAK κινασών τυροσίνης στο κυτταροπλασματικό μέρος του ομοδιμερούς. Τα μόρια αυτά στο καρβοξυτελικό τους άκρο φέρουν μια καταλυτική ρυθμιστική θέση και μια θέση με δράση κινάσης τυροσίνης. Η ενεργοποίηση των JAKs ξεκινά μετά από τον διμερισμό του υποδοχέα, έτσι ώστε δύο μόρια JAK κινασών να πλησιάσουν μεταξύ τους και να πραγματοποιηθεί trans-φωσφορυλίωση. Οι ενεργοποιημένες JAKs φωσφορυλιώνουν με τη σειρά τους, τους μεταγραφικούς παράγοντες STATs, οι οποίοι διατηρούνται ανενεργοί στο κυτταρόπλασμα μέχρι να ενεργοποιηθούν. Φωσφορυλίωση του κατάλοιπου τυροσίνης που φέρουν στο καρβοξυτελικό τους άκρο προκαλεί διμερισμό των STATs μέσω αλληλεπίδρασης με μια συντηρημένη SH2 αλληλουχία. Οι φωσφορυλιωμένοι παράγοντες STATs εισέρχονται στον πυρήνα του κυττάρου και προσδένονται σε ρυθμιστικές αλληλουχίες. Κατ αυτό τον τρόπο η ενεργοποίηση των STATs μέσω του EGFR είναι ικανή να ενεργοποιήσει ή να 28
30 καταστείλει τη μεταγραφή γονιδίων-στόχων τα οποία ελέγχουν τον πολλαπλασιασμό, τη διαφοροποίηση, τη μετανάστευση και την απόπτωση [47]. Εικόνα 8: Εκκίνηση σηματοδοτικών μονοπατιών από τον υποδοχέα EGFR μετά από τη δέσμευση του προσδέματος EGF κ.α. (Janku, F., D.J. Stewart, and R. Kurzrock, Targeted therapy in non-small-cell lung cancer--is it becoming a reality? Nat Rev Clin Oncol, : ) Φυσιολογική λειτουργία EGFR-EGF Ο ενεργοποιημένος EGFR είναι γνωστό ότι ελέγχει φυσιολογικές διαδικασίες όπως είναι ο κυτταρικός πολλαπλασιασμός, η διαφοροποίηση, η μετανάστευση και η επιβίωση. Η σημασία της έκφρασης του υποδοχέα στη φυσιολογική κυτταρική λειτουργία και στην ανάπτυξη φαίνεται από πειράματα που έχουν γίνει σε γενετικά τροποποιημένους μύες ποντίκια. Φυσιολογικά το σύστημα EGFR/EGF συμμετέχει στην πρώιμη εμβρυική ανάπτυξη και στην ανανέωση των βλαστικών κυττάρων σε φυσιολογικούς ιστούς, όπως είναι το δέρμα, το ήπαρ και το έντερο. Έτσι μεταλλάξεις 29
31 αποσιώπησης στο γονιδιακό τόπο του EGFR είναι τις περισσότερες φορές θανατηφόρες είτε κατά το στάδιο της κύησης είτε στα νεογνά, τα οποία παρουσιάζουν ανωμαλίες σε μεγάλο αριθμό οργάνων, συμπεριλαμβανομένου του εγκεφάλου, του δέρματος, του πνεύμονα, και της γαστρεντερικής οδού. Ο ρόλος του υποδοχέα είναι επίσης σημαντικός και στην ενήλικη ζωή. Ο μαστικός αδένας είναι ένα όργανο στο οποίο ο κυτταρικός πολλαπλασιασμός και η διαφοροποίηση συμβαίνουν κυρίως μεταγεννητικά. Κατά τη γέννηση ο μαστός φέρει ένα στοιχειώδες μόνο σύστημα λοβών, το οποίο υπόκειται σε εκτενή ανάπτυξη κατά τη διάρκεια της εφηβείας και της εγκυμοσύνης υπό την επήρεια στεροειδών και πεπτιδικών ορμονών. Σε όλη αυτή τη διαδρομή ανάπτυξης και διαφοροποίησης του αδένα παρατηρείται έκφραση του υποδοχέα με διαφορετικό μοτίβο ανάλογα με το εκάστοτε στάδιο. Διαγονιδιακά ποντίκια τα οποία φέρουν μετάλλαξη στη θέση κινάσης τυροσίνης του υποδοχέα δεν είναι ικανά να σχηματίσουν φυσιολογικούς μαστικούς λοβούς. EGFR-EGF και καρκίνος Σε ένα μεγάλο αριθμό νεοπλασιών έχει παρατηρηθεί διαταραγμένη έκφραση των επιπέδων του EGFR, λόγω υπερέκφρασης ή μεταλλάξεων. Αυξημένη σηματοδότηση μέσω του υποδοχέα είναι δυνατό να επάγει τον ανεξέλεγκτο πολλαπλασιασμό και να οδηγήσει σε νεοπλασματικό φαινότυπο. Η γονιδιακή ενίσχυση του EGFR παρατηρείται σε μεγάλο ποσοστό όγκων και μάλιστα στο γλοιοβλάστωμα αγγίζει το 40%, ενώ έχει παρατηρηθεί και σε άλλους όγκους όπως είναι ο καρκίνος του μαστού, της ουροδόχου, των νεφρών, των ωοθηκών και των πνευμόνων. Από πειράματα που έγιναν σε καρκινική σειρά οισοφάγου, όπου τα κύτταρα καλλιεργήθηκαν παρουσία EGF παρατηρήθηκε ότι επήλθαν αλλαγές τόσο μορφολογικές όσο και στα επίπεδα φωσφορυλίωσης της β-κατενίνης των κυττάρων. Σε διαφορετική σειρά καρκίνου του παχέος εντέρου, η οποία καλλιεργήθηκε παρουσία EGF και TGF-α, προκλήθηκε μείωση της E-καντχερίνης και αύξηση της α2-ιντεγκρίνης, του καρκινοεμβρυιονικού αντιγόνου (CEA, CarcinoEmbryonic Antigen) και του CD44, που όλα αποτελούν δείκτες αυξημένης μεταστατικότητας. Η μείωση της E-καντχερίνης οδηγεί σε μειωμένη προσκόλληση μεταξύ των κυττάρων, ενισχύοντας έτσι την αποκόλληση 30
32 των κυττάρων από τον αρχικό όγκο. Παράλληλα η αυξημένη παρουσία ιντεγκρίνης και CEA ενισχύει την προσκόλληση και την εξάπλωση των κυττάρων μέσω της εξωκυττάριας ουσίας, ενώ η υψηλή έκφραση CD44 ενισχύει την προσκόλληση των νεοπλασματικών κυττάρων στα ενδοθηλιακά κύτταρα και επάγει την εξαγγείωση τους και την πρόσβαση στην αιματική κυκλοφορία [48]. Πρόσφατα έχει αναδειχθεί ο ρόλος του EGFR και των προσδεμάτων του στον καρκίνο του μαστού. Κάποια δείγματα ανοσοϊστοχημείας υποστηρίζουν ότι ο EGFR υπερεκφράζεται σε πρωτογενείς όγκους και μάλιστα αποτελεί κακό προγνωστικό δείκτη, ενώ άλλες μελέτες δε βρίσκουν καμία πιθανή συσχέτιση. Στον τριπλά αρνητικά καρκίνο του μαστού, όπου δεν εκφράζονται οι υποδοχείς προγεστερόνης, οιστρογόνων και ο HER2, έχει παρατηρηθεί αυξημένη έκφραση του EGFR στο 50-70% αυτών. Ακόμα, στην ίδια ομάδα όγκων παρατηρείται αυξημένη έκφραση των EGFR προσδεμάτων όπως είναι ο TGFα και ο NRG2β, καθώς και των ADAMs και μεταλλοπρωτεϊνασών που είναι υπεύθυνες για την ωρίμανση των προσδεμάτων αυτών. Θετική συσχέτιση έχει αναγνωρισθεί και μεταξύ της έκφρασης του EGFR και του πληθυσμού των βλαστικών καρκινικών κυττάρων στο μαστό. Σε φυσιολογικό ιστό ή σε όγκους που εκφράζουν τον οιστρογονικό υποδοχέα ERα, όπου η έκφραση του EGFR είναι χαμηλή, ο βλαστικός πληθυσμός είναι επίσης μικρός. Αντίθετα στον τριπλά αρνητικά καρκίνο του μαστού, η αυξημένη έκφραση του EGFR συνοδεύεται από μεγαλύτερο αριθμό βλαστικών κυττάρων, ένδειξη της κακοήθειας του όγκου [49]. Σε ένα ορισμένους ασθενείς εμφανίζεται μετάσταση στα οστά μετά τη θεραπεία και τη λήψη αγωγής. Αυτό οφείλεται στην ύπαρξη ενός μικρού αριθμού διασπειρόμενων καρκινικών κυττάρων (DCCs, Disseminated Cancer Cells) που παρατηρούνται στο μυελό των οστών των ασθενών. Στα κύτταρα αυτά παρατηρείται αυξημένη έκφραση των υποδοχέων EGFR και HER2, υποδεικνύοντας έτσι μια συσχέτιση της έκφρασης τους με την ύπαρξη κυττάρων βλαστικού τύπου στον όγκο [50]. Ένα σημαντικό μοντέλο για την κατανόηση της μετάστασης στα οστά που παρατηρείται σε ασθενείς με καρκίνο του μαστού είναι τα κύτταρα MDA-MB-231, τα οποία χαρακτηρίζονται ως Basal-like ERα-αρνητικά. Tο εν λόγω πείραμα υποστηρίζει ότι τα καρκινικά κύτταρα στο μαστό ελέγχουν και καθοδηγούν τα κύτταρα που βρίσκονται στα οστά, με τρόπο τέτοιο ώστε να απορρυθμίζεται η φυσιολογική αποδόμηση του οστού και η 31
33 παραγωγή νέου. Τα MDA-MB-231 παράγουν κυτοκίνες και αυξητικούς παράγοντες που επηρεάζουν τη λειτουργία τόσο των οστεοβλαστών όσο και των οστεοκλαστών στα οστά. Η ωρίμανση των οστεοκλαστών, όπως ήδη αναφέρθηκε διαμεσολαβείται από το σύστημα RANK-RANKL. Οι οστεοβλάστες εκτός από RANKL και OPG εκκρίνουν και CSF-1 (Colony-Stimulating Factor-1), ένα μόριο το οποίο στρατολογεί μονοκύτταρα από τον μυελό των οστών και προκαλεί τη διαφοροποίηση τους σε οστεοκλάστες παρουσία υψηλής συγκέντρωσης RANKL. Τα καρκινικά κύτταρα του μαστού παράγουν κυτοκίνες οι οποίες απορρυθμίζουν την ισορροπία RANKL/OPG και αυξάνουν τον αριθμό των μονοκυττάρων που διαφοροποιούνται σε οστεοκλάστες. Στην οστεόλυση σημαντικό ρόλο παίζει η έκφραση του EGFR από τους οστεοβλάστες, καθώς από μελέτες που έγιναν με αναστολείς των κινασών τυροσίνης παρατηρήθηκε μείωση της έκφρασης του RANKL. Έτσι η σηματοδότηση μέσω του υποδοχέα EGFR στους οστεοβλάστες επάγει την οστεοκλαστογένεση μέσω απορρύθμισης της ισορροπίας RANK/RANKL [51]. Ακόμα οι Tacghee et al., [52] διερεύνησαν τους μοριακούς μηχανισμούς πίσω από τη ρύθμιση της οστεοκλαστογένεσης μέσω του EGFR. Μελέτησαν το ρόλο του σηματοδοτικού μονοπατιού του EGFR στη διαφοροποίηση και την επιβίωση των οστεοκλαστών και παρατήρησαν ότι η έκφραση του υποδοχέα ενισχύεται σημαντικά από τον παράγοντα RANKL. Παράλληλα η χρήση αναστολέων κινάσης τυροσίνης και αποσιώπηση του γονιδίου του EGFR απέτρεπε την εξαρτώμενη από RANKL δημιουργία οστεοκλαστών, υπογραμμίζοντας έτσι το ρόλο του EGFR στην οστεοκλαστογένεση. Υποδοχείς RANK EGFR και θεραπεία Αναστολείς του μονοπατιού RANK-RANKL Denosumab: Το Denosumab αποτελεί ένα πλήρως ανθρώπινο IgG2 μονοκλωνικό αντίσωμα το οποίο προσδένεται και αναστέλλει το πρόσδεμα RANKL, έτσι ώστε να μην μπορεί να αλληλεπιδράσει με τον υποδοχέα του στην επιφάνεια των οστεοκλαστών και των προγονικών τους κυττάρων. Όπως ήδη αναφέρθηκε ο RANKL είναι απαραίτητος για το σχηματισμό, την επιβίωση και τη λειτουργία των οστεοκλαστών και για το λόγο αυτό, ο αναστολέας αυτός δημιουργήθηκε ώστε να περιοριστεί η καταστροφή των οστών σε περιπτώσεις ρευματοειδούς αρθρίτιδας [53]. 32
34 Έπειτα η χρήση του ξεκίνησε να γίνεται περισσότερο ευρεία και χρησιμοποιήθηκε στον περιορισμό της καταστροφής των οστών κατά τις οστικές μεταστάσεις. Πολυάριθμα μοντέλα οστικής μετάστασης έχουν δείξει ότι οι RANKL αναστολείς περιορίζουν την οστεόλυση που προκαλείται από τους όγκους. Ζωικά μοντέλα τα οποία μιμούνται συνθήκες προχωρημένων καρκίνων προστάτη, μαστού και μημικροκυτταρικού καρκίνου του πνεύμονα με οστεολυτικές και οστεοβλαστικές σκελετικές αλλοιώσεις, έδειξαν ότι οι αναστολείς RANKL-Fc και OPG-Fc ήταν ικανοί να καθυστερήσουν οστικές μεταστάσεις και να μειώσουν την ανάπτυξη των όγκων στο σκελετό. Ακόμα προκλινικά μοντέλα πολλαπλού μυελώματος έδειξαν ότι η αναστολή του RANKL είναι δυνατό να μειώνει την οστεόλυση αυξάνοντας παράλληλα την επιβίωση του ασθενούς. Συνδυασμός αναστολέων RANKL και ορμονοθεραπείας ή χημειοθεραπείας έχει βρεθεί πως μειώνει σημαντικά τη μετάσταση στα οστά στην οποία εμπλέκεται το πρόσδεμα RANKL [54]. Εικόνα 9: Η ανάπτυξη των RANKL αναστολέων από το 1997 έως σήμερα (Narayanan, P., Denosumab: A comprehensive review. South Asian J Cancer, : 272-7) 33
35 Αναστολείς του μονοπατιού EGFR-EGF Στην ογκολογία ένας σημαντικός στόχος έχει αποδειχθεί ο EGFR, ο οποίος έχει βρεθεί να υπερεκφράζεται ή να είναι μεταλλαγμένος σε μια πληθώρα επιθηλιακών κακοηθειών και η ενεργοποίηση του υποδοχέα φαίνεται σημαντική για την ανάπτυξη και εξέλιξη των όγκων. Γνωρίζοντας τη βιολογία και τη λειτουργία του υποδοχέα κατασκευάστηκαν δύο ειδών αναστολείς, οι οποίοι περιλαμβάνουν μονοκλωνικά αντισώματα έναντι του εξωκυττάριου τμήματος του υποδοχέα καθώς και αναστολείς κινάσης τυροσίνης όπως το cetuximab (Erbitux), οι οποίοι στοχεύουν στην καταλυτική περιοχή του μορίου του EGFR όπως το gefitinib (Iressa) και το Erlotinib (Tarceva). Αντισώματα Τα αντί-egfr αντισώματα δρουν μέσω τεσσάρων μηχανισμών: α) σύνδεση στο εξωκυττάριο τμήμα του υποδοχέα και αναστολή σύνδεσης του προσδέτη β) σύνδεση στο εξωκυττάριο τμήμα του υποδοχέα και ενδοκυττάρωση του συμπλόκου υποδοχέααντισώματος γ) σύνδεση στο εξωκυττάριο τμήμα του υποδοχέα και αναστολή των σηματοδοτικών μονοπατιών του EGFR και δ) πιθανή διέγερση της ανοσολογικής απόκρισης [55]. Οι αναστολείς κινάσης τυροσίνης δρουν μέσω α) πρόσδεσης στο ενδοκυττάριο τμήμα του υποδοχέα β) αναστολή της ενεργοποίησης κινάσης τυροσίνης και γ) αναστολή της σηματοδότησης του υποδοχέα. 34
36 Εικόνα 10: Σχηματική αναπαράσταση των μονοπατιών σηματοδότησης του EGFR και τα πιθανά αποτελέσματα της αναστολής αυτών, έπειτα από την επίδραση μονοκλωνικών αντισώμάτων και αναστολέων κινάσης τυροσίνης. (Harari PM & Huang S- M 2001 Radiation response modification following molecular inhibition of epidermal growth factor receptor signaling. Seminars in Radiation Oncology ) Cetuximab: Αποτελεί ένα χιμαιρικό μονοκλωνικό αντίσωμα το οποίο αποτελείται από το συνδυασμό των μεταβλητών περιοχών του μονοκλωνικού αντισώματος του ποντικού, με τη σταθερή περιοχή της ανθρώπινης ανοσοσφαιρίνης G1, ώστε να μειωθεί η πιθανότητα ανοσολογικής απόκρισης στον άνθρωπο έναντι της ζωικής πρωτεΐνης. Αναστολείς κινάσης τυροσίνης Είναι συνθετικά μόρια παράγωγα κιναζολίνης, χαμηλού μοριακού βάρους που αλληλεπιδρούν με την ενδοκυττάρια περιοχή κινάσης τυροσίνης και αναστέλλουν τη φωσφορυλίωση του ενδοκυττάριου τμήματος του EGFR, ανταγωνιζόμενα για την περιοχή πρόσδεσης Mg-ATP. Τα τελευταία 20 χρόνια έχει κατασκευαστεί μια πληθώρα τέτοιων υποδοχέων, μεταξύ των οποίων βρίσκονται το Gefitinib και το Erlotinib. Gefitinib (Ιressa, AstraZeneca): Χρησιμοποιείται ευρέως στη θεραπεία κυρίως του Μη μικροκυτταρικού καρκίνου του πνεύμονα και αποτελεί παράγωγο ανιλινοκιναζολίνης που αναστέλλει πολυάριθμους υποδοχείς κινάσης τυροσίνης και ειδικότερα τον EGFR. Λόγω των υψηλών συγκεντρώσεων ΑΤΡ in vivo, απαιτούνται υψηλές συγκεντρώσεις του φαρμάκου για την αναστολή της δράσης του υποδοχέα. Σε αυτές τις συγκεντρώσεις όμως είναι δυνατό να αναστέλλει και άλλους υποδοχείς, όπως τον HER2, οπότε η δράση του μπορεί να μη θεωρηθεί ειδική. Συγχορηγούμενο με κυτταροτοξικές θεραπείες ή ραδιοθεραπεία έχει συνεργιστική επίδραση κι έτσι πια δεν απαιτείται υψηλή έκφραση EGFR από τον όγκο για να χορηγηθεί ως προτεινόμενη θεραπεία. Erlotinib (Tarceva): Αποτελεί έναν ικανό αναστρέψιμου τύπου αναστολέα της κινάσης τυροσίνης του ανθρώπινου EGFR και αποτελεί παράγωγο κιναζολίνης. Η δράση του σε μικρομοριακές δόσεις έγκειται στην αναστολή του κυτταρικού 35
37 πολλαπλασιασμού, επαγωγή της απόπτωσης και αναστολή του κυτταρικού κύκλου στη φάση G1. Σε μεγαλύτερες δόσεις είναι ικανό να αναστείλει πλήρως την επαγόμενη από EGF-φωσφορυλίωση του EGFR, ενώ δρα συνεργιστικά με την σισπλατίνη αυξάνοντας τη δράση της, χωρίς ταυτόχρονα να αυξάνεται η τοξικότητα της θεραπείας στον ασθενή [56]. 36
38 ΣΚΟΠΟΣ 37
39 Ο υποδοχέας RANK με τον προσδέτη του RANKL είναι γνωστό ότι συμμετέχουν στη φυσιολογική ανάπτυξη του μαστικού αδένα. Η μη φυσιολογική σηματοδότηση από το συγκεκριμένο υποδοχέα είναι δυνατό να οδηγεί σε παθολογική ανάπτυξη του μαστού και εμφάνιση νεοπλασίας. Ταυτόχρονα ο υποδοχέας EGFR είναι ένα από τα μόρια τα οποία ελέγχουν σημαντικές κυτταρικές διαδικασίες όπως ο πολλαπλασιασμός και η απόπτωση, ενώ οποιαδήποτε αλλαγή στη φυσιολογική λειτουργία συνδέεται με την εμφάνιση κακοηθειών. Με βάση τα ανωτέρω δεδομένα στην παρούσα εργασία μελετήθηκε η αλληλεπίδραση των γονιδίων των υποδοχέων RANK και EGFR στον καρκίνο του μαστού σε επίπεδο μεταγραφής, μετάφρασης και πρωτεϊνικής σηματοδότησης. 38
40 ΥΛΙΚΑ ΚΑΙ ΜΕΘΟΔΟΙ 39
41 ΚΥΤΤΑΡΑ ΚΑΙ ΚΥΤΤΑΡΟΚΑΛΛΙΕΡΓΕΙΕΣ 1. ΑΝΑΚΑΛΛΙΕΡΓΕΙΑ ΚΥΤΤΑΡΩΝ Σκοπός της διαδικασίας είναι η συνεχής παροχή του απαραίτητου προς μελέτη βιολογικού υλικού. Τα κύτταρα καλλιεργήθηκαν σε επωαστικό κλίβανο με σταθερές συνθήκες θερμοκρασίας και διοξειδίου του άνθρακα, στους 37 ο C και 5%, αντίστοιχα. Τα κύτταρα καλλιεργούνται σε τρυβλίο petri έως ότου φτάσουν να καλύπτουν το 80-90% της επιφάνειας του. Τότε με χημικά μέσα αποκολλώνται, Υλικά και διαλύματα Τρυψίνη/ΕDTA Dulbecco s Modified Eagle Medium (DMEM) MEM Earle s (EMEM) RPMI 1235 Ορός εμβρύου βοός (Fetal Bovine Serum, FBS) Φωσφορικό διάλυμα αλάτων 1x (Phosphate Buffer Saline, PBS) Πειραματική πορεία 1. Αφαίρεση θρεπτικού μέσου 2. Ξέπλυμα επιφάνειας κυττάρων με PBS 1x 3. Απομάκρυνση PBS 1x 4. Προσθήκη 1ml διαλύματος τρυψίνης. Επώαση για 5 min στον κλίβανο. 5. Μικροσκοπική παρατήρηση. Εάν τα κύτταρα έχουν αποκολληθεί από την επιφάνεια του τρυβλίου η τρυψίνη αδρανοποιείται με 5ml θρεπτικού μέσου το οποίο περιέχει ορό FBS 6. Μεταφορά κυτταρικού εναιωρήματος σε σωληνάκι φυγοκέντρησης. Φυγοκέντρηση στις 1600 rpm για 5 min 7. Απομάκρυνση υπερκειμένου, χωρίς διατάραξης ιζήματος. 8. Προσθήκη 5ml θρεπτικού και ήπια ανάμιξη, ώστε να μην σπάσουν τα κύτταρα. 9. Διαχωρισμός του κυτταρικού εναιωρήματος. Μεταφορά συγκεκριμένης ποσότητας κυττάρων σε νέο θρεπτικό μέσο. 2. ΨΥΞΗ ΚΥΤΤΑΡΩΝ 40
42 Η διατήρηση ζωικών κυττάρων για μεγάλο χρονικό διάστημα είναι δυνατή με την αποθήκευση τους σε υγρό άζωτο. Η ψύξη ξεκινά βαθμιαία (περίπου 1 0 C ανά ώρα) μέχρι η θερμοκρασία τους να φτάσει ένα κρίσιμο σημείο (-20 ο C) προκειμένου να αποφευχθεί ο σχηματισμός πάγου στο εσωτερικό τους και να ελαχιστοποιηθεί η απώλεια νερού. Για το λόγο αυτό, τα κύτταρα τοποθετούνται σε ειδικό δοχείο με ισοπροπανόλη, φυλάσσονται αρχικά στους -80 o C κι έπειτα μεταφέρονται σε υγρό άζωτο. Η διαδικασία πραγματοποιείται παρουσία διμέθυλο-σουλφοξειδίου (Dimethyl-Sulfoxide, DMSO). Υλικά και διαλύματα DMSO FBS Ειδικά φιαλίδια για βαθιά κατάψυξη (cryovials) Δοχείο ψύξης με ισοπροπανόλη (Mr. Frosty) 1. Βήματα 1-7 της διαδικασίας ανακαλλιέργειας. 2. Προσθήκη 900μl FBS και 100μl και ανάδευση 3. Μεταφορά σε cryovial και γρήγορα σε ειδικό δοχείο με ισοπροπανόλη. Διατηήρηση σε βαθιά κατάψυξη -80oC κι έπειτα σε υγρό άζωτο. 3. ΑΠΟΨΥΞΗ ΚΥΤΤΑΡΩΝ 1. Προετοιμασία τρυβλίου petri με 10ml θρεπτικού μέσου 2. Μεταφορά του cryovial σε υδατόλουτρο (37 ο C) και ανάδευση 3. Το εναιώρημα κυττάρων μεταφέρεται στο τρυβλίο petri 4. ΔΙΑΜΟΛΥΝΣΗ ΚΥΤΤΑΡΩΝ Υλικά και διαλύματα Turbofect (Thermo Scientific) Αντίδραση διαμόλυνσης Πλασμίδιο Turbofect ng 3μl 41
43 DMEM (χωρίς FBS) Έως 200μl Συνολικός όγκος 200 μl Τα συστατικά αναμιγνύονται καλά και επωάζονται για 20min σε θερμοκρασία δωματίου. Πλασμίδιο Αντιβιοτικό επιλογής Εταιρεία pcdna3.1/ WT-Rank Υγρομυκίνη Invitrogen MSCV-XZ066-EGFRvIII Αμπικιλίνη Addgene pcdna3.1 Υγρομυκίνη Invitrogen Πίνακας 3: Τα πλασμίδια που χρησιμοποιήθηκαν στην κυτταρική διαμόλυνση. Στον πίνακα παρουσιάζονται το ειδικό αντιβιοτικό επιλογής για το καθένα, καθώς και η εταιρεία παραγωγής τους. Εικόνα 11: Ο πλασμιδιακός φορεάς pcdna3.1. Πειραματική διαδικασία 1. Σε μικροπλακίδιο 6 κυψελίδων τοποθετούνται κύτταρα/ κυψελίδα. Σε κάθε κυψελίδα υπάρχουν 2ml καλλιεργητικού μέσου 2. Όταν τα κύτταρα καλύψουν το 70-80% της επιφάνειας της κυψελίδας, τότε μπορεί να πραγματοποιηθεί η διαμόλυνση. 42
44 3. Πριν την προσθήκη του διαμολυντικού, αλλάζουμε το θρεπτικό υλικό των κυττάρων 4. Προσθήκη του μίγματος διαμόλυνσης στάδειν σε όλη την επιφάνεια της μικροκυψελίδας. 5. Επώαση για h. 6. Πλύση με PBS 1x και αλλαγή θρεπτικού μέσου. 5. ΔΗΜΙΟΥΡΓΙΑ ΣΤΑΘΕΡΑ ΔΙΑΜΟΛΥΣΜΕΝΩΝ ΚΥΤΤΑΡΩΝ Μετά από 24 h από τη διαμόλυνση των κυττάρων, προστίθεται στο καλλιεργητικό μέσο το αντιβιοτικό επιλογής. Το εκάστοτε πλασμίδιο με το οποίο διαμολύνουμε τα κύτταρα φέρει ένα γονίδιο το οποίο προσφέρει αντίσταση σε ένα συγκεκριμένο αντιβιοτικό. Με βάση αυτό, όσα κύτταρα έχουν προσλάβει το πλασμίδιο θα μπορούν να επιβιώσουν παρουσία του αντιβιοτικού. Πειραματική διαδικασία 1. Μετά το πέρας 5-6 ημερών τα κύτταρα που δεν έχουν ενσωματώσει στο γενετικό τους υλικό το πλασμιδιακό DNA αποπίπτουν. 2. Τα θετικά κύτταρα που παραμένουν προσκολλημένα στον πάτο του τρυβλίου, τα ανακαλλιεργούμε αραιά και τα αφήνουμε ώστε να δημιουργηθούν μικρές αποικίες. Αφήνουμε τις αποικίες να μεγαλώσουν τόσο ώστε η απόσταση μεταξύ τους να διατηρείται μεγάλη και να αποφευχθεί ο κίνδυνος επιμόλυνσης μεταξύ των πληθυσμών. 3. Επιλέγουμε τις αποικίες μία μία και τις μεταφέρουμε σε ένα μικροπλακίδιο 24 κυψελίδων. 4. Όταν τα κύτταρα σε κάθε κυψελίδα καταλαμβάνουν περίπου τα 80-90% της επιφάνειας της τότε τα διαιρούμε σε δύο ίσα μέρη. 5. Η μισή ποσότητα κυττάρων μεταφέρεται σε μικροπλακέτα 12 κυψελίδων που φέρει καλυπτρίδα και η άλλη μισή σε μικροπλακέτα 12 κυψελίδων που δε φέρει. 6. Με χρήση ανοσοφθορισμού γίνεται μια πρώτη εκτίμηση του ποσοστού των κυττάρων που έχουν ενσωματώσει το πλασμίδιο. 43
45 7. Η διαδικασία από το βήμα 2 έως το βήμα 6 επαναλαμβάνεται για όσες φορές χρειαστεί ώστε όλα τα κύτταρα κάθε αποικίας να είναι θετικά στην έκφραση του γονιδίου. 8. Τέλος η θετική έκφραση επιβεβαιώνεται με πρωτεϊνική απομόνωση και ανοσοαποτύπωση κατά Western. 6. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΑΡΙΘΜΟΥ ΤΩΝ ΚΥΤΤΑΡΩΝ ΜΕ ΤΗ ΜΕΘΟΔΟ ΤΟΥ ΜΕΘΥΛ-ΤΕΤΡΑΖΟΛΙΟΥ (ΜΤΤ) Η αρχή της μεθόδου βασίζεται στην ικανότητα των ζωντανών κυττάρων να μεταβολίζουν το ΜΤΤ σε κρυστάλλους φορμαζάνης με χρώμα μπλε/μωβ. Έπειτα με ειδικό φωτόμετρο μετράται η ένταση του χρώματος στα 570nm, χρησιμοποιώντας ως μήκος κύματος αναφοράς τα 620nm. Με τη βοήθεια κατάλληλης πρότυπης καμπύλης, η οπτική απορρόφηση μετατρέπεται σε αριθμό κυττάρων. Υλικά και διαλύματα Μεθυλ-τετραζόλιο (ΜΤΤ): Σε 30ml PBS προστίθενται 150mg MTT και ακολουθεί διήθηση. Πειραματική διαδικασία 1. Σε μικροπλακίδιο 24 κυψελίδων όπου καλλιεργούνται κύτταρα, προστίθεται 10% ΜΤΤ στο θρεπτικό μέσο. Ακολουθεί επώαση 2 ωρών σε συνθήκες θερμοκρασίας 37 o C και διοξειδίου του άνθρακα 5%. 2. Το θρεπτικό μέσο απομακρύνεται. Στον πάτο της κυψελίδας οι μωβ κρύσταλλοι είναι ορατοί. 3. Προστίθεται 2-ισοπροπανόλη για να γίνει διαλυτοποίηση των κρυστάλλων. 4. Το έγχρωμο εκχύλισμα μεταφέρεται σε μικροπλακίδιο 96 κυψελίδων. 5. Φωτομέτρηση στα nm. ΒΑΚΤΗΡΙΑ ΚΑΙ ΒΑΚΤΗΡΙΑΚΕΣ ΚΑΛΛΙΕΡΓΕΙΕΣ 1. ΚΑΛΛΙΕΡΓΕΙΑ ΒΑΚΤΗΡΙΩΝ ΣΕ ΑΓΑΡ Το βακτηριακό στοκ διατηρείται σε γλυκερόλη στους -80 o C. Για την πλασμιδιακή απομόνωση είναι απαραίτητο να ξεκινήσουμε από μία μοναδιαία αποικία, ώστε να 44
46 είμαστε σίγουροι ότι το πλασμίδιο είναι καθαρό και δεν αποτελεί μίγμα διαφορετικών βακτηριακών προϊόντων. Υλικά και διαλύματα LB Broth with agar Σύσταση: 13,72g/lt Αγαρ 9,17g/lt Τρυπτόνη 4,57g/lt Εκχύλισμα ζύμης 4,57g/lt NaCl 1.6g/lt Αδρανείς παράγοντες δέσμευσης Προσθήκη 15gr άγαρ σε 1lt LB Broth. Αποστείρωση. Αμπικιλίνη 50mg/ml Πειραματική διαδικασία Η διαδικασία πραγματοποιείται παρουσία φλόγας ml αποστειρωμένου ρευστού LB άγαρ προστίθενται σε τρυβλίo petri, παρουσία αντιβιοτικού 2. Όταν σταθεροποιηθεί, με αποστειρωμένο ρύγχος πιπέτας, μεταφέρουμε μικρή ποσότητα από το στοκ και γλυκερόλης στην επιφάνεια του άγαρ. 3. Επωάζουμε στους 37 ο C για h. 2. ΠΑΡΑΣΚΕΥΗ ΥΓΡΗΣ ΒΑΚΤΗΡΙΑΚΗΣ ΚΑΛΛΙΕΡΓΕΙΑΣ Υλικά και διαλύματα LB Broth: Σύσταση: 10g/lt Τρυπτόνη 5g/lt Εκχύλισμα ζύμης 5g/lt NaCl Προσθήκη 20gr LB Broth σε 1lt dh 2 O, ανάμιξη και αποστείρωση Αμπικιλίνη 50mg/ml Πειραματική διαδικασία 45
47 Η διαδικασία πραγματοποιείται παρουσία φλόγας. Από την υγρή καλλιέργεια, θα γίνει πλασμιδιακή απομόνωση. με χρήση του kit NucleoSpin Bond (Macherey Nagel). 1. Μια μοναδιαία αποικία μεταφέρεται σε LB Broth παρουσία αμπικιλίνης. 2. Επώαση για 16 h, στους 37 o C υπό κίνηση 3. Ακολουθεί φυγοκέντρηση, ώστε να απομακρυνθεί η περίσσεια θρεπτικού 4. Τα κύτταρα διατηρούνται στους -80 o C ή γίνεται πλασμιδιακή απομόνωση. ΑΝΑΛΥΣΗ ΠΡΩΤΕΊΝΩΝ 1. ΠΑΡΑΣΚΕΥΗ ΟΛΙΚΟΥ ΠΡΩΤΕΪΝΙΚΟΥ ΕΚΧΥΛΙΣΜΑΤΟΣ ΑΠΟ ΚΥΤΤΑΡΙΚΕΣ ΣΕΙΡΕΣ Υλικά και διαλύματα 1. PBS 1x (παγωμένο) 2. Διάλυμα λύσης Stock 10mM Tris-HCl (ph=8) 1mM EDTA (ph=8) Για 50ml διαλύματος Λύσης 5ml 0.1ml 1% Triton-X ml 0.1% NaDOC 0.05gr 140mM NaCl 7ml 0.1% SDS 0.05gr 46
48 Πριν από κάθε χρήση στο διάλυμα λύσης προσθέτουμε: Stock Για 1ml διαλύματος λύσης 1mM NaF 0.5mM Na3VO4 5μl 5μl 1/100 αναστολέα πρωτεασών 10μl Πειραματική διαδικασία 1. Αφαίρεση θρεπτικού μέσου από το τρυβλίο και γρήγορο πλύσιμο με παγωμένο PBS 1x 2. Προσθήκη PBS 1x και μηχανική αποκόλληση των κυττάρων 3. Συλλογή του εναιωρήματος και φυγοκέντρηση στις 7000 rpm, 4 o C, 5 min 4. Απομάκρυνση υπερκειμένου και προσθήκη διαλύματος λύσης. Επώαση σε πάγο για 20min 5. Φυγοκέντρηση rpm, 4 o C, 20 min 6. Συλλογή υπερκειμένου που αντιστοιχεί στο πρωτεϊνικό εκχύλισμα 7. Διατήρηση στους -80 o C 2. ΠΟΣΟΤΙΚΟΠΟΪΗΣΗ ΠΡΩΤΕΊΝΩΝ Η διαδικασία πραγματοποιείται με φωτομέτρηση στα 595nM. Αρχικά φτιάχνεται μια πρότυπη καμπύλη για κάθε νέο διάλυμα Bradford. Για τη δημιουργία της πρότυπης καμπύλης γίνεται προετοιμασία 6 δειγμάτων γνωστής συγκέντρωσης BSA. Κάθε δείγμα από τα 6 ετοιμάζεται εις διπλούν για μεγαλύτερη ακρίβεια. Τα δείγματα φωτομετρούνται και η οπτική τους απορρόφηση αντιστοιχείται στη γνωστή συγκέντρωση BSA. Με τον τρόπο αυτό φτιάχνεται μια πρότυπη καμπύλη, από την οποία προκύπτει μια εξίσωση της μορφής y=ax+b, όπου y=οπτική απορρόφηση και x=συγκέντρωση. Στην εξίσωση αυτή τοποθετούνται οι οπτικές απορροφήσεις των υπό μελέτη δειγμάτων κι από εκεί υπολογίζονται οι συγκεντρώσεις τους. Υλικά και διαλύματα 47
49 Διάλυμα Bradford Πειραματική διαδικασία 1. Σε 1ml διαλύματος Bradford προστίθενται 2μl πρωτεϊνικού εκχυλίσματος 2. Ανάδευση 3. Επώαση σε σκοτάδι για 5min 4. Φωτομέτρηση 3. ΗΛΕΚΤΡΟΦΟΡΗΣΗ SDS-PAGE ΠΡΩΤΕΪΝΩΝ Η SDS PAGE ηλεκτροφόρηση (Sodium Dodecyl Sulfate PolyAcrylamide Gel Electrophoresis) χρησιμοποιείται για τον διαχωρισμό ενός πρωτεϊνικού μίγματος στα συστατικά του, με βάση την ηλεκτροφορητική κινητικότητα του κάθε μορίου. Η ικανότητα κάθε πρωτεΐνης να κινείται στο gel υπό την επίδραση ηλεκτρικού πεδίου εξαρτάται από το μέγεθος και το φορτίο του μορίου, τη δευτεροταγή του δομή καθώς και τις μετα-μεταφραστικές τροποποιήσεις που φέρει. Κάθε πρωτεϊνικό μόριο παρουσιάζει διαφορετικό μοριακό βάρος και διαφορετικό ισοηλεκτρικό σημείο. Επομένως δύο πρωτεΐνες με παρόμοια μοριακά βάρη δε θα είχαν τη δυνατότητα να διαχωριστούν με τη χρήση της SDS-PAGE, διότι λόγω διαφορετικής αναλογίας μάζας-φορτίου θα παρουσίαζαν και διαφορετική κινητικότητα στο ηλεκτρικό πεδίο. Για το λόγο αυτό χρησιμοποιείται το SDS (Sodim Dodecyl Sulfate) το οποίο προσδίδει σε κάθε πρωτεϊνικό μόριο αρνητικό φορτίο ανάλογα με το μοριακό της βάρος. Ταυτόχρονα συμβάλλει στην αποδιάταξη των πρωτεϊνικών αλυσίδων, ώστε η κίνηση των πρωτεϊνών να μην επηρεάζεται από το σχήμα τους. Περαιτέρω αποδιάταξη της τριτοταγούς δομής των πρωτεϊνών επιτυγχάνεται με τη χρήση DTT (DiThioThreitol), το οποίο ως αναγωγικός παράγοντας διασπά τους δισουλφιδικούς δεσμούς, ενώ για πλήρη αποδιάταξη απαιτείται η θέρμανση των δειγμάτων στους 95 o C για 5min. Οι ανωτέρω χειρισμοί των δειγμάτων, επιτρέπουν η κίνηση της εκάστοτε πρωτεΐνης στο gel πολυακρυλαμιδίου να γίνεται μόνο με βάση το μέγεθος της. Η αναλογία ακρυλαμιδίου και μέθυλο-bis-ακρυλαμιδίου είναι αυτή που θα καθορίσει το μέγεθος των πόρων του gel, ενώ η συγκέντρωση που συνήθως προτιμάται είναι 30%. Ο πολυμερισμός γίνεται παρουσία των καταλυτών ΝΝΝ Ν -τετραμεθυλενοδιαμίνης (TEMED) και Αmmonium Persulphate (APS). 48
50 Ανάλογα με το μοριακό βάρος της μια πρωτεΐνη κινείται στο πήκτωμα με διαφορετική ταχύτητα. Έτσι μετα από ορισμένο χρόνο εφαρμογής ηλεκτρικού πεδίου στην κορυφή του gel θα βρίσκονται πρωτεΐνες με μεγάλο μοριακό βάρος, ενώ στη βάση του τα μικρότερα μόρια. Πρωτεΐνες με μεσαία μοριακά βάρη θα βρίσκονται και σε ενδιάμεση θέση. Για την ανίχνευση των πολυπεπτιδικών αλυσίδων που έχουν αναλυθεί στο gel, γίνεται χρώση με κυανό του Coomassie. Υλικά και διαλύματα Πήκτωμα πακεταρίσματος 5% Stock Η 2 Ο Για 5ml διαλύματος 3,4ml 30% μίγμα acrylamide-bis acrylamide 0.83ml 1 M Tris (ph 6.8) 0.63ml 10% SDS 0.05ml 10% Ammonium persulfate 0.05ml TEMED 0.005ml Πήκτωμα διαχωρισμού 10% Stock Για 10ml διαλύματος Η 2 Ο 4ml 30% μίγμα acrylamide-bis acrylamide 3,3ml 1,5 M Tris (ph 8.8) 2,5ml 10% SDS 0,1ml 10% Ammonium persulfate 0.1ml TEMED 0.006ml Ρυθμιστικό διάλυμα Laemmli (10x) 49
51 Stock Για 1lt διαλύματος Tris base Glycine SDS 30.3gr 144.2gr 10gr Διάλυμα FSB Stock Για 40ml διαλύματος 160mM Tris ph=6.8 8ml 20% Glycerol 10ml 4% SDS 20ml 0.01% Bromophenol blue 500μl ddh ml ddh2o FSB Διάλυμα FSB-DTT 1x Stock Για 1ml διαλύματος 500μl 400μl DTT 1M 100μl FSB Διάλυμα FSB-DTT 2x Stock Για 1ml διαλύματος 800μl DTT 1M 200μl Μάρτυρας μοριακού βάρους (Page Ruler Plus Prestained Protein Ladder, Thermo Scientific) 50
52 Εικόνα 12: Page Ruler Plus Prestained Protein Ladder, Thermo Scientific Πειραματική διαδικασία 1. Προετοιμασία πηκτώματος i. To gel προετοιμάζεται μεταξύ δύο λεπτών τζαμιών που λειτουργούν ως καλούπι. Ανάλογα με την ποσότητα του δείγματος μας, έχουμε τη δυνατότητα να ετοιμάσουμε gel από 0,75mm 1,5mm. ii. Προετοιμασία του gel διαχωρισμού το οποίο θα βρίσκεται στη βάση του τελικού gel. Στην επιφάνεια αυτού προστίθεται μικρή ποσότητα νερού ώστε να εξομαλυνθεί η επιφάνεια του. iii. Όταν το πήκτωμα διαχωρισμού πήξει το νερό απομακρύνεται και προστίθεται το πήκτωμα πακεταρίσματος. Ειδικό χτενάκι τοποθετείται στη συσκευή για να δημιουργηθούν οι ειδικές θέσεις-πηγάδια (wells), όπου θα φορτωθούν τα δείγματα. iv. Όταν το gel πακεταρίσματος πήξει, τα χτενάκια αφαιρούνται και η συσκευή τοποθετείται στο δοχείο ηλεκτροφόρησης, που περιέχεται διάλυμα Laemmli 1x. 2. Προετοιμασία δειγμάτων i. Κατάλληλος όγκος πρωτεϊνικού εκχυλίσματος αναμιγνύεται με FSB-DTT ii. Θέρμανση για 5min στους 95 ο C και φυγοκέντρηση στις rpm για 1 min 3. Φόρτωση δειγμάτων i. Τα δείγματα φορτώνονται στα πηγαδάκια του πηκτώματος 51
53 ii. Επιπλέον φορτώνεται μάρτυρας μοριακού βάρους. Περιέχει μίγμα πρωτεϊνών με διαφορετικά μοριακά βάρη, καθένα από τα οποία αντιστοιχεί σε μια διακριτή ζώνη με χρώμα Η συσκευή κλείνει και εφαρμόζεται ηλεκτρικό πεδίο Volt 4. ΑΝΟΣΟΑΠΟΤΥΠΩΣΗ ΚΑΤΑ WESTERN Η τεχνική χρησιμοποιείται για την ανίχνευση συγκεκριμένων πρωτεϊνικών επιτόπων με τη χρήση αντισωμάτων, ειδικών για καθένα από αυτούς. Πραγματοποιείται μετά από διαχωρισμό του πρωτεϊνικού δείγματος με ηλεκτροφόρηση SDS-PAGE. Στη συνέχεια οι πρωτεΐνες μεταφέρονται σε ειδική μεμβράνη και επωάζονται με αντίσωμα ειδικό για την πρωτεΐνη ενδιαφέροντος. Ακολουθεί επώαση με δευτερογενές αντίσωμα το οποίο φέρει ένζυμο αλκαλικής υπεροξειδάσης. Η αλκαλική υπεροξειδάση, η οποία έχει τη δυνατότητα να διασπά το υπόστρωμα υπεροξειδίου, να οξειδώνει τη λουμινόλη και να οδηγεί στην εκπομπή ακτινοβολίας. Η παραγωγή ακτινοβολίας ανιχνεύεται από την αμαύρωση που προκαλεί στο φωτογραφικό φιλμ. Η μέθοδος αυτή ονομάζεται ενισχυμένη χημειοφωταύγεια (ECL, Enhanced ChemiLuminescence). Υλικά και διαλύματα Διάλυμα μεταφοράς Για 1lt διαλύματος 10x Tris base Glycine SDS 29gr 58gr 3.7gr Προσθήκη 10% μεθανόλης στο διάλυμα 1x πριν τη χρήση Διάλυμα TBS (ph 7.6) Για 1lt διαλύματος 10x NaCl Tris base 80gr 24.2gr 52
54 dh 2 O Διάλυμα TBS-Tween Σε 500ml διαλύματος TBS 1x προσθέτουμε 250μl Tween. Διάλυμα Developer (AGFA) Για 6lt διαλύματος 5lt Developer 1lt Διάλυμα Fixer (AGFA) Για 5lt διαλύματος dh 2 O Fixer 4lt 1lt Αντισώματα Πρωτογενή Αντισώματα Αντισώματα Οργανισμός Αραίωση Εταιρεία p44/42 κουνέλι 1/1000 Cell Signaling phospho-p44/42 κουνέλι 1/1000 Cell Signaling Akt κατσίκα 1/500 Santa Cruz phospho-akt κουνέλι 1/2000 Cell Signaling EGFR κουνέλι 1/5000 Millipore RANK κατσίκα 1/500 R&D actin ποντίκι 1/1000 Millipore 53
55 Δευτερογενή αντισώματα Αντισώματα Οργανισμός Αραίωση Εταιρεία a-rabbit IgG HRP κατσίκα 1/3000 Santa Cruz a-mouse IgG HRP κουνέλι 1/3000 Cell Signalling a-goat IgG HRP γάιδαρος 1/3000 Santa Cruz Πειραματική διαδικασία 1. Ενεργοποίηση της μεμβράνης PVDF (Merck) για 5min σε μεθανόλη 2. Μεταφορά των πρωτεϊνών από το πήκτωμα στη μεμβράνη με την εφαρμογή ηλεκτρικού πεδίου έντασης 300mA για 35-45min, ανάλογα με το πάχος του πηκτώματος. Η μεταφορά γίνεται σε συσκευή semi dry παρουσία διαλύματος Μεταφοράς 1x 3. Όταν η μεταφορά ολοκληρωθεί γίνεται κάλυψη αντιγονικών θέσεων με 5% γάλα ή BSA (Bovine Serum Albumin), ανάλογα με το πρωτογενές αντίσωμα που θα χρησιμοποιήσουμε. Η μεμβράνη επωάζεται για 1 ώρα σε θερμοκρασία δωματίου. 4. Επώαση με πρωτογενές αντίσωμα σε περιστρεφόμενο τροχό για ώες στους 4 o C. 5. Πλύση μεμβράνης 3x TBS-T για 5min 6. Επώαση με δευτερογενές αντίσωμα για 1 ώρα σε θερμοκρασία δωματίου σε περιστρεφόμενο τροχό. 7. Πλύση μεμβράνης 3x TBS-T για 5min 8. Επώαση με ECL για 4min 9. Μεταφορά σε ειδική κασετίνα. Η μεμβράνη καλύπτεται με φωτογραφικό φιλμ σε σκοτεινό θάλαμο. 10. Το φιλμ εμβαπτίζεται διαδοχικά σε διαλύματα Developer, Fixer και νερό βρύσης 5. ΑΝΟΣΟΦΘΟΡΙΣΜΟΣ Υλικά και διαλύματα 54
56 Διάλυμα φωσφορικών αλάτων (Phosphate Buffer Saline, PBS) Διάλυμα PBS-T (PBS-Tween 0.05%) Διάλυμα Carson s (ph 7.2) NaH 2 PO4 2H 2 O NaOH dh 2 O παραφορμαλδεΰδη Για 1lt διαλύματος 23.8gr 5.2gr 900ml 100ml Αντισώματα Πρωτογενές αντίσωμα Αντίσωμα Οργανισμός Αραίωση Εταιρεία RANK κατσίκα 1/80 R&D Δευτερογενές αντίσωμα Αντίσωμα Οργανισμός Αραίωση Εταιρεία a-goat 594 κουνέλι 1/500 R&D Πειραματική διαδικασία 1. Αποστειρωμένες καλυπτρίδες τοποθετούνται σε 12-well plate, όπου προστίθενται κύτταρα σε 1ml θρεπτικού μέσου 2. Επώαση για 24 h 3. Αφαίρεση θρεπτικού μέσου 4. Γρήγορο ξέπλυμα με παγωμένο PBS 5. Μονιμοποίηση με διάλυμα Carson s για 10min 6. Πλύση με PBS για 5min 7. Διατρητοποίηση των κυττάρων με TRITON-X 0.3% σε PBS για 5min 55
57 8. 3 πλύσεις με PBS για 5min 9. Κάλυψη μη ειδικών επιτόπων με 3% BSA και 10% FBS σε PBS για 1 ώρα σε θερμοκρασία δωματίου (διάλυμα blocking) 10. Προσθήκη πρωτογενούς αντισώματος και επώαση για h στους 4 o C. 11. Πλύση με PBS-T για 5min, 3 φορές 12. Προσθήκη δευτερογενούς αντισώματος και επώαση για 1 ώρα σε θερμοκρασία δωματίου, σε σκοτάδι 13. Πλύση με PBS-T για 5min, 3 φορές 14. Επώαση με Hoechst (βάφει μόνο πυρήνες) 1/2000 σε PBS για 2min σε σκοτάδι 15. Γρήγορη πλύση με dh 2 O 16. Σε αντικειμενοφόρο πλάκα προστίθεται mounting fluid που λειτουργεί ως κόλλα για την καλυπτρίδα. Η καλυπτρίδα τοποθετείται στην αντικειμενοφόρο. 17. Αφού στεγνώσουν ακολουθεί μικροσκοπική παρατήρηση. ΑΝΑΛΥΣΗ ΝΟΥΚΛΕΙΪΚΏΝ ΟΞΕΩΝ 1. ΑΠΟΜΟΝΩΣΗ ΝΟΥΚΛΕΙΚΩΝ ΟΞΕΩΝ (RNA) Α. Από κύτταρα: Η απομόνωση RNA έγινε από τις κυτταρικές σειρές SK-BR-3, MDA-MB-231, BT- 474, MCF-7, T47-D, MDA-MB-4175, MDA-MB-1183, HEK-293-T. Για τη διαδικασία αυτή χρησιμοποιήθηκε το σύστημα RNeasy της Qiagen, ακολουθώντας το πρωτόκολλο του κατασκευαστή. Πειραματική διαδικασία 1. Κυτταρική λύση i. Στο κυτταρικό ίζημα προστίθεται διάλυμα RLT και ακολουθεί έντονη ανατάραξη σε vortex, ώστε να σπάσουν τα συσσωματώματα. ii. Το δείγμα μεταφέρεται σε στήλη QIAshredder και φυγοκεντρείται για 2min, rpm. 2. Κατακρήμνιση DNA. i. Στο διάλυμα που εκλούεται προστίθεται 70% αιθανόλη και το δείγμα μεταφέρεται σε RNeasy mini στήλη. Φυγοκέντρηση 15sec, rpm. 3. Πλύσιμο της στήλης 56
58 i. Στη στήλη προστίθεται διάλυμα RW1. Φυγοκέντρηση 15sec, rpm. Το υγρό που εκλούεται απορρίπτεται. ii. Στη στήλη προστίθεται διάλυμα RΡΕ. Φυγοκέντρηση 2min, rpm. Tο υγρό που εκλούεται απορρίπτεται. 4. Έκλουση RNA i. Στη στήλη προστίθεται RNase free water. Φυγοκέντρηση 1min, rpm. Β. Από ιστούς εγκλεισμένους σε παραφίνη Η απομόνωση έγινε από τομές ιστών μονιμοποιημένων σε φορμόλη και εγκλεισμένους σε παραφίνη από 22 ασθενείς με καρκίνο μαστού. Για τη διαδικασία αυτή χρησιμοποιήθηκε το σύστημα RNeasy FFPE της Qiagen, ακολουθώντας το πρωτόκολλο του κατασκευαστή. Πειραματική διαδικασία 1. Αποπαραφινοποίηση των ιστών i. Στο δείγμα προστίθεται διάλυμα αποπαραφινοποίησης και ακολουθεί φυγοκέντρηση ii. Θέρμανση του δείγματος για την απομάκρυνση της περίσσειας παραφίνης. 2. Λύση των ιστών μέσω πέψης με πρωτεϊνάση Κ i. Στο δείγμα προστίθεται το διάλυμα PKD ii. Φυγοκέντρηση iii. Προσθήκη του ενζύμου πρωτεϊνάση Κ iv. Επώαση στους 56 o C για 15 min 3. Απομάκρυνση του DNA από το δείγμα i. Στη φάση του δείγματος που περιέχει το RNA προστίθεται διάλυμα DNase Booster Buffer και DNase I stock. ii. Επώαση σε θερμοκρασία δωματίου iii. Προσθήκη διαλύματος RBC iv. Προσθήκη διαλύματος αιθανόλης 4. Πρόσδεση του ολικού RNA στη στήλη RNeasy MinElute 57
59 i. Προσθήκη διαλύματος RBC και αιθανόλης για την πρόσδεση του RNA στη στήλη 5. Ξέπλυμα της στήλης i. Προσθήκη διαλύματος RPE στη στήλη και φυγοκέντρηση. Το μίγμα που προκύπτει απορρίπτεται. 6. Στέγνωμα της στήλης με φυγοκέντρηση 7. Έκλουση του RNA i. Προσθήκη RNase-free water στη στήλη και φυκοκέντρηση. Συλλογή του διαλύματος RNA. 2. ΣΥΝΘΕΣΗ ΣΥΜΠΛΗΡΩΜΑΤΙΚΟΥ DNA (cdna) Η σύνθεση του cdna πραγματοποιήθηκε με το SuperScript II, First Strand Synthesis System της Invitrogen. Ακολουθείται το πρωτόκολλο του κατασκευαστή από 500 ng RNA και ως εκκινητές τα τυχαία εξαμερή (Random Hexamers). Το πρωτόκολλο του κατασκευαστή παρουσιάζεται συνοπτικά παρακάτω. Εικόνα 13: Πειραματικό προτόκολλο της σύνθεσης συμπληρωματικού DNA με το σύστημα SuperScript II, First Strand Synthesis System της Invitrogen. 58
60 3. ΑΛΥΣΙΔΩΤΗ ΑΝΤΙΔΡΑΣΗ ΠΟΛΥΜΕΡΑΣΗΣ (PCR) Η PCR (Polymerase Chain Reaction) είναι μία in-vitro ενζυμική μέθοδος πολλαπλασιασμού αλληλουχιών του DNA. Για την ενζυμική αντίδραση χρησιμοποιούνται δύο ολιγονουκλεοτίδια τα οποία υβριδοποιούνται με τα άκρα των δύο συμπληρωματικών αλυσίδων της αλληλουχίας του DNA (cdna) την οποία θέλουμε να πολλαπλασιάσουμε. Το μέγεθος του επιλεγμένου προς πολλαπλασιασμό τμήματος DNA ορίζεται από τη θέση που κατέχουν τα 5 άκρα των ολιγονουκλεοτιδίων - εκκινητών. Η αντίδραση περιλαμβάνει τα ακόλουθα βήματα: Αποδιάταξη του DNA με θέρμανση στους 95 o C. Πρόσδεση του ζεύγους των ολιγονουκλεοτιδίων - εκκινητών με τις συμπληρωματικές αλληλουχίες του DNA (annealing). Η θερμοκρασία σύνδεσης συνήθως είναι χαμηλότερη κατά 5 o C από τη θερμοκρασία τήξης των ολιγονουκλεοτιδίων. Επιμήκυνση του ανασυνδυασμένου ολιγονουκλεοτιδίου από την Taq πολυμεράση στους 72 o C για 1min/1kb DNA. Οι κύκλοι αποδιάταξης, σύνδεσης και επιμήκυνσης επαναλαμβάνονται για φορές. Τα προϊόντα του DNA που δημιουργήθηκαν σε κάθε κύκλο χρησιμοποιούνται σαν μήτρα για τον επόμενο κύκλο. Το αποτέλεσμα είναι η εκθετική συσσώρευση του επιλεγμένου τμήματος DNA. 4. Real-Time PCR (RT-PCR) Οι αντιδράσεις της Real-Time PCR πραγματοποιήθηκαν στο μηχάνημα Rotor-Gene 3000 της εταιρείας Corbett Research. Αρχικά προετοιμάζεται το master mix για κάθε ζεύγος εκκινητών. Αυτό περιλαμβάνει το ζεύγος των δύο εκκινητών, το SYBR Green Master Mix και H2O. Η τελική συγκέντρωση των εκκινητών είναι 0.5 pmol/μl. Οι αντιδράσεις πραγματοποιούνται σε ειδικά διάφανα σωληνίδια. Σε κάθε θέση προστίθενται 18 μl από το master mix και 2 μl δείγματος cdna. Κάθε αντίδραση πραγματοποιείται τρείς φορές. Επίσης χρησιμοποιούνται ως δείγματα ελέγχου, δείγματα από RNA, τα οποία δεν έχουν υποστεί αντίστροφη μεταγραφή (RT-), καθώς και δείγματα στα οποία αντί cdna προστίθεται H2O (NTC). 59
61 Στη συνέχεια ενεργοποιείται η έναρξη των αντιδράσεων. Συνολικά πραγματοποιούνται 40 κύκλοι ενίσχυσης. Το πρόγραμμα που ακολουθείται αναλυτικά περιγράφεται παρακάτω: 5. Πλασμιδιακή απομόνωση με χρήση του kit NucleoSpin Bond (Macherey Nagel) Πραγματοποιείται έπειτα από υγρή καλλιέργεια και συλλογή βακτηριακού ιζήματος. 1. Κυτταρική λύση i. Στο ίζημα προστίθεται διάλυμα Α1. Ανάδευση ii. Προσθήκη διαλύματος Α2 και ήπια ανάδευση. Επώαση για 5min σε θερμοκρασία δωματίου iii. Προσθήκη διαλύματος Α3. Ήπια ανάδευση ώστε να μην κατακερματιστεί το γενομικό DNA. 2. Καθαρισμός εκχυλίσματος. i. Φυγοκέντρηση για 5min, g 3. Καθαρισμός DNA i. Το εκχύλισμα που προέκυψε από την φυγοκέντρηση διηθείται σε ειδική στήλη για 1min, g. Το διάλυμα που εκλούεται απομακρύνεται. Στη στήλη βρίσκεται τώρα προσδεδεμένο το πλασμιδιακό DNA. 4. Πλύση της στήλης i. Στη στήλη προστίθεται διάλυμα Α4. Φυγοκέντρηση για 1min, g. Διάλυμα που εκλούεται απομακρύνεται. ii. Ακολουθεί δεύτερη φυγοκέντρηση για να στεγνώσει η στήλη. 5. Έκλουση DNA i. Προσθήκη διαλύματος ΑΕ στη στήλη. Φυγοκέντρηση για 1min, g. Το διάλυμα που εκλούεται φέρει το πλασμιδιακό DNA. 6. ΠΟΣΟΤΙΚΟΠΟΙΗΣΗ ΝΟΥΚΛΕΙΚΩΝ ΟΞΕΩΝ Η ποσοτικοποίηση του RNA και των πλασμιδίων που απομονώθηκαν πραγματοποιήθηκε με το σύστημα Nanodrop σε μήκος κύματος 260nm. Απορρόφηση μιας μονάδας αντιστοιχεί σε πραγματική συγκέντρωση 40μg/ml για το RNA και 50μg/ml για το DNA. Για την εκτίμηση της καθαρότητας του εκάστοτε δείγματος, απαραίτητος είναι ο λόγος της απορρόφησης του προϊόντος στα 260nm και στα 60
62 280nm. Στα 280nm πραγματοποιείται απορρόφηση του υπεριώδους φωτός από άλλα μόρια όπως είναι οι πρωτεΐνες. Έτσι ένα προϊόν RNA ή DNA το οποίο έχει λόγο Α 260nm/280nm μεταξύ 1,9 και 2,1 θεωρείται ποιοτικά καθαρό. Ως τυφλό στη διαδικασία της ποσοτικοποίησης χρησιμοποιήθηκε RNase free water 7. ΗΛΕΚΤΡΟΦΟΡΗΣΗ ΝΟΥΚΛΕΙΚΩΝ ΟΞΕΩΝ ΣΕ ΠΗΚΤΩΜΑ ΑΓΑΡΟΖΗΣ Η ηλεκτροφόρηση σε πήκτωμα αγαρόζης επιτρέπει το διαχωρισμό τμημάτων DNA που μεταφέρουν μεταξύ τους από kb, ανάλογα με τη συγκέντρωση του πηκτώματος. Με την εφαρμογή ηλεκτρικού πεδίου στα άκρα του πηκτώματος, επιτρέπεται η κίνηση του DNA το οποίο είναι αρνητικά φορτισμένα προς την άνοδο. Η ηλεκτροφορητική κινητικότητα του DNA εξαρτάται πέντε παραμέτρους: α)από το μοριακό του βάρος. Όπως αναμένεται όσο μεγαλύτερο είναι ένα νουκλεοτιδικό τμήμα, τόσο πιο αργά κινείται ανάμεσα στους πόρους της αγαρόζης. β) Η ταχύτητα της μετανάστευσης επηρεάζεται από τη συγκέντρωση της αγαρόζης, γεγονός που ενισχύει την ανάλυση μορίων διαφορετικών μεγεθών. Για μικρότερα μόρια DNA χρησιμοποιούνται πηκτώματα υψηλότερης συγκέντρωσης σε σχέση με μεγαλύτερα μόρια. γ) Όπως συμβαίνει και στον πρωτεϊνικό διαχωρισμό, η στερεοδιαμόρφωση των τμημάτων DNA επηρεάζει την κινητικότητα των μορίων. Τμήματα DNA τα οποία είναι υπερελικωμένα (τύπος I), ανοικτά κυκλικά (τύπος II) και ευθύγραμμα (τύπος III) και τα οποία έχουν το ίδιο μοριακό βάρος, κινούνται με διαφορετικό ρυθμό σε ένα πήκτωμα αγαρόζης. Υπό συγκεκριμένες συνθήκες, η μορφή Ι του DNA μεταναστεύει γρηγορότερα από τη μορφή ΙΙΙ. Υπό άλλες συνθήκες, η σειρά αυτή μπορεί να αντιστραφεί. δ) Από την εφαρμοζόμενη τάση. Υπό χαμηλή διαφορά δυναμικού, ο ρυθμός μετανάστευσης γραμμικών μορίων DNA είναι ανάλογος της εφαρμοζόμενης τάσης. Αν όμως αυξηθεί η διαφορά δυναμικού στο κύκλωμα, η κινητικότητα των μεγάλου μοριακού βάρους τμημάτων DNΑ θα αυξηθεί διαφορικά. Το ικανοποιητικό λοιπόν εύρος διαχωρισμού σε πηκτώματα αγαρόζης μειώνεται όσο αυξάνεται η εφαρμοζόμενη διαφορά δυναμικού. Για να επιτύχουμε τη μέγιστη ανάλυση τμημάτων 61
63 DNA τα οποία διαφέρουν κατά 2kb, πρέπει να εφαρμόσουμε στο πήκτωμα όχι μεγαλύτερη τάση από 5V/cm. ε) Από τη σύνθεση του ρυθμιστικού διαλύματος ηλεκτροφόρησης. Η ηλεκτροφορητική κινητικότητα του DNA επηρεάζεται από τη σύνθεση και το βαθμό ιοντισμού του διαλύματος ηλεκτροφόρησης. Απουσία ιόντων η ηλεκτρική αγωγιμότητα είναι ελάχιστη και το DNA μετακινείται με πολύ αργό ρυθμό ή καθόλου. Διαλύματα με υψηλό βαθμό ιοντισμού δημιουργούν υψηλή ηλεκτρική αγωγιμότητα που σαν αποτέλεσμα έχει την ανάπτυξη θερμότητας στη συσκευή. Υλικά και διαλύματα ΝαΟΗ Διάλυμα βορικού νατρίου (SB Buffer) Για 1lt διαλύματοςsb 20x 8g Βορικό οξύ dh 2 O 45g έως 1lt Πήκτωμα αγαρόζης 10x διάλυμα χρωστικής (Loading Buffer) Μάρτυρας μοριακού βάρους (Thermo Scientific) 62
64 Πειραματική διαδικασία 1. Προετοιμασία πηκτώματος αγαρόζης. Σε 100ml ρυθμιστικού διαλύματος SB προστίθεται 1gr αγαρόζης. Ακολουθεί θέρμανση έως ότου το μίγμα διαυγάσει. Αφού κρυώσει γίνεται προσθήκη 10μl βρωμιούχου αιθιδίου και μεταφέρεται σε ειδικό καλούπι, μέχρι να σταθεροποιηθεί. 2. Το δείγμα που πρόκειται να αναλυθεί αναμιγνύεται με 10x διάλυμα χρωστικής και μεταφέρεται στις ειδικές θέσεις του πηκτώματος. 3. Η συσκευή ηλεκτροφόρησης κλείνει και εφαρμόζεται ρεύμα τάσης 100Volt. 4. Μετά το τέλος της ηλεκτροφόρησης το πήκτωμα παρατηρείται υπό UV φωτισμό και φωτογραφίζεται. 8. Κατάτμηση του DNA με ένζυμα περιορισμού Οι ενδονουκλεάσες περιορισμού είναι ένζυμα τα οποία απομονώνονται από προκαρυωτικούς οργανισμούς τα οποία αναγνωρίζουν και κατατέμνουν συγκεκριμένες αλληλουχίες δίκλωνων μορίων DNA. Υλικά και διαλύματα Στα πειράματα χρησιμοποιήθηκαν οι ενδονουκλεάσες Apa1 και Not1. Πειραματική διαδικασία 1. Προετοιμασία αντίδρασης Apa1 2μl Not1 2μl DNA 4μl React4 4μl BSA 3μl Triton100 1μl dh 2 O 14μl V τελικό 2. Το δείγμα επωάζεται παρουσία των περιοριστικών ενζύμων για 2 h στους 37 ο C 63
65 ΑΠΟΤΕΛΕΣΜΑΤΑ 64
66 Προσδιορισμός των ενδογενών επιπέδων mrna των RANK και EGFR σε καρκινικές σειρές μαστού και σε δείγματα ασθενών με καρκίνο μαστού Κυτταρική Υποδοχέας Υποδοχέας Υποδοχέας Τύπος σειρά οιστρογόνων(er) προγεστερόνης HER2 (PR) MDA-MB Basal SKBR HER2+ MCF Luminal A T-47D Luminal A BT Luminal B Με σκοπό τη μελέτη της πιθανής αλληλεπίδρασης των συστημάτων RANK-RANKL και EGFR-EGF, αρχικά έγινε ταυτοποίηση των ενδογενών επιπέδων mrna των μορίων RANK και EGFR σε καρκινικές κυτταρικές σειρές μαστού. Για το σκοπό αυτό χρησιμοποιήθηκαν επτά διαφορετικές καρκινικές σειρές μαστού, οι οποίες προέρχονται από διαφορετικούς ασθενείς με καρκίνο μαστού και παρουσιάζουν διαφορετικό λειτουργικό, ανοσοϊστοχημικά και μοριακό προφίλ. Οι κυτταρικές σειρές που χρησιμοποιήθηκαν ήταν οι MDA-MB-231, SKBR3, MCF-7, T-47D, BT- 474, MDA-MB-231 κλώνος 4175 και MDA-MB-231 κλώνος 1833, τα χαρακτηριστικά των οποίων παρουσιάζονται στον παρακάτω πίνακα. Οι κυτταρικοί κλώνοι 4175 και 1833 έχουν ίδια χαρακτηριστικά (isogenic) με την MDA-MB-231 σειρά, αλλά είναι κύτταρα επιλεγμένα να δίνουν μεταστάσεις στα οστά και στους πνεύμονες αντίστοιχα, όταν ενύονται σε ποντικούς. MDA-MB- 231-C4175 MDA-MB- 231-C Basal Basal 65
67 Πίνακας 4: Οι τύποι των καρκινικών σειρών μαστού MDA-MB-231, SKBR3, MCF-7, T-47D, BT-474, MDA-MB-231-C4175, MDA-MB-231-C1183 με βάση την έκφραση των υποδοχέων ER, PR, HER2. (Subik, K., et al., The Expression Patterns of ER, PR, HER2, CK5/6, EGFR, Ki-67 and AR by Immunohistochemical Analysis in Breast Cancer Cell Lines. Breast Cancer (Auckl), : p ) Για την ταυτοποίηση των επιπέδων mrna των γονιδίων RANK και EGFR έγινε χρήση της τεχνικής Real-time PCR. Απομονώθηκε ολικό RNA από κάθε κυτταρική σειρά με το σύστημα RNeasy kit της Qiagen και η συγκέντρωση του RNA τελικού προϊόντος ποσοτικοποιήθηκε σε συσκευή Nanodrop σε μήκος κύματος 260nm. Ακολούθησε σύνθεση cdna για κάθε δείγμα, με το σύστημα SuperScript II, First Strand Synthesis System της Invitrogen και το cdna προϊόν χρησιμοποιήθηκε ως υπόστρωμα στις αντιδράσεις PCR ενίσχυσης των γονιδίων RANK και EGFR. H διαδικασία πραγματοποιήθηκε δύο φορές έτσι ώστε να αποφευχθούν σφάλματα λόγω αποτυχίας ισοφόρτωσης και χρησιμοποιήθηκαν τα αρνητικά δείγματα ελέγχου NTC και RT-. Ως γονίδιο αναφοράς χρησιμοποιήθηκε το γονίδιο GAPDH. Έτσι για κάθε κυτταρική σειρά καταγράφηκαν δύο τιμές οι οποίες αντιστοιχούν στα επίπεδα mrna των RANK και EGFR. Κάθε τιμή εισήχθη σε ένα διάγραμμα με τις τιμές του mrna του RANK να αναγράφονται στον άξονα yy και τις τιμές του EGFR στον άξονα xx. Το σημείο όπου οι δύο τιμές συναντώνται για κάθε κυτταρική σειρά, φαίνεται στο παρακάτω διάγραμμα όπου παρουσιάζεται η σχετική έκφραση των mrna των δύο υποδοχέων. 66
68 Εικόνα 14: Σχηματική αναπαράσταση της συσχέτισης των mrna των RANK και EGFR στις κυτταρικές σειρές MDA-MB-231, SKBR3, MCF-7, T-47D, BT-474,, MDA-MB- 231-C4175, MDA-MB-231-C1833 Από το παραπάνω διάγραμμα παρατηρείται ότι υπάρχει τάση για θετική συσχέτιση μεταξύ των mrna των RANK και EGFR στις κυτταρικές σειρές μαστού. Υψηλά επίπεδα RANK συνεντοπίζονται με υψηλά επίπεδα EGFR ενώ χαμηλότερα επίπεδα RANK παρατηρούνται ταυτόχρονα με χαμηλά επίπεδα EGFR. Από την παρατήρηση αυτή προέκυψε το ερώτημα, εάν η ίδια παράλληλη πορεία ακολουθείται και στα mrna των RANK και EGFR ασθενών με καρκίνο του μαστού. Για το λόγο αυτό χρησιμοποιήθηκε δείγμα ιστού εγκλεισμένου σε παραφίνη από 22 ασθενείς, τα οποία παραχωρήθηκαν από το Γενικό Νοσοκομείο Πατρών και το Πανεπιστημιακό Γενικό Νοσοκομείο Πατρών, τα δεδομένα των οποίων παρουσιάζονται στον Πίνακα 5 που ακολουθεί. Από το δείγμα ιστού έγινε απομόνωση ολικού RNA με το σύστημα RNeasy FFPE Kit της Qiagen και ακολούθησε η τεχνική της Real Time PCR όπως αναφέρθηκε προηγουμένως. Τύπος κακοήθειας Βαθμός κακοήθειας ΕR PR HER2 1 ΛΔ ΙΙ
69 2 ΛΔ ΙΙ ΠΔ ΙΙ ΠΔ ΙΙ ΠΔ Ι ΠΔ ΙΙ ΠΔ ΙΙ ΑΠ Ι ΠΔ ΙΙ ΠΔ ΙΙ ΠΔ ΙΙ ΠΔ ΙΙ ΠΔ ΙΙ ΠΔ ΙΙΙ ΠΔ ΙΙ ΠΔ ΙΙΙ ΠΔ ΙΙ ΛΔ ΙΙ ΠΔ ΙΙ ΠΔ ΙΙ
70 21 ΠΔ ΙΙ ΠΔ ΙΙΙ Πίνακας 5: Δεδομένα ασθενών που χρησιμοποιήθηκαν στη μελέτη. Στον πίνακα παρουσιάζονται ο Τύπος καρκινώματος μαστού, όπου ΠΔ= Πορογενές Διηθητικό, ΛΔ= Λοβιακό Διηθητικό, ΑΠ= Αποκρινές Διηθητικό, ο Βαθμός κακοήθειας (Ι-ΙΙΙ), και η έκφραση των υποδοχέων προγεστερόνης (PR), οιστρογόνων (ER), καθώς και HER2. Για κάθε δείγμα ασθενούς έγινε έλεγχος των επιπέδων mrna των RANK και EGFR. Τα αποτελέσματα που προέκυψαν τοποθετήθηκαν σε ένα κοινό διάγραμμα όπως προηγουμένως για να γίνει η μεταξύ τους συσχέτιση. Όπως φαίνεται στην Εικόνα 15 και εδώ διατηρείται η θετική συσχέτιση μεταξύ των δύο υποδοχέων. Η αύξηση του RANK ακολουθείται από ταυτόχρονη αύξηση του EGFR και αντιστρόφως. Εικόνα 15: Σχηματική αναπαράσταση της συσχέτισης των mrna των RANK και EGFR σε δείγματα ιστού από ασθενείς με καρκίνο του μαστού. Από τα πειράματα αυτά προέκυψε μια πρώτη ένδειξη ότι υπάρχει θετική συσχέτιση μεταξύ των υποδοχέων RANK και EGFR τουλάχιστον σε επίπεδο mrna. Η σχέση αυτή ταυτοποιήθηκε τόσο στις κυτταρικές σειρές μαστού που μελετήθηκαν αλλά και σε δείγματα ασθενών με καρκίνο του μαστού. 69
71 Ταυτοποίηση του μορίου RANK ως επαγωγέα της έκφρασης του EGFR Έχοντας ως δεδομένο τη θετική συσχέτιση μεταξύ των υποδοχέων RANK και EGFR στο μεταγραφικό επίπεδο δημιουργήθηκε το ερώτημα εάν είναι ο RANK ο οποίος ελέγχει το μεταγραφικό ρυθμό του EGFR, ή αντιστρόφως. Έτσι έγινε μια προσπάθεια για την ταυτοποίηση του ενός εκ των δύο μορίων το οποίο πιθανώς ευθύνεται για την επαγωγή της μεταγραφής του άλλου. Για το σκοπό αυτό πραγματοποιήθηκε παροδική διαμόλυνση είτε με τον πλασμιδιακό φορέα pcdna3.1 που φέρει κλωνοποιημένο το γονίδιο TNFRSF11A, είτε με τον πλασμιδιακό φορέα MSCV-XZ066 που φέρει το γονίδιο EGFRvIII και κάθε φορά γινόταν έλεγχος ως προς τα επίπεδα mrna του δεύτερου υποδοχέα. Ως κυτταρικό μοντέλο χρησιμοποιήθηκε η φυσιολογική κυτταρική σειρά ΗΕΚ 293-Τ και ως διαμολυντικό μέσο το αντιδραστήριο Turbofect. Η συλλογή των κυττάρων έγινε σε τρία διαφορετικά χρονικά διαστήματα. Αρχικά στις 24, στις 48 και στις 72 h μετά τη διαμόλυνση. Αρχικά επιβεβαιώθηκε η επιτυχία της διαμόλυνσης, με απομόνωση πρωτεϊνικού εκχυλίσματος από τα διαμολυσμένα κύτταρα και ακολούθησε ανοσοαποτύπωση κατά Western, όπου έγινε έλεγχος θετικής έκφρασης RANK και EGFR στα κύτταρα που έλαβαν τα αντίστοιχα πλασμίδια. Ως αρνητικά δείγματα ελέγχου χρησιμοποιήθηκαν κύτταρα ΗΕΚ 293-Τ (ΗΕΚ 293-Τ mock) τα οποία υπέστησαν διαμόλυνση με τον πλασμιδιακό φορέα χωρίς αυτός να φέρει το εκάστοτε ένθετο. Η επιτυχία της διαμόλυνσης παρουσιάζεται στην Εικόνα
72 Εικόνα 16: Επιβεβαίωση παροδικής διαμόλυνσης των ΗΕΚ 293-Τ με τα πλασμίδια pcdna3.1-tnfrsf11a και MSCV-XZ066-EGFRvIII σε διαφορετικά χρονικά διαστήματα. Στη συνέχεια από τους ίδιους κυτταρικούς πληθυσμούς απομονώθηκε ολικό RNA στις χρονικές στιγμές 24, 48 και 72 h μετά τη διαμόλυνση και πραγματοποιήθηκε έλεγχος με Real Time PCR. Στα μεν κύτταρα που είχαν διαμολυνθεί με το πλασμίδιο pcdna3.1-tnfrsf11a έγινε έλεγχος των επιπέδων mrna του EGFR και στα κύτταρα που διαμολύνθηκαν με το MSCV-XZ066-EGFRvIII ελέγχθηκαν τα επίπεδα του mrna RANK. Η διακύμανση της έκφρασης των mrna των δύο υποδοχέων στις δύο κυτταρικές ομάδες παρουσιάζεται στα ραβδογράμματα που ακολουθούν. 71
73 Α Β Εικόνα 17: Παροδική έκφραση του RANK σε διαδοχικά χρονικά διαστήματα δείχνει να αυξάνει τη μεταγραφή του EGFR. Α. Παροδική διαμόλυνση των 293T κυττάρων με RANK, αυξάνουν τα επίπεδα mrna του EGFR Β. Παροδική διαμόλυνση των 293T κυττάρων με EGFR δεν επηρεάζει σημαντικά τη μεταγραφή του RANK. Από τα ανωτέρω διαγράμματα γίνεται φανερό ότι στην περίπτωση των κυττάρων ΗΕΚ 293-Τ που έλαβαν εξωγενώς το γονίδιο του ενεργοποιημένου EGFRvIII, δεν παρατηρείται σημαντική διαφοροποίηση στα επίπεδα του mrna του RANK. Η μεταγραφή του γονιδίου του RANK παραμένει σχεδόν σταθερή σε όλα τα χρονικά διαστήματα ενώ σε σχέση με το δείγμα ελέγχου παρατηρείται μια ελάχιστη μείωση. 72
74 Αντιθέτως η παροδική έκφραση του RANK στα ΗΕΚ 293-Τ επηρεάζει σαφώς τη μεταγραφή του γονιδίου του EGFR, η οποία παρουσιάζει και σταθερή αύξηση με την πάροδο του χρόνου. Τελικά στις 72 h μετά τη διαμόλυνση η μεταγραφή του EGFR έχει αυξηθεί κατά 6 φορές σε σχέση με το δείγμα ελέγχου. Συμπεραίνεται εύκολα επομένως ότι για την παράλληλη πορεία που παρατηρήθηκε προηγουμένως στην μεταγραφή των δύο γονιδίων, υπεύθυνος είναι ο RANK. Συμπερασματικά η αυξημένη σηματοδότηση μέσω του RANK λόγω υπερέκφρασης επάγει τη μεταγραφή του EGFR. Έλεγχος της ικανότητας του RANK να ελέγχει την έκφραση του EGFR σε πρωτεϊνικό επίπεδο στην κυτταρική σειρά καρκίνου μαστού SKBR3 Από τα προηγούμενα πειράματα προέκυψε το συμπέρασμα ότι η μεταγραφή του γονιδίου του EGFR εξαρτάται σε κάποιο βαθμό από την ενεργοποίηση του υποδοχέα RANK και πως υπάρχει θετική συσχέτιση της έκφρασης τους σε επίπεδο mrna. Συνεχίζοντας, έγινε έλεγχος της σχέσης που περιγράφηκε προηγουμένως, σε επίπεδο πρωτεΐνης αλλά αυτή τη φορά στην καρκινική μαστού SKBR3, καθώς η νόσος αυτή αποτελεί και το αντικείμενο ενδιαφέροντος της παρούσας μελέτης. Πραγματοποιήθηκε παροδική διαμόλυνση των SKBR3 κυττάρων με τον πλασμιδιακό φορέα pcdna3.1 που φέρει κλωνοποιημένο το γονίδιο TNFRSF11A (RANK), με το διαμολυντικό μέσο Turbofect. Η συλλογή του κυτταρικού ιζήματος έγινε 24, 48 και 72 h μετά τη διαμόλυνση, απ όπου απομονώθηκε ολική πρωτεΐνη. Χρησιμοποιώντας την τεχνική της ανοσοαποτύπωσης κατά Western ταυτοποιήθηκαν τα επίπεδα έκφρασης του EGFR στα κύτταρα που είχαν λάβει το γονίδιο του RANK στις τρεις διαφορετικές χρονικές στιγμές ως προς το δείγμα ελέγχου. Και στην περίπτωση αυτή ως αρνητικό δείγμα ελέγχου χρησιμοποιήθηκαν κύτταρα SKBR3 τα οποία είχαν υποστεί διαμόλυνση μόνο με τον πλασμιδιακό φορέα, χωρίς το γονιδιακό ένθετο. Τα αντισώματα και οι συγκεντρώσεις στις οποίες χρησιμοποιήθηκαν αναφέρονται στον Πίνακα 6. Ως μέτρο ισοφόρτωσης χρησιμοποιήθηκε η πρωτεϊνική έκφραση της ακτίνης. Στην Εικόνα 18 παρουσιάζεται η έκφραση του EGFR στις διαφορετικές χρονικές στιγμές, στα κύτταρα που έλαβαν ή όχι το γονίδιο του RANK μέσω της διαμόλυνσης. Ταυτόχρονα έγινε ποσοτικοποίηση της έκφρασης του EGFR ως προς 73
75 την ακτίνη, στις δύο κατηγορίες κυττάρων και η σχετική έκφραση του παρουσιάζεται στο ραβδόγραμμα που ακολουθεί. Εικόνα 18: Αυξημένα επίπεδα έκφρασης RANK, επάγουν την πρωτεϊνική έκφραση του EGFR. Α. Παροδική διαμόλυνση των καρκινικών κυττάρων μαστού SKBR3 με πλασμιδιακό φορέα (pcdna3.1) που φέρει κλωνοποιημένο το γονίδιο TNFRSF11A, δείχνει βαθμιαία αύξηση του EGFR σε διάστημα 72 ωρών, Β. Αντίθετα όταν τα κύτταρα διαμολύνθηκαν με πλασμίδιο που δε φέρει κανένα μόριο, δεν παρατηρείται καμία αύξηση του EGFR. Η αυξημένη έκφραση του RANK στα κύτταρα που έλαβαν το πλασμίδιο pcdna3.1- RANK, φαίνεται πως είναι ικανή να επάγει τη βαθμιαία αύξηση της πρωτεΐνης του EGFR, ενώ κάτι τέτοιο δεν παρατηρείται στα κύτταρα που δεν έλαβαν το γονιδιακό ένθετο. Αντιθέτως τα κύτταρα που έλαβαν μόνο τον πλασμιδιακό φορέα δεν παρουσίασαν καμία αλλαγή στη σχετική έκφραση του EGFR. Μάλιστα η διαφορά 74
76 στην έκφραση του παραγόμενου EGFR είναι ιδιαίτερα μεγάλη, αφού εμφανίζει μεγαλύτερη αύξηση σε σχέση με τα κύτταρα-ελέγχου. Συμπεραίνεται έτσι ότι η ρύθμιση της έκφρασης του EGFR από τον RANK που παρατηρήθηκε στο μεταγραφικό επίπεδο, συντηρείται και στο μεταφραστικό για την καρκινική σειρά μαστού SKBR3. Έλεγχος της επίδρασης της έκφρασης του RANK στο σηματοδοτικό μονοπάτι EGFR-EGF στα κύτταρα SKBR3 Τα ανωτέρω αποτελέσματα αποδεικνύουν την ικανότητα του RANK να επάγει την έκφραση του EGFR στα κύτταρα SKBR3, χωρίς όμως να παρατηρείται το αντίστροφο φαινόμενο. Έτσι ως επόμενο βήμα μελετήθηκε ο έλεγχος της σηματοδοτικής οδού EGFR-EGF από τον RANK. Τα παροδικά διαμολυσμένα κύτταρα SKBR3-RANK χρησιμοποιήθηκαν για τη μελέτη της επίδρασης του RANK στο σηματοδοτικό μονοπάτι EGFR-EGF. Η επαγωγή της σηματοδοτικής οδού έγινε με τη χρήση του ειδικού προσδέματος EGF σε διαφορετικά χρονικά διαστήματα (0, 10, 30 min). Για να ελεγχθεί η πιθανή ενεργοποίηση κομβικών μορίων στο μονοπάτι EGFR-EGF χρησιμοποιήθηκε η τεχνική της ανοσοαποτύπωσης κατά Western. Τα μόρια αυτά είναι οι Akt και p44/42, για τα οποία μελετήθηκε η ικανότητα ενεργοποίησης τους μέσω φωσφορυλίωσης και εντάσσονται στα σηματοδοτικά μονοπάτια τα οποία επάγονται από τον EGFR υποδοχέα. Η φωσφορυλίωση των δύο πρωτεϊνικών μορίων σηματοδοτεί την ενεργοποίηση του εν λόγω μονοπατιού και εμμέσως μας πληροφορεί για την ενεργοποίηση του υποδοχέα EGFR. Η πειραματική διαδικασία ξεκίνησε με αποστέρηση του ορού εμβρύου βοός από το θρεπτικό μέσο για 24 h. Μετά το πέρας της περιόδου αποστέρησης ορού τα κύτταρα υπέστησαν διέγερση με EGF σε συγκέντρωση 100ng/ml το οποίο προστέθηκε σε καλλιεργητικό μέσο άνευ ορού για 0, 10 και 30 min, τόσο στα κύτταρα SKBR3- RANK όσο και στα SKBR3-mock. Η σύγκριση μεταξύ των δύο κυτταρικών ομάδων έγινε ούτως ώστε να ταυτοποιηθούν οι αλλαγές σε επίπεδο φωσφορυλίωσης που είναι ικανός να προκαλέσει ο RANK στο σηματοδοτικό μονοπάτι του EGFR. 75
77 Μετά το πέρας της διέγερσης ακολούθησε πρωτεϊνική απομόνωση, ποσοτικοποίηση με τη μέθοδο Bradford και αναοσοαποτύπωση κατά Western. Επειδή η ανοσοαποτύπωση κατά Western αποτελεί ημιποσοτική μέθοδο, τα επίπεδα φωσφορυλίωσης κάθε πρωτεΐνης ποσοτικοποιήθηκαν ως προς την έκφραση της β- ακτίνης. Στις εικόνες που ακολουθούν φαίνεται η έκφραση των αντισωμάτων p44/42 και Akt καθώς και της φωσφορυλιωμένης μορφής τους, και στα ραβδογράμματα παρουσιάζεται η σχετική έκφραση των phospho-p44/42 (Thr202/Tyr204) και phospho-akt (Ser473) ως προς τη β-ακτίνη στις χρονικές στιγμές 0, 10 και 30 min διέγερσης με EGF. Α. EGF (100ng/ml) (min) SKBR RANK RANK p-p44/42 p44/42 p-akt AKT Actin 76
78 Εικόνα 21: Ανάλυση της πρωτεϊνικής έκφρασης των RANK, EGFR, phospho-p44/42, p44/42, phosphor-akt, Akt και β-ακτίνη στα κύτταρα SKBR3-RANK σε σχέση με τα SKBR3-mock κύτταρα. Α. Ποιοτικά με τη χρήση της ανοσοαποτύπωσης κατά Western Β. Ποσοτικοποίηση της έκφρασης των πρωτεϊνών phospho-p44/42 και phospho-akt ως προς τη β-ακτίνη. Όπως παρατηρείται από τις παραπάνω εικόνες η φωσφορυλιωμένη μορφή της πρωτεΐνης p44/42 υπάρχει ακόμα και πριν από τη διέγερση με EGF και βρίσκεται αυξημένη ήδη από τη χρονική στιγμή t= 0 στα κύτταρα SKBR3-RANK σε σχέση με τα SKBR3-mock. Η διαφορά αυτή ενισχύεται και συντηρείται σε όλη τη διάρκεια του πειράματος. Ακόμα ενώ μετά τα 30 min επώασης με EGF στην ομάδα SKBR3- RANK η φωσφορυλίωση μειώνεται σταδιακά, στα SKBR3-mock κύτταρα η αύξηση 77
79 συντηρείται, χωρίς ποτέ όμως να φτάνει τα επίπεδα των SKBR3-RΑΝΚ. Η φωσφορυλίωση της πρωτεΐνης Akt ακολουθεί ένα διαφορετικό πρότυπο. Στα κύτταρα που δεν εκφράζουν τον υποδοχέα RANK, η φωσφορυλιωμένη μορφή της Akt ανιχνεύεται ακόμα και χωρίς τη διέγερση με τον EGF, δηλαδή τη χρονική στιγμή t=0. Στα 10 min μετά την προσθήκη του ειδικού EGF διεγέρτη αυξάνεται η p-akt και για τις δύο κυτταρικές ομάδες, ενώ ένα μικρό προβάδισμα στην τελική ένταση της p-akt παρατηρείται στην ομάδα SKBR3-RANK. Το πιο σημαντικό όμως στο σημείο αυτό, δεν είναι ο απόλυτος αριθμός της σχετικής έκφρασης που παρατηρήθηκε, αλλά ότι από τη χρονική στιγμή t= 0 έως τη χρονική στιγμή t=10 min, η ομάδα που εκφράζει RANK παρουσιάζει αύξηση της φωσφορυλιωμένης Akt σε μεγαλύτερο ποσοστό σε σχέση με την ομάδα SKBR3-mock. Από τη χρονική στιγμή t=10 min έως τη χρονική στιγμή t=30 min υπάρχει μείωση της φωσφορυλίωσης και στις δύο κυτταρικές ομάδες, αλλά σε κάθε περίπτωση συντηρούνται υψηλότερα επίπεδα p-akt στην ομάδα που εκφράζει RANK. Έλεγχος της επίδρασης της έκφρασης του RANK στην ικανότητα πολλαπλασιασμού των SKBR3 κυττάρων Έχοντας επιβεβαιώσει την επαγωγή του EGFR από το RANK στα διαμολυσμένα με RANK SKBR3 κύτταρα, τέθηκε το ερώτημα της συμβολής του μορίου αυτού στην ικανότητα πολλαπλασιασμού των κυττάρων μέσω του EGFR. Για να πραγματοποιηθεί η συγκεκριμένη πειραματική διαδικασία, κατασκευάστηκαν προηγουμένως SKBR3 κύτταρα σταθερά διαμολυσμένα με τον RANK. Κύτταρα τα οποία εκφράζουν σταθερά ένα γονίδιο το οποίο έλαβαν εξωγενώς μέσω της διαμόλυνσης, έχουν ενσωματώσει το γονίδιο αυτό στο γονιδίωμα τους και η έκφραση του γίνεται με ρυθμό σταθερό και συνεχή χωρίς να χάνεται. Ταυτόχρονα τα επίπεδα έκφρασης δεν είναι τόσο υψηλά όπως παρατηρείται κατά την παροδική διαμόλυνση και προσομοιάζουν τα φυσιολογικά κυτταρικά επίπεδα. Για να πραγματοποιηθεί η κατασκευή τέτοιων κυττάρων που εκφράζουν σταθερά το γονίδιο TNFRSF11A, ακολουθήθηκε η ίδια διαδικασία όπως προηγουμένως και ως αντιβιοτικό επιλογής χρησιμοποιήθηκε η Υγρομυκίνη Β για την οποία το ίδιο το πλασμίδιο φέρει γονίδιο ανθεκτικότητας. Έπειτα τα κύτταρα καλλιεργήθηκαν αραιά για να δημιουργηθούν μοναδιαίες αποικίες. Όταν κάθε μοναδιαία έφτασε σε ικανό μέγεθος διαχωρίστηκε σε τρία μέρη, εκ των οποίων τα δύο χρησιμοποιήθηκαν για 78
80 ανοσοφθορισμό και ανοσοαποτύπωση κατά Western με σκοπό να ταυτοποιηθούν οι θετικές ομάδες κυττάρων. Η τρίτη ομάδα ήταν αυτή που διατηρήθηκε σε καλλιέργεια στην περίπτωση που ο κλώνος ήταν θετικός στην έκφραση του RANK. Η επιβεβαίωση πρόσληψης του γονιδίου του RANK από τα κύτταρα έγινε με την ανοσοαποτύπωση κατά Western, με τη χρήση αντι- RANK αντισώματος. Ως αρνητικό δείγμα ελέγχου χρησιμοποιήθηκαν εκχυλίσματα κυττάρων τα οποία είχαν απομονωθεί από SKBR3 που είχαν διαμολυνθεί μόνο με τον πλασμιδιακό φορέα και όχι το ένθετο RANK. Η κατασκευή των κυττάρων αυτών είχε πραγματοποιηθεί ήδη στο εργαστήριο για προηγούμενες μελέτες και τα κύτταρα αυτά διατηρούσαν την ικανότητα πολλαπλασιασμού παρουσία Υγρομυκίνης Β, μαρτυρώντας έτσι τη διατήρηση του πλασμιδίου στο γονιδίωμα τους. Στην Εικόνα 19 φαίνεται η θετική έκφραση του RANK στα σταθερά διαμολυσμένα κύτταρα SKBR3 (SKBR3-stable) σε σχέση με τα κύτταρα ελέγχου (SKBR3-mock). Μάρτυρας ισοφόρτωσης αποτελεί η ακτίνη, η οποία παρουσιάζει το ίδιο επίπεδο έκφρασης και στις δύο ομάδες κυττάρων. Εικόνα 19: Θετική έκφραση του υποδοχέα RANK στα σταθερά διαμολυσμένα κύτταρα (SKBR3-stable) σε σχέση με τα κύτταρα ελέγχου (SKBR3-mock). 79
81 Στους κλώνους που βρέθηκαν να είναι θετικοί στην έκφραση του RANK πραγματοποιήθηκε έλεγχος της θέσης του υποδοχέα στο κύτταρο, έτσι ώστε να επιβεβαιωθεί η τοποθέτησή του στην κυτταροπλασματική μεμβράνη, όπως θα ήταν αναμενόμενο. Ο έλεγχος αυτός έγινε με χρήση ανοσοφθορισμού και χρησιμοποιήθηκε πρωτογενές αντίσωμα αντι-rank 1/80 και δευτερογενές αντίσωμα anti-goat Alexa 594 (ερυθρό χρώμα) σε αραίωση 1/500, ενώ η χρώση των πυρήνων έγινε με Hoechst 1/2000 (κυανό χρώμα). Ακολούθησε παρατήρηση σε μικροσκόπιο φθορισμού, με τους πυρήνες να χρωματίζονται μπλε και το κυτταρόπλασμα κόκκινο. Κατά την παρατήρηση αυτή έγινε σύγκριση των πιθανά σταθερά διαμολυσμένων κλώνων με τα κύτταρα SKBR3-mock-stable, τα οποία είχαν ήδη κατασκευαστεί από το εργαστήριο για προηγούμενες μελέτες. Στην εικόνα που ακολουθεί παρουσιάζεται ο σταθερά διαμολυσμένος κλώνος SKBR3-RANK-stable-C1 A όπως φαίνεται στο κόκκινο και στο μπλε χρώμα του μικροσκοπίου φθορισμού, καθώς και η συγχώνευση των δύο πεδίων. Παράλληλα παρουσιάζεται και η κυτταρική ομάδα ελέγχου SKBR3- mock-stable, ώστε να γίνει εμφανώς κατανοητή η διαφορά μεταξύ της θετικής και της μη έκφρασης του υποδοχέα. 80
82 Εικόνα 20: Κατασκευή σταθερά διαμολυσμένων SKBR3 με πλασμιδιακό φορέα (pcdna3.1) που φέρει κλωνοποιημένο το γονίδιο TNFRSF11A. Η σωστή κυτταρική εντόπιση επιβεβαιώνεται με τη χρήση ανοσοφθορισμού. Η μελέτη έγινε μεταξύ των κυττάρων που είχαν λάβει μόνο τον πλασμιδιακό φορέα και όσων είχαν λάβει και το ένθετο RANK. Tα κύτταρα διατηρήθηκαν σε διαφορετικές συνθήκες καλλιέργειας, με ή χωρίς αποστέρηση ορού εμβρύου βοός, καθώς και παρουσία ή απουσία του προσδέματος EGF. Η αποστέρηση ορού εμβρύου βοός από το καλλιεργητικό μέσο είναι γνωστό πως περιορίζει την κυτταρική επιβίωση, επάγει την καταστροφή του γονιδιώματος ενώ ταυτόχρονα σταματά τον κυτταρικό κύκλο στη φάση G0/G1. Η καλλιέργεια απουσία ορού αποσκοπεί στην 81
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
Το μονοπάτι της κινάσης MAP- ERK
 Το μονοπάτι της κινάσης MAP- ERK 1 Σηματοδότηση μέσω μικρών GTPασών Η οικογένεια μορίων Ras (Rat Sarcoma virus) Ρύθμιση των πρωτεϊνών Ras Οι πρωτεΐνες Ras μετατρέπονται από την ανενεργή μορφή τους, που
Το μονοπάτι της κινάσης MAP- ERK 1 Σηματοδότηση μέσω μικρών GTPασών Η οικογένεια μορίων Ras (Rat Sarcoma virus) Ρύθμιση των πρωτεϊνών Ras Οι πρωτεΐνες Ras μετατρέπονται από την ανενεργή μορφή τους, που
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος
 Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
ΚΕΦΑΛΑΙΟ 15. Κυτταρική ρύθμιση. Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1
 ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
Μονοπάτια ενεργοποίησης κινασών MAP σε κύτταρα θηλαστικών
 Μονοπάτια ενεργοποίησης κινασών MAP σε κύτταρα θηλαστικών Εκτός από την ERK, τα κύτταρα των θηλαστικών διαθέτουν τις κινάσες MAP JNK και p38. Η ενεργοποίηση των κινασών JNK και p38 προκαλείται από μέλη
Μονοπάτια ενεργοποίησης κινασών MAP σε κύτταρα θηλαστικών Εκτός από την ERK, τα κύτταρα των θηλαστικών διαθέτουν τις κινάσες MAP JNK και p38. Η ενεργοποίηση των κινασών JNK και p38 προκαλείται από μέλη
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
Μοριακή βιολογία καρκίνου του πνεύμονα Ενότητα 1: Ογκολογία πνεύμονα. Κυριάκος Καρκούλιας, Επίκουρος Καθηγητής Σχολή Επιστημών Υγείας Τμήμα Ιατρικής
 Μοριακή βιολογία καρκίνου του πνεύμονα Ενότητα 1: Ογκολογία πνεύμονα Κυριάκος Καρκούλιας, Επίκουρος Καθηγητής Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Εισαγωγή Ο καρκίνος του πνεύμονα παρουσιάζει άφθονες
Μοριακή βιολογία καρκίνου του πνεύμονα Ενότητα 1: Ογκολογία πνεύμονα Κυριάκος Καρκούλιας, Επίκουρος Καθηγητής Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Εισαγωγή Ο καρκίνος του πνεύμονα παρουσιάζει άφθονες
Μοριακή Βιολογία. Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΚΕΧΑΓΙΑΣ ΒΑΣΙΛΕΙΟΣ ΑΘΗΝΑ, 16/11/10 A.M. :
 ΚΕΧΑΓΙΑΣ ΒΑΣΙΛΕΙΟΣ ΑΘΗΝΑ, 16/11/10 A.M. : 2010336 ΕΡΓΑΣΙΑ ΓΙΑ ΤΟ Μ.Π.Σ. ΜΕΤΑΒΟΛΙΚΑ ΝΟΣΗΜΑΤΑ ΟΣΤΩΝ ΚΥΤΟΚΙΝΕΣ ΠΑΡΑΓΟΜΕΝΕΣ ΑΠΟ ΤΑ Τ-ΚΥΤΤΑΡΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΠΟΥ ΕΜΠΛΕΚΟΝΤΑΙ ΣΤΗΝ ΟΣΤΕΟΚΛΑΣΤΟΓΕΝΕΣΗ
ΚΕΧΑΓΙΑΣ ΒΑΣΙΛΕΙΟΣ ΑΘΗΝΑ, 16/11/10 A.M. : 2010336 ΕΡΓΑΣΙΑ ΓΙΑ ΤΟ Μ.Π.Σ. ΜΕΤΑΒΟΛΙΚΑ ΝΟΣΗΜΑΤΑ ΟΣΤΩΝ ΚΥΤΟΚΙΝΕΣ ΠΑΡΑΓΟΜΕΝΕΣ ΑΠΟ ΤΑ Τ-ΚΥΤΤΑΡΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΠΟΥ ΕΜΠΛΕΚΟΝΤΑΙ ΣΤΗΝ ΟΣΤΕΟΚΛΑΣΤΟΓΕΝΕΣΗ
Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ. Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη
 Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη 2013 ΠΕΡΙΕΧΟΜΕΝΑ : Ορολογία και λίγα λόγια για τον καρκίνο Χαρακτηριστικά του καρκίνου Μεταλλάξεις Μεταλλάξεις και καρκίνος
Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη 2013 ΠΕΡΙΕΧΟΜΕΝΑ : Ορολογία και λίγα λόγια για τον καρκίνο Χαρακτηριστικά του καρκίνου Μεταλλάξεις Μεταλλάξεις και καρκίνος
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών
 Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος
 MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
Σύμφωνα με τον παγκόσμιο οργανισμό υγείας, κάθε χρόνο υπάρχουν 1.38 εκατομμύρια καινούρια περιστατικά και περίπου 458 000 θάνατοι από τον καρκίνο του
 1 Σύμφωνα με τον παγκόσμιο οργανισμό υγείας, κάθε χρόνο υπάρχουν 1.38 εκατομμύρια καινούρια περιστατικά και περίπου 458 000 θάνατοι από τον καρκίνο του μαστού. Ο καρκίνος του μαστού είναι με μεγάλη διαφορά
1 Σύμφωνα με τον παγκόσμιο οργανισμό υγείας, κάθε χρόνο υπάρχουν 1.38 εκατομμύρια καινούρια περιστατικά και περίπου 458 000 θάνατοι από τον καρκίνο του μαστού. Ο καρκίνος του μαστού είναι με μεγάλη διαφορά
Ομαδες μοριων κυτταρικης προσφυσης
 Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
Μόρια κυτταρικής πρόσφυσης
 Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΠΑΝΕΛΛΗΝΙΩΝ 2017 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII Δ Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Στους προκαρυωτικούς
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ ΠΑΝΕΛΛΗΝΙΩΝ 2017 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII Δ Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Στους προκαρυωτικούς
Ατυπία Υπερπλασία- Δυσπλασία. Κίττυ Παυλάκη
 Ατυπία Υπερπλασία- Δυσπλασία Κίττυ Παυλάκη Jeanne Calment Κάπνιζε µέχρι τα 117 Πέθανε στα 122 Η σωστή λειτουργία των οργανισµών απαιτεί τη δυνατότητα προσαρµογής των κυττάρων και κατά συνέπεια και των
Ατυπία Υπερπλασία- Δυσπλασία Κίττυ Παυλάκη Jeanne Calment Κάπνιζε µέχρι τα 117 Πέθανε στα 122 Η σωστή λειτουργία των οργανισµών απαιτεί τη δυνατότητα προσαρµογής των κυττάρων και κατά συνέπεια και των
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ
 27 Μαΐου 2016 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων (Νέο & Παλιό Σύστημα) ΘΕΜΑ Γ Γ.1 Ο χαρακτήρας της ομάδας αίματος στον άνθρωπο
27 Μαΐου 2016 ΒΙΟΛΟΓΙΑ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Απαντήσεις Θεμάτων Πανελλαδικών Εξετάσεων Ημερησίων Γενικών Λυκείων (Νέο & Παλιό Σύστημα) ΘΕΜΑ Γ Γ.1 Ο χαρακτήρας της ομάδας αίματος στον άνθρωπο
Μελέτη έκφρασης των αντιγόνων των οικογενειών Survivin και MAGE-A στον καρκίνο του πνεύμονα
 Μονάδα Ανοσολογίας Καρκίνου Εργαστήριο Ανοσολογίας-Ιστοσυμβατότητας Πανεπιστημιακό Νοσοκομείο Λάρισας Τμήμα Ιατρικής Πανεπιστήμιο Θεσσαλίας Μελέτη έκφρασης των αντιγόνων των οικογενειών Survivin και MAGE-A
Μονάδα Ανοσολογίας Καρκίνου Εργαστήριο Ανοσολογίας-Ιστοσυμβατότητας Πανεπιστημιακό Νοσοκομείο Λάρισας Τμήμα Ιατρικής Πανεπιστήμιο Θεσσαλίας Μελέτη έκφρασης των αντιγόνων των οικογενειών Survivin και MAGE-A
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
ΜΕΛΕΤΗ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΤΗ ΘΕΡΑΠΕΙΑ
 ΕΡΕΥΝΗΤΙΚΗ ΜΟΝΑΔΑ: ΜΟΡΙΑΚΗ ΒΙΟΛΟΓΙΑ ΥΠΕΥΘΥΝΟΣ: ΤΣΕΖΟΥ ΑΣΠΑΣΙΑ ΜΕΛΕΤΗ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΤΗ ΘΕΡΑΠΕΙΑ ΠΑΠΑΝΙΚΟΛΑΟΥ Βασίλης, PhD Λάρισα, 2012 ΚΑΡΚΙΝΟΣ ΜΑΣΤΟΥ Αποτελεί την πιο κοινή μορφή
ΕΡΕΥΝΗΤΙΚΗ ΜΟΝΑΔΑ: ΜΟΡΙΑΚΗ ΒΙΟΛΟΓΙΑ ΥΠΕΥΘΥΝΟΣ: ΤΣΕΖΟΥ ΑΣΠΑΣΙΑ ΜΕΛΕΤΗ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΤΗ ΘΕΡΑΠΕΙΑ ΠΑΠΑΝΙΚΟΛΑΟΥ Βασίλης, PhD Λάρισα, 2012 ΚΑΡΚΙΝΟΣ ΜΑΣΤΟΥ Αποτελεί την πιο κοινή μορφή
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ
 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 2 ο 1. Με ποιο μηχανισμό αντιγράφεται το DNA σύμφωνα με τους Watson και Crick; 2. Ένα κύτταρο που περιέχει ένα μόνο χρωμόσωμα τοποθετείται σε θρεπτικό υλικό που περιέχει ραδιενεργό
ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 2 ο 1. Με ποιο μηχανισμό αντιγράφεται το DNA σύμφωνα με τους Watson και Crick; 2. Ένα κύτταρο που περιέχει ένα μόνο χρωμόσωμα τοποθετείται σε θρεπτικό υλικό που περιέχει ραδιενεργό
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ. ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
1. Πού πραγματοποιούνται η αντιγραφή και η μεταγραφή; ΘΩΜΑΣ ΑΠΑΝΤΗΣΗ. 2. Ποιες είναι οι κατηγορίες γονιδίων με κριτήριο το προϊόν της μεταγραφής τους;
 Βιολογία Γ Ενιαίου Λυκείου / Θετική Κατεύθυνση κεφαλαιο 2ο: αντιγραφη, εκφραση και ρυθμιση τησ ΓενετικηΣ ΠληροφοριαΣ 1. Πού πραγματοποιούνται η αντιγραφή και η μεταγραφή; Ευκαρυωτικά κύτταρα: στον πυρήνα,
Βιολογία Γ Ενιαίου Λυκείου / Θετική Κατεύθυνση κεφαλαιο 2ο: αντιγραφη, εκφραση και ρυθμιση τησ ΓενετικηΣ ΠληροφοριαΣ 1. Πού πραγματοποιούνται η αντιγραφή και η μεταγραφή; Ευκαρυωτικά κύτταρα: στον πυρήνα,
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς. Οι φάσεις των Τ κυτταρικών απαντήσεων
 ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
Εξέλιξη και ανθρώπινος πολιτισμός: Η ρύθμιση του γονιδίου της λακτάσης
 Εξέλιξη και ανθρώπινος πολιτισμός: Η ρύθμιση του γονιδίου της λακτάσης Η διατήρηση του ενζύμου της λακτάσης στους ενήλικες είναι ένα παράδειγμα πρόσφατης εξέλιξης στον άνθρωπο. Μας δείχνει επίσης πώς μεταλλαγές
Εξέλιξη και ανθρώπινος πολιτισμός: Η ρύθμιση του γονιδίου της λακτάσης Η διατήρηση του ενζύμου της λακτάσης στους ενήλικες είναι ένα παράδειγμα πρόσφατης εξέλιξης στον άνθρωπο. Μας δείχνει επίσης πώς μεταλλαγές
13o Μεμβρανικοί υποδοχείς με εσωτερική δραστικότητα κινάσης Ser/Thr 1. Σηματοδότηση μέσω TGFβ
 13 o TGF-β Μεμβρανικοί υποδοχείς με εσωτερική δραστικότητα κινάσης Ser/Thr 1. Σηματοδότηση μέσω TGFβ Ωρίμανση του μορίου TGFβ Ενεργοποίηση των υποδοχέων TGFβ Οι μεταγραφικοί παράγοντες Smads Η ρύθμιση
13 o TGF-β Μεμβρανικοί υποδοχείς με εσωτερική δραστικότητα κινάσης Ser/Thr 1. Σηματοδότηση μέσω TGFβ Ωρίμανση του μορίου TGFβ Ενεργοποίηση των υποδοχέων TGFβ Οι μεταγραφικοί παράγοντες Smads Η ρύθμιση
Καραπέτσας Θανάσης. Διπλωματική Εργασία:
 Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος
 Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Κυτταρική επικοινωνία Τύποι επικοινωνίας
Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Κυτταρική επικοινωνία Τύποι επικοινωνίας
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
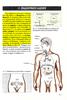 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
igenetics Mια Μεντελική προσέγγιση
 igenetics Mια Μεντελική προσέγγιση Κεφάλαιο 22 (+κεφ. 17 Hartwell) Γενετική του καρκίνου Η πρωτεΐνη p53 προσδένεται στο DNA. 2 ΕΙΚΟΝΑ 22.1 Μαστογραφία που απεικονίζει έναν όγκο. Όγκος 3 Κύρια σημεία: Καρκίνος
igenetics Mια Μεντελική προσέγγιση Κεφάλαιο 22 (+κεφ. 17 Hartwell) Γενετική του καρκίνου Η πρωτεΐνη p53 προσδένεται στο DNA. 2 ΕΙΚΟΝΑ 22.1 Μαστογραφία που απεικονίζει έναν όγκο. Όγκος 3 Κύρια σημεία: Καρκίνος
Μηχανισμοί Ογκογένεσης
 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΓΕΝΕΤΙΚΗΣ Μηχανισμοί Ογκογένεσης Δρ. Α. ΓΑΛΑΝΗΣ agalanis@mbg.duth.gr Μηχανισμοί Ογκογένεσης Ενότητα 4. Απορρύθμιση του κυτταρικού κύκλου και
ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΑΙ ΓΕΝΕΤΙΚΗΣ Μηχανισμοί Ογκογένεσης Δρ. Α. ΓΑΛΑΝΗΣ agalanis@mbg.duth.gr Μηχανισμοί Ογκογένεσης Ενότητα 4. Απορρύθμιση του κυτταρικού κύκλου και
 ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ: ΣΤΡΑΤΗΓΙΚΕΣ ΠΡΟΛΗΨΗΣ Αντωνίου Χαρά Διευθύντρια Β Χειρουργικής Κλινικής Γενικού Νοσοκομείου Χανίων ΣΕ ΤΙ ΘΑ ΑΝΑΦΕΡΘΟΥΜΕ??? Πόσο συχνός είναι ο καρκίνος του μαστού? Ποια αίτια τον προκαλούν?
ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ: ΣΤΡΑΤΗΓΙΚΕΣ ΠΡΟΛΗΨΗΣ Αντωνίου Χαρά Διευθύντρια Β Χειρουργικής Κλινικής Γενικού Νοσοκομείου Χανίων ΣΕ ΤΙ ΘΑ ΑΝΑΦΕΡΘΟΥΜΕ??? Πόσο συχνός είναι ο καρκίνος του μαστού? Ποια αίτια τον προκαλούν?
ΚΕΦΑΛΑΙΟ 11 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
 ΚΕΦΑΛΑΙΟ 11 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ 1o ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11207, 96ο ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11303 Ι. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν
ΚΕΦΑΛΑΙΟ 11 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ 1o ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11207, 96ο ΔΙΑΓΩΝΙΣΜΑ - ΓΗ_Α_ΒΙΟ_0_11303 Ι. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης
 ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
Αυτοφαγία & Ανοσολογικό Σύστημα. Χαράλαμπος Μ. Μουτσόπουλος
 Αυτοφαγία & Ανοσολογικό Σύστημα Χαράλαμπος Μ. Μουτσόπουλος Απρίλιος 2018 Αυτοφαγία & Ανοσολογικό Σύστημα Ευκαρυωτικά κύτταρα: Δυο μηχανισμούς αποδόμησης και ανακύκλωσης κυτταροπλασματικών αποβλήτων Πρωτεάσες
Αυτοφαγία & Ανοσολογικό Σύστημα Χαράλαμπος Μ. Μουτσόπουλος Απρίλιος 2018 Αυτοφαγία & Ανοσολογικό Σύστημα Ευκαρυωτικά κύτταρα: Δυο μηχανισμούς αποδόμησης και ανακύκλωσης κυτταροπλασματικών αποβλήτων Πρωτεάσες
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου
 Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Στα χρωμοσώματα ενός ανθρώπινου σωματικού κυττάρου στο στάδιο της μετάφασης της μίτωσης υπάρχουν: Α. 23 μόρια DNA Β. 92 μόρια DNA Γ. 46 μόρια DNA Δ.
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Στα χρωμοσώματα ενός ανθρώπινου σωματικού κυττάρου στο στάδιο της μετάφασης της μίτωσης υπάρχουν: Α. 23 μόρια DNA Β. 92 μόρια DNA Γ. 46 μόρια DNA Δ.
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β
 ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
Κυτταρική επικοινωνία
 Κυτταρική επικοινωνία Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Τύποι επικοινωνίας
Κυτταρική επικοινωνία Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Τύποι επικοινωνίας
ΑΝΟΣΟΛΟΓΙΑ. 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ
 ΑΝΟΣΟΛΟΓΙΑ 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ ΑΝΤΙΓΟΝΟ 3. Η πρόσληψη του αντιγόνου και η παρουσίασή του στα λεμφοκύτταρα 4. Η αναγνώριση του αντιγόνου. Αντιγονικοί
ΑΝΟΣΟΛΟΓΙΑ 1. Εισαγωγή (κυρίως στην επίκτητη ανοσία) 2. Φυσική ανοσία ΕΠΙΚΤΗΤΗ ΑΝΟΣΙΑ ΑΝΤΙΓΟΝΟ 3. Η πρόσληψη του αντιγόνου και η παρουσίασή του στα λεμφοκύτταρα 4. Η αναγνώριση του αντιγόνου. Αντιγονικοί
Kυτταρική Bιολογία. Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος ΔIAΛEΞΗ 20 (9/5/2017) Δρ. Xρήστος Παναγιωτίδης, Τμήμα Φαρμακευτικής Α.Π.Θ.
 Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
Kυτταρική Bιολογία ΔIAΛEΞΗ 20 (9/5/2017) Απόπτωση, ή Προγραμματισμένος Κυτταρικός Θάνατος Τι είναι απόπτωση; Απόπτωση είναι ο προγραμματισμένος κυτταρικός θάνατος Η καταστροφή του κυττάρου γίνεται «ήπια»
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
Βασικοί μηχανισμοί προσαρμογής
 ΣΥΓΚΡΙΤΙΚΗ ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ 23-24, 18/4/2016 Π.Παπαζαφείρη Βασικοί μηχανισμοί προσαρμογής Προσαρμογή σε μοριακό και γονιδιακό επίπεδο Επίπεδα ελέγχου 1. Πρωτεïνική δράση 2. Πρωτεïνοσύνθεση 3. Ρύθμιση της
ΣΥΓΚΡΙΤΙΚΗ ΦΥΣΙΟΛΟΓΙΑ ΖΩΩΝ 23-24, 18/4/2016 Π.Παπαζαφείρη Βασικοί μηχανισμοί προσαρμογής Προσαρμογή σε μοριακό και γονιδιακό επίπεδο Επίπεδα ελέγχου 1. Πρωτεïνική δράση 2. Πρωτεïνοσύνθεση 3. Ρύθμιση της
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα
 Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
Κεφάλαιο 20 Η ρύθμιση της γονιδιακής έκφρασης στους ευκαρυωτικούς οργανισμούς
 Κεφάλαιο 20 Η ρύθμιση της γονιδιακής έκφρασης στους ευκαρυωτικούς οργανισμούς Πυρίνας ανθρώπινου μεσοφασικού κυττάρου στον οποίο παρατηρούμε, με ανοσοφθορισμό, τη διάστικτη κατανομή της απακετυλάσης των
Κεφάλαιο 20 Η ρύθμιση της γονιδιακής έκφρασης στους ευκαρυωτικούς οργανισμούς Πυρίνας ανθρώπινου μεσοφασικού κυττάρου στον οποίο παρατηρούμε, με ανοσοφθορισμό, τη διάστικτη κατανομή της απακετυλάσης των
Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης. Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010
 ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
Έλεγχος κυτταρικού κύκλου Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος
 Έλεγχος κυτταρικού κύκλου Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Πως το κύτταρο διπλασιάζει τα συστατικά του; Πως γίνεται ο διαχωρισμός των συστατικών στα
Έλεγχος κυτταρικού κύκλου Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Πως το κύτταρο διπλασιάζει τα συστατικά του; Πως γίνεται ο διαχωρισμός των συστατικών στα
ΦΡΟΝΤΙΣΤΗΡΙΟ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΗΡΑΚΛΕΙΤΟΣ ΚΩΛΕΤΤΗ
 ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΟΥΝΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ε Ν Δ Ε Ι Κ Τ Ι Κ Ε Σ Α Π Α Ν Τ Η Σ Ε Ι Σ Θ Ε Μ Α Τ Ω Ν ΘΕΜΑ Α Α1-δ Α2-δ Α3-β
ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 ΙΟΥΝΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ε Ν Δ Ε Ι Κ Τ Ι Κ Ε Σ Α Π Α Ν Τ Η Σ Ε Ι Σ Θ Ε Μ Α Τ Ω Ν ΘΕΜΑ Α Α1-δ Α2-δ Α3-β
Μεταβολικές ανάγκες ανοσοκυττάρων
 Μεταβολικές ανάγκες ανοσοκυττάρων Στέργιος Κατσιουγιάννης PhD Μεταδιδακτορικός συνεργάτης Χαροκόπειο Πανεπιστήµιο Τµήµα Επιστήµης ιαιτολογίας και ιατροφής Μεταβολισµός και Ανοσολογία Ιστορικά το καλύτερο
Μεταβολικές ανάγκες ανοσοκυττάρων Στέργιος Κατσιουγιάννης PhD Μεταδιδακτορικός συνεργάτης Χαροκόπειο Πανεπιστήµιο Τµήµα Επιστήµης ιαιτολογίας και ιατροφής Μεταβολισµός και Ανοσολογία Ιστορικά το καλύτερο
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου
 Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Η αναλογία Α+G/T+C στο γενετικό υλικό ενός ιού είναι ίση με 2/3. Ο ιός μπορεί να είναι: α. ο φάγος λ. β. ο ιός της πολιομυελίτιδας. γ. φορέας κλωνοποίησης
Βιολογία Ο.Π. Θετικών Σπουδών Γ' Λυκείου ΘΕΜΑ Α Α1. Η αναλογία Α+G/T+C στο γενετικό υλικό ενός ιού είναι ίση με 2/3. Ο ιός μπορεί να είναι: α. ο φάγος λ. β. ο ιός της πολιομυελίτιδας. γ. φορέας κλωνοποίησης
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΛΙΝΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΚΑΙ ΜΕΛΕΤΗ ΙΣΟΜΟΡΦΩΝ ΤΗΣ L-DOPA ΑΠΟΚΑΡΒΟΞΥΛΑΣΗΣ ΚΑΙ ΤΟΥ
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΛΙΝΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΚΑΙ ΜΕΛΕΤΗ ΙΣΟΜΟΡΦΩΝ ΤΗΣ L-DOPA ΑΠΟΚΑΡΒΟΞΥΛΑΣΗΣ ΚΑΙ ΤΟΥ
Φλοιοτρόπος ορμόνη ή Κορτικοτροπίνη (ACTH) και συγγενή πεπτίδια
 ΕΠΙΝΕΦΡΙΔΙΑ Φλοιοτρόπος ορμόνη ή Κορτικοτροπίνη (ACTH) και συγγενή πεπτίδια 39 αμινοξέα Μ.Β. 4500 προοπιομελανοκορτίνη(pomc) 1. κορτικοτροπίνη (ACTH), 2. β λιποτροφίνη (β LPH), 3. γ λιποτροφίνη (γ LPH),
ΕΠΙΝΕΦΡΙΔΙΑ Φλοιοτρόπος ορμόνη ή Κορτικοτροπίνη (ACTH) και συγγενή πεπτίδια 39 αμινοξέα Μ.Β. 4500 προοπιομελανοκορτίνη(pomc) 1. κορτικοτροπίνη (ACTH), 2. β λιποτροφίνη (β LPH), 3. γ λιποτροφίνη (γ LPH),
ΦΡΟΝΤΙΣΤΗΡΙΑ ΠΡΟΟΠΤΙΚΗ
 Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
ΒΙΟΛΟΓΙΑ ΤΗΣ IDO ΚΕΡΕΝΙΔΗ ΝΟΡΑ
 ΒΙΟΛΟΓΙΑ ΤΗΣ IDO ΚΕΡΕΝΙΔΗ ΝΟΡΑ Η ύπαρξη του όγκου κινητοποιεί ανοσιακή απάντηση που περιλαμβάνει όλους τους ανοσοδραστικούς μηχανισμούς. Aυτόματη υποστροφή του καρκίνου είναι εξαιρετικά σπάνια Oι ανοσιακές
ΒΙΟΛΟΓΙΑ ΤΗΣ IDO ΚΕΡΕΝΙΔΗ ΝΟΡΑ Η ύπαρξη του όγκου κινητοποιεί ανοσιακή απάντηση που περιλαμβάνει όλους τους ανοσοδραστικούς μηχανισμούς. Aυτόματη υποστροφή του καρκίνου είναι εξαιρετικά σπάνια Oι ανοσιακές
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων. Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014. Απαντήσεις Θεμάτων
 Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Πανελλήνιες Εξετάσεις Ημερήσιων Γενικών Λυκείων Εξεταζόμενο Μάθημα: Βιολογία Θετικής Κατεύθυνσης, Ημ/νία: 04 Ιουνίου 2014 Απαντήσεις Θεμάτων ΘΕΜΑ Α A1. Τα πλασμίδια είναι: δ. κυκλικά δίκλωνα μόρια DNA
Η µελέτη της ρύθµισης της πρωτεινοσύνθεσης στο επίπεδο του Ριβοσώµατος εντοπίζεται σε τρία επίπεδα
 Η µελέτη της ρύθµισης της πρωτεινοσύνθεσης στο επίπεδο του Ριβοσώµατος εντοπίζεται σε τρία επίπεδα ΣτονΣτον ρόλο των διαφόρων οµάδων των ριβοσωµικών πρωτεινών. Κατά πόσο δηλαδή υπάρχει ετερογένεια στις
Η µελέτη της ρύθµισης της πρωτεινοσύνθεσης στο επίπεδο του Ριβοσώµατος εντοπίζεται σε τρία επίπεδα ΣτονΣτον ρόλο των διαφόρων οµάδων των ριβοσωµικών πρωτεινών. Κατά πόσο δηλαδή υπάρχει ετερογένεια στις
ΚΕΦΑΛΑΙΟ 11. Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα
 ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ. ΘΕΜΑ Β Β1. Στήλη Ι Στήλη ΙΙ 1 Α 2 Γ 3 Α 4 Β 5 Α 6 Α 7 Γ
 ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ 1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β) ΠΑΡΑΣΚΕΥΗ 27 ΜΑΪΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ ΣΥΣΤΗΜΑ) ΒΙΟΛΟΓΙΑ
ΘΕΜΑ Α Α1. β Α2. β Α3. δ Α4. γ Α5. γ 1 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΔΑ Β) ΠΑΡΑΣΚΕΥΗ 27 ΜΑΪΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ (ΝΕΟ ΣΥΣΤΗΜΑ) ΒΙΟΛΟΓΙΑ
ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ 2017 ΑΠΑΝΤΗΣΕΙΣ ËÁÌÉÁ
 ΘΕΜΑ Α Α1: δ Α2: δ Α3: β Α4: γ Α5: α ΘΕΜΑ Β ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ 2017 ΑΠΑΝΤΗΣΕΙΣ Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII - Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Αυτό
ΘΕΜΑ Α Α1: δ Α2: δ Α3: β Α4: γ Α5: α ΘΕΜΑ Β ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ 2017 ΑΠΑΝΤΗΣΕΙΣ Β1. Ι Α, ΙΙ Ε, ΙΙΙ ΣΤ, ΙV Β, V Ζ, VII Γ, VII - Β2. Η εικόνα 1 αντιστοιχεί σε προκαρυωτικό κύτταρο. Αυτό
ΑΠΑΝΤΗΣΕΙΣ ΣΤΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ 2107 ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ ΛΥΚΕΙΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ Β Β1. Ι: κωδική αλυσίδα (Δ) ΙΙ: μεταγραφόμενη αλυσίδα (Γ) ΙΙΙ: αμινομάδα (ΣΤ) ΙV: mrna (Β) V: RNA πολυμεράση (Ζ) VI: φωσφορική
ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ ΛΥΚΕΙΟΥ ΘΕΜΑ Β Β1. Ι: κωδική αλυσίδα (Δ) ΙΙ: μεταγραφόμενη αλυσίδα (Γ) ΙΙΙ: αμινομάδα (ΣΤ) ΙV: mrna (Β) V: RNA πολυμεράση (Ζ) VI: φωσφορική
«ΕΜΒΙΟΜΗΧΑΝΙΚΗ ΣΤΗΝ ΚΑΡΚΙΝΟΓΕΝΕΣΗ: ΒΙΟΧΗΜΙΚΑ ΜΟΝΟΠΑΤΙΑ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΟΠΤΙΚΕΣ»
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΚΗΣ ΧΗΜΕΙΑΣ ΜΟΝΑΔΑ ΚΥΤΤΑΡΙΚΗΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΕΜΒΙΟΜΗΧΑΝΙΚΗΣ «ΕΜΒΙΟΜΗΧΑΝΙΚΗ ΣΤΗΝ ΚΑΡΚΙΝΟΓΕΝΕΣΗ: ΒΙΟΧΗΜΙΚΑ ΜΟΝΟΠΑΤΙΑ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΟΠΤΙΚΕΣ»
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΚΗΣ ΧΗΜΕΙΑΣ ΜΟΝΑΔΑ ΚΥΤΤΑΡΙΚΗΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΕΜΒΙΟΜΗΧΑΝΙΚΗΣ «ΕΜΒΙΟΜΗΧΑΝΙΚΗ ΣΤΗΝ ΚΑΡΚΙΝΟΓΕΝΕΣΗ: ΒΙΟΧΗΜΙΚΑ ΜΟΝΟΠΑΤΙΑ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΟΠΤΙΚΕΣ»
Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΒΙΟΛΟΓΙΑ ΑΠΑΝΤΗΣΕΙΣ ÏÅÖÅ
 1 Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΒΙΟΛΟΓΙΑ ΘΕΜΑ 1 ο Α. 1 - Γ 2 - Β 3-4 - Γ 5 - Β. 1 - Σ 2 - Λ 3 - Λ 4 - Λ 5 - Σ ΘΕΜΑ 2 ο ΑΠΑΝΤΗΣΕΙΣ 1. Κάθε είδος αντισώµατος που αναγνωρίζει έναν αντιγονικό καθοριστή παράγεται
1 Γ' ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΒΙΟΛΟΓΙΑ ΘΕΜΑ 1 ο Α. 1 - Γ 2 - Β 3-4 - Γ 5 - Β. 1 - Σ 2 - Λ 3 - Λ 4 - Λ 5 - Σ ΘΕΜΑ 2 ο ΑΠΑΝΤΗΣΕΙΣ 1. Κάθε είδος αντισώµατος που αναγνωρίζει έναν αντιγονικό καθοριστή παράγεται
Τα ορμονικά μόρια και η διαχείριση τους μέσα στο φυτό
 Φυσιολογία Φυτών Διαχείριση ορμονικών μορίων Τα ορμονικά μόρια και η διαχείριση τους μέσα στο φυτό Φυσιολογία Φυτών 3 ου Εξαμήνου Δ. Μπουράνης, Σ. Χωριανοπούλου 1 Φυσιολογία Φυτών Διαχείριση ορμονικών
Φυσιολογία Φυτών Διαχείριση ορμονικών μορίων Τα ορμονικά μόρια και η διαχείριση τους μέσα στο φυτό Φυσιολογία Φυτών 3 ου Εξαμήνου Δ. Μπουράνης, Σ. Χωριανοπούλου 1 Φυσιολογία Φυτών Διαχείριση ορμονικών
ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΤΟΣ ΚΑΡΚΙΝΟΣ ΚΑΙ ΜΕΤΑΛΛΑΞΕΙΣ
 ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΤΟΣ 2012-2013 ΚΑΡΚΙΝΟΣ ΚΑΙ ΜΕΤΑΛΛΑΞΕΙΣ Τι είναι ο καρκίνος ; Ο Καρκίνος είναι ένα από τα σοβαρότερα προβλήματα υγείας που παρατηρούνται σήμερα στις αναπτυγμένες χώρες. Οι στατιστικές
ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΤΟΣ 2012-2013 ΚΑΡΚΙΝΟΣ ΚΑΙ ΜΕΤΑΛΛΑΞΕΙΣ Τι είναι ο καρκίνος ; Ο Καρκίνος είναι ένα από τα σοβαρότερα προβλήματα υγείας που παρατηρούνται σήμερα στις αναπτυγμένες χώρες. Οι στατιστικές
ΒΑΣΙΚΕΣ ΔΟΜΕΣ - ΤΟ ΚΥΤΤΑΡΟ
 ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ I ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιμος Π. Βανδώρος ΒΑΣΙΚΕΣ ΔΟΜΕΣ - ΤΟ ΚΥΤΤΑΡΟ Οι βασικές δομές που εξετάζουμε στην ανατομία μπορούν ιεραρχικά να ταξινομηθούν ως εξής:
ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ I ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιμος Π. Βανδώρος ΒΑΣΙΚΕΣ ΔΟΜΕΣ - ΤΟ ΚΥΤΤΑΡΟ Οι βασικές δομές που εξετάζουμε στην ανατομία μπορούν ιεραρχικά να ταξινομηθούν ως εξής:
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής
 Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
Ρύθµιση κυτταρικής λειτουργίας. Μεταγωγή σήµατος
 Ρύθµιση κυτταρικής λειτουργίας Μεταγωγή σήµατος 1 Εισαγωγή Η διαδικασία εξέλιξης των πολυκύτταρων οργανισµών (πρίν 2.5 δις χρόνια) άρχισε πολύ πιο αργά από την ύπαρξη των µονοκύτταρων οργανισµών (πρίν
Ρύθµιση κυτταρικής λειτουργίας Μεταγωγή σήµατος 1 Εισαγωγή Η διαδικασία εξέλιξης των πολυκύτταρων οργανισµών (πρίν 2.5 δις χρόνια) άρχισε πολύ πιο αργά από την ύπαρξη των µονοκύτταρων οργανισµών (πρίν
ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ. Σχηµατική απεικόνιση της µεγάλης και της µικρής κυκλοφορίας
 ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
Εισαγωγή στη Γενετική και στη Γονιδιωματική Τι είναι η κληρονομικότητα, και πώς μεταβιβάζεται η πληροφορία από γενιά σε γενιά;
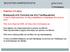 ΒΙΟΛΟΓΙΚΗ ΑΝΘΡΩΠΟΛΟΓΙΑ 12 26/10/2016 Κεφάλαιο 3 Α μέρος Εισαγωγή στη Γενετική και στη Γονιδιωματική Τι είναι η κληρονομικότητα, και πώς μεταβιβάζεται η πληροφορία από γενιά σε γενιά; Ποια είναι η δομή
ΒΙΟΛΟΓΙΚΗ ΑΝΘΡΩΠΟΛΟΓΙΑ 12 26/10/2016 Κεφάλαιο 3 Α μέρος Εισαγωγή στη Γενετική και στη Γονιδιωματική Τι είναι η κληρονομικότητα, και πώς μεταβιβάζεται η πληροφορία από γενιά σε γενιά; Ποια είναι η δομή
ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ
 Επαναληπτικό διαγώνισμα ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΑ 1-9 ΗΜΕΡΟΜΗΝΙΑ 1/3/2015 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ Σημείωση: η διπλή αρίθμηση στις σελίδες αφορά την παλιά και τη νέα έκδοση του σχολικού βιβλίου
Επαναληπτικό διαγώνισμα ΒΙΟΛΟΓΙΑΣ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΚΕΦΑΛΑΙΑ 1-9 ΗΜΕΡΟΜΗΝΙΑ 1/3/2015 ΕΝΔΕΙΚΤΙΚΕΣ ΑΠΑΝΤΗΣΕΙΣ Σημείωση: η διπλή αρίθμηση στις σελίδες αφορά την παλιά και τη νέα έκδοση του σχολικού βιβλίου
3. Η μέθοδος αλυσιδωτής αντίδρασης πολυμεράσης (PCR) επιτρέπει την επιλεκτική αντιγραφή μορίων DNA, χωρίς τη μεσολάβηση ζωικών κυττάρων.
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΘΕΜΑ 1ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 3 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΤΕΣΣΕΡΙΣ (4) Α. Να γράψετε τον αριθμό της
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΘΕΜΑ 1ο ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 3 ΙΟΥΝΙΟΥ 2003 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΤΕΣΣΕΡΙΣ (4) Α. Να γράψετε τον αριθμό της
Osteogenesis Imperfecta (Ατελής Οστεογένεση ) Ομάδα: Πατρασκάκη Μυρτώ Τσιτσικλή Μαγδαληνή
 Osteogenesis Imperfecta (Ατελής Οστεογένεση ) Ομάδα: Πατρασκάκη Μυρτώ Τσιτσικλή Μαγδαληνή Osteogenesis imperfecta Μενδελικό Νόσημα Συχνότητα στον πληθυσμό: 1:20.000 80-95% αυτοσωμικό επικρατές 10-15% αυτοσωμικό
Osteogenesis Imperfecta (Ατελής Οστεογένεση ) Ομάδα: Πατρασκάκη Μυρτώ Τσιτσικλή Μαγδαληνή Osteogenesis imperfecta Μενδελικό Νόσημα Συχνότητα στον πληθυσμό: 1:20.000 80-95% αυτοσωμικό επικρατές 10-15% αυτοσωμικό
ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ
 ΑΣΘΕΝΕΙΕΣ ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑΣ ΣΥΝΕΠΕΙΕΣ ΕΙΔΟΣ ΜΕΤΑΛΛΑΞΗΣ Οικογενή υπερχοληστερολαιμία Αυτοσωμική επικρατής κληρονομικότητα Σχετίζεται με αυξημένο
ΑΣΘΕΝΕΙΕΣ ΚΑΤΑΛΟΓΟΣ ΑΣΘΕΝΕΙΩΝ ΠΟΥ ΑΝΑΦΕΡΟΝΤΑΙ ΣΤΟ ΣΧΟΛΙΚΟ ΕΓΧΕΙΡΙΔΙΟ ΤΡΟΠΟΣ ΚΛΗΡΟΝΟΜΙΚΟΤΗΤΑΣ ΣΥΝΕΠΕΙΕΣ ΕΙΔΟΣ ΜΕΤΑΛΛΑΞΗΣ Οικογενή υπερχοληστερολαιμία Αυτοσωμική επικρατής κληρονομικότητα Σχετίζεται με αυξημένο
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΙ ΠΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΙ ΠΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ Αλληλεπιδράσεις πρωτεϊνών του ενδοσυμβιωτικού ιού του παρασιτοειδούς υμενόπτερου Cotesia congregata
ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΙ ΠΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ Αλληλεπιδράσεις πρωτεϊνών του ενδοσυμβιωτικού ιού του παρασιτοειδούς υμενόπτερου Cotesia congregata
ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ
 1 ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ Οι δύο πολυνουκλεοτιδικές αλυσίδες του DNA αποτελούνται από νουκλεοτίδια τα οποία ενώνονται με φωσφοδιεστερικούς δεσμούς. Πιο συγκεκριμένα
1 ΕΝΟΤΗΤΑ 14: Ο ΦΟΡΕΑΣ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ (DNA) 14.1 ΕΙΣΑΓΩΓΗ Οι δύο πολυνουκλεοτιδικές αλυσίδες του DNA αποτελούνται από νουκλεοτίδια τα οποία ενώνονται με φωσφοδιεστερικούς δεσμούς. Πιο συγκεκριμένα
HPV DNA, E6, E7, L1, L2, E2, p16, prb, κυκλίνες, κινάσες, Ki67. Τι από όλα αυτά πρέπει να γνωρίζει ο κλινικός γιατρός; Αλέξανδρος Λαµπρόπουλος
 HPV DNA, E6, E7, L1, L2, E2, p16, prb, κυκλίνες, κινάσες, Ki67. Τι από όλα αυτά πρέπει να γνωρίζει ο κλινικός γιατρός; Αλέξανδρος Λαµπρόπουλος δεν υπάρχει σύγκρουση συµφερόντων Ø Ποιό HPV τεστ είναι το
HPV DNA, E6, E7, L1, L2, E2, p16, prb, κυκλίνες, κινάσες, Ki67. Τι από όλα αυτά πρέπει να γνωρίζει ο κλινικός γιατρός; Αλέξανδρος Λαµπρόπουλος δεν υπάρχει σύγκρουση συµφερόντων Ø Ποιό HPV τεστ είναι το
Αύξηση. Αύξηση λόγω: -κυτταρικών διαιρέσεων (κυρίως) & κυτταρικού θανάτουαπόπτωσης
 Αύξηση Αύξηση λόγω: -κυτταρικών διαιρέσεων (κυρίως) & κυτταρικού θανάτουαπόπτωσης -αύξηση μεγέθους κυττάρων Ελάχιστα μελετημένος ο συνολικός έλεγχος της αύξησης Πώς ρυθμίζεται το μέγεθος ενός οργανισμού;
Αύξηση Αύξηση λόγω: -κυτταρικών διαιρέσεων (κυρίως) & κυτταρικού θανάτουαπόπτωσης -αύξηση μεγέθους κυττάρων Ελάχιστα μελετημένος ο συνολικός έλεγχος της αύξησης Πώς ρυθμίζεται το μέγεθος ενός οργανισμού;
Καρκίνος. Note: Σήμερα όμως πάνω από το 50% των διαφόρων καρκινικών τύπων είναι θεραπεύσιμοι
 Ο πιο απλός ορισμός είναι ότι ο καρκίνος είναι μια ομάδα ασθενειών που χαρακτηρίζεται από ανεξέλεγκτη ανάπτυξη και διασπορά ανώμαλων κυττάρων. Αν η εξάπλωση δεν ελεγχθεί θα οδηγήσει στο θάνατο. Ποσοστό
Ο πιο απλός ορισμός είναι ότι ο καρκίνος είναι μια ομάδα ασθενειών που χαρακτηρίζεται από ανεξέλεγκτη ανάπτυξη και διασπορά ανώμαλων κυττάρων. Αν η εξάπλωση δεν ελεγχθεί θα οδηγήσει στο θάνατο. Ποσοστό
ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ
 1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο 1. β 2. γ 3. α 4. γ 5. δ ΘΕΜΑ 2ο 1. Σχολικό
1 ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 1 ΙΟΥΛΙΟΥ 2004 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο 1. β 2. γ 3. α 4. γ 5. δ ΘΕΜΑ 2ο 1. Σχολικό
ΘΕΜΑ Α Α1. γ Α2. γ Α3. α Α4. β Α5. β ΘΕΜΑ B B1. B2.
 ΘΕΜΑ Α Α1. γ (το πριμόσωμα) Α2. γ (οι υποκινητές και οι μεταγραφικοί παράγοντες κάθε γονιδίου) Α3. α (μεταφέρει ένα συγκεκριμένο αμινοξύ στο ριβόσωμα) Α4. β (αποδιάταξη των δύο συμπληρωματικών αλυσίδων)
ΘΕΜΑ Α Α1. γ (το πριμόσωμα) Α2. γ (οι υποκινητές και οι μεταγραφικοί παράγοντες κάθε γονιδίου) Α3. α (μεταφέρει ένα συγκεκριμένο αμινοξύ στο ριβόσωμα) Α4. β (αποδιάταξη των δύο συμπληρωματικών αλυσίδων)
Ποιες είναι οι ομοιότητες και οι διαφορές μεταξύ της αντιγραφής και της
 ΚΕΦ. 2 ο ΕΡΩΤΗΣΕΙΣ ΚΡΙΣΕΩΣ Ποιες είναι οι ομοιότητες και οι διαφορές μεταξύ της αντιγραφής και της μεταγραφής; Διαφορές Αντιγραφή Μεταγραφή 1. Διατηρείται και μεταβιβάζεται η 1. Μεταβιβάζεται η γενετική
ΚΕΦ. 2 ο ΕΡΩΤΗΣΕΙΣ ΚΡΙΣΕΩΣ Ποιες είναι οι ομοιότητες και οι διαφορές μεταξύ της αντιγραφής και της μεταγραφής; Διαφορές Αντιγραφή Μεταγραφή 1. Διατηρείται και μεταβιβάζεται η 1. Μεταβιβάζεται η γενετική
 94 95 96 97 98 Ο ρόλος της αγγειογένεσης στη μετάσταση Η νεοαγγείωση αποτελεί ένα απαραίτητο τμήμα της ογκογόνου διεργασίας που διασφαλίζει τη γρηγορότερη και ανεμπόδιστη ανάπτυξη του όγκου. Η λειτουργική
94 95 96 97 98 Ο ρόλος της αγγειογένεσης στη μετάσταση Η νεοαγγείωση αποτελεί ένα απαραίτητο τμήμα της ογκογόνου διεργασίας που διασφαλίζει τη γρηγορότερη και ανεμπόδιστη ανάπτυξη του όγκου. Η λειτουργική
ΚΕΦΑΛΑΙΟ 16. Ο κυτταρικός κύκλος. Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1
 ΚΕΦΑΛΑΙΟ 16 Ο κυτταρικός κύκλος Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 16.1 Οι φάσεις του κυτταρικού κύκλου. Ο κύκλος διαίρεσης των περισσότερων ευκαρυωτικών κυττάρων χωρίζεται
ΚΕΦΑΛΑΙΟ 16 Ο κυτταρικός κύκλος Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 16.1 Οι φάσεις του κυτταρικού κύκλου. Ο κύκλος διαίρεσης των περισσότερων ευκαρυωτικών κυττάρων χωρίζεται
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΤΑΞΗ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 2 ΙΟΥΝΙΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΒΙΟΛΟΓΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Α. Για τις ημιτελείς προτάσεις
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Σ ΕΣΠΕΡΙΝΟΥ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 2 ΙΟΥΝΙΟΥ 2006 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ: ΒΙΟΛΟΓΙΑ ΣΥΝΟΛΟ ΣΕΛΙ ΩΝ: ΠΕΝΤΕ (5) ΘΕΜΑ 1ο Α. Για τις ημιτελείς προτάσεις
Αρχές μοριακής παθολογίας. Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ
 Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Μοριακή βάση του καρκίνου της ουροδόχου κύστεως
 Πανεπιστήμιο Αθηνών Τμήμα Βιολογίας Τομέας Βιοχημείας & Μοριακής Βιολογίας Μοριακή βάση του καρκίνου της ουροδόχου κύστεως Μαργαρίτης Αυγέρης, Ανδρέας Σκορίλας Τομέας Βιοχημείας και Μοριακής Βιολογίας,
Πανεπιστήμιο Αθηνών Τμήμα Βιολογίας Τομέας Βιοχημείας & Μοριακής Βιολογίας Μοριακή βάση του καρκίνου της ουροδόχου κύστεως Μαργαρίτης Αυγέρης, Ανδρέας Σκορίλας Τομέας Βιοχημείας και Μοριακής Βιολογίας,
ΑΝΟΣΟΒΙΟΛΟΓΙΑ. Εξεταστική Ιανουαρίου 2010
 Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
Εξεταστική Ιανουαρίου 2010 Ποιες είναι οι διαφορές μιας πρωτογενούς από μια δευτερογενή χυμική ανοσολογική απόκριση; Περιγράψετε τους μηχανισμούς ενεργοποίησης στις δυο περιπτώσεις. ΘΕΜΑ 2 (1 μονάδα) Περιγράψετε
Β1. Β2. ΘΕΜΑ 2ο 1. 2.
 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΠΑΡΑΣΚΕΥΗ 20 ΣΕΠΤΕΜΒΡΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: BΙΟΛΟΓΙΑ (ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο Α1.
1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΠΑΡΑΣΚΕΥΗ 20 ΣΕΠΤΕΜΒΡΙΟΥ 2002 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: BΙΟΛΟΓΙΑ (ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ) ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1ο Α1.
ΠΕΤΡΟΣ ΔΕΔΕΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΣΙ ΠΕΡΙΛΗΨΗ
 ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΣΙ ΠΕΡΙΛΗΨΗ Το οστό αποτελεί ένα ιδανικό περιβάλλον για μετάσταση, καθώς η συνεχής και δυναμική ανάπλασή τον παρέχει μια γόνιμη βάση για την παλιννόστηση και τον πολλαπλασιασμό των καρκινικών
ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΣΙ ΠΕΡΙΛΗΨΗ Το οστό αποτελεί ένα ιδανικό περιβάλλον για μετάσταση, καθώς η συνεχής και δυναμική ανάπλασή τον παρέχει μια γόνιμη βάση για την παλιννόστηση και τον πολλαπλασιασμό των καρκινικών
ΑΠΑΝΤΗΣΕΙΣ. ΘΕΜΑ Α Α1. γ Α2. α Α3. δ Α4. β Α5. α
 ΘΕΜΑ Α Α1. γ Α2. α Α3. δ Α4. β Α5. α 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 5 ΣΕΠΤΕΜΒΡΙΟΥ 2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ:
ΘΕΜΑ Α Α1. γ Α2. α Α3. δ Α4. β Α5. α 1 ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΤΕΤΑΡΤΗ 5 ΣΕΠΤΕΜΒΡΙΟΥ 2012 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ:
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
