ΤΟΜΟΓΡΑΦΙΑ ΕΚΠΟΜΠΗΣ ΠΟΖΙΤΡΟΝΙΩΝ (PET/CT SCAN) ΣΤΟ ΛΕΜΦΩΜΑ HODGKIN. ΣΥΣΧΕΤΙΣΗ ΜΕ ΤΗ ΘΕΡΑΠΕΥΤΙΚΗ ΣΤΡΑΤΗΓΙΚΗ ΚΑΙ ΤΗΝ ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ
|
|
|
- Θεοδοσία Λιακόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΑΙΜΑΤΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΤΟΜΟΓΡΑΦΙΑ ΕΚΠΟΜΠΗΣ ΠΟΖΙΤΡΟΝΙΩΝ (PET/CT SCAN) ΣΤΟ ΛΕΜΦΩΜΑ HODGKIN. ΣΥΣΧΕΤΙΣΗ ΜΕ ΤΗ ΘΕΡΑΠΕΥΤΙΚΗ ΣΤΡΑΤΗΓΙΚΗ ΚΑΙ ΤΗΝ ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ Ευτυχία Π. Μόσα Ιατρός Ακτινοθεραπεύτρια Ογκολόγος Διδακτορική Διατριβή Αθήνα, 2017
2 ΤΡΙΜΕΛΗΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗ ΕΠΙΤΡΟΠΗ Μ. Κ. ΑΓΓΕΛΟΠΟΥΛΟΥ Αναπληρώτρια Καθηγήτρια Αιματολογίας ( Επιβλέπουσα Καθηγήτρια) Θ. Π. ΒΑΣΙΛΑΚΟΠΟΥΛΟΣ Αναπληρωτής Καθηγητής Αιματολογίας Β. Ε. ΚΟΥΛΟΥΛΙΑΣ Αναπληρωτής Καθηγητής Ακτινοθεραπευτικής Ογκολογίας 2
3 Εθνικό και Καποδιστριακό Πανεπιστήμιο Αθηνών - Ιατρική Σχολή Αιματολογική Κλινική, Διευθυντής: Καθηγητής Κωνσταντόπουλος Κωνσταντίνος Υποψήφια Διδάκτορας: Ευτυχία Μόσα, Ιατρός Ακτινοθεραπεύτρια - Ογκολόγος Επιβλέπουσα Καθηγήτρια: Μαρία Αγγελοπούλου,Αναπληρώτρια Καθηγήτρια Αιματολογίας Τόπος εκπόνησης Διδακτορικής Διατριβής: Αιματολογική Κλινική Πανεπιστημίου Αθηνών Γνωστικό Αντικείμενο: «Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT SCAN) στο Λέμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία» Τριμελής Συμβουλευτική Επιτροπή: 1. Μαρία Αγγελοπούλου: Αναπληρώτρια Καθηγήτρια Αιματολογίας 2. Θεόδωρος Βασιλακόπουλος: Aναπληρωτής Καθηγητής Αιματολογίας 3. Βασίλειος Κουλουλίας: Αναπληρωτής Καθηγητής Ακτινοθεραπευτικής Ογκολογίας Ημερομηνία Υποβολής Αίτησης Διδακτορικής Διατριβής: 16/7/2010 Ημερομηνία Ορισμού Τριμελούς Επιτροπής: 26/7/2010 Ημερομηνία Υποβολής Πρωτοκόλλου Έρευνας: 19/11/2010 Ημερομηνία Υποβολής 1 ης Έκθεσης Προόδου: 24/7/2013 Ημερομηνία Υποβολής 2 ης Έκθεσης Προόδου: 26/6/2015 Ημερομηνία Υποβολής 3 ης Έκθεσης Προόδου: 20/10/2017 Ημερομηνία Ορισμού Επταμελούς Εξεταστικής Επιτροπής: 20/10/2017 Επταμελής Εξεταστική Επιτροπή: 1. Κωνσταντόπουλος Κων/νος, Καθηγητής Αιματολογίας 2. Μαρία Αγγελοπούλου,Αναπληρώτρια Καθηγήτρια Αιματολογίας 3. Θεόδωρος Βασιλακόπουλος, Αναπληρωτής Καθηγητής Αιματολογίας 4. Βασίλειος Κουλουλίας, Αναπληρωτής Καθηγητής Ακτινοθεραπευτικής Ογκολογίας 5. Χατζηίωαννου Σοφία, Αναπληρώτρια Καθηγήτρια Πυρηνικής Ιατρικής, Διευθύντρια ΡΕΤ/CT 6. Σιακαντάρη Μαρίνα, Αναπληρωτρια Καθηγήτρια Αιματολογίας 7. Τόλια Μαρία, Επίκουρη Καθηγήτρια Ακτινοθεραπείας 3
4 Στους Γονείς μου στον Άνθρωπο που υπήρξε ανεκτίμητος βοηθός και συμπαραστάτης στο εγχείρημα αυτό και στη Λι, το Νικόλα, την Αγγελίνα Στους Καθηγητές και Δασκάλους μου και στους Ασθενείς που δε σταματούν ποτέ να Ελπίζουν και να Αγωνίζονται 4
5 ΟΡΚΟΣ ΤΟΥ ΙΠΠΟΚΡΑΤΗ Ὄμνυμι Ἀπόλλωνα ἰητρὸν, καὶ Ἀσκληπιὸν, καὶ Ὑγείαν, καὶ Πανάκειαν, καὶ θεοὺς πάντας τε καὶ πάσας, ἵστορας ποιεύμενος, ἐπιτελέα ποιήσειν κατὰ δύναμιν καὶ κρίσιν ἐμὴν ὅρκον τόνδε καὶ ξυγγραφὴν τήνδε. Ἡγήσασθαι μὲν τὸν διδάξαντά με τὴν τέχνην ταύτην ἴσα γενέτῃσιν ἐμοῖσι, καὶ βίου κοινώσασθαι, καὶ χρεῶν χρηίζοντι μετάδοσιν ποιήσασθαι, καὶ γένος τὸ ἐξ ωὐτέου ἀδελφοῖς ἴσον ἐπικρινέειν ἄῤῥεσι, καὶ διδάξειν τὴν τέχνην ταύτην, ἢν χρηίζωσι μανθάνειν, ἄνευ μισθοῦ καὶ ξυγγραφῆς, παραγγελίης τε καὶ ἀκροήσιος καὶ τῆς λοιπῆς ἁπάσης μαθήσιος μετάδοσιν ποιήσασθαι υἱοῖσί τε ἐμοῖσι, καὶ τοῖσι τοῦ ἐμὲ διδάξαντος, καὶ μαθηταῖσι συγγεγραμμένοισί τε καὶ ὡρκισμένοις νόμῳ ἰητρικῷ, ἄλλῳ δὲ οὐδενί. Διαιτήμασί τε χρήσομαι ἐπ' ὠφελείῃ καμνόντων κατὰ δύναμιν καὶ κρίσιν ἐμὴν, ἐπὶ δηλήσει δὲ καὶ ἀδικίῃ εἴρξειν. Οὐ δώσω δὲ οὐδὲ φάρμακον οὐδενὶ αἰτηθεὶς θανάσιμον, οὐδὲ ὑφηγήσομαι ξυμβουλίην τοιήνδε. Ὁμοίως δὲ οὐδὲ γυναικὶ πεσσὸν φθόριον δώσω. Ἁγνῶς δὲ καὶ ὁσίως διατηρήσω βίον τὸν ἐμὸν καὶ τέχνην τὴν ἐμήν. Οὐ τεμέω δὲ οὐδὲ μὴν λιθιῶντας, ἐκχωρήσω δὲ ἐργάτῃσιν ἀνδράσι πρήξιος τῆσδε. Ἐς οἰκίας δὲ ὁκόσας ἂν ἐσίω, ἐσελεύσομαι ἐπ' ὠφελείῃ καμνόντων, ἐκτὸς ἐὼν πάσης ἀδικίης ἑκουσίης καὶ φθορίης, τῆς τε ἄλλης καὶ ἀφροδισίων ἔργων ἐπί τε γυναικείων σωμάτων καὶ ἀνδρῴων, ἐλευθέρων τε καὶ δούλων. Ἃ δ' ἂν ἐν θεραπείῃ ἢ ἴδω, ἢ ἀκούσω, ἢ καὶ ἄνευ θεραπηίης κατὰ βίον ἀνθρώπων, ἃ μὴ χρή ποτε ἐκλαλέεσθαι ἔξω, σιγήσομαι, ἄῤῥητα ἡγεύμενος εἶναι τὰ τοιαῦτα. Ὅρκον μὲν οὖν μοι τόνδε ἐπιτελέα ποιέοντι, καὶ μὴ ξυγχέοντι, εἴη ἐπαύρασθαι καὶ βίου καὶ τέχνης δοξαζομένῳ παρὰ πᾶσιν ἀνθρώποις ἐς τὸν αἰεὶ χρόνον. παραβαίνοντι δὲ καὶ ἐπιορκοῦντι, τἀναντία τουτέω 5
6 ΣΥΝΤΟΜΟ ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ Ευτυχίας Π. Μόσα MD, MSc Ακτινοθεραπεύτριας-Ογκολόγου 1. ΠΑΡΟΥΣΑ ΘΕΣΗ Σεπτέμβρης 2015-Σήμερα: Ακτινοθεραπευτρια Ογκολόγος, Επιμελήτρια Α, στη Μονάδα Επεμβατικής Ακτινοθεραπείας-Βραχυθεραπείας Ιridium Knife,Ιατρικό Αμαρουσίου 2. ΕΚΠΑΙΔΕΥΣΗ-ΜΕΤΕΚΠΑΙΔΕΥΣΗ-ΔΙΠΛΩΜΑΤΑ Εγκύκλιες Σπουδές 2 ο Γυμνάσιο-Λύκειο Νικαίας. Απολυτήριο με «Αριστα» Προπτυχιακή Εκπαίδευση: Σεπτέμβριος 1997-Ιούλιος 2003: Ιατρική Εκπαίδευση στην Ιατρική Σχολή του Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών.Βαθμός πτυχίου: «Λίαν Καλώς» Μεταπτυχιακή Εκπαίδευση: : Εκπαίδευση στην Ιατρική Ειδικότητα της Ακτινοθεραπευτικής Ογκολογίας, ως έμμισθη ειδικευόμενη στο Α.Ο.Ν.Α «Ο Άγιος Σάββας» : Κάτοχος τίτλου μεταπτυχιακών σπουδών της Ιατρικής Σχολής του Πανεπιστημίου Αθηνών με θέμα «Νεοπλασματική Νόσος στον Άνθρωπο: Σύγχρονη Κλινικοπαθολογοανατομική Προσέγγιση και Έρευνα». Βαθμός πτυχίου: «Άριστα». 6
7 : Εξειδίκευση στην Ενδοϊστική Βραχυθεραπεία (Γερμανία-Ελλάδα) με τις μεθόδους - Ενδοϊστική βραχυθεραπεία προστάτη με τη χρήση 3D ανακατασκευή υπερηχογράφου για το σχεδιασμό ακτινοθεραπείας - Ενδοϊστική βραχυθεραπεία υπό την καθοδήγηση πολυτομικού αξονικού τομογράφου,μετά από τρισδιαστατη ανασύνθεση των εικόνων και ανακατασκευή των καθετήρων, με βελτιστοποίηση του συστήματος ONCENTRA. 9/2015-Σήμερα: Εξειδίκευση στην Ενδοϊστική Βραχυθεραπεία (Γερμανία- Ελλάδα) με τις μεθόδους - Ενδοϊστική βραχυθεραπεία προστάτη με τη χρήση 3D ανακατασκευή υπερηχογράφου για το σχεδιασμό ακτινοθεραπείας - Ενδοϊστική βραχυθεραπεία υπό την καθοδήγηση πολυτομικού αξονικού τομογράφου,μετά από τρισδιαστατη ανασύνθεση των εικόνων και ανακατασκευή των καθετήρων, με βελτιστοποίηση του συστήματος ONCENTRA Σεμινάριο και εκπαίδευση μέσω διαδικτύου από τη NIDA για τη Διεξαγωγή Κλινικών Μελετών[ GCP Training: Online Training BY nida Clinical Trials Network, Certificate of Completion available 18/12/2015 Ξένες Γλώσσες Ελληνική γλώσσα (μητρική), Αγγλικά (γραπτώς και ομιλούμενα άπταιστα), Ισπανικά (γραπτώς και ομιλούμενα άπταιστα) 7
8 ΕΠΙΣΤΗΜΟΝΙΚΗ ΔΡΑΣΤΗΡΙΟΤΗΤΑ Α) Δημοσιεύσεις σε διεθνή περιοδικά: The Significance of PET/CT in the Initial Staging of Hodgkin Lymphoma: Experience Outside Clinical Trials. Angelopoulou MK, Mosa E, Pangalis GA, Rondogianni P, Chatziioannou S, Prassopoulos V, Moschogianni M, Tsirkinidis P, Asimakopoulos JV, Konstantinou I, Tsourouflis G, Sachanas S, Yiakoumis X, Boutsikas G, Arapaki M, Gainaru G, Kyrtsonis MC, Siakantaris MP, Datseris I, Panayiotidis P, Konstantopoulos K, VassilakopoulosTP. Anticancer Res Oct;37(10): Α Retrospective Analysis of Toxicity and Efficacy for 2 Hypofractionated Irradiation Schedules Versus a Conventional One for Post-Mastectomy Adjuvant Radiotherapy in Breast Cancer. Kouloulias Vassilis, Mosa Eftychia, Zygogianni Anna, Kypraiou Efrosini, Georgakopoulos John, Platoni Kalliopi, Antypas Christos, Kyrgias George, Tolia Maria, Papadimitriou Christos, Psyrri Amanda, Patatoukas George, Dilvoi Maria, Armpilia Christina, Theodorou Kyriaki, Kalogeridi Maria-Aggeliki, Beli Ivelina, Kouvaris John, Kelekis Nikolaos. Breast Care 2016;11: Attachment orientations of Greek cancer patients in palliative care. A validation study of the Experiences in Close Relationships scale (ECR-M16). Tsilika E, Parpa E, Galanopoulou N, Gennimata V, Mosa E, Galanos A, Mystakidou K. J BUON Jul-Aug;21(4): Prognostic Significance of Serum Inflammatory Response Markers in Newly Diagnosed Non-Small Cell Lung Cancer before Chemoirradiation Tolia Maria, Tsoukalas Nikolaos, Kyrgias George, Mosa Eftychia, Maras Apostolos, Kokakis Ioannis, Liakouli Zoi, Kouvaris John R., Liaskonis Konstantinos, Charalampakis Nikolaos, Pistevou-Gombaki Kyriaki, Kelekis Nikolaos and Kouloulias Vasileios. 8
9 Hindawi Publishing Corporation, Biomed Research International, Vol 2015,Article ID: , 5 pages 5. Prognostic Value of MRS Metabolites in Postoperative Irradiated High Grade Gliomas Tolia Maria, Verganelakis Dimitrios, Tsoukalas Nikolaos, Kyrgias George, Papathanasiou Matilda, Mosa Eftychia, Kokakis Ioannis, Kouvaris John R., Pissakas George, Pistevou- Gombaki Kyriaki, Kelekis Nikolaos and Kouloulias Vasileios. Hindawi Publishing Corporation, Biomed Research International, Vol 2015, Article ID , 6 PAGES, 6. Use of Hyaluronic Acid (Cystistat) for the Treatment of Late Radiation Induced Cystitis in Patient after Prostate Irradiation Kouloulias Vassilis, Mosa Eftychia, Fotineas Andreas, Beli Ivelina, Asimakoloulos Charalampos, Chaldeopoulos Dimitrios, Chysofos Michael, Siatelis Argyris and Kelekis Nikolaos Bioequiv Availlab 2014,6:1, 7. Adjuvant chemotherapy and acute toxicity in hypofractionated radiotherapy for early breast cancer. Kouloulias V, Zygogianni A, Kypraiou E, Georgakopoulos J, Thrapsanioti Z, Beli I, Mosa E, Psyrri A, Antypas C, Arkadopoulos N, Gennatas C, Zografos G, Kyrgias G, Dilvoi M, Patatoucas G, Kelekis N, Kouvaris J World J Clin Cases Nov 16; 2(11): Doi /wjcc.v2.i PMID: [PubMed] 8. A new hypofractionated schedule of weekly irradiation for basal cell carcinoma of the head and neck skin area in elderly patients. Koululias V,Papadavid E, Mosa E, Platoni K, Papadopoulos O, Rigopoulos D, Georgakopoulos J, Beli I, Karantonis F, Castana O, Dalamaga M, Kelekis N Dermatol Ther May-Jun; Vol 27(3): PMID: [Pubmed-as supplied by publisher] 9
10 9. "Three dimensional conformal radiotherapy for hepatocellular carcinoma in patients unfit for resection, ablation or chemotherapy: A retrospective study." Kouloulias V, Mosa E, Georgakopoulos J, Platoni K, Brountzos I, Zygogianni A, Antypas C, Kosmidis P, Mystakidou K, Tolia M, Beli I, Athanasios Gouliamos, John Kouvaris and Kelekis Nikolaos. Scientific World Journal, 2013 Nov 28;2013: doi: /2013/ Evaluation of efficacy and toxicity in two different hypofractionated 3D-conformal external beam radiotherapy schedules in localized muscle invasive bladder cancer. Kouloulias V, Mosa E, Tolia M,Kantzou I, Koliarakis N, Platoni K, Georgakopoulos I, Siatelis A, Sarris G, Beli I, Chrisofos M, Kelekis N. J BUON 2013 Oct-Dec;18(4): Evaluation of acute/late toxicity and local recurrence in T1-T2 glottic carcinoma treated with accelerated hypofractionated 3D-conformal external beam radiotherapy (3DCRT) Kouloulias VE, Zygogianni A, Mosa E., Platoni K, Georgakopoulos J, Antypas C, Beli I, Tolia M, Maragoudakis P,Giotakis I, Papas Z,Psyrri A, Kelekis N, Kouvaris J. Radiol Oncol May 21; 47(2): doi: /raon Print 2013 Jun 12. Efficacy and toxicity of radiotherapy for Graves ophthalmopathy: the University of Athens experience. Kouloulias V, Kouvaris J, Zygogianni A,Mosa E, Georgakopoulos J, Theodosiadis P, Antypas C, Platoni K, Tolia M, Beli I, Alonistiotis D, Dilvoi M, Patatoukas G, Asimakopoulos C, Efstathopoulos E, Kelekis N. Head Neck Oncol Feb 6;5(2): Efficacy, cosmesis and skin toxicity in a hypofractionated irradiation schedule for cutaneous basal cell carcinoma of the head and neck area. Kouloulias V, Kouvaris J, Mosa E,Georgakopoulos J, Platoni K, Papadopoulos O, Papadavid E, Zygogianni A, Rigoppoulos D, Antypas C, Beli I, Karantonis F, Kelekis N. Head Neck Oncol 2013 Dec 21;4(5):88. 10
11 14. Electrochemotherapy in cancer patients: first clinical trial in Greece. Skarlatos I, Kyrgias G, Mosa E, Provatopoulou X, Spyrou M, Theodorou K, Lepouras A, Gounaris A, Koukourakis M.In Vivo Mar-Apr;25(2): Paraneoplastic cerebellar degeneration in a patient with pseudomyxoma peritonei and breast cancer: case report and literature review. Ardavanis A, Sykoutri D, Kountourakis P, Doufexis D, Korkolis D, Tzerbini H, Skarlatos I, Mosa E, Rigatos G. In Vivo Sep-Oct;23(5): Epithelioid haemangioendothelioma of the lung presenting with pulmonary nocardiosis. Anagnostou V, Mossa E, Mihas S, Lepouras A, Tiniakos DG. In Vivo Nov- Dec;21(6): Β) Δημοσιεύσεις σε ελληνικά περιοδικά : 1 «Ηλεκτροχημειοθεραπεία: Mία Nέα Θεραπευτική Προσέγγιση Για Τον Έλεγχο Επιδερμικών Και Υποδορίων Όγκων» Σκαρλάτος Ι 1.,Προβατοπούλου Ξ. 4, Μόσα Ε. 1, Καλογερά Ε. 4, Λέπουρας Α. 3, Κύργιας Γ. 2, Γούναρη Α. 5, Μπερούκας Κ Ά Ακτινοθεραπευτικό Ογκολογικό Τμήμα Α.Ο.Ν.Α. O Aγιος Σάββας 2. Τμήμα Ατκτινοθεραπευτικής Ογκολογίας, Πανεπιστήμιο Λάρισας 3. Β Παθολογική Κλινική Ιατρικού Κέντρου Αθηνών 4. Ελληνικό Αντικαρκινικό Ινστιτοούτο Ερευνητικό Κέντρο 5.«Γ. Παπανικολάου», Ερευνητικό Κέντρο Α.Ο.Ν.Α. «Ο Άγιος Σάββας» Forum Of Clinical Oncology, 2009 Vol 8 ( B), No 3-4 Γ) Διαλέξεις ως προσκεκλημένος ομιλητής Συνολικά 11 διαλέξεις, 31 προφορικές και αναρτημένες ανακοινώσεις σε 40 ελληνικά και 2 διεθνή συνέδρια. 11
12 Δ) Παρακολουθήσεις σε Συνέδρια Συνολικά 87 συνέδρια, ημερίδες, συμπόσια και σεμινάρια (67 Ελληνικά και 20 Διεθνή) Ε) Λοιπό Επιστημονικό Έργο 1. Ομιλητής σε μετεκπαιδευτικά μαθήματα «Διατμηματικού Προγράμματος Μεταπτυχιακών Σπουδών στην Οργάνωση και Διαχείριση της Ανακουφιστικής και Υποστηρικτικής Φροντίδας Χρονίως Πασχόντων» του ΕΚΠΑ. 2. Εκπαιδευτρια ΑΚΕΣΩ 3. Εκπαιδευτρια σε κλινικό φροντιστήριο για τον καρκίνο του πνεύμονα στα πλαίσια του 25 ου Πανελληνίου Πνευμονολογικού Συνεδρίου 4. Συμμετοχή σε 4 Ερευνητικά Προγράμματα 5. Μέλος Οργανωτικής επιτροπής Επιστημονικών Συνεδρίων 6. Συμμετοχή σε προεδρεία Επιστημονικών Συνεδρίων 7. Σχολιαστής σε στρογγυλές τράπεζες ελληνικών Συνεδρίων 8. Μέλος σε Επιστημονικές Εταιρείες ΣΤ) Συγγραφικό Έργο Διπλωματική εργασία στα πλαίσια της απόκτησης μεταπτυχιακού τίτλου σπουδών, με θέμα: «Ορμονοεξάρτηση του καρκίνου του προστάτη και θεραπευτικές προοπτικές», Νοέμβριος
13 ΕΥΧΑΡΙΣΤΙΕΣ Η εκπόνηση μίας Διδακτορικής Διατριβής είναι ένα πολύπλοκο εγχείρημα. Είναι μία έρευνα επίπονη και μακροχρόνια, που προϋποθέτει συνεχή και καλή συνεργασία μεταξύ ιατρών διαφορετικών ειδικοτήτων και ασθενών. Στο δύσκολο αυτό εγχείρημα σύμμαχοί μου υπήρξαν σημαντικοί άνθρωποι, των οποίων τα λόγια και οι πράξεις συνέβαλαν ουσιαστικά, όχι μόνο στην επιτυχή περάτωση αυτού του επιστημονικού έργου, αλλά και στην πολυδιάστατη εξέλιξη μου ως ιατρός, καθώς και στη μύησή μου στο χώρο της έρευνας. Θερμότατες και Ειλικρινείς Ευχαριστίες οφείλω στην εμπνεύστρια και επιστημονική συντονίστρια της παρούσας Διδακτορικής Διατριβής, Αναπληρώτρια Καθηγήτρια Αιματολογίας της Ιατρικής Σχολής του ΕΚΠΑ, κ. Μαρία Αγγελοπούλου, που με εμπιστεύτηκε να ασχοληθώ με το συγκεκριμένο πρωτοποριακό θέμα. Μέσα από την έρευνα αυτή, κατάφερα να έρθω σε επαφή με ένα σημαντικό κεφάλαιο της ογκολογίας και είχα την ευκαιρία να αποκτήσω πολύτιμη εξειδίκευση για την περαιτέρω επιστημονική πορεία μου. Με την εμπειρία, τις γνώσεις και τα εποικοδομητικά σχόλια της, έδρασε καταλυτικά στην ολοκλήρωση αυτής της μελέτης. Οφείλω να επισημάνω ότι ο σχεδιασμός της διατριβής, η ανάλυση των αποτελεσμάτων της μελέτης και η εξαγωγή συμπερασμάτων πραγματοποιήθηκαν υπό τη στενή της επίβλεψη. Στάθηκε ως άξια καθηγήτρια ανεύρεσης επιστημονικής γνώσης και μοναδικός άνθρωπος ευγένειας και ήθους. Ευχαριστώ, ιδιαίτερα, τον Aναπληρωτή Καθηγητή Αιματολογίας της Ιατρικής Σχολής του ΕΚΠΑ, κ. Θεόδωρο Βασιλακόπουλο για την εμπιστοσύνη που μου επέδειξε και τις πολύτιμες συμβουλές που μου παρείχε καθ όλη τη διάρκεια εκπόνησης της Διατριβής. Η πολλαπλή βοήθεια, η αληθινή κατανόηση και η αμέριστη συμπαράσταση υπήρξαν κινητήριος δύναμη για την επίτευξη αυτού του πρωτοποριακού στόχου Η ουσιαστική συμβολή του και οι οξυδερκείς παρατηρήσεις του ήταν ανεκτίμητης αξίας. Ευχαριστώ πολύ τον Αναπληρωτή Καθηγητή της Ακτινοθεραπευτικής Ογκολογίας κ. Βασίλειο Κουλουλία για τη συμβολή του στην περάτωση της Διατριβής μου και τη συμπαράσταση του 13
14 ως μέλος της τριμελούς επιτροπής. Η γνώσεις και εμπειρία του πάνω στο αντικείμενο της ακτινοθεραπείας, ήταν σημαντικοί αρωγοί στο δρόμο για την ολοκλήρωση του δύσκολου αυτού έργου. Η βοήθεια και αληθινή κατανόηση του υπήρξαν πολύτιμες για την επιτυχή διεξαγωγή της μελέτης αυτής Με σεβασμό εκφράζω τις θερμότατες ευχαριστίες μου στον Ομότιμο Καθηγητή Αιματολογίας της Ιατρικής Σχολής του ΕΚΠΑ, κ. Γεράσιμο Πάγκαλη, για τη μοναδική ευκαιρία που μου έδωσε να διεξάγω μέρος της παρούσας μελέτης στην κλινική του. Είναι τιμή μου που έλαβα την αμέριστη συμπαράστασή του στην περάτωσή αυτής της έρευνας. Τέλος, θα ήθελα να ευχαριστήσω από τα βάθη της καρδιάς μου, τους ίδιους τους ασθενείς, αλλά και όλους όσους βοήθησαν με οποιοδήποτε τρόπο και μέσο στην περάτωση της παρούσας Διδακτορικής Διατριβής. 14
15 ΠΕΡΙΕΧΟΜΕΝΑ ΠΕΡΙΕΧΟΜΕΝΑ 15 ΠΡΟΛΟΓΟΣ 19 ΓΕΝΙΚΟ ΜΕΡΟΣ 1. ΛΕΜΦΩΜΑ HODGKIN 1.1 ΕΠΙΔΗΜΙΟΛΟΓΙΑ ΛΕΜΦΩΜΑΤΟΣ HODGKIN-ΙΣΤΟΛΟΓΙΚΗ ΕΙΚΟΝΑ ΙΣΤΟΛΟΓΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΚΑΙ ΤΑΞΙΝΟΜΗΣΗ Κλασικό Λέμφωμα Hodgkin Οζώδης Σκλήρυνση Μεικτή Κυτταροβρίθεια Κλασικός Τύπος Πλούσιος σε Λεμφοκύτταρα Λεμφοπενικός Τύπος Οζώδης Λεμφοεπικρατών Τύπος ΒΙΟΛΟΓΙΑ ΤΟΥ ΛΕΜΦΩΜΑΤΟΣ Hodgkin Τα κύτταρα προέλευσης στο Λέμφωμα Hodgkin Κύτταρα HRS και απώλεια έκφρασης του Β-φαινοτύπου Ο ρόλος του Epstein-Bar και η συνεχής ενεργοποίηση του NFκΒ Διαταραχή των μεταγραφικών παραγόντων ΑΡ-1 στο λέμφωμα Hodgkin Eνεργοποίηση οδών αγωγής σήματος Ο ρόλος των micro RNAs O ρόλος του αντιδραστικού περιβάλλοντος 40 15
16 1.4 ΚΛΙΝΙΚΗ ΕΙΚΟΝΑ ΕΡΓΑΣΤΗΡΙΑΚΑ ΕΥΡΗΜΑΤΑ Αιματολογικός και Βιοχημικός Έλεγχος Οστεομυελική Βιοψία ΑΠΕΙΚΟΝΙΣΤΙΚΟΣ ΕΛΕΓΧΟΣ Ακτινογραφία Θώρακος Αξονική Τομογραφία Σπινθηρογράφημα με Ραδιενεργό Γάλλιο, Σπινθηρογράφημα Οστών Μαγνητική Τομογραφία Τομογραφία Εκπομπής Ποζιτρονίων-ΡΕΤ Scan ( Positron Emission Tomography) ΑΔΡΗ ΠΡΟΓΝΩΣΤΙΚΗ ΤΑΞΙΝΟΜΗΣΗ ΘΕΡΑΠΕΙΑ ΠΡΩΤΗΣ ΓΡΑΜΜΗΣ Θεραπεία περιορισμένων σταδίων Θεραπεία ενδιάμεσων σταδίων Πεδίο Ακτινοθεραπείας Δόση Ακτινοθεραπείας Θεραπεία προχωρημένων σταδίων ΘΕΡΑΠΕΙΑ ΥΠΟΤΡΟΠΙΑΖΟΝΤΟΣ ΚΑΙ ΑΝΘΕΚΤΙΚΟΥ ΛΕΜΦΩΜΑΤΟΣ Μεγαθεραπεία και Αυτόλογη Μεταμόσχευση Αρχέγονων Αιμοποιητικών Κυττάρων Αίματος (ΜΘ/ΑΜΑΑΚ) Διάσωση ασθενών που αποτυγχάνουν μετά από ΜΘ/ΑΜΑΑΚ Ακτινοθεραπεία και Συμβατική Χημειοθεραπεία ως Θεραπεία Διάσωσης ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ Πεδίο Ακτινοθεραπείας στο Λέμφωμα Hodgkin Εκτεταμένο Πεδίο Ακτινοβόλησης (Extended Field Radiation Therapy) 71 16
17 Ακτινοθεραπεία Προσβεβλημένου Πεδίου (Involved Field Radiation Therapy- IFRT) Ακτινοθεραπεία Προσβεβλημένων Λεμφαδένα ή Λεμφαδένων (Involved Node Radiation Therapy- INRT) Δόση Ακτινοθεραπείας Δόση Ακτινοθεραπείας στα αρχικά και ενδιάμεσα στάδια Δόση Ακτινοθεραπείας στα προχωρημένα στάδια Τεχνικές Ακτινοθεραπείας Τοξικότητα Ακτινοθεραπείας ΥΠΟΛΟΓΙΣΤΙΚΗ ΤΟΜΟΓΡΑΦΙΑ ΕΚΠΟΜΠΗΣ ΠΟΖΙΤΡΟΝΙΩΝ (PET/CT) Συμβολη του PET/CT στις θεραπευτικες αποφασεις και την παρακολουθηση ασθενων με λεμφωμα hodgkin Εισαγωγή Τρόπος λειτουργίας του ΡΕΤ/CT ΡΕΤ/CT κατά τη σταδιοποίηση του HL ΡΕΤ/CT για την εκτίμηση της απάντησης στη θεραπεία HL ΡΕΤ-scan για την πρώïμη εκτίμηση της απάντησης και τροποποίηση της θεραπείας του HL Το ΡΕΤ-scan στην παρακολούθηση του HL PET/CT πριν από τη μεγαθεραπεία και αυτόλογη μεταμόσχευση στο HL Περιορισμοί -παγίδες στη χρήση του ΡΕΤ-scan
18 ΕΙΔΙΚΟ ΜΕΡΟΣ ΣΚΟΠΟΣ 112 ΥΛΙΚΟ ΚΑΙ ΜΕΘΟΔΟΙ 112 Προελευση συλλογη και διαχειριση του υλικου 112 Πρωτοκολλο PET/CT 112 Προσδιορισμος σταδιου νοσου- θεραπευτικο πρωτοκολλο 113 ΣΤΑΤΙΣΤΙΚΗ ΑΝΑΛΥΣΗ 116 Στατιστικη μεθοδολογια 116 ΑΠΟΤΕΛΕΣΜΑΤΑ 117 α. Συσχετιση μεταξυ κλινικης σταδιοποιησης (CS) και σταδιοποιησης με PET ( PET-S) 117 β. Aλλαγη θεραπευτικης αγωγης εξαιτιας της σταδιοποιησης με PET/CT 120 γ. Αλλαγη των πεδιων ακτινοθεραπειας εξαιτιας της σταδιοποιησης με PET/CT 125 δ. Αναλυση προγνωστικών παραγόντων 126 ε. Συμπεράσματα σύμφωνα με την τροποποίηση της θεραπευτικής στρατηγικής 133 ΣΥΖΗΤΗΣΗ 136 ΣΥΜΠΕΡΑΣΜΑΤΑ 143 ΠΕΡΙΛΗΨΗ 144 SUMMARY 146 ΒΙΒΛΙΟΓΡΑΦΙΑ
19 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία ΠΡΟΛΟΓΟΣ Το Λέμφωμα Hodgkin (HL), αποτελεί μία αιματολογική κακοήθεια, που προέρχεται από τα ώριμα Β λεμφοκύτταρα του βλαστικού κέντρου. Σύμφωνα με την ταξινόμηση του Παγκόσμιου Οργανισμού Υγείας (WHO) διακρίνεται σε δύο οντότητες: Το κλασσικό HL (chl, 95% των περιπτώσεων) και τον οζώδη λεμφοεπικρατούντα υπότυπο (NLPHL, 5% των περιπτώσεων). Το HL αποτελεί μοναδική περίπτωση νεοπλάσματος, καθώς τα νεοπλασματικά κύτταρα Hodgkin και Reed-Sternberg (HRS) στο κλασικό HL και τα κύτταρα του λεμφοεπικρατούντα τύπου (LP) στον NLP τύπο ανευρίσκονται εξαιρετικά σπάνια και συνήθως αφορούν ποσοστό μικρότερο του 1% του συνόλου των κυττάρων των προσβεβλημένων ιστών. Ειδικά τα HRS κύτταρα βρίσκονται ανάμεσα σε ένα αντιδραστικό μη νεοπλασματικό περιβάλλον και εμφανίζουν μία συνεχή αλληλεπίδραση με τα φλεγμονώδη κύτταρα που το απαρτίζουν, διαδικασία που θεωρείται απαραίτητη για την επιβίωση και την αύξησή τους. Η διάγνωση της ασθένειας επιτυγχάνεται με την ιστολογική εξέταση παθολογικού λεμφαδένα, που φέρει κύτταρα Reed-Sternberg. H σταδιοποίηση της νόσου προκύπτει από την κλινική εξέταση, την εκτίμηση του ιστορικού του ασθενούς, από την οστεομυελική βιοψία, καθώς επίσης και από την αξιολόγηση των απεικονιστικών ευρημάτων. Μέχρι πρότινος, η σταδιοποίηση γινόταν απεικονιστικά με την επικουρική διενέργεια αξονικών τομογραφιών τραχήλου, θώρακος, άνω και κάτω κοιλίας. Τα τελευταία χρόνια, ο ρόλος της τομογραφίας εκπομπής ποζιτρονίων φαίνεται να έχει κυρίαρχη θέση, όχι μόνο στον επανέλεγχο των ασθενών που έχουν λάβει θεραπεία, αλλά και στην ολοκληρωμένη αρχική σταδιοποίηση της νόσου. Η αξονική τομογραφία συνδυασμένη με το σπινθηρογράφημα εκπομπής ποζιτρονίων με 18- φθοριοδεοξυγλυκόζη (positron emission tomography-pet/ct), παρέχει ταυτόχρονα πληροφορίες για την απεικόνιση, αλλά και τη μεταβολική δραστηριότητα των 19
20 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή προσβεβλημένων περιοχών. Η κύρια εφαρμογή του ΡΕΤ/CT αφορά στο λέμφωμα Hodgkin, όπου έχει εφαρμοσθεί κυρίως στην εκτίμηση της ανταπόκρισης στην θεραπεία. Η χρήση του PET/CT scan έχει κατορθώσει να αυξήσει την ευαισθησία ανεύρεσης ενεργού νόσου σε σχέση με την συμβατική απεικόνιση. Κατά τη διάρκεια του προηγούμενου αιώνα, το HL μετατράπηκε από θανατηφόρα, σε μία νόσο ιάσιμη, περίπου στο 75% των ασθενών, παγκοσμίως. Ασθενείς με αρχικά στάδια της νόσου θεραπεύονται με συνδυασμό χημειοθεραπείας με ακτινοθεραπεία. Οι συνολικές δόσεις χημειοθεραπείας και ο σχεδιασμός και η συνολική δόση της ακτινοθεραπείας, διαφέρουν στους ασθενείς με ευνοϊκή πρόγνωση, από ότι σε αυτούς με δυσμενή πρόγνωση, ανάλογα με την προγνωστική κατηγορία που αυτοί εμπίπτουν. Στα προχωρημένα στάδια της νόσου, η κύρια θεραπεία είναι η χημειοθεραπεία. Η χορήγηση της ακτινοθεραπείας γίνεται σε επιλεγμένους ασθενείς στα πλαίσια σταθεροποίησης της νόσου. Σε πάσχοντες με ανθεκτική ή υποτροπιάζουσα νόσο, ακολουθείται τακτική με χημειοθεραπεία δεύτερης γραμμής που περιλαμβάνει χημειοθεραπευτικά φάρμακα, που δεν έχουν δοθεί κατά την αρχική θεραπεία και αυτόλογη μεταμόσχευση αιμοποιητικών κυττάρων διάσωσης. Εξαιτίας του γεγονότος ότι η έκβαση των ασθενών με HL έχει βελτιωθεί σημαντικά, ώστε το νόσημα να θεωρείται ιάσιμο στη μεγάλη πλειονότητα των ασθενών, η επιτυχής διαχείριση των ασθενών με HL απαιτεί σημαντική προσοχή στη σταδιοποίηση της νόσου και στην επιλογή θεραπευτικών πρωτοκόλλων, προκειμένου να μειωθούν οι δυνητικά σοβαρές απώτερες τοξικότητες σχετιζόμενες με τη θεραπεία. Είναι χαρακτηριστικό ότι μερικές από τις πιο σοβαρές παρενέργειες της θεραπείας, όπως οι δευτεροπαθείς κακοήθειες και τα καρδιολογικά νοσήματα δεν είναι εμφανή, παρά παρουσιάζονται χρόνια μετά την ολοκλήρωση της θεραπείας. Δυστυχώς, παρόλο που η πλειοψηφία των ασθενών κατορθώνουν να ιαθούν από το λέμφωμα από το οποίο πάσχουν, η τοξικότητα που συχνά σχετίζεται με τη θεραπεία τους, έχει γίνει μία σημαντική αιτία απώτερων θανάτων. Είναι επιτακτικό λοιπόν, η θεραπεία που 20
21 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία επιλέγεται, να εξισορροπεί την επιθυμία για διατήρηση υψηλού βαθμού ίασης, με την ανάγκη για μείωση των απώτερων επιπλοκών. Οι μέθοδοι αντιμετώπισης έχουν εξελιχθεί με τέτοιο τρόπο, ώστε ασθενείς με αρχικά στάδια της νόσου, να επιτυγχάνουν μακρά ύφεση με λιγότερο εντατική θεραπεία, ενώ πιο ενισχυμένη θεραπεία να χορηγείται σε ασθενείς με προχωρημένα στάδια της νόσου. Η εύρεση χρυσής τομής ανάμεσα στην αποτελεσματικότητα και την τοξικότητα της χημειοθεραπείας και της ακτινοθεραπείας αποτελεί τη σύγχρονη πρόκληση. Προς την κατεύθυνση αυτή μπορεί να συμβάλει και η ανάπτυξη προγνωστικών παραμέτρων που να επιτρέπουν την τροποποίηση της θεραπείας, ώστε να αποφεύγεται η υπερ-θεραπεία στα αρχικά και στα εκτεταμένα στάδια με καλή πρόγνωση, και να αντιμετωπίζονται πιο επιθετικά οι ασθενείς που αναμένεται να έχουν δυσμενή πρόγνωση. Σκοπός της παρούσας Διδακτορικής Διατριβής είναι η συσχέτιση των ευρημάτων της τομογραφίας εκπομπής ποζιτρονίων (PET/CT scan) με τα ευρήματα της συμβατικής σταδιοποίησης (κλινική εξέταση, αξονική τομογραφία) κατά την αρχική σταδιοποίηση σε ασθενείς με λέμφωμα Hodgkin. Η σύγκριση αυτή των δύο μορφών σταδιοποίησης γίνεται κατά τη διάγνωση. Μελετάται η συσχέτιση των ευρημάτων από τις δύο διαφορετικές μεθόδους με τo διάστημα ελεύθερο επιδείνωσης νόσου (FFP-Failure From Progression) και ερευνάται η δυνητική αλλαγή της θεραπευτικής προσέγγισης και η συσχέτιση με την ακτινοθεραπεία. Επιπλέον, αντικείμενο της αναδρομικής αυτής μελέτης είναι η διερεύνηση της προγνωστικής σημασίας των διαφόρων παραμέτρων του αρχικού PET/CT. 21
22 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ΓΕΝΙΚΟ ΜΕΡΟΣ 22
23 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία 1. ΛΕΜΦΩΜΑ HODGKIN 1.1 EΠΙΔΗΜΙΟΛΟΓΙΑ ΛΕΜΦΩΜΑΤΟΣ HODGKIN-ΙΣΤΟΛΟΓΙΚΗ ΕΙΚΟΝΑ To Λέμφωμα Hodgkin (HL) αποτελεί λεμφοϋπερπλαστικό νόσημα με ετήσια επίπτωση 2.4 περιπτώσεις ανά πληθυσμού. Παρουσιάζει μία ελαφρά μεγαλύτερη εμφάνιση στους άνδρες έναντι των γυναικών (1.1:1). Εμφανίζει διφασική ηλικιακή αιχμή, καθώς μπορεί να παρατηρείται σε μεγαλύτερη συχνότητα σε ηλικίες ετών και σε ηλικίες >55 ετών[1]. Η αιτία της νόσου Hodgkin παραμένει άγνωστη. Από μερικούς έχει προταθεί η έκθεση σε καρκινογόνα ή σε ιούς (διατροφή, λοιμώξεις, περιβαλλοντικοί/τοξικοί παράγοντες) και από άλλους έχουν θεωρηθεί γενετικοί ή ανοσολογικοί παράγοντες σαν πιθανή αιτία της νόσου[2,3]. Είναι χαρακτηριστικό ότι οι συγγενείς πρώτου βαθμού έχουν πενταπλάσια πιθανότητα εμφάνισης της νόσου του Hodgkin. Επιπρόσθετα, έχει συσχετιστεί με τον ιό του Epstein-Barr, που συχνά παρατηρείται σε άτομα με τον υπότυπο της μεικτής κυτταροβρίθειας. Στις περιπτώσεις αυτές, έχει απομονωθεί EBV DNA [1] στα κύτταρα Reed- Sternberg των ασθενών αυτών [2,3]. Στη συντριπτική του πλειοψηφία πρόκειται για νόσο Β-προέλευσης, καθώς το παθογνωμονικό εύρημα για το κλασσικό Λέμφωμα Hodgkin αποτελούν τα κύτταρα Reed- Sternberg. Το HL αποτελεί μοναδική περίπτωση νεοπλάσματος λόγω του γεγονότος ότι τα νεοπλασματικά κύτταρα Hodgkin και Reed-Sternberg στο κλασσικό HL και τα κύτταρα του λεμφοεπικρατούντα τύπου ανευρίσκονται εξαιρετικά σπάνια και συνήθως αφορούν ποσοστό μικρότερο του 1% του συνόλου των κυττάρων των προσβεβλημένων ιστών. Πιο συγκεκριμένα τα κύτταρα Reed-Sternberg βρίσκονται ανάμεσα σε ένα αντιδραστικό μη νεοπλασματικό περιβάλλον και εμφανίζουν μία συνεχή αλληλεπίδραση με τα φλεγμονώδη κύτταρα που το απαρτίζουν, διαδικασία που θεωρείται απαραίτητη για την επιβίωσή και την αύξησή τους. Στο 80% των περιπτώσεων εμφανίζεται με τραχηλική λεμφαδενοπάθεια. Το 50% των περιπτώσεων παρουσιάζονται με νόσο στο μεσοθωράκιο, κυρίως στον υποτύπο της οζώδους σκλήρυνσης. Β-συμπτώματα εμφανίζονται στο 33% των νοσούντων, αλλά μόνο το 15-20% από τους ασθενείς με στάδιο Ι-ΙΙ, πάσχουν από Β-συμπτώματα. 23
24 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή 1.2 ΙΣΤΟΛΟΓΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΚΑΙ ΤΑΞΙΝΟΜΗΣΗ Σύμφωνα με την ταξινόμηση του Παγκοσμίου Οργανισμού Υγείας (WHO), το Λέμφωμα Hodgkin διακρίνεται σε δύο ξεχωριστές νοσολογικές οντότητες: το κλασσικό HL (chl, 95% των περιπτώσεων) και τον οζώδη λεμφοεπικρατούντα υπότυπο (NLPHL, 5% των περιπτώσεων), με διαφορές τόσο σε μορφολογικό, όσο και σε κλινικό και προγνωστικό επίπεδο. Το κλασσικό λέμφωμα Hodgkin χαρακτηρίζεται από την παρουσία των γιγαντίων μονοπύρηνων κυττάρων Hodgkin,ή των τυπικών διπύρηνων ή πολυπύρηνων κυττάρων Reed-Sternberg (RS) και διακρίνεται σε 4 υποτύπους, με βάση τη σύνθεση του αντιδραστικού κυτταρικού περιβάλλοντος και κατά δεύτερο λόγο, με βάση τη μορφολογία των νεοπλασματικών κυττάρων Κλασικό Λέμφωμα Hodgkin Πρόκειται για κακόηθες λεμφικό νεόπλασμα, Β προέλευσης. Ιστολογικά διαγιγνώσκεται από την ανεύρευση κυττάρων Hodgkin και Reed-Sternberg (RS),με χαρακτηριστικό ανοσοφαινότυπο (CD30+, CD15+, CD45-,CD20-/+, PAX-5 αχνά +) μέσα σε πολύμορφο μη νεοπλασματικό κυτταρικό περιβάλλον, που περιλαμβάνει ποικίλου βαθμού λεμφοκύτταρα, ηωσινόφιλα, ουδετερόφιλα, ιστιοκύτταρα, ινοβλάστες και πλασματοκύτταρα. Τα κλασικά κύτταρα Reed-Sternberg είναι ευμεγέθη, με άφθονο βασεόφιλο κυτταρόπλασμα και τουλάχιστον δύο πυρήνες ή πυρηνικούς λοβούς, που περιέχουν χρωματίνη και ένα προβάλλον πυρήνιο, που μοιάζει με ιογενές έγκλειστο. Τα κύτταρα αυτά που παρουσιάζουν μόνο ένα πυρήνα αποτελούν τα κύτταρα Hodgkin. «Μομιοποιημένα κύτταρα» ονομάζονται είτε τα κύτταρα Reed-Sternberg είτε τα κύτταρα Hodgkin, που εμφανίζουν πυκνωτικούς πυρήνες. Είναι χαρακτηριστικό ότι τα νεοπλασματικά κύτταρα στο HL συνήθως αποτελούν το % του συνολικού πληθυσμού των κυττάρων, σε ένα παθολογικό λεμφαδένα. Όσον αφορά στον ανοσοφαινότυπο του κλασικού λεμφώματος Hodgkin αυτός αποτελείται από νεοπλασματικά κύτταρα, που είναι κατά κανόνα CD30 και CD15 (75-85% των περιπτώσεων) θετικά και αρνητικά για CD45 και J άλυσο. Η χρώση έχει μεμβρανική/στικτή 24
25 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία παραπυρηνική κατανομή. Είναι σύνηθες η έκφραση του CD15 να περιορίζεται σε μικρό αριθμό κυττάρων. Το CD20 εκφράζεται στο 30-40% των περιπτώσεων συνήθως με ποικίλλουσα ένταση και σε σχετικά μικρό ποσοστό των νεοπλασματικών κυττάρων. Αντίθετα, η έκφραση του CD79a είναι ακόμη πιο σπάνια, ενώ ο δείκτης ΡΑΧ-5 (Β-cell activator protein/bsap) εκφράζεται στο 95% των περιπτώσεων, ασθενέστερα σε σχέση με τα μικρά Β λεμφοκύτταρα. Ο μεταγραφικός παράγοντας των πλασματοκυττάρων IRF4/MUM-1 είναι κατά κανόνα έντονα θετικός σε αντίθεση με το CD13 που δεν εκφράζεται. Σπανιότατα, μικρό ποσοστό των νεοπλασματικών κυττάρων εκφράζει ένα ή περισσότερα Τ αντιγόνα ή το ΕΜΑ. Σπάνια (~10%) εκφράζεται ο μεταγραφικός παράγοντας ΟCT-2 ή το συνδιεγερτικό του μόριο ΒΟΒ-1. Στις περιπτώσεις με EBV λοίμωξη, τα νεοπλασματικά κύτταρα εμφράζουν ΕΒΝΑ-1 ή LMP-1 αλλά όχι ΕΒΝΑ-2. Η παρουσία του EBV είναι συχνότερη στη μικτή κυτταροβρίθεια (~75%) και στο λεμφοπενικό τύπο που αναπτύσσεται στο έδαφος HIV λοίμωξης. Για τη διαφορική διάγνωση από αναπλαστικό λέμφωμα ο συνδυασμός ΡΑΧ5+/ EBV+/ EMA-/ ΑLK-/ CD43- είναι συνηγορητικός της διάγνωσης HL. Η διαφορική διάγνωση από μεγαλοκυτταρικό Β λέμφωμα με αναπλαστική μορφολογία και έκφραση CD30 είναι συχνά δύσκολη και υπάρχουν περιπτώσεις με επικαλυπτόμενη μορφολογία ανοσοφαινότυπο (λεμφώματα γκρίζας ζώνης ). Όσον αφορά στο γονότυπο, τα κύτταρα του κλασικού HL είναι Β κύτταρα, τα οποία ωστόσο έχουν αποτελέσει σημαντικό μέρος του προγράμματος έκφρασης των Β γονιδίων. Χρειάζεται να σημειωθεί εδώ ότι στο 95% των περιπτώσεων, το Reed-Sternberg κύτταρο προέρχεται από ώριμο Β κύτταρο του βλαστικού κέντρου και σπάνιες είναι οι φορές που προέρχεται από ώριμο (μεταθυμικό) Τ λεμφοκύτταρο. Με την εξέλιξη των θεραπευτικών προσεγγίσεων της ακτινοθεραπείας και της χημειοθεραπείας, η πρόγνωση του κλασικού λεμφώματος Hodgkin είναι εξαιρετική, με ποσοστό ίασης που αγγίζει το 85%. Το στάδιο της νόσου είναι καθοριστικό για τη θεραπεία, 25
26 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ενώ για την πρόγνωση της νόσου υπάρχουν διάφορες κλινικές και εργαστηριακές παράμετροι, που παίζουν εξαιρετικά σημαντικό ρόλο. Το κλασικό HL αποτελεί το 95% των περιπτώσεων ΗL και εμφανίζει διφασική αιχμή: Οι ασθενείς μπορεί να είναι άτομα ηλικίας ετών, αλλά και άτομα> 55 ετών. Οι τέσσερις υπότυποι του Λεμφώματος Hodgkin είναι ο τύπος της οζώδους σκλήρυνσης (NSHL) (70%), της μεικτής κυτταροβρίθειας (20-25%), του κλασσικού τύπου πλούσιου σε λεμφοκύτταρα (5%) και του λεμφοπενικού τύπου (<1%) Οζώδης Σκλήρυνση Η οζώδης σκλήρυνση εμφανίζεται στο 70% των ασθενών και συνήθως παρατηρείται στους εφήβους και τους νεαρούς ενήλικες. Πρόκειται για υποτύπο του κλασικού HL που εμφανίζεται συνήθως σε αρχικά στάδια (Ι/ΙΙ). Χαρακτηρίζεται από την παρουσία όζων που περιβάλλονται από λωρίδες ινώδους συνδετικού ιστού, που ακτινοβολεί από την κάψα του λεμφαδένα. Στην οζώδη σκλήρυνση, τόσο τα κύτταρα Reed-Sternberg, όσο και τα κύτταρα Hodgkin εμφανίζουν έντονη λοβίωση του πυρήνα, μικρότερους πυρηνικούς λοβούς, μικρότερο πυρήνιο και άφθονο κυτταρόπλασμα, με ποικίλου βαθμού ηωσινόφιλα και ιστιοκύτταρα που συχνά δίνουν εικόνα νερώσεων και ηωσινοφιλικών αποστηματίων. Είναι συχνό φαινόμενο, σε μονιμοποιημένο παρασκεύασμα το κυτταρόπλασμα να συρρικνώνεται, με αποτέλεσμα τα κύτταρα να δίνουν την ψευδαίσθηση ότι βρίσκονται εντός κενού( lacunar RS κύτταρα). Ειδικά στην περίπτωση που τα lacunar Reed-Sternberg κύτταρα σχηματίζουν συμπαγείς αθροίσεις, εμφανίζεται ο «συγκυτιακός υπότυπος» της οζώδους σκλήρυνσης, ο οποίος δημιουργεί και προβλήματα διαφορικής διάγνωσης από το αναπλαστικό ή μεγαλοκυτταρικό λέμφωμα και από άλλους συμπαγείς όγκους. Ο διαχωρισμός της νόσου σε βαθμούς 1 και 2 γίνεται,σύμφωνα με τα κριτήρια του Βritish Νational Lymphoma Investigation (BNLI),με βάση τον αριθμό και την ατυπία των νεοπλασματικών κυττάρων. Απεικονιστικά η οζώδης σκλήρυνση παρουσιάζεται με εικόνα οζώδους λεμφαδενοπάθειας του μεσοθωρακίου. Το 1/3 αυτών των ασθενών εμφανίζει Β-συμπτώματα. 26
27 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Μεικτή Κυτταροβρίθεια Η μεικτή κυτταροβρίθεια (MCHL) εμφανίζεται σε ποσοστό 20-25% των πασχόντων και παρατηρείται κυρίως σε παιδιά. Στον συγκεκριμένο υπότυπο τα νεοπλασματικά κύτταρα είναι τυπικά σε μορφολογία. Η διήθηση είναι δυνατόν να έχει διαλεμφοζιδιακή κατανομή και το υπόστρωμα να εμφανίζει σκλήρυνση, χωρίς ωστόσο πάχυνση της κάψας όπως στην οζώδη σκλήρυνση. Ενίοτε τα ιστιοκύτταρα εμφανίζουν επιθηλιοειδή χαρακτηριστικά, συνήθως σε EBV+ περιπτώσεις. Η μεικτή κυτταροβρίθεια διαγιγνώσκεται συνήθως σε προχωρημένα στάδια, συχνά με υποκλινική υποδιαφραγματική νόσο σε ασθενείς με κλινική σταδιοποίηση Ι-ΙΙ πάνω από το διάφραγμα Γενικά, η προσβολή των λεμφαδένων είναι περιφερική, σε αυτό τον υποτύπο Κλασικός τύπος πλούσιος σε λεμφοκύτταρα Ο πλούσιος σε λεμφοκύτταρα τύπος (LRCHL) αποτελεί το 5% των περιπτώσεων. Το αρχιτεκτονικό πρότυπο είναι συνήθως οζώδες με παρουσία άφθονων μικρών Β λεμφοκυττάρων, που περικλείουν συχνά ατροφικά έκκεντρα τοποθετημένα βλαστικά κέντρα. Τα νεοπλασματικά κύτταρα ανευρίσκονται εντός των όζων, συνήθως στον εκπτυγμένο μανδύα των λεμφοζιδίων, αλλά όχι εντός των βλαστικών κυττάρων. Για τις περιπτώσεις αυτές που οι όζοι περιβάλλονται από λωρίδες κολλαγόνου, προτείνεται η διάγνωση της οζώδους σκλήρυνσης, ενώ σε άλλες περιπτώσεις έχει παρατηρηθεί μετάπτωση σε κλασσική οζώδη σκλήρυνση. Σπάνια το αρχιτεκτονικό πρότυπο είναι διάχυτο. Ο πλούσιος σε λεμφοκύτταρα τύπος, εμφανίζεται συχνότερα στους ενήλικες άνδρες, όπου παρατηρείται περιφερική λεμφαδενοπάθεια και σπανίως εντοπίζεται προσβολή του μεσοθωρακίου Λεμφοπενικός Τύπος Ο λεμφοπενικός τύπος (LDHL) δεν ξεπερνά το 5% των πασχόντων και συνήθως διαγιγνώσκεται σε προχωρημένο στάδιο, σε μεγαλύτερης ηλικίας ασθενείς, που 27
28 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή παρουσιάζουν Β-συμπτώματα, χειρότερη πρόγνωση και συχνή συσχέτιση με λοίμωξη από HIV. Τα νεοπλασματικά κύτταρα είναι αναλογικά αυξημένα σε σχέση με τον λεμφοκυτταρικό πληθυσμό. Ορισμένες φορές μοιάζουν με την εικόνα της μεικτής κυτταροβρίθειας με αυξημένο αριθμό νεοπλασματικών κυττάρων, ενώ άλλες χαρακτηρίζονται από έντονα πλειόμορφα νεοπλασματικά κύτταρα, με σαρκωματώδη μορφολογία, που δημιουργούν διαφοροδιαγνωστικό πρόβλημα από το αναπλαστικό λέμφωμα Οζώδης Λεμφοεπικρατών Τύπος Ο οζώδης λεμφοεπικρατής υπότυπος πλέον περιγράφεται ως ξεχωριστή οντότητα, σε σχέση με το κλασσικό λέμφωμα Hodgkin. Προγενέστερη ταξινόμηση αναγνώριζε αυτό τον υπότυπο, από ένα υποσύνολο ασθενών που παρουσίαζαν στις βιοψίες τους μικρά επικρατή λεμφοκύτταρα και σπάνια κύτταρα Reed-Sternberg. Ένα υποσύνολο αυτών των ασθενών έχει όγκους με οζώδη μορφολογία και κλινική συμπτωματολογία που διαφέρει από τους ασθενείς με το κλασσικό Λέμφωμα Hodgkin. Χαρακτηρίζεται από οζώδες (± διάχυτο) πρότυπο ανάπτυξης και παρουσία νεοπλασματικών κυττάρων, με μορφολογία τύπου «pop-corn»(lp κύτταρα), που αναπτύσσεται εντός δικτύου δενδριτικών κυττάρων πλούσιου σε μικρά Β και Τ (CD4+, CD57+) λεμφοκύτταρα. Γενικά, τα LP κύτταρα είναι θετικά στους Β δείκτες (CD20, CD79α, PAX-5), BCL-6,CD45, ΟΚΤ2 και ΒΟΒ-1 σε όλες τις περιπτώσεις. ΕΜΑ, J άλυσος και βαριές και ελαφρές άλυσοι ανοσοσφαιρινών ανιχνεύονται στα ίδια κύτταρα στην πλειοψηφία των περιπτώσεων. Αντίθετα, τα αντιγόνα CD15 και CD30 κατά κανόνα δεν εκφράζονται. Τα συνοδά μικρά λεμφοκύτταρα είναι Β και CD4+/CD57+/T κύτταρα. Τα τελευταία εκφράζουν δείκτες Τ βοηθητικών κυττάρων των βλαστικών κέντρων (PD1, BCL-6, MUM-1, CD134). Tα Τ λεμφοκύτταρα είναι πολυπληθέστερα στις διάχυτες περιοχές. Η παρουσία άφθονων LP κυττάρων εκτός των όζων έχει συσχετισθεί με τάση εξέλιξης σε εικόνες που μιμούνται διάχυτο μεγαλοκυτταρικό λέμφωμα πλούσιο σε Τ λεμφοκύτταρα (TCRBCL-like). Για τη διαφορική διάγνωση του οζώδους λεμφοεπικρατούντος από γνήσιο TCRBCL χρησιμοποιούνται η απουσία μικρών Β κυττάρων και η παρουσία CD8+ και ΤΙΑ-1+ κυττάρων στο τελευταίο. Φυσιολογικό αντίστοιχο είναι το Β κύτταρο του βλαστικού κέντρου στο στάδιο της κεντροβλάστης. 28
29 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Όσον αφορά στο γονότυπο, τα LP κύτταρα έχουν κλωνικά και λειτουργικά ανασυνδυασμένα γονίδια ανοσοσφαιρινών, τα οποία φέρουν στη μεταβλητή περιοχή σωματικές υπερμεταλλάξεις. Δεν παρατηρείται λανθάνουσα EBV λοίμωξη. Διαμεταθέσεις και ανασυνδυασμοί του γονιδίου BCL-6 παρατηρούνται στο 25% και 48% των περιπτώσεων αντίστοιχα. Σωματικές υπερμεταλλάξεις, κυρίως στο γονίδιο PAX-5 είναι πολύ συχνές. O οζώδης λεμφοεπικρατών τύπος πρόκειται για μία σπάνια κλινική οντότητα και αντιπροσωπεύει λιγότερο από 5% των περιπτώσεων με Λέμφωμα Hodgkin. Περιστασιακά παρουσιάζει απώτερη υποτροπή, αλλά καλύτερη ολική επιβίωση. Συνήθως, εμφανίζεται σε άνδρες, ηλικίας ετών, που παρουσιάζουν τραχηλική, μασχαλιαία ή βουβωνική λεμφαδενοπάθεια και έχουν Β-συμπτώματα σε ποσοστό<10%. Τα στάδια διάγνωσης είναι συνήθως αρχικά ( Ι ή ΙΙ). Στη βιβλιογραφία αναφέρονται ποικίλοι μορφολογικοί υπότυποι του οζώδους λεμφοεπικρατούντος HL, μεταξύ των οποίων οι πιο χαρακτηριστικοί είναι οι εξής: 1) «κλασικός» οζώδης υπότυπος (πλούσιος σε Β λεμφοκύτταρα), 2) υπότυπος με παρουσία συρρεόντων όζων, 3) οζώδης υπότυπος με παρουσία κυττάρων LP εκτός των όζων και 4) ο μικροοζώδης υπότυπος με παρουσία μικρών ή κατακερματισμένων βλαστικών κέντρων εντός των όζων. Ο τελευταίος μορφολογικός υπότυπος αναφέρεται ως πρώιμη αλλοίωση, κατ αντιστοιχία με το in situ λεμφοζιδιακό λέμφωμα, η οποία μπορεί δυνητικά να οδηγήσει σε κλινικά έκδηλο λέμφωμα.. Αυτό στοιχειοθετείται από το γεγονός ότι πρόκειται για μία αλλοίωση, που εντοπίζεται σε κατά τα άλλα φυσιολογικά βλαστικά κέντρα αποτελούμενα από CD20+, BCL-6+, μικρά Β λεμφοκύτταρα και Τ λεμφοκύτταρα διατασσόμενα εντός δικτύου δενδριτικών κυττάρων με CD23+.[4-13] Η πρόγνωση της νόσου στα αρχικά στάδια της φτάνει τη δεκαετή επιβίωση σε ποσοστό >90%. Είναι αξιοσημείωτο ότι και στην πιθανότητα υποτροπής, η νόσος παραμένει χημειοευαίσθητη. Δεν συμβαίνει το ίδιο όμως και στα προχωρημένα στάδια, που δύναται να παρατηρηθεί εκτροπή σε μεγαλοκυτταρικό Β-λέμφωμα, σε ποσοστό 3-5% των ασθενών. Σε αυτή την περίπτωση η πρόγνωση είναι δυσμενέστερη. Παρόλα αυτά, εφόσον η νόσος παραμένει εντοπισμένη, η πρόγνωση μπορεί να παραμείνει καλή. 29
30 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή 1.3 ΒΙΟΛΟΓΙΑ ΤΟΥ ΛΕΜΦΩΜΑΤΟΣ HODGKIN Το λέμφωμα Hodgkin αποτελεί ιδιάζουσα περίπτωση νεοπλάσματος. Λόγω των μοναδικών του χαρακτηριστικών, χρειάστηκε η ανάπτυξη σύγχρονων τεχνικών για να επιτρέψουν την απομόνωση και μελέτη των μεμονωμένων κυττάρων και να καταστεί εφικτή η αναγνώριση της προέλευσης των νεοπλασματικών κυττάρων από Β λεμφοκύτταρα, που να έχουν έρθει σε επαφή με αντιγόνο. Ιδιαίτερο γνώρισμα των κυττάρων του ΛΗ είναι τα νεοπλασματικά κύτταρα Hodgkin και τα κύτταρα Reed-Sternberg στον κλασικό τύπο του ΛΗ, καθώς και τα κύτταρα LP στον οζώδη λεμφοεπικρατούντα τύπο. Τα παθογνωμονικά αυτά κύτταρα ανευρίσκονται εξαιρετικά σπάνια, αφού αφορούν ποσοστό μικρότερο από 1% του συνόλου των κυττάρων του προσβεβλημένου ιστού. Είναι γεγονός ότι η πλειονότητα των κυττάρων που διηθούν τους προσβεβλημένους λεμφαδένες είναι φλεγμονώδη κύτταρα όπως Τ και Β λεμφοκύτταρα, ουδετερόφιλα, ηωσινόφιλα, πλασματοκύτταρα, ιστιοκύτταρα και μαστοκύτταρα, τα οποία και δημιουργούν και μία μοναδική ιστοπαθολογική εικόνα. Το λέμφωμα Hodgkin διαφοροποιείται από όλους τους άλλους ιστολογικούς τύπους λεμφωμάτων και σε ένα δεύτερο χαρακτηριστικό. Σε αντίθεση με όλους του άλλους τύπους λεμφωμάτων, όπου τα νεοπλασματικά κύτταρα διατηρούν κατά κανόνα την έκφραση των αντιγόνων που χαρακτηρίζουν τα φυσιολογικά κύτταρα από τα οποία προέρχονται, τα κύτταρα Reed-Sternberg στο κλασικό HL παρουσιάζουν ένα εξαιρετικά σύνθετο ανοσοφαινότυπο, με έκφραση αντιγόνων που φυσιολογικά χαρακτηρίζουν εντελώς διαφορετικούς πληθυσμούς. Έτσι τα κύτταρα Reed-Sternberg δύνανται να εκφράζουν σε ένα ποσοστό δείκτες Β λεμφοκυτταρικής διαφοροποίησης όπως το ΡΑΧ5, ή ενεργοποίησης όπως το CD30, ή και δείκτες διαφοροποίησης κοκκιοκυττάρων και μονοκυττάρων όπως το CD15. Επίσης μπορούν να εκφράσουν δείκτες διαφοροποίησης πλασματοκυττάρων όπως το MUM1 και το CD138, ή αντιγονο-παρουσιαστικών κυττάρων όπως τα MHC-II, CD40, CD80,CD86 και δενδριτικών κυττάρων όπως τα Fascin και TARC, ή ακόμα και κυτταροτοξικών Τ-κυττάρων, όπως η perforin και η grazyme-β. 30
31 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Τέλος η απορύθμιση πολλαπλών βασικών μοριακών μονοπατιών μεταβίβασης σήματος, φαίνεται να είναι μοναδική στο HL, κυρίως στον αριθμό των μονοπατιών που έχουν διαταραχθεί, προσλαμβάνοντας ιδιαίτερη σημασία για τον πολλαπλασιασμό και την επιβίωση των νεοπλασματικών κυττάρων.[14] Τα κύτταρα προέλευσης στο Λέμφωμα Hodgkin Σήμερα είναι αδιαμφισβήτητο ότι τα κύτταρα HRS και L&H εμφανίζουν στην συντριπτική πλειοψηφία των περιπτώσεων μονοκλωνικό ανασυνδυασμό των ανοσοσφαιρινών (Ιg) ο οποίος αποτελεί μοριακό δείκτη Β-κυτταρικής προέλευσης[15-18]. Βασική διαφορά των HRS από τα LP, είναι ότι σε ποσοστό περίπου 25% των περιπτώσεων, τα HRS κύτταρα παρουσιάζουν παθολογικές μεταλλάξεις με τελικό αποτέλεσμα την αδυναμία έκφρασης ανοσοσφαιρίνης[16,19,20]. Πιο συγκεκριμένα, ανιχνεύονται κωδικόνια τερματισμού, ελλείμματα και αντικαταστάσεις βάσεων που οδηγούν σε αλλαγή του πλαισίου ανάγνωσης και κανονικά θα έπρεπε να οδηγήσουν το φυσιολογικό Β-λεμφοκύτταρο σε απόπτωση. Φαίνεται όμως ότι τα κύτταρα HRS διαφεύγουν την απόπτωση, μέσω ενεργοποίησης αντιαποπτωτικών μηχανισμών και κατορθώνουν να επιβιώσουν. Με βάση τα προαναφερθέντα, προκύπτει ότι το κύτταρο HRS προέρχεται από ένα προ-αποπτωτικό, «εκτρωτικό», ώριμο Β- λεμφοκύτταρο του βλαστικού κέντρου[20,21]. Επίσης, βρέθηκε ότι τα κύτταρα LP στον NLP τύπο φέρουν σταθερές κλωνικές αναδιατάξεις και διαφορετικές σωματικές υπερμεταλλάξεις της μεταβλητής περιοχής του γονιδίου των ανοσοσφαιρινών σε κύτταρα του ίδιου κλώνου, γεγονός που υποδηλώνει ότι τα νεοπλασματικά κύτταρα διατηρούν ακέραιο το μηχανισμό των συνεχιζόμενων σωματικών υπερμεταλλάξεων στα πλαίσια του συνεχιζόμενου αντιγονικού ερεθισμού στο βλαστικό κέντρο[15,16-18]. Από τα παραπάνω συμπεραίνεται ότι και τα κύτταρα LP προέρχονται από ένα μετασχηματισμένο ώριμο Β-λεμφοκύτταρο του βλαστικού κέντρου. Τα κύτταρα LP έχουν ανοσοφαινότυπο ώριμου Β λεμφοκυττάρου με έκφραση μεταγραφικών παραγόντων και δεικτών διαφοροποίησης Β-σειράς (π.χ. PAX5, Oct-2, Bob1, bcl-6, CD20, CD19, CD79a, κ.α.)[21], σε αντίθεση με τα κύτταρα HRS του κλασικού HL, τα οποία έχουν χάσει το πρόγραμμα έκφρασης τους Β-κυτταρικού φαινοτύπου. 31
32 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Κύτταρα HRS και απώλεια έκφρασης του Β-φαινοτύπου Τα κύτταρα HRS, σε αντίθεση με τα LP, έχει βρεθεί ότι εκφράζουν ελάχιστους δείκτες Β- προέλευσης, ενώ διατηρούν δείκτες που κανονικά χαρακτηρίζουν άλλες κυτταρικές σειρές.[22,23] Η διαφοροποίηση αυτή, που περιγράφεται στην Εικόνα 1, αποτελεί μοναδικό χαρακτηριστικό και έχει ενοχοποιηθεί για την παθογένεση του κλασικού HL. Εικόνα 1. Απώλεια έκφρασης του φαινοτύπου των Β κυττάρων στα κύτταρα HRS. [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. Έχει παρατηρηθεί ότι στα κύτταρα HRS είναι κατεσταλμένη η έκφραση των μεταγραφικών παραγόντων Oct-2, Bob1 και PU.1 που χαρακτηρίζουν τη Β-κυτταρική σειρά, γεγονός που εξηγεί την απουσία έκφρασης πρωτεϊνών-στόχων όπως ο Β-κυτταρικός υποδοχέας (BCR)[24,25]. Η απουσία έκφρασης των παραπάνω μεταγραφικών παραγόντων γίνεται είτε με γενετικές είτε με επιγενετικές διαταραχές όπως η μεθυλίωση των υποκινητών των συγκεκριμένων γονιδίων.[26] 32
33 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Ένας άλλος σημαντικός μεταγραφικός παράγοντας των Β-λεμφοκυττάρων είναι ο Ε2Α, ο οποίος επάγει την έκφραση των γονιδίων CD19, CD79a, OCT2, AICDA και EBF, που προσδίδουν Β-φαινότυπο. Ο Ε2Α, μολονότι εξακολουθεί να εκφράζεται στα κύτταρα HRS, παρόλα αυτά αδρανοποιείται λόγω υπερέκφρασης των κυριότερων αναστολέων του, ABF-1 και ID2[27-29]. Στο σημείο αυτό χρειάζεται να σημειωθεί ότι ο ID2 φυσιολογικά εκφράζεται από τα κύτταρα φυσικούς φονείς (natural killer, NK) και τα δενδριτικά κύτταρα, γεγονός που υποστηρίζει την ανασταλτική τους δράση στην διαφοροποίηση και ανάπτυξη της Β- κυτταρικής σειράς. Επιπλέον, παρόλο που τα κύτταρα HRS διατηρούν την έκφραση του PAX5, του κυριότερου μεταγραφικού παράγοντα της Β-κυτταρικής σειράς, πολλά από τα γονίδιαστόχοι του δεν εκφράζονται, γεγονός που πιθανώς υποδηλώνει την ανάγκη ταυτόχρονης έκφρασης πολλών κρίσιμων μεταγραφικών παραγόντων[30,31]. Ένας άλλος πιθανός μηχανισμός καταστολής του Β-λεμφοκυτταρικού φαινοτύπου στα κύτταρα HRS είναι η ανώμαλη έκφραση και ενεργοποίηση των Notch1 και GATA3, που αποτελούν μεταγραφικούς παράγοντες της Τ-κυτταρικής σειράς. Νεότερα δεδομένα έχουν δείξει ότι τα κύτταρα HRS υπερεκφράζουν τον Notch1, που σε συνεργασία με αυξημένη δραστηριότητα του πυρηνικού παράγοντα-κβ (Nuclear factor-κβ, NF-κB) οδηγεί σε ανώμαλη έκφραση του GATA3, ο οποίος με τη σειρά του ενέχεται στην ανώμαλη παραγωγή κυτταροκινών από τα νεοπλασματικά κύτταρα[32]. Ανεξάρτητα από τους παράγοντες που εμπλέκονται στον «επαναπρογραμματισμό» της Β-λεμφοκυτταρικής διαφοροποίησης στα κύτταρα HRS, παραμένει αδιευκρίνιστο το πως ξεκινά η παραπάνω διαταραχή Ο ρόλος του Epstein-Bar και η συνεχής ενεργοποίηση του NFκΒ. Χαρακτηριστική γενετική ανωμαλία που να συνδέεται άμεσα με την παθογένεια στα νεοπλασματικά κύτταρα HRS δεν έχει ταυτοποιηθεί μέχρι σήμερα[33]. Από νωρίς η έρευνα των παθογενετικών μηχανισμών στράφηκε στη μελέτη των αντι-αποπτωτικών μηχανισμών που προστατεύουν τα κύτταρα HRS και τους επιτρέπουν να επιβιώνουν. Ο μηχανισμός αντιαπόπτωσης του κυττάρου μέσω ενεργοποίησης του παράγοντα NF-κB (Nuclear factor-κβ) φαίνεται ιδιαίτερα να λειτουργεί και να προσδίδει στα HRS ισχυρές ιδιότητες επιβίωσης (Εικόνα 2)[34]. Η σημασία της συνεχούς ενεργοποίησης του NF-κΒ στην παθογένεια του HL 33
34 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή προκύπτει από το γεγονός ότι η αναστολή έκφρασης του NF-κΒ σε κυτταρικές σειρές HL οδηγεί τα νεοπλασματικά κύτταρα σε απόπτωση [35]. Ενεργοποίηση του μηχανισμού NF-κB μπορεί να συμβεί μέσω σηματοδοτικών οδών που ξεκινούν από ενεργοποίηση επιφανειακών υποδοχέων του κυττάρου. Ο ενεργοποιημένος NF-κΒ επάγει την έκφραση σημαντικών αντιαποπτωτικών γονιδίων, τα οποία ρυθμίζουν τόσο την εξωγενή (c-flip), όσο και την ενδογενή (μιτοχονδριακή) αποπτωτική οδό (π.χ. BCL-XL, c-iaps, Survivin, XIAP). Συγκεκριμένα η πρωτεΐνη c-flip, που αποτελεί φυσιολογικό αναστολέα του εξωγενούς συστήματος απόπτωσης, υπερεκφράζεται στα κύτταρα HRS προσδίδοντάς τους πλεονέκτημα επιβίωσης[36,37]. Είναι χαρακτηριστικό ότι και η απορύθμιση της ενδογενούς (μιτοχονδριακής) οδού, οδηγεί σε ανάλογα αποτελέσματα [38]. Εκτός όμως από τις δύο αυτές οδούς, η ενεργοποίηση του NF-κΒ μπορεί να οδηγήσει και σε υπερέκφραση πρωτεϊνών που επάγουν τον ανεξέλεγκτο κυτταρικό πολλαπλασιασμό (π.χ. κυκλίνη D2), όπως επίσης και σε παραγωγή αυτοκρινών ή παρακρινών παραγόντων ανάπτυξης[39-40]. Η ενεργοποίηση του NF-κΒ φαίνεται ότι γίνεται μέσω πολλών μηχανισμών στα κύτταρα HRS (Πίνακας 1). Έτσι έχει παρατηρηθεί ενεργοποίηση του NF-κΒ μέσω έκφρασης επιφανειακών παραγόντων όπως είναι τα μόρια CD30 και CD40, που είναι μέλη της υπεροικογένειας των υποδοχέων του παράγοντα νέκρωσης του όγκου(tnf) καθώς και του υποδοχέα RANK[41-42]. Ένας άλλος τρόπος ενεργοποίησης του NF-κΒ των κυττάρων HRS παρατηρείται μέσω της πρωτεϊνης LMP1 του ιού EBV. Η τελευταία μιμείται τον ενεργοποιημένο υποδοχέα CD40 και ενεργοποιεί τον NF-κΒ[43]. Τρίτος τρόπος ενεργοποίησης παρατηρείται μέσω γενετικών διαταραχών στα κύτταρα HRS. Έτσι, διαταραχές περιλαμβάνουν ενισχύσεις (genomic gains) του γονιδίου Rel, (μέλος της οικογένειας του NF-κΒ) και του γονιδίου της NF-κΒ ενεργοποιητικής κινάσης NIK στο 40% και 20% των περιπτώσεων αντίστοιχα[44,45] και μεταλλάξεις που οδηγούν σε αδρανοποίηση των γονιδίων NFΚBIA και NFKBIE στο 10-20% περίπου των περιπτώσεων[46-48]. Νεότερα δεδομένα έχουν απομονώσει την παρουσία αδρανοποιητικών μεταλλάξεων στο γονίδιο TNFAIP3, το οποίο κωδικοποιεί τον αναστολέα Α20 του NF-κΒ, σε ποσοστό έως και 40% των περιπτώσεων[49,50], καθώς επίσης και σε αρκετές κυτταρικές σειρές HL[50]. Στο σημείο αυτό χρειάζεται να σημειωθεί ότι οι μεταλλάξεις αυτές συνυπάρχουν σε ποσοστό 34
35 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία 70% σε EBV-ασθενείς[50]. Στην περίπτωση του NLP-HL,τα κύτταρα LP παρουσιάζουν συνεχή ενεργοποίηση του NF-κΒ [51]. Ωστόσο, ο μηχανισμός ενεργοποίησής του είναι διαφορετικός από τους προαναφερθέντες και παραμένει ακόμα αδιευκρίνιστος.[52] Εικόνα 2. Ενεργοποίηση του πυρηνικού παράγοντα NF-κΒ στα κύτταρα HRS[Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3] Διαταραχή των μεταγραφικών παραγόντων ΑΡ-1 στο λέμφωμα Hodgkin Η οικογένεια ΑΡ-1 είναι μία άλλη ομάδα μεταγραφικών παραγόντων, που αποτελείται από τα διμερή ή ετερομερή που σχηματίζονται από τους παράγοντες JUN (c-jun, Jun-B, Jun-D), FOS (c-fos, FOS-B, FRA-1, FRA-2) και την οικογένεια των πρωτεϊνών ATF. Οι παράγοντες AP-1, 35
36 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ενεργοποιούνται από σήματα stress όπως η υπεριώδης ακτινοβολία αλλά και από μονοπάτια αυξητικών παραγόντων. Επιτυγχάνουν την προώθηση του κυτταρικού κύκλου και ρυθμίζουν την απόπτωση, μέσω της κυκλίνης D1 και της έκφρασης της p53.[53,54]. Η μελέτη της δραστηριότητας της οικογένειας AP-1 στο κλασικό HL έδειξε σταθερά αυξημένη έκφραση του συμπλέγματος του ΑΡ-1, που περιλαμβάνει το c-jun και το JUN-B[55-57]. Πίνακας 1. Μοριακά μονοπάτια που είναι ενεργοποιημένα στο HL, μηχανισμοί ενεργοποίησής τους και κυτταρικές λειτουργίες που επηρεάζονται. [Από Αίμα, Ιούλιος- Σεπτέμβριος 2012, τόμος3, τεύχος 3]. Μοριακό μονοπάτι Μηχανισμός ενεργοποίσης Κυτταρική λειτουργία NF-Κb JAK-STAT CD40, CD30, TNF, RANK LMP1 (30-40%) Γονιδιακές διαταραχές REL* (40%) ΝΙΚ* (20%) NFKBIA** (20%) NFKBIE** (15%) TNFAIP3** (40%, 70% EBV-) BCL3** (10%) IL-13 & IL-13R (STAT6) IL-21 &IL-21R (STAT5) Γονιδιακές διαταραχές JAK2* SOCS1** - Αναστολή απόπτωσης - Αύξηση κυτταρικού πολλαπλασιασμού - Επαγωγή κυτταρικής αύξησης - Αύξηση κυτταρικού πολλαπλασιασμού - Πλεονέκτημα επιβίωσης MAPK CD40, CD30, RANK -Αύξηση κυτταρικού Πολλαπλασιασμού PI3K/AKT/ Mtor RTKs CD40, CD30, RANK Υπερέκφραση HSP90 Σύνδεση με τον συνδέτη τους - Αυτοκρινκώς (PDGFRA, EPHB1) -Παρακρινικώς (DDR2, TRKA) - Ευόδωση σύνθεσης ογκοπρωτεϊνών - Προαγωγή κυτταρικού κύκλου. - Ανστολή απόπτωσης Ενεργοποίηση οδών μεταβίβασης σήματος * Γονιδιακή ενίσχυση( Gain or Amplification), ** Σημειακές μεταλλάξεις ( Point mutations)και γονιδιακά ελλείμματα (Deletions) 36
37 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Οι μεταγραφικοί παράγοντες της οικογένειας ΑP-1 σε συνεργασία με τον NFκB, αυξάνουν την έκφραση της κυκλίνης D2, του πρωτοογκογονιδίου c-met και του μορίου προσκόλλησης CCR7 (υποδοχέας homing των λεμφοκυττάρων), τα οποία είναι γνωστό ότι υπερεκφράζονται στα κύτταρα HRS. Επιπρόσθετα, έχει βρεθεί ότι ο Jun-B προάγει τη μεταγραφή του μορίου CD30, το οποίο χαρακτηρίζει το ΗL[58]. Στο συγκεκριμένο σημείο χρειάζεται να σημειωθεί ότι ο NLP-HL, ο οποίος στερείται της έκφρασης του CD30, χαρακτηρίζεται και από την απουσία του ΑΡ-1, καθώς και της έκφρασης του c-jun και του Jun-B[55,57]. Από την άλλη πλευρά ο παράγοντας ΑΡ-1 ενεργοποιεί στα κύτταρα HRS την ανοσοτροποποιητική πρωτείνη γκαλεκτίνη(galectin, Gal), η οποία συνδέεται με ομάδες γλυκάνης [59-61]. Η Gal-1 αποτελεί ένα πρωτότυπο μέλος, που έχει την ιδιότητα να ρυθμίζει την επιβίωση των Τ-λεμφοκυττάρων, την ομοιόσταση και την φλεγμονή[60] και εκφράζεται σχεδόν στο σύνολο των κυττάρων HRS (>90%). Επιπρόσθετα, συμβαδίζει με την αυξημένη έκφραση του ενεργοποιημένου μορίου AP-1, c-jun53 [61] Eνεργοποίηση οδών αγωγής σήματος Νεότερα δεδομένα έχουν αναδείξει ότι στο HL είναι ενεργοποιημένοι πολλοί από τους βασικούς κυτταρικούς μηχανισμούς αγωγής σήματος, με αποτέλεσμα την απορύθμιση του κυτταρικού κύκλου και της απόπτωσης και τελικά την ανάπτυξη του νεοπλασματικού φαινοτύπου ( Πίνακας 1). Χαρακτηριστικό εύρημα είναι η μη φυσιολογική συνεχής ενεργοποίηση της οδού JAK-STAT, που παίζει σημαίνοντα ρόλο στην ανάπτυξη του αιμοποιητικού συστήματος και στην ανοσολογική απάντηση[62,63]. Πιο συγκεκριμένα, στο HL έχει διαπιστωθεί συνεχής ενεργοποίηση διαφόρων μελών της ομάδας JAK-STAT όπως των STAT3, STAT5 και STAT6, οι οποίες προάγουν τον κυτταρικό πολλαπλασιασμό και την επιβίωση των νεοπλασματικών κυττάρων [64-66]. Ειδικά η ενεργοποίηση της STAT6 φαίνεται να προκαλείται με αυτοκρινή μηχανισμό, αφού τα κύτταρα HRS εκφράζουν την IL-13 και τον υποδοχέα της και η αναστολή της μετάδοσης σήματος μέσω της IL-13 καταστέλλει την δραστηριότητα της STAT6 [67]. Oι αναστολείς τυροσινικής κινάσης της οδού JAK-STAT παρεμποδίζουν την ενεργοποίηση των περισσοτέρων μελών της οικογένειας STAT σε κυτταρικές σειρές HL, και οδηγούν σε αναστολή του πολλαπλασιασμού και ευόδωση της 37
38 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή απόπτωσης[68,69]. Ο σημαντικός ρόλος της ενεργοποίησης της οδού JAK-STAT στην παθογένεια του HL ενισχύεται από την παρατήρηση ότι στο 1/3 των περιπτώσεων υπάρχει ενίσχυση (amplification) του γενετικού τόπου 9p24 που περιλαμβάνει το γονίδιο JAK2, ενώ σε ποσοστό 40% τα κύτταρα HRS φέρουν σωματικές αδρανοποιητικές μεταλλάξεις στα γονίδια που κωδικοποιούν τις πρωτεΐνες SOCS, τους κυριότερους αναστολείς της οδού JAK-STAT [70-72] Ένας έτερος ενεργοποιημένος καταρράκτης αγωγής σήματος, που παρατηρείται στο HL, είναι αυτός του συστήματος κινασών της οικογένειας ΜΑΡΚ. Πρόκειται για τρεις ομάδες κινασών (p38,jnk και ERK) που δρουν παράλληλα και ενεργοποιούνται από σήματα που προέρχονται από μεμβρανικούς υποδοχείς και τα οποία μεταβιβάζονται από κινάσεςυποστρώματα, μέσω διαδοχικών φωσφορυλιώσεων. Το αποτέλεσμα είναι η διέγερση μεταγραφικών παραγόντων που ελέγχουν την έκφραση ρυθμιστών του κυτταρικού κύκλου και την απόπτωση. Τα συστήματα JNK και ERK είναι ενεργοποιημένα στο κλασικό ΗL και οδηγούν σε ανεξέλεγκτο κυτταρικό πολλαπλασιασμό[73,74]. Ένα τρίτο μοριακό μονοπάτι που αποτελεί βασικό μηχανισμό επιβίωσης του κυττάρου και η συνεχής ενεργοποίησή του έχει συσχετιστεί με πολλές νεοπλασίες είναι η οδός ΡΙ3Κ/ΑΚΤ/Mtor [75]. Η αγωγή του σήματος μέσω της κινάσης mtor οδηγεί σε έλεγχο της πρωτεϊνοσύνθεσης και συνεπώς της σύνθεσης ογκοπρωτεϊνών καθώς και μορίων ρυθμιστικών του κυτταρικού κύκλου και της απόπτωσης. Η οδός PI3K/AKT/mTOR είναι ενεργοποιημένη στα λεμφώματα και αποτελεί βασικό θεραπευτικό στόχο [76-81]. H ενεργοποίηση των οδών ERK και PI3K/AKT/mTOR στο ΗL πιθανώς οφείλεται στην ενεργοποίηση των υποδοχέων CD30, CD40 και RANK. Τέλος υπάρχουν και οι υποδοχείς τυροσίνης κινάσης (RTKs) όπως είναι οι PDGFRA, DDR2, RON, EPHB1, TRKA, TRKB, που επίσης εκφράζονται στα κύτταρα HRS, ιδιαίτερα στον υπότυπο της οζώδους σκλήρυνσης και συμβάλλουν στη διαμόρφωση του νεοπλασματικού φαινοτύπου. Μελέτες με τη χρήση αντισωμάτων κατά φωσφορυλιωμένης τυροσινικής κινάσης έδειξαν ότι σε πολλές περιπτώσεις τα κύτταρα HRS έχουν αυξημένα ενδοκυττάρια μόρια φωσφορυλιωμένης τυροσινικής κινάσης υποδηλώνοντας την ύπαρξη ενεργού 38
39 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία μεταβίβασης του σήματος μέσω των RTKs. H ενεργοποίηση αυτών των κινασών τυροσίνης γίνεται μέσω σύνδεσης με το συνδετικό τους μόριο με αυτοκρινή (PDGFRA, EPHB1) ή παρακρινή τρόπο (DDR2, TRKA) και όχι μέσω μεταλλάξεων των αντίστοιχων γονιδίων[82]. Η συνέκφραση 3 ή περισσοτέρων κινασών είναι συχνότερη στις EBV-αρνητικές περιπτώσεις, όπου η αυξημένη δραστηριότητά τους μιμείται τη λειτουργία της LMP1 στις EBV-θετικές περιπτώσεις. Ωστόσο, η αναστολή της έκφρασης του PDGFRA από το imatinib δεν είχε επίδραση στον πολλαπλασιασμό και την απόπτωση των κυττάρων HRS [83]. Η συνέκφραση και η ενεργοποίηση πολλαπλών κινασών τυροσίνης στο HL αποτελεί μοναδικό παράδειγμα και υποδηλώνει ότι συμβάλλουν στην παθογένεια του HL Ο ρόλος των micro RNAs O ρόλος των micro RNAs έχει αποδειχθεί ότι είναι καίριος στην παθογένεια, στη διάγνωση και πρόγνωση διαφόρων κακοηθειών [84-86]. Τα mirnas αποτελούν μικρά μη κωδικοποιούντα μόρια RNA, τα οποία ρυθμίζουν την έκφραση διαφόρων γονιδίων-στόχων τους μέσω πλήρους ή ατελούς σύνδεσης με συμπληρωματικές αλληλουχίες βάσεων. Μετά την πλήρη σύνδεσή τους με το RNA-στόχο, το mrna διασπάται, ενώ στις περιπτώσεις ατελούς σύνδεσης επέρχεται αναστολή της μετάφρασης του mrna-στόχου[87]. Τα mirnas ασκούν σημαντική ρυθμιστική δράση στον κυτταρικό κύκλο, την απόπτωση και τη διαφοροποίηση, οι οποίες εμπλέκονται στην παθογένεια του καρκίνου[88]. Η έκφρασή τους διαφέρει σημαντικά μεταξύ φυσιολογικών και νεοπλασματικών ιστών. Επιπλέον, σε ορισμένα νεοπλάσματα έχει βρεθεί χαρακτηριστικό πρότυπο έκφρασης συγκεκριμένων mirnas, ενώ πιστεύεται ότι διαθέτουν είτε ογκοκατασταλτικές, είτε ογκογόνες ιδιότητες, γεγονός στο οποίο οφείλεται ο χαρακτηρισμός τους ως «oncomirs»[89]. Στο HL έχει διαπιστωθεί αυξημένη έκφραση του BIC/mir-155, που κωδικοποιείται από το τελικό τμήμα του γονιδίου BIC (B cell Integration Cluster)[90]. Η αυξημένη έκφραση του BIC/mir-155 στα Β-λεμφοκύτταρα σε ποντίκια οδηγεί σε πολυκλωνική προλευχαιμική υπερπλασία τους και στη συνέχεια σε λέμφωμα [91], ενώ η αναστολή της έκφρασής του σε knock-out ποντίκια έδειξε σημαντικές μεταβολές στο ανοσοποιητικό σύστημα με 39
40 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ελαττωματική λειτουργία δενδριτικών κυττάρων, παθολογική έκκριση κυτταροκινών και επαγωγή Τh2 τύπου ανοσολογικής απάντησης [92,93]. Αρκετές μελέτες σε κυτταρικές σειρές HL ανέδειξαν την ύπαρξη χαρακτηριστικού προτύπου έκφρασης mirnas [94-96], ενώ μελέτη λεμφαδένων στο κλασικό HL ανέδειξε πρότυπο έκφρασης 25 mirnas που διαφέρουν από τις αντιδραστικές λεμφαδενοπάθειες και 36 micrornas που διαχωρίζουν τον υπότυπο της οζώδους σκλήρυνσης από αυτόν της μικτής κυτταροβρίθειας. Επιπλέον, πιο πρόσφατη μελέτη από την ίδια ερευνητική ομάδα έδειξε ότι από τα 25 mirnas που εκφράζονται στο κλασικό HL η αυξημένη έκφραση του mir-135a σχετίζεται με σημαντικά καλύτερη επιβίωση ελεύθερη νόσου. Ένας από τους στόχους του mir-135a είναι το γονίδιο JAK2 που αποτελεί σημαντικό μέλος της οδού JAK-STAT, η οποία έχει βρεθεί ενεργοποιημένη στο HL. Ένας πιθανός μηχανισμός που ερμηνεύει την προγνωστική αξία του mir135-a είναι ότι η αναστολή του JAK2 από το mir-135a οδηγεί σε ελάττωση των επιπέδων του mrna και της πρωτεΐνης του αντιαποπτωτικού γονιδίου BclxL με αποτέλεσμα ευόδωση της απόπτωσης των νεοπλασματικών κυττάρων [97]. H συμμετοχή του mir-135a στην παθογένεια του HL, και η θετική προγνωστική του αξία το καθιστούν ενδιαφέροντα θεραπευτικό στόχο O ρόλος του αντιδραστικού περιβάλλοντος Το κλασικό HL χαρακτηρίζεται από ένα φλεγμονώδες κυτταρικό υπόστρωμα, το οποίο περιλαμβάνει λεμφοκύτταρα, πλασματοκύτταρα, ηωσινόφιλα, ουδετερόφιλα, μαστοκύτταρα, ιστιοκύτταρα και ινοβλάστες, ενώ τα κύτταρα HRS αποτελούν αδρά το 1% περίπου του συνολικού κυτταρικού πληθυσμού. Η πλειονότητα των κυττάρων του αντιδραστικού περιβάλλοντος είναι CD4+ Τ-λεμφοκύτταρα, η παρουσία των οποίων θεωρείται καίριας σημασίας για την επιβίωση των νεοπλασματικών HRS κυττάρων. H παρουσία του κυτταρικού αυτού υποστρώματος οφείλεται κατά κύριο λόγο στην προσέλκυση των κυττάρων που το απαρτίζουν λόγω παραγωγής πληθώρας κυτταροκινών και χημειοκινών από τα νεοπλασματικά κύτταρα (Εικόνα 3). 40
41 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Τα κύτταρα ΗRS παράγουν κυτταροκίνες που συμβάλλουν τόσο στη δημιουργία ενός περιβάλλοντος ευνοϊκού για την επιβίωσή τους, όσο και στον ίδιο τους τον πολλαπλασιασμό. Αρκετές κυτταροκίνες έχουν ανιχνευθεί σε μεταγραφικό ή μεταφραστικό επίπεδο τόσο στα κύτταρα HRS όσο και στα αντιδραστικό υπόστρωμα, όπως οι IL-1, IL-5, IL-6, IL-7, IL-9, IL-10, IL-13, IL-17 και TGFβ. Αυτές διαδραματίζουν σημαντικό ρόλο είτε στη δημιουργία του αντιδραστικού υποστρώματος (IL-5), είτε ως αυξητικοί παράγοντες (IL-6, IL-7, IL-9, IL-13, IL-17) είτε ως ανοσοκατασταλτικοί παράγοντες (IL-10, TGFβ)[98]. Τα κύτταρα HRS, καθώς και τα κύτταρα του αντιδραστικού περιβάλλοντος εκκρίνουν παράλληλα και χημειοκίνες, οι οποίες προάγουν την συσσώρευση διαφόρων κυττάρων, όπως είναι τα ηωσινόφιλα (eotaxin, CCL28), τα πλασματοκύτταρα (CCL28) και τα Τ- λεμφοκύτταρα.[99-100] Οι χημειοκίνες αποτελούν ένα σύνολο περίπου 40 μικρού μεγέθους εκκρινόμενων πρωτεϊνών. Ανήκουν σε 4 οικογένειες (CC, CXC, C και CX3C) και δρουν μέσω 18 διαμεμβρανικών υποδοχέων ως χημειοτακτικοί παράγοντες [101] Πιο συγκεκριμένα, Η χημειοκίνη TARC (CCL17) είναι ειδική και εκφράζεται μόνο στο κλασικό HL ενώ η MDC CCL22) εκφράζεται τόσο στο κλασικό όσο και στο NLP-HL. Και οι δύο αυτές χημειοκίνες δεσμεύονται στον CCR4 υποδοχέα των Th-2 κυττάρων, ερμηνεύοντας πιθανώς τη συγκέντρωση τέτοιων λεμφοκυττάρων γύρω από τα κύτταρα HRS [ ] φαίνεται ότι τα περισσότερα από τα λεμφοκύτταρα του αντιδραστικού περιβάλλοντος είναι προγραμματισμένα κατά τέτοιο τρόπο, ώστε καταστέλλουν την αποτελεσματική ανοσολογική απάντηση στους προσβεβλημένους από τη νόσο ιστούς παρεμποδίζοντας την εξόντωση των κυττάρων HRS μέσω κυτταροτοξικών Τ-λεμφοκυττάρων[98]. Αυτό έχει αποδειχθεί για τα CTLA-4+, CD4+ CD10+ και CD4+ CD25+ Τ-λεμφοκύτταρα[104] και πιθανώς και για αυτά που παράγουν TGFβ[105]. Τα CD4+ λεμφοκύτταρα της τύπου-1 ανοσολογικής απάντησης (Th-1) και τα κυτταροτοξικά CD8+ Τ-λεμφοκύτταρα συνήθως απουσιάζουν από το μικροπεριβάλλον του HL. Αυτό οφείλεται στο γεγονός ότι τα κύτταρα HRS εκκρίνουν αφ ενός κυτταροκίνες που σχετίζονται με την Th-2 απάντηση (IL-4, IL-13) και αφ ετέρου κυτταροκίνες που καταστέλλουν την Th-1 απάντηση (IL-10, TGFβ) και τα CD8+ Τ-λεμφοκύτταρα93. Επίσης, τα κύτταρα HRS εκφράζουν CD95-ligand, που προάγει την απόπτωση των ενεργοποιημένων Th-1 κυττάρων και των CD8+ Τ-λεμφοκυττάρων [106]. Το συγκεκριμένο προφίλ κυτταροκινών που εκκρίνουν τα κύτταρα HRS συμμετέχει ενεργά 41
42 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή στην ανάπτυξη ενός ανενεργού ανοσολογικά μικροπεριβάλλοντος το οποίο αναστέλλει την απόπτωση και εξασφαλίζει τελικά την επιβίωσή τους. Εικόνα 3. Αλληλεπιδράσεις μεταξύ των κυττάρων HRS και των κυττάρων του αντιδραστικού περιβάλλοντος. [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. 42
43 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία 1.4 ΚΛΙΝΙΚΗ ΕΙΚΟΝΑ Το HL προσβάλει συνήθως άτομα νεαρής ηλικίας. Στην πλειοψηφία τους οι ασθενείς είναι ασυμπτωματικοί με ανεύρεση συνήθως διογκωμένων λεμφαδένων στις τραχηλικές, υπερκλείδιες και τις μασχαλιαίες χώρες. Διόγκωση λεμφαδένων μπορεί να παρατηρηθεί επίσης στο μεσοθωράκιο, στην παραορτική χώρα, ενώ δύναται να παρατηρηθεί προσβολή σπληνός σε ποσοστό 20% των ασθενών. Μεταξύ των εξωλεμφαδενικών εντοπίσεων της νόσου, συχνότερες είναι οι εστίες στον πνεύμονα, στο μυελό των οστών και στο ήπαρ. Γενικά, οι παθολογικοί λεμφαδένες είναι κατά κανόνα ανώδυνοι, σκληροί και καθηλωμένοι, ενώ υπάρχει το ενδεχόμενο να σχηματίζουν μεγάλη μάζα με τη μορφή block κυρίως στο ανώτερο μεσοθωράκιο. Η κλινική εικόνα των ασθενών με Λέμφωμα Hodgkin ποικίλλει ανάλογα με την εντόπιση των ευρημάτων της νόσου και της ύπαρξης των γενικών συμπτωμάτων τους (Πίνακας 2). Πιο συγκεκριμένα, η παρουσία γενικών συμπτωμάτων, ορίζεται με το κεφαλαίο γράμμα Β. Στα Β- συμπτώματα περιλαμβάνονται ο πυρετός, οι νυχτερινές εφιδρώσεις και η απώλεια βάρους. Το 30-40% των ασθενών που πάσχουν από προχωρημένα στάδια της νόσου, παρουσιάζουν Β-συμπτώματα. Η κλασσική πυρετική καμπύλη είναι κυματοειδής και φέρει το όνομα Pel Epstein από τους ιατρούς που την περιέγραψαν. Πρόκειται για διαστήματα εμπυρέτου >38 C, κατά κανόνα διάρκειας μίας εβδομάδος, εναλλασσόμενων με διαστήματα απυρεξίας ίδιας διάρκειας. Η μορφή του εμπυρέτου του Λεμφώματος Hodgkin είναι τέτοια που μπορεί να φτάσει μέχρι και C, τις νυχτερινές ώρες, ενώ κατόπιν δύναται να μειώνεται μέχρι απυρεξίας ή και υποθερμίας, τις πρώτες πρωινές ώρες [ ]. Οι νυχτερινές εφιδρώσεις θεωρούνται ως Β-σύμπτωμα όταν είναι έντονες και ο ασθενής υποχρεούται να αλλάξει εσώρουχα και ενίοτε κλινοσκεπάσματα κατά τη διάρκεια της νύχτας. Η απώλεια βάρους, χρειάζεται να είναι>10% του συνολικού βάρους του ασθενούς και οφείλει να έχει μειωθεί το τελευταίο εξάμηνο. 43
44 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Παρόλο που ο κνησμός σα σύμπτωμα δεν εντάσσεται στα Β-συμπτώματα, εντούτοις μπορεί να υπάρχει, να είναι βασανιστικός, γενικευμένος και ενδεχομένως μπορεί να αποτελεί και το μοναδικό σύμπτωμα του ανθρώπου που νοσεί. Συχνά οδηγεί σε εκδορές, τις λεγόμενες δρυφάδες, που δίνουν την εικόνα δερματίτιδας[110,111]. Σπάνιο επίσης σύμπτωμα, που όμως είναι και αυτό ενδεικτικό της νόσου, αποτελεί η εμφάνιση πόνου σε διογκωμένους λεμφαδένες, μετά τη λήψη οινοπνευματωδών ποτών, ειδικά όταν οι διογκώσεις εντοπίζονται ενδοθωρακικά, ή ενδοκοιλιακά.[ ] Χρειάζεται να σημειωθεί ότι επί ογκώδους νόσου στο μεσοθωράκιο μπορεί να παρατηρηθεί ως σύμπτωμα βήχας, θωρακικό άλγος, δύσπνοια στην κόπωση, ή σπάνια σύνδρομο άνω κοίλης φλέβας, πλευριτική ή περικαρδιακή συλλογή. Επί οστικής προσβολής (όχι όμως του μυελού των οστών), ο ασθενής μπορεί να εμφανίσει πόνο στην ηρεμία, ή και μετά από πλήξη, λόγω πίεσης του περιοστέου. Επιπλέον, επί ενδοκοιλιακής ή και παρασπονδυλικής εντόπισης, ο ασθενής δύναται να πάσχει από οσφυαλγία. Πιο συγκεκριμένα, επί αναπτύξεως λεμφαδένων στην πύλη του ήπατος, θα εκδηλωθεί σημειολογία αποφρακτικού ικτέρου και επί πίεσης του νωτιαίου σωλήνα λόγω παρουσίας παρασπονδυλικής μάζας, θα αναζητηθεί η αντίστοιχη σημειολογία. Από πλευράς ευρημάτων, η νόσος εκδηλώνεται με ψηλαφητούς λεμφαδένες στις τραχηλικές, υπερκλείδιες, μασχαλιαίες χώρες, ή και στους βουβωνικούς λεμφαδένες, ανάλογα με το στάδιο της νόσου και την ανατομική εντόπισή της. Οι λεμφαδένες είναι κατά κανόνα ανώδυνοι, σκληροί και καθηλωμένοι, ενώ δύνανται και να σχηματίζουν μεγάλες μάζες, με τη μορφή block. Οι διογκωμένοι λεμφαδένες μπορεί να είναι ετερόπλευροι ή αμφοτερόπλευροι Η παρουσία μικρών δορυφόρων λεμφαδένων, που συνήθως δεν είναι προσβεβλημένοι από τη νόσο είναι σύνηθες φαινόμενο. H γνώση αυτή είναι απαραίτητη για τον χειρουργό που θα κληθεί να κάνει διαγνωστική βιοψία σε ασθενή, αφού είναι σημαντικό να επιλέξει την αφαίρεση παθολογικού λεμφαδένα και όχι του εύκολα προσβάσιμου, που μπορεί να αποτελεί αντιδραστικά διογκωμένος λεμφαδένας. H χρονική διάρκεια εντός της οποίας παρατηρείται η διόγκωση των λεμφαδένων στο ΗL, ποικίλλει από εβδομάδες, εώς και μήνες, ενώ δεν είναι σπάνια προσωρινά αυτόματη υποχώρηση της μάζας για άλλοτε 44
45 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία διαφορετικό χρονικό διάστημα. Σε αυτές τις περιπτώσεις δύναται να παρατηρηθεί επανεμφάνιση της μάζας που μπορεί να συνοδεύεται σε αρκετούς ασθενείς από πυρετικά κύματα. Πίνακας 2. Τρόποι εκδήλωσης-εμφάνισης του λεμφώματος Hodgkin (κατά σειρά συχνότητας) [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. Τρόπος Εκδήλωσης-εμφάνισης Ασυμπτωματική διόγκωση κλινικά ψηλαφητών λεμφαδένων (συνήθως τραχηλικών-υπερκλειδίων) Διόγκωση κλινικά ψηλαφητών λεμφαδένων με παρουσία Β-συμπτωμάτων Παρατεινόμενο εμπύρετο ή άλλα Β-συμπτώματα ή/και γενικευμένος κνησμός χωρίς κλινικά ψηλαφητούς λεμφαδένες Βήχας, δύσπνοια στην κόπωση ή σπανίως, σύνδρομο άνω κοίλης φλέβας Τυχαίο εύρημα διογκωμένων λεμφαδένων στο μεσοθωράκιο σε απλή ακτινογραφία θώρακος Συχνότητα 65% 30% 3% <2% <2% Πιο συχνή εντόπιση της νόσου παρατηρείται στους τραχηλικούς και υπερκλείδιους λεμφαδένες. Σπανίως η νόσος εντοπίζεται αποκλειστικά κάτωθεν του διαφράγματος. Ο σπλήνας είναι ψηλαφητός < 10% των περιπτώσεων, παρόλα αυτά, μελέτες έχουν δείξει ότι μπορεί να πάσχει σε ποσοστό εώς και 30%. Μεταξύ των εξωλεμφαδενικών εντοπίσεων τη νόσου, συχνότερες είναι εκείνες του πνεύμονα, του μυελού των οστών και του ήπατος. Η προσβολή του δακτυλίου Waldeyer, του γαστρεντερικού σωλήνα, του δέρματος και του κεντρικού νευρικού συστήματος από HL είναι σπάνια, εν αντιθέσει με ορισμένους ιστολογικούς τύπους non-hodgkin λεμφωμάτων στους οποίους η εντόπιση στα εν λόγω όργανα είναι συχνή (Πίνακας 3). 45
46 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Πίνακας 3. Συχνότητα προσβολής ανατομικών περιοχών και οργάνων, σε ασθενείς με λέμφωμα Hodgkin. Ανατομική περιοχή ή Όργανο Συχνότητα προσβολής (%) με βάση την κλινική σταδιοποίηση Τραχηλικοί-Υπερκλείδιοι) 80% Δακτύλιος Waldeyer 1% Λεμφαδένες Μεσοθωρακίου 50% Μασχαλιαίοι Λεμφαδένες 25% Παραορτικοί Λεμφαδένες * 25% Σπλήνας ** 9% Οπισθοσκελιαιοι Λεμφαδένες 2% Μεσεντέριοι Λεμφαδένες 1% Λαγόνιοι Λεμφαδένες 15% Βουβωνικοί/Μηριαίοι Λεμφαδένες 10% Πνεύμονας 7% Μυελός των Οστών 6% Ήπαρ 5% Οστά 3% Λοιπές εξωλεμφαδενικές εντοπίσεις <1% * Εφόσον αξιολογούνται με βιοψία μετά από ερευνητική λαπαροτομία το ποσοστό ανέρχεται σε 30-40%. ** Εφόσον αξιολογείται με ιστολογική εξέταση μετά από σπληνεκτομή στα πλαίσια ερευνητικής λαπαροτομίας, το ποσοστό ανέρχεται στο 30-35%. Από: ΑΙΜΑΤΟΛΟΓΙΑ στην Κλινική Πράξη, Γ.Α. Παγκαλή και συνεργάτες, σελίδα 620. Ιατρικές εκδόσεις Πσασχλίδης, Αθήνα 2008 ( Τροποποιηθέν). 46
47 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία 1.5 ΕΡΓΑΣΤΗΡΙΑΚΑ ΕΥΡΗΜΑΤΑ Αιματολογικός και Βιοχημικός Έλεγχος Ο αιματολογικός και βιοχημικός έλεγχος του ασθενούς με HL κατά τη διάγνωση είναι συνήθως φυσιολογικός, ιδίως στα αρχικά στάδια. Στα προχωρημένα στάδια είναι σύνηθες να παρατηρείται αναιμία, λευκοκυττάρωση με πολυμορφοπυρήνωση, λεμφοκυτταροπενία και θρομβοκυττάρωση. Η ΤΚΕ στο 45% των ασθενών ανευρίσκεται 50 mm/h, ενώ στο 15% των πασχόντων σε προχωρημένα στάδια, παρατηρείται ΤΚΕ 100mm/h, με ισχυρή συσχέτιση με τα Β-συμπτώματα. Η αυξημένη ΤΚΕ συνοδεύεται τυπικά και από αυξημένα επίπεδα C- Αντιδρώσας Πρωτεΐνης (CRP), που μπορεί να φθάνουν και το 60πλάσιο του φυσιολογικού (300 mg/l) χωρίς να υποκρύπτεται λοίμωξη, ενώ τα επίπεδα της επανέρχονται στο φυσιολογικό εντός των 2 πρώτων εβδομάδων από την έναρξη χημειοθεραπείας στην πλειονότητα των ασθενών [115]. Η προκαλσιτονίνη από την πλευρά της, είναι φυσιολογική στο 98% των περιπτώσεων σε απουσία λοίμωξης[116]. Κατά τη διάγνωση της νόσου μπορεί να παρατηρηθεί αύξηση των πρωτεϊνών οξείας φάσης (φερριτίνη, απτοσφαιρίνες, ινωδογόνο), αλλά και της εψιδίνης[115,117]. Ο βιοχημικός έλεγχος είναι συνήθως φυσιολογικός. Σε μία μικρή αναλογία ασθενών (κυρίως στα προχωρημένα στάδια της νόσου) ανευρίσκονται αυξημένα τα επίπεδα τιμών της LDH και της β 2 - μικροσφαιρίνης[118]. Ενίοτε μπορεί να παρατηρηθεί αύξηση της γ-gt και της αλκαλικής φωσφατάσης, χωρίς να υποδηλώνεται κατά ανάγκη προσβολή του ήπατος, όπως επίσης ενδέχεται να παρατηρηθεί και υπερχολερυθριναιμία και διαταραχή των ηπατικών ενζύμων. Η συχνότητα των παθολογικών μεταβολών των προαναφερθέντων ευρημάτων σε ασθενείς με HL, παρατίθεται στον Πίνακα 4. 47
48 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Πίνακας 4. Αιματολογικά και βιοχημικά ευρήματα ασθενών με λέμφωμα Hodgkin ΣΤΑΔΙΑ ΙΑ, ΙΙΑ ΣΤΑΔΙΑ ΙΒ, ΙΙΒ, ΙΙΙ, ΣΥΝΟΛΟ Εργαστηριακό Εύρημα IV ΑΣΘΕΝΩΝ Συχνότητα (%) Αναιμία Λευκοκυττάρωση ( /Ι) Λεμφοκυτταροπενία (<1x10 9 /l) Λεμφοκυτταροπενία (<1.5x10 9 /l) Ηωσινοφιλία ( /Ι) Θρομβοκυττάρωση (> /Ι) ΤΚΕ ΤΚΕ Αύξηση LDH Αύξηση αλκαλικής φωσφατάσης Υπολευκωματιναιμία (<3.5 gr/dl) Αύξηση β 2 μικροσφαιρίνης (>2.4mg/I) ** Aιμοσφαιρίνη <13gr/ dl και 15gr/dl για άρρενες και θήλεις αντιστοίχως Από: AIMAΤΟΛΟΓΙΑ στην Κλινική Πράξη. Γ.Α.Πάγκαλη και Συνεργατών, σελίδα 621. Ιατρικές Εκδόσεις Πασχαλίδη, Αθήνα 2008 (Τροποποιηθέν) Oστεομυελική Βιοψία (OMB) Όσον αφορά την επινέμεση του μυελού των οστών, η διήθηση του σε ασθενείς με HL είναι κατά κανόνα εστιακή. Αυτό συνεπάγεται ότι όσο μεγαλύτερο είναι το μέγεθος του προσβαλομένου οστικού κυλίνδρου, τόσο μεγαλύτερη είναι και η πιθανότητα ανεύρεσης νόσου. Η συχνότητα προσβολής μυελού των οστών κυμαίνεται από 6% εώς 8%, ανάλογα με το αν η βιοψία έχει γίνει μονόπλευρα ή αμφοτερόπλευρα, στις λαγόνιες άκανθες. Ασθενείς με Β-συμπτώματα, στάδια νόσου ΙΙΙ και IV, ηλικία 35 ετών, αναιμία (αιμοσφαιρίνη σε άνδρες <13g/dl ή σε γυναίκες <11.5g/dl), σχετικώς μειωμένο αριθμό λευκών αιμοσφαιρίων 48
49 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία (< /l) και βουβωνική/λαγόνιο εντόπιση της νόσου, έχουν στατιστικά μεγαλύτερη πιθανότητα προσβολής του μυελού των οστών [119]. Χρειάζεται να τονιστεί ότι η διάγνωση του HL από την οστεομυελική βιοψία είναι δυσχερής εώς αδύνατη, χωρίς την προϋπάρχουσα διάγνωση από βιοψία λεμφαδένα. 1.6 ΑΠΕΙΚΟΝΙΣΤΙΚΟΣ ΕΛΕΓΧΟΣ Ακτινογραφία Θώρακος Στην απλή ακτινογραφία θώρακος παρατηρείται διόγκωση των λεμφαδένων του πρόσθιου άνω μεσοθωρακίου, ειδικά στις πνευμονικές πύλες, σε ποσοστό περίπου 50% των ασθενών. Από την ακτινογραφία θώρακος επίσης, προσδιορίζεται και το μέγεθος της μάζας, ογκώδους ή μη (Εικόνα 4). Ο προσδιορισμός αυτός προκύπτει από το λόγο της μέγιστης διαμέτρου της μάζας, προς τη μέγιστη εγκάρσια διάμετρο του θωρακικού κλωβού. Όταν ο λόγος αυτός υπερβαίνει το «0.33» τότε η μάζα χαρακτηρίζεται ως ογκώδης, ενώ όταν η μάζα ξεπερνά τα «0,45», χαρακτηρίζεται ως πολύ ογκώδης. Εναλλακτικά, ο προσδιορισμός της ογκώδους μάζας υπολογίζεται και από την εγκάρσια διάμετρο της μάζας στο επίπεδο των σπονδύλων Θ5-Θ6. Σε αυτή την περίπτωση, ονομάζεται ογκώδης νόσος όταν ο λόγος υπερβαίνει το Εικόνα 4. Οπισθοπρόσθια ακτινογραφία θώρακος σε ασθενή με λέμφωμα Hodgkin και εντόπιση στο μεσοθωράκιο. [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. 49
50 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Αξονική Τομογραφία (CT) Ο απεικονιστικός έλεγχος ασθενούς με HL περιλαμβάνει τις περιοχές του τραχήλου, του θώρακος, της άνω και κάτω κοιλίας, συμπεριλαμβανομένου των παραορτικών λεμφαδένων, βουβωνικών και των μηριαίων τριγώνων άμφω. Η εξέταση προαπαιτεί τη λήψη σκιαγραφικού φαρμάκου από στόματος και ενδοφλεβίως. Η μελέτη της αξονικής τομογραφίας δύναται να αποκαλύψει λεμφαδενικές διογκώσεις, ύπαρξη οζιδίων στον πνεύμονα ή και εξωλεμφαδενικές εντοπίσεις, όπως επίσης και διηθήσεις στου ήπατος και του σπληνός. Εικόνα 5 α,β,γ,δ. Εικόνες CT ασθενών με ΗL και διόγκωση λεμφαδένων μεσοθωρακίου (α, β), διόγκωση παραορτικών λεμφαδένων (γ), προσβολή σπληνός με παρουσία υπόπυκνων αλλοιώσεων σπληνικού παρεγχύματος (δ). [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3] Σπινθηρογράφημα με Ραδιενεργό Γάλλιο, Σπινθηρογράφημα Οστών Πρόκειται για εξέταση που χρησιμοποιείτο την περίοδο στη μελέτη του λεμφώματος Hodgkin. Μετά την ανακάλυψη της τομογραφίας εκπομπής ποζιτρονίων, πλέον δεν εφαρμόζεται στην πράξη, παρά μόνο σπάνια όταν υπάρχει αμφιβολία για οστική εντόπιση της νόσου[120] Μαγνητική Τομογραφία (MRI) Η μαγνητική τομογραφία παίζει σημαντικό ρόλο στη σταδιοποίηση της νόσου του Hodgkin, όταν υπάρχουν υπόνοιες διήθησης του ήπατος, του σπληνός, οστικών εντοπίσεων καθώς και 50
51 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία ανάδειξη παρασπονδυλικής μάζας, από τον έλεγχο που έχει προηγηθεί με την CT Τομογραφία Εκπομπής Ποζιτρονίων-ΡΕΤ Scan ( Positron Epission Tomography) Η τομογραφία εκπομπής ποζιτρονίων (ΡΕΤ) αποτελεί μία σύγχρονη λειτουργική απεικονιστική μέθοδο, η οποία προέρχεται από τη σύντηξη δύο εξετάσεων, του ΡΕΤ και της CT. Κατά την εκτέλεση της συγκεκριμένης εξέτασης, ο ασθενής λαμβάνει ενδοφλέβια χορήγηση φθοριωμένης δεσοξυγλυκόζης (18FDG), η οποία και προσλαμβάνεται σε αυξημένο βαθμό από τα κύτταρα της νόσου, που παρουσιάζουν αυξημένη μεταβολική δραστηριότητα. Τα κριτήρια βάση των οποίων γίνεται η αξιολόγηση του αποτελέσματος του ΡΕΤ ποικίλλουν ανάλογα με τη χρονική στιγμή τέλεσης της εξέτασης, σε σχέση με τη θεραπεία (αρχική σταδιοποίηση,ενδιάμεσο, μεταθεραπευτικό ΡΕΤ). Τη δεδομένη στιγμή, παρόλο που το ΡΕΤ πραγματοποιείται σε όλους τους ασθενείς με HL μετά το πέρας της θεραπείας, δεν αποτελεί προαπαιτούμενη εξέταση για τον καθορισμό της έκτασης της νόσου κατά την αρχική σταδιοποίηση, παρόλο που η πραγματοποίηση της δύναται να αναδείξει εστίες της νόσου, μη ανιχνεύσιμες με τη συμβατική απεικόνιση. Ο ρόλος του ΡΕΤ CT στο HL αναλύεται διεξοδικά στο σχετικό κεφάλαιο του βιβλίου [121,122]. CT πριν τη χημειοθεραπεία CT μετά τη χημειοθεραπεία ΡΕΤ μετά τη χημειοθεραπεία Εικόνα 5. Αξονική τομογραφία (CT) προ χημειοθεραπείας, αξονική τομογραφία (CT) μετά χημειοθεραπείας, τομογραφία εκπομπής ποζιτρονίων (ΡΕT) μετά χημειοθεραπείας. [Από Andreou J, Kosmidis P, Gouliamos A et al. PET/CT in Lymphoma. 2016, pp43] 51
52 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή 1.7 ΑΔΡΗ ΠΡΟΓΝΩΣΤΙΚΗ ΤΑΞΙΝΟΜΗΣΗ Με βάση την κλινική σταδιοποίηση (Ann Arbor και τροποποίηση Cotswolds)[123,124] το HL ταξινομείται σε τέσσερα στάδια, που το καθένα αντιπροσωπεύεται από τους αντίστοιχους λατινικούς αριθμούς Ι,ΙΙ,ΙΙΙ,IV (Πίνακας 5). Με τη συνδρομή δε και ορισμένων προγνωστικών παραγόντων, το ΗL διακρίνεται περαιτέρω σε νόσο περιορισμένου σταδίου και νόσο προχωρημένου σταδίου. Τα περιορισμένα στάδια διαχωρίζονται επιμέρους σε αρχικά (ή αρχικά καλής πρόγνωσης) και ενδιάμεσα (ή αρχικά πτωχής πρόγνωσης) ανάλογα με την απουσία ή παρουσία συγκεκριμένων προγνωστικών παραγόντων (πίνακας 6). Πίνακας 5. Λέμφωμα Hodgkin. Σταδιοποίηση Ann-Arbor/Τροποποίηση Cotswolds Στάδιο Ι ΙΙ ΙΙΙ Περιγραφή Προσβολή μιας λεμφαδενικής περιοχής ή λεμφικού οργάνου (σπλήν, θύμος, κ.λπ.) ή μιας εξωλεμφαδενικής περιοχής [ΙΕ] Προσβολή δύο ή περισσότερων λεμφαδενικών περιοχών στην ίδια πλευρά του διαφράγματος ή εντοπισμένη προσβολή μιας εξωλεμφαδενικής περιοχής και λεμφαδένων στην ίδια πλευρά του διαφράγματος [ΙΙΕ]. Ο αριθμός των προσβεβλημένων ανατομικών περιοχών ή λεμφικών οργάνων υποδηλώνεται με δείκτη [π.χ. ΙΙ 2 ]. Όλες οι λεμφαδενικές ομάδες του μεσοθωρακίου λογίζονται ως μία μόνο ανατομική περιοχή, με εξαίρεση τις πνευμονικές πύλες που προσμετρώνται ξεχωριστά. Αμφοτερόπλευρη διόγκωση πυλαίων λεμφαδένων του πνεύμονος συν προσβολή μεσοθωρακίου συνιστά στάδιο ΙΙ 3 Προσβολή λεμφαδενικών περιοχών ή λεμφικών οργάνων σε αμφότερες τις πλευρές του διαφράγματος, που μπορεί να συνοδεύεται από προσβολή του σπληνός [ΙΙΙS], εντοπισμένη περιοχική προσβολή μιας εξωλεμφαδενικής περιοχής [ΙΙΙΕ] ή και των δύο [ΙΙΙSE]. ΙΙΙ 1 : Με προσβολή κοιλιακών λεμφαδένων ή/και λεμφαδένων πύλης ήπατος ή πύλης σπληνός ή/και του σπληνός καθεαυτού ΙΙΙ 2 : Με προσβολή παραορτικών, λαγονίων ή μεσεντερίων λεμφαδένων ΙV Διάχυτη ή εκτεταμένη προσβολή ενός ή περισσότερων εξωλεμφαδενικών ιστών ή οργάνων, με ή χωρίς συνοδό λεμφαδενική προσβολή Συμβολισμοί Εφαρμόσιμοι σε όλα τα στάδια Α Απουσία συμπτωμάτων Β Παρουσία συμπτωμάτων, πυρετός (>38 o C) σταθερός ή υποτροπιάζων κατά τον τελευταίο μήνα ή/και έντονες νυχτερινές εφιδρώσεις κατά τον τελευταίο μήνα ή/και απώλεια βάρους>10% του συνολικού βάρους, το προηγούμενο εξάμηνο Χ Ογκώδης νόσος (μάζα μεσοθωρακίου >1/3 της εγκάρσιας διαμέτρου του θωρακικού κλωβού στο επίπεδο Θ 5/6 ή/και λεμφαδενική μάζα 10εκ) Ε Προσβολή μιας εξωλεμφαδενικής περιοχής είτε εγγύς είτε κατά συνέχεια ιστού γνωστής προσβεβλημένης λεμφαδενικής περιοχής * Η προσβολή του ήπατος και του μυελού των οστών λογίζεται πάντοτε ως στάδιο IV ** Η τεκμηρίωση της διήθησης του ήπατος απαιτεί την ανάδειξη πολλαπλών εστιακών βλαβών (αποκλειόμενης της κυστικής ή αγγειακής τους φύσεως) με δύο τουλάχιστον απεικονιστικές μεθόδους. Ηπατομεγαλία βάσει της κλινικής εξέτασης με ή χωρίς διαταραχή της ηπατικής βιολογίας δεν επαρκεί. *** Η τεκμηρίωση της προσβολής του σπληνός απαιτεί είτε την αδιαμφισβήτητη ανεύρεση ψηλαφητού σπληνός με την κλινική εξέταση ή αμφιβόλως ψηλαφητού σπληνός, με ακτινολογική κατάδειξη σπληνομεγαλίας ή πολλαπλών παθολογικών εστιακών βλαβών. Κατάδειξη μόνο σπληνομεγαλίας με ακτινολογικές μεθόδους δεν επαρκεί. ΑΙΜΑΤΟΛΟΓΙΑ στην Κλινική Πράξη. Γ.Α. Πάγκαλη και Συν.,σελ Ιατρικές Εκδόσεις Πασχαλίδη, 2008 (Τροποποιηθέν) 52
53 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Γενικά τα στάδια Ι και ΙΙΑ ταξινομούνται ως αρχικά ή ενδιάμεσα αναλόγως προγνωστικών παραγόντων από όλες τις μείζονες ερευνητικές ομάδες, ενώ τα στάδια ΙΙΙ/IV θεωρούνται από όλους προχωρημένα. Το στάδιο ΙΙΒ αποτελεί αμφιλεγόμενο σημείο, όπως φαίνεται στον πίνακα 6 και αναλύεται παρακάτω, όπου δίδονται οι ορισμοί των αρχικών, ενδιαμέσων και προχωρημένων σταδίων σύμφωνα με τη Γερμανική Ομάδα Μελέτης του Λεμφώματος Hodgkin (German Hodgkin Study Group-GHSG) και τον EORTC (European Organization for the Research and Treatment of Cancer). Σύμφωνα με τη GHSG και τον EORTC, η διάκριση μεταξύ αρχικών και ενδιαμέσων σταδίων βασίζεται στην απουσία ή την παρουσία τουλάχιστον 1 παράγοντα κινδύνου (Α+ΤΚΕ 50 ή Β+ΤΚΕ 30, προσβολή 3 ή 4 λεμφαδενικών περιοχών, ογκώδες μεσοθωράκιο και εξωλεμφαδενική νόσος ή ηλικία >50 ετών) (πίνακας 6). Θα πρέπει να σημειωθεί ότι ο ορισμός της ογκώδους νόσου μεσοθωρακίου βάσει της απλής ακτινογραφίας θώρακος κατά GHSG ή EORTC διαφέρει (πίνακας 6). Οι ταξινομήσεις αυτές δεν έχουν επικυρωθεί επαρκώς σε προοπτικές μελέτες ασθενών που λαμβάνουν χημειοθεραπεία ως βασικό κορμό της θεραπείας τους[125]. Επίσης, η κατάταξη των ασθενών βασίζεται στην παρουσία τουλάχιστον ενός δυσμενούς παράγοντα, ενώ φαίνεται ότι η συρροή 2 δυσμενών παραγόντων [ ] ή η παρουσία συγκεκριμένων εξ αυτών (π.χ. ογκώδες μεσοθωράκιο ή/και αυξημένη ΤΚΕ)[128] επιβαρύνει περαιτέρω την πρόγνωση. Ευλόγως λοιπόν εγείρεται το ερώτημα κατά πόσον η εφαρμογή των ανωτέρω ταξινομήσεων είναι έγκυρη όταν χορηγείται συνδυασμός ΧΜΘ με βάση την ανθρακυκλίνη και ΑΚΘ και εάν υπό την αυτή αντιμετώπιση η πρόγνωση των αρχικών και ενδιαμέσων σταδίων διαφέρει όντως τόσο, ώστε να διαχωρίζονται και να τείνουν να αντιμετωπίζονται διαφορετικά (πίνακας 7) [ ]. Έτσι, υπό την ίδια σύγχρονη θεραπεία, η ταξινόμηση GHSG παρουσιάζει περιορισμένη διακριτική ικανότητα μεταξύ αρχικών και ενδιαμέσων σταδίων, ενώ επιπλέον υπάρχει μια ομάδα ενδιαμέσων σταδίων (χωρίς ογκώδες μεσοθωράκιο ή/και αυξημένη ΤΚΕ) με έκβαση ανάλογη αυτής των αρχικών[128]. Αντίθετα, η ταξινόμηση EORTC διαθέτει μεγαλύτερη διακριτική ικανότητα, γεγονός που οφείλεται στη δυσμενέστερη έκβαση των ενδιαμέσων σταδίων, λόγω της ενσωμάτωσης του συνόλου των ασθενών σταδίου ΙΙΒ[130,133]. 53
54 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Για τα προχωρημένα στάδια έχει επικρατήσει ο Διεθνής Προγνωστικός Δείκτης (International Prognostic score; IPS)[129]. Η εξ ίσου καλή ανταπόκρισή υπό τη σύγχρονη ΧΜΘ αποτελεί επίσης αμφιλεγόμενο σημείο, όπως θα αναλυθεί στη σχετική ενότητα, μαζί με την περαιτέρω προγνωστική ταξινόμηση και τους αναδυόμενους βιολογικούς προγνωστικούς παράγοντες. Πίνακας 6: Αδρή προγνωστική ταξινόμηση ασθενών με λέμφωμα Hodgkin Ερευνητικές Ομάδες GHSG EORTC Παράγοντες Κινδύνου α. 3 λεμφαδενικές περιοχές β. A + ΤΚΕ 50 ή B + ΤΚΕ 30 γ. Ογκώδης νόσος μεσοθωρακίου* δ. Ε-νόσος α. 4 λεμφαδενικές περιοχές β. A + ΤΚΕ 50 ή B + ΤΚΕ 30 γ. Ογκώδης νόσος μεσοθωρακίου** δ. Ηλικία 50 ετών Αδρή Προγνωστική Ταξινόμηση Αρχικά Στάδια I,II χωρίς π.κ. I,II χωρίς π.κ. Ενδιάμεσα Στάδια Προχωρημένα Στάδια I,IIA & 1 π.κ. IIB & π.κ. α ή/και β IIB & π.κ. γ ή/και δ III,IV I,II & 1 π.κ. III,IV * Κατά GHSG: 1/3 ( 0.33) της μεγίστης εγκαρσίας διαμέτρου του θωρακικού κλωβού, συνήθως περί το διάφραγμα ** Κατά EORTC: 0.35 της εγκαρσίας διαμέτρου του θωρακικού κλωβού στο επίπεδο Θ5-Θ6 π.κ.= Παράγοντες κινδύνου, E-νόσος= Εξωλεμφαδενική επέκταση νόσου. [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. 54
55 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Πίνακας 7: Είναι οι ταξινομήσεις της GHSG και του EORTC) επαρκείς; [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. Μελέτη Στάδια Θεραπεία Επιβίωση Ελεύθερη Αστοχίας (%) 5-ετής 8-ετής HD7 131 Αρχικά 2 x ABVD + (30+10) Gy ΑΘ-ΕΠ ~90 ~87 HD Αρχικά 2 x ABVD + 30 Gy ΑΘ-ΠΠ Δε δίδεται 86 HD Αρχικά 4 x ABVD + 30 Gy ΑΘ-ΠΠ ~93 87 Ενδιάμεσα χαμηλού κινδύνου HD (PFS) Με 3 περιοχές Ε-νόσο αλλά χωρίς ογκώδες μεσοθωράκιο ή ΤΚΕ 4 x ABVD + 30 Gy ΑΘ-ΠΠ 91 Δε δίδεται HD Ενδιάμεσα 4 x ABVD + 30 Gy ΑΘ-ΠΠ 85 ~83 HD (PFS) Ενδιάμεσα 4 x ABVD + 30 Gy ΑΘ-ΠΠ 89 Δε δίδεται Ενδιάμεσα υψηλού κινδύνου HD Με Ογκώδες μεσοθωράκιο ή (PFS) ΤΚΕ 4 x ABVD + 30 Gy ΑΘ-ΠΠ 88 Δε δίδεται με ή χωρίς 3 περιοχές Ε-νόσο H7F 133 Αρχικά 6 x EBVP + ΑΘ-ΠΠ Δε δίδεται Ενδιάμεσα H7U 133 (συμπεριλαμβανομένων όλων 6 x EBVP + ΑΘ-ΠΠ Δε δίδεται των ΙΙΒ) H8F 130 Αρχικά 3 x MOPP/ABV + ΑΘ-ΠΠ 98 Ενδιάμεσα H8U 130 (συμπεριλαμβανομένων όλων 4 x MOPP/ABV + ΑΘ-ΠΠ 88 των ΙΙΒ) 88 (10-ετής) 68 (10-ετής) 93 (10-ετής) 80 (10-ετής) Τα υψηλότερα ποσοστά στην HD14 μπορεί εν μέρει να οφείλονται στον περιορισμό ηλικίας (16-60 ετών έναντι στις HD10, HD11).Τα χαμηλότερα ποσοστά στην H8U οφείλονται στο ότι κατά τον EORTC στα ενδιάμεσα στάδια περιλαμβάνονται όλοι οι ασθενείς σταδίου ΙΙΒ. 55
56 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή 1.8 ΘΕΡΑΠΕΙΑ ΠΡΩΤΗΣ ΓΡΑΜΜΗΣ ΘΕΡΑΠΕΙΑ ΠΕΡΙΟΡΙΣΜΕΝΩΝ ΣΤΑΔΙΩΝ Η θεραπευτική αντιμετώπιση των ασθενών με HL περιορισμένου σταδίου περιλαμβάνει τη χορήγηση χημειοθεραπείας και επικουρικής ακτινοθεραπείας. Χημειοθεραπευτικός συνδυασμός εκλογής είναι το ABVD (Δοξορουβυκίνη, Μπλεομυκίνη, Βιμπλαστίνη, Ντακαρβαζίνη). Ωστόσο, παραμένουν βασικά ερωτήματα που αφορούν τον αριθμό των κύκλων ΧΜΘ, τη χρήση εντατικής ΧΜΘ τύπου BEACOPP ή τη χρήση συνδυασμών τύπου ABVD αλλά με λιγότερα φάρμακα, σε ασθενείς με ή χωρίς επιβαρυντικούς παράγοντες. Πιο συγκεκριμένα η χορήγηση 4 κύκλων ABVD υπήρξε μέχρι πρότινος η κλασσική θεραπευτική προσέγγιση από άποψη χημειοθεραπείας. Σύμφωνα όμως με τη μελέτη HD10 του GHSG, που παρουσιάζει αποτελέσματα ασθενών μετά από διάμεση παρακολούθηση 7.5 ετών, δεν παρατηρείται διαφορά μεταξύ 4 κύκλων και 2 κύκλων ABVD [134], αφού βρέθηκε ότι η 8- ετής FFTF (επιβίωση ελεύθερη αστοχίας της θεραπείας-freedom From treatment Failure; FFTF) είναι 88% και 86% αντίστοιχα, και η 8-ετής συνολική επιβίωση είναι 94.5% σε αμφότερες τις υποομάδες (πίνακας 8)[ ]. Επιπρόσθετα, η HD10 ανέδειξε ότι η χορήγηση 2 κύκλων ABVD είναι ασφαλέστερη όσον αφορά την αιματολογική και μη τοξικότητα. Η μελέτη της EORTC Η10 που εστίασε στον συνδυασμό ακτινοθεραπείαςχημειοθεραπείας, μελέτησε τη χορήγηση 3 κύκλων ABVD με ακτινοθεραπεία [136]. Ομοίως οι Radford et al, μέσα από τη μελέτη RAPID που πραγματοποιήθηκε σε 602 ασθενείς με HL περιορισμένου σταδίου, μελέτησαν την πιθανότητα της αποφυγής ακτινοθεραπείας μετά από 3 κύκλους ABVD, χωρίς όμως να καταφέρουν να απομονώσουν όφελος στην 3-ετή ελεύθερης εξέλιξης νόσου επιβίωση (progression free survival PFS), σε σχέση με την ομάδα που είχε υποβληθεί σε επικουρική ακτινοθεραπεία και είχε PFS 95%.[137]. Συμπερασματικά, στα αρχικά στάδια με καλή πρόγνωση, το πλήρες σχήμα ABVD παραμένει ως θεραπεία εκλογής, στην περίπτωση χορήγησης 2 κύκλων χημειοθεραπείας. Η δακαρμπαζίνη δε μπορεί να παραλειφθεί χωρίς ουσιαστική απώλεια θεραπευτικού αποτελέσματος. Η παράλειψη της μπλεομυκίνης (AVD) σχετίζεται με περίπου 4% FFTF απώλεια, χωρίς διαφοροποίηση στην επιβίωση. Όμως δεν κατάφερε να αποδείξει ότι δεν είναι κατώτερη του σχήματος ABVD. 56
57 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Πίνακας 8: Μελέτες Θεραπείας HL αρχικών αρχικών και ενδιάμεσων σταδίων [128,130,134,135,138,139]. [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. Επιβίωση Ελεύθερη Εξέλιξης Νόσου Μελέτη Σκέλη Γενικά Ασθενείς Χρόνος/FFTF Συγκρίσεις Χαρακτηριστικά HD10, GHSG, Αρχικά Στάδια 8 έτη ABVDx2 + ΑΘ-ΠΠ 30 Gy Αξιολογήσιμοι: vs 2 κύκλοι: ABVDx2 + ΑΘ-ΠΠ 20 Gy % vs 86%, HR 1.17 ABVDx4 + ΑΘ-ΠΠ 30 Gy ετών ( ) ABVDx4 + ΑΘ-ΠΠ 20 Gy Διάμεση Παρακ: 91 μήνες vs 20 Gy: 88% vs 89%, HR 1.00 ( ) HD13, GHSG, Αρχικά Στάδια ABVDx2 + ΑΘ-ΠΠ 30 Gy ABV x2 + ΑΘ-ΠΠ 30 Gy AVD x2 + ΑΘ-ΠΠ 30 Gy AV x2 + ΑΘ-ΠΠ 30 Gy Πρώιμη διακοπή των σκελών ABV και AV λόγω αυξημένου αριθμού αστοχιών της θεραπείας H8F, EORTC/GELA, Αρχικά Στάδια 10 έτη MOPP/ABVx3 + ΑΘ-ΠΠ Gy Αξιολογήσιμοι: % EFS, p<0.001 Υφολική Λεμφαδενική ΑΘ + Σπλην ετών, % OS, p=0.001 (97% vs %) Διάμεση Παρακ: 92 μήνες H9F, EORTC/GELA, Αρχικά 5 έτη Στάδια 57
58 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή EBVPx6 + ΑΘ-ΠΠ 36 Gy Αξιολογήσιμοι: ετών, έως % 36 Gy vs. 20 Gy vs. no RT: p<0.001 EBVPx6 + ΑΘ-ΠΠ 20 Gy % 36 Gy vs. 20 Gy: p=0.19 EBVPx6 χωρίς ΑΘ Διάμεση Παρακ: 60 μήνες % πρώιμη διακοπή του σκέλους άνευ RT HD11, GHSG, Ενδιάμεσα Στάδια 5 έτη ABVDx4 + ΑΘ-ΠΠ 30 Gy Αξιολογήσιμοι: BEACOPP vs ABVD (30Gy): p=0.65 ABVDx4 + ΑΘ-ΠΠ 20 Gy ετών BEACOPP vs ABVD (20Gy): p=0.02 BEACOPP-basex4 + ΑΘ-ΠΠ 30 Gy vs 20 Gy (BEACOPP): διαφορά -0.8% (-5.8 έως 4.2) BEACOPP-basex4 + ΑΘ-ΠΠ 20 Gy Διάμεση Παρακ: vs 20 Gy (ABVD): μήνες διαφορά -4.7% (-10.3 έως 0.8) HD14, GHSG, Ενδιάμεσα Στάδια 5 έτη ABVDx4 + ΑΘ-ΠΠ 30 Gy Αξιολογήσιμοι: % BEACOPP-esc vs ABVD: p<0.001 BEACOPP-esc x2 + ABVDx2 + ΑΘ-ΠΠ ετών, % HR 0.44 ( ) 30 Gy 2008 Διάμεση Παρακ: 43 μήνες H8U,EORTC/GELA, Ενδιάμεσα 10 έτη Στάδια MOPP/ABVx6 + ΑΘ-ΠΠ Gy Αξιολογήσιμοι: % EFS, p=0.80 MOPP/ABVx4 + ΑΘ-ΠΠ Gy ετών, % OS, p=0.93 MOPP/ABVx4 + Υφολική Λεμφαδενική ΑΘ 1999 Διάμεση Παρακ: 92 μήνες % 58
59 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία H9U,EORTC/GELA, Ενδιάμεσα 5 έτη Στάδια ABVDx6 + ΑΘ-ΠΠ Gy Αξιολογήσιμοι: % FFTF, p=0.27 ABVDx4 + ΑΘ-ΠΠ Gy ετών, έως % BEACOPP-basex4 + ΑΘ-ΠΠ Gy 2002 Διάμεση Παρακ: 67 μήνες % ΘΕΡΑΠΕΙΑ ΕΝΔΙΑΜΕΣΩΝ ΣΤΑΔΙΩΝ Σύμφωνα με την GHSG και τον EORTC, θεραπεία εκλογής για τα ενδιάμεσα στάδια του HL αποτέλεσε μέχρι πρότινος η χορήγηση 4 κύκλων εναλλασσομένου COPP/ABVD ή υβριδικού MOPP/ABV και η χορήγηση ακτινοθεραπείας με προσθιο-οπίσθια πεδία (ΑΚΘ-ΠΠ) [130,140]. Η αντιμετώπιση αυτή απέδιδε μακρά επιβίωση, χωρίς εξέλιξη νόσου σε ένα ποσοστό 80% των ασθενών. Τόσο το χαμηλό αυτό ποσοστό, όσο και η αυξημένη τοξικότητα της θεραπείας, οδήγησε στην αντικατάσταση του συγκεκριμένου σχήματος από το φαρμακευτικό σχήμα του ABVD. Στην περίπτωση των ασθενών με ενδιάμεσο στάδιο νόσου, τίθεται όμως το βασικό ερώτημα, του κατά πόσον υπερτερεί η χορήγηση των 6 κύκλων χημειοθεραπείας, έναντι των τεσσάρων. Στην τυχαιοποιημένη μελέτη Η8U του EORTC δε διαπιστώθηκε διαφορά μεταξύ MOPP/ABV x 4 + ΑΚΘ-ΠΠ, MOPP/ABV x 6 + ΑΚΘ-ΠΠ και MOPP/ABV x 4 σε συνδυασμό με ΑΚΘ εκτεταμένου πεδίου [130]. Στη μελέτη H9U του EORTC εξετάζεται το παραπάνω ερώτημα όσον αφορά το ABVD. Τόσο η σύγκριση μεταξύ ABVDx6 και ABVDx4, όσο και η σύγκριση ABVDx6 και BEACOPP-bx4 δεν έδειξε διαφορά στατιστικά σημαντική, ενώ παρατηρήθηκε ότι η τοξικότhτα ήταν μεγαλύτερη με τη χορήγηση BEACOPP-baseline. Η 5-ετής FFTF είναι 90% με ABVD x 6 + ΑΚΘ-ΠΠ έναντι 86% με ABVD x 4 + ΑΚΘ-ΠΠ, χωρίς η διαφορά να είναι στατιστικώς σημαντική, έτσι ώστε το ερώτημα να παραμένει ανοικτό[138]. Δεδομένης της ισοδυναμίας μεταξύ ABVD και εναλλασσομένων και υβριδικών συνδυασμών στο προχωρημένο HL και της τοξικότητος των τελευταίων όσον αφορά την εμφάνιση δευτεροπαθών λευχαιμιών και στειρότητος [141,142], η χορήγηση 4 κύκλων ABVD θα μπορούσε να είναι εξ ίσου 59
60 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή αποτελεσματική, εξ ου και η καθιέρωσή της ως μέτρο σύγκρισης (standard arm) στις μελέτες HD11, HD14 και H9U. Στη δημοσιευμένη μελέτη HD11 της GHSG, 4 κύκλοι ABVD με ΑKΘ-ΠΠ δεν υστερούν ως προς την Freedom From Treatment Failure (FTF) και τη συνολική επιβίωση των 4 κύκλων BEACOPPbaseline με ΑKΘ-ΠΠ, εφόσον η δόση ΑΚΘ είναι 30 Gy[135]. Ομοίως, τα αποτελέσματα της H9U του EORTC δε φαίνεται να δικαιολογούν την εφαρμογή του συνδυασμού BEACOPPbaseline έναντι του ABVD στα ενδιάμεσα στάδια της νόσου[138]. Αντιθέτως, η μελέτη HD14 της GHSG κατέδειξε διαφορά όσον αφορά την FFTF (χωρίς κλινικά σημαντική διαφορά στην τοξικότητα) μεταξύ ABVD x Gy ΑΘ-ΠΠ και 2 κύκλων BEACOPP escalated και ΑBVD x Gy ΑΘ-ΠΠ[128]. Σε αντίθεση με την GHSG και την EORTC, οι ιταλικές, βρετανικές και άλλες ερευνητικές ομάδες, αντιμετωπίζουν τους ασθενείς σταδίου ΙΙΒ, με τουλάχιστον 6 κύκλους ABVD.[ ]. Επιπλέον φαίνεται ότι το πλεονέκτημα της πλέον εντατικοποιημένης προσέγγισης είναι πιο εμφανές στους ασθενείς με πολλαπλούς δυσμενείς προγνωστικούς παράγοντες. Κατά συνέπεια η περαιτέρω προγνωστική ταξινόμηση των ενδιαμέσων σταδίων θα μπορούσε να κατευθύνει την εξατομίκευση της θεραπευτικής στρατηγικής. Σε καμμία περίπτωση δεν έχει αναδειχθεί όφελος ως προς τη συνολική επιβίωση με τη χρήση του BEACOPP-escalated, τουλάχιστον προς το παρόν. Συμπερασματικά, ο συνδυασμός χορήγησης 6 κύκλων ABVD και ΑΚΘ-ΠΠ αποτελεί την θεραπεία εκλογής για τα ενδιάμεσα στάδια του HL Πεδίο Ακτινοθεραπείας Δόση Ακτινοθεραπείας Η ακτινοθεραπεία αποτελεί τη θεραπεία εκλογής στα αρχικά και ενδιάμεσα στάδια HL σε συνδυασμό με χημειοθεραπεία με ABVD ή ισοδύναμους συνδυασμούς, καθώς σχετικές μελέτες κατέδειξαν ότι είναι εξίσου αποτελεσματική με την ΑΚΘ εκτεταμένου πεδίου σε αυτή την ομάδα ασθενών [130,140,148]. Έτσι, ενώ στο παρελθόν χορηγείτο μόνο θεραπεία με εκτεταμένα πεδία ακτινοβόλησης (πεδίο μανδύα, ανεστραμμένου «Υ», ολική ακτινοβόληση λεμφαδένων, υφολική ακτινοβόληση λεμφαδένων, τροποποιημένος και mini μανδύας), 60
61 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία βαθμιαία διαμορφώνεται η τάση τα πεδία ακτινοθεραπείας να περιλαμβάνουν μόνο τις περιοχές που πάσχουν (involved field radiotherapy-ifrt),ή και μόνο τους προσβεβλημένους λεμφαδένες( involved node radiotherapy-ινrt), όταν συνδυάζονται με χημειοθεραπεία. Η ισοδυναμία της τακτικής αυτής σε σχέση με την ακτινοθεραπεία ελέγχεται σε τυχαιοποιημένες μελέτες. Χρειάζεται να τονιστεί στο συγκεκριμένο σημείο, ότι ο συνδυασμός χημειοθεραπείας και ακτινοθεραπείας στα αρχικά και ενδιάμεσα στάδια της νόσου, έχει μειώσει και τη συνολική δόση ακτινοθεραπείας, που απαιτείται για την εκρίζωση του νοσήματος. Έτσι, ενώ ως μονοθεραπεία η δόση ακτινοθεραπείας που χορηγείτο για ριζική θεραπεία ήταν 36-45Gy, με την προσθήκη της χημειοθεραπείας έχει μειωθεί στα 30Gy. Ο ρόλος της ακτινοθεραπείας στo LH αναλύεται διεξοδικά στο σχετικό κεφάλαιο του βιβλίου ΘΕΡΑΠΕΙΑ ΠΡΟΧΩΡΗΜΕΝΩΝ ΣΤΑΔΙΩΝ Τα χαρακτηριστικά των ασθενών που συμμετέχουν σε μελέτες σχεδιασμένες για HL προχωρημένων σταδίων διαφέρουν ανάμεσα στις διάφορες ερευνητικές ομάδες. Τα κλινικά στάδια ΙΙΙ/ΙV θεωρούνται κατ εξοχήν ως προχωρημένα [142, ]. Η ταξινόμηση του σταδίου ΙΙΒ παραμένει αντιφατική: Ο EORTC, η GELA και οι ορισμένες αμερικανικές ομάδες εξαιρούν αυτούς τους ασθενείς από τον ορισμό του προχωρημένου HL[142, ]. Σύμφωνα με την GHSG το στάδιο ΙΙΒ μπορεί να αντιπροσωπεύει προχωρημένο HL, εάν συνδυάζεται με ογκώδες μεσοθωράκιο ή/και εξωλεμφαδενική εντόπιση[149]. Τέλος, Βρετανικές, Ιταλικές και Σουηδικές ομάδες συμπεριλαμβάνουν το στάδιο ΙΙΒ στα προχωρημένα στάδια [143,144,146,147,153,154]. Μερικές από τις τελευταίες ομάδες καθώς και σύγχρονες αμερικανικές και Βρετανικές μελέτες [[ ] αντιμετωπίζουν και τους ασθενείς σταδίου ΙΑ/ΙΙΑ με ογκώδη νόσο με πρωτόκολλα σχεδιασμένα για προχωρημένη νόσο. Ο συνδυασμός ABVD, αποτελεί την καθιερωμένη θεραπευτική αγωγή για το προχωρημένο HL, ενώ ο ρόλος της ΑΚΘ δεν είναι σαφώς καθορισμένος. Περίπου 60-70% των ασθενών 61
62 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή επιτυγχάνουν μακρές υφέσεις με ABVD±ΑΚΘ, ακόμη δε περισσότεροι με πιο εντατικοποιημένη ΧΜΘ τύπου BEACOPP-escalated. Οι ασθενείς στους οποίους η αρχική θεραπεία αποτυγχάνει ή υποτροπιάζουν μετά από πλήρη ύφεση (CR/CRu) υποβάλλονται σε ΧΜΘ διάσωσης και αυτόλογη μεταμόσχευση, εφ όσον το επιτρέπει η ηλικία και η φυσική κατάστασή τους[ ]. Χρειάζεται να σημειωθεί εδώ ότι το MOPP ήταν το πρώτο χημειοθεραπευτικό σχήμα σε ασθενείς κλινικών σταδίων ΙΙΙ/ΙV, που κατέδειξε 20-ετή FFTF σε ποσοστό περίπου 30% (ενημερωμένα αποτελέσματα της μελέτης της GALGB) [141]. Παρόλα αυτά το ABVD υπερτερεί έναντι του MOPP, τουλάχιστον όσον αφορά την FFTF. Στην προαναφερθείσα μελέτη, η 20-ετής FFTF μετά από ABVD χωρίς ΑΚΘ ήταν 40-45%. Είναι αξιοσημείωτο βέβαια ότι τα ποσοστά που επιτυγχάνουν οι εν λόγω συνδυασμοί σε αυτά τα στάδια της νόσου, τείνουν να υποεκτιμώνται, καθώς οι θάνατοι από οποιαδήποτε αιτία προσμετρούνται ως συμβάματα στον υπολογισμό της FFTF. Η σημασία αυτής της παρατήρησης επαυξάνεται όσο η παρακολούθηση γίνεται μακρότερη. Έτσι, εάν υπολογισθούν μόνο τα σχετιζόμενα με τη νόσο συμβάματα, το ποσοστό ελέγχου της νόσου στα 15 έτη μετά από ABVD±ΑΚΘ είναι της τάξεως του 60-65% (δεδομένα Αιματολογικής Κλινικής ΕΚΠΑ 2012). Απόπειρες να βελτιωθούν αυτά τα αποτελέσματα με εναλλασσόμενους κύκλους MOPP (ή COPP) και ABVD ή με υβριδικά σχήματα 7 (MOPP/ABV) ή 10 φαρμάκων (MOPP/EBV/CAD και COPP/ABV/IMEP) ήταν ανεπιτυχείς [ ,160,161]. Ένα άλλο σχήμα που χορηγήθηκε σε ασθενείς προχωρημένων σταδίων ήταν το Stanford V. Παρά όμως τα αρχικά πολύ ενθαρρυντικά αποτελέσματα, ούτε αυτός ο συνδυασμός αποδείχθηκε καλύτερος του ABVD, ενδέχεται δε και να υστερεί, ιδίως εάν το ενσωματωμένο πρόγραμμα ΑΚΘ δεν τηρείται πιστά [144,155,156]. Ως αποτέλεσμα το ABVD θεωρείται το μέτρο σύγκρισης (gold standard) στις τυχαιοποιημένες μελέτες για το προχωρημένο HL, σύμφωνα με τις περισσότερες ερευνητικές ομάδες. Κατά τη δεκαετία του 1990, η GHSG εισήγαγε τον συνδυασμό BEACOPP-escalated (BEACOPPesc), ο οποίος βασίζεται στη χρήση 7 φαρμάκων σε μεγαλύτερες δόσεις και βραχύτερα χρονικά διαστήματα. Το BEACOPPesc είναι ο μόνος μέχρι στιγμής συνδυασμός 62
63 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία που έχει βελτιώσει την FFTF σε σύγκριση με το ABVD. Επιπρόσθετα, έχει επιτύχει βελτίωση της συνολικής επιβίωσης σε σύγκριση με το COPP/ABVD, ένα ισοδύναμο του ABVD, όχι όμως και με το ίδιο το ABVD [149]. Το BEACOPPesc θεωρείται από τη GHSG ως θεραπεία εκλογής για τους νεότερους ασθενείς με προχωρημένο HL. Η επιλογή αυτή στηρίζεται στα αποτελέσματα της μελέτης HD9, που κατέδειξε ότι το BEACOPPesc υπερτερεί όσον αφορά την FFTF και τη συνολική επιβίωση σε σύγκριση με το COPP/ABVD, όπως επίσης και το BEACOPP-baseline, που περιέχει χαμηλότερες δόσεις φαρμάκων σε σχέση με το BEACOPPesc[149]. Ενημερωμένα αποτελέσματα της HD9 [162] κατέδειξαν ποσοστά 10-ετούς FFTF της τάξεως του 82%, 70% και 64% για το BEACOPPesc, το BEACOPP-baseline και το COPP/ABVD αντίστοιχα, ενώ τα ποσοστά 10-ετούς συνολικής επιβίωσης ήταν 86%, 80% και 75%. Όσον αφορά την τοξικότητα και την αποτελεσματικότητα, δεν προτείνεται η χρήση του BEACOPP-baseline, καθώς δε βελτίωσε τη συνολική επιβίωση σε σχέση με το COPP/ABVD. Το πλεονέκτημα του BEACOPPesc έναντι του COPP/ABVD ως προς την FFTF ήταν ανεξάρτητο του IPS, ενώ το πλεονέκτημα στη συνολική επιβίωση αφορούσε μόνο τους ασθενείς με IPS 2-3. Έτσι δε φαίνεται να παρέχεται σταθερή βάση που να δικαιολογεί την εντατικοποίηση της θεραπείας σε ασθενείς με υψηλότερο IPS. Στο σημείο αυτό χρειάζεται να αναφέρουμε ότι η αιματολογική τοξικότητα, οι λοιμώξεις και οι τοξικοί θάνατοι ήταν σαφώς συχνότεροι στους ασθενείς που έλαβαν BEACOPPesc σε σχέση με το COPP/ABVD. Επιπλέον, παρατηρήθηκε αυξημένο ποσοστό ασθενών που παρουσίασαν δευτεροπαθές Μυελοδυσπλαστικό Σύνδρομο, ή και Οξεία Μυελογενή Λευχαιμία (ΜΔΣ/ΟΜΛ), κάτι που δεν επιβεβαιώθηκε για την αθροιστική επίπτωση του συνόλου των δευτεροπαθών κακοηθειών. Αδρά, 2% των ασθενών απεβίωσαν από οξεία τοξικότητα του BEACOPPesc και επιπλέον 3% εμφάνισαν ΜΔΣ/ΟΜΛ (πίνακας 9). Το ποσοστό τοξικών θανάτων ήταν άμεσα συναρτημένο με την ηλικία, έτσι ώστε η χορήγηση BEACOPPesc να είναι απαγορευτική σε άτομα ετών (θνητότητα ~17%!) [ ]. 63
64 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Πίνακας 9. Σύγκριση συχνότητος τοξικών θανάτων και δευτεροπαθούς μυελοδυσπλασίας και οξείας μυελογενούς λευχαιμίας μεταξύ παραλλαγών του BEACOPP-escalated και του ABVD στις Γερμανικές Μελέτες HD9, HD12 και HD15 και στις 2 σχετικές Ιταλικές Μελέτες. [Από HAEMA, Ιούλ- Σεπτ 2012, τόμος 3, τεύχος 3]. Χημειοθεραπευτικό Σχήμα, Ασθενείς (#) Ηλικία (έτη) Διάμεση Παρακολούθη Τοξικοί Θάνατοι MDS/ANLL (%) Μελέτη ση (μήνες) (%) BEACOPP-esc x 8, HD BEACOPP-esc x 8, HD BEACOPP-esc x 8, HD BEACOPP-esc/base x (4+4), HD12 BEACOPP-esc/base x (4+4), Italian BEACOPP-esc x 6, HD BEACOPP-esc/base x (4+2), HD2000 GISL BEACOPP-14 x 8, HD BEACOPP-base x 8, HD COPP/ABVD x 8, HD ABVD x 6-8, Italian ABVD x 6, HD2000 GISL Στους ασθενείς <60 ετών η θνητότητα με συνδυασμούς τύπου BEACOPPesc είναι ~2%. Εύλογα, λοιπόν, ανακύπτει το ερώτημα κατά πόσο το BEACOPPesc αποτελεί τη νέα θεραπεία εκλογής για τους ασθενείς προχωρημένου σταδίου HL. Θα πρέπει ωστόσο πριν απαντηθεί, να ληφθούν υπ όψιν η σοβαρή οξεία και μακροχρόνια τοξικότητα που εμφανίζει το συγκεκριμένο σχήμα, η ανάγκη επαλήθευσης της αποτελεσματικότητάς του και από άλλες ερευνητικές ομάδες, ο καθορισμός υποομάδων που, ενδεχομένως, ωφελούνται ιδιαίτερα, το γεγονός ότι δεν υπερτερεί του COPP/ABVD σε ασθενείς ετών, η μεγάλη θνητότητα που 64
65 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία εμφανίζει στα έτη και η όχι αμελητέα θνητότητα στην ομάδα ετών, ενώ θα πρέπει να απαντηθούν και τα ερωτήματα εάν το BEACOPP esc μπορεί να αποκλιμακωθεί χωρίς σημαντική απώλεια ως προς την αποτελεσματικότητα, καθώς και ποια είναι η θέση του BEACOPPesc έναντι του ABVD, όταν επί αστοχίας, ακολουθεί σταθερά αυτόλογη μεταμόσχευση. 1.9 ΘΕΡΑΠΕΙΑ ΥΠΟΤΡΟΠΙΑΖΟΝΤΟΣ ΚΑΙ ΑΝΘΕΚΤΙΚΟΥ ΛΕΜΦΩΜΑΤΟΣ Το λέμφωμα Hodgkin (HL) είναι ιάσιμη νόσος στο 75% του συνόλου των ασθενών. Παρά την υψηλή πιθανότητα επιτυχούς έκβασης, η θεραπεία 1ης γραμμής αστοχεί στο 10% των ασθενών με αρχικά και στο 30% αυτών με προχωρημένα στάδια της νόσου. Οι ασθενείς εκείνοι στους οποίους αστοχεί η αρχική θεραπεία διακρίνονται στους πρωτοπαθώς ανθεκτικούς εκείνους δηλαδή που δεν επιτυγχάνουν πλήρη ύφεση με τη θεραπεία 1ης γραμμής και σε αυτούς που υποτροπιάζουν μετά από επίτευξη αρχικής ύφεσης. Η θεραπευτική στρατηγική για τις προαναφερόμενες κατηγορίες ασθενών έχει ως στόχο την επίτευξη ίασης, τουλάχιστον στους νέους. Η ακτινοθεραπεία με τη μορφή περιορισμένου ή και εκτεταμένου πεδίου μπορεί να οδηγήσει σε έλεγχο της νόσου σε ένα 30% των ασθενών, όταν αυτοί έχουν απώτερη υποτροπή, χωρίς Β- συμτώματα, με εντοπισμένη, μη εξωλεμφαδενική νόσο, που δεν έχει λάβει στο παρελθόν ακτινοθεραπεία. Η χημειοθεραπεία διάσωσης ακολουθούμενη από μεγαθεραπεία και αυτόλογη μεταμόσχευση αρχαίγονων αιμοποιητικών κυττάρων (ΑΜΑΑΚ) είναι η θεραπεία εκλογής για άτομα ηλικίας 65 ετών Μεγαθεραπεία και Αυτόλογη Μεταμόσχευση Αρχέγονων Αιμοποιητικών Κυττάρων Αίματος (ΜΘ/ΑΜΑΑΚ) Η θεραπευτική προσέγγιση με στόχο την ίαση σε ασθενείς με πρωτοπαθώς ανθεκτικό/υποτροπιάζον HL είναι η εφαρμογή χημειοθεραπευτικών συνδυασμών 2ης γραμμής, γνωστή ως θεραπεία διάσωσης, η συλλογή αρχέγονων αιμοποιητικών κυττάρων (ΑΑΚ) και στη συνέχεια η χορήγηση μεγαθεραπείας (ΜΘ), που αποτελεί μυελοαφανιστική χημειοθεραπεία,η οποία ακολουθείται από αυτόλογη μεταμόσχευση των συλλεχθέντων 65
66 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ΑΑΚ. Η υπεροχή της ΜΘ/ΑΜΑΑΚ έναντι της συμβατικής χημειοθεραπείας αποδείχθηκε σε 2 τυχαιοποιημένες μελέτες[165,166] Η πρώτη προέρχεται από τη Βρετανική Ομάδα (BNLI) και συνέκρινε 2-3 κύκλους του συνδυασμού mini-beam έναντι BEAM και ΑΜΑΑΚ. Η δεύτερη μελέτη διεξήχθη από την GHSG (HDR-1) και συνέκρινε 4 κύκλους Dexa-BEAM έναντι 2 κύκλων Dexa-BEAM ακολουθούμενων από ΒΕΑΜ και ΑΜΑΑΚ. Η 5-ετής επιβίωση ελεύθερη εξέλιξης νόσου (Progression Free Survival-PFS) ήταν 53% έναντι 10% στην πρώτη και 55% έναντι 34% στη δεύτερη,αντίστοιχα. Γενικότερα η πιθανότητα ίασης με ΜΘ/ΑΜΑΑΚ είναι της τάξεως 40-60% [ ]. Συχνά οι μελέτες αυτές υπερεκτιμούν την αποτελεσματικότητα της ΜΘ/ΑΜΑΑΚ, καθώς αφορούν επιλεγμένους ασθενείς και συνήθως εξαιρούν όσους δεν ανταποκρίνονται στη θεραπεία διάσωσης και δεν υποβάλλονται σε ΜΘ/ΑΜΑΑΚ. Οι αναλύσεις με μεθοδολογία intention to treat, έτσι ώστε να αντανακλάται το πραγματικό ποσοστό των ασθενών που διασώζονται με ΜΘ/ΑΜΑΑΚ [157,175,176] είναι ελάχιστες. Χρειάζεται να τονιστεί εδώ, ότι η ΜΘ/ΑΜΑΑΚ αποτελεί τη βέλτιστη θεραπευτική στρατηγική για ασθενείς ηλικίας <65 ετών, ενώ οι μεγαλύτεροι σε ηλικία ασθενείς αντιμετωπίζονται με συμβατική χημειοθεραπεία με ελάχιστες πιθανότητες ίασης. Ωστόσο, πρόσφατη αναδρομική μελέτη αναφέρει 3-ετή ΕΕ-ΕΝ και συνολική επιβίωση 73% και 88% αντίστοιχα σε ασθενείς >60 ετών μετά από ΜΘ/ΑΜΑΑΚ [177]. Η εφαρμογή χημειοθεραπείας 2ης γραμμής έχει τριπλό στόχο: τη μείωση του φορτίου της νόσου, τον έλεγχο της χημειοευαισθησίας του νοσήματος και τη συλλογή ΑΑΚ. Οι χημειοθεραπευτικοί συνδυασμοί που επιλέγονται περιλαμβάνουν πλατίνα και υψηλές δόσεις κυταραβίνης[168,174,178,179] (DHAP, ESHAP, ASHAP), ιφωσφαμίδη[175, ](ice, IEV, IGEV, ΜΙ ΝΕ, IVOx) ή συνδυασμό πλατίνας και γεμσιταμπίνης[183,184](gdp, GEM-P). Ένας άλλος συχνά χρησιμοποιούμενος συνδυασμός είναι ο mini-beam[165] ή ο Dexa-BEAM[166]. Η επιλογή του σχήματος διάσωσης εξαρτάται από την τακτική της εκάστοτε Αιματολογικής Μονάδος, καθώς δεν υπάρχουν συγκριτικές μελέτες φάσης ΙΙΙ. Ο σχετικά πρόσφατα χρησιμοποιούμενος συνδυασμός IGEV (γεμσιταμπίνη, ιφωσφαμίδη, βινορελμπίνη) παρουσιάζει ιδιαίτερα πλεονεκτήματα, καθώς έχει άριστο κινητοποιητικό 66
67 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία δυναμικό, σημαντική αποτελεσματικότητα και επιπλέον μπορεί να χορηγηθεί εξωνοσοκομειακά [181]. Η συλλογή των ΑΑΚ επιτελείται συνήθως μετά τον 2ο ή 3ο κύκλο της χημειοθεραπείας διάσωσης. Ο αριθμός των κύκλων της θεραπείας 2ης γραμμής δεν είναι καθορισμένος. Συνήθως χορηγούνται 3-4 κύκλοι ανάλογα με τον επιλεχθέντα συνδυασμό, το φορτίο της νόσου και την ανταπόκριση του ασθενούς. Εάν ο ασθενής είναι χημειοανθεκτικός μετά τον 2ο κύκλο θεραπείας, συνήθως γίνεται προσπάθεια επίτευξης τουλάχιστον μερικής ύφεσης προ της ΜΘ/ΑΜΑΑΚ με εναλλακτικό χημειοθεραπευτικό συνδυασμό. Η εντατικοποίηση της χημειοθεραπείας διάσωσης στην προσπάθεια βελτίωσης της χημειοευαισθησίας δεν έχει υιοθετηθεί ευρέως [168]. Σύμφωνα με την ομάδα του MSKCC η εντατικοποίηση του συνδυασμού ICE (augmented ICE και high dose ICE) βελτίωσε την πρόγνωση των ασθενών με παράγοντες κινδύνου [170], ενώ σε μεταγενέστερη μελέτη τους εφάρμοσαν τον συνδυασμό GDP στους ασθενείς εκείνους που δεν είχαν επαρκή ανταπόκριση μετά το σχήμα ICE [173]. Αντίθετα όμως, στην τυχαιοποιημένη μελέτη HDR2 της GHSG η εντατικοποίηση του συνδυασμού DHAP με διαδοχική προσθήκη υψηλών δόσεων κυκλοφωσφαμίδης, μεθοτρεξάτης/βινκριστίνης και ετοποσίδης δεν κατέδειξε όφελος, ακόμα και στις υψηλού κινδύνου ομάδες [168]. Η συλλογή ΑΑΚ μετά από αστοχία του συνδυασμού BEACOPPescalated στην 1η γραμμή φαίνεται εφικτή [185] παρά το γεγονός ότι δεν έχει διερευνηθεί εκτεταμένα. Οι χημειοανθεκτικοί ασθενείς αποκλείονται συνήθως από τις προοπτικές μελέτες, τα δεδομένα δε από τις αναδρομικές μελέτες αφορούν σε μικρό αριθμό πασχόντων. Έχει παρατηρηθεί παρόλα αυτά ότι ποσοστό 15-30% των ασθενών που εισέρχεται στην ΜΘ/ΑΜΑΑΚ με ανθεκτική νόσο μπορούν να διασωθούν και μάλιστα με επίτευξη plateau στις καμπύλες επιβίωσης [186,188]. Σε 2 αναδρομικές μελέτες 175 και 64 ασθενών που δεν ετέθησαν ποτέ σε ύφεση με οποιαδήποτε θεραπεία η PFS ήταν 32% και 17% αντίστοιχα[186,188]. Στην καθημερινή πρακτική οι ασθενείς αυτοί δεν πρέπει να αποκλείονται από την ΑΜΑΑΚ, καθώς είναι η μόνη τους ευκαιρία για μακροχρόνιο έλεγχο της νόσου. Αντίθετα οι ασθενείς με εξελισσόμενη νόσο ή κινητική αστοχία στα σχήματα διάσωσης δεν ωφελούνται από την ΜΘ/ΑΜΑΑΚ. Η εισαγωγή του μονοκλωνικού αντισώματος 67
68 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Brentuximab Vedotin (anti-cd30) φαίνεται να αλλάζει τη φυσική ιστορία και πρόγνωση των ασθενών αυτών, δίδοντάς τους τη δυνατότητα να υποβληθούν σε ΜΘ/ΑΜΑΑΚ, αφού ελεγχθεί το νόσημά τους. Έτσι, σε μελέτες φάσης ΙΙ, όταν το Brentuximab Vedotin χορηγηθεί ως πρώτης γραμμής θεραπεία διάσωσης πρίν την ΑΜΑΑΚ, δίνει 30% ανταπόκριση στο ΡΕΤ, με την ανταπόκριση των ασθενών πριν από τη ΑΜΑΑΚ να αγγιζει τα 2/3-3/4 και την 3ετή PFS >70% [189]. Στις περιπτώσεις αυτές έχει χορηγηθεί με σχήματα όπως τα ESHAP, DHAP,ICE. Συνήθως οι ανθεκτικοί ασθενείς υποβάλλονται σε αλλεπάλληλα σχήματα διάσωσης στην προσπάθεια να μειωθεί το φορτίο της νόσου προκειμένου να υποβληθούν σε ΑΜΑΑΚ. Επειδή όμως φαίνεται πώς με αυτό τον τρόπο τελικά οι ασθενείς χάνουν την ευκαιρία τους για ΜΘ/ΑΜΑΑΚ είτε λόγω επιπλοκών και κακής κατάστασης, ή λόγω προόδου της νόσου, συνίσταται η λήψη εώς και δύο διαφορετικών χημειοθεραπευτικών συνδυασμών διάσωσης, πριν από την ΑΜΑΑΚ, εφόσον δεν παρατηρείται προϊούσα νόσος [190]. Στα πλαίσια της μεγαθεραπείας, τα πιο συχνά χρησιμοποιούμενα σχήματα προετοιμασίας είναι ο συνδυασμός ολόσωμης ακτινοβόλησης (ΤΒΙ) με υψηλές δόσεις κυκλοφωσφαμίδης +/- ετοποσίδης [191] ή συνδυασμοί περιέχοντες μόνο χημειοθεραπεία υψηλών δόσεων, όπως οι CBV3 (κυκλοφωσφαμίδη, καρμουστίνη, ετοποσίδη), ΒΕΑΜ(C) [165,166] [καρμουστίνη, κυταραβίνη, ετοποσίδη, μελφαλάνη (κυκλοφωσφαμίδη)], χωρίς να υπάρχουν συγκριτικές μελέτες φάσης ΙΙΙ. Έτσι η επιλογή βασίζεται στην εμπειρία και την υποδομή του κάθε Κέντρου. Νεότερες παραλλαγές του BEAM αποτελούν οι συνδυασμοί TEAM, και BeAM με αντικατάσταση της καρμουστίνης από thiotepa ή μπενδαμουστίνη[192,193], ενώ έχουν πρόσφατα εισαχθεί και συνδυασμοί υψηλών δόσεων γεμσιταμπίνης[194] Διάσωση ασθενών που αποτυγχάνουν μετά από ΜΘ/ΑΜΑΑΚ Μελέτες έχουν αποδείξει ότι οι υποτροπές μετά την ΕΜΑΑΚ εμφανίζονται συνήθως εντός του πρώτου έτους και μάλιστα σε περιοχές που ήταν προσβεβλημένες [195] πριν τη ΜΘ, ή ήταν ογκώδεις στην υποτροπή[196]. Όσον αφορά στην ακτινοθεραπεία, όταν αυτή 68
69 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία συνδυάζεται με τη ΜΘ/ΑΜΑΑΚ, βελτιώνει τον τοπικό έλεγχο της νόσου, αν και η συμβολή της στην μακροχρόνια έκβαση δεν είναι επαρκώς τεκμηριωμένη[ ]. Η δόση που συστήνεται είναι 20Gy για τους ασθενείς που λαμβάνουν TBI και 30-40Gy για τους υπολοίπους, εφ όσον δεν έχουν ακτινοβοληθεί στο παρελθόν [195]. Στο σημείο αυτό χρειάζεται να τονιστεί ότι η συμπληρωματική ακτινοθεραπεία σχετίζεται με σημαντική πνευμονική τοξικότητα όταν το σχήμα προετοιμασίας περιέχει βουσουλφάνη[200]. Γενικά έχει παρατηρηθεί ότι η πρόγνωση των ασθενών που υποτροπιάζουν μετά την ΑΜΑΑΚ είναι ιδιαιτέρως πτωχή. Η θεραπευτική στρατηγική μπορεί να περιλαμβάνει ακτινοθεραπεία προσβεβλημένου πεδίου σε περιπτώσεις εντοπισμένης υποτροπής σε δόσεις 35Gy[201] ή χημειοθεραπεία με συνδυασμούς που δεν έχουν εφαρμοσθεί στο παρελθόν, είτε φάρμακα στα οποία είχαν ανταποκριθεί ικανοποιητικά οι ασθενείς σε πρότερη χρονική στιγμή, εφ όσον το επιτρέπει η αθροιστική τοξικότητά τους. Μπορεί να χρησιμοποιηθεί ο συνδυασμός γεμσιταμπίνης/βινορελμπίνης ± λιποσωμική δοξορουβικίνη[202,203], μονοθεραπεία με βινβλαστίνη[204] καθώς και οι συνδυασμοί BEACOPP-baseline, MOPP ή ChlVPP. Νέοι ασθενείς σε καλή φυσική κατάσταση με αργή εξέλιξη νόσου, στους οποίους η διάρκεια ύφεσης από την 1η ΑΜΑΑΚ είναι >1 έτος, οι οποίοι παραμένουν χημειοευαίσθητοι και δεν έχουν συμβατό δότη είναι υποψήφιοι για 2η ΑΜΑΑΚ[205,206]. Tο Brentuximab Vedotin μπορεί να χορηγηθεί σε ασθενείς που έχουν παρουσιάσει αποτυχία μετά από ΜΘ/ΑΜΑΑΚ, αλλά και σε ασθενείς που έχουν υποτροπιάσει μετά από τουλάχιστον 2 προηγηθέντα χημειοθεραπευτικά σχήματα. Επιπλέον, δύναται να χορηγηθεί και ως συντήρηση μετά από ΑΜΑΑΚ, σε ασθενείς υψηλού κινδύνου[ 207]. Ένα μικρό ποσοστό ασθενών που έχουν πλήρη ανταπόκριση με τηο Brentuximab Vedotin, δύνανται να ιαθούν. Επιπλέον, ασθενείς που στο παρελθόν έχουν λάβει Brentuximab Vedotin και έχουν παρουσιάσει υποτροπή ή επιδείνωση νόσου, δύνανται να λάβουν Nivolumab και Pembrolizumab. Οι συγκεκριμένοι PD-1 παράγοντες μπορούν να επάγουν γρήγορες και εντυπωσιακές ανταποκρίσεις. Στο σημείο αυτό χρειάζεται να τονιστεί ότι οι ασθενείς που έχουν λάβει στο παρελθόν PD-1 παράγοντες μπορούν να υποβληθούν σε αλλογενή μεταμόσχευση από αρχέγονα αιμοποιητικά κύτταρα. 69
70 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Ακτινοθεραπεία και Συμβατική Χημειοθεραπεία ως Θεραπεία Διάσωσης Αποτελεί θεραπευτική προσέγγιση για τους ασθενείς που δεν είναι υποψήφιοι για ΜΘ/ΑΜΑΑΚ κυρίως λόγω ηλικίας. Η εκτενέστερη μελέτη που εξετάζει την έκβαση ασθενών που αντιμετωπίσθηκαν μόνο με ακτινοθεραπεία στην υποτροπή, προέρχεται από μια αναδρομική ανάλυση της GHSG και αφορά σε 100 ασθενείς. Η 5-ετής ΕΕΕΝ ήταν 28% για το σύνολο των ασθενών[208], αλλά προκύπτει ότι ασθενείς με περιορισμένο κλινικό στάδιο υποτροπής (Ι/ΙΙ ), χωρίς Β-συμπτώματα και διάστημα πρώτης ύφεσης >1 έτους μπορούν να διασωθούν με ακτινοθεραπεία. Χρειάζεται να σημειωθεί ότι και η εντοπισμένη υπολειμματική νόσος μετά από θεραπεία 1ης γραμμής αντιμετωπίζεται με ακτινοθεραπεία. Είναι ευνόητο βέβαια ότι κάθε ένδειξη προόδου εντοπισμένης υπολειμματικής νόσου αποτελεί πρωτοπαθώς εξελισσόμενη νόσο και πρέπει να αντιμετωπίζεται με ΜΘ/ΑΜΑΑΚ. Όσον αφορά στη χημειοθεραπεία διάσωσης, εφόσον η διάρκεια της ύφεσης υπερβαίνει το ένα έτος, μπορεί να επαναληφθεί ο αρχικός χημειοθεραπευτικός συνδυασμός. Άλλες επιλογές αποτελούν οι συνδυασμοί MOPP, MOPP/ABVD, ChlVPP, γεμσιταμπίνη/βινορελμπίνη ± λιποσωμική δοξορουβικίνη, ενώ αναφέρεται ποσοστό 3-ετούς ΕΕΕΝ 50% μετά από BEACOPP ως θεραπεία 2ης γραμμής[209]. Συμπερασματικά η ΜΘ/ΑΜΑΑΚ διασώζει 40-60% των ασθενών με πρωτοπαθώς ανθεκτικό/σε υποτροπή λέμφωμα Hodgkin. Οι ασθενείς εκείνοι που ωφελούνται περισσότερο είναι εκείνοι με χημειοευαίσθητη όψιμη υποτροπή, χωρίς προχωρημένο κλινικό στάδιο ή εξωλεμφαδενικές εντοπίσεις στην υποτροπή. Αντίθετα για τους χημειοανθεκτικούς ασθενείς απαιτούνται νέες θεραπευτικές προσεγγίσεις. 70
71 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία 1.10 Ακτινοθεραπεία Η ακτινοθεραπεία παίζει καίριο ρόλο στη θεραπεία ασθενών με λέμφωμα Hodgkin. Στο παρελθόν, πριν από την ένταξη της χημειοθεραπείας, η ακτινοθεραπεία χορηγείτο ως μονοθεραπεία με εκτεταμένα πεδία ακτινοβόλησης (πεδίο μανδύα, τροποποιημένος και mini μανδύας, πεδίο ανεστραμμένου «Υ», ολική ακτινοβόληση λεμφαδένων, υφολική ακτινοβόληση λεμφαδένων,)[210]. Με την ένταξη όμως της χημειοθεραπείας βαθμιαία διαμορφώθηκε η τάση τα πεδία ακτινοθεραπείας να περιλαμβάνουν μόνο τις περιοχές που πάσχουν (involved field radiotherapy-ifrt),ή και μόνο τους προσβεβλημένους λεμφαδένες( involved node radiotherapy-ινrt), καθώς σχετικές μελέτες με συνδυασμό ακτινοθεραπείαςχημειοθεραπείας με ABVD ή ισοδύναμους συνδυασμούς, κατέδειξαν ότι είναι εξίσου αποτελεσματική η χορήγηση χημειοθεραπείας-ακτινοθεραπείας, με την ΑΚΘ εκτεταμένου πεδίου σε ασθενείς με νόσο Hodgkin περιορισμένου σταδίου [130,140,148]. Ο συνδυασμός χημειοθεραπείας και ακτινοθεραπείας, λόγω της επαυξημένης τοξικότητας, επιτάσσει την ανάλυση ζητημάτων όπως: την αλληλουχία των θεραπευτικών πράξεων, την επιλογή των πεδίων προς ακτινοβόληση και την απαιτούμενη συνολική δόση.[211,212] Η τοξικότητα της ακτινοθεραπείας σχετίζεται ευθέως ανάλογα με το μέγεθος του πεδίου ακτινοθεραπείας και τη συνολική δόση. Γενικά, σκοπός της ακτινοθεραπείας είναι η βελτιστοποίηση της ώστε με όσο το δυνατό πιο εντοπισμένο πεδίο ακτινοβόλησης και όσο το δυνατό μικρότερη συνολική δόση να επιτυγχάνεται ο καλύτερος έλεγχος της νόσου, με τη λιγότερη δυνατή τοξικότητα Πεδίο Ακτινοθεραπείας στο Λέμφωμα Hodgkin Εκτεταμένο Πεδίο Ακτινοβόλησης (Extended Field Radiation Therapy-EFRT) Στο παρελθόν, η χορήγηση ακτινοθεραπείας γινόταν με την παρωχημένη πλέον μέθοδο της δυσδιάστατης (2D) ακτινοθεραπείας. Αφορούσε την ακτινοβόληση της νόσου και ευρύτερων 71
72 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή γειτονικών λεμφαδενικών ομάδων, σύμφωνα με την αρχική σταδιοποίηση, με προσθιοπίσθιο και οπισθοπρόσθιο πεδίο φωτονίων. Με αυτή τη μέθοδο προέκυπταν εκτεταμένα πεδία ακτινοβόλησης (Extended Field Radiation Therapy-EFRT). Πιο συγκεκριμένα, ο μανδύας, αποτελούσε πεδίο ακτινοβόλησης που περιελάμβανε τραχηλικές, υπερκλείδιες, υποκλείδιες και μασχαλιαίες χώρες αμφοτερόπλευρα, καθώς επίσης και τους λεμφαδένες του μεσοθωρακίου και τις πνευμονικές πύλες. Ο ασθενής κατά την προσομοίωση της θεραπείας του ξάπλωνε σε μία επαναλείψιμη θέση, με τα χέρια πάνω από το κεφάλι, ή σε θέση μεσολαβής ( για να απομακρύνει τους μασχαλιαίους λεμφαδένες από τον θώρακα, ώστε να επιτρέπεται η προφύλαξη των πνευμόνων και για να προστατεύονται οι κεφαλές των βραχιονίων οστών) (Εικόνα 6). Το κεφάλι τοποθετείτο σε υπερέκταση. Για το σχεδιασμό των πεδίων χρησιμοποιούνταν ως οδηγά σημεία οστέινες δομές, ενώ συμβατικά blocks (στο λάρυγγα, το νωτιαίο μυελό, στον πνεύμονα), στόχευαν στον περιορισμό της ακτινοβόλησης σε υγιείς ιστούς και κυρίως σε ευαίσθητες δομές ή ευγενή όργανα [213,214] Εικόνα 6. Ψηφιακή ακτινογραφία DRR ( Digital reconstructive radiography-drr) πεδίου μανδύα, με block στην καρδιά μετά τα 30Gy ( γραμμή από μαύρες κουκίδες) [Hansen EK, Roach M III.Handbook of Evidence Based Radiation Oncology. 2 ond Edition, 2010, pp 556] Ο τροποποιημένος μανδύας αφορούσε στο ίδιο πεδίο με τον κλασικό μανδύα, χωρίς όμως να περιλαμβάνει τις μασχαλιαίες χώρες. Το πεδίο του ανεστραμμένου «Υ», επίσης περιελάμβανε τους παραορτικούς, λαγόνιους και μηροβουβωνικούς, με ή χωρίς τους σπληνικούς λεμφαδένες. Σε περιπτώσεις που η νόσος αναπτυσσόταν και από τις δύο πλευρές 72
73 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία του διαφράγματος, εφαρμοζόταν η ολική ή υφολική λεμφαδενική ακτινοβόληση ( Total ή Subtotal Lymph Node Irradiation-TLI ή STLI) με συνδυασμό των πεδίων μανδύα και ανεστραμμένου «Υ», με ή χωρίς τους πυελικούς λεμφαδένες (STLI) ανάλογα με την αρχική εντόπιση της νόσου. Σε αυτούς τους ασθενείς η υποδιαφραγματική θεραπεία ξεκινούσε 7-10 ημέρες μετά τη λήξη της ακτινοθεραπείας με πεδίο μανδύα Ακτινοθεραπεία Προσβεβλημένου Πεδίου (Involved Field Radiation Therapy- IFRT) Με την εισαγωγή νεώτερων τεχνολογιών και την ευρεία καθιέρωση της τρισδιάστατης σύμμορφης ακτινοθεραπείας (3 Dimensional Conformal Radiation Therapy 3DCRT), ήδη από τα τέλη της προηγούμενης δεκαετίας, υπήρχε εικόνα για την αποτελεσματικότητα της IFRT και πλήθος ερευνητών συνέκριναν την ακτινοθεραπεία εκτεταμένων πεδίων με την ακτινοβόληση προσβεβλημένου πεδίου για ασθενείς με HL αρχικών σταδίων τόσο ευνοϊκής όσο και δυσμενούς πρόγνωσης. Η Involved Field Radiation Therapy- IFRT, σύμφωνα με την ASTRO 2002, αφορά στη χορήγηση θεραπείας σε μία λεμφαδενική περιοχή που περιλαμβάνει τη νόσο και όχι σε ένα λεμφαδένα. Κύριες περιοχές στην ακτινοθεραπεία προσβεβλημένου πεδίου είναι ο τράχηλος (ετερόπλευρα), το μεσοθωράκιο (συμπεριλαμβανομένου και των πνευμονικών πυλών άμφω), η μασχαλιαία χώρα (συμπεριλαμβανομένου των υπερκλείδιων και υποκλείδιων λεμφαδένων), ο σπλήνας, οι παραορτικοί λεμφαδένες, οι βουβωνικοί λεμφαδένες (συμπεριλαμβανομένου των μηροβουβωνικών και των λαγόνιων λεμφαδένων). Τα πεδία ακτινοθεραπείας στην IFRT περιλαμβάνουν τις αρχικά και προ-χημειοθεραπείας διηθημένες περιοχές, με εξαίρεση τους λεμφαδένες μεσοθωρακίου και τους παραορτικούς, στους οποίους ακτινοθεραπεύονται οι εγκάρσιες διαστάσεις της νόσου μετά τη χημειοθεραπεία. Στην IFRT, ο τράχηλος ακτινοθεραπεύεται με ετερόπλευρο πεδίο, που περιλαμβάνει τους τραχηλικούς λεμφαδένες και τους σύστοιχους υπερκλείδιους. Στην ακτινοθεραπεία του μεσοθωρακίου με IFRT περιλαμβάνονται και οι πνευμονικές πύλες. Αν πάσχουν και οι υπερκλείδιες χώρες, περιλαμβάνονται τόσο οι υπερκλείδιες χώρες άμφω, όσο και οι 73
74 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή τραχηλικές περιοχές. Το πεδίο ακτινοθεραπείας με IFRT σε διηθημένη μασχαλιαία χώρα, περιλαμβάνει και τη σύστοιχη υπερκλείδια και υποκλείδια χώρα ( Εικόνα 7). Σε νόσο που εστιάζεται στη βουβωνική χώρα, το πεδίο περιλαμβάνει και τους έξω λαγόνιους και τους μηροβουβωνικούς λεμφαδένες. Γενικά στα πεδία ακτινοθεραπείας με IFRT δίνεται περιθώριο στο σχεδιασμό 2cm πάνω, και κάτω από τα όρια της νόσου, καθώς και 2cm από την εγκάρσια διάμετρο της βλάβης μετά τη χημειοθεραπεία ( στο μεσοθωράκιο και τους παραορτικούς λεμφαδένες).[215] Στη μελέτη EORTC GELA H8F, 542 ασθενείς με ευνοϊκής πρόγνωσης σταδίου Ι ΙΙ HL τυχαιοποιήθηκαν σε STLI ή χημειοθεραπεία (MOPP ABV x3) σε συνδυασμό με IFRT. Μετά από μεσοδιάστημα παρακολούθησης 92 μηνών, τόσο το ελεύθερο συμβάματος διάστημα (event free survival EFS) όσο και η συνολική επιβίωση υπερείχαν σαφέστατα στο σκέλος του συνδυασμού χημειοθεραπείας με IFRT [130]. Στην περίπτωση ασθενών με δυσμενούς πρόγνωσης HL αρχικών σταδίων, η μελέτη GHSG HD8 συνέκρινε ακτινοθεραπεία εκτεταμένων πεδίων, με ίδιας δόσης IFRT σε συνδυασμό με χημειοθεραπεία. Μετά από πολύμηνη μεταθεραπευτική παρακολούθηση, δεν φάνηκε διαφορά στην EFS ούτε στη συνολική 5-ετή επιβίωση, ενώ το σχήμα IFRT υπερείχε όσον αφορά στη μικρότερη συχνότητα εμφάνισης οξείας τοξικότητας της θεραπείας.[212] 74
75 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Εικόνα 7. Ψηφιακή ακτινογραφία DRR από πεδίο IFRT για στάδιο Ι, λεμφώματος Hodgkin που εντοπίζεται στη μασχαλιαία χώρα (α) και DRR από πεδίο IFRT για στάδιο Ι λεμφώματος Hodgkin που εντοπίζεται στη βουβωνική χώρα (β). [Hansen EK, Roach M III.Handbook of Evidence Based Radiation Oncology. 2 ond Edition, 2010, pp ] (α) (β) Η μελέτη EORTC-GELA H8U συνέκρινε 4 ή 6 κύκλους χημειοθεραπείας με το συνδυασμό MOPP/ABV ακολουθούμενη από STLI ή IFRT σε ασθενείς με εντοπισμένη νόσο δυσμενούς πρόγνωσης. Μετά από 5 έτη παρακολούθησης δεν παρατηρήθηκε διαφορά μεταξύ των δύο ακτινοθεραπευτικών σχημάτων όσον αφορά το EFS ή τη συνολική επιβίωση. [130] Πλήθος άλλων μελετών στη διεθνή βιβλιογραφία τεκμηριώνουν την αποτελεσματικότητα της IFRT ακτινοθεραπείας, καθιστώντας τη σε συνδυασμό με χημειοθεραπεία την ενδεδειγμένη θεραπεία σε ασθενείς με αρχικών σταδίων HL [125, 148, ] Ακτινοθεραπεία Προσβεβλημένου Λεμφαδένα ή Λεμφαδένων (Involved Νode Radiation Therapy- INRT) Νεότερα δεοδομένα στη διεθνή βιβλιογραφία, κατόπιν μετααναλύσεων και μακροχρόνιας παρακολούθησης ασθενών με HL, σε συνδυασμό με την εισαγωγή προηγμένων τεχνολογιών, έθεσαν σε αμφισβήτηση ακόμα και την ακτινοθεραπεία λεμφαδενικής περιοχής. Έτσι, μελέτη 75
76 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ανασκόπησης από τους Shahidi et al κατέδειξε ότι οι περισσότερες υποτροπές εντοπίζονταν στην περιοχή της αρχικής εστίας της νόσου[218]. Η χρήση επιπλέον της τομογραφίας εκπομπής ποζιτρονίων (FDG-PET) και ο συνδυασμός της με αξονική τομογραφία (PET-CT), καθώς και προηγμένα συστήματα σχεδιασμού και εφαρμογής της ακτινοθεραπείας κατέστησαν εφικτή την περαιτέρω εξατομικευμένη θεραπεία [ ]. Περάσαμε έτσι προοδευτικά από την IFRT στην ακτινοθεραπεία προσβεβλημένου λεμφαδένα ή λεμφαδένων (INRT) (Εικόνα 8). Eικόνα 8. Η εξέλιξη του σχεδιασμού της ακτινοθεραπείας στη θεραπεία του Λεμφώματος Hodgkin.[Presentation from ASTRO 2016, Contouring for Lymphoma, by Terezakis Stephanie, Figure of Dr Joachim Yahalom]] 1970-Oλική λεμφαδενική ακτινοβόληση (TLI) 1995-Ακτινοθεραπεία προσβεβλημένης περιοχής (IFRT) 2008-Ακτινοθεραπεία προσβεβλημένων λεμφαδένων (IΝRT) Όπως προαναφέρθηκε, η τοξικότητα της ακτινοθεραπείας σχετίζεται ευθέως ανάλογα με το μέγεθος του πεδίου και τη συνολική δόση. Μειώνοντας το μέγεθος του ακτινοβολητέου πεδίου, αυξάνεται όμως ο κίνδυνος γεωγραφικής απώλειας του όγκου-στόχου. Επομένως, ο περιορισμός των πεδίων ακτινοθεραπείας σε τόσο μεγάλο βαθμό, απαιτεί επιπρόσθετους ποιοτικούς ελέγχους και θεραπευτικούς αλγορίθμους, ώστε να συμπεριλαμβάνεται πάντα η νόσος, με ικανό περιθώριο. 76
77 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Δόση Ακτινοθεραπείας Δόση Ακτινοθεραπείας στα αρχικά και ενδιάμεσα στάδια Στο παρελθόν όταν η ακτινοθεραπεία αποτελούσε μονοθεραπεία για τους ασθενείς με λέμφωμα Hodgkin, συνολική δόση ανερχόταν σε 36-45Gy. Η προσθήκη της χημειοθεραπείας, επέτρεψε την ελάττωση της δόσης της ακτινοθεραπείας στα 30Gy, για την εκρίζωση του νοσήματος. Σε αναδρομική ανάλυση που έγινε σε 235 ασθενών σταδίων Ι/ΙΙ Α [125] και με ενημέρωση των δεδομένων επί 276 ασθενών[223], παρατηρήθηκε ότι οι ασθενείς που έλαβαν Gy εμφάνισαν σημαντικά λιγότερες υποτροπές σε σχέση με αυτούς που έλαβαν <28Gy (ως επί το πλείστον Gy). Η διαφορά κατά κύριο λόγο οφείλεται στον καλύτερο έλεγχο της νόσου εντός του προσβεβλημένου πεδίου. Στη μελέτη HD10 της GHSG απεδείχθη ότι σε ασθενείς αρχικών σταδίων, μετά από ABVD x 2, η δόση της ΑΚΘ μπορεί να ελαττωθεί από 30 σε 20 Gy χωρίς διαφορά στην αποτελεσματικότητα και με μικρότερη τοξικότητα [134]. Επίσης, στη μελέτη H9F του EORTC για ασθενείς αρχικών σταδίων, η 5-ετής FFTF για τους ασθενείς που έλαβαν 36 Gy και 20 Gy ακτινοθεραπείας μετά από CR/CRu που επετεύχθη με 6 κύκλους EBVP ήταν 89% έναντι 85% (p=0.19), ενώ η 5-ετής συνολική επιβίωση ήταν 100% έναντι 98% αντίστοιχα (p=0.41)[224]. Στα ενδιάμεσα στάδια, μετά από ABVD x 4, η μελέτη HD11 της GHSG κατέδειξε μικρού βαθμού αλλά στατιστικώς σημαντική διαφορά στην 5-ετή FFTF μεταξύ 30 Gy και 20 Gy ΑΘ- ΠΠ (85% έναντι 81%). Ωστόσο, η δόση της ΑΚΘ δε φαίνεται να επηρεάζει την FFTF, όταν η ΧΜΘ είναι πιο εντατική, δηλ. BEACOPP-baseline x 4. Σε καμμία περίπτωση δε διαπιστώθηκαν διαφορές στη συνολική επιβίωση[135]. Με βάση τα παραπάνω δεδομένα, η συνιστώμενη δόση ακτινοθεραπείας μετά από επαρκή ανταπόκριση στη ΧΜΘ με ABVD είναι προς το παρόν 30 Gy, με δυνατότητα ελάττωσης στα 20 Gy σε ασθενείς χωρίς δυσμενείς προγνωστικούς παράγοντες (πίνακας 7). 77
78 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Δόση Ακτινοθεραπείας στα προχωρημένα στάδια H χορήγηση ακτινοθεραπείας είναι υπό αμφισβήτηση στα προχωρημένα στάδια του λεμφώματος Hodgkin. Στην προ ΡΕΤ/CT εποχή και μετά από πλήρη ακτινολογική ύφεση σε ασθενείς που έχουν λάβει χημειοθεραπεία με ABVD, η ακτινοθεραπεία δε φαίνεται να προσφέρει επιπλεόν όφελος [152] ενώ δε φαίνεται να χρειάζεται και επί ακτινολογικής μερικής υφέσεως >75%, συγκρινόμενη στην τελευταία αυτή περίπτωση με 2 περαιτέρω κύκλους ΧΜΘ[225]. Είναι, ωστόσο, γεγονός, ότι η ακτινοθεραπεία μετατρέπει πολλές μερικές υφέσεις σε πλήρεις[226] και, ως εκ τούτου, φαίνεται ότι αποτελεί σημαντικό κομμάτι της θεραπείας σε ασθενείς με λιγότερο ικανοποιητικές μερικές υφέσεις(<75%), μετά από τη λήψη χημειοθεραπείας. Προκύπτει εύλογα το ερώτημα κατά πόσο οι τελευταίες αποτελούν (στην πλειονότητά τους) τις PET+ μερικές υφέσεις με υπόλειμμα >2.5 εκ της μελέτης HD15 της GHSG, οι οποίες θεωρείται ότι χρήζουν ακτινοβόλησης μετά από θεραπεία τύπου BEACOPPesc.[227] Στην προ ΡΕΤ/CT εποχή, η μελέτη HD12 της GHSG ερευνά την εφαρμογή ακτινοθεραπείας με συνολική δόση 30Gy, σε ασθενείς με ογκώδη νόσο 5 cm ή με υπόλειμμα 1.5cm και μετά από χορήγηση χημειοθεραπείας με BEACOPP[163]. Η χορήγηση ΑΚΘ στους ασθενείς αυτούς οδήγησε σε στατιστικώς σημαντική αύξηση της FFTF. Το όφελος προέκυψε από την ακτινοβόληση υπολειμμάτων 1.5cm και άνω, όπου η 5-ετής FFTF υπερτερούσε κατά 6%. Αντίθετα, δεν υπήρχε όφελος από την ακτινοβόληση επί ογκώδους νόσου, χωρίς τέτοιο υπόλειμμα. Η συνολική επιβίωση δε διέφερε. Χρειάζεται να επισημανθεί εδώ ότι στη συγκεκριμένη μελέτη ~23% των ασθενών που τυχαιοποιήθηκαν να μην ακτινοβοληθούν, τελικώς ακτινοβολήθηκαν, δυσχεραίνοντας έτσι την ερμηνεία των αποτελεσμάτων. Ξεχωριστό θέμα αποτελεί ο ρόλος της ΑΚΘ στην εποχή της λειτουργικής απεικόνισης με PET-Scan. Στη μελέτη HD15 της GHSG[228] ασθενείς με υπολειμματικές μάζες >2.5 εκ. και θετικό PET μετά το πέρας της θεραπείας με BEACOPPesc ή BEACOPP-14 υποβάλλονταν σε ακτινοβόληση. Η 5-ετής επιβίωση χωρίς εξέλιξη της νόσου ήταν 92% τόσο για τους ασθενείς που ευρίσκονταν σε CR/CRu, οι οποίοι δεν υποβλήθηκαν σε PET-scan, όσο και για όσους πέτυχαν μερική ύφεση με υπόλειμμα >2.5 εκ. και είχαν αρνητικό PET-scan, ενώ ήταν 86% για 78
79 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία τους ασθενείς με μερική ύφεση, υπόλειμμα >2.5 εκ. και θετικό PET-Scan, παρά την ακτινοβόληση. Έτσι η ακτινοβόληση φαίνεται ότι διασώζει την πλειονότητα των ασθενών που ανταποκρίνονται αλλά παραμένουν PET-θετικοί με υπόλειμμα >2.5 εκ. μετά από εντατική χημειοθεραπεία τύπου BEACOPPesc. Βεβαίως η μελέτη αυτή δεν απαντά στο ερώτημα σχετικά με τον ρόλο του PET σε ασθενείς που επιτυγχάνουν καλύτερες μερικές υφέσεις ή και πλήρεις καθώς και τον ενδεχόμενο ρόλο της ΑΚΘ στις εν λόγω ομάδες. Στην περίπτωση των ασθενών με προχωρημένο στάδιο λεμφώματος Hodgkin, οι οποίοι έχουν λάβει ABVD ή ισοδύναμους συνδυασμούς, η αναγκαιότητα χορήγησης επικουρικής ακτινοθεραπείας είναι υπό διερεύνηση. Τα προκαταρτικά δεδομένα μελετών δείχουν ότι η 5-ετής επιβίωση χωρίς νόσο σε ασθενείς που καθίστανται PET-αρνητικοί με ABVD (και ελάχιστοι ακτινοβολούνται) είναι περίπου 80%: ~88% για το στάδιο ΙΙΙ και 70-80% για το στάδιο IV[228]. Όταν οι ασθενείς ανταποκρίνονται στο ABVD αλλά παραμένουν PET(+), η πιθανότητα διάσωσης με ΑΚΘ είναι της τάξεως του 50%, ποσοστό που έρχεται σε αντίθεση με την πολύ επιτυχέστερη διάσωση μετά από BEACOPPesc. Στις περιπτώσεις υπολειμματικής μάζας, 80% περίπου των ασθενών είναι PET(-). Η παράληψη της ακτινοβόλησης δεν είναι σαφώς τεκμηριωμένη στην ομάδα αυτή, ιδίως εάν το μέγεθος της υπολειμματικής μάζας είναι σημαντικό ή/και υπήρχε ογκώδης νόσος. Από την άλλη 20% περίπου είναι PET(+) και σε αυτούς φαίνεται να χρειάζεται ακτινοβόληση, αλλά μένει να διευκρινισθεί κατά πόσον αυτή επαρκεί για την ίαση μετά το ABVD και κατά πόσο απαιτείται ακτινοβόληση προσβεβλημένου πεδίου ή μόνο στο υπόλειμμα. Στις περιπτώσεις που δεν υπάρχει υπολειμματική μάζα, η πλειονότητα των ασθενών είναι PET(-) και δεν ωφελούνται από την ακτινοβόληση[152], ενώ μια μικρή μειονότητα μπορεί να είναι PET(+), όπου η αξία της ακτινοβόλησης είναι άγνωστη Τεχνικές Ακτινοθεραπείας Ο ασθενής υποβάλλεται σε προ- και μεταχημειοθεραπευτικό απεικονιστικό έλεγχο με αξονική τομογραφία, η οποία να περιλαμβάνει όλες τις προσβεβλημένες λεμφαδενικές ομάδες. Σκόπιμη είναι και η διενέργεια PET-CT προ χημειοθεραπείας, κατά προτίμηση σε θέση θεραπείας, δηλαδή σε συνθήκες που προσομοιάζουν όσο το δυνατό με αυτές που 79
80 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή εφαρμόζονται κατά την ακτινοβόληση του ασθενούς. Με αυτό τον τρόπο δίνεται η δυνατότητα επιπροβολής και σύμπτυξης των εικόνων της αξονικής τομογραφίας σχεδιασμού θεραπείας με τις εικόνες της ποζιτρονιακής αξονικής, επιτυγχάνοντας ακριβέστερο καθορισμό της αρχικής εντόπισης της νόσου (Εικόνα 9). Η έναρξη της διαδικασίας σχεδιασμού της θεραπείας προϋποθέτει τη διενέργεια αξονικής τομογραφίας σχεδιασμού με τον ασθενή σε θέση θεραπείας και πλήρη σάρωση της ανατομικής περιοχής που υπάρχει η νόσος. Εν συνεχεία ακολουθεί σχεδιασμός-καθορισμός των ακτινοβολητέων όγκων: ο μακροσκοπικά ορατός όγκος (Gross Tumor Volume GTV), ο κλινικός όγκος (Clinical Target Volume - CTV), ο οποίος περιλαμβάνει την αρχική νόσο προ χημειοθεραπείας ή το GTV με περιθώριο ασφαλείας ανάλογα με την εντόπιση της νόσου και ο ακτινοβολητέος όγκος (Planning Target Volume - PTV), ο οποίος αναφέρεται στον κλινικό όγκο με ικανό περιθώριο ώστε να καλύπτονται μικρομεταβολές και μικροτροποποιήσεις κατά τη διάρκεια της θεραπείας, που οφείλονται στη φυσιολογική κινητικότητα των εσωτερικών οργάνων και στην αβεβαιότητα κατά την καθημερινή ακινητοποίηση του ασθενούς.[229,230] Ο ασθενής λαμβάνει τη θεραπεία, στα περισσότερα κέντρα παγκοσμίως μέσω της τεχνικής της τρισδιάστατης σύμμορφής ακτινοθεραπεία (3DCRT). Μέσα από σύνθετους υπολογισμούς που οδηγούν στο τελικό πλάνο ακτινοθεραπείας, επιτυγχάνεται η «συμμόρφωση» της χορηγηθείσας δόσης στον επιθυμητό όγκο-στόχο, με ταυτόχρονη προστασία των γειτονικών υγιών ιστών. Σε αυτό συμβάλλει πρώτιστα και η παρουσία των ιστογραμμάτων δόσης όγκου (DVH Dose Volume Histogram), με τα οποία γίνεται εφικτός ο υπολογισμός του ποσοστού των φυσιολογικών ιστών και των ακτινοβολητέων περιοχών που λαμβάνουν συγκεκριμένη δόση ακτινοβολίας. Με τον τρόπο αυτό μπορεί να προβλεφθεί τόσο η δραστικότητα όσο και η ασφάλεια της θεραπείας. Η ακτινοθεραπεία χορηγείται με γραμμικούς επιταχυντές εφοδιασμένους με πολλαπλούς κατευθυντήρες φύλλων, ικανών να κάνουν ακόμα πιο σύμμορφή τη δέσμη ακτινοβολίας, προστατεύοντας ακόμα περισσότερο τους υγιείς ιστούς. Στις μέρες μας, η χορήγηση της ακτινοθεραπείας σε ασθενείς με λέμφωμα Hodgkin δύναται να γίνει και με την τεχνική της ακτινοθεραπείας διαμορφούμενης έντασης (Intensity Modulated Radiation Therapy-IMRT). Με τη συγκεκριμένη τεχνική είναι εφικτή η κλιμάκωση της δόσης σε όγκους που γειτνιάζουν με ζωτικά όργανα. Η IMRT επιτρέπει τη λεγόμενη 80
81 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία γλυπτική της δόσης ακτινοβολίας (dose sculpture-dose painting). Με αυτό τον τρόπο μόνο οι υψηλής ενέργειας δέσμες ακτινοθεραπείας περιορίζονται να καλύπτουν τον όγκο-στόχο, ενώ οι γύρω φυσιολογικοί ιστοί προστατεύονται, λαμβάνοντας μόνο ένα μικρό μέρος της συνολικής χορηγηθείσας δόσης. Στην IMRT η ακτινοθεραπεία χορηγείται με πολλαπλά πεδία ακτινοβολίας, καθένα από τα οποία υποδιαιρείται σε υποπεδία. Με αυτό τον τρόπο εξασφαλίζεται ο βέλτιστος καθορισμός της έντασης κάθε δέσμης και κατ επέκταση η βέλτιστη κατανομή της δόσης[ ]. Η ΙΜRT επιτρέπει καλύτερη κάλυψη του όγκου στόχου και καλύτερη προστασία της καρδιάς και των στεφανιαίων αγγείων. Μειονέκτημα της τεχνικής αυτής όμως, είναι η ακτινοβόληση μεγάλης έκτασης υγιών ιστών με μικρή δόση ακτινοβολίας (dose bathing), αυξάνοντας έτσι δυνητικά τον κίνδυνο μεταγενέστερης εμφάνισης δευτερογενών κακοηθειών[234]. Πιο συγκεκριμένα η IMRT όταν χρησιμοποιηθεί για ακτινοθεραπεία που περιλαμβάνει το μεσοθωράκιο, χορηγεί σημαντικά μεγαλύτερες διάμεσες δόσεις ακτινοβολίας στους πνεύμονες και τους μαστούς. Το γεγονός αυτό την αποκλείει ως τεχνική θεραπείας του HL, στα πλαίσια ρουτίνας. Μία άλλη τεχνική με την οποία δύναται ο ασθενής να λάβει τη θεραπεία του είναι η καθοδηγούμενη από απεικόνιση ακτινοθεραπεία (Image Guided Radiation-IGRT). Με τη μέθοδο αυτή ο ασθενής, πρίν από κάθε συνεδρία και αφού τοποθετηθεί στη θέση θεραπείας, υποβάλλεται σε απεικόνιση για την επιβεβαίωση της τοποθέτησης του πεδίου πάνω στο σώμα του (Cone Beam Computed Tomography-CBCT). Με αυτό τον τρόπο ελέγχεται καθημερινά η σωστή κάλυψη του όγκου-στόχου από το πεδίο ακτινοθεραπείας, ενώ παράλληλα επιβεβαιώνεται και η προστασία των γειτνιαζόντων φυσιολογικών ιστών, μετά από σύγκριση των απεικονιστικών ευρημάτων με την αρχική αξονική πάνω στην οποία πραγματοποιήθηκε ο σχεδιασμός της θεραπείας.κατόπιν γίνονται οι τυχόν διορθώσεις και ακολουθεί η χορήγηση της συνεδρίας με μικρομετακινήσεις σε τρεις άξονες, ώστε να εξασφαλίζεται η ακόμα ακριβέστερη ακτινοβόληση[235]. Στο σημείο αυτό χρειάζεται να σημειωθεί ότι για την ακτινοθεραπεία του μεσοθωρακίου μία νεότερη τεχνική εστιάζεται στην ίδια την αναπνοή του ασθενούς(respiratory gating). Έτσι, μετά από μελέτη του αναπνευστικού κύκλου του ατόμου, η ακτινοβόληση του όγκου- 81
82 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή στόχου χορηγείται πάντα σε συγκεκριμένη φάση της αναπνοής, προστατεύοντας με αυτό τον τρόπο την έκθεση μεγάλου όγκου του υγιούς πνεύμονα από άσκοπη ακτινοβόληση[236]. Τέλος, στην ακτινοθεραπεία του μεσοθωρακίου έχει μελετηθεί και η τεχνική ακτινοβόλησης με πρωτόνια. Σύμφωνα με αυτή τη σωματιδιακή ακτινοβολία, η θεραπεία μπορεί να αποδοθεί με ακρίβεια σε ένα προκαθορισμένο στόχο ενδιαφέροντος, ενώ πέραν αυτού, η δόση ακτινοβόλησης είναι μηδενική. H συγκεκριμένη κατανομή ακτινοβολίας αποτελεί βιολογικό χαρακτηριστικό των πρωτονίων και λέγεται bragg peak. Το πλεονέκτημα της χορήγησης αυτού του είδους ακτινοθεραπείας είναι η βέλτιστη προστασία των υγιών δομών, όπως είναι ο πνεύμονας, η καρδιά, ο οισοφάγος και ο μαστός στην περίπτωση ακτινοβόλησης του μεσοθωρακίου[237,238]. Σε σύγκριση της συγκεκριμένης μεθόδου με την 3DCRT και την IMRT, η ακτινοθεραπεία με πρωτόνια φαίνεται να υπερέχει των άλλων δύο. Η χορήγηση της όμως στο HL είναι περιορισμένη, εξαιτίας των ανεπαρκών κλινικών δεδομένων της μεθόδου πάνω στη συγκεκριμένη νόσο,καθώς και της περιορισμένης διαθεσιμότητας εγκαταστάσεων πρωτονίων [238]. Εικόνα 9. Σύμπτυξη εικόνων αξονικής τομογραφίας και τομογραφίας εκπομπής ποζιτρονίων για το βέλτιστο σχεδιασμό του όγκου-στόχου. [Presentation from ASTRO 2016, Contouring for Lymphoma, by Terezakis Stephanie] 82
83 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Τοξικότητα Ακτινοθεραπείας Με τις σύγχρονες θεραπευτικές προσεγγίσεις, το HL αποτελεί μια από τις πλέον ιάσιμες κακοήθειες καθώς στις περισσότερες των περιπτώσεων επιτυγχάνεται διαρκής πλήρης ύφεση. Το γεγονός αυτό, σε συνδυασμό με το ότι αποτελεί νόσημα κυρίως των νέων ενηλίκων με μεγάλο προσδώκιμο επιβίωσης, καθιστά την εμφάνιση παρενεργειών, κυρίως χρόνιων σημαντικό πρόβλημα. Η τοξικότητα της ακτινοθεραπείας διακρίνεται σε οξεία, υποξεία και απώτερη. Στην οξεία τοξικότητα από ακτινοθεραπεία, παρατηρείται η εικόνα της αδυναμίας, της δερματίτιδας, της οισοφαγίτιδας, της διαταραχής της γεύσης, της ναυτίας, ή και της διάρροιας, ανάλογα με το αν το πεδίο ακτινοβόλησης εστιάζει στον τράχηλο, το μεσοθωράκιο, ή την άνω-κάτω κοιλία, αντίστοιχα. Η υποξεία τοξικότητα της ακτινοθεραπείας εμφανίζεται με την εικόνα της μετακτινικής πνευμονίτιδας (εφόσον εκτίθεται ο πνεύμονας στο πεδίο της ακτινοθεραπείας), ή του συνδρόμου Lermitte( εφόσον εκτίθεται ο νωτιαίος μυελός στο ακτινοβολητέο πεδίο). Οι απώτερες τοξικότητες περιλαμβάνουν τη στεφανιαία νόσο, τον υποθυρεοειδισμό, τα γαστρικά έλκη, την απώτερη μετακτινική πνευμονική τοξικότητα με τη μορφή πνευμονικής ίνωσης, τη στείρωση, τη μειωμένη ανοσία και την πιθανότητα δευτερογενών κακοηθειών. Η επίπτωση αυτών των απώτερων επιπλοκών αυξάνεται με το πέρασμα του χρόνου. Στις μέρες μας όμως, αυτός ο κίνδυνος φαίνεται να μειώνεται εξαιτίας των νεότερων θεραπευτικών τεχνικών και θεραπειών,που χρησιμοποιούνται σε σχέση με αυτά που χορηγούνταν 10 χρόνια πριν. Ειδικά για την ακτινοθεραπεία αυτό γίνεται εμφανές με την εξάλειψη της χορήγησης ακτινοθεραπείας με κοβάλτιο και τις πιο πρόσφατες τεχνικές που επιτρέπουν ακτινοβόληση του όγκου, με ταυτόχρονη βέλτιστη προστασία των γειτονικών υγιών ιστών. Στο σημείο αυτό, χρειάζεται να τονιστεί ότι η ακτινοθεραπεία ενοχοποιείται για την εμφάνιση λευχαιμίας, κυρίως με τη μορφή της οξείας μυελογενούς λευχαιμίας, με αιχμή στα 5-9 έτη από την ακτινοθεραπεία. Ασθενείς με ιστορικό ακτινοθεραπείας για HL έχουν σχετικό 83
84 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή κίνδυνο εμφάνισης 20 φορές περίπου υψηλότερο από το γενικό πληθυσμό. Συνήθεις είναι και οι κακοήθειες από το θυρεοειδή, τον πνεύμονα,το μαστό και το γαστρεντερικό,που εμφανίζονται μετά τα πρώτα 5 έτη από τη θεραπεία.μολονότι οι περισσότερες μελέτες στη διεθνή βιβλιογραφία συμφωνούν στο ότι η προσθήκη χημειοθεραπείας αυξάνει τον κίνδυνο για εμφάνιση συμπαγών όγκων, σημαντικότερος παράγοντας φαίνεται ότι είναι η μονοθεραπεία με ακτινοβολία, όπως φάνηκε και σε μεταανάλυση από τους Franklin et al, όπου ο κίνδυνος εμφάνισης κακοήθειας ήταν στατιστικά σημαντικά μικρότερος, κατά τη χορήγηση συνδυασμού χημειοθεραπείας - ακτινοθεραπείας συγκριτικά με τη χορήγηση ακτινοθεραπείας ως μονοθεραπεία, κυρίως σε ασθενείς σταδίου III. Οι ερευνητές απέδωσαν τα ευρήματα αυτά, στη σημαντικά αυξημένη συχνότητα υποτροπής ή προόδου νόσου και κατ επέκταση στην αναγκαιότητα θεραπείας διάσωσης στις περιπτώσεις εφαρμογής ακτινοθεραπείας μόνο. Ενδιαφέρον επίσης στοιχείο της μελέτης αυτής είναι η μη εμφάνιση στατιστικά σημαντικής διαφοράς στη συχνότητα εμφάνισης δευτεροπαθών κακοηθειών (με εξαίρεση τον καρκίνο του μαστού) σε περιπτώσεις εφαρμογής εκτεταμένων ή περιορισμένων πεδίων ακτινοθεραπείας. [239]. Έχει βρεθεί ότι ασθενείς που έλαβαν θεραπεία με προσθιοπίσθια πεδία και κοβάλτιο έχουν αθροιστικό κίνδυνο για εμφάνιση δευτεροπαθών κακοηθειών της του10-13% στα 15 έτη παρακολούθησης, ο οποίος μεγαλώνει με κάθε επιπλέον έτος επανελέγχου[240]. Επιπρόσθετα, ο Radford το 2015 ανέδειξε ότι ασθενείς που έχουν υποβληθεί στο παρελθόν σε θεραπεία για HL έχουν 4.6 φορές μεγαλύτερο κίνδυνο εμφάνισης δευτεροπαθών κακοηθειών, σε σχέση με το γενικό πληθυσμό. Ο αθροιστικός αυτός κίνδυνος εμφανίζεται σε ποσοστό 33.2% στα 30 έτη και στα 48.5% στα 40 έτη παρακολούθησης, αυξανόμενος κατά 9% και 19% σε σχέση με το γενικό πληθυσμό[241] Στη συγκεκριμένη μελέτη, 3905 ασθενείς είχαν λάβει θεραπεία από το 1965 έως το 2000 για HL. Είχαν υποβληθεί είτε μόνο σε ακτινοθεραπεία(27.3%) ή σε χημειοθεραπεία (12.1), ή και συνδυασμένη θεραπεία (60.5%). Τα αποτελέσματα της μελέτης έδειξαν ότι οι νέες θεραπείες δε φαίνεται να μειώνουν τον κίνδυνο εμφάνισης δευτεροπαθών κακοηθειών. Τα μικρότερα πεδία της ακτινοθεραπείας, συγκριτικά με το πεδίο ακτινοθεραπείας τύπου μανδύα, μείωναν σημαντικά τον κίνδυνο εμφάνισης καρκίνου μαστού, χωρίς όμως να επηρεάζουν την εμφάνιση καρκίνου του πνεύμονα. Ο συγγραφέας κατέλειξε στο γεγονός ότι η διατήρηση των υψηλών ποσοστών εμφάνισης δευτεροπαθών κακοηθειών οφείλεται σε μη πλήρη υιοθέτηση των νέων τεχνικών ακτινοθεραπείας, στο καλύτερο προληπτικό έλεγχο για τον καρκίνο 84
85 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία μαστού, που επιτρέπει την πολύ πρώιμη διάγνωσή του και στην ύπαρξη αλκυλιωτικών παραγόντων στα χημειοθεραπευτικά σχήματα.ειδικά στην περίπτωση δευτεροπαθούς κακοήθειας στο πάγκρεας και το στομάχι, ενοχοποιήθηκαν η χορήγηση υποδιαφραγματικής ακτινοθεραπείας στο παρελθόν, καθώς και η χορήγηση προκαρβαζίνης. Η τελευταία έχει βρεθεί ότι σχετίζεται και με την παρουσία δευτεροπαθών Non-Hodgkin νοσημάτων. Όπως αναφέρθηκε παραπάνω, η πνευμονική τοξικότητα είναι η συχνότερη παρενέργεια της ακτινοθεραπείας σε ασθενείς που έχουν υποβληθεί σε ακτινοβόληση του μεσοθωρακίου, ειδικά όταν αυτή συνδυάζεται με χημειοθεραπευτικά σχήματα που περιλαμβάνουν μπλεομυκίνη.οι σύγχρονες τεχνικές IMRT, IGRT,respiratory gating, proton beam radiotherapy έχουν ως στόχο τον περιορισμό ακτινοβόλησης υγιούς πνευμονικού παρεγχύματος όταν αυτό περιλαμβάνεται μέσα στο ακτινοβολητέο πεδίο. Προβλεπτικός δείκτης για πιθανή πνευμονική ίνωση και πνευμονίτιδα, οφειλόμενη στην ακτινοβολία, είναι το ποσοστό του υγιούς πνευμονικού παρεγχύματος που δέχεται δόση μεγαλύτερη από 20 Gy (V20).[233] Σημαντική τοξικότητα αποτελεί και η εμφάνιση καρδιαγγειακής νόσου, μετά από την ακτινοθεραπεία του μεσοθωρακίου και τη χορήγηση χημειοθεραπείας, βασισμένης στις ανθρακυκλίνες. Η νόσος δύναται να είναι ασυμπτωματική και να εμφανιστεί αρκετά χρόνια μετά τη θεραπεία[242,243] Τέλος, άλλη σημαντική και αρκετά συχνή παρενέργεια αποτελεί ο υποθυρεοειδισμός μετά τη χημειο-ακτινοθεραπεία για λέμφωμα Hodgkin, όταν αυτό περιλαμβάνει ακτινοβόληση του τραχήλου, οπότε ο αδένας βρίσκεται μέσα στο πεδίο ακτινοθεραπείας. Διαταραγμένη θυρεοειδική λειτουργία, αναφέρεται σε ποσοστό ως και 50% των ασθενών με μακρό χρονικό διάστημα ελεύθερο νόσου.[244] Συνίσταται προσεκτική κλινική εξέταση θυρεοειδούς αδένα και ο ετήσιος έλεγχος θυρεοειδικής λειτουργίας (TSH, T4) σε αυτά τα άτομα. Γενικά, περιορίζοντας το μέγεθος του ακτινοβολητέου πεδίου, μειώνοντας τη συνολική δόση στον όγκο - στόχο, και βελτιστοποιώντας τις τεχνικές θεραπείας, επαυξάνεται ο θεραπευτικός λόγος της ακτινοθεραπείας, αυξάνοντας την πιθανότητα του ελέγχου της νόσου και της ίασης, με την ίδια ή και ελαττωμένη τοξικότητα.[134,245] 85
86 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή 2. PET-CT 2.1 ΣΥΜΒΟΛΗ ΤΟΥ ΡΕΤ-CT ΣΤΙΣ ΘΕΡΑΠΕΥΤΙΚΕΣ ΑΠΟΦΑΣΕΙΣ ΚΑΙ ΤΗΝ ΠΑΡΑΚΟΛΟΥΘΗΣΗ ΑΣΘΕΝΩΝ ΜΕ ΛΕΜΦΩΜΑ HODGKIN Εισαγωγή Η Τομογραφία Εκπομπής Ποζιτρονίων (Positron Emission Tomography-PET) με δεσοξυγλυκόζη επισημασμένη με 18 F ( 18 FDG) και κυρίως η PET σε συνδυασμό με χαμηλής δόσης αξονική τομογραφία (CT) (PET/CT) είναι μια σύγχρονη απεικονιστική μέθοδος που χρησιμοποιείται ευρέως στη διερεύνηση των κακοήθων νεοπλασιών, ιδιαίτερα δε των λεμφωμάτων των οποίων οι περισσότεροι ιστολογικοί υπότυποι παρουσιάζουν λίαν υψηλή πρόσληψη 18 FDG.[246,247]. Ειδικά στο λέμφωμα Hodgkin, τα νεοπλασματικά κύτταρα Hodgkin και τα κύτταρα Reed-Sternberg αντιπροσωπεύουν ποσοστό μικρότερο του 1% του κυτταρικού πληθυσμού του διηθημένου λεμφαδένα, ενώ κυριαρχούν κύτταρα του αντιδραστικού «φλεγμονώδους» υποστρώματος, τα οποία είναι μεταβολικά πολύ ενεργά και σε αυτά οφείλεται κυρίως η πρόσληψη 18 FDG σε ποσοστό σχεδόν 100%, καθώς και η απουσία πρόσληψης μετά από θεραπεία παρά το γεγονός της παραμονής μεγάλων υπολειμματικών μαζών. Με τα νεότερα δεδομένα, η θεραπεία του λεμφώματος Hodgkin (HL) αποτελεί πρόκληση, καθώς απαιτεί συνεργασία του αιματολόγου, με τον παθολογοανατόμο, τον ακτινοθεραπευτή ογκολόγο, και τον πυρηνικό ιατρό.. Ωστόσο, η αδιάκοπα συνεχιζόμενη εξέλιξη των θεραπευτικών στρατηγικών και επιλογών που οδήγησε στη μεγάλη αύξηση του ποσοστού ίασης, έχουν καταστήσει σαφές πως η θεραπευτική προσέγγιση δεν θα πρέπει να βασίζεται μόνο στην αντινεοπλασματική αποτελεσματικότητα της αγωγής, αλλά παράλληλα και να αποτρέπει την εμφάνιση απώτερων επιπλοκών που θα επηρεάσουν αρνητικά την ποιότητα ζωής των ασθενών σε βάθος χρόνου[248].. Η διατήρηση αυτού του εύθραυστου ισοζυγίου, όπως και ο προσδιορισμός ασθενών που θα πρέπει να κατευθυνθούν εγκαίρως προς εντατικότερη θεραπεία, αποτελεί την κεντρική επιδίωξη της σύγχρονης θεραπείας του 86
87 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία HL και επιτυγχάνεται χρησιμοποιώντας μια σειρά προθεραπευτικών προγνωστικών παραγόντων, αλλά και την επανασταδιοποίηση της νόσου με τομογραφία εκπομπής ποζιτρονίων (ΡΕΤ/CT). Σημειώνεται πως από το 2001 και έπειτα παρασκευάζονται μόνο PET/CT τομογράφοι[249], οι οποίοι υπερτερούν έναντι του κλασσικού ΡΕΤ-scan [250,251] καθώς αποτελούν συσκευές που προσφέρουν την ίδια ώρα τόσο λειτουργικές όσο και μορφολογικές πληροφορίες Τρόπος λειτουργίας του ΡΕΤ/CT Η τομογραφία εκπομπής ποζιτρονίων αποτελεί μια μη επεμβατική, ποσοτική απεικονιστική τεχνική που κάνει ορατές in vivo βιοχημικές και βιολογικές διαδικασίες[252]. Πρόκειται για εξέταση που απεικονίζει την κατάσταση του μεταβολισμού του ασθενή. Οι μεταβολικές αλλαγές προηγούνται των ανατομικών/μορφολογικών αλλαγών. Ως εκ τούτου, επί του παρόντος, θεωρείται η πλέον ευαίσθητη μοριακή απεικονιστική τεχνική. Η απεικόνιση του ΡΕΤ βασίζεται στην ανίχνευση εκμηδενισμένων φωτονίων που παράγονται μετά από την εκπομπή ποζιτρονίων από ένα ραδιοσημασμένο ιχνηθέτη, που ακολουθεί και ανταποκρίνεται σε ένα συγκεκριμένο μοριακό βιολογικό περιβάλλον ή σε ένα βιοχημικό μονοπάτι. Γενικά η απεικόνιση με ΡΕΤ περιλαμβάνει ισότοπα, όπως είναι τα F-18, C-11, N-13, Ga-68, που εκπέμουν ποζιτρόνια. Τα ισότοπα αυτά έχουν έλλειμμα σε νετρόνια. Επιτυγχάνουν σταθερότητα μέσω μετατροπής ενός πρωτονίου σε νετρόνιο με ταυτόχρονη εκπομπή ενός ποζιτρονίου (β+) και ενός νετρίνου. Tο ποζιτρόνιο είναι ένα αντισωματίδιο ηλεκτρονίου με ίδια μάζα και αντίθετο φορτίο, με αυτά του ηλεκτρονίου. Μετά την εκπομπή του, το ποζιτρόνιo ταξιδεύει (φάσμα ποζιτρονίων) μεταξύ του υλικού και του νέφους ηλεκτρονίων μέχρι να χάσει σχεδόν όλη του την ενέργεια. Σε αυτό το σημείο το ποζιτρόνιο αλληλεπιδρά με ένα ελεύθερο ηλεκτρόνιο και αλληλοεξουδετερώνονται (εξαϋλωση), με αποτέλεσμα την παραγωγή δύο φωτονίων γάμμα ακτινοβολίας, με ενεργεια 511keV το καθένα (δίδυμη γένεση). Η ενέργεια αυτή αντιστοιχεί στη μάζα ηλεκτρονίων και ποζιτρονίων που εκπέμπονται σε αντίθετες κατευθύνσεις (~180 o )( Εικόνα 10). Τα φωτόνια ανιχνεύονται και μετά καταχωρούνται ως γεγονός, πρακτικά ταυτόχρονα, από ανιχνευτές του δακτυλίου της ΡΕΤ, σε αντιδιαμετρικά αντίθετη θέση. Πολλαπλές καταγραφές 87
88 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή γεγονότων εξαύλωσης επιτρέπουν με αρκετά μεγάλη ακρίβεια τον προσδιορισμό της θέσης προέλευσης τους και συνεπώς την ανατομική θέση όπου έχει συγκεντρωθεί το ραδιοϊσότοπο. Εικόνα 10. Πώς λειτουργεί η τομογραφία εκπομπής ποζιτρονίων; [Από Παρουσίαση: Κλινικές ενδείξεις της ποζιτρονικής τομογραφίας (PET/CT), Σκούρα Ευαγγελία] Παραγωγή δύο φωτονίων με αντίθετη κίνηση και ενέργεια 511KeV Ασταθής πυρήνας το πρωτόνιο διασπάται σε νετρόνιο, στον πυρήναποζιτρόνιο και σε νετρίνο που εκπέμπoνται το ποζιτρόνιο αλληλοεξουδετερώνεται αμοιβαία με ένα ελευθερο ηλεκτρόνιο Η πρακτικά ταυτόχρονη καταγραφή στους ανιχνευτές εντός συγκεκριμένου χρονικού πλαισίου ονομάζεται ανίχνευση από σύμπτωση. Θεωρείται ότι το γεγονός συμβαίνει κατά την ευθεία γραμμή μεταξύ των δύο ανιχνευτών ( γραμμή ανταπόκρισης, line of response, LOR). O χρόνος πλεύσης (time of flight, TOF) είναι μία νέα τεχνική στα καινούργια ΡΕΤ, που ενσωματώνει το χρόνο κατά τη διάρκεια της ανίχνευσης από σύμπτωση. Η ανίχνευση από σύμπτωση είναι η βασική αρχή της απεικόνισης του ΡΕΤ κατά την οποία ιδανικά μόνο τα φωτόνια που συμπίπτουν καταγράφονται τελικά, ενώ τα υπόλοιπα απορρίπτονται( Εικόνα 11). Τα φωτόνια χτυπούν πάνω στους ανιχνευτές και η ενέργεια τους μεταρέπεται σε φως, που πολλαπλασιάζεται μέσα από φωτοπολλαπλασιαστές και μετά μετατρέπεται σε ηλεκτρικό σήμα. Σε κάθε βήμα η ενέργεια που παράγεται (φως, ηλεκτρικό σήμα) είναι ανάλογη με 88
89 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία εκείνη που κατατέθηκε αρχικά από τα φωτόνια στους ανιχνευτές. Τα δεδομένα αποκτώνται σε μορφή λίστας ή σχεδιαγράμματος. Οι γραμμές ανταπόκρισης (LORs) αποθηκεύονται και διαμορφώνεται ένα ακατέργαστο ιστόγραμμα. H διόρθωση που γίνεται, λόγω χαμηλού σήματος, είναι η πιο σημαντική πηγή σφαλμάτων στην απεικόνιση με ΡΕΤ. Στους σαρωτές ΡET/CT, η διόρθωση επιτυγχάνεται μέσα από την εφαρμογή του CT. Τελικά, μέσα από την εφαρμογή μαθηματικών αλγορίθμων,οι τομογραφικές εικόνες ανακατασκεύαζονται και η βιοκατανομή του ιχνηθέτη οπτικοποιείται. Εικόνα 11. Ο τρόπος λειτουργίας της τομογραφίας εκπομπής ποζιτρονίων [Από Παρουσίαση:: Κλινικές ενδείξεις της ποζιτρονικής τομογραφίας (PET/CT), Σκούρα Ευαγγελία] Ισότοπο που εκπέμπει ποζιτρόνιο Σταθερό νουκλίδιο Το ποζιτρόνιο διασκορπίζεται στον ιστό χάνοντας ενέργεια Εξουδετέρωση φωτονίων με ενέργεια 511KeV Εξουδετέρωση φωτονίων με ενέργεια 511KeV Νετρίνο Διάφορες μέθοδοι ανοικοδόμησης έχουν χρησιμοποιηθεί. Στην περίπτωση του λεμφώματος Hodgkin,το ισότοπο που χορηγείται στον ασθενή ενδοφλεβίως, κατά τη διάρκεια της εξέτασης είναι η F-18 Fluorodeoxyglucose (FDG), ένα ανάλογο γλυκόζης που μεταφέρεται εντός των κυττάρων με τις πρωτείνες της κυτταρικής μεμβράνης, αλλά, αντίθετα με τη γλυκόζη, κατακρατείται ενδοκυτταρίως. To συγκεκριμένο ισότοπο έχει χρόνο ημίσειας ζωής 110 λεπτά. Εντός των κυττάρων η γλυκόζη φωσφορυλιώνεται μέσω εξοκινάσης. Στην F-18 89
90 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Fluorodeoxyglucose (FDG) η έλλειψη οξυγόνου στη θέση 2 εμποδίζει την περαιτέρω γλυκόλυση. Το φωσφορυλιωμένο μόριο παραμένει αδιάσπαστο και παγιδευμένο εντός του κυττάρου. Στα καρκινικά κύτταρα, η υψηλή συγκέντρωση F-18 Fluorodeoxyglucose (FDG) αντικατοπτρίζει αυξημένο μεταβολισμό της γλυκόζης. Βασική προϋπόθεση για τη λήψη σωστών πληροφοριών από το ΡΕΤ-scan είναι η αυξημένη πρόσληψη του ισοτόπου από τα λεμφωματικά κύτταρα (Εικόνες 12a,12b). Τα πλεονεκτήματα της PET/CT είναι πολλαπλά. Καταρχήν η διακριτική ικανότητα της μεθόδου είναι άκρως ικανοποιητική, καθώς μπορεί να ανιχνεύσει βλάβες με μέγεθος ακόμα και 4-6mm. Η διεξαγωγή της εξέτασης αφορά σε όλο το σώμα, με αποτέλεσμα ο ασθενής πάντα να υποβάλλεται σε ολόσωμη τομογραφική λήψη, από τη βάση του κρανίου εώς το μέσο των μηρών, πραγματοποιώντας με αυτό τον τρόπο πλήρη έλεγχο της νόσου του. Παράλληλα, ο χρόνος ημίσειας ζωής του F-18 είναι 110 min, ενώ ο μεταβολισμός της ουσίας και η απέκκριση της από το σώμα είναι ταχείς. Ένα επίσης σημαντικό γεγονός είναι ότι η διεξαγωγή της εξέτασης βασίζεται σε επισημασμένη γλυκόζη και όχι σε φαρμακευτικευτική ουσία που θα μπορούσε να προκαλέσει στον ασθενή ανεπιθύμητες ενέργειες. Επιπρόσθετα, η προετοιμασία της εξέτασης είναι εύκολη και απαιτεί σύντομη χρονική διάρκεια, καθώς ο ασθενής μετά την ενδοφλέβια χορήγηση του φαρμάκου, αναμένει μόλις μία ώρα πριν από τη διεξαγωγή της και οι λήψεις στις οποίες υποβάλλεται δεν ξεπερνούν τα min. Το μεγαλύτερο όμως πλεονέκτημα αυτής της μεθόδου είναι ότι το ΡΕΤ διαπιστώνει μεταβολικές αλλαγές, που προηγούνται των μορφολογικών. Στην περίπτωση δε του PET/CT, συνδυάζει τις μεταβολικές με τις μορφολογικές πληροφορίες. Εδώ χρειάζεται να σημειωθεί πως η πρόσληψη του FDG επηρεάζεται από μεγάλο αριθμό παραγόντων, οι κυριότεροι των οποίων είναι ο ιστολογικός τύπος, ο βαθμός επιθετικότητας του λεμφώματος, η βιωσιμότητα των κακοήθων κυττάρων, η παρουσία υποξίας και η τοπική αγγείωση, η οποία καθορίζει την μεταφορά του ισοτόπου στα λεμφωματικά κύτταρα[253]. Για τη διεξαγωγή του PET/CT συνηθέστερα χρησιμοποιείται το σύστημα Discovery ST PET/CT (GE Healthcare), που αποτελείται από ένα πλήρη σαρωτή γερμανικού βισμουθίου και ένα αξονικό τομογράφο 16 τομών. Οι ασθενείς που πρόκειται να υποβληθούν σε διαγνωστική 90
91 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία αυτή εξέταση παραμένουν νήστεις για τουλάχιστον 6 ώρες πριν την ενδοφλέβια χορήγηση της 18-FDG(~370-MBq). Η τομογραφία εκπομπής ποζιτρονίων λαμβάνει χώρα 60 λεπτά μετά την ενδοφλέβια χορήγηση 18-FDG.Kατά τη διάρκεια της αναμονής ο ασθενής αναπαύεται, δε μιλά, ούτε κάνει κινήσεις της κεφαλής. Η θερμοκρασία του περιβάλλοντος επίσης χρειάζεται να είναι ικανοποιητική για την αποφυγή του φαιού λίπους. Τα επίπεδα γλυκόζης στο αίμα πριν από την έγχυση του φαρμάκου, είναι απαραίτητο να είναι κάτω από 160mg/dl. Για τη διεξαγωγή της εξέτασης δε χρειάζεται η χορήγηση ενδοφλέβιου σκιαγραφικού. Πριν από την απεικόνιση, οι ασθενείς χρειάζεται να κενώσουν την κύστη και κατόπιν ακολουθεί η σάρωση από ένα υβριδικό FDG PET/CT σαρωτή. Εικόνα 12a. Η υβριδική-fusion τεχνική της ποζιτρονικής υπολογιστικής τομογραφίας,pet/ct [ AAndreou A, Kosmidis P, Gouliamos A. PET/CT in Lymphomas. Springer 2016] CT: δίνει ανατομικές λεπτομέρειες αλλα καθόλου μεταβολικές πληροφορίες ΡΕT: δίνει λειτουργικές πληροφορίες, αλλα είναι φτωχή σε ανατομικές λεπτομέρειες Συμπληρωματικές και όχι ανταγωνιστικές εξετάσεις 91
92 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Ακολουθεί η σάρωση της αξονικής τομογραφίας που εκτείνεται από τη βάση του κρανίου εώς τους εγγύς μηρούς. Αμέσως μετά την απόκτηση των εικόνων της αξονικής τομογραφίας, ακολουθεί η σάρωση με τομογραφία εκπομπής ποζιτρονίων, στις ίδιες ανατομικές θέσεις. Τα δεδομένα της αξονικής τομογραφίας χρησιμοποιούνται για τη διόρθωση εξασθένησης των εικόνων, για την ανασύσταση των οποίων χρησιμοποιείται ένας συμβατικός επαναληπτικός αλγόριθμος (OSEM). Οι υπερμεταβολικές βλάβες φαίνονται σαν ψευδώς χρωματικάκωδικοποιημένα εικονοστοχεία (pixels) ή ογκοστοιχεία (voxels) στη διαβαθμισμένη γκρι κλίμακα των εικόνων της αξονικής τομογραφίας. Στην εκτίμηση της εξέτασης υπάρχει η δυνατότητα της οπτικής ανάλυσης, αλλά και η δυνατότητα της ημιποσοτικής ανάλυσης, μέσω της μέτρησης του δείκτη SUV (Standardized uptake value, SUV). Εικόνα 12b.Η υβριδική-fusion τεχνική της ποζιτρονικής υπολογιστικής τομογραφίας, ΡΕΤ/CT. [Από: Κλινικές ενδείξεις της ποζιτρονικής τομογραφίας (PET/CT), Σκούρα Ευαγγελία] 92
93 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Οι τιμές πρόσληψης του ΡΕΤ/CT scan (Standardised Uptake Value-SUV) αντιπροσωπεύουν το λόγο της συγκέντρωσης του καρκινικού ιχνηθέτη, προς το μέσο όρο της συγκέντρωσης του ιχνηθέτη σε όλο το σώμα και χρησιμοποιούνται ως ημιποσοτική μέτρηση του βαθμού πρόσληψης του FDG προκειμένου να ερμηνευθεί η μέθοδος σάρωσης. Η τιμή του SUV υπολογίζεται από το συγκεκριμένο λογισμικό για κάθε μεταβολική περιοχή που εντοπίστηκε στην εξέταση. Όσον αφορά στην εκτίμηση του ΡΕΤ/CT για το HL, η εξέταση μπορεί να λάβει χώρα κατά την αρχική σταδιοποίηση, για τη μελέτη της έκτασης της νόσου, στην επανασταδιοποιήση της νόσου μετά το πέρας της αγωγής, αλλά και στην πρώιμη εκτίμηση του θεραπευτικού αποτελέσματος, για τη ενδεχόμενη τροποποίηση της θεραπείας, μέσω του interim PET. Οταν υπάρχει συμμετοχή λεμφαδένων στη νόσο, η ευαισθησία και η ειδικότητα του ΡΕΤ/CT είναι 94% και 100% αντίστοιχα. Στην περίπτωση που υπάρχει συμμετοχή και οργάνων, τότε η ευαισθησία και η ειδικότητα της μεθόδου είναι 88% και 100%, αντίστοιχα.σε αυτό το σημείο χρειάζεται να τονιστεί ότι συγκριτικά με τα επιθετικά non-hodgkin λεμφώματα, η μεταβολή στην πρόσληψη του FDG μετά από χημειοθεραπεία είναι σαφώς ταχύτερη στο HL[253]. Η αξιολόγηση της πρόσληψης της 18FDG γίνεται κατά κανόνα με ποιοτικά κριτήρια ιδίως στην αρχική διάγνωση. Παθολογική χαρακτηρίζεται οποιαδήποτε πρόσληψη παρατηρείται σε δομή που δεν υπάγεται στις γνωστές φυσιολογικές δομές. Υπάρχουν εντούτοις εργαστήρια που χρησιμοποιούν ποσοτικές παραμέτρους (κυρίως την SUV) ιδιαίτερα στις μεσοθεραπευτικές και μεταθεραπευτικές μελέτες. Από τη διεθνή βιβλιογραφία δεν προκύπτει εώς τώρα, σε καμμία περίπτωση ότι η ποσοτική αξιολόγηση υπερτερεί της ποιοτικής στο HL. Η θέσπιση εντούτοις ενιαίων αξιόπιστων κριτηρίων ερμηνείας των εικόνων PET/CT είναι σημαντική για τη σύγκριση των αποτελεσμάτων από διαφορετικά τμήματα και την αξιοπιστία των κλινικών δοκιμών. Έχει παρατηρηθεί ότι το 80% των ασθενών με HL παρουσιάζουν ακτινολογικά υπολειπόμενη μάζα μετά το πέρας της αρχικής θεραπείας. Από αυτούς το 10-20% αποδεικνύεται με βιοψία ότι έχει ενεργό νόσο. Επιπλέον έχει διαπιστωθεί ότι ασθενείς με ΡΕΤ (-) παρουσιάζουν ευνοϊκή πρόγνωση, σε αντίθεση με αυτούς που έχουν ΡΕΤ (+) και εμφανίζουν δυσμενέστερη πρόγνωση. 93
94 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Το 2007 δημοσιεύθηκαν για πρώτη φορά κριτήρια αξιολόγησης του μεταθεραπευτικού PET/CT βασισμένα στη συλλογική εμπειρία των μελών της διεθνούς επιτροπής που τα θέσπισε (International Harmonization Project - IHP) [254]. Τα κριτήρια αυτά είναι ποιοτικά, βασίζονται δηλαδή αποκλειστικά στην οπτική εκτίμηση της πρόσληψης (visual assessment). Για υπολειμματικές βλάβες μεγίστης διαμέτρου 2 cm,όπου κι αν αυτές εντοπίζονται, ως θετική αξιολογείται η πρόσληψη που υπερβαίνει αυτή των αγγειακών δομών του μεσοθωρακίου. Για βλάβες <2 cm ως θετική αξιολογείται η πρόσληψη που υπερβαίνει αυτή των περιβαλλόντων ιστών (background-bkg). Ειδικά κριτήρια προτάθηκαν επίσης για τις ηπατικές, σπληνικές και πνευμονικές βλάβες ως και την πρόσληψη από το μυελό των οστών. Παρά τη χρησιμότητα και αξιοπιστία των κριτηρίων αυτών για τις μελέτες μετά από την ολοκλήρωση της θεραπείας υπήρχαν περιορισμοί στη χρήση τους στις μεσοθεραπευτικές μελέτες. Στις μελέτες αυτές, ιδιαίτερα όταν πραγματοποιούνται στα πλαίσια κλινικών δοκιμών οπότε και στόχος είναι η εκτίμηση της πρώιμης ανταπόκρισης στη θεραπεία και η έγκαιρη τροποποίησή της σε μη ανταπόκριση, είναι προτιμότερο ως σημείο αναφοράς να χρησιμοποιείται ιστός με υψηλότερη πρόσληψη όπως π.χ. το ήπαρ. Το 2009 προτάθηκαν κατόπιν συναίνεσης στη Deauville της Γαλλίας κριτήρια για την αξιολόγηση της interim μελέτης και τα κριτήρια αυτά στη συνέχεια καθιερώθηκαν [255]. Σύμφωνα με αυτά πρέπει πάντα να προηγείται βασική μελέτη πριν από την έναρξη της θεραπείας που χρησιμεύει ως μελέτη αναφοράς. Στη συνέχεια η interim PET/CT αξιολογείται ποιοτικά με βάση μια 5-βάθμιο κλίμακα ανεξάρτητα από το μέγεθος της βλάβης (Πίνακας 10). Με βάση τα δεδομένα του 2009, ο ουδός θετικότητας τοποθετείται, ανάλογα με τη θεραπευτική τακτική που πρόκειται να ακολουθηθεί, στο score 2 ή 3 της κλίμακας. Έτσι αν ο θεραπευτικός στόχος είναι η αποκλιμάκωση της θεραπείας θετικές χαρακτηρίζονται οι μελέτες με score 2. Αν αντίθετα στόχος είναι η εντατικοποίηση της θεραπείας θετικές χαρακτηρίζονται οι μελέτες με score 3. Η θέσπιση της 5-βαθμίου αυτής κλίμακας παρουσιάζει δύο σημαντικά πλεονεκτήματα: 1) Η πρόσληψη αξιολογείται ανεξάρτητα από το μέγεθος της βλάβης και έτσι αποφεύγονται τα σφάλματα μέτρησης μικρών, κυρίως, βλαβών. 2) Κάθε εστία αξιολογείται και βαθμολογείται ανάλογα με την πρόσληψή της όσο μικρή και αν είναι αυτή. Παρά τις προσπάθειες προτυποποίησης της αξιολόγησης των ευρημάτων της 94
95 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία PET/CT και της θέσπισης ειδικών, διεθνώς αποδεκτών κριτηρίων, εξακολουθούν να υφίστανται προβλήματα αξιολόγησης ιδίως υπολειμματικών βλαβών με χαμηλή πρόσληψη. Στην εργασία των Zilstra et al. συγκρίθηκε η αξιολόγηση της PET/CT από 11 Πυρηνικούς Ιατρούς και έναν έμπειρο σε θέματα PET/CT Πυρηνικό Ιατρό. Υπήρχε 82%-94% συμφωνία όταν η μελέτη ήταν θετική αλλά μόνο 45% όταν ήταν αρνητική σύμφωνα με τον έμπειρο απεικονιστή. Οι μελετητές βρήκαν επίσης ότι όσο πιο έμπειρος είναι ο Πυρηνικός Ιατρός τόσο λιγότερα είναι τα ψευδώς θετικά ευρήματα.[256] Η ερώτηση που εύλογα προκύπτει είναι αν πρέπει μόνο έμπειροι Πυρηνικοί Ιατροί να γνωματεύουν τις PET/CT. Αυτό επιβάλλεται στις κλινικές μελέτες στα πλαίσια των οποίων τα αποτελέσματα των PET/CT αξιολογούνται τόσο στα κέντρα όπου αυτές εκτελούνται όσο και από μια κεντρική επιτροπή εμπειρογνωμόνων. Στις περιπτώσεις αυτές το ποσοστό ασύμφωνων ευρημάτων ανέρχεται σε 6% περίπου, όπως προκύπτει από τη διεθνή βιβλιογραφία, είναι δε ακόμη μικρότερο όταν υπάρχει βασική μελέτη.[257] Αν και είναι δύσκολο στην καθημερινή πράξη κάθε PET/CT μελέτη να αξιολογείται από κεντρική επιτροπή εμπειρογνωμόνων φαίνεται ότι η εμπειρία είναι απαραίτητη, σε αμφίβολες δε περιπτώσεις καλό είναι η τελική αξιολόγηση να γίνεται μετά από συναίνεση μεταξύ έμπειρων ιατρών. Η βασική μελέτη είναι απαραίτητη για την ελαχιστοποίηση των ψευδώς θετικών ευρημάτων. Πίνακας 10. Ποιοτική εκτίμηση της PET/CTσύμφωνα με την 5-βάθμιο κλίμακα της Deauville [NCCN Guidelines Version , Hodgkin Lymphoma] 1. Ουδεμία πρόσληψη 2. Πρόσληψη αυτής των αγγειακών δομών του μεσοθωρακίου 3. Πρόσληψη > των αγγειακών δομών του μεσοθωρακίου αλλά του ηπατικού παρεγχύματος 4. Ήπια αυξημένη πρόσληψη > ήπατος οπουδήποτε 5. Έντονα αυξημένη πρόσληψη > ήπατος οπουδήποτε ή/και νέες εστίες νόσου X. Πρόσληψη σε νέες περιοχές που δε σχετίζονται με το HD ΡΕΤ/CT κατά τη σταδιοποίηση του HL Η κλινική σταδιοποίηση του HL είναι καθοριστική για να προσδιορίσουμε τη θεραπευτική στρατηγική και πρόγνωση των ασθενών. Η φυσική εξέταση και η συλλογή πληροφοριών από 95
96 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή τις αξονικές τομογραφίες (CTs), τραχήλου, θώρακος, άνω και κάτω κοιλίας, σε συνδυασμό με την οστεομυελική ή άλλη βιοψία, όπου χρειάζεται, αποτελούν την κλασσική στρατηγική σταδιοποίησης των ασθενών με HL. Έχει βρεθεί ότι η μαγνητική τομογραφία δεν πλεονεκτεί έναντι της CT[258,259] ενώ το σπινθηρογράφημα με Γάλλιο(Ga -67 ) τείνει να εγκαταλειφθεί λόγω της μικρής ευαισθησίας του συγκριτικά με το ΡΕΤ-scan[260,120] Η ακριβής απεικόνιση αποτελεί ένα σημαντικό κριτήριο για τη σταδιοποίηση και κατ επέκταση για τον αρχικό σχεδιασμό της θεραπείας.στα πλαίσια της σταδιοποίησης, έχει βρεθεί ότι το PET-CT είναι ιδιαίτερα χρήσιμο στον εντοπισμό εξωλεμφαδενικών εστιών και οι διαθέσιμες έως σήμερα μελέτες δείχνουν πως αποτελεί ακριβέστερη μεθοδο για τη διάγνωση λεμφαδενικής και εξωλεμφαδενικής νόσου από ότι η CT. [261,262] Ωστόσο, εώς τώρα δεν έχει αποδειχθεί ότι το ΡΕΤ-CT σαν εξέταση είναι περισσότερο ευαίσθητη και ειδική σε σχέση με την τυφλή οστεομυελική βιοψία [263], αφού και η αντιδραστική υπερπλασία του μυελού μπορεί να δώσει θετική απεικόνιση [264]. Τα ανωτέρω δεδομένα επιβεβαιώνουν τη συχνή μεταβολή του σταδίου της νόσου σε ποσοστό 10-15% των ασθενών, μετά τη σταδιοποίηση με ΡΕΤ-scan [265]. Η μεταβολή του σταδίου της νόσου Hodgkin, μετά από χρήση του PET-CT δύναται να οδηγήσει και σε αλλαγή της θεραπευτικής προσέγγισης. Παρόλα αυτά είναι άγνωστο, προς το παρόν αν αυτή η τροποποίηση της θεραπείας βασισμένη στο ΡΕΤ- scan θα οδηγήσει και σε βελτίωση της επιβίωσης. Το ερώτημα αυτό ερευνάται με τρέχουσες τυχαιοποιημένες μελέτες. Αφενός, στο σημείο αυτό χρειάζεται να σημειωθεί ότι, οι μέχρι σήμερα μελέτες σχετικά με την αξία του ΡΕΤ-scan στη σταδιοποίηση του HL, παρουσιάζουν μεθοδολογικά προβλήματα. Ως κυριότερο μειονέκτημα παρουσιάζεται η απουσία μιας αξιόπιστης δοκιμασίας επαλήθευσης των ευρημάτων του PET-CT. Η λήψη διαγνωστικών βιοψιών από όλες τις υποπτες περιοχές θα μπορούσε να αποτελέσει μέθοδο επiβεβαίωσης, αυτό όμως δεν είναι εφικτό να δρομολογηθεί σε όλες τις ύποπτες περιοχές. 96
97 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Αφετέρου, είναι γεγονός ότι η σταδιοποίηση με PET-CT συμβάλλει ουσιαστικά και στο σχεδιασμό της ακτινοθεραπείας. Με τη βοήθεια των πληροφοριών που συλλέγονται από το ΡΕΤ-CT, η ακτινοθεραπεία στα πρώιμα στάδια του HL, χορηγείται στις μέρες μας, μόνο στις περιοχές που είναι διηθημένες στο PET, όπως αυτές ορίζονται μακροσκοπικά και προ χημειοθεραπείας. Όσον αφορά στα όψιμα στάδια της νόσου, η ακτινοθεραπεία με τη βοήθεια του ΡΕΤ εστιάζεται στις υπολειμματικές μάζες. Με τον τρόπο αυτό, έχουν εγκαταληφθεί πλέον τα εκτεταμένα πεδία ακτινοβόλησης, ως θεραπεία. Η σαφώς λεπτομερέστερη σταδιοποίηση της νόσου με το ΡΕΤ/CT ήταν επόμενο να δώσει προβάδισμα, έναντι της CT, στο σχεδιασμό της επικουρικής/περιοχικής ακτινοθεραπείας μετά τη χημειοθεραπεία. Από τη μία μεριά, έχει βρεθεί ότι στα πρώιμα στάδια του HL, εώς και το 75% των λεμφωματικών μαζών που απεικονίζονται στη CT, μπορεί να είναι αρνητικές στο PET/CT. Από την άλλη, θα πρέπει βέβαια να λαμβάνεται υπ όψιν ότι μια αρνητική PET/CT δεν αποκλείει την παρουσία μικροσκοπικής νόσου, καθώς είναι πεπερασμένες οι δυνατότητες του σπινθηρογράφου, που αδυνατεί να ανιχνεύσει βλάβες <5-10mm.Αυτό το γεγονός, ενέχει τον κίνδυνο της αστοχίας της ακτινοθεραπείας λόγω πιθανής απώλειας των μικροσκοπικών διηθήσεων που δεν απεικονίζονται στην εξέταση του ΡΕΤ-CT. Για το λόγο αυτό, παρόλο που ενθαρρυνεται η χρήση ΡΕΤ/CT στη σταδιοποίηση του HL προκειμένου να διευκολυνθεί η ερμηνεία αμφιλεγόμενων αποτελεσμάτων μετά τη θεραπεία πρώτης γραμμής, μέχρι τώρα δεν αποτελεί κατευθυντήρια οδηγία [255,266] και ο τελικός σχεδιασμός της πρώτης γραμμής θεραπείας θα πρέπει να λαμβάνει υπόψη όλες τις διαθέσιμες μεθόδους σταδιοποίησης[220] ΡΕΤ/CT για την εκτίμηση της απάντησης στη θεραπεία HL. Η απάντηση ενός όγκου στη χημειοθεραπεία χρησιμεύει σαν υποκατάστατο για την εκτίμηση άλλων παραμέτρων, όπως το ελεύθερο νόσου και το ολικό διάστημα επιβίωσης, ενώ αποτελεί και το γνώμονα σχεδιασμού των περαιτέρω θεραπευτικών αποφάσεων. Ωστόσο, η επανασταδιοποίηση του HL μετά το πέρας της θεραπείας εμποδίζεται από την αδυναμία της CT και λιγότερο του σπινθηρογραφήματος με Γάλλιο να χαρακτηρίσει σωστά τις υπολειμματικές μάζες, οι οποίες αποτελούν μείζον διαφοροδιαγνωστικό πρόβλημα που 97
98 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή το 1999 οδήγησε στη δημιουργία της ξεχωριστής κατηγορίας «πλήρης ύφεση μη επιβεβαιωμένη» (CRu) στα κριτήρια απάντησης των λεμφωμάτων στη χημειοθεραπεία [266]. Επισημαίνεται πως ακόμη και η συχνά δυσχερής βιοψία των ύποπτων περιοχών θα μπορούσε να δώσει υψηλό ποσοστό ψευδώς αρνητικών αποτελεσμάτων καθώς οι υπολειμματικές μάζες αποτελούνται συνήθως από μίγμα ινώδους ιστού και κακοήθων κυττάρων. Τα ενθαρρυντικά έως τώρα αποτελέσματα του ΡΕΤ/CT συνοψίσθηκαν σε δύο μετααναλύσεις[267,268] και μία συστηματική ανασκόπηση [269] των κυριότερων μελετών πάνω στην αξία του ΡΕΤ/CT στην εξακρίβωση υπολειμματικής νόσου μετά την ολοκλήρωση της χημειοθεραπείας πρώτης γραμμής. Αν και η μεθοδολογία και ο σχεδιασμός των περισσότερων μελετών ήταν πτωχής ποιότητας, καθώς η ετερογένεια αναφορικά με τα υπό μελέτη νοσήματα, τον ιστολογικό υπότυπο, το χημειοθεραπευτικό σχήμα και τον χρόνο εκτέλεσης του ΡΕΤ-scan ήταν ευρύτατα, το ΡΕΤ/CT παρουσίαζε σαφή υπεροχή έναντι της CT και του σπινθηρογραφήματος με Γάλλιο όσον αφορά τόσο την αρνητική, όσο και την θετική προγνωστική αξία. Φαίνεται λοιπόν πως το ΡΕΤ/CT μπορεί να ανιχνεύσει έγκαιρα τους ασθενείς που θα ωφεληθούν από περαιτέρω εντατικοποίηση της χημειοθεραπείας, γι αυτό, αν και σχετικά πρώιμα, ενσωματώθηκε στα πρόσφατα αναθεωρημένα κριτήρια της απάντησης των λεμφωμάτων στη χημειοθεραπεία [265,270]. Ωστόσο, το ΡΕΤ/CT δεν μπορεί επί του παρόντος να ανιχνεύσει την παρουσία μοριακής νόσου πιθανώς στο 15% των ασθενών, αριθμός που αντιπροσωπεύει τα ψευδώς αρνητικά αποτελέσματα του ΡΕΤ/CT[271,272]. Βάσει των παραπάνω, προτείνεται η εκτέλεση ΡΕΤ/CT σε όλους τους ασθενείς με HL μετά το πέρας της θεραπείας πρώτης γραμμής. Ο χρόνος διατέλεσης του ΡΕΤ/CT πρέπει να είναι τουλάχιστον 3 εβδομάδες μετά το πέρας της χημειοθεραπείας και μετά από 8-12 εβδομάδες αν έχει προηγηθεί ακτινοθεραπεία, προκειμένου να ελαχιστοποιηθεί η πιθανότητα ψευδώς θετικών αποτελεσμάτων [254]. Το αρνητικό ΡΕΤ/CT επιτρέπει την περαιτέρω παρακολούθηση ασθενών, ενώ το θετικό πρέπει κατά κανόνα να επιβεβαιώνεται με βιοψία της ύποπτης περιοχής εξαιτίας της 98
99 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία χαμηλής θετικής προγνωστικής αξίας. Εναλλακτικά, η επανάληψη του ΡΕΤ/CT μετά από 6-8 εβδομάδες αποτελεί μια λογική προσέγγιση, ανάλογα βέβαια με το επίπεδο κλινικής υποψίας [253]. Μία ακόμη πρόοδος στη θεραπεία του HL, που πιθανώς θα προέρθει από τη χρήση του ΡΕΤ/CT, είναι η καθοδήγηση της θεραπευτικής απόφασης για συμπληρωματική/περιοχική ακτινοθεραπεία. Με την εξαίρεση της εξωλεμφαδενικής προσβολής, που θα πρέπει να ακτινοβολείται ανεξαρτήτως του αποτελέσματος του ΡΕΤ/CT, φαίνεται πως το ΡΕΤ/CT έχει μεγάλη ικανότητα διάκρισης υπολειμματικής νόσου μετά τη χημειοθεραπεία [273]. Ωστόσο, αν και η αρνητική προγνωστική αξία του ΡΕΤ/CT είναι και σ αυτή τη περίπτωση υψηλότερη από το 85% [274], η παράλειψη της ακτινοθεραπείας βάσει μόνο ενός αρνητικού ΡΕΤ/CT δεν μπορεί να προταθεί ακόμη, λόγω ανεπαρκών κλινικών μελετών αλλά και ασυμφωνίας στον ορισμό της «ογκώδους» νόσου μεταξύ των διάφορων ερευνητικών ομάδων ΡΕΤ/CT για την πρώïμη εκτίμηση της απάντησης και τροποποίηση της θεραπείας του HL Μολονότι το κλινικό στάδιο και οι προγνωστικοί παράγοντες καθορίζουν την αρχική θεραπευτική στρατηγική, o καθοριστικός παράγοντας για την πρόγνωση της νόσου είναι η ανταπόκριση στη θεραπεία. Οι συμβατικές μέθοδοι για την εκτίμηση της ανταπόκρισης είναι η μορφολογία και ο βαθμός μείωσης της μετρητής νόσου στην CT. Εν τούτοις η μείωση των διαστάσεων της νόσου δεν είναι απαραίτητα αξιόπιστο κριτήριο ανταπόκρισης, καθώς τα νεοπλασματικά κύτταρα αποτελούν μόνο ένα μικρό ποσοστό του νεοπλασματικού όγκου, και τα κύτταρα του αντιδραστικού μικροπεριβάλλοντος επικρατούν στο HL. Είναι άλλωστε γνωστό ότι περίπου το 80% των ασθενών μετά την ολοκλήρωση της θεραπείας εμφανίζουν υπολειμματικές εστίες παθολογικών διαστάσεων, αλλά μόνον το 20% των ασθενών αυτών θα εμφανίσει υποτροπή της νόσου.[275] Στον αντίποδα, ένα 10-15% των ασθενών με εμφανή πλήρη ύφεση (ΠΥ) σε CT επίσης εμφανίζουν υποτροπή της νόσου.η διεξαγωγή ΡΕΤ/CT στο μεσοδιάστημα της θεραπείας πρώτης γραμμής και συνήθως μετά τα 2 πρώτα σχήματα (ABVD και BEACOPPesc), αποτελεί σήμερα το μείζον ερώτημα σχετικά με τη θεραπεία του HL. Η πρώιμη πρόβλεψη για την πορεία της νόσου βάσει των ευρημάτων του ΡΕΤ/CT θα μπορούσε 99
100 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή να ανιχνεύσει έγκαιρα τους ασθενείς με πτωχή απάντηση, που χρήζουν πρώïμη εντατικοποίηση της θεραπείας, αλλά και να περιορίσει την επιζήμια επιπλέον χημειοθεραπεία στους ταχείς απαντητές. Ακόμη, ασθενείς με βραδεία απάντηση αλλά με αρνητικό ΡΕΤ/CT στο πέρας της θεραπείας ίσως φέρουν επιθετικότερους κλώνους και ως εκ τούτου χρήζουν τακτικότερης παρακολούθησης. Αξίζει να σημειωθεί πως οι εφαρμογές του ΡΕΤ/CT στην πρόγνωση του HL έχουν βιολογική σημασία, καθώς οι μεταβολές στη λήψη του FDG αντικατοπτρίζουν την κινητική μείωσης του όγκου, αν και αυτό προϋποθέτει συγκεκριμένο αριθμό παραδοχών, όπως την λογαριθμική μείωση του κακοήθους φορτίου, την απουσία ανθεκτικών κλώνων και τη σταθερή αντιστοιχία πρόσληψης FDG και αριθμού καρκινικών κυττάρων[253]. Πέρα όμως από τα παραπάνω άλλοι δύο λόγοι προβληματίζουν στην αποδοχή της ένδειξης του ΡΕΤ/CT ενδιάμεσα της θεραπείας πρώτης γραμμής. Πρώτον, η τροποποίηση της θεραπευτικής στρατηγικής αναλόγως των ευρημάτων του ΡΕΤ/CT προϋποθέτει την ύπαρξη αποτελεσματικής εναλλακτικής θεραπείας, αλλά, επί του παρόντος, δεν υπάρχουν προοπτικές μελέτες που να καταδεικνύουν σαφές κλινικό όφελος από την πρώιμη επανασταδιοποίηση με ΡΕΤ/CT. Δεύτερον, η παροδική τοπική φλεγμονή μετά από χημειοθεραπεία [276], που είναι ιδιαίτερα χαρακτηριστική στο HL και σε συνδυασμό με τη πυκνή συχνότητα (ανά 15μερο) του χημειοθεραπευτικού σχήματος, δίνει αυξημένα ποσοστά ψευδώς θετικών ευρημάτων. Πέρα όλων αυτών, οι τρέχουσες μελέτες εμφανίζουν αδυναμία συμφωνίας σε πολλά θέματα μεθοδολογίας, αφού οι περισσότερες είναι αναδρομικές, συμπεριλαμβάνουν και ασθενείς με μη Hodgkin λέμφωμα και παρουσιάζουν ανομοιομορφία όσον αφορά την αγωγή, τις μεθόδους εκτίμησης και το στάδιο της νόσου [253,221]. Παρά τους παραπάνω περιορισμούς, το 80% περίπου των ασθενών με HL θα αρνητικοποιήσει το ΡΕΤ/CT μετά τα πρώτα 2 ABVD και φαίνεται πως αυτοί οι ασθενείς έχουν σημαντικά καλύτερη πρόγνωση από αυτούς με θετικά ευρήματα, με 95% πιθανότητα διετούς επιβίωσης ελεύθερης εξέλιξης νόσου (Progression Free Survival; PFS) [277].Το αρνητικό PET/CT μετά το πέρας της ΧΜΘ εξασφαλίζει άριστη, βραχυχρόνια τουλάχιστον, πρόγνωση με πιθανότητα υποτροπής <5% σε βάθος 2-3 ετών [ ] Αντίθετα το θετικό PET/CT μετά το πέρας της ΧΜΘ συνδυάζεται με σαφώς αυξημένη πιθανότητα υποτροπής που 100
101 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία πιθανώς υπερβαίνει το 50%, ακόμη και όταν ακολουθεί ακτινοθεραπεία, ενώ η διετής PFS δεν υπερβαίνει το 12.8% [279,280]. Είναι γεγονός λοιπόν, ότι το interim PET/CT αποτελεί ανεξαρτητο προγνωστικό παράγοντα για το HL. Η εμμενουσα πρόσληψη ραδιοφαρμάκου, προμηνύει φτωχή πρόγνωση και προβλέπει την υποτροπή σε ποσοστό 27%, σε αντίθεση με την περίπτωση που το ΡΕΤ είναι αρνητικό, οπότε τότε η πιθανότητα υποτροπής είναι μόλις 2.3% [281]. Με βάση τα προαναφερθέντα και με πιο πρόσφατα δεδομένα που δημοσιεύτηκαν το 2014 από τους Barrington et al, η ουδός θετικότητας τοποθετείται πλέον, ανάλογα με τη θεραπευτική επιλογή που θα ακολουθηθεί, στο score 3 ή 4 της κλίμακας Deauville. Τα ΡΕΤ score 1 και 2 αντιπροσωπεύουν την πλήρη μεταβολική ανταπόκριση (Complete Metabolic Response-CMR). Το PET score 3 επίσης αντιπροσωπεύει CMR στο interim PET και συνδέεται με καλή πρόγνωση στην ολοκλήρωση της προγραμματισμένης θεραπείας. Ωστόσο σε μελέτες που ερευνούν την αποκλιμάκωση της θεραπείας και βασίζονται στην ανταπόκριση στο ΡΕΤ, είναι προτιμότερο το score 3 να θεωρηθεί ως ανεπαρκής ανταπόκριση, ώστε να αποφευχθεί η υποθεραπεία [282]. Παράλληλα, σύμφωνα με τους Barrignton et al, η ενταντικοποίηση μίας θεραπείας ενδείκνυται όταν το ΡΕΤ score είναι >4. Ο ορισμός της πλήρους ύφεσης της νόσου έχει πλέον τροποποιηθεί, ώστε να απαιτεί αρνητικοποίηση του PET/CT ανεξάρτητα από την τυχόν παρουσία μετρητής υπολειμματικής βλάβης/βλαβών[283]. Επομένως, τίθεται το ερώτημα αν μπορούμε να προσαρμόσουμε τη θεραπεία ανάλογα με το αποτέλεσμα της πρώιμης εξέτασης με PET με στόχο τη μείωση της, στους ασθενείς με αρνητική PET και την εντατικοποίησή της σε ασθενείς με θετική PET, και απώτερο στόχο τη βελτίωση της επιβίωσης. Το γεγονός ότι περισσότεροι ασθενείς με πρώιμου σταδίου νόσο πεθαίνουν από απώτερες επιπλοκές της θεραπείας παρά από τη νόσο αυτή καθ εαυτή υποδηλώνει ότι ένας σημαντικός αριθμός ασθενών υπερθεραπεύονται,[209] και γίνεται πιο επιτακτική η ανάγκη να δοθούν απαντήσεις στα ερωτήματα αυτά. Ορισμένες μεγάλες προοπτικές τυχαιοποιημένες μελέτες σε ασθενείς με πρώιμου σταδίου νόσο εξετάζουν το ρόλο της θεραπείας που είναι προσαρμοσμένη στο αποτέλεσμα της πρώιμης PET/CT (Πίνακας 10), και ορισμένες από αυτές στοχεύουν την απάλειψη της ακτινοβολίας σε ασθενείς που είναι PET/ CT (-). 101
102 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Πίνακας 10. Τρέχουσες μελέτες με θεραπεία προσαρμοσμένη στην πρώιμη ΡΕΤανταπόκριση σε ασθενείς με πρώιμου σταδίου λέμφωμα Hodgkin Μελέτη Προέλευση Παράγοντες κινδύνου Χρόνος εκτέλεσης ΡΕΤ RAPID UK NCRI Μη ογκώδης Μετά 3xABVD Θεραπεία ΡΕΤ (-) Τυχαιοποίηση σε IFRT vs όχι άλλη θεραπεία ΡΕΤ(+) Ολοκλήρωση συνολικά 4xABVD+IFRT HD16 GHSG Μόνο ευνοϊκού κινδύνου Μετά 3xABVD H10 EORTC, Ανεξαρτήτως Μετά GELA IIL κινδύνου 2xABVD (ακόμη και ογκώδης) CALGB Μη ογκώδης Μετά 2xABVD CALGB Ογκώδης Μετά 2xABVD Συμβατικό σκέλος: 30Gy INRT ανεξαρτήτως αποτελέσματος ΡΕΤ Πειραματικό σκέλος: ΡΕΤ (-) Όχι άλλη θεραπεία ΡΕΤ (+) 30Gy INRT Συμβατικό σκέλος: 30Gy INRT ανεξαρτήτως αποτελέσματος ΡΕΤ Πειραματικό σκέλος: ΡΕΤ (-) συμπλήρωση 2 ή 4 ABVD αλλά όχι RT PET(+) 2 BEACOPPesc+ 30 Gy IFRT PET (-) Συνολικά 4x ABVD PET (+) 6x BEACOPPesc PET(-) Συμπλήρωση 4x ABVD PET(+) 4x BEACOPPesc+RT Μολονότι η ακτινοβόληση μετατρέπει το PET/CT σε αρνητικό σε μια αναλογία ασθενών, σε μια ακόμη μεγαλύτερη αναλογία το αποτέλεσμα παραμένει θετικό σε άλλες ή και τις ίδιες ανατομικές θέσεις κατά την επανεξέταση μετά την ακτινοβόληση. Συνήθη τακτική αποτελεί η χορήγηση 30 Gy IFRT με αύξηση σε θεραπευτική δόση (~40 Gy) στις περιοχές με θετικό PET. Το κατά πόσον η υιοθέτηση επιθετικότερης στρατηγικής με ΧΜΘ διάσωσης και αυτόλογη 102
103 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία μεταμόσχευση (μετά από ιστολογική τεκμηρίωση της εμμένουσας νόσου) υπερέχει συνολικά της ακτινοθεραπείας μένει να διερευνηθεί. Στα προχωρημένα στάδια της νόσου το θετικό ενδιάμεσο PET/CT μετά από 2 κύκλους ΧΜΘ αποτελεί δυσμενέστατο προγνωστικό παράγοντα [ ]. Κάτι ανάλογο πιθανώς ισχύει και για τα περιορισμένα στάδια με δυσμενείς προγνωστικούς παράγοντες δεν είναι όμως σαφές και για τους καλύτερης πρόγνωσης ασθενείς [286]. Οι περισσότερες από τις τρέχουσες τυχαιοποιημένες μελέτες που αφορούν τα περιορισμένα στάδια της νόσου εξετάζουν τη δυνατότητα παράληψης της ακτινοθεραπείας ή/και ελάττωσης της ΧΜΘ επί αρνητικού PET- Scan μετά από 2-3 κύκλους ABVD. Αντίθετα, επί θετικού PET/CT, δοκιμάζεται η διατήρηση της ακτινοθεραπείας με αύξηση ή εντατικοποίηση της ΧΜΘ (Πίνακας 11). Πίνακας 11. Τρέχουσες τυχαιοποιημένες μελέτες της GHSG και του EORTC για τους ασθενείς με λέμφωμα Hodgkin. [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. Σκέλος Καθιερωμένης Θεραπείας Ερευνητικό Σκέλος HD16, GHSG, Αρχικά Στάδια PET-Scan μετά ABVDx2 ABVDx2 + IFRT 30 Gy ABVDx2 χωρίς ΑΘ, επί PET (-) ABVDx2 + IFRT 30 Gy, επί PET(+) HD17, GHSG, Ενδιάμεσα Στάδια ABVDx4 + INRT 30 Gy ABVDx4 + IFRT 30 Gy EA50COPP-14 x 2+ ABVDx2 + IFRT 30 Gy EA50COPP-14 x 2+ ABVDx2 + INRT 30 Gy H10F, EORTC, Αρχικά Στάδια PET-Scan μετά ABVDx2 ABVDx3 + ΑΘ-ΠΛ 30 Gy ABVDx4 χωρίς ΑΘ, επί PET (-) ABVDx2 + BEACOPP-escx2 + INRT 30 Gy, επί PET(+) H10U, EORTC, Ενδιάμεσα Στάδια PET-Scan μετά ABVDx2 ABVDx4 + ΑΘ-ΠΛ 30 Gy ABVDx6 χωρίς ΑΘ, επί PET (-) ABVDx2 + BEACOPP-escx2 + INRT 30 Gy, επί PET(+) UK RAPID Trial, Στάδια ΙΑ/ΙΙΑ άνωθεν του διαφράγματος PET-Scan μετά ABVDx3 ABVDx3 + IFRT 30 Gy, επί PET(-) ABVDx3 χωρίς ΑΘ, επί PET(-) ABVDx4 + IFRT 30 Gy, επί PET(+) IFRT: Ακτινοθεραπεία Προσβεβλημένου Πεδίου (Involved Field Radiotherapy) INRT: Ακτινοθεραπεία Προσβεβλημένων Λεμφαδένων ( Involved Node Radiotherapy) 103
104 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Όσον αφορά στους ασθενείς προχωρημένου σταδίου, έχει παρατηρηθεί ότι η θετική προβλεπτική αξία της πρώιμης PET/CT είναι χαμηλότερη σε ασθενείς που έχουν αντιμετωπιστεί με τον επιθετικότερο συνδυασμό BEACOPPesc σε σύγκριση με τον συνδυασμό ABVD.[287] Είναι σαφές ότι ασθενείς με σταθερά θετική PET/CT μετά από 2-3 κύκλους θεραπείας έχουν μεγαλύτερη πιθανότητα αστοχίας της θεραπείας από ασθενείς με αρνητική PET, αλλά είναι επίσης σαφές ότι ένα σημαντικό ποσοστό ασθενών μπορούν να ιαθούν με συνέχιση της αρχικής θεραπείας παρά τη θετική PET, υποδηλώνοντας ότι τρεχόντως δεν είναι ενδεδειγμένη η αλλαγή σε πιο επιθετική θεραπεία. Μέχρι να ολοκληρωθούν προοπτικές τυχαιοποιημένες κλινικές που εξετάζουν τα ερωτήματα αυτά (Πίνακας 12), δε συνιστάται η μεταβολή της θεραπείας, καθώς οι ασθενείς μπορεί να εκτεθούν σε αδικαιολόγητο κίνδυνο αυξημένης πρώιμης και όψιμης τοξικότητας χωρίς να είναι βέβαιο ότι θα βελτιωθεί η έκβασή τους. 104
105 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Πίνακας 12. Τρέχουσες μελέτες με θεραπεία προσαρμοσμένη στην πρώιμη ΡΕΤ-ανταπόκριση σε ασθενείς με προχωρημένου σταδίου λέμφωμα Hodgkin. [Από HAEMA, Ιούλ-Σεπτ 2012, τόμος 3, τεύχος 3]. Mελέτη Προέλευση Προβλεπόμενος αρ. ασθενών Χρόνος εκτέλεσης ΡΕΤ HD18 GHSG 1500 Μετά 2xBEACOPPesc Θεραπεία ΡΕΤ(-) Τυχαιοποίηση σε 2vs 6 επιπλέον κύκλους ( όχι IFRT) PET(+) Τυχαιοποίηση σε 6BEACOPPesc με vs χωρίς Rituximab:Με το πέρας της θεραπεάς σε ΡΕT(+) υπολειμματικές εστίες>2.5cm HD06607 GITL 450 Μετά 2xABVD PET (-) Ολοκλήρωση ABVD. Aν ΡΕΤ(-) IFRT Τυχαιοποίηση σε IFRT vs όχι RT PET (+) τυχαιοποίηση σε BEACOPPesc ± Rituximab RATHL UK NCRI 1200 Μετά 2xABVD PET (-) τυχαιοποίηση σε 4 ABVD vs 4x AVD (όχι IFRT) PET (+) 6 BEACOPP14 ή BEACOPPesc HD0801 IIL 300 Μετά 2xABVD PET (-) ολοκλήρωση ABVD. Αν PET (-) τυχαιοποίηση σε ΙFRT vs όχι IFRT PET (+) μεγαθεραπεία και αυτόλογη ΜΑΚ S0816 SWOG 230 Μετά 2xABVD PET (-) συνολικά 4 ABVD PET (+) 6 BEACOPPesc Το ΡΕΤ/CT στην παρακολούθηση του HL Από τους ασθενείς με HL που επιτυγχάνουν ΠΥ μετά το πέρας της θεραπείας, μόνον 20% θα εμφανίσει υποτροπή της νόσου και ο κίνδυνος αυτός κατανέμεται σε μια περίοδο παρακολούθησης 5-10 ετών, με τον κίνδυνο στα πρώτα έτη να μην ξεπερνά το 5% κατ έτος. 105
106 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Για ασθενείς που παρακολουθούνται συστηματικά με CT μετά το πέρας της θεραπείας, το 75% των υποτροπών της νόσου ανιχνεύονται από τους ίδιους τους ασθενείς στα μεσοδιαστήματα μεταξύ των προγραμματισμένων ελέγχων της νόσου.[287] Αρκετές μελέτες διερεύνησαν την αξία του ΡΕΤ/CT στην παρακολούθηση των ασθενών με HL, με σκοπό την πρώιμη διάγνωση πιθανής υποτροπής της νόσου, υποδεικνύοντας την ισχυρή προβλεπτική αξία του PET/CT για την PFS και τη συνολική επιβίωση ασθενών με ή χωρίς υπολειμματική νόσο[267,268]. Οι αναδρομικές μελέτες που ακολούθησαν επιβεβαιώνουν την υπεροχή των νέων κριτηρίων ανταπόκρισης στο HL σε σύγκριση με τα προηγούμενα κριτήρια που βασίζονταν μόνο στη μορφολογική απεικόνιση.[288] Απαιτείται βέβαια μακρότερης διάρκειας παρακολούθηση των ασθενών και μεγαλύτερος αριθμός μελετών για να επιβεβαιωθούν και στην κλινική πράξη τα νέα αυτά κριτήρια ανταπόκρισης. Μία μελέτη σε 36 ασθενείς έδειξε πως το ΡΕΤ-scan ανίχνευσε την υποτροπή πριν την έναρξη συμπτωμάτων σε 3 περιπτώσεις, αλλά έδωσε ψευδώς θετικά αποτελέσματα σε άλλες 6, οι οποίες όμως αποδείχθηκαν αρνητικές κατά την επανάληψη του ΡΕΤ/CT[289]. Εξάλλου, δεν έχει καταδειχθεί βελτίωση της επιβίωσης μέσω της πρώιμης απεικονιστικής ανίχνευσης της υποτροπής, ενώ στο 80% των περιπτώσεων ο ασθενής ή/και ο γιατρός ανευρίσκει πρώτος την υποτροπή, ακόμη και αν έχει προηγηθεί CT έλεγχος [290]. Έτσι, προς το παρόν δεν συνιστάται η παρακολούθηση με ΡΕΤ-scan καθώς χρειάζονται προοπτικές μελέτες που να αποδεικνύουν το κλινικό όφελος ενός τέτοιου χειρισμού, οι οποίες θα είναι προτιμότερο να διενεργούνται με ΡΕΤ/CT, λόγω της σημαντικά μικρότερης συχνότητας ψευδώς θετικών ευρημάτων με την τελευταία μέθοδο [250,251] PET/CT πριν από τη μεγαθεραπεία και αυτόλογη μεταμόσχευση στο HL Παρά τα υψηλά ποσοστά ίασης με 1ης γραμμής θεραπεία στο HL, περίπου το 25% των ασθενών εμφανίζουν νόσο που είναι ανθεκτική στην αρχική θεραπεία ή υποτροπή αυτής. Οι ασθενείς αυτοί αντιμετωπίζονται με δεύτερης γραμμής θεραπεία διάσωσης και για τους ασθενείς με χημειοευαίσθητη νόσο η εδραίωση με μεγαθεραπεία και αυτόλογη μεταμόσχευση αιμοποιητικών κυττάρων αποτελεί τη θεραπεία εκλογής. Μελέτες έχουν υποδεξει ότι το αποτέλεσμα της PET/CT πριν τη μεταμόσχευση έχει προβλεπτική αξία για την 106
107 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία έκβαση των ασθενών. Για το HL οι μελέτες υποδεικνύουν ότι ασθενείς με θετική PET πριν τη μεταμόσχευση έχουν PFS 30-40% ενώ ασθενείς με αρνητική PET 70%-80% PFS στα 2-5 έτη. [170,291,292] Εντούτοις, ένα σημαντικό ποσοστό των PET (+) ασθενών παραμένει ελεύθερο νόσου μετά τη μεγαθεραπεία και επομένως η θετική PET δεν αποτελεί αιτία για να μην προσφερθεί η μεγαθεραπεία στους ασθενείς αυτούς Περιορισμοί-παγίδες στη χρήση του ΡΕΤ-scan Ο ορισμός του «θετικού» και «αρνητικού» ΡΕΤ-scan παρουσιάζει εγγενείς δυσκολίες αφού η πρόσληψη του FDG από τις περιοχές μεταβολικής δραστηριότητας αποτελεί μια συνεχή μεταβλητή. Ιδίως στην περίπτωση του HL, η μεγάλη ετερογένεια των κλινικών μελετών αναφορικά με τον ορισμό των θετικών ΡΕΤ-scan οδήγησε στη δημοσίευση κοινών αναθεωρημένων κριτηρίων ορισμού της θετικότητας των υπολειμματικών μαζών μετά από χημειοθεραπεία, συνδυάζοντας τη δομική απεικόνιση με το ΡΕΤ-/CT[254]. Διάφορες αιτίες άσχετες με τον όγκο μπορούν να προκαλέσουν αυξημένη πρόσληψη του FDG, παρουσιάζοντας ψευδώς θετικές εικόνες. Τέτοιες περιπτώσεις είναι οι φλεγμονές, oι κοκκιωματώδεις νόσοι και οι λοιμώξεις. Αυτή η εικόνα οφείλεται στην αυξημένη πρόσληψη ραδιοφαρμάκου από τα κύτταρα που συμμετέχουν στη φλεγμονώδη διεργασία (λευκά αιμοσφαίρια, μονοκύτταρα, μακροφάγα κτλ) [293,294]. Οι ασθενείς με λεμφώματα είναι επιρρεπείς σε λοιμώξεις και φλεγμονές λόγω της ανοσοκαταστολής που προκαλείται τόσο από τη νόσο όσο και από την εφαρμοζόμενη χημειοθεραπεία. Η διάκριση μεταξύ καλοήθους εξεργασίας και μεταβολικά ενεργού νόσου είναι συχνά αδύνατη στις περιπτώσεις αυτές. Σημαντική βοήθεια σε τέτοια περίπτωση μπορεί να προσφέρει το λεπτομερές ιστορικό, η αλλαγή της κατανομής των παθολογικών εστιών με την εμφάνιση νέων σε περιοχές που δεν είχαν αρχικά νόσο (ειδικά στα HL) καθώς και οι καθυστερημένες λήψεις (120 min) στις οποίες η πρόσληψη από τις καλοήθεις βλάβες μειώνεται ενώ στην ενεργό νόσο μένει σταθερή ή και αυξάνεται.[295] Ψευδώς θετική εικόνα παρουσιάζεται και με την έντονη απεικόνιση του φαιού λιπώδους ιστού στις τραχηλικές χώρες και παρασπονδυλικά στη θωρακική μοίρα,σε κατάσταση ψύχους 107
108 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή και σε άτομα με χαμηλό δείκτη μάζας σώματος. Το φαινόμενο αυτό είναι φυσιoλογικό και οφείλεται σε διέγερση από το συμπαθητικό νευρικό σύστημα και μπορεί να ανασταλεί με τη χορήγηση β-αναστολέα, ιδίως στις περιπτώσεις που η νόσος εντοπίζεται στον τράχηλο, αν και ο συνδυασμός PET/CT ελαχιστοποιεί το πρόβλημα αξιολόγησης εστιών αυξημένης πρόσληψης που δεν αντιστοιχούν σε συγκεκριμένες ανατομικές οντότητες. [296] Άλλες περιοχές που μπορεί να προσλαμβάνουν αυξημένη συγκέντρωση ραδιοφαρμάκου και να δείνουν ψευδώς θετικές εικόνες είναι η καρδιά, οι βουβωνικοί λεμφαδένες και το ΓΕΣ [256,271]. Σε νεαρά άτομα φυσιολογικά αυξημένη πρόσληψη παρατηρείται συχνά στις παρίσθμιες αμυγδαλές και στους σιελογόνους αδένες, η οποία μάλιστα μπορεί να επιταθεί μετά από τη χημειοθεραπεία ή ακτινοθεραπεία καθώς και στις δερματικές πτυχές και τους ιδρωτοποιούς αδένες της μασχάλης. Η πρόσληψη αυτή είναι συνήθως συμμετρική και δε δημιουργεί διαφοροδιαγνωστικά προβλήματα [297]. Επιπρόσθετα, η χρήση αυξητικών παραγόντων μπορεί να εντείνει την απεικόνιση του μυελού και του σπληνός, ενώ η αντιδραστική υπερπλασία του θύμου σε ασθενείς με HL δίνει εικόνα πρόσληψης στο μεσοθωράκιο. Φυσιολογικά αυξημένη πρόσληψη στο θύμο αδένα μπορεί να παρουσιαστεί σε άτομα νεότερα των 30 ετών, σε ποσοστό έως και 30%. [298] Η ένταση της πρόσληψης είναι αντιστρόφως ανάλογη του βαθμού λιπώδους εκφύλισης που παρουσιάζει ο αδένας στην CT. Απεικόνιση του θύμου αδένα μπορεί να παρατηρηθεί επίσης και σε μεγαλύτερης ηλικίας ασθενείς μετά από χημειοθεραπεία ή χορήγηση ραδιενεργού Ιωδίου (Ι 131 ) λόγω αντιδραστικής υπερπλασίας αυτού (thymic rebound) [299] Η χαρακτηριστική μορφολογία του θύμου αδένα υπό τη μορφή ανάστροφου V σε συνδυασμό με την εικόνα στην CT βοηθούν στην ταυτοποίησή του. Εντούτοις μερικές φορές η διάκριση μεταξύ φυσιολογικής πρόσληψης από το θύμο αδένα και νόσου του προσθίου μεσοθωρακίου μπορεί να είναι αρκετά δυσχερής. Διάχυτα ή και εστιακά αυξημένη πρόσληψη από το πνευμονικό παρέγχυμα μπορεί να οφείλεται σε τοξικότητα από τη χορήγηση μπλεομυκίνης ή ριτουξιμάμπης ή σε κυψελιδίτιδα λόγω χημειοθεραπείας.[300] Παθολογική πρόσληψη 18FDG σε λεμφαδένες του μεσοθωρακίου με την τυπική κατανομή της σαρκοείδωσης μπορεί να οφείλεται σε 108
109 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία σαρκοειδικού τύπου αντίδραση (sarcoid-like reaction). Στην τελευταία αυτή περίπτωση μόνο η βιοψία μπορεί να διευκρινίσει τη φύση του ευρήματος [301]. Αυξημένη πρόσληψη μπορεί επίσης να παρατηρηθεί μετά από ακτινοθεραπεία, στις κορυφές των πνευμόνων και οπισθοπεριτοναϊκά λόγω μετακτινικής φλεγμονής [302]. Η πρόσληψη αυτή μπορεί να εμμένει έως και 4-6 μήνες μετά την ακτινοθεραπεία σε ορισμένες περιπτώσεις. Για το λόγο αυτό συνιστάται αναμονή τουλάχιστον 3 μηνών μετά από ακτινοθεραπεία πριν την εκτέλεση PET/CT μελέτης. Το διάστημα αυτό θεωρείται ασφαλές για τους ασθενείς με λέμφωμα. Σε αυτό το σημείο χρειάζεται να σημειωθεί ότι και οι μετεγχειρητικές ουλές μπορεί να παρουσιάσουν αυξημένη πρόσληψη έως και 6 μήνες μετά από την επέμβαση ανάλογα με τον ιστό που έχει τραυματισθεί, αφού π.χ. τα οστά επουλώνονται πολύ αργότερα από τα μαλακά μόρια [303]. Στον αντίποδα, ψευδώς αρνητικά αποτελέσματα μπορεί να οφείλονται στη μη σωστή προετοιμασία με νηστεία, στο βραχύ χρόνο χορήγησης του FDG, στην υπεργλυκαιμία, ενώ οι νέες πνευμονικές εστίες σε ασθενή με κατά τα άλλα πλήρη ύφεση θεωρούνται εξ ορισμού φλεγμονώδεις. Σημαντικός περιορισμός του ΡΕΤ-scan είναι και η απεικόνιση των οστικών διηθήσεων λόγω του ότι η κινητική της πρόσληψης του FDG δεν έχει καθορισθεί με σαφήνεια [249]. Αιτία ψευδούς αρνητικής μελέτης- μολονότι δεν είναι τόσο συχνή στο λέμφωμα- αποτελεί και το μέγεθος της βλάβης. Επίσημα η διακριτική ικανότητα των PET/CT scanners είναι περίπου 6-7 mm. Εντούτοις, βλάβες μικρότερες του 1cm μπορεί να μην απεικονισθούν, ιδιαίτερα όταν περιβάλλονται από ιστούς με χαμηλή πρόσληψη 18FDG (π.χ. πνευμονικό παρέγχυμα), λόγω του φαινομένου του μερικού όγκου (Partial Volume Effect) ή όταν έχουν οι ίδιες χαμηλή πρόσληψη ή τέλος όταν βρίσκονται κοντά σε φυσιολογικές δομές με υψηλή πρόσληψη 18FDG (π.χ. ουροποιητικό σύστημα, μυοκάρδιο) [304,305]. Η εκτέλεση της μελέτης πολύ σύντομα μετά τη χημειοθεραπεία είναι μια επιπρόσθετη αιτία ψευδώς αρνητικών ευρημάτων. Οφείλεται σε προσωρινή αναστολή της πρόσληψης 18FDG από βιολογικά ενεργά καρκινικά κύτταρα ευθύς μετά την έναρξη της θεραπείας (φαινόμενο 109
110 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή stunning των καρκινικών κυττάρων). Μελέτες έχουν δείξει ότι κάποια κυτταροστατικά φάρμακα αναστέλλουν άμεσα την δράση της εξοκινάσης της γλυκόζης στο κυτταρόπλασμα και κατά συνέπεια την πρόσληψη 18FDG από το κύτταρο, ενώ αυτό είναι ακόμη μεταβολικά ενεργό [306]. Για το λόγο αυτό συνιστάται η PET/CT να μη γίνεται πριν περάσουν 10 τουλάχιστον ημέρες μετά από την τελευταία συνεδρία χημειοθεραπείας ή να γίνεται όσο πιο κοντά στον επόμενο κύκλο για τις μεσοθεραπευτικές (interim) μελέτες.για δε τις μελέτες μετά το πέρας της θεραπείας, κρίνεται σκόπιμη η διεξαγωγή του ΡΕΤ, ημέρες μετά τον τελευταίο κύκλο [254]. 110
111 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία ΕΙΔΙΚΟ ΜΕΡΟΣ 111
112 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ΣΚΟΠΟΣ Αντικείμενο του ειδικού μέρους της παρούσας Διδακτορικής Διατριβής είναι η διερεύνηση του ρόλου του PET/CT στην αρχική σταδιοποίηση, η συμμετοχή του στην τροποποίηση της θεραπευτικής στρατηγικής, καθώς και στην ενδεχόμενη αλλαγή του πεδίου ακτινοθεραπείας στην νόσο του Hodgkin, στην καθημερινή κλινική πράξη. Επιπλέον, αντικείμενο της αναδρομικής αυτής μελέτης είναι η διερεύνηση της προγνωστικής σημασίας του των διαφόρων παραμέτρων του αρχικού PET/CT, σε σύγκριση με τη συμβατική αξονική τομογραφία. ΥΛΙΚΟ ΚΑΙ ΜΕΘΟΔΟΙ ΠΡΟΕΛΕΥΣΗ ΣΥΛΛΟΓΗ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΤΟΥ ΥΛΙΚΟΥ Στην παρούσα πειραματική, αναδρομική μελέτη, συμμετείχαν 162 ασθενείς με Λέμφωμα Hodgkin, που εντάχθηκαν διαδοχικά, κατά το χρονικό διάστημα 12/12/2006 με 25/7/2014 και έλαβαν θεραπεία σε μία μόνο Αιματολογική Μονάδα. Ως μοναδικό κριτήριο ένταξης των ασθενών στη μελέτη ήταν η ύπαρξη εξέτασης PET/CT κατά τη διάγνωση. Η μελέτη εγκρίθηκε από την Επιτροπή Ηθικής και Δεοντολογίας του Λαϊκού Γενικού Νοσοκομείου, σύμφωνα με τη Διακήρυξη του Ελσίνκι. Όλοι οι συμμετέχοντες υποβλήθηκαν σε αρχική σταδιοποίηση με κλινική εξέταση και αξονική τομογραφία με ενδοφλέβιο σκιαγραφικό (Computed Tomography-CTs) τραχήλου, θώρακος, άνω και κάτω κοιλίας, καθώς και με οστεομυελική βιοψία. Επιπλέον, όλοι οι ασθενείς μελετήθηκαν με τομογραφία εκπομπής ποζιτρονίων (18- FDG PET/CT SCAN) κατά τη διάγνωση. ΠΡΩΤΟΚΟΛΛΟ PET/CT Για τη διεξαγωγή του PET/CT χρησιμοποιήθηκε το σύστημα Discovery ST PET/CT (GE Healthcare), που αποτελείται από ένα πλήρη σαρωτή γερμανικού βισμουθίου και ένα αξονικό τομογράφο 16 τομών. Οι ασθενείς παρέμεναν νήστεις για τουλάχιστον 6 ώρες πριν 112
113 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία την ενδοφλέβια χορήγηση της 18-FDG( MBq). Η τομογραφία εκπομπής ποζιτρονίων λάμβανε χώρα 60 λεπτά μετά την ενδοφλέβια χορήγηση 18-FDG. Τα επίπεδα γλυκόζης στο αίμα πριν από την έγχυση του φαρμάκου, έπρεπε να είναι κάτω από 160mg/dl. Δε χρειαζόταν να γίνει χορήγηση ενδοφλέβιου σκιαγραφικού. Οι ασθενείς ενθαρρύνονταν να κενώσουν την κύστη πριν την απεικόνιση και ακολουθούσε σάρωση από ένα υβριδικό FDG PET/CT σαρωτή. Ο χρόνος απόκτησης των εικόνων ήταν 4 λεπτά για κάθε θέση του κρεββατιού. Η σάρωση της αξονικής τομογραφίας εκτεινόταν από τη βάση του κρανίου εώς τους εγγύς μηρούς. Αμέσως μετά την απόκτηση των εικόνων της αξονικής τομογραφίας, ακολουθούσε η σάρωση με τομογραφία εκπομπής ποζιτρονίων, στις ίδιες ανατομικές θέσεις. Τα δεδομένα της αξονικής τομογραφίας χρησιμοποιούνταν για τη διόρθωση εξασθένησης των εικόνων,για την ανασύσταση των οποίων χρησιμοποιήθηκε ένας συμβατικός επαναληπτικός αλγόριθμος (OSEM). Οι υπερμεταβολικές βλάβες φαίνονταν σαν ψευδώς χρωματικά- κωδικοποιημένα εικονοστοχεία (pixels) ή ογκοστοιχεία (voxels) στη διαβαθμισμένη γκρι κλίμακα των εικόνων της αξονικής τομογραφίας. Οι τιμές πρόσληψης του ΡΕΤ/CT scan (Standardised Uptake Value-SUV) αντιπροσώπευαν το λόγο της συγκέντρωσης του καρκινικού ιχνηθέτη, προς το μέσο όρο της συγκέντρωσης του ιχνηθέτη σε όλο το σώμα και χρησιμοποιήθηκαν ως ημιποσοτική μέτρηση του βαθμού πρόσληψης του FDG προκειμένου να ερμηνευθεί η μέθοδος σάρωσης. Η τιμή του SUV υπολογίστηκε από το συγκεκριμένο λογισμικό για κάθε μεταβολική περιοχή που εντοπίστηκε στην εξέταση [283, ]. Η διεξαγωγή των PET/CT έλαβε χώρα σε τρία διαφορετικά κέντρα, όπου οι εξετάσεις μελετήθηκαν από τον αντίστοιχο πυρηνικό ιατρό. Ωστόσο, η πλειοψηφία των εξετάσεων πραγματοποιήθηκε στο Τμήμα Πυρηνικής Ιατρικής του Νοσοκομείου Ευαγγελισμός. Στο σημείο αυτό χρειάζεται να σημειωθεί ότι δεν έγινε κεντρική ανασκόπηση των PET/CT εξετάσεων. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΤΑΔΙΟΥ ΝΟΣΟΥ- ΘΕΡΑΠΕΥΤΙΚΟ ΠΡΩΤΟΚΟΛΛΟ Τόσο το κλινικό στάδιο (CS), όσο και η σταδιοποίηση με βάση την απεικόνιση με PET/CT (PET-S) προσδιορίστηκε σύμφωνα με το σύστημα σταδιοποίησης της Ann-Arbor και ανάλογα 113
114 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή με τις προσβεβλημένες περιοχές[311,312]. Ως διηθημένος μυελός των οστών, σύμφωνα με το PET/CT, ορίστηκε αυτός με εμφανή πολυεστιακή ή μονοεστιακή πρόσληψη στα οστά, χωρίς ωστόσο να συνυπάρχει εικόνα οστικών αλλοιώσεων στην αξονική τομογραφία. Ο μυελός των οστών που προσλάμβανε διάχυτα ραδιοφάρμακο ορίστηκε ως αρνητικός[265,307, ]. Ο αριθμός των προσβεβλημένων περιοχών (number of involved sites-nis) καταγράφηκε σύμφωνα με την εικόνα 1 και με τις δύο μορφές απεικόνισης. Ως ογκώδης νόσος ορίστηκε οποιοσδήποτε λεμφαδένας με διάμετρο μεγαλύτερη των 7cm, ή μάζα μεσοθωρακίου με διάμετρο μεγαλύτερη από 10cm, στην εγκάρσια διατομή της, στην αξονική τομογραφία. Eικόνα 1: Σχηματική απαρίθμηση των περιοχών που διηθούνται από τη νόσο. 1.Κάθε πλαίσιο αντιπροσωπεύει μία διηθημένη περιοχή. 2.Οι λεμφαδένες αριστερής και δεξιάς περιοχής απαριθμούνταν σαν ξεχωριστές περιοχές για τους τραχηλικούς, μασχαλιαίους, λαγόνιους,βουβωνικούς και μηριαίους λεμφαδένες. 3. Πολυεστιακή ή μονοεστιακή διήθηση απαριθμείτο ως μία εστία. 4. Ο αριστερός και δεξιός πνεύμονας απαριθμούνταν σαν ξεχωριστές περιοχές. 114
115 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Όλοι οι ασθενείς υποβλήθηκαν σε ενιαία θεραπεία, σύμφωνα με την ακόλουθη στρατηγική: Οι ασθενείς που έπασχαν από στάδια ΙΑ/ΙΒ, ΙΙΑ και ΙΙΒ χωρίς παρουσία ογκώδους νόσου, ή εξωλεμφαδενική νόσο, έλαβαν 4-6 κύκλους χημειοθεραπείας με το συνδυασμό ABVD (ανδριαμυκίνης 25mg/m 2, μπλεομυκίνης 10mg/m 2 με ανώτερο όριο τα 15mg, βινμπλαστίνη 6mg/m 2, δακαρμαζίνη 375mg/m 2 τις μέρες 1 και 15 κάθε κύκλου 30 ημερών), ακολουθούμενη από ακτινοθεραπεία προσβεβλημένου πεδίου (IFRT) με συνολική δόση 30-36Gy[ ]. Oι ασθενείς με στάδια ΙΙΙ και ΙV υποβάλλονταν μόνο σε χημειοθεραπεία, χωρίς να ακολουθεί προγραμματισμένη ακτινοθεραπεία, παρά επί υπολειμματικής νόσου. Χορηγούνταν 6-8 κύκλοι ABVD, ή 2 κύκλοι ABVD και ακολουθούσε θεραπεία καθοδηγούμενη από τα αποτελέσματα του ενδιάμεσου PET ως εξής:4-6 επιπλέον κύκλοι ABVD ( συνολικά οι ασθενείς λάμβαναν 6-8 κύκλους ABVD) εάν το ενδιάμεσο ΡΕΤ που λάμβανε χώρα μετά τους δύο πρώτους κύκλους, ήταν αρνητικό. Εφόσον το ενδιάμεσο ΡΕΤ ήταν θετικό (κλίμακα 5- σημείων των κριτηρίων Deauville 4), η θεραπεία άλλαζε σε 6 κύκλους BEACOPP-escalated (μπλεομυκίνη 10mg/m 2 - με ανώτερο όριο τα 10mg την ημέρα 8, ετοποσίδη 200 mg/m 2 -τις μέρες 1-3, ανδριαμυκίνη 35 mg/m 2 την ημέρα 1, κυκλοφωσφαμίδη 1250 mg/m 2, την ημέρα 1, βινκριστίνη 1.2 mg/m 2 -με ανώτερο όριο τα 2mg την ημέρα 8, προκαρβαζίνη 100 mg/m 2 - τις ημέρες 1-7 και πρεδνιζόνη 40 mg/m 2 τις ημέρες 1-14, από τις 21 ημέρες του κύκλου)[ ]. Ακολούθως, σε επιλεγμένους ασθενείς με θετική υπολειπόμενη νόσο στο μεταθεραπευτικό ΡΕΤ, χορηγείτο ακτινοθεραπεία μετά την χημειοθεραπεία. Οι ασθενείς με στάδιο ΙΙΒ, με ογκώδη νόσο ή με εξωλεμφαδενική επέκταση, ακολούθησαν το ίδιο πρόγραμμα με αυτό των ασθενών με προχωρημένα στάδια (ΙΙΙ και ΙV), με την προσθήκη IFRT στο τέλος της θεραπείας. 115
116 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ΣΤΑΤΙΣΤΙΚΗ ΑΝΑΛΥΣΗ ΣΤΑΤΙΣΤΙΚΗ ΜΕΘΟΔΟΛΟΓΙΑ Τo κύριο καταληκτικό σημείο της μελέτης ήταν το διάστημα ελεύθερο επιδείνωσης νόσου ( freedom from progression- FFP), το οποίο υπολογίστηκε από τη έναρξη της θεραπείας μέχρι την υποτροπή, την επιδείνωση, ή τον τελευταίο επανέλεγχο του ασθενούς. Οι θάνατοι από μη σχετιζόμενα αίτια, χωρίς προηγούμενη επιδείνωση της νόσου, εκτιμήθηκαν και λογοκρίθηκαν τη στιγμή του θανάτου. Για τη σύγκριση των παραμέτρων της νόσου, χρησιμοποιήθηκαν τα κατάλληλα μη παραμετρικά tests Η χρήση του Chi-Square test χρησιμοποιήθηκε για τις ποιοτικές μεταβλητές, ενώ για τις συνεχείς μεταβλητές χρησιμοποιήθηκε η μέθοδος Mann-Whitney ή η Wilcoxon, ανάλογα με την περίπτωση. Η ολική επιβίωση (overall survival-os) υπολογίστηκε ως το χρονικό διάστημα από την έναρξη της θεραπείας μέχρι το θάνατο από οποιαδήποτε αιτία, ή μέχρι τον τελευταίο επανέλεγχο του ασθενούς. Οι καμπύλες επιβίωσης σχεδιάστηκαν σύμφωνα με τη μέθοδο Κaplan-Meier και συγκρίθηκαν χρησιμοποιώντας το Log rank test. Το λογισμικό πρόγραμμα που χρησιμοποιήθηκε για τη στατιστική ανάλυση ήταν το SPPSv17 και τιμές p 0.05 θεωρήθηκαν ως στατιστικά σημαντικές. 116
117 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία AΠΟΤΕΛΕΣΜΑΤΑ α. Συσχέτιση μεταξύ κλινικής σταδιοποίησης (CS) και σταδιοποίησης με ΡΕΤ (ΡΕΤ-S) Στη συγκεκριμένη αναδρομική μελέτη συμπεριελήφθησαν 162 ασθενείς. Η διάμεση ηλικία ήταν τα 33 έτη και 83 (51%) από τους συμμετέχοντες ήταν άνδρες. Τα χαρακτηριστικά των ασθενών συνοψίζονται στον παρακάτω πίνακα 1. Πίνακας 1: Χαρακτηριστικά ασθενών N % Αριθμός ασθενών Διάμεση ηλικία σε έτη (εύρος) 33 (17-82) Άρρενες Διάμεσος αριθμός προσβεβλημένων περιοχών με βάση τη CS 4 (1-14) (εύρος) Διάμεσος αριθμός προσβεβλημένων περιοχών με βάση το PET-S 5 (1-15) (εύρος) Κλινική Σταδιοποίηση vs Σταδιοποίηση με PET/CT I II III IV 16 vs vs vs vs vs 6 42 vs 41 24vs vs 30 B-Συμπτώματα Συμμετοχή σπληνός: Από CS vs PET-S 32vs vs 27 Εξωλεμφαδενική νόσος: Από CS vs PET-S 54 vs vs 45 1 περιοχή 41 vs vs 34 2 περιοχές 10 vs 14 6 vs 9 3 περιοχές 3 vs 3 2 vs 2 Ογκώδης Νόσος Διάμεσο SUVmax (εύρος) 11.5 ( ) 117
118 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή CS: Σταδιοποίηση με βάση την αξονική τομογραφία PET-S: Σταδιοποίηση με βάση το ΡΕΤ/CT Σύμφωνα με την κλινική σταδιοποίηση (CS) 16,69,39 και 38 ασθενείς σταδιοποιήθηκαν ως στάδια Ι,ΙΙ, ΙΙΙ και IV, αντίστοιχα. Βάση της σταδιοποίησης με ΡΕΤ (ΡΕΤ-S) 10,66, 39 και 47 ασθενείς βρέθηκαν να είναι σταδίου Ι, ΙΙ, ΙΙΙ και IV, αντίστοιχα. Η κατανομή της σταδιοποίησης με ΡΕΤ έναντι της κλινικής σταδιοποίησης και ο αριθμός των διηθημένων περιοχών από την CS ή το ΡΕΤ-S, φαίνονται στους πίνακες 2 και 3. Πίνακας 2: Συσχέτιση μεταξύ κλινικής σταδιοποίησης (CS) και σταδιοποίησης με PET/CT Σταδιοποίηση με PET/CT Συνολικός N I II III IV Κλινική I Σταδιοποίηση II (CS) III IV Συνολικός N : Ασθενείς που έπεσαν στάδιο, : Ασθενείς που ανέβηκαν στάδιο, : Ασθενείς χωρίς αλλαγή σταδίου Πίνακας 3: Αριθμός διηθημένων περιοχών με CS ή PET/CT σε διαφορετικά κλινικά στάδιο Διάμεσος Αριθμός Διηθημένων περιοχών (εύρος) Κλινική Σταδιοποίηση CS PET/CT I 1 (1-1) 1.5 (1-5) II 2 (2-6) 4 (1-10) III 5.5 (2-14) 7 (1-15) IV 6 (3-11) 10.5 (3-14) CS: Κλινική σταδιοποίηση, PET/CT Σταδιοποίηση με βάση το PET/CT 118
119 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Οι ακόλουθες παρατηρήσεις ήταν προφανείς: Η κλινική σταδιοποίηση (CS) είχε υψηλή συσχέτιση με την σταδιοποίηση από ΡΕΤ (PET-S),(p-value<0.0001), ωστόσο συνολικά 35 ασθενείς άλλαξαν στάδιο: 26 ασθενείς (16%) ανέβηκαν στάδιο με βάση το ΡΕΤ, ενώ 9 συμμετέχοντες (6%) κατέβηκαν στάδιο. Η μεγαλύτερη συχνότητα αλλαγής σταδίου παρατηρήθηκε στα κλινικά στάδια Ι, όπου το 50% των ασθενών ανέβηκαν στάδιο, ακολουθούμενα από στο στάδιο ΙΙΙ (με βάση την κλινική σταδιοποίηση), όπου 11/39 ασθενείς (28%) των περιπτώσεων άλλαξαν στάδιο (5/39 μεταπήδησαν σε υψηλότερο στάδιο και 6/39 κατέβηκαν στάδιο). Το 20% των ασθενών με κλινικό στάδιο ΙΙ, άλλαξαν στάδιο με βάση το ΡΕΤ, με την πλειοψηφία να μεταπηδά σε πιο προχωρημένο στάδιο. Τέλος, μόνο το 5% των ασθενών με κλινικό στάδιο IV, έπεσε στάδιο. Παρατηρήθηκε στατιστικά σημαντική συσχέτιση μεταξύ του αριθμού των διηθημένων περιοχών που βρέθηκαν με CS και PET-S (p< , Spearman s rho=0.831). Ωστόσο, ο αριθμός των προσβεβλημένων περιοχών με βάση το ΡΕΤ ήταν σημαντικά μεγαλύτερος (p<0.0001) σε σχέση με τον αριθμό των περιοχών που απομονώθηκαν με την κλινική σταδιοποίηση (p=0.01 για το CS I και p< για όλα τα υπόλοιπα στάδια χωριστά). Συνολικά 88/161 (54%) ασθενείς είχαν επιπρόσθετες διηθημένες περιοχές από το ΡΕΤ, 13 (8%) είχαν λιγότερες περιοχές και 30 (19%) είχαν άλλες περιοχές που προστίθετο και άλλες που αφαιρούνταν με βάση τη σταδιοποίηση με ΡΕΤ. Τελικά, μόνο σε 30 (19%) ασθενείς, οι διηθημένες περιοχές ήταν ταυτόσημες τόσο στην κλινική, όσο και στη σταδιοποίηση με ΡΕΤ. Σε αυτή την τελευταία ομάδα, 25/30 ασθενείς είχαν αρχικά κλινικά στάδια CS. Η διήθηση του σπληνός και η εξωλεμφαδενική διήθηση αυξήθηκε από 20% και 34% αντίστοιχα με την CS, σε 27% και 45% με την PET/CT. Η ΡΕΤ/CT εντόπισε σημαντικά περισσότερους ασθενείς με διήθηση μυελού των οστών (p<0.0001) συγκριτικά με τη οστεομυελική βιοψία (ΒΜΒ). Έτσι, η διήθηση του μυελού των οστών αυξήθηκε από 8% με τη BMB σε 17% με το ΡΕΤ/CT. Αξίζει να σημειωθεί το γεγονός ότι δεν απομονώθηκε ούτε ένας ασθενής με αρνητικό ΡET/CT για διήθηση μυελού των οστών, που να έχει θετική ΒΜΒ, καταλήγοντας στο συμπέρασμα ότι το ΡΕΤ/CT έχει 100% αρνητική προγνωστική αξία. Σε 24 ασθενείς παρατηρήθηκε διάχυτη διήθηση του μυελού των οστών. Ωστόσο, κανένας από αυτούς δεν εμφάνισε θετική οστεομυελική βιοψία. 119
120 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Η συσχέτιση μεταξύ του ΡΕΤ/CT και της οστεομυελικής βιοψίας ήταν ιδιαίτερα στατιστικά σημαντική (p<0.0001) και απεικονίζεται στον πίνακα 4. Πίνακας 4: Συσχέτιση ευρημάτων διήθησης μυελού των οστών με βάση το PET/CT και με βάση την Οστεομυελική Βιοψία Οστεομυελική Βιοψία Αρνητική Θετική Αρνητική PET/CT Διάχυτη Πρόσληψη Μυελού Οστών Εστιακή Πρόσληψη Μυελού Οστών β. Αλλαγή Θεραπευτικής Αγωγής εξαιτίας της σταδιοποίησης με ΡΕΤ Σύμφωνα με την πολιτική της μονάδας μας, η θεραπευτική αγωγή για αρχικά και προχωρημένα στάδια νόσου, θα μπορούσε θεωρητικά να αλλάξει εξαιτίας της σταδιοποίησης με ΡΕΤ, σε 23 ασθενείς (14%). Τελικά, μόνο σε 10 συμμετέχοντες (το 6% του συνολικού πληθυσμού) ο θεράπων ιατρός αποφάσισε να αλλάξει τη θεραπευτική στρατηγική, εξαιτίας των ευρημάτων από τη σταδιοποίηση με ΡΕΤ, π.χ. η θεραπεία τροποποιήθηκε από θεραπεία αρχικού σταδίου, σε θεραπεία προχωρημένου σταδίου και αντίστροφα. Ανάμεσα σε αυτούς τους 10 ασθενείς, στους οποίους άλλαξε η θεραπευτική στρατηγική, 6 ανέβηκαν στάδιο και 4 πάσχοντες έπεσαν στάδιο νόσου, με βάση το PET/CT και έλαβαν IFRT ακτινοθεραπεία. Στους εναπομείναντες 13 ασθενείς, η θεραπεία στηρίχθηκε στη συμβατική σταδιοποίηση και παρόλο που η συντριπτική πλειοψηφία τους (12/13) είχε ανέβει στάδιο με βάση τη σταδιοποίηση με ΡΕΤ, η χορήγηση της ακτινοθεραπείας διατηρήθηκε ως αναπόσπαστο τμήμα της θεραπευτικής στρατηγικής. 120
121 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Η θεραπευτική στρατηγική και τα πεδία ακτινοθεραπείας που ακολουθήθηκαν στους 35 ασθενείς, στους οποίους υπήρξε αλλαγη σταδίου με την ΡΕΤ-S φαίνεται στον πίνακα 5. Πίνακας 5: Χαρακτηριστικά ασθενών που άλλαξαν κλινικό στάδτιο με το PET/CT Ασθενείς # CS PET-S Αίτιο για αλλαγή με CS Θεωρητική Τροποποίησ η της Θεραπευτική ς Στρατηγικής Τροποποίηση Θεραπευτικής Στρατηγικής Τροποποίηση του πεδίου RT Ασθενείς που ανέβηκαν στάδιο 3 IA IIIA Αριστερός Ναι Όχι Πάνω από το λαγόνιος LN διάφραγμα σύμφωνα με CS 5 IA IIIA Άμφω Ναι Όχι Πάνω από το λαγόνιοι LN διάφραγμα σύμφωνα με CS 7 IA IIA Μεσοθωράκιο Όχι Όχι Πάνω από το διάφραγμα σύμφωνα με PET-S 8 IA IIEA Δεξιό πλευρό Όχι Όχι Πάνω από το διάφραγμα σύμφωνα με CS 77 IB IIB LN Όχι Όχι Δεν είναι μεσοθωρακίου γνωστό το και αριστερός συγκεκριμένο Αποτέλεσμα CCR στους 61 μήνες CCR στους 77 μήνες CCR στους 86 μήνες CCR στους 70 μήνες CCR στους 80 μήνες 121
122 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή μασχαλιαίος πεδίο RT LN 108 IA IIIA Γαστροδωδεκα Δακτυλικός Ναι Όχι Πάνω από το διάφραγμα σύμφωνα με CS 155 IA IIA Δεξιός Όχι Όχι Πάνω από το τραχηλικός LN διάφραγμα σύμφωνα με PET-S 156 IB IIB Μεσοθωράκιο Όχι Όχι Δεν είναι γνωστό το συγκεκριμένο πεδίο RT 2 IIA IVA LΝ πύλης Ναι Όχι Αρχικά σπληνός και ανθεκτική εστιακή νόσος, RT σκελετική διάσωσης πρόσληψη 16 IIA IVA Ηπατική Ναι Όχι Πάνω από το βλάβη διάφραγμα σύμφωνα με CS 18 IIB IIIB Σπλήνας Ναι Ναι Δεν έλαβε RT λόγω διάγνωσης εκτεταμένου σταδίου 29* IIEA IVA Αριστερός LN, Ναι Ναι Δεν έλαβε RT μεσοθωράκιο, λόγω CCR στους 32 μήνες CCR στους 42 μήνες CCR στους 70 μήνες Υποτροπή στους 9 μήνες CCR στους 70 μήνες CCR στους 47 μήνες CCR στους 80 μήνες 122
123 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία άμφω λεμφαδένες πύλης διάγνωσης εκτεταμένου σταδίου 30 IIB IVB Ηπατικές βλάβες Ναι Όχι Πάνω από το διάφραγμα σύμφωνα με CS 31 IIB IVB Εστιακή Ναι Ναι Δεν έλαβε RT σκελετική λόγω πρόσληψη διάγνωσης εκτεταμένου σταδίου 69 IIB IIIB Μεσεντέριος Ναι Όχι Πάνω από το LN διάφραγμα σύμφωνα με CS 76 IIB IIIB Γαστρικός, Ναι Όχι Συμφωνα με Παραορτικός PET-S LN 79 IIA IIIA Σπλήνας Ναι Όχι Πάνω από το διάφραγμα σύμφωνα με PET-S 125 IIB IIIB Παραορτικός Ναι Όχι Πάνω από το LN διάφραγμα σύμφωνα με PET-S 135 IIA IIIA Παραορτικός, Ναι Όχι Πάνω από το Δεξιός διάφραγμα λαγόνιος LN σύμφωνα με CCR στους 72 μήνες CCR at 32 mo CCR στους 28 μήνες CCR στους 80 μήνες CCR στους 77 μήνες CCR στους 45 μήνες CCR στους 53 μήνες 123
124 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή CS 139 IIA IIIA Παραορτικός, ηπατογαστρικ Ναι Όχι Πάνω από το διάφραγμα CCR στους 56 μήνες ός LN σύμφωνα με CS 152 IIB IVB Εστιακή σκελετική Ναι Ναι Δεν έλαβε RT λόγω CCR στους 62 μήνες πρόσληψη διάγνωσης εκτεταμένου σταδίου 49 IIIB IVB Εστιακή σκελετική πρόσληψη Όχι No Όχι RT Υποτροπή στους 18 μήνες 60 IIIB IVB Εστιακή σκελετική Όχι Όχι Όχι RT CCR στους 82 μήνες πρόσληψη, άμφω πνευμονικοί όζοι 92 IIIB IVB Εστιακή σκελετική Όχι Όχι Όχι RT CCR στους 53 μήνες πρόσληψη 120 IIIA IVA Εστιακή σκελετική πρόσληψη Όχι Όχι Όχι RT Υποτροπή στους 10 μήνες 151 IIIA IVA Εστιακή σκελετική πρόσληψη Όχι Όχι Όχι RT CCR στους 59 μήνες Ασθενείς που Κατέβηκαν Στάδιο 78 IV IIIB Διήθηση Όχι Όχι Όχι RT CCR στους 124
125 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία B Οστών 82 μήνες 161 IV B 35 III B 41 III A 46 III B 71 III B 99 III B 117 III A IIB Διήθηση Οστών Ναι Ναι Πάνω από το διάφραγμα σύμφωνα με PET-S IIB Παραορτικός Ναι Ναι Πάνω από το LN διάφραγμα σύμφωνα με PET-S IIA Παραορτικός Ναι Ναι Πάνω από το LN διάφραγμα σύμφωνα με PET-S IIB Σπλήνας Ναι Ναι Πάνω από το διάφραγμα σύμφωνα με CS IIB Δεξιός Ναι Ναι Πάνω από το βουβωνικός διάφραγμα LN σύμφωνα με PET-S IIB Δεξιός Ναι Όχι Δεν έλαβα RT, βουβωνικός παρόλο που LN κατέβηκε στάδιο με το PET-S IA Παραορτικός, Ναι Ναι Πάνω από το Αριστερός διάφραγμα τραχηλικός LN σύμφωνα με PET-S Υποτροπή στους 12 μήνες Υποτροπή στους 11 μήνες CCR στους 89 μήνες CCR στους 82 μήνες CCR στους 56 μήνες CCR στους 77 μήνες CCR στους 26 μήνες 125
126 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή 81 IIA IA Αριστερός τραχηλικός LN Όχι Όχι Πάνω από το διάφραγμα σύμφωνα με PET-S CCR στους 46 μήνες *: Αυτός ο ασθενής είχε υποδιαφραγματική νόσο από το CS, CS: κλινική σταδιοποίηση, PET-S: Σταδιοποίηση με PET-S, CCR: Συνεχής πλήρης ύφεση, LN: Λεμφαδένες, RT: Ακτινοθεραπεία, IF-RT: Ακτινοθεραπεία περιορισμένων πεδίων, : Ασθενείς στους οποίους η θεραπεία δε θα άλλαζε θεωρητικά, : Ασθενείς στους οποίους η θεραπεία θα μπορούσε θεωρητικά να τροποποιηθεί σύμφωνα με το PET/CT, αλλά στην πραγματικότητα δεν τροποποιήθηκε και λήφθηκε υπόψη το CS, : Ασθενείς στους οποίους η θεραπεία μπορούσε θεωρητικά να τροποποιηθεί σύμφωνα με το PET/CT, και όντως άλλαξε. γ. Αλλαγή των Πεδίων Ακτινοθεραπείας εξαιτίας της σταδιοποίησης με ΡΕΤ. Βρέθηκαν 66 ασθενείς, στους οποίους τα πεδία της ακτινοθεραπείας IFRT θα μπορούσαν να έχουν θεωρητικά τροποποιηθεί, σύμφωνα με τη σταδιοποίηση με ΡΕΤ. Η πλειοψηφία τους (55) ανήκαν σε αρχικά στάδια της νόσου (Πίνακας 6). Ανάμεσα σε αυτούς τους ασθενείς, οι 20/66 (32%) συμμετέχοντες έλαβαν ακτινοθεραπεία χωρίς να γίνει αλλαγή των πεδίων της IFRT και ακτινοβολήθηκαν με βάση το προσβεβλημένο πεδίο ακτινοθεραπείας, που διαμορφώθηκε σύμφωνα με τις αξονικές, ενώ οι 36/66 ασθενείς (59%) έλαβαν ακτινοθεραπεία προσβεβλημένου πεδίου IFRT, σύμφωνα με τις διηθημένες περιοχές, που καθορίστηκαν από το PET/CT. Επιπλέον βρέθηκαν και 7 ασθενείς που θεωρήθηκαν ως μηαξιολογήσιμοι, κυρίως εξαιτίας της προόδου της νόσου τους ή λόγω πρόωρου θανάτου, πριν την έναρξη της ακτινοθεραπείας. Οι ασθενείς που παρουσίασαν επιδείνωση της νόσου έλαβαν χημειοθεραπεία διάσωσης. Τέλος, υπήρξαν και 3 ασθενείς για τους οποίους δεν υπάρχουν ακριβή στοιχεία για το πεδίο ακτινοθεραπείας τους. Ο πίνακας 6 δείχνει με λεπτομέρεια την ακτινοθεραπεία που έλαβαν στην πράξη οι ασθενείς μας. 126
127 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Πίνακας 6: Η ακτινοθεραπεία που χορηγήθηκε στους ασθενείς της μονάδας μας Πραγματική Κατάσταση Θεωρητική πιθανότητα για τροποποίηση των πεδίων της IFRT, σύμφωνα με το PET/CT Συνολικός Αριθμός Όχι Ναι Όλοι οι ασθενείς Καμμία αλλαγή των πεδίων IFRT (σύμφωνα με CS) Μη χορήγηση RT, μολονότι πτώση σταδίου με βάση το PET-S Πεδία RT σύμφωνα με CS, μολονότι αύξηση του σταδίου με βάση το PET-S Αλλαγή των πεδίων IFRT (σύμφωνα με PET-S) Καμμία RT εξαιτίας αύξηση του σταδίου νόσου με βάση το PET-S Μη RT εξαιτίας αύξησης του σταδίου τόσο με CS, όσο και με PET- S Μη αξιολογήσιμο Άγνωστο ακριβές πεδίο RT : Καμμία αλλαγή στο πεδίο RT, : Αλλαγή του πεδίου RT, σύμφωνα με το PET-S, RT: Ακτινοθεραπεία, IF-RT: ακτινοθεραπεία προσβεβλημένου πεδίου, CS: Διηθημένες περιοχές σύμφωνα με την κλινική σταδιοποίηση, PET-S: Διηθημένες περιοχές σύμφωνα με τη σταδιοποίηση με ΡΕΤ. δ. Ανάλυση προγνωστικών παραγόντων Σε διάμεσο χρόνο παρακολούθησης 56.7 μήνες (εύρος ), η 5-ετής FFP και η OS ήταν 81%±3 και 93%±2, αντίστοιχα. Οι ακόλουθοι προγνωστικοί παράμετροι εκτιμήθηκαν από μονοπαραγοντική ανάλυση: Το φύλο, η κλινική σταδιοποίηση, η σταδιοποίηση με ΡΕΤ, η 127
128 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή ύπαρξη Β-συμπτωμάτων, ο αριθμός των διηθημένων περιοχών, η εξωλεμφαδενική νόσος, η διήθηση του σπλήνα, η ογκώδης νόσος, η διήθηση του μυελού των οστών με βάση το ΡΕΤ, η μέγιστη πρόσληψη του SUV (SUVmax) και η τροποποίηση των πεδίων της IFRT,σύμφωνα με τη σταδιοποίηση με ΡΕΤ. Η παρουσία των Β-συμπτωμάτων είχε αρνητική προγνωστική αξία (5ετής FFP 86%, έναντι 74%, p=0.004).το στάδιο ήταν σημαντικός προγνωστικός παράγοντας για την FFP τόσο με τη συμβατική μέθοδο σταδιοποίησης (CS), όσο και με τη σταδιοποίηση με ΡΕΤ (ΡΕΤ/CT), (p<0.001 και για τις δύο μεθόδους). Η πενταετής FFP ήταν 100%, 85%, 86% και 59% για αυτούς με κλινικό στάδιο Ι,ΙΙ,ΙΙΙ,ΙV, έναντι 100%, 83%, 95% και 63% για αυτούς με ΡΕΤ σταδιοποίηση Ι,ΙΙ,ΙΙΙ,ΙV, αντίστοιχα (Διάγραμμα 1). Είναι αξιοσημείωτο ότι η πενταετής FFP για ασθενείς με στάδιο ΙΙΙ με βάση τη σταδιοποίηση με ΡΕΤ, ήταν καλύτερη από αυτή των ασθενών με στάδιο νόσου ΙΙ (95% έναντι 83%), μολονότι δεν ήταν στατιστικά σημαντική. Αυτό εξηγείται επειδή δεν καταγράφηκε κανένα συμβάν στους 10 ασθενείς με HL που ανέβηκαν επίπεδο από Ι/ΙΙ σύμφωνα με τη συμβατική σταδιοποίηση, σε ΡΕΤ στάδιο ΙΙΙ, ούτε και στο μοναδικό ασθενή που κατέβηκε στάδιο, από IV σε III, σύμφωνα με το ΡΕΤ. Οι ασθενείς που ανέβηκαν στάδιο με τη σταδιοποίηση με ΡΕΤ, είχαν εξαιρετική FFP. Αξίζει να σημειωθεί ότι αυτοί οι ασθενείς ανέβηκαν στάδιο κυρίως λόγω μικρών μεμονωμένων υποδιαφραγματικών υπερμεταβολικών λεμφαδενικών αλλοιώσεων και είχαν χαμηλό φορτίο νόσου, χωρίς ογκώδη νόσο. Η αύξηση ή μείωση του σταδίου με βάση τη σταδιοποίηση με PET δεν είχε καμμία προγνωστική σημασία, με πενταετή FFP 79% σε ασθενείς χωρίς διαφοροποίηση σταδίου, έναντι 89%, για αυτούς που ανέβηκαν στάδιο και 78% για αυτούς που κατέβηκαν στάδιο ( Διάγραμμα 2, p=0.547). 128
129 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Διάγραμμα 1: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom From Progression-FFP), σύμφωνα με την κλινική σταδιοποίηση (CS) (a) και τη σταδιοποίηση με την τομογραφία εκπομπής ποζιτρονίων/ αξονική τομογραφία (PET/CT) (b) 129
130 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Διάγραμμα 2: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom Fropm Progression-FFP) σύμφωνα με την άνοδο του σταδίου νόσου και την κάθοδο του σταδίου νόσου. Ο αριθμός των προσβεβλημένων περιοχών με βάση τη σταδιοποίηση με ΡΕΤ ήταν προγνωστικής σημασίας σε διάφορα όρια (cut-offs), όπως προσδιορίστηκε από την καμπύλη ROC. Απομονώθηκαν τρεις ομάδες ασθενών. Πιο συγκεκριμένα, ασθενείς με 2 περιοχές είχαν 5-ετή FFP 100%, έναντι 80% για αυτούς με 3-8 διηθημένες περιοχές και 69% για εκείνους με>8 προσβεβλημένες περιοχές (Διάγραμμα 3, p=0.004). Ο αριθμός των διηθημένων περιοχών σύμφωνα με την κλινική σταδιοποίηση ήταν λιγότερο σημαντικός συγκριτικά με τη σταδιοποίηση με ΡΕΤ, όντας στατιστικά σημαντικός μόνο στις περιπτώσεις με δύο και τρεις διηθημένες περιοχές ( p=0.02 και p=0.04, αντίστοιχα). Αξίζει να σημειωθεί ότι η έκβαση των 29 ασθενών στους οποίους η σταδιοποίηση με ΡΕΤ και η συμβατική σταδιοποίηση ανέδειξε ακριβώς τον ίδιο αριθμό εμπλεκόμενων περιοχών ήταν εξαιρετική, με 130
131 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία μία 5-ετή FFP 96% σε αντίθεση με τους υπόλοιπους ασθενείς, στους οποίους είτε προστέθηκαν, ή αφαιρέθηκαν περιοχές, ή και τα δύο. Οι ομάδες αυτές είχαν 5-ετή FFP 78%. Χρειάζεται να τονιστεί ότι ανάμεσα στην προηγούμενη ομάδα των 29 ασθενών, η συντριπτική πλειοψηφία (83%) είχαν αρχικό στάδιο νόσου ( συμβατική σταδιοποίηση CS I/II). Διάγραμμα 3: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom From Progression-FFP), σύμφωνα με τον αριθμό των προσβεβλημένων περιοχών PET/CT)(NIS by PET/CT) (Νumber of Involved Sites by Ομοίως, ο αριθμός των εξωλεμφαδενικών εντοπίσεων είχε στατιστική σημαντικότητα για την FFP τόσο με CS, όσο και με PET (p=0.001, p=0.003, αντίστοιχα) όπως ήταν και η πρόσληψη της FDG από το μυελό των οστών (Διάγραμμα 4, p< ). 131
132 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Διάγραμμα 4: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom From Progression-FFP), σύμφωνα με τον αριθμό των εξωλεμφαδενικών εντοπίσεων με βάση την CS(a) και με βάση το PET-S (b), σε ασθενείς με κλινικό στάδιο IV. Το SUVmax ήταν σημαντικό σε διάφορα σημεία (cut-offs), όπως προσδιορίστηκε από την καμπύλη ROC. Εντοπίστηκαν τρεις κατηγορίες ασθενών: οι ασθενείς με SUVmax 9 που είχαν 5-ετή FFP 93% έναντι 81% και 58% για τους συμμετέχοντες με SUVmax που κυμαινόταν μεταξύ 9 και 18, και αυτών με SUVmax> 18 αντίστοιχα (Διάγραμμα 5, p=0.009,). 132
133 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Διάγραμμα 5: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom From Progression-FFP), σύμφωνα με το SUVmax. Ακολούθως μελετήσαμε το γινόμενο του SUVmax x της μέγιστης διαμέτρου της βλάβης (Dmax), ως μία εκτίμηση της «συνολική γλυκόλυσης της βλάβης» (total lesion glycolysis-tlg). Mε βάση τις τιμές των ορίων (cut-offs) που προέκυψαν από την καμπύλη ROC, προσδιορίστηκαν τρεις ομάδες ασθενών με διαφορετική έκβαση: Βρέθηκαν 37 ασθενείς με μία τιμή του προαναφερθέντος γινομένου 35, 66 συμμετέχοντες παρουσίασαν μία τιμή που κυμαινόταν μεταξύ και 28 πάσχοντες με τιμή>100. Η έκβαση αυτών των τριών ομάδων ήταν σημαντικά διαφορετική, με τις αντίστοιχες τιμές 5-ετούς FFP να είναι 94%, 81% και 70% ( Διάγραμμα 6, p=0.04). 133
134 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή Διάγραμμα 6: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom From Progression-FFP), σύμφωνα με το αποτέλεσμα του γινομένου SUVmax x Dmax. ε. Συμπεράσματα σύμφωνα με την τροποποίηση της θεραπευτικής στρατηγικής Η αλλαγή της θεραπευτικής στρατηγικής σύμφωνα με τη σταδιοποίηση με ΡΕΤ δεν είχε καμμία επίπτωση στην έκβαση της νόσου. Μεταξύ των 23 ασθενών, στους οποίους η θεραπευτική στρατηγική μπορούσε να έχει αλλάξει σύμφωνα με τη σταδιοποίηση με ΡΕΤ, η 5-ετής FFP ήταν 92% για αυτούς που δεν άλλαξαν αγωγή έναντι 80% για εκείνους που άλλαξαν (Διάγραμμα 7, p=0.427). 134
135 Τομογραφία Εκπομπής Ποζιτρονίων (PET/CT) Στο Λεμφωμα Hodgkin. Συσχέτιση με τη Θεραπευτική Στρατηγική και την Ακτινοθεραπεία Διάγραμμα 7: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom From Progression-FFP), σύμφωνα με το αν η θεραπευτική στρατηγική βασίστηκε στην κλινική σταδιοποίηση (CS) ή στην σταδιοποίηση με ΡΕΤ (ΡΕΤ-S). Ακολούθως αξιολογήσαμε κατά πόσο η τροποποίηση των πεδίων της IFRT σύμφωνα με τις διηθημένες περιοχές με βάση το PEΤ/CT, επηρέαζε το αποτέλεσμα της θεραπείας. Ανάμεσα σε 63 ασθενείς, στους οποίους το πεδίο ακτινοθεραπείας μπορούσε να έχει αλλάξει σύμφωνα με τη σταδιοποίηση με ΡΕΤ, βρέθηκαν 20 ασθενείς, στους οποίους το πεδίο ακτινοθεραπείας πρακτικά δεν τροποποιήθηκε και 36 πάσχοντες, στους οποίους το πεδίο ακτινοθεραπείας, άλλαξε σύμφωνα με τη σταδιοποίηση με ΡΕΤ. Καταγράφηκαν επιπλέον και 7 ασθενείς που θεωρήθηκαν ως μη αξιολογήσιμοι, 5 εξαιτίας προόδου της νόσου και 2 λόγω τοξικού θανάτου, πριν τη χορήγηση ακτινοθεραπείας. Η FFP ήταν 90% για τους ασθενείς που δεν άλλαξαν πεδίο ακτινοθεραπείας με βάση τις εντοπίσεις του PET, έναντι 80% για τους ασθενείς στους οποίους τροποποιήθηκε ο 135
136 Ευτυχία Π. Μόσα, Διδακτορική Διατριβή σχεδιασμός της ακτινοθεραπείας ( Διάγραμμα 8a, p= 0.48), αντίστοιχα. Aυτή η διαφορά παρέμεινε στατιστικά μη-σημαντική, ακόμα και όταν μελετήθηκαν μεμονωμένα ασθενείς, με λέμφωμα Hodgkin αρχικών σταδίων (Διάγραμμα 8b, p=0.468). Διάγραμμα 8: Διάστημα ελεύθερο επιδείνωσης νόσου (Freedom From Progression-FFP), σύμφωνα με το πεδίο ακτινοθεραπείας με βάση την CS και τη PET-S, σε όλα τα στάδια της νόσου (a) στα αρχικά στάδια της νόσου(b). 136
ΛΕΜΦΩΜΑ HODGKIN. Τριανταφυλλιά Κολέτσα Λέκτορας Εργαστήριο Γενικής Παθολογίας και Παθολογικής Ανατομικής, ΑΠΘ
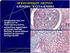 ΛΕΜΦΩΜΑ HODGKIN Τριανταφυλλιά Κολέτσα Λέκτορας Εργαστήριο Γενικής Παθολογίας και Παθολογικής Ανατομικής, ΑΠΘ Ταξινόμηση λεμφωμάτων- Βασικές αρχές Στην ταξινόμηση WHO: Λαμβάνονται υπόψη μορφολογικά, ανοσοϊστοχημικά,
ΛΕΜΦΩΜΑ HODGKIN Τριανταφυλλιά Κολέτσα Λέκτορας Εργαστήριο Γενικής Παθολογίας και Παθολογικής Ανατομικής, ΑΠΘ Ταξινόμηση λεμφωμάτων- Βασικές αρχές Στην ταξινόμηση WHO: Λαμβάνονται υπόψη μορφολογικά, ανοσοϊστοχημικά,
ΛΕΜΦΩΜΑ ΗΟDGKIN. Αλεξάνδρα Κουράκλη-Συμεωνίδου Απαρτιωμένη διδασκαλία 2015
 ΛΕΜΦΩΜΑ ΗΟDGKIN Αλεξάνδρα Κουράκλη-Συμεωνίδου Απαρτιωμένη διδασκαλία 2015 ΛΕΜΦΩΜΑ ΗΟDGKIN Επιδημιολογία - Αιτιοπαθογένεια Δικόρυφη καμπύλη εμφάνισης κορυφές: 15-40 έτη, >60 έτη : = Μικρή υπεροχή (1.5-2.0/1)
ΛΕΜΦΩΜΑ ΗΟDGKIN Αλεξάνδρα Κουράκλη-Συμεωνίδου Απαρτιωμένη διδασκαλία 2015 ΛΕΜΦΩΜΑ ΗΟDGKIN Επιδημιολογία - Αιτιοπαθογένεια Δικόρυφη καμπύλη εμφάνισης κορυφές: 15-40 έτη, >60 έτη : = Μικρή υπεροχή (1.5-2.0/1)
Ο Ιπποκράτης ως πατέρας της Ιατρικής και της Ιατρικής Δεοντολογίας και πρόδρομος της Βιοηθικής
 ΒΙΟΗΘΙΚΗ ΚΑΙ ΔΕΟΝΤΟΛΟΓΙΑ ΕΠΑΓΓΕΛΜΑΤΟΣ Ο Ιπποκράτης ως πατέρας της Ιατρικής και της Ιατρικής Δεοντολογίας και πρόδρομος της Βιοηθικής Ο Ιπποκράτης ο Κώος είναι ο πατέρας της ιατρικής επιστήμης, διδάσκοντας
ΒΙΟΗΘΙΚΗ ΚΑΙ ΔΕΟΝΤΟΛΟΓΙΑ ΕΠΑΓΓΕΛΜΑΤΟΣ Ο Ιπποκράτης ως πατέρας της Ιατρικής και της Ιατρικής Δεοντολογίας και πρόδρομος της Βιοηθικής Ο Ιπποκράτης ο Κώος είναι ο πατέρας της ιατρικής επιστήμης, διδάσκοντας
Λέµφωµα Hodgkin. Βλαχάκη Ευθυµία Επίκουρη Καθηγήτρια Αιµατολογίας-Αιµοσφαιρινοπαθειών ΑΠΘ
 Λέµφωµα Hodgkin Βλαχάκη Ευθυµία Επίκουρη Καθηγήτρια Αιµατολογίας-Αιµοσφαιρινοπαθειών ΑΠΘ Λεµφώµατα Κακοήθη νεοπλάσµατα του λεµφικού ιστού. Προσβάλλουν κυρίως τους λεµφαδένες, το σπλήνα και το µυελό των
Λέµφωµα Hodgkin Βλαχάκη Ευθυµία Επίκουρη Καθηγήτρια Αιµατολογίας-Αιµοσφαιρινοπαθειών ΑΠΘ Λεµφώµατα Κακοήθη νεοπλάσµατα του λεµφικού ιστού. Προσβάλλουν κυρίως τους λεµφαδένες, το σπλήνα και το µυελό των
ΠΑΡΟΥΣΙΑΣΗ ΠΕΡΙΣΤΑΤΙΚΟΥ
 ΠΑΡΟΥΣΙΑΣΗ ΠΕΡΙΣΤΑΤΙΚΟΥ ΠΟΥΛΙΑΝΙΤΗΣ ΝΙΚΟΛΑΟΣ ΕΙΔΙΚΕΥΟΜΕΝΟΣ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΓΝΑ Ο ΕΥΑΓΓΕΛΙΣΜΟΣ ΙΣΤΟΡΙΚΟ Βιοψίες κατά χρονολογική σειρά παραλαβής: 1. Βιοψία 2 ης μοίρας δωδεκαδακτύλου με αριθμό πρωτοκόλλου
ΠΑΡΟΥΣΙΑΣΗ ΠΕΡΙΣΤΑΤΙΚΟΥ ΠΟΥΛΙΑΝΙΤΗΣ ΝΙΚΟΛΑΟΣ ΕΙΔΙΚΕΥΟΜΕΝΟΣ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΓΝΑ Ο ΕΥΑΓΓΕΛΙΣΜΟΣ ΙΣΤΟΡΙΚΟ Βιοψίες κατά χρονολογική σειρά παραλαβής: 1. Βιοψία 2 ης μοίρας δωδεκαδακτύλου με αριθμό πρωτοκόλλου
Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας
 Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας Απαρτιωμένη διδασκαλία στην Αιματολογία 2015 Αργύρης Σ. Συμεωνίδης Οντότητες μη Hodgkin λεμφωμάτων που θα αναφερθούν Πρωτοπαθές Β-λέμφωμα
Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας Απαρτιωμένη διδασκαλία στην Αιματολογία 2015 Αργύρης Σ. Συμεωνίδης Οντότητες μη Hodgkin λεμφωμάτων που θα αναφερθούν Πρωτοπαθές Β-λέμφωμα
Λεμφώματα πνεύμονα (συνέχεια) Πηνελόπη Κορκολοπούλου Επ. Καθηγήτρια Εργαστήριο Παθολογικής Ανατομικής Πανεπιστημίου Αθηνών
 Λεμφώματα πνεύμονα (συνέχεια) Πηνελόπη Κορκολοπούλου Επ. Καθηγήτρια Εργαστήριο Παθολογικής Ανατομικής Πανεπιστημίου Αθηνών Αγγειοκεντρική ανοσοϋπερπλαστική νόσος / λέμφωμα πνεύμονος ΕΒV B T/NΚ Λεμφωματώδης
Λεμφώματα πνεύμονα (συνέχεια) Πηνελόπη Κορκολοπούλου Επ. Καθηγήτρια Εργαστήριο Παθολογικής Ανατομικής Πανεπιστημίου Αθηνών Αγγειοκεντρική ανοσοϋπερπλαστική νόσος / λέμφωμα πνεύμονος ΕΒV B T/NΚ Λεμφωματώδης
Aνασκόπηση. Ιστολογική εικόνα - Ταξινόμηση λεμφώματος Hodgkin. Πηνελόπη Κορκολοπούλου, Γεωργία Λεβίδου, Ευστράτιος Πατσούρης ΕΙΣΑΓΩΓΗ ΤΑΞΙΝΟΜΗΣΗ
 Aνασκόπηση Ιστολογική εικόνα - Ταξινόμηση λεμφώματος Hodgkin Πηνελόπη Κορκολοπούλου, Γεωργία Λεβίδου, Ευστράτιος Πατσούρης Περίληψη: Το λέμφωμα Hodgkin (HL) ταξινομείται σε δύο κύριους τύπους, τον οζώδη
Aνασκόπηση Ιστολογική εικόνα - Ταξινόμηση λεμφώματος Hodgkin Πηνελόπη Κορκολοπούλου, Γεωργία Λεβίδου, Ευστράτιος Πατσούρης Περίληψη: Το λέμφωμα Hodgkin (HL) ταξινομείται σε δύο κύριους τύπους, τον οζώδη
εοντολογία επαγγέλματος Professional Ethics
 εοντολογία επαγγέλματος Professional Ethics Εισηγητής: Μ. Βραχνάκης Σύγγραμμα: Καρατόλια-Μετζάκη Ζ. 2004. εοντολογία Επαγγέλματος Τεχνολόγων Γεωπόνων. Εκδόσεις Έλλην. Αθήνα. ΥΛΗ 1. Εισαγωγή Γενικά περί
εοντολογία επαγγέλματος Professional Ethics Εισηγητής: Μ. Βραχνάκης Σύγγραμμα: Καρατόλια-Μετζάκη Ζ. 2004. εοντολογία Επαγγέλματος Τεχνολόγων Γεωπόνων. Εκδόσεις Έλλην. Αθήνα. ΥΛΗ 1. Εισαγωγή Γενικά περί
PET/CT versus DWI-MRI στην ογκολογία του θώρακος. Ευθυμιάδου Ρωξάνη Τμήμα Αξονικής, Μαγνητικής Τομογραφίας & PET-CT ΔΘΚΑ «Υγεία»
 PET/CT versus DWI-MRI στην ογκολογία του θώρακος. Ευθυμιάδου Ρωξάνη Τμήμα Αξονικής, Μαγνητικής Τομογραφίας & PET-CT ΔΘΚΑ «Υγεία» Ca πνεύμονος Η πρώτη αιτία θανάτου από καρκίνο στο δ υτικό κόσμο. 3.000.000
PET/CT versus DWI-MRI στην ογκολογία του θώρακος. Ευθυμιάδου Ρωξάνη Τμήμα Αξονικής, Μαγνητικής Τομογραφίας & PET-CT ΔΘΚΑ «Υγεία» Ca πνεύμονος Η πρώτη αιτία θανάτου από καρκίνο στο δ υτικό κόσμο. 3.000.000
«Οὐ, μὰ τὸν ἁμετέρᾳ γενεᾷ παραδόντα τετρακτύν, παγάν ἀενάου φύσεως ῥιζώματ' ἔχουσαν»
 Όρκος Πυθαγορείων: «Οὐ, μὰ τὸν ἁμετέρᾳ γενεᾷ παραδόντα τετρακτύν, παγάν ἀενάου φύσεως ῥιζώματ' ἔχουσαν» [Οχι, μα τον παραδώσαντα και στη δική μας γενεά την τετρακτύν, την πηγή αιώνιας φύσεως που ριζώματα
Όρκος Πυθαγορείων: «Οὐ, μὰ τὸν ἁμετέρᾳ γενεᾷ παραδόντα τετρακτύν, παγάν ἀενάου φύσεως ῥιζώματ' ἔχουσαν» [Οχι, μα τον παραδώσαντα και στη δική μας γενεά την τετρακτύν, την πηγή αιώνιας φύσεως που ριζώματα
Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας
 Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας Απαρτιωμένη διδασκαλία στην Αιματολογία 2013 Αργύρης Σ. Συμεωνίδης Οντότητες μη Hodgkin λεμφωμάτων που θα αναφερθούν Πρωτοπαθές Β-λέμφωμα
Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας Απαρτιωμένη διδασκαλία στην Αιματολογία 2013 Αργύρης Σ. Συμεωνίδης Οντότητες μη Hodgkin λεμφωμάτων που θα αναφερθούν Πρωτοπαθές Β-λέμφωμα
ΕΙΔΙΚΗ ΠΑΘΟΛΟΓΙΚΗ ΑΝΑΤΟΜΙΚΗ
 ΕΙΔΙΚΗ ΠΑΘΟΛΟΓΙΚΗ ΑΝΑΤΟΜΙΚΗ Εργαστήριο Γεν. Παθολογίας και Παθολογικής Ανατομικής Α.Π.Θ. 5o ΦΡΟΝΤΙΣΤΗΡΙΟ ΛΕΜΦΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Διδάσκοντες: Αγγελική Χέβα Παθολογοανατόμος, ΠΓΝΘ «Γ. Παπανικολάου» Επιστημονικός
ΕΙΔΙΚΗ ΠΑΘΟΛΟΓΙΚΗ ΑΝΑΤΟΜΙΚΗ Εργαστήριο Γεν. Παθολογίας και Παθολογικής Ανατομικής Α.Π.Θ. 5o ΦΡΟΝΤΙΣΤΗΡΙΟ ΛΕΜΦΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Διδάσκοντες: Αγγελική Χέβα Παθολογοανατόμος, ΠΓΝΘ «Γ. Παπανικολάου» Επιστημονικός
HIV & Ca τραχήλου μήτρας. Άτομα μολυσμένα με HIV έχουν αυξημένη ροπή για την ανάπτυξη καρκίνου.
 HIV & Ca τραχήλου μήτρας Άτομα μολυσμένα με HIV έχουν αυξημένη ροπή για την ανάπτυξη καρκίνου. ΠΑΘΟΓΕΝΕΙΑ Πολλαπλοί παράγοντες μπορούν να συμβάλουν στην ανάπτυξη της κακοήθειας σε ασθενείς με AIDS. Οι
HIV & Ca τραχήλου μήτρας Άτομα μολυσμένα με HIV έχουν αυξημένη ροπή για την ανάπτυξη καρκίνου. ΠΑΘΟΓΕΝΕΙΑ Πολλαπλοί παράγοντες μπορούν να συμβάλουν στην ανάπτυξη της κακοήθειας σε ασθενείς με AIDS. Οι
ΛΕΜΦΑ ΕΝΙΚΟ ΛΕΜΦΩΜΑ ΟΡΙΑΚΗΣ ΖΩΝΗΣ ΙΣΤΟΛΟΓΙΚΗ ΕΙΚΟΝΑ
 ΛΕΜΦΑ ΕΝΙΚΟ ΛΕΜΦΩΜΑ ΟΡΙΑΚΗΣ ΖΩΝΗΣ ΙΣΤΟΛΟΓΙΚΗ ΕΙΚΟΝΑ Μικρά ή µεσαίου µεγέθους λεµφοειδή κύτταρα Πυρήνες στρογγυλοί ή ανωµάλου σχήµατος (µονοκυτταροειδείς ή σαν κεντροκύτταρα) ιαυγές κυτταρόπλασµα ΛΕΜΦΑ
ΛΕΜΦΑ ΕΝΙΚΟ ΛΕΜΦΩΜΑ ΟΡΙΑΚΗΣ ΖΩΝΗΣ ΙΣΤΟΛΟΓΙΚΗ ΕΙΚΟΝΑ Μικρά ή µεσαίου µεγέθους λεµφοειδή κύτταρα Πυρήνες στρογγυλοί ή ανωµάλου σχήµατος (µονοκυτταροειδείς ή σαν κεντροκύτταρα) ιαυγές κυτταρόπλασµα ΛΕΜΦΑ
Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις :
 Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις : Οι όρχεις αποτελούν κομμάτι του αναπαραγωγικού συστήματος (παραγωγή σπερματοζωάριων) του άνδρα αλλά
Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις : Οι όρχεις αποτελούν κομμάτι του αναπαραγωγικού συστήματος (παραγωγή σπερματοζωάριων) του άνδρα αλλά
Ενότητα 2011: Λεμφώματα
 Κλινικοεργαστηριακή Εκπαίδευση στην Αιματολογία Ενότητα 2011: Λεμφώματα 23-24 Σεπτεμβρίου 2011 Ηράκλειο, Κρήτη Διοργάνωση Ίδρυμα Ελληνικής Αιματολογικής Εταιρείας και Αιματολογική Κλινική Ιατρικής Σχολής
Κλινικοεργαστηριακή Εκπαίδευση στην Αιματολογία Ενότητα 2011: Λεμφώματα 23-24 Σεπτεμβρίου 2011 Ηράκλειο, Κρήτη Διοργάνωση Ίδρυμα Ελληνικής Αιματολογικής Εταιρείας και Αιματολογική Κλινική Ιατρικής Σχολής
Θα δoθεί πιστοποιητικό παρακολούθησης ΠΡΟΓΡΑΜΜΑ
 ΠΡΟΓΡΑΜΜΑ Θα δoθεί πιστοποιητικό παρακολούθησης Χαιρετισμός Αγαπητοί φίλοι και συνάδελφοι, Είναι χαρά μας να σας καλέσουμε στην Ημερίδα με τίτλο «Από τη στόχευση αντιγόνων στην ανοσοτροποποίηση και τη
ΠΡΟΓΡΑΜΜΑ Θα δoθεί πιστοποιητικό παρακολούθησης Χαιρετισμός Αγαπητοί φίλοι και συνάδελφοι, Είναι χαρά μας να σας καλέσουμε στην Ημερίδα με τίτλο «Από τη στόχευση αντιγόνων στην ανοσοτροποποίηση και τη
Συχνότητα. Άντρες Γυναίκες 5 1. Νεαρής και μέσης ηλικίας
 Η αιτιολογία της πάθησης είναι άγνωστη, αν και έχει μεγάλη σχέση με το κάπνισμα καθώς το 90% των ασθενών είναι ενεργείς καπνιστές Συχνότητα Άντρες Γυναίκες 5 1 Νεαρής και μέσης ηλικίας Στο 60% των περιπτώσεων
Η αιτιολογία της πάθησης είναι άγνωστη, αν και έχει μεγάλη σχέση με το κάπνισμα καθώς το 90% των ασθενών είναι ενεργείς καπνιστές Συχνότητα Άντρες Γυναίκες 5 1 Νεαρής και μέσης ηλικίας Στο 60% των περιπτώσεων
Γυναικολογικής Ογκολογίας
 3 o Masterclass Γυναικολογικής Ογκολογίας 2 18: Καρκίνος Ωοθηκών 8-9 Ιουνίου 2018 Electra Metropolis Hotel Αθήνα Διοργάνωση Ελληνικό Forum Ογκολογίας Με την συνεργασία της Ογκολογικής Μονάδας του Αρεταίειου
3 o Masterclass Γυναικολογικής Ογκολογίας 2 18: Καρκίνος Ωοθηκών 8-9 Ιουνίου 2018 Electra Metropolis Hotel Αθήνα Διοργάνωση Ελληνικό Forum Ογκολογίας Με την συνεργασία της Ογκολογικής Μονάδας του Αρεταίειου
ΜΕΛΕΤΗ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΤΗ ΘΕΡΑΠΕΙΑ
 ΕΡΕΥΝΗΤΙΚΗ ΜΟΝΑΔΑ: ΜΟΡΙΑΚΗ ΒΙΟΛΟΓΙΑ ΥΠΕΥΘΥΝΟΣ: ΤΣΕΖΟΥ ΑΣΠΑΣΙΑ ΜΕΛΕΤΗ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΤΗ ΘΕΡΑΠΕΙΑ ΠΑΠΑΝΙΚΟΛΑΟΥ Βασίλης, PhD Λάρισα, 2012 ΚΑΡΚΙΝΟΣ ΜΑΣΤΟΥ Αποτελεί την πιο κοινή μορφή
ΕΡΕΥΝΗΤΙΚΗ ΜΟΝΑΔΑ: ΜΟΡΙΑΚΗ ΒΙΟΛΟΓΙΑ ΥΠΕΥΘΥΝΟΣ: ΤΣΕΖΟΥ ΑΣΠΑΣΙΑ ΜΕΛΕΤΗ ΑΝΘΕΚΤΙΚΟΤΗΤΑΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΤΗ ΘΕΡΑΠΕΙΑ ΠΑΠΑΝΙΚΟΛΑΟΥ Βασίλης, PhD Λάρισα, 2012 ΚΑΡΚΙΝΟΣ ΜΑΣΤΟΥ Αποτελεί την πιο κοινή μορφή
ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΣΕ ΑΣΘΕΝΗ ΜΕ ΚΑΡΚΙΝΟ ΟΥΡΟΠΟΙΗΤΙΚΟΥ
 ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΣΕ ΑΣΘΕΝΗ ΜΕ ΚΑΡΚΙΝΟ ΟΥΡΟΠΟΙΗΤΙΚΟΥ ΜΠΑΡΚΟΥ ΑΝΑΣΤΑΣΙΑ ΑΝ Α Π Λ Η Ρ Ω Τ Ρ Ι Α Π Ρ Ο Ϊ Σ ΤΑΜ Ε Ν Η ΟΥ Ρ ΟΛΟ Γ Ι ΚΟΥ- Ο Γ ΚΟΛΟ Γ Ι ΚΟΥ Τ Μ Η Μ ΑΤΟ Σ ΑΝ Θ «Θ Ε ΑΓ Ε Ν Ε Ι Ο» ΠΟΙΟΤΗΤΑ ΖΩΗΣ Βασική
ΠΟΙΟΤΗΤΑ ΖΩΗΣ ΣΕ ΑΣΘΕΝΗ ΜΕ ΚΑΡΚΙΝΟ ΟΥΡΟΠΟΙΗΤΙΚΟΥ ΜΠΑΡΚΟΥ ΑΝΑΣΤΑΣΙΑ ΑΝ Α Π Λ Η Ρ Ω Τ Ρ Ι Α Π Ρ Ο Ϊ Σ ΤΑΜ Ε Ν Η ΟΥ Ρ ΟΛΟ Γ Ι ΚΟΥ- Ο Γ ΚΟΛΟ Γ Ι ΚΟΥ Τ Μ Η Μ ΑΤΟ Σ ΑΝ Θ «Θ Ε ΑΓ Ε Ν Ε Ι Ο» ΠΟΙΟΤΗΤΑ ΖΩΗΣ Βασική
ΠΑΘΟΓΕΝΕΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΚΟΙ ΤΥΠΟΙ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ
 ΠΑΘΟΓΕΝΕΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΚΟΙ ΤΥΠΟΙ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ Χρ.Τσοµπανίδου Παθολογοανατόµος Συντονίστρια Διευθύντρια Νοσοκοµείο Θεσ/νίκης «Άγιος Δηµήτριος» προέρχονται από το φυσιολογικό επιθήλιο µε την
ΠΑΘΟΓΕΝΕΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΚΟΙ ΤΥΠΟΙ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ Χρ.Τσοµπανίδου Παθολογοανατόµος Συντονίστρια Διευθύντρια Νοσοκοµείο Θεσ/νίκης «Άγιος Δηµήτριος» προέρχονται από το φυσιολογικό επιθήλιο µε την
ΠΡΟΛΗΨΗ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΣΕΓΓΙΣΕΙΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ ΕΠΙΔΗΜΙΟΛΟΓΙΑ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ
 ΠΡΟΛΗΨΗ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΣΕΓΓΙΣΕΙΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ ΕΠΙΔΗΜΙΟΛΟΓΙΑ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ Σοφία Τούσα, Ειδικευόµενη Γενικής Ιατρικής στο Γενικό Νοσοκοµείο Έδεσσας, MSc, υποψήφια διδάκτωρ
ΠΡΟΛΗΨΗ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΣΕΓΓΙΣΕΙΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ ΕΠΙΔΗΜΙΟΛΟΓΙΑ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ Σοφία Τούσα, Ειδικευόµενη Γενικής Ιατρικής στο Γενικό Νοσοκοµείο Έδεσσας, MSc, υποψήφια διδάκτωρ
Εξωτερική Ακτινοθεραπεία Προστάτη. Εξωτερική Ακτινοθεραπεία Προστάτη
 Εξωτερική Ακτινοθεραπεία Προστάτη Εξωτερική Ακτινοθεραπεία Προστάτη Σχεδιασμός Ακτινοθεραπείας Προστάτη Σχεδιασμός Ακτινοθεραπείας Προστάτη (Treatment Planning): σύγκριση απεικόνισης μεταξύ Αξονικής και
Εξωτερική Ακτινοθεραπεία Προστάτη Εξωτερική Ακτινοθεραπεία Προστάτη Σχεδιασμός Ακτινοθεραπείας Προστάτη Σχεδιασμός Ακτινοθεραπείας Προστάτη (Treatment Planning): σύγκριση απεικόνισης μεταξύ Αξονικής και
Δρ. Χριστίνα Γιαννάκη Γενική Διευθύντρια Υπουργείου Υγείας
 Δρ. Χριστίνα Γιαννάκη Γενική Διευθύντρια Υπουργείου Υγείας Το Υπουργείο Υγείας αναγνωρίζοντας την ανάγκη για βελτίωση των παρεχόμενων υπηρεσιών στους ασθενείς που χρήζουν ακτινοθεραπείας στην Κύπρο, προχώρησε
Δρ. Χριστίνα Γιαννάκη Γενική Διευθύντρια Υπουργείου Υγείας Το Υπουργείο Υγείας αναγνωρίζοντας την ανάγκη για βελτίωση των παρεχόμενων υπηρεσιών στους ασθενείς που χρήζουν ακτινοθεραπείας στην Κύπρο, προχώρησε
ΟΓΚΟΙ ΤΗΣ ΑΣΤΡΟΚΥΤΤΑΡΙΚΗΣ ΓΛΟΙΑΣ. Θωµάς Ζαραµπούκας. Αν. Καθ. Παθολογικής Ανατοµικής. Ιατρική Σχολή Α.Π.Θ.
 ΟΓΚΟΙ ΤΗΣ ΑΣΤΡΟΚΥΤΤΑΡΙΚΗΣ ΓΛΟΙΑΣ Θωµάς Ζαραµπούκας Αν. Καθ. Παθολογικής Ανατοµικής Ιατρική Σχολή Α.Π.Θ. Όγκοι της Αστροκυτταρικής Γλοίας Πιλοκυτταρικό αστροκύτωµα Πιλοµυξοειδές αστροκύτωµα Πλειόµορφο ξανθοαστροκύτωµα
ΟΓΚΟΙ ΤΗΣ ΑΣΤΡΟΚΥΤΤΑΡΙΚΗΣ ΓΛΟΙΑΣ Θωµάς Ζαραµπούκας Αν. Καθ. Παθολογικής Ανατοµικής Ιατρική Σχολή Α.Π.Θ. Όγκοι της Αστροκυτταρικής Γλοίας Πιλοκυτταρικό αστροκύτωµα Πιλοµυξοειδές αστροκύτωµα Πλειόµορφο ξανθοαστροκύτωµα
MRD ΠΜ ΧΛΛ. Σωσάνα Δελήμπαση ΓΝ<<Ο Ευαγγελισμός>>
 MRD ΠΜ ΧΛΛ Σωσάνα Δελήμπαση ΓΝ ΟΡΙΣΜΟΣ ΤΗΣ MRD Κάθε προσέγγιση που έχει σαν στόχο την ανίχνευση και αν είναι εφικτό τη μέτρηση των υπολειμματικών καρκινικών κυττάρων πέρα από την ευαισθησία
MRD ΠΜ ΧΛΛ Σωσάνα Δελήμπαση ΓΝ ΟΡΙΣΜΟΣ ΤΗΣ MRD Κάθε προσέγγιση που έχει σαν στόχο την ανίχνευση και αν είναι εφικτό τη μέτρηση των υπολειμματικών καρκινικών κυττάρων πέρα από την ευαισθησία
15/1/2018. Δρ. Σάββας Παρασκευόπουλος Χειρουργός Ουρολόγος Θεσσαλονίκη 2-5 /11/ ο Μακεδονικό Ουρολογικό Συμπόσιο
 Η χρήση του PET CT στην Ογκολογία και όχι μόνο Δρ. Σάββας Παρασκευόπουλος Χειρουργός Ουρολόγος Θεσσαλονίκη 2-5 /11/2017 11ο Μακεδονικό Ουρολογικό Συμπόσιο 1 Τι είναι το PET SCAN; Η Pet scan (pozitron emission
Η χρήση του PET CT στην Ογκολογία και όχι μόνο Δρ. Σάββας Παρασκευόπουλος Χειρουργός Ουρολόγος Θεσσαλονίκη 2-5 /11/2017 11ο Μακεδονικό Ουρολογικό Συμπόσιο 1 Τι είναι το PET SCAN; Η Pet scan (pozitron emission
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων
 Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Προληπτική Μαστογραφία Ανακαλύπτοντας το DCIS. Ιωάννης Θ. Νατσιόπουλος Ειδικός Χειρουργός Μαστού
 Προληπτική Μαστογραφία Ανακαλύπτοντας το DCIS Ιωάννης Θ. Νατσιόπουλος Ειδικός Χειρουργός Μαστού Ductal Carcinoma in Situ Πορογενές καρκίνωμα in Situ In Situ = επί τόπου Τοπικό πορογενές καρκίνωμα; Ductal
Προληπτική Μαστογραφία Ανακαλύπτοντας το DCIS Ιωάννης Θ. Νατσιόπουλος Ειδικός Χειρουργός Μαστού Ductal Carcinoma in Situ Πορογενές καρκίνωμα in Situ In Situ = επί τόπου Τοπικό πορογενές καρκίνωμα; Ductal
Μήπως έχω Σκληρόδερµα;
 Μήπως έχω Σκληρόδερµα; Για να πληροφορηθώ µýëïò ôçò Σπάνιος ναι... Μόνος όχι Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών σπανίων παθήσεων
Μήπως έχω Σκληρόδερµα; Για να πληροφορηθώ µýëïò ôçò Σπάνιος ναι... Μόνος όχι Η Πανελλήνια Ένωση Σπανίων Παθήσεων (Π.Ε.Σ.ΠΑ) είναι ο μόνος φορέας, μη κερδοσκοπικό σωματείο, συλλόγων ασθενών σπανίων παθήσεων
ΛΕΜΦΙΚΟΣ ΙΣΤΟΣ. Ιωάννης Κωστόπουλος Καθηγητής Εργαστήριο Γεν. Παθολογίας και Παθολογικής Ανατομικής Α.Π.Θ.
 ΛΕΜΦΙΚΟΣ ΙΣΤΟΣ Ιωάννης Κωστόπουλος Καθηγητής Εργαστήριο Γεν. Παθολογίας και Παθολογικής Ανατομικής Α.Π.Θ. ΛΕΜΦΑΔΕΝΕΣ ΛΕΜΦΑΔΕΝΕΣ Βλαστικά κέντρα ΛΕΜΦΑΔΕΝΕΣ Βλαστικά κέντρα ΛΕΜΦΑΔΕΝΕΣ Βλαστικά κέντρα CD20/L26
ΛΕΜΦΙΚΟΣ ΙΣΤΟΣ Ιωάννης Κωστόπουλος Καθηγητής Εργαστήριο Γεν. Παθολογίας και Παθολογικής Ανατομικής Α.Π.Θ. ΛΕΜΦΑΔΕΝΕΣ ΛΕΜΦΑΔΕΝΕΣ Βλαστικά κέντρα ΛΕΜΦΑΔΕΝΕΣ Βλαστικά κέντρα ΛΕΜΦΑΔΕΝΕΣ Βλαστικά κέντρα CD20/L26
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ. ΝΙΚΟΛΑΟΣ ΚΑΒΑΝΤΖΑΣ Επίκουρος Καθηγητής
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ ΝΙΚΟΛΑΟΣ ΚΑΒΑΝΤΖΑΣ Επίκουρος Καθηγητής ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ Επιφυσιοβλάστωµα Επιφυσιοκύττωµα Ογκος
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ ΝΙΚΟΛΑΟΣ ΚΑΒΑΝΤΖΑΣ Επίκουρος Καθηγητής ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ Επιφυσιοβλάστωµα Επιφυσιοκύττωµα Ογκος
ΣΥΝΟΠΤΙΚΟ ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ
 ΣΥΝΟΠΤΙΚΟ ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Μανούσος Μ. Κωνσταντουλάκης ΗΜΕΡΟΜΗΝΙΑ ΓΕΝΝΗΣΗΣ: 23 Ιουνίου 1965 ΤΟΠΟΣ ΓΕΝΝΗΣΗΣ: Αθήνα ΔΙΕΥΘΥΝΣΗ ΚΑΤΟΙΚΙΑΣ: Κάλβου 24, Π. Ψυχικό 15452 Αθήνα ΣΤΡΑΤΙΩΤΙΚΗ ΘΗΤΕΙΑ:
ΣΥΝΟΠΤΙΚΟ ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: Μανούσος Μ. Κωνσταντουλάκης ΗΜΕΡΟΜΗΝΙΑ ΓΕΝΝΗΣΗΣ: 23 Ιουνίου 1965 ΤΟΠΟΣ ΓΕΝΝΗΣΗΣ: Αθήνα ΔΙΕΥΘΥΝΣΗ ΚΑΤΟΙΚΙΑΣ: Κάλβου 24, Π. Ψυχικό 15452 Αθήνα ΣΤΡΑΤΙΩΤΙΚΗ ΘΗΤΕΙΑ:
ΠΑΡΟΞΥΣΜΙΚΗ ΝΥΚΤΕΡΙΝΗ ΑΙΜΟΣΦΑΙΡΙΝΟΥΡΙΑ (PNH) Αχιλλέας Θ. Καραμούτσιος Μονάδα Μοριακής Βιολογίας, Αιματολογικό Εργαστήριο ΠΓΝ Ιωαννίνων
 ΠΑΡΟΞΥΣΜΙΚΗ ΝΥΚΤΕΡΙΝΗ ΑΙΜΟΣΦΑΙΡΙΝΟΥΡΙΑ (PNH) Αχιλλέας Θ. Καραμούτσιος Μονάδα Μοριακής Βιολογίας, Αιματολογικό Εργαστήριο ΠΓΝ Ιωαννίνων Ιωάννινα, Σεπτέμβριος 2013 PNH Σπάνια διαταραχή του αρχέγονου αιμοποιητικού
ΠΑΡΟΞΥΣΜΙΚΗ ΝΥΚΤΕΡΙΝΗ ΑΙΜΟΣΦΑΙΡΙΝΟΥΡΙΑ (PNH) Αχιλλέας Θ. Καραμούτσιος Μονάδα Μοριακής Βιολογίας, Αιματολογικό Εργαστήριο ΠΓΝ Ιωαννίνων Ιωάννινα, Σεπτέμβριος 2013 PNH Σπάνια διαταραχή του αρχέγονου αιμοποιητικού
ΠΟΛΛΑΠΛΟΥΝ ΜΥΕΛΩΜΑ ΕΝΗΜΕΡΩΤΙΚΟ ΦΥΛΛΑΔΙΟ ΓΙΑ ΤΟΥΣ ΑΣΘΕΝΕΙΣ. Έκδοση του IΔPYMAΤΟΣ EΛΛHNIKHΣ AIMATOΛOΓIKHΣ ETAIPEIAΣ. Οκτώβριος 2016.
 ΠΟΛΛΑΠΛΟΥΝ ΜΥΕΛΩΜΑ 1 ΠΟΛΛΑΠΛΟΥΝ ΜΥΕΛΩΜΑ ΕΝΗΜΕΡΩΤΙΚΟ ΦΥΛΛΑΔΙΟ ΓΙΑ ΤΟΥΣ ΑΣΘΕΝΕΙΣ Έκδοση του IΔPYMAΤΟΣ EΛΛHNIKHΣ AIMATOΛOΓIKHΣ ETAIPEIAΣ Οκτώβριος 2016 2η Έκδοση ΠΟΛΛΑΠΛΟΥΝ ΜΥΕΛΩΜΑ 1 Πρόλογος Το Ίδρυμα της
ΠΟΛΛΑΠΛΟΥΝ ΜΥΕΛΩΜΑ 1 ΠΟΛΛΑΠΛΟΥΝ ΜΥΕΛΩΜΑ ΕΝΗΜΕΡΩΤΙΚΟ ΦΥΛΛΑΔΙΟ ΓΙΑ ΤΟΥΣ ΑΣΘΕΝΕΙΣ Έκδοση του IΔPYMAΤΟΣ EΛΛHNIKHΣ AIMATOΛOΓIKHΣ ETAIPEIAΣ Οκτώβριος 2016 2η Έκδοση ΠΟΛΛΑΠΛΟΥΝ ΜΥΕΛΩΜΑ 1 Πρόλογος Το Ίδρυμα της
Πανεπιστήμιο Θεσσαλίας Τμήμα Ιατρικής Εργαστήριο Ακτινολογίας Ιατρικής Απεικόνισης
 Πανεπιστήμιο Θεσσαλίας Τμήμα Ιατρικής Εργαστήριο Ακτινολογίας Ιατρικής Απεικόνισης Διδάσκοντες Ιωάννης Β. Φεζουλίδης Καθηγητής Μαριάννα Βλυχού Αναπλ. Καθηγήτρια Έφη Καψαλάκη Αναπλ. Καθηγήτρια Αικατερίνη
Πανεπιστήμιο Θεσσαλίας Τμήμα Ιατρικής Εργαστήριο Ακτινολογίας Ιατρικής Απεικόνισης Διδάσκοντες Ιωάννης Β. Φεζουλίδης Καθηγητής Μαριάννα Βλυχού Αναπλ. Καθηγήτρια Έφη Καψαλάκη Αναπλ. Καθηγήτρια Αικατερίνη
ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΕΙΔΙΚΕΥΣΗΣ: ΒΙΟΛΟΓΙΑ ΣΤΟΜΑΤΟΣ. Οδηγός Προγράμματος
 ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΕΙΔΙΚΕΥΣΗΣ: ΒΙΟΛΟΓΙΑ ΣΤΟΜΑΤΟΣ Οδηγός Προγράμματος του προγράμματος του προγράμματος είναι η ειδίκευση στη βιολογία των οδόντων και της στοματικής κοιλότητας, με εξέταση των δομών
ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΕΙΔΙΚΕΥΣΗΣ: ΒΙΟΛΟΓΙΑ ΣΤΟΜΑΤΟΣ Οδηγός Προγράμματος του προγράμματος του προγράμματος είναι η ειδίκευση στη βιολογία των οδόντων και της στοματικής κοιλότητας, με εξέταση των δομών
Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ. Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη
 Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη 2013 ΠΕΡΙΕΧΟΜΕΝΑ : Ορολογία και λίγα λόγια για τον καρκίνο Χαρακτηριστικά του καρκίνου Μεταλλάξεις Μεταλλάξεις και καρκίνος
Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη 2013 ΠΕΡΙΕΧΟΜΕΝΑ : Ορολογία και λίγα λόγια για τον καρκίνο Χαρακτηριστικά του καρκίνου Μεταλλάξεις Μεταλλάξεις και καρκίνος
Ethics. Derived from the Greek word ethos which means customs, habitual usage, conduct and character.
 Ethics Derived from the Greek word ethos which means customs, habitual usage, conduct and character. Moral principles that govern a person s behavior or the conducting of an activity Branch of knowledge
Ethics Derived from the Greek word ethos which means customs, habitual usage, conduct and character. Moral principles that govern a person s behavior or the conducting of an activity Branch of knowledge
TI NEOTEΡΟ ΣΤΟΥΣ ΝΕΥΡΟΕΝΔΟΚΡΙΝΕΙΣ ΟΓΚΟΥΣ ΤΟ 2015. Ορισμοί-Κατάταξη-Ιστολογία. Δ Ροντογιάννη
 TI NEOTEΡΟ ΣΤΟΥΣ ΝΕΥΡΟΕΝΔΟΚΡΙΝΕΙΣ ΟΓΚΟΥΣ ΤΟ 2015 Ορισμοί-Κατάταξη-Ιστολογία Δ Ροντογιάννη Νευροενδοκρινή νεοπλάσματα Ταξινόμηση Βιολογικοί δείκτες Μοριακή Παθολογία Νευροενδοκρινή νεοπλάσματα Ταξινόμηση
TI NEOTEΡΟ ΣΤΟΥΣ ΝΕΥΡΟΕΝΔΟΚΡΙΝΕΙΣ ΟΓΚΟΥΣ ΤΟ 2015 Ορισμοί-Κατάταξη-Ιστολογία Δ Ροντογιάννη Νευροενδοκρινή νεοπλάσματα Ταξινόμηση Βιολογικοί δείκτες Μοριακή Παθολογία Νευροενδοκρινή νεοπλάσματα Ταξινόμηση
Παθολογοανατομική προσέγγιση διάγνωση. Σχολιασμός Δημ. Σαμπαζιώτης, Ειδικευόμενος
 Παθολογοανατομική προσέγγιση διάγνωση Σχολιασμός Δημ. Σαμπαζιώτης, Ειδικευόμενος Παρασκευή Οστεομυελικής βιοψίας (ΟΜΒ) Επαρκής διαγνωστική ΟΜΒ πρέπει να είναι τουλάχιστον 1.5εκ, με απουσία crush artifact
Παθολογοανατομική προσέγγιση διάγνωση Σχολιασμός Δημ. Σαμπαζιώτης, Ειδικευόμενος Παρασκευή Οστεομυελικής βιοψίας (ΟΜΒ) Επαρκής διαγνωστική ΟΜΒ πρέπει να είναι τουλάχιστον 1.5εκ, με απουσία crush artifact
ΚΑΚΟΗΘΗ ΝΟΣΗΜΑΤΑ ΣΤΗΝ ΠΑΙΔΙΚΗ ΗΛΙΚΙΑ ΚΑΙ ΝΟΣΗΛΕΥΤΙΚΗ ΠΑΡΕΜΒΑΣΗ
 ΚΑΚΟΗΘΗ ΝΟΣΗΜΑΤΑ ΣΤΗΝ ΠΑΙΔΙΚΗ ΗΛΙΚΙΑ ΚΑΙ ΝΟΣΗΛΕΥΤΙΚΗ ΠΑΡΕΜΒΑΣΗ Επιβλέπουσα Α.ΤΕΙ.Θ Ε. ΔΙΑΜΑΝΤΟΠΟΥΛΟΥ Μέλη Επιτροπής Λαβδανίτη Μαρία Μινασίδου Ευγενία Αλεξιάδη Αθηνά Γεωργάκη Ελένη Αλεξάνδρειο Τεχνολογικό
ΚΑΚΟΗΘΗ ΝΟΣΗΜΑΤΑ ΣΤΗΝ ΠΑΙΔΙΚΗ ΗΛΙΚΙΑ ΚΑΙ ΝΟΣΗΛΕΥΤΙΚΗ ΠΑΡΕΜΒΑΣΗ Επιβλέπουσα Α.ΤΕΙ.Θ Ε. ΔΙΑΜΑΝΤΟΠΟΥΛΟΥ Μέλη Επιτροπής Λαβδανίτη Μαρία Μινασίδου Ευγενία Αλεξιάδη Αθηνά Γεωργάκη Ελένη Αλεξάνδρειο Τεχνολογικό
Διαχείριση της βιοχημικής υποτροπής στον καρκίνο του προστάτη
 Μωυσίδης Κυριάκος Λέκτορας Ουρoλογίας Β ουρολογική κλινική του Α.Π.Θ. Διευθυντής Καθηγητής Ε. Ιωαννίδης Διαχείριση της βιοχημικής υποτροπής στον καρκίνο του προστάτη Καρκίνος του προστάτη Yπάρχει κάποια
Μωυσίδης Κυριάκος Λέκτορας Ουρoλογίας Β ουρολογική κλινική του Α.Π.Θ. Διευθυντής Καθηγητής Ε. Ιωαννίδης Διαχείριση της βιοχημικής υποτροπής στον καρκίνο του προστάτη Καρκίνος του προστάτη Yπάρχει κάποια
Α ΜΑΙΕΥΤΙΚΗ & ΓΥΝΑΙΚΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΤΜΗΜΑ ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Γ.Ν.Α. «ΑΛΕΞΑΝΔΡΑ» ΝΟΣΟΣ PAGET ΑΙΔΟΙΟΥ
 Α ΜΑΙΕΥΤΙΚΗ & ΓΥΝΑΙΚΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΤΜΗΜΑ ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Γ.Ν.Α. «ΑΛΕΞΑΝΔΡΑ» ΝΟΣΟΣ PAGET ΑΙΔΟΙΟΥ Κουτρούµπα Ι, Χαϊδόπουλος Δ, Θωµάκος Ν, Σωτηροπούλου Μ, Καθοπούλης Ν, Βλάχος
Α ΜΑΙΕΥΤΙΚΗ & ΓΥΝΑΙΚΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΤΜΗΜΑ ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Γ.Ν.Α. «ΑΛΕΞΑΝΔΡΑ» ΝΟΣΟΣ PAGET ΑΙΔΟΙΟΥ Κουτρούµπα Ι, Χαϊδόπουλος Δ, Θωµάκος Ν, Σωτηροπούλου Μ, Καθοπούλης Ν, Βλάχος
Εντοπίζεται συνήθως τυχαία διότι δεν εκδηλώνεται με πόνο. Εξαίρεση αποτελούν κάποιες πολύ σπάνιες προχωρημένες περιπτώσεις.
 8SELIDO ENTIPO AGALIAZO.indd 1 Εισαγωγή Το έντυπο που κρατάτε στα χέρια σας έχει γραφτεί για να ρίξει φως στα σημαντικά σημεία για τον καρκίνου του θυρεοειδούς ο οποίος αποτελεί έναν από τους πιο σπάνιους
8SELIDO ENTIPO AGALIAZO.indd 1 Εισαγωγή Το έντυπο που κρατάτε στα χέρια σας έχει γραφτεί για να ρίξει φως στα σημαντικά σημεία για τον καρκίνου του θυρεοειδούς ο οποίος αποτελεί έναν από τους πιο σπάνιους
ΜΟΡΙΑΚΗ ΒΑΣΗ ΓΕΝΕΤΙΚΩΝ ΑΣΘΕΝΕΙΩΝ ΘΕΜΑ: ΠΟΛΛΑΠΛΗ ΝΕΥΡΟΙΝΩΜΑΤΩΣΗ. Ομάδα ΑΡΕΑΛΗ ΑΝΤΩΝΙΑ ΜΠΑΗ ΙΩΑΝΝΑ ΠΑΤΕΡΑΚΗ ΕΛΕΝΗ
 ΜΟΡΙΑΚΗ ΒΑΣΗ ΓΕΝΕΤΙΚΩΝ ΑΣΘΕΝΕΙΩΝ ΘΕΜΑ: ΠΟΛΛΑΠΛΗ ΝΕΥΡΟΙΝΩΜΑΤΩΣΗ Ομάδα ΑΡΕΑΛΗ ΑΝΤΩΝΙΑ ΜΠΑΗ ΙΩΑΝΝΑ ΠΑΤΕΡΑΚΗ ΕΛΕΝΗ ΑΠΡΙΛΙΟΣ 2015 ΣΚΟΠΟΣ Σκοπός της εργασίας αυτής είναι η παρουσίαση των χαρακτηριστικών της
ΜΟΡΙΑΚΗ ΒΑΣΗ ΓΕΝΕΤΙΚΩΝ ΑΣΘΕΝΕΙΩΝ ΘΕΜΑ: ΠΟΛΛΑΠΛΗ ΝΕΥΡΟΙΝΩΜΑΤΩΣΗ Ομάδα ΑΡΕΑΛΗ ΑΝΤΩΝΙΑ ΜΠΑΗ ΙΩΑΝΝΑ ΠΑΤΕΡΑΚΗ ΕΛΕΝΗ ΑΠΡΙΛΙΟΣ 2015 ΣΚΟΠΟΣ Σκοπός της εργασίας αυτής είναι η παρουσίαση των χαρακτηριστικών της
ΛΕΜΦΩΜΑΤΑ ΟΡΙΑΚΗΣ ΖΩΝΗΣ
 ΛΕΜΦΩΜΑΤΑ ΟΡΙΑΚΗΣ ΖΩΝΗΣ Πηνελόπη Κορκολοπούλου Αν. Καθηγήτρια Παθολογικής Ανατοµικής Παν/µίου Αθηνών 1 Β-ΛΕΜΦΩΜΑ ΑΠO ΤΟ ΚΥΤΤΑΡΟ ΤΗΣ ΟΡΙΑΚΗΣ ΖΩΝΗΣ (MZL) (WHO 2001) Tρεις τύποι λεµφωµάτων τα οποία αποτελούν
ΛΕΜΦΩΜΑΤΑ ΟΡΙΑΚΗΣ ΖΩΝΗΣ Πηνελόπη Κορκολοπούλου Αν. Καθηγήτρια Παθολογικής Ανατοµικής Παν/µίου Αθηνών 1 Β-ΛΕΜΦΩΜΑ ΑΠO ΤΟ ΚΥΤΤΑΡΟ ΤΗΣ ΟΡΙΑΚΗΣ ΖΩΝΗΣ (MZL) (WHO 2001) Tρεις τύποι λεµφωµάτων τα οποία αποτελούν
ΗPV και Καρκίνος Δέρµατος. Ηλέκτρα Νικολαΐδου Επ. Καθηγήτρια Δερµατολογίας ΕΚΠΑ Νοσ. «Α. Συγγρός»
 ΗPV και Καρκίνος Δέρµατος Ηλέκτρα Νικολαΐδου Επ. Καθηγήτρια Δερµατολογίας ΕΚΠΑ Νοσ. «Α. Συγγρός» ΓΕΝΗ HPV Α γένος: βλεννογόνοι αιτιολογική συσχέτιση µε καρκίνο τραχήλου µήτρας, πρωκτού, αιδοίου, πέους
ΗPV και Καρκίνος Δέρµατος Ηλέκτρα Νικολαΐδου Επ. Καθηγήτρια Δερµατολογίας ΕΚΠΑ Νοσ. «Α. Συγγρός» ΓΕΝΗ HPV Α γένος: βλεννογόνοι αιτιολογική συσχέτιση µε καρκίνο τραχήλου µήτρας, πρωκτού, αιδοίου, πέους
Ανι χνευση μεταλλα ξεων στον καρκι νο και εξατομικευμε νη θεραπει α
 Ανι χνευση μεταλλα ξεων στον καρκι νο και εξατομικευμε νη θεραπει α Περικλής Μακρυθανα σης, MD, PhD, FMH, PD Κλινικός γενετιστής Κύριος Ερευνητής Ίδρυμα Ιατροβιολογικών Ερευνών της Ακαδημι ας Αθηνών 4o
Ανι χνευση μεταλλα ξεων στον καρκι νο και εξατομικευμε νη θεραπει α Περικλής Μακρυθανα σης, MD, PhD, FMH, PD Κλινικός γενετιστής Κύριος Ερευνητής Ίδρυμα Ιατροβιολογικών Ερευνών της Ακαδημι ας Αθηνών 4o
Παράρτημα IV. Επιστημονικά πορίσματα
 Παράρτημα IV Επιστημονικά πορίσματα 1 Επιστημονικά πορίσματα Στις 10 Μαρτίου 2016, η Ευρωπαϊκή Επιτροπή πληροφορήθηκε ότι η Ανεξάρτητη Ομάδα Παρακολούθησης Δεδομένων Ασφαλείας παρατήρησε σε τρεις κλινικές
Παράρτημα IV Επιστημονικά πορίσματα 1 Επιστημονικά πορίσματα Στις 10 Μαρτίου 2016, η Ευρωπαϊκή Επιτροπή πληροφορήθηκε ότι η Ανεξάρτητη Ομάδα Παρακολούθησης Δεδομένων Ασφαλείας παρατήρησε σε τρεις κλινικές
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΛΙΝΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΚΑΙ ΜΕΛΕΤΗ ΙΣΟΜΟΡΦΩΝ ΤΗΣ L-DOPA ΑΠΟΚΑΡΒΟΞΥΛΑΣΗΣ ΚΑΙ ΤΟΥ
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΙΟΧΗΜΕΙΑΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΒΙΟΛΟΓΙΑΣ ΚΛΙΝΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΚΑΙ ΜΕΛΕΤΗ ΙΣΟΜΟΡΦΩΝ ΤΗΣ L-DOPA ΑΠΟΚΑΡΒΟΞΥΛΑΣΗΣ ΚΑΙ ΤΟΥ
ΔΙΑΓΝΩΣΗ ΛΕΜΦΩΜΑΤΟΣ ΣΤΗΝ ΚΥΗΣΗ. Βιβλιογραφική ενημέρωση, ΓΝΑ Ευαγγελισμός Θ. ΚΑΝΕΛΛΟΠΟΥΛΟΥ
 ΔΙΑΓΝΩΣΗ ΛΕΜΦΩΜΑΤΟΣ ΣΤΗΝ ΚΥΗΣΗ Βιβλιογραφική ενημέρωση, ΓΝΑ Ευαγγελισμός Θ. ΚΑΝΕΛΛΟΠΟΥΛΟΥ 17-10-2013 ΕΙΣΑΓΩΓΗ 1:6000 περιπτώσεις κακοήθειας κατά την κύηση / έτος στις ΗΠΑ 1:1000 κυήσεις Λέμφωμα 4 ο σε
ΔΙΑΓΝΩΣΗ ΛΕΜΦΩΜΑΤΟΣ ΣΤΗΝ ΚΥΗΣΗ Βιβλιογραφική ενημέρωση, ΓΝΑ Ευαγγελισμός Θ. ΚΑΝΕΛΛΟΠΟΥΛΟΥ 17-10-2013 ΕΙΣΑΓΩΓΗ 1:6000 περιπτώσεις κακοήθειας κατά την κύηση / έτος στις ΗΠΑ 1:1000 κυήσεις Λέμφωμα 4 ο σε
Τι είναι το Πολλαπλούν Μυέλωμα και σε τί διαφέρει από τους άλλους Αιματολογικούς καρκίνους
 Τι είναι το Πολλαπλούν Μυέλωμα και σε τί διαφέρει από τους άλλους Αιματολογικούς καρκίνους Δρ Ειρήνη Κατωδρύτου Αιματολόγος, Διευθύντρια ΕΣΥ Αιματολογική Κλινική Α.Ν.Θ. «Θεαγένειο» Πολλαπλούν Μυέλωμα Είδος
Τι είναι το Πολλαπλούν Μυέλωμα και σε τί διαφέρει από τους άλλους Αιματολογικούς καρκίνους Δρ Ειρήνη Κατωδρύτου Αιματολόγος, Διευθύντρια ΕΣΥ Αιματολογική Κλινική Α.Ν.Θ. «Θεαγένειο» Πολλαπλούν Μυέλωμα Είδος
Ανατομία του προστάτη σε ζώνες κατά McNeal
 15/1/2018 Νέα απεικονιστική προσέγγιση του καρκίνου του προστάτη. Θέσεις και περιορισμοί του σύγχρονου ακτινολόγου. ΠΑΠΑΪΩΑΝΝΟΥ ΣΟΦΙΑ ΕΠΙΜΕΛΗΤΡΙΑ Α Ακτινολογικό Εργαστήριο Νοσ.Παπαγεωργίου ΣΥΝΤΟΝΙΣΤΗΣ
15/1/2018 Νέα απεικονιστική προσέγγιση του καρκίνου του προστάτη. Θέσεις και περιορισμοί του σύγχρονου ακτινολόγου. ΠΑΠΑΪΩΑΝΝΟΥ ΣΟΦΙΑ ΕΠΙΜΕΛΗΤΡΙΑ Α Ακτινολογικό Εργαστήριο Νοσ.Παπαγεωργίου ΣΥΝΤΟΝΙΣΤΗΣ
ΕΑΡΙΝΟ ΣΧΟΛΕΙΟ ΑΙΜΑΤΟΛΟΓΙΑΣ
 ΠΡΟΓΡΑΜΜΑ ΕΑΡΙΝΟ ΣΧΟΛΕΙΟ ΑΙΜΑΤΟΛΟΓΙΑΣ ΤΟΥ ΤΟΣ Ε.Α.Ε. ΕΠΙΘΕΤΙΚΑ ΜΗ HODGKIN ΛΕΜΦΩΜΑΤΑ ΙΣΤΟΛΟΓΙΚΗ ΔΙΑΓΝΩΣΗ-ΘΕΡΑΠΕΙΑ-ΠΡΟΒΛΗΜΑΤΙΣΜΟΙ 28-29 ΑΠΡΙΛΙΟΥ 2017 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΑΛΕΞΑΝΔΡΟΥΠΟΛΗ Οργανωτικη
ΠΡΟΓΡΑΜΜΑ ΕΑΡΙΝΟ ΣΧΟΛΕΙΟ ΑΙΜΑΤΟΛΟΓΙΑΣ ΤΟΥ ΤΟΣ Ε.Α.Ε. ΕΠΙΘΕΤΙΚΑ ΜΗ HODGKIN ΛΕΜΦΩΜΑΤΑ ΙΣΤΟΛΟΓΙΚΗ ΔΙΑΓΝΩΣΗ-ΘΕΡΑΠΕΙΑ-ΠΡΟΒΛΗΜΑΤΙΣΜΟΙ 28-29 ΑΠΡΙΛΙΟΥ 2017 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΑΛΕΞΑΝΔΡΟΥΠΟΛΗ Οργανωτικη
ΜYΘΟΙ ΚΑΙ ΠΡΑΓΜΑΤΙΚΟΤΗΤΑ ΓΙΑ ΤΟΝ ΚΑΡΚΙΝΟ ΤΟΥ ΠΝΕΥΜΟΝΑ
 ΜYΘΟΙ ΚΑΙ ΠΡΑΓΜΑΤΙΚΟΤΗΤΑ ΓΙΑ ΤΟΝ ΚΑΡΚΙΝΟ ΤΟΥ ΠΝΕΥΜΟΝΑ ΑΜΠΕΛΙΔΟΥ ΒΑΡΒΑΡΑ ΕΙΔΙΚΕΥΜΟΝΕΝΗ ΠΝΕΥΜΟΝΟΛΟΓΟΣ-ΦΥΜΑΤΙΟΛΟΓΟΣ ΠΝΕΥΜΟΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΕΣΥ Γ.Ν.Θ Γ. ΠΑΠΑΝΙΚΟΛΑΟY Σκοπός Καταγραφή συχνών ερωτήσεων Εύλογων
ΜYΘΟΙ ΚΑΙ ΠΡΑΓΜΑΤΙΚΟΤΗΤΑ ΓΙΑ ΤΟΝ ΚΑΡΚΙΝΟ ΤΟΥ ΠΝΕΥΜΟΝΑ ΑΜΠΕΛΙΔΟΥ ΒΑΡΒΑΡΑ ΕΙΔΙΚΕΥΜΟΝΕΝΗ ΠΝΕΥΜΟΝΟΛΟΓΟΣ-ΦΥΜΑΤΙΟΛΟΓΟΣ ΠΝΕΥΜΟΝΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΕΣΥ Γ.Ν.Θ Γ. ΠΑΠΑΝΙΚΟΛΑΟY Σκοπός Καταγραφή συχνών ερωτήσεων Εύλογων
Δ.Ν.Έξαρχος Τμήμα CT-MRI&PET/CT Γ.N.Α «Ο Ευαγγελισμός»
 Δ.Ν.Έξαρχος Τμήμα CT-MRI&PET/CT Γ.N.Α «Ο Ευαγγελισμός» H μέθοδος εφαρμόζεται ευρέος τα τελευταία χρόνια στη σταδιοποίηση του καρκίνου του πνεύμονα και ιδιαίτερα στην επιλογή μεταξύ χειρουργήσιμου ή δυνητικά
Δ.Ν.Έξαρχος Τμήμα CT-MRI&PET/CT Γ.N.Α «Ο Ευαγγελισμός» H μέθοδος εφαρμόζεται ευρέος τα τελευταία χρόνια στη σταδιοποίηση του καρκίνου του πνεύμονα και ιδιαίτερα στην επιλογή μεταξύ χειρουργήσιμου ή δυνητικά
ΤΑ ΑΠΟΤΕΛΕΣΜΑΤΑ ΤΗΣ ΕΡΕΥΝΑΣ
 ΤΑ ΑΠΟΤΕΛΕΣΜΑΤΑ ΤΗΣ ΕΡΕΥΝΑΣ Γνώσεις, στάσεις και ποιότητα ζωής σε ασθενείς με λέμφωμα Οι ασθενείς που πάσχουν από λέμφωμα στην Ελλάδα εμφανίζονται ελλιπώς ενημερωμένοι σχετικά με ζητήματα που αφορούν στην
ΤΑ ΑΠΟΤΕΛΕΣΜΑΤΑ ΤΗΣ ΕΡΕΥΝΑΣ Γνώσεις, στάσεις και ποιότητα ζωής σε ασθενείς με λέμφωμα Οι ασθενείς που πάσχουν από λέμφωμα στην Ελλάδα εμφανίζονται ελλιπώς ενημερωμένοι σχετικά με ζητήματα που αφορούν στην
ΕΑΡΙΝΟ ΣΧΟΛΕΙΟ ΑΙΜΑΤΟΛΟΓΙΑΣ
 ΠΡΟΓΡΑΜΜΑ ΕΑΡΙΝΟ ΣΧΟΛΕΙΟ ΑΙΜΑΤΟΛΟΓΙΑΣ ΤΟΥ ΙΔΡΥΜΑΤΟΣ Ε.Α.Ε. ΕΠΙΘΕΤΙΚΑ ΜΗ HODGKIN ΛΕΜΦΩΜΑΤΑ ΙΣΤΟΛΟΓΙΚΗ ΔΙΑΓΝΩΣΗ-ΘΕΡΑΠΕΙΑ-ΠΡΟΒΛΗΜΑΤΙΣΜΟΙ 28-29 ΑΠΡΙΛΙΟΥ 2017 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΑΛΕΞΑΝΔΡΟΥΠΟΛΗ
ΠΡΟΓΡΑΜΜΑ ΕΑΡΙΝΟ ΣΧΟΛΕΙΟ ΑΙΜΑΤΟΛΟΓΙΑΣ ΤΟΥ ΙΔΡΥΜΑΤΟΣ Ε.Α.Ε. ΕΠΙΘΕΤΙΚΑ ΜΗ HODGKIN ΛΕΜΦΩΜΑΤΑ ΙΣΤΟΛΟΓΙΚΗ ΔΙΑΓΝΩΣΗ-ΘΕΡΑΠΕΙΑ-ΠΡΟΒΛΗΜΑΤΙΣΜΟΙ 28-29 ΑΠΡΙΛΙΟΥ 2017 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΑΛΕΞΑΝΔΡΟΥΠΟΛΗ
Επιστημονικό Πρόγραμμα
 Επιστημονικό Πρόγραμμα Χαιρετισμός Αγαπητές, αγαπητοί Συνάδελφοι Σας καλωσορίζω στο 4ο Σεμινάριο του 4ου Κύκλου Σπουδών της Ελληνικής Ακαδημίας Ογκολογίας με θέμα «Καρκίνος Ουροποιογεννητικού Συστήματος».
Επιστημονικό Πρόγραμμα Χαιρετισμός Αγαπητές, αγαπητοί Συνάδελφοι Σας καλωσορίζω στο 4ο Σεμινάριο του 4ου Κύκλου Σπουδών της Ελληνικής Ακαδημίας Ογκολογίας με θέμα «Καρκίνος Ουροποιογεννητικού Συστήματος».
Αρχική εμπειρία από την χορήγηση anakinra σε δέκα ενήλικες ασθενείς με ανθεκτική ιδιοπαθή υποτροπιάζουσα περικαρδίτιδα
 Αρχική εμπειρία από την χορήγηση anakinra σε δέκα ενήλικες ασθενείς με ανθεκτική ιδιοπαθή υποτροπιάζουσα περικαρδίτιδα Γ. Λάζαρος, Π. Βασιλείου, Κ. Αντωνάτου, Χ. Κουτσιανάς, Γ. Γεωργιόπουλος, Δ. Βασιλόπουλος,
Αρχική εμπειρία από την χορήγηση anakinra σε δέκα ενήλικες ασθενείς με ανθεκτική ιδιοπαθή υποτροπιάζουσα περικαρδίτιδα Γ. Λάζαρος, Π. Βασιλείου, Κ. Αντωνάτου, Χ. Κουτσιανάς, Γ. Γεωργιόπουλος, Δ. Βασιλόπουλος,
Οι σκοποί της Εταιρείας μας είναι επιστημονικοί και κοινωνικοί και αφορούν στην:
 Ο καρκίνος του μαστού αποτελεί τη συχνότερη νεοπλασματική νόσο που προσβάλλει τις γυναίκες, με αρνητικές επιπτώσεις όχι μόνο για την ίδια την ασθενή, αλλά και για το οικογενειακό και φιλικό της περιβάλλον.
Ο καρκίνος του μαστού αποτελεί τη συχνότερη νεοπλασματική νόσο που προσβάλλει τις γυναίκες, με αρνητικές επιπτώσεις όχι μόνο για την ίδια την ασθενή, αλλά και για το οικογενειακό και φιλικό της περιβάλλον.
ΣΗΜΕΡΙΝΗ ΘΕΣΗ: ΑΝΑΠΛΗΡΩΤΡΙΑ ΚΑΘΗΓΗΤΡΙΑ,ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΣΥΝΟΠΤΙΚΗ ΠΑΡΟΥΣΙΑΣΗ ΣΥΝΟΛΙΚΟΥ ΕΠΙΣΤΗΜΟΝΙΚΟΥ ΕΡΓΟΥ
 ΣΥΝΟΠΤΙΚΟ ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΑΙΚΑΤΕΡΙΝΗ ΠΑΥΛΑΚΗ ΗΜΕΡΟΜΗΝΙΑ ΓΕΝΝΗΣΗΣ: 23-10-1951 ΤΟΠΟΣ ΓΕΝΝΗΣΗΣ: ΑΘΗΝΑ ΔΙΕΥΘΥΝΣΗ ΚΑΤΟΙΚΙΑΣ: ΚΥΠΡΟΥ 9, ΚΗΦΙΣΙΑ ΕΙΔΙΚΟΤΗΤΑ: ΠΑΘΟΛΟΓΟΑΝΑΤΟΜΟΣ ΣΗΜΕΡΙΝΗ ΘΕΣΗ:
ΣΥΝΟΠΤΙΚΟ ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ ΟΝΟΜΑΤΕΠΩΝΥΜΟ: ΑΙΚΑΤΕΡΙΝΗ ΠΑΥΛΑΚΗ ΗΜΕΡΟΜΗΝΙΑ ΓΕΝΝΗΣΗΣ: 23-10-1951 ΤΟΠΟΣ ΓΕΝΝΗΣΗΣ: ΑΘΗΝΑ ΔΙΕΥΘΥΝΣΗ ΚΑΤΟΙΚΙΑΣ: ΚΥΠΡΟΥ 9, ΚΗΦΙΣΙΑ ΕΙΔΙΚΟΤΗΤΑ: ΠΑΘΟΛΟΓΟΑΝΑΤΟΜΟΣ ΣΗΜΕΡΙΝΗ ΘΕΣΗ:
Σχετιζομενος Με Το NLRP-12 Υποτροπιαζων Πυρετος
 www.printo.it/pediatric-rheumatology/cy/intro Σχετιζομενος Με Το NLRP-12 Υποτροπιαζων Πυρετος Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Ο ΣΧΕΤΙΖΟΜΕΝΟΣ ΜΕ ΤΟ NLRP12 ΥΠΟΤΡΟΠΙΑΖΩΝ ΠΥΡΕΤΟΣ 1.1 Τι είναι; Ο σχετιζόμενος με
www.printo.it/pediatric-rheumatology/cy/intro Σχετιζομενος Με Το NLRP-12 Υποτροπιαζων Πυρετος Έκδοση από 2016 1. ΤΙ ΕΙΝΑΙ Ο ΣΧΕΤΙΖΟΜΕΝΟΣ ΜΕ ΤΟ NLRP12 ΥΠΟΤΡΟΠΙΑΖΩΝ ΠΥΡΕΤΟΣ 1.1 Τι είναι; Ο σχετιζόμενος με
9 Ιανουαρίου 2016 ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ 2016. Νεώτερα Δεδομένα. 1 η Επιστημονική Ημερίδα. Ώρα προσέλευσης: 09:00 ΕΙΣΟΔΟΣ ΕΛΕΥΘΕΡΗ
 Οργάνωση: Απεικονιστικό Τμήμα Μαστού ΜΗΤΕΡΑ Α Κλινική Μαστού ΜΗΤΕΡΑ Β Κλινική Μαστού ΜΗΤΕΡΑ Ογκολογική Κλινική ΜΗΤΕΡΑ ΣΥΝΕΔΡΙΑΚΟ ΚΕΝΤΡΟ Ν. ΛΟΥΡΟΣ ΜΗΤΕΡΑ 1 η Επιστημονική Ημερίδα ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ 2016
Οργάνωση: Απεικονιστικό Τμήμα Μαστού ΜΗΤΕΡΑ Α Κλινική Μαστού ΜΗΤΕΡΑ Β Κλινική Μαστού ΜΗΤΕΡΑ Ογκολογική Κλινική ΜΗΤΕΡΑ ΣΥΝΕΔΡΙΑΚΟ ΚΕΝΤΡΟ Ν. ΛΟΥΡΟΣ ΜΗΤΕΡΑ 1 η Επιστημονική Ημερίδα ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ 2016
ΣΥΝΗΘΕΙΣ ΠΑΘΗΣΕΙΣ ΘΥΡΕΟΕΙΔΟΥΣ
 Οι όζοι του θυρεοειδούς είναι συχνοί και αποτελούν το συχνότερο ενδοκρινολογικό πρόβλημα σε πολλές χώρες. Οι πιθανότητες ότι κάποιος θα ανακαλύψει έναν τουλάχιστον όζο θυρεοειδούς είναι 1 στις 10 ενώ σε
Οι όζοι του θυρεοειδούς είναι συχνοί και αποτελούν το συχνότερο ενδοκρινολογικό πρόβλημα σε πολλές χώρες. Οι πιθανότητες ότι κάποιος θα ανακαλύψει έναν τουλάχιστον όζο θυρεοειδούς είναι 1 στις 10 ενώ σε
Εισαγωγή στην Ανοσολογία
 Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ
 ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ Βασικές γνώσεις I SBN 960-372-069-0 ΠΕΡΙΕΧΟΜΕΝΑ ΠΑΡΙΣ Α. ΚΟΣΜΙΔΗΣ ΓΕΩΡΓΙΟΣ ΤΣΑΚΙΡΗΣ Μ Ε Ρ Ο Σ Ι ΟΓΚΟΛΟΓΙΑ Κεφάλαιο 1 ΕΙΣΑΓΩΓΗ ΣΤΟΝ ΚΑΡΚΙΝΟ... 3 Το καρκινικό κύτταρο... 3 Κυτταρικός
ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ Βασικές γνώσεις I SBN 960-372-069-0 ΠΕΡΙΕΧΟΜΕΝΑ ΠΑΡΙΣ Α. ΚΟΣΜΙΔΗΣ ΓΕΩΡΓΙΟΣ ΤΣΑΚΙΡΗΣ Μ Ε Ρ Ο Σ Ι ΟΓΚΟΛΟΓΙΑ Κεφάλαιο 1 ΕΙΣΑΓΩΓΗ ΣΤΟΝ ΚΑΡΚΙΝΟ... 3 Το καρκινικό κύτταρο... 3 Κυτταρικός
Urogold III: Οι σημαντικότερες δημοσιεύσεις της χρονιάς (Προστάτης- όρχεις)
 Urogold III: Οι σημαντικότερες δημοσιεύσεις της χρονιάς (Προστάτης- όρχεις) Μουρμούρης Παναγιώτης MD, MSc, PhD, FEBU Πανεπιστημιακός Υπότροφος ΕΚΠΑ Β Ουρολογική Κλινική Σισμανόγλειο ΓΝΑ Καμία σύγκρουση
Urogold III: Οι σημαντικότερες δημοσιεύσεις της χρονιάς (Προστάτης- όρχεις) Μουρμούρης Παναγιώτης MD, MSc, PhD, FEBU Πανεπιστημιακός Υπότροφος ΕΚΠΑ Β Ουρολογική Κλινική Σισμανόγλειο ΓΝΑ Καμία σύγκρουση
ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ. Εισαγωγή στην αιματολογία
 ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ Εισαγωγή στην αιματολογία Αιματολογία Κλινική και εργαστηριακή Διαγνωστική και θεραπευτική Αυτόνομη και συνεργατική Αίμα-Λειτουργίες Μεταφορά οξυγόνου Απομάκρυνση
ΑΡΙΆΔΝΗ ΟΜΆΔΑ ΥΠΟΣΤΉΡΙΞΗΣ ΑΣΘΕΝΏΝ ΜΕ ΧΛΛ Εισαγωγή στην αιματολογία Αιματολογία Κλινική και εργαστηριακή Διαγνωστική και θεραπευτική Αυτόνομη και συνεργατική Αίμα-Λειτουργίες Μεταφορά οξυγόνου Απομάκρυνση
Δεκαπεντάλεπτη προετοιμασία του φοιτητή, για την παρακολούθηση του μαθήματος του καρκίνου του προστάτη.
 Δεκαπεντάλεπτη προετοιμασία του φοιτητή, για την παρακολούθηση του μαθήματος του καρκίνου του προστάτη. Καρκίνος του προστάτη Επιδημιολογία: Αποτελεί τον συχνότερα διαγνωσμένο καρκίνο στον άνδρα. 186.320
Δεκαπεντάλεπτη προετοιμασία του φοιτητή, για την παρακολούθηση του μαθήματος του καρκίνου του προστάτη. Καρκίνος του προστάτη Επιδημιολογία: Αποτελεί τον συχνότερα διαγνωσμένο καρκίνο στον άνδρα. 186.320
8Παρασκευή Ξενοδοχείο. Καρκίνος. Ημερίδα με θέμα. Κεφαλής -Τραχήλου Ουροδόχου Κύστης. Τελικό. πρόγραμμα. Λάρισα. Maίου 2015.
 Οργάνωση: Ερευνητική Εταιρεία Ουρογεννητικής Ογκολογίας Ημερίδα με θέμα Καρκίνος Κεφαλής -Τραχήλου Ουροδόχου Κύστης Xορηγoύνται 4 Μόρια Συνεχιζόμενης Ιατρικής Εκπαίδευσης (CΜE-CPD) 8Παρασκευή Ξενοδοχείο
Οργάνωση: Ερευνητική Εταιρεία Ουρογεννητικής Ογκολογίας Ημερίδα με θέμα Καρκίνος Κεφαλής -Τραχήλου Ουροδόχου Κύστης Xορηγoύνται 4 Μόρια Συνεχιζόμενης Ιατρικής Εκπαίδευσης (CΜE-CPD) 8Παρασκευή Ξενοδοχείο
VIN (Ενδοεπιθηλιακή νεοπλασία αιδοίου)
 VIN (Ενδοεπιθηλιακή νεοπλασία αιδοίου) Διαφορές μεταξύ τραχήλου και αιδοίου Κύτταρο-στόχος: κυρίως πλακώδες δεν υπάρχει εκτεθειμένος πολυδύναμος πληθυσμός, όπως στον τράχηλο Σχετιζόμενοι HPV: κυριαρχούν
VIN (Ενδοεπιθηλιακή νεοπλασία αιδοίου) Διαφορές μεταξύ τραχήλου και αιδοίου Κύτταρο-στόχος: κυρίως πλακώδες δεν υπάρχει εκτεθειμένος πολυδύναμος πληθυσμός, όπως στον τράχηλο Σχετιζόμενοι HPV: κυριαρχούν
Επιλεγόµενο µάθηµα:λευχαιµίες. Γεωργόπουλος Χρήστος Καρκατσούλης Μάριος Μπρίκος Νικήτας
 Επιλεγόµενο µάθηµα:λευχαιµίες Γεωργόπουλος Χρήστος Καρκατσούλης Μάριος Μπρίκος Νικήτας Ανοσολογία και καρκίνος Γενετικές και κυτταρικές αλλαγές που συµβαίνουν στον καρκίνο προσφέρουν στο ανοσιακό σύστηµα
Επιλεγόµενο µάθηµα:λευχαιµίες Γεωργόπουλος Χρήστος Καρκατσούλης Μάριος Μπρίκος Νικήτας Ανοσολογία και καρκίνος Γενετικές και κυτταρικές αλλαγές που συµβαίνουν στον καρκίνο προσφέρουν στο ανοσιακό σύστηµα
Adcetris (μπρεντουξιμάβη βεδοτίνη)
 EMA/996/2019 EMEA/H/C/002455 Ανασκόπηση του Adcetris και αιτιολογικό έγκρισης στην ΕΕ Τι είναι το Adcetris και σε ποιες περιπτώσεις χρησιμοποιείται; Το Adcetris είναι αντικαρκινικό φάρμακο που χρησιμοποιείται
EMA/996/2019 EMEA/H/C/002455 Ανασκόπηση του Adcetris και αιτιολογικό έγκρισης στην ΕΕ Τι είναι το Adcetris και σε ποιες περιπτώσεις χρησιμοποιείται; Το Adcetris είναι αντικαρκινικό φάρμακο που χρησιμοποιείται
Διάγνωση Λευχαιµίας Το λευχαιµικό κύτταρο. Επιλεγόµενο Μάθηµα Αιµατολογίας
 Διάγνωση Λευχαιµίας Το λευχαιµικό κύτταρο Επιλεγόµενο Μάθηµα Αιµατολογίας Εισαγωγή Η κατανόηση των αιµατολογικών παθήσεων συµπεριλαµβανοµένων των οξειών λευχαιµιών προϋποθέτει την γνώση του µηχανισµού
Διάγνωση Λευχαιµίας Το λευχαιµικό κύτταρο Επιλεγόµενο Μάθηµα Αιµατολογίας Εισαγωγή Η κατανόηση των αιµατολογικών παθήσεων συµπεριλαµβανοµένων των οξειών λευχαιµιών προϋποθέτει την γνώση του µηχανισµού
18. ΚΑΡΚΙΝΟΣ ΕΝΔΟΜΗΤΡΙΟΥ
 18. ΚΑΡΚΙΝΟΣ ΕΝΔΟΜΗΤΡΙΟΥ Ο καρκίνος του ενδομητρίου είναι η συχνότερη μορφή γυναικολογικού καρκίνου στις ΗΠΑ ( 6% όλων των νεοδιαγνωσθέντων καρκίνων στις γυναίκες). Η πρόγνωση είναι σχετικά καλή καθώς
18. ΚΑΡΚΙΝΟΣ ΕΝΔΟΜΗΤΡΙΟΥ Ο καρκίνος του ενδομητρίου είναι η συχνότερη μορφή γυναικολογικού καρκίνου στις ΗΠΑ ( 6% όλων των νεοδιαγνωσθέντων καρκίνων στις γυναίκες). Η πρόγνωση είναι σχετικά καλή καθώς
13-14. Αναδυόμενες. Επιλογές. στην ΑΙΜΑΤΟΛΟΓΙΑ ΦΕΒΡΟΥΑΡΙΟΥ 2 0 1 5 ΑΙΜΑΤΟΛΟΓΙΚΟ ΔΙΗΜΕΡΟ LARISSA IMPΕRIAL. Κεντρικής Ελλάδας.
 ΑΙΜΑΤΟΛΟΓΙΚΟ ΔΙΗΜΕΡΟ Κεντρικής Ελλάδας 1 η Νοσηλευτική Αιματολογική Ημερίδα Κεντρικής Ελλάδας Υπό την αιγίδα Ιατρική Σχολή Πανεπιστημίου Θεσσαλίας Τμήμα Νοσηλευτικής Ε.Κ.Π.Α. ΤΕΙ Νοσηλευτικής Λάρισας 13-14
ΑΙΜΑΤΟΛΟΓΙΚΟ ΔΙΗΜΕΡΟ Κεντρικής Ελλάδας 1 η Νοσηλευτική Αιματολογική Ημερίδα Κεντρικής Ελλάδας Υπό την αιγίδα Ιατρική Σχολή Πανεπιστημίου Θεσσαλίας Τμήμα Νοσηλευτικής Ε.Κ.Π.Α. ΤΕΙ Νοσηλευτικής Λάρισας 13-14
Χαράλαμπος Κ Σταθόπουλος. Ογκολογικό Τμήμα - ιευθυντής ΕΣΥ
 Γυναίκα 53 ετών με ιστορικό ca ωοθηκών, αυξανόμενη τιμή CA 125, και λεμφαδενοπάθεια τραχήλου - μεσοθωρακίου με μετρίου βαθμού ανοσολογική διέγερση. Χαράλαμπος Κ Σταθόπουλος Ογκολογικό Τμήμα - ιευθυντής
Γυναίκα 53 ετών με ιστορικό ca ωοθηκών, αυξανόμενη τιμή CA 125, και λεμφαδενοπάθεια τραχήλου - μεσοθωρακίου με μετρίου βαθμού ανοσολογική διέγερση. Χαράλαμπος Κ Σταθόπουλος Ογκολογικό Τμήμα - ιευθυντής
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας
 Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
Adcetris. μπρεντουξιμάβη βεδοτίνη. Τι είναι το Adcetris και σε ποιες περιπτώσεις χρησιμοποιείται; Περίληψη EPAR για το κοινό
 EMA/462209/2017 EMEA/H/C/002455 Περίληψη EPAR για το κοινό μπρεντουξιμάβη βεδοτίνη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο
EMA/462209/2017 EMEA/H/C/002455 Περίληψη EPAR για το κοινό μπρεντουξιμάβη βεδοτίνη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο
Ο ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΚΑΡΚΙΝΟΣ ΣΤΗΝ ΕΛΛΑΔΑ
 Ο ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΚΑΡΚΙΝΟΣ ΣΤΗΝ ΕΛΛΑΔΑ ΕΥΔΟΚΙΑ ΜΑΝΔΑΛΑ Αναπληρώτρια Καθηγήτρια Αιµατολογίας ΑΠΘ Δ Παθολογική Κλινική ΑΠΘ Ιπποκράτειο Νοσοκοµείο, Θεσσαλονίκη ΙΟΥΝΙΟΣ 2018 Ο καρκίνος η 2 η αιτία θανάτου (24,2%
Ο ΑΙΜΑΤΟΛΟΓΙΚΟΣ ΚΑΡΚΙΝΟΣ ΣΤΗΝ ΕΛΛΑΔΑ ΕΥΔΟΚΙΑ ΜΑΝΔΑΛΑ Αναπληρώτρια Καθηγήτρια Αιµατολογίας ΑΠΘ Δ Παθολογική Κλινική ΑΠΘ Ιπποκράτειο Νοσοκοµείο, Θεσσαλονίκη ΙΟΥΝΙΟΣ 2018 Ο καρκίνος η 2 η αιτία θανάτου (24,2%
ΚΑΡΚΙΝΟΣ ΤΟΥ ΛΑΡΥΓΓΑ
 ΚΩΝΣΤΑΝΤΙΝΟΣ ΒΛΑΧΤΣΗΣ ΙΑΤΡΟΣ ΩΤΟΡΙΝΟΛΑΡΥΓΓΟΛΟΓΟΣ Ι ΑΚΤΟΡΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΚΑΡΚΙΝΟΣ ΤΟΥ ΛΑΡΥΓΓΑ ΟΓΚΟΓΕΝΕΣΗ ΚΑΙ ΣΥΓΧΡΟΝΟΙ ΜΟΡΙΑΚΟΙ ΠΡΟΓΝΩΣΤΙΚΟΙ ΕΙΚΤΕΣ ΘΕΣΣΑΛΟΝΙΚΗ 2006 3 Κωνσταντίνος
ΚΩΝΣΤΑΝΤΙΝΟΣ ΒΛΑΧΤΣΗΣ ΙΑΤΡΟΣ ΩΤΟΡΙΝΟΛΑΡΥΓΓΟΛΟΓΟΣ Ι ΑΚΤΟΡΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΚΑΡΚΙΝΟΣ ΤΟΥ ΛΑΡΥΓΓΑ ΟΓΚΟΓΕΝΕΣΗ ΚΑΙ ΣΥΓΧΡΟΝΟΙ ΜΟΡΙΑΚΟΙ ΠΡΟΓΝΩΣΤΙΚΟΙ ΕΙΚΤΕΣ ΘΕΣΣΑΛΟΝΙΚΗ 2006 3 Κωνσταντίνος
ΚΑΡΔΙΟΤΟΞΙΚΟΤΗΤΑ ΧΗΜΕΙΟΘΕΡΑΠΕΥΤΙΚΩΝ ΦΑΡΜΑΚΩΝ
 ΚΑΡΔΙΟΤΟΞΙΚΟΤΗΤΑ ΧΗΜΕΙΟΘΕΡΑΠΕΥΤΙΚΩΝ ΦΑΡΜΑΚΩΝ Άννα Ιµπρισίµη, ΤΕ Νοσηλεύτρια, Δ Παθολογική κλινική, ΓΝΘ «Ιπποκράτειο» Δάφνη Μαυροπούλου, ΤΕ Νοσηλεύτρια, Δ Παθολογική κλινική, ΓΝΘ «Ιπποκράτειο» Ελένη Καλαϊτζή,
ΚΑΡΔΙΟΤΟΞΙΚΟΤΗΤΑ ΧΗΜΕΙΟΘΕΡΑΠΕΥΤΙΚΩΝ ΦΑΡΜΑΚΩΝ Άννα Ιµπρισίµη, ΤΕ Νοσηλεύτρια, Δ Παθολογική κλινική, ΓΝΘ «Ιπποκράτειο» Δάφνη Μαυροπούλου, ΤΕ Νοσηλεύτρια, Δ Παθολογική κλινική, ΓΝΘ «Ιπποκράτειο» Ελένη Καλαϊτζή,
ΧΡΟΝΙΑ ΔΥΣΛΕΙΤΟΥΡΓΙΑ/ΝΕΦΡΟΠΑΘΕΙΑ ΚΑΙ ΑΠΩΛΕΙΑ ΝΕΦΡΙΚΩΝ ΜΟΣΧΕΥΜΑΤΩΝ ΔΗΜΗΤΡΙΟΣ Σ. ΓΟΥΜΕΝΟΣ
 ΧΡΟΝΙΑ ΔΥΣΛΕΙΤΟΥΡΓΙΑ/ΝΕΦΡΟΠΑΘΕΙΑ ΚΑΙ ΑΠΩΛΕΙΑ ΝΕΦΡΙΚΩΝ ΜΟΣΧΕΥΜΑΤΩΝ ΔΗΜΗΤΡΙΟΣ Σ. ΓΟΥΜΕΝΟΣ Εισαγωγή Η πρόληψη των επεισοδίων οξείας απόρριψης και η μακροχρόνια διατήρηση του νεφρικού μοσχεύματος αποτελούν
ΧΡΟΝΙΑ ΔΥΣΛΕΙΤΟΥΡΓΙΑ/ΝΕΦΡΟΠΑΘΕΙΑ ΚΑΙ ΑΠΩΛΕΙΑ ΝΕΦΡΙΚΩΝ ΜΟΣΧΕΥΜΑΤΩΝ ΔΗΜΗΤΡΙΟΣ Σ. ΓΟΥΜΕΝΟΣ Εισαγωγή Η πρόληψη των επεισοδίων οξείας απόρριψης και η μακροχρόνια διατήρηση του νεφρικού μοσχεύματος αποτελούν
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά
 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
Μεθοδολογίες Αξιοποίησης Δεδομένων
 Μεθοδολογίες Αξιοποίησης Δεδομένων Βλάχος Σ. Ιωάννης Λέκτορας 407/80, Ιατρικής Σχολής Πανεπιστημίου Αθηνών Εργαστήριο Πειραματικής Χειρουργικής και Χειρουργικής Ερεύνης «Ν.Σ. Σ Χρηστέας» Στάδια Αξιοποίησης
Μεθοδολογίες Αξιοποίησης Δεδομένων Βλάχος Σ. Ιωάννης Λέκτορας 407/80, Ιατρικής Σχολής Πανεπιστημίου Αθηνών Εργαστήριο Πειραματικής Χειρουργικής και Χειρουργικής Ερεύνης «Ν.Σ. Σ Χρηστέας» Στάδια Αξιοποίησης
Επιστηµονικό Πρόγραµµα
 Επιστηµονικό Πρόγραµµα Χαιρετισµός ρ Αθανάσιος Αθανασιάδης Πρόεδρος της ΕΟΠΕ Επιστηµονικοί Υπεύθυνοι ιευθυντές Σπουδών Επιστηµονικό Πρόγραµµα. ΑΛΙΑΝΗ, Α. ΜΠΑΜΙΑΣ Ι. ΜΠΟΥΚΟΒΙΝΑΣ, Χ. ΠΑΝΟΠΟΥΛΟΣ ΠΑΡΑΣΚΕΥΗ
Επιστηµονικό Πρόγραµµα Χαιρετισµός ρ Αθανάσιος Αθανασιάδης Πρόεδρος της ΕΟΠΕ Επιστηµονικοί Υπεύθυνοι ιευθυντές Σπουδών Επιστηµονικό Πρόγραµµα. ΑΛΙΑΝΗ, Α. ΜΠΑΜΙΑΣ Ι. ΜΠΟΥΚΟΒΙΝΑΣ, Χ. ΠΑΝΟΠΟΥΛΟΣ ΠΑΡΑΣΚΕΥΗ
«ΕΜΒΙΟΜΗΧΑΝΙΚΗ ΣΤΗΝ ΚΑΡΚΙΝΟΓΕΝΕΣΗ: ΒΙΟΧΗΜΙΚΑ ΜΟΝΟΠΑΤΙΑ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΟΠΤΙΚΕΣ»
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΚΗΣ ΧΗΜΕΙΑΣ ΜΟΝΑΔΑ ΚΥΤΤΑΡΙΚΗΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΕΜΒΙΟΜΗΧΑΝΙΚΗΣ «ΕΜΒΙΟΜΗΧΑΝΙΚΗ ΣΤΗΝ ΚΑΡΚΙΝΟΓΕΝΕΣΗ: ΒΙΟΧΗΜΙΚΑ ΜΟΝΟΠΑΤΙΑ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΟΠΤΙΚΕΣ»
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΚΗΣ ΧΗΜΕΙΑΣ ΜΟΝΑΔΑ ΚΥΤΤΑΡΙΚΗΣ ΚΑΙ ΜΟΡΙΑΚΗΣ ΕΜΒΙΟΜΗΧΑΝΙΚΗΣ «ΕΜΒΙΟΜΗΧΑΝΙΚΗ ΣΤΗΝ ΚΑΡΚΙΝΟΓΕΝΕΣΗ: ΒΙΟΧΗΜΙΚΑ ΜΟΝΟΠΑΤΙΑ ΚΑΙ ΘΕΡΑΠΕΥΤΙΚΕΣ ΠΡΟΟΠΤΙΚΕΣ»
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς. Οι φάσεις των Τ κυτταρικών απαντήσεων
 ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
Επίδραση αναιμίας, λευκοκυττάρωσης και θρομβοκυττάρωσης στην επιβίωση ασθενών μετά από εκτομή καρκίνου του πνεύμονα
 Πρωτότυπη Εργασία Επίδραση αναιμίας, λευκοκυττάρωσης και θρομβοκυττάρωσης στην επιβίωση ασθενών μετά από εκτομή καρκίνου του πνεύμονα Tatjana N. Adžić 1, Gordana D. Radosavljević-Ašić 1, Jelena M. Stojšić
Πρωτότυπη Εργασία Επίδραση αναιμίας, λευκοκυττάρωσης και θρομβοκυττάρωσης στην επιβίωση ασθενών μετά από εκτομή καρκίνου του πνεύμονα Tatjana N. Adžić 1, Gordana D. Radosavljević-Ašić 1, Jelena M. Stojšić
Αρχές μοριακής παθολογίας. Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ
 Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Αρχές μοριακής παθολογίας Α. Αρμακόλας Αν. Καθηγητής Ιατρική Σχολή ΕΚΠΑ Μοριακή Παθολογία Ανερχόμενος κλάδος της Παθολογίας Επικεντρώνεται στην μελέτη και τη διάγνωση νοσημάτων Στον καθορισμό και την πιστοποίηση
Πρώιμος καρκίνος μαστού. Σπύρος Μηλιαράς MD, MRCS(Glasg), AFRCS(Edin) Αναπλ. Καθηγητής Χειρουργικής ΑΠΘ Α Χειρουργική Κλινική ΑΠΘ, ΠΓΝΘ Παπαγεωργίου
 Πρώιμος καρκίνος μαστού Σπύρος Μηλιαράς MD, MRCS(Glasg), AFRCS(Edin) Αναπλ. Καθηγητής Χειρουργικής ΑΠΘ Α Χειρουργική Κλινική ΑΠΘ, ΠΓΝΘ Παπαγεωργίου Ορισμός.. Πρώιμος καρκίνος του μαστού είναι η νόσος που
Πρώιμος καρκίνος μαστού Σπύρος Μηλιαράς MD, MRCS(Glasg), AFRCS(Edin) Αναπλ. Καθηγητής Χειρουργικής ΑΠΘ Α Χειρουργική Κλινική ΑΠΘ, ΠΓΝΘ Παπαγεωργίου Ορισμός.. Πρώιμος καρκίνος του μαστού είναι η νόσος που
Επιστημονικό Πρόγραμμα
 Επιστημονικό Πρόγραμμα Χαιρετισμός Αγαπητοί συνάδελφοι και μαθητές της Ακαδημίας Κλινικής Ογκολογίας, Με ιδιαίτερη χαρά σας καλωσορίζουμε στο 3 ο Εκπαιδευτικό Σεμινάριο του 5ου Κύκλου Σπουδών της Ελληνικής
Επιστημονικό Πρόγραμμα Χαιρετισμός Αγαπητοί συνάδελφοι και μαθητές της Ακαδημίας Κλινικής Ογκολογίας, Με ιδιαίτερη χαρά σας καλωσορίζουμε στο 3 ο Εκπαιδευτικό Σεμινάριο του 5ου Κύκλου Σπουδών της Ελληνικής
18 o ΠΑΝΕΛΛΗΝΙΟ ΣΥΝΕΔΡΙΟ ΟΓΚΟΛΟΓΙΑΣ. 19-22 Νοεμβρίου 2015 ΘΕΣΣΑΛΟΝΙΚΗ ΞΕΝΟΔΟΧΕΙΟ MAKEDONIA PALACE. Διοργάνωση
 18 o ΠΑΝΕΛΛΗΝΙΟ ΣΥΝΕΔΡΙΟ ΟΓΚΟΛΟΓΙΑΣ 19-22 Νοεμβρίου 2015 ΘΕΣΣΑΛΟΝΙΚΗ ΞΕΝΟΔΟΧΕΙΟ MAKEDONIA PALACE Διοργάνωση ΑΝΤΙΚΑΡΚΙΝΙΚΟ ΝΟΣΟΚΟΜΕΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ «ΘΕΑΓΕΝΕΙΟ» Σε συνεργασία με τα Ογκολογικά Νοσοκομεία «ΑΓΙΟΙ
18 o ΠΑΝΕΛΛΗΝΙΟ ΣΥΝΕΔΡΙΟ ΟΓΚΟΛΟΓΙΑΣ 19-22 Νοεμβρίου 2015 ΘΕΣΣΑΛΟΝΙΚΗ ΞΕΝΟΔΟΧΕΙΟ MAKEDONIA PALACE Διοργάνωση ΑΝΤΙΚΑΡΚΙΝΙΚΟ ΝΟΣΟΚΟΜΕΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ «ΘΕΑΓΕΝΕΙΟ» Σε συνεργασία με τα Ογκολογικά Νοσοκομεία «ΑΓΙΟΙ
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΕΛΕΥΘΕΡΩΝ ΕΛΑΦΡΩΝ ΑΛΥΣΕΩΝ ΣΤΟΝ ΟΡΟ ΚΑΙ ΣΤΑ ΟΥΡΑ. Χρυσούλα Νικολάου
 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΕΛΕΥΘΕΡΩΝ ΕΛΑΦΡΩΝ ΑΛΥΣΕΩΝ ΣΤΟΝ ΟΡΟ ΚΑΙ ΣΤΑ ΟΥΡΑ Χρυσούλα Νικολάου Μονοκλωνικές ελεύθερες ελαφρές αλύσεις Οι μονοκλωνικές ελεύθερες ελαφρές αλύσεις οι οποίες είναι γνωστές ως πρωτεΐνη Bence
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΕΛΕΥΘΕΡΩΝ ΕΛΑΦΡΩΝ ΑΛΥΣΕΩΝ ΣΤΟΝ ΟΡΟ ΚΑΙ ΣΤΑ ΟΥΡΑ Χρυσούλα Νικολάου Μονοκλωνικές ελεύθερες ελαφρές αλύσεις Οι μονοκλωνικές ελεύθερες ελαφρές αλύσεις οι οποίες είναι γνωστές ως πρωτεΐνη Bence
Prolaris : Ο Νέος Εξατομικευμένος Υπολογισμός της Επιθετικότητας του Καρκίνου του Προστάτη
 Prolaris : Ο Νέος Εξατομικευμένος Υπολογισμός της Επιθετικότητας του Καρκίνου του Προστάτη Τηλεφωνικό Κέντρο 210 69 66 000 Prolaris : Ο Νέος Εξατομικευμένος Υπολογισμός της Επιθετικότητας του Καρκίνου
Prolaris : Ο Νέος Εξατομικευμένος Υπολογισμός της Επιθετικότητας του Καρκίνου του Προστάτη Τηλεφωνικό Κέντρο 210 69 66 000 Prolaris : Ο Νέος Εξατομικευμένος Υπολογισμός της Επιθετικότητας του Καρκίνου
Η θέση της χημειοθεραπείας σε ασθενείς 3 ης ηλικίας. Θωμάς Μακατσώρης Λέκτορας Παθολογίας-Ογκολογίας Πανεπιστήμιο Πατρών 23-10-2010
 Η θέση της χημειοθεραπείας σε ασθενείς 3 ης ηλικίας Θωμάς Μακατσώρης Λέκτορας Παθολογίας-Ογκολογίας Πανεπιστήμιο Πατρών 23-10-2010 Το πεδίο αλλάζει Αύξηση του προσδόκιμου επιβίωσης παγκοσμίως Καλύτερη
Η θέση της χημειοθεραπείας σε ασθενείς 3 ης ηλικίας Θωμάς Μακατσώρης Λέκτορας Παθολογίας-Ογκολογίας Πανεπιστήμιο Πατρών 23-10-2010 Το πεδίο αλλάζει Αύξηση του προσδόκιμου επιβίωσης παγκοσμίως Καλύτερη
