Επιστήμη και Τεχνολογία Τροφίμων
|
|
|
- Άιμον Διαμαντόπουλος
- 5 χρόνια πριν
- Προβολές:
Transcript
1 Εργαστήριο Χημείας και Τεχνολογίας Τροφίμων ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΜΠ Επιστήμη και Τεχνολογία Τροφίμων Πέτρος Ταούκης Βασιλική Ωραιοπούλου 6 o Εξάμηνο Αθήνα, 2019
2
3 Περιεχόμενα Σελίδα 1. ΣΤΟΙΧΕΙΑ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ 1 ΠΡΩΤΕΪΝΕΣ 1 Αμινοξέα 2 Πεπτίδια-Πρωτεΐνες-Δομή 8 Ταξινόμηση πρωτεϊνών 19 Μετουσίωση πρωτεϊνών 22 Ρόλος πρωτεϊνών στα τρόφιμα 23 Χρησιμότητα-Λειτουργία πρωτεϊνών ως προστιθέμενο συστατικό 32 Πρωτεΐνες διαφόρων τροφίμων 33 ΥΔΑΤΑΝΘΡΑΚΕΣ 37 Μονοσακχαρίτες 37 Δισακχαρίτες 42 Πολυσακχαρίτες 44 ΛΙΠΙΔΙΑ 53 Λιπαρά οξέα 54 Τριγλυκερίδια 57 Ιδιότητες λιπαρών σωμάτων 60 Αλλοιώσεις λιπαρών 61 Βιβλιογραφία ΚΙΝΗΤΙΚΗ ΑΛΛΟΙΩΣΗΣ ΚΑΙ ΕΛΕΓΧΟΣ ΔΙΑΤΗΡΗΣΙΜΟΤΗΤΑΣ ΤΩΝ ΤΡΟΦΙΜΩΝ 66 Αρχές κινητικής αλλοίωσης των τροφίμων 70 Επίδραση παραμέτρων περιβάλλοντος 74 Χρήση των αρχών της κινητικής αλλοίωσης για την πρόβλεψη και τον έλεγχο της διατηρησιμότητας των τροφίμων 81 Βιβλιογραφία ΜΙΚΡΟΒΙΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ 84 Γενικές αρχές 84 Συνθήκες ανάπτυξης των μικροβίων στα τρόφιμα 94 Μέθοδοι απαρίθμησης μικροοργανισμών 99 Μικροβιολογία τροφίμων-νέες προσεγγίσεις 105 Κινητική μικροβιακής ανάπτυξης 113 Βιβλιογραφία 119
4 4. ΘΕΡΜΟΦΥΣΙΚΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΤΡΟΦΙΜΩΝ 121 Εισαγωγή 121 Πυκνότητα 121 Θερμική αγωγιμότητα 123 Ειδική θερμότητα 125 Λανθάνουσα θερμότητα πήξης και εξάτμισης του νερού 130 Θερμική διαχυτότητα 131 Ενεργότητα νερού-ισόθερμες ρόφησης 131 Σύμβολα 135 Βιβλιογραφία ΔΙΕΡΓΑΣΙΕΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΚΑΙ ΣΥΝΤΗΡΗΣΗΣ 138 Εισαγωγή 138 Οι κυριότερες διεργασίες στη βιομηχανία τροφίμων ΘΕΡΜΑΝΣΗ ΚΑΙ ΨΥΞΗ ΤΩΝ ΤΡΟΦΙΜΩΝ 141 Εισαγωγή 141 Μεταφορά θερμότητας με αγωγή 141 Αναλυτική επίλυση των εξισώσεων αγωγής θερμότητας 144 Εμπειρικές εξισώσεις-χρήση των παραμέτρων j και h 144 Προϊόντα με γνωστά γεωμετρικά σχήματα 149 Προϊόντα με ακανόνιστα γεωμετρικά σχήματα 152 Μεταφορά θερμότητας με συναγωγή 153 Εξαναγκασμένη συναγωγή 153 Φυσική (ελεύθερη) συναγωγή 155 Εναλλάκτες θερμότητας 155 Υπολογισμός της μεταβολής της θερμοκρασίας του τροφίμου στους εναλλάκτες θερμότητας 157 Συστήματα ασυνεχούς λειτουργίας 159 Συστήματα θέρμανσης και ψύξης για στερεά ή συσκευασμένα τρόφιμα 160 Παραδείγματα 163 Ασκήσεις 165 Σύμβολα 166 Βιβλιογραφία ΠΑΣΤΕΡΙΩΣΗ ΚΑΙ ΑΠΟΣΤΕΙΡΩΣΗ 169 Εισαγωγή 169 Κινητική καταστροφής μικροοργανισμών-ορισμοί 170 Ρυθμός καταστροφής υπό σταθερή θερμοκρασία-χρόνος υποδεκαπλασιασμού (D) 170 Χρόνος θερμικού θανάτου (F) 173 Επίδραση της θερμοκρασίας στο ρυθμό θανάτωσης-σταθερά θερμικής αντίστασης (z) 174 Σταθερά Q 176 Παράγοντες που επηρεάζουν τη θερμική αντίσταση των μικροοργανισμών 177 Θερμοκρασία 177 Ph 178 Οξυγόνο 179 Ενεργότητα νερού 180
5 Σύσταση υποστρώματος 181 Θερμική αδρανοποίηση ενζύμων 181 Μεταβολές των θρεπτικών συστατικών και των ποιοτικών χαρακτηριστικών κατά τη θέρμανση 182 Υπολογισμός καταστροφής μικροοργανισμών στις διεργασίες παστερίωσης και αποστείρωσης 184 Θέρμανση σε περιέκτες 185 Γενική μέθοδος 187 Υπολογιστικές μέθοδοι 189 Μέθοδος Ball 189 Μέθοδος Stumbo 193 Ασηπτική διεργασία 195 Εξοπλισμός θερμικών διεργασιών 198 Ζεμάτισμα 198 Παστερίωση 199 Αποστείρωση 200 Παραδείγματα 208 Ασκήσεις 213 Σύμβολα 214 Βιβλιογραφία ΚΑΤΑΨΥΞΗ 219 Εισαγωγή 219 Σχηματισμός κρυστάλλων πάγου 219 Ιδιότητες των κατεψυγμένων τροφίμων 222 Ταπείνωση σημείου πήξης 223 Μεταβολή ενθαλπίας κατά την κατάψυξη 226 Απαγωγή θερμότητας-υπολογισμός χρόνου κατάψυξης 229 Βασικές εξισώσεις 229 Ρυθμός κατάψυξης-πρόρρηση χρόνου κατάψυξης 230 Η εξίσωση Plank 231 Τροποποιήσεις της εξίσωσης Plank (εμπειρικές μέθοδοι) 234 Εξοπλισμός 239 Καταψυκτήρες με προσφύσηση αέρα 239 Καταψυκτήρες επαφής με στερεές επιφάνειες 241 Καταψυκτήρες επαφής με υγρά (με ψεκασμό ή εμβάπτιση) 244 Αποθήκευση κατεψυγμένων τροφίμων 245 Παραδείγματα 246 Ασκήσεις 251 Σύμβολα 252 Βιβλιογραφία 253
6 9. ΣΥΣΚΕΥΑΣΙΑ 255 Εισαγωγή 255 Παράγοντες του περιβάλλοντος που επιδρούν στην υποβάθμιση της 256 ποιότητας του τροφίμου Τύποι και υλικά συσκευασίας τροφίμων 259 Χαρτί-Χαρτόνι 260 Γυαλί 263 Μέταλλα 265 Μεταλλικά δοχεία 265 Μεταλλικά φύλλα 274 Ξύλο 275 Πλαστικά 275 Βιοδιασπώμενα και βρώσιμα υλικά 282 Πολυστρωματικά υλικά (laminates) 286 Διαπερατότητα υλικών συσκευασίας σε αέρια και ατμούς 288 Ορισμοί-Βασικές εξισώσεις 288 Διαπερατότητα υλικών συσκευασίας σε αέρια 290 Διαπερατότητα υδρατμών 292 Διαπερατότητα μέσω πολυστρωματικών υλικών 295 Διαπέραση από πόρους ή ανοίγματα συσκευασίας 297 Διαπέραση υλικών συσκευασίας από το φως 298 Έλεγχος βιολογικών προσβολών 299 Ικανότητα προστασίας από μηχανική φθορά 301 Επίδραση του υλικού συσκευασίας στις μεταβολές θερμοκρασίας του τροφίμου 302 Ενεργητική συσκευασία 303 Παραδείγματα 305 Ασκήσεις 309 Σύμβολα 310 Βιβλιογραφία 312
7 ΚΕΦΑΛΑΙΟ 1 ΣΤΟΙΧΕΙΑ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ 1. ΠΡΩΤΕΪΝΕΣ 1.1 Εισαγωγή Οι πρωτεΐνες είναι πολύπλοκα µακροµόρια που αποτελούν περισσότερο από το 50% του ξηρού βάρους των ζώντων κυττάρων. Παίζουν καθοριστικό ρόλο στη λειτουργία των κυττάρων κυρίως ως δοµικά στοιχεία και ως ένζυµα, που χρησιµεύουν για τα φαινόµενα του µεταβολισµού. Οι πρωτεΐνες είναι οργανικές αζωτούχες ενώσεις, αποτελούµενες από C, Η, Ο, Ν, S, και σε ορισµένες περιπτώσεις Ρ, Fe, Cu και Zn από τα οποία το περισσότερο χαρακτηριστικό στοιχείο είναι το άζωτο. Η περιεκτικότητα των πρωτεϊνών επί τοις εκατό στα στοιχεία αυτά κυµαίνεται ανάµεσα στα επόµενα όρια: C=50-55%, Η=6,5-7%, Ν= 15-17,6%, 0= 19-24%, και S=O,3-2,3%. Κάθε πρωτεΐνη χαρακτηρίζεται από τη φυσική της διαµόρφωση δηλαδή τη τρισδιάστατη οργάνωση της. Οι πρωτεΐνες εξυπηρετούν ένα µεγάλο εύρος λειτουργιών, και εµπειρικά µπορεί να καταταγούν σε τρεις µεγάλες κατηγορίες : δοµικές πρωτεΐνες, πρωτεΐνες µε βιολογική δράση και διατροφικές πρωτεΐνες ή πρωτεΐνες τροφίµων. Οι δοµικές πρωτεΐνες είναι ινώδεις πρωτεΐνες όπως η κερατίνη, το κολλαγόνο, η ελαστίνη κ.α., και υπάρχουν σε όλους τους ιστούς όπως οι µυς, τα οστά, το δέρµα, τα εσωτερικά όργανα, οι κυτταρικές µεµβράνες και τα ενδοκυτταρικά οργανίδια. Πρωτεΐνες µε βιολογική δράση εκτός από τα άνω των 2000 ένζυµα, που είναι βιολογικοί καταλύτες µε µεγάλη επιλεκτικότητα και εξειδίκευση, είναι οι ορµόνες (π.χ. ινσουλίνη, σωµατοτροπίνη) που ρυθµίζουν µεταβολικές αντιδράσεις, οι συστολικές πρωτεΐνες (µυοσίνη, ακτίνη και τροπονίνη), οι πρωτεΐνες µεταφοράς (αιµοσφαιρίνη, µυοσφαιρίνη και τρανσφερίνη), πρωτεΐνες µε προστατευτική δράση στο αίµα (ανοσοσφαιρίνες, θροµβίνες), αποθηκευτικές πρωτεΐνες (ωοαλβουµίνη, γλιαδίνη, ζεΐνη), τοξικές πρωτεΐνες (τοξίνη αλλαντίασης, σταφυλλοκοκοτοξίνες), αντιβιοτικές πρωτεΐνες, αντιγόνα και αντιθρεπτικές πρωτεΐνες (π.χ. αναστολείς τρυψίνης) Οι διατροφικές πρωτεΐνες ή πρωτεΐνες τροφίµων ουσιαστικά δεν αποτελούν ξεχωριστή κατηγορία καθώς οι περισσότερες από τις δοµικές και πρωτεΐνες µε βιολογική δράση που περιγράφηκαν παραπάνω είναι διατροφικές πρωτεΐνες. Πρωτεΐνες τροφίµων είναι απλά αυτές που είναι εύγευστες, µπορούν να µεταβολιστούν µε την πέψη, δεν είναι τοξικές και είναι οικονοµικά διαθέσιµες στον άνθρωπο. Οι πρωτείνες αποτελούν >50% ξ.β. ζώντων κυττάρων οµικά στοιχεία κολλαγόνο, κερατίνη, ελαστίνη Ενζυµα Βιολογική δράση Ορµόνες, συστολικές, µεταφοράς, τοξίνες, αποθήκη, προστασία 1
8 Με βάση τη µέση περιεκτικότητα των πρωτεϊνών σε άζωτο που είναι 16,5%, η περιεκτικότητα ενός τροφίµου σε πρωτεΐνες µπορεί να προσδιοριστεί µε τη µέθοδο Kjeldahl µε την οποία µετράται το συνολικό άζωτο: Πρωτεΐνη = Ν x 6,25 Στη σχέση αυτή βασίζεται και η σύσταση σε πρωτεΐνη που δηλώνεται στη διατροφική επισήµανση στις συσκευασίες των τροφίµων Αµινοξέα Με πλήρη υδρόλυση των πρωτεϊνών λαµβάνονται τα 20 αµινοξέα που αποτελούν τις δοµικές µονάδες (µονοµερή) των πρωτεϊνών. Ορισµένα άλλα αµινοξέα επίσης συναντώνται στη φύση αλλά ο ρόλος τους στις πρωτεΐνες τροφίµων είναι ασήµαντος. Πρωτείνη Υδρόλυση L α αµινοξέα Η φυσικοχηµική συµπεριφορά των αµινοξέων σε µεγάλο βαθµό καθορίζεται από την οµάδα R και από την ιδιότητα τους ως αµφολύτες. Αυτή η συµπεριφορά θα καθορίσει τις φυσικοχηµικές και λειτουργικές ιδιότητες της πρωτεΐνης στο τρόφιµο σε σχέση µε την σύστασή του και τις διεργασίες που θα υποστεί. Σε τιµές pη περί το ουδέτερο τα αµινοξέα σε υδατικά διαλύµατα έχουν ιοντισµένες τόσο τις άµινο όσο και τις καρβοξυλοµάδες. Το καρβοξύλιο χάνει ένα πρωτόνιο και αποκτά αρνητικό φορτίο, ενώ η αµινoµάδα προσλαµβάνει ένα πρωτόνιο και φορτίζεται θετικά. Η συνέπεια αυτού είναι ότι τα αµινοξέα έχουν χαρακτηριστικά διπόλου της ακόλουθης γενικής δοµής: 2
9 Τα αµινοξέα είναι αµφολύτες (Zwitterions) R C COO + NH 3 R ΟΞΥ + C NH 3 COO H + + R ΒΑΣΗ C NH 2 COO + - [H ][ αµινοξυ ] pka 2 = -log ± [ αµινοξυ ] R ΒΑΣΗ C COO + H + R ΟΞΥ C COOH + ± [H ][ αµινοξυ ] pka 1 = -log + [ αµινοξυ ] + NH 3 + NH 3 Τα αµινοξέα σε υδατικό διάλυµα συµπεριφέρονται σαν αµφολύτες, µε όξινο ή βασικό τρόπο, ανάλογο µε την τιµή του ρη τους. Τα µονοαµινοκαρβοξυλικά οξέα, όπως το γλουταµινικό οξύ, είναι ισχυρά οξέα, ενώ απότο άλλο µέρος τα διαµινοµονοκαρβοξυλικά οξέα όπως η λυσίνη, αντιδρούν σαφώς µε αλκαλικό τρόπο. Στην πλήρως πρωτονιωµένη του µορφή ένα α-αµινοξύ θα δώσει δύο Η + κατά την τιτλοδότηση του µε µία βάση (βλ. Σχ ) 3
10 Σχήµα Καµπύλη ογκοµέτρησης γλυκίνης (από. Μπόσκου, 1989) Ως ισοηλεκτρικό σηµείο pi ενός αµινοξέος ορίζεται το ph του διαλύµατος στο οποίο το συνολικό φορτίο του αµινοξέος είναι µηδέν, έχουµε δηλαδή κυρίως R + C NH 3 COO και ίσο αριθµό θετικά και αρνητικά φορτισµένων ιόντων. pi = pka pka Ισοηλεκτρικό σηµείο pi Η διαφορά στην ιοντική ισχύ επιτρέπει το διαχωρισµό και ποιοτικό προσδιορισµό των αµινοξέων, που βασίζεται στη δίοδο του µίγµατος των αµινοξέων από ιονοανταλλάκτες. Η έκλουση της στήλης µε ρυθµιστικά διαλύµατα που το ph τους µεταβάλλεται σταδιακά επιτρέπει την εκλεκτική εκρόφηση των αµινοξέων, τα οποία στη συνέχεια δίνουν χρωστική αντίδραση µε νινυδρίνη και µετρώνται φασµατοφωτοµετρικά. Η ένταση της προσρόφησης στην επιφάνεια της ρητίνης και συνεπώς η σειρά έκλουσης κάθε αµινοξέος εξαρτάται κυρίως από την ιοντική ισχύ, υπεισέρχονται όµως και άλλοι παράγοντες όπως το µέγεθος του µορίου, η αρωµατικότητα καθώς και η σχετική συγγένεια της ιοντοεναλλακτικής ρητίνης προς το κάθε αµινοξύ χωριστά. Ετσι λαµβάνεται το αµινογράφηµα το οποίο ανάλογα µε τον αριθµό των στηλών και τα χρησιµοποιούµενα ρυθµιστικά διαλύµατα περιλαµβάνουν είτε το σύνολο των αµινοξέων είτε χωριστά τα βασικά και χωριστά τα όξινα και ουδέτερα αµινοξέα, που συνήθως απαντούν σε µιά φυτική ή ζωική πρωτείνη ιαχωρισµός και ανάλυση των αµινοξέων γίνεται και µε HPLC. 1. Ασπαραγινικό οξύ 2.Θρεονίνη 3.Σερίνη 4.Γλουταµινικό οξύ 5.Προλίνη 6.Γλυκίνη 7.Αλανίνη 8.Κυστεΐνη 9.Βαλίνη 10. Μεθειονίνη 11. Ισολευκίνη 12.Λευκίνη 13.Τυροσίνη 14.Φαινυλαλανίνη 4
11 Σχήµα Aµινογράφηµα των ουδέτερων και όξινων αµινοξέων της πρωτείνης των σπορίων της τοµάτας (από Desrosier, 1984) Στήλη 70 cm. Ρητίνη JEOL-LC-R-I). Ρυθµιστικά διαλύµατα ph 3,31 και 4,25. Χρόνος αλλαγής 140 min. Θερµοκρασία 55 C. (από Desrosier, 1984) Ταξινόµηση αµινοξέων Τα 20 περίπου αµινοξέα, που απαντώνται στα υδρολύµατα των πρωτεϊνών µπορούν να χωρισθούν στις επόµενες δύο κύριες οµάδες: Α) αµινοξέα όπου το τµήµα R περιέχει µία αλειφατική αλυσίδα. Β) αµινοξέα όπου το R είναι ένα αρωµατικό ή ετεροκυκλικό τµήµα. Και οι δύο αυτές κύριες οµάδες µπορούν στη συνέχεια να υποδιαιρεθούν ως εξής: 1. αµινοξέα όπου το τµήµα R είναι ένας καθαρός υδρογονάνθρακας. 2. αµινοξέα όπου το τµήµα R περιέχει πολικές οµάδες όπως -SH ή -ΟΗ. 3. αµινοξέα, όπου το τµήµα R περιέχει µία δεύτερη αµινοµάδα (διαµινοκαρβοξυλικά οξέα, βασικά αµινοξέα). 4. αµινοξέα όπου το τµήµα R περιέχει µία δεύτερη καρβοξυλοµάδα (µονοαµινοδικαρβοξυλικά οξέα, όξινα αµινοξέα) 1. R = µη πολικό, υδροφοβο (Gly, Ala, Ile, Leu, Met, Phe, Pro, Trp, Val) 2. R= πολικό, υδρόφιλο (µη ιοντικό) Ser, Thr, Tyr (-OH) Asn, Gln (-Co-NH 2 ) Cys (-SH) 3. R= θετικά φορτισµένο (σε ph=7) Lys, His, Arg 4. R= αρνητικά φορτισµένο (σε ph=7) Asp, Glu Yδροφοβικότητα ενός αµινοξέος είναι η διαφορά ελεύθερης ενέργειας για τη µεταβολή της κατάστασής του από διάλυση σε υδατικό σε οργανικό διαλύτη : 0 G = RT ln S S EtOH H2O 5
12 Πίνακας Αµινοξέα Αµινοξύ Όνοµα pi pka1 pka2 Αλανίνη 6,02 2,35 9,69 Αργινίνη 10,76 2,17 9,04 12,48 (pka3) Σύµβολο 3 ή 1 γράµµατα Μοριακό βάρος Όνοµα (κατά IUPAC) Ala A 89.1 α-amino-propionic acid Arg R α-amino-δureinovalerianic acid οµή Ασπαραγίνη 5,41 2,02 8,80 Asn N amide of Asp Ασπαρτικό οξύ 2,97 2,09 9,82 3,86 (pka3) Asp D α-amino-succinic acid Κυστεΐνη 5,07 1,96 10,28 8,18 (pka3) Cys C α-amino-βmercaptopropionic acid Γλουταµίνη 5,65 2,17 9,13 Glu Q amide of Glu Γλουταµινικό οξύ Glu E α-amino-glutaric 3,22 2,19 9,67 acid 4,25 (pka3) Γλυκίνη 6,06 2,34 9,78 Gly G 75.1 α-amino-acetic acid Ιστιδίνη 7,58 1,82 9,17 6,00 (pka3) His H α-amino-βimidazol propionic acid Ισολευκίνη 6,02 2,36 9,68 Ile I α-amino-β-methyl valerianic acid 6
13 Λευκίνη 6,00 2,36 9,64 Leu L α-aminoisocaproic acid Λυσίνη 9,74 2,18 8,95 10,53 (pka3) Lys K α-ε-diaminocaproic acid Μεθειθονίνη 5,75 2,28 9,21 Φαινυλαλανίνη 5,53 1,83 9,24 Met M a-amino-α-methyl thiol-n-butyric acid Phe F a-amino-β-phenyl propionic acid Προλίνη 6,30 1,99 10,6 Pro P Pyrrolidine-2- carboxylic acid Σερίνη 5,68 2,21 9,15 Θρεονίνη 6,16 2,71 9,62 Τρυπτοφάνη 5,89 2,38 9,39 Τυροσίνη 5,65 2,20 9,11 10,07 (pka3) Ser S a-amino-βhydroxy propionic acid Thr T a-amino-βhydroxy n-butyric acidisocaproic acid Trp W a-amino-β-3- indolyl-propionic acid Tyr y a-amino-β-(ρhydroxy-phenyl propionic) acid Βαλίνη 5,97 2,32 9,62 Val V a-aminoisovalerianic acid 7
14 1.3 ΠΕΠΤΙ ΙΑ ΠΡΩΤΕΙΝΕΣ ΟΜΗ ΠΡΩΤΟΤΑΓΗΣ ΟΜΗ (PRIMARY STRUCTURE) Γραµµική αλληλουχία αµινοξέων Η σύνθεση των αµινοξέων για σχηµατισµό πεπτιδίων και πρωτεϊνών γίνεται µέσω πεπτιδικών δεσµών. Σ αυτούς η καρβοξυλική οµάδα ενός αµινοξέος αντιδρά µε την α-αµινονάδα ενός άλλου αµινοξέος και µε αποµάκρυνση ενός µορίου νερού σχηµατίζεται ένα διπεπτίδιο. Τα πεπτίδια ονοµάζονται δι-, τρι-, ή τετραπεπτίδια ανάλογα µε το αν προέρχονται από την ένωση δύο, τριών ή τεσσάρων αµινοξέων. Εάν έχουν συνδεθεί µε πεπτιδικούς δεσµούς µέχρι 10 αµινοξέα η ένωση που σχηµατίσθηκε ονοµάζεται ολιγοπεπτίδιο, όταν έχουν συνδεθεί περισσότερα από 10 αµινοξέα λέγεται πολυπεπτίδιο και όταν έχουν συνδεθεί περισσότερα από 100 αµινοξέα έχουµε τα µακροπεπτίδια και τις πρωτεΐνες. Τα πρωτεϊνικά µεγαλοµόρια αποτελούνται από εκατοντάδες αµινοξέα, το καθένα από τα οποία περιέχεται στο πρωτεϊνικό µόριο µία ή πολλές φορές. 8
15 Χαρακτηριστικά πεπτιδικού δεσµού: Ο πεπτιδικός δεσµός σταθεροποιείται µε συντονισµό δύο µεσοµερικών µορφών Αποτέλεσµα του ανωτέρω συντονισµού είναι ότι: ο C N δεσµός έχει 40% χαρακτήρα διπλού δεσµού και ο C=O 40% χαρακτήρα απλού δεσµού ο -NH δεν πρωτονιώνεται σε ανεξαρτήτως ph (από 0 ως 14) ο C N δεσµός δεν περιστρέφεται και είναι πολύ σταθερός (>400kJ/mol) τα 4 άτοµα του πεπτιδικού δεσµού + α άνθρακες στο ίδιο επίπεδο. Έτσι η πολυπεπτιδική αλυσίδα αποτελείται από αλληλουχία άκαµπτων επιπέδων και των οµάδων H-C-R n (βλ. Σχήµα 1.3.1) Σχήµα οµή ενός τµήµατος µιας α-l-πολυπεπτιδικής αλυσίδας (διαµόρφωσης trans). Απεικονίζονται οι ενδοατοµικές αποστάσεις (Å) και οι γωνίες µεταξύ των δεσµών ( ). Τα έξι άτοµα στα τετράγωνα είναι στο ίδιο επίπεδο. Το φ και ψ είναι οι δυνατές γωνίες συστροφής περί τον α-άνθρακα. Ο καθένας από τους πεπτιδικούς δεσµούς αµφίπλευρα του α-άνθρακα είναι σε ένα επίπεδο. Τα R1, R2, R3 είναι σε θέση trans. (φ=ψ=180 C) Πρωτοταγής δοµή µιας πρωτεΐνης είναι η γραµµική ακολουθία των αµινοξέων που την απαρτίζουν. Αυτή η συγκεκριµένη κατά περίπτωση αλληλουχία των αµινοξέων είναι εκείνη που προσδίδει πολλές από τις βασικές ιδιότητες στις διάφορες πρωτεΐνες και καθορίζει σε µεγάλο βαθµό τις δευτεροταγείς και τριτοταγείς δοµές τους. Η πρωτοταγής δοµή των περισσοτέρων πρωτεϊνών έχει προσδιορισθεί. 9
16 Σχήµα Πρωτοταγής δοµή της πρωτεΐνης β-λακτογλοβουλίνη του γάλακτος (αποτελείται από αλληλουχία 162 α-αµινοξέων, µε δύο δισουλφιδικούς δεσµούς). 10
17 1.3.2 ΕΥΤΕΡΟΤΑΓΗΣ ΟΜΗ (secondary structure) Τρισδιάστατος τρόπος διάταξης κατά τον άξονα. H φυσική διαµόρφωση (native) της πρωτεΐνης τείνει στην ελαχιστοποίηση της ελεύθερης ενέργειας : G=min Οι σηµαντικότερες και συνηθέστερες δευτεροταγείς δοµές είναι: α-έλικας (α-helix) Ιδιότητες: -3,6 αµινοξέα/περιστροφή (βήµα 0,54 nm- διάµετρος 0,6nm), δεξιόστροφος - οµάδες R στραµµένες προς τα έξω. εσµοί Η 2 µεταξύ πεπτιδικών δεσµών υψηλή σταθερότητα, µεγάλη «πυκνότητα», µικρές επιδράσεις µε άλλα µόρια Η 2 Ο. Το αµινοξύ προλίνη µε µη συµβατή µε α-έλικα, διακόπτει δοµή τµήµατα τυχαίας σπείρας π.χ. καζείνη. Τυχαία σπείρα (random coil) δηµιουργείται επίσης λόγω φορτισµένων ή ογκωδών πλευρικών αλύσων. Σχήµα α-έλικας 11
18 β-πτυχωµένα φύλλα (β- pleated sheets) οµή ζίγκ ζαγκ, πιο τεντωµένη από α έλικα. Πεπτιδικές αλυσίδες σχηµατίζουν µε ενδοαλυσικούς δεσµούς Η 2 πτυχωµένα φύλλα: παράλληλα ή αντιπαράλληλα R- οµάδες: πάνω και κάτω από τα φύλλα (εκτός Asn, Glu, His, Lys, Pro, Ser) Σχήµα β-πτυχωµένα φύλλα β-κάµψεις (β- bends) έλικας, υπερέλικας κολλαγόνου (πολυπρολίνηιι αριστερόστροφος, 3α.ο./περιστροφή) ΤΡΙΤΟΤΑΓΗΣ ΟΜΗ (tertiary structure) Η τριτοταγής δοµή αναφέρεται στην τρισδιάστατη οργάνωση µεγάλων τµηµάτων της πολυπεπτιδικής αλυσίδας που περιέχει περιοχές σαφώς καθορισµένης δευτεροταγούς δοµές και περιοχές µε ασαφή ή χωρίς δευτεροταγή δοµή. Ινώδεις πρωτείνες (κυρίως α- έλικες) Σφαιροειδείς (globular). Υδατοδιαλυτές σφαιροειδείς πρωτεΐνες τείνουν να αποκτήσουν διαµόρφωση ώστε τα υδρόφοβα αµινοξέα να διατάσσονται στο εσωτερικό και τα υδρόφιλα οµοιόµορφα στην επιφάνεια. Οι δεσµοί υδρογόνου παίζουν σηµαντικό ρόλο στη σταθεροποίηση τριτοταγών δοµών. 12
19 Σχήµα Απεικόνιση τριτοταγούς δοµής σφαιρικής πρωτεΐνης. Οι κύλινδροι συµβολίζουν τµήµατα α-έλικα και τα βέλη πτυχωµένα φύλλα ΤΕΤΑΡΤΟΤΑΓΗΣ ΟΜΗ (quaternary structure) Είναι αποτέλεσµα συσχετισµού πρωτεινικών µονάδων, όχι παραίτητα µε καθορισµένη συµµετρία. Ιδιες δυνάµεις ή δεσµοί που σταθεροποιούν την τριτοταγή δοµή + δισουλφιδικοί δεσµοί (-S-S-) ΠΑΡΑ ΕΙΓΜΑ ΤΕΤΑΡΤΟΤΑΓΟΥΣ ΟΜΗΣ Ακτοµυοσίνη: Μυοινίδια (myofibrils) Μυοσίνη 55%: 475,000, 6 υποµονάδες Ακτίνη 20% G-ακτίνη, σφαιροειδής 42,000 F- ακτίνη, ινώδης + Τροποµυοσίνη, τροπονίνες. 13
20 Σχήµα Σχηµατική αναπαράσταση της τεταρτοταγούς δοµής των µυοινικών πρωτεϊνών. (ae) Υποµονάδες της µυοσίνης και των µορίων της. (f) Τεταρτοταγής δοµή της F-ακτίνης (από Fennema, 1985) 14
21 Πίνακας Ιδιότητες δοµής σηµαντικών πρωτεϊνών τροφίµων Πρωτεΐνη ΜΒ (daltons) Τύπος: Σφαιρική (G) Ινώδης (F) Ελικοειδής (RC) ευτεροταγής δοµή α-έλικα (%) β- πτυχωτό φύλλο (%) Αριθµός αµινοξέων Αριθµός S-S Αριθµός SH pi Αριθµός υποµονάδων Αλληλουχία γνωστή (Γ) άγνωστη (Α) Προσθετική οµάδα (%, w/w) Μέση υδροφοβικότητα (kj/mol) Μυοσίνη b F Υψηλό Γ µερικώς Φωσφόρος 4,25 (κουνέλι) Ακτίνη b G F ,,4 (κουνέλι) Κολλαγόνο (τροποκολλαγόνο) b F Έλικα κολλαγόνου ~9 3 Γ µερικώς 4,5 (κοτόπουλο) αs 1 -Καζεΐνη Β b RC ,1 1 Γ Φωσφόρος 1,1 5,0 β-καζεΐνη Β b RC ,3 1 Γ Φωσφόρος 0,56 Υδρογονάνθρακες Κ-Καζεΐνη Β b 4, RC Γ 5 4,5 Φωσφόρος 0,22 β-λακτογλοβουλίνη b G ,2 Γ 5,15 α-λακτογλοβουλίνη Β b G ,1 Γ 4,8 Οβαλβουµίνη c G 1 ή 2 4 4,6 Υδρογονάνθρακες 3,3 Φωσφόρος Αλβουµίνη ορού b G ,8 1 Γ 4,7 Γλυαδίνη d (α,β,γ) G F Γ µερικώς 4,5 Γλουτενίνη d F Γλυκινίνη e G ,6 12 Α Κονγλυκινίνη e G ,6 9 Α b Αγελαδινό γάλα c Αυγό d Σιτάρι e Σόγια Υδρογονάνθρακες 4 4,65 15
22
23 1.3.5 ΑΛΛΗΛΕΠΙ ΡΑΣΕΙΣ ΚΑΙ ΕΣΜΟΙ ΠΟΥ ΚΑΘΟΡΙΖΟΥΝ ΤΗΝ ΠΡΩΤΕΙΝΙΚΗ ΟΜΗ 1. Στερεοχηµικοί περιορισµοί 2. Ηλεκτροστατικές αλληλεπιδράσεις (42-84 kj/mol) Οι πρωτεΐνες συµπεριφέρονται ως πολυηλεκτρολύτες λόγω ιοντικών R των αµινοξέων (Asp, Glu, Tyr, Lys, His, Arg, Cys). Τα αµινοξέα αυτά αντιπροσωπεύουν το 30-50% όλων των πρωτεϊνών στα τρόφιµα. Στο ισοηλεκτρικό σηµείο pi των πρωτεϊνών το µέσο φορτίο = 0. Αναλόγως του ph τα φορτία µεταβάλλονται και επηρεάζουν τη διαµόρφωση. Επίσης έχουµε επιδράσεις ιόντων-πρωτεΐνης π.χ. πρωτεΐνη-ca 2+ -πρωτεΐνη στα µικύλια της καζεΐνης του γάλακτος. 3. εσµοί Υδρογόνου (1,75Å, 8-40 kj/mol) Σταθεροποίηση δευτεροταγούς και τριτοταγούς δοµής. Οι δεσµοί είναι ενδοπρωτεΐνικοί αλλά και µε τα µόρια Η 2 Ο. 4. Υδρόφοβες αλληλλεπιδράσεις (4-12 kj/mol) Τα µη πολικά R τείνουν να «συσχετίζονται» σε εσωτερικές υδρόφοβες περιοχές της πρωτεΐνης. 5. ισουλφιδικοί δεσµοί ( kj/mol) S-S Οµοιοπολικοί δεσµοί µεταξύ -SH της κυστεϊνης. Πολύ σταθεροί. Πρωτεΐνες µε περισσότερους από 5 ισουλφιδικούς δεσµούς ανά 100 αµινοξέα είναι πολύ ανθεκτικές σε µετουσίωση. Σχήµα εσµοί και αλληλεπιδράσεις που καθορίζουν τη δευτεροταγή και τριτοταγή των πρωτεϊνών: (Α) εσµοί Η, (Β) ιπολικός δεσµός, (C) Υδρόφοβες αλληλεπιδράσεις, (D) ισουλφιδικός δεσµός, (Ε) Ιοντικός δεσµός 17
24 1.3.6 ΑΛΛΗΛΕΠΙ ΡΑΣΕΙΣ ΠΡΩΤΕΙΝΩΝ Η 2 0 Σχήµα Σχηµατική απεικίνιση αλληλεπιδράσεων νερού-πρωτεϊνών: (Α) εσµοί υδρογόνου µε πεπτιδικούς δεσµούς και οµάδες R, (Β) Υδρόφοβες αλληλεπιδράσεις, (C) Ιοντικοί δεσµοί ιαλυτότητα πρωτεϊνών (solubility): Παράγοντες που καθορίζουν τη διαλυτότητα: ph, ιοντική ισχύς, διαλύτης, θερµοκρασία (Τα). α) ph: Φορτίο ιαλυτότης Σε ph=pi, min διαλυτότητα, συχνά καταβύθιση Όταν ph>pi η αύξηση στο αρνητικό φορτίο είναι µεγαλύτερη από την αντίστοιχη αύξηση σε θετικό φορτίο για ph<pi. 1 2 β) Ιοντική ισχύς: µ = c i z i 2 ΕΝΑΛΑΤΩΣΗ: Αύξηση διαλυτότητας για χαµηλή συγκέντρωση αλάτων (0,5-1 Μ): S µ (λόγω µείωσης της ηλεκτροστατικής έλξης και αύξησης της διαλυτοποίησης) 18
25 ΕΝΑΛΑΤΩΣΗ: Μείωση της διαλυτότητας πρωτεϊνών λόγω υψηλής συγκέντρωσης αλάτων (>1 Μ): log S = log S k ' µ (ανταγωνισµός για µόρια Η 2 0) k = σταθερά εξαλάτωσης Ιδιότητες εναλάτωσης ιόντων: 0 SO 4 2- < F - < CH 3 COO - < CI - < Br - < NO 3 - < I - < CIO 4 - < EΞΑΛΑΤΩΣΗ < SCN - < NH 4 - < K + < Na + < Li + < Mg 2+ < Ca 2+ ΕΝΑΛΑΤΩΣΗ γ) ιαλύτες: Οργανικοί διαλύτες όπως EtOH, ακετόνη προκαλούν µείωση της διαλυτότητας λόγω µείωσης της διηλεκτρικής σταθεράς. δ) Θερµοκρασία: Από 0-50 C αύξηση της θερµοκρασίας προκαλεί αύξηση της διαλυτότητας, ενώ σε θερµοκρασίες >50 C η διαλυτότητα µειώνεται λόγω µετουσίωσης. 1.4 ΤΑΞΙΝΟΜΗΣΗ ΠΡΩΤΕΪΝΩΝ ΑΠΛΕΣ 1. Γλοβουλίνες ΑΠΛΕΣ (ΟΜΟΠΡΩΤΕΪΝΕΣ) ΣΥΝΘΕΤΕΣ (ΕΤΕΡΟΠΡΩΤΕΪΝΕΣ) Όξινη αντίδραση. Αδιάλυτες σε Η 2 0. ιαλυτές σε αραιά δ. αλάτων (ph=7). Καταβύθιση µε (NH 4 ) 2 SO 4 (ή οξίνιση). Περιέχουν Gly. Γαλακτο-, ωο-, ορογλοβουλίνη, µυοσίνη, αποθεµατικές φυτών. 2. Αλµπουµίνες ιαλυτές σε Η 2 0 (ph=6,6). Καταβύθιση µε (NH 4 ) 2 SO 4. εν περιέχουν Gly αλλά Cys.. Γαλακτο-, ωο-, οροαλµουµίνες. 3. Πρωταµίνες Απλές, λίγα αµινοξέα, Arg, όχι Cys ή αρωµατικά α.ο. Ζωικές κυρίως σε ψάρια, κλουπεΐνη (ρέγγα), σαλµίνη (σολωµό). 4. Ιστόνες Στους κυτταρικούς πυρήνες ως νουκλεοπρωτεΐνες. 19
26 5. Γλοιαδίνες (προλαµίνες). Αδιάλυτες H 2 O, EtOH. ιαλυτές σε 50-90% EtOH. Υψηλά ποσοστά Pro και Glu. Γλοιαδίνη σίτου, σίκαλης. Ζεΐνη καλαµποκιού. Χορδεΐνη κριθαριού. 6. Γλουτελίνες ιαλυτές σε αραιά δ. οξέων και βάσεων (Ph = 2 και 12) Γλουτελίνη + γλοιαδίνη γλουτένη ΣΥΝΘΕΤΕΣ (ΕΤΕΡΟΠΡΩΤΕΪΝΕΣ) Στην κατηγορία αυτή υπάγονται οι πολυπλοκώτερης συστάσεως πρωτείνες, οι οποίες περιλαµβάνουν στο µόριό τους και πρόσθετες οργανικές ή ανόργανες οµάδες, όπως υδατάνθρακες, λιπίδια, νoυκλεϊνικά οξέα, χρωστικές, µεταλλικά ιόντα, φωσφορικό οξύ. Οι οµάδες αυτές ονοµάζονται γενικά προσθετικές ουσίες και οι πρωτείνες που φέρουν προσθετική οµάδα συζευγµένες πρωτείνες. Οι σύνθετες πρωτείνες απαντώνται στη φύση σε µεγαλύτερη έκταση από ότι οι απλές πρωτείνες. Φωσφορoπρωτεινες. Στην οµάδα αυτή των πρωτεϊνών το ορθοφωσιρορικό οξύ αποτελεί την πρόσθετη οµάδα. Οι φωσψοροπρωτείνες (µε περιεκτικότητα 0,7% σε φωσφορικό οξύ) ε.ίναι σχεδόν αδιάλυτες στο νερό, ενώλόγω του όξινου χαρακτήρα τους είναι διαλυτές σε αραιά αλκάλια και τηναµµωνία. Ο κυριώτερος εκπρόσωπος της οµάδας των φωσιροροπρωτεϊνών είναι η καζείνη, που αποτελεί την κυριώτερη πρωτείνη του γάλακτος, µέσα στο οποίο βρίσκεται υπό µορφή κολλοειδούς διαλύµατος KαζεϊVΙKoύ ασβεστίου. Κατά.την οξίνιση του γάλακτος αποχωρίζεται το ασβέστιο από τοκαζεϊνικό ασβέστιο και σε ορισµένη τιµή ρη καθιζάνει η ελεύθερη καζείνη, ενώ µε την επίδραση της πυτιάς το διαλυµένο καζεϊνικό ασβέστιο µετατρέπεται σε αδιάλυτο παρακαζεϊνικό ασβέστιο. Νουκλεοπρωτείνες. Οι νουκλεοπρωτείνες είναι ένα από τα κύρια συστατικά του πυρήνα των ζωίκών και φυτικών κυττάρων. Ως προσθετική οµάδα έχουν τα νoυκλεϊνικά οξέα, που είναι ενώσεις µεγάλου µοριακού βάρους µε ισχυρά όξινό χαρακτήρα οφειλόµενο στην παρουσία του φωσφορικού οξέος. Γλυκοπρωτείνες. Συζευγµένες πρωτείνες που για προσθετική οµάδα έχουν ετεροσακχαρίτες, καθορίζονται ως γλυκοπρωτείνες (βλεννοπρωτείνες). Τα υδατανθρακικά συστατικά εί'!αι ενωµένα µε την πρωτείνη µέσω οµοιοπολικού δεσµού και µπορούν να αποτελούν 4-70% του συνολικούµορίου, ανάλογα µε το είδος της γλυκοπρωτείνης. Οι ετεροσακχαρίτεςπεριέχουν εξοζαµίνες και ένα ή περισσότερους από τους µονοσακχαρίτεςγαλακτόζη, µαννόζη, φυκόζη και σιαλικό οξύ, έχουν δε µοριακό βάροςκυµαινόµενο από ανάλογα µε τη γλυκοπρωτείνη. Οι γλυκοπρωτείνες απαντώνται στα βλεννώδη εκκρίµατα των θηλαστικών, όπου ενεργούν ως λιπαντικοί παράγοντες στις επιφάνειες των σωµατικών ιστών. Χρωµοπρωτείνες. Οι χρωµοπρωτείνες είναι ενώσεις πρωτείνη ς µε χαµηλού µοριακού βάρους προσθετικές οµάδες, παρόµοιες µε φυσικές χρωστικές, που σχεδόν πάντα περιέχουν ένα µέταλλο (Fe, Mg). Η φυσική χρωστική µπορεί να είναι ένα παράγωγο της πορφυρίνης (αίµη, χλωροφύλλη), αλλά και τα καροτινοειδή, που είναι λιποδιαλυτές χρωστικές, µπορούν να δράσουν ως προσθετικές οµάδες, ενώ το πρωτεϊνικό τµήµα του µορίου είναι µία απλή γλοβουλίνη. 20
27 Οι σηµαντικώτερες και περισσότερο διαδεδοµένες χρωµοπρωτείνες από τις περιέχουσες, ως πρόσθετη οµάδα, χρωστικές πορφυρίνης είναι η αιµοσφαιρίνη, η µυοσφαιρίνη, η χλωροπλαστίνη, Στο ήπαρ και τον σπλήνα απαντάται µία χρωµοπρωτείνη (µεταλλοπρωτείνη) η φεριτίνη, που περιέχει περίπου 20% σίδηρο και θεωρείται αποθεµατική πηγή σιδήρου του οργανισµού. Λιποπρωτείνες: Είναι σύνθετες πρωτείνες που περιέχουν λιπίδια ως πρόσθετη οµάδα και απαντώνται στα κύτταρα 'και τον ορό του αίµατος. Πιστεύεται ότι αυτά τα συµπλέγµατα λιπιδίων και πρωτεϊνών χρησιµεύουν ως µεταφορείς λιπιδίων στο αίµα και ως συστατικά των κυτταρικών µεµβρανών. Οι λιποπρωτείνες ταξινοµούνται ανάλογα µε την πυκνότητα τουςσε υψηλής πυκνότητας (H.D.L. High density lipoproteins), χάµηλής πυκνότητας (L.D.L. Low density lipoproteins) και σε πολύ χαµηλής πυκνότητας, και καθώς τα λιπίδια είναι λιγότερο πυκνά από τις πρωτείνες, όσο µεγαλύτερη είναι η περιεχόµενη ποσότητα λιπιδίων, τόσο µικρότερη είναι η πυκνότητα της λιποπρωτείνης. Τα απαντώµενα στις λιποπρωτείνες λιπίδια είναι τριγλυκερίδια, φωσφολιπίδια, χοληστερίνη και παράγωγά της. ΠΟΣΟΤΙΚΟΣ ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ Ο ακριβής προσδιορισµός των πρωτεϊνών, ιδίως στα πολύπλοκα µίγµατα που απαντώνται στα τρόφιµα, είναι ιδιαίτερα δύσκολος. Αυτό οφείλεται στις δυσκολίες διαχωρισµού, καθαρισµού και ξηράνσεώς τους, που συνδέονται µε τον επαµφοτερίζοντα χαρακτήρα τους, τη µεγάλη προσροφητική τους ικανότητα, την ιδιότητα ενυδατώσεώς τους, την ευαισθησία τους στους ηλεκτρολύτες, το pη, τη θέρµανση και τα διαλυτικά µέσα. Για τους λόγους αυτούς γίνεται συνήθως προσδιορισµός ολικού αζώτου µε τη µέθοδο Kjeldahl (1883), όπως έχει σήµερα τροποποιηθεί. Στη µέθοδο αυτή το τρόφιµο που περιέχει πρωτεϊνη, διασπάται µε χρήση πυκνού θειικού οξέος παρουσία καταλύτου, κατά τη διαδικασία δε αυτή τοάζωτο ανάγεται προς αµµωνία, που προσδιορίζεται µε τιτλοδότηση. Το ευρισκόµενο ποσό αζώτου πολλαπλασιαζόµενο επί 6,25 δίνει το ολικό ποσότης πρωτείνης, χωρίς να προκύπτει πληροφορία για το είδος των υπαρχουσών πρωτεϊνών. Ο συντελεστής 6,25 είναι ο συνήθως και γενικά χρησιµοποιούµενος στην αναλυτική πράξη, παρότι δεν είναι απόλυτα ακριβής. 'Ετσι για την καζείνη του γάλακτος ακριβέστερος είναι ο συντελεστής 6,37, για τη ζελατίνη η τιµή 5,55, για την πρωτείνη του κρόκου του αυγού η τιµή 6,67. εν πρέπει πάντως να διαφεύγει της προσοχής ότι η µέθοδος προσδιορίζει ολικό άζωτο, σε τρόπο που υπάρχει ενδεχόµενο να υπολογισθούν σανπρωτείνη, συστατικά αζωτούχα αλλά µη πρωτεϊνικά. Για τον προσδιορισµότης καθαρής πρωτείνης πρέπει να προηγηθεί διαχωρισµός της µε διάφορες αντιδράσεις καταβυθίσεως. '. 21
28 1.5 ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΙΝΩΝ (denaturation) ΟΡΙΣΜΟΣ: Κάθε µεταβολή της διαµόρφωσης της φυσικής πρωτεΐνης (δευτεροταγής, τριτοταγής ή τεταρτοταγής δοµή) που δεν ενέχει διάσπαση πεπτιδικών δεσµών (πρωτοταγής δοµή). Μπορεί να φτάσει µέχρι πλήρες ξετύλιγµα της αλύσου. Αντιστρεπτή ή αναντίστρεπτη. Παράγοντες που προκαλούν ή επηρεάζουν τη µετουσίωση είναι ΦΥΣΙΚΟΙ και ΧΗΜΙΚΟΙ: Θερµότητα, οξέα, βάσεις, πυκνά άλατα, διαλύτες, ακτινοβόληση, ψύξη, µηχανικήκαταπόνηση, υψηλή πίεση, ρόφηση σε διεπιφάνειες. Συνέπειες µετουσίωσης: 1. Μείωση διαλυτότητας (λόγω έκθεσης υδρόφοβων οµάδων) 2. Μεταβολή ικανότητας ρόφησης H 2 O 3. Απώλεια βιολογικής δράσης (ενζυµικής ή ανοσολογικής). 4. Αυξηµένη ευπάθεια σε πρωτεολυτικά ένζυµα. 5. Αυξηµένο ιξώδες. 6. Απώλεια ικανότητας κρυστάλλωσης. Η µετουσίωση συµβαίνει σε στενό θερµοκρασιακό εύρος Μικρή Τ Μεγάλο k (µεταβολή στο ρυθµό µετουσίωσης). Αυτό µεταφράζεται σε πολύ µεγάλες τιµές ενέργειας ενεργοποίησης στη σχέση Arrhenius που εκφράζει την εξάρτηση του ρυθµού µετουσίωσης, k, από την θερµοκρασία, T. π.χ. η τιµή ενέργειας ενεργοποίησης, Εα = 550 kj/mol για µετουσίωση συναλβουµίνης αυγού στο εύρος 57 C - 67 C k x k 57 22
29 1.6 ΡΟΛΟΣ ΠΡΩΤΕΙΝΩΝ ΣΤΑ ΤΡΟΦΙΜΑ: Α. ΘΡΕΠΤΙΚΟΤΗΤΑ Β. ΛΕΙΤΟΥΡΓΙΚΟΤΗΤΑ Α. ΘΡΕΠΤΙΚΟΤΗΤΑ Οι πρωτεΐνες παρέχουν στον οργανισµό Ν 2 και αµινοξέα για σύνθεση πρωτεΐνών και άλλων Ν- ενώσεων. Πρωτεΐνες σώµατος: kg / 70 kg. Καταβολισµός αναβολισµός (βλ. Σχ. Ανάγκες σε πρωτεΐνη: 0,8 g / kg /day ή 56 g / 70 kg. Συνιστώµενη Ηµερήσια όση: ΣΗ (RDA) 1 g / kg /day Η υτική δίαιτα περιέχει υπερβάλλουσα ποσότητα πρωτεΐνών: g /day, έτσι το 10-15% θερµίδων προέρχεται από πρωτεΐνες (4kcal/g) Σχήµα Ηµερήσιες ροές και ισοζύγιο αµινοξέων και πρωτεϊνών για ενήλικα 70kg 23
30 ΑΠΑΡΑΙΤΗΤΑ ΑΜΙΝΟΞΕΑ (Essential aminoacids) Ο οργανισµός µε την καθηµερινή τροφή προσλαµβάνει πρωτεΐνες, που περιέχουν ποικίλα ποσά αµινοξέων. Πολλά από τα αµινοξέα αυτά µπορούν να συντεθούν από τον οργανισµό για τις θρεπτικές του ανάγκες, ενώ εκείνα που ο οργανισµός δεν µπορεί να συνθέσει, πρέπει να τα παραλαµβάνει από τις τροφές τακτικά και σε επαρκείς ποσότητες. Τα αµινοξέα αυτά χαρακτηρίζονται ως «ουσιώδη» ή «απαραίτητα» αµινοξέα, γιατί η δράση τους δεν µπορεί να αντικατασταθεί από άλλα θρεπτικά συστατικά των τροφίµων. Τα αµινοξέα αυτά είναι τα επόµενα: λευκίνη, ισολευκίνη, λυσίνη, µεθειονίνη, θρεονίνη, φαινυλαλανίνη, τρυποφάνη, βαλίνη, ιστιδίνη (Ile, Leu, Lys, Met, Thr, Phe, Trp, Val, His). Η ιστιδίνη είναι απαραίτητo αµινοξύ για τους αναπτυσσόµενους οργανισµούς αλλά όχι και για τους ενήλικους. Η ανάγκη για απαραίτητα αµινοξέα (λόγος ΑΑ/ΣΑ απαραίτητων προς συνολικά αµινοξέα) είναι µεγαλύτερη στα παιδιά: ΑΑ/ΣΑ= 37% (βρέφη) 15% (ενήλικες) ΠΕΡΙΟΡΙΣΤΙΚΟ ΑΜΙΝΟΞΥ Ο οργανισµός του ανθρώπου χρειάζεται καθηµερινά την πρόσληψη µιας ποσότητας από κάθε απαραίτητο αµινοξύ και έτσι η θρεπτική βιολογική αξία µιας πρωτεΐνης περιορίζεται από εκείνα τα αµινοξέα, που περιέχονται σε ποσότητα κάτω από το ελάχιστο απαιτούµενο όριο και που αποτελούν τα περιοριστικά ουσιώδη αµινοξέα. Ως περιοριστικό αµινοξύ ή παράγοντας µιας πρωτεΐνης ορίζεται το απαραίτητο αµινοξύ που βρίσκεται στην πρωτεΐνη στη µικρότερη αναλογία σε σχέση µε την ποσότητα του αµινοξέος στην πρώτυπη πρωτεΐνη αναφοράς του FAO. Όταν στις πρωτεΐνες της διατροφής υπάρχει ανεπαρκής ποσότητα ή έλλειψη, ακόµα και ενός απαραίτητου αµινοξέος, ο οργανισµός παρουσιάζει διαταραχές της αναπτύξεως, µεταβολές του δέρµατος και γενικές διαταραχές του πρωτεϊνικού και του γενικού µεταβολισµού. ΠΟΙΟΤΗΤΑ ΠΡΩΤΕΙΝΗΣ Όταν είναι γνωστή η σύνθεση των πρωτεϊνών ενός τροφίµου, είναι δυνατό να συναχθούν ορισµένα συµπεράσµατα σχετικά µε τη βιολογική του αξία, σαν ένα µέτρο του βαθµού που ο οργανισµός µπορεί να χρησιµοποιήσει τις πρωτεΐνες της διατροφής. Οι φυτικές πρωτεΐνες που έχουν χαµηλή βιολογική αξία λόγω ανεπαρκείας ουσιωδών αµινοξέων, µπορούν να γίνουν βιολογικά πλήρεις όταν αναµιχθούν µε άλλες φυτικές πρωτεΐνες, ώστε να αλληλοσυµπληρωθούν τα περιοριστικά απαραίτητα αµινοξέα τους. Σε ορισµένες άλλες περιπτώσεις, όπως στα άλευρα των δηµητριακών, η βιολογική αξία των πρωτεϊνών βελτιώνεται µε εµπλουτισµό τους µε τα σε ανεπαρκή περιεκτικότητα απαραίτητα αµινοξέα, κυρίως δε µε προσθήκη λυσίνης. 24
31 Ως δείκτες ποιότητας µιας πρωτεΐνης χρησιµοποιούνται οι εξής: - Βιολογική αξία (BV) = συγκρ. Ν / αποροφ. Ν % (συνήθως από 85-98) - Συντελεστής αποτελεσµατικότητας (PER) = αύξηση βάρους / βάρος πρωτεΐνης (συνήθως 2,5) - Καθαρή χρησιµοποιήσιµη πρωτεΐνη (NPU) = συγκρατούµενη Ν/ Ντροφίµου % = (Nbody- Nbodyfr)/Ni - Χηµικό σκόρ (chemical score): [(mg/g πρωτεΐνης) περιοριστικού α.ο.] / [ mg ιδίου α.ο./ g πρωτεΐνης FAO] Πίνακας Απαιτήσεις σε απαραίτητα αµινοξέα για την ανθρώπινη διατροφή και υποθετική ιδανική πρωτεΐνη ανά ηλικία Αµινοξέα Απαιτήσεις για νεογνά mg/day/kg Προσωρινά Πρότυπα Μοντέλα mg/g πρωτ. Απαιτήσεις για παιδιά mg/day/kg Προσωρινά Πρότυπα Μοντέλα mg/g πρωτ. Απαιτήσεις για ενήλικες mg/day/kg Προσωρινά Πρότυπα Μοντέλα mg/g πρωτ. Ιστιδίνη Ισολευκίνη Λευκίνη Λυσίνη Μεθειονίνη Φαινυλαλανίνη (+ τυροσίνη) Θρεονίνη Τρυπτοφάνη Βαλλίνη , , , ,5 18 Συνολικά Απαραίτητα Αµινοξέα Συνολική Απαίτηση Πρωτεϊνών : άνδρες 520: γυναίκες 25
32 Πίνακας Περιεχόµενο σε απαραίτητα αµινοξέα και ποιότητα πρωτεϊνών σηµαντικών ζωικών και φυτικών τροφίµων (σε κύκλο το περιοριστικό αµινοξύ της πρωτεΐνης ΑΜΙΝΟΞΕΑ Ιστιδίνη Ισολευκίνη Λευκίνη Λυσίνη Μεθειονίνη + κυστεΐνη Φαινυλαλανίνη + τυροσίνη Θρεονίνη Τρυπτοφάνη Βαλλίνη Συνολικά απαραίτητα αµινοξέα (χωρίς His) ΠΡΟΤΥΠΗ FAO Error! Ανθρώπινο γάλα Αγελαδινό γάλα Αυγά Κότας Βοδινό κρέας Πρωτεϊνικό περιεχόµενο % Χηµικό Σκορ Συντελεστής Αποτελεσµατικότητας (4) (3) (PER) Βιολογική Αξία (BV) (95) Καθαρή Χρησιµοποιήσιµη Πρωτεΐνη (NPU) (87) ΑΜΙΝΟΞΕΑ Ιστιδίνη Ισολευκίνη Λευκίνη Λυσίνη Μεθειονίνη + κυστεΐνη Φαινυλαλανίνη + τυροσίνη Θρεονίνη Τρυπτοφάνη Βαλλίνη Συνολικά απαραίτητα αµινοξέα (χωρίς His) ΠΡΟΤΥΠΗ FAO Error! Ψάρια Σιτάρι Ρύζι (καφέ) Σόγια Πρωτεϊνικό περιεχόµενο % Χηµικό Σκορ Συντελεστής Αποτελεσµατικότητας (PER) Βιολογική Αξία (BV) Καθαρή Χρησιµοποιήσιµη Πρωτεΐνη (NPU)
33 Β. ΛΕΙΤΟΥΡΓΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΠΡΩΤΕΙΝΩΝ Ο όρος λειτουργικότητα (functionality) για τα συσταικά των τροφίµων ορίζεται ως το σύνολο των ιδιοτήτων, εκτός από τις θρεπτικές, οι οποίες επηρεάζουν τη χρησιµοποίησή τους στα τρόφιµα. Οι λειτουργικές ιδιότητες (functional properties) των πρωτεϊνών είναι εκείνες οι φυσικοχηµικές ιδιότητες που καθορίζουν τη συµπεριφορά των πρωτεϊνών στα συστήµατα τροφίµων, κατά την παραγωγή, αποθήλευση, προετοιµασία και κατανάλωση, και κατά συνέπεια επηρεάζουν την ποιότητα και την αποδοχή του τροφίµου. Μερικές τυπικές κατηγορίες λειτουργικών ιδιοτήτων παρουσιάζονται στον επόµενο πίνακα. Πίνακας Λειτουργικές ιδιότητες πρωτεϊνών σε συστήµατα τροφίµων Γενική Ιδιότητα Λειτουργικά χαρακτηριστικά Οργανοληπτική Χρώµα, γεύση, οσµή Κιναισθητική Υφή, απαλότητα, στοµατική αίσθηση, κοκκώδης αίσθηση, θολότητα Ενυδάτωση ιαλυτότητα, διαβρεκτικότητα, απορρόφηση νερού, διόγκωση, πάχυνση, ζελοποίηση, συναίρεση, ιξώδες Επιφανειακή Γαλακτοµατωποίηση, αφρισµός, σχηµατισµός µεµβράνης έσµευση έσµευση λιπαρών, γευστικών οσµηρών ουσιών οµική Ελαστικότητα, συνεκτικότητα, καταλληλότητα για µάσηση, συνάφεια, δηµιουργία πλέγµατος, συσσωµάτωση, σχηµατισµός ζύµης και ινών, ικανότητα αναδιαµόρφωσης και εκβολής Ρεολογική Ιξώδες, πήξη Ενζυµική Πρόσδοση τρυφερότητας, ωρίµανση Αναµιξιµότητα Συµπληρωµατικότητα Αντιοξειδωτική Παρεµπόδιση ανάπτυξης δυσάρεστης γεύσης - οσµής Επίδραση H 2 O πρωτεΐνης. Επίδραση πρωτεΐνης πρωτεΐνης. Επιφανειακές ιδιότητες. 1. Ικανότητα διαβροχής και διασποράς (wettability and dispersability) παράγοντες: c, ph, T, t, µ, other compounds 2. ιόγκωση (swelling) (swelling µέθοδος: συσκευή Bauman) 3. ιαλυτότητα (solubility) 4. Αλληλεπιδράσεις σε ξηρή κατάσταση µε H 2 O (ισόθερµος ρόφησης) (protein water interactions in the dry state) 5. Ιξώδες και πάχυνση (viscosity and thickening) (ιξωδοµετρία) Ψευδοπλασικά, θιξοτροπικά 6. Απορρόφηση νερού και λιπαρών (water and fat absorption) (φυγοκέντρηση) 7. Συνάφεια και συνεκτικότητα (adhesion and cohesion) 8. Ζελοποίηση και πήξη (gelation and coagulation) σχηµατισµός τακτικού «δικτύου». Τ, Τ, οξίνιση, ιόντα. 27
34 9. Γαλακτωµατοποιητικές ιδιότητες (emulsifying properties) 10. Αφριστικές ιδιότητες (foaming properties) 11. έσµευση γευστικών/αρωµατικών ουσιών (flavor binding) 12. Ικανότητα δηµιουργίας φιλµ (film formation) 13. Αναδιαµόρφωση (texturization) Α. ΖΕΛΟΠΟΙΗΣΗ (ΣΧΗΜΑΤΙΣΜΟΣ ΠΗΓΜΑΤΟΣ) Ο σχηµατισµός πήγµατος είναι ένα πολύ σηµαντικό φαινόµενο στη χηµεία τροφίµων. Τα χαρακτηριστικά των ζωντανών κυττάρων αλλά και πολλές ιδιότητες των τροφίµων, όπως και η συµπεριφορά τους κατά το µαγείρεµα, εξαρτώνται από τη δοµή του υπάρχοντος πήγµατος. Οι πρωτεΐνες έχουν την ικανότητα να συγκρατούν µε ενυδάτωση περίπου 1 g νερό ανά 5 g ξηρής πρωτεΐνης. Μερικές όµως πρωτεΐνες µπορούν να σχηµατίζουν πήγµατα, στα οποία «ακινητοποιούν» νερό σε ποσότητα περίπου δεκαπλάσια του µικτού βάρους της ενυδατωµένης πρωτεΐνης. Στο σχηµατιζόµενο πήγµα, αυτό το ακινητοποιηµένο νερό έχει χαλαρή σύνδεση µε τις πρωτεΐνες και είναι µάλλον φυσικά παγιδευµένο, για το λόγο δε αυτό µπορεί να αποβληθεί από το πήγµα πολύ ευκολότερα από ότι αποµακρύνεται το νερό ενυδατώσης. Η ακινητοποίηση συνίσταται στο ότι το νερό δεν ρέει ελεύθερα από το πήγµα, αν και φυσικά τα µόριά του κινούνται ελεύθερα µέσα σε αυτό. Προϋπόθεση για το σχηµατισµό πήγµατος: Μετουσίωση και ξετύλιγµα αλύσου. Κατόπιν σχµατισµός δικτύου, αποτέλεσµα ισορροπίας των Π-Η 2 Ο και Π-Π αλληλεπιδράσεων. δηλ. ελκτικών και απωστικών δυνάµεων µεταξύ αλύσων. Ελκτικές δυνάµεις: υδρόφοβες, ηλεκτροστατικές (γέφυρες Ca 2+ ), δεσµοί Η 2, δεσµοί S-S Απωστικές δυνάµεις: ηλεκτροστατικές Π - Η 2 Ο Παράµετροι: συγκέντρωση πρωτεΐνης, MW, ph ΙΑ ΙΚΑΣΙΑ ΣΧΗΜΑΤΙΣΜΟΥ ΠΗΓΜΑΤΟΣ Θέρµανση ψύξη (ζελατίνη) Ελαφρά οξίνιση και Ca 2+ ενισχύει τα πήγµατα (π. σόγιας, ορού γάλακτος) Επίσης ορισµένα πήγµατα σχηµατίζονται µε ενζυµική υδρόλυση (µικύλια καζεΐνης, λευκό αυγού). Έχουµε δύο τύπους πρωτεΐνικών πηγµάτων: 1. Αντιστρεπτά πήγµατα (βασίζονται σε δεσµούς Η 2 π.χ. ζελατίνη) 2. Αναντίστρεπτα πήγµατα (δεσµοί S-S π.χ. ωοαλβουµίνη, β-γαλακτογλοβουλίνη) Οι πρωτείνες που σχηµατίζουν εύκολα πήγµατα, έχουν δοµές µε µεγάλο βαθµό ασυµµετρίας. Οι επιµήκεις πρωτεϊνικές ίνες σχηµατίζουν ένα τρισδιάστατο πλέγµα κυρίως µε διαµοριακούς δεσµούς υδρογόνου και η προκύπτουσα δοµή είναι ικανή να συγκρατεί το νερό σε µη ρέουσα κατάσταση. Στα πήγµατα έχουµε µεγάλη κατακράτηση φυσικά εγκλωβισµένου Η 2 Ο (10g Η 2 Ο ως 50g Η 2 Ο/g πρωτεΐνης). Η συγκράτηση του νερού υποβοηθείται και από ιοντισµένα τµήµατα των πρωτεϊνικών µορίων, επηρεάζεται δε από το pη και τη θερµοκρασία. Με αύξηση των ελκτικών δυνάµεων µεταξύ των πρωτεϊνικών µορίων όπως π.χ. µε µεταβολή του pη σε τιµή πλησιέστερη προς το ισοηλεκτρικό σηµείο, το πήγµα συστέλλεται αποβάλλοντας µέρος του συγκρατούµενου νερού. Το φαινόµενο αυτό ονοµάζεται συναίρεση, σε πολλά δε πήγµατα παρουσιάζεται και µε την πάροδο του χρόνου. 28
35 Σχήµα Μικρογράφηµα από ηλεκτρονικό µικροσκόπιο (SEM) πήγµατος tofu από πρωτεΐνη σόγιας Β. ΓΑΛΑΚΤΩΜΑΤΟΠΟΙΗΣΗ Σχήµα Σχηµατική απεικόνιση της διαµόρφωσης της επιφάνειας µιας πρωτεΐνης στη διεπιφάνεια του γαλακτώµατος 29
36 Γαλακτοµατοποιητική ικανότητα (Emulsion capacity, EC) 0,65<Φ<0,85 (ποσοστό διεσπαρµένης φάσης) Σταθερότητα γαλακτώµατος (Emulsion stability, ES) ES = Vf x 100 / Vi max ES για 0,77<Φ<0,88 Εκτός της γαλακτωµατοποιητικής ικανότητας της πρωτεΐνης, άλλες παράµετροι που επηρεάζουν το γαλάκτωµα: ενέργεια, ρυθµός προσθήκης λαδιού, Φ, Τ, ph, µ, παρουσία σακχάρων, παρουσία surfactants χαµηλού MW, τύπος λαδιού, C διαλύτης πρωτεΐνης. Καλοί γαλακτωµατοποιητές = εύκαµπτες πρωτεΐνες ικανές να «ξετυλιχτούν» και να σχηµατίσουν υδρόφοβους δεσµούς στην επιφάνεια των σταγονιδίων λίπους. Σφαιρικές πρωτεΐνες, όχι καλές. (ωοαλβουµίνη, πρωτ. ορού) Καζεϊνικά, ψηλό EC: S, φυσικά «ξετυλιγµένη» δοµή, υδρόφοβα τµήµατα. Επίσης: ακτοµυοσίνη, υπερσυµπυκνώµατα σόγιας, πλάσµατος. Σχήµα Ηλεκτρονικό µικρογράφηµα γαλακτώµατος µαγιονέζας. Στη διεπιφάνεια νερού σταγονιδίων λαδιού φαίνεται η συγκεντρωµένη πρωτεΐνη. 30
37 Γ. ΙΚΑΝΟΤΗΤΑ ΑΦΡΙΣΜΟΥ (FOAMING) ΑΦΡΟΣ = ιασπορά φυσσαλίδων αέρα σε συνεχή υγρή ή ηµιστερεή φάση περιέχουσα διαλυτή επιφ. ενεργή ουσία (surfactant) π.χ. παγωτά, µαρέγκες, mousse, αφρός µπύρας, σουφλέ, κέικ και ψωµί. Καλοί αφροποιητές: χαµηλή επιφανειακή τάση, ψηλό ιξώδες συνεχούς φάσης, ισχυρά, ελαστικά προσροφηµένα φιλµ. Πρωτεΐνες λευκώµατος αυγού, αλβουµίνη πλάσµατος, ζελατίνη, πρωτεΐνες ορού γάλακτος, µικύλια καζεΐνης, πρωτεΐνες σόγιας.. ΙΚΑΝΟΤΗΤΑ ΣΧΗΜΑΤΙΣΜΟΥ ΖΥΜΗΣ Οι πρωτεΐνες γλουτένης δηµιουργούν ισχυρά συνεκτική και βισκοελαστική «πάστα» (ζύµη) κατά την ανάµειξη και µηχανική ζύµωση, παρουσία νερού και σε θερµοκρασία περιβάλλοντος. ίκτυο που «συγκρατεί» τα υπόλοιπα στοιχεία του αλεύρου. Γλοιαδίνη (gli) + Γλουτένη (glut) λόγω των παρακάτω χαρακτηριστικών: υψηλό ΜW και µικρός αριθµός πολικών αµινοξέων µικρή διαλυτότητα σε ουδέτερο ph Μεγάλο ποσοστό Γλουταµίνης (33%), και αµινοξέων µε -ΟΗ (Ser, Thr, Tyr) µεγάλος αριθµός δεσµών -OH Μεγάλος αριθµός µη πολικών, υδρόφοβων αµινοξέων συντελεί σε τάση για πρωτεϊνικούς (Π-Π) δεσµούς και δεσµούς µε λιπαρά Ιδιαίτερα µεγάλη ικανότητα σχηµατισµού S-S Για να έχουµε βέλτιστη αρτοποιητική ικανότητα πρέπει να έχει το άλευρο τη σωστή αναλογία γλοιαδίνης-γλουτένης: Glut ελαστικότητα, συνοχή Gli εκτατικότητα, ρευστότητα 31
38 1.7 ΧΡΗΣΙΜΟΤΗΤΑ ΛΕΙΤΟΥΡΓΙΑ ΠΡΩΤΕΙΝΩΝ ΩΣ ΠΡΟΣΤΙΘΕΜΕΝΟ ΣΥΣΤΑΤΙΚΟ Πίνακας Χρησιµότητα λειτουργία πρωτεϊνών ως προστιθέµενο συστατικό ΛΕΙΤΟΥΡΓΙΑ ΕΦΑΡΜΟΓΗ ΤΥΠΟΣ ΠΡΩΤΕΙΝΗΣ ΘΡΕΠΤΙΚΟΤΗΤΑ Παιδικές τροφές, Πρωτεΐνες σόγιας, γάλακτος εµπλουτισµένα µε πρωτεΐνη τρόφιµα ΙΑΛΥΤΟΤΗΤΑ Υγρά τρόφιµα, αναψυκτικά Πρωτεΐνες ορού, σόγιας ΙΞΩ ΕΣ Σούπες, σάλτσες, dressing, Καζεϊνικά, ορού, σόγιας, κ.α. γιαούρτια ΚΑΤΑΚΡΑΤΗΣΗ ΝΕΡΟΥ Προϊόντα κρέατος και ιχθυηρών, αρτοσκευάσµατα, γιαούρτι Πρωτεΐνες κρέατος, αυγού, γάλακτος, σόγιας ΖΕΛΟΠΟΙΗΣΗ ΣΥΝΑΦΕΙΑ / ΣΥΝΕΚΤΙΚΟΤΗΤΑ ΓΑΛΑΚΤΩΜΑΤΟΠΟΙΗΣΗ ΑΦΡΙΣΜΟΣ/ΦΙΛΜ Προϊόντα κρέατος, αρτοσκευάσµατα, γαλακτοκοµικά, ζελέδες Κρέατα, αλλαντικά, ζυµαρικά, αρτοσκευάσµατα Αλλαντικά, dressings, µαγιονέζα, σάλτσες, αρτοσκευάσµατα Ζαχαρωτά, αρτοσκευάσµατα, mousse, παγωτά Ζελατίνη, αυγού, σόγιας, γάλακτος κρέατος, γάλακτος, αυγού, σόγιας κρέατος, γάλακτος, αυγού, σόγιας αυγού, γάλακτος και σόγιας 32
39 1.8 ΠΡΩΤΕΙΝΕΣ ΙΑΦΟΡΩΝ ΤΡΟΦΙΜΩΝ Κατά τη µελέτη των πρωτεϊνών των τροφίµων πρέπει να λαµβάνεται υπόψη, πως αυτές οι βασικές για τη διατροφή µας ουσίες είναι συγχρόνως απαραίτητες στα φυτά και τα ζώα για την ανάπτυξη και την επιβίωσή τους. Πολλές πρωτεΐνες πρέπει να θεωρούνται ως πρώτες ύλες που χρειάζονται κάποια επεξεργασία ή τροποποίηση πριν χρησιµοποιηθούν από τον άνθρωπο. Πρωτεΐνες ζωϊκής προελεύσεως Κρέας. Αποτελείται από τους σκελετικούς µύες των ζώων, που χρησιµοποιούνται ως τρόφιµα. Το κρέας της αγελάδας, του αρνιού και του χοίρου χαρακτηρίζονται σαν «κόκκινα κρέατα» σε αντιδιαστολή προς το χρώµα του κρέατος των πουλερικών. Ένας τυπικός µυϊκός ιστός απαλλαγµένος από όλο το εξωτερικό λίπος, περιέχει 18-20% πρωτείνη επί υγρής βάσεως. Γάλα. Το γάλα αγελάδας περιέχει 3-4% πρωτεΐνη, που παραδοσιακά χωρίζεται σε δύο είδη: την καζεΐνη που αποτελεί το 80% και την πρωτεΐνη του ορού που αποτελεί το υπόλοιπο. Η καζεΐνη είναι µία φωσφοροπρωτεΐνη, που µπορεί να διαχωρισθεί από το απουβουτυρωµένο γάλα µε οξίνιση σε τιµή pη 4,6. Αυγά. Τα αυγά της όρνιθας αποτελούνται από 11% φλοιό, 31% κρόκο και 58% λευκό. Έτσι στο ρευστό τµήµα του αυγού ο κρόκος αποτελεί το 35% και το λευκό το 65%. Η κύρια λειτουργία των πρωτεϊνών του αυγού είναι η διατροφή του εµβρύου και φαίνεται ότι πρώτα χρησιµοποιείται ο κρόκoς, ενώ το λευκό τµήµα δρα αρχικά ως µέσο προστασίας πριν καταναλωθεί και αυτό ως πρωτεΐνη. Στις πρωτεΐνες του λευκού του αυγού υπάγονται η ωοαλµπουµίνη που είναι µία φωσφοροπρωτεΐνη µε µοριακό βάρος περίπου , η κοναλ-. µπουµίνη, το ωοµυκοειδές που δρα ως αντιένζυµο της τρυψίνης, οι γλοβουλίνες ανάµεσα στις οποίες η µε αντιβιοτική δράση λυσοζύµη, η ωοµυκίνη µε µοριακό βάρος Στις πρωτείνες του κρόκου του αυγού υπάγονται δύο λιποπρωτεΐνες, η βιτελλίνη και η λιποβιτελλενίνη και οι υδατoδ~αλυτές λιβετίνες. Ψάρια. Τα ψάρια περιέχουν 40-60% εδώδιµη σάρκα, η περιεκτικότητα της οποίας για τα περισσότερο κοινά είδη κυµαίνεται µεταξύ 10-20%. Οι πρωτεΐνες των ψαριών έχουν πολλές οµοιότητες µε τις πρωτεΐνες των σκελετικών µυών των θηλαστικών, αλλά δεν είναι τόσο σταθερές όσο αυτές και µε τις διάφορες κατεργασίες υπόκεινται εύκολα σε αλλοιώσεις (διάσπαση, µετουσίωση, πήξη). Πρωτεΐνες φυτικής προελεύσεως - Φρούτα λαχανικά 1-2% - ηµητριακά 10-15% ΣΙΤΟΣ: Το 80% των πρωτεϊνών αποτελεί η ΓΛΟΥΤΕΝΗ : Γλοιαδίνη/Γλουτενίνη 1/1 Υστερεί σε λυσίνη. Καθορίζει την αρτοποιητική ικανότητα του αλευριού. Πλούσια σε Gln, Pro. Αποτελείται από πολυπεπτιδικές άλυσους Dalton που µε τη µηχανική καταπόνηση κατά το ζύµωµα της ζύµης του ψωµιού συνδέονται µε S-S- και δίνουν δίκτυα µορίων των Dalton. Γλουτενίνη συντελεί στην ελαστικότητα, συνεκτικότητα, αντοχή του ψωµιού Γλοιαδίνη συντελεί στη ρευστότητα, «φούσκωµα», αφράτη υφή του ψωµιού. 33
40 - ΟΣΠΡΙΑ Ελαιούχοι σπόροι 20-40% πρωτεΐνης Αλευρα (50%) Συµπυκνώµατα (70%) Υπερσυµπυκνώµατα (90%) Πρόβληµα: Η περιεκτικότητα σε αντιθρεπτικούς παράγοντες: αναστολείς ενζύµων, αιµατογλουτινίνες, σαπωνίνες Πίνακας Κατά προσέγγιση περιεκτικότητα διαφόρων τροφίµων σε πρωτεΐνη Τρόφιµο Πρωτεΐνη (%) Τρόφιµο Πρωτεΐνη (%) Λαχανικά και φρούτα Ζωικά Πατάτες 2 Τυρός σκληρός 25 Τοµάτες 1 Κρέας (ωµό) Μαρούλι 1 Ψάρι (ωµό) Πορτοκάλια 1 Αυγά 12 Γάλα 3 Οσπρια και ελαιούχοι ηµητριακά σπόροι Μπιζέλια Σίτος Σόγια Βρώµη Φασόλια Κριθή Φυστίκια Σϊκαλη Ηλιόσπορος Ρύζι 7-9 Σησαµόσπορος Καλαµπόκι 9-10 Βαµβακόσπορος ιάφορα Ψωµί 8 Μακαρόνια Νέες πηγές πρωτεϊνών Εξωσυµβατικές Πρωτεΐνες Οι νέες κατευθύνσεις για την αύξηση των διαθέσιµων πηγών πρωτεϊνών είναι: α) η παραγωγή πρωτεΐνης από µονοκύτταρους οργανισµούς κυτταρική πρωτεΐνη (single cell protein) (SCP) και β) η εφαρµογή νέων µεθόδων που επιτρέπουν την καλύτερη αξιοποίηση φυτών πλούσιων σε πρωτεΐνες. Μεγάλες ερευνητικές προσπάθειες γίνονται για την παραλαβή πρωτεϊνών από ελαιούχους σπόρους επειδή αυτοί υπάρχουν σε µεγάλες ποσότητες, έχουν µεγάλη περιεκτικότητα σε πρωτεΐνες και µάλιστα υψηλής θρεπτικής αξίας. η αξιοποίηση των πρωτεϊνών για ανθρώπινη διατροφή των υψηλών σε πρωτεϊνικό περιεχόµενο πρίόντων από πίτες ελαιούχων σπόρων περιορίζεται από την παρουσία φαινολικών ενώσεων και ζυµώσιµων σακχάρων. Ορισµένα από αυτά τα ανεπιθυµητα συσταικά είναι αντιθρεπτικά (αναστολείς τρυψίνης της σόγιας) ή τοξικά (γκοσσυπόλη του βαµβακόσπορου), ενώ άλλα είναι υπεύθυνα για τον άσχηµο χρωµατισµό των 34
41 πρωτεϊνικών προϊόντων (χλωρογενικό οξύ του ηλιόσπορου) ή προκαλούν γαστρεντερικές διαταραχές (ζυµώσιµοι ολιγοσακχαρίτες). Ορισµένοι από τους αντιθρεπτικούς αυτούς παράγοντες µπορούν να καταστραφούν ή να αδρανοποιηθούν µε κατάλληλη θερική κατεργαία, µε προφανείς συνέπειες για τη θρεπτική αξία του προίόντος. Οταν κάτι τέτοιο δεν αίναι δυνατόν, το πρόβληµα χρειάζεται πλέον ειδική αντιµετώπιση π.χ. αποµάκρυνση µε οργανικούς διαλύτες. Για την παραλαβή των πρωτεϊνών από τους σπόρους έχουν αναπτυχθεί διάφορες τεχνικές ανάλογα µε τις οποίες λαµβάνονται πρωτείνικά άλευρα (flours), συµπυκνώµατα (concentrates) και υπερσυµπυκνώµατα (isolates) µε περιεκτικότητα περίπου 50, 70 και 90% πρωτεΐνης εδώδιµης ποιότητας. Οι διάφορες τεχνικές που υπάρχουν µπορούν να ταξινοµηθούν ανάλογα µε το προϊόν που προκύπτει ή τη φύση της κατεργασίας (υγρές τεχνικές, ξηρές τεχνικές). Ως πρωτείνικό άλευρο ορίζεται το λεπτά αλεσµένο προϊόν που παράγεται από αποφλοιωµένο και πλήρως απελαιωµένοσπόρο. ο σπόρος αποφλοιώνεται, υφίσταται ορισµένες προκατεργασίες που διευκολύνουν την εκχύλιση του ελαίου και στη συνέχεια πιέζεται και εκχυλίζεται ή εκχυλίζεται απευθείας µε ένα οργανικό διαλύτη, συνήθως εξάνιο. οι κατεργασίες πραγµατοποιούνται γενικά σε ήπιες συνθήκες (θερµοικρασίας, υγρασίας, πίεσης), ώστε να µην αλλιωθούν οι λειτουργικές ιδιότητες των πρωτεϊνών. Το άλευρο που προκύπτει έχει συνήθως περιεκτικότητα σε πρωτεΐνες µεγαλύτερη από 45%. Για την παραλαβή ενός προίόντος ακόµη πιο πλόυσιου σε πρωτεϊνικό συµπύκνωµα, µπορούν να χρησιµοποιηθούν ξηρές ή υγρές µέθοδοι. Οι ξηρές µέθοδοι χρησιµοποιούν κύρια αέριους κυκλώνες και βασίζονται σε παραµέτρους, όπως το ειδικό βάρος, το µέγεθος ή το σχήµα των άθικτων πρωτείνικών σωµατιδίων. Με τον επιτυγχανόµενο πνευµατικό διαχωρισµό προκύπτουν δύο κλάσµατα: ένα λεπτόκοκκο εµπλουτισµένο σε πρωτεΐνες και ανόργανα συστατικά, συνήθως για ανθρώπινη διατροφή και ένα χονδρόκοκκο µε αυξηµένη περιεκτικότητα σε κυτταρικές µεµβράνες, ολιγοσακχαρίτες και αντιθρεπτικά συστατικά, προοριζόµενο για ζωοτροφές. οι υγρές µέθοδοι βασίζονται στη διαλυτοποίηση και αποµάκρυνση µη πρωτείνικών συστατικών. Οι ολιγοσακχαρίτες και τα ανόργανα άλατα µπορούν να παοµακρυνθούν έως ένα βαθµό µε όξινο διάλυµα, µε υδατικό διάλυµα αλκοόλης ή µε θερµό νερό. Οι περισσότερες πρωτεΐνες των σπόρων παραµένουν αδιάλυτες υπό αυτές τις συνθήκες, όπως είναι επιθυµητό, αλλά η χρήση οξινισµένουνερού στο ισοηλεκτρικό σηµείο της πρωτεΐνης αποτελή την καλύτερη τεχνική (εµποδίζονται όσο το συνατόν η µετουσίωση και η απώλεια λειτουργικών ιδιοτήτων). Το πρωτεϊνικό συµπύκνωµα που προκύπτει περιέχει, µετά από την ξηρανση περίπου 65-75% πρωτεΐνες, αδιάλυτους υδατάνθρακες, 4% ανόργανα άλατα και 0,3-1,2% λιπαρά. Για την παραλαβή πρωτεϊνικών υπερσυµπυκνωµάτων χρησιµοποιείται κύρια η µέθοδος της διαλυτοποίησης καταβύθισης των αζωτούχων συστατικών. Οι πρωτεΐνες εκχυλίζονται συνήθως µε αλκαλικό διάλυµα, και στη συνέχεια καταβυθίζονται στο ισοηλεκτρικό τους σηµείο. η µέθοδος της διαλυτοποίησης καταβύθισης µπορεί να εφαρµοστεί σε άλευρο ή ακόµα σε σµπύκνωµα. Για την αποτελεσµατική ακχύλιση των πρωτεϊνών απαιτείται καταστροφή της κυτταρικής δοµής. Η διάσπαση της κυτταρικής δοµής είναι δυνατόν να γίνει µηχανικά, µε χηµική ή ενζυµική κατεργασία, µε υπέρηχους ή µικροκύµατα, µε κατάψυξη απόψυξη, µε ενυδάτωση κ.λ.π. Από τις παραπάνω µεθόδους προτιµάται η µηχανική καταστροφή των κυτταρικών τοιχωµάτων µε άλεση, γιατί είναι τεχνολογικά παλή και δεν προκαλεί πρωτεϊνική µετουσίωση. Η λεπτότητα της άλεσης του υλικού παίζει ρόλο στην εκχύλιση, συνήθως ικανοποιητικές εκχυλίσεις επιτυγχάνονται µε µέγεθος σωµατιδίων µm. Οι πρωτεΐνες του αλεύρου µπορούν να διαλυτοποιηθούν σε αλκαλικό διάλυµα και έκπλυση του πρωτεϊνικού ιζήµατος, ώστε να αποµακρυνθούν ολιγοσακχαρίτες, άλατα και άλλες διαλυτές ουσίες που συγκαταβυθίζονται µε τις πρωτεΐνες. Η ξήρανση πραγµατοποιείται µε διάφορες τεχνικές υπό κενό, µε ψεκασµό, υπό κατάψυξη. Μετά την ξήρανση παραλαµβάνεται ένα πρωτεϊνικό 35
42 υπερσυµπύκνωµα που περιέχει 90% πρωτεΐνη ή και περισσότερο. Τα πρωτεϊνικά υπερσυµπυκνώµατα είναι ακριβότερα από τα συµπυκνώµατα λόγω των πρόσθετων φυσικών και χηµικών διεργασιών, αλλά και λόγω της επιτυγχανόµενης ανάκτησης των πρωτεϊνών του αρχικού υλικού, η οποία µπορεί να φτάσει το πολύ σε 75%. Η αποµάκρυνση των ανεπιθύµητων συστατικών και η γνώση της καµπύλης διαλυτότητας της πρωτεΐνης είναι οι κυριότερες παράµετροι που πρέπεινα ληφθούν υπόψη προκειµένου να επιτευχθεί υψηλή ανάκτηση και ικανοποιητικός καθαρισµός των πρωτεϊνικών συστατικών. Με τις περισσότερες πίτες ή άλευρα, οι µέθοδοι µε την υγρή κατεργασία αποµακρύνουν ένα µεγάλο µέρος των αντιθρεπτικών ή τοξικών παραγόντων (γκοσσυπόλη, αφλατοξίνες), αλλά αυξάνουν τη συγκέντρωση αντιθρεπτικών παραγόντων πρωτεϊνικής φύσης (αναστολείς τρυψίνης, αιµατογλουτίνες). Η αδρανοποίηση αυτών δε γίνεται σε υγρή κατάσταση µε θέρµανση προς αποφυγή της µεταβολής των λειτουργικών ιδιότητων, αλλά εφαρµόζεται µετά την προσθήκη του συµπυκνώµατος στο τρόφιµο κατά το ψήσιµο. Με την εφαρµογή πρόσθετων επεξεργασιών οι πρωτεΐνες µπορούν να σχηµατοποιηθούν προς προϊόντα µε οργανωµένη ινώδη δοµή. Κατά µία µέθοδο παράγεται ινοποιηµένο πρωτεϊνικό υλικό µε άµεση θερµοπλαστική εκβολή πρωτεϊνικών αλεύρων ή συµπυκνωµάτων κάτω από ελγχόµενες συνθήκες θερµοκρασίας και υγρασίας. Σϋµφωνα µε άλλη µέθοδο οι πρωτεΐνες διαλύονται σε άλκαλι και το διάλυµα συµπιέζεται µέσα από λεπτότατες ίνες. Αυτές οι σχηµατουργηµένες πρωτεΐνες παρέχουν µεγάλη ευελιξία στην παρασκευή τροφίµων. Η παραλαβή αλεύρων και συµπυκνωµάτων είναι σχετικά δυνατή απ όλους σχεδόν τους ελαιούχους σπόρους. Μέχρι σήµερα για οικονοµικούς κυρίως λόγους οι σπόροι της σόγιας αποτελούν τη σπουδαιότερη βιοµηχανική πρώτη ύλη για τέτοια προϊόντα. Αυτά χρησιµοποιούνται για τον εµπλουτισµό διάφορων τροφίµων, για τη µερική αντικατάσταση του κρέατος σε σχετικά προϊόντα και γενικότερα για τις λειτουργικές ιδιότητες που προσδίδουν στα τρόφιµα στα οποία ενσωµατώνονται. 36
43 ΚΕΦΑΛΑΙΟ 1 ΣΤΟΙΧΕΙΑ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ 2. Υ ΑΤΑΝΘΡΑΚΕΣ Οι υδατάνθρακες έχουν ευρεία διάδοση στη φύση, συνιστώντας τα 3/4 του βιολογικού κόσµου. Οι υδατάνθρακες σχηµατίζονται στα φυτά µε τη διαδικασία της φωτοσύνθεσης. Υπό τη µορφή του αµύλου οι υδατάνθρακες αποτελούν το αποταµιευτικό υλικό στα φυτά. Είναι εξαιρετικά σηµαντικοί ως συστατικό των τροφίµων, στα οποία αποτελούν πηγή ενέργειας, παράγοντα γεύσης και στοιχείο δοµής. Το 80% της ενέργειας στην ανθρώπινη δίαιτα προέρχεται από υδατάνθρακες. Ο όρος «υδατάνθρακας» χρησιµοποιήθηκε αρχικά για να δείξει ότι αυτές οι ενώσεις στοιχειακά περιγράφονται από το γενικό τύπο C x (H 2 O) y, πρόκειται δηλαδή για «ενυδατωµένο» άνθρακα, όπου το οξυγόνο και το υδρογόνο περιέχονται στην ίδια όπως και στο νερό αναλογία. Υπάρχουν όµως γνωστοί υδατάνθρακες που δεν ανταποκρίνονται στον τύπο αυτό καθώς ενώσεις του τύπου C x (H 2 O) y που δεν έχουν τα χαρακτηριστικά υδατανθράκων όπως π.χ. το οξικό οξύ (C 2 H 4 Ο 2 ) και το γαλακτικό οξύ (C 3 H 6 Ο 3 ) ΜΟΝΟΣΑΚΧΑΡΙΤΕΣ Οι µονοσακχαρίτες, οι απλούστεροι υδατάνθρακες, που αποτελούν και τη δοµική µονάδα όλων των υπόλοιπων είναι αλειφατικές πολυυδροξυαλδεΰδες (αλδόζες) ή αλειφατικές πολυυδροξυκετόνες (κετόζες): ΗΟ-(CHOH) n -CHO ή ΟΗ-(CHOH) n-1 -CO-CH 2 OH Οι µονοσακχαρίτες ταξινοµούνται σύµφωνα µε τον αριθµό των ατόµων του άνθρακα στο µόριό τους. Έτσι έχουµε τριόζες, τετρόζες, πεντόζες, εξόζες, από τις οποίες οι περισσότερο ενδιαφέρουσες τη χηµεία των τροφίµων είναι ορισµένες εξόζες (γλυκόζη, φρουκτόζη, γαλακτόζη, µανόζη) και πεντόζες (αραβινόζη, ξυλόζη). Η αρίθµηση των ατόµων του άνθρακα στο µόριό τους αρχίζει από το πλησιέστερο προς την ανάγουσα οµάδα ακραίο άτοµο άνθρακα. Τα απλούστερα σάκχαρα είναι οι τριόζες, και είναι η γλυκεριναλδεύδη από τις αλδόζες και η διϋδροξυακετόνη από τις κετόζες. Η ύπαρξη στα µόρια των σακχάρων ασύµµετρων ατόµων άνθρακα έχει ως συνέπεια την εµφάνιση στερεοϊσοµερών µορφών και στροφική ικανότητα του επιπέδου του πολωµένου φωτός. Μία ένωση που είναι δεξιόστροφη αναφέρεται µε το σύµβολο (+) ή (d) ενώ µία ένωση που είναι αριστερόστροφη αναφέρεται µε το σύµβολο (-) ή (l). Τα κεφαλαία γράµµατα D και L αποτελούν ένδειξη εναντιοµέρειας που χρησιµοποιείται στα σάκχαρα και άλλα οργανικά µόρια µε βιολογική σηµασία όπως τα αµινοξέα και δεν χαρακτηρίζουν στροφική ικανότητα. Η γλυκεριναλδεϋδη που λαµβάνεται ως ουσία αναφοράς έχει ένα ασύµµετρο άτοµο άνθρακα (τό C2) και κατά συνέπεια έχει δύο ισοµερή που αναγράφονται µε τα σύµβολα D και L. Με βάση τη γλυκεριναλδεϋδη τα φυσικά σάκχαρα έχουν διαµόρφωση D (βλ. Πίνακα 2.1). Η διεύθυνση στροφής του επιπέδου του πολωµένου φωτός είναι ανεξάρτητη από το αν το σάκχαρο ανήκει στην D ή στην L σειρά. Για παράδειγµα αναφέρεται η D-φρουκτόζη που είναι αριστερόστροφη (D (-) φρουκτόζη). Η διεύθυνση και το µέγεθος της στροφής έχουν σηµαντική σηµασία, τόσο 37
44 για την αναγνώριση, όσο και για τον ποσοτικό προσδιορισµό των σακχάρων. Μετράται η ειδική στροφική ικανότητα [α] D 20 σε θερµοκρασία 20 C και µονοχρωµατικό φως της γραµµής D του νατρίου δηλ. η γωνία στροφής που προκαλείται µετά από διαδροµή της φωτεινής δέσµης 10cm µέσα από σακχαροδιάλυµα περιεκτικότητας 1g/ml. Πίνακας 2.1 Σειρά των D- αλδοζών ΑΛ ΟΖΕΣ Είναι γνωστό ότι το καρβονύλιο των αλδεϋδών και των κετονών αντιδρά µε ένα ή δύο µόρια µε υδροξύλια για την παραγωγή ηµιακετάλης ή κετάλης αντίστοιχα. Τέτοιος ηµιακεταλικός δεσµός δηµιουργείται ενδοµοριακά µεταξύ του καρβονυλίου (στη θέση 1 στις αλδόζες, στη θέση 2 στις κετόζες) και του υδροξυλίου στη θέση ν-1 (π.χ. θέση 5 στις εξόζες) των µονοσακχαριτών. Έτσι ο πραγµατικός συντακτικός τύπος είναι κυκλοηµιακεταλικής µορφής και όχι η ανοικτή αλυσίδα. Με την παραδοχή της ηµιακεταλικής µορφής το άτοµο του άνθρακα C1, προκειµένου για τις αλδόζες, και το C2, προκειµένου για τις κετόζες, γίνεται ασύµµετρο και έτσι παρουσιάζονται δυο ισοµερείς µορφές. Στην περίπτωση της γλυκόζης σχηµατίζονται η α-γλυκόζη και η β- γλυκόζη, οι οποίες είναι κατοπτρικά ισοµερή ως προς το άτοµο C1 ενώ κατά το υπόλοιπο µόριο είναι επιθέσιµες. Οι µορφές αυτές της D-γλυκόζης µπορούν να αποµονωθούν: η µεν α-dγλυκόζη κρυσταλλώνεται από υδατικό της διάλυµα και σε πρόσφατο υδατικό της διάλυµα έχει ειδική στροφή[α]: + 112,2 που τείνει βαθµιαία να πάρει την τιµή +52,5 η δε β-d-γλυκόζη κρυσταλλώνεται από διάλυµά της σε πυριδίνη και σε πρόσφατο υδατικό της διάλυµα έχει ειδική στροφή [α]: + 18,7 που και αυτή τείνει σταδιακά να πάρει την τιµή + 52,5. Η παρουσία των δύο αυτών µορφών της γλυκόζης εξηγεί τον πολυστροφισµό των υδατικών της διαλυµάτων, γιατί κατά την παραµονή του σακχαρούχου διαλύµατος η µία µορφή µεταπίπτει στην άλλη και τελικά αποκαθίσταται ισορρoπία, οπότε η στροφή του πολωµένου φωτός παίρνει τη σταθερή 38
45 τελική της τιµή. Στη γλυκόζη η ισορροπία είναι σε αναλογία περίπου 38% α- και 62% β- ενώ υπάρχει και ένα ελάχιστο ποσοστό 0,0026% σε άκυκλη µορφή που εξηγεί την δυνατότητα των σακχάρων να αντιδρούν ως άκυκλες αλδεύδες ή κετόνες. Γενικά οι κυκλικές ηµιακετάλες των σακχάρων έχουν δακτυλίους µε 5 ή 6 άτοµα, και τα σάκχαρα µε αυτές τις δοµές είναι γνωστά µε τα ονόµατα φουρανόζες και πυρανόζες αντίστοιχα. Από τις δoµές αυτές η µορφή της πυρανόζης µε εξαµελή δακτύλιο είναι η συνήθως απαντώµενη στη φύση λόγω της σταθερότητάς της. Απεικονίζεται συνήθως µε τον τύπο Haworth, αν και στο χώρο ο τύπος διαµόρφωσης ανακλίντρου είναι ο ορθότερος. Οι πενταµελούς δακτυλίου φουρανόζες απαντώνται συχνά σε κετόζες ενωµένες µε άλλα µόρια σακχάρων όπως π.χ. στην περίπτωση της φρουκτόζης στο µόριο της σακχαρόζης. ΠΙΝΑΚΑΣ Οι κυριότεροι υδατάνθρακες που απαντούν στα τρόφιµα Είδος Μονοσακχαρίτες από τους οποίους Πηγές αποτελείται Μονοσακχαρίτες Γλυκόζη Φρουκτόζη Φρούτα, φυτικά µέρη, αίµα, γλεύκος, µέλι κ.λ.π Χυµοί φρούτων, µέλι, αίµα ισακχαρίτες 39
46 (Καλαµοσάκχαρο) Σακχαρόζη D-γλυκόζη, D-φρουκτόζη Σακχαροκάλαµο, τεύτλα, φρούτα, λαχανικά, µέλι. Μαλτόζη D-γλυκόζη Προϊόντα υδρόλυσης αµύλου, µέλι Λακτόζη D-γαλακτόζη, D-γλυκόζη Γάλα, τυρός, γαλακτοκοµικά προϊόντα Ολιγοσακχαρίτες Ραφινόζη, Σταχυόζη D-γαλακτόζη, D-γλυκόζη, D- φρουκτόζη Οσπρια, δηµητριακά, βαµβακόσπορος, σακχαρότευτλα. Πολυσακχαρίτες Αµυλο, δεξτρίνες D-γλυκόζη ηµητριακά, όσπρια, βολβοί, ρίζες Κυτταρίνη D-γλυκόζη Τοιχώµατα κυττάρων φυτών Γλυκογόνο D-γλυκόζη Συκώτι, ζωικοί ιστοί Ηµικυτταρίνες L-αραβινόζη, D-ξυλόζη, L-ραµνόζη, D-γαλακτόζη, D-µανόζη, D- γλυκόζη, D-γλυκουρονικό οξύ, D- Κυτταρικά τοιχώµατα φυτών, δηµητριακά, όσπρια, ξηροί καρποί, αλεύρι γαλακτουρονικό οξύ Πεντοζάνες L-αραβινόζη, D-ξυλόζη όπου και οι ηµικυτταρίνες Πηκτινικές ύλες D-γαλακτουρονικό οξύ, L- Φρούτα, λαχανικά, σακχαρότευτλα. αραβινόζη, D-γαλακτόζη, L- ραµνόζη, L-φουκόζη Ινουλίνη D-φρουκτόζη chicory Κόµµεα ετεροπολυσακχαρίτες Σπόροι, εκκρίµατα φυτών, φύκη, µικροοργανισµοί ΑΝΤΙ ΡΑΣΕΙΣ ΜΟΝΟΣΑΚΧΑΡΙΤΩΝ Οξείδωση των µονοσακχαριτών. Με ήπια οξειδωτικά µέσα (βρωµιούχο νερό, αραιό νιτρικό οξύ) οι αλδόζες µετατρέπονται στα αλδονικά οξέα, ενώ οι κετόζες κάτω από ορισµένες συνθήκες δεν προσβάλλονται. Με εντονώτερα οξειδωτικά µέσα (πυκνό νιτρικό οξύ) οξειδώνονται και οι δύο ακραίες οµάδες του µορίου και σχηµατίζονται τα διβασικά αλδαρικά οξέα. Επιλεκτική οξείδωση στη θέση C6 µπορεί να γίνει µόνον µε ενζυµική κατάλυση µε επακόλουθο σχηµατισµό των σηµαντικών στη φύση ουρονικών οξέων (π.χ. το γαλακτουρονικό οξύ, συστατικό στοιχείο των πηκτινών) Οξείδωση Αλδονικό οξύ (Br 2, a.hno 3 ) Ουρονικό οξύ καταλυτική Αλδαρικό οξύ π. ΗΝΟ 3 COOH COOH COOH COOH Η ανίχνευση και ο ποσοτικός προσδιορισµός των µονοσακχαριτών βασίζεται στις αναγωγικές τους ιδιότητες. Το φελίγγειο υγρό (Fehling) π.χ. που περιέχει άλας του οξειδίου του χαλκού σε αλκαλικό διάλυµα, ανάγεται από τα σάκχαρα αυτά σε υποξείδιο του χαλκού. Για τον ποσοτικό 40
47 προσδιορισµό των σακχάρων χρησιµοποιείται ακόµα και αλκαλικό διάλυµα ιωδίου, το οποίο οξειδώνει µε στοιχειοµετρική αναλογία τις αλδόζες, ενώ δεν προσβάλλει τις κετόζες και τους µη ανάγοντες δισακχαρίτες όπως τη σακχαρόζη. Αναγωγή των µονοσακχαριτών. Οι αλδόζες και οι κετόζες µε αναγωγικά µέσα και κυρίως µε αµάλγαµα νατρίου ανάγονται στο σηµείο της καρβονυλικής οµάδας και παρέχουν πολυσθενείς αλκοόλες, τις αλδιτόλες, όπως οι πεντιτόλες από τις πεντόζες (π.χ ξυλιτόλη) και οι εξιτόλες από τις εξόζες (π.χ. σορβιτόλη), µερικές από τις οποίες έχουν γλυκειά γεύση. Αναγωγή - Αλδιτόλες CH 2 OH CH 2 OH (σορβιτόλη, µαννιτόλη) -Η 2 Ο SPAN, TWEEN εστεροποιηµένοι αιθέρες H D-σορβιτόλη είναι η περισσότερο διαδεδοµένη στη φύση πολυαλκοόλη. Τα φρέσκα φρούτα περιέχουν ως 5-10% σορβιτόλη. Η σορβιτόλη δεν ανάγει το διάλυµα Fehling και δεν ζυµώνεται από τους ζυµοµύκητες. Με καταλυτική αφυδάτωση της σορβιτόλης σχηµατίζονται εσωτερικοί αιθέρες της, των οποίων οι εστέρες µε ανώτερα λιπαρά οξέα, υπό την ονοµασία SPAN και TWEEN χρησιµοποιούνται ως γαλακτωµατοποιητές από τη βιοµηχανία τροφίµων. Η σορβιτόλη όπως η διαλκοόλη γλυκόλη και η τριαλκοόλη γλυκερόλη χαρακτηρίζεται από υγροσκοπικότητα. Για το λόγο αυτό χρησιµοποιείται για τη διατήρηση της νωπότητας και της µαλακότητας προϊόντων ζαχαροπλαστικής. Χρησιµοποιείται από τους διαβητικούς αντί για ζάχαρη, γιατί όπως και µε τη ξυλιτόλη, σε ελεγχόµενα ποσά ο µεταβολισµός της είναι ανεξάρτητος από την ινσουλίνη. Επίδραση οξέων και αλκαλίων. Με επίδραση υδροχλωρικού ή θειικού οξέος σχηµατίζονται δισακχαρίτες και ανώτεροι σακχαρίτες από διαµoριακή απόσπαση νερού, ενώ από ενδοµοριακή αποµάκρυνση νερού από τις πεντόζες και τις εξόζες σχηµατίζονται αντίστοιχα φουρφουράλη και υδροξυµεθυλοφουρφουράλη Η επίδραση αραιών αλκαλίων στα απλά σάκχαρα επιφέρει ισοµερισµούς, χωρίς να προκαλείται καταστροφή του µορίου. Σηµαντική παρουσιάζεται η εµφάνιση ενδιάµεσων ενολικών µορφών, που οδηγεί σε αλλαγή της θέσεως υδροξυλιοµάδας σε άτοµο άνθρακα και αποτελεί µία διαδικασία που ονοµάζεται ενολοποίηση, που ακολουθούµενη από οξίνιση οδηγεί σε επιµερίωση (ισοµερίωση) αλδόζης-κετόζης. οξίνιση γλυκόζη, µαννόζη, φρουκτόζη επιµερίωση εν-διόλη 41
48 Γλυκοζίτες Οι γλυκοζίτες είναι ενώσεις που προκύπτουν από την ένωση αναγόντων απλών σακχάρων µε άλλα διαφορετικής φύσεως σώµατα Στην κυκλική ηµιακεταλική µορφή ενός σακχάρου σχηµατίζεται από την αλδεϋδική ή κετονική οµάδα µια υδροξυλοµάδα, που ονοµάζεται ακεταλικό ή γλυκοζιτικό υδροξύλιο. Η οµάδα αυτή αποτελεί το σηµείο συνδέσεως µε άλλες ενώσεις προς σχηµατισµό των γλυκοζιτών. Το µη σακχαρούχο συστατικό ονοµάζεται άγλυκον. Ανάλογα µε το άγλυκο συστατικό οι γλυκοζίτες διακρίνονται σε Ο-γλυκοζίτες, Ν-γλυκοζίτες και S-γλυκοζίτες. Οι γλυκοζίτες µε όξινη υδρόλυση διασπώνται σε σάκχαρο και άγλυκο τµήµα. Είναι ενώσεις µε ευρύτατη διάδοση στα φυτά. Για παράδειγµα αναφέρεται η φυσική χρωστική ανθοκυανίνη που είναι Ο-γλυκοζίτης και ο S-γλυκοζίτης σινιγρίνη, που µε ενζυµική υδρόλυση δίνει ως άγλυκο το ισοθειοκυανικό αλλύλιο ή σιναπέλαιο µε τη χαρακτηριστική οσµή της µουστάρδας. Ο-γλυκοζίτες (φαινόλες, φλαβόνες, ανθοκυάνες, στερεοειδή, τερπενοειδή) Ν-γλυκοζίτες (νουκλεοτίδια) S-γλυκοζίτες (σινιγρίνη AITC) Κυανογενετικοί γλυκοζίτες (µε υδρόλυση HCN ΑΜΥΓ ΑΛΙΝΗ) 'Οταν στη θέση του άγλυκου υπάρξει ένα άλλο απλό σάκχαρο, τότε το προϊόν της ενώσεως δεν λέγεται πλέον γλυκοζίτης αλλά δισακχαρίτης. Οι ολιγοσακχαρίτες και οι πολυσακχαρίτες είναι και αυτοί γλυκοζίτες ΙΣΑΚΧΑΡΙΤΕΣ Η ένωση µεταξύ δύο µονοσακχαριτών µπορεί να προκύψει κατά δύο τρόπους και έτσι διακρίνουµε δύο διαφόρους τύπους δισακχαριτών 1. ισακχαρίτες του τύπου της τρεχαλόζης ή και σακχαρόζης, όπου οι δύο µονοσακχαρίτες είναι ενωµένοι µε αιθερικό δεσµό των υδροξυλίων της αναγωγικής τους οµάδας. Οι δισακχαρίτες αυτοί δεν είναι ανάγοντες και δεν παρουσιάζουν πολυστροφισµό. 2. ισακχαρίτες του τύπου της µαλτόζης, στους οποίους το ηµιακεταλικό υδροξύλιο του ενός µορίου είναι ενωµένο µε αιθερικό δεσµό µε ένα από τα υπόλοιπα µη ακεταλικά υδροξύλια του άλλου µορίου µονοσακχαρίτη. Στην περίπτωση αυτή η αναγωγική οµάδα του ενός µορίου παραµένει ελεύθερη και ο σχηµατιζόµενος δισακχαρίτης είναι ανάγον σάκχαρο και παρουσιάζει πολυστροφισµό. Στην οµάδα αυτή ανήκουν οι περισσότεροι δισακχαρίτες όπως η µαλτόζη, η κελλοβιόζη και η λακτόζη. ΙΣΑΚΧΑΡΙΤΕΣ ΓΛΥΚΟΖΗΣ Μαλτόζη: α (1 4) γλυκοζιτικός δεσµός 42
49 Ισοµαλτόζη: α (1 6) γλυκοζιτικός δεσµός Κελλοβιόζη: β (1 4) γλυκοζιτικός δεσµός Γεντοβιόζη: β (1 6) γλυκοζιτικός δεσµός Τρεχαλόζη: α,α (1 1) γλυκοζιτικός δεσµός ΑΛΛΟΙ ΣΗΜΑΝΤΙΚΟΙ ΙΣΑΚΧΑΡΙΤΕΣ Σακχαρόζη = Γλυκόζη + Φρουκτόζη : α (1 2) γλυκοζιτικός δεσµός ή β (2 1) φρουκτοζιτικός δεσµός. Είναι ευρύτατα διαδεδοµένη στη φύση ιδιαίτερα στο σακχαροκάλαµο και τα σακχαρότευτλα. Τα καλλιεργούµενα σακχαρότευτλα περιέχουν 16-20% σακχαρόζη. Υδρολυόµενη µε οξύ δίνει µίγµα γλυκόζης και φρουκτόζης, το οποίο λόγω της επικρατήσεως της αριστερής στροφικής ικανότητας της φρουκτόζης είναι αριστερόστροφο, δηλαδή έχει αντίθετη στροφή από τη σακχαρόζη. Η µεταβολή αυτή ονοµάζεται αναστροφή (inversion) και το ισοµοριακό µίγµα των δύο σακχάρων (γλυκόζη και φρουκτόζη) ονοµάζεται ιµβερτοσάκχαρο. Η υδρόλυση της σακχαρόζης γίνεται και µε το ένζυµο ιµβερτάση. Πίνακας 2.2. Σχετική γλυκύτητα σακχάρων σε σύγκριση µε τη σακχαρόζη. ΣΑΚΧΑΡΟ ΣΑΚΧΑΡΟ Σακχαρόζη 100 Γαλακτόζη 63 Φρουκτόζη 115 Λακτόζη 39 Γλυκόζη 65 Σορβιτόλη 54 Μαλτόζη 46 Ξυλιτόλη 100 Λακτόζη = Γαλακτόζη + Γλυκόζη: β (1 4) γαλακτοζιτικός δεσµός Είναι το µοναδικό σάκχαρο του γάλακτος των θηλαστικών. Βιοµηχανικά παρασκευάζεται από τον ορό της τυροκοµίας δηλ. το τυρογάλα, που παραµένει µετά την πήξη του γάλακτος. Η λακτόζη δεν ζυµώνεται από όλα τα είδη ζυµοµυκήτων, αλλά µόνο από ορισµένους µε σχηµατισµό οινοπνεύµατος. Τα γαλακτικά βακτήρια ζυµώνουν τη λακτόζη προς γαλακτικό οξύ. 43
50 2.3. ΠΟΛΥΣΑΚΧΑΡΙΤΕΣ Ανάλογα µε τη χηµική τους σύσταση οι πολυσακχαρίτες διακρίνονται σε οµοπολυσακχαρίτες (άµυλο, κυτταρίνη, γλυκογόνο) όταν το µόριό τους αποτελείται από ένα είδος απλού σακχάρου, και σε ετεροπολυσακχαρίτες (ηµικυτταρίνες, πηκτινικές ύλες, κόµµεα) όταν το µόριό τους αποτελείται από δύο ή περισσότερα συστατικά. Το συστηµατικό τους όνοµα προκύπτει από το όνοµα του µονοσακχαρίτη από τον οποίο προέρχονται µε αντικατάσταση της καταλήξεως -όζη από την κατάληξη -ανη. Π.χ. πεντόζη-πεντοζάνη, µαννόζη-µαννάνη, γλυκόζη-γλυκάνη. Οι πολυσακχαρίτες είναι πολύ διαφορετικοί από τις βασικές δοµικές µονάδες, που τους αποτελούν. Μακροσκοπικά και µικροσκοπικά εµφανίζονται άµορφοι, αλλά εξεταζόµενοι µε ακτίνες Χ αποκαλύπτουν µικροκρυσταλλική δοµή. εν έχουν γλυκειά γεύση και δεν ανάγουν το φελίγγειο υγρό. Με όξινη ή ενζυµική υδρόλυση οι πολυσακχαρίτες διασπώνται στα βασικά δοµικά τους συστατικά ΑΜΥΛΟ (Starch) Το άµυλο είναι γλυκάνη, και αποτελεί το σηµαντικότερο τελικό προϊόν της φωτοσύνθεσης και σε αντίθεση µε την κυτταρίνη, η γλυκόζη που το αποτελεί, µπορεί µε τη βοήθεια των αµυλασών να επανέλθει στο µεταβολισµό του ανθρώπου για κάλυψη ενεργειακών αναγκών ή για σύνθεση άλλων υλικών. Το άµυλο ευρίσκεται υπό µορφή κόκκων (granules) δηλ. «πακέτα» χαρακτηριστικού µεγέθους και σχήµατος. Οι κόκκοι του αµύλου ανάλογα µε την προέλευσή τους διαφέρουν ως προς το µέγεθος και τη µορφή, πράγµα που επιτρέπει τη µικροσκοπική αναγνώριση του αµύλου διαφόρων πρoελεύσεων Η δοµή του κόκκου είναι ψευδοκρυσταλλική, δεν υπάρχει δηλαδή µια σαφής επαναλαµβανόµενη συµµετρία αλλά εµφανίζει περισσότερο τη µορφή ενός θυσάνου από στενά «πλεγµένους» έλικες αµυλόζης και µόρια αµυλοπηκτίνης µε ένα κεντρικό σηµείο έναρξης. Σχήµα 2.1. Κόκκοι αµύλου από διάφορες πηγές. Η Αµυλόζη αποτελεί περίπου το 25% του αµύλου. Είναι άλυσος µορίων γλυκόζης (MW=50, ,000) διαλυτή στο νερό χωρίς διόγκωση. Τα µόρια γλυκόζης είναι ενωµένα µε α(1-4) δεσµούς, σε ευθεία δοµή (διαµόρφωση α έλικα σε διάλυµα). Έχει την ικανότητα φυσικού εγκλεισµού άλλων µορίων π.χ. λιπαρά, ιώδιο (δείκτης αµύλου). 44
51 Σχήµα 2.2. Μόριο αµυλόζης. Η αµυλοπηκτίνη είναι διακλαδωµένη άλυσος, µε πλευρικές αλύσους γλυκοζών και βαθµό πολυµερισµού (DP) = χιλιάδες γλυκόζες (MW = 1-10 εκατοµύρια). Έχει α(1-4) δεσµούς και α(1-6) δεσµούς (διακλαδώσεις). Βρίσκεται κυρίως στο εξωτερικό του κόκκου του αµύλου. ε διαλύεται στο νερό αλλά διογκώνεται και µε θέρµανση δίνει αµυλόκολλα. Σχήµα 2.3. Μόριο αµυλοπηκτίνης. Το άµυλο (αµυλόζη και αµυλοπηκτίνη µαζί) είναι σώµα λευκό, αδιάλυτο στο ψυχρό νερό και στο οινόπνευµα. Στο ζεστό νερό εξ αιτίας της περιεχόµενης αµυλοπηκτίνης το άµυλο διογκώνεται, οι κόκκοι του διαρρηγνύονται και λαµβάνεται ιξώδες υγρό, που κατά την ψύξη γίνεται ζελατινώδες και αποτελεί την κοινή αµυλόκολλα. Η υδρόλυση του αµύλου µπορεί να γίνει µε οξέα ή ενζυµικά. Κατά την ενζυµική υδρόλυση του αµύλου µε διάφορες αµυλάσες (α-αµυλάση, β-αµυλάση, γλυκοαµυλάση) σχηµατίζονται ανάλογα µε την περίπτωση; µαλτόζη, γλυκόζη και οριοδεξτρίνες, που ονοµάζονται έτσι γιατί βρίσκονται στο όριο της υδρολυτικής ικανότητας του χρησιµοποιουµένου ενζύµου. Κατά την υδρόλυση του αµύλου µε οξέα λαµβάνεται. ως τελικό προϊόν σχεδόν ποσοτικά η γλυκόζη, που αποτελεί το απλούστερο δοµικό τµήµα του µορίου του αµύλου. Κατά την όξινη υδρόλυση του αµύλου σχηµατίζονται µερικά ενδιάµεσα προϊόντα µε κοµµιώδη σύσταση και χωρίςκαθορισµένη σύνθεση, που ονοµάζονται δεξτρίνες. Οι δεξτρίνες είναι ένας γενικός όρος για ~ρoϊόντα αποικοδοµήσεως του αµύλου, που αποτελούν ενδιάµεση βαθµίδα, µε ελ,α:ττούµενο µοριακό µέγεθος, ανάµεσα στο άµυλο και τους ολιγοσακχαρίτες. ΟΙ δεξτρίνες είναι διαλυτές στο νερό και αδιάλυτες στο οινόπνευµα. Οι δεξτρίνες δεν έχουν γλυκειά γεύση ούτε ζυµώνονται κατ' ευθείαν από τους ζυµοµύκητες. Με πλήρη υδρόλυση µετατρέπονται τελικά σε γλυκόζη. Κατά την όξινη υδρόλυση του αµύλου λαµβάνεται πρώτα το διαλυτό άµυλο ή αµυλοδεξτρινη, που σχηµατίζει ακόµα µπλέ χρώµα µε ιώδιο. Καθώς προχωρεί η υδρόλυση σχηµατίζονται οι ερυθροδεξτρίνες, που µε ιώδιο δίνουν κόκκινο χρώµα. Στη συνέχεια της υδρόλυσης σχηµατίζονται οι µαλτοδεξτρίνες που δεν δίνουν κανένα χρώµα µε το ιώδιο, κατόmν σχηµατίζεται µαλτόζη και τελικά γλυκόζη. 45
52 Ευρεία χρήση στη βιοµηχανία τροφίµων έχουν τα σιρόπια γλυκόζης που παράγονται από την υδρόλυση αµύλου, κυρίως από καλαµπόκι. Ιδιαίτερο ενδιαφέρον παρουσιάζουν στα σιρόπια υψηλής περιεκτικότητας σε φρουκτόζη (High Fructose Corn Syrup- HFCS) που παράγονται µε περαιτέρω ενζυµική κατεργασία των σιροπιών γλυκόζης µε ισοµεράση φρουκτόζης. Παραγωγή αµύλου Πρώτη ύλη: καλαµπόκι ιαβροχή µε νερό και 0,2% SO 2 στους 15 C για h. Αλεση, αποφλοίωση. Πολτός. Προσθήκη SO 2 και αύξηση της θερµοκρασίας σε C. ιαχωρισµός κόκκων αµύλου µε φυγοκέντρηση, φιλτράρισµα. Ξήρανση. ΖΕΛΑΤΙΝΟΠΟΙΗΣΗ ΑΜΥΛΟΥ (gelatinization): Η τεχνολογική χρησιµότητα του αµύλου στα συστήµατα τροφίµων προκύπτει από την ιδιότητα του να ζελατινοποιείται. ΟΡΙΣΜΟΣ: Ως ζελατινοποποίηση ορίζεται η µη αντιστρεπτή διόγκωση των κόκκων του αµύλου µε νερό κατά την θέρµανση του πάνω από µια κρίσιµη θερµοκρασία. Παρ όλον ότι αναφερόµαστε στην θερµοκρασία ζελατινοποίησης, Τ ζ, στην πραγµατικότητα το φαινόµενο συµβαίνει σε ένα εύρος περίπου 10 C. Κάθε είδος αµύλου χαρακτηρίζεται από την θερµοκρασία ζελατινοποίησης του η οποία µπορεί και να µεταβληθεί µε τις συνθήκες επεξεργασίας και τη σύνθεση του τροφίµου. Θερµοκρασία ζελατινοποίησης Καλαµπόκι C Πατάτα C Σίτος C Ρύζι C Οι παράγοντες που µπορούν να επηρεάσουν το Τ ζ είναι το ph, ο ρυθµός θέρµανσης (dq/dt), και η παρουσία σακχάρων και λιπαρών. Στάδια ζελατινοποίησης: α) Κρύο νερό. Κόκκοι αδιάλυτοι. Απορροφούν νερό αντιστρεπτά (µέχρι 25%) και διογκώνονται ελαφρά (9-20%) β) Με την αύξηση της θερµοκρασίας η δοµή του κόκκου σταδιακά µειώνεται, µέχρι το σηµείο ζελατινοποιήσεως Τ ζ. Στο Τ ζ έχουµε απώλεια «κρυσταλλικότητας», αύξηση ιξώδους, ταχεία διόγκωση, µεγάλη συγκράτηση νερού. ιαλυτά µόρια αµυλόζης διαρρέουν από τον κόκκο. Στο σηµείο αυτό το φαινόµενο της ζελατινοποίησης είναι αναντίστρεπτο. γ) Με συνέχιση της θέρµανσης έχουµε αύξηση διόγκωσης και το διαλυτό άµυλο αυξάνει. Τελικά οι κόκκοι διαρρηγνύονται, το ιξώδες µειώνεται απότοµα και οι κόκκοι «συγκολούνται» αναντίστρεπτα. Στο σηµείο αυτό έχουµε σχηµατισµό πήγµατος (gel). 46
53 Τα πήγµατα του αµύλου διασπώνται εύκολα µε µεγάλες διατµητικές τάσεις και «υγροποιούνται». Το φαινόµενο είναι εν µέρει αντιστρεπτό δηλ. το πήγµα «επανέρχεται». Με παλαίωση προκαλείται έντονη συναίρεση του πήγµατος (gel). Όταν το ζελατινοποιηµένο άµυλο ψυχθεί, µε τον χρόνο γίνεται συσσωµάτωση και καθίζηση: αναδιαµόρφωση (retrogradation). Η αναδιαµόρφωση οφείλεται κυρίως στην αµυλόζη. Στην αναδιαµόρφωση του ζελατινοποιηµένου αµύλου οφείλεται εν µέρει το «µπαγιάτεµα» (staling) του ψωµιού και των αρτοποιηµάτων. ΤΡΟΠΟΠΟΙΗΜΕΝΑ ΑΜΥΛΑ ΟΡΙΣΜΟΣ: Ως τροποποποίηση του αµύλου ορίζουµε την ήπια αποικοδόµιση ή φυσική κατεργασία ή αντίδραση των ΟΗ µε διάφορες ουσίες (οξικό ανυδρίτη, οξικό βινύλιο, φωσφορικά άλατα) µε στόχο τη µεταβολή και βελτίωση των φυσικοχηµικών και λειτουργικών ιδιοτήτων του φυσικού αµύλου. Έχουµε διάφορους τύπους τροποποιηµένων αµύλων. Στη συνέχεια παρουσιάζονται συνοπτικά τα τροποποιηµένα άµυλα και οι ιδιότητες τους. Τροποποιηµένα µε οξύ (Acid modified thin boiling) Παρουσιάζουν µείωση ιξώδους, αύξηση Τ ζ, δυνατότητα διάλυσης υψηλής συγκέντρωσης και δίνουν µε ψύξη ισχυρά gel. Εφαρµογές: τσίχλες, ζαχαρωτά. Εστεροποιηµένα Αιθεροποιηµένα Υδροξυαιθυλιωµένα (hydroexyethylated) Βαθµός υποκατάστασης (DS): 0,05-0,1 (Παραγωγή: άµυλο + οξείδιο αιθυλενίου, 50 C). Παρουσιάζουν µείωση Τ ζ, διόγκωση κόκκων, και δίνουν διαφανή διαλύµατα υψηλού ιξώδους που δεν σχηµατίζουν gel. Εφαρµογή: δηµιουργία πυκνόρευστων τροφίµων (food thickening). Φωσφορικοί µονοεστέρες (DS ~0,25) (Παραγωγή: ξηρό άµυλο + όξινα άλατα όρθο, πυρο ή τρι φωσφορικά, 60 C) Παρουσιάζουν µείωση Τ ζ, αυξηµένο ιξώδες διαφάνεια. Σταθερότητα σε ψύξη απόψυξη. Φωσφορικοί διεστέρες ( cross-linked starch) (Παραγωγή: πολτός αµύλου + 2% τριµεταφωσφορικό για 1h στους 50 C) Εµποδίζουν τη διόγκωση κόκκων. Η δηµιουργία πλέγµατος συνεπάγεται σταθερότητα σε θερµοκρασία, ph, µηχανική ανάδευση. Αυξάνεται το Τ ζ και προκύπτουν µη διαφανή πήγµατα. Εφαρµογές όταν απαιτείται σταθερότητα σε θέρµανση, ψύξη απόψυξη. Οξικοί εστέρες (DS ~0,5) (Παραγωγή: αντίδραση µε οξικό ανυδρίτη, 25 C, ph 7-11) Εµποδίζει το συσχετισµό µορίων αµυλόζης και γραµµικών µερών αµυλοπηκτίνης Παρουσιάζουν µείωση Τ ζ και ανίσταση σε δηµιουργία gel και αναδιαµόρφωση. ίνουν σταθερά και διαφανή ιξώδη διαλύµατα στεθερά σε ψύξη απόψυξη. 47
54 Λευκασµένο άµυλο (bleached starch) (Παραγωγή: αντίδραση µε υποχλωρικά άλατα ήπιος αποπολυµερισµός). Αυξάνει τη λευκότητα για εφαρµογές σαν σκόνη, και όταν χρειάζεται να είναι αποστειρωµένο από σπόρια βακτηρίων όπως π.χ. για προσθήκη σε κονσέρβες. Με υψηλή αµυλόζη (high amylose) ίνουν πολύ ισχυρά, ταχέως σχηµατιζόµενα πήγµατα (gels). Εφαρµογές: καραµέλες, «κουρκούτια» τηγανίσµατος. εξτρινιωµένο (Παράγεται µε υδρόλυση µέχρι διαλυτότητας σε κρύο νερό) ίνουν χαµηλό ιξώδες. Φορέας αφυδατούµενων συστατικών. ΚΥΤΤΑΡΙΝΗ (Cellulose) Αποτελεί ως κύριο συστατικό των κυτταρικών τοιχωµάτων των φυτών, δοµικό συστατικό των φυτικών ιστών µαζί µε ηµικυτταρίνες, πηκτινικές ουσίες και λιγνίνη. Σε καθαρή κατάσταση βρίσκεται στις ίνες του βαµβακιού, ενώ στο ξύλο των κωνοφόρων και των φυλλοβόλων δένδρων που χρησιµοποιούνται για τη βιοµηχανική της παρασκευή, η περιεχόµενη κυτταρίνη είναι 40-60%. Η κυτταρίνη δεν είναι µία θρεπτική ουσία για τον άνθρωπο, που δεν διαθέτει τα κατάλληλα ένζυµα για την πέψη της. Παρά ταύτα η κυτταρίνη είναι χρήσιµη στην ανθρώπινη διατροφή µαζί µε τους άλλους µη µεταβολίσιµους σύνθετους υδατάνθρακες ως διαιτητική ίνα (dietary fiber) συντελώντας στην οµαλή λειτουργία του εντερικού συστήµατος. Όπως και το άµυλο η κυτταρίνη είναι οµοπολυσακχαρίτης και συγκεκριµένα γλυκάνη. Κατά την υδρολυτική διάσπαση της σχηµατίζεται ως ενδιάµεσο προϊόν ο δισακχαρίτης κελλοβιόζη, πράγµα που δείχνει ότι η σύνδεση των µορίων της γλυκόζης που την αποτελούν γίνεται µε β (1 4) δεσµούς. Ο βαθµός πολυµερισµού (DP) ποικίλει (π.χ για βαµβάκι). Η δοµή της κυτταρίνης διευκρινίσθηκε σηµαντικά µε έρευνες µε ακτίνες Χ. Παρουσιάζει δοµή κρυσταλλική από παράλληλη διάταξη των επιµήκων ευθυγράµµων αλυσίδων γλυκάνης διακοπτόµενη από άµορφες περιοχές άτακτης διάταξης των αλυσίδων. Η καθαρή κυτταρίνη είναι άσπρη όµορφη µάζα, αδιάλυτη στο νερό, το οινόπνευµα, τον αιθέρα, τα ψυχρά αραιά αλκάλια και τα αραιά οξέα. ιαλύεται στο αµµωνιακό διάλυµα οξειδίου του χαλκού (αντιδραστήριο Schweitzer). Καθαρή κρυσταλλική κυτταρίνη σε λεπτοδιαµερισµένους κόκκους χρησιµοποιείται ως πηκτικό µέσο στη βιοµηχανία ως «µικροκρυσταλλική κυτταρίνη». 48
55 Αιθέρες ή εστέρες της κυτταρίνης (το ανάλογο των τροποποιηµένων αµύλων) είναι χρήσιµοι σαν πρώτες ύλες στη βιοµηχανία τροφίµων για σταθεροποίηση υφής, αύξηση ιξώδους ή πήξη: Σηµαντικότεροι είναι οι: Μεθυλοκυτταρίνη (Methylcellulose MC) Έχει τη χαρακτηριστική ιδιότητα να δηµιουργεί πήγµατα κατά τη θέρµανση (thermogelation). Καρβοξυµεθυλοκυτταρίνη (Carboxymethylcellulose, CMC) ΓΛΥΚΟΓΟΝΟ Αποθεµατικός CHO σε ήπαρ µύες. Οµοια δοµή µε αµυλοπηκτίνη. >MW και διακλαδώσεις ΗΜΙΚΥΤΤΑΡΙΝΗ Ολοκυτταρίνη = κυτταρίνη + ηµικυτταρίνη (διαλυτή σε άλκαλι) ουδέτερο Α κλάσµα: Ξυλάνη µε α D-(1 4) δεσµούς µε διακλαδώσεις αραβινόζης όξινο Β κλάσµα: Ξυλάνη µε α D-(1 4) δεσµούς µε δ. 4-0-µεθυλο-γλυκουρονικό οξύ ΚΟΜΜΕΑ (GUMS) Τα κόµµεα ή υδροκολλοειδή είναι υδατοδιαλυτοί ετεροπολυσακχαρίτες εκχυλιζόµενοι από φυτά και φύκη ή και µικροοργανισµούς και συντελούντες στην αύξηση του ιξώδους ή στη δηµιουργία gel. Κόµµεα από σπόρους: ΓΑΛΑΚΤΟΜΑΝΝΑΝΕΣ. Κόµµι γκουάρ (guar), χαουπάλευρο (locust bean gum). Γκουάρ (πηγή Cyamopsis tetragonolobus) β-(1 α) µαννοζικοί δεσµοί µε µια οµάδα α (1 6) γαλακτόζη ανά δύο µαννόζες MW= % σε διάλυµα δίνει ιξώδες n=6000cps. 49
56 Με την αύξηση της θερµοκρασίας αυξάνεται η διαλυτότητά του. εν επηρεάζεται από µεταβολές ph, άλατα. Συνεργισµός µε άµυλο, και άλλα κόµµεα. Χρήσεις: για αύξηση ιξώδους «σώµατος», µείωση συναίρεσης. Τυριά, παγωτά, κρέµες, αλλαντικά, σάλτσες. Χαρουπάλευρο (πηγή χαρουπιά: Ceratonia silique). Αλυσίδα µαννάνης µε οµάδες γαλακτόζης όχι οµοιόµορφα κατανεµηµένες (4:1). Μεγάλα τµήµατα µαννάνης χωρίς διακλάδωση. Συνεργισµός µε καραγεννάνες σε σχηµατισµό gel. ιαλύεται µόνο σε ζεστό νερό και δίνει πολύ υψηλά ιξώδη, όπως το γκουάρ, από το οποίο έχει χαµηλότερο κόστος. Εκκρίµατα φυτών: Αραβικό κόµµι, τραγακανθικό κόµµι (tragacanth), κόµµι καράγια. Αραβικό κόµµι (έκκριµα Acacia). Πολύπλοκος ετεροπολυσακχαρίτης µε MW Κορµός (1 3) γαλακτοπυρανόζης µε (1 6) διακλαδώσεις γαλακτόζης, γλυκόζης, ραµνόζης, αραβινόζης. ίνει διαλύµατα µε νευτωνική συµπεριφορά ως 40%. Στα 50% gel παρόµοια µε του αµύλου. Επηρεάζεται από ph. Ασύµβατο µε ζελατίνη, αλγινικά. Χρήση για ιξώδες, σταθεροποίηση γαλακτωµάτων, αποτροπή κρυστάλλωση. ΚΥΡΙΩΣ ως φορέας αφυδατωµένων αρωµατικών α υλών (encapsulated). Εκχυλίσµατα φυκών: Καραγεννάνη, αλγινικά, άγαρ-άγαρ. Καραγεννάνες (πηγή: φύκη Irish moss - Chondrus crispus) Μίγµα πολυµερών ι-, κ-, λ-, µ- και ν- καραγεννάνη. Θειικοί εστέρες β(1 4) γαλακτόζης, 3,6-άνυδρο-β-γαλακτόζης (1 3) Η εµπορική καραγενάνη είναι συνήθως µείγµα 60% κ-καραγεννάνης (που δηµιουργεί πήγµατα :gelling) και 40% λ-καραγεννάνης (που δηµιουργεί ιξώδη ρευστά: non gelling). Με άλατα Κ + η καραγεννάνη δίνει εύθραυστα gel. Συνεργισµός µε χαρουπάλευρο. Με άλατα Na + η καραγεννάνη δίνει υψηλό ιξώδες. ιαλυτότητα εν ψυχρώ. 50
57 ΧΡΗΣΕΙΣ: Σταθεροποίηση γαλακτοκοµικών προϊόντων: Κρέµες, τυριά, παγωτά, γάλατα. Επίσης µε αρτοποιήµατα, κέικ. Συνεργισµοί µε CMC, γκουάρ, χαρουπάλευρο. εν είναι συµβατή µε αλγινικά και πηκτίνη. Σε ph µικρότερο από 5 υφίσταται υδρόλυση. Αλγινικά άλατα (πηγή φαιοφύκη, Macrocystis pyrifera) Γραµµικοί πολυσακχαρίτες αποτελούµενοι από D-µαννουρονικό οξύ (Μ) και L-γουλουρονικό οξύ (Γ). Ο λόγος Μ/Γ καθορίζει τις ιδιότητες του διαλύµατος. Συνήθως έχουµε τµήµατα πολύ- Μ, πολύ-γ συνδεδεµένα µε εναλλασόµενα Μ-Γ. Αλγινικά άλατα Κ, Na.NH 4 και αµινών είναι διαλυτά σε κρύο νερό. Τα άλατα µε δι- και τρισθενή µέταλλα είναι αδιάλυτα. Τα διαλύµατα είναι υψηλού ιξώδους που µειώνεται µε αύξηση της θερµοκρασίας. Σταθερά σε ph ηµιουργούν gel εν ψυχρώ µε την προσθήκη Ca 2+ ή ph<3. χρησιµοποιούνται για σταθεροποίηση επιδορπίων, γαλακτοποιηµένων σαλτσών, σταθεροποίηση αφρού. Κόµµεα από µικροοργανισµούς: Ξανθάνη, κόµµι τζέλλαν. Ξανθάνη (xanthan gum) (Πηγή: Xanthomonas campestris) Η ξανθάνη έχει κορµό κυτταρίνης µε διακλαδώσεις εστεροποιηµένων ολιγοσακχαριτών. Είναι ευδιάλυτη σε κρύο και ζεστό νερό. ίνει πολύ υψηλό ιξώδες (το υψηλότερο από οποιοδήποτε άλλο κόµµι) και δεν επηρεάζεται από τη θερµοκρασία και το ph! Με το γκουάρ παρουσιάζει συνεργισµό και µε το χαρουπάλευρο δίνει θερµοαντιστρεπτό gel. ΧΡΗΣΕΙΣ: Αναψυκτικά, κονσερβοποιηµένα τρόφιµα, κατεψυγµένα τρόφιµα, τρόφιµα σταθεροποιηµένα µε άµυλο για να µειώσει τη συναίρεση, επιδόρπια, γαλακτοποιηµένες σάλτσες. ΠΗΚΤΙΝΕΣ Είναι συστατικά του µεσοκυτταρικού χώρου των φυτικών ιστών. Συνίστανται κυρίως από πολυµερή γαλακτουρονικού οξέος, α-d(1 4) γαλακτουρονικοί δεσµοί, που έχουν υποστεί εστεροποίηση προς µεθυλεστέρες σε διαφορετικό βαθµό (DE: degree of εsterification). Με σειρά µειούµενου DE έχουµε τις: Πρωτοπηκτίνες Πηκτινικά οξέα ΗΜΡ αδ. Σε νερό Πηκτινικά οξέα LMP διαλυτά σε νερό Πηκτικά οξέα (DE=0) Κατά την ωρίµανση των φρούτων δρουν διάφορες πηκτινάσες (Πρωτοπηκτινάση, πηκτινοµεθυλεστεράση, πολυγαλακτουρονάση) που µετατρέπουν τις πρωτοπηκτίνες στις άλλες 51
58 πηκτίνες και τέλος υδρολύουν την πολυγαλακτουρονική άλυσο µε αποτέλεσµα την µεταβολή της δοµής και της υφής: ΧΡΗΣΕΙΣ: Οι πηκτίνες χρησιµοποιούνται για την Παρασκευή ισχυρών gel (µαρµελάδες, πήκτες) Συνθήκες σχηµατισµού gel: Α. DE>50%. Πηκτίνη 0,3% min 1% optimum Απαιτείται ph= και 60-65% ζάχαρη DE= 50-70%: αργός σχηµατισµός πήγµατος - DE>70%: ταχύς Σχηµατισµός κατά την ψύξη. Αναντίστρεπτος µέχρι 100 C. Χρήση: Μαρµελάδες φρούτων. Β. DE<50%. Απαιτείται προσθήκη Ca 2+ ph= χωρίς ζάχαρη (συνήθως προστίθεται 10-20% για πλαστικότητα) Ταχύς σχηµατισµός πήγµατος. Χρήση: Κονσερβοποίηση κύβων τοµάτας, µαρµελάδες diet. 52
59 3.ΛΙΠΙ ΙΑ Με τον όρο λιπίδια περιγράφεται µια ευρεία κατηγορία ενώσεων διαλυτών σε οργανικούς διαλύτες και ελάχιστα διαλυτών σε Η 2 Ο, που µαζί µε τις πρωτεΐνες και τους υδατάνθρακες αποτελούν τα κύρια συστατικά της βιολογικής ύλης. Αντίθετα µε τις πρωτείνες και τους υδατάνθρακες, που απαρτίζονται από βασικές δοµικές µονάδες, τα αµινοξέα και τους µονοσακχαρίτες αντίστοιχα, τα λιπίδια έχουν ετερογενή φύση και είναι δύσκολα στην ταξινόµηση. Ταξινόµηση ΑΠΛΑ ΛΙΠΙ ΙΑ Λιπαρά σώµατα (γλυκερίδια ή ακυλογλυκερόλες) : εστέρες γλυκερόλης µε λιπαρά οξέα. Αποτελούν το 99% των λιπιδίων και αναλόγως αν είναι στερεά ή υγρά ΥΚΣ χαρακτηρίζονται σε λίπη και έλαια. Κηροί: λιπαρά οξέα + αλκοόλες µεγάλου MW ΣΥΝΘΕΤΑ ΛΙΠΙ ΙΑ Φωσφολιπίδια (φωσφατίδια): εστέρες γλυκερόλης µε λιπαρά οξέα + Ρ οξύ + Ν βάσεις (χολίνη, κολαµίνη) Σφιγγολιπίδια (σφιγγοµυελίνες): εστέρες σφιγγοσίνης µε λιπαρά οξέα + Ρ οξύ + χολίνη Γλυκολιπίδια (σερεβροζίδια και γαγγλιοζίδια): εστέρες σφιγγοσίνης µε λιπαρά οξέα + απλό ή σύνθετος υδατάνθρακα (δεν περιέχουν φωσφορικό οξύ). ΤΕΡΠΕΝΟΕΙ Η: Στεροειδή - Λιποδιαλυτές βιταµίνες - Φυτικές χρωστικές Τη χηµεία τροφίµων απασχολούν κυρίως τα λιπαρά σώµατα. ιακρίνονται σε φυτικά λίπη και έλαια (περιέχουν φυτοστερόλες) και σε ζωικά λίπη και έλαια (περιέχουν ζωοστερόλες όπως η χοληστερόλη) Τα λιπαρά χρησιµεύουν ως συµπυκνωµένη πηγή ενέργειας (9 kcal/g), ενώ κάποια λιπαρά οξέα θεωρούνται απαραίτητα και πρέπει να περιέχονται στη δίαιτα σε ένα ελάχιστο ποσό. Τα λιπαρά είναι φορείς των λιποδιαλυτών βιταµινών. 53
60 3.1. ΛΙΠΑΡΑ ΟΞΕΑ Τα λιπαρά σώµατα (γλυκερίδια ή ακυλογλυκερόλες) είναι εστέρες της γλυκερόλης µε λιπαρά οξέα και για το λόγο αυτό οι ιδιότητές τους εξαρτώνται σε µεγάλο βαθµό από τη δοµή και τη διαµόρφωση των περιεχόµενων λιπαρών οξέων. Τα λιπαρά οξέα αναλόγως του αν έχουν ακόρεστους διπλούς δεσµούς ή όχι διακρίνονται σε ακόρεστα και κορεσµένα. Κορεσµένα λιπαρά οξέα Οι ιδιότητές τους προσδιορίζονται από τον αριθµό C. Οσο µικρότερο είναι το µήκος της αλύσου του λιπαρού οξέος, τόσο χαµηλότερο είναι το σηµείο τήξης του Τα κορεσµένα λιπαρά οξέα που µετέχουν στη δοµή των λιπαρών σωµάτων είναι κατά κανόνα ευθείας αλύσου, ενώ τα διακλαδισµένης αλύσου σπάνια απαντώνται. Από πλευράς µεγέθους µορίου απαντώνται οξέα µε άρτιο αριθµό ατόµων άνθρακα από 4 έως 24. Λιπαρά οξέα µε 4-10 άτοµα άνθρακα απαντώνται στη λιπαρή ουσία του γάλακτος, µαζί µε οξέα µε µεγαλύτερο µήκος αλύσου. Λιπαρά οξέα µε περισσότερα από 24 άτοµα άνθρακα σπάνια απαντώνται σε τριγλυκερίδια τροφίµων, ενώ απαντώνται στους κηρούς. Στις περιπτώσεις που λιπαρά οξέα µε περιττό αριθµό ατόµων άνθρακα απαντώνται σε ζωικά ή φυτικά λιπαρά σώµατα η αναλογία τους δεν υπερβαίνει το 1-2%. Τα επικρατέστερα κορεσµένα λιπαρά οξέα είναι το δαφνικό (Cl2), το µυριστικό (Cl4), το παλµιτικό (Cl6) και το στεατικό (C18) Πίνακας 3.1 Κορεσµένα λιπαρά οξέα C Όνοµα Χηµικός τύπος Σ.Τ. ( C) 4 Βουτυρικό οξύ CH 3 (CH 2 ) 2 COOH -5,3 12 αφνικό ή λωρικό οξύ CH 3 (CH 2 ) 10 COOH 44,8 14 Μυριστικό οξύ CH 3 (CH 2 ) 12 COOH 54,4 16 Παλµιτικό οξύ CH 3 (CH 2 ) 14 COOH 62,9 18 Στεατικό οξύ CH 3 (CH 2 ) 16 COOH 70,1 Ακόρεστα λιπαρά οξέα Οι ιδιότητές τους προσδιορίζονται από τον αριθµό C και τα χαρακτηριστικά των διπλών δεσµών - αριθµός διπλών δεσµων (1-6) - θέση - γεωµετρική διαµόρφωση - συζυγία Η αρίθµηση των ατόµων του άνθρακα και των διπλών δεσµών των λιπαρών οξέων γίνεται είτε αρχίζοντας από το άτοµο άνθρακα του καρβοξυλίου ( αρίθµηση), είτε από τη µεθυλική οµάδα στο άκρο του µορίου τους (ω αρίθµηση). Στα λιπαρά σώµατα τα ακόρεστα οξέα αυτά βρίσκονται υπό τη µορφή cis. 54
61 Πίνακας 3.2 Ακόρεστα λιπαρά οξέα C Θέσεις διπλών δεσµών Όνοµα Χηµικός τύπος Αριθµός ιωδίου Σ.Τ. ( C) 18:1 9/ω-9 Ελαϊκό 90 13,4 18:2 9,12/ω-6 Λινελαϊκό :3 9,12,15/ω-3 Λινολενικό :4 5,8,11,14/ω-6 Αραχιδονικό ,5 20:5 5,8,11,14,17 /ω-3 Εικοσιπεντενοϊκό (ΕΡΑ) 22:6 4,7,10,13,16,19/ω-3 Εικοσιδυοεξενοϊκό (DHA) Το ευρύτερα διαδεδοµένο ακόρεστο λιπαρό οξύ είναι το ελαϊκό οξύ, που στη συνήθη θερµοκρασία είναι υγρό. Απαντάται σε όλα τα λιπαρά σώµατα των τροφίµων και είναι το κύριο συστατικό των φυτικών ελαίων. Είναι µονοακόρεστο λιπαρό οξύ και οι σύγχρονες θεωρίες ορθής διατροφής, που βασίζονται τόσο σε επιδηµιολογικές µελέτες όσο και σε κλινικές, συνιστούν την κατανάλωση του τόσο έναντι των κορεσµένων, που θεωρούνται υπέυθυνα για την αύξηση της LDL-χοληστερόλης και της αθηροσκλήρωσης, όσο και των πολυακορέστων, που µπορεί να έχουν µακροχρόνια αρνητικές επιδράσεις λόγω του ότι είναι ευοξείδωτα. Το ελαϊκό οξύ είναι το κύριο λιπαρό οξύ του ελαιολάδου ( περίπου 80%) (βλ. Πίνακα 3.3). Έχουν βρεθεί διάφορα ισοµερή του ελαϊκού οξέος (ισοελαϊκά οξέα), που ταξινοµούνται ανάλογα µε τη θέση του διπλού δεσµού στο µόριό τους, όπως το πετροσελινικό οξύ (C18 cis 6,7) και βαξενικό oξύ (C18 trans 11,12). Κατά την υδρογόνωση των ελαίων το ελαϊκό οξύ υφίσταται µεταβολές στο διπλό δεσµό, η έκταση των οποίων εξαρτάται από το βαθµό της υδρογόνωσης. Οι µεταβολές αυτές αναφέρονται τόσο στη δοµή cis-trans των µορίων, όσο και στη θέση του διπλού δεσµού: Τα σχηµατιζόµενα ισοµερή (ισοµερή θέσεως και στερεοϊσοµερή) τού ελαϊκού οξέος χαρακτηρίζονται ως ισοελαϊκά οξέα. Ειδικώτερα το trans ελαϊκό οξύ ονοµάζεται ελαϊδινικό οξύ και είναι στερεό στη συνήθη θερµοκρασία. Η µετατροπή αυτή του ελαϊκού οξέος (τόσο του ελεύθερου, όσο και του ενωµένου σε γλυκερίδια) γίνεται όχι µόνο κατά την υδρογόνωση των λιπαρών σωµάτων, αλλά επίσης και κατά τη διάρκεια της οξείδωσης και τη διαδικασία του θερµικού πολυµερισµού κατά το τηγάνισµα. Σηµαντική διάδοση έχει και το λινελαϊκό οξύ, που απαντάται σε µεγάλα ποσά σε φυτικά έλαια όπως το αραβοσιτέλαιο, το ηλιέλαιο και το σογιέλαιο. Το πολυακόρεστο λινολενικό βρίσκεται σε σηµαντική αναλογία στα ίδια φυτικά έλαια. Σήµερα ιδιαίτερη µνεία γίνεται στα ω3 λιπαρά οξέα και ιδιαίτερα στα ευρισκόµενα στα ιχθυέλαια, εικοσιπεντενοϊκό (ΕΡΑ) και εικοσιδυοεξενοϊκό (DHA), στα οποία αποδίδουν ευεργετικές επιδράσεις στο κυκλοφορικό. 55
62 Πίνακας 3.3 Αναλογία (%) των λιπαρών οξέων σε φυτικά λίπη και έλαια και ζωικά λίπη Λιπαρά Σογιέ- Ηλιαν- Κραµ- Βαµβα- Αραβο- Σησαµέ- Κακαό- Ελαιό- Φοινικο- Κοκό- Αραχιδέ- Οξέα λαιο θέλαιο βέλαιο κέλαιο σιτέλαιο λαιο λιπος λαδο πυρηνέλαιο λιπος λαιο 8: : : ίχνη : ίχνη 0.6 ίχνη ίχνη :0 - ίχνη ίχνη - ίχνη : ,8 9, : ,5 ίχνη ίχνη :0 0.1 ίχνη ίχνη ίχνη :1 0.1 ίχνη ίχνη : , , : , , : , , : , ,1 0.2 ίχνη : , : : : :0 0.3 ίχνη ίχνη : : :0 - - ίχνη : Λιπαρά Οξέα Χοίρειο λίπος Βόειο λίπος Λίπος προβάτου Λίπος βουτύρου γάλακτος (αγελάδας) 10:0 και µικρότερα : : : : : : : : : : : : : : : :
63 3.2 ΤΡΙΓΛΥΚΕΡΙ ΙΑ Τα λιπαρά σώµατα που βρίσκονται στη φύση είναι εστέρες αποτελούµενοι κυρίως από γλυκερόλη και τρία µόρια λιπαρών οξέων, µε συνέπεια να επικρατούν στη σύστασή τους τα τριγλυκερίδια. ιγλυκερίδια και µονογλυκερίδια, στα οποία µόνο δύο ή µία οµάδες υδροξυλίου της γλυκερόλης είναι εστεροποιηµένες µε λιπαρά οξέα, βρίσκονται σε µικρή αναλογία(0,1-0,4%) στα φυσικά λιπαρά σώµατα. Πάντως µονογλυκερίδια και διγλυκερίδια παρασκευάζονται βιοµηχανικά σε µεγάλα ποσά και χρησιµοποιούνται ευρύτατα στη βιοµηχανία τροφίµων ως γαλακτωµατοποιητές. Σε ένα τριγλυκερίδιο οι τρεις υδροξυλιοµάδες της γλυκερόλης είναι δυνατό να είναι εστεροποιηµένες µε το ίδιο λιπαρό οξύ, οπότε έχουµε τα απλά τριγλυκερίδια, ή µε διάφορα λιπαρά οξέα, οπότε έχουµε τα µικτά τριγλυκερίδια. Στη φύση, σχεδόν όλα τα γλυκερίδια περιέχουν µίγµα λιπαρών οξέων εστεροποιηµένων µε τη γλυκερόλη, δηλαδή είναι µικτά τριγλυκερίδια. Στα µικτά τριγλυκερίδια ο τρόπος σύνδεσης των λιπαρών οξέων στις θέσεις 1, 2, 3 της γλυκερόλης οδηγεί στο σχηµατισµό ισοµερών θέσης. 1. CH 2 O COR 1 2. CHO COR 2 3. CH 2 O COR 3 Η διάταξη των πολλών και διαφορετικών µεταξύ τους φυσικών λιπαρών οξέων στα γλυκερίδια καθορίζει τη χηµική ποικιλία και την φυσική συµπεριφορά των φυσικών λιπαρών σωµάτων. Για την κατανοµή έχουν προταθεί διάφορα στατιστικά µοντέλα µε αυτό της µερικής τυχαίας κατανοµής να εξηγεί καλύτερα τις παρατηρούµενες κατανοµές στα διάφορα λιπαρά σώµατα (Πίνακας 3.4). Θεωρίες κατανοµής των λιπαρών οξέων στα τριγλυκερίδια α) Θεωρία οµοιόµορφης κατανοµής (even distribution) π.χ. αν S 33% ==> µόνο XXX και SXX τριγλυκερίδια, αν 33% S 66% µόνο SXX και SSX τριγλυκερίδια. β) Θεωρία τυχαίας κατανοµής (random distribution) %ΧΥΖ = [mol % X] x [mol%y] x [mol% Z] x 10-4 (n 3 τριγλυκερίδια) γ) Θεωρία µερικής τυχαίας κατανοµής (1,3 -random distribution, 2-random distribution) %ΧΥΖ = [mol % X] at1,3 x [mol%y] at2 x [mol% Z] at1,3 x 10-4 (n 3 τριγλυκερίδια) Παρότι δεν είναι απόλυτα κατανοητή η κατανοµή των λιπαρών οξέων στα ουδέτερα γλυκερίδια, εν τούτοις είναι γνωστό ότι στα περισσότερα έλαια και λίπη η κατανοµή αυτή δεν είναι τυχαία και πιθανώς εξαρτάται από τα ενζυµικά συστήµατα των κυττάρων. 'Ελαια και λίπη από διάφορες πηγές διαφέρουν σηµαντικά µεταξύ τους, σε ότι αφορά τη σχετική θέση των κορεσµένων και ακόρεστων λιπαρών οξέων στα µόρια των τριγλυκεριδίων τους. Στα φυτικά λιπαρά σώµατα τα κορεσµένα λιπαρά οξέα παρουσιάζουν µία προτίµηση προς την 1 θέση σε σχέση προς τη 2 θέση, ενώ στα ζωικά λιπαρά σώµατα µπορεί να παρουσιασθεί το αντίθετο. Κάτω από κατάλληλες συνθήκες θερµοκρασίας, σε άνυδρο περιβάλλον και µε παρουσία καταλύτη, οι ρίζες των λιπαρών οξέων των τριγλυκεριδίων µπορούν να εναλλάσσονται µεταξύ τους, είτε µέσα στο µόριο του τριγλυκεριδίου, είτε µεταξύ διαφορετικών τριγλυκεριδίων. Στην πρώτη περίπτωση έχουµε την ενδοµοριακή µετεστεροποίηση, ενώ στη δεύτερη περίπτωση τη 57
64 διαµοριακή µετεστεροποίηση. Η µετεστεροποίηση µπορεί να είναι µη κατευθυνόµενη ή κατευθυνόµενη. Η µη κατευθυνόµενη µετεστεροποίηση προκαλεί αναδιάταξη των ριζών των λιπαρών οξέων στις τρεις υδροξυλιοµάδες των µορίων της γλυκερίνης, πoυ γίνεται µε στατιστική κατανοµή, πράγµα που επιτρέπει πρόβλεψη της σύστασης του µίγµατος στο σηµείο ισορροπίας. Σε ότι αφορά την ονοµατολογία των τριγλυκεριδίων ισχύουν ορισµένοι γενικοί κανόνες: 1) Το όνοµα των µε µικρότερο µήκος αλύσου λιπαρών οξέων µπαίνει πριν από το όνοµα των λιπαρών οξέων µε µεγαλύτερο µήκος αλύσου, π.χ. παλµιτοδιστεατίνη. 2) Όταν κορεσµένα και ακόρεστα λιπαρά οξέα έχουν το ίδιο µήκος αλύσου, µπαίνει πρώτο το κορεσµένο λιπαρό οξύ, π.χ. παλµιτοστεατοολείνη. 3) Οταν τα ακόρεστα οξέα έχουν το ίδιο µήκος αλύσου, αλλά διάφορο βαθµό ακορεστότητας, µπαίνει πρώτο το περισσότερο κορεσµένο οξύ, π.χ. ελαϊνολινελαϊνολινολενίνη. Πίνακας 3.4 Κατανοµή (%) των λιπαρών οξέων στα τριγλυκερίδια φυτικών λιπών και ελαίων και ζωικών λιπών Καρύδα Πηγήc Γάλα αγελάδος Βούτυρο κακάο Αραβόσιτος Σόγια Ελιά Χοιρινό Πηγή Φυστίκι Βοδινό Θέση Θέση : :0 6: ,3 3 6:0 8: :0 10: :0 12: :0 14: : : : : ,5 0, : : : : , : : ,6 0,8 1 18: :0 20: :1 20: :0 22: :0 24:0 1 0,5 3 58
65 ΠΟΛΥΜΟΡΦΙΣΜΟΣ Τα ρευστά γλυκερίδια όπως επίσης τα µόνο και τα διγλυκερίδια έχουν την ιδιότητα να κρυσταλλώνονται σε διάφορες κρυσταλλικές µορφές. Αυτός ο πολυµορφισµός υπάρχει σε κάθε γλυκερίδιο µε εµφάση των µορφών α, β' και β (εξαγωνικό, ορθοροµβικό, τρικλινές σύστηµα αντίστοιχα). Από τις µορφές αυτές σταθερότερη είναι η β, ενώ οι ασταθείς α και β' µεταβάλλονται σε σταθερή µορφή β µε την πάροδο του χρόνου (24 ώρες ή και περισσότερο σε χαµηλή θερµοκρασία). Με ταχεία ψύξη ρευστών γλυκεριδίων λαµβάνεται η ασταθής µορφή α, ενώ µε βραδεία ψύξη λαµβάνεται η σταθερή β µορφή. Οι διάφορες κρυσταλλικές µορφές έχουν διαφορετικά σηµεία τήξεως, από τα οποία η β µορφή έχει το υψηλότερο και η α µορφή το χαµηλότερο Η διαφοροποίηση στην κρυσταλλική δοµή επηρεάζεται από την καθαρότητα, τη θερµοκρασία, το ρυθµό ψύξης, την παρουσία πυρηνών κρυστάλλωσης, τους διαλύτες, την κατανοµή λιπαρών οξέων και την ακορεστότητα. Για παράδειγµα το βούτυρο κακάο της σοκολάτας µπορεί να κρυσταλλωθεί στις µορφές α-2, β - 2, β-3v. Η τελευταία είναι αυτή που δίνει την επιθυµητή υφή και τη στιλπνότητα της καλής ποιότητας σοκολάτας. Επιτυγχάνεται µε τη σωστή ωρίµανση του τήγµατος της σοκολάτας στους 32 C. Σχήµα 3.1. Κρυσταλλική δοµή ελαϊκού οξέος 59
66 3.3 ΦΥΣΙΚΕΣ ΚΑΙ ΧΗΜΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΛΙΠΑΡΩΝ ΣΩΜΑΤΩΝ Οι φυσικές ιδιότητες των φυσικών ελαίων και λιπών χρησιµεύουν συχνά για το χαρακτηρισµό τους. Συνήθως, µετρώνται περισσότερες από µία ιδιότητες, ώστε ο χαρακτηρισµός να γίνει µε αρκετή βεβαιότητα, γιατί τα φυσικά λιπαρά σώµατα παρουσιάζουν ορισµένες διακυµάνσεις στα γνωρίσµατά τους. Οι φυσικές ιδιότητες παρέχουν χρήσιµα στοιχεία για την εκτίµηση του σταδίου της επεξεργασίας και της καταλληλότητας ενός λιπαρού σώµατος για µία συγκεκριµένη χρήση. Σηµείο τήξεως. Το σηµείο τήξεως ή η περιοχή τήξεως των λιπαρών σωµάτων ποικίλλει από µία σχετικά στενή θερµοκρασιακή περιοχή µε άµεση τήξη τους, όπως στα λιπαρά σώµατα που χρησιµοποιούνται στη ζαχαροπλαστική, µέχρι µία ευρεία θερµοκρασιακή περιοχή, µε σταδιακή τήξη τους, όπως στα µαγειρικά λίπη. Επειδή τα λιπαρά σώµατα είναι µίγµατα διαφόρων τριγλυκεριδίων, το κάθε ένα από τα οποία έχει το δικό του σηµείο τήξεως, είναι φυσικό να παρουσιάζουν µία περιοχή τήξεως, στην οποία το σηµείο στο οποίο τήκεται το τελευταίο ίχνος στερεού αντιστοιχεί συνήθως στη θερµοκρασία τήξεως του µε υψηλότερο σηµείο τήξεως συστατικού. Το γεγονός αυτό εξηγεί γιατί τα στερεά λιπαρά σώµατα είναι πλαστικά σε µία ευρεία θερµοκρασιακή ζώνη. Σε µικροσκοπική εξέταση στερεών λιπαρών σωµάτων, παρατηρείται ότι αποτελούνται από µία µάζα πολύ µικρών κρυστάλλων µέσα σε µία ποσότητα ρευστού λιπαρού σώµατος. Οι κρύσταλλοι έχουν διάταξη που τους επιτρέπει να ολισθαίνουν µεταξύ τους, µε συνέπεια η όλη µάζα να έχει πλαστική δοµή, πράγµα που δεν θα συνέβαινε, αν η λιπαρή ουσία αποτελείτο από ένα µόνο είδος γλυκεριδίου, το οποίο σε κάθε θερµοκρασία θα έπρεπε να είναι στο σύνολό του είτε στερεό, είτε ρευστό. Καθώς το λιπαρό σώµα θερµαίνεται, ελαττώνεται ο αριθµός των κρυστάλλων στη ρευστή µάζα και η ουσία γίνεται πιο µαλακή, όταν δε το ποσοστό του ρευστού υπερβεί ένα κρίσιµο όριο, η λιπαρή ουσία γίνεται ρέουσα. Ειδικό βάρος. Ο προσδιορισµός του ειδικού βάρους πρέπει να γίνεται υπό προσεκτικά ελεγχόµενη θερµοκρασία (στους 25 C για τα ρευστά και στους 40 C ή 60 C για τα δύστηκτα λιπαρά σώµατα), γιατί έστω και µικρές µεταβολές της θερµοκρασίας προκαλούν σηµαντικές µεταβολές στα σώµατα αυτά. Γενικά το ειδικό βάρος αυξάνει µε αύξηση της ακορεστότητας και του µήκους της αλύσου των περιεχόµενων στα τριγλυκερίδια λιπαρών οξέων. είκτης διάθλασης. Ο δείκτης διάθλασης των λιπαρών σωµάτων αυξάνει µε την αύξηση του µήκους της αλύσου των λιπαρών οξέων στα τριγλυκερίδια και µε την αύξηση της ακορεστότητας. Ο αριθµός ιωδίου, που αποτελεί ένα µέτρο του βαθµού της ακορεστότητας, συνδέεται µε τον δείκτη διάθλασης και έτσι η µέτρηση του δείκτη διάθλασης µπορεί να χρησιµοποιηθεί για την παρακολούθηση της υδρογόνωσης των ελαίων. Οι χηµικές ιδιότητες ενός φυσικού λιπαρού σώµατος, καθορίζονται από τα περιεχόµενα λιπαρά οξέα. Η διαµόρφωση των γλυκεριδίων είναι επίσης σηµαντική, όπως και τα επί µέρους συστατικά, το µοριακό µέγεθος και ιδιαίτερα ο βαθµός ακορεστότητας. Υδρολυτική διάσπαση. Στα µόρια των γλυκεριδίων οι εστερικοί δεσµοί είναι θέσεις αντιδράσεως. Η υδρολυτική διάσπαση µπορεί να πραγµατοποιηθεί µε τη βοήθεια νερού, αραιών οξέων, καυστικών αλκαλίων, λιπολυτικών ενζύµων. Η υδρολυτική διάσπαση των γλυκεριδίων µε νερό σε θερµοκρασία C και πίεση at χωρίς παρουσία καταλύτη έχει εφαρµοσθεί σε µεγάλη έκταση. Τόσο τα λαµβανόµενα λιπαρά οξέα, όσο και η γλυκερόλη βρίσκουν εκτεταµένες βιοµηχανικές εφαρµογές. Υδρολυτική διάσπαση γίνεται ακόµα και κατά τη διάρκεια αλλοιώσεως των λιπαρών σωµάτων. Η υδρόλυση και σαπωνοποίηση των λιπαρών σωµάτων χρησιµοποιείται για τον αναλυτικό προσδιορισµό τους. Ο αριθµός σαπωνοποίησης εκφράζει τα mg ΚΟΗ που απαιτούνται για την πλήρη σαπωνοποίηση 1g λιπαρής ουσίας. Ο αριθµός σαπωνοποίησης είναι τόσο µεγαλύτερος, 60
67 όσο µεγαλύτερη είναι η περιεκτικότητα του λιπαρού σώµατος σε λιπαρά οξέα µικρού µοριακού βάρους και γι' αυτό απoτελεί ένα δείκτη του µέσου µοριακού βάρους των λιπαρών οξέων. Αντιδράσεις προσθήκης και διάσπασης. Προκειµένου για λιπαρά σώµατα µε ακόρεστα λιπαρά οξέα, οι θέσεις διπλών δεσµών είναι θέσεις όπου µπορούν να γίνουν αντιδράσεις προσθήκης και διάσπασης. Μερικές από τις αντιδράσεις αυτές, όπως η υδρογόνωση, η αλογόνωση, ο πολυµερισµός µε θέρµανση, η οξείδωση µε προσφύσηση αέρα είναι ελεγχόµενες, ενώ άλλες όπως η αυτοξείδωση είναι ανεπιθύµητες. Η κάτω από καθορισµένες συνθήκες προσθήκη ιωδίου στους διπλούς δεσµοίις των ακόρεστων λιπαρών οξέων των λιπαρών σωµάτων, χρησιµοποιείται για τον αναλυτικό προσδιορισµό τους. Ο αριθµός ιωδίου εκφράζει τα γραµµάρια ιωδίου που προστίθενται στους διπλούς δεσµούς 100 g λιπαρής ουσίας. Εξευγενισµός Το σύνολο των διεργασιών µε τις οποίες ένα ακατέργαστο λίπος ή έλαιο γίνεται εδώδιµο. Καθίζηση και αποκοµµίωση Εξουδετέρωση Αποχρωµατισµός Απόσµηση Αποµαργαρίνωση (winterization) 3.4 ΑΛΛΟΙΩΣΕΙΣ ΛΙΠΑΡΩΝ Κατά την αποθήκευσή τους τα λιπαρά σώµατα παρουσιάζουν ανεπιθύµητες αλλαγές γεύσης και οσµής, που συνολικά χαρακτηρίζονται ως ταγγισµός. Παράγοντες που επηρεάζουν τον ταγγισµό είναι η θερµοκρασία, το Ο 2, η υγρασία, οι καταλύτες, το φως, τα ένζυµα. Μηχανισµοί Ταγγισµού 1. Υδρολυτική διάσπαση C 3 H 5 (OCOR) H 2 O CH 3 H 5 (OH) HOOCR Καταλύεται από οξέα, αλκαλικές ενώσεις (Ca, Mg, Zn) και λιπάσες 2. Αυτοξειδωτικός ταγγισµός Η οξείδωση από το οξυγόνο του αέρα, που είναι µία αυτοκαταλυόµενη αντίδραση, είναι η συνηθέστερη αιτία ταγγισµού. Και στην περίπτωση αυτή η ύπαρξη περίσσειας οξυγόνου, φωτός, υγρασίας και ουσιών µε καταλυτική προοξειδωτική δράση, επιταχύνει την αλλοίωση Η αρχή της οξειδώσεως παρατηρείται πάντοτε στα ακόρεστα λιπαρά οξέα στο σηµείο του διπλού δεσµού. Η πορεία της αυτοξείδωσης ακολουθεί τρεις σαφώς διακρινόµενες µεταξύ τους φάσεις. Κατά την πρώτη η οξείδωση προχωρεί µε βραδύ ρυθµό, ενώ µετά από ένα σηµείο επιταχύνεται κατά πολύ, εξ αιτίας της καταλυτικής δράσης των ουσιών που σχηµατίζονται. 61
68 ΦΑΣΕΙΣ ΑΥΤΟΞΕΙ ΩΣΗΣ k 1 1. ΕΝΑΡΞΗ (Ωρίµανση) Παράγοντας έναρξης ελεύθερη ρίζα (R, ROO ) (ενέργεια, Fe, Cu) ΙΑ ΟΣΗ k 2 R + O 2 ROO k 3 ROO + RH ROOH + R k 4 ΤΕΡΜΑΤΙΣΜΟΣ R + R R-R k 5 ROO + R ROOH k 6 ROO + ROO ROOR + O 2 Αναλόγως του αν ο περιοριστικός παράγοντας είναι η συγκέντρωση (µερική πίεση) του Ο 2 ο ρυθµός εκφράζεται ως ακολούθως: Ρ Ο2 υψηλή: k1 1/2 Ρυθµός = k3( ) [ ROOH ][ RH ] k 6 Ρ Ο2 χαµηλή: k1 1/2 Ρυθµός = k2( ) [ ROOH ][ O2] k 4 Ο ρυθµός οξείδωσης αυξάνεται εκθετικά µε τον αριθµό των συζυγών διπλών δεσµών λόγω σταθεροποίησης των ριζών µε συντονισµό. Για παράδειγµα έχουµε: 62
69 Σταθεροποίηση ελεύθερων ριζών λόγω συζυγίας διπλών δεσµών Σχηµατισµός υδρουπεροξειδίων Λινελαϊκό οξύ Τα υδρουπεροξείδια διασπώνται στη συνέχεια προς ενώσεις στις οποίες οφείλεται η χαρακτηριστική ταγγή γεύση. Για να γίνει αντιληπτός ο οξειδωτικός ταγγισµός αρκεί να υποστεί αλλοίωση ένα µικρό µόνο ποσοστό της λιπαρής ουσίας, γιατί οι κατώτερες λιπαρές αλδεϋδες έχοντας πολύ ισχυρή οσµή γίνονται αντιληπτές και σε πολύ µικρές συγκεντρώσεις. διάσπαση Υδρουπεροξείδια οξείδωση αλδεΰδες, κετόνες, εστέρες, υδρογονάνθρακες, πολυµερή ΜΕΘΟ ΟΙ ΜΕΤΡΗΣΗΣ ΟΞΕΙ ΩΤΙΚΟΥ ΤΑΓΓΙΣΜΟΥ 1. Κατανάλωση Ο 2 2. Αριθµός υπεροξειδίων (ROOH I 2 ). Εκφράζεται σε meq O 2 /kg λίπους. Max Αριθµός ανισιδίνης (ανισιδίνη + 2-αλκενάλες κίτρινο χρώµα). Αριθµός Totox = 2A.Y. + A.A. 4. οκιµή θειοβερβιτουρικού οξέος (αριθµός ΤΒΑ). ΤΒΑ + µηλονική διαλδεϋδη 63
70 5. οκιµή Kreis. Ρεσορκινόλη + 2,3-εποξυπροπανάλη 6. Απορρόφηση στο UV ΑΝΑΣΧΕΣΗ ΟΞΕΙ ΩΣΗΣ ΠΑΡΑΓΟΝΤΕΣ 1. Αποκλεισµός Ο 2 2. Έλεγχος a w και Τα 3. Μείωση ακορεστότητας 4. Αντιοξειδωτικά Τα αντιοξειδωτικά λειτουργούν µε τρεις µηχανισµούς. Κυρίως µέσω δέσµευσης των ελευθέρων ριζών µέσω συµπλοκοποίησης των µεταλλοϊόντων που προκαλούν έναρξη της αυτοξείδωσης. Φαινολικές ουσίες. εσµευτές ελεύθερων ριζών. Τοκοφερόλες. Γαλλικό προπύλιο. Βουτυλιωµένη υδροξυανισόλη (ΒΗΑ), βουτυλιωµένη υδροξυτονόλη (ΒΗΤ), βουτυλιωµένη υδροξυτολουόλη (TBHQ) BHA BHT Συµπλοκοποιητές EDTA, κιτρικό οξύ 64
71 Συνεργιστικά Ασκορβικό οξύ, παλµιτικό ασκορβύλιο (ascorbyl palmitate), κιτρικό οξύ Τέλος πρέπει να αναφερθεί ότι φαινόµενα ταγγισµού εµφανίζονται σε λίπη και έλαια ή τρόφιµα µε λιπαρά και λόγω αναστροφής και ενζυµικής οξείδωσης. Αναστροφή υσάρεστη οσµή οφειλόµενη σε περιορισµένη οξείδωση (λινελαϊκού ή >) προς καρβονυλικές ενώσεις. Σογιέλαιο, ιχθυέλαια. Ενζυµική οξείδωση Οι λιποξυγενάσες, που έχουν αποµονωθεί από σπόρους φυτών, είναι ένζυµα που καταλύουν την άµεση οξείδωση προς υδροϋπεροξείδια, λιπαρών σωµάτων που περιέχουν τµήµατα cis-cis 1-4 πενταδιενίου. Αυτό σηµαίνει ότι προσβάλλουν πολυακόρεστα λιπαρά οξέα και όχι το ελαϊκό οξύ ή τα κορεσµένα λιπαρά οξέα. Οι λιποξυγενάσες είναι δραστικές και σε χαµηλές θερµοκρασίες, και έτσι αποτελούν ένα πρόβληµα στη συντήρηση κατεψυγµένων τροφίµων που περιέχουν λιπαρά σώµατα. ΒΙΒΛΙΟΓΡΑΦΙΑ Food Chemistry / ed. O. Fenemma Marcel Dekker Inc., 1996 Introduction to Food Chemistry / Richard Owusu-Apenten, 2005 Food lipids : chemistry, nutrition, and biotechnology / edited by Casimir C. Akoh, David B. Min., 2002 Food Chemistry / H.-D. Belitz, W. Grosch, translation from the 4th German edition by M. M., 1999 Analytical chemistry of foods / C.S. James, 1999 Food : the chemistry of its components / T. P. Coultate, 1996 Biochemistry of food proteins / edited by B. J. F. Hudson, 1992 Επιστήµη και Τεχνική των Τροφίµων / Χ.. Θωµόπουλος, Εκδόσεις ΕΜΠ, 1986 Χηµεία Τροφίµων/. Μπόσκου, Εκδόσεις Γαργατάνη, Θεσ/νικη,
72 ΚΕΦΑΛΑΙΟ 2 ΚΙΝΗΤΙΚΗ ΑΛΛΟΙΩΣΗΣ ΚΑΙ ΕΛΕΓΧΟΣ ΔΙΑΤΗΡΗΣΙΜΟΤΗΤΑΣ ΤΩΝ ΤΡΟΦΙΜΩΝ Με την ολοκλήρωση της επισκόπησης της χημείας τροφίμων έχει γίνει σαφές ότι το τρόφιμο είναι ένα πολύπλοκο, φυσικοχημικά και βιολογικά ενεργό σύστημα. Τα βασικά συστατικά του τροφίμου, δηλαδή οι πρωτεΐνες, οι υδατάνθρακες και τα λιπαρά, συμμετέχουν σε πολλές αντιδράσεις που έχουν σαν τελικό αποτέλεσμα την αλλοίωση των οργανοληπτικών χαρακτηριστικών, της θρεπτικής αξίας και της ασφάλειας του τροφίμου. Ενδεικτικά μόνον δινονται στο σχήμα 2.1 οι διαφορετικοί δρόμοι αντίδρασης των βασικών αυτών συστατικών. Η ποιότητα τροφίμου γενικά ορίζεται σαν το σύνολο των χαρακτηριστικών που επιτρέπουν το διαχωρισμό του και καθορίζουν το βαθμό αποδοχής του από τον καταναλωτή ή τον χρήστη. Πρόκειται για μια δυναμική κατάσταση που κινείται προς φθίνουσα κατεύθυνση (με εξαίρεση ορισμένα τρόφιμα που βελτιώνεται η ποιότητά τους με την ωρίμανση ή παλαίωση). Για το λόγο αυτό τα τρόφιμα έχουν πεπερασμένη διατηρησιμότητα ή διάρκεια ζωής (shelf life). Δεν έχει διατυπωθεί κάποιος γενικά εφαρμόσιμος ορισμός της διατηρησιμότητας των τροφίμων. Ο καθορισμός της διάρκειας ζωής και των κριτηρίων που οριοθετούν το τέλος της εξαρτώνται απο το προϊόν και από τη χρήση για την οποία προορίζεται. Από το Διεθνές Ινστιτούτο Ψυγμένων Προϊόντων (International Institute of Refrigeration, IIR) υποδεικνύονται δυο διαφορετικοί ορισμοί. Χρόνος υψηλής ποιότητας (HQL: High Quality Life) είναι ο χρόνος μετά την επεξεργασία του προϊόντος για την πρώτη αντιληπτή οργανοληπτική διαφορά (70-80% θετική απάντηση σε τριγωνικό τέστ). Ένας αλλος ορισμός είναι ο χρόνος πρακτικής διατήρησης (PSL: Practical Shelf Life). PSL είναι ο χρόνος αποθήκευσης μετά την παραγωγή, προϊόντος υψηλής αρχικής ποιότητας, στον οποίο το τρόφιμο είναι οργανοληπτικά κατάλληλο για χρήση ή κατανάλωση. Ο χρόνος πρακτικής διατήρησης (PSL) είναι συνήθως δύο ή τρείς φορες μεγαλύτερος απο το χρόνο υψηλής ποιότητας (HQL). H Ευρωπαϊκή Κοινότητα εισήγαγε, για την επισήμανση των προϊόντων, τον χρόνο ελάχιστης διατηρησιμότητας (minimum durability), ο οποίος ορίζεται ως ο χρόνος στον οποίο το τρόφιμο διατηρεί τα χαρακτηριστικά του, υπό κατάλληλες συνθήκες αποθήκευσης. Ο τελευταίος αυτός ορισμός διαφέρει από τους προαναφερθέντες στο ότι αναφέρεται στο τρόφιμο και τις ιδιότητες του χωρίς να λαμβάνει καθόλου υπόψη τη χρήση για την οποία προορίζεται. Από τους επιστήμονες που ασχολούνται με τα τρόφιμα πολλές φορές επιβεβαιώνεται η βασική παραδοχή ότι το υψηλότερης ποιότητας τρόφιμο είναι εκείνο που έχει παρακευασθεί ή συλλεχθεί πρόσφατα. Παρ' όλα αυτά, μια και τα διάφορα χαρακτηριστικά των τροφίμων αλληλοεπικαλύπτονται, πρέπει να αποφασιστεί μέχρι ποιού σημείου ένα ορισμένο χαρακτηριστικό ή η εμφάνιση κάποιου ανεπιθύμητου μπορεί να ανιχνευτεί από τον καταναλωτή. Για παράδειγμα, αν η εμφάνιση κάποιου συγκεκριμένου αρώματος ή γεύσης σημαίνει την απουσία άλλων γεύσεων, πρέπει να αποφασιστεί μέχρι ποιό επίπεδο μπορεί να γίνει αυτό αντιληπτό από τον καταναλωτή. Ένας τέτοιος ορισμός πλησιάζει αρκετά με εκείνον που ορίσαμε πρίν ως χρόνο υψηλής ποιότητας (HQL). 66
73 67
74 68
75 69
76 Πάντως όποιος ορισμός και αν χρησιμοποιηθεί τελικά, είναι απαραίτητο να συνοδεύεται από περαιτέρω διευκρινήσεις και οδηγίες π.χ. πρέπει να γίνεται σαφές τι σημαίνει οργανοληπτική ποιότητα και ποιές είναι οι εκάστοτε μέθοδοι μέτρησης και τα κριτήρια που χρησιμοποιούνται για να θεσμοθετηθούν τα επιτρεπτά όρια αποδοχής. 2.2 ΑΡΧΕΣ ΚΙΝΗΤΙΚΗΣ ΑΛΛΟΙΩΣΗΣ ΤΩΝ ΤΡΟΦΙΜΩΝ Εφαρμόζοντας τις βασικές αρχές της χημικής κινητικής ο ρυθμός υποβάθμισης της ποιότητας μπορεί να εκφρασθεί σαν συνάρτηση ενδογενών και εξογενών παραγόντων: όπου: dq dt F C, E (1) i j C i = παράμετροι σύστασης (αντιδρώντα συστατικά, ανόργανοι καταλύτες, ένζυμα, παρεμποδιστές, ph, ενεργότητα νερού, μικροβιακή χλωρίδα) E j = παράμετροι περιβάλλοντος (θερμοκρασία, σχετική υγρασία, ολική πίεση, μερική πίεση περιβαλλόντων αερίων π.χ. CO 2, N 2, O 2, φως, μηχανικές καταπονήσεις) Όπως είναι γνωστό, για μη αντιστρεπτές αντιδράσεις ισχύει γενικά το σχήμα: μ 1 Α 1 +μ 2 Α 2 +μ 3 Α μ m A m O ρυθμός της παραπάνω αντίδρασης δίνεται από τη σχέση: 1 r j d A dt j k f P (2) m k A A... A f n n n όπου n j η τάξη αντίδρασης ως προς Α j (για πραγματικές μοριακές αντιδράσεις n j =μ j ). Για ισορροπίες αντίστοιχα ισχύει: m (3) k f αα+ββ γc+δd (4) και k b d B d C d D d A r k f A B k C D dt dt dt dt b (5) Γενικά αναζητούνται ποσοτικά μετρήσιμοι και αποτελεσματικοί δείκτες, Α ή Β, οι οποίοι είτε καθορίζουν την ποιότητα του τροφίμου είτε την χαρακτηρίζουν έμμεσα μεταβαλλόμενοι με τον ίδιο ρυθμό. Για τους δείκτες αυτούς θεωρείται ότι ισχύει: 70
77 d A ra k A dt m (6) r B B d k dt B m (7) όπου: Α=επιθυμητή ποιοτική παράμετρος π.χ. θρεπτικό συστατικό, άρωμα Β=παράμετρος που υποβαθμίζει το τρόφιμο π.χ. ανεπιθύμητο άρωμα, χρώμα, μικροβιακό φορτίο Οι σχέσεις αυτές μπορούν να προκύψουν από την (3) αν οι συγκεντρώσεις των Α j είναι σε στοιχοιομετρική αναλογία και m=σn j ή από την (5) για k f >>k b ή [C] και [D] αμελητέες. Tα k, k' (φαινόμενες σταθερές ρυθμού αντίδρασης) και τα m, m' (φαινόμενες τάξεις των αντιδράσεων) προσδιορίζονται πειραματικά με δύο τρόπους: 1) Διαφορικές μέθοδοι : Στην κινητική μελέτη των συστημάτων των τροφίμων δεν είναι δυνατόν να υπολογιστεί πειραματικά ο ρυθμός της αντίδρασης για αυτό μετρώνται οι συγκεντρώσεις των Α, Β (άμεσα ή έμμεσα) ως συνάρτηση του χρόνου. Με γραφική ή με κάποια στατιστική μέθοδο προσαρμογής των καμπύλων που προκύπτουν απο τα παραπάνω δεδομένα (π.χ. γραμμική ή πολυωνυμική προσαρμογή) είναι δυνατόν να υπολογιστούν γραφικά ή αναλυτικά οι ρυθμοί των αντιδράσεων. Αν λογαριθμήσουμε τις εξισώσεις (6), (7) παίρνουμε τις παρακάτω γραμμικές σχέσεις: log r Α = log k + m log [A] (8) log r Β = log k' + m' log [B] (9) Με γραμμική προσαρμογή των δεδομένων, χρησιμοποιώντας τη μέθοδο των ελαχίστων τετραγώνων για τις παραπάνω εξισώσεις, είναι δυνατόν να υπολογιστούν οι σταθερές k, k', m, m'. 2) Μέθοδοι με ολοκλήρωση Στις μεθόδους ολοκλήρωσης, διαχωρίζονται οι μεταβλητές των εξισώσεων (6), (7) και ακολουθεί ολοκλήρωση. Για παράδειγμα για την εξίσωση (6) έχουμε: A d[a] m [A] A0 kt (10) Η παραπάνω σχέση είναι της μορφής : Q(A) = kt (11) όπου το Q(Α) ορίζεται ως η συνάρτηση ποιότητας του τροφίμου. 71
78 Ανάλογα με την τάξη της αντίδρασης προκύπτουν διαφορετικές συναρτήσεις ποιότητας για κάθε τρόφιμο, όπως φαίνεται στον παρακάτω Πίνακα 2.1. Περιλαμβάνεται επίσης στον πίνακα και ο χρόνος ημιζωής, ο οποίος αντιπροσωπεύει το χρόνο στον οποίο η τιμή της συγκέντρωσης του δείκτη Α έχει μειωθεί στο μισό της αρχικής τιμής της. Πίνακας 2.1 : Εξισώσεις της ποιοτικής αλλοίωσης των τροφίμων και του χρόνου ημιζωής τους για διαφορετικές τάξεις αντιδράσεων. Φαινόμενη τάξη αντίδρασης Συνάρτηση Ποιότητας Q(A) t Χρόνος ημιζωής t 1/2 0 A o -A t A o /(2k o ) 1 ln(a o /A t ) ln2/k 1 2 1/A o -1/A t 1/(k 2 A o ) m (m 1) 1 1 m 1 m ( At A0 ) m 1 m k (m 1) A m 1 m o Στη μέθοδο με ολοκλήρωση γίνεται ποσοτικός προσδιορισμός της τιμής του δείκτη Α, την οποία υπολογίζουμε με κατάλληλες φυσικοχημικές μεθόδους, σε τακτά χρονικά σημεία και επιλέγουμε από τον πιο πάνω πίνακα, την εξίσωση που δίνει την καλύτερη στατιστική προσαρμογή στα πειραματικά σημεία (μέθοδοι ελαχίστων τετραγώνων). Ακολουθεί στατιστική ανάλυση του επιλεγμένου μοντέλου, όπου μας ενδιαφέρουν η διασπορά των μετρήσεων, ο συντελεστής συσχετίσεως και το διάστημα εμπιστοσύνης της προσδιοριζόμενης παραμέτρου. Στα σχήματα (2.2) και (2.3) φαίνεται ο τρόπος με τον οποίο ο βαθμός μετατροπής της κρίσιμης παραμέτρου και η ακρίβεια ποσοτικού προσδιορισμού της, καθορίζουν την αποτελεσματικότητα του προσδιοριζόμενου μοντέλου. Αναφερόμενοι στο σχήμα 2.2 πρέπει να επισημανθεί ότι το τέλος της διατηρησιμότητας για πολλά τρόφιμα αντιστοιχεί σε απώλεια του δείκτη ποιότητας Α λιγότερο του 30% και ως εκ τούτου μικρή πρακτικά σημασία θα είχε αν το φαινόμενο περιγραφεί με μηδενική ή πρώτη τάξη. Όπως όμως είναι φανερό από το σχήμα 2.3, δεδομένου ότι η ακρίβεια μέτρησης συνήθως κυμαίνεται στο 5%, η αντίδραση πρέπει να μετρηθεί τουλάχιστον μέχρι μετατροπής 50%, οπότε η διαφορά προσαρμογής των δύο μοντέλων είναι πλέον σημαντική. 72
79 Σχήμα 2.2 : Απώλεια της ποιότητας του τροφίμου ως συνάρτηση του χρόνου, όπου παρουσιάζεται η διαφορά μεταξύ της αντίδρασης πρώτης και μηδενικής τάξης. Σχήμα 2.3 : Επίδραση του αναλυτικής ακρίβειας και του βαθμού μετατροπής του μετρούμενου δείκτη Α στο σφάλμα υπολογισμού της σταθεράς του ρυθμού αντίδρασης. 73
80 Τις περισσότερες αντιδράσεις αλλοίωσης που έχουμε μελετήσει και χρησιμοποιήσει για την ποσοτική περιγραφή της διατηρησιμότητας των τροφίμων τις χαρακτηρίζουμε ως μηδενικής ή πρώτης τάξης και φαίνονται στον πίνακα 2.2. Πίνακας 2.2 : Σημαντικές συναρτήσεις ποιότητας που ακολουθούν μηδενικής και πρώτης τάξης κινητική. ΚΙΝΗΤΙΚΗ Αλλοίωση κατεψυγμένων 0 ης ΤΑΞΗΣ ΚΙΝΗΤΙΚΗ 1 ης ΤΑΞΗΣ Μη ενζυμικό μαύρισμα Απώλεια βιταμινών Μικροβιακή μείωση/ανάπτυξη Οξειδωτική απώλεια χρώματος Απώλεια υφής κατά τη θερμική κατεργασία Πρέπει ακόμη να σημειωθεί το γεγονός ότι συνήθως η κινητική μελέτη δεν αναφέρεται στον συχνά πολύπλοκο πραγματικό μηχανισμό των αντιδράσεων, οπότε κάποια μεταβολή στη σύσταση του συστήματος μπορεί να επηρεάσει το ρυθμό αντίδρασης του δείκτη ποιότητας χωρίς αυτό να μπορεί να προβλεφθεί. Γι' αυτό, η αναγωγή των αποτελεσμάτων σε σύστημα διαφορετικής σύστασης πρέπει να γίνεται με ιδιαίτερη προσοχή. Γι' αυτό είναι σκόπιμο, σε ορισμένα συστήματα τροφίμων να μελετάται σε βάθος ο αληθινός μηχανισμός ορισμένων, καθοριστικών για την ποιότητα του τροφίμου, αντιδράσεων ώστε να μπορούν να μελετηθούν αλλαγές στη σύστασή του. Τέτοια διερεύνηση γίνεται συνήθως σε μοντέλα συστημάτων, για αντιδράσεις ιδιαίτερης διατροφικής και τοξικολογικής σημασίας παρά σε πραγματικά τρόφιμα ΕΠΙΔΡΑΣΗ ΠΑΡΑΜΕΤΡΩΝ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Ένα κινητικό μοντέλο που περιγράφει την απώλεια της διάρκειας ζωής ενός προϊόντος είναι χαρακτηριστικό για κάθε τρόφιμο, αλλά επηρεάζεται άμεσα και από περιβαλλοντικούς παράγοντες (π.χ. θερμοκρασία, σχετική υγρασία, ενεργότητα νερού, πίεση και μερική πίεση περιβαλλόντων αερίων), οι οποίοι θα πρέπει να λαμβάνονται υπ' όψην κατά τον σχεδιασμό του. Κατά την προηγούμενη ανάλυση θεωρήθηκε ότι οι περιβαλλοντικοί παράγοντες Ε j παραμένουν σταθεροί. Στην πραγματικότητα όμως μεταβάλλονται συνεχώς και επηρεάζουν τους ρυθμούς των αντιδράσεων που συμβαίνουν μέσα σε ένα σύστημα. Γι' αυτό το λόγο πρέπει να γενικευτούν τα μοντέλα, έτσι ώστε να περιλαμβάνουν ως μεταβλητές και τους περιβαλλοντικούς παράγοντες που επιδρούν ισχυρά στο ρυθμό αντίδρασης. Η επίδραση των παραμέτρων αυτών μπορεί να ενσωματωθεί στα παραπάνω μοντέλα αν η σταθερά ρυθμού αντίδρασης της συνάρτησης ποιότητας εκφραστεί σαν συνάρτηση των παραμέτρων αυτών: k=k (Εj) (12) 74
81 Από τις παραπάνω παραμέτρους, εκείνη η οποία ελέγχεται λιγότερο από τη συσκευασία, καθορίζεται αποκλειστικά από τις συνθήκες αποθήκευσης και έχει σημαντική επίδραση στο k είναι η θερμοκρασία. Επίδραση της θερμοκρασίας Η αύξηση της θερμοκρασίας έχει σαν αποτέλεσμα την αύξηση στο ρυθμό των αντιδράσεων. Η επίδραση αυτή εξηγείται από την σχέση του Arrhenius : EA k k A exp (13) RT E lnk lnk A A R 1 (14) T όπου: k: η σταθερά του ρυθμού της αντιδράσεως, k A: συντελεστής Arrhenius ή σταθερά Arrhenius, Ε Α: ενέργεια ενεργοποιήσης σε cal/mol, R: η παγκόσμια σταθερά των αερίων (1,9872 cal/mol.κ=8,314 J/mol.Κ ), Τ: απόλυτη θερμοκρασία σε Κ Μέθοδοι προσδιορισμού παραμέτρων Arrhenius: Από την σχέση (14), γνωρίζοντας τις τιμές των k σε διαφορετικές θερμοκρασίες (min 3, optimum 5 ή 6), με απεικόνιση του lnk ως προς το 1/Τ θα πάρουμε ευθεία με κλίση -Ε Α /R (σχήμα 2.3). ln k /T ln k Te m p e ra tu re ( C) Σχήμα 2.4 : (α) Τυπικό διάγραμμα Arrhenius της απεικόνιση του lnk συναρτήσει του 1/Τ και (β) γραφική απεικόνιση του lnk με τη θερμοκρασία Με την εφαρμογή αριθμητικών μεθόδων προσαρμογής (στατιστική ανάλυση) προσδιορίζονται οι παράμετροι της σχέσης του Arrhenius με ακρίβεια 95%. Αν όμως διαθέτουμε τρείς μόνο τιμές του k, το διάστημα εμπιστοσύνης είναι συνήθως πολύ μεγάλο. Γι' αυτό, προκειμένου να ληφθούν αξιόπιστες εκτιμήσεις των Ε Α και k A απαιτούνται δεδομένα σε περισσότερες θερμοκρασίες. Μια εκτίμηση του βέλτιστου αριθμού πειραμάτων που δίνει αξιόπιστα αποτελέσματα ήταν 5 ή 6 θερμοκρασίες. Όταν τα πειραματικά σημεία περιορίζονται σε τρείς μόνο θερμοκρασίες, τότε συμπεριλαμβάνοντας και τα άνω και κάτω όρια εμπιστοσύνης κάθε 75
82 σημείου στην γραμμική προσαρμογή ή με τη μέθοδο σημείου προς σημείο (point by point), μπορεί κανείς να υπολογίσει τις παραμέτρους της σχέσης του Arrhenius με μικρότερα διαστήματα εμπιστοσύνης. Εναλλακτικά, ο υπολογισμός του k χρησιμοποιώντας πολυβάθμια γραμμική προσαρμογή των συγκεντρώσεων A ως προς το χρόνο σε όλες τις εξεταζόμενες θερμοκρασίες, περιορίζει την ανάγκη υπολογισμού ξεχωριστά του Αο για καθε πείραμα, οπότε και αυξάνονται οι βαθμοί ελευθερίας, με αποτέλεσμα να υπολογίζεται με μεγαλύτερη ακρίβεια το k σε κάθε θερμοκρασία Εφόσον επίσης ακολουθείται από γραμμική προσαρμογή του lnk ως προς το 1/Τ, έχουμε τότε μια μέθοδο δύο σταδίων. Επίσης, είναι δυνατόν να γίνει και ανάλυση σε ένα στάδιο, χρησιμοποιώντας στατιστικές μεθόδους μη γραμμικής παλινδρόμησης στην εξίσωση που προκύπτει απο την αντικατάσταση της (13) στις συναρτήσεις ποιότητας του πίνακα 2.1. Για παράδειγμα για πρώτης τάξης συνάρτηση ποιότητας προκύπτει η ακόλουθη εξίσωση: A A exp[ k exp(- E A RT )t] 0 A (15) Η παραπάνω εξίσωση έχει ως μεταβλητές τόσο το χρόνο όσο και τη θερμοκρασία και με μη γραμμική προσαρμογή υπολογίζονται τα Α 0, k A, E A. Τα πειραματικά δεδομένα που χρησιμοποιούνται είναι συγκεντρώσεις των δεικτών ποιότητας ως προς το χρόνο, για όλες τις εξεταζόμενες θερμοκρασίες με αποτέλεσμα να αυξάνονται οι βαθμοί ελευθερίας και να λαμβάνονται στενότερα διαστήματα εμπιστοσύνης για τα υπολογιζόμενα μεγέθη. Τα μειονεκτήματα αυτής της μεθόδου εκτός απο την πολυπλοκότητα της εφαρμογής της είναι ότι απαιτεί προηγούμενη γνώση της τάξης αντίδρασης και δεν επιτρέπει την εύκολη αναγνώριση των ακραίων τιμών που οφείλονται σε πειραματικά σφάλματα και θα έπρεπε να εξαιρεθούν. Q 10 Ένας άλλος εναλλακτικός τρόπος έκφρασης της επίδρασης της θερμοκρασίας στη διατηρησιμότητα, πολύ συνήθης στην παλαιότερη βιβλιογραφία και στη βιομηχανία είναι ο όρος Q 10. Το Q 10 ορίζεται ως ο λόγος της σταθεράς του ρυθμού αντίδρασης σε δυο θερμοκρασίες που διαφέρουν κατα 10 βαθμούς Κ ή C. Ακόμα το Q 10 εναλλακτικά ορίζεται και ως η μεταβολή στο χρόνο ζωής ενός προϊόντος, θ s, δηλ. στο χρόνο στον οποίο οι δείκτες ποιότητας Α και Β φτάνουν σε μη αποδεκτά όρια, όταν το τρόφιμο αποθηκεύεται σε θερμοκρασία κατα 10 βαθμούς υψηλότερη. Q 10 k( T 10) s ( T) k( T) ( T 10) Δηλαδή το Q 10 εισάγει την παρακάτω εξίσωση εξάρτησης της θερμοκρασίας: k(t) s (16) k o e bt ή lnk lnk o bt (17) δηλ. η γραφική απεικόνιση του lnk με τη θερμοκρασία (σε αντίθεση με το 1/Τ στην εξίσωση του Arrhenius) μας δίνει ευθεία (Σχ. 2.4(β)). Αντίστοιχα και η απεικόνιση του lnθ s με τη 76
83 θερμοκρασία. Αυτές οι γραφικές παραστάσεις ονομάζονται διάγραμμα της διάρκειας ζωής (shelf-life plot). Το Q 10 και το b δίνονται συναρτήσει της ενέργειας ενεργοποίησης της αντίδρασης που καθορίζει την ποιοτική υποβάθμιση του τροφίμου από την παρακάτω σχέση : ln Q E A 10 b R T( T 10) (18) Η εξάρτηση του Q 10 από τη θερμοκρασία γίνεται πιο έντονη όσο πιο μεγάλη είναι η ευαισθησία της αντίδρασης ως προς τη θερμοκρασία. Πίνακας 2.3 : Εξάρτηση του Q 10 από την θερμοκρασία και το Ε Α Ε Α Q 10 Q 10 Q 10 kcal/mol στους 5 C στους 20 C στους 40 C Αποκλίσεις από τη συμπεριφορά κατά Arrhenius 1. Σε ορισμένες περιπτώσεις, την ποιότητα του τροφίμου την επηρεάζουν περισσότερες απο μία αντιδράσεις. Όταν αυτές οι αντιδράσεις (π.χ. μη ενζυματικό μαύρισμα, αυτοξείδωση λιπαρών) έχουν διαφορετική θερμοκρασιακή συμπεριφορά (διαφορετική Ε Α ) επηρεάζουν την ολική ποιότητα ανάλογα με το θερμοκρασιακό εύρος σε άλλο βαθμό, με αποτέλεσμα η συνάρτηση της τελευταίας με τη θερμοκρασία να αποκλίνει από τη σχέση Arrhenius. Για παράδειγμα, αν η ποιότητα του τροφίμου εξαρτάται απο δύο κυρίως αντιδράσεις τότε η γραφική απεικόνιση της μεταβολής της με το 1/Τ θα έχει διαφορετική κλίση σε κάθε μια απο τις διαφορετικές θερμοκρασιακές περιοχές όπως φαίνεται και στο Σχήμα
84 Σχήμα 2.5 : Τυπική θερμοκρασιακή εξάρτηση της ποιότητας τροφίμου απο τη θερμοκρασία όταν αυτή επηρεάζεται απο δυο αντιδράσεις με διαφορετική Ε Α. 2. Επίσης έχουμε αποκλίσεις από τη συμπεριφορά Arrhenius από μεταβολές στη φυσική κατάσταση του τροφίμου π.χ. στα κατεψυγμένα τρόφιμα στη περιοχή απόψυξης-κατάψυξης, αλλαγή στη κρυσταλλική δομή των υδατανθράκων, ρευστοποίηση λιπαρών κ.λ.π., όπως φαίνεται και στο παρακάτω Σχήμα 2.6 Σχήμα 2.6 : Αποκλίσεις από τη συμπεριφορά κατά Arrhenius για κατεψυγμένα τρόφιμα. 78
85 3. Στις ενζυματικές και μικροβιολογικές αντιδράσεις ο ρυθμός των αντιδράσεων παρουσιάζει θερμοκρασιακό μέγιστο κάτω και άνω του οποίου ακολουθείται συμπεριφορά Arrhenius. Αυτό παρουσιάζεται στο παρακάτω Σχήμα 2.7 Σχήμα 2.7 : Τυπική καμπύλη θεμοκρασιακής εξάρτησης του ρυθμού σε ενζυμικές και μικροβιολογικές αντιδράσεις. 79
86 Επίδραση της ενεργότητας του νερού (a w ) Η περιεχόμενη υγρασία και η ενεργότητα του νερού στα τρόφιμα είναι οι αμέσως πιο σημαντικοί περιβαλλοντικοί παράγοντες μετά τη θερμοκρασία που επιδρούν στο ρυθμό των αντιδράσεων που καθορίζουν την ποιοτική υποβάθμιση του τροφίμου. Η ενεργότητα του νερού είναι ένα μέτρο της διαθεσιμότητας του νερού στα διάφορα τρόφιμα. Δηλαδή περιγράφει το πόσο ισχυρά συγκρατείται μέσα στο τρόφιμο και σε ποιό ποσοστό είναι διαθέσιμο να συμπεριφερθεί ως διαλύτης ή να λάβει μέρος σε χημικές δράσεις. Ως κρίσιμα όρια του a w λαμβάνονται εκείνα πάνω απο τα οποία παρατηρούνται ανεπιθύμητες μεταβολές στα τρόφιμα σε σχέση με την ασφάλεια και τη ποιότητα τους. Ο έλεγχος του a w αποτελεί βασικό παράγοντα για τη διατήρηση των ξηρών και μέσης υγρασίας τροφίμων (IMF). Από άποψη ασφάλειας ενδιαφερόμαστε για την ανάπτυξη μικροοργανισμών. Η ικανότητα ανάπτυξής τους σε συγκεκριμένο περιβάλλον εξαρτάται απο το συνδυασμό αλληλεπιδράσεων πλήθους παραγόντων όπως: a w, ph, θερμοκρασία, κ.λ.π. Για δεδομένες τιμές των άλλων παραγόντων, μπορούμε να καθορίσουμε ελάχιστη a w για την ανάπτυξη συγκεκριμένων μικροοργανισμών. Το κρίσιμο όριο παθογένεσης στα τρόφιμα ορίζεται σε ενεργότητα a w (το πιο ανθεκτικό παθογόνο βακτήριο είναι το Staphylococcus aureus ). Η υφή και η ποιότητα του τροφίμου επηρεάζεται σημαντικά απο την περιεκτικότητα σε υγρασία και a w. Τα ξηρά τρόφιμα όπως τσίπς, ποπ-κόρν, κράκερς και κορν φλείκς χάνουν τη τραγανότητά τους όταν αυξάνεται η περιεχόμενη υγρασία τους συνήθως σε διάστημα a w απο 0.35 έως 0.5. Τρόφιμα μέσης υγρασίας όπως αποξηραμένα φρούτα, ζωοτροφές, προϊόντα αρτοποιίας και ζαχαροπλαστικής, χάνοντας υγρασία σε διάστημα a w μεταξύ , γίνονται πολύ σκληρά. Ένα άλλο σημαντικό πρόβλημα εμφανίζεται στα τρόφιμα που περιέχουν άμορφα ζάκχαρα όταν η a w αυξάνει πάνω απο 0.35 με 0.4, οπότε τα άμορφα ζάχαρα ανακρυσταλλώνονται απελευθερώνοντας νερό με επιπτώσεις στη ποιότητα και την υφή του τροφίμου. Εκτός απο τα συγκεκριμένα κρίσιμα όρια του a w, η ενεργότητα του νερού επιδρά και και στις χημικές δράσεις. Η επίδραση αυτή παίζει καθοριστικό ρόλο στη διατηρησιμότητα των ξηρών και μέσης υγρασίας τροφίμων. Γενικά, η ιδιότητα του νερού να συμπεριφέρεται ως διαλύτης και να παίρνει μέρος σε διάφορα χημικά φαινόμενα, αυξάνεται αυξανομένης της τιμής της a w. H επίδραση αυτή οφειλεται στο γεγονός οτι το νερό που αντιστοιχεί στη περιοχή του μονομοριακού στρώματος είναι ισχυρά δεσμευμένο και δεν είναι ικανό να λάβει μέρος σε δράσεις που υποβαθμίζουν το τρόφιμο ή ο ρυθμός των δράσεων αυτών είναι τόσο μικρός ώστε να θεωρείται αμελητέα η επιδραση του νερού στη σταθερότητα του τροφίμου. Ακριβώς πάνω απο το μονομοριακό στρώμα νερού ΒΕΤ αρχίζει η διάλυση των αντιδρώντων με αποτέλεσμα την κίνηση τους που συνοδεύεται απο μικρή επιτάχυνση του ρυθμόυ πολλών αντιδράσεων. Αυξανομένης της τιμής a w πάνω απο την τιμή που αντιστοιχεί στο μονομοριακό στρώμα νερού έχουμε την εκθετική αύξηση του ρυθμού πολλών αντιδράσεων που επιδρούν στη διατηρησιμότητα των τροφίμων. Εμπειρικά στην περιοχή τιμών a w ( 0,2-0,9 ) έχουμε σε πολλές αντιδράσεις διπλασιασμό του ρυθμού αντίδρασης για κάθε αύξηση της ενεργότητας κατά 0,1. Οι περισσότερες αντιδράσεις παρουσιάζουν ελάχιστους ρυθμούς ακριβώς στο όριο του μονομοριακού στρώματος, ενώ ειδικά η οξείδωση των λιπαρών παρουσιάζει ελάχιστο ρυθμό 80
87 στη περιοχή του μονομοριακού στρώματος και αυξανόμενους ρυθμούς τόσο πρίν όσο και μετά απο αυτό. Έχουν διατυπωθεί διάφορες προσεγγίσεις εξήγησης της επίδρασης της ενεργότητας νερού a w στη διατηρησιμότητα των τροφίμων. Η περιεχόμενη υγρασία και η ενεργότητα του νερού μπορούν να επιδράσουν στις κινητικές παραμέτρους των συναρτήσεων ποιότητας (k A, E A ), στις συγκεντρώσεις των αντιδρώντων σωμάτων και σε μερικές περιπτώσεις ακόμα και στη φαινόμενη τάξη αντίδρασης, m. Ο προεκθετικός παράγοντας ή σταθερά Arrhenius k A ταυτίζεται με τη πιθανότητα ή τη συχνότητα των ενεργών συγκρούσεων που οδηγούν στη διάσπαση των ενεγροποιημένων μοριών σε μια αντίδραση. Αυτό σημαίνει οτι το k A είναι αντιστόφως ανάλογο της πυκνότητας της υδατικής φάσης. Αν μειωμένης της ενεργότητας νερού αυξάνεται η πυκνότητα, καθώς το νερό δεσμευέται ισχυρότερα, θα αναμένονταν το k A αλλά και η συνολική σταθερά του ρυθμού αντίδρασης να μειώνεται. Μεταβολή όμως της ενεργότητας νερού ίσως να επηρεάζει και την ενέργεια ενεργοποίησης E A, εφόσον αυτή αποτελεί συνάρτηση των θερμοδυναμικών σταθερών κάθε αντίδρασης. Επίδραση άλλων παραγόντων Για να εκφραστεί η επίδραση των διαφόρων παραγόντων σε μια απλή μαθηματική σχέση, η αρχή της συνάρτησης ποιότητας μπορεί να χρησιμοποιηθεί σε μια πιο γενική προσέγγιση. Αν υποθέσουμε ότι η ποιότητα ενός τροφίμου εξαρτάται από i διαφορετικούς παράγοντες Α i, τότε: Q ( A ) i i k t (19) i Η σταθερά του ρυθμού k i για κάθε ένα παράγοντα ποιότητας είναι συνάρτηση διαφόρων παραγόντων: k f ( T, a, ph, P, P...) i i w O CO 2 2 (20) οι τιμές των οποίων είναι με τη σειρά τους εξαρτώμενες από το χρόνο. Η σταθερά ρυθμού είναι επομένως επίσης μια συνάρτηση του χρόνου, k i k i ( t). Στην περίπτωση αυτή, η τιμή της συνάρτησης ποιότητας σε μια δεδομένη χρονική στιγμή δίνεται από την έκφραση: Q i ( A i ) k idt 0 t (21) 81
88 Αν η ελάχιστη αποδεκτή τιμή για την παράμετρο ποιότητας Α i είναι γνωστή (Α m ), τότε το αναλωθέν ( ci ) και το υπολειπόμενο ( ri ) ποσοστό διατηρησιμότητας σε χρόνο t, ορίζονται ως εξής: και Q i(a0) Q i(a i) c i (23) Q (A ) Q (A ) i 0 i m Q i(a i) Q i(am) r i (24) Q (A ) Q (A ) i 0 i m Η εναπομένουσα διάρκεια ζωής του τροφίμου σε μια θερμοκρασία Τ υπολογίζεται από την έκφραση: min[( Q (A ) Q (A ))/k ] (25) r i i i m i 2.4. ΧΡΗΣΗ ΤΩΝ ΑΡΧΩΝ ΤΗΣ ΚΙΝΗΤΙΚΗΣ ΑΛΛΟΙΩΣΗΣ ΓΙΑ ΤΗΝ ΠΡΟΒΛΕΨΗ ΚΑΙ ΤΟΝ ΕΛΕΓΧΟ ΤΗΣ ΔΙΑΤΗΡΗΣΙΜΟΤΗΤΑΣ ΤΩΝ ΤΡΟΦΙΜΩΝ Μέθοδος επιταχυνόμενου ελέγχου διατηρησιμότητας (ΜΕΕΔ) (A.S.L.T.: Accelerated shelf life testing). Η διατηρησιμότητα και η διάρκεια ζωής ενός προϊόντος εξαρτάται, όπως αναπτύχθηκε παραπάνω, από ένα πλήθος παραγόντων όπως είναι η σύστασή του, η επεξεργασία του, η συσκευασία και εξωγενείς παράγοντες, με σημαντικότερο τη θερμοκρασία. Με βάση τις αρχές της κινητικής, όπως περιγράφτηκαν παραπάνω, μπορεί να προβλεφτεί η διάρκεια ζωής ενός προϊόντος χωρίς τον άμεσο πειραματικό προσδιορισμό της, με τη μέθοδο επιταχυνόμενου ελέγχου της διατηρησιμότητας (ΜΕΕΔ). Η μέθοδος επιταχυνόμενου ελέγχου της διατηρησιμότητας (ΜΕΕΔ) χρησιμοποιεί εκτιμήσεις της διάρκειας ζωης του τροφίμου σε πειράματα που γίνονται σε υψηλές θερμοκρασίες και στη συνέχεια τα αποτελέσματα προεκβάλονται σε συνήθεις συνθήκες αποθήκευσης με τη χρήση της σχέσης του Arrhenius. Η χρήση αυτής της μεθόδου επιτυγχάνει σύντμηση του χρόνου των δοκιμών και είναι ιδαίτερα χρήσιμη για προϊόντα μακράς διατηρησιμότητας (μήνες ή έτη). Τα βασικά βήματα που ακολουθούνται στη ΜΕΕΔ είναι τα παρακάτω : 1. Προσδιορισμός των παραμέτρων που προσδιορίζουν την ποιότητα και την ασφαλή απο μικροβιολογικής άποψης κατανάλωση του προϊόντος. 82
89 2. Προσδιορισμό των αντιδράσεων που επιδρούν άμεσα στη ποιότητα του τροφίμου και άρα στο χρόνο ζωής του, ο οποίος γίνεται μετά από εκτενή μελέτη των συστατικών του τροφίμου, της επεξεργασίας του και των συνθηκών αποθήκευσής του. Είναι απαραίτητη η αναδρομή σε βιβλιογραφικά δεδομένα. 3. Επιλογή του υλικού συσκευασίας. Τα κατεψυγμένα και κoνσερβοποιημένα τρόφιμα μπορούν να συσκευάζονται κατ'ευθείαν στη τελική τους συσκευασία. Τα ξηρά τρόφιμα πρέπει να αποθηκεύονται σε αεροστεγή γυάλινα δοχεία ή σε μη διαπερατά φάκελλα στις επιθυμητές συνθήκες υγρασίας και a w. 4. Επιλέγονται οι θερμοκρασίες του πειράματος (τουλάχιστον δύο). Οι πιο συνήθεις επιλογές είναι οι εξής, όπως φαίνεται στον πιο κάτω Πίνακα 2.6. Πίνακας 2.6 Τύπος Προϊόντος Θερμοκρασίες πειράματος ( o C) Δείγμα αναφοράς ( o C) Κονσερβοποιημένο 25, 30, 35, 40 4 Ξηρό, αφυδατωμένο 25, 30, 35, 40, Ψυγείου 5, 10, 15, 20 0 Κατεψυγμένο -5, -10, -15 < Γνωρίζοντας τον επιθυμητό χρόνο ζωής του προϊόντος στις ακραίες συνθήκες θεμοκρασίας και βασιζόμενοι σε βιβλιογραφικά στοιχεία για το Q 10 υπολογίζουμε τον απαραίτητο χρόνο παραμονής του προϊόντος σε κάθε μια απο τις επιλεγόμενες θερμοκρασίες. Αν δεν υπάρχουν πληροφορίες για το Q 10 απαιτούνται περισσότερες απο δύο θερμοκρασίες. 6. Αποφασίζεται το είδος και η συχνότητα των ελέγχων που θα χρησιμοποιηθούν για κάθε θερμοκρασία. Χρησιμοποιώντας δεδομένα σε μεγαλύτερη θερμοκρασία μπορεί να υπολογίσει κανείς την ελάχιστη συχνότητα των ελέγχων (μετρήσεων) σε κάθε θερμοκρασία σύμφωνα με τη παρακάτω σχέση: f f Q T/ (26) όπου: f 1 : ο χρόνος μεταξύ των ελέγχων (π.χ. μέρες ή εβδομάδες) στη μέγιστη θερμοκρασία Τ 1, f 2 : ο χρόνος μεταξύ σημείων σε χαμηλότερη θερμοκρασία Τ 2 και ΔΤ: η διαφορά θερμοκρασίας μεταξύ του Τ 1 και Τ 2 σε βαθμούς Κελσίου. Για παράδειγμα έστω ότι η θερμοκρασιακή εξάρτηση του ρυθμού ποιοτικής υποβάθμισης για ένα κονσερβοποιημένο προϊόν εκφράζεται με τιμή Q 10 =3. Όταν διατηρείται στους 25 C ελέγχεται ανά 90 ημέρες για δύο έτη. Αν η μελέτη γίνει στους 35 C (ΔΤ=10) με Q 10 =3, το προϊόν θα πρέπει να ελέγχεται κάθε 30 ημέρες για 240 ημέρες. Αντίστοιχα, αν η μελέτη 83
90 γίνει στους 45 C (ΔΤ=20) με Q 10 =3, το προϊόν θα πρέπει να ελέγχεται κάθε 10 ημέρες για 80 ημέρες. Σε ορισμένες περιπτώσεις είναι προτιμότερο να γίνονται συχνότερα οι έλεγχοι ειδικά αν δεν είναι με ακρίβεια γνωστό το Q 10. Mεγάλα χρονικά διαστήματα μεταξύ των πειραματικών σημείων μπορεί να έχουν ως αποτέλεσμα τον μη ακριβή προσδιορισμό της διάρκειας ζωής. Γενικά πρέπει να λαμβάνονται τουλάχιστον έξι πειραματικά σημεία σε κάθε θερμοκρασία, ώστε να μειωθούν στο ελάχιστο τα σφάλματα. Διαφορετικά μειώνεται πολύ ο βαθμός βεβαιότητας της διάρκειας ζωής t s. 7. Tα δεδομένα τοποθετούνται σε διάγραμμα ώστε να μπορεί να προσδιοριστεί η τάξη του αντιδρώντος συστήματος και να εκτιμηθεί αν πρέπει να αυξηθεί ή να μειωθεί ο αριθμός των ελέγχων. Συνίσταται να αποφεύγεται αυτό που συχνά παρατηρείται, να εξετάζονται δηλαδή τα δεδομένα, αφού έχει τελειώσει η πειραματική διαδικασία, οπότε διαπιστώνεται ότι έπρεπε να έχουν γίνει νωρίτερα αλλαγές στον προγραμματισμό του πειράματος. 8. Για τα πειραματικά δεδομένα κάθε θερμοκρασίας προσδιορίζεται η τάξη και το k του συστήματος, κατασκευάζεται το διάγραμμα Arrhenius, και εκτιμάται η διάρκεια ζωής του προϊόντος στις πραγματικές συνθήκες αποθήκευσης. Πολλές φορές συνηθίζεται σε ερευνητικά εργαστήρια να τοποθετείται το προϊόν και στην πραγματική θερμοκρασία ώστε να διαπιστωθεί η ακρίβεια των υπολογισμών. Βέβαια αυτό δεν συνηθίζεται στη βιομηχανία, γιατί είναι τόσο χρονικά όσο και οικονομικά ασύμφορο. ΥΠΟΛΟΓΙΣΤΙΚΟ ΠΑΡΑΔΕΙΓΜΑ Πρόβλημα Ο ρυθμός αλλοίωσης των τροφίμων και η διατηρησιμότητά τους μετά την επεξεργασία εξαρτάται από τη συσκευασία και από τις συνθήκες διανομής και αποθήκευσης, κυρίως τη θερμοκρασία. Για τα αφυδατωμένα τρόφιμα οι δράσεις υποβάθμισης είναι φυσικοχημικές. Mελετήθηκε η διατηρησιμότητα τσιπς πατάτας. Η αντίδραση που θεωρείται βασικά υπεύθυνη για τη μείωση της ποιότητας είναι ο αυτοξειδωτικός ταγγισμός, που μετράται με προσδιορισμό της τιμής των υπεροξειδίων. Μετρήθηκε με το χρόνο η παραγωγή υπεροξειδίων σε διάφορες θερμοκρασίες. Η σταθερά ρυθμού αντίδρασης k στους 25 C υπολογίστηκε σε 0,03 (μονάδες υπεροξειδίων/ημέρα) αντίστοιχα. Η αρχική τιμή υπεροξειδίων είναι 1 και η φαινόμενη τάξη αντίδρασης μηδενική. Η επίδραση της θερμοκρασίας εκφράστηκε από τη σχέση Arrhenius με ενέργεια ενεργοποίησης Ε Α 15 kcal/mol. Να υπολογιστεί η διατηρησιμότητα του τροφίμου στους 25, 30 και 35 C. Θεωρήστε ότι η μέγιστη αποδεκτή τιμή υπεροξειδίων είναι 10. (R=1,987 cal/mol.κ) Τα παραπάνω ισχύουν όταν τα συσκευασμένα τσιπς έχουν ενεργότητα νερού a w = 0,2. Αν η σταθερά ρυθμού του αυτοξειδωτικού ταγγισμού αυξάνει κατά 50% για κάθε 0,05 αύξηση στην a w, ποια θα είναι η διάρκεια ζωής ενός προϊόντος που λόγω κακής συσκευασίας έχει a w =0,3 και αποθηκεύεται στους 30 C (η σχετική αύξηση του ρυθμού λόγω αύξησης της a w είναι ίδια σε όλες τις θερμοκρασίες). Λύση Στη περίπτωση του τροφίμου που εξετάζεται(συσκευασμένα τσιπς πατάτας) έχουμε σαν κύριο δείκτη ποιότητας την τιμή υπεροξειδίων, που είναι μέτρο του αυτοξειδωτικού ταγγισμού. Έχουμε δηλαδή την περίπτωση της εξίσωσης (7) (σελ. 71 σημειώσεων) που η υποβάθμιση της 84
91 ποιότητας εκφράζεται με το ρυθμό αύξησης μιας ανεπιθύμητης παραμέτρου που υποβαθμίζει το τρόφιμο. Δεδομένου ότι η φαινόμενη τάξη αντίδρασης είναι μηδενική, η συνάρτηση ποιότητας (εξ. 11, Πιν 2.1) εκφράζεται ως: Q(Β) = B t -B o = k t Στη αρχή της ζωής του τροφίμου έχουμε B o = 1 μονάδα υπεροξειδίων και στο τέλος έχουμε B t = 10 μονάδες υπεροξειδίων. Η σταθερά ρυθμού αντίδρασης k στους 25 C είναι k 25 =0,03 (μονάδες υπεροξειδίων/ημέρα) επομένως η διατηρησιμότητα (διάρκεια ζωής) στους 25 C είναι t= (B t -B o )/k= (10-1)/ 0,03 = 300 d. Για τον υπολογισμό της διατηρησιμότητας (διάρκειας ζωής) στους 30 και 35 C πρέπει να υπολογίσουμε τις σταθερές ρυθμού αντίδρασης k 30 και k 35. Ισχύει η σχέση Arrhenius (εξ.13, σελ. 75) με ενέργεια ενεργοποίησης Ε Α 15 kcal/mol. Έχουμε: k 25 = k A exp (-E A /R 298) (1) k 30 = k A exp (-E A /R 303) (2) k 35 = k A exp (-E A /R 308) (3) Από (2):(1) έχουμε: k 30 = k 25 exp [(E A /R) ((1/298)-(1/303))]= 0,03 exp [(15000/1,9871) ((1/298)-(1/303))]= 0,03 exp(0,4180)= 0,03. 1,519 = 0,04557 (μονάδες υπεροξειδίων/ημέρα) Αντίστοιχα έχουμε k 35 = k 25 exp [(E A /R) ((1/298)-(1/308))]= 0,03 exp [(15000/1,9871) ((1/298)-(1/308))]= 0,03 exp(0,8224)= 0,03. 2,276 = 0,06828 (μονάδες υπεροξειδίων/ημέρα) Επομένως η διατηρησιμότητα στους 30 C είναι t= (B t -B o )/k 30 = (10-1)/ 0,04557 = 197,5 d και η διατηρησιμότητα στους 35 C είναι t= (B t -B o )/k 35 = (10-1)/ 0,06828 = 131,8 d. Τα παραπάνω ισχύουν όταν τα συσκευασμένα τσιπς έχουν ενεργότητα νερού a w = 0,2. Για να υπολογίσουμε τη διάρκεια ζωής ενός προϊόντος που λόγω κακής συσκευασίας έχει a w =0,3 και αποθηκεύεται στους 30 C πρέπει να υπολογίσουμε τη σταθερά ρυθμού του αυτοξειδωτικού ταγγισμού k 30-0,3 στoυς 30 C και a w =0,3. Αν η σταθερά ρυθμού αυξάνει κατά 50% για κάθε 0,05 αύξηση στην a w (δηλ. x1,5) έχουμε για 0,1 αύξηση: k 30-0,3 = k 30 x1,5 x1,5 = 0,04557 x1,5 x1,5 = 0,1025(μονάδες υπεροξειδίων/ημέρα). Επομένως η διατηρησιμότητα στους 30 C και a w =0,3 είναι: t= (B t -B o )/ k 30-0,3 = (10-1)/ 0,1025 = 87,8 d (δηλ. λιγότερο από 3 μήνες). ΒΙΒΛΙΟΓΡΑΦΙΑ Taoukis, P. and Labuza, T. P. Summary: Integrative Concepts (Shelf-life testing and modelling). In: "FOOD CHEMISTRY", 3rd Edition, O. Fennema (editor), Marcel Dekker, New York, Chapter 17, pp , Taoukis, P.S., Labuza, T. P. and Saguy, I. Kinetics of Food Deterioration and Shelf-Life prediction. In: "THE HANDBOOK OF FOOD ENGINEERING PRACTICE", K.J. Valentas, E. Rotstein, R. P. Singh (ed.), CRC Press, Chapter 10, p , Taoukis PS, Giannakourou MC. Temperature and food stability: analysis and control. In: Understanding and measuring the shelf-life of food, R. Steele (ed), Woodhead Publishing Ltd, Cambridge, England and CRC Press LLC, Boca Raton FL, USA, Ch. 3, p ,
92 ΚΕΦΑΛΑΙΟ 3 ΜΙΚΡΟΒΙΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ 3.1. Γενικές αρχές Τα τρόφιµα, λόγω της υψηλής περιεκτικότητάς τους σε θρεπτικά συστατικά και της ευκολίας µολύνσεως και ρυπάνσεώς τους, είναι πάντοτε φορείς µικροoργανισµών. Τα µικρόβια αυτά συµµετέχουν στις φυσικοχηµικές και βιολογικές µεταβολές που συµβαίνουν στα τρόφιµα. Αυτό αποτελεί και το αντικείµενο της επιστήµης της µικροβιολογίας των τροφίµων. Ο όρος "µικρόβιο" ή "µικροοργανισµός" είναι όρος της τεχνολογίας και αφορά ένα σύνολο εµβίων όντων από διάφορες ταξινοµικές οµάδες µε ορισµένα κοινά χαρακτηριστικά. Οι µικροοργανισµοί είναι αόρατοι µε γυµνό οφθαλµό, µε µικροσκοπικές διαστάσεις µεγαλύτερες από τη διακριτική ικανότητα του µικροσκοπίου (0.16 µ). Γενικά, πρόκειται για µονοκύτταρους οργανισµούς ή κοινοκυτταρικούς χωρίς εγκάρσια τοιχώµατα ή και πολυκυτταρικούς χωρίς όµως διαφοροποίηση των κυττάρων για σχηµατισµό οργάνων ή ιστών. Σύµφωνα µε τον Haeckel, οι µικροοργανισµοί κατατάσσονται στα πρώτιστα, τα οποία διακρίνονται σε δύο µεγάλες κατηγορίες: α) τα ευκαρυωτικά (φύκη, πρωτόζωα, µύκητες, µυξοµύκητες) και β) τα προκαρυωτικά (βακτήρια, κυανοπράσινα φύκη, µυκοπλάσµατα). Ανάλογα µε την πηγή άνθρακα, αζώτου και ενέργειας, τα µικρόβια διαιρούνται σε τέσσερις οµάδες: α)τα φωτοαυτότροφα, τα οποία χρησιµοποιούν ως πηγή ενέργειας την ηλιακή ακτινοβολία και ως πηγή άνθρακα το CO 2, β)τα φωτοετερότροφα, τα οποία χρησιµοποιούν ως πηγή ενέργειας την ηλιακή ακτινοβολία και ως πηγή άνθρακα οργανικές ενώσεις, γ) τα χηµειοαυτότροφα, τα οποία χρησιµοποιούν το CO 2 ως µοναδική πηγή άνθρακα και αντλούν ενέργεια από τις οξειδοαναγωγικές αντιδράσεις ανοργάνων ουσιών, και δ)τα χηµειοετερότροφα, τα οποία χρησιµοποιούν ως πηγή άνθρακα οργανικές ουσίες και αντλούν ενέργεια από οξειδοαναγωγικές αντιδράσεις οργανικών πάντα ουσιών. Τα µικρόβια της τελευταίας οµάδας, τα χηµειοετερότροφα, είναι αυτά που ενδιαφέρουν κυρίως τη µικροβιολογία τροφίµων και διαιρούνται σε τρεις κατηγορίες ανάλογα µε τη σχέση τους προς το υπόστρωµα ή τον ξενιστή πάνω στον οποίο αναπτύσσονται. Έτσι, διακρίνονται σε: 84
93 α) παθογόνα µικρόβια, τα οποία αναπτύσσονται πάνω σε ζωντανούς οργανισµούς και δηµιουργούν µε την ανάπτυξη και τον πολλαπλασιασµό τους παθολογικές καταστάσεις. Στην περίπτωσή µας ενδιαφέρον παρουσιάζουν µόνο όσα µικρόβια µεταφέρονται µε τα τρόφιµα και το πόσιµο νερό, φθάνουν ως τον άνθρωπο και τα ανώτερα ζώα, τον µολύνουν και δηµιουργούν παθολογικές καταστάσεις. β) παράσιτα µικρόβια, που αναπτύσσονται πάνω σε ζωντανούς οργανισµούς χωρίς να δηµιουργούν νοσηρές ή παθολογικές καταστάσεις, τουλάχιστον υπό οµαλές συνθήκες. Αν όµως µειωθεί η αντοχή του οργανισµού (π.χ. λοιµώξεις), τότε εξελίσσονται σε ισχυρά παθογόνα και προξενούν σοβαρές παθολογικές καταστάσεις. γ) σαπρόφυτα µικρόβια, που αναπτύσσονται πάνω σε νεκρή οργανική ουσία (όπως είναι πολλά τρόφιµα) και όχι πάνω σε ζωντανούς οργανισµούς. Αναπτυσσόµενα όµως πάνω στα τρόφιµα προξενούν αλλοιώσεις, οπότε είναι ανεπιθύµητα, ή διασπάσεις προς ενδιάµεσα προϊόντα που είναι πολύτιµα για τον άνθρωπο, οπότε είναι ωφέλιµα. Στο ταξινοµικό σύστηµα των µικροβίων αναγνωρίζονται οι ακόλουθες ταξινοµικές κατηγορίες: τάξη, γένος (genus), είδος (species), στέλεχος (strain). Το είδος παρουσιάζει µια υψηλή βαθµίδα φαινοτυπικής οµοιότητας και σηµαντικής ανοµοιότητας ως προς άλλα αθροίσµατα συγγενών πληθυσµών. Τα διάφορα στελέχη έχουν µεγάλη σηµασία για την Μικροβιολογία Τροφίµων. Γένος και είδος συµβολίζονται µε µια διώνυµη λατινική ονοµασία (σε πλάγια γραφή). Για παράδειγµα στο Saccharomyces cerevisiae, ο όρος Saccharomyces αντιπροσωπεύει το γένος, ο όρος cerevisiae το είδος, ενώ χρησιµοποιούνται περισσότερα από 1000 διαφορετικά στελέχη της ζύµης S. cerevisiae ως µαγιές ψωµιού, κρασιού ή µπύρας. Μια κατηγοριοποίηση των µικροοργανισµών, η οποία είναι πρακτική για τα τρόφιµα, είναι η εξής: Α. Βακτήρια, Β. Ζυµοµύκητες, Γ. Ευρωτοµύκητες. Οι µικροοργανισµοί των τροφίµων µπορεί να είναι είτε ανεπιθύµητοι (παθογόνοι ή αλλοιωγόνοι), είτε χρήσιµοι (ζυµώσεις, ωρίµανση). Α. Βακτήρια Πρόκειται για µικροσκοπικούς µονοκύτταρους οργανισµούς, που πολλαπλασιάζονται µε διαίρεση. Είναι ετερότροφοι, αγενείς, χωρίς διάκριτο κυτταρικό πυρήνα, χωρίς 85
94 χλωροφύλλη και µε σφαιρικό (κοκκώδες), ραβδόµορφο ή σπειροειδές σχήµα. Τα σφαιρικά διαιρούνται προς κάθε επίπεδο και διακρίνονται σε διπλόκοκκους, τετράκοκκους, σαρκίνες, στρεπτόκοκκους και σταφυλόκοκκους. Τα ραβδόµορφα διαιρούνται εγκάρσια και διακρίνονται σε λεπτοτριχοειδή κλωστρίδια (διόγκωση στο µέσο) κεφαλοσπόρια (διόγκωση στο άκρο). Τα σπειροειδή είναι σαν τα ραβδόµορφα παρουσιάζουν όµως απολήξεις ή ελικοειδή περιστροφή και διακρίνονται σε δονάκια και σπειρύλια. Τα βακτήρια που παρουσιάζουν σπορίωση ονοµάζονται βάκιλλοι. Σχήµα 3.1. Μορφολογία διαφόρων βακτηρίων Τα βακτήρια, ανάλογα µε τη χρώση τους κατά Gram, διακρίνονται σε θετικά (+) αν η τελική χρώση τους είναι κυανοϊώδης και σε αρνητικά (-) αν είναι κόκκινη. Η χρώση κατά Gram είναι µια διαδικασία προσθήκης διαλυµάτων Α (κρυσταλλοϊώδες σε οινόπνευµα) και Β (Lugol: υδατικό διάλυµα I 2 και ΚΙ) και τέλος φουξίνης. Η χρώση κατά Gram εξαρτάται από τη σύσταση και τη στρωµάτωση του βακτηριακού τοιχώµατος και είναι θεµελιακή ιδιότητα που συνδέεται µε διαφορετική συµπεριφορά όσον αφορά την παθογένεια, την αντοχή στα αντιβιοτικά και άλλους παράγοντες. Η κυτταρική οργάνωση των βακτηρίων παρουσιάζει ορισµένες ιδιαιτερότητες: - ύσκαµπτο κυτταρικό τοίχωµα µε κύριο συστατικό την πεπτιδογλυκάνη (µε επιπλέον πολυσακχαρίτες για τα Gram (+) και πρωτεΐνες και λιποπρωτεΐνες για τα Gram (-) ). - ιαχωρισµός περιεχοµένου σε κυτόπλασµα και πυρηνόπλασµα (κυκλικό διπλής περιελίξεως DNA, χωρίς µεµβράνη και οργανίδια). -Πλασµίδια -Έλλειψη γένους και µείξη κληρονοµικής ουσίας µέσω συζευκτικών µηχανισµών. -Έλυτρο: πηκτώδης περιβάλλουσα πολυσακχαρική µάζα µε γλοιώδη υφή (χαρακτηριστική στα χαλασµένα από βακτήρια τρόφιµα). -Βλεφαρίδες (ή µαστίγια): Εκφύσεις χαρακτηριστικές του βακτηρίου -Σπόρια: συµπύκνωση κυτταρικού υλικού, που αποτελεί ένα µέσο άµυνας των κυττάρων. Τα σπόρια αντέχουν σε υψηλές θερµοκρασίες, ενώ κάτω από ευνοϊκές συνθήκες δίδουν εκ νέου βλαστικά βακτήρια (germination). Όσον αφορά την ταξινόµηση των βακτηρίων, η πιο πρόσφατη και περισσότερο αποδεκτή καλύπτεται από αυτήν των προκαρυωτικών κατά Bergey (1984) σε 17 οµάδες. 86
95 Πρόκειται για µια εµπειρική ταξινόµηση µε βάση τη µορφολογία, τη χρώση κατά Gram, την παθογένεια, το άθροισµα αζωτούχων βάσεων στο DNA, κ.λ.π. Από το σύνολο των βακτηρίων µόνο ορισµένα είδη αφορούν τη βιοµηχανία τροφίµων. Αυτά ανήκουν στις οµάδες 2, 4, 5, 12, 13, 14 και 15. Βάσει της δράσης τους µπορούν πρακτικά να κατηγοριοποιηθούν σε: ΠΑΡΑΓΟΝΤΕΣ ΠΑΘΟΓΟΝΟΥ ΜΟΛΥΝΣΕΩΣ : εκδήλωση παθογένειας δια προσβολής του δέκτη ή µέσω τοξίνης ΠΑΡΑΓΟΝΤΕΣ ΑΛΛΟΙΩΣΕΩΝ : ανεπιθύµητες αλλαγές οργανοληπτικών χαρακτηριστικών, µη παθογόνες, ΠΑΡΑΓΟΝΤΕΣ ΩΦΕΛΙΜΙΣΤΙΚΗΣ ΧΡΗΣΗΣ : για την παραγωγή χρήσιµων για τον άνθρωπο προϊόντων του µεταβολισµού τους όπως γαλακτικό οξύ (σε τρόφιµα όπως γιαούρτια, τυριά, βουτυρόγαλα, ελιές, τουρσιά, πίκλες, σαλάµι αέρος), προπιονικό οξύ ( σε τυριά ελβετικού τύπου Emmenthaler), οξεικό οξύ (παραγωγή ξυδιού) κτλ ΠΙΝΑΚΑΣ 3.1 ΟΜΑ Α 1. Οι Σπειροχαίτες (Spirochetes) Γένη: Spirocaeta, Treponema, Borrelia κ.λ.π. ΟΜΑ Α 2. Αερόβια / Μικροαερόφιλα, Κινούµενα, Ελικοειδή / Βιµπριοειδή. Αρνητικά κατά Gram βακτήρια (Aerobic / Microaerophilic, Motile, Helical / Vibrioid Gram - Negative Bacteria). Γένη: Spirillum, Campylobacter κ.λ.π. ΟΜΑ Α 3. Μη κινούµενα (ή σπανίως κινούµενα), αρνητικά κατά Gram, καµπύλα βακτήρια (Νonmotile or Rarely Motile, Gram Negative Curved Bacteria). ΟΜΑ Α 4. Αρνητικά κατά Gram, αερόβια ραβδία και κόκκοι (Gram Negative Aerobic Rods and Cocci). Οικογένειες: Pseudomonadacae, Halobacteriaceae, Acetobacteriaceae, κ.λ.π. Γένη: Alcaligenes, Brucella κ.λ.π. ΟΜΑ Α 5. Προαιρετικώς αναερόβια αρνητικά κατά Gram ραβδία (Facultatively Anaerobic Gram - Negative Rods). Οικογένειες: Enterobacteriaceae, Vibrionaceae κ.λ.π. Γένη: Zymomonas, Streptobacillus κ.λ.π. ΟΜΑ Α 6. Αναερόβια, αρνητικά κατά Gram, ευθέα, καµπύλα ή ελικοειδή ραβδία (Αναεροβιψ Γραµ - Νεγατιωε Στραιγητ, Ψθρωεδ ανδ Ηελιψαλ Ροδσ). ΟΜΑ Α 7. Αποικοδοµούντατα θειικά και ανάγοντα το θείο βακτήρια (Dissimilatory Sulfate - or - Sulfur - Reducing Bacteria). Γένη: Desulfovibrio, Desulfomonas κ.λ.π ΟΜΑ Α 8. Αναερόβιοι αρνητικοί κατα Gram κόκκοι (Anaerobic Gram - negative Cocci). ΟΜΑ Α 9. Ρικέττσιες και Χλαµύδια (Rickettsias and Chlamydias). ΟΜΑ Α 10. Μυκοπλάσµατα (Mycoplasmas). ΟΜΑ Α 11. Ενδοσυµβιωτές (Endosymbionts). ΟΜΑ Α 12. Κόκκοι θετικοί κατά Gram (Gram - positive Cocci). Οικογένεια: Micrococcaceae. Γένη: Streptococcus, Leuconostoc, Pediococcus Sarcina κ.λ.π. ΟΜΑ Α 13. Σποριογόνα θετικά κατά Gram ραβδία και κόκκοι (Endospore - forming Gram positive Rods and Cocci). Γένη: Bacillus, Clostridium, Sporosarcina κ.λ.π. ΟΜΑ Α 14. Κανονικά ασποριογόνα, θετικά κατά Gram ραβδία (Regular, Non-sporing, Gram - positive Rods). Γένη: Lactobacillus, Listeria, Brochothrix κ.λ.π. ΟΜΑ Α 15. Ακανόνιστα, ασποριογόνα, θετικά κατά Gram ραβδία (Irregular, Nonsporing, Gram- Positive Rods). Γένη: Corynebacterium, Actinomyces, Bifidobacterium κ.λ.π. ΟΜΑ Α 16. Mycobacteria (Μυκοβακτήρια). Οικογένεια: Mycobacteriaceae.Γένος: Mycobacterium. ΟΜΑ Α 17. Nocardioforms (Νοκαρδιότυπα). Γένη: Nocardia, Rhodococcus, Saccharopolyspora κ.λ.π. Τα βακτήρια είναι η κυριότερη πηγή µολύνσεως και αλλοίωσης των τροφίµων. Η συγκριτική υπεροχή τους αυτή έναντι των άλλων µικροβίων οφείλεται: 87
96 I. Στη µεγάλη παραλλακτικότητα των διαφόρων ειδών τους ως προς τις απαιτήσεις σε ph, θρεπτικά συστατικά, θερµοκρασία, ERH. II. Στη δυνατότητα σχηµατισµού ενδοσπορίων III.Στη δυνατότητα αναερόβιας ανάπτυξης IV.Στην έκκριση τοξινών ΠΑΘΟΓΟΝΑ ΒΑΚΤΗΡΙΑ Εµπειρικός κανόνας: Τα Gram ( - ) βακτήρια εκδηλώνουν παθογένεια δια προσβολής του δέκτη (ανθρώπου). Η εκδήλωση των συµπτωµάτων συµβαίνει µετά από τουλάχιστον 24h. Τα συµπτώµατα διαρκούν και καταπονούν αλλά είναι σπανίως θανατηφόρα. π.χ. Salmonellα spp. Εξαίρεση: Τα Escherichia coli είναι Gram ( - ) βακτήρια αλλά παράγουν τοξίνη. Τα Gram (+) βακτήρια εκδηλώνουν παθογένεια µέσω τοξίνης. Η εκδήλωση των συµπτωµάτων συµβαίνει εντός 1-6 ωρών. Τα συµπτώµατα διαρκούν h και καταπονούν αλλά δέν είναι επικίνδυνα π.χ. Staphylococcus aureus. Σηµαντική εξαίρεση στον κανόνα αυτό είναι το Gram (+)Clostridium botulinum που παράγει µια ισχυρότατη θανατηφόρο νευροτοξίνη. Παθογόνα G (-) βακτήρια: Salmonella, spp., Shigella spp., Escherichia coli, Campylobacter jejuni, Vibrio parahemolyticus Βρίσκονται: σε έντερα, κόπρανα, έδαφος, γάλα, κρέας (πουλερικά), θαλασσινά. Είναι δείκτες µη τήρησης ορθής βιοµηχανικής πρακτικής και καλής υγιεινής πρακτικής- Good Manufacturing Practices (GMP) και Good Hygiene Practices (GHP). Ελέγχονται µε θερµική κατεργασία, διαχωρισµό α υλών - ετοίµων, GHP, άλλα "εµπόδια". Παθογόνα G (+) βακτήρια: Clostridium botulinum, Clostridium perfringens, Bacillus cereus, Staphylococcus aureus, Listeria monocytogenes, Bacillus subtilis. Emerging pathogens ( αναδυόµενα παθογόνα: βακτήρια και των δύο παραπάνω κατηγοριών η επικινδυνότητα και η επιδηµιολογική σηµασία των οποίων καθώς και η ανάγκη λήψεως ειδικών µέτρων κατά την παραγωγή των σχετικών τροφίµων αναγνωρίστηκε πρόσφατα): Yersinia enterocolitica, Aeromonas hydrophila, Plesiomonas shigelloides, Vibrio vulnificus, Escherichia coli Ο157 Η7 Στους επόµενους δύο πίνακες δίνονται υπό µορφή συστηµατοποιηµένης βάσης δεδοµένων τα στοιχεία των κυριοτέρων παθογόνων βακτηρίων περιλαµβανοµένων της προέλευσης τους, των τροφίµων που συναντώνται, της επικινδυνότητας τους, της παθογόνου δόσης, περιόδου επώασης και συµπτωµάτων, της µορφολογίας και των συνθηκών ανάπτυξης. Τα στοιχεία αυτά διευκολύνουν την εκτίµηση της επικινδυνότητας και τον ορισµό κρισίµων ορίων και προληπτικών µέτρων, κατά την ανάπτυξη ενός σχεδίου διασφάλισης ασφάλειας (ΗACCP) διεργασίας συγκεκριµµένου τροφίµου. 88
97 89
98 ΠΙΝΑΚΑΣ 3.2. ΠΙΝΑΚΑΣ ΣΤΟΙΧΕΙΩΝ ΠΑΘΟΓΟΝΩΝ ΒΑΚΤΗΡΙΩΝ Βακτήριο Salmonella Listeria monocytogenes Yersinia enterolitica Clostridium botulinum Clostridium perfringens Ιδιότητα Φυσικό περιβάλλον Πουλερικά, κατοικίδια και άγρια ζώα, άνθρωπος, έντοµα, πουλιά Εδαφος, βλάστηση, άνθρωπος, λύµατα, νερό, ζώα (ευρεία διάδοση) Νερό, χοιρίδια, τρωκτικά Εδαφος, φερτές ύλες γλυκού νερού, βλαστηση (ευρεία διάδοση) Εδαφος, θαλάσσια ιζήµατα, σκόνη, περιττώµατα Τρόφιµα σχετιζόµενα Γάλα, ωµά πουλερικά, αυγά,ωµό κρέας γάλα, µαλακά τυριά, ωµό κρέας, παγωτά, λαχανικά γάλα, παγωτά, λαχανικά, ωµό χοιρινό. ανεπαρκώς επεξεργασµένες ή επιµολυσµένες κονσέρβες Κιµάς, πουλερικά, χοιρινό, γαλακτοκοµικά προϊόντα Σηµαντικότητα Παθογόνος δόση Συνήθης υπεύθυνος τροφικής παθογένειας λόγω κακής υγιεινής ή ανεπαρκούς επεξεργασίας Έντονα συµπτώµατα. Σπάνια θανατηφόρο Χαµηλή: 5-24/ml γάλα, 4/kg γάλα σκόνη, 1-5/100gτυρί υνατότητα ανάπτυξης σε Τ ψυγείου. Μικροοργανισµός ευρείας διάδοσης. Θανατηφόρο σε 30% των προσβαλοµένων χαµηλότερη για άτοµα µε επιβαρυµένο ανοσοποιητικό σύστηµα Αυξανόµενος αριθµός κρουσµάτων. Συµπτώµατα παρεµφερή µε κρίση σκωληκοειδίτιδας. Αγνωστη - πιθανόν υψηλή (> 10 6 ) Σπόρια πολύ ανθεκτικά σε θέρµανση - ξήρανση και χηµικούς παράγοντες. Τοξίνη ευαίσθητη στη θέρµανση αλλά πολύ θανατηφόρος. Συνήθης αίτιος τροφικής παθογένειας. Θερµοάντοχα σπόρια. Παράγει τοξίνη αφού εισέλθει στο έντερο διά του µολυσµένου τροφίµου πολύ χαµηλή 0.2 µg τοξίνης Υψηλή /g τροφίµου (8-10 mg τοξίνης) Περίοδος επώασης hr 8 µέρες - 3 µήνες 1-10 µέρες <18-96 ώρες 8-24 ώρες Συµπτώµατα Ναυτία, εµετοί, κοιλιακοί πόνοι, πονοκέφαλοι, ρίγη,πυρετός. ιάρκεια: 2-3 µέρες. Από γρίππης έως µηνιγγίτιδας. Προκαλεί αποβολές. ιάρροια, πυρετός, έµετοι, οξύς πόνος στο δεξί χαµηλό µέρος της κοιλίας. Σκοτοδίνη, διαταραχές όρασης, αδυναµία κατάποσης παράλυση και θάνατος ιάρροια, ναυτία, αέρια Μορφολογία Gram(-) κοντά ραβδία µε περιµετρικές βλεφαρίδες, x µ Gram(+) κοντά ραβδία, x µ Gram(-) κοντά ραβδία, x µ Gram(+) σπορογόνα ραβδία, x µ Gram(+) σπορογόνα ραβδία, x µ Απαιτήσεις σε Ο 2 Προαιρετικά αναερόβιο Αερόβιο ή µικροαερόφιλο Προαιρετικά αναερόβιο Αναερόβιο Αναερόβιο (µπορεί να αναπτυχθεί παρουσία Ο 2 στη λογαριθµική φάση) Θερµοκρασίες ανάπτυξης ( C) Μέγιστη Βέλτιστη 37 Ελάχιστη 5.1 Περιοχή τιµών ph Μέγιστη 9.0 Βέλτιστη Ελάχιστη 4(HCl/κιτρικό) 4.4( γαλακτικό) 5.4(οξεικό) Ελάχιστο aw για ανάπτυξη Μέγιστο % NaCl για ανάπτυξη στους 30 C (ph 5.0 στους 4 C) (µη πρωτεολυτικός τύπος Ε) 10.0(πρωτεολυτικοί τύποι Α,Β...) (µη πρωτεολυτικός τύπος Ε) 4.6 (πρωτεολυτικοί τύποι Α,Β,...) (µη πρωτεολυτικός τύπος Ε) 0.94 (πρωτεολυτικοί τύποι Α,Β,..) (µη πρωτεολυτικός τύπος Ε) 10 (πρωτεολυτικοί τύποι Α,Β,...)
99 Βακτήριο Ιδιότητα Φυσικό περιβάλλον Τρόφιµα σχετιζόµενα Σηµαντικότητα Παθογόνος δόση Staphylococcus aureus Bacillus Cereus Escherichia coli 0157 Η7 έρµα, αµυχές, βλενογόνος. Εδαφος, βλάστηση, γάλα βοοειδή, κοπριά, κρέας, γάλα. Ψάρια, κρέας, γάλα, τυρί, Ρύζι, µπαχαρικά, κρέας, Κιµάς, κρέατα, γάλα. ζυµαρικά, αλλαντικά. γάλα, λαχανικά, ξηροί Μπορεί εύκολα να περάσει από τους ανθρώπους στο τρόφιµο σε συνθήκες µη σωστών χειρισµών. Παράγει θερµοάντοχη τοξίνη. 1 mg τοξίνης (για παραγωγή τοξίνης απαιτούνται 10 6 /g κύτταρα) καρποί. Θερµοάντοχα σπόρια. υνατότητα µόλυνσης µε παραγωγή τοξίνης ή µε πολλαπλασιασµό στο έντερο. Περίοδος επώασης 2-6 ώρες ιαρροϊκή τοξίνη 6-15 ώρες Εµετική τοξίνη 1/2-6 ώρες Συµπτώµατα Ναυτία, έµετοι και διάρροια Ναυτία, έµετοι, διάρροια που διαρκούν 1-2 µέρες Μορφολογία Gram(+) σταφυλόκοκκοι διαµέτρου µ εντεροαιµορραγικό έντονα συµπτώµατα - πιθανόν θανατηφόρα Αγνωστη Αγνωστη Gram(+) σπορογόνα ραβδία x µ 3-9 µέρες Αγνωστη Αιµορραγική κολίτιδα, αιµορραγική διάρριοια, νεφρική ανεπάρκεια, θάνατος. Gram(-) ραβδία x 2-6 µ Aeromonas hydrophila Γλυκά νερό, λύµατα, θαλάσσιο νερό. Θαλασσινά, κόκκινο κρέας, πουλερικά, γάλα. Ασθενείς µε επιβαρυένο ανοσοποιητικό σε κίνδυνο. υνατότητα ανάπτυξης σε Τ ψυγείου παράγει δύο τύπους τοξίνης. ιάρροια, έµετοι, κοιλιακοί πόνοι, πυρετός. Μπορεί να προκαλέσει µηνιγγίτιδα και σηψαιµία. Gram(-) ραβδία µε στρογγυλεµένα άκρα x µ Απαιτήσεις σε Ο 2 Προαιρετικά αναερόβιο Προαιρετικά αναερόβιο Προαιρετικά αναερόβιο Προαιρετικά αναερόβιο Θερµοκρασίες Μέγιστη ανάπτυξης ( C) Βέλτιστη Ελάχιστη 7-11 Περιοχή τιµών ph Μέγιστη Βέλτιστη Ελάχιστη 4.0 Ελάχιστο aw για ανάπτυξη Μέγιστο % NaCl για ανάπτυξη 0.86 (για παραγωγή τοξίνης 0.9) 18.2 (για παραγωγή τοξίνης 10%) άγνωστη
100 Β. Ζυµοµύκητες Πρόκειται για ελλειψοειδείς, σφαιρικούς ή ραβδόµορφους µικροοργανισµούς. Το µέγεθός τους ποικίλλει από 2-6 µm, ενώ ο πολλαπλασιασµός τους γίνεται µε εκβλάστηση, διχοτόµηση (σχιζοµύκητες) ή σπορογονία (δυσµενείς συνθήκες). Μπορεί να είναι σπορογόνοι ή και άσποροι. Η κυτταρική οργάνωση των ζυµοµυκήτων περιλαµβάνει: -Κυτταρικό τοίχωµα από ηµικυτταρίνη, χιτίνη. (Συχνά γλοιώδες περίβληµα που προκαλεί συγκόλληση). -Κυτταρική µεµβράνη -Κυτταρόπλασµα µε πυρήνα, χυµοτόπια και σπειρωτά κοκκία. Οι ζυµοµύκητες είναι αερόβιοι, ανθεκτικοί σε χαµηλό ph και ενεργότητα νερού, αλλά είναι ευαίσθητοι στη θερµοκρασία. Οι ζυµοµύκητες προκαλούν αλλοιώσεις, αλλά όχι παθογένεια. Γ. Ευρωτοµύκητες (Μούχλες) Είναι πολυκύτταροι µικροοργανισµοί νηµατοειδούς µορφής. Όσον αφορά την οργάνωσή τους, αποτελούνται από ένα βλαστικό κι ένα καρποφόρο µέρος. Το βλαστικό µέρος περιλαµβάνει διακλαδωµένα νηµατοειδή κύτταρα (νηµατώδη υφή) που σχηµατίζουν µυκήλια. Το καρποφόρο µέρος αποτελεί µια νηµατώδης υφή που σχηµατίζει σπόρια (γονιδιοφόρος). Οι ευρωτοµύκητες όπως και ζυµοµύκητες είναι αερόβιοι, ανθεκτικοί σε χαµηλές θερµοκρασίες, χαµηλό ph και ενεργότητα νερού, και συνήθως ευαίσθητοι σε ψηλές θερµοκρασίες. Σχήµα 3.2. Aspergillus niger a) Γονίδια b)μυκήλιο µε γονιδιοφόρα c)γονιδιοφόρα d,e) ιακλαδωµένα στηρίγµατα 92
101 Οι ευρωτοµύκητες διακρίνονται σε παθογόνους και κοινούς. Οι τελευταίοι µπορεί να είναι ευρωτοµύκητες εδάφους, αλλοίωσης ή ωφέλιµοι (ωρίµανση τυριού, οργανικά οξέα, αντιβιοτικά, ένζυµα). Οι ευρωτοµύκητες που αναπτύσσονται στα τρόφιµα δεν είναι παθογόνοι µε εξαίρεση την κάτω από ορισµένες ακραίες συνθήκες κακής πρακτικής δυνατότητα παραγωγής από ορισµένους µυκοτοξινών που είναι ιδιαίτερα τοξικές. Οι κυριότερες µυκοτοξίνες είναι: Αφλατοξίνες ( από Aspergillus flavus και Aspergillus parasiticus) Τύποι: B 1, B 2, G 1, G 2 (σε ξηρούς καρπούς, δηµητριακά) και Μ 1, Μ 2 (µεταβολίτες των Β 1, Β 2 σε γάλα) Με αποθήκευση σε υγρές συνθήκες ή ανάπτυξη του καρπού σε συνθήκες ξηρασίας. Προκαλούν ηπατοπάθειες. Οχρατοξίνες ( από Aspergillus ochraceus, Penicillium spp.) Σε καλαµπόκι, φασόλια, φυστίκια. Προκαλούν νεφροπάθειες. Πατσουλίνη (patulin) (από Penicillium) Σε µουχλιασµένα φρούτα, φρουτοχυµούς. Καρκινογόνο, αιµοραγίες. Τριχοθεσίνες (trichothecenes) (Fusarium graminearum) Τύποι: Ζεαραλινόνη, δεοξυνιβαλενόλη (DON). Σε σίτο, καλαµπόκι Συνθήκες ανάπτυξης των µικροβίων στα τρόφιµα Τα µικρόβια, όπως αναφέρθηκε, είναι διαδεδοµένα παντού. Τα τρόφιµα όµως φέρουν κατά κανόνα µεγαλύτερο µικροβιακό φορτίο απ' ότι οι άλλες µορφές οργανικής και πολύ περισσότερο ανόργανης ύλης. Οι διάφορες πηγές µόλυνσης των τροφίµων είναι οι εξής: 1) ο άνθρωπος, 2) το πεπτικό σύστηµα αγροτικών ζώων, 3) τα έντοµα (µύγες, κολεόπτερα), 4) τα τρωκτικά, 5) τα σπλάχνα και τα βράγχια θαλασσινών, 6) τα αστικά λύµατα, 7) η κοπριά των ζώων, 8) η σκόνη, 9) το έδαφος, 10) το νερό. Η µόλυνση όµως του τροφίµου µε µικροργανισµούς δεν συνεπάγεται αναγκαστικά και την αλλοίωσή του. Για να αλλοιώσουν το τρόφιµο που έχουν µολύνει, θα πρέπει τα µικρόβια να αυξηθούν σε αριθµό (να πολλαπλασιαστούν). Για να είναι εφικτός όµως ο πολλαπλασιασµός των µικροβίων πρέπει να συντρέξουν ορισµένες προϋποθέσεις και να εξασφαλισθούν ορισµένες περιβαλλοντικές συνθήκες. Ο απρόσκοπτος πολλαπλασιασµός των µικροβίων επιζητείται στις καλλιέργειες που έχουν ως στόχο την εκτίµηση του µικροβιακού φορτίου ενός τροφίµου, στις επιθυµητές και ελεγχόµενες από τον άνθρωπο ζυµώσεις και οξειδώσεις και όταν τα µικρόβια χρησιµοποιούνται στην παρασκευή µονοκυτταρικής πρωτεΐνης (single cell protein). 93
102 Αντίθετα, για τη συντήρηση των τροφίµων µε οποιαδήποτε µέθοδο, επιζητείται η παρεµπόδιση του πολλαπλασιασµού των µικροβίων. Γενικά οι παράγοντες που επηρεάζουν τον µεταβολισµό και κατ' επέκταση τον πολλαπλασιασµό των µικροβίων στα τρόφιµα διακρίνονται σε: α) ενδογενείς, που σχετίζονται µε τη σύσταση του τροφίµου (ph, Eh, a w, θρεπτικά συστατικά, αντιµικροβιακοί παράγοντες, ανταγωνιστική χλωρίδα) και β) εξωγενείς, που σχετίζονται µε τις συνθήκες συντήρησης (Τ, RH, P, p O2, p CO2, κ.λ.π.) Οι παράγοντες που επηρεάζουν, ή ορθότερα, προσδιορίζουν το ρυθµό πολλαπλασιασµού των µικροβιακών κυττάρων, βρίσκονται σε συνεχή µεταξύ τους αλληλεξάρτηση και αλληλεπίδραση. Έτσι, το τελικό αποτέλεσµα δεν εξαρτάται µόνο από την απόλυτη τιµή καθενός από τους υπεύθυνους για την ανάπτυξη των µικροβίων παράγοντες, αλλά και από τον βαθµό στον οποίο ο παράγοντας αυτός επηρεάζει ή επηρεάζεται από όλους τους άλλους. Για κάθε παράγοντα που επηρεάζει τον πολλαπλασιασµό των κυττάρων οποιουδήποτε µικροβίου, έχουν προσδιορισθεί τρεις τιµές, η ελάχιστη (minimum), η άριστη (optimum) και η µέγιστη (maximum). Οι τιµές αυτές για κάποιους µικροοργανισµούς για τη θερµοκρασία, το ph και την ενεργότητα του νερού φαίνονται αντίστοιχα στους πίνακες 3.3, 3.4, και 3.5. Τα κύτταρα του µικροβίου πολλαπλασιάζονται σ' όλο το εύρος της διακυµάνσεως, µεταξύ των δύο ακραίων τιµών, ο ρυθµός όµως του πολλαπλασιασµού µειώνεται συνεχώς µε την µετακίνηση από το µέσο προς τα δύο άκρα. Η φάση δηλαδή της καθυστέρησης (lag phase) και ο χρόνος µέσα στον οποίο ολοκληρώνεται µια κυτταρική διαίρεση επιµηκύνεται συνεχώς µέχρι που πρακτικά ο πολλαπλασιασµός των κυττάρων και ο µεταβολισµός µηδενίζονται υπό αντίξοες συνθήκες. Πίνακας 3.3 Ευρος διακύµανσης της θερµοκρασίας αναπτύξης για επιλεγµένα µικρόβια Μικροοργανισµοί Θερµοκρασία ( C) Minimum Optimum Maximum Bacteria 5-42 Acetobacter Aeromonas Bacillus cereus 5-42 Brevibacterium Clostridium C. botulinum C. perfringens C. thermosaccharolyticum Escherichia coli Lactobacillus Leuconostoc Micrococcus Moraxella
103 Propionibacterium Proteus Pseudomonas P. aeruginosa 8-42 P. fluorescens Salmonella Staphylococcus S. aureus Streptococcus cremoris S. faecalis S. lactis S. thermophilus Vibrio V. parahaemolyticus Xanthomonas Yersinia enterocolitica Molds Aspergillus fumigatus Botrytis cinerea Cladosporium Penicillium rubrum Rhizopus stolonifer 5-25 Yeasts Candida C. lipolytica Hansenula Saccharomyces Torulopsis Πίνακας 3.4 ιακύµανση της τιµής του ph για την ανάπτυξη επιλεγµένων µικροβίων Oργανισµός ph Minimum Optimum Maximum Bacteria (most) Acetobacter Bacillus subtilis Clostridium botulinum C. perfringens C. sporogenes Erwinia carotovora Escherichia coli Gluconobacter oxydans Lactobacillus (most) L. acidophilus L. plantarum Leuconostoc cremoris L. oenos Pediococcus cerevisiae Propionibacterium Proteus vulgaris Pseudomonas (most) P. aeruginosa Salmonella (most) S. typhi S. choleraesuis Srratia marcescens
104 Staphylococcus aureus Streptococcus lactis Vibrio V. cholerae V. parahaemolyticus Yeasts Hansenula Kluyveromyces Pichia Saccharomyces cerevisiae S. rouxii Molds Aspergillus niger A. oryzae Botrytis cinerea Mucor Penicillium Rhizopus nigricus
105 Πίνακας 3.5 Ελάχιστη τιµή a w για την ανάπτυξη διαφόρων µικροοργανισµών Οργανισµός minimum a w Σπουδαιότερα βακτήρια προκαλούντα αλλοιώσεις Acinrtobacter Aeromonas Alcaligenes Arthrobacter Bacillus B. cereus Citrobacter Clostridium botulinum Type A Type B Type E C. perfringens Corynebacterium Enterobacter Escherichia coli Flovobacterium Klebsiela Lactobacillus Leuconostoc Micrococcus M. roseus Pseudomonas aeruginosa P. fluorescens Salmonella Streptococcus Staphylococcus albus S. aureus Vibrio parahaemolyticus Halophilic bacteria 0.75 Most yeasts Osmophilic yeasts Most molds Xeromyces bisporus Aspergillus A. glaucus A. flavus A. halophilicus 0.68 A. niger Botrytis cinereea 0.93 Debaryomyces Fusarium Hansenula Mucor Penicillium Rhodotorula Saccharomyces cerevisiae S. rouxii Xerophilic molds
106 Θερµοκρασία: Η θερµοκρασία αποτελεί πιθανώς τον σπουδαιότερο περιβαλλοντικό παράγοντα που επηρεάζει την ανάπτυξη, αλλά και τη δραστικότητα των διαφόρων τύπων µικροβίων. Γενικά, η µικροβιακή ανάπτυξη µπορεί να λάβει χώρα σ' όλη την κλίµακα µεταξύ -8 C και 90 C. Συνήθως η ανάπτυξη και ο πολλαπλασιασµός των µικροβίων λαµβάνει χώρα σε θερµοκρασιακό εύρος περίπου 40 C, χαρακτηριστικό για κάθε µικρόβιο (δηλαδή Τ max - T min 40 C). Τα µικρόβια, µε βάση το εύρος διακύµανσης της θερµοκρασίας µέσα στο οποίο µπορούν να αναπτυχθούν, χωρίζονται σε τέσσερις οµάδες, δηλαδή τα θερµόφιλα, τα µεσόφιλα, τα ψυχρόφιλα και τα ψυχρότροφα, όπως παρουσιάζονται στον πίνακα 3.6. Πίνακας 3.6: Κατηγορία µικροβίων ιακύµανση της θερµοκρασίας αναπτύξεως στις διάφορες κατηγορίες µικροβίων Θερµοκρασία ( C) Ελαχίστη Αρίστη Μεγίστη Θερµόφιλα Μεσόφιλα Ψυχρόφιλα -5 έως Ψυχρότροφα 0 έως Μέθοδοι απαρίθµησης µικροοργανισµών Υπάρχουν αρκετές διαδικασίες οι οποίες µπορούν να χρησιµοποιηθούν για τον υπολογισµό ενός µικροβιακού πληθυσµού. Αυτές περιλαµβάνουν: µικροσκοπικές µετρήσεις, ηλεκτρονικές µετρήσεις σωµατιδίων, µετρήσεις σε τρυβλία (pour or spread plates), διάλυση (αραίωση) σε σωλήνες (tube dilution), τεχνική του πιο πιθανού αριθµού µικροβίων (ΜΡΝ), καλλιέργεια από µεµβράνη διήθησης, χηµικούς δείκτες, τριφωσφορική αδενοσίνη (ΑΤΡ), µέθοδοι οπτικής πυκνότητας, κ.ά. Ένα ιδανικό τεστ πρέπει να είναι ακριβές, γρήγορο, χρήσιµο για τους περισσότερους τύπους δειγµάτων και όχι ακριβό. 1. Κατ' ευθείαν µέτρηση στο µικροσκόπιο (Direct Microscopic Count, DMC) Η DMC είναι µια άµεση µέθοδος, η οποία όµως µετρά τον συνολικό αριθµό των κυττάρων χωρίς να διακρίνει τα ζωντανά από τα νεκρά κύτταρα. Με τη µέθοδο αυτή τα αποτελέσµατα αποκτούνται νωρίτερα από οποιαδήποτε άλλη διαδικασία αφού δεν χρειάζεται περίοδος επώασης για τον µεταβολισµό και τον πολλαπλασιασµό των κυττάρων. Πρόκειται δηλαδή για µια ταχεία µικροβιολογική µεθοδο, εφόσον ο υπολογισµός του βακτηριακού φορτίου γίνεται σε µικρό χρονικό διάστηµα, η οποία επιτρέπει την άµεση επέµβαση στον χειρισµό της διεργασίας για την αποκατάσταση οποιουδήποτε προβλήµατος. Η άµεση παρατήρηση και απαρίθµηση των µικροοργανισµών σε γνωστό όγκο τροφίµου είναι η ποσοτική αρχή στην οποία βασίζεται η DMC. Στα υγρά τρόφιµα ο προσδιορισµός είναι άµεσος, ενώ τα στερεά τρόφιµα πρέπει να διαλυθούν κατάλληλα πριν την ανάλυση. Κατά τη µέθοδο αυτή, µια γνωστή ποσότητα τροφίµου απλώνεται οµοιόµορφα σε µια προκαθορισµένη περιοχή πάνω σε πλάκα µικροσκοπίου. Το φιλµ ξηραίνεται, σταθεροποιείται, βάφεται µε χρωστική και ο αριθµός των µικροβίων προσδιορίζεται µε τη βοήθεια του µικροσκοπίου. Παρά τα πλεονεκτήµατα της DMC η εφαρµογή της περιορίζεται σε δείγµατα µε υψηλό αριθµό µικροβίων, ενώ δεν δίνει πληροφορίες για δείγµατα µε χαµηλό αριθµό µικροοργανισµών. Επίσης 98
107 µετρά και τα νεκρά και τα ζωντανά κύτταρα. Το γεγονός ότι εξετάζεται µόνο µικρή ποσότητα τροφίµου περιορίζει την ακρίβεια της µεθόδου. Η αξία της DMC εξαρτάται από το είδος του τροφίµου και των µικροοργανισµών που σχετίζονται µε το τρόφιµο. Έτσι, για προϊόντα που έχουν υποστεί κατεργασία για τον έλεγχο των µικροβίων, όπως π.χ. θέρµανση, είναι αµφίβολο αν η DMC µπορεί να προβλέψει την διατηρησιµότητα του προϊόντος ή να προσδιορίσει την επικινδυνότητά του για τη δηµόσια υγεία 2. Ηλεκτρονική µέτρηση σωµατιδίων (Coulter) Ο ηλεκτρονικός µετρητής βασίζεται στην αρχή ότι τα κύτταρα έχουν µικρή ηλεκτρική αγωγιµότητα σε σχέση µ' ένα ηλεκτρολυτικό διάλυµα. Ένα διάλυµα µικροβιακών κυττάρων σε κατάλληλο ηλεκτρολύτη φέρεται δια µέσου ενός ανοίγµατος, το οποίο µεταφέρει ηλεκτρικό ρεύµα µεταξύ δύο ηλεκτροδίων. Τα κύτταρα που περνούν µέσα από το άνοιγµα εκτοπίζουν ίσο όγκο διαλύµατος προκαλόντας παλµούς ανάλογους του µεγέθους ή του όγκου τους που ενισχύονται και µετρώνται. Η µέθοδος αυτή µετράει επίσης τον συνολικό αριθµό των κυττάρων κι όχι των ζωντανών. 3. Μέθοδοι µέτρησης αριθµού ζωντανών κυττάρων Υπάρχουν αρκετές µέθοδοι που έχουν σχεδιασθεί για τον υπολογισµό του αριθµού των ζωντανών µικροοργανισµών. Μερικές απ' αυτές είναι: 3.1. Αερόβια µέτρηση σε τρυβλία (aerobic plate count) Η µέθοδος αυτή (pour plate count) είναι η πιο συνηθισµένη τεχνική για την µέτρηση των ζωντανών µικροοργανισµών στα τρόφιµα. Βασίζεται στην υπόθεση ότι τα µικροβιακά κύτταρα που υπάρχουν σε ένα δείγµα αναµειγµένο µε άγαρ και θρεπτικά υλικά (πεπτόνες (αλµπουµίνη, πεπτόνη, πολυπεπτίδια, αµινοξέα), εκχύλισµα κρέατος (πεπτόνες + P, k), ζελατίνη, CHO, ανόργανα συστατικά), σχηµατίζουν ξεχωριστές και ορατές αποικίες. H µέθοδος όµως αυτή δεν µετρά απαραίτητα τον πραγµατικό συνολικό αριθµό των ζωντανών κυττάρων ανά γραµµάριο δείγµατος, αφού τα βακτηριακά κύτταρα υφίστανται µόνα τους ή σε ζευγάρια, αλυσίδες, συµπλέγµατα και οµάδες. Έτσι, οι µετρήσεις που προκύπτουν από τη µέθοδο αυτή δεν πρέπει να αναφέρονται ως µετρήσεις ζωντανών κυττάρων, αλλά ως µετρήσεις αποικιών ανά µονάδα ή µονάδες σχηµατισµού αποικιών ανά µονάδα (Colony Forming Units, cfu). Επίσης χρησιµοποιείται ο όρος TPC (Total Plate Count). Η διαδικασία είναι σχετικά απλή. Κατάλληλες αραιώσεις του δείγµατος, ώστε τελικά να έχουµε αριθµό CFU µεταξύ 30 και 300, απλώνονται σ' ένα αποστειρωµένο τρυβλίο Petri και προστίθεται αποστειρωµένο, τηγµένο, ψυχρό άγαρ. Αν πρόκειται να προσδιοριστούν ειδικοί τύποι µικροβίων, εκτός των θρεπτικών υλικών το άγαρ φέρει και ουσίες που επιτρέπουν επιλεκτικά την ανάπτυξη των προς µέτρηση µικροοργανισµών (εκλεκτικό υπόστρωµα). Το άγαρ πρέπει να αναµειχθεί πλήρως µε το εµβόλιο για να κατανεµηθούν τα κύτταρα οµοιόµορφα. Ύστερα από την στερεοποίηση, τα τρυβλία αναποδογυρίζονται για να εµποδίσουν την συµπύκνωση της υγρασίας στην επιφάνεια του άγαρ και στη συνέχεια επωάζονται. Η θερµοκρασία και ο χρόνος της επώασης ποικίλλουν ανάλογα µε το είδος του µικροοργανισµού που ο ερευνητής θέλει να απαριθµήσει (ψυχρότροφα, µεσόφιλα ή θερµόφιλα). Η διαδικασία αυτή (pour plate count) είναι απλή, µπορεί να καλύψει µία ευρεία περιοχή συγκεντρώσεων και προς το παρόν είναι ίσως η πιο ακριβής µέθοδος για τον προσδιορισµό των βακτηρίων που αναπτύσσονται σε άγαρ. Επίσης, οι µικροοργανισµοί µπορούν να ανακτηθούν για παραπέρα µελέτη. Τα αποτελέσµατα πρέπει να αντικατοπτρίζουν το επίπεδο των ζωντανών µικροβίων του τροφίµου τη χρονική στιγµή που πάρθηκε το δείγµα. Υπάρχουν όµως και πολλές πλευρές της µεθόδου αυτής οι οποίες είναι ανεπιθύµητες. Αυτές που µας ενδιαφέρουν κυρίως είναι ο χρόνος, το κόστος, οι τεχνικές απαιτήσεις, οι πληροφορίες που αποκτούνται και η ακρίβεια. Έτσι, η περίοδος επώασης µπορεί να κυµαίνεται από δύο έως δέκα ηµέρες, έτσι ώστε οι µικροοργανισµοί να µπορούν να παράγουν µία ορατή αποικία πριν την απαρίθµηση. Η µέθοδος αυτή είναι αρκετά ακριβή. Αν και η τεχνική αυτή φαίνεται αρκετά απλή, στην πραγµατικότητα χρειάζεται ένας πολύ καλά εκπαιδευµένος τεχνικός για να πραγµατοποιήσει αυτό το τεστ. Η ακρίβεια εποµένως της µεθόδου εξαρτάται από την ικανότητα του τεχνικού, όσο κι από τις παραδοχές και τα σφάλµατα που περικλείονται στην συγκεκριµένη µέθοδο. 99
108 Μια παραλλαγή της παραπάνω µεθόδου είναι η επιφανειακή ανάπτυξη σε τρυβλία (spread plate count). Στο σύστηµα αυτό, το αποστειρωµένο, τηγµένο και ψυχρό άγαρ απλώνεται πρώτα σε αποστειρωµένο τρυβλίο Petri. Ύστερα από την στερεοποίηση, τα τρυβλία προεπωάζονται κατά τη διάρκεια της νύχτας. Η επώαση ξηραίνει την επιφάνεια του άγαρ, έτσι ώστε οι µικροοργανισµοί να µην συνενωθούν κατά το άπλωµά τους πάνω στο άγαρ. Η µέθοδος αυτή παρουσιάζει κάποια σηµαντικά πλεονεκτήµατα σε σχέση µε την κλασσική µέθοδο απαρίθµησης σε τρυβλία (pour plate count). Έτσι, δεν είναι απαραίτητη η χρήση ηµιδιαφανούς µέσου, όπως στην κλασσική µέθοδο για την διευκόλυνση της εύρεσης των αποικιών. Η µορφολογία των αποικιών µπορεί να παρατηρηθεί καλύτερα στις επιφανειακές αποικίες, βελτιώνοντας την ικανότητα του αναλυτή να διακρίνει ανάµεσα σε διαφορετικά είδη αποικιών. Οι µικροοργανισµοί δεν εκτίθενται στην θερµότητα του τηγµένου άγαρ που µπορεί σε ορισµένες περιπτώσεις να οδηγήσει σε χαµηλότερες τιµές µετρήσεων. Απ' την άλλη µεριά, η µέθοδος αυτή υστερεί σε ακρίβεια για δείγµατα που περιέχουν λίγους µικροοργανισµούς, αφού πρέπει να χρησιµοποιηθούν σχετικά µικροί όγκοι δείγµατος Καλλιέργεια από µεµβράνη διήθησης (membrane filters) Όταν γίνεται διήθηση ρευστών µέσα από µεµβράνη, όλα τα σωµατίδια, βακτήρια ή κύτταρα, που είναι µεγαλύτερα από τους πόρους κατακρατούνται στην επιφάνεια της µεµβράνης. Τα µικροβιακά κύτταρα που έχουν κατακρατηθεί µπορούν να εξεταστούν και να µετρηθούν µ' ένα µικροσκόπιο µε τρόπο παρόµοιο της DMC. Οι µικροοργανισµοί που κατακρατήθηκαν µπορούν να καλλιεργηθούν αν η µεµβράνη µεταφερθεί ασηπτικά σ' ένα αποστειρωµένο τρυβλίο Petri, µε υγρά θρεπτικά συστατικά διπλής αξίας που διαχέονται µέσα από την πορώδη µεµβράνη και εφοδιάζοντας τους ώστε να αναπτυχθούν. Ύστερα από επώαση έξι έως οχτώ ωρών οι αποικίες µπορούν να µετρηθούν µε ένα µικροσκόπιο ιάλυση σε σωλήνες (tube dilution) H µέθοδος αυτή περιλαµβάνει βασικά τον εµβολιασµό µιας σειράς σωλήνων, που περιέχουν αποστειρωµένο θρεπτικό ζωµό, µε µια σειρά διαλυµάτων του τροφίµου. Ύστερα από την επώαση των εµβολιασµένων σωλήνων, ο ζωµός παρατηρείται ως προς τη θολότητα η οποία υποδεικνύει την ανάπτυξη των µικροοργανισµών. Αν δεν υπάρχει καθόλου θολότητα, τότε συµπεραίνεται ότι δεν υπήρχαν µικροοργανισµοί ή δεν µπόρεσαν να πολλαπλασιαστούν. Συνήθως συνδιάζεται µε την επόµενη τεχνική Τεχνική του πιο πιθανού αριθµού µικροβίων (Most Probable Number, ΜΡΝ) Η τεχνική αυτή βασίζεται στην παραδοχή ότι τα διάφορα δείγµατα του ιδίου βάρους ή όγκου που προέρχονται από την ίδια πηγή θα πρέπει να περιέχουν κατά µέσο όρο τον ίδιο αριθµό µικροβίων που είναι ο περισσότερο πιθανός αριθµός µικροβίων που αποτελούν τη µικροχλωρίδα της αρχικής πηγής (τρόφιµο ή πόσιµο νερό). Χρησιµοποιώντας αρκετούς σωλήνες για κάθε διάλυµα και καταγράφοντας τους σωλήνες που παρουσιάζουν ανάπτυξη των µικροβίων (θετικοί) κι αυτούς που δεν παρουσιάζουν (αρνητικοί), παίρνουµε έναν πιο ακριβή αριθµό των παρόντων µικροοργανισµών. Η σχέση ανάµεσα στους θετικούς και τους αρνητικούς σωλήνες έχει προσδιορισθεί µαθηµατικά κι έτσι έχουν προκύψει οι πίνακες του πιο πιθανού αριθµού µικροβίων. Για τη χρήση της µεθόδου αυτής χρειάζονται τουλάχιστον τρία διαλύµατα. Στην ιδανική περίπτωση, οι σωλήνες µε την µικρότερη αραίωση πρέπει να είναι θετικοί, ενώ αυτοί µε τη µεγαλύτερη αρνητικοί. Όσο περισσότεροι σωλήνες χρησιµοποιούνται σε κάθε διάλυµα, τόσο πιο ακριβής είναι ο υπολογισµός, αλλά για λόγους ευκολίας έχει καθιερωθεί η χρήση µιας σειράς τριων ή πέντε σωλήνων. Ύστερα από την επιλογή των τριων σειρών διαλυµάτων, πρέπει κανείς να συµβουλευτεί τον κατάλληλο ΜΡΝ πίνακα, να βρει τον πιο πιθανό αριθµό µικροβίων που ικανοποιεί τον αριθµό των θετικών σωλήνων και να τον πολλαπλασιάσει µε τον συντελεστή διάλυσης, ώστε να προκύψει ο πιο πιθανός αριθµός µικροβίων ανά γραµµάριο προϊόντος. Η µέθοδος ΜΡΝ είναι λιγότερο ακριβής από τις µεθόδους µέτρησης σε τρυβλία, αλλά είναι πιο εύκολη και απλή από αυτές. Η µέθοδος αυτή είναι ιδιαίτερα χρήσιµη για δείγµατα µε λίγους µόνο µικροοργανισµούς και µπορεί να χρησιµοποιηθεί για τον προσδιορισµό µικροοργανισµών σε δείγµατα µεγαλύτερα του ενός gr. 4. Μέθοδοι που βασίζονται στο µεταβολισµό των µικροοργανισµών 100
109 Ο µεταβολισµός των µικροοργανισµών και η παραγωγή µεταβολικών προϊόντων στα τρόφιµα µπορεί να µετρηθεί και να χρησιµοποιηθεί για τον υπολογισµό του βακτηριακού πληθυσµού ή της µικροβιακής ποιότητας των τροφίµων. Μερικές από τις µεθόδους που βασίζονται στο µεταβολισµό είναι: -Οι χηµικοί δείκτες αποσύνθεσης (Chemical Indicators of Decomposition) Τα τρόφιµα συντίθενται από ποικίλλες χηµικές ενώσεις, οι οποίες υπόκεινται σε διάφορες βιοχηµικές µεταβολές, επιθυµητές ή όχι. Η αποσύνθεση των τροφίµων που οδηγεί σε αλλοίωση της ποιότητάς τους αποτελεί µια ανεπιθύµητη µεταβολή. Ένα πλήθος χηµικών ουσιών έχουν µελετηθεί ως δείκτες της αλλοίωσης αυτής της ποιότητας των τροφίµων. Ο βαθµός της µεταβολικής δραστηριότητας µπορεί να σχετίζεται ή να µην σχετίζεται µε τον αριθµό των παρόντων µικροοργανισµών. -Τα φυσικά τεστ Η µικροβιακή ανάπτυξη προκαλεί µεταβολές στα τρόφιµα, όπως στην περιεκτικότητα των οξέων ή στο ph. Καθώς το ph αλλάζει, µεταβάλλεται και η ικανότητα των πρωτεϊνών για την δέσµευση του νερού. Η διαφορά αυτή µπορεί να προσδιορισθεί µε το ΕRV τεστ (Extract Release Volume). -Η τριφωσφορική αδενοσίνη Κατά τη διάρκεια του µεταβολισµού, τα κύτταρα σχηµατίζουν φωσφορικούς δεσµούς υψηλής ενέργειας, η οποία αποθηκεύεται στο ΑΤΡ. Το ΑΤΡ στα βακτηριακά κύτταρα εξαφανίζεται όταν αυτά πεθαίνουν. Απ' τη στιγµή που όλα τα ζωντανά βακτηριακά κύτταρα περιέχουν ΑΤΡ είναι δυνατός ο υπολογισµός του αριθµού των κυττάρων µε την ποσοτικοποίηση του ΑΤΡ σ' ένα σύστηµα. 5. Άλλες µέθοδοι Εκτός από τις µεθόδους που περιγράφηκαν, πολλά άλλα συστήµατα χρησιµοποιήθηκαν από τους µικροβιολόγους για την ανάπτυξη ταχείων µεθόδων για τον προσδιορισµό των µικροβίων. Μερικές από αυτές είναι: η αέρια χρωµατογραφία ή η αέρια-υγρή χρωµατογραφία, η µέτρηση της ηλεκτρικής αντίστασης, που επηρεάζεται από την µεταβολή στην σύνθεση του υποστρώµατος ανάπτυξης λόγω της µεταβολικής δραστηριότητας, η µικροσκοπία φθορισµού, ο προσδιορισµός του βάρους ή της µάζας των κυττάρων, της οπτικής πυκνότητας ή της θολότητας, κ.ά. Ταχείες µικροβιολογικές µέθοδοι Τα τελευταία 20 χρόνια, η µεγαλύτερη προσπάθεια έχει συγκεντρωθεί στην εξέλιξη ταχείων µικροβιολογικών µεθόδων για τον έλεγχο των τελικών προϊόντων, των συστατικών, του εξοπλισµού και του περιβάλλοντος κατά την διαδικασία παραγωγής. Οι ταχείες µικροβιολογικές µέθοδοι βασίζονται σε ενόργανες και βιοτεχνολογικές µεθόδους. Απ' τη µια µεριά, οι µέθοδοι αυτές διευκολύνουν σηµαντικά ελέγχους ρουτίνας, ενώ απ' την άλλη απαιτούν σηµαντικά αυξηµένη ευαισθησία της µεθοδολογίας, η οποία συχνά συγκρούεται µε την απαιτούµενη ταχύτητα. Στην πραγµατικότητα, ένας αναλυτής αναζητά τουλάχιστον πέντε στοιχεία στις µεθόδους που αποσκοπούν στην εκτίµηση της µικροβιολογικής ακεραιότητας δειγµάτων τελικών προϊόντων ή της συµµόρφωσης των δειγµάτων γραµµής µε κάποια πρότυπα υγιεινής. Τα στοιχεία αυτά είναι: (1) ευκολία, (2) ταχύτητα, (3) αξιοπιστία, (4) πραγµατικές εγγυήσεις για την αποφυγή λαθών και (5) µηχανοποίηση ή και αυτοµατοποίηση. Οι ταχείες µικροβιολογικές µέθοδοι έχουν όµως κι αυτές µειονεκτήµατα. Απαιτούν ανάπτυξη των µικροοργανισµών σε υψηλά επίπεδα προτού τα αποτελέσµατα είναι φανερά. Η πλειοψηφία των σηµαντικών µικροοργανισµών υφίστανται µε την επεξεργασία του τροφίµου τραυµατισµό, σαν αποτέλεσµα της έκθεσής τους σε αντίξοες εξωτερικές συνθήκες, άµεσα, όπως µε την θέρµανση, ή έµµεσα, όπως µε την ελάττωση του ph ή της ενεργότητας του τροφίµου. Το γεγονός αυτό οδηγεί σε λανθασµένα χαµηλά αποτελέσµατα κι εποµένως στην αποτυχία να πάρουµε διορθωτικά µέτρα, όπου αυτά απαιτούνται. Ένα άλλο µειονέκτηµα σχετίζεται µε την ίδια την φύση των τροφίµων. Μέθοδοι που δουλεύουν αξιοσηµείωτα καλά µε απλές καλλιέργειες ή µικροοργανισµούς στόχους, απέτυχαν αρχικά όταν εφαρµόστηκαν σε πραγµατικά δείγµατα τροφίµων λόγω παρουσίας σε πολλά τρόφιµα 101
110 µολυσµατικού απαγορευτικού υλικού. Τέτοιες παρεµβολές ξεπερνώνται µε προηγούµενη συµπύκνωση και καθαρισµό των µικροοργανισµών στόχων, σε βάρος όµως της απλότητας και της ταχύτητας. Τέλος οι νέες ταχείες µέθοδοι µετρούν παραµέτρους διαφορετικές από τις κλασσικά αποδεκτές θέτοντας πρόβληµα της ερµηνείας των αποτελεσµάτων. Ένας διαχωρισµός των ταχείων µεθόδων µπορεί να γίνει µε βάση την ικανότητα διάκρισης ανάµεσα στα διάφορα είδη µικροοργανισµών. Έτσι, διακρίνονται σε: α) Μεθόδους χαρακτηρισµού/αναγνώρισης και β) Μεθόδους απαρίθµησης Παρακάτω αναπτύσσονται συνοπτικά ορισµένες από τις µεθόδους αυτές. Μέθοδοι χαρακτηρισµού/αναγνώρισης Αλυσιδωτή αντίδραση της πολυµεράσης (Polymerase Chain Reaction, PCR) Η µέθοδος αυτή βασίζεται στην παρουσία πολλαπλών αντιγράφων ορισµένων ακολουθιών νουκλεοτιδίων του χρωµοσώµατος. Η αντίδραση PCR ενισχύει µια συγκεκριµένη ακολουθία-στόχο του χρωµοσώµατος µε µέγεθος µέχρι περίπου 4kb. Τα δύο άκρα της ακολουθίας, που πρόκειται να αντιγραφεί, ορίζονται από δύο µικρά τµήµατα DNA, που καλούνται "primers", ένα για κάθε κλώνο. Επειδή όµως η ακολουθία αυτή δεν είναι µοναδική µέσα στο χροµόσωµα, η αντίδραση PCR ενισχύει όχι µόνο τη στενή ακολουθία-στόχο, αλλά και ευρύτερες περιοχές. Παράγονται έτσι τεµάχια διαφορετικού µεγέθους, που διαχωρίζονται µε ηλεκτροφόρηση, δηµιουργώντας ένα αποτύπωµα πάνω σε ταινία, χαρακτηριστικό του συγκεκριµένου στελέχους. Aνιχνευτές DNA (DNA probes) Οι ανιχνευτές DNA είναι µικρού µήκους επισηµασµένα τµήµατα DNA, τα οποία υβριδίζονται ή ζευγαρώνουν µε συµπληρωµατικές ακολουθίες DNA, που έχουν εξαχθεί από µικροβιακές καλλιέργειες των προς εξέταση δειγµάτων. Το ζευγάρωµα γίνεται όπως και στο δίκλωνο DNA (αδενίνη µε θυµίνη και γουανίνη µε κυτοσίνη). Αν η ακολουθία των βάσεων του DNA-ανιχνευτή συµπληρώνει µια ειδική ακολουθία του µικροοργανισµούστόχου, τότε ο ανιχνευτής προσδένεται µόνο µε το µικροοργανισµό αυτό. Enzyme-linked Immunosorbent Assay (ELISA) Η µέθοδος αυτή περιλαµβάνει τη "σύλληψη" του αντιγόνου από ένα αντίσωµα, που βρίσκεται ακινητοποιηµένο πάνω σε στερεή µήτρα. Μετά το πλύσιµο για την αποµάκρυνση των µη προσδεδεµένων υλικών, προστίθεται ένα δεύτερο αντίσωµα, που αναγνωρίζει ένα διαφορετικό τµήµα του συλληφθέντος αντιγόνου και αφήνεται να αντιδράσει µε το σύµπλεγµα αντισώµατος-αντιγόνου. Εάν το δεύτερο αντίσωµα είναι επισηµασµένο µε ένα ένζυµο, το υπόστρωµα του ενζύµου προστίθεται µετά το ξέπλυµα της περίσσειας του δεύτερου αντισώµατος, που δεν έχει προσδεθεί, και ο αναλυτής παρατηρεί οπτικά το σχηµατισµό χρώµατος ή τον ποσοτικοποιεί φασµατοφωτοµετρικά. Μέθοδοι απαρίθµησης 102
111 Αλλαγές στην αντίσταση (ή την αγωγιµότητα ή το ηλεκτρικό φορτίο) Καθώς τα βακτήρια πολλαπλασιάζονται σε µία καλλιέργεια, οι µεταβολικές τους δραστηριότητες προκαλούν αλλαγές στη χηµική σύσταση του µέσου. Αυτές οι αλλαγές µπορούν να παρακολουθούνται συνεχώς, χρησιµοποιώντας ηλεκτρόδια για τη µέτρηση της αντίστασης που παρουσιάζεται σε ένα εναλλασσόµενο ρεύµα που εφαρµόζεται στο µέσο. Ο χρόνος που απαιτείται για µια ανάλυση ποικίλλει ανάλογα µε τον αρχικό αριθµό των µικροοργανισµών στο δείγµα. Όσο περισσότεροι µικροοργανισµοί παρευρίσκονται στο εξεταζόµενο δείγµα, τόσο µικρότερος είναι ο χρόνος που χρειάζεται για να σηµειωθούν ανιχνεύσιµες µεταβολές. Απ' όλες τις τεχνικές για ταχεία και αυτόµατη µικροβιολογία που περιγράφηκαν τη δεκαετία του 1970, αυτές που βασίζονται στις άµεσες ηλεκτρικές µετρήσεις των διαφόρων µέσων είναι οι πιο επιτυχηµένες. Η προσέγγιση αυτή έχει αναπτυχθεί εµπορικά και τώρα υπάρχει µια ποικιλία οργάνων διαθέσιµων και σε χρήση σε εργαστήρια σε όλο τον κόσµο. Έχουν γίνει πολλές προσπάθειες για την εµποροποίηση οργάνων για τη µέτρηση της αγωγιµότητας ή της αντίστασης και σήµερα υπάρχουν τέσσερις κατασκευαστές: Τα Bactometer, BacTrac, Malthus, RABIT. Όλα είναι υψηλά αυτοµατοποιηµένα συστήµατα ικανά να µετρήσουν πολλαπλά δείγµατα και να παρουσιάσουν αυτόµατα αναλυτικές αναφορές. ΑΤΡ-Bιοφωτεινότητα (ΑΤΡ-Bioluminescence) H µέθοδος αυτή βασίζεται στο γεγονός ότι όλοι οι ζωντανοί οργανισµοί περιέχουν τριφωσφορική αδενοσίνη (ΑΤΡ), η οποία αποτελεί την πηγή ενέργειας όλων των µεταβολικών δράσεων. Παρουσία ΑΤΡ, το οργανικό συστατικό λουσιφερίνη οξειδώνεται σε οξυλουσιφερίνη, εκπέµποντας φωτόνια ως ένα από τα προϊόντα της αντίδρασης. Το ένζυµο που συµµετέχει είναι η λουσιφεράση. Οι αντιδράσεις του παραπάνω ενζύµου είναι ταχείες, ολοκληρώνονται µέσα σε λίγα λεπτά και ποσοτικοποιώντας µε ένα φωτόµετρο το ποσό των εκπεµπόµενων φωτονίων είναι δυνατόν να υπολογιστεί ο αριθµός των βακτηριακών κυττάρων στο δείγµα. Τεχνική του άµεσα επιφθορίζοντος φίλτρου (Direct Epifluorescent Filter Technique - DEFT) Κατά τη µέθοδο αυτή, το προς εξέταση δείγµα υφίσταται µια προκατεργασία, ώστε να µπορεί να φιλτραριστεί. Στη συνέχεια, το δείγµα φιλτράρεται πάνω σε πολυανθρακικές µεµβράνες, χρωµατίζεται µε τη φθορίζουσα χρωστική acridine orange, και εξετάζεται µε µικροσκόπιο φθορισµού. Η ακριδίνη, όταν προσδένεται µε DNA -κυρίαρχη αντίδραση στα νεκρά κύτταρα- εκπέµπει πράσινο φθορισµό, ενώ όταν προσδένεται µε RNA, το οποίο αφθονεί στα ζωντανά κύτταρα, φθορίζει πορτοκαλί χρώµα. Ο αριθµός των ζωντανών µικροοργανισµών προσδιορίζεται από τον αριθµό των πορτοκαλοκίτρινων κυττάρων που µετρούνται πάνω στο φίλτρο. 103
112 3.4. ΚΛΑΣΣΙΚΗ ΜΙΚΡΟΒΙΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ - ΦΙΛΟΣΟΦΙΑ - ΠΡΟΣΕΓΓΙΣΕΙΣ Τα τρόφιµα, όπως προαναφέρθηκε, αποτελούν άριστα υποστρώµατα για την ανάπτυξη των µικροβίων και πολλά απ' αυτά αποκτούν ένα µεγάλο εύρος µολυσµατικών µικροοργανισµών, σαν αποτέλεσµα των διαδικασιών παραγωγής και µεταχείρισής τους. Συνήθως, µόνο ένα µέρος αυτών θα αναπτυχθούν και τελικά θα κυριαρχήσουν ως µικροοργανισµοί αλλοίωσης του τροφίµου. Η ανάπτυξη των µικροοργανισµών, παθογόνων ή αλλοιoγόνων, στα τρόφιµα ενδιαφέρει οποιονδήποτε σχετίζεται µε την αλυσίδα παραγωγής, από τους αρχικούς παραγωγούς µέχρι τους υπεύθυνους βιοµηχανικής παρασκευής, τους υπεύθυνους διανοµής, τους πωλητές και τέλος τους καταναλωτές. Στα πλαίσια των προσπαθειών και µέτρων που είναι δυνατό και πρέπει να ληφθούν, για λόγους υγιεινής και ασφάλειας, µε στόχο να περιορισθεί η ανάπτυξη των µικροοργανισµών, απαιτείται συστηµατική γνώση της σχέσης µικρόβιο - υπόστρωµα - περιβάλλον. Είναι επίσης σηµαντικό να είµαστε σε θέση να υπολογίσουµε τον χρόνο ζωής που αποµένει ή την µικροβιολογική ασφάλεια ενός συγκεκριµένου προϊόντος σ' ένα συγκεκριµένο στάδιο της αλυσίδας. Τα παραπάνω γίνονται ακόµα πιο σηµαντικά για τρόφιµα που πρόκειται να µεταφερθούν σε µεγάλες αποστάσεις ή να αποθηκευτούν για µεγάλο χρονικό διάστηµα. Η παραδοσιακή προσέγγιση για τον µικροβιολογικό έλεγχο των τροφίµων ήταν συγκεντρωµένη κυρίως στην εξέταση του τελικού προϊόντος (µε εξαίρεση την αποστείρωση σε αυτόκλειστα για τα κονσερβοποιηµένα τρόφιµα και την παστερίωση του γάλακτος και των γαλακτοκοµικών προϊόντων). Τα διάφορα τρόφιµα παρασκευάζονταν και στη συνέχεια εξετάζονταν για το αν συµβαδίζουν µε κάποια προκαθορισµένα µικροβιολογικά κριτήρια. Ο έλεγχος της µικροβιολογικής σταθερότητας γίνονταν πειραµατικά µε εµβολιασµό των τροφίµων µε µικροοργανισµούς που θα µπορούσαν να προκαλέσουν πρόβληµα (challenge testing) και καταγραφή της ανάπτυξης ή της µείωσης των µικροοργανισµών αυτών κατά τη διάρκεια της αποθήκευσης µε επαναλαµβανόµενη λήψη δειγµάτων. Ακόµα κι αν ο µικροβιολογικός έλεγχος βασίζεται σ' ένα ασφαλές σχέδιο όσον αφορά τα δείγµατα, οι παραδοσιακές µικροβιολογικές µέθοδοι είναι γενικά τόσο αργές και κοπιαστικές που δεν µπορούν να ανταποκριθούν στις σηµερινές ανάγκες παραγωγής τροφίµων, που περιλαµβάνουν άµεση διανοµή, έλεγχο της διαδικασίας σε πραγµατικό χρόνο και υγειονοµικό έλεγχο. Επίσης οι µεθόδοι αυτοί δεν επιτρέπουν την ποσοτική εκτίµηση σε συνθήκες διαφορετικές από αυτές που έχουν εξεταστεί, ιδιαίτερα όταν αλληλεπιδρούν δύο ή περισσότεροι παράγοντες. 104
113 3.5. ΜΙΚΡΟΒΙΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ -NΕΕΣ ΠΡΟΣΕΓΓΙΣΕΙΣ Τη δεκαετία του 1980 σηµειώθηκε µια σηµαντική αύξηση στον αριθµό τροφικών δηλητηριάσεων, η οποία οδήγησε σε µια αυξηµένη απαίτηση για εξασφάλιση ασφαλών και υγιεινών τροφίµων από το κοινό. Την ίδια περίοδο πολλοί µικροβιολόγοι άρχισαν να δέχονται ότι οι παραδοσιακές µικροβιολογικές µέθοδοι για τον προσδιορισµό της ποιότητας και της ασφάλειας των τροφίµων περιορίζονται από τον χρόνο που απαιτείται για να δώσουν αποτελέσµατα, ενώ οι έµµεσες µέθοδοι, που βασίζονται σε χηµικές, φυσικές ή φυσικοχηµικές αλλαγές, δεν δίνουν αποτελέσµατα αν δεν υπάρχει µεγάλος αριθµός κυττάρων. Στην περίπτωση των µικροοργανισµών αλλοίωσης, απαιτούνται 10 7 κύτταρα / g ή ml του προϊόντος, που σηµαίνει ότι το τρόφιµο βρίσκεται ήδη στο αρχικό στάδιο αλλοίωσης και χρειάζεται µόνο µικρή εξάπλωση των µικροβίων για να γίνει ορατή η αλλοίωση. Παροµοίως, ακόµα και πολλές ταχείες µέθοδοι που έχουν προταθεί απαιτούν ανάπτυξη των µικροοργανισµών σε υψηλά επίπεδα προτού τα αποτελέσµατα είναι φανερά, ενώ άλλες µέθοδοι εξαρτώνται από τη χρήση πολύπλοκου και ακριβού εξοπλισµού. Η µέθοδος που θα επιλεγεί για να είναι πρακτικά χρήσιµη πρέπει να παρέχει γρήγορα αποτελέσµατα, να είναι αναπαραγωγίσιµη, και ιδιαίτερα για τον υπολογισµό της διατηρησιµότητας, να δίνει ένα µέτρο του βαθµού της αλλοίωσης του τροφίµου κι όχι απλά να επιβεβαιώνει την έναρξη της αλλοίωσης, η οποία ούτως ή άλλως µπορεί να προσδιοριστεί οργανοληπτικά. Το τελευταίο κριτήριο δεν ακολουθείται από τις περισσότερες φυσικές και χηµικές µεθόδους που έχουν προταθεί για τον υπολογισµό της διατηρησιµότητας, που σηµαίνει ότι είναι περισσότερο διαγνωστικές, παρά προρρητικές. Σήµερα, περισσότερο από ποτέ, ο αποτελεσµατικός έλεγχος των µικροβιολογικών παραµέτρων κατά τη διάρκεια της παραγωγής τροφίµων είναι απαραίτητος για την παρασκευή και διανοµή ασφαλών και υγιεινών προϊόντων, τα οποία έχουν την επιθυµητή διατηρησιµότητα. Η επιστήµη και η µικροβιολογία τροφίµων αντιµετωπίζει την πρόκληση της νέας γενιάς προϊόντων που προτιµώνται από τους καταναλωτές, των οποίων τα χαρακτηριστικά είναι η ευκολία χρήσης και µεγαλύτερη διατηρησιµότητα, σε συνδυασµό µε την επίτευξη µεγαλύτερης φρεσκάδας. Γενικά, τα προϊόντα αυτά είναι ελάχιστα επεξεργασµένα (minimally processed), περιέχουν ελάχιστα ή καθόλου συντηρητικά και χρησιµοποιούν τεχνικές όπως η συσκευασία υπό τροποποιηµένη ατµόσφαιρα αερίων προκειµένου να επεκταθεί η διατηρησιµότητά τους. Παράλληλα οι κατασκευαστές τροφίµων δεν ενδιαφέρονται µόνο για την παραγωγή προϊόντων απαλλαγµένων από παθογόνους µικροοργανισµούς, αλλά που ανθίστανται στην µικροβιολογική αλλοίωση. Μόνο στις ΗΠΑ η οικονοµική απώλεια λόγω της µικροβιολογικής αλλοίωσης έχει εκτιµηθεί γύρω στα $30 δισεκατοµύρια το χρόνο. 105
114 Οι φαινοµενικά αντικρουόµενοι στόχοι ελάχιστης επεξεργασίας και µέγιστης διατηρησιµότητας απαιτούν βελτιστοποίηση όλων των παραµέτρων παραγωγής και συντήρησης σε συνδυασµό µε πρωτότυπες τεχνικές, για να εξασφαλιστεί η ασφάλεια και η ελάχιστη υποβάθµιση µέχρι το χρόνο ανάλωσης του τροφίµου. Τρεις νέες προσεγγίσεις, που στοχεύουν στη συστηµατοποίηση και βέλτιστη αξιοποίηση της έρευνας και της αποκτούµενης γνώσης της µικροβιολογίας τροφίµων, ώστε να διασφαλίζεται η υγιεινή και η ποιότητα των τροφίµων από το σχεδιασµό ως την κατανάλωση είναι η τεχνολογία εµποδίων, το σύστηµα διασφάλισης ασφάλειας και υγιεινής HACCP και η προρρητική µικροβιολογία (predictive microbiology). Τεχνολογία εµποδίων (Hurdle Technology) Οι Leistner (1977) και οι Rodel and Leistner (1982) εισήγαγαν την ιδέα των εµποδίων (hurdles), για την περιγραφή των επιδράσεων διαφόρων εσωτερικών παραγόντων σύνθεσης του τροφίµου (food composition factors) και εξωτερικών περιβαλλοντικών συνθηκών (environmental conditions) στην µικροβιακή ανάπτυξη και επιβίωση, που συνοψίζονται στον Πίνακα 3.6. ΠΙΝΑΚΑΣ 3.6. ΦΥΣΙΚΑ ΕΜΠΟ ΙΑ ΦΥΣΙΚΟΧΗΜΙΚΑ ΕΜΠΟ ΙΑ 1. Θερµική επεξεργασία (π.χ. απο- 1. a w στείρωση,παστερίωση,λεύκανση) 2. ph 2. Θερµοκρασία συντήρησης 3. Eh 3. Ακτινοβόληση 4. NaCl 4. Ηλεκτροµαγνητική ενέργεια 5. NaNO 2 5. Υπερυψηλή πίεση 6. CO 2 6. Ultrasonication 7. Οργανικά οξέα 7. Συσκευασία 8. Συντηρητικά 8. ΜΑΡ 9. Κάπνισµα 9. Ασηπτική συσκευασία 10. Μπαχαρικά 10. Μικροϋφή 11. Ανταγωνιστική µικροχλωρίδα 12. Βακτηριοσίνες H προσέγγιση αυτή έχει σαν σκοπό την επίτευξη της συντήρησης των τροφίµων µε την συνεργιστική επίδραση διαφόρων παραµέτρων συντήρησης (εµποδίων), που 106
115 διαταράσσουν την οµοιοστασία (κατάσταση σταθερότητας και εσωτερικής ισορροπίας) των µικροοργανισµών, έτσι ώστε να µην αναπτύσσονται ή να εξαλείφονται. Ποσοτικά πάντως δεδοµένα για το ζητούµενο επίπεδο οποιουδήποτε εµποδίου και της συνεργιστικής του επίδρασης µε άλλα εµπόδια είναι περιορισµένη. Στο παρακάτω Σχήµα 3.3 απεικονίζεται η δράση διαφόρων εµποδίων όπως π.χ. θέρµανση, ψύξη, a w, ph, Eh (οξειδοαναγωγικό δυναµικό), συντηρητικά, βιταµίνες, θρεπτικά συστατικά και ανταγωνιστική µικροχλωρίδα σε οχτώ διαφορετικά παραδείγµατα. Σχήµα 3.3. Απεικόνιση της δράσης των εµποδίων σε οχτώ παραδείγµατα 107
116 HACCP Το ακρωνύµιο HACCP αποτελεί συντοµογραφία του Hazard Analysis Critical Control Points, ενός συστήµατος διασφάλισης της ασφάλειας των τροφίµων που βασίζεται στην Ανάλυση Κινδύνων και τον προσδιορισµό των Κρίσιµων Σηµείων Ελέγχου. Το σύστηµα HACCP αναπτύχθηκε από την αµερικανική εταιρία τροφίµων Pillsburry σε συνεργασία µε την NASA µε στόχο τη µέγιστη δυνατή διασφάλιση της µικροβιολογικής ασφάλειας των τροφίµων των πρώτων επανδρωµένων διαστηµικών πτήσεων. Βασίστηκε στις αρχές του συστήµατος FMEA (Failure, Mode and Effect Analysis) που µελετά σε κάθε στάδιο µιας διεργασίας τι µπορεί να πάει στραβά, τις πιθανές αιτίες και το αναµενόµενο αποτέλεσµα, µε σκοπό να εγκαταστήσει αποτελεσµατικούς µηχανισµούς ελέγχου. Το HACCP χρησιµοποιεί την ίδια προσέγγιση αλλά µε έµφαση στην ασφάλεια του προϊόντος. Πρωτοπαρουσιάστηκε επίσηµα το 1971 στο Εθνικό Συνέδριο για την Ασφάλεια Τροφίµων των ΗΠΑ και από τότε οι αρχές και η αναγκαιότητα του συστήµατος συνειδητοποιήθηκαν σταδιακά από τη βιοµηχανία τροφίµων. Από τα τέλη της δεκαετίας του 1980, περίοδο που συµπίπτει µε την επικράτηση της φιλοσοφίας των συστηµάτων ποιότητας που δίνουν έµφαση στην πρόληψη έναντι του ελέγχου του τελικού προϊόντος, η αναγνώριση του συστήµατος HACCP, ως την πλέον αποτελεσµατική προσέγγιση για τη διασφάλιση της ασφάλειας, αποκτά νέα δυναµική. Σήµερα το HACCP αποτελεί για την ασφάλεια των τροφίµων το διεθνές σύστηµα αναφοράς. Με βάση την εµπειρία της εφαρµογής, όσον αφορά την µεθοδολογία εγκατάστασης του συστήµατος και την αποτελεσµατικότητά του, οι αρχές του HACCP κωδικοποιήθηκαν και αναπτύσσονται λεπτοµερώς σε δύο δηµοσιεύσεις που αποτελούν διεθνώς το σηµείο αναφοράς. Η πρώτη από την Εθνική Επιτροπή για τα Μικροβιολογικά Κριτήρια στα Τρόφιµα των ΗΠΑ (National Advisory Committee on Microbiological Criteria for Foods - NACMCF, 1992) και η δεύτερη από την Επιτροπή για την Υγιεινή Τροφίµων του Codex Alimentarius (Codex Alimentarius Committee on Food Hygiene, 1993). To σύστηµα HACCP, όπως περιγράφεται στις παραπάνω πηγές, βασίζεται σε επτά Αρχές, που συνοψίζουν τον τρόπο εγκατάστασης, εφαρµογής και συντήρησής του στην υπό µελέτη µονάδα (πίνακας 1.7). Το σύστηµα HACCP είναι συµβατό µε τη σύγχρονη φιλοσοφία πρόληψης και διασφάλισης της ποιότητας µέσω κατάλληλων διαδικασιών και όχι µε έλεγχο του τελικού προϊόντος. Αναφέρεται όχι µόνο στους µικροβιολογικούς, αλλά και στους φυσικούς και χηµικούς κινδύνους, που πιθανόν να υπεισέλθουν στη διαδικασία παραγωγής του τροφίµου. 108
117 ΠΙΝΑΚΑΣ 1.7 : Αρχές Συστήµατος HACCP Aρχή HACCP 1 ιεξαγωγή ανάλυσης κινδύνων. Περιγραφή προληπτικών µέτρων ελέγχου. Aρχή HACCP 2 Αναγνώριση Κρίσιµων Σηµείων Ελέγχου (CCP) στη διεργασία. Aρχή HACCP 3 Καθορισµός Κρίσιµων Ορίων για τα προληπτικά µέτρα που συνδέονται µε κάθε αναγνωρισµένο CCP. Aρχή HACCP 4 Καθορισµός απαιτήσεων παρακολούθησης και καταγραφής των CCP. Καθορισµός διαδικασιών για τη ρύθµιση και διατήρηση εντός ελέγχου της διεργασίας. Aρχή HACCP 5 Καθορισµός διορθωτικών ενεργειών που ακολουθούνται όταν υπάρχει ένδειξη απόκλισης απο ένα κρίσιµο όριο. Aρχή HACCP 6 Καθορισµός διαδικασιών αποτελεσµατικής καταγραφής που αποδεικνύουν έγγραφα την εφαρµογή του συστήµατος HACCP. Aρχή HACCP 7 Καθορισµός διαδικασιών για την επαλήθευση ορθής λειτουργίας του συστήµατος HACCP. Η προσέγγιση της ασφάλειας και υγιεινής µε τη φιλοσοφία HACCP επιβάλει µια ουσιαστική επαναξιολόγηση κάθε διεργασίας της βιοµηχανίας τροφίµων. Το σύστηµα απαιτεί ενδελεχή εξέταση των κινδύνων σε όλα τα στάδια και αναγνώριση των σηµείων που είναι κρίσιµα για τον έλεγχο. H συστηµατοποίηση της διαδικασίας αυτής γίνεται µε τη χρήση λεπτοµερών οδηγιών βασισµένων στις Aρχές HACCP. Ο τρόπος ανάπτυξης του συστήµατος HACCP έχει διεθνώς παγιωθεί βάσει των ταυτόσηµων οδηγιών του NACMCF (1992) και του Codex Committee on Food Hygiene (1993) βασισµένες στις 7 Αρχές HACCP (Πίνακας 1.7). Επαρκής βιβλιογραφία και εγχειρίδια αναλύουν τις οδηγίες αυτές και δίδουν πρακτικές εφαρµογές (Mortimore and Wallace, Τζιά και Τσιαπούρης, 1996). Της διεξαγωγής της Ανάλυσης Κινδύνων της Αρχής 1 προηγείται η συγκρότηση Οµάδας HACCP, η περιγραφή του τροφίµου και της διανοµής του, η αναγνώριση χρήσης και καταναλωτών και η σύνταξη και επαλήθευση του διαγράµµατος ροής της διεργασίας. Κατά την ανάλυση κινδύνων, και για ένα συγκριτικό καθορισµό της επικινδυνότητας (risk), του κάθε συστατικού, σταδίου διεργασίας ή προϊόντος, είχε προταθεί από την NACMCF ένα σύστηµα κατηγοριοποιήσης (assignment of risk categories) από VI ως 0, βάσει των χαρακτηριστικών των κινδύνων (hazard characteristics) Α ως F (NACMCF 1992, Appendix B). Η προσέγγιση αυτή δεν χρησιµοποιείται πλέον από την NACMCF έχοντας υποκατασταθεί από µια διαδικασία εξαντλητικού ερωτηµατολογίου (NACMCF 1992, 109
118 Appendix A). Η αναγνώριση των Κρισίµων Σηµείων Ελέγχου (CCP) που ακολουθεί είναι καθοριστική για την αποτελεσµατικότητα του συστήµατος. Είναι απόλυτα σηµαντικό να αναγνωριστούν όλα τα CCP χωρίς να παραληφθεί κανένα αλλά και χωρίς να επιβαρυνθεί το σύστηµα µε επι πλέον Σηµεία. Το δένδρο απόφασης των Κρισίµων Σηµείων Ελέγχου (Σχήµα 1.5) δίνει τον αλγόριθµο για µια συστηµατική αναγνώριση. Με τη ολοκλήρωση της διαδικασίας ανάπτυξης του συστήµατος HACCP βάσει και των υπολοίπων Αρχών συµπληρώνεται το Έντυπο Ελέγχου HACCP (HACCP Control Chart) που µαζί µε τα σχετικά διαγράµµατα ροής δίνει συνοπτικά αλλά περιεκτικά την καταγραφή του συστήµατος. ΒΙΒΛΙΟΓΡΑΦΙΑ HACCP Codex Committee on Food Hygiene (1993). Guidelines for the Application of the HACCP System in Training Considerations for the Application of the HACCP System to Food Processing and Manufacturing, World Health Organization. WHO/FNU/FOS/93.3II. Μortimore, S. and Wallace, C. (1994) HACCP, A practical approach, Chapman & Hall, London. National Advisory Committee on Microbiological Criteria of Foods (1992) Hazard Analysis and Critical Control Points System (adopted March 20, 1992), International Journal of Food Microbiology, 16, Τζιά, Κ.και Τσιαπούρης, Α. (1996) Ανάλυση Επικινδυνότητας στα κρίσιµα σηµεία ελέγχου (HACCP) στη βιοµηχανία τροφόµων, Εκδ. Παπασωτηρίου, Αθήνα. Προρρητική Μικροβιολογία Μια εναλλακτική µέθοδος στην αναπτυσσόµενη τεχνολογία, που παρέχει τη δυνατότητα για γρήγορες µικροβιολογικές εκτιµήσεις, χωρίς την απαίτηση για χρονοβόρες και δαπανηρές αναλύσεις, είναι η προρρητική µικροβιολογία. Πρόκειται για έναν αναπτυσσόµενο τοµέα έρευνας που συνδυάζει στοιχεία µικροβιολογίας, µαθηµατικών και στατιστικής. Η προρρητική µικροβιολογία βασίζεται στην ανάπτυξη µαθηµατικών µοντέλων, τα οποία µπορούν να προβλέψουν το ρυθµό ανάπτυξης ή µείωσης των µικροοργανισµών κάτω από συγκεκριµένες περιβαλλοντικές συνθήκες, επιτρέποντας έτσι την ποσοτικοποίηση πολλαπλών ανεξάρτητων µεταβλητών και των αλληλεπιδράσεων τους. εν περιορίζεται δηλαδή στη µελέτη συγκεκριµένων συστηµάτων αλλά επιχειρεί να µαθηµατικοποιήσει την επίδραση των καθοριστικών παραγόντων όπως η θερµοκρασία, το ph, η ενεργότητα νερού, η συγκέντρωση αλάτων, οργανικών οξέων, η µερική πίεση οξυγόνου, διοξειδίου του άνθρακος και άλλων αερίων, η παρουσία αντιµικροβιακών παραγόντων και άλλων εµποδίων, έτσι ώστε να επιτρέπεται η συναγωγή συµπερασµάτων για διαφορετικά συστήµατα και διεργασίες. Αναµφισβήτητα, ένας µεγάλος αριθµός παραγόντων επηρεάζει τους µικροοργανισµούς. Στα περισσότερα όµως τρόφιµα λίγοι µόνο από αυτούς τους παράγοντες ασκούν τη µεγαλύτερη επίδραση στην ανάπτυξη ή την µείωση των µικροοργανισµών. 110
119 ΣΧΗΜΑ 1.5. ένδρο απόφασης Κρισίµων Σηµείων Ελέγχου E1. Υπάρχουν προληπτικά µέτρα για τον αναγνωρισµένο κίνδυνο; προϊόν Αναθεώρησε στάδιο, βήµα ή ΝΑΙ ΟΧΙ Είναι απαραίτητος ο έλεγχος στο στάδιο για την ασφάλεια ; ΝΑΙ ΟΧΙ εν είναι CCP Τέλος* E2. Eίναι αυτό το στάδιο ειδικά σχεδιασµένο για την εξάλειψη ή τη µείωση σε αποδεκτό επίπεδο του κινδύνου; OΧΙ ΝΑΙ Ε3. Μπορεί ο κίνδυνος στο στάδιο αυτό να προκύψει ή να αυξηθεί πάνω απο το κρίσιµο όριο ; ΝΑΙ ΟΧΙ εν είναι CCP Tέλος * Ε4. Ο κίνδυνος θα εξαληφθεί ή µειωθεί σε αποδεκτό επίπεδο σε παρεπόµενο στάδιο ή βήµα ; ΟΧΙ CCP NAI έν είναι CCP Τέλος * Κρίσιµο Σηµείο Ελέγχου * Προχώρησε µε τον επόµενο κίνδυνο στο ίδιο στάδιο ή στο επόµενο στάδιο της διεργασίας. Η προρρητική µικροβιολογία είναι στην ουσία µια κινητική προσέγγιση στα πλαίσια της γενικών αρχών της κινητικής αλλοίωσης των τροφίµων που αναπτύσσεται στο επόµενο κεφάλαιο. Στη συνέχεια αναφέρεται συνοπτικά το θέµα της κινητικής ανάπτυξης των µικροοργανισµών ΚΙΝΗΤΙΚΗ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΑΠΤΥΞΗΣ Γενική καµπύλη ανάπτυξης - Φάσεις ανάπτυξης µικροβιακού πληθυσµού 111
120 Σ' ένα περιβάλλον, στο οποίο τα θρεπτικά συστατικά δεν αποτελούν περιοριστικό παράγοντα, ένα βακτήριο ή ένας µικροβιακός πληθυσµός θα αναπαραχθεί και θα αυξηθεί στον αριθµό. Γενικά, για οποιοδήποτε οµοιογενή µικροβιακό πληθυσµό κάτω από συνθήκες σταθερής κατάστασης, η ανάπτυξη σ' ένα θρεπτικό µέσο ή σ' ένα πραγµατικό σύστηµα τροφίµου µπορεί να τυποποιηθεί από την καµπύλη του Σχήµατος 3.5, η οποία προκύπτει αν κανείς σχεδιάσει το λογάριθµο της πυκνότητας των βακτηρίων συναρτήσει του χρόνου. ανώτερη ασύµπτωτη 1 9 διαφορά Lo g cf u/ κατώτερη ασύµπτωτη log κύκλος=3,32 διπλασιασµοί Χρόνος για 3,32 διπλασιασµούς ΧΡΟΝΟΣ h Χρόνος Προσαρµογής Σχήµα 3.5. Τυπική καµπύλη βακτηριακής ανάπτυξης Όπως φαίνεται, υπάρχει ένας αρχικός αργός ρυθµός αύξησης του λογαρίθµου της πυκνότητας των κυττάρων, που αυξάνεται σ' έναν σχεδόν σταθερό ρυθµό ανάπτυξης, µειώνεται ξανά στο µηδέν και τελικά ο ρυθµός γίνεται αρνητικός. Αυτές οι τέσσερις φάσεις της καµπύλης αναφέρονται αντίστοιχα ως: λανθάνουσα φάση, εκθετική φάση, φάση στασιµότητας και φάση κάµψης ή θανάτου. Είναι γενικώς αποδεκτό ότι η λανθάνουσα φάση είναι µια χρονική περίοδος, στην οποία τα κύτταρα προσαρµόζουν τη φυσιολογία και βιοχηµεία τους στο καινούριο περιβάλλον που βρίσκονται, ενώ κατά την διάρκεια της εκθετικής φάσης τα κύτταρα αναπτύσσονται όσο πιο γρήγορα είναι δυνατό σ' αυτό το περιβάλλον. Κατά την φάση αυτή τα κύτταρα επιδεικνύουν εξισορροπηµένη ανάπτυξη, κατά την οποία ο ρυθµός σύνθεσης κάθε συστατικού του κυττάρου (ένζυµα, δοµικά µόρια, DNA, κ.ά.) είναι τέτοιος ώστε να µην γίνεται µεγαλύτερη σύνθεση απ' αυτή που απαιτείται για την παραγωγή νέων κυττάρων, δηλαδή ολόκληρη η µεταβολική δραστηριότητα των κυττάρων κατευθύνεται στην αναπαραγωγή. Στην εκθετική φάση όλα τα συστατικά των κυττάρων βρίσκονται σε σταθερές αναλογίες και τα κύτταρα θεωρούνται, για πρακτικούς σκοπούς, φυσιολογικά ταυτόσηµα (πανοµοιότυπα). Καθώς ο πληθυσµός συνεχίζει να αυξάνεται, η συσσώρευση των µεταβολιτών µέσα στο περιβάλλον γίνεται αρκετά απαγορευτική (παρεµποδιστική), ώστε να προκαλεί µείωση στο ρυθµό αύξησης του αριθµού των κυττάρων. Κατά την διάρκεια αυτής της φάσης, οι συνθήκες µπορεί να γίνουν τόσο απαγορευτικές ώστε να οδηγήσουν στο θάνατο και την λύση των κυττάρων, οπότε ο καθαρός ρυθµός αύξησης του πληθυσµού µειώνεται συνεχώς µέχρι την τιµή µηδέν (φάση στασιµότητας). Η διάρκεια αυτής της φάσης 112
121 ποικίλλει, αλλά τελικά καθώς όλο και περισσότερες τοξίνες συσσωρεύονται, ο ρυθµός θανάτου των κυττάρων γίνεται µεγαλύτερος από την ικανότητα του περιβάλλοντος να υποστηρίξει την κυτταρική διαίρεση, µε αποτέλεσµα την µείωση του µεγέθους της βακτηριακής πυκνότητας και την είσοδο των µικροβίων σε µια νέα φάση, που αναγνωρίζεται ως φάση θανάτου της καλλιέργειας. Η σύνθεση του τροφίµου, οι περιβαλλοντικές συνθήκες, η ηλικία και η κατάσταση των µικροβίων, µπορεί να επηρεάσουν τη µορφή της καµπύλης ανάπτυξης. Υπάρχουν πολλές περιγραφικές µέθοδοι που έχουν προταθεί στη βιβλιογραφία για την περιγραφή µιας καµπύλης µικροβιακής ανάπτυξης, όπου οι κύριες υποθέσεις είναι ότι ο πληθυσµός είναι οµοιογενής και ο ρυθµός ανάπτυξης ή ο χρόνος διπλασιασµού είναι ανεξάρτητοι της ηλικίας. Για ένα βακτήριο, τα τρόφιµα αποτελούν ένα νέο περιβάλλον το οποίο µπορεί να εκµεταλλευτεί. Το βακτήριο θα αναπτυχθεί και θα αναπαραχθεί στο περιβάλλον αυτό όπως και σε ένα εργαστηριακό υπόστρωµα. Για το λόγο αυτό οι µικροβιολόγοι τροφίµων ενδιαφέρονται για την κινητική της ανάπτυξης των βακτηρίων, ιδιαίτερα για την λανθάνουσα και εκθετική φάση. Αν οι µικροοργανισµοί σ' ένα τρόφιµο αναγκαστούν να παραµείνουν στη λανθάνουσα φάση, τότε ο χρόνος ζωής (διατηρησιµότητα) του τροφίµου θα επιµηκυνθεί. Αν τελικά φτάσουν στην εκθετική φάση, τότε ο ρυθµός ανάπτυξης κάτω από συγκεκριµένες συνθήκες αποθήκευσης θα καθορίσουν τη διατηρησιµότητα του προϊόντος. Έτσι λοιπόν, για τους σκοπούς της προρρητικής µικροβιολογίας είναι χρήσιµο να µπορούµε να µοντελοποιήσουµε την καµπύλη ανάπτυξης του µικροβιακού πληθυσµού, ιδιαίτερα τη διάρκεια της λανθάνουσας φάσης και την κλίση της εκθετικής φάσης, που αντιπροσωπεύει το ρυθµό ανάπτυξης του οργανισµού. Ο προσδιορισµός των δύο αυτών κινητικών παραµέτρων και η µοντελοποίηση των ποσοτικών επιδράσεων διαφόρων εµποδίων σε αυτές αποτελούν κρίσιµα σηµεία για την µικροβιακή πρόρρηση της διατηρησιµότητας και την ανάλυση επικινδυνότητας. Η φάση στασιµότητας είναι λιγότερου άµεσου ενδιαφέροντος γιατί τα περισσότερα τρόφιµα θα έχουν ήδη αλλοιωθεί και θα είναι µη αποδεκτά πριν το µικροβιακό φορτίο φτάσει στη φάση στασιµότητας. Με τον παραδοσιακό τρόπο, ο χρόνος λανθάνουσας φάσης και ο εκθετικός ρυθµός ανάπτυξης προσδιορίζονται από την εφαπτοµένη της καµπύλης στο σηµείο της εκθετικής φάσης µε την µεγαλύτερη κλίση. Ο χρόνος που απαιτείται για τον διπλασιασµό του πληθυσµού (generation time) µπορεί να προσδιορισθεί από την κλίση αυτής της γραµµής. Όταν ο δεκαδικός λογάριθµος απεικονίζεται γραφικά συναρτήσει του χρόνου, τότε η σχέση ανάµεσα στην κλίση (k) και στο χρόνο διπλασιασµού (GT) είναι: k = log 2 10 GT. H κλίση αντιπροσωπεύει τον εκθετικό ρυθµό µικροβιακής ανάπτυξης.για τον υπολογισµό της διάρκειας της λανθάνουσας φάσης, η εφαπτοµένη προεκτείνεται µέχρι την πυκνότητα των µικροοργανισµών σε χρόνο µηδέν και ο χρόνος στο σηµείο αυτό θεωρείται ως το τέλος της λανθάνουσας φάσης. Μοντέλα ανάπτυξης µικροοργανισµών Έχει προταθεί ένας αριθµός µαθηµατικών συναρτήσεων, οι οποίες περιγράφουν σιγµοειδείς καµπύλες και έχουν χρησιµοποιηθεί για τη δηµιουργία µοντέλων ανάπτυξης των µικροβίων. Το πλεονέκτηµα τέτοιων συναρτήσεων είναι ότι τεχνικές µη γραµµικής παλινδόµησης µπορούν να χρησιµοποιηθούν ώστε να προσδιοριστεί µαθηµατικά η γραµµή καλύτερης προσαρµογής (line of best fit), η γραµµή δηλαδή εκείνη που περνά απ' όλα τα σηµεία των δεδοµένων, όσο αυτό είναι δυνατό, µ' έναν αντικειµενικό και αναπαραγωγίσιµο τρόπο. Την εξίσωση προσαρµογής µπορούµε να την επεξεργαστούµε 113
122 παραπέρα ώστε να υπολογίσει όσο το δυνατό καλύτερα το χρόνο λανθάνουσας φάσης και το χρόνο διπλασιασµού χρησιµοποιώντας όλα τα δεδοµένα. Ένα µειονέκτηµα αποτελεί το γεγονός ότι οι τεχνικές µη γραµµικής παλινδρόµησης δεν µπορούν να εφαρµοστούν χωρίς την βοήθεια υπολογιστών και κατάλληλου λογισµικού. Μερικές από αυτές τις συναρτήσεις είναι οι παρακάτω: Μοντέλο Monod: O ρυθµός µε τον οποίο αυξάνεται ο µικροβιακός πληθυσµός είναι ανάλογος µε τον αριθµό των µελών του πληθυσµού, δηλαδή ο ειδικός ρυθµός ανάπτυξης ή ο χρόνος διπλασιασµού θεωρείται σταθερός για σταθερές περιβαλλοντικές συνθήκες. Αυτό είναι αποτελεσµατικό µέσα σ' ένα µικρό χρονικό διάστηµα, πριν δηλαδή αρχίσει να µειώνεται σηµαντικά το διαθέσιµο υπόστρωµα ή να µεταβάλλεται το περιβάλλον (π.χ µείωση ph). Η ολοκληρωµένη µορφή του µοντέλου Monod είναι: [ ] N= N0 exp k( t t L ) (1) όπου Ν:ο αριθµός των µικροοργανισµών σε χρόνο t, N 0 :το αρχικό φορτίο, k:ο ειδικός ρυθµός ανάπτυξης και t L :ο χρόνος λανθάνουσας φάσης Ο ειδικός ρυθµός ανάπτυξης είναι η κλίση του διαγράµµατος του lnn συναρτήσει του t, για t>t L. Ο χρόνος λανθάνουσας φάσης µπορεί να προσδιορισθεί γραφικά και αντιστοιχεί στο σηµείο τοµής της ευθείας Ν 0 µε την ευθεία γραµµικής παλινδρόµησης της εκθετικής φάσης ανάπτυξης. Το µοντέλο αυτό είναι απλό και συνήθως επαρκές και έχει χρησιµοποιηθεί αρκετά, ακόµα και για µεικτούς πληθυσµούς. Η λογιστική συνάρτηση µπορεί να χρησιµοποιηθεί για την ανάπτυξη οποιουδήποτε πληθυσµού σ' ένα απεριόριστο περιβάλλον, µε την παραδοχή ότι ο απόλυτος ρυθµός ανάπτυξης, δηλαδή η µεταβολή του αριθµού µικροβίων µε το χρόνο, είναι ανάλογος µε την πυκνότητα τους σε οποιοδήποτε χρόνο. Αυτό συµπίπτει µε την εξίσωση για την εκθετική ανάπτυξη. Πρακτικά όµως τις περισσότερες φορές το περιβάλλον δεν είναι απεριόριστο και ο ειδικός ρυθµός ανάπτυξης δεν είναι σταθερός, αλλά µειώνεται συναρτήσει της πυκνότητας του πληθυσµού, εξαιτίας της µείωσης των θρεπτικών συστατικών ή της συσσώρευσης τοξικών µεταβολιτών. Έτσι ο παρατηρούµενος ειδικός ρυθµός ανάπτυξης, k', είναι συνάρτηση του Ν, δηλαδή k'=f(n). Οι παραδοχές πάνω στις οποίες βασίζεται το µοντέλο υπαγορεύουν ότι ο ειδικός ρυθµός ανάπτυξης γίνεται µέγιστος (k), για Ν=0, δηλ. k'=k. Στη φάση στασιµότητας, το k' µειώνεται στο 0. Η λογιστική εξίσωση έτσι µπορεί να γραφεί: N () t C = (2) 1 + exp ( ) { Bt M} όπου: t: χρόνος, Ν(t): πυκνότητα πληθυσµού σε χρόνο t, C: η τιµή της ανώτερης ασύµπτωτης, δηλ. η µέγιστη πυκνότητα πληθυσµού που δίνεται από το Ν( ), Μ: ο χρόνος στον οποίο ο απόλυτος ρυθµός ανάπτυξης είναι µέγιστος, Β/2: ειδικός ρυθµός ανάπτυξης στο t=m και όπου Ν(0)<<C, B:ειδικός ρυθµός ανάπτυξης στο t=0. Η λογιστική συνάρτηση είναι συµµετρική ως προς το σηµείο (Μ,C/2). Όπως παρατηρούµε η εξίσωση αυτή δεν έχει κανένα σαφή όρο που να αναφέρεται στο αρχικό εµβόλιο Ν (0). Αυτό συµβαίνει γιατί το µοντέλο αυτό προβλέπει ότι ο ειδικός ρυθµός ανάπτυξης είναι συνάρτηση του µεγέθους του πληθυσµού, κι έτσι για κάθε τιµή της πυκνότητας του εµβολίου ο ρυθµός ανάπτυξης θα είναι ο ίδιος όπως θα ήταν κι αν ο πληθυσµός είχε φτάσει σ' αυτό το µέγεθος απ' οποιαδήποτε άλλη αρχική πυκνότητα εµβολίου. 114
123 Συνάρτηση του Gompertz: Ενώ τα µοντέλα λογιστικού τύπου βασίζονται στη γραµµική µείωση του ειδικού ρυθµού ανάπτυξης συναρτήσει της πυκνότητας του πληθυσµού, η συνάρτηση του Gompertz βασίζεται στην εκθετική σχέση αυτών των δύο ιδιοτήτων. Η συνάρτηση του Gompertz µπορεί να εκφραστεί ως εξής: { [ ]} Nt () = Cexpexp Bt ( M) (3) όπου: t: χρόνος, Ν(t): πυκνότητα πληθυσµού σε χρόνο t, C: η τιµή της ανώτερης ασύµπτωτης, δηλ. η µέγιστη πυκνότητα πληθυσµού που δίνεται από το Ν( ), Μ: ο χρόνος στον οποίο ο απόλυτος ρυθµός ανάπτυξης είναι µέγιστος, Β: ο σχετικός ρυθµός ανάπτυξης στο Μ Οι Gibson et al. (1987) εισήγαγαν εξισώσεις παρόµοιες στην εµφάνιση µε τη λογιστική συνάρτηση και τη συνάρτηση Gompertz, οι οποίες περιγράφουν καµπύλες βακτηριακής ανάπτυξης µε τη µορφή του λογαρίθµου της πυκνότητας των κυττάρων συναρτήσει του χρόνου, σε όρους ρυθµού εκθετικής ανάπτυξης και διάρκειας λανθάνουσας φάσης. Η τροποποίηση του λογιστικού µοντέλου µπορεί να γραφεί ως εξής: D log N() t = A+ (4) 1 + exp ( ) [ Bt M] ενώ η τροποποίηση της συνάρτησης του Gompertz γράφεται: { [ ]} log N() t = A+ Dexp exp B( t M) (5) όπου: t: χρόνος, Ν(t): πυκνότητα πληθυσµού σε χρόνο t, Α: η τιµή της κατώτερης ασύµπτωτης (logn (- ) ), D: η διαφορά µεταξύ των τιµών ανώτερης και κατώτερης ασύµπτωτης (logn ( ) -logn (- ) ), M: ο χρόνος στον οποίο ο εκθετικός ρυθµός ανάπτυξης είναι µέγιστος και Β: σχετίζεται µε την κλίση της καµπύλης στο Μ και είναι :για την εξίσωση (4): ΒD/4 =κλίση της εφαπτοµένης στο Μ και για την εξίσωση (5):BD/e = κλίση της εφαπτοµένης στο Μ Μετά την µαθηµατική περιγραφή της καµπύλης ανάπτυξης µπορούµε να υπολογίσουµε τις κινητικές παραµέτρους, όπως το χρόνο διπλασιασµού, το χρόνο λανθάνουσας φάσης ή το χρόνο ώστε οι µικροοργανισµοί να φτάσουν σ' ένα συγκεκριµένο επίπεδο. Με διαφοροποίηση µιας εξίσωσης µπορούν να προκύψουν εκφράσεις για τον µέγιστο ρυθµό εκθετικής ανάπτυξης, τον χρόνο διπλασιασµού, κ,ά. Έτσι, για την τροποποιηµένη εξίσωση του Gompertz, έχουµε: µ= BD e, GT = log N( 0) A, tlag = M + BD B BD e όπου µ: µέγιστος ρυθµός εκθετικής ανάπτυξης, GT:ο χρόνος διπλασιασµού και t lag :η διάρκεια της λανθάνουσας φάσης. Μοντέλα επίδρασης θερµοκρασίας Η µεγάλη σηµασία της θερµοκρασίας για την µικροβιακή ανάπτυξη έχει οδηγήσει στην δηµοσίευση διαφόρων µοντέλων. Τα µοντέλα αυτά χρησιµοποιούνται για την περιγραφή της επίδρασης της θερµοκρασίας στον ειδικό ρυθµό ανάπτυξης κατά την εκθετική φάση (µ max ). Τα µοντέλα παρουσιάζουν επίσης ενδιαφέρον για την δυνατότητα µιας συνεχούς περιγραφής µε παρεµβολή και την πρόρρηση µε προεκβολή. Για την περιγραφή της επίδρασης της θερµοκρασίας στην ανάπτυξη µικροβίων έχουν προταθεί δύο τύποι µοντέλων, τα µοντέλα τύπου Arrhenius και τα µοντέλα τύπου Belehradek. (6) 115
124 Τα µοντέλα τύπου Belehradek γράφονται µε τη γενική µορφή: d k = α( t t0 ) (7) όπου: k: ρυθµός, t: θερµοκρασία και α, d, t 0 : παράµετροι προσαρµογής Το t 0 θεωρείται ως βιολογικό µηδέν, δηλαδή η θερµοκρασία στην οποία (και φυσικά κάτω από την οποία) δεν είναι δυνατή η ανάπτυξη των µικροβίων. Μεγάλη εφαρµογή στην προρρητική µικροβιολογία έχει το απλό µοντέλο της τετραγωνικής ρίζας που προκύπτει από την (7) k = b( T T ) min (8) το οποίο εφαρµόζεται µόνο στην περιοχή χαµηλών θερµοκρασιών, οι οποίες κυµαίνονται από την ελάχιστη θερµοκρασία στην οποία µπορεί να παρατηρηθεί ανάπτυξη µικροοργανισµών έως αυτήν ακριβώς πριν τη βέλτιστη θερµοκρασία. Η βέλτιστη θερµοκρασία είναι αυτή στην οποία η σταθερά ειδικού ρυθµού ανάπτυξης γίνεται µέγιστη. Στην ελάχιστη θερµοκρασία Τ min, ο ρυθµός ανάπτυξης εξ ορισµού είναι µηδέν. Πρόκειται δηλαδή για την ελάχιστη θερµοκρασία µικροβιακής ανάπτυξης όπου η γραµµή παλινδρόµησης κόβει τον άξονα των θερµοκρασιών στο k = 0. Συνήθως, η ελάχιστη θερµοκρασία T min είναι 2-3 C µικρότερη από τη θερµοκρασία στην οποία πραγµατικά παρατηρείται η ανάπτυξη των µικροοργανισµών. Μια επέκταση της προηγούµενης εξίσωσης, που επιτρέπει την χρησιµοποίηση δεδοµένων απ' όλο το βιοκινητικό θερµοκρασιακό εύρος είναι: { [ max ]} k = b( T T ) 1 exp c( T T ) (9) min Όπως ακριβώς το Τ min είναι το "βιολογικό µηδέν" στο χαµηλό άκρο της θερµοκρασιακής περιοχής, έτσι και το Τ max αποτελεί το "βιολογικό µηδέν" στο υψηλό άκρο της περιοχής. Κάτω δηλαδή από το Τ min και πάνω από το Τ max δεν παρατηρείται ανάπτυξη µικροβίων. Η Τ max είναι η µεγαλύτερη θερµοκρασία όπου η γραµµή παρεµβολής κόβει τον άξονα θερµοκρασίας στο k = 0. Οι παράµετροι c και b δεν έχουν µικροβιολογική ερµηνεία, αλλά απλά βοηθούν στην προσαρµογή δεδοµένων για θερµοκρασίες µεγαλύτερες της βέλτιστης. Απ' τη στιγµή που το να αποκτήσει κανείς ακριβή δεδοµένα σε πολύ χαµηλούς ρυθµούς ανάπτυξης είναι δύσκολο, οι Τ min και Τ max συνήθως δεν είναι οι πραγµατικές θερµοκρασίες, στις οποίες η ανάπτυξη είναι µηδενική. Καθώς η µικροβιακή ανάπτυξη είναι µία βιοχηµική διαδικασία, είναι αναµενόµενο για ένα συγκεκριµένο θερµοκρασιακό εύρος να µπορεί να εφαρµοστεί ο νόµος του Arrhenius. Η πιο απλή σχέση του τύπου Arrhennius είναι : k = Aexp( Eα / RT) (10) όπου k: η σταθερά µικροβιακού ρυθµού ανάπτυξης, Εα: η ενέργεια ενεργοποίησης και Α: εµπειρική σταθερά και χρησιµοποιείται για την προσαρµογή δεδοµένων σε θερµοκρασίες µικρότερες της βέλτιστης. Σε διάγραµµα lnk συναρτήσει του αντιστρόφου της απόλυτης θερµοκρασίας 1/Τ προκύπτει ευθεία γραµµή αν τα Ε α και Α δεν µεταβάλλονται µε τη θερµοκρασία. Η σχέση Arrhenius µπορεί επίσης να εφαρµοστεί για την µοντελοποίηση της θερµοκρασιακής εξάρτησης της λανθάνουσας φάσης, η οποία είναι σηµαντική για την πρόρρηση της διατηρησιµότητας κάτω από µεταβλητές συνθήκες θερµοκρασίας όπου υπάρχει χαµηλό αρχικό µικροβιακό φορτίο. 116
125 Στην περίπτωση αυτή για τη δηµιουργία της γραφικής παράστασης του Arrhenius χρησιµοποιείται το αντίστροφο του χρόνου λανθάνουσας φάσης, 1/t L. O Davey (1989) πρότεινε ένα γραµµικό µοντέλο τύπου Arrhenius για να περιγράψει την επίδραση της θερµοκρασίας και της ενεργότητας του νερού στο ρυθµό µικροβιακής ανάπτυξης. Όταν η ενεργότητα του νερού διατηρείται σχεδόν σταθερή, το οποίο µπορεί να συµβαίνει για τα περισσότερα νωπά τρόφιµα αφού απαιτείται σηµαντική αλλαγή της περιεχόµενης υγρασίας γαι ν' αλλάξει η ενεργότητα του νερού σηµαντικά, ο όρος αυτός C1 C2 παραλείπεται και καταλήγει στην εξίσωση: ln k = C T T (11) όπου k: ρυθµός, Τ: θερµοκρασία (Κ), C 0,C 1 και C 2 παράµετροι προσαρµογής ΜΟΝΤΕΛΑ ΣΥΝ ΥΑΣΤΙΚΗΣ ΕΠΙ ΡΑΣΗΣ ΤΗΣ ΘΕΡΜΟΚΡΑΣΙΑΣ, ΤΗΣ ΕΝΕΡΓΟΤΗΤΑΣ ΝΕΡΟΥ ΚΑΙ ΑΛΛΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΟ ΡΥΘΜΟ ΜΙΚΡΟΒΙΑΚΗΣ ΑΝΑΠΤΥΞΗΣ Σε ορισµένα τρόφιµα, όπως ψάρι, κρέας, γάλα και πουλερικά, τα οποία παρουσιάζουν υψηλά επίπεδα ενεργότητας νερού και σχεδόν ουδέτερες τιµές ph, η θερµοκρασία είναι ο µοναδικός ή ο σηµαντικότερος παράγοντας που ελέγχει το ρυθµό µικροβιακής ανάπτυξης. Σε πολλά όµως προϊόντα η θερµοκρασία αποτελεί µόνο τον ένα από µια σειρά παραγόντων που επιδρούν στο ρυθµό της αλλοίωσης του προϊόντος. Η συνδυαστική επίδραση διαφορετικών περιορισµών στην ανάπτυξη µικροβίων περιγράφηκε στην τεχνολογία των εµποδίων. Σε λίγες περιπτώσεις έχουν γίνει προσπάθειες για την µοντελοποίηση των συνδυαστικών επιδράσεων δύο ή περισσότερων παραγόντων στο ρυθµό ανάπτυξης. Τις περισσότερες φορές οι προσπάθειες περιορίστηκαν στην απλή παρουσίαση ενός συγκεκριµένου συνδυασµού εµποδίων για να αποτρέψουν την µικροβιακή ανάπτυξη. Θερµοκρασία και ενεργότητα νερού: Λαµβάνοντας ως αρχικό σηµείο τα µοντέλα τετραγωνικής ρίζας δοκιµάστηκαν οι εξισώσεις: k = d( T Tmin ) ( aw aw ) (12) min και { [ ]} k = d( T T ) 1 exp c( T T ) ( a a ) (13) min max w wmin H µορφή των παραπάνω εξισώσεων φανερώνει ότι οι επιδράσεις της θερµοκρασίας και της ενεργότητας του νερού είναι προσθετικές και όχι συνεργιστικές. Βάσει της σχέσης Arrhenius προτάθηκε η: όπου C1 C2 ln k = C Ca 3 w + Ca 4 T T 2 w k:ο ρυθµός ανάπτυξης και C i µε i=0,1,2,3,4 :συντελεστές που προσδιορίζονται µε τεχνικές πολλαπλής γραµµικής παλινδρόµησης Η εξίσωση αυτή έχει επίσης χρησιµοποιηθεί για δεδοµένα σχετικά µε το χρόνο λανθάνουσας φάσης αντικαθιστώντας το k µε το 1/t L. Θερµοκρασία και ph: k = C ph ph ( T T ) (15) Το ph min είναι η χαµηλότερη τιµή ph στην οποία παρατηρείται ανάπτυξη µικροβίων και εξαρτάται από το συγκεκριµένο οξύ (οξικό, γαλακτικό, κιτρικό, κ.ά.) που χρησιµοποιείται. Η θερµοκρασία και το ph, όπως φαίνεται από την παραπάνω σχέση, επίσης δρουν ανεξάρτητα. Θερµοκρασία, ενεργότητα νερού και ph min min (14) 117
126 k = C a a ph ph ( T T ) (16) w wmin min min Ανακεφαλαιώνοντας, την τελευταία δεκαετία έχουν αναπτυχθεί ολοκληρωµένα µοντέλα πρόρρησης και ικανός αριθµός δεδοµένων που επιτρέπουν την ανάπτυξη λογισµικού µε τη δυνατότητα πρόρρησης του ρυθµού ανάπτυξης και αδρανοποίησης της µικροχλωρίδας του τροφίµου και συνεπώς ποσοτικής εκτίµησης του κινδύνου απο παθογόνους µικροοργανισµούς, στις συγκεκριµένες συνθήκες της διεργασίας. Τα θεωρούµενα ως ελέγχοντα χαρακτηριστικά του τροφίµου, όπως το ph, η ενεργότητα νερού, η συγκέντρωση χλωριούχου νατρίου και πιθανόν και οργανικών οξέων ή άλλων αντιµικροβιακών παραγόντων αποτελούν τα προς εισαγωγή δεδοµένα (input) για το τρόφιµο. Επι πλέον τροφοδοτούνται τα χαρακτηριστικά του εξεταζόµενου σταδίου της διεργασίας όπως ο χρόνος, η θερµοκρασία και η µερική πίεση οξυγόνου και άλλων αερίων. Τέτοιο λογισµικό έχει αναπτυχθεί απο τη USDA (U.S. Department of Agriculture) (Pathogen Μodeling Program v.4) και στο Ηνωµένο Βασίλειο από ένα µεγάλο ερευνητικό πρόγραµµα του Υπουργείου Γεωργίας µεταξύ άλλων στο Institute of Food Research, το Campden και το Leatherhead Food Research Association (Food MicroModel). Το Pathogen Μodeling Program v.4 στηρίζεται στην προσοµοίωση των καµπυλών αύξησης των µικροοργανισµών µε την συνάρτηση Gompertz στις διάφορες ελέγχουσες συνθήκες που αναφέρθηκαν. Χρησιµοποιήθηκε η µεγαλύτερη δυνατή βάση δεδοµένων από εκτεταµµένα πειράµατα για τους βασικούς παθογόνους µικροοργανισµούς (Salmonellae, Listeria monocytogenes, Clostridium perfringens, Staphylococcus aureus, Shigella dysentereae κ.λ.π) και εµπλουτίζεται συνεχώς µε δεδοµένα για νέους σηµαντικούς µικροοργανισµούς όπως ο E.coli O157:H7. Το πρόγραµµα επιτρέπει την ποσοτική πρόρρηση της δυνατότητας και της έκτασης ανάπτυξης των κρίσιµων µικροοργανισµών στις συνθήκες και παραµέτρους της διεργασίας παραγωγής. Το Food MicroModel (Food Micromodel Ltd., Surrey, UK) είναι διαθέσιµο ως εµπορικό λογισµικό και βασίζεται σε παρόµοια ως άνω προσέγγιση. ίνει µεγαλύτερες δυνατότητες όσον αφορά το διάστηµα τιµών ορισµένων ελεγχουσών παραµέτρων π.χ. NaCl και τον συνυπολογισµό περισσοτέρων αντιµικροβιακών παραγόντων. ΒΙΒΛΙΟΓΡΑΦΙΑ Food microbiology / M.R. Adams and M.O. Moss, 2000 The Microbiology of safe food / S. J. Forsythe, 2000 Modern food microbiology / James M. Jay, 2000 The microbiological safety and quality of food / Edited by Barbara M. Lund, Tony C. Baird- Parker, 2000 Food hygiene, microbiology and HACCP / S.J. Forsythe and P.R. Hayes, 1998 HACCP : a practical approach / Sara Mortimore, Carol Wallace
127 International Commission on Microbiological Specifications for Foods. Microorganisms in foods 5 : characteristics of microbial pathogens / ICMSF, 1996 International Commission on Microbiological Specifications for Foods of the International Union, Characteristics of microbial pathogens / International Commission on Microbiological Specification for Food, 1996 Food biotechnology : microorganisms / Edited by Y. H. Hui, George G. Khachatourians, 1995 HACCP : establishing hazard analysis critical control point programs / edited by Kenneth E. S., 1995 Μικροβιολογία τροφίµων : βακτήρια-ζύµες-µύκητες, Μπαλατσούρας Γεώργιος,
128 ΚΕΦΑΛΑΙΟ 4 ΘΕΡΜΟΦΥΣΙΚΕΣ Ι ΙΟΤΗΤΕΣ ΤΩΝ ΤΡΟΦΙΜΩΝ Εισαγωγή Η µελέτη και ο σχεδιασµός όλων των διεργασιών των τροφίµων απαιτούν τη γνώση των θερµοφυσικών ιδιοτήτων τους. Τα τρόφιµα είναι γενικά ανοµοιογενή υλικά, µε κύρια συστατικά το νερό, τις πρωτεΐνες, τους υδατάνθρακες και τα λιπαρά. Οι ιδιότητές τους εξαρτώνται άµεσα από τη σύστασή τους. Η µακροδοµή των τροφίµων, π.χ. το πορώδες, το µέγεθος και το σχήµα των σωµατιδίων στα στερεά ή ηµιστερεά τρόφιµα, το µέγεθος των σταγονιδίων ή διασπαρµένων σωµατιδίων και η περιεκτικότητά τους (v/v) σε υγρά τρόφιµα επηρεάζει επίσης τις ιδιότητές τους. Οι θερµοφυσικές ιδιότητες των τροφίµων µπορούν να µετρηθούν µε διάφορες πειραµατικές τεχνικές ή να υπολογισθούν κατά προσέγγιση µε βάση τη σύσταση και τη δοµή τους και βιβλιογραφικά δεδοµένα των ιδιοτήτων των επί µέρους συστατικών. Η απλούστερη παραδοχή θεωρεί ότι το τρόφιµο αποτελείται από n συστατικά, χωρίς αλληλεπιδράσεις οπότε η µάζα και ο όγκος αυτού αποδίδονται από τις σχέσεις: m = V = n m i i= 1 n V i i= 1 (4.1) (4.2) Το κλάσµα µάζας κάθε συστατικού ορίζεται ως Y i : mi Yi = (4.3) m και οι ιδιότητες του τροφίµου µπορούν να εκφρασθούν συναρτήσει των κλασµάτων µάζας και των ιδιοτήτων των επί µέρους συστατικών. Σε ορισµένες διεργασίες µπορεί να µεταβάλλεται η σύσταση ή/και η µακροδοµή του τροφίµου, π.χ. µε αποµάκρυνση ενός συστατικού, όπως του νερού κατά την ξήρανση, µε αλλαγή της κατάστασης ενός συστατικού, όπως πήξη του νερού κατά την κατάψυξη. Σε αυτές τις περιπτώσεις για τον υπολογισµό της µεταβολής των ιδιοτήτων του τροφίµου κατά την κατεργασία και του τελικού προϊόντος µπορούµε να θεωρήσουµε ως βασικά συστατικά του το νερό και τα λοιπά στερεά συστατικά. Πυκνότητα Η πραγµατική πυκνότητα (true density) (ρ) ενός τροφίµου µπορεί να υπολογισθεί από τις πυκνότητες των επί µέρους συστατικών (ρ i ) µε βάση τα κλάσµατα µάζας αυτών (Y i ) ως: 121
129 1 = ρ n i= 1 Y i ρ i (4.4) Η πυκνότητα ενός συστατικού (substance density) είναι η µετρούµενη πυκνότητα αυτού σε µορφή που δεν περιέχει καθόλου πόρους (π.χ. µετά από άλεση σε πολύ µικρά σωµατίδια. Τιµές πυκνότητας των βασικών συστατικών των τροφίµων δίνονται στον Πίνακα 4.1. Η φαινόµενη πυκνότητα (apparent density) (ρ ap ) σχετίζεται µε το πορώδες ή φαινόµενο πορώδες (porosity) του υλικού: ε ap =V a /V ap (4.5) όπου V a, V ap όγκος του υλικού (ολικός) και όγκος των πόρων, αντίστοιχα. Στην περίπτωση των τροφίµων υπάρχουν συχνά αλληλεπιδράσεις φάσεων και πρέπει στον υπολογισµό της φαινόµενης πυκνότητας να ληφθεί υπ όψιν και ο παράγοντας διόρθωσης του όγκου λόγω αυτών των αλληλεπιδράσεων: ε ex =V ex /V ap (4.6) όπου V ex µεταβολή του όγκου που οφείλεται στις αλληλεπιδράσεις και µπορεί να είναι θετική ή αρνητική. Εποµένως µία γενικευµένη σχέση που µπορεί να αποδώσει τη φαινόµενη πυκνότητα του τροφίµου είναι η (4.7), ενώ εάν το πορώδες ή µεταβολή όγκου λόγω αλληλεπιδράσεων είναι αµελητέα οι αντίστοιχοι όροι µπορούν να παραληφθούν. m ρv ρ( Vap Va Vex ) ρ( Vap ε apvap ε exvap ) ρ ap = = = = = ρ(1 ε ap ε V V V V και 1 ρ ap ap ap 1 = 1 ε ε ap n ex i= 1 Y i ρ i ap ap ex ) (4.7) Ο ακριβής ορισµός της φαινόµενης πυκνότητας είναι η πυκνότητα ενός υλικού που περιλαµβάνει όλο τον αέρα ή τα κενά διαστήµατα που σχηµατίζονται εντός του υλικού, και τα οποία ορίζουν το φαινόµενο πορώδες (apparent porosity) του υλικού. Όταν ένα υλικό σωρεύεται ή συσκευάζεται χύµα δηµιουργούνται επί πλέον κενά αέρα που καθορίζουν το πορώδες της κλίνης του υλικού (bulk porosity). Σε αυτή την περίπτωση το ολικό πορώδες είναι το άθροισµα των δύο ανωτέρω. Η πυκνότητα της κλίνης του υλικού (bulk density) προσδιορίζεται από τη σχέση (4.6) µε βάση το ολικό πορώδες. Σε ορισµένες διεργασίες όπως στην ξήρανση µπορεί να συµβαίνει συρρίκνωση του τροφίµου. Σε αυτή την περίπτωση η φαινόµενη πυκνότητα του συρρικνωµένου υλικού µπορεί να υπολογισθεί µε βάση την αρχική φαινόµενη πυκνότητα από τη σχέση: 1 ρ ap 1 = [ ρ apit w + β ]/[1 + w] ρ w (4.8) 122
130 όπου ρ ap, ρ αpit φαινόµενη πυκνότητα του συρρικνωµένου και του αρχικού υλικού, αντίστοιχα (kg/m 3 ) ρ w πυκνότητα του νερού (kg/m 3 ) β συντελεστής συρρίκνωσης: (v IT -v)/[(w IT -w)/ρ w ] v, v IT ειδικός όγκος του συρρικνωµένου και του αρχικού υλικού, αντίστοιχα (m 3 /kg ξηρού στερεού) w, w IT υγρασία του συρρικνωµένου και του αρχικού υλικού σε ξηρή βάση, αντίστοιχα (kg νερού/kg ξηρού στερεού) Πίνακας 4.1. Θερµοφυσικές ιδιότητες συστατικών των τροφίµων Συστατικό Συµβολισµός Πυκνότητα (kg/m 3 ) Ειδική θερµότητα (kj/kg) Θερµική αγωγιµότητα (W/m C) Νερό w Πρωτεΐνες p Ζελατίνη ge Υδατάνθρακες ca Άµυλο st Σακχαρόζη su Λιπαρά fa Ίνες fi Ανόργανα as πάγος I αέρας a Πηγή: Rahman, 1995 και Hallstrom et al, 1990 Θερµική αγωγιµότητα Η θερµική αγωγιµότητα των τροφίµων µεταβάλλεται µε τη σύσταση και στα ετερογενή τρόφιµα επηρεάζεται και από τη δοµή. Ιδιαίτερα τα ινώδη τρόφιµα (π.χ. κρέας) παρουσιάζουν θερµική αγωγιµότητα παράλληλα µε τις ίνες 15-20% µεγαλύτερη από τη θερµική αγωγιµότητα κάθετα προς τις ίνες. Τιµές του συντελεστή θερµικής αγωγιµότητας των βασικών συστατικών των τροφίµων δίνονται στον Πίνακα 4.1. Γενικά, η θερµική αγωγιµότητα µειώνεται καθώς µειώνεται η υγρασία του τροφίµου, λόγω της µεγαλύτερης θερµικής αγωγιµότητας του νερού σε σύγκριση µε τα άλλα συστατικά. Στα ξηρά τρόφιµα η θερµική αγωγιµότητα µειώνεται απότοµα όταν αυξάνει το πορώδες. Η επίδραση του πορώδους στη θερµική αγωγιµότητα είναι πολύ πιο σύνθετη από την επίδρασή του στην πυκνότητα του τροφίµου. Αντίθετα η 123
131 θερµική αγωγιµότητα αυξάνεται κατά την κατάψυξη καθώς ο πάγος έχει πολύ µεγαλύτερη θερµική αγωγιµότητα από το νερό (2.22 έναντι 0.57 W/m C). Ο συντελεστής θερµικής αγωγιµότητας του πάγου αυξάνει µε µείωση της θερµοκρασίας (Πίνακας 4.2), ενώ του νερού µειώνεται. Επί πλέον η κατάψυξη µπορεί να µεταβάλει το πορώδες και επίσης η κατεύθυνση ανάπτυξης των κρυστάλλων του πάγου επηρεάζει τη θερµική αγωγιµότητα του τροφίµου. Για τους παραπάνω λόγους η διατύπωση µαθηµατικών µοντέλων για τον υπολογισµό του συντελεστή θερµικής αγωγιµότητας κατά τη διάρκεια της κατάψυξης είναι ιδιαίτερα δύσκολη. Συνήθως χρησιµοποιούνται οι σχέσεις που χρησιµοποιούνται και στα µη κατεψυγµένα τρόφιµα θεωρώντας τον πάγο ένα επί πλέον συστατικό ή µία επί πλέον φάση σε διασπορά. Ως πρώτη προσέγγιση των συντελεστών θερµικής αγωγιµότητας νωπών, και των αντίστοιχων κατεψυγµένων και αφυδατωµένων τροφίµων, µπορούν να θεωρηθούν οι εµπειρικοί κανόνες (Kostaropoulos): νωπά τρόφιµα υγρασίας >30-40%: k f = W/m C κατεψυγµένα τρόφιµα υγρασίας >30-40%: k ff 2.5k f αφυδατωµένα τρόφιµα: k df 0.1k f όπου k f, k ff, k df συντελεστές θερµικής αγωγιµότητας του αρχικού, του κατεψυγµένου και του ξηρού τροφίµου, αντίστοιχα Πίνακας 4.2. Μεταβολή ιδιοτήτων του πάγου µε τη θερµοκρασία Θερµοκρασία ( C) Πυκνότητα (kg/m 3 ) Ειδική θερµότητα (kj/kg C) Θερµική αγωγιµότητα (W/m C) Πηγή: Heldman and Singh,1981 Για τον ακριβέστερο υπολογισµό του συντελεστή θερµικής αγωγιµότητας έχουν διατυπωθεί διάφορες εξισώσεις µε βάση τη σύσταση του τροφίµου, οι οποίες έχουν καλύτερη ακρίβεια πρόβλεψης στα οµογενή υλικά. Ο Sweat ανέπτυξε µία τέτοια εξίσωση, στηριζόµενος σε δεδοµένα από 430 υγρά και στερεά τρόφιµα, που έχει ικανοποιητική ακρίβεια: k = 0. 58Y Y Y Y Y (4.9) w p ca as fa 124
132 Για τα ετερογενή υλικά έχουν προταθεί µοντέλα µε βάση τη δοµή του υλικού. Θεωρώντας ότι το υλικό αποτελείται από συστατικά ή φάσεις διατεταγµένες σε στρώσεις κλάσµατος όγκου ε i η κάθε µία εάν οι στρώσεις των συστατικών είναι παράλληλες στη ροή θερµότητας: k = ε k (parallel model) (4.10) pa i i εάν οι στρώσεις των συστατικών είναι κάθετες στη ροή θερµότητας (σε σειρά): 1 i = ε (series model) (4.11) k k se i εάν οι στρώσεις των συστατικών διατάσσονται τυχαία ως προς τη ροή θερµότητας: ε1 ε2 ε k k k... k (random model) (4.12) ra = 1 2 n n εάν οι στρώσεις έχουν µικτή διάταξη µε ποσοστό f κάθετο στη ροή θερµότητας και 1-f παράλληλο: 1 f f = 1 + k k k (mixed model) (4.13) mix pa se Στην περίπτωση που το τρόφιµο αποτελείται από δύο φάσεις, µία συνεχή και µία διεσπαρµένη, µε συντελεστή θερµικής αγωγιµότητας k c και k d, αντίστοιχα και κλάσµα όγκου της διεσπαρµένης φάσης ε d, o Maxwell πρότεινε την εξίσωση: k k k k k k d + 2 c 2ε d( c d) m = c (Maxwell model) (4.14) k + 2k + ε ( k k ) d c d c d Η εξίσωση Maxwell προβλέπει ικανοποιητικά τη θερµική αγωγιµότητα όταν η διεσπαρµένη φάση αποτελεί µικρό ποσοστό, ώστε τα σωµατίδια αυτής να είναι αποµακρυσµένα και να µην αλληλεπιδρούν. Εκτός των παραπάνω υπάρχουν και άλλες σχέσεις που στηρίζονται σε θεωρητικές προσεγγίσεις της µετάδοσης θερµότητας ή είναι εµπειρικές σχέσεις που προκύπτουν µε βάση δεδοµένα. Οι περισσότερες εµπειρικές εξισώσεις συσχετίζουν τη θερµική αγωγιµότητα µε την υγρασία του τροφίµου. Οι συντελεστές θερµικής αγωγιµότητας µεταβάλλονται µε µεταβολή της θερµοκρασία, αν και η µεταβολή αυτή είναι µικρή µε την προϋπόθεση ότι δεν υπάρχει αλλαγή φάσης. Στη βιβλιογραφία δίνονται συσχετίσεις του τύπου 2 k = a+ bt + ct για τα βασικά συστατικά των τροφίµων καθώς και για ορισµένα τρόφιµα. (4.15) Τιµές συντελεστών θερµικής αγωγιµότητας για ορισµένα τρόφιµα δίνονται στον Πίνακα 4.3. Ειδική θερµότητα Η ειδική θερµότητα είναι µια αθροιστική ιδιότητα και µπορεί να εκφρασθεί µε βάση τις τιµές ειδικής θερµότητας των επί µέρους συστατικών: 125
133 Πίνακας 4.3. Συντελεστές θερµικής αγωγιµότητας τροφίµων Τρόφιµο Υγρασία (%) Θερµοκρασία ( C) Θερµική αγωγιµότητα (W/m C) Μήλα Χυµός µήλου Φράουλες (-14) Πατάτες Πήγµα αµύλου πατάτας Φασόλια Σιτάρι Αλεύρι σιταριού Μέλι Γάλα νωπό Γάλα συµπυκνωµένο Γάλα σκόνη Κρόκος αυγού Λεύκωµα αυγού Αυγό κατεψυγµένο (-10)-(-6) Βούτυρο Ελαιόλαδο Σπορέλαια Βοδινό κάθετα στις ίνες Βοδινό παράλληλα στις ίνες Χοιρινό κάθετα στις ίνες Χοιρινό παράλληλα στις ίνες Πηγή: Heldman and Singh,
134 n c = cy i i 1 i= (4.16) Η τιµή της ειδικής θερµότητας µεταβάλλεται πολύ µε τη σύσταση του τροφίµου, ιδιαίτερα µε την περιεκτικότητα σε νερό, καθώς η ειδική θερµότητα του νερού είναι 4.18 kj/kg C, ενώ των στερεών συστατικών πολύ µικρότερη 1-2 kj/kg C (Πίνακας 4.1). Οι τιµές που υπολογίζονται θεωρητικά µέσω της εξίσωσης (4.16) εµφανίζουν απόκλιση σε σχέση µε τις πειραµατικές τιµές διαφόρων τροφίµων επειδή η ειδική θερµότητα των συστατικών ποικίλει ανάλογα µε την προέλευση, το δεσµευµένο νερό έχει διαφορετική ειδική θερµότητα από το ελεύθερο νερό και η αλληλεπίδραση των φάσεων µπορεί να προκαλεί µεταβολή στην ειδική θερµότητα. Έτσι µπορεί στην εξίσωση (4.16) να προστεθεί ένας συντελεστής διόρθωσης που πρέπει να προσδιορισθεί πειραµατικά για το κάθε τρόφιµο. Επίσης η ειδική θερµότητα αλλάζει σηµαντικά µε την αλλαγή φάσης, όπως στην κατάψυξη των τροφίµων, λόγω της µεγάλης διαφοράς των τιµών ειδικής θερµότητας πάγου και νερού. Μία κατά προσέγγιση εκτίµηση της ειδικής θερµότητας, προ του σηµείου έναρξης κατάψυξης, για τρόφιµα µεγάλης περιεκτικότητας σε νερό µπορεί να γίνει µέσω της σχέσης: c = 4.18Y w + 2Y s (4.17) όπου Y s =1-Y w Άλλες σχέσεις για προσεγγιστική εκτίµηση της ειδικής θερµότητας διαφόρων κατηγοριών τροφίµων, µε βάση κυρίως την περιεκτικότητα σε νερό, µπορούν να βρεθούν στη βιβλιογραφία. Οι πιο γνωστές είναι του Siebel για τρόφιµα χωρίς λιπαρά και µε ψηλό περιεχόµενο υγρασίας Μ (% επί υγρής βάσης): c = M (4.18) του Charm για τρόφιµα µε στερεό λίπος: c= Y Y Y (4.19) fa s w όπου 2.094, και είναι οι τιµές ειδικής θερµότητας (kj/kg) του λίπους, των στερεών και του νερού των Choi & Okos µε βάση τα βασικά συστατικά του τροφίµου: c= Y Y Y Y Y (4.20) p ca fa as w Τιµές ειδικής θερµότητας διαφόρων τροφίµων, όπως υπολογίζονται µε τις εξισώσεις (4.18), (4.19) και (4.20), σε σύγκριση µε εκείνες που προσδιορίστηκαν πειραµατικά δίνονται στον Πίνακα 4.4. Σε εύρος θερµοκρασιών όπου δεν παρατηρείται αλλαγή φάσης η ειδική θερµότητα µεταβάλλεται λίγο µε τη θερµοκρασία και η µέση τιµή µπορεί να υπολογισθεί µέσω της µεταβολής της ενθαλπίας: 127
135 Πίνακας 4.4. Σύσταση και τιµές ειδικής θερµότητας τροφίµων Τρόφιµο Νερό (%) Πρωτεΐνες (%) Υδατ/κες (%) Λιπαρά (%) Τέφρα (%) Ειδική θερµότητα (kj/kg K) Εξ Εξ Εξ Πειραµατική Μήλα Πορτοκαλοχυµός Πατάτες Αγγούρια Καρότα Γάλα παστερεριωµένο Γάλα αποβουτυρωµένο Γάλα σκόνη Βούτυρο Τυρί άπαχο Άµυλο Κρόκος αυγού Κρέας µόσχου Βοδινό Βοδινό ψητό Ψάρια Γαρίδες Μπέικον Πηγή: Heldman and Singh,
136 H 1 c = = T T T T T1 cdt (4.21) Τιµές µεταβολής της ειδικής θερµότητας των συστατικών των τροφίµων µε τη θερµοκρασία, που µπορούν να χρησιµοποιηθούν για τον υπολογισµό της µέσης ειδικής θερµότητας του κάθε συστατικού από την εξίσωση (4.21), δίνονται στον Πίνακα 4.5. Η µέση ειδική θερµότητα του τροφίµου µπορεί να υπολογισθεί στη συνέχεια από την (4.16). Επίσης στη βιβλιογραφία προτείνονται διάφορες σχέσεις που αποδίδουν την ειδική θερµότητα ως συνάρτηση της θερµοκρασίας και της σύστασης του τροφίµου, ιδιαίτερα κάτω του σηµείου έναρξης κατάψυξης. Πίνακας 4.5. Συσχέτιση της ειδικής θερµότητας των συστατικών των τροφίµων µε τη θερµοκρασία σε εύρος -40 έως 150 C Συστατικό Εξίσωση Νερό α c w = T T Νερό β cw = T T Πάγος ci = T Πρωτεΐνες c 3 p T T Λιπαρά c = + fa T T Υδατάνθρακες cca = T T Ινες cfi = T T Τέφρα cas = T T α :Τ:-40 έως 0 C, β :Τ:0 έως 150 C Πηγή: Rahman, Στην περιοχή θερµοκρασιών όπου συµβαίνει αλλαγή φάσης η ειδική θερµότητα αποδίδεται ως φαινόµενη ειδική θερµότητα και συµπεριλαµβάνει τη λανθάνουσα θερµότητα της αλλαγής φάσης. Η συνήθης προσέγγιση είναι η έκφραση της ενθαλπίας του κατεψυγµένου τροφίµου, που περιέχει την αισθητή και τη λανθάνουσα θερµότητα, ως συνάρτησης της θερµοκρασίας και ακολούθως η έκφραση της ειδικής θερµότητας µέσω του διαφορικού dh/dt. Με βάση αυτή την προσέγγιση έχουν προταθεί διάφορες σχέσεις. Σύµφωνα µε τον Van Beek (από Rahman, 1995): 2 c = c ( 1 Y ) + c Y ( T / T) + c Y ( 1 T / T) LY T / T (4.22) so wo w wo F I wo F wo F όπου Τ σε C και το κλάσµα µάζας του δεσµευµένου νερού πρέπει να προστεθεί στο κλάσµα µάζας των στερεών. Ο Schwartzberg (1976) για τον προσδιορισµό της ειδικής θερµότητας και της ενθαλπίας κάτω του σηµείου έναρξης κατάψυξης κατέληξε στις εξισώσεις: 129
137 2 M RT w Fw c = cfo + ( Yw Ywo )( cw ci ) + ( 1 Ywo ) 2 08.( cw ci) (4.23) M so ( T TFw ) H = ( T T )[ c + ( Y Y )( c c )] + ref Fo w wo w I M 2 RT (4.24) w Fw ( T Tref )( 1 Ywo ) 08.( cw ci) M so ( TFw T)( TFw Tref ) όπου c Fo η ειδική θερµότητα του τροφίµου αµέσως πριν την έναρξη κατάψυξης Τ σε Κ και T ref θερµοκρασία αναφοράς, θεωρούµενη συνήθως ίση µε 233 K (-40 C). Ο Chen (1985) πρότεινε τις ακόλουθες εξισώσεις για τον προσδιορισµό της ειδικής θερµότητας και της ενθαλπίας των τροφίµων σε θερµοκρασίες χαµηλότερες και ψηλότερες του σηµείου έναρξης κατάψυξης: 2 RM T w Fw c = Yso + Yso 2 για T<T F (4.25) Mso ( T TFw ) [ so so ] c = Y 015. Y 3 για T>T F (4.26) H = ( T T ) Y + Y ref so so [ Fo F so so ] 2 RM T w Fw για T<T F Mso ( T TFw )( Tref TFw ) (4.27) H = H + ( T T )( Y 015. Y 3 ) για T>T F (4.28) όπου H Fo η ενθαλπία του τροφίµου αµέσως πριν την έναρξη κατάψυξης. Ανάλογες εξισώσεις έχουν προταθεί και από άλλους ερευνητές. Λανθάνουσα θερµότητα πήξης και εξάτµισης του νερού Η λανθάνουσα θερµότητα πήξης του καθαρού νερού µεταβάλλεται µε τη θερµοκρασία και η γραµµική συσχέτιση αυτών είναι: Lw = ( T ) (4.29) όπου L w σε kj/kg και Τ σε Κ. Για τη λανθάνουσα θερµότητα πήξης του νερού στα τρόφιµα έχουν προταθεί από τους Schwartzberg (1976, από Rahman, 1995) και Riedel (1978, από Rahman, 1995), αντίστοιχα οι σχέσεις: L = L ( c c )( T T ) (4.30) wf w w I Fw 3 2 L wf = T T (4.31) όπου Τ σε C. Η λανθάνουσα θερµότητα εξάτµισης του νερού στα τρόφιµα εξαρτάται από τη σύσταση των προϊόντων και τη θερµοκρασία. Η διαφορά της από τη λανθάνουσα θερµότητα εξάτµισης του καθαρού νερού έχει συσχετισθεί µε το κλάσµα µάζας επί 130
138 ξηρής βάσης (Μ w ) ή επί υγρής βάσης (Y w )µε εµπειρικές σχέσεις του τύπου: Q = ξ exp( M / η) (4.32) w Q = (4.33) b am w Q = L w 1+ ξ[exp( ηy )]} (4.34) { w όπου ξ, η, α, b σταθερές που εξαρτώνται από το τρόφιµο Θερµική διαχυτότητα Η θερµική διαχυτότητα α=k/ρc των τροφίµων επηρεάζεται προφανώς από τις παραµέτρους που επηρεάζουν τις τρεις προαναφερθείσες ιδιότητες. Στη βιβλιογραφία µπορούν να βρεθούν εµπειρικές σχέσεις για τον προσδιορισµό του συντελεστή θερµικής διαχυτότητας διαφόρων τροφίµων ως συνάρτηση της σύστασης και της θερµοκρασίας. Γενικά µπορεί να θεωρηθεί ότι ισχύουν οι εµπειρικοί κανόνες (Kostaropoulos): νωπά τρόφιµα υγρασίας >30: α f 1.4x10-7 m 2 /s κατεψυγµένα τρόφιµα υγρασίας >30-40%: a ff 3a f ξηρά τρόφιµα: a df 0.8a f λάδια και λίπη: α fa 0.6a f όπου a f, a ff, a df, a fa συντελεστές θερµικής διαχυτότητας του αρχικού, του κατεψυγµένου, του ξηρού τροφίµου και των λιπαρών, αντίστοιχα Ενεργότητα νερού-ισόθερµες ρόφησης Η ενεργότητα νερού (a ή a w ) σε ένα τρόφιµο σε ισορροπία µε το περιβάλλον του ορίζεται ως ο λόγος της µερικής πίεσης ατµών του περιβάλλοντος σε ισορροπία µε το τρόφιµο (p) προς την τάση ατµών του καθαρού νερού (πίεση κορεσµού) (p o ): p RH a = o p = 100 (4.35) όπου RH σχετική υγρασία του χώρου σε ισορροπία µε το τρόφιµο Η ενεργότητα νερού σε ένα ιδανικό διάλυµα ισούται µε το µοριακό κλάσµα του νερού στο διάλυµα (Χ w ) α = (4.36) X w Τα διαλύµατα µεγαλύτερης συγκέντρωσης διαλυτού συστατικού αποκλίνουν από την ιδανική συµπεριφορά και για τον υπολογισµό της ενεργότητας του νερού εισάγεται ο συντελεστής ενεργότητας του διαλυµένου συστατικού (γ) στην εξίσωση (4.36): α = γx w (4.37) 131
139 Τα τρόφιµα απέχουν από την ιδανική συµπεριφορά επειδή υπάρχουν αλληλεπιδράσεις µεταξύ των διαλυµένων συστατικών και ορισµένα διαλυτά συστατικά δεν βρίσκονται σε πραγµατική διάλυση επειδή είναι συνδεδεµένα µε αδιάλυτα συστατικά, όπως π.χ. ορισµένα άλατα µε τις πρωτεΐνες. Για τον υπολογισµό της ενεργότητας νερού τροφίµων έχουν διατυπωθεί διάφορες εµπειρικές εξισώσεις, οι οποίες στηρίζονται στη θεώρηση του τροφίµου ως µίγµα πολλών συστατικών και συνυπολογίζουν τη συνεισφορά αυτών των συστατικών στη µείωση της ενεργότητας. Μία από τις πλέον αποδεκτές είναι η εξίσωση Norrish που υπολογίζει την ενεργότητα διαλύµατος ενός συστατικού: 2 α = X w [exp( kx s )] (4.38) όπου X s µοριακό κλάσµα του διαλυµένου συστατικού k σταθερά εξαρτώµενη από το διαλυµένο συστατικό Η σταθερά k έχει προσδιορισθεί για πολλά διαλυτά συστατικά που απαντώνται σε τρόφιµα και στο γεγονός αυτό οφείλεται η ευρεία χρησιµοποίηση της εξίσωσης Norrish. Τιµές της σταθεράς k δίνονται στον Πίνακα 4.6. Για διάλυµα περισσοτέρων συστατικών ο Ross, µε την παραδοχή ότι οι αλληλεπιδράσεις µεταξύ των διαλυτών συστατικών είναι ασήµαντες στο µίγµα, κατέληξε στη σχέση: α = α α α... (4.39) α n όπου a i η ενεργότητα νερού του συστατικού i εάν θεωρηθεί διαλυµένο σε όλο το νερό του διαλύµατος. Η σχέση ισορροπίας του νερού µεταξύ του τροφίµου και της αέριας φάσης σε σταθερή θερµοκρασία µπορεί να αποδοθεί από τις ισόθερµες ρόφησης. Αυτές συσχετίζουν την περιεκτικότητα του νερού στο τρόφιµο (υγρασία του τροφίµου) µε τη µερική πίεση ατµών στην αέρια φάση (p), ή µε την ενεργότητα του νερού (a). Οι ισόθερµες ρόφησης και η ενεργότητα νερού του τροφίµου προσδιορίζονται συνήθως στα τρόφιµα µε δύο βασικές µεθόδους. Στην πρώτη ένα τρόφιµο γνωστής υγρασίας τοποθετείται σε ένα αεροστεγή µικρό θάλαµο και αφήνεται να έρθει σε ισορροπία µε το περιβάλλον του. Η σχετική υγρασία του χώρου ( ή η ενεργότητα νερού) µετριέται µετά την αποκατάσταση της ισορροπίας µε κατάλληλους αισθητήρες. Στη δεύτερη µέθοδο µικρά δείγµατα τροφίµου τοποθετούνται σε χώρους σταθερής σχετικής υγρασίας. Μετά την αποκατάσταση της ισορροπίας προσδιορίζεται η υγρασία του τροφίµου σταθµικά µετά από ξήρανση, ή µε άλλη κατάλληλη µέθοδο. Η σταθερή σχετική υγρασία στο χώρο επιτυγχάνεται µε χρήση κορεσµένων διαλυµάτων αλάτων ή διαλυµάτων θειικού οξέος. 132
140 Πίνακας 4.6. Τιµές της σταθεράς k της εξίσωσης (4.38) για διάφορα διαλυτά συστατικά Συστατικό k Συστατικό k Σάκχαρα Γαλακτόζη Ξυλόζη Γλυκόζη Σακχαρόζη Λακτόζη Φρουκτόζη Μαλτόζη DE a Πολυόλες Γλυκερόλη Προπυλενογλυκόλη Μανιτόλη ,3 βουτυλενογλυκόλη Ξυλιτόλη Σορβιτόλη Αµίδια Αλανίνη Γλυκολαµίδιο β-αλανίνη Λακταµίδιο Γλυκίνη Ουρία Οξέα Α-Αµυνοβουτυρικό Μηλικό Γαλακτικό Τρυγικό Κιτρικό Άλατα KCl NaCl a DE: Dextrose equivalent (ισοδύναµο δεξτρόζης) Πηγή: Rahman, Οι ισόθερµες των τροφίµων είναι συνήθως σιγµοειδείς καµπύλες, όπως φαίνονται στο σχήµα 4.1. και έχουν αποδοθεί προσεγγιστικά από διάφορες µαθηµατικές εξισώσεις. Στο σχήµα 4.1 φαίνεται και η υστέρηση που παρουσιάζουν τα περισσότερα τρόφιµα µεταξύ ρόφησης και εκρόφησης. Στο φαινόµενο της υστέρησης, τα τρόφιµα, κατά τη ρόφηση υγρασίας, εµφανίζουν µικρότερη περιεκτικότητα νερού από ότι κατά την εκρόφηση, σε ισορροπία µε περιβάλλον της ίδιας σχετικής υγρασίας. Το φαινόµενο της υστέρησης ερµηνεύεται από τη δηµιουργία µη αντιστρεπτών µεταβολών κατά τη ρόφηση υγρασίας από το τρόφιµο. Η σχέση της υγρασίας του τροφίµου µε τη µερική πίεση ατµών στην αέρια φάση σε ισορροπία εξαρτάται από τον τρόπο µε τον οποίο το νερό συγκρατείται από το τρόφιµο. Ένα τµήµα του νερού είναι ισχυρά δεσµευµένο στο τρόφιµο ως µονοµοριακό στρώµα. Οι ειδικές θέσεις στις οποίες δεσµεύεται αυτό το νερό περιλαµβάνουν τις οµάδες υδροξυλίων των πολυσακχαριτών, τις καρβονυλοµάδες και αµινοµάδες των πρωτεϊνών κ.ά. Η εκτίµηση της ποσότητας αυτού του ισχυρά δεσµευµένου νερού που καλείται και τιµή µονοµοριακού στρώµατος (monolayer value) µπορεί να γίνει µέσω της εξίσωσης BET (Brunauer-Emmet-Teller), η οποία είναι µία από τις εξισώσεις που προσεγγίζουν την ισόθερµη ρόφησης: wbmca w = (4.40) ( 1 a)[ 1+ ( C 1) a] 133
141 Σχήµα 4.1. Τυπική ισόθερµη ρόφησης-εκρόφησης τροφίµου ή a 1 C 1 = + w( 1 a) w C w C a bm bm (4.41) όπου a ενεργότητα νερού w υγρασία του τροφίµου (kg H 2 O/kg ξηρού στερεού) w bm τιµή µονοµοριακού στρώµατος (kg H 2 O/kg ξηρού στερεού) C σταθερά Για τον υπολογισµό της τιµής µονοµοριακού στρώµατος κατασκευάζεται η ισόθερµη ΒΕΤ µε άξονες την ενεργότητα νερού (a) και το λόγο a/w(1-a). Η µονοστρωµατική τιµή (w bm ) και η σταθερά C υπολογίζονται από την αποτέµνουσα (1/w bm C) και την κλίση [(C-1)/w bm C] της ευθείας. Η εξίσωση ΒΕΤ συνήθως θεωρείται ότι εκφράζει µε καλή προσέγγιση τα δεδοµένα της ισοθέρµου ρόφησης µέχρι τιµή ενεργότητας Επίσης η τιµή µονοµοριακού στρώµατος που υπολογίζεται µε την εξίσωση ΒΕΤ αποδίδει ικανοποιητικά το νερό το δεσµευµένο σε πολικές θέσεις των ξηρών τροφίµων. Πιο ικανοποιητική προσέγγιση της ισοθέρµου ρόφησης για τα περισσότερα τρόφιµα και για µεγαλύτερο εύρος τιµών ενεργότητας νερού (µέχρι 0.90 ή 0.95) δίνεται από την εξίσωση GAB (Guggenheim-Anderson-de Boer): wgmyka w = (4.42) ( 1 Ka)( 1 Ka + YKa) όπου w gm τιµή µονοµοριακού στρώµατος (kg H 2 O/kg ξηρού στερεού) K, Y σταθερές που σχετίζονται µε την επίδραση της θερµοκρασίας Ο υπολογισµός των σταθερών της εξίσωσης GAB στηρίζεται στο µετασχηµατισµό της εξίσωσης 4.42 στην: a K = 1 a + 1 a + (4.43) w w Y w Y w YK gm gm gm 134
142 Οι συντελεστές του πολυονύµου της (4.43) προσδιορίζονται µε πολυονιµική προσέγγιση της καµπύλης που προκύπτει αν κατασκευασθεί διάγραµµα a/w ως προς α µε βάση τα πειραµατικά δεδοµένα. Τιµές του µονοµοριακού στρώµατος κατά ΒΕΤ και GAB και των αντίστοιχων σταθερών των δύο εξισώσεων υπάρχουν στη βιβλιογραφία για διάφορα τρόφιµα και συστατικά τροφίµων. Το µονοµοριακό στρώµα νερού αντιστοιχεί στο πρώτο τµήµα των ισοθέρµων ρόφησης (ζώνη Ι, σχήµα 4.1) και ανέρχεται σε g/g στερεών και οι τιµές ενεργότητας που αντιστοιχούν σε αυτό δεν υπερβαίνουν συνήθως το Το λιγότερο ισχυρά δεσµευµένο νερό αποτελεί τις πολυστρωµατικές στοιβάδες και αντιστοιχεί στη ζώνη ΙΙ της ισοθέρµου σε τιµές ενεργότητας µέχρι 0.75 περίπου. Επί πλέον του δεσµευµένου νερού υπάρχει ένα µέρος νερού παγιδευµένο σε τριχοειδείς πόρους, το οποίο παρουσιάζει µειωµένη τάση ατµών. Η ενεργότητα νερού µειώνεται όσο µειώνεται η ακτίνα των πόρων ενός υλικού. Η ακριβής µείωση της ενεργότητας νερού λόγω της ύπαρξης τριχοειδών πόρων στα τρόφιµα δεν είναι εύκολο να υπολογισθεί, αλλά έχει εκτιµηθεί από εξισώσεις και πίνακες που υπάρχουν στη βιβλιογραφία. Το ελεύθερο νερό στα τρόφιµα εµφανίζει µειωµένη τάση ατµών λόγω των διαφόρων συστατικών που είναι διαλυµένα σε αυτό και αντιστοιχεί στη ζώνη ΙΙΙ των ισοθέρµων ρόφησης. Για τρόφιµα µε µεγάλη περιεκτικότητα σε ελεύθερο νερό (α>0.9) η ενεργότητα νερού µπορεί κατά προσέγγιση να υπολογισθεί µέσω των εξισώσεων ( ) λαµβάνοντας υπ όψιν µόνο τα διαλυτά συστατικά. Σύµβολα α=k/ρc θερµική διαχυτότητα (m 2 /s) a ή α w ενεργότητα νερού β συντελεστής συρρίκνωσης γ συντελεστής ενεργότητας c ειδική θερµότητα (J/kg C) C σταθερά της εξίσωσης (4.40) Η µεταβολή ενθαλπίας (kj/kg) ε πορώδες ή παράγοντας διόρθωσης όγκου ή κλάσµα όγκου H ενθαλπία του τροφίµου (J/kg) k συντελεστής αγωγής θερµότητας (W/m Κ) k σταθερά της εξίσωσης (4.38) K σταθερά της εξίσωσης (4.42) L λανθάνουσα θερµότητα πήξης ή εξάτµισης (kj/kg) m µάζα (kg) M µοριακό βάρος 135
143 Μ w κλάσµα µάζας νερού επί ξηρής βάσης p µερική πίεση ατµών (atm) p o τάση ατµών του καθαρού νερού (πίεση κορεσµού) (atm) ρ πυκνότητα (kg/m 3 ) R=8.314 J/mole K (σταθερά των αερίων) RH σχετική υγρασία Τ θερµοκρασία ( C ή K) T ref θερµοκρασία αναφοράς, θεωρούµενη συνήθως ίση µε -40 C v ειδικός όγκος (m 3 /kg ξηρού στερεού) V όγκος (m 3 ) w υγρασία (kg H 2 O/kg ξηρού στερεού) w bm τιµή µονοµοριακού στρώµατος κατά BET (kg H 2 O/kg ξηρού στερεού) w gm τιµή µονοµοριακού στρώµατος κατά GAB (kg H 2 O/kg ξηρού στερεού) Χ µοριακό κλάσµα Y κλάσµα µάζας (υγρή βάση) Y σταθερά της εξίσωσης (4.42) είκτες α αέρας ap φαινόµενη τιµή as ανόργανα συστατικά c διεσπαρµένη φάση ca υδατάνθρακας d συνεχής φάση df αφυδατωµένο τρόφιµο ex λόγω αλληλεπιδράσεων f τρόφιµο fa λιπαρό fi ίνες ff κατεψυγµένο τρόφιµο F έναρξη κατάψυξης Fο τιµή αµέσως πριν την έναρξη κατάψυξης Fw σηµείο πήξης του νερού i συστατικό i Ι πάγος IT αρχική τιµή p πρωτεΐνη s στερεό 136
144 so w wo wf στερεά ή διαλυµένα συστατικά νερό νερό πριν την έναρξη κατάψυξης νερό στο τρόφιµο Βιβλιογραφία Hallstrom B. Skjolderbrand C and Tragardh C (1990) Heat Transfer and Food Products, Elsevier Applied Sci., London, pp Heldman D.R. and Singh R.P. (1981) Food Process Engineering, 2 nd ed., The AVI Publishing Co. Inc., Westport, Connecticut. Rahman S. (1995) Food Properties Handbook, CRC Press, Boca Raton, pp Saravacos G.D. and Maroulis Z.B. (2001) Transport Properties of Foods, Marcel Dekker Inc., New York, pp ,
145 138
146 ΚΕΦΑΛΑΙΟ 5 ΙΕΡΓΑΣΙΕΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΚΑΙ ΣΥΝΤΗΡΗΣΗΣ ΤΩΝ ΤΡΟΦΙΜΩΝ Εισαγωγή Η βιοµηχανία τροφίµων επεξεργάζεται διαφορετικές πρώτες ύλες για να παράγει µία µεγάλη ποικιλία προϊόντων τα οποία να ικανοποιούν τον καταναλωτή. Οι βασικοί στόχοι της επεξεργασίας είναι: Η παραγωγή τροφίµων που θα παρέχουν τα απαραίτητα θρεπτικά συστατικά για τον άνθρωπο. Η παραγωγή προϊόντων µε βελτιωµένα οργανοληπτικά χαρακτηριστικά (άρωµα, γεύση, χρώµα, υφή) που θα τύχουν µεγαλύτερης αποδοχής από τον καταναλωτή. Η αύξηση της ποικιλίας των προϊόντων για να προσελκύσουν περισσότερους καταναλωτές. Με την ευρύτερη έννοια εδώ εντάσσεται και η µεταποίηση ενός τροφίµου σε άλλη µορφή που µπορεί να επεξεργασθεί περαιτέρω προς τελικό προϊόν (π.χ. η άλεση σπόρων προς αλεύρι). Η παράταση της διάρκειας ζωής του προϊόντος µε διατήρηση αποδεκτής ποιότητας. Καθένας από τους παραπάνω στόχους υπάρχει σε µικρότερο ή µεγαλύτερο βαθµό στην παραγωγή όλων των τροφίµων, αλλά η παραγωγή ενός συγκεκριµένου προϊόντος µπορεί να στηρίζεται περισσότερο σε έναν από αυτούς. Για παράδειγµα τα κατεψυγµένα λαχανικά πρέπει να έχουν οργανοληπτικά και θρεπτικά χαρακτηριστικά όσο το δυνατόν πλησιέστερα στα νωπά, αλλά και διάρκεια ζωής µερικών µηνών αντί ηµερών. Εποµένως στόχος της κατάψυξης είναι η παράταση της διάρκειας ζωής του προϊόντος. Αντίθετα στην παραγωγή προϊόντων ζαχαροπλαστικής, καραµελοποιίας, σοκολατοποιίας κ.α. βασικός στόχος είναι η αύξηση της ποικιλίας των προϊόντων (προϊόντα µε διαφορετικό άρωµα, νέες γεύσεις, άλλη µορφή κλπ.) που θα προσελκύσουν τον καταναλωτή. Οι κυριότερες διεργασίες στη βιοµηχανία τροφίµων Οι διεργασίες που χρησιµοποιεί η βιοµηχανία τροφίµων διαφέρουν πολύ, ανάλογα µε τις πρώτες ύλες, το στόχο της επεξεργασίας και τα προϊόντα που πρόκειται να παραχθούν. Ένα συνοπτικό διάγραµµα διάφορων πιθανών διεργασιών δίνεται στο σχήµα 5.1. Οι πρώτες ύλες που φθάνουν στη βιοµηχανία µπορεί να έχουν διάφορες µορφές: από υγρά χαµηλού ιξώδους έως στερεά. Αυτές πρέπει να µεταφερθούν µε κατάλληλα σχεδιασµένα συστήµατα. Στο σχεδιασµό των συστηµάτων διακίνησης των υγρών τροφίµων είναι απαραίτητη η γνώση των ρεολογικών ιδιοτήτων τους, καθώς τα 139
147 περισσότερα τρόφιµα έχουν µη νευτονικά ρεολογικά χαρακτηριστικά. Η διακίνηση των στερεών µπορεί να γίνει µε πολύ διαφορετικές διατάξεις: πνευµατική µεταφορά για άλευρα και σκόνες, µεταφορά σε κανάλια για καρπούς κλπ. Νευτωνικά Υγρά Υγρά χαµηλής συνεκτικότητας Παχύρευστα υγρά Μαλακά στερεά Σκληρά στερεά Είσοδος µονάδας Ροή ρευστών ιακίνηση στερεών ιαχωρισµός Άλεση Ανάµιξη Θέρµανση Ψύξη Συµπύκνωση Αφυδάτωση Κατάψυξη Υγρά µεγάλης συνεκτικότητας Ξηρά στερεά Υγρά Στερεά Κατεψυγµένα στερεά Έξοδος µονάδας Συσκευασία Σχήµα 5.1. ιάγραµµα πιθανών διεργασιών σε µία βιοµηχανία τροφίµων Στη συνέχεια είναι πιθανόν να υπεισέρχονται διεργασίες διαχωρισµού των πρώτων υλών σε συστατικά. Αυτές οι διεργασίες περιλαµβάνουν µηχανικούς διαχωρισµούς µε φυγοκέντριση, διήθηση ή καταβύθιση στερεών και φυσικούς διαχωρισµούς µε εξάτµιση, εκχύλιση ή µεµβράνες. Επίσης είναι πιθανόν να απαιτείται άλεση των στερεών προς µικρότερα µεγέθη ή µείωση του µεγέθους των σταγονιδίων της διεσπαρµένης φάσης (γαλακτωµατοποίηση) σε τρόφιµα τύπου γαλακτώµατος. Συχνά ακολουθεί ανάµιξη ορισµένων πρώτων υλών (στερεών, υγρού/στερεού ή υγρού/υγρού). 140
148 Οι φυσικές διεργασίες που απαντώνται σχεδόν σε όλες τις βιοµηχανίες τροφίµων είναι οι διεργασίες µεταφοράς θερµότητας. Σχεδόν κάθε επεξεργασµένο τρόφιµο έχει υποστεί θέρµανση ή ψύξη σε κάποιο σηµείο της επεξεργασίας από την πρώτη ύλη µέχρι το τελικό προϊόν. Ειδικότερα οι διεργασίες µεταφοράς θερµότητας περιλαµβάνουν τη θέρµανση ή ψύξη σε εναλλάκτες ή θαλάµους (αεροψυκτήρες, υδροψυκτήρες), την παστερίωση, αποστείρωση και το ζεµάτισµα των τροφίµων. Ο σχεδιασµός και η εφαρµογή αυτών των διεργασιών σε ένα τρόφιµο γίνεται µε ιδιαίτερη προσοχή, δεδοµένης της θερµοευαισθησίας του και της υποβάθµισης της ποιότητας σε υψηλές θερµοκρασίες. Η κατάψυξη είναι επίσης µια διεργασία µεταφοράς θερµότητας που εφαρµόζεται συχνά στη βιοµηχανία τροφίµων, καθώς όλο και περισσότερα προϊόντα διατίθενται κατεψυγµένα. Η συµπύκνωση και η αφυδάτωση (ξήρανση) εµπλέκουν µεταφορά θερµότητας και µάζας, µε στόχο τη µείωση του όγκου (και της περιεκτικότητας σε νερό) υγρών τροφίµων ή την παραγωγή αφυδατωµένων τροφίµων µε αυξηµένη διάρκεια ζωής. Τέλος η κρυστάλλωση εφαρµόζεται για τον διαχωρισµό και την παραλαβή προϊόντων από διαλύµατα (π.χ. της ζάχαρης) ή για την επίτευξη ορισµένων ρεολογικών χαρακτηριστικών (π.χ. ελεγχόµενη κρυστάλλωση των λιπαρών στις µαργαρίνες και τη σοκολάτα). Βέβαια κρυστάλλωση (του νερού) συµβαίνει και κατά την κατάψυξη ή τη συµπύκνωση µε κατάψυξη. Η συσκευασία των προϊόντων ακολουθεί τις προαναφερθείσες διεργασίες ή µπορεί να γίνεται σε ένα ενδιάµεσο στάδιο, όπως συσκευασία τροφίµων πριν την αποστείρωση ή πριν την κατάψυξή τους. Επί πλέον των βασικών διεργασιών που αναφέρθηκαν παραπάνω στη βιοµηχανία τροφίµων εφαρµόζονται πολλές βοηθητικές κατεργασίες, όπως ο καθαρισµός των πρώτων υλών, η αποφλοίωση ή αποστέωση, η ταξινόµηση πρώτων υλών και προϊόντων, ο καθαρισµός και η απολύµανση του εξοπλισµού και των χώρων. 141
149 ΚΕΦΑΛΑΙΟ 6 ΘΕΡΜΑΝΣΗ ΚΑΙ ΨΥΞΗ ΤΩΝ ΤΡΟΦΙΜΩΝ Εισαγωγή Η θέρµανση και η ψύξη των τροφίµων είναι οι διεργασίες που απαντώνται συχνότερα από όλες τις άλλες στη βιοµηχανία τροφίµων. Σχεδόν όλα τα επεξεργασµένα τρόφιµα θερµαίνονται ή/και ψύχονται σε κάποιο στάδιο µεταξύ της παραλαβής της πρώτης ύλης και της διάθεσης του τελικού προϊόντος. Επί πλέον διεργασίες µεταφοράς θερµότητας προς ή από το τρόφιµο είναι οι διεργασίες που σχετίζονται µε τη συντήρηση του τροφίµου, όπως η ψύξη, η κατάψυξη, η παστερίωση, η αποστείρωση, το ζεµάτισµα και η ξήρανση. Επίσης µεταφορά θερµότητας έχουµε σε διεργασίες παρασκευής ορισµένων προϊόντων όπως το ψήσιµο και το τηγάνισµα. Οι ιδιαιτερότητες που πρέπει να λαµβάνονται υπ όψιν στο σχεδιασµό και την εφαρµογή µιας διεργασίας µεταφοράς θερµότητας στα τρόφιµα είναι: -Η καταστροφή θρεπτικών συστατικών και οργανοληπτικών χαρακτηριστικών στις υψηλές θερµοκρασίες. -Η καταστροφή µικροοργανισµών και ενζύµων σε υψηλές θερµοκρασίες, που είναι εξ άλλου και ο στόχος των θερµικών διεργασιών συντήρησης. -Η δυνατότητα επιβίωσης και ο ρυθµός ανάπτυξης µικροοργανισµών, δράσης των ενζύµων και πραγµατοποίησης χηµικών δράσεων στο τρόφιµο σε συνάρτηση µε τη θερµοκρασία. Για τους υπολογισµούς µεταφοράς θερµότητας στις διεργασίες που προαναφέρθηκαν λαµβάνονται υπ όψιν οι θερµοφυσικές ιδιότητες των τροφίµων, που µπορούν να προσδιορισθούν πειραµατικά στο ίδιο το τρόφιµα ή να υπολογισθούν προσεγγιστικά µε βάση τη σύστασή του. Μεταφορά θερµότητας µε αγωγή Κατά τη θέρµανση ή ψύξη πολλών τροφίµων, συσκευασµένων ή µη, η ροή θερµότητας από την επιφάνεια στο εσωτερικό του τροφίµου γίνεται µε αγωγή σε µη µόνιµη κατάσταση. Η µεταβολή της θερµοκρασίας στο τρόφιµο, θεωρώντας την πιο γενική περίπτωση της αγωγής και στις τρεις διαστάσεις και παραγωγή θερµότητας (q, J/s) στο εσωτερικό του τροφίµου, δίνεται από την εξίσωση: T T T T ρ c p k x k y + k z + q t = + x x y y z z (6.1) Η πυκνότητα (ρ, kg/m 3 ), η ειδική θερµότητα (c p, J/kg C) και ο συντελεστής θερµικής αγωγιµότητας (k, W/m C) του τροφίµου εξαρτώνται από τη θερµοκρασία. 141
150 Επί πλέον, ο συντελεστής θερµικής αγωγιµότητας είναι συνάρτηση του χώρου σε τρόφιµα τα οποία δεν είναι οµογενή και ισότροπα ως προς την αγωγή θερµότητας. Παρ όλα αυτά, αν το εύρος της θερµοκρασίας είναι µικρό, για απλούστερη επίλυση της εξίσωσης, συχνά γίνεται οι παραδοχή ότι τα τρόφιµα είναι οµογενή και ισότροπα και οι ιδιότητες τους σταθερές. Παραγωγή θερµότητας στο εσωτερικό του τροφίµου µπορεί να έχουµε λόγω της αναπνοής (που είναι εξώθερµη) ή ως λανθάνουσα θερµότητα κατά την αλλαγή φάσης του νερού, π. χ. κατά την κατάψυξη. Σε άλλες διεργασίες, όπου δεν παράγεται θερµότητα στο τρόφιµο και θεωρώντας το οµογενές και ισότροπο η εξίσωση (6.1) µπορεί να γραφεί ως: α T T T T = t (6.2) x y z όπου a=k/ρc p (m 2 /s) η θερµική διαχυτότητα του τροφίµου. Η αγωγή θερµότητας σε πλάκα ορισµένου πάχους και απείρου µήκους και πλάτους, κύλινδρο απείρου µήκους και σφαίρα αντιµετωπίζεται συνήθως µε οµοιόµορφο τρόπο θεωρώντας αγωγή σε µία διάσταση και συµµετρία περί τον άξονα ή το κέντρο του αντικειµένου. Οπότε η εξίσωση (6.1) γίνεται: ρ T c t r k T Zk T p = r + r r (6.3) όπου Z=0 για πλάκα Z=1 για κύλινδρο απείρου µήκους Z=2 για σφαίρα r απόσταση από το κέντρο ή τον άξονα συµµετρίας του αντικειµένου Αρχικές και οριακές συνθήκες Η αρχική θερµοκρασία του τροφίµου, πριν τη θέρµανση ή την ψύξη, είναι συνήθως σταθερή. Εποµένως ως αρχική συνθήκη για την επίλυση των παραπάνω εξισώσεων θεωρούµε Τ=Τ IT για κάθε r, για t=0 όπου T IT αρχική θερµοκρασία του τροφίµου ( C) Η συνήθης οριακή συνθήκη είναι η πρόσδοση ή απαγωγή θερµότητας από την επιφάνεια του τροφίµου µε συναγωγή, η οποία γράφεται: T hc A( Tm Tr = R ) = ka r (6.4) r= R όπου h c επιφανειακός συντελεστής συναγωγής (W/m 2 C) Α επιφάνεια εναλλαγής θερµότητας (m) T m θερµοκρασία του µέσου θέρµανσης ή ψύξης ( C) 142
151 Η οριακή συνθήκη όπως δίνεται στην εξίσωση (6.4) µπορεί να καλύψει και την περίπτωση που η θερµοκρασία στην επιφάνεια του τροφίµου (Τ s ) διατηρείται σταθερή: T r= R = Ts (6.5) θεωρώντας h =. c Στην πραγµατικότητα η πρόσδοση ή απαγωγή θερµότητας από την επιφάνεια του τροφίµου εξαρτάται κυρίως από το σύστηµα θέρµανσης ή ψύξης και µπορεί να ακολουθήσει τους βασικούς µηχανισµούς: αγωγή, συναγωγή ή ακτινοβολία, ενώ ιδιαίτερα στην ψύξη µπορεί να συµβαίνει και εξάτµιση νερού στην επιφάνεια. Στην περίπτωση της αγωγής, όπως στην ψύξη σε επαφή µε ψυχόµενες πλάκες µπορεί να χρησιµοποιηθεί η εξίσωση (6.4) στην ίδια µαθηµατική µορφή επιλέγοντας την κατάλληλη τιµή για τον επιφανειακό συντελεστή µεταφοράς θερµότητας από το τρόφιµο προς την ψυκτική πλάκα. Στα υπόλοιπα συστήµατα θέρµανσης ή ψύξης, η µεταφορά θερµότητας γίνεται βασικά µε συναγωγή αλλά µπορεί να παράλληλα να συµβαίνει µεταφορά τόσο µε ακτινοβολία όσο και µε εξάτµιση νερού. Η οριακή συνθήκη σε αυτές τις περιπτώσεις µπορεί να εκφρασθεί ως: T Σ(θερµότητας που απάγεται από την επιφάνεια = ka r r= R (6.6) Ο ρυθµός µεταφοράς θερµότητας µε ακτινοβολία είναι συνήθως ασήµαντος καθώς απαιτείται µεγάλη διαφορά θερµοκρασίας της επιφάνειας του προϊόντος και της θερµαντικής ή ψυκτικής επιφάνειας για την επίτευξη ικανοποιητικού ρυθµού. Εξαίρεση αποτελεί ψήσιµο τροφίµων ή το αρχικό στάδιο ψύξης των προϊόντων αρτοποιίας, καθώς και περιορισµένες άλλες περιπτώσεις. Η θερµότητα που µεταφέρεται µε ακτινοβολία µπορεί να αποδοθεί ως: 4 4 q F Aσ ( T + 273) ( T (6.7) [ ] rad = 1 2 m s ) όπου σ η σταθερά Stefan-Boltzmann (W/m 2 K 4 ) F 1-2 συντελεστής που εξαρτάται από την ικανότητα εκποµπής και τις επιφάνειες των δύο σωµάτων Η εξίσωση (6.7) µπορεί να γραφεί σε µορφή παρόµοια µε τη συναγωγή ως: q = h A( T T ) (6.8) rad rad m s 2 2 όπου hrad = F1 2 Tm + Ts [ Tm Ts ] σ ( ) ( ) ( ) (6.9) Εποµένως στην περίπτωση παράλληλης συναγωγής και ακτινοβολίας εάν οι θερµοκρασίες του µέσου εναλλαγής θερµότητας και της επιφάνειας που προκαλεί τη µεταφορά θερµότητας µε ακτινοβολία είναι ίδιες, µπορεί να χρησιµοποιηθεί η εξίσωση (6.4), µε επιφανειακό συντελεστή h=h c +h rad αντί του h c. Όσον αφορά στην εξάτµιση νερού, η οποία µπορεί να συµβαίνει κατά την ψύξη, η θερµότητα που απάγεται µέσω αυτής από την επιφάνεια του τροφίµου είναι επίσης πολύ µικρή για τα περισσότερα τρόφιµα. Εξάλλου η απώλεια υγρασίας κατά την 143
152 ψύξη είναι ανεπιθύµητη και οι λειτουργικές παράµετροι ρυθµίζονται έτσι ώστε να αποφεύγεται. Εάν η θερµότητα που απάγεται µε εξάτµιση είναι σηµαντική, πρέπει να συνυπολογισθεί στην εξίσωση (3.6) και είναι: q = k A( p p L (6.10) evap g a s ) όπου k g συντελεστής µεταφοράς µάζας (s/m) p a µερική πίεση ατµών στον περιβάλλοντα αέρα (Pa) p s µερική πίεση ατµών στο οριακό στρώµα που περιβάλει το τρόφιµο (Pa) L λανθάνουσα θερµότητα εξάτµισης του νερού στη θερµοκρασία της επιφάνειας (J/kg) Ο συντελεστής µεταφοράς µάζας µπορεί να µετρηθεί ή να υπολογισθεί από τον συντελεστή συναγωγής µέσω του αριθµού Lewis (Le=θερµική διαχυτότητα/διαχυτότητα µάζας). Η µερική πίεση ατµών στον περιβάλλοντα αέρα µπορεί να υπολογισθεί από την τάση ατµών του νερού στη θερµοκρασία του αέρα T a, που συµβολίζεται p a o και τη σχετική υγρασία του αέρα RH: p a =p a o RH. Η µερική πίεση ατµών στο οριακό στρώµα που περιβάλει το τρόφιµο υπολογίζεται από την τάση ατµών του νερού στη θερµοκρασία T s, που συµβολίζεται p s o και την ενεργότητα νερού του τροφίµου α w : p s =p s o a w. Αναλυτική επίλυση των εξισώσεων αγωγής θερµότητας Η εξίσωση µεταφοράς θερµότητας (6.3) έχει επιλυθεί αναλυτικά, για σταθερές θερµικές ιδιότητες, σταθερές εξωτερικές συνθήκες (θερµαντικού ή ψυκτικού µέσου), οµοιόµορφες αρχικές συνθήκες και οριακή συνθήκη όπως εκφράζεται από την εξίσωση (6.4), για πλάκα, κύλινδρο απείρου µήκους και σφαίρα. Η γενική µορφή της λύσης είναι µια σειρά, που συµπεριλαµβάνει όρους που εκφράζουν την επίδραση του αριθµού Biot και δίνει τη θερµοκρασία ως συνάρτηση του χρόνου, συγκεκριµένα του αδιάστατου χρόνου όπως εκφράζεται από τον αριθµό Fourier. Οι εξισώσεις αυτές µπορούν να χρησιµοποιηθούν για την πρόβλεψη της θερµοκρασίας Τ σε οποιοδήποτε σηµείο ενός στερεού, το οποίο είχε µια οµοιόµορφη αρχική θερµοκρασία Τ ΙΤ σε χρόνο µηδέν και θερµαίνεται ή ψύχεται σε ένα µέσο σταθερής θερµοκρασίας Τ m µε επιφανειακό συντελεστή µεταφοράς θερµότητας h. Τα k, c p και ρ θεωρούνται σταθερά και το στερεό ορίζεται από r=0 στην κεντρική θέση ή άξονα έως r=r στην επιφάνεια όπου ισχύει η οριακή συνθήκη της εξίσωσης (6.4). Σε r=0 ισχύει η οριακή T συνθήκη συµµετρίας: = 0. Συνήθως οι λύσεις δίνονται περιέχοντας τους r r =0 αδιάστατους αριθµούς: αριθµός Biot hr Bi = k αριθµός Fourier kt αt Fo = = 2 2 ρc R R p 144
153 T Tm αδιάστατη θερµοκρασία Y = T T Η γενική µορφή τους είναι : T T r Y = m = Φ A( n) exp( B( n) Fo) T T n = 1 R IT m IT m (6.11) όπου η συνάρτηση Φ και οι συναρτήσεις A(n) και Β(n) είναι διαφορετικές για κάθε στερεό. Για την περίπτωση του κυλίνδρου απείρου µήκους π.χ. η λύση παίρνει τη µορφή: T Tm 2BiJ o ( ir / R) 2 Y = β = exp( β Fo) 2 2 i (6.12) T T i = ( β + Bi ) J ( β ) IT m όπου οι τιµές του β είναι οι ρίζες της: βj ( β) Bi ( β) = 1 J o 0 1 i o i και J o, J 1 συναρτήσεις Bessel µηδενικής και πρώτης τάξης αντίστοιχα. Όταν ο αριθµός Fourier είναι µεγαλύτερος από 0.1 περίπου, τότε µόνο ο πρώτος όρος της σειράς των εξισώσεων (6.11), (6.12) είναι σηµαντικός, ενώ οι υπόλοιποι µπορούν να αγνοηθούν. Ένας σηµαντικός παράγοντας για την εκτίµηση της µεταφοράς θερµότητας σε µη µόνιµες συνθήκες είναι η σχέση της εσωτερικής προς την εξωτερική αντίσταση στη µεταφορά θερµότητας, η οποία εκφράζεται µέσω του αριθµού Biot. Όταν Bi>40, ο επιφανειακός συντελεστής µεταφοράς θερµότητας προς το τρόφιµο είναι αρκετά µεγάλος, η αντίσταση στην επιφάνεια θεωρείται αµελητέα και η θερµοκρασία στην επιφάνεια του τροφίµου µπορεί να θεωρηθεί ίση µε τη θερµοκρασία του µέσου θέρµανσης ή ψύξης. Σε αυτή την περίπτωση ισχύει η εξίσωση (6.11) µε T m =T s. Όταν 0.1<Bi <40, τόσο η αντίσταση µεταφοράς θερµότητας προς την επιφάνεια όσο και η αντίσταση στο εσωτερικό του τροφίµου είναι σηµαντικές. Επειδή η χρήση των εξισώσεων της µορφής (6.11) για τον υπολογισµό της κατανοµής της θερµοκρασίας συναρτήσει του χρόνου είναι πολύπλοκες, χρησιµοποιούνται νοµογραφήµατα που έχουν αναπτυχθεί για τη µεταφορά θερµότητας σε µη µόνιµη κατάσταση. Τα ίδια νοµογραφήµατα χρησιµοποιούνται και για Bi>40. Σε αυτά δίνεται η σχετική (αδιάστατη) διαφορά θερµοκρασίας, Y=(T-T m )/(T IT -T m ), ως συνάρτηση του αδιάστατου χρόνου ή αριθµού Fourier (αt/r 2 ) σε διάφορες αποστάσεις από το κέντρο του στερεού και για διάφορες τιµές 1/Bi. Αντιπροσωπευτικά διαγράµµατα για πλάκα, κύλινδρο απείρου µήκους και σφαίρα δίνονται στα σχήµατα του Παραρτήµατος, όπου m=1/bi και η χαρακτηριστική διάσταση για τον υπολογισµό του Bi θεωρείται το ½ του πάχους της πλάκας, η ακτίνα του κυλίνδρου ή της σφαίρας. Στη βιβλιογραφία υπάρχουν επίσης διαγράµµατα που δίνουν τη µέση θερµοκρασία για τα τρία βασικά στερεά. 145
154 Οι υπολογισµοί για ορθογώνια ράβδο απείρου µήκους και για τα πεπερασµένα σχήµατα, ορθογώνιο παραλληλεπίπεδο ή κύλινδρο προκύπτουν µε τη µέθοδο Newman όπου το Y υπολογίζεται ως το γινόµενο των αντιστοίχων τιµών των επιµέρους διευθύνσεων: Υ=Υ x Y y για ορθογώνια ράβδο, Υ=Υ x Y y Y z για ορθογώνιο παραλληλεπίπεδο και Υ=Υ x Y r για κύλινδρο. Οι σχέσεις αυτές µπορούν να χρησιµοποιηθούν και στην περίπτωση που οι συντελεστές µεταφοράς θερµότητας δεν είναι ίδιοι σε όλες τις πλευρές, αρκεί να διατηρείται η συµµετρία. Εάν δεν ισχύουν οι παραπάνω συνθήκες και υπάρχει σηµαντική µεταβολή των ιδιοτήτων του τροφίµου µε τη θερµοκρασία κατά τη διάρκεια της θέρµανσης ή ψύξης πρέπει να ακολουθηθεί αριθµητική επίλυση των διαφορικών εξισώσεων (6.1) ή (6.3). Για αριθµούς Biot µικρότερους από 0.1 (Bi<0.1), θεωρείται αµελητέα η εσωτερική αντίσταση, η θερµοκρασία στο τρόφιµο θεωρείται οµοιόµορφη και ο ρυθµός µεταφοράς θερµότητας προς το τρόφιµο ελέγχεται από τη µεταφορά θερµότητας προς την επιφάνεια του τροφίµου. Το ισοζύγιο θερµότητας σε αυτή την περίπτωση µπορεί να εκφρασθεί ως: c ρ VdT = ha( T T dt (6.13) p m ) όπου c p ειδική θερµότητα του τροφίµου (J/kg C) ρ πυκνότητα του τροφίµου (kg/m 3 ) V όγκος του τροφίµου (m 3 ) h επιφανειακός συντελεστής µεταφοράς θερµότητας (W/m 2 C) A επιφάνεια εναλλαγής θερµότητας (m 2 ) T m θερµοκρασία του µέσου θέρµανσης ή ψύξης ( C) και Τ θερµοκρασία του τροφίµου σε χρόνο t ( C) Η εξίσωση (6.13) ισχύει και για τη µεταφορά θερµότητας σε υγρά, οµογενή και πλήρως αναµίξιµα τρόφιµα συσκευασµένα σε περιέκτες, όπου αντί του συντελεστή h µπορεί να θεωρηθεί ο συνολικός συντελεστής µεταφοράς θερµότητας U. Με ολοκλήρωση της εξίσωσης (6.13) προκύπτει: T Tm ha Y = = exp( ) t (6.14) T Tm c ρv IT p Εµπειρικές εξισώσεις - χρήση των παραµέτρων j και h Η ποικιλία των σχηµάτων που απαντάται στην πράξη στα τρόφιµα οδήγησε στην ανάγκη επέκτασης των αναλυτικών λύσεων σε γενική, εµπειρικής µορφής, εξίσωση που να µπορεί να χρησιµοποιηθεί για όλα τα τρόφιµα. Αυτή στηρίζεται στο γεγονός ότι η θερµοκρασία σε οποιοδήποτε σηµείο του τροφίµου, µεταβάλλεται εκθετικά µε το χρόνο θέρµανσης ή ψύξης, όπως προκύπτει και από τις εξισώσεις (6.11) και (6.14). Παρόλα αυτά στις περισσότερες περιπτώσεις παρατηρείται µια αρχική περίοδος 146
155 υστέρησης. Εποµένως η ανοιγµένη διαφορά θερµοκρασίας τροφίµου και µέσου εναλλαγής θερµότητας µπορεί να αποδοθεί µε την γενικής µορφής εξίσωση: Y t Tc Tm t f c = = jc ) = jc10 TIT Tm f exp( (6.15) για τη θερµοκρασία T c στο θερµικό κέντρο του τροφίµου (σηµείο µε τη µεγαλύτερη διαφορά θερµοκρασίας από το µέσο θέρµανσης ή ψύξης), και Y t Tav Tm t f av = = jav ) = jav10 TIT Tm f exp( (6.16) για τη µέση θερµοκρασία του τροφίµου, Τ av όπου j c, j av παράγοντες υστέρησης για το θερµικό κέντρο και τη µέση θερµοκρασία, f αντίστοιχα, και χρόνος που εκφράζει το ρυθµό θέρµανσης και συγκεκριµένα ο χρόνος που απαιτείται για να υποδεκαπλασιασθεί η διαφορά θερµοκρασίας µεταξύ του τροφίµου και του µέσου θέρµανσης ή ψύξης (s). Οι παράµετροι j και f µπορούν να προσδιορισθούν από την καµπύλη µεταβολής της θερµοκρασίας του τροφίµου µε το χρόνο σε ηµιλογαριθµικό διάγραµµα (καµπύλη θερµικής διείσδυσης), που έχει γενικά τη µορφή του σχήµατος 6.1. Ο παράγοντας υστέρησης ισούται µε: TA Tm j = T Tm IT (6.17) όπου T A ψευδοαρχική θερµοκρασία που προκύπτει από την αποτέµνουσα της καµπύλης θέρµανσης ή ψύξης Η παράµετρος f προσδιορίζεται από την κλίση της ευθείας, η οποία ισούται µε -1/f. Oι εξισώσεις (6.15) και (6.16) µπορούν να χρησιµοποιηθούν ως µία εµπειρική προσέγγιση, γενικής εφαρµογής για τρόφιµα διαφόρων σχηµάτων, εφόσον είναι οµογενή και ισχύει η οριακή συνθήκη (6.4). Ο υπολογισµός των f και j που είναι συναρτήσεις του Bi και του σχήµατος, µπορεί να γίνει πειραµατικά, αλλά έχουν προταθεί και εναλλακτικές λύσεις βασιζόµενες στις αναλυτικές λύσεις του ισοζυγίου θερµότητας. Στην περίπτωση που h 0 και εποµένως Bi 0, η σύγκριση των εξισώσεων (6.15) και (6.16) µε την (6.14) δίνει για οποιοδήποτε σχήµα: j c 1, j av 1 και f= 2.303(ρc p /h) (V/A) = 2.303(Rρc p /h) (V/AR) (6.18) Επίσης η σχέση (6.14) µπορεί να γραφεί και ως: ht AR Y = Yav = exp( ) (6.19) Rρc V p 147
156 Σχήµα 6.1. Καµπύλες θέρµανσης και ψύξης κονσερβοποιηµένου τροφίµου 148
157 Ο λόγος AR/V είναι ένας αδιάστατος δείκτης σχήµατος µε τιµές 1 για πλάκα, 2 για κύλινδρο απείρου µήκους και 3 για σφαίρα. Μπορεί να χρησιµοποιηθεί για τα τρία βασικά σχήµατα και µέσω αυτού να υπολογισθούν οι τιµές f και Y όταν Bi 0. Η συνθήκη αυτή µπορεί να ισχύει στη θέρµανση και στην ψύξη οµογενών, υγρών πλήρως αναµίξιµων, συσκευασµένων τροφίµων όπου αντί του συντελεστή h πρέπει να χρησιµοποιηθεί ο συνολικός συντελεστής µεταφοράς θερµότητας προς την επιφάνεια του τροφίµου U. Είναι όµως σπάνια στη θέρµανση ή στην ψύξη στερεών τροφίµων, όπου συνήθως Bi>0.1. Στην περίπτωση όπου Bi>0.1, ο συνδυασµός των εξισώσεων (6.15) και (6.16) µε την (6.12) παίρνοντας υπ όψιν µόνο τον πρώτο όρο της σειράς δίνει: f=2.303r 2 /(αβ 2 ) για κύλινδρο απείρου µήκους (6.20) Η ίδια σχέση µε διαφορετικές τιµές β προκύπτει και για πλάκα ή σφαίρα. Οι τιµές των j προκύπτουν µε τον ίδιο τρόπο και είναι διαφορετικές για τα τρία σχήµατα. Εποµένως οι τιµές των f και j εξαρτώνται από τον αριθµό Bi, και το σχήµα του τροφίµου και ειδικότερα το f επί πλέον από τη χαρακτηριστική διάσταση και τη θερµική διαχυτότητα. Οι τιµές αυτές έχουν υπολογισθεί, µε βάση τις αναλυτικές λύσεις, για τα ηµιάπειρα στερεά και τη σφαίρα. Σχετικά διαγράµµατα έχουν δηµοσιευθεί από τον Pflug και δίνονται στα σχήµατα 6.2 και 6.3. Προϊόντα µε γνωστά γεωµετρικά σχήµατα Για πεπερασµένα αντικείµενα µορφής κυλίνδρου ή ορθογώνιου παραλληλεπιπέδου µε βάση τη µέθοδο Newman, όπου το Y υπολογίζεται ως το γινόµενο των αντιστοίχων τιµών των επιµέρους διευθύνσεων: Υ=Υ x Y y Y z για ορθογώνιο παραλληλεπίπεδο και Υ=Υ x Y r για κύλινδρο προκύπτει αντικαθιστώντας στην εξίσωση (6.16): 1 1 = f όπου f i f i = f κατά τη διεύθυνση i (6.21) και j = jx jy jz για ορθογώνιο παρ/µο ή j = j j για κύλινδρο (6.22) Στην πράξη για τα τρόφιµα που πλησιάζουν το σχήµα του ορθογωνίου παραλληλεπιπέδου ή του κυλίνδρου µπορεί να γίνει προσεγγιστικός υπολογισµός των f και j µε βάση το πλησιέστερο σχήµα και τη χρήση των διαγραµµάτων του Pflug και των εξισώσεων (6.21) και (6.22). Επίσης από τα δεδοµένα θερµικής διείσδυσης, f και j, που έχουν προσδιορισθεί για ένα προϊόν ορισµένων διαστάσεων µπορούν να υπολογισθούν αντίστοιχα δεδοµένα για το ίδιο προϊόν άλλων διαστάσεων. Είναι προφανές ότι η µεταβολή των x r 149
158 διαστάσεων του τροφίµου επηρεάζει σηµαντικά την παράµετρο f καθώς η τιµή της εξαρτάται από τις διαστάσεις και τη φύση του τροφίµου. Σχήµα 6.2. Επίδραση του Bi στον παράγοντα f. Σχήµα 6.3. Επίδραση του Bi στον παράγοντα υστέρησης στο κέντρο του τροφίµου j c. 150
159 Για εναλλαγή θερµότητας σε προϊόντα µε Bi<0.1 ισχύει f=2.303ρc p V/(hA). Οπότε η µετατροπή π.χ. για τρόφιµα κυλινδρικού σχήµατος διαφορετικών διαστάσεων µπορεί να γίνει µε ικανοποιητική προσέγγιση σύµφωνα µε τη σχέση: f V / A 2br 2b + r = = f V / A 2b + r 2b r όπου f η παράµετρος θερµικής διείσδυσης για ένα µέγεθος κυλινδρικού τροφίµου f η αντίστοιχη παράµετρος για κυλινδρικό τρόφιµο άλλου µεγέθους r, r οι αντίστοιχες ακτίνες των κυλίνδρων 2b, 2b τα αντίστοιχα ύψη των κυλίνδρων (6.23) Όταν η αντίσταση στη µεταφορά θερµότητας στην επιφάνεια του τροφίµου µπορεί να θεωρηθεί αµελητέα (Bi>40), συνθήκη η οποία συνήθως ισχύει στις θερµικές κατεργασίες, η παράµετρος f εξαρτάται από τις διαστάσεις και το συντελεστή θερµικής διαχυτότητας του τροφίµου. Το γινόµενο fα(1/r 2 ), όπου r η χαρακτηριστική διάσταση του προϊόντος είναι σταθερό και ίσο µε για πλάκα και για ηµιάπειρο κύλινδρο, όπως φαίνεται από το διάγραµµα 6.2. Ο συντελεστής θερµικής διαχυτότητας εκφράζει τη ροή θερµοκρασίας και είναι ανεξάρτητος των διαστάσεων του τροφίµου και της διεύθυνσης ροής θερµότητας για ισότροπα υλικά. Κατά συνέπεια για τα πεπερασµένα αντικείµενα και µετάδοση θερµότητας και από τις τρεις διαστάσεις η παράµετρος f µπορεί να προσδιορισθεί σύµφωνα µε τη σχέση (6.21) για κυλινδρικό τρόφιµο: f = α 2 1/ r / b 2 [ ] και για τρόφιµο σχήµατος ορθογωνίου παραλληλεπιπέδου: f = α / r + 1/ b + 1/ c [ ] όπου r η ακτίνα του κυλίνδρου ή το µισό πάχος του ορθογωνίου b το µισό του ύψους του κυλίνδρου ή του ορθογωνίου c το µισό του πλάτους του ορθογωνίου (6.24) (6.25) Εάν αντίσταση στη µεταφορά θερµότητας στην επιφάνεια του προϊόντος δεν είναι αµελητέα, το γινόµενο fα(1/r 2 ) µεταβάλλεται µε τη µεταβολή του Bi και µπορεί να υπολογισθεί κατά προσέγγιση από το διάγραµµα Pflug ή η παράµετρος f να προσδιορισθεί πειραµατικά. Η µετατροπή για άλλες διαστάσεις του ίδιου προϊόντος γίνεται µε τις σχέσεις (6.24) και (6.25) θέτοντας τους κατάλληλους συντελεστές που προκύπτουν, αντί του και Όλες οι παραπάνω σχέσεις χρησιµοποιούνται και για τη µετατροπή των παραµέτρων θερµικής διείσδυσης σε τρόφιµα συσκευασµένα σε δοχεία. Αν προσδιορισθούν οι παράµετροι f h και f c για τη θέρµανση και ψύξη, αντίστοιχα ενός 151
160 τροφίµου συσκευασµένου σε ορισµένο δοχείο, είναι δυνατόν να υπολογισθούν οι αντίστοιχες παράµετροι για άλλο δοχείο ίδιου σχήµατος και διαφορετικών διαστάσεων, δεδοµένου ότι η θερµική διαχυτότητα του τροφίµου είναι η ίδια. Ο παράγοντας υστέρησης επηρεάζεται πολύ λίγο από τις διαστάσεις του τροφίµου σε Bi<0.1 (αµελητέα αντίσταση µεταφοράς θερµότητας στο εσωτερικό του τροφίµου) και µπορεί να θεωρηθεί κατά προσέγγιση σταθερός. Σε Bi>40 το j στο επίπεδο συµµετρίας πλάκας ισούται µε 1.27 και στον άξονα ηµιάπειρου κυλίνδρου µε Για πεπερασµένα σχήµατα ο παράγοντας υστέρησης ισούται µε το γινόµενο των τιµών που αντιστοιχούν στη µονοδιάστατη ροή θερµότητας και εποµένως προκύπτει για: κύλινδρο: j = = 203. ορθογώνιο παραλληλόγραµµο: j = = 205. Αν και θεωρητικά οι τιµές του j έπρεπε να είναι σταθερές ανεξάρτητες των διαστάσεων του τροφίµου στην πράξη οι υπολογιζόµενες τιµές από τις καµπύλες θερµικής διείσδυσης µεταβάλλονται µε τη µεταβολή του ύψους ως προς τη διάµετρο σε τρόφιµο κυλινδρικού σχήµατος. Ένας λόγος είναι η προσέγγιση µε την οποία υπολογίζεται η κλίση του ευθύγραµµου τµήµατος της καµπύλης θερµικής διείσδυσης. Με βάση δεδοµένα θερµοκρασίας-χρόνου για κυλινδρικές κονσέρβες µε αυξανόµενο λόγο ύψους/διαµέτρου βρέθηκε ότι η παράµετρος j µεταβάλλεται σύµφωνα µε τα θεωρητικά αναµενόµενα µεταξύ των ορίων 2.03 και Εάν αντίσταση στη µεταφορά θερµότητας στην επιφάνεια του προϊόντος δεν είναι αµελητέα, το j µεταβάλλεται µε τη µεταβολή του Bi και µπορεί να προσδιορισθεί από τα σχετικά διαγράµµατα που υπάρχουν στη βιβλιογραφία, όπως το 6.3. Προϊόντα µε ακανόνιστα γεωµετρικά σχήµατα Για ακανόνιστα σχήµατα έχει προταθεί η χρήση γενικευµένων γεωµετρικών δεικτών. Τέτοιος είναι ο δείκτης που προτάθηκε από τον Smith και τους συνεργάτες του (1967) και ορίζεται από την ακόλουθη σχέση: G = β 2 / π 2 (6.26) Για οποιοδήποτε σχήµα, όταν Bi, από τη στιγµή που η θερµοκρασία στο κέντρο αρχίζει να µειώνεται εκθετικά, το διάγραµµα ln(y c ) ως προς Fo θα έχει κλίση - β 2 σύµφωνα µε την εξίσωση (6.12) και τις αντίστοιχες που ισχύουν για τα άλλα σχήµατα. Χρησιµοποιώντας αυτές τις εξισώσεις οι τιµές του G βρέθηκαν ίσες µε 0.25, και 1.00 για πλάκα, κύλινδρο απείρου µήκους και σφαίρα, αντίστοιχα. Με βάση αυτά οι τιµές του G που προκύπτουν για ορθογώνιο παραλληλεπίπεδο διαστάσεων L x, L y, L z (όπου L x η µικρότερη διάσταση) είναι: 2 2 [ x y x z ] G = ( L / L ) + ( L / L ) (6.27) ενώ για ελλειψοειδή σχήµατα προτάθηκε: 152
161 2 2 G = ( L / L ) ( L / L ) (6.28) x y x z Τα ακανόνιστα σχήµατα σχετίζονται µε το πλησιέστερο ελλειψοειδές µοντέλο που έχει ίσες ορθογωνικές διατοµές. Με βάση τον γεωµετρικό δείκτη G, έχουν σχεδιαστεί διαγράµµατα που σχετίζουν την ανοιγµένη θερµοκρασία Y µε τους αριθµούς Fo και m=1/bi, για διάφορες τιµές του G. Αυτά τα διαγράµµατα µπορούν να χρησιµοποιηθούν για την πρόβλεψη της θερµοκρασίας στο κέντρο ή της µέσης θερµοκρασίας, µετά από ορισµένο χρόνο ψύξης ή το αντίστροφο, µε σχετικά ικανοποιητική ακρίβεια. ιαγράµµατα για προσδιορισµό της θερµοκρασίας στο κέντρο αντικειµένων µε διάφορες τιµές G δίνονται στο παράρτηµα. Μεταφορά θερµότητας µε συναγωγή Η ροή θερµότητας µε συναγωγή σε ένα ρευστό τρόφιµο που βρίσκεται σε επαφή µε µια θερµή ή ψυχρή επιφάνεια αποδίδεται από τη σχέση: q = h A T T ) (6.29) c ( s f όπου h c συντελεστής συναγωγής (W/m 2 C) Τ s θερµοκρασία της επιφάνειας T f θερµοκρασία του κύριου όγκου του ρευστού, µακριά από την επιφάνεια Ο συντελεστής συναγωγής µπορεί να εκτιµηθεί από µαθηµατικές σχέσεις που εξαρτώνται από το είδος της ροής και συνοψίζονται στη συνέχεια. Οι αδιάστατοι αριθµοί που χρησιµοποιούνται σε αυτές είναι: h αριθµός Nusselt c D Nu = k uρd αριθµός Reynolds Re = µ c p µ αριθµός Prandtl Pr = k 2 π ρud c p π D αριθµός Graetz Gz = = Re Pr 4 kl 4 L 2 3 ρ βgd αριθµός Grashof Gr o T = 2 µ Εξαναγκασµένη συναγωγή Σε στρωτή ροή ρευστού που θερµαίνεται από µια επίπεδη πλάκα σταθερής θερµοκρασίας ισχύει: 1/ 2 1/ 3 Nu = Re Pr (6.30) Σε στρωτή ροή ρευστού µέσα σε κυλινδρικό αγωγό µε σταθερή θερµοκρασία τοιχώµατος: 153
162 0.085Gz Nu = Gz Nu = 1/ 3 2.0Gz µ µ w / 3 µ µ w 0.14 για Gz<20 (6.31) για Gz>20 (6.32) Σε µικρούς αριθµούς Graetz (π.χ. για πολύ µεγάλου µήκους κυλινδρικούς αγωγούς) ο αριθµός Nusselt προσεγγίζει την τιµή 3.66 όταν είναι σταθερή η θερµοκρασία του τοιχώµατος και την τιµή 4.36 όταν είναι σταθερός ο ρυθµός ροής θερµότητας. n Σε µη νευτονικά τρόφιµα που ακολουθούν την εξίσωση τ = K γ η εξίσωση (6.32) γίνεται : Nu 1/ 3 n 1 = 3n + 1 1/ 3 K8 2.0 Gz 1 4 n n K 8 w 0.14 όπου n δείκτης ρεολογικής συµπεριφοράς Κ δείκτης συνοχής της ροής (6.33) Οι συντελεστές συναγωγής που υπολογίζονται από τις παραπάνω εξισώσεις είναι οι µέσοι συντελεστές σε όλο το µήκος του αγωγού και βασίζονται σε µια µέση λογαριθµική τιµή της διαφοράς θερµοκρασίας µε βάση τη σχέση: p ( IT q = h π DL T = m c T out T ) (6.34) c L ( Tw TIT ) ( Tw T out ) όπου TL = (6.35) ln[( T T ) /( T T out )] w IT w Για τυρβώδη ροή σε κυλινδρικό αγωγό µπορεί να χρησιµοποιηθεί η εµπειρική σχέση: Nu = 0.023Re 0,8 Pr 1/ 3 µ µ w 0.14 (6.36) Η σχέση (6.36) αποτελεί ικανοποιητική προσέγγιση (µε αποκλίσεις µέχρι 20% από τα πειραµατικά δεδοµένα) για αριθµούς Prandtl µεταξύ 0.7 και 700 και λόγο L/D µεγαλύτερο του 60. Για τον εκθέτη του παράγοντα διόρθωσης του ιξώδους έχουν προταθεί οι τιµές 0.36 για θέρµανση και 0.2 για ψύξη από τους Kays & London, ή 0.25 και 0.11, αντίστοιχα (Mills). Για υγρά χαµηλού ιξώδους, όπως το νερό µπορεί να αγνοηθεί ο παράγοντας διόρθωσης του ιξώδους και χρησιµοποιείται η εµπειρική σχέση: Nu 0,8 n = 0.023Re Pr (6.37) όπου n=0.4 όταν το υγρό θερµαίνεται και n=0.3 όταν ψύχεται. Για µη νευτονικά ρευστά έχουν προταθεί ορισµένες σχέσεις η ακρίβειά τους όµως στην πρόβλεψη πειραµατικών τιµών είναι µικρή. 154
163 Οι αριθµοί Reynolds και Prandtl υπολογίζονται µε βάση τις ιδιότητες του ρευστού στη µέση θερµοκρασία του κύριου όγκου αυτού, και ο συντελεστής συναγωγής που υπολογίζεται από τις (6.36) και (6.37) είναι ο µέσος σε όλο το µήκος του σωλήνα. Στην περιοχή µετάβασης ανάµεσα στη στρωτή και τυρβώδη ροή 2100<Re<6000 χρησιµοποιούνται διαγράµµατα για τον υπολογισµό του συντελεστή συναγωγής συναρτήσει του αριθµού Reynolds. Για ροή σε µη κυλινδρικούς αγωγούς µπορούν να χρησιµοποιηθούν οι παραπάνω εξισώσεις µε την ισοδύναµη διάµετρο (=4xδιατοµή/διαβρεχόµενη περίµετρο) του αγωγού, αντί της διαµέτρου D. Φυσική (ελεύθερη) συναγωγή Στη φυσική συναγωγή χρησιµοποιούνται εµπειρικές σχέσεις της µορφής: n Nu = b(gr Pr) (6.40) όπου b και n σταθερές που εξαρτώνται από τη γεωµετρία και τον προσανατολισµό της επιφάνειας που βρίσκεται σε επαφή µε το υγρό που θερµαίνεται ή ψύχεται µε φυσική συναγωγή. Για τον υπολογισµό των αριθµών της εξίσωσης (6.40) οι ιδιότητες του ρευστού υπολογίζονται στη θερµοκρασία του υµένα (µέση θερµοκρασία µεταξύ επιφάνειας και κύριου όγκου του ρευστού) και όχι στη µέση θερµοκρασία του ρευστού, όπως στις εξισώσεις για εξαναγκασµένη συναγωγή. Η επίδραση της φυσικής συναγωγής στη µεταφορά θερµότητας περιορίζεται στη στρωτή ροή. Σ αυτή την περίπτωση ο συντελεστής συναγωγής που προκύπτει από την εξίσωση (6.32) πολλαπλασιάζεται µε ένα διορθωτικό παράγοντα. Εναλλάκτες θερµότητας Οι εναλλάκτες που χρησιµοποιούνται στη βιοµηχανία τροφίµων είναι είτε έµµεσης εναλλαγής θερµότητας όπως αυλωτοί, µε πλάκες, ή αποξεόµενης επιφάνειας, είτε άµεσης µε διαβίβαση ατµού στη µάζα του τροφίµου ή αντίστροφα. Οι πρώτοι χρησιµοποιούνται για θέρµανση ή ψύξη των τροφίµων, ενώ οι δεύτεροι µόνο για θέρµανση. Γενικά ο σχεδιασµός οποιουδήποτε εναλλάκτη στηρίζεται στην εκτίµηση των συντελεστών συναγωγής τόσο από την πλευρά του τροφίµου όσο και από την πλευρά του θερµαντικού ή ψυκτικού υγρού. O συνολικός συντελεστής µεταφοράς θερµότητας υπολογίζεται λαµβάνοντας υπ όψιν την αντίσταση στη µεταφορά θερµότητας δια µέσου του τροφίµου, του θερµαντικού ή ψυκτικού υγρού και του τοιχώµατος: 1 1 x 1 = + + (6.41) U h k o h i 155
164 όπου h o, h i συντελεστές µεταφοράς θερµότητας στο εξωτερικό και το εσωτερικό των αυλών (ή πλακών), αντίστοιχα, (W/m 2 C) x πάχος του τοιχώµατος (m) k συντελεστής θερµικής αγωγιµότητας του τοιχώµατος (W/m C) Στην περίπτωση πολύ ιξωδών τροφίµων η µεταφορά θερµότητας στην πλευρά του τροφίµου ελέγχει τη διεργασία και λαµβάνεται: U = h i (6.42) Στους εναλλάκτες µε αυλούς το τρόφιµο ρέει συνήθως εντός των αυλών και ο συντελεστής h i υπολογίζεται από τις εξισώσεις (6.31) - (6.33) και (6.36) - (6.37). Για το θερµαντικό ή ψυκτικό µέσο δίδονται κατάλληλες σχέσεις στη βιβλιογραφία. Ορισµένες φορές χρησιµοποιούνται εναλλάκτες τριπλού σωλήνα, στους οποίους το µέσο εναλλαγής θερµότητας διαβιβάζεται στον εσωτερικό και εξωτερικό σωλήνα και το τρόφιµο στον ενδιάµεσο δακτύλιο. Γι αυτή την περίπτωση έχουν προταθεί εξισώσεις που συσχετίζουν τον εξωτερικό και τον εσωτερικό συντελεστή µεταφοράς θερµότητας µε τις ιδιότητες των ρευστών και τις διαµέτρους των αυλών (Heldman & Singh, 1980). Στους εναλλάκτες µε πλάκες τόσο για τον εξωτερικό όσο και για τον εσωτερικό συντελεστή συναγωγής µπορεί να χρησιµοποιηθεί η σχέση: hd Nu = e = 0.37 Re Pr k (6.43) όπου D e η ισοδύναµη διάµετρος ισούται µε το διπλάσιο της απόστασης µεταξύ των πλακών του εναλλάκτη. Για µη νευτονικά υγρά που ακολουθούν την εκθετική εξίσωση ροής, όπως είναι πολλά τρόφιµα έχει προταθεί η σχέση: hd e / 2 6 n + 1 = k ς 2n + 1 (6.44) όπου: 5 2n 3n n ς = + (6.45) 4 2n + 1 4n + 1 5n + 1 Οι εναλλάκτες αποξεόµενης επιφάνειας χρησιµοποιούνται στη βιοµηχανία τροφίµων για µη νευτονικά υγρά µε µεγάλο ιξώδες, όπως είναι οι µαργαρίνες. Για τον υπολογισµό του συντελεστή µεταφοράς θερµότητας στο εσωτερικό του αποξεόµενου αυλού, όπου διαβιβάζεται το τρόφιµο, έχει διατυπωθεί µία εµπειρική εξίσωση που περιλαµβάνει όλα τα χαρακτηριστικά µεγέθη και τις µεταβλητές λειτουργίας του εναλλάκτη καθώς και τις ιδιότητες του ρευστού. Στις περιπτώσεις άµεσης εναλλαγής θερµότητας είτε διαβιβάζεται ατµός στη µάζα του τροφίµου είτε το τρόφιµο στην µάζα του ατµού. Η ανάµιξη γίνεται στις 156
165 κατάλληλες αναλογίες ατµού και τροφίµου, ώστε όλη η ποσότητα του ατµού να υγροποιηθεί αποδίδοντας τη λανθάνουσα θερµότητα στο τρόφιµο του οποίου η θερµοκρασία ανέρχεται στη θερµοκρασία του ατµού. Η αναλογία ατµού/τροφίµου µπορεί να υπολογισθεί από το ισοζύγιο ενθαλπίας: όπου mc p ( T T m v IT ) = m v L ( T ) mv m c p = ( T T m, µαζική ροή του τροφίµου και του ατµού αντίστοιχα (kg/s) L ( T ) Τ ΙΤ, Τ αρχική και τελική θερµοκρασία του τροφίµου, αντίστοιχα ( C) L (Τ) θερµότητα εξάτµισης του νερού στη θερµοκρασία Τ (J/kg) IT (6.46) H τιµή του συνολικού συντελεστή µεταφοράς θερµότητας (U) υπό αυτές τις συνθήκες είναι πολύ µεγάλη και η θέρµανση του τροφίµου θεωρείται σχεδόν στιγµιαία. Η εξάτµιση του νερού και ο διαχωρισµός του από το τρόφιµο υπό µορφή ατµού γίνεται σε δοχείο εκτόνωσης, το οποίο λειτουργεί σε µειωµένη πίεση ίση µε την τάση ατµών στη θερµοκρασία του δοχείου εκτόνωσης. Το αντίστοιχο ισοζύγιο ενθαλπίας είναι: p ( T Te ) + mv c pw ( T Te ) = m v L( Te ) m c (6.47) όπου c pw ειδική θερµότητα του νερού (J/kg C) Τ e θερµοκρασία του δοχείου εκτόνωσης ( C) L (Τe) θερµότητα εξάτµισης του νερού στη θερµοκρασία Τ e (J/kg) Υπολογισµός της µεταβολής της θερµοκρασίας του τροφίµου στους εναλλάκτες θερµότητας Στους εναλλάκτες έµµεσης θέρµανσης ή ψύξης η µεταβολή της θερµοκρασίας του τροφίµου µπορεί να βρεθεί ολοκληρώνοντας τη βασική εξίσωση για τη µεταφορά θερµότητας. Στην απλούστερη περίπτωση, όπου η θερµοκρασία του µέσου εναλλαγής θερµότητας διατηρείται σταθερή (Τ m ) προκύπτει: m c dt = UdA( T T ) m T( t ) p dt T T = A( t ) UdA TIT m 0 mc p T ( t ) T m UA ( t ) ln T Αλλά IT T A( t ) = A m t t ολ = m c p 157
166 Εποµένως: όπου Τ (t) T( t) Tm UAt UA ln = = t (6.48) TIT Tm mc t mc p p ολ µέση θερµοκρασία του τροφίµου µετά από χρόνο παραµονής t στον εναλλάκτη ( C) T IT θερµοκρασία εισόδου στον εναλλάκτη ( C) m µάζα του προϊόντος που βρίσκεται σε επαφή µε την επιφάνεια A (kg) A επιφάνεια του εναλλάκτη (m 2 ) U συνολικός συντελεστής µεταφοράς θερµότητας (W/m 2 C) Η εξίσωση (6.48) µοιάζει µε την εξίσωσή (6.16), µε j=1 λόγω εναλλαγής θερµότητας σε µόνιµη κατάσταση. Εποµένως η εξίσωση που δίνει τη µέση θερµοκρασία του τροφίµου συναρτήσει του χρόνου παραµονής στον εναλλάκτη µπορεί να γραφεί ως: T Tm log = t / f (6.49) TIT Tm mcp όπου: f = (6.50) UA Η περίπτωση σταθερής θερµοκρασίας του µέσου θέρµανσης (T m ) συµβαίνει όταν χρησιµοποιείται συµπυκνούµενος ατµός ή όταν ο ρυθµός ροής του θερµαντικού υγρού είναι πολύ µεγαλύτερος από του τροφίµου. Εάν η θερµοκρασία του θερµαντικού µέσου µειώνεται καθώς αυξάνεται η θερµοκρασία του τροφίµου τότε το ισοζύγιο θερµότητας σε εναλλάκτη αντιρροής γίνεται: ( T TmIT ) ( T UA ( T T ln ( T T IT IT mit m T ) Από το οποίο προκύπτει: ) m ) = mc p ( T T IT ) = m m ( T T m mit ) UA m c pm m c p ln = (6.51) ( T IT T m ) m c p m m c pm Η αντίστοιχη εξίσωση της (6.49) για την περίπτωση αυτή δίνει την ανοιγµένη διαφοράς θερµοκρασίας ως προς τη θερµοκρασία εισόδου των δύο ρευστών µε παράγοντα f ίσο µε: όπου mc f = UA m p m m c pm m m c pm m c p c pm ( T mit T m ) (6.52) m m, µαζική ροή του θερµαντικού ή ψυκτικού υγρού και του τροφίµου, αντίστοιχα (kg/s) 158
167 c pm, c p ειδική θερµότητα του θερµαντικού ή ψυκτικού υγρού και του τροφίµου, αντίστοιχα (J/kg C) Ειδικότερα στην περίπτωση ανάκτησης θερµότητας, τόσο το θερµαινόµενο όσο και το ψυχόµενο υγρό είναι το ίδιο το τρόφιµο, οπότε: mc p = m m c pm (6.53) p ( T TIT ) = m m c pm ( TmIT Tm ) = UA T (6.54) mc T T = T T = T ct (6.55) m IT mit = t T = Tout ( Tout TIT ) (6.56) t oλ όπου λ = V m t o / V όγκος που καταλαµβάνει το τρόφιµο στον εναλλάκτη Στις περιπτώσεις άµεσης εναλλαγής θερµότητας όπως αναφέρθηκε η τιµή του συνολικού συντελεστή µεταφοράς θερµότητας (U) είναι πολύ µεγάλη και η ανύψωση της θερµοκρασίας του τροφίµου πολύ γρήγορη, συνήθως της τάξης του ενός δευτερολέπτου ή λιγότερο. Έτσι σε αυτή τη µέθοδο η θέρµανση θεωρείται στιγµιαία. Συστήµατα ασυνεχούς λειτουργίας Συνήθως αποτελούνται από ανοξείδωτα δοχεία τα οποία φέρουν µανδύα ή/και εσωτερική σπείρα κυκλοφορίας του θερµαντικού ή ψυκτικού µέσου. Το θερµαντικό µέσο είναι νερό ή ατµός, ενώ το ψυκτικό µέσο είναι νερό, µίγµα νερού/πάγου ή κάποιο ψυκτικό υγρό. Τα περισσότερα δοχεία είναι εφοδιασµένα µε αναδευτήρες για την αύξηση του ρυθµού µεταφοράς θερµότητας µε συναγωγή. Στα τρόφιµα που περιέχουν στερεά ο σχεδιασµός και η λειτουργία των αναδευτήρων ρυθµίζεται ώστε να αποφευχθεί η θραύση των στερεών, εάν είναι πιθανή. Η µεταβολή της θερµοκρασίας στα στερεά που περιέχει το µίγµα γίνεται µε αγωγή και ο ρυθµός της είναι πολύ βραδύτερος του αντίστοιχου ρυθµού της υγρής µάζας του µίγµατος. Ο ρυθµός ψύξης σε κλειστά δοχεία µπορεί να αυξηθεί µε την εφαρµογή κενού για την εξάτµιση µέρους του υγρού. Η µέθοδος παρουσιάζει προβλήµατα σε τρόφιµα που έχουν τάση αφρισµού. 159
168 Συστήµατα θέρµανσης και ψύξης για στερεά ή συσκευασµένα τρόφιµα Η θέρµανση στα περισσότερα συσκευασµένα τρόφιµα γίνεται µε στόχο την παστερίωση ή την αποστείρωσή τους και ο χρησιµοποιούµενος εξοπλισµός θα αναπτυχθεί στο κεφάλαιο 7. Στη συνέχεια θα αναφερθούν τα συστήµατα ψύξης (πρόψυξης) που χρησιµοποιούνται για τρόφιµα χύµα ή συσκευασµένα τα οποία συντηρούνται υπό ψύξη για παράταση του χρόνου ζωής µέχρι την κατανάλωσή τους. Στα περισσότερα συστήµατα η απαγωγή θερµότητας από την επιφάνεια του ψυχόµενου τροφίµου γίνεται µε συναγωγή. Τα συνήθη ψυκτικά µέσα είναι ο αέρας και το νερό, αν και χρησιµοποιούνται και ορισµένα διαλύµατα αλατιού ή ζαχάρων. Ο συντελεστής συναγωγής θερµότητας εξαρτάται από το σχήµα και την τραχύτητα της επιφάνειας του τροφίµου και κυρίως από τις θερµοφυσικές ιδιότητες και την ταχύτητα του µέσου ψύξης. Μεταφορά θερµότητας µε αγωγή συµβαίνει στα συστήµατα όπου το τρόφιµο βρίσκεται σε επαφή µε τις ψυκτικές επιφάνειες, όπως οι ψυκτήρες πλακών. Τυπικές τιµές επιφανειακών συντελεστών µεταφοράς θερµότητας για ορισµένα από τα συστήµατα που θα παρουσιασθούν στη συνέχεια δίνονται στον πίνακα 8.2 (κεφάλαιο 8). Κατά κανόνα, σε όλα τα συστήµατα, ο ρυθµός ψύξης των τροφίµων επιδιώκεται να είναι ταχύς. Ο κύριος λόγος για όλα τα τρόφιµα, πέραν του οικονοµικού οφέλους, είναι η ταχύτερη αντιµετώπιση της ανάπτυξης και δράσης των µικροοργανισµών. Υπάρχουν όµως και άλλοι λόγοι ανάλογα µε το τρόφιµο. Στα φρούτα η ταχεία ψύξη επιβραδύνει το ρυθµό ωρίµανσης. Στο κρέας επιβραδύνει το ρυθµό µετουσίωσης των πρωτεϊνών, η οποία αρχίζει αµέσως µετά τη σφαγή λόγω µείωσης του ph. Στα ψάρια αποτρέπει τη συρρίκνωση και σε διάφορα άλλα τρόφιµα έχει παρατηρηθεί επιβράδυνση διαφόρων ανεπιθύµητων δράσεων (απώλεια σακχάρων κ.λ.π.). Επίσης µε την ταχεία ψύξη η απώλεια υγρασίας είναι µικρότερη. Παρ όλα αυτά ο υπερβολικά ταχύς ρυθµός ψύξης µπορεί να προκαλέσει προβλήµατα υφής σε ορισµένα τρόφιµα, όπως φρούτα, λαχανικά και κρέας, ενώ η ανάπτυξη τοπικά χαµηλής θερµοκρασίας οδηγεί στο σχηµατισµό λεκέδων και στην αλλοίωση της υφής σε φρούτα και λαχανικά. Αεροψυκτήρες Η χρήση αεροψυκτήρων σε συστήµατα συνεχούς ή ασυνεχούς λειτουργίας είναι η ευρύτερα χρησιµοποιούµενη µέθοδος ψύξης επειδή είναι οικονοµική, υγιεινή και παρουσιάζει σχετικά περιορισµένα προβλήµατα διάβρωσης του εξοπλισµού. Το µεγαλύτερο µειονέκτηµα της ψύξης µε αέρα είναι η αφυδάτωση των µη συσκευασµένων τροφίµων. Επίσης η οµοιόµορφη κατανοµή του αέρα αποτελεί 160
169 πρόβληµα που πρέπει να αντιµετωπισθεί κατά το σχεδιασµό και τη λειτουργία του συστήµατος. Στα συστήµατα ασυνεχούς λειτουργίας τα τρόφιµα µεγάλου µεγέθους (σφάγια, µπανάνες κ.λ.π.) αναρτώνται σε ράγες στην οροφή ενώ τα µικρότερου µεγέθους τοποθετούνται σε παλέτες ή σε µεγάλες λεκάνες και η ψύξη γίνεται µε αεροψυκτήρες οροφής ή δαπέδου. Οι λειτουργικές παράµετροι που ελέγχονται κατά τη διάρκεια της ψύξης είναι η θερµοκρασία και η ταχύτητα του αέρα. Μείωση της θερµοκρασίας και αύξηση της ταχύτητας µειώνει το χρόνο ψύξης, ο οποίος βέβαια εξαρτάται από το µέγεθος του ψυχόµενου τροφίµου και το συντελεστή θερµικής αγωγιµότητας αυτού. Ο κίνδυνος επιφανειακής κατάψυξης του ψυχόµενου τροφίµου περιορίζει την ελάχιστη θερµοκρασία του αέρα που µπορεί να χρησιµοποιηθεί. Ιδιαίτερο πρόβληµα παρουσιάζουν τα συσκευασµένα έτοιµα γεύµατα που περιέχουν δύο ή περισσότερα προϊόντα (π.χ. κρέας µε ζυµαρικά) µε διαφορετικές θερµικές ιδιότητες. Η αύξηση της ταχύτητας του αέρα επιταχύνει τη συναγωγή θερµότητας. Σε χαµηλές ταχύτητες η συναγωγή θερµότητας από την επιφάνεια του τροφίµου µπορεί να αποτελεί το βραδύτερο στάδιο (Bi<0.1) και εποµένως η αύξησή της επιταχύνει την ψύξη του τροφίµου. Σε µεγάλες τιµές ταχύτητας του αέρα το ελέγχον στάδιο είναι η αγωγή θερµότητας στο εσωτερικό του τροφίµου και η αύξηση της ταχύτητας επιφέρει ασήµαντη µείωση του χρόνου ψύξης. Η απαιτούµενη ισχύς του αεροψυκτήρα για την κίνηση του αέρα είναι ανάλογη του κύβου της ταχύτητας εποµένως για οικονοµικούς λόγους στην ψύξη µεγάλων τεµαχίων τροφίµων δεν χρησιµοποιείται ταχύτητα αέρα µεγαλύτερη από 1m/s. Η µη οµοιόµορφη κατανοµή του αέρα στο θάλαµο ψύξης οδηγεί σε µη αποτελεσµατική ψύξη µέρους των προϊόντων. Εάν τα τρόφιµα δεν τοποθετηθούν σωστά, µε οµοιόµορφα διάκενα µεταξύ τους, ο αέρας θα µετακινηθεί στα µεγαλύτερα ανοίγµατα αντί να περάσει δια µέσου όλων των προϊόντων. Παρόµοια προβλήµατα εµφανίζονται σε µεγάλα σιλό µε σπόρους ή φρούτα που ψύχονται µε αέρα υπό πίεση. Στα συστήµατα συνεχούς λειτουργίας το πρόβληµα ανοµοιόµορφης κατανοµής του αέρα ελαχιστοποιείται. Σε αυτά τα συστήµατα τα τρόφιµα διακινούνται, αναρτώµενα από την οροφή, δια µέσου του θαλάµου ψύξης ή µεταφέρονται µέσω µίας σήραγγας ψύξης. Στις σήραγγες ψύξης υπάρχει η δυνατότητα της µεταβολής των συνθηκών του αέρα κατά µήκος της σήραγγας µε χρήση µεγάλης ψυκτικής ισχύος στην αρχή της σήραγγας για ταχύ ρυθµό απαγωγής θερµότητας και µικρότερης στο τέλος. Οι σήραγγες είναι επίπεδες ή έχουν ελικοειδή διάταξη για οικονοµία χώρου. Υδροψυκτήρες Η υδρόψυξη είναι η φθηνότερη µέθοδος ταχείας ψύξης σε προϊόντα µικρών διαστάσεων. Γίνεται µε εµβάπτιση προϊόντος ή ψεκασµό αυτού µε ψυχρό νερό, στο 161
170 οποίο συνήθως προστίθεται χλώριο ως αντισηπτικό. Τα συστήµατα ποικίλουν από απλές ή αναδευόµενες δεξαµενές ψυχρού νερού όπου εµβαπτίζεται το τρόφιµο έως διατάξεις µε συνεχή µεταφορά του τροφίµου µέσω αναδευόµενης δεξαµενής ή κάτω από ψεκαστήρες ψυχρού νερού. Με την υδρόψυξη συνήθως συµβαίνει µικρή αύξηση του βάρους και υπάρχει σχετική νοµοθεσία της Ευρωπαϊκής Ένωσης για τη µέγιστη επιτρεπτή αύξηση σε διάφορα προϊόντα. Η µέθοδος εφαρµόζεται κυρίως σε λαχανικά, όπως σέλινο, σπαράγγια, αρακά, καρότα και σε ορισµένα φρούτα, όπως ροδάκινα. Για µεγαλύτερα τρόφιµα όπως πουλερικά ή χοιρινά εφαρµόζεται εµβάπτιση σε ψυχρό νερό ή σε µίγµα νερού/πάγου. Επίσης µπορεί να χρησιµοποιηθεί αλατοδιάλυµα, οπότε τα προϊόντα ψύχονται συσκευασµένα για να ελαχιστοποιηθεί η απορρόφηση άλατος. Στην υδρόψυξη µε εµβάπτιση µη συσκευασµένων τροφίµων κύριο πρόβληµα µπορεί να αποτελέσει η αλληλοµόλυνση µε µικροοργανισµούς, ιδιαίτερα στα ζωικής προέλευσης και µπορεί να αντιµετωπισθεί µε συνεχή συστήµατα διαβίβασης του νερού και του τροφίµου κατ αντιρροή. Η υδρόψυξη µε ψεκασµό έχει συνδυασθεί και µε ψύξη µε αέρα. Συνήθως εναλλάσσεται ο ψεκασµός νερού και η διοχέτευση ψυχρού αέρα για ορισµένα χρονικά διαστήµατα η κάθε µία. Το κύριο πλεονέκτηµα είναι η µικρότερη απώλεια υγρασίας. Η χρήση ψυχρού αέρα στο τελικό στάδιο της ψύξης εξασφαλίζει στεγνές επιφάνειες των τροφίµων που είναι ο σηµαντικότερος παράγοντας για τον περιορισµό της µικροβιακής ανάπτυξης. Ψυκτήρες πλακών Σε τρόφιµα µικρού πάχους η ψύξη µε επαφή µε ψυχόµενες πλάκες µπορεί να µειώσει περίπου στο µισό τον απαιτούµενο χρόνο συγκρινόµενη µε ένα σύστηµα µε αεροψυκτήρες. Τα συστήµατα αυτά είναι συνεχούς λειτουργίας. Χρησιµοποιούνται για τη γρήγορη ψύξη συσκευασµένων τροφίµων, ή ιδιαίτερα ευαλλοίωτων τροφίµων, όπως το αποστεωµένο κρέας. Σ αυτές τις περιπτώσεις η πρόψυξη αποτελεί συχνά το πρώτο στάδιο µιας διεργασίας κατάψυξης. Ψύξη µε πάγο ή µίγµα νερού/πάγου Η ψύξη µε θρυµµατισµένο πάγο είναι απλή και χρησιµοποιείται κυρίως σε ψάρια. Τα ψάρια συσκευάζονται σε κιβώτια µε στρώσεις θρυµµατισµένου πάγου µεταξύ τους. Ο πάγος απορροφά θερµότητα από το τρόφιµο για την τήξη του και το ψυκτικό µίγµα διατηρείται στους 0 ο C όσο υπάρχει ακόµα πάγος. Η ελάχιστη ποσότητα πάγου που απαιτείται για την ψύξη ενός τροφίµου είναι: m= Q/ (6.57) όπου m η µάζα του πάγου (kg) Q το ποσό θερµότητας που πρέπει να απονακρυνθεί (kj) 162
171 kj/kg η λανθάνουσα θερµότητα τήξης του πάγου στους 0 C Ψύξη υπό µειωµένη πίεση Τρόφιµα που έχουν µεγάλη επιφάνεια προς όγκο και τη δυνατότητα αποµάκρυνσης νερού µε εξάτµιση µπορούν να ψυχθούν σε χώρους µε µειωµένη πίεση. Οι θάλαµοι ψύξης λειτουργούν σε 4-5 mm Hg και επιτυγχάνεται µείωση της θερµοκρασίας κατά 5 ο C περίπου για εξάτµιση 1 % του νερού. Η θερµότητα που απάγεται µε εξάτµιση υπολογίζεται σύµφωνα µε την εξίσωση (6.10). Με αυτή τη µέθοδο ψύχονται λαχανικά, όπως µαρούλι, σέλινο, λάχανο κ.ά. Συνήθως τα προϊόντα καταβρέχονται πριν την ψύξη για να αποφευχθεί η απώλεια βάρους. Κρυογόνος ψύξη Η χρήση ψυκτικών µέσων, όπως υγρό άζωτο και υγρό ή στερεό διοξείδιο του άνθρακα ( κρυογόνος) εφαρµόζεται κυρίως στην κατάψυξη αλλά έχει αναφερθεί και στην ψύξη κρέατος. Το κύριο πρόβληµα σε αυτή τη µέθοδο είναι η επιφανειακή κατάψυξη του προϊόντος. Οι επιφανειακοί συντελεστές µεταφοράς θερµότητας µεταβάλλονται πολύ καθώς το υγρό βράζει ερχόµενο σε επαφή µε την επιφάνεια του τροφίµου και εξαρτώνται από τη θερµοκρασία αυτής της επιφάνειας (Πιν. 8.2). Παραδείγµατα 1. Κατά τη θερµική κατεργασία κονσερβοποιηµένου προϊόντος σε αυτόκλειστο θερµοκρασίας 250 F, µε χρόνο ανόδου της θερµοκρασίας του αυτοκλείστου 3 min, καταγράφηκαν τα ακόλουθα δεδοµένα θερµοκρασίας του θερµικού κέντρου του προϊόντος ως συνάρτηση του χρόνου παραµονής στο αυτόκλειστο: Χρόνος (min) Θερµοκρασία F Χρόνος (min) Θερµοκρασία F (ψύξη) α) Να υπολογισθούν οι τιµές των f h και j h Λύση Θα κατασκευασθεί το διάγραµµα log (T r -T) ως προς t. 163
172 T r -T time (min) log (T r -T) , , ,9 2, , , , , , , ,6 45 1, ,5 50 1, , , ,5 65 0, , ,7 75 0, ,7 80 0, ,5 log (Tr-T) 2 log (Tr-T) 1,5 1 0, time (min) 2,5 2 log (Tr-T) 1,5 1 0,5 y = -0,0248x + 2, time (min) Από την κλίση της ευθείας που προκύπτει εξαιρώντας τα τρία αρχικά σηµεία (υστέρηση) υπολογίζουµε τον παράγοντα f h =1/0.0248=40.32 min. Ο παράγοντας υστέρησης υπολογίζεται από την αποτέµνουσα της ευθείας log (T r -T A )= και T r -T A =268 j h =(T r -T A )/(T r -T IT )=268/( )= Λουκάνικα µήκους 0.4 m και διαµέτρου 0.03 m ψύχονται από αρχική θερµοκρασία 21 C στους 4 C σε θάλαµο µε ρεύµα αέρα θερµοκρασίας 1 C. Να εκτιµηθεί ο χρόνος που χρειάζεται για να φθάσει η θερµοκρασία στο γεωµετρικό άξονα του προϊόντος τους 4 C. ίδονται επιφανειακός συντελεστής µεταφοράς 164
173 θερµότητας h=13 W/m 2 C, θερµική αγωγιµότητα k=0.4 W/m C, ειδική θερµότητα c p =3.1 kj/kg C και πυκνότητα ρ=950 kg/m 3. Λύση Υπολογίζεται ο αριθµός Biot h. Bi = R = = > 01. k 04. Αρα για τη µεταφορά θερµότητας τόσο η αγωγή στο τρόφιµο όσο και η συναγωγή από την επιφάνεια του τροφίµου προς το µέσο ψύξης είναι σηµαντικές. Επειδή το µήκος του λουκάνικου είναι υπερδεκαπλάσιο της διαµέτρου µπορούµε να θεωρήσουµε ότι προσεγγίζει κύλινδρο απείρου µήκους και να χρησιµοποιήσουµε το αντίστοιχο σχήµα του Παραρτήµατος. T Tm 4 1 = TIT Tm 21 1 = 015. και m= 1 Bi = 205. Από σχήµα Π.2: 2 at = 25. t = = 4140 s=69 min. R Λάχανο ψύχεται από τους 32.2 C στους 4.4 C σε 4 h. Να υπολογισθεί η θερµότητα που πρέπει να αποµακρυνθεί. Λύση Η συνολική θερµότητα ανά µονάδα µάζας (Q) που πρέπει να αποµακρυνθεί θα είναι η αισθητή θερµότητα Θεωρώντας µία µέση τιµή περιεχόµενης υγρασίας στο λάχανο 90 % επί υγρής βάσης µπορούµε να υπολογίσουµε την ειδική θερµότητα αυτού από τη σχέση Siebel: c p =33.49x =3851 J/kg C Εποµένως η συνολική αισθητή θερµότητα που πρέπει να αποµακρυνθεί είναι: Q = c p T = 3.851( ) = kj/kg Ασκήσεις 1. Πατάτες διαστάσεων 0.08x0.04x0.065 mxmxm ψύχονται από αρχική θερµοκρασία 27 C σε θάλαµο µε ρεύµα αέρα θερµοκρασίας 2 C. Να εκτιµηθεί ο χρόνος που χρειάζεται για να φθάσει η θερµοκρασία στο κέντρο του προϊόντος τους 8 C. ίδονται επιφανειακός συντελεστής µεταφοράς θερµότητας h=40 W/m 2 C, και πυκνότητα ρ=1030 kg/m Ροδάκινα ψύχονται από τους 21 C στους 4 C σε ρεύµα ψυχρού νερού θερµοκρασίας 1.5 C. Να υπολογισθεί ο απαιτούµενος χρόνος για να φθάσει το γεωµετρικό κέντρο του ροδάκινου τους 4 C εάν ο επιφανειακός συντελεστής µεταφοράς θερµότητας στο ρεύµα νερού είναι 50 W/m 2 C, η µέση ακτίνα των φρούτων είναι m, η πυκνότηα αυτών ρ=975 kg/m 3 και η θερµική αγωγιµότητα k=0.52 W/m C. Για τον υπολογισµό της ειδικής θερµότητας δίνεται η µέση σύσταση των ροδακίνων ως υδατάνθρακες 14.6%, πρωτεaνες 0.4%, λιπαρά 0.3%, τέφρα 0.5%, νερό 84.2%. 165
174 Σύµβολα a=k/ρc p θερµική διαχυτότητα του τροφίµου (m 2 /s) α σταθερά της εξίσωσης (3.33) Α επιφάνεια εναλλαγής θερµότητας (m 2 ) α w ενεργότητα νερού b σταθερά της εξίσωσης (3.33) β µέγεθος οριζόµενο από τις εξισώσεις (3.11), (3.12) Βi αριθµός Biot: hr/k c ειδική θερµότητα (J/kg K) f χρόνος υποδεκαπλασιασµού της διαφοράς θερµοκρασίας µεταξύ του τροφίµου και του ψυκτικού µέσου (s) Fo αριθµός Fourier kt/(ρc p R 2 ) ή αt/r 2 F 1-2 συντελεστής στην εξίσωση (3.7) h επιφανειακός συντελεστής µεταφοράς θερµότητας (W/m 2 C) H d ύψος πόρτας (m) j παράγοντας υστέρησης k συντελεστής θερµικής αγωγιµότητας (W/m K) k g L m συντελεστής µεταφοράς µάζας (s/m) λανθάνουσα θερµότητα εξάτµισης του νερού (J/kg) µάζα (kg) Μ περιεχόµενη υγρασία (% επί υγρής βάσης) N εισροή υδρατµών (kg/s) N t εισροή υδρατµών από διάφορες πηγές εντός του θαλάµου (kg/s) p a µερική πίεση ατµών στον περιβάλλοντα αέρα (Pa) p s o p a o p s q Q r R µερική πίεση ατµών στο οριακό στρώµα που περιβάλει το τρόφιµο (Pa) τάση ατµών του νερού σε θερµοκρασία T a (Pa) τάση ατµών του νερού σε θερµοκρασία T s (Pa) ρυθµός ροής ή παραγωγής θερµότητας (W) µεταφερόµενη ή παραγώµενη θερµότητα (J) απόσταση από το κέντρο ή τον άξονα συµµετρίας (m) χαρακτηριστική διάσταση του τροφίµου (m) ρ πυκνότητα (kg/m 3 ) σ σταθερά Stefan-Boltzmann (W/m 2 K 4 ) T θερµοκρασία ( C) U συνολικός συντελεστής µεταφοράς θερµότητας (W/m 2 C) v a µέση ταχύτητα του αέρα δια µέσου του ανοίγµατος (m/s) V όγκος (m) 166
175 W υγρασία αέρα (kg υδρατµών/kg ξηρού αέρα) W d πλάτος πόρτας (m) Y=(T-T m )/(T IT -T m ) ανοιγµένη θερµοκρασία Z σταθερά της εξίσωσης (3.3) είκτες α αέρας (εντός του ψυκτικού θαλάµου) av µέση τιµή b υλικό εξισορρόπησης θερµοκρασιακών µεταβολών c θερµικό κέντρο d πόρτα ψυκτικού θαλάµου ext εξωτερικό περιβάλλον του θαλάµου IT αρχική τιµή m µέσο ψύξης p τρόφιµο r αναπνοή rad ακτινοβολία s επιφάνεια τροφίµου w τοίχος θαλάµου Βιβλιογραφία Brown M.H. and Gould G.W. (1992) Processing in Chilled Foods A Comrehensive Guide, ed. C. Dennis and M. Stringer, Ellis Horwood, N.Y., pp Cleland A.C. (1990) Food Refrigeration Processes Analysis, Design and Simulation, Elsevier Applied Science, London-N.Y., pp. 1-32, Fennema O. (1975) Preservation of food by storage at chilling temperatures in Physical Principles of Food Preservation, ed. O. Fennema, Marcel Dekker Ink., N.Y., pp Gorini F.L., Eccher Zerbini P. and Testoni A. (1990) The contolled atmosphere storage of fruit and vegetables in Chilled Foods The State of the Art, ed. T.R.Gormley, Elsevier Applied Science, London-N.Y., pp Heldman D.R. and Singh R.P. (1981) Food Process Engineering, 2 nd ed., The AVI Publishing Co. Inc., Westport, Connecticut, pp , James S.J. and Bailey C. (1990) Chilling systems for foods in Chilled Foods The State of the Art, ed. T.R.Gormley, Elsevier Applied Science, London-N.Y., pp Θωµόπουλος Χ.. (1981) Τεχνολογία Γεωργικών Βιοµηχανιών, Λύχνος ΕΠΕ, Αθήνα, σελ
176 Μαρκάκης Π. (1996) Στοιχεία Τεχνολογίας Τροφίµων, Τρίαινα Εκδοτική, Αθήνα, σελ O Beirne D. (1990) Modified atmosphere packaging of fruits and vegetables in Chilled Foods The State of the Art, ed. T.R.Gormley, Elsevier Applied Science, London-N.Y., pp Rahman S. (1995) Food Properties Handbook, CRC Press, Boca Raton, pp Singh R.P. and Mannapperuma J.D. (1990) Developments in food freezing in Biotechnology and Food Process Engineering, ed. H.G. Schwartzberg aand M.A. Rao, Marcel Dekker, N.Y., pp Toledo R.T. (1991) Fundamentals of Food Process Engineering, 2 nd ed, The AVI Publishing Co. Inc., Westport, Connecticut, pp Walker S.J. (1992) Chilled foods microbiology in Chilled Foods A Comrehensive Guide, ed. C. Dennis and M. Stringer, Ellis Horwood, N.Y., pp Woolfe M.L. (1992) Temperature monotoring and measurement in Chilled Foods A Comrehensive Guide, ed. C. Dennis and M. Stringer, Ellis Horwood, N.Y., pp
177 ΚΕΦΑΛΑΙΟ 7 ΠΑΣΤΕΡΙΩΣΗ ΚΑΙ ΑΠΟΣΤΕΙΡΩΣΗ Εισαγωγή Η παστερίωση και η αποστείρωση (αναφερόµενες και ως θερµικές διεργασίες) των τροφίµων έχουν ως στόχο την καταστροφή µικροοργανισµών ή και την αδρανοποίηση των ενζύµων που υπάρχουν στο τρόφιµο. Παράλληλα όµως στη διάρκεια των διεργασιών αυτών, λόγω υψηλής θερµοκρασίας, εξελίσσονται µε ταχύτερο ρυθµό δράσεις υποβάθµισης της ποιότητας του τροφίµου (αλλοίωση οργανοληπτικών χαρακτηριστικών, µεταβολές των συστατικών). Εποµένως οι συνθήκες της κάθε θερµικής κατεργασίας επιλέγονται έτσι ώστε να δίνουν σταθερό προϊόν µε τη µικρότερη δυνατή υποβάθµιση της ποιότητας. Επί πλέον της παστερίωσης και αποστείρωσης, θερµική διεργασία αποτελεί και το ζεµάτισµα των τροφίµων. Οι βασικοί στόχοι και οι διαφορές µεταξύ αυτών των διεργασιών συνοψίζονται στη συνέχεια Παστερίωση Η παστερίωση είναι σχετικά ήπια θερµική διεργασία που καταστρέφει µέρος των µικροοργανισµών του τροφίµου και συνεπώς συνδυάζεται µε συνθήκες αποθήκευσης που περιορίζουν την ανάπτυξη των επιζώντων µικροοργανισµών. Σε πολλές περιπτώσεις ο κύριος στόχος της παστερίωσης είναι η καταστροφή των παθογόνων µικροοργανισµών (π.χ. στο γάλα), αλλά εφαρµόζεται και για την καταστροφή αλλοιογόνων µικροοργανισµών (π.χ. στη µπύρα). Αποστείρωση Η αποστείρωση είναι η θερµική διεργασία που στοχεύει στην καταστροφή όλων των µικροοργανισµών και των σπορίων τους. Στείρο είναι το προϊόν στο οποίο δεν έχει επιβιώσει κανένας µικροοργανισµός, ώστε να είναι ικανός να αναπτυχθεί όταν βρεθεί σε ευνοϊκές συνθήκες. Εποµένως οι όροι στείρο και αποστείρωση δεν είναι δόκιµοι για τα τρόφιµα και τη θερµική κατεργασία αυτών που στοχεύει στην πραγµατικότητα στη µείωση της πιθανότητας επιβίωσης των µικροοργανισµών και των σπορίων τους, ώστε υπό τις προβλεπόµενες συνθήκες συντήρησης του τροφίµου να µειώνεται σηµαντικά η πιθανότητα ανάπτυξης αυτών των µικροοργανισµών. Πιο δόκιµος θα ήταν ο όρος εµπορικά στείρο (commercially sterile). Παρ όλα αυτά ο όρος αποστείρωση έχει επικρατήσει για τη θερµική διεργασία που εφαρµόζεται σε τρόφιµα µε στόχο να µειώσει τους πληθυσµούς όλων των µικροοργανισµών και των σπορίων τους. Τα σπόρια είναι τα πλέον θερµοάντοχα και η ένταση της κατεργασίας εξαρτάται κυρίως από την αντίσταση αυτών στη θερµική καταστροφή. 169
178 Ζεµάτισµα Το ζεµάτισµα είναι µία θερµική διεργασία που εφαρµόζεται κυρίως σε φρούτα και λαχανικά πριν από την κατάψυξη, την ξήρανση ή την κονσερβοποίηση. Ο σκοπός του ζεµατίσµατος εξαρτάται από τη διεργασία που θα ακολουθήσει. Το ζεµάτισµα πριν από την κατάψυξη ή την ξήρανση γίνεται κυρίως για την αδρανοποίηση των ενζύµων που προκαλούν ανεπιθύµητες µεταβολές στο χρώµα, τη γεύση, το άρωµα ή και τη θρεπτική αξία του τροφίµου. ύο από τα πιο θερµοάντοχα ένζυµα που υπάρχουν στους φυτικούς ιστούς είναι η περοξειδάση και η καταλάση. Η αποτελεσµατικότητα του ζεµατίσµατος συχνά ελέγχεται µέσω της ενεργότητας αυτών των ενζύµων. Κατά το ζεµάτισµα καταστρέφεται και ένα ποσοστό µικροοργανισµών του τροφίµου, το οποίο σε ορισµένες περιπτώσεις σε τρόφιµα που πρόκειται να καταψυχθούν έχει παρατηρηθεί ότι ανέρχεται µέχρι και σε 98% του συνολικού πληθυσµού. Πριν την κονσερβοποίηση το ζεµάτισµα εφαρµόζεται κυρίως για την αποµάκρυνση των αερίων από τους φυτικούς ιστούς, τη συρρίκνωση του φλοιού, το µαλάκωµα της σάρκας του τροφίµου που διευκολύνει τη συσκευασία και τον καθαρισµό του τροφίµου. Η απενεργοποίηση των ενζύµων δεν αποτελεί συνήθως στόχο σε αυτή την περίπτωση, δεδοµένου ότι θα ακολουθήσει µία θερµική κατεργασία ικανή να αδρανοποιήσει τα ένζυµα. Κινητική καταστροφής µικροοργανισµών- Ορισµοί Ρυθµός καταστροφής υπό σταθερή θερµοκρασία- Χρόνος υποδεκαπλασιασµού (D) Όταν ένα αιώρηµα µικροοργανισµών θερµανθεί υπό σταθερή θερµοκρασία η καταστροφή των µικροοργανισµών ακολουθεί κινητική πρώτης τάξης, δηλ. ο ρυθµός καταστροφής είναι ανάλογος της συγκέντρωσης των ζώντων µικροοργανισµών: dc = kc (7.1) dt όπου C συγκέντρωση των ζώντων µικροοργανισµών (L -1 ) k σταθερά του ρυθµού της δράσης (s -1 ) Αντί της συγκέντρωσης συχνά χρησιµοποιείται ο πληθυσµός των µικροοργανισµών ανά περιέκτη, που συµβολίζεται µε Ν. Ολοκληρώνοντας την εξίσωση (7.1) µεταξύ των ορίων C o σε χρόνο t o = 0 και C σε χρόνο t προκύπτει: ln C = kt (7.2) C ή log o C Co = k t = 1 t ή log N = 1 2,303 D N D t (7.3) o 170
179 Η εξίσωση (7.3) ορίζει το µέγεθος D, το οποίο καλείται χρόνος υποδεκαπλασιασµού (Decimal reduction time) και είναι ο χρόνος (s) που απαιτείται για να υποδεκαπλασιασθεί η συγκέντρωση των µικροοργανισµών (C = C o /10). Σύµφωνα µε την εξίσωση (7.3) ο χρόνος υποδεκαπλασιασµού των µικροοργανισµών σχετίζεται µε τη σταθερά k του ρυθµού θανάτωσης των µικροοργανισµών µέσω της σχέσης: D = 2, 303 (7.4) k Εποµένως εάν αντί της σταθεράς k χρησιµοποιηθεί ο χρόνος υποδεκαπλασιασµού D η εξίσωση (7.1) γράφεται και ως: d(logc) 1 = (7.5) dt D Η εξίσωση (7.3) δείχνει ότι µηδενική συγκέντρωση µικροοργανισµών δεν µπορεί να επιτευχθεί σε ορισµένο χρόνο θερµικής κατεργασίας. Εποµένως απόλυτη ασφάλεια έναντι της ανάπτυξης µικροοργανισµών, δηλ. η παραγωγή στείρου προϊόντος, δεν µπορεί να υπάρξει. Μπορεί όµως να µειωθεί στα επιθυµητά επίπεδα η πιθανότητα επιβίωσης και εποµένως και ανάπτυξης αυτών. Έτσι η αποµένουσα συγκέντρωση µετά από χρόνο t θερµικής κατεργασίας, συχνά αποδίδεται ως σπόρια ανά δοχείο συσκευασίας και εκφράζει την πιθανότητα µικροβιακής αλλοίωσης στο θερµικά κατεργασµένο τρόφιµο. Εάν π.χ. η αποµένουσα συγκέντρωση είναι 10-4 σπόρια ανά δοχείο συσκευασίας, αυτό σηµαίνει ότι 1 σπόριο έχει επιβιώσει σε 10 4 δοχεία και το περιεχόµενο του αντίστοιχου δοχείου µπορεί να αλλοιωθεί ή γενικότερα να υπάρξει ανάπτυξη του µικροοργανισµού σε αυτό. Οποιαδήποτε τιµή της συγκέντρωσης C 1 σηµαίνει αλλοίωση όλων των δοχείων. Η καταστροφή των µικροοργανισµών σε ηµιλογαριθµικό διάγραµµα ως προς το χρόνο αποδίδεται συνήθως από απλή ευθεία γραµµή, όπως στο σχήµα 7.1Α. Οι πειραµατικές µετρήσεις όµως έχουν δείξει διάφορες αποκλίσεις. Η καµπύλη του σχήµατος 7.1Β δείχνει µια αρχική αύξηση της συγκέντρωσης των µικροοργανισµών που ακολουθείται από αδρανοποίηση πρώτης τάξης. Αυτή η συµπεριφορά έχει παρατηρηθεί σε πολύ θερµοανθεκτικά σπόρια που ενεργοποιούνται µε αύξηση της θερµοκρασίας και πολλαπλασιάζονται αρχικά, ενώ αυτό δεν θα είχε συµβεί χωρίς τη θερµική κατεργασία. Το σχήµα 7.1C δείχνει µια αρχική υστέρηση στην καµπύλη θερµικής αδρανοποίησης. Στις περισσότερες περιπτώσεις αυτή η υστέρηση δεν επεκτείνεται πέραν του χρόνου ενός λογαριθµικού κύκλου δηλ. του χρόνου που απαιτείται για να αδρανοποιηθεί το 90% του πληθυσµού. Έτσι η καµπύλη του σχήµατος 7.1C µπορεί να αποδοθεί από την εξίσωση: log C t tl = 1, C D t > t L (.6) o 171
180 όπου t L ο χρόνος υστέρησης που ορίζεται ίσος µε το χρόνο αδρανοποίησης του αρχικού 90% του πληθυσµού. Ο ορισµός του χρόνου υστέρησης όπως στην εξίσωση (7.6) περιορίζει τα λάθη που µπορεί να γίνουν στην επιλογή του µε βάση τις πειραµατικές µετρήσεις. Οι πειραµατικές µετρήσεις δείχνουν ότι ο χρόνος υστέρησης µεταβάλλεται για διαφορετικές αρχικές συγκεντρώσεις µικροοργανισµών και διαφορετικές θερµοκρασίες. Συνήθως ο t L πλησιάζει το D όσο η αρχική συγκέντρωση µειώνεται και η θερµοκρασία αυξάνεται. Όταν t L = D η εξίσωση (7.6) µεταπίπτει στην εξίσωση (7.3) και η καταστροφή των µικροοργανισµών ακολουθεί κινητική πρώτης τάξης από την αρχή της διεργασίας. Η εξίσωση (7.6) δεν χρησιµοποιείται συνήθως στους υπολογισµούς στις θερµικές διεργασίες εκτός εάν προσδιορισθεί ποσοτικά η εξάρτηση του χρόνου υστέρησης από την αρχική συγκέντρωση και τη θερµοκρασία. Σχήµα 7.1. Καµπύλες µεταβολής της συγκέντρωσης των µικροοργανισµών µε το χρόνο θερµικής κατεργασίας. 172
181 Το σχήµα 7.1D αντιπροσωπεύει την καµπύλη αδρανοποίησης µιας µικτής καλλιέργειας. Η αδρανοποίηση κάθε είδους µικροοργανισµών θεωρείται ανεξάρτητη της αδρανοποίησης του άλλου. Εάν υπάρχουν δύο είδη µικροοργανισµών Α και Β µε χρόνους υποδεκαπλασιασµού D A και D B, αντίστοιχα η συγκέντρωση του κάθε πληθυσµού µετά από οποιδήποτε χρονικό διάστηµα µπορεί να υπολογισθεί µε βάση την εξίσωση (7.3): t D C = C ( 10 ) ( / ) A t D, C = C ( 10 ) ( / ) B και A Ao B Bo ( t/ DA) ( t/ DB) Bo C = C + C = C ( 10) + C ( 10 ) A B Ao Εάν D A <<D B ο δεύτερος όρος είναι κατά προσέγγιση σταθερός σε µικρές τιµές t και υπερισχύει ο πρώτος όρος, όπως φαίνεται από την αρχική ευθεία του σχήµατος 7.1D µε κλίση -1/D A. Σε µεγάλες τιµές t ο πρώτος όρος πλησιάζει το µηδέν και ο συνολικός πληθυσµός εκφράζεται από το δεύτερο όρο που αντιστοιχεί στη ευθεία µε κλίση -1/D B. Ο χρόνος θερµικής κατεργασίας για να επιτευχθεί µία ορισµένη τελική συγκέντρωση, ή πιθανότητα αλλοίωσης, από µικτούς πληθυσµούς µε γνωστές αρχικές συγκεντρώσεις και τιµές D, λαµβάνεται ως ο µέγιστος χρόνος που υπολογίζεται µέσω της εξίσωσης (7.3) για κάθε πληθυσµό χωριστά µε τελική συγκέντρωση την ορισθείσα. Το σχήµα 7.1Ε δείχνει µια απόκλιση από την ευθεία σε µεγάλους χρόνους θερµικής αδρανοποίησης η οποία µπορεί να εµφανισθεί όταν οι αρχικές συγκεντρώσεις είναι πολύ µεγάλες και οι µικροοργανισµοί έχουν την τάση να σχηµατίζουν συστάδες. Στον υπολογισµό του χρόνου κατεργασίας η απόκλιση αυτή δεν λαµβάνεται υπόψη, όπως και στην περίπτωση της αρχικής υστέρησης, εκτός εάν υπάρχουν δεδοµένα αναπαραγωγισιµότητας της καµπύλης και ποσοτικής συσχέτισης µε την αρχική συγκέντρωση και τη θερµοκρασία. Χρόνος θερµικού θανάτου (F) Ο χρόνος διατήρησης σε σταθερή θερµοκρασία που απαιτείται για την επίτευξη προκαθορισµένης µείωσης της συγκέντρωσης ενός πληθυσµού καλείται χρόνος θερµικού θανάτου (thermal death time, TDT) και συµβολίζεται µε F. Η τιµή του F συνήθως αποδίδεται ως πολλαπλάσιο του χρόνου υποδεκαπλασιασµού D. Εάν π.χ. είναι επιθυµητή η µείωση του πληθυσµού κατά % ή 10-6 του αρχικού απαιτείται χρόνος F = 6D. Για την έκφραση της µείωσης ενός πληθυσµού χρησιµοποιείται και ο όρος τιµή αποστείρωσης (sterilization value, SV) όπου N o Co SV = log = log (7.7) N C 173
182 Εποµένως για µείωση του πληθυσµού κατά %, όπως στο προηγούµενο παράδειγµα, SV = 6 και ο απαιτούµενος χρόνος υπό σταθερή θερµοκρασία F = SV * D (7.8) Επίδραση της θερµοκρασίας στο ρυθµό θανάτωσης- Σταθερά θερµικής αντίστασης (z) Η εξάρτηση της σταθεράς του ρυθµού θανάτωσης από τη θερµοκρασία µπορεί να αποδοθεί είτε από την εξίσωση Arrhenius είτε µέσω της σταθεράς θερµικής αντίστασης (thermal resistance constant) z. Σύµφωνα µε την εξίσωση Arrhenius: Ea 1 1 k = k o exp( Ea / RT ) ή log( k / k ref ) = ( 2.303R T T ) (7.9) όπου E a ενέργεια ενεργοποίησης (J/mol) T απόλυτη θερµοκρασία (Κ) Η χρήση της σταθεράς z στηρίζεται στις παρατηρήσεις του Bigelow, σύµφωνα µε τις οποίες ο λογάριθµος του χρόνου θερµικού θανάτου (του ελάχιστου χρόνου για επίτευξη πλήρους καταστροφής ενός πληθυσµού, όπως τον όρισε) µεταβάλλεται µε τη θερµοκρασία γραµµικά, όπως φαίνεται στο σχήµα 7.2. Εκφράζοντας το χρόνο θερµικού θανάτου µε F όπως ορίσθηκε παραπάνω, η εξίσωση που αποδίδει τη σχέση αυτού µε τη θερµοκρασία είναι: Tref T log( F / Fref ) = (7.10) z όπου F, F ref χρόνοι θερµικού θανάτου σε θερµοκρασία T και T ref ( F ή C) αντίστοιχα (s) z σταθερά θερµικής αντίστασης, η οποία ισούται µε τη διαφορά θερµοκρασίας ( F ή C) που απαιτείται για να δεκαπλασιασθεί ή υποδεκαπλασιασθεί ο χρόνος θερµικού θανάτου. Εάν αντί του χρόνου θερµικού θανάτου χρησιµοποιήσουµε το χρόνο υποδεκαπλασιασµού του πληθυσµού ενός µικροοργανισµού ή εξίσωση (7.10) γράφεται ως: Tref T log( D / Dref ) = (.11) z Η σταθερά θερµικής αντίστασης ενός µικροοργανισµού µπορεί να υπολογισθεί από ηµιλογαριθµικό διάγραµµα του χρόνου θερµικού θανάτου ή του χρόνου υποδεκαπλασιασµού συναρτήσει της θερµοκρασίας, ως το αντίστροφο της αρνητικής κλίσης της προκύπτουσας ευθείας (σχήµα 7.2): z = ( T1 T2) / log( F2 / F1 ) ή z = ( T1 T2) / log( D2 / D1 ) ref 174
183 Η τιµή του z εκφράζει την επίδραση της θερµοκρασίας στο ρυθµό καταστροφής κάθε συγκεκριµένου µικροοργανισµού και είναι προφανές ότι χαµηλή τιµή σηµαίνει µεγάλη µεταβολή του ρυθµού µε τη θερµοκρασία και αντιστρόφως. Η έκφραση της εξάρτησης της σταθεράς του ρυθµού καταστροφής k από τη θερµοκρασία µε βάση τη σταθερά z µπορεί να προκύψει µε συνδυασµό των εξισώσεων (7.4) και (7.11): Σχήµα 7.2. Μεταβολή του χρόνου θερµικού θανάτου µε τη θερµοκρασία. T Tref log( k / k ref ) = (7.12) z Η εξίσωση (7.12) δίνει την εξάρτηση του k από τη θερµοκρασία όπως και η εξίσωση Arrhenius (7.9). Πρέπει να αναφερθεί ότι υπάρχει ασυµφωνία µεταξύ των δύο εξισώσεων και ότι επίσης καµία από τις δύο δεν µπορεί να εκφράσει την επίδραση της θερµοκρασίας στην καταστροφή των µικροοργανισµών για µεγάλο θερµοκρασιακό εύρος. Παρ όλα αυτά είναι γενικά αποδεκτό ότι και οι δύο εξισώσεις µπορούν να χρησιµοποιηθούν µε ικανοποιητική ακρίβεια σε σχετικά στενό εύρος θερµοκρασιών για το οποίο υπάρχουν πειραµατικά δεδοµένα. 175
184 Στη θερµοβακτηριολογία και στις θερµικές διεργασίες στα τρόφιµα χρησιµοποιούνται συχνότερα οι σταθερές D και z, αντί των k και E a. Τιµές D και z διαφόρων µικροοργανισµών υπάρχουν στη βιβλιογραφία για διάφορα υποστρώµατα. Ως θερµοκρασία αναφοράς συνήθως χρησιµοποιούνται οι 250 F ή C και ο χρόνος υποδεκαπλασιασµού σε άλλη θερµοκρασία µπορεί να υπολογισθεί σύµφωνα µε την εξίσωση (7.11) ως: T log( D T / D ) = , T, z F ή z T log( D T / D121. 1) =, T, z C z O χρόνος υποδεκαπλασιασµού στους 250 F συχνά συµβολίζεται και µε D o. Είναι προφανές από τα παραπάνω ότι ο απαιτούµενος χρόνος F για την επίτευξη µιας καθορισµένης µείωσης συγκέντρωσης ενός µικροοργανισµού, ή τιµής αποστείρωσης, σε µια ισοθερµοκρασιακή κατεργασία εξαρτάται από τη θερµοκρασία και η µεταβολή του µε τη θερµοκρασία εξαρτάται από τη θερµική αντίσταση του µικροοργανισµού. Γι αυτό ο χρόνος θερµικού θανάτου επισηµαίνεται συνήθως µε δύο δείκτες, εκ των οποίων ο ένας δείχνει τη θερµοκρασία στην οποία αναφέρεται και ο άλλος την τιµή του z που χαρακτηρίζει το συγκεκριµένο µικροοργανισµό. Για τους 250 F (θερµοκρασία αναφοράς) χρησιµοποιείται το σύµβολο F z 250 ή F o z. Ο όρος F o χρησιµοποιείται ορισµένες φορές χωρίς την επισήµανση µε z και αναφέρεται σε z=18 F=10 C. Εποµένως η εξίσωση (7.10) µπορεί να γραφεί και ως: T FT Fo = T log( / ), όπου T, z F ή log( FT / Fo ) =, όπου T, z C z z Σταθερά Q Ένας άλλος όρος που χρησιµοποιείται για να εκφράσει την επίδραση της µεταβολής της θερµοκρασίας σε βιολογικά συστήµατα είναι η τιµή Q, η οποία δείχνει την αύξηση του ρυθµού µιας δράσης µε τη θερµοκρασία. Συνήθως χρησιµοποιείται η τιµή Q για διαφορά θερµοκρασίας 10 C, η οποία συµβολίζεται Q 10 και ορίζεται ως: k( T ) = Q10 (7.13) k ( T 10) όπου k (T), k (T-10) σταθερές του ρυθµού της δράσης σε θερµοκρασία T και 10) C, αντίστοιχα (s -1 ) Η σχέση που συνδέει το Q 10 µε το z, όπως προκύπτει από τις εξισώσεις (7.12) και (7.13) είναι: 18 log Q 10 = ή z (7.14α) 10 log Q 10 = z (7.14β) όπου z σε F και C στην (7.14α) και (7.14β), αντίστοιχα. (T- 176
185 Παράγοντες που επηρεάζουν τη θερµική αντίσταση των µικροοργανισµών Πολλοί παράγοντες επηρεάζουν τη θερµική αντίσταση των µικροοργανισµών. Τα δηµοσιευµένα αποτελέσµατα ερευνών συχνά παρουσιάζουν διαφορές που οφείλονται στις διαφορετικές τεχνικές που χρησιµοποιούνται για τη µέτρηση της θερµικής αντίστασης και στα διαφορετικά υποστρώµατα που χρησιµοποιούνται τόσο για την ανάπτυξη των µικροοργανισµών όσο και κατά την υποβολή τους στη θερµική κατεργασία. Αν και είναι δύσκολο να ποσοτικοποιηθεί η επίδραση κάθε ενός παράγοντα στη θερµική αντίσταση είναι κοινά αποδεκτό ότι τρεις κατηγορίες παραγόντων επιδρούν σε αυτήν: 1. Η ενυπάρχουσα αντίσταση του µικροοργανισµού 2. Το περιβάλλον ανάπτυξης του µικροοργανισµού 3. Το περιβάλλον στο οποίο βρίσκεται ο µικροοργανισµός στη διάρκεια της θερµικής κατεργασίας. Η ενυπάρχουσα αντίσταση ποικίλει ακόµη και µεταξύ διαφορετικών στελεχών του ίδιου είδους µικροοργανισµού τα οποία έχουν αναπτυχθεί στις ίδιες συνθήκες όπως διαπιστώθηκε από πολλούς ερευνητές. Τα σπόρια ή τα κύτταρα µε τη µεγαλύτερη αντίσταση πιστεύεται ότι περιέχουν πρωτεΐνες µεγαλύτερης σταθερότητας. Οι περιβαλλοντικοί παράγοντες κατά την ανάπτυξη των µικροοργανισµών έχει βρεθεί ότι επηρεάζουν σηµαντικά τη θερµική τους αντίσταση. Το ίδιο ισχύει και για τους περιβαλλοντικούς παράγοντες κατά τη θέρµανση αυτών. Με βάση τα στοιχεία που δίνονται στη βιβλιογραφία οι κύριοι παράγοντες είναι οι ακόλουθοι: Θερµοκρασία Τόσο η θερµοκρασία ανάπτυξης όσο και η θερµική αντίσταση ποικίλει στα διάφορα είδη µικροοργανισµών. Με βάση το εύρος διακύµανσης της θερµοκρασίας µέσα στο οποίο µπορούν να αναπτυχθούν οι µικροοργανισµοί χωρίζονται σε 4 κατηγορίες όπως παρουσιάζονται στον Πίνακα 7.1. Πίνακας 7.1. Θερµοκρασία ανάπτυξης διαφόρων κατηγοριών µικροοργανισµών Κατηγορία Θερµοκρασία ανάπτυξης ( C) µικροοργανισµών Ελάχιστη Άριστη Μέγιστη Θερµόφιλοι Μεσόφιλοι Ψυχρόφιλοι -5 έως Ψυχρότροφοι
186 Σε θερµοκρασία ανώτερη από τη µέγιστη θερµοκρασία ανάπτυξης των µικροοργανισµών αρχίζει ο θερµικός θάνατος των κυττάρων. Τα σπόρια όµως των µικροοργανισµών και ιδιαίτερα των βακτηρίων µπορούν να επιβιώσουν σε θερµοκρασία πολύ ανώτερη από τη µέγιστη θερµοκρασία ανάπτυξης του αντίστοιχου µικροοργανισµού. Όσο µεγαλύτερη είναι η θερµοκρασία ανάπτυξης ενός µικροοργανισµού τόσο µεγαλύτερη είναι και η θερµική αντίσταση αυτού. Εποµένως µεγαλύτερη αντίσταση στη θερµική θανάτωση εµφανίζουν οι θερµόφιλοι µικροοργανισµοί και τα σπόριά τους, ακολουθούµενοι από τους µεσόφιλους µικροοργανισµούς. Οι περισσότεροι ζυµοµύκητες και ευρωτοµύκητες που αναπτύσσονται στα τρόφιµα έχουν µικρή αντοχή στη θερµοκρασία. Αντίθετα ορισµένα βακτήρια παρουσιάζουν µεγάλη θερµική αντοχή. Επίσης έχει παρατηρηθεί ότι για τον ίδιο µικροοργανισµό η θερµική αντίσταση επηρεάζεται από τη θερµοκρασία στην οποία αναπτύχθηκε. Γενικά για τα θεµόφιλα και ορισµένα µεσόφιλα βακτήρια µεγαλύτερη αντίσταση εµφανίζουν τα σπόρια τα oποία έχουν παραχθεί σε ψηλότερες θερµοκρασίες. Για τα µη σπορογόνα βακτήρια έχει παρατηρηθεί ότι µεγαλύτερη θερµική αντίσταση εµφανίζουν τα κύτταρα που έχουν παραχθεί στη βέλτιστη θερµοκρασία ανάπτυξης. ph Η ικανότητα επιβίωσης των µικροοργανισµών αλλά και η θερµική αντίσταση αυτών εξαρτάται από το ph του υποστρώµατος στο οποίο βρίσκονται. Για το λόγο αυτό τα τρόφιµα ταξινοµούνται συνήθως σε: τρόφιµα χαµηλής οξύτητας: ph > 4.5 όξινα τρόφιµα: 4.5 > ph > 4.0 ή 3.7 τρόφιµα υψηλής οξύτητας: ph < 4.0 ή 3.7 Συνήθως χρησιµοποιείται η τιµή 4.0 του ph ως διαχωριστικό όριο για τα τρόφιµα υψηλής οξύτητας γιατί σε τιµές χαµηλότερες από αυτήν σπανίως επιβιώνουν θερµοάντοχα σπορογόνα βακτήρια. Παρ όλα αυτά έχει παρατηρηθεί η επιβίωση του Βacillus thermoacidurans µέχρι και τιµή ph 3.7. Στα τρόφιµα υψηλής οξύτητας µπορούν να επιβιώσουν κυρίως ευρωτοµύκητες και ζύµες που εµφανίζουν πολύ χαµηλή θερµοανθεκτικότητα και εποµένως µπορούν να αντιµετωπισθούν µε ήπια θερµική κατεργασία. Στα όξινα τρόφιµα επιβιώνουν και ορισµένα σπορογόνα βακτήρια, ενώ στα τρόφιµα χαµηλής οξύτητας επιβιώνουν σπορογόνα βακτήρια µεταξύ των οποίων πολλά είναι παθογόνα. Το όριο του ph 4.5 καθορίσθηκε µε βάση την ικανότητα επιβίωσης και παραγωγής τοξίνης του Clostridium botulinum, ο οποίος είναι ένας από τους πλέον επικίνδυνους αναερόβιους µικροοργανισµούς µε τοξίνη ικανή να επιφέρει το θάνατο σε συγκέντρωση 0.2 µg/άτοµο. Για το λόγο αυτό σε τρόφιµα αυτής της κατηγορίας γίνεται θερµική 178
187 επεξεργασία µε στόχο την καταστροφή αυτού του µικροοργανισµού. Εποµένως στα τρόφιµα χαµηλής και µέσης οξύτητας (ph > 4.0 ή 3.7) τα σπορογόνα βακτήρια είναι εκείνα στα οποία επικεντρώνεται το ενδιαφέρον της θερµικής κατεργασίας διότι εµφανίζουν τη µεγαλύτερη θερµική αντίσταση. Επίσης έχει βρεθεί ότι το ph ανάπτυξης επηρεάζει την ικανότητα σχηµατισµού σπορίων. Οξυγόνο Ένας άλλος σηµαντικός παράγοντας για την ανάπτυξη των µικροοργανισµών είναι το οξυγόνο. Οι ζυµοµύκητες και οι ευρωτοµύκητες είναι αερόβοι µικροοργανισµοί, δηλαδή χρειάζονται µοριακό οξυγόνο για την ανάπτυξή τους. Τα βακτήρια ταξινοµούνται όσον αφορά στις απαιτήσεις σε οξυγόνο σε υποχρεωτικά αερόβια, προαιρετικά αναερόβια και υποχρεωτικά αναερόβια. Τα υποχρεωτικά αερόβια βακτήρια χρειάζονται µοριακό οξυγόνο για την ανάπτυξή τους και τα σπόρια των περισσότερων από αυτά εµφανίζουν πολύ µικρότερη θερµική αντίσταση συγκρινόµενα µε τα σπόρια των άλλων δύο οµάδων. Στις σύγχρονες µεθόδους κονσερβοποίησης εφαρµόζεται απαέρωση των δοχείων και η συγκέντρωση του µοριακού οξυγόνου είναι πολύ χαµηλή για να επιτρέψει την ανάπτυξη αερόβιων βακτηρίων. Εποµένως από την άποψη της αποστείρωσης των τροφίµων τα αερόβια βακτήρια έχουν τη µικρότερη σηµασία. Τα προαιρετικά αναερόβια σπορογόνα βακτήρια έχουν ιδιαίτερη σηµασία στην αποστείρωση, καθώς µερικά από αυτά είναι θερµόφιλα και παράγουν σπόρια µε µεγαλύτερη θερµική αντίσταση από τα υποχρεωτικά αναερόβια. Στα τρόφιµα χαµηλής οξύτητας ο Βacillus stearothermiphilus και τα συγγενή είδη παράγουν τα πιο θερµοάντοχα σπόρια, µε χρόνους υποδεκαπλασιασµού µεγαλύτερους από 4 min στους 250 F. Η βέλτιστη θερµοκρασία ανάπτυξης αυτών των θερµόφιλων βακτηρίων κυµαίνεται µεταξύ 49 C και 55 C και η ελάχιστη συνήθως δεν υπερβαίνει τους 38 C. Στα όξινα τρόφιµα αναπτύσσονται ορισµένα είδη προαιρετικά αναερόβιων βακτηρίων, µε σηµαντικότερο από άποψη θερµοανθεκτικότητας το Bacillus coagulans, του οποίου πάντως ο χρόνος υποδεκαπλασιασµού στους 250 F είναι της τάξης του 0.1 min. Τα υποχρεωτικά αναερόβια βακτήρια που έχουν µεγάλη σηµασία στην αποστείρωση είναι τα θερµόφιλα ή µεσόφιλα καθώς ορισµένα παράγουν επίσης σπόρια µε µεγάλη θερµική αντίσταση. Από τα θερµόφιλα τα σηµαντικότερα είναι το Clostridium thermosaccharolyticum, το οποίο αναπτύσσσεται σε ph > 4.5 και θερµοκρασία > 32 C αλλά παράγει ιδιαίτερα θερµοάντοχα σπόρια και το Clostridium nigrificans, το οποίο αναπτύσσσεται επίσης σε ph > 4.5 αλλά εµφανίζει µικρότερη θερµοανθεκτικότητα. Από τα µεσόφιλα το σηµαντικότερο είναι το 179
188 Clostridium botulinum λόγω της πολύ επικίνδυνης τοξίνης που παράγει. Όπως έχει ήδη αναφερθεί το Clostridium botulinum δεν αναπτύσσεται σε ph < 4.5. Σε όξινα τρόφιµα (4.0 < ph < 4.5) αναπτύσσονται ορισµένα µεσόφιλα βακτήρια µε σηµαντικότερα το Clostridium pasteurianum και το Clostridium butyricum. Στον Πίνακα 7.2 παρουσιάζεται η θερµική αντίσταση των σηµαντικότερων µικροοργανισµών στις διάφορες κατηγορίες κονσερβοποιηµένων τροφίµων. Πίνακας 7.2. Θερµική αντίσταση των σηµαντικότερων µικροοργανισµών σε διάφορες κατηγορίες κονσερβοποιηµένων τροφίµων. Οµάδες Μικροοργανισµών D C (min) z ( C) Τρόφιµα χαµηλής οξύτητας (ph>4.5) Θερµόφιλα (σπόρια) Βακτήρια που παράγουν οξέα (B. stearothermophilus) Bακτήρια αεριογόνα (C. thermosaccharolyticum) Βακτήρια που παράγουν H 2 S (C. nigrificans) Μεσόφιλα (σπόρια) C. botulinum (τύπος Α και Β) οµάδα C. sporogenes (συµπεριλ. του P.A. 3679) Όξινα τρόφιµα (4.0<pH<4.5 Θερµόφιλα (σπόρια) B. coagulans) Μεσόφιλα (σπόρια) B. polymyxa και B. macerans Βουτυρικά αναερόβια (C. pastiurianum) Τρόφιµα υψηλής οξύτητας (ph<4.0) Μεσόφιλα µη σπορογόνα βακτήρια Lactobacillus, Leuconostoc Ζύµες και ευρωτοµύκητες α : D 100 C, β : D 65.6 C Πηγή: Stumbo, 1973, µε µετατροπή στις µονάδες α α β β Ενεργότητα νερού Τόσο τα σπόρια όσο και τα κύτταρα των µικροοργανισµών είναι πιο ανθεκτικά στη θέρµανση σε ξηρό από ότι σε υγρό περιβάλλον. Η διαφορά σχετίζεται µε το µηχανισµό καταστροφής στα δύο περιβάλλοντα: µετουσίωση των πρωτεϊνών µε θέρµανση σε υγρό περιβάλλον και οξείδωση σε ξηρό περιβάλλον. Η οξείδωση εξελίσσεται µε βραδύτερο ρυθµό και απαιτεί µεγαλύτερη προσφορά ενέργειας από τη θερµική µετουσίωση, εποµένως χρειάζεται µεγαλύτερος χρόνος κατεργασίας σε ξηρό περιβάλλον σε σύγκριση µε το υγρό στην ίδια θερµοκρασία (π.χ. 120 min στους 248 F για αδρανοποίηση σπορίων του C. botulinum µε χρήση ξηρού αέρα και 4-10 min στους 250 F σε υδατικό περιβάλλον). 180
189 Η ενεργότητα του νερού είναι παράγων µε µικρή σηµασία στη θερµική κατεργασία των περισσοτέρων τροφίµων καθώς αυτά περιέχουν σηµαντικές ποσότητες νερού. Αντίθετα σηµαντικός είναι ο παράγων αυτός στα αποξηραµένα τρόφιµα. Σύσταση του υποστρώµατος Πολλά από τα συστατικά του υποστρώµατος επιδρούν στη θερµική αντίσταση των µικροοργανισµών. Η επίδραση αυτή ποικίλει για τα διάφορα είδη και στελέχη και δεν είναι δυνατόν να διατυπωθούν γενικευµένα συµπεράσµατα. Αυξηµένη συγκέντρωση διαλυτών υδατανθράκων γενικά αυξάνει τη θερµική αντίσταση. Το ίδιο έχει παρατηρηθεί ότι ισχύει για αυξηµένη συγκέντρωση πρωτεϊνών και λιπαρών. Χαµηλή συγκέντρωση NaCl (έως 4 %) τείνει να αυξήσει τη θερµική αντίσταση πολλών µικροοργανισµών, ενώ ψηλότερες συγκεντρώσεις τείνουν να τη µειώσουν. Τα νιτρικά και νιτρώδη άλατα όπως και τα συντηρητικά και αντιβιοτικά µειώνουν επίσης την αντίσταση των µικροοργανισµών. Ακόµη επίδραση στη θερµική αντίσταση φαίνεται να έχουν και διάφορα ιόντα όπως του ασβεστίου του µαγνησίου και του σιδήρου. Η επίδραση αυτών των ιόντων µελετήθηκε όχι µόνο όσον αφορά στην παρουσία τους στο υπόστρωµα που βρίσκεται ο µικροοργανισµός κατά τη θερµική κατεργασία αλλά και στο υπόστρωµα που αναπτύσσεται. Άλλα συστατικά του υποστρώµατος ανάπτυξης που πιθανώς επιδρούν στη θερµική αντίσταση είναι οι πρωτεΐνες, οι πεπτόνες και τα λιπαρά. Επειδή η σύσταση του υποστρώµατος ανάπτυξης µπορεί να επηρεάσει σηµαντικά τη θερµική αντίσταση οι τιµές θερµικής αντίστασης που προσδιορίζονται για σπόρια που καλλιεργήθηκαν σε τεχνητά υποστρώµατα δεν πρέπει να θεωρούνται αντιπροσωπευτικές για τα σπόρια που υπάρχουν στα τρόφιµα. Για τους υπολογισµούς στις θερµικές κατεργασίες πρέπει η θερµική αντίσταση να προσδιορίζεται σε σπόρια που καλλιεργούνται σε υπόστρωµα που δίνει τη µεγαλύτερη θερµική αντίσταση. Θερµική αδρανοποίηση των ενζύµων Η θέρµανση σε σχετικά υψηλές θερµοκρασίες (>45 C) προκαλεί αδρανοποίηση των ενζύµων, λόγω µετουσίωσης των πρωτεϊνών τους. Η αδρανοποίηση αυτή είναι επιθυµητή ώστε να µην εµφανισθεί ενζυµική αλλοίωση σε ένα προϊόν που είναι µικροβιακά σταθερό. Η θερµική αντίσταση των ενζύµων εξαρτάται από πολλούς παράγοντες. Στην πραγµατικότητα οι περισσότεροι παράγοντες που επηρεάζουν τη θερµική αντίσταση των µικροοργανισµών επηρεάζουν και τη θερµική αντίσταση των ενζύµων. 181
190 Ο ρυθµός αδρανοποίησης των ενζύµων µπορεί να εκφρασθεί µέσω των µεγεθών D και z, όπως και στους µικροοργανισµούς. Η τιµή του z που εκφράζει την εξάρτηση του ρυθµού από τη θερµοκρασία είναι για πολλά ένζυµα πολύ µεγαλύτερη από την αντίστοιχη των µικροοργανισµών (ή η ενέργεια ενεργοποίησης πολύ µικρότερη). Αυτό σηµαίνει ότι η αύξηση της θερµοκρασίας επιφέρει πολύ µικρότερη αύξηση του ρυθµού αδρανοποίησης των ενζύµων από εκείνη των µικροοργανισµών. Για την καταστροφή των µικροοργανισµών µπορούν να επιλεγούν διάφορα ζεύγη τιµών θερµοκρασίας χρόνου τα οποία θα επιφέρουν ισοδύναµο αποτέλεσµα. Είναι προφανές ότι όσο µεγαλύτερη είναι η θερµοκρασία τόσο µικρότερος είναι ο απαιτούµενος χρόνος. Όταν χρησιµοποιούνται χαµηλές θερµοκρασίες ο απαιτούµενος χρόνος για την καταστροφή των µικροοργανισµών είναι υπερεπαρκής και για την πλήρη αδρανοποίηση των ενζύµων. Εάν όµως χρησιµοποιηθούν πολύ υψηλές θερµοκρασίες µπορεί η αδρανοποίηση των ενζύµων να απαιτεί µεγαλύτερο χρόνο από εκείνη των µικροοργανισµών (επειδή ο ρυθµός της έχει αυξηθεί πολύ λιγότερο) και εποµένως να αποτελεί τον παράγοντα µε βάση τον οποίο θα σχεδιασθεί η διεργασία. Η καταλάση και η περοξειδάση είναι από τα πιο θερµοάντοχα ένζυµα που προκαλούν αλλοιώσεις στα τρόφιµα. Ενδεικτικά αναφέρεται τιµή z για την περοξειδάση σε λαχανικά 30.5 C, όταν για τους περισσότερους µικροοργανισµούς κυµαίνεται µεταξύ 4.4 C και 12.2 C. Μεταβολές των θρεπτικών συστατικών και των ποιοτικών χαρακτηριστικών κατά τη θέρµανση Με την αύξηση της θερµοκρασίας επιταχύνονται ορισµένες αντιδράσεις καταστροφής ή υποβάθµισης των θρεπτικών συστατικών, όπως οξειδώσεις ή αντιδράσεις δέσµευσης των βιταµινών και των αµινοξέων, οξειδώσεις λιπαρών, κ.λ.π. Επίσης επιταχύνονται δράσεις υποβάθµισης των ποιοτικών χαρακτηριστικών, όπως µεταβολές του χρώµατος, µεταβολές των αρωµατικών συστατικών των τροφίµων, µεταβολές λειτουργικών χαρακτηριστικών µέσω της µετουσίωσης των πρωτεϊνών ή των φυσικοχηµικών δράσεων που λαµβάνουν χώρα στο άµυλο ή στις διαιτητικές ίνες. Μία τρίτη κατηγορία δράσεων περιλαµβάνει επιθυµητές δράσεις, όπως η καταστροφή ορισµένων φυσικών ή µικροβιακών τοξινών, η καταστροφή αναστολέων ενζύµων, η αύξηση της τρυφερότητας και της ευπεπτότητας του τροφίµου, κλπ. Πολλοί παράγοντες επηρεάζουν όλες αυτές τις δράσεις και εάν είναι επιθυµητός ο έλεγχος κάποιας δράσης (π.χ. της απώλειας µιας βιταµίνης) κατά τη θερµική κατεργασία ενός τροφίµου πρέπει να µελετηθεί η κινητική που ακολουθεί στο συγκεκριµένο τρόφιµο και η εξάρτηση από τη θερµοκρασία. 182
191 Για τη βιταµίνη C που αποτελεί ένα από τα πιο ευαίσθητα θρεπτικά συστατικά έχουν γίνει αρκετές µελέτες: Ορισµένοι ερευνητές βρήκαν ότι η απώλειά της ακολουθεί κινητική πρώτης τάξης, ενώ άλλοι χρησιµοποιώντας άλλα τρόφιµα δεν κατέληξαν στο ίδιο αποτέλεσµα. Οι διαφορές αποδίδονται σε διαφορετικούς µηχανισµούς που ακολουθεί η δράση σε διαφορετικά τρόφιµα (επίδραση περιεχόµενης υγρασίας, οξυγόνου, αντιοξειδωτικών ουσιών κτλ.). Η θειαµίνη έχει επίσης µελετηθεί σε πολλά συστήµατα τροφίµων και υπάρχουν αρκετά δεδοµένα για το ρυθµό της καταστροφής της και την εξάρτηση από τη θερµοκρασία για κινητική πρώτης τάξης. Πίνακας 7.3. Κινητικές παράµετροι δράσεων υποβάθµισης κατά τη θερµική κατεργασία των τροφίµων. Συστατικό Μέσο ph α θερµοκρασίας Εύρος ( C) E a (kcal/mole) z ( C) D C (min) θειαµίνη αρακάς ολόκληρος φυσ θειαµίνη πολτός χοιρινού θειαµίνη πολτός σπανακιού θειαµίνη πολτός αρακά φυσ C υγρό παρασκεύασµα β Β 12 υγρό παρασκεύασµα β Α υγρό παρασκεύασµα β φολικό οξύ υγρό παρασκεύασµα β χλωροφύλλη πολτός σπανακιού χλωροφύλλη πολτός αρακά ανθοκυανίνη χυµός φράουλας φυσ ανθοκυανίνη χυµός γκρέιπφρουτ φυσ καροτενοειδή πάπρικα φυσ καστάνωση γάλα υφή αρακάς φυσ ποιότητα αρακάς φυσ (δοκιµαστές) αναστολείς γάλα σόγιας _ τρυψίνης εντεροτοξίνη σταφυλόκοκ α φυσ. είχνει το φυσικό ph του τροφίµου β οι τιµές αναφέρονται σε µέρες Πηγή: Karel et al., 1975, µε µετατροπή στις µονάδες. Στον Πίνακα 7.3 δίνονται οι κινητικές παράµετροι της υποβάθµισης ορισµένων συστατικών ή ποιοτικών χαρακτηριστικών σε διάφορα τρόφιµα. Όπως φαίνεται από 183
192 τις τιµές του z ή της ενέργειας ενεργοποίησης, η επίδραση της θερµοκρασίας στις δράσεις υποβάθµισης είναι πολύ µικρότερη σε σύγκριση µε την καταστροφή των µικροοργανισµών. Αυτό σηµαίνει ότι η επιλογή υψηλής θερµοκρασίας µικρού χρόνου κατά τη θερµική διεργασία θα δώσει προϊόν καλύτερης ποιότητας από εκείνο που θα προκύψει µετά από κατεργασία χαµηλής θερµοκρασίας και µεγάλου χρόνου. Υπολογισµοί καταστροφής µικροοργανισµών στις διεργασίες αποστείρωσης και αποστείρωσης Η παστερίωση ή αποστείρωση των τροφίµων γίνεται µε δύο τρόπους. Είτε το τρόφιµο τοποθετείται σε περιέκτη, σφραγίζεται και ακολούθως υφίσταται θερµική διεργασία για να επιτευχθεί η επιθυµητή µείωση µικροοργανισµών, είτε αρχικά υφίσταται θερµική διεργασία και στη συνέχεια τοποθετείται σε ένα στείρο περιέκτη και σφραγίζεται. Η πρώτη µέθοδος αποτελεί την κλασσική κονσερβοποίηση (θέρµανση σε περιέκτες), ενώ η δεύτερη καλείται ασηπτική διεργασία. Η κλασσική κονσερβοποίηση βρίσκει ακόµη ευρεία εφαρµογή, ιδιαίτερα σε τρόφιµα που περιέχουν στερεά κοµµάτια, αν και µειονεκτεί ως προς την εφαρµογή υψηλής θερµοκρασίας-µικρού χρόνου που εξασφαλίζει καλύτερη ποιότητα στα τρόφιµα. Και στους δύο παραπάνω τύπους διεργασιών η θερµοκρασία του τροφίµου µεταβάλλεται κατά τη διάρκεια της διεργασίας. Εποµένως για τον υπολογισµό της µείωσης της συγκέντρωσης ενός πληθυσµού µικροοργανισµών πρέπει να εισαχθεί η επίδραση της θερµοκρασίας στο χρόνο υποδεκαπλασιασµού (εξίσωση (7.11)) στην εξίσωση (7.5), για να υπολογισθεί η µείωση του πληθυσµού. Οπότε η ολοκλήρωση µεταξύ του χρόνου έναρξης και τέλους της θερµικής κατεργασίας δίνει: C t 1 ( T ( t) Tref ) / z d(log C) = dt D 10 (7.15) Co Με βάση τον ορισµό του χρόνου F ως χρόνου θερµικού θανάτου ισχύει: z F = D (log C log C) (7.16) ref ref o Συνδυάζοντας την εξίσωση (7.16) µε την εξίσωση (7.15) λαµβάνονται δύο εκφράσεις για το χρόνο θερµικού θανάτου F: F z ref = D ref ref 0 t ( T ( t) T ) / z ref (log C logc) = 10 dt (7.17) o 0 Η πρώτη έκφραση που δίνεται και από την εξίσωση (7.16) καθορίζει ουσιαστικά την τιµή στόχο του F, ή την απαιτούµενη τιµή, δηλ. το χρόνο σε σταθερή θερµοκρασία αναφοράς που απαιτείται για την επιθυµητή µείωση της συγκέντρωσης των µικροοργανισµών. Η δεύτερη έκφραση που δίνεται από την εξίσωση (7.18) 184
193 F z ref = t 0 ( T ( t) T ) / z ref 10 dt (7.18) καθορίζει την τιµή F της διεργασίας, δηλ. τον ισοδύναµο χρόνο σε σταθερή θερµοκρασία αναφοράς που θα επιφέρει την ίδια µείωση του µικροβιακού πληθυσµού µε την πραγµατική θερµική διεργασία. Η εξίσωση (7.18) είναι η βασική εξίσωση σχεδιασµού των θερµικών διεργασιών. Είναι φανερό ότι για τον υπολογισµό του αποτελέσµατος της θερµικής κατεργασίας σύµφωνα µε τις παραπάνω εξισώσεις απαιτείται, εκτός των κινητικών δεδοµένων καταστροφής των µικροοργανισµών, και η γνώση της µεταβολής της θερµοκρασίας του τροφίµου συναρτήσει του χρόνου της διεργασίας. Η επίδραση της µεταβολής της θερµοκρασίας µε το χρόνο στη µείωση της συγκέντρωσης των µικροοργανισµών δίνεται από την εξίσωση (7.15) ή την ισοδύναµή της (7.17) και είναι ανεξάρτητη από το εάν η θερµική κατεργασία γίνεται µε το τρόφιµο να βρίσκεται σε ένα περιέκτη ή σε ένα σύστηµα συνεχούς ροής. Η µεταβολή όµως της θερµοκρασίας µε το χρόνο εξαρτάται από το είδος της διεργασίας. Θέρµανση σε περιέκτες Στην κλασσική κονσερβοποίηση, όπου το τρόφιµο υφίσταται θερµική κατεργασία ενώ βρίσκεται σε σφραγισµένους περιέκτες, η θέρµανση γίνεται συνήθως σε αυτόκλειστα ασυνεχούς λειτουργίας µε διαβίβαση ατµού ή σπανιότερα θερµού νερού. Μετά το τέλος της θέρµανσης ανοίγεται η βάνα διαφυγής του ατµού (ή του νερού) και το συσκευασµένο τρόφιµο ψύχεται µε καταιονισµό ψυχρού νερού. Υπάρχουν επίσης και διατάξεις συνεχούς λειτουργίας στις οποίες επίσης το συσκευασµένο τρόφιµο ακολουθεί ένα κύκλο θέρµανσης και ένα κύκλο ψύξης. Η θανάτωση των µικροοργανισµών πρέπει να υπολογισθεί κατά τη θέρµανση αλλά και κατά τα αρχικά στάδια της ψύξης, οπότε η θερµοκρασία είναι υψηλή και ο ρυθµός θανάτωσης σηµαντικός. Όταν ο περιέκτης µε το τρόφιµο χαµηλής θερµοκρασίας έρθει σε επαφή µε το µέσο θέρµανσης µεταφέρεται θερµότητα από το µέσο θέρµανσης στην επιφάνεια του περιέκτη, δια µέσου του τοιχώµατος του περιέκτη και στο εσωτερικό αυτού δηλ. στο τρόφιµο. Η µεταφορά θερµότητας γίνεται σε µη µόνιµες συνθήκες δεδοµένου ότι η θερµοκρασία µεταβάλλεται µε το χρόνο σε όλα τα σηµεία στο εσωτερικό του περιέκτη. Το ίδιο συµβαίνει και κατά την ψύξη. Η µεταφορά θερµότητας στην επιφάνεια του περιέκτη γίνεται µε συναγωγή και ο επιφανειακός συντελεστής στην περίπτωση που χρησιµοποιείται ατµός είναι σηµαντικά µεγαλύτερος από το συντελεστή µεταφοράς θερµότητας στο εσωτερικό του τροφίµου. Η αντίσταση στην αγωγή θερµότητας δια µέσου του τοιχώµατος του περιέκτη είναι αµελητέα όταν 185
194 πρόκειται για µεταλλικούς περιέκτες µε λεπτά τοιχώµατα, όπως αυτοί που κυρίως χρησιµοποιούνται σε τρόφιµα που υφίστανται θερµική κατεργασία. Η µεταφορά θερµότητας στο εσωτερικό του τροφίµου µπορεί να γίνει µε αγωγή ή και µε συναγωγή, ανάλογα µε τη φύση του τροφίµου. Στερεά ή υπερβολικά ιξώδη τρόφιµα θερµαίνονται µε αγωγή. Υγρά τρόφιµα, χαµηλού ιξώδους θερµαίνονται κυρίως µε συναγωγή. Η φυσική κυκλοφορία µπορεί να ενισχυθεί µέσω ανακίνησης ή περιστροφής της κονσέρβας αυξάνοντας το ρυθµό µεταφοράς θερµότητας. Ακόµη υπάρχουν τρόφιµα στα οποία η µεταφορά θερµότητας µεταβάλλεται από συναγωγή σε αγωγή κατά τη θέρµανση, όπως τρόφιµα που περιέχουν µεγάλες ποσότητες αµύλου, το οποίο ζελατινοποιείται πάνω από ορισµένη θερµοκρασία. Η θέρµανση µε συναγωγή είναι πολύ ταχύτερη από τη θέρµανση µε αγωγή, ο ρυθµός διείσδυσης θερµότητας µεταβάλλεται από τον ένα µηχανισµό στον άλλο και εάν παρασταθεί γραφικά η θερµοκρασία συναρτήσει του χρόνου θέρµανσης η καµπύλη παρουσιάζει µία ασυνέχεια δείχνοντας δύο ή και περισσότερους ρυθµούς διείσδυσης της θερµότητας. Σε κάθε περίπτωση για τη θέρµανση και την ψύξη του τροφίµου ισχύουν όσα αναπτύχθηκαν στο κεφάλαιο 6. Συνήθως για τη συσχέτιση της µεταβολής της θερµοκρασίας του τροφίµου µε το χρόνο χρησιµοποιείται η εξίσωση (6.15). Οι παράµετροι f και j υπολογίζονται θεωρητικά ή προσδιορίζονται πειραµατικά µε µέτρηση της θερµοκρασίας συναρτήσει του χρόνου και κατασκευή των καµπυλών θερµικής διείσδυσης, όπως στο σχήµα (6.1). Συνήθως µετράται η θερµοκρασία και υπολογίζονται τα f και j σε ένα µόνο σηµείο, το κρίσιµο σηµείο ή το θερµικό κέντρο του προϊόντος, το οποίο είναι το σηµείο µε την ελάχιστη επίδραση της θερµικής κατεργασίας. Η χρήση του κρίσιµου σηµείου στηρίζεται στο ότι εάν επιτευχθεί εµπορική στειρότητα στο κρίσιµο σηµείο µε τη θερµική κατεργασία, τότε το υπόλοιπο προϊόν (το οποίο µε βάση τον ορισµό του κρίσιµου σηµείου υφίσταται εντονότερη κατεργασία) θα είναι επίσης εµπορικά στείρο. Προφανώς η γνώση της θέσης του κρίσιµου σηµείου ή της κρίσιµης περιοχής είναι απαραίτητη και έχει αποτελέσει αντικείµενο έρευνας. Συνήθως για µεταλλικούς περιέκτες ως κρίσιµο σηµείο θεωρείται το γεωµετρικό κέντρο του προϊόντος όταν η µεταφορά θερµότητας γίνεται µε αγωγή, ενώ όταν γίνεται µε συναγωγή θεωρείται ότι βρίσκεται στο χαµηλότερο 25 % του ύψους του περιέκτη. Η ακριβής θέση του κρίσιµου σηµείου εξαρτάται από πολλούς παράγοντες, όπως από το είδος του προϊόντος, το είδος και τις διαστάσεις του περιέκτη, τα χαρακτηριστικά του κύκλου θέρµανσης και ψύξης, το βαθµό ανακίνησης, την κατανοµή της µικροβιακής συγκέντρωσης και την έκταση της διεργασίας. Η ακριβής θέση πρέπει να προσδιορισθεί προκειµένου να σχεδιασθεί η θερµική κατεργασία. 186
195 Η µέτρηση της θερµοκρασίας γίνεται µε χρήση θερµοστοιχείων που τοποθετούνται στο εσωτερικό της κονσέρβας. Σε ορισµένες περιπτώσεις όµως, όπως π.χ. στην περίπτωση αξονικά περιστρεφόµενης κονσέρβας που περιέχει µίγµα υγρού τροφίµου µε στερεά κοµµάτια, υπάρχουν πρακτικές δυσκολίες στη µέτρηση της θερµοκρασίας των στερεών και έχουν προταθεί πιο σύνθετες µέθοδοι όπως η χρήση υγρών κρυστάλλων ως αισθητήρων θερµοκρασίας. Οµοίως τα µαθηµατικά µοντέλα µπορεί να είναι απλά όπως στην περίπτωση οµογενούς, πλήρως αναµίξιµου υγρού τροφίµου ή αρκετά σύνθετα όπως σε τρόφιµα που περιέχουν στερεά κοµµάτια. Έτσι συνήθως οι πειραµατικές µετρήσεις και τα µαθηµατικά µοντέλα χρησιµοποιούνται συµπληρωµατικά για τον προσδιορισµό της συνάρτησης της θερµοκρασίας από το χρόνο θερµικής κατεργασίας. Συνήθως τα µαθηµατικά µοντέλα προκύπτουν από την επεξεργασία πειραµατικών δεδοµένων σε ορισµένες συνθήκες και γενικεύουν τα συµπεράσµατα σε ορισµένο εύρος συνθηκών ώστε να αποφεύγονται µη αναγκαία πειράµατα. Για την επίλυση της εξίσωσης (7.18) έχουν προταθεί διάφορες µαθηµατικές προσεγγίσεις. Στη συνέχεια θα αναπτυχθεί η γενική µέθοδος (general method) που ήταν η πρώτη µαθηµατική προσέγγιση που χρησιµοποιήθηκε για υπολογισµούς θερµικών διεργασιών και ορισµένες από τις υπολογιστικές µεθόδους (formula method) που είναι οι ευρύτερα χρησιµοποιούµενες. Γενική µέθοδος Το κύριο χαρακτηριστικό της γενικής µεθόδου είναι ότι δεν απαιτείται ακριβής γνώση της συνάρτησης θερµοκρασίας χρόνου η οποία υπεισέρχεται στην εξίσωση (7.18). Αντ αυτής µπορούν να χρησιµοποιηθούν τιµές θερµοκρασίας που αντιστοιχούν σε διακριτά χρονικά σηµεία της θερµικής κατεργασίας. Ο υπολογισµός του ολοκληρώµατος της εξίσωσης (7.18) γίνεται γραφικά ή αριθµητικά. Ο Bigelow ήταν ο πρώτος που εφάρµοσε τη γραφική µέθοδο ολοκλήρωσης. Για θερµοκρασία αναφοράς τους 250 F εξίσωση (7.18) µπορεί να γραφεί και ως: F t z ( T( t) 250)/ z 250 = 10 0 Η συνάρτηση 10 dt ( T( t) 250)/ z (7.19) καλείται και συνάρτηση θερµικής καταστροφής (Lethality function) ή ρυθµός θερµικής καταστροφής (Lethal rate) και συµβολίζεται µε L. Όσον αφορά στη φυσική της σηµασία είναι ο ισοδύναµος χρόνος θερµικής κατεργασίας στους 250 F µε 1 min θερµικής κατεργασίας σε θερµοκρασία T ( F). Με βάση τα δεδοµένα θερµοκρασίας-χρόνου προσδιορίζεται η συνάρτηση θερµικής καταστροφής (L) και κατασκευάζεται διάγραµµα L συναρτήσει του χρόνου t (σχήµα 7.3). Το εµβαδόν της επιφάνειας µεταξύ της καµπύλης που προκύπτει και του άξονα των τετµηµένων (t) αντιστοιχεί στην τιµή του χρόνου θερµικής καταστροφής (F z 250 ). 187
196 Για την απλοποίηση της µεθόδου προτάθηκε η χρήση χαρτιού µε κατάλληλες συντεταγµένες καθώς και η αριθµητική ολοκλήρωση µε διάφορες µεθόδους. Η γενική µέθοδος µπορεί να εφαρµοσθεί για οποιοδήποτε σχήµα της καµπύλης θέρµανσης και εποµένως είναι η πιο ακριβής και κατάλληλη για την επεξεργασία πολύπλοκων δεδοµένων θερµοκρασίας-χρόνου. Η ακρίβειά της εξαρτάται µόνο από την µέθοδο ολοκλήρωσης στην περίπτωση που χρησιµοποιούνται πειραµατικά δεδοµένα θερµοκρασίας-χρόνου. Έτσι µπορεί και πρέπει να χρησιµοποιείται για τον έλεγχο της ακρίβειας οποιασδήποτε άλλης µεθόδου στον υπολογισµό του ισοδύναµου χρόνου θερµικής καταστροφής ( F z 250 ). Σχήµα 7.3. Γραφική µέθοδος προσδιορισµού του χρόνου αποστείρωσης (Bigelow) Η εφαρµογή όµως της µεθόδου για τον προσδιορισµό του απαιτούµενου χρόνου θερµικής κατεργασίας για τη επίτευξη ορισµένης τιµής F z 250 δηµιουργεί ορισµένα προβλήµατα. Έχοντας πειραµατικά δεδοµένα µόνο για ένα χρόνο θερµικής κατεργασίας πρέπει να γίνουν ορισµένες παραδοχές για το τι συµβαίνει σε διαφορετικούς χρόνους. Ο Bigelow θεώρησε ότι το σχήµα της καµπύλης της συνάρτησης L ως προς το χρόνο, µετά το τέλος της θέρµανσης, είναι γεωµετρικά το ίδιο ανεξάρτητα από το χρόνο που σταµατά η θέρµανση. Αυτή η παραδοχή όµως δεν είναι πάντα σωστή καθώς το σχήµα της καµπύλης της συνάρτησης L κατά την ψύξη εξαρτάται από τη διαφορά θερµοκρασίας µεταξύ του προϊόντος και του µέσου θέρµανσης. Εποµένως µόνο στην περίπτωση που το προϊόν έχει φθάσει σε θερµοκρασιακή ισορροπία µε το µέσο θέρµανσης µπορεί να θεωρηθεί ότι η καµπύλη 188
197 της συνάρτησης L θα έχει το ίδιο σχήµα, ανεξάρτητα από το χρόνο θερµικής κατεργασίας. Για πλήρως αναµίξιµα, υγρά προϊόντα που θερµαίνονται µε συναγωγή η παραδοχή της γεωµετρικής οµοιότητας παρέχει ικανοποιητική ακρίβεια στον υπολογισµό του χρόνου της κατεργασίας. Για προϊόντα όµως που θερµαίνονται µε αγωγή αυτή η παραδοχή δεν πρέπει να χρησιµοποιείται και είναι απαραίτητη η ύπαρξη πειραµατικών δεδοµένων για διάφορους χρόνους θερµικής κατεργασίας. Οι εκτενείς υπολογισµοί που απαιτούνται στη γενική µέθοδο για κάθε σειρά δεδοµένων θερµοκρασίας-χρόνου οδήγησαν σε περιορισµένη εφαρµογή αυτής και σε ανάπτυξη των υπολογιστικών µεθόδων (formula methods). Υπολογιστικές µέθοδοι Η αρχική υπολογιστική µέθοδος του Ball αναπτύχθηκε για να απλοποιήσει τους υπολογισµούς στις θερµικές κατεργασίες κονσερβοποιηµένων τροφίµων. Σε αυτή τη βάση αναπτύχθηκαν και άλλες υπολογιστικές µέθοδοι, οι οποίες στηρίζονται σε ορισµένες παραδοχές, όπως και η µέθοδος του Ball. Όλες αυτές οι µέθοδοι στηρίζονται σε µία σχέση (formula) που δίνει τη θερµοκρασία του τροφίµου ως συνάρτηση του χρόνου. Αυτή η σχέση χρησιµοποιείται στην εξίσωση (7.18) για την ολοκλήρωση. Από την ολοκλήρωση προκύπτουν τιµές της ισοδύναµης θερµικής καταστροφής σε µια θερµοκρασία αναφοράς για διάφορες συνθήκες θέρµανσης και ψύξης, οι οποίες δίνονται σε πίνακες ή διαγράµµατα συναρτήσει των παραµέτρων θέρµανσης και ψύξης. Οι κύριες πηγές λαθών των υπολογιστικών µεθόδων προκύπτουν από λάθος παραδοχές στη σχέση θερµοκρασίας-χρόνου. Mέθοδος Ball Ο Ball αναπτύσσοντας την πρώτη υπολογιστική µέθοδο στηρίχθηκε στην παρατήρηση ότι σε ηµιλογαριθµικό διάγραµµα η διαφορά θερµοκρασίας µεταξύ του µέσου θέρµανσης και του θερµικού κέντρου της κονσέρβας ως συνάρτηση του χρόνου, µετά από µία αρχική περίοδο υστέρησης, ήταν ευθεία γραµµή, όπως αναπτύχθηκε αναλυτικά στο κεφάλαιο 6 και φαίνεται στο σχήµα 6.1. Με βάση αυτό χρησιµοποίησε µία γενική εξίσωση για όλο τον κύκλο θέρµανσης η οποία είναι αντίστοιχη της εξίσωσης (6.15): t / f T ( t) = T j ( T T )10 h (7.20) RT h RT IT όπου T(t) θερµοκρασία του θερµικού κέντρου του τροφίµου σε χρόνο t ( C ή F) T RT θερµοκρασία του µέσου θέρµανσης ή του αυτοκλείστου ( C ή F) T IT αρχική θερµοκρασία του θερµικού κέντρου του τροφίµου ( C ή F) j h παράγοντας υστέρησης όπως φαίνεται στο σχήµα 6.1 f h χρόνος που απαιτείται για να υποδεκαπλασιασθεί η διαφορά θερµοκρασίας µεταξύ του τροφίµου και του µέσου θέρµανσης (s) 189
198 Η αρχική υστέρηση δεν λήφθηκε υπ όψη από τον Ball στον υπολογισµό του ισοδύναµου χρόνου θερµικής καταστροφής. Στην πραγµατικότητα, σε συνήθεις συνθήκες κατεργασίας, η θερµοκρασία του τροφίµου σε αυτό το αρχικό διάστηµα θέρµανσης είναι τόσο χαµηλή ώστε η θερµική καταστροφή είναι ασήµαντη. Αντίθετα όταν αρχίζει ο επόµενος κύκλος, της ψύξης, η θερµοκρασία του τροφίµου είναι υψηλή και η θερµική καταστροφή που προκαλεί σηµαντική. Έτσι οι σχέσεις που θα αποδίδουν τη θερµοκρασία ως συνάρτηση του χρόνου πρέπει να είναι ακριβείς και από αυτές ουσιαστικά εξαρτάται η ακρίβεια της κάθε υπολογιστικής µεθόδου. Κατά την ψύξη η θερµοκρασία του τροφίµου ακολουθεί µια πορεία ανάλογη της θέρµανσης, όπως φαίνεται και από το σχήµα 6.1, και µπορεί να αποδοθεί από µία εξίσωση παρόµοια µε τη (7.20). Η θερµοκρασία όµως κατά την αρχική περίοδο υστέρησης πρέπει να προβλεφθεί µε ακρίβεια από µία κατάλληλη σχέση επειδή έχει υψηλές τιµές. Ο Ball µε βάση τα πειραµατικά δεδοµένα θεώρησε ότι η θερµοκρασία κατά την αρχική περίοδο της ψύξης µπορεί να αποδοθεί ικανοποιητικά από µία καµπύλη σχήµατος υπερβολής και ότι η αρχική αυτή περίοδος τελειώνει όταν η θερµοκρασία του τροφίµου γίνει: Tt ( c1) = Tg ( Tg TCW) (7.21) Έτσι χρησιµοποίησε δύο διαφορετικές εξισώσεις για να περιγράψει την καµπύλη ψύξης. Μία για την αρχική καµπύλη σχήµατος υπερβολής στην περίοδο υστέρησης, δηλ. για 0 t < t = f log( j / ) : c c1 c c tc Tt () = Tg +.( Tg TCW) log( jc / (7.22) f c και µία για την ευθεία γραµµή, δηλ για tc tc1 = fc log( jc / ) : t c / f T ( t) = T + j ( T T )10 c (7.23) CW c g CW όπου T g θερµοκρασία του τροφίµου στο τέλος της θέρµανσης του αυτοκλείστου (µερικές φορές θεωρείται ως η µέγιστη θερµοκρασία του τροφίµου) ( C ή F) T CW θερµοκρασία του νερού ψύξης ( C ή F) j c παράγοντας υστέρησης της καµπύλης ψύξης, όπως φαίνεται στο σχ. 6.1 f c t c χρόνος που απαιτείται για να υποδεκαπλασιασθεί η διαφορά θερµοκρασίας µεταξύ του τροφίµου και του νερού ψύξης (s) χρόνος παραµονής σε ψύξη (s) Ο χρόνος t c1 στον οποίο αρχίζει το ευθύγραµµο τµήµα της καµπύλης ψύξης υπολογίζεται µέσω της εξίσωσης (7.23) θέτοντας σύµφωνα µε την παραδοχή (7.21): t c Tt ( c1) = Tg ( Tg TCW) c / f = TCW + jc ( Tg TCW )10 1 (7.24) από την οποία προκύπτει: tc1 = fc log( jc / ) (7.25) 190
199 Στην αρχική µέθοδο ο Ball θεώρησε ότι ο παράγων υστέρησης j c έχει τη σταθερή τιµή 1.41, η οποία και χρησιµοποιήθηκε σε όλες τις εξισώσεις. Επίσης αρχικά θεώρησε ότι f = f, στη συνέχεια όµως παρουσίασε δεδοµένα για f f. c h Η υποκατάσταση των συναρτήσεων της θερµοκρασίας από τις εξισώσεις (7.20), (7.22) και (7.23) στην (7.18) οδηγεί σε µία εξίσωση µέσω της οποίας µπορεί να υπολογισθεί ο χρόνος θερµικού θανάτου (σε οποιαδήποτε θερµοκρασία αναφοράς) που επιτυγχάνεται στη διεργασία. Ο Ball προχώρησε σε γραφική εκτίµηση των ολοκληρωµάτων και παρουσίασε τα αποτελέσµατά του σε µορφή πινάκων και διαγραµµάτων. Για τους υπολογισµούς αυτούς έκανε ορισµένες επί πλέον απλοποιήσεις, µικρότερης όµως σηµασίας, όπως ότι δεν υπάρχει θερµική καταστροφή σε θερµοκρασία χαµηλότερη από 80 F. Οι παράµετροι που επηρεάζουν τις τιµές του F για διάφορους χρόνους κατεργασίας είναι οι z, T RT, T IT, j c, f h, f c και T CW. H θερµοκρασία αναφοράς (T ref ) δεν θεωρείται µία επί πλέον παράµετρος δεδοµένου ότι µέσω της εξίσωσης (7.18) µπορούν εύκολα να µετατραπούν οι τιµές του F από µία θερµοκρασία αναφοράς σε άλλη. Επίσης, εάν είναι γνωστός ο χρόνος θέρµανσης, η θερµοκρασία του τροφίµου στο τέλος της θέρµανσης (T g ) µπορεί να υπολογισθεί από την εξίσωση (7.20), στη συνέχεια η θερµοκρασία στο τέλος του αρχικού καµπύλου τµήµατος της καµπύλης ψύξης µπορεί να υπολογισθεί σύµφωνα µε την παραδοχή του Ball και στη συνέχεια να υπολογισθεί ο χρόνος ψύξης. Ο συνολικός χρόνος προκύπτει αθροίζοντας τους χρόνους θέρµανσης και ψύξης. Έτσι η θερµοκρασία T g δεν είναι ανεξάρτητη παράµετρος που απαιτείται για τους υπολογισµούς. Υπάρχουν διάφοροι τρόποι να παρουσιασθούν τα αποτελέσµατα της ολοκλήρωσης. Περισσότερο εύχρηστα όµως είναι δεδοµένα τιµών του F της πλήρους θερµικής κατεργασίας ως προς το χρόνο θέρµανσης, αντί του ολικού χρόνου της κατεργασίας, επειδή δίνουν άµεσες τιµές του χρόνου στον οποίο πρέπει να διακοπεί η θέρµανση (π.χ. η παροχή ατµού στο αυτόκλειστο). Σε αντίθετη περίπτωση θα πρέπει να υπάρχει µια απλή εξίσωση εργασίας που να συνοδεύει τους πίνακες, η οποία θα επιτρέπει τον υπολογισµό του χρόνου θέρµανσης από τον ολικό χρόνο της κατεργασίας. Ο Ball χρησιµοποίησε την ακόλουθη ονοµατολογία για την παρουσίαση των αποτελεσµάτων του: g = ( T T ) (7.26) RT g (διαφορά θερµοκρασίας µεταξύ του αυτοκλείστου και του θερµικού κέντρου του τροφίµου στο τέλος της θέρµανσης) m= T T (7.27) g CW (διαφορά θερµοκρασίας µεταξύ του θερµικού κέντρου στο τέλος της θέρµανσης και του νερού ψύξης) m + g = T RT T CW (7.28) c h 191
200 I = T RT T IT (7.29) ( Tref TRT ) / z ( Tref TRT ) / z U = F 10 = D (logc log C)10 (7.30) ref ref o To U καθορίζεται από το στόχο της διεργασίας: είναι ο χρόνος θερµικού θανάτου σε σταθερή θερµοκρασία ίση µε την T RT για να επιτευχθεί η επιθυµητή µείωση πληθυσµού µικροοργανισµών. Εποµένως συνδέεται µε το χρόνο στη θερµοκρασία αναφοράς F ref και µε τη συγκέντρωση των µικροοργανισµών µε τη σχέση (7.30) Ο Ball δηµοσίευσε τους πρώτους πίνακες όπου το g δίνεται ως συνάρτηση του f h /U, για ορισµένη τιµή z και (m+g). O χρόνος θέρµανσης (τον οποίο αποδίδει µε το σύµβολο Β) για την επίτευξη ορισµένου g µπορεί να υπολογισθεί µέσω της εξίσωσης (7.20) ως: t = B = f log[ j ( T T )] log g = f log[ j I] log g (7.31) h h [ ] [ ] h RT IT Ο παράγοντας j c θεωρήθηκε σταθερός και ίσος µε 1.41 στους υπολογισµούς του, όπως ήδη αναφέρθηκε. Τα διαγράµµατα που προκύπτουν µε βάση τους πίνακες του Ball δίνονται στα σχήµατα Π.8-Π.10 στο παράρτηµα. Υπάρχουν δύο επί πλέον σηµεία που πρέπει να αναφερθούν όσον αφορά στη µέθοδο του Ball. Το πρώτο αναφέρεται στην περίπτωση µεταβαλλόµενου ρυθµού θέρµανσης, όπου η καµπύλη θέρµανσης µπορεί να αποτελείται από δύο ή περισσότερες ευθείες (broken-line curve). Αυτή η περίπτωση αντιµετωπίσθηκε θεωρώντας την κάθε ευθεία µε µία νέα κλίση και µία νέα αποτέµνουσα και το συνολικό αποτέλεσµα της θέρµανσης ως συνιστάµενο των επιµέρους αποτελεσµάτων. Το δεύτερο σηµείο σχετίζεται µε την παραδοχή που εµπεριέχεται στις εξισώσεις του Ball ότι η θερµοκρασία του µέσου θέρµανσης και του νερού ψύξης είναι σταθερή. Στην περίπτωση που η κατεργασία γίνεται σε αυτόκλειστα ασυνεχούς λειτουργίας υπάρχει ένας χρόνος ανόδου της θερµοκρασίας µέχρι την τελική της τιµή. Για να συµπεριλάβει αυτό το χρόνο ανόδου ο Ball θεώρησε (στηριζόµενος σε πειραµατικές παρατηρήσεις) ότι η έκθεση στη σταθερή θερµοκρασία λειτουργίας για ένα χρόνο ίσο µε το 42 % του χρόνου ανόδου της θερµοκρασίας, δίνει ισοδύναµα αποτελέσµατα µε την έκθεση στην ανερχόµενη θερµοκρασία, η οποία συµβαίνει στην πράξη. Αυτό το εφάρµοσε στη µέθοδό του µετατοπίζοντας τον άξονα του µηδενικού χρόνου θέρµανσης στο 0.58 του χρόνου ανόδου της θερµοκρασίας. Παρ όλα αυτά σηµείωσε ότι ο παράγοντας 42 % δεν είναι πάντα εφαρµόσιµος. Η επίδραση του χρόνου ανόδου έχει στη συνέχεια µελετηθεί και από άλλους ερευνητές. Για το χρόνο που απαιτείται για τη σταθεροποίηση της θερµοκρασίας ψύξης ο Ball δεν παρουσίασε αντίστοιχες διορθώσεις. Στη συνέχεια οι Ball και Olson παρουσίασαν µία νέα µέθοδο στην οποία λαµβάνεται υπ όψιν η µεταβολή του παράγοντα j c. Η µεταβολή αυτού του παράγοντα επηρεάζει σηµαντικά το αποτέλεσµα θερµικής καταστροφής κατά την ψύξη εποµένως και το συνολικό F ref της διεργασίας. h h 192
201 Μέθοδος Stumbo Μια τροποποιηµένη υπολογιστική µέθοδος παρουσιάστηκε από τον Stumbo, ο οποίος δηµοσίευσε πίνακες του g ως συνάρτηση του f h /U για διάφορες τιµές του j c και του z. Οι πίνακες του Stumbo συνυπολογίζουν τη θερµική καταστροφή κατά τη θέρµανση και την ψύξη και η διαδικασία που ακολουθείται για τον υπολογισµό της θερµικής καταστροφής ή του χρόνου µιας διεργασίας είναι ταυτόσηµη µε τη µέθοδο του Ball. Βασική παραδοχή των υπολογισµών είναι ότι f c = f h. Εάν αυτή η παραδοχή δεν ισχύει η προσέγγιση της µεθόδου δεν είναι ικανοποιητική. Εάν δεν υπάρχουν δεδοµένα του j c µπορεί να χρησιµοποιηθεί το j h. Οι τιµές του j c είναι συνήθως µεγαλύτερες από τις τιµές του j h, οπότε το σφάλµα του υπολογισµού θα είναι προς κατεργασία µεγαλύτερου χρόνου, άρα ασφαλέστερη. Με βάση τους πίνακες του Stumbo o Toledo δηµοσίευσε διαγράµµατα συσχέτισης του f h /U µε το log g. Επίσης δηµοσιεύσε τροποποιηµένους πίνακες εργασίας, όπως ο Πίνακας 7.4, για διάφορα j = j c - 1 και z. Για ενδιάµεσες τιµές των παραµέτρων είναι δυνατόν να χρησιµοποιηθεί γραµµική παρεµβολή µεταξύ των τιµών των πινάκων. Μία βασική διαφορά είναι ότι µέθοδος του Stumbo για προϊόντα που θερµαίνονται µε αγωγή χρησιµοποιεί τις εξισώσεις αγωγής θερµότητας ως εµπειρικό εργαλείο για τον υπολογισµό µιας ολοκληρωµένης τιµής F του προϊόντος µε βάση την τιµή F του θερµικού κέντρου. Σφάλµατα υπολογισµού µπορεί να προκύψουν όταν η µέθοδος χρησιµοποιείται για τρόφιµα που δεν προσεγγίζουν τις παραδοχές του εµπειρικού µοντέλου. Οι πίνακες και τα διαγράµµατα που προαναφέρθηκαν είναι εύκολο να χρησιµοποιηθούν µε δεδοµένο το επιθυµητό F ref µιας διεργασίας για προσδιορισµό του απαιτούµενου χρόνου παραµονής σε σταθερή θερµοκρασία στον αποστειρωτήρα, εάν είναι γνωστά τα δεδοµένα των καµπυλών θερµικής διείσδυσης. Μέσω της εξίσωσης (7.30) προσδιορίζεται το U και υπολογίζεται το f h /U. Από τους πίνακες ή τα διαγράµµατα προσδιορίζεται το g = T RT - T g και στη συνέχεια ο απαιτούµενος χρόνος παραµονής t h σε σταθερή θερµοκρασία T RT στον αποστρειρωτήρα µέσω της εξίσωσης (7.31). Ο χρόνος t συµπεριλαµβάνει το 42 % του χρόνου ανόδου της θερµοκρασίας (t αν ) που παρουσιάζεται στα αυτόκλειστα ασυνεχούς λειτουργίας. Εποµένως ο χρόνος παραµονής στον αποστειρωτήρα σε σταθερή θερµοκρασία θα είναι: tconst = t 04. tαν. Πολλές φορές η διόρθωση αυτή δεν γίνεται για λόγους ασφαλείας. Αντίθετα το 42 % του χρόνου ανόδου ως ισοδύναµου χρόνου ισοθερµοκρασιακής κατεργασίας, όπως ήταν στην αρχική παραδοχή του Ball, χρησιµοποιείται για τον προσδιορισµό 193
202 του j h, που γίνεται προσδιορίζοντας την αποτέµνουσα της καµπύλης θέρµανσης (σχήµα 6.1) σε χρόνο ίσο µε το 58% του χρόνου ανόδου της θερµοκρασίας. Για τον προσδιορισµό του επιτυγχανόµενου F ref (και εποµένως της µείωσης πληθυσµού που επιτυγχάνεται) µέσω µιας διεργασίας ορισµένου χρόνου παραµονής σε T RT µε γνωστές τις παραµέτρους των καµπυλών θερµικής διείσδυσης ακολουθείται η αντίστροφη πορεία. Πίνακας 7.4. Συσχέτιση τιµών g µε f h /U σύµφωνα µε τη µέθοδο Stumbo z =14 F z =18 F z =22 F f h /U g j=1 ( F) g / j g j=1 ( F) g / j g j=1 ( F) g / j * * * * * * g= TRT Tg, U ο χρόνος θερµικού θανάτου σε θερµοκρασία T RT Υπολογισµός τιµών για j 1: gj = gj=1 + ( j 1)( g / j) Πηγή: Toledo,
203 Ασηπτική διεργασία Στην ασηπτική διεργασία το τρόφιµο -θερµαίνεται σε εναλλάκτη συνεχούς λειτουργίας µέχρι την επιθυµητή θερµοκρασία παστερίωσης ή αποστείρωσης, -διοχετεύεται σε ένα σωλήνα όπου η θερµοκρασία του διατηρείται σταθερή και ο χρόνος παραµονής ρυθµίζεται ώστε να επιτευχθεί η απαιτούµενη µείωση της συγκέντρωσης των µικροοργανισµών, και ακολούθως -ψύχεται σε θερµοκρασία περιβάλλοντος ή χαµηλότερη και συσκευάζεται ασηπτικά. Συνήθως η ψύξη γίνεται µε διαβίβαση του θερµικά κατεργασµένου τροφίµου στον εναλλάκτη εισόδου, αποδίδοντας τη θερµότητά του στο εισερχόµενο προς κατεργασία τρόφιµο. Οι εναλλάκτες που χρησιµοποιούνται είναι είτε έµµεσης θέρµανσης όπως αυλωτοί, µε πλάκες, ή αποξεόµενης επιφάνειας, είτε άµεσης θέρµανσης µε διαβίβαση ατµού στη µάζα του τροφίµου ή αντίστροφα. Το πρόβληµα που προκύπτει και έχει ιδιαίτερη σηµασία για τη θερµική κατεργασία των τροφίµων είναι η κατανοµή των χρόνων παραµονής του τροφίµου στο σύστηµα και η µεταβολή της θερµοκρασίας µε το χρόνο παραµονής. Η κατανοµή ταχυτήτων και χρόνων παραµονής στους εναλλάκτες και στις σωληνώσεις εξαρτώνται από το είδος της ροής και τη ρεολογική συµπεριφορά του ρευστού. Για λόγους ασφαλείας ως χρόνος θερµικής κατεργασίας θεωρείται ο ελάχιστος χρόνος παραµονής του τροφίµου στο σύστηµα, που εξαρτάται από το ισοδύναµο µήκος που διατρέχει και τη µέγιστη ταχύτητα του ρευστού. Π.χ. ο ελάχιστος χρόνος παραµονής στις σωληνώσεις σταθερής θερµοκρασίας είναι: L t min = (7.32) v max όπου L το µήκος του σωλήνα (m). Για νευτονικά ρευστά σε στρωτή ροή (Re<2100) v max = 2 v, όπου v : η µέση ταχύτητα. Σε πλήρως αναπτυγµένη τυρβώδη ροή (Re>8000) v / v max 082,. εποµένως v max 122. v και η οριακή τιµή µπορεί να ληφθεί ως τιµή ασφαλείας. 1+ 3n Για µη νευτονικά ρευστά σε στρωτή ροή v max = v( ), όπου n ο δείκτης 1+ n ρεολογικής συµπεριφοράς. Για τα ψευδοπλαστικά ρευστά (n<1), στα οποία ανήκουν τα περισσότερα τρόφιµα, προκύπτει ότι v max < 2 v, αλλά για τα πηγνυόµενα ρευστά (n>1) v max > 2 v. Σε τυρβώδη ροή όλα τα µη νευτονικά ρευστά εµφανίζουν v max < 2 v. Το είδος της ροής στα µη νευτονικά ρευστά καθορίζεται από την τιµή του γενικευµένου αριθµού Reynolds: Re = d n v 2 n ρ ( n 3 n n / 1+ 3n ) 2, όπου d η διάµετρος του αγωγού και K ο K συντελεστής συνοχής της ροής του ρευστού. 195
204 Ο λόγος v σχήµα 7.4. / v max συναρτήσει του γενικευµένου αριθµού Reynolds δίνεται στο Εποµένως σε στρωτή ροή η οριακή συνθήκη v max = 2 v (7.33) µπορεί να θεωρηθεί ως συνθήκη ασφαλείας για τον υπολογισµό του ελάχιστου χρόνου παραµονής σε σωληνώσεις για τα περισσότερα τρόφιµα, εκτός των πηγνυόµενων ρευστών. v Σε τυρβώδη ροή λαµβάνεται η οριακή τιµή = 125 v (7.34) max. ή και µικρότερη για ψευδοπλαστικά ρευστά ώστε η διεργασία να µην οδηγεί σε υπερκατεργασµένα τρόφιµα. Σχήµα 7.4. Συσχέτιση v 1976). / vmax µε το γενικευµένο αριθµό Reynolds (Palmer and Jones, Όσα αναφέρθηκαν για την κατανοµή των ταχυτήτων αφορούν ροή σε ισοθερµοκρασιακές συνθήκες. Στις συνθήκες θέρµανσης ή ψύξης η µεταβολή της θερµοκρασίας επηρεάζει τις ρεολογικές ιδιότητες του τροφίµου και εποµένως την κατανοµή των ταχυτήτων και των χρόνων παραµονής. 196
205 Η µεταφορά θερµότητας εξαρτάται επίσης από το είδος της ροής, τις ρεολογικές ιδιότητες του τροφίµου και το σύστηµα εναλλαγής θερµότητας, όπως αναπτύχθηκε στο κεφάλαιο 6. Η µεταβολή της µέσης θερµοκρασίας του τροφίµου µε το χρόνο παραµονής στους εναλλάκτες µπορεί να αποδοθεί από τις σχέσεις που παρατέθηκαν εκεί. Η έλλειψη επαρκών σχέσεων για τη µεταφορά θερµότητας ιδιαίτερα σε µη πλήρως αναπτυγµένη τυρβώδη ροή, η µικρή συνεισφορά του ισοδύναµου χρόνου θέρµανσης και ψύξης στον ολικό χρόνο θερµικού θανάτου και οι απαιτήσεις ασφαλείας οδήγησαν στο να υπολογίζεται ως θερµική καταστροφή στις ασηπτικές διεργασίες µόνο εκείνη που συµβαίνει σε ισοθερµοκρασιακές συνθήκες, δηλ. στους σωλήνες παραµονής του ρευστού. Για παράδειγµα, ο Οργανισµός Τροφίµων και Φαρµάκων (FDA) των ΗΠΑ έως πρόσφατα ενέκρινε ως χρόνο θερµικής καταστροφής µόνο το χρόνο διατήρησης σε ισοθερµοκρασιακές συνθήκες, ενώ θεωρούσε τη θερµική καταστροφή που προκαλείται κατά τη θέρµανση και την ψύξη ως παράγοντα ασφαλείας. Τώρα ο FDA δέχεται τον συνυπολογισµό της θερµικής καταστροφής κατά τη θέρµανση και την ψύξη µόνο εφ όσον υπάρχουν επαρκή, αξιόπιστα δεδοµένα. Με βάση όσα αναφέρθηκαν για το σχεδιασµό της ασηπτικής διεργασίας για την επίτευξη ορισµένου στόχου σύµφωνα µε την εξίσωση (7.16) γίνονται οι ακόλουθες δύο βασικές παραδοχές: 1. Υπολογίζεται µόνο η θερµική καταστροφή που συµβαίνει στους σωλήνες παραµονής σε σταθερή θερµοκρασία (Τ) 2. Ως χρόνος κατεργασίας σε σταθερή θερµοκρασία θεωρείται ο ελάχιστος χρόνος παραµονής (t min ) στους σωλήνες σταθερής θερµοκρασίας. Εποµένως ο ισοδύναµος χρόνος στις ασηπτικές διεργασίες υπολογίζεται µέσω της ως: z ( T Tref ) / z F = 10 t (7.35) ref min Η εξίσωση (7.35) µπορεί να χρησιµοποιηθεί για τον υπολογισµό του ελάχιστου χρόνου παραµονής που απαιτείται για την επίτευξη ορισµένου αποτελέσµατος θανάτωσης µικροοργανισµών, όπως ορίζεται από την εξίσωση (7.16), ή για τον z υπολογισµό της τιµής F ref που επιτυγχάνεται σε ορισµένη διεργασία. Για την ασηπτική διεργασία ανοµοιογενών τροφίµων (µίγµατα υγρού και σωµατιδίων) έχει γίνει αρκετή έρευνα και έχουν διατυπωθεί ορισµένα µοντέλα για την πρόβλεψη της θερµοκρασίας του υγρού και των σωµατιδίων. Οι τιµές F που προκύπτουν για το υγρό και τα σωµατίδια έχουν διαφορά µεταξύ τους, η οποία αυξάνει όσο αυξάνει το µέγεθος των σωµατιδίων και µειώνεται ο χρόνος παραµονής. Αυτό σηµαίνει ότι για τρόφιµα µε σχετικά µεγάλα στερεά κοµµάτια η ασηπτική διεργασία οδηγεί σε υπερθέρµανση του υγρού ή ανεπαρκή θερµική κατεργασία των 197
206 στερεών. Για την αντιµετώπιση τέτοιων προβληµάτων έχει προταθεί η χωριστή θερµική κατεργασία του υγρού σε εναλλάκτες συνεχούς λειτουργίας και των στερεών σε ασυνεχή συστήµατα θερµαινόµενα µε ατµό. Στις περιπτώσεις που είναι επιθυµητός ο συνυπολογισµός της θερµικής καταστροφής κατά τη θέρµανση και την ψύξη πρέπει από τις εξισώσεις µεταφοράς θερµότητας να προσδιορισθεί η συνάρτηση θερµοκρασίας-χρόνου κατά τη θέρµανση και την ψύξη για να χρησιµοποιηθεί στην εξίσωση (7.18) ώστε να γίνει η ολοκλήρωση. Η υποβάθµιση των θρεπτικών συστατικών στις θερµικές διεργασίες, µπορεί να γίνει µέσω των κινητικών δεδοµένων καταστροφής τους µε τη θερµοκρασία, του υπολογισµού των ισοδυνάµων χρόνων (αντιστοίχων των F ref ) και της µείωσης της συγκέντρωσης που αντιστοιχεί σε αυτούς τους χρόνους. Στην ασηπτική διεργασία θεωρείται ο µέσος χρόνος παραµονής στο σωλήνα ισοθερµοκρασιακής κατεργασίας. Εξοπλισµός θερµικών διεργασιών Ζεµάτισµα Στις περισσότερες περιπτώσεις το ζεµάτισµα γίνεται µε άµεση επαφή του τροφίµου µε θερµό νερό ή ατµό. Η χρήση ατµού συνεπάγεται µικρότερες απώλειες υδατοδιαλυτών συστατικών και µικρότερο όγκο και φορτίο αποβλήτων. Το ζεµάτισµα µε νερό µπορεί να γίνει σε συστήµατα ασυνεχούς λειτουργίας µε εµβάπτιση των τροφίµων σε προθερµασµένο νερό. Συνήθως το τρόφιµο τοποθετείται σε διάτρητα τύµπανα, τα οποία έχουν δυνατότητα περιστροφής. Τα συστήµατα συνεχούς λειτουργίας είναι τύπου κοχλιωτού µεταφορέα, διάτρητου τυµπάνου ή σωλήνων. Τα συστήµατα διάτρητου τυµπάνου φέρουν συνήθως εσωτερικά κοχλία µεταφοράς. Τα συστήµατα σωλήνων χρησιµοποιούνται µόνο για τρόφιµα µικρών διαστάσεων τα οποία µπορούν να αντληθούν µαζί µε το νερό και να παραµένουν σε αιώρηση σε µικρές σχετικά ταχύτητες µεταφοράς, ώστε να µην προκαλείται φθορά. Το νερό µετά το διαχωρισµό του τροφίµου ανακυκλώνεται. Σε όλα τα συστήµατα µε νερό υπάρχει το πρόβληµα της αύξησης των διαλυτών στερεών στο νερό µε το χρόνο επαφής µε το τρόφιµο. Αύξηση της συγκέντρωσης περισσότερο από 2-3 % σε στερεά µπορεί να προκαλέσει δυσάρεστες οσµές στο τελικό προϊόν. Εποµένως είναι απαραίτητη η συνεχής προσθήκη φρέσκου νερού. Το ζεµάτισµα µε ατµό µπορεί να γίνει σε συστήµατα ασυνεχούς λειτουργίας, αλλά κυρίως χρησιµοποιούνται ζεµατιστήρες συνεχούς λειτουργίας. Τα τρόφιµα µεταφέρονται µε ιµάντες ή κοχλίες δια µέσου σήραγγας στην οποία διαβιβάζεται ατµός. Για τη µεταφορά τροφίµων ευαίσθητων σε µηχανική φθορά χρησιµοποιείται 198
207 ως µέσο µεταφοράς θερµό νερό. Επίσης έχουν αναπτυχθεί συστήµατα δύο σταδίων. Στο πρώτο στάδιο το τρόφιµο θερµαίνεται, ενώ το δεύτερο είναι ένα αδιαβατικό στάδιο όπου η διαφορά θερµοκρασίας µέσα στο τρόφιµο εξαλείφεται. Εκτός από τα συστήµατα που αναφέρθηκαν έχουν χρησιµοποιηθεί και ζεµατιστήρες θερµού αερίου. Το κύριο πλεονέκτηµά τους είναι η απουσία αποβλήτων, ενώ µειονεκτήµατα είναι η αφυδάτωση των προϊόντων, η οποία αντιµετωπίζεται µε ύγρανση του αερίου, και το επιφανειακό µαύρισµα σε ορισµένα προϊόντα. Επειδή η µέθοδος προκαλεί µερική αφυδάτωση είναι κατάλληλη για ζεµάτισµα τροφίµων πριν την ξήρανση. Παστερίωση Η παστερίωση γίνεται συνήθως σε θερµοκρασία χαµηλότερη από 100 C. Μπορεί να γίνει σε τρόφιµα ήδη συσκευασµένα ή να προηγηθεί της συσκευασίας, η οποία θα πρέπει να γίνει σε ασηπτικές συνθήκες. Η παστερίωση υγρών προϊόντων γίνεται στις σύγχρονες µονάδες σε εναλλάκτες συνεχούς λειτουργίας και ακολουθείται από ασηπτική συσκευασία. Το βασικό πλεονέκτηµα είναι η ταχύτερη µεταφορά θερµότητας και η µικρότερη υποβάθµιση των ποιοτικών χαρακτηριστικών του τροφίµου συγκρινόµενη µε την παστερίωση ήδη συσκευασµένων προϊόντων. Γενικά υπάρχει η τάση της εφαρµογής κατεργασίας υψηλής θερµοκρασίας-µικρού χρόνου (HTST: High Temperature Short Time) για την παραγωγή προϊόντων καλύτερης ποιότητας, όπως ήδη αναπτύχθηκε. Οι εναλλάκτες που χρησιµοποιούνται για προϊόντα χαµηλού ιξώδους, όπως το γάλα και η µπύρα, είναι κυρίως µε πλάκες. Σε αυτούς τους εναλλάκτες επιτυγχάνεται ανάκτηση θερµότητας µέχρι και 94 % µε θέρµανση του εισερχόµενου τροφίµου από το ήδη παστεριωµένο προϊόν (σχήµα 7.5). Για την αποµένουσα θέρµανση µέχρι την επιθυµητή θερµοκρασία χρησιµοποιείται ζεστό νερό ή ατµός χαµηλής πίεσης. Σε εφαρµογές ιδιαίτερα υψηλών θερµοκρασιών χρησιµοποιούνται εναλλάκτες µε σωλήνες στους οποίους η θέρµανση γίνεται µε διαβίβαση ατµού. Για ιξώδη προϊόντα χρησιµοποιούνται εναλλάκτες αποξεόµενης επιφάνειας. Στερεά τρόφιµα χύµα µπορούν να παστεριωθούν σε συστήµατα ίδια µε αυτά που χρησιµοποιούνται για το ζεµάτισµα Τρόφιµα τα οποία είναι ήδη συσκευασµένα παστεριώνονται σε συστήµατα συνεχούς ή ασυνεχούς λειτουργίας. Οι συσκευές ασυνεχούς λειτουργίας µπορεί να είναι δοχεία θερµού νερού, ή αυτόκλειστα θερµαινόµενα µε διαβίβαση ατµού κυρίως για µεταλλικούς περιέκτες. Συστήµατα συνεχούς λειτουργίας µε ψεκασµό διαδοχικά θερµού και ψυχρού νερού χρησιµοποιούνται στην παστερίωση συσκευασµένης µπύρας, χυµών ή αναψυκτικών. Παστεριωτές ατµού ή ατµού/νερού συνεχούς λειτουργίας χρησιµοποιούνται για µεταλλικούς περιέκτες και λειτουργούν συνήθως 199
208 σε ατµοσφαιρική πίεση. Τα δοχεία µεταφέρονται δια µέσου του παστεριωτήρα µε κοχλία. Επίσης χρησιµοποιούνται σήραγγες που θερµαίνονται µε µίγµα ατµού/αέρα. Σχήµα 7.5. ιάγραµµα ροής για παστερίωση σε εναλλάκτη µε πλάκες. Αποστείρωση Η αποστείρωση όπως και η παστερίωση µπορεί να γίνει σε προϊόντα ήδη συσκευασµένα, ή σε µη συσκευασµένα προϊόντα οπότε ακολουθεί ασηπτική συσκευασία. Για την κατεργασία µη συσκευασµένων προϊόντων (ασηπτική κατεργασία) χρησιµοποιείται είτε έµµεση θέρµανση, είτε άµεση. Η λειτουργία είναι συνεχής και το προϊόν συσκευάζεται στη γραµµή, αµέσως µετά τη διεργασία, σε αποστειρωµένους περιέκτες. Η ασηπτική κατεργασία εφαρµόζεται σε υγρά τρόφιµα που µπορεί να περιέχουν µικρά τεµάχια αιωρούµενων στερεών. Για µεγαλύτερα τεµάχια στερεών τα κυρίως προβλήµατα είναι η υποκατεργασία στο κέντρο των τεµαχίων, η µηχανική φθορά που προκαλείται από την ανάδευση που είναι αναγκαία για ταχύτερη µεταφορά θερµότητας και η κατακάθιση στερεών στους σωλήνες παραµονής. Στην έµµεση θέρµανση χρησιµοποιούνται οι ίδιοι εναλλάκτες που αναφέρθηκαν στην παστερίωση, µε τη διαφορά ότι ως µέσο θέρµανσης λόγω των υψηλότερων θερµοκρασιών χρησιµοποιείται συχνότερα ο ατµός. Οι εναλλάκτες µε πλάκες χρησιµοποιούνται κυρίως για τρόφιµα χαµηλού ιξώδους. Πλεονεκτούν ως προς την ανάκτηση ενέργειας (περισσότερο από 90 %), την ευελιξία στη λειτουργία και τον καθαρισµό. Οι εναλλάκτες µε σωλήνες χρησιµοποιούνται επίσης για τρόφιµα σχετικά χαµηλού ιξώδους. Κύριο πλεονέκτηµά τους είναι η δυνατότητα λειτουργίας σε µεγαλύτερη πίεση και µεγαλύτερη παροχή τροφίµου που εξασφαλίζει τυρβώδη ροή, πιο οµοιόµορφη µεταφορά θερµότητας και λιγότερες αποθέσεις στα τοιχώµατα σε σύγκριση µε τους εναλλάκτες µε πλάκες. Οι εναλλάκτες αποξεόµενης επιφάνειας χρησιµοποιούνται σε ιξώδη τρόφιµα ή µε στερεά τεµαχίδια, είναι ευέλικτοι στη λειτουργία αλλά υστερούν στην ανάκτηση θερµότητας. 200
209 Η άµεση εναλλαγή θερµότητας γίνεται µε ανάµιξη ατµού µε το τρόφιµο, προκαλεί σχεδόν στιγµιαία ανύψωση της θερµοκρασίας και χρησιµοποιείται σε διεργασίες πολύ υψηλής θερµοκρασίας και µικρού χρόνου. Η ψύξη γίνεται επίσης σχεδόν στιγµιαία µε εκτόνωση σε θάλαµο χαµηλής πίεσης στους 70 C περίπου. Ένα διάγραµµα ροής µε χρήση άµεσης θέρµανσης δίνεται στο σχήµα 7.6. Κατά την εκτόνωση συµπαρασύρονται και πτητικά συστατικά που µπορεί να είναι επιθυµητό για ορισµένα τρόφιµα (π.χ. το γάλα). Το βασικό πλεονέκτηµα έναντι της έµµεσης εναλλαγής θερµότητας είναι οι µικρότεροι χρόνοι ανύψωσης και µείωσης της θερµοκρασίας. Η µέθοδος είναι κατάλληλη µόνο για τρόφιµα χαµηλού ιξώδους. Απαιτεί ατµό πόσιµο από πλευράς ποιότητας. Η ανάκτηση ενέργειας ανέρχεται µέχρι 50 % και ο έλεγχος των συνθηκών της διεργασίας υστερεί έναντι των έµµεσων εναλλακτών θερµότητας. Οι διεργασίες αποστείρωσης των µη συσκευασµένων τροφίµων, που γίνονται σε υψηλή θερµοκρασία και για µικρό χρονικό διάστηµα, ανεξάρτητα του εάν γίνονται µε άµεση ή έµµεση θέρµανση, καλούνται διεργασίες υπερηψηλής θερµοκρασίας (UHT: Ultra High Temperature). Για παράδειγµα στο γάλα η κατεργασία UHT γίνεται στους 140 C περίπου µε διάρκεια 2-5 sec. Σχήµα 7.6. ιάγραµµα ροής µονάδας UHT µε άµεση θέρµανση του προϊόντος. Η αποστείρωση συσκευασµένων τροφίµων γίνεται σε αυτόκλειστα ασυνεχούς λειτουργίας τα οποία θερµαίνονται συνήθως µε ατµό. Τα παλαιότερου τύπου αυτόκλειστα είναι ακίνητα ενώ στα νεότερα υπάρχει η δυνατότητα ανακίνησης των περιεκτών για ταχύτερη µεταφορά θερµότητας. Τα ακίνητα αυτόκλειστα είναι κυλινδρικά µε κατακόρυφο ή οριζόντιο προσανατολισµό του άξονά τους. Για τη διευκόλυνση της φόρτωσης και εκφόρτωσης των κονσερβών χρησιµοποιούνται καλάθια. Οι κονσέρβες τοποθετούνται κατακόρυφα στο καλάθι που φέρει διάτρητα µεταλλικά χωρίσµατα για διαχωρισµό των στοιβάδων των κονσερβών. Στα κατακόρυφα αυτόκλειστα τα καλάθια τοποθετούνται στο αυτόκλειστο και 201
210 αποµακρύνονται από αυτό µε ηλεκτρικούς ανυψωτήρες. Στα οριζόντια αυτόκλειστα τα καλάθια έχουν σχήµα ορθογωνίου παραλληλογράµµου µε κοίλες τις δύο πλευρικές επιφάνειες και µετακινούνται εντός και εκτός του αυτοκλείστου πάνω σε ράγες (σχήµα 7.7). Το κάλυµα των αυτοκλείστων στερεώνεται µε κοχλίες ή µε δακτύλιο κλειδώµατος που κλειδώνει και ξεκλειδώνει µε µοχλό. Στα αυτόκλειστα µε ανακίνηση των περιεκτών εφαρµόζεται είτε περιστροφή των δοχείων περί τον άξονά τους, είτε ταλάντωση σε διεύθυνση παράλληλη ή κάθετη προς τον άξονα του δοχείου (σχήµα 7.8). Σχήµα 7.7. ιάταξη φόρτωσης σε οριζόντιο σταθερό αυτόκλειστο (Toledo, 1991). Τα αυτόκλειστα ασυνεχούς λειτουργίας φέρουν βαλβίδες εισόδου και εξόδου ατµού, ψυχρού νερού και πιθανώς αέρα, βαλβίδα ασφαλείας, ρυθµιστή θερµοκρασίας, θερµόµετρο και µανόµετρο. Ένα τυπικό κατακόρυφο αυτόκλειστο δίνεται στο σχήµα 7.9. Κατά τη λειτουργία το αυτόκλειστο κλείνεται µετά τη φόρτωση των δοχείων και απαερώνεται µε διαβίβαση ατµού. Η αποµάκρυνση του αέρα πρέπει να είναι πλήρης για να µην υπάρξει µείωση του συντελεστή µεταφοράς θερµότητας, λόγω σχηµατισµού εγκλωβισµένου στρώµατος αέρα στις επιφάνειες των δοχείων. Η διαβίβαση ατµού συνεχίζεται µέχρι να επιτευχθεί η επιθυµητή θερµοκρασία. Ο χρόνος από την αρχή της εισαγωγής ατµού µέχρι την επίτευξη της επιθυµητής θερµοκρασίας καλείται χρόνος ανόδου της θερµοκρασίας του αποστειρωτήρα (retort come-up time). Τα δοχεία παραµένουν στη σταθερή θερµοκρασία για χρονικό διάστηµα που έχει προκαθορισθεί κατά το σχεδιασµό της διεργασίας. Ο απαιτούµενος χρόνος παραµονής που υπολογίζεται µε τις 202
211 υπολογιστικές µεθόδους µετριέται από τη στιγµή που το αυτόκλειστο θα αποκτήσει την επιθυµητή θερµοκρασία, χωρίς να προσµετράται ο χρόνος ανόδου της θερµοκρασίας. Ακολουθεί η ψύξη µε εκτόνωση του ατµού και διαβίβαση συνήθως ψυχρού νερού, ενώ µπορεί να χρησιµοποιηθεί ταυτόχρονα και ορισµένη υπερπίεση αέρα για να αποφευχθεί η διόγκωση των µεταλλικών δοχείων ή το άνοιγµα των πωµάτων σε γυάλινα δοχεία. Σχήµα 7.8. Μέθοδοι ανακίνησης κονσερβών σε αυτόκλειστα. (α) ταλάντωση σε διεύθυνση παράλληλη ή κάθετη προς τον άξονα του δοχείου (b) περιστροφή των δοχείων περί τον άξονά τους (Brennan et al, 1976). Η πίεση στο εσωτερικό των δοχείων κατά τη θέρµανση είναι µικρότερη από την πίεση στο χώρο του αυτοκλείστου, λόγω χαµηλότερης θερµοκρασίας. Με την αύξηση της θερµοκρασίας το περιεχόµενο του δοχείου διαστέλλεται και εποµένως µειώνεται ο κενός τροφίµου χώρος µέσα στο δοχείο. Παράλληλα αυξάνεται η τάση ατµών καθώς και η πίεση του αέρα και άλλων αερίων που έχουν παραµείνει στο δοχείο κατά τη σφράγιση αυτού ή υπάρχουν στο τρόφιµο. Έτσι προς το τέλος της αποστείρωσης και ιδιαίτερα κατά τη διάρκεια της ψύξης, οπότε η θερµοκρασία και η πίεση στο χώρο του αυτοκλείστου µειώνεται πολύ ταχύτερα από ότι στο εσωτερικό του δοχείου, η εσωτερική πίεση του δοχείου είναι πολύ µεγαλύτερη από την εξωτερική και µπορεί να επιφέρει διόγκωση ή άνοιγµα. Για την εξισορρόπηση της πίεσης, εκτός της χρήσης πιεσµένου αέρα κατά την ψύξη, οι περιέκτες φέρουν δακτύλιους διαστολής ή κοίλα πώµατα, ώστε να µπορούν να διασταλούν και να επανέλθουν στη συνέχεια στο αρχικό τους σχήµα. Για τον ίδιο λόγο οι περιέκτες δεν γεµίζονται πλήρως αλλά αφήνεται ορισµένος κενός χώρος ο οποίος απαερώνεται πριν από τη σφράγιση. Ο χώρος αυτός διευκολύνει επίσης τη µεταφορά θερµότητας σε διεργασίες µε ανακίνηση των περιεκτών. Για γυάλινα δοχεία και γενικώς για δύσκαµπτους περιέκτες που θα αποστειρωθούν στους C συνιστάται ο κενός χώρος να 203
212 είναι τουλάχιστο το 6 % του συνολικού όγκου στη συµβατική θερµοκρασία σφράγισης (55 C). Κατά γενικό κανόνα ο κενός χώρος δεν πρέπει να υπερβαίνει το 10 % του συνολικού όγκου. Η µερική πίεση του αέρα εντός του δοχείου µειώνεται µε αποµάκρυνση των αερίων που είναι εγκλωβισµένα στα τρόφιµο (µε ζεµάτισµα ή εφαρµογή κενού) και µε απαέρωση του δοχείου πριν τη σφράγιση (µε εφαρµογή κενού ή διαβίβαση ατµού ή θέρµανση στους C). Επί πλέον της µείωσης της εσωτερική πίεσης, η απαέρωση συµβάλλει στον περιορισµό της διάβρωσης στο εσωτερικό του δοχείου, της οξείδωσης του τροφίµου και της ανάπτυξης αερόβιων µικροοργανισµών. Σχήµα 7.9. Κατακόρυφο αυτόκλειστο ασυνεχούς λειτουργίας µε δυνατότητα ψύξης υπό πίεση αέρα. 1: βαλβίδα ασφαλείας, 2: ανακουφιστικές βαλβίδες διαρροής ατµού κατά τη λειτουργία, 3-6: όργανα µέτρησης και ελέχου των παραµέτρων λειτουργίας. 7: διασκορπιστήρας ατµού, 8: είσοδος αέρα για ψύξη υπό πίεση (Brennan et al, 1976). Ιδιαίτερα για την αποστείρωση τροφίµων συσκευασµένων σε γυάλινους περιέκτες, που δεν αντέχουν σε απότοµες µεταβολές θερµοκρασίας, τα αυτόκλειστα ασυνεχούς λειτουργίας γεµίζονται αρχικά µε νερό. Το νερό θερµαίνεται µε ατµό και ανακυκλοφορεί διαβιβαζόµενο στον πυθµένα του αποστειρωτήρα εξασφαλίζοντας οµοιόµορφη θέρµανση των δοχείων. Η ψύξη γίνεται αργά µε εισαγωγή κρύου νερού. Ο χρόνος ανόδου της θερµοκρασίας του αποστειρωτήρα και ψύξης αυτού είναι 204
213 µεγάλος και λαµβάνεται υπ όψιν στο σχεδιασµό της διεργασίας. Η εκτίµηση της θερµικής καταστροφής γίνεται µε καλύτερη προσέγγιση µε χρήση της γενικής µεθόδου. Σε µεγάλες εγκαταστάσεις χρησιµοποιούνται και αυτόκλειστα συνεχούς λειτουργίας διαφόρων τύπων. Ένας τύπος είναι τα οριζόντια κυλινδρικά δοχεία που φέρουν περιστρεφόµενες ελικοειδείς διατάξεις διακίνησης των δοχείων (σχήµα 7.10). Τα δοχεία ανάλογα µε τη διάταξη µπορεί να περιστρέφονται περί τον άξονά τους ή να είναι σταθερά. Η είσοδος και η έξοδος των κονσερβών στο αυτόκλειστο γίνεται µε περιστροφικές βαλβίδες πιέσεως (σχήµα 7.11). Σχήµα Οριζόντιο αυτόκλειστο συνεχούς λειτουργίας (Brennan,1976). Σε άλλο τύπο συνεχούς αποστειρωτήρα η βαλβίδα πιέσεως λειτουργεί µε συνδυασµό φραγής νερού και µηχανικής φραγής. Ο αποστειρωτήρας είναι κυλινδρικό οριζόντιο δοχείο στο κάτω τµήµα του οποίου υπάρχει νερό στο οποίο προθερµαίνονται τα δοχεία κατά την είσοδό τους και ψύχονται κατά την έξοδο. Ο χώρος που καταλαµβάνεται από ατµό αποµονώνεται από το κάτω τµήµα µε διαχωριστικό και ο χρόνος παραµονής ρυθµίζεται µέσω της ταχύτητας του φορέα που µεταφέρει τα δοχεία (σχήµα 7.12). Μπορεί να υπάρχει συνεχής περιστροφή των δοχείων µε κατάλληλη τοποθέτηση κυλινδρικών ράβδων κάτω από το φορέα. 205
214 Σχήµα Οριζόντιο αυτόκλειστο συνεχούς λειτουργίας µε περιστροφική βαλβίδα εισόδου κονσερβών (Toledo, 1991). Σχήµα Αποστειρωτήρας Hydrolock. α: φραγή νερού, b: µεταφορική αλυσίδα, c: στάθµη νερού, d: χώρος ατµού, e: στήριξη δοχείων στο µεταφορέα, f: διαδροµή δοχείων, g: αναστροφή πορείας, h: εισαγωγέας µίγµατος ατµού αέρα, I: διαχωριστικό µόνωσης χώρων ατµού-νερού, j: νερό πρόψυξης, k: σχισµή µεταφοράς, l: περιστροφική βαλβίδα µε φραγή νερού, m: ψύξη µε αέρα ( Brennan, 1976). Ένας άλλος τύπος είναι ο υδροστατικός αποστειρωτήρας, ο οποίος έχει µεγάλο ύψος και η πίεση του ατµού συγκρατείται µε την υδροστατική πίεση στηλών νερού κατάλληλου ύψους, ανοικτών στην ατµόσφαιρα, στην είσοδο και στην έξοδο του αποστειρωτήρα (σχήµα 7.13). 206
215 Σχήµα Υδροστατικός αποστειρωτήρας (Lund, 1975). Τα δοχεία µε το προϊόν µεταφέρονται µε ταινία δια µέσου της στήλης προθέρµανσης, στο θάλαµο του ατµού σταθερής θερµοκρασίας και τέλος στη στήλη ψύξης. Η ταχύτητα της ταινίας καθορίζει το χρόνο παραµονής στο θάλαµο του ατµού που πρέπει να ισούται µε τον προκαθορισµένο κατά το σχεδιασµό χρόνο της διεργασίας. Για διεργασία στους 121 C η τάση ατµών είναι kpa και δεδοµένου ότι η ατµοσφαιρική πίεση είναι kpa απαιτείται στήλη νερού 10.7 m για τη διατήρηση της πίεσης στο εσωτερικό του αποστειρωτήρα. Έτσι η συνολική εγκατάσταση του αποστειρωτήρα µπορεί να φθάνει και τα 20 m ύψος και γίνεται σε υπαίθριο χώρο. Καταλαµβάνει όµως µικρό εµβαδό και λόγω της ευελιξίας για διάφορους τύπους κονσερβοποιηµένων τροφίµων, της ελαχιστοποίησης του θερµικού σοκ που υφίσταται το τρόφιµο και ο περιέκτης και του υψηλού βαθµού αυτοµατισµού ο υδροστατικός αποστειρωτήρας είναι ευρέως διαδεδοµένος σε µεγάλες βιοµηχανικές µονάδες. Σε κονσέρβες µικρού µεγέθους γίνεται αποστείρωση και µε άµεση επαφή µε φλόγες. Η µέθοδος εφαρµόζεται σε προϊόντα θερµαινόµενα µε συναγωγή, τα οποία µετακινούνται περιστρεφόµενα γρήγορα για ταχύτερη µεταφορά θερµότητας. Επειδή 207
216 στο σύστηµα δεν υπάρχει υπερπίεση τα δοχεία πρέπει να αντέχουν την εσωτερική πίεση που αναπτύσσεται γι αυτό και η µέθοδος περιορίζεται σε µικρού µεγέθους περιέκτες. Παραδείγµατα 1. Σε κονσερβοποιηµένο τρόφιµο υπάρχουν στελέχη του PA 3679 (D o =1.2 min) και του Clostridium botulinum (D o =0.22 min). Εάν η θερµική κατεργασία που υφίσταται το τρόφιµο µειώνει τον πληθυσµό του Clostridium botulinum σε της αρχικής τιµής, να βρεθεί η πιθανότητα επιβίωσης του PA 3679 όταν το αρχικό του φορτίο ήταν 2 µικρ./δοχείο, µε δεδοµένο ότι οι δύο µικροοργανισµοί έχουν την ίδια τιµή z. Λύση Έστω ότι η θερµική κατεργασία του τροφίµου γίνεται σε θερµοκρασία Τ F. Οι χρόνοι υποδεκαπλασιασµού για τους δύο µικροοργανισµούς θα είναι: D ( )= D PA T PAo T z 250 T z DCb( T )= DCbo10 Εποµένως D PA( T ) DPAo = DCb( T ) DCbo Ο χρόνος που απαιτείται για µείωση του πληθυσµού του Clostridium botulinum σε της αρχικής τιµής θα είναι: N Cbo 12 t = DCb( T ) log = DCb( T ) log10 = 12DCb( T ) N Cb Η µείωση του πληθυσµού του PA σε αυτό το χρόνο θα είναι: N t D PA Cb( T ). log = = 12 = = 22. N PAo DPA( T ) DPA( T ) 12. log N = log N 22. = log = 19. PA PAo N PA = = Άρα υπάρχει πιθανότητα να επιβιώσουν 13 µικροοργανισµοί ανά 1000 κονσέρβες. 2. Κατά τη θερµική κατεργασία κονσερβοποιηµένου προϊόντος σε αυτόκλειστο θερµοκρασίας 250 F, µε χρόνο ανόδου της θερµοκρασίας του αυτοκλείστου 3 min, καταγράφηκαν τα ακόλουθα δεδοµένα θερµοκρασίας του θερµικού κέντρου του προϊόντος ως συνάρτηση του χρόνου παραµονής στο αυτόκλειστο: Χρόνος (min) Θερµοκρασία Χρόνος (min) Θερµοκρασία F F
217 (ψύξη) α) Να υπολογισθεί, σύµφωνα µε τη γενική µέθοδο, ο ισοδύναµος χρόνος F o αυτής της κατεργασίας για ένα µικροοργανισµό µε z=18 F. β) Να υπολογισθούν οι τιµές των f h και j h και ο ισοδύναµος χρόνος F o σύµφωνα µε την υπολογιστική µέθοδο του Stumbo. γ) Να υπολογισθεί η απαιτούµενη διάρκεια κατεργασίας στους 240 F, 250 F και 260 F για F o =8 min όταν z=18 F, j h =j c και αρχική θερµοκρασία προϊόντος 120 F. Λύση α) Η γενική µέθοδος στηρίζεται στον υπολογισµό του ολοκληρώµατος t 0 t 0 T Fo = Ldt = 10 dt γραφικά ή υπολογιστικά. Η γραφική ολοκλήρωση για τον υπολογισµό της επιφάνειας κάτω από την καµπύλη L µπορεί να γίνει σύµφωνα µε τον κανόνα του Simpson. Κατά τη διάρκεια της θέρµανσης το διάστηµα από t=0 min σε t=80 min θεωρώντας δt=5 min χωρίζεται σε 16 τµήµατα. Το εµβαδόν δίνεται από τη σχέση δt A = L + 4L + 2L + 4L + 2L L + 4L + L [ ] 3 όπου L 0 η τιµή σε t=0 min, L 1 η τιµή σε t=δt=5 min κ.ο.κ. Οι τιµές L που υπολογίζονται είναι: L o =10-110/18 =0=L 1 =L 2 =L 3 L 10 = /18 = L 4 =10-87/18 =1.5*10-5 L 11 =10-12/18 = L 5 =10-65/18 =2.45*10-4 L 12 =10-9/18 = L 6 =10-54/18 =1.001*10-3 L 13 =10-6.5/18 = L 7 =10-37/18 = L 14 =10-5/18 = L 8 =10-26/18 = L 15 =10-3.7/18 = L 9 = /18 = L 16 =10-2.7/18 = Άρα Α=13.57 min. Αντίστοιχα για την ψύξη: L ο =10-2.7/18 = L 4 =10-75/18 =6.8*10-5 L 1 =10-3/18 = L 5 =10-97/18 =0 L 2 =10-4.8/18 = L 6 =0 L 3 = /18 = Άρα Α=7.75 min Το F o αντιστοιχεί στη συνολική επιφάνεια. Εποµένως F o = =21.32 min. Η ψύξη σε αυτό το παράδειγµα συµβάλλει περισσότερο από το ένα τρίτο της συνολικής θερµικής καταστροφής. β) Θα κατασκευασθεί το διάγραµµα log (Tr-T) ως προς t. Tr-T time (min) log (Tr-T) 209
218 , , ,9 2, , , , , , , ,6 45 1, ,5 50 1, , , ,5 65 0, , ,7 75 0, ,7 80 0, ,5 log (Tr-T) 2 log (Tr-T) 1,5 1 0, time (min) 2,5 2 log (Tr-T) 1,5 1 0,5 y = -0,0248x + 2, time (min) Από την κλίση της ευθείας που προκύπτει εξαιρώντας τα τρία αρχικά σηµεία (υστέρηση) υπολογίζουµε τον παράγοντα f h =1/0.0248=40.32 min. Ο παράγοντας υστέρησης υπολογίζεται από την αποτέµνουσα της ευθείας σε t=0.6xt αν =0.6x3=1.8 min: log (T r -T A )= x = και T r -T A =242 j h =(T r -T A )/(T r -T IT )=242/( )=2.2 Το F o θα υπολογισθεί µε γραµµική παρεµβολή από τον πίνακα 7.4 για z=18 για τελική διαφορά θερµοκρασίας Τ r -T g =g=2.7 µεταξύ των τιµών g=0.523+(2.2-1)x0.192=0.753 και g=1.93+(2.2-1)x0.68= Σε g=0.753 αντιστοιχεί τιµή f h /U=1 Σε g=2.746 αντιστοιχεί τιµή f h /U=2 Για g=2.7 προκύπτει f h /U=1.977 και U=40.32/1.977=20.45 min. 210
219 Επειδή η κατεργασία γίνεται στους 250 F το U συµπίπτει µε το F o. Εποµένως F o =20.45 min. γ) Για την κατεργασία στους 240 F υπολογίζεται αρχικά ο απαιτούµενος χρόνος σε ισοθερµοκρασιακή κατεργασία σε αυτή τη θερµοκρασία: U 240 = F o 10 = min Εποµένως f h /U=40.32/28.75=1.40 Από Πίνακα 7.4 για f h /U=1.40 j c =2.2 και z=18 F µε γραµµική παρεµβολή µεταξύ των τιµών (2.2-1)0.192=0.753 και 1.93+(2.2-1)0.68=2.746 βρίσκουµε g= ( )=1.550 Ο απαιτούµενος χρόνος θα υπολογισθεί µέσω της εξίσωσης (7.31): t = fh{log[ jh( Tr TIT)] log g} = {log[ 2. 2( )] log } = 90 min Ο χρόνος αυτός περιλαµβάνει το 40 % του χρόνου ανόδου της θερµοκρασίας του αποστειρωτήρα στη θερµοκρασία των 240 F. Για λόγους ασφαλείας όµως µπορεί αυτός ο χρόνος να µην αφαιρεθεί και η ψύξη να αρχίσει 90 min µετά από τη στιγµή που ο αποστειρωτήρας έφτασε τους 240 F. Οµοίως υπολογίζουµε για τους 250 F και τους 260 F. U 250 =F o =8 min f h /U=5.04 g=7.308 F t=64.2 min στους 250 F U 260 =2.226 min f h /U=18.11 g=16.64 F t=51 min στους 260 F 3. Κατά την ασηπτική κατεργασία χυµού φρούτων επιδιώκεται η µείωση πληθυσµού µικροοργανισµών, µε χρόνο υποδεκαπλασιασµού στους 100 C: D 100 C =30 s και z=10 C, στο 10-5 της αρχικής συγκέντρωσης και η µείωση ενζύµων, µε D 100 C =5 s και z=30 C, στο 10-3 της αρχικής συγκέντρωσης. Ζητείται η απαιτούµενη θερµοκρασία παραµονής (σε ισοθερµοκρασιακές συνθήκες) για την επίτευξη των δύο στόχων στον ίδιο χρόνο και ο απαιτούµενος χρόνος παραµονής. Λύση Ο απαιτούµενος χρόνος για τη µείωση του πληθυσµού των µικροοργανισµών σε θερµοκρασία Τ θα είναι: 100 T 100 T Co F( T) µ = D( T) µ log = D o 10 log10 = s 100 Cµ C Οµοίως για τα ένζυµα: 100 T 100 T Co F( T) ε = D( T) ε log = D o 10 log10 = s 100 Cε C Εφόσον θέλουµε να πετύχουµε τους δύο στόχους στον ίδιο χρόνο, ο οποίος θα είναι και ο χρόνος της κατεργασίας θα πρέπει: 100 T 10 F (T)µ = F (T)ε = T 30 Τ=115 C 211
220 και F 115 C =4.74 s 4. Ποιοι χρόνοι παραµονής τροφίµου σε ασηπτική κατεργασία απαιτούνται για τη µείωση πληθυσµού µικροοργανισµών στο της αρχικής τιµής όταν η κατεργασία γίνει στους 120 C ή στους 140 C. ίδεται: D 120 C =30 s και z=10 C. Να συγκριθεί ο λόγος του ρυθµού καταστροφής των µικροοργανισµών προς τον ρυθµό καταστροφής της βιταµίνης C στις δύο κατεργασίες, αν είναι γνωστό ότι η θερµική καταστροφή της ακολουθεί κινητική πρώτης τάξης µε ενέργεια ενεργοποίησης 125 kj/mol K. Λύση D 140 C = D 120 C 10 ( )/10 =0.3 s F 120 C = D 120 C log(n o /N)=30x10=300 s F 140 C = D 140 C log(n o /N)=0.3x10=3 s Ρυθµός καταστροφής µικροοργανισµών: dn = dt D N Ρυθµός καταστροφής βιταµίνης C E dc RT = kc = koe C dt Εποµένως ο λόγος των ρυθµών καταστροφής στους 140 C προς τον αντίστοιχο λόγο στους 120 C θα είναι: R393 Nkoe C Λ140 D140 30e = 125 = =15. 6 Λ e R413 Nkoe C D120 Το αποτέλεσµα δείχνει ότι στην µεγαλύτερη θερµοκρασία θα έχουµε 15.6 φορές ταχύτερη καταστροφή των µικροοργανισµών ως προς απώλεια βιταµίνης C από ότι στη χαµηλότερη θερµοκρασία. Εποµένως η κατεργασία στην µεγαλύτερη θερµοκρασία θα οδηγήσει σε µικρότερη απώλεια βιταµίνης. Tην απώλεια βιταµίνης σε κάθε µία κατεργασία µπορούµε να την υπολογίσουµε εάν γνωρίζουµε το k o. Με δεδοµένο ότι οι απαιτούµενοι χρόνοι κατεργασίας στους 120 C και στους 140 C είναι 300 s και 3 s, αντίστοιχα απώλεια στους 120 C: C C o k koexp( ) = 1 e = 1 e C o απώλεια στους 140 C: C C o C o k = 1 e = 1 e 3 3koexp( ) 5. Μίγµα παγωτού µε ιξώδες 70 cp και πυκνότητα 1015 kg/m 3 κατεργάζεται ασηπτικά µε ογκοµετρική παροχή 20 L/min. Το µίγµα θερµαίνεται στους 140 C, διαβιβάζεται σε σωλήνα εξωτερικής διαµέτρου 1 in και µήκους 30 m, όπου και παραµένει στη θερµοκρασία των 140 C και στη συνέχεια ψύχεται. Να υπολογισθεί η τιµή αποστείρωσης (Sterilizing Value, SV) της κατεργασίας για τον µικροοργανισµό PA 3679 (D o =1.83 min, z=24 F). ίδεται εσωτερική διάµετρος του σωλήνα in. 212
221 Λύση Θα υπολογισθεί η τιµή αποστείρωσης µόνο µε βάση το χρόνο παραµονής στο σωλήνα σταθερής θερµοκρασίας 140 C. Η µέση ταχύτητα στο σωλήνα θα είναι: 3 3 Q / 60( m / s) v avg = = = 0.82m / s πr π ( / 2) ( m ) Ιξώδες µ=70cp=0.07 Pa s dv avg ρ Re = = = 263 µ 007. Άρα η ροή είναι στρωτή και η µέγιστη ταχύτητα στο σωλήνα παραµονής θα είναι vmax = 2vavg = = 164. m/ s Εποµένως ο ελάχιστος χρόνος παραµονής θα είναι tmin = L/ vmax = 30 / 164. = s Η κατεργασία γίνεται στους 140 C ή 140x9/5+32=284 F Με βάση τα κινητικά δεδοµένα καταστροφής του PA 3679 (D o =1.83 min, z=24 F): D284 = Do = = 4. 21s και N o t SV = log = = = 435. N D Ασκήσεις 1. Να υπολογισθεί ο χρόνος υποδεκαπλασιασµού στους 250 F (D 250 ή D o ) ενός µικροοργανισµού, όταν επιβιώνουν 30 µικροοργανισµοί από ένα αρχικό φορτίο 5x10 6 µικροοργανισµών µετά από παραµονή για 10 min στους 250 F. 2. Εάν ο µικροοργανισµός της άσκησης 1 έχει τιµή z=20 F να υπολογισθεί ο απαιτούµενος χρόνος στους 250 F (F 250 ή F o ) καθώς και στους 240 F (F 240 ) για πιθανότητα µικροβιακής αλλοίωσης 1 ανά δοχεία από αρχικό φορτίο 100 µικρ./δοχείο. 3. Κατά τη θερµική κατεργασία προϊόντος κρέατος σε αυτόκλειστο θερµοκρασίας 250 F, µε χρόνο ανόδου της θερµοκρασίας του αυτοκλείστου 5 min, καταγράφηκαν τα ακόλουθα δεδοµένα θερµοκρασίας του θερµικού κέντρου του προϊόντος ως συνάρτηση του χρόνου παραµονής στο αυτόκλειστο: Χρόνος (min) θερµοκρασία ( F)
222 Να υπολογισθεί, σύµφωνα µε τη γενική µέθοδο, ο ισοδύναµος χρόνος F o αυτής της κατεργασίας για ένα µικροοργανισµό µε z=18 F. 4. Να υπολογισθούν οι τιµές των f h και j h για το προϊόν της άσκησης 3. Να βρεθεί σύµφωνα µε τη µέθοδο του Ball η απαιτούµενη διάρκεια κατεργασίας στους 230 F και 265 F για SV=8 όταν D 250 F =75 s, z=18 F, m+g=160 F και αρχική θερµοκρασία προϊόντος 120 F. 5. Υγρό τρόφιµο συσκευασµένο σε µεταλλικά δοχεία 0.5 L αποστειρώνεται σε αποστειρωτήρα συνεχούς λειτουργίας σε θερµοκρασία 110 C. Να υπολογισθεί η πιθανότητα µικροβιακής αλλοίωσης µετά από χρόνο παραµονής των δοχείων στον αποστειρωτήρα 30 min. ίδονται: αρχική θερµοκρασία τροφίµου 30 C, αρχικό µικροβιακό φορτίο 2000 µικροοργανισµοί και σπόρια ανά λίτρο, µέσος χρόνος υποδεκαπλασιασµού D 120 C =0.5s, z=10 C, f h =30 min, J h =1.4, J c = Κονσερβοποιηµένο τρόφιµο µε κλίση καµπύλης θερµικής διείσδυσης f h =30 min και υστέρηση j h =j c =1.07 περιέχει αρχικό µικροβιακό φορτίο 50 µικρ./δοχείο µε D o =1.2 min. Για το τρόφιµο αυτό σχεδιάσθηκε θερµική κατεργασία σε αυτόκλειστο στους 250 F για επίτευξη F o =6 min βασισµένη σε τιµή z=18 F και αρχική θερµοκρασία τροφίµου 150 F. Οι πειραµατικές µετρήσεις έδειξαν ότι η πραγµατική τιµή z για τους µικροοργανισµούς στο τρόφιµο ήταν 14 F αντί για 18 F και η θερµοκρασία στο αυτόκλειστο 248 F αντί 250 F. Να υπολογισθεί η πιθανότητα αλλοίωσης για τη θερµική κατεργασία στην οποία υποβάλλεται το τρόφιµο. Σύµβολα α=k/ρc p θερµική διαχυτότητα (m 2 /s) Α επιφάνεια εναλλαγής θερµότητας (m 2 ) b ½ ύψους κυλίνδρου ή ορθογωνίου παρ/µου (m) c ½ πλάτους ορθογωνίου παρ/µου (m) c p ειδική θερµότητα (J/kg C) C συγκέντρωση ζώντων µικροοργανισµών ή θρεπτικών συστατικών (L -1 ) d διάµετρος σωλήνα (m) d p χαρακτηριστική διάσταση του τροφίµου (m) D χρόνος υποδεκαπλασιασµού (s) D o χρόνος υποδεκαπλασιασµού στους C ή 250 F (s) E a ενέργεια ενεργοποίησης (J/mol) f χρόνος που απαιτείται για να υποδεκαπλασιασθεί η διαφορά θερµοκρασίας µεταξύ του τροφίµου και του µέσου θέρµανσης ή ψύξης (s) 214
223 F χρόνος θερµικού θανάτου (s) F o χρόνος θερµικού θανάτου στους C ή 250 F για z = 10 C ή 18 F (s) g=t RT -T g διαφορά θερµοκρασία αποστειρωτήρα θερµικού κέντρου τροφίµου στο τέλος της θέρµανσης ( C ή F) g bh διαφορά θερµοκρασία αποστειρωτήρα θερµικού κέντρου τροφίµου τη στιγµή που h h i αλλάζει η κλίση της καµπύλης θέρµανσης ( C ή F) επιφανειακός συντελεστής µεταφοράς θερµότητας (W/m 2 C) επιφανειακός συντελεστής µεταφοράς θερµότητας του τροφίµου (W/m 2 C) h o επιφανειακός συντελεστής µεταφοράς θερµότητας του θερµαντικού υγρού (W/m 2 C) j παράγοντας υστέρησης όπως ορίζεται στο σχήµα 6.1. J o, J συναρτήσεις Bessel i k σταθερά ρυθµού δράσης (s -1 ) k K L L συντελεστής αγωγής θερµότητας (W/m C) συντελεστής συνεκτικότητας ρευστού µήκος σωλήνα (m) ρυθµός ή συνάρτηση θερµικής καταστροφής (s ή min) m=t g -T CW διαφορά θερµοκρασία του θερµικού κέντρου τροφίµου στο τέλος της n N θέρµανσης και του νερού ψύξης ( C ή F) δείκτης ρεολογικής συµπεριφοράς πληθυσµός µικροοργανισµών N o αρχικός πληθυσµός µικροοργανισµών Q Q 10 ογκοµετρική ροή (m 3 /s) λόγος της σταθεράς του ρυθµού µιας δράσης σε θερµοκρασία Τ ( C) προς τη σταθερά σε θερµοκτασία Τ-10 ( C) ρ πυκνότητα (kg/m 3 ) r ακτίνα κυλίνδρου ή ½ πάχους ορθογωνίου παρ/µου (m) R ακτίνα κυλινδρικού δοχείου (m) N o SV = log τιµή αποστείρωσης (sterilization value) N t χρόνος (s) t L χρόνος υστέρησης όπως ορίζεται στην εξίσωση (7.6) (s) t min ελάχιστος χρόνος παραµονής στους σωλήνες ασηπτικής διεργασίας (s) T θερµοκρασία ( C ή F) Τ g θερµoκρασία του τροφίµου στο τέλος της θέρµανσης (έναρξη της ψύξης) ( C ή F) U συνολικός συντελεστής µεταφοράς θερµότητας (W/m 2 C) 215
224 U v v χρόνος θερµικού θανάτου στη θερµοκρασία του αποστειρωτήρα όπως ορίζεται από την εξίσωση 7.30 (s) ταχύτητα ρευστού (m/s) µέση ταχύτητα ρευστού (m/s) v max µέγιστη ταχύτητα ρευστού (m/s) V όγκος (m 3 ) V p όγκος προϊόντος (m 3 ) w x z µαζική ροή (kg/s) πάχος τοιχώµατος (m) σταθερά θερµικής αντίστασης ( C ή F) αδιάστατοι αριθµοί Bi αριθµός Biot: hd p / Gr αριθµός Grashof: d ρ gβ T / η Nu αριθµός Nusselt: hd / k Pr αριθµός Prandtl: cpη / k Re αριθµός Reynolds: ρdv / η k είκτες c ψύξη cw νερό ψύξης h θέρµανση ΙΤ αρχική τιµή m θερµαντικό µέσο o αρχική κατάσταση ή θερµοκρασία 250 F RT αποστειρωτήρα s επιφάνεια τροφίµου T στη θερµοκρασία Τ ref στη θερµοκρασία αναφοράς Βιβλιογραφία Brennan J.G, Butters J.R., Cowell N.D. and Lilly A.E.V. (1976) Food Engineering Operations, 2 nd ed., Applied Science Publishers Ltd., London, pp Heldman D.R. and Singh R.P. (1981) Food Process Engineering, 2 nd ed., The AVI Publishing Co. Inc., Westport, Connecticut, pp Holdsworth S.D. (1997) Thermal Processing of Packaged Foods, Blackie Academic and Professional, London. Κουµούτσος Ν. Λυγερού Β. (1991) Μεταφορά Θερµότητας, Εκδόσεις ΕΜΠ, σελ
225 Lund D. (1975) Heat processing in Physical Principles of Food Preservation, ed. O. Fennema, Marcel Dekker Ink., N.Y., pp Lund D.B. and Singh R.K. (1993) The system and its elements in Principles of Aseptic Processing and Packaging, 2 nd ed., ed. J.V. Champers and P.E. Nelson, The Food Processors Institute, Washington, D.C., pp Merson R.L., Sing R.P. and Carroad P.A. (1978) An evaluation of Ball s formula method of thermal process calculations Food Technol. 32:66. National Canners Association (1968) Laboratory Manual for Food Canners and Processors, Vol. 1, Westport, AVI, pp. 336 Palmer J.A. and JonesV.A. (1976) Prediction of holding times for continuous thermal processing of power-law fluids J. Food Sci. 41: Σαραβάκος Γ. (1979) Τεχνική Θερµικών ιεργασιών, Β Έκδοση, Αθήνα, σελ Singh R.K. (1993) Residence time distribution in aseptic processing in Principles of Aseptic Processing and Packaging, 2 nd ed., ed. J.V. Champers and P.E. Nelson, The Food Processors Institute, Washington, D.C., pp Stoforos N.G. (1995) Thermal process design Food Control 6(2):81. Stoforos N.G., Noronha J., Hendrickx M. and Tobback P. (1997) A critical analysis of mathematical procedures for the evaluation and design of in-container thermal processes of foods Crit. Rev. Food Sci. Nutr. 37(5):411. Stumbo C.R. (1973) Thermobacteriology in Food Processing, 2 nd ed., Academic Press, N.Y. Ταούκης Π. (1997) Επιστήµη και Τεχνική των Τροφίµων Σηµειώσεις από τις Παραδόσεις, Αθήνα, σελ Toledo R.T. (1980) Fundamentals of Food Process Engineering, The AVI Publishing Co. Inc., Westport, Connecticut, pp Zechman L.G. and Pflug I.J. (1989) Location of the slowest heating zone for naturalconvection-heating fluids in metal containers J. Food Sci. 54:
226 218
227 ΚΕΦΑΛΑΙΟ 8 ΚΑΤΑΨΥΞΗ Εισαγωγή Η συντήρηση µε κατάψυξη στηρίζεται στη µείωση της ανάπτυξης και δράσης των µικροοργανισµών όσο µειώνεται η θερµοκρασία. Παθογόνοι και µη παθογόνοι µικροοργανισµοί αδρανοποιούνται πλήρως στους 18 C, ενώ πολλοί πεθαίνουν. Επίσης όσο χαµηλότερη είναι η θερµοκρασία τόσο βραδύτερα εξελίσσονται οι διάφορες ενζυµικές και χηµικές δράσεις που συµβαίνουν στο τρόφιµο. Ορισµένες ενζυµικές δράσεις συνεχίζονται ακόµα και σε θερµοκρασία 30 C γι αυτό συνίσταται το ζεµάτισµα ορισµένων τροφίµων πριν την κατάψυξη. Επί πλέον της επίδρασης της µείωσης της θερµοκρασίας η κατάψυξη µέσω της κρυστάλλωσης του νερού στο τρόφιµο µειώνει το ποσό του υγρού διαθέσιµου νερού και έτσι επιβραδύνει και µε αυτό τον τρόπο την ανάπτυξη µικροοργανισµών και την ενζυµική δραστηριότητα. Οι βασικές τεχνολογικές εξελίξεις στην κατάψυξη των τροφίµων έχουν συντελεσθεί τον τελευταίο αιώνα και πρόσφατα η µέθοδος αυτή βρίσκει όλο και ευρύτερη εφαρµογή. Για να παραχθεί κατεψυγµένο τρόφιµο άριστης ποιότητας επιλέγονται νωπά τρόφιµα αντίστοιχης ποιότητας τα οποία καταψύχονται στην επιθυµητή θερµοκρασία χρησιµοποιώντας διάφορα συστήµατα καταψύξεως και στη συνέχεια φυλάσσονται σε θαλάµους οι οποίοι πρέπει να διατηρούνται σε σταθερή θερµοκρασία µε τις µικρότερες δυνατές διακυµάνσεις. Για το σχεδιασµό ενός συστήµατος κατάψυξης πρέπει κατ αρχήν να εκτιµηθούν οι ενεργειακές απαιτήσεις ή αλλιώς η µεταβολή ενθαλπίας του τροφίµου κατά την κατάψυξη. Αυτή η µεταβολή εξαρτάται από το ίδιο το τρόφιµο το οποίο καταψύχεται. Ο δεύτερος σηµαντικός παράγοντας για ένα τέτοιο σύστηµα είναι ο ρυθµός µε τον οποίο προχωρεί η κατάψυξη του τροφίµου. Ο ρυθµός κατάψυξης σχετίζεται µε τις ενεργειακές απαιτήσεις τη διαφορά θερµοκρασίας µεταξύ του τροφίµου και του µέσου κατάψυξης και τις ιδιότητες του τροφίµου. Ο ρυθµός κατάψυξης επηρεάζει τον τρόπο σχηµατισµού του πάγου και εποµένως τις ιδιότητες και την ποιότητα του προϊόντος. Επίσης ο ρυθµός κατάψυξης καθορίζει και το ρυθµό παραγωγής µιας µονάδας κατάψυξης, εποµένως είναι επιθυµητός ο ταχύτερος ρυθµός κατάψυξης εφόσον δεν υποβαθµίζεται η ποιότητα του προϊόντος. 219
228 Σχηµατισµός κρυστάλλων πάγου Ο τρόπος που σχηµατίζονται οι κρύσταλλοι του πάγου κατά την κατάψυξη ενός τροφίµου έχει µεγάλη σηµασία λόγω της επίδρασης του µεγέθους των κρυστάλλων στην ποιότητα του προϊόντος. Ο σχηµατισµός του πάγου προχωρά σε δύο στάδια: (α) την πυρηνογένεση ή το σχηµατισµό του αρχικού κρυστάλλου και (β) την αύξηση του µεγέθους του κρυστάλλου. Η πυρηνογένεση είναι το εναρκτήριο στάδιο το οποίο περικλείει την παρουσία ή το σχηµατισµό των πυρήνων που θα αποτελέσουν τα κέντρα των κρυστάλλων που θα σχηµατισθούν. Μπορεί να ορισθεί ως η γένεση, σε ένα µετασταθές σύστηµα ή φάση, µικρών σωµατιδίων µίας νέας σταθερής φάσης τα οποία µπορούν να µεγαλώνουν αυτοφυώς. υνητικά µπορεί να συµβούν δύο τύποι πυρηνογένεσης η οµογενής και η ετερογενής. Η πρώτη περίπτωση συµβαίνει σπανιώτερα, σε συστήµατα όπως το πολύ καθαρό νερό, όπου οι πυρήνες αποτελούνται από τυχαίες συναθροίσεις ικανών µορίων νερού. Η οµογενής πυρηνογένεση στο νερό δεν ξεκινά στους 0 C, αλλά σε αρκετά χαµηλότερη θερµοκρασία. Η µείωση της θερµοκρασίας κάτω του σηµείου πήξης χωρίς τον σχηµατισµό κρυστάλλων καλείται υπέρψηξη (supercooling). Στην ετερογενή πυρηνογένεση µικρότατα σωµατίδια που υπάρχουν µέσα στο υγρό δρουν σαν πυρήνες για την εκκίνηση του σχηµατισµού των κρυστάλλων. Στα διαλύµατα ετερογενής πυρηνογένεση δηµιουργείται επίσης από τοπικές διακυµάνσεις της συγκέντρωσης της διαλυµένης ουσίας αλλά και από µηχανικά αίτια (δυνάµεις κρούσης). Και η ετερογενής πυρηνογένεση συνήθως συµβαίνει αφού η θερµοκρασία του υγρού µειωθεί κάτω από το σηµείο πήξης, αλλά είναι πιο πιθανή από την οµογενή πυρηνογένεση. Προσωρινή υπέρψηξη µέχρι και 10 C έχει παρατηρηθεί σε µεγάλα βιολογικά δείγµατα. Ο ρυθµός της πυρηνογένεσης παίζει σηµαντικό ρόλο στο µέγεθος και τη δοµή των κρυστάλλων που θα διαµορφωθούν. Η δηµιουργία λίγων πυρήνων οδηγεί στο σχηµατισµό λίγων και µεγάλων κρυστάλλων πάγου, ενώ η δηµιουργία πολλών πυρήνων οδηγεί σε µεγάλο αριθµό µικρών κρυστάλλων. Εποµένως το µέγεθος των κρυστάλλων εξαρτάται άµεσα από το ρυθµό πυρηνογένεσης. Η επίδραση της θερµοκρασίας στο ρυθµό πυρηνογένεσης στην κατάψυξη φαίνεται στο σχήµα 8.1. Η πυρηνογένεση αρχίζει µετά από κάποια χαρακτηριστική µείωση της θερµοκρασίας κάτω του σηµείου πήξης και ο ρυθµός της αυξάνεται ταχύτατα καθώς µειώνεται περαιτέρω η θερµοκρασία. Εποµένως ο ταχύς ρυθµός πυρηνογένεσης και η δηµιουργία πολλών µικρών κρυστάλλων σχετίζεται άµεσα µε τον ταχύ ρυθµό µείωσης της θερµοκρασίας κάτω του σηµείου πήξης ή µε τον ταχύ ρυθµό κατάψυξης. Το δεύτερο στάδιο είναι η αύξηση του µεγέθους των κρυστάλλων του πάγου, η οποία µπορεί να συµβεί µόνον αφού σχηµατισθούν οι πυρήνες και περάσουν ένα κρίσιµο µέγεθος. Ο ρυθµός αύξησης του µεγέθους των κρυστάλλων εξαρτάται από το 220
229 ρυθµό διάχυσης των µορίων του νερού από το διάλυµα στην επιφάνεια του κρυστάλλου, το ρυθµό µε τον οποίο εναποτίθενται τα µόρια του νερού στην επιφάνεια του κρυστάλλου και το ρυθµό αποµάκρυνσης της θερµότητας. Η θερµότητα που πρέπει να αποµακρυνθεί είναι η θερµότητα κρυστάλλωσης. Η επίδραση της θερµοκρασίας στο ρυθµό αύξησης του µεγέθους των κρυστάλλων φαίνεται επίσης στο σχήµα 8.1. Η αύξηση του µεγέθους των κρυστάλλων ξεκινά σε θερµοκρασίες πολύ κοντά στο σηµείο πήξης και ο ρυθµός της αυξάνεται πολύ λιγότερο µε µείωση της θερµοκρασίας από ότι ο ρυθµός πυρηνογένεσης. Σε πολύ χαµηλές θερµοκρασίες το ιξώδες του διαλύµατος αυξάνεται πολύ και ο ρυθµός αύξησης του µεγέθους των κρυστάλλων µειώνεται. Σχήµα 8.1. Επίδραση της υπέρψυξης στο ρυθµό πυρηνογένεσης και αύξησης του µεγέθους των κρυστάλλων του πάγου. (Fennema and Powrie, 1964) Εποµένως, όπως φαίνεται από το σχήµα 8.1, εάν η απαγωγή θερµότητας είναι βραδεία και το τρόφιµο παραµείνει για µεγάλο χρονικό διάστηµα µεταξύ των 0 C και του σηµείου Α οι κρύσταλλοι που δηµιουργούνται θα µεγαλώσουν σηµαντικά. Αντίθετα, µε ταχεία απαγωγή θερµότητας η θερµοκρασία του τροφίµου θα µειωθεί γρήγορα κάτω του σηµείου Α και θα σχηµατισθούν πολλοί κρύσταλλοι µικρού µεγέθους. Συµπερασµατικά το µέγεθος των κρυστάλλων του πάγου και η ποιότητα του κατεψυγµένου τροφίµου µπορεί να ελεγχθεί µέσω του ρυθµού απαγωγής θερµότητας. Ο ρυθµός απαγωγής θερµότητας επηρεάζει και το χώρο (εσωκυτταρικό ή εξωκυτταρικό) όπου σχηµατίζονται οι κρύσταλλοι του πάγου στο τρόφιµο που καταψύχεται. Ο χώρος σχηµατισµού των κρυστάλλων εξαρτάται επίσης από τη θερµοκρασία του δείγµατος και τη φύση των κυττάρων. Η κρυστάλλωση στους περισσότερους ιστούς έχει παρατηρηθεί ότι αρχίζει στον εξωκυτταρικό χώρο ανεξάρτητα από το ρυθµό κατάψυξης. Η συνέχιση της διεργασίας µπορεί να περιλαµβάνει είτε σχηµατισµό κρυστάλλων αποκλειστικά στον εξωκυτταρικό χώρο, είτε σχηµατισµό κρυστάλλων και στον εσωκυτταρικό χώρο µέσω πυρηνογένεσης στο 221
230 εσωτερικό του κυττάρου ή µέσω αύξησης του µεγέθους των εξωκυτταρικών κρυστάλλων δια µέσου της κυτταρικής µεµβράνης η οποία σχίζεται. Ο βραδύς ρυθµός κατάψυξης ευνοεί τον σχηµατισµό κρυστάλλων στον εξωκυτταρικό χώρο. Με τον σχηµατισµό των αρχικών κρυστάλλων η συγκέντρωση των διαλυτών συστατικών στον εξωκυτταρικό χώρο αυξάνει και διαχέεται νερό από το εσωτερικό του κυττάρου (που βρίσκεται σε κατάσταση υπέρψυξης) προς τον εξωκυτταρικό χώρο, όπου και εναποτίθεται στους εξωκυτταρικούς κρυστάλλους. Η αφυδάτωση αυτή του κυττάρου προκαλεί αύξηση των διαλυµένων συστατικών και περαιτέρω ταπείνωση του σηµείου πήξης µε αποτέλεσµα να ελαχιστοποιείται η πιθανότητα πυρηνογένεσης µέσα στο κύτταρο. Η συνέχιση της κατάψυξης οδηγεί σε µεγάλους εξωκυτταρικούς κρυστάλλους και συρρίκνωση των κυττάρων, η οποία µπορεί να είναι µη αντιστρεπτή κατά την απόψυξη. Ιδιαίτερα στην περίπτωση της ρήξης των κυτταρικών µεµβρανών καταστρέφεται η υφή των ιστών και συµβαίνει απώλεια κυτταρικού χυµού κατά την απόψυξη. Αντίθετα όταν η κατάψυξη γίνει µε ταχύ ρυθµό παράγονται οµοιόµορφοι µικροί κρύσταλλοι στον εσωκυτταρικό και εξωκυτταρικό χώρο, η µετακίνηση του νερού ελαχιστοποιείται, η µικροσκοπική εικόνα των παγωµένων ιστών είναι παρόµοια µε την αρχική και η ποιότητα του τροφίµου µετά την απόψυξη είναι ανώτερη. Ένα άλλο σηµαντικό φαινόµενο για την ποιότητα των κατεψυγµένων τροφίµων είναι η ανακρυστάλλωση. Οι κρύσταλλοι πάγου που σχηµατίζονται στο κατεψυγµένο τρόφιµο είναι ασταθείς και επηρεάζονται από τις διακυµάνσεις της θερµοκρασίας κατά την αποθήκευση. Η ανακρυστάλλωση οφείλεται στην τάση του συστήµατος να µειώσει την ελεύθερη ενέργειά του, η οποία ελαχιστοποιείται στην κρυσταλλική φάση όταν η δοµή της προς όλες τις κατευθύνσεις είναι τέλεια και το µέγεθός της άπειρο. Η ανακρυστάλλωση στα κατεψυγµένα τρόφιµα περιλαµβάνει µεταβολή της επιφάνειας και της εσωτερικής δοµής των κρυστάλλων, µετανάστευση µορίων από τους µικρούς κρυστάλλους στους µεγαλύτερους και συνένωση µικρών κρυστάλλων. Οι δύο τελευταίες περιπτώσεις έχουν ως συνέπεια την αύξηση του µεγέθους των κρυστάλλων Ο ρυθµός ανακρυστάλλωσης είναι µεγάλος σε θερµοκρασίες κοντά στο αρχικό σηµείο κατάψυξης και µειώνεται δραστικά σε πολύ χαµηλές θερµοκρασίες. Η ανακρυστάλλωση µπορεί να ελεγχθεί αποτελεσµατικά διατηρώντας χαµηλή και σταθερή θερµοκρασία κατά την αποθήκευση των κατεψυγµένων τροφίµων. Ιδιότητες των κατεψυγµένων τροφίµων Οι ιδιότητες του τροφίµου και ιδιαίτερα οι θερµικές ιδιότητες µεταβάλλονται κατά την κατάψυξη. Οι ιδιότητες του νερού µεταβάλλονται σηµαντικά καθώς αλλάζει 222
231 κατάσταση και µετατρέπεται από υγρό σε στερεό (πάγο) και επηρεάζουν τις ιδιότητες του τροφίµου που µεταβάλλονται και αυτές σηµαντικά µε την κατάψυξη. Οι εµπειρικές σχέσεις για τον προσδιορισµό των ιδιοτήτων των τροφίµων, που αναπτύχθηκαν στο κεφάλαιο 5, χρησιµοποιούνται και στα κατεψυγµένα τρόφιµα, διακρίνοντας τα συστατικά τους σε στερεά, νερό και πάγο. Εποµένως πρέπει να είναι γνωστό το ποσοστό νερού του τροφίµου που έχει µετατραπεί σε πάγο για να προσδιορισθούν οι ιδιότητες του. Οι ιδιότητες των λοιπών στερεών συστατικών δεν µεταβάλλονται πολύ στο θερµοκρασιακό εύρος 0 C έως 40 C και συνήθως µπορούµε να θεωρήσουµε τις µέσες τιµές αυτών στους υπολογισµούς. Η πυκνότητα, η θερµική αγωγιµότητα και η ειδική θερµότητα του µη κατεψυγµένου ή του κατεψυγµένου τροφίµου µεταβάλλονται λίγο µε τη θερµοκρασία εφόσον δεν αλλάζει το ποσοστό νερού σε υγρή κατάσταση και πάγου, αλλά µεταβάλλονται µε τη µετάβαση από τη µία κατάσταση στην άλλη και σχετίζονται άµεσα µε το ποσοστό νερού και πάγου. Ταπείνωση σηµείου πήξης Τα τρόφιµα περιέχουν σχετικά µεγάλες ποσότητες νερού στο οποίο είναι διαλυµένα διάφορα συστατικά. Εποµένως το σηµείο έναρξης της πήξης του νερού στο τρόφιµο θα είναι χαµηλότερο από αυτό του καθαρού νερού. Το µέγεθος ταπείνωσης του σηµείου πήξης εξαρτάται από το µοριακό βάρος και τη συγκέντρωση των διαλυµένων συστατικών στο νερό. Το σηµείο πήξης ενός διαλύµατος (Τ Α ) σε σχέση µε το σηµείο πήξης του καθαρού διαλύτη (Τ Αο ), εκφρασµένα σε απόλυτη θερµοκρασία, δίνεται από τη σχέση: λ 1 1 = ln X A = ln( 1 Xsi) (8.1) R TAo TA όπου λ λανθάνουσα θερµότητα πήξης του διαλύτη (J/mole) R=8.314 J/mole K Χ Α µοριακό κλάσµα του διαλύτη στο διάλυµα X si µοριακά κλάσµατα των διαλυµένων συστατικών στο διάλυµα Για αραιά διαλύµατα όπου ΣX si <<1 και για µικρή διαφορά θερµοκρασίας (T Ao - T A ) η εξίσωση (8.1) απλοποιείται σε: RT 2 Ao TAo TA = X si λ (8.2) 223
232 Η εξίσωση (8.2) για ένα διάλυµα ενός συστατικού γραµµοµοριακότητας m (moles της διαλυµένης ουσίας ανά kg διαλύτη) µπορεί να διατυπωθεί ως: 2 RTAo M Am TF = TAo TA = (8.3) 1000L όπου L λανθάνουσα θερµότητα πήξης ανά µονάδα µάζας (kj/kg) R εκφρασµένο ανά µονάδα µάζας (J/g Κ) M A µοριακό βάρος του διαλύτη. Με την εξίσωση (8.2) ή (8.3) µπορεί να υπολογισθεί το σηµείο έναρξης της κατάψυξης ενός τροφίµου. Στην εξίσωση (8.3) όλοι οι παράγοντες του δεξιού σκέλους, εκτός της γραµµοµοριακότητας m αποτελούν την κρυοσκοπική σταθερά, ή µοριακή ταπείνωση του σηµείου πήξης (β), η οποία για το νερό υπολογίζεται β=1.86 kg K/mole. Για τα περισσότερα πραγµατικά διαλύµατα η ταπείνωση του σηµείου πήξης δεν ακολουθεί τις ιδανικές εξισώσεις, εκτός εάν οι συγκεντρώσεις των διαλυµένων στερεών είναι πολύ µικρές. Στα πραγµατικά διαλύµατα µέρος του νερού δεσµεύεται στα στερεά συστατικά, δεν µπορεί να δράσει ως διαλύτης και δεν καταψύχεται σε οποιαδήποτε θερµοκρασία. Το ποσό του δεσµευµένου νερού για οποιοδήποτε συστατικό εξαρτάται από τη συγκέντρωση και τη θερµοκρασία. Με βάση το δεσµευµένο νερό έχει προταθεί η ακόλουθη εξίσωση για την ταπείνωση του σηµείου ψύξης: β 1 BYsi T = ln M 1 BY + EY w si si (8.4) όπου Β δεσµευµένο νερό ανά kg στερεών (kg νερού/kg ξηρών στερεών) Y si κλάσµα µάζας των στερεών (υγρή βάση) M w µοριακό βάρος του νερού Ε λόγος των µοριακών βαρών (M w /M si ) Για διαλύµατα έχουν προταθεί και άλλες εξισώσεις, παρόµοιες µε την (8.4), µε εµπειρικές σταθερές που εξαρτώνται από τη συγκέντρωση των διαλυµένων συστατικών. Επίσης για διάφορες κατηγορίες τροφίµων έχουν προταθεί εµπειρικές σχέσεις µε βάση την προσαρµογή στα πειραµατικά δεδοµένα. Οι Chang & Tao (1981) πρότειναν για κρέατα: T = (8.5) Y w για λαχανικά και φρούτα: T = Y Y 2 (8.6) w w για χυµούς: 2 T = Y w Yw (8.7) Ο Rahman (1995) πρότεινε: 224
233 για κρέατα: T = ( Y 1)/( Y ) (8.8) w w για ιχθυρά: T = ( Y 1)/( Y ) (8.9) w w όπου Y w κλάσµα µάζας του νερού (υγρή βάση) Με ανάλογο τρόπο οι Chen & Nagy (1987, από Rahman, 1995) απέδωσαν το Τ ως πολυωνυµική συνάρτηση τρίτου βαθµού του κλάσµατος µάζας των στερεών συστατικών µε σταθερές που µεταβάλλονται για τα διάφορα τρόφιµα ή τις διαλυµένες ουσίες (σε περίπτωση υδατικών διαλυµάτων). Καθώς το νερό αρχίζει να καταψύχεται η συγκέντρωση των διαλυµένων συστατικών στο νερό που έχει παραµείνει σε υγρή κατάσταση συνεχώς αυξάνεται προκαλώντας επί πλέον ταπείνωση του σηµείου πήξης του µη κατεψυγµένου τµήµατος. Εποµένως η θερµοκρασία πήξης στο τρόφιµο συνεχώς µειώνεται έως το ευτηκτικό σηµείο, σε αντίθεση µε το νερό, όπως φαίνεται στο σχήµα 8.2. Σε ένα διάλυµα ενός συστατικού η απαγωγή θερµότητας µετά το ευτηκτικό σηµείο δεν συνεπάγεται µείωση της θερµοκρασίας, αλλά κρυστάλλωση της διαλυµένης ουσίας παράλληλα µε το σχηµατισµό κρυστάλλων πάγου µέχρι την πλήρη κρυστάλλωση όλου του διαλύµατος. Στην πραγµατικότητα στα τρόφιµα συνήθως υπάρχουν περισσότερες από µία διαλυµένες ουσίες και εποµένως εµφανίζονται περισσότερα του ενός ευτηκτικά σηµεία, τα οποία δεν είναι εµφανή. Η µάζα του νερού που παραµένει σε υγρή φάση σε οποιαδήποτε θερµοκρασία T χαµηλότερη του σηµείου έναρξης κατάψυξης µπορεί να υπολογισθεί µέσω της εξίσωσης (8.1). Σηµαντικές αποκλίσεις εµφανίζονται σε τρόφιµα τα οποία έχουν µεγάλη ποσότητα δεσµευµένου νερού. Σε αυτή την περίπτωση το συνολικό νερό σε υγρή φάση µπορεί κατά προσέγγιση να αποδοθεί από το άθροισµα του υπολογιζόµενου από την εξίσωση (8.1) και του δεσµευµένου νερού. Σχήµα 8.2. Σύγκριση καµπυλών ψύξης για καθαρό νερό και υδατικό διάλυµα ενός συστατικού. 225
234 Επίσης έχει προταθεί ο υπολογισµός του κλάσµατος νερού που παραµένει σε υγρή φάση µέσω της απλοποιηµένης σχέσης: Y Y w wo TF = T (8.10) όπου Y w, Y wo κλάσµα µάζας του νερού στη θερµοκρασία Τ ( C) και πριν την έναρξη της κατάψυξης, αντίστοιχα T F η θερµοκρασία έναρξης κατάψυξης ( C) Άλλες προτεινόµενες σχέσεις στηρίζονται στο διάγραµµα φάσεων ή στην εξίσωση Clausius-Clapeyron και στο νόµο Raoult, όπως: Y Y L M R T T L M R T T wo 1 exp( w Fw w / )( 1/ Fw 1/ F ) exp( Fw w / )( 1/ Fw 1/ ) = 1 Y 1 exp( L M / R)( 1/ T 1/ T) exp( L M / R)( 1/ T 1/ T ) Y Y w wo wo BY BY so so T = T [ ][ ] [ Fw w Fw ][ Fw w Fw F ] Fw Fw TF T (8.11) (8.12) όπου L Fw λανθάνουσα θερµότητα πήξης του νερού στο τρόφιµο σε θερµοκρασία T F (kj/kg) T Fw σηµείο πήξης του νερού (Κ) Η συνεχής αύξηση της συγκέντρωσης των διαλυµένων συστατικών όσο προχωρεί η κατάψυξη προκαλεί και σηµαντικές µεταβολές των φυσικοχηµικών ιδιοτήτων της µη κατεψυγµένης φάσης, όπως του ph, της οξύτητας, της ιοντικής ισχύος, του ιξώδους, της επιφανειακής και διεπιφανειακής τάσης και του δυναµικού οξειδοαναγωγής. Επίσης µπορεί να αποβληθεί διαλυτό οξυγόνο ή διοξείδιο του άνθρακα. Η αύξηση της συγκέντρωσης και η µεταβολή του ph µπορεί να προκαλέσουν την καταβύθιση συστατικών που βρίσκονται σε κολλοειδή διασπορά. Μεταβολή ενθαλπίας κατά την κατάψυξη Όπως ήδη αναφέρθηκε για το σχεδιασµό ενός συστήµατος κατάψυξης χρειάζεται η γνώση των ενεργειακών απαιτήσεων ή αλλιώς της θερµότητας που πρέπει να αποµακρυνθεί για τη µείωση της θερµοκρασίας του τροφίµου στο επιθυµητό επίπεδο. Η συνολική µεταβολή της ενθαλπίας του τροφίµου ( Η, kj/kg) που απαιτείται για να µειωθεί η θερµοκρασία του, από κάποια τιµή ψηλότερη του σηµείου έναρξης πήξης στην επιθυµητή θερµοκρασία αποθήκευσης, µπορεί να εκφρασθεί ως άθροισµα των επί µέρους µεταβολών της ενθαλπίας διαφόρων φάσεων ή καταστάσεων: H = Hso + H w + H L + HI (8.13) όπου Η so η µεταβολή ενθαλπίας των στερεών συστατικών του τροφίµου 226
235 Η w η µεταβολή ενθαλπίας του νερού που παραµένει σε υγρή κατάσταση Η L η µεταβολή ενθαλπίας λόγω της λανθάνουσας θερµότητας Η Ι η µεταβολή ενθαλπίας του πάγου Λόγω των διαλυµένων συστατικών στο νερό που υπάρχει στο τρόφιµο υπάρχει µία συνεχής ταπείνωση του σηµείου πήξης όπως αναπτύχθηκε παραπάνω και εποµένως η µάζα του νερού που αποµένει σε υγρή κατάσταση και η µάζα του πάγου που σχηµατίζεται µεταβάλλονται καθώς µειώνεται η θερµοκρασία. Η µεταβολή ενθαλπίας των στερεών συστατικών του τροφίµου από µία αρχική θερµοκρασία Τ ΙΤ σε µία τελική Τ, χαµηλότερη του σηµείου έναρξης κατάψυξης (Τ F ) δίνεται από την εξίσωση: ή: ( ) H = Y c T T + Y c T T (8.14) H H IT so so so IT F so so F ( ) dh = Y c T T + Y c dt (8.15) so so so IT F so so T T F Ο υπολογισµός των τριών άλλων όρων που εκφράζουν τις µεταβολές ενθαλπίας της εξίσωσης (8.13) δεν είναι εύκολος δεδοµένου ότι µεταβάλλεται τόσο η µάζα του νερού και του πάγου σε θερµοκρασία κάτω του σηµείου Τ F, όσο και η ειδική θερµότητα του νερού που έχει παραµείνει σε υγρή κατάσταση και του πάγου. Ο κάθε ένας από αυτούς τους όρους µπορεί εποµένως να εκφρασθεί ως: H F ( ) w( ) w( ) (8.16) H = dh = Y c T T + Y Tc TdT w w wo w IT F H IT T T HL = YI( T) Lw( T) (8.17) H = dhi = Y( Tc ) ( TdT ) (8.18) I H 0 TF T I I Εποµένως για τον υπολογισµό της µεταβολής της ενθαλπίας απαιτείται η συσχέτιση του κατεψυγµένου και µη κατεψυγµένου νερού µε τη θερµοκρασία και των ειδικών θερµοτήτων αυτών. Όσον αφορά στην ειδική θερµότητα του πάγου αυτή µπορεί να θεωρηθεί σταθερή για σχετικά µικρές µεταβολές της θερµοκρασίας. Επίσης η εξάρτηση της ειδικής θερµότητας όλων των συστατικών από τη θερµοκρασία µπορεί να εκφρασθεί όπως στον Πίνακα 5.5. Οι υπολογισµοί ειδικής θερµότητας και ενθαλπίας µπορούν να γίνουν και µε σχέσεις όπως οι (5.22) - (5.28). Ο υπολογισµός του ποσοστού του κατεψυγµένου και µη κατεψυγµένου νερού σε οποιαδήποτε θερµοκρασία χαµηλότερη του σηµείου έναρξης της κατάψυξης µπορεί να γίνει µέσω των εξισώσεων (8.1) και (8.10) - (8.12). Για την εξάρτηση της λανθάνουσας θερµότητας από τη θερµοκρασία µπορούν να χρησιµοποιηθούν οι σχέσεις (5.30) ή (5.31). 227
236 Ο βασικός περιορισµός στην εφαρµογή αυτής της προσέγγισης για τον υπολογισµό της µεταβολής της ενθαλπίας κατά την κατάψυξη ενός τροφίµου είναι η πολυπλοκότητα του ίδιου του τροφίµου το οποίο περιέχει πολλά διαλυµένα συστατικά και η έλλειψη επαρκούς γνώσης για τις διαλυµένες ουσίες που υπάρχουν στο κάθε τρόφιµο και το βαθµό που επηρεάζει κάθε µια την ταπείνωση του σηµείου πήξης. Εάν υπάρχουν διαθέσιµα πειραµατικά δεδοµένα για την ταπείνωση του σηµείου πήξης η εξίσωση (8.1) µπορεί να χρησιµοποιηθεί για τον υπολογισµό του µοριακού κλάσµατος του διαλύτη και µέσω αυτού ενός φαινόµενου µοριακού κλάσµατος της διαλυµένης ουσίας. Θεωρώντας ένα αντιπροσωπευτικό µοριακό βάρος για τις διαλυµένες ουσίες που ευθύνονται για την ταπείνωση του σηµείου πήξης µπορεί να υπολογισθεί από το µοριακό κλάσµα του διαλύτη (νερού) η µάζα αυτού που παραµένει σε υγρή κατάσταση και εποµένως και η µάζα που έχει µετατραπεί σε πάγο. Σχήµα 8.3. Ενθαλπία βοδινού κρέατος σε διάφορες περιεκτικότητες νερού και θερµοκρασίες. (Heldman and Singh, 1981) 228
237 Η µεταβολή της ενθαλπίας κατά την κατάψυξη διαφόρων τροφίµων έχει µετρηθεί πειραµατικά µε χρήση αδιαβατικού θερµιδοµέτρου και τα αποτελέσµατα έχουν παρουσιασθεί σε νοµογραφήµατα ενθαλπίας περιεκτικότητας σε υγρασία όπως δείχνει αντιπροσωπευτικά το σχήµα 8.3. Σε αυτό δίνεται η ενθαλπία βοδινού κρέατος συναρτήσει της περιεκτικότητας σε υγρασία για εύρος θερµοκρασιών µεταξύ 40 C και 40 C ενώ παράλληλα παρουσιάζεται και το ποσοστό του νερού που έχει καταψυχθεί. Η επιλογή των 40 C ως θερµοκρασίας βάσης στηρίζεται στο γεγονός ότι αµελητέα ποσότητα νερού καταψύχεται κάτω από αυτή τη θερµοκρασία και το νερό που παραµένει σε υγρή κατάσταση αποτελεί το δεσµευµένο νερό του τροφίµου. Αντίστοιχα νοµογραφήµατα έχουν αναπτυχθεί και για άλλα τρόφιµα. Τιµές ενθαλπίας διαφόρων τροφίµων σε θερµοκρασίες χαµηλότερες των 0 C δίνονται στον Πίνακα 8.1. Απαγωγή θερµότητας-υπολογισµός χρόνου κατάψυξης Βασικές εξισώσεις Υπάρχουν δύο προσεγγίσεις για τη διατύπωση της απαγωγής θερµότητας κατά την κατάψυξη. Η πρώτη στηρίζεται στη συνεχή µεταβολή της πυκνότητας (ρ), της ειδικής θερµότητας (c) και του συντελεστή θερµικής αγωγιµότητας (k) του τροφίµου και είναι η περισσότερο ρεαλιστική. Σύµφωνα µε αυτή, η µεταβολή της θερµοκρασίας στα διάφορα σχήµατα θα ακολουθεί τις κλασσικές εξισώσεις (6.1) και (6.3) όπου τα k, ρ και c µεταβάλλονται µε τη θερµοκρασία. Για πλάκα (x= -R έως x=r) π.χ. η εξίσωση µε τις οριακές και αρχικές της συνθήκες γίνεται: T ρ( TcT ) ( ) ( ) t x T = x για -R<x<R και t>0 (8.19) T ht ( m T) = kt ( ) x σε x= -R για t>0 (8.20) T ht ( m T) = kt ( ) x σε x=r για t>0 (8.21) T = 0 x σε x=0 για t>0 (8.22) T=T IT για -R x R σε t=0 (8.23) Η δεύτερη δέχεται ένα κινούµενο µέτωπο κατάψυξης και µεταβολή των ιδιοτήτων του τροφίµου από τη µη κατεψυγµένη στην κατεψυγµένη κατάσταση. Οι εξισώσεις που προκύπτουν σύµφωνα µε αυτή την προσέγγιση για πλάκα είναι: 2 T T ρscs = k s 2 για -R<x<x s -R και t>0 t x (8.24) 2 T T ρlcl = kl 2 για x s -R<x<0 και t>0 t x (8.25) 229
238 ht ( T k T m ) = σε x= -R για t>0 (8.26) x T = 0 σε x=0 για t>0 (8.27) x s ρs L dx T T = kl k s dt x x σε x=x s -R για t>0 (8.28) x + x s s x s =0, T=T IT για -R x R σε t=0 (8.29) k=k s εάν x s >0 και k=k l εάν x s =0 (8.30) Οι δείκτες l και s αναφέρονται στη µη κατεψυγµένη και στην κατεψυγµένη φάση, αντίστοιχα. Η εξίσωση (8.28) εκφράζει την οριακή συνθήκη για το κινούµενο µέτωπο κατάψυξης που βρίσκεται σε απόσταση x s από την επιφάνεια και οι όροι x s +, x s - συµβολίζουν τις θέσεις σε απειροστά µικρή απόσταση εκατέρωθεν του µετώπου. Με αντίστοιχο τρόπο µπορούν να διατυπωθούν οι εξισώσεις και για τα άλλα βασικά σχήµατα. Η επίλυση της εξίσωσης (8.19) γίνεται µε αριθµητικές µεθόδους. Στην προσέγγιση του κινούµενου µετώπου κατάψυξης µπορεί να ακολουθηθεί αναλυτική επίλυση για τα βασικά σχήµατα και σταθερές εξωτερικές συνθήκες, ενώ για ακανόνιστα σχήµατα ή αν οι συνθήκες αλλάζουν µε το χρόνο χρειάζονται αριθµητικές µέθοδοι. Οι εξισώσεις αγωγής θερµότητας έχουν επιλυθεί για διάφορα προϊόντα ακανόνιστου σχήµατος και καλύπτουν µε ικανοποιητική ακρίβεια όλες τις περιπτώσεις των σχηµάτων που απαντώνται συνήθως. Για απλοποίηση των υπολογισµών έχουν προταθεί εµπειρικές µέθοδοι που στηρίζονται στις αναλυτικές αλλά χρησιµοποιούν ορισµένες απλοποιητικές παραδοχές. Ρυθµός κατάψυξης-πρόρρηση χρόνου κατάψυξης Ο ρυθµός µε τον οποίο καταψύχεται ένα τρόφιµο καθορίζει την δοµή και την ποιότητα του τροφίµου, όπως ήδη αναφέρθηκε, αλλά και το χρόνο που απαιτείται για να καταψυχθεί το τρόφιµο ο οποίος είναι βασική παράµετρος για το σχεδιασµό του συστήµατος. Για τον ρυθµό κατάψυξης έχουν διατυπωθεί διάφοροι ορισµοί µε σηµαντικές διαφορές. Το ιεθνές Ινστιτούτο Κατάψυξης (International Institute of Refrigeration) πρότεινε το 1971 τον ακόλουθο ορισµό: «Ο ρυθµός κατάψυξης µιας µάζας τροφίµου είναι ο λόγος της ελάχιστης απόστασης από την επιφάνεια έως το θερµικό κέντρο προς το χρόνο που µεσολαβεί από τη στιγµή που η επιφάνεια φθάσει τους 0 C έως τη στιγµή που η θερµοκρασία του θερµικού κέντρου θα γίνει 5 C χαµηλότερη από την αρχική θερµοκρασία σχηµατισµού πάγου στο θερµικό κέντρο. Όπου η απόσταση µετράται σε cm και ο χρόνος σε h, ο ρυθµός κατάψυξης θα εκφράζεται σε cm/h». Τέσσερις παράγοντες επηρεάζουν το ρυθµό κατάψυξης: (α) η διαφορά θερµοκρασίας µεταξύ του τροφίµου και του µέσου ψύξης, (β) οι τρόποι µεταφοράς 230
239 θερµότητας από το τρόφιµο προς το µέσο ψύξης και µέσα στο ίδιο το τρόφιµο, (γ) το µέγεθος, το σχήµα και οι θερµικές ιδιότητες του τροφίµου και (δ) το µέγεθος, ο τύπος και το σχήµα της συσκευασίας του τροφίµου, εάν είναι συσκευασµένο. Η βασική δυσκολία στην επίλυση των εξισώσεων για το ρυθµό µεταφοράς θερµότητας και την πρόβλεψη του ρυθµού κατάψυξης και του χρόνου κατάψυξης έγκειται στην εξάρτηση της ειδικής θερµότητας της πυκνότητας και της θερµικής αγωγιµότητας του τροφίµου από τη θερµοκρασία, η οποία είναι σηµαντική στη ζώνη κατάψυξης ή σε θερµοκρασίες χαµηλότερες από το αρχικό σηµείο κατάψυξης του τροφίµου. Οι αναλυτικές και εµπειρικές µέθοδοι που χρησιµοποιούνται για την πρόρρηση του ρυθµού κατάψυξης και του χρόνου που απαιτείται για την κατάψυξη ενός τροφίµου περιέχουν απλοποιητικές παραδοχές, όπως σταθερές τιµές των θερµικών ιδιοτήτων µε τη θερµοκρασία, για την επίτευξη προσεγγιστικών λύσεων. Η εξίσωση Plank Ο Plank (1913) διατύπωσε µία εξίσωση για τον υπολογισµό του χρόνου κατάψυξης η οποία µπορεί να χρησιµοποιηθεί για προϊόντα διαφόρων γεωµετρικών σχηµάτων. Η εξίσωση στηρίζεται στη µεταφορά θερµότητας κατά µία διεύθυνση όπως φαίνεται στο σχήµα 8.4 για ένα στερεό µε σχήµα πλάκας πάχους d. Το ισοζύγιο θερµότητας εκφράζεται από την εξίσωση: AL dx AT ( m TF) ρ = (8.31) dt 1/ h+ x/ k όπου Α επιφάνεια εναλλαγής θερµότητας (m 2 ) L λανθάνουσα θερµότητα πήξης (J/kg στερεού) ρ πυκνότητα του στερεού (kg/m 3 ) Τ m θερµοκρασία του ψυκτικού µέσου ( C) T F σηµείο έναρξης κατάψυξης ( C) h συντελεστής µεταφοράς θερµότητας από την επιφάνεια του τροφίµου προς το ψυκτικό µέσο (W/m 2 C) k συντελεστής αγωγής θερµότητας δια µέσου της κατεψυγµένης φάσης (W/m C) Το διαφορικό dx/dt αντιπροσωπεύει την ταχύτητα του µετώπου κατάψυξης. O πρώτος όρος της εξίσωσης (8.31) εκφράζει τη θερµότητα που παράγεται στο µέτωπο κατάψυξης και ο δεύτερος τη µεταφορά θερµότητας µε αγωγή δια µέσου του κατεψυγµένου τµήµατος του τροφίµου και συναγωγή, αγωγή ή ακτινοβολία από την επιφάνεια του τροφίµου προς το µέσο κατάψυξης. Με ολοκλήρωση προκύπτει η ακόλουθη εξίσωση για το χρόνο κατάψυξης: 2 ρl d d t F = + (8.32) T T 2h 8k F m 231
240 Το d είναι το πάχος της πλάκας (m) και µε την εισαγωγή κατάλληλων σταθερών λαµβάνεται η γενική µορφή της εξίσωσης Plank: 2 ρl Pd Rd t F = + T T h k F m κατεψυγµένο τµήµα (8.33) µη κατεψυγµένο τµήµα Τ T m T S T F T S x d Σχήµα 8.4. Σχηµατική απεικόνιση µονοδιάστατης κατάψυξης σε πλάκα πάχους d. Οι σταθερές P και R εξαρτώνται από το σχήµα και σύµφωνα µε την εξίσωση (8.32) σε πλάκα ισούνται µε 1/2 και 1/8 αντίστοιχα. Για κύλινδρο απείρου µήκους παίρνουν τις τιµές P=1/4 και R=1/16 και για σφαίρα P=1/6 και R=1/24, µε d τη διάµετρο του κυλίνδρου ή της σφαίρας. Εποµένως η εξίσωση Plank στη γενική της µορφή εµπεριέχει τον παράγοντα σχήµατος και είναι προφανές από τις τιµές που παίρνουν οι σταθερές ότι εάν πλάκα πάχους d, κύλινδρος διαµέτρου d και σφαίρα διαµέτρου d εκτεθούν στις ίδιες συνθήκες θα έχουν χρόνους κατάψυξης ανάλογους προς 6:3:2. Αυτή η αναλογία συµφωνεί µε τον παράγοντα σχήµατος V/AR που αναφέρθηκε στην ψύξη. Στην πραγµατικότητα αυτή η σχέση µεταξύ των τριών σχηµάτων έχει πολύ ευρύτερη εφαρµογή από την εξίσωση του Plank και µπορεί να χρησιµοποιηθεί για την εφαρµογή οποιασδήποτε µεθόδου πρόρρησης από το ένα σχήµα στο άλλο. Ο Cleland µε περισσότερες από 100 δοκιµές που κάλυπταν µεγάλο εύρος συνθηκών προσδιόρισε την αναλογία χρόνων κατάψυξης και τα διαστήµατα εµπιστοσύνης σε επίπεδο 95% : πλάκας/σφαίρα =3.02±0.20 πλάκας/κύλινδρο=2.01±0.07 κυλίνδρου/σφαίρα=1.50±
241 Εποµένως η αναλογία 6:3:2 είναι ικανοποιητική για να εφαρµοσθεί µία οµοιόµορφη προσέγγιση για τα τρία σχήµατα. Όταν η εξίσωση Plank εφαρµόζεται σε τρόφιµο ορθογώνιου σχήµατος πρέπει να χρησιµοποιηθεί για τον προσδιορισµό των σταθερών ένα νοµογράφηµα όπως αυτό του σχήµατος 8.5. Σ αυτή την περίπτωση η διάσταση d της εξίσωσης Plank είναι η µικρότερη διάσταση του ορθογωνίου. Η σταθερά β 1 είναι το πηλίκο της αµέσως µεγαλύτερης διάστασης του ορθογωνίου προς το d και η σταθερά β 2 το πηλίκο της µεγαλύτερης διάστασης του ορθογωνίου προς το d. Σχήµα 8.5. Προσδιορισµός των σταθερών P και R της εξίσωσης Plank σε τρόφιµο ορθογωνίου σχήµατος. (Heldman and Singh, 1981) H εξίσωση Plank είναι η πιο γνωστή απλοποιηµένη αναλυτική µέθοδος για την πρόρρηση του χρόνου κατάψυξης. Οι βασικές απλοποιητικές παραδοχές της είναι οι ακόλουθες: Η εξίσωση χρησιµοποιεί µία τιµή λανθάνουσας θερµότητας πήξης και δεν λαµβάνει υπ όψιν ότι η απαγωγή της λανθάνουσας θερµότητας γίνεται σε ένα θερµοκρασιακό εύρος κατά την κατάψυξη του τροφίµου. Η τιµή του συντελεστή θερµικής αγωγιµότητας θεωρείται επίσης σταθερή, ενώ καθώς µεταβάλλεται η 233
242 θερµοκρασία της κατεψυγµένης ζώνης κατά τη διεργασία και ο συντελεστής θερµικής αγωγιµότητας αυτής µεταβάλλεται. Επίσης η εξίσωση λαµβάνει υπ όψιν τη µεταφορά θερµότητας µετά την επίτευξη του αρχικού σηµείου κατάψυξης του τροφίµου και δεν υπολογίζει το χρόνο που απαιτείται για την απαγωγή θερµότητας πριν την κατάψυξη. Παρ όλα αυτά η εξίσωση Plank είναι µια απλή εξίσωση που έχει αποδεκτή ακρίβεια στον υπολογισµό του χρόνου κατάψυξης µε την προϋπόθεση το τρόφιµο να βρίσκεται αρχικά στη θερµοκρασία έναρξης της κατάψυξής του. Τροποποιήσεις της εξίσωσης Plank (εµπειρικές µέθοδοι) Τροποποιήσεις και βελτιώσεις της εξίσωσης έχουν προταθεί από διάφορους ερευνητές, ώστε να συνυπολογισθεί και η απαγωγή θερµότητας πριν από το σηµείο έναρξης κατάψυξης: ρ H Pd t F = + T T h F m Rd k 2 (8.34) Ο όρος Η εκφράζει τη συνολική µεταβολή της ενθαλπίας από την αρχική θερµοκρασία στην οποία βρίσκεται το τρόφιµο έως την τελική. Για την κατάψυξη ψαριών η µεταβολή αυτή της ενθαλπίας µπορεί να υπολογισθεί από την εξίσωση (Nagaoka et al, 1955): [ IT F ][ l IT F s F ] H = +, ( T T ) c ( T T ) + L+ c ( T T) (8.35) όπου Τ IT και Τ, η αρχική και τελική θερµοκρασία του τροφίµου αντίστοιχα. Επίσης η µεταβολή της ενθαλπίας στην εξίσωση (8.34) για διάφορα τρόφιµα µπορεί να υπολογισθεί προσεγγιστικά από πίνακες που υπάρχουν στη βιβλιογραφία, όπως ο Πίνακας 8.1 ή από εµπειρικές εξισώσεις, όπως έχει αναφερθεί. Αν και η τροποποιηµένη εξίσωση που προκύπτει λαµβάνει υπ όψιν την απαγωγή θερµότητας πριν από το σηµείο έναρξης κατάψυξης και σε χαµηλότερες θερµοκρασίες από αυτό, στηρίζεται και πάλι στην παραδοχή ότι η λανθάνουσα θερµότητα αποµακρύνεται σε σταθερή θερµοκρασία και οι θερµικές ιδιότητες είναι σταθερές. Η αριθµητική επίλυσή των εξισώσεων αγωγής θερµότητας για τον προσδιορισµό του χρόνου κατάψυξης και η σύγκριση των αποτελεσµάτων µε εκείνα που προέκυψαν από την τροποποιηµένη εξίσωση του Plank έδειξε ότι η εξίσωση του Plank µπορεί να οδηγήσει σε σφάλµα υπολογισµού το µέγεθος του οποίου εξαρτάται από την αρχική θερµοκρασία του τροφίµου πριν την κατάψυξη. Έχουν επίσης προταθεί αρκετές εµπειρικές µέθοδοι, οι περισσότερες από τις οποίες αποτελούν τροποποιήσεις της εξίσωσης Plank. Οι εµπειρικές σχέσεις χρησιµοποιούν συνήθως αδιάστατους αριθµούς, ώστε να έχουν ευρύτερη εφαρµογή. Οι θερµικές ιδιότητες εµπεριέχονται στους αδιάστατους αριθµούς, έτσι ώστε µία σχέση που προκύπτει από δεδοµένα για ένα τρόφιµο σε ορισµένες συνθήκες να 234
243 µπορεί θεωρητικά να εφαρµοσθεί και σε άλλα. Η εξίσωση (8.34) µπορεί να γραφεί σε αδιάστατη µορφή ως: 1 1 Fo = P + R Bi*Ste Ste (8.36) όπου Fo = αt F /d 2 (αριθµός Fourier) (8.37) Bi = hd/k (αριθµός Biot ) (8.38) Ste = c s (T F -T m )/ Η (αριθµός Stephan) (8.39) και α ο συντελεστής θερµικής διαχυτότητας. Εισάγοντας ένα νέο αδιάστατο αριθµό, τον αριθµό Plank µπορεί να εισαχθεί και η επίδραση της απαγωγής θερµότητας πριν το αρχικό σηµείο κατάψυξης: Pk = c l (T IT -T F )/ H (αριθµός Plank) (8.40) και Fo= f (Bi, Ste, Pk) (8.41) Οι Cleland και Earle (1977, 1979) µέσω πειραµατικών µετρήσεων και στατιστικής ανάλυσης των αποτελεσµάτων έδωσαν τις ακόλουθες ηµιεµπειρικές εξισώσεις για τους παράγοντες P και R της εξίσωσης (8.36): Για πλάκα: P= Pk+Ste(0.3224Pk Bi ) (8.42) R= Ste(0.274Pk ) (8.43) Για κύλινδρο: P= Pk+Ste(0.4008Pk+0.071Bi ) (8.44) R= Ste(0.0415Pk ) (8.45) Για σφαίρα: P= Pk+Ste(0.231Pk Bi ) (8.46) R= Ste(0.0386Pk ) (8.47) Οι εξισώσεις (8.42) - (8.47) ισχύουν για αρχική θερµοκρασία τροφίµου µέχρι 40 C, θερµοκρασία ψυκτικού µέσου µεταξύ 15 C και 45 C και εύρος των αριθµών: Ste Bi 10 για πλάκες και 0.5 Bi 4.5 για κυλίνδρους και σφαίρες 0 Pk 0.55 Για περιεχόµενο υγρασίας περίπου 77% παρουσιάζουν ακρίβεια ±3% για πλάκες, ±5.2% για κυλίνδρους και ±3.8% για σφαίρες. 235
244 Πίνακας 8.1. Ενθαλπία κατεψυγµένων τροφίµων (Πηγή: Heldman and Singh, 1981) Προϊόν Υγρασία Μέση α Θερµοκρασία C % (νωπού) ειδική θερµότητα kj/kg Φρούτα και λαχανικά Αγγούρι Ενθαλπία (kj/kg) % υγρό νερό Αρακάς Ενθαλπία (kj/kg) % υγρό νερό Αχλάδι Ενθαλπία (kj/kg) % υγρό νερό αµάσκηνο β Ενθαλπία (kj/kg) % υγρό νερό Καρότο Ενθαλπία (kj/kg) % υγρό νερό Κεράσι β Ενθαλπία (kj/kg) % υγρό νερό Κρεµµύδι Ενθαλπία (kj/kg) % υγρό νερό Μήλο πολτός Ενθαλπία (kj/kg) % υγρό νερό Ροδάκινο β Ενθαλπία (kj/kg) % υγρό νερό Σπανάκι Ενθαλπία (kj/kg) % υγρό νερό Σπαράγγι Ενθαλπία (kj/kg) % υγρό νερό Τοµατοπολτό ς Ενθαλπία (kj/kg) % υγρό νερό Φράουλα Ενθαλπία (kj/kg) % υγρό νερό Φραµπουάζ Ενθαλπία (kj/kg) % υγρό νερό Αυγά Ασπράδι Ενθαλπία (kj/kg) % υγρό νερό Κρόκος Ενθαλπία (kj/kg) % υγρό νερό Ολόκληρα γ Ενθαλπία (kj/kg) % υγρό νερό Κρέατα και Ιχθυρά Μπακαλιάρος Ενθαλπία (kj/kg) % υγρό νερό Πέρκα Ενθαλπία (kj/kg) % υγρό νερό Βοδινό φρέσκο δ Ενθαλπία (kj/kg) % υγρό νερό Βοδινό αφυδατωµένο Ενθαλπία (kj/kg) % υγρό νερό Ψωµί Λευκό Ενθαλπία (kj/kg) % υγρό νερό - Ολικής άλεσης Ενθαλπία (kj/kg) % υγρό νερό α Μέση τιµή µεταξύ 4 C και 32 C, εκτός των κρεάτων µεταξύ 0 C και 20 C και του κρόκου αυγού µεταξύ 20 C και 40 C. β Χωρίς πυρήνα. γ Υπολογισµένο µε βάση 58 % ασπράδι (86.5 % νερό) και 32 % κρόκο (50 % νερό). Τα δεδοµένα για µοσχάρι και κοτόπουλο πλησιάζουν πολύ αυτά του βοδινού για την ίδια περιεκτικότητα σε υγρασία 236
245
246 Επίσης οι ίδιοι ερευνητές (Cleland και Earle, 1984) έδωσαν µια πιο γενικευµένη εξίσωση για το χρόνο κατάψυξης και για τα τρία βασικά σχήµατα: 2 H 10 Pd Rd 1.65N Ste T Tm t = + F 1 ln E( T F Tm ) h k s k s Tref Tm όπου: (8.48) P=0.5[ Pk+Ste(0.2296Pk )] (8.49) R=0.125[1.202+Ste(3.410Pk )] (8.50) H 10 µεταβολή ενθαλπίας από T F σε -10 C (J/m 3 ) T τελική θερµοκρασία στο θερµικό κέντρο T ref θερµοκρασία αναφοράς = -10 C Ε=1 για πλάκα, 2 για κύλινδρο απείρου µήκους και 3 για σφαίρα. Μία άλλη εµπειρική διόρθωση της εξίσωσης Plank η οποία συνυπολογίζει το χρόνο µέχρι το σχηµατισµό πάγου, το χρόνο κατάψυξης του τροφίµου και το χρόνο ψύξης του κατεψυγµένου τροφίµου µέχρι την τελική θερµοκρασία είναι η προσέγγιση Pham: t F = όπου T V ha 1 = cl ( TIT T T1 Fav ) ( T w sf Fav av ( 1+ Bi / 6) + ( 1+ Bi / 4) + ( 1+ Bi / 6) 1 ( TIT Tm )( TFav Tm ) ln[( T T ) / ( T T )] IT m Fav m L T 2 2 c T T 3 ) 3 (8.51) (8.52) Bi 1 = 0.5( hd / k s + hd / k l ) (8.53) T2 = TFav Tm (8.54) Bi 2 = Bi 3 = hd / k s (8.55) ( TFav Tm )( Tav Tm ) T3 = ln[( T T ) / ( T T )] (8.56) Fav m av m TFav = TF 15. (8.57) T = T ( T T )/( 2+ 4/ N 3 ) (8.58) av fin fin m Bi Η Τ Fav υπολογίζεται και µέσω µιας εξίσωσης µε ολοκλήρωση που δίνει καλύτερη προσέγγιση λόγω της βαθµιαίας αλλαγής φάσης. Όταν το προϊόν που θα καταψυχθεί είναι συσκευασµένο ο συντελεστής (h) στις παραπάνω εξισώσεις αντικαθίσταται από ένα συνολικό συντελεστή µεταφοράς θερµότητας (U) που συµπεριλαµβάνει και την αντίσταση στη µεταφορά θερµότητας δια µέσου του υλικού συσκευασίας: 1 U = (8.59) xp 1 + kp h 238
247 όπου x p, το πάχος και k p, ο συντελεστής θερµικής αγωγιµότητας του υλικού συσκευασίας. Εξοπλισµός Οι καταψυκτήρες που χρησιµοποιούνται για τα τρόφιµα διακρίνονται σε τρεις τύπους: (α) τους καταψυκτήρες µε προσφύσηση αέρα, (β) τους καταψυκτήρες επαφής µε στερεές επιφάνειες και (γ) τους καταψυκτήρες εµβάπτισης σε υγρά ή ψεκασµού µε υγρά. Kαταψυκτήρες µε προσφύσηση αέρα Οι καταψυκτήρες αυτού του τύπου χρησιµοποιούν ψυχρό αέρα σε διάφορες ταχύτητες και έχουν διαφορετικό σχεδιασµό ανάλογα µε τα προϊόντα που πρόκειται να καταψυχθούν. Χρησιµοποιούνται ευρύτατα στη βιοµηχανία λόγω της ευελιξίας χρήσης τους για διάφορα προϊόντα. Η θερµοκρασία του αέρα κυµαίνεται µεταξύ 20 C και 40 C και η ταχύτητά του σε ευρύτατα όρια από 0.5 έως 18 m/s. Το ρεύµα αέρα δηµιουργείται από ισχυρούς ανεµιστήρες και διέρχεται από τα καταψυχόµενα προϊόντα κατ αντιρροή ή εγκάρσια προς αυτά. Η µεταφορά θερµότητας από την επιφάνεια του τροφίµου προς τον αέρα γίνεται µε συναγωγή και ο επιφανεικός συντελεστής εξαρτάται από τη ροή και την ταχύτητα του αέρα. Η τιµή του σε κάθε περίπτωση µπορεί να υπολογισθεί από εµπειρικές εξισώσεις ή από πίνακες της βιβλιογραφίας. Γενικά στους καταψυκτήρες µε προσφύσηση αέρα κυµαίνεται µεταξύ 10 και 67 W/m 2 C. Καταψυκτήρες ασυνεχούς λειτουργίας χρησιµοποιούνται σε µονάδες µικρής δυναµικότητας. Αποτελούνται από µονωµένους θαλάµους που φέρουν τα ψυκτικά στοιχεία και τους απαραίτητους ανεµιστήρες. Τα προϊόντα φορτώνονται συνήθως χειρωνακτικά σε τελάρα ή δίσκους που είναι προσαρµοσµένα σε κυλιόµενα φορεία, τα οποία µετακινούνται µέσα στο θάλαµο πάνω σε ράγες-οδηγούς. Σε µεγαλύτερες µονάδες χρησιµοποιούνται συστήµατα συνεχούς λειτουργίας που είτε αποτελούνται από µία σήραγγα µέσω της οποίας διακινείται το τρόφιµο µε κατάλληλη διάταξη, είτε χρησιµοποιούν την αρχή της ρευστοαιώρησης. Στις σήραγγες κατάψυξης τα προϊόντα µεταφέρονται είτε σε κυλιόµενα φορεία µε ράφια προωθούµενα µηχανικά, είτε πάνω σε διάτρητες µεταφορικές ταινίες, είτε, στην περίπτωση τεµαχίων κρέατος µεγάλων διαστάσεων, αναρτηµένα από ράγες στην οροφή. Μία διάταξη µε κυλιόµενα φορεία απεικονίζεται σχηµατικά στο σχήµα 8.6. Στην περίπτωση που χρησιµοποιείται µεταφορική ταινία, αντί για κυλιόµενα φορεία µε ράφια, απαιτείται µεγάλο µήκος της ταινίας µέσα στο θάλαµο. Για εξοικονόµηση 239
248 χώρου χρησιµοποιείται κατάλληλη ελικοειδής διάταξη, όπως π.χ. του σχήµατος 8.7. Οι µεταφορικές ταινίες κατασκευάζονται συνήθως από µεταλλικό πλέγµα. Σχήµα 8.6. Σήραγγα κατάψυξης µε προσφύσηση αέρα. 1: Ψυκτικά στοιχεία, 2: Ανεµιστήρες, 3: Φορεία µε προϊόντα, 4: Μεταφορική διάταξη, 5: Θύρες εισόδουεξόδου, 6: Κενός χώρος υπό το δάπεδο. (Θωµόπουλος, 1981) Σχήµα 8.7. Καταψυκτήρας προσφύσησης αέρα µε ελικοειδή µεταφορική ταινία. 1: Ψυκτικά στοιχεία, 2: Πρώτος κύλινδρος µε ανοδική πορεία της µεταφορικής ταινίας, 3: εύτερος κύλινδρος µε καθοδική πορεία της µεταφορικής ταινίας, 4: Έξοδος, 5: ιάταξη αυτόµατου πλυσίµατος της ταινίας, 6: Στεγνωτήριο, 7: Ρυθµιστής κίνησης και τάσης της ταινίας, 8: Κύλινδρος αναστροφής. (Brennan et al, 1976) Για την κατάψυξη τροφίµων µικρού µεγέθους (µπιζέλια, κύβοι καρότου, γαρίδες κ.ά.) χωρίς να κολλούν µεταξύ τους χρησιµοποιείται ρευστοστερεά κλίνη. Τα τρόφιµα µεταφέρονται σε διάτρητο ιµάντα και η ρευστοαιώρηση επιτυγχάνεται µε εµφύσηση αέρα µε µεγάλη ταχύτητα εγκάρσια από το κάτω µέρος του ιµάντα (σχ. 240
249 8.8). Φρούτα και λαχανικά καταψύχονται µε αυτή τη µέθοδο εντός 3 έως 5 min γι αυτό και χρησιµοποιείται εµπορικά ο όρος IQF: instant quick frozen. Σχήµα 8.8. Σχηµατική απεικόνιση καταψυκτήρα ρευστοστερεάς κλίνης. (Brennan et al, 1976) Καταψυκτήρες επαφής µε στερεές επιφάνειες Οι καταψυκτήρες αυτοί αποτελούνται από κοίλες πλάκες στο εσωτερικό των οποίων κυκλοφορεί το ψυκτικό υγρό και ανάµεσα στις οποίες πιέζονται τα προς κατάψυξη τρόφιµα. Χρησιµοποιούνται κυρίως για στερεά τρόφιµα συσκευασµένα σε λεπτά χάρτινα κιβώτια. Οι καταψυκτήρες αυτού του τύπου έχουν µικρότερη απαίτηση σε χώρο και µικρότερη κατανάλωση ισχύος σε σύγκριση µε τους καταψυκτήρες µε προσφύσηση αέρα. Η λειτουργία τους µπορεί να είναι ασυνεχής ή συνεχής. Οι καταψυκτήρες µε οριζόντιες πλάκες ασυνεχούς λειτουργίας φέρουν επάλληλες πλάκες και τα προϊόντα φορτώνονται σε µεταλλικούς δίσκους µε διαστάσεις κατάλληλες ώστε να χρησιµοποιηθεί αποτελεσµατικά όλη η επιφάνεια των πλακών (σχ. 8.9). Μετά τη φόρτωση οι πλάκες κλείνουν µε υδραυλικό έµβολο και διατηρείται µία χαµηλή πίεση (10-30 kn/m 2 ) κατά τη διάρκεια της κατάψυξης για να εξασφαλίζει καλή επαφή των πλακών µε τα προϊόντα. Η απόσταση µεταξύ των πλακών καθορίζεται µε ράβδους για να αποφευχθεί η µηχανική κάκωση των προϊόντων σε περίπτωση εσφαλµένου κλεισίµατος. Καταψυκτήρες µε κατακόρυφες πλάκες ασυνεχούς λειτουργίας (σχ. 8.10) είναι κατάλληλοι για ψύξη µη συσκευασµένων τροφίµων όπως ψαριών και κρέατος. Τα τρόφιµα τροφοδοτούνται απευθείας ανάµεσα στις πλάκες και σχηµατίσουν συµπαγή στερεά κοµµάτια. Μετά το πέρας της διεργασίας οι πλάκες θερµαίνονται για να αποκολληθούν τα κατεψυγµένα τρόφιµα και ταυτόχρονα να καθαριστούν οι επιφάνειες των πλακών. 241
250 Σχήµα 8.9. Σχηµατική απεικόνιση καταψυκτήρα µε οριζόντιες πλάκες. Α: Έµβολο µετακίνησης των πλακών, Β: Κοίλες ψυχόµενες πλάκες, C: Προϊόντα, D: Ράβδος για ρύθµιση της απόστασης, Ε: ίσκοι, F: Μόνωση. (Brennan et al, 1976) Σχήµα Καταψυκτήρας µε κατακόρυφες πλάκες. Α: Ψυκτικές πλάκες, Β: Θέσεις φόρτωσης, C: Χειριστήριο υδραυλικής ρύθµισης, D: Έµβολο µετακίνησης των πλακών, Ε: Μηχανισµός εκφόρτωσης, F: Έµβολο ανύψωσης του µηχανισµού εκφόρτωσης, G: Σωλήνες κυκλοφορίας του ψυκτικού υγρού. (Brennan et al, 1976) 242
251 Στα συνεχή συστήµατα οι πλάκες φορτώνονται και εκφορτώνονται ανά στοιβάδα µε κατάλληλες διατάξεις. Τα προϊόντα τροφοδοτούνται µε µεταφορικό ιµάντα ανάµεσα σε δύο πλάκες και µετά την κατάψυξη εκφορτώνονται, µε άνοιγµα των δύο πλακών, σε ιµάντα αποµάκρυνσης. Ο συντελεστής µεταφοράς θερµότητας µεταξύ των επιφανειών των πλακών και των τροφίµων πρέπει να είναι υψηλός και οµοιόµορφος για αποτελεσµατική λειτουργία. Αυτό εξασφαλίζεται µε καλή επαφή µεταξύ των επιφανειών και ανυπαρξία πάγου ή αποθεµάτων στις επιφάνειες των πλακών. Επίσης εξαρτάται από το σχεδιασµό των ίδιων των πλακών του καταψυκτήρα. Η χρήση πλακών από κράµατα αλουµινίου έχει βελτιώσει πολύ την αποτελεσµατικότητα των καταψυκτήρων. Ενδεικτικές τιµές συντελεστών µεταφοράς θερµότητας δίνονται στον πίνακα 8.2. Στους καταψυκτήρες επαφής µε στερεή επιφάνεια µπορούν να καταταχθούν και οι εναλλάκτες θερµότητας αποξεόµενης επιφάνειας ή τυµπάνου που χρησιµοποιούνται για την κατάψυξη ρευστών προϊόντων, όπως µίγµατος παγωτού, συµπυκνωµένων χυµών φρούτων και πολτών διαφόρων τροφίµων. Πίνακας 8.2. Επιφανειακοί συντελεστές µεταφοράς θερµότητας Ψυκτικό µέσο / συνθήκες Συντελεστής µεταφοράς θερµότητας (W/m 2 C) αέρας / φυσική κυκλοφορία 5 α αέρας / βεβιασµένη κυκλοφορία α,β ψυκτήρας πλακών 56 α ψυκτήρας πλακών αλουµινίου / ψύξη πλίνθου 481 γ χαλκού άλµη / βραδεία κυκλοφορία 56 α άλµη / βεβιασµένη κυκλοφορία 85 α, β υγρό άζωτο β υγρό άζωτο / κάτω επιφάνεια οριζόντιας πλάκας (σχηµατίζεται στρώµα αερίου) υγρό άζωτο / άνω επιφάνεια οριζόντιας πλάκας υγρό άζωτο / ψεκασµός freon R-12 (εξαρτάται από T s τροφίµου) 170 α, 200 β 425 α 175 β β (εξαρτάται από T s τροφίµου) freon R-12 / ψεκασµός 1190 β Πηγή α : Heldman and Singh, 1981, β : Singh and Mannapperuma, 1990, γ : Rahman,
252 Καταψυκτήρες επαφής µε υγρά (µε ψεκασµό ή εµβάπτιση) Η µέθοδος αυτή στηρίζεται στην άµεση επαφή του προϊόντος µε ένα ψυκτικό υγρό χαµηλής θερµοκρασίας που συνεπάγεται την ταχύτατη κατάψυξή του. Στην περίπτωση χρήσης υγρών µε πολύ χαµηλό σηµείο βρασµού χρησιµοποιείται ο όρος κρυογόνος κατάψυξη. Τα ψυκτικά µέσα που χρησιµοποιούνται στην κρυογόνο κατάψυξη είναι κυρίως το υγρό άζωτο (σ.β. 196 C) και δευτερευόντως το υγρό διοξείδιο του άνθρακα (σ.β. 78 C). Στις περισσότερες περιπτώσεις αξιοποιείται και η λανθάνουσα και η αισθητή θερµότητα του κρυογόνου µέσου µε διακίνηση του καταψυχόµενου προϊόντος κατ αντιρροή προς αυτό. Έτσι το προϊόν έρχεται αρχικά σε επαφή µε το ψυχρό αέριο και η θερµοκρασία του µειώνεται σηµαντικά πριν να έρθει σε επαφή µε το ψεκαζόµενο υγρό (σχήµα 8.11). Εµβάπτιση σε υγρό άζωτο δεν χρησιµοποιείται επειδή ο ρυθµός κατάψυξης δεν είναι ελεγχόµενος και δεν αξιοποιείται και η αισθητή θερµότητα του ψυκτικού µέσου. Ένα άλλο κρυογόνο µέσο που έχει χρησιµοποιηθεί είναι το Freon 12 ειδικής καθαρότητας µε σηµείο βρασµού 30 C. Λόγω της πολύ ψηλότερης τιµής του σηµείου βρασµού συνήθως το προϊόν εµβαπτίζεται αρχικά σε υγρό Freon 12 για επιφανειακή κατάψυξη και στη συνέχεια ψεκάζεται µε αυτό για την ολοκλήρωση της κατάψυξης. Η χρήση του Freon 12 έχει απαγορευθεί για περιβαλλοντικούς λόγους. Σχήµα ιαγραµµατική απεικόνηση καταψυκτήρα µε υγρό άζωτο. (Brennan et al, 1976) Εκτός της κρυογόνου κατάψυξης στην κατάψυξη µε εµβάπτιση χρησιµοποιούνται κυρίως αλατοδιαλύµατα, υδατικά διαλύµατα ζαχάρων και γλυκερίνης. Τα διαλύµατα αυτά ψύχονται µε καθ αυτό κρυογόνα. Στην κατάψυξη ασυσκεύαστων τροφίµων πρέπει το ψυκτικό υγρό να είναι συµβατό µε τη γεύση του τροφίµου. Συνήθως αλατοδιαλύµατα χρησιµοποιούνται για την κατάψυξη ψαριών και ζαχαροδιαλύµατα για την κατάψυξη φρούτων. Τα συσκευασµένα τρόφιµα καταψύχονται σε διατάξεις 244
253 συνεχούς λειτουργίας όπου τα δοχεία προωθούνται (περιστρεφόµενα για ταχύτερη µεταφορά θερµότητας) κατ αντιρροή προς το ψυκτικό υγρό. Το κύριο πρόβληµα στους καταψυκτήρες εµβάπτισης είναι η διατήρηση σταθερής πυκνότητας του ψυκτικού µέσου και η σταδιακή ρύπανσή του κατά τη χρήση. Η µεταφορά θερµότητας από την επιφάνεια του καταψυχόµενου τροφίµου σε αυτούς τους καταψυκτήρες γίνεται µε συναγωγή και οι συντελεστές µεταφοράς θερµότητας υπολογίζονται από εµπειρικές εξισώσεις όπως και στους καταψυκτήρες προσφύσησης αέρα η από πίνακες της βιβλιογραφίας. Ενδεικτικές τιµές κυµαίνονται µεταξύ 420 και 440 W/m 2 C για έντονα αναδευόµενο αλατοδιάλυµα. Πιο πολύπλοκο είναι το φαινόµενο µεταφοράς θερµότητας στην κρυογόνο κατάψυξη όπου τα υγρά βράζουν σε επαφή µε την επιφάνεια του τροφίµου. Ο ρυθµός απαγωγής θερµότητας σε αυτή την περίπτωση εξαρτάται από τη θερµοκρασία της επιφάνειας του τροφίµου. Οι συντελεστές µεταφοράς θερµότητας έχουν υπολογισθεί ως συνάρτηση της διαφοράς θερµοκρασίας µεταξύ της επιφάνειας του τροφίµου και της θερµότητας κορεσµού του κρυογόνου µέσου, και κυµαίνονται από 200 έως 5000 W/m 2 K για υγρό άζωτο και από 200 έως 8000 W/m 2 K για Freon 12. Αποθήκευση κατεψυγµένων τροφίµων Οι συνθήκες αποθήκευσης των κατεψυγµένων τροφίµων είναι εξ ίσου σηµαντικές για την ποιότητα αυτών µε την κατάψυξη. Ο στόχος της αποθήκευσης υπό κατάψυξη είναι να διατηρηθεί η θερµοκρασία στα επίπεδα που θα περιορίσουν το ρυθµό όλων των µεταβολών που υποβαθµίζουν την ποιότητα του τροφίµου. Στις χαµηλές θερµοκρασίες που χρησιµοποιούνται ( 18 ο C έως 40 ο C ) στην αποθήκευση κατεψυγµένων τροφίµων οι µικροβιακές δράσεις πρακτικά αναστέλλονται. Οι ενζυµικές και χηµικές δράσεις συνεχίζονται µε βραδύτερο ρυθµό όσο µειώνεται η θερµοκρασία, ενώ µπορεί να παρατηρηθούν και ορισµένες φυσικές µεταβολές, όπως κρυστάλλωση ή ανακρυστάλλωση του πάγου και απώλεια υγρασίας. Οι κύριες ενζυµικές δράσεις που υποβαθµίζουν την ποιότητα των κατεψυγµένων τροφίµων περιλαµβάνουν το ενζυµικό µαύρισµα και οι κύριες χηµικές δράσεις την οξείδωση των λιπαρών, την αλλοίωση αρωµατικών και χρωστικών συστατικών και τη µερική καταστροφή των βιταµινών. Λόγω µεταβολής του ph και αύξησης της συγκέντρωσης των αλάτων µπορεί να προκληθεί µερική αδιαλυτοποίηση των πρωτεϊνών. Επίσης καθίζηση ουσιών µε µικρή διαλυτότητα, όπως η λακτόζη. Τα µη συσκευασµένα τρόφιµα µπορεί να χάσουν πολλή υγρασία µε το χρόνο και να παρουσιάσουν κηλίδες που µοιάζουν µε εγκαύµατα. Για το λόγο αυτό προκειµένου για µακροχρόνια διατήρηση είναι απαραίτητη η συσκευασία µε υλικά µικρής διαπερατότητας σε υγρασία. 245
254 Λόγω των µεταβολών που αναφέρθηκαν η διάρκεια αποθήκευσης υπό κατάψυξη είναι περιορισµένη και εξαρτάται από τη θερµοκρασία. Υπάρχουν ενδεικτικοί πίνακες διάρκειας συντήρησης χωρίς σηµαντική υποβάθµιση της ποιότητας, για διάφορα τρόφιµα, σε διαφορετικές θερµοκρασίες. Παραδείγµατα 1. Μίγµα παγωτού έχει την ακόλουθη σύσταση: λιπαρά 10 %, στερεά γάλακτος µη λιπαρά 12 % εκ των οποίων λακτόζη (ΜΒ=342) 54.5 %, ζάχαρη (ΜΒ=342) 15 %, σταθεροποιητής 0.22 %. Να υπολογισθεί το σηµείο έναρξης κατάψυξης θεωρώντας τα ζάχαρα ως τα κύρια συστατικά που επηρεάζουν τη µείωση του σηµείου πήξης. Να υπολογισθεί ποιο ποσοστό νερού µένει στην υγρή φάση στους 20 C. Λύση Εάν θεωρήσουµε ότι κυρίως τα σάκχαρα επηρεάζουν το σηµείο πήξης και ότι η συγκέντρωση των σακχάρων στο νερό είναι αρκετά µικρή µπορούµε να χρησιµοποιήσουµε την εξίσωση (8.3) για τον υπολογισµό ταπείνωσης του σηµείου πήξης. Η γραµµοµοριακότητα του διαλύµατος ως προς τα σάκχαρα θα είναι m= m / M s s όπου m s η µάζα του κάθε σακχάρου που είναι διαλυµένη σε 1000 g νερού και M s το µοριακό βάρος του. Σύµφωνα µε τα δεδοµένα της σύστασης σε 100 g παγωτού περιέχονται 12x0.545=6.54 g λακτόζης, 15 g ζάχαρης και ( )=62.78 g νερού. ( / ) 1000 ( 15 / ) 1000 Άρα m = + = mole/kg διαλύτη Από την (8.3) µε γνωστή την κρυοσκοπική σταθερά του νερού β=1.86 προκύπτει TF = 186. m= = Εποµένως το σηµείο έναρξης κατάψυξης του παγωτού θα είναι C ή Κ. Το νερό που παραµένει σε υγρή φάση στους 20 C (253 K) µπορεί να υπολογισθεί µέσω της (8.1) θεωρώντας το δεσµευµένο νερό στα διάφορα συστατικού του παγωτού αµελητέο. λ (νερού)=6003 J/mole R=8.314 J/mole K ln X A = = = X A Εάν καλέσουµε m w τη µάζα του νερού ανά 100 g που παραµένει σε µη κατεψυγµένη κατάσταση στους 20 C, σύµφωνα µε τον ορισµό του µοριακού κλάσµατος θα ισχύει: mw / = mw = 487. g m / / 342 w 246
255 Άρα το ποσοστό του αρχικού νερού που µένει σε µη κατεψυγµένη κατάσταση είναι: = % Εναλλακτικά µπορεί να χρησιµοποιηθεί η εξίσωση (8.10) Yw T Y = F wo T = 187. = = 9. 35% και η ποσότητα νερού που παραµένει υγρή ανά g παγωτού θα είναι = 59. g H διαφορά αποτελέσµατος µε τους δύο υπολογισµούς είναι σχετικά µικρή. 2. Να υπολογισθεί η απαίτηση σε ψύξη για κατάψυξη 50 kg βοδινού κρέατος υγρασίας 74.5 % από 5 C σε 15 C. Τι ποσοστό τροφίµου είναι κατεψυγµένο στους -15 C; Λύση Μπορούµε να χρησιµοποιήσουµε το διάγραµµα (8.3) ή τον Πίνακα (8.1). Από το διάγραµµα (8.3) για περιεκτικότητα σε νερό 74.5 % βρίσκουµε: Ενθαλπία στους 5 C: 330 kj/kg Ενθαλπία στους 15 C: 55 kj/kg Συνολική απαίτηση σε ψύξη H m= ( ) 50 = kj Το ποσοστό του νερού που είναι κατεψυγµένο σύµφωνα µε το ίδιο διάγραµµα είναι 86 %. Αφού η συνολική περιεκτικότητα νερού ανέρχεται σε 74.5 % και το νερό είναι το µόνο συστατικό του κρέατος που καταψύχεται το ποσοστό του κρέατος που θα είναι κατεψυγµένο είναι: = %. Από τον Πίνακα 8.1. Ενθαλπία στους 5 C: = kj/kg Ενθαλπία στους 15 C: 55 kj/kg όπως προκύπτει µε γραµµική παρεµβολή. Συνολική απαίτηση σε ψύξη H m= ( ) 50 = kj Το ποσοστό του νερού που παραµένει µη κατεψυγµένο είναι 13.5 %, εποµένως το κατεψυγµένο ποσοστό θα είναι 86.5 %. Και το κατεψυγµένο ποσοστό του κρέατος: = %. 3. Φράουλες καταψύχονται σε καταψυκτήρα µε προσφύσηση αέρα θερµοκρασίας -35 C. Να υπολογισθεί ο απαιτούµενος χρόνος για την κατάψυξη του προϊόντος από τους 5 C στους 20 C αν θεωρηθεί ότι τα τεµάχια έχουν σχήµα σφαίρας µε µέση διάµετρο 2 cm. ίνονται: επιφανειακός συντελεστής συναγωγής h=80 W/m 2 C, θερµοκρασία έναρξης κατάψυξης -1.1 C, πυκνότητα φράουλας 1030 kg/m 3, συντελεστής αγωγής θερµότητας του κατεψυγµένου τµήµατος 1.85 W/m C. Εάν ο καταψυκτήρας φέρει ιµάντα συνεχούς λειτουργίας πλάτους 1.5 m και µήκους 6 m να υπολογισθεί η ταχύτητα του ιµάντα και η δυναµικότητα του καταψυκτήρα. Λύση Θα χρησιµοποιηθεί η τροποποιηµένη εξίσωση Plank (8.34). H Η θα υπολογισθεί από τον Πίνακα 8.1 Ενθαλπία στους 5 C: = kj/kg Ενθαλπία στους 20 C: 44 kj/kg H = kj/kg 247
256 (8.34): ( kg / m ) ( J / kg) 002. ( m) 002. ( m ) t F = o 2o + o = ( )( C) 6 80( W / m C) ( W / m C) 527.() 7 s = 88.(min) Οι φράουλες πρέπει να παραµείνουν στον καταψυκτήρα 8.8 min. εδοµένου ότι ο ιµάντας του καταψυκτήρα έχει µήκος 6 m η ταχύτητά του πρέπει να είναι: 6 = 068. m/min 88. Αν θεωρήσουµε ότι οι φράουλες διατάσσονται σε οµοιόµορφες σειρές στον ιµάντα στο πλάτος αυτού µπορούν να τοποθετηθούν τεµάχια και στην επιφάνεια 1-m µήκους ιµάντα 1 75 = 3750 τεµάχια / m ιµάντα ή 3750 π( d / 2) ρ = 3750 π( 0. 01) 1030 = kg/m ιµάντα 3 3 Με βάση την ταχύτητα ιµάντα που υπολογίσθηκε η δυναµικότητα θα είναι: = kg/min ή 660 kg/h 4. Βοδινό διαστάσεων 1x0.25x0.6 m καταψύχεται σε καταψυκτήρα µε προσφύσηση αέρα θερµοκρασίας 30 C (h=30 W/m 2 C). Η αρχική θερµοκρασία του βοδινού είναι 5 C. Να υπολογισθεί ο χρόνος που απαιτείται για κατάψυξη του προϊόντος στους 10 C α) µέσω της εξίσωσης Plank, β) µέσω της εξίσωσης Nagaoka et al. H µέση σύσταση του βοδινού να θεωρηθεί: νερό 74.5 %, πρωτεΐνες 20 %, λιπαρά 5.5 %. Λύση Για τον υπολογισµό µε βάση οποιαδήποτε από τις δύο εξισώσεις πρέπει να είναι γνωστή η πυκνότητα, το σηµείο έναρξης κατάψυξης και ο συντελεστής θερµικής αγωγιµότητας του κατεψυγµένου βοδινού. Με βάση τη σύσταση του βοδινού η πυκνότητα µπορεί κατά προσέγγιση να υπολογισθεί από τα δεδοµένα του Πίνακα 5.1 του κεφαλαίου 5: = + + ρ = 1055 kg/m 3 ρ O συντελεστής θερµικής αγωγιµότητας του νωπού βοδινού µπορεί να θεωρηθεί ίσος προς W/m C (Πίνακας 5.3, κεφάλαιο 5) και του κατεψυγµένου µε βάση τον εµπειρικό κανόνα k = 25. k = = 108. W/m C. ff f Η ταπείνωση του σηµείου πήξης µπορεί να εκτιµηθεί µε την εξίσωση (8.5) ή την εξίσωση (8.8) οπότε για Υ w =0.745 T = = 080. T = ( )/( ) = 087. Οι τιµές είναι παραπλήσιες και µπορούµε να δεχθούµε το µέσο όρο αυτών. Εποµένως Τ F = 0.84 C. Οι σταθερές της εξίσωσης Plank θα προσδιορισθούν µέσω του διαγράµµατος 8.5 για β 1 =0.6/0.25=2.4, β 2 =1.0/0.25=4 P=
257 R=0.085 Για την εφαρµογή της εξίσωσης Plank θα θεωρήσουµε σύµφωνα µε τον Πίνακα 8.1 ότι το 16 % του νερού παραµένει σε υγρή κατάσταση άρα το 84 % καταψύχεται. Εποµένως L = = kj/kg βοδινού t F = + + = s =15.5 h H εξίσωση Nagaoka υπολογίζει τη µεταβολή ενθαλπίας σύµφωνα µε τη σχέση (8.35). Η ειδική θερµότητα του βοδινού πριν την κατάψυξη µπορεί να ληφθεί από τον Πίνακα 8.1 c l = 3.52 kj/kg C Η ειδική θερµότητα του κατεψυγµένου τροφίµου είναι δύσκολο να υπολογισθεί µε ακρίβεια και µία πρώτη προσέγγιση σε τρόφιµα µε µεγάλη περιεκτικότητα νερού είναι να θεωρηθεί ίση µε την ειδική θερµότητα του πάγου. Ένας πιο ακριβής υπολογισµός µπορεί να γίνει µε βάση τη σύσταση του τροφίµου και τις µεταβολές της ειδικής θερµότητας των συστατικών µε τη θερµοκρασία, όπως δίνονται στον Πίνακα 5.5. Σύµφωνα µε τον Πίνακα 8.1 το ποσοστό του µη κατεψυγµένου νερού στο κατεψυγµένο βοδινό ( 10 C) ανέρχεται σε 16 % του ολικού νερού, εποµένως το ποσοστό του πάγου σε 84 % του ολικού νερού και η λοιπή σύσταση όπως δίνεται. Η µέση ενθαλπία του κατεψυγµένου βοδινού θα υπολογισθεί ως: T 1 c = cy i i = Yi cdt T T i F TF νερό T cw = a T T T T + β + γ = T T at T β T T γ T T F TF F [ ( F) + / 2( F ) + / 3( F) ] = 4.10 kj/kg οµοίως για πάγο c I =2.03 kj/kg πρωτεΐνες c p =2,00 kj/kg λιπαρά c fa =1.98 kj/kg και c s = = kj/kg [ ][ ] H = ( ) 352. ( ) ( ) = και αντικαθιστώντας το Η στην εξίσωση (8.34): t F = s =19.1 h 5. Για τα ίδια δεδοµένα της άσκησης 4 να υπολογισθεί ο χρόνος που απαιτείται για κατάψυξη φέτας βοδινού διαστάσεων 0.33x0.025x0.20 m µέσω της τροποποίησης Cleland and Earle. Λύση Η φέτα βοδινού έχει πολύ µικρότερο πάχος σε σύγκριση µε τις άλλες δύο διαστάσεις και µπορούµε να θεωρήσουµε ότι η αγωγή θερµότητας προσοµοιάζει την περίπτωση πλάκας ορισµένου πάχους και απείρου µήκους και πλάτους. Θα υπολογισθούν οι αριθµοί Bi, Ste, Pk και µέσω αυτών οι παράγοντες P και R για να χρησιµοποιηθούν στην εξίσωση (8.36). Η µεταβολή ενθαλπίας θα υπολογισθεί σύµφωνα µε τον Πίνακα 8.1. H = ( ) = kj/kg 249
258 hd Bi = = = k 108. cs( TF Tm) ( ) Ste = = = H cl( TIT TF) 352. ( ) Pk = = = H Οι τιµές των αδιάστατων αριθµών καθώς και της θερµοκρασίας του τροφίµου και του ψυκτικού µέσου βρίσκονται εντός των ορίων υπολογισµών των Cleland and Earle, εποµένως µπορούν να χρησιµοποιηθούν οι εξισώσεις (8.42) και (8.43) για τον υπολογισµό των P και R. Με αντικατάσταση των παραπάνω τιµών προκύπτει: P = R = Ο συντελεστής θερµικής διαχυτότητας υπολογίζεται ως: k a = c = 108. m 2 /s ρ s Ο χρόνος κατάψυξης θα υπολογισθεί από την εξίσωση (8.36): t F = = s = 143. h Καταψυκτήρας µε πλάκες, συνεχούς λειτουργίας χρησιµοποιείται για την κατάψυξη συσκευασµένων φιλέτων µπακαλιάρου µε ρυθµό παραγωγής 500 kg/h. Το προϊόν εισέρχεται στον καταψυκτήρα στους 5 C και εξέρχεται στους 25 C. Η συσκευασία είναι 0.5 kg και έχει διαστάσεις 0.04x0.1x0.14 m. Οι πλάκες του καταψυκτήρα έχουν πλάτος 1 m θερµοκρασία 30 C και ο επιφανειακός συντελεστής µεταφοράς θερµότητας είναι 56 W/m 2 C. Το υλικό συσκευασίας έχει πάχος 0.8 mm και συντελεστή θερµικής αγωγιµότητας 0.05 W/m C. Εάν είναι γνωστό ότι το ύψος του καταψυκτήρα δεν µπορεί να υπερβεί τα 2.5 m και η απόσταση µεταξύ των βαθµίδων είναι 0.3 m να βρεθούν κατά προσέγγιση οι διαστάσεις του. ίδεται ο συντελεστής θερµικής αγωγιµότητας του κατεψυγµένου τροφίµου 2.08 W/m C. Λύση Θα προσδιορισθεί ο χρόνος κατάψυξης σύµφωνα µε την εξίσωση (8.34) θεωρώντας τα φιλέτα πλάκες ορισµένου πάχους. Ο συνολικός συντελεστής µεταφοράς θερµότητας στην επιφάνεια του τροφίµου θα υπολογισθεί σύµφωνα µε την εξίσωση (8.59): x p = + = + = U = 29. 5W/m 2 C U h k p Από Πίνακα 8.1 H = ( ) = 311 kj/kg Από την εξίσωση (8.9) µε Υ w = 0.8 T = (. 08 1)/( ) = 19. T F = 19. C ρ = 950 kg/m 3 (πυκνότητα των φιλέτων µπακαλιάρου µε βάση βιβλιογραφικά δεδοµένα) k = 2.08 W/m C 250
259 t F = + + = 8078s = h Για να λειτουργεί µε δυναµικότητα 500 kg/h ο καταψυκτήρας θα πρέπει να περιέχει 500 (kg/h) x 2.24 (h)=1120 kg προϊόντος, ή 1120 (kg) / 0.5 (kg/πακέτο) = 2240 πακέτα. Στο 1 m πλάτους των πλακών θα διαταχθούν 1/0.14 = 7.14 = 7 συσκευασίες. Κατακόρυφα υπάρχουν 2.5/0.3 = 8.33 = 8 βαθµίδες. Ανά µέτρο πλάτους των πλακών και στις 8 βαθµίδες θα διατάσσονται 7x8 = 56 συσκευασίες. Άρα στο συνολικό µήκος θα πρέπει να βρίσκονται 2240/56 = 40 συσκευασίες. Και το συνολικό µήκος θα είναι 40x0.1 m = 4 m. Ασκήσεις 1. Να υπολογισθεί το σηµείο έναρξης κατάψυξης πορτοκαλοχυµού µε σύσταση 87.5 % νερό, 1.8 % γλυκόζη, 2.6 % φρουκτόζη, 6.0 % σακχαρόζη και 2.1 % µη υδατοδιαλυτά συστατικά. Επίσης να βρεθεί το ποσοστό νερού του πορτοκαλοχυµού που έχει καταψυχθεί στους 12 C. 2. Να υπολογισθεί η απαίτηση σε ψύξη ανά kg πορτοκαλοχυµού της άσκησης 1 για µείωση της θερµοκρασίας από 25 C σε 12 C. 3. Κεράσια µέσης διαµέτρου 1.5 cm καταψύχονται σε καταψυκτήρα ρευστοστερεάς κλίνης (IQF) µε αέρα θερµοκρασίας 30 C και µε επιφανειακό συντελεστή συναγωγής h=60 W/m 2 C. Να υπολογισθεί ο απαιτούµενος χρόνος για την κατάψυξη του προϊόντος από τους 5 C στους 15 C. ίνονται: µέση περιεκτικότητα σε νερό 77 %, πυκνότητα 1050 kg/m 3, συντελεστής αγωγής θερµότητας του κατεψυγµένου τµήµατος 1.80 W/m C. 4. Κρόκος αυγού, συσκευασµένος σε δοχεία από λαµιναρισµένο χαρτί διαστάσεων 7x10x15 cm, καταψύχεται από τους 4 C στους 10 C. Η θερµοκρασία έναρξης κατάψυξης του προϊόντος είναι 0.5 C και η πυκνότητα αυτού 950 kg/m 3. Το υλικό συσκευασίας έχει πάχος 0.65 mm και συντελεστή θερµικής αγωγιµότητας W/m C. Εάν η κατάψυξη γίνεται σε καταψυκτήρα µε ελικοειδή µεταφορική ταινία, µε ρεύµα ψυχρού αέρα θερµοκρασίας 25 C και ο επιφανειακός συντελεστής είναι h=20 W/m 2 C, να υπολογισθεί το µήκος της απαιτούµενης ταινίας (πλάτους 0.5 m) στον καταψυκτήρα για παραγωγή 100 kg/h προϊόντος. 5. Μπάλες βοδινού διαµέτρου 15 cm καταψύχονται στον καταψυκτήρα της άσκησης 4 µε προσφύσηση αέρα θερµοκρασίας 30 C και h=25 W/m 2 C. Η αρχική θερµοκρασία του βοδινού είναι 5 C. Να υπολογισθεί ο χρόνος που απαιτείται για κατάψυξη του προϊόντος στους 10 C µέσω της εξίσωσης Plank, β) της τροποποίησης Cleland and Earle. Επίσης να υπολογισθεί η δυναµικότητα του καταψυκτήρα αν το πλάτος της µεταφορικής ταινίας είναι 0.5 m και το συνολικό µήκος αυτής 550 m. 251
260 6. Κέικ (διαµέτρου 23 cm και πάχους 4 cm) βάρους kg καταψύχονται µε υγρό άζωτο. Η θερµοκρασία έναρξης κατάψυξης του προϊόντος είναι 0.7 C και ο συντελεστής αγωγής θερµότητας του κατεψυγµένου κέικ 1.73 W/m C. Εάν το προϊόν χρειάσθηκε 1.6 min για µείωση της θερµοκρασίας του από 0 C σε 18 C και χρησιµοποιήθηκαν kg N 2 /kg προϊόντος να εκτιµηθεί ο επιφανειακός συντελεστής µεταφοράς θερµότητας. ίνονται λανθάνουσα θερµότητα εξάτµισης αζώτου kj/kg, µέση ειδική θερµότητα αζώτου kj/kg C. Σύµβολα α=k/ρc θερµική διαχυτότητα (m 2 /s) Α επιφάνεια εναλλαγής θερµότητας (m 2 ) β κρυοσκοπική σταθερά, ή µοριακή ταπείνωση του σηµείου πήξης (C kg/mole) β 1 σταθερά διαγράµµατος 8.5 β 2 σταθερά διαγράµµατος 8.5 Β δεσµευµένο νερό ανά kg στερεών (kg νερού/kg ξηρών στερεών) c ειδική θερµότητα (J/kg C) d πάχος πλάκας, διάµετρος κυλίνδρου ή σφαίρας (m) Η µεταβολή ενθαλπίας (kj/kg) Ε λόγος των µοριακών βαρών (M w /M si ) h επιφανειακός συντελεστής µεταφοράς θερµότητας (W/m 2 C) H ενθαλπία του τροφίµου (J/kg) k συντελεστής αγωγής θερµότητας (W/m C) λ λανθάνουσα θερµότητα τήξης του διαλύτη (J/mole) L λανθάνουσα θερµότητα πήξης ανά µονάδα µάζας (kj/kg) L Fw λανθάνουσα θερµότητα πήξης του νερού στο τρόφιµο σε θερµοκρασία T F (kj/kg) m γραµµοµοριακότητα διαλύµατος (mole διαλυµένης ουσίας / kg διαλύτη) M µοριακό βάρος M A µοριακό βάρος του διαλύτη P σταθερά εξίσωσης Plank ρ πυκνότητα (kg/m 3 ) R=8.314 J/mole K (σταθερά των αερίων) R σταθερά εξίσωσης Plank R ακτίνα (m) t F χρόνος κατάψυξης (s) Τ θερµοκρασία ( C ή K) T A σηµείο πήξης διαλύµατος (Κ) T Ao σηµείο πήξης διαλύτη (Κ) T Fw σηµείο πήξης του νερού (Κ) T ref θερµοκρασία αναφοράς, θεωρούµενη συνήθως ίση µε 40 C V όγκος (m 3 ) 252
261 V/AR παράγοντας σχήµατος (αδιάστατος) x απόσταση (m) Χ Α µοριακό κλάσµα του διαλύτη στο διάλυµα X si µοριακό κλάσµα του διαλυµένου συστατικού i στο διάλυµα Y κλάσµα µάζας (υγρή βάση) Αδιάστατοι αριθµοί Bi αριθµός Biot: hd/k Fo αριθµός Fourier: αt F /d 2 Pk αριθµός Plank: c l (T IT -T F )/ H Ste αριθµός Stephan: c s (T F -T m )/ Η είκτες α αέρας ap φαινόµενη τιµή av µέση τιµή F έναρξη κατάψυξης Fο τιµή αµέσως πριν την έναρξη κατάψυξης i συστατικό i Ι πάγος ΙΤ αρχική τιµή l µη κατεψυγµένη φάση L οφειλόµενη στη λανθάνουσα θερµότητα m ψυκτικό µέσο s κατεψυγµένη φάση si στερεό ή διαλυµένο συστατικό i so στερεά ή διαλυµένα συστατικά w νερό wo νερό πριν την έναρξη κατάψυξης Βιβλιογραφία Bender A.E. (1993) Nutritional aspects of frozen foods in Frozen Food Technology ed. C.P. Mallet, Blackie A&P, London. Brennan J.G, Butters J.R., Cowell N.D. and Lilly A.E.V. (1976) Food Engineering Operations, 2 nd ed., Applied Science Publishers Ltd., London, pp Chang H.D. and Tao L.C. (1981) Correlation of enthalpies in food systems J. Food Sci. 46: Chen C.S. Thermodynamic analysis of freezing and thawing of foods. Enthalpy and apparent specific heat J. Food Sci. 50:
262 Choi Υ. and Okos M.R. (1986) Effects of temperature and composition on the thermal properties of foods in Food Engineering and Process Applications, Vol. 1, Transport Phenomena, eds M. Maguer and P. Jelen, Elsevier Applied Sci. London. Cleland A.C. (1990) Food Refrigeration Processes Analysis, Design and Simulation, Elsevier Applied Science, London-N.Y., pp , Cleland A.C. and Earle R.L. (1977) A comparison of analytical and numerical methods for predicting the freezing time of foods J. Food Sci. 42: Cleland A.C. and Earle R.L. (1979a) A comparison of methods for predicting the freezing time of cylindrical and spherical foodstufs J. Food Sci. 44: 958. Cleland A.C. and Earle R.L. (1979b) Prediction of freezing time of foods in rectangular packages J. Food Sci. 44: 964. Fennema O. (1975) Freezing preservation in Physical Principles of Food Preservation, ed. O. Fennema, Marcel Dekker Ink., N.Y., pp Fennema O. and Powrie W.D. (1964) Fundamentals of low-temperature food preservation Advan. Food Res. 13: 219. Heldman D.R. and Singh R.P. (1981) Food Process Engineering, 2 nd ed., The AVI Publishing Co. Inc., Westport, Connecticut, pp Θωµόπουλος Χ.. (1981) Τεχνολογία Γεωργικών Βιοµηχανιών, Λύχνος ΕΠΕ, Αθήνα, σελ Μαρκάκης Π. (1996) Στοιχεία Τεχνολογίας Τροφίµων, Τρίαινα Εκδοτική, Αθήνα, σελ Nagaoka J., Takagi S. and Hotani S. (1955) Experiments of freezing of fish in an airblast freezer Proc. 9 th Int. Congr. Refrig., Paris, 2:4. Persson P.O. and Londahl G. (1993) Freezing Technology in Frozen Food Technology ed. C.P. Mallet, Blackie A&P, London. Rahman S. (1995) Food Properties Handbook, CRC Press, Boca Raton, pp , Reid D.S. (1993) Basic physical phenomena in the freezing and thawing of plant and animal tissues in Frozen Food Technology ed. C.P. Mallet, Blackie A&P, London. Sing R.P. and Mannapperuma J.D. (1990) Developments in Food Freezing in Biotechnology and Food Process Engineering, ed. HG. Schwartzberg and M.A. Rao, Marcel Dekker Inc., N.Y. and Basel, pp Schwartzberg H. (1976) Effective heat capacities for the freezing and thawing of food J. Food Sci. 41:
263 ΚΕΦΑΛΑΙΟ 9 ΣΥΣΚΕΥΑΣΙΑ ΤΡΟΦΙΜΩΝ Η συσκευασία επιτελεί κυρίως δύο βασικές λειτουργίες στο τρόφιµο: την προστασία του τροφίµου σε προκαθορισµένο βαθµό για τον αναµενόµενο χρόνο ζωής και την διαφήµιση αυτού στο σηµείο πώλησης. Η προστασία του τροφίµου είναι πρωταρχικής σηµασίας, αλλά η προσέλκυση του καταναλωτή και ή αναγνώριση της ταυτότητας του προϊόντος είναι επίσης ιδιαίτερα σηµαντικά για τις πωλήσεις και συχνά παίζουν καθοριστικό ρόλο στην επιλογή και το σχεδιασµό της συσκευασίας. Επί πλέον η συσκευασία εξυπηρετεί την διακίνηση και αποθήκευση των τροφίµων µέσω της τοποθέτησης της επιθυµητής ποσότητας σε ένα περιέκτη (άµεση συσκευασία) και της συγκέντρωσης περισσότερων µονάδων περιεκτών σε ένα σύνολο (εξωτερική συσκευασία), ώστε να διευκολύνεται και να είναι περισσότερο ασφαλής η µεταφορά και η αποθήκευσή τους. Για παράδειγµα υγρά τρόφιµα συσκευάζονται σε φιάλες, οι οποίες στη συνέχεια τοποθετούνται σε κιβώτια που µπορούν εύκολα να συγκεντρωθούν σε παλέτες και να διακινηθούν ή να στοιβαχθούν σε αποθήκες. Συχνά χρησιµοποιείται, για λόγους προώθησης στην αγορά και ενδιάµεση συσκευασία, π.χ. συσκευασία µικρού αριθµού µονάδων περιεκτών µε φύλλο πλαστικού και προσφορά του πακέτου σε ελκυστικότερη τιµή. Η συσκευασία µπορεί επίσης να λειτουργήσει ως βοηθητικό µέσο µιας διεργασίας. Για παράδειγµα τα µεταλλικά δοχεία που χρησιµοποιούνται σε θερµικές κατεργασίες τροφίµων εξασφαλίζουν όχι µόνο την προστασία τους, αλλά, µε τη σταθερότητα των διαστάσεων τους, διατηρούν το περιεχόµενο τρόφιµο σε ορισµένο σχήµα και θέση και επιτρέπουν τον υπολογισµό της διείσδυσης θερµότητας. Τέλος ο περιέκτης πρέπει να παρέχει ευκολία χρήσης στον καταναλωτή. Συχνά ο ίδιος ο περιέκτης χρησιµοποιείται ως σκεύος από το οποίο καταναλώνουµε το τρόφιµο, π.χ. φιάλες ή µεταλλικά κουτιά µπίρας και αναψυκτικών. Ο σωστός σχεδιασµός της συσκευασίας διευκολύνει τους χειρισµούς του καταναλωτή και τον προστατεύει από πιθανούς τραυµατισµούς. Το κόστος των ίδιων των υλικών συσκευασίας, της µεταφοράς τους στη µονάδα συσκευσίας των τροφίµων, των µηχανηµάτων συσκευασίας κ.λ.π. αυξάνει την τελική τιµή του τροφίµου που φθάνει στον καταναλωτή. Επί πλέον δεν πρέπει να παραβλέπεται το κόστος που επιβαρύνει το κοινωνικό σύνολο: κόστος συγκέντρωσης των απορριµάτων (χρησιµοποιηµένων υλικών συσκευασίας), κόστος διαχείρησης των απορριµάτων και πρόληψης της οικολογικής διαταραχής. Παρ όλα αυτά η συσκευασία, αν χρησιµοποιηθεί σωστά, µπορεί να επιφέρει οικονοµικό όφελος επειδή µειώνει τις απώλειες και τις φθορές των τροφίµων, παρεµποδίζει τη µόλυνση, 255
264 διευκολύνει τη µεταφορά και µειώνει το εργατικό κόστος. Παράλληλα προστατεύοντας το τρόφιµο µέχρι την κατανάλωσή του, µειώνει τον όγκο των απορριµάτων που δηµιουργούν τα ίδια τα ακατάλληλα για κατανάλωση τρόφιµα. Ο ρόλος της συσκευασίας στην προστασία του τροφίµου και τη διατήρηση της ποιότητάς του είναι πρωταρχικής σηµασίας, όπως ήδη αναφέρθηκε και γι αυτό η συσκευασία θα εξετασθεί στη συνέχεια από αυτήν κυρίως τη σκοπιά Παράγοντες του περιβάλλοντος που επιδρούν στην υποβάθµισης της ποιότητας του τροφίµου κατά την αποθήκευση. Για να εξετασθεί ο ρόλος της συσκευασίας στην προστασία του τροφίµου πρέπει αρχικά να εξετασθούν οι παράγοντες που µπορούν να επιφέρουν υποβάθµιση της ποιότητας του τροφίµου. Η ποιότητα του τροφίµου που φθάνει στον καταναλωτή εξαρτάται από την κατάσταση της πρώτης ύλης, τη µέθοδο και τις συνθήκες επεξεργασίας και τις συνθήκες αποθήκευσης. Κατά την αποθήκευση η ποιότητα του τροφίµου υποβαθµίζεται, εκτός ορισµένων εξαιρέσεων όπως η ωρίµανση του κρασιού και της µπίρας. Ο ρυθµός και η έκταση αυτής της υποβάθµισης εξαρτάται από τις συνθήκες του περιβάλλοντος στο οποίο βρίσκεται το τρόφιµο. Το εσωτερικό περιβάλλον στο οποίο βρίσκεται το τρόφιµο µπορεί να διατηρηθεί σε συνθήκες πιο ευνοϊκές για τη διατήρηση του, από ότι το εξωτερικό περιβάλλον, χρησιµοποιώντας µία κατάλληλη προστατευτική φραγή που την αποτελεί το ίδιο το υλικό συσκευασίας. Οι κύριοι παράγοντες που επιδρούν στην ποιότητα του τροφίµου και µπορούν να ελεγχθούν µε τη συσκευασία είναι η µηχανική καταπόνηση, το φως, το οξυγόνο και τα άλλα αέρια του περιβάλλοντος, οι υδρατµοί, οι µικροοργανισµοί και διάφορες ουσίες από το περιβάλλον που µπορεί να το µολύνουν. Παράλληλα η συσκευασία µπορεί να επηρεάσει τη µεταφορά θερµότητας από και προς το τρόφιµο. Οι παράγοντες αυτοί, οι επιπτώσεις τους στο τρόφιµο και η σχετιζόµενη ιδιότητα της συσκευασίας δίνονται στον πίνακα 9.1. Μηχανική καταπόνηση Η µηχανική καταπόνηση προκαλεί µηχανικές φθορές στα τρόφιµα, οι οποίες τα καθιστούν πιο ευάλωτα στην προσβολή από µικροοργανισµούς. Η ικανότητα του υλικού συσκευασίας να προστατεύσει το τρόφιµο εξαρτάται από τις µηχανικές αντοχές αυτού (αντοχή σε κρούση, συµπίεση, διάτµηση κ.λ.π.). Επίσης οι µηχανικές αντοχές καθορίζουν και τη διατήρηση της ακεραιότητας της συσκευασίας απέναντι σε µηχανικές καταπονήσεις, που είναι απαραίτητη για να µην προσβληθεί το τρόφιµο από εξωτερικούς παράγοντες. Εκτός από τις αντοχές που αναφέρθηκαν, άλλες, όπως 256
265 η αντοχή σε εφελκυσµό, είναι επίσης σηµαντικές στην κατασκευή των δοχείων συσκευασίας. Πίνακας 9.1. Επιπτώσεις περιβαλλοντικών παραγόντων στο τρόφιµο και ιδιότητες της συσκευασίας σχετιζόµενες µε την προστασία από τον αντίστοιχο παράγοντα. Επιπτώσεις στο τρόφιµο Περιβαλλοντικός παράγοντας Σχετιζόµενη ιδιότητα της συσκευασίας Χηµικές Μεταβολές Ο 2, CO 2, Ν 2 ιαπερατότητα από αέρια (οξειδώσεις, καταστροφή βιταµινών κ.λ.π.) Φυσικές µεταβολές (πρόσληψη-απώλεια Υγρασία ιαπερατότητα από υδρατµούς υγρασίας, κρυσταλλώσεις) Φυσιολογικές µεταβολές Φως ιαπερατότητα από φως (αναπνοή) Μικροβιολογικές µεταβολές, επιµόλυνση από βιολογικούς παράγοντες Επιµόλυνση από χηµικές ουσίες Μικροοργανισµοί και έντοµα από το περιβάλλον Επικίνδυνες ουσίες στο περιβάλλον ή στη συσκευασία Πορώδες, ακεραιότητα συσκευασίας, διατρησιµότητα από έντοµα Ύπαρξη ακατάλληλων προσθέτων ή συστατικών στη συσκευασία, ιαπερατότητα από χηµικά Μηχανική φθορά Μηχανική καταπόνηση Μηχανικές ιδιότητες Θερµοκρασία Θερµική αγωγιµότητα, Πορώδες, Ικανότητα ανάκλασης Οξυγόνο και άλλα αέρια Το οξυγόνο συµµετέχει σε ορισµένες αντιδράσεις που υποβαθµίζουν την ποιότητα των τροφίµων, όπως η οξείδωση των λιπαρών, οξειδώσεις βιταµινών, οξειδώσεις χρωστικών κ.λ.π. Ο ρυθµός αυτών των δράσεων εξαρτάται από τη συγκέντρωση του οξυγόνου στο τρόφιµο, η οποία µε τη σειρά της εξαρτάται από τη µερική πίεση του οξυγόνου στον αέρα που περιβάλλει το τρόφιµο. Άλλη δράση στην οποία συµµετέχει το οξυγόνο είναι η αναπνοή φρούτων και λαχανικών. Η επιβράδυνση της αναπνοής είναι επιθυµητή για την παράταση του χρόνου ζωής των προϊόντων και µπορεί να επιτευχθεί µε µείωση της συγκέντρωσης του οξυγόνου. Πολύ χαµηλή συγκέντρωση όµως οδηγεί σε αναερόβια αναπνοή και γρήγορη αλλοίωση. Η χρήση υλικών συσκευασίας µε διαφορετική διαπερατότητα σε οξυγόνο βοηθά στον έλεγχο όλων των δράσεων που αναφέρθηκαν. Εκτός του οξυγόνου µπορεί να ενδιαφέρει η διαπερατότητα της συσκευασίας σε διοξείδιο του άνθρακα και άζωτο, ιδιαίτερα στις συσκευασίες φρέσκων φρούτων και λαχανικών και στις συσκευασίες σε τροποποιηµένη ατµόσφαιρα. 257
266 Σε τρόφιµα πλούσια σε πτητικά αρωµατικά συστατικά απαιτείται συσκευασία µη περατή από αυτά ώστε να διατηρηθεί το άρωµα του προϊόντος. Επίσης η συσκευασία πρέπει να προστατεύει το τρόφιµο από την πρόσληψη οσµών από το περιβάλλον. Υδρατµοί Ο ρόλος του νερού στην ανάπτυξη ανεπιθύµητων δράσεων στα τρόφιµα αναπτύχθηκε σε προηγούμενη παράγραφο. Επί πλέον η πρόσληψη υγρασίας µπορεί να επιφέρει ανεπιθύµητες µεταβολές της υφής (απώλεια τραγανότητας) και η απώλεια υγρασίας απώλεια βάρους, κρυσταλλώσεις, µεταβολές στην υφή και την εµφάνιση. Η υγρασία του τροφίµου εξαρτάται από την υγρασία του περιβάλλοντος αέρα, εποµένως η διατήρηση σταθερής υγρασίας σε συσκευασµένο τρόφιµο προϋποθέτει τη χαµηλή διαπερατότητα από υδρατµούς του υλικού συσκευασίας. Σε ορισµένα προϊόντα, όπως στα φρέσκα φρούτα και λαχανικά που αναπνέουν, είναι επιθυµητή η αποµάκρυνση των παραγόµενων υδρατµών από το περιβάλλον της συσκευασίας ώστε να µην υπάρχει τοπική συµπύκνωσή τους. Σε αυτές τις περιπτώσεις απαιτούνται υλικά συσκευασίας διαπερατά από τους υδρατµούς. Φως Το φως καταλύει και επιταχύνει διάφορες ανεπιθύµητες αντιδράσεις στα τρόφιµα. Για παράδειγµα την οξείδωση των λιπαρών που οδηγεί σε οξειδωτικό ταγγισµό, την οξείδωση του γάλακτος προς σχηµατισµό δύσοσµων µερκαπτανών, τις αντιδράσεις αλλοίωσης διαφόρων χρωστικών ουσιών, τις αντιδράσεις ορισµένων βιταµινών (ριβοφλαβίνη, βιταµίνη C) που οδηγούν σε απώλεια της αξίας τους, κ.λ.π. Η καταλυτική επίδραση του φωτός είναι γενικά εντονότερη όσο χαµηλότερο το µήκος κύµατος της ακτινοβολίας, δηλ. στην περιοχή του υπεριώδους και στα χαµηλότερα µήκη κύµατος του ορατού φάσµατος. Οι επί µέρους αντιδράσεις υποβάθµισης των τροφίµων, παρ όλα αυτά, µπορεί να εµφανίζουν βέλτιστο σε ορισµένο µήκος κύµατος. Ειδικά η παρουσία φωτοευαισθητοποιητών, όπως ριβοφλαβίνης, β-καροτενίου, βιταµίνης Α, ή υπεροξειδίων µπορεί να αυξήσει σηµαντικά το φάσµα της δραστικής ακτινοβολίας. Επίσης η κατεργασία του τροφίµου µπορεί να επηρεάσει την ευαισθησία σε διάφορα µήκη κύµατος, π.χ. κρέας συντηρηµένο µε νιτρώδη χάνει το φυσικό του χρώµα γρήγορα µε έκθεση σε ορατό ή υπεριώδες φώς, ενώ το νωπό κρέας µόνο στο υπεριώδες. Εκτός του µήκους κύµατος η ένταση της ακτινοβολίας και η διάρκεια της έκθεσης είναι σηµαντικές. Η διείσδυση της ακτινοβολίας στο τρόφιµο εξαρτάται από το ίδιο το τρόφιµο και ακολουθεί την εκθετική σχέση (νόµος Beer-Lambert): kx I = I e x o όπου I x ένταση του φωτός σε βάθος x του τροφίµου (Cd) (9.1) 258
267 I o ένταση του φωτός στην επιφάνεια του τροφίµου (Cd) k χαρακτηριστική σταθερά απορρόφησης του τροφίµου σε ορισµένο µήκος κύµατος (m -1 ) Μεγαλύτερη διείσδυση παρουσιάζει η ακτινοβολία µεγαλύτερου µήκους κύµατος. Στα στερεά τρόφιµα η µικρή διείσδυση της ακτινοβολίας τα προστατεύει σε µεγάλο βαθµό από τις ανεπιθύµητες φωτοκαταλυόµενες αντιδράσεις. Αντίθετα στα υγρά τρόφιµα, ακόµη και εάν η διείσδυση είναι µικρή η διάχυση των αντιδρώντων συστατικών προς την επιφάνεια και των σχηµατιζόµενων από τη φωτοκατάλυση ελεύθερων ριζών προς το εσωτερικό οδηγεί σε σηµαντική υποβάθµιση. Η διαπερατότητα του υλικού συσκευασίας από το φως καθορίζει την ένταση του φωτός στην επιφάνεια του τροφίµου και εποµένως µπορεί να χρησιµοποιηθεί για τον έλεγχο των φωτοκαταλυόµενων δράσεων. Μόλυνση µε µικροοργανισµούς ή µε διάφορες ουσίες από το περιβάλλον Η ποιότητα των τροφίµων υποβαθµίζεται σε όλες τις περιπτώσεις αν αυτά µολυνθούν από εξωτερικούς παράγοντες. Ιδιαίτερα η προσβολή από µικροοργανισµούς µπορεί να προκαλέσει τη γρήγορη αλλοίωση ή την ανάπτυξη παθογόνων µικροοργανισµών στο τρόφιµο. Η συσκευασία, εφόσον αποµονώνει το τρόφιµο από το περιβάλλον µπορεί να το προστατεύσει από τη µόλυνση. Η απαίτηση προστασίας εξαρτάται από το προϊόν. Στα προϊόντα που έχουν υποστεί κάποια κατεργασία µε στόχο την καταστροφή των µικροοργανισµών απαιτείται απόλυτη προστασία από επιµόλυνση. Η συσκευασία µπορεί επίσης να προστατεύσει τα τρόφιµα από τα έντοµα ή και από τα τρωκτικά. Αυτή η προστασία επιτυγχάνεται απόλυτα µόνο µε τα µεταλλικά και τα γυάλινα δοχεία Τύποι και υλικά συσκευασίας τροφίµων Η προστασία που προσφέρεται στο τρόφιµο από τη συσκευασία εξαρτάται από τη φύση του υλικού συσκευασίας και από τον τύπο κατασκευής του περιέκτη. Οι συσκευασίες των τροφίµων διακρίνονται σε δύο βασικές κατηγορίες ανάλογα µε την εξυπηρέτηση της πώλησης και διακίνησης του τροφίµου: Α. Συσκευασίες λιανικής πώλησης που έρχονται απ ευθείας σε επαφή µε το τρόφιµο, αναγράφουν στοιχεία που προσδιορίζουν και διαφηµίζουν το περιεχόµενο και προστατεύουν το τρόφιµο στα σηµεία λιανικής πώλησης και στην αποθήκευση στο σπίτι. Β. Συσκευασίες που χρησιµοποιούνται για τη µεταφορά και τη διανοµή των τροφίµων και οι οποίες µπορεί να έρχονται σε άµεση επαφή µε το τρόφιµο, 259
268 περιέχοντας µεγάλες ποσότητες τροφίµου χύµα, π.χ. σάκοι, βαρέλια κ.λ.π. ή να περιέχουν µονάδες συσκευασµένων τροφίµων, π.χ. κιβώτια. Από την άποψη προστασίας του τροφίµου ιδιαίτερο ενδιαφέρον παρουσιάζουν οι συσκευασίες της πρώτης κατηγορίας και εκείνες από τη δεύτερη κατηγορία που έρχονται σε άµεση επαφή µε το τρόφιµο. Εκτός της απαίτησης προστασίας αυτές οι συσκευασίες πρέπει να είναι αδρανείς απέναντι του τροφίµου και να µη µολύνουν οι ίδιες το τρόφιµο. Η συσκευασία µπορεί να είναι ήδη προσχηµατισµένη (π.χ. γυάλινα και µεταλλικά δοχεία) ή να σχηµατίζεται στη γραµµή συσκευασίας πριν από το γέµισµα (π.χ. χαρτονένια κουτιά, πλαστικά σακίδια). Μία άλλη ταξινόµηση των συσκευασιών αφορά στον τύπο του περιέκτη και συγκεκριµένα το εάν έχει ορισµένο σχήµα και την ικανότητά του να αλλάζει σχήµα όταν πιεστεί µε τα χέρια: Α. ύσκαµπτες (rigid) και ηµίσκληρες (semi-rigid) συσκευασίες που έχουν ορισµένο σχήµα. Από αυτές οι ηµίσκληρες µπορούν να παραµορφωθούν όταν πιεστούν µε τα χέρια (χαρτονένια κουτιά, ορισµένα πλαστικά δοχεία) ενώ οι δύσκαµπτες διατηρούν το σχήµα τους (γυάλινα και µεταλλικά δοχεία). Β. Εύκαµπτες (flexible) που δεν έχουν ορισµένο σχήµα και κατασκευάζονται από φύλλο εύκαµπτου υλικού Και στις δύο κατηγορίες µπορεί να χρησιµοποιηθούν διάφορα υλικά όσον αφορά στη φύση του υλικού. Οι κυριότεροι τύποι υλικών συσκευασίας µε βάση τη φύση του υλικού είναι: Χαρτί για εύκαµπτη συσκευασία Χαρτόνι για δύσκαµπους περιέκτες Μεταλλικά δοχεία Μεταλλικά φύλλα για εύκαµπτη συσκευασία Γυάλινα δοχεία Πλαστικές µεµβράνες Πλαστικοί περιέκτες δύσκαµπτοι Ξύλινοι περιέκτες Χαρτί-Χαρτόνι Το χαρτί ή χαρτόνι και τα υλικά συσκευασίας που έχουν ως βάση αυτά αποτελούν µεγάλο ποσοσοστό των υλικών συσκευασίας. Οι κύριες αιτίες είναι το χαµηλό κόστος, η διαθεσιµότητα, η εύκολη διαµόρφωση και η χαµηλή ρύπανση, λόγω αποικοδόµησης. Οι ιδιότητες του χαρτιού, ως υλικού συσκευασίας, µπορούν να µεταβληθούν πολύ ανάλογα µε τη διεργασία παραγωγής, την προσθήκη ουσιών βελτίωσης στην 260
269 κατασκευή του φύλλου, ή την επίστρωση των φύλλων µε κηρούς, άσφαλτο, πλαστικά κ.λ.π. Το απλό χαρτί (χωρίς βελτιωτικά και επιστρώσεις) που χρησιµοποιείται για εύκαµπτη συσκευασία έχει γενικά µικρή µηχανική αντοχή και µεγάλη διαπερατότητα από υδρατµούς και αέρια. Οι πιο σηµαντικοί τύποι αυτού του χαρτιού είναι: Χαρτί Kraft: παρουσιάζει βελτιωµένη µηχανική αντοχή. Λαδόχαρτο και περγαµηνό χαρτί: έχει µικρούς πόρους λόγω πυκνού πλέγµατος ινών κυτταρίνης και εποµένως µικρή διαπερατότητα από λιπαρά. Τσιγαρόχαρτο: µαλακό χαρτί µε µεγάλους πόρους και µικρό βάρος ανά επιφάνεια που µπορεί να προστατεύσει από τριβές Χαρτί κρέπ: παρουσιάζει µεγάλη ικανότητα επιµήκυνσης και είναι κατάλληλο για περιτυλίξεις Χαρτί µε πρόσθετες ουσίες µπορεί να παρουσιάσει πολύ βελτιωµένες ιδιότητες. Ένας σηµαντικός τύπος αυτού του χαρτιού είναι το: Αδιαβροχοποιηµένο χαρτί (wet-strength paper): παρασκευάζεται µε προσθήκη ρητινών ουρίας-φορµαλδεΰδης ή µελαµίνης-φορµαλδεΰδης στο χαρτοπολτό, οπότε τα παραγόµενα προϊόντα συµπύκνωσης που δηµιουργούνται κατά την ξήρανση του χαρτιού, είναι αδιάλυτα στο νερό και αυξάνουν πολύ την αντοχή του χαρτιού όταν απορροφήσει υγρασία. Τα επικαλυµµένα χαρτιά (coated papers) παρασκευάζονται µε επικάλυψη του φύλλου µε διάφορα υλικά µέσω διαβίβασής του σε λουτρό τηγµένου υλικού ή αιωρήµατος του υλικού, ή µέσω εξώθησης του υλικού µε εκβολέα. Οι κυριότεροι τύποι επικαλυµµένων χαρτιών είναι: Χαρτί µε επικάλυψη κηρού: παρασκευάζεται µε εµβάπτιση σε λουτρό τηγµένης παραφίνης και παρουσιάζει µειωµένη διαπερατότητα νερού και υδρατµών. Χαρτί µε επικάλυψη ασφάλτου: Η επικάλυψη γίνεται στη µία πλευρά του φύλλου µε ρολό ηµιεµβαπτισµένο σε λουτρό ασφάλτου και δύο επικαλυµµένα φύλλα πιέζονται ανάµεσα σε περιστρεφόµενους κυλίνδρους, για τη δηµιουργία ενός σύνθετου φύλλου µε την επικάλυψη στο εσωτερικό. Το σύνθετο φύλλο έχει πολύ µειωµένη διαπερατότητα σε νερό και υδρατµούς και χρησιµοποιείται για την κατασκευή σάκων ιδιαίτερα για θαλάσσια µεταφορά. Χαρτί µε επικάλυψη πολυεθυλενίου (PE): Το PE είναι το ευρύτερα χρησιµοποιούµενο πλαστικό για την επικάλυψη χαρτιού. Η επικάλυψη γίνεται µε µεµβράνη PE που σχηµατίζεται από εκβολέα και τα δύο υλικά συµπιέζονται ανάµεσα σε κυλίνδρους. Το επικαλυµµένο φύλλο έχει πολύ µικρή διαπερατότηττα νερού και υδρατµών και σχετικά µικρή διαπερατότητα λιπαρών. Επίσης έχει την ικανότητα θερµοσυρραφής. 261
270 Χαρτί µε επικάλυψη πολυβινυλιδενοχλωριδίου (PVdC): Η επικάλυψη γίνεται απο λουτρό αιωρήµατος PVdC. Το φύλλο παρουσιάζει ανάλογες ιδιότητες µε εκείνο του PE. Το χαρτόνι διαφέρει από το χαρτί ως προς το βάρος ανά µονάδα επιφάνειας. ιεθνώς ως χαρτόνι χαρακτηρίζεται το προϊόν βάρους µεγαλύτερου των 250 g/m 2, ενώ το µικρότερου βάρους χαρακτηρίζεται ως χαρτί. Το πάχος του χαρτονιού είναι µεγαλύτερο από 0.30 mm. Υπάρχουν τρεις τύποι χαρτονιού που διαφέρουν ως προς την πρώτη ύλη κατασκευής: Chipboard: Χαρτόνι που παράγεται από ανακυκλωµένο χαρτί, έχει σκούρο χρώµα, µικρή µηχανική αντοχή και δεν χρησιµοποιείται για άµεση επαφή µε το τρόφιµο. Duplex board: Χαρτόνι που παράγεται από µίγµα ηµιλευκασµένου χηµικού και µηχανικού πολτού ή πολτού από ανακύκλωση και επικαλύπτεται και από τις δύο πλευρές µε χηµικό πολτό. Μπορεί να χρησιµοποιηθεί σε ορισµένες περιπτώσεις σε επαφή µε τα τρόφιµα. Solid white board: Χαρτόνι που παράγεται από λευκασµένο χηµικό πολτό και χρησιµοποιείται σε άµεση επαφή µε τα τρόφιµα. Για υγρά ή λιπαρά τρόφιµα και γενικά για προϊόντα που απαιτούν ειδική προστασία χρησιµοποιούνται χαρτόνια επικαλυµµένα µε κηρούς, PE ή PVdC ή πολυστρωµατικά φύλλα (laminates) µε χαρτόνι, PE και φύλλο αλουµινίου. Τα χαρτονένια κουτιά κατασκευάζονται από συµπαγές ηµίσκληρο χαρτόνι ή πολυστρωµατικό φύλλο. Τα χαρτοκιβώτια που χρησιµοποιούνται για χονδρική συσκευασία και για µεταφορά προϊόντων (π.χ. φρούτα) κατασκευάζονται από συµπαγές χαρτόνι ή από κυµατοειδές χαρτόνι. Σχήµα 9.1. ιάφοροι τύποι κυµατοειδούς χαρτονιού (πραγµατικό µέγεθος) (Παπαδάκης, 1997) 262
271 Το κυµατοειδές χαρτόνι αποτελείται εσωτερικά από ένα ή περισσότερα στρώµατα κυµατοειδούς χαρτιού και εξωτερικά από επίπεδα χαρτόνια. Η κυµάτωση συνεισφέρει στην απόσβεση των κρούσεων και οι µηχανικές αντοχές αυτών των χαρτονιών εξαρτώνται τόσο από τον τύπο της κυµάτωσης (πλάτος και αριθµός κυµατώσεων ανά τρέχον µέτρο χαρτιού), όσο και από τον αριθµό και τις πυκνότητες των εσωτερικών και εξωτερικών στρωµάτων (τρίφυλλο, πεντάφυλλο, επτάφυλλο). Οι τύποι των κυµατοειδών χαρτονιών δίνονται στο σχήµα Γυαλί Τα γυάλινα δοχεία χρησιµοποιούνται από πολύ παλιά για τη συσκευασία των τροφίµων και αποτελούν και σήµερα ένα από τα σπουδαιότερα µέσα συσκευασίας. Από φυσική άποψη το γυαλί χαρακτηρίζεται ως ένα υπόψυκτο υγρό πολύ υψηλού ιξώδους. Από χηµική άποψη είναι µίγµα ανόργανων οξειδίων ποικίλων αναλογιών. Το κύριο συστατικό είναι το SiO 2 (70-75%) ακολουθούµενο από τα Na 2 O και CaO (6-13%, το κάθε ένα). Άλλα οξείδια, Al 2 O 3, BaO, MgO, προστίθενται σε πολύ µικρότερες αναλογίες, Για τον χρωµατισµό του γυαλιού προστίθενται διάφορα οξείδια µετάλλων, όπως χρωµίου και σιδήρου (πράσινες φιάλες), ή οξείδια σιδήρου, θείου και άνθρακας (φαιοκίτρινες φιάλες). Τα κύρια πλεονεκτήµατα των γυάλινων δοχείων συσκευασίας είναι: Αδιαπερατότητα: Το γυαλί αποτελεί εξαίρετο φραγµό στερεών, υγρών και αερίων και εποµένως είναι ιδιαίτερα κατάλληλο για τη συσκευασία αεριούχων ποτών, ενώ προσφέρει πολύ καλή προστασία σε όλα τα τρόφιµα. Αδράνεια: Το γυαλί δεν αντιδρά µε τα συστατικά του τροφίµου και παραµένει χηµικά σταθερό. ιαφάνεια: Η διαφάνεια του γυαλιού επιτρέπει περιεχοµένου και συντελεί στην ελκυστική εµφάνιση. την καλή ορατότητα του Χρώµα: Το γυαλί µπορεί να χρωµατισθεί για τον περιορισµό της διαπερατότητας της υπεριώδους κυρίως ακτινοβολίας, που επιταχύνει δράσεις υποβάθµισης ποιότητας σε ορισµένα τρόφιµα. υνατότητα κατασκευής περιεκτών διαφόρων σχηµάτων: Με χρήση κατάλληλων τεχνικών το γυαλί µπορεί να διαµορφωθεί σε διάφορους περιέκτες. Γενικά διακρίνονται σε φιάλες (µεγάλο ύψος προς διάµετρο) και βάζα (ύψος παραπλήσιο της διαµέτρου). Το σχήµα του περιέκτη σχεδιάζεται µε διάφορα κριτήρια, αλλά ένα βασικό είναι η ελκυστικότητα της εµφάνισης. υνατότητα ανακύκλωσης και επαναπλήρωσης: Το γυάλινο δοχείο προσφέρει τη δυνατότητα καθαρισµού και επαναπλήρωσης. Η δυνατότητα αυτή µπορεί να αξιοποιηθεί οικονοµικά σε προϊόντα ευρείας κατανάλωσης µε εκτεταµένο δίκτυο διανοµής και συγκέντρωσης των άδειων περιεκτών. Κλασσικό παράδειγµα αποτελούν 263
272 οι φιάλες της µπίρας και οι φιάλες αναψυκτικών µε µέσο όρο επαναπλήρωσης 20 και 35 φορές, αντίστοιχα. Για προϊόντα µικρότερης κατανάλωσης ή εκείνα που διατίθενται σε εκτεταµένες γεωγραφικές περιοχές χρησιµοποιούνται περιέκτες µιας χρήσης, οι οποίοι µπορούν να ανακυκλωθούν επιστρεφόµενοι στα εργοστάσια παραγωγής γυαλιού. υνατότητα θερµικής κατεργασίας: Τα τρόφιµα συσκευασµένα σε γυάλινα δοχεία µπορούν να υποστούν θερµική κατεργασία παστερίωσης ή αποστείρωσης. Για την αποφυγή προβληµάτων που µπορεί να δηµιουργηθούν από υπερπίεση στο εσωτερικό των δοχείων πρέπει ο κενός χώρος κατά το κλείσιµο να είναι µεγαλύτερος του 6% του συνολικού όγκου (στους 55 C). Εκτός των πλεονεκτηµάτων που αναφέρθηκαν πρέπει να προστεθεί ότι οι καταναλωτές έχουν συνδέσει τη γυάλινη συσκευασία µε την καλύτερη ποιότητα του προϊόντος. Έτσι υπάρχει µεγαλύτερη αποδοχή της γυάλινης συσκευασίας έναντι οποιασδήποτε άλλης σε προϊόντα υψηλής τιµής. Τα κυριότερα µειονεκτήµατα των γυάλινων δοχείων είναι: Ευθραυστότητα: Τα γυάλινα δοχεία έχουν τη µέγιστη αντοχή αµέσως µετά την κατασκευή τους, αλλά η επαφή µεταξύ τους ή µε άλλα αντικείµενα δηµιουργεί µικροσκοπικές ρωγµές στην επιφάνεια που µειώνουν σηµαντικά την αντοχή. Η θραύση των γυάλινων δοχείων οφείλεται σε κρούση, συµπίεση, εσωτερική πίεση ή απότοµη µεταβολή της θερµοκρασίας (θερµικό σοκ). Η αντοχή σε κρούση συµπίεση και εσωτερική πίεση είναι µεγαλύτερη όσο πιο οµοιόµορφη είναι η κατανοµή του γυαλιού στο δοχείο, λιγότερα τα ελαττώµατα ή ασθενή σηµεία στην κατασκευή και µικρότερες οι βλάβες λόγω επαφής µε διάφορα αντικείµενα. Το πάχος του δοχείου αυξάνει την αντοχή σε εσωτερική πίεση αλλά µειώνει την αντοχή σε κρούση, όπως και την αντοχή σε απότοµη µεταβολή της θερµοκρασίας. Τα κοινά γυαλιά δεν αντέχουν σε απότοµες µεταβολές της θερµοκρασίας σε αντίθεση µε τα γυαλιά pyrex που περιέχουν µεγάλη ποσότητα βορίου. Βελτίωση της αντοχής σε κρούση και περιορισµός των επιφανειακών βλαβών που συνεπάγεται βελτίωση και των άλλων αντοχών επιτυγχάνεται µε επικάλυψη µε διάφορα επιχρίσµατα. Μεγάλο βάρος ανά επιφάνεια: Το βάρος της γυάλινης συσκευασίας αυξάνει σηµαντικά το κόστος µεταφοράς των προϊόντων. Τα δοχεία µε λεπτότερα τοιχώµατα έχουν µικρότερες µηχανικές αντοχές, αν και τα τελευταία χρόνια οι τεχνολογικές βελτιώσεις στην κατασκευή τους έχουν επιτύχει την οµοιόµορφη κατανοµή του γυαλιού και τη διατήρηση των µηχανικών αντοχών µε σηµαντική µείωση του βάρους. Οι γυάλινοι περιέκτες µορφοποιούνται µε πίεση σε καλούπια (βάζα) ή µε εµφύσηση (φιάλες) και µεταφέρονται έτοιµοι στη βιοµηχανία συσκευασίας. Τα πώµατά τους κατασκευάζονται από λευκοσίδηρο ή κοινό σίδηρο, αλουµίνιο, φελλό ή πλαστικά. ιακρίνονται σε πώµατα πιέσεως, τα οποία χρησιµοποιούνται όταν η πίεση 264
273 στο εσωτερικό των φιαλών είναι µεγαλύτερη της ατµοσφαιρικής, πώµατα κενού που χρησιµοποιούνται σε βάζα που σφραγίζονται υπό µειωµένη πίεση και συνήθως υφίστανται θερµική επεξεργασία, και κοινά πώµατα. Τα πώµατα πιέσεως είναι τα µεταλλικά τύπου κορώνα, τα πώµατα αλουµινίου µε εγκοπές και τα βιδωτά πώµατα πλαστικά ή µεταλλικά. Τα πώµατα κενού φέρουν ελαστικό παρέµβυσµα και είναι βιδωτά µε προεξοχές, ή βιδώνουν στο εξωτερικό σπείρωµα του βάζου, ή είναι παραβιαζόµενα χωρίς τη δυνατότητα επανακλεισίµατος. Τα κοινά πώµατα είναι πώµατα από φελλό, πλαστικά ή µεταλλικά και µπορεί να είναι βιδωτά καθώς και να φέρουν ελαστικό παρέµβυσµα. ιάφορα είδη πωµάτων δίνονται στο σχήµα 9.2. Σχήµα 9.2. ιάφορα είδη πωµάτων. (Θωµόπουλος, 1986) Α: Σφράγιση περιεχοµένου υπό συνήθη πίεση 1.Κοινό πώµα από φελλό, 2. Βιδωτό ασφαλείας, 3. Απλό πώµα αλουµινίου, 4. Μεταλλικό βιδωτό Β. Σφράγιση περιεχοµένου υπό κενό 5. Βιδωτό C. Σφράγιση περιεχοµένου υπό πίεση 6. Πώµα τύπου κορώνα, 7. Πώµα αλουµινίου, 8. Βιδωτό Μέταλλα Μεταλλικά δοχεία Η συσκευασία τροφίµων σε µεταλλικά δοχεία άρχισε το 19ο αιώνα µε την ανάπτυξη της κονσερβοποιίας και έκτοτε διαδόθηκε ευρύτατα. Αυτή η διάδοση οφείλεται στα σηµαντικά πλεονεκτήµατα των µεταλλικών δοχείων, όπως: µηχανική αντοχή που διευκολύνει τη διακίνηση δυνατότητα ερµητικού κλεισίµατος που εξασφαλίζει την προστασία του τροφίµου από µολύνσεις 265
274 αδιαπερατότητα από αέρια υγρασία και φως αντοχή σε ψηλές θερµοκρασίες που επιτρέπει την χρήση τους σε θερµικές κατεργασίες των τροφίµων σχετικά χαµηλή τοξικότητα εύκολη µορφοποίηση και δυνατότητα κατασκευής διαφόρων σχηµάτων καλή εµφάνιση λόγω της δυνατότητας βερνικώµατος και διακόσµησης της επιφάνειας ευχέρια γεµίσµατος και κλεισίµατος µε µηχανικά µέσα και σχετικά χαµηλό βάρος. Τα υλικά που χρησιµοποιούνται στην κατασκευή των δοχείων είναι ο επικασσιτερωµένος χάλυβας ή λευκοσίδηρος, ο επιχρωµιωµένος χάλυβας και το αλουµίνιο. Λευκοσίδηρος Ο λευκοσίδηρος είναι το ευρύτερα χρησιµοποιούµενο υλικό µε µεγάλη διαφορά από τα άλλα δύο. Ο χάλυβας που χρησιµοποιείται για την κατασκευή των φύλλων έχει µικρή περιεκτικότητα σε άνθρακα και η σύνθεσή του έχει σηµαντική επίδραση στην αντοχή σε διάβρωση και στις µηχανικές ιδιότητες του λευκοσιδήρου. Για την κατασκευή δοχείων κονσερβών χρησιµοποιούνται κυρίως τρεις τύποι χάλυβα: Ο τύπος L είναι υψηλής καθαρότητας και παρουσιάζει µεγάλη αντοχή σε διάβρωση γι αυτό χρησιµοποιείται για έντονα διαβρωτικά προϊόντα. Τα µέγιστα επιτρεπτά όρια συστατικών στον τύπο L είναι C: 0.13%, Mg: 0.60%, P: 0.15%, S: 0.05%, Si: 0.010% και Cu: 0.06%. Η αντίσταση σε διάβρωση εξαρτάται και από τον τύπο του τροφίµου. Για παράδειγµα σε αεριούχα ποτά η αναλογία Cu/S καθορίζει την αντίσταση σε διάβρωση. Ο τύπος MR είναι λιγότερο καθαρός και η αντοχή του στη διάβρωση είναι µέτρια γι αυτό χρησιµοποιείται σε λιγότερο διαβρωτικά τρόφιµα. Είναι ο ευρύτερα χρησιµοποιούµενος χάλυβας στην κονσερβοποιία. Ο τύπος MC είναι παρόµοιος µε τον MR, αλλά έχει µεγαλύτερη περιεκτικότητα σε φωσφόρο που του προσδίδει µεγαλύτερη µηχανική αντοχή και δυσκαµψία. Η επικασσιτέρωση των φύλλων του χάλυβα αυξάνει την αντοχή σε διάβρωση. Γίνεται ηλεκτρολυτικά και στις δύο επιφάνειες του φύλλου και το σχηµατιζόµενο στρώµα έχει πάχος µm ( g/m 2 ). Η επικάλυψη στην εξωτερική επιφάνεια µπορεί να έχει το ίδιο πάχος ή να είναι λεπτότερη από την επικάλυψη στην εσωτερική επιφάνεια. Εκτός της επικασσιτέρωσης το φύλλο του λευκοσιδήρου προστατεύεται επί πλέον µε δύο επιφανειακές κατεργασίες, την αδρανοποίηση και τη λίπανση. Η αδρανοποίηση σταθεροποιεί την επιφάνεια του κασσιτέρου µέσω του ελέγχου του σχηµατισµού των φυσικών οξειδίων. Γίνεται µε ηλεκτρολυτική απόθεση ενός λεπτότατου στρώµατος χρωµικών ή φωσφορικών αλάτων. Η λίπανση γίνεται µε πολύ 266
275 µικρή ποσότητα λιπαντικού και προστατεύει το φύλλο από εκδορές, ενώ παράλληλα διευκολύνει τη µορφοποίηση. Η τοµή του τελικού φύλλου δίνεται στο σχήµα 9.3 Μία νεότερη εξέλιξη στα φύλλα του λευκοσιδήρου είναι η κατασκευή λεπτότερων φύλλων διπλής εξέλασης (DR, double reduced). Με την τεχνική αυτή το φύλλο έχει µεγαλύτερη µηχανική αντοχή και είναι πιο δύσκαµπτο, έτσι µπορεί να χρησιµοποιηθεί λεπτότερο φύλλο για την κατασκευή του δοχείου. Τα κοινά φύλλα λευκοσιδήρου έχουν πάχος mm, ενώ τα φύλλα διπλής εξέλασης mm. Τα φύλλα αυτά χρησιµοποιήθηκαν αρχικά σε αεριούχα ποτά αλλά σήµερα επεκτείνονται και σε άλλα κονσερβοποιηµένα προϊόντα. Επιχρωµιωµένος χάλυβας (TFS) Ο επιχρωµιωµένος χάλυβας καλείται και χάλυβας ελεύθερος κασσιτέρου (tin free steel, TFS). Κατασκευάζεται όπως ακριβώς και ο λευκοσίδηρος, αλλά µε ηλεκτρολυτική επικάλυψη µε χρώµιο. Η αδρανοποίηση γίνεται µε σχηµατισµό λεπτότατου στρώµατος οξειδίου του χρωµίου. Η τοµή του δίνεται στο σχήµα 9.3. Το κύριο πλεονέκτηµα του TFS είναι η χαµηλότερη τιµή. Παρουσιάζει όµως µικρότερη αντίσταση σε διάβρωση από ότι ο λευκοσίδηρος, µεγαλύτερη δυσκολία στη διαµόρφωση δοχείων και αδυναµία κασσιτεροκόλλησης στις ραφές. Η στεγανότητα στη ραφή των δοχείων γίνεται µε ηλεκτροκόλληση ή µε οργανικές κόλλες. Λόγω της µικρής αντοχής σε διάβρωση τα δοχεία από TFS επικαλύπτονται πάντα µε βερνίκι. Η επιφάνειά τους δέχεται καλύτερα τα βερνίκια και τα µελάνια εκτύπωσης και το υψηλότερο σηµείο τήξης επιτρέπει τη στερεοποίηση των βερνικιών σε ψηλότερη θερµοκρασία και µικρότερο χρόνο απ ότι ο λευκοσίδηρος. Σχήµα 9.3 Τοµή φύλλων λευκοσιδήρου και επιχρωµιωµένου χάλυβα (TFS). (Malin, 1980) Αλουµίνιο Το αλουµίνιο είναι ελαφρύτερο, λιγότερο σκληρό και περισσότερο εύκαµπτο από τα άλλα δύο υλικά. Tο καθαρό αλουµίνιο είναι πολύ ευλύγιστο και µαλακό και είναι κατάλληλο για την παραγωγή λεπτών φύλλων. Για την παρασκευή δύσκαµπτων περιεκτών χρησιµοποιούνται κράµατά του µε διάφορα στοιχεία, κυρίως µε µαγνήσιο και µαγγάνιο. Η προσθήκη αυτών των µετάλλων, ιδιαίτερα του µαγνησίου αυξάνει 267
276 σηµαντικά τη µηχανική αντοχή του υλικού αλλά µειώνει την αντίστασή του σε διάβρωση. Το αλουµίνιο εµφανίζει ικανοποιητική αντίσταση στην ατµοσφαιρική διάβρωση, λόγω του σχηµατισµού επιφανειακού προστατευτικού στρώµατος οξειδίου του αργιλίου. Άλλα πλεονεκτήµατά του, εκτός του ότι είναι ελαφρύ, εύκαµπτο και εποµένως εύκολα διαµορφώσιµο, είναι η µεγαλύτερη θερµική αγωγιµότητα από το λευκοσίδηρο και η αδράνειά του σε προϊόντα που περιέχουν θείο. Επίσης χαράσσεται εύκολα και µπορεί να χρησιµοποιηθεί σε κονσέρβες µε εύκολο άνοιγµα. Τα κύρια µειονεκτήµατά του είναι η ακριβή τιµή, η µικρότερη µηχανική αντοχή, η γρηγορότερη διάβρωση από υδαρή προϊόντα και η αντίδρασή του µε ορισµένα προϊόντα στα οποία προκαλεί αποχρωµατισµό. Για το λόγο αυτό τα δοχεία από αλουµίνιο προστατεύονται συνήθως µε κατάλληλο βερνίκι. Χρησιµοποιούνται ευρύτατα στη συσκευασία µπίρας και αναψυκτικών (στην Ελλάδα αποτελούν το αποκλειστικό µεταλλικό κουτί συσκευασίας αυτών των προϊόντων) σε συσκευασία θαλασσινών και προϊόντων κρέατος. Επίσης ως πώµατα εύκολου ανοίγµατος σε δοχεία από λευκοσίδηρο. Τα δοχεία αυτά έχουν χρησιµοποιηθεί για συσκευασία µπίρας και χυµών φρούτων χωρίς να εµφανίζεται ηλεκτρολυτική δράση του άκρου από αλουµίνιο και του κορµού από λευκοσίδηρο. Αντίθετα έντονη ηλεκτρολυτική δράση και γρήγορη διάτρηση του δοχείου παρατηρείται στην περίπτωση συσκευασίας προϊόντων που περιέχουν χλωριούχο νάτριο. Το αλουµίνιο χρησιµοποιείται και στην κατασκευή σωληναρίων που περιέχουν τρόφιµα. Κατασκευή µεταλλικών δοχείων Τα µεταλλικά δοχεία διακρίνονται σε δοχεία τριών τεµαχίων και δοχεία δύο τεµαχίων. Τα δοχείο τριών τεµαχίων αποτελείται από ένα ορθογώνιο φύλλο το οποίο σχηµατίζει το πλευρικό τοίχωµα που κλείνει µε διπλή πλάγια ραφή, τον πυθµένα που στερεώνεται στο πλευρικό τοίχωµα µε διπλή ραφή στο εργοστάσιο κατασκευής του δοχείου και το πώµα που στερεώνεται µε τον ίδιο τρόπο στο κονσερβοποιείο (σχήµα 9.4). Η πλάγια ραφή συγκολλάται µε κασσιτεροκόλληση µε κράµα Pb, Sn, Bi (soldering), ή µε ηλεκτροσυγκόλληση (welding). Η ηλεκτροσυγκόλληση είναι νεότερη τεχνική, δίνει ισχυρότερη ραφή και έχει τα πλεονεκτήµατα της απουσίας µολύβδου που είναι ιδιαίτερα τοξικό στοιχείο, της οικονοµίας µετάλλου, της καλύτερης εµφάνισης, της δυνατότητας επικάλυψης µε βερνίκι και τυπώµατος της ραφής. Η ηλεκτροσυγκόλληση γίνεται µε διαβίβαση ηλεκτρικού ρεύµατος σε δύο κυλινδρικά ηλεκτρόδια που προκαλεί σύντηξη των δύο άκρων του µεταλλικού 268
277 φύλλου ενώ ταυτόχρονα αυτά πιέζονται από τα ηλεκτρόδια ώστε να συγκολληθούν. Η επικάλυψη των δύο άκρων του φύλλου µπορεί να περιορίζεται σε πλάτος από 2-3 mm µέχρι και 0.4 mm (σχήµα 9.5). Η ηλεκτροσυγκόλληση µπορεί να εφαρµοσθεί και σε δοχεία από TFS στα οποία δεν είναι δυνατή η κασσιτεροσυγκόλληση. Σχήµα 9.4. Κύρια στάδια της κατασκευής λευκοσιδηρού δοχείου µε κασσιτεροσυγκόλληση. (Robertson, 1993) Σχήµα 9.5. ιαστάσεις κασσιτεροκολληµένης και ηλεκτροσυγκολληµένης πλάγιας ραφής. (Καρακασίδης, 1989) Μία νεότερη τεχνική, που όµως έχει περιορισµένη εφαρµογή είναι η συγκόλληση µε laser (laser welding). Τα πλεονεκτήµατα της τεχνικής είναι η µείωση του πλάτους της επικάλυψης σε mm και η ικανότητα χρήσης και σε TFS ενώ το κύριο µειονέκτηµα είναι η χαµηλή ταχύτητα συγκόλλησης. Μία άλλη τεχνική που 269
278 αναπτύχθηκε για δοχεία από TFS είναι η συγκόλληση µε χρήση θερµοπλαστικής κονίας πολυαµιδίου. Το δοχείο δύο τεµαχίων αποτελείται από ενιαίο κορµό και πυθµένα στον οποίο στερεώνεται το καπάκι µετά το γέµισµα του δοχείου στο κονσερβοποιείο. Το ενιαίο σώµα του δοχείου σχηµατίζεται από ένα µεταλλικό δίσκο ακολουθώντας δύο τεχνικές. Στην τενική DRD (draw and redraw) σχηµατίζεται αβαθές κύπελλο που διαµορφώνεται από διαδοχικές πρέσσες σε δοχείο µε ίδιο πάχος τοιχώµατος και πυθµένα που συµπίπτει µε το πάχος του αρχικού µεταλλικού δίσκου (σχήµα 9.6). Στην τεχνική DWI (drawn and wall ironed) σχηµατίζεται πάλι αβαθές κύπελλο του οποίου τα τοιχώµατα σιδερώνονται περνώντας από διαδοχικά περιστρεφόµενα ράουλα µειούµενης διαµέτρου ώστε το τελικό τους πάχος είναι περίπου το 1/3 του αρχικού και το ύψος του δοχείου υπερδιπλάσιο της διαµέτρου (σχήµα 9.7). Τα δοχεία DWI είναι τα ψηλότερα δοχεία που χρησιµοποιούνται στη µπίρα και τα αναψυκτικά, ενώ τα DRD είναι σχετικά αβαθή και χρησιµοποιούνται σε διάφορα τρόφιµα. Η τεχνική DRD µπορεί να χρησιµοποιηθεί για διαµόρφωση δοχείων από όλα τα υλικά, ενώ η τεχνική DWI µόνο από λευκοσίδηρο και αλουµίνιο. Το υλικό µπορεί να είναι ήδη λακαρισµένο στα DRD, αντίθετα η τεχνική DWI προκαλεί ρωγµές στο βερνίκι και εποµένως η επικάλυψη πρέπει να γίνει µετά. Ανεξάρτητα της τεχνικής διαµόρφωσης τα δοχεία δύο τεµαχίων παρουσιάζουν ορισµένα πλεονεκτήµατα: Έχουν μόνο µία διπλή ραφή εποµένως είναι ευκολότερο να διασφαλισθεί η ακεραιότητα της συσκευασίας. Σχήµα 9.6. ιαδοχικά στάδια κατασκευής δοχείων DRD. 1: Αρχικός δίσκος, 2: Τραβηγµένο κύπελλο, 3 και 4: Ξανατραβηγµένα κύπελλα, 5: Τελικό δοχείο. (Malin, 1980) 270
279 Σχήµα 9.7. ιαδοχικά στάδια κατασκευής δοχείων DWI. 1: Αρχικός δίσκος, 2 και 3: Τραβηγµένα και ξανατραβηγµένα κύπελλα, 4, 5 και 6: Πρώτο, δεύτερο και τρίτο στάδιο σιδερώµατος των τοιχωµάτων και σχηµατισµού του πυθµένα, 7: Τελειωµένο δοχείο. (Malin,1980) Η επικάλυψη µε βερνίκι και η προστασία από αυτό είναι πιο αποτελεσµατική. Η ραφή προκαλεί µια ανώµαλη επιφάνεια που δεν επικαλύπτεται εύκολα. Γίνεται οικονοµία υλικού, ιδιαίτερα σε σχέση µε τη διπλή ραφή µε κασσιτεροσυγκόλληση. Εφ όσον λείπει η ανωµαλία στην επιφάνεια που δηµιουργεί η ραφή, η διακόσµηση και εκτύπωση του δοχείου είναι πιο εύκολη και δηµιουργείται πολύ καλύτερο αισθητικό αποτέλεσµα. ιάβρωση-επικάλυψη µεταλλικών δοχείων Με την πάροδο του χρόνου το εσωτερικό των δοχείων διαβρώνεται και διαλύεται µέταλλο στο τρόφιµο µε τη µορφή άλατος ή επικάθεται ως υµένιο στα τοιχώµατα του δοχείου σε µορφή οξειδίου ή υδροξειδίου που µπορεί να υποστεί περαιτέρω οξείδωση. Στα λευκοσιδηρά δοχεία διαλύεται συνήθως πρώτα ο κασσίτερος που αποτελεί την εξωτερική επίστρωση του φύλλου µε ρυθµό που εξαρτάται από τη διαβρωτικότητα του τροφίµου, τον τύπο του λευκοσιδήρου και τη θερµοκρασία αποθήκευσης. Στην επιφάνεια του επικασσιτερωµένου φύλλου υπάρχουν πόροι και πιθανώς εκδορές που έχουν δηµιουργηθεί κατά την κατασκευή των δοχείων. Έτσι υπάρχουν µικρές περιοχές εκτεθειµένου κράµατος κασσιτέρου-σιδήρου ή και σιδήρου. Όταν λοιπόν ο λευκοσίδηρος έρθει σε επαφή µε το προϊόν δηµιουργείται γαλβανικό στοιχείο µεταξύ κασσιτέρου σιδήρου, µε τον σίδηρο να είναι ανοδικός ως προς τον κασσίτερο και να οξειδώνεται και διαλύεται αυτός επειδή είναι ηλεκτροθετικότερος. 271
280 Αυτό συµβαίνει κατά τη διάβρωση στην εξωτερική επιφάνεια του δοχείου και στο εσωτερικό του όταν είναι συσκευασµένα προϊόντα, όπως αλκοολούχα ποτά που δεν περιέχουν οξέα ή διαλύµατα που δεν περιέχουν συστατικά µε τα οποία να αντιδρά ο κασσίτερος. Η διάβρωση αυτή ονοµάζεται διάβρωση µε βελονισµό και καταλήγει σε τρύπηµα του δοχείου και επιµόλυνση του προϊόντος (σχήµα 9.8 δ-στ). Αντίθετα όταν το προϊόν περιέχει περιέχει οργανικά οξέα ή αµινοξέα, όπως συµβαίνει µε τα περισσότερα τρόφιµα, µε τα οποία ο κασσίτερος µπορεί να σχηµατίσει σταθερά σύµπλοκα, συµβαίνει αναστροφή της πολικότητας και εποµένως οξειδώνεται και διαλύεται κατά προτίµηση ο κασσίτερος, ενώ προστατεύεται ο σίδηρος. Αυτή είναι η πιο συνηθισµένη περίπτωση διάβρωσης στο εσωτερικό του δοχείου. Εάν η διάβρωση προχωρήσει πολύ εκτίθεται µεγάλη επιφάνεια σιδήρου, η προστασία από τον κασσίτερο δεν είναι πλέον επαρκής και αρχίζει να διαλύεται και σίδηρος (σχήµα 9.8 α-γ). Οι αναγωγικές δράσεις που συµβαίνουν στα πρώτα στάδια της διάβρωσης είναι η αναγωγή οξυγόνου, νιτρικών, θείου κ.λ.π. Το οξυγόνο που πιθανώς είναι διαλυµένο στο τρόφιµο ή που υπάρχει στον κενό χώρο, στο άνω µέρος της κονσέρβας προκαλεί έντονη διάβρωση και τη δηµιουργία συχνά µιας γραµµής στη διαχωριστική επιφάνεια τροφίµου/κενού χώρου όπου έχει αποκαλυφθεί ο χάλυβας. Εάν το συµπύκνωµα που σχηµατίζεται στον κενό χώρο µετά τη θερµική επεξεργασία είναι ελαφρά όξινο µπορεί να σχηµατισθεί και σκουριά. Τα προβλήµατα αυτά µπορούν να αποφευχθούν µε καλή απαέρωση πριν το κλείσιµο του δοχείου και αποµάκρυνση του αέρα από τους ιστούς του τροφίµου µε ζεµάτισµα. Η διάβρωση επιταχύνεται από το θείο που υπάρχει στα τρόφιµα (π.χ. σε θειούχα αµινοξέα). Το θείο αντιδρά γρήγορα µε το σίδηρο προς σχηµατισµό θειούχου σιδήρου που προκαλεί µαύρες κηλίδες στα τρόφιµα, ενώ σε εκτεταµένη διάλυση υπάρχει κίνδυνος διάτρησης του δοχείου. Επίσης το διοξείδιο του θείου που προστίθεται στα τρόφιµα ως συντηρητικό ή ως µέσο αποχρωµατισµού µπορεί να αναχθεί από τον κασσίτερο προς ιόντα θείου ή θείο με ταυτόχρονη οξείδωση-διάλυση του κασσιτέρου και σχηματισμό μαύρων κηλίδων. Σχήµα 9.8. ιάβρωση λευκοσιδηρών δοχείων. (α)-(γ): διαλύεται κατά προτίµηση ο κασσίτερος, (δ)-(στ): διαλύεται κατά προτίµηση ο σίδηρος. (Καρακασίδης, 1989) 272
281 Τα νιτρικά ιόντα που περιέχονται σε τρόφιµα (προερχόµενα από λίπανση) είναι έντονα οξειδωτικά σε ph<6 και προκαλούν διάλυση του στρώµατος του κασσιτέρου πάρα πολύ γρήγορα. Αφού εξαντληθούν οι αποπολωτές η µόνη αντίδραση που συµβαίνει είναι η αναγωγή υδρογονοκατιόντων και η παραγωγή υδρογόνου. Εάν η µεταλλική κονσέρβα διογκωθεί από την πίεση του εκλυόµενου υδρογόνου το περιεχόµενο σε µεταλλοϊόντα έχει περάσει τα επιτρεπόµενα όρια και επί πλέον είναι αδύνατο να πωληθεί. Τα επιχρωµιωµένα δοχεία υφίστανται ευκολότερα διάβρωση από τα λευκοσιδηρά, ενώ τα αλουµινένια έχουν αντοχή σε διάβρωση η οποία όµως µειώνεται όταν χρησιµοποιούνται κράµατα ιδιαίτερα µε προσθήκη Mg για την αύξηση της µηχανικής αντοχής. Για προστασία του τροφίµου από διάλυση των µετάλλων της κονσέρβας και αντίστροφα γίνεται επικάλυψη. Η επικάλυψη γίνεται σε όλα τα επιχρωµιωµένα και αλουµινένια δοχεία, ενώ δεν γίνεται πάντα στα λευκοσιδηρά. Εντούτοις και στα λευκοσιδηρά εφαρµόζεται επικάλυψη όταν υπάρχει κίνδυνος σχηµατισµού µαύρων κηλίδων. Τα επικαλυπτικά που χρησιµοποιούνται ανήκουν στους ακόλουθους βασικούς τύπους: ολεορητίνες, φαινολικά, βινυλικά και εποξειδικές ρητίνες. Όλα αυτά αποδίδονται από τη βιοµηχανία µε το γενικό όρο σµάλτα (enamels) ή βερνίκια (lacquers). Οι ολεορητίνες είναι τα πιο κοινά επικαλυπτικά. Ο τύπος R είναι ο κοινός τύπος, ενώ ο τύπος C περιέχει 15% ZnO που αντιδρά µε τα σουλφίδια και προστατεύει από τις αµαυρώσεις. Τα φαινολικά επικαλυπτικά είναι λιγότερο διαπερατά και ανθεκτικότερα σε χηµικά από τις ολεορητίνες και δεν µαλακώνουν από τα λίπη. Είναι όµως λιγότερο εύκαµπτα και δίνουν οσµή σε ορισµένα τρόφιµα. Χρησιµοποιούνται κυρίως για θαλασσινά, κρέας, ζωοτροφές και γενικά προϊόντα πλούσια σε λιπαρά Οι εποξειδικές ρητίνες εµφανίζουν αντοχή σε υψηλές θερµοκρασίες, είναι εύκαµπτες και δεν προσδίδουν οσµή στα τρόφιµα. Τα βινυλικά είναι σκληρά και άοσµα, µε ιδιαίτερα υψηλή αντοχή σε όξινα προϊόντα. Επειδή έχουν µικρή αντοχή σε ατµό δεν µπορούν να χρησιµοποιηθούν µόνα τους ως επικαλυπτικά σε προϊόντα που υποβάλλονται σε θερµική κατεργασία ανώτερης θερµοκρασίας από τους 95 C και συνήθως επιστρώνονται σε άλλο επικαλυπτικό, όπως ολεορητίνες ή φαινολικά ή χρησιµοποιούνται για πρόσθετη επικάλυψη στη ραφή. Εκτός των παραπάνω τύπων χρησιµοποιούνται και τροποποιηµένα επικαλυπτικά που προκύπτουν από συνδυασµούς των παραπάνω. Η επικάλυψη γίνεται πριν τη διαµόρφωση του δοχείου στα δοχεία τριών τεµαχίων και στα δοχεία DRD, και µετά τη διαµόρφωση στα δοχεία DWI, επειδή το επικαλυπτικό 273
282 σπάει κατά τη διαµόρφωση. Στη ραφή δηµιουργείται ανώµαλη επιφάνεια και ασυνέχεια της επικάλυψης, από την οποία συχνά αρχίζει η διάβρωση του δοχείου. Έτσι συνήθως γίνεται πρόσθετη επικάλυψη για προστασία. Η διάβρωση στα λακαρισµένα κουτιά αρχίζει από πόρους και σκασίµατα του επικαλυπτικού. Ο κασσίτερος διαλύεται αρχικά στους πόρους. Εάν συνεχίσει να διαλύεται ο κασσίτερος έναντι του σιδήρου παρατηρείται τοπική αποφλοίωση του επικαλυπτικού, γρήγορη τοπική απώλεια της προστατευτικής επιφάνειας του κασσιτέρου και προσβολή του σιδήρου ταχύτερη από ότι στα αλακάριστα δοχεία. Εάν διαλύεται ο σίδηρος έναντι του κασσιτέρου µπορεί και πάλι γρήγορα να παρατηρηθεί διάτρηση του δοχείου. Στο σχήµα 9.9 φαίνονται οι δύο τύποι της διάβρωσης σε λακαρισµένα δοχεία. Τα προβλήµατα διάβρωσης λύνονται µε αύξηση του πάχους του επικαλυπτικού σε όξινα προϊόντα (µέχρι 12 µm) επιλογή κατάλληλου ανθεκτικού επικαλυπτικού και καλή επικάλυψη της ραφής (συχνά διπλή). Σχήµα 9.9. ιάβρωση λακαρισµένων δοχείων. Α: ιάλυση κασσιτέρου, τοπική αποφλοίωση, Β: ιάλυση σιδήρου, διάτρηση δοχείου. (Καρακασίδης,1989) Μεταλλικά φύλλα Τα µεταλλικά φύλλα που χρησιµοποιούνται στη συσκευασία τροφίµων είναι κυρίως φύλλα αλουµινίου. Στην κατασκευή τους χρησιµοποιείται αλουµίνιο καθαρότητας >99.4% και το πάχος τους κυµαίνεται µεταξύ 4.3 και 152 µm. Σε πάχος µεγαλύτερο από 25 µm είναι αδιαπέραστο από υδρατµούς, αέρια, φως χηµικούς και βιολογικούς ρυπαντές, ενώ σε µικρότερα πάχη εµφανίζει ορισµένη διαπερατότητα λόγω πόρων του φύλλου. Άλλα πλεονεκτήµατα του αλουµινόφυλλου, σε σύγκριση µε άλλα εύκαµπτα υλικά συσκευασίας είναι ότι δεν προσβάλλεται από το φως, από λίπη και έλαια και από έντοµα και µικροοργανισµούς, δεν απορροφά οσµές, δεν καίγεται και δεν είναι τοξικό. Τα λεπτά φύλλα αλουµινίου χρησιµοποιούνται παραδοσιακά στην περιτύλιξη σοκολάτας, διαφόρων γλυκών, τσίχλας και τεµαχίων κατεργασµένου τυριού. Τα φύλλα µεγαλύτερου πάχους (50 µm) χρησιµοποιούνται στην κατασκευή πωµάτων για φιάλες. Ηµίσκληροι περιέκτες κατασκευάζονται από φύλλο πάχους μm και χρησιμοποιούνται σε κατεψυγμένα τρόφιμα, είδη αρτοποιίας, έτοιμα και ημιέτοιμα γεύματα. 274
283 Τα τελευταία χρόνια τα φύλλα αλουµινίου χρησιµοποιούνται πολύ στην κατασκευή πολυστρωµατικών φύλλων (laminates) από χαρτί/αλουµίνιο, πλαστικό/αλουµίνιο ή χαρτί/αλουµίνιο/πλαστικό, τα οποία αξιοποιούν τις εξαιρετικές ιδιότητες φραγής του αλουµινόφυλλου και τις µηχανικές αντοχές των άλλων υλικών Ξύλο. Η χρήση του ξύλου για την κατασκευή κιβωτίων ήταν πολύ διαδεδοµένη παλαιότερα, λόγω της χαµηλής τιµής του υλικού. Σήµερα, λόγω του υψηλού κόστους και της προσφοράς φθηνών υποκαταστάτων, η χρήση του ξύλου έχει περιορισθεί πάρα πολύ. Τα ξύλινα σκελετοκιβώτια (καφάσια) για τη συσκευασία νωπών οπωροκηπευτικών έχουν αντικατασταθεί σε µεγάλο βαθµό από πλαστικά ή χαρτοτελλάρα. Ξύλο χρησιµοποιείται κυρίως για κατασκευή βαρελιών κρασιού, µπίρας, ή φέτας και για κατασκευή κιβωτίων για ξηρά φρούτα Πλαστικά Τα πλαστικά υλικά συσκευασίας είναι πολυµερή υλικά διαφόρου χηµικής σύστασης, δοµής και φυσικών ιδιοτήτων. Σε αυτά ταξινοµούνται και τα φυσικά πολυµερή, όπως τα φύλλα αναγεννηµένης κυτταρίνης (σελοφάν), τα πολυµερή µε βάση το άµυλο, τις πρωτεΐνες κ.λ.π. Στη συσκευασία τροφίµων χρησιµοποιούνται δύσκαµπτοι πλαστικοί περιέκτες και εύκαµπτες πλαστικές µεµβράνες. Ορισµένα πολυµερή υλικά χρησιµοποιούνται και για τις δύο κατηγορίες περιεκτών, αλλά στις εύκαµπτες συσκευασίες χρησιµοποιούνται πολύ περισσότερα είδη από ότι στις δύσκαµπτες. Στον Πίνακα 9.2 παρουσιάζονται τα κυριότερα υλικά που χρησιµοποιούνται στις εύκαµπτες και δύσκαµπτες συσκευασίες και οι συνήθεις συντµήσεις τους, οι οποίες χρησιµοποιούνται και στο κείµενο. Με βάση τη χηµική σύσταση µπορούµε να διακρίνουµε τις παρακάτω κατηγορίες πλαστικών: Πολυολεφίνες Ως υλικά συσκευασίας χρησιµοποιούνται το πολυαιθυλένιο (-CH 2 -CH 2 -) n και το πολυπροπυλένιο (-CH 2 -CHCH 3 -) n. To πολυαιθυλένιο είναι το ευρύτερα χρησιµοποιούµενο από όλα τα πλαστικά υλικά συσκευασίας για τα τρόφιµα. ιακρίνεται σε πολυαιθυλένιο χαµηλής πυκνότητας (LDPE) και πολυαιθυλένιο υψηλής πυκνότητας (HDPE) ανάλογα µε την ύπαρξη διακλαδώσεων µεταξύ των µακροµοριακών αλυσίδων. Και τα δύο υλικά χρησιµοποιούνται στην κατασκευή δύσκαπτων περιεκτών και σε µορφή µεµβράνης για εύκαµπτες συσκευασίες. Το πολυαιθυλένιο χαµηλής πυκνότητας είναι εύκαµπτο, έχει µεγάλη αντοχή σε κρούση, ενώ µαλακώνει σε θερµοκρασία >100 C. Η διαπερατότητά του σε υδρατμούς είναι μικρή, αλλά η διαπερατότητά του σε αέρια μεγάλη. Είναι ανθεκτικό σε οξέα, βάσεις και διαλύματα αλάτων, απορροφά όμως πτητικά συστατικά από ορισμένα 275
284 συσκευασµένα τρόφιµα και είναι ακατάλληλο για τη συσκευασία χυµών και παρόµοιων τροφίµων. Πίνακας 9.2. Πολυµερή υλικά που χρησιµοποιούνται σε δύσκαµπτους και εύκαµπτους περιέκτες ύσκαµπτοι περιέκτες Εύκαµπτοι περιέκτες ABS ακρυλινιτρίλιο-βουταδιένιο-στυρένιο ABS ακρυλινιτρίλιο-βουταδιένιο-στυρένιο Cellulose acetate οξεική κυτταρίνη ΕVA αιθυλένιο-οξεικός βινυλεστέρας HDPE πολυαιθυλένιο χαµηλής πυκνότητας EVAl αιθυλένιο-βινυλική αλκόλη LDPE πολυαιθυλένιο υψηλής πυκνότητας HDPE πολυαιθυλένιο χαµηλής πυκνότητας PETP πολυαιθυλενοτερεφθαλικός εστέρας LDPE πολυαιθυλένιο υψηλής πυκνότητας PP πολυπροπυλένιο MS σελοφάν επικαλυµένο µε νιτροκυτταρίνη PS πολυστυρένιο MXDT σελοφάν επικαλυµένο µε PVdC στη µία πλευρά PVC πολυβινυλοχλωρίδιο MXXT σελοφάν επικαλυµένο µε PVdC στις δύο πλευρές Nylon πολυαµίδιο OPP προσανατολισµένο πολυπροπυλένιο OPS προσανατολισµένο πολυστυρένιο PET πολυεστέρας PETP πολυαιθυλενοτερεφθαλικός εστέρας PP πολυπροπυλένιο PS πολυστυρένιο PVAl πολυβινυλική αλκόλη PVC πολυβινυλοχλωρίδιο PVdC πολυβινυλιδενοχλωρίδιο Saran PVC-PVdC SAN στυρένιο-ακρυλονιτρίλιο Το πολυαιθυλένιο υψηλής πυκνότητας έχει πέντε φορές µικρότερη διαπερατότητα σε υδρατµούς και αέρια από το LDPE, παρουσιάζει θερµική σταθερότητα µέχρι τους 120 C, αλλά έχει µικρότερη αντοχή σε κρούση. Οι λοιπές ιδιότητες του είναι παρόµοιες µε το LDPE. Οι µεµβράνες πολυαιθυλενίου παρέχουν δυνατότητα θερµικής συγκόλλησης και συνδυάζονται άριστα µε άλλα υλικά, όπως το χαρτί και το αλουµινόφυλλο για την παραγωγή σύνθετων πολυστρωµατικών υλικών. Το πολυπροπυλένιο (PP) χρησιµοποιείται επίσης σε εύκαµτες και δύσκαµτες συσκευασίες. Παρουσιάζει στεγανότητα ενδιάµεση των LDPE και HDPE, πολύ χαµηλή διαπερατότητα από λίπη, θερµική σταθερότητα έως τους C, αλλά µικρότερη αντοχή σε κρούση. Η αντοχή του σε αντιδραστήρια είναι παρόµοια µε των πολυαιθυλενίων. Βασικό πλεονέκτημά του είναι η καλή εμφάνιση που οφείλεται στη στιλπνότητα και τη διαύγεια καθώς και η αντοχή του στο τσάκισμα. 276
285 Σε µορφή µεµβρανών χρησιµοποιείται συχνά µετά από διεργασία προσανατολισµού (OPP, oriented poly-propylene) για βελτίωση των αντοχών και της εµφάνισης και παρουσιάζει µέτρια δυνατότητα θερµοσυγκόλλησης. Πολυβινυλοπαράγωγα Τα πολυβινυλοπαράγωγα έχουν το γενικό τύπο (-CH 2 -CXY-) n όπου τα Χ και Y είναι είτε άτοµα υδρογόνου είτε άλλοι υποκαταστάτες, όπως χλώριο, βενζολικός δακτύλιος, υδροξύλιο κ.λ.π. Οι ιδιότητες των πολυβινυλοπαραγώγων εξαρτώνται από τη φύση του υποκαταστάτη, τη διαµόρφωση των οµάδων στην αλυσίδα, το µοριακό βάρος του πολυµερούς, την κρυσταλλικότητα και τον προσανατολισµό. Επίσης οι ιδιότητες εξαρτώνται από την προσθήκη πλαστικοποιητή, οπότε αυξάνεται η διαπερατότητα και η διαλυτότητα του πλαστικού. Γενικά η ύπαρξη πολικών υποκαταστατών αυξάνει τη διαπερατότητα από υδρατµούς και πολικά µόρια. Η µηχανική αντοχή, η αντοχή σε υψηλές θερµοκρασίες και σε προσβολή από χηµικά και η στεγανότητα αυξάνονται µε το βαθµό κρυσταλλικότητας. Τα πολυβινυλοπαράγωγα που χρησιµοποιούνται στη συσκευασία τροφίµων είναι: Πολυστυρένιο (PS) (-CH 2 -CH-o-) n : Είναι διαυγές, σκληρό και εύθραυστο, µε µικρή στεγανότητα σε υδρατµούς και µέση σε αέρια και θερµοκρασία ευπλαστότητας C. Η αντοχή του δύσκαµπτου διαυγούς υλικού µπορεί να βελτιωθεί µε προσθήκη πολυβουταδιενίου, χάνεται όµως η διαύγειά του. Οι µεµβράνες πολυστυρενίου χρησιµοποιούνται σε απλή µορφή ή κατόπιν προσανατολισµού σε ορισµένη θερµοκρασία (ΟPS). Πολυβινυλοχλωρίδιο (PVC) (-CH 2 -CHCl-) n : Είναι σκληρό και εύθραυστο υλικό, µε προσθήκη όµως πλαστικοποιητών γίνεται µαλακό και εύκαµπτο και µπορεί να χρησιµοποιηθεί στην κατασκευή ηµίσκληρων περιεκτών ή µεµβρανών. Το μη πλαστικοποιηµένο υλικό παρουσιάζει εξαιρετική αντοχή στα λιπαρά. Η διαπερατότητα του στους υδρατµούς είναι µεγαλύτερη των πολυολεφινών, σε αέρια όµως πολύ µικρή. Οι λεπτές µεµβράνες έχουν µεγάλη διαύγεια και µεγάλη διαπερατότητα σε αέρια. Το PVC γίνεται εύπλαστο σε χαµηλή θερµοκρασία (82 C) και αρχίζει να αποικοδοµείται σε λίγο ψηλότερη, ενώ προσβάλλεται και από το ηλιακό φως. Γι αυτό προστίθενται σταθεροποιητές. Οι πλαστικοποιητές και οι σταθεροποιητές είναι ουσίες τοξικές που µεταναστεύουν στα τρόφιµα και εποµένως είναι απαραίτητος ο έλεγχος καταλληλότητας της συσκευασίας για χρήση σε τρόφιµα. Πολυβινυλιδενοχλωρίδιο (PVdC) µεµβρανών, σε συνδυασµό συνήθως (-CH 2 -CCl 2 -) n : Χρησιµοποιείται σε μορφή µε άλλα υλικά, λόγω της εξαιρετικής στεγανότητας που παρουσιάζει και της άριστης θερμοσυγκόλησης. Είναι κατάλληλο, όπως και το PVC για συρρικνούμενο περιτύλιγμα. Συμπολυμερές βινυλοχλωριδίου- 277
286 βινυλιδενοχλωριδίου, γνωστό ως Saran, χρησιµοποιείται για την κατασκευή µεµβρανών µε πολύ µικρή διαπερατότητα σε αέρια και υδρατµούς. Πολυβινυλική αλκοόλη (PVAl) (-CH 2 -CHOH-) n : Χρησιµοποιείται ως µεµβράνη. Το συµπολυµερές α ιθυλενίου-βινυλικής α λκοόλης ( EVAl) έχει πολύ µικρή διαπερατότητα σε αέρια αλλά µεγάλη ευαισθησία σε υδρατµούς. Για το λόγο αυτό χρησιµοποιείται στο εσωτερικό σύνθετων πολυστρωµατικών υλικών. Οξεικός πολυβινυλεστέρας (-CH 2 -CHOCOCH 3 -) n : Mορφοποιείται ως εύκαµπτη µεµβράνη. Επίσης µε µορφή µεµβράνης χρησιµοποιείται και συµπολυµερές βινυλοχλωριδίου-οξεικού βινυλεστέρα. Πολυεστέρες Οι πολυεστέρες (PET) έχουν το γενικό τύπο HO(-CO-R-CO-O-R -O-) n H. Ο πολυεστέρας που χρησιµοποιείται συνήθως στη συσκευασία τροφίµων είναι ο πολυαιθυλενο-τερεφθαλικός (PETP). Έχει άριστη διαφάνεια, καλές µηχανικές αντοχές, ελάχιστη διαπερατότητα υδρατµών και αερίων, αντοχή σε οξέα, βάσεις, λιπαρά και διαλύτες και σταθερότητα σε υψηλές θερµοκρασίες. Οι φιάλες από PETP αντέχουν σε πίεση µέχρι 4 atm και δεν µαλακώνουν µέχρι τους 250 C. Οι µεµβράνες διατηρούν επίσης τις ιδιότητές τους σε υψηλές θερµοκρασίες και µπορούν να χρησιµοποιηθούν στη συσκευασία τροφίµων που πρέπει να θερµανθούν συσκευασµένα πριν την κατανάλωση. Τα πλεονεκτήµατα του PETP οδηγούν σε συνεχή διεύρυνση της χρήσης τους παρ όλο το µεγάλο κόστος. Στις εύκαµπτες συσκευασίες εκτός του PETP χρησιµοποιείται και ο πολυβουτυλενο-τερεφθαλικός εστέρας (PBTP). Πολυακρυλικά Οι κύριοι εκπρόσωποι αυτής της κατηγορίας είναι ο πολυµεθακρυλικός εστέρας (-CH 2 -CCH 3 COOCH 3 -) n, το πολυακρυλονιτρίλιο (-CH 2 -CHCΝ-) n και το συµπολυµερές ακρυλονιτριλίου-µεθακρυλικού εστέρα (Barex). Έχουν καλές µηχανικές και χηµικές ιδιότητες και πολύ µικρή διαπερατότητα σε αέρια. Ο πολυµεθακρυλικός εστέρας είναι πολύ ακριβό υλικό και γι αυτό χρησιµοποιείται ελάχιστα στη συσκευασία τροφίµων. Το πολυακριλονιτρίλιο έχει απαγορευθεί για χρήση στα τρόφιµα λόγω µετανάστευσης του µονοµερούς ακρυλονιτριλίου που είναι καρκινογόνο. Το συµπολυµερές Barex αναπτύχθηκε αρχικά για την κατασκευή φιαλών συσκευασίας αεριούχων αναψυκτικών, αλλά έχει και αυτού απαγορευθεί η χρήση στις ΗΠΑ. Ένα άλλο συµπολυµερές µε εξ ίσου καλές ιδιότητες, είναι το συµπολυµερές ακρυλινιτριλίου-βουταδιενίου-στυρενίου (ABS) το οποίο χρησιµοποιείται στην κατασκευή ηµίσκληρων περιεκτών και του οποίου η χρήση επιτρέπεται στις ΗΠΑ µε την προϋπόθεση ότι η µεταφερόµενη ποσότητα ακρυλονιτριλίου στο τρόφιµο δεν 278
287 υπερβαίνει τα 50 ppb. Παρόµοιες απαγορεύσεις δεν ισχύουν στην ΕΕ. Ανάλογες ιδιότητες και χρήσεις έχει και το συµπολυµερές στυρενίου-ακρυλονιτριλίου (SAN). Πολυαµίδια Τα πολυαµίδια που χρησιµοποιούνται στη συσκευασία τροφίµων είναι τα: nylon 6 (-ΝΗ-(CH 2 ) 5 -CO-) n nylon 6.6 (-ΝΗ-(CH 2 ) 6 -NH-CO-(CH 2 ) 4 -CO-) n nylon 11 (-ΝΗ-(CH 2 ) 10 -CO-) n Χρησιµοποιούνται σε µορφή µεµβρανών και έχουν µικρή διαπερατότητα σε αέρια, καλές µηχανικές αντοχές και αντοχή σε λιπαρά, αλλά η ιδιαίτερα σηµαντική ιδιότητά τους είναι η αντοχή σε υψηλή θερµοκρασία (µέχρι 250 C) που επιτρέπει τη χρήση τους σε συσκευασία τροφίµων που πρόκειται να ψηθούν συσκευασµένα. Τα πολυαµίδια είναι ευαίσθητα στην υγρασία και διαπερατά από υδρατµούς γι αυτό χρησιµοποιούνται κυρίως σε πολυστρωµατικά υλικά µε πολυαιθυλένιο. Ιονοµερή Είναι ιονικά πολυµερή. Το µόνο ιονοµερές που παράγεται εµπορικά είναι το πολυµερές του αιθυλενίου που περιέχει και καρβοξυλοµάδες και έχει το εµπορικό όνοµα Surlyn A. Χρησιµοποιείται κυρίως µε τη µορφή µεµβράνης. Αναγεννηµένη κυτταρίνη (σελοφάν) Η αναγεννηµένη κυτταρίνη ανοίκει στα φυσικά πολυµερή. Είναι λεπτή διαφανής µεµβράνη, µε µικρή διαπερατότητα σε αέρια, αλλά µεγάλη ευαισθησία και διαπερατότητα σε υδρατµούς, καθώς και αδυναµία θερµοσυγκόλλησης. Τα µειονεκτήµατα αυτά µπορούν να υπερνικηθούν µε διάφορες επικαλύψεις. Σελοφάν επικαλυµµένο µε νιτροκυτταρίνη (MS) έχει µικρή διαπερατότητα σε υδρατµούς και επικαλυµµένο µε PVdC (MXDT, MXXT) ακόµα µικρότερη, ενώ παράλληλα επιδέχονται θερµοσυγκόλληση. Άλλα επικαλυπτικά που χρησιµοποιούνται είναι το Saran και το LDPE. Μη επικαλυµµένες µεµβάνες χρησιµοποιούνται σε προϊόντα που είναι απαραίτητη η διέλευση υγρασίας για να αποφευχθεί η ανάπτυξη µυκήτων, ενώ επικαλυµµένες µεµβράνες για υγροσκοπικά προϊόντα. Οξεική κυτταρίνη Παρουσιάζει εξαιρετική διαφάνεια και εµφάνιση και χρησιµοποιείται σε δύσκαµπτους περιέκτες ή σε εύκαµπτες συσκευασίες σαν απλή µεµβράνη ή σε πολυστρωµατικά υλικά. Είναι ευαίσθητη στην υγρασία και δεν θερµοσυγκολλάται. Έχει µέση διαπερατότητα σε αέρια και υδρατµούς και γι αυτό χρησιµοποιείται σε προϊόντα που αναπνέουν, όπως φρούτα. 279
288 Μορφοποίηση και κατεργασίες πλαστικών υλικών συσκευασίας Οι δύσκαµπτοι πλαστικοί περιέκτες µορφοποιούνται µε έγχυση σε καλούπι (διαφόρων µορφών δοχεία) ή µε εµφύσηση σε συνδυσµό µε έγχυση ή εξώθηση (φιάλες). Η διαδικασία της εκτατικής εµφύσησης που βρίσκει µεγάλη εφαρµογή στην παραγωγή φιαλών από PET φαίνεται στο σχήµα Αντί για απλή εξώθηση µπορεί να χρησιµοποιηθεί συνεξώθηση δύο ή περισσότερων υλικών οπότε η παραγόµενη φιάλη εµφανίζει το συνδυασµό των ιδιοτήτων αυτών. Κεσεδάκια, δίσκοι και ρηχοί περιέκτες σχηµατίζονται επίσης µε θερµοµορφοποίηση. Μορφοποίηση µε συµπίεση χρησιµοποιείται στην κατασκευή πωµάτων από θερµοσκληρόµενα υλικά. Σχήµα ιαδικασία εκτατικής εµφύσησης για την παραγωγή φιαλών από PET. (Παπαδάκης, 1997) Οι µεµβράνες για τις εύκαµπτες συσκευασίες παράγονται µε εξώθηση µέσω λεπτής σχισµής ή συµπίεση ανάµεσα σε περιστρεφόµενους κυλίνδρους. Στο σχήµα 9.11 παρουσιάζονται τα βασικά στοιχεία ενός εκβολέα για την παραγωγή επίπεδης µεµβράνης, ενώ στο σχήµα 9.12 η παραγωγή µεµβράνης σε σχήµα κυλίνδρου για κατασκευή εύκαµπτων σακιδίων. Συχνά για την παρασκευή µεµβρανών προστίθεται στην πρώτη ύλη πλαστικοποιητής. 280
 1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
ΑΛΛΗΛΕΠΙ ΡΑΣΕΙΣ ΚΑΙ ΕΣΜΟΙ ΠΟΥ ΚΑΘΟΡΙΖΟΥΝ ΤΗΝ ΠΡΩΤΕΪΝΙΚΗ ΟΜΗ
 ΑΛΛΗΛΕΠΙ ΡΑΣΕΙΣ ΚΑΙ ΕΣΜΟΙ ΠΟΥ ΚΑΘΟΡΙΖΟΥΝ ΤΗΝ ΠΡΩΤΕΪΝΙΚΗ ΟΜΗ 1. Στερεοχηµκοί περιορισµοί 1 2. Ηλεκτροστατικές Αλληλεπιδράσεις (42-84 kj/mol) Πρωτεΐνες = πολυηλεκτρολύτες λόγω ιοντικών R των aµινοξέων (Asp,
ΑΛΛΗΛΕΠΙ ΡΑΣΕΙΣ ΚΑΙ ΕΣΜΟΙ ΠΟΥ ΚΑΘΟΡΙΖΟΥΝ ΤΗΝ ΠΡΩΤΕΪΝΙΚΗ ΟΜΗ 1. Στερεοχηµκοί περιορισµοί 1 2. Ηλεκτροστατικές Αλληλεπιδράσεις (42-84 kj/mol) Πρωτεΐνες = πολυηλεκτρολύτες λόγω ιοντικών R των aµινοξέων (Asp,
www.chemeng.ntua.gr/courses/trbio
 1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
1 ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΒΙΟΛΟΓΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΚΑΙ ΠΡΟΪΟΝΤΩΝ (ΤΡΟΦΙΜΑ-ΒΙΟΤΕΧΝΟΛΟΓΙΑ) Περιεχόµενο - Σκοπός του Μαθήµατος 6 ο ΕΞΑΜΗΝΟ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Ο ΗΓΙΕΣ ΜΑΘΗΜΑΤΟΣ Το µάθηµα Επιστήµη και Μηχανική Βιολογικών
πρωτεΐνες πολυμερείς ουσίες δομούν λειτουργούν λευκώματα 1.Απλές πρωτεΐνες 2.Σύνθετες πρωτεΐνες πρωτεΐδια μη πρωτεϊνικό μεταλλοπρωτεΐνες
 ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΠΡΩΤΕΙΝΕΣ Οι πρωτεΐνες είναι πολυμερείς ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Πρωτεΐνες είναι οι ουσίες που κυρίως δομούν και λειτουργούν τους οργανισμούς. Λέγονται και λευκώματα λόγω του λευκού
ΚΕΦΑΛΑΙΟ 1 ΣΤΟΙΧΕΙΑ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ
 ΚΕΦΑΛΑΙΟ 1 ΣΤΟΙΧΕΙΑ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ 1. ΠΡΩΤΕΪΝΕΣ 1.1 Εισαγωγή Οι πρωτεΐνες είναι πολύπλοκα µακροµόρια που αποτελούν περισσότερο από το 50% του ξηρού βάρους των ζώντων κυττάρων. Παίζουν καθοριστικό ρόλο
ΚΕΦΑΛΑΙΟ 1 ΣΤΟΙΧΕΙΑ ΧΗΜΕΙΑΣ ΤΡΟΦΙΜΩΝ 1. ΠΡΩΤΕΪΝΕΣ 1.1 Εισαγωγή Οι πρωτεΐνες είναι πολύπλοκα µακροµόρια που αποτελούν περισσότερο από το 50% του ξηρού βάρους των ζώντων κυττάρων. Παίζουν καθοριστικό ρόλο
Θρεπτικές ύλες Τρόφιµα - Τροφή
 ΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ 1 Θρεπτικές ύλες Τι καλούµε θρεπτικές ύλες; Ποιες είναι; Τρόφιµα Τι καλούµε τρόφιµο; Χηµεία Τροφίµων Θρεπτικές ύλες Τρόφιµα - Τροφή Προϋπόθεση για να χαρακτηριστεί ένα προϊόν τρόφιµο; 2
ΧΗΜΕΙΑ ΤΡΟΦΙΜΩΝ 1 Θρεπτικές ύλες Τι καλούµε θρεπτικές ύλες; Ποιες είναι; Τρόφιµα Τι καλούµε τρόφιµο; Χηµεία Τροφίµων Θρεπτικές ύλες Τρόφιµα - Τροφή Προϋπόθεση για να χαρακτηριστεί ένα προϊόν τρόφιµο; 2
Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου
 Πρωτεΐνες 1 Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου Οι πρωτεΐνες είναι πολύπλοκα µόρια που περιέχουν 2 Είναι πηγές αµινοξέων (απαραίτητα, µη απαραίτητα)
Πρωτεΐνες 1 Από το Ελληνικό ρήµα «πρωτεύω» που αποδεικνύει τη σηµασία των πρωτεϊνών στην διατροφή του ανθρώπου Οι πρωτεΐνες είναι πολύπλοκα µόρια που περιέχουν 2 Είναι πηγές αµινοξέων (απαραίτητα, µη απαραίτητα)
MAΘΗΜΑ 4 ο AMINOΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ
 MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν;
 Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ: ΣΥΣΤΑΤΙΚΑ-Ι ΙΟΤΗΤΕΣ-ΡΕΟΛΟΓΙΑ-ΜΙΚΡΟΒΙΟΛΟΓΙΑ- ΠΟΙΟΤΗΤΑ- ΣΥΚΕΥΑΣΙΑ
 E. M. ΠΟΛΥΤΕΧΝΕΙΟ ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ: ΣΥΣΤΑΤΙΚΑ-Ι ΙΟΤΗΤΕΣ-ΡΕΟΛΟΓΙΑ-ΜΙΚΡΟΒΙΟΛΟΓΙΑ- ΠΟΙΟΤΗΤΑ- ΣΥΚΕΥΑΣΙΑ Κ. Τζιά, Π. Ταούκης, Β. Ωραιοπούλου ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΣΗΜΕΙΩΣΕΙΣ ΑΠΟ ΤΙΣ ΠΑΡΑ
E. M. ΠΟΛΥΤΕΧΝΕΙΟ ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ: ΣΥΣΤΑΤΙΚΑ-Ι ΙΟΤΗΤΕΣ-ΡΕΟΛΟΓΙΑ-ΜΙΚΡΟΒΙΟΛΟΓΙΑ- ΠΟΙΟΤΗΤΑ- ΣΥΚΕΥΑΣΙΑ Κ. Τζιά, Π. Ταούκης, Β. Ωραιοπούλου ΕΠΙΣΤΗΜΗ ΚΑΙ ΜΗΧΑΝΙΚΗ ΤΡΟΦΙΜΩΝ ΣΗΜΕΙΩΣΕΙΣ ΑΠΟ ΤΙΣ ΠΑΡΑ
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
Σύσταση του αυγού Λευκό Κρόκος Βάρος 38 g 17 g Πρωτείνη 3,9 g 2,7 g Υδατάνθρακες 0,3 g 0,3 g Λίπος 0 6 g Χοληστερόλη 0 213 mg
 Αυγό Τα αυγά αποτελούνται από το κέλυφος (10 %), το ασπράδι ή λευκό (50-60 %), τον κρόκο ή κίτρινο (30 %). Το κέλυφος αποτελείται κατά 95 % από ανόργανα συστατικά όπως ανθρακικό ασβέστιο, ανθρακικό μαγνήσιο
Αυγό Τα αυγά αποτελούνται από το κέλυφος (10 %), το ασπράδι ή λευκό (50-60 %), τον κρόκο ή κίτρινο (30 %). Το κέλυφος αποτελείται κατά 95 % από ανόργανα συστατικά όπως ανθρακικό ασβέστιο, ανθρακικό μαγνήσιο
αποτελούν το 96% κ.β Ποικιλία λειτουργιών
 ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
ΧΗΜΙΚΑ ΣΤΟΙΧΕΙΑ ΠΟΥ ΣΥΝΘΕΤΟΥΝ ΤΟΥΣ ΟΡΓΑΝΙΣΜΟΥΣ 92 στοιχεία στο φλοιό της Γης 27 απαραίτητα για τη ζωή H, Ο, Ν, C αποτελούν το 96% κ.β S, Ca, P, Cl, K, Na, Mg αποτελούν το 4% κ.β. Fe, I Ιχνοστοιχεία αποτελούν
COOH R 2. H α-αμινοξύ 2
 7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
ΠΡΩΤΕΪΝΕΣ. Φατούρος Ιωάννης Αναπληρωτής Καθηγητής
 ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
Κεφάλαιο 22 Πρωτεΐνες
 Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Κεφάλαιο 22 Πρωτεΐνες Σύνοψη Οι πρωτεΐνες είναι μακρομόρια που προκύπτουν από την ένωση α-αμινοξέων. Τα α-αμινοξέα είναι οργανικές ενώσεις που έχουν μία αμινομάδα (ΝΗ 2 ) και καρβοξύλιο (COOH) συνδεδεμένα
Η πλειοψηφία των αμινοξέων είναι του τύπου :
 ΚΕΦΑΛΑΙΟ 5 Η πλειοψηφία των αμινοξέων είναι του τύπου : H 2 NCHCOOH R O συνδυασμός καρβοξυλίου και αμινομάδας στο μόριό τους έχει ως αποτέλεσμα να συμπεριφέρονται είτε ως οξέα είτε ως βάσεις (αμφολύτες).
ΚΕΦΑΛΑΙΟ 5 Η πλειοψηφία των αμινοξέων είναι του τύπου : H 2 NCHCOOH R O συνδυασμός καρβοξυλίου και αμινομάδας στο μόριό τους έχει ως αποτέλεσμα να συμπεριφέρονται είτε ως οξέα είτε ως βάσεις (αμφολύτες).
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
ΤΡΟΦΟΓΝΩΣΙΑ. Υπεύθυνος Καθηγητής: Παπαμιχάλης Αναστάσιος
 ΤΡΟΦΟΓΝΩΣΙΑ Υπεύθυνος Καθηγητής: Παπαμιχάλης Αναστάσιος ΚΑΤΗΓΟΡΙΕΣ ΘΡΕΠΤΙΚΩΝ ΥΛΩΝ Υδατάνθρακες Λίπη Πρωτεΐνες Νερό Ανόργανα συστατικά Βιταμίνες Υπευθ. Καθηγητής: Παπαμιχάλης Αναστάσιος ΥΔΑΤΑΝΘΡΑΚΕΣ Οι
ΤΡΟΦΟΓΝΩΣΙΑ Υπεύθυνος Καθηγητής: Παπαμιχάλης Αναστάσιος ΚΑΤΗΓΟΡΙΕΣ ΘΡΕΠΤΙΚΩΝ ΥΛΩΝ Υδατάνθρακες Λίπη Πρωτεΐνες Νερό Ανόργανα συστατικά Βιταμίνες Υπευθ. Καθηγητής: Παπαμιχάλης Αναστάσιος ΥΔΑΤΑΝΘΡΑΚΕΣ Οι
Απώλειες των βιταμινών κατά την επεξεργασία των τροφίμων
 Απώλειες των βιταμινών κατά την επεξεργασία των τροφίμων Αποφλοίωση και καθαρισμός Πολλά φυτικά προϊόντα π.χ, μήλα, πατάτες χρειάζονται αποφλοίωση ή καθαρισμό μερικών τμημάτων τους πριν από την κατεργασία.
Απώλειες των βιταμινών κατά την επεξεργασία των τροφίμων Αποφλοίωση και καθαρισμός Πολλά φυτικά προϊόντα π.χ, μήλα, πατάτες χρειάζονται αποφλοίωση ή καθαρισμό μερικών τμημάτων τους πριν από την κατεργασία.
Δρ. Ιωάννης Τσαγκατάκης Σύμβουλος Διατροφικής Αγωγής. Οι Πρωτεΐνες. Ένωση Ελλήνων Χημικών Περιφερειακό Τμήμα Κρήτης
 Δρ. Ιωάννης Τσαγκατάκης Σύμβουλος Διατροφικής Αγωγής Οι Πρωτεΐνες Ένωση Ελλήνων Χημικών Περιφερειακό Τμήμα Κρήτης Αμινοξέα, Πεπτίδια, Πρωτεΐνες, Ένζυμα Πεπτιδικός δεσμός Αμινοξέα Πεπτίδια (
Δρ. Ιωάννης Τσαγκατάκης Σύμβουλος Διατροφικής Αγωγής Οι Πρωτεΐνες Ένωση Ελλήνων Χημικών Περιφερειακό Τμήμα Κρήτης Αμινοξέα, Πεπτίδια, Πρωτεΐνες, Ένζυμα Πεπτιδικός δεσμός Αμινοξέα Πεπτίδια (
Ποια η χρησιμότητα των πρωτεϊνών;
 ΠΡΩΤΕΪΝΕΣ Τι είναι οι πρωτεϊνες; Η ονομασία πρωτεϊνες προέρχεται από το ρήμα πρωτεύω και σημαίνει την εξαιρετική σημασία που έχουν οι πρωτεϊνες για την υγεία του ανθρώπινου σώματος. Από την εποχή των Ολυμπιακών
ΠΡΩΤΕΪΝΕΣ Τι είναι οι πρωτεϊνες; Η ονομασία πρωτεϊνες προέρχεται από το ρήμα πρωτεύω και σημαίνει την εξαιρετική σημασία που έχουν οι πρωτεϊνες για την υγεία του ανθρώπινου σώματος. Από την εποχή των Ολυμπιακών
Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων. 1/10/2015 Δ.Δ. Λεωνίδας
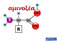 αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
τα βιβλία των επιτυχιών
 Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
Τα βιβλία των Εκδόσεων Πουκαμισάς συμπυκνώνουν την πολύχρονη διδακτική εμπειρία των συγγραφέων μας και αποτελούν το βασικό εκπαιδευτικό υλικό που χρησιμοποιούν οι μαθητές των φροντιστηρίων μας. Μέσα από
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
Διαλέξεις Χημείας Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων
 Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
Διαλέξεις Χημείας -2014 Αγγελική Μαγκλάρα, PhD Εργαστήριο Κλινικής Χημείας Ιατρική Σχολή Πανεπιστημίου Ιωαννίνων 1. Κατάταξη 2. Λειτουργίες 1. Πεπτιδικές ορμόνες 3. Πεπτιδικός δεσμός 1. Χαρακτηριστικά
Καλλιεργούνται πολλές ποικιλίες σιταριών, οι οποίες χωρίζονται σε δύο κατηγορίες: α) σε σκληρά σιτάρια τα οποία έχουν υψηλότερο ποσοστό σε πρωτεΐνη
 Δημητριακά Δημητριακά ή σιτηρά είναι αποξηραμένοι ώριμοι καρποί φυτών. Τα πιο σημαντικά δημητριακά είναι το σιτάρι ή σίτος, το ρύζι, το καλαμπόκι ή αραβόσιτος, το κριθάρι, η σίκαλη και η βρώμη. Ο κόκκος
Δημητριακά Δημητριακά ή σιτηρά είναι αποξηραμένοι ώριμοι καρποί φυτών. Τα πιο σημαντικά δημητριακά είναι το σιτάρι ή σίτος, το ρύζι, το καλαμπόκι ή αραβόσιτος, το κριθάρι, η σίκαλη και η βρώμη. Ο κόκκος
Υγιεινή. Πρωτεΐνες. Λεοτσινίδης Μιχάλης Καθηγητής Υγιεινής Ιατρική Σχολή Πανεπιστήμιο Πατρών
 Υγιεινή Πρωτεΐνες Λεοτσινίδης Μιχάλης Καθηγητής Υγιεινής Ιατρική Σχολή Πανεπιστήμιο Πατρών Αποτελούνται από αμινοξέα ενωμένα με πεπτιδικούς δεσμούς. Μέση σύσταση: Ν: 16 % C: 50 % H: 7 % O: 22 % S: 0,5-3%
Υγιεινή Πρωτεΐνες Λεοτσινίδης Μιχάλης Καθηγητής Υγιεινής Ιατρική Σχολή Πανεπιστήμιο Πατρών Αποτελούνται από αμινοξέα ενωμένα με πεπτιδικούς δεσμούς. Μέση σύσταση: Ν: 16 % C: 50 % H: 7 % O: 22 % S: 0,5-3%
Κεφάλαιο 1. Οι δομικοί λίθοι
 Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ»
 «ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ
 ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ 1 6 ο ΕΞΑΜΗΝΟ. https://courses.chemeng.ntua.gr/food_science_and_technology/ ΔΙΔΑΣΚΩΝ Πέτρος Ταούκης, Καθηγητής ΕΜΠ, Γρ. 301, τηλ. 210 772 3171, taoukis@chemeng.ntua.gr
ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ 1 6 ο ΕΞΑΜΗΝΟ. https://courses.chemeng.ntua.gr/food_science_and_technology/ ΔΙΔΑΣΚΩΝ Πέτρος Ταούκης, Καθηγητής ΕΜΠ, Γρ. 301, τηλ. 210 772 3171, taoukis@chemeng.ntua.gr
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ / Γ ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 21 / 09 /2014 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως και Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ
 ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
ΔΟΜΗ ΚΑΙ ΔΡΑΣΗ ΠΡΩΤΕΙΝΩΝ ΠPΩTEINEΣ Οι πρωτεΐνες παίζουν σημαντικό ρόλο σε όλες σχεδόν τις βιολογικές διεργασίες. H σημασία τους φαίνεται στις παρακάτω περιπτώσεις: 1. Κατάλυση (πχ. ένζυμα) 2. Μεταφορά
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α
 Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
Α μ ι ν ο ξ έ α - π ε π τ ί δ ι α 2.1. Χημική δομή και ταξινόμηση των αμινοξέων Τα αμινοξέα, όπως υποδηλώνει και το όνομά τους, περιέχουν στο μόριό τους δύο χαρακτηριστικές ομάδες: την αμινομάδα και την
ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ
 ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ 1 6 ο ΕΞΑΜΗΝΟ. https://courses.chemeng.ntua.gr/food_science_and_technology/ ΔΙΔΑΣΚΩΝ Πέτρος Ταούκης, Καθηγητής ΕΜΠ, Γρ. 301, τηλ. 210 772 3171, taoukis@chemeng.ntua.gr
ΕΠΙΣΤΗΜΗ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΤΡΟΦΙΜΩΝ 1 6 ο ΕΞΑΜΗΝΟ. https://courses.chemeng.ntua.gr/food_science_and_technology/ ΔΙΔΑΣΚΩΝ Πέτρος Ταούκης, Καθηγητής ΕΜΠ, Γρ. 301, τηλ. 210 772 3171, taoukis@chemeng.ntua.gr
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ. Πηκτίνες
 ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ Πηκτίνες Γενικά Πολυσακχαρίτης ο οποίος βρίσκεται σε διάφορες συγκεντρώσεις στα κυτταρικά τοιχώματα των ανώτερων φυτικών ιστών μαζί με την κυτταρίνη. Η πηκτίνη
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ Πηκτίνες Γενικά Πολυσακχαρίτης ο οποίος βρίσκεται σε διάφορες συγκεντρώσεις στα κυτταρικά τοιχώματα των ανώτερων φυτικών ιστών μαζί με την κυτταρίνη. Η πηκτίνη
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ. ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ 1 Δομή των αμινοξέων Τα αμινοξέα περιέχουν στο μόριο τους: Καρβοξύλιο και αμινομάδα. Τα αμινοξέα των πρωτεϊνών είναι α-αμινοξέα. Συνέπειες:
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΑΣΚΗΣΗ ΠΡΑΞΗΣ 10η ΕΙΣΑΓΩΓΗ ΣΤΙΣ ΠΡΩΤΕΪΝΕΣ 1 Δομή των αμινοξέων Τα αμινοξέα περιέχουν στο μόριο τους: Καρβοξύλιο και αμινομάδα. Τα αμινοξέα των πρωτεϊνών είναι α-αμινοξέα. Συνέπειες:
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
Βιολογία Β Λυκείου θέματα
 Ι. Οι υδατάνθρακες διακρίνονται σε μονοσακχαρίτες, δισακχαρίτες και πολυσακχαρίτες. α) Να αναφέρετε από δύο παραδείγματα μονοσακχαριτών, δισακχαριτών και πολυσακχαριτών. (6μ) β) Σε ένα κύτταρο συναντώνται
Ι. Οι υδατάνθρακες διακρίνονται σε μονοσακχαρίτες, δισακχαρίτες και πολυσακχαρίτες. α) Να αναφέρετε από δύο παραδείγματα μονοσακχαριτών, δισακχαριτών και πολυσακχαριτών. (6μ) β) Σε ένα κύτταρο συναντώνται
ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ
 ΚΕΦΑΛΑΙΟ 1ο ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ 2010-11 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 1 ο : ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΚΑΙ ΒΙΟΧΗΜΕΙΑ 1. Τι είναι η Βιοχημεία και με ποιες ενώσεις ασχολείται. 2. Πόσα και ποια στοιχεία
ΚΕΦΑΛΑΙΟ 1ο ΒΙΟΤΕΧΝΟΛΟΓΙΑ 1 ο ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΒΟΛΟΥ 2010-11 ΕΡΩΤΗΣΕΙΣ ΚΑΤΑΝΟΗΣΗΣ ΚΕΦΑΛΑΙΟ 1 ο : ΟΡΓΑΝΙΚΗ ΧΗΜΕΙΑ ΚΑΙ ΒΙΟΧΗΜΕΙΑ 1. Τι είναι η Βιοχημεία και με ποιες ενώσεις ασχολείται. 2. Πόσα και ποια στοιχεία
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ
 Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
Απομόνωση Καζεΐνης ΆΣΚΗΣΗ 6 Η ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ Θεωρητικό μέρος ΠΡΩΤΕΪΝΕΣ ΚΑΖΕΪΝΗ Πρωτεΐνες Είναι μεγάλα σύνθετα βιομόρια. Έχουν μοριακό βάρος από 10.000 μέχρι πάνω από 1 εκατομμύριο.
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ
 ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
ΙΑΤΡΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ (ΕΚΠΑ) ΚΑΤΑΤΑΚΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΑΚ.ΕΤΟΥΣ 2017-2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ 1. Σε ποια μορφή της αιμοσφαιρίνης συνδέεται το 2,3, BPG, ποιο είναι το ηλεκτρικό του φορτίο, με
Θέµατα ιάλεξης ΜΕΤΑΒΟΛΙΣΜΟΣ ΛΙΠΩΝ- Λίπη και αθηροσκλήρυνση. Μεσογειακή ίαιτα. Λίπη και αθηροσκλήρυνση: Ο ρόλος της άσκησης
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΜΕΤΑΒΟΛΙΣΜΟΣ ΛΙΠΩΝ- ΠΡΩΤΕΪΝΩΝ Θέµατα ιάλεξης Ο ρόλος της διατροφής στην εµφάνιση ασθενειών της καρδιάς Επίδραση
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΜΕΤΑΒΟΛΙΣΜΟΣ ΛΙΠΩΝ- ΠΡΩΤΕΪΝΩΝ Θέµατα ιάλεξης Ο ρόλος της διατροφής στην εµφάνιση ασθενειών της καρδιάς Επίδραση
Θέµατα ιάλεξης ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ ΠΡΩΤΕΪΝΕΣ. ιαχωρισµός Αµινοξέων
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΠΡΩΤΕΪΝΕΣ - ΕΝΖΥΜΑ Θέµατα ιάλεξης οµή, αριθµός και διαχωρισµός των αµινοξέων Ένωση αµινοξέων µε τον πεπτιδικό δεσµό
ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ
 ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ Παππάς Χρήστος Επίκουρος καθηγητής ΑΜΙΝΟΞΕΑ Αμινοξέα είναι οργανικά μόρια που διαθέτουν καρβοξύλιο (-α) και αμινομάδα (-ες). Πλευρική αλυσίδα R NH 2 α O α- αμινοξύ OH Είναι
ΑΜΙΝΟΞΕΑ ΠΕΠΤΙΔΙΑ ΠΡΩΤΕΪΝΕΣ Παππάς Χρήστος Επίκουρος καθηγητής ΑΜΙΝΟΞΕΑ Αμινοξέα είναι οργανικά μόρια που διαθέτουν καρβοξύλιο (-α) και αμινομάδα (-ες). Πλευρική αλυσίδα R NH 2 α O α- αμινοξύ OH Είναι
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ. Καρβουντζή Ηλιάνα Βιολόγος
 Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Χημικά στοιχεία που συνθέτουν τους οργανισμούς Ο C, το H 2, το O 2 και το N 2 είναι τα επικρατέστερα στους οργανισμούς σε ποσοστό 96% κ.β. Γιατί; Συμμετέχουν σε σημαντικό βαθμό στη σύνθεση
ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του
 ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του ΤΑ ΜΟΝΟΜΕΡΗ ΣΥΝΔΕΟΝΤΑΙ ΜΕ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ. 1. ΠΡΩΤΕΪΝΕΣ
ΣΥΜΠΥΚΝΩΣΗ: αφαίρεση ενός μορίου νερού - σύνθεση ενός διμερούς ΥΔΡΟΛΥΣΗ : προσθήκη ενός μορίου νερού - διάσπαση του διμερούς στα συστατικά του ΤΑ ΜΟΝΟΜΕΡΗ ΣΥΝΔΕΟΝΤΑΙ ΜΕ ΟΜΟΙΟΠΟΛΙΚΟ ΔΕΣΜΟ. 1. ΠΡΩΤΕΪΝΕΣ
Οργανική Χημεία. Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες
 Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
Οργανική Χημεία Κεφάλαιο 27: Βιομόρια, αμινοξέα, πεπτίδια και πρωτεΐνες 1. Γενικά Πρωτεΐνες: μεγάλα βιομόρια που απαντούν σε όλους τους ζωντανούς οργανισμούς Διαφορετικά είδη πρωτεϊνών με ποικίλη βιολογική
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής
 Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Δομή πρωτεϊνών: Τριτοταγής διαμόρφωση της δομής - Αναφέρεται στην αναδίπλωση της πολυπεπτιδικής αλυσίδας πάνω στον εαυτό της και στο τελικό σχήμα που θα πάρει στο χώρο -Σ αυτή τη διαμόρφωση σημαντικό ρόλο
Τα χημικά στοιχεία που είναι επικρατέστερα στους οργανισμούς είναι: i..
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 1 ο ΚΕΦΑΛΑΙΟ «XHMIKH ΣΥΣΤΑΣΗ ΤΟΥ ΚΥΤΤΑΡΟΥ» ΕΙΣΑΓΩΓΗ ΚΑΙ Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Όταν αναφερόμαστε στον όρο «Χημική Σύσταση του Κυττάρου», τί νομίζετε ότι
Αρχές Επεξεργασίας Τροφίμων
 Αρχές Επεξεργασίας Τροφίμων Κατάψυξη τροφίμων Κατάψυξη Απομάκρυνση θερμότητας από ένα προϊόν με αποτέλεσμα την μείωση της θερμοκρασίας του κάτω από το σημείο πήξης. Ως μέθοδος συντήρησης βασίζεται: Στην
Αρχές Επεξεργασίας Τροφίμων Κατάψυξη τροφίμων Κατάψυξη Απομάκρυνση θερμότητας από ένα προϊόν με αποτέλεσμα την μείωση της θερμοκρασίας του κάτω από το σημείο πήξης. Ως μέθοδος συντήρησης βασίζεται: Στην
Για τον άνθρωπο π.χ. το 85% περίπου των στερεών συστατικών του σώματός του αποτελείται από πρωτεΐνες. Έτσι οι πρωτεΐνες της τροφής χρησιμοποιούνται :
 PΟΛΟΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ ΣΤΗ ΔΙΑΤΡΟΦΗ Oι πρωτεΐνες είναι τάξη θρεπτικών υλών με ιδιαίτερη σημασία για τους ζωντανούς οργανισμούς, γιατί αποτελούν την κύρια δομική ύλη τους. Περιεκτηκότητα μερικών τροφίμων σε
PΟΛΟΣ ΤΩΝ ΠΡΩΤΕΪΝΩΝ ΣΤΗ ΔΙΑΤΡΟΦΗ Oι πρωτεΐνες είναι τάξη θρεπτικών υλών με ιδιαίτερη σημασία για τους ζωντανούς οργανισμούς, γιατί αποτελούν την κύρια δομική ύλη τους. Περιεκτηκότητα μερικών τροφίμων σε
3.1. Γενικά για τις πρωτείνες
 Π ρ ω τ ε ί ν ε ς 3.1. Γενικά για τις πρωτείνες Οι πρωτεΐνες είναι ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Αλλωστε το όνομά τους υποδηλώνει το ρόλο αυτό. Αποτελούν απαραίτητο στοιχείο για κάθε
Π ρ ω τ ε ί ν ε ς 3.1. Γενικά για τις πρωτείνες Οι πρωτεΐνες είναι ουσίες με κυρίαρχο και πρωταρχικό ρόλο στη ζωή. Αλλωστε το όνομά τους υποδηλώνει το ρόλο αυτό. Αποτελούν απαραίτητο στοιχείο για κάθε
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01%
 ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
ΔΙΑΚΡΙΣΗ ΣΤΟΙΧΕΙΩΝ ΜΑΚΡΟΘΡΕΠΤΙΚΑ (C, H, N, O) 96% ΜΙΚΡΟΘΡΕΠΤΙΚΑ (πχ. Na, K, P, Ca, Mg) 4% ΙΧΝΟΣΤΟΙΧΕΙΑ (Fe, I) 0,01% Ο άνθρακας, το υδρογόνο, το οξυγόνο και το άζωτο συμμετέχουν, σε σημαντικό βαθμό, στη
ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ
 ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το
ΘΕΜΑ A ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) 24 ΜΑΪΟΥ 2013 ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 ΕΚΦΩΝΗΣΕΙΣ Ζήτηµα 1ο 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α.
οµή και λειτουργία των µεγάλων βιολογικών µορίων
 οµή και λειτουργία των µεγάλων βιολογικών µορίων οµή και λειτουργία των µεγάλων βιολογικών µορίων κατηγορίες υδατάνθρακες πρωτεΐνες νουκλεϊνικά οξέα λιπίδια Οι πρωτεΐνες, υδατάνθρακες, νουκλεϊνικά οξέα
οµή και λειτουργία των µεγάλων βιολογικών µορίων οµή και λειτουργία των µεγάλων βιολογικών µορίων κατηγορίες υδατάνθρακες πρωτεΐνες νουκλεϊνικά οξέα λιπίδια Οι πρωτεΐνες, υδατάνθρακες, νουκλεϊνικά οξέα
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΠΡΩΤΕΙΝΕΣ ΑΛΕΥΡΩΝ
 ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΠΡΩΤΕΙΝΕΣ ΑΛΕΥΡΩΝ ΓΕΝΙΚΑ ΚΥΡΙΕΣ ΠΡΩΤΕΙΝΕΣ 80-90% ΓΛΟΥΤΕΝΙΝΕΣ ΓΛΟΙΑΔΙΝΕΣ ΔΕΥΤΕΡΕΥΟΥΣΕΣ ΠΡΩΤΕΙΝΕΣ 10-20% ΛΕΥΚΟΣΙΝΗ ΕΔΕΣΤΙΝΗ ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΚΟΤΗΤΑ ΤΗΣ ΓΛΟΥΤΕΝΙΝΗΣ
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΠΡΩΤΕΙΝΕΣ ΑΛΕΥΡΩΝ ΓΕΝΙΚΑ ΚΥΡΙΕΣ ΠΡΩΤΕΙΝΕΣ 80-90% ΓΛΟΥΤΕΝΙΝΕΣ ΓΛΟΙΑΔΙΝΕΣ ΔΕΥΤΕΡΕΥΟΥΣΕΣ ΠΡΩΤΕΙΝΕΣ 10-20% ΛΕΥΚΟΣΙΝΗ ΕΔΕΣΤΙΝΗ ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΚΟΤΗΤΑ ΤΗΣ ΓΛΟΥΤΕΝΙΝΗΣ
Βιολογία Γενικής Παιδείας Β Λυκείου
 Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
Απρίλιος Μάιος 12 Βιολογία Γενικής Παιδείας Β Λυκείου Βιολογία Γενικής Παιδείας Β Λυκείου (Ερωτήσεις που παρουσιάζουν ενδιαφέρον) 1. Τι είναι τα βιομόρια και ποια είναι τα βασικά χαρακτηριστικά τους; Βιομόρια
Αλληλεπιδράσεις θρεπτικών συστατικών των τροφίμων
 Αλληλεπιδράσεις θρεπτικών συστατικών των τροφίμων Τα τρόφιμα είναι σύνθετοι συνδυασμοί που προέρχονται από πολλές πηγες. Όλα τα τρόφιμα έχουν τη δυνατότητα αλλεπίδρασης (χημικής) σε διαφορετικό βαθμό.
Αλληλεπιδράσεις θρεπτικών συστατικών των τροφίμων Τα τρόφιμα είναι σύνθετοι συνδυασμοί που προέρχονται από πολλές πηγες. Όλα τα τρόφιμα έχουν τη δυνατότητα αλλεπίδρασης (χημικής) σε διαφορετικό βαθμό.
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001
 Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
Ζήτηµα 1ο Χηµεία-Βιοχηµεία Τεχνολογικής Κατεύθυνσης Γ Λυκείου 2001 1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 25 ο C έχει τιµή 10-14 : α. µόνο στο
ΔΙΑΤΡΟΦΗ ΚΑΙ ΕΦΗΒΕΙΑ
 ΔΙΑΤΡΟΦΗ ΚΑΙ ΕΦΗΒΕΙΑ ΕΦΗΒΕΙΑ- ΑΝΑΓΚΕΣ v Επιτάχυνση ρυθμού ανάπτυξης v Ωρίμανση και αύξηση ιστών v Αποκτά το 20% του ύψους και το 50% του βάρους του ενήλικα, ενώ οι μύες, ο όγκος του αίματος και γενικά
ΔΙΑΤΡΟΦΗ ΚΑΙ ΕΦΗΒΕΙΑ ΕΦΗΒΕΙΑ- ΑΝΑΓΚΕΣ v Επιτάχυνση ρυθμού ανάπτυξης v Ωρίμανση και αύξηση ιστών v Αποκτά το 20% του ύψους και το 50% του βάρους του ενήλικα, ενώ οι μύες, ο όγκος του αίματος και γενικά
ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
 ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
ΕΠΕΞΕΡΓΑΣΙΑ ΤΡΟΦΙΜΩΝ
 ΕΠΕΞΕΡΓΑΣΙΑ ΤΡΟΦΙΜΩΝ Συμπύκνωση Τι είναι η συμπύκνωση Είναι η διαδικασία με την οποία απομακρύνουμε μέρος της υγρασίας του τροφίμου, αφήνοντας όμως αρκετή ώστε αυτό να παραμένει ρευστό (> 20-30%). Εφαρμόζεται
ΕΠΕΞΕΡΓΑΣΙΑ ΤΡΟΦΙΜΩΝ Συμπύκνωση Τι είναι η συμπύκνωση Είναι η διαδικασία με την οποία απομακρύνουμε μέρος της υγρασίας του τροφίμου, αφήνοντας όμως αρκετή ώστε αυτό να παραμένει ρευστό (> 20-30%). Εφαρμόζεται
1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΘΕΜΑ 1o 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση: Η σταθερά Κ w στους 5 ο C έχει τιµή 10-14 : α. µόνο στο καθαρό νερό β. σε οποιοδήποτε υδατικό διάλυµα γ. µόνο σε υδατικά
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΕΤΟΥΣΙΩΣΗ ΠΡΩΤΕΪΝΩΝ (άσκηση 7 του εργαστηριακού οδηγού) Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ Εργαλεία
ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ, Ε.Μ. ΠΟΛΥΤΕΧΝΕΙΟ
 Μαρία Σ. Τσεβδού, Πέτρος Σ. Ταούκης ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ, Ε.Μ. ΠΟΛΥΤΕΧΝΕΙΟ «...γιαούρτι (πλήρες ή, κατά περίπτωση, ημιαποβουτυρωμένο)...(όνομα ζώου) χαρακτηρίζεται
Μαρία Σ. Τσεβδού, Πέτρος Σ. Ταούκης ΕΡΓΑΣΤΗΡΙΟ ΧΗΜΕΙΑΣ & ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ, Ε.Μ. ΠΟΛΥΤΕΧΝΕΙΟ «...γιαούρτι (πλήρες ή, κατά περίπτωση, ημιαποβουτυρωμένο)...(όνομα ζώου) χαρακτηρίζεται
Είναι σημαντικές επειδή: Αποτελούν βασικά δοµικά συστατικά του σώµατος Εξυπηρετούν ενεργειακές ανάγκες Ασκούν έλεγχο σε όλες τις βιοχηµικές διεργασίες
 ΕΞΕΤΑΣΤΕΑ ΥΛΗ ΕΝΟΤΗΤΑ 2: Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ, 5 9 (απλή αναφορά) 2.2 ΤΟ ΝΕΡΟ ΚΑΙ Η ΒΙΟΛΟΓΙΚΗ ΤΟΥ ΣΗΜΑΣΙΑ, 9 14 (απλή αναφορά), 2.4 ΟΡΓΑΝΙΚΕΣ ΟΥΣΙΕΣ, σελ. 20 36 Οργανικές Ουσίες
ΕΞΕΤΑΣΤΕΑ ΥΛΗ ΕΝΟΤΗΤΑ 2: Η ΧΗΜΕΙΑ ΤΗΣ ΖΩΗΣ 2.1 ΒΑΣΙΚΕΣ ΧΗΜΙΚΕΣ ΕΝΝΟΙΕΣ, 5 9 (απλή αναφορά) 2.2 ΤΟ ΝΕΡΟ ΚΑΙ Η ΒΙΟΛΟΓΙΚΗ ΤΟΥ ΣΗΜΑΣΙΑ, 9 14 (απλή αναφορά), 2.4 ΟΡΓΑΝΙΚΕΣ ΟΥΣΙΕΣ, σελ. 20 36 Οργανικές Ουσίες
ΒΙΟΛΟΓΙΑ. Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ.
 ΒΙΟΛΟΓΙΑ Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ. Ηλιούπολης Κεφάλαιο 1ο ΒΙΟΛΟΓΙΚΑ ΜΑΚΡΟΜΟΡΙΑ Η ΙΕΡΑΡΧΙΑ ΤΩΝ ΒΙΟΜΟΡΙΩΝ ΠΡΟΔΡΟΜΕΣ
ΒΙΟΛΟΓΙΑ Παραδόσεις του μαθήματος γενικής παιδείας (Β λυκείου) Επιμέλεια: ΑΡΓΥΡΗΣ ΙΩΑΝΝΗΣ Βιολόγος M.Sc. Καθηγητής 3 ου λυκ. Ηλιούπολης Κεφάλαιο 1ο ΒΙΟΛΟΓΙΚΑ ΜΑΚΡΟΜΟΡΙΑ Η ΙΕΡΑΡΧΙΑ ΤΩΝ ΒΙΟΜΟΡΙΩΝ ΠΡΟΔΡΟΜΕΣ
ΥΔΑΤΑΝΘΡΑΚΕΣ. Τι είναι οι υδατάνθρακες;
 ΥΔΑΤΑΝΘΡΑΚΕΣ Τι είναι οι υδατάνθρακες; Οι υδατάνθρακες είναι τα νομίσματα ενέργειας του σώματός μας. Τα περισσότερα τρόφιμα που τρώμε καθημερινά αποτελούνται από υδατάνθρακες. Ο οργανισμός μας, σπα τους
ΥΔΑΤΑΝΘΡΑΚΕΣ Τι είναι οι υδατάνθρακες; Οι υδατάνθρακες είναι τα νομίσματα ενέργειας του σώματός μας. Τα περισσότερα τρόφιμα που τρώμε καθημερινά αποτελούνται από υδατάνθρακες. Ο οργανισμός μας, σπα τους
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράμμα που αντιστοιχεί στη σωστή απάντηση:
 ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) : ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό
ΒΙΟΧΗΜΕΙΑ ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ. Στοιχείο O C H N Ca P K S Na Mg περιεκτικότητα % ,5 1 0,35 0,25 0,15 0,05
 ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
ΒΙΟΧΗΜΕΙΑ Βιοχημεία: είναι η επιστήμη που ασχολείται με τη μελέτη των οργανικών ενώσεων που συναντώνται στον οργανισμό, καθώς και με τον μεταβολισμό τους. ΧΗΜΙΚΗ ΣΥΣΤΑΣΗ ΤΩΝ ΒΙΟΛΟΓΙΚΩΝ ΜΟΡΙΩΝ 108 στοιχεία
ΔΗΜΗΤΡΙΑΚΑ Οι τροφές αυτές βρίσκονται στη βάση της διατροφικής πυραμίδας, είναι πλούσιες σε σύνθετους υδατάνθρακες, βιταμίνες της ομάδας Β, πρωτεΐνες,
 ΟΜΑΔΕΣ ΤΡΟΦΙΜΩΝ ΔΗΜΗΤΡΙΑΚΑ Οι τροφές αυτές βρίσκονται στη βάση της διατροφικής πυραμίδας, είναι πλούσιες σε σύνθετους υδατάνθρακες, βιταμίνες της ομάδας Β, πρωτεΐνες, άπεπτες φυτικές ίνες, σίδηρο και άλλα
ΟΜΑΔΕΣ ΤΡΟΦΙΜΩΝ ΔΗΜΗΤΡΙΑΚΑ Οι τροφές αυτές βρίσκονται στη βάση της διατροφικής πυραμίδας, είναι πλούσιες σε σύνθετους υδατάνθρακες, βιταμίνες της ομάδας Β, πρωτεΐνες, άπεπτες φυτικές ίνες, σίδηρο και άλλα
Βιοχημεία Τροφίμων Ι. Ενότητα 7 η Δημητριακά Ι (μέρος β) Όνομα καθηγητή: Έφη Τσακαλίδου. Τμήμα: Επιστήμης Τροφίμων & Διατροφής του Ανθρώπου
 Βιοχημεία Τροφίμων Ι Ενότητα 7 η Δημητριακά Ι (μέρος β) Όνομα καθηγητή: Έφη Τσακαλίδου Τμήμα: Επιστήμης Τροφίμων & Διατροφής του Ανθρώπου Στόχοι ενότητας Κατανόηση της δομής και της σύστασης του σπόρου
Βιοχημεία Τροφίμων Ι Ενότητα 7 η Δημητριακά Ι (μέρος β) Όνομα καθηγητή: Έφη Τσακαλίδου Τμήμα: Επιστήμης Τροφίμων & Διατροφής του Ανθρώπου Στόχοι ενότητας Κατανόηση της δομής και της σύστασης του σπόρου
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
Κωνσταντίνος Π. (Β 2 ) ΚΕΦΑΛΑΙΟ 3: ΜΕΤΑΒΟΛΙΣΜΟΣ Βιοενεργητική είναι ο κλάδος της Βιολογίας που μελετά τον τρόπο με τον οποίο οι οργανισμοί χρησιμοποιούν ενέργεια για να επιβιώσουν και να υλοποιήσουν τις
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΘΕΜΑ 1 ο 1.1. Να γράψετε στο τετράδιό σας το γράµµα που αντιστοιχεί στη σωστή απάντηση:
 ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
ΑΡΧΗ 1ΗΣ ΣΕΛΙ ΑΣ Γ ΤΑΞΗ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 5 ΙΟΥΝΙΟΥ 2001 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ): ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ ΣΥΝΟΛΟ ΣΕΛΙ
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ
 ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ
 ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου. Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση:
 KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
KΕΦΑΛΑΙΟ 1ο Χημική σύσταση του κυττάρου Ενότητα 1.1: Χημεία της ζωής Ενότητα 2.1: Μακρομόρια Να απαντήσετε σε καθεμιά από τις παρακάτω ερωτήσεις με μια πρόταση: 1. Για ποιο λόγο θεωρείται αναγκαία η σταθερότητα
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ
 Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
Κεφάλαιο 3 ΜΕΤΑΒΟΛΙΣΜΟΣ 3.1 Ενέργεια και οργανισμοί Όλοι οι οργανισμοί, εκτός από αυτούς από αυτούς που έχουν την ικανότητα να φωτοσυνθέτουν, εξασφαλίζουν ενέργεια διασπώντας τις θρεπτικές ουσιές που περιέχονται
οµή και Αναδίπλωση πρωτεϊνών
 οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 5 ΣΕΛΙΔΕΣ
 Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
3.2 ΕΝΖΥΜΑ ΒΙΟΛΟΓΙΚΟΙ ΚΑΤΑΛΥΤΕΣ
 ΠΕΡΙΛΗΨΗ ΣΤΟ 3 Ο ΚΕΦΑΛΑΙΟ: ΜΕΤΑΒΟΛΙΣΜΟΣ ΚΥΡΙΑΚΟΣ Γ. Β1 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί
ΠΕΡΙΛΗΨΗ ΣΤΟ 3 Ο ΚΕΦΑΛΑΙΟ: ΜΕΤΑΒΟΛΙΣΜΟΣ ΚΥΡΙΑΚΟΣ Γ. Β1 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Όλοι οι οργανισμοί προκειμένου να επιβιώσουν και να επιτελέσουν τις λειτουργίες τους χρειάζονται ενέργεια. Οι φυτικοί
Τάξη. Γνωστικό αντικείµενο: Ειδικοί διδακτικοί στόχοι
 Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ. Πηκτίνες
 ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ Πηκτίνες Γενικά Πολυσακχαρίτης ο οποίος βρίσκεται σε διάφορες συγκεντρώσεις στα κυτταρικά τοιχώματα των ανώτερων φυτικών ιστών μαζί με την κυτταρίνη. Η πηκτίνη
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ Πηκτίνες Γενικά Πολυσακχαρίτης ο οποίος βρίσκεται σε διάφορες συγκεντρώσεις στα κυτταρικά τοιχώματα των ανώτερων φυτικών ιστών μαζί με την κυτταρίνη. Η πηκτίνη
ΠΑΡΑΡΤΗΜΑ. του ΚΑΤ ΕΞΟΥΣΙΟΔΟΤΗΣΗ ΚΑΝΟΝΙΣΜΟΥ
 ΕΥΡΩΠΑΪΚΗ ΕΠΙΤΡΟΠΗ Βρυξέλλες, 31.1.2017 C(2017) 403 final ANNEX 1 ΠΑΡΑΡΤΗΜΑ του ΚΑΤ ΕΞΟΥΣΙΟΔΟΤΗΣΗ ΚΑΝΟΝΙΣΜΟΥ για τη συμπλήρωση του κανονισμού (ΕΕ) αριθ. 251/2014 του Ευρωπαϊκού Κοινοβουλίου και του Συμβουλίου
ΕΥΡΩΠΑΪΚΗ ΕΠΙΤΡΟΠΗ Βρυξέλλες, 31.1.2017 C(2017) 403 final ANNEX 1 ΠΑΡΑΡΤΗΜΑ του ΚΑΤ ΕΞΟΥΣΙΟΔΟΤΗΣΗ ΚΑΝΟΝΙΣΜΟΥ για τη συμπλήρωση του κανονισμού (ΕΕ) αριθ. 251/2014 του Ευρωπαϊκού Κοινοβουλίου και του Συμβουλίου
Ποιοτικά Χαρακτηριστικά Λυµάτων
 Ποιοτικά Χαρακτηριστικά Λυµάτων µπορούν να καταταχθούν σε τρεις κατηγορίες: Φυσικά Χηµικά Βιολογικά. Πολλές από τις παραµέτρους που ανήκουν στις κατηγορίες αυτές αλληλεξαρτώνται π.χ. η θερµοκρασία που
Ποιοτικά Χαρακτηριστικά Λυµάτων µπορούν να καταταχθούν σε τρεις κατηγορίες: Φυσικά Χηµικά Βιολογικά. Πολλές από τις παραµέτρους που ανήκουν στις κατηγορίες αυτές αλληλεξαρτώνται π.χ. η θερµοκρασία που
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 5 ΣΕΛΙΔΕΣ
 Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
Θέμα Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΜΟΝΟ ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ-ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ
Γκύζη 14-Αθήνα Τηλ : 210.64.52.777
 ΘΕΜΑ Α Α1. α Α2. γ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΑΠΑΝΤΗΣΕΙΣ
ΘΕΜΑ Α Α1. α Α2. γ ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 24 ΜΑΪΟΥ 2013 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΚΥΚΛΟΣ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΠΑΡΑΓΩΓΗΣ) ΑΠΑΝΤΗΣΕΙΣ
ÔÏÕËÁ ÓÁÑÑÇ ÊÏÌÏÔÇÍÇ
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗ (1ος Κύκλος) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 16 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: ΘΕΜΑ Α Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΕΧΝΟΛΟΓΙΚΗ (1ος Κύκλος) ΧΗΜΕΙΑ - ΒΙΟΧΗΜΕΙΑ Ηµεροµηνία: Τετάρτη 16 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ Στις ερωτήσεις Α1 και Α2 να γράψετε
 ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑ Α Β ) ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) Θέμα Α Για τις προτάσεις
ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑ Α Β ) ΤΕΤΑΡΤΗ 1 ΙΟΥΝΙΟΥ 2016 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΒΙΟΧΗΜΕΙΑ ΤΕΧΝΟΛΟΓΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ (ΠΑΛΑΙΟ ΣΥΣΤΗΜΑ) Θέμα Α Για τις προτάσεις
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες
 Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
Οι πρωτεΐνες συμμετέχουν σε όλες τις κυτταρικές λειτουργίες Γένωμα vs Πρωτέωμα Όλη η αλληλουχία βάσεων στο DNA Τι είναι δυνατόν Συγκεκριμένο Στατικό Οι πρωτεΐνες που κωδικοποιούνται από το γένωμα Τι είναι
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΑΜΥΛΟ ΚΑΙ ΑΡΤΟΣΚΕΥΑΣΜΑΤΑ
 ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΑΜΥΛΟ ΚΑΙ ΑΡΤΟΣΚΕΥΑΣΜΑΤΑ Βιοσύνθεση και χημική δομή Είναι ένας από τους σπουδαιότερους φυσικούς υδατάνθρακες. Δομείται στα πλαστίδια των φυτικών κυττάρων που ονομάζονται
ΤΕΧΝΟΛΟΓΙΑ ΚΑΙ ΑΡΧΕΣ ΠΑΡΑΣΚΕΥΗΣ ΤΡΟΦΙΜΩΝ ΑΜΥΛΟ ΚΑΙ ΑΡΤΟΣΚΕΥΑΣΜΑΤΑ Βιοσύνθεση και χημική δομή Είναι ένας από τους σπουδαιότερους φυσικούς υδατάνθρακες. Δομείται στα πλαστίδια των φυτικών κυττάρων που ονομάζονται
ενζυμική αμαύρωση. Η ενζυμική αμαύρωση είναι το μαύρισμα τις μελανίνες
 Ενζυμική αμαύρωση Όταν καθαρίζουμε ή κόβουμε λαχανικά και φρούτα συμβαίνουν μια σειρά αντιδράσεων που μεταβάλουν το χρώμα της σάρκας τους σε σκούρο. Αυτές οι μεταβολές ονομάζονται ενζυμική αμαύρωση. Η
Ενζυμική αμαύρωση Όταν καθαρίζουμε ή κόβουμε λαχανικά και φρούτα συμβαίνουν μια σειρά αντιδράσεων που μεταβάλουν το χρώμα της σάρκας τους σε σκούρο. Αυτές οι μεταβολές ονομάζονται ενζυμική αμαύρωση. Η
ΑΠΑΝΤΗΣΕΙΣ. Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
 ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Το συζυγές οξύ της ΝΗ 3 είναι: α. ΝΗ 2 - β.νa
ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Το συζυγές οξύ της ΝΗ 3 είναι: α. ΝΗ 2 - β.νa
Επιδραση της αλατισης και καπνισης στα θρεπτικα συστατικά των ζωικών προιοντων Εκτός από το χλωριούχο νάτριο, για συντηρηση για τα ψαρια και το
 Επιδραση της αλατισης και καπνισης στα θρεπτικα συστατικά των ζωικών προιοντων Εκτός από το χλωριούχο νάτριο, για συντηρηση για τα ψαρια και το κρεας, γίνεται και χρήση άλλων αλατων όπως νιτρικών και νιτρωδών.
Επιδραση της αλατισης και καπνισης στα θρεπτικα συστατικά των ζωικών προιοντων Εκτός από το χλωριούχο νάτριο, για συντηρηση για τα ψαρια και το κρεας, γίνεται και χρήση άλλων αλατων όπως νιτρικών και νιτρωδών.
