Μεταπτυχιακή Εργασία
|
|
|
- Όφελος Ζαχαρίου
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΤΜΗΜΑ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΕΡΓΑΣΤΗΡΙΟ ΑΝΟΡΓΑΝΗΣ ΚΑΙ ΑΝΑΛΥΤΙΚΗΣ ΧΗΜΕΙΑΣ Μεταπτυχιακή Εργασία Ανάκτηση Φωσφόρου από Υδατικά Απόβλητα σε Ρευστοποιημένες Κλίνες Θεανώ Μαυρίκου Χημικός Επιβλέπων Καθηγητής Π. Κουτσούκος Πάτρα 212
2 2
3 Ευχαριστίες Η παρούσα μεταπτυχιακή εργασία εκπονήθηκε στο εργαστήριο Ανόργανης και Αναλυτικής Χημείας του Τμήματος Χημικών Μηχανικών του Πανεπιστήμιου Πατρών στα πλαίσια του μεταπτυχιακού προγράμματος σπουδών στον τομέα Περιβάλλον και Ενέργεια κατά το χρονικό διάστημα Θα ήθελα να εκφράσω τις θερμές ευχαριστίες μου στον Επιβλέποντα Καθηγητή μου κ. Πέτρο Κουτσούκο Καθηγητή του Τμήματος Χημικών Μηχανικών για την ευκαιρία που μου έδωσε να συνεργαστώ μαζί του και την υποστήριξη που μου παρείχε σε όλα τα στάδια αυτής της εργασίας. Η καθοδήγηση του, καθώς και οι πολύτιμες επιστημονικές συμβουλές υπήρξαν καθοριστικές. Επίσης, θα ήθελα να ευχαριστήσω τον Επίκουρο Καθηγητή του Τμήματος Χημικών Μηχανικών κ. Χριστάκη Παρασκευά για τη συμμετοχή του στην εξεταστική επιτροπή, καθώς και για την πρόσβαση που μου παρείχε στο εργαστήριο Φαινομένων Μεταφοράς και Φυσικοχημικής Υδροδυναμικής. Εκφράζω επίσης ευχαριστίες στον Επίκουρο Καθηγητή κ. Μιχάλη Κορνάρο, γιατί δέχτηκε να συμμετάσχει στην αξιολόγηση της παρούσας εργασίας. Δε θα μπορούσα να παραλείψω ένα μεγάλο ευχαριστώ στους συναδέλφους στο εργαστήριο για το ευχάριστο περιβάλλον και ιδιαίτερα τη διδάκτορα Σταματία Ροκίδη για τη φιλία και τις επιστημονικές συμβουλές που μου παρείχε. Θα ήθελα να ευχαριστήσω τον υποψήφιο διδάκτορα Γιάννη Μπούντα για την επιστημονική του συμβολή, τη συμπαράσταση και για την φιλία του στην πραγματοποίηση αυτής της εργασίας. Τέλος, το μεγαλύτερο ευχαριστώ και την ευγνωμοσύνη μου αξίζει να τα εκφράσω στην οικογένεια μου για την αγάπη και τη στήριξη που μου πρόσφεραν σε όλη τη διάρκεια των σπουδών μου. 3
4 Περιεχόμενα Περίληψη - Summary... 7 Kεφάλαιο 1: Εισαγωγή Ο Φώσφορος στα Υδατικά Απόβλητα Απομάκρυνση του Φωσφόρου Ανάκτηση Φωσφόρου Ο Στρουβίτης ως Εναπόθεση στις Βιομηχανίες (Scale Formation) Εφαρμογές Ανάκτησης Φωσφόρου από Βιομηχανίες Επεξεργασίας αποβλήτων Ο Στρουβίτης ως Λίπασμα Οικονομική Αξιολόγηση στην Ανάκτηση Φωσφόρου υπό μορφή Στρουβίτη Σκοπός της εργασίας Κεφάλαιο 2: Θεωρητικό Μέρος Εισαγωγή της Κρυστάλλωσης Διαλύματα δυσδιάλυτων Αλάτων Διάγραμμα Διαλυτότητας Γινόμενο Διαλυτότητας Υπερκορεσμός Πυρηνογένεση Ομογενής Πυρηνογένεση Ετερογενής Πυρηνογένεση Δευτερογενής Πυρηνογένεση Κρυσταλλική Ανάπτυξη Θεωρίες επιφανειακής ενέργειας Προσρόφησης υποστρώματος Θεωρίες Διάχυσης Καθορισμός μηχανισμού που ελέγχει τη Κρυσταλλική Ανάπτυξη Επίδραση παρουσίας ξένων ιόντων ή ενώσεων (Επιμολύνσεις)
5 2.5 Χρήση Αντιδραστήρων στη κρυστάλλωση Αντιδραστήρας Διαλείποντος Έργου (Batch) Αντιδραστήρας Ρευστοποιημένης κλίνης (FBR) Υδροδυναμική του Συστήματος Φάσεις ρευστοποίησης Ιδιότητες του Πληρωτικού Υλικού Kεφάλαιο 3: Πειραματική Διαδικασία Αντιδραστήρια και σύσταση του συνθετικού αποβλήτου Πειραματικές Διατάξεις Αντιδραστήρας Διαλείποντος Έργου Αντιδραστήρας Ρευστοποιημένης Κλίνης Πειραματική Διαδικασία και επεξεργασία Αποτελεσμάτων Αναλυτικές Τεχνικές Φασματομετρία Μοριακής Απορρόφησης Υπεριώδους/Ορατού (UV/VIS) για τη μέτρηση της συγκέντρωσης των φωσφορικών στα διαλύματα Φασματοσκοπία Ατομικής Απορρόφησης (ΑΑS) για τη μέτρηση της συγκέντρωσης του μαγνησίου στα διαλύματα Περίθλαση Ακτίνων-Χ (ΧRD) Ηλεκτρονική Μικροσκοπία Σάρωσης (SEM) Kεφάλαιο 4: Aποτελέσματα Πειραμάτων Αυθόρμητης Καταβύθισης Διαγράμματα σταθερότητας για την αυθόρμητη καταβύθιση του στρουβίτη Αυθόρμητη καταβύθιση στρουβίτη σε αντιδραστήρα διαλείποντος έργου Αυθόρμητη καταβύθιση στρουβίτη σε αντιδραστήρα ρευστοποιημένης κλίνης Συμπεράσματα
6 Kεφάλαιο 5: Κρυστάλλωση Στρουβίτη σε Υποστρώματα Καταβύθιση Στρουβίτη σε υπόστρωμα Quartz Καταβύθιση στρουβίτη σε αντιδραστήρα διαλείποντος έργου Καταβύθιση στρουβίτη σε αντιδραστήρα ρευστοποιημένης κλίνης Καταβύθιση Στρουβίτη σε υπόστρωμα Άμμου Καταβύθιση στρουβίτη σε αντιδραστήρα διαλείποντος έργου Καταβύθιση στρουβίτη σε αντιδραστήρα ρευστοποιημένης κλίνης Καταβύθιση Στρουβίτη σε υπόστρωμα Στρουβίτη Καταβύθιση στρουβίτη σε αντιδραστήρα διαλείποντος έργου Καταβύθιση στρουβίτη σε αντιδραστήρα ρευστοποιημένης κλίνης Ποσοστό Ανάκτησης Φωσφόρου και Καταβύθισης Στρουβίτη Σε υπόστρωμα Quartz Σε υπόστρωμα Άμμου Σε υπόστρωμα Στρουβίτη Χρόνος Παραμονής Ρευστού στον Αντιδραστήρα Συμπεράσματα και Ερευνητικές Προτάσεις για το μέλλον Kεφάλαιο 6: Βιβλιογραφία Παράρτημα Ι
7 Περίληψη O Φώσφορος είναι βασικό συστατικό των αστικών αποβλήτων, ο οποίος συγκεντρώνεται στους υδάτινους αποδέκτες προκαλώντας κυρίως προβλήματα ευτροφισμού. Τα παγκόσμια αποθέματα ορυκτού φωσφόρου μειώνονται λόγω της αυξημένης ζήτησης, έτσι κρίνεται απαραίτητο η κατά κάποιον τρόπο ανακύκλωση του. Μια από τις εναλλακτικές και πολλά υποσχόμενες μεθόδους για την ανάκτηση του φωσφόρου από την επεξεργασία των υγρών αποβλήτων είναι η δέσμευση του φωσφόρου, μέσω της κρυστάλλωσης, υπό την μορφή φωσφορικών αλάτων όπως ο στρουβίτης (ΜgNH4PO4.6H2O). O στρουβίτης χρησιμοποιείται απευθείας ως βραδέως αποδεσμευόμενο λίπασμα, το οποίο λόγω της χαμηλής του διαλυτότητας, εξασφαλίζει, την ελεγχόμενη παροχή θρεπτικών συστατικών φωσφόρου και αζώτου, απαραίτητων για την ανάπτυξη των φυτών. Στη παρούσα εργασία, δοκιμάστηκαν δύο τύποι αντιδραστήρων, ένας αντιδραστήρας ρευστοποιημένης κλίνης (FBR) και ένας αντιδραστήρας διαλείποντος έργου (Batch) με συνθετικό απόβλητο σε ph 6.5 στους 25 ο C. Η στοιχειομετρική αναλογία 1:1:1 των πλεγματικών ιόντων του στρουβίτη, Mg:N:P, διατηρήθηκε σε όλα τα πειράματα. Η καταβύθιση στρουβίτη σε υπέρκορα διαλύματα εξαρτάται κυρίως από τον υπερκορεσμό της καταβυθιζόμενης φάσης, τη θερμοκρασία και τη παρουσία ξένων ιόντων ή επιμολύνσεων. Πραγματοποιήθηκαν πειράματα αυθόρμητης καταβύθισης του στρουβίτη σε συνθήκες σταθερού ph για τον καθορισμό του εύρους της μετασταθούς περιοχής. Η γνώση αυτή είναι απαραίτητη για τον καθορισμό των συνθηκών διεξαγωγής πειραμάτων. Τα αποτελέσματα από τους δύο τύπους αντιδραστήρων, δεν παρουσίασαν διαφορές στους χρόνους επαγωγής γεγονός το οποίο υποδεικνύει την αυξημένη σημασία της πυρηνογένεσης και την μικρότερη σημασία της ρευστοδυναμικής του συστήματος. Στους δύο τύπους αντιδραστήρων μελετήθηκε ο ετερογενής σχηματισμός του στρουβίτη σε συνθήκες σταθερού ph 6.5, σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου, χρησιμοποιώντας ως φύτρα για την εκκίνηση της κρυσταλλικής ανάπτυξης, quartz, άμμο και στρουβίτη. Με υπόστρωμα quartz, παρατηρήθηκε μείωση του ρυθμού καταβύθισης αυξανομένης της ποσότητας τόσο σε αντιδραστήρα batch όσο και σε FBR, λόγω της επιβραδυντικής δράσης των πυριτικών ιόντων. Με υπόστρωμα άμμου, παρατηρήθηκε υπερδιπλάσια αύξηση του ρυθμού καταβύθισης για τη 7
8 διπλάσια ποσότητα φύτρων, το οποίο συνηγορεί στην υπόθεση της δευτερογενούς πυρηνογένεσης. Τα μεγαλύτερα ποσοστά ανάκτησης φωσφόρου της τάξεως ~4% και καταβύθισης στρουβίτη από 7-1% είχαμε σε αντιδραστήρα ρευστοποιημένης κλίνης με υπόστρωμα στρουβίτη. Η χρήση υποστρώματος άμμου είχε αποτελέσματα παραπλήσια με τα αντίστοιχα τα οποία ελήφθησαν με την χρησιμοποίηση φύτρων κρυσταλλικού στρουβίτη. Η εισαγωγή σωματιδίων quartz στα υπέρκορα διαλύματα για την δημιουργία πυρήνων κρυστάλλωσης στρουβίτη είχε ως αποτέλεσμα την συγκριτικά μικρότερη απομάκρυνση φωσφόρου και κρυστάλλωση στρουβίτη. Σε λιγότερα από 7min λειτουργίας των αντιδραστήρων, στα υπέρκορα διαλύματα στα οποία είχαν εισαχθεί φύτρα στρουβίτη, η καταβυθιζόμενη ποσότητα στρουβίτη ήταν η μέγιστη δυνατή. Συγκρίσιμα αποτελέσματα ελήφθησαν με την εισαγωγή άμμου στα υπέρκορα διαλύματα. Το καταβυθιζόμενο στερεό χαρακτηρίστηκε με μεθόδους περίθλασης ακτίνων- X και ηλεκτρονική μικροσκοπία σάρωσης. Στα πειράματα batch, το καταβυθιζόμενο στερεό ήταν στρουβίτης, ενώ στα FBR σε υπόστρωμα 2g quartz σε χαμηλό υπερκορεσμό καταβυθίστηκε μικρή ποσότητα φωσφορικού μαγνησίου και σε υπόστρωμα 5g στρουβίτη σε υπερκορεσμό Ω=1.65 παρατηρήθηκε μικρή ποσότητα newberyite. 8
9 Summary Phosphorus is one of the main components in the municipal wastewater, which can lead to problems such as eutrophication in the water reservoirs. The known reserves of phosphorus rocks are decreasing because of the high worldwide demands. Thus, it is necessary to recycle phosphorus from wastewater. Τhe crystallization of struvite is An attractive and new alternative method for phosphorus recovery. Struvite may be used as a slow-release fertilizer because of its relatively low solubility and the presence of both ammonia and phosphorus which through dissolution nutrients available to plants. In the present work, two types of reactors, a fluidized bed reactor (FBR) and a stirred tank reactor were used for the investigation of phosphorus recovery in synthetic wastewater at pη 6.5, 25 ο C. The stoichiometric molar ratio at the constituent ions was 1:1:1 through out the experiments of the present work. The extent of struvite precipitation depends on the solution supersaturation with respect to the precipitating solid, the temperature and the presence of foreign ions or substrates in the solution. The spontaneous precipitation of struvite was studied in both types of reactors at a constant ph 6.5 in order to determine the metastable zone width. This provided knowledge of the stable supersaturated solutions domain where heterogenous nucleation experiments can be done, in order to evaluate nucleation experiments can be done, in order to evaluate the relative ability of substrates to induce the crystallization of struvite. For the two type s reactors, no significant differences were measured for the induction time, preceding precipitation. This suggested that hydrodynamics is not very important for the conditions of the present work. The heterogeneous formation of struvite was investigated at constant supersaturation and of ph in synthetic wastewater in both types of reactors. The seeds included quartz, sand and synthetic struvite. A decrease in the rate of struvite precipitation was found in both reactors with the use of quartz seeds due to the retardation effect of silicon ions. The use of sand seeds increased the rate of precipitation, while increasing the amount of substrate, resulted in a disproportionate increase at the respective rates of precipitation, suggesting a secondary nucleation process. Phosphorus recovery reached almost 4% and precipitation of struvite from 7 to 1% in the FBR filled with struvite. Sand gave similar results with struvite. The recovery of 9
10 phosphorus and precipitation with quartz seeds were low, perhaps because of the inhibition effect of the silicon ions. Experiments, in which struvite seeds were used to seed supersaturated solutions, resulted in the precipitation the maximum amount of struvite in less than 7min. The experiments with sand seeds were quite close from the previous experiments especially in high supersaturation values. Finally, the precipitated solid characterized with XRD and SEM. In the batch series, the precipitated solid was struvite but for the FBR experiments a small amount of magnesium phosphate, for supersaturation Ω= 1.65 with 2g quartz seeds and a small amount of newberyite for 5g struvite seeds in supersaturation value 1.65, were obtained. These findings suggested that the problem is complex and kinetic stabilization of metastable mineral phases may be formed at very specific conditions. 1
11 Κεφάλαιο 1 Εισαγωγή 1.1 O Φώσφορος στα υδατικά απόβλητα Στη σύγχρονη κοινωνία, οι αστικές, οι βιομηχανικές και οι γεωργικές δραστηριότητες προκαλούν την ρύπανση των υδάτινων πόρων με τα αέρια και τα στερεά αλλά κυρίως με τα υγρά απόβλητα τους. Τα αστικά και γεωργικά λύματα περιέχουν ως επί το πλείστον οργανικές ύλες και ορισμένα ανόργανα άλατα όπως τα αμμωνιακά, νιτρικά και φωσφορικά. Τα υγρά απόβλητα των βιομηχανιών περιέχουν κατά κανόνα ρύπους ανάλογους με τα αστικά λύματα αλλά ορισμένες φορές έχουν επιπλέον τοξικές ουσίες και διάφορα μέταλλα όπως ο μόλυβδος, το χρώμιο κλπ. Συγκεκριμένα, ο φώσφορος στα υγρά απόβλητα βρίσκεται κυρίως στις οργανικές ενώσεις και αποτελεί το 75% περίπου του συνολικά υπάρχοντος φωσφόρου. To υπόλοιπο 25% περίπου, βρίσκεται κυρίως με τη μορφή ορθοφωσφορικών (PO4 3-, HPO4 2-, H2PO4 - ) διαλυτών ιόντων από 7-9% και πολυφωσφορικών (P2O7 2- ) ιόντων τα οποία είναι περίπλοκα μόρια, καθώς και με τη μορφή οργανικών φωσφορικών ενώσεων. Τα κάθε είδους απόβλητα καταλήγουν κυρίως στους υγρούς αποδέκτες που είναι επιφανειακοί ή υπόγειοι. Η μεταφορά του φωσφόρου από τα εδάφη στα επιφανειακά νερά οδηγεί στην υποβάθμιση της ποιότητας των φυσικών νερών και στην αύξηση του φαινομένου του ευτροφισμού. Το φαινόμενο του ευτροφισμού χρησιμοποιείται για να εκφράσει τη δυσμενής απόκριση ενός οικοσυστήματος στην περίσσεια θρεπτικών συστατικών, κυρίως αζώτου και φωσφόρου είτε λόγω ανθρωπογενών δραστηριοτήτων είτε λόγω φυσιολογικής εποχιακής αύξησης των στοιχείων αυτών [Harper, 1991]. Ο εμπλουτισμός του νερού σε άλατα φωσφόρου και αζώτου προκαλεί αύξηση της φυτικής (πρωτογενούς) παραγωγικότητας. Η υπέρμετρη παραγωγή φυτικών οργανισμών οδηγεί στη συνέχεια σε αυξημένη δραστηριότητα των αποικοδομητών που δρουν για την αποσύνθεση των φυτικών οργανισμών, και τελικά επηρεάζεται η ποιότητα του νερού (αύξηση θολερότητας, μείωση διαθέσιμου οξυγόνου) [Pierzynski, 2]. Οι ζωικοί οργανισμοί (ψάρια, γαρίδες, βένθος) πεθαίνουν από ασφυξία, με αποτέλεσμα πολλά είδη να εξαφανίζονται, να αντικαθίστανται από άλλα πιο ανθεκτικά (π.χ. πολύχαιτους) και να διαταράσσεται η ισορροπία και η βιοποικιλότητα των υδάτινων συστημάτων 11
12 Σχήμα 1.1: Χαρακτηριστικό παράδειγμα ευτροφισμού στο Shelburne, του Vermont. [Clean water Initiative: Restoring and protecting America s Waters (1998)] 1.2 Απομάκρυνση του Φωσφόρου Κατά την πρωτοβάθμια επεξεργασία των υγρών αποβλήτων είναι δυνατό να απομακρυνθεί το 5-1% του φωσφόρου, ο οποίος συνδέεται με τα οργανικά αιωρούμενα σωματίδια τα οποία περιέχονται στο απόβλητο. Κατά τη δευτεροβάθμια επεξεργασία απομακρύνεται το 2-4% του φωσφόρου σύμφωνα με την μεταβολική δράση των μικροοργανισμών. Τέλος για την απομάκρυνση του φωσφόρου από τα από τα απόβλητα κατά την τριτοβάθμια επεξεργασία ακολουθούνται βιολογικές ή χημικές διεργασίες με ποσοστά απομάκρυνσης 8-95% αντίστοιχα [Τchobanoglous, 23]. Κατά την επεξεργασία των υγρών αποβλήτων, η απομάκρυνση του φωσφόρου απαιτεί τη μεταφορά του φωσφορικού άλατος από την υγρή σε μια στερεά μορφή. Στη συνέχεια γίνεται ο διαχωρισμός από τα υγρά-στερεά και στο τέλος, απομακρύνεται φωσφόρος στην περίσσεια της ιλύος. Δύο μέθοδοι χρησιμοποιούνται για να μετατρέψουν το φώσφορο σε μια στερεά μορφή: η χημική κατακρήμνιση και η ενισχυμένη βιολογική αφαίρεση του φωσφόρου. Η χημική επεξεργασία για την απομάκρυνση φωσφόρου από την υγρή φάση περιλαμβάνει την προσθήκη των αλάτων μετάλλων που αντιδρούν με τον διαλυτό φώσφορο και σχηματίζουν στερεά ιζήματα του αντίστοιχου φωσφορικού άλατος, τα οποία αφαιρούνται με τις διαδικασίες διαχωρισμού στερεών από υγρά όπως η διαύγαση και η διήθηση [Parsons, 23]. Για τον σκοπό αυτό, χρησιμοποιούνται κυρίως άλατα χλωριούχου ή θειικού αλουμινίου ή σιδήρου και σε αρκετές περιπτώσεις και υδροξείδιο του ασβεστίου. Οργανικά φωσφορικά προσροφούνται στο καταβυθιζόμενο στερεό ενισχύοντας και αυτά την απομάκρυνση του φωσφόρου. Η χημική επεξεργασία χρησιμοποιείται ευρύτατα με επιτυχία και υψηλή απόδοση χωρίς να εξαρτάται η λειτουργία της από την ποιότητα, το φορτίο και τις θερμοκρασιακές συνθήκες του αποβλήτου. 12
13 Τα τελευταία χρόνια, η βιολογική απομάκρυνση του χρησιμοποιείται ευρύτατα καθώς μεταξύ των κυριότερων πλεονεκτημάτων συμπεριλαμβάνονται οι μειωμένες δαπάνες σε χημικά και η μικρότερη παραγωγή ιλύος, συγκριτικά με τη χημική καθίζηση. Τα εισερχόμενα λύματα έρχονται σε επαφή με την επανακυκλοφορούμενη λάσπη (βιομάζα) υπό αναερόβιες συνθήκες, οπότε σε ανταγωνιστικό περιβάλλον αναπτύσσεται μια κατηγορία ετεροτροφικών βακτηριδίων τα οποία ερχόμενα σε επαφή με τον φώσφορο, που περιέχεται στα λύματα, τον ελευθερώνουν υδρολύοντας τον με την μορφή διαλυτών φωσφορικών αλάτων. Στη συνέχεια γίνεται πρόσληψη του φωσφόρου από την κυτταρική μάζα των μικροοργανισμών στη δεξαμενή αερισμού. Οι μικροοργανισμοί αυτοί προσροφούν και συσσωρεύουν ενδοκυτταρικά περισσότερο φώσφορο από όσο απαιτείται συνήθως για την κυτταρική ανάπτυξη και συντήρηση τους [Λυμπεράτος, 1999]. Τελικά ο φώσφορος απομακρύνεται με το ρεύμα της λάσπης που απάγεται από τις δεξαμενές τελικής καθίζησης. Η αποφωσφόρωση συνήθως γίνεται μόνη της αλλά πολλές φορές συνδυάζεται και με την απομάκρυνση του αζώτου (Νιτροποίηση- Απονιτροποίηση). Η μέθοδος της βιολογικής απομάκρυνσης επιτυγχάνει απομάκρυνση φωσφόρου της τάξεως του 9-95% με χαμηλό λειτουργικό κόστος. Με τις δύο αυτές μεθόδους ο φώσφορος απομακρύνεται μαζί με άλλα προϊόντα των λυμάτων, δεν ανακυκλώνεται ως ένα πραγματικά διατηρήσιμο προϊόν. Οι ποσότητες του φωσφόρου οι οποίες απομακρύνονται από τα υδατικά απόβλητα είναι σημαντικές και αν γινόταν ανάκτηση θα ήταν δυνατό να καλύψουν σημαντικές ανάγκες της βιομηχανίας παραγωγής φωσφόρου σε πρώτη ύλη. Aποθέματα Φωσφόρου Η κατανάλωση και η παραγωγή φωσφόρου σε παγκόσμια κλίμακα παρουσιάζεται στο σχήμα 1.2. Όπως φαίνεται η βόρειος Αμερική καλύπτει τις ανάγκες της σε φώσφορο. Η Αφρική και η Μέση Ανατολή παρουσιάζουν αυξημένη παραγωγή συγκριτικά με την κατανάλωση τους. Τα ποσά που περισσεύουν εξάγονται σε άλλες χώρες ανά τον κόσμο με αποτέλεσμα η Βόρειος Αφρική να είναι από τους πιο σημαντικούς εξαγωγείς φωσφόρου στον κόσμο. Στην Ασία, η κατανάλωση φωσφόρου υπερβαίνει την παραγωγή του με αποτέλεσμα να απαιτούνται εισαγωγές του ορυκτού. Στην Ευρώπη, η παραγωγή φωσφόρου περιορίζεται στην Ανατολική Ευρώπη καλύπτοντας την κατανάλωση της. 13
14 Σχήμα 1.2 : Παγκόσμια παραγωγή Φωσφόρου [Adam, 29] Από την U.S. Geological Survey (USGS) το 21, εκτιμήθηκε ότι τα φωσφορικά ορυκτά αποθέματα έχουν χρονικό ορίζοντα για 9 έτη [Roberts and Stewart, 22], εν αντίθεση με το 1996 όπου είχαν υπολογιστεί για 16 έτη [Steen and Agro, 1998]. Το 28, η τιμή του ορυκτού φωσφόρου ανέβηκε παγκοσμίως λόγω της αυξημένης γεωργικής ζήτησης και των περιορισμένων κοιτασμάτων. Η τιμή στις ΗΠΑ σχεδόν διπλασιάστηκε και η μέση τιμή των εξαγωγών από χώρες όπως η Βόρειος Αφρική ανήλθε στα 4 ευρώ/τόνος, τιμή πενταπλάσια σε σύγκριση με την μέση τιμή στις ΗΠΑ το 27. Έτσι, είναι ιδιαίτερα ανησυχητικό για τη βιομηχανία λιπάσματος της βόρειας Αμερικής ότι η χρονική διάρκεια των αποθεμάτων έχει εκτιμηθεί στα 25 χρόνια, μετατρέποντας έτσι την Αμερική από κυρίαρχο εξαγωγέα φωσφόρου σε μεγαλύτερο παγκόσμιο καταναλωτή. Κρίνεται έτσι αναγκαίο η εύρεση μιας μεθόδου αξιοποίησης του φωσφόρου που προέρχεται από τα απόβλητα. 1.3 Ανάκτηση του Φωσφόρου Η εύρεση μεθόδου για την ανάκτηση του φωσφόρου από τα υδατικά απόβλητα κρίνεται απαραίτητη για τους εξής λόγους. Ο πρώτος είναι αναγκαιότητα της περιστολής της συγκέντρωσης του φωσφόρου για την καλύτερη ποιότητα των φυσικών νερών για την προστασία του περιβάλλοντος. Ο δεύτερος λόγος αφορά στην αειφόρο ανάπτυξη μέσω εξοικονόμησης πρώτων υλών. Ο τρίτος λόγος προέκυψε μετά από την παρουσία λειτουργικών προβλημάτων στις μονάδες επεξεργασίας υγρών αποβλήτων, τα οποία οφείλονταν σε επικαθίσεις φωσφορικών αλάτων σε τμήματα εξοπλισμού των μονάδων [Κοφινά, 26]. Η καλύτερη δυνατή λύση στα πλαίσια αυτά είναι η ανάκτηση του φωσφόρου με την μορφή του 14
15 εξάνυδρου εναμμώνιου φωσφορικού μαγνησίου, MgNH4PO4. 6H2O με την κοινή ονομασία στρουβίτης (Struvite) Ο Στρουβίτης ως Εναπόθεση στις Βιομηχανικές Μονάδες (Scale Formation) Σε μονάδα επεξεργασίας αποβλήτων παρατηρήθηκε για πρώτη φορά το 1939 ο σχηματισμός στρουβίτη, ένα λευκό κρυσταλλικό στερεό, στην υπερκείμενη υγρή φάση αναερόβιας χωνευμένης λάσπης[rawn, 1939]. Ο σχηματισμός εναποθέσεων στρουβίτη παρουσιάστηκε επίσης το 1963 σε μονάδα επεξεργασίας αποβλήτων του Hyperion στο Los Angeles, όπου χειριστές της εγκατάστασης παρατήρησαν επικαθίσεις κρυστάλλων στο κάτω μέρος των σχαρών χώνευσης [Borgerding, 1972]. To ρεύμα της χωνευμένης ιλύος αραιώθηκε, αλλά σε διάστημα 5 ετών, η φυσική ροή, λόγω βαρύτητας της λάσπης, είχε μειωθεί σε τέτοιο βαθμό, ώστε η χρήση αντλίας κρίθηκε απαραίτητη. Στις περιπτώσεις αυτές, η εσωτερική διάμετρος των σωληνώσεων είχε μειωθεί από τις εναποθέσεις από 12 σε 6 in. Η δημιουργία επικαθίσεων στρουβίτη εξαρτάται από την χημική σύσταση του ρεύματος των αποβλήτων, το ph και από το υλικό και την τραχύτητα των επιφανειών των σωληνώσεων [Doyle, 22]. Από το σχηματισμό του στρουβίτη επηρεάζονται εκτός από τις σωληνώσεις, όλα τα σημεία στα οποία η ροή είναι ιδιαίτερα έντονη όπως οι αντλίες, οι φυγόκεντροι και οι αεριστήρες. Σε ορισμένες περιπτώσεις, η έκταση της ζηµιάς είναι τόσο µεγάλη ώστε η µόνη εφικτή και οικονοµική λύση είναι η αντικατάσταση των σωληνώσεων. Με την επικάθηση του στρουβίτη στις σωληνώσεις μειώνεται η διάμετρος τους και έτσι απαιτείται μεγαλύτερη ενέργεια για την μετακίνηση της λάσπης με τη χρήση αντλίας αυξάνοντας το κόστος λειτουργίας της. Επίσης, αυξάνεται ο χρόνος κυκλοφορίας της λάσπης στους σωλήνες, με αποτέλεσμα τη μείωση της δυναμικότητας της εγκατάστασης. Οι Σχήμα 1.3: Επικαθίσεις στρουβίτη σε σωλήνωση σε μονάδα επεξεργασίας αποβλήτων [Shao, 1999] περισσότερες μονάδες έχουν καταρτίσει προγράμματα συντήρησης κατά τη διάρκεια της λειτουργίας τους με μεγάλο όμως κόστος σε εργατοώρες. Χαρακτηριστικό παράδειγμα είναι το Pongol Pig waste της Σιγκαπούρης και 15
16 το Slough STW του Ηνωμένου Βασιλείου, όπου με τα προγράμματα τακτικής συντήρησης έχουν απώλειες 8-1 εργατοωρών κάθε φορά [Μohajit, 1989] Eφαρμογές ανάκτησης φωσφόρου από βιομηχανίες επεξεργασίας αποβλήτων Έχει αναπτυχθεί μια σειρά μεθόδων για την ανάκτηση του φωσφόρου υπό μορφή στρουβίτη. Έχουν πραγματοποιηθεί πειράματα τόσο σε εργαστηριακή όσο και σε πιλοτική και πραγματική κλίμακα. Στο συγκεκριμένο κεφάλαιο περιγράφονται διάφορες βιομηχανικές μέθοδοι για την ανάκτηση του φωσφόρου. Χαρακτηριστικά παραδείγματα των μεθόδων είναι τα εξής; Crystalactor, Air Prex και η διεργασία Pearl Process. Διεργασία Κρυστάλλωσης μέσω της μεθόδου DHV-Crystalactor H μέθoδος DHV-Crystalactor βασίζεται στην κρυστάλλωση ενώσεων του φωσφόρου όπως φωσφορικό ασβέστιο, φωσφορικό μαγνήσιο και στρουβίτης, επάνω σε φύτρα πληρωτικού υλικού (πχ. άμμος ή quartz), σε αντιδραστήρα ρευστοποιημένης κλίνης (σχήμα 1.4). Η διεργασία της κρυστάλλωσης πραγματοποιείται με την είσοδο του αποβλήτου με κατεύθυνση από κάτω προς τα πάνω ώστε να ρευστοποιείται όλο το μήκος της κλίνης και με την κατάλληλη προσθήκη αντιδραστηρίων και ρύθμιση του ph. Με την επιλογή των κατάλληλων συνθηκών, ελαχιστοποιείται η πιθανότητα επιμολύνσεων και επιτυγχάνεται λήψη κρυστάλλων υψηλής καθαρότητας. Τα παραγόμενα μεγαλύτερης διαμέτρου σφαιρίδια (pellets) συλλέγονται από το κάτω μέρος του αντιδραστήρα και αντικαθίστανται με μικρότερης διαμέτρου φύτρα πληρωτικού υλικού. Τα pellets αυτά ξηραίνονται σε θερμοκρασία δωματίου. Ένα από τα κυριότερα πλεονεκτήματα της συγκεκριμένης μεθόδου είναι η δυνατότητα να παράγονται καθαρά και απαλλαγμένα από οργανικά κατάλοιπα σφαιρίδια στρουβίτη με Σχήμα 1.4 : Αντιδραστήρας Crystalactor [Giesen, 29] 16
17 μειωμένες συγκεντρώσεις βαρέων μετάλλων και φιλικά προς το περιβάλλον. Στον πίνακα 1.1 συγκρίνονται τα σφαιρίδια που προκύπτουν από την επεξεργασία με την λυματολάσπη που προκύπτει από καθίζηση. Πίνακας 1.1: Σύγκριση χαρακτηριστικών [Giesen, 29] DHV-Crystalactor Συμβατική Καθίζηση Μορφολογία Σφαιρίδια.8-1.mm Λυματολάσπη Ποσοστό σε νερό 1-5% 6-85% (μετά την αφυδάτωση) Υλικό ανάπτυξης <5% -- Ενώσεις Φωσφόρου 9-98% 2-3% (μετά την αφυδάτωση) Λόγω της εξαιρετικής σύστασης τους τα σφαιρίδια είτε ανακυκλώνονται είτε χρησιμοποιούνται σε άλλες διεργασίες. Δηλαδή: Πρώτες ύλες για την παραγωγή φωσφορικών οξέων Πρώτη ύλη για την παρασκευή λιπασμάτων Πρώτη ύλη για την παρασκευή συγκεκριμένων τροφών Λίπασμα Μέθοδος Airprex Η διαδικασία Αir Prex αναπτύχθηκε από την γερμανική εταιρία Berliner Wasserbetriebe (BWB) και η συγκεκριμένη μέθοδος χρησιμοποιείται στην εγκατάσταση επεξεργασίας αστικών λυμάτων στο Waβmanndorf κοντά στο αεροδρόμιο Schönefeld. Η μονάδα βιολογικού καθαρισμού Waβmanndorf είναι μια από τις έξι εγκαταστάσεις επεξεργασίας αστικών λυμάτων της εταιρίας ΒWB που έχουν το μεγαλύτερο φορτίο BOD5 και η δεύτερη μεγαλύτερη μονάδα με τη μεγαλύτερη ροή λυμάτων προς επεξεργασία. Η εγκατάσταση έχει τη δυνατότητα επεξεργασίας 23 m 3 /d, με έναν μέσο ρυθμό εισροής της τάξεως των 18. m 3 /d εφόσον επικρατούν ξηρές κλιματολογικές συνθήκες. Η BWB διαθέτει μια μονάδα επεξεργασίας λυμάτων στην οποία πραγματοποιείται βιολογική αφαίρεση του φωσφόρου από τα λύματα. Ένα σημαντικό πρόβλημα που αντιμετωπίζει η εγκατάσταση είναι η καταβύθιση του στρουβίτη που έχει ως αποτέλεσμα να επηρεάζει την απόδοση και τη λειτουργία του εξοπλισμού. Η χωνευμένη λυματολάσπη περιείχε συγκέντρωση μαγνησίου 1mg/L. Στο σχήμα 1.5 παρουσιάζεται μια αντλία και ο σωλήνας εισόδου ροής από το σταθμό άντλησης νερών της φυγοκέντρησης, όπου καταβυθίστηκε στρουβίτης μετά από 319 h λειτουργίας. Η ανάλυση δείγματος έδειξε ότι το υλικό που καταβυθίστηκε ήταν στρουβίτης και ένα μικρό ποσοστό ήταν φωσφορικό ασβέστιο [Heinzmann, 29]. 17
18 Σχήμα 1.5: Αντλία και σωλήνας εισόδου ρευστού χρησιμοποιείται στην εγκατάσταση επεξεργασίας αστικών λυμάτων στο Waβmanndorf [Heinzmann, 29] Το πρόβλημα λύθηκε αναπτύσσοντας μια μέθοδο ελεγχόμενης καταβύθισης του στρουβίτη, η οποία αναπτύχθηκε σε συνεργασία με το Τεχνικό Πανεπιστήμιο του Βερολίνου. Η διαδικασία Air Prex απεικονίζεται στο σχήμα 1.6 στην οποία η καταβύθιση στρουβίτη πραγματοποιείται με αφαίρεση CO2 με μεθόδους αερισμού και ρύθμιση του ph αλλά και δόση MgCl2. O Στρουβίτης αφαιρείται συνεχώς από τον πυθμένα του αντιδραστήρα καθιστώντας την ανάκτηση φωσφόρου περισσότερο αποτελεσματική. Σχήμα 1.6 : Αντιδραστήρα μεθόδου Air Prex [Heinzmann, 29] Όπως φαίνεται στο σχήμα 1.6 η αρχή της μεθόδου έγκειται στην κυκλική κίνηση που υφίσταται η λυματολάσπη εντός του αντιδραστήρα. Οι φυσαλίδες αέρα που δημιουργούνται μετακινούν τη λυματολάσπη προς τα πάνω στην περιοχή αερισμού η οποία βρίσκεται στη μέση του αντιδραστήρα. Αφού η λυματολάσπη φτάσει στην επιφάνεια τότε εναποτίθεται στη ζώνη ηρεμίας στο εξωτερικό μέρος του αντιδραστήρα. Ο καταβυθιζόμενος 18
19 στρουβίτης εναποτίθεται στον πυθμένα της δεξαμενής καθώς η λυματολάσπη εισέρχεται και πάλι στην ζώνη αερισμού [Νieminen, 21]. H παραγωγή του στρουβίτη είναι 2.5 t/d καθώς και η ποιότητα του πληροί τις προϋποθέσεις της γερμανικής νομοθεσίας. Ο στρουβίτης πωλείται στις βιομηχανίες λιπασμάτων ώστε να χρησιμοποιηθεί και εκεί σε συνδυασμό με άλλες πρώτες ύλες. Η επένδυση της συγκεκριμένης διαδικασίας κοστίζει 2.5 εκατομμύρια ευρώ και η ιδανική τιμή πώλησης του στρουβίτη είναι 5 /t. Στον υπολογισμό αυτής της τιμής συμπεριλαμβάνεται και το κόστος της νέας εγκατάστασης. Η τιμή ως προς τον φώσφορο είναι 4 /t P [Nieminen, 21], [Hannenman, 29]. Διαδικασία Pearl Process H συγκεκριμένη διαδικασία αναπτύχθηκε από το πανεπιστήμιο του Καναδά, British Columbia. Σε αυτήν πραγματοποιείται ανάκτηση φωσφορικών και άλλων θρεπτικών συστατικών από τα υπερκείμενα υγρά της ιλύος. Το ανακτώμενο προϊόν διατίθεται στο εμπόριο ως λίπασμα με την ονομασία Crystal Green (σχήμα 1.7) από την εταιρία Ostara. Aπό το 21 έχουν διεξαχθεί πιλοτικά τεστ και στα έξι διαφορετικά εργοστάσια για μια περίοδο ενός με οκτώ μηνών. Ο πρώτος αντιδραστήρας βιομηχανικής κλίμακας λειτούργησε στο Edmonton του Καναδά τον Μάιο του 27 και άλλοι αντιδραστήρες όπως αυτοί που είναι στις Ηνωμένες Πολιτείες της Αμερικής στο Portland του Οregon και στο Suffolk της Virginia ξεκίνησαν να λειτουργούν το Ο τέταρτος στη Νέα Υόρκη το φθινόπωρο του Σχήμα 1.7: Προιόν Crystal Green [Ostara]
20 Σχήμα 1.8: Αντιδραστήρας για την καταβύθιση στρουβίτη στην Ostara του Καναδά [Britton 21] Η τεχνολογία Pearl βασίζεται στην χρήση ενός κατάλληλου αντιδραστήρα ρευστοποιημένης κλίνης. Όπως φαίνεται στο σχήμα 1.8 η διάμετρος του αντιδραστήρα μεγαλώνει από κάτω προς τα πάνω. Η λυματολάσπη, που εισέρχεται για επεξεργασία στον αντιδραστήρα προέρχεται από τη διαδικασία αφυδάτωσης και περιέχει περίπου 1-9 mg/l φωσφόρου PO4-P σε περίπτωση που η εγκατάσταση έχει μονάδα βιολογικής αφαίρεσης φωσφόρου και αναερόβια χώνευση. Με τη συμβατική μεθόδου της ενεργός ιλύος και αναερόβια χώνευση, η συγκέντρωση του φωσφόρου είναι περίπου 6-15mg/L. Στο εσωτερικό του αντιδραστήρα εισάγεται ένας τόνος από πληρωτικό υλικό στρουβίτη διαμέτρου 1mm που είχαν παραχθεί από τη μονάδα παραγωγής του Edmonton Alberta στον Καναδά. Καλλιεργήθηκαν για μια περίοδο δύο έως τεσσάρων εβδομάδων έτσι ώστε να φθάσουν στο επιθυμητό μέγεθος. Το προϊόν αποστέλλεται στη συνέχεια σε ειδικά δονούμενα φίλτρα για την αφαίρεση του νερού. Έπειτα συλλέγονται και διαχωρίζονται και πακετάρονται ανάλογα το μέγεθος τους. Η εφαρμογή αυτής της τεχνολογία προσφέρει μια καλή απόδοση ανάκτησης φωσφόρου >85%. 2
21 1.3.3 Στρουβίτης ως λίπασμα Ο στρουβίτης μπορεί να χρησιμοποιηθεί ως λίπασμα για αγροτική χρήση (Potjer, 21). Yπάρχουν αρκετές βιβλιογραφικές αναφορές για τη χρήση του στρουβίτη ως βραδέως αποδεσμευόμενο λίπασμα, λόγω της χαμηλής διαλυτότητας του νερό [Bridger et al., 1961]. Ο στρουβίτης διαθέτει χαμηλή περιεκτικότητα σε βαρέα μέταλλα και άλλους μικρορυπαντές [Βattistoni, 2]. Η ελεγχόμενη παροχή των θρεπτικών συστατικών του όπως του φωσφόρου και του αζώτου, απαραίτητων για την ανάπτυξη φυτών, το καθιστά μια ελκυστική επιλογή για την γεωργία [Μunch and Barr, 21]. Επίσης, ο στρουβίτης εκτιμάται ότι έχει τη δυνατότητα να σταθεροποιεί ελαφρά το έδαφος χωρίς να φράσσονται όλοι οι πόροι αυτού, ούτως ώστε να παρέχεται η δυνατότητα στο νερό και στον αέρα να εισέρχονται στο έδαφος και παράλληλα να εμπλουτίζεται με τα απαραίτητα θρεπτικά συστατικά για να μπορούν τα φυτά να αναπτύσσονται ανεμπόδιστα. Ένα μειονέκτημα του στρουβίτη ως λίπασμα είναι η έλλειψη καλίου [Gaterall et al., 2]. To κάλιο, είναι απαραίτητο για την αποτελεσματική ανάπτυξη των καρπών. Σε πολλές περιπτώσεις, απαιτείται η επιπλέον προσθήκη του για να χρησιμοποιηθεί ο στρουβίτης ως λίπασμα. Τέλος, η ανάκτηση του φωσφόρου και του αζώτου μέσω της κρυστάλλωσης υπό μορφή στρουβίτη, μπορεί να δώσει ένα πολύτιμο λίπασμα μειώνοντας έτσι το κόστος της διαχείρισης των λυμάτων και συνεισφέροντας στην ανάκτηση μιας σημαντικής πρώτης ύλης. 1.4 Oικονομική Αξιολόγηση Ανάκτησης Φωσφόρου υπό μορφή στρουβίτη Ο φώσφορος αποτελεί μια πρώτη ύλη, η οποία βρίσκεται σε πεπερασμένες ποσότητες. Οι ολοένα αυξανόμενες ανάγκες χρήσης του καθιστούν την ανάκτηση του φωσφόρου αναγκαία. Επειδή ο στρουβίτης περιέχει θρεπτικά στοιχεία όπως είναι ο φώσφορος και το άζωτο, είναι επωφελές να υπάρχει ανάκτηση τους υπό τη μορφή στρουβίτη, έτσι ώστε το προϊόν αυτό να χρησιμοποιείται στη βιομηχανία λιπασμάτων. H παραγωγή στρουβίτη έχει ως αποτέλεσμα τη μείωση κόστους των χημικών που χρησιμοποιούνται στη μονάδα επεξεργασίας λυμάτων. Ακόμη, μειώνεται και η παραγωγή λυματολάσπης (λόγω χημικής καθίζησης του φωσφόρου) και εξοικονομούνται εκτάσεις, οι οποίες απαιτούνται για την απόθεση της. Έρευνες υποδεικνύουν πώς πάνω από το 9% του διαλυμένου φωσφόρου μπορεί να ανακτηθεί μετά την 21
22 αναερόβια χώνευση μέσω της κρυστάλλωσης του στρουβίτη [Battistoni et al., 21]. Απαλλαγμένος από τοξικές ακαθαρσίες, αποτιμάται στα 25 /t ξηρού υλικού από Ιαπωνικές εταιρίες λιπασμάτων [Verstraete, 29]. To κόστος παραγωγής από τη λυματολάσπη μπορεί να κυμαίνεται από 22 έως 73 /t στην Αυστραλία και στην Ιαπωνία [Doyle and Parsons, 22] και να φτάνει μέχρι 275 /t στην Ολλανδία [Verstraete, 29]. Σύμφωνα με έρευνα που πραγματοποιήθηκε από τους Munch and Barr [21], υπολογίστηκε ότι το λειτουργικό κέρδος από την παραγωγή στρουβίτη σε μονάδες επεξεργασίας λυμάτων που παράγουν 55. m 3 /d κυμαίνεται από -13. έως 149. ανά έτος δολάρια Αυστραλίας (με το αρνητικό πρόσημο να υποδηλώνει κόστος). Εάν υποθέσουμε πως μια μονάδα επεξεργασίας λυμάτων μπορεί να ανακτήσει περίπου 1κg στρουβίτη από 1 m 3 λυμάτων [Munch and Barr, 21] τότε το κέρδος μπορεί να κυμαίνεται από -.7 έως.74 δολάρια Αυστραλίας ανά Kg στρουβίτη που ανακτάται κάθε μέρα. Στον πίνακα 1.2 παρουσιάζεται το κόστος ανάκτησης φωσφόρου ως στρουβίτη. Παρατηρούμε ότι το αρχικό λειτουργικό κόστος δεν μπορεί να καλυφθεί πλήρως πουλώντας μόνο στρουβίτη. Παρόλα αυτά όσο αυξάνονται οι γνώσεις μας γύρω από την κρυστάλλωση του στρουβίτη τόσο δύναται να καλυφθεί πλήρως το λειτουργικό κόστος αλλά και να υπάρξει επίσης και κέρδος. Όπως φαίνεται στον πίνακα 1.1 το ποσό του φωσφόρου που ανακτάται από 1 m 3 /d αποτελεί μόλις τα 2.6 δισεκατομμυριοστά της παγκόσμιας κατανάλωσης σε φώσφορο. Πίνακας 1.2: Εκτιμώμενο κόστος ανάκτησης φωσφόρου ώς στρουβίτη από χωνευτές λυμάτων [Shu et al. 25] Εκροές Λυμάτων (m 3 /d) (Oxley WWTP) 6 (λεκάνη απορροής GBR) Στρουβίτης (Kg/d) Ζημιά ($/d) Κέρδος ($/d) Ζημιά ($/yr) Κέρδος ($/yr) Στρουβίτης (Kg/yr) Φώσφορος (P2O3) (Kg/yr)
23 Όσον αφορά στο παράδειγμα της Αυστραλίας, δηλαδή τις μονάδες επεξεργασίας λυμάτων στην περιοχή του μεγάλου κοραλλιογενούς ύφαλου, το ποσοστό του φωσφόρου που ανακτάται αποτελεί το.16% της παγκόσμιας κατανάλωσης. Η ανάκτηση φωσφόρου έχει τη δυναμική να μειώσει το λειτουργικό κόστος με τη μείωση της χρήσης χημικών, τη διάθεση της λυματολάσπης αλλά και τη μείωση του χρόνου καθαρισμού των εναποθέσεων του στρουβίτη στη βιομηχανία. 1.5 Σκοπός της Παρούσας εργασίας Σκοπός της παρούσας εργασίας ήταν η μελέτη της κινητικής της καταβύθισης και η βελτιστοποίηση των συνθηκών ανάκτησης φωσφόρου με τη μορφή του στρουβίτη σε ένα συνθετικό αστικό απόβλητο. Η κινητική της καταβύθισης του στρουβίτη μελετήθηκε σε συνθήκες σταθερού ph 6.5 και σε θερμοκρασία 25 C με στοιχειομετρική αναλογία 1:1:1 των συγκεντρώσεων των ιόντων Mg 2+, PO4 3- και NH4 +. Τα πειράματα πραγματοποιήθηκαν σε αντιδραστήρα διαλείποντος έργου (Batch) και σε αντιδραστήρα ρευστοποιημένης κλίνης (FBR). Διερευνήθηκε η καταβύθιση στρουβίτη από υπέρκορα διαλύματα ομογενώς με αυθόρμητη καταβύθιση, για τον καθορισμό των αρχικών συνθηκών και στους δύο αντιδραστήρες. Επίσης, στους δύο τύπους αντιδραστήρα πραγματοποιείται μελέτη της κινητικής της ετερογενούς καταβύθισης χρησιμοποιώντας ως ξένα υποστρώματα κρυσταλλικά φύτρα συνθετικά παρασκευασμένου στρουβίτη, quartz και άμμου. Με βάση τα ποσοστά ανάκτησης φωσφόρου και καταβύθισης στρουβίτη που υπολογίζονται, επιλέγεται ο κατάλληλος αντιδραστήρας και πληρωτικό υλικό για την κρυστάλλωση του στρουβίτη. 23
24 Κεφάλαιο 2 Θεωρητικό Μέρος 2.1 Εισαγωγή της Κρυστάλλωσης Η κρυστάλλωση είναι μια διεργασία που χρησιμοποιείται ευρέως στη χημική βιομηχανία, είτε ως μέθοδος παραγωγής είτε ως μέθοδος καθαρισμού ή ανάκτησης στερεών υλικών. Είναι από τις καλύτερες και φτηνότερες μεθόδους παραγωγής καθαρών στερεών από μη καθαρά διαλύματα, προσφέροντας ένα τελικό προϊόν με το πλεονέκτημα καθορισμού επιθυμητών ιδιοτήτων (σχήμα, μέγεθος σωματιδίων κ.α.). Εφαρμογές των μεθόδων και των αρχών της κρυστάλλωσης γίνονται στις βιομηχανίες παραγωγής χημικών προϊόντων, φαρμάκων, κεραμικών, χρωμάτων, πολυμερών υλικών, στη μεταλλουργία, στη σύνθεση ημιαγωγών, στη παρασκευή καταλυτών, στις βιομηχανίες τροφίμων, λιπασμάτων και πετρελαίου [ ]. H ανακάλυψη της τεράστιας σημασίας της κρυστάλλωσης, των νόμων που τη διέπουν και των παραγόντων που την επηρεάζουν, καθυστέρησε αρκετά και για μεγάλο χρονικό διάστημα χαρακτηριζόταν περισσότερο ως τέχνη παρά ως επιστήμη. Στα τέλη του 18 ου και τις αρχές του 19 ου αιώνα άρχισε να παρατηρείται μια μετάβαση από την τέχνη στην επιστήμη, η οποία συνεχίζεται μέχρι σήμερα, δεδομένου ότι πολλές από τις σύγχρονες θεωρίες δεν έχουν ακόμη εφαρμοστεί πλήρως από την τεχνολογία [Mullin, 21]. Η κρυστάλλωση περιλαμβάνει μια σειρά διεργασιών το τελικό αποτέλεσμα των οποίων είναι ο σχηματισμός μιας νέας φάσης μέσα σε ομογενές διάλυμα. Αναγκαία αλλά όχι ικανή συνθήκη για το σχηματισμό νέας φάσης είναι η ύπαρξη του υπερκορεσμού, μιας κατάστασης θερμοδυναμικά ασταθούς. Οι δομικές μονάδες της διαλυμένης ουσίας αρχίζουν να διατάσσονται με τρόπο που από δομικής άποψης, είναι χαρακτηριστικό της νέας φάσης. Σχηματίζεται μια νέα διαχωριστική επιφάνεια μεταξύ του διαλύματος και της νέας στερεάς φάσης. Η νέα φάση εμφανίζεται πρώτα με τη μορφή κρυσταλλικών εμβρύων (πλειάδες δομικών μονάδων) μέσα στο υπέρκορο διάλυμα, οι οποίες είτε επαναδιαλύονται στο διάλυμα είτε ξεπερνώντας ένα ενεργειακό φράγμα, αναπτύσσονται και δημιουργούν τη νέα φάση. Οι διεργασίες που οδηγούν στο σχηματισμό της νέας φάσης (υπερκορεσμός, πυρηνογένεση, κρυσταλλική ανάπτυξη), πολλές φορές 24
25 συμβαίνουν σχεδόν ταυτόχρονα καθιστώντας δύσκολη την επιμέρους μελέτη τους και αναγκαία την παράλληλη επεξεργασία τους. 2.2 Διαλύματα δυσδιάλυτων Αλάτων Διάγραμμα Διαλυτότητας Ως διάγραμμα διαλυτότητας ενός δυσδιάλυτου άλατος ορίζεται το διάγραμμα στο οποίο παρίσταται γραφικά η συγκέντρωση του άλατος σε συναρτήσει της θερμοκρασίας σε σταθερό ph ή συναρτήσει του ph όταν η θερμοκρασία είναι σταθερή. Σε ένα τέτοιο διάγραμμα, διακρίνονται τρείς περιοχές, η φυσική σημασία των οποίων καθορίζεται από την καμπύλη διαλυτότητας και από την καμπύλη υπερδιαλυτότητας. α) Σταθερή περιοχή: Είναι η περιοχή κάτω από τη καμπύλη διαλυτότητας. Στη περιοχή αυτή το διάλυμα είναι ακόρεστο, η μόνη φάση που υπάρχει είναι η υδατική και λαμβάνει χώρα η διεργασία της διάλυσης. Η καμπύλη διαλυτότητας περιγράφει την ισορροπία μεταξύ υγρής και στερεής φάσης. Η καμπύλη διαλυτότητας αντιστοιχεί στον γεωμετρικό τόπο των σημείων που ικανοποιούν τη συνθήκη του γινομένου διαλυτότητας και καθορίζεται από το θερμοδυναμικό γινόμενο διαλυτότητας. β) Μετασταθής Σταθερή περιοχή: Βρίσκεται πάνω από τη καμπύλη διαλυτότητας, στην οποία τα διαλύματα είναι μεν υπέρκορα αλλά μπορεί να είναι σταθερά έπ άπειρον με την προϋπόθεση ότι δεν εισάγονται πυρήνες κρυστάλλωσης. Η καμπύλη υπερδιαλυτότητας αποτελεί το άνω όριο της μετασταθούς περιοχής και καθορίζεται από την κινητική του σχηματισμού της στερεάς φάσης, δηλαδή προσδιορίζεται μόνο πειραματικά. Η διαχωριστική αυτή γραμμή μεταξύ της μετασταθούς και της ασταθούς περιοχής δεν είναι σαφής και επηρεάζεται σημαντικά από παράγοντες όπως η ύπαρξη ανωμαλιών στα τοιχώματα του δοχείου που περιέχει το υπέρκορο διάλυμα, η ύπαρξη ξένων σωματιδίων όπως σκόνη κλπ. Τα σημεία της καμπύλης υπερδιαλυτότητας, αντιστοιχούν σε διαλύματα στα οποία η έναρξη της καταβύθισης γίνεται με τη πάροδο ενός χρονικού διαστήματος που ονομάζεται χρόνος επαγωγής. Ο χρόνος αυτός είναι αντιστρόφως ανάλογος του υπερκορεσμού του διαλύματος. γ) Μετασταθής- Ασταθής περιοχή: Είναι η περιοχή πέρα από την μετασταθή περιοχή όπου τα διαλύματα είναι αρκετά υπέρκορα. Στην ασταθή περιοχή συμβαίνει αυθόρμητη καταβύθιση του δυσδιάλυτου άλατος με τη δημιουργία των πυρήνων κρυστάλλωσης αυθόρμητα στο υπέρκορο διάλυμα. 25
26 Σχήμα 2.1: Διάγραμμα διαλυτότητας δυσδιάλυτου άλατος [Mullin, 21] Γινόμενο Διαλυτότητας Η θερμοδυναμική ισορροπία μεταξύ της κρυσταλλικής φάσης και ενός διαλύματος ορίζεται με τη βοήθεια του γινομένου διαλυτότητας. Για τα δυσδιάλυτα άλατα της μορφής ΑmBn που διίστανται σύμφωνα με την πιο κάτω γενική αντίδραση: 2.1 το χημικό δυναμικό των ιόντων στο διάλυμα δίνεται από τις σχέσεις: όπου και είναι τα πρότυπα χημικά δυναμικά και οι ενεργότητες των πλεγματικών ιόντων και, k η σταθερά του Boltzmann και T η απόλυτη θερμοκρασία. Όμοια για την στερεά φάση: 2.4 H μεταβολή του χημικού δυναμικού κατά την κρυστάλλωση είναι ίση με:
27 Στην κατάσταση ισορροπίας (κορεσμένο διάλυμα) Δμ= οπότε: 2.6 Και ανά mole: 2.7 Όμως για την στερεά κατάσταση έχουμε απλοποιείται στη μορφή:. Έτσι η πιο πάνω σχέση 2.8 Άρα = 2.9 Όπου είναι οι ενεργότητες των ιόντων και στην κατάσταση ισορροπίας, διαλυτότητας. Η θερμοκρασίας και την πίεση Υπερκορεσμός είναι η θερμοδυναμική σταθερά του γινομένου για κάθε δυσδιάλυτο άλας εξαρτάται από την Ο υπερκορεσμός ενός διαλύματος ως προς ένα άλας, για ορισμένη θερμοκρασία και πίεση είναι το μέτρο της απομάκρυνσης από την κατάσταση ισορροπίας ενός διαλύματος. Ορίζεται ως η διαφορά ανάμεσα στην συγκέντρωση της ένωσης στο υπέρκορο διάλυμα C και στην διαλυτότητα της ένωσης δηλαδή τη συγκέντρωση ισορροπίας C. : Υπερκορεσμός 2.1 Σχετικός υπερκορεσμός, σχ, ορίζεται ως: 2.11 Και ο βαθμός ή λόγος υπερκορεσμού, S, : 2.12 Στις παραπάνω εκφράσεις αναφερόμαστε σε αραιά διαλύματα με αποτέλεσμα οι ενεργότητες να αντικαθίστανται από τις αντίστοιχες συγκεντρώσεις. Επειδή τα διαλύματα των ηλεκτρολυτών είναι μη ιδανικά αντί των συγκεντρώσεων χρησιμοποιούνται οι ενεργότητες των ιόντων. 27
28 Η κινητήριος δύναμη για τον σχηματισμό δυσδιάλυτων αλάτων σε υπέρκορα διαλύματα τους είναι η μεταβολή του χημικού δυναμικού κατά τη μετατροπή της υγρής φάσης σε κρυσταλλική φάση, όπου α και αs είναι η ενεργότητες της διαλυμένης ένωσης στο υγρό και στην στερεά κατάσταση αντίστοιχα [House, 1989]: 2.13 Στη περίπτωση διαλυμάτων αλάτων ηλεκτρολυτών, η ενεργότητα είναι η μέση ιονική ενεργότητα: όπου, είναι ο αριθμός των ιόντων που περιέχονται στην ένωση ΑmBn. Οπότε η εξίσωση 2.13 γράφεται: ktln όπου IAP = 2.14 Για τους ηλεκτρολύτες ο λόγος του ιοντικού γινομένου των ενεργοτήτων προς το θερμοδυναμικό γινόμενο διαλυτότητας είναι η έκφραση του βαθμού υπερκορεσμού. Άρα: Στην ισορροπία, δηλαδή πάνω στη καμπύλη διαλυτότητας, το ιοντικό γινόμενο ενεργοτήτων ισούται με το θερμοδυναμικό γινόμενο διαλυτότητας όπου ισχύει Ω = 1 και συνεπώς το διάλυμα είναι κορεσμένο. Για Ω > 1, το διάλυμα είναι υπέρκορο όπου πραγματοποιείται η καταβύθιση στερεού, ενώ για Ω < 1, το διάλυμα είναι ακόρεστο και είναι δυνατή η διάλυση του στερεού. Ο υπερκορεσμός συνδέεται με τον σχετικό υπερκορεσμό, σύμφωνα με τη σχέση: Η κινητήριος δύναμη (driving force) για την κρυστάλλωση της ένωσης ΑmBn εκφράζεται συνήθως σαν μεταβολή της ελεύθερης ενέργειας Gibbs (ΔG) για την μετάβαση από το υπέρκορο διάλυμα στην κατάσταση ισορροπίας ( κορεσμένο διάλυμα) και δίνεται από τη σχέση:
29 2.3Πυρηνογένεση Η επίτευξη του υπερκορεσμού είναι το αρχικό στάδιο στην διεργασία της κρυστάλλωσης. Η δημιουργία ενός υπέρκορου διαλύματος μπορεί να γίνει με πολλούς τρόπους όπως με αλλαγή στην θερμοκρασία, εξάτμιση του διαλύτη, αλλαγή της σύστασης του διαλύτη ή με χημική αντίδραση. Ο σχηματισμός μιας νέας στερεής φάσης στο υπέρκορο διάλυμα εκτός από την επίτευξη του υπερκορεσμού προϋποθέτει την δημιουργία τρισδιάστατων πυρήνων κρυστάλλωσης κατά το στάδιο της πυρηνογένεσης. Ο σχηματισμός αυτός συνοδεύεται από μεταβολή της ελεύθερης ενέργειας του συστήματος. Η πυρηνογένεση μπορεί να λάβει χώρα αυθόρμητα ή να προκληθεί εξωγενώς με εισαγωγή φύτρων νέας φάσης ή ακόμα και με τοπικές μηχανικές αναταράξεις. Ανάλογα με τις συνθήκες που επικρατούν στο υπέρκορο διάλυμα, η πυρηνογένεση διακρίνεται στα ακόλουθα είδη, τα οποία παρουσιάζονται στο σχήμα 2.2. Είναι δυνατόν τα τρία αυτά στάδια να λαμβάνουν χώρα ταυτόχρονα σε διαφορετικές περιοχές του διαλύματος, στο οποίο συμβαίνει η κρυστάλλωση, αλλά πάντα έχουμε αυστηρή διαδοχή αυτών. Σχήμα 2.2: Είδη Πυρηνογένεσης Κατά την πρωτογενή πυρηνογένεση απουσιάζουν οι κρύσταλλοι της σχηματιζόμενης νέας φάσης, ενώ η δευτερογενής προκαλείται από την παρουσία τέτοιων κρυστάλλων. Η πρωτογενής πυρηνογένεση διακρίνεται στην ομογενή και στην ετερογενή. 29
30 Η ομογενής πυρηνογένεση λαμβάνει χώρα σε απολύτως καθαρά διαλύματα απουσία κάθε ξένου σωματιδίου ή επιφάνειας. Θεωρείται ότι είναι το αποτέλεσμα διμοριακών αντιδράσεων ανάμεσα σε μόρια ή ιόντα της διαλυμένης ουσίας που δημιουργούν μοριακές πλειάδες ή έμβρυα. Για να γίνει αυθόρμητος σχηματισμός κρυστάλλων, θα πρέπει το διάλυμα να είναι επαρκώς υψηλού υπερκορεσμού. Αντιθέτως, η ετερογενής πυρηνογένεση που προκαλείται από την παρουσία ξένων σωματιδίων (πχ σκόνη) ή ανωμαλιών στα τοιχώματα του δοχείου που περιέχει το υπέρκορο διάλυμα, και είναι το είδος της πυρηνογένεσης, το οποίο συναντάται κατά κανόνα στη πράξη. Η ενέργεια ενεργοποίησης στην ετερογενή είναι μικρότερη από την αντίστοιχη της ομογενούς και λαμβάνει χώρα σε χαμηλότερες τιμές υπερκορεσμού συγκριτικά με την ομογενή πυρηνογένεση. Κατά τη δευτερογενή πυρηνογένεση προϋπάρχουν στο διάλυμα κρύσταλλοι της ίδιας φάσης με τους σχηματιζόμενους πυρήνες της νέας φάσης. Οι κρύσταλλοι της σχηματιζόμενης νέας φάσης είτε εισάγονται στο υπέρκορο διάλυμα είτε δημιουργούνται πχ από την θραύση των κρυστάλλων λόγω ανάδευσης και δρουν ως νέα πρόσθετα ενεργά κέντρα για την κρυστάλλωση. Αυτό συνεπάγεται τον σχηματισμό των πυρήνων πάνω στην επιφάνεια των εισαγόμενων κρυστάλλων Ομογενής Πυρηνογένεση Ο σχηματισμός του κρίσιμου πυρήνα είναι μια διαδικασία, κατά την οποία οι δομικές μονάδες όχι μόνο πρέπει να συσσωματωθούν υπερνικώντας την τάση τους να επαναδιαλυθούν, αλλά πρέπει και να προσανατολιστούν σε ένα συγκεκριμένο κρυσταλλικό πλέγμα. Οι αλληλεπιδράσεις μεταξύ των ιόντων ή μορίων οδηγούν στο σχηματισμό καταρχήν ενός πυρήνα αρκετά μικρού, ώστε το μέγεθος του να είναι μικρότερο από κάποιο κρίσιμο μέγεθος. Η αύξηση ως προς το μέγεθος των μικρών αυτών πυρήνων, τελικά οδηγεί στην ανάπτυξη του κρυστάλλου. Οι διεργασίες αυτές μπορούν να συγκριθούν με τις χημικές αντιδράσεις, στις οποίες ο σχηματισμός προϊόντων της αντίδρασης προϋποθέτει την υπέρβαση του ενεργειακού φράγματος μεταξύ προϊόντων και αντιδρώντων. Συνεπώς, για να υπάρξει κρυσταλλική ανάπτυξη θα πρέπει να υπερνικηθεί το ενεργειακό φράγμα της πυρηνογένεσης. Ο σχηματισμός ενός σταθερού πυρήνα είναι το αποτέλεσμα μιας σειράς αυτοκαταλυόμενων διμοριακών αντιδράσεων μεταξύ πλειάδων δομικών μονάδων, όπως αποδίδεται σχηματικά στο σχήμα 2.3. Αποτέλεσμα της σειράς 3
31 αυτής των αντιδράσεων είναι ο σχηματισμός διαδοχικά μεγαλύτερου μεγέθους πλειάδων, οι οποίες είτε επαναδιαλύονται είτε αυξάνουν σε μέγεθος μέχρι του σχηματισμού μιας πλειάδας δομικών μονάδων η οποία έχει ένα κρίσιμο μέγεθος (critical nucleus). Η κρίσιμη αυτή πλειάδα αναπτύσσεται περαιτέρω σαν κρύσταλλος με την προσθήκη νέων δομικών μονάδων [Walton 1967]. Η διαδικασία αυτή δημιουργίας του πυρήνα κρίσιμου μεγέθους γίνεται ταχύτατα και συμβαίνει σε περιοχές υψηλού υπερκορεσμού του διαλύματος. (Κρίσιμος Πυρήνας) Σχήμα 2.3: Διμοριακές αντιδράσεις προσθήκης δομικών μονάδων διαλυμένης ουσίας κατά τον σχηματισμό του κρίσιμου πυρήνα Η δομή του κρίσιμου πυρήνα δεν είναι γνωστή καθώς το πολύ μικρό του μέγεθος καθιστά δύσκολη την παρατήρησή τους. Ο κρίσιμος πυρήνας θεωρείται ότι είναι είτε ένας μικροσκοπικός κρύσταλλος με σχεδόν τέλεια μορφή ή ένα μάλλον διάχυτο σωματίδιο με μη σαφώς καθορισμένη επιφάνεια. Οι ιδιότητες των εμβρύων κρίσιμου μεγέθους είναι οι αυτές με τις αντίστοιχες ιδιότητες της συνεχούς φάσεως και η επιφανειακή τους ενέργεια είναι η αυτή με την αντίστοιχη τιμή μιας άπειρης έκτασης επίπεδης στερεάς επιφάνειας. Οι εργασίες των Gibbs, Volmer, Becker και Doring [Nielsen 1964] αποτέλεσαν τη βάση για την κατανόηση της πυρηνογένεσης δημιουργώντας το υπόβαθρο για την κλασσική θεωρία της πυρηνογένεσης. Η δημιουργία των πυρήνων συνοδεύεται από μεταβολή της ελεύθερης ενέργειας του συστήματος. Στη μεταβολή αυτή συνεισφέρουν δύο όροι: ο ένας όρος αντιστοιχεί στην δημιουργία του όγκου της νέας φάση, ΔGv και ο δεύτερος στη μεταβολή της ενέργειας που αντιστοιχεί στο σχηματισμό της νέας επιφάνειας, ΔGs. ΔG = ΔGv + ΔGs 2.18 H μεταβολή της ελεύθερης ενέργειας η οποία αντιστοιχεί στη δημιουργία του όγκου της νέας φάσης, ΔGv, είναι πάντοτε αρνητική, αφού το 31
32 πλήθος των ελεύθερα κινούμενων δομικών μονάδων υποχρεώνονται να βρεθούν σε ολοενά μικρότερο χώρο. Η μεταβολή αυτή οφείλεται σε μετάβαση από μια ασταθή σε μια σταθερή κατάσταση και έχει τη μορφή: 2.19 όπου a ο παράγοντας σχήματος με βάση των όγκο βασισμένο στο χαρακτηριστικό μήκος L, Vm ο γραμμομοριακός όγκος της ουσίας που κρυσταλλώνεται και Δμ η μεταβολή του χημικού δυναμικού κατά το σχηματισμό του πυρήνα η οποία δίνεται από την: 2.2 H μεταβολή της ελεύθερης ενέργειας η οποία αντιστοιχεί στο σχηματισμό της επιφάνειας του πυρήνα, ΔGs, είναι πάντα θετική αφού για την μεταφορά μιας δομικής μονάδας από το κυρίως διάλυμα στην επιφάνεια του πυρήνα απαιτείται ενέργεια. Η μεταβολή αυτή εξαρτάται από την επιφανειακή τάση και δίνεται από την έκφραση: 2.21 όπου b ο παράγοντας σχήματος με βάση την επιφάνεια βασισμένος στο χαρακτηριστικό μήκος L, και γs η διεπιφανειακή τάση. Η μεταβολή της ελεύθερης ενέργειας του συστήματος, από τον συνδιασμό των εξισώσεων 2.18, 2.19 και 2.21 γίνεται: 2.22 Για σφαιρικό του σχήματος πυρήνα με ακτίνα r, η μεταβολή της ελεύθερης ενέργειας του συστήματος γράφεται: 2.23 Η φυσική σημασία της εξισώσεως 2.23 φαίνεται καλύτερα στο σχήμα 2.4 το οποίο δείχνει την εξάρτηση της μεταβολής της ελεύθερης ενέργειας ΔG από την ακτίνα, r. 32
33 Σχήμα 2.4 Μεταβολή της ελεύθερης ενέργειας ΔG του συστήματος συναρτήσει της ακτίνας του σχηματιζόμενου πυρήνα [Mullin, 21] Από τη στιγμή που θα δημιουργηθεί ο κρίσιμος πυρήνας σύμφωνα με το σχήμα 2.4, η ανάπτυξη συνοδεύεται από ελάττωση της ελεύθερης του ενέργειας του συστήματος. Η ελεύθερη ενέργεια η οποία απαιτείται για την δημιουργία και σταθεροποίηση του κρίσιμου πυρήνα, οφείλεται σε στατιστικές διακυμάνσεις της συγκεντρώσεως της διαλελυμένης ουσίας σε ορισμένα σημεία του διαλύματος [Gardner 1975]. O σχηματισμός πυρήνα με μέγεθος μικρότερο από τον κρίσιμο δεν ευνοείται θερμοδυναμικά αφού η μεταβολή της ελεύθερης ενέργειας είναι θετική. Στη περίπτωση αυτή ο σχηματιζόμενος πυρήνας είναι ασταθής και επαναδιαλύεται. Αντίθετα αν ο πυρήνας έχει μέγεθος μεγαλύτερο από τον κρίσιμο, ο πυρήνας μπορεί να αναπτυχθεί περισσότερο καθώς η αύξηση του μεγέθους συνοδεύεται με μείωση της ελεύθερης ενέργειας. Η τιμή του μέγιστου στη μεταβολή της ελεύθερης ενέργειας αντιστοιχεί στον κρίσιμο πυρήνα. Προκύπτει από την παραγώγιση της εξ. (2-22) ως προς το χαρακτηριστικό μέγεθος, L ή για την περίπτωση σφαιρικού σχήματος πυρήνα από την εξ. (2-23) ως προς την ακτίνα, r και θέτοντας την παράγωγο ίση με το μηδέν ( συνθήκη μεγίστου): 33
34 Από την τελευταία σχέση προκύπτει το χαρακτηριστικό μεγέθος ή η ακτίνα του κρίσιμου πυρήνα: 2.24 Αντικατάσταση στις 2.22 και 2.24 δίνει την τιμή της μεταβολής της ελεύθερης ενέργειας, η οποία αντιστοιχεί στο απαιτούμενο ενεργειακό φράγμα για την πυρηνογένεση: 2.25 όπου β ο παράγοντας σχήματος ο οποίος εξαρτάται από την επιφάνεια και τον όγκο του σχηματιζόμενου πυρήνα. Για σφαιρικούς πυρήνες β=16π/3, για πυρήνες κυβικού σχήματος ράβδου β=11 και για πυρήνες σχήματος πλάκας β=25 [N vlt 1985]. Ως ταχύτητα πυρηνογένεσης, J, ορίζεται ο αριθμός των πυρήνων που σχηματίζονται ανά μονάδα όγκου και χρόνου, μπορεί δε να εκφραστεί από μια εξίσωση τύπου Arrhenius: 2.26 όπου Αο ένας προεκθετικός παράγοντας εξαρτώμενος από την θερμοκρασία, k η σταθερά Boltzmann και T η απόλυτη θερμοκρασία. Η εξ. (2-26) με αντικατάσταση της μεταβολής της ελεύθερης ενέργειας, ΔG, από την εξ. (2-25) και αντικαθοστώντας σε αυτή τη μεταβολή του χημικού δυναμικού, Δμ, από την εξ. (2-2) γράφεται: 2.27 Από την εξίσωση 2.27 παρατηρούμε ότι η ταχύτητα πυρηνογένεσης εξαρτάται από τρεις παράγοντες: τη θερμοκρασία Τ, τον υπερκορεσμό S και την διεπιφανειακή ενέργεια γs. H ταχύτητα πυρηνογένεσης αυξάνεται με αύξηση του υπερκορεσμού και της θερμοκρασίας ενώ μειώνεται με αύξηση της διεπιφανειακής ενέργειας. Η εξίσωση 2.27 στη λογαριθμική της μορφή έχει επιβεβαιωθεί και πειραματικά [Turnbull 1956]. Στο σχήμα 2.5 φαίνεται η εξάρτηση του παράγοντα exp(-δg/kt) και της ταχύτητας πυρηνογένεσης, J, από τον λόγο υπερκορεσμού, Ω. 34
35 Σχήμα 2.5: Εξάρτηση της ταχύτητας πυρηνογένεσης, J, από τον λόγο υπερκορεσμού Ω Παράλληλα με την κλασσική θεωρία της πυρηνογένεσης έχουν αναπτυχθεί και μια σειρά από εμπειρικές σχέσεις μεταξύ μετρήσιμων ή παρατηρήσιμων μεγεθών κατά την πυρηνογένεση. Μια σημαντική παράμετρος που χρησιμοποιείται στην πυρηνογένεση είναι ο χρόνος επαγωγής, τ. Ο χρόνος επαγωγής ορίζεται, ως ο χρόνος ο οποίος μεσολαβεί ανάμεσα στην χρονική στιγμή κατά κανόνα επιτυγχάνεται η υπέρκορος κατάσταση και στην χρονική στιγμή κατά την οποία ανιχνεύεται η έναρξη της καταβύθισης από την μεταβολή κάποιας χαρακτηριστικής φυσικοχημικής ιδιότητας του διαλύματος ή της φάσης η οποία αποχωρίζεται από το διάλυμα. Ο χρόνος επαγωγής εξαρτάται από τον υπερκορεσμό, την θερμοκρασία, τον τρόπο ανάδευσης, το ιξώδες του συστήματος, την παρουσία ακαθαρσιών κ.α. Η παράμετρος αυτή, μετρείται είτε με οπτική μέθοδο είτε με παρακολούθηση της συγκέντρωσης στο υπέρκορο διάλυμα ενός από τα χημικά είδη που σχετίζονται άμεσα ή έμμεσα με το καταβυθιζόμενο στερεό. Ο χρόνος επαγωγής εξαρτάται από την μέθοδο με την οποία προσδιορίζεται, διότι οι μέθοδοι έχουν ορισμένη ευαισθησία ως προς την μετρούμενη μεταβολή. Μια γενική έκφραση του χρόνου επαγωγής συναρτήσει της χρονικά εξαρτώμενης ταχύτητας πυρηνογένεσης, J, για καταβύθιση σε διαλύματα [Kaschiev and van Rosmalen, 23] δίνεται από την: Όπου q παράμετρος, Κ κινητικός παράγοντας, Β θερμοδυναμική σταθερά και G χρονικά εξαρτώμενη συνάρτηση του ρυθμού ανάπτυξης των
36 υπερκρίσιμων πυρήνων. Η παράμετρος q και ο κινητικός παράγοντας Κ, λαμβάνουν διαφορετικές τιμές ανάλογα με την τεχνική μέτρησης του χρόνου επαγωγής που χρησιμοποιείται. Για μέτρηση του χρόνου επαγωγής με βάση έναν υπερκρίσιμο πυρήνα q = και Κ=, ενώ με βάση πολλούς υπερκρίσιμους πυρήνες μέσω παρακολούθησης της συγκέντρωσης στο υπέρκορο διάλυμα ενός από τα πλεγματικά ιόντα q = 3 και Κ= όπου αν το ανιχνεύσιμο κλάσμα του όγκου της σχηματιζόμενης νέας φάσης στο υπέρκορο διάλυμα. Ο χρόνος επαγωγής μπορεί να θεωρηθεί ότι αποτελείται από τρείς συνεισφορές: α) τον χρόνο χαλάρωσης, tr, που χρειάζεται για να επιτευχθεί στο σύστημα μια ημισταθερή κατανομή συσσωματωμάτων, β) από τον χρόνο, tn, που χρειάζεται για τον σχηματισμό του σταθερού πυρήνα και γ) από τον χρόνο tg, που χρειάζεται για την ανάπτυξη του πυρήνα σε ανιχνεύσιμο μέγεθος. Έτσι ο χρόνος επαγωγής ισούται με το άθροισμα των χρόνων: Πειραματικά προσδιορίζεται ο συνολικός χρόνος επαγωγής,τ γιατί ο ακριβής προσδιορισμός κάθε επιμέρους χρόνου είναι αδύνατος. Σύμφωνα με την κλασσική θεωρία της πυρηνογέννεσης, ο χρόνος επαγωγής είναι αντιστρόφως ανάλογος της ταχύτητας πυρηνογένεσης, ενώ το μέγεθος των κρίσιμου πυρήνα ανεξάρτητο του υπερκορεσμού. Η εξίσωση 2.27 μπορεί κατ αναλογία να γραφεί: Για δεδομένη θερμοκρασία η γραφική παράσταση του λογαρίθμου του χρόνου επαγωγής συνάρτηση του αντίστροφου τετραγώνου του λογαρίθμου του υπερκορεσμού δίνει ευθεία γραμμή από την κλίση της οποίας υπολογίζεται η διεπιφανειακή ενέργεια, γs με την προυπόθεση ότι τα δεδομένα αναφέρονται σε ομογενή πυρηνογένεση [Μullin 21]. Στη πράξη όμως, σε αρκετές περιπτώσεις τα πειραματικά δεδομένα, μπορεί να προσαρμόζονται σε δύο διαφορετικές ευθείες με διαφορετικές κλίσεις. Ο υπολογισμός της διεπιφανειακής ενέργειας πραγματοποιείται από την κλίση της ευθείας στην περιοχή των υψηλότερων υπερκορεσμών, περιοχή η οποία αντιστοιχεί στην ομογενή πυρηνογένεση. Η αλλαγή της κλίσης των δυο ευθειών σε συγκεκριμένη τιμή υπερκορεσμού αντιστοιχεί στη μετάβαση από την κυρίως ομογενή στην κυρίως ετερογενή πυρηνογένεση [S hnel and 36
37 Mullin 1978; Mullin and Ang. 1976]. Oι τυπικές τιμές της διεπιφανειακής ενέργειας για δυσδιάλυτα άλατα κυμαίνονται μεταξύ 5 1 mj*m 2- ενώ για πιο ευδιάλυτα άλατα οι τιμές της διεπιφανειακής ενέργειας είναι αρκετά μικρότερες. Μια πιο ημί-εμπειρική έκφραση για το χρόνο επαγωγής συναρτήσει της αρχικής συγκέντρωσης της διαλυμένης ουσίας στο υπέρκορο διάλυμα δόθηκε από τους Christiansen [1951] και Nielsen [1964]: 2.31 όπου p είναι ο αριθμός των δομικών μονάδων που απαρτίζουν τον κρίσιμο πυρήνα και kp μια σταθερά. Η εξίσωση 2.31 ισχύει για υδατικά διαλύματα και στη λογαριθμική της μορφή δίνει ευθεία γραμμή με κλίση (1-p) από όπου υπολογίζεται ο αριθμός των δομικών μονάδων που συγκροτούν τον κρίσιμο πυρήνα. Τέλος, ο χρόνος επαγωγής μειώνεται αυξανομένου του υπερκορεσμού, με αύξηση της θερμοκρασίας για δεδομένη τιμή του υπερκορεσμού, με την παρουσία ξένης φάσης που οδηγεί σε ετερογενή πυρηνογένεση και με αύξηση της ταχύτητας ανάδευσης Ετερογενής πυρηνογένεση H ετερογενής πυρηνογένεση είναι αυτή που συνήθως λαμβάνει χώρα στη φύση ενώ η ομογενής πυρηνογένεση είναι πάρα πολύ δύσκολο να συμβεί σε μη απόλυτα ελεγχόμενες συνθήκες. Σε τιμές υπερκορεσμού μικρότερες από τις αντίστοιχες της ομογενούς πυρηνογένεσης, η παρουσία μιας ξένης επιφάνειας μπορεί να προκαλέσει πυρηνογένεση. Οι ξένες αυτές επιφάνειες κατά κανόνα διευκολύνουν την πυρηνογένεση λόγω μείωσης της ενέργειας Gibbs για τον σχηματισμό νέας φάσης σε υπέρκορα διαλύματα. Ένας από του τρόπους και οπωσδήποτε όχι ο μοναδικός, με τον οποίο μπορεί να αρχίσει η κρυστάλλωση σε ένα σύστημα είναι είτε η εισαγωγή κρυσταλλιτών του υλικού που πρόκειται να κρυσταλλωθεί σε υπέρκορα διαλύματα. Ισόμορφα υλικά με αυτό που πρόκειται να κρυσταλλωθεί χρησιμοποιούνται επίσης πολλές φορές για την έναρξη της διεργασίας, ενώ επίσης χρησιμοποιούνται και υλικά τα οποία παρουσιάζουν λιγότερη ή περισσότερη συμβατότητα πλέγματος με τα προς κρυστάλλωση υλικά. Στη περίπτωση αυτή ιδιότητες όπως το επιφανειακό φορτίο, η δομή της επιφάνειας ή η συνάφεια του κρυσταλλικού πλέγματος των αναπτυσσόμενων 37
38 κρυστάλλων με αυτό του υποστρώματος, παίζουν καθοριστικό ρόλο [Μullin 21, Sohnel 1992]. Tέλος, πυρηνογένεση λαμβάνει χώρα σε πολλές περιπτπώσεις τόσο σε εργαστηριακής όσο και σε μεγάλης κλίμακας κρυσταλλωτήρες σε σημεία στα οποία παρατηρείται τοπική αύξηση του βαθμού υπερκορεσμού όπως δίπλα σε μια ψυχόμενη ή θερμαινόμενη επιφάνεια, στην επιφάνεια ενός υγρού. Η πυρηνογένεση σε πολλές περιπτώσεις αρχίζει πάνω στα τοιχώματα του κρυσταλλωτήρα ή επάνω στον αναδευτήρα, λόγω των μικροσκοπικών ατελειών των επιφανειών τους. Ο μηχανισμός με τον οποίο λαμβάνει χώρα η ετερογενής πυρηνογένεση είναι αποτέλεσμα αλληλεπιδράσεων των δομικών μονάδων στο υπέρκορο διάλυμα με το στερεό στην επιφάνεια επαφής υποστρώματος διαλύματος. Ο μηχανισμός της ετερογενούς πυρηνογένεσης είναι ανάλογος με την διαφορά ότι οι διαδοχικές διμοριακές αντιδράσεις λαμβάνουν χώρα στη διεπιφάνεια υποστρώματος/ υπέρκορου διαλύματος. Έτσι, όταν ένας ικανός αριθμός δομικών μονάδων συγκεντρωθεί στην επιφάνεια του υποστρώματος θα δημιουργηθεί ο πυρήνας ο οποίος μόλις ξεπεράσει το κρίσιμο μέγεθος θα αναπτυχθεί περαιτέρω. Η παρουσία ενός ξένου υποστρώματος ή μιας κατάλληλης επιφάνειας, μπορεί να προκαλέσει πυρηνογένεση σε ένα διάλυμα σε υπερκορεσμούς μικρότερους εκείνων που χρειάζονται για την ομογενή πυρηνογένεση, με αποτέλεσμα το εύρος της μετασταθούς περιοχής να είναι μικρότερο από το αντίστοιχο για την ομογενή πυρηνογένεση [Τavare 1995, Kashchiev 2]. To όριο της μετασταθούς περιοχής καθορίζεται από την τιμή του κρίσιμου υπερκορεσμού. Κάτω από το οποίο, το διάλυμα παραμένει υπέρκορο για μεγαλύτερο διάστημα από ένα αυθαίρετο οριζόμενο χρόνο επώασης. Η ελεύθερη ενέργεια η οποία σχετίζεται με το σχηματισμό πυρήνα κρίσιμου μεγέθους κατά την ετερογενή πυρηνογένεση, ΔGET, είναι μικρότερη της αντίστοιχης για ομογενή πυρηνογένεση, ΔGOM, κατά ένα παράγοντα φ ( φ 1): Ένας από τους παράγοντες που επηρεάζουν την πυρηνογένεση, είναι η διαφασική επιφανειακή ενέργεια κατά την δημιουργία ενός πυρήνα σε ένα ξένο υπόστρωμα. Στο σχήμα 2.5 απεικονίζονται σχηματικά τα διανύσματα των διαφασικών επιφανειακών ενεργειών στο σύστημα: στερεό αναπτυσσόμενος κρύσταλλος διάλυμα
39 Σχήμα 2.6: Διανύσματα διαφασικών ενεργειών στις διεπιφάνειες μεταξύ τριών φάσεων : διαλύματος, κρυστάλλου και στερεού υποστρώματος Οι τρεις διαφασικές ενέργειες σημειώνονται στο σχήμα 2.5 είναι: Διφασική επιφανειακή ενέργεια μεταξύ του υγρού και της κρυσταλλικής φάσης που δημιουργείται, Διφασική επιφανειακή ενέργεια μεταξύ της επιφάνειας του στερεού υποστρώματος και του υγρού, Διφασική επιφανειακής ενέργεια μεταξύ της κρυσταλλικής φάσης και της φάσης του υποστρώματος. Διανυσματική ανάλυση των τριών διφασικών επιφανειακών ενεργειών, δίνει: 2.33 Η γωνία θ είναι η γωνία επαφής μεταξύ της κρυσταλλικής φάσης και της στερεής επιφάνειας και η τιμή της καθορίζει τη διαβροχή σε συστήματα υγρού-στερεού. Έτσι ο παράγοντας φ της εξίσωσης 2.32 μπορεί να εκφραστεί ως συνάρτηση της γωνίας επαφής, θ: 2.34 Από την εξίσωση 2.34 προκύπτει ότι: Για θ=18 ο, πλήρη διαβροχή cosθ=-1, φ=1 οπότε ΔGΕΤ=ΔGΟΜ. Υπάρχει δηλαδή πλήρης κρυσταλλική συμβατότητα. Έτσι η ελεύθερη ενέργεια για ετερογενή πυρηνογένεση είναι ίδια με αυτή για ομογενή πυρηνογένεση. 39
40 Για <θ<18 ο, φ<1 οπότε ΔGΕΤ<ΔGΟΜ Η πυρηνογένεση είναι πιθανότερη όσο μικρότερη η τιμή του παράγοντα φ. Η ξένη φάση μειώνει το ενεργειακό φράγμα για τη δημιουργία του κρίσιμου πυρήνα, λειτουργώντας καταλυτικά για την πυρηνογένεση. Για θ= και φ= οπότε ΔGΕΤ= Η περίπτωση αυτή αντιστοιχεί στην εισαγωγή σε υπέρκορο διάλυμα κρυσταλλικών φύτρων της προς κρυστάλλωση νέας φάσης. Με τον τρόπο αυτό, η πυρηνογένεση είναι ταχύτατη, περιορίζεται στα ενεργά κέντρα των εισαγόμενων κρυσταλλικών φυτρών (υπό προυποθέσεις) και λαμβάνει χώρα κατά κύριο λόγο κρυσταλλική ανάπτυξη των φύτρων. Στο σχήμα 2.6 φαίνεται η σχέση μεταξύ του παράγοντα φ και της γωνίας θ: Σχήμα 2.7: Εξάρτηση του λόγου της μεταβολής των ελεύθερων ενεργειών ετερογενούς προς της ομογενούς πυρηνογένεσης από τη γωνία θ Στην έως τώρα ανάλυση θεωρήθηκε η επιφάνεια του υποστρώματος επίπεδη. Η επιφάνεια του κρυσταλλικού υποστρώματος περιλαμβάνει ατέλειες στις οποίες σχηματίζονται οι κρίσιμοι πυρήνες και σταθεροποιούνται ευκολότερα [Turnbull 195]. Η μέγιστη διάμετρος σφαιρικού σχήματος ατέλειας η οποία είναι ικανή να σταθεροποιήσει ένα πυρήνα, δίνεται από την έκφραση της μορφής:
41 όπου η ελεύθερη ενέργεια για το σχηματισμό ενός πυρήνα ορισμένου όγκου. Παρόμοιες εκφράσεις έχουν εξαχθεί και για ατέλειες διαφορετικής γεωμετρίας. Όπως και στην ομογενή πυρηνογένεση, ο χρόνος επαγωγής είναι αντιστρόφως ανάλογος της ταχύτητας πυρηνογένεσης Δευτερογενής Πυρηνογένεση Οι μηχανισμοί πυρηνογένεσης που προκύπτουν από την παρουσία των κρυστάλλων στα υπέρκορα διαλύματα περιγράφονται στην δευτερογενή πυρηνογένεση. Στη περίπτωση αυτή, κρύσταλλοι της ίδιας φάσης με τους σχηματιζόμενους πυρήνες της νέας φάσης προυπάρχουν στο διάλυμα. Οι κρύσταλλοι της σχηματιζόμενης νέας φάσης είτε εισάγονται στο υπέρκορο διάλυμα είτε δημιουργούνται από θραύση των κρυστάλλων λόγω ανάδευσης και δρούν ως πρόσθετα κέντρα κρυστάλλωσης στα υπέρκορα διαλύματα. Οι μηχανισμοί της δευτερογενούς πυρηνογένεσης χωρίζονται σε τρείς κατηγορίες [Botsaris 1976] Ι. Φαινόμενη δευτερογενής πυρηνογένεση, η οποία λαμβάνει χώρα με την εισαγωγή στο σύστημα κρυσταλλικών φύτρων. ΙΙ. Αληθής δευτερογενής πυρηνογένεση, κατά την οποία σχηματίζονται νέοι πυρήνες λόγω των αλληλεπιδράσεων των κρυστάλλων που προυπάρχουν στο σύστημα με το υπέρκορο διάλυμα, ΙΙΙ. Πυρηνογένεση επαφής, κατά την οποία οι νέοι πυρήνες σχηματίζονται μετά από συγκρούσεις των κρυστάλλων μεταξύ τους ή με επιφάνειες του δοχείου κρυστάλλωσης. Η δευτερογενής πυρηνογένεση εξαρτάται, πέραν του υπερκορεσμού και από την θερμοκρασία, την ταχύτητα ανάδευσης, το μέγεθος, το σχήμα, και την ανθεκτικότητα των κρυστάλλων καθώς και από την παρουσία προσμίξεων. Tέλος, είναι σημαντική στην κρυστάλλωση ευδιάλυτων αλάτων, στα οποία οι σχηματιζόμενοι κρυστάλλοι είναι κατά κανόνα μεγάλου μεγέθους (αρκετές δεκάδες ή εκατοντάδες μm). Αντίθετα, κατά την καταβύθιση δυσδιάλυτων αλάτων, δευτερογενής πυρηνογένεση δεν λαμβάνει χώρα γιατί τα σχηματιζόμενα σωματίδια είναι πολύ μικρά για να συμμετέσχουν στους μηχανισμούς της δευτερογενής πυρηνογένεσης. Στις περισσότερες 41
42 περιπτώσεις καταβύθισης η δευτερογενής πυρηνογένεση δεν λαμβάνεται υπόψη, αλλά μπορεί να είναι σημαντική στα τελευταία στάδια της αυθόρμητης καταβύθισης αν ο αρχικός υπερκορεσμός είναι χαμηλός [S hnel and Garside, 1992]. 2.4 Κρυσταλλική Ανάπτυξη Κατά τη κρυσταλλική ανάπτυξη, οι σταθεροί υπερκρίσιμοι πυρήνες αναπτύσσονται και δημιουργούν μακροσκοπικούς κρυστάλλους. Οι συνθήκες και ο ρυθμός της κρυσταλλικής ανάπτυξης επηρεάζουν τα χαρακτηριστικά των κρυστάλλων και του τελικού προιόντος της διεργασίας. Μια βασική δυσκολία, είναι ότι η κρυσταλλική ανάπτυξη μπορεί να γίνεται με περισσότερους του ενός μηχανισμούς με ανάλογες επιπτώσεις στις μετρούμενες ταχύτητες κρυστάλλωσης. Στην προσπάθεια να εξηγηθεί ο μηχανισμός της κρυσταλλικής ανάπτυξης και να βρεθούν μαθηματικές εκφράσεις οι οποίες συσχετίζουν τους ρυθμούς ανάπτυξης των κρυστάλλων, με τον υπερκορεσμό των διαλυμάτων προτάθηκαν πολλές θεωρίες οι οποίες περιγράφουν την κρυσταλλική ανάπτυξη τόσο από τη θερμοδυναμική άποψη όσο και από κινητική. Τρείς είναι οι βασικές κατηγορίες των θεωριών κρυσταλλικής ανάπτυξης: Ι. θεωρίες επιφανειακής ενέργειας ΙΙ. θεωρίες προσρόφησης στρώματος ΙΙΙ. θεωρίες διάχυσης Οι θεωρίες επιφανειακής ενέργειας βασίζονται κυρίως σε κρυσταλλογραφικά και δομικά δεδομένα, και η κρυσταλλική ανάπτυξη θεωρείται κατά κύριο λόγο οδηγείται από την ελαχιστοποίηση της επιφανειακής ενέργειας. Σύμφωνα με τις θεωρίες προσρόφησης στρώματος άτομα ή μόρια από ένα συνεχές μέσον, ενσωματώνονται στον κρύσταλλο συμβάλλοντας έτσι στην ανάπτυξη του. Η διαδικασία είναι ασυνεχής και πραγματοποιείται με προσρόφηση κατά στρώματα πάνω στην κρυσταλλική επιφάνεια. Τέλος, οι θεωρίες διάχυσης στηρίζονται στην υπόθεση ότι η εναπόθεση μάζας στην επιφάνεια ενός κρυστάλλου είναι μια συνεχής διεργασία με ταχύτητα ανάλογη της διαφοράς συγκέντρωσης μεταξύ του σημείου εναπόθεσης και της κύριας μάζας του διαλύματος. 42
43 2.4.1 Θεωρίες επιφανειακής ενέργειας Οι θεωρίες επιφανειακής ενέργειας στηρίζονται στην υπόθεση των Curie [Curie, 1885] και Gibbs [Gibbs, 1928], δηλαδή η μορφοτροπία του αναπτυσσόμενου κρυστάλλου είναι αυτή στην οποία αντιστοιχεί η ελάχιστη επιφανειακή ενέργεια. Η ολική ελεύθερη ενέργεια ενός κρυστάλλου σε ισορροπία με το περιβάλλον του, σε σταθερή θερμοκρασία και πίεση, είναι ελάχιστη για δεδομένο όγκο. Επομένως, το σχήμα ενός κρυστάλλου σε ισορροπία με το περιβάλλον του, σε σταθερή θερμοκρασία και πίεση είναι το μικρότερο δυνατό για ένα δεδομένο όγκο. Αυτό σημαίνει ότι το σχήμα ενός κρυστάλλου λοιπόν ο οποίος αναπτύσσεται σε ένα υπέρκορο ρευστό είναι το σχήμα ισορροπίας και η ανάπτυξη των εδρών του κρυστάλλου γίνεται με τέτοιο τρόπο ώστε η συνολική ενέργεια του να είναι ελάχιστη. Σύμφωνα με τις θεωρίες επιφανειακής ενέργειας οι διάφορες κρυσταλλικές έδρες αναπτύσσονται με ταχύτητες ανάλογες των αντίστοιχων επιφανειακών τους ενεργειών. Όταν κατά την ανάπτυξη του κρυστάλλου το σχήμα του παραμένει σταθερό και ίδιο με το αρχικό, θεωρείται ότι ο κρύσταλλος αυτός αναπτύσσεται ιδανικά (σχήμα 2.7 α ). Στη περίπτωση αυτή οι τρείς ίδιες έδρες Α αναπτύσσονται με τον ίδιο ρυθμό, ενώ οι μικρότερες έδρες Β, αναπτύσσονται γρηγορότερα και η ακόμα μικρότερη έδρα C αναπτύσσεται πιο γρήγορα από όλες. Οι έδρες των κρυστάλλων αναπτύσονται με διαφορετικούς ρυθμούς, λόγω τόσο της διαφορετικής πυκνότητας ύλης όσο και λόγω της διαφορετικής κατανομής ατελειών. Έτσι, οι ταχύτερα αναπτυσσόμενες έδρες εξαφανίζονται. Η ανάπτυξη αυτή όπως απεικονίζεται στο σχήμα 2.7b, δείχνει ότι οι μικρότερες έδρες Β αναπτύσσονται πιο γρήγορα. Οι έδρες αύτες όσο αναπτύσσεται ο κρύσταλλος γίνονται ολοενά και μικρότερες εώς ότου τελικά εξαφανίζονται. Αντίθετα, οι μεγαλύτερες έδρες Α, αναπτύσσονται με μικρότερες ταχύτητες τελικά καθορίζουν και τη μορφοτροπία των αναπτυσσόμενων κρυστάλλων. 43
44 Σχήμα 2.8: Ταχύτητες ανάπτυξης των κρυσταλλικών εδρών (α) για κρύσταλλο σταθερού σχήματος και (b) για κρύσταλλο μεταβλητού σχήματος (περίπτωση επικαλυπτόμενης κρυσταλλικής ανάπτυξης) [Gibbs, 1928] Το σημείο αμφισβήτησης αυτών των θεωριών επιφανειακής διάχυσης είναι ότι δεν μπορούν να εξηγήσουν την επίδραση του υπερκορεσμού στις ταχύτητες ανάπτυξης Θεωρίες προσρόφησης υποστρώματος Οι θεωρίες προσρόφησης υποστρώματος αναπτύχθηκαν από τον Volmer [Volmer, 1939], ο οποίος υποστήριξε την ιδέα ότι η κρυσταλλική ανάπτυξη, είναι μια συνεχής διαδικασία, η οποία λαμβάνει χώρα κατά στρώματα προσροφημένων ατόμων ή μορίων της διαλυμένης ουσίας στην κρυσταλλική επιφάνεια. Για την επιφάνεια του κρυστάλλου, η κρυσταλλική ανάπτυξη επιτυγχάνεται με διαδοχικές ενσωματώσεις δομικών μονάδων σε κόγχες και βαθμίδες [Kossel, 1934]. Καθώς η αναπτυσσόμενη βαθμίδα φτάνει το όριο της επιφάνειας, η ενσωμάτωση νέων δομικών μονάδων σταματά, γιατί δεν υπάρχουν πλέον άλλες ευνοικές θέσεις κρυστάλλωσης. Η κρυσταλλική ανάπτυξη συνεχίζεται με την ανάπτυξη ενός μηχανισμού επιφανειακής δισδιάστατης πυρηνογένεσης όπως φαίνεται στο σχήμα 2.8. Όταν ένα κρυσταλλικό επίπεδο ολοκληρώνεται, δομικές μονάδες μεταφέρονται στην επιφάνεια του κρυστάλλου και καθώς κινούνται τυχαία, συγκρούονται μεταξύ τους. Αν αυτές οι συγκρούσεις είναι μη ελαστικές, τότε δημιουργούνται επιφανειακά δισδιάστατα έμβρυα τα οποία οδηγούν στο σχηματισμό κρίσιμων πυρήνων. 44
45 Σχήμα 2.9: Κρυσταλλική ανάπτυξη. α) Μεταφορά της δομικής μονάδας στο σημείο ενσωμάτωσης της στο κρυσταλλικό πλέγμα b) Ολοκλήρωση του μονομοριακού στρώματος, c) Επιφανειακή πυρηνογέννεση. Για να σταθεροποιηθεί ο πυρήνας αυτός, θα πρέπει ικανός αριθμός δομικών μονάδων που βρίσκονται προσροφημένες στην επιφάνεια, να σχηματίσουν ένα δισδιάστατο πυρήνα, κάτι που προυποθέτει τη δημιουργία δεσμών μεταξύ των δομικών μονάδων αλλά και με την επιφάνεια του κρυστάλλου [Nielsen 1964]. Έτσι με υπολογισμούς παρόμοιους με αυτούς για τον υπολογισμό του κρίσιμου πυρήνα κατά την ομογενή πυρηνογένεση, αποδείχθηκε ότι η κρίσιμη ακτίνα του δισδιάστατου πυρήνα και η αντίστοιχη κρίσιμη ελεύθερη ενέργεια πυρηνογένεσης δίνονται από τις σχέσεις: όπου hn το ύψος του δισδιάστατου πυρήνα. Η ταχύτητα πυρηνογένεσης δίδεται από μια σχέση τύπου Arhenius [Ohara and Reid, 1973]: 2.39 όπου Β 2D προεκθετικός παράγοντας συνάρτηση της τετραγωνικής ρίζας του lns. Η ταχύτητα ανάπτυξης του κρυστάλλου δίδεται από την εξίσωση[freche, 1989]:
46 To πρότυπο αυτό κρυσταλλικής ανάπτυξης, αναφέρεται πολλές φορές και ως πρότυπο μονοπυρηνικής ανάπτυξης, ενώ η σχηματική απεικόνιση της ανάπτυξης ενός κρυστάλλου σύμφωνα με το πρότυπο αυτό δίνεται στο σχήμα 2.9α. Συνήθως, στην επιφάνεια του κρυστάλλου σχηματίζονται περισσότερα του ενός πυρήνες οι οποίοι και αναπτύσσονται. Ο απαιτούμενος χρόνος για να δημιουργηθεί το μονόστρωμα παραμένει μικρότερος από το χρόνο που χρειάζεται για να δημιουργηθούν οι πυρήνες. Η επιφανειακή διάχυση των δομικών μονάδων και η τακτοποίηση τους στα ενεργά κέντρα είναι το καθορίζον την ταχύτητα στάδιο. Ο μηχανισμός ανάπτυξης ονομάζεται πολυπυρηνικός, σχηματικά απεικονίζεται στο σχήμα 2.9b. Η ταχύτητα ανάπτυξης του κρυστάλλου στην περίπτωση αυτή δίνεται από την σχέση [Hilling, 1966]: 2.41 Όπου C2 σταθερά και f(s) είναι μια συνάρτηση που εξαρτάται από τον υπερκορεσμό και δίνεται από την σχέση: 2.42 Εκτός από τις δύο προηγούμενες περιπτώσεις υπάρχει και μια ενδιάμεση: Όταν ο χρόνος σχηματισμού ενός πυρήνα είναι σχετικά μικρότερος από το χρόνο σχηματισμού του μονοστρώματος τότε νέοι πυρήνες, και άρα καινούργια επίπεδα, αρχίζουν να σχηματίζονται πριν ολοκληρωθεί ο σχηματισμός των προηγούμενων. Ο μηχανισμός αυτός ανάπτυξης των κρυστάλλων ονομάζεται μηχανισμός γέννησης- εξάπλωσης ή πρότυπο σχηματισμού επάλληλων πυρήνων [ birth-spread model ή nuclei above nuclei model (ΝΑΝ)]. Σχηματικά, το πρότυπο αυτό παρουσιάζεται στο σχήμα 2.9c. H ταχύτητα κρυσταλλικής ανάπτυξης συναρτήσει του υπερκορεσμού με βάση αυτόν το μηχανισμό δίδεται από τη σχέση: 2.43 όπου us η ταχύτητα εξάπλωσης του πυρήνα και σταθερά. 46
47 Σχήμα 2.1: Πρότυπα κρυσταλλικής ανάπτυξης με δισδιάστατη πυρηνογένεση. (α) Μονοπυρηνικό πρότυπο, (b) Πολυπυρηνικό πρότυπο, (c) πρότυπο Γέννεσης και Εξάπλωσης [Hilling, 1966]. Σύμφωνα με, από το μονοπυρηνικό πρότυπο και την εξίσωση 2.4 ο ρυθμός κρυσταλλικής ανάπτυξης μιας έδρας είναι ευθέως ανάλογος της επιφάνειας της έδρας. Κατά το πρότυπο αυτό οι μεγαλύτερες έδρες αναπτύσσονται πιο γρήγορα σε σχέση με τις μικρότερες, γεγονός που αντιτίθεται στην παρατήρηση ότι οι γρηγορότερα αναπτυσσόμενες έδρες ενός κρυστάλλου έχουν μικρότερες επιφάνειες. Αυτό το γεγονός καθιστά το μονοπυρηνικό πρότυπο μη ρεαλιστικό για τις περισσότερες των περιπτώσεων. Σύμφωνα με την εξίσωση 2.41, το πολυπυρηνικό πρότυπο υποδεικνύει ότι ο ρυθμός κρυσταλλικής ανάπτυξης αυξάνεται αυξανομένου του ρυθμού πυρηνογένεσης ενώ με αύξηση του υπερκορεσμού, πέραν ενός ορίου ελλατώνεται, μετατρέποντας την έκφραση του ρυθμού κρυσταλλικής ανάπτυξης σε πολύπλοκη συνάρτηση του υπερκορεσμού. Από την εξίσωση 2.41, ο ρυθμός κρυσταλλικής ανάπτυξης φαίνεται ότι δεν αυξάνεται συνεχώς συναρτήσει του υπερκορεσμού. Αντίθετα υπάρχει μια τιμή υπερκορεσμού, για την οποία ο ρυθμός γίνεται μέγιστος, ενώ ελαττώνεται με περαιτέρω αύξηση ή μείωση του υπερκορεσμού. Ένα τέτοιο αποτέλεσμα φαίνεται απίθανο και δεν έχει επαληθευτεί πειραματικά τουλάχιστον σε αραία διαλύματα. Πιθανόν να ισχύει σε τήγματα ή σε υψηλές συγκετρώσεις λόγω της μεταβολής του ιξώδους του συνεχούς μέσου στο οποίο λαμβάνει χώρα η κρυσταλλική ανάπτυξη. 47
48 Κατά το πρότυπο γέννησης-εξάπλωσης ο ρυθμός κρυσταλλικής ανάπτυξης αυξάνεται με αύξηση του υπερκορεσμού και της θερμοκρασίας. Η εξάρτηση του ρυθμού από τις μεταβλητές αυτές δεν είναι απλή συνάρτηση του υπερκορεσμού και το πρότυπο αυτό δε φαίνεται να παρουσιάζει τα προβλήματα των δυο απλούστερων μοντέλων. Φαινόμενα όμως κρυστάλλωσης, είναι δυνατό να παρατηρηθούν και σε υπερκορεσμούς κατά πολύ μικρότερους από αυτούς οι οποίοι προβλέπονται για επιφανειακή πυρηνογένεση. Σύμφωνα με την κλασσική θεωρία και μάλιστα οι ταχύτητες ανάπτυξης των κρυστάλλων στις συνθήκες αυτές είναι αρκετά ψηλές. Η εξήγηση στη φαινομενικά απρόβλεπτη αυτή συμπεριφορά κάποιων υπέρκορων διαλυμάτων δόθηκε από τους Burton, Cabrera και Frank [Burton et al., 1951], οι οποίοι ανέπτυξαν και την ομώνυμη θεωρία, BCF. Σύμφωνα με τη θεωρία αυτή, πολύ λίγοι κρύσταλλοι είναι αυτοί οι οποίοι αναπτύσσονται κατά αλληλοδιαδεχόμενα στρώματα. Στην πραγματικότητα, στην επιφάνεια των αναπτυσσόμενων κρυστάλλων δημιουργούνται γραμμοαταξίες έλικας (screw dislocations) οι οποίες παρέχουν μόνιμα κέντρα κρυστάλλωσης χωρίς να είναι απαραίτητη η δισδιάστατη πυρηνογένεση. Δομικές μονάδες προσροφούνται στην επιφάνεια του κρυστάλλου και διαχέονται στη κορυφή του βήματος των γραμμοαταξιών έλικας. Αυτές οι γραμμοαταξίες έλικας έχουν το ένα άκρο τους σε κάποιο σημείο της επιφάνειας του κρυστάλλου και δημιουργούν ένα βήμα, το οποίο στη συνέχεια αυτοπεριστρέφεται και αναπτύσσεται σε σπείρα γύρω από το σταθερό σημείο. Στο σχήμα 2.1 παρουσιάζεται η σπειροειδής ανάπτυξη σύμφωνα με το πρότυπο Burton, Cabrera και Frank (BCF). Η καλύτερη προσέγγιση για την κατεύθυνση της σπείρας είναι αυτή της αρχιμήδειας έλικας, υπό την προυπόθεση ότι τα βήματα ισαπέχουν και δεν είναι πολύ κοντά στο κέντρο της. Συχνό είναι επίσης το φαινόμενο να αναπτύσσονται παράλληλα πολλές έλικες της ίδιας φοράς κυρίως όταν υπάρχουν πολλές γραμμοαταξίες έλικας στην επιφάνεια του κρυστάλλου. 48
49 Σχήμα 2.11: Κρυσταλλική ανάπτυξη σύμφωνα με το πρότυπο Burton, Cabrera και Frank. Η γραμμοαταξία έλικας της επιφάνειας αυτοπεριστρέφεται και δημιουργεί μια έλικα. Σύμφωνα με το πρότυπο BCF η επιφανειακή διάχυση είναι το καθορίζον την ταχύτητα στάδιο. Η σχέση μεταξύ του ρυθμού κρυστάλλωσης, R BCF, και του σχετικού υπερκορεσμού δίνεται από την εξίσωση: 2.44 όπου Αj και Βj σταθερές οι οποίες εξαρτώνται από την θερμοκρασία και το μέγεθος των βημάτων στην επιφανεία των κρυστάλλων. Σε χαμηλές τιμές υπερκορεσμού,σ, σύμφωνα με την εξίσωση (2-43) προκύπτει, οπότε η ταχύτητα κρυστάλλωσης είναι ανάλογη του τετραγώνου του σχετικού υπερκορεσμού: 2.45 Αντίθετα σε υψηλές τιμές υπερκορεσμού,. Στην περίπτωση αυτή η ταχύτητα κρυστάλλωσης είναι ανάλογη της πρώτης δύναμης του υπερκορεσμού: 2.46 Σύμφωνα με την θεωρία ΒCF οι ρυθμοί κρυσταλλικής ανάπτυξης μεταβάλλονται από παραβολική εξάρτηση με τον υπερκορεσμό σε γραμμική εξάρτηση καθώς ο υπερκορεσμός αυξάνεται. Η μεταβολή αυτή παρίσταται γραφικά στο σχήμα Σχήμα 2.12: Εξάρτηση της ταχύτητας κρυσταλλικής ανάπτυξης από τον υπερκορεσμό σύμφώνα με την εξίσωση
50 2.4.3 Θεωρίες Διάχυσης Η αρχική πρόταση των Noyes και Whitney [Noyes and Whitney, 1897] πάνω στην οποία αναπτύχθηκαν οι διάφορες θεωρίες διάχυσης ήταν ότι η εναπόθεση του στερεού ( διαλυμένες δομικές μονάδες) επάνω στην επιφάνεια ενός αναπτυσσόμενου κρυστάλλου είναι ουσιαστικά μια διαδικασία διάχυσης. Σύμφωνα με αυτή την πρόταση η διάλυση είναι αντίστροφη προς την κρυσταλλική διεργασία, ενώ οι ταχύτητες των δύο διεργασιών εξαρτώνται από τη διαφορά συγκέντρωσης μεταξύ της στερεάς επιφάνειας και της κύριας μάζας του διαλύματος. Υποθέτoντας ότι υπάρχει ένα στάσιμο στρώμα υγρού γύρω από τον αναπτυσσόμενο κρύσταλλο, στον οποίο οι προς εναπόθεση στην επιφάνεια δομικές μονάδες (μόρια, ιόντα του διαλυμένου σώματος) θα πρέπει να διαχυθούν, η εξίσωση που περιγράφει τη διεργασία κρυστάλλωσης δίνεται από τη σχέση [Nernst 194]: 2.47 όπου m η μάζα του στερεού που εναποτίθεται σε χρόνο t, D ο συντελεστής διάχυσης του μητρικού υγρού, δ το πάχος του στρώματος διάχυσης, Α το εμβαδόν της επιφάνειας του κρυστάλλου, C η συγκέντρωση της διαλυμένης ουσίας στο διάλυμα και Cs η συγκέντρωση ισορροπίας ( διαλυτότητα). Το πάχος του στρώματος διάχυσης εξαρτάται από την ταχύτητα ανάδευσης του διαλύματος, δηλαδή την σχετική ταχύτητα στερεού-υγρού. Έχει βρεθεί ότι το πάχος του στρώματος αυτού κυμαίνεται από 2μm έως 15μm σε μη αναδευόμενα διαλύματα, ενώ σε ισχυρά αναδευόμενα σχεδόν μηδενίζεται. Η αδυναμία της θεωρίας αυτής να ερμηνεύσει πειραματικά δεδομένα έγκειται στο γεγονός ότι θα έπρεπε σε αναδευόμενα διαλύματα να παρατηρούνται θεωρητικά σχεδόν άπειρες ταχύτητες ανάπτυξης των κρυστάλλων, καθώς και στο γεγονός ότι εν τέλει η διάλυση ενός κρυστάλλου δεν αποτελεί την αντίστροφη διεργασία της κρυστάλλωσης. Έτσι, προτάθηκε ότι η κρυσταλλική ανάπτυξη λαμβάνει χώρα σε δυο στάδια, εκ των οποίων το πρώτο περιλαμβάνει τη μεταφορά μορίων του διαλυμένου σώματος από το διάλυμα στη στερεή επιφάνεια, ενώ το δεύτερο την τακτοποίηση των μοριων του διαλυμένου σώματος στο πλέγμα του κρυστάλλου με μια αντίδραση πρώτης τάξης. Κινητήρια δύναμη και στα δυο αυτά στάδια είναι η διαφορά συγκέντρωσης. Οι μαθηματικές εκφράσεις του ρυθμού μεταφοράς μάζας σε κάθε στάδιο έχουν ως εξής: 5
51 (διάχυση) όπου Κd ο συντελεστής μεταφοράς μάζας λόγω διάχυσης, Κr η σταθερά ταχύτητας για την αντίδραση και Cin η συγκέντρωση της διαλυμένης ουσίας στη διεπιφάνεια στερεού- υγρού. Η εξάρτηση της συγκέντρωσης συναρτήσει της απόστασης από την επιφάνεια του κρυστάλλου παρουσιάζεται στο σχήμα Σχήμα 2.13: Μεταβολή της συγκέντρωσης συναρτήσει της απόστασης από την επιφάνεια ενός αναπτυσσόμενου κρυστάλλου Επειδή όμως πρακτικά είναι δύσκολος ο προσδιορισμός της συγκέντρωσης στη διαφασική επιφάνεια διάλυμα/κρύσταλλος, χρησιμοποιείται αντί των επί μέρους διαφορών συγκέντρωσης (ανάλογες με τις επι μέρους κινητήριες δυνάμεις για κάθε διεργασία) η ολική διαφορά συγκέντρωσης (ολική κινητήρια δύναμη). Έτσι: 2.5 Και η ταχύτητα κρυσταλλικής ανάπτυξης, RG, είναι: 51
52 όπου ΚG ο ολικός συντελεστής κρυσταλλικής ανάπτυξης και n η τάξη της αντίδρασης. Εάν n = 1, δηλαδή η επιφανειακή αντίδραση είναι πρώτης τάξης, τότε η συγκέντρωση στη διαφασική επιφάνεια, Cin απαλείφεται από τις παραπάνω εξισώσεις δίνοντας: όποτε: 2.53 Αν η επιφανειακή αντίδραση είναι ταχύτατη (Κr πολύ μεγάλο) τότε θα ισχύει ΚG Κd οπότε και η ταχύτητα κρυστάλλωσης καθορίζεται από τα φαινόμενα διάχυσης. Ομοίως όταν Κd πολύ μεγάλο,έχουμε Κr ΚG οπότε και η συνολική ταχύτητα καθορίζεται από την επιφανειακή αντίδραση. Πρέπει να σημειωθεί ότι όποια και να είναι τα σχετικά μεγέθη των Κd και Κr, πάντοτε συμβάλλουν μερικώς στην τιμή της σταθεράς ΚG Καθορισμός Μηχανισμού που Ελέγχει τη Κρυσταλλική Ανάπτυξη Πέρα από τις καθαρά θερμοδυναμικές προσεγγίσεις οι οποίες έγιναν κατά καιρούς στη προσπάθεια να εξηγηθούν οι διάφοροι μηχανισμοί της κρυστάλλωσης, αναπτύχθηκαν ημιεμπειρικές σχέσεις για την προσαρμογή των πειραματικών δεδομένων. Μια εκτίμηση για το είδος του μηχανισμού κρυστάλλωσης, προκύπτει από την ημιεμπειρική σχέση η οποία εκφράζει την εξάρτηση του ρυθμού καταβύθισης, Rp, από τον σχετικό υπερκορεσμό, σ [Nancollas and Reddy, 1971]: Όπου n φαινόμενη τάξη της καταβύθισης, Κ η φαινόμενη σταθερά ταχύτητας η οποία εξαρτάται από τη θερμοκρασία και s μια συνάρτηση του αριθμού των ενεργών κέντρων των κρυστάλλων, τα οποία χρησιμοποιούνται ως φύτρα για την εκκίνηση της κρυσταλλικής ανάπτυξης. Η φαινόμενη τάξη της καταβύθισης σχετίζεται άμεσα με το μηχανισμό ανάπτυξης [Freche, 1989 ; Sangwal, 1994]. Έτσι αν: 52
53 Ι. n=1. H ανάπτυξη των κρυστάλλων καθορίζεται από την διάχυση των δομικών μονάδων από το κυρίως διάλυμα ( μεταφορά μάζας). Της ίδιας τάξεως επίσης είναι και η διάχυση των δομικών μονάδων στην αναπτυσσόμενη κρυσταλλική επιφάνεια και η ενσωμάτωση τους στα ενεργά κέντρα αυτής, καθώς και η κρυστάλλωση με ελικοειδή μετατόπιση βήματος- μοντέλο B.C.F., (γραμμική εξάρτηση της ταχύτητας από τον σχετικό υπερκορεσμό). ΙΙ. n=2. Οι κρύσταλλοι αναπτύσσονται σύμφωνα με τον μηχανισμό ελικοειδούς ανάπτυξης-μοντέλο B.C.F. (παραβολική εξάρτηση της ταχύτητας από το σχετικό υπερκορεσμό). ΙΙΙ. n>2. Οι κρύσταλλοι αναπτύσσονται μέσω μηχανισμού επιφανειακής πυρηνογέννεσης ( πολυπυρηνικό πρότυπο). Συνήθως σε μια διαδικασία κρυσταλλικής ανάπτυξης συμμετέχουν περισσότεροι του ενός μηχανισμοί. Αν οι μηχανισμοί αυτοί συμβαίνουν παράλληλα τότε ο ταχύτερος εξ αυτών καθορίζει τον ρυθμό της διεργασίας. Αν οι μηχανισμοί πραγματοποιούνται σε σειρά τότε ο βραδύτερος είναι αυτός ο οποίος καθορίζει τον ρυθμό κρυστάλλωσης Επίδραση παρουσίας ξένων ιόντων ή ενώσεων ( Επιμολύνσεις) Η διεργασία της κρυστάλλωσης επηρεάζεται σημαντικά από την παρουσία ξένων ιόντων ή ενώσεων στα υπέρκορα διαλύματα. Η παρουσία των επιμολύνσεων αυτών ακόμα και σε πολύ μικρές συγκεντρώσεις μεταβάλλει την ταχύτητα πυρηνογένεσης, τον ρυθμό κρυσταλλικής ανάπτυξης αλλά και την μορφολογία, το σχήμα ή το μέγεθος των σχηματιζόμενων κρυστάλλων. Κάθε ουσία διαφορετική από αυτή που κρυσταλλώνεται μπορεί να θεωρηθεί ως επιμόλυνση. Οι επιμολύνσεις επηρεάζουν τους ρυθμούς της κρυστάλλωσης είτε αλλάζοντας τις φυσικοχημικές ιδιότητες του διαλύματος αλλά και του στερεού προιόντος, είτε μεταβάλλοντας τα χαρακτηριστικά της ηλεκτρικής διπλοστιβάδας που περιβάλλει τα σωματίδια κρυστάλλων [Khamskii, 1979]. Oι επιμολύνσεις μπορούν επίσης να προσροφηθούν στα ενεργά κέντρα ή ακόμα να σχηματίσουν ξεχωριστό στρώμα στην επιφάνεια των αναπτυσσόμενων κρυστάλλων το οποίο έχει ορισμένο προσανατολισμό και κρυσταλλογραφική συνάφεια με το υπόστρωμα. Σύμφωνα με το πρότυπο του Kossel υπάρχουν τρείς πιθανές θέσεις όπου οι επιμολύνσεις μπορούν να προσροφηθούν επιφέροντας αποδιοργάνωση 53
54 στην κρυσταλλική ανάπτυξη του κρυστάλλου και μείωση του ρυθμού κρυσταλλικής ανάπτυξης [Davey, 1979]. Μερικές επιμολύνσεις προσροφούνται μη αντιστρεπτά ενώ τα προσροφούμενα μόρια παραμένουν στην επιφάνεια πρακτικώς ακίνητα. Έτσι λοιπόν, τα αποτελέσματα της παρουσίας επιμολύνσεων τις κατηγοριοποιεί σε δύο ακραίες περιπτώσεις αναλόγως των θέσεων προσροφήσεως: ευκίνητες επιμολύνσεις, οι οποίες προσροφούνται στις κόγχες ή στις ακμές και ακίνητες επιμολύνσεις οι οποίες προσροφούνται σε επίπεδες επιφάνειες των βαθμίδων. Σχήμα 2.14: Θέσεις προσρόφησης επιμολύνσεων στην επιφάνεια του κρυστάλλου σύμφωνα με το πρότυπο Κossel: (α) σε κόγχη (b) σε ακμή και (c) σε βαθμίδα Η παρουσία επιμολύνσεων στο σύστημα επηρεάζει και την πυρηνογένεση, είτε επιταχύνοντας την αν δράσουν ως ετερογενή υποστρώματα, είτε ανασταλτικά [Sarig, 1976]. Στη δεύτερη περίπτωση, η μείωση της ταχύτητας πυρηνογένεσης είναι δυνατόν να οφείλεται στον σχηματισμό σύμπλοκων ενώσεων με κάποιο από τα συστατικά του πυρήνα ή στην προσρόφηση των επιμολύνσεων στην επιφάνεια του υποκρίσιμου πυρήνα αλλάζοντας την δομή του ή στην στερεοχημική παρεμπόδιση συστατικών που ενσωματώνονται στον πυρήνα. Οι μεταβολές της ταχύτητας πυρηνογένεσης γίνονται αντιληπτές από ανάλογες μεταβολές του χρόνου επαγωγής [Verdoes, 1992]. Tόσο στην πυρηνογέννεση όσο και στη κρυσταλλική ανάπτυξη η διεπιφανειακή ενέργεια, γs, μεταξύ των σχηματιζόμενων κρυστάλλων και διαλύματος, είναι εκείνη η θερμοδυναμική παράμετρος, η οποία εμφανίζεται σε όλα τα κινητικά πρότυπα και επηρεάζεται από φαινόμενα προσρόφησης. Η προσρόφηση μιας ένωσης στην επιφάνεια του κρυστάλλου μειώνει τη διεπιφανειακή ενέργεια. Η μείωση της διεπιφανειακής ενέργειας έχει ως συνέπεια την μείωση του μεγέθους του κρίσιμου πυρήνα ή του δισδιάστατου 54
55 πυρήνα ή της ακτίνας της σπείρας και τη μείωση της ελεύθερης ενέργειας Gibbs. Αποτέλεσμα της μείωσης της ελεύθερης ενέργειας είναι η αύξηση της ταχύτητας πυρηνογένεσης ή της κρυσταλλικής ανάπτυξης αντίστοιχα. Από τα παραπάνω προκύπτει ότι τα θεωρητικά πρότυπα της κρυσταλλικής ανάπτυξης προβλέπουν αντίθετες τάσεις των επιμολύνσεων στην κινητική της κρυσταλλικής ανάπτυξης. Από θερμοδυναμική άποψη η ταχύτητα κρυσταλλικής ανάπτυξης τείνει να αυξηθεί ενώ από κινητική η προσρόφηση μειώνει την ταχύτητα. Η επιφανεική συγκέντρωση της επιμόλυνσης Γ, μπορεί να προσδιοριστεί από την εξίσωση[lyklema, 1995]: 2.55 Όπου V o όγκος του διαλύματος, Co η συγκέντρωση της επιμόλυνσης πριν την προσρόφηση, Ceq η συγκέντρωση της επιμόλυνσης στην ισορροπία δηλαδή μετά την προσρόφηση, W το βάρος και SSA η ειδική επιφάνεια του υποστρώματος. Η γραφική παράσταση της επιφανειακής συγκέντρωσης Γ, έναντι της συγκέντρωσης ισορροπίας στο διάλυμα, Ceq σε σταθερή θερμοκρασία, δίνει την ισόθερμο προσρόφησης της επιμόλυνσης στο δεδομένο υπόστρωμα. Ανάλογα με τη θέση που καταλαμβάνουν τα προσροφημένα μόρια ή ιόντα στην διφασική επιφάνεια κρυστάλλου-διαλύματος καθώς και την συμπεριφορά τους στην θέση αυτή υπάρχουν αρκετά πρότυπα τα οποία ερμηνεύουν τα φαινόμενα προσρόφησης. Για την ερμηνεία των κινητικών αποτελεσμάτων και δεδομένου του ότι η δράση των επιμολύνσεων εντοπίζεται στην προσρόφηση τους στην επιφάνεια των κρυστάλλων μπορεί να υιοθετηθεί το πρότυπο προσρόφησης Langmuir. Σύμφωνα με το πρότυπο αυτό, τα προσροφημένα μόρια σχηματίζουν επιφανειακό μονόστρωμα, δεν αλληλεπιδρούν μεταξύ τους, τα ενεργά κέντρα του υποστρώματος είναι ενεργειακά ισοδύναμα και η προσρόφηση θεωρείται αντιστρεπτή. Οι ταχύτητες προσρόφησης και εκρόφησης δίνονται αντίστοιχα από τις εξισώσεις 2.56 και 2.57:
56 Όπου kad η σταθερά ταχύτητας προσρόφησης, C η συγκέντρωση της επιμόλυνσης στο διάλυμα, Cm η συγκέντρωση που απαιτείται για να γίνει ένα μονόστρωμα, Ca η εκάστοτε πραγματική συγκέντρωση της επιμόλυνσης και kdes η σταθερά ταχύτητας εκρόφησης. Στην κατάσταση ισορροπίας οι δύο ταχύτητες είναι ίσες οπότε προκύπτει: 2.58 To κλάσμα των ενεργών θέσεων της επιφάνεια του κρυστάλλου που καλύπτεται από τις επιμολύνσεις, θ και η σταθερά συνάφειας kaff ορίζεται από την εξίσωση Η ταχύτητα της κρυσταλλικής ανάπτυξης, Ri παρουσία επιμόλυνσης η οποία προσροφείται στην επιφάνεια του κρυστάλλου είναι μικρότερη από την ταχύτητα κρυσταλλικής ανάπτυξης, Ro, απουσία επιμόλυνσης λόγω δέσμευσης ορισμένων ενεργών κέντρων κρυστάλλωσης και δίνεται από έκφραση της μορφής [Nancollas, 1984]: 2.59 Όπου bro η οριακή ταχύτητα ανάπτυξης παρουσία επιμολύνσεων και b σταθερά (<b<1). Συνδιάζοντας τις 2.59 και 2.58 προκύπτει το κινητικό πρότυπο για την κρυσταλλική ανάπτυξη με προσρόφηση Langmuir: 2.6 H γραφική παράσταση του συναρτήσει του αντιστρόφου της συγκέντρωσης της επιμόλυνσης στο υπέρκορο διάλυμα, δίνει ευθεία γραμμή με κλίση και τεταγμένη επί την αρχή. Από την οποία υπολογίζεται η τιμή της σταθεράς συνάφειας, η οποία αποτελεί μέτρο της συνάφειας της προσροφημένης επιμόλυνσης προς το υπόστρωμα [Koutsoukos, 198]. Αν η τεταγμένη επί την αρχή είναι μεγαλύτερη της μονάδας τότε η επιμόλυνση προκαλεί μερική παρεμπόδιση της κρυσταλλικής ανάπτυξης ακόμα και σε υψηλές συγκεντρώσεις. Στη περίπτωση αυτή είναι δυνατόν να παρατηρηθούν αλλαγές στην μορφολογία του αναπτυσσόμενου κρυστάλλου καθώς αναπτύσσονται οι έδρες εκείνες με τις οποίες οι αλληλεπιδράσεις της επιμόλυνσης είναι μικρότερες. Αν η τεταγμένη επί την αρχή είναι μικρότερη της μονάδας τότε η επιμόλυνση προκαλεί πλήρη παρεμπόδιση της 56
57 κρυσταλλικής ανάπτυξης ακόμα και σε συγκεντρώσεις μικρότερες από την απαιτούμενη για πλήρη μονοστρωματική κάλυψη της κρυσταλλικής επιφάνειας. 2.5 Χρήση αντιδραστήρων στη κρυστάλλωση Η κρυστάλλωση είναι μια πολύπλοκή διαδικασία ο σκοπός της οποίας είναι η παραγωγή του προιόντος από ένα μίγμα αντιδρώντων. Κατά τη διάρκεια της κρυστάλλωσης ιδιαίτερη έμφαση δίνεται στην ποιότητα του παραγόμενου προιόντος (καθαρότητα, σχήμα και μέγεθος κρυστάλλων). Εξετάστηκαν δύο τύποι αντιδραστήρων για την ανάκτηση του φωσφόρου μέσω κρυστάλλωσης του στρουβίτη, οι οποίοι παρουσιάζονται παρακάτω Αντιδραστήρες διαλείποντος έργου (Batch) H απλούστερη μορφή αντιδραστήρα που υπάρχει είναι o αντιδραστήρας διαλείποντος έργου με ανάδευση. Η γεωμετρία του αναδευτήρα και η ταχύτητα, καθώς και η γεωμετρία του δοχείου και τα φυσικά χαρακτηριστκά του συστήμαος είναι οι σημαντικότερες παράμετροι. Είναι δύσκολο να προβλεφθεί με ακρίβεια ο τύπος του κατάλληλου αναδευτήρα και ταχύτητας για την ομογενής ανάμειξη στερεού και ρευστού. Η ανάδευση πραγματοποιείται είτε με μηχανικό αναδευτήρα σε σταθερή ταχύτητα, ανακυκλώνοντας τα αντιδρώντα στον αντιδραστήρα [Ali and Schneider, 26], είτε με αερισμός του διαλύματος εργασίας με αέρα [Jaffer et al., 21]. Αυτές οι διαδικασίες επιτρέπουν την ισοκατανομή των χημικών στο σύστημα δηλαδή σε όλα τα σημεία κρυσταλλικής ανάπτυξης [Αli and Schneider, 26]. H φύση της κρυσταλλικής ανάπτυξης απαιτεί τη σταθερή παροχή αντιδραστηρίων για τη συνεχή ανάπτυξη των κρυστάλλων [Ohlinger et al., 1999] Aντιδραστήρες Ρευστοποιημένης κλίνης (FBR) Με τη διέλευση ενός ρευστού μέσα από μια συμπαγή κλίνη με στερεά σωματίδια, δημιουργείται μια πτώση πίεσης λόγω της έλκουσας του ρευστού. Όταν η δύναμη του ρευστού γίνει ίση με το βάρος της κλίνης, τα σωματίδα αιωρούνται και έτσι δημιουργείται μια κίνηση που θυμίζει την κίνηση ρευστού (ρεύστωση). Στην ορολογία της χημικής μηχανικής μια κλίνη σε αυτή την κατάσταση ονομάζεται ρευστοποιημένη (Fluidized bed). Tα βασικά πλεονεκτήματα των ρευστοποιημένων κλίνων είναι[r. Shankar, 211]: Ι. Oμοιόμορφη ανάμειξη των σωματιδίων και του ρευστού: Με τον τρόπο αυτό επιτυγχάνεται πιο αποτελεσματική μεταφορά θερμότητας και μάζας, άρα 57
58 ταχύτερες χημικές αντιδράσεις και ομοιόμορφη κατανομή θερμοκρασιών και συγκεντρώσεων των συστατικών. ΙΙ. Ισοθερμοκρασιακές συνθήκες λειτουργίας: Σε άλλους τύπου αντιδραστήρα ένα συχνό φαινόμενο που παρατηρείται είναι η ανισοκατανομή της θερμοκρασίας δημιουργώντας τοπικά θερμά ή ψυχρά σημεία. Αυτές οι διαφορές μπορεί να οδηγησούν σε υποβάθμιση της ποιότητας του τελικού προιόντος. Το πληρωτικό υλικό παρουσιάζει υψηλούς συντελεστές μεταφοράς θερμότητας λόγω της ρεύστωσης και της φύσης του, έτσι ο αντιδραστήρας ρευστοποιημένης κλίνης είναι κατάλληλος ΙΙΙ. Ρεύστωση μικρού μεγέθους σωματιδίων: Οι ρευστοποιημένες κλίνες προτιμούνται για διεργασίες με σωματίδια μικρού σχετικά μεγέθους, όπου οι σταθερές κλίνες (steady state) παρουσιάζουν σημαντικές δυσκολίες λόγω αυξημένης πτώσης της πίεσης και χαμηλής θερμικής αγωγιμότητας. ΙV. Δυνατότητα συνεχούς λειτουργίας του αντιδραστήρα: Το σχέδιο κατασκευής ενός τέτοιου τύπου αντιδραστήρα δίνει τη δυνατότητα για συνεχή απομάκρυνση των προιόντων και την εισαγωγή νέων αντιδρώντων Υδροδυναμική του συστήματος Κατά τη ροή των ρευστών όταν οι δυνάμεις τριβής μεταξύ σωματιδίωνρευστού ισούται με τη δύναμη βαρύτητας, τα σωματίδια παραμένουν αιωρούμενα. Η ρευστοποιημένη κλίνη συμπεριφέρεται συνήθως ως ψευδοπλαστικό ρευστό (μη Νευτωνικό). Τα υγρά προκαλούν ρευστοποίηση σχετικά εύκολα και δημιουργούν ομοιογενή συστήματα, στα οποία ο όγκος της κλίνης μεταβάλλεται συνεχώς με την ταχύτητα του υγρού. Η ταχύτητα του ρευστού, υ, πρέπει να είναι μεγαλύτερη από την ταχύτητα έναρξης της ρευστοποίησης, υμ, και μικρότερη από την ταχύτητα παράσυρσης ή οριακή ταχύτητα, υt των σωματιδίων. Συνήθως χρησιμοποιείται η φαινομενική ταχύτητα του ρευστού στη κλίνη που βασίζεται στη διατομή, Α του δοχείου που είναι κάθετη στη ροή. Η ρευστοποίηση ορισμένης μάζας στερεών σωματιδίων που συνήθως βρίσκονται σε κυλινδρικό δοχείο χαρακτηρίζεται από την πτώση πίεσης, ΔP, συναρτήσει της φαινόμενης ταχύτητας του ρευστού, υ, όπως φαίνεται στο σχήμα
59 Σχήμα 2.15: Πτώση πίεσης και ύψος κλίνης συναρτήσει της φαινόμενης ταχύτητας [Ergun, 1952] Αρχικά, για μηδενική παροχή, η πτώση πίεσης είναι μηδέν και η κλίνη έχει ένα συγκεκριμένο ύψος. Για τη διαδρομή ABCD, η πτώση πίεσης σταδιακά αυξάνεται ενώ το ύψος της στήλης παραμένει σταθερό. Μεταξύ των σημείων Α και Β η στήλη διαστέλλεται και στο σημείο Β αρχίζει η ρευστοποίηση, δηλαδή τα σωματίδια αρχίζουν να κινούνται και η κλίνη συμπεριφέρεται σαν ρευστό υψηλού ιξώδους. Η ταχύτητα στο σημείο Β είναι η ταχύτητα έναρξης ρευστοποίησης. Αν η ταχύτητα του ρευστού αυξηθεί περισσότερο, η ΔΡ αυξάνει κατά πολύ λιγότερο και η κλίνη αραιώνει. Στο σημείο C περίπου παρατηρείται παράσυρση των σωματιδίων στο ρευστό. Στο σημείο έναρξης της ρευστοποίησης οι δυνάμεις βαρύτητας και πτώσης πίεσης του ρευστού μέσα στην κλίνη ισορροπούν, δηλαδή: / L (1 )( ) g 2.61 M Όπου LM, το μήκος της κλίνης κατά την έναρξη της ρευστοποίησης, εμ το πορώδες κατά την έναρξη της ρευστοποίησης και, ρ η πυκνότητα των σωματιδίων και του ρευστού αντίστοιχα. Το πορώδες της κλίνης, εμ, κατά την έναρξη της ρευστοποίησης εξαρτάται από το είδος του υλικού και γενικώς αυξάνει όταν το μέγεθος των σωματιδίων ελλατώνεται. M 59
60 Η πτώση πίεσης του ρευστού στη μόνιμη κλίνη μέχρι τη ρευστοποίηση δίνεται από την σχέση του Εrgun [Εrgun, 1952]: 3 [( Po PL ) / L][ Dp / L][ /1 ] 15(1 ) / ( DpGo ) Όπου L το μήκος της σταθερής κλίνης, ψ παράγοντας που εξαρτάται από την σφαιρικότητα των σωματιδίων, DP η διάμετρος των σωματιδίων, μ ιξώδες ρευστού και Go η μαζική παροχή στην κλίνη (Go= ρυο). Στο σημείο ρεύστωσης ισχύει συγχρόνως η εξίσωση Συνδυάζοντας τις δύο αυτές εξισώσεις μπορεί να απαλειφθεί η πτώση πίεσης και να προκύψει μια εξίσωση για τον υπολογισμό της ταχύτητας υm. H εξίσωση αυτή απλοποιείται στις ακόλουθες δύο μορφές για δύο διαφορετικές περιοχές τιμών του αριθμού Reynolds, Re: για Re < { Dp( ) g }/{15 (1 )} {[ D ( ) g]/1.75 } για Re > /2 p H φαινομενική ταχύτητα έναρξης ρευστοποίησης, υ Μ, είναι πολύ μικρότερη από την οριακή ταχύτητα παράσυρσης, υt, η οποία στην περιοχή στρωτής ροής δίνεται από την εξίσωση Stokes : 2 t [ d ( ) g]/ Για μικρές τιμές του αριθμού Re και οι δύο ταχύτητες υ Μ και υt εξαρτώνται από Dp 2, (ρρ-ρ) και 1/μ. Έτσι, ο λόγος τους εξαρτάται μόνο από το πορώδες στην έναρξη ρεύστοποίησης: / [8.33(1 )]/ 2.66 t 2 3 Σε μεγαλύτερα σφαιρικά (ψ=1) σωματίδια, επομένως μεγαλύτερες τιμές του αριθμούς Re, η οριακή ταχύτητα δίνεται από τον Newton: 1/2 t 1.75[ gdp( ) / ] 2.67 Οπότε για Re > 1 / 2.32[ ] 2.68 t 3 1/2 Σε ενδιάμεσες τιμές Re χρησιμοποιούντι ενδιάμεσες τιμές του λόγου υ Μ και υt. Σε κλίνες με ευρεία κατανομή μεγεθών των κόκκων του πληρωτικού υλικού αντιστοιχούν διαφορετικές ταχύτητες έναρξης ρευστοποίησης και παράσυρσης. Στη περίπτωση αυτή η ταχύτητα λειτουργίας επιλέγεται έτσι 6
61 ώστε να επιτυγχάνεται η ρευστοποίηση των μεγαλύτερων σωματιδίων χωρίς να παρασύρονται τα μικρότερα σωματίδια Φάσεις Ρευστοποίησης Το στερεό υπόστρωμα τυπικά υποστηρίζεται από μια πορώδη επιφάνεια γνωστή και ως κατανομέας. Το ρευστό διέρχεται μέσω του κατανομέα προς τα επάνω μέσω του πληρωτικού υλικού. Συγκεκριμένα, στον πίνακα 2.1 παρουσιάζονται τα βασικά οπτικά χαρακτηριστικά για πέντε φάσεις ρευστοποίηση. Οι τελευταίες τέσσερις φάσεις αναφέρονται συχνά ως ρευστοποίηση με συσσωμάτωση (aggregative fluidization). Δεν παρατηρούνται όλες οι φάσεις που αναφέρονται παρακάτω σε κάθε περίπτωση. Αυτό συμβαίνει γιατί τα σημεία μετάβασης ανάμεσα στις φάσεις δεν εξαρτώνται αυστηρά και μόνο από την φύση του συστήματος ρευστόστερεό, αλλά και από εξωγενείς παράγοντες. Τα σύμβολα υmb, υms, υk και υtr αναφέρονται στις φαινομενικές ταχύτητες ροής, στο σημείο εμφάνισης φυσαλίδων, στο σημείο έναρξης ροής τύπου βλήματος (slugging), στο σημείο εμφάνισης τυρβώδους ροής και για κάθετη μεταφορά των σωματιδίων του πληρωτικού υλικού, αντίστοιχα. Πίνακας 2.1: Φάσεις ρευστοποίησης με αυξανόμενη φαινόμενη ταχύτητα αερίου, υ Εύρος Ταχύτητας Φάση Εμφάνιση και βασικά χαρακτηριστικά υ υμ Σταθερή κλίνη Τα σωματίδια είναι ήρεμα: το ρευστό ρέει στα κενά διαστήματα ανάμεσα στα σωματίδια. υμ υ υmb Μερική Ρευστοποίηση Η κλίνη διαστέλλεται ομαλά με έναν ομογενή τρόπο, μερική κίνηση σωματιδίων, μικρή τάση για τα σωματίδια να ενοποιηθούν. υmb υ υms Ρευστοποίηση με σχηματισμός φυσαλίδας Σχηματίζονται τμήματα κενού κοντά στην είσοδο, αναπτύσσονται κυρίως από συνένωση, και ανυψώνονται προς την επιφάνεια, η κορυφή της κλίνης είναι καλά καθορισμένη με 61
62 υms υ υκ Ροή τύπου βλήματος (Slugging) φυσαλίδες που τη σπάζουν περιοδικά, ανώμαλη διακύμανση πίεσης. Kενά γεμίζουν περισσότερο τη στήλη, η κορυφή της κλίνης ανυψώνεται και καταρρέει με λογικά κανονική συχνότητα, μεγάλες και ομαλές διακυμάνσεις πίεσης. υκ υ υtr Τυρβώδης φάση Μικρά κενά και ομάδες σωματιδίων εξακοντίζονται, η κορυφή της κλίνης δύσκολα διακρίνεται, μικρή έκταση σε διακυμάνσεις πίεσης. υtr υ Γρήγορη Ρευστοποίηση Απουσία σαφούς άνω επιφάνειας στην κλίνη, σωματίδια μεταφέρονται έξω από την κορυφή και πρέπει να αναπληρωθούν με προσθήκη στερεών στη βάση. Ομάδες σωματιδίων κινούνται προς τα κάτω, κυρίως προς τον τοίχο, ενώ το ρευστό που περιέχει ευρέως διασπαρμέν σωματίδια, κινείται προς τα πάνω, τα σταθερά σωματίδια διαρκώς αραιώνονται καθώς η υ αυξάνει. Ενώ η υmb και η υκ ορίζονται ακριβώς, οι άλλες μεταβάσεις είναι συνήθως βαθμιαίες. Στις στήλες που εξοπλίζονται με εσωτερικά διαφράγματα ή σωλήνες, δύο φάσεις μπορούν να συνυπάρχουν σε διαφορετικά μέρη της ίδιας στήλης. Ωστόσο, είναι χρήσιμο να καθοριστούν τα διαφορετικά είδη σωματιδίων που τείνουν να δώσουν διαφορετική συμπεριφορά ρευστοποίησης. 62
63 Ιδιότητες του Πληρωτικού υλικού Τα πληρωτικά υλικά που χρησιμοποιούνται στις FBR έχουν σχήμα σφαιρικό, κυλινδρικό ή διάφορα άλλα σχήματα που έχει βρεθεί οτι συντελουν στην καλύτερη επαφή στερεού και ρευστού, με διάμετρο σημαντικά μικρότερη από αυτή της στήλης. Κυρίως τα πληρωτικά υλικά πρέπει να είναι ομοιόμορφα κατανεμημένα έτσι ώστε να μην δημιουργούνται δίαυλοι μέσα από τους οποίους δίνεται η δυνατότητα στο ρευστό να περάσει πιο εύκολα [Τσέβης, 21]. Το 1973, ο D. Geldart πρότεινε την ομαδοποίηση των σωματιδίων σε τέσσερις ομάδες ανάλογα με τις ιδιότητες τους. Στο σχήμα 2.14 φαίνεται το διάγραμμα που πρότεινε ο Geldart για τις τέσσερις ομάδες σωματιδίων. Σχήμα 2.16: Ομάδες σωματιδίων κατά Geldart (για ατμοσφαιρικές συνθήκες πίεσης και θερμοκρασίας του ρευστού ρευστοποίησης) [Geldart, 1973] Συγκεκριμένα οι ομάδες κατα Geldart και τα χαρακτηριστικά τους είναι τα εξής: Ομάδα Α: Τα σωματίδια αυτά έχουν διάμετρο μεταξύ 2 και 1μm και τυπικά πυκνότητα 14 Kg/m 3. Ρευστοποιούνται πολύ εύκολα σε χαμηλές ταχύτητες ρευστού, ενώ σε υψηλότερες ταχύτητες εμφανίζουν φυσαλίδες μικρού μεγέθους. Τυπική εφαρμογή τέτοιων σωματιδίων πραγματοποιείται στην καταλυτική διάσπαση Fcc ( Fluidized Catalyst Cracking). Ομάδα B: Είναι τα σωματίδια με διάμετρο από 4 έως 5 μm (πχ άμμος) και πυκνότητα από 14 έως 45 Kg/m 3. Τα σωματίδια αυτά ρευστοποιούνται έντονα σχηματίζοντας μεγάλες φυσαλίδες. 63
64 Ομάδα C: Αυτή η ομάδα περιλαμβάνει τα πιο λεπτόκοκκα και συνπώς τα πιο συνεκτικά σωματίδια. Με μέγεθος από 2 έως 3 μm, η ρεύστωση των σωματιδίων αυτών γίνεται κάτω από συνθήκες που είναι πολύ δύσκολο να επιτευχθούν και μπορεί να χρειαστεί η εφαρμογή εξωτερικής δύναμης όπως είναι η μηχανική ταλάντωση. Ομάδα D: Τα σωματίδια σε αυτή την ομάδα έχουν μέγεθος μεγαλύτερο από 6 μm και κατά κανόνα έχουν υψηλές πυκνότητες. Η ρεύστωση για να επιτευχθεί απαιτεί πολύ υψηλές ενέργειες ρευστού και είναι συνδεδεμένη με υψηλά επίπεδα τριβών. Συχνά οι ιδιότητες των στερεών είναι καθορισμένες για μια συγκεκριμένη εφαρμογή. Όπου πρέπει να γίνει κάποια επιλογή υλικών, οι ιδιότητες που είναι γενικά επιθυμητές είναι οι παρακάτω: Ι. Το υλικό θα πρέπει να ρέει εύκολα. Αυτό υποδηλώνει ότι τα σωματίδια θα πρέπει να είναι στρογγυλά ή χωρίς πολλές ακμές, αρκετά ξηρά και μεγάλα για να μη συσσωματώνονται ή να δημιουργούν φορτία λόγω των διασωματιδιακών ελκτικών δυνάμεων. ΙΙ. Θα πρέπει να υπάρχει ένα λογικά ευρύ φάσμα των μεγεθών των σωματιδίων. Κατά κανόνα, ο λόγος των ισοδύναμων διαμέτρων ανάμεσα στα μεγαλύτερα και στα μικρότερα κλάσματα θα πρέπει να κυμαίνεται μεταξύ ΙΙΙ. Τα σωματίδια δεν θα πρέπει να είναι εύθραυστα. 64
65 Κεφάλαιο 3 Πειραματική Διαδικασία 3.1 Αντιδραστήρια και σύσταση συνθετικού αποβλήτου Τα διαλύματα παρασκευάσθηκαν με τριπλά απεσταγμένο νερό. Προτυποποιήθηκαν, όπου ήταν απαραίτητο με αναλυτικές τεχνικές, οι οποίες παρουσιάζονται στη συνέχεια. Τα πειράματα έγιναν σε υπέρκορα προς το στρουβίτη διαλύματα με υπόβαθρο συνθετικό απόβλητο το οποίο προσομοίαζε στη χημική σύσταση ένος τυπικού αστικού αποβλήτου. Η χημική σύσταση συνοψίζεται στον πίνακα 3.1: Πίνακας 3.1: Σύσταση συνθετικού αποβλήτου Συστατικό MgCl2. 6H2O NH4H2PO4 Glucose NaCl NaNO3 Συγκέντρωση 2.1 * 1-2 M 1.7 * 1-2 M 2.1 * 1-2 M 1.7 * 1-2 M * 1-4 M 5 * 1-2 M * 1-4 M Όπως φαίνεται από τον πίνακα 3.1, οι συγκεντρώσεις Mg, NH4 και PO4 3- χρησιμοποιήθηκαν σαν μεταβλητές. Χρησιμοποιήθηκαν stock διαλύματα MgCl2. 6H2O συγκέντρωσης 1M και NH4H2PO4 συγκέντρωσης 1Μ, τα οποία προτυποποιήθηκαν με τουλάχιστον δυο αναλυτικές μεθόδους το καθένα. Το διάλυμα του μαγνησίου βαθμονομήθηκε με συμπλοκομετρική τιτλοδότηση με πρότυπο διάλυμα EDTA και με τη μέθοδο της ατομικής απορρόφησης με φλόγα. Το διάλυμα των φωσφορικών βαθμονομήθηκε με ποτενσιομετρική τιτλοδότηση με πρότυπο διάλυμα ΝαOH.1 M και φασματοφωτομετρικά. Στo διάλυμα καυστικού νατρίου η προτυποποίηση έγινε με όξινο φθαλικό κάλιο C8H5KO4, του οποίου το κρυσταλλικό στερεό προηγουμένως είχε ξηραθεί, για μια νύχτα,στους 15 C, με τιτλοδότηση με πρότυπο διάλυμα HCl.1 M. Παρασκευάστηκαν διαλύματα NaCl 1 Μ και ΝαΝΟ3.59 Μ. Η συγκέντρωση της γλυκόζης αντιστοιxούσε σε τιμή χημικά απαιτούμενου οξυγόνου (COD) 1ppm. Τέλος, χρησιμοποιήθηκαν πρότυπα ρυθμιστικά 65
66 διαλύματα, με τιμές ph 4.8 και στους 25 C, τα οποία απαιτούντο για τη βαθμονόμηση του ηλεκτροδίου μέτρησης ph. Για την παρασκευή τους χρησιμοποιήθηκαν τα κρυσταλλικά στερεά C8H5KO4, ΚΗ2PO4 και Νa2HPO4, τα οποία πριν τη ζύγιση τους είχαν ξηρανθεί για 24 h στους 15 C [Bates 1973]. Όλα τα παραπάνω διαλύματα μετά την παρασκευή τους διηθούνταν υπό κενό από φίλτρο μεμβράνης διαμέτρου πόρων.2μm. To πρότυπο διάλυμα φωσφορικών καθώς και τα ρυθμιστικά διαλύματα φυλάσσονταν στο ψυγείο στους 4 C, για να αποφευχθεί η ανάπτυξη μικροβιακής δράσης, η οποία είναι πολύ πιθανή σε θερμοκρασία περιβάλλοντος. 3.2 Πειραματικές Διατάξεις Αντιδραστήρας Διαλείποντος Έργου Για τα πειράματα καταβύθισης στρουβίτη από υπέρκορα διαλύματα σε συνθήκες σταθερού ph στους 25 ο C χρησιμοποιήθηκε η παρακάτω πειραματική διάταξη η οποία παρουσιάζεται στο σχήμα 3.1: Σχήμα 3.1: Πειραματική διάταξη για τα πειράματα κρυστάλλωσης στρουβίτη σε αντιδραστήρα διαλείποντος έργου 66
67 Τα πειράματα πραγματοποιήθηκαν σε διπλότοιχο δοχείο κατασκευασμένο από γυαλί (pyrex), όγκου 1L. O αντιδραστήρας σφραγιζόταν με ειδικά σχεδιασμένο και κατασκευασμένο καπάκι από πολυαμίδιο το οποίο διέθετε τέσσερις οπές. Η πρώτη χρησιμοποιούταν για την είσοδο του ηλεκτροδίου στο διάλυμα εργασίας και η δεύτερη για τους σωλήνες οι οποίοι είναι απαραίτητοι για την μεταφορά του διαλύματος τιτλοδότησης από τις μηχανικά συνδεδεμένες προχοϊδες στο διάλυμα εργασίας. Η τρίτη οπή χρησιμοποιήθηκε ως θύρα δειγματοληψίας. Η ανάδευση του διαλύματος γινόταν με μηχανικό αναδευτήρα με σταθερή ταχύτητα στα 22 rpm, έτσι ώστε το διάλυμα εργασίας να αναμειγνύεται ομογενώς. Ο αναδευτήρας είχε σχήμα προπέλας. Το συνδυασμένο ηλεκτρόδιο υάλου/αg/agcl χρησιμοποιήθηκε για τις μετρήσεις του ph σε συνδυασμό με το κατάλληλο όργανο (ph-meter, Metrohm 627). Το πεχάμετρο ήταν συνδεδεμένο με τον αυτόματο τιτλοδότη του οποίου το σημείο ρύθμισης ήταν το ph 6.5. Όταν μειωνόταν το ph, ενεργοποιείτο ο κινητήρας με τις δυο μηχανικά συνδεδεμένες σύριγγες για την προσθήκη βάσης πρότυπου διαλύματος NaOH έτσι ώστε να διατηρηθεί σταθερό το ph στο 6.5. Σε όλη τη διάρκεια της καταβύθισης καταγραφόταν το δυναμικό του ηλεκτροδίου συναρτήσει του χρόνου, προκειμένου να διαπιστωθεί η διατήρηση σταθερής τιμής, η οποία είχε επιλεγεί Αντιδραστήρας Ρευστοποιημένης Κλίνης Για τα πειράματα καταβύθισης στρουβίτη σε υπέρκορα διαλύματα, τα οποία ρευστοποιούσαν τη κλίνη από το πληρωτικό υλικό το οποίο επιλέγετε σε συνθήκες σταθερού ph και 25 ο C χρησιμοποιήθηκε η πειραματική διάταξη του σχήματος 3.2. Η πειραματική διάταξη αποτελείται από μια γυάλινη δεξαμενή (pyrex), στην οποία παρασκευαζόταν το υπέρκορο διάλυμα, το οποίο αναδευόταν με μαγνητική ράβδο από teflon. Στην κλίνη εισερχόταν και ανακυκλωνόταν το διάλυμα μέσω μιας φυγοκεντρικής αντλίας. Η ροή μετρείτο ογκομετρικά καθ όλη τη διάρκεια του πειράματος στην έξοδο του αντιδραστήρα. Το διάλυμα κατέληγε στη δεξαμενή και με τον τρόπο αυτό ανακυκλωνόνταν. 67
68 Σχήμα 3.2: Πειραματική διάταξη ρευστοποιημένης κλίνης Ο αντιδραστήρας ρευστοποιημένης κλίνης αποτελείτο από ένα γυάλινο κυλινδρικό σωλήνα το πάνω μέρος του οποίου κατέληγε σε χοάνη. Η είσοδος της κλίνης περιλάμβανε στρόφιγγα ενώ η έξοδος του ρευστού γίνεται από ένα πλαστικό βιδωτό καπάκι, τα οποία έφεραν ακροφύσια και προσαρμόζονταν σε αυτά οι σωλήνες σιλικόνης, οι οποίοι χρησιμοποιήθηκαν για την κυκλοφορία του υπέρκορου διαλύματος. Το ύψος της στήλης με το πληρωτικό υλικό μεταβαλλόταν ανάλογα με το πείραμα. Αυτό συνεπάγεται μεταβολή στον ωφέλιμο όγκο της κλίνης άρα και στον χρόνο παραμονής των αντιδρώντων στην κλίνη. Τα χαρακτηριστικά της στήλης είναι τα εξής: Πίνακας 3.2: Διαστάσεις ρευστοποιημένης κλίνης Μήκος σωλήνα (κάτω μέρος) Διάμετρος σωλήνα (κάτω μέρος) Μήκος κώνου (πάνω μέρος) Διάμετρος κώνου (πάνω μέρος) 43.5 cm 1.8 cm 21.2 cm 3.7 cm Όγκος 55 cm 3 68
69 Στο σχήμα 3.3 παρατίθεται και η φωτογραφική απεικόνιση της πειραματικής διάταξης. Σχήμα 3.3: Φωτογραφία της πειραματικής διάταξης για την ρευστοποιημένη κλίνη στους 25 ο C. Διακρίνονται: (1) Δεξαμενή υπό ανάδευση (2) Ηλεκτρόδιο, (3) Φυγοκεντρική Αντλία, (4) ph-στάτης, (5) ph-μετρο, (6) Αντιδραστήρας. Πείραμα καθορισμού ροής Για τον κατάλληλο σχεδιασμό των διαστάσεων της κλίνης σημαντικό ρόλο έχει η γνώση της κλίμακας της παροχής που διαθέτει η αντλία με σκοπό την επίτευξη ρευστοποίησης της κλίνης. Επομένως, πραγματοποιήθηκαν μια σειρά από πειραματικές μετρήσεις. Η διαδικασία ήταν η εξής: Η στήλη πληρώνονταν αρχικά με σωματίδια quartz γνωστού βάρους. Καταγραφόταν το αρχικό ύψος της κλίνης και στη συνέχεια διοχετεύονταν νερό στην κλίνη με συγκεκριμένη αρχική παροχή. Η παροχή αυξανόταν 69
70 σταδιακά μέχρι την παρατήρηση ρευστοποίησης του πληρωτικού υλικού στην κλίνη. Στο σημείο αυτό καταγραφόταν η παροχή και το ύψος της στήλης αφού σταθεροποιούνταν η επιφάνεια στη κορυφή της κλίνης. Στη συνέχεια αυξανόταν η παροχή περαιτέρω μέχρι να παρατηρηθεί παράσυρση των σωματιδίων. Τα πειράματα επαναλήφθηκαν με διαφορετική ποσότητα πληρωτικού υλικού. Τα αποτελέσματα συνοψίζονται στον πίνακα 3.3: Πίνακας 3.3: Πειραματικές μετρήσεις ρευστοποιημένης κλίνης με πληρωτικό υλικό quartz και νερό Βάρος πληρωτικού υλικού (gr) 1 2 Αρχικό ύψος στήλης (cm) 4 8 Aρχική παροχή (ml/min) 1 1 Παροχή ρευστοποίησης (ml/min) Ύψος στήλης ρευστοποίησης (cm) Παροχή Παράσυρσης (ml/min) Κάποιες χαρακτηριστικές παράμετροι για την λειτουργία της ρευστοποιημένης κλίνης είναι: A s Q f 3.1 u f Όπου Qf η συνολική παροχή και υf η ταχύτητα ρευστού. Το ύψος της ρευστοποιημένης κλίνης: V Le 3.2 A Όπου V ο όγκος της ρευστοποιημένης κλίνης. Ο χρόνος επαφής των αντιδρώντων στον κρυσταλλωτήρα: f s V 3.3 Q Με τη βοήθεια των παραπάνω αυτών μετρήσεων του πίνακα 3.3 προσδιορίσθηκε το εύρος των τιμών της παροχής ρευστού για την διεξαγωγή των πειραμάτων. Οι τιμές αυτές κυμάνθηκαν μεταξύ 1-3 ml/min. To χαμηλότερο όριο επιλέχθηκε για την περίπτωση που η κλίνη λειτουργούσε για 7
71 μακρές χρονικές περιόδους, ενώ το υψηλότερο όριο ήταν πάνω από τα όρια ρεύστωσης της κλίνης. Κύριος στόχος ήταν η επίτευξη ικανοποιητικών χρόνων επαφής (εξίσωση 3.3). Οι χρόνοι επαφής κυμάνθηκαν μεταξύ min. Κύριος στόχος στην παρούσα εργασία των ρυθμίσεων λειτουργίας της κλίνης,, προτιμήθηκαν συνθήκες λειτουργίας της κλίνης οι οποίες εξασφάλιζαν μέση τιμή χρόνου επαφής στα 2.5 min. Η ροή του ρευστού ρυθμίστηκε στα 22 ml/min και διατηρήθηκε σταθερή σε όλα τα πειράματα. 3.3 Πειραματική διαδικασία και επεξεργασία Αποτελεσμάτων Τα πειράματα πραγματοποιήθηκαν στις παραπάνω πειραματικές διατάξεις σε σταθερή θερμοκρασία 25 C και σταθερό ph 6.5. H στοιχειομετρική αναλογία των πλεγματικών ιόντων Mg 2+, PO4 3- και NH4 +. Τα υπέρκορα διαλύματα παρασκευάσθηκαν με αναλογία 1:1:1. Η καταβύθιση στρουβίτη περιγράφεται από την ακόλουθη αντίδραση: Mg 2+ (aq) + NH4 + (aq) + H2PO4 - (aq) MgNH4PO4.6H2O(s) + 2H + (aq) Η κινητήρια δύναμη για τον σχηματισμό του στερεού είναι η διαφορά μεταξύ του χημικού δυναμικού του στερεού στο υπέρκορο διάλυμα, από το αντίστοιχο στην ισορροπία. Θεωρώντας ότι τα πρότυπα χημικά δυναμικά στο υπέρκορο διάλυμα και στην ισορροπία είναι ίσα, η διαφορά στα χημικά δυναμικά είναι: ο 1/3 ο 1/3 Δμ= μ +ktln(a Mg 2+ *a + *a 3- ) s Mg NH s 4 PO - μ +ktln(a *a *a ) 4 NH4 PO4 3.4 Όπου Ω ο βαθμός υπερκορεσμός ως προς στρουβίτη που ορίζεται από την σχέση: 3.5 Όπου το θερμοδυναμικό γινόμενο διαλυτότητας του στρουβίτη. Ο υπερκορεσμός είναι ένα μέτρο της απόκλισης του συστήματος από την ισορροπία και ένα μέτρο της κινητήριας δύναμης για την καταβύθιση. Ο σχετικός υπερκορεσμός ως προς στρουβίτη ορίζεται ως: 71
72 Οι συγκεντρώσεις των χημικών ειδών του διαλύματος και ο υπερκορεσμός των διαλυμάτων ως προς στρουβίτη υπολογίστηκαν με την βοήθεια του λογισμικού PHREEQC λαμβάνοντας υπόψη όλες τις δυνατές χημικές ισορροπίες στο διάλυμα σε συνδυασμό με τα ισοζύγια μάζας και φορτίου. Οι χημικές ισορροπίες και οι τιμές των σταθερών οι οποίες χρησιμοποιήθηκαν στους υπολογισμούς για κάθε επιμέρους σειρά πειραμάτων, παρουσιάζονται στο παράρτημα I. To διάλυμα εργασίας για τη μελέτη καταβύθισης κρυστάλλων στρουβίτη σε αντιδραστήρα τύπου batch είχε συνολικό όγκο.5l, ενώ για τον αντιδραστήρα ρευστοποιημένης κλίνης είχε 2L και παρασκευαζόταν από την ανάμειξη κατάλληλων όγκων από τα stock διαλύματα των αντιδραστηρίων σύστασης του συνθετικού αποβλήτου. Τα υπέρκορα διαλύματα πριν τη μεταφορά τους στον αντιδραστήρα διηθούντο από ηθμούς μεμβράνης.2μm για να αφαιρεθούν τυχόν ακαθαρσίες (πχ σκόνη). Το ηλεκτρόδιο βαθμονομείτο, πριν από κάθε πείραμα, με πρότυπα ρυθμιστικά διαλύματα ph 4.8 και ph To διάλυμα εργασίας εισαγόταν στον αντιδραστήρα, ο οποίος στη συνέχεια ασφαλιζόταν με καπάκι πάνω στο οποίο ήταν προσαρμοσμένο το ηλεκτρόδιο. Η αρχική τιμή ph ήταν περίπου 4.3, ενώ στη συνέχεια ρυθμιζόταν στο 6.5 με προσθήκη κατάλληλης ποσότητας προτύπου διαλύματος ΝαΟΗ 1Μ. Η στιγμή επίτευξης του υπερκορεσμού ήταν εκείνη στην οποία το ph του διαλύματος ρυθμιζόταν στην επιθυμητή τιμή. Από εκείνη ακριβώς τη χρονική στιγμή ξεκινούσε η καταγραφή της τιμής του δυναμικού του ηλεκτροδίου συναρτήσει του χρόνου. Στα πειράματα η μόνη παράμετρος που διατηρούταν σταθερή ήταν το ph στην τιμή 6.5. Κατά την αντίδραση καταβύθισης του στρουβίτη, τα πρωτόνια που απελευθερώνονταν, τα οποία γίνονταν αντιληπτά με μείωση στην τιμή του ph του διαλύματος, εξουδετερώνονταν με την προσθήκη πρότυπου διαλύματος βάσης. Το χρονικό διάστημα που μεσολαβούσε από την επίτευξη του υπερκορεσμού μέχρι την πρώτη πτώση της τιμής του ph σε σύγκριση με την προκαθορισμένη τιμή ph 6.5 οριzόταν ως χρόνος επαγωγής, τ. Μετά την πάροδο του χρόνου αυτού ξεκινούσε η καταβύθιση του στρουβίτη, η οποία και συνοδευόταν με προσθήκες πρότυπου διαλύματος καυστικού νατρίου με ρυθμό ο οποίος υπαγορευόταν με τον ρυθμό καταβύθισης. Τη στιγμή επίτευξης του υπερκορεσμού λαμβανόταν το πρώτο δείγμα. Στη συνέχεια, ένα δεύτερο εντός της χρονικής περιόδου η οποία οριζόταν ως
73 χρόνος επαγωγής. Κατά τη καταβύθιση, συλλέγονταν περίπου εφτά δείγματα, έτσι ώστε ο όγκος του διαλύματος εργασίας να μη μεταβάλλεται σημαντικά. Τα δείγματα διηθούνταν από ηθμούς μεμβράνης.22 μm (Whatman). Tα διηθήματα αναλύονταν για μαγνήσιο με φασματοσκοπία ατομικής απορρόφησης και για φωσφορικά φασματοφωτομετρικά με την μέθοδο του βαναδομολυβδαινικού συμπλόκου. Η στερεά κρυσταλλική φάση, μετά τη ξήρανση σε θερμοκρασία δωματίου, χαρακτηριζόταν με περίθλαση ακτίνων- Χ και με ηλεκτρονική μικροσκοπία σάρωσης. Από τις αναλύσεις των διηθημάτων των δειγμάτων προέκυπταν οι συγκεντρώσεις των πλεγματικών ιόντων στα διαλύματα. Στα πειράματα της παρούσας εργασίας ο αρχικός ρυθμός της καταβύθισης υπολογίσθηκε από την μεταβολή της συγκέντρωσης του μαγνησίου και του φωσφόρου συναρτήσει του χρόνου. Συγκεκριμένα, ο ρυθμός σχηματισμού στρουβίτη, Rst, στη μονάδα του χρόνου ήταν: Όπου V ο όγκος του διαλύματος εργασίας και Ci η συγκέντρωση των ιόντων μαγνησίου ή φωσφορικών κατά τη χρονική στιγμή t. Ο υπολογισμός της κλίσης dci/dt γινόταν με πολυωνυμική προσαρμογή της καμπύλης του διαγράμματος και υπολογισμό της πρώτης παραγώγου αυτού για χρόνο t= (αρχική ταχύτητα) Αναλυτικές Τεχνικές Φασματομετρία Μοριακής Απορρόφησης Υπεριώδους/Ορατού (UV/VIS) για τη μέτρηση της συγκέντρωσης των φωσφορικών στα διαλύματα Η φασματοφωτομετρία αναφέρεται στη χρησιμοποίηση του φωτός για μέτρηση των συγκεντρώσεων χημικών ενώσεων ή στοιχείων που βρίσκονται υπό μορφή διαλυμάτων. Η απορρόφηση της ηλεκτρομαγνητικής ακτινοβολίας από ιόντα και μόρια αποτελεί τη βάση για ποιοτική ανίχνευση και για ποσοτικό προσδιορισμό των ενώσεων αυτών. Επιπλέον, μελέτες των φασμάτων απορρόφησης δίνουν τη δυνατότητα εξαγωγής συμπερασμάτων για τη δομή και τη σταθερότητα πολλών χημικών ενώσεων, έτσι ώστε να επιλεγούν οι πλέον κατάλληλες συνθήκες και το βέλτιστο μήκος κύματος για την ανάλυση. 73
74 Τα διαλύματα τοποθετούνταν σε γυάλινες κυψελίδες οπτικής διαδρομής 1 cm. Όταν μονοχρωματική ακτινοβολία διέρχεται από το διάλυμα,το οποίο περιέχει την ουσία που απορροφά σε μήκος κύματος που έχει επιλεγεί, η ισχύς της ακτινοβολίας ελαττώνεται προοδευτικά κατά μήκος της διαδρομής ως αποτέλεσμα της απορροφήσεως της από αυτήν. Η συγκέντρωση της ουσίας που απορροφά ακτινοβολία στο διάλυμα εξαρτάται από την ελάττωση της ισχύος της προσπίπτουσας ακτινοβολίας και συνήθως συνδέεται γραμμικά με την διαπερατότητα Τ, ή την απορρόφηση Α και ακολουθεί τον νόμο των Beer-Lambert: 3.8 Όπου Α η απορρόφηση, Po η ισχύς της προσπίπτουσας ακτινοβολίας, P η ισχύς της εξερχόμενης ακτινοβολίας από το διάλυμα, Τ η διαπερατότητα, b το μήκος της οπτικής διαδρομής της ακτινοβολίας μέσα στο διάλυμα, α η απορροφητικότητα, ε η μοριακή απορροφητικότητα και c η συγκέντρωση της ουσίας που απορροφά την ακτινοβολία του μήκους κύματος το οποίο έχει επιλεγεί. Σύμφωνα με το νόμο του Beer η απορρόφηση είναι ευθέως ανάλογη με τη συγκέντρωση των μορίων που απορροφούν. Η σχέση 3.8 είναι ικανοποιητική για αραιά διαλύματα σε περιοχές συγκεντρώσεων.1 Μ για τις περισσότερες ενώσεις. Αποκλίσεις από την γραμμική συμπεριφορά σε υψηλότερες συγκεντρώσεις μπορούν να οδηγήσουν σε σημαντικές αλλαγές στην απορρόφηση της ακτινοβολίας και σε μικρότερη αναλυτική ευαισθησία. Οργανολογία Τα όργανα για τη μέτρηση της απορρόφησης διαλυμάτων στην υπεριώδη και ορατή ακτινοβολία αποτελούνται από: (i) μια πηγή ακτινοβολίας σταθερή ισχύος, (ii) ένα σύστημα φακών, κατόπτρων και σχισμών που ορίζουν, ευθυγραμμίζουν και εστιάζουν τη δέσμη, (iii) έναν μονοχρωμάτορα για την ανάλυση της ακτινοβολίας σε επί μέρους μήκη κύματος, (iv) μια διαφανή κυψελίδα για τη τοποθέτηση δείγματος, (v) έναν ανιχνευτή ακτινοβολίας που μετατρέπει το οπτικό σήμα σε ηλεκτρικό (vi) ένα σύστημα μέτρησης το οποίο διαθέτει ενισχυτή σήματος και όργανο ανάγνωσης. 74
75 Χαρακτηριστικό παράδειγμα είναι ένας γενικός τύπος φασματοφωτομέτρου απλής δέσμης, όπως φαίνεται στο σχήμα 4.4: Σχήμα 3.4: Φασματοφωτόμετρο απλής δέσμης [Skoog, 22]. Για μετρήσεις μοριακής απορρόφησης απαιτείται μια πηγή συνεχούς φάσματος εκπομπής, της οποίας η ισχύς δεν μεταβάλλεται απότομα για μια μεγάλη περιοχή τιμών μήκους κύματος. Με ηλεκτρική διέγερση δευτερίου ή υδρογόνου υπό χαμηλή πίεση παράγεται ένα συνεχές φάσμα εκπομπής στην υπεριώδη περιοχή (16-34nm). Η συνηθέστερη πηγή ορατής (34-78nm) ακτινοβολίας είναι η λυχνία νήματος βολφραμίου. Το νήμα βολφραμίου, ευρισκόμενο σε γυάλινο περίβλημα, παρουσία ευγενούς αερίου σε χαμηλή πίεση, πυρακτώνεται με ηλεκτρικό ρεύμα και φωτοβολεί. Η ακτινοβολία που εκπέμπεται από την πηγή κατευθύνεται μέσω κατόπτρων στον μονοχρωμάτορα. Ο μονοχρωμάτορας διαχωρίζει την πολυχρωματική ακτινοβολία σε επί μέρους μήκη κύματος και απομονώνει αυτά σε στενές ζώνες ή καλύτερα σε μονοχρωματική ακτινοβολία. Σχήμα 3.5: (α) Μονοχρωμάτορας φράγματος, (β)μονοχρωμάτορας Πρίσματος [Skoog, 22] 75
76 Ένας μονοχρωμάτορας αποτελείται από μια σχισμή εισόδου, μια διάταξη ευθυγράμμισης (φακός ή καθρέφτης), μια διάταξη διασποράς (πρίσμα ή φράγμα), έναν φακό ή καθρέφτη εστίασης και μια σχισμή εξόδου. Ολόκληρο το σύστημα είναι τοποθετημένο σε φωτοστεγανό θάλαμο. Η ανάλυση της πολυχρωματικής ακτινοβολίας βασίζεται στα φαινόμενα περίθλασης και συμβολής των ακτίνων της, δηλαδή όταν οι ακτινοβολίες με διαφορετικά μήκη κύματος ανακλώνται σε διαφορετικές γωνίες. Οι διαχωρισμένες πλέον ακτινοβολίες κατευθύνονται προς την έξοδο όπου μόνο αυτή με το επιθυμητό μήκος κύματος εξέρχεται. Το φασματοφωτόμετρο με το οποίο έγιναν οι μετρήσεις στην εργασία αυτή, ήταν διπλής δέσμης της εταιρίας HITAHI (Model U-21 UV/VIS Spectrophotometer). Το σχηματικό διάγραμμα της οργανολογίας, η οποία χρησιμοποιήθηκε, φαίνεται στο σχήμα 4.6: Σχήμα 3.6: Όργανο διπλής δέσμης με δέσμες διαχωρισμένες στον χώρο [Skoog, 22] Στο φασματοφωτόμετρο της διπλής δέσμης, το φώς περνά διαδοχικά μέσα από το δείγμα και την κυψελίδα αναφοράς. Αυτό επιτυγχάνεται με έναν κινητήρα ο οποίος περιστρέφει ένα κάτοπτρο μέσα στην οπτική δέσμη, έτσι υπάρχει η δυνατότητα σύγκρισης των εντάσεων Po και P τν δύο οπτικών δεσμών. Η οπτική δέσμη εναλλάσσεται ανάμεσα στις δυο κυψελίδες αρκετές φορές ανά sec και το ηλεκτρονικό κύκλωμα αυτόματα συγκρίνει τις εντάσεις αυτές και από τη γνωστή σχέση του Beer υπολογίζεται η συγκέντρωση του άγνωστου διαλύματος. Ως ανιχνευτές στο φασματοφωτόμετρο U-21 UV/VIS χρησιμοποιούνται φωτοδίοδοι πυριτίου. Το ηλεκτρικό σήμα του ανιχνευτή ενισχύεται, μετράται από όργανο μέτρησης και καταγράφεται ως ένδειξη σε ανάλογο σύστημα ανάγνωσης. 76
77 Μέτρηση συγκέντρωσης φωσφορικών ιόντων Η μέτρηση της συγκέντρωσης των φωσφορικών στα διαλύματα πραγματοποιήθηκε σε μήκος κύματος 42 nm όπου απορροφά το σύμπλοκο των φωσφορικών με τα βαναδικά και μολυβδαινικά ιόντα σε ph= 1. Σε ένα αραιό διάλυμα φωσφορικών, το μολυβδαινικό αμμώνιο αντιδρά υπό όξινες συνθήκες για να σχηματίσει ένα ετεροπολικό οξύ, το μολυβδαινοφωσφορικό οξύ. Παρουσία βαναδίου, ένα κιτρινόχρωμο βαναδομολυβδαινοφωσφορικό οξύ σχηματίζεται. Η ένταση του κίτρινου χρώματος είναι ανάλογη της συγκέντρωσης των φωσφορικών. Το ελάχιστο όριο ανίχνευσης της μεθόδου είναι 2 μg P/L. Παρασκευάστηκαν πρότυπα διαλύματα με γραμμική περιοχή μέτρησης έως 1*1-4 Μ, με αραίωση κατάλληλων όγκων πρότυπου διαλύματος ΝΗ4Η2PO4.1 M και διαλύματος HCl 2.5 Μ σε τελικό όγκο 1 ml, όπως φαίνεται στον πίνακα 4.3. Το διάλυμα των βαναδομολυβδαινικών ιόντων (Εμφανιστικό Διάλυμα) παρασκευαζόταν με ανάμειξη διαλυμάτων ΗCl 2.5 M, μολυβδαινικού αμμωνίου (NH4)6Mo7.O % και ΝΗ4VO3.234% σε αναλογία 2:2:1. Πίνακας 3.4: Πρότυπα διαλύματα για τη μέτρηση της συγκέντρωσης των φωσφορικών Πρότυπα (M) ΝΗ4Η2PO4 (ml) HCl (ml) Blank - 4 2* * * * * Αναμίχθηκαν ίσοι όγκοι σε αναλογία 1:1 τυφλού, προτύπων και δειγμάτων με το εμφανιστικό διάλυμα. Η μέτρηση πραγματοποιούταν τουλάχιστον 12 ώρες μετά την παρασκευή τους και παρέμεναν σταθερά για ώρες. Μετά τη μέτρηση της απορρόφησης του τυφλού και των προτύπων, κατασκευάζεται το διάγραμμα της συγκέντρωσης των φωσφορικών συναρτήσει της απορρόφησης. Η άγνωστη συγκέντρωση των φωσφορικών στα δείγματα προσδιοριζόταν από την μετρούμενη απορρόφηση και από την αντίστοιχη καμπύλη βαθμονόμησης (σχήμα 3.7). 77
78 Σχήμα 3.7: Καμπύλη βαθμονόμησης Φασματοσκοπία Ατομικής Απορρόφησης (ΑΑS) για τη μέτρηση της συγκέντρωσης του μαγνησίου Οι ατομικές φασματοσκοπικές τεχνικές ανάλυσης στηρίζονται στο γεγονός ότι τα φάσματα των ατόμων, σε αντίθεση με αυτά των μορίων, έχουν μορφή οξείας γραμμής εύρους μικρότερου από.1 nm, σε συνδυασμό με το γεγονός ότι κάθε στοιχείο έχει το δικό του χαρακτηριστικό φάσμα με αποτέλεσμα τη μικρή πιθανότητα αλληλοεπικάλυψης των φασματικών γραμμών διαφόρων στοιχείων του ίδιου δείγματος. Αρχικά το δείγμα εκτίθεται σε ηλεκτρική ή θερμική ενέργεια με σκοπό την διάσπαση των μορίων του σε άτομα. Η ατομοποίηση του δείγματος γίνεται είτε σε φλόγα είτε σε φούρνο ηλεκτροθερμικά. Όπως παρουσιάζεται στο σχήμα 4.8, ένα κλάσμα των μορίων, ατόμων και ιόντων διεγείρονται από τη θερμότητα της φλόγας και παρέχουν ατομικά, ιοντικά και μοριακά φάσματα εκπομπής. Είναι από το κρισιμότερο στάδιο στη φασματοσκοπία φλόγας λόγω των πολύπλοκων φαινομένων που πραγματοποιούνται στη φλόγα και είναι εκείνο που καθορίζει την επαναληψιμότητα της μεθόδου. 78
79 Σχήμα 3.8: Μεταβολές καταστάσεων κατά την ατομοποίηση ενός δείγματος [Skoog, 22] Όταν η ακτινοβολία διέρχεται από τα άτομα της θεμελιώδους καταστάσεως,η ένταση της μειώνεται καθώς μέρος της ακτινοβολίας απορροφείται από τα άτομα, τα οποία με τη διαδικασία αυτή διεγείρονται. Η ένταση της απορροφούμενης ακτινοβολίας εξαρτάται από τον αριθμό των ατόμων που συμμετέχουν στο φαινόμενο. Υπολογίζοντας την απορρόφηση της ακτινοβολίας, η οποία ακολουθεί το νόμο του Beer,γίνεται ποσοτικός προσδιορισμός των ατόμων του στοιχείου του δείγματος: Όπου Α η απορρόφηση, Ιο η ισχύς της προσπίπτουσας ακτινοβολίας, Ι η ισχύς της εξερχόμενης ακτινοβολίας, Τ η διαπερατότητα, b το μήκος της οπτικής διαδρομής της ακτινοβολίας, α η απορροφητικότητα, και c η συγκέντρωση των ατόμων που απορροφούν. Στις μεθόδους ατομικής απορρόφησης απαντώνται δύο τύποι παρεμποδίσεων: Φασματικές παρεμποδίσεις, οι οποίες προκύπτουν, όταν η απορρόφηση ή η εκπομπή ενός παρεμποδίζοντος συστατικού του δείγματος επικαλύπτει ή βρίσκεται τόσο κοντά στις γραμμές απορρόφησης ή εκπομπής
80 του αναλυτή, ώστε να καθίσταται αδύνατη η διάκριση τους από τον μονοχρωμάτορα. Χημικές παρεμποδίσεις, οι οποίες οφείλονται στις διάφορες διαδικασίες, που συμβαίνουν κατά τη διάρκεια της ατομοποίησης οι οποίες αλλάζουν τα χαρακτηριστικά της απορρόφησης του αναλυτή. Για παράδειγμα, προσθήκη περίσσειας ιόντων λανθανίου ελαχιστοποιεί τη παρεμπόδιση των φωσφορικών κατά τον προσδιορισμό του μαγνησίου. Οργανολογία Το φασματόμετρο ατομικής απορρόφησης με φλόγα, που πραγματοποιηθήκαν, οι μετρήσεις ήταν το ΑΑnalyst- 3 της Perkin- Elmer. Ένα φασματοφωτόμετρο ατομικής απορρόφησης, όπως φαίνεται στο σχηματικό περίγραμμα του σχήματος 3.9 αποτελείται από μία πηγή ακτινοβολίας, μια συσκευή ατομοποίησης, έναν μονοχρωμάτορα, ο οποίος απομονώνει το κατάλληλο για το στοιχείο που αναλύεται, έναν ανιχνευτή στον οποίο φτάνει η ακτινοβολία από τον μονοχρωμάτορα και την μετατρέπει σε ηλεκτρικό σήμα και ένα σύστημα μέτρησης το οποίο διαθέτει ενισχυτή του σήματος και όργανο ανάγνωσης. Ο συχνότερα χρησιμοποιούμενος ανιχνευτής στα φασματόμετρα ατομικής απορρόφησης είναι ένας φωτοπολλαπλασιαστής (PMT). Σχήμα 3.9: Φασματοφωτόμετρο ατομικής απορρόφησης [Skoog, 22] Για να υπάρξει γραμμική σχέση μεταξύ του σήματος απορρόφησης και της συγκέντρωσης, δηλαδή για να ισχύει ο νόμος του Beer, είναι αναγκαίο οι γραμμές της ακτινοβολίας της πηγής να είναι στενές σε σχέση με το εύρος μιας κορυφής απορρόφησης. Η συνηθέστερη πηγή ακτινοβολίας για μετρήσεις ατομικής απορρόφησης είναι η λυχνία κοίλης καθόδου (hollow cathode lamp, HCL). Η συσκευή ατομοποίησης δημιουργεί ένα νέφος από τα άτομα του στοιχείου που αναλύεται με χρήση φλόγας ή ηλεκτροθερμαινόμενου 8
81 φούρνου. Σε κάθε περίπτωση η συσκευή ατομοποίησης είναι ευθυγραμμισμένη με την οπτική διαδρομή της ακτινοβολίας. Το σήμα που φτάνει στον μονοχρωμάτορα πρέπει να προέρχεται αποκλειστικά από την πηγή και όχι από εκπομπή ακτινοβολίας από το σύστημα ατομοποίησης. Αυτό επιτυγχάνεται με την παρεμβολή ενός περιστρεφόμενου τεμαχιστή στην πορεία της δέσμης μεταξύ πηγής και φλόγας. Μέτρηση της συγκέντρωσης μαγνησίου στα διαλύματα Η συγκέντρωση του μαγνησίου μετρήθηκε με φασματομετρία ατομικής απορρόφησης με χρήση ατομοποιητή σε φλόγα αέρα/ασετυλίνης. Η μέτρηση γίνεται με κατάλληλη λυχνία Mg στα nm. Ο προσδιορισμός της συγκέντρωσης έγινε με τη βοήθεια σειράς προτύπων διαλυμάτων. Η γραμμική περιοχή του νόμου Βeer-Lambert περιελάμβανε διαλύματα έως συγκέντρωση ως 2 ppm. Τα πρότυπα διαλύματα παρασκευάσθηκαν έτσι ώστε να έχουν όσο το δυνατό παρόμοια φυσική και χημική σύσταση με τα αντίστοιχα διαλύματα των δειγμάτων. Τα πρότυπα διαλύματα παρασκευάσθηκαν σε τελικό όγκο 1 ml, όπως φαίνεται στον πίνακα 4.4. Τόσο στα πρότυπα όσο και στα δείγματα απαιτείται η προσθήκη διαλύματος οξειδίου του λανθανίου, La2O3, 2.5 M. Πίνακας 3.5: Πρότυπα διαλύματα για τον προσδιορισμό της συγκέντρωσης μαγνησίου Πρότυπα (ppm) Μg(1ppm) (ml) ΝΗ4Η2PO4 (ml) NaCl (ml) La2O3 (ml) Blank Περίθλαση Ακτίνων Χ (XRD) Η περίθλαση των ακτίνων Χ παρέχει μια απλή και πρακτική μέθοδο για την ταυτοποίηση κρυσταλλικών ενώσεων. Η τεχνική της περίθλασης των ακτίνων Χ από κονιοποιημένα δείγματα είναι μοναδική και αποτελεί τη μόνη αναλυτική τεχνική, η οποία μπορεί να δώσει ποιοτικές και ποσοτικές πληροφορίες ως προς το είδος των κρυσταλλικών ενώσεων που υπάρχουν σε ένα στερεό δείγμα. Οι τεχνικές περίθλασης ακτίνων Χ από κονιοποιημένα δείγματα βασίζονται στο ότι το περιθλασιόγραμμα (diffraction pattern) των ακτίνων Χ είναι μοναδικό για κάθε κρυσταλλική ουσία. Επομένως, εάν υπάρχει πλήρης 81
82 ταύτιση μεταξύ των περιθλασιογραμμάτων του με πρότυπη ουσία είναι δυνατή η ταυτοποίηση του. Το κρυσταλλικό δείγμα λειοτριβείται μέχρις ότου μετατραπεί σε λεπτή ομοιογενή σκόνη. Στην κατάσταση αυτή οι απειράριθμοι μικροκρυσταλλίτες προσανατολίζονται προς κάθε δυνατή κατεύθυνση. Έτσι, όταν μια δέσμη ακτίνων Χ προσπέσει στο υλικό, αναμένεται ότι ένας σημαντικός αριθμός σωματιδίων θα είναι προσανατολισμένα έτσι ώστε να ικανοποιούν τη συνθήκη Bragg για ανάκλαση από κάθε δυνατό κρυσταλλικό επίπεδο. Η ταυτοποίηση από τα περιθλασιογράμματα βασίζεται στον προσδιορισμό της γωνίας (σε μονάδες θ ή 2θ) και της έντασης της αντίστοιχης ανάκλασης. Η απόσταση d μεταξύ των πλεγματικών επιπέδων τα οποία αντιστοιχούν σε μια ανάκλαση υπολογίζεται από την εξίσωση του Bragg, από το γνωστό μήκος κύματος της πηγής και από τη μετρούμενη γωνία. Οι εντάσεις των γραμμών εξαρτώνται από τον αριθμό και το είδος των ατομικών ανακλαστικών κέντρων σε κάθε σειρά επιπέδων του κρυσταλλικού πλέγματος. Σε ένα κρυσταλλικό πλέγμα η διάταξη των ατόμων είναι περιοδική. Όταν οι ακτίνες Χ πέσουν πάνω σε παράλληλα πλεγματικά επίπεδα ενός κρυστάλλου, κάποιες από αυτές περιθλώνται από το πρώτο επίπεδο, κάποιες από το δεύτερο και κάποιες από τα χαμηλότερα επίπεδα. Από τις ακτίνες που εξέρχονται από το δείγμα ανιχνεύονται μόνο αυτές που βρίσκονται σε φάση, δηλαδή αυτές που συμβάλλουν ενισχυτικά, παράγοντας έτσι δέσμη περίθλασης ισχυρότερη από την αρχική. Η συνθήκη για την ενισχυτική συμβολή των περιθλώμενων ακτίνων είναι, η διαφορά δεσμού τους στο εσωτερικό του κρυστάλλου να είναι ακέραιο πολλαπλάσιο, του μήκους κύματος των ακτίνων. Σε κάθε άλλη περίπτωση συμβάλλουν αποσβεστικά και η έντασή τους μηδενίζεται. Όπως φαίνεται από το διάγραμμα του σχήματος 3.1 κοντά στην πρόσπτωση δέσμη ακτίνων-χ σε παράλληλα πλεγματικά επίπεδα ενός κρυστάλλου, τουλάχιστον εν μέρει ανακλώντα και εν μέρει διεισδύοντα στο υλικό. 82
83 Σχήμα 3.1: Περίθλαση των ακτίνων Χ από ένα κρυσταλλικό πλέγμα [Skoog, 22]. Οι ακτίνες Χ1 και Χ2 μήκους κύματος λ προσπίπτουν στο δείγμα υπό γωνία θ. Η Χ1 ανακλάται στο σημείο Β1 και η Χ2 στο Β2 υπό γωνία θ και οι δύο. Οι δύο ακτίνες, που εξέρχονται από το πλέγμα βρίσκονται στην ίδια διεύθυνση Χ1,2 και δίνουν φαινόμενα περίθλασης με αύξηση της εντάσεως τους καθώς βρίσκονται σε φάση. Η ακτίνα Χ1,2 έχει μήκος κύματος ακέραια πολλαπλάσια λ. Συμβολή υπάρχει όταν: 3.1 Όπου λ είναι το μήκος κύματος της ακτινοβολίας, d η απόσταση των επίπεδων στην εξεταζόμενη κρυσταλλογραφική διεύθυνση, θ η γωνία περίθλασης και m ένας ακέραιος που δείχνει την τάξη της περιθλώμενης ακτινοβολίας. Η εξίσωση 3.1 είναι γνωστή ως εξίσωση του Bragg και δηλώνει ότι η γωνία περίθλασης εξαρτάται από την απόσταση των επιπέδων ενός κρυσταλλικού πλέγματος για την αντίστοιχη κρυσταλλογραφική διεύθυνση. Απαιτούνται εκφράσεις που να συνδέουν την γωνία θ με τα κρυσταλλογραφικά χαρακτηριστικά του στερεού. Διαφορετικές ομάδες επιπέδων σε ένα πλέγμα έχουν διαφορετικές τιμές της μεταξύ τους απόστασης. Η απόσταση d μεταξύ δύο επιπέδων, μετρημένη από την κατακόρυφο στα επίπεδα, εξαρτάται από τους δείκτες Miller (hkl) του επιπέδου από παραμέτρους της μοναδιαίας κυψελίδας του αντίστοιχου πλέγματος (α,b,c,α,β,γ). Η ακριβής σχέση εξαρτάται από το κρυσταλλογραφικό σύστημα. Για το απλό κυβικό σύστημα η σχέση μεταξύ d και των διαστάσεων της μοναδιαίας κυψελίδας είναι: 83
84 3.11 Ανάλογες αλλά πιο περίπλοκες σχέσεις ισχύουν για τα αλλά κρυσταλλικά συστήματα. Συνδυάζοντας τις εξισώσεις 3.1 και 3.11, είναι δυνατός ο υπολογισμός της γωνίας περίθλασης για τα διάφορα κρυσταλλικά επίπεδα του στερεού. Έτσι για ένα στερεό που κρυσταλλώνεται στο κυβικό σύστημα ισχύει: 3.12 Και με τον τρόπο αυτό κάθε επίπεδο στο πλέγμα που χαρακτηρίζεται από τους δείκτες Miller (hkl) δίνει χαρακτηριστική ανάκλαση σε συγκεκριμένη γωνία θ. Οργανολογία Ένα περιθλασίμετρο ακτίνων Χ αποτελείται από μια πηγή παραγωγής ακτίνων Χ, μια διάταξη περιορισμού της περιοχής μήκους κύματος της εισερχόμενης ακτινοβολίας, έναν χώρο τοποθέτησης του δείγματος, έναν ανιχνευτή και ένα σύστημα επεξεργασίας και ανάγνωσης του αναλυτικού σήματος. Η συνηθέστερη πηγή ακτίνων Χ για αναλυτικές εφαρμογές είναι ο σωλήνας ή η λυχνία ακτίνων Χ ή σωλήνας Coolidge. Αποτελείται από ένα σωλήνα-περίμβλημα με υψηλό κενό, στο οποίο βρίσκεται μια θερμαινόμενη κάθοδος νήματος βολφραμίου και μια άνοδος αποτελούμενη από ένα συμπαγές τεμάχιο χαλκού. Στην επιφάνεια του χαλκού ηλεκτροαποτίθεται το μεταλλοστόχος ( βολφράμιο,χρώμιο κ.α). Για τον περιορισμό του εύρους της περιοχής τιμών μήκους κύματος χρησιμοποιούνται φίλτρα και μονοχρωμάτορες. Το φιλτράρισμα της ακτινοβολίας πραγματοποιείται με λεπτές μεταλλικές λωρίδες, ενώ ο μονοχρωμάτορας αποτελείται από ένα ζεύγος κατευθυντήρων δέσμης και ένα στοιχείο διασποράς. Το στοιχείο αυτό είναι ένας μονοκρύσταλλος προσαρμοσμένος σε ένα γωνιόμετρο, που επιτρέπει την μεταβολή και την ακριβή μέτρηση ή ρύθμιση της γωνίας θ, μεταξύ της μετωπικής επιφάνειας του κρυστάλλου και της εισερχόμενης δέσμης. Για την λήψη του περιθλασιογράμματος προσαρμόζεται ο κατευθυντήρας εξόδου και ο ανιχνευτής σε περιστροφική τράπεζα, που περιστρέφεται με διπλάσια ταχύτητα από το γωνιόμετρο. Οι κατευθυντήρες αποτελούνται συνήθως από μια σειρά πυκνά τοποθετημένων μεταλλικών πλακών οι οποίες απορροφούν όλη την εκτός παραλληλότητας ακτινοβολία της δέσμης. 84
85 Το περιθλασίμετρο το οποίο χρησιμοποιήθηκε στις αναλύσεις των κρυσταλλικών στερεών στην παρούσα εργασία, ήταν Siemens D5. Η ακτινοβολία X παραγόταν από λυχνία Coolidge (Cu Ka) η οποία λειτουργούσε στα 4 kv και 3 ma. Το μήκος κύματος της ακτινοβολίας ήταν λ= Ǻ. Σχήμα 3.11: Διάταξη του περιθλασιμέτρου ακτίνων Χ [Skoog, 22]. Η ακτινοβολία αφού περάσει από τον μονοχρωμάτορα εστίασης καθίσταται πλήρως μονοχρωματική και ευθυγραμμισμένη. Καθώς η ευθυγραμμισμένη ακτινοβολία προσπίπτει στο δείγμα, το οποίο περιστρέφεται με τη βοήθεια του γωνιομέτρου,δημιουργούνται διαφορετικές γωνίες πρόσπτωσης θ. Με τον τρόπο αυτό οι ακτίνες Χ δε ακτινοβολούν το δείγμα μόνο υπό μία γωνία, αλλά το σαρώνουν σε ένα φάσμα γωνιών που επιλέγεται. Μετά την περίθλασή τους από τους κρυσταλλίτες του δείγματος οι ακτίνες εστιάζονται στον ευθυγραμμιστή εξόδου, ο οποίος βρίσκεται σε γωνία θ γύρω από τον άξονα του περιθλασίμετρου. Έτσι η απόκλιση της προσπίπτουσας σε σχέση με την περιθλώμενη ακτινοβολία είναι συνολικά 2θ. Ο ανιχνευτής με ταυτόχρονη στροφή κατά γωνία 2θ συλλέγει τις διάφορες περιθλάσεις αφού πρώτα περάσουν από φίλτρο Ni. Το φίλτρο χρησιμοποιείται για τη λήψη καλύτερων κορυφών των ανακλάσεων στα φάσματα. Όταν το άνοιγμα του φίλτρου είναι μικρό τότε οι μικρές κορυφές είναι πιθανό να μη φαίνονται, ενώ αν το άνοιγμα είναι μεγάλο τότε είναι πολύ πιθανό να υπάρχει θόρυβος και πολύ υψηλές κορυφές. Ο ανιχνευτής μετατρέπει την ακτινοβολία σε ηλεκτρικό ρεύμα και τα αποτελέσματα συλλέγονται με το κατάλληλο λογισμικό δίνοντας το περιθλασιόγραμμα του δείγματος, το οποίο και αναλύεται περαιτέρω Ηλεκτρονική Μικροσκοπία Σάρωσης (SEM) Η ηλεκτρονική μικροσκοπία σάρωσης παρέχει πληροφορίες σχετικά με το σχήμα και το μέγεθος των κρυσταλλικών στερεών σωματιδίων. Επιπλέον 85
86 δίνει λεπτομέρειες για την επιφάνεια των στερεών και υπάρχει και η δυνατότητα ποιοτική ή και ημιποσοτική ανάλυση των στοιχείων του υλικού. Στο ηλεκτρονικό μικροσκόπιο σάρωσης η επιφάνεια του στερεού δείγματος σαρώνεται παλινδρομικά με δέσμη ηλεκτρονίων υψηλής ενέργειας. Με τη διαδικασία αυτή λαμβάνονται πολλά είδη σημάτων από την επιφάνεια τα οποία χρησιμοποιούνται για μελέτες επιφανειών και για στοιχειακή ανάλυση. Η αυξημένη διακριτική ικανότητα του ηλεκτρονικού μικροσκοπίου σάρωσης έναντι του οπτικού μικροσκοπίου οφείλεται αφενός στο μικρότερο μήκος κύματος της δέσμης των ηλεκτρονίων σε σχέση με το μήκος κύματος του φωτός και αφετέρου στην δυνατότητα εξέτασης του δείγματος σε μεγαλύτερο βάθος πεδίου. Οι αλληλεπιδράσεις ενός στερεού με μια δέσμη ηλεκτρονίων διακρίνονται σε ελαστικές και ανελαστικές. Οι ελαστικές αλληλεπιδράσεις επηρεάζουν τις τροχιές των ηλεκτρονίων της δέσμης, χωρίς να μεταβάλλουν σημαντικά τις ενέργειές τους. Οι ανελαστικές έχουν ως αποτέλεσμα τη μεταφορά μέρους ή όλης της ενέργειας των ηλεκτρονίων στο στερεό. Το διεγερμένο στερεό εκπέμπει δευτερογενή ηλεκτρόνια, ηλεκτρόνια Auger, ακτίνες Χ και μερικές φορές φωτόνια μεγαλύτερου μήκους κύματος. Όταν ένα ηλεκτρόνιο συγκρούεται με ένα άτομο, η κατεύθυνση του ηλεκτρονίου αλλάζει, αλλά η ταχύτητα του δεν επηρεάζεται σχεδόν καθόλου και έτσι η κινητική ενέργειά του παραμένει ουσιαστικά αμετάβλητη. Η γωνία εκτροπής για μια δεδομένη σύγκρουση είναι τυχαία και ποικίλει μεταξύ -18 ο. Μερικά από τα ηλεκτρόνια τελικά χάνουν ενέργεια από ανελαστικές συγκρούσεις και παραμένουν στο στερεό. Ωστόσο, η πλειονότητά τους υφίσταται πολυάριθμες ελαστικές συγκρούσεις με αποτέλεσμα να εξέρχονται τελικά από την επιφάνεια ως οπισθοσκεδαζόμενα ηλεκτρόνια (Backscattered Electrons, BS). Σχήμα 3.12: Αλληλεπιδράσεις μεταξύ δέσμης ηλεκτρονίων και δείγματος [Skoog, 22]. 86
87 Η δέσμη των οπισθοσκεδαζόμενων ηλεκτρονίων έχει πολύ μεγαλύτερη διάμετρο από την προσπίπτουσα δέσμη και είναι ένας από τους παράγοντες που περιορίζουν την διακριτική ικανότητα ενός ηλεκτρονικού μικροσκοπίου. Η ένταση των οπισθοσκεδαζόμενων ηλεκτρονίων εξαρτάται από την τοπογραφία του δείγματος, από τον ατομικό αριθμό των στοιχείων που το αποτελούν και από την ένταση της δέσμης των ηλεκτρονίων. Οι ελαστικές συγκρούσεις αυξάνονται σε υλικά τα οποία περιέχουν υψηλούς ατομικούς αριθμούς και όταν η ένταση της δέσμης των ηλεκτρονίων είναι χαμηλή. Τα οπισθοσκεδαζόμενα ηλεκτρόνια είναι ηλεκτρόνια υψηλής ενέργειας και έχουν προκύψει από διείσδυση της προσπίπτουσας δέσμης σε βάθος μερικών μm. Μαζί με τα οπισθοσκεδαζόμενα ηλεκτρόνια εκπέμπονται από την επιφάνεια του στερεού και ηλεκτρόνια ενέργειας μικρότερης των 5 kev. Τα ηλεκτρόνια αυτά ονομάζονται δευτερογενή (Secondary Electrons, SE), προέρχονται από ανελαστικές αλληλεπιδράσεις και είναι λιγότερα από τα οπισθοσκεδαζόμενα ηλεκτρόνια. Εξαιτίας της χαμηλής ενέργειάς τους παράγονται από βάθος μερικών νανομέτρων και εξέρχονται σε δέσμη, η οποία είναι ελαφρά μεγαλύτερη σε διάμετρο από την προσπίπτουσα δέσμη. Η ένταση των δευτερογενών ηλεκτρονίων εξαρτάται από την γωνία της προσπίπτουσας δέσμης ως προς την επιφάνεια του δείγματος. Σχήμα 3.13: Εκπομπή οπισθοσκεδαζόμενου (BS) και δευτερογενών (SE) ηλεκτρονίων από την προσπίπτουσα δέσμη ηλεκτρονίων, Β [Skoog, 22]. Σχήμα 3.14: Σχηματική παρουσίαση παραγωγής χαρακτηριστικών ακτίνων Χ [Skoog, 22]. 87
88 Χαρακτηριστικές ακτίνες Χ παράγονται κατά την αλληλεπίδραση της δέσμης των ηλεκτρονίων με το δείγμα όταν διεγερμένα ηλεκτρόνια επιστρέφουν σε επίπεδα χαμηλότερης ενέργειας των ατομικών τροχιακών τους. Αν η ενέργεια της δέσμης των ηλεκτρονίων είναι αρκετά υψηλή τότε είναι δυνατή η απομάκρυνση ενός ηλεκτρονίου από κάποιο εσωτερικό φλοιό του ατόμου. Η σύγκρουση έχει ως αποτέλεσμα την δημιουργία ενός διεγερμένου ιόντος, το οποίο έχει χάσει ηλεκτρόνιο από εσωτερικό τροχιακό. Επειδή μια τέτοια δομή είναι ασταθής άλλο ηλεκτρόνιο από εξωτερικό τροχιακό υψηλότερης ενέργειας μεταπίπτει και συμπληρώνει το κενό τροχιακό υπό την εκπομπή ενός φωτονίου. Το φωτόνιο αυτό αντιστοιχεί σε ηλεκτρομαγνητική εκπομπή στην περιοχή ακτίνων Χ. Οι χαρακτηριστικές ακτίνες Χ έχουν προέλθει από την διείσδυση της δέσμης των ηλεκτρονίων σε πολύ μεγαλύτερο βάθος πεδίου. Οργανολογία Το ηλεκτρονικό μικροσκόπιο σάρωσης αποτελείται από τη πηγή ηλεκτρονίων, το μαγνητικό σύστημα εστίασης, τον θάλαμο δείγματος εφοδιασμένο με το κατάλληλο σύστημα κενού και από τους ανιχνευτές. Την πηγή των ηλεκτρονίων αποτελεί ένα λεπτό σχήματος V νήμα από μέταλλο το οποίο διαρρέεται από ρεύμα, θερμαίνεται σε υψηλή θερμοκρασία (27Κ) και εκπέμπει ηλεκτρόνια. Για να ελευθερωθεί ένα ηλεκτρόνιο θα πρέπει να πάρει ενέργεια μεγαλύτερη από το έργο εξόδου του μετάλλου. Το μέταλλο που χρησιμοποιείται κυρίως είναι το βολφράμιο, γιατί παρουσιάζει χαμηλό έργο εξόδου και η δέσμη που παράγεται χαρακτηρίζεται από σταθερότητα. Στα ηλεκτρονικά μικροσκόπια σάρωσης εκπομπής πεδίου ( field emission), όπως και στην περίπτωση του ΗΜ το οποίο χρησιμοποιήθηκε και στην παρούσα εργασία, η εκπομπή ηλεκτρονίων δημιουργείται μέσω φαινομένου σήραγγος. Τα παραγόμενα ηλεκτρόνια λόγω της μεγάλης διαφοράς δυναμικού που εφαρμόζεται μεταξύ καθόδου ( νήμα βολφραμίου) και ανόδου ( μεταλλική πλάκα) επιταχύνονται μέσω οπής προς την άνοδο. Η διάμετρος της οπής και επομένως και της παραγόμενης δέσμης ηλεκτρονίων είναι 1-5 μm ενώ τα ηλεκτρόνια επιταχύνονται με τάση που φτάνει τα 35 kev. Η διάμετρος της δέσμης ηλεκτρονίων είναι εξαιρετικής σημασίας για την διακριτική ικανότητα του ηλεκτρονικού μικροσκοπίου. Η διάμετρος δέσμης μειώνεται με το μαγνητικό σύστημα εστίασης, το οποίο αποτελείται από ζεύγη μαγνητών ευθυγραμμισμένα μεταξύ πηγής ηλεκτρονίων και δείγματος τα οποία λειτουργούν ως συγκεντρωτικοί και αντικειμενικοί φακοί. Τα ζεύγη μαγνητών που αποτελούν το συγκεντρωτικό φακό. Το σύστημα του αντικειμενικού φακού βρίσκεται ακριβώς πριν από το 88
89 δείγμα και είναι υπεύθυνο για την μείωση της διαμέτρου της δέσμης στα 5-2nm και για την εκτροπή της δέσμης προκειμένου να σαρώσει περιοχή του δείγματος. Η σάρωση επιτυγχάνεται με δυο ζεύγη ηλεκτρομαγνητικών πηνίων που βρίσκονται στον αντικειμενικό φακό. Το ένα ζεύγος εκτρέπει την ακτίνα κατά μήκος του δείγματος στη διεύθυνση x και το άλλο στην διεύθυνση y. Έτσι με εφαρμογή ηλεκτρικού σήματος στο ένα ζεύγος των πηνίων η δέσμη των ηλεκτρονίων κινείται σε ευθεία γραμμή κατά μήκος του δείγματος και στη συνέχεια επιστρέφει στην αρχική της θέση. Με την ολοκλήρωση το άλλο ζεύγος πηνίων εκτρέπει κατακόρυφα τη δέσμη για διάστημα ίσο με την διάμετρό της και επαναλαμβάνεται η κατά μήκος κίνηση της δέσμης από το πρώτο ζεύγος πηνίων. Με τον τρόπο αυτό ακτινοβολείται με την δέσμη των ηλεκτρονίων όλη η επιφάνεια του δείγματος. Το δείγμα είναι τοποθετημένο στο θάλαμο δείγματος η ατμόσφαιρα του οποίου ελέγχεται από το σύστημα κενού. Χρησιμοποιείται κενό για να αποφεύγονται οι ανελαστικές σκεδάσεις των ηλεκτρονίων με τα μόρια του αέρα, για να αποφεύγεται η οξείδωση των μαγνητών και να διατηρείται το σύστημα καθαρό. Το δείγμα τοποθετείται σε ειδική βάση (stage) που επιτρέπει τη μετακίνηση, την κλίση και την περιστροφή του δείγματος, για μεγαλύτερη ελευθερία επιλογής της περιοχής που θα σαρωθεί. Τα δείγματα, απαιτείται να είναι καλοί αγωγοί του ηλεκτρικού ρεύματος και της θερμότητας για να αποφευχθεί η ανάπτυξη επιφανειακών φορτίων και η πιθανότητα θερμικής αποσύνθεσής τους. Η τεχνική που χρησιμοποιείται για την λήψη εικόνων από το ηλεκτρονικό μικροσκόπιο σάρωσης μη αγώγιμων δειγμάτων είναι η επικάλυψή τους με λεπτό μεταλλικό υμένιο. Τα υλικά που κυρίως χρησιμοποιούνται είναι ο χρυσός, ο γραφίτης και ο λευκόχρυσος και το υμένιο παράγεται με επίπαση εξαχνωμένου μετάλλου σε υψηλό κενό (sputtering). 89
90 Σχήμα 3.15: Σχεδιάγραμμα ηλεκτρονικού μικροσκοπίου σάρωσης (SEM) [Skoog, 22]. Όταν τα ηλεκτρόνια διεισδύσουν στο δείγμα θα λάβουν χώρα οι αλληλεπιδράσεις που περιγράφηκαν παραπάνω. Κατά την διάρκεια της σάρωσης κατάλληλοι ανιχνευτές συλλέγουν τα ηλεκτρόνια και λαμβάνεται σήμα το οποίο αντιστοιχεί στο δεδομένο σημείο της επιφάνειας. Το σήμα αποθηκεύεται στον υπολογιστή, όπου τελικά μετατρέπεται σε εικόνα. Στην εικόνα με υψηλή λάμψη απεικονίζονται οι περιοχές που δίνουν ισχυρό σήμα στον ανιχνευτή, ενώ σκοτεινές είναι οι περιοχές με ασθενές σήμα. Η προβαλλόμενη εικόνα έχει μια σαφή τρισδιάστατη ποιότητα, επειδή τα ηλεκτρονικά μικροσκόπια σάρωσης εστιάζουν σε μεγάλο βάθος. Τα οπισθοσκεδαζόμενα ηλεκτρόνια συλλέγονται από ανιχνευτή διόδου ημιαγωγού, τα δευτερογενή ηλεκτρόνια από σπινθηριστή και φωτοπολλαπλασιαστή και οι χαρακτηριστικές ακτίνες Χ από φασματόμετρα διασποράς ενέργειας (EDS). Από πίνακες χαρακτηριστικών ενεργειών όλων των στοιχείων γίνεται ταυτοποίηση των κορυφών του φάσματος των ακτίνων Χ. Οι φωτογραφίες των δειγμάτων στην παρούσα εργασία ελήφθησαν με ηλεκτρονικό μικροσκόπιο σάρωσης LEO VP-35 FEM. Τα πρώτα δύο ήταν εφοδιασμένα με ανιχνευτή χαρακτηριστικών ακτίνων Χ (Bruker) και λογισμικό σύστημα στοιχειακής ανάλυσης των δειγμάτων (Esprit). 9
91 Κεφάλαιο 4 Πειράματα αυθόρμητης καταβύθισης 4.1 Διαγράμματα Σταθερότητας για την αυθόρμητη καταβύθιση του στρουβίτη σε υπέρκορα διαλύματα Στη σειρά αυτή των πειραμάτων μελετήθηκε η κινητική της αυθόρμητης καταβύθισης του στρουβίτη από υπέρκορα διαλύματα στους 25 o C προκειμένου να ληφθούν πληροφορίες για τον μηχανισμό της. Με τα πειράματα αυτά προσδιορίστηκαν τα όρια των συγκεντρώσεων των ιόντων του καταβυθιζόμενου στερεού για την αυθόρμητη καταβυθισή του μετά την παρέλευση ορισμένου χρόνου (χρόνος επαγωγής) σε αντιδραστήρες διαλείποντος έργου και σε ρευστοποιημένη κλίνη Αυθόρμητη καταβύθιση στρουβίτη σε αντιδραστήρα διαλείποντος έργου Πραγματοποιήθηκαν πειράματα αυθόρμητης καταβύθισης στρουβίτη σε συνθήκες σταθερού ph 6.5 στους 25 ο C σε αντιδραστήρα διαλείποντος έργου. Προσδιορίσθηκε η περιοχή σταθερότητας των διαλυμάτων, στην οποία η κρυστάλλωση πραγματοποιείται μόνον όταν εισάγουμε πυρήνες κρυστάλλωσης (Μετασταθής Περιοχή). Στον πίνακα 4.1 παρουσιάζονται οι αρχικές συγκεντρώσεις, υπερκορεσμός, σχετικός υπερκορεσμός και λογάριθμος της συγκέντρωσης των ιόντων Μg 2+, όπως προσδιορίσθηκαν από το λογισμικό υπολογισμού ειδομορφών σε υδατικά διαλύματα σε ισορροπία, PHREEQC [U.S. Geological Survey]. Τέλος, οι χρόνοι επαγωγής προσδιορίστηκαν από τα διαγράμματα μεταβολής των συγκεντρώσεων των πλεγματικών ιόντων έναντι του χρόνου. Πίνακας 4.1: Πειραματικές συνθήκες σε συνθετικό υδατικό απόβλητο υπέρκορο ως προς στρουβίτη στους 25 C C/*1-2 M ph Ω σ log[mg 2+ ]/M τ /min
92 Χρόνος Επαγωγής τ/ min Στο σχήμα 4.1 απεικονίζεται η εξάρτηση του χρόνου επαγωγής από τον υπερκορεσμό για την αυθόρμητη καταβύθιση του στρουβίτη, γνωστό και ως διάγραμμα σταθερότητας. Από διαγράμματα αυτού του είδους καθορίζονται τα όρια της ασταθούς και της σταθεράς τιμών υπερκορεσμών περιοχής. Από το διάγραμμα φαίνεται ότι ο χρόνος επαγωγής μειώνεται με την αύξηση του υπερκορεσμού, σύμφωνα με την κλασσική θεωρία της πυρηνογένεσης (εξ. 2.3) ,6,8 1, 1,2 1,4 1,6 1,8 2, 2,2 2,4 2,6 2,8 Υπερκορεσμός, Ω Σχήμα 4.1: Μεταβολή του χρόνου επαγωγής συναρτήσει του υπερκορεσμού ως προς στρουβίτη, Ω, για την αυθόρμητη καταβύθιση του στρουβίτη σε διαλύματα συνθετικού αποβλήτου σε συνθήκες σταθερού ph 6.5, 25 ο C Για τιμές υπερκορεσμού ως προς στρουβίτη μεγαλύτερες από Ω=3, ο χρόνος επαγωγής ήταν αρκετά μικρός (ασταθής περιοχή) ενώ για τιμές υπερκορεσμού μικρότερες του Ω= 1.6, ο χρόνος επαγωγής ήταν αρκετά μεγάλος, ώστε τα αντίστοιχα υπέρκορα διαλύματα να θεωρούνται σταθερά. Εφαρμογή της εξίσωσης 2.3 στα δεδομένα του σχήματος 4.1, λαμβάνοντας για το β συντελεστής σχήματος των κρυστάλλων την τιμή (=32), Vm ο μοριακός όγκος της καταβυθιζόμενης φάσης (= cm 3 ) είναι δυνατόν από την κλίση της ευθείας logτ log 2- Ω να υπολογισθεί η διεπιφανειακή ενέργεια. Η γραμμική προσαρμογή των δεδομένων, όπως φαίνεται στο σχήμα 4.2, διακρίνονται δύο περιοχές. Η περιοχή συνθηκών των υπέρκορων διαλυμάτων με Ω > 2 αντιστοιχούν σε συνθήκες στις οποίες η πυρηνογένεση είναι κατά κύριο λόγο ομογενής. Από την κλίση της ευθείας η οποία αντιστοιχεί στα σημεία αυτά και η οποία είναι μεγαλύτερη, 92
93 log (τ/min) log(τ/min) υπολογίσθηκε η τιμή της διεπιφανειακής ενέργειας και βρέθηκε γs= 1 mj*m -2 για ph ,2 1 3, 2,8 8 2,6 2,4 2,2 2, 1,8 1,6 1, /log 2 Ω Σχήμα 4.2: Μεταβολή του λογάριθμου του χρόνου επαγωγής, logτ συναρτήσει του αντιστρόφου του τετραγώνου του υπερκορεσμού 1/log 2 Ω για την αυθόρμητη καταβύθιση του στρουβίτη σε υπέρκορα διαλύματα συνθετικού αποβλήτου σε σταθερό ph 6.5 στους 25 o C σε αντιδραστήρα διαλείποντος έργου 3, ,8 2,6 8 2,4 6 2,2 2, 4 1,8 1,6 2 1,4-1,78-1,76-1,74-1,72-1,7-1,68 log[mg 2+ /M] Σχήμα 4.3: Μεταβολή του λογαρίθμου του χρόνου επαγωγής, logτ συναρτήσει του λογαρίθμου της συγκέντρωσης των ελεύθερων ιόντων μαγνησίου, log[mg 2+ ] σε υπέρκορα διαλύματα συνθετικού αποβλήτου για σταθερό ph 6.5 σε αντιδραστήρα διαλείποντος έργου, 25 C. Η εξίσωση 2.31 σε λογαριθμική μορφή είναι: 93
94 Χρόνος Επαγωγής, τ/min Από την προσαρμογή των δεδομένων του πίνακα 4.1, στην γραμμική εξίσωση 4.1 υπολογίσθηκε ο αριθμός των δομικών μονάδων του κρίσιμου πυρήνα, p= 16, για ph Αυθόρμητη καταβύθιση στρουβίτη σε αντιδραστήρα ρευστοποιημένης κλίνης Πραγματοποιήθηκαν πειράματα αυθόρμητης καταβύθισης στρουβίτη σε συνθήκες σταθερού ph 6.5 σε αντιδραστήρα ρευστοποιημένης κλίνης με ροή 22 ml*min -1. Στον πίνακα 4.2 παρουσιάζονται οι αρχικές συγκεντρώσεις, ο υπερκορεσμός, ο σχετικός υπερκορεσμός ως προς στρουβίτη και ο λογάριθμος της συγκέντρωσης των ιόντων Μg 2+ όπως υπολογίσθηκαν από το λογισμικό phreeqc. Τέλος, οι τιμές του χρόνου επαγωγής μετρήθηκαν από τα αντίστοιχα διαγράμματα μεταβολής των συγκεντρώσεων των ιόντων Μg 2+, NH4 + και PO4 3- συναρτήσει του χρόνου. Πίνακας 4.2: Πειραματικές συνθήκες και οι τιμές του χρόνου επαγωγής που μετρήθηκαν σε συνθετικό υδατικό απόβλητο σε ph 6.5 στους 25 C C/*1-2 M ph Ω σ log[mg 2+ ]/M τ /min Υπερκορεσμός, Ω 94
95 log (τ/min) Σχήμα 4.4: Μεταβολή του χρόνου επαγωγής έναντι του υπερκορεσμού Ω για την αυθόρμητη καταβύθιση του στρουβίτη σε διαλύματα συνθετικού αποβλήτου σε συνθήκες σταθερού ph 6.5 στους 25 ο C Από το διάγραμμα σταθερότητας του σχήματος 4.4 φαίνεται ότι και στη περίπτωση αυτή ο χρόνος επαγωγής μειώθηκε με την αύξηση του υπερκορεσμού. Στο σχήμα 4.5 φαίνεται η μεταβολή του λογαρίθμου του χρόνου επαγωγής, logτ έναντι του αντίστροφου του τετραγώνου του λογαρίθμου του υπερκορεσμού, 1/log 2 Ω για την αυθόρμητη καταβύθιση στρουβίτη σε αντιδραστήρα ρευστοποιημένης κλίνης. Από τη κλίση της ευθείας, η οποία αντιστοιχεί στην περιοχή της κυρίως ομογενούς πυρηνογένεσης υπολογίσθηκε η τιμή της διεπιφανειακής ενέργειας, γs= 11.2mJ*m -2. Η τιμή αυτή δεν διαφοροποιείται από την τιμή η οποία υπολογίσθηκε από τα πειραματικά δεδομένα σε αντιδραστήρα διαλείποντος έργου. Για τη σειρά αυτή των πειραμάτων, η γραφική παράσταση του λογαρίθμου του χρόνου επαγωγής από τον λογάριθμο της συγκέντρωσης του ελεύθερου μαγνησίου φαίνεται στο σχήμα 4.6. Από την κλίση της ευθείας του διαγράμματος υπολογίσθηκε ο αριθμός των δομικών μονάδων του κρίσιμου πυρήνα, p = 19, σε πολύ καλή συμφωνία με την τιμή η οποία προέκυψε από την προσαρμογή των πειραματικών δεδομένων από αντιδραστήρα διαλείποντος έργου ,2 3, 2,8 2,6 2,4 2, , 1,8 2 1,6 1, /log 2 Ω Σχήμα 4.5: Μεταβολή του λογάριθμου του χρόνου επαγωγής συναρτήσει του αντίστροφου του τετραγώνου του υπερκορεσμού για την αυθόρμητη καταβύθιση του στρουβίτη σε σταθερό ph 6.5 σε αντιδραστήρα ρευστοποιημένης κλίνης στους 25 ο C 95
96 log (τ/min) 3,2 3, 2,8 2,6 2,4 2, , 1,8 2 1,6 1,4-1,78-1,76-1,74-1,72-1,7-1,68 log([mg 2+ ]/M) Σχήμα 4.6: Μεταβολή του λογαρίθμου του χρόνου επαγωγής, logτ συναρτήσει του λογαρίθμου της συγκέντρωσης των ελεύθερων ιόντων μαγνησίου, log[mg 2+ ] για σταθερό ph 6.5 σε αντιδραστήρα ρευστοποιημένης κλίνης στους 25 ο C 4.2 Συμπεράσματα Η μόνη καταβυθιζόμενη φάση σε πειράματα αυθόρμητης καταβύθισης σε θερμοκρασία 25 ο C και σε σταθερό ph 6.5 είναι ο στρουβίτης σε όλο το εύρος των τιμών υπερκορεσμού που μελετήθηκαν. Ο χρόνος επαγωγής είναι μειωνόταν αυξανόμενων των τιμών του υπερκορεσμού του διαλύματος ως προς στρουβίτη. Παρατηρήθηκε ότι σε τιμές υπερκορεσμού μεγαλύτερες του Ω=2.63 η έναρξη της καταβύθισης ήταν ταχύτατη (ασταθής περιοχή), ενώ σε τιμές υπερκορεσμού μικρότερες του Ω=1.65, τα διαλύματα ήσαν πρακτικώς σταθερά. Από τις μετρήσεις των τιμών του χρόνου επαγωγής συναρτήσει του υπερκορεσμού και της συγκέντρωσης των ιόντων μαγνησίου, Mg 2+, στα υπέρκορα διαλύματα υπολογίσθηκαν η τιμή της διεπιφανειακής ενέργειας για τους αναπτυσσόμενους πυρήνες στρουβίτη (γs= 1 mj*m -2 ) και το μέγεθος του κρίσιμου πυρήνα (περίπου 18 δομικές μονάδες). Υπήρξε συμφωνία των υπολογισμών αυτών τόσο για τις μετρήσεις σε αντιδραστήρα διαλείποντος έργου όσο και σε αντιδραστήρα ρευστοποιημένης κλίνης, γεγονός το οποίο υποδηλώνει η πυρηνογένεση και στις δύο περιπτώσεις είναι παρόμοια. 96
97 Κεφάλαιο 5 Ετερογενής Καταβύθιση του Στρουβίτη Τα πειράματα καταβύθισης στρουβίτη πραγματοποιήθηκαν σε αντιδραστήρες διαλείποντος έργου και ρευστοποιημένης κλίνης χρησιμοποιώντας σταθερά υπέρκορα διαλύματα (σχήμα 4.1) στα οποία εισήχθησαν ως φύτρα κρυσταλλικής ανάπτυξης του στρουβίτη ξένα (ως προς την χημική τους σύσταση) υποστρώματα. Τα αποτελέσματα αυτά συγκρίθηκαν με πειράματα στα οποία χρησιμοποιήθηκαν κρυσταλλικά φύτρα στρουβίτη. Κατά τα λοιπά, κατά την διεξαγωγή των πειραμάτων, ακολουθήθηκε η ίδια διαδικασία όπως περιγράφηκε στα πειράματα αυθόρμητης καταβύθισης. Στα πειράματα καταβύθισης στρουβίτη σε αντιδραστήρα διαλείποντος έργου μετά την επίτευξη του υπερκορεσμού εισαγόταν στο διάλυμα προζυγισμένη ποσότητα καλά χαρακτηρισμένων κρυσταλλικών φύτρων. Στα πειράματα ρευστοποιημένης κλίνης μετά την πλήρωση της κλίνης με τα σωματίδια φύτρων ρυθμιζόταν η ροή στα 22 ml min -1. Η ροή αυτή εξασφάλιζε τη ρεύστωση των σωματιδίων σε όλο το μήκος της κλίνης και διατηρούταν σταθερή καθ ολή τη διάρκεια διεξαγωγής του πειράματος. Ο χρόνος επαγωγής εμετρείτο από την έναρξη του πειράματος ως τη πρώτη πτώση της τιμής του ph του διαλύματος. Η μεταβολή αυτή συνόδευε την έναρξη της κρυσταλλικής ανάπτυξης. Κατά τη διάρκεια των πειραμάτων αυτών γινόταν δειγματοληψία. Τα δείγματα διηθούνταν και στα διηθήματα γινόταν ανάλυση για μαγνήσιο και φωσφορικά. Από τις αναλύσεις των δειγμάτων υπολογιζόταν ο ρυθμός της κρυσταλλικής ανάπτυξης. Tα φύτρα που χρησιμοποιήθηκαν για τα πειράματα καταβύθισης στρουβίτη ήταν quartz, άμμος και κρύσταλλοι παρασκευασμένου στρουβίτη (MgNH4PO4.6H2O). Η παρασκευή του στρουβίτη έγινε με βραδεία προσθήκη διαλύματος NH4H2PO4 σε διάλυμα MgCl2 με ταυτόχρονη προσθήκη διαλύματος NaOH έτσι ώστε η τιμή του ph να διατηρείται στην τιμή 9.. Οι κρύσταλλοι στρουβίτη και τα υπόλοιπα κρυσταλλικά στερεά, χαρακτηρίστηκαν με περίθλαση ακτίνων-χ. Οι κόκκοι του διοξειδίου του πυριτίου ήταν μεγέθους 2-8 μm. Η άμμος προερχόταν από παραλία της Πάτρας, είχε καθαριστεί με βρασμό σε διάλυμα HCl, εκτεταμένη έκπλυση με νερό και ξήρανση στην ατμόσφαιρα. Οι κόκκοι μεγέθους 18-5 μm διαχωρίσθηκαν με την βοήθεια κόσκινων. Τα σωματίδια αυτά χρησιμοποιήθηκαν ως υπόστρωμα για την ανάπτυξη του στρουβίτη. 97
98 5.1 Καταβύθιση στρουβίτη σε υπόστρωμα quartz Στην ενότητα αυτή παρουσιάζεται η μελέτη της κινητικής καταβύθισης του στρουβίτη σε σταθερά υπέρκορα διαλύματα με προσθήκη κρυσταλλικών φύτρων quartz σε αντιδραστήρα διαλείποντος έργου και ρευστοποιημένης κλίνης. Διατηρήθηκαν οι αυτές συνθήκες και για τους δυο τύπους αντιδραστήρα Καταβύθιση στρουβίτη σ ε αντιδραστήρα διαλείποντος έργου Οι αρχικές συγκεντρώσεις των πλεγματικών ιόντων του στρουβίτη, το ph του διαλύματος εργασίας το οποίο παρέμενε σταθερό με την προσθήκη ΝaOH, οι τιμές του υπερκορεσμού και του σχετικού υπερκορεσμού ως προς στρουβίτη, ο λογάριθμος της συγκέντρωσης των ιόντων μαγνησίου στο διάλυμα, οι τιμές του χρόνου επαγωγής και οι αρχικές ταχύτητες καταβύθισης συνοψίζονται στους πίνακες 5.1 και 5.2 για δυο διαφορετικές ποσότητες υποστρώματος. Πίνακας 5.1: Πειραματικές συνθήκες και αποτελέσματα μετρήσεων για την καταβύθιση στρουβίτη σε σταθερά διαλύματα συνθετικού αποβλήτου με φύτρα 5mg quartz, ph 6.5, 25 ο C σε αντιδραστήρα διαλείποντος έργου C/1-2 M Ω ph σ log[mg 2+ ] τ/min R CG/1-5 molmin -1 g Πίνακας 5.2: Πειραματικές συνθήκες και αποτελέσματα μετρήσεων για την καταβύθιση στρουβίτη σε σταθερά διαλύματα συνθετικού αποβλήτου με φύτρα 1mg quartz,ph 6.5, 25 ο C σε αντιδραστήρα διαλείποντος έργου C/1-2 M Ω ph σ log[mg 2+ ] τ/min R CG /1-6 molmin -1 g Στο σχήμα 5.1 απεικονίζεται η εξάρτηση του χρόνου επαγωγής από τον υπερκορεσμό για την καταβύθιση στρουβίτη από υπέρκορα διαλύματα, για τις δυο ποσότητες υποστρώματος. Όπως φαίνεται ο χρόνος επαγωγής μειώνεται με την αύξηση του υπερκορεσμού του διαλύματος και για τις δυο 98
99 χρόνος επαγωγής, τ/min ποσότητες φύτρων, ενώ παρουσιάζει εξάρτηση από την ποσότητα του υποστρώματος. Συγκεκριμένα, αύξηση της συγκέντρωσης του quartz στα υπέρκορα διαλύματα είχε ως αποτέλεσμα μεγαλύτερους χρόνους επαγωγής mg quartz 1mg quartz ,6 1,8 2, 2,2 2,4 2,6 2,8 Υπερκορεσμός, Ω Σχήμα 5.1: Μεταβολή του χρόνου επαγωγής συναρτήσει του υπερκορεσμού Ω ως προς στρουβίτη, για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου σε συνθήκες σταθερού ph 6.5, 25 ο C με φύτρα quartz 5mg ( )1mg ( ) quartz Στα διαγράμματα των σχημάτων 5.2 και 5.3 απεικονίζεται η εξάρτηση του λογάριθμου του χρόνου επαγωγής, logτ από το αντίστροφο τετράγωνου του λογαρίθμου του υπερκορεσμού, 1/log 2 Ω. Οι γραφικές παραστάσεις έγιναν με βάση την εξίσωση 4.1 από την οποία υπολογίσθηκε η ενέργεια που απαιτείται για τη δημιουργία της νέας επιφάνειας του στρουβίτη πάνω στο ξένο υπόστρωμα. Ο υπολογισμός της διεπιφανειακής ενέργειας έγινε από την κλίση της ευθείας στην περιοχή των υψηλότερων τιμών υπερκορεσμού, η οποία αντιστοιχεί κυρίως στην ομογενή πυρηνογένεση. Η τιμή της διεπιφανειακής ενέργειας η οποία υπολογίστηκε ήσαν γs= 8 mj. m -2 με φύτρα quartz.5 και 1g. Η τιμή αυτή σε σύγκριση με την αντίστοιχη τιμή γs= 1 mj*m -2, η οποία υπολογίσθηκε από τα πειράματα αυθόρμητης καταβύθισης, ήταν παραπλήσια γεγονός που υποδηλώνει ότι η καταβύθιση και στις δύο περιπτώσεις ήταν ετερογενής ή ότι οι κρυσταλλίτες του quartz δεν παίζουν σημαντικό ρόλο στην πυρηνογένεση. 99
100 log(τ/min) log(τ/min) 2, ,6 2,4 8 2,2 6 2, 1,8 4 1,6 2 1,4 5 mg quartz /log 2 Ω Σχήμα 5.2: Μεταβολή του logτ συναρτήσει του 1/log 2 Ω για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου με την εισαγωγή φύτρων 5mg quartz, ph 6.5, 25 o C 2, ,4 8 2,2 6 2, 4 1,8 1,6 1mg quartz /log 2 Ω 2 Σχήμα 5.3: Μεταβολή του logτ συναρτήσει του 1/log 2 Ω για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου με την εισαγωγή 1mg φύτρων quartz, ph 6.5, 25 o C 1
101 logτ/min Στο σχήμα 5.4 παρουσιάζεται η εξάρτηση του logτ από τον λογάριθμο της συγκέντρωσης των ιόντων Mg 2+. Ο αριθμός των δομικών μονάδων του κρίσιμου πυρήνα βρέθηκε για.5 και 1 g που μελετήθηκαν ίσος με p= 14 και p = 11 αντίστοιχα, τιμές παραπλήσιες. 2, ,6 2,4 5 mg quartz 1mg quartz 8 2,2 6 2, 1,8 4 1,6 2 1,4-1,78-1,76-1,74-1,72-1,7-1,68 log[mg 2+ ]/(M) Σχήμα 5.4 : Μεταβολή του logτ συναρτήσει του log[mg 2+ ] για την καταβύθιση στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου με την εισαγωγή 5mg ( ) και 1mg ( ) φύτρων quartz, ph 6.5, 25 o C Ο ρυθμός κρυσταλλικής ανάπτυξης, RCG, εκφράζεται ως η ποσότητα του σχηματιζόμενου στρουβίτη στη μονάδα του χρόνου προς τη μάζα των εισαγόμενων κρυσταλλικών φύτρων στο διάλυμα εργασίας. Ο ρυθμός κρυσταλλικής ανάπτυξης, RCG, υπολογίστηκε από την μεταβολή της συγκέντρωσης ενός πλεγματικού ιόντος συναρτήσει του χρόνου (εξ. 3.7). Η εξάρτηση των αρχικών ρυθμών καταβύθισης του στρουβίτη από τον σχετικό υπερκορεσμό του διαλύματος εκφράζεται από τη σχέση: όπου μια σταθερά και n η φαινόμενη τάξη της καταβύθισης. Η αριθμητική τιμή της τάξης σχετίζεται με το μηχανισμό της αντίδρασης όπως παρουσιάστηκε στην υποενότητα στο κεφάλαιο 2. Η εξάρτηση των αρχικών ρυθμών καταβύθισης από τον σχετικό υπερκορεσμό όπως φαίνεται στο διάγραμμα 5.5, είναι παραβολική. Σύμφωνα
102 Ρυθμός Καταβύθισης R ' CG / molmin-1 g -1 με τα πρότυπα κρυσταλλικής ανάπτυξης, η παραβολική εξάρτηση υποδηλώνει ότι το καθορίζον την αντίδραση στάδιο είναι η διάχυση των δομικών μονάδων στην επιφάνεια του αναπτυσσόμενου κρυστάλλου και η ενσωμάτωση τους στα ενεργά κέντρα κρυσταλλικής ανάπτυξης. Από το ίδιο διάγραμμα φαίνεται ότι ο ρυθμός σχηματισμού στρουβίτη μειώνεται με την αύξηση της ποσότητας του υποστρώματος. Εκ τούτου, λοιπόν συνάγεται το συμπέρασμα ότι το υπόστρωμα έχει επιβραδυντική δράση στη κρυσταλλική ανάπτυξη, πιθανώς λόγω μόλυνσης των κρυστάλλων από ιόντα πυριτικών ειδών τα οποία απελευθερώνονται στο διάλυμα λόγω της μερικής διάλυσης του quartz ,x1-5 5mg SiO 2 2,5x1-5 1mg SiO 2 8 2,x ,5x1-5 1,x ,x1-6 2,,15,2,25,3,35,4 Σχετικός υπερκορεσμός, σ Σχήμα 5.5: Μεταβολή της αρχικής ταχύτητας καταβύθισης, R CG συναρτήσει του σχετικού υπερκορεσμού, σ ως προς στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου με φύτρα 5mg ( ) και 1mg ( ) quartz σε σταθερό ph 6.5 στους 25 o C Στο σχήμα 5.6 απεικονίζεται το περιθλασιόγραμμα των ακτίνων- Χ του σχηματιζόμενου στρουβίτη με το quartz. Παρατηρούμε ταύτιση των κορυφών της καταβυθιζόμενης φάσης με το πρότυπο διάγραμμα για τον στρουβίτη. Εκ τούτου συμπεραίνεται ότι η καταβυθιζόμενη φάση είναι ο στρουβίτης. Aνάλογα περιθλασιογράμματα ακτίνων-χ ελήφθησαν για όλα τα στερεά που καταβυθίσθηκαν και για τις δυο διαφορετικές ποσότητες φύτρων. 12
103 Ένταση Στρουβίτης Καταβυθιζόμενη φάση θ Σχήμα 5.6: Περιθλασιογράμματα ακτίνων-χ σχηματιζόμενου στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου με την εισαγωγή φύτρων quartz σε υπερκορεσμό Ω=2.45 ως προς στρουβίτη, σταθερό ph 6.5, 25 o C Στο σχήμα 5.7 παρατίθενται οι φωτογραφίες από το ηλεκτρονικό μικροσκόπιο σάρωσης σάρωσης και τα αποτελέσματα της μικροανάλυσης με EDX. Παρατηρήθηκε ο σχηματισμός πρισματικών κρυστάλλων στρουβίτη, οι οποίοι δε κάλυπταν όλη την επιφάνεια των μεγάλων ακανόνιστου σχήματος κρυστάλλων quartz. Στην μικροανάλυση χαρακτηρισμού του υποστρώματος και του αναπτυσσόμενου σε αυτό στρουβίτη διακρίνουμε τα στοιχεία του μαγνησίου, του πυριτίου και του αζώτου. 13
104 Σχήμα 5.7: (α),(β) Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης σε καταβυθιζόμενο στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου σε υπόστρωμα quartz σε ph 6.5 στους 25 και (γ) αποτελέσματα μικροανάλυσης Καταβύθιση στρουβίτη σε αντιδραστήρα ρευστοποιημένης κλίνης Σε αντιδραστήρα ρευστοποιημένης κλίνης χρησιμοποιήθηκαν δύο διαφορετικές ποσότητες υποστρώματος 1 και 2g quartz. Στους πίνακες 5.3 και 5.4 συνοψίζονται οι αρχικές συγκεντρώσεις, υπερκορεσμός, σχετικός υπερκορεσμός και λογάριθμος συγκέντρωσης ιόντων Μg 2+ όπως υπολογίσθηκαν από το λογισμικό phreeqc. Οι χρόνοι επαγωγής μετρήθηκαν από τα διαγράμματα μεταβολής των συγκεντρώσεων των πλεγματικών ιόντων συναρτήσει του χρόνου. Πίνακας 5.3: Πειραματικές συνθήκες και αποτελέσματα μετρήσεων για την καταβύθιση στρουβίτη σε σταθερά υπέρκορα ως προς στρουβίτη διαλύματα συνθετικού αποβλήτου με την εισαγωγή 1g φύτρων quartz, ph 6.5, 25 ο C C/1-2 M Ω ph σ Log([Mg 2+ ]/M) τ/min R CG/*1-6 molmin -1 g
105 Χρόνος Επαγωγής τ/ min Πίνακας 5.4: Πειραματικές συνθήκες και αποτελέσματα μετρήσεων για την καταβύθιση στρουβίτη σε σταθερά υπέρκορα ως προς στρουβίτη διαλύματα συνθετικού αποβλήτου με την εισαγωγή 2g φύτρων quartz, ph 6.5, 25 ο C C/1-2 M Ω ph σ log[mg 2+ ] τ/min R CG /*1-7 molmin -1 g Στο σχήμα 5.8 απεικονίζεται η εξάρτηση του χρόνου επαγωγής από τον υπερκορεσμό για την καταβύθιση του στρουβίτη από υπέρκορα διαλύματα του για τις δύο διαφορετικές ποσότητες υποστρώματος. Οι χρόνοι επαγωγής παρουσιάζουν εξάρτηση από την ποσότητα του quartz,το οποίο είναι πιο εμφανές σε τιμές υπερκορεσμού Ω< g quartz 1 g quartz ,6 1,8 2, 2,2 2,4 2,6 2,8 Υπερκορεσμός, Ω Σχήμα 5.8: Μεταβολή του χρόνου επαγωγής συναρτήσει του υπερκορεσμού, Ω, ως προς στρουβίτη για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου σε συνθήκες σταθερού ph 6.5, 25 ο C σε υπόστρωμα quartz 2g ( ) και 1g ( ) Στο σχήμα 5.9 από τα διαγράμματα επιβεβαιώθηκε η γραμμική εξάρτηση μεταξύ του λογαρίθμου του χρόνου επαγωγής και του αντίστροφου τετραγώνου του υπερκορεσμού. Από την κλίση των ευθειών υπολογίσθηκε η τιμή της διεπιφανειακής ενέργειας, η οποία και βρέθηκε ίση προς 6 mj. m -2 και για τις δύο ποσότητες φύτρων που χρησιμοποιήθηκαν, γεγονός το οποίο υποδηλώνει ταυτότητα του μηχανισμού και στις δύο περιπτώσεις. 15
106 log τ/min logτ/min ,2 2, 8 1,8 6 1,6 4 1,4 1, /log 2 Ω (α) ,6 2,4 8 2,2 6 2, 4 1,8 2 1, /log 2 Ω (β) Σχήμα 5.9: Μεταβολή του logτ συναρτήσει του 1/log 2 Ω για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα ως προς στρουβίτη διαλύματα συνθετικού αποβλήτου για υπόστρωμα quartz (α) 1g, (β) 2g, ph 6.5, 25 ο C Στο διάγραμμα του σχήματος 5.1 παρουσιάζεται η εξάρτηση του logτ από τον λογάριθμο της συγκέντρωσης των ελεύθερων ιόντων Mg 2+. Ο αριθμός των δομικών μονάδων για 1 και 2gr υποστρώματος είναι p=12 κρίσιμου πυρήνα, p=19 κατά την αυθόρμητη καταβύθιση του στρουβίτη σε ρευστοποιημένη κλίνη. O αριθμός αυτός είναι μικρότερος από τον αντίστοιχο ο οποίος υπολογίσθηκε για την αυθόρμητη καταβύθιση στρουβίτη σε ρευστοποιημένη κλίνη, προφανώς λόγω της παρουσίας του υποστρώματος, το οποίο διευκολύνει την διεργασία. 16
107 log τ/min 2,8 2,6 2,4 2,2 2, 1, g quartz 2g quartz ,6 1,4 2 1,2 1, -1,78-1,76-1,74-1,72-1,7-1,68 log([mg 2+ ]/M) Σχήμα 5.1: Μεταβολή του logτ συναρτήσει του log([mg 2+ ]/Μ) για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα ως προς στρουβίτη διαλύματα συνθετικού αποβλήτου με την εισαγωγή φύτρων quartz 1g ( ) και 2g ( ), ph 6.5, 25 ο C Στο σχήμα 5.11 απεικονίζεται η εξάρτηση του ρυθμού σχηματισμού του στρουβίτη από τον σχετικό υπερκορεσμό και για τις δυο διαφορετικές ποσότητες υποστρωμάτων quartz. O ρυθμός σχηματισμού στρουβίτη μειώθηκε σημαντικά αυξανόμενης της ποσότητας των φύτρων quartz. Η φαινόμενη τάξη της καταβύθισης του στρουβίτη σε υπόστρωμα quartz σε ρευστοποιημένη κλίνη ήταν ίση με n=1 (γραμμική εξάρτηση). Όπως στην περίπτωση των πειραμάτων σε αντιδραστήρα διαλείποντος έργου, έχει επιβραδυντική δράση στη καταβύθιση του στρουβίτη λόγω μερικής διαλυτοποίησης του. Προφανώς τα ιόντα των πυριτικών ειδών παρεμποδίζουν τον ρυθμό κρυσταλλικής ανάπτυξης του στρουβίτη. 17
108 Ρυθμός Καταβύθισης R CG '/ molmin -1 g -1 3,x g SiO 2 2,5x1-6 2g SiO 2 8 2,x1-6 1,5x ,x ,x1-7 2,,15,2,25,3,35,4 Σχετικός Υπερκορεσμός, σ Σχήμα 5.11: Μεταβολή της αρχικής ταχύτητας καταβύθισης, R CG συναρτήσει του σχετικού υπερκορεσμού, σ για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα ως προς στρουβίτη διαλύματα συνθετικού αποβλήτου με την εισαγωγή φύτρων quartz 1g ( ) και 2g ( ) quartz, ph 6.5, 25 ο C Προκειμένου να επιβεβαιωθεί η υπόθεση της επιβραδυντικής δράσης των ιόντων των πυριτικών ειδών στα υπέρκορα, πραγματοποιήθηκε μια νέα σειρά πειραμάτων: Μελετήθηκε η επίδραση της αυξανόμενης συγκέντρωσης πυριτικών για δεδομένη τιμή υπερκορεσμού του διαλύματος εργασίας. Στην σειρά αυτή των πειραμάτων, στα υπέρκορα ως προς στρουβίτη διαλύματα προστέθηκε Na2SiO3 (Sodium Silicate) σε διάφορες συγκεντρώσεις όπως φαίνεται στον πίνακα 5.5. Πίνακας 5.5: Συγκεντρώσεις Si και αρχικοί ρυθμοί καταβύθισης παρουσίας πυριτικών ιόντων κατά την αυθόρμητη καταβύθιση του στρουβίτη σε συνθετικό απόβλητο σε υπερκορεσμό Ω=2.63, ph 6.5, 25 ο C Συγκέντρωση Si/*1-5 M Ri/*1-5 molmin Όπως φαίνεται στο διάγραμμα του σχήματος 5.12 αυξανόμενης της συγκέντρωσης των πυριτικών ειδών ο ρυθμός καταβύθισης μειώνεται. 18
109 Ρυθμός Ri/ molmin -1 5,x ,x ,x ,x ,x1-5 2,, 2,x1-5 4,x1-5 6,x1-5 8,x1-5 1,x1-4 C Si /M Σχήμα 5.12: Εξάρτηση του ρυθμού καταβύθισης στρουβίτη σε αντιδραστήρα διαλείποντος έργου από την συγκέντρωση πυριτικών ιόντων σε υπέρκορα διαλύματα συνθετικού αποβλήτου, υπερκορεσμού Ω=2.63 ph 6.5, 25 ο C Άρα, επιβεβαιώνεται η υπόθεση μας ότι τα ιόντα του πυριτίου που απελευθερώνονται στο διάλυμα από το υπόστρωμα έχουν επιβραδυντική δράση. Η επιβραδυντική δράση των πυριτικών ιόντων κατ αναλογία προς τη δράση ανάλογων αναστολέων, πιθανότατα οφείλεται στην προσρόφηση τους στα ενεργά κέντρα της κρυσταλλικής επιφάνειας. Σύμφωνα με το κινητικό πρότυπο για την κρυσταλλική ανάπτυξη με προσρόφηση τύπου Langmuir, τα δεδομένα είναι δυνατόν να προσαρμοστούν στην εξ Σύμφωνα με αυτή την εξίσωση η γραφική παράσταση του λόγου συναρτήσει του αντιστρόφου της συγκέντρωσης της επιμόλυνσης στο υπέρκορο διάλυμα, δίνει ευθεία γραμμή. Τα δεδομένα της παρούσας εργασίας έδωσαν ικανοποιητική προσαρμογή, όπως φαίνεται στο σχήμα
110 Ένταση R o /(R o -R) 4, ,5 8 3, 2,5 6 2, 4 1,5 2 1, 1x1 4 2x1 4 3x1 4 4x1 4 5x1 4 1/C Si Σχήμα 5.13: Κινητικό πρότυπο με την υπόθεση ρόφησης σύμφωνα με το πρότυπο Langmuir για την αυθόρμητη καταβύθιση του στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου παρουσία πυριτικών ιόντων, ph 6.5, 25 ο C. Ο χαρακτηρισμός των στερεών που σχηματίσθηκαν από σταθερά υπέρκορα διαλύματα ως προς στρουβίτη με φύτρα quartz σε ρευστοποιημένη κλίνη πραγματοποιήθηκε με περιθλασιόγραμμα ακτίνων-χ και ηλεκτρονική μικροσκοπία σάρωσης. Στο σχήμα 5.14 απεικονίζεται το φάσμα περίθλασης ακτίνων-χ του σχηματιζόμενου στερεού με το quartz και του στρουβίτη, τα οποία ταυτίζονται Καταβυθιζόμενη Φάση Στρουβίτης θ 11
111 Σχήμα 5.14: Περιθλασιόγραμμα ακτίνων-χ σχηματιζόμενου στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου με φύτρα quartz. Υπερκορεσμός ως προς στρουβίτη Ω=1.65, σταθερό ph 6.5, 25 o C Στις φωτογραφίες που ακολουθούν στο σχήμα 5.15 απεικονίζεται η μορφολογία των καταβυθιζόμενων κρυστάλλων σε υπόστρωμα quartz σε υπερκορεσμό Ω= 2.45 σε 1g υποστρώματος. Σχήμα 5.15: Φωτογραφίες ηλεκτρονικής σάρωσης (SEM) καταβυθιζόμενων κρυστάλλων στρουβίτη με υπόστρωμα quartz για την καταβύθιση του στρουβίτη σε σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου, ph 6.5, 25 ο C 111
112 Σε υπερκορεσμό Ω= 1.65 σε υπόστρωμα 2g υποστρώματος διοξειδίου του πυριτίου καταβυθίζεται μαζί με στρουβίτη και φωσφορικό μαγνήσιο όπως φαίνεται από τις φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης (SEM) του σχήματος Στη μικροανάλυση ΕDX φαίνεται η παρουσία του αζώτου αλλά δεν είναι συναρμοσμένο στον κρύσταλλο αφού η μορφολογία που παρατηρήθηκε είναι του φωσφορικού μαγνησίου. Θα πρέπει να σημειωθεί ωστόσο, ότι το περιθλασιόγραμμα των ακτίνων Χ, έδειξε τον αποκλειστικό σχηματισμό στρουβίτη. Σχήμα 5.16 : Φωτογραφίες ηλεκτρονικής μικροσκοπίας σάρωσης (SEM) και μικροανάλυση EDX των καταβυθιζόμενων κρυστάλλων στρουβίτη με εισαγωγή 2g quartz σε υπερκορεσμό Ω=1.65 για την καταβύθιση του στρουβίτη από σταθερά υπέρκορα διαλύματα συνθετικού αποβλήτου, ph 6.5, 25 ο C. 112
ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΟΥ ΑΠΟ ΤΑ ΣΤΡΑΓΓΙΣΜΑΤΑ ΤΗΣ ΑΦΥΔΑΤΩΣΗΣ ΙΛΥΟΣ ΜΕΣΩ ΚΑΤΑΚΡΗΜΝΙΣΗΣ ΣΤΡΟΥΒΙΤΗ
 ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΟΥ ΑΠΟ ΤΑ ΣΤΡΑΓΓΙΣΜΑΤΑ ΤΗΣ ΑΦΥΔΑΤΩΣΗΣ ΙΛΥΟΣ ΜΕΣΩ ΚΑΤΑΚΡΗΜΝΙΣΗΣ ΣΤΡΟΥΒΙΤΗ Αλίκη Κόκκα και Ευάγγελος Διαμαντόπουλος Τμήμα Μηχανικών Περιβάλλοντος Πολυτεχνείο Κρήτης PhoReSe: Ανάκτηση Φωσφόρου
ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΟΥ ΑΠΟ ΤΑ ΣΤΡΑΓΓΙΣΜΑΤΑ ΤΗΣ ΑΦΥΔΑΤΩΣΗΣ ΙΛΥΟΣ ΜΕΣΩ ΚΑΤΑΚΡΗΜΝΙΣΗΣ ΣΤΡΟΥΒΙΤΗ Αλίκη Κόκκα και Ευάγγελος Διαμαντόπουλος Τμήμα Μηχανικών Περιβάλλοντος Πολυτεχνείο Κρήτης PhoReSe: Ανάκτηση Φωσφόρου
Ανάκτηση φωσφόρου από επεξεργασμένα αστικά λύματα Αξιολόγηση εναλλακτικών διεργασιών
 Ανάκτηση φωσφόρου από επεξεργασμένα αστικά λύματα Αξιολόγηση εναλλακτικών διεργασιών 1525-ΒΕΤ-2013 PhoReSΕ: Ανάκτηση φωσφόρου από τη δευτεροβάθμια εκροή εγκαταστάσεων επεξεργασίας αστικών λυμάτων ΠΡΑΞΗ
Ανάκτηση φωσφόρου από επεξεργασμένα αστικά λύματα Αξιολόγηση εναλλακτικών διεργασιών 1525-ΒΕΤ-2013 PhoReSΕ: Ανάκτηση φωσφόρου από τη δευτεροβάθμια εκροή εγκαταστάσεων επεξεργασίας αστικών λυμάτων ΠΡΑΞΗ
Χαρακτηρισμός των στερεών ιζημάτων ανάκτησης φωσφόρου Μελέτη βιοδιαθεσιμότητας του παραγόμενου προϊόντος
 ΠΡΑΞΗ ΕΘΝΙΚΗΣ ΕΜΒΕΛΕΙΑΣ «Πρόγραμμα Ανάπτυξης Βιομηχανικής Έρευνας και Τεχνολογίας (ΠΑΒΕΤ) 2013» Δευτέρα 25 Μαΐου, 2015 Ημερίδα - Κ.Ε.Δ.Ε.Α. Θεσσαλονίκη Χαρακτηρισμός των στερεών ιζημάτων ανάκτησης φωσφόρου
ΠΡΑΞΗ ΕΘΝΙΚΗΣ ΕΜΒΕΛΕΙΑΣ «Πρόγραμμα Ανάπτυξης Βιομηχανικής Έρευνας και Τεχνολογίας (ΠΑΒΕΤ) 2013» Δευτέρα 25 Μαΐου, 2015 Ημερίδα - Κ.Ε.Δ.Ε.Α. Θεσσαλονίκη Χαρακτηρισμός των στερεών ιζημάτων ανάκτησης φωσφόρου
Μπούντας Ιωάννης Πανεπιστήμιο Πατρών Τμήμα Χημικών Μηχανικών και ITE/IΕXΜΗ jmpountas@chemeng.upatras.gr
 Ανάκτηση φωσφορικών από αστικά λύματα με τη μορφή MgNH 4 PO 4.6H 2 O (στρουβίτη) Μπούντας Ιωάννης Πανεπιστήμιο Πατρών Τμήμα Χημικών Μηχανικών και ITE/IΕXΜΗ jmpountas@chemeng.upatras.gr Πανεπιστήμιο Πατρών
Ανάκτηση φωσφορικών από αστικά λύματα με τη μορφή MgNH 4 PO 4.6H 2 O (στρουβίτη) Μπούντας Ιωάννης Πανεπιστήμιο Πατρών Τμήμα Χημικών Μηχανικών και ITE/IΕXΜΗ jmpountas@chemeng.upatras.gr Πανεπιστήμιο Πατρών
Πρόλογος Το περιβάλλον Περιβάλλον και οικολογική ισορροπία Η ροή της ενέργειας στο περιβάλλον... 20
 Πίνακας περιεχομένων Πρόλογος... 7 1. Το περιβάλλον... 19 1.1 Περιβάλλον και οικολογική ισορροπία... 19 1.2 Η ροή της ενέργειας στο περιβάλλον... 20 2. Οι μικροοργανισμοί... 22 2.1 Γενικά... 22 2.2 Ταξινόμηση
Πίνακας περιεχομένων Πρόλογος... 7 1. Το περιβάλλον... 19 1.1 Περιβάλλον και οικολογική ισορροπία... 19 1.2 Η ροή της ενέργειας στο περιβάλλον... 20 2. Οι μικροοργανισμοί... 22 2.1 Γενικά... 22 2.2 Ταξινόμηση
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (1) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΕΙΣΑΓΩΓΗ (1) Αφορά ετερογενείς ισορροπίες µεταξύ δυσδιάλυτων ηλεκτρολυτών και των ιόντων τους σε κορεσµένα
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5
 ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
ΕΝΟΤΗΤΑ ΕΡΓΑΣΙΑΣ (Ε.Ε.) 5 Μοντελοποίηση της ροής σε ένα πόρο μεταβλητής γεωμετρίας και σε τρισδιάστατα δίκτυα παρουσία νερού ή οργανικής φάσης Ε.Ε. 5.1. : Μοντελοποίηση της ροής σε ένα πόρο απλής και μεταβλητής
Διάλεξη 5. Δευτεροβάθμια ή Βιολογική Επεξεργασία Υγρών Αποβλήτων - Συστήματα Βιολογικών Κροκύδων - Σύστημα Ενεργοποιημένης Λάσπης
 Διάλεξη 5 Δευτεροβάθμια ή Βιολογική Επεξεργασία Υγρών Αποβλήτων - Συστήματα Βιολογικών Κροκύδων - Σύστημα Ενεργοποιημένης Λάσπης Στάδια Επεξεργασίας Υγρών Αποβλήτων Πρωτοβάθμια ή Μηχανική Επεξεργασία Δευτεροβάθμια
Διάλεξη 5 Δευτεροβάθμια ή Βιολογική Επεξεργασία Υγρών Αποβλήτων - Συστήματα Βιολογικών Κροκύδων - Σύστημα Ενεργοποιημένης Λάσπης Στάδια Επεξεργασίας Υγρών Αποβλήτων Πρωτοβάθμια ή Μηχανική Επεξεργασία Δευτεροβάθμια
ΑΝΤΙΔΡΑΣΤΗΡΕΣ ΕΙΣΑΓΩΓΗ
 ΑΝΤΙΔΡΑΣΤΗΡΕΣ ΕΙΣΑΓΩΓΗ TM150 Διαχείριση περιβάλλοντος Θεωρούμε ως χημικό αντιδραστήρα κάθε συσκευή όπου συμβαίνει μια αντίδραση (χημική ή βιοχημική). Η χημική ή βιοχημική αντίδραση Σχεδιασμός χημικού αντιδραστήρα
ΑΝΤΙΔΡΑΣΤΗΡΕΣ ΕΙΣΑΓΩΓΗ TM150 Διαχείριση περιβάλλοντος Θεωρούμε ως χημικό αντιδραστήρα κάθε συσκευή όπου συμβαίνει μια αντίδραση (χημική ή βιοχημική). Η χημική ή βιοχημική αντίδραση Σχεδιασμός χημικού αντιδραστήρα
Ορισμός το. φλψ Στάδια επεξεργασίας λυμάτων ΘΕΜΑ: ΒΙΟΛΟΓΙΚΟΣ ΚΑΘΑΡΙΣΜΟΣ ΣΤΗΝ ΚΩ ΤΙ ΕΙΝΑΙ Ο ΒΙΟΛΟΓΙΚΟΣ ΚΑΘΑΡΙΣΜΟΣ?
 ΘΕΜΑ: ΒΙΟΛΟΓΙΚΟΣ ΚΑΘΑΡΙΣΜΟΣ ΣΤΗΝ ΚΩ ΤΙ ΕΙΝΑΙ Ο ΒΙΟΛΟΓΙΚΟΣ ΚΑΘΑΡΙΣΜΟΣ? Ο βιολογικος καθαρισμος αφορα την επεξεργασια λυματων, δηλαδη τη διαδικασια μεσω της οποιας διαχωριζονται οι μολυσματικες ουσιες από
ΘΕΜΑ: ΒΙΟΛΟΓΙΚΟΣ ΚΑΘΑΡΙΣΜΟΣ ΣΤΗΝ ΚΩ ΤΙ ΕΙΝΑΙ Ο ΒΙΟΛΟΓΙΚΟΣ ΚΑΘΑΡΙΣΜΟΣ? Ο βιολογικος καθαρισμος αφορα την επεξεργασια λυματων, δηλαδη τη διαδικασια μεσω της οποιας διαχωριζονται οι μολυσματικες ουσιες από
Η βιολογική κατάλυση παρουσιάζει παρουσιάζει ορισμένες ορισμένες ιδιαιτερότητες ιδιαιτερότητες σε
 Η βιολογική κατάλυση παρουσιάζει ορισμένες ιδιαιτερότητες σε σχέση με τη μη βιολογική που οφείλονται στη φύση των βιοκαταλυτών Οι ιδιαιτερότητες αυτές πρέπει να παίρνονται σοβαρά υπ όψη κατά το σχεδιασμό
Η βιολογική κατάλυση παρουσιάζει ορισμένες ιδιαιτερότητες σε σχέση με τη μη βιολογική που οφείλονται στη φύση των βιοκαταλυτών Οι ιδιαιτερότητες αυτές πρέπει να παίρνονται σοβαρά υπ όψη κατά το σχεδιασμό
Έλεγχος Σχηματισμού Στρουβίτη σε Αναερόβιους Χωνευτές με Προσθήκη FeCl 3. Βραγγάλας Κωνσταντίνος Επιβλέπων: Καθηγητής Δ. Μαμάης Αθήνα Οκτώβριος 2008
 Έλεγχος Σχηματισμού Στρουβίτη σε Αναερόβιους Χωνευτές με Προσθήκη FeCl 3 Βραγγάλας Κωνσταντίνος Επιβλέπων: Καθηγητής Δ. Μαμάης Αθήνα Οκτώβριος 2008 Ονομασία - Προέλευση Ένυδρο Εναμμώνιο Φωσφορικό Μαγνήσιο
Έλεγχος Σχηματισμού Στρουβίτη σε Αναερόβιους Χωνευτές με Προσθήκη FeCl 3 Βραγγάλας Κωνσταντίνος Επιβλέπων: Καθηγητής Δ. Μαμάης Αθήνα Οκτώβριος 2008 Ονομασία - Προέλευση Ένυδρο Εναμμώνιο Φωσφορικό Μαγνήσιο
Επίκουρος Καθηγητής Π. Μελίδης
 Χαρακτηριστικά υγρών αποβλήτων Επίκουρος Καθηγητής Π. Μελίδης Τμήμα Μηχανικών Περιβάλλοντος Εργαστήριο Διαχείρισης και Τεχνολογίας Υγρών Αποβλήτων Τα υγρά απόβλητα μπορεί να προέλθουν από : Ανθρώπινα απόβλητα
Χαρακτηριστικά υγρών αποβλήτων Επίκουρος Καθηγητής Π. Μελίδης Τμήμα Μηχανικών Περιβάλλοντος Εργαστήριο Διαχείρισης και Τεχνολογίας Υγρών Αποβλήτων Τα υγρά απόβλητα μπορεί να προέλθουν από : Ανθρώπινα απόβλητα
ΠΡΟΤΥΠΟ ΠΕΙΡΑΜΑΤΙΚΟ ΛΥΚΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΠΑΤΡΩΝ 2013-14
 ΘΕΜΑΤΑ ΟΙΚΟΛΟΓΙΑΣ Μπορεί να λειτουργήσει ένα οικοσύστημα α) με παραγωγούς και καταναλωτές; β) με παραγωγούς και αποικοδομητές; γ)με καταναλωτές και αποικοδομητές; Η διατήρηση των οικοσυστημάτων προϋποθέτει
ΘΕΜΑΤΑ ΟΙΚΟΛΟΓΙΑΣ Μπορεί να λειτουργήσει ένα οικοσύστημα α) με παραγωγούς και καταναλωτές; β) με παραγωγούς και αποικοδομητές; γ)με καταναλωτές και αποικοδομητές; Η διατήρηση των οικοσυστημάτων προϋποθέτει
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 11 η : Χημική ισορροπία. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 11 η : Χημική ισορροπία Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Η Κατάσταση Ισορροπίας 2 Πολλές αντιδράσεις δεν πραγματοποιούνται
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 11 η : Χημική ισορροπία Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Η Κατάσταση Ισορροπίας 2 Πολλές αντιδράσεις δεν πραγματοποιούνται
Εργασία στο μάθημα: ΟΙΚΟΛΟΓΙΑ ΓΙΑ ΜΗΧΑΝΙΚΟΥΣ. Θέμα: ΕΥΤΡΟΦΙΣΜΟΣ
 ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργασία στο μάθημα: ΟΙΚΟΛΟΓΙΑ ΓΙΑ ΜΗΧΑΝΙΚΟΥΣ Θέμα: ΕΥΤΡΟΦΙΣΜΟΣ 1 Ονομ/μο φοιτήτριας: Κουκουλιάντα Στυλιανή Αριθμός μητρώου: 7533 Υπεύθυνος καθηγητής:
ΔΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΠΟΛΙΤΙΚΩΝ ΜΗΧΑΝΙΚΩΝ Εργασία στο μάθημα: ΟΙΚΟΛΟΓΙΑ ΓΙΑ ΜΗΧΑΝΙΚΟΥΣ Θέμα: ΕΥΤΡΟΦΙΣΜΟΣ 1 Ονομ/μο φοιτήτριας: Κουκουλιάντα Στυλιανή Αριθμός μητρώου: 7533 Υπεύθυνος καθηγητής:
2.4 Ρύπανση του νερού
 1 Η θεωρία του μαθήματος με ερωτήσεις 2.4 Ρύπανση του νερού 4-1. Ποια ονομάζονται λύματα; Έτσι ονομάζονται τα υγρά απόβλητα από τις κατοικίες, τις βιομηχανίες, τις βιοτεχνίες και τους αγρούς. 4-2. Ποιοι
1 Η θεωρία του μαθήματος με ερωτήσεις 2.4 Ρύπανση του νερού 4-1. Ποια ονομάζονται λύματα; Έτσι ονομάζονται τα υγρά απόβλητα από τις κατοικίες, τις βιομηχανίες, τις βιοτεχνίες και τους αγρούς. 4-2. Ποιοι
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΑΞΙΟΛΟΓΗΣΗ ΤΟΥ ΚΙΝΔΥΝΟΥ ΥΠΟΒΑΘΜΙΣΗΣ ΤΟΥ ΥΔΡΟΒΙΟΤΟΠΟΥ ΤΗΣ ΑΛΥΚΗΣ ΛΑΡΝΑΚΑΣ ΑΠΟ ΤΗΝ ΕΠΙΦΑΝΕΙΑΚΗ ΑΠΟΡΡΟΗ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή εργασία ΑΞΙΟΛΟΓΗΣΗ ΤΟΥ ΚΙΝΔΥΝΟΥ ΥΠΟΒΑΘΜΙΣΗΣ ΤΟΥ ΥΔΡΟΒΙΟΤΟΠΟΥ ΤΗΣ ΑΛΥΚΗΣ ΛΑΡΝΑΚΑΣ ΑΠΟ ΤΗΝ ΕΠΙΦΑΝΕΙΑΚΗ ΑΠΟΡΡΟΗ
COMPACT ΜΟΝΑΔΕΣ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ
 COMPACT ΜΟΝΑΔΕΣ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ με τη μέθοδο SBR COMPACT ΜΟΝΑΔΕΣ ΒΙ ΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ Η εταιρεία ΣΥΡΜΕΤ ΜΟΝ. Ε.Π.Ε. με την πολύχρονη εμπειρία της στο χώρο της επεξεργασίας λυμάτων, προσφέρει
COMPACT ΜΟΝΑΔΕΣ ΒΙΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ με τη μέθοδο SBR COMPACT ΜΟΝΑΔΕΣ ΒΙ ΟΛΟΓΙΚΗΣ ΕΠΕΞΕΡΓΑΣΙΑΣ Η εταιρεία ΣΥΡΜΕΤ ΜΟΝ. Ε.Π.Ε. με την πολύχρονη εμπειρία της στο χώρο της επεξεργασίας λυμάτων, προσφέρει
Ποιοτικά Χαρακτηριστικά Λυµάτων
 Ποιοτικά Χαρακτηριστικά Λυµάτων µπορούν να καταταχθούν σε τρεις κατηγορίες: Φυσικά Χηµικά Βιολογικά. Πολλές από τις παραµέτρους που ανήκουν στις κατηγορίες αυτές αλληλεξαρτώνται π.χ. η θερµοκρασία που
Ποιοτικά Χαρακτηριστικά Λυµάτων µπορούν να καταταχθούν σε τρεις κατηγορίες: Φυσικά Χηµικά Βιολογικά. Πολλές από τις παραµέτρους που ανήκουν στις κατηγορίες αυτές αλληλεξαρτώνται π.χ. η θερµοκρασία που
Ζουμπούλης Αναστάσιος
 ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΟΥ ΑΠΟ ΤΗ ΔΕΥΤΕΡΟΒΑΘΜΙΑ ΕΚΡΟΗ ΕΓΚΑΤΑΣΤΑΣΕΩΝ ΕΠΕΞΕΡΓΑΣΙΑΣ ΑΣΤΙΚΩΝ ΛΥΜΑΤΩΝ ΓΕΝΙΚΗ ΠΕΡΙΓΡΑΦΗ ΤΟΥ ΕΡΕΥΝΗΤΙΚΟΥ ΕΡΓΟΥ PhoReSE Ζουμπούλης Αναστάσιος Καθηγητής Περιβαλλοντικής Χημείας και Χημικής
ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΟΥ ΑΠΟ ΤΗ ΔΕΥΤΕΡΟΒΑΘΜΙΑ ΕΚΡΟΗ ΕΓΚΑΤΑΣΤΑΣΕΩΝ ΕΠΕΞΕΡΓΑΣΙΑΣ ΑΣΤΙΚΩΝ ΛΥΜΑΤΩΝ ΓΕΝΙΚΗ ΠΕΡΙΓΡΑΦΗ ΤΟΥ ΕΡΕΥΝΗΤΙΚΟΥ ΕΡΓΟΥ PhoReSE Ζουμπούλης Αναστάσιος Καθηγητής Περιβαλλοντικής Χημείας και Χημικής
Για την αντιμετώπιση του προβλήματος της διάθεσης των παραπάνω αποβλήτων, τα Ελληνικά τυροκομεία ως επί το πλείστον:
 Ο κλάδος της τυροκόμησης είναι παραδοσιακά ο κλάδος με τη μικρότερη απόδοση προϊόντων σε σχέση με την πρώτη ύλη. Για κάθε τόνο γάλακτος παράγονται περίπου 350 κιλά προϊόντος και περίπου 2,6 τόνοι απόβλητα
Ο κλάδος της τυροκόμησης είναι παραδοσιακά ο κλάδος με τη μικρότερη απόδοση προϊόντων σε σχέση με την πρώτη ύλη. Για κάθε τόνο γάλακτος παράγονται περίπου 350 κιλά προϊόντος και περίπου 2,6 τόνοι απόβλητα
ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ ΠΡΟΪΟΝ
 Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ
Σχολή Γεωτεχνικών Επιστημών και Διαχείρισης Περιβάλλοντος Πτυχιακή εργασία ΑΠΟΜΑΚΡΥΝΣΗ ΜΕΓΑΛΩΝ ΣΥΓΚΕΝΤΡΩΣΕΩΝ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΠΟΒΛΗΤΑ ΧΡΗΣΙΜΟΠΟΙΩΝΤΑΣ ΔΙΑΠΥΡΩΜΕΝΑ ΤΣΟΦΛΙΑ ΑΥΓΩΝ ΚΑΙ Η ΣΥΝΘΕΣΗ BRUSHITE ΩΣ ΤΕΛΙΚΟ
ΠΡΟΤΑΣΗ ΕΦΑΡΜΟΓΗΣ. aquabio.gr ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ AQUABIO SBR ΓΙΑ ΤΗΝ ΕΠΕΞΕΡΓΑΣΙΑ ΛΥΜΑΤΩΝ ΞΕΝΟΔΟΧΕΙΑΚΩΝ ΣΥΓΚΡΟΤΗΜΑΤΩΝ ΜΙΚΡΗΣ ΔΥΝΑΜΙΚΟΤΗΤΑΣ
 aquabio.gr Αντώνης Χουρδάκης & ΣΙΑ Ε.Ε. a.chourdakis@aquabio.gr Διδώς Σωτηρίου 15, Ηράκλειο, 71305 τηλ.: (+30) 2810 372 899 κιν.: (+30) 697 22 22 981 fax: (+30) 2810 372 901 ΠΡΟΤΑΣΗ ΕΦΑΡΜΟΓΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ
aquabio.gr Αντώνης Χουρδάκης & ΣΙΑ Ε.Ε. a.chourdakis@aquabio.gr Διδώς Σωτηρίου 15, Ηράκλειο, 71305 τηλ.: (+30) 2810 372 899 κιν.: (+30) 697 22 22 981 fax: (+30) 2810 372 901 ΠΡΟΤΑΣΗ ΕΦΑΡΜΟΓΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ
ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ
 ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ Η αξιοποίηση της γεωθερμικής ενέργειας συναντά ορισμένα τεχνικά προβλήματα, Τα προβλήματα αυτά είναι: (α) ο σχηματισμός επικαθίσεων (ή καθαλατώσεις
ΤΕΧΝΙΚΑ ΠΡΟΒΛΗΜΑΤΑ ΚΑΤΑ ΤΗΝ ΑΞΙΟΠΟΙΗΣΗ ΤΗΣ ΓΕΩΘΕΡΜΙΑΣ Η αξιοποίηση της γεωθερμικής ενέργειας συναντά ορισμένα τεχνικά προβλήματα, Τα προβλήματα αυτά είναι: (α) ο σχηματισμός επικαθίσεων (ή καθαλατώσεις
ΑΠΟΜΑΚΡΥΝΣΗ ΟΡΓΑΝΙΚΟΥ ΑΖΩΤΟΥ από υγρά βιομηχανικά απόβλητα
 ΑΠΟΜΑΚΡΥΝΣΗ ΟΡΓΑΝΙΚΟΥ ΑΖΩΤΟΥ από υγρά βιομηχανικά απόβλητα Βλυσίδης Απόστολος Καθηγητής ΕΜΠ Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης reative ommons. Για εκπαιδευτικό υλικό, όπως
ΑΠΟΜΑΚΡΥΝΣΗ ΟΡΓΑΝΙΚΟΥ ΑΖΩΤΟΥ από υγρά βιομηχανικά απόβλητα Βλυσίδης Απόστολος Καθηγητής ΕΜΠ Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης reative ommons. Για εκπαιδευτικό υλικό, όπως
ΜΑΘΗΜΑ: ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΠΕΞΕΡΓΑΣΙΑΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΕΡΓΑΣΙΕΣ
 ΜΑΘΗΜΑ: ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΠΕΞΕΡΓΑΣΙΑΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΕΡΓΑΣΙΕΣ Υποβοηθητική Άσκηση-Χρήση ημιαντιδράσεων (υποχρεωτική η υποβολή για όσους δεν επέλεξαν το μάθημα Βιοχημικές Διεργασίες στο υδάτινο Περιβάλλον)
ΜΑΘΗΜΑ: ΠΡΟΧΩΡΗΜΕΝΕΣ ΜΕΘΟΔΟΙ ΕΠΕΞΕΡΓΑΣΙΑΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΕΡΓΑΣΙΕΣ Υποβοηθητική Άσκηση-Χρήση ημιαντιδράσεων (υποχρεωτική η υποβολή για όσους δεν επέλεξαν το μάθημα Βιοχημικές Διεργασίες στο υδάτινο Περιβάλλον)
Τα βασικά της διεργασίας της
 Τα βασικά της διεργασίας της ενεργού ιλύος Επίκουρος Καθηγητής Π. Μελίδης Τμήμα Μηχανικών Περιβάλλοντος Εργαστήριο Διαχείρισης και Τεχνολογίας Υγρών Αποβλήτων 1 Γιατί είναι απαραίτητη η επεξεργασία Για
Τα βασικά της διεργασίας της ενεργού ιλύος Επίκουρος Καθηγητής Π. Μελίδης Τμήμα Μηχανικών Περιβάλλοντος Εργαστήριο Διαχείρισης και Τεχνολογίας Υγρών Αποβλήτων 1 Γιατί είναι απαραίτητη η επεξεργασία Για
ΑΠΟΜΑΚΡΥΝΣΗ ΦΩΣΦΟΡΟΥ από υγρά βιομηχανικά απόβλητα
 ΑΠΟΜΑΚΡΥΝΣΗ ΦΩΣΦΟΡΟΥ από υγρά βιομηχανικά απόβλητα Βλυσίδης Απόστολος Καθηγητής ΕΜΠ Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό υλικό, όπως εικόνες,
ΑΠΟΜΑΚΡΥΝΣΗ ΦΩΣΦΟΡΟΥ από υγρά βιομηχανικά απόβλητα Βλυσίδης Απόστολος Καθηγητής ΕΜΠ Άδεια Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό υλικό, όπως εικόνες,
Κροκίδωση Συσσωμάτωση Χημική κατακρήμνιση Πηγή: Μαρία Λοϊζίδου, ΕΜΠ, Αθήνα 2006
 Κροκίδωση Συσσωμάτωση Χημική κατακρήμνιση Πηγή: Μαρία Λοϊζίδου, ΕΜΠ, Αθήνα 2006 Η χημική κατακρήμνιση βασίζεται στη λειτουργία της συσσωμάτωσης και κροκίδωσης των κολλοειδών σωματιδίων που υπάρχουν αρχικά
Κροκίδωση Συσσωμάτωση Χημική κατακρήμνιση Πηγή: Μαρία Λοϊζίδου, ΕΜΠ, Αθήνα 2006 Η χημική κατακρήμνιση βασίζεται στη λειτουργία της συσσωμάτωσης και κροκίδωσης των κολλοειδών σωματιδίων που υπάρχουν αρχικά
Χημεία και Τεχνολογία Υλικών
 Χημεία και Τεχνολογία Υλικών Σύνθεση στερεών καταλυτών Χρήστος Κορδούλης Καταλύτες Σώματα που επιταχύνουν επιθυμητές χημικές αντιδράσεις χωρίς τα ίδια να καταναλώνονται Καταλυτικός Μετατροπέας 2 CO + O
Χημεία και Τεχνολογία Υλικών Σύνθεση στερεών καταλυτών Χρήστος Κορδούλης Καταλύτες Σώματα που επιταχύνουν επιθυμητές χημικές αντιδράσεις χωρίς τα ίδια να καταναλώνονται Καταλυτικός Μετατροπέας 2 CO + O
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων. Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης
 Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
Να σχεδιάστε ένα τυπικό διάγραμμα ροής μιας εγκατάστασης επεξεργασίας αστικών λυμάτων και να περιγράψτε τη σημασία των επιμέρους σταδίων.
 Τεχνολογία και Διαχείριση Υγρών Αποβλήτων Ι Ακαδημαϊκό έτος 2017-2018 Σημαντικά ζητήματα μαθήματος (Β. Διαμαντής) Βασικές αρχές Από τι αποτελούνται τα αστικά λύματα? Ποιες είναι οι τυπικές συγκεντρώσεις
Τεχνολογία και Διαχείριση Υγρών Αποβλήτων Ι Ακαδημαϊκό έτος 2017-2018 Σημαντικά ζητήματα μαθήματος (Β. Διαμαντής) Βασικές αρχές Από τι αποτελούνται τα αστικά λύματα? Ποιες είναι οι τυπικές συγκεντρώσεις
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες
 Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Χημικές αντιδράσεις καταλυμένες από στερεούς καταλύτες Σε πολλές χημικές αντιδράσεις, οι ταχύτητές τους επηρεάζονται από κάποια συστατικά τα οποία δεν είναι ούτε αντιδρώντα ούτε προϊόντα. Αυτά τα υλικά
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
Προσδιορισμός φυσικοχημικών παραμέτρων υγρών αποβλήτων και υδάτων
 Προσδιορισμός φυσικοχημικών παραμέτρων υγρών αποβλήτων και υδάτων (DO - BOD - COD - TOC) Χ. Βασιλάτος Οργανική ύλη Αποξυγόνωση επιφανειακών και υπογείων υδάτων Οι οργανικές ύλες αποτελούν πολύ σοβαρό ρύπο,
Προσδιορισμός φυσικοχημικών παραμέτρων υγρών αποβλήτων και υδάτων (DO - BOD - COD - TOC) Χ. Βασιλάτος Οργανική ύλη Αποξυγόνωση επιφανειακών και υπογείων υδάτων Οι οργανικές ύλες αποτελούν πολύ σοβαρό ρύπο,
Διαχείριση και Τεχνολογίες Επεξεργασίας Αποβλήτων
 Διαχείριση και Τεχνολογίες Επεξεργασίας Αποβλήτων Απόβλητα Ν. 1650/1986 Απόβλητο θεωρείται κάθε ποσότητα ουσιών, θορύβου, αντικειμένων ή άλλων μορφών ενέργειας σε οποιαδήποτε φυσική κατάσταση από τις οποίες
Διαχείριση και Τεχνολογίες Επεξεργασίας Αποβλήτων Απόβλητα Ν. 1650/1986 Απόβλητο θεωρείται κάθε ποσότητα ουσιών, θορύβου, αντικειμένων ή άλλων μορφών ενέργειας σε οποιαδήποτε φυσική κατάσταση από τις οποίες
Όσα υγρά απόβλητα μπορούν να επαναχρησιμοποιηθούν, πρέπει να υποστούν
 7. Επαναχρησιμοποίηση νερού στο δήμο μας! Όσα υγρά απόβλητα μπορούν να επαναχρησιμοποιηθούν, πρέπει να υποστούν επεξεργασία πριν την επανάχρησή τους. Ο βαθμός επεξεργασίας εξαρτάται από την χρήση για την
7. Επαναχρησιμοποίηση νερού στο δήμο μας! Όσα υγρά απόβλητα μπορούν να επαναχρησιμοποιηθούν, πρέπει να υποστούν επεξεργασία πριν την επανάχρησή τους. Ο βαθμός επεξεργασίας εξαρτάται από την χρήση για την
Διαχείριση Αποβλήτων
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ Διαχείριση Αποβλήτων Ενότητα 11 : Βιομηχανικά Στερεά και Υγρά Απόβλητα Δρ. Σταυρούλα Τσιτσιφλή Τμήμα Μηχανικών Χωροταξίας, Πολεοδομίας και Περιφερειακής Ανάπτυξης Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ Διαχείριση Αποβλήτων Ενότητα 11 : Βιομηχανικά Στερεά και Υγρά Απόβλητα Δρ. Σταυρούλα Τσιτσιφλή Τμήμα Μηχανικών Χωροταξίας, Πολεοδομίας και Περιφερειακής Ανάπτυξης Άδειες Χρήσης Το
Επίπλευση με αέρα (Dissolved Air Flotation)
 Επίπλευση με αέρα (Dissolved Air Flotation) Προσκόλληση των στερεών σε αιώρηση πάνω σε ανερχόμενες φυσαλλίδες αέρα Πολλές και μικρές Αποσυμπίεση αέρα από υψηλότερη πίεση στην ατμοσφαιρική Σύγκρουση φυσαλλίδων/στερεών
Επίπλευση με αέρα (Dissolved Air Flotation) Προσκόλληση των στερεών σε αιώρηση πάνω σε ανερχόμενες φυσαλλίδες αέρα Πολλές και μικρές Αποσυμπίεση αέρα από υψηλότερη πίεση στην ατμοσφαιρική Σύγκρουση φυσαλλίδων/στερεών
E.E.4 Πειράματα σε κλίνες με κοκκώδες υλικό Διάρκεια: 12 μήνες Έναρξη: 4 ος μήνας- Λήξη 15 ος μήνας
 E.E.4 Πειράματα σε κλίνες με κοκκώδες υλικό Διάρκεια: 12 μήνες Έναρξη: 4 ος μήνας- Λήξη 15 ος μήνας Τίτλος Παραδοτέου: Πειράματα σε κλίνες άμμου Κατάσταση Παραδοτέου: Σε εξέλιξη 1 ΠΕΡΙΛΗΨΗ Στην Ε.Ε.4 πραγματοποιήθηκαν
E.E.4 Πειράματα σε κλίνες με κοκκώδες υλικό Διάρκεια: 12 μήνες Έναρξη: 4 ος μήνας- Λήξη 15 ος μήνας Τίτλος Παραδοτέου: Πειράματα σε κλίνες άμμου Κατάσταση Παραδοτέου: Σε εξέλιξη 1 ΠΕΡΙΛΗΨΗ Στην Ε.Ε.4 πραγματοποιήθηκαν
7. Βιοτεχνολογία. α) η διαθεσιμότητα θρεπτικών συστατικών στο θρεπτικό υλικό, β) το ph, γ) το Ο 2 και δ) η θερμοκρασία.
 7. Βιοτεχνολογία Εισαγωγή Τι είναι η Βιοτεχνολογία; Η Βιοτεχνολογία αποτελεί συνδυασμό επιστήμης και τεχνολογίας. Ειδικότερα εφαρμόζει τις γνώσεις που έχουν αποκτηθεί για τις βιολογικές λειτουργίες των
7. Βιοτεχνολογία Εισαγωγή Τι είναι η Βιοτεχνολογία; Η Βιοτεχνολογία αποτελεί συνδυασμό επιστήμης και τεχνολογίας. Ειδικότερα εφαρμόζει τις γνώσεις που έχουν αποκτηθεί για τις βιολογικές λειτουργίες των
Βελτίωση αναερόβιων χωνευτών και αντιδραστήρων µεθανογένεσης
 Βελτίωση αναερόβιων χωνευτών και αντιδραστήρων µεθανογένεσης Τι είναι; BI-CHEM XP146 βιο-ενζυµατικό προϊόν σε σκόνη που περιέχει: Ένζυµα: τύποι πρωτεάσης, αµυλάσης, κυτταρινάσης και λιπάσης Αναερόβια βακτήρια
Βελτίωση αναερόβιων χωνευτών και αντιδραστήρων µεθανογένεσης Τι είναι; BI-CHEM XP146 βιο-ενζυµατικό προϊόν σε σκόνη που περιέχει: Ένζυµα: τύποι πρωτεάσης, αµυλάσης, κυτταρινάσης και λιπάσης Αναερόβια βακτήρια
Υδατικοί Πόροι -Ρύπανση
 Υδατικοί Πόροι -Ρύπανση Γήινη επιφάνεια Κατανομή υδάτων Υδάτινο στοιχείο 71% Ωκεανοί αλμυρό νερό 97% Γλυκό νερό 3% Εκμεταλλεύσιμο νερό 0,01% Γλυκό νερό 3% Παγόβουνα Υπόγεια ύδατα 2,99% Εκμεταλλεύσιμο νερό
Υδατικοί Πόροι -Ρύπανση Γήινη επιφάνεια Κατανομή υδάτων Υδάτινο στοιχείο 71% Ωκεανοί αλμυρό νερό 97% Γλυκό νερό 3% Εκμεταλλεύσιμο νερό 0,01% Γλυκό νερό 3% Παγόβουνα Υπόγεια ύδατα 2,99% Εκμεταλλεύσιμο νερό
Τεχνική Περιβάλλοντος
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 4: Αμμοσυλλέκτες Ευθύμιος Νταρακάς Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 4: Αμμοσυλλέκτες Ευθύμιος Νταρακάς Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για
Φοιτητες: Σαμακός Φώτιος Παναγιώτης 7442 Ζάπρης Αδαμάντης 7458
 Φοιτητες: Σαμακός Φώτιος Παναγιώτης 7442 Ζάπρης Αδαμάντης 7458 1.ΕΙΣΑΓΩΓΗ 2.ΣΤΟΙΧΕΙΑΡΥΠΑΝΣΗΣ 2.1 ΠΑΘΟΦΟΝΟΙ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΙ 2.1.1 ΒΑΚΤΗΡΙΑ 2.1.2 ΙΟΙ 2.1.3 ΠΡΩΤΟΖΩΑ 2.2 ΑΝΟΡΓΑΝΕΣ ΚΑΙ ΟΡΓΑΝΙΚΕΣ ΔΙΑΛΥΤΕΣ ΣΤΟ
Φοιτητες: Σαμακός Φώτιος Παναγιώτης 7442 Ζάπρης Αδαμάντης 7458 1.ΕΙΣΑΓΩΓΗ 2.ΣΤΟΙΧΕΙΑΡΥΠΑΝΣΗΣ 2.1 ΠΑΘΟΦΟΝΟΙ ΜΙΚΡΟΟΡΓΑΝΙΣΜΟΙ 2.1.1 ΒΑΚΤΗΡΙΑ 2.1.2 ΙΟΙ 2.1.3 ΠΡΩΤΟΖΩΑ 2.2 ΑΝΟΡΓΑΝΕΣ ΚΑΙ ΟΡΓΑΝΙΚΕΣ ΔΙΑΛΥΤΕΣ ΣΤΟ
Ανάκτηση φωσφόρου από Υδατικά Απόβλητα με Κρυστάλλωση. Ο ρόλος Ανιοντικών και Κατιοντικών Ρύπων.
 ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΙΣ ΠΕΡΙΒΑΛΛΟΝΤΙΚΕΣ ΕΠΙΣΤΗΜΕΣ Μεταπτυχιακή εργασία Ανάκτηση φωσφόρου από Υδατικά Απόβλητα με Κρυστάλλωση. Ο ρόλος Ανιοντικών και Κατιοντικών Ρύπων. Νίκος Χατζηπέτρος
ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΙΣ ΠΕΡΙΒΑΛΛΟΝΤΙΚΕΣ ΕΠΙΣΤΗΜΕΣ Μεταπτυχιακή εργασία Ανάκτηση φωσφόρου από Υδατικά Απόβλητα με Κρυστάλλωση. Ο ρόλος Ανιοντικών και Κατιοντικών Ρύπων. Νίκος Χατζηπέτρος
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΚΑΙ ΒΙΟΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ
 ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΚΑΙ ΒΙΟΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Διδάσκοντες:Ν. Καλογεράκης Π. Παναγιωτοπούλου Γραφείο: K.9 Email: ppanagiotopoulou@isc.tuc.gr Μέρες/Ώρες διδασκαλίας: Δευτέρα (.-3.)-Τρίτη (.-3.) ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΚΑΙ ΒΙΟΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Διδάσκοντες:Ν. Καλογεράκης Π. Παναγιωτοπούλου Γραφείο: K.9 Email: ppanagiotopoulou@isc.tuc.gr Μέρες/Ώρες διδασκαλίας: Δευτέρα (.-3.)-Τρίτη (.-3.) ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ
ΑΠΟΧΕΤΕΥΣΗ. Λεοτσινίδης Μιχάλης Καθηγητής Υγιεινής
 ΑΠΟΧΕΤΕΥΣΗ Λεοτσινίδης Μιχάλης Καθηγητής Υγιεινής ΑΠΟΧΕΤΕΥΣΗ Το σύστημα που απομακρύνει τα ακάθαρτα νερά από το περιβάλλον που ζει και εργάζεται ο άνθρωπος και τα διαθέτει τελικά, με τρόπο υγιεινό και
ΑΠΟΧΕΤΕΥΣΗ Λεοτσινίδης Μιχάλης Καθηγητής Υγιεινής ΑΠΟΧΕΤΕΥΣΗ Το σύστημα που απομακρύνει τα ακάθαρτα νερά από το περιβάλλον που ζει και εργάζεται ο άνθρωπος και τα διαθέτει τελικά, με τρόπο υγιεινό και
ΥΔΑΤΙΝΗ ΡΥΠΑΝΣΗ ΥΔΑΤΙΝΗ ΡΥΠΑΝΣΗ-ΟΡΙΣΜΟΣ
 Τι είναι ρύπανση: Ρύπανση μπορεί να θεωρηθεί η δυσμενής μεταβολή των φυσικοχημικών ή βιολογικών συνθηκών ενός συγκεκριμένου περιβάλλοντος ή/και η βραχυπρόθεσμη ή μακροπρόθεσμη βλάβη στην ευζωία, την ποιότητα
Τι είναι ρύπανση: Ρύπανση μπορεί να θεωρηθεί η δυσμενής μεταβολή των φυσικοχημικών ή βιολογικών συνθηκών ενός συγκεκριμένου περιβάλλοντος ή/και η βραχυπρόθεσμη ή μακροπρόθεσμη βλάβη στην ευζωία, την ποιότητα
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (2) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (2) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΤΗΤΑΣ (1) Επίδραση κοινού ιόντος Εάν σε κορεσµένο διάλυµα δυσδιάλυτου ηλεκτρολύτη (π.χ. AgCl) προστεθεί
ΓΙΝΟΜΕΝΟ ΙΑΛΥΤΟΤΗΤΑΣ (2) ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΙΑΛΥΤΟΤΗΤΑΣ (1) Επίδραση κοινού ιόντος Εάν σε κορεσµένο διάλυµα δυσδιάλυτου ηλεκτρολύτη (π.χ. AgCl) προστεθεί
ΠΡΟΤΑΣΗ ΕΦΑΡΜΟΓΗΣ. aquabio.gr ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ AQUABIO SBR ΓΙΑ ΤΗΝ ΕΠΕΞΕΡΓΑΣΙΑ ΛΥΜΑΤΩΝ ΣΥΓΚΡΟΤΗΜΑΤΟΣ ΠΟΛΥΤΕΛΩΝ ΚΑΤΟΙΚΙΩΝ
 aquabio.gr Αντώνης Χουρδάκης & ΣΙΑ Ε.Ε. a.chourdakis@aquabio.gr Διδώς Σωτηρίου 15, Ηράκλειο, 71305 τηλ.: (+30) 2810 372 899 κιν.: (+30) 697 22 22 981 fax: (+30) 2810 372 901 ΠΡΟΤΑΣΗ ΕΦΑΡΜΟΓΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ
aquabio.gr Αντώνης Χουρδάκης & ΣΙΑ Ε.Ε. a.chourdakis@aquabio.gr Διδώς Σωτηρίου 15, Ηράκλειο, 71305 τηλ.: (+30) 2810 372 899 κιν.: (+30) 697 22 22 981 fax: (+30) 2810 372 901 ΠΡΟΤΑΣΗ ΕΦΑΡΜΟΓΗΣ ΤΟΥ ΣΥΣΤΗΜΑΤΟΣ
ΤΕΧΝΟΛΟΓΙΕΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΑΣΤΙΚΩΝ ΛΥΜΑΤΩΝ
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ Σχολή Χηµικών Μηχανικών ΤΕΧΝΟΛΟΓΙΕΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΑΣΤΙΚΩΝ ΛΥΜΑΤΩΝ ΒΛΥΣΙ ΗΣ ΑΠΟΣΤΟΛΟΣ Καθηγητής ΑΘΗΝΑ 2007 1 ΤΕΧΝΟΛΟΓΙΑ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ 1. Εισαγωγή Ο ι ρύποι που πρέπει να
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ Σχολή Χηµικών Μηχανικών ΤΕΧΝΟΛΟΓΙΕΣ ΕΠΕΞΕΡΓΑΣΙΑΣ ΑΣΤΙΚΩΝ ΛΥΜΑΤΩΝ ΒΛΥΣΙ ΗΣ ΑΠΟΣΤΟΛΟΣ Καθηγητής ΑΘΗΝΑ 2007 1 ΤΕΧΝΟΛΟΓΙΑ ΕΠΕΞΕΡΓΑΣΙΑΣ ΛΥΜΑΤΩΝ 1. Εισαγωγή Ο ι ρύποι που πρέπει να
ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Ι & ΙΙ Εργαστηριακή Άσκηση 1: ΚΡΥΣΤΑΛΛΩΣΗ
 Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
συστήματα προαπονιτροποίησης είναι η δημιουργία ευνοϊκών συνθηκών για την ανάπτυξη νηματοειδών μικροοργανισμών.
 ΠΕΡΙΛΗΨΗ Το σύστημα ενεργού ιλύος είναι το πιο διαδεδομένο και αποτελεσματικό σύστημα βιολογικής επεξεργασίας αστικών λυμάτων, όσον αφορά τόσο στην ποιότητα εκροής όσο και στην οικονομία του. Αναπτύχθηκε
ΠΕΡΙΛΗΨΗ Το σύστημα ενεργού ιλύος είναι το πιο διαδεδομένο και αποτελεσματικό σύστημα βιολογικής επεξεργασίας αστικών λυμάτων, όσον αφορά τόσο στην ποιότητα εκροής όσο και στην οικονομία του. Αναπτύχθηκε
Τεχνική Περιβάλλοντος
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 5: Καθίζηση Δεξαμενές καθίζησης Ευθύμιος Νταρακάς Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 5: Καθίζηση Δεξαμενές καθίζησης Ευθύμιος Νταρακάς Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative
ΠΡΑΓΜΑΤΙΚΑ ΕΙΓΜΑΤΑ ΠΡΟΕΤΟΙΜΑΣΙΑ ΤΩΝ ΕΙΓΜΑΤΩΝ ΓΙΑ ΑΝΑΛΥΣΗ. ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ
 ΠΡΑΓΜΑΤΙΚΑ ΕΙΓΜΑΤΑ ΠΡΟΕΤΟΙΜΑΣΙΑ ΤΩΝ ΕΙΓΜΑΤΩΝ ΓΙΑ ΑΝΑΛΥΣΗ ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΠΡΑΓΜΑΤΙΚΑ ΕΙΓΜΑΤΑ (1) - Οι χηµικοί σε ακαδηµαϊκά ιδρύµατα και βιοµηχανία
ΠΡΑΓΜΑΤΙΚΑ ΕΙΓΜΑΤΑ ΠΡΟΕΤΟΙΜΑΣΙΑ ΤΩΝ ΕΙΓΜΑΤΩΝ ΓΙΑ ΑΝΑΛΥΣΗ ΕΡΗ ΜΠΙΖΑΝΗ 4 ΟΣ ΟΡΟΦΟΣ, ΓΡΑΦΕΙΟ 2 eribizani@chem.uoa.gr 2107274573 1 ΠΡΑΓΜΑΤΙΚΑ ΕΙΓΜΑΤΑ (1) - Οι χηµικοί σε ακαδηµαϊκά ιδρύµατα και βιοµηχανία
Ειδικές παραγγελίες για εξυπηρέτηση των ατομικών αναγκών πελατών. Επεξεργασία σε ανώτατο επίπεδο π.χ. 10:10:2 για BOD:SS:NH4
 Η σειρά HiPAF είναι ένα σύστημα επεξεργασίας αστικών αποβλήτων σχεδιασμένο ειδικά για να ικανοποιήσει και τους πιο απαιτητικούς πελάτες. Συνδυάζοντας ευελιξία, αξιοπιστία, ικανή προεργασία και στιβαρή
Η σειρά HiPAF είναι ένα σύστημα επεξεργασίας αστικών αποβλήτων σχεδιασμένο ειδικά για να ικανοποιήσει και τους πιο απαιτητικούς πελάτες. Συνδυάζοντας ευελιξία, αξιοπιστία, ικανή προεργασία και στιβαρή
Κροκίδωση - Συσσωµάτωση
 ΕΠΕΞΕΡΓΑΣΙΑ ΝΕΡΟΥ ΚΑΙ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ Αχαρνών 364 & Γλαράκι 10Β, Αθήνα, 11145 Τηλ: 211 1820 163-4-5 Φαξ: 211 1820 166 e-mail: enerchem@enerchem.gr web site: www.enerchem.gr Κροκίδωση - Συσσωµάτωση Πηγή:
ΕΠΕΞΕΡΓΑΣΙΑ ΝΕΡΟΥ ΚΑΙ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ Αχαρνών 364 & Γλαράκι 10Β, Αθήνα, 11145 Τηλ: 211 1820 163-4-5 Φαξ: 211 1820 166 e-mail: enerchem@enerchem.gr web site: www.enerchem.gr Κροκίδωση - Συσσωµάτωση Πηγή:
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ
 ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
aquabio.gr ΜΕΤΑΤΡΟΠΗ ΣΤΕΓΑΝΗΣ ΔΕΞΑΜΕΝΗΣ (ΔΕΞ. ΒΟΘΡΟΥ) ΣΕ ΜΟΝΑΔΑ ΒΙΟΛΟΓΙΚΟΥ ΚΑΘΑΡΙΣΜΟΥ ΔΙΑΚΟΠΤΟΜΕΝΗΣ ΛΕΙΤΟΥΡΓΙΑΣ (SBR)
 aquabio.gr Αντώνης Χουρδάκης & ΣΙΑ Ε.Ε. a.chourdakis@aquabio.gr Διδώς Σωτηρίου 15, Ηράκλειο, 71305 τηλ.: (+30) 2810 372 899 κιν.: (+30) 697 22 22 981 fax: (+30) 2810 372 901 aquabio SBR ΜΕΤΑΤΡΟΠΗ ΣΤΕΓΑΝΗΣ
aquabio.gr Αντώνης Χουρδάκης & ΣΙΑ Ε.Ε. a.chourdakis@aquabio.gr Διδώς Σωτηρίου 15, Ηράκλειο, 71305 τηλ.: (+30) 2810 372 899 κιν.: (+30) 697 22 22 981 fax: (+30) 2810 372 901 aquabio SBR ΜΕΤΑΤΡΟΠΗ ΣΤΕΓΑΝΗΣ
ΠΕΡΙΕΧΟΜΕΝΑ. Περιεχόμενα
 ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ... 1 1. ΕΙΣΑΓΩΓΗ... 3 1.1 ΤΟ ΒΙΟΑΕΡΙΟ ΣΤΗΝ ΕΥΡΩΠΗ... 3 1.1.1 Το βιοαέριο στην Ελλάδα... 6 1.2 ΛΥΜΑΤΑ ΧΟΙΡΟΣΤΑΣΙΟΥ... 8 1.2.1 Σύσταση των λυμάτων χοιροστασίου... 8 1.2.1.1 Νερό... 8
ΠΕΡΙΕΧΟΜΕΝΑ ΠΡΟΛΟΓΟΣ... 1 1. ΕΙΣΑΓΩΓΗ... 3 1.1 ΤΟ ΒΙΟΑΕΡΙΟ ΣΤΗΝ ΕΥΡΩΠΗ... 3 1.1.1 Το βιοαέριο στην Ελλάδα... 6 1.2 ΛΥΜΑΤΑ ΧΟΙΡΟΣΤΑΣΙΟΥ... 8 1.2.1 Σύσταση των λυμάτων χοιροστασίου... 8 1.2.1.1 Νερό... 8
Διαδικασίες Υψηλών Θερμοκρασιών
 Διαδικασίες Υψηλών Θερμοκρασιών Θεματική Ενότητα 4: Διαδικασίες σε υψηλές θερμοκρασίες Τίτλος: Διαδικασίες μετασχηματισμού των φάσεων Ονόματα Καθηγητών: Κακάλη Γλυκερία, Ρηγοπούλου Βασιλεία Σχολή Χημικών
Διαδικασίες Υψηλών Θερμοκρασιών Θεματική Ενότητα 4: Διαδικασίες σε υψηλές θερμοκρασίες Τίτλος: Διαδικασίες μετασχηματισμού των φάσεων Ονόματα Καθηγητών: Κακάλη Γλυκερία, Ρηγοπούλου Βασιλεία Σχολή Χημικών
Το πρόβλημα της ιλύς. Η λύση GACS
 Το πρόβλημα της ιλύς Κατά την επεξεργασία των υγρών αποβλήτων παράγονται ταυτόχρονα και ορισμένα παραπροϊόντα, όπως τα εσχαρίσματα, η άμμος, τα ξαφρίσματα και η περίσσεια ιλύς από τις δεξαμενές καθίζησης
Το πρόβλημα της ιλύς Κατά την επεξεργασία των υγρών αποβλήτων παράγονται ταυτόχρονα και ορισμένα παραπροϊόντα, όπως τα εσχαρίσματα, η άμμος, τα ξαφρίσματα και η περίσσεια ιλύς από τις δεξαμενές καθίζησης
ΟΙ ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΟΞΙΝΗΣ ΒΡΟΧΗΣ ΣΤΟ ΠΕΡΙΒΑΛΛΟΝ
 !Unexpected End of Formula l ΟΙ ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΟΞΙΝΗΣ ΒΡΟΧΗΣ ΣΤΟ ΠΕΡΙΒΑΛΛΟΝ ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Παραδεισανός Αδάμ ΠΡΟΛΟΓΟΣ Η εργασία αυτή εκπονήθηκε το ακαδημαϊκό έτος 2003 2004 στο μάθημα «Το πείραμα στη
!Unexpected End of Formula l ΟΙ ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΟΞΙΝΗΣ ΒΡΟΧΗΣ ΣΤΟ ΠΕΡΙΒΑΛΛΟΝ ΘΕΩΡΗΤΙΚΟ ΜΕΡΟΣ Παραδεισανός Αδάμ ΠΡΟΛΟΓΟΣ Η εργασία αυτή εκπονήθηκε το ακαδημαϊκό έτος 2003 2004 στο μάθημα «Το πείραμα στη
Σήµερα οι εξελίξεις στην Επιστήµη και στην Τεχνολογία δίνουν τη
 ΚΕΦΑΛΑΙΟ 7ο: ΑΡΧΕΣ & ΜΕΘΟ ΟΛΟΓΙΑ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Συνδυασµός ΤΕΧΝΟΛΟΓΙΑΣ & ΕΠΙΣΤΗΜΗΣ Προσφέρει τη δυνατότητα χρησιµοποίησης των ζωντανών οργανισµών για την παραγωγή χρήσιµων προϊόντων 1 Οι ζωντανοί οργανισµοί
ΚΕΦΑΛΑΙΟ 7ο: ΑΡΧΕΣ & ΜΕΘΟ ΟΛΟΓΙΑ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Συνδυασµός ΤΕΧΝΟΛΟΓΙΑΣ & ΕΠΙΣΤΗΜΗΣ Προσφέρει τη δυνατότητα χρησιµοποίησης των ζωντανών οργανισµών για την παραγωγή χρήσιµων προϊόντων 1 Οι ζωντανοί οργανισµοί
Τι είναι άμεση ρύπανση?
 ΡΥΠΑΝΣΗ ΝΕΡΟΥ Τι είναι ρύπανση; Ρύπανση μπορεί να θεωρηθεί η δυσμενής μεταβολή των φυσικοχημικών ή βιολογικών συνθηκών ενός συγκεκριμένου περιβάλλοντος ή/και η βραχυπρόθεσμη ή μακροπρόθεσμη βλάβη στην
ΡΥΠΑΝΣΗ ΝΕΡΟΥ Τι είναι ρύπανση; Ρύπανση μπορεί να θεωρηθεί η δυσμενής μεταβολή των φυσικοχημικών ή βιολογικών συνθηκών ενός συγκεκριμένου περιβάλλοντος ή/και η βραχυπρόθεσμη ή μακροπρόθεσμη βλάβη στην
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
ΦΥΣΙΚΟΧΗΜΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΟΥ ΝΕΡΟΥ
 ΦΥΣΙΚΟΧΗΜΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΟΥ ΝΕΡΟΥ Η ΡΟΗ ΤΟΥ ΝΕΡΟΥ Η ροή του νερού μεταξύ των άλλων καθορίζει τη ζωή και τις λειτουργίες των έμβιων οργανισμών στο ποτάμι. Διαμορφώνει το σχήμα του σώματός τους, τους
ΦΥΣΙΚΟΧΗΜΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΟΥ ΝΕΡΟΥ Η ΡΟΗ ΤΟΥ ΝΕΡΟΥ Η ροή του νερού μεταξύ των άλλων καθορίζει τη ζωή και τις λειτουργίες των έμβιων οργανισμών στο ποτάμι. Διαμορφώνει το σχήμα του σώματός τους, τους
Αρχές Επεξεργασίας Τροφίμων
 Αρχές Επεξεργασίας Τροφίμων Κατάψυξη τροφίμων Κατάψυξη Απομάκρυνση θερμότητας από ένα προϊόν με αποτέλεσμα την μείωση της θερμοκρασίας του κάτω από το σημείο πήξης. Ως μέθοδος συντήρησης βασίζεται: Στην
Αρχές Επεξεργασίας Τροφίμων Κατάψυξη τροφίμων Κατάψυξη Απομάκρυνση θερμότητας από ένα προϊόν με αποτέλεσμα την μείωση της θερμοκρασίας του κάτω από το σημείο πήξης. Ως μέθοδος συντήρησης βασίζεται: Στην
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ
 ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
ΣΥΝΘΕΣΗ ΝΑΝΟΣΩΛΗΝΩΝ ΑΝΘΡΑΚΑ ΜΕΣΩ ΘΕΡΜΟΛΥΣΗΣ ΟΡΓΑΜΟΜΕΤΑΛΛΙΚΗΣ ΕΝΩΣΗΣ ΣΕ ΣΤΕΡΕΑ ΚΑΤΑΣΤΑΣΗ Α.Μ. Νέτσου 1, Ε. Χουντουλέση 1, Μ.Περράκη 2, Α.Ντζιούνη 1, Κ. Κορδάτος 1 1 Σχολή Χημικών Μηχανικών, ΕΜΠ 2 Σχολή
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΠΕΡΙΒΑΛΛΟΝΤΟΣ. Πτυχιακή διατριβή
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΘΟΔΟΙ ΠΡΟΕΠΕΞΕΡΓΑΣΙΑΣ ΤΩΝ ΛΙΠΩΝ ΚΑΙ ΕΛΕΩΝ ΠΡΟΣ ΠΑΡΑΓΩΓΗ ΒΙΟΑΕΡΙΟΥ Ανδρέας Φράγκου Λεμεσός 2015
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή ΜΕΘΟΔΟΙ ΠΡΟΕΠΕΞΕΡΓΑΣΙΑΣ ΤΩΝ ΛΙΠΩΝ ΚΑΙ ΕΛΕΩΝ ΠΡΟΣ ΠΑΡΑΓΩΓΗ ΒΙΟΑΕΡΙΟΥ Ανδρέας Φράγκου Λεμεσός 2015
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ. Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια.
 ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
ΚΕΦΑΛΑΙΟ 7 Τι είναι οι καλλιέργειες μικροοργανισμών; Τι είναι το θρεπτικό υλικό; Ποια είναι τα είδη του θρεπτικού υλικού και τι είναι το καθένα;
 ΚΕΦΑΛΑΙΟ 7 Τι είναι οι καλλιέργειες μικροοργανισμών; Καλλιέργεια είναι η διαδικασία ανάπτυξης μικροοργανισμών με διάφορους τεχνητούς τρόπους στο εργαστήριο ή σε βιομηχανικό επίπεδο. Με τη δημιουργία καλλιεργειών
ΚΕΦΑΛΑΙΟ 7 Τι είναι οι καλλιέργειες μικροοργανισμών; Καλλιέργεια είναι η διαδικασία ανάπτυξης μικροοργανισμών με διάφορους τεχνητούς τρόπους στο εργαστήριο ή σε βιομηχανικό επίπεδο. Με τη δημιουργία καλλιεργειών
Ανακύκλωση & διατήρηση Θρεπτικών
 Ανακύκλωση & διατήρηση Θρεπτικών 30-12-2014 EVA PAPASTERGIADOU Ανακύκλωση των Θρεπτικών είναι η χρησιμοποίηση, ο μετασχηματισμός, η διακίνηση & η επαναχρησιμοποίηση των θρεπτικών στοιχείων στα οικοσυστήματα
Ανακύκλωση & διατήρηση Θρεπτικών 30-12-2014 EVA PAPASTERGIADOU Ανακύκλωση των Θρεπτικών είναι η χρησιμοποίηση, ο μετασχηματισμός, η διακίνηση & η επαναχρησιμοποίηση των θρεπτικών στοιχείων στα οικοσυστήματα
Στοιχειμετρικοί υπολογισμοί σε διαλύματα
 Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Ολοκληρωµένες λύσεις διαχείρισης
 Ολοκληρωµένες λύσεις διαχείρισης λυµάτων µικρής & µεσαίας κλίµακας Προβλήµατα στα οποία δίνεται λύση Οι λύσεις που προτείνει η Agrologistics, έρχονται να δώσουν απάντηση σε πολλά προβλήµατα σχετικά µε
Ολοκληρωµένες λύσεις διαχείρισης λυµάτων µικρής & µεσαίας κλίµακας Προβλήµατα στα οποία δίνεται λύση Οι λύσεις που προτείνει η Agrologistics, έρχονται να δώσουν απάντηση σε πολλά προβλήµατα σχετικά µε
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΤΟ ΝΕΡΟ
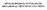 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΤΟ ΝΕΡΟ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΕ ΝΕΡΟ ΓΕΝΙΚΑ Με το πείραμα αυτό μπορούμε να προσδιορίσουμε δύο βασικές παραμέτρους που χαρακτηρίζουν ένα
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΤΟ ΝΕΡΟ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΕ ΝΕΡΟ ΓΕΝΙΚΑ Με το πείραμα αυτό μπορούμε να προσδιορίσουμε δύο βασικές παραμέτρους που χαρακτηρίζουν ένα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 01 03 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Τι ονομάζουμε χημική αντίδραση; Πότε μια χημική αντίδραση
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: 1 ΗΜΕΡΟΜΗΝΙΑ: 01 03 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Τι ονομάζουμε χημική αντίδραση; Πότε μια χημική αντίδραση
ΔΙΑΘΕΣΗ ΣΤΕΡΕΩΝ ΚΑΙ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΣΤΟ ΓΕΩΛΟΓΙΚΟ ΠΕΡΙΒΑΛΛΟΝ
 ΔΙΑΘΕΣΗ ΣΤΕΡΕΩΝ ΚΑΙ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΣΤΟ ΓΕΩΛΟΓΙΚΟ ΠΕΡΙΒΑΛΛΟΝ Ενότητα 9: Υγρά αστικά απόβλητα Διάθεση λυμάτων στο έδαφος (φυσικά συστήματα επεξεργασίας) (Μέρος 1 ο ) Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών
ΔΙΑΘΕΣΗ ΣΤΕΡΕΩΝ ΚΑΙ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΣΤΟ ΓΕΩΛΟΓΙΚΟ ΠΕΡΙΒΑΛΛΟΝ Ενότητα 9: Υγρά αστικά απόβλητα Διάθεση λυμάτων στο έδαφος (φυσικά συστήματα επεξεργασίας) (Μέρος 1 ο ) Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών
ΑΝΑΕΡΟΒΙΑ ΣΥΝΕΠΕΞΕΡΓΑΣΙΑ ΑΓΡΟΤΟΒΙΟΜΗΧΑΝΙΚΩΝ ΑΠΟΒΛΗΤΩΝ ΜΕ ΠΕΡΙΣΣΕΙΑ ΙΛΥ ΒΙΟΛΟΓΙΚΩΝ ΚΑΘΑΡΙΣΜΩΝ
 ΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΙΑΧΕΙΡΙΣΗΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΑΝΑΕΡΟΒΙΑ ΣΥΝΕΠΕΞΕΡΓΑΣΙΑ ΑΓΡΟΤΟΒΙΟΜΗΧΑΝΙΚΩΝ ΑΠΟΒΛΗΤΩΝ ΜΕ ΠΕΡΙΣΣΕΙΑ ΙΛΥ ΒΙΟΛΟΓΙΚΩΝ ΚΑΘΑΡΙΣΜΩΝ
ΗΜΟΚΡΙΤΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΡΑΚΗΣ ΤΜΗΜΑ ΜΗΧΑΝΙΚΩΝ ΠΕΡΙΒΑΛΛΟΝΤΟΣ ΕΡΓΑΣΤΗΡΙΟ ΤΕΧΝΟΛΟΓΙΑΣ ΚΑΙ ΙΑΧΕΙΡΙΣΗΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ ΑΝΑΕΡΟΒΙΑ ΣΥΝΕΠΕΞΕΡΓΑΣΙΑ ΑΓΡΟΤΟΒΙΟΜΗΧΑΝΙΚΩΝ ΑΠΟΒΛΗΤΩΝ ΜΕ ΠΕΡΙΣΣΕΙΑ ΙΛΥ ΒΙΟΛΟΓΙΚΩΝ ΚΑΘΑΡΙΣΜΩΝ
ΣΥΝΔΥΑΣΜΟΣ ΤΗΣ ΑΝΤΙΣΤΑΣΗΣ ΔΙΑΧΥΣΗΣ ΣΤΟΥΣ ΠΟΡΟΥΣ ΜΕ ΚΙΝΗΤΙΚΗ ΕΠΙΦΑΝΕΙΑΚΗΣ ΑΝΤΙΔΡΑΣΗΣ
 ΣΥΝΔΥΑΣΜΟΣ ΤΗΣ ΑΝΤΙΣΤΑΣΗΣ ΔΙΑΧΥΣΗΣ ΣΤΟΥΣ ΠΟΡΟΥΣ ΜΕ ΚΙΝΗΤΙΚΗ ΕΠΙΦΑΝΕΙΑΚΗΣ ΑΝΤΙΔΡΑΣΗΣ Παράγοντας Αποτελεσματικότητας Ειδικά για αντίδραση πρώτης τάξης, ο παράγοντας αποτελεσματικότητας ισούται προς ε = C
ΣΥΝΔΥΑΣΜΟΣ ΤΗΣ ΑΝΤΙΣΤΑΣΗΣ ΔΙΑΧΥΣΗΣ ΣΤΟΥΣ ΠΟΡΟΥΣ ΜΕ ΚΙΝΗΤΙΚΗ ΕΠΙΦΑΝΕΙΑΚΗΣ ΑΝΤΙΔΡΑΣΗΣ Παράγοντας Αποτελεσματικότητας Ειδικά για αντίδραση πρώτης τάξης, ο παράγοντας αποτελεσματικότητας ισούται προς ε = C
Πανεπιστήμιο Δυτικής Μακεδονίας. Τμήμα Μηχανολόγων Μηχανικών. Χημεία. Ενότητα 15: Διαλύματα
 Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Τμήμα Μηχανολόγων Μηχανικών Χημεία Ενότητα 15: Διαλύματα Αν. Καθηγητής Γεώργιος Μαρνέλλος e-mail: gmarnellos@uowm.gr Τμήμα Μηχανολόγων Μηχανικών Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες
Χημικές Διεργασίες: Εισαγωγή
 : Εισαγωγή Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση - Αφυδρογόνωση - Πυρόλυση - Ενυδάτωση κλπ Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση
: Εισαγωγή Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση - Αφυδρογόνωση - Πυρόλυση - Ενυδάτωση κλπ Ορολογία Μοναδιαίες Διεργασίες ( Unit Processes ) - Οξείδωση - Υδρογόνωση
Τεχνική Περιβάλλοντος
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 9: Απομάκρυνση αζώτου Ευθύμιος Νταρακάς Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 9: Απομάκρυνση αζώτου Ευθύμιος Νταρακάς Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons.
Υδροχημεία. Ενότητα 10: Οξείδωση - Αναγωγή. Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών Τμήμα : Γεωλογίας
 Υδροχημεία Ενότητα 10: Οξείδωση - Αναγωγή Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών Τμήμα : Γεωλογίας Σκοποί ενότητας Κατανόηση των οξειδοαναγωγικών φαινομένων, δυναμικό οξειδοαναγωγής Κατανόηση της διαδικασίας
Υδροχημεία Ενότητα 10: Οξείδωση - Αναγωγή Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών Τμήμα : Γεωλογίας Σκοποί ενότητας Κατανόηση των οξειδοαναγωγικών φαινομένων, δυναμικό οξειδοαναγωγής Κατανόηση της διαδικασίας
Περιβαλλοντική Τεχνολογία και Διαχείριση
 Περιβαλλοντική Τεχνολογία και Διαχείριση Απόστολος Βλυσίδης Καθηγητής ΕΜΠ Σχολή Χημικών Μηχανικών Εργαστήριο Οργανικής Χημικής Τεχνολογίας ΒΙΟΛΟΓΙΚΗ ΟΞΕΙΔΩΣΗ ΑΠΟΒΛΗΤΩΝ ΑΕΡΟΒΙΑ ΧΩΝΕΥΣΗ ΣΥΣΤΗΜΑΤΑ ΕΝΕΡΓΟΥ
Περιβαλλοντική Τεχνολογία και Διαχείριση Απόστολος Βλυσίδης Καθηγητής ΕΜΠ Σχολή Χημικών Μηχανικών Εργαστήριο Οργανικής Χημικής Τεχνολογίας ΒΙΟΛΟΓΙΚΗ ΟΞΕΙΔΩΣΗ ΑΠΟΒΛΗΤΩΝ ΑΕΡΟΒΙΑ ΧΩΝΕΥΣΗ ΣΥΣΤΗΜΑΤΑ ΕΝΕΡΓΟΥ
Εφαρμογές βιοαντιδραστήρων μεμβρανών (MBR) για την επεξεργασία υγρών αποβλήτων και προβλήματα έμφραξης. Π. Σαμαράς
 ΤΜΗΜΑ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΑΣ ΓΕΩΠΟΝΙΑΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ ΚΑΙ ΔΙΑΤΡΟΦΗΣ ΤΕΙ ΘΕΣΣΑΛΟΝΙΚΗΣ Εφαρμογές βιοαντιδραστήρων μεμβρανών (MBR) για την επεξεργασία υγρών αποβλήτων και προβλήματα
ΤΜΗΜΑ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ ΣΧΟΛΗ ΤΕΧΝΟΛΟΓΙΑΣ ΓΕΩΠΟΝΙΑΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΤΡΟΦΙΜΩΝ ΚΑΙ ΔΙΑΤΡΟΦΗΣ ΤΕΙ ΘΕΣΣΑΛΟΝΙΚΗΣ Εφαρμογές βιοαντιδραστήρων μεμβρανών (MBR) για την επεξεργασία υγρών αποβλήτων και προβλήματα
Θεωρία. Γενική Χημεία. Χημεία
 Θεωρία Εργαστη- Γενική ριακές Χημεία Ασκήσεις Γενική Χημεία Αντωνία Χίου Επίκουρη Καθηγήτρια Η κατανόηση του υλικού κόσμου και Στόχοι των βασικών αρχών που τον διέπουν. Στο πλαίσιο ασο αυτό μελετώνται
Θεωρία Εργαστη- Γενική ριακές Χημεία Ασκήσεις Γενική Χημεία Αντωνία Χίου Επίκουρη Καθηγήτρια Η κατανόηση του υλικού κόσμου και Στόχοι των βασικών αρχών που τον διέπουν. Στο πλαίσιο ασο αυτό μελετώνται
Κεφάλαιο 1: Εισαγωγή. Κεφάλαιο 2: Η Βιολογία των Ιών
 Κεφάλαιο 1: Εισαγωγή 1.1 Μικροοργανισμοί, Μικροβιολογία και Μικροβιολόγοι... 19 1.1.1 Μικροοργανισμοί... 19 1.1.2 Μικροβιολογία... 20 1.1.3 Μικροβιολόγοι... 21 1.2 Σύντομη Ιστορική Εξέλιξη της Μικροβιολογίας...
Κεφάλαιο 1: Εισαγωγή 1.1 Μικροοργανισμοί, Μικροβιολογία και Μικροβιολόγοι... 19 1.1.1 Μικροοργανισμοί... 19 1.1.2 Μικροβιολογία... 20 1.1.3 Μικροβιολόγοι... 21 1.2 Σύντομη Ιστορική Εξέλιξη της Μικροβιολογίας...
ΜΟΝΤΕΛΟΠΟΙΗΣΗ ΤΩΝ ΦΑΙΝΟΜΕΝΩΝ ΡΟΗΣ, ΜΕΤΑΦΟΡΑΣ ΚΑΙ ΕΛΕΓΧΟΜΕΝΗΣ ΚΑΤΑΒΥΘΙΣΗΣ ΚΑΤΑ ΤΗΝ ΑΝΑΜΕΙΞΗ ΑΛΑΤΟΥΧΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΕ ΔΙΚΤΥΑ ΠΟΡΩΝ ΣΥΝΘΕΤΗΣ ΓΕΩΜΕΤΡΙΑΣ
 10 ο ΠΑΝΕΛΛΗΝΙΟ ΕΠΙΣΤΗΜΟΝΙΚΟ ΣΥΝΕΔΡΙΟ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ, ΠΑΤΡΑ, 4-6 ΙΟΥΝΙΟΥ, 2015. ΜΟΝΤΕΛΟΠΟΙΗΣΗ ΤΩΝ ΦΑΙΝΟΜΕΝΩΝ ΡΟΗΣ, ΜΕΤΑΦΟΡΑΣ ΚΑΙ ΕΛΕΓΧΟΜΕΝΗΣ ΚΑΤΑΒΥΘΙΣΗΣ ΚΑΤΑ ΤΗΝ ΑΝΑΜΕΙΞΗ ΑΛΑΤΟΥΧΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΕ ΔΙΚΤΥΑ
10 ο ΠΑΝΕΛΛΗΝΙΟ ΕΠΙΣΤΗΜΟΝΙΚΟ ΣΥΝΕΔΡΙΟ ΧΗΜΙΚΗΣ ΜΗΧΑΝΙΚΗΣ, ΠΑΤΡΑ, 4-6 ΙΟΥΝΙΟΥ, 2015. ΜΟΝΤΕΛΟΠΟΙΗΣΗ ΤΩΝ ΦΑΙΝΟΜΕΝΩΝ ΡΟΗΣ, ΜΕΤΑΦΟΡΑΣ ΚΑΙ ΕΛΕΓΧΟΜΕΝΗΣ ΚΑΤΑΒΥΘΙΣΗΣ ΚΑΤΑ ΤΗΝ ΑΝΑΜΕΙΞΗ ΑΛΑΤΟΥΧΩΝ ΔΙΑΛΥΜΑΤΩΝ ΣΕ ΔΙΚΤΥΑ
ΕΦΑΡΜΟΓΗ ΜΟΝΑ Α ΑΝΑΚΥΚΛΩΣΗΣ ΝΕΡΟΥ ΚΑΙ ΜΗ ΕΝΙΚΗΣ ΑΠΟΡΡΙΨΗΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ
 ΕΦΑΡΜΟΓΗ ΜΟΝΑ Α ΑΝΑΚΥΚΛΩΣΗΣ ΝΕΡΟΥ ΚΑΙ ΜΗ ΕΝΙΚΗΣ ΑΠΟΡΡΙΨΗΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ Πηγή: Mr.Matteo Villa HAR srl. Επιµέλεια: Κων/νος I. Νάκος SHIELCO Ltd Σελίδα 1/5 O οίκος HAR srl, Ιταλίας εξειδικεύεται στον σχεδιασµό
ΕΦΑΡΜΟΓΗ ΜΟΝΑ Α ΑΝΑΚΥΚΛΩΣΗΣ ΝΕΡΟΥ ΚΑΙ ΜΗ ΕΝΙΚΗΣ ΑΠΟΡΡΙΨΗΣ ΥΓΡΩΝ ΑΠΟΒΛΗΤΩΝ Πηγή: Mr.Matteo Villa HAR srl. Επιµέλεια: Κων/νος I. Νάκος SHIELCO Ltd Σελίδα 1/5 O οίκος HAR srl, Ιταλίας εξειδικεύεται στον σχεδιασµό
Λυμένες ασκήσεις: 36. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λανθασμένες;
 ΧΗΜΕΙΑ: Εισαγωγή στην Χημεία - από το νερό στο άτομο- από το μακρόκοσμο στον μικρόκοσμο 41 Λυμένες ασκήσεις: 36. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λανθασμένες; α. Το νερό χαρακτηρίζεται
ΧΗΜΕΙΑ: Εισαγωγή στην Χημεία - από το νερό στο άτομο- από το μακρόκοσμο στον μικρόκοσμο 41 Λυμένες ασκήσεις: 36. Ποιες από τις παρακάτω προτάσεις είναι σωστές και ποιες λανθασμένες; α. Το νερό χαρακτηρίζεται
Πείραμα 2 Αν αντίθετα, στο δοχείο εισαχθούν 20 mol ΗΙ στους 440 ºC, τότε το ΗΙ διασπάται σύμφωνα με τη χημική εξίσωση: 2ΗΙ(g) H 2 (g) + I 2 (g)
 Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Ο πυρήνας του ατόμου
 Ο πυρήνας του ατόμου Αρχές 19 ου αιώνα: Η ανακάλυψη της ραδιενέργειας, (αυθόρμητης εκπομπής σωματιδίων και / ή ακτινοβολίας από στοιχεία), βοήθησε τα μέγιστα στην έρευνα της δομής του ατόμου. Ποια είδη
Ο πυρήνας του ατόμου Αρχές 19 ου αιώνα: Η ανακάλυψη της ραδιενέργειας, (αυθόρμητης εκπομπής σωματιδίων και / ή ακτινοβολίας από στοιχεία), βοήθησε τα μέγιστα στην έρευνα της δομής του ατόμου. Ποια είδη
(Chemical Oxygen Demand) C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O /180= 1.06 = 1.06 go 2 /ggluc
 COD BOD TS VS F/M (Chemical Oxygen Demand) C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O 180 192 192/180= 1.06 = 1.06 go 2 /ggluc Βιοχημικά απαιτούμενο οξυγόνο (Biochemical Oxygen Demand) Ολικά στερεά (Total Solids)
COD BOD TS VS F/M (Chemical Oxygen Demand) C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O 180 192 192/180= 1.06 = 1.06 go 2 /ggluc Βιοχημικά απαιτούμενο οξυγόνο (Biochemical Oxygen Demand) Ολικά στερεά (Total Solids)
ΒΙΟΓΕΩΧΗΜΙΚΟΙ ΚΥΚΛΟΙ Βιογεωχημικός κύκλος
 ΒΙΟΓΕΩΧΗΜΙΚΟΙ ΚΥΚΛΟΙ Βιογεωχημικός κύκλος ενός στοιχείου είναι, η επαναλαμβανόμενη κυκλική πορεία του στοιχείου στο οικοσύστημα. Οι βιογεωχημικοί κύκλοι, πραγματοποιούνται με την βοήθεια, βιολογικών, γεωλογικών
ΒΙΟΓΕΩΧΗΜΙΚΟΙ ΚΥΚΛΟΙ Βιογεωχημικός κύκλος ενός στοιχείου είναι, η επαναλαμβανόμενη κυκλική πορεία του στοιχείου στο οικοσύστημα. Οι βιογεωχημικοί κύκλοι, πραγματοποιούνται με την βοήθεια, βιολογικών, γεωλογικών
Μεταπτυχιακή Εργασία ΗΣ
 ΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥ ΩΝ ΣΤΙΣ ΠΕΡΙΒΑΛΛΟΝΤΙΚΕΣ ΕΠΙΣΤΗΜΕΣ ΠΑΝ/ΜΙΟ ΠΑΤΡΩΝ Μεταπτυχιακή Εργασία ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΣΤΙΚΑ Υ ΑΤΙΚΑ ΑΠΟΒΛΗΤΑ ΜΕ ΤΗ ΧΡΗΣΗ ΡΕΥΣΤΟΠΟΙΗΜΕΝΗΣ ΚΛΙΝ ΗΣ ΝΗ Γεώργιος.
ΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥ ΩΝ ΣΤΙΣ ΠΕΡΙΒΑΛΛΟΝΤΙΚΕΣ ΕΠΙΣΤΗΜΕΣ ΠΑΝ/ΜΙΟ ΠΑΤΡΩΝ Μεταπτυχιακή Εργασία ΑΝΑΚΤΗΣΗ ΦΩΣΦΟΡΟΥ ΑΠΟ ΑΣΤΙΚΑ Υ ΑΤΙΚΑ ΑΠΟΒΛΗΤΑ ΜΕ ΤΗ ΧΡΗΣΗ ΡΕΥΣΤΟΠΟΙΗΜΕΝΗΣ ΚΛΙΝ ΗΣ ΝΗ Γεώργιος.
Αντλία Θερμότητας με Θερμική Συμπίεση και Παραγωγή Ενέργειας από Θερμότητα
 Αντλία Θερμότητας με Θερμική Συμπίεση και Παραγωγή Ενέργειας από Θερμότητα Τεχνολογικό πεδίο Η μελέτη αναφέρετε σε αντλίες θερμότητας, δηλαδή μεταφορά θερμότητας σε ψηλότερη θερμοκρασία με συνηθέστερη
Αντλία Θερμότητας με Θερμική Συμπίεση και Παραγωγή Ενέργειας από Θερμότητα Τεχνολογικό πεδίο Η μελέτη αναφέρετε σε αντλίες θερμότητας, δηλαδή μεταφορά θερμότητας σε ψηλότερη θερμοκρασία με συνηθέστερη
panagiotisathanasopoulos.gr
 Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
