ΤΟΜΕΑΣ ΜΕΤΑΛΛΟΥΡΓΙΑΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Εργαστήριο Επιστήμης και Τεχνολογίας Προστασίας Περιβάλλοντος στη Μεταλλουργία και Τεχνολογία Υλικών
|
|
|
- Μελαινη Διαμαντόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ ΜΕΤΑΛΛΟΥΡΓΩΝ ΤΟΜΕΑΣ ΜΕΤΑΛΛΟΥΡΓΙΑΣ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑΣ ΥΛΙΚΩΝ Εργαστήριο Επιστήμης και Τεχνολογίας Προστασίας Περιβάλλοντος στη Μεταλλουργία και Τεχνολογία Υλικών Προσδιορισμός συντελεστή μεταφοράς οξυγόνου σε νερό Εργαστηριακή άσκηση μαθήματος Περιβάλλον Ι Εισαγωγή στην Επιστήμη και Τεχνολογία Προστασίας του Περιβάλλοντος Παυλίνα Κούση ΑΘΗΝΑ 2015
2
3 3 Προσδιορισμός συντελεστή μεταφοράς οξυγόνου σε νερό Σκοπός της άσκησης και σύνοψη της μεθόδου Σκοπός της άσκησης είναι ο πειραματικός προσδιορισμός του συντελεστή μεταφοράς μάζας οξυγόνου σε γνωστό όγκο νερού, με τη βοήθεια συστήματος αερισμού που λειτουργεί με γνωστή παροχή. Η μέθοδος βασίζεται στη δέσμευση του διαλελυμένου οξυγόνου από τον όγκο του νερού με θειώδες νάτριο και στη μετέπειτα ανα-οξυγόνωση του νερού σχεδόν μέχρι του σημείου κορεσμού Εισαγωγή Η παρουσία διαλελυμένου οξυγόνου (dissolved oxygen, DO) στα υδατικά συστήματα είναι απαραίτητη για την επιβίωση και την ανάπτυξη πολλών υδρόβιων (αερόβιων) οργανισμών και χρησιμοποιείται ως δείκτης της γεωχημικής ποιότητας των συστημάτων επιφανειακών και υπόγειων υδάτων (Τσέζος et al., 2006). Για παράδειγμα, η συγκέντρωση διαλελυμένου οξυγόνου σε γλυκά επιφανειακά νερά κατάλληλα για υδροληψία πόσιμου νερού πρέπει να είναι >70% της συγκέντρωσης κορεσμού (ΦΕΚ 438/Β, 1986). Η συγκέντρωση του διαλελυμένου οξυγόνου στα φυσικά νερά δεν είναι σταθερή, αλλά βρίσκεται σε μια «εύθραυστη» ισορροπία μεταξύ κατανάλωσης και συνεχούς αναοξυγόνωσης, με αποτέλεσμα να εξαρτάται από τις φυσικές, χημικές και βιοχημικές διεργασίες που λαμβάνουν χώρα μέσα στο κάθε υδάτινο σώμα (Hitchman, 1978). Προέλευση διαλελυμένου οξυγόνου στο νερό: ατμοσφαιρικός αερισμός και φωτοσύνθεση υδρόβιων φυτών. Ο αερισμός είναι η σημαντικότερη από τις δυο διαδικασίες στα ρεύματα που κινούνται γρήγορα, ενώ στις λίμνες επικρατεί ο μηχανισμός της φωτοσύνθεσης. Στην 1
4 πρώτη περίπτωση, η ημερήσια διακύμανση της συγκέντρωσης διαλελυμένου οξυγόνου είναι μικρή ενώ, στη δεύτερη περίπτωση, παρατηρείται σημαντική διακύμανση μεταξύ ημέρας και νύκτας. Επίσης, το τρεχούμενο νερό, λόγω της ροής του, διαλυτοποιεί περισσότερο οξυγόνο από το στάσιμο νερό. Κατανάλωση διαλελυμένου οξυγόνου στο νερό: αναπνοή, αερόβιες διεργασίες αποικοδόμησης, διάφορες χημικές και βιολογικές αντιδράσεις. Αν καταναλώνεται περισσότερο οξυγόνο από ό,τι παράγεται, η συγκέντρωση του διαλελυμένου οξυγόνου μειώνεται, με επακόλουθες συνέπειες στη βιοποικιλότητα. Η μέτρηση του διαλελυμένου οξυγόνου είναι κρίσιμης σημασίας για τον έλεγχο της ρύπανσης των υδάτων αλλά και των διεργασιών βιολογικής επεξεργασίας υγρών αποβλήτων Ορισμοί Συγκέντρωση διαλελυμένου οξυγόνου Ο όρος «διαλελυμένο οξυγόνο» (DO) αναφέρεται στο μοριακό (αέριο) οξυγόνο (Ο 2 ) που είναι διαλυμένο στο νερό. Η συγκέντρωση του διαλελυμένου οξυγόνου στο νερό (δίνεται συνήθως σε mg/l) επηρεάζεται από πολλούς παράγοντες, όπως η θερμοκρασία περιβάλλοντος, η ατμοσφαιρική πίεση (υψόμετρο) και η ενεργότητα των ιόντων (ιοντική ισχύς του υδάτινου σώματος). Εκτός της φυσικής, εποχικής αλλά και της ημερήσιας, διακύμανσης στη συγκέντρωση διαλελυμένου οξυγόνου, κρίσιμης σημασίας είναι οι περιπτώσεις ρύπανσης, όπως οι απορροές που περιέχουν οργανικό φορτίο, το οποίο διασπάται από μικροοργανισμούς. Κατά τη διαδικασία της βιοαποικοδόμησης, οι μικροοργανισμοί καταναλώνουν οξυγόνο 1. Παραδείγματα τέτοιων αποβλήτων που προκαλούν την κατανάλωση του διαλελυμένου οξυγόνου είναι, μεταξύ άλλων, το ρεύμα εξόδου των εγκαταστάσεων βιολογικής επεξεργασίας λυμάτων, οι απορροές όμβριων υδάτων από αγροτικές καλλιέργειες, αστικούς δρόμους ή κτηνοτροφικές εγκαταστάσεις. οι απορροές θερμού νερού, όπως αυτές των εγκαταστάσεων ψύξης εξοπλισμού εργοστασίων, που αυξάνουν τη θερμοκρασία του υδάτινου σώματος, μειώνοντας έτσι την περιεκτικότητά του σε οξυγόνο. Συμπερασματικά, για την κατανόηση και την τεκμηρίωση των επιπτώσεων των φυσικών φαινομένων και των ανθρωπογενών δραστηριοτήτων στους υδατικούς πόρους, απαιτούνται ακριβή δεδομένα για τη συγκέντρωση του διαλελυμένου οξυγόνου. 1 Το οξυγόνο που καταναλώνεται από τους μικροοργανισμούς για την αποικοδόμηση των οργανικών υλικών ονομάζεται βιοχημικά απαιτούμενο οξυγόνο (BOD). Περισσότερα για τον ορισμό και τον προσδιορισμό του BOD θα δείτε στην Εργαστηριακή Άσκηση 1 και στην ενότητα των Βοηθητικών Σημειώσεων του μαθήματος. 2
5 Συγκέντρωση κορεσμού Συγκέντρωση κορεσμού του οξυγόνου στο νερό είναι η μέγιστη συγκέντρωση διαλελυμένου οξυγόνου ευρισκόμενη σε ισορροπία με την περιεκτικότητα του αέρα σε οξυγόνο. Η συγκέντρωση κορεσμού εξαρτάται κυρίως από τη θερμοκρασία, την αλατότητα του νερού (συγκέντρωση χλωριόντων, (Benson et al., 1984)) και την ατμοσφαιρική πίεση. Γενικά, η διαλυτότητα του οξυγόνου στο νερό μειώνεται καθώς αυξάνεται η θερμοκρασία και η συγκέντρωση χλωριόντων ενώ αυξάνεται καθώς αυξάνεται η πίεση. Γι αυτό, η διαλυτότητα του οξυγόνου είναι υψηλότερη στο ψυχρό νερό και σε χαμηλότερο υψόμετρο. Σχηματικά, η επίδραση της αύξησης των παραπάνω παραγόντων στη διαλυτότητα του οξυγόνου στο νερό απεικονίζεται ως εξής: Θερμοκρασία Αλατότητα Πίεση Διαλυτότητα Ο 2 Η διαλυτότητα του οξυγόνου στο νερό είναι «χαμηλή», της τάξης των 9,2 mg/l για καθαρό νερό στους 20 C και σε πίεση 1 atm Έλλειμμα διαλελυμένου οξυγόνου Ως έλλειμμα ορίζεται η διαφορά μεταξύ της συγκέντρωσης κορεσμού και της πραγματικής συγκέντρωσης διαλελυμένου οξυγόνου. Δηλαδή, Έ 2 CO ύ C O ή (3.1) Ρυθμός και συντελεστής μεταφοράς οξυγόνου Η παλαιότερη και απλούστερη θεωρία που περιγράφει τη μεταφορά αερίου σε υγρό είναι αυτή των δυο στρωμάτων (two-film theory, (Whitman, 1962)). Η αρχή της θεωρίας παρουσιάζεται στο Σχήμα 3.1. Σχήμα 3.1. Σχηματικό διάγραμμα θεωρίας δύο στρωμάτων για τη μεταφορά (απορρόφηση) αερίου σε υγρό (Lin et al., 2007) 3
6 Η μεταφορά του οξυγόνου από τον όγκο της αέριας φάσης στην υγρή φάση ακολουθεί τα εξής διαδοχικά βήματα (Villadsen et al., 2011): 1. Διάχυση του οξυγόνου από τον όγκο της αέριας φάσης στη διεπιφάνεια αερίου-υγρού (φυσαλίδα) 2. Μεταφορά μέσω της διεπιφάνειας αερίου-υγρού 3. Διάχυση του οξυγόνου μέσω ενός σχετικά στάσιμου υγρού στρώματος που περικλείει τη φυσαλίδα του αερίου, δηλαδή από τη διεπιφάνεια αερίου-υγρού προς τον καλά αναμεμιγμένο όγκο της υγρής φάσης Το βήμα (2) είναι μια διαδικασία που φθάνει γρήγορα σε ισορροπία ενώ, στην περίπτωση αερίων χαμηλής διαλυτότητας, το βήμα (1) εξελίσσεται πολύ ταχύτερα από το βήμα (3). Έτσι, στην περίπτωση του οξυγόνου, ο ρυθμός μεταφοράς του οξυγόνου μέσω της διεπιφάνειας αερίου-υγρού ελέγχεται από την αντίσταση του στρώματος υγρού στη διάχυση των μορίων του οξυγόνου. Οπότε, με εφαρμογή των νόμων του Henry 2 και του Fick 3, προκύπτει η σχέση (Lin et al., 2007): dc A dc K C* C K a C* C dt V dt L t L t όπου K L συντελεστής μεταφοράς μάζας, cm/h A επιφάνεια διεπιφάνειας μεταφοράς, cm 2 V όγκος που περιέχει τη διεπιφάνεια μεταφοράς, cm 3 C t συγκέντρωση στον όγκο του υγρού τη χρονική στιγμή t, mg/l C* συγκέντρωση ισορροπίας με το αέριο τη χρονική στιγμή t, mg/l a ειδική επιφάνεια της διεπιφάνειας ανά μονάδα όγκου συστήματος, cm -1 K L a συντελεστής μεταφοράς μάζας ανά μονάδα όγκου στο υγρό, h -1 (3.2) Έτσι, αν θεωρήσουμε ότι C* ισοδυναμεί με τη συγκέντρωση κορεσμού, προκύπτει ότι ο ρυθμός με τον οποίο το οξυγόνο διαλύεται στο νερό είναι ανάλογος του ελλείμματος διαλελυμένου οξυγόνου. Δηλαδή, dc Ka L Cύ C ή (3.3) dt όπου K L a ο συντελεστής μεταφοράς οξυγόνου ανά μονάδα όγκου (σε μονάδες time -1 ) ο οποίος εξαρτάται κυρίως από: τη θερμοκρασία, σύμφωνα με τη σχέση Ka T20 L (T) Ka L (20) (3.4) όπου θ ο συντελεστής διόρθωσης για τη θερμοκρασία με τυπικές τιμές μεταξύ 1,015 και 2 Σε σταθερή θερμοκρασία, η διαλυτότητα ενός αερίου σε συγκεκριμένο υγρό είναι ανάλογη της μερικής πίεσης του αερίου που βρίσκεται σε ισορροπία με το υγρό αυτό. 3 Η ροή της μάζας που μεταφέρεται ανά μονάδα χρόνου μέσω συγκεκριμένης επιφάνειας (flux) είναι ανάλογη της δύναμης που προκαλεί τη διάχυση (διαφορά συγκέντρωσης). 4
7 1, Συνήθως, για το νερό βρύσης, λαμβάνεται θ = 1,024 (Ramalho, 1983). τον όγκο του νερού την επιφάνεια της διεπιφάνειας νερού-φυσαλίδων (η οποία εξαρτάται από την παροχή αέρα και την ταχύτητα ανάδευσης) Επιλύοντας τη διαφορική εξίσωση (3.2) και ολοκληρώνοντας για χρονικό διάστημα από 0 έως t, με αντίστοιχη συγκέντρωση οξυγόνου C 0 και C t, προκύπτει (Lin et al., 2007) dc με αποτέλεσμα (αν C*=C κορεσμού ) C* C C* C Ct t t t Kat L Ka L dtln Ka L t e C0 0 C* C (3.5) C* C C* C Kat L C C* C* C e t Kat L L C C e C 1e t 0 ύ Αν θεωρήσουμε ότι τη στιγμή t=0 το σύστημα είναι πλήρως απο-οξυγονωμένο (δηλαδή C 0 =0), τότε η μεταβολή της συγκέντρωσης του οξυγόνου κατά τη φάση της οξυγόνωσης δίνεται από τη σχέση: Kat (3.6) Kat L C C 1 e (3.7) ύ Ικανότητα οξυγόνωσης Η ικανότητα οξυγόνωσης R ενός συστήματος αερισμού ορίζεται ως ο ρυθμός απορρόφησης οξυγόνου κατά τον αερισμό ενός πλήρως απο-οξυγονωμένου υγρού ως εξής: όπου V ο όγκος του νερού. R KLa V C ύ (3.8) 4 Στην περίπτωση υπολογισμού του συντελεστή μεταφοράς οξυγόνου ανά μονάδα όγκου αποβλήτου (αντί νερού βρύσης), πρέπει να ληφθεί υπόψη και (1) συντελεστής διόρθωσης α για τα ολικά διαλελυμένα στερεά με 0,3<α<1,2 και (2) συντελεστής διόρθωσης β για τα σωματίδια, τα άλατα και τις επιφανειακά ενεργές ουσίες με 0,7<β<0,98 (Lin et al., 2007). 5
8 3.3. Πειραματική διαδικασία Ο πειραματικός προσδιορισμός του συντελεστή μεταφοράς οξυγόνου σε νερό βασίζεται στη μέτρηση της συγκέντρωσης διαλελυμένου οξυγόνου. Για το σκοπό αυτό, επιλέγεται κατάλληλη μέθοδος μέτρησης, διαμορφώνεται κατάλληλη διάταξη και εκτελείται πείραμα σε τρία στάδια όπως περιγράφεται στις παραγράφους που ακολουθούν Μέθοδος μέτρησης διαλελυμένου οξυγόνου Για τη μέτρηση του διαλελυμένου οξυγόνου κατά την πειραματική διαδικασία της παρούσας άσκησης, εφαρμόζεται η ηλεκτρομετρική μέθοδος που βασίζεται στο ρυθμό διάχυσης του μοριακού οξυγόνου μέσω της μεμβράνης ενός πολαρογραφικού αισθητήρα που συνδέεται σε κατάλληλο όργανο μέτρησης. Γενικά, η μέθοδος αυτή προτιμάται έναντι της ιωδομετρικής (Winkler) σε εφαρμογές πεδίου ή όταν χρειάζεται συνεχής παρακολούθηση ή επί τόπου μέτρηση της συγκέντρωσης του διαλελυμένου οξυγόνου (APHA et al., 1998; ASCE, 2007; ASTM, 2012; EPA, 2002; Hitchman, 1978; Rounds et al., 2013). Επίσης, σημαντικό πλεονέκτημα της μεθόδου είναι ότι δεν επηρεάζεται από την παρουσία χημικών ειδών που αλλοιώνουν το αποτέλεσμα της χημικής μεθόδου (ASTM, 2012; EPA, 2002). Πολαρογραφικός αισθητήρας μέτρησης διαλελυμένου οξυγόνου Οι ηλεκτροχημικοί, πολαρογραφικοί αισθητήρες (Σχήμα 3.2) αποτελούνται από μια άνοδο και μια κάθοδο, οι οποίες βρίσκονται μέσα σε διάλυμα ηλεκτρολύτη και περικλείονται από μεμβράνη. Το υλικό της μεμβράνης (teflon, πολυαιθυλένιο, καουτσούκ, PVC ) είναι περατό από τα μόρια του οξυγόνου. Συνήθως, η κάθοδος είναι από χρυσό και η άνοδος από άργυρο. Το σύστημα συμπληρώνεται με κύκλωμα που εφαρμόζει συνεχή τάση 0,8 V στον αισθητήρα, η οποία πολώνει τα δυο ηλεκτρόδια, και ένα αμπερόμετρο που ανιχνεύει την απόκριση του αισθητήρα. Ο ηλεκτρολύτης (KCl), που υπάρχει κάτω από τη μεμβράνη, επιτρέπει την κίνηση του ηλεκτρικού ρεύματος από την άνοδο προς την κάθοδο (YSI, 2009). Αρχή λειτουργίας του πολαρογραφικού αισθητήρα μέτρησης διαλελυμένου οξυγόνου Τα μόρια του διαλελυμένου οξυγόνου διαχέονται, μέσω της μεμβράνης, προς τον αισθητήρα με ρυθμό ανάλογο της διαφοράς πίεσης που υπάρχει μεταξύ των δυο πλευρών της μεμβράνης. Στη συνέχεια, τα μόρια του οξυγόνου ανάγονται στην κάθοδο (αντίδραση (3.9)) ενώ ο άργυρος οξειδώνεται στη θετικά φορτισμένη άνοδο (αντίδραση (3.10)), παράγοντας ηλεκτρικό ρεύμα (ηλεκτρόνια) που κινούνται προς την κάθοδο και το όργανο μέτρησης. Σύμφωνα με τη συνολική αντίδραση οξειδοαναγωγής και λόγω της παρουσίας του ηλεκτρολύτη (αντίδραση (3.11)), σχηματίζεται στερεός χλωριούχος άργυρος. Η διαδικασία απεικονίζεται στο Σχήμα
9 O 2H O4e 4OH (3.9) 2 2 4Ag 4Ag 4e (3.10) O2 2H2O4Ag4KCl 4AgCl 4KOH (3.11) Σχήμα 3.2. Σχηματική απεικόνιση ηλεκτροχημικού, πολαρογραφικού αισθητήρα μέτρησης διαλελυμένου οξυγόνου (YSI, 2009) Σχήμα 3.3. Απεικόνιση της διαδικασίας οξειδοαναγωγής στο εσωτερικό του πολαρογραφικού αισθητήρα μέτρησης διαλελυμένου οξυγόνου (Walker, 1987) Εφόσον, το οξυγόνο ανάγεται (καταναλώνεται) γρήγορα στην κάθοδο, μπορεί να θεωρηθεί ότι η πίεση του οξυγόνου κάτω από τη μεμβράνη ισούται με μηδέν. Επομένως, η ποσότητα του οξυγόνου που διαχέεται μέσω της μεμβράνης είναι ανάλογη της μερικής πίεσης του οξυγόνου που βρίσκεται εκτός της μεμβράνης. Καθώς μεταβάλλεται η πίεση (συγκέντρωση) του οξυγόνου, σημειώνεται αντίστοιχη μεταβολή και στη διάχυση του οξυγόνου μέσω της 7
10 μεμβράνης, η οποία προκαλεί ανάλογη μεταβολή στην ένταση του ρεύματος που φθάνει στον αισθητήρα. Έτσι, όσο περισσότερο οξυγόνο περνά από τη μεμβράνη και ανάγεται στην κάθοδο, τόσο μεγαλύτερη είναι η ένταση του ρεύματος (το σήμα) που ανιχνεύει ο αισθητήρας: όταν αυξάνεται η συγκέντρωση του οξυγόνου, το σήμα αυξάνεται ενώ, αντίθετα, όταν μειώνεται η συγκέντρωση του διαλελυμένου οξυγόνου, το σήμα ελαττώνεται (YSI, 2009). Είναι σημαντικό να τονίσουμε ότι, κατά τη διάρκεια της μέτρησης, το διαλελυμένο οξυγόνο καταναλώνεται. Επομένως, είναι σημαντικό να υπάρχει συνεχής ανάδευση για να εξασφαλίζεται επαρκής ροή οξυγόνου στο άκρο του αισθητήρα. Αν δεν υπάρχει ροή, οι ενδείξεις θα είναι εσφαλμένα χαμηλές. ο χλωριούχος άργυρος που σχηματίζεται κατά την αντίδραση οξειδοαναγωγής, επικάθεται στην άνοδο. Επομένως, είναι απαραίτητο ανά τακτά διαστήματα να απομακρύνονται οι επικαθίσεις αυτές και να συμπληρώνεται ηλεκτρολύτης ώστε να διατηρείται η απόκριση του αισθητήρα. Βαθμονόμηση του πολαρογραφικού αισθητήρα μέτρησης διαλελυμένου οξυγόνου Η βαθμονόμηση του αισθητήρα διαλελυμένου οξυγόνου πραγματοποιείται με μέτρηση της συγκέντρωσης σε δυο σημεία (ASCE, 2007; ASTM, 2012): στο 0: σε πλήρως απο-οξυγονωμένο νερό (όπου η συγκέντρωση διαλελυμένου οξυγόνου ισούται με 0) και στη μέγιστη τιμή: σε νερό του οποίου η συγκέντρωση διαλελυμένου οξυγόνου προσεγγίζει το επίπεδο κορεσμού ή, εναλλακτικά, στον αέρα Πειραματική διάταξη Η πειραματική διάταξη (Εικόνα 3.1) περιλαμβάνει: ορθογώνιο δοχείο (1) με γνωστό όγκο νερού βρύσης οξυγονόμετρο (WTW oxi196) (2) με πολαρογραφικό αισθητήρα (3) για τη μέτρηση της συγκέντρωσης του διαλελυμένου οξυγόνου (σε mg/l ή % της συγκέντρωσης κορεσμού) και με δυνατότητα μέτρησης θερμοκρασίας (σε C) σύστημα αερισμού, το οποίο περιλαμβάνει: - αεροσυμπιεστή για την παραγωγή συμπιεσμένου αέρα - παροχόμετρο μεταβλητής διατομής (4) για τη ρύθμιση της παροχής (Ζαννής, 2013) - σωλήνα με διαχυτήρα τύπου δίσκου (Εικόνα 3.2) στο άκρο του (5) για τη δημιουργία φυσαλίδων αέρα μηχανικό αναδευτήρα (6) που εξασφαλίζει ομοιόμορφη κατανομή οξυγόνου και αέρα (φυσαλίδων) στο χώρο του δοχείου 5 Σε συνθήκες ισορροπίας, η μερική πίεση του οξυγόνου σε νερό κορεσμένο με αέρα ισούται με την μερική πίεση του οξυγόνου σε αέρα κορεσμένο με νερό (ASTM, 2012). 8
11 (α) (β) Εικόνα 3.1. Πειραματική διάταξη (αριστερά) και κάτοψη του δοχείου (δεξιά) κατά (α) το αρχικό στάδιο και (β) το στάδιο ανα-οξυγόνωσης.
12 Εικόνα 3.2. Διαχυτήρας αέρα τύπου δίσκου Στάδιο 1: Καταγραφή αρχικών συνθηκών Καταγράφονται οι αρχικές συνθήκες του πειράματος, δηλαδή η θερμοκρασία και η συγκέντρωση διαλελυμένου οξυγόνου του νερού. Για το σκοπό αυτό, ακολουθούνται τα εξής βήματα: Πλήρωση του δοχείου με συγκεκριμένο όγκο νερού βρύσης. Θέση σε λειτουργία του αναδευτήρα σε μέση ταχύτητα. Βαθμονόμηση του αισθητήρα του οξυγονόμετρου και εγκατάστασή του μέσα στο δοχείο. Καταγραφή των ενδείξεων του οργάνου (Πίνακας 3.1). Με βάση τις τιμές αυτές, υπολογίζεται η συγκέντρωση κορεσμού για το εξεταζόμενο σύστημα και συγκρίνεται η τιμή που προκύπτει με τη θεωρητική (βλ. Συμπληρωματικό υλικό 1). Πίνακας 3.1: Αρχικές συνθήκες πειράματος απo-οξυγόνωσης / ανα-οξυγόνωσης Παράμετρος Όγκος νερού (L) Θερμοκρασία (C) Συγκέντρωση διαλελυμένου οξυγόνου (mg/l) Συγκέντρωση διαλελυμένου οξυγόνου (% C κορεσμού ) Τιμή Στάδιο 2: Απο-οξυγόνωση του νερού Η απο-οξυγόνωση του νερού πραγματοποιείται με διάλυμα θειώδους νατρίου, σύμφωνα με την αντίδραση: 2 Co Na SO O 2Na SO (3.12) 10
13 Το θειώδες νάτριο είναι έντονα αναγωγικό, με αποτέλεσμα την οξείδωση του θείου και την αναγωγή του στοιχειακού οξυγόνου. Το οξυγόνο σε μορφή Ο 2- δεν ανιχνεύεται από τον αισθητήρα (Σχήμα 3.3). Η αντίδραση απο-οξυγόνωσης καταλύεται με διάλυμα CoCl 2 *6H 2 O καθώς τα ενυδατωμένα ιόντα κοβαλτίου (Co 2+ ) εκκινούν την αλυσιδωτή αντίδραση οξείδωσης του θείου από τη μορφή 2 SO 3 προς τη μορφή 2 SO (Chen et al., 1972). 4 Με βάση τη στοιχειομετρία της αντίδρασης (3.12), υπολογίζεται ο απαιτούμενος όγκος του διαλύματος Na 2 SO 3 10% κ.ό. 6 για τη δέσμευση του διαθέσιμου διαλελυμένου οξυγόνου (ατομικό βάρος Na: 23, S: 32, O: 16). Επίσης, υπολογίζεται ο απαιτούμενος όγκος του διαλύματος CoCl 2 *6H 2 O 1% κ.ό. έτσι ώστε η συγκέντρωση των ιόντων κοβαλτίου στο νερό να κυμαίνεται μεταξύ 0,5-1,5 mg/l (ατομικό βάρος Co: 59, Cl: 35,5, H: 1, O: 16). Παρατήρηση Ενώ για την προσθήκη του καταλύτη ισχύει ευρεία περιοχή συγκεντρώσεων, το διάλυμα θειώδους νατρίου προστίθεται με ακρίβεια και σε ποσότητα μικρότερη από τη στοιχειομετρικά απαιτούμενη έτσι ώστε η τελική συγκέντρωση του διαλελυμένου οξυγόνου να προσεγγίζει το 1 mg/l. Διαφορετικά, επιτυγχάνεται μεν πλήρης απο-οξυγόνωση του νερού αλλά τυχόν περίσσεια αντιδραστηρίου που δεν καταναλώνεται σύμφωνα με την αντίδραση (3.12) αντιδρά κατά το στάδιο της ανα-οξυγόνωσης, με αποτέλεσμα τη λήψη εσφαλμένων μετρήσεων! Στάδιο 3: Ανα-οξυγόνωση του νερού Για την ανα-οξυγόνωση του νερού, μειώνεται η ταχύτητα ανάδευσης, τίθεται σε λειτουργία το σύστημα αερισμού και ρυθμίζεται το παροχόμετρο ώστε να διοχετεύεται στο δοχείο συμπιεσμένος αέρας με σταθερή παροχή 2 L/min. Παρακολουθείται η ένδειξη του οξυγονόμετρου και, με τη βοήθεια χρονομέτρου, καταγράφονται οι χρονικές στιγμές οπότε παρατηρείται μεταβολή της συγκέντρωσης του διαλελυμένου οξυγόνου. Έτσι, συμπληρώνεται πίνακας με ζεύγη τιμών χρόνου-συγκέντρωσης (όπως ο Πίνακας 3.2) μέχρι η συγκέντρωση του διαλελυμένου οξυγόνου να φθάσει στο 80-90% της συγκέντρωσης κορεσμού. Πίνακας 3.2. Καταγραφή μετρήσεων Χρόνος (s) 0 Συγκέντρωση διαλελυμένου οξυγόνου (mg/l) 6 Περιεκτικότητα επί τοις εκατό κατ όγκο (w/v, % κ.ό.) g διαλυμένης ουσίας ανά 100 ml διαλύματος 11
14 3.4. Επεξεργασία και σχολιασμός πειραματικών δεδομένων Ζητούμενο 1: Μεταβολή της συγκέντρωσης του διαλελυμένου οξυγόνου σε σχέση με το χρόνο Για το σκοπό αυτό, ακολουθούνται τα εξής βήματα: Αποτύπωση των αποτελεσμάτων των μετρήσεων που συλλέχθηκαν κατά τη φάση αναοξυγόνωσης (Πίνακας 3.2) σε διάγραμμα C-t, όπου θα εμφανίζεται και η συγκέντρωση κορεσμού του μελετούμενου συστήματος. Ποιοτικός σχολιασμός του διαγράμματος ως προς τη μορφή της σχηματιζόμενης καμπύλης, το ρυθμό οξυγόνωσης σε σχέση με το έλλειμμα σε οξυγόνο κ.λπ. Υπολογισμός των παραμέτρων της εξίσωσης (3.6) με ανάλυση των πειραματικών δεδομένων μέσω μη γραμμικής παλινδρόμησης στο MS Excel (Brown, 2001) ή με χρήση διαθέσιμων υπολογιστικών φύλλων (βλ. Συμπληρωματικό υλικό 3 και 4) Ζητούμενο 2: Γραφικός υπολογισμός του συντελεστή μεταφοράς οξυγόνου στο νερό Το K L a δίνεται από την κλίση του διαγράμματος lnδc-t, όπου ΔC το έλλειμμα οξυγόνου. Για το σκοπό αυτό, ακολουθούνται τα εξής βήματα: Υπολογισμός του ελλείμματος οξυγόνου και του φυσικού λογαρίθμου του ελλείμματος για όλα τα ζεύγη τιμών (t,c) του πίνακα μετρήσεων και αποτύπωση των τιμών σε διάγραμμα lnδc-t. Αποτύπωση στο διάγραμμα της βέλτιστης ευθείας που ικανοποιεί τα πειραματικά σημεία με τη μέθοδο των ελαχίστων τετραγώνων (ή γραμμική γραμμή τάσης, με τη βοήθεια του MS Excel), δηλαδή της ευθείας y=ax+b, r 2 1. Υπολογισμός του συντελεστή μεταφοράς οξυγόνου στο νερό (K L a) από την κλίση της ευθείας και υπολογισμός της ικανότητας οξυγόνωσης R (βλ. Συμπληρωματικό υλικό 2). Σύγκριση του αποτελέσματος με το αποτέλεσμα της παραγράφου Πώς θα επηρεαστεί το γράφημα (και η τιμή του K L a) αν το ίδιο ακριβώς πείραμα εκτελεστεί σε μεγαλύτερο ή μικρότερο υψόμετρο; Αν εκτελεστεί με θαλασσινό νερό; 12
15 Το K L a δίνεται από την κλίση του διαγράμματος lnδc-t, όπου ΔC το έλλειμμα οξυγόνου. Απόδειξη: dc dc dcκορ Ka L Cκορ C Ka L dt Ka L dt dt C C C C κορ κορ 1 ln Cκορ C dcκορ C KLadt lncκορ C KLat KLa C C t κορ C Για C αρχικό = C 1 (τη χρονική στιγμή t 1 ) και C τελικό = C 2 (τη χρονική στιγμή t 2 ), είναι: κορ 1 κορ 2 ln C C ln C C Ka L t t 2 1 Η έκφραση αυτή του K L a ισοδυναμεί με την εφαπτομένη της γωνίας ω του διαγράμματος ln(δc)- t, δηλαδή με την κλίση της ευθείας y=ax+b, ως εξής: Ζητούμενο 3: Απόδοση συστήματος αερισμού Η απόδοση του εφαρμοζόμενου συστήματος αερισμού (ε) αξιολογείται με βάση την αξιοποίηση του παρεχόμενου αέρα για την οξυγόνωση του συστήματος. Για το σκοπό αυτό, υπολογίζεται το ποσοστό του οξυγόνου που απορροφήθηκε από το νερό κατά τη διαδικασία της ανα-οξυγόνωσης σε σχέση με τη συνολική ποσότητα του οξυγόνου που διοχετεύθηκε (δίνεται η περιεκτικότητα του αέρα σε οξυγόνο ίση με 21% κ.ό.), ως εξής: ά 2 ή 100% ά ύ 2 (3.13) Να σχολιάσετε το αποτέλεσμα και να συγκρίνετε την τιμή με τις αποδόσεις τυπικών συστημάτων αερισμού που χρησιμοποιούνται στους βιολογικούς αντιδραστήρες για την επεξεργασία λυμάτων. 13
16 Ζητούμενο 4: Ερωτήσεις κατανόησης Απαντήστε τις παρακάτω ερωτήσεις κατανόησης, αιτιολογώντας την απάντησή σας. (1) Αν η συγκέντρωση του διαλελυμένου οξυγόνου σε ένα δείγμα νερού είναι 9,07 mg/l, τότε: (α) η θερμοκρασία του νερού είναι 20 C με βάση τον πίνακα διαλυτότητας του οξυγόνου. (β) το νερό είναι κορεσμένο σε διαλελυμένο οξυγόνο. (γ) αν η θερμοκρασία του νερού είναι 15 C (συγκέντρωση κορεσμού οξυγόνου 10,07 mg/l), το δείγμα είναι: i) κατά 90% κορεσμένο ii) κατά 60% κορεσμένο iii) κατά 40% κορεσμένο iv) κατά 1% κορεσμένο v) κατά 1 mg/l ελλειμματικό σε οξυγόνο σε σχέση με την τιμή κορεσμού (2) Αν ένα δείγμα νερού έχει θερμοκρασία 25 C, η συγκέντρωση του διαλελυμένου οξυγόνου σε αυτό είναι: 8,24 mg/l (τιμή κορεσμού στους 25 C) το 60% της αντίστοιχης τιμής κορεσμού μικρότερο ή οριακά ίσο από 8,24 mg/l μηδέν περίπου μηδέν δεν γνωρίζουμε (3) Ποιο από τα παρακάτω δείγματα νερού έχει μεγαλύτερη συγκέντρωση διαλελυμένου οξυγόνου: Νερό 60% κορεσμένο σε οξυγόνο σε θερμοκρασία 25 C Νερό 80% κορεσμένο σε οξυγόνο σε θερμοκρασία 25 C Νερό 60% κορεσμένο σε οξυγόνο σε θερμοκρασία 20 C Νερό κορεσμένο σε οξυγόνο σε θερμοκρασία 25 C Νερό στους 25 C στο οποίο έχει γίνει απο-οξυγόνωση 14
17 Συμπληρωματικό υλικό 1. Πίνακες διαλυτότητας οξυγόνου στο νερό, U.S. Geological Survey: 2. Υπόδειγμα επεξεργασίας πειραματικών δεδομένων (Τσέζος et al., 2005) 3. Εικονικό πείραμα αποξυγόνωσης-αναοξυγόνωσης και επεξεργασία των αποτελεσμάτων, Michigan Technological University 2003: 4. Πρόγραμμα εκτίμησης παραμέτρων κατά ASCE (ASCE, 2007): 5. Παρουσίαση YSI, Dissolved Oxygen Technologies - Part 1. Selecting the Right Sensor: 6. Παρουσίαση YSI, Dissolved Oxygen Technologies - Part 2. Getting the Best DO Data: 7. Παρουσίαση KROHNE, Measuring Principle of Variable Area Flowmeters: Βιβλιογραφία APHA, AWWA & WEF (1998). Dissolved oxygen. in: Standard methods for the examination of water and wastewater, 20th ed. ASCE (2007). Measurement of oxygen transfer in clean water: ASCE standard, ASCE/EWRI Reston, Va.: American Society of Civil Engineers. ASTM (2012). Standard test methods for dissolved oxygen in water: ASTM standard D888-12e1. West Conshohocken, PA: ASTM International. Benson, B.B. & Krause, D. (1984). The concentration and isotopic fractionation of oxygen dissolved in freshwater and seawater in equilibrium with the atmosphere. Limnology and Oceanography 29(3): Brown, A.M. (2001). A step-by-step guide to non-linear regression analysis of experimental data using a Microsoft Excel spreadsheet. Computer Methods and Programs in Biomedicine 65(3): Chen, T.-I. & Barron, C.H. (1972). Some aspects of the homogeneous kinetics of sulfite oxidation. Industrial & Engineering Chemistry Fundamentals 11(4): EPA (2002). Dissolved Oxygen, EPA Method US Environmental Protection Agency. Hitchman, M.L. (1978). Measurement of dissolved oxygen. New York: Wiley. Lin, S. & Lee, C.C. (2007). Water and wastewater calculations manual, 2nd ed. New York: McGraw-Hill. Ramalho, R.S. (1983). Theory and practice of aeration in wastewater treatment. in: Introduction to wastewater treatment processes, 2nd ed. New York: Academic Press, pp Rounds, S.A., Wilde, F.D. & Ritz, G.F. (2013). Dissolved oxygen (ver. 3.0). in: Wilde, F.D. (Ed.) 15
18 USGS Techniques of Water-Resources Investigations, Book 9: National Field Manual for the Collection of Water-Quality Data, Chapter A6: Field Measurements. U.S. Geological Survey, pp Villadsen, J., Nielsen, J.H. & Lideń, G. (2011). Bioreaction engineering principles, 3rd ed. New York: Springer. Walker, D. (1987). The use of the oxygen electrode and fluorescence probes in simple measurements of photosynthesis. Sheffield: Research Institute for Photosynthesis, University of Sheffield. Whitman, W.G. (1962). The two film theory of gas absorption. International Journal of Heat and Mass Transfer 5(5): YSI (2009). The Dissolved Oxygen Handbook. Yellow Springs, Ohio: YSI Inc. Απαιτούμενη ποιότητα των επιφανειακών νερών που προορίζονται για: «πόσιμα», «κολύμβηση», «διαβίωση ψαριών σε γλυκά νερά» και «καλλιέργεια και αλιεία οστρακοειδών», μέθοδοι μέτρησης, συχνότητα δειγματοληψίας και ανάλυση των επιφανειακών νερών που προορίζονται για πόσιμα, σε συμμόρφωση με τις οδηγίες του Συμβουλίου των Ευρωπαϊκών Κοινοτήτων 75/440/ΕΟΚ, 76/160/ΕΟΚ, 78/659/ΕΟΚ, 79/293/ΕΟΚ και 79/869/ΕΟΚ (1986), Υ.Α. οικ /1352/1986, Ελλάδα: Εφημερίς της Κυβερνήσεως της Ελληνικής Δημοκρατίας, Τεύχος Β, Αρ. φύλλου 438, pp Ζαννής, Γ. (2013): Παροχόμετρα πλωτήρα (ροτάμετρα). Ιούνιος Τσέζος, Μ., Ρεμουντάκη, Ε., Χατζηκιοσεγιάν, Α. & Βιδάλη, Ρ. (2005). Βοηθητικές σημειώσεις εργαστηριακών ασκήσεων για το μάθημα "Περιβάλλον Ι - Εισαγωγή στην Επιστήμη και Τεχνολογία Προστασίας του Περιβάλλοντος". Αθήνα: Εθνικό Μετσόβιο Πολυτεχνείο. Τσέζος, Μ. & Ρεμουντάκη, Ε. (2006). Βοηθητικές σημειώσεις για το μάθημα "Περιβάλλον Ι - Εισαγωγή στην Επιστήμη και Τεχνολογία Προστασίας του Περιβάλλοντος". Αθήνα: Εθνικό Μετσόβιο Πολυτεχνείο. 16
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΤΟ ΝΕΡΟ
 ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΤΟ ΝΕΡΟ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΕ ΝΕΡΟ ΓΕΝΙΚΑ Με το πείραμα αυτό μπορούμε να προσδιορίσουμε δύο βασικές παραμέτρους που χαρακτηρίζουν ένα
ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΤΟ ΝΕΡΟ ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΣΥΝΤΕΛΕΣΤΗ ΜΕΤΑΦΟΡΑΣ ΟΞΥΓΟΝΟΥ ΣΕ ΝΕΡΟ ΓΕΝΙΚΑ Με το πείραμα αυτό μπορούμε να προσδιορίσουμε δύο βασικές παραμέτρους που χαρακτηρίζουν ένα
Προσδιορισμός φυσικοχημικών παραμέτρων υγρών αποβλήτων και υδάτων
 Προσδιορισμός φυσικοχημικών παραμέτρων υγρών αποβλήτων και υδάτων (DO - BOD - COD - TOC) Χ. Βασιλάτος Οργανική ύλη Αποξυγόνωση επιφανειακών και υπογείων υδάτων Οι οργανικές ύλες αποτελούν πολύ σοβαρό ρύπο,
Προσδιορισμός φυσικοχημικών παραμέτρων υγρών αποβλήτων και υδάτων (DO - BOD - COD - TOC) Χ. Βασιλάτος Οργανική ύλη Αποξυγόνωση επιφανειακών και υπογείων υδάτων Οι οργανικές ύλες αποτελούν πολύ σοβαρό ρύπο,
Χημική Τεχνολογία. Ενότητα 6: Διαλυμένο Οξυγόνο. Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε.
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Ενότητα 6: Διαλυμένο Οξυγόνο Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες Χρήσης Το παρόν
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Ενότητα 6: Διαλυμένο Οξυγόνο Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες Χρήσης Το παρόν
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα. Χημική Τεχνολογία. Εργαστηριακό Μέρος
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 6: Διαλυμένο Οξυγόνο Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 6: Διαλυμένο Οξυγόνο Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων Μηχανικών Τ.Ε. Άδειες
ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ II
 4-1 ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ II Θέμα ασκήσεως: Ποτενσιομετρική τιτλοδότηση, προσδιορισμός κανονικού δυναμικού ηλεκτροδίου, πειραματική επαλήθευση της εξισώσεως Nernst. Αρχή μεθόδου: Μετρείται η ΗΕΔ γαλβανικού
4-1 ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ II Θέμα ασκήσεως: Ποτενσιομετρική τιτλοδότηση, προσδιορισμός κανονικού δυναμικού ηλεκτροδίου, πειραματική επαλήθευση της εξισώσεως Nernst. Αρχή μεθόδου: Μετρείται η ΗΕΔ γαλβανικού
Πείραμα 2 Αν αντίθετα, στο δοχείο εισαχθούν 20 mol ΗΙ στους 440 ºC, τότε το ΗΙ διασπάται σύμφωνα με τη χημική εξίσωση: 2ΗΙ(g) H 2 (g) + I 2 (g)
 Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
Α. Θεωρητικό μέρος Άσκηση 5 η Μελέτη Χημικής Ισορροπίας Αρχή Le Chatelier Μονόδρομες αμφίδρομες αντιδράσεις Πολλές χημικές αντιδράσεις οδηγούνται, κάτω από κατάλληλες συνθήκες, σε κατάσταση ισορροπίας
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ ΧΗΜΕΙΑ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Η σωστή τετράδα κβαντικών αριθμών για το μονήρες
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Α1. Η σωστή τετράδα κβαντικών αριθμών για το μονήρες
Δείτε εδώ τις Διαφάνειες για την Άσκηση 8. Περιγραφή υπολογισμών της Άσκησης 8 του Εργαστηρίου ΜΧΔ
 Δείτε εδώ τις Διαφάνειες για την Άσκηση 8 Περιγραφή υπολογισμών της Άσκησης 8 του Εργαστηρίου ΜΧΔ Διάγραμμα Ροής Βήμα 1. Υπολογισμός της πραγματικής αρχικής συγκέντρωσης του διαλύματος κιτρικού οξέος στη
Δείτε εδώ τις Διαφάνειες για την Άσκηση 8 Περιγραφή υπολογισμών της Άσκησης 8 του Εργαστηρίου ΜΧΔ Διάγραμμα Ροής Βήμα 1. Υπολογισμός της πραγματικής αρχικής συγκέντρωσης του διαλύματος κιτρικού οξέος στη
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων. Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης
 Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
Ταξινόμηση της ύλης Διαλύματα Περιεκτικότητες διαλυμάτων Χημεία Α Λυκείου Διδ. Εν. 1.5 π. Ευάγγελος Μαρκαντώνης 2 ο ΓΕΛ Αργυρούπολης Μακροσκοπική ταξινόμηση της ύλης ΥΛΗ Καθορισµένη (καθαρή) ουσία όχι
ΑΣΚΗΣΗ 8 - Μελέτη της ηλεκτρόλυσης CuSO 4 ΑΣΚΗΣΗ 8. Μελέτη της ηλεκτρόλυσης CuSO 4
 ΑΣΚΗΣΗ 8 Μελέτη της ηλεκτρόλυσης CuSO 4 Συσκευές: Ένα τροφοδοτικό συνεχούς τάσης, ένα αμπερόμετρο, ένα χρονόμετρο και ένα βολτάμετρο. Το βολτάμετρο ή κουλομβόμετρο αποτελείται από ένα γυάλινο δοχείο που
ΑΣΚΗΣΗ 8 Μελέτη της ηλεκτρόλυσης CuSO 4 Συσκευές: Ένα τροφοδοτικό συνεχούς τάσης, ένα αμπερόμετρο, ένα χρονόμετρο και ένα βολτάμετρο. Το βολτάμετρο ή κουλομβόμετρο αποτελείται από ένα γυάλινο δοχείο που
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα. Χημική Τεχνολογία
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Ενότητα 8.1: Βιοχημικά Απαιτούμενο Οξυγόνο (Biochemical Oxygen Demand, BOD) Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Ενότητα 8.1: Βιοχημικά Απαιτούμενο Οξυγόνο (Biochemical Oxygen Demand, BOD) Ευάγγελος Φουντουκίδης Τμήμα Μηχανολόγων
Από πού προέρχεται η θερμότητα που μεταφέρεται από τον αντιστάτη στο περιβάλλον;
 3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
3. ΗΛΕΚΤΡΙΚΗ ΕΝΕΡΓΕΙΑ Ένα ανοικτό ηλεκτρικό κύκλωμα μετατρέπεται σε κλειστό, οπότε διέρχεται από αυτό ηλεκτρικό ρεύμα που μεταφέρει ενέργεια. Τα σπουδαιότερα χαρακτηριστικά της ηλεκτρικής ενέργειας είναι
ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Ι & ΙΙ Εργαστηριακή Άσκηση 4: ΞΗΡΑΝΣΗ (σε ρεύμα αέρα)
 Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
Γενική Χημεία. Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής
 Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
Γενική Χημεία Νίκος Ξεκουκουλωτάκης Επίκουρος Καθηγητής Πολυτεχνείο Κρήτης Τμήμα Μηχανικών Περιβάλλοντος Γραφείο Κ2.125, τηλ.: 28210-37772 e-mail:nikosxek@gmail.com Περιεχόμενα Διαλύματα Γραμμομοριακή
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ. ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ
 ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
ΤΕΧΝΙΚΗ ΧΗΜΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ ΕΡΓΑΣΤΗΡΙΑΚΕΣ ΑΣΚΗΣΕΙΣ 5 ο ΕΞΑΜΗΝΟ Μελέτη της κινητικής αποχρωματισμού πρότυπων διαλυμάτων αζωχρωμάτων μέσω της καταλυτικής διάσπασης υπεροξειδίου του υδρογόνου σε αντιδραστήρα
5.1 ΥΠΟΛΟΓΙΣΜΟΣ ΤΟΥ ΓΡΑΜΜΟΙΣΟΔΥΝΑΜΟΥ ΙΟΝΤΟΣ ΟΞΥΓΟΝΟΥ, ΥΔΡΟΓΟΝΟΥ ΚΑΙ ΧΑΛΚΟΥ ΜΕ ΗΛΕΚΤΡΟΛΥΣΗ
 5.1 ΑΣΚΗΣΗ 5 ΥΠΟΛΟΓΙΣΜΟΣ ΤΟΥ ΓΡΑΜΜΟΙΣΟΔΥΝΑΜΟΥ ΙΟΝΤΟΣ ΟΞΥΓΟΝΟΥ, ΥΔΡΟΓΟΝΟΥ ΚΑΙ ΧΑΛΚΟΥ ΜΕ ΗΛΕΚΤΡΟΛΥΣΗ Α' ΜΕΡΟΣ: Ηλεκτρόλυση του νερού. ΘΕΜΑ: Εύρεση της μάζας οξυγόνου και υδρογόνου που εκλύονται σε ηλεκτρολυτική
5.1 ΑΣΚΗΣΗ 5 ΥΠΟΛΟΓΙΣΜΟΣ ΤΟΥ ΓΡΑΜΜΟΙΣΟΔΥΝΑΜΟΥ ΙΟΝΤΟΣ ΟΞΥΓΟΝΟΥ, ΥΔΡΟΓΟΝΟΥ ΚΑΙ ΧΑΛΚΟΥ ΜΕ ΗΛΕΚΤΡΟΛΥΣΗ Α' ΜΕΡΟΣ: Ηλεκτρόλυση του νερού. ΘΕΜΑ: Εύρεση της μάζας οξυγόνου και υδρογόνου που εκλύονται σε ηλεκτρολυτική
ΚΕΦΑΛΑΙΟ 8: ΜΕΤΡΗΣΗ ΑΤΜΟΣΦΑΙΡΙΚΩΝ ΣΥΣΤΑΤΙΚΩΝ ΚΑΘ ΥΨΟΣ (ΟΖΟΝΤΟΒΟΛΙΣΗ)
 ΚΕΦΑΛΑΙΟ 8: ΜΕΤΡΗΣΗ ΑΤΜΟΣΦΑΙΡΙΚΩΝ ΣΥΣΤΑΤΙΚΩΝ ΚΑΘ ΥΨΟΣ (ΟΖΟΝΤΟΒΟΛΙΣΗ) 8.1 Γενικά Η γνώση της κατακόρυφης κατανομής της συγκέντρωσης του ατμοσφαιρικού όζοντος είναι ιδιαίτερα σημαντική για την κατανόηση
ΚΕΦΑΛΑΙΟ 8: ΜΕΤΡΗΣΗ ΑΤΜΟΣΦΑΙΡΙΚΩΝ ΣΥΣΤΑΤΙΚΩΝ ΚΑΘ ΥΨΟΣ (ΟΖΟΝΤΟΒΟΛΙΣΗ) 8.1 Γενικά Η γνώση της κατακόρυφης κατανομής της συγκέντρωσης του ατμοσφαιρικού όζοντος είναι ιδιαίτερα σημαντική για την κατανόηση
Θέµατα προηγούµενων εξεταστικών περιόδων. 1 ο Θέµα Ιανουαρίου 2005
 Θέµατα προηγούµενων εξεταστικών περιόδων 1 ο Θέµα Ιανουαρίου 2005 Σε ένα επίπεδο ηλεκτρόδιο ενεργού επιφάνειας 2 cm 2, που χρησιµοποιείται ως άνοδος σε µία ηλεκτρολυτική κυψέλη που περιέχει διάλυµα 2*10-3
Θέµατα προηγούµενων εξεταστικών περιόδων 1 ο Θέµα Ιανουαρίου 2005 Σε ένα επίπεδο ηλεκτρόδιο ενεργού επιφάνειας 2 cm 2, που χρησιµοποιείται ως άνοδος σε µία ηλεκτρολυτική κυψέλη που περιέχει διάλυµα 2*10-3
Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ
 ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΤΟΧΟΙ Εργαστηριακή άσκηση 1: ΠΑΡΑΓΟΝΤΕΣ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΤΑΧΥΤΗΤΑ ΔΙΑΛΥΣΗΣ Στο τέλος του πειράματος αυτού θα πρέπει να μπορείς : 1. Να αναγνωρίζεις ότι το φαινόμενο της διάλυσης είναι
Η ΑΝΑΓΚΗ ΓΙΑ ΠΟΣΟΤΙΚΟΠΟΙΗΣΗ ΣΤΗΝ ΕΝΟΡΓΑΝΗ ΑΝΑΛΥΣΗ
 Η ΑΝΑΓΚΗ ΓΙΑ ΠΟΣΟΤΙΚΟΠΟΙΗΣΗ ΣΤΗΝ ΕΝΟΡΓΑΝΗ ΑΝΑΛΥΣΗ Οι Ενόργανες Μέθοδοι Ανάλυσης είναι σχετικές μέθοδοι και σχεδόν στο σύνολο τους παρέχουν την αριθμητική τιμή μιας φυσικής ή φυσικοχημικής ιδιότητας, η
Η ΑΝΑΓΚΗ ΓΙΑ ΠΟΣΟΤΙΚΟΠΟΙΗΣΗ ΣΤΗΝ ΕΝΟΡΓΑΝΗ ΑΝΑΛΥΣΗ Οι Ενόργανες Μέθοδοι Ανάλυσης είναι σχετικές μέθοδοι και σχεδόν στο σύνολο τους παρέχουν την αριθμητική τιμή μιας φυσικής ή φυσικοχημικής ιδιότητας, η
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2019 Β ΦΑΣΗ ΧΗΜΕΙΑ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α4 να γράψετε στο τετράδιό
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Σάββατο 20 Απριλίου 2019 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α4 να γράψετε στο τετράδιό
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ. Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια.
 ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
ΦΥΣΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ Οι φυσικές καταστάσεις της ύλης είναι η στερεή, η υγρή και η αέρια. Οι μεταξύ τους μεταβολές εξαρτώνται από τη θερμοκρασία και την πίεση και είναι οι παρακάτω: ΣΗΜΕΙΟ ΤΗΞΗΣ ΚΑΙ ΣΗΜΕΙΟ
Πειραματική διαδικασία προσδιορισμού ιοντικής σύστασης ατμοσφαιρικών σωματιδίων
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ ΜΕΤΑΛΛΟΥΡΓΩΝ Τομέας Μεταλλουργίας και Τεχνολογίας Υλικών Εργαστήριο Επιστήμης και Τεχνολογίας Προστασίας του Περιβάλλοντος στη Μεταλλουργία και Τεχνολογία
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΜΗΧΑΝΙΚΩΝ ΜΕΤΑΛΛΕΙΩΝ ΜΕΤΑΛΛΟΥΡΓΩΝ Τομέας Μεταλλουργίας και Τεχνολογίας Υλικών Εργαστήριο Επιστήμης και Τεχνολογίας Προστασίας του Περιβάλλοντος στη Μεταλλουργία και Τεχνολογία
M M n+ + ne (1) Ox + ne Red (2) i = i Cdl + i F (3) de dt + i F (4) i = C dl. e E Ecorr
 Επιταχυνόμενες μέθοδοι μελέτης της φθοράς: Μέθοδος Tafel και μέθοδος ηλεκτροχημικής εμπέδησης Αντώνης Καραντώνης, και Δημήτρης Δραγατογιάννης 1 Σκοπός της άσκησης Στην άσκηση αυτή θα μελετηθεί η διάβρωση
Επιταχυνόμενες μέθοδοι μελέτης της φθοράς: Μέθοδος Tafel και μέθοδος ηλεκτροχημικής εμπέδησης Αντώνης Καραντώνης, και Δημήτρης Δραγατογιάννης 1 Σκοπός της άσκησης Στην άσκηση αυτή θα μελετηθεί η διάβρωση
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ. ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΤΕΣΣΕΡΕΙΣ (4) ΕΠΙΜΕΛΕΙΑ ΘΕΜΑΤΩΝ: ΚΑΛΑΜΑΡΑΣ ΓΙΑΝΝΗΣ xhmeiastokyma.
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΤΕΣΣΕΡΕΙΣ (4) ΕΠΙΜΕΛΕΙΑ ΘΕΜΑΤΩΝ: ΚΑΛΑΜΑΡΑΣ ΓΙΑΝΝΗΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α5 να γράψετε τον αριθμό της ερώτησης και δίπλα
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Α ΛΥΚΕΙΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΤΕΣΣΕΡΕΙΣ (4) ΕΠΙΜΕΛΕΙΑ ΘΕΜΑΤΩΝ: ΚΑΛΑΜΑΡΑΣ ΓΙΑΝΝΗΣ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α5 να γράψετε τον αριθμό της ερώτησης και δίπλα
Θέμα: Έρευνα για την αλατότητα του νερού
 Τίτλος: Έρευνα για την αλατότητα του νερού Θέμα: Έρευνα για την αλατότητα του νερού Χρόνος: 90 λεπτά (2 μαθήματα) Ηλικία: μαθητές 14 15 χρονών Διαφοροποίηση: Οι χαρισματικοί μαθητές καλούνται να καταγράψουν
Τίτλος: Έρευνα για την αλατότητα του νερού Θέμα: Έρευνα για την αλατότητα του νερού Χρόνος: 90 λεπτά (2 μαθήματα) Ηλικία: μαθητές 14 15 χρονών Διαφοροποίηση: Οι χαρισματικοί μαθητές καλούνται να καταγράψουν
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2019 A ΦΑΣΗ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Πέμπτη 3 Ιανουαρίου 2019 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α4 να γράψετε στο τετράδιό
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Πέμπτη 3 Ιανουαρίου 2019 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α4 να γράψετε στο τετράδιό
Άσκηση 7η. Χημική Ισορροπία. Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών
 Άσκηση 7η Χημική Ισορροπία Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Η έννοια της Χημικής Ισορροπίας Υπάρχουν χηµικές αντιδράσεις που εξελίσσονται προς µία µόνο μόνο κατεύθυνση, όπως π.χ. η σύνθεση
Άσκηση 7η Χημική Ισορροπία Εργαστήριο Χημείας Τμήμα ΔΕΑΠΤ Πανεπιστήμιο Πατρών Η έννοια της Χημικής Ισορροπίας Υπάρχουν χηµικές αντιδράσεις που εξελίσσονται προς µία µόνο μόνο κατεύθυνση, όπως π.χ. η σύνθεση
ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ - ΠΑΡΑΔΕΙΓΜΑ
 ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ - ΠΑΡΑΔΕΙΓΜΑ ΘΕΜΑ 1ο Για τις παρακάτω ερωτήσεις Α1-Α3 να μεταφέρετε στο φύλλο απαντήσεων τον αριθμό της ερώτησης και δίπλα μόνο το γράμμα που αντιστοιχεί στη σωστή απάντηση.
ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ Α ΛΥΚΕΙΟΥ - ΠΑΡΑΔΕΙΓΜΑ ΘΕΜΑ 1ο Για τις παρακάτω ερωτήσεις Α1-Α3 να μεταφέρετε στο φύλλο απαντήσεων τον αριθμό της ερώτησης και δίπλα μόνο το γράμμα που αντιστοιχεί στη σωστή απάντηση.
ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ (Α. Χημική Θερμοδυναμική) 1 η Άσκηση
 ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 004-05 (Α. Χημική Θερμοδυναμική) η Άσκηση Στερεό CO, βάρους 6 g, εισάγεται μέσα σε κενό δοχείο όγκου 00 cm 3 που βρίσκεται συνεχώς σε θερμοκρασία δωματίου (300
ΘΕΜΑΤΑ ΤΕΛΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 004-05 (Α. Χημική Θερμοδυναμική) η Άσκηση Στερεό CO, βάρους 6 g, εισάγεται μέσα σε κενό δοχείο όγκου 00 cm 3 που βρίσκεται συνεχώς σε θερμοκρασία δωματίου (300
3 η Εργαστηριακή άσκηση Γαλβανικά στοιχεία
 Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Εργαστηριακές Ασκήσεις Φυσικοχημείας 3 η Εργαστηριακή άσκηση Γαλβανικά στοιχεία Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό
Τμήμα Διαχείρισης Περιβάλλοντος & Φυσικών Πόρων, Πολυτεχνική Σχολή Εργαστηριακές Ασκήσεις Φυσικοχημείας 3 η Εργαστηριακή άσκηση Γαλβανικά στοιχεία Γαλάνη Απ. Αγγελική, Χημικός PhD Εργαστηριακό Διδακτικό
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΘΕΜΑ Α ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ & Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 3 ΙΟΥΛΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΘΕΜΑ Α ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ & Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΔΕΥΤΕΡΑ 3 ΙΟΥΛΙΟΥ 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ:
Ημερομηνία: Σάββατο 5 Ιανουαρίου 2019 Διάρκεια Εξέτασης: 3 ώρες
 ΤΑΞΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ημερομηνία: Σάββατο 5 Ιανουαρίου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις ημιτελείς προτάσεις Α1 Α4 να γράψετε στο τετράδιό σας τον αριθμό
ΤΑΞΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ημερομηνία: Σάββατο 5 Ιανουαρίου 2019 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις ημιτελείς προτάσεις Α1 Α4 να γράψετε στο τετράδιό σας τον αριθμό
Διάβρωση και Προστασία. Εαρινό εξάμηνο Ακ. Έτους Μάθημα 6ο
 Διάβρωση και Προστασία Εαρινό εξάμηνο Ακ. Έτους 2016-17 Μάθημα 6ο Διάγραμμα δυναμικού Ε- ph για σίδηρο εμβαπτισμένο σε διάλυμα Fe 2+ με ενεργότητα = 1 Σε ph=2 για διάλυμα περιεκτικότητας σε ιόντα Fe 2+
Διάβρωση και Προστασία Εαρινό εξάμηνο Ακ. Έτους 2016-17 Μάθημα 6ο Διάγραμμα δυναμικού Ε- ph για σίδηρο εμβαπτισμένο σε διάλυμα Fe 2+ με ενεργότητα = 1 Σε ph=2 για διάλυμα περιεκτικότητας σε ιόντα Fe 2+
Όνομα :... Ημερομηνία:... /... /...
 Όνομα :... Ημερομηνία:... /... /... Επαναληπτικό Διαγώνισμα Χημείας Γ Λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών (1 ο + 2 ο + 3 ο + 4 ο + 5 ο ΚΕΦ.) Διάρκεια 180 min ΘΕΜΑ Α Στις ερωτήσεις Α1 εως Α4
Όνομα :... Ημερομηνία:... /... /... Επαναληπτικό Διαγώνισμα Χημείας Γ Λυκείου Ομάδας Προσανατολισμού Θετικών Σπουδών (1 ο + 2 ο + 3 ο + 4 ο + 5 ο ΚΕΦ.) Διάρκεια 180 min ΘΕΜΑ Α Στις ερωτήσεις Α1 εως Α4
Υδατικοί Πόροι -Ρύπανση
 Υδατικοί Πόροι -Ρύπανση Γήινη επιφάνεια Κατανομή υδάτων Υδάτινο στοιχείο 71% Ωκεανοί αλμυρό νερό 97% Γλυκό νερό 3% Εκμεταλλεύσιμο νερό 0,01% Γλυκό νερό 3% Παγόβουνα Υπόγεια ύδατα 2,99% Εκμεταλλεύσιμο νερό
Υδατικοί Πόροι -Ρύπανση Γήινη επιφάνεια Κατανομή υδάτων Υδάτινο στοιχείο 71% Ωκεανοί αλμυρό νερό 97% Γλυκό νερό 3% Εκμεταλλεύσιμο νερό 0,01% Γλυκό νερό 3% Παγόβουνα Υπόγεια ύδατα 2,99% Εκμεταλλεύσιμο νερό
Περιβαλλοντική Χημεία
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Περιβαλλοντική Χημεία Ενότητα 8.2: Χημικώς Απαιτούμενο Οξυγόνο (Chemical Oxygen Demand, COD) Ευάγγελος Φουντουκίδης Τμήμα Πολιτικών
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Περιβαλλοντική Χημεία Ενότητα 8.2: Χημικώς Απαιτούμενο Οξυγόνο (Chemical Oxygen Demand, COD) Ευάγγελος Φουντουκίδης Τμήμα Πολιτικών
ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ. 9 - Δεκεμβρίου
 1 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ 9 - Δεκεμβρίου - 2017 2 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ..... 1 η Δραστηριότητα Παρασκευή δυο υδατικών διαλυμάτων ΝaCl με
1 ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 ΧΗΜΕΙΑ 9 - Δεκεμβρίου - 2017 2 ΕΚΦΕ ΑΛΙΜΟΥ ΤΟΠΙΚΟΣ ΔΙΑΓΩΝΙΣΜΟΣ EUSO 2018 Εξεταζόμενο μάθημα: ΧΗΜΕΙΑ ΟΜΑΔΑ..... 1 η Δραστηριότητα Παρασκευή δυο υδατικών διαλυμάτων ΝaCl με
ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΑΝΑΛΗΠΤΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ (Α. Χημική Θερμοδυναμική) H 298
 ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΑΝΑΛΗΠΤΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 4-5 (Α. Χημική Θερμοδυναμική) η Άσκηση Από τα δεδομένα του πίνακα που ακολουθεί και δεχόμενοι ότι όλα τα αέρια είναι ιδανικά, να υπολογίσετε: α)
ΛΥΣΕΙΣ ΘΕΜΑΤΩΝ ΕΠΑΝΑΛΗΠΤΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΣΤΗ ΦΥΣΙΚΟΧΗΜΕΙΑ 4-5 (Α. Χημική Θερμοδυναμική) η Άσκηση Από τα δεδομένα του πίνακα που ακολουθεί και δεχόμενοι ότι όλα τα αέρια είναι ιδανικά, να υπολογίσετε: α)
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΘΕΜΑ Α Ηµεροµηνία: Τετάρτη 23 Απριλίου 2014 ιάρκεια Εξέτασης: 2 ώρες ΕΚΦΩΝΗΣΕΙΣ Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A4 και δίπλα
ΜΗΧΑΝΙΚΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΔΙΕΡΓΑΣΙΩΝ
 ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΜΗΧΑΝΙΚΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΔΙΕΡΓΑΣΙΩΝ ΟΔΗΓΙΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΥΓΡΗΣ ΕΚΧΥΛΙΣΗΣ Ελένη Παντελή, Υποψήφια Διδάκτορας Γεωργία Παππά, Δρ. Χημικός Μηχανικός
ΕΘΝΙΚΟ ΜΕΤΣΟΒΙΟ ΠΟΛΥΤΕΧΝΕΙΟ ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΜΗΧΑΝΙΚΗ ΚΑΙ ΑΝΑΠΤΥΞΗ ΔΙΕΡΓΑΣΙΩΝ ΟΔΗΓΙΕΣ ΕΡΓΑΣΤΗΡΙΑΚΗΣ ΑΣΚΗΣΗΣ ΥΓΡΗΣ ΕΚΧΥΛΙΣΗΣ Ελένη Παντελή, Υποψήφια Διδάκτορας Γεωργία Παππά, Δρ. Χημικός Μηχανικός
ΚΕΦΑΛΑΙΟ 5 : ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ, ΗΕΔ, ΓΕΦΥΡΑ ΑΛΑΤΟΣ, ΣΤΟΙΧΕΙΟ DANIELL, ΛΕΙΤΟΥΡΓΙΑ ΣΤΟΙΧΕΙΟΥ, ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΚΑΙ ΕΦΑΡΜΟΓΕΣ.
 ο ΚΕΦΑΛΑΙΟ 5 : ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ, ΗΕΔ, ΓΕΦΥΡΑ ΑΛΑΤΟΣ, ΣΤΟΙΧΕΙΟ DANIELL, ΛΕΙΤΟΥΡΓΙΑ ΣΤΟΙΧΕΙΟΥ, ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΚΑΙ ΕΦΑΡΜΟΓΕΣ. Διδακτικοί στόχοι: Μετά την ολοκλήρωση του 5ου κεφαλαίου οι φοιτητές θα πρέπει
ο ΚΕΦΑΛΑΙΟ 5 : ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ, ΗΕΔ, ΓΕΦΥΡΑ ΑΛΑΤΟΣ, ΣΤΟΙΧΕΙΟ DANIELL, ΛΕΙΤΟΥΡΓΙΑ ΣΤΟΙΧΕΙΟΥ, ΠΡΟΤΥΠΑ ΔΥΝΑΜΙΚΑ ΚΑΙ ΕΦΑΡΜΟΓΕΣ. Διδακτικοί στόχοι: Μετά την ολοκλήρωση του 5ου κεφαλαίου οι φοιτητές θα πρέπει
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα. Χημική Τεχνολογία. Εργαστηριακό Μέρος
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 8.2: Χημικώς Απαιτούμενο Οξυγόνο (Chemical Oxygen Demand, COD) Ευάγγελος Φουντουκίδης
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 8.2: Χημικώς Απαιτούμενο Οξυγόνο (Chemical Oxygen Demand, COD) Ευάγγελος Φουντουκίδης
Διαλύματα ασθενών οξέων ασθενών βάσεων.
 Διαλύματα ασθενών οξέων ασθενών βάσεων. Η ισχύς ενός οξέος σε υδατικό διάλυμα περιγράφεται από τη σταθερά ισορροπίας ιοντισμού του οξέος. Σε ένα αραιό υδατικό διάλυμα ασθενούς μονοπρωτικού οξέος ΗΑ, έχουμε
Διαλύματα ασθενών οξέων ασθενών βάσεων. Η ισχύς ενός οξέος σε υδατικό διάλυμα περιγράφεται από τη σταθερά ισορροπίας ιοντισμού του οξέος. Σε ένα αραιό υδατικό διάλυμα ασθενούς μονοπρωτικού οξέος ΗΑ, έχουμε
ΥΔΡΟΧΗΜΕΙΑ. Ενότητα 8: Μετρήσεις και υπολογισμοί φυσικοχημικώνυδροχημικών. Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών Τμήμα : Γεωλογία
 ΥΔΡΟΧΗΜΕΙΑ Ενότητα 8: Μετρήσεις και υπολογισμοί φυσικοχημικώνυδροχημικών παραμέτρων (Μέρος 1ο) Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών Τμήμα : Γεωλογία Σκοποί ενότητας Κατανόηση των φυσικοχημικών παραμέτρων
ΥΔΡΟΧΗΜΕΙΑ Ενότητα 8: Μετρήσεις και υπολογισμοί φυσικοχημικώνυδροχημικών παραμέτρων (Μέρος 1ο) Ζαγγανά Ελένη Σχολή : Θετικών Επιστημών Τμήμα : Γεωλογία Σκοποί ενότητας Κατανόηση των φυσικοχημικών παραμέτρων
Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου 2000
 Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό νερό διαλύεται
Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό νερό διαλύεται
ΟΞΕΙΔΟΑΝΑΓΩΓΙΚEΣ ΓΕΩΧΗΜΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ. Αριάδνη Αργυράκη
 1 ΟΞΕΙΔΟΑΝΑΓΩΓΙΚEΣ ΓΕΩΧΗΜΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ Αριάδνη Αργυράκη Περιεχόμενα 2 1. Ορισμοί 2. Εξισορρόπηση αντιδράσεων οξειδοαναγωγής 3. Διαγράμματα Eh-pH 4. Σημαντικές βιο-γεωχημικές αντιδράσεις ΑΝΤΙΔΡΑΣΕΙΣ ΟΞΕΙΔΟΑΝΑΓΩΓΗΣ
1 ΟΞΕΙΔΟΑΝΑΓΩΓΙΚEΣ ΓΕΩΧΗΜΙΚΕΣ ΔΙΕΡΓΑΣΙΕΣ Αριάδνη Αργυράκη Περιεχόμενα 2 1. Ορισμοί 2. Εξισορρόπηση αντιδράσεων οξειδοαναγωγής 3. Διαγράμματα Eh-pH 4. Σημαντικές βιο-γεωχημικές αντιδράσεις ΑΝΤΙΔΡΑΣΕΙΣ ΟΞΕΙΔΟΑΝΑΓΩΓΗΣ
F el = z k e 0 (3) F f = f k v k (4) F tot = z k e 0 x f kv k (5)
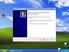 Κίνηση των ιόντων υπό την επίδραση ηλεκτρικού πεδίου Αντώνης Καραντώνης 15 Μαρτίου 2011 1 Σκοπός της άσκησης Σκοπός της άσκησης είναι ο προσδιορισμός της οριακής ταχύτητας των ιόντων υπό την επίδραση ηλεκτρικού
Κίνηση των ιόντων υπό την επίδραση ηλεκτρικού πεδίου Αντώνης Καραντώνης 15 Μαρτίου 2011 1 Σκοπός της άσκησης Σκοπός της άσκησης είναι ο προσδιορισμός της οριακής ταχύτητας των ιόντων υπό την επίδραση ηλεκτρικού
ΠΡΟΔΙΑΓΡΑΦΕΣ - ΟΔΗΓΙΕΣ ΔΙΑΜΟΡΦΩΣΗΣ ΘΕΜΑΤΩΝ ΓΙΑ ΤΟ ΜΑΘΗΜΑ
 ΠΡΟΔΙΑΓΡΑΦΕΣ - ΟΔΗΓΙΕΣ ΔΙΑΜΟΡΦΩΣΗΣ ΘΕΜΑΤΩΝ ΓΙΑ ΤΟ ΜΑΘΗΜΑ Χημεία Α ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ και Α, Β ΤΑΞΕΙΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Α ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ και Α ΤΑΞΗ ΕΣΠΕΡΙΝΟΥ ΕΠΑΛ ΚΕΝΤΡΙΚΗ ΕΠΙΣΤΗΜΟΝΙΚΗ ΕΠΙΤΡΟΠΗ ΤΡΑΠΕΖΑΣ
ΠΡΟΔΙΑΓΡΑΦΕΣ - ΟΔΗΓΙΕΣ ΔΙΑΜΟΡΦΩΣΗΣ ΘΕΜΑΤΩΝ ΓΙΑ ΤΟ ΜΑΘΗΜΑ Χημεία Α ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ και Α, Β ΤΑΞΕΙΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ Α ΤΑΞΗ ΗΜΕΡΗΣΙΟΥ και Α ΤΑΞΗ ΕΣΠΕΡΙΝΟΥ ΕΠΑΛ ΚΕΝΤΡΙΚΗ ΕΠΙΣΤΗΜΟΝΙΚΗ ΕΠΙΤΡΟΠΗ ΤΡΑΠΕΖΑΣ
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα. Χημική Τεχνολογία. Εργαστηριακό Μέρος
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 8.1: Βιοχημικά Απαιτούμενο Οξυγόνο (Biochemical Oxygen Demand, BOD) Ευάγγελος Φουντουκίδης
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ Ανώτατο Εκπαιδευτικό Ίδρυμα Πειραιά Τεχνολογικού Τομέα Χημική Τεχνολογία Εργαστηριακό Μέρος Ενότητα 8.1: Βιοχημικά Απαιτούμενο Οξυγόνο (Biochemical Oxygen Demand, BOD) Ευάγγελος Φουντουκίδης
ΣΥΣΤΗΜΑΤΑ ΑΕΡΙΣΜΟΥ ΒΙΟΛΟΓΙΚΩΝ ΚΑΘΑΡΙΣΜΩΝ
 Περιβαλλοντική Τεχνολογία και Διαχείριση Απόστολος Βλυσίδης Καθηγητής ΕΜΠ Σχολή Χημικών Μηχανικών Εργαστήριο Οργανικής Χημικής Τεχνολογίας ΣΥΣΤΗΜΑΤΑ ΑΕΡΙΣΜΟΥ ΒΙΟΛΟΓΙΚΩΝ ΚΑΘΑΡΙΣΜΩΝ Άδεια Χρήσης Το παρόν
Περιβαλλοντική Τεχνολογία και Διαχείριση Απόστολος Βλυσίδης Καθηγητής ΕΜΠ Σχολή Χημικών Μηχανικών Εργαστήριο Οργανικής Χημικής Τεχνολογίας ΣΥΣΤΗΜΑΤΑ ΑΕΡΙΣΜΟΥ ΒΙΟΛΟΓΙΚΩΝ ΚΑΘΑΡΙΣΜΩΝ Άδεια Χρήσης Το παρόν
2-1. I I i. ti (3) Q Q i. όπου Q το συνολικό ηλεκτρικό φορτίο που μεταφέρεται και είναι: (4)
 2-1 ΑΡΙΘΜΟΙ ΜΕΤΑΦΟΡΑΣ ΙΟΝΤΩΝ Θέμα ασκήσεως: Προσδιορισμός αριθμού μεταφοράς ιόντων με την μέθοδο Horf. Θεωρία Κατά την εφαρμογή ηλεκτρικού πεδίου σε ιοντικό διάλυμα, ηλεκτρικό ρεύμα διέρχεται από αυτό
2-1 ΑΡΙΘΜΟΙ ΜΕΤΑΦΟΡΑΣ ΙΟΝΤΩΝ Θέμα ασκήσεως: Προσδιορισμός αριθμού μεταφοράς ιόντων με την μέθοδο Horf. Θεωρία Κατά την εφαρμογή ηλεκτρικού πεδίου σε ιοντικό διάλυμα, ηλεκτρικό ρεύμα διέρχεται από αυτό
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 A ΦΑΣΗ ΧΗΜΕΙΑ ΑΛΓΟΡΙΘΜΟΣ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Πέμπτη 4 Ιανουαρίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α4 να γράψετε στο τετράδιό
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Πέμπτη 4 Ιανουαρίου 2018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α ΕΚΦΩΝΗΣΕΙΣ Για τις προτάσεις Α1 έως και Α4 να γράψετε στο τετράδιό
Ημερομηνία: 29 Δεκεμβρίου 2017 Διάρκεια Εξέτασης: 3 ώρες
 ΤΑΞΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ημερομηνία: 29 Δεκεμβρίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις ημιτελείς προτάσεις Α1 Α5 να γράψετε στο τετράδιό σας τον αριθμό της
ΤΑΞΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Ημερομηνία: 29 Δεκεμβρίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Στις ημιτελείς προτάσεις Α1 Α5 να γράψετε στο τετράδιό σας τον αριθμό της
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΚΑΙ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 7 ΣΕΠΤΕΜΒΡΙΟΥ 2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ & Δ ΕΣΠΕΡΙΝΩΝ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΚΑΙ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΕΜΠΤΗ 7 ΣΕΠΤΕΜΒΡΙΟΥ 2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου 2000
 Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου ΕΚΦΩΝΗΕΙ τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό
Ζήτηµα 1ο Θέµατα Χηµείας Θετικής Κατεύθυνσης Β Λυκείου ΕΚΦΩΝΗΕΙ τις ερωτήσεις 1-3,να γράψετε στο τετράδιο σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. 1. ε καθαρό
f = c p + 2 (1) f = 3 1 + 2 = 4 (2) x A + x B + x C = 1 (3) x A + x B + x Γ = 1 3-1
 ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΣΥΣΤΗΜΑΤΟΣ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΑΜΟΙΒΑΙΑ ΙΑΛΥΤΟΤΗΤΑ Θέµα ασκήσεως Προσδιορισµός καµπύλης διαλυτότητας σε διάγραµµα φάσεων συστήµατος τριών υγρών συστατικών που το ένα ζεύγος παρουσιάζει περιορισµένη
ΙΣΟΡΡΟΠΙΑ ΦΑΣΕΩΝ ΣΥΣΤΗΜΑΤΟΣ ΠΟΛΛΩΝ ΣΥΣΤΑΤΙΚΩΝ ΑΜΟΙΒΑΙΑ ΙΑΛΥΤΟΤΗΤΑ Θέµα ασκήσεως Προσδιορισµός καµπύλης διαλυτότητας σε διάγραµµα φάσεων συστήµατος τριών υγρών συστατικών που το ένα ζεύγος παρουσιάζει περιορισµένη
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα
 Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
Διαλύματα - Περιεκτικότητες διαλυμάτων Γενικά για διαλύματα Μάθημα 6 6.1. SOS: Τι ονομάζεται διάλυμα, Διάλυμα είναι ένα ομογενές μίγμα δύο ή περισσοτέρων καθαρών ουσιών. Παράδειγμα: Ο ατμοσφαιρικός αέρας
5. ΟΞΕΙΔΟΑΝΑΓΩΓΗ- ΗΛΕΚΤΡΟΛΥΣΗ
 83 5. ΟΞΕΙΔΟΑΝΑΓΩΓΗ- ΗΛΕΚΤΡΟΛΥΣΗ 84 85 ΔΙΔΑΚΤΙΚΗ ΩΡΑ: 19 ΔΙΔΑΚΤΙΚΗ ΕΝΟΤΗΤΑ: Οξειδοαναγωγή - Ηλεκτρόλυση 5.1 Αριθμός οξείδωσης. Οξείδωση Αναγωγή ΣΤΟΧΟΙ Στο τέλος αυτής της διδακτικής ώρας θα πρέπει ο μαθητής
83 5. ΟΞΕΙΔΟΑΝΑΓΩΓΗ- ΗΛΕΚΤΡΟΛΥΣΗ 84 85 ΔΙΔΑΚΤΙΚΗ ΩΡΑ: 19 ΔΙΔΑΚΤΙΚΗ ΕΝΟΤΗΤΑ: Οξειδοαναγωγή - Ηλεκτρόλυση 5.1 Αριθμός οξείδωσης. Οξείδωση Αναγωγή ΣΤΟΧΟΙ Στο τέλος αυτής της διδακτικής ώρας θα πρέπει ο μαθητής
ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ
 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ ΘΕΜΑ Α Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το ιόν 56 Fe +2 περιέχει:
ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: XHMEIA A ΛΥΚΕΙΟΥ ΘΕΜΑ Α Να γράψετε στο τετράδιο σας τον αριθµό κάθε µίας από τις ερωτήσεις A1 έως A5 και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση. Α1. Το ιόν 56 Fe +2 περιέχει:
Επίπλευση με αέρα (Dissolved Air Flotation)
 Επίπλευση με αέρα (Dissolved Air Flotation) Προσκόλληση των στερεών σε αιώρηση πάνω σε ανερχόμενες φυσαλλίδες αέρα Πολλές και μικρές Αποσυμπίεση αέρα από υψηλότερη πίεση στην ατμοσφαιρική Σύγκρουση φυσαλλίδων/στερεών
Επίπλευση με αέρα (Dissolved Air Flotation) Προσκόλληση των στερεών σε αιώρηση πάνω σε ανερχόμενες φυσαλλίδες αέρα Πολλές και μικρές Αποσυμπίεση αέρα από υψηλότερη πίεση στην ατμοσφαιρική Σύγκρουση φυσαλλίδων/στερεών
Στοιχειμετρικοί υπολογισμοί σε διαλύματα
 Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Στοιχειμετρικοί υπολογισμοί σε διαλύματα 23-1. Τι εκφράζουν οι συντελεστές μιας χημικής αντίδρασης; Οι συντελεστές σε μία χημική εξίσωση καθορίζουν την αναλογία mol των αντιδρώντων και προϊόντων στην αντίδραση.
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις
 Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις Άσκηση 6: Ισορροπία φάσεων συστήματος πολλών συστατικών αμοιβαία διαλυτότητα Βασιλική Χαβρεδάκη Τμήμα Χημείας 1. Θεωρία... 3 2. Μετρήσεις... 5 3. Επεξεργασία Μετρήσεων...
Φυσικοχημεία 2 Εργαστηριακές Ασκήσεις Άσκηση 6: Ισορροπία φάσεων συστήματος πολλών συστατικών αμοιβαία διαλυτότητα Βασιλική Χαβρεδάκη Τμήμα Χημείας 1. Θεωρία... 3 2. Μετρήσεις... 5 3. Επεξεργασία Μετρήσεων...
Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ. Ηµεροµηνία: Τρίτη 5 Ιανουαρίου 2016 ιάρκεια Εξέτασης: 3 ώρες ΑΠΑΝΤΗΣΕΙΣ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ηµεροµηνία: Τρίτη 5 Ιανουαρίου 06 ιάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α Α.. γ Α.. β Α.3. γ Α.4. γ Α.5. α ΑΠΑΝΤΗΣΕΙΣ Α.6.. Σ. Λ (Σύµφωνα
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ηµεροµηνία: Τρίτη 5 Ιανουαρίου 06 ιάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α Α.. γ Α.. β Α.3. γ Α.4. γ Α.5. α ΑΠΑΝΤΗΣΕΙΣ Α.6.. Σ. Λ (Σύµφωνα
panagiotisathanasopoulos.gr
 Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ. + SO 4 Βάσεις είναι οι ενώσεις που όταν διαλύονται σε νερό δίνουν ανιόντα υδροξειδίου (ΟΗ - ). NaOH Na
 ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ ΙΔΙΟΤΗΤΕΣ ΟΞΕΩΝ Αλλάζουν το χρώμα των δεικτών. Αντιδρούν με μέταλλα και παράγουν αέριο υδρογόνο (δες απλή αντικατάσταση) Αντιδρούν με ανθρακικά άλατα και παράγουν αέριο CO2. Έχουν όξινη
ΧΗΜΕΙΑ Γ' ΓΥΜΝΑΣΙΟΥ ΙΔΙΟΤΗΤΕΣ ΟΞΕΩΝ Αλλάζουν το χρώμα των δεικτών. Αντιδρούν με μέταλλα και παράγουν αέριο υδρογόνο (δες απλή αντικατάσταση) Αντιδρούν με ανθρακικά άλατα και παράγουν αέριο CO2. Έχουν όξινη
Mεταφορά διαλυμένου ρύπου σε κορεσμένο έδαφος: Μαθηματική περιγραφή
 Mεταφορά διαλυμένου ρύπου σε κορεσμένο έδαφος: Μαθηματική περιγραφή Βασικό ερώτημα: Πού θα πάει ο ρύπος; Παρουσίαση 1 από 4 Μεταφορά λόγω διάχυσης Κύριος στόχος παρουσίασης Γιατί ασχολούμαστε εδώ με τη
Mεταφορά διαλυμένου ρύπου σε κορεσμένο έδαφος: Μαθηματική περιγραφή Βασικό ερώτημα: Πού θα πάει ο ρύπος; Παρουσίαση 1 από 4 Μεταφορά λόγω διάχυσης Κύριος στόχος παρουσίασης Γιατί ασχολούμαστε εδώ με τη
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΠΕΜΠΤΗ 7 ΣΕΠΤΕΜΒΡΙΟΥ 2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ
ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ ΕΙΣΑΓΩΓΙΚΕΣ ΕΞΕΤΑΣΕΙΣ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΤΟΥ ΕΞΩΤΕΡΙΚΟΥ ΚΑΙ ΤΕΚΝΩΝ ΕΛΛΗΝΩΝ ΥΠΑΛΛΗΛΩΝ ΠΟΥ ΥΠΗΡΕΤΟΥΝ ΣΤΟ ΕΞΩΤΕΡΙΚΟ ΠΕΜΠΤΗ 7 ΣΕΠΤΕΜΒΡΙΟΥ 2017 - ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ
Generated by Foxit PDF Creator Foxit Software http://www.foxitsoftware.com For evaluation only. ΑΣΚΗΣΗ ΜΕΤΡΗΣΗ ΤΗΣ ΕΙΔΙΚΗΣ ΘΕΡΜΟΤΗΤΑΣ ΥΓΡΟΥ
 ΑΣΚΗΣΗ 13 ΜΕΤΡΗΣΗ ΤΗΣ ΕΙΔΙΚΗΣ ΘΕΡΜΟΤΗΤΑΣ ΥΓΡΟΥ ΜΕΡΟΣ ΠΡΩΤΟ ΒΑΣΙΚΕΣ ΘΕΩΡΗΤΙΚΕΣ ΓΝΩΣΕΙΣ 1.1. Εσωτερική ενέργεια Γνωρίζουμε ότι τα μόρια των αερίων κινούνται άτακτα και προς όλες τις διευθύνσεις με ταχύτητες,
ΑΣΚΗΣΗ 13 ΜΕΤΡΗΣΗ ΤΗΣ ΕΙΔΙΚΗΣ ΘΕΡΜΟΤΗΤΑΣ ΥΓΡΟΥ ΜΕΡΟΣ ΠΡΩΤΟ ΒΑΣΙΚΕΣ ΘΕΩΡΗΤΙΚΕΣ ΓΝΩΣΕΙΣ 1.1. Εσωτερική ενέργεια Γνωρίζουμε ότι τα μόρια των αερίων κινούνται άτακτα και προς όλες τις διευθύνσεις με ταχύτητες,
ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ. Εισαγωγή. 3.1 Γενικά για τη χημική κινητική και τη χημική αντίδραση - Ταχύτητα αντίδρασης
 3 ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ 3 ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ Εισαγωγή Στην μέχρι τώρα γνωριμία μας με τη χημεία υπάρχει μια «σημαντική απουσία»: ο χρόνος... Είναι λοιπόν «καιρός» να μπει και ο χρόνος ως παράμετρος στη μελέτη ενός
3 ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ 3 ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ Εισαγωγή Στην μέχρι τώρα γνωριμία μας με τη χημεία υπάρχει μια «σημαντική απουσία»: ο χρόνος... Είναι λοιπόν «καιρός» να μπει και ο χρόνος ως παράμετρος στη μελέτη ενός
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2016 Α ΦΑΣΗ
 ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 06 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑ Α Α.. Α.. Α.3. Α.4. Α.5. Α.6. γ β γ γ α ΘΕΜΑ Β Β.. Ηµεροµηνία: Τρίτη 5 Ιανουαρίου 06 ιάρκεια Εξέτασης:
ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 06 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥ ΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ ΘΕΜΑ Α Α.. Α.. Α.3. Α.4. Α.5. Α.6. γ β γ γ α ΘΕΜΑ Β Β.. Ηµεροµηνία: Τρίτη 5 Ιανουαρίου 06 ιάρκεια Εξέτασης:
Τράπεζα Χημεία Α Λυκείου
 Τράπεζα Χημεία Α Λυκείου 1 ο Κεφάλαιο Όλα τα θέματα του 1 ου Κεφαλαίου από τη Τράπεζα Θεμάτων 25 ερωτήσεις Σωστού Λάθους 30 ερωτήσεις ανάπτυξης Επιμέλεια: Γιάννης Καλαμαράς, Διδάκτωρ Χημικός Ερωτήσεις
Τράπεζα Χημεία Α Λυκείου 1 ο Κεφάλαιο Όλα τα θέματα του 1 ου Κεφαλαίου από τη Τράπεζα Θεμάτων 25 ερωτήσεις Σωστού Λάθους 30 ερωτήσεις ανάπτυξης Επιμέλεια: Γιάννης Καλαμαράς, Διδάκτωρ Χημικός Ερωτήσεις
ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ
 Επιμέλεια: Νίκος Δάκος ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έω ς και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
Επιμέλεια: Νίκος Δάκος ΠΡΟΤΕΙΝΟΜΕΝΑ ΘΕΜΑΤΑ ΠΑΝΕΛΛΑΔΙΚΩΝ ΕΞΕΤΑΣΕΩΝ ΧΗΜΕΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΜΑ Α Για τις ερωτήσεις Α1 έω ς και Α5 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα το γράμμα
ΜΙΑ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΔΟΣ ΤΗ ΒΔΟΜΑΔΑ ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ
 ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ - B ΤΑΞΗ ΓΥΜΝΑΣΙΟΥ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΜΙΑ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΔΟΣ ΤΗ ΒΔΟΜΑΔΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ
ΑΝΑΛΥΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΧΗΜΕΙΑΣ - B ΤΑΞΗ ΓΥΜΝΑΣΙΟΥ ΥΠΟΥΡΓΕΙΟ ΠΑΙΔΕΙΑΣ ΚΑΙ ΠΟΛΙΤΙΣΜΟΥ ΓΡΑΦΕΙΑ ΕΠΙΘΕΩΡΗΤΩΝ ΜΕΣΗΣ ΕΚΠΑΙΔΕΥΣΗΣ ΛΕΥΚΩΣΙΑ ΜΙΑ ΔΙΔΑΚΤΙΚΗ ΠΕΡΙΟΔΟΣ ΤΗ ΒΔΟΜΑΔΑ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2007-2008 ΔΙΔΑΚΤΕΑ ΥΛΗ ΣΤΟΧΟΙ
ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ Ι Θέμα ασκήσεως Αρχή μεθόδου Θεωρία
 3-1 ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ Ι Θέμα ασκήσεως: Προσδιορισμός κανονικού δυναμικού (Ε) ηλεκτροδίου. Προσδιορισμός του θερμικού συντελεστή ( Ε/ Τ) P. Προσδιορισμός του γινομένου διαλυτότητας του Agl. Αρχή μεθόδου:
3-1 ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ Ι Θέμα ασκήσεως: Προσδιορισμός κανονικού δυναμικού (Ε) ηλεκτροδίου. Προσδιορισμός του θερμικού συντελεστή ( Ε/ Τ) P. Προσδιορισμός του γινομένου διαλυτότητας του Agl. Αρχή μεθόδου:
ΥΠΟΛΟΓΙΣΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΧΩΡΟ-ΧΡΟΝΙΚΗΣ ΑΠΟΚΡΙΣΗΣ ΤΑΛΑΝΤΟΥΜΕΝΩΝ ΗΛΕΚΤΡΟΧΗΜΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΣΕ ΔΙΑΜΟΡΦΩΣΕΙΣ ΔΥΟ ΚΑΙ ΤΡΙΩΝ ΗΛΕΚΤΡΟΔΙΩΝ
 ΥΠΟΛΟΓΙΣΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΧΩΡΟ-ΧΡΟΝΙΚΗΣ ΑΠΟΚΡΙΣΗΣ ΤΑΛΑΝΤΟΥΜΕΝΩΝ ΗΛΕΚΤΡΟΧΗΜΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΣΕ ΔΙΑΜΟΡΦΩΣΕΙΣ ΔΥΟ ΚΑΙ ΤΡΙΩΝ ΗΛΕΚΤΡΟΔΙΩΝ Παναγιώτης Σταματόπουλος, Αντώνης Καραντώνης Τομέας Επιστήμης και Τεχνικής
ΥΠΟΛΟΓΙΣΤΙΚΗ ΜΕΛΕΤΗ ΤΗΣ ΧΩΡΟ-ΧΡΟΝΙΚΗΣ ΑΠΟΚΡΙΣΗΣ ΤΑΛΑΝΤΟΥΜΕΝΩΝ ΗΛΕΚΤΡΟΧΗΜΙΚΩΝ ΣΥΣΤΗΜΑΤΩΝ ΣΕ ΔΙΑΜΟΡΦΩΣΕΙΣ ΔΥΟ ΚΑΙ ΤΡΙΩΝ ΗΛΕΚΤΡΟΔΙΩΝ Παναγιώτης Σταματόπουλος, Αντώνης Καραντώνης Τομέας Επιστήμης και Τεχνικής
Επίκουρος Καθηγητής Π. Μελίδης
 Χαρακτηριστικά υγρών αποβλήτων Επίκουρος Καθηγητής Π. Μελίδης Τμήμα Μηχανικών Περιβάλλοντος Εργαστήριο Διαχείρισης και Τεχνολογίας Υγρών Αποβλήτων Τα υγρά απόβλητα μπορεί να προέλθουν από : Ανθρώπινα απόβλητα
Χαρακτηριστικά υγρών αποβλήτων Επίκουρος Καθηγητής Π. Μελίδης Τμήμα Μηχανικών Περιβάλλοντος Εργαστήριο Διαχείρισης και Τεχνολογίας Υγρών Αποβλήτων Τα υγρά απόβλητα μπορεί να προέλθουν από : Ανθρώπινα απόβλητα
Ενεργότητα και συντελεστές ενεργότητας- Οξέα- Οι σταθερές ισορροπίας. Εισαγωγική Χημεία
 Ενεργότητα και συντελεστές ενεργότητας- Οξέα- Οι σταθερές ισορροπίας 1 Εισαγωγική Χημεία 2013-14 Από τον ορισμό της Ιοντικής Ισχύος (Ι) τα χημικά είδη ψηλού φορτίου συνεισφέρουν περισσότερο στην ιοντική
Ενεργότητα και συντελεστές ενεργότητας- Οξέα- Οι σταθερές ισορροπίας 1 Εισαγωγική Χημεία 2013-14 Από τον ορισμό της Ιοντικής Ισχύος (Ι) τα χημικά είδη ψηλού φορτίου συνεισφέρουν περισσότερο στην ιοντική
Ηλεκτρόλυση νερού ή ηλεκτρόλυση αραιού διαλύματος θειικού οξέος με ηλεκτρόδια λευκοχρύσου και με χρήση της συσκευής Hoffman.
 Σύντομη περιγραφή του πειράματος Ηλεκτρόλυση νερού ή ηλεκτρόλυση αραιού διαλύματος θειικού οξέος με ηλεκτρόδια λευκοχρύσου και με χρήση της συσκευής Hoffman. Διδακτικοί στόχοι του πειράματος Στο τέλος
Σύντομη περιγραφή του πειράματος Ηλεκτρόλυση νερού ή ηλεκτρόλυση αραιού διαλύματος θειικού οξέος με ηλεκτρόδια λευκοχρύσου και με χρήση της συσκευής Hoffman. Διδακτικοί στόχοι του πειράματος Στο τέλος
Εισαγωγή στις Ετερογενείς Χημικές Αντιδράσεις
 Στα ετερογενή συστήματα υπάρχουν δύο παράγοντες, οι οποίοι περιπλέκουν την ανάλυση και την περιγραφή τους, και οι οποίοι πρέπει να ληφθούν υπόψη επιπλέον αυτών που εξετάζονται στα ομογενή συστήματα. Καταρχήν
Στα ετερογενή συστήματα υπάρχουν δύο παράγοντες, οι οποίοι περιπλέκουν την ανάλυση και την περιγραφή τους, και οι οποίοι πρέπει να ληφθούν υπόψη επιπλέον αυτών που εξετάζονται στα ομογενή συστήματα. Καταρχήν
Κεφάλαιο 20. Θερμότητα
 Κεφάλαιο 20 Θερμότητα Εισαγωγή Για να περιγράψουμε τα θερμικά φαινόμενα, πρέπει να ορίσουμε με προσοχή τις εξής έννοιες: Θερμοκρασία Θερμότητα Θερμοκρασία Συχνά συνδέουμε την έννοια της θερμοκρασίας με
Κεφάλαιο 20 Θερμότητα Εισαγωγή Για να περιγράψουμε τα θερμικά φαινόμενα, πρέπει να ορίσουμε με προσοχή τις εξής έννοιες: Θερμοκρασία Θερμότητα Θερμοκρασία Συχνά συνδέουμε την έννοια της θερμοκρασίας με
Να σχεδιάστε ένα τυπικό διάγραμμα ροής μιας εγκατάστασης επεξεργασίας αστικών λυμάτων και να περιγράψτε τη σημασία των επιμέρους σταδίων.
 Τεχνολογία και Διαχείριση Υγρών Αποβλήτων Ι Ακαδημαϊκό έτος 2017-2018 Σημαντικά ζητήματα μαθήματος (Β. Διαμαντής) Βασικές αρχές Από τι αποτελούνται τα αστικά λύματα? Ποιες είναι οι τυπικές συγκεντρώσεις
Τεχνολογία και Διαχείριση Υγρών Αποβλήτων Ι Ακαδημαϊκό έτος 2017-2018 Σημαντικά ζητήματα μαθήματος (Β. Διαμαντής) Βασικές αρχές Από τι αποτελούνται τα αστικά λύματα? Ποιες είναι οι τυπικές συγκεντρώσεις
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
ΜΑΘΗΜΑ / ΤΑΞΗ : ΧΗΜΕΙΑ / Β ΓΥΜΝΑΣΙΟΥ ΣΕΙΡΑ: ΗΜΕΡΟΜΗΝΙΑ: 26 04 2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: Θεοδοσία Τσαβλίδου, Μαρίνος Ιωάννου ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ 1 1.1 Στον επόμενο πίνακα δίνονται τα σημεία τήξης και τα
ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΟΓΚΟΜΕΤΡΗΣΕΙΣ
 ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΟΓΚΟΜΕΤΡΗΣΕΙΣ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ - ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Γαλβανικά στοιχεία-στοιχείο Daniel Zn (s) + Cu +2 (aq) Zn +2 + Cu (s) Zn(s) Zn +2 (aq) + 2e - (ημιαντίδραση οξείδωσης)
ΟΞΕΙΔΟΑΝΑΓΩΓΙΚΕΣ ΟΓΚΟΜΕΤΡΗΣΕΙΣ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ - ΤΜΗΜΑ ΒΙΟΧΗΜΕΙΑΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ Γαλβανικά στοιχεία-στοιχείο Daniel Zn (s) + Cu +2 (aq) Zn +2 + Cu (s) Zn(s) Zn +2 (aq) + 2e - (ημιαντίδραση οξείδωσης)
1.Εισαγωγή. 2.Επιλεκτικά ηλεκτρόδια ιόντων(εηι)
 ΑΜΕΣΗ ΜΕΤΡΗΣΗ ΙΟΝΤΩΝ Κ + ΣΤΟ ΠΟΣΙΜΟ ΝΕΡΟ ΜΕ ΕΠΙΛΕΚΤΙΚΟ ΗΛΕΚΤΡΟΔΙΟ 1.Εισαγωγή Χημικοί αισθητήρες είναι όργανα τα οποία μπορούν να παρακολουθούν την ενεργότητα φορτισμένων ή μη ουσιών σε υγρή ή αέρια φάση.
ΑΜΕΣΗ ΜΕΤΡΗΣΗ ΙΟΝΤΩΝ Κ + ΣΤΟ ΠΟΣΙΜΟ ΝΕΡΟ ΜΕ ΕΠΙΛΕΚΤΙΚΟ ΗΛΕΚΤΡΟΔΙΟ 1.Εισαγωγή Χημικοί αισθητήρες είναι όργανα τα οποία μπορούν να παρακολουθούν την ενεργότητα φορτισμένων ή μη ουσιών σε υγρή ή αέρια φάση.
Στοιχειομετρικοί υπολογισμοί
 Στοιχειομετρικοί υπολογισμοί Σε κάθε χημική αντίδραση οι ποσότητες των χημικών ουσιών που αντιδρούν και παράγονται έχουν ορισμένη σχέση μεταξύ τους, η οποία καθορίζεται από τους συντελεστές των ουσιών
Στοιχειομετρικοί υπολογισμοί Σε κάθε χημική αντίδραση οι ποσότητες των χημικών ουσιών που αντιδρούν και παράγονται έχουν ορισμένη σχέση μεταξύ τους, η οποία καθορίζεται από τους συντελεστές των ουσιών
panagiotisathanasopoulos.gr
 Παναγιώτης Αθανασόπουλος. Κεφάλαιο 3ο Χημική Κινητική Παναγιώτης Αθανασόπουλος Χημικός, 35 Διδάκτωρ Πανεπιστημίου Πατρών Χηµικός ιδάκτωρ Παν. Πατρών 36 Γενικα για τη χημικη κινητικη και τη χημικη Παναγιώτης
Παναγιώτης Αθανασόπουλος. Κεφάλαιο 3ο Χημική Κινητική Παναγιώτης Αθανασόπουλος Χημικός, 35 Διδάκτωρ Πανεπιστημίου Πατρών Χηµικός ιδάκτωρ Παν. Πατρών 36 Γενικα για τη χημικη κινητικη και τη χημικη Παναγιώτης
ΟΜΟΣΠΟΝΔΙΑ ΕΚΠΑΙΔΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑΔΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2018 Β ΦΑΣΗ ΧΗΜΕΙΑ
 ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α Α1. β Α. γ Α3. δ Α4. γ Α5. α Λ, β Λ, γ Λ, δ Σ, ε Λ. ΘΕΜΑ Β Β1.
ΤΑΞΗ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ: ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΜΑΘΗΜΑ: ΧΗΜΕΙΑ Ημερομηνία: Τετάρτη 11 Απριλίου 018 Διάρκεια Εξέτασης: 3 ώρες ΘΕΜΑ Α Α1. β Α. γ Α3. δ Α4. γ Α5. α Λ, β Λ, γ Λ, δ Σ, ε Λ. ΘΕΜΑ Β Β1.
ΧΗΜΕΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Σε κάθε μία από τις επόμενες ερωτήσεις να επιλέξετε τη σωστή απάντηση
 Κανάρη 36, Δάφνη Τηλ. 210 9713934 & 210 9769376 ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ ΧΗΜΕΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑ Α Σε κάθε μία από τις επόμενες ερωτήσεις να επιλέξετε τη σωστή απάντηση Α1. Σε δοχείο σταθερού όγκου
Κανάρη 36, Δάφνη Τηλ. 210 9713934 & 210 9769376 ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ ΧΗΜΕΙΑ Ο.Π. ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ ΘΕΜΑ Α Σε κάθε μία από τις επόμενες ερωτήσεις να επιλέξετε τη σωστή απάντηση Α1. Σε δοχείο σταθερού όγκου
Αγωγιμότητα στα μέταλλα
 Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Ονοματεπώνυμο: Χημεία Γ Λυκείου Υλη: Χημική Κινητική Χημική Ισορροπία Ιοντισμός (K a K b ) Επιμέλεια διαγωνίσματος: Τσικριτζή Αθανασία Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Χημεία Γ Λυκείου Υλη: Χημική Κινητική Χημική Ισορροπία Ιοντισμός (K a K b ) Επιμέλεια διαγωνίσματος: Τσικριτζή Αθανασία Αξιολόγηση : Θέμα Α Να επιλέξετε τη σωστή απάντηση σε καθεμία
Ονοματεπώνυμο: Μάθημα: Χημεία Γ Λυκείου Υλη: Χημική Κινητική Χημική Ισορροπία Ιοντισμός (K a K b ) Επιμέλεια διαγωνίσματος: Τσικριτζή Αθανασία Αξιολόγηση : Θέμα Α Να επιλέξετε τη σωστή απάντηση σε καθεμία
Πολυτεχνείο Κρήτης Τµήµα Μηχανικών Περιβάλλοντος ΥΔΑΤΙΚΗ ΧΗΜΕΙΑ. Σηµειώσεις
 Πολυτεχνείο Κρήτης Τµήµα Μηχανικών Περιβάλλοντος ΥΔΑΤΙΚΗ ΧΗΜΕΙΑ Σηµειώσεις Κεφάλαιο : Καθορισµός της έννοιας του p των φυσικών νερών (Ισορροπία Ανθρακικών) Το p ως κύρια µεταβλητή Ο Νόµος δράσης των µαζών
Πολυτεχνείο Κρήτης Τµήµα Μηχανικών Περιβάλλοντος ΥΔΑΤΙΚΗ ΧΗΜΕΙΑ Σηµειώσεις Κεφάλαιο : Καθορισµός της έννοιας του p των φυσικών νερών (Ισορροπία Ανθρακικών) Το p ως κύρια µεταβλητή Ο Νόµος δράσης των µαζών
ΔΙΕΘΝΕΣ ΣΥΣΤΗΜΑ ΜΟΝΑΔΩΝ (S.I.)
 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ ΔΙΕΘΝΕΣ ΣΥΣΤΗΜΑ ΜΟΝΑΔΩΝ (S.I.) Το 1960 καθορίστηκε μετά από διεθνή συμφωνία το Διεθνές Σύστημα Μονάδων S.I. (από τα αρχικά των γαλλικών λέξεων Système International d Unités). Το σύστημα
ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ ΔΙΕΘΝΕΣ ΣΥΣΤΗΜΑ ΜΟΝΑΔΩΝ (S.I.) Το 1960 καθορίστηκε μετά από διεθνή συμφωνία το Διεθνές Σύστημα Μονάδων S.I. (από τα αρχικά των γαλλικών λέξεων Système International d Unités). Το σύστημα
1 Ο ΚΕΦΑΛΑΙΟ ΕΡΩΤΗΣΕΙΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΜΕ ΑΠΑΝΤΗΣΗ
 1 Ο ΚΕΦΑΛΑΙΟ ΕΡΩΤΗΣΕΙΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΜΕ ΑΠΑΝΤΗΣΗ 1. Το στοιχείο Χ έχει 17 ηλεκτρόνια. Αν στον πυρήνα του περιέχει 3 νετρόνια περισσότερα από τα πρωτόνια, να υπολογισθούν ο ατομικός και ο μαζικός του
1 Ο ΚΕΦΑΛΑΙΟ ΕΡΩΤΗΣΕΙΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΜΕ ΑΠΑΝΤΗΣΗ 1. Το στοιχείο Χ έχει 17 ηλεκτρόνια. Αν στον πυρήνα του περιέχει 3 νετρόνια περισσότερα από τα πρωτόνια, να υπολογισθούν ο ατομικός και ο μαζικός του
l R= ρ Σε ηλεκτρικό αγωγό µήκους l και διατοµής A η αντίσταση δίνεται από την εξίσωση: (1)
 ΑΓΩΓΙΜΟΤΗΤΑ ΗΕΚΤΡΟΥΤΩΝ Θέµα ασκήσεως Μελέτη της µεταβολής της αγωγιµότητας ισχυρού και ασθενούς ηλεκτρολύτη µε την συγκέντρωση, προσδιορισµός της µοριακής αγωγιµότητας σε άπειρη αραίωση ισχυρού οξέος,
ΑΓΩΓΙΜΟΤΗΤΑ ΗΕΚΤΡΟΥΤΩΝ Θέµα ασκήσεως Μελέτη της µεταβολής της αγωγιµότητας ισχυρού και ασθενούς ηλεκτρολύτη µε την συγκέντρωση, προσδιορισµός της µοριακής αγωγιµότητας σε άπειρη αραίωση ισχυρού οξέος,
Αγωγιμότητα στα μέταλλα
 Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
Η κίνηση των ατόμων σε κρυσταλλικό στερεό Θερμοκρασία 0 Θερμοκρασία 0 Δ. Γ. Παπαγεωργίου Τμήμα Μηχανικών Επιστήμης Υλικών Πανεπιστήμιο Ιωαννίνων dpapageo@cc.uoi.gr http://pc164.materials.uoi.gr/dpapageo
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ
 ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 1. Σε δοχείο σταθερού όγκου και σε σταθερή θερμοκρασία, εισάγονται κάποιες ποσότητες των αερίων Η 2(g) και Ι 2(g) τα οποία αντιδρούν σύμφωνα με
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 1. Σε δοχείο σταθερού όγκου και σε σταθερή θερμοκρασία, εισάγονται κάποιες ποσότητες των αερίων Η 2(g) και Ι 2(g) τα οποία αντιδρούν σύμφωνα με
ΜΗΧΑΝΙΚΗ ΦΥΣΙΚΩΝ ΔΙΕΡΓΑΣΙΩΝ Ι & ΙΙ Εργαστηριακή Άσκηση 1: ΚΡΥΣΤΑΛΛΩΣΗ
 Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
Ε Θ Ν Ι Κ Ο Μ Ε Τ Σ Ο Β Ι Ο Π Ο Λ Υ Τ Ε Χ Ν Ε Ι Ο ΣΧΟΛΗ ΧΗΜΙΚΩΝ ΜΗΧΑΝΙΚΩΝ ΤΟΜΕΑΣ ΙΙ: Σχεδιασμού, Ανάλυσης & Ανάπτυξης Διεργασιών και Συστημάτων ΕΡΓΑΣΤΗΡΙΟ ΣΧΕΔΙΑΣΜΟΥ & ΑΝΑΛΥΣΗΣ ΔΙΕΡΓΑΣΙΩΝ Διευθυντής: Ι.
