ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΔΙΑΜΑΝΤΗΣ ΒΙΟΛΟΓΟΣ
|
|
|
- Διονυσόδωρος Δημητρακόπουλος
- 7 χρόνια πριν
- Προβολές:
Transcript
1 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΖΩΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΖΩΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΕΠΙΔΡΑΣΗ ΤΗΣ ΛΕΠΤΙΝΗΣ ΣΤΟΥΣ ΕΝΔΟΚΥΤΤΑΡΙΚΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ ΚΑΙ ΣΤΙΣ ΑΘΗΡΟΓΟΝΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΟΝΟΚΥΤΤΑΡΩΝ ΑΝΘΡΩΠΟΥ ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΔΙΑΜΑΝΤΗΣ ΒΙΟΛΟΓΟΣ ΘΕΣΣΑΛΟΝΙΚΗ 2009
2 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΖΩΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΖΩΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΕΠΙΔΡΑΣΗ ΤΗΣ ΛΕΠΤΙΝΗΣ ΣΤΟΥΣ ΕΝΔΟΚΥΤΤΑΡΙΚΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ ΚΑΙ ΣΤΙΣ ΑΘΗΡΟΓΟΝΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΟΝΟΚΥΤΤΑΡΩΝ ΑΝΘΡΩΠΟΥ ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ ΔΙΑΜΑΝΤΗΣ ΒΙΟΛΟΓΟΣ ΘΕΣΣΑΛΟΝΙΚΗ 2009
3 ARISTOTLE UNIVERSITY OF THESSALONIKI FACULTY OF SCIENCES SCHOOL OF BIOLOGY DEPARTMENT OF ZOOLOGY LABORATORY OF ANIMAL PHYSIOLOGY DOCTORAL THESIS THE EFFECT OF LEPTIN ON INTRACELLULAR SIGNAL TRANSDUCTION AND THE PRO-ATHEROSCLEROTIC PROPERTIES OF HUMAN MONOCYTES DIAMANTIS KONSTANTINIDIS BIOLOGIST/RESEARCHER THESSALONIKI 2009
4 Επιβλέπουσα Καθηγήτρια Καλογιάννη-Δημητριάδη Μάρθα (Καθηγήτρια Τμήματος Βιολογίας, ΑΠΘ) Τριμελής Συμβουλευτική Επιτροπή Καλογιάννη-Δημητριάδη Μάρθα (Καθηγήτρια Τμήματος Βιολογίας, ΑΠΘ) Κολιάκος Γεώργιος (Αναπληρωτής Καθηγητής Τμήματος Ιατρικής, ΑΠΘ) Θεοφιλίδης Γεώργιος (Καθηγητής Τμήματος Βιολογίας, ΑΠΘ) Επταμελής Εξεταστική Επιτροπή Καλογιάννη-Δημητριάδη Μάρθα (Καθηγήτρια Τμήματος Βιολογίας, ΑΠΘ) Κολιάκος Γεώργιος (Αναπληρωτής Καθηγητής Τμήματος Ιατρικής, ΑΠΘ) Θεοφιλίδης Γεώργιος (Καθηγητής Τμήματος Βιολογίας, ΑΠΘ) Κοκόλης Νικόλαος (Καθηγητής Τμήματος Κτηνιατρικής, ΑΠΘ) Παλέτας Κωνσταντίνος (Αναπληρωτής Καθηγητής Τμήματος Ιατρικής, ΑΠΘ) Μιχαηλίδης Βασίλειος (Αναπληρωτής Καθηγητής Τμήματος Βιολογίας, ΑΠΘ) Παπαδόπουλος Αθανάσιος (Αναπληρωτής Καθηγητής Τμήματος Βιολογίας, ΑΠΘ)
5 Η έγκριση της παρούσας διδακτορικής διατριβής από το τμήμα Βιολογίας της σχολής Θετικών Επιστημών του Αριστοτελείου Πανεπιστημίου Θεσσαλονίκης δεν υποδηλώνει αποδοχή των απόψεων του συγγραφέα
6 Το παρών έργο υλοποιείται στο πλαίσιο του Μέτρου 8.3 του Ε.Π. Ανταγωνιστικότητα Γ Κοινοτικό Πλαίσιο Στήριξης και συγχρηματοδοτείται κατά: 75% της Δημόσιας Δαπάνης από την Ευρωπαϊκή Ενωση - Ευρωπαϊκό Κοινωνικό Ταμείο 25% της Δημόσιας Δαπάνης από το Ελληνικό Δημόσιο - Υπουργείο Ανάπτυξης - Γενική Γραμματεία Έρευνας και Τεχνολογίας
7 ΕΠΙΔΡΑΣΗ ΤΗΣ ΛΕΠΤΙΝΗΣ ΣΤΟΥΣ ΕΝΔΟΚΥΤΤΑΡΙΚΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ ΚΑΙ ΣΤΙΣ ΑΘΗΡΟΓΟΝΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΑΝΘΡΩΠΙΝΩΝ ΜΟΝΟΚΥΤΤΑΡΩΝ ΔΙΑΜΑΝΤΗΣ ΚΩΝΣΤΑΝΤΙΝΙΔΗΣ Εργαστήριο Φυσιολογίας Ζώων, Τομέας Ζωολογίας, Τμήμα Βιολογίας, Σχολή Θετικών Επιστημών, Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης, Θεσσαλονίκη, ΤΚ Η αθηρωμάτωση είναι μια ασθένεια η οποία τείνει να εξελιχθεί σε μάστιγα για τους κατοίκους των αναπτυγμένων χωρών. Οι αρνητικές επιπτώσεις που επιφέρει στην ποιότητα της ζωής του ατόμου, αλλά και ευρύτερα σε κοινωνικό και οικονομικό επίπεδο την έχουν καταστήσει σπουδαίο ερευνητικό στόχο παγκοσμίως. Στόχος της παρούσας μελέτης ήταν η διερεύνηση της επίδρασης της ορμόνης λεπτίνης στις αθηρογόνες ιδιότητες των ανθρώπινων μονοκυττάρων. Η λεπτίνη είναι μια ορμόνη που παράγεται από το λιπώδη ιστό η οποία μέσω επίδρασης στον υποθάλαμο έχει ως πρωταρχικό στόχο την παύση της λήψης τροφής από τον οργανισμό όταν τα ενεργειακά αποθέματα επαρκούν. Ως εκ τούτου, τα επίπεδά της στο αίμα εμφανίζονται ιδιαιτέρως αυξημένα σε καταστάσεις παχυσαρκίας. Η δράση της λεπτίνης, δεν περιορίζεται στην ανορεκτική της δράση, αλλά έχει ποικίλες δράσεις επιδρώντας σε μεγάλη ποικιλία κυτταρικών τύπων. Ένας από τους τύπους κυττάρων στους οποίους επιδρά η λεπτίνη είναι τα μονοκύτταρα, κύτταρα του ανοσοποιητικού συστήματος τα οποία συμμετέχουν στους αθηρωματικούς μηχανισμούς. Στην παρούσα εργασία μελετήθηκε η επίδραση της λεπτίνης σε ιδιότητες των μονοκυττάρων που μπορούν να χαρακτηριστούν αθηρογόνες. Χρησιμοποιήθηκαν συγκεντρώσεις λεπτίνης οι οποίες κυμαίνονταν από χαμηλές κανονικές (1,6ng/ml) εώς υψηλές υπερλεπτιναιμικές (1600ng/ml). Διαπιστώθηκε ότι σε υπερλεπτιναιμικές συγκεντρώσεις η λεπτίνη ενίσχυε αθηρογόνες ιδιότητες των μονοκυττάρων όπως την προσκόλληση στο συστατικό της εξωκυττάριας ουσίας λαμινίνη-1, καθώς και τη μετανάστευση διαμέσου αυτής. Οι ιδιότητες αυτές σχετίζονται με την αλληλεπίδραση των μονοκυττάρων με τα ενδοθηλιακά κύτταρα και τη μετακίνησή τους στον υποενδοθηλιακό χώρο. Επίσης, στις ίδιες συγκεντρώσεις ενίσχυσε την επιφανειακή έκφραση των υποδοχέων 7
8 ρακοσυλλεκτών CD36 και μέσω αυτών τη φαγοκύττωση μετρίως οξειδωμένων λιποπρωτεϊνων χαμηλής πυκνότητας (oxldl 3 ), ιδιότητες που σχετίζονται με τη μετατροπή των μονοκυττάρων προς αφρώδη κύτταρα, βασικά συστατικά της αθηρωματικής πλάκας. Η ενίσχυση των παραπάνω ιδιοτήτων από τη λεπτίνη υποδηλώνουν ότι υπερλεπτιναιμικά άτομα, όπως οι παχύσαρκοι ασθενείς, είναι ιδιαιτέρως ευάλωτα σε αθηρωματικά γεγονότα. Αντιθέτως, η λεπτίνη δεν φάνηκε να ενισχύει την επιφανειακή έκφραση του υποδοχέα ρακοσυλλέκτη CD68, καθώς και των υπομονάδων των ιντεγκρινών CD11a, CD11b, CD18, CD29 και CD49b τουλάχιστον για το χρονικό διάστημα επώασης που εφαρμόστηκε. Όσον αφορά στα μονοπάτια μεταγωγής σήματος που εκκινούνται από τη λεπτίνη και εντείνουν τις παραπάνω αθηρωματικές ιδιότητες των μονοκυττάρων, στην προσκόλληση στη λαμινίνη-1 φαίνεται να συμμετέχουν ο ΝΗΕ1, η PI3K, συμβατικές PKC, ο κυτταροσκελετός της ακτίνης και η NADPH οξειδάση, στη μετανάστευση στη λαμινίνη-1 οι ίδιες πρωτεϊνες πλην της NADPH οξειδάσης, ενώ στις διαδικασίες επιφανειακής έκφρασης του υποδοχέα CD36 και στη φαγοκύττωση των oxldls συμμετέχουν ο ΝΗΕ1, η PI3K, συμβατικές PKC και η NADPH οξειδάση. Παράλληλα σε κανονικές εώς υψηλές κανονικές συγκεντρώσεις η λεπτίνη αύξησε το οξειδωτικό στρες που παρήγαγαν τα μονοκύτταρα μέσω ενός μηχανισμού που περιλαμβάνει τον ΝΗΕ1, την PI3K, συμβατικές PKCs και τη NADPH οξειδάση. Ταυτόχρονα, στις ίδιες συγκεντρώσεις λεπτίνης παρατηρήθηκε αύξηση της δραστικότητας του ενζύμου δισμουτάση του σουπεροξειδίου, καθώς και ενεργοποίηση του ΝΗΕ1 που έγινε αντιληπτή ως αύξηση του ενδοκυτταρικού ph. Όλα αυτά μαζί, υποδηλώνουν ότι σε κανονικές εώς υψηλές κανονικές συγκεντρώσεις η λεπτίνη αυξάνει την παραγωγή οξειδωτικού στρες από τα μονοκύτταρα, κάτι που δυνητικά μπορεί να τους προκαλέσει βλάβες ή/και να προκαλέσει οξείδωση συστατικών όπως οι LDLs και στοιχεία της εξωκυττάριας ουσίας συμβάλλοντας έτσι στη δημιουργία αθηρωματικών γεγονότων. Επιπρόσθετα, διαπιστώθηκε ότι η λεπτίνη δεν επέδρασε στα επίπεδα σύνδεσης της προστατευτικής πρωτεϊνης Hsp70 στον NHE1, αύξησε όμως, τα επίπεδα γλουταθειονυλίωσης των ήδη συνδεδεμένων στον ΝΗΕ1 μορίων της Hsp70. Συνοψίζοντας, στην παρούσα εργασία διαπιστώθηκε ότι η λεπτίνη πράγματι ενισχύει ορισμένες αθηρογόνες ιδιότητες των ανθρώπινων μονοκυττάρων κατά δοσοεξαρτώμενο τρόπο. Στους μηχανισμούς μεταγωγής σήματος που εκκινεί η λεπτίνη και 8
9 που σχετίζονται με τις παραπάνω αθηρογόνες ιδιότητες συμμετέχουν ο ΝΗΕ1, η PI3K, οι συμβατικές PKCs, η NADPH οξειδάση και ο κυτοσκελετός της ακτίνης. 9
10 THE EFFECT OF LEPTIN ON INTRACELLULAR SIGNAL TRANSDUCTION AND THE PRO-ATHEROSCLEROTIC PROPERTIES OF HUMAN MONOCYTES DIAMANTIS KONSTANTINIDIS Laboratory of Animal Physiology, Department of Zoology, School of Biology, Faculty of Sciences, Aristotle Univeristy of Thessaloniki, Thessaloniki, Atherosclerosis is a disease which is threatening to reach pandemic proportions in the developed world. Its negative effects on the quality of life of the individual, as well as its socioeconomic impact have led to it being a major research target worldwide. The present study focuses on the effects of the hormone leptin on the atherogenic properties of human monocytes. Leptin is an adipose tissue-derived hormone which lowers food intake when energy stores are high by acting on the hypothalamus. Consequently, its blood levels are particularly high in obese patients. Apart from its anorectic action leptin, leptin has many other modes of action, affecting a wide variety of cell types. Monocytes are cells of the immune system participating in atherogenic procedures and which are affected by leptin. In the present study, the effect of leptin on the atherogenic properties was studied. Leptin was used at concentrations which ranged from low normal (1.6ng/ml) to high hyperleptinaemic (1600ng/ml). It was oobserved that leptin at hyperleptinaemic concentrations enhanced such atherogenic properties of monocytes as adhesion to and migration through the extracellular matrix protein laminin-1. These properties are pertinent to monocyteendothelial cell interaction and the migration of monocytes to the subendothelial space. Additionally, at the same hyperleptinaemic concentrations leptin increased surface expression of the scavenger receptor CD36 and through it, oxidized low density lipoprotein (oxldl 3 ) phagocytosis. These properties are related to monocytes becoming foam cells, fundamental components of atheromatous plaques. The above mentioned leptin-induced effects imply that hyperleptinaemic individuals, such as obese patients, are particularly vulnerable to these atherogenous properties of monocytes. In other experiments, leptin was not found to increase surface expression 10
11 of CD68, another scavenger receptor, as well as that of integrin subunits CD11a, CD11b, CD18, CD29 and CD49b, at least for the incubation time implemented. Regarding the signal transduction pathways through which leptin enhanced the above mentioned properties, monocyte adhesion to laminin-1 involved NHE1, PI3K, conventional PKCs, the actin cytoskeleton and NADPH oxidase, migration through laminin-1 involved the same proteins but not NADPH oxidase. Leptin induced surface expression of CD36 and oxldl phagocytosis involved NHE1, PI3K, conventional PKCs and NADPH oxidase. Moreover, at normal to high normal concentrations, leptin increased oxidative stress produced by monocytes through a mechanism involving NHE1, PI3K, conventional PKCs and NADPH oxidase. At the same time, at the same concentrations leptin increased the activity of superoxide dismutase, as well as of NHE1. The latter being visualized as an increase in intracellular ph. Taken altogether these results indicate that leptin increases oxidative stress produced by monocytes, something which could have detrimental effects on the cells themselves or/and induce oxidative damage to LDLs and extracellular matrix components, thus contributin to atherogenous phenomena. Additionally, leptin did not have any effect on the binding levels of the protective protein Hsp70 on NHE1, however it did increase glutahtionylation levels of Hsp70 molecules already bound to NHE1. In conclusion, in the present study it was demonstrated that leptin enhances certain human monocyte atherogenous properties in a dose-dependent manner. The signalling pathways induced by leptin in order to convey these atherogenous properties involves NHE1, PI3K, conventional PKCs, NADPH oxidase and the actin cytoskeleton. 11
12 Πρόλογος Τεσσαράμισι χρόνια προσπάθειας οδήγησαν στο σύγγραμμα που κρατάτε στα χέρια σας. Η δουλειά αυτή υπογράφεται ως είθισται από ένα μόνο άτομο, σαφέστατα όμως, μερίδιο κατέχουν και όλοι οι άνθρωποι οι οποίοι βοήθησαν, συμβούλεψαν, συνεργάστηκαν και διαμόρφωσαν το κατάλληλο περιβάλλον ώστε να καταστεί εφικτή η υλοποίησή της. Κατά συνέπεια, ένα ευχαριστώ είναι το λιγότερο που μπορώ να προσφέρω σε αυτούς τους ανθρώπους. Όμως, ας πάρουμε τα πράγματα από την αρχή Οφείλω να ομολογήσω ότι το καλοκαίρι του 2004, αμέσως μετά την απόκτηση του πτυχίου του Βιολογικού τμήματος του ΑΠΘ, η εκπόνηση διδακτορικής διατριβής δεν ήταν στα άμεσα σχέδιά μου. Όμως, η ευκαιρία που μου πρόσφερε η κ. Μάρθα Καλογιάννη, στα πλαίσια του ερευνητικού προγράμματος ΠΕΝΕΔ 2003, να μελετήσω υπό πολύ καλές συνθήκες την αθηρωμάτωση, ένα πολύπλοκο φαινόμενο που επηρεάζει αρνητικά την ποιότητα ζωής εκατομμυρίων ανθρώπων ανά τον κόσμο ήταν ιδιαιτέρως δελεαστική. Η γνωριμία μου με την κ. Μάρθα Καλογιάννη ξεκίνησε το 2002 όταν με δέχτηκε ως διπλωματικό της φοιτητή σε μια διπλωματική εργασία που αφορούσε την επίδραση της αναστολής του ΝΗΕ1 σε καρκινικά κύτταρα ανθρώπου και που περιελάμβανε συνεργασία με το εργαστήριο του κ. Γεώργιου Κολιάκου στην Ιατρική σχολή του ΑΠΘ. Η εμπειρία που αποκόμισα από τη διπλωματική μου εργασία ήταν άκρως θετική και ήταν έτσι ένας πρόσθετος παράγοντας ώστε το ενδεχόμενο να συνεχίσω στα γνώριμα εργαστήρια με διδακτορική διατριβή να μη με αφήσει αδιάφορο. Κατά συνέπεια, οφείλω ένα πολύ μεγάλο ευχαριστώ καταρχήν στην καθηγήτρια του τομέα Ζωολογίας του τμήματος Βιολογίας του ΑΠΘ κ. Μάρθα Καλογιάννη για την εμπιστοσύνη και την κατανόηση που μου έδειξε όλα αυτά τα χρόνια. Όσον αφορά την πραγματοποίηση της παρούσας εργασίας, οι συμβουλές και επισημάνσεις της υπήρξαν υπερπολύτιμες. Δίχως υπερβολή, η καθοδήγησή της έχει υπάρξει καθοριστική, όχι μόνο για την εκπόνηση της παρούσας διατριβής αλλά και για την έως τώρα πορεία μου στο χώρο της Βιολογίας. Ένα μεγάλο ευχαριστώ οφείλω και στον αναπληρωτή καθηγητή του εργαστηρίου Βιολογικής Χημείας της Ιατρικής σχολής του ΑΠΘ κ. Γεώργιο Κολιάκο. Πέρα από 12
13 τη φιλοξενία που μου παρείχε στο εργαστήριό του, η συμβολή του στην ερευνητική κατεύθυνση που πήρε η διατριβή είναι ανεκτίμητη. Μέσω γόνιμων συζητήσεων υπήρξε πηγή ρηξικέλευθων ερευνητικών ιδεών και ευελπιστώ ότι έστω εν μέρει κατάφερα να αφομοιώσω την ικανότητά του ορισμένες φορές να σκέφτεται με έναν εποικοδομητικά ανορθόδοξο τρόπο. Ευχαριστώ ακόμα τον αναπληρωτή καθηγητή Παθολογίας του τμήματος Ιατρικής του ΑΠΘ, κ. Κωνσταντίνο Παλέτα για την άμεση βοήθεια όποτε του ζητήθηκε, καθώς επίσης και την προϊσταμένη του κέντρου αιμοδοσίας του Ιπποκρατείου νοσοκομείου Θεσσαλονίκης κ. Μέγα για τη διαχρονική παροχή πειραματικού υλικού που πληρούσε τις απαραίτητες προδιαγραφές. Στο σημείο αυτό θα ήθελα να ευχαριστήσω και τα τμήματα Βιολογίας και Ιατρικής του ΑΠΘ. Το μεν πρώτο έχει αποτελέσει κομμάτι της ζωής μου εδώ και σχεδόν μία δεκαετία, το δε δεύτερο με έχει φιλοξενήσει σε μεγάλο μέρος της ερευνητικής μου δραστηριότητας. Η εκπόνηση της παρούσας διδακτορικής διατριβής υπήρξε η αφορμή να γνωρίσω και να συνεργαστώ με πραγματικά ικανούς και αξιόλογους ανθρώπους. Έτσι, θα ήθελα καταρχήν να ευχαριστήσω τη διδάκτορα Ζαχαρούλα Ζολώτα που ως η αμέσως προηγούμενη διπλωματικός της κ. Καλογιάννη με εκπαίδευσε το 2002 στις βασικές εργαστηριακές τεχνικές και που όλα αυτά τα χρόνια με τιμάει με τη φιλία της. Παράλληλα, θα ήθελα να ευχαριστήσω τις υποψήφιες διδάκτορες Χριστίνα Μπεφάνη, Κωνσταντίνα Τοπουρίδου και Μαρία Σαρηγιάννη για την άριστη συνεργασία. Συνέβαλλαν τα μέγιστα στη δημιουργία ενός πολύ καλού, φιλικού αλλά και επιστημονικού κλίματος στο εργαστήριο και η γνωριμία μου μαζί τους συγκαταλέγεται σαφέστατα στα πρόσθετα κέρδη από την εκπόνηση της διδακτορικής μου διατριβής. Δεν πρέπει να παραλείψω να ευχαριστήσω τους φίλους μου οι οποίοι μου συμπαραστάθηκαν σε αυτή την προσπάθεια, έδειξαν κατανόηση και με συμβούλεψαν όποτε αυτό χρειάστηκε. Άφησα για το τέλος τα πλέον αγαπημένα μου πρόσωπα, τα μέλη της οικογένειάς μου. Θα ήθελα να ευχαριστήσω με όλη μου την καρδιά τους γονείς μου Γιώργο και Δάφνη και τον αδερφό μου Ανδρέα για τη διαχρονική υποστήριξη και αγάπη που μου έχουν παράσχει. Τα λόγια είναι λίγα για να εκφράσω τη σημασία που έχει για μένα η στήριξη και η πίστη προς τις επιλογές μου που αισθάνομαι από την οικογένειά μού. 13
14 Τελειώνοντας, εύχομαι το παρών σύγγραμμα να πληροί τα κριτήρια μιας τουλάχιστον ενδιαφέρουσας διατριβής. 14
15 Περιεχόμενα Εισαγωγή 1.Αθηρωμάτωση Γενικά στοιχεία Αθηρωματική διαδικασία.21 2.Χημοκίνες.32 3.Μόρια Κυτταραικής Προσκόλλησης (CAMs) IgSF CAMs Σελεκτίνες (Selectins) Ιντεγκρίνες (Integrins) Καντερίνες (Cadherins) Υποδοχείς ρακοσυλλέκτες CD Άλλοι υποδοχείς ρακοσυλλέκτες Μονοκύτταρα Ορμόνες που σχετίζονται με την παχυσαρκία Λεπτίνη Άλλες ορμόνες που σχετίζονται με την παχυσαρκία Ιοντοανταλλάκτης Na + /H + (NHE1) Ελεύθερες ρίζες και αντιοξειδωτικοί μηχανισμοί Σκοπός της εργασίας...51 Παράρτημα Εισαγωγής 1. Λιποπρωτεϊνες χαμηλής πυκνότητας (LDLs) Εξωκυττάρια ουσία Δείκτης μάζας σώματος (BMI) Μονοπάτι μεταγωγής σήματος JAK/STAT..56 Υλικά και Μέθοδοι 1.1 Απομόνωση, κρυοαπoθήκευση και επαναφορά μονοκυττάρικο από ολικό αίμα Διαδικασία απομόνωσης μονοκυττάρων από ολικό αίμα Κρυοαποθήκευση μονοκυττάρων σε υγρό άζωτο.63 15
16 1.1.3 Μέτρηση βιωσιμότητας και αριθμού μονοκυττάρων Μέτρηση βιωσιμότητας με τη μέθοδο του Trypan Blue Μέτρηση βιωσιμότητας σε κυτταρόμετρο ροής (με χρήση της...64 φθορίζουσας ουσίας 7-AAD και αντισώματος κατά του επιφανειακού δείκτη CD Απόψυξη μονοκυττάρων από το υγρό άζωτο Προσκόλληση μονοκυττάρων σε υπόστρωμα λαμινίνης Μετανάστευση μονοκυττάρων σε υπόστρωμα λαμινίνης Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD68, CD49b, 68 CD29, CD18, CD11a, CD11b Προσδιορισμός σε φθορισμόμετρο Προσδιορισμός με κυτταρομετρία ροής Προσδιορισμός επιπέδων φαγοκύττωσης οξειδωμένων λιποπρωτεϊνών 70 χαμηλής πυκνότητας (oxidized low-density lipoproteins, oxldls) Παρασκευή οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας (oxldls) Πείραμα φαγοκύττωσης των oxldls από μονοκύτταρα Προσδιορισμός τιμής ενδοκυτταρικού ph (phi) Προσδιορισμός ελευθέρων ριζών με H 2 DCFDA Προσδιορισμός του ανιόντος σουπεροξειδίου Προσδιορισμός του ανιόντος σουπεροξειδίου με ΝΒΤ Προσδιορισμός του ανιόντος σουπεροξειδίου με DΗΕ Προσδιορισμός δραστικότητας της δισμουτάσης του σουπεροξειδίου (SOD) Συνανοσοκαθίζηση του ΝΗΕ Ηλεκτροφόρηση δειγμάτων που προήλθαν από ανοσοκαθίζηση του ΝΗΕ Western Blotting και εμφάνιση με τη μέθοδο ECL δειγμάτων που προήλθαν.81 από ανοσοκαθίζηση του ΝΗΕ Στατιστική ανάλυση πειραματικών αποτελεσμάτων.82 Παράρτημα Υλικών και Μεθόδων 1.Παρασκευή PBS 1x Παρασκευή 500ml θρεπτικού διαλύματος πλήρους IMDM 85 3.Βασική αρχή φθορισμού
17 4.Προ-καθαρισμός (Pre-clearance).86 5.Μέτρηση συγκέντρωσης πρωτεϊνης Μέτρηση συγκέντρωσης πρωτεϊνης με BCA Μέτρηση συγκέντρωσης πρωτεϊνης με τη μέθοδο Bradford.87 6.Σύσταση gel.88 7.SDS.89 8.Ανίχνευση πρωτεϊνών σε gel με τη μέθοδο silver staining Χρήση blocking buffer Ενισχυμένη χημειοφωταύγεια (ECL) Dot blot.91 Πειραματικά αποτελέσματα 1. Προσκόλληση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 93 Α) Καμπύλη δόσης-απόκρισης λεπτίνης..93 Β) Πειραματικά αποτελέσματα Μετανάστευση μονοκυττάρων σε υπόστρωμα λαμινίνης Α) Καμπύλη δόσης-απόκρισης λεπτίνης.97 Β) Πειραματικά αποτελέσματα Προσδιορισμός της επιφανειακής έκφρασης υποδοχέων-ρακοσυλλεκτών Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD36 99 Α) Καμπύλη δόσης-απόκρισης λεπτίνης..99 Β) Πειραματικά αποτελέσματα Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD Προσδιορισμός της επιφανειακής έκφρασης υπομονάδων των ιντεγκρινών Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD49b Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD11a Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD11b Προσδιορισμός φαγοκύττωσης των oxldl 3 από μονοκύτταρα Α) Καμπύλη δόσης-απόκρισης λεπτίνης 107 Β) Πειραματικά αποτελέσματα Προσδιορισμός φαγοκύττωσης των oxldl 24 από μονοκύτταρα
18 7. Προσδιορισμός τιμής ενδοκυτταρικού ph (phi) Προσδιορισμός ελευθέρων ριζών με H 2 DCFDA 116 Α) Καμπύλη δόσης-απόκρισης λεπτίνης..116 Β) Πειραματικά αποτελέσματα Προσδιορισμός του ανιόντος σουπεροξειδίου Προσδιορισμός του ανιόντος σουπεροξειδίου με ΝΒΤ 119 Α) Καμπύλη δόσης-απόκρισης λεπτίνης..119 Β) Πειραματικά αποτελέσματα Προσδιορισμός του ανιόντος σουπεροξειδίου με DHE.121 Α) Καμπύλη δόσης-απόκρισης λεπτίνης Β) Πειραματικά αποτελέσματα Προσδιορισμός δραστικότητας της δισμουτάσης του σουπεροξειδίου (SOD) Ανοσοκαθίζηση της ΝΗΕ1 και ανίχνευση της Hsp70 και της γλουταθειόνης Παράρτημα Αποτελεσμάτων Πίνακες.129 Συζήτηση Μέρος Α Μελέτη της επίδρασης της λεπτίνης σε δυνητικά αθηρωματικές δράσεις των μονοκυττάρων ανθρώπου Γενικός ρόλος των μονοκυττάρων κατά την αθηρωμάτωση Επίδραση της λεπτίνης στην ικανότητα προσκόλλησης των μονοκυττάρων ανθρώπου στο συστατικό της εξωκυττάριας ουσίας λαμινίνη Επίδραση της λεπτίνης στην ικανότητα μετανάστευσης των μονοκυττάρων ανθρώπου διαμέσου του συστατικού της εξωκυττάριας ουσίας λαμινίνη Επίδραση της λεπτίνης στην επιφανειακή έκφραση των υποδοχέων ρακοσυλλεκτών CD36 και CD68 από μονοκύτταρα ανθρώπου Επίδραση της λεπτίνης στην επιφανειακή έκφραση των υπομονάδων των ιντεγκρινών CD11a, CD11b, CD18, CD29 και CD49b από μονοκύτταρα ανθρώπου Επίδραση της λεπτίνης στην ικανότητα φαγοκύττωσης μετρίως (oxldl 3 ) και πλήρως οξειδωμένων (oxldl 24 ) λιποπρωτεϊνών χαμηλής πυκνότητας 18
19 από μονοκύτταρα ανθρώπου.142 Σύνοψη Α Μέρους 143 Μέρος Β Μελέτη της επίδρασης της λεπτίνης σε οξειδωτικές-αντιοξειδωτικές λειτουργίες των μονοκυττάρων ανθρώπου Επίδραση της λεπτίνης στην τιμή του ενδοκυτταρικού ph (phi) μονοκυττάρων ανθρώπου Επίδραση της λεπτίνης στην παραγωγή δραστικών μορφών οξυγόνου (ROS) και αζώτου (RNS) από μονοκύτταρα ανθρώπου Επίδραση της λεπτίνης στην παραγωγή του ανιόντος σουπεροξειδίου από μονοκύτταρα ανθρώπου Επίδραση της λεπτίνης στη δραστικότητα του ενζύμου δισμουτάση του σουπεροξειδίου των μονοκυττάρων ανθρώπου Επίδραση της λεπτίνης στη σύνδεση της Hsp70 με τον NHE1 και στα επίπεδα γλουταθειονυλίωσης της Hsp70 σε μονοκύτταρα ανθρώπου.153 Σύνοψη Β Μέρους 156 Μέρος Γ Σκιαγράφηση μονοπατιών μεταγωγής σήματος που εκκινούνται από τη λεπτίνη σε μονοκύτταρα ανθρώπου και σχετίζονται με τις αθηρογόνες ιδιότητες αυτών 158 Συμπεράσματα..161 Βιβλιογραφία.164 Εργασίες.165 Βιβλία.182 Στατιστικές αναφορές 183 Αντιδραστήρια (Συντμήσεις Προμηθευτές)
20 1.Αθηρωμάτωση 1.1.Γενικά στοιχεία Η αθηρωμάτωση (ή αθηρογένεση) είναι μια ασθένεια ευρύτατα διαδεδομένη στις αναπτυγμένες χώρες όπου μέσω των καρδιαγγειακών προβλημάτων που προκαλεί αποτελεί και την κυρίαρχη αιτία θανάτου (Lefkowitz & Willerson, 2001). Η διάδοσή της οφείλεται σε πλήθος παραγόντων με κυριότερους το κάπνισμα, την πλούσια σε κακά λιπαρά και γλυκόζη δυτικού τύπου διατροφή, την έλλειψη σωματικής άσκησης και την παράλληλη εκδήλωση διαβήτη (Kuller, 2006; Mallika et al., 2007). Η αθηρωμάτωση εμφανίζεται με τη μορφή συμπαγών πλακών (αθηρωματικές πλάκες) οι οποίες μέσω μιας πολύπλοκης διαδικασίας, αρχίζουν να σχηματίζονται από το τοίχωμα μιας αρτηρίας και επεκτείνονται διαρκώς προς τον αυλό της (εικ.1). Αυτό έχει ως αποτέλεσμα μερική έως ολική στένωση της παθούσας αρτηρίας και κατά συνέπεια αντίστοιχο περιορισμό της ικανότητάς της να επιτρέπει τη διέλευση του αίματος. Η παθογένεια που προκαλείται από αυτή την κατάσταση εξαρτάται από το εύρος της στένωσης της αρτηρίας, καθώς και από το σημείο του σώματος στο οποίο βρίσκεται αυτή. Έτσι, ολική στένωση μιας αρτηρίας της οποίας όμως η λειτουργία μπορεί να αναπληρωθεί με περαιτέρω φυσιολογική διαστολή μιας γειτονικής υγιούς αρτηρίας δύναται να μην προκαλέσει κανένα σύμπτωμα. Αντίθετα, ακόμα και μερική στένωση αρτηριών που επωμίζονται το έργο της αιμάτωσης ζωτικών οργάνων όπως για παράδειγμα περιοχών του εγκεφάλου οδηγεί σε άμεση εμφάνιση συμπτωμάτων, συχνά μη αναστρέψιμων (λόγω των μόνιμων βλαβών που μπορούν να υποστούν ευαίσθητες περιοχές ακόμα και έπειτα από βραχύχρονη διακοπή της αιμάτωσης-οξυγόνωσής τους). Κατά συνέπεια, η υποβόσκουσα αθηρωμάτωση είναι η κυριότερη αιτία καρδιαγγειακών επιπλοκών όπως τα εγκεφαλικά επεισόδια και το έμφραγμα του μυοκαρδίου (Lefkowitz & Willerson, 2001). Ένα άλλο ενδεχόμενο είναι η διάρρηξη και αποκόλληση των αθηρωματικών πλακών με αποτέλεσμα τη μεταφορά τους μέσω της αρτηριακής κυκλοφορίας σε σημεία όπου σχηματίζουν θρόμβους (Glass & Witztum, 2001). Αυτό εμποδίζει σε μεγάλο βαθμό τη διέλευση του αίματος προς τους ιστούς που βρίσκονται μετά το σημείο του θρόμβου και πολύ συχνά αποτελεί επείγον ιατρικό περιστατικό. Αξίζει να σημειωθεί ότι οι έννοιες αθηρωμάτωση και αρτηριοσκλήρυνση δεν είναι πάντοτε ταυτόσημες, καθότι η πρώτη αφορά τη σκλήρυνση του αρτηριακού 20
21 τοιχώματος συγκεκριμένα λόγω του σχηματισμού αθηρωματικών πλακών, ενώ η δεύτερη αφορά τη σκλήρυνση του αρτηριακού τοιχώματος για οποιονδήποτε λόγο (συμπεριλαμβανομένου του σχηματισμού αθηρωματικών πλακών, συνεπώς πρόκειται για πιο γενικό όρο). Εικόνα 1. Απεικόνιση της σταδιακής εξέλιξης της αθηρωματικής πλάκας (Libby, 2002). Picture 1. Schematic of the life history of an atheroma (Libby, 2002). 1.2.Αθηρωματική διαδικασία Είναι γενικά αποδεκτό ότι η αθηρογένεση ξεκινάει σε σημεία στα οποία το αρτηριακό τοίχωμα έχει υποστεί μικροτραυματισμούς. Οι μικροτραυματισμοί αυτοί είναι πολύ πιο συχνοί σε περιοχές του αρτηριακού τοιχώματος με ενεργοποιημένο ενδοθήλιο (Ross, 1999). Ανάμεσα στα σημαντικότερα αίτια της ενεργοποίησης του ενδοθηλίου θεωρείται ότι συγκαταλέγονται τα υψηλά επίπεδα λιποπρωτεϊνών χαμηλής πυκνότητας (LDLs 1 ), καθώς και των τροποποιημένων μορφών τους, των ελάχιστα τροποποιημένων LDLs (mmldls) και των οξειδωμένων LDLs (oxldls) στη γύρω περιοχή, οι υψηλές συγκεντρώσεις ελευθέρων ριζών που παράγονται υπό φυσιολογικές συνθήκες, αλλά και επιτείνονται από συνήθειες όπως το κάπνισμα, 21
22 ασθένειες όπως η υπέρταση και ο διαβήτης και χρόνιες μικροβιακές μολύνσεις (Østerud & Bjørklid, 2003). Η παρουσία των τροποποιημένων μορφών των LDLs (mmldls και oxldls) στον υποενδοθηλιακό χώρο εκκινεί τη διαδικασία φλεγμονής του ενδοθηλίου (Itabe et al., 2003) (εικ.2). Οι μηχανισμοί παραγωγής οξειδωτικών ριζών που μπορούν να προκαλέσουν οξείδωση των LDLs περιλαμβάνουν την αναπνευστική έκρηξη (respiratory burst), καθώς και διάφορα ενζυμικά συστήματα όπως η NADPH οξειδάση, η μυελοϋπεροξειδάση, η 15-λιποξυγενάση (15-LO) και οι συνθάσες του μονοξειδίου του αζώτου των μονοκυττάρων/μακροφάγων (inos, inducible nitric oxide synthase) και των ενδοθηλιακών κυττάρων (enos, endothelial nitric oxide synthase) (Heinecke, 1998). Με τον όρο αναπνευστική έκρηξη περιγράφεται η ταχύτατη απελευθέρωση μεγάλων ποσοτήτων ελεύθερων ριζών οξυγόνου από ουδετερόφιλα κοκκιοκύτταρα και μονοκύτταρα/μακροφάγα ενάντια σε εισβάλλοντα μικρόβια (βακτήρια και μύκητες) με στόχο την καταστροφή τους (Babior, 1984). Η NADPH οξειδάση συμμετέχει στη δημιουργία της αναπνευστικής έκρηξης μέσω τη παραγωγής της ελεύθερης ρίζας σουπεροξείδιο (Ο -. 2 ), ενώ η μυελοϋπεροξειδάση καταλύει την παραγωγή της οξειδωτικής ουσίας υποχλωριώδες οξύ (HOCl) από υπεροξείδιο (Η 2 Ο 2, που προήλθε από την αναπνευστική έκρηξη) και Cl - (Clifford & Repine, 1982; Bellavite, 1988). H 15-λιποξυγενάση μπορεί να δράσει απευθείας στις LDLs, προκαλώντας την οξείδωσή τους (Belkner et al., 1993). Όσον αφορά τις συνθάσες του μονοξειδίου του αζώτου, στα μεν μακροφάγα/μονοκύτταρα το μονοξείδιο του αζώτου δρα απευθείας ως αντιμικροβιακό οξειδωτικό, στα δε ενδοθηλιακά κύτταρα δρα ως αγγειοδιασταλτικός παράγοντας (Hibbs et al., 1988; Wallace, 2005). Και στις δύο περιπτώσεις το μονοξείδιο του αζώτου δύναται να συμβάλλει στην οξείδωση των LDLs. Οι oxldls που εν τέλει παράγονται έχουν την ικανότητα από μόνες τους να προσελκύουν μονοκύτταρα στο σημείο όπου βρίσκονται (Steinberg et al., 1989). Ταυτόχρονα όμως, οι oxldls επάγουν την έκκριση χημοκινών από τα ενδοθηλιακά κύτταρα, δηλαδή κυτοκινών όπως η MCP-1 (Monocyte Chemotactic Protein-1, χημειοτακτική πρωτεΐνη των μονοκυττάρων-1), οι οποίες προσελκύουν κύτταρα του ανοσοποιητικού συστήματος και κυρίως μονοκύτταρα και Τ-λεμφοκύτταρα, κατά χημειοτακτικό τρόπο (Navab et al., 1996). H ανίχνευση της MCP-1 (γνωστή και ως 22
23 CCL2, Chemokine C-C motif Ligand 2) πραγματοποιείται από τους υποδοχείς CCR2 των μονοκυττάρων και των Τ-λεμφοκυττάρων (Boisvert, 2004). Παράλληλα, τα ενδοθηλιακά κύτταρα εκφράζουν στην επιφάνειά τους συγκεκριμένα μόρια κυτταρικής προσκόλλησης (Cell Adhesion Molecules, CAMs) όπως τo VCAM-1 (Vascular CAM-1), το ICAM-1 (Intercellular CAM-1), την Ε- σελεκτίνη (E-selectin) και την P-σελεκτίνη (P-selectin) (Hansson, 2001). Η σύνδεση των μονοκυττάρων με τα μόρια VCAM-1 και ICAM-1 των ενδοθηλιακών κυττάρων πραγματοποιείται μέσω συγκεκριμένων μορίων κυτταρικής προσκόλλησης που εκφράζουν στην επιφάνειά τους, τις ιντεγκρίνες (integrins) Στην προκειμένη περίπτωση την α 4 β 1 -ιντεγκρίνη (γνωστή και ως VLA-4, Very Late Antigen-4) και την α L β 2 -ιντεγκρίνη (γνωστή και ως LFA-1, Lymphocyte Function-associated Antigen-1) αντίστοιχα. Με παρόμοιο τρόπο, η σύνδεση των μονοκυττάρων με τα μόρια σελεκτινών των ενδοθηλιακών κυττάρων πραγματοποιείται μέσω της πρωτεΐνης PSGL1 (P-Selectin Glycoprotein Ligand 1) η οποία εκφράζεται στην επιφάνεια των μονοκυττάρων και σχεδόν όλων των λευκοκυττάρων. Έτσι, μέσω συνδέσεων VCAM-1 α 4 β 1 -ιντεγκρίνη, ICAM-1 α L β 2 -ιντεγκρίνη και PSGL1-σελεκτίνης τα μονοκύτταρα προσδένονται σε πρώτη φάση στην περιοχή του ενδοθηλίου στην οποία έχει ξεκινήσει φλεγμονή (Ley et al., 2007). Αξίζει να αναφερθεί ακόμα ότι την πρωτεΐνη PSGL1, την εκφράζουν και τα ενδοθηλιακά κύτταρα, ενώ με τη σειρά τους τα λευκοκύτταρα εκφράζουν την δικιά τους σελεκτίνη, την L-selectin, δημιουργώντας έτσι μια επιπρόσθετη δυνατότητα σύνδεσης για την πρόσδεση των μονοκυττάρων στο ενδοθήλιο. Η πρόσδεση όμως αυτή είναι απλώς το αρχικό στάδιο της διαδικασίας προσκόλλησης των μονοκυττάρων, και γενικότερα των λευκοκυττάρων, στο ενδοθήλιο. Σχεδόν αμέσως ξεκινάει η κύλιση των μονοκυττάρων πάνω στα ενδοθηλιακά κύτταρα, μια διαδικασία στην οποία συμβάλλουν κυρίως συνδέσεις PSGL1-σελεκτινών και VCAM-1 α 4 β 1 -ιντεγκρίνης (Kansas, 1996). Κατόπιν, με την επίδραση χημοκινών τα μονοκύτταρα επιβραδύνονται και ακινητοποιούνται. Στην διαδικασία ακινητοποίησης παίζουν σπουδαίο ρόλο συνδέσεις VCAM-1 α 4 β 1 - ιντεγκρίνης, ICAM-1 α L β 2 -ιντεγκρίνης μεταξύ των μονοκυττάρων και των ενδοθηλιακών κυττάρων (και MADCAM1 α 4 β 7 -ιντεγκρίνης μεταξύ λεμφοκυττάρων και ενδοθηλιακών κυττάρων) (Campbell et al., 1996). 23
24 Εικόνα 2. Στην εικόνα φαίνονται τα τρία βήματα που παλαιότερα θεωρούνταν αρκετά για την προσκόλληση των λευκοκυττάρων στο ενδοθήλιο. Αυτά ήταν η κύλιση, η ενεργοποίηση και η ακινητοποίηση. Πλέον αναγνωρίζονται και πρόσθετα βήματα στην όλη διαδικασία όπως είναι η πρόσδεση, η αργή κύλιση, η ενίσχυση της προσκόλλησης, το άπλωμα και το ενδοαγγειακό σύρσιμο των κυττάρων. Ακολουθεί στη συνέχεια η μετανάστευση. Στα κουτιά αναφέρονται τα μόρια που παίζουν πρωτεύοντα ρόλο για την εκτέλεση του κάθε βήματος (Ley et al., 2007). Picture 2. The three steps that in the past were thought to be sufficient for leukocyte adhesion to the endothelium can be seen in the picture. These are rolling (κύλιση, as seen in Greek on the picture), activation (ενεργοποίηση) and arrest (ακινητοποίηση). Nowadays, more steps are recognized as taking place such as capture (πρόσδεση), slow rolling (αργή κύλιση), adhesion strengthening (ενίσχυση της προσκόλλησης), spreading (άπλωμα) and intravascular crawling (σύρσιμο), followed by migration. The boxes indicate the molecules that participate in every step (Ley et al., 2007). Ακολουθούν η ενίσχυση της προσκόλλησης, το άπλωμα των κυττάρων και στη συνέχεια το σύρσιμό τους επάνω στα ενδοθηλιακά κύτταρα. Οι διαδικασίες αυτές ελέγχονται από αυστηρά ρυθμιζόμενα μονοπάτια μεταγωγής σήματος, ενώ ρόλο παίζουν και οι συνδέσεις ICAM-1 α Μ β 2 -ιντεγκρίνης. Εν συνεχεία, πραγματοποιείται η διαδικασία της μετανάστευσης προς τον έσω χιτώνα, στην οποία τα λευκοκύτταρα αντιμετωπίζουν κυρίως τρία εμπόδια, το στρώμα ενδοθηλιακών κυττάρων (το διαπερνούν σε 2-5 min), τη βασική μεμβράνη των ενδοθηλιακών κυττάρων (το διαπερνούν σε 5-15 min) και τυχόν περικύτταρα (σχετικά αδιαφοροποίητα κύτταρα των αγγειακών τοιχωμάτων) που θα συναντήσουν. Ο πιο κοινός τύπος μετανάστευσης είναι η παρακυτταρική μετανάστευση 24
25 (paracellular migration) κατά την οποία τα λευκοκύτταρα διέρχονται από τα σημεία στα οποία έρχονται σε επαφή δύο γειτονικά ενδοθηλιακά κύτταρα. Κατά τη διάρκεια της παρακυτταρικής μετανάστευσης συμμετέχουν επιφανειακά μόρια των ενδοθηλιακών κυττάρων όπως τα PECAM-1 (Platelet Endothelial Cell Adhesion Molecule-1), ICAM-1, ICAM-2, JAMs (JAM-A, JAM-B, JAM-C, Junctional Adhesion Molecule-1), ESAM (Endothelial cell-selective Adhesion Molecule) και CD99 που συνδέονται με αντίστοιχα μόρια της επιφάνειας των λευκοκυττάρων (Vestweber, 2002). Τα ICAM-1, ICAM-2 συνδέονται με ιντεγκρίνες όπως η α L β 2 - ιντεγκρίνη, ενώ τα PECAM-1 και CD99 πραγματοποιούν ομοτυπικές συνδέσεις (PECAM-1 PECAM-1 και CD99 CD99). Οι JAMs πραγματοποιούν τόσο ομοτυπικές συνδέσεις (JAMs-JAMs), όσο και ετεροτυπικές (JAMs-ιντεγκρίνες). Έχει παρατηρηθεί ότι μερικά μόρια συμβάλουν στην μετανάστευση με ένα ειδικό για το ερέθισμα τρόπο. Έτσι για παράδειγμα, τα PECAM-1, ICAM-2 και JAM-A συμμετέχουν στη μετανάστευση μόνο όταν στα κύτταρα που τα εκφράζουν έχει επιδράσει ιντερλευκίνη-1β και όχι TNF-α (Nourshargh et al., 2006). Αντίστοιχα υπάρχουν μόρια που συμμετέχουν στη μετανάστευση με έναν ειδικό για τα κύτταρα τρόπο. Ένα τέτοιο μόριο είναι το ESAM που βοηθάει στη μετανάστευση των ουδετερόφιλων κοκκιοκυττάρων, αλλά όχι των Τ-λεμφοκυττάρων (Wegmann et al., 2006). Ένας σπανιότερος τρόπος μετανάστευσης είναι η διακυτταρική μετανάστευση (transcellular migration), η οποία παρατηρείται σε λευκοκύτταρα που έρχονται σε επαφή με στοιχεία του κεντρικού νευρικού συστήματος (Engelhardt & Wolburg, 2004). Στη συνέχεια, τα λευκοκύτταρα πρέπει να διαπεράσουν τη βασική μεμβράνη (basement membrane ή/και basal lamina, πρόκειται για τμήμα της εξωκυττάριας ουσίας 2 ) και τα διάσπαρτα περικύτταρα. Η βασική μεμβράνη των ενδοθηλιακών κυττάρων, όπως και των περισσότερων τύπων κυττάρων, αποτελείται κυρίως από δύο πρωτεϊνικά δίκτυα, αυτό των λαμινινών και αυτό του κολλαγόνου τύπου IV, που συνδέονται μεταξύ τους με διάφορα μόρια όπως η πρωτεογλυκάνη περλεκάνη. Σε γενικές γραμμές τα λευκοκύτταρα περνούν από τα σημεία λιγότερης αντίστασης, αποφεύγοντας έτσι τα περικύτταρα και τις περιοχές με υψηλή συγκέντρωση πρωτεΐνης (Wang et al., 2006). Έχει προταθεί ότι ορισμένα συστατικά της βασικής μεμβράνης όπως η θειική ηπαράνη (heparan sulfate) μπορούν και δεσμεύουν χημοκίνες με αποτέλεσμα να δημιουργείται μια χημειοτακτική οδός την οποία 25
26 μπορούν να ακολουθήσουν τα λευκοκύτταρα (Miyasaka & Tanaka, 2004). Επίσης, έχει προταθεί ότι μόρια κυτταρικής προσκόλλησης μπορούν να συμβάλλουν στη μετανάστευση όχι μόνο με τον παραδοσιακό τρόπο της σύνδεσής τους σε αντίστοιχα μόρια της επιφάνειας των λευκοκυττάρων, αλλά και μέσω επαγωγής της έκφρασης άλλων σχετικών μορίων. Έτσι, για παράδειγμα, το PECAM-1 έχει την ικανότητα να επάγει την έκφραση της α 6 β 1 -ιντεγκρίνης, του κύριου υποδοχέα λαμινίνης των λευκοκυττάρων, στην επιφάνεια των ουδετερόφιλων κοκκιοκυττάρων, καθιστώντας τα ικανά να δεσμεύονται σε μόρια λαμινίνης και κατά συνέπεια να μεταναστεύουν πιο εύκολα διαμέσου της βασικής μεμβράνης (Dangerfield et al., 2002). Μετά τη μετανάστευση στον έσω χιτώνα του αρτηριακού τοιχώματος, τα μονοκύτταρα βρίσκονται πλέον σε περιβάλλον πλούσιο σε oxldls, την αρχική αιτία προσέλκυσής τους στο συγκεκριμένο σημείο (εικ.3). Παράλληλα, τα μονοκύτταρα, υπό την επίδραση της κυτοκίνης-παράγοντα διαφοροποίησης M-CSF (Macrophage Colony-Stimulating Factor) που εκκρίνεται από τα γύρω κύτταρα, διαφοροποιούνται προς μακροφάγα (Glass & Witztum, 2001). Μέσω υποδοχέων γνωστών ως υποδοχείς ρακοσυλλέκτες (scavenger receptors), με κυριότερους τους CD36 και SR-AΙ/ΙΙ, τα μακροφάγα εσωτερικεύουν oxldls, η συσσώρευση των οποίων τα μετατρέπει σταδιακά σε αφρώδη κύτταρα. Οι δύο μηχανισμοί που διαθέτουν τα μακροφάγα για την απομάκρυνση της περίσσειας χοληστερόλης που έχουν εσωτερικεύσει είναι η ενζυματική μετατροπή της προς πιο ευδιάλυτες μορφές ή/και η απέκκριση της διαμέσου πρωτεϊνώνμεταφορέων της πλασματικής μεμβράνης. Όσον αφορά τον πρώτο τρόπο, το ένζυμο υδροξυλάση της χοληστερόλης-27 (cholesterol 27 hydroxylase) εκφράζεται στα μακροφάγα και πθανότατα μετατρέπει τη χοληστερόλη προς την πιο διαλυτή μορφή χοληστερόλη-27-οη (Bjorkhem, 1992). Ο δεύτερος τρόπος είναι ο πιο κοινός, μεσολαβείται από υποδοχείς όπως ο ABC-A1 (ATP-binding cassette A1 transporter) και έχει ως αποδέκτη της χοληστερόλης τις λιποπρωτεϊνες υψηλής πυκνότητας (HDLs, High Density Lipoproteins) (εικ.3). Το γεγονός αυτό ίσως εξηγεί, τουλάχιστον εν μέρει, την παρατήρηση ότι άτομα με υψηλά ποσοστά των HDLs (τη λεγόμενη καλή χοληστερίνη ) έχουν μικρότερα ποσοστά αθηροσκλήρωσης (Tall et al, 2000). Παρόλα αυτά, οι δύο αυτοί μηχανισμοί δεν αρκούν για να αποτραπεί η μετατροπή των μακροφάγων προς αφρώδη κύτταρα. 26
27 Εικόνα 3. Λιποπρωτεϊνες χαμηλής πυκνότητας (LDLs) περνούν στον υποενδοθηλιακό χώρο (έσω χιτώνας) όπου και σταδιακά οξειδώνονται πρώτα προς ελάχιστα οξειδωμένες λιποπρωτεΐνες χαμηλής πυκνότητας (mmldls) και στη συνέχεια προς πλήρως οξειδωμένες λιποπρωτεϊνες χαμηλής πυκνότητας (oxldls). Ήδη ως mmldls, οι λιποπρωτεϊνες επάγουν την παραγωγή χημοκινών από τα ενδοθηλιακά κύτταρα, καθώς και την έκφραση μορίων κυτταρικής προσκόλλησης (CAMs) στην επιφάνειά τους. Έτσι, αφενός προσελκύονται μονοκύτταρα στις συγκεκριμένες περιοχές και αφετέρου βοηθείται η προσκόλλησή τους στα ενδοθηλιακά κύτταρα. Εν συνεχεία, τα μονοκύτταρα μεταναστεύουν στον υποενδοθηλιακό χώρο όπου και διαφοροποιούνται προς μακροφάγα κύτταρα, τα οποία μέσω υποδοχέων ρακοσυλλεκτών όπως ο CD36 φαγοκυτταρώνουν τις oxldls. Λόγω της συσσώρευσης των oxldls στο κυτταρόπλασμά τους, τα μακροφάγα μετατρέπονται σε αφρώδη κύτταρα. Μόρια χοληστερόλης από τις oxldls μεταφέρονται σε λιποπρωτεϊνες υψηλής πυκνότητας (HDLs) μέσω υποδοχέων όπως ο ABC A1 (Glass & Witztum, 2001). Picture 3. Low density lipoproteins (LDLs) infiltrate the subendothelial space (intima) and are gradually oxidized towards minimally modified LDLs (mmldls) and in time, oxidized LDLs (LDLs). Already as mmldls they induce chemokine production by endothelial cells, as well as cell adhesion molecule (CAMs) expression on their surface. As a result, monocytes are drawn towards these areas and their adhesion to endothelial cells is facilitated. Following this, monocytes migrate to the subendothelial 27
28 space where they differentiate into macrophages whose scavenger receptors, such as CD36, scavenge oxldls. Due to oxldl accumulation in their cytoplasm, macrophages become foam cells. Cholesterol molecules from oxldls are loaded to high density lipoproteins (HDLs) through receptors such as ABC A1 (Glass & Witztum, 2001). Σε αυτή τη φάση στο σημείο της αρτηρίας όπου έχει ξεκινήσει φλεγμονή έχει σχηματιστεί η λεγόμενη λιπώδης γράμμωση (fatty streak). Η λιπώδης γράμμωση ονομάστηκε έτσι διότι η αλλαγή του χρώματος της αρτηρίας που παρατηρείται στο σημείο της φλεγμονής από ερυθρό προς λευκό ή υποκίτρινο, θεωρήθηκε αρχικά ότι οφειλόταν στην έντονη παρουσία λίπους. Μικροσκοπική παρατήρηση όμως έδειξε ότι παρά την ονομασία της, η λιπώδης γράμμωση αποτελείται κυρίως από μακροφάγα κύτταρα τα οποία έχουν ξεκινήσει τη μετατροπή τους προς αφρώδη κύτταρα και τα οποία εντοπίζονται ακριβώς κάτω από το ενδοθήλιο. Γενικά, η ύπαρξη λιπώδους γράμμωσης σε κάποια περιοχή μιας αρτηρίας υποδηλώνει ισχυρή πιθανότητα δημιουργίας αθηρωματικής πλάκας, χωρίς όμως αυτή να είναι πάντα η εξέλιξη (Stary et al., 1994). Μαζί με τα μακροφάγα έχουν μεταναστεύσει και Τ-λεμφοκύτταρα. Τα τελευταία αλληλεπιδρούν με τα μακροφάγα, ενεργοποιούνται και παράγουν κυτοκίνες Th1 (TNF-α, IFN-γ) και Τh2 (IL-4, IL-5, IL-6, IL-10, IL-13) (Hansson, 1997) (εικ.4). Παράλληλα, όπως αναγνωρίζεται από την έκφραση αντιγόνων ιστοσυμβατότητας τάξης II (MHC class ΙΙ) ενεργοποιούνται και τα μακροφάγα, τα ενδοθηλιακά κύτταρα και τα λεία μυικά κύτταρα παράγοντας μόρια όπως ο ΤNF-α, η IL-6 και η MCP-1. Πλέον η συγκεκριμένη περιοχή της αρτηρίας βρίσκεται σε κατάσταση μόνιμης φλεγμονής. Την ίδια στιγμή, πολλά από τα λεία μυικά κύτταρα αρχίζουν να μεταναστεύουν από τον μέσω χιτώνα προς τον υποενδοθηλιακό χώρο (εικ.4). Εκεί ενδέχεται να υποστούν διαίρεση, ενώ ταυτόχρονα μπορούν να εσωτερικεύσουν oxldls μετατρεπόμενα έτσι σε αφρώδη κύτταρα προερχόμενα από λεία μυικά κύτταρα. Επίσης, τα λεία μυικά κύτταρα παράγουν συστατικά της εξωκυττάριας ουσίας όπως κολλαγόνο, τα οποία σχηματίζουν το περίβλημα της αθηρωματικής πλάκας, το οποίο είναι γνωστό ως ινώδες κάλυμμα (fibrous cap) (Ross, 1999; Paulsson et al., 2000). Με την πάροδο του χρόνου αφρώδη κύτταρα συσσωρεύονται κάτω από το ινώδες κάλυμμα και πολλά από αυτά, λόγω της 28
29 υπερβολικής ενδοκυτταρικής συσσώρευσης λιπιδίων πεθαίνουν, δίνοντας γένεση σε έναν νεκρωτικό πυρήνα από λιπίδια και κύτταρα (εικ.4). Εικόνα 4. Αλληλεπιδράσεις μεταξύ των αφρώδων κυττάρων που προέρχονται από μακροφάγα και των Τ-λεμφοκυττάρων βοηθών μονιμοποιούν την κατάσταση φλεγμονής. Κυτοκίνες που παράγονται τόσο από τα μακροφάγα όσο και από τα Τ-λεμφοκύτταρα επιδρούν σε όλους τους κυτταρικούς τύπους της γύρω περιοχής. Λεία μυικά κύτταρα μεταναστεύουν από τον μέσο χιτώνα προς τον έσω χιτώνα, διαιρούνται και παράγουν πρωτεϊνες της εξωκυττάριας ουσίας οι οποίες στη συνέχεια σχηματίζουν ένα ινώδες κάλυμμα (Glass & Witztum, 2001). Picture 4. Interactions between macrophage-derived foam cells and T-cells result in the establishment of an inflammatory state. Cytokines produced by macrophages and T- cells exert effects on all cell types of the surrounding area. Smooth muscle cells migrate from the media to the intima, proliferate and produce extracellular matrix proteins which begin to form the fibrous cap (Glass & Witztum, 2001). Παρόλο που ονομάζεται νεκρωτικός, ο πυρήνας αυτός δεν προκύπτει από νέκρωση των κυττάρων, αλλά από τον προγραμματισμένο κυτταρικό θάνατό τους, γνωστό και 29
30 ως απόπτωση, που επάγεται από αλληλεπιδράσεις μεταξύ των κυττάρων (Bennet, 1999). Η αθηρωματική πλάκα διογκώνεται διαρκώς και λόγω εξασθένισης του υπερκείμενου ενδοθηλίου αρχίζει να προβάλλει μέσα στον αυλό της αρτηρίας μειώνοντας τη ροή του αίματος. Η στένωση της αρτηρίας που πραγματοποιείται συχνά επιχειρείται να αντισταθμιστεί με ανάλογη διόγκωση και τάνυση του μέσου χιτώνα των λείων μυικών κυττάρων και άρα της διαμέτρου της αρτηρίας (Glagov et al., 1987). Αυτό όμως μπορεί να γίνει μέχρις ενός ορίου με αποτέλεσμα αργά ή γρήγορα ο ρυθμός αύξησης της αθηρωματικής πλάκας να ξεπεράσει το ρυθμό των όποιων αντίμετρων. Η διόγκωση της αθηρωματικής πλάκας θεωρήθηκε αρχικά ότι γίνεται σταδιακά και με αργό ρυθμό, όμως σχετικά νέα δεδομένα οδηγούν στο συμπέρασμα ότι αυτή πραγματοποιείται με ξαφνικές εκρήξεις (bursts) κάθε φορά που το ινώδες κάλυμμα υφίσταται επαρκώς ισχυρό μηχανικό ερέθισμα (Libby, 2002). Εν τέλει το ινώδες κάλυμμα υφίσταται διάρρηξη και τα συστατικά του έρχονται σε επαφή με το αίμα (εικ.5). Αυτό έχει ως αποτέλεσμα, ο ιστικός παράγοντας που παράχθηκε από λευκοκύτταρα που βρίσκονταν κάτω από το ινώδες κάλυμμα μέσα και γύρω από την αθηρωματική πλάκα, να δώσει το έναυσμα για την έναρξη της διαδικασίας της θρόμβωσης έπειτα και από την προσέλκυση αιμοπεταλίων (Lee & Libby, 1997). Ο θρόμβος που σχηματίζεται μπορεί να φράξει περαιτέρω την αρτηρία εμποδίζοντας την ροή του αίματος σε εκείνο το σημείο ή να αποκολληθεί και να μεταφερθεί σε άλλο σημείο όπου θα προκαλέσει το ίδιο ή και μεγαλύτερο πρόβλημα. Παράλληλα, αξίζει να σημειωθεί ότι κατά τη διάρρηξη του ινώδους καλύμματος απελευθερώνονται και θραύσματα της αθηρωματικής πλάκας, συχνά ικανού μεγέθους ώστε μεταφερόμενα με το αίμα να προκαλέσουν φράξιμο μικρότερων αρτηριών που βρίσκονται στη διαδρομή της αρτηρίας. Οι λόγοι για τους οποίους το αρχικά παχύ και πυκνό ινώδες κάλυμμα εξασθενεί και διαρρηγνύεται αποτελούν αντικείμενο εντατικής έρευνας. Σημαντικό ρόλο θεωρείται ότι παίζουν κολλαγενάσες και μεταλλοπρωτεϊνάσες της εξωκυττάριας ουσίας (matrix metalloproteinases, MMPs), οι οποίες αποικοδομούν συστατικά του ινώδους καλύμματος (Galis et al., 1994). 30
31 Εικόνα 5. Η νέκρωση των αφρώδων κυττάρων που προέρχονται από μακροφάγα ή λεία μυικά κύτταρα οδηγεί στο σχηματισμό ενός νεκρωτικού πυρήνα και στη συσσώρευση χοληστερίνης εξωκυτταρικά. Η έκκριση μεταλλοπρωτεϊνασών από λειτουργικά ακόμα μακροφάγα αποσταθεροποιεί το ινώδς κάλυμμα που έχει σχηματιστεί. Ρήξη του ινώδους καλύμματος φέρνει σε επαφή στοιχεία του αίματος με τον ιστικό παράγοντα με αποτέλεσμα την προσέλκυση αιμοπεταλίων και τη δημιουργία θρόμβου (Glass & Witztum, 2001). Picture 5. Necrosis of macrophage- or smooth muscle cell-derived foams cells leads to the formation of a necrotic core and the accumulation of extracellular cholesterol. The expression of matrix metalloproteinases (MMPs) by still functional macrophages destabilizes the fibrous cap. Plaque rupture exposes blood components to the tissue factor resulting in platelet recruitment and the formation of a thrombus (Glass & Witztum, 2001). Τα ένζυμα αυτά παράγονται από ενεργοποιημένα από κυτοκίνες μακροφάγα, ενδοθηλιακά και λεία μυικά κύτταρα. Άλλα ένζυμα με παρόμοιο τρόπο δράσης είναι πιθανότατα και η ελαστάση των ουδετερόφιλων κοκκιοκυττάρων και η καθεψίνη S. Σπουδαίο ρόλο στην έναρξη της παραγωγής κολλαγενασών και μεταλλοπρωτεϊνασών της εξωκυττάριας ουσίας φαίνεται ότι παίζει ο υποδοχέας CD40 και o ligand του (CD40L) που εκφράζονται στην επιφάνεια μακροφάγων, Τ-λεμφοκυττάρων, 31
32 ενδοθηλιακών και λείων μυικών κυττάρων. Σύνδεση του CD40 με τον ligand του προκαλεί την παραγωγή μεταλλοπρωτεϊνασών της εξωκυττάριας ουσίας, ιστικού παράγοντα, καθώς και κυτοκινών και χημοκινών όπως TNF-α, IFN-γ, IL-1, IL-6 και MCP-1 (Mach et al., 1998). Συνεπώς, το σύστημα του υποδοχέα CD40 φαίνεται να συμμετέχει σε πλήθος αθηρωματικών διεργασιών όπως η μετανάστευση των λευκοκυττάρων, η διατήρηση της φλεγμονής, η εξασθένιση του ινώδους καλύμματος και η θρόμβωση. 2.Χημοκίνες Οι χημοκίνες ή χημειοτακτικές κυτοκίνες (chemokines, chemotactic cytokines) είναι μια οικογένεια μικρών πρωτεϊνών (8-10kDa) οι οποίες παίζουν σπουδαίο ρόλο στην μετακίνηση και καθοδήγηση των λευκοκυττάρων (κατά χημειοτακτικό τρόπο όπως υποδηλώνει και το όνομά τους). Χωρίζονται σε 4 τύπους ανάλογα με τη θέση των πρώτων δύο έως τεσσάρων συντηρημένων υπολειμμάτων κυστεΐνης στο μόριο τους (Fernandez & Lolis, 2002) (εικ.6). Εικόνα 6. Η δομή των τεσσάρων τύπων χημοκινών (C κυστεΐνη, Χ οποιοδήποτε αμινοξύ) Picture 6. The structures of the four types of chemokines (C cysteine, X any amino acid) Στον πίνακα που ακολουθεί φαίνονται ορισμένες από τις πιο σημαντικές χημοκίνες, ο τύπος στον οποίο ανήκουν με βάση τη δομή τους και οι εναλλακτικές ονομασίες τους (αυτές συνήθως αποτελούνται από τον τύπο της χημοκίνης, π.χ. CXC, το γράμμα L για τη λέξη ligand και τον χαρακτηριστικό αριθμό τους): 32
33 Τύπος Χημοκίνης Μέλη Συνώνυμα C Λεμφοτακτίνη α (Lymphotactin-α) XCL1 MCP-1 (Χημειοτακτική πρωτεϊνη των μονοκυττάρων-1, Monocyte chemotactic protein-1) CCL2 CC MIP-1α (Πρωτεϊνη φλεγμονής των μακροφάγων α, Macrophage inflammatory protein-1α) CCL3 MIP-1β (Πρωτεϊνη φλεγμονής των μακροφάγων β, Macrophage inflammatory protein-1β) CCL4 RANTES (Regulated on activation normal T-cell expressed and secreted) CCL5 CXC IL-8 (Ιντερλευκίνη-8, Interleukin-8) MIG (Mονοκίνη που επάγεται από την IFN-γ, Monokine induced by IFN-gamma) CXCL8 / Gro-α CXCL9 CX 3 C Φρακταλκίνη (Fractalkine) CX3CL1 Πίνακας 1. Ορισμένες από τις σχετικές με αθηρωμάτωση χημοκίνες Table 1. Some of the chemokines involved in atheroma progression (type of chemokine, members of this type, synonyms). Οι υποδοχείς των χημοκινών είναι συζευγμένοι με G-proteins (GPCRs, G-protein coupled receptors) και μετά τη δέσμευση των μορίων χημοκίνης με αυτούς, μεταβιβάζουν ταχύτατα τα κατάλληλα σήματα στα κύτταρα, όπως της έκφρασης ιντεγκρινών στην επιφάνειά τους (Allen et al., 2007). 3.Μόρια κυτταρικής προσκόλλησης (CAMs) Τα μόρια κυτταρικής προσκόλλησης (Cell Adhesion Molecules, CAMs) είναι πρωτεΐνες που εκφράζονται στην επιφάνεια μεγάλης ποικιλίας κυτταρικών τύπων όπως σε μονοκύτταρα, λεμφοκύτταρα, αιμοπετάλια, ενδοθηλιακά κύτταρα, επιθηλιακά κύτταρα, νευρώνες και άλλους τύπους και σχετίζονται τόσο με τη σύνδεση κυττάρων-κυττάρων, όσο και κυττάρων-εξωκυττάριας ουσίας. Κατά συνέπεια παίζουν σπουδαίο ρόλο στις διαδικασίες κυτταρικής προσκόλλησης και κυτταρικής μετανάστευσης, καθώς και στη διατήρηση της δομικής ακεραιότητας των ιστών (Krieglstein & Granger, 2001). Ως εκ τούτου, για κάθε συγκεκριμένη κυτταρική διαδικασία που επιχειρείται (π.χ. κυτταρική μετανάστευση) εκφράζονται και τα αντίστοιχα συγκεκριμένα μόρια κυτταρικής προσκόλλησης στην κυτταρική επιφάνεια. Χωρίζονται σε τέσσερις κυρίως οικογένειες πρωτεϊνών, στα μόρια κυτταρικής προσκόλλησης που ανήκουν στην υπεροικογένεια των ανοσοσφαιρινών 33
34 (Ig SuperFamily CAMs, IgSF CAMs), στις σελεκτίνες, στις ιντεγκρίνες και στις καντερίνες. 3.1.IgSF CAMs Το κοινό χαρακτηριστικό αυτών των μορίων κυτταρικής προσκόλλησης είναι η ύπαρξη της χαρακτηριστικής περιοχής Ιg (Ig domain) των ανοσοσφαιρινών (αντισωμάτων) στη δομή τους. Οι πιο σημαντικές όσον αφορά τα φαινόμενα αθηρωμάτωσης είναι οι VCAM-1 (Vascular Cell Adhesion Molecule-1 ή CD106), ICAM-1 (Intercellular Cell Adhesion Molecule-1 ή CD54), PECAM-1 (Platelet Endothelial Cell Adhesion Molecule-1 ή CD31) και MADCAM1 (Mucosal Addressin Cell Adhesion Molecule-1) (Krieglstein & Granger, 2001). To VCAM-1 εκφράζεται στην επιφάνεια ενδοθηλιακών κυττάρων τα οποία έχουν ενεργοποιηθεί έπειτα από την επίδραση κυτοκινών όπως ο TNF-α (Tumour Necrosis Factor alpha, παράγοντας νέκρωσης όγκου άλφα) και η ιντερλευκίνη-1 (IL-1). Συνδέεται κυρίως με την α 4 β 1 - ιντεγκρίνη (γνωστή και ως VLA-4, Very Late Antigen-4) που εκφράζεται στην επιφάνεια των μονοκυττάρων συμβάλλοντας έτσι στην προσκόλληση των τελευταίων στο ενδοθήλιο (Berlin et al., 1995). To ICAM-1 εκφράζεται στην επιφάνεια των ενδοθηλιακών κυττάρων, αλλά και των μονοκυττάρων και των Τ-λεμφοκυττάρων (Bevilacqua et al., 1987). H έκφρασή του επάγεται επίσης από κυτοκίνες όπως ο TNF-α και η IL-1. Συνδέεται με την α L β 2 -ιντεγκρίνη (γνωστή και ως LFA-1, Lymphocyte Function-associated Antigen-1). Το PECAM-1 εκφράζεται σε πλήθος κυτταρικών τύπων όπως στα ενδοθηλιακά κύτταρα, στα αιμοπετάλια, στα μονοκύτταρα, στα Τ-λεμφοκύτταρα και στα ουδετερόφιλα κοκκιοκύτταρα (Albelda et al., 1991). Όσον αφορά τα αθηρωματικά γεγονότα, το PECAM-1 συμμετέχει μέσω ομομερών συνδέσεων PECAM-1 PECAM-1 στη μετανάστευση των μονοκυττάρων προς τον έσω χιτώνα, καθώς και στην προσκόλληση των μονοκυττάρων κατά τον σχηματισμό θρόμβου. To MADCAM1 σχετίζεται κυρίως με την προσκόλληση των λεμφοκυττάρων στο ενδοθήλιο. 3.2.Σελεκτίνες (Selectins) Τα τρία μέλη της οικογένειας των σελεκτινών είναι η E-σελεκτίνη που εκφράζεται στα ενδοθηλιακά κύτταρα, η L-σελεκτίνη που εκφράζεται στα λευκοκύτταρα (συμπεριλαμβανομένων των μονοκυττάρων) και η P-σελεκτίνη που 34
35 εκφράζεται στα αιμοπετάλια και στα ενδοθηλιακά κύτταρα (Kansas, 1996). Η έκφρασή τους στην επιφάνεια των κυττάρων επάγεται από κυτοκίνες όπως ο TNF-α και η IL-1. Το κύριο μόριο στο οποίο συνδέονται οι σελεκτίνες είναι η πρωτεϊνη PSGL-1 (P-Selectin Glycoprotein Ligand 1) η οποία εκφράζεται στην επιφάνεια σχεδόν όλων των λευκοκυττάρων, καθώς και στα ενδοθηλιακά κύτταρα (McEver & Cummings, 1997). Οι συνδέσεις σελεκτίνης PSGL-1 παίζουν σπουδαίο ρόλο κατά την προσκόλληση των μονοκυττάρων στο ενδοθήλιο. 3.3.Ιντεγκρίνες (Integrins) Οι ιντεγκρίνες είναι πρωτεΐνες της πλασματικής μεμβράνης οι οποίες συμμετέχουν σε διαδικασίες προσκόλλησης τόσο μεταξύ κυττάρων όσο και μεταξύ κυττάρων και εξωκυττάριας ουσίας. Συμμετέχουν σε διαδικασίες μεταγωγής σήματος, μεταβιβάζοντας τόσο πληροφορίες από τον εξωκυτταρικό χώρο προς το ίδιο το κύτταρο, όσο και πληροφορίες σχετικά με την κατάσταση του κυττάρου προς άλλα κύτταρα. Οι ιντεγκρίνες είναι ετεροδιμερή αποτελούμενα από μία α-υπομονάδα και μία β-υπομονάδα (Mousa, 2008). Στα θηλαστικά έχουν χαρακτηριστεί 19 α- υπομονάδες και 8 β-υπομονάδες. Οι α 4 β 1 -ιντεγκρίνη (γνωστή και ως VLA-4 ή CD49d-CD29) και α L β 2 -ιντεγκρίνη (γνωστή και ως LFA-1 ή CD11a-CD18) που βρίσκονται στην επιφάνεια των μονοκυττάρων αλληλεπιδρούν με τα μόρια κυτταρικής προσκόλλησης VCAM-1 και ICAM-1 αντίστοιχα των ενδοθηλιακών κυττάρων, επιτρέποντας έτσι την προσκόλληση των μονοκυττάρων στο ενδοθήλιο (Sigal et al., 2000; Chan et al., 2001). Την ίδια λειτουργία επιτελούν και οι α 4 β 7 - ιντεκρίνη και α Μ β 2 -ιντεγκρίνη (γνωστή και ως MAC-1 ή CD11b-CD18) που συμμετέχουν στις διαδικασίες προσκόλλησης των Τ-λεμφοκυττάρων και των μονοκυττάρων στο επιθήλιο και της μετανάστευσης διαμέσου αυτού (Dunne et al., 2002). Όσον αφορά τις αθηρωματικές διαδικασίες, ιδιαίτερη σημασία έχουν και οι ιντεγκρίνες α 1 β 1 -ιντεγκρίνη, α 2 β 1 -ιντεγκρίνη (CD49b-CD29) και α 6 β 1 -ιντεγκρίνη που συνδέονται στα συστατικά της εξωκυττάριας ουσίας λαμινίνη και κολλαγόνο. 3.4.Καντερίνες (Cadherins) Οι καντερίνες (ή καδερίνες) είναι Ca 2+ -εξαρτώμενες διαμεμβρανικές πρωτεΐνες της κυτταρικής επιφάνειας που συνδέουν κύτταρα μεταξύ τους συμβάλλοντας στην συνοχή των ιστών. Μερικές χαρακτηριστικές καντερίνες είναι οι Ε-καντερίνες που 35
36 εντοπίζονται στον επιθηλιακό ιστό, οι Ν-καντερίνες που εντοπίζονται στον νευρικό ιστό και η Τ-καντερίνη που εντοπίζεται στην καρδιά (Angst et al., 2001). 4.Υποδοχείς ρακοσυλλέκτες Οι υποδοχείς ρακοσυλλέκτες είναι πρωτεΐνες της πλασματικής μεμβράνης που εκφράζονται κυρίως από κύτταρα του ανοσοποιητικού συστήματος (αλλά όχι μόνο) και χρησιμεύουν στην απομάκρυνση από το μικροπεριβάλλον των κυττάρων ουσιών ή σωμάτων που είναι ξένα ή δυνητικά τοξικά (Goldstein et al., 1979). Τέτοιες ουσίεςσώματα είναι για παράδειγμα οι oxldls, βακτήρια ή γηρασμένα κύτταρα. Συνήθως μετά τη δέσμευση της ουσίας-σώματος στον υποδοχέα, ακολουθεί η εσωτερίκευσή του με φαγοκυττάρωση και η διάσπαση του είτε από πλήθος ενζύμων, είτε με οξειδωτικό τρόπο μέσω βομβαρδισμού με ελεύθερες ρίζες. Στις περιπτώσεις που η ουσία-σώμα δεν μπορεί να διασπαστεί παρά πέρα, όπως συμβαίνει στην περίπτωση των oxldls, αναγκαστικά ακολουθεί η συσσώρευσή του ενδοκυτταρικά. Ανάλογα με τη δομή τους (τα χαρακτηριστικά domains τους) οι υποδοχείς ρακοσυλλέκτες χωρίζονται στους τύπους Α (π.χ. SR-AI, SR-AII, SR-AIII, MARCO), B (π.χ. CD36), C, D (π.χ. CD68), E (π.χ. LOX-1), F, G, H και I (van Berkel et al., 2005). 4.1.CD36 Ο υποδοχέας ρακοσυλλέκτης CD36 (88kDa, τύπου Β) είναι μια ισχυρά γλυκοσυλιωμένη πρωτεΐνη της πλασματικής μεμβράνης. Εκφράζεται κυρίως από μονοκύτταρα/μακροφάγα, ενδοθηλιακά κύτταρα, λιπώδη κύτταρα και αιμοπετάλια (Silverstein & Febbraio, 2000). Διαθέτει ειδικότητα δέσμευσης για πλήθος υποστρωμάτων όπως τροποποιημένες ακετυλιωμένες (acldls) ή οξειδωμένες (oxldls) LDLs και μόρια κολλαγόνου τύπου Ι και IV. Ειδικά όσον αφορά τις oxldls, οι υποδοχείς CD36 αποτελούν μία από τις σημαντικότερες οδούς ενδοκυτταρικής εισόδου τους (Endemann et al., 1993). 4.2.Άλλοι υποδοχείς ρακοσυλλέκτες Ο SR-AI/II (δύο υποτύποι Ι και ΙΙ, παράγονται με διαφορικό splicing) είναι ένας υποδοχέας ρακοσυλλέκτης τύπου Α που μεταξύ των άλλων, επίσης δεσμεύει acldls και oxldls, διαθέτει όμως μεγαλύτερη ειδικότητα για τις πρώτες. Εκφράζεται 36
37 κυρίως στα μονοκύτταρα/μακροφάγα και στα ενδοθηλιακά κύτταρα (Kunjathoor et al., 2002). Άλλοι υποδοχείς ρακοσυλλέκτες που εκφράζονται σε μονοκύτταρα/μακροφάγα και έχουν την ικανότητα να δεσμεύουν τροποποιημένες LDLs (mmldls, acldls, oxldls) είναι ο MARCO (MAcrophage Receptor with COllagenous structure, τύπου Α), ο LOX-1 (Lectin-like oxidized LDL receptor, τύπου Ε) και ο CD68 (γνωστός και ως macrosialin, τύπου D) (Dhaliwal & Steinbrecher, 1999). Από αυτούς τους τρεις, όσον αφορά την εσωτερίκευση των oxldls, πιο σημαντικός φαίνεται να είναι ο CD68, που μάλιστα αποτελεί και καλό δείκτη των μακροφάγων, καθότι εκφράζεται ειδικά σε αυτά τα κύτταρα (με πολύ μικρή έκφραση στα μονοκύτταρα και μηδενική σε άλλους τύπους κυττάρων). 5.Μονοκύτταρα Τα μονοκύτταρα είναι κύτταρα του ανοσοποιητικού συστήματος τα οποία παράγονται στο μυελό των οστών από κύτταρα τα οποία αποτελούν ταυτόχρονα προγονικά κύτταρα και των ουδετερόφιλων κοκκιοκυττάρων (εικ.7). Είναι γνωστό εδώ και πολλά χρόνια ότι μετά την είσοδό τους στην περιφερική κυκλοφορία, τα μονοκύτταρα παραμένουν εκεί για μερικές μέρες μέχρις ότου δεχτούν κατάλληλα ερεθίσματα (π.χ. χημοκίνες, κυτοκίνες, παράγοντες διαφοροποίησης από κύτταρα περιοχών στις οποίες έχει ξεκινήσει φλεγμονή) προκειμένου να εισέλθουν σε συγκεκριμένες ιστούς όπου και διαφοροποιούνται (Volkman & Gowans, 1965). Ανάλογα με τον ιστό, τα παράγωγα κύτταρα της διαφοροποίησής τους μπορεί να είναι μακροφάγα κύτταρα, δενδριτικά κύτταρα, κύτταρα Langerhans (ειδικός τύπος δενδριτικών κυττάρων της επιδερμίδας), οστεοκλάστες (μεγάλα, πολυπύρηνα κύτταρα που πραγματοποιούν την απορρόφηση των οστών χάρις στα ισχυρά ένζυμα που παράγουν) και άλλοι τύποι κυττάρων (Agel et al., 1987). Τα μονοκύτταρα, τα μακροφάγα και τα δενδριτικά κύτταρα έχουν την ικανότητα να φαγοκυτταρώνουν και να διασπούν με ποικιλία ενζύμων που παράγουν, τόσο ξένα προς τον οργανισμό στοιχεία όπως βακτήρια και βακτηριακά προϊόντα, όσο και στοιχεία του ίδιου του οργανισμού που πρέπει να απομακρυνθούν όπως αποπτωτικά κύτταρα. 37
38 Εικόνα 7. Προέλευση μονοκυττάρων και των παραγώγων τους στον ποντικό (παρόμοια και στον άνθρωπο). Από τα πρώτα στάδια της ανάπτυξης, κύτταρα με φαινότυπο μακροφάγου που εκφράζουν χαρακτηριστικούς επιφανειακούς υποδοχείς εντοπίζονται στον λεκυθικό ασκό. Στο εμβρυικό στάδιο, η αιμοποίηση που πραγματοποιείται στο ήπαρ αποτελεί την κύρια πηγή μονοκυττάρων/μακροφάγων. Στα ενήλικα άτομα, τα μονοκύτταρα παράγονται στον μυελό των οστών. Τα νεαρά μονοκύτταρα που εισέρχονται στην κυκλοφορία φέρουν τον υποδοχέα Ly6C (Ly6C + ) ο οποίος με την πάροδο του χρόνου μετατρέπεται προς μια ενδιάμεση μορφή Ly6C int. Μέσω ενός μηχανισμού που δεν είναι ακόμα γνωστός, και απουσία φλεγμονής, τόσο τα Ly6C + όσο και τα Ly6C int, χάνουν τον υποδοχέα Ly6C (Ly6C - ) και εισέρχονται στους ιστούς προκειμένου να αναπληρώσουν τους εκεί πληθυσμούς εγκατεστημένων μακροφάγων και δενδριτικών κυττάρων. Άσχετα με την κατάσταση του Ly6C όλοι οι παραπάνω τύποι μονοκυττάρων μπορούν να μετατραπούν προς τα παράγωγα κύτταρα των μονοκυττάρων. HSC (Haemotopoietic stem cell, Αιματοποιητικό βλαστοκύτταρο), GM-CFU (Granulocyte/Macrophage Colony-Forming Unit, Μονάδα σχηματισμού αποικίας κοκκιοκυττάρων/μονοκυττάρων), M-CFU (Macrophage Colony-Forming Unit, Μονάδα σχηματισμού αποικίας μακροφάγων), G-CFU (Granulocyte Colony- Forming Unit, Μονάδα σχηματισμό κοκκιοκυττάρων) (Gordon & Taylor, 2005). 38
39 Picture 7. Origins of monocytes and cells derived from them in the mouse (practically the same as in humans). From the first stages of development, in the yolk sac, cells with a monocyte-like phenotype expressing particular surface markers can be identified. In the fetal stage, haematopoiesis taking part in the liver is the main source of monocytes/macrophages. In adults, monocytes are produced in the bone marrow. Young monocytes released into the circulation express the surface marker Ly6C (Ly6C + ) which in time progresses to become the intermediate form Ly6C int. Through a mechanism which is not fully understood and in the absence of inflammation both Ly6C + and Ly6C int stop expressing Ly6C (Ly6C - ) and begin entering tissues in order to replenish the established populations of macrophages and dendritic cells. Irrespective of their Ly6C state, all the previously mentioned monocyte types can differentiate into any type of monocyte-derived cell. HSC (Haemotopoietic Stem Cell), GM-CFU (Granulocyte/Macrophage Colony-Forming Unit), M-CFU (Macrophage Colony-Forming Unit), G-CFU (Granulocyte Colony-Forming Unit) (Gordon & Taylor, 2005). Έτσι για παράδειγμα μετά τη φαγοκύττωση και διάσπαση ενός παθογόνου βακτηρίου, συστατικά του (ξένα αντιγόνα) μεταφέρονται στην επιφάνεια των παραπάνω κυττάρων και σε συνδυασμό με κατάλληλα αντιγόνα ιστοσυμβατότητας (MHC, αντιγόνα εαυτού) παρουσιάζονται σε Τ-λεμφοκύτταρα εκπαιδεύοντάς τα να αντιδράσουν απέναντι στη συγκεκριμένη απειλή την επόμενη φορά που θα τη συναντήσουν (Zeigler-Heitbrock, 2007). Τα μονοκύτταρα ανήκουν στην κατηγορία των λευκοκυττάρων και αποτελούν το 5-10% αυτού του πληθυσμού στο αίμα ( x 10 6 / L αίματος). Αν και μέσα στον συνολικό πληθυσμό μπορεί να υπάρχουν εξαιρέσεις, τα μονοκύτταρα συνήθως είναι τα μεγαλύτερα λευκοκύτταρα διαθέτοντας διάμετρο μm (έως 21 μm ως μακροφάγα) και μηδαμινή κοκκίωση (Daniels et al., 1979). Μικροσκοπικά αναγνωρίζονται έπειτα από κατάλληλη χρώση χάριν στον χαρακτηριστικό τους δίλοβο πυρήνα. Ο πιο χαρακτηριστικός υποδοχέας της επιφάνειας (επιφανειακός δείκτης, surface marker) των μονοκυττάρων είναι ο CD14, ο οποίος όπως προαναφέρθηκε χρησιμεύει κυρίως για την ανίχνευση των λιποπολυσακχαριτών (LPS), δομικών συστατικών των εξωτερικών κυτταρικών μεμβρανών αρνητικών κατά Gram βακτηρίων. Έχει διαπιστωθεί ότι οι πιο πολυπληθείς υποπληθυσμοί των μονοκυττάρων είναι οι CD14 ++ CD16 - και CD14 + CD16 +. Υπάρχουν ενδείξεις ότι ο τύπος CD14 ++ CD16 - αντιπροσωπεύει νεαρά μονοκύτταρα που μόλις εισήλθαν στην 39
40 κυκλοφορία του αίματος, ενώ ο τύπος CD14 + CD16 + αντιπροσωπεύει πιο ώριμα μονοκύτταρα (Ziegler-Heitbrock, 2007). Ένας άλλος σημαντικός επιφανειακός υποδοχέας που έχει ήδη αναφερθεί και ως υποδοχέας τροποποιημένων LDLs είναι ο CD68, χαρακτηριστικός των μακροφάγων με ελάχιστη έκφραση στα μονοκύτταρα. Ακόμα αξίζει να αναφερθεί ο υποδοχέας Ly6C των μονοκυττάρων του ποντικού ο οποίος εκφράζεται στα νεαρά μονοκύτταρα, αλλά κατά την ωρίμανση έως και την τελική διαφοροποίησή τους εξαφανίζεται από την επιφάνεια των κυττάρων (Gordon & Taylor, 2005). 6.Ορμόνες που σχετίζονται με παχυσαρκία Σπουδαίο ρόλο στη ρύθμιση της λήψης και κατανάλωσης ενέργειας από τον οργανισμό παίζει μια ομάδα ορμονών που είναι γνωστές ως αδιποκίνες (adipokines). Οι ορμόνες αυτές είναι κυτοκίνες που παράγονται ως επί το πλείστον από το λιπώδη ιστό και εκκρίνονται κατόπιν στην κυκλοφορία του αίματος. Με την αυστηρή έννοια του όρου, αδιποκίνες χαρακτηρίζονται εκείνες οι κυτοκίνες που επηρεάζουν και το ανοσοποιητικό σύστημα. Κάτι τέτοιο είναι γνωστό για τη λεπτίνη και την αδιπονεκτίνη, οι οποίες έχουν μελετηθεί περισσότερο, αλλά όχι για άλλες ορμόνες που προέρχονται από το λιπώδη ιστό όπως η ρεζιστίνη (Tilg & Moschen, 2006). Πέρα από τις αδιποκίνες παρόμοιο ρόλο παίζουν και άλλες ορμόνες που δεν παράγονται από το λιπώδη ιστό, όπως η γκρελίνη που παράγεται από το επιθήλιο του στομάχου (Meier & Gressner, 2004). 6.1 Λεπτίνη Η λεπτίνη (16kDa) είναι μια ορμόνη που παράγεται κυρίως από το λιπώδη ιστό και συμμετέχει σε ποικίλες κυτταρικές και σωματικές διεργασίες με κυριότερη ίσως τη ρύθμιση του ισοζυγίου ενέργειας του οργανισμού (Sweeney, 2002). Η σύνθεση της καθορίζεται και ρυθμίζεται από το γονίδιο ob (το όνομά του προέρχεται από την αγγλική λέξη obese, που σημαίνει παχύσαρκος, και αυτό διότι παρατηρήθηκε ότι ποντίκια με μετάλλαξη στο συγκεκριμένο γονίδιο εμφάνιζαν ισχυρή ροπή προς την παχυσαρκία). Η ανακάλυψη του γονιδίου ob στο ποντίκι το 1994 και στη συνέχεια ο χαρακτηρισμός του ομόλογου γονιδίου του στον άνθρωπο, οδήγησε στο βιαστικό συμπέρασμα ότι η λεπτίνη θα μπορούσε από μόνη της να αποτελέσει το μαγικό φάρμακο κατά της παχυσαρκίας (Zhang et al. 1994; Auwerx and Staels 1998). Όπως 40
41 όμως έγινε γρήγορα αντιληπτό, η παχυσαρκία είναι ένα πολυπαραγοντικό νόσημα και απλή χορήγηση λεπτίνης δεν ήταν δυνατό να αντιστρέψει την κατάσταση της συντριπτικής πλειοψηφίας των ασθενών. Έτσι με την πάροδο του χρόνου διαπιστώθηκε ότι η παχυσαρκία στις περισσότερες περιπτώσεις δεν οφείλεται σε ποσοτική έλλειψη λεπτίνης τουναντίον μάλιστα, οι περισσότεροι παχύσαρκοι είναι παράλληλα και υπερλεπτιναιμικοί (Banks, 2004). Αμέσως μετά την ανακάλυψή της, η λεπτίνη και οι δράσεις της στον οργανισμό έγιναν ένα ιδιαίτερα δημοφιλές ερευνητικό αντικείμενο. Έτσι, διαπιστώθηκε ότι πέρα από τη ρύθμιση του ισοζυγίου της ενέργειας του οργανισμού, η λεπτίνη συμμετέχει στη ρύθμιση τόσο διαφορετικών μεταξύ τους μηχανισμών όπως είναι η αγγειογένεση, οι δράσεις του ανοσοποιητικού συστήματος και οι ρυθμοί του αναπαραγωγικού συστήματος (Ahima & Osei, 2004). Τουλάχιστον έξι ισομορφές του υποδοχέα της λεπτίνης (ObRa, ObRb, ObRc, ObRd, ObRe, ObRf) έχουν χαρακτηριστεί έως τώρα με τους ObRa, ObRb και ObRc να συμμετέχουν στον μηχανισμό ενεργειακής ρύθμισης που επιτελεί η λεπτίνη. Συγκεκριμένα, διαχρονικά ερεθίσματα όπως η υπερβολική συσσώρευση λίπους στον οργανισμό (παχυσαρκία) σε βάθος χρόνου, αλλά και στιγμιαία ερεθίσματα όπως η υπερβολική κατανάλωση τροφής ή/και αυξημένα επίπεδα ινσουλίνης και γλυκοκορτικοειδών (π.χ. κορτιζόλη) στο αίμα, ενεργοποιούν τη σύνθεση και έκκριση της λεπτίνης από το λιπώδη ιστό (Koutkia et al., 2003). Σε γενικές γραμμές, παρατηρείται συσχέτιση μεταξύ της συγκέντρωσης της λεπτίνης στο αίμα του ατόμου τόσο με τον δείκτη μάζας σώματός 3 (BMI, Body Mass Index) του όσο και με το ολικό του σωματικό λίπος (Frühbeck, 2001). Αντίστοιχα, η νηστεία, αυξημένη ενδοκυτταρική συγκέντρωση κυκλικού ΑΜΡ (camp) και αγωνιστές των β 3 - αδρενεργικών υποδοχέων (οι υποδοχείς αυτοί εντοπίζονται κυρίως στο λιπώδη ιστό και ενεργοποίησή τους ενισχύει τα επίπεδα λιπόλυσης) αναστέλλουν τη σύνθεση και έκκριση της λεπτίνης (Slieker et al., 1996; Leibel, 2002). 41
42 Οι μέσες συγκεντρώσεις λεπτίνης στον ορό του αίματος φαίνονται στον παρακάτω πίνακα: Μέση συγκέντρωση λεπτίνης στον ορό (ng/ml) Εύρος συγκέντρωσης λεπτίνης στον ορό (ng/ml) Άτομα κανονικού BMI ανεξαρτήτως φύλου 7,5 ± 9,3 0 16,8 Παχύσαρκα άτομα ανεξαρτήτως φύλου 31,3 ± 24,1 7,2 55,4 Πίνακας 1. Μέσες συγκεντρώσεις λεπτίνης και εύρος αυτών στον ορό του αίματος ατόμων με κανονικό BMI ή υψηλό BMI (παχύσαρκα άτομα) ανεξαρτήτως φύλου (Considine et al., 1996). Table 1. Mean concentrations of leptin and their range in the plasma of individuals with normal BMI and high BMI (obese individuals) irrespective of their sex (Considine et al., 1996). Αξίζει να σημειωθεί ότι οι γυναίκες εμφανίζουν μεγαλύτερη συγκέντρωση λεπτίνης στο αίμα σε σχέση με άνδρες παρόμοιας λιπιδικής μάζας, ενώ σε περιπτώσεις υπερλεπτιναιμίας η συγκέντρωση της λεπτίνης στο αίμα δύναται να ξεπεράσει ακόμα και τα 200 ng/ml (Dagogo-Jack et al. 1998; La Cava & Matarese, 2004). Μετά την έκκρισή της στην κυκλοφορία του αίματος, η λεπτίνη φτάνει στο χοριοειδές πλέγμα του εγκεφάλου (choroid plexus) όπου δεσμεύεται από τους υποδοχείς της ObRa και ObRc, διαπερνά έτσι τον αιματοεγκεφαλικό φραγμό και μεταφέρεται στο εγκεφαλονωτιαίο υγρό. Από εκεί φτάνει στον υποθάλαμο όπου δεσμεύεται στον υποδοχέα της ObRb μεταβιβάζοντας το μήνυμα για μείωση της όρεξης για λήψη τροφής και για αύξηση της κατανάλωσης ενέργειας από τον οργανισμό (Meier & Gressner, 2004). Παράλληλα, η λεπτίνη επάγει τη σύνθεση και έκκριση τόσο της ωχρινοτρόπου ορμόνης (LH, Luteinizing Hormone), όσο και της ωοθηλακιοτρόπου ορμόνης (FSH, Follicle-Stimulating Hormone) από την υπόφυση (Carro et al., 1997; Yu et al., 1997). Συνεπώς φαίνεται να υπάρχει ένας άξονας επικοινωνίας μεταξύ λιπώδους ιστού, υποθαλάμου-υπόφυσης και αναπαραγωγικού συστήματος, με τον πρώτο να εκκρίνει λεπτίνη όταν επαρκούν τα ενεργειακά αποθέματα, δίνοντας έτσι το σήμα από τη μία πλευρά για αναστολή της λήψης 42
43 τροφής και από την άλλη παρέχοντας το πράσινο φως για τη διαδικασία της αναπαραγωγής (Meier & Gressner, 2004). Από τις ισομορφές του υποδοχέα λεπτίνης μόνο ο ObRb έχει βρεθεί να διαθέτει τις απαραίτητες κυτταροπλασματικές περιοχές (domains) ώστε να συμμετάσχει σε μεταγωγή σήματος (Sweeney, 2002). Ο ΟbRb ανήκει στην κατηγορία των τύπου Ι υποδοχέων κυτοκινών, εκφράζεται σε πολύ μεγάλη ποικιλία κυτταρικών τύπων και σύνδεση της λεπτίνης με αυτόν εκκινεί το μονοπάτι JAK/STAT 4 μέσω του οποίου το σήμα μετακινείται κατά μήκος συγκεκριμένων μονοπατιών μεταγωγής σήματος καταλήγοντας στην ενεργοποίηση συγκεκριμένων γονιδίων όπως του c-myc που ανάλογα με τις συνθήκες συμβάλλει στην κυτταρική διαίρεση ή στον προγραμματισμένο κυτταρικό θάνατο (απόπτωση) (εικ.10). Όσον αφορά τους κυτταρικούς τύπους που σχετίζονται με φαινόμενα αθηρωμάτωσης, έχει διαπιστωθεί ότι ο ObRb εκφράζεται ισχυρά στην επιφάνεια ορισμένων κυτταρικών συστατικών των αθηρωματικών πλακών όπως στα ενδοθηλιακά κύτταρα και στα μονοκύτταρα και σε μικρότερο βαθμό στα λεία μυικά κύτταρα (Peelman et al., 2004; Schroeter et al., 2007). 6.2 Άλλες ορμόνες που σχετίζονται με παχυσαρκία Η αδιπονεκτίνη παράγεται, όπως προαναφέρθηκε, από το λιπώδη ιστό. Έχει αντιφλεγμονώδη χαρακτήρα, επάγει την απόπτωση των μονοκυττάρων, ενώ εμποδίζει και τη φαγοκύττωση που επιτελείται από τα μακροφάγα. Τα επίπεδά της στο αίμα είναι αρκετά υψηλά (κανονική συγκέντρωση 5-10mg/ml) και μείωσή τους αποτελεί ένδειξη αντίστασης στην ινσουλίνη, διαβήτη τύπου ΙΙ και αθηρωμάτωσης (Arita et al., 1999; Kawano et al., 2005). Η ρεζιστίνη επίσης παράγεται από το λιπώδη ιστό και εμφανίζει φλεγμονώδη δράση, καθώς αυξάνει την παραγωγή TNFα και ιντερλευκίνη-6 από λευκοκύτταρα. Παράλληλα, αυξάνει την έκφραση των μορίων κυτταρικής προσκόλλησης VCAM-1 και ICAM-1 από τα ενδοθηλιακά κύτταρα (Meier & Gressner, 2004; Tilg & Moschen, 2006). Η γκρελίνη έχει το χαρακτηριστικό ότι παράγεται από το επιθήλιο του στομάχου. Φαίνεται να έχει φλεγμονώδη δράση, ενώ ταυτόχρονα έχει αντίθετη δράση από τη λεπτίνη καθώς αυξάνει την όρεξη για λήψη τροφής (Meier & Gressner, 2004) 43
44 7.Ιοντοανταλλάκτης Νa + /H + (ΝΗΕ1) Οι ιοντοανταλλάκτες Νa + /H + (Na + /H + exchangers, NHEs) είναι διαμεμβρανικές πρωτεΐνες της πλασματικής μεμβράνης που πραγματοποιούν ηλεκτροουδέτερη ανταλλαγή εξωκυτταρικών ιόντων Na + με ενδοκυτταρικά Η + σε αναλογία 1:1 (Putney et al., 2002). Στα θηλαστικά έχουν χαρακτηριστεί 10 ισομορφές των ιοντοανταλλακτών Νa + /H + (ΝΗΕ1-ΝΗΕ10), οι οποίες διαφέρουν μεταξύ τους ως προς τις αμινοξικές τους ακολουθίες και την ενδοκυτταρική τους θέση. Ανάλογα με τις ισομορφές που θα συγκριθούν παρατηρείται ομοιότητα στην αμινοξική ακολουθία τους που κυμαίνεται μεταξύ 25-70%. Η δομή όλων των ισομορφών περιλαμβάνει 12 διαμεμβρανικά τμήματα προς το Ν-τελικό άκρο στα οποία επιτελείται η ιοντοανταλλακτική λειτουργία, καθώς και ένα κυτταροπλασματικό ρυθμιστικό C- τελικό άκρο (Orlowski & Grinstein, 2004) (εικ.8). Η ισομορφή-1 του ιοντοανταλλάκτη Νa + /H + (ΝΗΕ1) είναι η μόνη η οποία απαντάται σε κάθε τύπο κυττάρου στον οποίο έχει αναζητηθεί. Οι ΝΗΕ2 και ΝΗΕ4 εκφράζονται κυρίως στους νεφρούς και στο γαστρεντερικό σωλήνα (Bookstein et al., 1997). Ο NHE2 εντοπίζεται στο κορυφαίο τμήμα των κυττάρων και συμμετέχει στην επαναρρόφηση Na +, ενώ ο ΝΗΕ4 εντοπίζεται στο βασεοπλευρικό τμήμα συμμετέχοντας στην κυτταρική οσμωρύθμιση (Tse et al., 1993; Pizzonia et al., 1998). Ο NHE3 εντοπίζεται κυρίως στους νεφρούς και στο εντερικό επιθήλιο (Biemesderfer et al., 1993; Hoogerwerf et al., 1996). Ο NHE5 εντοπίζεται στον νευρικό ιστό όπου συμμετέχει στη ρύθμιση του ενδοκυτταρικού ph των νευρώνων. Οι ΝΗΕ6-ΝΗΕ9 έχουν βρεθεί σχεδόν σε όλους τους κυτταρικούς τύπους και χαρακτηρίζονται από το γεγονός ότι σε αντίθεση με τους ΝΗΕ1-ΝΗΕ5 εντοπίζονται σε ενδοκυτταρικά διαμερίσματα και όχι στην πλασματική μεμβράνη (Nakamura et al., 2005). O ΝΗΕ6 θεωρήθηκε αρχικά ότι εντοπίζεται στα μιτοχόνδρια όπου συμμετέχει στη ρύθμιση του ενδομιτοχονδριακού ph, παρόλα αυτά νεότερα δεδομένα αμφισβητούν τη μιτοχονδριακή υπόθεση και υποστηρίζουν ότι ο ΝΗΕ6 εκφράζεται αποκλειστικά στα αρχικά ενδοσώματα ή ενδοσώματα ανακύκλωσης (early endosomes ή recycling endosomes) (Raley-Susman et al., 1991; Numata et al., 1998; Brett et al., 2002). O NHE7 εντοπίζεται κυρίως στο trans-golgi δίκτυο και έχει την ιδιαιτερότητα ότι δεν πραγματοποιεί μόνο ανταλλαγή Na + /H +, αλλά και K + /H + πάντα σε αναλογία 1:1 (Numata and Orlowski, 2001). O NHE8 εντοπίζεται κυρίως στο μέσο- και στο trans- Golgi δίκτυο, ενώ ο ΝΗΕ9 εντοπίζεται στα τελικά ενδοσώματα (Nakamura et al., 44
45 2005). Πολύ πρόσφατα χαρακτηρίστηκε και ο ΝΗΕ10, ο οποίος βρέθηκε ότι συμμετέχει στη διαφοροποίηση και επιβίωση των οστεοκλαστών (Lee, 2008). O NHE1 αποτελείται από 815 αμινοξέα με μοριακό βάρος kDa ανάλογα με τα επίπεδα γλυκοσυλίωσής του και διαδραματίζει πρωτεύοντα ρόλο στη ρύθμιση σημαντικών διεργασιών όπως του ενδοκυτταρικού ph (phi) (Moolenaar et al., 1983; Bianchini & Pouyssegur, 1994), του κυτταρικού όγκου (Cala, 1983a; Cala 1983b), της οργάνωσης του κυτταροσκελετού (Simchowitz & Cragoe, 1986; Lagana et al., 2000) και της κυτταρικής διαίρεσης (Putney et al., 2002). Τα διαμεμβρανικά τμήματα IV, VII, IX, XI φαίνεται ότι είναι τα πιο σημαντικά όσον αφορά την επιτέλεση της ιοντοανταλλακτικής λειτουργίας (Slepkov et al., 2007). Η κύρια αιτία ενεργοποίησης του ΝΗΕ1 είναι η πτώση του ενδοκυτταρικού ph πέρα από κάποιο όριο ασφαλείας (κυτταροπλασματική οξέωση) (Karmazyn et al., 2001). Η δράση του ΝΗΕ1 ρυθμίζεται έμμεσα (με μη απευθείας σύνδεση στoν ΝΗΕ1) από μεγάλη ποικιλία παραγόντων όπως τη γλυκόζη, ορμόνες (με την αδρεναλίνη, την ινσουλίνη και τη λεπτίνη να είναι μόνο μερικές) (Ceolotto et al., 1997), βαρέα μέταλλα (κάδμιο) και δευτερογενείς μηνύτορες (Tse et al., 1993), που ενεργοποιούν κατάλληλα μονοπάτια μεταγωγής σήματος. 45
46 Εικόνα 8. Δομή του ΝΗΕ1. Πάνω φαίνεται μεγεθυμένο το Ν-τελικό διαμεμβρανικό τμήμα που επιτελεί τη λειτουργία της ιοντοανταλλαγής, ενώ κάτω φαίνεται το ρυθμιστικό C- τελικό άκρο με ορισμένες από τις πρωτεΐνες που δύναται να δεσμευτούν σε αυτό. Ροζ κύκλοι, αμινοξέα που συμμετέχουν στη δέσμευση ιόντων Na +, H + και αποτελούν στόχο των φαρμακευτικών αναστολέων του ΝΗΕ1 Πορτοκαλί κύκλοι, αμινοξέα που συμμετέχουν στη δέσμευση και μεταφορά ιόντων Na +, H + Κίτρινοι κύκλοι, αμινοξέα που αποτελούν στόχο των φαρμακευτικών αναστολέων του ΝΗΕ1 Πράσινοι κύκλοι, αμινοξέα απαραίτητα για την απόκτηση σωστής διαμόρφωσης από τον ΝΗΕ1, καθώς και την στοχοποίησή της για μεταφορά στην πλασματική μεμβράνη Ρ μέσα σε κύκλο, θέση φωσφορυλίωσης από κινάσες. EL (Extracellular Loop, εξωκυτταρικός βρόγχος), IL (Intracellular Loop, ενδοκυτταρικός βρόγχος) (Slepkov et al., 2007). Picture 8. Structure of NHE1. Visible at the top is the enlarged N-terminal transmembrane section which mediates ion exchange, while at the bottom there is the C-terminal regulatory section along with some of the proteins that can bind to it. Pink circles, amino acids which take part in Na +, H + binding and are targeted during pharmacological inhibition of NHE1 Orange circles, amino acids that take part in Na +, H + binding, as well as transport Yellow circles, amino acids that are targeted during pharmacological inhibition of NHE1 Green circles, amino acids essential for proper NHE1 folding, as well as for it being targeted for transport to the plasma 46
47 membrane P inside a circle, site of phosphorylation by kinases. EL (extracellular loop), IL (intracellular loop) (Slepkov et al., 2007) Στο τέλος αυτών των μονοπατιών βρίσκονται πρωτεΐνες που μπορούν να επιδράσουν άμεσα στο C-τελικό ρυθμιστικό άκρο του ΝΗΕ1 (αμινοξέα ). Έτσι, έχει διαπιστωθεί ότι ένας μεγάλος αριθμός κινασών όπως η ERK1/2 (extracellular signal-regulated kinase 1/2), η p90 RSK (p90 ribosomal S6 kinase) και η NIK (Nck-Interacting Kinase) μπορούν και ενεργοποιούν τον ΝΗΕ1 μέσω της φωσφορυλίωσής του σε συγκεκριμένες θέσεις σερίνης και θρεονίνης του C-τελικού άκρου. Αντίστοιχα υπάρχουν και κινάσες όπως η p38 που φωσφορυλιώνουν τον ΝΗΕ1 σε άλλες θέσεις δρώντας ανασταλτικά (Slepkov et al., 2007). Ένας άλλος τρόπος ρύθμισης της δράσης του ΝΗΕ1 είναι με απευθείας σύνδεση μιας πρωτεΐνης στο C-τελικό άκρο του. Μερικές από τις πρωτεϊνες που δρουν κατά αυτόν τον τρόπο είναι η καλμοδουλίνη (CaM, Calmodulin), η πρωτεΐνη προσαρμογής και η Hsp70 (Heat Shock Protein 70kDa, πρωτεΐνη θερμικού σοκ 70kDa) (Bertrand et al., 1994; Silva et al., 1995; Lehoux et al., 2001). Το C-τελικό άκρο του ΝΗΕ1 χρησιμεύει και ως σκαλωσιά (scaffold) πάνω στην οποία συναρμολογούνται πρωτεϊνικά σύμπλοκα, ένα εκ των οποίων είναι το σύμπλοκο ERM. Αυτό αποτελείται από τις πρωτεϊνες εζρίνη, ραδιξίνη και μοεσίνη (Ezhrin, Radixin, Moesin ERM complex). Ταυτόχρονα, το σύμπλοκο ERM συνδέεται και με τον κυτταροσκελετό της ακτίνης φέρνοντάς τον έτσι σε επαφή με τον ΝΗΕ1. Με αυτόν τον τρόπο o ΝΗΕ1 μπορεί να δίνει και να λαμβάνει πληροφορία από το κυτταρόπλασμα, συμμετέχοντας ταχύτατα στις κυτταρικές λειτουργίες που σχετίζονται με τον κυτταροσκελετό της ακτίνης όπως είναι η κυτταρική μετανάστευση, το κυτταρικό σχήμα και κατ επέκταση ο κυτταρικός όγκος (Denker et al., 2000; Baumgartner et al., 2004). 8.Ελεύθερες ρίζες και αντιοξειδωτικοί μηχανισμοί Οι ελεύθερες ρίζες (free radicals) είναι άτομα ή μόρια που φέρουν ένα ή περισσότερα ασύζευκτα ηλεκτρόνια στα τροχιακά τους (Halliwell & Gutteridge, 1990). Έτσι έχουν μια ισχυρή τάση να ζευγαρώσουν τα ασύζευκτα ηλεκτρόνιά τους, κάτι που τις καθιστά ιδιαίτερα δραστικές απέναντι σε άλλα μόρια που βρίσκονται κοντά τους. Η δραστικότητά τους αυτή μπορεί να τις καταστήσει επικίνδυνες για το κύτταρο, καθότι μπορούν να προκαλέσουν βλάβες όπως τροποποίηση του DNA ή του 47
48 RNA, οξείδωση λιπιδίων ή/και διαταραχή της δομής και κατά συνέπεια λειτουργίας πρωτεϊνών. Γίνεται αντιληπτό ότι όλες αυτές οι βλάβες μπορούν να οδηγήσουν σε ασθένειες όπως ο καρκίνος, η αθηρωμάτωση και άλλες. Ταυτόχρονα όμως, υπάρχουν κύτταρα του ανοσοποιητικού συστήματος όπως τα μονοκύτταρα, τα μακροφάγα και τα ουδετερόφιλα κοκκιοκύτταρα, τα οποία εκμεταλλεύονται τις ελεύθερες ρίζες για την άμυνα του οργανισμού (Demaurex et al.,1996; Sanchez-Pozo et al., 2003). Έτσι, μέσω μιας διαδικασίας που ονομάζεται αναπνευστική έκρηξη (respiratory burst), όταν δεχθούν τα κατάλληλα ερεθίσματα παράγουν μεγάλες ποσότητες ελεύθερων ριζών τις οποίες και διοχετεύουν ταχύτατα ενάντια σε στόχους όπως εισβάλλοντα βακτήρια προκειμένου να τους καταστρέψουν. Η διαδικασία αυτή όμως, δεν είναι απόλυτα ελεγχόμενη με αποτέλεσμα συχνά να οξειδώνονται και μόρια που τυχαίνει να βρίσκονται πλησίον της περιοχής της αναπνευστικής έκρηξης όπως για παράδειγμα οι LDLs που μπορούν οξειδωθούν προς oxldls αυξάνοντας έτσι την πιθανότητα εκδήλωσης αθηρωματικών γεγονότων (Cathcart, 2004). Σχετικά πρόσφατα και καθώς το πεδίο των ελευθέρων ριζών ερευνάται όλο και περισσότερο, άρχισε να γίνεται αντιληπτό ότι ορισμένες ελεύθερες ρίζες δεν έχουν μόνο δυνητικά καταστροφικές ιδιότητες, αλλά μπορούν να συμμετέχουν και σε μηχανισμούς μεταγωγής σήματος (Gutierrez et al., 2006) (εικ.9). Από τις ελεύθερες ρίζες, οι πιο σημαντικές όσον αφορά τα βιολογικά συστήματα είναι οι δραστικές μορφές οξυγόνου (ROS, reactive oxygen species) και αζώτου (RNS, reactive nitrogen species). Στις δραστικές μορφές οξυγόνου συγκαταλέγονται το ανιόν του σουπεροξειδίου (Ο.- 2 ), η υδροξυλική ρίζα (ΟΗ. ), το υπεροξείδιο του υδρογόνου (Η 2 Ο 2 ) και το υπεροξυνιτρώδες ή υπεροξυνιτρίτης (ΟΝΟΟ - ), ενώ από τις δραστικές μορφές αζώτου αξίζει να αναφερθεί το μονοξείδιο του αζώτου (ΝΟ. ). Το ανιόν σουπεροξειδίου παράγεται κυρίως από το ένζυμο NADPH οξειδάση που εντοπίζεται στην πλασματική μεμβράνη ή/και στα φαγοσώματα κυττάρων του ανοσοποιητικού συστήματος (Touyz, 2003). Ακόμα, μπορεί να παραχθεί στα μιτοχόνδρια ως παραπροϊόν της αναπνευστικής αλυσίδας (κυρίως στα συμπλέγματα Ι και ΙΙΙ) ή ως αποτέλεσμα της δράσης ορισμένων ενζύμων όπως της οξειδάσης της ξανθίνης. 48
49 Εικόνα 9. Δραστικές μορφές οξυγόνου που παράγονται κατά την αναγωγή του μοριακού οξυγόνου. Στο σχήμα φαίνεται ότι η υδροξυλική ρίζα είναι η πιο δραστική και κατά συνέπεια διαθέτει και τον μικρότερο χρόνο ημιζωής. Σε ένα συγκεκριμένο εύρος συγκεντρώσεων ( Μ) το υπεροξείδιο του υδρογόνου μπορεί να συμμετάσχει στη μεταγωγή σήματος επιδρώντας σε κυτταρικές διαδικασίες (Giorgio et al., 2007). Picture 9. Reactive oxygen species produced during reduction of molecular oxygen. The hydroxyl radical is the most reactive hence its very small half-life. Hydrogen peroxide at concentrations of Μ can affect cellular processes by participating in intracellular signaling (Giorgio et al., 2007). Η ιδιαιτέρως δραστική υδροξυλική ρίζα μπορεί να παραχθεί από την αποδόμηση του υπεροξυνιτρώδους ή ως προϊόν της αντίδρασης Fenton μεταξύ ιόντων σιδήρου και του υπεροξειδίου του υδρογόνου ( [1] Fe 2+ + H 2 O 2 Fe 3+ + OH. + OH, [2] Fe 3+ + H 2 O 2 Fe 2+ + OOH. + H + ) (Touyz, 2003). Το υπεροξείδιο του υδρογόνου παράγεται κατά την εξουδετέρωση του ανιόντος σουπεροξειδίου από το ένζυμο δισμουτάση του σουπεροξειδίου (SOD, superoxide dismutase, σύμφωνα με την αντίδραση 2O H + H 2 O 2 + O 2 ) (Hancock et al., 2001). Το υπεροξινιτρώδες παράγεται από την αντίδραση του ανιόντος σουπεροξειδίου με το μονοξείδιο του αζώτου (Ο ΝΟ. ΟΝΟΟ - ) (Darley-Usmar et al., 1995). Τέλος, το μονοξείδιο του αζώτου παράγεται από την αντίδραση του αμινοξέος αργινίνη με το οξυγόνο που καταλύεται από τα ένζυμα συνθάσες του ΝΟ (NOS, NO synthase). 49
50 Αναπόφευκτο αποτέλεσμα της λειτουργίας των κυττάρων είναι η συνεχής παραγωγή ελευθέρων ριζών. Ως εκ τούτου έχουν εξελιχθεί διάφοροι αντιοξειδωτικοί μηχανισμοί προκειμένου να εξουδετερώνονται οι ελεύθερες ρίζες προτού προκαλέσουν βλάβες. Έτσι, όπως προαναφέρθηκε, το ένζυμο δισμουτάση του σουπεροξειδίου εξουδετερώνει άμεσα το ανιόν του σουπεροξειδίου, ενώ μπορεί να θεωρηθεί ότι με αυτόν τον τρόπο εξουδετερώνει έμμεσα και παράγωγα του ανιόντος του σουπεροξειδίου, όπως το υπεροξυνιτρώδες. Το υπεροξείδιο του υδρογόνου αντιμετωπίζεται με το ένζυμο καταλάση (που καταλύει την αντίδραση 2H 2 O 2 2H 2 O + O 2 ) (Touyz, 2003). Ένας άλλος αντιοξειδωτικός μηχανισμός ενάντια στο υπεροξείδιο του υδρογόνου είναι αυτός της υπεροξειδάσης της γλουταθειόνης (που καταλύει την αντίδραση 2GSH + H 2 O 2 GS SG + 2H 2 O). Η γλουταθειόνη είναι ένα τριπεπτίδιο (αποτελείται από γλυκίνη-γλουταμινικό οξύ-κυστεϊνη) που μπορεί και εξουδετερώνει ελεύθερες ρίζες μέσω της παροχής σε αυτές ενός ηλεκτρονίου, ενώ η ίδια διμερίζεται προς την οξειδωμένη της μορφή, τη δισουλφιδική γλουταθειόνη (GS- SG) (Pompella et al., 2003). Ταυτόχρονα, η γλουταθειόνη, μέσω μιας διαδικασίας γνωστή ως γλουταθειονυλίωση μπορεί και δεσμεύεται σε ενεργές κυστεϊνες ευαίσθητων πρωτεϊνών προστατεύοντάς τες από τη βλαβερή επίδραση των ελευθέρων ριζών. Κατόπιν, η δράση του ενζύμου ρεδουκτάση της γλουταθειόνης την επαναφέρει στην ανηγμένη της μορφή (GSH), απελευθερώνοντάς την από τις πρωτεΐνες στις οποίες είχε δεσμευτεί (Pompella et al., 2003). Ένας άλλος αντιοξειδωτικός μηχανισμός που επιστρατεύεται από το κύτταρο όταν βρεθεί σε κατάσταση οξειδωτικού στρες είναι η πρωτεΐνη Hsp70 (Heat-shock protein 70kDa, πρωτεϊνη θερμικού σοκ 70kDa) (Suzuki et al., 2005). H Hsp70 δεσμεύεται σε υδρόφοβες περιοχές πρωτεϊνών προστατεύοντας τη διαμόρφωσή τους από την επίδραση των ελευθέρων ριζών, εμποδίζοντας παράλληλα τη δημιουργία δυνητικά τοξικών πρωτεϊνικών συσσωματωμάτων στο κυτταρόπλασμα. Αντιοξειδωτικός μηχανισμός ενάντια στην υδροξυλική ρίζα δεν υπάρχει, και αυτό διότι είναι τόσο δραστική που αντιδράει αμέσως με το πρώτο βιολογικό μακρομόριο που θα συναντήσει. Ακόμα όμως και στις περιπτώσεις που υπάρχουν αντιοξειδωτικοί μηχανισμοί, αυτοί δεν δύναται να δράσουν ενάντια σε όλες τις ελεύθερες ρίζες που παράγονται. Έτσι, μια ενδιαφέρουσα θεωρία υποστηρίζει ότι η γήρανση οφείλεται τουλάχιστον εν μέρει στη συσσώρευση βλαβών που προκαλούνται από ελεύθερες ρίζες στη διάρκεια της ζωής του οργανισμού (Wei et al., 1998). 50
51 9. Σκοπός της εργασίας Σκοπός της παρούσης εργασίας ήταν η μελέτη της επίδρασης της ορμόνης λεπτίνης επί των ανθρωπίνων μονοκυττάρων με έμφαση στην επιρροή που αυτή ασκεί στη συμμετοχή τους στην πορεία της διαδικασίας της αθηρωμάτωσης. Για αυτό το σκοπό, μονοκύτταρα, κύτταρα του ανοσοποιητικού συστήματος που είτε κυκλοφορούν περιπολώντας στο αίμα, είτε εγκαθίστανται σε ιστούς όπου και διαφοροποιούνται προς μακροφάγα και άλλους κυτταρικούς τύπους, απομονώνονταν από ολικό αίμα παραχωρημένο από υγιείς δότες. Είναι γνωστό ότι τα μονοκύτταρα διαδραματίζουν πρωταγωνιστικό ρόλο στα φαινόμενα αθηρωμάτωσης. Η αθηρωμάτωση είναι μια ιδιαιτέρως πολύπλοκη διαδικασία, η προοδευτική εξέλιξη της οποίας μπορεί να διαχωριστεί σε διάφορα σχετικά καλά χαρακτηρισμένα στάδια ή βήματα. Έτσι, μελετήθηκε η επίδραση της λεπτίνης σε πολλά από αυτά τα στάδια και συγκεκριμένα στην ικανότητα των μονοκυττάρων να προσκολλώνται στην πρωτεΐνη της εξωκυττάριας ουσίας λαμινίνη-1, καθώς και στη μετανάστευση διαμέσου αυτής, στην παραγωγή δραστικών μορφών οξυγόνου από τα μονοκύτταρα και στην ικανότητα των μονοκυττάρων να εκφράζουν στην επιφάνειά τους τον υποδοχέα ρακοσυλλέκτη CD36 και μέσω αυτού να φαγοκυτταρώνουν οξειδωμένες λιποπρωτεΐνες χαμηλής πυκνότητας (oxldls). Τα πειράματα προσκόλλησηςμετανάστευσης στη λαμινίνη-1 αποτελούν καλή αναπαράσταση των πραγματικών διαδικασιών πρόσδεσης των μονοκυττάρων στο ενδοθήλιο αγγείων και της μετανάστευσης διαμέσου αυτού προς τον υποενδοθηλιακό χώρο. Από τα πειράματα μέτρησης της παραγωγής δραστικών μορφών οξυγόνου μπορεί να εξαχθεί το κατά πόσον η λεπτίνη επηρεάζει την καταγεγραμμένη ικανότητα των μονοκυττάρων να οξειδώνουν μόρια του μικροπεριβάλλοντός τους, όπως για παράδειγμα τις LDLs προς oxldls. Παράλληλα, η φαγοκύττωση των oxldls μέσω υποδοχέων ρακοσυλλεκτών όπως ο CD36 είναι επίσης μια διαδικασία που είναι γνωστό ότι συμβαίνει στον υποενδοθηλιακό χώρο και είναι ένα από τα βασικά βήματα για τη μετατροπή των μονοκυττάρων προς αφρώδη κύτταρα. Σε όλα τα προαναφερθέντα πειράματα όπου και διαπιστώθηκε επίδραση της λεπτίνης στη δράση των μονοκυττάρων, πραγματοποιήθηκε και επιλεγμένη φαρμακολογική αναστολή συγκεκριμένων πρωτεϊνών προκειμένου να παραχθεί έμμεση πληροφορία σχετικά με τους μηχανισμούς μεταγωγής σήματος που αξιοποιεί η λεπτίνη. Έτσι, πραγματοποιήθηκε αναστολή της ισομορφής-1 του ιοντοανταλλάκτη 51
52 Na + /H + (NHE1), της κινάσης της φωσφατίδυλοϊνοσιτόλης-3 (PI3K), όλων των ισομορφών της πρωτεϊνικής κινάσης C (PKC), καθώς και πιο ειδικά μόνο των λεγόμενων συμβατικών ισομορφών της (α-, β i - και β ii -), της NADPH οξειδάσης, της συνθάσης του ΝΟ, ενώ σε μερικά πειράματα εφαρμόστηκε και αναστολή του πολυμερισμού των ινιδίων της ακτίνης του κυτοσκελετού. Ταυτόχρονα, σε κάθε πείραμα όπου κρίθηκε απαραίτητο, συλλέχθηκαν δεδομένα προς σχηματισμό της καμπύλης δόσης-απόκρισης της λεπτίνης προκειμένου να επιλεγεί η πιο δραστική συγκέντρωσή της για την περαιτέρω διερεύνηση του φαινομένου. Αυτό είχε ιδιαίτερη σημασία καθότι με αυτόν τον τρόπο μπορούσε να διαπιστωθεί εάν κάποια επίδραση της λεπτίνης συνέβαινε υπό κανονικές συγκεντρώσεις, υπό υπερλεπτιναιμικές (χαρακτηριστικές των παχύσαρκων ατόμων) ή και στις δύο περιπτώσεις. Στη συνέχεια δόθηκε μεγαλύτερη έμφαση στον ΝΗΕ1 και στη θέση που κατέχει στο μηχανισμό δράσης της λεπτίνης. Έτσι, μελετήθηκε καταρχήν, η επίδραση της λεπτίνης στην τιμή του ενδοκυτταρικού ph (phi) των μονοκυττάρων, μιας ιδιαιτέρως σημαντικής παραμέτρου που ρυθμίζεται κυρίως από τον ΝΗΕ1. Κατόπιν, μελετήθηκε η επίδραση της λεπτίνης σε αντι-οξειδωτικούς μηχανισμούς των μονοκυττάρων σε σχέση με τον ΝΗΕ1, μέσω της ανίχνευσης τόσο των επιπέδων σύνδεσης του ΝΗΕ1 με την πρωτεΐνη Hsp70, όσο και των επιπέδων γλουταθειονυλίωσης της Hsp70 που αποτελούν έμμεσο δείκτη των ενδοκυτταρικών επιπέδων οξειδωτικού στρες. Τέλος, μελετήθηκε η επίδραση της λεπτίνης στη δραστικότητα του ενζύμου δισμουτάση του σουπεροξειδίου (SOD), ενός ακόμα σημαντικού αντι-οξειδωτικού μηχανισμού. Τα αποτελέσματα της παρούσης εργασίας ελπίζουμε να συμβάλλουν στην καλύτερη κατανόηση του ομολογουμένως πολύπλοκου μηχανισμού μέσω του οποίου η λεπτίνη κατευθύνει τα μονοκύτταρα στη διαδικασία της αθηρωμάτωσης. 52
53 Παράρτημα Εισαγωγής 1.Λιποπρωτεΐνες χαμηλής πυκνότητας (LDLs) Οι λιποπρωτεΐνες είναι υδατοδιαλυτές πρωτεΐνες που χρησιμεύουν στη μεταφορά χοληστερόλης, τριγλυκεριδίων, φωσφολιπιδίων και άλλων λιπών διαμέσου του αίματος, επιτρέποντάς έτσι σε αυτά να μετακινούνται στο υδατικής σύστασης αίμα παρά τη λιπαρή τους φύση (Smith et al., 1978). Έχουν συνήθως σφαιρικό σχήμα, διαθέτοντας ένα μη πολικό ηλεκτροουδέτερο πυρήνα αποτελούμενο από εστέρες χοληστερόλης και τριγλυκερίδια, και περιφερειακά στρώματα σχετικά πολικών ουσιών όπως φωσφολιπίδια και χοληστερόλη. Βασικό συστατικό τους είναι ορισμένες πρωτεΐνες, γνωστές ως αποπρωτεΐνες, που έχουν την ιδιότητα να δεσμεύουν μεγάλες ποσότητες λιπιδίων. Παραδοσιακά αναγνωρίζονται πέντε κύριες ομάδες λιποπρωτεϊνών και αυτές είναι (κατά σειρά μεγέθους από τη μεγαλύτερη προς τη μικρότερη) τα χυλομικρά, οι λιποπρωτεΐνες πολύ χαμηλής πυκνότητας (VLDLs, Very Low-Density Lipoproteins), οι λιποπρωτεΐνες ενδιάμεσης πυκνότητας (IDLs, Intermediate-Density Lipoproteins), οι LDLs (LDLs, Low-Density Lipoproteins) και οι λιποπρωτεΐνες υψηλής πυκνότητας (HDLs, High-Density Lipoproteins) (πίνακας 3) (Loscalzo, 2005) (Πίνακας 2). Οι LDLs προέρχονται από VLDLs οι οποίες χάνουν την πρωτεΐνη apoe από τη δομή τους, διατηρώντας έτσι μόνο την χαρακτηριστική των LDLs πρωτεΐνη apob-100, ενώ παράλληλα η αναλογία μεταξύ των τριγλυκεριδίων και της χοληστερόλης που φέρουν αυξάνει δραματικά υπέρ της δεύτερης (Gleissner et al., 2007). Κύτταρα τα οποία χρειάζονται χοληστερόλη εκφράζουν στην επιφάνειά τους υποδοχείς για τις LDLs. Έπειτα από τη δέσμευση των LDLs, ακολουθεί η ενδοκύττωση τους μέσα σε κυστίδια καλυμμένα με την πρωτεΐνη κλαθρίνη τα οποία στη συνέχεια ενώνονται με ενδοσώματα. Εν τέλει, οι LDLs φτάνουν στα λυοσώματα όπου με τη δράση υδρολυτικών ενζύμων αφαιρούνται τα μόρια εστεροποιημένης χοληστερόλης για να χρησιμοποιηθούν για τις ανάγκες του κυττάρου. Οι LDLs είναι γνωστές και ως κακή χοληστερίνη διότι υψηλές συγκεντρώσεις τους στον ορό έχουν συσχετιστεί με αυξημένη πιθανότητα εκδήλωσης αθηρωμάτωσης. Η ικανότητα των LDLs να επάγουν αθηρωματικά φαινόμενα αυξάνει ακόμα περισσότερο όταν αυτές υποστούν οξειδωτική τροποποίηση προς ελάχιστα τροποποιημένες (mmldls) και οξειδωμένες LDLs (oxldls) (Berliner et al., 1990). 53
54 Χυλομικρά VLDLs LDLs HDLs Θέση σύνθεσης (πηγή) Έντερο Ήπαρ VLDLs Ήπαρ και έντερο Μέγεθος (Å, m) Πυκνότητα (g/ml) <0,94 0,94-1,006 1,019-1,063 1,063-1,21 MB (kda) Τριγλυκερίδια (% κ.β.) Φωσφολιπίδια (% κ.β.) Ελεύθερη χοληστερόλη (% κ.β.) Εστεροποιημένη χοληστερόλη (% κ.β.) Πρωτεΐνη (% κ.β.) apoa-i, apoa-iv, apob-100, apoe, apob-100 apoa-i, apoa-ii Κύριες apob-48, apoci, apoci, apocii, Απολιποπρωτεΐνες apociii, apoe apociii apoa-ii, apocii apoa-i, apoa-ii, apoci, apoci, apocii, Δευτερεύουσες απολιποπρωτεΐνες apoa-iv, apociv, apoav apocii, apociii, apoe apociii, apod, apoe, apoj, apoav Πίνακας 2. Οι κύριες λιποπρωτεΐνες, οι ιδιότητες και τα συστατικά τους στοιχεία. Οι IDLs εμφανίζουν χαρακτηριστικά ενδιάμεσα των VLDLs και των LDLs (Loscalzo, 2005). Table 2. The main types of lipoproteins, their properties and composition. IDLs exhibit characteristics intermediate of VLDLs and LDLs (Loscalzo, 2005). 2.Εξωκυττάρια ουσία Η εξωκυττάρια ουσία (ECM, extracellular matrix) είναι ένα εξωκυτταρικό δίκτυο πρωτεϊνών και πρωτεογλυκανών (πρωτεΐνες που έχουν υποστεί εκτεταμένη γλυκοσυλίωση μέσω της προσθήκης γλυκοζαμινογλυκανών σε αυτές) που καλύπτει τους χώρους μεταξύ των ιστών (Rees et al., 2008). Αποτελεί βασικό χαρακτηριστικό του συνδετικού ιστού, με τα συστατικά της να παράγονται και να εκκρίνονται από τα ίδια τα κύτταρα τα οποία περιβάλλει. Η βασική μεμβράνη που προαναφέρθηκε και την οποία πρέπει να διαπεράσουν τα μονοκύτταρα κατά τη μετανάστευσή τους προς τον υποενδοθηλιακό χώρο, αποτελεί τμήμα της εξωκυττάριας ουσίας. Ο ρόλος της εξωκυττάριας ουσίας είναι πολλαπλός. Περιλαμβάνει, μεταξύ των άλλων, το διαχωρισμό των ιστών, την επικοινωνία μεταξύ κυττάρων, την προστασία των 54
55 κυττάρων από μηχανικό στρες και την παροχή θέσεων πρόσδεσης για κύτταρα (όπως συμβαίνει με τα λευκοκύτταρα). Στα πρωτεϊνικά συστατικά (που δεν υπόκεινται υποχρεωτικά σε εκτεταμένη γλυκοσυλίωση) συγκαταλέγονται οι διάφορες ισομορφές του κολλαγόνου, η ελαστίνη, η φιμπρονεκτίνη και οι διάφορες ισομορφές των λαμινινών (π.χ. η λαμινίνη-1) (Hayden et al., 2005). Τόσο η φιμπρονεκτίνη, όσο κι οι λαμινίνες έχουν την ικανότητα να συνδέονται με τις ιντεγκρίνες κυττάρων που επιχειρούν να προσκολληθούν στην εξωκυττάρια ουσία (όπως π.χ. των λευκοκυττάρων). Οι κυριότερες γλυκοζαμινογλυκάνες (πρόκειται για μεγάλου μήκους, αδιακλάδωτους πολυσακχαρίτες που αποτελούνται από συγκεκριμένες, επαναλαμβανόμενες δισακχαριτικές μονάδες ο καθένας) που συμβάλλουν στη δομή της εξωκυττάριας ουσίας με το να συνδέονται σε πρωτεΐνες της είναι η θειική ηπαράνη (heparan sulfate, συνδέεται σε λαμινίνες, στην πρωτεΐνη περλεκάνη και αλλού), η θειική χονδροϊτίνη (chondroitin sulfate), η θειική δερματάνη (dermatan sulfate), η θειική κερατάνη (keratan sulfate) και η ηπαρίνη (Hayden et al., 2005). Εξαίρεση μεταξύ των γλυκοζαμινογλυκάνών αποτελεί το υαλουρονικό οξύ, το οποίο παρόλο που παίζει πολύ σπουδαίο ρόλο στη δομή της εξωκυττάριας ουσίας, δεν συνδέεται με πρωτεΐνες προς σχηματισμό πρωτεογλυκάνων. Κύτταρα που μπορούν και προσδένονται στο υαλουρονικό οξύ (π.χ. λευκοκύτταρα), το κάνουν μέσω του επιφανειακού υποδοχέα CD44 που εκφράζουν. Ορισμένες από τις πιο σημαντικές πρωτεογλυκάνες που συμμετέχουν στη δομή της εξωκυττάριας ουσίας είναι η περλεκάνη που προαναφέρθηκε, η αγγρεκάνη (aggrecan), η βερσικάνη (versican) και η φιμπρομοντουλίνη (fibromodulin). Η εξωκυττάρια ουσία αποτελεί ένα δυναμικό σύστημα του οποίου τα συστατικά διαρκώς συντίθενται και διασπώνται. Τη διάσπαση των συστατικών της εξωκυττάριας ουσίας την επιτελούν ένζυμα που συχνά εμφανίζουν ειδικότητα, όπως οι υαλουρονιδάσες για το υαλουρονικό οξύ ή ένζυμα με πιο γενική δράση όπως οι μεταλλοπρωτεϊνάσες της εξωκυττάριας ουσίας (MMPs, Matrix Metalloproteinases) που διασπούν τα πρωτεϊνικά συστατικά της (Murphy & Nagase, 2008). 55
56 3.Δείκτης μάζας σώματος (BMI) O δείκτης μάζας σώματος (BMI, body mass index) αποτελεί γενικό δείκτη των επιπέδων παχυσαρκίας ενός ατόμου και λόγο της ευκολίας με την οποία υπολογίζεται έχει καθιερωθεί ευρύτατα. Ισούται με το αποτέλεσμα της παρακάτω εξίσωσης: Βάρος ΒΜΙ =,όπου το βάρος σε kg και το ύψος σε m. 2 Ύψος Τα αποτελέσματα της μέτρησης του ΒΜΙ ερμηνεύονται με βάση τον παρακάτω πίνακα: ΒΜΙ <18,5 18,5 24, ,9 >30 Κατάσταση Λιποβαρής Κανονικός Υπέρβαρος Παχύσαρκος Πίνακας 2. Αντιστοίχιση ΒΜΙ και κατάστασης ατόμου Table 2. BMI and state of the individual. <18,5 underweight, 18,5-24,9 normal, 25-29,9 overweight, >30 obese. 4.Μονοπάτι μεταγωγής σήματος JAK/STAT Το μονοπάτι αυτό στις διάφορες εκφάνσεις του περιλαμβάνει 4 διαφορετικές κινάσες τυροσίνης JAK (Janus kinases) και 7 διαφορετικούς μεταγραφικούς παράγοντες STAT (Signal Transducer and Activator of Transcription protein) και αξιοποιείται από κυτοκίνες όπως οι ιντερφερόνες και οι ιντερλευκίνες των οποίων οι υποδοχείς δε διαθέτουν ενδογενή ικανότητα φωσφορυλίωσης άλλων πρωτεϊνών (Frühbeck, 2006). Έτσι, τον φωσφορυλιωτικό ρόλο τον αναλαμβάνουν οι κινάσες JAK που στρατολογούνται στα κυτταροπλασματικά άκρα των υποδοχέων έπειτα από την ενεργοποίηση των τελευταίων (εικ.10). Ειδικότερα όσον αφορά τη λεπτίνη, ο υποδοχέας της ObRb στρατολογεί κυρίως την JAK2 (Ghilardi & Skoda, 1997). Τα όρια μεταξύ ορμονών και κυτοκινών μερικές φορές δεν είναι ευδιάκριτα και η λεπτίνη αποτελεί μία από αυτές τις περιπτώσεις καθώς φέρει ιδιότητες και των δύο (συμμετέχει στη διακυτταρική επικοινωνία και μπορεί να δράσει σε πολύ μικρές συγκεντρώσεις της τάξης των pm). H JAK2 φωσφορυλιώνει υπολείμματα τυροσίνης τόσο πρωτεϊνών που βρίσκονται κοντά της, όσο και του ίδιου του ObRb καθιστώντας τον έτσι ικανό να δεσμεύσει μεταγραφικούς παράγοντες STATs. Μελέτες έχουν δείξει ότι ο ObRb μπορεί και δεσμεύει τους STAT3, STAT5 και STAT6, 56
57 αλλά όχι τους STAT1, STAT2 ή STAT4, με τη δέσμευση του STAT3 να είναι η πιο συχνή (Sweeney, 2002). Εν συνεχεία οι ενεργοποιημένοι μεταγραφικοί παράγοντες μετατοπίζονται στον πυρήνα όπου διεγείρουν τη μεταγραφή συγκεκριμένων γονιδίων (εικ.10). Η δράση του μονοπατιού JAK/STAT που εκκινείται από τη λεπτίνη αναστέλλεται από πρωτεΐνες γνωστές ως SOCS (Suppressors of Cytokine Signalling) (Müller et al., 2005). Ενδιαφέρον προκαλεί το γεγονός ότι η ίδια η λεπτίνη ενισχύει την έκφραση της SOCS-3, υποδηλώνοντας έτσι την ύπαρξη ενός τουλάχιστον επιπέδου ελέγχου της δράσης της λεπτίνης μέσω διαδικασίας αυτοαναστολής (Bjørbaeck et al., 1998). Ένας άλλος αρνητικός ρυθμιστής της δράσης της λεπτίνης είναι πρωτεΐνη PTP1B (Protein Tyrosine Phosphatase 1B) η οποία δρα κυρίως μέσω αποφωσφορυλίωσηςαπενεργοποίησης της JAK2 (Zabolotny et al., 2002). Εικόνα 10. Ενεργοποίηση του μονοπατιού JAK/STAT από τη λεπτίνη. Δέσμευση της λεπτίνης στον υποδοχέα της ObRb οδηγεί σε αλλαγή της διαμόρφωσης του τελευταίου (Α). Η αλλαγή της διαμόρφωσης επιτρέπει στις JAKs να ενεργοποιηθούν και να φωσφορυλιώσουν πολλά υπολείμματα τυροσίνης του ObRb παρέχοντας έτσι στις STATs τη δυνατότητα να δεσμευτούν και αυτές στον ObRb (B). Μετά τη φωσφορυλίωση των STATs ακολουθεί αποκόλλησή τους από τον ObRb και διμερισμός τους (Γ). Τέλος, τα διμερή των STATs μετατοπίζονται στον πυρήνα όπου επάγουν τη μεταγραφή συγκεκριμένων 57
58 γονιδίων (Δ). Στην εικόνα φαίνονται επίσης οι αναστολείς του μονοπατιού που εκκινεί η λεπτίνη, SOCS-3 και PTP1B. L σε κόκκινο κύκλο, η λεπτίνη (Frühbeck, 2006). Picture 10. Activation of the JAK/STAT pathway by leptin. Leptin binding to its receptor ObRb leads it to a conformation change (A). The conformation change allows activation of JAKs, which in turn phosphorylate many tyrosine residues of ObRb thus providing STATs with the appropriate sites for their own binding to ObRb (B). Following their phosphorylation, STATs detach from ObRb and form dimers (Γ). Finally, STAT dimers translocate to the nucleus where they induce transcription of particular genes (Δ). The inhibitors of this leptin-induced pathway SOCS-3 and PTP1B are also depicted. L in a red circle is leptin (Frühbeck, 2006). 58
59 Υλικά και Μέθοδοι 1.1 Απομόνωση, κρυοαποθήκευση και επαναφορά μονοκυττάρων από ολικό αίμα Διαδικασία απομόνωσης μονοκυττάρων από ολικό αίμα Ολικό αίμα παραλαμβανόταν από το κέντρο αιμοδοσίας του νοσοκομείου Ιπποκράτειο. Αφορούσε ασκούς που περιείχαν μειωμένη ποσότητα ολικού αίματος (συνήθως 200 ml) και συνεπώς δεν επρόκειτο να χρησιμοποιηθούν σε μεταγγίσεις, αλλά προέρχονταν από υγιείς δότες. Το ολικό αίμα ήταν τουλάχιστον τριών ημερών προκειμένου να έχει προηγηθεί ιολογικός έλεγχος. Η απομόνωση των μονοκυττάρων από το ολικό αίμα γινόταν με βάση τη μέθοδο των Seager-Danciger et al, Η μέθοδος αυτή μέσω δύο κύριων φυγοκεντρήσεων εκμεταλλεύεται τις διαφορές στις πυκνότητες ανάμεσα στα μονοκύτταρα (<1,068 g/ml), λεμφοκύτταρα (1,066-1,076 g/ml), ερυθροκύτταρα (>1,086 g/ml) και τα υπόλοιπα κυτταρικά συστατικά του αίματος (εικ.1). Εικόνα 1. Πυκνότητες και ποσότητες κυτταρικών συστατικών του αίματος Picture 1. Densities and quantities of blood cells. Colour code: Monocytes (Blue), Lymphocytes (Green), Basophil granulocytes (Cyan), Neutrophil granulocytes (Purple), Eosinophil granulocytes (Yellow), Erythrocytes (Red). Περιληπτικά, αίμα επιστοιβαζόταν σε διάλυμα Ficoll-Paque Plus (1,077 g / ml) και φυγοκεντρούνταν με αποτέλεσμα να διαπεράσουν το διάλυμα Ficoll-Paque Plus και 59
60 να βρεθούν στο ίζημα, όλα τα κυτταρικά συστατικά του αίματος με πυκνότητα μεγαλύτερη του 1,077 g/ml. Τα μονοκύτταρα με τα λεμφοκύτταρα λόγω της χαμηλότερης πυκνότητάς τους δεν μπορούσαν να διαπεράσουν το διάλυμα Ficoll- Paque Plus, οπότε έμεναν στο υπερκείμενο και συλλέγονταν. Αυτά στη συνέχεια επιστοιβάζονταν σε διάλυμα 46% iso-osmotic Percoll (1,067 g/ml) και φυγοκεντρούνταν, με αποτέλεσμα τα περισσότερα λεμφοκύτταρα να βρεθούν στο ίζημα, ενώ τα μονοκύτταρα και ελάχιστα πολύ χαμηλής πυκνότητας λεμφοκύτταρα έμεναν στο υπερκείμενο και συλλέγονταν, ολοκληρώνοντας έτσι τη διαδικασία. Πιο αναλυτικά, με αυτή τη μέθοδο 30 ml αίματος από έναν ασκό μεταφέρονταν σε δοχείο falcon των 50 ml όπου κατόπιν προσθέτονταν 6 ml PBS 1x 1. Έπειτα από ελαφρά και περιστροφική ανακίνηση γινόταν αργή και προσεκτική υποστοίβαξη με 10 ml Ficoll- Paque Plus (1,077 g/ml) με τη χρήση μιας 18 gauge σύριγγας (18 gauge spinal needle, χρησιμοποιείται για τη λήψη μυελού των οστών) (κοινώς, το Ficoll-Paque Plus τοποθετούνταν από κάτω από το αίμα). Ακολουθούσε φυγοκέντρηση 400 g / 20 min / RT (δινόταν προσοχή ώστε όλες οι φυγοκεντρήσεις να γίνονταν χωρίς φρένο ή επιτάχυνση, διότι σε αντίθετη περίπτωση καταστρέφονταν τα κύτταρα). Σε έκτακτες περιπτώσεις έλλειψης διαθέσιμων ασκών, γινόταν λήψη ποσότητας 20 ml ολικού αίματος από τον γράφοντα και τοποθετούνταν σε δοχείο falcon των 50 ml στο οποίο είχε ήδη τοποθετηθεί 1 ml αντιπηκτικού διαλύματος 200 mm EDTA. Αυτό αραιωνόταν έως τα 30 ml με πλήρες θρεπτικό υλικό IMDM 2 και κατόπιν ακολουθούνταν η ίδια διαδικασία που περιγράφηκε παραπάνω (προσθήκη PBS 1x, υποστοίβαξη με Ficoll-Paque Plus και φυγοκέντρηση). Μετά το πέρας της φυγοκέντρησης σχηματίζονταν χαρακτηριστικές ζώνες με τα περισσότερα ερυθροκύτταρα να έχουν διαπεράσει το διάλυμα Ficoll-Paque Plus και να βρίσκονται στο ίζημα (εικ.2α). Πάνω από το ίζημα βρισκόταν η ζώνη του διαλύματος Ficoll- Paque Plus, ενώ πάνω πάνω βρισκόταν η υποκίτρινη ζώνη του πλάσματος. Μεταξύ της ζώνης του Ficoll-Paque Plus και του πλάσματος βρισκόταν μια λεπτή, αλλά πυκνή, υπόλευκη στοιβάδα η οποία περιείχε τα κύτταρα που μας ενδιέφεραν, τα PBMCs (Peripheral Blood Mononuclear Cells, μονοπύρηνα κύτταρα περιφερικού αίματος), που αποτελούνταν κυρίως από μονοκύτταρα και λεμφοκύτταρα (εικ.2α). Ποσότητα ml από τη ζώνη των PBMCs συλλέγονταν (εικ. 2Β) σε ένα δοχείο falcon των 50 ml και αραιώνονταν με PBS 1x (που περιείχε 1mM EDTA) προς τελικό όγκο ml. Έπειτα από ελαφρά ανακίνηση ακολουθούσε φυγοκέντρηση 150 g / 60
61 10 min / RT και απομάκρυνση του υπερκείμενου. Το ίζημα επαναδιαλυόταν σε 40 ml PBS 1x (που περιείχε 1 mm EDTA) και φυγοκεντρούνταν ξανά στα 150g / 10min / RT. Μετά από μία ακόμα όμοια πλύση (απομάκρυνση υπερκείμενου, διάλυση σε PBS 1x και φυγοκέντρηση), το ίζημα διαλυόταν σε 50 ml πλήρους θρεπτικού διαλύματος IMDM. Σε δύο δοχεία falcon των 50 ml προσθέτονταν από 25 ml 46% iso-osmotic Percoll. Το 46% iso-osmotic Percoll παράγονταν με καταρχήν ανάμειξη 23,125 ml Percoll (1,130 g / ml) με PBS 10x (ph 7,0) και παρασκευή έτσι του διαλύματος γνωστού ως iso-osmotic Percoll. Στη συνέχεια, από τα 25 ml του iso-osmotic Percoll που προέκυπταν και έπειτα από ελαφρά ανακίνηση, απορρίπτονταν τα 2 ml προκειμένου να φτάσουμε στον επιθυμητό όγκο των 23 ml. Εικόνα 2. A. Οι χαρακτηριστικές ζώνες που σχηματίζονται μετά τη φυγοκέντρηση (400 g / RT / 20 min) του αίματος με Ficoll-Paque Plus (1,077 g / ml) B. Το ίδιο δοχείο falcon έπειτα από τη συλλογή της υπόλευκης στοιβάδας. Picture 2. A. The characteristic zones formed after centrifugation (400 g / RT / 20 min) of blood overlayered on Ficoll-Paque Plus (1.077 g/ml) B. The same falcon tube after the extraction of the buffy coat. Τέλος, το 46% iso-osmotic Percoll προέκυπτε με την προσθήκη 27 ml πλήρους θρεπτικού υλικού IMDM στα 23 ml του iso-osmotic Percoll. Πάνω από το 46% iso- 61
62 osmotic Percoll στα δύο δοχεία falcon των 50 ml γινόταν επιστοίβαξη με 25 ml διαλύματος κυττάρων (δηλαδή με ίζημα που ήταν διαλυμένο σε πλήρες θρεπτικό υλικό IMDM) και στη συνέχεια πραγματοποιούνταν φυγοκέντρηση 550 g / 30 min / RT (εικ.3α). Γινόταν λήψη ml από κάθε λευκή ζώνη (τα λεμφοκύτταρα και τα όποια εναπομείναντα ερυθροκύτταρα καθιζάναν, ενώ τα μονοκύτταρα ήταν αυτά που σχημάτιζαν μια λευκή ζώνη ανάμεσα στις ζώνες του 46% iso-osmotic Percoll και του IMDM πλήρους) και μεταφορά τους σε νέα δοχεία falcon των 50 ml (εικ.3β). Εκεί αραιώνονταν με παγωμένο PBS 1x (που περιείχε 1 mm EDTA) προς τελικό όγκο ml. Ακολουθούσε φυγοκέντρηση 400 g / 10 min / 4 o C και απομάκρυνση του υπερκείμενου. Στο ίζημα βρίσκονταν τα απομονωμένα μονοκύτταρα. Στη συνέχεια τα μονοκύτταρα είτε διαλύονταν σε PBS 1x ή IMDM πλήρες και χρησιμοποιούνταν άμεσα σε πείραμα, είτε ακολουθούσε κρυοαποθήκευσή τους στο υγρό άζωτο. Με τη χρήση κυτταρομετρίας ροής επαληθεύτηκε ποσοστό >85% μονοκυττάρων στο τελικό δείγμα με τη βιωσιμότητα των κυττάρων να είναι >95% (βλ. παρ ). Εικόνα 3. Α. Επιστοίβαξη διαλύματος κυττάρων πάνω από 46% iso-osmotic Percoll (1,067 g / ml). B. Το ίδιο δοχείο falcon μετά τη φυγοκέντρηση (550 g / RT / 30 min). Picture 3. A. Overlayering of cells on 46% iso-osmotic Percoll (1.067 g / ml). B. The same falcon tube after centrifugation (550 g / RT / 30 min). The monocyte layer is the one situated exactly on the 25 ml mark. 62
63 1.1.2 Κρυοαποθήκευση μονοκυττάρων σε υγρό άζωτο Το ίζημα διαλύονταν καλά (προς αποφυγή συσσωματωμάτων) σε freezing medium (αποτελούμενο από 75% IMDM, 15% FCS, 10% DMSO) και μεταφέρονταν σε κατάλληλο αριθμό αμπουλών (1-2 αμπούλες ανά 30 ml ολικού αίματος). Μια ποσότητα 10 μl λαμβάνονταν προκειμένου να μετρηθεί επί τόπου ο αριθμός και η βιωσιμότητα των μονοκυττάρων με τη μέθοδο του Trypan Blue. Κατόπιν, οι αμπούλες τοποθετούνταν σε ειδικό δοχείο Mr. Frosty (NALGENE TM Cryo 1 o C Freezing Container) που περιείχε ισοπροπυλική αλκοόλη και τοποθετούνταν στους - 70 o C για 2,5-3 h (το δοχείο Mr. Frosty επιτρέπει την πτώση της θερμοκρασίας στο εσωτερικό του κατά 1 o C / min, με αποτέλεσμα τα κύτταρα να ψύχονται σταδιακά και έτσι να αυξάνονται τα ποσοστά επιβίωσής). To διμεθυλοσουλφοξείδιο (dimethyl sulfoxide, DMSO) που περιέχεται στο freezing medium, είναι αυτό που παρέχει κρυοπροστασία στα κύτταρα αποτρέποντας σε μεγάλο βαθμό το σχηματισμό ιδιαιτέρως βλαβερών παγοκρυστάλλων στο κυτταρόπλασμά τους (Branch et al, 1994). Μετά το πέρας των 2,5-3 h οι αμπούλες μεταφέρονταν σε ειδικά κάνιστρα και τοποθετούνταν στο υγρό άζωτο (δηλαδή σε θερμοκρασία -196 o C) Μέτρηση βιωσιμότητας και αριθμού μονοκυττάρων Μέτρηση βιωσιμότητας και αριθμού μονοκυττάρων με τη μέθοδο του Trypan Blue Η προαναφερθείσα ποσότητα των 10 μl κυττάρων διαλυμένων σε freezing medium αναμιγνυόταν με τη χρήση μικροπιπέττας με 10 μl Trypan Blue. To Trypan Blue είναι μια χημική ένωση που έχει την ικανότητα να διαπερνά την πλασματική μεμβράνη μόνο των νεκρών κυττάρων (και όχι των ζωντανών) με αποτέλεσμα να τα χρωματίζει μπλε. Στη συνέχεια λαμβάνονταν 10 μl από το μίγμα, τοποθετούνταν κατάλληλα υπό καλυπτρίδα σε πλάκα Neubauer (αιμοκυτταρόμετρο) και γινόταν η μέτρηση των ζωντανών κυττάρων (δηλαδή όσων δεν ήταν χρωματισμένα μπλε) με τη χρήση οπτικού μικροσκοπίου (μεγέθυνση 10x). Έπειτα από μέτρηση όλων των ζωντανών μονοκυττάρων στα τέσσερα μεγάλα τετράγωνα της πλάκας Neubauer, υπολογιζόταν ο συνολικός αριθμός τους ανά αμπούλα ή στο διάλυμα με βάση τον τύπο: (Ν/4) x 2 x 10 4 x V = αριθμός μονοκυττάρων στο δείγμα 63
64 όπου: Ν ο αριθμός των μονοκυττάρων στα 4 τετράγωνα της πλάκας Neubauer δια 4 για να βρούμε το μέσο όρο των τετραγώνων επί 2 λόγω της αραίωσης που πραγματοποιήθηκε με Trypan Blue V ο όγκος του διαλύματος (του συνολικού αρχικού εναιωρήματος κυττάρων σε ml) Μέτρηση βιωσιμότητας και αριθμού μονοκυττάρων σε κυτταρόμετρο ροής (με χρήση της φθορίζουσας ουσίας 7-AAD και αντισώματος κατά του επιφανειακού δείκτη CD14) Ο επιφανειακός υποδοχέας CD14 εκφράζεται ειδικά στα μονοκύτταρα και στα παράγωγά τους τα μακροφάγα (και σε πολύ μικρότερο βαθμό στα ουδετερόφιλα, βασεόφιλα και ηωσινόφιλα κοκκιοκύτταρα) και χρησιμεύει στα κύτταρα αυτά, κυρίως για την ανίχνευση λιποπολυσακχαριτών (lipolysaccharides, LPS), οι οποίοι είναι συστατικά των εξωτερικών κυτταρικών μεμβρανών αρνητικών κατά Gram βακτηρίων (Schutt, 1999). Η φθορίζουσα ουσία 3 7-ΑΑD (7-amino-actinomycin D) έχει την ικανότητα να διαπερνά την πλασματική μεμβράνη μόνο νεκρών κυττάρων και να συνδέεται σε περιοχές του DNA πλούσιες σε GC (γουανίνη-κυτοσίνη). Έτσι, κύτταρα από αμπούλα (έπειτα από απόψυξή τους, βλ. τμήμα 1.1.4) επωάστηκαν για 15 min στους 37 o C με αντίσωμα κατά του CD14 (αντί-cd14) που ήταν συνδεδεμένο με φυκοερυθρίνη (Phycoerythrine ή PE, διεγείρεται στα 542nm και εκπέμπει στα 575nm), καθώς και με 7-ΑΑD (όταν έχει δεσμευτεί σε τμήμα DNA διεγείρεται στα 543nm και εκπέμπει στα 655nm) και κατόπιν μετρήθηκαν σε κυτταρόμετρο ροής (Beckman Coulter EPICS XL-MCL). Με αυτό τον τρόπο ήταν δυνατό να μετρηθεί ο αριθμός των μονοκυττάρων που περιεχόταν σε μια αμπούλα (CD14+ κύτταρα), η καθαρότητα του δείγματος σε μονοκύτταρα (βρέθηκε συστηματικά >85% περιεκτικότητα σε μονοκύτταρα) και η βιωσιμότητα των κυττάρων (βρέθηκε >95% βιωσιμότητα ή με άλλα λόγια βρέθηκε συστηματικά <5% χρώση με 7-AAD) Απόψυξη μονοκυττάρων από το υγρό άζωτο Μια αμπούλα μονοκυττάρων λαμβανόταν από το υγρό άζωτο και τοποθετούνταν αμέσως στο υδατόλουτρο στους 37 o C. Προτού λιώσει εντελώς ο πάγος, τα κύτταρα διαλύονταν σε 7 ml θερμό πλήρες IMDM σε δοχείο falcon των 15 ml και ακολουθούσε φυγοκέντρηση 1500 rpm / 8 min / RT. Έπειτα από απόρριψη του 64
65 υπερκείμενου, τα κύτταρα επαναδιαλύονταν σε 3-5 ml πλήρους IMDM και ακολουθούσε μια ακόμα όμοια πλύση. Κατόπιν τα κύτταρα μπορούσαν να χρησιμοποιηθούν για πείραμα. Όπως προαναφέρθηκε (βλ. τμήμα 1.1.3), μετρήσεις σε κυτταρόμετρο ροής έδειξαν >85% καθαρότητα σε μονοκύτταρα και >95% ζωντανά κύτταρα έπειτα από απόψυξη. 1.2 Προσκόλληση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 H μέθοδος αυτή επιτρέπει τον έμμεσο προσδιορισμό του ποσοστού των μονοκυττάρων που προσκολλώνται σε υπόστρωμα λαμινίνης-1 μέσω της άμεσης ανίχνευσης της δράσης του ειδικού για τα μονοκύτταρα ενζύμου, μυελοϋπεροξειδάση (MPO, myeloperoxidase) [Verdegaal et al, 1996]. Συγκεκριμένα, η μυελοϋπεροξειδάση καταλύει τη μετατροπή της χημικής ένωσης O-dianisidine προς την οξειδωμένη της μορφή η οποία απορροφάει στα 405 nm (η αντίδραση που καταλύεται από την MPO μπορεί να γραφεί ως : Ο-dianisidine + H 2 O 2 οξειδωμένη O-dianisidine). Χρησιμοποιώντας ειδικά κυτταρικά δείγματα ελέγχου (MPO 100% controls) γίνεται η αναγωγή των τιμών δράσης της μυελοϋπεροξειδάσης (τιμές απορρόφησης προϊόντος της αναφερόμενης παραπάνω αντίδρασης) σε τιμές αριθμού κυττάρων. Πιο αναλυτικά, κατά τη μέθοδο αυτή κατάλληλη ποσότητα λαμινίνης-1 (αγορασμένη από εταιρεία) διαλυόταν σε PBS 1x (ph 7,2) προς τελική συγκέντρωση 37,5 μg/ml. Στη συνέχεια, 50μl διαλυμένης λαμινίνης-1 τοποθετούνταν σε τόσα πηγαδάκια 96άρας διαφανούς πλάκας, όσα και τα δείγματά μου. Η πλάκα αφηνόταν ελαφρώς καλυμμένη overnight σε θερμοκρασία δωματίου προκειμένου να εξατμιστεί το νερό και να μείνει μόνο η λαμινίνη-1 στα πηγαδάκια. Την επόμενη μέρα, τα μονοκύτταρα διαλύονταν κατάλληλα σε PBS 1x ώστε να είναι 10 6 / ml. Σε κάθε πηγαδάκι στο οποίο είχε τοποθετηθεί λαμινίνη-1 εναποθέτονταν από 100μl διαλύματος κυττάρων (που περιείχαν δηλαδή 10 5 κύτταρα). Παράλληλα από 100μl διαλύματος κυττάρων μεταφέρονταν σε 2-4 δοχεία eppendorf τα οποία χρησίμευαν ως ΜPO 100% controls (τα δείγματα αυτά, στο τέλος του πειράματος παρέχουν τις τιμές δράσης της μυελοϋπεροξειδάσης που θα λαμβάνονταν εάν προσκολλούνταν και τα 10 5 μονοκύτταρα και έτσι με κατάλληλη αναγωγή γίνεται ο υπολογισμός του αριθμού των μονοκυττάρων που προσκολλήθηκαν στα δείγματά μας). Σε κάθε πηγαδάκι που χρησιμοποιούνταν προσθέτονταν οι επιλεγμένοι φαρμακολογικοί αναστολείς και ακολουθούσε επώαση για 15 min / 37 o C. Στη συνέχεια προσθέτονταν 65
66 στα κατάλληλα πηγαδάκια οι ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) για 30 min / 37 o C. Μετά το πέρας της επώασης γινόταν απομάκρυνση των υπερκείμενων από τα πηγαδάκια (όπου εμπεριέχονταν τα μη προσκολλημένα κύτταρα) και κατόπιν αυτά πλένονταν μία φορά με PBS 1x (ph 6,0). H ίδια διαδικασία ακολουθούνταν για τα κύτταρα που κρατήθηκαν ως MPO 100% controls, τα οποία φυγοκεντρούνταν και πλένονταν με PBS 1x (ph 6,0). Έπειτα από την απομάκρυνση των υπερκειμένων τόσο από τα πηγαδάκια όσο και από τα MPO 100% controls, προσθέτονταν σε αυτά από 50 μl 0,5% w/v hexadecyltrimethylammonium bromide διαλυμένου σε PBS ph 6,0, προς λύση των κυττάρων. Τα δείγματα των MPO 100% controls μεταφέρονταν σε ξεχωριστά πηγαδάκια και η πλάκα επωάζονταν 30 min / 37 o C. Στο ενδιάμεσο παρασκευάζονταν 0,2 mg/ml dianisidine dihydrochloride διαλυμένο σε PBS 1x (ph 6,0) στο οποίο και γινόταν προσθήκη κατάλληλης ποσότητας H 2 O 2 ώστε η τελική του συγκέντρωση να ήταν 0,4 mm. Από αυτό το διάλυμα προσθέτονταν 50 μl σε κάθε πηγαδάκι που χρησιμοποιούνταν. Ακολουθούσε επώαση 15 min / RT με ελαφρά ανάδευση. Με την πραγματοποίηση της αντίδρασης τα δείγματα αποκτούσαν χρώμα πορτοκαλί (λόγω του προϊόντος που παράγεται από τη δράση της μυελοϋπεροξειδάσης επί της O-dianisidine). Τέλος, γινόταν μέτρηση της μυελοϋπεροξειδάσης των μονοκυττάρων μέσω της απορρόφησης των δειγμάτων στα 405 nm σε ELISA reader. 1.3 Μετανάστευση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 Η μέθοδος αυτή έγκειται στην καταρχήν προσκόλληση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 και στη συνέχεια στη μετανάστευσή τους διαμέσου του ίδιου υποστρώματος λόγω χημειοτακτικού ερεθίσματος. Συγκεκριμένα, βασίζεται στην χημειοτακτική μετανάστευση των μονοκυττάρων στην κάτω πλευρά ειδικών φίλτρων διαμέσου της λαμινίνης-1 λόγω της απουσίας του FCS (Fetal Calf Serum, ορός εμβρύου μόσχου) στο θρεπτικό τους υλικό και στην παρουσία του FCS στις κυκλικές υποδοχές που εφάπτονται με τις κάτω επιφάνειες των φίλτρων. Πιο αναλυτικά, ειδικά κυλινδρικά φίλτρα, τόσα όσα και τα δείγματά μου, τοποθετούνταν σε ειδικές υποδοχές πλάκας 24 πηγαδιών. Μέσα στα φίλτρα εναποθέτονταν από 150 μl λαμινίνης-1 20 μg / ml και αφήνονταν overnight / 4 ο C. Την επόμενη μέρα, απομακρυνόταν με προσοχή (προκειμένου να μη διαταραχθεί η καθιζάνουσα λαμινίνη-1) το όποιο υπερκείμενο είχε απομείνει στα φίλτρα και προσθέτονταν σε 66
67 αυτά από 150 μl BSA 0,5% w/v (bovine serum albumin, αλβουμίνη ορού βοοειδούς) προκειμένου να δεσμευτούν και οι λιγοστές περιοχές των φίλτρων που δεν είχαν καλυφθεί με λαμινίνη-1 διότι δεν θέλαμε τα μονοκύτταρα να περάσουν με τη ροή του υγρού διαμέσου των οπών των φίλτρων). Ακολουθούσε επώαση σε κλίβανο για 1 h / 37 ο C προκειμένου να επιτευχθεί η προσκόλληση των μονοκυττάρων στη λαμινίνη-1 και κατόπιν γινόταν απομάκρυνση των υπερκειμένων. Στις κυκλικές υποδοχές της πλάκας 24 πηγαδιών (bottom chambers) προσθέτονταν 500 μl IMDM πλήρες (που περιείχε 10% FCS), ενώ μέσα στα φίλτρα τοποθετούνταν 250 μl εναιωρήματος μονοκυττάρων (2 x 10 6 μονοκύτταρα / ml) σε IMDM σκέτο (που δεν περιείχε 10% FCS). Μέσα στα φίλτρα προσθέτονταν οι επιλεγμένοι φαρμακολογικοί αναστολείς για 15 min / 37 o C και κατόπιν οι ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) και ακολουθούσε επώαση για 30 min / 37 o C. Στη συνέχεια, με μικροπιπέττα αφαιρούνταν από τα φίλτρα τα υπερκείμενα και με μπατονέττες εμποτισμένες με PBS 1x (ph 7,0) αφαιρούνταν τα κύτταρα που είχαν μείνει στην άνω επιφάνεια των φίλτρων και άρα δεν είχαν μεταναστεύσει. Κατόπιν, γινόταν μονιμοποίηση και χρώση των μονοκυττάρων που βρίσκονταν στην κάτω επιφάνεια των φίλτρων (και άρα είχαν μεταναστεύσει) με το Hemacolor Staining Kit (Merck) σύμφωνα με τις οδηγίες του κατασκευαστή. Συγκεκριμένα, τα φίλτρα με τα κύτταρα εμποτίζονταν σε ένα διάλυμα μονιμοποίησης, κατόπιν σε ένα διάλυμα που περιείχε την ερυθρή χρωστική εωσίνη Υ και τέλος σε ένα διάλυμα που περιείχε τη χρωστική azure B. Έπειτα από αφαίρεση του IMDM πλήρους από τις κυκλικές υποδοχές της πλάκας 24 πηγαδιών, τα φιλτράκια επανατοποθετούνταν σε αυτές και στις υποδοχές προσθέτονταν από 200 μl οξικό οξύ 10% προκειμένου να λυθούν τα κύτταρα και να διαλυθεί το σύμπλοκο των δύο χρωστικών (εωσίνη Υ και azure B) που κατακρατήθηκε από αυτά. Η πλάκα 24 πηγαδιών ανακινούνταν για 3-4 min στον αναδευτήρα και στη συνέχεια τα περιεχόμενα των κυκλικών υποδοχών μεταφέρονταν σε ξεχωριστά πηγαδάκια πλάκας 96 πηγαδιών διαφανούς πλάκας. Τέλος, σε ELISA reader γινόταν η μέτρηση της απορρόφησης των δειγμάτων σε μήκος κύματος 590nm [Hussein and Taylor, 2002]. Όσο μεγαλύτερες οι τιμές, τόσο μεγαλύτερος ο αριθμός των μονοκυττάρων που μετανάστευσαν. 67
68 1.4 Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD36 Ο προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD36 γινόταν μέσω μιας διαδικασίας ανοσοφθορισμού (Coons, 1960; Koliakos et al, 2004). Τα κύτταρα διαλύονταν σε πλήρες θρεπτικό υλικό IMDM και μοιράζονταν ισόποσα σε τόσα σωληνάκια falcon των 15ml όσα και τα δείγματά μας. Ακολουθούσε φυγοκέντρηση, απόρριψη των υπερκείμενων και επαναδιάλυση των κυττάρων που βρίσκονται στο ίζημα σε PBS 1x. Ακολουθούσε άλλη μία όμοια πλύση με PBS 1x και τα κύτταρα επωάζονταν πρώτα με τους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν με τους ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) για 30 min / 37 o C. Φυσικά διατηρούνταν και τα απαραίτητα δείγματα ελέγχου (controls) στα οποία δεν γινόταν καμία επίδραση. Στη συνέχεια κάθε δείγμα επωάζονταν με 10 μl αντισώματος anti-cd36 (mouse anti-human IgM, 0,1 mg/ml) που ήταν συνδεδεμένο με τη φθορίζουσα ουσία FITC (Fluorescein Isothiocyanate) για 10 min / 37 o C στο σκοτάδι. Έπειτα από τρεις πλύσεις με PBS 1x προς απομάκρυνση της περίσσειας του αντισώματος, τα δείγματα μεταφέρονταν διαδοχικά σε κυψελίδα από χαλαζία και πραγματοποιούνταν μέτρηση σε φθορισμόμετρο (Shimadzu RF-5000) με τιμή διέγερσης (excitation) 495nm και τιμή εκπομπής (emission) στα 525nm. 1.5 Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD68, CD49b, CD29, CD18, CD11a και CD11b Προσδιορισμός σε φθορισμόμετρο Ο προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD49b, CD29, CD18, CD11a και CD11b (όχι όμως του CD68) έγινε καταρχήν σε φθορισμόμετρο (LS-55 Perkin-Elmer fluorescence spectrometer) με μεθοδολογία παρόμοια με αυτή που χρησιμοποιήθηκε παραπάνω για την ανίχνευση των επιπέδων του υποδοχέα CD36. Συγκεκριμένα, τα κύτταρα διαλύονταν σε πλήρες θρεπτικό υλικό IMDM και μοιράζονταν ισόποσα σε τόσα σωληνάκια falcon των 15ml όσα και τα δείγματά μας. Ακολουθούσε φυγοκέντρηση, απόρριψη των υπερκείμενων και επαναδιάλυση των κυττάρων που βρίσκονται στο ίζημα σε PBS 1x. Ακολουθούσε άλλη μία όμοια πλύση με PBS 1x και τα κύτταρα επωάζονταν με τον ενεργοποιητή (στην προκειμένη περίπτωση, λεπτίνη) σε διάφορες συγκεντρώσεις για 30 min / 37 o C. Φυσικά διατηρούνταν και τα απαραίτητα δείγματα ελέγχου (controls) στα οποία δεν γινόταν καμία επίδραση. Στη συνέχεια, τα αντίστοιχα δείγματα επωάζονταν με anti-cd49b 68
69 (mouse anti-human IgG1, 0,1 mg/ml), anti-cd29 (mouse anti-human IgG1, 0,1 mg/ml), anti-cd18 (rat anti-human IgG2b, 0,1 mg/ml), anti-cd11b (mouse antihuman IgG1, 0,1 mg/ml) που ήταν συνδεδεμένα με τη φθορίζουσα ουσία FITC (Fluorescein Isothiocyanate) και anti-cd11a (mouse anti-human IgG2a, 0,1 mg/ml) που ήταν συνδεδεμένο με τη φθορίζουσα ουσία RPE (R-Phyco-Erythrin) για 10 min / 37 o C στο σκοτάδι υπό ανακίνηση. Έπειτα από τρεις πλύσεις με PBS 1x προς απομάκρυνση της περίσσειας του αντισώματος, τα δείγματα μεταφέρονταν σε αντίστοιχα πηγαδάκια μαύρης πλάκα (ειδικής για μετρήσεις φθορισμού) στο φθορισμόμετρο σε τιμή διέγερσης (excitation) 495nm και τιμή εκπομπής (emission) στα 525nm προς ανίχνευση της FITC και τιμή διέγερσης (excitation) 542nm και τιμή εκπομπής (emission) στα 575nm προς ανίχνευση της RPE Προσδιορισμός με κυτταρομετρία ροής Τα αποτελέσματα επιβεβαιώθηκαν και με χρήση κυτταρομετρίας ροής (ταυτόχρονα εδώ χρησιμοποιήθηκε και το αντίσωμα για την πρωτεΐνη CD68). Καταρχήν, τα κύτταρα διαλύονταν σε πλήρες θρεπτικό υλικό IMDM και μοιράζονταν ισόποσα σε τόσα σωληνάκια falcon των 15ml όσα και τα δείγματά μας. Ακολουθούσε φυγοκέντρηση, απόρριψη των υπερκείμενων και επαναδιάλυση των κυττάρων που βρίσκονται στο ίζημα σε PBS 1x. Ακολουθούσε άλλη μία όμοια πλύση με PBS 1x, τα κύτταρα μεταφέρονταν σε σωληνάκια RIA (radioimmunoassay tubes, χρησιμοποιούνται μεταξύ των άλλων για μετρήσεις σε κυτταρόμετρο ροής) και επωάζονταν με τον ενεργοποιητή (στην προκειμένη περίπτωση, τη λεπτίνη) για 30 min / 37 o C. Φυσικά διατηρούνταν και τα απαραίτητα δείγματα ελέγχου (controls) στα οποία δεν γινόταν καμία επίδραση. Στη συνέχεια, τα αντίστοιχα δείγματα επωάζονταν με 10 μl αντισώματος anti-cd68 (mouse anti-human IgG1, 0,1 mg/ml), anti-cd49b (mouse anti-human IgG1, 0,1 mg/ml), anti-cd29 (mouse anti-human IgG1, 0,1 mg/ml), anti-cd18 (rat anti-human IgG2b, 0,1 mg/ml), anti-cd11b (mouse antihuman IgG1, 0,1 mg/ml) που ήταν συνδεδεμένα με τη φθορίζουσα ουσία FITC (Fluorescein Isothiocyanate) και anti-cd11a (mouse anti-human IgG2a, 0,1 mg/ml) που ήταν συνδεδεμένο με τη φθορίζουσα ουσία RPE (R-Phyco-Erythrin) για 10 min / 37 o C στο σκοτάδι υπό ανακίνηση. Τα σωληνάκια RIA που περιείχαν τα δείγματα τοποθετούνταν σε καρουζέλ (εξάρτημα κυτταρομέτρου ροής με ειδικές θήκες για σωληνάκια RIA) και πραγματοποιούνταν εν συνεχεία οι μετρήσεις σε κυτταρόμετρο 69
70 ροής (Beckman Coulter EPICS XL-MCL) στα κατάλληλα φίλτρα μήκους κύματος ανάλογα με τη φθορίζουσα ουσία που χρησιμοποιούνταν. Οι μετρήσεις πραγματοποιούνταν μέχρι τη μέτρηση κυττάρων (events). 1.6 Προσδιορισμός επιπέδων φαγοκύττωσης οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας (oxidized low-density lipoproteins, oxldls) Παρασκευή οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας (oxldls) Παράχθηκαν δύο τύποι οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας (oxldls), οι oxldl 3 και οι oxldl 24, οι οποίες στη συνέχεια σημάνθηκαν με τη φθορίζουσα ουσία DiI (1,1 -dioctadecyl-3,3,3,3 -tetramethyl-indocarbocyanine perchlorate) [Stephan and Yurachek, 1993; Itabe et al, 2003]. Οι oxldl 3 χαρακτηρίζονται ως μετρίως οξειδωμένες LDLs, ενώ οι oxldl 24 ως πλήρως οξειδωμένες LDLs. Οι oxldl 3 παράχθηκαν μέσω οξείδωσης λιποπρωτεϊνών χαμηλής πυκνότητας (LDLs, συγκέντρωσης 0,2 mg / ml) με 5 μμ CuSO 4 διαλυμένο σε PBS 1x (ph 7,0) για 3 h / 37 o C. Αντίστοιχα, οι oxldl 24 παράχθηκαν μέσω οξείδωσης λιποπρωτεϊνών χαμηλής πυκνότητας (LDLs, συγκέντρωσης 2 mg/ml) με 50 μμ CuSO 4 διαλυμένο σε PBS 1x (ph 7,0) για 24 h / 37 o C. Και στις δύο περιπτώσεις οι αντιδράσεις διακόπτονταν με την προσθήκη υδατικού διαλύματος EDTA ώστε η τελική συγκέντρωσή του να ήταν 250 μμ. Κατόπιν γινόταν σήμανση και των δύο τύπων oxldls με την φθορίζουσα ουσία DiI. Αυτό γινόταν με επώαση DiI (100 mg / ml) με τους δύο τύπους των οxldls σε αναλογία 300 μg : 1 mg αντίστοιχα για 18 h / 37 o C, ακολουθούμενο από τρεις διαδοχικές διαπιδύσεις των 24 h σε PBS 1x (ph 7,0) / 4 o C, ολοκληρώνοντας με πέρασμα από φίλτρο ειδικό για σύριγγες με οπές διαμέτρου 0,22 μm. Στο τέλος γινόταν μέτρηση της συγκέντρωσης των DiI-oxLDL με τη μέθοδο Bradford και αυτές ήταν πλέον έτοιμες προς χρήση σε πείραμα Πείραμα φαγοκύττωσης των oxldls από μονοκύτταρα Τα μονοκύτταρα διαλύονταν σε θρεπτικό υλικό IMDM που δεν περιείχε FCS και επωάζονταν για 15 min / 37 o C με τους φαρμακολογικούς αναστολείς που είχαν επιλεγεί. Στη συνέχεια προσθέτονταν στα δείγματα ταυτόχρονα οι ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) και DiI-oxLDLs (είτε DiI-oxLDL 3, είτε DiIoxLDL 24, ανάλογα με το σκεπτικό του πειράματος) και γινόταν επώαση για 1 h, 3 h, 5 h / 37 o C. Ακολουθούσαν τρεις πλύσεις των δειγμάτων με PBS 1x (ph 7,0) 70
71 προκειμένου να απομακρυνθεί η περίσσεια των DiI-oxLDLs. Κατόπιν, τα δείγματα μεταφέρονταν σε δόσεις των 200 μl σε πηγαδάκια μαύρης (ειδικής για μετρήσεις φθορισμού) πλάκας ELISA 96 πηγαδιών. Τέλος, ο υπολογισμός των επιπέδων φαγοκύττωσης των oxldls γινόταν με ανίχνευση του φθορισμού της φθορίζουσας ουσίας DiI με την οποία είχαν σημανθεί σε φθορισμόμετρο (LS-55 Perkin-Elmer fluorescence spectrometer) με τιμή διέγερσης (excitation) 520nm και τιμή εκπομπής (emission) στα 578 nm. 1.7 Προσδιορισμός τιμής ενδοκυτταρικού ph (phi) Για τον προσδιορισμό του ενδοκυτταρικού ph μονοκυττάρων εφαρμόστηκε σε τροποποιημένη μορφή η μέθοδος των Incerpi et al, Συγκεκριμένα, αυτή η μέθοδος αφορά τη χρήση της ουσίας BCECF-AM (Bis-(carboxyethyl)-5(6)-carboxyfluorescein acetoxymethylester, διεγείρεται στα 495nm και εκπέμπει στα nm). Η μη φθορίζουσα ουσία ΒCECF-AM μπορεί και διαπερνά εύκολα την πλασματική μεμβράνη των κυττάρων όπου και υδρολύεται από κυτταροπλασματικές εστεράσες προς το φθορίζον παράγωγό της, το BCECF. Αυτό πλέον δεν μπορεί να διαπεράσει την πλασματική μεμβράνη με αποτέλεσμα να συσσωρεύεται μέσα στα κύτταρα. Όσο πιο αλκαλικό είναι το ενδοκυτταρικό ph, τόσο μεγαλύτερες τιμές φθορισμού παρέχει το BCECF. Κατά τη διάρκεια του πειράματος παρασκευάστηκαν τρία διαλύματα που περιείχαν 130 mm KCl, 1 mm MgCl 2, 30 mm Hepes διαλυμένα σε 100 ml dh 2 O. Τα ph τους ρυθμίστηκαν στις τιμές 6,7, 7,0 και 7,3 αντίστοιχα. Τα διαλύματα αυτά θα χρησιμοποιούνταν στη συνέχεια για τη δημιουργία της πρότυπης καμπύλης phi φθορισμού (χρησιμεύει για τη μετάφραση των τιμών φθορισμού προς τιμές phi). Παράλληλα, παρασκευάστηκαν τα διαλύματα όπως φαίνονται στον πίνακα 1. Συγκεκριμένα, το ιωδοξικό Na παρεμποδίζει τη γλυκόλυση (συγκεκριμένα, παρεμποδίζει την οξείδωση της γλυκεριναλδεϋδης-3-ρ προς γλυκερινικό οξύ-1-p-3-p από το ένζυμο δεϋδρογονάση της 3-φωσφορικής γλυκεριναλδεϋδης, γνωστό και ως GAPDH), το DIDS αναστέλλει τον ιοντοανταλλάκτη HCO - 3 /Cl - (γνωστός και ως ανιονικός ανταλλάκτης-1, anion exchanger-1, AE1 ή/και Band 3) και η μεθαζολαμίδη αναστέλλει το ένζυμο καρβονική ανυδράση (το οποίο καταλύει την αντίδραση: CO 2 + H 2 O HCO H + ) (Gray et al., 1958; Sabri & Ochs, 1971; Salhany, 1996). Προστέθηκαν προκειμένου η οποιαδήποτε μεταβολή του phi να οφείλεται στη δράση του NHE1και μόνο (και όχι σε κάποιο άλλο phi-ρυθμιστικό σύστημα). Όσον αφορά 71
72 τη νιγερισίνη, πρόκειται για ένα ιονοφόρο που ανοίγει κανάλια ιόντων K + /H + στα κύτταρα με τελικό αποτέλεσμα το ενδοκυτταρικό ph να εξισώνεται με το εξωκυτταρικό ph, δηλαδή το ph του ρυθμιστικού μας διαλύματος. Η νιγερισίνη είναι απαραίτητη για τη χάραξη της πρότυπης καμπύλης phi-φθορισμού (Thomas et al, 1979). Ουσία Διαλύτης Ποσότητα oυσίας Ποσότητα διαλύτη Συγκέντρωση oυσίας στο διάλυμα Ιωδοξικό Na dh 2 O 0,062 g 1 ml 300 mm Υδατικό δ/μα 0,025 g 1 ml 50 mm DIDS NaHCO 3 0,1M ph 8,0 Μεθαζολαμίδη DMSO 0,028 g 1 ml 120 mm 5% DMSO 1 mg 1 ml 1 mg/ml BCECF-AM 95% dh 2 O Νιγερισίνη DMSO 5 mg 1 ml 6,7 mm Πίνακας 1. Υπόλοιπα διαλύματα για μέτρηση του ενδοκυτταρικού ph. Table 1. Other solutions necessary for measuring intracellular ph (phi). Τέλος, παρασκευάστηκε και ένα υδατικό διάλυμα (διάλυμα ph 7,3 + NaCl, 200 ml) που περιείχε 135 mm NaCl, 5 mm KCl, 1 mm CaCl 2, 5 mm γλυκόζη, 1 mm MgCl 2 και 20 mm Hepes. Έπειτα από δύο πλύσεις με το διάλυμα ph 7,3 + NaCl, τα κύτταρα επωάζονταν με 10 μμ BCECF-AM στο ίδιο διάλυμα για 30 min στους 37 ο C στο σκοτάδι. Ακολουθούσαν τρεις πλύσεις με διάλυμα ph 7,3 + NaCl υπό όσο το δυνατόν πιο σκοτεινές συνθήκες, προκειμένου να απομακρυνθεί το περισσευούμενο BCECF-AM (η ποσότητα που δεν εισήλθε στα κύτταρα). Στη συνέχεια τα κύτταρα ισομοιράζονταν σε ποσότητες των 3 ml σε κατάλληλο αριθμό δοχείων falcon των 15 ml και όλα πλην τριών επωάζονταν για 15min / 37 ο C με τους αναστολείς των phiρυθμιστικών μηχανισμών (300 mm ιωδοξικό Na, 50 mm DIDS, 120 mm μεθαζολαμίδη προσθέτονταν και στο δείγμα ελέγγχου), καθώς και με τους επιλεγμένους φαρμακολογικούς αναστολείς (εδώ 20 nm cariporide). Κατόπιν, τα κύτταρα επωάζονταν για 30 min / 37 ο C με τον διεγέρτη που στην προκειμένη περίπτωση ήταν η λεπτίνη σε διάφορες συγκεντρώσεις. Στο ενδιάμεσο, στα τρία 72
73 δοχεία falcon των 15 ml που είχαν κρατηθεί πραγματοποιούνταν από δύο πλύσεις με τα διαλύματα των ph 6,7, 7,0 και 7,3 αντίστοιχα και κατόπιν προσθέτονταν 13 μμ νιγερισίνης και επωάζονταν για 15 min στο σκοτάδι σε RT. Τέλος, τα δείγματα μεταφέρονταν σε κυψελίδα από χαλαζία (quartz cuvette) και υπό συνεχή ανάδευση γινόταν μέτρηση σε φθορισμόμετρο (Shimadzu RF-5000) πρώτα των τριών δειγμάτων της πρότυπης καμπύλης και εν συνεχεία των πειραματικών δειγμάτων σε εναλλασσόμενες τιμές διέγερσης (excitation) 495nm (τιμή ευαίσθητη στο phi) και 440nm (τιμή ευαίσθητη στον αριθμό των κυττάρων) με σταθερή τιμή εκπομπής (emission) στα 530 nm. Τα αποτελέσματα εξάγονταν από τον λόγο των μετρήσεων φθορισμού 495nm / 440nm υπό την ίδια τιμή εκπομπής των 530nm και στη συνέχεια μέσω της πρότυπης καμπύλης μετατρέπονταν σε τιμές ενδοκυτταρικού ph. 1.8 Προσδιορισμός ελευθέρων ριζών με H 2 DCFDA Με τη χρήση της φθορίζουσας ουσίας H 2 DCFDA (2',7'-dichlorodihydrofluorescein diacetate) πραγματοποιείται ένας γενικός προσδιορισμός της συνολικής παραγωγής H 2 O 2 και ελευθέρων ριζών οξυγόνου (π.χ. ΟΗ., ROO., αλλά όχι Ο -. 2 ), αλλά και αζώτου (ΝΟ., ONOO - ) (Rothe & Valet, 1990; Gomes et al., 2005). Τα κύτταρα διαλύονταν σε πλήρες θρεπτικό υλικό IMDM και ακολουθούσε φυγοκέντρηση, απόρριψη των υπερκείμενων και επαναδιάλυση των κυττάρων που βρίσκονται στο ίζημα σε PBS 1x. Ακολουθούσε άλλη μία όμοια πλύση με PBS 1x και τα κύτταρα φορτώνονταν με τη φθορίζουσα ουσία H 2 DCFDA (C τελ 5 μg/ml) για 20 min / 37 o C στο σκοτάδι. Κατόπιν τα δείγματα φυγοκεντρούνταν, τα υπερκείμενα απορρίπτονταν και η διαδικασία αυτή επαναλαμβανόταν άλλες δύο φορές με PBS 1x προκειμένου να απομακρυνθεί η περίσσεια της φθορίζουσας ουσίας που δεν εισήλθε στα κύτταρα. Στη συνέχεια τα κύτταρα μοιράζονταν ισόποσα σε τόσα σωληνάκια falcon των 15 ml ή δοχεία eppendorf όσα και τα δείγματά μας. Έπειτα από επώαση με τους φαρμακολογικούς αναστολείς για 15 min / 37 o C στο σκοτάδι, τα κύτταρα εν συνεχεία επωάζονταν με τους ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) για 30 min / 37 o C πάλι στο σκοτάδι. Παράλληλα, διατηρούνταν και τα απαραίτητα δείγματα ελέγχου (controls) στα οποία δεν γινόταν καμία επίδραση. Κατόπιν τα δείγματα πλένονταν δύο φορές με PBS 1x και σε δόσεις των 200 μl μεταφέρονταν σε πηγαδάκια μαύρης (ειδικής για μετρήσεις φθορισμού) 96άρας πλάκας ELISA (96 πηγαδιών). Τα δείγματα μετρούνταν σε φθορισμόμετρο (LS-55 Perkin-Elmer 73
74 fluorescence spectrometer) με τιμή διέγερσης (excitation) 498nm και τιμή εκπομπής (emission) στα 522nm. 1.9 Προσδιορισμός του ανιόντος σουπεροξειδίου Προσδιορισμός του ανιόντος σουπεροξειδίου με NBT Επιχειρήθηκε μέτρηση της παραγωγής ανιόντων σουπεροξειδίου (Ο -. 2 ) όπως αυτά μετρούνται με την ουσία ΝΒΤ (Nitro Blue Tetrazolium). Η όλη διαδικασία αποτελεί τροποποίηση προηγούμενης μεθόδου (Müller et al. 1989). Η αρχή της μεθόδου βασίζεται στην αναγωγή του ΝΒΤ από ανιόντα σουπεροξειδίου προς το παράγωγό του diformazan, του οποίου η παραγωγή μπορεί στη συνέχεια να μετρηθεί ως οπτική απορρόφηση σε φωτόμετρο. Τα κύτταρα ( 10 6 κύτταρα/ml) μοιράζονταν ισόποσα σε τόσα σωληνάκια falcon των 15 ml (1 ml στο καθένα) ή δοχεία eppendorf όσα και τα δείγματά μας. Έπειτα από επώαση με τους φαρμακολογικούς αναστολείς για 15 min / 37 o C στο σκοτάδι, τα κύτταρα εν συνεχεία επωάζονταν με τους ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) για 30 min / 37 o C πάλι στο σκοτάδι. Ακολουθούσε φυγοκέντρηση 1500 rpm / 10 min, απομάκρυνση του υπερκειμένου και κατόπιν σε κάθε δείγμα προσθέτονταν 200 μl υδατικού διαλύματος NBT (1 mg/ml). Σε ένα κενό δοχείο falcon προσθέτονταν επίσης 200 μl ΝΒΤ και διατηρούνταν στο σκοτάδι ώστε στο τέλος να χρησιμοποιηθεί ως τυφλό. Τα δείγματα επωάζονταν 1,5-2 h / 37 ο C στο σκοτάδι και κατόπιν φυγοκεντρούνταν 1500 rpm / 10 min και τα υπερκείμενα απομακρύνονταν. Σε κάθε δείγμα προσθέτονταν από 500 μl TBS (Tris-buffered saline, παρασκευάζονταν ως εξής: σε 50 ml υδατικού διαλύματος Tris 0,05 Μ προσθέτονταν πρώτα HCl 0,05 M μέχρι τελικού ph 7,6 και στη συνέχεια 2 g NaCl και τέλος συμπληρωνόταν με dη 2 O έως τελικού όγκου 100ml) και εν συνεχεία γινόταν φυγοκέντρηση 1500 rpm / 10 min και απόρριψη των υπερκειμένων. Ακολουθούσε προσθήκη 500 μl μεθανόλης 100% με ελαφρά ανάδευση με μικροπιπέττα. Σε αυτό το στάδιο γινόταν μέτρηση της συγκέντρωσης πρωτεΐνης σε κάθε δείγμα με τη χρήση της μεθόδου του BCA. Ακολουθούσε πάλι φυγοκέντρηση 1500 rpm / 10 min, απόρριψη των υπερκειμένων, προσθήκη 500 μl μεθανόλης 50% αυτή τη φορά και φυγοκέντρηση ξανά. Μετά το πέρας της φυγοκέντρησης, τα υπερκείμενα απομακρύνονταν και τα δοχεία falcon με τα δείγματα αφήνονταν χωρίς καπάκια προκειμένου να εξατμιστεί η μεθανόλη. Τέλος, σε κάθε δείγμα προσθέτονταν από 270 ml ΚΟΗ 2Μ και 345 μl DMSO και επωάζονταν 30 min / RT 74
75 σε σχετικά σκοτεινές συνθήκες. Η παραγωγή του diformazan αναγνωρίζεται από την ένταση του γαλάζιου χρώματος που παρατηρούνταν στα δείγματα. Η μέτρηση γινόταν σε φωτόμετρο σε μήκος κύματος 620nm και αφού πρώτα πραγματοποιούνταν καλιμπράρισμά του με το τυφλό (200 μl NBT 1 mg/ml) που είχε διατηρηθεί Προσδιορισμός του ανιόντος σουπεροξειδίου με DHE Με τη χρήση της φθορίζουσας ουσίας διυδροαιθίδιο (dihydroethidium, DHE), γινόταν η μέτρηση της παραγωγής του ανιόντος σουπεροξειδίου (Ο -. 2 ) (Peshavariya et al, 2007). Λόγω της ευκολίας με την οποία η ουσία αυτή οξειδώνεται στον αέρα, ο χειρισμός της γινόταν υπό ατμόσφαιρα αργού (Ar). Τα κύτταρα διαλύονταν σε πλήρες θρεπτικό υλικό IMDM και ακολουθούσε φυγοκέντρηση, απόρριψη των υπερκείμενων και επαναδιάλυση των κυττάρων που βρίσκονται στο ίζημα σε PBS 1x. Ακολουθούσε άλλη μία όμοια πλύση με PBS 1x και τα κύτταρα φορτώνονταν με τη φθορίζουσα ουσία DHE (C τελ 25 μm) για 20 min / 37 o C στο σκοτάδι. Κατόπιν τα δείγματα φυγοκεντρούνταν, τα υπερκείμενα απορρίπτονταν και η διαδικασία αυτή επαναλαμβανόταν άλλες δύο φορές με PBS 1x προκειμένου να απομακρυνθεί η περίσσεια της φθορίζουσας ουσίας που δεν είχε εισέλθει στα κύτταρα. Στη συνέχεια τα κύτταρα μοιράζονταν ισόποσα σε τόσα σωληνάκια falcon των 15 ml ή δοχεία eppendorf όσα και τα δείγματά μας. Έπειτα από επώαση με τους φαρμακολογικούς αναστολείς για 15 min / 37 o C στο σκοτάδι, τα κύτταρα εν συνεχεία επωάζονταν με τους ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) για 30 min / 37 o C πάλι στο σκοτάδι. Παράλληλα, διατηρούνταν και τα απαραίτητα δείγματα ελέχου (controls) στα οποία δεν γινόταν καμία επίδραση. Κατόπιν, τα δείγματα πλένονταν δύο φορές με PBS 1x και σε δόσεις των 200 μl μεταφέρονταν σε πηγαδάκια μαύρης (ειδικής για μετρήσεις φθορισμού) 96άρας πλάκας ELISA. Τα δείγματα μετρούνταν σε φθορισμόμετρο (LS-55 Perkin-Elmer fluorescence spectrometer) με τιμή διέγερσης (excitation) 490nm και τιμή εκπομπής (emission) στα 567nm (Zhao et al, 2005) Προσδιορισμός δραστικότητας της δισμουτάσης του σουπεροξειδίου (SOD) Η δισμουτάση του σουπεροξειδίου (SOD, superoxide dismutase) είναι ένα ένζυμο υπεύθυνο για την εξουδετέρωση του επιβλαβούς για το κύτταρο ανιόντος σουπεροξειδίου (O -. 2 ). Καταλύει την αντίδραση: 2O H + H 2 O 2 + O 2 (Hancock 75
76 et al. 2001), δηλαδή τη μετατροπή του ανιόντος σουπεροξειδίου προς το λιγότερο τοξικό υπεροξείδιο του υδρογόνου. Συγκεκριμένα, η πειραματική διαδικασία βασιζόταν στην μετατροπή της χημικής ένωσης WST-1 (4-[3-(4-iodophenyl)-2-(4- nitrophenyl)-2h-5-tetrazolio]-1,3-benzene disulfonate ή πιο σύντομα water soluble tetrazolium salt) προς το WST-1 formazan, το οποίο απορροφάει ικανοποιητικά στα 450nm και συνεπώς η παραγωγή του μπορεί να μετρηθεί και να ποσοτικοποιηθεί (Peskin & Winterbourn, 2000). Η μετατροπή πραγματοποιούνταν με τη μεσολάβηση ανιόντων σουπεροξειδίου που παράγονταν λόγω της οξείδωσης της ξανθίνης (ή όπως εδώ του παραγώγου της, υποξανθίνης) από το ένζυμο οξειδάση της ξανθίνης προς ουρικό οξύ και υπεροξείδιο του υδρογόνου. Αναστολή της SOD αύξανε τη συγκέντρωση των ανιόντων σουπεροξειδίου με αποτέλεσμα μεγαλύτερη παραγωγή WST-1 formazan. Έτσι με την ανίχνευση του WST-1 formazan γινόταν ο υπολογισμός τη αναστολής της SOD στα πειραματικά δείγματα, ενώ με τη βοήθεια πρότυπης καμπύλης υπολογιζόταν η δραστικότητά της σε U/ml. Στην εικόνα 6 φαίνεται η βασική αρχή της πειραματικής διαδικασίας με την οποία προσδιοριζόταν η επίδραση αναστολέων και ενεργοποιητών στη δραστικότητα της δισμουτάσης του σουπεροξειδίου. Συγκεκριμένα όσον αφορά την πειραματική διαδικασία, τα μονοκύτταρα διαλύονταν σε PBS 1x (ph 7,0) και ακολούθως πλένονταν δύο φορές (φυγοκέντρηση, απόρριψη υπερκειμένου, επαναδιάλυση) με το ίδιο διάλυμα. Σε αυτό το στάδιο γινόταν μέτρηση της ζωτικότητας και του αριθμού των μονοκυττάρων με τη μέθοδο του Trypan Blue. Στη συνέχεια τα μονοκύτταρα ισομοιράζονταν σε τόσα σωληνάκια falcon των 15ml όσα και τα πειραματικά μας δείγματα και εκεί γινόταν επίδραση πρώτα με τους φαρμακολογικούς αναστολείς που είχαν επιλεγεί για 15 min / 37 o C και στη συνέχεια με τους ενεργοποιητές (στην προκειμένη περίπτωση, λεπτίνη) για 30 min / 37 o C. 76
77 Εικόνα 4. Βασική αρχή μεθόδου προσδιορισμού δραστικότητας της SOD (ΟΞ, οξειδάση της ξανθίνης). Picture 6. Basic principle of the superoxide dismutase (SOD) activity assay (ΟΞ, xanthine oxidase). Έπειτα από μία πλύση με παγωμένο PBS 1x, το ίζημα των κυττάρων του κάθε δείγματος επαναδιαλυόταν με διάλυμα λύσης 1x (lysis buffer 1% Nonidet P-40, 0,5% δεοξυχολικό οξύ, 0,05% SDS, 50 mm Tris-HCl (ph 8.0), 150 mm NaCl, 3 mm KCl, 1 mm EDTA) στο οποίο είχαν προστεθεί οι απαραίτητοι αναστολείς πρωτεασών [10 μg / ml απροτινίνη, 10 μg / ml λευπεπτίνη, 1 mm PMSF]). Η αναλογία που χρησιμοποιούνταν ήταν 500 μl διαλύματος λύσης 1x / 10 6 κύτταρα. Αμέσως (και με καλή ανάδευση με τη μικροπιπέττα) γινόταν μεταφορά των δειγμάτων σε σωληνάκια eppendorf και επωάζονταν στον πάγο για 20 min προκειμένου να ολοκληρωθεί η λύση των κυττάρων. Έπειτα από φυγοκέντρηση g / 10 min / 4 o C, τα υπερκείμενα μεταφέρονταν σε νέα σωληνάκια eppendorf. Σε 96άρα διαφανή πλάκα προσθέτονταν σε πηγαδάκια πρώτα από 20 μl από τα standards που θα χρησίμευαν για τη χάραξη της πρότυπης καμπύλης και σε χωριστά πηγαδάκια από 20 μl από τα δείγματά μας. Τα standards παρασκευάζονταν από πριν με καταρχήν διάλυση 26,67 μl bovine Cu, ZnSOD (7,5 ku/ml) σε 973,33 μl διαλύματος buffer 100 mm KH 2 PO 4 (ph 7,5, ρυθμίζεται με KOH) έτσι ώστε να παραχθεί 1 ml διαλύματος 200 U/ml bovine Cu, ZnSOD. Με συνεχόμενες αραιώσεις με buffer 100 mm KH 2 PO 4 (ph 7,5) παρασκευάζονταν και τα υπόλοιπα standards (πέραν αυτού των 200 U/ml) των 100 U/ml, 50 U/ml, 25 U/ml, 10 U/ml, 5 U/ml, 1 U/ml, 0,1 U/ml, 0,05 U/ml, 0,01 U/ml, 0,001 U/ml και 0 U/ml (μόνο διάλυμα buffer 100 mm KH 2 PO 4 ). Στη συνέχεια της πειραματικής διαδικασίας παρασκευάζονταν τα τρία απαραίτητα δείγματα ελέγχου 77
78 (controls) και προσθέτονταν σε χωριστά πηγαδάκια. Τα δείγματα ελέγχου ήταν το blank (χωρίς SOD, με WST-1, χωρίς οξειδάση της ξανθίνης) και το Α (χωρίς SOD, με WST-1, με οξειδάση της ξανθίνης [μέγιστη τιμή]). Κατόπιν, παρασκευάζονταν το μείγμα αντιδραστηρίων (σε 19,3 ml assay buffer [50 mm Tris-HCl, ph 8.0, 0,1 mm Diethylene triamine-penta-acetic acid ή DTPA, 0.1 mm υποξανθίνη], προσθέτονταν 100 μl διαλύματος WST-1 και 17,37 μl διαλύματος οξειδάσης της ξανθίνης) και προσθέτονταν από 200 μl σε κάθε πηγαδάκι και όσο πιο γρήγορα γινόταν (διότι λόγω της παρουσίας της οξειδάσης της ξανθίνης στο μείγμα αντιδραστηρίων, η αντίδραση ξεκινούσε αμέσως). Τέλος, έπειτα από επώαση / RT υπό ελαφρά ανακίνηση, μετρούνταν η απορρόφηση των δειγμάτων στα 450nm σε ELISA reader. Ο υπολογισμός της αναστολής της SOD σε κάθε δείγμα γινόταν με την εφαρμογή του εξής τύπου (με το αποτέλεσμα να πολλαπλασιάζεται επί του 100): SOD activity (inhibition %) = [(Α blank) (δείγμα μου blank)] / (Α blank) Όπου όπως προαναφέρθηκε: Α (χωρίς SOD, με WST-1, με οξειδάση της ξανθίνης [μέγιστη τιμή]). blank (χωρίς SOD, με WST-1, χωρίς οξειδάση της ξανθίνης) Στη συνέχεια, με τη χρήση της πρότυπης καμπύλης που προέκυπτε από τη χρήση των standards υπολογίζονταν και τα U/ml της SOD στα δείγματά μας Συνανοσοκαθίζηση του ΝΗΕ1 Με τη διαδικασία της συνανοσοκαθίζησης (Co-IP, co-immunoprecipitation) είναι δυνατή η απομόνωση μιας συγκεκριμένης πρωτεΐνης σε συνδυασμό με άλλες πρωτεΐνες με τις οποίες βρίσκεται σε σύμπλοκο. Στην προκειμένη περίπτωση, πραγματοποιήθηκε ανοσοκαθίζηση του ΝΗΕ1 προκειμένου στη συνέχεια αφενός να μελετηθεί η επίδραση της λεπτίνης και των επιλεγμένων φαρμακολογικών αναστολέων στη σύνδεση της Hsp70 στην ΝΗΕ1 και αφετέρου να διαπιστωθεί το επίπεδο της γλουταθειονυλίωσης της συνδεδεμένης με τον ΝΗΕ1-Hsp70 πάλι έπειτα από την επίδραση των παραπάνω παραγόντων. Έτσι, τα μονοκύτταρα διαλύονταν σε PBS 1x, ισομοιράζονταν σε falcon των 15 ml και επωάζονταν αρχικά με τους φαρμακολογικούς αναστολείς για 15 min / 37 o C και εν συνεχεία με λεπτίνη για 30 78
79 min / 37 o C. Ακολουθούσε μια πλύση με παγωμένο PBS 1x, απόρριψη του υπερκείμενου και διάλυση των ιζημάτων των κυττάρων σε 500 μl διαλύματος λύσης 1x (lysis buffer 1% Nonidet P-40, 0,5% δεοξυχολικό οξύ, 0,05% SDS, 50 mm Tris- HCl (ph 8.0), 150 mm NaCl, 3 mm KCl, 1 mm EDTA, αναστολείς πρωτεασών [10 μg / ml απροτινίνη, 10 μg / ml λευπεπτίνη, 1mM PMSF]) το καθένα. Αμέσως, τα δείγματα μεταφέρονται σε νέα καθαρά δοχεία eppendorf και γινόταν επώασή τους με περιστροφική ανάδευση για 1 h / 4 o C. Στη συνέχεια πραγματοποιούνταν η διαδικασία που είναι γνωστή με τον όρο pre-clearance 4 προκειμένου να μειωθεί το background που μπορεί να προκληθεί από τη μη ειδική δέσμευση πρωτεϊνών στo αντίσωμα ενάντια στον ΝΗΕ1. Τα δείγματα μεταφέρονταν στον πάγο, προσθέτονταν σε όλα από 1 μg control IgG (IgG ελέγχου, εδώ rabbit IgG) / 500 μl δείγματος μαζί με 20 μl Protein A/G Plus-Agarose (το Protein A/G Plus-Agarose έχει την ιδιότητα να δεσμεύει ανοσοσφαιρίνες και να τις κατακρημνίζει) και επωάζονταν με περιστροφική ανάδευση για 30 min / 4 o C. Ακολουθούσε φυγόκεντρηση 1000 g / 5 min / 4 o C, μεταφορά των υπερκειμένων σε νέα καθαρά δοχεία eppendorf (στο ίζημα βρίσκονταν όλες οι πρωτεΐνες που δεσμεύτηκαν τυχαία στο control IgG)και συνέχιση της διαδικασίας στον πάγο. Εν συνεχεία με BCA 5 (Bicinchoninic acid) ή με τη μέθοδο Bradford 5 μετρούνταν οι συγκεντρώσεις των πρωτεϊνών στα δείγματα. Με κατάλληλη προσθήκη διαλύματος λύσης, εξισώνονταν οι συγκεντρώσεις των πρωτεϊνών των δειγμάτων. Κατόπιν, σε μg πρωτεΐνης που υπήρχε σε κάθε δείγμα προσθέτονταν 1-10 μl πρωτεύοντος αντισώματος (primary antibody), δηλαδή αντι-νηε1 (συγκεκριμένα rabbit anti-nhe1) και γινόταν επώαση 1 h / 4 o C υπό περιστροφική ανάδευση. Μετά το πέρας της μίας ώρας προσθέτονταν σε κάθε δείγμα από 20 μl Protein A/G Plus-Agarose και ακολουθούσε επώαση υπό περιστροφική ανάδευση overnight / 4 o C. Την επόμενη μέρα τα δείγματα φυγοκεντρούνταν 1000 g / 5 min / 4 o C και διατηρούνταν τόσο τα ιζήματα όσο και τα υπερκείμενα (τα υπερκείμενα μεταφέρονταν σε νέα eppendorf και διατηρούνταν στους 4 o C, προκειμένου να μελετηθούν τα επίπεδα γλουταθειονυλίωσης της ελεύθερης Hsp70). Τα ιζήματα υπόκειντο σε τρεις πλύσεις με διάλυμα λύσης που περιείχε αναστολείς πρωτεασών. Στην τελευταία πλύση δεν απορρίπτονταν όλο το υπερκείμενο, αλλά διατηρούνταν μια ποσότητα 30 μl σε κάθε δοχείο eppendorf με το οποίο επαναδιαλύονταν τα ιζήματα. Κατόπιν, με τη μέθοδο του BCA πραγματοποιούνταν μέτρηση της περιεκτικότητας κάθε δείγματος σε πρωτεΐνη. 79
80 Ηλεκτροφόρηση δειγμάτων που προήλθαν από ανοσοκαθίζηση του ΝΗΕ1 Η συσκευή ηλεκτροφόρησης συναρμολογούνταν (μικρά τζαμάκια-short plates πάνω σε μεγάλα τζαμάκια-spacer plates with 1mm spacers) και στη συνέχεια σε μικρές κωνικές φιάλες παρασκευάζονταν τα running gel 8% 6 (για 2 gel απαιτούνταν: [όλα τα συστατικά στον πάγο προτού προστεθούν] - 2,66 ml ακρυλαμίδιο 30%, 1,06 ml bis-ακρυλαμίδιο 2%, 100 μl SDS 10% 7, 3,75 ml 1M Tris ph 8,8, 2,40 ml dh 2 O, 10 μl TEMED [μπαίνει στο τέλος μαζί με το APS], 75 μl APS [μπαίνει στο τέλος μαζί με το TEMED] σύνολο 10,005 ml). Το TEMED (tetramethylethylenediamine) σε συνδυασμό με το APS (ammonium persulfate) καταλύουν τον πολυμερισμό του ακρυλαμίδιου και αυτός είναι ο λόγος για τον οποίον κατά την παρασκευή των running gel μπαίνουν μαζί στο τέλος της. Tα running gel φορτώνονταν στη συσκευή και όσο έπηζαν παρασκευάζονταν τα stacking gel 4% (για 2 gel απαιτούνταν: [όλα τα συστατικά στον πάγο προτού να προστεθούν] - 0,66 ml ακρυλαμίδιο 30%, 0,27 ml bis-ακρυλαμίδιο 2%, 25 μl SDS 10%, 0,63 ml Tris 1M ph 6,8, 3,40 ml dh 2 O, 5 μl TEMED [μπαίνει στο τέλος μαζί με το APS], 38 μl APS [μπαίνει στο τέλος μαζί με το TEMED] σύνολο 5,028 ml). Τα stacking gel φορτώνονταν πάνω από τα πηγμένα running gel και τα ειδικά χτενάκια πιέζονταν μέσα προκειμένου να γίνει ο σχηματισμός των πηγαδιών. Μετά το πήξιμο και των stacking gel, τα gel μεταφέρονταν στην ειδική συσκευή και καλύπτονταν με running buffer 1x (για stock διάλυμα 10x 10 g SDS 0,1%, 144,25 g γλυκίνη (glycine), 30,25 g Tris-base, 1 lt dh 2 O, ph 8,3, διατήρηση στους 4 o C). Έπειτα από μέτρηση της περιεκτικότητας των δειγμάτων σε πρωτεΐνη με BCA, αυτά διαλύονταν περαιτέρω με κατάλληλη ποσότητα loading buffer (SDS 3%, 0,08 M Tris-HCl ph 6,8, glycerol 15%, bromophenol blue 0,01%), ώστε όλα να περιέχουν την ίδια συγκέντρωση πρωτεΐνης (η οποία συγκέντρωση αντιστοιχούσε πάντα με την μικρότερη συγκέντρωση πρωτεΐνης που ανιχνεύονταν με βάση την προηγούμενη μέτρηση με BCA). Κατόπιν επωάσεως στους 3-5 min / 100 ο C και ακόλουθης φυγοκέντρησης rpm / 5 min / 4 o C, δείγματα των 25 μl φορτώνονταν στα πηγαδάκια των gel. Σε ξεχωριστό πηγαδάκι και αφού υπόκειντο την ίδια διαδικασία (επώαση 3-5 min / 100 ο C, φυγοκέντρηση rpm / 5 min / 4 o C), φορτώνονταν οι markers (πρωτεΐνες γνωστού μοριακού βάρους). Τα δείγματα ηλεκτροφορούνταν στα 70 V (ή 25 ma, εάν χρησιμοποιούνταν ο διακόπτης της έντασης του ρεύματος) έως ότου να εισερχόντουσαν στα running gel οπότε και η τάση αυξανόταν στα 200 V (ή 40 ma, 80
81 εάν χρησιμοποιούνταν ο διακόπτης της έντασης του ρεύματος) μέχρι τα δείγματα να έφταναν σχεδόν στο κάτω άκρο των gel Western Blotting και εμφάνιση με τη μέθοδο ECL δειγμάτων που προήλθαν από ανοσοκαθίζηση του ΝΗΕ1 Κατά τη διαδικασία του Western Blotting γινόταν μεταφορά των πρωτεϊνών από τα gel πολυακρυλαμιδίου σε μεμβράνες νιτροκυτταρίνης, ανίχνευσή τους με ειδικά αντισώματα και οπτικοποίησή τους με τη μέθοδο ECL. Έτσι, στην αρχή πραγματοποιήθηκε η μέθοδος του semi-dry blotting σε συσκευή της Fisher Scientific που περιελάμβανε καπάκι (άνοδος -) τιτανίου επικαλυμμένο με πλατίνα και βάση (κάθοδος +) από ανοξείδωτο ατσάλι (εικ. 4). Εικόνα 5. Διάταξη συσκευής για semi-dry blotting εν ώρα λειτουργίας Picture 4. Semi-dry blotting apparatus while in use. Συγκεκριμένα, δύο χαρτάκια Whatmann βρέχονταν πλήρως με transfer buffer 1x (1 όγκος transfer buffer 10x : 7 όγκοι dh 2 O : 2 όγκους μεθανόλη (CΗ 3 OH) για stock διάλυμα transfer buffer 10x [30,3 g Tris, 144 g γλυκίνη, 1 lt dh 2 O, ph 8,3, διατήρηση στους 4 o C]) και τοποθετούνταν επάνω στη βάση της συσκευής. Από τα gel κόβονταν το τμήμα του stacking gel και το υπόλοιπο μεταφέρονταν επάνω στα δύο βρεγμένα χαρτάκια Whatmann. Κατάλληλου εμβαδού κομμάτι μεμβράνης 81
82 νιτροκυτταρίνης βρεχόταν ελαφρά με transfer buffer 1x και τοποθετούνταν από πάνω από το gel. Το σάντουιτς ολοκληρωνόταν με την τοποθέτηση από πάνω άλλων δύο βρεγμένων χαρτιών Whatmann. H διαδικασία αυτή πραγματοποιούνταν για τρία gel, ενώ το τέταρτο διατηρούνταν σε transfer buffer προκειμένου την επόμενη μέρα να υποστεί silver staining 8. H συσκευή κλεινόταν σφιχτά και το blotting πραγματοποιούνταν στα 400 ma για 60 min / RT (εικ. 4). Εικόνα 6. Η συσκευή για semi-dry blotting μετά το πέρας του blotting. Στα αριστερά (κάθοδος +) φαίνονται τα σάντουιτς που περιέχουν τα gel και τις μεμβράνες νιτροκυτταρίνης. Δεξιά η άνοδος -. Picture 5. Semi-dry blotting apparatus after blotting has been completed. On the left (cathode +) the sandwiches containing the gels and the nitrocellulose membranes can be seen. On the right, the anode (-) can be seen. Στη συνέχεια (εικ. 5), οι μεμβράνες νιτροκυτταρίνης αφαιρούνταν από τα σάντουιτς και επωάζονταν σε δοχεία που περιείχαν ml blocking buffer 9 (10 ml TBS 10x, 100 μl Tween, 5 g σκόνη γάλακτος, 90 ml dh 2 O για stock διάλυμα TBS 10x [12,1 g Tris, 40 g NaCl, 500 ml dh 2 O, ph 7,6, διατήρηση στους 4 o C]) για 60 min / RT υπό ήπια ανάδευση. Κατόπιν προσθέτονταν πρωτεύον αντίσωμα (primary antibody, εδώ anti-nhe1, anti-hsp70 και anti-gsh) σε αναλογία 1:2000 (όπως όριζε ο προμηθευτής) απευθείας στο blocking buffer και οι μεμβράνες νιτροκυτταρίνης επωάζονταν overnight / 4 o C υπό ήπια ανάδευση. Την επόμενη μέρα, οι μεμβράνες 82
83 νιτροκυτταρίνης πλένονταν τρεις φορές με TBS 1x / Tween για 6 min / RT υπό ήπια ανάδευση προς απομάκρυνση των πρωτευόντων αντισωμάτων. Ακολουθούσε επώαση με τα δευτερεύοντα αντισώματα (secondary antibodies, εδώ anti-rabbit για NHE1, anti-goat για Hsp70, anti-mouse για GSH, όλα συνδεδεμένα με το ένζυμο horseradish peroxidase, HRP, στα ελληνικά υπεροξειδάση του αγριοράπανου) σε αναλογία 1: (όπως όριζε ο προμηθευτής), καθώς και με anti-biotin HRPσυνδεδεμένο αντίσωμα (προς εμφάνιση των markers) σε αναλογία 1:1000. Ακολουθούσαν άλλες τρεις πλύσεις με TBS 1x / Tween για 6 min / RT υπό ήπια ανάδευση. Η διαδικασία συνεχιζόταν στο φωτογραφικό θάλαμο υπό συνθήκες σκότους πλην της χρήσης ερυθράς λυχνίας. Οι μεμβράνες νιτροκυτταρίνης επωάζονταν με διάλυμα ECL (enhanced chemiluminescence, ενισχυμένη χημειοφωταύγεια) 10 (18,8 ml dh 2 O, 600 μl Lumiglo πρώτα, 600 μl H 2 O 2 κατόπιν) για 1 min / RT με ελαφρά ανάδευση. Εν συνεχεία, το διάλυμα ECL απορρίπτονταν, η κάθε μεμβράνη νιτροκυτταρίνης τοποθετούνταν σε διαφανή, στεγνή, ζελατινοειδή θήκη και μετά σε φωτογραφική κασετίνα. Πάνω από τη θήκη που περιείχε τη μεμβράνη τοποθετούνταν φιλμ και η κασετίνα έκλεινε για περίπου 15 sec (ο χρόνος έκθεσης μπορούσε να αυξηθεί ή μειωθεί ανάλογα με την ένταση των ιχνών που εμφανίζονταν). Αμέσως μετά το φιλμ αναδεύονταν μέσα σε developer μέχρι την εμφάνιση επαρκώς ευκρινών ιχνών και στη συνέχεια μεταφέρονταν στο fixer. Αυτό είχε ως αποτέλεσμα την μονιμοποίηση των ιχνών και το φιλμ δεν ήταν πλέον ευαίσθητο στο φως. Τα φιλμ αφήνονταν για 5-10 min σε dh 2 O και κατόπιν αφήνονταν όρθια να στεγνώσουν. Στην περίπτωση που σε συνεχόμενα πειράματα δεν λαμβανόταν ικανοποιητική τελική εικόνα από το blot, πραγματοποιούνταν η διαδικασία του dot blot αντιδραστηρίων που χρησιμοποιούνταν. 11 προς επαλήθευση της σωστής λειτουργίας των 1.12 Στατιστική ανάλυση πειραματικών αποτελεσμάτων Για την επεξεργασία των αποτελεσμάτων των πειραμάτων προσδιορισμού του ενδοκυτταρικού ph (phi), προσδιορισμού της επιφανειακής έκφρασης CD36, προσδιορισμού ελευθέρων ριζών με H 2 DCFDA, προσδιορισμού ανιόντος σουπεροξειδίου με DHE, προσκόλλησης μονοκυττάρων σε υπόστρωμα λαμινίνης-1, μετανάστευσης σε υπόστρωμα λαμινίνης-1, προσδιορισμού επιπέδων φαγοκύττωσης των oxldls και του προσδιορισμού της δραστικότητας της δισμουτάσης του 83
84 σουπεροξειδίου χρησιμοποιήθηκε η one-way ANOVA (analysis of variance) με το Student-Newman-Keuls test που εμπεριεχόταν στο στατιστικό λογισμικό GraphPad Instat version 3.00 (GraphPad Software, San Diego, CA, USA, Η στατιστική επεξεργασία εφαρμόστηκε στα αποτελέσματα τουλάχιστον έξι επαναλήψεων καθενός εκ των παραπάνω πειραματικών διαδικασιών. Το μικρότερο επίπεδο σημαντικότητας που γινόταν αποδεκτό ήταν το P<0,05. 84
85 Παράρτημα Υλικών και Μεθόδων 1.Παρασκευή PBS 1x Το PBS (phosphate buffered saline) είναι ένα διάλυμα αλάτων που χρησιμοποιήθηκε ευρέως κατά τη διάρκεια πειραμάτων για την πλύση κυττάρων προς απομάκρυνση διεγερτών-αναστολέων-θρεπτικού υλικού, κτλ. από το περιβάλλον τους. Για την παρασκευή 100 ml PBS 1x διαλύονταν 0,8 g NaCl (C τελ 137 mm), 0,02 g KCl (C τελ 2,7 mm), 0,02 g KH 2 PO 4 (C τελ 147 mm) και 0,115 g Na 2 HPO 4 (C τελ 8,1 mm) σε 100 ml dh 2 O. To ph ρυθμιζόταν στο 7,2 και το διάλυμα αποστειρωνόταν στο αυτόκαυστο. Για ευκολία συνήθως παρασκευάζονταν PBS 10x (με δεκαπλασιασμό όλων των ποσοτήτων των συστατικών στα 100 ml) από το οποίο κατόπιν γινόταν αραίωση προς PBS 1x. 2.Παρασκευή 500ml θρεπτικού διαλύματος πλήρους IMDM Το χαρακτηριζόμενο ως πλήρες IMDM είναι θρεπτικό υλικό IMDM (Iscove s Modified Dulbecco s Medium) το οποίο περιέχει 1% αντιβιοτικά (πενικιλλίνη / στρεπτομυκίνη), 1% L-γλουταμίνη (L-gln), 1% διάλυμα Hepes 1M και 10% FCS (Fetal Calf Serum). Χρησιμοποιήθηκε ως θρεπτικό υλικό για μονοκύτταρα. Παρασκευαζόταν με την προσθήκη 5ml πενικιλλίνης / στρεπτομυκίνης (10000 U / ml, άρα C τελ 100U/ml), 5 ml L-γλουταμίνης (200 mm, άρα C τελ 2 mm), 5ml διαλύματος Hepes 1M (άρα C τελ 10 mm) και 50 ml FCS (Fetal Calf Serum, ορός εμβρύου μοσχαριού) σε 435 ml IMDM. Προς αποφυγή μολύνσεων, η παρασκευή του πλήρους IMDM γινόταν στον απαγωγό (hood) και η μεταφορά όλων των συστατικών στο IMDM γινόταν με σύριγγα στην οποία είχε εφαρμοστεί φίλτρο οπών διαμέτρου 0,22μm. Τα 500 ml του πλήρους IMDM διατηρούνταν στους 4 ο C μέχρι την ημερομηνία λήξης που όριζε ο προμηθευτής. 3.Βασική αρχή φθορισμού Ορισμένες χημικές ενώσεις, γνωστές ως φθορίζουσες ουσίες, διαθέτουν μοριακή δομή η οποία τους επιτρέπει να διεγείρονται, απορροφώντας ενέργεια (φως) ενός συγκεκριμένου μήκους κύματος (excitation wavelength). Η νέα, όμως, αυτή κατάσταση υψηλής ενέργειας είναι ασταθής και προσωρινή με αποτέλεσμα σχεδόν αμέσως οι φθορίζουσες ουσίες να επανέρχονται στην αρχική τους κατάσταση μέσω της εκπομπής ενέργειας (φωτός) πάλι σε συγκεκριμένο μήκος κύματος (emission wavelength, διαφορετικού όμως, του αρχικού που τους οδήγησε στη διεγερμένη κατάσταση). Έτσι για παράδειγμα, η φθορίζουσα ουσία H 2 DCFDA που χρησιμοποιήθηκε στα πειράματα 85
86 μέτρησης της παραγωγής οξειδωτικών ριζών απορροφάει-διεγείρεται στα 498nm και εκπέμπει στα 522nm. 4. Προ-καθαρισμός (Pre-Clearance) Ο προ-καθαρισμός του lysate συνέβαλλε στη μείωση του background που μπορούσε να προκληθεί από τη μη ειδική δέσμευση πρωτεϊνών στα beads αγαρόζης ή σεφαρόζης Με άλλα λόγια, προσθέτοντας αντίσωμα IgG μη ειδικό για την πρωτεΐνη που μας ενδιέφερε, καθώς και beads αγαρόζης, καθαριζόταν το lysate από πρωτεΐνες οι οποίες θα μπορούσαν δυνητικά να συνδεθούν μη ειδικά, δηλ. σε άλλες περιοχές πλην της αντιγονο-δεσμευτικής, στο αντίσωμα. Βασικός κανόνας που ακολουθήθηκε ήταν το αντίσωμα που χρησιμοποιούνταν για pre-clearance να ήταν απαραιτήτως του ίδιου τύπου Ig και από το ίδιο είδος ζώου από το οποίο θα ήταν και το primary antibody, δηλ. εδώ rabbit IgG) 5.Μέτρηση συγκέντρωσης πρωτεΐνης 5.1 Μέτρηση συγκέντρωσης πρωτεΐνης με BCA Η αρχή λειτουργίας αυτής της μεθόδου βασίζεται σε δύο αντιδράσεις. Η πρώτη αφορά την αναγωγή ιόντων Cu 2+ προς Cu 1+ έπειτα από την αλληλεπίδρασή τους με τους πεπτιδικούς δεσμούς των πρωτεϊνών. Τα επίπεδα αυτής της αναγωγής είναι ανάλογα της συγκέντρωσης της πρωτεΐνης στο διάλυμα. Η δεύτερη αντίδραση αφορά στην ιδιότητα του BCA (bicinchoninic acid) να σχηματίζει χηλικές ενώσεις με τα ιόντα Cu 1+ με αναλογία δύο μορίων BCA προς ένα ιόν Cu 1+. Αυτά τα σύμπλοκα BCA-Cu 1+ δίνουν ιώδες χρώμα στο διάλυμα και απορροφούν ισχυρά στα 562nm [Smith et al, 1985]. To διάλυμα BCA (bicinchoninic acid) ή working solution παρασκευαζόταν με ανάμειξη των Reagent A και Reagent B σε αναλογία 50 όγκοι Reagent A : 1 όγκο Reagent B (50:1) σύμφωνα με τις οδηγίες του προμηθευτή (Pierce). Αρχικά, παρασκευάζονταν συνολικά [(n + 2) x 200 μl] όγκος διαλύματος BCA, όπου n ο συνολικός αριθμός δειγμάτων (πρότυπων και πειραματικών). Κατόπιν, παρασκευάζονταν τα πρότυπα δείγματα (standards), απαραίτητα για τη χάραξη της πρότυπης καμπύλης. Σε 5 ml PBS 1x (ph 7,0) (ή γενικότερα σε 5 ml του διαλύματος στο οποίο βρίσκεται η πρωτεΐνη που μελετάται) προσθέτονταν με αργό ρυθμό 10 mg αλβουμίνης (BSA, bovine serum albumin και έτσι παρασκευαζόταν διάλυμα BSA 2 mg / ml. Εννέα σωληνάκια eppendorf σημειώνονταν με αριθμούς από 1 έως το 9 και σε όλα πλην του πρώτου 86
87 προσθέτονταν από 100 μl PBS 1x (ph 7,0). Στη συνέχεια στο πρώτο προσθέτονταν 200μl BSA 2mg/ml και από αυτά, τα 100 μl μεταφέρονταν στο σωληνάκι eppendorf 2 (έτσι στο σωληνάκι eppendorf 1 έμεναν 100μl διαλύματος ΒSA 2mg/ml και παράλληλα στο eppendorf 2 το BSA ήταν πλέον αραιωμένο 1:2, ήταν δηλαδή 1 mg / ml). Αντίστοιχα, 100 μl από το eppendorf 2 μεταφέρονταν στο eppendorf 3 και ούτω καθεξής, μέχρι το eppendorf 8 από το οποίο λαμβάνονταν τα 100 μl και απορρίπτονταν, έτσι ώστε το περιεχόμενο του σωληνακιού eppendorf 9 να είναι μόνο 100 μl PBS 1x (και άρα να αποτελεί το τυφλό). Με αυτό τον τρόπο ήταν διαθέσιμα πρότυπα δείγματα των 2 mg / ml, 1 mg / ml, 0,5 mg / ml, 0,25 mg / ml, 0,125 mg / ml, 0,0625 mg / ml, 0,03125 mg / ml, 0, mg / ml και 0 mg / ml. Από αυτά τα πρότυπα δείγματα, καθώς και από τα πειραματικά λαμβάνονταν 10 μl και τοποθετούνταν σε χωριστά πηγαδάκια διάφανης πλάκας 96 πηγαδιών. Στη συνέχεια σε κάθε πηγαδάκι που χρησιμοποιούνταν προσθέτονταν από 200 μl διαλύματος BCA. H πλάκα καλυπτόταν με αλουμινόχαρτο, ανακινούνταν ελαφρά για 30sec στο plate shaker και επωάζονταν στο υδατόλουτρο για 30 min / 37 o C. Τέλος, γινόταν μέτρηση της απορρόφησης στα 562nm σε ELISA reader. Με βάση την πρότυπη καμπύλη γνωστών συγκεντρώσεων υπολογίζονταν οι συγκεντρώσεις σε πρωτεΐνη των πειραματικών δειγμάτων. Γενικά, το εύρος ανίχνευσης του BCA είναι μg πρωτεΐνης/ml διαλύματος. Αυτό μπορεί να μειωθεί και στα 6μg/ml εάν παραταθεί ο χρόνος επώασης των δειγμάτων με BCA στις 2h. 5.2 Mέτρηση συγκέντρωσης πρωτεΐνης με τη μέθοδο Bradford Η μέθοδος Bradford εκμεταλλεύεται τις ιδιότητες της χρωστικής Coomassie (Bradford, 1976). H χρωστική αυτή δρα μέσω της δέσμευσής της με δυνάμεις Van der Waals σε περιοχές των πρωτεϊνών όπου υπάρχουν συγκεκριμένα αμινοξέα όπως η αργινίνη, η ιστιδίνη, καθώς και τα αρωματικά αμινοξέα (τρυπτοφάνη, τυροσίνη, φαινυλαλανίνη). Το αποτέλεσμα αυτής της δέσμευσης είναι η μετατόπιση του σημείου απορρόφησης της Coomassie από τα 465nm στα 595nm. H διαδικασία μέτρησης της συγκέντρωσης πρωτεϊνών με τη μέθοδο Bradford είναι όμοια έως ενός σημείου με τη διαδικασία που εφαρμόζεται προς μέτρηση της συγκέντρωσης πρωτεϊνών με τη χρήση του BCA. Έτσι, σε 5 ml PBS 1x (ph 7,0) (ή γενικότερα σε 5 ml του διαλύματος στο οποίο βρίσκεται η πρωτεΐνη που μελετάται) προσθέτονταν με αργό ρυθμό 10 mg αλβουμίνης (BSA, bovine serum albumin και έτσι παρασκευαζόταν διάλυμα BSA 2 mg / ml. Σε εννέα σωληνάκια 87
88 eppendorf σημειώνονταν οι αριθμοί από το 1 έως το 9 και σε όλα πλην του πρώτου προσθέτονταν από 100 μl PBS 1x (ph 7,0). Στη συνέχεια στο πρώτο προσθέτονταν 200 μl BSA 2 mg / ml και από αυτά, τα 100 μl μεταφέρονταν στο σωληνάκι eppendorf 2 (έτσι στο σωληνάκι eppendorf 1 έμεναν 100 μl διαλύματος ΒSA 2 mg / ml και παράλληλα στο eppendorf 2 το BSA ήταν πλέον αραιωμένο 1:2, ήταν δηλαδή 1mg/ml). Αντίστοιχα, 100 μl από το eppendorf 2 μεταφέρονταν στο eppendorf 3 και ούτω καθεξής, μέχρι το eppendorf 8 από το οποίο λαμβάνονταν τα 100 μl και απορρίπτονταν, έτσι ώστε το περιεχόμενο του σωληνακιού eppendorf 9 να είναι μόνο 100 μl PBS 1x (και άρα να αποτελεί το τυφλό). Με αυτό τον τρόπο ήταν διαθέσιμα πρότυπα δείγματα των 2 mg / ml, 1 mg / ml, 0,5 mg / ml, 0,25 mg / ml, 0,125 mg / ml, 0,0625 mg / ml, 0,03125 mg / ml, 0, mg / ml και 0 mg / ml. Από αυτά τα πρότυπα δείγματα, καθώς και από τα πειραματικά λαμβάνονταν 5 μl και τοποθετούνταν σε χωριστά πηγαδάκια διάφανης πλάκας 96 πηγαδιών. Στη συνέχεια σε κάθε πηγαδάκι που χρησιμοποιούνταν προσθέτονταν από 145μl διαλύματος Coomassie-Plus. Ακολουθούσε ανάδευση της πλάκας για 2-3min σε plate shaker και μέτρηση της απορρόφησης στα 595nm σε ELISA reader. Με βάση την πρότυπη καμπύλη γνωστών συγκεντρώσεων υπολογίζονταν οι συγκεντρώσεις σε πρωτεΐνη των πειραματικών δειγμάτων. Ένα μειονέκτημα της μεθόδου Bradford είναι ότι η ανίχνευση της συγκέντρωσης των πρωτεϊνών εξαρτάται άμεσα από την αμινοξική τους σύνθεση και ειδικότερα από το αν περιέχουν τα συγκεκριμένα αμινοξέα στα οποία μπορεί να δεσμευθεί η χρωστική Coomassie. Η μέθοδος Bradford επίσης επηρεάζεται και μπορεί να δώσει πλαστά αποτελέσματα εάν τα δείγματα περιέχουν >0,1% SDS, >0,1% Τriton Χ-100, φαινόλη ή ακετόνη. 6.Σύσταση Gel Η πυκνότητα του running gel (γνωστό και ως resolving gel) που θα χρησιμοποιηθεί καθορίζεται από το ΜΒ της πρωτεΐνης που μας ενδιαφέρει, έτσι gel 8% => kda, gel 10% => kda, gel 12,5% => kda, gel 15% => kda, gel 20% => 4-40 kda. Οι διαφορετικές πυκνότητες του running gel οδηγούν και σε διαφορετικά μεγέθη πόρων που επιτρέπουν μόνο σε πρωτεΐνες συγκεκριμένων ΜΒ να το διατρέξουν. 88
89 7.SDS To SDS διασπά όλους τους μη ομοιοπολικούς δεσμούς (δηλαδή ΔΕΝ διασπά πεπτιδικούς και δισουλφιδικούς δεσμούς, για τους τελευταίους χρησιμοποιείται 2- μερκαπτοαιθανόλη) που μπορεί να υπάρχουν στις πρωτεΐνες με αποτέλεσμα να διαταράσσεται η διαμόρφωσή τους. Επιπρόσθετα, ανιόντα SDS δεσμεύονται στην αμινοξική αλυσίδα σε αναλογία 1 ανιόν SDS : 2 αμινοξέα (αναλογία μάζας 1,4 g SDS : 1 g πρωτεΐνης), με αποτέλεσμα οι πρωτεΐνες να αποκτούν ισχυρό αρνητικό φορτίο (λόγω ηλεκτροστατικών απώσεων οι πρωτεΐνες αποκτούν σχετικά ραβδοειδές σχήμα). Έτσι, κατευθύνονται προς τον θετικό πόλο, με ταχύτητα που δεν καθορίζεται από το σχήμα τους, αλλά μόνο από το μέγεθός τους (όσο πιο μικρό ΜΒ έχουν, τόσο πιο γρήγορα κινούνται). 8.Ανίχνευση πρωτεϊνών σε gel με τη μέθοδο του Silver Staining Με τη χρώση Silver Staining (χρώση με άργυρο) γινόταν οπτικοποίηση πρωτεϊνών που βρίσκονταν πάνω σε gel έπειτα από ηλεκτροφόρηση. Όλες οι επωάσεις που αναφέρονται παρακάτω πραγματοποιούνται υπό συνεχή ανάδευση. Καταρχήν, το gel τοποθετούνταν σε κατάλληλο δοχείο (συνήθως γυάλινο, διαφανές μπωλ) και επωάζονταν με 25 ml fixative (11,4 ml dh 2 O, 15 ml μεθανόλη και 3,6 ml οξικό οξύ) για 10 min. Έπειτα από απόρριψη του fixative, πραγματοποιούνταν δύο πλύσεις με dh 2 O για 5 min κάθε φορά και ακολουθούσε επώαση με 30 ml υδατικού διαλύματος sodium thiosulfate 0,02% για 1 min ακριβώς (φροντίζαμε να περισσέψει μια μικρή ποσότητα για να προστεθεί στο developer μετά). Έπειτα από απόρριψη του υπερκείμενου υγρού γινόταν άλλη μια πλύση με dh 2 O για 1 min. Στη συνέχεια το gel επωάζονταν με 25 ml υδατικού διαλύματος νιτρικού αργύρου (AgNO 3 ) 0,2% για 10 min και πλένονταν μετά με dh 2 O για 5 min. Ακολουθούσε επώαση με 25 ml developer (0,75 g Na 2 CO 3 σε 25 ml dh 2 O, στα οποία προσθέτονται στη συνέχεια 20 μl διαλύματος sodium thiosulfate 0,02% και στο τέλος 12,5 μl φορμαλδεΰδης) έως την εμφάνιση ευκρινών μπαντών. Κατόπιν, το υπερκείμενο υγρό απορρίπτονταν και το gel επωάζονταν με 25 ml υδατικού διαλύματος οξικού οξέος 10% για 10 min. Έπειτα από την απόρριψη και αυτού του υγρού, στο gel προσθέτονταν 25 ml υδατικού διαλύματος γλυκερόλης 10% προκειμένου να αποφευχθεί η ξήρανσή του και να επιτευχθεί έτσι η συντήρησή του. Σε αυτή την κατάσταση του gel λαμβάνονταν φωτογραφία του προς 89
90 αρχειοθέτηση και πιθανή χρήση του στην ερμηνεία των αποτελεσμάτων των πειραμάτων. 9.Χρήση blocking buffer H μεμβράνη νιτροκυτταρίνης διαθέτει την πολύ σημαντική ιδιότητα να δεσμεύει πρωτεΐνες και ήδη πάνω στην επιφάνειά της (ως αποτέλεσμα της διαδικασίας του semidry blotting) έχει δεσμευτεί η πρωτεΐνη που μας ενδιαφέρει. Όμως, πρωτεΐνη είναι και το αντίσωμα που θα προστεθεί προκειμένου να την ανιχνεύσει. Έτσι, με τη χρήση του blocking buffer, δεσμεύονται από τις πρωτεΐνες του γάλακτος όλες οι θέσεις στην επιφάνεια της μεμβράνης νιτροκυτταρίνης όπου θα μπορούσε να γίνει μη-ειδική δέσμευση του αντισώματος. Έτσι, πλέον οι μόνες θέσεις στις οποίες μπορεί να δεσμευτεί το αντίσωμα είναι οι θέσεις όπου βρίσκεται η πρωτεΐνη για την οποία έχουν ειδικότητα. 10. Ενισχυμένη χημειοφωταύγεια (ECL) Η ενισχυμένη χημειοφωταύγεια (enhanced chemiluminescence, ECL) βασίζεται στη σύζευξη της υπεροξειδάσης του αγριοράπανου (HRP, horseradish peroxidase) στο μόριο που μας ενδιαφέρει (συνήθως με σύζευξή της με αντίσωμα ειδικό για το μόριο που μας ενδιαφέρει). Η HRP στη συνέχεια καταλύει την οξείδωση του υποστρώματος της ECL από Η 2 Ο 2 προς έναν ενδιάμεσο παράγοντα ο οποίος περιέχει τριπλό (διεγερμένο) καρβονύλιο το οποίο κατά τη μετάπτωση προς μονό καρβονύλιο εκλύει φως (που καταγράφεται έτσι στο φιλμ). Στη συγκεκριμένη περίπτωση η HRP καταλύει την εξής αντίδραση: Lumiglo + H 2 O 2 ενδιάμεσο προϊόν [ ] ενδιάμεσο προϊόν + φως Με την ενισχυμένη χημειοφωταύγεια γίνεται δυνατή η ανίχνευση βιομορίων ακόμα και σε συγκέντρωση της τάξης των Μ. 90
91 11. Dot Blot Η διαδικασία του dot blot είναι ένας οικονομικός τρόπος (καθότι καταναλώνονται λίγα υλικά), προκειμένου να γίνει επαλήθευση της ομαλής λειτουργίας των αντιδραστηρίων που απαιτούνται για την απεικόνιση ενός western blot. Συγκεκριμένα, με κατάλληλο σχεδιασμό του πειράματος μπορεί να ελεγχθεί η ποιότητα των πρωτευόντων και δευτερευόντων αντισωμάτων και η ικανότητα σύνδεσης μεταξύ τους, καθώς επίσης και η ποιότητα των αντιδραστηρίων που χρησιμοποιούνται στη διαδικασία ενισχυμένης χημειοφωταύγειας (ECL). Όσον αφορά την πειραματική διαδικασία, έπειτα από τις απαραίτητες πλύσεις με PBS 1x, το ίζημα των κυττάρων επωαζόταν στον πάγο με 500 μl lysis buffer 1x (που περιείχε [10 μg / ml απροτινίνη, 10 μg / ml λευπεπτίνη, 1 mm PMSF]) για 1 h / 4 ο C υπό περιστροφή. Ακολούθως, 5 μl από διάλυμα γνωστής πρωτεΐνης (για παράδειγμα 5 μl κάποιου από τα πρωτεύοντα αντισώματα που ελέγχονταν) τοποθετούνταν σε όσα σημεία μεμβράνης νιτροκυτταρίνης κρινόταν απαραίτητο και αφήνονταν να στεγνώσουν. Με μολύβι σημαδεύονταν οι θέσεις στις οποίες είχε γίνει η εναπόθεση του όποιου διαλύματος πρωτεΐνης προκειμένου στο τέλος να είναι δυνατή η ερμηνεία των αποτελεσμάτων. Δινόταν προσοχή ώστε οι διάφορες θέσεις απόθεσης του διαλύματος πρωτεΐνης να μην βρίσκονται πολύ κοντά μεταξύ τους, έτσι ώστε να μην έρχονται σε επαφή. Στη συνέχεια, η μεμβράνη νιτροκυτταρίνης επωαζόταν με blocking buffer για 1 h σε θερμοκρασία δωματίου και κατόπιν πλενόταν τρεις φορές με TBS 1x / Tween για 5 min κάθε φορά. Εν συνεχεία γινόταν επώαση της μεμβράνης νιτροκυτταρίνης με πρωτεύον αντίσωμα ειδικό για την πρωτεΐνη που είχε εναποτεθεί, overnight στους 4 ο C. Στην περίπτωση που είχε εναποτεθεί πρωτεύον αντίσωμα απευθείας στη μεμβράνη, τότε γινόταν απλώς επώαση με το blocking buffer, δίχως την προσθήκη κάποιου άλλου αντισώματος σε αυτή τη φάση). Την επόμενη μέρα, ακολουθούσαν πάλι τρεις πλύσεις με TBS 1x / Tween για 5 min κάθε φορά και μετά επώαση με το κατάλληλο δευτερεύον αντίσωμα. Έπειτα πάλι από τρεις πλύσεις με TBS 1x / Tween για 5 min κάθε φορά, γινόταν εμφάνιση των κουκκίδων πρωτεΐνης (dots) σε φωτογραφικό φιλμ με εκμετάλλευση της μεθόδου της ενισχυμένης χημειοφωταύγειας (βλ. 1.5). 91
92 Εικόνα 7. Dot blot προς επαλήθευση της σωστής λειτουργίας ορισμένων αντιδραστηρίων που χρησιμοποιούνται στη διαδικασία του Western Blotting Picture 7. Dort blot conducted in order to verify whether certain reagents used in the Western blotting procedure were in working condition. Στην εικόνα 7 φαίνεται το αποτέλεσμα πειράματος dot blot κατά το οποίο κατέστη σαφές ότι το πρωτεύον αντίσωμα ενάντια στην ΝΗΕ1, το δευτερεύον αντίσωμα ενάντια στο συγκεκριμένο πρωτεύον, καθώς και τα αντιδραστήρια της μεθόδου ενισχυμένης χημειοφωταύγειας ήταν σε καλή κατάσταση και λειτουργούσαν κανονικά. Λόγω της χρήσης lysates και όχι συμπυκνωμένου διαλύματος που να περιείχε μόνο ΝΗΕ1, δεν εμφανίστηκαν ευκρινείς κουκκίδες στα ενδιάμεσα τέσσερα σημεία. 92
93 Πειραματικά αποτελέσματα 1. Προσκόλληση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 Α) Καμπύλη δόσης-απόκρισης λεπτίνης Η προσκόλληση των μονοκυττάρων στο ενδοθήλιο που έχει υποστεί μικροτραυματισμό και στην εξωκυττάρια ουσία που παράγεται από αυτό είναι ένα από τα πρωταρχικά στάδια της αθηρωματικής διαδικασίας. Έτσι αποφασίστηκε η μελέτη της επίδρασης της λεπτίνης στην ικανότητα των μονοκυττάρων να προσκολλώνται σε ένα από τα κύρια συστατικά της εξωκυττάριας ουσίας, την λαμινίνη-1. Πριν την κυρίως πειραματική διαδικασία πραγματοποιήθηκε υπολογισμός της καμπύλης δόσης-απόκρισης (dose-response curve) της λεπτίνης στη διαδικασία προσκόλλησης των μονοκυττάρων σε υπόστρωμα λαμινίνης-1 προκειμένου να επιλεγεί η πιο αποτελεσματική συγκέντρωσή της. Διαπιστώθηκε ότι η λεπτίνη, σε όλες τις συγκεντρώσεις που χρησιμοποιήθηκαν (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml), αύξησε τα επίπεδα προσκόλλησης των μονοκυττάρων στη λαμίνινη-1 έπειτα από 30 min επώασης και μάλιστα αυτή η αύξηση ήταν σε όλες τις περιπτώσεις στατιστικά σημαντικά διαφορετική σε σχέση με το δείγμα ελέγχου (διάγραμμα 1). Συγκεκριμένα, η λεπτίνη προκάλεσε αυξήσεις στην προσκόλληση των μονοκυττάρων της τάξης του 38,5 ± 6,33% (1,6 ng/ml), 50,36 ± 6,11% (16 ng/ml), 54,91 ± 4,12% (160 ng/ml) και 41,06 ± 5,89% (1600 ng/ml). Η μέγιστη τιμή σημειώθηκε σε συγκέντρωση λεπτίνης 160 ng/ml, οπότε αυτή ήταν και η συγκέντρωση που χρησιμοποιήθηκε στην κυρίως πειραματική διαδικασία. 93
94 Διάγραμμα 1. Καμπύλη δόσης-απόκρισης της λεπτίνης για το πείραμα προσκόλλησης των μονοκυττάρων στη λαμινίνη-1. Τα μονοκύτταρα επωάστηκαν με τέσσερις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml) για 30 min / 37 o C. Τα αποτελέσματα της καμπύλης αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test και εκφράζονται ως τιμές επί τοις εκατό (%) μεγαλύτερες του δείγματος ελέγχου. Τα αποτελέσματα και στις τέσσερις συγκεντρώσεις λεπτίνης που ελέγχθηκαν εμφάνισαν στατιστικά σημαντική αύξηση σε σχέση με το δείγμα ελέγχου (P<0,05). Η κλίμακα στον x άξονα είναι λογαριθμική. * P<0,05 σε σχέση τόσο με το δείγμα συγκέντρωσης 1,6 ng/ml, όσο και με το δείγμα συγκέντρωσης 1600 ng/ml. Figure 1. Dose response curve of leptin for the experiment of monocyte adhesion to laminin-1. Monocytes were incubated with leptin at four different concentrations (1.6 ng/ml, 16 ng/ml, 160 ng/ml, 1600 ng/ml) for 30 min / 37 o C. The results of the curve are presented as the mean percent increases ± standard deviations versus the control sample of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. The increase caused by leptin was statistically significant (P<0.05) compared to the control sample at all four leptin concentrations which were used. The logarithmic scale is used on the x axis. * P<0.05 versus leptin samples 1.6ng/ml and 1600 ng/ml. Β) Πειραματικά αποτελέσματα Η λεπτίνη (160 ng/ml) όπως είχε διαπιστωθεί και από τα αποτελέσματα της καμπύλης δόσης-απόκρισης αύξησε κατά στατιστικά σημαντικό τρόπο τα επίπεδα προσκόλλησης των μονοκυττάρων σε υπόστρωμα λαμινίνης-1 (διάγραμμα 2). Συγκεκριμένα, στο δείγμα που επωάστηκε με λεπτίνη σε αυτή τη συγκέντρωση, προσκολλήθηκαν στη λαμινίνη ± κύτταρα, έναντι ±
95 κυττάρων στο δείγμα ελέγχου. Υπενθυμίζεται ότι ο μέγιστος αριθμός μονοκυττάρων που θα μπορούσαν να προσκολληθούν είναι όπως συνέβη στο δείγμα μυελοϋπεροξειδάσης 100% (ΜΡΟ 100%). Η δράση της λεπτίνης περιορίστηκε κατά στατιστικά σημαντικό τρόπο όταν προηγήθηκε κατάλληλη μεμονωμένη φαρμακολογική αναστολή του ΝΗΕ1, του κυτοσκελετού της ακτίνης, της PI3K, των πρωτεϊνικών κινασών C (και πιο συγκεκριμένα των ισομορφών α-, β i - και β ii - αυτής) και της NADPH οξειδάσης (διάγραμμα 2). Από τα προαναφερθέντα, τη μέγιστη αρνητική επίδραση στο μηχανισμό της λεπτίνης την είχε η αναστολή του ΝΗΕ1, της οποίας το δείγμα ήταν το μόνο στο οποίο τα επίπεδα προσκόλλησης των μονοκυττάρων στη λαμινίνη-1 δεν ξεπέρασαν τα επίπεδα του δείγματος ελέγχου. Αξίζει να σημειωθεί ότι αναστολή της συνθάσης του ΝΟ δεν παρατηρήθηκε να επιδρά στη δράση της λεπτίνης. Μέτρηση της μεμονωμένης δράσης των αναστολέων έναντι του δείγματος ελέγχου απουσία λεπτίνης δεν παρουσίασε στατιστικά σημαντικές διαφορές (Πίνακας 1). Διάγραμμα 2. Προσκόλληση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 έπειτα από την επώαση με λεπτίνη με ή χωρίς αναστολείς. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 160 ng/ml. Το δείγμα MPO 100% δεν αποτελεί πειραματικό δείγμα, για αυτό το λόγο δεν επισημαίνονται στο διάγραμμα οι 95
96 στατιστικά σημαντικές διαφορές της τιμής του με αυτές του δείγματος ελέγχου και του δείγματος λεπτίνης 160ng/ml. Figure 2. Monocyte adhesion to laminin-1 after incubation with leptin in the presence or absence of pharmacological inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 160 ng/ml for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. ** P<0,05 versus leptin sample 160 ng/ml. The MPO 100% sample is not considered an experimental sample, thus the levels of statistical significance of its value versus the control sampl and the leptin 160 ng/ml sample are not depicted in the figure. 2. Μετανάστευση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 Α) Καμπύλη δόσης-απόκρισης λεπτίνης Αμέσως μετά την προσκόλληση των μονοκυττάρων στο ενδοθήλιο που έχει υποστεί μικροτραυματισμούς, εκκινείται η διαδικασία μετανάστευσης των μονοκυττάρων προς τον υποενδοθηλιακό χώρο. Η μετανάστευσή τους προϋποθέτει αλληλεπιδράσεις με στοιχεία της εξωκυττάριας ουσίας. Έτσι, αποφασίστηκε η μελέτη της επίδρασης της λεπτίνης στην μετανάστευση των μονοκυττάρων διαμέσου του στοιχείου της εξωκυττάριας ουσίας λαμινίνη-1. Όπως και προηγουμένως, πριν την κυρίως πειραματική διαδικασία πραγματοποιήθηκε υπολογισμός της καμπύλης δόσης-απόκρισης της λεπτίνης στη διαδικασία μετανάστευσης των μονοκυττάρων σε υπόστρωμα λαμινίνης-1 προκειμένου να επιλεγεί η πιο αποτελεσματική συγκέντρωσή της. Διαπιστώθηκε ότι η λεπτίνη, σε όλες τις συγκεντρώσεις που χρησιμοποιήθηκαν (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml), αύξησε τα επίπεδα μετανάστευσης των μονοκυττάρων στη λαμίνινη-1 έπειτα από 30min επώασης και μάλιστα αυτή η αύξηση ήταν σε όλες τις περιπτώσεις στατιστικά σημαντική σε σχέση με το δείγμα ελέγχου (διάγραμμα 3). Συγκεκριμένα, η λεπτίνη προκάλεσε αυξήσεις στην μετανάστευση των μονοκυττάρων της τάξης του 11,04 ± 1,46% (1,6 ng/ml), 17,31 ± 1,30% (16 ng/ml), 27,66 ± 3,32% (160 ng/ml) και 30,75 ± 3,40% (1600 ng/ml). Η μέγιστη τιμή σημειώθηκε σε συγκέντρωση λεπτίνης 1600 ng/ml, παρόλα αυτά επιλέχθηκε η συγκέντρωση 160 ng/ml για την πειραματική διαδικασία. Αυτό έγινε διότι αφενός μεν η συγκέντρωση των 1600 ng/ml είναι υπερφυσιολογική και είναι δύσκολο να 96
97 απαντηθεί ακόμα και σε υπερλεπτιναιμικά άτομα, αφετέρου δε η συγκέντρωση των 160 ng/ml προκαλεί σχεδόν το ίδιο αποτέλεσμα, είναι φυσιολογική για υπερλεπτιναιμικά άτομα και χρησιμοποιήθηκε ήδη στο πείραμα της προσκόλλησης των μονοκυττάρων σε υπόστρωμα λαμινίνης-1. Διάγραμμα 3. Καμπύλη δόσης-απόκρισης της λεπτίνης για το πείραμα μετανάστευσης των μονοκυττάρων στη λαμινίνη-1. Τα μονοκύτταρα επωάστηκαν με τέσσερις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml) για 30 min / 37 o C. Τα αποτελέσματα της καμπύλης αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test και εκφράζονται ως τιμές επί τοις εκατό (%) μεγαλύτερες του δείγματος ελέγχου. Τα αποτελέσματα και στις τέσσερις συγκεντρώσεις λεπτίνης που ελέγχθηκαν εμφάνισαν στατιστικά σημαντική αύξηση σε σχέση με το δείγμα ελέγχου (P<0,05). Η κλίμακα στον x άξονα είναι λογαριθμική. * P<0,05 σε σχέση τόσο με το δείγμα συγκέντρωσης 1,6 ng/ml, όσο και με το δείγμα συγκέντρωσης 16 ng/ml. Figure 3. Dose response curve of leptin for the experiment of monocyte migration through laminin-1. Monocytes were incubated with leptin at four different concentrations (1.6 ng/ml, 16 ng/ml, 160 ng/ml, 1600 ng/ml) for 30 min / 37 o C. The results of the curve are presented as the mean percent increases ± standard deviations versus the control sample of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. The increase caused by leptin was statistically significant (P<0.05) compared to the control sample at all four leptin concentrations which were used. The logarithmic scale is used on the x axis. * P<0.05 versus leptin samples 1.6ng/ml and 16 ng/ml. 97
98 Β) Πειραματικά αποτελέσματα Η λεπτίνη (160 ng/ml) όπως είχε διαπιστωθεί και από τα αποτελέσματα της καμπύλης δόσης-απόκρισης αύξησε κατά στατιστικά σημαντικό τρόπο τα επίπεδα μετανάστευσης των μονοκυττάρων σε υπόστρωμα λαμινίνης-1 (διάγραμμα 4). Συγκεκριμένα, στο δείγμα που επωάστηκε με λεπτίνη σε αυτή τη συγκέντρωση, μετανάστευσαν διαμέσου της λαμινίνης ± κύτταρα, έναντι ± κυττάρων στο δείγμα ελέγχου. Υπενθυμίζεται ότι ο μέγιστος αριθμός μονοκυττάρων που θα μπορούσαν να μεταναστεύσουν είναι (ο αριθμός των μονοκυττάρων που τοποθετούνταν αρχικά στα φίλτρα). Η δράση της λεπτίνης περιορίστηκε κατά στατιστικά σημαντικό τρόπο όταν προηγήθηκε κατάλληλη μεμονωμένη φαρμακολογική αναστολή του ΝΗΕ1, του κυτοσκελετού της ακτίνης, της PI3K και των πρωτεϊνικών κινασών C (και πιο συγκεκριμένα των επονομαζόμενων συμβατικών ισομορφών α-, β i - και β ii - αυτής) (διάγραμμα 4). Από τα προαναφερθέντα, τη μέγιστη αρνητική επίδραση στο μηχανισμό της λεπτίνης την είχε η αναστολή του ΝΗΕ1, καθώς και των συμβατικών ισομορφών της PKC που δεν επέτρεψαν στα επίπεδα μετανάστευσης των μονοκυττάρων στη λαμινίνη-1 να ξεπεράσουν τα επίπεδα του δείγματος ελέγχου. Αξίζει να σημειωθεί ότι αναστολή είτε της NADPH οξειδάσης, είτε της συνθάσης του ΝΟ δεν παρατηρήθηκε να επιδρά στη δράση της λεπτίνης. Μέτρηση της μεμονωμένης δράσης των αναστολέων έναντι του δείγματος ελέγχου απουσία λεπτίνης δεν οδήγησε σε στατιστικά σημαντικές διαφορές (Πίνακας 2). Διάγραμμα 4. Μετανάστευση μονοκυττάρων σε υπόστρωμα λαμινίνης-1 έπειτα από την επώαση με λεπτίνη με ή χωρίς αναστολείς. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους 98
99 φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 160 ng/ml. Figure 4. Monocyte migration through laminin-1 after incubation with leptin in the presence or absence of pharmacological inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 160 ng/ml for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. ** P<0,05 versus leptin sample 160 ng/ml. 3. Προσδιορισμός της επιφανειακής έκφρασης υποδοχέων-ρακοσυλλεκτών Στον υποενδοθηλιακό χώρο, τα μονοκύτταρα έρχονται σε επαφή με οξειδωμένες λιποπρωτεϊνες χαμηλής πυκνότητας (oxldls) τις οποίες μπορούν και φαγοκυτταρώνουν μέσω εξειδικευμένων υποδοχέων της επιφάνειάς τους, πραγματοποιώντας έτσι το πρώτο βήμα για τη μετατροπή τους προς αφρώδη κύτταρα. Κατά συνέπεια αποφασίστηκε καταρχήν η μελέτη της επίδρασης της λεπτίνης στην επιφανειακή έκφραση του υποδοχέα CD36, ίσως του κυριότερου όσον αφορά την φαγοκύττωση των oxldls, στα μονοκύτταρα. Εν συνεχεία μελετήθηκε η επίδραση της λεπτίνης στην επιφανειακή εξωτερίκευση ενός άλλου σημαντικού υποδοχέα ρακοσυλλέκτη, του CD Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD36 Α) Καμπύλη δόσης-απόκρισης λεπτίνης Όπως και προηγουμένως, πριν την κυρίως πειραματική διαδικασία πραγματοποιήθηκε υπολογισμός της καμπύλης δόσης-απόκρισης της λεπτίνης στη διαδικασία εξωτερίκευσης των υποδοχέων CD36 στην επιφάνεια των μονοκυττάρων προκειμένου να επιλεγεί η πιο αποτελεσματική συγκέντρωσή της. Διαπιστώθηκε ότι η λεπτίνη, σε όλες τις συγκεντρώσεις που χρησιμοποιήθηκαν (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml), αύξησε τα επίπεδα επιφανειακής έκφρασης των υποδοχέων CD36 έπειτα από 30min επώασης και μάλιστα αυτή η αύξηση ήταν σε όλες τις περιπτώσεις στατιστικά σημαντική σε σχέση με το δείγμα ελέγχου (διάγραμμα 5). Συγκεκριμένα, η λεπτίνη προκάλεσε αυξήσεις στην εξωτερίκευση των 99
100 υποδοχεών CD36 της τάξης του 22,50 ± 4,36% (1,6 ng/ml), 27,30 ± 5,51% (16 ng/ml), 47,01 ± 7,91% (160 ng/ml) και 41,96 ± 8,38% (1600 ng/ml). Η μέγιστη τιμή σημειώθηκε σε συγκέντρωση λεπτίνης 160 ng/ml, οπότε αυτή επιλέχθηκε για την πειραματική διαδικασία. Διάγραμμα 5. Καμπύλη δόσης-απόκρισης της λεπτίνης για το πείραμα μέτρησης των επιπέδων επιφανειακής έκφρασης των υποδοχέων CD36. Τα μονοκύτταρα επωάστηκαν με τέσσερις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml) για 30 min / 37 o C. Τα αποτελέσματα της καμπύλης αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test και εκφράζονται ως τιμές επί τοις εκατό (%) μεγαλύτερες του δείγματος ελέγχου. Τα αποτελέσματα και στις τέσσερις συγκεντρώσεις λεπτίνης που ελέγχθηκαν εμφάνισαν στατιστικά σημαντική αύξηση σε σχέση με το δείγμα ελέγχου (P<0,05). Η κλίμακα στον x άξονα είναι λογαριθμική. * P<0,05 σε σχέση τόσο με το δείγμα συγκέντρωσης 1,6 ng/ml, όσο και με το δείγμα συγκέντρωσης 16 ng/ml. Figure 5. Dose response curve of leptin for the experiment of CD36 receptor expression on the surface of monocytes. Monocytes were incubated with leptin at four different concentrations (1.6 ng/ml, 16 ng/ml, 160 ng/ml, 1600 ng/ml) for 30 min / 37 o C. The results of the curve are presented as the mean percent increases ± standard deviations versus the control sample of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. The increase caused by leptin was statistically significant (P<0.05) compared to the control sample at all four leptin concentrations which were used. The logarithmic scale is used on the x axis. * P<0.05 versus leptin samples 1.6ng/ml and 16 ng/ml. 100
101 Β) Πειραματικά αποτελέσματα Η λεπτίνη (160 ng/ml) όπως είχε διαπιστωθεί και από τα αποτελέσματα της καμπύλης δόσης-απόκρισης αύξησε κατά στατιστικά σημαντικό τρόπο τα επίπεδα επιφανειακής έκφρασης των υποδοχέων CD36 (διάγραμμα 6). Συγκεκριμένα, στο δείγμα που επωάστηκε με λεπτίνη σε αυτή τη συγκέντρωση, η επιφανειακή έκφραση των υποδοχέων CD36 ήταν αυξημένη κατά 50% σε σχέση με το δείγμα ελέγχου. Η δράση της λεπτίνης περιορίστηκε κατά στατιστικά σημαντικό τρόπο όταν προηγήθηκε κατάλληλη μεμονωμένη φαρμακολογική αναστολή του ΝΗΕ1, της PI3K, των πρωτεϊνικών κινασών C (και πιο συγκεκριμένα των επονομαζόμενων συμβατικών ισομορφών α-, β i - και β ii - αυτής) και της NADPH οξειδάσης (διάγραμμα 6). Η αναστολή καθενός εκ των προαναφερθέντων δεν επέτρεψε στα επίπεδα επιφανειακής έκφρασης των υποδοχέων CD36 να ξεπεράσουν τα επίπεδα του δείγματος ελέγχου, παρά την επίδραση της λεπτίνης. Αξίζει να σημειωθεί ότι η αναστολή της συνθάσης του ΝΟ για άλλη μια φορά δεν παρατηρήθηκε να επιδρά στη δράση της λεπτίνης. Μέτρηση της μεμονωμένης δράσης των αναστολέων έναντι του δείγματος ελέγχου απουσία λεπτίνης δεν οδήγησε σε στατιστικά σημαντικές διαφορές (Πίνακας 3). Διάγραμμα 6. Επιφανειακή έκφραση των υποδοχέων CD36 σε μονοκύτταρα έπειτα από επώαση με λεπτίνη με ή χωρίς αναστολείς. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική 101
102 επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 160 ng/ml. Figure 6. Expression of the CD36 receptor on the surface of monocytes after incubation with leptin in the presence or absence of pharmacological inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 160 ng/ml for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. ** P<0,05 versus leptin sample 160 ng/ml. 3.2 Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD68 Η λεπτίνη (160 ng/ml, χρησιμοποιήθηκε η συγκέντρωση η οποία προηγουμένως προκάλεσε μέγιστη επιφανειακή έκφραση του υποδοχέα CD36) δεν διαπιστώθηκε να αυξάνει κατά στατιστικά σημαντικό τρόπο την εξωτερίκευση του υποδοχέαρακοσυλλέκτη CD68 (διάγραμμα 7). Διάγραμμα 7. Επίπεδα έκφρασης του υποδοχέα-ρακοσυλλέκτη CD68 στην επιφάνεια μονοκυττάρων ανθρώπου. Τα μονοκύτταρα επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα είναι ενδεικτικά τουλάχιστον τριών πειραμάτων με τη χρήση κυτταρομετρίας ροής. Figure 7. Surface expression levels of scavenger receptor CD29 in human monocytes. Cells were incubated with leptin 160 ng/ml for 30 min /37 o C. Results are indicative of at least three experiments in which flow cytometry was utilized. 4. Προσδιορισμός της επιφανειακής έκφρασης υπομονάδων των ιντεγκρινών Όπως διαπιστώθηκε, η λεπτίνη (160 ng/ml) προκάλεσε στατιστικά σημαντική αύξηση των επίπεδων τόσο της προσκόλλησης, όσο και της μετανάστευσης των 102
103 μονοκυττάρων ανθρώπου σε υπόστρωμα λαμινίνης-1. Είναι γνωστό ότι οι διαδικασίες της προσκόλλησης και της μετανάστευσης απαιτούν πολύπλοκες αλληλεπιδράσεις μεταξύ επιφανειακών πρωτεϊνών των μονοκυττάρων (π.χ. τις ιντεγκρίνες) και των επιφανειακών πρωτεϊνών άλλων κυττάρων (π.χ. των ενδοθηλιακών κυττάρων) ή/και συστατικών της εξωκυττάριας ουσίας (π.χ. λαμινίνη-1). Έτσι, μελετήθηκε κατά πόσον η αύξηση των επιπέδων προσκόλλησηςμετανάστευσης που προκαλεί η λεπτίνη (160 ng/ml) οφείλονται στην αύξηση των επιπέδων επιφανειακής έκφρασης υπομονάδων των ιντεγκρινών και συγκεκριμένα των CD29, CD49b, CD18, CD11a και CD11b. Αρχικές μετρήσεις δόσης απόκρισης της λεπτίνης διενεργήθηκαν με μετρήσεις σε φθορισμόμετρο χωρίς η λεπτίνη να φαίνεται να επηρεάζει την εξωτερίκευση των παραπάνω πρωτεϊνών κατά στατιστικά σημαντικό τρόπο (Πίνακας 4). Παρόλα αυτά κρίθηκε σκόπιμη η επιβεβαίωση αυτού του αποτελέσματος με μετρήσεις σε κυτταρόμετρο ροής. 4.1 Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD29 Η επιφανειακή πρωτεΐνη CD29 (γνωστή και ως β 1 υπομονάδα των ιντεγκρινών) αποτελεί μία από τις δύο υπομονάδες των ιντεγκρινών α 2 β 1 και α 6 β 1 που θεωρούνται υποδοχείς των λαμινινών, καθώς και της α 4 β 1 (γνωστής και ως VLA-4).Η λεπτίνη (160 ng/ml) δεν διαπιστώθηκε να αυξάνει κατά στατιστικά σημαντικό τρόπο την επιφανειακή έκφραση της CD29 (διάγραμμα 8). Τα αποτελέσματά αυτά υποδηλώνουν ότι παρά το ρόλο των ιντεγκρινών α 2 β 1 και α 6 β 1 ως υποδοχείς λαμινίνης, η λεπτίνη δεν φαίνεται να τις αξιοποιεί κατά την ενίσχυση της προσκόλλησης και της μετανάστευσης των μονοκυττάρων σε υπόστρωμα λαμινίνης-1 που προκαλεί. 103
104 Διάγραμμα 8. Επίπεδα έκφρασης της πρωτεϊνης CD29 στην επιφάνεια μονοκυττάρων ανθρώπου. Τα μονοκύτταρα επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα είναι ενδεικτικά τουλάχιστον τριών πειραμάτων με τη χρήση κυτταρομετρίας ροής. Figure 8. Surface expression levels of protein CD29 in human monocytes. Cells were incubated with leptin 160 ng/ml for 30 min /37oC. Results are indicative of at least three experiments in which flow cytometry was utilized Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD49b Η επιφανειακή πρωτεΐνη CD49b (γνωστή και ως α 2 υπομονάδα των ιντεγκρινών) αποτελεί συστατικό της ιντεγκρίνης α 2 β 1 που όπως αναφέρθηκε παραπάνω αποτελεί υποδοχέα των λαμινινών. Διαπιστώθηκε ότι όπως και στην περίπτωση της β 1 υπομονάδας (CD29) η λεπτίνη δεν προκάλεσε στατιστικά σημαντική μεταβολή της έκφρασης της CD49b στην επιφάνεια των μονοκυττάρων (διάγραμμα 9). Διάγραμμα 9. Επίπεδα έκφρασης της πρωτεΐνης CD49b στην επιφάνεια μονοκυττάρων ανθρώπου. Τα μονοκύτταρα επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα είναι ενδεικτικά τουλάχιστον τριών πειραμάτων με τη χρήση κυτταρομετρίας ροής. Figure 9. Surface expression levels of protein CD49b in human monocytes. Cells were incubated with leptin 160 ng/ml for 30 min /37 o C. Results are indicative of at least three experiments in which flow cytometry was utilized Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD18 Η επιφανειακή πρωτεΐνη CD18 (γνωστή και ως β 2 υπομονάδα των ιντεγκρινών) συμμετέχει στη δομή των ιντεγκρινών α L β 2 (γνωστή ως LFA-1) και α Μ β 2 (γνωστή και ως Mac-1). Από τα πειράματά μας διαπιστώθηκε ότι η λεπτίνη (160 ng/ml) δεν 104
105 προκάλεσε στατιστικά σημαντική μεταβολή της έκφρασης της CD49b στην επιφάνεια των μονοκυττάρων (διάγραμμα 10). Διάγραμμα 10. Επίπεδα έκφρασης της πρωτεϊνης CD18 στην επιφάνεια μονοκυττάρων ανθρώπου. Τα μονοκύτταρα επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα είναι ενδεικτικά τουλάχιστον τριών πειραμάτων με τη χρήση κυτταρομετρίας ροής. Figure 10. Surface expression levels of protein CD18 in human monocytes. Cells were incubated with leptin 160 ng/ml for 30 min /37 o C. Results are indicative of at least three experiments in which flow cytometry was utilized. 4.4 Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD11a Η επιφανειακή πρωτεΐνη CD11a (γνωστή και ως a L υπομονάδα των ιντεγκρινών) συμμετέχει στη δομή της ιντεγκρίνης α L β 2 (γνωστής ως LFA-1). Από τα πειράματά μας διαπιστώθηκε ότι η λεπτίνη (160 ng/ml) δεν προκάλεσε στατιστικά σημαντική μεταβολή της έκφρασης της CD11a στην επιφάνεια των μονοκυττάρων (διάγραμμα 11). 105
106 Διάγραμμα 11. Επίπεδα έκφρασης της πρωτεϊνης CD11a στην επιφάνεια μονοκυττάρων ανθρώπου. Τα μονοκύτταρα επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα είναι ενδεικτικά τουλάχιστον τριών πειραμάτων με τη χρήση κυτταρομετρίας ροής. Figure 11. Surface expression levels of protein CD11a in human monocytes. Cells were incubated with leptin 160 ng/ml for 30 min /37 o C. Results are indicative of at least three experiments in which flow cytometry was utilized. 4.5 Προσδιορισμός της επιφανειακής έκφρασης των υποδοχέων CD11b Η επιφανειακή πρωτεΐνη CD11b (γνωστή και ως a M υπομονάδα των ιντεγκρινών) συμμετέχει στη δομή των ιντεγκρινών α L β 2 (γνωστή ως LFA-1) και α Μ β 2 (γνωστή και ως Mac-1). Από τα πειράματά μας διαπιστώθηκε ότι η λεπτίνη (160 ng/ml) δεν προκάλεσε στατιστικά σημαντική μεταβολή της έκφρασης της CD49b στην επιφάνεια των μονοκυττάρων (διάγραμμα 12). Διάγραμμα 12. Επίπεδα έκφρασης της πρωτεϊνης CD11b στην επιφάνεια μονοκυττάρων ανθρώπου. Τα μονοκύτταρα επωάστηκαν με λεπτίνη 160 ng/ml για 30 min / 37 o C. Τα αποτελέσματα είναι ενδεικτικά τουλάχιστον τριών πειραμάτων με τη χρήση κυτταρομετρίας ροής. Figure 12. Surface expression levels of protein CD29 in human monocytes. Cells were incubated with leptin 160 ng/ml for 30 min /37 o C. Results are indicative of at least three experiments in which flow cytometry was utilized. 5. Προσδιορισμός φαγοκύττωσης των oxldl 3 από μονοκύτταρα Α) Καμπύλη δόσης-απόκρισης λεπτίνης Μετά τη διαπίστωση ότι η λεπτίνη αυξάνει την επιφανειακή έκφραση του υποδοχέα CD36, μελετήθηκε η επίδραση της στο αμέσως επόμενο στάδιο της 106
107 διαδικασίας, δηλαδή την φαγοκύττωση των oxldls. Όπως και στις προηγούμενες περιπτώσεις, πριν την κυρίως πειραματική διαδικασία πραγματοποιήθηκε υπολογισμός της καμπύλης δόσης-απόκρισης της λεπτίνης στην φαγοκύττωση των μετρίων οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας (oxldl 3 ) από τα μονοκύτταρα προκειμένου να επιλεγεί η πιο αποτελεσματική συγκέντρωσή της. Διαπιστώθηκε ότι η λεπτίνη, σε όλες τις συγκεντρώσεις που χρησιμοποιήθηκαν (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml), αύξησε τα επίπεδα εσωτερίκευσης των oxldl 3 από τα μονοκύτταρα έπειτα από 1 h και 3 h επώασης και μάλιστα αυτή η αύξηση ήταν σε όλες τις περιπτώσεις στατιστικά σημαντικά διαφορετική σε σχέση με το δείγμα ελέγχου. Συγκεκριμένα, έπειτα από 1 h επώασης η λεπτίνη προκάλεσε αυξήσεις στα επίπεδα φαγοκύττωσης των oxldl 3 από τα μονοκύτταρα της τάξης του 36,60 ± 3,00% (1,6 ng/ml), 44,5 ± 3,03% (16 ng/ml), 42,00 ± 3,52% (160 ng/ml) και 55,12 ± 3,46% (1600 ng/ml) (διάγραμμα 13). Αντίστοιχα έπειτα από 3 h επώασης η λεπτίνη προκάλεσε αυξήσεις στα επίπεδα φαγοκύττωσης των oxldl 3 από τα μονοκύτταρα της τάξης του 48,11 ± 2,99% (1,6 ng/ml), 57,10 ± 2,32% (16 ng/ml), 62,98 ± 4,81% (160 ng/ml) και 43,50 ± 4,98% (1600 ng/ml) (διάγραμμα 14). Με δεδομένο ότι οι μετρήσεις εξωτερίκευσης των υποδοχέων CD36 (ενός από τους κυριότερους υποδοχείς για τις oxldls) έγιναν με επίδραση λεπτίνης σε συγκέντρωση 160 ng/ml και σε συνάρτηση με το γεγονός ότι αυτή η συγκέντρωση είχε το μέγιστο αποτέλεσμα έπειτα από 3 h, καθώς και ικανοποιητικό αποτέλεσμα έπειτα από 1 h, αποφασίστηκε η επιλογή της για τα πειράματα με τη χρήση φαρμακολογικής αναστολής που ακολούθησαν. Επιπρόσθετα, η επιλογή των χρόνων επώασης της 1 h και των 3 h έγινε με γνώμονα το γεγονός ότι όπως διαπιστώθηκε από το προηγούμενο πείραμα, για την επιφανειακή έκφραση των υποδοχέων CD36, η οποία είναι απαραίτητο να προηγηθεί προκειμένου να γίνει η φαγοκύττωση των oxldl 3, απαιτούνται τουλάχιστον 30 min. 107
108 Διάγραμμα 13. Καμπύλη δόσης-απόκρισης της λεπτίνης έπειτα από 1 h επώασης για το πείραμα μέτρησης των επιπέδων φαγοκύττωσης των μετρίως οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας από τα μονοκύτταρα. Τα μονοκύτταρα επωάστηκαν με τέσσερις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml) για 1 h / 37 o C. Τα αποτελέσματα της καμπύλης αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test και εκφράζονται ως τιμές επί τοις εκατό (%) μεγαλύτερες του δείγματος ελέγχου. Τα αποτελέσματα και στις τέσσερις συγκεντρώσεις λεπτίνης που ελέγχθηκαν εμφάνισαν στατιστικά σημαντική αύξηση σε σχέση με το δείγμα ελέγχου (P<0,05). Η κλίμακα στον x άξονα είναι λογαριθμική. * P<0,05 σε σχέση τόσο με το δείγμα συγκέντρωσης 1,6 ng/ml, όσο και με το δείγμα συγκέντρωσης 16 ng/ml, αλλά και με το δείγμα συγκέντρωσης 160 ng/ml. Figure 13. Dose response curve of leptin after 1 h of incubation for the measurement of moderately oxidized lipoproteins (oxldl 3 ) by monocytes. Monocytes were incubated with leptin at four different concentrations (1.6 ng/ml, 16 ng/ml, 160 ng/ml, 1600 ng/ml) for 1 h / 37 o C. The results of the curve are presented as the mean percent increases ± standard deviations versus the control sample of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. The increase caused by leptin was statistically significant (P<0.05) compared to the control sample at all four leptin concentrations which were used. The logarithmic scale is used on the x axis. * P<0.05 versus leptin samples 1.6ng/ml, 16 ng/ml and 160 ng/ml. 108
109 Διάγραμμα 14. Καμπύλη δόσης-απόκρισης της λεπτίνης έπειτα από 3h επώασης για το πείραμα μέτρησης των επιπέδων φαγοκύττωσης των μετρίως οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας από τα μονοκύτταρα. Τα μονοκύτταρα επωάστηκαν με τέσσερις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml, 160 ng/ml και 1600 ng/ml) για 3 h / 37 o C. Τα αποτελέσματα της καμπύλης αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test και εκφράζονται ως τιμές επί τοις εκατό (%) μεγαλύτερες του δείγματος ελέγχου. Τα αποτελέσματα και στις τέσσερις συγκεντρώσεις λεπτίνης που ελέγχθηκαν εμφάνισαν στατιστικά σημαντική αύξηση σε σχέση με το δείγμα ελέγχου (P<0,05). Η κλίμακα στον x άξονα είναι λογαριθμική. * P<0,05 σε σχέση τόσο με το δείγμα συγκέντρωσης 1,6 ng/ml, όσο και με το δείγμα συγκέντρωσης 1600 ng/ml. Figure 14. Dose response curve of leptin after 3 h of incubation for the measurement of moderately oxidized lipoproteins (oxldl 3 ) by monocytes. Monocytes were incubated with leptin at four different concentrations (1.6 ng/ml, 16 ng/ml, 160 ng/ml, 1600 ng/ml) for 3 h / 37 o C. The results of the curve are presented as the mean percent increases ± standard deviations versus the control sample of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. The increase caused by leptin was statistically significant (P<0.05) compared to the control sample at all four leptin concentrations which were used. The logarithmic scale is used on the x axis. * P<0.05 versus leptin samples 1.6ng/ml and 1600 ng/ml. 109
110 Β) Πειραματικά αποτελέσματα Ως γνωστόν, ο υποδοχέας CD36 είναι ένας από τους κυρίαρχους υποδοχείς όσον αφορά στη δέσμευση και φαγοκύττωση των oxldl 3 από τα μονοκύτταρα. Με βάση τα αποτελέσματα του πειράματος επίδρασης της λεπτίνης στην επιφανειακή έκφραση των υποδοχέων CD36, έγινε η υπόθεση ότι η αναστολή της επιφανειακής έκφρασης αυτών των υποδοχέων θα είχε ως αποτέλεσμα τη μείωση των επιπέδων φαγοκύττωσης των oxldl 3 από τα μονοκύτταρα. Για αυτό το λόγο στο συγκεκριμένο πείραμα χρησιμοποιήθηκαν μόνο οι φαρμακολογικοί αναστολείς που φάνηκε να επιδρούν στο μηχανισμό της λεπτίνης στο πείραμα επιφανειακής έκφρασης των υποδοχέων CD36. Η λεπτίνη (160 ng/ml) όπως είχε διαπιστωθεί και από τα αποτελέσματα της καμπύλης δόσης-απόκρισης αύξησε κατά στατιστικά σημαντικό τρόπο τα επίπεδα φαγοκύττωσης των oxldl 3 από τα μονοκύτταρα για χρονικά διαστήματα επώασης 1 h και 3 h. Συγκεκριμένα, επώαση με λεπτίνη (160 ng/ml) για 1 h αύξησε τα επίπεδα φαγοκύττωσης των oxldl 3 κατά 54% σε σχέση με το δείγμα ελέγχου. Η δράση της λεπτίνης περιορίστηκε κατά στατιστικά σημαντικό τρόπο όταν προηγήθηκε κατάλληλη μεμονωμένη φαρμακολογική αναστολή του ΝΗΕ1, της PI3K, των πρωτεϊνικών κινασών C (και πιο συγκεκριμένα των επονομαζόμενων συμβατικών ισομορφών α-, β i - και β ii - αυτής) και της NADPH οξειδάσης (διάγραμμα 15). Αντίστοιχα ήταν τα αποτελέσματα επώασης με λεπτίνη (160 ng/ml) για 3 h, όπου παρατηρήθηκε αύξηση των επιπέδων φαγοκύττωσης των oxldl 3 κατά 64% σε σχέση με το δείγμα ελέγχου, ενώ πάλι κατάλληλη μεμονωμένη φαρμακολογική αναστολή του ΝΗΕ1, της PI3K, των πρωτεϊνικών κινασών C (και πιο συγκεκριμένα των επονομαζόμενων συμβατικών ισομορφών α-, β i - και β ii - αυτής) και της NADPH οξειδάσης περιόρισε κατά στατιστικά σημαντικό τρόπο τη δράση της λεπτίνης (διάγραμμα 16). Μέτρηση της μεμονωμένης δράσης των αναστολέων έναντι του δείγματος ελέγχου απουσία λεπτίνης δεν οδήγησε σε στατιστικά σημαντικές διαφορές (Πίνακες 5, 6). 110
111 Διάγραμμα 15. Μέτρηση των επιπέδων φαγοκύττωσης των oxldl 3 από μονοκύτταρα έπειτα από επώαση με λεπτίνη με ή χωρίς αναστολείς για 1 h. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 160 ng/ml για 1 h / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 160 ng/ml. Figure 15. Measurement of oxldl 3 uptake levels by monocytes after incubation for 1 h with leptin in the presence or absence of pharmacological inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 160 ng/ml for 1 h / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0,05 versus the control sample. ** P<0.05 versus leptin sample 160 ng/ml. 111
112 Διάγραμμα 16. Μέτρηση των επιπέδων φαγοκύττωσης των oxldl 3 από μονοκύτταρα έπειτα από επώαση με λεπτίνη με ή χωρίς αναστολείς για 3 h. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 160 ng/ml για 3 h / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 160 ng/ml. Figure 16. Measurement of oxldl 3 uptake levels by monocytes after incubation for 3 h with leptin in the presence or absence of pharmacological inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 160 ng/ml for 1 h / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0,05 versus the control sample. ** P<0.05 versus leptin sample 160 ng/ml. 6. Προσδιορισμός φαγοκύττωσης των oxldl 24 από μονοκύτταρα Ελέγχθηκε επίσης η επίδραση της ίδιας συγκέντρωσης λεπτίνης (160 ng/ml) στα επίπεδα φαγοκύττωσης των πλήρως οξειδωμένων λιποπρωτεϊνών χαμηλής πυκνότητας (oxldl 24 ) από τα μονοκύτταρα. Δεν διαπιστώθηκε στατιστικά σημαντική επίδραση της λεπτίνης στη φαγοκύττωση των oxldl 24 έπειτα από επώαση για 1 h, 3 h και 5 h σε σχέση με το δείγμα ελέγχου (διάγραμμα 17). 112
113 Διάγραμμα 17. Μέτρηση των επιπέδων φαγοκύττωσης των oxldl 24 από μονοκύτταρα έπειτα από επώαση με και χωρίς λεπτίνη (160 ng/ml) για 1 h, 3 h και 5 h. Τα μονοκύτταρα επωάστηκαν με λεπτίνη 160 ng/ml για 1 h, 3 h, 5 h / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. Τα δείγματα λεπτίνης δεν εμφάνισαν στατιστικά σημαντικές διαφορές σε σχέση με τα δείγματα ελέγχου και στεις τρεις χρονικές περιόδους που ελέγχθηκαν. Figure 17. Measurement of oxldl 24 uptake levels by monocytes after incubation for 1 h, 3 h and 5 h / 37 o C with leptin 160 ng/ml. Monocytes were incubated leptin 160 ng/ml for 1 h, 3 h, 5 h / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. No statistically significant differences were observed between the leptin samples and the control samples for all three time periods that were measured. 7. Προσδιορισμός τιμής ενδοκυτταρικού ph (phi) To ενδοκυτταρικό ph (phi) είναι ένας σπουδαίος ρυθμιστικός παράγοντας του ενδοκυτταρικού περιβάλλοντος, καθώς ανάλογα με την τιμή του ορισμένες πρωτεΐνες μεταπίπτουν στην ενεργή τους μορφή, ενώ άλλες απενεργοποιούνται. Ο ιοντοανταλλάκτης Na + -H + (NHE1) διαδραματίζει καίριο ρόλο στη ρύθμιση του ενδοκυτταρικού ph. Επιπρόσθετα, ο ΝΗΕ1 έχει καταδειχθεί ότι συμμετέχει σε μονοπάτια μεταγωγής σήματος. Με βάση τα προηγούμενα κρίθηκε σκόπιμο να 113
114 μελετηθεί η επίδραση της λεπτίνης στην τιμή του phi και κατά συνέπεια στην ενεργότητα του ΝΗΕ1. Έτσι, πραγματοποιήθηκε πείραμα δόσης-απόκρισης της λεπτίνης στη μεταβολή της τιμής του ενδοκυτταρικού ph. Η λεπτίνη, σε όλες τις συγκεντρώσεις της που χρησιμοποιήθηκαν (1,6 ng/ml, 16 ng/ml και 160 ng/ml), αύξησε στατιστικά σημαντικά την τιμή του phi των μονοκυττάρων. Συγκεκριμένα, μετρήθηκαν τιμές phi της τάξης των 7.09 ± 0.12 (1,6 ng/ml), 7.18 ± 0.22 (16 ng/ml) και 7.11 ± 0.14 (160 ng/ml) σε σχέση με τιμή phi 6.85 ± 0.05 για το δείγμα ελέγχου (διάγραμμα 18). Προηγούμενη αναστολή του ΝΗΕ1 απέτρεψε την αυξητική επίδραση της λεπτίνης στο phi. Υπενθυμίζεται ότι όπως αναφέρθηκε αναλυτικά και στο τμήμα Υλικά και Μέθοδοι, ελήφθησαν όλα τα απαραίτητα μέτρα ώστε οι όποιες μεταβολές του phi να είναι αποτέλεσμα μόνο της λειτουργίας του ΝΗΕ1 και όχι κάποιου από τους υπόλοιπους phi-ρυθμιστικούς μηχανισμούς των κυττάρων. H συγκέντρωση λεπτίνης 1600 ng/ml δεν χρησιμοποιήθηκε στο συγκεκριμένο πείραμα δόσης-απόκρισης και γενικότερα η χρήση της εγκαταλείφθηκε στα επόμενα πειράματα, καθότι κρίθηκε ως υπερβολικά υψηλή, μια ακραία περίπτωση που απαντάται πάρα πολύ σπάνια σε ασθενείς. Διάγραμμα 18. Απεικόνιση αποτελεσμάτων πειράματος δόσης-απόκρισης της λεπτίνης στη μεταβολή της τιμής του ενδοκυτταρικού ph (phi) σε συνδυασμό με αποτελέσματα αναστολής του ΝΗΕ1. Τα μονοκύτταρα επωάστηκαν με cariporide για 15 min / 37 o C και στη συνέχεια με τρεις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml και 160 ng/ml) για 30 min / 114
115 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το αντίστοιχο δείγμα ελέγχου. ** P<0,05 σε σχέση με το αντίστοιχο δείγμα συγκέντρωσης λεπτίνης. Figure 18. Dose response curve of leptin for the measurement of intracellular ph (phi) in conjunction with NHE1 inhibition. Monocytes were incubated with cariporide for 15 min / 37 o C followed by incubation with leptin at three diffenet concentrations (1,6 ng/ml, 16 ng/ml, 160ng/ml) for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. ** P<0,05 versus the respective leptin sample. Παράλληλα με την επίδραση της λεπτίνης στο phi ανθρώπινων μονοκυττάρων, μελετήθηκε και η επίδραση στο phi των ορμονών ρεζιστίνη και γκρελίνη, δύο ακόμα ορμονών των οποίων τα επίπεδα στο αίμα διαφοροποιούνται στους παχύσαρκους ασθενείς σε σχέση με ό,τι συμβαίνει σε άτομα κανονικού βάρους. Καμία από τις δύο αυτές ορμόνες δεν διαπιστώθηκε να έχει στατιστικά σημαντική επίδραση στο phi των ανθρώπινων μονοκυττάρων. Συγκεκριμένα, το δείγμα ελέγχου εμφάνισε τιμή phi 6,77 ± 0,07, ενώ τα δείγματα ρεζιστίνης σε συγκεντρώσεις 12ng/ml και 18ng/ml εμφάνισαν τιμές phi 6,80 ± 0,18 και 6,72 ± 0,21 αντίστοιχα και της γκρελίνης σε συγκεντρώσεις 0,5ng/ml, 1ng/ml και 2 ng/ml είχαν αντίστοιχα τιμές 6,80 ± 0,12, 6,87 ± 0,14 και 6,80 ± 0,17 (διάγραμμα 19). Λόγω του γεγονότος ότι η ρεζιστίνη και η γκρελίνη δεν επηρέασαν το phi και άρα την ενεργότητα του ΝΗΕ1, δεν μελετήθηκαν περαιτέρω. 115
116 Διάγραμμα 19. Απεικόνιση αποτελεσμάτων πειράματος δόσης-απόκρισης της ρεζιστίνης και της γκρελίνης στη μεταβολή της τιμής του ενδοκυτταρικού ph (phi). Τα μονοκύτταρα επωάστηκαν με δύο διαφορετικές συγκεντρώσεις ρεζιστίνης (12ng/ml και 18ng/ml) και τρεις διαφορετικές συγκεντρώσεις γκρελίνης (0,5ng/ml, 1ng/ml και 2ng/ml) για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. Δεν υπήρξαν στατιστικά σημαντικές διαφορές μεταξύ των δειγμάτων. Figure 19. Dose response experiment of resistin and ghrelin for the measurement of intracellular ph (phi). Monocytes were incubated with resistin at two different concentrations (12ng/ml and 18ng/ml) and with ghrelin at three diffenet concentrations (0.5 ng/ml, 1 ng/ml, 2ng/ml) for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. No statistically significant differences between the samples were observed. 8. Προσδιορισμός ελευθέρων ριζών με H 2 DCFDA Α) Καμπύλη δόσης-απόκρισης λεπτίνης Η υψηλή συγκέντρωση ελευθέρων ριζών στον υποενδοθηλιακό χώρο αποτελεί συχνά καταλυτικό παράγοντα της μετατροπής των λιποπρωτεϊνών χαμηλής πυκνότητας (LDLs) προς τις οξειδωμένες μορφές τους (oxldls), συμβάλλοντας έτσι στην αθηρωματική διαδικασία. Κατά συνέπεια αποφασίστηκε η μελέτη της επίδρασης της λεπτίνης στην παραγωγή οξειδωτικών ριζών από τα μονοκύτταρα. Όπως και στις προαναφερθείσες περιπτώσεις, έτσι και εδώ, πριν την κύρια πειραματική διαδικασία πραγματοποιήθηκε υπολογισμός της καμπύλης δόσηςαπόκρισης της λεπτίνης στη διαδικασία προσδιορισμού ελευθέρων ριζών με H 2 DCFDA προκειμένου να επιλεγεί η πιο αποτελεσματική συγκέντρωσή της. Διαπιστώθηκε ότι η λεπτίνη έπειτα από 30 min επώασης στις συγκεντρώσεις των 16 ng/ml και 160 ng/ml (αλλά όχι σε συγκέντρωση 1,6 ng/ml), αύξησε τα επίπεδα των ελευθέρων ριζών που ανιχνεύονται με τη χρήση του H 2 DCFDA κατά στατιστικά σημαντικό τρόπο σε σχέση με το δείγμα ελέγχου (διάγραμμα 20). Συγκεκριμένα, η λεπτίνη προκάλεσε αύξηση στα επίπεδα ελευθέρων ριζών της τάξης του 117,11% (16 ng/ml) και του 70,83% (160 ng/ml). Κατά συνέπεια, επιλέχθηκε η συγκέντρωση λεπτίνης 16 ng/ml για τη συνέχεια της πειραματικής διαδικασίας. 116
117 Διάγραμμα 20. Απεικόνιση αποτελεσμάτων πειράματος δόσης-απόκρισης της λεπτίνης σε μονοκύτταρα όσον αφορά τα επίπεδα των ελευθέρων ριζών που μπορούν να ανιχνευθούν με H 2 DCFDA. Τα μονοκύτταρα επωάστηκαν με τρεις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml και 160 ng/ml) για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman- Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Figure 20. Dose response curve of leptin for the measurement of oxidative species through the use of H 2 DCFDA. Monocytes were incubated with leptin at three different concentrations (1.6 ng/ml, 16 ng/ml, and 160 ng/ml) for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. Β) Πειραματικά αποτελέσματα Η λεπτίνη (16 ng/ml) όπως είχε διαπιστωθεί και από τα αποτελέσματα δόσηςαπόκρισης αύξησε κατά στατιστικά σημαντικό τρόπο τα επίπεδα των ελευθέρων ριζών που ανιχνεύονται με H 2 DCFDA (διάγραμμα 20). Συγκεκριμένα, το δείγμα που επωάστηκε με λεπτίνη σε αυτή τη συγκέντρωση είχε τιμή 126,38% μεγαλύτερη από το δείγμα ελέγχου. Η δράση της λεπτίνης περιορίστηκε κατά στατιστικά σημαντικό τρόπο όταν προηγήθηκε κατάλληλη μεμονωμένη φαρμακολογική αναστολή της PI3K και της NADPH οξειδάσης (διάγραμμα 21). Ιδιαίτερο ενδιαφέρον έχει το γεγονός ότι μεμονωμένη φαρμακολογική αναστολή του NHE1 ενίσχυσε περαιτέρω την επίδραση 117
118 της λεπτίνης με αποτέλεσμα τιμές επιπέδων ελευθέρων ριζών κατά 197,16% και 32,44% αυξημένες σε σχέση με το δείγμα ελέγχου και το δείγμα λεπτίνης (16 ng/ml) αντίστοιχα. Μεμονωμένη αναστολή της ΝΗΕ1 (χωρίς προσθήκη λεπτίνης στη συνέχεια) δεν επηρέασε τα επίπεδα ελευθέρων ριζών που ανιχνεύονται με H 2 DCFDA σε σχέση με το δείγμα ελέγχου (πίνακας 1). Κατά συνέπεια, η αναστολή του ΝΗΕ1 ενισχύει με κάποιο τρόπο τη δράση της λεπτίνης. Αξίζει να σημειωθεί ότι αναστολή των πρωτεϊνικών κινασών C και της συνθάσης του ΝΟ δεν παρατηρήθηκε να έχουν επίδραση στη δράση της λεπτίνης. Μέτρηση της μεμονωμένης δράσης των αναστολέων έναντι του δείγματος ελέγχου απουσία λεπτίνης δεν οδήγησε σε στατιστικά σημαντικές διαφορές (Πίνακας 7). Διάγραμμα 21. Μέτρηση των επιπέδων των ελευθέρων ριζών που μπορούν να ανιχνευθούν με H 2 DCFDA έπειτα από επώαση μονοκυττάρων με λεπτίνη παρουσία ή απουσία φαρμακολογικών αναστολέων. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 16 ng/ml για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 16 ng/ml. Figure 21. Measurement of oxidative species through the use of H 2 DCFDA after incubation of monocytes with leptin in the presence or absence of pharmacological inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 16 ng/ml for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences 118
119 between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls posttest. * P<0.05 versus the control sample. ** P<0,05 versus leptin sample 16 ng/ml. 9. Προσδιορισμός του ανιόντος σουπεροξειδίου Το H 2 DCFDA είναι μια φθορίζουσα ουσία με την οποία μπορεί να γίνει ικανοποιητική ανίχνευση μεγάλης ποικιλίας οξειδωτικών ριζών τόσο οξυγόνου (ROS) όσο και αζώτου (RNS) και είναι συνεπώς ένας καλός δείκτης για τη μέτρηση γενικού οξειδωτικού στρες. Ένα αδύνατο σημείο της χρήσης του όμως, είναι η μη δυνατότητα ικανοποιητικής ανίχνευσης του πολύ σημαντικού ανιόντος του σουπεροξειδίου (Ο -. 2 ). Έτσι, αποφασίστηκε η μελέτη της επίδρασης της λεπτίνης στην παραγωγή του ανιόντος του σουπεροξειδίου από τα μονοκύτταρα με τη χρήση καταρχήν της ουσίας ΝΒΤ (Nitro Blue Tetrazolium). Μετά τη λήψη των αποτελεσμάτων με ΝΒΤ, κρίθηκε απαραίτητη η επιβεβαίωσή τους με την πολύ ειδική για το ανιόν σουπεροξειδίου φθορίζουσα ουσία DHE (διυδροαιθίδιο). 9.1 Προσδιορισμός του ανιόντος σουπεροξειδίου με ΝΒΤ Α) Καμπύλη δόσης-απόκρισης λεπτίνης Όπως και στις προηγούμενες περιπτώσεις έτσι και εδώ, πριν την κύρια πειραματική διαδικασία πραγματοποιήθηκε υπολογισμός της καμπύλης δόσηςαπόκρισης της λεπτίνης στη διαδικασία προσδιορισμού της συγκέντρωσης των ανιόντων σουπεροξειδίου (Ο -. 2 ) με τη χρήση της ουσίας ΝΒΤ προκειμένου να επιλεγεί η πιο αποτελεσματική συγκέντρωσή της. Διαπιστώθηκε ότι η λεπτίνη έπειτα από 30 min επώασης στις συγκεντρώσεις των 1,6 ng/ml, 16 ng/ml και 160 ng/ml, αύξησε τα επίπεδα των ανιόντων σουπεροξειδίου που ανιχνεύονται με τη χρήση του ΝΒΤ κατά στατιστικά σημαντικό τρόπο σε σχέση με το δείγμα ελέγχου (διάγραμμα 22). Συγκεκριμένα, η λεπτίνη προκάλεσε αύξηση στα επίπεδα ελευθέρων ριζών της τάξης του 21,37% (1,6 ng/ml), του 48,16% (16 ng/ml) και του 32,52% (160 ng/ml). Κατά συνέπεια, επιλέχθηκε η συγκέντρωση λεπτίνης 16 ng/ml για τη συνέχεια της πειραματικής διαδικασίας. 119
120 Διάγραμμα 22. Απεικόνιση αποτελεσμάτων πειράματος δόσης-απόκρισης της λεπτίνης σε μονοκύτταρα όσον αφορά τα επίπεδα των ανιόντων σουπεροξειδίου (Ο -. 2 ) όπως ανιχνεύονται με την ουσία ΝΒΤ. Τα μονοκύτταρα επωάστηκαν με τρεις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml και 160 ng/ml) για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman- Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Figure 22. Dose response curve of leptin for the measurement of superoxide anions (O -. 2 ) through the use of NBT. Monocytes were incubated with leptin at three different concentrations (1.6 ng/ml, 16 ng/ml, and 160 ng/ml) for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls posttest. * P<0.05 versus the control sample. Β) Πειραματικά αποτελέσματα Η λεπτίνη (16 ng/ml) όπως είχε διαπιστωθεί και από τα αποτελέσματα δόσηςαπόκρισης αύξησε κατά στατιστικά σημαντικό τρόπο τα επίπεδα των ανιόντων σουπεροξειδίου (Ο -. 2 ) όπως ανιχνεύτηκαν με τη χρήση της ουσίας ΝΒΤ (διάγραμμα 22). Συγκεκριμένα, το δείγμα που επωάστηκε με λεπτίνη σε αυτή τη συγκέντρωση είχε τιμή 34,49% μεγαλύτερη από το δείγμα ελέγχου. Η δράση της λεπτίνης περιορίστηκε κατά στατιστικά σημαντικό τρόπο όταν προηγήθηκε κατάλληλη μεμονωμένη φαρμακολογική αναστολή του ΝΗΕ1, της PI3K, των πρωτεϊνικών κινασών C (και πιο συγκεκριμένα των επονομαζόμενων συμβατικών ισομορφών α-, β i - και β ii - αυτής), αλλά περιέργως όχι της NADPH οξειδάσης (διάγραμμα 23). Αξίζει 120
121 να σημειωθεί ότι αναστολή της συνθάσης του ΝΟ δεν παρατηρήθηκε να έχει επίδραση στη δράση της λεπτίνης. Διάγραμμα 23. Μέτρηση των επιπέδων των ανιόντων σουπεροξειδίου (Ο -. 2 ) όπως ανιχνεύονται με ΝΒΤ έπειτα από επώαση μονοκυττάρων με λεπτίνη παρουσία ή απουσία φαρμακολογικών αναστολέων. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 16 ng/ml για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 16 ng/ml. Figure 23. Measurement of superoxide anions (O -. 2 ) through the use of ΝΒΤ after incubation of monocytes with leptin in the presence or absence of pharmacological inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 16 ng/ml for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls posttest. * P<0.05 versus the control sample. ** P<0,05 versus leptin sample 16 ng/ml. 9.2 Προσδιορισμός του ανιόντος σουπεροξειδίου με DHE Με δεδομένο ότι η κύρια πηγή παραγωγής ανιόντων σουπεροξειδίου του κυττάρου είναι η NADPH οξειδάση αποτέλεσε παράδοξο η αναστολή της να μην έχει επίδραση στο φαινόμενο αυτό. Γενικώς, το ΝΒΤ δεν είναι τόσο ειδικό στην ανίχνευση ανιόντων σουπεροξειδίου όσο θα ήταν επιθυμητό και επιπρόσθετα δύναται να 121
122 τροποποιηθεί από ένζυμα του κυττάρου με αποτέλεσμα την παραγωγή παραπλανητικού αποτελέσματος (Μünzel et al. 2002). Έτσι, το ΝΒΤ τείνει να αντικατασταθεί στη βιβλιογραφια από νέες ουσίες, η κυριότερη από τις οποίες είναι η φθορίζουσα ουσία διυδροαιθίδιο (DHE). Το DHE υπερτερεί του ΝΒΤ καθότι είναι πολύ πιο ειδικό για το ανιόν σουπεροξειδίου, ενώ και η πειραματική διαδικασία που ακολουθείται είναι πολύ πιο απλή αφήνοντας λίγα περιθώρια για λάθη. Α) Καμπύλη δόσης-απόκρισης λεπτίνης Όπως και στις προηγούμενες περιπτώσεις έτσι και εδώ, πριν την κύρια πειραματική διαδικασία πραγματοποιήθηκε υπολογισμός της καμπύλης δόσηςαπόκρισης της λεπτίνης στη διαδικασία προσδιορισμού της συγκέντρωσης των ανιόντων σουπεροξειδίου (Ο -. 2 ) με τη χρήση της ουσίας DHE προκειμένου να επιλεγεί η πιο αποτελεσματική συγκέντρωσή της. Διαπιστώθηκε ότι η λεπτίνη έπειτα από 30 min επώασης στις συγκεντρώσεις των 1,6 ng/ml, 16 ng/ml και 160 ng/ml, αύξησε τα επίπεδα των ανιόντων σουπεροξειδίου που ανιχνεύονται με τη χρήση του DHE κατά στατιστικά σημαντικό τρόπο σε σχέση με το δείγμα ελέγχου (διάγραμμα 24). Συγκεκριμένα, η λεπτίνη προκάλεσε αύξηση στα επίπεδα ελευθέρων ριζών της τάξης του 31,71% (1,6 ng/ml), του 36,59% (16 ng/ml) και του 33,29% (160 ng/ml). Τα αποτελέσματα της λεπτίνης συγκέντρωσης 160 ng/ml διαφέρουν από τα αντίστοιχα με NBT, καθότι εδώ δεν φαίνεται να διαφέρουν από τις τιμές του δείγματος ελέγχου. Πάντως η συγκέντρωση λεπτίνης 16 ng/ml η οποία και επιλέχθηκε για τη συνέχεια της πειραματικής διαδικασίας είναι και στις δύο περιπτώσεις αυτή που προκαλεί τη μεγαλύτερη αύξηση στην παραγωγή ανιόντων σουπεροξειδίου. 122
123 Διάγραμμα 24. Απεικόνιση αποτελεσμάτων πειράματος δόσης-απόκρισης της λεπτίνης σε μονοκύτταρα όσον αφορά τα επίπεδα των ανιόντων σουπεροξειδίου (Ο -. 2 ) όπως ανιχνεύονται με διυδροαιθίδιο (DHE). Τα μονοκύτταρα επωάστηκαν με τρεις διαφορετικές συγκεντρώσεις λεπτίνης (1,6 ng/ml, 16 ng/ml και 160 ng/ml) για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student- Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Figure 24. Dose response curve of leptin for the measurement of superoxide anions (O -. 2 ) through the use of dihydroethidium (DHE). Monocytes were incubated with leptin at three different concentrations (1.6 ng/ml, 16 ng/ml, and 160 ng/ml) for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman- Keuls post-test. * P<0.05 versus the control sample. Β) Πειραματικά αποτελέσματα Η λεπτίνη (16 ng/ml) όπως είχε διαπιστωθεί και από τα αποτελέσματα δόσηςαπόκρισης αύξησε κατά στατιστικά σημαντικό τρόπο τα επίπεδα των ανιόντων σουπεροξειδίου (Ο -. 2 ) όπως ανιχνεύτηκαν με τη χρήση της ουσίας DHE (διάγραμμα 24). Συγκεκριμένα, το δείγμα που επωάστηκε με λεπτίνη σε αυτή τη συγκέντρωση είχε τιμή 32,74% μεγαλύτερη από το δείγμα ελέγχου. Η δράση της λεπτίνης περιορίστηκε κατά στατιστικά σημαντικό τρόπο όταν προηγήθηκε κατάλληλη μεμονωμένη φαρμακολογική αναστολή του ΝΗΕ1, της PI3K, των πρωτεϊνικών κινασών C (και πιο συγκεκριμένα των επονομαζόμενων συμβατικών ισομορφών α-, 123
124 β i - και β ii - αυτής) και της NADPH οξειδάσης (διάγραμμα 25). Διαπιστώθηκε έτσι αναντιστοιχία μεταξύ των αποτελεσμάτων των μεθόδων με DHE και ΝΒΤ όσον αφορά το δείγμα στο οποίο πραγματοποιήθηκε αναστολή της NADPH οξειδάσης. Στα άλλα δείγματα δεν παρατηρήθηκαν διαφοροποιήσεις. Όπως έχει ήδη αναφερθεί, οι μετρήσεις της παραγωγής ανιόντων σουπεροξειδίου με DHE υπερτερούν έναντι αυτών με NBT, με το τελευταίο να τείνει να αντικατασταθεί στη βιβλιογραφία από το πρώτο, τουλάχιστον όσον αφορά τη συγκεκριμένη εφαρμογή. Κατά συνέπεια, στο τμήμα συζήτηση θα συζητηθούν τα αποτελέσματα έπειτα από τη χρήση του DHE μόνο. Αξίζει επίσης να σημειωθεί ότι αναστολή της συνθάσης του ΝΟ δεν παρατηρήθηκε να έχει επίδραση στη δράση της λεπτίνης. Μέτρηση της μεμονωμένης δράσης των αναστολέων έναντι του δείγματος ελέγχου απουσία λεπτίνης δεν οδήγησε σε στατιστικά σημαντικές διαφορές (Πίνακας 8). Διάγραμμα 25. Μέτρηση των επιπέδων των ανιόντων σουπεροξειδίου (Ο -. 2 ) όπως ανιχνεύονται με DHE έπειτα από επώαση μονοκυττάρων με λεπτίνη παρουσία ή απουσία φαρμακολογικών αναστολέων. Τα μονοκύτταρα επωάστηκαν με τους κατάλληλους φαρμακολογικούς αναστολείς για 15 min / 37 o C και κατόπιν επωάστηκαν με λεπτίνη 16 ng/ml για 30 min / 37 o C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. ** P<0,05 σε σχέση με το δείγμα συγκέντρωσης 16 ng/ml. Figure 25. Measurement of superoxide anions (O -. 2 ) through the use of dihydroethidium (DHE) after incubation of monocytes with leptin in the presence or absence of pharmacological 124
125 inhibitors. Monocytes were incubated with the appropriate pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 16 ng/ml for 30 min / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student- Newman-Keuls post-test. * P<0.05 versus the control sample. ** P<0,05 versus leptin sample 16 ng/ml. 10. Προσδιορισμός δραστικότητας της δισμουτάσης του σουπεροξειδίου (SOD) Λαμβάνοντας υπόψιν την ικανότητα της λεπτίνης να αυξάνει την παραγωγή ελευθέρων ριζών (όπως μετρήθηκαν με H 2 DCFDA και DHE), κρίθηκε σκόπιμο να μετρηθεί η επίδραση της λεπτίνης στη δράση του ενζύμου δισμουτάση σουπεροξειδίου (SOD, superoxide dismutase) που αποτελεί έναν από τους πιο σημαντικούς αντι-οξειδωτικούς μηχανισμούς των κυττάρων. Η δισμουτάση του σουπεροξειδίου καταλύει την αντίδραση 2O H + H 2 O 2 + O 2 (Hancock et al. 2001). Έτσι έχει την ιδιαιτερότητα ότι από τη μία πλευρά εξουδετερώνει την οξειδωτική απειλή που αντιπροσωπεύουν τα ανιόντα σουπεροξειδίου, αλλά ταυτόχρονα αυξάνει τα επίπεδα μιας άλλης οξειδωτικής ουσίας, του υπεροξειδίου του υδρογόνου. Στο συγκεκριμένο πείραμα τα μονοκύτταρα επωάστηκαν με λεπτίνη σε συγκεντρώσεις 16 ng/ml και 160 ng/ml για χρονικά διαστήματα 30 min, 1 h και 2 h. Διαπιστώθηκε ότι η λεπτίνη στη συγκέντρωση των 16 ng/ml αύξησε στα πρώτα 30 min τη δράση της δισμουτάσης του σουπεροξειδίου (όπως αυτή μετρήθηκε σε U/ml) κατά 37,26% σε σχέση με το αντίστοιχο δείγμα ελέγχου. Στη συνέχεια η δράση της δισμουτάσης του σουπεροξειδίου μειώθηκε και επέστρεψε στα επίπεδα του δείγματος ελέγχου όπου και παρέμεινε μέχρι και τις 2 h (διάγραμμα 26). Επώαση με λεπτίνη σε συγκέντρωση 160 ng/ml προκάλεσε πάλι μια ταχεία αύξηση της τάξης του 47% στη δραστικότηα της δισμουτάσης του σουπεροξειδίου. Σε αυτή την περίπτωση, η δράση της λεπτίνης είχε πιο μεγάλη διάρκεια καθότι οι τιμές δραστικότητας της δισμουτάσης του σουπεροξειδίου μέχρι και τις 2 h παρέμειναν σε στατιστικά σημαντικά πιο υψηλά επίπεδα σε σχέση με τα αντίστοιχα δείγματα έλεγχου (διάγραμμα 26). 125
126 Διάγραμμα 26. Μέτρηση της δραστικότητας της δισμουτάσης του σουπεροξειδίου μονοκυττάρων με και χωρίς την επίδραση λεπτίνης. Τα μονοκύτταρα επωάστηκαν με λεπτίνη στις συγκεντρώσεις 16 ng/ml και 160 ng/ml για 30 min, 1 h και 2 h / 37 ο C. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου για το αντίστοιχο χρονικό σημείο. Figure 26. Measurement of superoxide dismutase (SOD) activity in the presence or absence of leptin. Monocytes were incubated with leptin at concentrations of 16 ng/ml and 160 ng/ml for 30 min, 1 h, 2 h / 37 o C. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample for the respective time period. 11. Ανοσοκαθίζηση της ΝΗΕ1 και ανίχνευση της Hsp70 και της γλουταθειόνης Από τα προηγούμενα πειράματα διαπιστώθηκε ότι η λεπτίνη προκαλεί την ενεργοποίηση του ΝΗΕ1 των μονοκυττάρων, ενώ αυξάνει και την παραγωγή οξειδωτικών ριζών από αυτά. Έτσι στη συνέχεια μελετήθηκε η επίδραση της λεπτίνης και του συνοδευτικού της οξειδωτικού στρες στην αλληλεπίδραση του ΝΗΕ1 με τους αντι-οξειδωτικούς μηχανισμούς της Hsp70 και της γλουταθειόνης. Επιλέχθηκε συγκέντρωση λεπτίνης 16 ng/ml, καθότι αυτή χρησιμοποιήθηκε στα πειράματα ενδοκυτταρικού ph (ή αλλιώς ενεργοποίησης του ΝΗΕ1) και στα πειράματα μέτρησης της παραγωγής οξειδωτικών ριζών που προηγήθηκαν. Η λεπτίνη (16 ng/ml) 126
127 δεν φάνηκε να επηρεάζει τη σύνδεση της Hsp70 στον ΝΗΕ1, αύξησε όμως τα επίπεδα γλουταθειονυλίωσης των μορίων Hsp70 που ήταν ήδη συνδεδεμένα με τον ΝΗΕ1 (εικόνα 1, σύγκριση στηλών 1 και 2). Αναστολή του ΝΗΕ1 πριν την επώαση με λεπτίνη προκάλεσε αύξηση τόσο των επιπέδων σύνδεσης των Hsp70-NHE1 όσο και στα επίπεδα γλουταθειονυλίωσης των μορίων Hsp70 που συμμετέχουν σε αυτή τη σύνδεση σε σχέση με το αποτέλεσμα μεμονωμένης δράσης λεπτίνης (εικόνα 1, σύγκριση στηλών 2 και 3). Αναστολή της PI3K ή των πρωτεϊνικών κινασών C πριν την επώαση με λεπτίνη είχε το αντίστροφο αποτέλεσμα από αυτό της μεμονωμένης δράσης της λεπτίνης, καθότι αύξησε τα επίπεδα της σύνδεσης Hsp70-NHE1 μειώνοντας όμως τα επίπεδα γλουταθειονυλίωσης των μορίων Hsp70 που συμμετέχουν σε αυτή τη σύνδεση (εικόνα 1, σύγκριση στηλών 4 και 5 με τη στήλη 2). Εικόνα 1. Ανίχνευση των ΝΗΕ1, Hsp70 και γλουταθειόνης (GSH) έπειτα από ανοσοκαθίζηση με αντίσωμα αντι-νηε1 στο προϊόν λύσης (lysate) μονοκυττάρων. Τα μονοκύτταρα επωάστηκαν με τους φαρμακολογικούς αναστολείς για 15 min / 37 o C, ακολούθησε επώαση με λεπτίνη 16 ng/ml για 30 min / 37 o C και στη συνέχεια λύση. Στο προϊόν λύσης των μονοκυττάρων πραγματοποιήθηκε ανοσοκαθίζηση με αντίσωμα αντι-νηε1 και εν συνεχεία ανάλυση μέσω Western blot. Επεξήγηση δειγμάτων: 1. Control, 2. Λεπτίνη 16 ng/ml, 3. Λεπτίνη 16 ng/ml + 127
128 Cariporide 20 nm, 4. Λεπτίνη 16 ng/ml + Wortmannin 50 nm, 5. Λεπτίνη 16 ng/ml + GF109203X 10 μμ. Picture 1. Detection of NHE1, Hsp70 and glutathione (GSH) after immunoprecipitation with anti-nhe1 antibody of monocyte lysates. Monocytes were incubated with the pharmacological inhibitors for 15 min / 37 o C followed by incubation with leptin 16 ng/ml for 30 min / 37 o C and finally lysis. Monocyte lysates were immunoprecipitated with anti-nhe1 antibody followed by analysis through Western blotting. Samples: 1. Control, 2. Leptin 16 ng/ml, 3. Leptin 16 ng/ml + Cariporide 20 nm, 4. Leptin 16 ng/ml + Wortmannin 50 nm, 5. Leptin 16 ng/ml + GF109203X 10 μμ. 128
129 Παράρτημα Αποτελεσμάτων Πίνακες Πίνακας 1. Μέτρηση της προσκόλλησης των μονοκυττάρων σε υπόστρωμα λαμινίνης-1, προκειμένου να προσδιοριστεί η επίδραση των φαρμακολογικών αναστολέων στο δείγμα ελέγχου απουσία λεπτίνης. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Table 1. Measurement of monocyte adhesion to laminin-1 in order to determine the effect of the pharmacological inhibitors on the control sample in the absence of leptin. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. Δείγμα Αριθμός προσκολλημένων μονοκυττάρων Control ± Λεπτίνη (160 ng/ml) ± * Cariporide (20 nm) ± Cytochalasin D (2 μμ) ± Wortmannin (50 nm) ± GF109203X (10 μμ) ± Gö6976 (500 nm) ± DPI (10 μμ) ± L-NAME (100 μμ) ± MPO 100% Control ± Πίνακας 2. Μέτρηση της μετανάστευσης των μονοκυττάρων διαμέσου υποστρώματος λαμινίνης-1, προκειμένου να προσδιοριστεί η επίδραση των φαρμακολογικών αναστολέων στο δείγμα ελέγχου απουσία λεπτίνης. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Table 2. Measurement of monocyte migration through laminin-1 in order to determine the effect of the pharmacological inhibitors on the control sample in the absence of leptin. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman- Keuls post-test. * P<0.05 versus the control sample. 129
130 Δείγμα Αριθμός μεταναστευόντων μονοκυττάρων Control ± Leptin (16 ng/ml) ± * Cariporide (20 nm) ± Cytochalasin D (2 μμ) ± Wortmannin (50 nm) ± GF109203X (10 μμ) ± Gö6976 (500 nm) ± DPI (10 μμ) ± L-NAME (100 μμ) ± Πίνακας 3. Μέτρηση της έκφρασης των υποδοχέων CD36 στην επιφάνεια των μονοκυττάρων, προκειμένου να προσδιοριστεί η επίδραση των φαρμακολογικών αναστολέων στο δείγμα ελέγχου απουσία λεπτίνης. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Table 3. Measurement of monocyte migration through laminin-1 in order to determine the effect of the pharmacological inhibitors on the control sample in the absence of leptin. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman- Keuls post-test. * P<0.05 versus the control sample. Δείγμα Ένταση φθορισμού EX495nm / EX525nm Control ± Leptin (16 ng/ml) ± * Cariporide (20 nm) ± Cytochalasin D (2 μμ) ± Wortmannin (50 nm) ± GF109203X (10 μμ) ± Gö6976 (500 nm) ± DPI (10 μμ) ± L-NAME (100 μμ) ± Πίνακας 4. Αποτελέσματα πειραμάτων δόσης-απόκρισης της λεπτίνης σε μονοκύτταρα ανθρώπου όσον αφορά την επιφανειακή έκφραση των πρωτεϊνών CD11a, CD11b, CD18, CD29 και CD49b. Οι τιμές εκφράζουν ένταση φθορισμού σε μήκος κύματος διέγερσης 495nm προς μήκος κύματος εκπομπής 525nm για όλες τις πρωτεϊνες (αντισώματα συζευγμένα με τη φθορίζουσα ουσία FITC), πλην της CD11a όπου εκφράζουν ένταση φθορισμού σε μήκος κύματος διέγερσης 542nm προς μήκος κύματος εκπομπής 575nm (αντίσωμα συζευγμένο με τη φθορίζουσα ουσία RPE). Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα 130
131 αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω oneway ANOVA με το Student-Newman-Keuls test. Table 4. Dose response results of leptin concerning surface expression of proteins CD11a, CD11b, CD18, CD29 και CD49b on human monocytes. Values express fluorescence intensity at an excitation wavelength of 495nm and an emission wavelength of 525nm for all proteins tested (antibodies conjugated with the fluorescence substance FITC), except for protein CD11a where values express fluorescence intensity at an excitation wavelength of 542nm and an emission wavelength of 575nm for all proteins tested (antibody conjugated with the fluorescence substance RPE). The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. Αντίσωμα Δείγμα Control Leptin (1,6 ng/ml) Leptin (16 ng/ml) Leptin (160 ng/ml) CD11a CD11b CD18 CD29 CD49b 110,86 ± 8,05 112,87 ± 36,31 114,40 ± 25,96 91,80 ± 23,93 55,13 ± 8,87 56,15 ± 10,11 56,57 ± 12,62 45,80 ± 9,73 136,77 ± 21,91 142,40 ± 52,93 144,49 ± 35,64 114,63 ± 29,12 51,80 ± 11,03 47,80 ± 8,67 61,42 ± 18,65 46,97 ± 12,21 39,69 ± 9,36 37,53 ± 16,27 38,42 ± 13,51 47,02 ± 30,40 Πίνακας 5. Μέτρηση της φαγοκύττωσης των oxldl 3 από τα μονοκύτταρα έπειτα από έκθεση 1 h σε αυτές, προκειμένου να προσδιοριστεί η επίδραση των φαρμακολογικών αναστολέων στο δείγμα ελέγχου απουσία λεπτίνης. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Table 5. Measurement of oxldl 3 uptake by monocytes after 1 h incubation with them in order to determine the effect of the pharmacological inhibitors on the control sample in the absence of leptin. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. 131
132 Δείγμα Ένταση φθορισμού EX520nm / EX578nm Control ± Leptin (16 ng/ml) ± * Cariporide (20 nm) ± Wortmannin (50 nm) ± GF109203X (10 μμ) ± Gö6976 (500 nm) ± DPI (10 μμ) ± Πίνακας 6. Μέτρηση της φαγοκύττωσης των oxldl 3 από τα μονοκύτταρα έπειτα από έκθεση 3 h σε αυτές, προκειμένου να προσδιοριστεί η επίδραση των φαρμακολογικών αναστολέων στο δείγμα ελέγχου απουσία λεπτίνης. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Table 6. Measurement of oxldl 3 uptake by monocytes after 3 h incubation with them in order to determine the effect of the pharmacological inhibitors on the control sample in the absence of leptin. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by one-way ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. Δείγμα Ένταση φθορισμού EX520nm / EX578nm Control ± Leptin (16 ng/ml) ± * Cariporide (20 nm) ± Wortmannin (50 nm) ± GF109203X (10 μμ) ± Gö6976 (500 nm) ± DPI (10 μμ) ± Πίνακας 7. Μέτρηση των επιπέδων των ελευθέρων ριζών που παράγονται από μονοκύτταρα με τη χρήση H 2 DCFDA προκειμένου να προσδιοριστεί η επίδραση των φαρμακολογικών αναστολέων στο δείγμα ελέγχου απουσία λεπτίνης. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Table 7. Measurement of oxidative species production by monocytes through the use of H 2 DCFDA in order to determine the effect of the pharmacological inhibitors on the control sample in the absence of leptin. The results are presented as the means ± standard deviations of at least six 132
133 experiments. The level of significance of the differences between the samples was calculated by oneway ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. Δείγμα Ένταση Φθορισμού EX498nm / EM522nm Control 4,529 ± 0,136 Leptin (16 ng/ml) 9,034 ± 0,532 * Cariporide (20 nm) 4,765 ± 0,280 Wortmannin (50 nm) 4,443 ± 0,310 DPI (10 μμ) 4,632 ± 0,407 Πίνακας 8. Μέτρηση των επιπέδων των ανιόντων σουπεροξειδίου (Ο -. 2 ) που παράγονται από μονοκύτταρα με τη χρήση DHE προκειμένου να προσδιοριστεί η επίδραση των φαρμακολογικών αναστολέων στο δείγμα ελέγχου απουσία λεπτίνης. Τα αποτελέσματα αποτελούν τους μέσους όρους ± τυπικές αποκλίσεις που προέκυψαν από τα αποτελέσματα τουλάχιστον έξι πειραμάτων στα οποία και έγινε στατιστική επεξεργασία μέσω one-way ANOVA με το Student-Newman-Keuls test. * P<0,05 σε σχέση με το δείγμα ελέγχου. Table 8. Measurement of superoxide anion (Ο -. 2 ) levels produced by monocytes through the use of DHE in order to determine the effect of the pharmacological inhibitors on the control sample in the absence of leptin. The results are presented as the means ± standard deviations of at least six experiments. The level of significance of the differences between the samples was calculated by oneway ANOVA with a Student-Newman-Keuls post-test. * P<0.05 versus the control sample. Δείγμα Ένταση Φθορισμού EX480nm / EM567nm Control 7,954 ± 0,424 Leptin (16 ng/ml) 10,283 ± 0,754 * Cariporide (20 nm) 7,645 ± 0,675 Wortmannin (50 nm) 7,776 ± 0,499 GF109203X (10 μμ) 8,034 ± 0,578 Gö6976 (500 nm) 8,213 ± 0,534 DPI (10 μμ) 8,001 ± 0,
134 Συζήτηση Μέρος Α Μελέτη της επίδρασης της λεπτίνης σε δυνητικά αθηρωματικές δράσεις των μονοκυττάρων ανθρώπου Σύμφωνα με πρόσφατα στοιχεία, το 75% των θανάτων στις ΗΠΑ οφείλεται σε καρδιαγγειακά νοσήματα, τα οποία σχετίζονται με αθηρωμάτωση (American Heart Association, 2005). Το συνολικό κόστος περίθαλψης όλων των ασθενών με καρδιαγγειακά νοσήματα στις ΗΠΑ το 2000 ήταν 326,6 δισεκατομμύρια δολάρια ($) (Lefkowitz & Willerson, 2001). Επιπρόσθετα, πάλι στις ΗΠΑ, προηγούμενη έρευνα είχε διαπιστώσει ότι η αθηρωμάτωση (είτε σε πολύ αρχικό, είτε σε πιο προχωρημένο στάδιο) ενυπήρχε στο 80-90% των ενηλίκων 30 ετών (Berenson & Pickoff, 1995). Με δεδομένη, τα τελευταία χρόνια, την απομάκρυνση των Ελλήνων από το μεσογειακό πρότυπο διατροφής και την υιοθέτηση σε μεγάλο ποσοστό του αμερικανικού προτύπου, σε συνδυασμό με τα υψηλά ποσοστά καπνιστών στον πληθυσμό, γίνεται αντιληπτό ότι η ελληνική πραγματικότητα τείνει να ταυτιστεί με αυτή των ΗΠΑ με αντίστοιχες συνέπειες για την ελληνική κοινωνία και οικονομία. Μεταξύ των κυριοτέρων τρόπων μείωσης του ενδεχομένου της αθηρωμάτωσης ή τουλάχιστον της προόδου της, περιλαμβάνονται η τροποποίηση της διατροφής του άτομου (μείωση της λήψης λιπαρών τροφών), η αύξηση της σωματικής άσκησης και η διακοπή του καπνίσματος. Επίσης, έχει διαπιστωθεί ότι ευεργετική προς την κατεύθυνση της πρόληψης της αθηρωμάτωσης είναι η μείωση των επιπέδων των LDLs και των τροποποιημένων τους μορφών στο αίμα. Το τελευταίο επιτυγχάνεται μέσω κατάλληλης διατροφής, αλλά και με τη χρήση σχετικά νέων και ιδιαίτερα αποτελεσματικών φαρμάκων, των στατινών. Οι στατίνες δρουν μέσω της αναστολής του ενζύμου αναγωγάση του μεθυλο-γλουτάμυλο συνενζύμου Α (ή HMG-CoA reductase) που έχει ως αποτέλεσμα τη μείωση της σύνθεσης χοληστερόλης από το ήπαρ, ενώ παράλληλα αυξάνουν την επιφανειακή έκφραση υποδοχέων των LDLs, συμβάλλοντας έτσι στην απομάκρυνση των τελευταίων από το αίμα (Lewis, 2009). Η τροποποίηση της διατροφής που αναφέρθηκε παραπάνω αφορά στη μείωση της πρόσληψης χοληστερόλης και τριγλυκεριδίων που ευνοούν την αύξηση της συγκέντρωσης των LDLs (και άρα και των πιο επικίνδυνων τροποιημένων τους μορφών) στο αίμα. Είναι πλέον πλήρως αποδεκτή η συσχέτιση 134
135 υπερχοληστερολαιμίας και αθηρογένεσης (Libby, 2002). Ταυτόχρονα, συνίσταται συνδυασμός σωματικής άσκησης και σωστής διατροφής προκειμένου να αποφευχθούν φαινόμενα παχυσαρκίας που θα είχαν ως αποτέλεσμα την καταπόνηση του καρδιαγγειακού συστήματος, αυξάνοντας παράλληλα την πιθανότητα για ασθένειες όπως ο διαβήτης και το μεταβολικό σύνδρομο (Lewis, 2009). Το τελευταίο είναι μία σχετικά πρόσφατα αναγνωρισμένη πολυπαραγοντική ασθένεια, η οποία χαρακτηρίζεται από τη συνύπαρξη στον ασθενή της παχυσαρκίας, της αθηρωμάτωσης, της αντίστασης στην ινσουλίνη με επακόλουθη υπερισνουλιναιμία και διαβήτη τύπου ΙΙ, της υπερλιπιδαιμίας και της στεφανιαίας νόσου (Sorrentino, 2005). Η αντίσταση στην ινσουλίνη που συνοδεύει τον διαβήτη τύπου ΙΙ, την παχυσαρκία και το μεταβολικό σύνδρομο υποστηρίζεται από ορισμένους ερευνητές ότι έχει ως αφετηρία βλάβες που προκαλούνται από οξειδωτικές ρίζες (Houstis et al, 2006). Η επακόλουθη αύξηση των επιπέδων δεικτών φλεγμονής όπως η κυτοκίνη TNF-α και γλυκοκορτικοειδή επιτείνει μια κατάσταση χρόνιας φλεγμονής που ευνοεί αθηρωματικές διαδικασίες. Το 2002 ο Παγκόσμιος Οργανισμός Υγείας (World Health Organization - W.H.O.) υπολόγισε την ύπαρξη παγκοσμίως περισσοτέρων του ενός δισεκατομμυρίου υπέρβαρων ενηλίκων, με τα 300 εκατομμύρια εξ αυτών να είναι επίσης κλινικά παχύσαρκοι (BMI >30) (Hotamisligil, 2006). Σύνηθες χαρακτηριστικό της παχυσαρκίας είναι η υπερλεπτιναιμία, δηλαδή η υψηλή συγκέντρωση της ορμόνης λεπτίνης στο αίμα. Η έκκριση της λεπτίνης στην κυκλοφορία είναι ανάλογη της ποσότητας του λιπώδους ιστού του ατόμου και μία από τις πρώτες δράσεις της που αναγνωρίστηκε ήταν η ικανότητά της να μειώνει την όρεξη, αποτρέποντας έτσι τη λήψη και άλλων θερμίδων από τον οργανισμό. Στην παρούσα εργασία μελετήθηκε η επίδραση της λεπτίνης σε πλήθος δυνητικά αθηρωματικών ιδιοτήτων των μονοκυττάρων, κυττάρων του ανοσοποιητικού συστήματος που εμπλέκονται σε διάφορα στάδια της αθηρωματικής διαδικασίας. 1.Γενικός ρόλος των μονοκυττάρων κατά την αθηρωμάτωση Το υγιές ενδοθήλιο, μέσω της δράσης αγγειοδιασταλτικών και αγγειοσυσταλτικών ουσιών όπως το ΝΟ, η ενδοθηλίνη κα η αγγειοτασίνη ΙΙ, ρυθμίζει τον αγγειακό τόνο και δρα αντιπηκτικά (Drexler, 1998). Δυσλειτουργία του ενδοθηλίου λόγω μικροτραυματισμών ή/και διαταραχής της ιδιότητάς του να ρυθμίζει 135
136 τον αγγειακό τόνο αυξάνουν τη διαπερατότητά του, τη συσσώρευση αιμοπεταλίων, καθώς και την προσκόλληση λευκοκυττάρων στο σημείο. Κατά τη διάρκεια των αρχικών σταδίων της αθηρογένεσης, τα μονοκύτταρα προσδένονται σε σημεία των αγγειακών τοιχωμάτων όπου τα τελευταία έχουν υποστεί μικροτραυματισμούς. Κατευθύνονται εκεί χημειοτακτικά χάρις στη δράση των χημοκινών που εκκρίνονται από τα γειτονικά στους μικροτραυματισμούς ενδοθηλιακά κύτταρα. Παράλληλα, τα μονοκύτταρα προσελκύονται και από παράγοντες όπως οι λιποπρωτεΐνες χαμηλής πυκνότητας (LDLs) που συσσωρεύονται εκεί και στον υποενδοθηλιακό χώρο. Μετά την ολοκλήρωση της προσκόλλησής τους ακολουθεί η μετανάστευσή τους προς τον υποενδοθηλιακό χώρο. Τα μονοκύτταρα, μέσω υπερβολικής παραγωγής δραστικών μορφών οξυγόνου (ROS) και αζώτου (RNS) μπορούν να προκαλέσουν βλάβη στο ενδοθήλιο, δημιουργώντας έτσι νέους μικροτραυματισμούς ή μεγεθύνοντας προϋπάρχοντες. Ο συνδυασμός των οξειδωτικών δραστικών μορφών, των οξειδωμένων LDLs και των κυτοκινών που εκκρίνονται από μονοκύτταρα, λεμφοκύτταρα, ενδοθηλιακά κύτταρα και λεία μυικά κύτταρα επιτείνουν μια κατάσταση φλεγμονής, απαραίτητη για τη συνέχιση της αθηρωματικής διαδικασίας που εν τέλει οδηγεί στη δημιουργία των αφρωδών κυττάρων, βασικών συστατικών των αθηρωματικών πλακών (Ross, 1999). 2.Επίδραση της λεπτίνης στην ικανότητα προσκόλλησης των μονοκυττάρων ανθρώπου στο συστατικό της εξωκυττάριας ουσίας λαμινίνη-1 Οι πειραματικές διατάξεις προσκόλλησης στη λαμινίνη-1 και μετανάστευσης διαμέσου αυτής που ακολουθεί αποτελούν καλές αναπαραστάσεις της βασικής διαδικασίας που πραγματοποιείται κατά την άφιξη των μονοκυττάρων στο σημείο της φλεγμονής. In vivo, έπειτα από τη χημειοτακτική προσέλκυσή τους τα μονοκύτταρα προσκολλώνται στο αγγειακό ενδοθήλιο μέσω αλληλεπιδράσεων με συστατικά της εξωκυττάριας ουσίας, όπως η λαμινίνη-1. Τα δεδομένα μιας πρόσφατης μελέτης κατέδειξαν ότι μακρόχρονη επώαση με λεπτίνη (1-100ng/ml για 7 ημέρες) αύξησε τα επίπεδα προσκόλλησης πρόδρομων ενδοθηλιακών κυττάρων (endothelial progenitor cells) σε πρωτεϊνες της εξωκυττάριας ουσίας (φιμπρονεκτίνη και βιτρονεκτίνη) και ώριμα ενδοθηλιακά κύτταρα (Schroeter et al. 2008). Έχει επίσης ενδιαφέρον το γεγονός ότι επώαση για το ίδιο χρονικό διάστημα με πολύ μεγάλη συγκέντρωση 136
137 λεπτίνης (1000ng/ml) είχε το αντίθετο αποτέλεσμα αναστέλλοντας τις δύο παραπάνω ιδιότητες. Αντίστοιχα, από τα αποτελέσματα της παρούσας εργασίας συμπεραίνεται ότι η λεπτίνη σε συγκέντρως 160ng/ml ευνοεί σημαντικά την προσκόλληση των μονοκυττάρων στην πρωτεϊνη της εξωκυττάριας ουσίας λαμινίνη-1. Η συγκέντρωση αυτή απαντάται σε υπερλεπτιναιμικούς ασθενείς και οφείλεται σχεδόν πάντα στην προσπάθεια του οργανισμού να αντιμετωπίσει την εκδηλούμενη παχυσαρκία αυτών των ασθενών. Αξίζει να παρατηρηθεί ότι στην ακόμη μεγαλύτερη συγκέντρωση των 1600ng/ml λεπτίνης τα επίπεδα προσκόλλησης των μονοκυττάρων δεν διαφέρουν από αυτά του δείγματος ελέγχου, κάτι που συμπίπτει με τις παρατηρήσεις των Schroeter et al. που προαναφέρθηκαν. Επιπρόσθετα, στα μονοπάτια μεταγωγής σήματος που εκκινούνται από τη λεπτίνη κατά τη διάρκεια της διαδικασίας προσκόλλησης συμμετέχουν ο ΝΗΕ1, ο κυτταροσκελετός της ακτίνης, η PI3K, συμβατικές ισομορφές της πρωτεϊνικής κινάσης C (α-, β I - και β II -), καθώς και η NADPH οξειδάση. Η ΝΗΕ1 είναι γνωστό ότι συνδέεται με τον κυτταροσκελετό της ακτίνης και μέσω αυτού μπορεί να λάβει και να μεταδώσει πληροφορία (Baumgartner et al., 2004). Έχει δειχθεί ότι τα μονοκύτταρα μπορούν και οξειδώνουν στοιχεία της εξωκυττάριας ουσίας και μάλιστα φαίνεται να προσκολλώνται ακόμα πιο εύκολα σε οξειδωμένη λαμινίνη-1 (Ahmed et al., 2003). Η οξείδωση της λαμινίνης-1 από ανιόντα σουπεροξειδίου, ως φαινόμενο του μικροπεριβάλλοντος, θα μπορούσε να εξηγήσει το ρόλο της NADPH οξειδάσης κατά την κυτταρική προσκόλληση. Γενικά, έχει δειχθεί ότι οξειδωτική βλάβη, κυρίως έπειτα από την επίδραση ισχυρών ριζών όπως το ΟΗ. και το HOCl, μπορούν να υποστούν τόσο πολυσακχαρίτες, όσο και πρωτεϊνες της εξωκυττάριας ουσίας (όπως το κολλαγόνο, η ελαστίνη, η φιμπρονεκτίνη και φυσικά οι λαμινίνες, κυρίως μέσω οξείδωσης των πλευρικών τους αλυσίδων) (Gilbert et al., 1984; Rees et al., 2008). Πρωτεΐνες της εξωκυττάριας ουσίας που περιέχουν αμινοξέα με ομάδα θειόλης, όπως η κυστεϊνη και η μεθειονίνη, είναι ιδιαίτερα ευαίσθητες στην οξειδωτική τροποποίηση δίνοντας τόσο αντιστρεπτά (π.χ. δισουλφίδια), όσο και μη αντιστρεπτά προϊόντα (π.χ. σουλφινικό οξύ), ο σχηματισμός των οποίων φυσικά και επηρεάζει την αρχική λειτουργία τους (Hawkins & Davies, 2001). Επιπρόσθετα, έχει παρατηρηθεί ότι η οξειδωτική τροποποίηση συστατικών της εξωκυττάριας ουσίας, αποτελεί παράγοντα 137
138 αποσταθεροποίησης του ινώδους καλύμματος, συμβάλλοντας έτσι στη ρήξη της αθηρωματικης πλάκας (Rees et al., 2008). 3.Επίδραση της λεπτίνης στην ικανότητα μετανάστευσης των μονοκυττάρων ανθρώπου διαμέσου του συστατικού της εξωκυττάριας ουσίας λαμινίνη-1 Έπειτα από την επιτυχημένη προσκόλληση των μονοκυττάρων στην εξωκυττάρια ουσία, ακολουθεί η μετανάστευσή τους προς τον ενδοθηλιακό χώρο. Πρόκειται για μια ιδιαιτέρως πολύπλοκη διαδικασία που περιλαμβάνει την αλληλεπίδραση με ένα άλλο τμήμα της εξωκυττάριας ουσίας, τη βασική μεμβράνη, υπό την καθοδήγηση χημοκινών όπως η MCP-1 (monocyte chemotactic protein-1, χημειοτακτική πρωτεΐνη-1 των μονοκυττάρων) και η CX3CL1 (γνωστή και ως fractalkine) (Ley et al., 2007; Ziegler-Heitbrock, 2007). Επίσης, περιλαμβάνει ποικίλες αλληλεπιδράσεις μεταξύ μορίων κυτταρικής προσκόλλησης που εκφράζονται στην επιφάνεια των μονοκυττάρων (κυρίως σελεκτίνες και ιντεγκρίνες) με τους ligands τους που εκφράζονται στην επιφάνεια των ενδοθηλιακών κυττάρων, καθώς και με στοιχεία της εξωκυττάριας ουσίας. Σε μια προηγούμενη μελέτη διαπιστώθηκε ότι η λεπτίνη μπορεί και ενεργοποιεί τα προερχόμενα από το λιπώδη ιστό ενδοθηλιακά κύτταρα, επάγοντας τη μετακίνηση των μονοκυττάρων ανάμεσά τους και τη μετατροπή τους προς μακροφάγα των ιστών (Curat et al., 2004). Συνεπώς, η λεπτίνη θα μπορούσε να έχει παρόμοια δράση και επί των ενδοθηλιακών κυττάρων των αγγείων συμβάλλοντας έτσι έμμεσα στη μετατροπή των περιπολούντων στο αίμα μονοκυττάρων προς μακροφάγα που εντοπίζονται ακριβώς κάτω από το ενδοθήλιο. Πράγματι, σε μια πρόσφατη μελέτη διαπιστώθηκε ότι η λεπτίνη σε συγκεντρώσεις 10ng/ml και 100ng/ml αύξησε την ικανότητα πρόδρομων ενδοθηλιακών κυττάρων να μεταναστεύουν διαμέσου ενεργοποιημένων κυττάρων HUVECs (ενδοθηλιακά κύτταρα από φλέβα ομφαλίου λώρου) (Schroeter et al., 2008). Όσον αφορά την απευθείας επίδραση της λεπτίνης στα μονοκύτταρα, στην παρούσα εργασία διαπιστώθηκε ότι η λεπτίνη (160ng/ml και 1600ng/ml) ενίσχυσε την ικανότητα των μονοκυττάρων να μεταναστεύουν διαμέσου της λαμινίνης-1. Όπως είναι φανερό, η δράση αυτή της λεπτίνης μετουσιώνεται μόνο σε υπερλεπτιναιμικές συγκεντρώσεις, υποδηλώνοντας ότι οι παχύσαρκοι ασθενείς είναι πιο ευαίσθητοι στη συγκεκριμένη αθηρογόνο ιδιότητα των μονοκυττάρων. Θεωρήθηκε πιθανό αυτή η δράση της λεπτίνης να μεσολαβείται από τις κατάλληλες 138
139 ιντεγκρίνες, καθότι είναι γνωστή η δυνατότητα αλληλεπίδρασης ορισμένων ιντεγκρινών με τη λαμινίνη-1 (Desban et al., 2006), κάτι που μελετήθηκε στη συνέχεια. Παράλληλα, στη δράση της λεπτίνης επί του φαινομένου της μετανάστευσης φάνηκε να συμμετέχουν ο ΝΗΕ1, ο κυτταροσκελετός της ακτίνης, η PI3K και συμβατικές ισομορφές της πρωτεϊνικής κινάσης C (α-, β I - και β II -). Η ενεργοποίηση του ΝΗΕ1 και ο πολυμερισμός της ακτίνης αποτελούν απαραίτητες προϋποθέσεις για την ομαλή διεξαγωγή τόσο της προσκόλλησης όσο και της μετανάστευσης με αποτέλεσμα να ρυθμίζονται με ακρίβεια μέσω ενός μηχανισμού που περιλαμβάνει ορισμένες GTPάσες όπως η RhoA (Raftopoulou & Hall, 2004; Cardone et al., 2005). Μια μελέτη που είναι σύμφωνη με τα αποτελέσματά μας αναφέρει ότι μια άλλη GTPάση, η Rac, συμμετέχει σε έναν κύκλο θετικής ανάδρασης (positive feedback loop) με την PI3K επάγοντας έτσι την κυτταρική μετανάστευση (Stephens et al., 2002). H Rac μαζί με μια άλλη πρωτεϊνη, την Cdc42, κατά τη διάρκεια της μετανάστευσης εντοπίζονται στο πρόσθιο τμήμα του κυττάρου (προς την κατεύθυνση της κίνησης) όπου συμβάλουν στον πολυμερισμό του κυτοσκελετού της ακτίνης (Nobes & Hall, 1999). Αυτό το πραγματοποιούν μέσω της ρύθμισης της δράσης μιας κινάσης, της p65pak η οποία είναι γνωστό ότι συμμετέχει στο δυναμικό φαινόμενο της συναρμολόγησης και αποσυναρμολόγησης του κυτοσκελετού της ακτίνης. Σπουδαίο ρόλο στη ρύθμιση του κυτοσκελετού της ακτίνης παίζουν και οι πρωτεϊνες μέλη της οικογένειας WASp/SCAR/WAVE (Takenawa & Miki, 2001). H Cdc42 είναι γνωστό ότι ενεργοποιεί την WASp, ενώ η Rac επιτελεί την ίδια εργασία για τις SCAR/WAVE (Rohatgi et al., 1999; Eden et al., 2002). Ο NHE1 κατά τη διάρκεια της κυτταρικής κίνησης δρα ως μόριο σκαλωσιά (protein scaffold) πάνω στο οποίο επιτελείται ο διαρκής πολυμερισμός και αποπολυμερισμός της ακτίνης (Stock & Schwab, 2006). Όσον αφορά το ρόλο των PKCs στη μετανάστευση, πέρα από τη ρύθμιση της δράσης του ΝΗΕ1, οι PKCs έχει δειχθεί ότι μπορούν να επάγουν την έκφραση των μορίων κυτταρικής προσκόλλησης VCAM-1 και ICAM-1 σε ενδοθηλιακά κύτταρα (Kouroedov et al., 2004). Συνεπώς είναι πολύ πιθανό να έχουν την ίδια επίδραση στα μονοκύτταρα και έτσι να συμμετέχουν στη μετανάστευση μέσω αυτού του μηχανισμού. 139
140 4.Επίδραση της λεπτίνης στην επιφανειακή έκφραση των υποδοχέων ρακοσυλλεκτών CD36 και CD68 από μονοκύτταρα ανθρώπου Η εσωτερίκευση των oxldls πραγματοποιείται σε μεγάλο ποσοστό από τον υποδοχέα ρακοσυλλέκτη CD36 που εκφράζεται στην επιφάνεια των μονοκυττάρων, των μακροφάγων και άλλων κυττάρων στην περιοχή της φλεγμονής (Dhaliwal & Steinbrecher, 1999; Silverstein & Febbraio, 2000). Ο CD36 θα μπορούσε να θεωρηθεί ότι έχει τόσο αθηρογόνο, όσο και προστατευτική ενάντια στην αθηρογένεση δράση. Από τη μια πλευρά, μέσω του CD36 και της επακόλουθης φαγοκύττωσης που αυτός επιτελεί, μειώνεται η συγκέντρωση των oxldls από τον ενδοθηλιακό χώρο και άρα αφαιρείται ένα ερέθισμα που προσελκύει μονοκύτταρα στο σημείο της φλεγμονής (Steinberg et al., 1989). Από την άλλη πλευρά, αυτή η φαγοκύττωση των oxldls είναι που οδηγεί προς αφρώδη κύτταρα, καθώς τα κύτταρα που την πραγματοποιούν αδυνατούν να διασπάσουν πλήρως ενζυματικά τις oxldls με τελικό αποτέλεσμα αυτές να συσσωρεύονται ενδοκυτταρικά (van Berkel et al., 2005). Από τα αποτελέσματα των πειραμάτων της παρούσας εργασίας εξάγεται ότι η λεπτίνη (160ng/ml και 1600ng/ml) αυξάνει την έκφραση του υποδοχέα ρακοσυλλέκτη CD36 στην επιφάνεια των μονοκυττάρων, κάτι που είναι σε συμφωνία με τα αποτελέσματα μιας πρόσφατης εργασίας που αφορούσε την επίδραση της λεπτίνης στην έκφραση του CD36 στην επιφάνεια καρδιομυοκυττάρων ποντικού (Palanivel et al., 2006). Όπως και προηγουμένως στο πείραμα μετανάστευσης διαμέσου της λαμινίνης-1, έτσι και εδώ, η λεπτίνη ενισχύει τη συγκεκριμένη αθηρογόνο ιδιότητα μόνο σε υπερλεπτιναιμικές συγκεντρώσεις επαληθεύοντας έτσι ξανά τη συσχέτιση μεταξύ παχυσαρκίας και αθηρωμάτωσης. Τα πειράματά μας, έπειτα από κατάλληλη φαρμακολογική αναστολή, έδειξαν συμμετοχή των ΝΗΕ1, PI3K, συμβατικών ισομορφών της πρωτεϊνικής κινάσης C (α-, β I - και β II -) και NADPH οξειδάση στη συγκεκριμένη λειτουργία που επάγεται από τη λεπτίνη. Με δεδομένο ότι η επίδραση με λεπτίνη γινόταν για επαρκές χρονικό διάστημα (30min), οι παραπάνω πρωτεϊνες πιθανότατα συμμετέχουν είτε στη μεταγωγή σήματος που απαιτείται για τη μεταγραφή-μετάφρασή και μεταφορά μορίων υποδοχέα CD36 στην κυτταρική επιφάνεια είτε στη μεταφορά στην κυτταρική επιφάνεια προαποθηκευμένων στο κυτταρόπλασμα υποδοχέων CD36. Ρόλο στην εσωτερίκευση των oxldls έχει και ένας άλλος υποδοχέαςρακοσυλλέκτης, ο CD68. Ο υποδοχέας αυτός αποτελεί ταυτόχρονα και δείκτη της 140
141 μετατροπής των μονοκυττάρων προς μακροφάγα, καθότι εκφράζεται σε υψηλό ποσοστό στα δεύτερα, αλλά ελάχιστα στα πρώτα. Από τα αποτελέσματα των πειραμάτων μας διαπιστώθηκε ότι η λεπτίνη, στην ίδια συγκέντρωση (160 ng/ml) στην οποία αύξανε στο μέγιστο βαθμό την επιφανειακή έκφραση του υποδοχέαρακοσυλλέκτη CD36, δεν προκαλούσε το ίδιο αποτέλεσμα στην επιφανειακή έκφραση του υποδοχέα CD68 σε σχέση με το δείγμα ελέγχου. Συνεπώς, η λεπτίνη, σε αυτή τη συγκέντρωση τουλάχιστον, δεν φαίνεται να επηρεάζει ούτε την εσωτερίκευση των oxldls μέσω του υποδοχέα CD68, ούτε τη διαδικασία μετατροπής των μονοκυττάρων προς μακροφάγα κύτταρα. 5.Επίδραση της λεπτίνης στην επιφανειακή έκφραση των υπομονάδων των ιντεγκρινών CD11a, CD11b, CD18, CD29 και CD49b από μονοκύτταρα ανθρώπου Όπως διαπιστώθηκε, η λεπτίνη, στις συγκεντρώσεις που χρησιμοποιήθηκαν, ενίσχυσε την ικανότητα των μονοκυττάρων να προσκολλώνται στη λαμινίνη-1 και να μεταναστεύουν διαμέσου αυτής. Η πραγματοποίηση των διεργασιών της προσκόλλησης και της μετανάστευσης από τα μονοκύτταρα απαιτεί πολύπλοκες αλληλεπιδράσεις μεταξύ συστατικών της εξωκυττάριας ουσίας (όπως η λαμινίνη-1) ή/και κυττάρων (π.χ. ενδοθηλιακά κύτταρα) και επιφανειακών πρωτεϊνών των μονοκυττάρων που ονομάζονται μόρια κυτταρικής προσκόλλησης (CAMs, cell adhesion molecules). Στην παρούσα εργασία μελετήθηκε η ικανότητα της λεπτίνης να προκαλεί την έκφραση στην επιφάνεια των μονοκυττάρων, υπομονάδων μιας σημαντικής κατηγορίας μορίων κυτταρικής προσκόλλησης, των ιντεγκρινών. Οι υπομονάδες που μελετήθηκαν ήταν οι CD11a (γνωστή και ως υπομονάδα a L, η οποία σε συνδυασμό με τη CD18 σχηματίζει την ιντεγκρίνη LFA-1), CD11b (γνωστή και ως υπομονάδα a M, η οποία σε συνδυασμό με τη CD18 σχηματίζει την ιντεγκρίνη Mac-1), CD18 (γνωστή και ως υπομονάδα β 2 η οποία όπως αναφέρθηκε συμμετέχει στη δομή των LFA-1 και Mac-1), CD49b (γνωστή και ως υπομονάδα α 2, η οποία σε συνδυασμό με τη CD29 σχηματίζει την ιντεγκρίνη α 2 β 1, γνωστή για τη συμμετοχή της κατά την αλληλεπίδραση με τη λαμινίνη-1) και CD29 (γνωστή και ως υπομονάδα β 1, η οποία σε συνδυασμό με τη CD49d σχηματίζει την ιντεγκρίνη VLA-4, ενώ όπως προαναφέρθηκε συμμετέχει και στη δομή της ιντεγκρίνης με ικανότητα υποδοχέα 141
142 λαμινίνης-1, α 2 β 1 ). Η ιντεγκρίνη VLA-4 έχει στοχοποιηθεί σε θεραπευτικές προσεγγίσεις για την αντιμετώπιση ασθενειών που αφορούν χρόνιες φλεγμονές (όπως π.χ. η αθηρωμάτωση). Συγκεκριμένα, οι προσεγγίσεις που μελετώνται είναι η χρήση αντισωμάτων ή ανταγωνιστών μικρού μοριακού βάρους προκειμένου να αποτραπεί η αλληλεπίδραση της ιντεγκρίνης VLA-4 με την VCAM-1 ή/και την MADCAM1 (Mousa, 2008). Διαπιστώθηκε ότι η λεπτίνη, στη συγκέντρωση που χρησιμοποιήθηκε (160 ng/ml, συγκέντρωση που οδήγησε σε μέγιστη αύξηση των επιπέδων προσκόλλησης και μετανάστευσης των μονοκυττάρων στα αντίστοιχα πειράματα) δεν προκάλεσε στατιστικά σημαντική μεταβολή στην επιφανειακή έκφραση σε σχέση με το δείγμα ελέγχου καμίας εκ των υπομονάδων ιντεγκρίνης που μελετήθηκε και κατ επέκταση και των ιντεγκρινών στη δομή των οποίων συμμετέχουν. Τα αποτελέσματα αυτά φαίνονται να έρχονται σε αντίθεση με μια πρόσφατη μελέτη στην οποία επίδραση με λεπτίνη σε συγκεντρώσεις 10ng/ml και 100ng/ml αύξησε την επιφανειακή έκφραση των υπομονάδων των ιντεγκρινών CD11a, CD11b και CD18 σε πρόδρομα ενδοθηλιακά κύτταρα (endothelial progenitor cells) (Schroeter et al., 2008). Πέρα όμως από τον διαφορετικό τύπο κυττάρου που χρησιμοποιήθηκε, στη συγκεκριμένη εργασία πραγματοποιήθηκε επώαση με λεπτίνη για 7 ημέρες, σε αντίθεση με την επώαση για 30min που πραγματοποιήθηκε στη δική μας πειραματική διαδικασία. Κατά συνέπεια, όσον αφορά τα δικά μας αποτελέσματα, είναι πολύ πιθανό η λεπτίνη να ενισχύει τις διαδικασίες προσκόλλησης και μετανάστευσης των μονοκυττάρων στη λαμινίνη-1 σε αρχικό στάδιο μέσω κάποιου άλλου μηχανισμού ανεξάρτητου των ιντεγκρινών με πιο πιθανή τη δράση άλλων μορίων κυτταρικής προσκόλλησης όπως οι IgSF CAMs ή/και οι σελεκτίνες. 6.Επίδραση της λεπτίνης στην ικανότητα φαγοκύττωσης μετρίως (oxldl 3 ) και πλήρως οξειδωμένων (oxldl 24 ) λιποπρωτεϊνών χαμηλής πυκνότητας από μονοκύτταρα ανθρώπου Λόγω των υψηλών συγκεντρώσεων των ROS στην περιοχή της φλεγμονής, οι LDLs σταδιακά οξειδώνονται προς oxldls. ROS που απελευθερώνονται από τη NADPH οξειδάση των ενδοθηλιακών, των λείων μυικών κυττάρων και πιθανότατα και των μονοκυττάρων θεωρείται ότι παίζουν σημαντικό ρόλο στη διαδικασία αυτή (Irani, 2000). Επιπρόσθετα, μονοξείδιο του αζώτου (ΝΟ) που παράγεται από τη ΝΟ 142
143 συνθάση των γειτονικών κυττάρων (την enos των ενδοθηλιακών κυττάρων ή την inos των λευκοκυττάρων) δύναται να αντιδράσει με μοριακό οξυγόνο και ανιόντα σουπεροξειδίου προς παραγωγή RNS οι οποίες επίσης είναι ικανές να οξειδώσουν τις LDLs προς oxldls (Davis et al., 2001; Gutierrez et al., 2006). Η φαγοκύττωση των oxldls από τα μακροφάγα και μονοκύτταρα αποτελεί βασικό παράγοντα ώστε τα τελευταία να μετατραπούν σε αφρώδη κύτταρα. Αυτά αυξάνουν διαρκώς σε μέγεθος λόγω της συνεχούς συσσώρευσης των oxldls στο εσωτερικό τους και της ταυτόχρονης αδυναμίας τους να τις μεταβολίσουν επαρκώς, καταλήγοντας εν τέλει σε κυτταρικό θάνατο, κάτι που ενισχύει περαιτέρω την αθηρογόνο διαδικασία φλεγμονής (Ross, 1999). Με βάση τις προηγούμενες παρατηρήσεις μας, ερευνήσαμε περαιτέρω τη φαγοκύττωση των oxldls από τα μονοκύτταρα ανθρώπου, την κυριότερη αιτία μετατροπής τους προς αφρώδη κύτταρα. Η λεπτίνη, έπειτα από χρόνους επώασης 1 h και 3 h βρέθηκε να αυξάνει τη φαγοκύττωση των μετρίως οξειδωμένων oxldls (oxldl 3 ) από τα μονοκύτταρα. Αντίθετα, έπειτα από χρόνους επώασης 1 h, 3 h και 5 h δεν φάνηκε να επηρεάζει τα επίπεδα φαγοκύττωσης των πλήρως οξειδωμένων LDLs (oxldl 24 ). Η προτίμηση για τις oxldl 3 πιθανότατα σχετίζεται με τη μεγαλύτερη ειδικότητα δέσμευσης που διαθέτει ο CD36 απέναντι στις oxldl 3 σε σχέση με τις oxldl 24 (Kunjathoor et al., 2002). Η αυξητική δράση της λεπτίνης επί της φαγοκύττωσης των oxldl 3 ανεστάλη έπειτα από φαρμακολογική αναστολή των ΝΗΕ1, PI3K, συμβατικών ισομορφών της πρωτεϊνικής κινάσης C (α-, β I - και β II -) και NADPH οξειδάση. Οι oxldls φαίνεται να παίζουν και ρόλο ενεργοποιητή, καθώς είναι γνωστή η ιδιότητά τους να ενεργοποιούν τις συμβατικές PKCs των ενδοθηλιακών κυττάρων, συνεπώς είναι πιθανή παρόμοια επίδραση και σε λευκοκύτταρα (Sugiyama et al., 1994). Είναι άξιο αναφοράς ότι η αναστολή των ίδιων ακριβώς πρωτεϊνών ανέστειλε και την επαγόμενη από τη λεπτίνη αύξηση της επιφανειακή έκφρασης του CD36. Συνεπώς, η αύξηση των επιπέδων φαγοκύττωσης των oxldl 3 που προκαλεί η λεπτίνη σε μονοκύτταρα ανθρώπου είναι πολύ πιθανό να σχετίζεται με την αντίστοιχη αύξηση της επιφανειακής έκφρασης του CD36 που η ίδια επίσης προκαλεί. Αξίζει να αναφερθεί ότι έπειτα από 5 h επίδρασης με λεπτίνη παρατηρήθηκε σημαντική μείωση στη φαγοκύττωση των oxldl 3 από τα μονοκύτταρα ανθρώπου. Το γεγονός αυτό θα μπορούσε να αποδοθεί σε αποπτωτικά ή νεκρωτικά φαινόμενα που προκαλούνται από την ενδοκυτταρική συσσώρευση των 143
144 αποδεδειγμένα τοξικών oxldls ή ακόμα και σε κορεσμό της δυνατότητας των μονοκυττάρων να αποθηκεύουν oxldls. Σε προηγούμενη μελέτη είχε παρατηρηθεί ότι οι oxldls μπορούσαν να επάγουν σε μονοκύτταρα τη σύνθεση μιας συγγενικής της Hsp70 πρωτεϊνης θερμικού σοκ, της Hsp60, της οποίας τα μόρια εκφράζονταν επιφανειακά ή/και εκκρίνονταν στην κυκλοφορία του αίματος (Frostegard et al., 1996). Αυτό είχε ως αποτέλεσμα την προσέλκυση Τ-λεμφοκυττάρων στην περιοχή και τη διατήρηση-επιδείνωση έτσι μιας φλεγμονώδους κατάστασης στη συγκεκριμένη περιοχή του αγγειακού τοιχώματος η οποία και ευνοούσε την εμφάνιση αθηρωματικών γεγονότων. H Hsp60 είναι ιδιαίτερα συντηρημένη δομικά ανάμεσα στους οργανισμούς με αποτέλεσμα να διατυπωθεί η άποψη ότι τα μόρια Hsp60 βακτηρίων που δύνανται να κυκλοφορήσουν στο αίμα έπειτα από μόλυνση, ίσως να είναι αυτά που δίνουν το αρχικό ερέθισμα για τη δημιουργία φλεγμονής και εν συνεχεία αθηρωμάτωσης (Hansson, 2001). Με βάση αυτό, ο ίδιος ερευνητής προτείνει τον εμβολιασμό με κατάλληλα τροποποιημένες oxldls ή την μερική ανοσοκαταστολή ως μεθόδους πρόληψης της αθηρωμάτωσης, τουλάχιστον για τα πιο ευαίσθητα στη νόσο άτομα. 144
145 Σύνοψη Α Μέρους Συνοψίζοντας, τα αποτελέσματα που παρουσιάστηκαν έως αυτό το σημείο υποδηλώνουν ότι η λεπτίνη, κυρίως σε υπερλεπτιναιμικές συγκεντρώσεις (160ng/ml), ενισχύει ορισμένες από τις αθηρωματικές ιδιότητες των μονοκυττάρων. Συγκεκριμένα, αυξάνει την προσκόλληση και τη μετανάστευσή τους στο συστατικό της εξωκυττάριας ουσίας λαμινίνη-1. Επιπλέον, παρατηρήθηκε ότι οι ενισχυμένες ικανότητες προσκόλλησης και μετανάστευσης των μονοκυττάρων λόγω της λεπτίνης δεν πραγματοποιούνται, στα πολύ αρχικά στάδια τουλάχιστον, μέσω αντίστοιχης αύξησης της εξωτερίκευσης των υπομονάδων CD11a, CD11b, CD18, CD29 ή/και CD49b των ιντεγκρινών. Αύξηση επίσης παρατηρήθηκε στην επιφανειακή έκφραση των υποδοχών CD36 που σχετίζονται κυρίως με τη δέσμευση και εσωτερίκευση των oxldls. Αντιθέτως, δεν παρατηρήθηκε αύξηση της επιφανειακής έκφρασης των υποδοχέων CD68. Με δεδομένο ότι η επώαση με λεπτίνη οδήγησε σε αύξηση της εσωτερίκευσης των oxldl 3, κύριος υπεύθυνος θα πρέπει συνεπώς να θεωρηθεί ο υποδοχέας CD36. Αυτό υποδηλώνεται και από το γεγονός ότι φαρμακολογική αναστολή των ίδιων επιλεγμένων πρωτεϊνών (ΝΗΕ1, PI3K, συμβατικές PKCs και NADPH οξειδάση), οδήγησε τόσο σε αναστολή της επιφανειακής έκφρασης των υποδοχέων CD36, όσο και στην εξωτερίκευση των oxldls. Αντίστοιχα από τη μη αύξηση της επιφανειακής έκφρασης των υποδοχέων CD68 εξάγεται το συμπέρασμα ότι στα 30min της επώασης με λεπτίνη στη συγκέντρώση που χρησιμοποιήθηκε (160ng/ml), δεν παρατηρείται έστω έναρξη της μετατροπής των μονοκυττάρων προς μακροφάγα. Όσον αφορά στα μονοπάτια μεταγωγής σήματος που εκκινούνται από τη λεπτίνη και εντείνουν τις συγκεκριμένες αθηρωματικές ιδιότητες των μονοκυττάρων, στην προσκόλληση στη λαμινίνη-1 φαίνεται να συμμετέχουν ο ΝΗΕ1, η PI3K, η PKC, ο κυτταροσκελετός της ακτίνης και η NADPH οξειδάση, στη μετανάστευση στη λαμινίνη-1 οι ίδιες πρωτεϊνες πλην της NADPH οξειδάσης, ενώ στις διαδικασίες επιφανειακής έκφρασης του υποδοχέα CD36 και στη φαγοκύττωση των oxldls συμμετέχουν ο ΝΗΕ1, η PI3K, η PKC και η NADPH οξειδάση (Σχήμα 1). Κοινό χαρακτηριστικό των παραπάνω αθηρογόνων ιδιοτήτων των ανθρώπινων μονοκυττάρων αποτελεί το γεγονός ότι επάγονται από τη λεπτίνη σε υπερλεπτιναιμικές συγκεντρώσεις υποδηλώνοντας ότι υπερλεπτιναιμικά άτομα όπως οι παχύσαρκοι ασθενείς είναι ιδιαιτέρως ευάλωτοι σε αθηρωματικά γεγονότα. 145
146 Σχήμα 1. Επισκόπηση Α Μέρους.
147 Μέρος Β Μελέτη της επίδρασης της λεπτίνης σε οξειδωτικές-αντιοξειδωτικές λειτουργίες των μονοκυττάρων ανθρώπου Με δεδομένη την ικανότητα των μονοκυττάρων να οξειδώνουν στοιχεία του μικροπεριβάλλοντός τους, με πιο σημαντικό για την αθηρωμάτωση γεγονός την οξείδωση των LDLs προς oxldls, κρίθηκε σκόπιμο να μελετηθεί η επίδραση της λεπτίνης στην παραγωγή οξειδωτικών ριζών από αυτά. Παράλληλα, μελετήθηκε η επίδραση της λεπτίνης σε αντιοξειδωτικούς μηχανισμούς των μονοκυττάρων με τη μεγαλύτερη έμφαση να δίνεται στο ρόλο του ΝΗΕ1 σε αυτούς. 1.Επίδραση της λεπτίνης στην τιμή του ενδοκυτταρικού ph (phi) μονοκυττάρων ανθρώπου Σε μια προηγούμενη εργασία είχε δειχθεί ότι η λεπτίνη μπορούσε να ενεργοποιήσει τον ΝΗΕ1 ερυθροκυττάρων ανθρώπου, προκαλώντας μέσω αυτού αύξηση του ενδοκυτταρικού ph (phi) (Konstantinou-Tegou et al., 2001). Αντίστοιχα μελέτες έχουν καταστήσει πλέον σαφές ότι ορμόνες όπως η αδρεναλίνη, η ενδοθηλίνη και άλλες μπορούν και ενεργοποιούν τον ΝΗΕ1 (Ceolotto et al., 1997; Koliakos et al., 2007). Από τα πειράματά μας διαπιστώθηκε ότι η λεπτίνη είχε την ίδια επίδραση και σε μονοκύτταρα ανθρώπου. Ταυτόχρονα, διαπιστώθηκε ότι δύο άλλες ορμόνες σχετικές με παχυσαρκία, η ρεζιστίνη και η γκρελίνη δεν επηρέασαν το phi και άρα την ενεργότητα του ΝΗΕ1 στις συγκεντρώσεις που χρησιμοποιήθηκαν. Όσον αφορά τη λεπτίνη, αυτή ενεργοποίησε τον ΝΗΕ1 και στις τρεις συγκεντρώσεις που χρησιμοποιήθηκαν και οι οποίες κυμαίνονταν από χαμηλές κανονικές έως υπερλεπτιναιμικές (1.6ng/ml, 16ng/ml and 160ng/ml). Το γεγονός ότι ενεργοποιούνταν ακόμα και σε χαμηλές συγκεντρώσεις (1,6 ng/ml) υποδηλώνει ότι ο ΝΗΕ1 είναι ιδιαιτέρως ευαίσθητος στη μεταγωγή σήματος που εκκινείται από τη λεπτίνη. Η αύξηση του phi που προκαλείται από την ενεργοποίηση του ΝΗΕ1 είναι πιθανότατα απαραίτητη προκειμένου να είναι εφικτή η ενεργοποίηση ή απενεργοποίηση ή/και μετατόπιση συγκεκριμένων πρωτεϊνων που συμμετέχουν στα μονοπάτια μεταγωγής σήματος που εκκινούνται από τη λεπτίνη, καθότι είναι γνωστό ότι το phi αποτελεί σημαντικό παράγοντα που καθορίζει τη διαμόρφωση μιας πρωτεϊνης στο χώρο και άρα και τη λειτουργικότητά της, ενώ συχνά παίζει ρόλο και στην ενδοκυτταρική της θέση όπως έχει δειχθεί για την PKC (Ho et al., 2000; Matsuyama et al., 2000). Σε μια προηγούμενη εργασία μας είχαμε δείξει την ύπαρξει
148 ενός μηχανισμού θετικής ανάδρασης (feedback loop) μεταξύ της ΝΗΕ1 και της κινάσης ERK (Konstantinidis et al., 2006). Η λεπτίνη είναι γνωστό ότι ενεργοποιεί την ERK, συνεπώς είναι πιθανό η ενεργοποίηση της ΝΗΕ1 από την λεπτίνη να μεσολαβείται από την ERK (Berti & Gammeltoft, 1999). 2.Επίδραση της λεπτίνης στην παραγωγή δραστικών μορφών οξυγόνου (ROS) και αζώτου (RNS) από μονοκύτταρα ανθρώπου Οι δραστικές μορφές οξυγόνου και αζώτου που παράγονται εξωκυτταρικά από αγγειακά κύτταρα (ενδοθηλιακά κύτταρα, λεία μυικά κύτταρα, κ.α.), αλλά και οι αντίστοιχες που παράγονται από τα μεταναστεύοντα λευκοκύτταρα πιθανότατα παίζουν σπουδαίο ρόλο αφενός στη μετατροπή της εξωκυττάριας ουσίας (ECM remodeling) προς μια πιο ευνοϊκή για αθηρωματικά γεγονότα κατάσταση και αφετέρου στην αποσταθεροποίηση του ινώδους καλύμματος (Griendling et al., 2000). Παράλληλα, οι ίδιες οξειδωτικές ρίζες δύνανται ενδοκυτταρικά και υπό κατάλληλες προϋποθέσεις να έχουν είτε έναν καταστροφικό για τα κύτταρα ρόλο, είτε να συμμετέχουν σε διαδικασίες μεταγωγής σήματος, καθότι έστω και σε μικρές ποσότητες, οξειδωτικές ρίζες παράγονται από τα περισσότερα, αν όχι όλα, τα κύτταρα (Lambeth, 2004; Gutierrez et al., 2006). Στη συνεχεία της παρούσας εργασίας, μελετήθηκε η επίδραση της λεπτίνης στην παραγωγή δραστικών μορφών οξυγόνου (με εξαίρεση τα ανιόντα σουπεροξειδίου) και αζώτου. Διαπιστώθηκε αύξηση της παραγωγής τους από μονοκύτταρα ανθρώπου έπειτα από επίδραση με λεπτίνη. Αυτό παρατηρήθηκε στην υψηλή κανονική και στην υπερλεπτιναιμική συγκέντρώση που χρησιμοποιήθηκαν (16 ng/ml και 160 ng/ml), αλλά όχι στη χαμηλή συγκέντρωση που ήταν εντός των κανονικών ορίων (1,6 ng/ml). Είναι γνωστό ότι η λεπτίνη επάγει την παραγωγή οξειδωτικού στρες σε ενδοθηλιακά κύτταρα ανθρώπου από φλέβα ομφαλιου λώρου (human umbilical vein endothelial cells ή HUVECs) (Bouloumie et al., 1999). Επιπρόσθετα, πρόσφατα πειράματα στα ίδια κύτταρα, αλλά και σε ποντίκια, κατέγραψαν αύξηση του οξειδωτικού στρες σε περιπτώσεις υπερλεπτιναιμίας συνοδευτικής της παχυσαρκίας (Korda et al., 2008). Στα αρχικά στάδια της αθηρωματικής διαδικασίας τα μονοκύτταρα και τα ενδοθηλιακά κύτταρα βρίσκονται πάρα πολύ κοντά μεταξύ τους. Κατά συνέπεια, αυξήσεις στην παραγωγή οξειδωτικών ριζών και από τους δύο τύπους κυττάρων θα μπορούσαν να συμβάλλουν στη 148
149 δημιουργία μικροπεριβαλλόντων όπου οι LDLs θα μπορούσαν να οξειδωθούν προς τις πιο αθηρογόνες μορφές τους τις oxldls. Επιπρόσθετα, η διατήρηση του οξειδωτικού στρες σε υψηλά επίπεδα εγκυμονεί τον κίνδυνο πρόκλησης ανεπανόρθωτης βλάβης στα γύρω κύτταρα οδηγώντας στην απόπτωσή τους (Dimmeler & Zeiher, 2000). Τα κύτταρα που μετατρέπονται σε αφρώδη λόγω της υπερβολικής ενδοκυτταρικής συσσώρευσης των oxldls, καθώς και κύτταρα που έχουν εισέλθει στη φάση της απόπτωσης (με πολλά κύτταρα να ανήκουν και στους δύο προαναφερθέντες τύπους κυττάρων) αποτελούν βασικούς δομικούς λίθους των αθηρωματικών πλακών (Choudhury et al., 2005). Επιπρόσθετα, τα στοιχεία μιας πρόσφατης μελέτης υποδηλώνουν έναν αθηρωματικό ρόλο για τη λεπτίνη κατά τη διάρκεια της αγγειακής αναδιαμόρφωσης (vascular remodeling), της διαδικασίας δηλαδή κατά την οποία λόγω κατάλληλων μηνυμάτων (ένα εκ των οποίων υποστηρίζεται ότι είναι και η λεπτίνη) αλλάζει η κυτταρική σύσταση του αγγειακού τοιχώματος καθιστώντας έτσι είτε ευκολότερη είτε δυσκολότερη την εμφάνιση αθηρωματικού γεγονότος (Schroeter et al., 2008). Στην παρούσα εργασία, τα αποτελέσματά μας υποδηλώνουν ότι σε υπερλεπτιναιμικούς ασθενείς, αλλά και γενικότερα ακόμα και σε υγιή άτομα με υψηλές κανονικές συγκεντρώσεις λεπτίνης, οι περιοχές των αγγείων στις οποίες ξεκινάει φλεγμονή είναι ακόμα περισσότερο ευάλωτες στην εμφάνιση αθηρωματικών φαινομένων, όπως της δημιουργίας αθηρωματικών πλακών. Στο μονοπάτι μεταγωγής σήματος που εκκινείται από τη λεπτίνη οδηγώντας σε παραγωγή οξειδωτικών ριζών φαίνεται να συμμετέχουν οι PI3K και NADPH οξειδάση, καθώς η φαρμακευτική αναστολή τους ανέστειλε και την παραγωγή οξειδωτικών ριζών. Ταυτόχρονα, η ίδια διαδικασία ήταν ανεξάρτητη της PKC. Μια πολύ ενδιαφέρουσα παρατήρηση σε αυτή τη σειρά πειραμάτων ήταν ότι η αναστολή του ΝΗΕ1 ενίσχυε την επαγόμενη από τη λεπτίνη παραγωγή οξειδωτικών ριζών, υποδηλώνοντας ότι η ενεργή ΝΗΕ1 έχει προστατευτικό ρόλο ενάντια στο οξειδωτικό στρες. Σε μια προηγούμενη εργασία μας, είχαμε παρατηρήσει το ίδιο φαινόμενο σε καρκινικά επιθηλιακά κύτταρα ανθρώπου στα οποία αναστέλλονταν ο ΝΗΕ1 (Konstantinidis et al., 2006). Σε εκείνη την εργασία δεν είχε χρησιμοποιηθεί ουσία ενεργοποιητής όπως στην προκειμένη περίπτωση η λεπτίνη, έτσι είχαμε προτείνει ότι το καταστροφικό για τα κύτταρα αποτέλεσμα που προκαλούσε η αναστολή του ΝΗΕ1 οφειλόταν σε υπερβολικό κυτταρικό στρες λόγω της μη δυνατότητας των 149
150 κυττάρων να φτάσουν στο phi που ήταν απαραίτητο προκειμένου να πραγματοποιήσουν μίτωση. Με δεδομένο ότι η παρούσα εργασία πραγματοποιήθηκε σε μη καρκινικά κύτταρα, είναι πιθανό η μη δυνατότητα της λεπτίνης να αυξήσει τη δράση του ΝΗΕ1, λόγω της φαρμακευτικής αναστολής του, να μεταφράζεται σε πρόσθετο οξειδωτικό στρες (πέρα από αυτό που παράγεται ήδη μόνο από τη δράση της λεπτίνης). Στην πορεία των πειραμάτων, και αφού μετρήθηκε και η επίδραση της λεπτίνης στο ένζυμο δισμουτάση του σουπεροξειδίου (SOD), καταλήξαμε σε μια ακόμα πιθανή εξήγηση (που δεν έρχεται σε αντίθεση με την παραπάνω και είναι μάλλον συμπληρωματική της) της αύξησης των επιπέδων οξειδωτικού στρες έπειτα από την αναστολή του ΝΗΕ1 και η οποία θα αναλυθεί παρακάτω. 3.Επίδραση της λεπτίνης στην παραγωγή του ανιόντος σουπεροξειδίου από μονοκύτταρα ανθρώπου Στη συνέχεια της παρούσης εργασίας μελετήθηκε η επίδραση της λεπτίνης στην παραγωγή του ανιόντος σουπεροξειδίου. Η συγκεκριμένη μελέτη έγινε χωριστά από τη μελέτη των υπόλοιπων οξειδωτικών ριζών λόγω του γεγονότος ότι η φθορίζουσα ουσία H 2 DCFDA που χρησιμοποιήθηκε προηγουμένως, σε αντίθεση με τη φθορίζουσα ουσία DHE που χρησιμοποιήθηκε εδώ, δε διαθέτει την ειδικότητα να ανιχνεύει το ανιόν σουπεροξειδίου (Rothe & Valet, 1990; Gomes et al., 2005). Αξίζει να σημειωθεί ότι για την ανίχνευση του σουπεροξειδίου χρησιμοποιήθηκε αρχικά η ουσία NBT, η οποία όμως δεν είναι τόσο ειδική ως προς το σουπεροξείδιο, συνεπώς κρίθηκε σκόπιμο να επιβεβαιωθούν με τη χρήση του DHE τα αποτελέσματα που πάρθηκαν με NBT (Münzel et al., 2002). Οι οξειδωτικές ρίζες που διοχετεύονται εξωκυτταρικά δεν είναι απαραίτητα οι ίδιες που παράγονται ενδοκυτταρικά τόσο ποιοτικά, όσο και ποσοτικά (Rees et al., 2008). Έτσι, τα ανιόντα σουπεροξειδίου που παράγονται από τη NADPH οξειδάση διοχετεύονται κυρίως εξωκυτταρικά (Babior, 1987). Τα ανιόντα σουπεροξειδίου είναι μέτριας τοξικότητας και σε συνδυασμό με διάφορα μόρια δίνουν γένεση σε άλλες οξειδωτικές ρίζες (για παράδειγμα, αντιδρώντας με το ΝΟ παράγουν υπεροξυνιτρίτη γνωστό και ως ONOO - ) (Radi et al., 2001). Ταυτόχρονα, με τη δράση του ενζύμου SOD (δισμουτάση του σουπεροξειδίου) επί του σουπεροξειδίου αυξάνονται τα επίπεδα του Η 2 Ο 2, το οποίο μπορεί να αποτελέσει πηγή οξειδωτικών ριζών. Έτσι, για παράδειγμα, το ένζυμο μυελοϋπεροξειδάση το οποίο εκκρίνεται και εξωκυτταρικά από μονοκύτταρα και 150
151 ουδετερόφιλα, υποστηρίζεται ότι έχει έναν ευνοϊκό για την αθηρωμάτωση ρόλο (Nicholls & Hazen, 2005; Davies et al., 2008). Συγκεκριμένα, έχει διαπιστωθεί η ύπαρξη της μυελοϋπεροξειδάσης υποενδοθηλιακά, στις αρχικές θέσεις μικροτραυματισμού του ενδοθηλίου όπου έχει προταθεί ότι μέσω της παραγωγής HOCl από Η 2 Ο 2 συμβάλλει στην οξείδωση στοιχείων της εξωκυττάριας ουσίας (Daugherty et al. 1994; Fu et al., 1998; Woods et al., 2003). Το εξωκυτταρικό ανιόν σουπεροξειδίου και τα παράγωγά του μπορούν να οξειδώσουν στοιχεία της εξωκυττάριας ουσίας ευνοώντας έτσι, όπως προαναφέρθηκε, ακόμα περισσότερο την προσκόλληση μονοκυττάρων στην περιοχή. Συγκεντρώσεις λεπτίνης που κυμαίνονταν εντός του ορίου του φυσιολογικού (1,6 ng/ml και 16 ng/ml) αύξησαν την παραγωγή του ανιόντος σουπεροξειδίου από τα μονοκύτταρα. Παρόλα αυτά η λεπτίνη σε υπερλεπτιναιμική συγκέντρωση (160 ng/ml) δεν είχε το ίδιο αποτέλεσμα κάτι που έρχεται σε αντίθεση με μια προηγούμενη μελέτη που διενεργήθηκε σε καρδιομυοκύτταρα ποντικού (Dong et al., 2006). Κατάλληλη φαρμακολογική αναστολή οδήγησε στο συμπέρασμα ότι ο ΝΗΕ1, η PI3K, συμβατικές ισομορφές της πρωτεϊνικής κινάσης C (α-, β I - και β II -) και η NADPH οξειδάση συμμετέχουν στο μηχανισμό της επαγόμενης από λεπτίνη παραγωγής ανιόντος σουπεροξειδίου. Συγκεκριμένα, η NADPH οξειδάση είναι γνωστό ότι παράγει μέσω της δράσης της ανιόντα σουπεροξειδίου, συνεπώς αποτελεί πιθανό σημείο τερματισμού του σήματος που επάγει η λεπτίνη. Είναι επίσης γνωστό ότι η ισομορφή α- της πρωτεϊνικής κινάσης C (PKCα) των μονοκυττάρων είναι απαραίτητη για τη συναρμολόγηση των πρωτεϊνικών υπομονάδων που αποτελούν τη NADPH οξειδάση, συνεπώς είναι λογικό αναστολή της PKCα να έχει αρνητική επίδραση στην παραγωγή ανιόντων σουπεροξειδίου (Cathcart, 2004). Επίσης, η PI3K έχει δειχθεί ότι μπορεί να ενεργοποιηθεί από τη λεπτίνη σε μονοπύρηνα κύτταρα του περιφερικού αίματος (ένας πληθυσμός κυττάρων που περιλαμβάνει τα μονοκύτταρα) (Martin- Romero & Sanchez-Margalet, 2001). Παράλληλα, ο ΝΗΕ1 ρυθμίζεται τόσο άμεσα, όσο και έμμεσα και από την PI3K, και από την PKC (Maly et al., 2002; Wu et al., 2004). Το γεγονός ότι η παραγωγή του ανιόντος σουπεροξειδίου μειώθηκε έπειτα από αναστολή του ΝΗΕ1 υποδηλώνει την ύπαρξη επικοινωνίας μεταξύ του ΝΗΕ1 και της NADPH οξειδάσης. Αξίζει επίσης να αναφερθεί ότι η συνθάση του ΝΟ δεν φαίνεται να συμμετέχει στο επαγόμενο από λεπτίνη οξειδωτικό στρες, καθώς η αναστολή της 151
152 δεν επηρέασε κατά στατιστικά σημαντικό τρόπο ούτε την παραγωγή γενικά οξειδωτικών ριζών, ούτε την παραγωγή του ανιόντος σουπεροξειδίου. 4.Επίδραση της λεπτίνης στη δραστικότητα του ενζύμου δισμουτάση του σουπεροξειδίου των μονοκυττάρων ανθρώπου Κάναμε την υπόθεση ότι η λεπτίνη μπορεί να μη δρα μόνο μέσω της αύξησης της παραγωγής ανιόντων σουπεροξειδίου, αλλά να δρα και μέσω της μείωσης της εξουδετέρωσής τους από το ένζυμο δισμουτάση του σουπεροξειδίου (SOD). Ως επακόλουθο αυτής της υπόθεσης, μετρήσαμε τη δραστικότητα της SOD με και χωρίς την επίδραση λεπτίνης. H SOD υπάρχει σε διάφορες ισομορφές στο κύτταρο με κυριότερες την Cu/Zn SOD του κυτταροπλάσματος και την Mn SOD του μιτοχονδρίου, ενώ υπάρχει και μια διαλυτή στο πλάσμα ισομορφή, η EC-SOD, η οποία προφανώς κυκλοφορεί εξωκυτταρικά. Με τη μεθοδολογία που χρησιμοποιήσαμε μετρήσαμε συνολική ενδοκυτταρική SOD (Fattman et al., 2003). Παρά το γεγονός ότι η λεπτίνη αυξάνει την παραγωγή ανιόντων σουπεροξειδίου, φαίνεται επίσης, σε υψηλές κανονικές και υπερλεπτιναιμικές συγκεντρώσεις (16 ng/ml και 160 ng/ml, αντίστοιχα) να αυξάνει την ενεργότητα της SOD. Η SOD καταλύει την ακόλουθη αντίδραση: 2O H + H 2 O 2 + O 2 (Hancock et al., 2001). Με βάση τα αποτελέσματά μας, η λεπτίνη με το να αυξάνει τη συγκέντρωση των ανιόντων σουπεροξειδίου, καθώς και την ενεργότητα της SOD, μετατοπίζει την αντίδραση προς τα δεξιά. Αυτό θα είχε ως αποτέλεσμα μεγαλύτερες ενδοκυτταρικές συγκεντρώσεις H 2 O 2 και των οξειδωτικών παραγώγων του. Από την άλλη πλευρά, η λεπτίνη ενεργοποιεί τον ΝΗΕ1 με αποτέλεσμα τη μείωση της ενδοκυτταρικής συγκέντρωσης Η +, κάτι που περιορίζει την παραπάνω αντίδραση. Αυτό ίσως να εξηγεί την αύξηση των επιπέδων του επαγόμενου από τη λεπτίνη οξειδωτικού στρες έπειτα από παράλληλη αναστολή του ΝΗΕ1. Πράγματι, η αναστολή του ΝΗΕ1 οδηγεί την αντίδραση προς τα δεξιά, οδηγώντας σε μεγαλύτερη κατανάλωσηεξουδετέρωση των ανιόντων σουπεροξειδίου. Αυτό με τη σειρά του ίσως να εξηγεί τη μείωση των επιπέδων της επαγόμενης από τη λεπτίνη παραγωγής ανιόντος σουπεροξειδίου έπειτα από παράλληλη αναστολή του ΝΗΕ1. Εν κατακλείδι, η λεπτίνη σε υπερλεπτιναιμικές συγκεντρώσεις φαίνεται να ευνοεί τη μετακίνηση προς τα δεξιά της ισορροπίας της παραπάνω αντίδρασης, οδηγώντας σε μεγαλύτερες ενδοκυτταρικές συγκεντρώσεις H 2 O 2. Σε σχέση με άλλα οξειδωτικά στοιχεία, το 152
153 H 2 O 2 διαθέτει πολλές από τις ιδιότητες που είναι απαραίτητες ώστε να λειτουργήσει ως μόριο μεταγωγής σήματος, όπως μεγαλύτερη σταθερότητα και χρόνο ημιζωής. Πράγματι, φαίνεται να παίζει έναν τέτοιο ρόλο, καθώς όλο και περισσότερα από τα ενδοκυτταρικά μόρια στόχοι του γίνονται γνωστά. (Giorgio et al., 2007). Συγκεκριμένα, τα ενδοκυτταρικά επίπεδα του H 2 O 2 έχει δειχθεί έως τώρα ότι ρυθμίζονται από αυξητικούς παράγοντες όπως ο EGF (epidermal growth factor), o PDGF (platelet-derived growth factor) και η ινσουλίνη (Stone & Young, 2006). Το H 2 O 2 με τη σειρά του συμμετέχει στη ρύθμιση της μεταγωγής σήματος μέσω της αναστολής φωσφατασών όπως η PTP1B και η PTEN, ενώ μεταξύ των άλλων στόχων του συγκαταλέγονται η φωσφολιπάση Α2 (διασπά φωσφολιπίδια οδηγώντας στη σύνθεση φλεγμονώδων παραγώγων τους όπως οι προσταγλανδίνες και τα λευκοτριένια) και ο HSF-1 (heat shock factor 1, μεταγραφικός παράγοντας που σχετίζεται με τη μεταγραφή των πρωτεϊνών Hsp) (Lee et al., 1998; Ahn & Thiele, 2003; Yu et al., 2005; Song et al., 2006). Η κύρια ρυθμιστική δράση του H 2 O 2 πραγματοποιείται μέσω της αντιστρεπτής οξείδωσης των πρωτεϊνών στόχων του σε θέσεις κυστεϊνης ή μέσω της σουλφοξείδωσης θέσεων μεθειονίνης με αποτέλεσμα την τροποποίηση της λειτουργίας τους (Giorgio et al., 2007). 5.Επίδραση της λεπτίνης στη σύνδεση της Hsp70 με τον NHE1 και στα επίπεδα γλουταθειονυλίωσης της Hsp70 σε μονοκύτταρα ανθρώπου Εν συνεχεία μελετήθηκε η επίδραση της λεπτίνης και του ενδοκυτταρικού οξειδωτικού στρες που παράγει, στον ΝΗΕ1 και στις αλληλεπιδράσεις του τελευταίου με αντι-οξειδωτικούς κυτταρικούς μηχανισμούς και συγκεκριμένα την πρωτεϊνη Hsp70 και το αντιοξειδωτικό τριπεπτίδιο γλουταθειόνη. Η εξελικτικά συντηρημένη οικογένεια των πρωτεϊνών Hsp70 (οι Hsp70 του E.coli και του ανθρώπου εμφανίζουν 50% ομολογία στις αμινοξικές τους αλληλουχίες και ουσιαστικά όμοια λειτουργία) είναι γνωστή για το ρόλο της στην ορθή αναδίπλωση νέων πρωτεϊνών στο χώρο, στην προστασία τους από ακραίες συνθήκες (θερμικό σοκ, οξειδωτικό στρες, κ.α.), καθώς επίσης και στη μετατόπισή τους στα σημεία του κυττάρου για τα οποία προορίζονται (Beckmann et al., 1990; Schlesinger, 1990). Είναι γνωστό ότι η Hsp70 μπορεί και συνδέεται στο C-τελικό άκρο του ΝΗΕ1 μέσω ενός ATP-εξαρτώμενου μηχανισμού (όλες οι Hsp70s έχουν την ιδιότητα να δεσμεύουν και να υδρολύουν ΑΤΡ) (Silva et al., 1995). Η λεπτίνη σε 153
154 υψηλές κανονικές συγκεντρώσεις (16 ng/ml) δεν φάνηκε να αυξάνει τη σύνδεση της Hsp70 στον ΝΗΕ1. Αύξησε, όμως, τα επίπεδα γλουταθειονυλίωσης των μορίων Hsp70 που είχαν ήδη συνδεθεί στον ΝΗΕ1. Πρόσφατα αναφέρθηκε ότι η Hsp70 μπορεί και ρυθμίζει τα επίπεδα γλουταθειονυλίωσης μέσω τη ρύθμισης της δράσης των ενζύμων υπεροξειδάση της γλουταθειόνης (glutathione peroxidase) και αναγωγάση της γλουταθειόνης (glutathione reductase, GSR) (Guo et al., 2007). Τα ένζυμα αυτά βρίσκονται και στο πλάσμα του αίματος, αλλά σε σχεδόν αμελητέες συγκεντρώσεις. Αντίστοιχα, η γλουταθειόνη βρίσκεται και αυτή σε μικρές συγκεντρώσεις στο πλάσμα (1-3μΜ) (Halliwell & Gutridge, 1990; Halliwell & Gutridge, 1991) υποδηλώνοντας ότι ο ρόλος της στην προστασία του εξωκυτταρικού περιβάλλοντος και πιο συγκεκριμένα εδώ, της εξωκυττάριας ουσίας, από οξειδωτικό στρες είναι ασήμαντος. Ενδοκυτταρικά, η συγκέντρωση της γλουταθειόνης βρίσκεται στα επίπεδα των mm και διαδραματίζει καίριο ρόλο στην προστασία από οξειδωτικό στρες. Η υπεροξειδάση της γλουταθειόνης καταλύει σε γενικές γραμμές την αντίδραση: 2GSH + H 2 O 2 GS SG + 2H 2 O. Μέσω αυτού του μηχανισμού εξουδετερώνεται το δυνητικά επιβλαβές κυτταροπλασματικό H 2 O 2. Εν συνεχεία η αναγωγάση της γλουταθειόνης επιδρά επί της δισουλφιδικής γλουταθειόνης σύμφωνα με την αντίδραση GS-SG + NADPH + H + 2 GSH + NADP + απελευθερώνοντας έτσι τη γλουταθειόνη. Αντίστοιχα, μέσω του ενζύμου S-τρανσφεράση της γλουταθειόνης, η γλουταθειόνη δεσμεύεται σε εκτεθειμένες κυστεϊνες πρωτεϊνών προστατεύοντάς τες κατά αντιστρεπτό τρόπο (καθότι όπως περιγράφηκε παραπάνω, με τη δράση της αναγωγάσης της γλουταθειόνης η γλουταθειόνη απελευθερώνεται ξανά στο κυτταρόπλασμα) (Dalle-Donne et al., 2007; Shelton & Mieyal, 2008). Η αναστολή του ΝΗΕ1 πριν την επίδραση με λεπτίνη αύξησε τόσο τη δέσμευση μορίων Hsp70 στον ΝΗΕ1, όσο και τα επίπεδα γλουταθειονυλίωσής τους. Αυτό που προκύπτει από τα πειράματά μας είναι ότι ως απάντηση στο επαγόμενο από τη λεπτίνη οξειδωτικό στρες, το κύτταρο αυξάνει τα επίπεδα γλουταθειονυλίωσης των μορίων Hsp70 που είναι ήδη συνδεδεμένα με τον ΝΗΕ1, αλλά δεν αυξάνει τα ίδια τα επίπεδα σύνδεσης Hsp70-NHE1. Όπως φάνηκε και από τις μετρήσεις γενικού οξειδωτικού στρες που έγιναν με τη φθορίζουσα ουσία Η 2 DCFDA, είναι πιθανό ότι όταν συμβαίνει ταυτόχρονα επίδραση με λεπτίνη και αναστολή του ΝΗΕ1, τα επίπεδα οξειδωτικού στρες ξεπερνούν κάποιο όριο πέρα από το οποίο η αύξηση των επιπέδων 154
155 γλουταθειονυλίωσης δεν επαρκεί για να προστατεύσει από σοβαρές βλάβες με αποτέλεσμα το κύτταρο να αυξάνει και τα επίπεδα δέσμευσης Hsp70-NHE1. Αναστολή των PI3K και PKC πριν την επίδραση με λεπτίνη προκάλεσε αποτέλεσμα αντίστροφο από αυτό της απλής επίδρασης με λεπτίνη, καθώς παρατηρήθηκε αύξηση των επιπέδων σύνδεσης Hsp70-NHE1, αλλά μείωση των επιπέδων γλουταθειονυλίωσης των μορίων Hsp70 που είχαν συνδεθεί με τον ΝΗΕ. Αυτό πιθανότατα οφείλεται σε παρόμοια επίδραση αυτών των δύο πρωτεϊνών επί του ΝΗΕ1 και άρα συμμετοχή και των δύο στο ίδιο μονοπάτι μεταγωγής σήματος που σχετίζεται με σύνδεση των Hsp70-NHE1 και γλουταθειονυλίωση της πρώτης. Όπως αναφέρθηκε παραπάνω, τόσο η Hsp70 όσο και η γλουταθειόνη έχουν αμελητέο ρόλο στην προστασία του εξωκυττάριου χώρου από οξειδωτικό στρες. Εξωκυτταρικά φαίνεται ότι παίζει σπουδαίο ρόλο το ασκορβικό οξύ (κοινώς γνωστό ως βιταμίνη C) το οποίο κυκλοφορεί στο πλάσμα του αίματος σε συγκεντρώσεις μΜ και μπορεί και εξουδετερώνει άμεσα ιδιαίτερα δραστικές ρίζες όπως για παράδειγμα το HOCl (Halliwell & Gutridge, 1990). Παράλληλα, το ασκορβικό αποτελεί απαραίτητο συμπαράγοντα ενζύμων που συμμετέχουν στη συντήρηση και επιδιόρθωση της εξωκυττάριας ουσίας όπως της λυσιλο-οξειδάσης (lysil oxidase). Συνεπώς, γίνεται αντιληπτό ότι έλλειψη του ασκορβικού οξέος λόγω της εξουδετέρωσής του από υπερπαραγωγή οξειδωτικών ριζών θα είχε άμεσα αρνητική επίδραση στην εξωκυττάρια ουσία (Lucero & Kagan, 2006). Σε γενικές γραμμές, εξωκυτταρικά, τόσο οι προστατευτικοί αντι-οξειδωτικοί μηχανισμοί, όσο και οι μηχανισμοί επιδιόρθωσης είναι ιδιαίτερα περιορισμένοι σε σχέση με ό,τι συμβαίνει ενδοκυτταρικά (Rees et al., 2008). 155
156 Σύνοψη Β Μέρους Συνοψίζοντας, διαπιστώθηκε ότι η λεπτίνη ενεργοποιεί τον ΝΗΕ1 προκαλώντας αύξηση του ενδοκυτταρικού ph των ανθρώπινων μονοκυττάρων. Επίσης, διαπιστώθηκε ότι η επώαση των μονοκυττάρων ανθρώπου με λεπτίνη σε υψηλή κανονική συγκέντρωση (16ng/ml) αύξησε την παραγωγή οξειδωτικών ριζών οξυγόνου και αζώτου. Έχει ενδιαφέρον το γεγονός ότι αναστολή του ΝΗΕ1 ενίσχυσε το οξειδωτικό στρες που παραγόταν από τη λεπτίνη (όχι όμως όσον αφορά την παραγωγή ανιόντος σουπεροξειδίου, όπου φάνηκε να έχει την αντίθετη δράση). Σε γενικές γραμμές, ο μηχανισμός μέσω του οποίου η λεπτίνη αυξάνει το οξειδωτικό στρες περιλαμβάνει τον ΝΗΕ1, την PI3K, συμβατικές PKCs και τη NADPH οξειδάση (Σχήμα 2). Παράλληλα, όμως, η επώαση με λεπτίνη αύξησε και την ενεργότητα του αντι-οξειδωτικού μηχανισμού του ενζύμου δισμουτάση του σουπερξειδίου (SOD). Πιθανότατα, η αύξηση της δραστικότητας της SOD, σε συνδυασμό με την αύξηση της παραγωγής ανιόντος σουπεροξειδίου, αλλά και του πλεονάσματος υδρογονοκατιόντων λόγω της αναστολής του ΝΗΕ1, οδηγούν σε αύξηση της παραγωγής υπεροξειδίου του υδρογόνου και των παραγώγων του. Επιπρόσθετα, η επώαση με λεπτίνη δεν είχε επίδραση στα επίπεδα σύνδεσης Hsp70-NHE1, αύξανε όμως, τα επίπεδα γλουταθειονυλίωσης των ήδη συνδεδεμένων στον ΝΗΕ1 μορίων της Hsp70. Αναστολή του ΝΗΕ1 ταυτόχρονα με την επώαση με λεπτίνη, πιθανότατα λόγω του υψηλού οξειδωτικού στρες, οδηγούσε τόσο σε αύξηση σύνδεσης των μορίων Hsp70 με τον ΝΗΕ1 όσο και σε ενίσχυση των επιπέδων γλουταθειονυλίωσής τους. 156
157 Σχήμα 2. Επισκόπηση Β Μέρους.
158 Μέρος Γ Σκιαγράφηση μονοπατιών μεταγωγής σήματος που εκκινούνται από τη λεπτίνη σε μονοκύτταρα ανθρώπου και σχετίζονται με τις αθηρογόνες ιδιότητες αυτών Η λεπτίνη, παρόμοια με πολλές κυτοκίνες, πραγματοποιεί μεταγωγή σήματος μέσω του μονοπατιού JAK/STAT. Η κινάση JAK2 συνδέεται με τον υποδοχέα της λεπτίνης ObRb, κάτι που της δίνει τη δυνατότητα να ενεργοποιήσει στη συνέχεια τον μεταγραφικό παράγοντα STAT3 ο οποίος έτσι μετατοπίζεται στον πυρήνα όπου ενεργοποιεί τη μεταγραφή πλήθους γονιδίων (Σχήμα 3). Έχει διαπιστωθεί ότι η δράση της STAT3 (δηλ. τα γονίδια των οποίων τη μεταγραφή ενεργοποιεί) είναι κυτταροειδική. Έτσι, για παράδειγμα, στα Β-λεμφοκύτταρα επάγει μίτωση, ενώ στα μονοκύτταρα επάγει μηχανισμούς διαφοροποίησης (Levy & Lee, 2002). Ταυτόχρονα, η JAK2 μπορεί, μέσω του IRS-2 (Insulin Receptor Substrate-2, υπόστρωμα-2 του υποδοχέα της ινσουλίνης), να ενεργοποιεί την PI3K (Sweeney, 2002) (Σχήμα 3). H PI3K με τη σειρά της είναι γνωστό ότι ενεργοποιεί τις Ca 2+ -εξαρτώμενες ισομορφές της πρωτεϊνικής κινάσης C, δηλαδή τις α-, β I - και β II -, οι οποίες στη συνέχεια μετατοπίζονται προς την πλασματική μεμβράνη όπου αλληλεπιδρούν με τον ΝΗΕ1 (Attoub et al., 2000; Maly et al., 2002; Li et al., 2005), ενώ ταυτόχρονα επάγει τη συναρμολόγηση της NADPH οξειδάσης από τα συστατικά της στοιχεία (Cosentino et al., 2003) (Σχήμα 3). Μέσω ενός άλλου μονοπατιού μεταγωγής σήματος το οποίο περιλαμβάνει Rho GTPάσες, η PI3K επιδρά στον κυτταροσκελετό της ακτίνης, ο οποίος με τη σειρά του είναι συνδεδεμένος με τον ΝΗΕ1 μέσω του πρωτεϊνικού συμπλόκου ERM (αποτελούμενο από τις πρωτεΐνες εζρίνη, ραδιξίνη, μοεσίνη) (Cardone et al., 2005; Meima et al., 2007) (Σχήμα 3). Είναι επίσης γνωστό ότι η λεπτίνη αυξάνει τη μεταγραφή και εν συνεχεία επιφανειακή έκφραση του κύριου ινσουλινο-εξαρτώμενου μεταφορέα γλυκόζης, του GLUT4, μέσω σηματοδοτικών μονοπατιών που περιλαμβάνουν τις ERK και PI3K (Berti & Gammeltoft, 1999). Παράλληλα, μια εργασία σε μακροφάγα ποντικού διαπίστωσε ότι η αδιπονεκτίνη μπορούσε και ανέστελλε τη φλεγμονώδη δράση της λεπτίνης (συγκεκριμένα τη σύνθεση TNFα) μέσω παρεμπόδισης της φωσφορυλίωσης και άρα ενεργοποίησης των ERK και p38, δύο πρωτεϊνών που ανήκουν στην ευρύτερη κατηγορία των MAPκινασών (MAPKs) (Zhao et al., 2005). Στην ίδια εργασία παρατηρήθηκε ότι η λεπτίνη πραγματοποιούσε την ίδια φλεγμονώδη δράση και μέσω αύξησης του camp και της δράσης της PKA, γεγονότων που δεν επηρεάζονταν από την αδιπονεκτίνη (Σχήμα 3). Επιπρόσθετα, προηγούμενη εργασία μας είχε δείξει επικοινωνία μεταξύ
159 ERK και NHE1 (Konstantinidis et al., 2006) (Σχήμα 3). Τα αποτελέσματά μας δείχνουν ότι η αθηρογόνος δράση της λεπτίνης πραγματοποιείται είτε μέσω ενός ή και των δύο προαναφερθέντων μονοπατιών που ξεκινούν από την PI3K και καταλήγουν στον ΝΗΕ1, είτε μέσω ενός νέου, αχαρτογράφητου μονοπατιού που περιλαμβάνει τον ΝΗΕ1, την PI3K, συμβατικές ισομορφές της πρωτεϊνικής κινάσης C (α-, β I - και β II -) και την NADPH οξειδάση. Εξίσου πιθανή είναι η ύπαρξη ενός σηματοδοτικού δικτύου στα πλαίσια του οποίου ενεργοποιούνται σε διαφορετικό βαθμό όλα τα προηγούμενα μονοπάτια. Αξίζει να σημειωθεί ότι με βάση τα αποτελέσματά μας η ΝΟ συνθάση δε φαίνεται να συμμετέχει στις διαδικασίες προσκόλλησης στη λαμινίνη-1 και μετανάστευσης διαμέσου αυτής, καθώς και στη διαδικασία φαγοκύττωσης των oxldls. 159
160 Σχήμα 3. Επισκόπηση μονοπατιών μεταγωγής σήματος που σχετίζονται με τη δράση της λεπτίνης.
Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3], Δ. Καραμήτσος[1]
![Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3], Δ. Καραμήτσος[1] Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3], Δ. Καραμήτσος[1]](/thumbs/20/414553.jpg) Ολόγοςλεπτίνης/αδιπονεκτίνης ως ανεξάρτητος προγνωστικός παράγοντας 10ετούς καρδιαγγειακού κινδύνου σε ινσουλινοθεραπευόμενους ασθενείς με διαβήτη τύπου 2 Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1],
Ολόγοςλεπτίνης/αδιπονεκτίνης ως ανεξάρτητος προγνωστικός παράγοντας 10ετούς καρδιαγγειακού κινδύνου σε ινσουλινοθεραπευόμενους ασθενείς με διαβήτη τύπου 2 Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1],
ΛΙΠΩΔΗΣ ΙΣΤΟΣ ΚΑΙ ΕΝΔΟΘΗΛΙΟ: ΜΙΑ ΔΥΝΑΜΙΚΗ ΣΧΕΣΗ. Κ. ΜΑΚΕΔΟΥ, Ιατρός Βιοπαθολόγος
 ΛΙΠΩΔΗΣ ΙΣΤΟΣ ΚΑΙ ΕΝΔΟΘΗΛΙΟ: ΜΙΑ ΔΥΝΑΜΙΚΗ ΣΧΕΣΗ Κ. ΜΑΚΕΔΟΥ, Ιατρός Βιοπαθολόγος ΛΙΠΩΔΗΣ ΙΣΤΟΣ Απόδοση λιπαρών οξέων μετά από υδρόλυση των τριγλυκεριδίων, σε περίοδο νηστείας, με σκοπό: Την παραγωγή ενέργειας
ΛΙΠΩΔΗΣ ΙΣΤΟΣ ΚΑΙ ΕΝΔΟΘΗΛΙΟ: ΜΙΑ ΔΥΝΑΜΙΚΗ ΣΧΕΣΗ Κ. ΜΑΚΕΔΟΥ, Ιατρός Βιοπαθολόγος ΛΙΠΩΔΗΣ ΙΣΤΟΣ Απόδοση λιπαρών οξέων μετά από υδρόλυση των τριγλυκεριδίων, σε περίοδο νηστείας, με σκοπό: Την παραγωγή ενέργειας
Οξειδωτικό Stress, άσκηση και υπερπροπόνηση
 Οξειδωτικό Stress, άσκηση και υπερπροπόνηση Τζιαμούρτας Ζ. Αθανάσιος Επίκουρος Καθηγητής Βιοχημείας της Άσκησης, ΠΘ Ερευνητής, Ινστιτούτο Σωματικής Απόδοσης και Αποκατάστασης Οξειδωτικό στρες Γενικός όρος
Οξειδωτικό Stress, άσκηση και υπερπροπόνηση Τζιαμούρτας Ζ. Αθανάσιος Επίκουρος Καθηγητής Βιοχημείας της Άσκησης, ΠΘ Ερευνητής, Ινστιτούτο Σωματικής Απόδοσης και Αποκατάστασης Οξειδωτικό στρες Γενικός όρος
στη λειτουργία του ενδοθηλίου, το οποίο δέχεται την επίδραση ενδογενών και εξωγενών στρεσογόνων παραγόντων. Η απόκρισή του στους εν λόγω
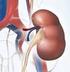 Περίληψη Το φαινόμενο της φλεγμονής φαίνεται ότι διαδραματίζει καθοριστικό ρόλο στη λειτουργία του ενδοθηλίου, το οποίο δέχεται την επίδραση ενδογενών και εξωγενών στρεσογόνων παραγόντων. Η απόκρισή του
Περίληψη Το φαινόμενο της φλεγμονής φαίνεται ότι διαδραματίζει καθοριστικό ρόλο στη λειτουργία του ενδοθηλίου, το οποίο δέχεται την επίδραση ενδογενών και εξωγενών στρεσογόνων παραγόντων. Η απόκρισή του
Φλεγμονή. Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ
 Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
Φλεγμονή Α. Χατζηγεωργίου Επίκουρος Καθηγητής Φυσιολογίας Ιατρικής Σχολής ΕΚΠΑ Μη ειδική ανοσολογική άμυνα ΑΝΑΤΟΜΙΚΟΙ ΦΡΑΓΜΟΙ Φυσικοί: δέρμα, βλεννογόνοι, βλέννα, βήχας Χημικοί: λυσοζύμη, αντιμικροβιακά
ΚΥΚΛΟΦΟΡΙΚΕΣ ΔΙΑΤΑΡΑΧΕΣ
 ΚΥΚΛΟΦΟΡΙΚΕΣ ΔΙΑΤΑΡΑΧΕΣ ΑΡΤΗΡΙΟΣΚΛΗΡΥΝΣΗ ΑΘΗΡΟΣΚΛΗΡΩΣΗ Κολέτσα Τριανταφυλλιά Eπικ. Καθηγήτρια Παθολογικής Ανατομικής ΑΠΘ Aρτηριοσκλήρωση * Αρτηριδιοσκλήρωση (Υπερτασική) * Τύπου Mockemberg
ΚΥΚΛΟΦΟΡΙΚΕΣ ΔΙΑΤΑΡΑΧΕΣ ΑΡΤΗΡΙΟΣΚΛΗΡΥΝΣΗ ΑΘΗΡΟΣΚΛΗΡΩΣΗ Κολέτσα Τριανταφυλλιά Eπικ. Καθηγήτρια Παθολογικής Ανατομικής ΑΠΘ Aρτηριοσκλήρωση * Αρτηριδιοσκλήρωση (Υπερτασική) * Τύπου Mockemberg
ΚΑΡΔΙΑΓΓΕΙΑΚΕΣ ΠΑΘΗΣΕΙΣ Ι
 ΚΑΡΔΙΑΓΓΕΙΑΚΕΣ ΠΑΘΗΣΕΙΣ Ι MK1118 ΑΣΚΗΣΗ ΣΕ ΚΛΙΝΙΚΟΥΣ ΠΛΗΘΥΣΜΟΥΣ ΔΙΑΛΕΞΗ 4 ΑΝΤΩΝΙΑ ΚΑΛΤΣΑΤΟΥ, PHD ΣΥΓΧΡΟΝΕΣ ΑΙΤΙΕΣ ΘΝΗΤΟΤΗΤΑΣ ΑΡΙΘΜΟΣ ΘΑΝΑΤΩΝ 450,000 400,000 350,000 300,000 250,000 200,000 150,000 100,000
ΚΑΡΔΙΑΓΓΕΙΑΚΕΣ ΠΑΘΗΣΕΙΣ Ι MK1118 ΑΣΚΗΣΗ ΣΕ ΚΛΙΝΙΚΟΥΣ ΠΛΗΘΥΣΜΟΥΣ ΔΙΑΛΕΞΗ 4 ΑΝΤΩΝΙΑ ΚΑΛΤΣΑΤΟΥ, PHD ΣΥΓΧΡΟΝΕΣ ΑΙΤΙΕΣ ΘΝΗΤΟΤΗΤΑΣ ΑΡΙΘΜΟΣ ΘΑΝΑΤΩΝ 450,000 400,000 350,000 300,000 250,000 200,000 150,000 100,000
«ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΒΙΟΪΑΤΡΙΚΗ ΜΗΧΑΝΙΚΗ»
 ΜΑΘΗΜΑ ETY-494 «ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΒΙΟΪΑΤΡΙΚΗ ΜΗΧΑΝΙΚΗ» Τμήμα Επιστήμης και Τεχνολογίας Υλικών, Σχολή Θετικών Επιστημών, Πανεπιστήμιο Κρήτης ρ. Γεώργιος Βλαστός (E-mail: vlastos@materials.uoc.gr) Ιστοσελίδα
ΜΑΘΗΜΑ ETY-494 «ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΒΙΟΪΑΤΡΙΚΗ ΜΗΧΑΝΙΚΗ» Τμήμα Επιστήμης και Τεχνολογίας Υλικών, Σχολή Θετικών Επιστημών, Πανεπιστήμιο Κρήτης ρ. Γεώργιος Βλαστός (E-mail: vlastos@materials.uoc.gr) Ιστοσελίδα
ΠΑΖΑΪΥΟΥ-ΠΑΝΑΓΙΩΤΟΥ Κ.
 Γιατί μας απασχολεί Ο σακχαρώδης διαβήτης τύπου 1 και 2 συνοδεύονται από μικρο και μακροαγγειακές επιπλοκές Σημαντικότερη αιτία νοσηρότητας και θνητότητας του διαβητικού πληθυσμού Ο κίνδυνος για καρδιαγγειακή
Γιατί μας απασχολεί Ο σακχαρώδης διαβήτης τύπου 1 και 2 συνοδεύονται από μικρο και μακροαγγειακές επιπλοκές Σημαντικότερη αιτία νοσηρότητας και θνητότητας του διαβητικού πληθυσμού Ο κίνδυνος για καρδιαγγειακή
8 η Παρουσίαση Εισαγωγή στο Αίμα
 ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ 8 η Παρουσίαση Εισαγωγή στο Αίμα ΠΗΓΕΣ :ADAM,AMERICAN SOCIETY OF HEMATOLOGY, www.blood.co.uk Συστατικά του κυκλοφορικού
ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ
 ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ ΧΡΙΣΤΙΝΑ ΚΑΛΟΓΕΡΟΠΟΥΛΟΥ ΑΘΗΝΑ 2010 1 ΣΚΟΠΟΣ Η ανάλυση και μελέτη της μοριακής δομής των καρωτίδων αρτηριών με υπέρυθρη φασματοσκοπία. Η εξαγωγή συμπερασμάτων
ΦΑΣΜΑΤΟΣΚΟΠΙΚΗ ΑΝΑΛΥΣΗ ΚΑΡΩΤΙΔΩΝ ΕΠΙΔΡΑΣΗ ΣΑΚΧΑΡΟΥ ΧΡΙΣΤΙΝΑ ΚΑΛΟΓΕΡΟΠΟΥΛΟΥ ΑΘΗΝΑ 2010 1 ΣΚΟΠΟΣ Η ανάλυση και μελέτη της μοριακής δομής των καρωτίδων αρτηριών με υπέρυθρη φασματοσκοπία. Η εξαγωγή συμπερασμάτων
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ. Εργαστήριο Γενετικής, ΓΠΑ
 ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
ΑΝΟΣΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΜΟΝΟΚΛΩΝΙΚΑ ΑΝΤΙΣΩΜΑΤΑ ΕΜΒΟΛΙΑ Στάδια μικροβιακής λοίμωξης δημιουργία αποικίας σε εξωτερική επιφάνεια διείσδυση στον οργανισμό τοπική μόλυνση συστηματική (γενικευμένη) μόλυνση H σημασία
Πανεπιστήμιο Ιωαννίνων. Ερευνητικό Κέντρο Αθηροθρόμβωσης. Σ. Παπαδάκη 1, Σ. Σιδηροπούλου 1, Β. Χαντζηχρήστος 1, Μ. Πασχόπουλος 2, Α.
 Πανεπιστήμιο Ιωαννίνων Ερευνητικό Κέντρο Αθηροθρόμβωσης Σ. Παπαδάκη 1, Σ. Σιδηροπούλου 1, Β. Χαντζηχρήστος 1, Μ. Πασχόπουλος 2, Α. Τσελέπης 1 1 Ερευνητικό Κέντρο Αθηροθρόμβωσης/Εργαστήριο Βιοχημείας, Τμήμα
Πανεπιστήμιο Ιωαννίνων Ερευνητικό Κέντρο Αθηροθρόμβωσης Σ. Παπαδάκη 1, Σ. Σιδηροπούλου 1, Β. Χαντζηχρήστος 1, Μ. Πασχόπουλος 2, Α. Τσελέπης 1 1 Ερευνητικό Κέντρο Αθηροθρόμβωσης/Εργαστήριο Βιοχημείας, Τμήμα
Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C.
 Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
Βιταμίνη C - Ενισχύει το ανοσοποιητικό με 20 διαφορετικούς τρόπους - ΚΑΛΑΜΠΑΚΑ CITY KALAMP Επιστημονικά Δεδομένα για τη βιοχημική δράση της αντιοξειδωτικής Βιταμίνης C. Η βιταμίνη C, γνωστή και ως ασκορβικό
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ. ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή εργασία Η ΚΑΤΑΘΛΙΨΗ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 1
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία Η ΚΑΤΑΘΛΙΨΗ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 1 ΑΝΔΡΕΑΣ ΑΝΔΡΕΟΥ Φ.Τ:2008670839 Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία Η ΚΑΤΑΘΛΙΨΗ ΣΕ ΕΦΗΒΟΥΣ ΜΕ ΣΑΚΧΑΡΩΔΗ ΔΙΑΒΗΤΗ ΤΥΠΟΥ 1 ΑΝΔΡΕΑΣ ΑΝΔΡΕΟΥ Φ.Τ:2008670839 Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ
 ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
Διαβητική περιφερική αρτηριοπάθεια και νευροπάθεια Οφέλη από τη ρύθμιση των λιπιδίων. Σ. Λιάτης
 Διαβητική περιφερική αρτηριοπάθεια και νευροπάθεια Οφέλη από τη ρύθμιση των λιπιδίων Σ. Λιάτης Δομή της παρουσίασης Διαβητική δυσλιπιδαιμία Περιφερική αρτηριοπάθεια και δυσλιπιδαιμία Περιφερική νευροπάθεια
Διαβητική περιφερική αρτηριοπάθεια και νευροπάθεια Οφέλη από τη ρύθμιση των λιπιδίων Σ. Λιάτης Δομή της παρουσίασης Διαβητική δυσλιπιδαιμία Περιφερική αρτηριοπάθεια και δυσλιπιδαιμία Περιφερική νευροπάθεια
ΔΕΙΚΤΕΣ ΦΛΕΓΜΟΝΗΣ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΜΗ ΑΛΛΕΡΓΙΚΟ ΣΟΒΑΡΟ ΒΡΟΓΧΙΚΟ ΑΣΘΜΑ
 ΔΕΙΚΤΕΣ ΦΛΕΓΜΟΝΗΣ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΜΗ ΑΛΛΕΡΓΙΚΟ ΣΟΒΑΡΟ ΒΡΟΓΧΙΚΟ ΑΣΘΜΑ ΠΑΡΑΣΚΕΥΗ ΚΑΤΣΑΟΥΝΟΥ ΛΕΚΤΟΡΑΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΠΝΕΥΜΟΝΟΛΟΓΙΑΣ ΚΑΙ ΑΝΑΠΝΕΥΣΤΙΚΗΣ ΑΝΕΠΑΡΚΕΙΑΣ- Κ.Ε.Θ. ΝΟΣΟΚΟΜΕΙΟ
ΔΕΙΚΤΕΣ ΦΛΕΓΜΟΝΗΣ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΜΗ ΑΛΛΕΡΓΙΚΟ ΣΟΒΑΡΟ ΒΡΟΓΧΙΚΟ ΑΣΘΜΑ ΠΑΡΑΣΚΕΥΗ ΚΑΤΣΑΟΥΝΟΥ ΛΕΚΤΟΡΑΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΠΝΕΥΜΟΝΟΛΟΓΙΑΣ ΚΑΙ ΑΝΑΠΝΕΥΣΤΙΚΗΣ ΑΝΕΠΑΡΚΕΙΑΣ- Κ.Ε.Θ. ΝΟΣΟΚΟΜΕΙΟ
Μεταβολικές ανάγκες ανοσοκυττάρων
 Μεταβολικές ανάγκες ανοσοκυττάρων Στέργιος Κατσιουγιάννης PhD Μεταδιδακτορικός συνεργάτης Χαροκόπειο Πανεπιστήµιο Τµήµα Επιστήµης ιαιτολογίας και ιατροφής Μεταβολισµός και Ανοσολογία Ιστορικά το καλύτερο
Μεταβολικές ανάγκες ανοσοκυττάρων Στέργιος Κατσιουγιάννης PhD Μεταδιδακτορικός συνεργάτης Χαροκόπειο Πανεπιστήµιο Τµήµα Επιστήµης ιαιτολογίας και ιατροφής Μεταβολισµός και Ανοσολογία Ιστορικά το καλύτερο
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς. Οι φάσεις των Τ κυτταρικών απαντήσεων
 ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΚΥΤΟΚΙΝΕΣ, ΜΥΟΚΙΝΕΣ ΚΑΙ ΑΣΚΗΣΗ Χαρά Κ. Δελή, PhD
 Σχολή Επιστήμης Φυσικής Αγωγής και Αθλητισμού Πανεπιστήμιο Θεσσαλίας ΚΥΤΟΚΙΝΕΣ, ΜΥΟΚΙΝΕΣ ΚΑΙ ΑΣΚΗΣΗ Χαρά Κ. Δελή, PhD Εργαστήριο Φυσιολογίας, Βιοχημείας και Διατροφής της Άσκησης Σχολή Επιστήμης Φυσικής
Σχολή Επιστήμης Φυσικής Αγωγής και Αθλητισμού Πανεπιστήμιο Θεσσαλίας ΚΥΤΟΚΙΝΕΣ, ΜΥΟΚΙΝΕΣ ΚΑΙ ΑΣΚΗΣΗ Χαρά Κ. Δελή, PhD Εργαστήριο Φυσιολογίας, Βιοχημείας και Διατροφής της Άσκησης Σχολή Επιστήμης Φυσικής
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Ο ρόλος του οξειδωτικού stress στην έναρξη της αθηρωμάτωσης. Αλληλεπιδράσεις μονοκυττάρων και ενδοθηλιακών
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Ο ρόλος του οξειδωτικού stress στην έναρξη της αθηρωμάτωσης. Αλληλεπιδράσεις μονοκυττάρων και ενδοθηλιακών
Μικροοργανισμοί. Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς
 Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
Μικροοργανισμοί Οι μικροοργανισμοί διακρίνονται σε: Μύκητες Πρωτόζωα Βακτήρια Ιούς Παθογόνοι μικροοργανισμοί Παθογόνοι μικροοργανισμοί ονομάζονται οι μικροοργανισμοί που χρησιμοποιούν τον άνθρωπο ως ξενιστή
Κυκλοφορικό σύστημα. Από μαθητές και μαθήτριες του Στ 1
 Κυκλοφορικό σύστημα Από μαθητές και μαθήτριες του Στ 1 Η καρδία Χτύπα 2 δισεκατομμύρια φορές σε όλη μας τη ζωή. Βρίσκεται στο θώρακα, κέντρο προς αριστερά. Έχει το μέγεθος μιας γροθιάς. Αλεξάνδρα, Αναστασία,
Κυκλοφορικό σύστημα Από μαθητές και μαθήτριες του Στ 1 Η καρδία Χτύπα 2 δισεκατομμύρια φορές σε όλη μας τη ζωή. Βρίσκεται στο θώρακα, κέντρο προς αριστερά. Έχει το μέγεθος μιας γροθιάς. Αλεξάνδρα, Αναστασία,
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΦΥΣΙΚΗΣ ΑΓΩΓΗΣ & ΑΘΛΗΤΙΣΜΟΥ. 9η Διάλεξη: «Άσκηση και ελεύθερες ρίζες»
 ΕΠΕΑΕΚ ΑΝΑΜΟΡΦΩΣΗ ΤΟΥ ΠΡΟΓΡΑΜΜΑΤΟΣ ΣΠΟΥΔΩΝ ΤΟΥ Τ.Ε.Φ.Α.Α.ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΙΑΣ - ΑΥΤΕΠΙΣΤΑΣΙΑ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΦΥΣΙΚΗΣ ΑΓΩΓΗΣ & ΑΘΛΗΤΙΣΜΟΥ ΚΕ 0918 «Βιοχημική Αξιολόγηση Αθλητών»
ΕΠΕΑΕΚ ΑΝΑΜΟΡΦΩΣΗ ΤΟΥ ΠΡΟΓΡΑΜΜΑΤΟΣ ΣΠΟΥΔΩΝ ΤΟΥ Τ.Ε.Φ.Α.Α.ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΙΑΣ - ΑΥΤΕΠΙΣΤΑΣΙΑ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΗΣ ΦΥΣΙΚΗΣ ΑΓΩΓΗΣ & ΑΘΛΗΤΙΣΜΟΥ ΚΕ 0918 «Βιοχημική Αξιολόγηση Αθλητών»
Μόρια κυτταρικής πρόσφυσης
 Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
Βιολογικές Μεμβράνες και Μεταγωγή Σήματος
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογικές Μεμβράνες και Μεταγωγή Σήματος Τερματισμός σηματοδότησης Διδάσκουσα: Καθ. Μαρία - Ελένη Ε. Λέκκα Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογικές Μεμβράνες και Μεταγωγή Σήματος Τερματισμός σηματοδότησης Διδάσκουσα: Καθ. Μαρία - Ελένη Ε. Λέκκα Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό
ΑΣΚΗΣΙΟΓΕΝΗΣ ΜΥΙΚΟΣ ΤΡΑΥΜΑΤΙΣΜΟΣ ΚΑΙ ΦΛΕΓΜΟΝΗ
 ΒΙΟΧΗΜΕΙΑ ΤΗΣ ΑΣΚΗΣΗΣ κωδ. μαθήματος Ν314 Τίτλος 9 ης Διάλεξης ΑΣΚΗΣΙΟΓΕΝΗΣ ΜΥΙΚΟΣ ΤΡΑΥΜΑΤΙΣΜΟΣ ΚΑΙ ΦΛΕΓΜΟΝΗ Εισήγηση: Χατζηνικολάου Α.,Επίκουρος Καθηγητής Δημιουργείται συνήθως σε: Μυοσκελετικό τραυματισμό
ΒΙΟΧΗΜΕΙΑ ΤΗΣ ΑΣΚΗΣΗΣ κωδ. μαθήματος Ν314 Τίτλος 9 ης Διάλεξης ΑΣΚΗΣΙΟΓΕΝΗΣ ΜΥΙΚΟΣ ΤΡΑΥΜΑΤΙΣΜΟΣ ΚΑΙ ΦΛΕΓΜΟΝΗ Εισήγηση: Χατζηνικολάου Α.,Επίκουρος Καθηγητής Δημιουργείται συνήθως σε: Μυοσκελετικό τραυματισμό
ΜΕΛΕΤΗ ΤΗΣ ΔΡΑΣΤΗΡΙΟΤΗΤΑΣ ΤΗΣ ΝΗΕ 1 ΚΑΙ ΟΙ ΑΘΗΡΟΓΟΝΕΣ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΜΟΝΟΚΥΤΤΑΡΩΝ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΑΝΤΙΣΤΑΣΗ ΣΤΗΝ ΙΝΣΟΥΛΙΝΗ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΜΕΑΣ ΠΑΘΟΛΟΓΙΑΣ Β ΠΑΘΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΔΙΕΥΘΥΝΤΡΙΑ: ΚΑΘΗΓΗΤΡΙΑ ΜΑΡΙΑ ΡΑΠΤΟΠΟΥΛΟΥ ΓΙΓΗ ΠΑΝΕΠ. ΕΤΟΣ 2008 2009 Αριθμ. 2883 ΜΕΛΕΤΗ ΤΗΣ ΔΡΑΣΤΗΡΙΟΤΗΤΑΣ ΤΗΣ
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΜΕΑΣ ΠΑΘΟΛΟΓΙΑΣ Β ΠΑΘΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΔΙΕΥΘΥΝΤΡΙΑ: ΚΑΘΗΓΗΤΡΙΑ ΜΑΡΙΑ ΡΑΠΤΟΠΟΥΛΟΥ ΓΙΓΗ ΠΑΝΕΠ. ΕΤΟΣ 2008 2009 Αριθμ. 2883 ΜΕΛΕΤΗ ΤΗΣ ΔΡΑΣΤΗΡΙΟΤΗΤΑΣ ΤΗΣ
4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ. περιλαμβάνονται ο σπλήνας και ο θύμος αδένας (εικ.4.1). Το λεμφικό σύστημα είναι πολύ σημαντικό γιατί:
 ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
ΚΕΧΑΓΙΑΣ ΒΑΣΙΛΕΙΟΣ ΑΘΗΝΑ, 16/11/10 A.M. :
 ΚΕΧΑΓΙΑΣ ΒΑΣΙΛΕΙΟΣ ΑΘΗΝΑ, 16/11/10 A.M. : 2010336 ΕΡΓΑΣΙΑ ΓΙΑ ΤΟ Μ.Π.Σ. ΜΕΤΑΒΟΛΙΚΑ ΝΟΣΗΜΑΤΑ ΟΣΤΩΝ ΚΥΤΟΚΙΝΕΣ ΠΑΡΑΓΟΜΕΝΕΣ ΑΠΟ ΤΑ Τ-ΚΥΤΤΑΡΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΠΟΥ ΕΜΠΛΕΚΟΝΤΑΙ ΣΤΗΝ ΟΣΤΕΟΚΛΑΣΤΟΓΕΝΕΣΗ
ΚΕΧΑΓΙΑΣ ΒΑΣΙΛΕΙΟΣ ΑΘΗΝΑ, 16/11/10 A.M. : 2010336 ΕΡΓΑΣΙΑ ΓΙΑ ΤΟ Μ.Π.Σ. ΜΕΤΑΒΟΛΙΚΑ ΝΟΣΗΜΑΤΑ ΟΣΤΩΝ ΚΥΤΟΚΙΝΕΣ ΠΑΡΑΓΟΜΕΝΕΣ ΑΠΟ ΤΑ Τ-ΚΥΤΤΑΡΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΠΟΥ ΕΜΠΛΕΚΟΝΤΑΙ ΣΤΗΝ ΟΣΤΕΟΚΛΑΣΤΟΓΕΝΕΣΗ
Υγεία και Άσκηση Ειδικών Πληθυσμών ΜΚ0958. Περιεχόμενο
 Υγεία και Άσκηση Ειδικών Πληθυσμών ΜΚ0958 Υπεύθυνη Μαθήματος: Χ. Καρατζαφέρη Διδάσκοντες: Χ. Καρατζαφέρη, Γ. Σακκάς,Α. Καλτσάτου 2013-2014 Διάλεξη 3 ΤΕΦΑΑ, ΠΘ Περιεχόμενο Συνδεση με τα προηγουμενα Πριν
Υγεία και Άσκηση Ειδικών Πληθυσμών ΜΚ0958 Υπεύθυνη Μαθήματος: Χ. Καρατζαφέρη Διδάσκοντες: Χ. Καρατζαφέρη, Γ. Σακκάς,Α. Καλτσάτου 2013-2014 Διάλεξη 3 ΤΕΦΑΑ, ΠΘ Περιεχόμενο Συνδεση με τα προηγουμενα Πριν
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ TOMEAΣ ΖΩΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΖΩΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ TOMEAΣ ΖΩΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΖΩΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Επίδραση της ινσουλίνης και της γλυκόζης σε ενδοκυτταρικούς
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΘΕΤΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΜΗΜΑ ΒΙΟΛΟΓΙΑΣ TOMEAΣ ΖΩΟΛΟΓΙΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΖΩΩΝ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ Επίδραση της ινσουλίνης και της γλυκόζης σε ενδοκυτταρικούς
ΜΕΣΟΘΕΡΑΠΕΙΑ ΕΝΕΣΙΜΗ ΤΟΠΙΚΗ ΘΕΡΑΠΕΙΑ
 ΜΕΣΟΘΕΡΑΠΕΙΑ ΕΝΕΣΙΜΗ ΤΟΠΙΚΗ ΘΕΡΑΠΕΙΑ ΜΕΣΟΘΕΡΑΠΕΙΑ Αυτό σημαίνει ότι χρησιμοποιούμε μόνο ενέσιμα φάρμακα και μόνο στο σημείο που πάσχει. ΜΕΣΟΘΕΡΑΠΕΙΑ Ξεκίνησε στη λογική του γιατί να μη χορηγήσω ένα αντιφλεγμονώδες
ΜΕΣΟΘΕΡΑΠΕΙΑ ΕΝΕΣΙΜΗ ΤΟΠΙΚΗ ΘΕΡΑΠΕΙΑ ΜΕΣΟΘΕΡΑΠΕΙΑ Αυτό σημαίνει ότι χρησιμοποιούμε μόνο ενέσιμα φάρμακα και μόνο στο σημείο που πάσχει. ΜΕΣΟΘΕΡΑΠΕΙΑ Ξεκίνησε στη λογική του γιατί να μη χορηγήσω ένα αντιφλεγμονώδες
6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών
 6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών Οι δύο τύποι της κυτταρικής ανοσίας Η µετανάστευση των δραστικών Τ κυττάρων στις εστίες της λοίµωξης (εντόπιση
6. ΡΑΣΤΙΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΤΗΣ ΚΥΤΤΑΡΙΚΗΣ ΑΝΟΣΙΑΣ: Εξάλειψη των ενδοκυττάριων µικροοργανισµών Οι δύο τύποι της κυτταρικής ανοσίας Η µετανάστευση των δραστικών Τ κυττάρων στις εστίες της λοίµωξης (εντόπιση
ΦΑΓΟΚΥΤΤΑΡΩΣΗ ΟΞΕΙΔΩΤΙΚΗ ΕΚΡΗΞΗ. Αλεξάνδρα Φλέβα Ph.D Βιολόγος Τμήμα Ανοσολογίας-Ιστοσυμβατότητας Γ.Ν. «Παπαγεωργίου»
 ΦΑΓΟΚΥΤΤΑΡΩΣΗ ΟΞΕΙΔΩΤΙΚΗ ΕΚΡΗΞΗ Αλεξάνδρα Φλέβα Ph.D Βιολόγος Τμήμα Ανοσολογίας-Ιστοσυμβατότητας Γ.Ν. «Παπαγεωργίου» ΦΥΣΙΚΗ-ΜΗ ΕΙΔΙΚΗ ΑΝΟΣΙΑ Φυσιολογικοί φραγμοί Κύτταρα Χημικές ουσίες Αποτελεί τη πρώτη
ΦΑΓΟΚΥΤΤΑΡΩΣΗ ΟΞΕΙΔΩΤΙΚΗ ΕΚΡΗΞΗ Αλεξάνδρα Φλέβα Ph.D Βιολόγος Τμήμα Ανοσολογίας-Ιστοσυμβατότητας Γ.Ν. «Παπαγεωργίου» ΦΥΣΙΚΗ-ΜΗ ΕΙΔΙΚΗ ΑΝΟΣΙΑ Φυσιολογικοί φραγμοί Κύτταρα Χημικές ουσίες Αποτελεί τη πρώτη
Ομαδες μοριων κυτταρικης προσφυσης
 Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
Η ΕΠΙΔΡΑΣΗ ΤΩΝ ΠΡΟΔΙΑΘΕΣΙΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΗΝ ΕΞΕΛΙΞΗ ΤΗΣ ΣΤΕΦΑΝΙΑΙΑΣ ΝΟΣΟΥ. Γαργάνη Κωνσταντίνα: ΤΕ Νοσηλεύτρια Σ/Μ ΓΝΘ Παπανικολάου
 Η ΕΠΙΔΡΑΣΗ ΤΩΝ ΠΡΟΔΙΑΘΕΣΙΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΗΝ ΕΞΕΛΙΞΗ ΤΗΣ ΣΤΕΦΑΝΙΑΙΑΣ ΝΟΣΟΥ Γαργάνη Κωνσταντίνα: ΤΕ Νοσηλεύτρια Σ/Μ ΓΝΘ Παπανικολάου Η στεφανιαία νόσος είναι µία πάθηση των αρτηριών της καρδιάς που οφείλεται
Η ΕΠΙΔΡΑΣΗ ΤΩΝ ΠΡΟΔΙΑΘΕΣΙΚΩΝ ΠΑΡΑΓΟΝΤΩΝ ΣΤΗΝ ΕΞΕΛΙΞΗ ΤΗΣ ΣΤΕΦΑΝΙΑΙΑΣ ΝΟΣΟΥ Γαργάνη Κωνσταντίνα: ΤΕ Νοσηλεύτρια Σ/Μ ΓΝΘ Παπανικολάου Η στεφανιαία νόσος είναι µία πάθηση των αρτηριών της καρδιάς που οφείλεται
Άσκηση, Οξειδωτικό στρες και ανοσιακό σύστημα. Θανάσης Ζ. Τζιαμούρτας Αναπληρωτής Καθηγητής Βιοχημείας της Άσκησης
 Άσκηση, Οξειδωτικό στρες και ανοσιακό σύστημα Θανάσης Ζ. Τζιαμούρτας Αναπληρωτής Καθηγητής Βιοχημείας της Άσκησης Θέματα παρουσίασης Λοιμώξεις του ανώτερου αναπνευστικού συστήματος (URTI) και άσκηση (γιατί;)
Άσκηση, Οξειδωτικό στρες και ανοσιακό σύστημα Θανάσης Ζ. Τζιαμούρτας Αναπληρωτής Καθηγητής Βιοχημείας της Άσκησης Θέματα παρουσίασης Λοιμώξεις του ανώτερου αναπνευστικού συστήματος (URTI) και άσκηση (γιατί;)
ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera
 Α1. 1. β Βιολογία ΘΕΜΑ Α γενιικής παιιδείίας 2. γ 3. γ 4. γ 5. δ Α2. ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera Ηπατίτιδα C + Candida albicans
Α1. 1. β Βιολογία ΘΕΜΑ Α γενιικής παιιδείίας 2. γ 3. γ 4. γ 5. δ Α2. ΣΤΗΛΗ Α Αντιβιοτικό Αντισώματα ιντερφερόνες Τ- Τ- (αντιγόνα) κυτταροτοξικά βοηθητικά Τοξίνες Vibrio cholera Ηπατίτιδα C + Candida albicans
2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις μεμβράνες 2. Φυσιολογικοί φραγμοί
2 Ο ΜΑΘΗΜΑ ΣΥΣΤΗΜΑ ΣΥΜΠΛΗΡΩΜΑΤΟΣ ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις μεμβράνες 2. Φυσιολογικοί φραγμοί
Άσκηση και Καρδιοπάθειες
 Συμμαχία για την υγεία - Άσκηση Άσκηση και Καρδιοπάθειες Συγγραφική ομάδα: Φλουρής Ανδρέας, Ερευνητής Βογιατζής Ιωάννης, Αναπληρωτής Καθηγητής ΤΕΦΑΑ, ΕΚΠΑ Σταυρόπουλος- Καλίνογλου Αντώνης, Ερευνητής Σύγχρονες
Συμμαχία για την υγεία - Άσκηση Άσκηση και Καρδιοπάθειες Συγγραφική ομάδα: Φλουρής Ανδρέας, Ερευνητής Βογιατζής Ιωάννης, Αναπληρωτής Καθηγητής ΤΕΦΑΑ, ΕΚΠΑ Σταυρόπουλος- Καλίνογλου Αντώνης, Ερευνητής Σύγχρονες
Μεταβολικό σύνδρομο και νόσος Alzheimer
 Μεταβολικό σύνδρομο και νόσος Alzheimer Καλλιόπη Παζαΐτου -Παναγιώτου Ενδοκρινολόγος Τμήμα Ενδοκρινολογίας- Ενδοκρινικής Ογκολογίας ΑΝΘ «Θεαγένειο» Μεταβολικό σύνδρομο και νόσος Alzheimer Ορισμός μεταβολικού
Μεταβολικό σύνδρομο και νόσος Alzheimer Καλλιόπη Παζαΐτου -Παναγιώτου Ενδοκρινολόγος Τμήμα Ενδοκρινολογίας- Ενδοκρινικής Ογκολογίας ΑΝΘ «Θεαγένειο» Μεταβολικό σύνδρομο και νόσος Alzheimer Ορισμός μεταβολικού
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ Με βάση τη θέση στο ανθρώπινο σώμα Με βάση την ιδιότητα για γενικευμένη ή εξειδικευμένη δράση Εξωτερικοί εσωτερικοί μη ειδικοί μηχανισμοί ειδικοί
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ
 ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ Ερωτήσεις πολλαπλής επιλογής: επιλέξτε το γράμμα που αντιστοιχεί στη σωστή συνέχεια της πρότασης. 1. Δυσμενές χημικό περιβάλλον στην επιδερμίδα προκαλείται από:
ΕΦΑΡΜΟΓΕΣ ΑΣΚΗΣΕΙΣ ΣΤΟΥΣ ΜΗΧΑΝΙΣΜΟΥΣ ΑΜΥΝΑΣ Ερωτήσεις πολλαπλής επιλογής: επιλέξτε το γράμμα που αντιστοιχεί στη σωστή συνέχεια της πρότασης. 1. Δυσμενές χημικό περιβάλλον στην επιδερμίδα προκαλείται από:
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ. Πετρολιάγκης Σταμάτης Τμήμα Γ4
 ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Πετρολιάγκης Σταμάτης Τμήμα Γ4 ΕΝΝΟΙΑ ΤΗΣ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Η κυτταρική μεμβράνη ή πλασματική μεμβράνη είναι η εξωτερική μεμβράνη που περιβάλλει το κύτταρο
ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Πετρολιάγκης Σταμάτης Τμήμα Γ4 ΕΝΝΟΙΑ ΤΗΣ ΠΛΑΣΜΑΤΙΚΗΣ ΜΕΜΒΡΑΝΗΣ Η κυτταρική μεμβράνη ή πλασματική μεμβράνη είναι η εξωτερική μεμβράνη που περιβάλλει το κύτταρο
ΓΡΑΠΤΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2018
 ΓΥΜΝΑΣΙΟ ΕΠΙΣΚΟΠΗΣ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2017-2018 ΓΡΑΠΤΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2018 ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΤΑΞΗ: Β ΗΜΕΡΟΜΗΝΙΑ: Βαθμός:.. Ολογράφως: Υπογραφή:... ΧΡΟΝΟΣ: 45 λεπτά ΟΝΟΜΑΤΕΠΩΝΥΜΟ:. ΤΜΗΜΑ:. ΑΡ.. ΤΟ ΕΞΕΤΑΣΤΙΚΟ
ΓΥΜΝΑΣΙΟ ΕΠΙΣΚΟΠΗΣ ΣΧΟΛΙΚΗ ΧΡΟΝΙΑ 2017-2018 ΓΡΑΠΤΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2018 ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΤΑΞΗ: Β ΗΜΕΡΟΜΗΝΙΑ: Βαθμός:.. Ολογράφως: Υπογραφή:... ΧΡΟΝΟΣ: 45 λεπτά ΟΝΟΜΑΤΕΠΩΝΥΜΟ:. ΤΜΗΜΑ:. ΑΡ.. ΤΟ ΕΞΕΤΑΣΤΙΚΟ
ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ. Σχηµατική απεικόνιση της µεγάλης και της µικρής κυκλοφορίας
 ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΛΙΠΗ. ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΛΙΠΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Τα λίπη αποτελούν μια συμπυκνωμένη πηγή ενέργειας Ενεργούν σαν διαλύτες
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΛΙΠΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Τα λίπη αποτελούν μια συμπυκνωμένη πηγή ενέργειας Ενεργούν σαν διαλύτες
AIΜΟΣΤΑΣΗ Τι είναι η αιμόσταση? Ποια είναι τα κύρια στάδια?
 AIΜΟΣΤΑΣΗ Τι είναι η αιμόσταση? Ποια είναι τα κύρια στάδια? Aιμόσταση=πρόληψη απώλειας αίματος Aιμόσταση=πρόληψη απώλειας Tο αίμα: αίματος Πρέπει να είναι υγρό Δεν έρχεται σε επαφή με αρνητικά φορτισμένες
AIΜΟΣΤΑΣΗ Τι είναι η αιμόσταση? Ποια είναι τα κύρια στάδια? Aιμόσταση=πρόληψη απώλειας αίματος Aιμόσταση=πρόληψη απώλειας Tο αίμα: αίματος Πρέπει να είναι υγρό Δεν έρχεται σε επαφή με αρνητικά φορτισμένες
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα
 Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
Επίκτητη Ανοσιακή Απάντηση (χυμικό σκέλος) Β λεμφοκύτταρα φυσική ή μη ειδική ανοσία δεν απαιτεί προηγούμενη έκθεση στο παθογόνο και δεν διαθέτει μνήμη. σε επίκτητη ή ειδική ανοσία χυμική ανοσία με παραγωγή
Επίπεδα λεπτίνης και γκρελίνης σε ασθενείς με διαβήτη τύπου 2 πριν και 6 μήνες μετά την έναρξη ινσουλινοθεραπείας
 Επίπεδα λεπτίνης και γκρελίνης σε ασθενείς με διαβήτη τύπου 2 πριν και 6 μήνες μετά την έναρξη ινσουλινοθεραπείας Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3],
Επίπεδα λεπτίνης και γκρελίνης σε ασθενείς με διαβήτη τύπου 2 πριν και 6 μήνες μετά την έναρξη ινσουλινοθεραπείας Ν. Κατσίκη[1], Α. Γκοτζαμάνη-Ψαρράκου[2], Φ. Ηλιάδης[1], Τρ. Διδάγγελος[1], Ι. Γιώβος[3],
«Τρώτε μήλα για δέκα λόγους υγείας!», από την Χριστίνα Ι. Μπουντούρη, Γενικό Οικογενειακό Ιατρό και τo iatropedia.gr!
 «Τρώτε μήλα για δέκα λόγους υγείας!», από την Χριστίνα Ι. Μπουντούρη, Γενικό Οικογενειακό Ιατρό και τo iatropedia.gr! Όλοι γνωρίζουν την παροιμία»ένα μήλο την ημέρα τον γιατρό τον κάνει πέρα». Πλέον έχει
«Τρώτε μήλα για δέκα λόγους υγείας!», από την Χριστίνα Ι. Μπουντούρη, Γενικό Οικογενειακό Ιατρό και τo iatropedia.gr! Όλοι γνωρίζουν την παροιμία»ένα μήλο την ημέρα τον γιατρό τον κάνει πέρα». Πλέον έχει
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ
 ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ Η πρώτη γραπτή αναφορά στο φαινόμενο της ανοσίας μπορεί να αναζητηθεί στον Θουκυδίδη, τον μεγάλο ιστορικό του Πελοποννησιακού Πολέμου Ανάπτυξη και επιβίωση o
ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ Η πρώτη γραπτή αναφορά στο φαινόμενο της ανοσίας μπορεί να αναζητηθεί στον Θουκυδίδη, τον μεγάλο ιστορικό του Πελοποννησιακού Πολέμου Ανάπτυξη και επιβίωση o
Ο ρόλος του λιπώδους ιστού
 Ο ρόλος του λιπώδους ιστού Γιώργος Βαλσαμάκης Ενδοκρινολόγος Eπιστημονικός συνεργάτης Ενδοκρινολογικήs Μονάδαs Β Μαιευτικής και Γυναικολογικής κλινικής Αρεταίειο Νοσοκομείο Θέματα συζήτησης Α. Ο λιπώδης
Ο ρόλος του λιπώδους ιστού Γιώργος Βαλσαμάκης Ενδοκρινολόγος Eπιστημονικός συνεργάτης Ενδοκρινολογικήs Μονάδαs Β Μαιευτικής και Γυναικολογικής κλινικής Αρεταίειο Νοσοκομείο Θέματα συζήτησης Α. Ο λιπώδης
Πτυχιακή διατριβή. Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN) στην ατμόσφαιρα
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN)
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΓΕΩΤΕΧΝΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗΣ ΠΕΡΙΒΑΛΛΟΝΤΟΣ Πτυχιακή διατριβή Η επίδραση της τασιενεργής ουσίας Ακεταλδεΰδης στη δημιουργία πυρήνων συμπύκνωσης νεφών (CCN)
ΦΡΟΝΤΙΣΤΗΡΙΑ ΜΗΤΑΛΑΣ ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ
 ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΚΕΦΑΛΑΙΟ 1.3 : ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ ΘΕΜΑ 1 Χαρακτηρίστε τις προτάσεις ως σωστές ή λανθασµένες. 1. Οι βλεννογόνοι
ΙΑΓΩΝΙΣΜΑ ΒΙΟΛΟΓΙΑΣ Γ ΛΥΚΕΙΟΥ ΓΕΝΙΚΗΣ ΠΑΙ ΕΙΑΣ ΚΕΦΑΛΑΙΟ 1.3 : ΜΗΧΑΝΙΣΜΟΙ ΑΜΥΝΑΣ ΤΟΥ ΑΝΘΡΩΠΙΝΟΥ ΟΡΓΑΝΙΣΜΟΥ ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΑΝΟΣΙΑΣ ΘΕΜΑ 1 Χαρακτηρίστε τις προτάσεις ως σωστές ή λανθασµένες. 1. Οι βλεννογόνοι
ΓΡΑΠΤΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015
 ΓΥΜΝΑΣΙΟ ΑΡΧ. ΜΑΚΑΡΙΟΥ Γ - ΠΛΑΤΥ ΣΧΟΛΙΚΟ ΕΤΟΣ 2014-2015 ΓΡΑΠΤΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ-ΧΗΜΕΙΑ ΗΜΕΡΟΜΗΝΙΑ: 12/6/2015 ΒΑΘΜΟΣ ΒΑΘΜΟΣ:... ΤΑΞΗ: Γ Αριθμητικά.. ΧΡΟΝΟΣ: 2 ώρες Ολογράφως:...
ΓΥΜΝΑΣΙΟ ΑΡΧ. ΜΑΚΑΡΙΟΥ Γ - ΠΛΑΤΥ ΣΧΟΛΙΚΟ ΕΤΟΣ 2014-2015 ΓΡΑΠΤΕΣ ΑΠΟΛΥΤΗΡΙΕΣ ΕΞΕΤΑΣΕΙΣ ΙΟΥΝΙΟΥ 2015 ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ-ΧΗΜΕΙΑ ΗΜΕΡΟΜΗΝΙΑ: 12/6/2015 ΒΑΘΜΟΣ ΒΑΘΜΟΣ:... ΤΑΞΗ: Γ Αριθμητικά.. ΧΡΟΝΟΣ: 2 ώρες Ολογράφως:...
Φαρµακολογική αξιολόγηση της επίδρασης ελληνικών οινοποιητικών προϊόντων στο καρδιαγγειακό σύστηµα ασθενών µε στεφανιαία νόσο.
 Φαρµακολογική αξιολόγηση της επίδρασης ελληνικών οινοποιητικών προϊόντων στο καρδιαγγειακό σύστηµα ασθενών µε στεφανιαία νόσο. Iωάννα Ανδρεάδου Τοµέας Φαρµακευτικής Χηµείας, Τµήµα Φαρµακευτικής, ΕΚΠΑ,
Φαρµακολογική αξιολόγηση της επίδρασης ελληνικών οινοποιητικών προϊόντων στο καρδιαγγειακό σύστηµα ασθενών µε στεφανιαία νόσο. Iωάννα Ανδρεάδου Τοµέας Φαρµακευτικής Χηµείας, Τµήµα Φαρµακευτικής, ΕΚΠΑ,
www.cirse.org Περιφερική Αγγειοπάθεια Ενημέρωση Ασθενών Επεμβατική Ακτινολογία: Η εναλλακτική σου στη χειρουργική
 Περιφερική Αγγειοπάθεια Ενημέρωση Ασθενών Επεμβατική Ακτινολογία: Η εναλλακτική σου στη χειρουργική www.cirse.org Cardiovascular and Interventional Radiological Society of Europe Cardiovascular and Interventional
Περιφερική Αγγειοπάθεια Ενημέρωση Ασθενών Επεμβατική Ακτινολογία: Η εναλλακτική σου στη χειρουργική www.cirse.org Cardiovascular and Interventional Radiological Society of Europe Cardiovascular and Interventional
Εισαγωγή στην Ανοσολογία
 Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
Εισαγωγή στην Ανοσολογία ρ. Γιώργος Κρασιάς Ινστιτούτο Νευρολογίας και Γενετικής Κύπρου Τµήµα Μοριακής Ιολογίας Τι είναι το Ανοσοποιητικό Σύστηµα (ΑΣ)? Το ΑΣ (Immune System) είναι ένα σύστηµα άµυνας του
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ. physiology.med.uoa.gr
 ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΑΣΙΚΩΝ ΙΑΤΡΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ( ΜΟΡΦΟΛΕΙΤΟΥΓΙΚΟΣ ) physiology.med.uoa.gr ekvalai@med.uoa.gr mkoutsil@med.uoa.gr ΕΠΙΔΙΟΡΘΩΣΗ DNA GADD45 P21 MDM-2 p53 G1 S G 0 ΔΙΑΦΟΡΟΠΟΙΗΣΗ BAX
ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ ΤΟΜΕΑΣ ΒΑΣΙΚΩΝ ΙΑΤΡΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ( ΜΟΡΦΟΛΕΙΤΟΥΓΙΚΟΣ ) physiology.med.uoa.gr ekvalai@med.uoa.gr mkoutsil@med.uoa.gr ΕΠΙΔΙΟΡΘΩΣΗ DNA GADD45 P21 MDM-2 p53 G1 S G 0 ΔΙΑΦΟΡΟΠΟΙΗΣΗ BAX
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή διατριβή. Ονοματεπώνυμο: Αργυρώ Ιωάννου. Επιβλέπων καθηγητής: Δρ. Αντρέας Χαραλάμπους
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή διατριβή Διερεύνηση της αποτελεσματικότητας εναλλακτικών και συμπληρωματικών τεχνικών στη βελτίωση της ποιότητας της ζωής σε άτομα με καρκίνο
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή διατριβή Διερεύνηση της αποτελεσματικότητας εναλλακτικών και συμπληρωματικών τεχνικών στη βελτίωση της ποιότητας της ζωής σε άτομα με καρκίνο
MΕΣΟΓΕΙΑΚΗ ΔΙΑΙΤΑ H διατροφή του ανθρώπου, από την εμφάνισή του μέχρι σήμερα, διαμορφώθηκε από την εξελικτική εμπειρία του και από πολλούς άλλους
 MΕΣΟΓΕΙΑΚΗ ΔΙΑΙΤΑ H διατροφή του ανθρώπου, από την εμφάνισή του μέχρι σήμερα, διαμορφώθηκε από την εξελικτική εμπειρία του και από πολλούς άλλους παράγοντες όπως το περιβάλλον, οι συνήθειες ζωής, οι θρησκευτικές
MΕΣΟΓΕΙΑΚΗ ΔΙΑΙΤΑ H διατροφή του ανθρώπου, από την εμφάνισή του μέχρι σήμερα, διαμορφώθηκε από την εξελικτική εμπειρία του και από πολλούς άλλους παράγοντες όπως το περιβάλλον, οι συνήθειες ζωής, οι θρησκευτικές
< (0.999) Graft (0.698) (0.483) <0.001 (0.698) (<0.001) (<0.001) 3 months (0.999) (0.483) (<0.001) 6 months (<0.
 Supplementary table 1. Correlation of endothelial cell density among graft, 3, 6, and 12 months after Descemet s automated stripping endothelial keratoplasty. Graft 3 months 6 months 12 months Graft
Supplementary table 1. Correlation of endothelial cell density among graft, 3, 6, and 12 months after Descemet s automated stripping endothelial keratoplasty. Graft 3 months 6 months 12 months Graft
ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΘΝΙΚΟΥ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΕΡΕΥΝΑΣ Β'ΠΡΟΠΑΙΔΕΥΤΙΚΗΣ ΠΑΘΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΚΑΘΗΓΗΤΗΣ Θ.
 ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΘΝΙΚΟΥ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΕΡΕΥΝΑΣ Β'ΠΡΟΠΑΙΔΕΥΤΙΚΗΣ ΠΑΘΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΚΑΘΗΓΗΤΗΣ Θ. ΟΙΚΟΝΟΜΟΠΟΥΛΟΣ 1 ΙΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΒΙΟΛΟΓΟΣ: ΕΡΙΦΥΛΗ ΚΥΡΙΑΖΗ
ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΘΝΙΚΟΥ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΜΟΝΑΔΑ ΕΡΕΥΝΑΣ Β'ΠΡΟΠΑΙΔΕΥΤΙΚΗΣ ΠΑΘΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΚΑΘΗΓΗΤΗΣ Θ. ΟΙΚΟΝΟΜΟΠΟΥΛΟΣ 1 ΙΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΒΙΟΛΟΓΟΣ: ΕΡΙΦΥΛΗ ΚΥΡΙΑΖΗ
Αποφρακτική αρτηριακή νόσος που εντοπίζεται στον καρωτιδικό διχασμό ή στην αρχική μοίρα της έσω καρωτίδας και χαρακτηρίζεται από το σχηματισμό
 Αποφρακτική αρτηριακή νόσος που εντοπίζεται στον καρωτιδικό διχασμό ή στην αρχική μοίρα της έσω καρωτίδας και χαρακτηρίζεται από το σχηματισμό αθηρωματικής πλάκας που προκαλεί στένωση του αγγειακού αυλού,
Αποφρακτική αρτηριακή νόσος που εντοπίζεται στον καρωτιδικό διχασμό ή στην αρχική μοίρα της έσω καρωτίδας και χαρακτηρίζεται από το σχηματισμό αθηρωματικής πλάκας που προκαλεί στένωση του αγγειακού αυλού,
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά
 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά 10 ο Κεφάλαι ο Όλοι ευχόμαστε να υπήρχε ένα μαγικό χάπι που να μας έλυνε όλα τα προβλήματα. Έπειτα από 25 χρόνια έρευνας, οι
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «Ιατρική Ερευνητική Μεθοδολογία»
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «Ιατρική Ερευνητική Μεθοδολογία» «Μελέτη των αλληλεπιδράσεων των ενδοθηλιακών κυττάρων ανθρώπου με την λαμινίνη σε διεργασίες
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΠΟΥΔΩΝ «Ιατρική Ερευνητική Μεθοδολογία» «Μελέτη των αλληλεπιδράσεων των ενδοθηλιακών κυττάρων ανθρώπου με την λαμινίνη σε διεργασίες
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ
 ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΕΡΓΑΣΙΑ ΒΙΟΛΟΓΙΑΣ 3.1 ΕΝΕΡΓΕΙΑ ΚΑΙ ΟΡΓΑΝΙΣΜΟΙ Οι οργανισμοί εξασφαλίζουν ενέργεια, για τις διάφορες λειτουργίες τους, διασπώντας θρεπτικές ουσίες που περιέχονται στην τροφή τους. Όμως οι φωτοσυνθετικοί
ΒΑΣΙΚΑ ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ Μάθημα 7 Το κυκλοφορικό μας σύστημα
 jk ΒΑΣΙΚΑ ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ Μάθημα 7 Το κυκλοφορικό μας σύστημα Εισαγωγή στο Κυκλοφορικό μας Σύστημα (ΚΣ) Το ΚΣ αποτελείται από - τα αιμοφόρα αγγεία την καρδιά Αέρας που εισπνέουμε Αέρας που εκπνέουμε
jk ΒΑΣΙΚΑ ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ Μάθημα 7 Το κυκλοφορικό μας σύστημα Εισαγωγή στο Κυκλοφορικό μας Σύστημα (ΚΣ) Το ΚΣ αποτελείται από - τα αιμοφόρα αγγεία την καρδιά Αέρας που εισπνέουμε Αέρας που εκπνέουμε
Εφαρμοσμένη Διατροφική Ιατρική
 Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
Γλωσσάρι για το Μάθημα της Διατροφικής Ιατρικής Λιπαρά οξέα: περιέχουν μακριές αλυσίδες μορίων που αποτελούν σχεδόν όλο το σύμπλεγμα λιπιδίων τόσο για τα ζωικά όσο και για τα φυτικά λίπη. Αν αποκοπούν
Παθοφυσιολογία της επούλωσης των ελκών στο διαβήτη και αιτίες αποτυχίας
 Παθοφυσιολογία της επούλωσης των ελκών στο διαβήτη και αιτίες αποτυχίας Ιωάννα Ελευθεριάδου Επιστημονικός Συνεργάτης Διαβητολογικού Κέντρου ΓΝΑ Λαϊκό Σακχαρώδης διαβήτης και έλκη κάτω άκρων 25% των ασθενών
Παθοφυσιολογία της επούλωσης των ελκών στο διαβήτη και αιτίες αποτυχίας Ιωάννα Ελευθεριάδου Επιστημονικός Συνεργάτης Διαβητολογικού Κέντρου ΓΝΑ Λαϊκό Σακχαρώδης διαβήτης και έλκη κάτω άκρων 25% των ασθενών
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
Βιολογία Α Λυκείου Κεφ. 3. Κυκλοφορικό Σύστημα. Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα
 Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010
 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 Μεγεθυντική ικανότητα και διακριτική ικανότητα ή ανάλυση Μέγιστη ανάλυση
CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 CAMPBELL REECE, ΒΙΟΛΟΓΙΑ ΤΟΜΟΣ Ι, ΠΕΚ 2010 Μεγεθυντική ικανότητα και διακριτική ικανότητα ή ανάλυση Μέγιστη ανάλυση
Εφαρμοσμένη Διατροφική Ιατρική
 Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Σημείωση: Το κείμενο αποτελεί απόσπασμα του κεφαλαίου «Χοληστερίνη και φλεγμονή». Έχει αναπαραχθεί λόγω των πολύτιμων πληροφοριών
Απόσπασμα από το βιβλίο «Πως να ζήσετε 150 χρόνια» του Dr. Δημήτρη Τσουκαλά Σημείωση: Το κείμενο αποτελεί απόσπασμα του κεφαλαίου «Χοληστερίνη και φλεγμονή». Έχει αναπαραχθεί λόγω των πολύτιμων πληροφοριών
«Ο ΑΝΤΙΘΡΟΜΒΩΤΙΚΟΣ ΡΟΛΟΣ ΤΗΣ ΑΣΚΗΣΗΣ»
 «ΙΠΠΟΚΡΑΤΕΙΕΣ ΗΜΕΡΕΣ ΚΑΡΔΙΟΛΟΓΙΑΣ» 21 22 ΜΑΡΤΙΟΥ 2014 Macedonia Palace, Θεσσαλονίκη «Ο ΑΝΤΙΘΡΟΜΒΩΤΙΚΟΣ ΡΟΛΟΣ ΤΗΣ ΑΣΚΗΣΗΣ» ΚΑΡΑΒΑΣΙΛΕΙΑΔΟΥ ΣΑΒΒΑΤΩ Νοσηλεύτρια ΤΕ Παθολογίας, Msc, PhD ΤΕΦΑΑ -ΑΠΘ. Μονάδα
«ΙΠΠΟΚΡΑΤΕΙΕΣ ΗΜΕΡΕΣ ΚΑΡΔΙΟΛΟΓΙΑΣ» 21 22 ΜΑΡΤΙΟΥ 2014 Macedonia Palace, Θεσσαλονίκη «Ο ΑΝΤΙΘΡΟΜΒΩΤΙΚΟΣ ΡΟΛΟΣ ΤΗΣ ΑΣΚΗΣΗΣ» ΚΑΡΑΒΑΣΙΛΕΙΑΔΟΥ ΣΑΒΒΑΤΩ Νοσηλεύτρια ΤΕ Παθολογίας, Msc, PhD ΤΕΦΑΑ -ΑΠΘ. Μονάδα
οµή Ανοσιακού Συστήµατος Ελένη Φωτιάδου-Παππά Τµήµα Ανοσολογίας Γ.Ν. Νίκαιας-Πειραιά
 οµή Ανοσιακού Συστήµατος Ελένη Φωτιάδου-Παππά Τµήµα Ανοσολογίας Γ.Ν. Νίκαιας-Πειραιά Ανοσολογικό σύστηµα Βασικό σύστηµα του οργανισµού Λειτουργικές µονάδες του ανοσολογικού συστήµατος Οργανωµένος λεµφικός
οµή Ανοσιακού Συστήµατος Ελένη Φωτιάδου-Παππά Τµήµα Ανοσολογίας Γ.Ν. Νίκαιας-Πειραιά Ανοσολογικό σύστηµα Βασικό σύστηµα του οργανισµού Λειτουργικές µονάδες του ανοσολογικού συστήµατος Οργανωµένος λεµφικός
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΘΗΝΑΣ ΓΙΑΓΚΙΝΗ ΧΗΜΙΚΟΥ Μελέτη των ιστολογικών και βιοχημικών αλλοιώσεων
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΘΗΝΑΣ ΓΙΑΓΚΙΝΗ ΧΗΜΙΚΟΥ Μελέτη των ιστολογικών και βιοχημικών αλλοιώσεων
ΟΡΜΟΝΕΣ ΥΠΟΔΟΧΕΙΣ ΟΡΜΟΝΙΚΗ ΔΡΑΣΗ
 ΟΡΜΟΝΕΣ ΥΠΟΔΟΧΕΙΣ ΟΡΜΟΝΙΚΗ ΔΡΑΣΗ Μιχαήλ Κουτσιλιέρης MD (NKUA), Ph.D (McGill Un.) ΚΑΘΗΓΗΤΗΣ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ, ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΕΘΝΙΚΟ & ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ mkoutsil@med.uoa.gr
ΟΡΜΟΝΕΣ ΥΠΟΔΟΧΕΙΣ ΟΡΜΟΝΙΚΗ ΔΡΑΣΗ Μιχαήλ Κουτσιλιέρης MD (NKUA), Ph.D (McGill Un.) ΚΑΘΗΓΗΤΗΣ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ, ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΕΘΝΙΚΟ & ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ mkoutsil@med.uoa.gr
ΚΑΠΝΙΣΜΑ ΚΑΙ ΣΥΝΔΡΟΜΟ ΑΙΦΝΙΔΙΟΥ ΒΡΕΦΙΚΟΥ ΘΑΝΑΤΟΥ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΚΑΠΝΙΣΜΑ ΚΑΙ ΣΥΝΔΡΟΜΟ ΑΙΦΝΙΔΙΟΥ ΒΡΕΦΙΚΟΥ ΘΑΝΑΤΟΥ Ονοματεπώνυμο: Λοϊζιά Ελένη Λεμεσός 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ ΚΑΠΝΙΣΜΑ ΚΑΙ ΣΥΝΔΡΟΜΟ ΑΙΦΝΙΔΙΟΥ ΒΡΕΦΙΚΟΥ ΘΑΝΑΤΟΥ Ονοματεπώνυμο: Λοϊζιά Ελένη Λεμεσός 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ
Ειδικές μέθοδοι ανάλυσης κυτταρικών διεργασιών Επίδραση εξωγενών παραγόντων στη λειτουργία κυτταρικών μεμβράνων
 ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ Ειδικές μέθοδοι ανάλυσης κυτταρικών διεργασιών Επίδραση εξωγενών παραγόντων στη λειτουργία κυτταρικών μεμβράνων Αναστασία Παπαδάκη Τμήμα Βιολογίας To φυτικό κύτταρο
ΕΛΛΗΝΙΚΗ ΔΗΜΟΚΡΑΤΙΑ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΡΗΤΗΣ Ειδικές μέθοδοι ανάλυσης κυτταρικών διεργασιών Επίδραση εξωγενών παραγόντων στη λειτουργία κυτταρικών μεμβράνων Αναστασία Παπαδάκη Τμήμα Βιολογίας To φυτικό κύτταρο
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
Κορινθιακή σταφίδα: ένα υπερτρόφιμο υψηλής διατροφικής αξίας για μικρούς και μεγάλους. 25 Αυγούστου 2016, Ψηλά Αλώνια, Αίγιο
 Κορινθιακή σταφίδα: ένα υπερτρόφιμο υψηλής διατροφικής αξίας για μικρούς και μεγάλους 25 Αυγούστου 2016, Ψηλά Αλώνια, Αίγιο Η Κορινθιακή σταφίδα είναι ένα μοναδικό προϊόν που παράγεται σχεδόν αποκλειστικά
Κορινθιακή σταφίδα: ένα υπερτρόφιμο υψηλής διατροφικής αξίας για μικρούς και μεγάλους 25 Αυγούστου 2016, Ψηλά Αλώνια, Αίγιο Η Κορινθιακή σταφίδα είναι ένα μοναδικό προϊόν που παράγεται σχεδόν αποκλειστικά
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ. Πτυχιακή εργασία
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή εργασία ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΚΑΚΗΣ ΔΙΑΤΡΟΦΗΣ ΣΤΗ ΠΡΟΣΧΟΛΙΚΗ ΗΛΙΚΙΑ ΜΕ ΑΠΟΤΕΛΕΣΜΑ ΤΗ ΠΑΧΥΣΑΡΚΙΑ Έλλη Φωτίου 2010364426 Επιβλέπουσα
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ Πτυχιακή εργασία ΕΠΙΠΤΩΣΕΙΣ ΤΗΣ ΚΑΚΗΣ ΔΙΑΤΡΟΦΗΣ ΣΤΗ ΠΡΟΣΧΟΛΙΚΗ ΗΛΙΚΙΑ ΜΕ ΑΠΟΤΕΛΕΣΜΑ ΤΗ ΠΑΧΥΣΑΡΚΙΑ Έλλη Φωτίου 2010364426 Επιβλέπουσα
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος
 Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I. Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ.
 Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 14/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Γενικά στοιχεία
Εισαγωγή στην Ανοσολογία Επίκτητη Ανοσία I Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 14/10/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Γενικά στοιχεία
Bιολογία γενικής παιδείας
 Bιολογία γενικής παιδείας Α1. 1. δ 2. α 3. β 4. δ ΘΕΜΑ Α Α2. ΟΛΑ ΚΑΠΟΙΑ Τοξίνες + Πλασματική μεμβράνη + Κυτταρικό τοίχωμα + Αποικίες + Κάψα + Πλασμίδια + Μαστίγια + Ριβοσώματα + Πυρηνοειδές + Ενδοσπόρια
Bιολογία γενικής παιδείας Α1. 1. δ 2. α 3. β 4. δ ΘΕΜΑ Α Α2. ΟΛΑ ΚΑΠΟΙΑ Τοξίνες + Πλασματική μεμβράνη + Κυτταρικό τοίχωμα + Αποικίες + Κάψα + Πλασμίδια + Μαστίγια + Ριβοσώματα + Πυρηνοειδές + Ενδοσπόρια
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ. Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΟΥ ΚΛΙΜΑΤΟΣ ΑΣΦΑΛΕΙΑΣ ΤΩΝ ΑΣΘΕΝΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΟ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΟΥ ΚΛΙΜΑΤΟΣ ΑΣΦΑΛΕΙΑΣ ΤΩΝ ΑΣΘΕΝΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΟ ΑΝΔΡΕΑΣ ΛΕΩΝΙΔΟΥ Λεμεσός, 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ Πτυχιακή εργασία ΔΙΕΡΕΥΝΗΣΗ ΤΟΥ ΚΛΙΜΑΤΟΣ ΑΣΦΑΛΕΙΑΣ ΤΩΝ ΑΣΘΕΝΩΝ ΣΤΟ ΝΟΣΟΚΟΜΕΙΟ ΑΝΔΡΕΑΣ ΛΕΩΝΙΔΟΥ Λεμεσός, 2012 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ
Χρόνια φλεγμονή. Βαλεντίνη Τζιούφα-Ασημακοπούλου. Νοέμβριος 2018
 Χρόνια φλεγμονή Βαλεντίνη Τζιούφα-Ασημακοπούλου Νοέμβριος 2018 Οξεία φλεγμονή Ταχεία εισβολή και λύση Εξιδρωματικά στοιχεία Πολυμορφοπύρηνα Χρόνια φλεγμονή Ύπουλη εισβολήπαρατεταμένη πορείαβραδεία λύση
Χρόνια φλεγμονή Βαλεντίνη Τζιούφα-Ασημακοπούλου Νοέμβριος 2018 Οξεία φλεγμονή Ταχεία εισβολή και λύση Εξιδρωματικά στοιχεία Πολυμορφοπύρηνα Χρόνια φλεγμονή Ύπουλη εισβολήπαρατεταμένη πορείαβραδεία λύση
Πεπτικός σωλήνας Κύρια λειτουργία του είναι η εξασφάλιση του διαρκούς ανεφοδιασμού του οργανισμού με νερό, ηλεκτρολύτες και θρεπτικά συστατικά.
 Πεπτικός σωλήνας Κύρια λειτουργία του είναι η εξασφάλιση του διαρκούς ανεφοδιασμού του οργανισμού με νερό, ηλεκτρολύτες και θρεπτικά συστατικά. Στον πεπτικό σωλήνα πραγματοποιείται ο τεμαχισμός της τροφής
Πεπτικός σωλήνας Κύρια λειτουργία του είναι η εξασφάλιση του διαρκούς ανεφοδιασμού του οργανισμού με νερό, ηλεκτρολύτες και θρεπτικά συστατικά. Στον πεπτικό σωλήνα πραγματοποιείται ο τεμαχισμός της τροφής
Η θέση ύπνου του βρέφους και η σχέση της με το Σύνδρομο του αιφνίδιου βρεφικού θανάτου. ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ
 ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Η θέση ύπνου του βρέφους και η σχέση της με το Σύνδρομο του αιφνίδιου βρεφικού θανάτου. Χρυσάνθη Στυλιανού Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ
ΤΕΧΝΟΛΟΓΙΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΚΥΠΡΟΥ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Η θέση ύπνου του βρέφους και η σχέση της με το Σύνδρομο του αιφνίδιου βρεφικού θανάτου. Χρυσάνθη Στυλιανού Λεμεσός 2014 ΤΕΧΝΟΛΟΓΙΚΟ
Δομή και λειτουργία προκαρυωτικού κυττάρου
 Δομή και λειτουργία προκαρυωτικού κυττάρου Ιωσήφ Παπαπαρασκευάς Βιοπαθολόγος, Επ. Καθηγητής ΕΚΠΑ Εργαστήριο Μικροβιολογίας, Ιατρική Σχολή ipapapar@med.uoa.gr Γιατί πρέπει να γνωρίζουμε την δομή και τη
Δομή και λειτουργία προκαρυωτικού κυττάρου Ιωσήφ Παπαπαρασκευάς Βιοπαθολόγος, Επ. Καθηγητής ΕΚΠΑ Εργαστήριο Μικροβιολογίας, Ιατρική Σχολή ipapapar@med.uoa.gr Γιατί πρέπει να γνωρίζουμε την δομή και τη
Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki M.
 10th Panhellenic Conference of Alzheimer's Disease and Related Disorders (PICAD) and 2nd Mediterranean Conference of Neurodegenerative Diseases (MeCOND) Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki
10th Panhellenic Conference of Alzheimer's Disease and Related Disorders (PICAD) and 2nd Mediterranean Conference of Neurodegenerative Diseases (MeCOND) Malamidou A., Pantazaki A.A. *, Koliakos G., Tsolaki
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ»
 «ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
«ΠΡΩΤΕΪΝΕΣ: ΧΗΜΙΚΗ ΔΟΜΗ ΚΑΙ ΒΙΟΛΟΓΙΚΟΣ ΡΟΛΟΣ» Τι είναι οι πρωτεΐνες; Από τι αποτελούνται; Ποιος είναι ο βιολογικός του ρόλος; Ας ρίξουμε μία ματιά σε όλα αυτά τα ερωτήματα που μας απασχολούν ΚΕΦΑΛΑΙΟ 1:
