Ραδιοεπισημασμένα Ανάλογα Σωματοστατίνης με Διευρυμένο Φάσμα Κλινικών Ενδείξεων στην Διαγνωστική Ογκολογία-Ραδιοσημασμένες Πανσωματοστατίνες
|
|
|
- Ἄδραστος Κουβέλης
- 9 χρόνια πριν
- Προβολές:
Transcript
1 Εργαστήριο Φαρμακογνωσίας & Χημείας Φυσικών Προϊόντων Τμήμα Φαρμακευτικής Πανεπιστήμιο Πατρών ΔΙΑΤΜΗΜΑΤΙΚΟ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΙΑΤΡΙΚΗ ΧΗΜΕΙΑ: Σχεδιασμός και Ανάπτυξη Φαρμακευτικών Προϊόντων Ραδιοεπισημασμένα Ανάλογα Σωματοστατίνης με Διευρυμένο Φάσμα Κλινικών Ενδείξεων στην Διαγνωστική Ογκολογία-Ραδιοσημασμένες Πανσωματοστατίνες ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΑΙΚΑΤΕΡΙΝΗ ΤΑΤΣΗ ΧΗΜΙΚΟΣ, ΔΙΠΛΩΜΑΤΟΥΧΟΣ Μ.Δ.Ε Πάτρα, 2012
2
3 Laboratory of Pharmacognosy & Chemistry of atural Products Department of Pharmacy University of Patras ITERDEPARTMETAL PRGRAM F PSTGRADUATE STUDIES MEDICIAL CEMISTRY: Design and Development of Pharmaceutical products Radiolabeled Somatostatin Analogs with Expanded Clinical Indications in Diagnostic ncology Radiolabeled Pansomatostatins Phd TESIS AIKATERII TATSI M.Sc. CEMIST Patras, 2012
4
5 ΤΡΙΜΕΛΗΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗ ΕΠΙΤΡΟΠΗ 1. Καθηγητής Παύλος Κορδοπάτης (Επιβλέπων - Τμήμα Φαρμακευτικής, Πανεπιστήμιο Πατρών) 2. Διευθυντής Ερευνών Berthold ock (Μέλος Τριμελούς Συμβουλευτικής Επιτροπής - Ε.Κ.Ε.Φ.Ε. Δημόκριτος ) 3. Καθηγήτρια Marion de Jong (Μέλος Τριμελούς Συμβουλευτικής Επιτροπής - Erasmus MC Rotterdam) TREE MEMBER ADVISRY CMMITTEE 1. Professor Paul Cordopatis (Supervisor Department of Pharmacy, University of Patras) 2. Director of Research Berthold ock (Member of Advisory Committee.C.S.R.. Demokritos ) 3. Professor Marion de Jong (Member of Advisory Committee - Erasmus MC Rotterdam)
6
7 ΕΠΤΑΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ 1. Καθηγητής Παύλος Κορδοπάτης (Επιβλέπων - Τμήμα Φαρμακευτικής, Πανεπιστήμιο Πατρών) 2. Διευθυντής Ερευνών Berthold ock (Μέλος Τριμελούς Συμβουλευτικής Επιτροπής - Ε.Κ.Ε.Φ.Ε. Δημόκριτος ) 3. Καθηγήτρια Marion de Jong (Μέλος Τριμελούς Συμβουλευτικής Επιτροπής- Erasmus MC Rotterdam) 4. Καθηγητής Παύλος Βασιλάκος (Μέλος Επταμελούς Επιτροπής - Τμήμα Ιατρικής Πανεπιστημίου Πατρών) 5. Επίκουρη Καθηγήτρια Βασιλική Μαγκαφά (Μέλος Επταμελούς Επιτροπής - Τμήμα Φαρμακευτικής, Πανεπιστήμιο Πατρών) 6. Επίκουρη Καθηγήτρια Φωτεινή Λάμαρη (Μέλος Επταμελούς Επιτροπής - Τμήμα Φαρμακευτικής, Πανεπιστήμιο Πατρών) 7. Διευθύντρια Ερευνών Θεοδοσία Μάινα-ock (Μέλος Επταμελούς Επιτροπής - Ε.Κ.Ε.Φ.Ε. Δημόκριτος )
8
9 Στην Οικογένειά μου
10
11 ΠΡΟΛΟΓΟΣ Η παρούσα Διδακτορική Διατριβή εκπονήθηκε στο Εργαστήριο Φαρμακογνωσίας και Χημείας Φυσικών Προϊόντων, στο Τμήμα Φαρμακευτικής του Πανεπιστημίου Πατρών και στο Εργαστήριο Μοριακής Ραδιοφαρμακευτικής του Ινστιτούτου Ραδιοϊσοτόπων & Ραδιοδιαγνωστικών Προϊόντων του ΕΚΕΦΕ «Δημόκριτος» στο πλαίσιο του Διατμηματικού Μεταπτυχιακού Προγράμματος Ιατρική Χημεία, "Σύνθεση και Ανάπτυξη Φαρμακευτικών Προϊόντων". Θερμές ευχαριστίες θα ήθελα να απευθύνω στον Επιβλέποντα Καθηγητή Παύλο Κορδοπάτη για τη συμβολή του στην υλοποίηση της Διατριβής από την ανάθεση του θέματος μέχρι και την ολοκλήρωσή της. Τον ευχαριστώ θερμά για την καθοδήγηση, την ενθάρρυνση, την καθοριστική βοήθειά του στην αντιμετώπιση προβλημάτων κατά την σύνθεση των πεπτιδικών αναλόγων και τα εφόδια που μου προσέφερε. Ένα μεγάλο ευχαριστώ οφείλω στον Διευθυντή Ερευνών Berthold ock (Μέλος Τριμελούς Συμβουλευτικής Επιτροπής - ΕΚΕΦΕ «Δημόκριτος») για την καθοριστική συμβολή του στη διαμόρφωση και υλοποίηση του θέματος και για το χρόνο που μου αφιέρωνε για να μου προσφέρει τις γνώσεις και τις συμβουλές του. Ευχαριστώ θερμά τη Διευθύντρια Ερευνών Θεοδοσία Μάϊνα-ock για τη συμβολή της στη διαμόρφωση και υλοποίηση του θέματος, την πολύτιμη καθοδήγησή της, το συνεχές ενδιαφέρον για την πρόοδο μου, την καθοριστική συμβολή της κατά τη συγγραφή της Διδακτορικής Διατριβής και για τις αμέτρητες ώρες εποικοδομητικής έρευνας που περάσαμε στο εργαστήριο. Θερμότατα ευχαριστώ την Καθηγήτρια Marion de Jong (Μέλος Τριμελούς Συμβουλευτικής Επιτροπής- Erasmus MC Rotterdam) για την καθοδήγησή, τις συμβουλές, την οικονομική υποστήριξη και τη φιλοξενία της κατά τη διάρκεια του Molecular Medicine Postgraduate School στο Erasmus MC στο Rotterdam. Ευχαριστώ θερμά τον Καθηγητή Παύλο Βασιλάκο για τη συμβολή του κατά τη συγγραφή της Διδακτορικής Διατριβής. Θα ήθελα να ευχαριστήσω θερμά την Επίκουρη Καθηγήτρια Βασιλική Μαγκαφά για την καθοδήγησή και τις συμβουλές της στην πεπτιδική σύνθεση. Επίσης θα ήθελα να ευχαριστήσω θερμά την Επίκουρη Καθηγήτρια Φωτεινή Λάμαρη για την συμπαράστασή, την καθοδήγησή και τις συμβουλές της κατά τη διάρκεια της Διδακτορικής Διατριβής.
12 Θα ήθελα να ευχαριστήσω θερμά τον Καθηγητή Jean-Claude Reubi και την ομάδα του (Ινστιτούτο Παθολογίας, Πανεπιστημίου Βέρνης) για τη συνεργασία του και τη διεξαγωγή των πειραμάτων ανταγωνιστικής δέσμευσης με αυτοραδιογραφία υποδοχέων και επαγωγής εσωτερίκευσης των sst 1-5 με μικροσκοπία ανοσοφθορισμού. Ευχαριστώ τους φίλους/συναδέλφους στο Εργαστήριο Φαρμακογνωσίας και Χημείας Φυσικών Προϊόντων και στο Εργαστήριο Μοριακής Ραδιοφαρμακευτικής για τη συμπαράσταση και τη βοήθεια που μου προσέφεραν. Για το λόγο αυτό θα ήθελα ιδιαιτέρως να ευχαριστήσω τον Δρ. Αθανάσιο Γαλάνη, την Δρ. Αικατερίνη Ζώμπρα, τον Δρ. Χρίστο Πέτρου, την Δρ. Δήμητρα Χρυσάνθη, τον M.Sc. Δαυίδ Χαραλαμπίδη, τον M.Sc. Παντελή Μαρσουβανίδη και την M.Sc. Αικατερίνη Καλούδη, οι οποίοι με βοήθησαν ο καθένας με το δικό του τρόπο καθ όλη τη διάρκεια της Διδακτορικής Διατριβής. Επίσης, ευχαριστώ πολύ τον Δρ. Γεώργιο Δεράο και την Δρ. Δέσποινα Λαιμού για τη βοήθεια τους στη λήψη φασμάτων μάζας. Τέλος, ένα μεγάλο ευχαριστώ οφείλω στην οικογένειά μου που με στήριζε και με εμψύχωνε σε όλη τη διάρκεια της Διδακτορικής Διατριβής.
13 ΠΕΡΙΕΧΟΜΕΝΑ Α. ΕΙΣΑΓΩΓΗ 1 Α.1 ΣΤΟΧΕΥΜΕΝΗ ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ 1 Α.1.1 ΡΑΔΙΟΦΑΡΜΑΚΑ ΣΤΗ ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ 1 Α.1.2 ΣΥΓΧΡΟΝΑ ΡΑΔΙΟΦΑΡΜΑΚΑ-ΜΟΡΙΑΚΗ ΣΤΟΧΕΥΣΗ 5 Α.1.3 ΡΑΔΙΟΠΕΠΤΙΔΙΑ 16 Α ΤΜΗΜΑ ΑΝΑΓΝΩΡΙΣΗΣ ΥΠΟΔΟΧΕΑ-ΠΕΠΤΙΔΙΟ 17 Α ΡΑΔΙΟΜΕΤΑΛΛΟ 24 Α ΧΗΜΙΚΟΣ ΥΠΟΚΑΤΑΣΤΑΤΗΣ 27 Α ΣΥΝΔΕΤΗΣ 32 Α.2 ΣΥΝΘΕΣΗ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ 34 Α.2.1 ΕΙΣΑΓΩΓΗ 34 Α.2.2 ΠΕΠΤΙΔΙΚΟΣ ΔΕΣΜΟΣ 35 Α.2.3 ΜΕΘΟΔΟΙ ΣΥΖΕΥΞΗΣ ΑΜΙΝΟΞΕΩΝ 35 A ΜΕΘΟΔΟΣ ΑΖΙΔΙΩΝ 35 A ΜΕΘΟΔΟΣ ΑΝΥΔΡΙΤΩΝ 36 A ΜΕΘΟΔΟΣ ΕΝΕΡΓΩΝ ΕΣΤΕΡΩΝ 36 A ΜΕΘΟΔΟΣ ΚΑΡΒΟΔΙΙΜΙΔΙΩΝ 37 A ΦΩΣΦΟΝΙΚΑ ΚΑΙ ΟΥΡΟΝΙΚΑ ΠΑΡΑΓΩΓΑ 38 Α.2.4 ΡΑΚΕΜΙΩΣΗ 39 Α.2.5 ΠΡΟΣΤΑΤΕΥΤΙΚΕΣ ΟΜΑΔΕΣ 40 Α ΠΡΟΣΤΑΣΙΑ ΤΗΣ α-αμινομαδασ 41 Α ΠΡΟΣΤΑΣΙΑ ΚΑΡΒΟΞΥΛΟΜΑΔΑΣ 41 Α ΠΡΟΣΤΑΣΙΑ ΠΛΕΥΡΙΚΩΝ ΟΜΑΔΩΝ 42 Α.2.6 ΣΥΝΘΕΣΗ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ ΣΕ ΣΤΕΡΕΗ ΦΑΣΗ 45 Α ΤΟ ΣΤΕΡΕΟ ΥΠΟΣΤΡΩΜΑ 47 Α ΣΥΖΕΥΞΗ ΑΜΙΝΟΞΕΩΝ ΣΕ ΣΤΕΡΗ ΦΑΣΗ ΕΠΙΜΗΚΥΝΣΗ ΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ 48 Α ΑΠΟΜΑΚΡΥΝΣΗ ΠΕΠΤΙΔΙΚΟΥ ΑΝΑΛΟΓΟΥ ΑΠΟ ΤΗ ΡΗΤΙΝΗ ΚΑΙ ΤΙΣ ΠΛΑΓΙΕΣ ΠΡΟΣΤΑΤΕΥΤΙΚΕΣ ΟΜΑΔΕΣ 49 Α ΣΧΗΜΑΤΙΣΜΟΣ ΔΙΣΟΥΛΦΙΔΙΚΟΥ ΔΕΣΜΟΥ 49 Α ΚΑΘΑΡΙΣΜΟΣ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ 50 Α.3 ΣΩΜΑΤΟΣΤΑΤΙΝΗ 52 Α.3.1 ΣΩΜΑΤΟΣΤΑΤΙΝΗ 52 Α.3.2 ΑΝΑΛΟΓΑ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ 56 Α.3.3 ΡΑΔΙΟΕΠΙΣΗΜΑΣΜΕΝΑ AΝΑΛΟΓΑ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ 60 Β. ΣΚΟΠΟΣ ΣΧΕΔΙΑΣΜΟΣ 69 Β.1 ΣΚΟΠΟΣ ΤΗΣ ΔΙΑΤΡΙΒΗΣ 69 Β.2 ΣΧΕΔΙΑΣΜΟΣ ΑΝΑΛΟΓΩΝ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ 73
14 Γ. ΠΕΙΡΑΜΑΤΙΚΟ ΜΕΡΟΣ 83 Γ.1 ΠΕΙΡΑΜΑΤΙΚΑ ΔΕΔΟΜΕΝΑ ΠΕΠΤΙΔΙΚΗΣ ΣΥΝΘΕΣΗΣ 83 Γ.1.1 ΣΥΣΚΕΥΕΣ/ΟΡΓΑΝΑ-ΥΛΙΚΑ 83 Γ.1.2 ΓΕΝΙΚΗ ΠΟΡΕΙΑ ΤΗΣ ΣΥΝΘΕΣΗΣ ΠΕΠΤΙΔΙΩΝ 85 Γ.1.3 ΣΥΝΘΕΣΗ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ 91 Γ. 2 ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΡΑΔΙΟΧΗΜΙΚΟΣ ΕΛΕΓΧΟΣ 110 Γ.2.1 ΣΥΣΚΕΥΕΣ/ΟΡΓΑΝΑ-ΥΛΙΚΑ 110 Γ.2.2 ΕΠΙΣΗΜΑΝΣΗ ΜΕ 111 In 111 Γ.2.3 ΠΡΟΕΤΟΙΜΑΣΙΑ ΤΟΥ ΕΠΙΣΗΜΑΣΜΕΝΟΥ ΑΝΑΛΟΓΟΥ [ 111 Ιn]ΑΤΧΣ 112 Γ.2.4 ΡΑΔΙΟΧΗΜΙΚΟΣ ΕΛΕΓΧΟΣ 112 Γ. 3 ΒΙΟΛΟΓΙΚΗ ΑΞΙΟΛΟΓΗΣΗ 114 Γ.3.1 ΑΥΤΟΡΑΔΙΟΓΡΑΦΙΑ ΥΠΟΔΟΧΕΩΝ 114 Γ.3.2 ΕΠΑΓΩΓΗ ΕΣΩΤΕΡΙΚΕΥΣΗΣ ΤΩΝ SST 1-5 ΜΕ ΜΙΚΡΟΣΚΟΠΙΑ ΑΝΟΣΟΦΘΟΡΙΣΜΟΥ 117 Γ.3.3 ΚΥΤΤΑΡΟΚΑΛΛΙΕΡΓΕΙΕΣ 119 Γ ΚΑΛΛΙΕΡΓΕΙΑ ΚΥΤΤΑΡΙΚΩΝ ΣΕΙΡΩΝ 120 Γ ΑΠΟΘΗΚΕΥΣΗ ΚΥΤΤΑΡΩΝ 122 Γ ΜΕΤΡΗΣΗ ΑΡΙΘΜΟΥ ΚΥΤΤΑΡΩΝ 123 Γ.3.4 ΕΣΩΤΕΡΙΚΕΥΣΗ ΤΩΝ [ 111 Ιn]ΑΤΧΣ 123 Γ.3.5 ΜΕΤΑΒΟΛΙΣΜΟΣ ΤΩΝ 111 Ιn]ΑΤΧΣ ΣΕ ΥΓΙΗ ΠΟΝΤΙΚΙΑ 126 Γ.3.6 ΒΙΟΚΑΤΑΝΟΜΗ ΤΩΝ 111 Ιn]ΑΤΧΣ 128 Γ ΒΙΟΚΑΤΑΝΟΜΗ ΣΕ ΥΓΙΗ ΠΟΝΤΙΚΙΑ 129 Γ ΒΙΟΚΑΤΑΝΟΜΗ ΣΕ ΠΟΝΤΙΚΙΑ SCID 132 Δ. ΑΠΟΤΕΛΕΣΜΑΤΑ-ΣΥΖΗΤΗΣΗ 137 Δ.1 ΑΠΟΤΕΛΕΣΜΑΤΑ ΠΕΠΤΙΔΙΚΗΣ ΣΥΝΘΕΣΗΣ 137 Δ.1.1 ΠΕΠΤΙΔΙΚΗ ΣΥΝΘΕΣΗ 137 Δ.1.2 ΣΥΖΗΤΗΣΗ ΕΠΙ ΤΩΝ ΑΠΟΤΕΛΕΣΜΑΤΩΝ ΤΗΣ ΠΕΠΤΙΔΙΚΗΣ ΣΥΝΘΕΣΗΣ 153 Δ.2. ΕΠΙΣΗΜΑΝΣΗ - ΡΑΔΙΟΧΗΜΙΚΟΣ ΕΛΕΓΧΟΣ 156 Δ.3. ΑΠΟΤΕΛΕΣΜΑΤΑ ΒΙΟΛΟΓΙΚΗΣ ΑΞΙΟΛΟΓΗΣΗΣ 161 Δ.3.1 ΣΥΓΓΕΝΕΙΑ ΔΕΣΜΕΥΣΗΣ ΣΤΟΥΣ SST Δ.3.2 ΕΠΑΓΩΓΗ ΕΣΩΤΕΡΙΚΕΥΣΗΣ ΤΩΝ SST Δ.3.3 ΕΣΩΤΕΡΙΚΕΥΣΗ ΤΩΝ [ 111 In]ΑΤΧΣ 175 Δ.3.4 ΜΕΤΑΒΟΛΙΚΗ ΣΤΑΘΕΡΟΤΗΤΑ ΤΩΝ [ 111 In]ΑΤΧΣ 181 Δ.3.5 ΒΙΟΚΑΤΑΝΟΜΗ ΤΩΝ [ 111 In]ΑΤΧΣ ΣΕ ΠΡΟΤΥΠΑ ΠΕΙΡΑΜΑΤΟΖΩΩΝ 189 Δ ΥΓΙΗ ΠΟΝΤΙΚΙΑ 190 Δ ΠΕΙΡΑΜΑΤΙΚΟΙ ΟΓΚΟΙ ΣΕ ΠΟΝΤΙΚΙΑ SCID 195 Ε. ΣΥΜΠΕΡΑΣΜΑΤΑ 209
15 ΠΕΡΙΛΗΨΗ 215 SYPSIS 219 ΒΙΒΛΙΟΓΡΑΦΙΑ 223 ΒΙΟΓΡΑΦΙΚΟ ΣΗΜΕΙΩΜΑ 247
16
17 Συντμήσεις-Γλωσσάριο Οι συντμήσεις που χρησιμοποιούνται στην παρούσα διατριβή έχουν προταθεί από την Διεθνή Ένωση Καθαρής και Εφαρμοσμένης Χημείας (IUPAC) και την Διεθνή Ένωση Βιοχημείας (IUB) [IUPAC-IUB Joint Commission on Biochemical omenclature (JCB), omenclature and Symbolism for Amino Acids and Peptides, Recommendations, Eur. J. Biochem. 138 (1984) 9 and J. Biol. Chem., 264 (1989) 663. Τα αμινοξέα τα οποία αναγράφονται στο κείμενο, είναι L- στερεοχημικής διάταξης, εκτός αν χαρακτηρίζονται διαφορετικά. Σύντμηση 2-Cl-Trt AA Acm Ac Ala Arg Asn Asp Boc Bu CCl 4 Cys C 3 C DCM DIC DMF DMS DTA DTA-tris(tBu)ester Πλήρης ονομασία 2-χλωροτριτυλοχλωρίδιο ρητίνη Αμινοξύ Ακεταμιδο-μεθυλ-ομάδα Οξικό οξύ Αλανίνη Αργινίνη Ασπαραγίνη Ασπαραγινικό οξύ Τριτοταγής βουτυλοξυκαρβονυλομάδα Βουτανόλη Τετραχλωράνθρακας Κυστεΐνη Ακετονιτρίλιο Διχλωρομεθάνιο Ν,Ν -διϊσοπροπυλοκαρβοδιιμίδιο Διμεθυλοφορμαμίδιο Διμεθυλοσουλφοξείδιο 1,4,7,10-τετρααζακυκλοδωδεκαν- 1,4,7,10-τετραοξικό οξύ 2-(4,7,10-τρις(2-τερτ-βουτοξυ-2- οξοαιθυλ)-1,4,7,10-τετρααζακυκλο-1- δωδεκαν)οξικό οξύ
18 Σύντμηση DTB EDT Et 2 Et Fmoc Fmoc--PEG 1 -C 2 C/ Fmoc-AEA Πλήρης ονομασία 5,5 -διθειοδις(2-νιτροβενζοϊκό οξύ) 1,2-αιθανοδιθειόλη Διαιθυλεθέρας Αιθανόλη 9-φλουορενυλο-μεθοξυκαρβονυλομάδα Fmoc-5-αμινο-3-οξαπεντανοϊκό οξύ Fmoc--PEG 2 -C 2 C/ Fmoc-AEEA GΗ Gln Glu Gly is Bt I 2 IC 50 (Inhibitory Concentration 50%) Ile ipr Leu Lys Me Met le Pbf Fmoc-8-αμινο-3,6-διοξαοκτανοϊκό οξύ Αυξητική ορμόνη Γλουταμίνη Γλουταμινικό οξύ Γλυκίνη Ιστιδίνη 1-υδροξυβενζοτριαζόλιο Ιώδιο Η συγκέντρωση του προσδέτη η οποία αναστέλλει το 50% της ειδικής δέσμευσης του ραδιοπροσδέτη Ισολευκίνη Ισοπροπανόλη Λευκίνη Λυσίνη Μεθανόλη Μεθειονίνη Νορλευκίνη 2,2,4,6,7-πενταμεθυλοδιυδροβενζοφουρανο-5 σουλφονυλομάδα
19 Σύντμηση PEG Phe Pro RP-PLC Ser SPPS SS sst tbu ΤΕS TFA TFE Thr TIS TLC Trt Tyr Val Πλήρης ονομασία Πολυαιθυλενογλυκόλη Φαινυλαλανίνη Προλίνη Υγρή χρωματογραφία υψηλής απόδοσης ανάστροφης φάσης Σερίνη Σύνθεση πεπτιδίων σε στερεή φάση Σωματοστατίνη, Somatotropin Releasing Inhibiting Factor Υπότυπος του υποδοχέα της σωματοστατίνης Τριτοταγής βουτυλομάδα Τριαιθυλσιλάνιο Τριφθοροξικό οξύ Τριφθοροαιθανόλη Θρεονίνη Τριϊσοπροπυλοσιλάνιο Χρωματογραφία λεπτής στιβάδας τριτυλομάδα Τυροσίνη Βαλίνη
20
21 Α. Εισαγωγή
22
23 Α.1 Εισαγωγή Α.1 ΣΤΟΧΕΥΜΕΝΗ ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ Α.1.1 ΡΑΔΙΟΦΑΡΜΑΚΑ ΣΤΗ ΔΙΑΓΝΩΣΗ ΚΑΙ ΘΕΡΑΠΕΙΑ Τα ραδιοφάρμακα (radiopharmaceuticals) είναι ενώσεις που περιέχουν ένα ραδιονουκλίδιο και χρησιμοποιούνται στην πυρηνική ιατρική. Η χορήγηση των ραδιοφαρμάκων στον άνθρωπο γίνεται κυρίως ενδοφλέβια, αλλά μπορεί να γίνει και από το στόμα ή με εισπνοή. Σχήμα Α. 1: Ενδοφλέβια χορήγηση του ραδιοφαρμάκου στον άνθρωπο και εντόπιση του στις παθολογικές εστίες Τα διαγνωστικά ραδιοφάρμακα μετά τη χορήγηση και εντόπιση τους στην παθολογική εστία (Σχήμα Α. 1) εκπέμπουν ακτινοβολία η οποία διαπερνά το σώμα του ασθενούς και ανιχνεύεται εξωτερικά από κατάλληλες ανιχνευτικές διατάξεις (SPECT, PET). Στις τεχνικές της πυρηνικής ιατρικής (SPECT, PET) η πηγή ακτινοβολίας βρίσκεται μέσα στο σώμα του ασθενούς, σε αντίθεση με τις τεχνικές ακτίνων-χ (ραδιογραφία και αξονική τομογραφία) όπου η πηγή ακτινοβολίας είναι έξω από το σώμα του ασθενούς. Όταν το διαγνωστικό ραδιοφάρμακο περιέχει ραδιονουκλίδιο το οποίο εκπέμπει ηλεκτρομαγνητική ακτινοβολία (γ ή Χ) τότε χρησιμοποιείται η τεχνική SPECT (Single Photon Emission Computed Tomography) με την οποία ανιχνεύονται τα φωτόνια γ. Η ανίχνευση της ακτινοβολίας γ γίνεται από τη γ-camera, η οποία αποτελείται από τον κατευθυντήρα, τον σπινθηριστικό κρύσταλλο, τον φωτοπολλαπλασιαστή και το υπολογιστικό σύστημα ανάλυσης ηλεκτρονικών δεδομένων. Βάσει της αρχής λειτουργίας της γ-camera αρχικά τα φωτόνια γ προσπίπτουν στον κατευθυντήρα. Ο κατευθυντήρας αποτελείται από πολλές παράλληλες οπές, τις οποίες διαπερνούν μόνο τα φωτόνια που εκπέμπονται παράλληλα ως προς τη διεύθυνση των οπών, ενώ τα φωτόνια που προσπίπτουν με διαφορετική γωνία απορροφώνται από το υλικό των οπών (συνήθως μόλυβδος ή βολφράμιο) [1,2]. Στη συνέχεια η φωτονιακή ακτινοβολία προσκρούει στον σπινθηριστικό κρύσταλλο και διεγείρει το υλικό του προκαλώντας την 1
24 Α.1 Εισαγωγή δημιουργία σπινθηρισμών. Οι σπινθηρισμοί συναντούν την κάθοδο του φωτοπολλαπλασιαστή και παράγονται ηλεκτρόνια. Τα ηλεκτρόνια αυτά ενισχύονται στη διαδρομή τους κατά μήκος του φωτοπολλαπλασιαστή και μετατρέπονται σε ηλεκτρονικό σήμα. Το σύνολο των ηλεκτρικών σημάτων επεξεργάζεται από το υπολογιστικό σύστημα, δίνοντας έτσι την απεικόνιση της μελετώμενης περιοχής του σώματος (Σχήμα Α.2.Α). Η διάταξη της SPECT περιλαμβάνει μία ή περισσότερες κεφαλές γ-camera (ταχύτερη λήψη δεδομένων), οι οποίες μπορεί να περιστρέφονται γύρω από το σώμα του ασθενούς, παρέχοντας τρισδιάστατη τομογραφική απεικόνιση (Σχήμα Α.2.Β). Τα κυριότερα ραδιονουκλίδια με εφαρμογή στην τεχνική SPECT είναι τα 99m Tc, 111 In και 67 Ga (αναλυτικά Α ). Η βέλτιστη περιοχή τιμών ενέργειας της ακτινοβολίας γ για τις οργανολογικές διατάξεις που διαθέτει σήμερα η Πυρηνική Ιατρική είναι kev. Α Β Σχήμα Α. 2: Α. Σχηματική αναπαράσταση της γ-camera και Β. Σύγχρονη διάταξη SPECT με τρεις κεφαλές Όταν το διαγνωστικό ραδιοφάρμακο περιέχει ραδιονουκλίδιο το οποίο εκπέμπει ποζιτρόνια (β + ) τότε χρησιμοποιείται η τεχνική PET (Positron Emission Tomography). Μετά την εκπομπή του, κατά την πορεία του στο βιολογικό υπόστρωμα το ποζιτρόνιο συναντά και αλληλεπιδρά με ένα ηλεκτρόνιο. Προκαλείται εξαΰλωση και παραγωγή ενός ζεύγους φωτονίων γ-ακτινοβολίας με ενέργεια 511 kev, τα οποία κινούνται αντιδιαμετρικά. Το ζεύγος φωτονίων ανιχνεύεται και έτσι έμμεσα προσδιορίζεται το σημείο προέλευσης του ποζιτρονίου (Σχήμα Α.3.Α). Η αρχή λειτουργίας της PET camera είναι ανάλογη με αυτή της SPECT. Η κύρια διαφορά με τη SPECT εντοπίζεται στον τρόπο διαλογής των φωτονίων. Στην PET η επιλογή των φωτονίων βασίζεται στην ταυτόχρονη ανίχνευση των αντιδιαμετρικών φωτονίων (coincidence detection). Για το σκοπό αυτό η διάταξη PET διαθέτει πολλούς ανιχνευτές διατεταγμένους σε δακτύλιο. Για την απεικόνιση επιλέγονται μόνο τα φωτόνια που προσπίπτουν ταυτόχρονα σε δύο ανιχνευτές, οι οποίοι βρίσκονται σε αντιδιαμετρική θέση μεταξύ τους [3]. Τα κυριότερα παραδείγματα ραδιονουκλιδίων με 2
25 Α.1 Εισαγωγή εφαρμογή στην τεχνική PET είναι τα 18 F, 68 Ga, 86 Y, 94m Tc και 64 Cu (αναλυτικά A.1.3.2). Α Β Σχήμα Α. 3: Α. Σχηματική απεικόνιση της απεικονιστικής διάταξης PET Β. Σύγχρονη διάταξη PET Συγκριτικά, η PET είναι πιο ευαίσθητη τεχνική σε σύγκριση με τη SPECT, καθώς η διαλογή των φωτονίων γίνεται με ταυτόχρονη ανίχνευση, ενώ στη SPECT ένα μέρος μόνο των συνολικών φωτονίων γ που εκπέμπονται οδηγούνται μέσω του κατευθυντήρα στο ανιχνευτικό σύστημα. Όμως, η SPECT έχει το πλεονέκτημα να ανιχνεύει συγκεκριμένο εύρος τιμών ενέργειας ακτινοβολίας γ και επομένως να μπορεί να διαχωρίσει τις ενέργειες διαφορετικών ραδιονουκλιδίων. Ως εκτούτου, μπορεί να εφαρμοστεί στη συλλογή διαφορετικών λειτουργικών πληροφοριών με συγχορήγηση πολλαπλών ραδιοϊχνηθετών. Σε αντίθεση, η PET ανιχνεύει σε κάθε περίπτωση φωτόνια γ της ίδιας ενέργειας (511 kev) και δεν έχει αυτή τη δυνατότητα [4]. Οι τεχνικές SPECT και PET παρέχουν σημαντικές πληροφορίες για τη φυσιολογία και παθολογικές αλλιώσεις λειτουργιών ιστών και συστημάτων του οργανισμού. Όμως, δεν παρέχουν ανατομικές πληροφορίες, δηλαδή δεν δίνουν τη δυνατότητα ακριβούς χωροταξικής εντόπισης των παθολογικών εστιών στο σώμα του ασθενούς. Η ανάγκη για μεγαλύτερη ακρίβεια στη διάγνωση οδήγησε στην ανάπτυξη υβριδικών απεικονιστικών διατάξεων, οι οποίες συνδυάζουν μία λειτουργική (SPECT, PET) με μία ανατομική απεικονιστική τεχνική, όπως η αξονική τομογραφία (CT) και η μαγνητική τομογραφία (MRI). Οι υβριδικές διατάξεις SPECT/CT (Σχήμα Α.4.Α) και PET/CT (Σχήμα Α.4.Β) χρησιμοποιούνται ήδη στη διαγνωστική ογκολογία και μάλιστα με ιδιαίτερη επιτυχία καθώς συμβάλλουν στον αποτελεσματικότερο εντοπισμό της καρκινικής εστίας και στο σχεδιασμό και την παρακολούθηση της θεραπείας [5]. Επιπλέον, έχει ήδη αρχίσει η ανάπτυξη συστημάτων SPECT/MRI και PET/MRI [6]. 3
26 Α.1 Εισαγωγή Α Β Σχήμα Α. 4: Α. Διάταξη SPET/CT και Β. Διάταξη PET/CT A B B C C Σχήμα Α. 5: Αριστερά:. Διάγνωση φαιοχρωμοκυττώματος με 99m Tc-MIBG (metaiodobenzyl-guanidine) με τεχνική SPECT (A), CT (B) και SPET/CT (C). Δεξιά: Απεικόνιση με 68 Ga-DTA-TATE ενός άνδρα με παγκρεατικό ΝΕΤ και ηπατικές μεταστάσεις με την τεχνική CT (A), PET (B) και PET/CT (C). [oracio A, et al. Gallium-68 (68Ga); The revival of an old Positron Emission Tomography (PET) agent. The Leading Experience in Chile. Alasbimn Journal 10 (41): July Article AJ Τα θεραπευτικά ραδιοφάρμακα περιέχουν ραδιονουκλίδιο το οποίο εκπέμπει σωματιδιακή ακτινοβολία (α, β - και ηλεκτρόνια Auger) και χρησιμοποιούνται στην ογκολογία λόγω της κυτοτοξικής δράσης της σωματιδιακής ακτινοβολίας. Τα σωματίδια α έχουν χαμηλή διεισδυτική ικανότητα μm, όμως όταν εισέλθουν στο κύτταρο επιφέρουν θραύση μονόκλωνου ή δίκλωνου DA (single or double strand DA damage). Τα ηλεκτρόνια Auger έχουν χαμηλή διεισδυτική ικανότητα 10 nm, επομένως για να προκαλέσουν βλάβη πρέπει να είναι όσο το δυνατόν πιο κοντά στο γενετικό υλικό του κυττάρου. Όταν όμως αυτό επιτευχθεί προκαλούν μεγαλύτερη βλάβη από τα σωματίδια α. 4
27 Α.1 Εισαγωγή Τα σωματίδια β - έχουν διεισδυτική ικανότητα τάξης mm έως cm και μπορούν να προκαλέσουν βλάβη στο κύτταρο χωρίς να βρίσκονται κοντά στον πυρήνα και ταυτόχρονα και σε γειτονικά καρκινικά κύτταρα με το φαινόμενο των διασταυρούμενων πυρών (cross-fire effect). Σχήμα Α. 6: Καταστροφή του DA από τα σωματίδια α, β - και τα ηλεκτρόνια Auger Επομένως, θα πρέπει ανάλογα με το στάδιο και τον τύπο της νεοπλασίας να επιλεγεί και το κατάλληλο θεραπευτικό ραδιονουκλίδιο που ενσωματώνεται στο ραδιοφάρμακο. Έτσι, για μικρομεταστάσεις επιλέγονται ραδιονουκλίδια με μικρή διεισδυτική ικανότητα ( 111 In, Auger e - ), για μεσαίου μεγέθους μεταστάσεις ραδιονουκλίδια μέσης ενέργειας όπως το 177 Lu (β - emitter), ενώ για μεγαλύτερες μεταστάσεις με νεκρωτικές περιοχές επιλέγονται ραδιονουκλίδια με υψηλή ενέργεια και με μεγάλη διεισδυτική ικανότητα ακτινοβολίας όπως το 90 Y (β - emitter), ώστε να ακτινοβολείται όλη η μάζα του όγκου. Για την αποτελεσματικότερη αντιμετώπιση ταυτόχρονα μικρών και μεγαλύτερων μεταστατικών εστιών έχει προταθεί συνδυασμός (cocktail) ραδιονουκλιδίων χαμηλής, μεσαίας και υψηλής ενέργειας. Αντιπροσωπευτικά ραδιονουκλίδια που έχουν προταθεί για την ανάπτυξη θεραπευτικών ραδιοφαρμάκων είναι το 111 In (Auger e - ), το 213 Bi (αemitter), και τα 90 Υ, 177 Lu (β - emitters) (αναλυτικά Α.1.3.2). Α.1.2 ΣΥΓΧΡΟΝΑ ΡΑΔΙΟΦΑΡΜΑΚΑ-ΜΟΡΙΑΚΗ ΣΤΟΧΕΥΣΗ Η στοχευμένη διάγνωση και θεραπεία επιτυγχάνεται με επιλεκτική αλληλεπίδραση σύγχρονων ραδιοφαρμάκων με βιομόρια-στόχους του βιολογικού υποστρώματος. Στα τέλη του 19ου αιώνα ο Paul Ehrlich διατύπωσε την αρχή της «μαγικής σφαίρας» που αφορούσε στην ανάγκη ανάπτυξης φαρμάκων μοριακής στόχευσης [7]. Το πρώτο ραδιοφάρμακο για στοχευμένη διάγνωση και θεραπεία παθήσεων του θυρεοειδούς (που ανταποκρίνονται στο ιώδιο) είναι το 131 I-aI, το οποίο στοχεύει και δεσμεύεται επιλεκτικά στο μεταφορέα του ιωδίου (I-symporter). Το 131 I-aI χορηγήθηκε για πρώτη 5
28 Α.1 Εισαγωγή φορά το 1941 σε ασθενείς με υπερθυρεοειδισμό και μέχρι και σήμερα θεωρείται το κύριο ραδιοφάρμακο για τη στοχευμένη διάγνωση και θεραπεία υπερθυρεοειδισμού και του καρκίνου του θυρεοειδούς [8]. Επιπλέον, το 99m - Tc 4 είναι από τα πρώτα ραδιοφάρμακα του Tc που χρησιμοποιήθηκε για τη στοχευμένη διάγνωση παθήσεων του θυρεοειδούς και στοχεύει επιλεκτικά και αυτό τον μεταφορέα του ιωδίου (Isymporter) [9]. Αξίζει να σημειωθεί ότι η εφαρμογή αυτή προέκυψε τυχαία και χωρίς γνώση του υποστρώματος και κατάλληλο σχεδιασμό του ραδιοφαρμάκου. Η αρχή της «μαγικής σφαίρας» εφαρμόστηκε σε καρκινοπαθείς το 1975 στο Cambridge από τους Kohler και Milstein με τη χορήγηση μονοκλωνικών αντισωμάτων [10]. Τα πρώτα μόρια που χρησιμοποιήθηκαν για την ανάπτυξη ραδιοφαρμάκων μοριακής στόχευσης ήταν μονοκλωνικά αντισώματα (MAbs). Τα ραδιοεπισημασμένα μονοκλωνικά αντισώματα στοχεύουν μοριακά αποτυπώματα στην επιφάνεια των νεοπλασματικών κυττάρων, τα οποία αναγνωρίζουν και δεσμεύονται σε αυτά, δηλαδή ειδικά αντιγόνα που εκφράζονται στον καρκίνο. Tο 1993 εγκρίθηκε για πρώτη φορά από το FDA (Food and Drug Administration) ένα επισημασμένο με 111 In μονοκλωνικό αντίσωμα από ποντίκι για διάγνωση της επανεμφάνισης καρκίνου του παχέος εντέρου και καρκίνου των ωοθηκών (ncoscint ) [11]. Τα ραδιοεπισημασμένα μονοκλωνικά αντισώματα χαρακτηρίζονται από υψηλή συγγένεια δέσμευσης για το αντιγόνο. Παρολ αυτά, τα ραδιοεπισημασμένα μονοκλωνικά αντισώματα έχουν σημαντικά μειονεκτήματα: 1. υψηλή αντιγονικότητα όταν προέχονται από άλλα είδη π.χ. από ποντίκια, οπότε υπάρχει ο κίνδυνος παραγωγής ανθρώπινων αντισωμάτων τύπου antimouse (AMA, uman AntiMouse Antibodies) και αναφυλακτικού σοκ 2. υψηλό κόστος παραγωγής 3. μεγάλο μοριακό βάρος (~ Da) με αποτέλεσμα τη δύσκολη διείσδυση στον καρκινικό ιστό 4. αργή αιματική κάθαρση 5. επίτευξη χαμηλών λόγων όγκου/υποστρώματος και άρα χαμηλή απεικονιστική ευκρίνεια στα αρχικά χρονικά διαστήματα μετά τη χορήγηση, που καθιστά ασύμβατη τη χρήση βραχύβιων ραδιονουκλιδίων 6. ευαίσθητα σε ακραίες συνθήκες επισήμανσης 6
29 Α.1 Εισαγωγή Τα ραδιοεπισημασμένα πεπτίδια γνώρισαν μεγάλη εξέλιξη τα τελευταία 30 χρόνια και συνέβαλαν σημαντικά στην πειραματική και κλινική ογκολογία. Η στοχευμένη απεικονιστική διάγνωση και ραδιονουκλιδική θεραπεία του καρκίνου με διαμεσολάβηση υποδοχέων πεπτιδίων (Peptide Receptor Imaging and Radiotherapy, PRΙ και PRRT) βρίσκει ολοένα μεγαλύτερη εφαρμογή. Βασική προϋπόθεση για την αποτελεσματικότητα της στρατηγικής αυτής είναι η υπερέκφραση υποδοχέων πεπτιδίων στα καρκινικά κύτταρα-στόχους σε αντίθεση με την ελάχιστη ή απουσία έκφρασης στους υγιείς παρακείμενους ιστούς [12]. Τα πλεονεκτήματα των πεπτιδίων είναι: 1. το μικρό μοριακό βάρος 2. η εύκολη σύνθεση και το χαμηλό κόστος παραγωγής 3. η δυνατότητα χημικής τροποποίησης της δομής 4. η εύκολη πρόσδεση ενός υποκαταστάτη για τη συναρμογή του ραδιονουκλιδίου 5. η ανθεκτικότητα σε συνθήκες της ραδιοεπισήμανσης 6. η υψηλή συγγένεια δέσμευσης με τον αντίστοιχο υποδοχέα 7. η ταχύτερη διείσδυση στον καρκινικό ιστό 8. η ικανότητα εσωτερίκευσης (ραδιοπεπτίδια-αγωνιστές) στα κύτταρα-στόχους διαμέσου των αντίστοιχων υποδοχέων (ενίσχυση διαγνωστικού σήματος ή του θεραπευτικού αποτελέσματος) 9. η απουσία πρόκλησης ανοσολογικών αντιδράσεων κατά τη χορήγησή τους 10. η ταχεία αιματική κάθαρση και απομάκρυνση από τους παρακείμενους ιστούς, η οποία οδηγεί σε υψηλούς λόγους όγκου/υποστρώματος σε σύντομο χρονικό διάστημα Λόγω των παραπάνω πλεονεκτημάτων τα ραδιοπεπτίδια μπορούν να χρησιμοποιηθούν με επιτυχία στην απεικονιστική διάγνωση ή ραδιονουκλιδική θεραπεία καρκίνου. Παρόλ αυτά τα ραδιοπεπτίδια εμφανίζουν κάποια μειονεκτήματα: 1. συχνά εμφανίζουν μικρή μεταβολική σταθερότητα 2. η εισαγωγή του ραδιονουκλιδίου στο πεπτίδιο μπορεί να προκαλέσει αλλαγές στις φυσικοχημικές του ιδιότητες και στη διαμόρφωση του και επομένως στην βιοκινητική και την αλληλεπίδρασή του με τον υποδοχέα 7
30 Α.1 Εισαγωγή Βιομόρια-στόχοι Τα βιομόρια-στόχοι των πεπτικών ραδιοφαρμάκων βρίσκονται στη κυτταρική μεμβράνη (υποδοχείς, αντιγόνα). Οι υποδοχείς πεπτιδίων που χρησιμοποιούνται στη ραδιοφαρμακευτική ανήκουν κατά κύριο λόγο στην υπεροικογένεια των συζευγμένων με G πρωτεΐνες υποδοχέων (Gprotein coupled receptors, GPCRs). Οι GPCRs συνιστούν την μεγαλύτερη οικογένεια μεμβρανικών υποδοχέων που εμπλέκονται στη μεταγωγή σήματος (signal transduction) [13,14]. Βασικό γνώρισμα των GPCRs είναι η διαμόρφωση των επτά διαμεμβρανικών α-ελίκων, οι οποίες συνδέονται μεταξύ τους με τρεις εξωκυττάριους και τρεις ενδοκυττάριους βρόγχους [15]. Σε ορισμένους υποδοχείς η διαμόρφωση των βρόγχων σταθεροποιείται με δισουλφιδικούς δεσμούς που σχηματίζονται μεταξύ καταλοίπων κυστεΐνης. Η περιοχή σύνδεσης του υποδοχέα με το πεπτίδιο αντιστοιχεί στο εξωκυτταρικό αμινοτελικό άκρο του υποδοχέα, ενώ η περιοχή αλληλεπίδρασης με την G πρωτεΐνη περιλαμβάνει το ενδοκυτταρικό καρβοξυ-τελικό άκρο, καθώς και τους ενδοκυτταρικούς βρόχους του διαμεμβρανικού τμήματος του υποδοχέα [16,17]. Σχήμα Α. 7: 3D κρυσταλλική δομή της ροδοψίνης Α. παράλληλα και Β. κάθετα στο επίπεδο της κυτταρικής μεμβράνης. [Meng EC, Bourne R. (2001) Receptor activation: what does the rhodopsin structure tell us? Trends Pharmacol Sci. (11): ] Οι GPCRs οφείλουν την ονομασία τους στην αλληλεπίδρασή τους με ετεροτριμερείς G πρωτεΐνες. Οι G πρωτεΐνες αποτελούνται από την α υπομονάδα που παρουσιάζει υψηλή συγγένεια για νουκλεοτίδια της γουανίνης, καθώς και τις β και γ υπομονάδες που συνδέονται στενά μεταξύ τους σχηματίζοντας διμερή. Όταν ο υποδοχέας είναι ανενεργός, η υπομονάδα G α είναι συζευγμένη με ένα μόριο διφωσφορικής γουανοσίνης (GDP). 8
31 Α.1 Εισαγωγή Η πρόσδεση του πεπτιδίου στον υποδοχέα προκαλεί αλλαγές στη διαμόρφωση της G πρωτεΐνης, που οδηγούν στην ανταλλαγή του GDP με GTP και στην απόσπαση της υπομονάδας G βγ. Στη συνέχεια, τόσο το σύμπλεγμα Gα-GTP όσο και το G βγ, διεγείρουν μια σειρά από σηματοδοτικά μόρια (όπως αδενυλική κυκλάση, φωσφολιπάση Α 2, φωσφολιπάση C), τα οποία με τη σειρά τους διεγείρουν ή αναστέλλουν την παραγωγή δεύτερων μηνυμάτων (όπως camp, διακυλογλυκερόλη, 1,3,5-τριφωσφορική ινοσιτόλη), την αύξηση των ενδοκυτταρικών επιπέδων Ca 2+ ή τη διάνοιξη ή κλείσιμο ιοντικών καναλιών (Σχήμα Α.8) [18]. Τα δευτεροταγή μηνύματα στη συνέχεια ενεργοποιούν άλλους ενδοκυττάριους στόχους όπως μικρές πρωτεΐνες-gtp των οικογενειών ras και rho και μέλη των κινασών ΜΑΡΚ (mitogen activated protein kinases), δημιουργώντας πληθώρα σηματοδοτικών δικτύων με τελικό αποδέκτη τον πυρήνα του κυττάρου. Στον πυρήνα του κυττάρου η φωσφορυλίωση μεταγραφικών παραγόντων λαμβάνει μέρος στη ρύθμιση σημαντικών κυτταρικών λειτουργιών, π.χ. κυτταρικός πολλαπλασιασμός, κυτταρικός θάνατος, διαφοροποίηση, υπερτροφία και καρκινογένεση. Σχήμα Α. 8: Πορεία μεταγωγής εξωκυττάριου σήματος διαμέσου των GPCRs (signal transduction) [18] Οι GPCRs εμπλέκονται σε ένα ευρύ φάσμα ανθρώπινων λειτουργιών, όπως η νευροδιαβίβαση, η απελευθέρωση ορμονών και ενζύμων από ενδοκρινείς και εξωκρινείς αδένες, ανοσολογικές αντιδράσεις, ο έλεγχος του καρδιακού ρυθμού και η κυτταρική μετανάστευση. Οι GPCRs διαδραματίζουν επίσης σημαντικό ρόλο στην καρκινογένεση, στον πολλαπλασιασμό και στην εξέλιξη της νόσου (αγγειογένεση, μετάσταση). Τα καρκινικά κύτταρα έχουν την ικανότητα να υπονομεύουν τις φυσιολογικές λειτουργίες των GPCRs 9
32 Α.1 Εισαγωγή με αποτέλεσμα να πολλαπλασιάζονται αυτόνομα ικανοποιώντας τις αυξημένες ανάγκες σε οξυγόνο, να αποφεύγουν την ανίχνευση από το ανοσοποιητικό σύστημα και να εισβάλουν σε παρακείμενους ή μη ιστούς. Έχει παρατηρηθεί ότι υποδοχείς ρυθμιστικών πεπτιδίων υπερεκφράζονται (δηλαδή εκφράζονται σε υψηλότερη πυκνότητα σε σχέση με τους υγιείς ιστούς) σε διάφορους τύπους ανθρώπινων νεοπλασιών [19]. Οι υποδοχείς συνεισφέρουν στη διαδικασία ανάπτυξης του όγκου μέσω ενεργοποίησης τους από αγωνιστές που διεγείρουν τον κυτταρικό πολλαπλασιασμό και απελευθερώνονται είτε από τα ίδια τα καρκινικά κύτταρα (αυτοκρινείς οδοί) είτε από κύτταρα του στρώματος (παρακρινείς οδοί). Πολλές τεχνικές έχουν αναπτυχθεί για τη μελέτη της έκφρασης υποδοχέων πεπτιδορμονών σε φυσιολογικούς και νεοπλασματικούς ιστούς ώστε να γίνει προσδιορισμός και in vivo χαρτογράφηση υποδοχέων πεπτιδορμονών κατάλληλων για μοριακή στόχευση στην κλινική ογκολογία. Μερικές από αυτές τις τεχνικές είναι: α. σε επίπεδο πρωτεΐνης: η αυτοραδιογραφία υποδοχέων (με χρήση ραδιοπροσδετών επιλεκτικών για έναν συγκεκριμένο υποδοχέα) και η ανοσοϊστοχημεία (με αντισώματα έναντι υποδοχέων) και β. σε επίπεδο mra: mra υβριδισμός in situ, η αλυσιδωτή αντίδραση της ανάστροφης μεταγραφάσης (RT-PCR) και η ανάλυση κατά orthern. Η υπερέκφραση των υποδοχέων ρυθμιστικών πεπτιδίων σε καρκινικά κύτταρα τους καθιστά ιδανικούς στόχους για την διαγνωστική απεικόνιση ή ραδιοθεραπεία του καρκίνου. Τα μόρια στόχευσης υποδοχέων πεπτιδορμονών χρησιμοποιούνται σαν φορείς διαγνωστικών ή θεραπευτικών ραδιονουκλιδίων [12] είτε κυτταροτοξικών φαρμάκων [20], καθώς το μόριο στόχευσης αναγνωρίζει και αλληλεπιδρά με τον υποδοχέα που υπερεκφράζεται στον όγκο. Οι κυριότεροι τύποι υποδοχέων που υπερεκφράζονται σε διάφορους τύπους καρκίνου παρουσιάζονται στον πίνακα Α.1. Τα κριτήρια επιλογής βιομορίου-στόχου για επιτυχή εφαρμογή στη στοχευμένη διάγνωση και θεραπεία του καρκίνου είναι: 1. η πυκνότητα έκφρασης του βιομορίου-στόχου στον καρκινικό όγκο 2. η συχνότητα έκφρασης του (σε διαφορετικές περιπτώσεις ασθενών με τον ίδιο καρκίνο) 3. η διατήρηση της έκφρασης τους κατά την εξέλιξη της νόσου 4. η χαμηλή έκφραση σε φυσιολογικούς ιστούς. Στην υπεροικογένεια των GPCRs ιδιαίτερο ενδιαφέρον στην ογκολογία παρουσιάζουν οι υποδοχείς σωματοστατίνης (sst). 10
33 Α.1 Εισαγωγή Πίνακας Α.1: Χαρακτηριστικά παραδείγματα έκφρασης υποδοχέων ενδογενών πεπτιδίων με και η έκφραση τους σε τύπους καρκίνου Πεπτίδιο Υποδοχέας Όγκος που εκφράζει τον υποδοχέα SS14 ή SS28 sst 1-5 ΝΕΤ, λέμφωμα non-odgin, MTC, SCLC, όγκοι του νευρικού συστήματος α-ms α-ms-r Μελάνωμα CCK/γαστρίνη CCK 1-R, CCK 2-R MTC, SCLC, παγκρεατικοί όγκοι, αστροκύτωμα VIP/PACAP VPAC 1-R, VPAC 2-R /PAC 1-R SCLC, καρκίνος παχέος εντέρου, στομάχου, παγκρέατος LR LR-R καρκίνος μαστού, προστάτη T TS 1-R, TS 2-R, TS 3-R Ποροειδές εξωκρινικό καρκίνωμα του παγκρέατος, σάρκωμα Ewing, μενιγγίωμα, αστροκύτωμα, ΒΒΝ BB 1-R (MB-R), BB 2-R (GRP-R), BB 3-R SCLC, καρκίνος προστάτη, καρκίνος μαστού, καρκίνος παχέος εντέρου GRP BB 2-R (GRP-R) SCLC, καρκίνος προστάτη, καρκίνος μαστού, καρκίνος παχέος εντέρου Ουσία P K 1-R γλοιοβλάστωμα, αστροκύτωμα, MTC, καρκίνος μαστού, δια- και περινεοπλαστικά αγγεία SS: σωματοστατίνη, ΝΕΤ: νευροενδοκρινικοί όγκοι, MS: ορμόνη διέγερσης των μελανοκυττάρων, CCK: χολοκυστοκινίνη, VIP: αγγειοδραστικό εντερικό πολυπεπτίδιο, PACAP: υποφυσιακό πεπτίδιο ενεργοποίησης της αδενυλικής κυκλάσης, LR: εκλυτική ορμόνη της ωχρινοτρόπου ορμόνης, T: νευροτενσίνη, ΒΒΝ: μπομπεσίνη, GRP: πεπτίδιο απελευθέρωσης της γαστρίνης, SCLC: μικροκυτταρικός καρκίνος των πνευμόνων, MTC: μυελλοειδές καρκίνωμα του θυροειδούς, R: υποδοχέας (receptor). Υποδοχείς σωματοστατίνης. Οι βιολογικές δράσεις της σωματοστατίνης (SS) και των αναλόγων της εκδηλώνονται μετά από αλληλεπίδραση με υψηλής συγγένειας μεμβρανικούς υποδοχείς (sst). Μέχρι σήμερα έχουν κλωνοποιηθεί και χαρακτηριστεί πέντε υπότυποι του υποδοχέα της σωματοστατίνης, οι sst 1-5. Οι sst κωδικοποιούνται από πέντε μη αλληλικά γονίδια τα οποία βρίσκονται σε πέντε διαφορετικά χρωμοσώματα. Τα γονίδια των sst 1 και sst 3-5 δεν φέρουν ιντρόνια (introns) σε αντίθεση με τα γονίδια του sst 2. Επιπλέον, ο υποδοχέας sst 2 εκφράζεται με δύο διαφορετικές μορφές [23], sst 2A (369 ΑΑ) και sst 2B (156 ΑΑ), οι οποίες διαφέρουν μόνο ως προς το μήκος του κυτταροπλασματικού C-άκρου [24]. Μέχρι σήμερα στον άνθρωπο έχει εντοπιστεί μόνο ο sst 2A ενώ στα τρωκτικά και οι δύο (ο sst 2A κυρίως σε αρουραίους και ο sst 2B κυρίως σε ποντίκια). 11
34 Α.1 Εισαγωγή Σχήμα Α. 9: Σχηματική αναπαράσταση της δομής των ανθρώπινων υποδοχέων hsst 1-5 [37] Το μήκος της αλληλουχίας των sst 1-5 κυμαίνεται από 356 (sst 2 ) έως 418 αμινοξέα (sst 3 ) και οι αλληλουχίες των υποτύπων sst εμφανίζουν σημαντική ομολογία (39-57%). Ιδιαίτερα υψηλή είναι η ομολογία αντίστοιχων υποδοχέων σε διαφορετικά είδη π.χ % ομολογία για τον sst 1 μεταξύ ανθρώπου, αρουραίου και ποντικιού, 93-96% ομολογία για τον sst 2 μεταξύ ανθρώπου, αρουραίου, ποντικού, χοίρου και βοοειδών, 88% ομολογία για τον sst 4 μεταξύ του ανθρώπου και του αρουραίου και 82-83% ομολογία για τους sst 3 και sst 5 μεταξύ του ανθρώπου και των τρωκτικών [24,25]. Η ομολογία μεταξύ των διαμεμβρανικών περιοχών των ανθρώπινων υποτύπων hsst 1-5 κυμαίνεται μεταξύ 55-70%. Η υψηλότερη ομολογία εμφανίζεται μεταξύ των hsst 1 και hsst 4 (70%), ακολουθούμενη από αυτών μεταξύ hsst 3 και hsst 5 (69%) [24,25]. Όλοι οι υπότυποι sst που έχουν κλωνοποιηθεί μέχρι σήμερα, όχι μόνο από τον άνθρωπο αλλά και από άλλα είδη, έχουν μια αυστηρά συντηρημένη ακολουθία, YASCAPI/VLY, στην έβδομη διαμεμβρανική περιοχή, η οποία είναι η υπογραφή αυτής της οικογένειας υποδοχέων. Και οι δύο φυσικές μορφές της σωματοστατίνης SS14 και SS28 παρουσιάζουν υψηλή συγγένεια δέσμευσης και για τους πέντε sst 1-5. Οι υποδοχείς hsst 1-4 παρουσιάζουν μεγαλύτερη συγγένεια δέσμευσης για την SS14 (σε σύγκριση με την SS28) [26,27,28]. Αντίθετα, ο hsst 5 παρουσιάζει μεγαλύτερη συγγένεια δέσμευσης για την SS28 (σε σύγκριση με την SS14) [26,27,29]. Μετά τη δέσμευση της SS ή αναλόγων της στους sst 1-5, ενεργοποιούνται οι G- πρωτεΐνες και ακολουθεί η μεταγωγή σήματος μέσω διαφόρων μονοπατιών. Στη συνέχεια ενεργοποιούνται ένζυμα κλειδιά όπως είναι η αδενυλική κυκλάση, οι φωσφοτυροσινο-φωσφατάσες (ΡΤΡases) και οι ΜΑΡ κινάσες και επέρχονται αλλαγές στα ενδοκυττάρια επίπεδα ιόντων ασβεστίου και καλίου [24,25,30-32]. Η εξέλιξη των 12
35 Α.1 Εισαγωγή ενδοκυττάριων γεγονότων εξαρτάται από τον συγκεκριμένο υπότυπο sst 1-5 και από τον προσδέτη. Επιπλέον συνδέεται με την επαγωγή ή μη της εσωτερίκευσης του υποδοχέα και σε περιπτώσεις συνέκφρασης υποτύπων sst 1-5 στην κυτταρική μεμβράνη από την μεταξύ τους αλληλεπίδραση (receptor cross-talking). Η επαγωγή εσωτερίκευσης των πέντε sst 1-5 μετά την δέσμευση του προσδέτηαγωνιστή διαφέρει [32]. Στην περίπτωση των sst 2, sst 3 και sst 5 παρατηρείται μεγαλύτερη ικανότητα εσωτερίκευσης από τους sst 1 και sst 4 [33,34]. Η έκφραση των υποδοχέων της σωματοστατίνης sst 1-5 έχει διαπιστωθεί σε πολλούς υγιείς και νεοπλασματικούς ιστούς. Στον ανθρώπινο οργανισμό οι hsst εκφράζονται στο ΚΝΣ και σε ιστούς της περιφέρειας, όπως το γαστρεντερικό σύστημα, το πάγκρεας και τα επινεφρίδια. Οι πιο συχνά απαντώμενοι υπότυποι είναι ο hsst 1 και ο hsst 2 [35]. Η έκφραση των hsst 1-5 σε υγιείς ιστούς περιγράφεται στον παρακάτω πίνακα [31,32]. Πίνακας Α.2: Έκφραση των hsst 1-5 σε υγιείς ιστούς σε επίπεδο mra και επίπεδο πρωτεΐνης Όργανο mra Πρωτεΐνη Επινεφρίδια hsst 2 hsst 2 Καρδιά hsst 1,3,4,5 hsst 1,3,4,5 Νήστιδα hsst 1-5 hsst 1-5 Στομάχι hsst 1-5 hsst 1-5 Πνεύμονες hsst 1,2,4 hsst 1,2,4 Νεφροί hsst 1-5 hsst 1-5 Ήπαρ hsst 1-3 hsst 1-3 Πάγκρεας hsst 1-5 hsst 1-5 Σπλήνας hsst 1-5 hsst 1-5 Παρεγκεφαλίδα hsst 1-5 hsst 1-5 Υπόφυση hsst 1,2,3,5 hsst 1,2,3,5 Ιππόκαμπος hsst 1-4 hsst 1-4 Αμυγδαλή hsst 1-5 hsst 1-5 Υποθάλαμος hsst 1-5 hsst 1-5 Επιπλέον, οι sst 1-5 εκφράζονται μόνοι τους ή σε διάφορους συνδυασμούς σε πολλούς ανθρώπινους όγκους και σε μεγαλύτερη πυκνότητα από τους φυσιολογικούς ιστούς 13
36 Α.1 Εισαγωγή (Πίνακας Α.3). Οι sst 1-5 εκφράζονται σε μεγάλο βαθμό στους νευροενδοκρινούς όγκους (ETs), συμπεριλαμβανομένων των γαστροεντεροπαγκρεατικών όγκων (GEP). Ο πιο συχνά απαντώμενος υπότυπος στους νεοπλασματικούς ιστούς είναι ο sst 2 και ακολουθούν οι sst 1,3,5, ενώ ο sst 4 απαντάται σπάνια [35]. Ο sst 2 εκφράζεται στα νευροβλαστώματα, στα μυελοβλαστώματα, καρκινώματα του μαστού, τα μηνιγγιώματα, παραγαγγλιώματα, λεμφώματα, μικροκυτταρικό καρκίνο του πνεύμονα, ηπατώματα και καρκινώματα των νεφρών. Πίνακας Α.3: Υπερέκφραση των sst 1-5 σε ανθρώπινους καρκίνους Τύποι καρκίνου sst 1 sst 2 sst 3 sst 4 sst 5 Νευροβλάστωμα ne hd ne ne ne Μηνιγγίωμα ne hd ne ne ne Μυελοβλάστωμα ne hd ne ne ne Καρκίνος μαστού 1/31 hd 29/31 hd 1/31 md ne ne ne Λέμφωμα ne 7/7 hd ne ne 3/7 ld Καρκίνος νεφρών ne 5/7 hd 2/7 md ne ne ne Παραγαγγλίωμα 2/10 hd 8/10 hd 2/10 ld ne ne Μικροκυτταρικός καρκίνος του πνεύμονα ne 2/2 hd ne ne ne Ηπάτωμα ne 2/2 hd ne ne ne Καρκίνος του προστάτη Σάρκωμα Ανενεργό αδένωμα υπόφυσης 4/6 hd 2/6 md 6/9 hd 2/9 md 1/30 hd ne ne ne 1/6 ld 1/9 md ne 1/9 md ne 8/30 hd 4/30 md 4/30 ld 16/30 hd 1/30 md ne 1/30 md 3/30 ld Αδένωμα με υπερέκκριση G GEP όγκοι Φαιοχρωμοκύττωμα Καρκίνος στομάχου ne 3/22 hd 3/22 md 3/19 hd 2/19 md 2/5 hd 1/5 ld 9/24 hd 12/24 md 1/24 ld 1/22 hd 12/22 md 13/19 2/22 ld hd 2/19 md 2/24 ld ne 2/24 hd 8/24 md (x/y): x=αριθμός περιστατικών που εκφράζεται ο συγκεκριμένος υπότυπος, y=συνολικός αριθμός περιστατικών, hd= υψηλή πυκνότητα, md= μέτρια πυκνότητα, ld= χαμηλή πυκνότητα, ne= απουσία έκφρασης ne ne 3/22 md 1/22 ld ne ne 1/19 ld 1/5 hd ne ne 2/5 hd Επενδύδωμα 1/2 hd ne ne ne 1/2 hd 14
37 Α.1 Εισαγωγή Λίγοι όγκοι με σαφή υπεροχή των sst 1 έχουν εντοπιστεί, όπως είναι τα καρκινώματα του προστάτη και τα σαρκώματα. Ο sst 3 εκφράζεται κυρίως στα ανενεργά υποφυσιακά αδενώματα ενώ ο sst 4 εκφράζεται εξαιρετικά σπάνια και σε μέτρια πυκνότητα στα σαρκώματα [35]. Ο sst 5 εκφράζεται συχνά σε αδενώματα της υπόφυσης και σε μέτρια πυκνότητα σε σαρκώματα, στον καρκίνο του προστάτη, σε GEP-ETs και σε γαστρικά καρκινώματα. Συχνά οι sst 2 και sst 5 και εκφράζονται μαζί σε αδενώματα με υπερέκκριση αυξητικής ορμόνης (G) [35,36]. Επιπλέον, οι sst 1 και sst 2 εκφράζονται σε GEP-ETs και σε μικρότερο βαθμό σε φαιοχρωμοκυττώματα. Έτσι, παρά την επικράτηση της έκφρασης των sst 2 σε πολλούς καρκινικούς όγκους, συνέκφραση των sst 2 με άλλους sst υποτύπους είναι αρκετά συχνή. Επιπλέον σε όγκους που δεν εκφράζεται ο sst 2 είναι δυνατόν να εκφράζεται ένας ή περισσότεροι από τους υπόλοιπους sst. Τα δύο αυτά ευρήματα έχουν κλινική σημασία για την sstστοχευμένη διάγνωση και θεραπεία καρκίνου, για τα οποία έχουν χρησιμοποιηθεί μέχρι τώρα αποκλειστικά πεπτιδικά ανάλογα επιλεκτικά για τον sst 2. Είναι λογικό να υποθέσουμε ότι πεπτίδια με χαρακτηριστικά πανσωματοστατίνης, δηλαδή ανάλογα με υψηλή συγγένεια δέσμευσης σε όλους τους sst 1-5, θα διευρύνουν τις κλινικές ενδείξεις δεδομένου ότι θα εντοπίζονται σε μεγαλύτερο φάσμα ανθρώπινων όγκων. Επιπλέον, η χρήση τους θα ενισχύσει τη διαγνωστική ευαισθησία ή/και θεραπευτική αποτελεσματικότητα σε όγκους που υπάρχει συνέκφραση των sst
38 Α.1 Εισαγωγή Α.1.3 ΡΑΔΙΟΠΕΠΤΙΔΙΑ Τα ραδιοπεπτίδια που προορίζονται για εφαρμογή στην απεικονιστική διάγνωση και ραδιονουκλιδική θεραπεία συνήθως αποτελούνται από τα εξής μέρη: α) Τμήμα αναγνώρισης του υποδοχέα (πεπτίδιο) β) Μεταλλικό ραδιονουκλίδιο το οποίο εκπέμπει το ραδιενεργό σήμα ή κυτοτοξική ακτινοβολία γ) Διλειτουργικό χημικό υποκαταστάτη ο οποίος προσδένεται στο πεπτίδιο και δεσμεύει σταθερά το μεταλλικό ραδιονουκλίδιο δ) Συνδέτη Σχήμα Α. 10: Σχηματική αναπαράσταση ραδιοπεπτιδίου Το ραδιοπεπτίδιο για επιτυχή εφαρμογή στην κλινική ογκολογία θα πρέπει : α) Να διατηρεί την ικανότητα δέσμευσης στον αντίστοιχο υποδοχέα μετά την εισαγωγή του χημικού υποκαταστάτη και την επισήμανση με το ραδιομέταλλο β) Να μπορεί να σχηματίζεται σε υψηλή ειδική ραδιενέργεια. Καθώς ο αριθμός θέσεων δέσμευσης είναι συγκεκριμένος για κάθε καρκινικό όγκο η χορήγηση μεγάλης ποσότητας μη ραδιοεπισημασμένου πεπτιδίου μπορεί να επιφέρει μερικό ή ολικό κορεσμό των θέσεων δέσμευσης, με αποτέλεσμα την μείωση της αποτελεσματικότητας ή την πλήρη αποτυχία της in vivo στόχευσης. Επιπλέον, δεδομένου ότι πολλά πεπτίδια μπορεί να προκαλέσουν ανεπιθύμητα συμπτώματα (τοξικότητα, παρενέργειες) μετά την in vivo χορήγησή τους, η επιτρεπτή δόση χορήγησης περιορίζεται. Στην περίπτωση της SS και των αναλόγων της δεν υφίσταται τέτοιο πρόβλημα καθώς η δράση της είναι κατασταλτική. 16
39 Α.1 Εισαγωγή γ) Να είναι μεταβολικά σταθερό στο βιολογικό περιβάλλον (πεπτιδική αλληλουχία και σύμπλοκο ραδιομετάλλου-χημικού υποκαταστάτη), ώστε να εξασφαλίζεται η επαρκής πρόσβαση του μεταλλικού ραδιονουκλιδίου στα κύτταρα στόχους. δ) Να έχει υψηλή υδροφιλικότητα ώστε να απεκκρίνεται γρήγορα από τους νεφρούς και το ουροποιητικό σύστημα και να ελαχιστοποιείται η πρόσληψη στο ήπαρ και τα έντερα. Με αυτό τον τρόπο επιτυγχάνεται ευκρινής απεικόνιση νεοπλασματικών εστιών στην κοιλιακή χώρα. ε) Να εσωτερικεύεται στα κύτταρα-στόχους (ραδιοπροσδέτης-αγωνιστής). Αυτό έχει ως αποτέλεσμα τη συσσώρευση του ραδιονουκλιδίου στο εσωτερικό του κυττάρου και επομένως την αύξηση του διαγνωστικού σήματος ή της κυτοτοξικής σωματιδιακής ακτινοβολίας (ραδιονουκλιδική θεραπεία) στα κύτταρα στόχους. Α ΤΜΗΜΑ ΑΝΑΓΝΩΡΙΣΗΣ ΥΠΟΔΟΧΕΑ - ΠΕΠΤΙΔΙΟ Ανάλογα με τον υποδοχέα-στόχο επιλέγεται και το αντίστοιχο ενδογενές πεπτίδιο - προσδέτης ή ανάλογο του για το σχεδιασμό του ραδιοπεπτιδίου. Έτσι για την στόχευση των sst 1-5 επιλέγουμε ανάλογα της SS14. Το πεπτιδικό τμήμα των ραδιοπεπτιδίων αυτών πρέπει να πληροί τα εξής κριτήρια: α) να έχει υψηλή συγγένεια δέσμευσης στον υποδοχέα-στόχο β) να έχει υψηλή ικανότητα εσωτερίκευσης γ) να έχει σταθερότητα στο βιολογικό περιβάλλον δ) να είναι υδρόφιλο ώστε να ευνοείται η απέκκριση των τελικών ραδιοπεπτιδίων από τα νεφρά και το ουροποιητικό σύστημα. Τα κριτήρια αυτά για το πεπτιδικό τμήμα αναλύονται διεξοδικά παρακάτω: α) Η ικανότητα δέσμευσης του πεπτιδίου στον υποδοχέα. Η ικανότητα του πεπτιδίου να αλληλεπιδρά και να δεσμεύεται στον αντίστοιχο υποδοχέα είναι βασική προϋπόθεση για επιτυχή στόχευση. Η ικανότητα δέσμευσης ενός πεπτιδίου μπορεί να αξιολογηθεί με μελέτες ανταγωνιστικής δέσμευσης. Με τα πειράματα ανταγωνιστικής δέσμευσης προσδιορίζεται το ποσοστό εκτόπισης ενός γνωστού ραδιοπροσδέτη (γνωστής υψηλής συγγένειας και σε σταθερή 17
40 Α.1 Εισαγωγή συγκέντρωση) από τις θέσεις δέσμευσης (υποδοχείς) παρουσία αυξανόμενων συγκεντρώσεων του πεπτιδίου (προσδέτη) που μελετάμε. Όταν η συγκέντρωση του πεπτιδίου είναι μηδενική, όλες οι θέσεις δέσμευσης (δηλαδή οι υποδοχείς) καταλαμβάνονται από τον ραδιοπροσδέτη. Καθώς αυξάνεται η συγκέντρωση του πεπτιδίου εκτοπίζεται σταδιακά ο ραδιοπροσδέτης από τις θέσεις δέσμευσης. Η συγκέντρωση του πεπτιδίου (προσδέτη) που εκτοπίζει το 50% του ραδιοπροσδέτη μας δίνει τη σταθερά IC 50 (Inhibitory Concentration 50%). τιμή IC 50 είναι χαρακτηριστική για κάθε πεπτίδιο και τον εκάστοτε ραδιοπροσδέτη. Ειδικά για τα ανάλογα SS, όπως το octreotide και τα ανάλογα του, οι τιμές IC 50 κυμαίνονται σε ~2-4 nm για τον sst 2 (με ραδιοπροσδέτη την [Leu 8,DTrp 22, 125 I- Tyr 25 ]SS28) [38]. Για τη μελέτη ανταγωνιστικής δέσμευσης χρησιμοποιούνται ιστοί ή κύτταρα ή μεμβράνες κυττάρων ως πηγές θέσεων ειδικής δέσμευσης, δηλαδή υποδοχέων ( Γ.3.1 και Δ.3.1) γ) Εσωτερίκευση. Πρόσφατες μελέτες έδειξαν ότι τόσο οι ραδιοπροσδέτες-αγωνιστές όσο και οι ραδιοπροσδέτες-ανταγωνιστές μπορούν να χρησιμοποιηθούν για τη μοριακή στόχευση του καρκίνου [39-41]. Μετά από δέσμευση στον υποδοχέα, οι ραδιοπροσδέτες-αγωνιστές εσωτερικεύονται στα κύτταρα. Με τον τρόπο αυτό οι αγωνιστές συσσωρεύονται στο εσωτερικό του κυττάρου αυξάνοντας το διαγνωστικό σήμα ή την κυτοτοξική ακτινοβολία στα κύτταρα στόχους [40]. Η εσωτερίκευση του αγωνιστή ραδιοπροσδέτη διαμέσου του υποδοχέα είναι ένας ισχυρός, ειδικός μηχανισμός και αποτελεί σημαντικό παράγοντα για την επιτυχή in vivo στόχευση των υποδοχέων με ραδιοπεπτίδια αγωνιστές. Η διαδικασία της εσωτερίκευσης μπορεί να γίνει με τρείς τρόπους: α) μέσω κυστιδίων επικαλυμμένων με κλαθρίνη β) μέσω κυστιδίων που αποτελούνται από διπλοστοιβάδα χοληστερόλης και γλυκολιπιδίων και γ) μέσω απογυμνωμένων κυστιδίων [43]. Ο πιο χαρακτηριστικός μηχανισμός εσωτερίκευσης των GPCRs είναι αυτός που πραγματοποιείται μέσω κυστιδίων επικαλυμμένων με κλαθρίνη [43]. Μετά την ενεργοποίηση ενός GPCR από ένα προσδέτη-αγωνιστή η μετατροπή ενός GDP σε GTP, με ανταλλαγή ενός νουκλεοτιδίου, οδηγεί σε διαχωρισμό των υπομονάδων α (G α ) και βγ (G βγ ). Η υπομονάδα βγ ενεργοποιεί τις κινάσες των υποδοχέων που συζεύγνυνται με τις πρωτεΐνες G (G protein-coupled receptor kinases ή GRKs) και στη συνέχεια οι GRKs φωσφορυλιώνουν τον υποδοχέα (Σχήμα Α. 11). 18
41 Α.1 Εισαγωγή Σχήμα Α. 11: Ενεργοποίηση των GRKs από την υπομονάδα G βγ και φωσφορυλίωση του υποδοχέα. [49] Με τη βοήθεια της β-αρρεστίνης το φωσφορυλιωμένο σύμπλοκο υποδοχέα - προσδέτη ενσωματώνεται σε κυστίδια επικαλλυμένα με κλαθρίνη και ακολουθεί μεταφορά στα ενδοσωμάτια [30,44-46]. Το όξινο περιβάλλον του ενδοσωματίου προκαλεί την αποδέσμευση του προσδέτη από τον υποδοχέα και ακολουθεί είτε αποικοδόμηση του υποδοχέα στα λυσοσώματα είτε αποφωσφορυλίωση του υποδοχέα και επιστροφή στη κυτταρική μεμβράνη [49] (Σχήμα Α. 12). Σχήμα Α. 12: Μηχανισμός εσωτερίκευσης των GPCRs μέσω κυστιδίων επικαλυμμένων με κλαθρίνη. [49] Πιο ειδικά, οι ραδιοπροσδέτες (ραδιοπεπτίδια), μετά την αποδέσμευση από τον υποδοχέα στα ενδοσωμάτια μπορεί να οδηγηθούν για αποικοδόμηση στα λυσοσώματα είτε να διαφύγουν την αποικοδόμηση (μέσω άλλων ενδοκυττάριων οδών). Οι ραδιομεταβολίτες συνήθως παγιδεύονται και συσσωρεύονται στο εσωτερικό του κυττάρου και μπορούν να ανιχνευθούν στον πυρήνα ή ακόμα και στα μιτοχόνδρια (Σχήμα Α. 13) [50,51]. 19
42 Α.1 Εισαγωγή Σχήμα Α. 13: Εσωτερίκευση ραδιοπεπτιδίου σε καρκινικό κύτταρο Αξιοσημείωτο είναι ότι η εσωτερίκευση των υποδοχέων της σωματοστατίνης επάγεται μόνο από αγωνιστές αλλά όχι από ανταγωνιστές [40,42]. Επιπλέον, για τους υποδοχείς της SS έχει αποδειχτεί ότι ο sst 2 εσωτερικεύεται πολύ γρήγορα [38]. Για τον sst 4 έχει αποδειχθεί ότι επιδεικνύει ασθενή εσωτερίκευση [52], ενώ για τον sst 1 οι απόψεις για το αν εσωτερικεύεται διίστανται [53]. Στη βιβλιογραφία ορίζεται η εξής φθίνουσα σειρά ικανότητας εσωτερίκευσης των υποδοχέων: sst 2 >sst 3, sst 5 >sst 4 >sst 1. Η υψηλή ικανότητα εσωτερίκευσης του sst 2 (σε συνδυασμό με την υπερέκφραση του σε πολλούς ανθρώπινους όγκους) καθιστά τον sst 2 ελκυστικό βιομόριο-στόχο για ραδιοεπισημασμένα ανάλογα σωματοστατίνης για εφαρμογή στην κλινική πράξη. Γι αυτό το σκοπό αναπτύχθηκαν ανάλογα της σωματοστατίνης με υψηλή συγγένεια για τον sst 2, τα οποία και εσωτερικεύονται ταχύτατα και σε υψηλό ποσοστό. Η συσσώρευση της ραδιενέργειας στον ενδοκυττάριο χώρο έχει ως αποτέλεσμα την αποτελεσματικότερη σπινθηρογραφική απεικόνιση λόγω της παρατεταμένης παραμονής και ενίσχυσης του ραδιενεργού σήματος στο εσωτερικό του κυττάρου. Επίσης, λόγω της προσέγγισης στο γενετικό υλικό του κυττάρου και της παρατεταμένης έκθεσης στην κυτοτοξική σωματιδιακή ακτινοβολία έχουμε αποτελεσματικότερη ραδιονουκλιδική θεραπεία. γ) Μεταβολική σταθερότητα. Συνήθως τα φυσικά πεπτίδια έχουν μικρό χρόνο ημιζωής στην κυκλοφορία. Το γεγονός αυτό αποτελεί ένα σημαντικό πρόβλημα για τη δράση των πεπτιδίων καθώς τις περισσότερες φορές μόνο μικρή ποσότητα της αρχικής ένωσης φθάνει στα όργανα-στόχους. Για την εφαρμογή των πεπτιδικών αναλόγων στην κλινική πράξη συχνά απαιτείται αύξηση της μεταβολικής τους σταθερότητας. Για το σκοπό αυτό τα πεπτίδια τροποποιούνται με μια από τις παρακάτω μεθόδους: 20
43 Α.1 Εισαγωγή 1) Κυκλοποίηση γραμμικών πεπτιδίων. Η τεχνική αυτή έχει εφαρμοστεί με επιτυχία στο πεπτίδιο [Leu 5 ]εγκεφαλίνη (-Tyr-Gly-Gly-Phe-Leu-). Συγκεκριμένα, το κυκλικό ανάλογο DADLE (c[tyr-dala-gly-phe-dleu]) έδειξε εντυπωσιακή αύξηση της σταθερότητας σε σχέση με το γραμμικό ανάλογο [Leu 5 ]εγκεφαλίνη (t 1/2 = 100 min και t 1/2 = 6.1 min αντίστοιχα, μετά από επώαση σε ομογενοποίημα ήπατος αρουραίου) [54]. 2) Eισαγωγή δεύτερου δακτυλίου στο μονοκυκλικό πεπτίδιο. Έχει αναφερθεί στο δικυκλικό ανάλογο c(aha-lys-c(cys-phe-phe-dtrp-lys-thr-phe-cys)-ser) υψηλή in vivo σταθερότητα [55]. Σχήμα Α. 14: Η δομή του αναλόγου c(aha-lys-c(cys-phe-phe-dtrp-lys-thr-phe-cys)-ser) [55] 3) Μείωση του αριθμού αμινοξέων στο δακτύλιο κυκλικών αναλόγων. Ανάλογα της SS14 (δωδεκαμελής δακτύλιος) με μικρότερο δακτύλιο όπως π.χ. το octreotide και άλλα ανάλογα του με εξαμελή δακτύλιο, έδειξαν μεγαλύτερη σταθερότητα σε σχέση με τη SS14 (από t 1/2 = 3 min η SS14 και t 1/2 = 1.7 h το octreotide, σε πλάσμα αίματος ανθρώπου) [56,57]. Σχήμα Α. 15: Η αλληλουχία της SS14 και του αναλόγου octreotide 4) Αντικατάσταση επιλεγμένων φυσικών L-αμινοξέων από D- αμινοξέα. Σε πολλά ανάλογα της εκλυτικής ορμόνης της ωχρινοτρόπου ορμόνης (LR) η αντικατάσταση L-αμινοξέων από D- αμινοξέα οδήγησε σε πολύ σταθερά ανάλογα με αυξημένη και παρατεταμένη δράση [58-60]. 5) Προσθήκη πολυαιθυλενογλυκόλης (PEGx). Προσθήκη PEG 2,40K στην ιντερφερόνη α-2b (IF-α2b) αύξησε σημαντικά τη σταθερότητα της φυσικής πρωτεΐνης έναντι της θρυψίνης [61]. Επίσης σε ανάλογο της μπομπεσίνης (ΒΒΝ) 21
44 Α.1 Εισαγωγή Lys 4 -BΒ έγινε προσθήκη των PEG 5, PEG 10, PEG 20 και παρατηρήθηκε σημαντικά αυξημένη μεταβολική σταθερότητα των PEG-αναλόγων. Επώαση των αναλόγων σε πλάσμα αίματος ανθρώπου στους 37ºC για 24 h έδειξε ότι 16% του αρχικού Lys 4 -BΒ έμεινε σταθερό, ενώ όλα τα PEG X -Lys 4 -BΒ παρέμειναν 100% σταθερά [62]. Σχήμα Α. 16: Προσθήκη PEGx στο ανάλογο Lys 4 -BΒ [62] 6) Τροποποίηση του Ν- ή C- τελικού άκρου του πεπτιδίου. Στο ανοσογονικό πεπτίδιο MART-I αυξήθηκε σημαντικά η σταθερότητα έναντι των εξωπεπτιδασών στο πλάσμα του αίματος με ακετυλίωση στο Ν-τελικό άκρο ή αμιδίωση στο C-τελικό άκρο [63]. Σχήμα Α. 17: Σταθερότητα του πεπτιδίου MART-I και των αναλόγων του σε πλάσμα αίματος [63] 7) Ν-μεθυλίωση. Στο πεπτίδιο της LR (pglu-is-trp-ser-tyr-dleu-leu-arg-pro- Et) η μεθυλίωση ξεχωριστά των πεπτιδικών δεσμών 3, 4 και 5 οδήγησε σε σταθερά ανάλογα έναντι της χυμοθρυψίνης (t 1/2 > 60 min έναντι της LR με t 1/2 = 1 min) [64]. 8) Αναγωγή πεπτιδικού δεσμού. Αντικατάσταση των πεπτιδικών δεσμών με μεθυλαμινο-δεσμούς (C 2 ) σε ανάλογα νευροτενσίνης (ΝΤ(8-13)) οδήγησε σε 22
45 Α.1 Εισαγωγή ανάλογα με αυξημένη σταθερότητα και βιολογική δραστικότητα (70-90% σταθερά έναντι του ΝΤ(8-13) που μένει 20-40% σταθερό, μετά από 2 h σε ομογενοποίημα εγκεφάλου αρουραίου) [65,66]. 9) Σχηματισμός ολιγομερών πεπτιδίων. Το τετραμερές του πεπτιδίου Η2009 (δεσμεύεται επιλεκτικά στην ιντεγκρίνη α ν β 6 ) ήταν πιο σταθερό από το μονομερές σε ορό αρουραίου στις 4 h (69% και 46% παρέμεινε σταθερό αντίστοιχα) [67]. Σχήμα Α. 18: Σχηματισμός του τετραμερούς του πεπτιδίου Η2009 [67] 10) Σύνθεση retro-inverso. Μερική τροποποίηση με αναστροφή (retro-inverso) πεπτιδικών δεσμών σε αρχικό πεπτίδιο της ουσίας P (Substance P ή SP) οδήγησε στο ανάλογο [pglu 6,gPhe 8,mGly 9 ]SP(6-11) με αυξημένη σταθερότητα (100% σταθερό σε 1 h σε αντίθεση με το μητρικό πεπτίδιο που παραμένει 10% σταθερό σε 45 min, μετά από επώαση σε τομές υποθαλάμου και παρωτίδες αρουραίου) [68]. Σχήμα Α. 19: Σχηματική αναπαράσταση από μερική τροποποίηση retro-inverso ενός μητρικού πεπτιδίου [68] 23
46 Α.1 Εισαγωγή Για την καλύτερη σχεδίαση των τροποποιήσεων σε κάθε ανάλογο είναι σημαντική η γνώση των ενζύμων που αποικοδομούν το πεπτίδιο καθώς και οι εκλεκτικές θέσεις αποικοδόμησης στην πεπτιδική αλυσίδα. Φυσικά όλες αυτές οι μεταβολές για τη σταθεροποίηση του πεπτιδίου δε θα πρέπει να επηρεάσουν αρνητικά τη συγγένεια δέσμευσης του στον αντίστοιχο υποδοχέα καθώς και την ικανότητα του να εσωτερικεύεται στα κύτταρα-στόχους. δ) Υδροφιλικότητα. Τα πεπτιδικά ανάλογα θα πρέπει να είναι υδρόφιλα ώστε να συμβάλουν στη γρήγορη απέκκριση των τελικών ραδιοπεπτιδίων από τα νεφρά και το ουροποιητικό σύστημα και να ελαχιστοποιείται η πρόσληψη στο ήπαρ και τα έντερα. Συνεπώς με τη χορήγηση των αντίστοιχων ραδιοπεπτιδίων επιτυγχάνεται ευκρινής απεικόνιση νεοπλασματικών εστιών στην κοιλιακή χώρα (διαγνωστική απεικόνιση) και ελαχιστοποίηση της επιβάρυνσης του ασθενούς με κυτοτοξική ακτινοβολία (θεραπεία). Α ΡΑΔΙΟΜΕΤΑΛΛΟ Για την επιλογή του κατάλληλου ραδιομετάλλου λαμβάνονται υπόψη τα εξής κριτήρια: 1. το κόστος ραδιονουκλιδίου 2. οι πυρηνικές ιδιότητες (χρόνος υποδιπλασιασμού, τρόπος διάσπασης (σωματιδιακή β + ή γ ακτινοβολία), εμβέλεια ακτινοβολίας) 3. η διαθεσιμότητα του (π.χ. αν παράγεται από γεννήτρια είναι εύκολα διαθέσιμο) 4. η ειδική ραδιενέργεια (εκφράζει τη ραδιενέργεια ανά μονάδα μάζας του ραδιονουκλιδίου, Ci/mol) 5. η ραδιενεργός συγκέντρωση (εκφράζει τη ραδιενέργεια ανά μονάδα όγκου του διαλύματος του ραδιονουκλιδίου, mci/ml) Ανάλογα με την ακτινοβολία που εκπέμπουν τα ραδιονουκλίδια χωρίζονται σε διαγνωστικά (φωτόνια γ ή β + ) ή θεραπευτικά (α, β - και ηλεκτρόνια Auger). Όταν το διαγνωστικό ραδιονουκλίδιο εκπέμπει ηλεκτρομαγνητική ακτινοβολία (γ ή Χ) εφαρμόζεται η τεχνική SPECT π.χ. 111 In ή 99m Tc ή 67 Ga ( Α.1.1). Όταν το διαγνωστικό ραδιονουκλίδιο εκπέμπει ποζιτρόνια (β + ) εφαρμόζεται η τεχνική PET π.χ. 64 Cu ή 68 Ga ( Α.1.1). Τα μεταλλικά ραδιονουκλίδια 90 Y και 177 Lu εκπέμπουν β - ακτινοβολία και είναι χρήσιμα για την ανάπτυξη θεραπευτικών ραδιοφαρμάκων (Πίνακας Α.4) [69]. Το 111 In είναι ραδιονουκλίδιο που παράγεται σε κυκλοτρόνιο από την πυρηνική αντίδραση 111 Cd (p, n) 111 In και έχει χρόνο υποδιπλασιασμού 67.9 h). Εκπέμπει χαμηλής εμβέλειας ηλεκτρόνια Auger και γ-ακτινοβολία με την ενέργεια των δύο φωτονίων να 24
47 Α.1 Εισαγωγή ανέρχεται σε 172 και 247 kev. Έχει χρησιμοποιηθεί ευρέως στην ιατρική ως διαγνωστικό ραδιονουκλίδιο (σπινθηρογραφική απεικόνιση). Συχνά τα ραδιοπεπτίδια επισημασμένα με 111 In χρησιμοποιούνται για τον προσδιορισμό των χαρακτηριστικών βιοκατανομής και δοσιμετρίας του αντίστοιχου θεραπευτικού 90 Y-αναλόγου, καθώς το 90 Y δεν εκπέμπει γ-ακτινοβολία και επομένως δεν ανιχνεύεται [69]. Πίνακας Α. 4: Μεταλλικά ραδιονουκλίδια για την ανάπτυξη διαγνωστικών ραδιοπεπτιδίων με εφαρμογή στην τεχνική SPECT και PET. Ραδιονουκλίδιο (SPECT) t 1/2 (h) Τρόπος διάσπασης (%) Εγ (kev) Τρόπος Παραγωγής 111 In 67.2 Auger, EC (100%) 172, 247 Κυκλοτρόνιο, 112 Cd(p,2n) 111 In 99m Tc 6.0 ΙΤ (100%) 141 Γεννήτρια 99 Mo/ 99m Tc 99 Μο/ 99m Tc 67 Ga 78.1 Auger, EC (100%) 91,93,185,296, (21),0.3(16) Κυκλοτρόνιο, 68z Zn(p,2n) 67 Ga Ραδιονουκλίδιο (PET) t 1/2 (h) Τρόπος διάσπασης (%) Εβ + (kev) Τρόπος Παραγωγής 68 Ga 1.1 β + (90%), EC(10%) 820,1895 Γεννήτρια 68 Ge/ 68 Ga 64 Cu 12.9 β + (19%), β - (40%), EC(41%) 654 Αντιδραστήρας, Κυκλοτρόνιο, 64 i(p,n) 64 Cu 86 Y 14.7 β + (33%), EC(66%) 1043,1248,1603, 2019,2335 Κυκλοτρόνιο, 86 Sr(p,n) 86 Y Όπου Εγ: ενέργεια φωτονίων γ, Εβ + : ενέργεια ποζιτρονίων, EC: σύλληψη ηλεκτρονίου (electron capture), β - : σωματιδιακή ακτινοβολία ηλεκτρονίων, ΙΤ: εσωτερική μετάδοση (internal transmission) Το 68 Ga εκπέμπει ποζιτρόνια (β + ), έχει χρόνο υποδιπλασιασμού 68 min και χρησιμοποιείται για απεικόνιση PET [69]. Η τεχνική αυτή επιτρέπει την καλύτερη ποσοτικοποίηση αποτελεσμάτων. Έτσι επισημαίνοντας το αντίστοιχο ραδιοπεπτίδιο με 68 Ga μπορούμε να παραλάβουμε ποσοτικά δοσιμετρικά δεδομένα. Το 68 Ga παράγεται από γεννήτρια (υψηλή διαθεσιμότητα). Όμως η διαφορετική χημεία συναρμογής του 68 Ga από τα 90 Y και 177 Lu καθιστά τη χρήση ραδιοπεπτιδίων επισημασμένων με 68 Ga για τον προσδιορισμό των χαρακτηριστικών βιοκατανομής των αντίστοιχων 90 Y ή 177 Lu-αναλόγων όχι απόλυτα θεμιτή, καθώς συχνά υπάρχουν αποκλίσεις στη βιοκατανομή. Επιπλέον, ο χρόνος υποδιπλασιασμού του 68 Ga είναι μικρός και επομένως, δεν είναι εφικτή η μελέτη βιοκινητικής σε μεγαλύτερα χρονικά διαστήματα μετά τη χορήγηση, οπότε και αναμένεται αποτελεσματικότερη κάθαρση της ακτινοβολίας από τους παρακείμενους ιστούς. 25
48 Α.1 Εισαγωγή Ένα άλλο ραδιονουκλίδιο για απεικόνιση PET είναι το 86 Y. Με ραδιοπεπτίδια επισημασμένα με 86 Y έχουμε σαφώς καλύτερο προσδιορισμό των χαρακτηριστικών βιοκατανομής και της δοσιμετρίας ακτινοβολίας των αντίστοιχων 90 Y-αναλόγων. Επιπλέον, ο χρόνος υποδιπλασιασμού του 86 Y (t 1/2 = 14.7 h) επαρκεί για την παρακολούθηση της βιοκινητικής του αντίστοιχου ραδιοπεπτιδίου σε μεγαλύτερα χρονικά διαστήματα μετά τη χορήγηση. Όμως το 86 Y είναι ακριβό και δύσκολα διαθέσιμο (παράγεται σε κυκλοτρόνιο). To 90 Y παράγεται από γεννήτρια, εκπέμπει υψηλής ενέργειας σωματίδια β - (E max = 2,27 MeV, 100% αφθονία), έχει χρόνο υποδιπλασιασμού 2.7 d και χρησιμοποιείται στη ραδιονουκλιδική θεραπεία. Το 177 Lu εκπέμπει σωματίδια β - με μέγιστη ενέργεια 0.5 MeV και συνοδά φωτόνια γ επιτρέποντας την παρακολούθηση της ραδιονουκλιδικής θεραπείας καθώς εξελίσσεται (real time). Επιπλέον, καθίσταται άμεσα εφικτή η δυνατότητα δοσιμετρίας. Πίνακας Α.5: Μεταλλικά ραδιονουκλίδια για την ανάπτυξη θεραπευτικών ραδιοπεπτιδίων Ραδιονουκλίδιο t 1/2 Τρόπος διάσπασης Εmax β - (MeV) Εγ (kev) Μέγιστη εμβέλεια (mm) Τρόπος Παραγωγής 90 Y 64.1 h 2.27 (100%) Γεννήτρια 90 Sr/ 90 Y 177 Lu 6.7 d 0.5 (79%) 208, Αντιδραστήρας 99 Μο/ 99m Tc 67 Cu 61.9 h 0.58 (20%) 91,93,185, 395,484,577 Όπου Εmax β - : μέγιστη ενέργεια β - σωματιδίων, Εγ: ενέργεια φωτονίων γ Επιταχυντής 26
49 Α.1 Εισαγωγή Α ΧΗΜΙΚΟΣ ΥΠΟΚΑΤΑΣΤΑΤΗΣ Όπως προαναφέρθηκε, στο σχεδιασμό ραδιοπεπτιδίων γίνεται τροποποίηση του αρχικού πεπτιδίου με δέσμευση κατάλληλου διλειτουργικού χημικού υποκαταστάτη ο οποίος θα δεσμεύσει το ραδιομέταλλο. Ο χημικός υποκαταστάτης συζεύγνυται ομοιοπολικά συνήθως στο Ν-τελικό άκρο του πεπτιδίου μέσω ενός πεπτιδικού δεσμού μεταξύ της καρβοξυλικής ομάδας του υποκαταστάτη και της Ν-τελικής αμινομάδας του πεπτιδίου. Ο χημικός υποκαταστάτης θα πρέπει να πληροί τις εξής προϋποθέσεις: α) Να σχηματίζει σύμπλοκο ραδιομετάλλου-χημικού υποκαταστάτη σταθερό στο βιολογικό περιβάλλον β) Να σχηματίζει υδρόφιλο σύμπλοκο με το ραδιομέταλλο ώστε να ευνοείται η γρήγορη απέκκριση από τα νεφρά στα ούρα γ) Να δεσμεύει το ραδιονουκλίδιο με υψηλή ραδιοχημική απόδοση υπό συνθήκες πρακτικά εύκολα εφαρμόσιμες στην κλινική πράξη δ) Να σχηματίζει σύμπλοκο με το ραδιονουκλίδιο σε υψηλή ειδική ραδιενέργεια και υψηλή καθαρότητα Ανάλογα με το μεταλλικό ραδιονουκλίδιο επιλέγουμε και τον κατάλληλο υποκαταστάτη για τη σταθερή συναρμογή του. Ο υποκαταστάτης DTA (1,4,7,10-τετρααζακυκλοδωδεκαν-1,4,7,10-τετραοξεικό οξύ) αποτελείται από ένα δωδεκαμελή δακτύλιο με τέσσερα άτομα αζώτου, στα οποία συνδέονται τέσσερις ομάδες οξικού οξέος (Πίνακας Α.6). Θεωρείται καθολικός καθώς σχηματίζει σύμπλοκα με μέταλλα 2 + και 3 + διαφόρων ιοντικών ακτίνων με πολύ υψηλές σταθερές σχηματισμού. Γι αυτό το λόγο χρησιμοποιείται για την συναρμογή μεγάλου φάσματος διαγνωστικών ή θεραπευτικών ραδιομετάλλων σε πεπτιδικά ανάλογα π.χ. [ 111 In / 67 Ga / 68 Ga / 86 Y / 90 Υ / 177 Lu -DTA,Tyr 3 ]octreotide [70-75]. Ο υποκαταστάτης DTA σχηματίζει σύμπλοκα με αριθμό ένταξης από έξι έως εννέα. Συνήθως σχηματίζει σύμπλοκα με αριθμό ένταξης οκτώ (Ν 4 Ο 4 ), όμως με τις λανθανίδες σχηματίζει σύμπλοκα και με αριθμό ένταξης εννέα με επιπλέον υποκαταστάτη ένα μόριο νερού. Πιο αναλυτικά, η χημεία συναρμογής των ραδιομετάλλων με τον υποκαταστάτη DTA είναι συχνά διαφορετική λόγω του διαφορετικού μεγέθους τους. Για παράδειγμα τα 90 Y, 68 Ga και 111 In είναι τρισθενή μεταλλικά κατιόντα και η κύρια διαφορά τους είναι το μέγεθος τους. 27
50 Α.1 Εισαγωγή Συγκεκριμένα, το Ga(ΙΙΙ) έχει ιοντική ακτίνα pm [76] και ο αριθμός ένταξης του σε σύμπλοκα με το DTA είναι έξι (Ν 4 Ο 2 ). Ειδικά, στο Ga-DTA-DPhe- 2 που μελετήθηκε, έχει ψευδο-οκταεδρική δομή και αριθμό ένταξης έξι (Σχήμα Α. 20) [76,78]. Το Y(ΙΙΙ) έχει ιοντική ακτίνα pm [76], η οποία ταιριάζει απόλυτα με την κοιλότητα του DTA σχηματίζοντας σταθερά σύμπλοκα με αριθμό ένταξης οχτώ ή εννέα [78-80]. Συγκεκριμένα, το Υ-DTA-D-Phe- 2 υιοθετεί τετραγωνική αντιπρισματική γεωμετρία με αριθμό ένταξης οχτώ (Σχήμα Α. 20) [76,78]. Η χημεία συναρμογής του Lu(III) (λανθανίδα) με τον υποκαταστάτη DTA μοιάζει πολύ με αυτή του Y(ΙΙΙ) (ψευδο-λανθανίδα). Το Lu(III) σχηματίζει πολύ σταθερά σύμπλοκα με τον υποκαταστάτη DTA με αριθμό ένταξης οχτώ ή εννέα. Α Β Σχήμα Α. 20: Δομή Α. του Ga-DTA-DPhe- 2 και Β. του Υ-DTA-DPhe- 2 [76] Το In(ΙΙΙ) έχει ιοντική ακτίνα pm [76] και ο αριθμός ένταξης του σε σύμπλοκα με το DTA είναι επτά και μερικές φορές οχτώ [78,79]. Δεν έχει γίνει ακόμα μελέτη της δομής του συμπλόκου In-DTA. Ωστόσο έχει αποσαφηνιστεί η δομή του In-DTA-ΑΑ (ΑΑ=p-αμινο-ανιλίδη). Το σύμπλοκο αυτό βρέθηκε να έχει μια τετραγωνικήαντιπρισματική γεωμετρία (με περιστροφή ~ 28 ) και αριθμό ένταξης επτά σε υγρή φάση και οχτώ σε στερεή φάση (Σχήμα Α. 21) [76,77]. Α Β Σχήμα Α. 21: Δομή Α. του In-DTA-ΑΑ και Β. σε στερεή φάση και σε υγρή φάση [76,77] Μεγάλος αριθμός παραγώγων του DTA έχει αναπτυχθεί λόγω της ευρείας χρήσης του (Πίνακας Α.6). Έτσι, για τη δέσμευση του υποκαταστάτη στο υπό σύνθεση πεπτίδιο 28
51 Α.1 Εισαγωγή στη ρητίνη αναπτύχθηκε ο προστατευμένος υποκαταστάτης DTA-tris(tBu) που είναι συμβατός στις συνθήκες SPPS. Η δέσμευση του DTA-tris(tBu) στο ορθογωνικά προστατευμένο πεπτίδιο μπορεί να γίνει είτε στο Ν-τελικό άκρο είτε στην πλευρική αμινομάδα μιας Lys. Ένα άλλο παράγωγο του DTA,το α-αμινο-dta, επιτρέπει την δέσμευση του στο C-τελικό άκρο του πεπτιδίου [81]. Η δέσμευση του DTA στο πεπτίδιο γίνεται μέσω ενός από τα τέσσερα καρβοξύλια του με αποτέλεσμα τη μείωση του αριθμού ένταξης (Ν 4 Ο 3 ). Για να αυξηθεί ο αριθμός ένταξης στα σύμπλοκα του DTA, ειδικά για τα ραδιομέταλλα 90 Υ και 177 Lu που έχουν μεγαλύτερη ιοντική ακτίνα (αριθμός ένταξης 8 ή 9), αναπτύχθηκαν παράγωγα του τα οποία επιτρέπουν τη συμμετοχή και του τέταρτου καρβοξυλίου (Ν 4 Ο 4 ) για τη δημιουργία πιο σταθερών συμπλόκων. Τα DTAGA, DTASA και DTA-S ester είναι από τα πιο σημαντικά παράγωγα DTA για σταθερή συναρμογή ραδιομετάλλων όπως το 90 Υ και το 177 Lu [82,83]. Στην επισήμανση DTA-αναλόγων οι συνθήκες διαφέρουν ανάλογα με ραδιομέταλλο που επιλέγουμε. Συγκεκριμένα, η επισήμανση αναλόγων DTA με 111 In απαιτεί θέρμανση στους 90 C για 30 min [84]. Η περιοχή του p 4-5 θεωρείται βέλτιστη για την επισήμανση του DTA με 111 In καθώς σε p<4 είναι πολύ αργή η αντίδραση επισήμανσης ενώ σε p>5 έχουμε σχηματισμό υδροξειδίων του 111 In [84]. Μετά την είσοδο τους στην κυκλοφορία τα υδροξείδια του 111 In εντοπίζονται σε παρακείμενους ιστούς όπως στο ήπαρ, στη σπλήνα και στους πνεύμονες αλλοιώνοντας το αποτέλεσμα της απεικόνισης. Γι αυτό το λόγο είναι απαραίτητη η χρήση ρυθμιστικού διαλύματος οξικού νατρίου p 4.6 [85]. Μετά την επισήμανση των DTA-αναλόγων με 111 In προστίθεται διάλυμα a 2 EDTA (free 111 In scavenger) για τη δέσμευση τυχόν ελεύθερου 111 In. Το σχηματιζόμενο υδρόφιλο σύμπλοκο απεκκρίνεται γρήγορα από τα ούρα και έτσι αποφεύγεται η εναπόθεση ελεύθερου 111 In στα οστά. Μελέτη που έγινε για την εύρεση βέλτιστων συνθηκών επισήμανσης DTA-αναλόγων με 177 Lu και 90 Y έδειξε ότι η περιοχή του p θεωρείται βέλτιστη, και για τα δύο ραδιονουκλίδια, και απαιτεί θέρμανση στους 80 C για 20 min, ενώ με το 111 In όπως είπαμε απαιτεί θέρμανση στους 90 C για 30 min [84]. 29
52 Α.1 Εισαγωγή Α Β Σχήμα Α. 22: Α. Ο σχηματισμός του 177 Lu-DTATC σε συνάρτηση με το p, μετά από 20 min στους 80 C. Παρόμοια αποτελέσματα είχε και ο σχηματισμός του 90 Υ-DΟΤΑ-ΤΑΤΕ. B. σχηματισμός του επισημασμένου DTATC (p 4) σε συνάρτηση με το χρόνο με: Lu (80 C), 177 Lu (100 C), 90 Y (80 C), 90 Y (100 C) 111 In (80 C), 111 In (100 C) [84] Αντίστοιχη μελέτη για την επισήμανση του DTATC με 68 Ga έδειξε ότι η περιοχή του p θεωρείται βέλτιστη και απαιτείται θέρμανση στους 80 C για 5-10 min [86]. Α Β Σχήμα Α. 23: Α. Ο σχηματισμός του 68 Ga-DTATC σε συνάρτηση με το p και το χρόνο, στους 80 C. Β. σε συνάρτηση με τη θερμοκρασία και το χρόνο, σε p [86] Είναι σημαντικό να σημειωθεί ότι το ελεύθερο 68 Ga και 111 In τείνουν να εντοπίζoνται στο ήπαρ και τους πνεύμονες, λόγω της υψηλής ενέργειας σχηματισμού με την τρανσφερίνη, ενώ το ελεύθερο 90 Y και 111 In εναποτίθενται στα οστά [87]. Η οστική εναπόθεση τους οφείλεται στην ανταλλαγή των κατιόντων Ca 2+ στον υδροξυαπατίτη (Ca 10 (P 4 ) 6 () 2 ) με κατιόντα του ραδιονουκλιδίου [77]. Είναι λοιπόν σημαντικό τα ραδιοεπισημασμένα ανάλογα να παραλαμβάνονται σε υψηλή καθαρότητα και απόδοση επισήμανσης και το σύμπλοκο του ραδιομετάλλου να έχει υψηλή in vivo σταθερότητα, ώστε να αποφευχθεί η εναπόθεση ελεύθερου ραδιομετάλλου στα οστά και ανεπιθύμητη ακτινοβόληση του αιμοποιητικού συστήματος (μυελός των οστών). 30
53 Α.1 Εισαγωγή Πίνακας Α.6: Οι σημαντικότεροι υποκαταστάτες για τη συναρμογή ραδιονουκλιδίων Όνομα (Σύντμηση) Χημικός Τύπος Όνομα (Σύντμηση) Χημικός Τύπος DTA DTPA t-bu 2 C C 2 t-bu 2 DTAGA C 2 t-bu α-amino-dta t-bu 2 C t-bu 2 C C 2 t-bu DTASA C 2 t-bu DTA-S ester t-bu 2 C TA DASA TETA CTPA DF (C 2 ) 5 (C 2 ) 2 (C 2 ) 5 2 (C 2 ) (C 2 2 ) 5 31
54 Α.1 Εισαγωγή Ο υποκαταστάτης DTPA (διαιθυλενοτριαμινο πενταοξεικό οξύ) σχηματίζει πολύ σταθερά σύμπλοκα με το 111 In (αριθμός ένταξης 7 ή 8) και η επισήμανση του με 111 In γίνεται σε θερμοκρασία δωματίου (RT). Το ctreoscan ([ 111 In]DTPA-octreotide) [88] είναι το πρώτο ραδιοπεπτίδιο που εγκρίθηκε για κλινική εφαρμογή. Όμως o υποκαταστάτης DTPA δεν δημιουργεί σταθερά σύμπλοκα με άλλα ραδιομέταλλα π.χ. 68 Ga, 90 Y, 177 Lu. Σχήμα Α. 24: Δομή του In-DTPA [76] Για την επισήμανση πεπτιδίων με 67 Ga και 68 Ga χρησιμοποιούνται και οι υποκαταστάτες ΝΟΤΑ (1,4,7-τριαζακυκλονοεναν-1,4,7-τριοξεικό οξύ), (DASA (1,4,7-τριαζακυκλοεναν-1-ηλεκτρικό οξύ-4,7-διοξεικό οξύ) και DF (desferrioxamine-b) π.χ. [ 67 Ga ή 68 Ga DF]octreotide [89]. Το Ga(ΙΙΙ) δημιουργεί πολύ σταθερά σύμπλοκα με το ΝΟΤΑ με αριθμό ένταξης 6 (Ν 3 Ο 3 ) [90]. Για την επισήμανση πεπτιδίων με 64 Cu, εκτός από τον υποκαταστάτη DTA, χρησιμοποιούνται και οι υποκαταστάτες CTPA (4-[1,4,8,11- τετρααζακυκλοδεκατετρανο-1-1μεθυλο]βενζοϊκό οξύ) και TETA (1,4,8,11- τετρααζακυκλοδεκατετραν-1,4,8,11 τετραοξικό οξύ) π.χ. [ 64 Cu]TETA-octreotide [91]. Α ΣΥΝΔΕΤΗΣ Σε πολλές περιπτώσεις μεταξύ του χημικού συμπλόκου (υποκαταστάτης-μεταλλικό ραδιονουκλίδιο) και πεπτιδικού τμήματος παρεμβάλλεται ένα μόριο-συνδέτης. Η προσθήκη συνδέτη γίνεται ώστε να αποφευχθεί πιθανή μείωση της ικανότητας δέσμευσης του ραδιοπεπτιδίου με στερεοχημική παρεμπόδιση. Επίσης η προσθήκη συνδέτη βελτιώνει πολλές φορές τις φυσικοχημικές ιδιότητες, όπως την υδροφιλικότητα αλλά και τη μεταβολική σταθερότητα του ραδιοπεπτιδίου. Επιπλέον, κάποιοι συνδέτες, όπως η Lys, παρέχουν τη δυνατότητα σχηματισμού διακλαδώσεων στο πεπτίδιο (branched peptide linkers). Για παράδειγμα, όπως φαίνεται και στο Σχήμα Α. 25, στο ανάλογο ΤC (για τη δέσμευση του αναλόγου στους υποδοχείς sst 2 και εσωτερίκευση στα καρκινικά 32
55 Α.1 Εισαγωγή κύτταρα) προστείθεται μια Lys στο Ν-τελικό του άκρο. Μέσω της α-αμινομάδας της Lys συνδέεται ο υποκαταστάτης DTA (για τη δέσμευση του ραδιομετάλλου) και στην ε- αμινομάδα συνδέεται το εξαπεπτίδιο (SV40 large T antigen) -Pro-Lys-Lys-Lys-Arg- Lys-Val- (nuclear localization signal, LS) για μεταφορά του αναλόγου στον πυρήνα του καρκινικού κυττάρου. Αυτό το τριλειτουργικό ανάλογο σχεδιάστηκε με σκοπό την μεγαλύτερη συσσώρευση της ραδιενέργειας στον πυρήνα των κυττάρων-στόχων και την παρατεταμένη παραμονή των ραδιοπροσδετών στο εσωτερικό τους [92]. Σχήμα Α. 25: Σχηματική αναπαράσταση του πεπτιδικού αναλόγου LS [92] Στο ανάλογο α -(1-δεοξυ-D-φρουκτοζυλ)- ε -(2-φλουοροπροπιόνυλ)-Lys 0 -Tyr 3 - octreotate (Σχήμα Α. 26) στην α-αμινομάδα της Lys συνδέεται ένα σάκχαρο (τροποποιητής φαρμακοκινητικής), ενώ στην στην ε-αμινομάδα συνδέεται μια προσθετική ομάδα για την επισήμανση με 18 F [93]. Σχήμα Α. 26: Δομή του α -(1-δεοξυ-D-φρουκτοζυλ)- ε -(2-[ 18 F]φλουοροπροπιόνυλ)-Lys 0 -Tyr 3 -octreotate [93] Συχνά χρησιμοποιούνται υδρόφιλα αμινοξέα ή πολυαιθυλενογλυκόλη (PEG Χ ) ως συνδέτες. Προσθήκη PEG 5 και PEG 10 σε ανάλογο της μπομπεσίνης (ΒΒΝ) Lys-BΒ είχε σαν αποτέλεσμα την παραλαβή δύο υδρόφιλων αναλόγων PEG χ -Lys-BΒ. Μελέτη βιοκατανομής των 99m Tc-Lys-BΒ, 99m Tc- PEG 5 -Lys-BΒ και 99m Tc- PEG 10 -Lys-BΒ σε άθυμα ποντίκια με καρκινικούς όγκους PC-3 έδειξε ταχύτερη απέκκριση του 99m Tc- PEG 10 -Lys-BΒ σε σχέση με το 99m Tc-Lys-BΒ από τα νεφρά και αυξημένη πρόσληψη του 99m Tc- PEG 5 -Lys-BΒ στον όγκο σε σχέση με το 99m Tc-Lys-BΒ [62]. 33
56 Α.2 Πεπτιδική σύνθεση Α.2 ΣΥΝΘΕΣΗ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ Α.2.1 ΕΙΣΑΓΩΓΗ Αρχικά τα πεπτίδια απομονώνονταν από φυσικούς πόρους, όμως οι ποσότητες που παραλαμβάνονταν δεν ήταν ικανοποιητικές [94]. Η ανάπτυξη της χημικής σύνθεσης των πεπτιδίων στις αρχές του 20ου αιώνα από τους Theodor Curtius και Emil Fischer έδωσε τη δυνατότητα παραλαβής πεπτιδίων σε επαρκή ποσότητα [95,96]. Επιπλέον, έγινε δυνατή η σύνθεση τροποποιημένων αναλόγων που δεν υπάρχουν στη φύση. Τα ανάλογα αυτά αποτέλεσαν σημαντικά εργαλεία για την ανάπτυξη φαρμάκων. Η σύνθεση πεπτιδίων γίνεται με τις εξής μεθόδους. α) Με τη μέθοδο σύνθεσης σε διάλυμα. Στην αρχή χρησιμοποιήθηκε η μέθοδος αυτή, αλλά για μεγάλου μήκους πεπτίδια είναι χρονοβόρα και επίπονη καθώς μετά από κάθε αντίδραση το προϊόν πρέπει να απομονωθεί και να καθαριστεί. β) Με τη μέθοδο σύνθεσης πεπτιδίων σε στερεή φάση. Η εισαγωγή της μεθόδου αυτής το 1963 από τον B. Merrifield ήταν ένα πολύ σημαντικό βήμα και επιτάχυνε την εξέλιξη της πεπτιδικής χημείας [97]. Για την ανοικοδόμηση της πεπτιδικής αλυσίδας σε στερεή φάση χρησιμοποιείται η στρατηγική σύνθεσης κατά στάδια (step by step) στην οποία η ανοικοδόμηση της πεπτιδικής αλυσίδας γίνεται με την προσθήκη ενός κατάλληλα προστατευμένου αμινοξέος σε κάθε βήμα. Στο εργαστήριο χρησιμοποιείται η πορεία επιμήκυνσης της πεπτιδικής αλυσίδας η οποία ξεκινά από το C τελικό άκρο. Η εν λόγω στρατηγική δεν ενδείκνυται για την σύνθεση μεγάλων πεπτιδίων και πρωτεϊνών λόγω της μικρής καθαρότητας του τελικού προϊόντος. γ) Με συνδυασμό σύνθεσης μικρών πεπτιδικών τμημάτων σε στερεή φάση (με τη στρατηγική σύνθεσης κατά στάδια) και συμπύκνωση των πεπτιδικών τμημάτων σε υγρή φάση (fragment condensation) δίνεται η δυνατότητα σύνθεσης μεγάλου μήκους πεπτιδίων σε μικρότερο χρονικό διάστημα, καθώς οι συνθέσεις των πεπτιδικών τμημάτων μπορούν να γίνουν ταυτόχρονα. Είναι σημαντικό τα πεπτιδικά τμήματα να περιέχουν στο C-τελικό αμινοξύ κατάλληλα αμινοξέα (Gly ή Pro) ώστε να αποφεύγεται η ρακεμίωση. 34
57 Α.2 Πεπτιδική σύνθεση Α.2.2 ΠΕΠΤΙΔΙΚΟΣ ΔΕΣΜΟΣ Ο σχηματισμός ενός πεπτιδικού δεσμού δημιουργείται με την αντίδραση της νουκλεόφιλης α-αμινομάδας ενός αμινοξέος και της α-καρβοξυλομάδας ενός άλλου αμινοξέος. Σχήμα Α. 27: Σχηματισμός πεπτιδικού δεσμού και διαστάσεις δεσμών τμήματος της πεπτιδικής αλυσίδας Ο πεπτιδικός δεσμός αποτελεί μια άκαμπτη και επίπεδη περιοχή του μορίου. Το υδρογόνο της αμινομάδας βρίσκεται συνήθως σε θέση trans ως προς το οξυγόνο του καρβονυλίου, ενώ η δομή cis είναι λιγότερο σταθερή λόγω στερεοχημικών παρεμποδίσεων. Με χρήση κρυσταλλογραφίας ακτίνων Χ οι Pauling και Corey ανακάλυψαν ότι δεν υπάρχει δυνατότητα περιστροφής γύρω από το δεσμό του καρβονυλικού ατόμου του άνθρακα και του αζώτου, τα οποία βρίσκονται στο ίδιο επίπεδο, καθώς ο δεσμός αυτός παίρνει το χαρακτήρα μερικού διπλού δεσμού [98,99]. Το μήκος του δεσμού είναι Å, μεταξύ δηλαδή ενός απλού C- (1.49 Å) και ενός διπλού C= (1.27 Å). Οι δεσμοί μεταξύ του α-άνθρακα και του ατόμου άνθρακα του καρβονυλίου και μεταξύ α-άνθρακα και του ατόμου του αζώτου του πεπτιδικού δεσμού είναι απλοί δεσμοί και μπορούν να περιστραφούν. Η αντίδραση σχηματισμού του πεπτιδικού δεσμού δεν ευνοείται θερμοδυναμικά. Συνεπώς η δημιουργία πεπτιδικού δεσμού δεν πραγματοποιείται αυθόρμητα και απαιτεί προσφορά ενέργειας. Γι αυτό και έχουν αναπτυχθεί πολλές μέθοδοι για την δημιουργία πεπτιδικού δεσμού με ενεργοποίηση της καρβοξυλομάδας του Ν α - προστατευμένου αμινοξέος ώστε να ευνοείται η πυρηνόφιλη προσβολή της αμινομάδας. Α.2.3 ΜΕΘΟΔΟΙ ΣΥΖΕΥΞΗΣ ΑΜΙΝΟΞΕΩΝ A ΜΕΘΟΔΟΣ ΑΖΙΔΙΩΝ. Η μέθοδος των αζιδίων πρωτοπαρουσιάστηκε στη πεπτιδική χημεία κατά το 1902 από το Curtius [96]. Για αρκετό καιρό η μέθοδος των 35
58 Α.2 Πεπτιδική σύνθεση αζιδίων θεωρούνταν η μοναδική με μικρά ποσοστά ρακεμίωσης. Αρχικά, τα Ν α - προστατευμένα αμινοξέα ή πεπτιδικά κλάσματα μετατρέπονται σε υδραζίδια και τελικά σε αζίδια, μετά από αντίδραση με νιτρώδη παράγωγα. Η αντίδραση των αζιδίων με την αμινομάδα του αμινο-συστατικού οδηγεί στο σχηματισμό του πεπτιδικού δεσμού. Σχήμα Α. 28: Σχηματισμός πεπτιδικού δεσμού με τη μέθοδο αζιδίων A ΜΕΘΟΔΟΣ ΑΝΥΔΡΙΤΩΝ. Το 1951 ο Theodor Wieland, βασιζόμενος στη θεωρία του Curtius, εισήγαγε για πρώτη φορά τη μέθοδο των μεικτών ανυδριτών για τη σύνθεση πεπτιδίων [100]. χρήση των απλών ή συμμετρικών ανυδριτών έχει συνδυαστεί κυρίως με τη Boc/Bzl μεθοδολογία. Μειονέκτημα της μεθόδου είναι ότι τα διαλύματα των ανυδριτών στις συγκεντρώσεις που απαιτούνται για την αντίδραση, έστω και αν φυλαχθούν σε παγωμένα δοχεία έως ότου αντιδράσουν, είτε καθιζάνουν είτε παίρνουν μια ζελατινώδη μορφή [101]. Οι μικτοί ανυδρίτες, χρησιμοποιούνται κυρίως στην σύνθεση πεπτιδίων σε υγρή φάση και παρασκευάζονται από το άλας του Ν α -προστατευμένου αμινοξέος με τριτοταγή βάση, σε θερμοκρασία υπό το μηδέν. πυρηνόφιλη προσβολή από το αμινοσυστατικό μπορεί να οδηγήσει σε δύο διαφορετικά προϊόντα. Για το λόγο αυτό, χρησιμοποιούνται οξέα με ογκώδεις αλκυλομάδες ή ισχυρούς ηλεκτρονιοδότες ώστε να διευκολύνεται η εκλεκτική προσβολή της καρβονυλομάδας του καρβοξυ-συστατικού. R 1 + R R 1 Cl _ R 2 2 R R 1 CR 2 + C 2 + R Σχήμα Α. 29: Αντίδραση σύζευξης με μικτούς καρβονικούς ανυδρίτες A ΜΕΘΟΔΟΣ ΕΝΕΡΓΩΝ ΕΣΤΕΡΩΝ. Οι Bodansky και Seeman ήταν οι πρώτοι που εφάρμοσαν τη μέθοδο των ενεργών εστέρων [102]. Απαιτεί περισσότερο χρόνο αντίδρασης σε σχέση με τις μεθόδους των συμμετρικών ανυδριτών και καρβοδιιμιδίων 36
59 Α.2 Πεπτιδική σύνθεση και χρησιμοποιείται μεγαλύτερη περίσσεια του Ν α -προστατευμένου αμινοξέος. Μεταξύ των άλλων τύπων εστέρων που χρησιμοποιούνται είναι και αυτοί του π- νιτροφαινυλεστέρων και οι εστέρες του Ν-υδροξυ-ηλεκτριμιδίου. Οι σημαντικότεροι ενεργοί εστέρες δίνονται παρακάτω στον πίνακα Α. 7. Πίνακας Α.7: Οι σημαντικότεροι ενεργοί εστέρες Όνομα (Σύντμηση) Χημικός Τύπος Όνομα (Σύντμηση) Χημικός Τύπος p-νιτροφαινυλεστέρες ΟΝp R C 2 Ν-υδροξυ-ηλεκτριμιδικοί εστέρες ΟΝSu R C 2,4,5-τριχλωροφαινυλεστέρες Tcp R C Cl Cl Cl 1-υδροξυβενζοτριαζολυλεστέρες Bt R C πενταχλωροφαινυλεστέρες Pcp R C Cl Cl Cl Cl Cl 1-υδροξυ-7-αζαβενζοτριαζολυλεστέρες At R C A ΜΕΘΟΔΟΣ ΚΑΡΒΟΔΙΙΜΙΔΙΩΝ. Ο σημαντικότερος εκπρόσωπος της κατηγορίας αυτής είναι το Ν,Ν-δικυκλοεξυλκαρβοδιιμίδιο (DCC) που χρησιμοποιήθηκε με επιτυχία κατά τη σύνθεση πεπτιδίων σε στερεά φάση [103]. Αρχικά σχηματίζεται ένα ενδιάμεσο, η Ο-ακυλισοουρία, ένα ισχυρό ακυλιωτικό μέσο, που μπορεί είτε να δημιουργήσει ενεργοποιημένα καρβοξυπαράγωγα είτε να υποστεί νουκλεόφιλη προσβολή προς δημιουργία του πεπτιδίου. Μειονέκτημα της μεθόδου αυτής είναι ο σχηματισμός της Ν-ακυλισοουρίας, που μειώνει την απόδοση και διαχωρίζεται δύσκολα από τα επιθυμητά προϊόντα. Το πρόβλημα αυτό καθώς και η ρακεμίωση του καρβοξυ-συστατικού περιορίζονται με τη χρήση νουκλεόφιλων, όπως το 1-υδροξυβενζοτριαζόλιο (Bt) [104]. Πρόβλημα αποτελεί επίσης ο σχηματισμός της δυσδιάλυτης Ν,Ν-δικυκλοεξυλουρίας (DCU), που διαχωρίζεται δύσκολα από το επιθυμητό προϊόν καθώς και η τοξικότητα του DCC. Για το λόγο αυτό χρησιμοποιείται το δϊισοπροπυλοκαρβοδιιμίδιο (DIC), του οποίου η ουρία είναι ευδιάλυτη στους διαλύτες που χρησιμοποιούνται κατά τις πλύσεις της ρητίνης. 37
60 Α.2 Πεπτιδική σύνθεση Τελευταία χρησιμοποιείται το 1-υδροξυ-7-αζαβενζοτριαζόλιο (At) [105] ως πρόσθετο αντιδραστήριο σύζευξης για υψηλότερες αποδόσεις και χαμηλότερα επίπεδα ρακεμίωσης. RC + C DCC R -Ακυλισoουρία C R -Ακυλουρία RC 2 R Bt R R 2 R 2 R R Bt + DCU + DCU R + R DCU Σχήμα Α. 30: Αντιδράσεις δημιουργίας πεπτιδικού δεσμού με χρήση DCC (Ίδια πορεία ισχύει και για το DIC). A ΦΩΣΦΟΝΙΚΑ ΚΑΙ ΟΥΡΟΝΙΚΑ ΠΑΡΑΓΩΓΑ. Τα τελευταία χρόνια αναπτύχθηκαν νέα αντιδραστήρια με δυνατότητα in situ δημιουργίας ενεργοποιημένων παραγώγων. Τα αντιδραστήρια αυτά αντιδρούν με καρβοξυλικά ανιόντα. Ως εκτούτου, είναι απαραίτητη η παρουσία βάσης στο μίγμα της αντίδρασης, όπως η δϊισοπροπυλαιθυλαμίνη (DIPEA) [106] ή κολλιδίνη [105]. Οι βασικές συνθήκες στις οποίες πραγματοποιείται η ενεργοποίηση και σύζευξη οδηγούν σε ταχύτατες συζεύξεις μεγαλύτερες από αυτές που παρατηρούνται σε συζεύξεις με DCC/Bt. Οι βασικές συνθήκες όμως αυξάνουν τον κίνδυνο ρακεμίωσης μέσω 5-(4Η)οξαζολόνης (αζλακτόνης). Πρόσθετα, για μείωση της ρακεμίωσης χρησιμοποιούνται Bt ή At τα οποία πρωτονιώνουν τη σχηματιζόμενη αζλακτόνη. Τα πιο σημαντικά από αυτά τα αντιδραστήρια σύζευξης δίνονται στον πίνακα που ακολουθεί. 38
61 Α.2 Πεπτιδική σύνθεση Πίνακας Α.8: Φωσφονικά και ουρονικά παράγωγα Όνομα (Σύντμηση) Χημικός Τύπος Εξαφθοροφωσφορικό άλας του βενζοτριαζολυλοξυ-τρις(διμεθυλαμινο)- φωσφονίου (ΒΟΡ) [107] Me 2 + P Me2 Me 2.PF 6 _ Εξαφθοροφωσφορικό άλας του βενζοτριαζολυλοξυ-τρις-πυρρολιδινοφωσφονίου (PyΒΟΡ) [108] + P _.PF 6 Εξαφωσφορικό άλας της 2-(1Η βενζοτριαζολυλ)-1,1,3,3- τετραμεθυλουρίας (ΗBTU) [109] Me 2 _ + C.PF 6 Me 2 Εξαφωσφορικό άλας της Ο-(7- αζαβενζοτριαζολυλ)-1,1,3,3- τετραμεθυλουρίας (ΗATU) [110] + C Me 2 _.PF 6 Me 2 Τετραφθοροβορικό άλας της 2-(1Η βενζοτριαζολυλ)-1,1,3,3- τετραμεθυλουρίας (ΤBTU) [109] + C Me 2 _.BF 4 Me 2 Α.2.4 ΡΑΚΕΜΙΩΣΗ Αποτελεί σημαντικό πρόβλημα κατά την ενεργοποίηση και τη σύζευξη αμινοξέος παρουσία βάσης. Ο διαχωρισμός των διαστερεοϊσομερών είναι δύσκολος και η απώλεια της οπτικής καθαρότητας μεταβάλλει τη βιολογική δράση του πεπτιδίου. Ο βαθμός της ρακεμίωσης εξαρτάται από μία σειρά παραγόντων, όπως τη μέθοδο ενεργοποίησης, τη χρησιμοποιούμενη Ν προστατευτική ομάδα και τις συνθήκες της αντίδρασης (θερμοκρασία, διαλύτη). Δύο βασικοί μηχανισμοί οδηγούν σε ρακεμίωση: Α) Απόσπαση του α-πρωτονίου προς σχηματισμό ενός καρβανιόντος (ενδιάμεσο), στο οποίο το α-άτομο άνθρακα επαναπροσλαμβάνει ένα πρωτόνιο χάνοντας την οπτική του καθαρότητα. B A- R C C-X -B -A R C C-X -B A- R C C-X Σχήμα Α. 31: Μηχανισμός ρακεμίωσης με απευθείας απόσπαση α-πρωτονίου. 39
62 Α.2 Πεπτιδική σύνθεση Β) Ο σχηματισμός αζλακτόνης. Ο μηχανισμός αυτός περιλαμβάνει το σχηματισμό ενδιάμεσου κυκλικού παραγώγου (αζλακτόνης), μέσω απόσπασης του όξινου πρωτονίου της προστατευμένης αμινομάδας υπό την επίδραση βάσης [111]. R X R' + L B R X R' L B - X R L R' B R R R B + + B R' R' R' L 2 R 2 D R' [D] + [ L] Σχήμα Α.32: Μηχανισμός ρακεμίωσης μέσω σχηματισμού αζλακτόνης Α.2.5 ΠΡΟΣΤΑΤΕΥΤΙΚΕΣ ΟΜΑΔΕΣ Ο Emil Ficher πιθανών να είναι ο πρώτος που αναγνώρισε τη αναγκαιότητα χρήσης προστατευτικών ομάδων στη πεπτιδική χημεία, αλλά η πρώτη προστατευτική ομάδα αναπτύχθηκε από τους Bergmann και Ζέρβα [112]. Η προστασία των πλευρικών ομάδων των αμινοξέων παίζει πολύ σημαντικό ρόλο επιτρέποντας τη σύνθεση μεγάλης καθαρότητας πεπτιδίων τα οποία διαφορετικά θα ήταν πολύ δύσκολο να συντεθούν. Τα χαρακτηριστικά που θα πρέπει να έχουν οι προστατευτικές ομάδες στη πεπτιδική σύνθεση είναι: Να εισάγονται εύκολα Να είναι σταθερές στις συνθήκες πεπτιδικής σύνθεσης Να ελαχιστοποιούν τη δραστικότητα της ομάδας που προστατεύουν Να μην ευνοούν τη ρακεμίωση του χειρόμορφου κέντρου του αμινοξέoς Να αυξάνουν τη διαλυτότητα των αμινοξέων ή των πεπτιδικών τμημάτων στους οργανικούς διαλύτες που χρησιμοποιούνται κατά τη διάρκεια της πεπτιδικής σύνθεσης Να απομακρύνονται εύκολα, γρήγορα, ποσοτικά και εκλεκτικά ανάλογα με το πεπτίδιο που θέλουμε να συνθέσουμε χωρίς την δημιουργία παραπροϊόντων. 40
63 Α.2 Πεπτιδική σύνθεση Α ΠΡΟΣΤΑΣΙΑ ΤΗΣ α-αμινομαδασ Η προστασία της α-αμινομάδας είναι πολύ σημαντική στην πεπτιδική σύνθεση και είναι υποχρεωτική για να αποτρέψει τον πολυμερισμό των αμινοξέων κατά την ενεργοποίησή τους. Επειδή στις περισσότερες των περιπτώσεων η σύνθεση γίνεται από το καρβoξυ- στο αμινο-τελικό άκρο είναι πολύ σημαντικό οι προσωρινές αμινοπροστατευτικές ομάδες να απομακρύνονται σε ήπιες συνθήκες και να μην επηρεάζουν τις πλάγιες ομάδες οι οποίες θα απομακρυνθούν στο τέλος της σύνθεσης. Οι Ν α -προστατευτικές ομάδες θα πρέπει να ελαττώνουν τον πυρηνόφιλο χαρακτήρα του αζώτου της αμινομάδας. Ομάδες που προτιμώνται για το σκοπό αυτό θα πρέπει να : α) μειώνουν την ηλεκτρονική πυκνότητα του αζώτου λόγω μεσομέρειας (π.χ. ουρεθανικού τύπου), ή μέσω επαγωγικού φαινομένου (π.χ. ο- νιτροφαινυλσουλφονυλομάδα) και β) μειώνουν τη δραστικότητα της αμινομάδας μέσω στερεοχημικής παρεμπόδισης (π.χ. τριφαινυλο-μεθυλ-ομάδα). Οι πιο σημαντικές προστατευτικές ομάδες που χρησιμοποιούνται για την προστασία της α-αμινομάδας είναι η τριτοταγής βουτυλοξυκαρβονυλομάδα (Boc) και η 9- φλουορενυλμεθοξυκαρβονυλομάδα (Fmoc). Η Boc ομάδα χρησιμοποιείται στην Boc/Bzl μεθοδολογία ενώ η Fmoc ομάδα χρησιμοποιείται στην Fmoc/tBu μεθοδολογία όπως αναπτύσσεται αναλυτικά στο Α.2.6. Χαρακτηριστικές αμινο-προστατευτικές ομάδες αναφέρονται στον Πίνακα Α. 9. Α ΠΡΟΣΤΑΣΙΑ ΚΑΡΒΟΞΥΛΟΜΑΔΑΣ Παρόλο που οι καρβοξυλομάδες των αμινοξέων δεν είναι τόσο δραστικά νουκλεόφιλα όσο οι αμινομάδες τους, η προστασία αυτών που δεν συμμετέχουν στο πεπτιδικό δεσμό γίνεται για αύξηση της διαλυτότητας σε οργανικούς διαλύτες, ευκολότερη απομόνωση των προϊόντων και ελαχιστοποίηση της ρακεμίωσης. Προστατεύονται με μετατροπή τους σε εστέρες. Σημαντική είναι η προστασία των πλευρικών καρβοξυλομάδων στα αμινοξέα Glu και Asp προς αποφυγή διακλαδισμένων πεπτιδίων-παραπροϊόντων. Οι κυριότερες καρβοξυ-προστατευτικές ομάδες είναι η τριτοταγής βουτυλ-ομάδα (tbu), η μεθυλ-ομάδα (Me), η αιθυλ-ομάδα (Et), και η 9- φλουορενυλ-μεθυλομάδα (Fm) (Πίνακας Α. 10). 41
64 Α.2 Πεπτιδική σύνθεση Πίνακας Α. 9: Μερικές αμινο-προστατευτικές ομάδες και οι συνθήκες απομάκρυνσής τους Όνομα (Σύντμηση) Χημικός Τύπος Αποπροστασία Σταθερότητα Βενζυλοξυκαρβονυλομάδα(Ζ-ομάδα) [112] Pd/ 2, Br/Cl Σε διοξάνη Βασικές συνθήκες, μερικώς όξινες Τριτοταγή βουτυλοξυκαρβονυλομάδα(boc-ομάδα) [113] 40% TFA, F Βασικές συνθήκες, καταλυτική υδρογόνωση 2-(π-Διφαινυλο)-2- προπυλοξυκαρβονυλομάδα(bpoc-ομάδα) [114] 1% TFA Βασικές συνθήκες 9-φλουρενυλομεθοξυκαρβονυλ-ομάδα (Fmocομάδα) [115,116] 4Ν Νa, 20-40% Piperidine/DMF Όξινες συνθήκες, καταλυτική υδρογόνωση Τριφαινυλομεθυλ-ομάδα ή τριτυλομάδα (Trt-ομάδα) [117,118] ~5% C 3C Βασικές συνθήκες Α ΠΡΟΣΤΑΣΙΑ ΠΛΕΥΡΙΚΩΝ ΟΜΑΔΩΝ Προστασία της Αργινίνης. Λόγω του ισχυρά βασικού και πυρηνόφιλου χαρακτήρα της η γουανιδινομάδα συνήθως προστατεύεται στο ένα άτομο αζώτου. Οι κυριότερες ομάδες που χρησιμοποιούνται για τη προστασία της γουανιδινομάδας είναι η 4- μεθυλοβενζυλσουλφoνυλομάδα (Tos), η 2,2,5,7,9-πενταμεθυλο-χρωμαν-6- σουλφονυλομάδα (Pmc) και η 2,2,4,6,7-πενταμεθυλο-διυδροβενζοφουρανο-5- σουλφονυλομάδα (Pbf). Προστασία της Ασπαραγίνης και της Γλουταμίνης. ι τρεις κύριες παράπλευρες αντιδράσεις που παρατηρούνται στη χρήση αυτών των αμινοξέων στη πεπτιδική χημεία είναι α) η αφυδάτωση του καρβαξαμιδίου κατά την διάρκεια της ενεργοποίησης της καρβοξυλομάδας με καρβοδιιμίδια και μετατροπής του σε νιτρίλιο β) η δημιουργία πυρογλουταμινικού οξέος (pglu) όταν η Gln είναι το Ν-τελικό αμινοξύ κατά την διάρκεια της τελικής αποπροστασίας σε όξινες συνθήκες και γ) η κυκλοποίηση της Asn ή της 42
65 Α.2 Πεπτιδική σύνθεση Gln (μίγμα α- και β- ασπαρτυλ- πεπτιδίων) η οποία μπορεί να συνοδεύεται και από υδρόλυση του πεπτιδικού δεσμού. Η τριφαινυλομεθυλομάδα (Trt) χρησιμοποιείται κατά κύριο λόγο καθώς απομακρύνεται εύκολα με τριφθοροξικό οξύ. Πίνακας Α. 10: Οι σημαντικότερες καρβοξυλο-προστατευτικές ομάδες Όνομα (Σύντμηση) Χημικός Τύπος Αποπροστασία Σταθερότητα Βενζυλ- (Bzl) Η 2/Pd, F, Br/Ac Βασικές, μερικώς όξινες συνθήκες Τριτοταγής βουτυλ- (tbu) TFA, ισχυρά οξέα Βασικές, όξινες συνθήκες, καταλυτική υδρογόνωση μεθυλ- (Me) Σαπωνοποίηση, Όξινες συνθήκες C 3 9-Φλουορενυλμεθυλομάδα (Fm ομάδα) 4Ν ΝaΗ, 20-40% Piperidine/DMF Όξινες συνθήκες, καταλυτική υδρογόνωση Πίνακας Α. 11: Μερικές προστατευτικές ομάδες της γουανιδομάδας της Arg Όνομα (Σύντμηση) Χημικός Τύπος Αποπροστασία 4-τολουολο-σουλφονυλο ομάδα (Tos) S F/ανισόλη, TFMSA/TFA/θειοανισόλη 2,2,5,7,8 πεντα-μεθυλχρωμαν- 6-σουλφονυλο ομάδα (Pmc) [119] 50%TFA/DCM TFA/Ανισόλη (9 / 1) S 2,2,4,6,7-πενταμεθυλο-διϋδροβενζοφουρανο-5-σουλφονυλο ομάδα (Pbf) [120] S TFA/DCM 43
66 Α.2 Πεπτιδική σύνθεση Προστασία του Ασπαραγινικού και του Γλουταμινικού οξεός. πλάγια καρβοξυλομάδα του ασπαραγινικού και του γλουταμινικού προστατεύονται με ομάδες όπως η -Bzl και η tbu στην Boc και στην Fmoc μεθοδολογία αντίστοιχα. Προστασία της Λυσίνης. Η πλευρική ε-αμινομάδα της Lys μπορεί να μετατραπεί σε ιμίνη με ισοδύναμη ποσότητα βενζαλδεΰδης παρουσία Li. Η ε-αμινομάδα της μπορεί να αντιδράσει με ενεργοποιημένα καρβοξυπαράγωγα, δίνοντας έτσι διακλαδισμένα πεπτίδια. Μια άλλη παράπλευρη αντίδραση που μπορεί να παρατηρηθεί, είναι η ενδομοριακή ακυλίωση κατά τη διάρκεια της ενεργοποίησης προς λακτάμη. Οι ομάδες που χρησιμοποιούνται πιο πολύ για τη πλευρική προστασία της Lys είναι οι 2-χλωρο-βενζυλοξυκαρβονυλ (2-Cl-Z), 4-μεθυλτριτυλ (Mtt) και η τριτοταγής βουτυλοξυ-καρβονυλομάδα (Βοc). Προστασία της Σερίνης, Θρεονίνης και Τυροσίνης. Οι πλευρικές υδροξυλομάδες των παραπάνω αμινοξέων είναι δυνατόν να υποστούν ακυλίωση στη περίπτωση που δεν χρησιμοποιηθεί προστασία, παρά το γεγονός ότι είναι ασθενέστερα πυρηνόφιλα σε σχέση με τις α-αμινομάδες τους. Η tbu-, η τριτυλομάδα (Trt) [121] και η χλωροτριτυλομάδα (Clt) [122] είναι αυτές που χρησιμοποιούνται περισσότερο για τη προστασία των πλευρικών ομάδων στην Fmoc-μεθοδολογία οι οποίες απομακρύνονται σε ήπια όξινες συνθήκες (TFA/DCM). Προστασία της Ιστιδίνης. Ο ιμιδαζολικός δακτύλιος της is πρέπει να προστατευθεί στη πεπτιδική σύνθεση. Μπορεί εύκολα να ακυλιωθεί από ενεργοποιημένα καρβοξυπαράγωγα και το π-άτομο αζώτου μπορεί να δώσει υψηλά ποσοστά ρακεμίωσης. Για την προστασία του ιμιδαζολίου στην Fmoc-χημεία χρησιμοποιούνται οι Trt-, Mmt- και Mtt- ομάδες οι οποίες φεύγουν με διάλυμα TFA σε DCM [122]. Προστασία της Τρυπτοφάνης. Ο ινδολικός δακτύλιος της Trp μπορεί εύκολα να οξειδωθεί κατά τη διάρκεια της σύνθεσης και να ακυλιωθεί από ηλεκτρόφιλα κατιόντα κατά την τελική αποπροστασία, με επίδραση οξέων. Για το λόγο αυτό προστατεύται με κατάλληλες ομάδες που απενεργοποιούν το αρωματικό δακτύλιο έλκοντας ηλεκτρόνια συνδεδεμένες με το άτομο του αζώτου του ινδολικού δακτυλίου. Στην Fmoc/tBu μεθοδολογία χρησιμοποιείται η Boc-ομάδα ως πιο αποτελεσματική για την πλευρική προστασία της Trp [ ]. Προστασία της Κυστεΐνης. Οι κυριότερες προστατευτικές ομάδες που χρησιμοποιούνται στην Fmoc-χημεία είναι οι tbu-, Trt-, Mmt- και Acm. Αν χρησιμοποιήσουμε την Acm ομάδα σε δύο Cys, η προσθήκη I 2 οδηγεί κατευθείαν στο κυκλικό πεπτίδιο με ταυτόχρονη αποπροστασία των Acm ομάδων [126,127]. Για την 44
67 Α.2 Πεπτιδική σύνθεση απομάκρυνση των Trt-, Mmt-, χρησιμοποιούνται διαλύματα TFA σε DCM. Στην αντίδραση αποπροστασίας είναι απαραίτητη η χρήση δεσμευτών κατιόντων για την αποφυγή επαναπροσβολής της θειολομάδας [128]. Πίνακας Α. 12: Μερικές προστατευτικές ομάδες για την Cys. Όνομα (Σύντμηση) Χημικός Τύπος Αποπροστασία Τριφαινυλομεθυλ-ομάδα ή τριτυλομάδα (Trt) [117,118] 90% v/v TFA, 30 min 4-μεθοξυ-τριτυλομάδα (Mmt) 0.5-1% TFA in DCM-TES (95:5), 30 min 3%v/v TFA, 5-10 min ακεταμιδο-μεθυλ-ομάδα (Acm) I 2 in Ac: 2 (4:1), g(iii), Ag(I),Tl(III) Α.2.6 ΣΥΝΘΕΣΗ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ ΣΕ ΣΤΕΡΕΗ ΦΑΣΗ Η μέθοδος της σύνθεσης σε στερεή φάση αποτελεί σταθμό στην πεπτιδική χημεία. Περιγράφηκε για πρώτη φορά από τον Merrifield το 1963 [97]. Αρχικά έχουμε ομοιοπολική δέσμευση του C-τελικού αμινοξέος σε μια χαρακτηριστική ομάδα ενός αδιάλυτου στερεού υποστρώματος (πολυμερές). Ο δεσμός αυτός πρέπει να είναι σταθερός στην διάρκεια των διεργασιών της σύνθεσης και να διασπάται στο τέλος σε συνθήκες που δεν επηρεάζουν την πεπτιδική αλυσίδα. Οι δραστικές ομάδες των αμινοξέων είναι προστατευμένες με ομάδες οι οποίες δεν επηρεάζονται από τις συνθήκες της αντίδρασης. Η προσωρινή προστατευτική ομάδα της α-αμινομάδας απομακρύνεται πριν την σύνδεση του επόμενου αμινοξέος. Στη συνέχεια έχουμε επαναλαμβανόμενες διεργασίες σύζευξης με το επόμενο αμινοξύ και απομάκρυνσης της Ν α -προστατευτικής του ομάδας. Οι πλύσεις σε κάθε κύκλο είναι αρκετές, ώστε να απομακρυνθούν με κατάλληλους διαλύτες οι περίσσειες αντιδρώντων και τυχόν παραπροϊόντα και για να προετοιμαστεί η ρητίνη για το επόμενο στάδιο. Η ευκολία, η ταχύτητα καθώς και ο αυτοματισμός της μεθόδου, οδήγησαν στην μεγάλη ανάπτυξη της τεχνικής αυτής. 45
68 Α.2 Πεπτιδική σύνθεση Μέθοδος Boc/Bzl. Μια από τις βασικές αρχές της μεθόδου περιλαμβάνει την σύνδεση του πρώτου αμινοξέος στο στερεό υπόστρωμα μέσω σχηματισμού βενζυλ-εστέρα. Ως προσωρινή προστατευτική ομάδα χρησιμοποιείται η τριτοταγής βουτυλοξυκαρβονυλομάδα (Boc). Η απομάκρυνσή της επιτυγχάνεται με χρήση τριφθοροξικού οξέος (TFA) ή με χρήση διαλύματος TFA σε διχλωρομεθάνιο (DCM) και είναι σταθερή σε βάσεις, νουκλεόφιλα και στη καταλυτική υδρογόνωση. Ως μόνιμες προστατευτικές ομάδες χρησιμοποιούνται ομάδες βενζυλ-τύπου όπως η βενζυλομάδα (Bzl). Η απομάκρυνση του πεπτιδίου από την ρητίνη καθώς και η απομάκρυνση των προστατευτικών ομάδων επιτυγχάνεται με χρήση άνυδρου υδροφθορίου (F). Η μέθοδος αυτή παρουσιάζει μειονεκτήματα τα οποία έχουν σχέση με την χρήση του τοξικού και ιδιαίτερα επικίνδυνου F, ενώ η παρασκευή προστατευμένων πεπτιδίων παρουσιάζει δυσκολίες και ιδιαιτερότητες. Η μέθοδος Boc/Bzl σήμερα βρίσκει περιορισμένη χρήση C Σχήμα Α. 33: Μηχανισμός απόσπασης της Βoc-ομάδας με επίδραση οξέων Μέθοδος Fmoc/tBu. Σε αντίθεση με την μέθοδο Boc/Bzl, η μέθοδος Fmoc/tBu έχει το πλεονέκτημα ότι η απομάκρυνση της Ν α -αμινο-προστατευτικής ομάδας γίνεται σε βασικές συνθήκες. Έτσι χρησιμοποιείται η ομάδα Fmoc [115,116], η οποία απομακρύνεται με διάλυμα 20% πιπεριδίνης σε διμεθυλοφορμαμίδιο (DMF). - + C 2 2 C C 2 2 Σχήμα Α. 34: Μηχανισμός απόσπασης της Fmoc-ομάδας με πιπεριδίνη. 46
69 Α.2 Πεπτιδική σύνθεση Τόσο οι ρητίνες όσο και οι πλάγιες προστατευτικές ομάδες που χρησιμοποιούνται είναι ευαίσθητες έναντι των οξέων και μάλιστα σε ηπιότερες συνθήκες (TFA) σε σχέση με την μέθοδο Boc/Bzl. Η απόσπαση του πεπτιδίου από το στερεό υπόστρωμα καθώς και η πλήρης απομάκρυνση των προστατευτικών ομάδων επιτυγχάνεται με TFA. Η μέθοδος Fmoc/tBu λόγω των πλεονεκτημάτων της προτιμάται έναντι της μεθόδου Boc/Bzl. Α ΤΟ ΣΤΕΡΕΟ ΥΠΟΣΤΡΩΜΑ Το στερεό υπόστρωμα παίζει σπουδαίο ρόλο στην επιτυχία της μεθόδου σύνθεσης σε στερεή φάση. Βασικά κριτήρια που καθορίζουν την καταλληλότητα του υποστρώματος, όπως η μηχανική αντοχή και η καλή διόγκωση σε διαλύτες που χρησιμοποιούνται ευρέως στην πεπτιδική σύνθεση. Σε ένα καλά διογκωμένο πολυμερές τα αντιδραστήρια διαχέονται στο εσωτερικό του επιτυγχάνοντας τοπικά υψηλές συγκεντρώσεις που εξασφαλίζουν την πρόοδο των αντιδράσεων και μάλιστα με μεγάλες ταχύτητες. Το επικρατέστερο πολυμερές που χρησιμοποιείται στην πεπτιδική σύνθεση είναι ένα συμπολυμερές πολυστυρολίου και διβινυλοβενζολίου (PS-DVB). Το ποσοστό του διβινυλοβενζολίου (DVB) για καλύτερη δράση είναι 1%. Κάθε πολυμερές έχει συνδεδεμένη μια χαρακτηριστική ομάδα ρητίνης που τη διαφοροποιεί από όλες τις υπόλοιπες. Πρόκειται για τη δραστική ομάδα η οποία, με τις κατάλληλες αντιδράσεις, συνδέεται με την καρβοξυλομάδα του αμινοξέος για τη σύνθεση του πεπτιδίου. Πίνακας Α. 13: Ρητίνες που χρησιμοποιούνται στην πεπτιδική σύνθεση σε στερεή φάση Όνομα (Σύντμηση) Χημικός Τύπος Αποπροστασία CLTR-Cl [ ] Cl Cl 1% TFA/DCM Wang [132] TFA (50-100%) MBA [133] Fmoc F/TMFSA 47
70 Α.2 Πεπτιδική σύνθεση Μια από τις πιο σημαντικές ρητίνες αυτές είναι η 2-χλωροτριτυλοχλωριδιο-ρητίνη (CLTR-Cl), η οποία συνδυάζεται με την μεθοδολογία Fmoc-tBu και μπορεί να οδηγήσει στη σύνθεση πεπτιδίων με μεγάλη απόδοση και υψηλή καθαρότητα [ ]. Α ΣΥΖΕΥΞΗ ΑΜΙΝΟΞΕΩΝ ΣΕ ΣΤΕΡΕΗ ΦΑΣΗ ΕΠΙΜΗΚΥΝΣΗ ΠΕΠΤΙΔΙΚΗΣ ΑΛΥΣΙΔΑΣ Η πρόσδεση του πρώτου αμινοξέος στο πολυμερές γίνεται με αντίδραση της καρβοξυλομάδας του αμινοξέος με τη δραστική ομάδα του πολυμερούς ή με μια ενδιάμεση ομάδα που παίζει το ρόλο του συνδέσμου (linker) για σχηματισμό πεπτιδίων αμιδίων. Όλες οι ρητίνες που χρησιμοποιούνται στη στερεή φάση διαθέτουν ως δραστική ομάδα ένα αλογόνο (κυρίως Cl) ή μια υδροξυλομάδα. Mε τη χρήση της ρητίνης CLTR-Cl, η εστεροποίηση πραγματοποιείται με απ ευθείας αντίδραση του Ν α -Fmoc προστατευμένου αμινοξέος πάνω στο πολυμερές παρουσία DIPEA. To ποσοστό υποκατάστασης του πολυμερούς εξαρτάται από την ποσότητα του αντιδρώντος αμινοξέος και πρέπει να είναι ανάλογο του μεγέθους του παρασκευαζόμενου πεπτιδίου. Για την σύνθεση μικρών πεπτιδίων (<15 αμινοξέα), επιλέγονται μεγάλες υποκαταστάσεις (>0,5 mmol/g), ενώ στη σύνθεση μεγάλων πεπτιδίων (>15 αμινοξέα) επιλέγονται μικρές υποκαταστάσεις (<0,5 mmol/g), γιατί καθώς αυξάνεται το μήκος της πεπτιδικής αλυσίδας αυξάνεται και η στερεοχημική παρεμπόδιση των συνθετικών διεργασιών. Κατά την επιμήκυνση της πεπτιδικής αλυσίδας απομακρύνεται η Ν α -προστατευτική ομάδα του C-τελικού αμινοξέος και ακολουθούν διαδοχικοί κύκλοι σύζευξηςαποπροστασίας, μέχρι να συντεθεί το τελικό πεπτίδιο. Μια σημαντική παράπλευρη αντίδραση πραγματοποιείται κατά την προσθήκη του τρίτου αμινοξέος σε ένα διπεπτίδιο. Οι εστέρες των διπεπτιδίων υφίστανται αυθόρμητη κυκλοποίηση και παράγουν 2,5 δικετοπιπεραζίνες με αποτέλεσμα την απομάκρυνση του πεπτιδίου από την ρητίνη. Ο σχηματισμός δικετοπιπεραζίνης εμφανίζεται πιο συχνά σε πεπτίδια που το C-τελικό άκρο τους είναι η Pro λόγω της διαμόρφωσης που παίρνει κατά τη σύνδεση με το υπόστρωμα. Ωστόσο ο κίνδυνος μειώνεται αισθητά με τη χρήση ρητινών τύπου τριτυλ (στερεοχημική παρεμπόδιση). 48
71 Α.2 Πεπτιδική σύνθεση 2 R 1 + R 1 R 2 R 2 Σχήμα Α. 35: Μηχανισμός σχηματισμού δικετοπιπεραζινών Μετά την ολοκλήρωση της σύνθεσης της πεπτιδικής αλληλουχίας πραγματοποιείται η σύζευξη του προστατευμένου υποκαταστάτη DTA-tris(tBu)ester. Συνήθως για τη σύζευξη του DTA-tris(tBu)ester χρησιμοποιούνται τα αντιδραστήρια ATU, DIPEA ή DIC, Bt και ακολουθεί η απομάκρυνση του πεπτιδικού αναλόγου από τη ρητίνη και τις πλάγιες προστατευτικές ομάδες. Α ΑΠΟΜΑΚΡΥΝΣΗ ΠΕΠΤΙΔΙΚΟΥ ΑΝΑΛΟΓΟΥ ΑΠΟ ΤΗ ΡΗΤΙΝΗ ΚΑΙ ΤΙΣ ΠΛΑΓΙΕΣ ΠΡΟΣΤΑΤΕΥΤΙΚΕΣ ΟΜΑΔΕΣ Μόλις η σύνθεση ολοκληρωθεί απομακρύνουμε το πεπτίδιο από το στερεό υπόστρωμα με επίδραση οξέος. Το είδος της ρητίνης είναι αυτό που καθορίζει και το οξύ το οποίο θα χρησιμοποιηθεί. Κατά τη διαδικασία απομάκρυνσης των πλάγιων προστατευτικών ομάδων σε όξινες συνθήκες λόγω της δημιουργίας κατιόντων απαιτείται η χρήση δεσμευτών κατιόντων (cation scavengers). Οι ενώσεις αυτές δεσμεύουν τα παραγόμενα κατιόντα τα οποία μπορούν να δημιουργήσουν παραπροϊόντα με επίπτωση στην απόδοση και την καθαρότητα των προϊόντων. Χαρακτηριστικά παραδείγματα δεσμευτών κατιόντων είναι η ανισόλη, η θειοανισόλη [134], το διμεθυλοσουλφίδιο [135], το αιθυλομεθυλοσουλφίδιο [135], η 2-μερκαπτοαιθανόλη [136], η 1,2-αιθανοδιθειόλη [137], η διθειοθρεϊτόλη [138], η 2-μερκαπτοπυριδίνη [139], η π-κρεζόλη και π-θειοκρεζόλη [140], ενώ η προσθήκη νερού στο διάλυμα έχει αποδειχθεί ότι είναι πολλές φορές χρήσιμη [141]. Η επιλογή του μίγματος δεσμευτών εξαρτάται από τα αμινοξέα που απαρτίζουν το πεπτίδιο και τις προστατευτικές του ομάδες. Α ΣΧΗΜΑΤΙΣΜΟΣ ΔΙΣΟΥΛΦΙΔΙΚΟΥ ΔΕΣΜΟΥ Οι δισουλφιδικοί δεσμοί οι οποίοι δημιουργούνται μέσω οξείδωσης δύο θειολομάδων συχνά απαντώνται σε πεπτίδια και πρωτεΐνες στη φύση. Όπως έχει παρατηρηθεί, οι δεσμοί αυτοί χρησιμεύουν στον σχηματισμό και σταθεροποίηση τρισδιάστατων δομών 49
72 Α.2 Πεπτιδική σύνθεση πρωτεϊνών και πεπτιδίων. Η δημιουργία δισουλφιδικού δεσμού μπορεί να γίνει με πολλές διαφορετικές μεθόδους : Οξείδωση από τον αέρα. Είναι από τις πιο εύκολες μεθόδους. Πραγματοποιείται σε ατμοσφαιρικό αέρα και το πεπτίδιο πρέπει να είναι διαλυμένο με μεγάλη αραίωση και σε ελαφρώς αλκαλικές συνθήκες. Τα μειονεκτήματα της μεθόδου είναι ο πιθανός διμερισμός και η μεγάλη διάρκεια για την ολοκλήρωση της αντίδρασης [142]. Οξείδωση με ιώδιο σε διάλυμα Ac. Είναι πολύ γρήγορη και εύκολη μέθοδος. Χρησιμοποιείται κυρίως με τις προστατευτικές ομάδες Trt, Mmt και Acm. Ιδιαίτερη προσοχή χρειάζεται όταν το πεπτίδιο περιέχει ευοξείδωτα αμινοξέα όπως Met και Trp. Γι αυτό απαιτούνται συνεχείς έλεγχοι για την πορεία της αντίδρασης [126,127,143] Χρήση υδατικού διαλύματος DMS (20% (v/v)). Η μέθοδος αυτή χρησιμοποιείται αρκετά συχνά. Το DMS διαλύεται σε νερό μέχρι 20% (v/v). Βασικό μειονέκτημα είναι η δύσκολη απομάκρυνση του DMS. [144,145] Οξείδωση με DMS σε ελαφρά βασικές συνθήκες. Χρησιμοποιείται εναλλακτικά με την προηγούμενη μέθοδο καθώς προστίθεται μόνο 1% (v/v) DMS στο φωσφορικό ρυθμιστικό διάλυμα (p 7.5) στο οποίο έχουμε διαλύσει το πεπτίδιο [146]. Οξείδωση με διάλυμα τριφθοροξικού θαλίου. Η οξείδωση με τριφθοροξικό θάλιο είναι ήπια και δίνει καλές αποδόσεις. Αν το πεπτίδιο περιέχει Met και Trp θα πρέπει να είναι προστατευμένες κατά την οξείδωση αυτή. Ο κύριος περιορισμός αυτής της μεθόδου είναι η υψηλή τοξικότητα του αντιδραστηρίου [147]. Για τη δημιουργία δύο δισουλφιδικών δεσμών μπορεί να γίνει συνδυασμός της Acm ομάδας (για τις δύο Cys) και της Trt ή Mmt ομάδας (για τις άλλες δύο Cys). Η Acm ομάδα είναι σταθερή σε όξινες συνθήκες στις οποίες απομακρύνονται οι Trt και Mmt ομάδες. Έτσι μπορεί να γίνει επιλεκτική αποπροστασία ανά δύο Cys και συνδυάζοντας δύο από τις παραπάνω μεθόδους (π.χ. οξείδωση με DMS σε ελαφρά βασικές συνθήκες για τις Cys που προστατεύονται με Trt ή Mmt ομάδες και οξείδωση με ιώδιο σε διάλυμα Ac για τις Cys που προστατεύονται με Acm ομάδες) ώστε να παραλάβουμε το επιθυμητό δικυκλικό πεπτίδιο. Α ΚΑΘΑΡΙΣΜΟΣ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ Η απομόνωση του πεπτιδίου από τα παραπροϊόντα (καθαρισμός) πραγματοποιείται με τη χρήση χρωματογραφίας υψηλής αποδόσης ανάστροφης φάσης (RP-PLC). Στην RP-PLC το υλικό πλήρωσης των στηλών είναι silica, όπου αλκυλομάδες είναι 50
73 Α.2 Πεπτιδική σύνθεση ομοιοπολικά συνδεδεμένες στις ομάδες σιλανόλης στην επιφάνειά της. Όσο μεγαλύτερη είναι η αλκυλομάδα που δεσμεύεται στην επιφάνεια της στατικής φάσης τόσο αυξάνεται η υδροφοβικότητά της. Οι στήλες που χρησιμοποιούνται στην RP- PLC είναι C8 - C18, ανάλογα με τον μήκος της αλυσίδας των αλκυλίων που προστίθενται στη silica. Ένα από τα πλεονεκτήματα της είναι η σχετική αδράνεια των σωματιδίων της silica και έτσι οι μόνες αλληλεπιδράσεις είναι αυτές μεταξύ της ουσίας και των ομοιοπολικά συνδεδεμένων υδρόφοβων, αλκυλικών αλυσίδων. Στην RP-PLC χρησιμοποιούμε μίγμα διαλυτών (πολικός/άπολος), οι οποίοι πρέπει να αναμιγνύονται πλήρως και να μην απορροφούν στο UV. Συνήθως ως πολικός διαλύτης χρησιμοποιείται το Η 2 Ο και ως άπολοι οι διαλύτες ακετονιτρίλιο (C 3 C), μεθανόλη (Me), τετραϋδροφουράνιο (TF), προπανόλη (Pr) ή ισοπροπανόλη (ipr). Για τον καθαρισμό πεπτιδίων χρησιμοποιείται μεταβαλλόμενη σύσταση διαλυτών Η 2 Ο και C 3 C (gradient separation). Όσο μειώνεται η πολικότητα της κινητής φάσης αυξάνει η ισχύς της έκλουσης και ελαττώνεται η συγκράτηση στην στατική φάση. 51
74 Α.3 Σωματοστατίνη Α.3 ΣΩΜΑΤΟΣΤΑΤΙΝΗ Α.3.1 ΣΩΜΑΤΟΣΤΑΤΙΝΗ Η σωματοστατίνη (SS) απομονώθηκε για πρώτη φορά από τον υποθάλαμο προβάτου. Η SS χαρακτηρίστηκε ως αναστολέας της έκκρισης της αυξητικής ορμόνης από την υπόφυση από τον Brazeau και τους συνεργάτες του το 1973 [148]. Υπάρχουν δύο ενδογενείς βιοδραστικές μορφές σωματοστατίνης, η σωματοστατίνη 14 (SS14) και η σωματοστατίνη 28 (SS28). Η SS28 περιέχει ολόκληρη την ακολουθία της SS14 στο καρβοξυτελικό τμήμα της, αμέσως μετά από ένα διπλό ζευγάρι βασικών αμινοξέων Arg 13 -Lys 14 [149]. Σχήμα Α. 36: Η αλληλουχία των SS14 και SS28 Και οι δύο μορφές της σωματοστατίνης στα θηλαστικά προέρχονται από ένα μεγαλύτερο ανενεργό πρόδρομο μόριο, την προπροσωματοστατίνη (preprosomatostatin ή PPSST, 116 ΑΑ), από το οποίο με ενδοπρωτεόλυση προκύπτει η προσωματοστατίνη (prosomatostatin ή PSST, 96 ΑΑ). Στη συνέχεια η PSST ενδοπρωτεολύεται και προκύπτουν τα εν λόγω δραστικά πολυπεπτίδια SS14 και SS28 (Σχήμα Α. 37). Η SS14 παράγεται με ενδοπρωτεόλυση (με αναγνώριση του διπεπτιδίου Arg 13 -Lys 14 της SS28), ενώ με ενδοπρωτεόλυση στο αμινοξύ Arg 90 της PPSST παράγεται η SS-28 [150,151]. 52
75 Α.3 Σωματοστατίνη Σχήμα Α. 37: Το πρόδρομο μόριο PPSST από το οποίο παράγονται οι SS14 και SS28 Επιπλέον η SS14 αποικοδομείται με τη δράση ενδοπεπτιδασών, π.χ. EC και EC , προς μικρότερα αδρανή πεπτίδια [152]. Οι SS14 και SS28 είναι τα μόνα γνωστά βιοενεργά μεταβολικά προϊόντα [153]. Σχήμα Α. 38: Θέσεις αποικοδόμησης της SS14 από τις ενδοπεπτιδάσες Η σωματοστατίνη απαντάται σε μεγάλη πυκνότητα στο κεντρικό και περιφερικό νευρικό σύστημα, στο πάγκρεας και στα έντερα, και λιγότερο στο θυρεοειδή, τα επινεφρίδια, τα νεφρά και τον προστάτη [ ]. Οι βιολογικές δράσεις της SS και των αναλόγων της εκδηλώνονται μετά από αλληλεπίδραση με τους υποδοχείς της (sst 1-5 ). Μετά τη δέσμευση της SS ή αναλόγων της στους sst 1-5, ενεργοποιούνται οι G- πρωτεΐνες και ακολουθεί η μεταγωγή σήματος μέσω διαφόρων μονοπατιών (αναλυτικά στο Α.1.2). 53
76 Α.3 Σωματοστατίνη Σχήμα Α. 39: Ο υπότυπος sst 2A του υποδοχέα της SS [47] Ο κυριότερος ρόλος της σωματοστατίνης είναι η αναστολή της G από τον πρόσθιο λοβό της υπόφυσης [160]. Η σωματοστατίνη αναστέλλει την έκκριση της αυξητικής ορμόνης απευθείας με αλληλεπίδραση στην υπόφυση και έμμεσα μέσω της καταστολής της απελευθέρωσης της GR (Growth hormone-releasing hormone) [162,163]. Επιπλέον, η λειτουργία της σωματοστατίνης ως νευροδιαβιβαστή στον εγκέφαλο έχει επίδραση στις γνωστικές, κινητικές, αισθητηριακές και αυτόνομες λειτουργίες [158, ]. Η ανασταλτική δράση της σωματοστατίνης επεκτείνεται στην αναστολή έκκρισης μεγάλου αριθμού ορμονών, όπως της ντοπαμίνης, της ινσουλίνης, του γλυκαγόνου, της νορεπινεφρίνης καθώς και την αναστολή της δικής της έκκρισης από τον υποθάλαμο. Όταν η σωματοστατίνη συντίθεται και απελευθερώνεται από τα δ-κύτταρα των παγκρεατικών νησιδίων, προκαλεί καταστολή της σύνθεσης και της έκκρισης της ινσουλίνης και του γλυκαγόνου [ ]. Στο γαστρεντερικό σωλήνα σχεδόν κάθε ορμόνη του εντέρου έχει αποδειχθεί ότι αναστέλλεται από την σωματοστατίνη, όπως το γαστρικό οξύ, η πεψίνη και η χολή. Η σωματοστατίνη έχει άμεση επίπτωση στο θυρεοειδή, αναστέλλοντας την απελευθέρωση των Τ3, Τ4 και της καλσιτονίνης. Σε αντίθεση, η σωματοστατίνη δεν έχει επίδραση στην απελευθέρωση της ωχρινοτρόπου ορμόνης, της ωοθυλακιοτρόπου ορμόνης, της προλακτίνης ή της κορτικοτροπίνης των επινεφριδίων υπό φυσιολογικές συνθήκες. 54
77 Α.3 Σωματοστατίνη Σχήμα Α. 40: Βιολογικές δράσεις της SS [48] Ιδιαίτερα σημαντικό είναι το γεγονός ότι η ανασταλτική δράση της SS επεκτείνεται και στα καρκινικά κύτταρα. Η αντινεοπλασματική δράση της πραγματοποιείται με άμεσους ή με έμμεσους μηχανισμούς. Η SS αναστέλλει την έκκριση παραγόντων που ευνοούν την κυτταρική ανάπτυξη (π.χ. αναστολή της επαγόμενης από τη G παραγωγή του IGF-1) και την αγγειογένεση. Επιπλέον, ασκεί άμεση αναστολή του κυτταρικού πολλαπλασιασμού με μηχανισμούς παύσης της κυτταρικής ανάπτυξης ή με μηχανισμούς που οδηγούν στην απόπτωση [ ]. Σχήμα Α. 41: Αντινεοπλασματική δράση της SS [ 55
78 Α.3 Σωματοστατίνη Πολλοί ασθενείς με ETs υποφέρουν από συμπτώματα τα οποία επάγονται από ορμόνες που παράγονται και απελευθερώνονται μαζικά από τα καρκινικά κύτταρα. Για ορισμένους ασθενείς, τα συμπτώματα αυτά μπορεί να απειλούν ακόμα και τη ζωή τους, όπως ασθενείς με καρκινοειδές του μεσεντερίου που πάσχουν από κρίσεις με εκτεταμένες εξάψεις και υπόταση, ασθενείς με σοβαρή διάρροια που προκαλείται από όγκους που παράγουν το αγγειοδραστικό εντερικό πολυπεπτίδιο (VIP) ή ασθενείς με ινσουλινώματα, στους οποίους λόγω υπερέκκρισης ινσουλίνης προκαλείται υπογλυκαιμία έως και υπογλυκαιμικό σοκ. Σε άλλους ασθενείς τα συμπτώματα επηρεάζουν την ικανότητα τους να πραγματοποιούν απλές καθημερινές δραστηριότητες. Οι υποδοχείς της SS (sst 1-5 ) και ιδιαίτερα ο sst 2, εκφράζονται σε υψηλή πυκνότητα στους ETs, συμπεριλαμβανομένων των GEP-ETs (Σχήμα Α.Χ) (αναλυτικά Α.1.2). Σχήμα Α. 42 Έκφραση υποδοχέων sst 2Α στην κυτταρική μεμβράνη καρκινοειδούς και σωματοστατινώματος (μέθοδος ανοσοφθορισμού). [Liu Q, Reubi JC, Wang Y, Knoll BJ, Schonbrunn A. (2003) In vivo phosphorylation of the somatostatin 2A receptor in human tumors. J Clin Endocrinol Metab.88(12): ] Η εισαγωγή αναλόγων της SS (π.χ. octreotide, LAR) στη θεραπεία των περισσοτέρων από αυτά τα ορμονοεξαρτώμενα συμπτώματα κατέστησε δυνατό τον περιορισμό τους και έχει βελτιώσει σημαντικά την ποιότητα ζωής των ασθενών [176]. Παράλληλα η χορήγηση αναλόγων SS αναστέλλει ή σταθεροποιεί την ανάπτυξη των όγκων, όπως προείπαμε. Α.3.2 ΑΝΑΛΟΓΑ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ Η SS14 έχει χρόνο ημιζωής στο πλάσμα του αίματος <3 min λόγω της αποικοδόμησης της στους δεσμούς μεταξύ των αμινοξέων Ala 1 -Gly 2, Gly 2 -Cys 3, Phe 6 -Phe 7, Trp 8 -Lys 9 και Thr 10 -Phe 11 (Σχήμα Α. 38), γεγονός που περιορίζει την κλινική της χρήση. Ως εκτούτου κατέστη αναγκαία η ανάπτυξη μεταβολικά σταθεροποιημένων αναλόγων της SS14 με βελτιωμένες φαρμακοκινητκές ιδιότητες με σκοπό την εφαρμογή στην κλινική πράξη. 56
79 Α.3 Σωματοστατίνη Η μελέτη γραμμικών ανάλογων της SS14 έδειξε την μειωμένη δράση τους στην αναστολή έκκρισης της G in vitro σε σχέση με την SS14, καθιστώντας σαφές πόσο σημαντικό ρόλο παίζει ο δισουλφιδικός δεσμός στη βιολογική δράση των αναλόγων SS [177,178]. Συστηματική αντικατάσταση L-αμινοξέων της SS14 από τα D-ισομερή τους έδειξε ότι η αντικατάσταση της LTrp 8 με DTrp 8 αύξησε τη δραστικότητα του αναλόγου 8 φορές, ενώ αντικατάσταση της LCys 14 με DCys 14 αύξησε τη δραστικότητα του αναλόγου ~3 φορές ως προς την αναστολή έκκρισης της G in vitro σε σχέση με την SS14. Η αντικατάσταση της LTrp 8 με DTrp 8 θεωρείται πολύ σημαντική γι αυτό και διατηρείται στα περισσότερα ανάλογα της SS14 [179,180]. Συστηματική αντικατάσταση αμινοξέων της SS14 με Ala επέδειξε ποια αμινοξέα είναι σημαντικά για την εκδήλωση βιολογικής δράσης των αναλόγων της SS14. Αντικατάσταση των αμινοξέων Phe 6, Phe 7, Trp 8, Lys 9 και Phe 11 με Ala είχε ως αποτέλεσμα τη δραματική μείωση της ανασταλτικής τους δράσης στην έκκρισης της G in vitro σε σχέση με την SS14 [179]. Επιπλέον, με σταδιακή και επιλεκτική μείωση αμινοξέων της πεπτιδικής αλυσίδας της SS14 διαπιστώθηκε ότι το κυκλικό εξαπεπτίδιο c(cys-phe-dtrp-lys-thr-cys) είναι το μικρότερο πεπτιδικό ανάλογο της SS14 που έχει ανασταλτική δράση στην έκκριση της G in vitro [178,179]. Μετά από διαμορφωτικές μελέτες MR αποδείχθηκε ότι η αλληλουχία Phe 7 -Trp 8 -Lys 9 -Thr 10 είναι η φαρμακοφόρος ομάδα. Γι αυτό το λόγο η αλληλουχία αυτή, και μάλιστα με DTrp 8, διατηρήθηκε στα περισσότερα συνθετικά ανάλογα SS14 [181,182]. Το octreotide ή SMS (DPhe 1 -c(cys 2 -Phe 3 -DTrp 4 -Lys 5 -Thr 6 -Cys 7 )-Thr(ol) 8 ) είναι ένα κυκλικό οκταπεπτιδικό ανάλογο της SS14 το οποίο φέρει την φαρμακοφόρο ομάδα στην πεπτιδική του αλληλουχία. Αντικατάσταση της LTrp 4 με DTrp 4 προσέδωσε σταθερότητα στη β-στροφή του αναλόγου, ενώ η προσθήκη DPhe 1 στο Ν-τελικό του άκρο και η αναγωγή της Thr στο C-τελικό άκρο σε αλκόολη Thr(ol) 8 (Σχήμα Α. 44) αύξησαν τη μεταβολική σταθερότητα του αναλόγου. To octreotide επέδειξε μεγαλύτερη δραστικότητα ως προς την αναστολή έκκρισης της G in vitro (70 φορές πιο δραστικό), μεγαλύτερη μεταβολική σταθερότητα με χρόνο ημιζωής (t 1/2 = 90 min στο πλάσμα του αίματος) σε σχέση με την SS14. Επίσης παρουσιάζει πολύ υψηλή συγγένεια δέσμευσης για τον sst 2 και μικρότερη για τους sst 3 και sst 5 σε αντίθεση με την SS14 που έχει υψηλή συγγένεια δέσμευσης και για τους πέντε sst 1-5 [ ]. Το octreotide (εμπορικό όνομα Sandostatin ) βρήκε εφαρμογή στην κλινική πράξη στη θεραπεία της μεγαλακρίας (ελέγχοντας την υπερέκκριση της G από αδενώματα της υπόφυσης). 57
80 Α.3 Σωματοστατίνη Επίσης ήταν αποτελεσματικό στη μείωση των συμπτωμάτων που επάγονται από ορμόνες οι οποίες παράγονται και απελευθερώνονται από τα καρκινικά κύτταρα των GEP-ETs (βελτίωση ποιότητας ζωής στους ασθενείς) [185]. Το octreotide LAR (Sandostatin LAR ) είναι μια φαρμακοτεχνική μορφή του octreotide (Σχήμα Α. 43) βραδείας απελευθέρωσης (χορήγηση 1 φορά το μήνα ενδομυϊκά) για τη θεραπεία της μεγαλακρίας. Η χορήγηση του octreotide LAR σε ασθενείς με μεγαλακρία μειώνει τα επιπέδα της αυξητικής ορμόνης (σταθερή και διαρκής μείωση), βελτιώνει την εμφάνιση του προσώπου, μειώνει ή εξαλείφει τη συχνότητα εμφάνισης συμπτωμάτων όπως πονοκέφαλο, κόπωση, αρθραλγία και υπερβολική εφίδρωση και ορισμένες φορές οδηγεί σε συρρίκνωση του όγκου [186,187]. Σχήμα Α. 43: Sandostatin LAR [ Αντικατάσταση της Phe 3 με Tyr 3 και της Thr(ol) 8 με Thr 8 στο octreotide οδήγησε στο ανάλογο [Tyr 3 ]octreotate (TATE, DPhe 1 -c(cys 2 -Tyr 3 -DTrp 4 -Lys 5 -Thr 6 -Cys 7 )-Thr 8 -) το οποίο παρουσίασε υψηλή και επιλεκτική συγγένεια δέσμευσης για τον sst 2 (μεγαλύτερη από το octreotide) [188]. Εκτός από το octreotide αναπτύχθηκαν και άλλα κυκλικά οκταπεπτίδια όπως το lanreotide ή BIM (Somatuline LA, D-β-al-c(Cys-Tyr-DTrp Lys-Val-Cys)-Thr- 2 ) και το vapreotide (RC160, DPhe-c(Cys-Tyr-DTrp-Lys-Val-Cys)-Trp- 2 ). Τα δύο αυτά ανάλογα παρουσίασαν υψηλή συγγένεια δέσμευσης για τους sst 2 και sst 5 και χαμηλότερη για τους sst 3 και sst 4. Το lanreotide παρουσιάζει ανάλογες θεραπευτικές ιδιότητες με το octreotide όμως, η φαρμακοτεχνική μορφή του βραδείας απελευθέρωσης (που χρησιμοποείται στη θεραπεία της μεγαλακρίας) έχει διάρκεια δράσης το πολύ 2 εβδομάδες [184,189]. 58
81 Α.3 Σωματοστατίνη Σχήμα Α. 44: Η δομή των αναλόγων octreotide, lanreotide και vapreotide Τα τελευταία χρόνια έχει προσελκύσει μεγάλο ενδιαφέρον η ανάπτυξη μεταβολικά σταθεροποιημένων αναλόγων με χαρακτηριστικά πανσωματοστατίνης (ικανότητα δέσμευσης και στους πέντε sst 1-5, όπως η SS14) με σκοπό τη διεύρυνση των κλινικών ενδείξεων αυτών των αναλόγων. Το SM230 είναι ένα κυκλικό εξαπεπτιδικό ανάλογο με υψηλή συγγένεια δέσμευσης για τους sst 1, sst 2, sst 3 και sst 5. Το SM230 (Σχήμα Α.45) παρουσιάζει υψηλή ανασταλτική δράση in vitro στην έκκριση της G και IGF-1 και υψηλή μεταβολική σταθερότητα στο πλάσμα του αίματος (23 h) [190,191]. Παρόλο που το SM230 έχει πολύ υψηλή συγγένεια δέσμευσης για τον sst 2 (παρόμοια με του octreotide) αδυνατεί να επάγει την εσωτερίκευση του υποδοχέα in vitro και in vivo [192]. Όμως, επάγει την εσωτερίκευση των sst 3 και sst 5 πιο αποτελεσματικά σε σχέση με το octreotide. Το KE108 (Σχήμα Α.45) είναι ένα κυκλικό εννιαπεπτίδιο με οκταμελή δακτύλιο με συγγένεια δέσμευσης και για τους πέντε sst 1-5 [193]. Το ανάλογο αυτό παρά την υψηλή συγγένεια δέσμευσης για τους sst 2, sst 3 και sst 5, επάγει την εσωτερίκευση των sst 3 αλλά αδυνατεί να επάγει την εσωτερίκευση των sst 2 (ακόμα και σε συγκεντρώσεις nm δεν επάγει επαρκώς την εσωτερίκευση των sst 2 ) και sst 5 [38]. Και τα δύο ανάλογα έδειξαν αγωνιστική δράση στους sst 2 για την αναστολή της αδενυλικής κυκλάσης. Από τα παραπάνω γίνεται σαφές ότι τα ΚΕ108 και SM230 δεν αποτελούν γνήσιους μιμητές της ενδογενούς ορμόνης SS14 και είναι αγωνιστές με λειτουργική επιλεκτικότητα (biased agonists) [194]. Σχήμα Α. 45: Η δομή των αναλόγων SM230 και KE108 59
82 Α.3 Σωματοστατίνη Α.3.3 ΡΑΔΙΟΕΠΙΣΗΜΑΣΜΕΝΑ AΝΑΛΟΓΑ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ ΔΙΑΓΝΩΣΤΙΚΑ ΡΑΔΙΟΠΕΠΤΙΔΙΑ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ Tο ctreoscan είναι το πρώτο πεπτιδικό ραδιοφάρμακο που εγκρίθηκε (στις ΗΠΑ το 1994) και χρησιμοποιείται με επιτυχία στην απεικονιστική διάγνωση ΝΕΤs [195,196]. Το ctreoscan αποτελείται από το κυκλικό οκταπεπτιδικό ανάλογο της SS octreotide το οποίο έχει υψηλή συγγένεια δέσμευσης για τον sst 2 και μικρότερη για τον sst 5 (οι οποίοι εκφράζονται σε ΝΕΤs). Στο Ν-τελικό άκρο του octreotide έχει προσδεθεί ο υποκαταστάτης DTPA για τη σταθερή συναρμογή του 111 In. Διατίθεται εμπορικά ως τυποποιημένο λυόφιλο προσκεύασμα (kit) και με απλή προσθήκη διαλύματος 111 InCl 3 πραγματοποιείται η ανασύσταση του και ο σχηματισμός του ραδιοφαρμάκου. C 3 S S C InCl 3 In C 3 S S C 3 2 [DTPA 0 ]octreotide ctreoscan (R) Σχήμα Α. 46: Μετά από επισήμανση του [DTPA 0 ]octreotide με 111 In παραλαμβάνεται το ραδιοφαρμάκο ctreoscan. Το ctreoscan έχει υψηλή ευαισθησία (>75%) στην ανίχνευση καρκινοειδών, όγκων των νησιδίων, γαστρινώματος, γλυκαγονώματος, παραγαγγλιώματος, ενδοκρινικών όγκων του παγκρέατος (εκτός από ινσουλινώματος) και χαμηλότερη ευαισθησία (40-75%) στην ανίχνευση ινσουλινώματος, καρκίνου μαστού, λεμφώματος, φαιοχρωμοκυττώματος και αστροκυτώματος [196]. Λόγω κάποιων μειονεκτημάτων του 111 In, π.χ. σχετικά υψηλό κόστος περιορισμένη διαθεσιμότητα λόγω παραγωγής του στο κυκλοτρόνιο και χαμηλότερης ευκρίνειας απεικονίσεις λόγω της μη ιδανικής ενέργειας των εκπεμπόμενων φωτονίων (172 και 247 kev) το ενδιαφέρον των επιστημόνων στράφηκε και σε άλλα διαγνωστικά ραδιονουκλίδια, όπως το 99m Tc (SPECT) και το 68 Ga (PET). Τα τελευταία είναι εύκολα διαθέσιμα καθώς παραλαμβάνονται από γεννήτρια. 60
83 Α.3 Σωματοστατίνη Σχήμα Α. 47: Ολόσωμη απεικόνιση μετά τη χορήγηση ctreoscan σε ασθενή με νευροενδοκρινικό όγκο παγκρέατος. Πρωτοπαθής εστία στην κεφαλή του παγκρέατος (μικρό βέλος) και πολλαπλές εστίες παθολογικής πρόσληψης του ραδιοφαρμάκου στο ήπαρ, που αντιστοιχούν σε ηπατικές μεταστάσεις (μεγάλο βέλος) [ nown.html] Ο υποκαταστάτης DTPA σχηματίζει πολύ σταθερά σύμπλοκα με το 111 In και η επισήμανση του με 111 In γίνεται σε θερμοκρασία δωματίου, όμως δεν σχηματίζει σταθερά σύμπλοκα με σημαντικά στην ιατρική ραδιομέταλλα. Γι αυτό και χρησιμοποιήθηκε ευρέως ο υποκαταστάτης DTA, ο οποίος σχηματίζει σταθερά σύμπλοκα με μεγάλο φάσμα διαγνωστικών και θεραπευτικών ραδιομετάλλων π.χ. 111 In, 67/68 Ga, 86/90 Υ, 177 Lu (αναλυτικά Α.1.3.2). Το 68 Ga-DTA-[Tyr 3 ]octreotide ( 68 Ga-DTATC) χρησιμοποιήθηκε για PET απεικόνιση sst + 2 όγκων και παρουσίασε υψηλή απεικονιστική ευκρίνεια και ανίχνευση μεγαλύτερου αριθμού μεταστάσεων σε σύγκριση με το ctreoscan (Σχήμα Α.48) [197,198]. Η επιτυχία αυτή του 68 Ga-DTATC οφείλεται τόσο στο ραδιονουκλίδιο 68 Ga το οποίο επιτρέπει την εφαρμογή της PET απεικόνισης, η οποία είναι πιο ευαίσθητη τεχνική σε σύγκριση με τη SPECT, καθώς και στο πεπτιδικό ανάλογο TC, το οποίο έχει υψηλότερη συγγένεια δέσμευσης στους sst 2 σε σύγκριση με το octreotide. Επιπλέον, η συγγένεια δέσμευσης του 68 Ga-DTATC για τον sst 2 (2.5 ± 0.5 nm) είναι δέκα φορές μεγαλύτερη από αυτή του ctreoscan (22 ± 3.6 nm) [199]. Σχήμα Α. 48: Α. Ολόσωμη απεικόνιση SPECT μετά τη χορήγηση ctreoscan και Β. Απεικόνιση PET μεταστατικών εστιών ΝΕΤ μετά τη χορήγηση 68 Ga- DTATC. Με 68 Ga-DTATC επιτυγχάνεται απεικόνιση με μεγάλη ευκρίνεια σε ασθενή με πολλαπλές μεταστάσεις ΝΕΤ σε αντίθεση με το ctreoscan που ανιχνεύει μικρότερο αριθμό μεταστάσεων [199] 61
84 Α.3 Σωματοστατίνη Λόγω των πλεονεκτημάτων του 99m Tc (χαμηλό κόστος, εύκολη διάθεση (γεννήτρια) και ιδανικές πυρηνικές, όπως μονοενεργειακά φωτόνια 140 kev ιδανικά για απεικόνιση με SPECT camera) έγιναν προσπάθειες ανάπτυξης διαγνωστικών ραδιοπεπτιδίων SS. Δύο από τα πιο επιτυχημένα ραδιοπεπτίδια είναι το 99m Tc-Demotate 1 και το 99m Tc- YIC-TC, τα οποία στην κλινική χρήση έδειξαν βελτιωμένα χαρακτηριστικά σε σύγκριση με το ctreoscan. To 99m Tc-Demotate 1 (Demotate 1: [ 0 4,Tyr 3 ]octreotate) είναι ένα καινούργιο πολλά υποσχόμενο ραδιοφάρμακο για κλινική εφαρμογή. Τα ενθαρρυντικά προκλινικά δεδομένα για το 99m Tc-Demotate 1 (υψηλή συγγένεια δέσμευσης στον sst 2, υψηλή ικανότητα εσωτερίκευσης σε sst κύτταρα και υψηλή και ειδική πρόσληψη σε sst 2 όγκους AR4-2J) [57] επιβεβαιώθηκαν και κλινικά σε μικρό αριθμό ασθενών με καρκινοειδείς όγκους και ενδοκρινικούς όγκους του παγκρέατος [201]. Σχήμα Α. 49: Α. Η δομή του 99m Tc-Demotate 1. Ολόσωμη απεικόνιση μετά τη χορήγηση Β. 99m Tc- Demotate 1 (1 και 4 h) και Γ. ctreoscan (4 και 24 h). Και με τα δύο ανιχνεύθηκε η ηπατική μετάσταση από παγκρεατικό όγκο, όμως μια ακόμα μετάσταση δεν ανιχνεύεται από το ctreoscan λόγω παρεμβολής των νεφρών αλλά ανιχνεύεται από το 99m Tc-Demotate 1 [201] Το ραδιοπεπτίδιο 99m Tc- YIC-TC περιέχει το ανάλογο Tyr 3 -octreotide (TC), τον υποκαταστάτη YIC (6-υδραζινο-νικοτινικό οξύ) και τον συμπληρωματικό υποκαταστάτη EDDA (αιθυλενοδιαμινοδιοξικό οξύ) για τη συναρμογή του 99m Tc. Το ραδιοπεπτίδιο αυτό είχε και αυτό ενθαρρυντικά προκλινικά δεδομένα (υψηλή συγγένεια δέσμευσης στον sst 2, υψηλή ικανότητα εσωτερίκευσης σε sst + 2 κύτταρα, υψηλή και ειδική πρόσληψη σε sst + 2 όγκους AR4-2J και χαμηλή πρόσληψη στα νεφρά) [202]. 62
85 Α.3 Σωματοστατίνη Επιπλέον, συγκριτική μελέτη που έγινε σε μικρή ομάδα ασθενών με χορήγηση είτε 99m Tc-YIC-TC είτε 99m Tc-Demotate 1 έδειξε ότι τα δύο ραδιοπεπτίδια έχουν παρόμοια ικανότητα απεικόνισης στους περισσότερους ασθενείς [203]. Α Β Σχήμα Α. 50: Α. Η δομή του 99m Tc-YIC-TC και Β. SPECT απεικόνιση (τομές) σε ασθενή με ηπατική μετάσταση καρκινοειδούς μετά από χορήγηση 99m Tc- YIC-TC (4 h) και 99m Tc-Demotate 1 (1 h). Με το υπερηχογράφημα και την αξονική τομογραφία είναι αμυδρά ορατή η μετάσταση αυτή στο ήπαρ [203] ΘΕΡΑΠΕΥΤΙΚΑ ΡΑΔΙΟΠΕΠΤΙΔΙΑ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ Το ctreoscan βρήκε εφαρμογή και στη θεραπεία των ΝΕΤs, καθώς το 111 In εκπέμπει εκτός από γ-ακτινοβολία και ηλεκτρόνια Auger. Όμως λόγω της μικρής διεισδυτικής ικανότητας τους, το ctreoscan έχει μικρή θεραπευτική ικανότητα σε μεγάλες μεταστάσεις. Ως εκτούτου, η έρευνα προσανατολίστηκε και σε άλλα θεραπευτικά ραδιομέταλλα τα οποία εκπέμπουν μεγαλύτερης εμβέλειας σωματίδια β - και κυρίως στο 90 Y και 177 Lu. Η συναρμογή αυτών των θεραπευτικών ραδιομετάλλων από τον υποκαταστάτη DTA, ο οποίος είναι συνδεδεμένος στο πεπτιδικό ανάλογο SS, καθιστά εφικτή τη θεραπεία μεγάλου μεγέθους μεταστάσεων και πρόκληση βλάβης και σε γειτονικά καρκινικά κύτταρα (αναλυτικά στο Α.1.3.2). Το 90 Y-DTATC (ctreother ) έχει χρησιμοποιηθεί ευρέως στη ραδιονουκλιδική θεραπεία μεταστατικών ΝΕΤs. Περιέχει το ανάλογο TC, το οποίο έχει υψηλή συγγένεια δέσμευσης για τον sst 2 και τον υποκαταστάτη DTA για τη σταθερή συναρμογή του 90 Y. Αρκετές κλινικές δοκιμές φάσης 1 και 2 έχουν πραγματοποιηθεί για αυτό το θεραπευτικό ραδιοπεπτίδιο SS (Πίνακας Α.14) [ ]. 63
86 Α.3 Σωματοστατίνη Πίνακας Α.14 Ανταπόκριση ραδιονουκλιδικής θεραπείας σε ασθενείς με GEP-ETs με διαφορετικά ραδιοεπισημασμένα ανάλογα SS Βιβλιογραφία Ραδιοπεπτίδιο Ασθενείς (νούμερο) ΠΑ ΜΑ ΑΑ ΣΑ ΕΑ ΠΑ+ΜΑ (%) [207] 90 Y-DTATC (29%) ΜΔ 11(52%) 4(19%) 29 [204,205] 90 Y-DTATC 74 3(4%) 15(20%) ΜΔ 48(65%) 8(11%) 24 [206] 90 Y-DTATC 33 2(6%) 9(27%) ΜΔ 19(57%) 3(9%) 33 [208] 90 Y-DTATC (9%) 7(12%) 33(61%) 10(19%) 9 [213] [ 177 Lu-DTA 0,Tyr 3 ]octreotate 310 5(2%) 86(28%) 51(16%) 107(35%) 61(20%) 29 ΠΑ: πλήρης ανταπόκριση, ΜΑ: μερική ανταπόκριση, AΑ: ασήμαντη ανταπόκριση, ΣΑ: σταθεροποίηση ασθένειας, ΕΑ: επιδείνωση ασθένειας, ΜΔ: μη διαθέσιμο 64
87 Α.3 Σωματοστατίνη Γενικά, η ανταπόκριση (πλήρης και μερική) της ραδιονουκλιδικής θεραπείας των GEP-ETs σε 90 Y-DTATC κυμαίνεται μεταξύ 10-30% (Πίνακας Α. 14). Όμως, διαπιστώθηκε νεφροτοξικότητα ή/και αιματολογική τοξικότητα (20% ασθενών) [207,209]. Η νεφροτοξικότητα μπορεί να αποτραπεί μειώνοντας την νεφρική κατακράτηση του ραδιοπεπτιδίου με έγχυση μίγματος κατιονικών αμινοξέων (Lys και Arg) ή Lys και Gelofusine [210,211]. Σχήμα Α. 51: Αξονική τομογραφία (Α) πριν και (Β) μετά τη θεραπεία με 90 Y-DTATC σε ασθενή με μετάσταση στο ήπαρ. Μετά τη θεραπεία δεν είναι πλέον ορατή η κακοήθεια στο ήπαρ [207] Το [ 177 Lu-DTA 0,Tyr 3 ]octreotate περιέχει το ανάλογο [Tyr 3 ]octreotate, το οποίο έχει υψηλότερη συγγένεια δέσμευσης στον sst 2 από το octreotide και μεγαλύτερη ικανότητα εσωτερίκευσης διαμέσου του sst 2 και τον υποκαταστάτη DTA για τη σταθερή συναρμογή του 177 Lu. Το ραδιοπεπτίδιο αυτό είχε εντυπωσιακά αποτελέσματα όταν χορηγήθηκε σε ασθενείς (σύγκριση με το ctreoscan ) καθώς η πρόσληψη στους όγκους ήταν 3-4 φορές υψηλότερη απ ότι του ctreoscan, ενώ στα νεφρά, στη σπλήνα και στο ήπαρ ήταν παρόμοια [212]. Γενικά, η ανταπόκριση (πλήρης και μερική) της ραδιονουκλιδικής θεραπείας των GEP-ETs (σε 310 ασθενείς) σε [ 177 Lu-DTA 0,Tyr 3 ]octreotate είναι 29% (αναλυτικά δεδομένα στον Πίνακα Α. 14). Κάποιες παρενέργειες όπως ναυτία (25%), εμετός (10%) και ενοχλήσεις ή πόνο στην κοιλιακή χώρα (10%) παρατηρήθηκαν για 24 h μετά τη χορήγηση [213]. 65
88 Α.3 Σωματοστατίνη Σχήμα Α. 52: Ολόσωμη απεικόνιση ασθενούς με ΝΕΤ παγκρεατικό όγκο και μεταστάσεις στο ήπαρ. Πρώτη εικόνα απεικόνιση καρκινικών εστιών με ctreoscan πριν τη θεραπεία, (2η-4η) συνεδρία με [ 177 Lu-DTA 0,Tyr 3 ]octreotate και στη τελευταία εικόνα απεικόνιση με ctreoscan μετά τη θεραπεία. Ο ασθενής είχε μερική ανταπόκριση (μείωση του μεγέθους του όγκου περισσότερο από 50%) στη θεραπεία με [ 177 Lu-DTA 0,Tyr 3 ]octreotate [de Jong M, Breeman WAP, Kwekkeboom DJ, Valkema R, Krenning EP. (2009) Tumor Imaging and Therapy Using Radiolabeled Somatostatin Analogues. Acc. Chem. Res. 42(7): ] Επιπρόσθετα, με ραδιοευαισθητοποιητές χημειοθεραπευτικούς παράγοντες, όπως η καπεσιταβίνη (ανενεργή μορφή), μπορεί να βελτιωθεί η ραδιονουκλιδική θεραπεία όγκων. Το ένζυμο θυμιδινική φωσφορυλάση (ΤΡ), είναι απαραίτητο για την μετατροπή της καπεσιταβίνης στην ενεργή μορφή της (5-φλουορορουρακίλη ή 5-FU). Το ΤΡ υπάρχει σε μεγαλύτερη ποσότητα σε πολλούς όγκους σε σύγκριση με τους φυσιολογικούς ιστούς [214]. Η ακτινοβολία πυροδοτεί την ΤΡ να προάγει την μετατροπή της καπεσιταβίνης σε 5-FU. Μελέτη που έγινε σε 33 ασθενείς με GEP- ETs με χορήγηση [ 177 Lu-DTA 0,Tyr 3 ]octreotate και καπεσιταβίνη έδειξε μερική ανταπόκριση στην θεραπεία ασθενών σε ποσοστό 24% και σταθεροποίηση της ασθένειας σε ποσοστό 70% των ασθενών [215]. 66
89 Α.3 Σωματοστατίνη ΡΑΔΙΟΕΠΙΣΗΜΑΣΜΕΝΑ ΑΝΑΛΟΓΑ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ ΔΙΕΥΡΥΜΕΝΟΥ ΦΑΣΜΑΤΟΣ Τα προηγούμενα ραδιοπεπτίδια SS έχουν βελτιωμένα χαρακτηριστικά στην απεικόνιση ή στη θεραπεία κυρίως των sst + 2 όγκων. Παρά την επικράτηση της έκφρασης των sst 2 σε πολλούς καρκινικούς όγκους, συνέκφραση των sst 2 με άλλους sst-υποτύπους είναι αρκετά συχνή. Επιπλέον, σε αρκετούς όγκους όπου απουσιάζει ο sst 2 εκφράζεται συχνά ένας ή περισσότεροι από τους υπόλοιπους sst ( Α.1.2). Έτσι γίνεται αντιληπτό ότι ανάπτυξη πεπτιδίων με χαρακτηριστικά πανσωματοστατίνης θα διευρύνει τις κλινικές ενδείξεις των sst 2 -επιλεκτικών αναλόγων, δεδομένου ότι τα αντίστοιχα ραδιοπεπτίδια θα εντοπίζονται ή θα θεραπεύουν μεγαλύτερο φάσμα ανθρώπινων όγκων. Επιπλέον, λόγω αλληλεπίδρασης με αυξημένο αριθμό υποδοχέων (συνέκφραση των sst) θα επιτευχθεί αύξηση του διαγνωστικού σήματος και του θεραπευτικού αποτελέσματος. Τα τελευταία χρόνια γίνονται προσπάθειες για την ανάπτυξη ραδιοπεπτιδίων με υψηλή συγγένεια δέσμευσης στους πέντε sst 1-5. Τέσσερα νέα ανάλογα SS αναπτύχθηκαν: DTA-C (DTA-al 3 -C), DTA-BC (DTA-BzThi 3 -C), DTA-C-ATE (DTA-al 3,Thr 8 -C) και DTA-BC-ATE (DTA- BzThi 3,Thr 8 -C) τα οποία έχουν υψηλή συγγένεια δέσμευσης για τους sst 2,sst 3 και sst 5. Όλα τα παραπάνω ανάλογα επισημασμένα με 111 In έχουν υψηλή συγγένεια δέσμευσης για τους sst 2, sst 3 και sst 5 και πολύ μικρότερη για τους sst 1 και sst 4. Επιπλέον, όλα έδειξαν μεγαλύτερη ικανότητα εσωτερίκευσης διαμέσου των sst 2 και sst 3 (σε κύτταρα AR4-2J, EK293-hsst 2 και EK393-hsst 3 ) σε σύγκριση με το [ 111 In]DTA-ΤC. Η μελέτη των παραπάνω 111 In και 68 Ga ραδιοεπισημασμένων αναλόγων βρίσκεται σε κλινική φάση [216,217]. \ Σχήμα Α. 53: Η δομή των αναλόγων DTA-C, DTA-BC, DTA-C-ATE και DTA-ΒC-ATE [217] 67
90 Α.3 Σωματοστατίνη Τα επισημασμένα DTA-ανάλογα του KE108 [ 90 Υ]KE88, [ 111 In]KE88 και [ 67 Ga]KE88 (KE88: DTA-KE108) διατηρούν την υψηλή συγγένεια για τους sst 1-5. Τα ραδιοπεπτίδια αυτά εσωτερικεύονται διαμέσου των sst 3 (~32%) αλλά παρατηρήθηκε μειωμένη εσωτερίκευση διαμέσου των sst 2 (<0.4%). Ακολούθως, στη βιοκατανομή των [ 111 In]KE88 και [ 67 Ga]KE88, σε ποντίκια με πειραματικούς όγκους EK293-hsst 2 ή -hsst 3 ή AR4-2J, παρατηρήθηκε υψηλή πρόσληψη στους sst + 3 πειραματικούς + όγκους (η οποία παρέμενε και μετά από 24 h), ενώ η πρόσληψη στους sst 2 πειραματικούς όγκους ήταν χαμηλότερη και μειώθηκε στις 24 h [218]. Παρόμοια δεδομένα προκύπτουν από μελέτη των ραδιοπεπτιδίων [ 99m Tc]Demopan 1 ( 99m Tc- 4 -des-tyr 0 -KE108) και [ 99m Tc]Demopan 2 ( 99m Tc- 4 -KE108), τα οποία έχουν υψηλή συγγένεια δέσμευσης και για τους πέντε hsst 1-5 και ικανότητα εσωτερίκευσης διαμέσου των sst 3. Προκλινική μελέτη για τα δύο αυτά ραδιοπεπτίδια πραγματοποιήθηκε σε επίμυες με AR4-2J πειραματικούς όγκους. Σε αντίθεση με το [ 99m Tc]Demopan 1, το [ 99m Tc]Demopan 2 είχε υψηλή και ειδική πρόσληψη τόσο στον πειραματικό όγκο όσο και σε φυσιολογικούς sst + ιστούς όπως το πάγκρεας και τα επινεφρίδια [219]. 68
91 Β. Σκοπός- Σχεδιασμός
92
93 Β.1 Σκοπός της διατριβής Β.1 ΣΚΟΠΟΣ ΤΗΣ ΔΙΑΤΡΙΒΗΣ Σκοπός της παρούσας διατριβής ήταν η ανάπτυξη ραδιοπεπτιδίων SS με χαρακτηριστικά πανσωματοστατίνης. Τα νέα πεπτιδικά ανάλογα SS επιδιώκεται να έχουν τις εξής ιδιότητες: 1. α έχουν υψηλή συγγένεια δέσμευσης και για τους πέντε sst Να έχουν υψηλή ικανότητα εσωτερίκευσης για όλους τους sst 1-5 και ιδιαίτερα για τον sst 2 o οποίος είναι ο πιο συχνά απαντώμενος υπότυπος στους νεοπλασματικούς ιστούς 3. Να είναι μεταβολικά σταθερά 4. Να είναι υδρόφιλα 5. Να μπορούν να επισημανθούν με το ευρύ φάσμα διαγνωστικών (για εφαρμογή στην τεχνική SPECT και PET) και θεραπευτικών ραδιονουκλιδίων Πιο αναλυτικά: 1. Η ικανότητα των πεπτιδικών αναλόγων SS να αλληλεπιδρούν και να δεσμεύονται και στους πέντε sst 1-5 μπορεί να διευρύνει τις κλινικές ενδείξεις των sst 2 -επιλεκτικών αναλόγων, δεδομένου ότι τα αντίστοιχα ραδιοπεπτίδια θα εντοπίζονται σε μεγαλύτερο φάσμα ανθρώπινων όγκων. Επιπλέον, θα ενισχύσει τη διαγνωστική ευαισθησία ή/και τη θεραπευτική αποτελεσματικότητα σε όγκους με έκφραση και άλλων υποτύπων εκτός των sst 2. Γι αυτό το σκοπό στα πεπτιδικά ανάλογα που αναπτύξαμε διατηρήσαμε τον αριθμό των αμινοξέων της SS14, καθώς η φυσική ορμόνη παρουσιάζει υψηλή ικανότητα δέσμευσης και για τους πέντε hsst 1-5. Το πρώτο ανάλογο που σχεδιάστηκε είναι το DTA-SS14 (ΑΤ1Σ). Η αντικατάσταση της LTrp8 με DTrp 8 πραγματοποιήθηκε σε όλα τα υπόλοιπα ανάλογα καθώς στη βιβλιογραφία έχει αναφερθεί ότι η DTrp σταθεροποιεί τη β-στροφή σε πολλά ανάλογα σωματοστατίνης ευνοώντας την συγγένεια δέσμευσης στον sst 2. Η ικανότητα δέσμευσης των πεπτιδικών αναλόγων αξιολογήθηκε με πειράματα αυτοραδιογραφίας υποδοχέων σε μεμβράνες κυττάρων που υπερεκφράζουν επιλεκτικά καθ έναν από τους πέντε hsst 1-5 με ανταγωνιστική δέσμευση του ραδιοπροσδέτη [Leu 8,DTrp 22, 125 I-Tyr 25 ]SS28. 69
94 Β.1 Σκοπός της διατριβής 2. Η δέσμευση του ραδιοπροσδέτη-αγωνιστή στους υποδοχείς εκτός από τη μεταγωγή σήματος ενδοκυττάρια προκαλεί και την εσωτερίκευση του συμπλόκου υποδοχέα-ραδιοπροσδέτη στα κύτταρα. Η εσωτερίκευση των ραδιοπεπτιδίων έχει μεγάλη σημασία στην επιτυχή εφαρμογή τους in vivo καθώς αυξάνεται η συγκέντρωση του ραδιενεργού σήματος στο εσωτερικό του κυττάρου-στόχου. Αυτό έχει ως αποτέλεσμα την αύξηση του διαγνωστικού σήματος ή της κυτοτοξικής σωματιδιακής ακτινοβολίας (ραδιονουκλιδική θεραπεία) στα κύτταρα στόχους. Η μελέτη της επαγωγής της εσωτερίκευσης των sst από τα ΑΤΧΣ έγινε με μικροσκοπία ανοσοφθορισμού σε κύτταρα EK293-hsst 2 και EK293-hsst 3, ενώ η μελέτη εσωτερίκευσης των [ 111 In]ΑΤΧΣ έγινε σε επίπεδο ραδιοϊχνηθέτη σε κύτταρα AR4-2J, EK293-hsst 3 και EK293-hsst Η SS14 έχει μικρό χρόνο ημιζωής στο πλάσμα του αίματος (<3 min) γεγονός που περιορίζει την κλινική της χρήση. Αύξηση της μεταβολικής σταθερότητας στα νέα συνθετικά ανάλογα της SS (ATXΣ) θα εξασφαλίσει την πρόσβαση τους στα όργαναστόχους μετά την χορήγηση και την είσοδο τους στην κυκλοφορία. Για την επίτευξη αυτού του σκοπού έγιναν κάποιες τροποποιήσεις στη δομή και την αλληλουχία της SS14. Σε όλα τα πεπτιδικά ανάλογα ΑΤΧΣ έχει προσδεθεί ομοιοπολικά στο Ν-τελικό άκρο ο υποκαταστάτης DTA για τη δέσμευση του ραδιομετάλλου και παράλληλα για την προστασία της αμινομάδας στο Ν-τελικό άκρο. Επίσης έγιναν οι παρακάτω τροποποιήσεις: α) σταδιακή μείωση του αριθμού αμινοξέων στο δακτύλιο από δώδεκα σε έξι αμινοξέα β) αντικατάσταση επιλεγμένων L-αμινοξέων από D- ή μη φυσικά αμινοξέα γ) εισαγωγή δεύτερης δισουλφιδικής γέφυρας και δ) αντικατάσταση αμινοξέων από PEG Χ στο Ν-τελικό άκρο. Για τα [ 111 In]ΑΤΧΣ πραγματοποιήθηκε μελέτη της in vivo σταθερότητας σε ποντίκια. Μετά από κατεργασία του δείγματος αίματος ποντικού, το οποίο συλλέχθηκε 5 min μετά από χορήγηση των [ 111 In]ΑΤΧΣ, ακολούθησε ανάλυση με PLC για ανίχνευση τυχόν ραδιομεταβολιτών. 4. Τα [ 111 In]ΑΤΧΣ θα πρέπει να είναι υδρόφιλα, ώστε να απεκκρίνονται γρήγορα από τα νεφρά και το ουροποιητικό σύστημα και να ελαχιστοποιείται η πρόσληψη στο ήπαρ και τα έντερα. Ως εκτούτου, σε πιθανή εφαρμογή τους στην απεικονιστική διάγνωση SPECT θα επιτυγχάνεται ευκρινής απεικόνιση των νεοπλασματικών εστιών στην κοιλιακή χώρα. 70
95 Β.1 Σκοπός της διατριβής Η αξιολόγηση της ταχύτητας και της οδού απομάκρυνσης των [ 111 In]ΑΤΧΣ καθώς και της ταχύτητας αποβολής τους από τα νεφρά στα ούρα έγινε με μελέτες βιοκατανομής σε υγιή και παθολογικά πρότυπα πειραματοζώων. Στις μελέτες αυτές έγινε και αξιολόγηση της πρόσληψης των [ 111 In]ΑΤΧΣ σε φυσιολογικούς ιστούς-στόχους, π.χ. το πάγκρεας που εκφράζει κυρίως τον sst 2, καθώς και της απομάκρυνσης τους από τους παρακείμενους ιστούς. Επιπλέον, πραγματοποιήθηκαν πειράματα βιοκατανομής των [ 111 In]ΑΤΧΣ σε SCID ποντίκια για αξιολόγηση της πρόσληψης των αναλόγων σε πειραματικούς όγκους EK293-hsst 2 / -hsst 3 / -hsst 5 ή/και AR4-2J (rsst 2A ). 5. Σε όλα τα πεπτιδικά ανάλογα ΑΤΧΣ έχει προσδεθεί στο Ν-τελικό άκρο ο καθολικός υποκαταστάτης DTA ο οποίος σχηματίζει σταθερά σύμπλοκα με μεγάλο φάσμα διαγνωστικών ή θεραπευτικών ραδιομετάλλων. Η επισήμανση των ATΧΣ έγινε με 111 In για μια πρώτη συγκριτική αξιολόγηση (screening), ώστε να αναδείξει τυχόν ανάλογα επιλογής για περαιτέρω μελέτη και εφαρμογή είτε στην τεχνική PET (επισήμανση π.χ. με 68 Ga) είτε στη ραδιονουκλιδική θεραπεία (επισήμανση π.χ. με 90 Y ή 177 Lu). Στην παρούσα διατριβή η διαδρομή από το σχεδιασμό τον αναλόγων ΑΤΧΣ μέχρι την αξιολόγηση της χρησιμότητά τους στην απεικονιστική διάγνωση περιλαμβάνει με τη σειρά τα εξής στάδια: Σχεδιασμός των αναλόγων ΑΤΧΣ Σύνθεση, απομόνωση, ταυτοποίηση και έλεγχος καθαρότητας των ΑΤΧΣ Πειράματα αυτοραδιογραφίας υποδοχέων σε μεμβράνες κυττάρων που υπερεκφράζουν επιλεκτικά καθ έναν από τους πέντε hsst 1-5 για τον προσδιορισμό της συγγένειας δέσμευσης των ΑΤΧΣ με ραδιοπροσδέτη την [Leu 8,DTrp 22, 125 I-Tyr 25 ]SS28 - Σύγκριση με SS14 και SS28 Μελέτη επαγωγής εσωτερίκευσης των hsst 2 και hsst 3 από τα ΑΤΧΣ με τη μέθοδο ανοσοφθορισμού Επισήμανση με 111 In και ανάλυση των [ 111 In]ΑΤΧΣ με PLC για εξακρίβωση της καθαρότητας και σταθερότητας των επισημασμένων προϊόντων Μελέτη εσωτερίκευσης των [ 111 In]ΑΤΧΣ σε επίπεδο ραδιοϊχνηθέτη σε κύτταρα AR4-2J, EK293-hsst 3 και EK293-hsst 5 71
96 Β.1 Σκοπός της διατριβής Μελέτη της in vivo σταθερότητας των [ 111 In]ΑΤΧΣ σε ποντίκια. Μετά από κατεργασία του δείγματος αίματος ποντικού, το οποίο συλλέχθηκε 5 min μετά από χορήγηση των [ 111 In]ΑΤΧΣ ακολούθησε ανάλυση με PLC για ανίχνευση τυχόν ραδιομεταβολιτών. Πειράματα βιοκατανομής των [ 111 In]ΑΤΧΣ σε υγιή ποντίκια για την μελέτη της φαρμακοκινητικής συμπεριφοράς των αναλόγων Πειράματα βιοκατανομής των [ 111 In]ΑΤΧΣ σε SCID ποντίκια για επιπλέον αξιολόγηση της πρόσληψης των αναλόγων σε πειραματικούς όγκους EK293-hsst 2 / - hsst 3 / -hsst 5 ή/και AR4-2J. 72
97 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης Β.2 ΣΧΕΔΙΑΣΜΟΣ ΑΝΑΛΟΓΩΝ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ Η φυσική ορμόνη SS14 έχει χρόνο ημιζωής στο πλάσμα του αίματος <3 min, γεγονός που περιορίζει την κλινική της χρήση. Το μειονέκτημα αυτό κατέστησε αναγκαία την ανάπτυξη μεταβολικά σταθεροποιημένων αναλόγων SS. Η ανάπτυξη του σταθερού κυκλικού οκταπεπτιδίου octreotide, το οποίο είναι επιλεκτικό για τον sst 2, απετέλεσε επίτευγμα σταθμό των προσπαθειών αυτών. Με πρόσδεση του υποκαταστάτη DTPA στο Ν-τελικό άκρο του octreotide και τη συναρμογή του 111 In προέκυψε το ctreoscan. Το ctreoscan είναι το πρώτο πεπτιδικό ραδιοφάρμακο που εγκρίθηκε (1994) και χρησιμοποιείται με επιτυχία στην απεικονιστική διάγνωση των ΝΕΤs (Σχήμα Α. 46). Έκτοτε σε όλα τα πεπτιδικά ανάλογα SS, τα οποία είναι τροποποιημένα με χημικό υποκαταστάτη για σταθερή δέσμευση μεταλλικού ραδιονουκλιδίου, διατηρήθηκε ο μικρός αριθμός αμινοξέων (6-8) αλλά και ο δακτύλιος των 6 αμινοξέων. Οι κυριότερες τροποποιήσεις στην αλληλουχία του octreotide που έχουν επιχειρηθεί αφορούσαν αντικαταστάσεις επιλεγμένων αμινοξέων (π.χ. του Phe 3 από Tyr 3 ή της Thr(ol) 8 από Thr 8 ). Τα (ραδιο)πεπτίδια SS που προέκυψαν όμως έδειξαν ικανότητα αλληλεπίδρασης μόνο για τον sst 2 και χρησιμοποιήθηκαν με επιτυχία στην απεικόνιση ή στη θεραπεία κυρίως των sst + 2 όγκων. Με άλλα λόγια, δεν αποτελούν γνήσιους μιμητές της ενδογενούς ορμόνης SS14. Παρόλο που ο sst 2 είναι ο πιο συχνά απαντώμενος υπότυπος στους νεοπλασματικούς ιστούς, αρκετά συχνά υπάρχει συνέκφραση των sst 2 με άλλους sst-υποτύπους σε καρκινικούς όγκους. Επιπλέον, σε αρκετούς όγκους που δεν εκφράζεται ο sst 2 εκφράζεται ένας ή περισσότεροι από τους υπόλοιπους sst. Γίνεται λοιπόν αντιληπτό ότι ανάπτυξη πεπτιδίων με χαρακτηριστικά πανσωματοστατίνης θα διευρύνει τις κλινικές ενδείξεις των sst 2 -επιλεκτικών αναλόγων, δεδομένου ότι τα αντίστοιχα ραδιοπεπτίδια θα απεικονίζουν ή θα θεραπεύουν μεγαλύτερο φάσμα ανθρώπινων όγκων. Επιπλέον, λόγω αλληλεπίδρασης με αυξημένο αριθμό υποδοχέων (συνέκφραση των sst) θα επιτυγχάνεται αύξηση του διαγνωστικού σήματος και του θεραπευτικού αποτελέσματος. Σε αντίθεση με τα προηγούμενα sst 2 -επιλεκτικά και μεταβολικά σταθεροποιημένα ανάλογα, η ξεχασμένη SS14 έχει την ικανότητα όχι μόνο να δεσμεύεται με υψηλή συγγένεια και στους πέντε hsst 1-5 αλλά και να αναπτύσσει πλήρη φαρμακολογική 73
98 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης δράση στους sst 1-5. Δεν έχει μελετηθεί συστηματικά μέχρι τώρα πώς η σταδιακή μείωση των αμινοξέων του δακτυλίου της μητρικής ορμόνης επιδρά: 1. Στη διατήρηση της συγγένειας δέσμευσης και για τους sst Στη φαρμακολογική απόκριση της μητρικής ορμόνης (π.χ. επαγωγή εσωτερίκευσης + σε καθέναν από τους sst 1-5 και εσωτερίκευση των ραδιοπροσδετών σε sst 1-5 κύτταρα) 3. Στη μεταβολική σταθερότητα 4. Σε φαρμακοκινητικά χαρακτηριστικά (π.χ. ταχύτητα και ικανότητα στόχευσης των sst 1-5 in vivo και ταχύτητα απομάκρυνσης από παρακείμενους ιστούς). Στη διατριβή αυτή σχεδιάστηκαν δώδεκα νέα πεπτιδικά ανάλογα (ΑΤΧΣ) στα οποία διατηρήθηκε ο αρχικός αριθμός των αμινοξέων της SS14. Όλες οι αλλαγές που επιχειρήθηκαν αφορούσαν μόνο τη σταδιακή μείωση του δακτυλίου (από δωδεκαμελή σε εξαμελή) ή/και αντικατάσταση αμινοξέων-κλειδιών (key amino acids) στις παραπάνω βιολογικές παραμέτρους. Βεβαίως παρόμοιες προσπάθειες επιχειρήθηκαν και παλιότερα, οι οποίες όμως δεν απαντούν επαρκώς στα ερωτήματα αυτά δεδομένου ότι δεν είχαν ακόμα κλωνοποιηθεί και μελετηθεί οι sst 1-5. Οι παλιότερες αυτές προσπάθειες έχουν ληφθεί υπόψη στην επιλογή και στο σχεδιασμό των αναλόγων της διατριβής αυτής με στόχο πάντα την αποσαφήνιση των δομικών παραμέτρων που θα οδηγήσουν στο σχεδιασμό ραδιοπεπτιδίων αληθινών μιμητών της SS14. Συγκεκριμένα, στην παρούσα διατριβή σε όλα τα πεπτιδικά ανάλογα έχει προσδεθεί ομοιοπολικά στο Ν-τελικό άκρο ο υποκαταστάτης DTA για τη δυνατότητα δέσμευσης με 111 In άλλα και άλλων ραδιομετάλλων με κλινικό ενδιαφέρον (αναλυτικά Α.1.3.2) και παράλληλα για την προστασία της αμινομάδας στο Ν-τελικό άκρο. Επιπλέον, στα ΑΤΧΣ έγιναν οι παρακάτω τροποποιήσεις: 1. Σταδιακή μείωση του αριθμού αμινοξέων στο δακτύλιο από δώδεκα σε έξι αμινοξέα 2. Αντικατάσταση επιλεγμένων L-αμινοξέων από D- ή μη φυσικά αμινοξέα 3. Εισαγωγή δεύτερης δισουλφιδικής γέφυρας 4. Αντικατάσταση αμινοξέων από PEG Χ στο Ν-τελικό άκρο. Τα ανάλογα που σχεδιάστηκαν κατηγοριοποιήθηκαν με βάση τα αμινοξέα που περιέχονται στο δακτύλιο και αναλύονται παρακάτω. 74
99 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης ΚΑΤΗΓΟΡΙΑ ΑΝΑΛΟΓΩΝ ΜΕ ΔΩΔΕΚΑΜΕΛΗ ΔΑΚΤΥΛΙΟ Στα ανάλογα ΑΤ1Σ, ΑΤ2Σ και ΑΤ8Σ διατηρήσαμε το δωδεκαμελή δακτύλιο της SS14. Το ΑΤ1Σ διαφέρει από την SS14 μόνο ως προς τον υποκαταστάτη DTA. Στο ανάλογο ΑΤ2Σ έχει αντικατασταθεί η LTrp 8 με DTrp 8 (η αντικατάσταση αυτή διατηρήθηκε και σε όλα τα υπόλοιπα ΑΤΧΣ) καθώς στη βιβλιογραφία έχει αναφερθεί ότι η DTrp σταθεροποιεί τη β-στροφή σε πολλά ανάλογα σωματοστατίνης ευνοώντας την συγγένεια δέσμευσης στον sst 2 [56,180]. Ala 1 Gly 2 Cys 3 Lys 4 Asn 5 Phe 6 Phe 7 2 C C C S S 2 C 3 C 3 Lys 9 2 L /DTrp 8 Cys 14 Ser 13 Thr 12 Phe 11 Thr 10 Σχήμα Β. 1: Δομή των αναλόγων ΑΤ1Σ/ΑΤ2Σ (DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -Phe 6 -Phe 7 -L/DTrp 8 -Lys 9 - Thr 10 -Phe 11 -Thr 12 -Ser 13 -Cys 14 ]) Στο τρίτο ανάλογο της κατηγορίας με δωδεκαμελή δακτύλιο ΑΤ8Σ, έχουν γίνει οι εξής επιπλέον αλλαγές: α) η Lys 4 έχει αντικατασταθεί από την Arg 4 που είναι επίσης βασικό αμινοξύ και έχει απεντοπισμένο θετικό φορτίο και β) η LCys 14 έχει αντικατασταθεί με τη DCys 14. Έχει αναφερθεί ότι η αντικατάσταση της LCys14 με DCys 14 επηρεάζει τη διαμόρφωση του δακτυλίου της SS14. Επιπλέον, η αντικατάσταση της LTrp 8 και της LCys 14 από τα D-ισομερή τους αυξάνει τη δράση του αναλόγου (~6.5 φορές) ως προς την αναστολή της G σε σύγκριση με τη SS14 [179]. Σε πολλά πεπτιδικά ανάλογα (π.χ. τα ανάλογα της α-ms (Alpha-melanocyte stimulating hormone)) η αντικατάσταση της Lys από την Arg μειώνει σημαντικά την πρόσληψη τους στα νεφρά [220]. Επιπλέον, αντικατάσταση της Lys 4 από την Arg 4 στην SS14 έχει αναφερθεί ότι δεν επηρεάζει τη δραστικότητα του αναλόγου ως προς την αναστολή της G in vitro και του γλυκαγόνου in vivo [221]. 75
100 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης Ala 1 Gly 2 Cys 3 Arg 4 Asn 5 Phe 6 Phe 7 C C C S S 2 2 C 3 C 3 Lys 9 DTrp 8 2 DCys 14 Ser 13 Thr 12 Phe 11 Thr 10 Σχήμα Β. 2: Δομή του αναλόγου ΑΤ8Σ (DTA-Ala 1 -Gly 2 -c[cys 3 -Arg 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 - Phe 11 -Thr 12 -Ser 13 -DCys 14 ]) ΚΑΤΗΓΟΡΙΑ ΑΝΑΛΟΓΩΝ ΜΕ ΔΕΚΑΜΕΛΗ ΔΑΚΤΥΛΙΟ Στο ΑΤ12Σ με δεκαμελή δακτύλιο έχει αντικατασταθεί η Lys 4 από την Arg 4 για τυχόν μείωση της πρόσληψης στα νεφρά. Επιπλέον, τα Ν-τελικά αμινοξέα Ala 1 και Gly 2 έχουν αντικατασταθεί από PEG 1. Με αυτό τον τρόπο ο υποκαταστάτης DTA διατηρείται στην ίδια θέση, μακριά από τη φαρμακοφόρο ομάδα, όπως και στα ανάλογα ΑΤ1Σ/ΑΤ2Σ. PEG 1 1,2 Cys 3 Arg 4 Asn 5 Phe 6 Phe 7 C 2 C C S S 2 C 3 Lys 9 2 DTrp 8 Cys 12 Phe 11 Thr 10 Σχήμα Β. 3: Δομή του αναλόγου ΑΤ12Σ (DTA-PEG 1 1,2 -c[cys 3 -Arg 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 - Phe 11 -Cys 12 ]) 76
101 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης ΚΑΤΗΓΟΡΙΑ ΑΝΑΛΟΓΩΝ ΜΕ ΕΝΝΕΑΜΕΛΗ ΔΑΚΤΥΛΙΟ Τα κυκλικό εννεαπεπτίδιο des-aa 1,2,4,5,12 SS14 (DT-9) με εννεαμελή δακτύλιο έδειξε παρατεταμένη συμπτωματική ανασταλτική δράση (για δύο ημέρες) όταν χορηγήθηκε σε ασθενή με καρκινοειδές σύνδρομο [222]. Cys 5 Phe 6 Phe 7 2 DTrp 8 S S C 3 Lys 9 2 Cys 13 Ser 12 Phe 11 Thr 10 Β. 4: Δομή του αναλόγου DT-9 Βασιζόμενοι σε αυτά τα δεδομένα σχεδιάσαμε δύο ανάλογα με εννεαμελή δακτύλιο (ΑΤ10Σ και ΑΤ11Σ). Τα εξωκυκλικά Ν-τελικά αμινοξέα των δύο αυτών αναλόγων έχουν αντικατασταθεί με PEG 2. Και στα δύο ανάλογα η Lys (το αμινοξύ αυτό έχει συχνά ενοχοποιηθεί για αύξηση της νεφρικής κατακράτησης σε πολλά πεπτιδικά ανάλογα) έχει αντικατασταθεί είτε με Gly (ΑΤ10Σ) είτε με το βασικό αμινοξύ Arg (ΑΤ11Σ) με την προοπτική μείωσης της νεφρικής πρόσληψης χωρίς όμως να μειωθεί η συγγένεια δέσμευσης για τους sst 1-5. PEG 2 1,2,3 Xaa 4 Cys 5 Phe 6 Phe 7 C C C R S S C 3 Lys 9 DTrp 8 2 (AT10S): R= (AT11S): R= C 2 C 2 C 2 C() 2 Cys 13 Ser 12 Phe 11 Thr 10 Σχήμα Β. 5: Δομή των αναλόγων ΑΤ10Σ (DTA-PEG 2 1,2,3 -Gly 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 - Ser 12 -Cys 13 ]) και ΑΤ11Σ (DTA-PEG 2 1,2,3 - Arg 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Ser 12 -Cys 13 ]. 77
102 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης ΚΑΤΗΓΟΡΙΑ ΑΝΑΛΟΓΩΝ ΜΕ ΟΚΤΑΜΕΛΗ ΔΑΚΤΥΛΙΟ Το κυκλικό οκταπεπτιδικό ανάλογο -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]- (DT-8) με οκταμελή δακτύλιο διατηρεί τη συγγένεια δέσμευσης και για τους πέντε sst 1-5 (IC 50 s : sst 1 = 27 ± 3.4 nm, sst 2 = 41 ± 8.7 nm, sst 3 = 13 ± 3.2 nm, sst 4 = 1.8 ± 0.7 nm, sst 5 = 46 ± 27 nm). Η αντικατάσταση της LCys 3 από DCys 3 αύξησε περαιτέρω τη συγγένεια δέσμευσης σε όλους τους hsst 1-5, ειδικά για τον hsst 2 (IC 50 s : sst 1 = 14 nm, sst 2 = 14.5 nm, sst 3 = 4.5 nm, sst 4 = 1.0 nm, sst 5 = 9.5 nm) [223]. Επιπλέον, το κυκλικό ανάλογο ΚΕ108 (Tyr-c[DDab-Arg-Phe-Phe-DTrp-Lys-Thr-Phe]) με οκταμελή δακτύλιο έχει συγγένεια δέσμευσης και για τους πέντε sst 1-5. Το ΚΕ108 έχει υψηλή συγγένεια δέσμευσης για τους sst 2, sst 3 και sst 5 και χαμηλότερη για τους sst 1 και sst 4 (IC 50 s : sst 1 = 2.6 ± 0.4 nm, sst 2 = 0.9 ± 0.1 nm, sst 3 = 1.5 ± 0.2 nm, sst 4 = 1.6 ± 0.1 nm, sst 5 = 0.65 ± 0.1 nm) [193]. Βασιζόμενοι στα παραπάνω δεδομένα σχεδιάσαμε δύο ανάλογα με οκταμελή δακτύλιο (ΑΤ4Σ και ΑΤ9Σ) τα οποία θα έχουν όμως δεκατέσσερα αμινοξέα (όπως η SS14). Στα ανάλογα με οκταμελή δακτύλιο, ΑΤ4Σ και ΑΤ9Σ έχει αντικατασταθεί η LCys 3 με le 3. Το αμινοξύ αυτό μιμείται το δισουλφιδικό δεσμό [224]. Τα δύο αυτά ανάλογα διαφέρουν στη θέση 5 όπου το ΑΤ4Σ φέρει LCys ενώ το ΑΤ9Σ φέρει DCys, ώστε να συγκριθεί η επίδραση στη συγγένεια δέσμευσης στους sst 1-5 (σε αντιστοιχία με τα παραπάνω ευρήματα των οκταπεπτίδιων DT-8 και [DCys 3 ]DT-8). Ala 1 Gly 2 le 3 Lys 4 L/DCys 5 Phe 6 Phe 7 2 C C C S S C 3 Lys 9 2 DTrp 8 Gly 14 Ser 13 Cys 12 Phe 11 Thr 10 Σχήμα Β. 6: Δομή των αναλόγων ΑΤ4Σ/ΑΤ9Σ (DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -c[l/dcys 5 -Phe 6 -Phe 7 -DTrp 8 - Lys 9 -Thr 10 -Phe 11 -Cys 12 ]-Ser 13 -Gly 14 ) 78
103 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης ΚΑΤΗΓΟΡΙΑ ΑΝΑΛΟΓΩΝ ΜΕ ΕΞΑΜΕΛΗ ΔΑΚΤΥΛΙΟ Το ανάλογο [Tyr 3 ]octreotate (TATE, DPhe 1 -c(cys 2 -Tyr 3 -DTrp 4 -Lys 5 -Thr 6 -Cys 7 )-Thr 8 -) παρουσίασε υψηλότερη συγγένεια δέσμευσης για τον sst 2 σε σύγκριση με το octreotide [188]. Επεκτείνοντας το ανάλογο αυτό με τα αντίστοιχα αμινοξέα της SS14 σχεδιάσαμε το ανάλογο ΑΤ3Σ. Ο σχεδιασμός αυτός αποσκοπεί σε αύξηση της συγγένειας δέσμευσης στον sst 2 αλλά και με πιθανή συγγένεια δέσμευσης και για τους υπόλοιπους υπότυπους sst λόγω της διατήρησης των δεκατεσσάρων αμινοξέων της SS14. Σε πολλά ανάλογα της SS η αντικατάσταση της Phe 7 από Tyr 7 αυξάνει σημαντικά τη συγγένεια δέσμευσης για τον sst 2 αλλά και την ικανότητα εσωτερίκευσης του διαμέσου του sst 2 [225]. Το ΑΤ3Σ και το ΑΤ7Σ διαφέρουν στη θέση 7 όπου φέρουν Tyr και Phe αντίστοιχα. Ala 1 Gly 2 le 3 Lys 4 2 Asn 5 Cys 6 R Xaa 7 C C C (AT3S): R= 2 Gly 14 Ser 13 Thr 12 S C 3 S Cys 11 Thr 10 C 3 Lys 9 DTrp 8 2 (AT7S): R= Σχήμα Β. 7: Δομή των αναλόγων ΑΤ3Σ (DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -Asn 5 -c[cys 6 -Tyr 7 -DTrp 8 -Lys 9 -Thr 10 - Cys 11 ]-Thr 12 -Ser 13 -Gly 14 ) και ΑΤ7Σ (DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -Asn 5 -c[cys 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Cys 11 ]- Thr 12 -Ser 13 -Gly 14 ) ΚΑΤΗΓΟΡΙΑ ΔΙΚΥΚΛΙΚΩΝ ΑΝΑΛΟΓΩΝ To 1978 αναπτύχθηκε μια σειρά από δικυκλικά ανάλογα από τον Veber και την ομάδα του [226]. Από αυτά, οι ενώσεις III (c(aha-lys-c(cys-phe-phe-dtrp-lys-thr-phe-cys)- Ser) και VI (c(aha-lys-abu-c(cys-phe-dtrp-lys-thr-cys)-thr-ser) (Σχήματα Β. 9 και Β. 11) έδειξαν να είναι οι πιο δραστικές στην αναστολή έκκρισης του γλυκαγόνου, της ινσουλίνης και της G και παρουσίασαν παρατεταμένη in vivo σταθερότητα [226]. Aha: 7-αμινο-επτανοϊκό οξύ Abu: 2-αμινο-βουτυρικό οξύ 79
104 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης Στην ένωση III τα αμινοξέα Asn 5 και Thr 12 έχουν αντικατασταθεί από Cys, ενώ στην ένωση VI έχουν αντικατασταθεί τα αμινοξέα Phe 6 και Phe 11. Συμπέραναν λοιπόν ότι οι πλευρικές ομάδες των Asn 5 και Thr 12 και Phe 6 και Phe 11 είναι πολύ κοντά. Επιπλέον, οι αρωματικοί δακτύλιοι των Phe 6 και Phe 11 παίζουν σημαντικό ρόλο στη σταθεροποίηση της ενεργής διαμόρφωσης της ένωσης VI, λόγω της αλληλεπίδρασης π-stacking μεταξύ τους (Σχήμα Β. 8). Σχήμα B. 8: Η προτεινόμενη δομή του αναλόγου des-αα 1,2,3,14 dicarba 3,14 SS14 [226] Βασιζόμενοι στα παραπάνω δεδομένα των δύο αυτών αναλόγων, σχεδιάσαμε δύο δικυκλικά ανάλογα, με δύο δισουλφιδικούς δεσμούς. Τα δύο δικυκλικά ανάλογα, ΑΤ5Σ και ΑΤ6Σ, είναι τα πρώτα DTA-ανάλογα SS με δύο δισουλφιδικές γέφυρες. Ο σχεδιασμός του δικυκλικού ΑΤ5Σ στηρίχθηκε στη δομή του αναλόγου (c(aha-lys- Abu-c(Cys-Phe-DTrp-Lys-Thr-Cys)-Thr-Ser) (VI) και περιέχει ένα εξαμελή (όπως το octreotide) και ένα δωδεκαμελή δακτύλιο (όπως η SS14) (Σχήμα Β. 10). Aha 3 Lys 4 2 Abu 5 Cys 6 Phe 7 2 C C 2 S C 3 S C 3 Lys 9 DTrp 8 2 Ser 13 Thr 12 Cys 11 Thr 10 Σχήμα B. 9: Η δομή του αναλόγου (c(aha-lys-abu-c(cys-phe-dtrp-lys-thr-cys)-thr-ser) (VI) 80
105 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης Ala 1 Gly 2 Cys 3 Lys 4 Asn 5 Cys 6 Phe 7 2 C C C S S 2 S C 3 S C 3 Lys 9 2 DTrp 8 Cys 14 Ser 13 Thr 12 Cys 11 Thr 10 Σχήμα Β. 10: Δομή του αναλόγου ΑΤ5Σ (DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -c[cys 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 - Cys 11 ]-Thr 12 -Ser 13 -Cys 14 ]) Ο σχεδιασμός του δικυκλικού ΑΤ6Σ στηρίχθηκε στη δομή του αναλόγου (c(aha-lysc(cys-phe-phe-dtrp-lys-thr-phe-cys)-ser) (ΙΙΙ) και περιέχει ένα οκταμελή και ένα δωδεκαμελή δακτύλιο (Σχήμα Β. 12). Aha 3 Lys 4 2 Cys 5 Phe 6 Phe 7 2 C C 2 S S C 3 Lys 9 DTrp 8 2 Ser 13 Cys 12 Phe 11 Thr 10 Σχήμα B. 11: Α. Η δομή του αναλόγου c(aha-lys-c(cys-phe-phe-dtrp-lys-thr-phe-cys)-ser) (ΙΙΙ) 81
106 Β.2 Σχεδιασμός αναλόγων σωματοστατίνης Ala 1 Gly 2 Cys 3 Lys 4 Cys 5 Phe 6 Phe 7 2 C S S S S C C C 3 Lys 9 DTrp 8 2 Cys 14 Ser 13 Cys 12 Phe 11 Thr 10 Σχήμα Β. 12: Δομή του αναλόγου ΑΤ6Σ (DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 - Phe 11 -Cys 12 ]-Ser 13 -Cys 14 ]) Πίνακας Β. 1 Αλληλουχία των DTA-πεπτιδικών αναλόγων σωματοστατίνης (ΑΤΧΣ) Κωδικος IS 0503/02- Αλληλουχία Αριθμός ΑΑ στο δακτύλιο ΑΤ1Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -Phe 6 -Phe 7 -Trp 8 -Lys 9 -Thr 10 -Phe 11 -Thr 12 -Ser 13 -Cys 14 ] 12 ΑΤ2Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Thr 12 -Ser 13 -Cys 14 ] 12 ΑΤ3Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -Asn 5 -c[cys 6 -Tyr 7 -DTrp 8 -Lys 9 -Thr 10 -Cys 11 ]-Thr 12 -Ser 13 -Gly 14 6 ΑΤ4Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]-Ser 13 -Gly 14 8 ΑΤ5Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -c[cys 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Cys 11 ]-Thr 12 -Ser 13 -Cys 14 ] 6, 12 ΑΤ6Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]-Ser 13 -Cys 14 ] 8, 12 ΑΤ7Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -Asn 5 -c[cys 6 -Phe7-DTrp 8 -Lys 9 -Thr 10 -Cys 11 ]-Thr 12 -Ser 13 -Gly 14 6 ΑΤ8Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Arg 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Thr 12 -Ser 13 -DCys 14 ] 12 AT9Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -c[dcys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]-Ser 13 -Gly ΑΤ10Σ DTA-PEG 1,2,3-Gly -c[cys -Phe -Phe -DTrp -Lys -Thr -Phe -Ser -Cys ] 9 2 ΑΤ11Σ DTA-PEG 2 1,2,3 -Arg 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Ser 12 -Cys 13 ] 9 ΑΤ12Σ DTA-PEG 1 1,2 -c[cys 3 -Arg 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ] 10 82
107 Γ. Πειραματικό Μέρος
108
109 Γ. Πειραματικό Μέρος Γ.1 ΠΕΙΡΑΜΑΤΙΚΑ ΔΕΔΟΜΕΝΑ ΠΕΠΤΙΔΙΚΗΣ ΣΥΝΘΕΣΗΣ Γ.1.1 ΣΥΣΚΕΥΕΣ/ΟΡΓΑΝΑ-ΥΛΙΚΑ Η πεπτιδική σύνθεση αναλόγων της σωματοστατίνης πραγματοποιήθηκε σύμφωνα με την Fmoc/tBu μεθοδολογία σύνθεσης πεπτιδίων σε στερεή φάση χρησιμοποιώντας την 2-χλωροτριτυλο-χλωρίδιο ρητίνη (2-Cl-Trt). Η σύνθεση των πεπτιδίων έγινε μέσα σε υάλινο αντιδραστήρα (Σχήμα Γ. 1) με πορώδη ηθμό (P2) στο κάτω μέρος του. Τα αμινοξέα τα οποία χρησιμοποιήθηκαν προέρχονταν από την εταιρεία ova-biochem (Darmstadt, Germany) και CBL Patras (Patras,Greece) όπως αναλυτικά αναφέρεται στους αντίστοιχους Πίνακες Γ. 4 - Γ. 18. Η 2-Cl-Trt ρητίνη με προσδεδεμένο το ανάλογο C-τελικό αμινοξύ ήταν της CBL Patras (Patras, Greece). Τα αντιδραστήρια Fmoc-- PEG 1 -C 2 C (Fmoc-ΑΕΑ) και Fmoc--PEG 2 -C 2 C (Fmoc-ΑΕΕΑ) (Σχήμα Γ. 2) προμηθεύτηκαν από την ChemPep (Wellington, USA) και ο προστατευμένος υποκαταστάτης DTA-tris(tBu)ester (Σχήμα Γ. 3) από την CheMatech (Dijon, France). Τα αντιδραστήρια σύζευξης και οξείδωσης και οι οργανικοί διαλύτες που χρησιμοποιήθηκαν καταγράφονται στον Πίνακα Γ. 1. Σχήμα Γ. 1: Υάλινος αντιδραστήρας σύνθεσης πεπτιδίων Σχήμα Γ. 2: Τα αντιδραστήρια Fmoc-- PEG 1-C 2C και Fmoc- -PEG 2-C 2C Σχήμα Γ. 3: Ο υποκαταστάτης DTAtris(tBu)ester 83
110 Γ. Πειραματικό Μέρος Πίνακας Γ. 1: Αντιδραστήρια και διαλύτες που χρησιμοποιήθηκαν στην πεπτιδική σύνθεση Αντιδραστήρια/Διαλύτες Εταιρεία Bt DIC I 2 DMF ipr Et 2 DCM C 3C TFA CCl 4 DMS Merck (ohenbrunn, Germany) Sigma Aldrich (Steinheim, Germany) Panreac (Barcelona, Spain) SDS (Val de Reuil, France) SDS (Val de Reuil, France) Merck (ohenbrunn, Germany) SDS (Val de Reuil, France) SDS (Val de Reuil, France) Acros rganics (ew Jersey, USA) Acros rganics (ew Jersey, USA) Merck (ohenbrunn, Germany) Ο έλεγχος της προόδου των αντιδράσεων κατά τη σύνθεση των πεπτιδίων γινόταν με τα δοκιμή Kaiser ή δοκιμή Chloranil και με χρωματογραφία λεπτής στοιβάδας (TLC) σε πλάκες silica gel 60 με δείκτη φθορισμού F 254. Τα συστήματα ανάπτυξης που χρησιμοποιήθηκαν για την ανάπτυξη των χρωματογραφημάτων είναι τα εξής: A. Bu/ C 3 C/ 2 / Πυριδίνη (4:1:1:2, v/v) B. C 3 C/ 2 (5:1, v/v) C. Bu/ C 3 C/ 2 (4/1/1, v/v ) Η εμφάνιση των χρωματογραφημάτων λεπτής στοιβάδας έγινε i) σε θάλαμο υπεριώδους ακτινοβολίας (UV), ii) με ψεκασμό με διάλυμα νινυδρίνης και θέρμανση στους 100 C. Ο έλεγχος για την πορεία της οξείδωσης των σουλφυδρυλομάδων προς σχηματισμό ενός δισουλφιδικού δεσμού έγινε με τη δοκιμή Ellman. Ο καθαρισμός των πεπτιδίων επιτεύχθηκε με χρήση της υγρής χρωματογραφίας υψηλής απόδοσης ανάστροφης φάσης (RP-PLC) με τη συσκευή ÄΚΤΑ purifier 10 της Amersham Pharmacia Biotech με ανιχνευτή UV-900, χρησιμοποιώντας στήλη Supelcosil C18 (5 μm, 8 mm 250 mm) από τη Sigma Aldrich (Steinheim, Germany). Το μίγμα διαλυτών ήταν Η 2 Ο + 0.1% TFA (Διαλύτης A) και C 3 C + 0.1% TFA (Διαλύτης B) και το σύστημα έκλουσης γραμμικά μεταβαλλόμενης σύστασης: 10% σε 84
111 Γ. Πειραματικό Μέρος 60% Διαλύτη B σε 50 min και ροή 2 ml/min (Σύστημα Α). Για την ανίχνευση των προϊόντων μετρήθηκε η απορρόφηση στα 214 και 254 nm. Ο έλεγχος για την καθαρότητα των πεπτιδίων και την πρόοδο των αντιδράσεων της οξείδωσης πραγματοποιήθηκε με RP-PLC, χρησιμοποιώντας τη συσκευή Waters 2695 με ανιχνευτή Waters 2487 και αναλυτική στήλη Symmetry Shield C18 (3.5 μm, 4.6 mm 75 mm) της Waters (Milford, USA). Το μίγμα διαλυτών ήταν Η 2 Ο + 0.1% TFA (Διαλύτης A) και C 3 C + 0.1% TFA (Διαλύτης B) και το σύστημα έκλουσης γραμμικά μεταβαλλόμενης σύστασης: 20% σε 50% Διαλύτη B σε 30 min και ροή 1 ml/min (Σύστημα Β). Για την ανίχνευση των προϊόντων μετρήθηκε η απορρόφηση στα 220 και 280 nm. Η λυοφιλοποίηση των υδατικών διαλυμάτων των πεπτιδίων πραγματοποιήθηκε σε λυοφιλοποιητή της Labconco με αντλία Edwards (West Sussex, UK). Η ταυτοποίηση των πεπτιδίων πραγματοποιήθηκε με φασματογράφο μάζας κάτω από συνθήκες ιοντισμού με ψεκασμό ηλεκτρονίων (ESI-MS) Micromass-Platform LC της Waters Micromass Technologies. Γ.1.2 ΓΕΝΙΚΗ ΠΟΡΕΙΑ ΤΗΣ ΣΥΝΘΕΣΗΣ ΠΕΠΤΙΔΙΩΝ Για την επιμήκυνση της πεπτιδικής αλυσίδας χρησιμοποιήθηκε η 2-Cl-Trt ρητίνη με συζευγμένο το ανάλογο C-τελικό αμινοξύ για κάθε πεπτίδιο, όπως προαναφέρθηκε. Η ρητίνη παραμένει σε θερμοκρασία δωματίου για min και προστίθεται DMF για να διογκωθεί πριν ξεκινήσει η επιμήκυνση του πεπτιδίου. ΜΕΘΟΔΟΣ ΣΥΖΕΥΞΗΣ ΜΕ DIC/Bt Το Fmoc-αμινοξύ (3 mmol περίσσεια) και Bt (4.5 mmol περίσσεια) διαλύονται σε DMF (ελάχιστος όγκος). Το διάλυμα ψύχεται σε παγόλουτρο υπό ήπια ανάδευση και προστίθεται DIC (3.3 mmol περίσσεια). Το διάλυμα παραμένει στο παγόλουτρο για 10 min και σε θερμοκρασία δωματίου για άλλα 10 min. Το διάλυμα προστίθεται στη ρητίνη και η αντίδραση σύζευξης ολοκληρώνεται σε περίπου 4-6 h. Ο έλεγχος της πορείας σύζευξης γίνεται με δοκιμή Kaiser, με δοκιμή Chloranil ή/και με χρωματογραφία TLC. Μετά από κάθε σύζευξη η ρητίνη πλένεται με DMF και ipr και ξηραίνεται με Et 2 (Πίνακας Γ. 2). Αν η αντίδραση δεν έχει ολοκληρωθεί η διαδικασία επαναλαμβάνεται. ΜΕΘΟΔΟΣ ΑΠΟΜΑΚΡΥΝΣΗΣ ΤΗΣ ΟΜΑΔΑΣ Ν α -Fmoc Η απομάκρυνση της ομάδας Fmoc επιτυγχάνεται με διάλυμα 25% (v/v) πιπεριδίνης σε DMF σε 3 ή 4 δόσεις συνολικής χρονικής διάρκειας min. Ο έλεγχος της πορείας της αντίδρασης γίνεται με δοκιμή Kaiser ή με δοκιμή Chloranil. Μετά την 85
112 Γ. Πειραματικό Μέρος ολοκλήρωση της απομάκρυνσης της ομάδας Fmoc ακολουθεί πλύσιμο της ρητίνης με DMF και ipr και ξήρανση με Et 2 (Πίνακας Γ. 2). Πίνακας Γ. 2: Επαναλαμβανόμενη πορεία σύνθεσης πεπτιδίων για κάθε αμινοξύ που προστίθεται στη ρητίνη Διαδικασία Αντιδραστήρια/Διαλύτες Αριθμός επαναλήψεων/διάρκεια 1. Διόγκωση ρητίνης DMF (2x1 min) 2. Ενεργοποίηση ΑΑ Fmoc-AA/ Bt/DIC σε DMF (1x20 min) 3. Σύζευξη Ενεργοποιημένο Fmoc-ΑΑ 4-6 h 4. Έκπλυση ρητίνης DMF ipr x2 (3x1 min) (2x2 min) x2 αιθέρας (2x3 min) 5. Fmocαποπροστασία 25% πιπεριδίνη σε DMF σε 3-4 δόσεις (30-40 min) 6.Έκπλυση ρητίνης DMF ipr x2 (3x1 min) (2x2 min) x2 αιθέρας (2x3 min) ΕΛΕΓΧΟΣ ΠΟΡΕΙΑΣ ΣΥΝΘΕΣΗΣ Δοκιμή Kaiser και Chloranil Για τον έλεγχο της πορείας αντίδρασης σύζευξης κάθε αμινοξέος και αποπροστασίας της ομάδας Fmoc χρησιμοποιείται η δοκιμή Kaiser για την ανίχνευση ελεύθερων πρωτοταγών αμινομάδων και η δοκιμή Chloranil για την ανίχνευση ελεύθερων δευτεροταγών αμινομάδων. Για τη δοκιμή Kaiser, δείγμα πεπτιδορητίνης μεταφέρεται σε δοκιμαστικό σωλήνα και προστίθενται 3 σταγόνες από κάθε διάλυμα. Διάλυμα 1: 500 mg νινυδρίνης σε 10 ml Bu Διάλυμα 2: 80 g φαινόλης σε 20 ml Bu Διάλυμα 3: 2 ml υδατικού διαλύματος M KC σε 98 ml πυριδίνης 86
113 Γ. Πειραματικό Μέρος Το μίγμα θερμαίνεται για 5 min στους 100 C. Εφόσον το διάλυμα είναι κίτρινο και οι κόκκοι της ρητίνης λευκοί η δοκιμή θεωρείται αρνητική (-) ως προς την ύπαρξη ελεύθερων αμινομάδων. Αν το χρώμα των κόκκων και το διάλυμα γίνει μπλε-μωβ η δοκιμή είναι θετική (+) στην ύπαρξη ελεύθερων αμινομάδων (Σχήμα Γ. 4). Στην περίπτωση ελέγχου σύζευξης αμινοξέος στη ρητίνη, η αντίδραση πρέπει να επαναληφθεί. Σχήμα Γ. 4: Αντίδραση νινυδρίνης με τα αμινοξέα με τρανσαμίνωση-αποκαρβοξυλίωση δίνοντας το ιώδες του Ruhemann Για τον προσδιορισμό ελεύθερων ιμινομάδων όπως της προλίνης χρησιμοποιείται τη δοκιμή Chloranil. Δείγμα πεπτιδορητίνης μεταφέρεται σε δοκιμαστικό σωλήνα και προστίθενται 50 μl κορεσμένου διαλύματος αντιδραστηρίου Chloranil σε τολουόλιο και 200 μl ακετόνης. Το μίγμα αναδεύεται για 10 min σε θερμοκρασία δωματίου. Ο χρωματισμός των κόκκων της ρητίνης σε μπλε υποδηλώνει την παρουσία ελεύθερων δευτεροταγών αμινομάδων. Σχήμα Γ. 5: Αντίδραση δευτεροταγούς αμίνης με ακετόνη και το αντιδραστήριο Chloranil 87
114 Γ. Πειραματικό Μέρος Χρωματογραφία λεπτής στοιβάδας (TLC) Η χρωματογραφία λεπτής στοιβάδας χρησιμοποιείται επίσης για τον έλεγχο ολοκλήρωσης κάθε σύζευξης αμινοξέος και αποπροστασίας από την Fmoc ομάδα. Δείγμα πεπτιδορητίνης μεταφέρεται σε δοκιμαστικό σωλήνα και προστίθενται μερικές σταγόνες από το διάλυμα απόσπασης DCM/TFE/Ac (7:2:1 ν/ν/ν) ή TFE/ 2 (7:3 ν/ν). Μετά από 10 min απελευθερώνεται στο διάλυμα ένα μέρος του πεπτιδίου. Από το διάλυμα αυτό τοποθετείται δείγμα στην πλάκα χρωματογραφίας και αναπτύσσεται στο κατάλληλο σύστημα διαλυτών. Η πλάκα εμφανίζεται σε UV ακτινοβολία και ψεκάζεται με διάλυμα νινυδρίνης. Μετά από θέρμανση στους C η ύπαρξη μωβ κηλίδων υποδηλώνει την ύπαρξη ελεύθερων αμινομάδων. ΑΠΟΣΠΑΣΗ ΚΑΙ ΑΠΟΠΡΟΣΤΑΣΙΑ ΤΟΥ ΠΕΠΤΙΔΙΟΥ ΑΠΟ ΤΗ ΡΗΤΙΝΗ ΚΑΙ ΤΙΣ ΠΡΟΣΤΑΤΕΥΤΙΚΕΣ ΟΜΑΔΕΣ Μετά την ολοκλήρωση της σύνθεσης του πεπτιδίου ακολουθεί η απομάκρυνση του από τη ρητίνη και αποπροστασία από τις πλάγιες προστατευτικές ομάδες. Η πεπτιδορητίνη μεταφέρεται σε μια σφαιρική φιάλη και προστίθεται διάλυμα TFA/TES ή TIS/EDT/Anisole/ 2. Η αναλογία του διαλύματος αλλάζει σύμφωνα με τις προστατευτικές ομάδες του εκάστοτε πεπτιδίου προς αποπροστασία. Το διάλυμα αφήνεται για 4 h υπό ανάδευση σε θερμοκρασία δωματίου. Ακολουθεί διήθηση και πλύσιμο της ρητίνης με DCM πάνω στον ηθμό. Το διήθημα συμπυκνώνεται υπό ελαττωμένη πίεση προς σχηματισμό ελαιώδους υπολείμματος και το προϊόν καταβυθίζεται με την προσθήκη άνυδρου διαιθυλαιθέρα σε παγόλουτρο. Το στερεό διηθείται και πλένεται πάνω στον ηθμό με διαιθυλαιθέρα. ΚΥΚΛΟΠΟΙΗΣΗ ΤΟΥ ΓΡΑΜΜΙΚΟΥ ΠΕΠΤΙΔΙΟΥ Οξείδωση με ιώδιο σε διάλυμα προς σχηματισμό ενός δισουλφιδικού δεσμού Το DTA-πεπτίδιο, μετά την αποπροστασία, μεταφέρεται σε σφαιρική φιάλη όπου διαλύεται σε Ac/ 2 Ο (4:1 ν/ν) με τελική συγκέντρωση 2 mg/ml. Στο διάλυμα προστίθενται 10 eq ιωδίου (Σχήμα Γ. 6). Η αντίδραση παραμένει υπό ανάδευση για 10 min μέχρι 1 h σε θερμοκρασία δωματίου και ελέγχεται τακτικά με δοκιμή Ellman. Μετά την ολοκλήρωση της οξείδωσης προστίθεται διπλός όγκος 2 για να σταματήσει η αντίδραση. Η απομάκρυνση του ιωδίου επιτυγχάνεται με εκχυλίσεις με CCl 4 (5-6 φορές). Η υδατική φάση λυοφιλοποιείται για να παραλάβουμε το προϊόν σε στερεή μορφή. Ακολουθεί ανάλυση με PLC και MS για να πιστοποιηθεί ότι παραλάβαμε το κυκλικό πεπτίδιο. 88
115 Γ. Πειραματικό Μέρος Σχήμα Γ. 6: Πορεία σχηματισμού ενός δισουλφιδικού δεσμού Σχηματισμός δικυκλικού πεπτιδίου Για τον σχηματισμό δύο δισουλφιδικών δεσμών χρησιμοποιήθηκαν δύο διαφορετικές προστατευτικές πλευρικές ομάδες για τις τέσσερις σουλφυδρυλικές ομάδες. Η τριτυλομάδα (Trt), η οποία απομακρύνεται με 90% TFA, και η ακεταμιδο-μεθυλ-ομάδα (Acm), η οποία απομακρύνεται με ιώδιο και είναι σταθερή σε TFA. Το DTA-πεπτίδιο, μετά την αποπροστασία, μεταφέρεται σε σφαιρική φιάλη όπου διαλύεται σε ρυθμιστικό διάλυμα φωσφορικών 0.01Μ, p 7.5, με τελική συγκέντρωση 1 mg/ml. Στο διάλυμα προστίθεται 1% v/v DMS. Η αντίδραση παραμένει υπό ανάδευση σε θερμοκρασία δωματίου και ελέγχεται με δοκιμή Ellman. Όταν ολοκληρωθεί η αντίδραση το διάλυμα λυοφιλοποιείται. Ακολουθεί ανάλυση με PLC και MS για να πιστοποιηθεί ότι έχει σχηματιστεί ο πρώτος δισουλφιδικός δεσμός. Ακολουθεί οξείδωση σε διάλυμα με ιώδιο με το προϊόν της προηγούμενης αντίδρασης (Σχήμα Γ. 7). Με την οξείδωση με ιώδιο επιτυγχάνουμε την ταυτόχρονη αποπροστασία των σουλφυδρυλομάδων από τις ομάδες Acm και τον σχηματισμό ενός δεύτερου δισουλφιδικού δεσμού ο οποίος πιστοποιείται με ανάλυση με PLC και MS. 89
116 Γ. Πειραματικό Μέρος Σχήμα Γ. 7: Πορεία σχηματισμού δύο δισουλφιδικών δεσμών Δοκιμή Ellman Σε μια πλάκα χρωματογραφίας TLC μεταφέρουμε μια σταγόνα από το διάλυμα της αντίδρασης. Αφού στεγνώσει προσθέτουμε μια σταγόνα αιθανολικού διαλύματος Ellman (DTB) και η πλάκα θερμαίνεται. Η ύπαρξη κίτρινης κηλίδας υποδηλώνει την ύπαρξη ελεύθερων σουλφυδρυλομάδων, ενώ η ύπαρξη άχρωμης κηλίδας το σχηματισμό δισουλφιδικού δεσμού. ΤΕΛΙΚΟΣ ΚΑΘΑΡΙΣΜΟΣ - ΤΑΥΤΟΠΟΙΗΣΗ Ο καθαρισμός των πεπτιδίων πραγματοποιήθηκε με RP-PLC με ημιπαρασκευαστική στήλη Supelcosil C18 (5 μm, 8 mm 250 mm) (Σύστημα Α) και ο έλεγχος καθαρότητας με RP-PLC με αναλυτική στήλη Symmetry C18 (3.5 μm, 4.6 mm 75 mm) (Σύστημα Β) ( Γ.1.1). Η ταυτοποίηση των πεπτιδίων έγινε με ESI-MS. 10% σε 60% Διαλύτη Β σε 50 min και ροή 2 ml/ min (Σύστημα Α) 20% σε 50% Διαλύτη Β σε 30 min και ροή 1 ml/ min (Σύστημα Β) (Διαλύτης Α: Η 2 Ο + 0.1% TFA και Διαλύτης B: C 3 C + 0.1% TFA) 90
117 Γ. Πειραματικό Μέρος Γ.1.3 ΣΥΝΘΕΣΗ ΠΕΠΤΙΔΙΚΩΝ ΑΝΑΛΟΓΩΝ ΣΩΜΑΤΟΣΤΑΤΙΝΗΣ Κατά την εκπόνηση της διατριβής συντέθηκαν δώδεκα νέα πεπτιδικά ανάλογα της σωματοστατίνης 14, AT1Σ-ΑΤ12Σ, τα οποία φέρουν στο Ν-τελικό αμινοξύ τον καθολικό υποκαταστάτη DTA. εισαγωγή του υποκαταστάτη DTA στα πεπτιδικά ανάλογα έγινε για τη σταθερή συναρμογή τρισθενών ραδιομετάλλων χρήσιμων στην απεικoνιστική διάγνωση με SPECT ( 111 In) ή PET ( 68 Ga) και στη ραδιοθεραπεία ( 90 Υ, 177 Lu). Για την προσθήκη του υποκαταστάτη DTA χρησιμοποιήθηκε η μεθοδολογία Fmoc/tBu. Εκτός από τα ΑΤ5Σ και ΑΤ6Σ τα οποία φέρουν δύο δισουλφιδικές γέφυρες (δικυκλικά) τα υπόλοιπα ανάλογα φέρουν μία δισουλφιδική γέφυρα (Πίνακας Γ. 3). Πίνακας Γ. 3: Αλληλουχία των συντεθέντων πεπτιδικών αναλόγων σωματοστατίνης και το μοριακό τους βάρος Κωδικος IS 0503/02- Αλληλουχία Αριθμός ΑΑ στο δακτύλιο ΜΒ ΑΤ1Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -Phe 6 -Phe 7 -Trp 8 -Lys 9 -Thr 10 -Phe 11 -Thr 12 -Ser 13 -Cys 14 ] ΑΤ2Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Thr 12 -Ser 13 -Cys 14 ] ΑΤ3Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -Asn 5 -c[cys 6 -Tyr 7 -DTrp 8 -Lys 9 -Thr 10 -Cys 11 ]-Thr 12 -Ser 13 -Gly ΑΤ4Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]-Ser 13 -Gly ΑΤ5Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -Asn 5 -c[cys 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Cys 11 ]-Thr 12 -Ser 13 -Cys 14 ] 6, ΑΤ6Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Lys 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]-Ser 13 -Cys 14 ] 8, ΑΤ7Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -Asn 5 -c[cys 6 -Phe7-DTrp 8 -Lys 9 -Thr 10 -Cys 11 ]-Thr 12 -Ser 13 -Gly ΑΤ8Σ DTA-Ala 1 -Gly 2 -c[cys 3 -Arg 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Thr 12 -Ser 13 -DCys 14 ] AT9Σ DTA-Ala 1 -Gly 2 -le 3 -Lys 4 -c[dcys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]-Ser 13 -Gly ΑΤ10Σ DTA-PEG 2 1,2,3 -Gly 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Ser 12 -Cys 13 ] ΑΤ11Σ DTA-PEG 2 1,2,3 -Arg 4 -c[cys 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Ser 12 -Cys 13 ] ΑΤ12Σ DTA-PEG 1 1,2 -c[cys 3 -Arg 4 -Asn 5 -Phe 6 -Phe 7 -DTrp 8 -Lys 9 -Thr 10 -Phe 11 -Cys 12 ]
118 Γ. Πειραματικό Μέρος ΣΥΝΘΕΣΗ ΤΩΝ ΑΝΑΛΟΓΩΝ ΑΤ1Σ ΚΑΙ ΑΤ2Σ Τα δύο ανάλογα διαφέρουν στη θέση 8 όπου η LTrp στο ΑΤ1Σ έχει αντικατασταθεί από τη DTrp στο ΑΤ2Σ. Ως εκτούτου, ξεκίνησε κοινή πορεία σύνθεσης των δύο αναλόγων μέχρι και την προσθήκη της Lys στη θέση 9. Χρησιμοποιήθηκαν 306 mg από την - Cys(Trt)-2-Cl-Trt ρητίνη με υποκατάσταση 0.55 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.504 mmol) (Πίνακας Γ. 4), 116 mg Bt (0.76 mmol) και 86 μl DIC (0.56 mmol). Μετά την ολοκλήρωση της σύζευξης του αμινοξέος Fmoc-Lys(Boc)- ακολούθησε απομάκρυνση της ομάδας Fmoc με 25% πιπεριδίνη σε DMF, πλύσεις και ξήρανση της πεπτιδορητίνης - Lys(Boc)-Thr(tBu)-Phe-Thr(tBu)-Ser(tBu)-Cys(Trt)--Cl-Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε, μοιράστηκε σε δύο μέρη και τοποθετήθηκε σε δύο υάλινους αντιδραστήρες σύνθεσης ώστε να συνεχίσουν οι συνθέσεις των δύο αναλόγων χωριστά. Πίνακας Γ. 4: Αμινοξέα σύζευξης κατά τη σύνθεση του -Lys(Boc)-Thr(tBu)-Phe-Thr(tBu)-Ser(tBu)- Cys(Trt)--Cl-Trt-R Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Phe-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- *CBL Patras (Patras, Greece) Για την ολοκλήρωση της σύνθεσης του αναλόγου ΑΤ1Σ χρησιμοποιήθηκαν τα 9/17 της πεπτιδορητίνης. Βάσει του ποσοστού αυτού υπολογίστηκαν οι νέες ποσότητες του κάθε αμινοξέος (0.267 mmol), Bt (61.3 mg, 0.36 mmol) και DIC (45.5 μl, 0.26 mmol). Μετά την ολοκλήρωση της επιμήκυνσης του πεπτιδίου ακολούθησε απομάκρυνση της ομάδας Fmoc και σύζευξη του DTA-tris(tBu)ester (τριπλή περίσσεια) όπως ακριβώς και για τα αμινοξέα. Ακολούθησε επανασύζευξη του DTAtris(tBu)ester με mmol καθώς οι δοκιμές έδειξαν ότι η πρώτη αντίδραση ήταν ημιτελής (Πίνακας Γ. 5). 92
119 Γ. Πειραματικό Μέρος Πίνακας Γ. 5: Αμινοξέα σύζευξης για την ολοκλήρωση της σύνθεσης του ΑΤ1Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Trp(Boc)-* /-/- Fmoc-Phe- * /-/- Fmoc-Phe-* /-/- Fmoc-Asn(Trt)- * /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany),***Chematech (Dijon, France) Για την ολοκλήρωση της σύνθεσης του αναλόγου ΑΤ2Σ χρησιμοποιήθηκαν τα 8/17 της πεπτιδορητίνης. Βάσει του ποσοστού αυτού υπολογίστηκαν οι νέες ποσότητες του κάθε αμινοξέος (0.237 mmol), Bt (54.4 mg) και DIC (40.3 μl). Μετά την ολοκλήρωση της επιμήκυνσης του πεπτιδίου ακολούθησε απομάκρυνση της ομάδας Fmoc και σύζευξη του DTA-tris(tBu)ester (τριπλή περίσσεια) όπως ακριβώς και για τα αμινοξέα. Ακολούθησε επανασύζευξη του DTA-tris(tBu)ester με mmol καθώς οι δοκιμές έδειξαν ότι η πρώτη αντίδραση ήταν ημιτελής (Πίνακας Γ. 6). Όταν η επιμήκυνση των πεπτιδίων ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση των πεπτιδορητινών σε κενό με αιθέρα. Στη συνέχεια πραγματοποιήθηκε η απόσπαση των πεπτιδίων από τη ρητίνη και η αποπροστασία τους από τις πλάγιες προστατευτικές ομάδες με 10 ml διάλυμα TFA/TES/EDT/Anisole/ 2 (93:3:2:1:1), για κάθε ανάλογο, για 4 h σε θερμοκρασία δωματίου όπως προαναφέρθηκε ( Γ.1.2). Ακολούθησε οξείδωση των πεπτιδίων με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να σχηματιστεί ο δισουλφιδικός δεσμός μεταξύ των σουλφυδρυλομάδων Cys 3 -Cys
120 Γ. Πειραματικό Μέρος Πίνακας Γ. 6: Αμινοξέα σύζευξης για την ολοκλήρωση της σύνθεσης του ΑΤ2Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe- * /-/- Fmoc-Phe- * /-/- Fmoc-Asn(Trt)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France) Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ1Σ % ΑΤ2Σ % (M+2 + /2) (M+3 + /3) (M+2 + /2) (M+3 + /3) Α: 0.53 B: 0.50 A: 0.57 B: 0.57 ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ3Σ Χρησιμοποιήθηκαν 200 mg από την -Gly-2-Cl-Trt ρητίνη με υποκατάσταση 0.35 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.21 mmol), mg Bt (0.32 mmol) και 36 μl (0.23 mmol) DIC. Μετά την ολοκλήρωση της σύζευξης της Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Ala-Gly-le-Lys(Boc)-Asn(Trt)- Cys(Trt)-Tyr(tBu)-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Cys(Trt)-Thr(tBu)-Ser(tBu)-Gly--Cl- Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε τη σύνθεση του αναλόγου. Η σύζευξη του DTA-tris(tBu)ester (0.105 mmol, 3 eq) πραγματοποιήθηκε με mg Bt (0.16 mmol) και 18 μl DIC (0.12 mmol). Ακολούθησε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 7). Όταν η επιμήκυνση του 94
121 Γ. Πειραματικό Μέρος πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TES/EDT/Anisole/ 2 (93:3:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθεί το πεπτίδιο μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 6 - Cys 11. Πίνακας Γ. 7: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ3Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Tyr(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Asn(Trt)- * /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-le-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France) Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ3Σ % (M+2 + /2) (M+3 + /3) Α: 0.84 C:
122 Γ. Πειραματικό Μέρος ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ4Σ Χρησιμοποιήθηκαν 200 mg από την -Gly-2-Cl-Trt ρητίνη με υποκατάσταση 0.35 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.27 mmol), 62 mg Bt (0.4 mmol) και 46 μl DIC (0.3 mmol). Μετά την ολοκλήρωση της σύζευξης της Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Ala-Gly-le-Lys(Boc)-Cys(Trt)-Phe- Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Phe-Cys(Trt)-Ser(tBu)-Gly--Cl-Trt-R. Πίνακας Γ. 8: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ4Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Phe-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe-* /-/- Fmoc-Phe-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-le-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France) Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε τη σύνθεση του αναλόγου Η σύζευξη του DTA-tris(tBu)ester (0.135 mmol, 3 eq) πραγματοποιήθηκε με 31 mg Bt (0.2 mmol) και 23 μl DIC (0.15 mmol). Ακολούθησε επανασύζευξη του DTAtris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 8). 96
123 Γ. Πειραματικό Μέρος Όταν η επιμήκυνση του πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TES/EDT/Anisole/ 2 (93:3:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθεί το πεπτίδιο μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 5 -Cys 12. Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ4Σ ,9% (M+ + ) (M+2 + /2) (M+3 + /3) C: 0.28 ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ5Σ Χρησιμοποιήθηκαν 250 mg από την -Cys(Acm)-2-Cl-Trt ρητίνη με υποκατάσταση 0.40 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.3 mmol), 69 mg Bt (0.45 mmol) και 51.1 μl DIC (0.33 mmol). Μετά την ολοκλήρωση της σύζευξης της Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Ala-Gly-Cys(Acm)-Lys(Boc)-Asn(Trt)- Cys(Trt)-Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Cys(Trt)-Thr(tBu)-Ser(tBu)-Cys(Acm)--Cl- Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε τη σύνθεση του αναλόγου. Η σύζευξη του DTA-tris(tBu)ester (0.15 mmol, 3 eq) πραγματοποιήθηκε με 35 mg Bt (0.23 mmol) και 25.6 μl DIC (0.17 mmol). Ακολούθησε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 9). Όταν η επιμήκυνση του πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TIS/EDT/Anisole/ 2 (93:3:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ρυθμιστικό διάλυμα φωσφορικών 0.01 Μ, p 7.5, και 1% DMS, ώστε να πραγματοποιηθεί η πρώτη κυκλοποίηση του πεπτιδίου μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 6 -Cys 11 ( Γ.1.2). Η ταυτοποίηση της πρώτης δισουλφιδικής γέφυρας έγινε με ανάλυση με PLC (Σύστημα Β) και MS. Στη συνέχεια το μονοκυκλικό προϊόν οξειδώθηκε για δεύτερη φορά με ιώδιο 97
124 Γ. Πειραματικό Μέρος σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) επιτυγχάνοντας ταυτόχρονη αποπροστασία των σουλφυδρυλομάδων Cys 3 -Cys 14 από τις ομάδες Acm και σχηματισμό ενός δεύτερου δισουλφιδικού δεσμού. Η ταυτοποίηση του δικυκλικού πεπτιδίου έγινε με ανάλυση με PLC (Σύστημα Β) και MS. Πίνακας Γ. 9: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ5Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Asn(Trt)- * /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-Cys(Acm)-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France) Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ5Σ % (M+2 + /2) (M+3 + /3) (M+4 + /4) C:
125 Γ. Πειραματικό Μέρος ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ6Σ Χρησιμοποιήθηκαν 250 mg από την -Cys(Acm)-2-Cl-Trt ρητίνη με υποκατάσταση 0.4 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.3 mmol), 69 mg Bt (0.45 mmol) και 51.1 μl DIC (0.33 mmol). Μετά την ολοκλήρωση της σύζευξης της Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Ala-Gly-Cys(Acm)-Lys(Boc)-Cys(Trt)- Phe-Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Phe-Cys(Trt)-Ser(tBu)-Cys(Acm)--Cl-Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε τη σύνθεση του αναλόγου. Η σύζευξη του DTA-tris(tBu)ester (0.15 mmol, 3 eq) πραγματοποιήθηκε με 35 mg Bt (0.23 mmol) και 25.6 μl DIC (0.17 mmol). Ακολούθησε επανασύζευξη του DTAtris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 10). Όταν η επιμήκυνση του AT6Σ ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TIS/EDT/Anisole/ 2 (93:3:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ρυθμιστικό διάλυμα φωσφορικών 0.01 Μ, p 7.5 και 1% DMS ώστε να πραγματοποιηθεί η πρώτη κυκλοποίηση του πεπτιδίου μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 5 -Cys 12. Η ταυτοποίηση της πρώτης δισουλφιδικής γέφυρας έγινε με ανάλυση με PLC (Σύστημα Β) και MS. Στη συνέχεια το μονοκυκλικό προϊόν οξειδώθηκε για δεύτερη φορά με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) επιτυγχάνοντας ταυτόχρονη αποπροστασία των σουλφυδρυλομάδων Cys 3 -Cys 14 από τις ομάδες Acm και σχηματισμό ενός δεύτερου δισουλφιδικού δεσμού. Η ταυτοποίηση του δικυκλικού πεπτιδίου έγινε με ανάλυση με PLC (Σύστημα Β) και MS. 99
126 Γ. Πειραματικό Μέρος Πίνακας Γ. 10: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ6Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Phe-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe- * /-/- Fmoc-Phe-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-Cys(Acm)-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France) Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ6Σ % (M+2 + /2) (M+3 + /3) (M+4 + /4) C: 0.56 ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ7Σ Χρησιμοποιήθηκαν 300 mg από την -Gly-2-Cl-Trt ρητίνη με υποκατάσταση 0.35 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.315 mmol), 72.4 mg Bt (0.47 mmol) και 53.6 μl DIC (0.35 mmol). Μετά την ολοκλήρωση της σύζευξης της Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Ala-Gly-le-Lys(Boc)-Asn(Trt)- Cys(Trt)-Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Cys(Trt)-Thr(tBu)-Ser(tBu)-Gly--Cl-Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε τη σύνθεση του αναλόγου. Η 100
127 Γ. Πειραματικό Μέρος σύζευξη του DTA-tris(tBu)ester (0.158 mmol, 3 eq) πραγματοποιήθηκε με 36.2 mg Bt (0.24 mmol) και 26.8 μl DIC (0.17 mmol). Ακολούθησε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 11). Όταν η επιμήκυνση του πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TIS/EDT/Anisole/ 2 (93:3:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθεί το πεπτίδιο μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 6 - Cys 11. Πίνακας Γ. 11: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ7Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe- * /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Asn(Trt)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-le-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France) 101
128 Γ. Πειραματικό Μέρος Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ7Σ % (M+2 + /2) (M+3 + /3) A: 0.83 ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ8Σ Χρησιμοποιήθηκαν 205 mg από την -DCys(Trt)-2-Cl-Trt ρητίνη με υποκατάσταση 0.60 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.3 mmol), 69 mg Bt (0.45 mmol) και 51.1 μl DIC (0.33 mmol). Μετά την ολοκλήρωση της σύζευξης της Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Ala-Gly-Cys(Trt)-Arg(Pbf)-Asn(Trt)- Phe-Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Phe-Thr(tBu)-Ser(tBu)-DCys(Trt)--Cl-Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε η σύνθεση του αναλόγου. Η σύζευξη του DTA-tris(tBu)ester (0.15 mmol, 3 eq) πραγματοποιήθηκε με 34.5 mg Bt (0.23 mmol) και 25.6 μl DIC (0.17 mmol). Ακολούθησε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 12). Όταν η επιμήκυνση του πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TIS/EDT/Anisole/ 2 (93:2:2:2:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθεί το πεπτίδιο μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 3 -DCys
129 Γ. Πειραματικό Μέρος Πίνακας Γ. 12: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ8Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Phe-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe-* /-/- Fmoc-Phe-* /-/- Fmoc-Asn(Trt)-* /-/- Fmoc-Arg(Pbf)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTAtris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany),***Chematech (Dijon, France) Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ8Σ % (M+2 + /2) (M+3 + /3) C: 0.2 ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ9Σ Χρησιμοποιήθηκαν 286 mg από την -Gly-2-Cl-Trt ρητίνη με υποκατάσταση 0.3 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.3 mmol), 69 mg Bt (0.45 mmol) και 51.1 μl DIC (0.33 mmol). Μετά την ολοκλήρωση της σύζευξης της Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Ala-Gly-le-Lys(Boc)-DCys(Trt)-Phe- Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Phe-Cys(Trt)-Ser(tBu)-Gly--Cl-Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε τη σύνθεση του αναλόγου. Η σύζευξη του DTA-tris(tBu)ester (0.15 mmol, 3 eq) 103
130 Γ. Πειραματικό Μέρος πραγματοποιήθηκε με 34.5 mg Bt (0.23 mmol) και 25.6 μl DIC (0.17 mmol). Ακολούθησε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 13). Όταν η επιμήκυνση του πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TIS/EDT/Anisole/ 2 (93:3:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθεί το πεπτίδιο μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 5 -DCys 12. Πίνακας Γ. 13: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ9Σ στη ρητίνη Fmoc-αμινοξύ mg (για eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-Phe-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe-* /-/- Fmoc-Phe-* /-/- Fmoc-DCys(Trt)-** /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-le-** /-/- Fmoc-Gly-* /-/- Fmoc-Ala-* /-/- DTA-tris(tBu)ester*** *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France) /+/+ -/-/- Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ9Σ % (M+2 + /2) (M+3 + /3) B:
131 Γ. Πειραματικό Μέρος ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ10Σ ΚΑΙ ΑΤ11Σ Τα δύο ανάλογα διαφέρουν στη θέση 1 καθώς το ΑΤ10Σ έχει Gly ενώ το ΑΤ11Σ έχει Arg. Γι αυτό ξεκίνησε κοινή πορεία σύνθεσης των δύο αναλόγων μέχρι και την προσθήκη της Fmoc-Cys(Trt)- στη θέση 2. Χρησιμοποιήθηκαν 436 mg από την - Cys(Trt)-2-Cl-Trt ρητίνη με υποκατάσταση 0.55 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.72 mmol) (Πίνακας Γ. 14), 166 mg Bt (1.08 mmol) και 123 μl DIC (0.79 mmol). Μετά την ολοκλήρωση της σύζευξης του αμινοξέος Fmoc-Cys(Trt)- ακολούθησε απομάκρυνση της ομάδας Fmoc με 25% πιπεριδίνη σε DMF, πλύσεις και ξήρανση της πεπτιδορητίνης -Cys(Trt)- Phe-Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Phe-Ser(tBu)-Cys(Trt)--Cl-Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε, μοιράστηκε σε δύο ίσα μέρη και τοποθετήθηκε σε δύο υάλινους αντιδραστήρες σύνθεσης ώστε να συνεχίσουν οι συνθέσεις των δύο αναλόγων χωριστά. Πίνακας Γ. 14: Αμινοξέα σύζευξης κατά τη σύνθεση του -Cys(Trt)-Phe-Phe-DTrp(Boc)-Lys(Boc)- Thr(tBu)-Phe-Ser(tBu)-Cys(Trt)--Cl-Trt-R. Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Ser(tBu)-* /-/- Fmoc-Phe-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe-* /-/- Fmoc-Phe-* /-/- Fmoc-Cys(Trt)-** /-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany) Για την ολοκλήρωση της σύνθεσης του αναλόγου ΑΤ10Σ χρησιμοποιήθηκε το 1/2 της πεπτιδορητίνης. Βάσει του ποσοστού αυτού υπολογίστηκαν οι νέες ποσότητες του κάθε αμινοξέος (0.36 mmol), Bt (83 mg, 0.54 mmol) και DIC (61.5 μl, 0.4 mmol). Μετά την ολοκλήρωση της σύζευξης του Fmoc-Ala- ακολούθησε απομάκρυνση της ομάδας Fmoc. Η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε η σύνθεση του αναλόγου. σύζευξη του Fmoc--PEG 2 -C 2 C (0.36 mmol, 6eq) 105
132 Γ. Πειραματικό Μέρος πραγματοποιήθηκε με 83 mg Bt (0.54 mmol) και 61.5 μl DIC (0.4 mmol). Πραγματοποιήθηκε επανασύζευξη του Fmoc--PEG 2 -C 2 C με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη. Ακολούθησε η σύζευξη του DTA-tris(tBu)ester (0.18mmol, 3eq) με 42 mg Bt (0.27 mmol)και 30.8 μl DIC (0.2 mmol). Πραγματοποιήθηκε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 15). Πίνακας Γ. 15: Αμινοξέα σύζευξης για την ολοκλήρωση της σύνθεσης του ΑΤ10Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Gly-* /-/- Fmoc--PEG 2-C 2C** /+/+ -/-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **Chem Pep (Wellington, USA), ***Chematech (Dijon, France) Για την ολοκλήρωση της σύνθεσης του αναλόγου ΑΤ11Σ χρησιμοποιήθηκε το 1/2 της πεπτιδορητίνης. Βάσει του ποσοστού αυτού υπολογίστηκαν οι νέες ποσότητες του κάθε αμινοξέος (0.36 mmol), Bt (83 mg, 0.54 mmol) και DIC (61.5 μl, 0.4 mmol). Μετά την ολοκλήρωση της σύζευξης του Fmoc-Arg(Pbf)- ακολούθησε απομάκρυνση της ομάδας Fmoc. πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε η σύνθεση του αναλόγου. σύζευξη του Fmoc--PEG 2 -C 2 C (0.36 mmol, 6 eq) πραγματοποιήθηκε με 83 mg Bt (0.54 mmol) και 61.5 μl DIC (0.4 mmol). Πραγματοποιήθηκε επανασύζευξη του Fmoc--PEG 2 -C 2 C με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη. Ακολούθησε η σύζευξη του DTA-tris(tBu)ester (0.18 mmol, 3 eq) με 42 mg Bt (0.27 mmol)και 30.8 μl DIC (0.2 mmol). Πραγματοποιήθηκε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 16). 106
133 Γ. Πειραματικό Μέρος Πίνακας Γ. 16: Αμινοξέα σύζευξης για την ολοκλήρωση της σύνθεσης του ΑΤ11Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Arg(Pbf)-* /-/- Fmoc--PEG 2-C 2C** /+/+ -/-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **Chem Pep (Wellington, USA), ***Chematech (Dijon, France) Όταν η επιμήκυνση των πεπτιδίων ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση των πεπτιδορητινών σε κενό με αιθέρα. Στη συνέχεια πραγματοποιήθηκε η απόσπαση των πεπτιδίων από τη ρητίνη και η αποπροστασία τους από τις πλάγιες προστατευτικές ομάδες με 10 ml διάλυμα TFA/TES/EDT/Anisole/ 2 (93:3:2:1:1) για το ΑΤ10Σ και (92:3:2:2:1) για το ΑΤ11Σ, για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση των πεπτιδίων με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθούν τα πεπτίδια μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 2 -Cys 10. Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ10Σ % ΑΤ11Σ % (M+2 + /2) (M+3 + /3) (M+2 + /2) (M+3 + /3) C: 0.86 C: 0.87 ΣΥΝΘΕΣΗ ΤΟΥ ΑΝΑΛΟΓΟΥ ΑΤ12Σ Χρησιμοποιήθηκαν 200 mg από την -Cys(Trt)-2-Cl-Trt ρητίνη με υποκατάσταση 0.55 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.33 mmol), 76 mg Bt (0.5 mmol) και 56.2 μl DIC (0.36 mmol). Μετά την ολοκλήρωση της σύζευξης της Fmoc-Cys(Trt)- ακολούθησε απομάκρυνση της ομάδας Fmoc, πλύσεις και ξήρανση της πεπτιδορητίνης Cys(Trt)-Arg(Pbf)-Asn(Trt)- Phe-Phe-DTrp(Boc)-Lys(Boc)-Thr(tBu)-Phe-Cys(Trt)--Cl-Trt-R. Στη συνέχεια η πεπτιδορητίνη ζυγίστηκε και μοιράστηκε σε δύο ίσα μέρη. Το ένα μέρος αποθηκεύτηκε στους 20 C και με το άλλο συνεχίστηκε τη σύνθεση του αναλόγου. σύζευξη του Fmoc--PEG 1 -C 2 C (0.33 mmol, 6 eq) πραγματοποιήθηκε με 76 mg Bt (
134 Γ. Πειραματικό Μέρος mmol) και 56.2 μl DIC (0.36 mmol). Πραγματοποιήθηκε επανασύζευξη του Fmoc-- PEG 1 -C 2 C με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη. Ακολούθησε η σύζευξη του DTA-tris(tBu)ester (0.165 mmol, 3 eq) με 38 mg Bt (0.25 mmol) και 28.1 μl DIC (0.18 mmol). Πραγματοποιήθηκε επανασύζευξη του DTA-tris(tBu)ester με μισές ποσότητες αντιδραστηρίων καθώς οι δοκιμές έδειξαν ότι δεν ολοκληρώθηκε η πρώτη σύζευξη (Πίνακας Γ. 17). Όταν η επιμήκυνση του πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 10 ml διάλυμα TFA/TIS/EDT/Anisole/2 (93:2:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθεί το πεπτίδιο μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 1 -DCys 10. Πίνακας Γ. 17: Αμινοξέα σύζευξης για τη σύνθεση του ΑΤ12Σ στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Phe-* /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Phe-* /-/- Fmoc-Phe-* /-/- Fmoc-Asn(Trt)-* /-/- Fmoc-Arg(Pbf)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc--PEG 1- C 2C**** /+/+ -/-/- DTA-tris(tBu)ester*** /+/+ -/-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany), ***Chematech (Dijon, France), ****Chem Pep (Wellington, USA) Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf ΑΤ12Σ % (M+2 + /2) C:
135 Γ. Πειραματικό Μέρος ΣΥΝΘΕΣΗ ΤΟΥ TATE Το [Tyr 3 ]ctreotate (ΤΑΤΕ) (DPhe 1 -Cys 2 -Tyr 3 -DTrp 4 -Lys 5 -Thr 6 -Cys 7 -Thr 8 -) συντέθηκε De ovo [227] ώστε να χρησιμοποιηθεί στα βιολογικά πειράματα για τον αποκλεισμό του sst 2. Χρησιμοποιήθηκαν 304 mg από την -Thr(tBu)-2-Cl-Trt ρητίνη με υποκατάσταση 0.5 mmol/g. Για τη σύζευξη του κάθε αμινοξέος χρησιμοποιήθηκε τριπλή περίσσεια αμινοξέος (0.45 mmol), 103 mg Bt (0.68 mmol) και 77 μl DIC (0.5 mmol) (Πίνακας Γ. 18). Πίνακας Γ. 18: Αμινοξέα σύζευξης για τη σύνθεση του TATE στη ρητίνη Fmoc-αμινοξύ mg (για 3 eq) Χρόνος αντίδρασης (h) Kaiser/Chloranil/TLC Fmoc-Cys(Trt)-** /-/- Fmoc-Thr(tBu)-* /-/- Fmoc-Lys(Boc)-* /-/- Fmoc-DTrp(Boc)-* /-/- Fmoc-Tyr(tBu)-* /-/- Fmoc-Cys(Trt)-** /-/- Fmoc-DPhe-* /-/- *CBL Patras (Patras, Greece), **ovabiochem (Darmstadt, Germany) Όταν η επιμήκυνση του πεπτιδίου ολοκληρώθηκε, ακολούθησε πλύσιμο και ξήρανση της πεπτιδορητίνης σε κενό με αιθέρα. Η απόσπαση του πεπτιδίου από τη ρητίνη και η αποπροστασία του από τις πλάγιες προστατευτικές ομάδες πραγματοποιήθηκε με 20 ml διάλυμα TFA/TIS/EDT/Anisole/ 2 (93:3:2:1:1) για 4 h σε θερμοκρασία δωματίου. Ακολούθησε οξείδωση του πεπτιδίου με ιώδιο σε διάλυμα Ac/ 2 Ο (4:1 ν/ν) για να κυκλοποιηθεί το πεπτίδιο μέσω του δισουλφιδικού δεσμού μεταξύ των σουλφυδρυλομάδων Cys 2 -DCys 7. Κωδικός ΜΒ PLC: %C 3C στην έκλουση ES-MS TLC: Rf TATE % (M+2 + /2) C:
136 Γ. Πειραματικό Μέρος Γ. 2 ΕΠΙΣΗΜΑΝΣΗ ΚΑΙ ΡΑΔΙΟΧΗΜΙΚΟΣ ΕΛΕΓΧΟΣ Γ.2.1 ΣΥΣΚΕΥΕΣ/ΟΡΓΑΝΑ-ΥΛΙΚΑ Αντιδραστήρια 111 InCl 3 Biomedica Life Sciences S.A., Greece Ανάλογο ΑΤΧΣ Ρυθμιστικό διάλυμα οξικού νατρίου 1 Μ p 4.6 Διάλυμα ασκορβικού νατρίου 0.1 M Διάλυμα a 2EDTA 0.1 Μ Ρυθμιστικό διάλυμα φωσφορικών: 0.5 M a 2P 4/0.5 M a 3P 4 2/1 (p 12) PBS p~7.4 (10 mm a 2P 4, 1.8 mm K 2P0 4, 2.7 mm KCl, 140 mm acl) +0.5%BSA Δ1 Δ2 Δ3 Δ4 Δ5 Et Όργανα Χρωματογράφος Waters με σύστημα ανάμιξης διαλυτών Waters 600 συνδεδεμένο με ανιχνευτή UV- Vis διάταξης φωτοδιόδων Waters PDA 2998, Ραδιομετρικός ανιχνευτής Gabi Αναλυτικές στήλες ανάστροφης φάσης: XTerra RP-18 (5 μm, 3.9 mm 20 mm) Waters, Vienna, Austria Raytest, RSM Analytische Instrumente Gmb, Germany Waters, Milford, USA Αυτόματος μετρητής γ-ακτινοβολίας με κρύσταλλο ai(tl), τύπου Canberra Packard Auto-Gamma 5000 Series Manchester, UK Α Β Σχήμα Γ.8: Α. Απαγωγός με τούβλα μολύβδου όπου γίνονται οι επισημάνσεις. Β. PLC χρωματογράφος Waters με ραδιομετρικό ανιχνευτή Gabi 110
137 Γ. Πειραματικό Μέρος Γ.2.2 ΕΠΙΣΗΜΑΝΣΗ ΜΕ 111 In Για την επισήμανση των DTA αναλόγων ΑΤΧΣ χρησιμοποιήθηκαν 30 μl 111 InCl 3 σε 50 mm Cl (10-20 mci/ml) και προστέθηκαν 1 μl διαλύματος Δ2, 2 μl διαλύματος Δ1 και 2.5 nmol κάθε αναλόγου ΑΤΧΣ (LSA). Το διάλυμα θερμάνθηκε στους 90 C για 20 min. Μετά τη θέρμανση 2 μl από το LSA αναμίχθηκαν με 24 μl Η 2 Ο, 2 μl διαλύματος Δ1 και 2 μl διαλύματος Δ3 (Διάλυμα QC). Ακολούθησε επώαση για 10 min σε RT και μετά ανάλυση με PLC (Σχήμα Γ. 8. Β) για τον έλεγχο του ποσοστού καθαρότητας του επισημασμένου πεπτιδίου. Στη συνέχεια στο LSA προστέθηκαν 2 μl διαλύματος Δ3, Et (και 5 μl διαλύματος Δ4 μόνο στα διαλύματα που προορίζονται για βιοκατανομή) (Διάλυμα Β ή ΔΒ). Σχήμα Γ.9: Σχηματική απεικόνιση διαλυμάτων LSA και QC Σχήμα Γ.10: Επισήμανση με 111 In- Σχηματισμός [ 111 Ιn]ΑΤ1Σ 111
138 Γ. Πειραματικό Μέρος Γ.2.3 ΠΡΟΕΤΟΙΜΑΣΙΑ ΤΟΥ ΕΠΙΣΗΜΑΣΜΕΝΟΥ ΑΝΑΛΟΓΟΥ [ 111 Ιn]ΑΤΧΣ ΓΙΑ : ΒΙΟΚΑΤΑΝΟΜΗ ΠΕΙΡΑΜΑΤΟΖΩΩΝ Στο ΔΒ προστέθηκαν 7 ml διαλύματος φυσιολογικού ορού/et (90/10), ώστε σε κάθε ζώο να χορηγηθούν 100 μl διαλύματος που να αντιστοιχούν σε 10 pmol [ 111 Ιn]ΑΤXΣ και ραδιενέργεια 1-2 μci. ΕΣΩΤΕΡΙΚΕΥΣΗ Πέντε μl του ΔΒ αραιώθηκαν με Δ5 ώστε σε 150 μl του τελικού διαλύματος να περιέχονται 2 pmol [ 111 Ιn]ΑΤXΣ και ραδιενέργεια μci. ΜΕΤΑΒΟΛΙΣΜΟΣ Ειδικά για τα πειράματα μεταβολισμού χρησιμοποιήθηκε το ίδιο πρωτόκολλο επισήμανσης όπως αναφέρθηκε παραπάνω με τις εξής δύο διαφορές. Χρησιμοποιήθηκαν 120 μl 111 InCl 3 ( mci) και 10 nmol κάθε αναλόγου ΑΤΧΣ. Στο ΔΒ προστέθηκε φυσιολογικός ορός με τελικό όγκο 500 μl ώστε σε κάθε ζώο να χορηγηθούν μl διαλύματος που να αντιστοιχούν σε 3 nmol [ 111 Ιn]ΑΤXΣ και ραδιενέργεια μci. Γ.2.4 ΡΑΔΙΟΧΗΜΙΚΟΣ ΕΛΕΓΧΟΣ Η απόδοση της επισήμανσης των αναλόγων μελετήθηκε με ανάλυση με PLC σε στήλη XTerra RP-18 (5 μm, 3.9 mm 20 mm) και συστήματα έκλουσης γραμμικά μεταβαλλόμενης σύστασης : 0% σε 50% Διαλύτη Β σε 20 min (Σύστημα Α) 10% σε 50% Διαλύτη Β σε 20 min (Σύστημα Β) 20% σε 50% Διαλύτη Β σε 30 min (Σύστημα Γ) 20% σε 30% Διαλύτη Β σε 20 min (Σύστημα Δ) (Διαλύτης Α : Η 2 Ο + 0.1% TFA και Διαλύτης B: C 3 C) 112
139 Γ. Πειραματικό Μέρος Πίνακας Γ.19: Συγκεντρωτικός πίνακας της απόδοσης και του χρόνου έκλουσης των επισημασμένων αναλόγων [ 111 In]ATXΣ t R (min) Σύστημα Απόδοση % [ 111 In]AT1Σ 13.5 Β 97 [ 111 In]AT2Σ 19.4 Γ 97 [ 111 In]AT3Σ 8.8 Β 98 [ 111 In]AT4Σ 14.4 Β 94 [ 111 In]AT5Σ 9,7 Δ 94 [ 111 In]AT6Σ 14 Β 94 [ 111 In]AT8Σ 15 Α 97 [ 111 In]AT9Σ 13.5 Β 96 [ 111 In]AT10Σ 12.5 Β 98 [ 111 In]AT11Σ 12 Β 95.5 [ 111 In]AT12Σ 18.6 Γ
140 Γ. Πειραματικό Μέρος Γ. 3 ΒΙΟΛΟΓΙΚΗ ΑΞΙΟΛΟΓΗΣΗ Γ.3.1 ΑΥΤΟΡΑΔΙΟΓΡΑΦΙΑ ΥΠΟΔΟΧΕΩΝ Αντιδραστήρια C (Chinese hamster ovary) κύτταρα επιμολυσμένα με σταθερή έκφραση του hsst 1 CCL39 (Chinese hamster lung cell line of fibroblasts) με σταθερή έκφραση του hsst 2/hsst 3/hsst 4 EK293: εμβρυονικά κύτταρα από ανθρώπινο νεφρό με σταθερή έκφραση του hsst 5 am s F-12 θρεπτικό υλικό Dulbecco s modified Eagle s medium θρεπτικό υλικό Ορός εμβρύου βοός (FBS) Πενικιλλίνη 100 U/mL / στρεπτομυκίνη μg/ml G418 [Leu 8,DTrp 22, 125 I-Tyr 25 ]SS28 Τρις(υδροξυμεθυλο)-αμινομεθάνιο (Tris) Drs. T. Reisine και G. Singh, (University of Pennsylvania, Philadelphia, USA) Dr. D. oyer (ovartis Pharma, Basel, Switzerland) Dr. S. Schulz ( University of Jena, Germany) Gibco, Grand Island, USA Gibco, Grand Island, USA Gibco, Grand Island, USA Biochrom AG, Berlin, Germany Gibco, Carlsbad, CA, USA Anawa, Wangen, Switzerland Merck, Darmstadt, Germany PBS p~7.4 (10 mm a 2P 4, 1.8 mm K 2P0 4, 2.7 mm KCl, 140 mm acl) Αλβουμίνη εμβρύου βοός (BSA) Sigma Diagnostics, St. Louis, USA Όργανα Κρυοστατικός τομογράφος Leitz 1720, Rockleigh, J, USA Α Β Σχήμα Γ.11: Αποικίες κυττάρων Α. C και Β. CCL 39 επιμολυσμένα με τον hsst 2 114
141 Γ. Πειραματικό Μέρος Οι μελέτες αυτές πραγματοποιήθηκαν στο Ινστιτούτο Παθολογίας του Πανεπιστημίου της Βέρνης από την ομάδα του Καθηγητή Jean-Claude Reubi. Χρησιμοποιήθηκαν κύτταρα C (Σχήμα Γ. 11. Α), τα οποία έχουν επιμολυνθεί ώστε να εκφράζουν μόνιμα τον υπότυπο hsst 1 (προσφορά των Drs. T. Reisine και G. Singh, University of Pennsylvania, Philadelphia, USA), τα κύτταρα CCL39 (Σχήμα Γ. 11. Β) τα οποία έχουν επιμολυνθεί ώστε να εκφράζουν μόνιμα τους υπότυπους hsst 2, hsst 3 και hsst 4 (προσφορά των Dr. D. oyer, ovartis Pharma, Basel, Switzerland) και τα κύτταρα EK293 τα οποία έχουν επιμολυνθεί ώστε να εκφράζουν τον υπότυπο hsst 5 (προσφορά του Dr. S. Schultz, Institute of Pharmacology and Toxicology, University ospital, Friedrich Schiller University Jena, Germany). Για τα κύτταρα C χρησιμοποιήθηκε το θρεπτικό υλικό am s F-12 και για τα κύτταρα CCL39 μίγμα δύο θρεπτικών υλικών: Dulbecco s modified Eagle s medium/am s F-12 (1:1). Για τα κύτταρα EK293 χρησιμοποιήθηκε το θρεπτικό υλικό Dulbecco s modified Eagle s medium. Το θρεπτικό υλικό και των τριών κυτταροσειρών περιείχε επίσης 10% (v/v) FBS, 100 U/mL πενικιλλίνη, 100 μg/ml στρεπτομυκίνη. Για τις καλλιέργειες των κυττάρων χρησιμοποιήθηκε επωαστικός κλίβανος ρυθμισμένος σε θερμοκρασία 37 0 C και υγρή ατμόσφαιρα 5% C 2. Το αντιβιοτικό γενετισίνη (G418-sulfate; Gibco, USA) χρησιμοποιήθηκε για τα επιμολυσμένα κύτταρα που εκφράζουν τους υπότυπους hsst 2, hsst 3 και hsst 4 σε τελική συγκέντρωση 400 μg/ml και για τα επιμολυσμένα κύτταρα που εκφράζουν τον υπότυπο hsst 5 σε τελική συγκέντρωση 500 μg/ml. Τα κύτταρα αποκολλήθηκαν από τον πυθμένα των φλασκών με ειδική ξύστρα, πλύθηκαν δύο φορές με ψυχρό διάλυμα 0.05 Μ Tris-Cl (p 7.4) και φυγοκεντρήθηκε το κυτταρικό εναιώρημα στα 120 g για 5 min στους 40 0 C. Τα κύτταρα επαναιωρήθηκαν σε ψυχρό διάλυμα 0.05 Μ Tris-Cl (p 7.4) και ακολούθησε η λύση τους με ομογενοποιητή (Polytron, Kinematica Inc., Littau, Switzerland). Ακολούθησε δεύτερη φυγοκέντρηση στα 120 g για 5 min στους 40 0 C, συλλέχθηκε το υπερκείμενο και φυγοκεντρήθηκε στα g για 30 min στους 40 0 C. Αφού απομακρύνθηκε το υπερκείμενο, το κυτταρικό παρασκεύασμα επαναιωρήθηκε σε ψυχρό διάλυμα 0.05 Μ Tris-Cl (p 7.4) και φυγοκεντρήθηκε στα g για 15 min στους 40 0 C. 115
142 Γ. Πειραματικό Μέρος Απομακρύνθηκε το υπερκείμενο και το κυτταρικό παρασκεύασμα αποθηκεύτηκε στους -80 C. Για τη μελέτη αυτοραδιογραφίας υποδοχέων πραγματοποιήθηκαν τομές πάχους 20 μm στο κυτταρικό παρασκεύασμα με τη βοήθεια κρυοστατικού τομογράφου (Leitz 1720, Rockleigh, J, USA). Οι τομές τοποθετήθηκαν σε αντικειμενοφόρες πλάκες μικροσκοπίου και αποθηκεύτηκαν στους -20 C πριν τη χρήση τους [41, 199]. Για κάθε ανάλογο χρησιμοποιήθηκε ως ραδιοπροσδέτης [Leu 8,DTrp 22, 125 I- Tyr 25 ]SS28 ( 125 I-[LTT]SS28) (2,000 Ci/mmol; Anawa, Wangen, Switzerland) 15,000 cpm/100 L. Το ανάλογο προς μελέτη προστέθηκε σε αυξανόμενες συγκεντρώσεις εύρους από 0.1 μέχρι 1000 nm. Η φυσική ορμόνη SS14 χρησιμοποιήθηκε ως ένωση αναφοράς. Οι τομές επωάστηκαν με 125 I-[LTT]SS28 για 2 h σε θερμοκρασία δωματίου σε μίγμα ρυθμιστικού διαλύματος Tris-Cl (170 mmol, p 8.2), 1% BSA, 40 mg/l βακιτρακίνη και 10 mmol/l MgCl 2. Στη συνέχεια οι τομές πλύθηκαν 2 5 min με ψυχρό διάλυμα Tris-Cl (170 mmol, p 8.2) που περιείχε 0.25% BSA. Ακολούθησε γρήγορο πλύσιμο με Tris-Cl (170 mmol, p 8.2), γρήγορο στέγνωμα και τα κύτταρα εκτέθηκαν για 1 εβδομάδα πάνω σε φιλμ υψηλής ευαισθησίας Kodak BioMax MR film. Ο προσδιορισμός των τιμών IC 50 έγινε μετά από ποσοτικοποίηση των δεδομένων χρησιμοποιώντας ειδική διάταξη ανάλυσης εικόνας με τη βοήθεια ηλεκτρονικού υπολογιστή. Για την ποσοτικοποίηση χρησιμοποιήθηκαν τα πρότυπα ιστών (Autoradiographic [ 125 I] and/or [ 14 C] microscales, GE ealthcare; Little Chalfont, UK), τα οποία περιείχαν γνωστές ποσότητες του ραδιονουκλιδίου, βαθμονομημένες ως προς ισοδύναμες συγκεντρώσεις προσδέτη [41]. 116
143 Γ. Πειραματικό Μέρος Γ.3.2 ΕΠΑΓΩΓΗ ΕΣΩΤΕΡΙΚΕΥΣΗΣ ΤΩΝ SST 1-5 ΜΕ ΜΙΚΡΟΣΚΟΠΙΑ ΑΝΟΣΟΦΘΟΡΙΣΜΟΥ Αντιδραστήρια EK293: εμβρυονικά κύτταρα από ανθρώπινο νεφρό με σταθερή έκφραση των hsst 2/hsst 3 Δισκία καλλιέργειας κυττάρων 4 φρεατίων (35 mm) Poly-D-Lysine Dulbecco s modified Eagle s medium θρεπτικό υλικό PS (100 mm φωσφορικό ρυθμιστικό διάλυμα και 0.15 M σακχαρόζη) Αλβουμίνη εμβρύου βοός (BSA) SS14 sst 2-ειδικό αντίσωμα R2-88 sst 3-ειδικό αντίσωμα SS-850 Aντίσωμα Alexa Fluor 488 goat anti-rabbit IgG (+L) Dr. S. Schulz ( University of Jena, Germany) Cellstar; Greiner Bio-ne Gmb Sigma-Aldrich, St. Louis, M Gibco, Grand Island, USA Ref.3 Sigma Diagnostics, St. Louis, USA J.E. Rivier, The Salk Institute, La Jolla, California, USA Agnes Schönbrunn, ouston, Texas, USA Gramsch Laboratories, Schwabhausen, Germany Molecular Probes, Inc., Eugene, R, USA Όργανα Leica DM RB μικροσκόπιο ανοσοφθορισμού Ref.3 lympus DP10 φωτογραφική μηχανή Ref.3 Α Β Σχήμα Γ.12: Αποικίες κυττάρων EK293 (εμβρυονικά κύτταρα από ανθρώπινο νεφρό) που εκφράζουν τον Α. hsst 2 και Β. hsst 3 όπως φαίνονται με μικροσκοπία ανοσοφθορισμού 117
144 Γ. Πειραματικό Μέρος Τα κύτταρα EK293-hsst 2 και EK293-hsst 3 (Σχήμα Γ. 12.Α και Β) τοποθετήθηκαν σε δισκία καλλιέργειας κυττάρων 4 φρεατίων επικαλυμμένα με Poly-D-Lysine. Σε κάθε πείραμα προστέθηκε στα κύτταρα το ανάλογο προς μελέτη αυξανόμενης συγκέντρωσης εύρους από 1 μέχρι 1000 nm για 30 min στους 37 0 C και παράλληλα η φυσική ορμόνη SS14 ως ένωση αναφοράς. Μετά το πέρας των 30 min τα κύτταρα ξεπλύθηκαν με PS. Στη συνέχεια προστέθηκε στα κύτταρα ψυχρή μεθανόλη (-20 0 C) για 7 min, ώστε να γίνουν διαπερατά, και ξεπλύθηκαν δύο φορές με PS. Για τη μείωση της μη ειδικής δέσμευσης πραγματοποιήθηκε επώαση των κυττάρων με PS το οποίο περιείχε 0.1% BSA σε θερμοκρασία δωματίου για 60 min. Ακολούθησε επώαση των κυττάρων για 60 min σε θερμοκρασία δωματίου με το sst 2 -ειδικό αντίσωμα R2-88 ή το sst 3 -ειδικό αντίσωμα SS-850 (και τα δύο διαλυτοποιημένα 1:1000 σε PS). Τα κύτταρα πλύθηκαν τρείς φορές (5 min για κάθε φορά) με PS που περιείχε 0.1% BSA. Τα κύτταρα επωάστηκαν για 60 min σε θερμοκρασία δωματίου σε σκοτεινό δωμάτιο με το αντίσωμα Alexa Fluor 488 goat anti-rabbit IgG (+L) διαλυμένο (1:600) σε PS. Τα κύτταρα πλύθηκαν τρείς φορές (5 min για κάθε φορά) με PS που περιείχε 0.1% BSA, ενσωματώθηκαν με PS/γλυκερόλη 1:1 και καλύφθηκαν με γυάλινη καλυπτρίδα. Η απεικόνιση των κυττάρων πραγματοποιήθηκε με μικροσκόπιο ανοσοφθορισμού Leica DM RB και φωτογραφική μηχανή lympus DP10 [38, 228]. 118
145 Γ. Πειραματικό Μέρος Γ.3.3 ΚΥΤΤΑΡΟΚΑΛΛΙΕΡΓΕΙΕΣ Αντιδραστήρια Κύτταρα AR4-2J από εξωκρινή καρκίνο του παγκρέατος επίμυα EK293: εμβρυονικά κύτταρα από ανθρώπινο νεφρό με σταθερή έκφραση των hsst 2A/hsst 3/hsst 5 Θρεπτικό υλικό F-12K Θρεπτικό υλικό Dulbecco s MEM GLUTAMAX-I Ορός εμβρύου βοός (FBS) Πενικιλλίνη U/mL / στρεπτομυκίνη μg/ml (PE/STREP) Θρυψίνη/EDTA 0.05 %/0.02 % (w/v) L-γλουταμίνη DMS YBRI-MAX G418 Αποστειρωμένα φίλτρα Millex-GS 0.22 μm Millipore Φλάσκες καλλιέργειας 75 cm 2 Ξύστρα για κύτταρα Πλαστικά κρυογονικά φιαλίδια Τρις(υδροξυμεθυλο)-αμινομεθάνιο (Tris) Δινάτριο άλας του αιθυλενοδιαμινοτετραοξικού οξέος (a 2EDTA) PBS p~7.4 (10 mm a 2P 4, 1.8 mm K 2P0 4, 2.7 mm KCl, 140 mm acl) Αλβουμίνη εμβρύου βοός (BSA) Prof. S. Mather ( St. Bartholomew s ospital, London, UK) Dr. S. Schulz ( University of Jena, Germany) Gibco, Grand Island, USA Gibco, Grand Island, USA Gibco, Grand Island, USA Biochrom AG, Berlin, Germany Biochrom AG, Berlin, Germany Biochrom AG, Berlin, Germany Sigma-Aldrich Chemie Gmb, Steinheim, Germany Gibco, Carlsbad, CA, USA Millipore, Milford, USA Greiner Bio-n, Frickenhausen, Germany Greiner Bio-n, Frickenhausen, Germany Greiner Bio-n, Frickenhausen, Germany Merck, Darmstadt, Germany Carlo Erba, Milan, Italy Sigma Diagnostics, St. Louis, USA Όργανα pμετρο p 211 microprocessor p meter Επωαστικός κλίβανος C 2 anna Instruments Srl, Sarmeola di Rubano, Italy Smart Cell- eal Force, ong Kong Εστία κάθετης νηματικής ροής αέρος Safe 2000-class II Ψυχόμενη Φυγόκεντρος Universal 32R με κεφαλή 1617 olten, Denmark ettich Intertnational Kirchlengern, Germany 119
146 Γ. Πειραματικό Μέρος Όργανα Ανάστροφο μικροσκόπιο τύπου 7002 Αιματοκυτταρόμετρο eubauer-improved, βάθος θαλάμου 0.1 mm Cryo 1 0 C freezing container Wang Biomedical, etherlands Poly-ptik Gmb, Germany algene Brand Products, Y, USA Δοχείο Dewars Β 2035 Cryo Diffusion, Lery, France Α Β Γ Σχήμα Γ.13: Α. Εστία κάθετης νηματικής ροής αέρος Safe 2000-class II. Β. Επωαστικός κλίβανος C 2 Smart Cell. Γ. Ψυχόμενη Φυγόκεντρος Universal 32R Γ ΚΑΛΛΙΕΡΓΕΙΑ ΚΥΤΤΑΡΙΚΩΝ ΣΕΙΡΩΝ Το κρυογονικό φιαλίδιο με τα κύτταρα ανασύρθηκε από το δοχείο υγρού αζώτου (Σχήμα Γ. 14. Β) και έμεινε για λίγα λεπτά σε θερμοκρασία δωματίου μέχρι να ξεπαγώσει. Το φιαλίδιο μεταφέρθηκε μέσα στην εστία κάθετης νηματικής ροής (Laminar Air Flow) (Σχήμα Γ. 13. Α) και στη συνέχεια τα κύτταρα που περιείχε μεταφέρθηκαν σε φλάσκα με θρεπτικό υλικό καλλιέργειας. Η φλάσκα τοποθετήθηκε στον επωαστικό κλίβανο (Σχήμα Γ. 13. Β) ρυθμισμένο σε θερμοκρασία 37 0 C και υγρή ατμόσφαιρα 5% C 2. Α Β Σχήμα Γ.14: Α. Δοχεία υγρού αζώτου. Β. Το κρυογονικό φιαλίδιο με τα κύτταρα ανασύρεται από το δοχείο υγρού αζώτου. 120
147 Γ. Πειραματικό Μέρος Κυτταρική σειρά AR4-2J Για τα κύτταρα AR4-2J χρησιμοποιήθηκε το θρεπτικό υλικό F-12K στο οποίο είχαν προστεθεί 10% (v/v) FBS, 1 mm L-γλουταμίνη, 100 U/mL πενικιλλίνη και 100 μg/ml στρεπτομυκίνη. Το FBS χρησιμοποιήθηκε μετά από θερμική απενεργοποίηση στους 56 0 C για 30 min. Κύτταρα ΗΕΚ293 για σταθερή έκφραση των hsst 2A / hsst 3 / hsst 5 Για τα κύτταρα EK293 χρησιμοποιήθηκε το θρεπτικό υλικό Dulbecco s MEM GLUTAMAX-I εμπλουτισμένο με 10% (v/v) FBS, 100 U/mL πενικιλλίνη, 100 μg/ml στρεπτομυκίνη και 0.75 mg/ml αντιβιοτικό G418. Όλη η διαδικασία της καλλιέργειας των καρκινικών κυττάρων έγινε σε άσηπτες συνθήκες μέσα σε θάλαμο νηματικής ροής. Το αντιβιοτικό G418 διαλυτοποιήθηκε με λίγα ml θρεπτικού υλικού και το διάλυμα πέρασε από αποστειρωμένο φίλτρο Millex-GS με διάμετρο 0.22 μm Millipore πριν προστεθεί στο θρεπτικό υλικό. Την επόμενη μέρα έγινε αλλαγή θρεπτικού υλικού ώστε να απομακρυνθεί το DMS που χρησιμοποιείται για την ψύξη των κυττάρων και η φλάσκα τοποθετήθηκε ξανά στον επωαστικό κλίβανο. Κάθε 2 μέρες γινόταν αλλαγή στο θρεπτικό υλικό των καλλιεργειών και κάθε 2-3 μέρες γινόταν ανακαλλιέργεια σε αναλογία 1:3 ή 1:4 ανάλογα με τον αριθμό κυττάρων που περιείχε η φλάσκα και με το ρυθμό πολλαπλασμού των κυττάρων, ο οποίος ελεγχόταν με οπτικό μικροσκόπιο. Όλες οι διαδικασίες γίνονταν μέσα σε θάλαμο νηματικής ροής. Για την ανακαλλιέργεια των κυττάρων, απομακρύνθηκε το θρεπτικό υλικό της καλλιέργειας και έγινε πλύση με αποστειρωμένο PBS. Ακολούθησε προσθήκη 4 ml διαλύματος θρυψίνης/edta σε κάθε φλάσκα και τοποθετήθηκαν για 5-10 min στον επωαστικό κλίβανο για να πραγματοποιηθεί η αποκόλληση των κυττάρων από τις φλάσκες. Οι φλάσκες μεταφέρθηκαν πάλι στο θάλαμο νηματικής ροής όπου και προστέθηκαν 8-10 ml θρεπτικού υλικού για να ανασταλεί η δράση της θρυψίνης. Ακολούθησε ανακατανομή σε νέες φλάσκες σε αναλογία 1:3 ή 1:4 και προστέθηκε επιπλέον θρεπτικό υλικό στην κάθε μια (Σχήμα Γ. 15. Β). 121
148 Γ. Πειραματικό Μέρος Οι φλάσκες τοποθετήθηκαν στον επωαστικό κλίβανο (Σχήμα Γ. 15. Γ). Α Β Γ Σχήμα Γ.15: Α. F-12K θρεπτικό υλικό, θρυψίνη/edta 0.05 %/0.02 % (w/v) και πιπέττα Greiner Maxipette. Β. Προσθήκη θρεπτικού υλικού στις φλάσκες. Γ. Τοποθέτηση φλασκών στον επωαστικό κλίβανο. Γ ΑΠΟΘΗΚΕΥΣΗ ΚΥΤΤΑΡΩΝ Απομακρύνθηκε το θρεπτικό υλικό της καλλιέργειας μέσα στο θάλαμο νηματικής ροής. Ακολούθησε προσθήκη 4 ml διαλύματος θρυψίνης/edta στις φλάσκες και έπειτα τοποθετήθηκαν για 5-10 min στον επωαστικό κλίβανο. Οι φλάσκες μεταφέρθηκαν πάλι στο θάλαμο νηματικής ροής όπου και προστέθηκαν 5 ml θρεπτικού υλικού για να ανασταλεί η δράση της θρυψίνης και ακολούθησε ήπια φυγοκέντρηση για 10 min (Σχήμα Γ. 13. Γ). Στη συνέχεια τα κύτταρα επαναιωρήθηκαν με προσθήκη 1 ml, ανά φλάσκα, ψυχρού διαλύματος κατάψυξης FBS + 5% DMS και το μίγμα μοιράστηκε σε κρυογονικά φιαλίδια. Τα κρυογονικά φιαλίδια τοποθετήθηκαν στο cryofreezing container ώστε να γίνει σταδιακή ψύξη και μεταφέρθηκαν σε καταψύκτη στους -80 C για 24 h. Την επόμενη ημέρα τα φιαλίδια αποθηκεύτηκαν σε δοχείο Dewars που περιείχε υγρό Ν 2 (Σχήμα Γ. 14. Α). 122
149 Γ. Πειραματικό Μέρος Γ ΜΕΤΡΗΣΗ ΑΡΙΘΜΟΥ ΚΥΤΤΑΡΩΝ Από μια φλάσκα απομακρύνθηκε το θρεπτικό υλικό της καλλιέργειας μέσα στο θάλαμο νηματικής ροής και ακολούθησε πλύση με αποστειρωμένο PBS και προσθήκη 4 ml διαλύματος θρυψίνης/edta (Σχήμα Γ. 16. Β). Η φλάσκα τοποθετήθηκε για 5-10 min στον επωαστικό κλίβανο Η φλάσκα μεταφέρθηκε πάλι στο θάλαμο νηματικής ροής όπου και προστέθηκαν 5 ml θρεπτικού υλικού. Σε φιαλίδιο τύπου Eppendorf αναμείχθηκαν 50 μl του παραπάνω εναιωρήματος κυττάρων από τη φλάσκα και 50 μl διαλύματος χρωστικής (0.25% (w/v) Trypan blue σε PBS), το οποίο χρωματίζει τα νεκρά κύτταρα. Η μεταφορά δείγματος από το μίγμα στο αιματοκυτόμετρο έγινε με πιπέτα και η μέτρηση των βιώσιμων κυττάρων (μη χρωματισμένα κύτταρα) με τη βοήθεια μικροσκοπίου (Σχήμα Γ. 16. Α). Α Β Σχήμα Γ.16: Α. Ανάστροφο μικροσκόπιο τύπου Β. Απομάκρυνση θρεπτικού υλικού από τις φλάσκες και προσθήκη διαλύματος θρυψίνης/edta. Γ.3.4 ΕΣΩΤΕΡΙΚΕΥΣΗ ΤΩΝ [ 111 In]ΑΤΧΣ Αντιδραστήρια Kύτταρα AR4-2J από εξωκρινή καρκίνο του παγκρέατος επίμυα EK293: εμβρυονικά κύτταρα από ανθρώπινο νεφρό με σταθερή έκφραση των hsst 2A/hsst 3/hsst 5 Prof. S. Mather ( St. Bartholomew s ospital, London, UK) Dr. S. Schulz ( University of Jena, Germany) 123
150 Γ. Πειραματικό Μέρος Αντιδραστήρια Θρεπτικό υλικό F-12K Gibco, Grand Island, USA Διάλυμα εσωτερίκευσης: F-12K + 1% FBS Θρεπτικό υλικό Dulbecco s MEM GLUTAMAX-I Gibco, Grand Island, USA Διάλυμα εσωτερίκευσης: Dulbecco s MEM GLUTAMAX-I + 1% FBS Ορός εμβρύου βοός (FBS) Gibco, Grand Island, USA PBS p~7.4 (10 mm a 2P 4, 1.8 mm K 2P0 4, 2.7 mm KCl, 140 mm acl)+ 0.5% BSA Αλβουμίνη εμβρύου βοός (BSA) Sigma Diagnostics, St. Louis, USA Ρυθμιστικό διάλυμα γλυκίνης, p 2.8 (50 mm γλυκίνη, 0.1 M acl) Διάλυμα 1 a Δοκιμαστικοί σωλήνες RIA διαστάσεων 75 mm 12 mm Δισκία καλλιέργειας κυττάρων 6 φρεατίων, επικαλυμμένα με Poly-D-Lysine Biosigma S.r.l, Cona (VE), Italy Greiner Bio-ne, Frickenhausen, Germany Όργανα Επωαστικός κλίβανος C 2 Εστία κάθετης νηματικής ροής αέρος Safe class II Ανάστροφο μικροσκόπιο τύπου 7002 pμετρο p 211 microprocessor p meter Αντλία RV3 Rotary Vane Pump Αυτόματος μετρητής γ-ακτινοβολίας πολλαπλών δειγμάτων κρυστάλλου ai(tl) Auto-Gamma 5000 Series Θερμαινόμενος θάλαμος-shaker τύπου Μ 201-R Smart Cell- eal Force, ong Kong olten, Denmark Wang Biomedical, etherlands anna Instruments Srl, Sarmeola di Rubano, Italy Edwards igh Vacuum International, West Sussex, UK Canberra Packard, Manchester, UK MPM Instruments Srl, Bernareggio, Italy Α Β Σχήμα Γ.17: Α. Θερμαινόμενος θάλαμος-shaker. Β. Δισκία καλλιέργειας κυττάρων 6 φρεατίων, επικαλυμμένα με Poly- D-Lysine 124
151 Γ. Πειραματικό Μέρος Στα πειράματα της εσωτερίκευσης χρησιμοποιήθηκαν τα κύτταρα AR4-2J, τα οποία ενδογενώς εκφράζουν τον rsst 2 και τα κύτταρα EK293 ώστε να εκφράζουν σταθερά τους hsst 3 ή hsst 5. Η καλλιέργεια των κυττάρων έγινε σε άσηπτες συνθήκες. Χρησιμοποιήθηκε 1 φλάσκα για 2 δισκία καλλιέργειας κυττάρων 6 φρεατίων (Σχήμα Γ. 17. Γ). Στο θάλαμο νηματικής ροής απομακρύνθηκε το θρεπτικό υλικό της φλάσκας, έγινε πλύση με αποστειρωμένο PBS και προστέθηκαν 4 ml διαλύματος θρυψίνης/edta. Η φλάσκα τοποθετήθηκε για 5-10 min στον επωαστικό κλίβανο. Η φλάσκα μεταφέρθηκε στο θάλαμο νηματικής ροής όπου και προστέθηκαν 5 ml θρεπτικού υλικού. Το εναιώρημα κυττάρων μεταφέρθηκε στα δισκία και μεταφέρθηκαν στο επωαστικό κλίβανο όπου και παρέμειναν για 48 h μέχρι πληρότητας κυττάρων στον πυθμένα των φρεατίων. Την ημέρα του πειράματος τα δισκία βγήκαν από τον επωαστικό κλίβανο και όλη η υπόλοιπη διαδικασία πραγματοποιήθηκε σε μη άσηπτες συνθήκες. Τα δισκία τοποθετήθηκαν σε πάγο και αφαιρέθηκε το υπερκείμενο. Ακολούθησε πλύσιμο των κυττάρων 2 φορές με 2 ml ψυχρού διαλύματος εσωτερίκευσης και μετά προσθήκη 1.2 ml (2 x 600 μl) διαλύματος εσωτερίκευσης σε θερμοκρασία 37 C. Στην επάνω τριπλέτα φρεατίων προστέθηκαν 150 μl διαλύματος εσωτερίκευσης θερμοκρασίας 37 C ανά φρεάτιο. Στην κάτω τριπλέτα προστέθηκαν 150 μl διαλύματος ΤΑΤΕ ή ΚΕ108 ή octreotide (σε διάλυμα εσωτερίκευσης με τελική συγκέντρωση 1 μμ) για τον προσδιορισμό της μη ειδικής δέσμευσης. Στη συνέχεια προστέθηκαν 150 μl (2 pmol πεπτιδίου και ραδιενέργεια μci) επισημασμένου αναλόγου [ 111 In]ATΧΣ, διαλυτοποιημένο σε PBS + 0.5% BSA, σε όλα τα φρεάτια και τα κύτταρα επωάστηκαν για 1 h στους 37 C (Σχήμα Γ. 17. Α). 125
152 Γ. Πειραματικό Μέρος Ο τερματισμός της επώασης πραγματοποιήθηκε με τοποθέτηση των δισκίων σε πάγο. Ακολούθησε συλλογή του υπερκειμένου σε αντίστοιχους δοκιμαστικούς σωλήνες RIA, προσθήκη 1 ml ψυχρού διαλύματος PSA + 0.5% BSA και ξανά συλλογή. Τα κύτταρα επωάστηκαν σε θερμοκρασία δωματίου με προσθήκη 0.6 ml ρυθμιστικού διαλύματος γλυκίνης p 2.8 για 5 min και συλλέχθηκε το υπερκείμενο το οποίο περιέχει το ποσοστό του ραδιοπεπτιδίου που δεσμεύτηκε στη κυτταρική μεμβράνη. Η διαδικασία αυτή επαναλήφθηκε και δεύτερη φορά και ακολούθησε πλύσιμο των κυττάρων με 1 ml διαλύματος PBS+ 0.5% BSA. Με προσθήκη 0.6 ml διαλύματος 1 a για λίγα λεπτά και κυκλική ανάδευση του δισκίου προκλήθηκε η αποκόλληση και η λύση των κυττάρων. Το προκύπτον εναιώρημα, το οποίο περιέχει το ποσοστό του εσωτερικευμένου πεπτιδίου, συλλέχθηκε στoυς αντίστοιχους δοκιμαστικούς σωλήνες RIA. Η διαδικασία επαναλήφθηκε άλλη μία φορά. Οι δοκιμαστικοί σωλήνες RIA μεταφέρθηκαν σε μετρητή γ ακτινοβολίας όπου και μετρήθηκε η ραδιενέργεια των κλασμάτων που συλλέχθηκαν (Σχήμα Γ. 18. Β). Με χρήση του λογισμικού προγράμματος Microsoft Excel υπολογίστηκε το ποσοστό της εσωτερικευμένης ραδιενέργειας ως προς την ολική ραδιενέργεια. Γ.3.5 ΜΕΤΑΒΟΛΙΣΜΟΣ ΤΩΝ 111 Ιn]ΑΤΧΣ ΣΕ ΥΓΙΗ ΠΟΝΤΙΚΙΑ Αντιδραστήρια Αρσενικά ποντίκια Swiss albino (7-8 εβδομάδων, g) Αποστειρωμένα φίλτρα Millex-GS 0.22 μm Millipore Σωληνάκια Eppendorf Σύριγγες αποστειρωμένες 1 ml Δινάτριο άλας του αιθυλενοδιαμινοτετραοξικού οξέος (a 2EDTA) Εκτροφείο πειραματοζώων ΕΚΕΦΕ «Δημόκριτος» Millipore, Milford, USA Eppendorf (Y, USA) PentaFerte, Campli, Italy Carlo Erba, Milan, Italy 126
153 Γ. Πειραματικό Μέρος Όργανα Χρωματογράφος Waters Ραδιομετρικός ανιχνευτής Gabi Αναλυτικές στήλες ανάστροφης φάσης: Symmetry Shield (RPM 5 μm, 3.9 mm 20 mm) Ψυχόμενη Φυγόκεντρος Universal 32R με κεφαλή 1617 Waters, Vienna, Austria Raytest, RSM Analytische Instrumente Gmb, Germany Waters, Milford, USA ettich Intertnational Kirchlengern, Germany Σε υγιή αρσενικά ποντίκια τύπου Swiss albino χορηγήθηκαν ενδοφλέβια στην ουρά 150 μl ραδιοπεπτιδίου [ 111 In]ATΧΣ (3 nmol πεπτιδίου και ραδιενέργεια μci). Τα πειραματόζωα παρέμειναν για 5 min σε κλουβί με ελεύθερη πρόσβαση σε νερό. Χρησιμοποιήθηκε αιθέρας για την αναισθητοποίηση των πειραματόζωων και ακολούθησε θανάτωση με καρδιεκτομή. Η συλλογή του αίματος έγινε με σύριγγα του 1 ml, το αίμα τοποθετήθηκε σε σωληνάκι Eppendorf που είχε ψυχθεί και περιείχε 8-10 μl EDTA. Αμέσως μετά τη συλλογή του αίματος το σωληνάκι τοποθετήθηκε σε πάγο. Το δείγμα αίματος φυγοκεντρήθηκε για 10 min στις 2000 g στους 4ºC. Το υπερκείμενο συλλέχθηκε σε προψυγμένο σωληνάκι Eppendorf και προστέθηκε ίση ποσότητα C 3 C. Το μίγμα φυγοκεντρήθηκε για 10 min στις g στους 4ºC. Το υπερκείμενο συλλέχθηκε σε άλλο σωληνάκι Eppendorf και με χρήση υγρού αζώτου απομακρύνθηκε ο διαλύτης. Έγινε επαναδιαλυτοποίηση με ορό και το διάλυμα πέρασε από φίλτρο τύπου 0.22 µm Millex-GS. Στη συνέχεια έγινε ανάλυση του διαλύματος με PLC (Σχήμα Γ. 8. Β) για να διαπιστωθεί αν υπάρχουν μεταβολίτες. Επιπλέον πραγματοποιήθηκε συν-ένεση του προτύπου [ 111 In]ΑΤΧΣ για τον προσδιορισμό του χρόνου έκλουσης του Χρησιμοποιήθηκε στήλη τύπου Symmetry Shield (RPM 5 μm, 3.9 mm 20 mm) και συστήματα έκλουσης γραμμικά μεταβαλλόμενης σύστασης : 127
154 Γ. Πειραματικό Μέρος 0% σε 40% Διαλύτη Β σε 40 min (Σύστημα Α) 0% σε 50% Διαλύτη Β σε 50 min (Σύστημα Β) (Διαλύτης Α : Η 2 Ο + 0.1% TFA και Διαλύτης B: C 3 C) Γ.3.6 ΒΙΟΚΑΤΑΝΟΜΗ ΤΩΝ 111 Ιn]ΑΤΧΣ Αντιδραστήρια Κύτταρα AR4-2J από εξωκρινή καρκίνο του παγκρέατος επίμυα EK293: εμβρυονικά κύτταρα από ανθρώπινο νεφρό με σταθερή έκφραση των hsst 2A/hsst 3/hsst 5 Ποντίκια Swiss albino (7-8 εβδομάδων, g) Ποντίκια τύπου SCID (6-8 εβδομάδων, g) Θρεπτικό υλικό F-12K Prof. S. Mather ( St. Bartholomew s ospital, London, UK) Dr. S. Schulz ( University of Jena, Germany) Εκτροφείο πειραματοζώων ΕΚΕΦΕ «Δημόκριτος» Εκτροφείο πειραματοζώων ΕΚΕΦΕ «Δημόκριτος Gibco, Grand Island, USA Θρεπτικό υλικό Dulbecco s MEM GLUTAMAX-I Gibco, Grand Island, USA Ορός εμβρύου βοός (FBS) Gibco, Grand Island, USA Αλβουμίνη εμβρύου βοός (BSA) Sigma Diagnostics, St. Louis, USA Πενικιλλίνη U/mL / στρεπτομυκίνη μg/ml (PE/STREP) Biochrom AG, Berlin, Germany Θρυψίνη/EDTA 0.05 %/0.02 % (w/v) Biochrom AG, Berlin, Germany L-γλουταμίνη Biochrom AG, Berlin, Germany PBS p~7.4 (10 mm a 2P 4, 1.8 mm K 2P0 4, 2.7 mm KCl, 140 mm acl) Σύριγγες αποστειρωμένες 1 ml Δοκιμαστικοί σωλήνες RIA διαστάσεων 75 mm 12 mm Χειρουργικές λεπίδες Τροφή αποστειρωμένη Κλουβιά 1284L με κάλυμμα εφοδιασμένο με ειδικό μικροβιοκρατές φίλτρο από 100% πολυεστέρα Σωληνάκια Eppendorf PentaFerte, Campli, Italy Biosigma S.r.l, Cona (VE), Italy Penta Ferte, Campli, Italy Mucedola Srl, Milano, Italy Tecniplast LAB-CEM, Αθήνα Eppendorf, Y, USA 128
155 Γ. Πειραματικό Μέρος Όργανα Ψυχόμενη Φυγόκεντρος Universal 32R Εστία κάθετης νηματικής ροής αέρος Safe class II Θάλαμος οριζόντιας νηματικής ροής (laminair) GELAIRE Class 100 Αυτόματος μετρητής γ-ακτινοβολίας πολλαπλών δειγμάτων κρυστάλλου ai(tl) Auto-Gamma 5000 Series ettich Intertnational Kirchlengern, Germany olten, Denmark Gelman Instrument S.p.A., Milano, Italy Canberra Packard, Manchester, UK Τα πρωτόκολλα πειραματισμού με ποντίκια SCID και Swiss albino πραγματοποιήθηκαν σύμφωνα με τους Εθνικούς και Ευρωπαϊκούς κανονισμούς χρήσης πειραματόζωων και είχαν εγκριθεί από το Ελληνικό Υπουργείο Αγροτικής Ανάπτυξης και Τροφίμων. Α Β Σχήμα Γ.18: Α. Θάλαμος οριζόντιας νηματικής ροής (laminair) GELAIRE Class 100. Β. Αυτόματος μετρητής γ- ακτινοβολίας πολλαπλών δειγμάτων κρυστάλλου ai(tl) Auto-Gamma 5000 Series Α Β Σχήμα Γ.19: Α. Ποντίκι Swiss albino. Β. Ποντίκι τύπου SCID Γ ΒΙΟΚΑΤΑΝΟΜΗ ΣΕ ΥΓΙΗ ΠΟΝΤΙΚΙΑ Για τα πειράματα βιοκατανομής χρησιμοποιήθηκαν ποντίκια Swiss albino (Σχήμα Γ. 19. Α) σε ομάδες των τριών ή τεσσάρων ποντικών για κάθε χρονικό σημείο. Σε κάθε πειραματόζωο χορηγήθηκε ενδοφλέβια στην ουρά 100 μl διαλύματος [ 111 In]ATΧΣ (10 pmol πεπτιδίου και ραδιενέργεια 1 2 μci). 129
156 Γ. Πειραματικό Μέρος Σε ομάδα πειραματοζώων συγχορηγήθηκε μαζί με το ραδιοπεπτίδιο 100 μl περίσσεια ψυχρού πεπτιδίου Tate (50 nmol) ή octreotide (50 nmol) ή KE108 (15 nmol), για τον in vivo αποκλεισμό υποδοχέων. Τα πειραματόζωα παρέμειναν σε κλουβί με ελεύθερη πρόσβαση σε νερό. Χρησιμοποιήθηκε αιθέρας για την αναισθητοποίηση των πειραματόζωων και ακολούθησε θανάτωση με καρδιεκτομή μετά από 1, 4 και 24 h. Αμέσως συλλέχθηκε το αίμα σε προζυγισμένα σωληνάκια αιματοκρίτη τα οποία μεταφέρθηκαν σε δοκιμαστικούς σωλήνες RIA και ζυγίστηκαν. Η ουρά των πειραματοζώων κόπηκε και ζυγίστηκε το βάρος τους. Ακολούθησε ανατομή (Σχήμα Γ. 23. Γ) και αφαίρεση-συλλογή των οργάνων ενδιαφέροντος: ήπατος, καρδιάς, νεφρών, στομαχιού, εντέρων, σπλήνα, δείγματος μυός, πνευμόνων, μηριαίου οστού και παγκρέατος (Σχήμα Γ. 24). Τα όργανα ζυγίστηκαν, μεταφέρθηκαν σε δοκιμαστικούς σωλήνες RIA και μετρήθηκε η ραδιενέργεια του κάθε δείγματος σε μετρητή γ-ακτινοβολίας (Σχήμα Γ. 25 Α και Β). Για τον υπολογισμό των αποτελεσμάτων ετοιμάστηκε πρότυπο διάλυμα του ραδιοπεπτιδίου το οποίο αντιστοιχεί στο 10% της χορηγούμενης δόσης. Από το διάλυμα αυτό μεταφέρθηκε 1 ml σε δοκιμαστικούς σωλήνες RIA, οι οποίοι τοποθετήθηκαν στην αρχή και στο τέλος κάθε σειράς δειγμάτων. Τα αποτελέσματα της βιοκατανομής υπολογίστηκαν ως ποσοστό της χορηγούμενης δόσης ανά γραμμάριο ιστού (%ID/g) σύμφωνα με τις παρακάτω εξισώσεις με την βοήθεια του λογισμικού προγράμματος Microsoft Excel. Για να υπολογίσουμε το % δόσης στο αίμα πολλαπλασιάζουμε με τον συντελεστή 0.07, καθώς ο όγκος του αίματος αποτελεί το 7% του βάρους του σώματος του πειραματοζώου. Αντίστοιχα για το % δόσης στους μυς πολλαπλασιάζουμε με 0.43, καθώς ο όγκος των μυών αποτελεί το 43% του βάρους του σώματος του πειραματοζώου. 130
157 Γ. Πειραματικό Μέρος Για την διόρθωση των μετρήσεων σε σχέση με τον χρόνο υποδιπλασιασμού του ραδιονουκλιδίου χρησιμοποιείται πρότυπο διάλυμα που αντιστοιχεί στο 10% της χορηγούμενης δόσης. Κατόπιν 1 ml από αυτό το διάλυμα μεταφέρεται σε σωληνάκια και τοποθετείται στο μετρητή γ- ακτινοβολίας στην αρχή και στο τέλος των δειγμάτων προς μέτρηση (Σχήμα Γ. 20. Α και Β). Η εξίσωση που δίνει το πρότυπο 10% είναι η: όπου: Σ: σύνολο cpm δειγμάτων προτύπου Ν: σύνολο δειγμάτων προτύπου D: συντελεστής αραίωσης της χορηγούμενης δόσης κατά την ετοιμασία του προτύπου διαλύματος Όταν η χορήγηση του ραδιοπεπτιδίου γίνεται από την φλέβα της ουράς, αφαιρούνται οι κρούσεις της ουράς γιατί ποσότητα του ραδιοπεπτιδίου μπορεί να παραμείνει στην ουρά χωρίς να εισέλθει στην κυκλοφορία του αίματος. Α Β Σχήμα Γ.20: Α. Προετοιμασία πρότυπου διαλύματος του ραδιοπεπτιδίου. Β. Δοκιμαστικοί σωλήνες RIA με πρότυπο διάλυμα ραδιοπεπτιδίου. 131
Ραδιοεπισηµασµένα Πεπτίδια στην Ογκολογία
 Ραδιοεπισηµασµένα Πεπτίδια στην Ογκολογία Θεοδοσία Μάϊνα Berthold ock Εργαστήριο Ραδιοφαρµάκων Ινστιτούτο Ραδιοϊσοτόπων - Ραδιοδιαγνωστικών Προϊόντων, ΕΚΕΦΕ «ηµόκριτος», Αθήνα Στόχευση µε ραδιοπεπτίδια
Ραδιοεπισηµασµένα Πεπτίδια στην Ογκολογία Θεοδοσία Μάϊνα Berthold ock Εργαστήριο Ραδιοφαρµάκων Ινστιτούτο Ραδιοϊσοτόπων - Ραδιοδιαγνωστικών Προϊόντων, ΕΚΕΦΕ «ηµόκριτος», Αθήνα Στόχευση µε ραδιοπεπτίδια
ιάγνωση και Θεραπεία µε Ραδιονουκλίδια
 ιάγνωση και Θεραπεία µε Ραδιονουκλίδια Θεοδοσία Μάϊνα Εργαστήριο Ραδιοφαρµάκων Ινστιτούτο Ραδιοϊσοτόπων - Ραδιοδιαγνωστικών Προϊόντων, ΕΚΕΦΕ «ηµόκριτος», Αθήνα Απεικόνιση µε ακτίνες-χ Wilhelm Röntgen,
ιάγνωση και Θεραπεία µε Ραδιονουκλίδια Θεοδοσία Μάϊνα Εργαστήριο Ραδιοφαρµάκων Ινστιτούτο Ραδιοϊσοτόπων - Ραδιοδιαγνωστικών Προϊόντων, ΕΚΕΦΕ «ηµόκριτος», Αθήνα Απεικόνιση µε ακτίνες-χ Wilhelm Röntgen,
HY 673 - Ιατρική Απεικόνιση. Στέλιος Ορφανουδάκης Κώστας Μαριάς. Σημειώσεις II: Πυρηνική Ιατρική
 HY 673 - Ιατρική Απεικόνιση Στέλιος Ορφανουδάκης Κώστας Μαριάς Σημειώσεις II: Πυρηνική Ιατρική Σεπτέμβριος 2003-Φεβρουάριος 2004 Πυρηνική Ιατρική Εισαγωγή Η Πυρηνική Ιατρική είναι κλάδος της ιατρικής που
HY 673 - Ιατρική Απεικόνιση Στέλιος Ορφανουδάκης Κώστας Μαριάς Σημειώσεις II: Πυρηνική Ιατρική Σεπτέμβριος 2003-Φεβρουάριος 2004 Πυρηνική Ιατρική Εισαγωγή Η Πυρηνική Ιατρική είναι κλάδος της ιατρικής που
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν;
 Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
Ποια είναι κατά τη γνώμη σας τα 30 μικρομόρια που συνιστούν τα πρόδρομα μόρια των βιομακρομορίων; Πώς μπορούν να ταξινομηθούν; Γενικά Για να προσδιορίσουμε τα 30 πρόδρομα μόρια των βιομακρομορίων θα πρέπει
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ
 ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
ΕΦΑΡΜΟΓΕΣ ΤΗΣ ΒΙΟΤΕΧΝΟΛΟΓΙΑΣ ΣΤΗΝ ΙΑΤΡΙΚΗ Καθώς η επιστημονική γνώση και κατανόηση αναπτύσσονται, ο μελλοντικός σχεδιασμός βιοτεχνολογικών προϊόντων περιορίζεται μόνο από τη φαντασία μας Βιοτεχνολογία
Ραδιοεπισηµασµένα βιοµόρια στη διάγνωση και στη θεραπευτική αντιµετώπιση του καρκίνου Μ. Φάνη, Π. Μπουζιώτη
 Ραδιοεπισηµασµένα βιοµόρια στη διάγνωση και στη θεραπευτική αντιµετώπιση του καρκίνου Μ. Φάνη, Π. Μπουζιώτη Εργαστήριο Ραδιοφαρµακολογικών Μελετών Ινστιτούτο Ραδιοϊσοτόπων-Ραδιοδιαγνωστικών Προϊόντων Ε.Κ.Ε.Φ.Ε
Ραδιοεπισηµασµένα βιοµόρια στη διάγνωση και στη θεραπευτική αντιµετώπιση του καρκίνου Μ. Φάνη, Π. Μπουζιώτη Εργαστήριο Ραδιοφαρµακολογικών Μελετών Ινστιτούτο Ραδιοϊσοτόπων-Ραδιοδιαγνωστικών Προϊόντων Ε.Κ.Ε.Φ.Ε
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Δ ΕΣΠΕΡΙΝΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Δ ΤΑΞΗΣ ΕΣΠΕΡΙΝΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΗΜΕΡΙΔΑ ΧΗΜΕΙΑΣ 2017 Ραδιενέργεια και εφαρμογές στην Ιατρική
 ΗΜΕΡΙΔΑ ΧΗΜΕΙΑΣ 2017 Ραδιενέργεια και εφαρμογές στην Ιατρική Μαριάννα Κοκόλη Ραδιενέργεια: εκπομπή σωματιδίων ή ηλεκτρομαγνητικής ακτινοβολίας από ορισμένους ασταθείς πυρήνες ατόμων στοιχείων που ονομάζονται
ΗΜΕΡΙΔΑ ΧΗΜΕΙΑΣ 2017 Ραδιενέργεια και εφαρμογές στην Ιατρική Μαριάννα Κοκόλη Ραδιενέργεια: εκπομπή σωματιδίων ή ηλεκτρομαγνητικής ακτινοβολίας από ορισμένους ασταθείς πυρήνες ατόμων στοιχείων που ονομάζονται
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών
 Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
Χηµική Μεταβίβαση Σήµατος Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τµήµα Γεωπονικής Βιοτεχνολογίας, Γεωπονικό Πανεπιστήµιο Αθηνών 1 Η Επικοινωνία στα Ζωϊκά Κύτταρα 1. Δίκτυα εξωκυτταρικών και ενδοκυτταρικών
ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
 ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
ΜΙΝΟΠΕΤΡΟΣ ΚΩΝΣΤΑΝΤΙΝΟΣ ΦΥΣΙΚΟΣ - Ρ/Η ΚΑΘΗΓΗΤΗΣ ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΥΠΕΥΘΥΝΟΣ ΣΕΦΕ 2 ου ΕΝΙΑΙΟΥ ΛΥΚΕΙΟΥ ΠΕΡΑΜΑΤΟΣ ΕΡΓΑΣΤΗΡΙΑΚΗ ΑΣΚΗΣΗ ΒΙΟΛΟΓΙΑΣ ΚΑΤΕΥΘΥΝΣΗΣ Γ ΛΥΚΕΙΟΥ ΑΝΤΙΓΡΑΦΗ ΚΑΙ ΕΚΦΡΑΣΗ ΤΗΣ ΓΕΝΕΤΙΚΗΣ ΠΛΗΡΟΦΟΡΙΑΣ
MAΘΗΜΑ 4 ο AMINOΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ
 MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
MAΘΗΜΑ 4 ο AMIΞΕΑ-ΠΕΠΤΙ ΙΑ-ΠΡΩΤΕΪΝΕΣ Αλανίνη (Αla) Αλανυλοσερίνη (Αla-Ser) Αλβουµίνη ρα. Κουκουλίτσα Αικατερίνη Χηµικός Εργαστηριακός Συνεργάτης Τ.Ε.Ι Αθήνας ckoukoul@teiath.gr AMIΞΕΑ 2 λειτουργικές οµάδες
Συστήματα επικοινωνίας Ανθρωπίνου σώματος. ενδοκρινολογικό νευρικό σύστημα
 Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κύτταρο Το κύτταρο αποτελείται από μέρη τα οποία έχουν συγκεκριμένη δομή και επιτελούν μία συγκεκριμένη λειτουργία στην όλη οργάνωση του κυττάρου. Δομή κυτταροπλασματικής μεμβράνης Συστήματα επικοινωνίας
Κανονικη Εξεταστικη
 Κανονικη Εξεταστικη 29-1-2015 1ο: - Ποιοι παραγοντες επηρεαζουν τη δοση που χορηγειται στον εξεταζομενο κατα την ακτινογραφια 2ο: - Που οφειλεται το γραμμικο φασμα ακτινων χ, και να κανουμε το σχημα της
Κανονικη Εξεταστικη 29-1-2015 1ο: - Ποιοι παραγοντες επηρεαζουν τη δοση που χορηγειται στον εξεταζομενο κατα την ακτινογραφια 2ο: - Που οφειλεται το γραμμικο φασμα ακτινων χ, και να κανουμε το σχημα της
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ. ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ
 ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΘΕΩΡΙΑ 3 η ΠΑΡΟΥΣΙΑΣΗ ΚΥΤΤΑΡΟΚΙΝΕΣ ή ΚΥΤΤΟΚΙΝΕΣ Dr ΠΑΠΑΓΙΑΝΝΗΣ ΔΗΜΗΤΡΗΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΤΕΙ ΘΕΣΣΑΛΙΑΣ Είδαμε ότι οι ΜΗΧΑΝΙΣΜΟΙ ΜΗ ΕΙΔΙΚΗΣ ΑΝΟΣΙΑΣ είναι 1. Ανατομικοί φραγμοί - Δέρμα - Βλεννώδεις
ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ
 2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
2. ΜΕΤΑΒΟΛΙΚΟ ΜΟΝΤΕΛΟ ΑΠΕΙΚΟΝΙΣΗΣ ΤΩΝ ΟΓΚΩΝ Οι όγκοι χαρακτηρίζονται από πολλαπλές αλλαγές του μεταβολισμού. Η χαρακτηριστική μεταβολική λειτουργία μπορεί να μετρηθεί in vivo με τη βοήθεια ενός ραδιοσημασμένου
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΟΡΜΟΝΕΣ ΚΑΙ ΑΣΚΗΣΗ. ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.
 MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΟΡΜΟΝΕΣ ΚΑΙ ΑΣΚΗΣΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Αδένες Έκκρισης Ορμονών Υπόφυση Θυρεοειδής Αδένας Παραθυροειδείς
MANAGING AUTHORITY OF THE OPERATIONAL PROGRAMME EDUCATION AND INITIAL VOCATIONAL TRAINING ΟΡΜΟΝΕΣ ΚΑΙ ΑΣΚΗΣΗ ΘΑΝΑΣΗΣ ΤΖΙΑΜΟΥΡΤΑΣ, Ph.D., C.S.C.S Αδένες Έκκρισης Ορμονών Υπόφυση Θυρεοειδής Αδένας Παραθυροειδείς
ΚΕΦΑΛΑΙΟ 15. Κυτταρική ρύθμιση. Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1
 ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
ΚΕΦΑΛΑΙΟ 15 Κυτταρική ρύθμιση Ακαδημαϊκές Εκδόσεις 2011 Το κύτταρο-μια Μοριακή Προσέγγιση 1 ΕΙΚΟΝΑ 15.1 Μηχανισμοί διακυτταρικής σηματοδότησης. Η διακυτταρική σηματοδότηση μπορεί να συμβαίνει είτε απευθείας
ΦΑΡΜΑΚΟ ΥΝΑΜΙΚΗ ΙΙ. Γενικές έννοιες (Θεωρία υποδοχέων - Αγωνιστής ανταγωνιστής) Σηµεία ράσης Μοριακοί Μηχανισµοί ράσης Φαρµάκων
 ΦΑΡΜΑΚΟ ΥΝΑΜΙΚΗ ΙΙ Γενικές έννοιες (Θεωρία υποδοχέων - Αγωνιστής ανταγωνιστής) Σηµεία ράσης Μοριακοί Μηχανισµοί ράσης Φαρµάκων Υποδοχείς (φαρµάκων) και ενδοκυττάριες σηµατοδοτικές πορείες - Συστήµατα Μεταγωγής
ΦΑΡΜΑΚΟ ΥΝΑΜΙΚΗ ΙΙ Γενικές έννοιες (Θεωρία υποδοχέων - Αγωνιστής ανταγωνιστής) Σηµεία ράσης Μοριακοί Μηχανισµοί ράσης Φαρµάκων Υποδοχείς (φαρµάκων) και ενδοκυττάριες σηµατοδοτικές πορείες - Συστήµατα Μεταγωγής
Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων. 1/10/2015 Δ.Δ. Λεωνίδας
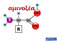 αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
αμινοξέα Οι πρωτεΐνες δομούνται από ένα σύνολο αμινοξέων Λυσίνη CORN Ισομερές L Ισομερές D R = πλευρική αλυσίδα (side chain) Τα περισσότερα αμινοξέα είναι ασύμμετρα Όλα τα αμινοξέα που βρίσκονται στις
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
Ραδιενεργές διασπάσεις. Ραδιονουκλίδια στην ιατρική
 Ραδιενεργές διασπάσεις Ραδιονουκλίδια στην ιατρική Νουκλίδια Οι πυρήνες µε διαφορετικό αριθµό πρωτονίων ή/και νετρονίων ονοµάζονται νουκλίδια. Υπάρχουν 1500 περίπου νουκλίδια (φυσικά +τεχνητά). Η ενέργεια
Ραδιενεργές διασπάσεις Ραδιονουκλίδια στην ιατρική Νουκλίδια Οι πυρήνες µε διαφορετικό αριθµό πρωτονίων ή/και νετρονίων ονοµάζονται νουκλίδια. Υπάρχουν 1500 περίπου νουκλίδια (φυσικά +τεχνητά). Η ενέργεια
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ
 ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΚΕΦΑΛΑΙΟ 9 ο ΣΤΡΑΤΗΓΙΚΕΣ ΚΑΤΑΛΥΣΗΣ Είδαμε τους μηχανισμούς με τους οποίους καταλύονται οι χημικές/βιολογικές αντιδράσεις (θα επανέλθουμε αν έχουμε χρόνο) Θα εξετάσουμε δύο παραδείγματα ενζύμων και του
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ. Οι ρυθμιστές του οργανισμού
 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
Καραπέτσας Θανάσης. Διπλωματική Εργασία:
 Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
Διαπανεπιστημιακό Πρόγραμμα Μεταπτυχιακών Σπουδών «Κλινική Φαρμακολογία & Θεραπευτική» Επιβλέπων: Δρ. Αλ. Γαλάνης, Λέκτορας Μορ. Βιολογίας, «Σχεδιασμός Ειδικών Πεπτιδίων Αναστολέων της Αλληλεπίδρασης του
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ
 ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΕΙΣΑΓΩΓΗ ΣΤΗ ΔΙΑΤΡΟΦΗ Ενότητα 8η - Μέρος Α ΠΡΩΤΕΪΝΕΣ Όνομα καθηγητή: Μ. ΚΑΨΟΚΕΦΑΛΟΥ Όνομα καθηγητή: Α. ΖΑΜΠΕΛΑΣ Τμήμα: Επιστήμης τροφίμων και διατροφής του ανθρώπου ΣΤΟΧΟΙ ΤΟΥ ΜΑΘΗΜΑΤΟΣ Η δομή των πρωτεϊνών
ΡΑΔΙΟΒΙΟΛΟΓΙΑ. Εξάμηνο Υ/Ε Ώρες Θεωρίας Ώρες Ασκήσης Διδακτικές μονάδες ECTS Ζ Ε Διδάσκων
 ΡΑΔΙΟΒΙΟΛΟΓΙΑ Εξάμηνο Υ/Ε Ώρες Θεωρίας Ώρες Ασκήσης Διδακτικές μονάδες ECTS Ζ Ε 2 0 2 2 Διδάσκων Α. Ζησιμόπουλος, Επίκουρος Καθηγητής Πυρηνικής Ιατρικής, Τμήμα Ιατρικής ΔΠΘ. Aντικειμενικοί στόχοι του μαθήματος
ΡΑΔΙΟΒΙΟΛΟΓΙΑ Εξάμηνο Υ/Ε Ώρες Θεωρίας Ώρες Ασκήσης Διδακτικές μονάδες ECTS Ζ Ε 2 0 2 2 Διδάσκων Α. Ζησιμόπουλος, Επίκουρος Καθηγητής Πυρηνικής Ιατρικής, Τμήμα Ιατρικής ΔΠΘ. Aντικειμενικοί στόχοι του μαθήματος
 ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΛΑ Β ) ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από
ΘΕΜΑ Α ΠΑΝΕΛΛΗΝΙΕΣ ΕΞΕΤΑΣΕΙΣ Γ' ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΚΑΙ ΕΠΑΛ (ΟΜΑΛΑ Β ) ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από
Φυσιολογία ΙΙ Ενότητα 2:
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 2: Ορμόνες Ανωγειανάκις Γεώργιος Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Ενότητα 2: Ορμόνες Ανωγειανάκις Γεώργιος Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης Creative Commons. Για εκπαιδευτικό
ΠΥΡΗΝΙΚΗ ΙΑΤΡΙΚΗ ΚΑΙ ΤΟΜΟΓΡΑΦΙΑ SPECT
 ΠΥΡΗΝΙΚΗ ΙΑΤΡΙΚΗ ΚΑΙ ΤΟΜΟΓΡΑΦΙΑ SPECT ΚΑΘΗΓΗΤΗΣ Δ. ΚΟΥΤΣΟΥΡΗΣ Εισαγωγή Πυρηνική Ιατρική: διαγνωστικές και θεραπευτικές διαδικασίες που απαιτούν την εισαγωγή ραδιενέργειας στον οργανισμό με ενδοφλέβια ένεση,
ΠΥΡΗΝΙΚΗ ΙΑΤΡΙΚΗ ΚΑΙ ΤΟΜΟΓΡΑΦΙΑ SPECT ΚΑΘΗΓΗΤΗΣ Δ. ΚΟΥΤΣΟΥΡΗΣ Εισαγωγή Πυρηνική Ιατρική: διαγνωστικές και θεραπευτικές διαδικασίες που απαιτούν την εισαγωγή ραδιενέργειας στον οργανισμό με ενδοφλέβια ένεση,
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας
 ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 12 ο Κυτταρική Βιολογία (νανομετρικό μέγεθος) - Βιοδείκτες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ)
ΒΙΟΤΕΧΝΟΛΟΓΙΑ ΣΤ ΕΞΑΜΗΝΟΥ Τμήμα Ιατρικών Εργαστηρίων Τ.Ε.Ι. Αθήνας Μάθημα 12 ο Κυτταρική Βιολογία (νανομετρικό μέγεθος) - Βιοδείκτες Διδάσκων Δρ. Ιωάννης Δρίκος Απόφοιτος Ιατρικής Σχολής Ιωαννίνων (ΠΙ)
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
Μοριακή Bιολογία ΔIAΛEΞΕΙΣ 11-13 OΔΟΙ ΚΑΙ ΜΗΧΑΝΙΣΜΟΙ ΕΥΚΑΡΥΩΤΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Χρήστος Παναγιωτίδης, Ph.D. Καθηγητής Κυτταρικής/Μοριακής
15/1/2018. Δρ. Σάββας Παρασκευόπουλος Χειρουργός Ουρολόγος Θεσσαλονίκη 2-5 /11/ ο Μακεδονικό Ουρολογικό Συμπόσιο
 Η χρήση του PET CT στην Ογκολογία και όχι μόνο Δρ. Σάββας Παρασκευόπουλος Χειρουργός Ουρολόγος Θεσσαλονίκη 2-5 /11/2017 11ο Μακεδονικό Ουρολογικό Συμπόσιο 1 Τι είναι το PET SCAN; Η Pet scan (pozitron emission
Η χρήση του PET CT στην Ογκολογία και όχι μόνο Δρ. Σάββας Παρασκευόπουλος Χειρουργός Ουρολόγος Θεσσαλονίκη 2-5 /11/2017 11ο Μακεδονικό Ουρολογικό Συμπόσιο 1 Τι είναι το PET SCAN; Η Pet scan (pozitron emission
Τάξη. Γνωστικό αντικείµενο: Ειδικοί διδακτικοί στόχοι
 Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
Αµινοξέα και πεπτίδια Τάξη Μάθηµα Γνωστικό αντικείµενο: ιδακτική ενότητα Απαιτούµενος χρόνος Χηµεία,Βιοχηµεία. Αµινοξέα και πεπτίδια 2 διδακτικές ώρες Ειδικοί διδακτικοί στόχοι Οι διδακτικοί στόχοι αυτών
ΠΟΖΙΤΡΟΝΙΑΚΗ ΤΟΜΟΓΡΑΦΙΑ (PET) ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΚΑΙ ΕΦΑΡΜΟΓΕΣ
 ΠΟΖΙΤΡΟΝΙΑΚΗ ΤΟΜΟΓΡΑΦΙΑ (PET) ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΚΑΙ ΕΦΑΡΜΟΓΕΣ Η Ποζιτρονιακή τομογραφία (PET) είναι μια μοριακή τομογραφική τεχνική η οποία μελετά με τη βοήθεια ειδικών ραδιοφαρμάκων που εκπέμπουν ποζιτρόνια
ΠΟΖΙΤΡΟΝΙΑΚΗ ΤΟΜΟΓΡΑΦΙΑ (PET) ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΚΑΙ ΕΦΑΡΜΟΓΕΣ Η Ποζιτρονιακή τομογραφία (PET) είναι μια μοριακή τομογραφική τεχνική η οποία μελετά με τη βοήθεια ειδικών ραδιοφαρμάκων που εκπέμπουν ποζιτρόνια
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
Ηεξέλιξη της πολυκυτταρικότητας
 ΚΥΤΤΑΡΙΚΗ ΕΠΙΚΟΙΝΩΝΙΑ Τα κύτταρα επικοινωνούν µεταξύ τους και µε το περιβάλλον προκειµένου να συντονίζουν τις λειτουργίες που απαιτούνται για την αύξηση, ανάπτυξη και λειτουργία ενός οργανισµού Η επικοινωνία
ΚΥΤΤΑΡΙΚΗ ΕΠΙΚΟΙΝΩΝΙΑ Τα κύτταρα επικοινωνούν µεταξύ τους και µε το περιβάλλον προκειµένου να συντονίζουν τις λειτουργίες που απαιτούνται για την αύξηση, ανάπτυξη και λειτουργία ενός οργανισµού Η επικοινωνία
Γαστρεντερικές ορμόνες, νεύρωση & αιμάτωση. Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ.
 Γαστρεντερικές ορμόνες, νεύρωση & αιμάτωση Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 02/12/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Οικογένεια
Γαστρεντερικές ορμόνες, νεύρωση & αιμάτωση Σωτήρης Ζαρογιάννης Επίκ. Καθηγητής Φυσιολογίας Εργαστήριο Φυσιολογίας Τμήμα Ιατρικής Π.Θ. 02/12/2016 Φυσιολογία Συστημάτων Ακαδημαϊκό Ετος 2016-2017 Οικογένεια
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ
 ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
ΒΙΟΧΗΜΕΙΑ ΤΟΥ ΜΕΤΑΒΟΛΙΣΜΟΥ ΠΑΡΟΥΣΙΑΣΗ 6 Η ΚΑΤΑΝΑΛΩΣΗ ΥΔΑΤΑΝΘΡΑΚΩΝ ΚΑΙ ΡΥΘΜΙΣΗ ΤΗΣ ΓΛΥΚΑΙΜΙΑΣ 1 Έλεγχος της ενέργειας Τα πραγματικά «Βιοκαύσιμα» 2 Υδατανθρακούχα τρόφιμα 3 Σημασία της ρύθμισης κατανάλωσης
COOH R 2. H α-αμινοξύ 2
 7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
7 Χαρακτηριστικές χημικές αντιδράσεις των πρωτεϊνών Στόχος της άσκησης: Κατανόηση της χημικής σύστασης των πρωτεϊνών. Η εξοικείωση με σημαντικές ιδιότητες των πρωτεϊνών και αμινοξέων: παρουσία των ιοντικών
Κυτταρική Βιολογία. Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής ΑΠΘ
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Κυτταρική Βιολογία Ενότητα 12 : Απόπτωση ή Προγραμματισμένος κυτταρικός θάνατος Παναγιωτίδης Χρήστος ΑΠΘ Άδειες Χρήσης Το παρόν εκπαιδευτικό
Η κυτταρική µετατόπιση των πρωτεϊνών
 9-1 Κεφάλαιο 9 Η κυτταρική µετατόπιση των πρωτεϊνών Εισαγωγή Στο κύτταρο η έκφραση των πρωτεϊνών γίνεται από µόνο ένα τύπο ριβοσώµατος (εκτός των µιτοχονδριακών και των χλωροπλαστικών που µοιάζουν µε αυτά
9-1 Κεφάλαιο 9 Η κυτταρική µετατόπιση των πρωτεϊνών Εισαγωγή Στο κύτταρο η έκφραση των πρωτεϊνών γίνεται από µόνο ένα τύπο ριβοσώµατος (εκτός των µιτοχονδριακών και των χλωροπλαστικών που µοιάζουν µε αυτά
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ
 ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
ΜΟΝΟΠΑΤΙΑ ΕΝΔΟΚΥΤΤΑΡΙΚΗΣ ΜΕΤΑΓΩΓΗΣ ΣΗΜΑΤΟΣ Το ένζυμο Αδενυλική κυκλάση, υπεύθυνο για τη βιοσύνθεση του camp. Το camp είναι ένα παράδειγμα μορίου «αγγελιοφόρου» καθοδικά των G πρωτεινών Αύξηση του camp
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ
 11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
11. ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Στον ανθρώπινο οργανισμό υπάρχουν δύο είδη αδένων, οι εξωκρινείς και οι ενδοκρινείς. Οι εξωκρινείς (ιδρωτοποιοί αδένες, σμηγματογόνοι αδένες κ.ά.) εκκρίνουν το προϊόν τους στην επιφάνεια
University of Cyprus Biomedical Imaging and Applied Optics. HMY 370 Εισαγωγή στη Βιοϊατρική Μηχανική. Πυρηνική Απεικόνιση
 University of Cyprus Biomedical Imaging and Applied Optics HMY 370 Εισαγωγή στη Βιοϊατρική Μηχανική Πυρηνική Απεικόνιση Πυρηνική Ιατρική Ακόμα ένας τρόπος για να βλέπουμε μέσα στο ανθρώπινο σώμα Χρησιμοποιούνται
University of Cyprus Biomedical Imaging and Applied Optics HMY 370 Εισαγωγή στη Βιοϊατρική Μηχανική Πυρηνική Απεικόνιση Πυρηνική Ιατρική Ακόμα ένας τρόπος για να βλέπουμε μέσα στο ανθρώπινο σώμα Χρησιμοποιούνται
ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ
 ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ Βασικές γνώσεις I SBN 960-372-069-0 ΠΕΡΙΕΧΟΜΕΝΑ ΠΑΡΙΣ Α. ΚΟΣΜΙΔΗΣ ΓΕΩΡΓΙΟΣ ΤΣΑΚΙΡΗΣ Μ Ε Ρ Ο Σ Ι ΟΓΚΟΛΟΓΙΑ Κεφάλαιο 1 ΕΙΣΑΓΩΓΗ ΣΤΟΝ ΚΑΡΚΙΝΟ... 3 Το καρκινικό κύτταρο... 3 Κυτταρικός
ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ Βασικές γνώσεις I SBN 960-372-069-0 ΠΕΡΙΕΧΟΜΕΝΑ ΠΑΡΙΣ Α. ΚΟΣΜΙΔΗΣ ΓΕΩΡΓΙΟΣ ΤΣΑΚΙΡΗΣ Μ Ε Ρ Ο Σ Ι ΟΓΚΟΛΟΓΙΑ Κεφάλαιο 1 ΕΙΣΑΓΩΓΗ ΣΤΟΝ ΚΑΡΚΙΝΟ... 3 Το καρκινικό κύτταρο... 3 Κυτταρικός
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2015 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Τι είναι οι πρωτεΐνες Βασικά σημεία Οργανικά μεγαλομόρια που αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΤΕΛΟΣ 1ΗΣ ΑΠΟ 6 ΣΕΛΙΔΕΣ
 ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
ΘΕΜΑ Α ΑΡΧΗ 1ΗΣ ΣΕΛΙΔΑΣ Γ ΗΜΕΡΗΣΙΩΝ ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΤΡΙΤΗ 19 ΙΟΥΝΙΟΥ 2018 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΣΥΝΟΛΟ ΣΕΛΙΔΩΝ: ΕΞΙ (6) Να γράψετε στο τετράδιό
Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης. Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010
 ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
ΠΕΡΙΛΗΨΗ Υποψήφιος διδάκτορας: Καββαδάς Παναγιώτης Έτος ολοκλήρωσης διδακτορικής διατριβής: 2010 Μελέτη τοπ ρόλοπ της ιντεγκρινοσπνδεόμενης κινάσης στην πνεπμονική ίνσση, Διδακτορική Διατριβή, Πανεπιστήμιο
Hormones and GI εντερο-ενδοκρινικά (εντεροχρωμοφινικά ECU κύτταρα)
 Hormones and GI 15 τύποι ορμονο-εκκριτικά εντερο-ενδοκρινικά κύτταρα Στο βλεννογόνου: στομάχου, λεπτού και παχέος εντέρου Πολλά εξ αυτών εκκρίνουν μόνο μια ορμόνη Ταυτοποιούνται με τα γράμματα G κύτταρα,
Hormones and GI 15 τύποι ορμονο-εκκριτικά εντερο-ενδοκρινικά κύτταρα Στο βλεννογόνου: στομάχου, λεπτού και παχέος εντέρου Πολλά εξ αυτών εκκρίνουν μόνο μια ορμόνη Ταυτοποιούνται με τα γράμματα G κύτταρα,
Ραδιοφάρµακα του Τεχνητίου και του Ρηνίου. Εργαστήριο Ραδιοφαρµακευτικής Χηµείας, Ινστιτούτο Ραδιοϊσοτόπων και Ραδιοδιαγνωστικών Προϊόντων
 Ραδιοφάρµακα του Τεχνητίου και του Ρηνίου Μηνάς Παπαδόπουλος, Ιωάννης Πιρµεττής Εργαστήριο Ραδιοφαρµακευτικής Χηµείας, Ινστιτούτο Ραδιοϊσοτόπων και Ραδιοδιαγνωστικών Προϊόντων Ραδιοφάρµακα Είναι οργανικές
Ραδιοφάρµακα του Τεχνητίου και του Ρηνίου Μηνάς Παπαδόπουλος, Ιωάννης Πιρµεττής Εργαστήριο Ραδιοφαρµακευτικής Χηµείας, Ινστιτούτο Ραδιοϊσοτόπων και Ραδιοδιαγνωστικών Προϊόντων Ραδιοφάρµακα Είναι οργανικές
Κεφάλαιο 1. Οι δομικοί λίθοι
 Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
Κεφάλαιο 1 Οι δομικοί λίθοι Κεφάλαιο 1 Οι Δομικοί Λίθοι των Πρωτεϊνών Εικόνα 1.1 Η αμινοξική αλληλουχία μιας πρωτεϊνικής πολυπεπτιδικής αλυσίδας ονομάζεται πρωτοταγής δομή. Διαφορετικές περιοχές της αλληλουχίας
και χρειάζεται μέσα στο ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. ενζύμων κύτταρο τρόπους
 Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
Για να εξασφαλιστεί η σωστή και αρμονική έκφραση των ενζύμων μέσα στο κύτταρο χρειάζεται ρύθμιση εναρμόνιση των διαφόρων ενζυμικών δραστηριοτήτων. και Η εναρμόνιση αυτή επιτυγχάνεται με διάφορους τρόπους
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ
 ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΣΥΝΟΨΗ ΠΑΡΑΓΩΓΗΣ ΕΝΕΡΓΕΙΑΣ ΤΡΟΦΗ Λίπη Πολυσακχαρίτες Γλυκόζη κι άλλα σάκχαρα Πρωτεΐνες Αμινοξέα Λιπαρά Οξέα Γλυκόλυση Πυροσταφυλικό Οξύ Ακέτυλο-oA Αλυσίδα μεταφοράς ηλεκτρονίων / Οξειδωτική φωσφορυλίωση
ΦΡΟΝΤΙΣΤΗΡΙΑ ΠΡΟΟΠΤΙΚΗ
 Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Απαντήσεις του κριτηρίου αξιολόγησης στη βιολογία γενικής παιδείας 1 ο ΚΕΦΑΛΑΙΟ ΘΕΜΑ 1 ο Να γράψετε τον αριθμό καθεμίας από τις ημιτελείς προτάσεις 1 έως και 5, και δίπλα σε αυτόν το γράμμα που αντιστοιχεί
Καρκίνος. Note: Σήμερα όμως πάνω από το 50% των διαφόρων καρκινικών τύπων είναι θεραπεύσιμοι
 Ο πιο απλός ορισμός είναι ότι ο καρκίνος είναι μια ομάδα ασθενειών που χαρακτηρίζεται από ανεξέλεγκτη ανάπτυξη και διασπορά ανώμαλων κυττάρων. Αν η εξάπλωση δεν ελεγχθεί θα οδηγήσει στο θάνατο. Ποσοστό
Ο πιο απλός ορισμός είναι ότι ο καρκίνος είναι μια ομάδα ασθενειών που χαρακτηρίζεται από ανεξέλεγκτη ανάπτυξη και διασπορά ανώμαλων κυττάρων. Αν η εξάπλωση δεν ελεγχθεί θα οδηγήσει στο θάνατο. Ποσοστό
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης
 Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Επίδραση και άλλων παραγόντων στην Αλλοστερική συμπεριφορά της Αιμοσφαιρίνης Καθώς το οξυγόνο χρησιμοποιείται στους ιστούς παράγεται CO2 το οποίο πρέπει να μεταφερθεί πίσω στους πνεύμονες ή τα βράγχια
Μοριακή Βιολογία. Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος. Παναγιωτίδης Χρήστος Τμήμα Φαρμακευτικής
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Μοριακή Βιολογία Ενότητα # (6): Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος Παναγιωτίδης Χρήστος Άδειες Χρήσης Το παρόν εκπαιδευτικό
Ραδιοϊσοτοπική Απεικόνιση Νεοπλασμάτων - Φλεγμονών
 Εργαστήριο Πυρηνικής Ιατρικής Ιατρική Σχολή Πανεπιστημίου Θεσσαλίας ΠΑΡΑΔΟΣΕΙΣ ΠΥΡΗΝΙΚΗΣ ΙΑΤΡΙΚΗΣ 2014-2015 Ραδιοϊσοτοπική Απεικόνιση Νεοπλασμάτων - Φλεγμονών Παναγιώτης Αν. Γεωργούλιας Αν. Καθηγητής Πυρηνικής
Εργαστήριο Πυρηνικής Ιατρικής Ιατρική Σχολή Πανεπιστημίου Θεσσαλίας ΠΑΡΑΔΟΣΕΙΣ ΠΥΡΗΝΙΚΗΣ ΙΑΤΡΙΚΗΣ 2014-2015 Ραδιοϊσοτοπική Απεικόνιση Νεοπλασμάτων - Φλεγμονών Παναγιώτης Αν. Γεωργούλιας Αν. Καθηγητής Πυρηνικής
οµή και Αναδίπλωση πρωτεϊνών
 οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
οµή και Αναδίπλωση πρωτεϊνών Νηφόρου Κατερίνα Μεταδιδακτορική Ερευνήτρια, Οµάδα Μοριακής Καρκινογένεσης, Εργ/ριο Ιστολογίας-Εµβρυολογίας, Ιατρική Σχολή Αθηνών Σηµασία των πρωτεϊνών Ενζυµική κατάλυση Μεταφορά
Εξωκυττάριο στρώμα (ΕΣ)
 Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Εξωκυττάριο στρώμα (ΕΣ) 1 Παραδείγματα εξωκυτταρικού στρώματος. Στιβάδες επιθηλιακών κυττάρων στηρίζονται σε μια λεπτή στιβάδα εξωκυτταρικού στρώματος που ονομάζεται βασικός υμένας. Κάτω από τον βασικό
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής
 Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
Κ Ε Φ Α Λ Α Ι Ο 22 : Η ενεργοποίηση της µεταγραφής Εικόνα 22.1 Η γονιδιακή έκφραση ελέγχεται κυρίως κατά την έναρξη της µεταγραφής και σπάνια στα επόµενα στάδια της γονιδιακής έκφρασης, παρόλο που ο έλεγχος
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος
 Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
Έλεγχος κυτταρικού κύκλου-απόπτωση Πεφάνη Δάφνη Επίκουρη καθηγήτρια, Ιατρική σχολή ΕΚΠΑ Μιχαλακοπούλου 176, 1 ος όροφος Κυτταρικός κύκλος Φάσεις του κυτταρικού κύκλου G1:Αύξηση του κυττάρου και προετοιμασία
Ομαδες μοριων κυτταρικης προσφυσης
 Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
Ομαδες μοριων κυτταρικης προσφυσης Μόρια κυτταρικής πρόσφυσης 2 Πρόσφυση μεταξύ λευκοκυττάρων και ενδοθηλιακών κυττάρων Το πρώτο βήμα αυτής της αλληλεπίδρασης είναι η δέσμευση των σελεκτινών των λευκοκυττάρων
μιας χημικής ουσίας. Θα πρέπει όμως η ουσία να μπορεί να χρησιμοποιηθεί κλινικά. Το 99m Tc ένας από τους πιο διαδεδομένους ιχνηθέτες
 Ιδιότητες ραδιοφαρμάκου Ασφαλής χορήγηση ραδιοφαρμάκου Ασφάλεια για τον ασθενή και μη τοξικότητα για τον οργανισμό. Η ποσότητα της χημικής ουσίας που χορηγείται για να έχουμε την επιθυμητήδόσηναείναιμικρήώστεναμηνέχουμεπρόβληματοξικής
Ιδιότητες ραδιοφαρμάκου Ασφαλής χορήγηση ραδιοφαρμάκου Ασφάλεια για τον ασθενή και μη τοξικότητα για τον οργανισμό. Η ποσότητα της χημικής ουσίας που χορηγείται για να έχουμε την επιθυμητήδόσηναείναιμικρήώστεναμηνέχουμεπρόβληματοξικής
Μόρια κυτταρικής πρόσφυσης
 Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
Μόρια κυτταρικής πρόσφυσης 1 Ομαδες μοριων κυτταρικης προσφυσης Καντχερίνες -CAMs Σελεκτίνες ΙντεγκρίνεςCAMs Σελεκτίνες Ιντεγκρίνες Συνδέσεις μεταξύ πρωτεινών με ομοιοφιλικό είτε με ετεροφιλικό τρόπο Κυτταρικές
ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΑΚΤΙΝΟΛΟΓΙΑ. Λία Ε. Μουλοπούλου Καθηγήτρια Ακτινολογίας Διευθύντρια Α Εργαστηρίου Ακτινολογίας
 ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΑΚΤΙΝΟΛΟΓΙΑ Λία Ε. Μουλοπούλου Καθηγήτρια Ακτινολογίας Διευθύντρια Α Εργαστηρίου Ακτινολογίας ΤΙ ΕΙΝΑΙ Η ΑΚΤΙΝΟΛΟΓΙΑ; Μία 5ετής ιατρική ειδικότητα που χρησιμοποιεί διάφορες απεικονιστικές
ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΑΚΤΙΝΟΛΟΓΙΑ Λία Ε. Μουλοπούλου Καθηγήτρια Ακτινολογίας Διευθύντρια Α Εργαστηρίου Ακτινολογίας ΤΙ ΕΙΝΑΙ Η ΑΚΤΙΝΟΛΟΓΙΑ; Μία 5ετής ιατρική ειδικότητα που χρησιμοποιεί διάφορες απεικονιστικές
Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών
 Μοριακή Αναγνώριση Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών 1 Μοριακή Αναγνώριση Με τον όρο μοριακή αναγνώριση περιγράφουμε την αλληλεπίδραση μεταξύ δύο
Μοριακή Αναγνώριση Ηλίας Ηλιόπουλος Εργαστήριο Γενετικής, Τμήμα Βιοτεχνολογίας, Γεωπονικό Πανεπιστήμιο Αθηνών 1 Μοριακή Αναγνώριση Με τον όρο μοριακή αναγνώριση περιγράφουμε την αλληλεπίδραση μεταξύ δύο
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Γ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ
 ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Γ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ Ορίζουμε ως διαβιβαστή μια ουσία που απελευθερώνεται από έναν νευρώνα σε μια σύναψη και που επηρεάζει ένα άλλο κύτταρο, είτε έναν νευρώνα είτε ένα κύτταρο
ΜΑΘΗΜΑ 3ο ΜΕΡΟΣ Γ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ ΝΕΥΡΟΔΙΑΒΙΒΑΣΤΕΣ Ορίζουμε ως διαβιβαστή μια ουσία που απελευθερώνεται από έναν νευρώνα σε μια σύναψη και που επηρεάζει ένα άλλο κύτταρο, είτε έναν νευρώνα είτε ένα κύτταρο
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β
 ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΡΩΤΗΣΕΙΣ ΤΗΣ ΤΡΑΠΕΖΑΣ ΘΕΜΑΤΩΝ ΣΤΟ 11 Ο ΚΕΦΑΛΑΙΟ ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ ΘΕΜΑ Β 1. Το σύστημα των ενδοκρινών αδένων είναι το ένα από τα δύο συστήματα του οργανισμού μας που συντονίζουν και
Φαρμακοκινητική. Χρυσάνθη Σαρδέλη
 Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
Φαρμακοκινητική Χρυσάνθη Σαρδέλη Αναπληρώτρια Καθηγήτρια Κλινικής Φαρμακολογίας Εργαστήριο Κλινικής Φαρμακολογίας Τμήμα Ιατρικής, Σχολή Επιστημών Υγείας, ΑΠΘ Φαρμακοκινητική Η Φαρμακοκινητική είναι η επιστήμη
ΡΑΔΙΟΧΗΜΕΙΑ 4. ΠΥΡΗΝΙΚΗ ΙΑΤΡΙΚΗ ΠΥΡΗΝΙΚΗ ΦΑΡΜΑΚΕΥΤΙΚΗ ΚΕΦΑΛΑΙΟ 3. ΡΑΔΙΕΝΕΡΓΑ ΣΤΟΙΧΕΙΑ
 ΡΑΔΙΟΧΗΜΕΙΑ ΔΙΑΧΕΙΡΙΣΗ ΡΑΔΙΕΝΕΡΓΩΝ ΑΠΟΒΛΗΤΩΝ ΤΟΞΙΚΟΤΗΤΑ ΡΑΔΙΕΝΕΡΓΩΝ ΙΣΟΤΟΠΩΝ Τμήμα Χημικών Μηχανικών ΚΕΦΑΛΑΙΟ 3. ΡΑΔΙΕΝΕΡΓΑ ΣΤΟΙΧΕΙΑ 4. ΠΥΡΗΝΙΚΗ ΙΑΤΡΙΚΗ ΠΥΡΗΝΙΚΗ ΦΑΡΜΑΚΕΥΤΙΚΗ Ιωάννα Δ. Αναστασοπούλου Βασιλική
ΡΑΔΙΟΧΗΜΕΙΑ ΔΙΑΧΕΙΡΙΣΗ ΡΑΔΙΕΝΕΡΓΩΝ ΑΠΟΒΛΗΤΩΝ ΤΟΞΙΚΟΤΗΤΑ ΡΑΔΙΕΝΕΡΓΩΝ ΙΣΟΤΟΠΩΝ Τμήμα Χημικών Μηχανικών ΚΕΦΑΛΑΙΟ 3. ΡΑΔΙΕΝΕΡΓΑ ΣΤΟΙΧΕΙΑ 4. ΠΥΡΗΝΙΚΗ ΙΑΤΡΙΚΗ ΠΥΡΗΝΙΚΗ ΦΑΡΜΑΚΕΥΤΙΚΗ Ιωάννα Δ. Αναστασοπούλου Βασιλική
Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος
 Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Κυτταρική επικοινωνία Τύποι επικοινωνίας
Κυτταρα ζυμομύκητα αποκρίνονται σε σήμα ζευγαρώματος Στους πολυκύτταρους οργανισμούς οι θεμελιώδεις κυτταρικές λειτουργίες εξαρτώνται από σύνθετα σηματοδοτικά μονοπάτια Κυτταρική επικοινωνία Τύποι επικοινωνίας
PET-CT : περιορισμοίpitfalls. Ευθυμιάδου Ρωξάνη Διευθύντρια τμήματος PET-CT Θεραπευτήριο «Υγεία»
 PET-CT : περιορισμοίpitfalls Ευθυμιάδου Ρωξάνη Διευθύντρια τμήματος PET-CT Θεραπευτήριο «Υγεία» PET/CT CT PET Κλινικές εφαρμογές PET-CT Καρδιολογία 5% Νευρολογία 5% Ογκολογία 90% PET-CT PET CT PET-CT Περιορισμοί
PET-CT : περιορισμοίpitfalls Ευθυμιάδου Ρωξάνη Διευθύντρια τμήματος PET-CT Θεραπευτήριο «Υγεία» PET/CT CT PET Κλινικές εφαρμογές PET-CT Καρδιολογία 5% Νευρολογία 5% Ογκολογία 90% PET-CT PET CT PET-CT Περιορισμοί
Ασφάλεια για τον ασθενή και μη τοξικότητα για τον οργανισμό. Η ποσότητα της χημικής ουσίας που χορηγείται για να έχουμε την
 Ασφαλής χορήγηση ραδιοφαρμάκου Ιδιότητες ραδιοφαρμάκου Ασφάλεια για τον ασθενή και μη τοξικότητα για τον οργανισμό. Η ποσότητα της χημικής ουσίας που χορηγείται για να έχουμε την επιθυμητή δόση να είναι
Ασφαλής χορήγηση ραδιοφαρμάκου Ιδιότητες ραδιοφαρμάκου Ασφάλεια για τον ασθενή και μη τοξικότητα για τον οργανισμό. Η ποσότητα της χημικής ουσίας που χορηγείται για να έχουμε την επιθυμητή δόση να είναι
ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ Β ΚΥΚΛΟΥ
 ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ Β ΚΥΚΛΟΥ ΜΑΘΗΜΑ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΤΑΞΗ Γ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ 25/4/2016 ΘΕΜΑ Α Α1. Μέσω του καρυότυπου δεν μπορούν να ανιχνευτούν : α. οι δομικές χρωμοσωμικές ανωμαλίες β.
ΔΙΑΓΩΝΙΣΜΑ ΠΡΟΣΟΜΟΙΩΣΗΣ Β ΚΥΚΛΟΥ ΜΑΘΗΜΑ ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΤΑΞΗ Γ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ 25/4/2016 ΘΕΜΑ Α Α1. Μέσω του καρυότυπου δεν μπορούν να ανιχνευτούν : α. οι δομικές χρωμοσωμικές ανωμαλίες β.
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ
 ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
ΠΡΩΤΕΙΝΕΣ ΚΑΙ ΔΙΑΤΡΟΦΗ Σεπτέμβριος 2016 Αντωνία Ματάλα Χαροκόπειο Πανεπιστήμιο Βασικά στοιχεία Πρωτεΐνες και διατροφή Οργανικά μεγαλομόρια τα οποία αποτελούνται από αμινοξέα (περιέχουν C, H, O & Ν) Απαραίτητες
(10%) Υαιοχρωμοκύττωμα Όγκος του μυελού των επινεφριδίων. Μπορεί να εμφανισθεί ως: ποραδικό Οικογενές
 Υαιοχρωμοκύττωμα Όγκος του μυελού των επινεφριδίων Μπορεί να εμφανισθεί ως: ποραδικό Οικογενές ΜΕΝ-2Α και ΜΕΝ-2Β Νόσος von Hippel-Lindau Νευρο-ινωμάτωση Oικογενές χωρίς άλλη συνοδό νόσο (10%) Υαιοχρωμοκύττωμα
Υαιοχρωμοκύττωμα Όγκος του μυελού των επινεφριδίων Μπορεί να εμφανισθεί ως: ποραδικό Οικογενές ΜΕΝ-2Α και ΜΕΝ-2Β Νόσος von Hippel-Lindau Νευρο-ινωμάτωση Oικογενές χωρίς άλλη συνοδό νόσο (10%) Υαιοχρωμοκύττωμα
ΚΕΦΑΛΑΙΟ 11. Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα
 ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
ΚΕΦΑΛΑΙΟ 11 Βιοενεργητική & Μεταβολισµός: Μιτοχόνδρια, Χλωροπλάστες & Υπεροξειδιοσώµατα Τα ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΑ Μέρος Ε ΤΑ ΒΑΣΙΚΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΤΩΝ ΥΠΕΡΟΞΕΙΔΙΟΣΩΜΑΤΩΝ - Περιέχουν ένζυµα για ποικίλες µεταβολικές
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΑΝΟΙΚΤΑ ΑΚΑΔΗΜΑΪΚΑ ΜΑΘΗΜΑΤΑ Βιολογία ΙI Κυτταρική Επικοινωνία Διδάσκοντες: Σ. Γεωργάτος, Θ. Τζαβάρας, Π. Κούκλης, Χ. Αγγελίδης Υπεύθυνος μαθήματος: Σ. Γεωργάτος Άδειες Χρήσης Το
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης
 ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
ΚΕΦΑΛΑΙΟ 10. Στρατηγικές ρύθμισης Oι μεταβολικές πορείες, όπως και η κυκλοφοριακή κίνηση ρυθμίζονται από σήματα. Η CTP, το τελικό προϊόν μιας πορείας πολλών βημάτων, ελέγχει τη ροή των αντιδράσεων σύνθεσής
ΜΑΘΗΜΑ: ΡΑΔΙΟΒΙΟΛΟΓΙΑ ΘΕΜΑ: ΒΙΟΪΑΤΡΙΚΕΣ ΕΦΑΡΜΟΓΕΣ ΤΩΝ ΙΟΝΤΙΖΟΥΣΩΝ ΑΚΤΙΝΟΒΟΛΙΩΝ
 ΜΑΘΗΜΑ: ΡΑΔΙΟΒΙΟΛΟΓΙΑ ΘΕΜΑ: ΒΙΟΪΑΤΡΙΚΕΣ ΕΦΑΡΜΟΓΕΣ ΤΩΝ ΙΟΝΤΙΖΟΥΣΩΝ ΑΚΤΙΝΟΒΟΛΙΩΝ ΧΡΗΣΕΙΣ ΑΚΤΙΝΩΝ-Χ ΚΑΙ ΡΑΔΙΟΝΟΥΚΛΙΔΙΩΝ ΣΤΙΣ ΒΙΟΪΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ Η χρήση ακτίνων-χ και ραδιοϊχνηθετών συνηθίζεται: Στην Ιατρική:
ΜΑΘΗΜΑ: ΡΑΔΙΟΒΙΟΛΟΓΙΑ ΘΕΜΑ: ΒΙΟΪΑΤΡΙΚΕΣ ΕΦΑΡΜΟΓΕΣ ΤΩΝ ΙΟΝΤΙΖΟΥΣΩΝ ΑΚΤΙΝΟΒΟΛΙΩΝ ΧΡΗΣΕΙΣ ΑΚΤΙΝΩΝ-Χ ΚΑΙ ΡΑΔΙΟΝΟΥΚΛΙΔΙΩΝ ΣΤΙΣ ΒΙΟΪΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ Η χρήση ακτίνων-χ και ραδιοϊχνηθετών συνηθίζεται: Στην Ιατρική:
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ Πρωτεΐνες Οι πρωτεΐνες είναι τα εργαλεία των ζωντανών οργανισμών Οι πρωτεΐνες είναι υπεύθυνες για όλες τις αντιδράσεις και τις δραστηριότητες του κυττάρου
ΑΡΧΕΣ ΜΕΤΡΗΣΗΣ ΠΥΡΗΝΙΚΗΣ ΑΚΤΙΝΟΒΟΛΙΑΣ
 ΑΡΧΕΣ ΜΕΤΡΗΣΗΣ ΠΥΡΗΝΙΚΗΣ ΑΚΤΙΝΟΒΟΛΙΑΣ 1. ΧΡΗΣΕΙΣ ΚΑΙ ΠΛΕΟΝΕΚΤΗΜΑΤΑ ΡΑΔΙΟΝΟΥΚΛΙΔΙΩΝ 2. ΠΡΟΪΟΝΤΑ ΡΑΔΙΕΝΕΡΓΟΥ ΔΙΑΣΠΑΣΗΣ 3. ΠΡΟΕΛΕΥΣΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΑΚΤΙΝΩΝ-γ 4. ΑΝΙΧΝΕΥΣΗ ΑΚΤΙΝΩΝ-γ (ΑΝΟΡΓΑΝΟΙ ΚΡΥΣΤΑΛΛΙΚΟΙ
ΑΡΧΕΣ ΜΕΤΡΗΣΗΣ ΠΥΡΗΝΙΚΗΣ ΑΚΤΙΝΟΒΟΛΙΑΣ 1. ΧΡΗΣΕΙΣ ΚΑΙ ΠΛΕΟΝΕΚΤΗΜΑΤΑ ΡΑΔΙΟΝΟΥΚΛΙΔΙΩΝ 2. ΠΡΟΪΟΝΤΑ ΡΑΔΙΕΝΕΡΓΟΥ ΔΙΑΣΠΑΣΗΣ 3. ΠΡΟΕΛΕΥΣΗ ΚΑΙ ΙΔΙΟΤΗΤΕΣ ΤΩΝ ΑΚΤΙΝΩΝ-γ 4. ΑΝΙΧΝΕΥΣΗ ΑΚΤΙΝΩΝ-γ (ΑΝΟΡΓΑΝΟΙ ΚΡΥΣΤΑΛΛΙΚΟΙ
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς. Οι φάσεις των Τ κυτταρικών απαντήσεων
 ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
ΚΥΤΤΑΡΙΚΕΣ ΑΝΟΣΟΑΠΑΝΤΗΣΕΙΣ: Ενεργοποίηση των Τ κυττάρων από τους µικροοργανισµούς Οι φάσεις των Τ κυτταρικών απαντήσεων Αναγνώριση του αντιγόνου και συνδιέγερση Αναγνώριση πεπτιδίων συνδεδεµένων µε το
Φλοιοτρόπος ορμόνη ή Κορτικοτροπίνη (ACTH) και συγγενή πεπτίδια
 ΕΠΙΝΕΦΡΙΔΙΑ Φλοιοτρόπος ορμόνη ή Κορτικοτροπίνη (ACTH) και συγγενή πεπτίδια 39 αμινοξέα Μ.Β. 4500 προοπιομελανοκορτίνη(pomc) 1. κορτικοτροπίνη (ACTH), 2. β λιποτροφίνη (β LPH), 3. γ λιποτροφίνη (γ LPH),
ΕΠΙΝΕΦΡΙΔΙΑ Φλοιοτρόπος ορμόνη ή Κορτικοτροπίνη (ACTH) και συγγενή πεπτίδια 39 αμινοξέα Μ.Β. 4500 προοπιομελανοκορτίνη(pomc) 1. κορτικοτροπίνη (ACTH), 2. β λιποτροφίνη (β LPH), 3. γ λιποτροφίνη (γ LPH),
Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος
 MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
MOPIAKH BIOΛOΓIA ΦAPMAKEYTIKHΣ ΔIAΛEΞΕΙΣ 10-12 Oδοί και μηχανισμοί ευκαρυωτικής μεταγωγής σήματος (Πως γίνονται αντιληπτά τα μηνύματα και πως δίδονται οι απαντήσεις) Δρ. Xρήστος Παναγιωτίδης, Tµήµα Φαρµακευτικής
Εφαρμογές αρχών φαρμακολογίας
 Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
Εφαρμογές αρχών φαρμακολογίας Χριστίνα Δάλλα Λέκτορας Φαρμακολογίας Ιατρική Σχολή, Πανεπιστήμιο Αθηνών cdalla@med.uoa.gr www.med.uoa.gr/pharmacology Ισχύς (potency) ενός φαρμάκου (συνήθως εκφράζεται σε
Φαρμακολογία Τμήμα Ιατρικής Α.Π.Θ.
 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΧΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Α.Π.Θ. Ενότητα 3: Φαρμακοδυναμική Μαρία Μυρωνίδου-Τζουβελέκη Α.Π.Θ. Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΑΝΟΙΧΤΑ ΑΚΑΔΗΜΑΙΚΑ ΜΑΘΗΜΑΤΑ Α.Π.Θ. Ενότητα 3: Φαρμακοδυναμική Μαρία Μυρωνίδου-Τζουβελέκη Α.Π.Θ. Άδειες Χρήσης Το παρόν εκπαιδευτικό υλικό υπόκειται σε άδειες χρήσης
Ενότητα: Κυτταρική Σηματοδότηση. Σ. Ταραβήρας Αναπληρωτής Καθηγητής ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ
 Ενότητα: Κυτταρική Σηματοδότηση Σ. Ταραβήρας Αναπληρωτής Καθηγητής ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ Κυτταρική σηματοδότηση Στόχοι Αρχές φυσιολογικής ρύθμισης Μορφές επικοινωνίας και σηματοδότησης Μοριακή βάση κυτταρικής
Ενότητα: Κυτταρική Σηματοδότηση Σ. Ταραβήρας Αναπληρωτής Καθηγητής ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΟΛΟΓΙΑΣ Κυτταρική σηματοδότηση Στόχοι Αρχές φυσιολογικής ρύθμισης Μορφές επικοινωνίας και σηματοδότησης Μοριακή βάση κυτταρικής
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ
 BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
BIOXHMEIA, TOMOΣ I ΠANEΠIΣTHMIAKEΣ EKΔOΣEIΣ KPHTHΣ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΑΠΕΙΚΟΝΙΣΗ ΜΟΡΙΑΚΩΝ ΔΟΜΩΝ ΜΟΡΙΑΚΑ ΜΟΝΤΕΛΑ 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING) 1: ΧΩΡΟΠΛΗΡΩΤΙΚΟ ΜΟΝΤΕΛΟ (SPACE-FILLING)
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ
 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΠΑΡΑΣΚΕΥΗ 16 IOYNIOY 2017 ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: ΒΙΟΛΟΓΙΑ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΑΠΑΝΤΗΣΕΙΣ ΘΕΜΑ Α Α1. δ Α2. δ Α3. β Α4. γ Α5. α ΘΕΜΑ Β Β1. Α I Β IV Γ VI
 94 95 96 97 98 Ο ρόλος της αγγειογένεσης στη μετάσταση Η νεοαγγείωση αποτελεί ένα απαραίτητο τμήμα της ογκογόνου διεργασίας που διασφαλίζει τη γρηγορότερη και ανεμπόδιστη ανάπτυξη του όγκου. Η λειτουργική
94 95 96 97 98 Ο ρόλος της αγγειογένεσης στη μετάσταση Η νεοαγγείωση αποτελεί ένα απαραίτητο τμήμα της ογκογόνου διεργασίας που διασφαλίζει τη γρηγορότερη και ανεμπόδιστη ανάπτυξη του όγκου. Η λειτουργική
ΠΡΩΤΕΪΝΕΣ. Φατούρος Ιωάννης Αναπληρωτής Καθηγητής
 ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΠΡΩΤΕΪΝΕΣ Φατούρος Ιωάννης Αναπληρωτής Καθηγητής Θέματα Διάλεξης Δομή, αριθμός και διαχωρισμός των αμινοξέων Ένωση αμινοξέων με τον πεπτιδικό δεσμό για τη δημιουργία πρωτεΐνης Λειτουργίες των πρωτεϊνών
ΟΜΟΣΠΟΝ ΙΑ ΕΚΠΑΙ ΕΥΤΙΚΩΝ ΦΡΟΝΤΙΣΤΩΝ ΕΛΛΑ ΟΣ (Ο.Ε.Φ.Ε.) ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ ΕΠΑΝΑΛΗΠΤΙΚΑ ΘΕΜΑΤΑ 2014
 ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
ΤΑΞΗ: ΚΑΤΕΥΘΥΝΣΗ: ΜΑΘΗΜΑ: Γ ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΘΕΤΙΚΗ ΒΙΟΛΟΓΙΑ Ηµεροµηνία: Παρασκευή 25 Απριλίου 2014 ιάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω
Ενδοκρινής Μοίρα του Παγκρέατος. 21/5/18 Ε. Παρασκευά, Εργ. Φυσιολογίας, Τµήµα Ιατρικής Π.Θ.
 Ενδοκρινής Μοίρα του Παγκρέατος 1 Εξωκρινής µοίρα: πέψη 80% του όγκου του οργάνου Ενδοκρινής µοίρα (νησίδια Langerhans): µεταβολισµός της γλυκόζης 2% του όγκου του οργάνου 1-2 εκατ. νησίδια 2 Κύτταρα &
Ενδοκρινής Μοίρα του Παγκρέατος 1 Εξωκρινής µοίρα: πέψη 80% του όγκου του οργάνου Ενδοκρινής µοίρα (νησίδια Langerhans): µεταβολισµός της γλυκόζης 2% του όγκου του οργάνου 1-2 εκατ. νησίδια 2 Κύτταρα &
Έλεγχος της λειτουργίας της εξωκρινούς μοίρας του παγκρέατος
 Έλεγχος της λειτουργίας της εξωκρινούς μοίρας του παγκρέατος Φλεγμονή Ανεπάρκεια ΠΑΘΟΛΟΓΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ ΠΑΓΚΡΕΑΤΟΣ ΦΛΕΓΜΟΝΗ ΤΟΥ ΠΑΓΚΡΕΑΤΟΣ Φλεγμονή που συνοδεύεται από διάφορα συμπτώματα στο σκύλο και
Έλεγχος της λειτουργίας της εξωκρινούς μοίρας του παγκρέατος Φλεγμονή Ανεπάρκεια ΠΑΘΟΛΟΓΙΚΕΣ ΚΑΤΑΣΤΑΣΕΙΣ ΠΑΓΚΡΕΑΤΟΣ ΦΛΕΓΜΟΝΗ ΤΟΥ ΠΑΓΚΡΕΑΤΟΣ Φλεγμονή που συνοδεύεται από διάφορα συμπτώματα στο σκύλο και
