Alumna/o Medida-unidades Erro absoluto. Valor medio: Erro relativo: EXPERIENCIA 2: DETERMINACION DE SUPERFICIES POR MEDIDA DIRECTA
|
|
|
- Ευστοργιος Καραβίας
- 7 χρόνια πριν
- Προβολές:
Transcript
1 PRÁCTICA 1 REALIZACIÓN DE MEDIDAS OBXECTIVOS: 1. Construír táboas de datos 2. Expresar correctamente o resultado das medidas 3. Aplicar a noción de que o valor medio é o que mais se aproxima ó valor verdadeiro. 4. Calcular erros absolutos e relativos 5. Utilizar instrumentos de medida (regra, calibre, probeta...) 6. Adquirir espírito de colaboración e de traballo en equipo 7. Valorar a limpeza e a orde na presentación da libreta de laboratorio. CUESTIÓNS PREVIAS: Qué instrumentos coñeces para medir lonxitudes? É algún deles mais preciso que a túa regra? Cando ti e mais un compañeiro ou compañeira facedes unha medida obteredes sempre o mesmo resultado? No caso de non obter o mesmo resultado cal delas está mal? Cómo podes medi-lo volume dunha bóla empregando auga? Cómo medirías o volume dunha gota de auga? EXPERIENCIA 1: MEDIDA DE LONXITUDES Elixe distintas lonxitudes que podas medir cunha regra (pode ser a lonxitude da mesa, o ancho da aula...) Dentro de cada grupo de traballo deberedes realizar cada un a mesma determinación e anotar o resultado na táboa de datos indicada. O terminar tedes que calcular o valor medio de tódalas medidas do grupo, así coma o erro relativo da medida. OLLO: o valor medio non pode ter mais cifras decimais das que obtivestes coa regra! Alumna/o Medida-unidades Erro absoluto Valor medio: Erro relativo: EXPERIENCIA 2: DETERMINACION DE SUPERFICIES POR MEDIDA DIRECTA CUESTIÓNS PREVIAS: Sabes cando é 1 cm 2? Cómo construirías un patrón de 1 cm 2? Cómo podes averiguar cantos cm 2 ten una folla de papel sen utilizar a regra? Primeiro debedes construír un cadrado de 1 cm de lado e o utilizaredes para medir a superficie dunha folla da vosa libreta mediante determinación directa. Organiza os valores obtidos nunha táboa e calcula o valor medio obtido no grupo de traballo, así coma o erro cometido. Alumna/o Medida-unidades Erro absoluto Valor medio: Erro relativo:
2 EXPERIENCIA 3: MEDIDA DE LONXITUDES CUN INSTRUMENTO DE PRECISIÓN: O CALIBRE Como actividade voluntaria. Para practicar a realización de medidas co calibre podes axudarte do simulador que aparecen estas páxinas. Vamos a medir o diámetro dunha moeda, primeiro cunha regra e despois co calibre. O procedemento é similar ó feito anteriormente. Cada alumna/o realiza a súa propia medida e anota o resultado na táboa de datos. Despois calculamos o valor medio, a imprecisión e o erro relativo. Alumna/o Coa regra Erro absoluto Co calibre Erro absoluto Valor medio: Erro relativo:
3 EXPERIENCIA 4: DETERMINACIÓN DO VOLUME DUNHA ESFERA CUESTIÓNS PREVIAS: Cómo definías volume? Cómo se pode medir o volume dunha canica? REALIZACIÓN A) DETERMINACIÓN INDIRECTA Neste caso vamos a medir o diámetro da esfera (e a partir de este o radio) e calcular o volume mediante cálculo matemático. Utilizaremos a expresión matemática. Expresar o resultado en cm πR V = 3 B) DETERMINACIÓN DIRECTA Vamos a comparar directamente o volume co incremento de volume de auga nunha probeta. Expresar o resultado en cm 3. Debemos completar a táboa seguinte, expresando as unidades de medida e o valor medio. Alumna/o diámetro radio Volume (m.indirecta) Volume (m. directa) Valor medio: CUESTIONARIO Qué diferenza hai ente unha medida directa e unha indirecta? É preciso o calibre? Máis que unha regra? Por qué? Qué é máis preciso, un reloxo dixital, un segundeiro ou un de area? Cómo se debe facer para que unha medida sexa o mais precisa posible? EXPERIENCIA 5: DETERMINACIÓN DO VOLUME DUNHA GOTA DE AUGA MATERIAL: Pipeta, vaso de precipitados. PROCEDEMENTO: Tomaremos auga coa pipeta e enrasaremos no cero. Deixamos caer un número determinado de gotas de auga que iremos contando. Anotamos o número de gotas, o volume de auga total e o dividir, anotamos o volume que obtemos para unha gota. Alumna/o Volume total (ml) Nº gotas Volume dunha gota Erro absoluto Valor medio: Erro absoluto medio Erro relativo CUESTIONARIO Cantas cifras significativas obtemos ó medir o volume de auga? Cal é a unidade mais pequena que podes apreciar coa pipeta? Si medimos o volume de unha única gota, sería máis o menos exacta a medida? Indica a precisión da pipeta utilizada.
4 EXPERIENCIA 6: DETERMINACIÓN DA DENSIDADE DUN SÓLIDO CUESTIÓNS PREVIAS: Qué é a densidade? En qué unidades se expresa? Qué tipo de magnitude é? É unha propiedade intensiva (característica) ou extensiva (xeral)? Por qué? MATERIAL: Balanza, Probeta, Canicas PROCEDEMENTO: Introducimos unha cantidade de auga na probeta, enrasandoa ata un determinado valor, que anotaremos como volume inicial (V 0 ). Deberemos evitar os erros de paralaxe. Nunha balanza medimos a masa dun determinado número de bólas. Engadimos as bólas á probeta e anotamos o volume de auga que ocupan as bólas engadidas. A continuación determinamos, por diferenza, o volume de auga que ocupan as bólas que pesamos. RESULTADOS Alumna/o Nº de canicas Masa (g) Volume (cm 3 ) Densidade = m/v (g/cm 3 ) Erro absoluto (...) Valor medio: Erro absoluto medio Erro relativo CUESTIONARIO Calcula o erro relativo Expresa correctamente o resultado da densidade. Representa graficamente os valores da masa fronte os do volume Explica si o valor da densidade obtido pode ser moi diferente dos que se obtiveron nos outros grupos. Depende o valor da densidade da cantidade de bólas? Explica se o valor obtido pode ser menor de 1g/cm 3. Expresa o valor medio obtido da densidade en kg/m 3. Cal é a precisión da probeta que utilizaches?. e da balanza?
5 AUTOAVALIACIÓN Marca cunha X según corresponda OBXECTIVOS 1. Aprender a manexar distintos instrumentos de medida 2. Diferenciar entre medida directa e indirecta 3. Entender o concepto de precisión dun instrumento de medida. 4. Aplicar o cálculo de erros para determinar o erro absoluto e relativo 5. Facer táboas de datos.
6 PRÁCTICA 2 ESTADOS DA MATERIA OBXECTIVOS: 1. Identificar as características dos tres estados da materia 2. Comprobar a natureza corpuscular da materia 3. Diferenciar entre propiedades xerais e específicas 4. Utilizar instrumentos de medida (regla, calibre, probeta, termómetro, balanza) para determinar algunha das propiedades xerais (masa, volume) e específicas da materia (densidade, temperatura de fusión e de ebulición) 5. Representar gráficamente os datos recollidos. 6. Adquirir espírito de colaboración e de traballo en equipo 7. Valorar a limpeza e a orde na presentación da libreta de laboratorio. 8. Recoñece-la importancia da ciencia na vida cotiá CUESTIÓNS PREVIAS: Cómo é a distancia entre as partículas de sólidos, líquidos e gases? Cómo é o movemento das partículas en sólidos, líquidos e gases? EXPERIENCIA 1: EXPLICAR AS CARACTERÍSTICAS DE SÓLIDOS, LÍQUIDOS E GASES Sólido: deixa que as bólas se coloquen nunha esquina da caixa, sen mover esta. Cómo se dispoñen as partículas nun sólido? Qué tipo de movemento teñen? Líquido: move suavemente a caixa ata ver cómo as bólas se deslizan unhas arredor das outras. Cómo se dispoñen as partículas nun líquido? Qué tipo de movemento teñen? Gas: incrementa agora a axitación das partículas. Cómo se dispoñen as partículas nun gas? Qué tipo de movemento teñen? Qué ocorre coa distancia entre as partículas comparada co sólido e o líquido?
7 EXPERIENCIA 2: DIFUSIÓN A TRAVÉS DUN LÍQUIDO Utiliza unhas pinzas para coller uns poucos cristais de permanganato potásico (KMnO 4 ). Colócaos suavemente no fondo dun vaso de precipitados con auga e observa o que ocorre durante varios minutos. Observa de novo o recipiente ó final da clase Describe o que cres que lle ocorre as partículas violetas. Utiliza as palabras partículas e difusión na túa resposta. Fai un debuxo explicativo. Repite a experiencia con auga fría e con auga quente. Qué diferenzas atopas nos tres casos? EXPERIENCIA 3: MOVEMENTO BROWNIANO Utiliza o microscopio para observar as partículas de pó nunha caixa petri. Qué observas? Cómo explicas este movemento de axitación? Repite o mesmo experimento cunha gota de leite situada nun portaobxectos recuberto por un cubreobxectos. Fíxate nas pequenas gotas de graxa. O movemento que acabas de observar chámase movemento Browniano. Por qué se produce este movemento? Quén explicou en que consiste o movemento browniano? EXPERIENCIA 3: DETERMINACIÓN DA DENSIDADE DUN LÍQUIDO E DUN SÓLIDO DENSIDADE DO LÍQUIDO 1º Medi la masa do vaso de precipitados vacío: mvaso = g 2º Verte lo líquido no vaso de precipitados e determina la nova masa: m vaso + líquido = g 3º Calcula la masa do líquido por diferencia: m líquido =..g 4º Transvasa lo líquido á probeta e medi lo seu volume: V =..ml 5º Calcula la densidade do líquido e expresala en g/ml e en unidades do SI:. DENSIDADE DO SÓLIDO Medi la masa do sólido: m sólido = g Verter auga na probeta e medi lo seu volume: V auga = ml Introduci lo sólido na probeta e medi lo novo volume: V sólido+auga =. ml Calcula lo volume do sólido por diferencia: V sólido = ml CUESTIÓNS 1. Debuxa los aparatos e material utilizado. Identificaos. No caso da balanza, indica lo nome das súas partes fundamentais. 2. Define o termo balanza: 3. Identifica las posibles fontes de erros nesta práctica. 5. Determinouse a densidade de 8 moedas de un euro. A masa das oito moedas foi de 60,05 g e o volume,tamén das oito, foi de 6,7 ml. a. Obte la densidade en g/ml e en unidades do SI. b. Canto vale a densidade dunha soa moeda de euro?
8 EXPERIENCIA 4: DETERMINACIÓN DA TEMPERATURA DE FUSIÓN DUN SÓLIDO 1. Colle a sustancia sólida que che indiquen e anota o seu nome. 2. Pón o sólido no tubo de ensaio e coloca un termómetro en contacto co sólido. Unha vez estabilizada a temperatura do termómetro, anota a súa temperatura. 3. Colóca o tubo de ensaio no interior dun vaso con auga e quenta o sistema sobre a placa calefactora e vai anotando a súa temperatura cada 2 min. Cando comence a fundir, anota a súa temperatura en intervalos mais pequenos. CUESTIÓNS 1. A qué temperatura funde o sólido? 2. Coincide coa temperatura de fusión que marca a etiqueta do recipiente do sólido? 3. Si colleramos outro sólido (sal), fundiría a mesma temperatura? 5. Qué cambios lle ocorren ó solido ó fundir? 5. Representa unha gráfica para explicar cómo varía a temperatura no vaso de precipitados co tempo. EXPERIENCIA 5: DETERMINACIÓN DA TEMPERATURA DE EBULICIÓN DUN LÍQUIDO 1. Unha vez realizado o montaxe para a ebulición, deberás observa-las características do fenómeno e realizar as medidas. 2. Colócase unha pequena cantidade de líquido (aprox. 75 ml) no matrás erlenmeyer e intróduce o termómetro nel. Non debemos esquecer o soporte e a pinza para suxeta-lo matrás. Non se debe aplica-lo calor de forma directa sobre o matrás erlenmeyer, senón a través dun baño María. 3. Quéntase o matrás erlenmeyer e anótanse os valores da temperatura cada 2 min. 4. No momento da ebulición anotaranse os valores da temperatura en intervalos de tempo máis curtos. CUESTIÓNS 1. A qué temperatura ferve o líquido? 2. Si quentásemos outro líquido, fervería a mesma temperatura? 3. Sube a temperatura de maneira continua cando se quenta un líquido? Deixa de subir en algún momento? 4. Cómo é a ebulición, rápida ou lenta? Só na superficie ou en toda a masa? 5. En qué se diferenza a ebulición da evaporación? 6. Representa unha gráfica temperatura/tempo cos teus datos. AUTOAVALIACIÓN Marca cunha X según corresponda OBXECTIVOS 1. Identificar as características dos tres estados da materia 2. Comprobar a natureza corpuscular da materia 3. Diferenciar entre propiedades xerais e específicas 4. Utilizar instrumentos de medida 5. Representar gráficamente os datos recollidos. 6. Diferenciar entre medidas directas e indirectas 7. Entender o concepto de precisión dun instrumento de medida. 8. Facer táboas de datos 9. Representar gráficamente os datos recollidos
9 PRÁCTICA 3 SEPARACIÓN DOS COMPOÑENTES DUNHA MESTURA OBXECTIVOS: 1. Identificar as características dos distintos tipos de mesturas 2. Coñecer e utilizar o material de laboratorio 3. Diferenciar entre mesturas homoxéneas e heteroxéneas 4. Respecta-las normas de seguridade nun laboratorio 5. Adquirir espírito de colaboración e de traballo en equipo 6. Valorar a limpeza e a orde na presentación da libreta de laboratorio. 7. Recoñece-la importancia da ciencia na vida cotiá CUESTIÓNS PREVIAS: Qué son sistemas homoxéneos e heteroxéneos? Qué tipo de propiedades se poden empregar para separar unhas substancias de outras? EXPERIENCIA 1: SEPARACION DUNHA MESTURA HETEROXENEA. Material: imán vaso de precipitados funil papel de filtro axitador Mestura de sal, area e trozos de ferro Procedemento: 1) Separación magnética : Coa axuda dun iman se separan os trozos de ferro. 2) Para separar a area da sal será necesario facer uso da solubilidade da sal en auga. Engadirase auga ata que o sal se disolva. 3) Filtración: pasar a mestura a través dun papel de filtro, colocado no funil. 4) Cristalización: para recuperar o sal disolto na auga, temos que evaporar a auga quentando a disolución ata que esta desapareza, non quedando máis que o sal. Cuestións : 1) Por qué se considera esta mestura como heteroxénea? 2) Contesta verdadeiro ou falso ás afirmacións seguintes: a) Despois da filtración, un liquido turbio queda transparente b) A auga filtrada é auga pura. c) O filtro retén tódalas impurezas dun liquido. d) O filtrado é un liquido homoxeneo. 3) Remplaza cada letra pola palabra que conveña: Palabras a utilizar: Depósito, Filtrado, Axitador, Filtro, Erlenmeyer, Mestura heteroxenea, Funil.
10 EXPERIENCIA 2: SEPARACIÓN DE MESTURAS E DISOLUCIÓNS. 1º SEPARACIÓN MAGNÉTICA: Material: Vaso de precipitados Imán Reactivos: Mestura de area e puntas Procedemento: 1) Achega o imán á mestura 2) Separa as puntas que quedaron adheridas ó imán. 2º FILTRACIÓN: A) FILTRACIÓN SIMPLE: Material: Soporte Noz Pinza Funil 2 Vasos de precipitados Variña de vidro Frasco lavador Reactivos : Mestura de auga e area Procedemento : 1) Dobra o papel de filtro como se che indica e introdúceo no funil (aproximadamente 1 cm por debaixo do borde). 2) Engade auga co frasco lavador para axustar o papel ás paredes do funil. 3) Monta o dispositivo da figura e verte a mestura lentamente coa axuda da variña. A) FILTRACIÓN A BALEIRO: Material : Matraz Kitasato Funil Büchner Trompa de baleiro Variña de vidro Vaso de precipitados Reactivos : Mestura auga e ioduro de chumbo (II) Procedemento : 1) Recorta o papel de filtro de maneira que axuste no funil Büchner. 2) Abre a billa.cando notes que a trompa de baleiro realiza a súa función, comeza a verter a mestura despacio e coa axuda da variña. 3) Cando remates de filtrar, retira o Büchner, e despois pecha a billa.
11 3º DECANTACIÓN: Material : Soporte Noz Aro Funil de decantación 2 Vasos de precipitados Reactivos : Mestura auga e aceite Procedemento : 1) Introduce a mestura no funil de decantación e axítaa suavemente. 2) Suxeita o funil no soporte e pon un vaso de precipitados debaixo da saída. 3) Déixao en repouso ata que se separen claramente as dúas fases. 4) Abre a chave con coidado e deixa saír unicamente o líquido da parte inferior. 4º DESTILACIÓN: Observa con detenimento o aparato de destilación que se che amosa e non toques nada. Contesta ás preguntas que tes debaixo do esquema. 1) Pon o nome do material que aparece no esquema. 2) Que circula polo circuito interno do refrixerante? e polo externo? 3) Que temperatura marca o termómetro? 4) Por que, sendo o viño tinto,se obtén un líquido incoloro? De que líquido se trata?. AUTOAVALIACIÓN Marca cunha X según corresponda OBXECTIVOS 1. Identificar as características dos distintos tipos de mesturas 2. Coñecer e utilizar o material de laboratorio 3. Diferenciar entre mesturas homoxéneas e heteroxéneas 4. Respecta-las normas de seguridade nun laboratorio 5. Adquirir espírito de colaboración e de traballo en equipo 6. Valorar a limpeza e a orde na presentación da libreta de laboratorio. 7. Recoñece-la importancia da ciencia na vida cotiá
12 PRÁCTICA 5 IDENTIFICACIÓN DE SUBSTANCIAS OBXECTIVOS: Algunha propiedades dos materiais poden aproveitarse para identificar de qué tipo de substancias se trata. É o caso do estado de agregación, a solubilidade en auga ou a condutividade eléctrica. EXPERIENCIA 1: ESTADO DE AGREGACIÓN Coloca unha pequena mostra de cada unha das substancia que imos analizar nun recipiente adecuado: as substancias sólidas en vidros de reloxo, e as líquidas en tubos de ensaio. CUESTIÓNS a) Observa o estado de agregación de cada substancia e completa a táboa no teu caderno Auga Cloruro Alcol Arame Aceite Permanganato Sílice de sodio etílico de cobre de potasio Estado de agregación b) As substancias iónicas e metálicas son habitualmente sólidas. As covalentes, en cambio, poden ser sólidas, líquidas ou gasosas. Cales das analizadas son, sen dúbida, covalentes? c) Tendo en conta o seu aspecto, de qué substancia podemos afirmar que é metálica?. Razoa a resposta. EXPERIENCIA 2: SOLUBILIDADE Enche un tubo de ensaio ata a metade con auga. Engade unha pequena cantidade de cloruro de sodio e axita a mestura. Fai o mesmo co permanganato de potasio. Repite a experiencia en diferentes tubos de ensaio co arame de cobre e coa sílice Enche a cuarta parte dun tubo de ensaio con auga destilada. Completa o tubo ata a metade con alcol etílico e axita a mestura. Repite a experiencia noutro tubo de ensaio cunha cantidade equivalente de aceite. CUESTIÓNS a) Observa a solubilidade en auga de cada substancia e completa a táboa. Auga Cloruro de sodio Alcol etílico Aceite Solubilidade en auga X Arame de cobre Permanganato de potasio Sílice
13 EXPERIENCIA 3: CONDUCTIVIDADE ELÉCTRICA Introduce os extremos de dous cables (conectados a un equipo de corrente eléctrica continua que dispoña dun voltímetro para medir o paso da corrente), en cada un dos líquidos seguintes: - auga destilada - disolución de cloruro de sodio - alcol etílico - aceite Acciona o interruptor e observa si hai paso da corrente. CUESTIÓNS a)observa a condutividade eléctrica de cada líquido e completa a táboa. Auga Cloruro de sodio Alcol etílico Aceite Condutividade eléctrica Arame de cobre Permanganato de potasio Sílice b) Analiza os resultados das tres experiencias e clasifica as substancias segundo sexan iónicas, covalentes ou metálicas. Xustifica a túa resposta en cada caso.
14 REACCIÓNS QUÍMICAS OBXECTIVOS: Nestas experiencias pretendemos, sobre todo, familiarizarnos coa realización de reaccións químicas no laboratorio, tratando de comprender por qué se producen, familiarizarse coas ecuacións químicas e o seu axuste, e comprender as posibles consecuencias derivadas do seu uso. Ademais tentaremos de achegarnos ao fascinante mundo da química, ó mesmo tempo máxico e racional. CUESTIÓNS PREVIAS: Qué diferenzas hai entre un proceso físico e un proceso químico? Cómo se pode saber si hai ou non unha reacción química? Qué precaucións cres que debes tomar cando fagas unha reacción química no laboratorio? Qué é a lei de conservación da masa? EXPERIENCIA 1: LUME VERDE ESPONTÁNEO Moitas das reaccións químicas que estades acostumados a ver suceden en disolución acuosa, por iso resulta chamativo comprobar como reaccionan os reactivos en estado sólido que aquí se empregan. Dos reactivos empregados vamos a centrarnos na reacción de descomposición do nitrato de amonio, por ser unha sustancia de utilidade recoñecida, tanto como fertilizante como explosivo. O nitrato de amonio (NH 4 NO 3 ) descomponse en nitróxeno, auga (vapor) e osíxeno. a. Escribe e axusta a ecuación química correspondente, indicando o estado físico de cada unha das sustancias que interveñen. Indica o tipo de enlace de cada unha das sustancias que intervén na reacción b. Por qué cres que se produce a explosión? c. Qué función fai a auga pulverizada? e o cinc? d. A qué se debe o lume verde que aparece? EXPERIENCIA 2: VOLCÁN Nesta reacción, que intenta simular unha erupción volcánica, o dicromato de amonio (NH 4 ) 2 Cr 2 O 7 descomponse pola acción do calor para dar trióxido de dicromo, nitróxeno e auga. a. Escribe e axusta a ecuación química correspondente, indicando o estado físico de cada unha das sustancias que interveñen. Indica o tipo de enlace de cada unha das sustancias que intervén na reacción b. Cal dos sólidos que se forman cres que é mais denso, o de partida (dicromato de amonio) ou o producto final (trióxido de dicromo) c. Para qué se emprega a cinta de magnesio?
15 EXPERIENCIA 3: SODIO E AUGA UNHA MESTURA EXPLOSIVA? O sodio reacciona rápida e violentamente coa auga debido a que a súa reacción é fortemente exotérmica. Pero poderíamos realizar esa reacción evitando a súa perigosidade? Ademais de observar coidadosamente os cambios de color, emisión de gases, incremento de temperatura, etc, que acompañan á reacción, debes respostar as seguintes cuestións. 1. O sodio reacciona coa auga para producir hidróxido de sodio é hidróxeno. a. Escribe e axusta a ecuación química correspondente, indicando o estado físico de cada unha das sustancias que interveñen b. Indica o tipo de enlace de cada unha das sustancias que intervén na reacción. c. Os disolventes orgánicos arden con facilidade (p.e. a gasolina) sen embargo nesta reacción podemos empregalos para facer mais segura a reacción. Por qué? Poderíase empregar calquera disolvente orgánico? d. Por qué aparece a coloración rosada na fase acuosa? EXPERIENCIA 4: DECIBELIOS A GO-GO Esta reacción explosiva basease na formación e posterior descomposición dun composto moi sinxelo. 2. Primeiramente fanse reaccionar o iodo con amoníaco concentrado (disolución do 30%) para formar triioduro de nitróxeno sólido e hidróxeno molecular. a. Escribe e axusta a ecuación química correspondente, indicando o estado físico de cada unha das sustancias que interveñen. Indica o tipo de enlace de cada unha das sustancias que intervén na reacción A continuación, o triioduro de nitróxeno descomponse en nitróxeno e iodo. a. Escribe e axusta a ecuación química correspondente, indicando o estado físico de cada unha das sustancias que interveñen. Indica o tipo de enlace de cada unha das sustancias que intervén na reacción Por qué cres que se produce esa explosión? EXPERIENCIA 5: QUÉN FOI ANTES: O OVO OU A SERPE? O ser humano creou o ovo e logo empregou a calor dun volcán para a súa incubación, de aí saíu unha gran serpe que se multiplicou ata os nosos días Simplemente observa e disfruta.
Procedementos operatorios de unións non soldadas
 Procedementos operatorios de unións non soldadas Técnicas de montaxe de instalacións Ciclo medio de montaxe e mantemento de instalacións frigoríficas 1 de 28 Técnicas de roscado Unha rosca é unha hélice
Procedementos operatorios de unións non soldadas Técnicas de montaxe de instalacións Ciclo medio de montaxe e mantemento de instalacións frigoríficas 1 de 28 Técnicas de roscado Unha rosca é unha hélice
Tema: Enerxía 01/02/06 DEPARTAMENTO DE FÍSICA E QUÍMICA
 Tema: Enerxía 01/0/06 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: 1. Unha caixa de 150 kg descende dende o repouso por un plano inclinado por acción do seu peso. Se a compoñente tanxencial do peso é de 735
Tema: Enerxía 01/0/06 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: 1. Unha caixa de 150 kg descende dende o repouso por un plano inclinado por acción do seu peso. Se a compoñente tanxencial do peso é de 735
Química 2º Bacharelato Equilibrio químico 11/02/08
 Química º Bacharelato Equilibrio químico 11/0/08 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: PROBLEMAS 1. Nun matraz de,00 litros introdúcense 0,0 10-3 mol de pentacloruro de fósforo sólido. Péchase, faise
Química º Bacharelato Equilibrio químico 11/0/08 DEPARTAMENTO DE FÍSICA E QUÍMICA Nome: PROBLEMAS 1. Nun matraz de,00 litros introdúcense 0,0 10-3 mol de pentacloruro de fósforo sólido. Péchase, faise
Química prácticas (selectividad)
 Departamento de Ciencias Páxina 1 material de laboratorio Embudo Buchner conectado a un matraz Kitasato y a una bomba de vacío Embudo Buchner Departamento de Ciencias Páxina 2 Nome Usos Vaso de precipitados
Departamento de Ciencias Páxina 1 material de laboratorio Embudo Buchner conectado a un matraz Kitasato y a una bomba de vacío Embudo Buchner Departamento de Ciencias Páxina 2 Nome Usos Vaso de precipitados
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA
 Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. O nafaleno (C₁₀H₈) é un composto aromático sólido que se vende para combater a traza. A combustión completa deste composto para producir
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. O nafaleno (C₁₀H₈) é un composto aromático sólido que se vende para combater a traza. A combustión completa deste composto para producir
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS
 Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS PROBLEMAS M.H.S.. 1. Dun resorte elástico de constante k = 500 N m -1 colga unha masa puntual de 5 kg. Estando o conxunto en equilibrio, desprázase
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS PROBLEMAS M.H.S.. 1. Dun resorte elástico de constante k = 500 N m -1 colga unha masa puntual de 5 kg. Estando o conxunto en equilibrio, desprázase
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amonuíaco de concentración 0,01 mol/dm³ está ionizada nun 4,2 %. a) Escribe a reacción de disociación e calcula
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amonuíaco de concentración 0,01 mol/dm³ está ionizada nun 4,2 %. a) Escribe a reacción de disociación e calcula
Tema 3. Espazos métricos. Topoloxía Xeral,
 Tema 3. Espazos métricos Topoloxía Xeral, 2017-18 Índice Métricas en R n Métricas no espazo de funcións Bólas e relacións métricas Definición Unha métrica nun conxunto M é unha aplicación d con valores
Tema 3. Espazos métricos Topoloxía Xeral, 2017-18 Índice Métricas en R n Métricas no espazo de funcións Bólas e relacións métricas Definición Unha métrica nun conxunto M é unha aplicación d con valores
EXERCICIOS AUTOAVALIABLES: RECTAS E PLANOS. 3. Cal é o vector de posición da orixe de coordenadas O? Cales son as coordenadas do punto O?
 EXERCICIOS AUTOAVALIABLES: RECTAS E PLANOS Representa en R os puntos S(2, 2, 2) e T(,, ) 2 Debuxa os puntos M (, 0, 0), M 2 (0,, 0) e M (0, 0, ) e logo traza o vector OM sendo M(,, ) Cal é o vector de
EXERCICIOS AUTOAVALIABLES: RECTAS E PLANOS Representa en R os puntos S(2, 2, 2) e T(,, ) 2 Debuxa os puntos M (, 0, 0), M 2 (0,, 0) e M (0, 0, ) e logo traza o vector OM sendo M(,, ) Cal é o vector de
EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm³ contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm³ contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
PAU XUÑO 2011 MATEMÁTICAS II
 PAU XUÑO 2011 MATEMÁTICAS II Código: 26 (O alumno/a debe responder só os exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio 2= 3 puntos, exercicio
PAU XUÑO 2011 MATEMÁTICAS II Código: 26 (O alumno/a debe responder só os exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio 2= 3 puntos, exercicio
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
EXERCICIOS DE REFORZO: RECTAS E PLANOS
 EXERCICIOS DE REFORZO RECTAS E PLANOS Dada a recta r z a) Determna a ecuacón mplícta do plano π que pasa polo punto P(,, ) e é perpendcular a r Calcula o punto de nterseccón de r a π b) Calcula o punto
EXERCICIOS DE REFORZO RECTAS E PLANOS Dada a recta r z a) Determna a ecuacón mplícta do plano π que pasa polo punto P(,, ) e é perpendcular a r Calcula o punto de nterseccón de r a π b) Calcula o punto
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO
 Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
Química P.A.U. EQUILIBRIO QUÍMICO 1 EQUILIBRIO QUÍMICO PROBLEMAS FASE GAS 1. A 670 K, un recipiente de 2 dm 3 contén unha mestura gasosa en equilibrio de 0,003 moles de hidróxeno, 0,003 moles de iodo e
QUÍMICA EXERCICIOS RESOLTOS. Segundo Curso de Bacharelato. Manuela Domínguez Real
 QUIMICA º BACHARELATO QUÍMICA Segundo Curso de Bacharelato Manuela Domínguez Real 1ª Edición Setembro 003 003 Manuela Domínguez Real 003 BAÍA Edicións Polígono de Pocomaco, ª Avda. Parcela G18 Nave posterior
QUIMICA º BACHARELATO QUÍMICA Segundo Curso de Bacharelato Manuela Domínguez Real 1ª Edición Setembro 003 003 Manuela Domínguez Real 003 BAÍA Edicións Polígono de Pocomaco, ª Avda. Parcela G18 Nave posterior
O MÉTODO CIENTÍFICO. ten varias etapas 2. BUSCA DE REGULARIDADES. cifras significativas
 PROGRAMACIÓN DE AULA MAPA DE CONTIDOS 1. OBTENCIÓN DA INFORMACIÓN O MÉTODO CIENTÍFICO ten varias etapas 2. BUSCA DE REGULARIDADES 3. EXPLICACIÓN DAS LEIS PROGRAMACIÓN DE AULA E mediante utilizando na análise
PROGRAMACIÓN DE AULA MAPA DE CONTIDOS 1. OBTENCIÓN DA INFORMACIÓN O MÉTODO CIENTÍFICO ten varias etapas 2. BUSCA DE REGULARIDADES 3. EXPLICACIÓN DAS LEIS PROGRAMACIÓN DE AULA E mediante utilizando na análise
EXERCICIOS DE ÁLXEBRA. PAU GALICIA
 Maemáicas II EXERCICIOS DE ÁLXEBRA PAU GALICIA a) (Xuño ) Propiedades do produo de marices (só enuncialas) b) (Xuño ) Sexan M e N M + I, onde I denoa a mariz idenidade de orde n, calcule N e M 3 Son M
Maemáicas II EXERCICIOS DE ÁLXEBRA PAU GALICIA a) (Xuño ) Propiedades do produo de marices (só enuncialas) b) (Xuño ) Sexan M e N M + I, onde I denoa a mariz idenidade de orde n, calcule N e M 3 Son M
CRITERIOS DE AVALIACIÓN. QUÍMICA (Cód. 27)
 CRITERIOS DE AVALIACIÓN QUÍMICA (Cód. 7) CRITERIOS XERAIS DE AVALIACIÓ DO EXAME DE QUÍMICA - As respostas deben axustarse ao enunciado da pregunta. - Terase en conta a claridade da exposición dos conceptos,
CRITERIOS DE AVALIACIÓN QUÍMICA (Cód. 7) CRITERIOS XERAIS DE AVALIACIÓ DO EXAME DE QUÍMICA - As respostas deben axustarse ao enunciado da pregunta. - Terase en conta a claridade da exposición dos conceptos,
Resorte: estudio estático e dinámico.
 ESTUDIO DO RESORTE (MÉTODOS ESTÁTICO E DINÁMICO ) 1 Resorte: estudio estático e dinámico. 1. INTRODUCCIÓN TEÓRICA. (No libro).. OBXECTIVOS. (No libro). 3. MATERIAL. (No libro). 4. PROCEDEMENTO. A. MÉTODO
ESTUDIO DO RESORTE (MÉTODOS ESTÁTICO E DINÁMICO ) 1 Resorte: estudio estático e dinámico. 1. INTRODUCCIÓN TEÓRICA. (No libro).. OBXECTIVOS. (No libro). 3. MATERIAL. (No libro). 4. PROCEDEMENTO. A. MÉTODO
Ano 2018 FÍSICA. SOL:a...máx. 1,00 Un son grave ten baixa frecuencia, polo que a súa lonxitude de onda é maior.
 ABAU CONVOCAT ORIA DE SET EMBRO Ano 2018 CRIT ERIOS DE AVALI ACIÓN FÍSICA (Cód. 23) Elixir e desenvolver unha das dúas opcións. As solución numéricas non acompañadas de unidades ou con unidades incorrectas...
ABAU CONVOCAT ORIA DE SET EMBRO Ano 2018 CRIT ERIOS DE AVALI ACIÓN FÍSICA (Cód. 23) Elixir e desenvolver unha das dúas opcións. As solución numéricas non acompañadas de unidades ou con unidades incorrectas...
PAU XUÑO 2010 MATEMÁTICAS II
 PAU XUÑO 010 MATEMÁTICAS II Código: 6 (O alumno/a deber responder só aos eercicios dunha das opcións. Punuación máima dos eercicios de cada opción: eercicio 1= 3 punos, eercicio = 3 punos, eercicio 3 =
PAU XUÑO 010 MATEMÁTICAS II Código: 6 (O alumno/a deber responder só aos eercicios dunha das opcións. Punuación máima dos eercicios de cada opción: eercicio 1= 3 punos, eercicio = 3 punos, eercicio 3 =
NÚMEROS REAIS. Páxina 27 REFLEXIONA E RESOLVE. O paso de Z a Q. O paso de Q a Á
 NÚMEROS REAIS Páxina 7 REFLEXIONA E RESOLVE O paso de Z a Q Di cales das seguintes ecuacións se poden resolver en Z e para cales é necesario o conxunto dos números racionais, Q. a) x 0 b) 7x c) x + d)
NÚMEROS REAIS Páxina 7 REFLEXIONA E RESOLVE O paso de Z a Q Di cales das seguintes ecuacións se poden resolver en Z e para cales é necesario o conxunto dos números racionais, Q. a) x 0 b) 7x c) x + d)
PROBLEMAS E CUESTIÓNS DE SELECTIVIDADE
 PROBLEMAS E CUESTIÓNS DE SELECTIVIDADE O KMnO en presenza de H SO transforma o FeSO en Fe (SO ), formándose tamén K SO, MnSO e auga: a) Axusta a reacción molecular. b) Cantos cm de disolución de KMnO 0,5
PROBLEMAS E CUESTIÓNS DE SELECTIVIDADE O KMnO en presenza de H SO transforma o FeSO en Fe (SO ), formándose tamén K SO, MnSO e auga: a) Axusta a reacción molecular. b) Cantos cm de disolución de KMnO 0,5
QUÍMICA. Cualificación: Cuestións =2 puntos cada unha; problemas: 2 puntos cada un; práctica: 2 puntos
 31 QUÍMICA Cualificación: Cuestións =2 puntos cada unha; problemas: 2 puntos cada un; práctica: 2 puntos CUESTIÓNS (Responda SAMENTE a DÚAS das seguintes cuestións) 1 Indique xustificando a resposta, se
31 QUÍMICA Cualificación: Cuestións =2 puntos cada unha; problemas: 2 puntos cada un; práctica: 2 puntos CUESTIÓNS (Responda SAMENTE a DÚAS das seguintes cuestións) 1 Indique xustificando a resposta, se
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA
 Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. Para o proceso Fe 2O 3 (s) + 2 Al (s) Al 2O 3 (s) + 2 Fe (s), calcule: a) A entalpía da reacción en condicións estándar e a calor desprendida
Química P.A.U. TERMOQUÍMICA 1 TERMOQUÍMICA PROBLEMAS TERMOQUÍMICA 1. Para o proceso Fe 2O 3 (s) + 2 Al (s) Al 2O 3 (s) + 2 Fe (s), calcule: a) A entalpía da reacción en condicións estándar e a calor desprendida
MATEMÁTICAS. (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 puntos)
 21 MATEMÁTICAS (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 Dada a matriz a) Calcula os valores do parámetro m para os que A ten inversa.
21 MATEMÁTICAS (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 Dada a matriz a) Calcula os valores do parámetro m para os que A ten inversa.
A proba constará de vinte cuestións tipo test. As cuestións tipo test teñen tres posibles respostas, das que soamente unha é correcta.
 Páxina 1 de 9 1. Formato da proba Formato proba constará de vinte cuestións tipo test. s cuestións tipo test teñen tres posibles respostas, das que soamente unha é correcta. Puntuación Puntuación: 0.5
Páxina 1 de 9 1. Formato da proba Formato proba constará de vinte cuestións tipo test. s cuestións tipo test teñen tres posibles respostas, das que soamente unha é correcta. Puntuación Puntuación: 0.5
CADERNO Nº 2 NOME: DATA: / / Os números reais
 CADERNO Nº NOME: DATA: / / Os números reais Contidos. Os números reais Números irracionais Números reais Aproximacións Representación gráfica Valor absoluto Intervalos. Radicais Forma exponencial Radicais
CADERNO Nº NOME: DATA: / / Os números reais Contidos. Os números reais Números irracionais Números reais Aproximacións Representación gráfica Valor absoluto Intervalos. Radicais Forma exponencial Radicais
MÓDULO 3 SEMIPRESENCIAL NATUREZA UNIDADE 2: MESTURAS E DISOLUCIÓNS 1. UNIDADE 2 Mesturas e disolucións
 MÓDULO 3 SEMIPRESENCIAL NATUREZA UNIDADE 2: MESTURAS E DISOLUCIÓNS 1 UNIDADE 2 Mesturas e disolucións 2.1. Coñecer as características dos tres estados da materia. 2.2. Diferenciar substancias puras e mesturas.
MÓDULO 3 SEMIPRESENCIAL NATUREZA UNIDADE 2: MESTURAS E DISOLUCIÓNS 1 UNIDADE 2 Mesturas e disolucións 2.1. Coñecer as características dos tres estados da materia. 2.2. Diferenciar substancias puras e mesturas.
CALCULO DA CONSTANTE ELASTICA DUN RESORTE
 11 IES A CAÑIZA Traballo de Física CALCULO DA CONSTANTE ELASTICA DUN RESORTE Alumno: Carlos Fidalgo Giráldez Profesor: Enric Ripoll Mira Febrero 2015 1. Obxectivos O obxectivo da seguinte practica é comprobar,
11 IES A CAÑIZA Traballo de Física CALCULO DA CONSTANTE ELASTICA DUN RESORTE Alumno: Carlos Fidalgo Giráldez Profesor: Enric Ripoll Mira Febrero 2015 1. Obxectivos O obxectivo da seguinte practica é comprobar,
ln x, d) y = (3x 5 5x 2 + 7) 8 x
 EXERCICIOS AUTOAVALIABLES: CÁLCULO DIFERENCIAL. Deriva: a) y 7 6 + 5, b) y e, c) y e) y 7 ( 5 ), f) y ln, d) y ( 5 5 + 7) 8 n e ln, g) y, h) y n. Usando a derivada da función inversa, demostra que: a)
EXERCICIOS AUTOAVALIABLES: CÁLCULO DIFERENCIAL. Deriva: a) y 7 6 + 5, b) y e, c) y e) y 7 ( 5 ), f) y ln, d) y ( 5 5 + 7) 8 n e ln, g) y, h) y n. Usando a derivada da función inversa, demostra que: a)
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2 %. a) Escriba a reacción de disociación e calcule
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2 %. a) Escriba a reacción de disociación e calcule
Química 2º Bacharelato Cálculos elementais e Termoquímica 14/01/08
 Química 2º Bacharelato álculos elementais e Termoquímica 14/1/8 DEPARTAMENTO DE FÍSIA E QUÍMIA Nome: UALIFIAIÓN: UESTIÓNS =2 PUNTOS ADA UNHA; PROBLEMAS: 2 PUNTOS ADA UN; PRÁTIA: 2 PUNTOS PROBLEMAS (Responda
Química 2º Bacharelato álculos elementais e Termoquímica 14/1/8 DEPARTAMENTO DE FÍSIA E QUÍMIA Nome: UALIFIAIÓN: UESTIÓNS =2 PUNTOS ADA UNHA; PROBLEMAS: 2 PUNTOS ADA UN; PRÁTIA: 2 PUNTOS PROBLEMAS (Responda
Física P.A.U. ELECTROMAGNETISMO 1 ELECTROMAGNETISMO. F = m a
 Física P.A.U. ELECTOMAGNETISMO 1 ELECTOMAGNETISMO INTODUCIÓN MÉTODO 1. En xeral: Debúxanse as forzas que actúan sobre o sistema. Calcúlase a resultante polo principio de superposición. Aplícase a 2ª lei
Física P.A.U. ELECTOMAGNETISMO 1 ELECTOMAGNETISMO INTODUCIÓN MÉTODO 1. En xeral: Debúxanse as forzas que actúan sobre o sistema. Calcúlase a resultante polo principio de superposición. Aplícase a 2ª lei
TRIGONOMETRIA. hipotenusa L 2. hipotenusa
 TRIGONOMETRIA. Calcular las razones trigonométricas de 0º, º y 60º. Para calcular las razones trigonométricas de º, nos ayudamos de un triángulo rectángulo isósceles como el de la figura. cateto opuesto
TRIGONOMETRIA. Calcular las razones trigonométricas de 0º, º y 60º. Para calcular las razones trigonométricas de º, nos ayudamos de un triángulo rectángulo isósceles como el de la figura. cateto opuesto
CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA
 QQuímica P.A.U. CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA 1 CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA PROBLEMAS GASES 1. Nun matraz de 10 dm³ introdúcense 2,0 g de hidróxeno; 8,4 g de nitróxeno e 4,8 g de
QQuímica P.A.U. CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA 1 CÁLCULOS NUMÉRICOS ELEMENTAIS EN QUÍMICA PROBLEMAS GASES 1. Nun matraz de 10 dm³ introdúcense 2,0 g de hidróxeno; 8,4 g de nitróxeno e 4,8 g de
Expresións alxébricas
 Expresións alxébricas Contidos 1. Expresións alxébricas Que son? Como as obtemos? Valor numérico 2. Monomios Que son? Sumar e restar Multiplicar 3. Polinomios Que son? Sumar e restar Multiplicar por un
Expresións alxébricas Contidos 1. Expresións alxébricas Que son? Como as obtemos? Valor numérico 2. Monomios Que son? Sumar e restar Multiplicar 3. Polinomios Que son? Sumar e restar Multiplicar por un
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
A circunferencia e o círculo
 10 A circunferencia e o círculo Obxectivos Nesta quincena aprenderás a: Identificar os diferentes elementos presentes na circunferencia e o círculo. Coñecer as posicións relativas de puntos, rectas e circunferencias.
10 A circunferencia e o círculo Obxectivos Nesta quincena aprenderás a: Identificar os diferentes elementos presentes na circunferencia e o círculo. Coñecer as posicións relativas de puntos, rectas e circunferencias.
Volume dos corpos xeométricos
 11 Volume dos corpos xeométricos Obxectivos Nesta quincena aprenderás a: Comprender o concepto de medida do volume e coñecer e manexar as unidades de medida do S.M.D. Obter e aplicar expresións para o
11 Volume dos corpos xeométricos Obxectivos Nesta quincena aprenderás a: Comprender o concepto de medida do volume e coñecer e manexar as unidades de medida do S.M.D. Obter e aplicar expresións para o
PAU XUÑO 2011 QUÍMICA OPCIÓN A
 AU XUÑO 011 Código: 7 QUÍMICA Cualificación: O alumno elixirá UNA das dúas opcións. Cada pregunta cualificarase con puntos OCIÓN A 1. 1.1. Que sucedería se utilizase unha culler de aluminio para axitar
AU XUÑO 011 Código: 7 QUÍMICA Cualificación: O alumno elixirá UNA das dúas opcións. Cada pregunta cualificarase con puntos OCIÓN A 1. 1.1. Que sucedería se utilizase unha culler de aluminio para axitar
EXPERIENCIAS 1. O A A
 EXPERIENCIAS. O movemento............................... 46. As forzas.................................. 48. Forzas gravitatorias.......................... 50 4. Forzas e presións en fluídos....................
EXPERIENCIAS. O movemento............................... 46. As forzas.................................. 48. Forzas gravitatorias.......................... 50 4. Forzas e presións en fluídos....................
TEMA 5. O EQUILIBRIO QUÍMICO
 TEMA 5. O EQUILIBRIO QUÍMICO 1. Para a reacción: N (g) + 3 H (g) NH 3 (g), a constante de equilibrio, K c, a certa temperatura, é,38 10 3. Calcula a constante de equilibrio, á mesma temperatura, para as
TEMA 5. O EQUILIBRIO QUÍMICO 1. Para a reacción: N (g) + 3 H (g) NH 3 (g), a constante de equilibrio, K c, a certa temperatura, é,38 10 3. Calcula a constante de equilibrio, á mesma temperatura, para as
CADERNO Nº 2 NOME: DATA: / / Polinomios. Manexar as expresións alxébricas e calcular o seu valor numérico.
 Polinomios Contidos 1. Monomios e polinomios Expresións alxébricas Expresión en coeficientes Valor numérico dun polinomio 2. Operacións Suma e diferenza Produto Factor común 3. Identidades notables Suma
Polinomios Contidos 1. Monomios e polinomios Expresións alxébricas Expresión en coeficientes Valor numérico dun polinomio 2. Operacións Suma e diferenza Produto Factor común 3. Identidades notables Suma
PROBLEMAS DE SELECTIVIDADE: EQUILIBRIO QUÍMICO
 PROBLEMAS DE SELECTIVIDADE: EQUILIBRIO QUÍMICO 3013 2. Para a seguinte reacción: 2NaHCO 3(s) Na 2 CO 3(s) + CO 2(g) + H 2 O (g) ΔH
PROBLEMAS DE SELECTIVIDADE: EQUILIBRIO QUÍMICO 3013 2. Para a seguinte reacción: 2NaHCO 3(s) Na 2 CO 3(s) + CO 2(g) + H 2 O (g) ΔH
Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA
 Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA PROBLEMAS REACCIÓNS 1. Por oxidación do ión bromuro con ión permanganato [tetraoxomanganato(vii)] no medio ácido, obtense bromo (Br 2) e o sal de manganeso(ii):
Química P.A.U. ELECTROQUÍMICA 1 ELECTROQUÍMICA PROBLEMAS REACCIÓNS 1. Por oxidación do ión bromuro con ión permanganato [tetraoxomanganato(vii)] no medio ácido, obtense bromo (Br 2) e o sal de manganeso(ii):
Problemas xeométricos
 Problemas xeométricos Contidos 1. Figuras planas Triángulos Paralelogramos Trapecios Trapezoides Polígonos regulares Círculos, sectores e segmentos 2. Corpos xeométricos Prismas Pirámides Troncos de pirámides
Problemas xeométricos Contidos 1. Figuras planas Triángulos Paralelogramos Trapecios Trapezoides Polígonos regulares Círculos, sectores e segmentos 2. Corpos xeométricos Prismas Pirámides Troncos de pirámides
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES
 Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
Química P.A.U. ÁCIDOS E BASES 1 ÁCIDOS E BASES PROBLEMAS ÁCIDO/BASE DÉBIL 1. Unha disolución de amoníaco de concentración 0,01 mol/dm 3 está ionizada nun 4,2%. a) Escriba a reacción de disociación e calcule
A actividade científica. Tema 1
 A actividade científica Tema 1 A ciencia trata de coñecer mellor o mundo que nos rodea. Para poder levar a cabo a actividade científica necesitamos ter un método que nos permita chegar a unha conclusión.
A actividade científica Tema 1 A ciencia trata de coñecer mellor o mundo que nos rodea. Para poder levar a cabo a actividade científica necesitamos ter un método que nos permita chegar a unha conclusión.
XEOMETRÍA NO ESPAZO. - Se dun vector se coñecen a orixe, o módulo, a dirección e o sentido, este está perfectamente determinado no espazo.
 XEOMETRÍA NO ESPAZO Vectores fixos Dos puntos do espazo, A e B, determinan o vector fixo AB, sendo o punto A a orixe e o punto B o extremo, é dicir, un vector no espazo é calquera segmento orientado que
XEOMETRÍA NO ESPAZO Vectores fixos Dos puntos do espazo, A e B, determinan o vector fixo AB, sendo o punto A a orixe e o punto B o extremo, é dicir, un vector no espazo é calquera segmento orientado que
5.2 PRÁCTICAS PARA COMPRENDER AS DISOLUCIÓNS
 Manual práctico dun laboratorio de química 52 5.2 PRÁCTICAS PARA COMPRENDER AS DISOLUCIÓNS O traballo no laboratorio de química esixe, entre outros requisitos, saber realizar de maneira correcta algunhas
Manual práctico dun laboratorio de química 52 5.2 PRÁCTICAS PARA COMPRENDER AS DISOLUCIÓNS O traballo no laboratorio de química esixe, entre outros requisitos, saber realizar de maneira correcta algunhas
NÚMEROS COMPLEXOS. Páxina 147 REFLEXIONA E RESOLVE. Extraer fóra da raíz. Potencias de. Como se manexa k 1? Saca fóra da raíz:
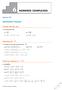 NÚMEROS COMPLEXOS Páxina 7 REFLEXIONA E RESOLVE Extraer fóra da raíz Saca fóra da raíz: a) b) 00 a) b) 00 0 Potencias de Calcula as sucesivas potencias de : a) ( ) ( ) ( ) b) ( ) c) ( ) 5 a) ( ) ( ) (
NÚMEROS COMPLEXOS Páxina 7 REFLEXIONA E RESOLVE Extraer fóra da raíz Saca fóra da raíz: a) b) 00 a) b) 00 0 Potencias de Calcula as sucesivas potencias de : a) ( ) ( ) ( ) b) ( ) c) ( ) 5 a) ( ) ( ) (
Física P.A.U. ÓPTICA 1 ÓPTICA
 Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10 14 Hz incide, cun ángulo de incidencia de 30, sobre unha lámina de vidro de caras plano-paralelas de espesor
Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10 14 Hz incide, cun ángulo de incidencia de 30, sobre unha lámina de vidro de caras plano-paralelas de espesor
Física P.A.U. ÓPTICA 1 ÓPTICA
 Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10¹⁴ Hz incide cun ángulo de incidencia de 30 sobre unha lámina de vidro de caras plano-paralelas de espesor 10
Física P.A.U. ÓPTICA 1 ÓPTICA PROBLEMAS DIOPTRIO PLANO 1. Un raio de luz de frecuencia 5 10¹⁴ Hz incide cun ángulo de incidencia de 30 sobre unha lámina de vidro de caras plano-paralelas de espesor 10
PAU SETEMBRO QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos.
 PAU SETEMBRO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Indique razoadamente, si son verdadeiras ou falsas as seguintes
PAU SETEMBRO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Indique razoadamente, si son verdadeiras ou falsas as seguintes
PAU XUÑO 2012 MATEMÁTICAS II
 PAU Código: 6 XUÑO 01 MATEMÁTICAS II (Responder só aos exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio = 3 puntos, exercicio 3= puntos, exercicio
PAU Código: 6 XUÑO 01 MATEMÁTICAS II (Responder só aos exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio = 3 puntos, exercicio 3= puntos, exercicio
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS
 Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS INTRODUCIÓN MÉTODO 1. En xeral: a) Debúxanse as forzas que actúan sobre o sistema. b) Calcúlase cada forza. c) Calcúlase a resultante polo principio
Física P.A.U. VIBRACIÓNS E ONDAS 1 VIBRACIÓNS E ONDAS INTRODUCIÓN MÉTODO 1. En xeral: a) Debúxanse as forzas que actúan sobre o sistema. b) Calcúlase cada forza. c) Calcúlase a resultante polo principio
IX. ESPAZO EUCLÍDEO TRIDIMENSIONAL: Aplicacións ao cálculo de distancias, áreas e volumes
 IX. ESPAZO EUCLÍDEO TRIDIMENSIONAL: Aplicacións ao cálculo de distancias, áreas e volumes 1.- Distancia entre dous puntos Se A e B son dous puntos do espazo, defínese a distancia entre A e B como o módulo
IX. ESPAZO EUCLÍDEO TRIDIMENSIONAL: Aplicacións ao cálculo de distancias, áreas e volumes 1.- Distancia entre dous puntos Se A e B son dous puntos do espazo, defínese a distancia entre A e B como o módulo
EQUILIBRIOS ÁCIDO-BASE
 EQUILIBRIOS ÁCIDO-BASE 1- ÁCIDOS E BASES. DEFINICIÓN SEGUNDO AS TEORÍAS DE ARRHENIUS E BRÖNSTED-LOWRY. Arrhenius.- Ácido. substancia que en disolución acuosa disóciase producindo ións H. ( auga) AH H (aq.)
EQUILIBRIOS ÁCIDO-BASE 1- ÁCIDOS E BASES. DEFINICIÓN SEGUNDO AS TEORÍAS DE ARRHENIUS E BRÖNSTED-LOWRY. Arrhenius.- Ácido. substancia que en disolución acuosa disóciase producindo ións H. ( auga) AH H (aq.)
PAU XUÑO 2016 QUÍMICA
 PAU Código: 7 XUÑO 016 QUÍICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con puntos. Todas as cuestións teóricas deberán ser razoadas. OPCIÓN A 1. 1.1. Xustifique,
PAU Código: 7 XUÑO 016 QUÍICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con puntos. Todas as cuestións teóricas deberán ser razoadas. OPCIÓN A 1. 1.1. Xustifique,
Números reais. Obxectivos. Antes de empezar.
 1 Números reais Obxectivos Nesta quincena aprenderás a: Clasificar os números reais en racionais e irracionais. Aproximar números con decimais ata unha orde dada. Calcular a cota de erro dunha aproximación.
1 Números reais Obxectivos Nesta quincena aprenderás a: Clasificar os números reais en racionais e irracionais. Aproximar números con decimais ata unha orde dada. Calcular a cota de erro dunha aproximación.
I.E.S. CADERNO Nº 6 NOME: DATA: / / Semellanza
 Semellanza Contidos 1. Semellanza Figuras semellantes Teorema de Tales Triángulos semellantes 2. Triángulos rectángulos. Teoremas Teorema do cateto Teorema da altura Teorema de Pitágoras xeneralizado 3.
Semellanza Contidos 1. Semellanza Figuras semellantes Teorema de Tales Triángulos semellantes 2. Triángulos rectángulos. Teoremas Teorema do cateto Teorema da altura Teorema de Pitágoras xeneralizado 3.
PAU XUÑO 2014 QUÍMICA. Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
 PAU Código: 27 XUÑO 2014 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. 1.1. Dados os seguintes elementos: B, O, C e F, ordéneos en
PAU Código: 27 XUÑO 2014 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. 1.1. Dados os seguintes elementos: B, O, C e F, ordéneos en
ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS
 Química P.A.U. ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS CUESTIÓNS NÚMEROS CUÁNTICOS. a) Indique o significado dos números cuánticos
Química P.A.U. ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS ESTRUTURA ATÓMICA E CLASIFICACIÓN PERIÓDICA DOS ELEMENTOS CUESTIÓNS NÚMEROS CUÁNTICOS. a) Indique o significado dos números cuánticos
1_2.- Os números e as súas utilidades - Exercicios recomendados
 1_.- Os números e as súas utilidades - Exercicios recomendados 1. Ordena de menor a maior as seguintes fraccións: 1 6 3 5 7 4,,,,, 3 5 4 8 6 9. Efectúa as seguintes operacións e simplifica o resultado:
1_.- Os números e as súas utilidades - Exercicios recomendados 1. Ordena de menor a maior as seguintes fraccións: 1 6 3 5 7 4,,,,, 3 5 4 8 6 9. Efectúa as seguintes operacións e simplifica o resultado:
PAU XUÑO 2011 MATEMÁTICAS II
 PAU XUÑO 2011 MATEMÁTICAS II Código: 26 (O alumno/a debe responder só os exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio 2= 3 puntos, exercicio
PAU XUÑO 2011 MATEMÁTICAS II Código: 26 (O alumno/a debe responder só os exercicios dunha das opcións. Puntuación máxima dos exercicios de cada opción: exercicio 1= 3 puntos, exercicio 2= 3 puntos, exercicio
Proba de Avaliación do Bacharelato para o Acceso á Universidade XUÑO 2018
 Proba de Avaliación do Bacharelato para o Acceso á Universidade Código: 24 XUÑO 2018 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1.
Proba de Avaliación do Bacharelato para o Acceso á Universidade Código: 24 XUÑO 2018 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1.
MEDIDAS EXPERIMENTAIS DE DIVERSOS CAMPOS MAGNÉTICOS Xosé Peleteiro Salgado Área de Física Aplicada. Facultade de Ciencias. Ourense
 MEDIDAS EXPERIMENTAIS DE DIVERSOS CAMPOS MAGNÉTICOS Xosé Peleteiro Salgado Área de Física Aplicada. Facultade de Ciencias. Ourense Se presentan tres procedementos diferentes nos que coas medidas realizadas
MEDIDAS EXPERIMENTAIS DE DIVERSOS CAMPOS MAGNÉTICOS Xosé Peleteiro Salgado Área de Física Aplicada. Facultade de Ciencias. Ourense Se presentan tres procedementos diferentes nos que coas medidas realizadas
Física e Química 4º ESO
 Física e Química 4º ESO DEPARTAMENTO DE FÍSICA E QUÍMICA Física: Temas 1 ao 6. 01/03/07 Nome: Cuestións 1. Un móbil ten unha aceleración de -2 m/s 2. Explica o que significa isto. 2. No medio dunha tormenta
Física e Química 4º ESO DEPARTAMENTO DE FÍSICA E QUÍMICA Física: Temas 1 ao 6. 01/03/07 Nome: Cuestións 1. Un móbil ten unha aceleración de -2 m/s 2. Explica o que significa isto. 2. No medio dunha tormenta
CADERNO Nº 11 NOME: DATA: / / Estatística. Representar e interpretar gráficos estatísticos, e saber cando é conveniente utilizar cada tipo.
 Estatística Contidos 1. Facer estatística Necesidade Poboación e mostra Variables 2. Reconto e gráficos Reconto de datos Gráficos Agrupación de datos en intervalos 3. Medidas de centralización e posición
Estatística Contidos 1. Facer estatística Necesidade Poboación e mostra Variables 2. Reconto e gráficos Reconto de datos Gráficos Agrupación de datos en intervalos 3. Medidas de centralización e posición
Física P.A.U. GRAVITACIÓN 1 GRAVITACIÓN
 Física P.A.U. GRAVITACIÓN 1 GRAVITACIÓN PROBLEMAS SATÉLITES 1. O período de rotación da Terra arredor del Sol é un año e o radio da órbita é 1,5 10 11 m. Se Xúpiter ten un período de aproximadamente 12
Física P.A.U. GRAVITACIÓN 1 GRAVITACIÓN PROBLEMAS SATÉLITES 1. O período de rotación da Terra arredor del Sol é un año e o radio da órbita é 1,5 10 11 m. Se Xúpiter ten un período de aproximadamente 12
PAU XUÑO QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
 PAU XUÑO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. 1.1. Dados os seguintes elementos: B, O, C e F, ordéneos en
PAU XUÑO 2014 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. 1.1. Dados os seguintes elementos: B, O, C e F, ordéneos en
Caderno de traballo. Proxecto EDA 2009 Descartes na aula. Departamento de Matemáticas CPI A Xunqueira Fene
 Departamento de Matemáticas CPI A Xunqueira Fene Nome: 4º ESO Nº Páx. 1 de 36 FIGURAS SEMELLANTES 1. CONCEPTO DE SEMELLANZA Intuitivamente: Dúas figuras son SEMELLANTES se teñen a mesma forma pero distinto
Departamento de Matemáticas CPI A Xunqueira Fene Nome: 4º ESO Nº Páx. 1 de 36 FIGURAS SEMELLANTES 1. CONCEPTO DE SEMELLANZA Intuitivamente: Dúas figuras son SEMELLANTES se teñen a mesma forma pero distinto
PAU XUÑO Código: 25 FÍSICA OPCIÓN A OPCIÓN B
 PAU XUÑO 013 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU XUÑO 013 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
Probas de acceso a ciclos formativos de grao medio CMPM001. Proba de. Código. Matemáticas. Parte matemática. Matemáticas.
 Probas de acceso a ciclos formativos de grao medio Proba de Matemáticas Código CMPM001 Páxina 1 de 9 Parte matemática. Matemáticas 1. Formato da proba Formato A proba consta de vinte cuestións tipo test.
Probas de acceso a ciclos formativos de grao medio Proba de Matemáticas Código CMPM001 Páxina 1 de 9 Parte matemática. Matemáticas 1. Formato da proba Formato A proba consta de vinte cuestións tipo test.
MATEMÁTICAS. (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 puntos)
 1 MATEMÁTICAS (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 puntos) Opción 1. Dada a matriz a) Calcula os valores do parámetro m para os
1 MATEMÁTICAS (Responder soamente a unha das opcións de cada bloque temático). BLOQUE 1 (ÁLXEBRA LINEAL) (Puntuación máxima 3 puntos) Opción 1. Dada a matriz a) Calcula os valores do parámetro m para os
ELECTROTECNIA. BLOQUE 1: ANÁLISE DE CIRCUÍTOS (Elixir A ou B) A.- No circuíto da figura determinar o valor da intensidade na resistencia R 2
 36 ELECTROTECNIA O exame consta de dez problemas, debendo o alumno elixir catro, un de cada bloque. Non é necesario elixir a mesma opción (A ou B ) de cada bloque. Todos os problemas puntúan igual, é dicir,
36 ELECTROTECNIA O exame consta de dez problemas, debendo o alumno elixir catro, un de cada bloque. Non é necesario elixir a mesma opción (A ou B ) de cada bloque. Todos os problemas puntúan igual, é dicir,
FÍSICA OPCIÓN 1. ; calcula: a) o período de rotación do satélite, b) o peso do satélite na órbita. (Datos R T. = 9,80 m/s 2 ).
 22 Elixir e desenrolar unha das dúas opcións propostas. FÍSICA Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Non se valorará a simple
22 Elixir e desenrolar unha das dúas opcións propostas. FÍSICA Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Non se valorará a simple
b) Segundo os datos do problema, en tres anos queda a metade de átomos, logo ese é o tempo de semidesintegración.
 FÍSICA MODERNA FÍSICA NUCLEAR. PROBLEMAS 1. Un detector de radioactividade mide unha velocidade de desintegración de 15 núcleos min -1. Sabemos que o tempo de semidesintegración é de 0 min. Calcula: a)
FÍSICA MODERNA FÍSICA NUCLEAR. PROBLEMAS 1. Un detector de radioactividade mide unha velocidade de desintegración de 15 núcleos min -1. Sabemos que o tempo de semidesintegración é de 0 min. Calcula: a)
INICIACIÓN AO CÁLCULO DE DERIVADAS. APLICACIÓNS
 INICIACIÓN AO CÁLCULO DE DERIVADAS. APLICACIÓNS Páina 0 REFLEXIONA E RESOLVE Coller un autobús en marca Na gráfica seguinte, a liña vermella representa o movemento dun autobús que arranca da parada e vai,
INICIACIÓN AO CÁLCULO DE DERIVADAS. APLICACIÓNS Páina 0 REFLEXIONA E RESOLVE Coller un autobús en marca Na gráfica seguinte, a liña vermella representa o movemento dun autobús que arranca da parada e vai,
Tema 1. Espazos topolóxicos. Topoloxía Xeral, 2016
 Tema 1. Espazos topolóxicos Topoloxía Xeral, 2016 Topoloxía e Espazo topolóxico Índice Topoloxía e Espazo topolóxico Exemplos de topoloxías Conxuntos pechados Topoloxías definidas por conxuntos pechados:
Tema 1. Espazos topolóxicos Topoloxía Xeral, 2016 Topoloxía e Espazo topolóxico Índice Topoloxía e Espazo topolóxico Exemplos de topoloxías Conxuntos pechados Topoloxías definidas por conxuntos pechados:
PAU Setembro 2010 FÍSICA
 PAU Setembro 010 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU Setembro 010 Código: 5 FÍSICA Puntuación máxima: Cuestións 4 puntos (1 cada cuestión, teórica ou práctica). Problemas 6 puntos (1 cada apartado). Non se valorará a simple anotación dun ítem como solución
PAU XUÑO QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A
 PAU XUÑO 2012 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Cos seguintes datos E (Fe 2+ /Fe) = -0,44 e E (Ag + /Ag) =
PAU XUÑO 2012 Código: 27 QUÍMICA Cualificación: O alumno elixirá UNHA das dúas opcións. Cada pregunta cualificarase con 2 puntos. OPCIÓN A 1. Cos seguintes datos E (Fe 2+ /Fe) = -0,44 e E (Ag + /Ag) =
Expresións alxébricas
 5 Expresións alxébricas Obxectivos Crear expresións alxébricas a partir dun enunciado. Atopar o valor numérico dunha expresión alxébrica. Clasificar unha expresión alxébrica como monomio, binomio,... polinomio.
5 Expresións alxébricas Obxectivos Crear expresións alxébricas a partir dun enunciado. Atopar o valor numérico dunha expresión alxébrica. Clasificar unha expresión alxébrica como monomio, binomio,... polinomio.
1 Experimento aleatorio. Espazo de mostra. Sucesos
 V. PROBABILIDADE E ESTATÍSTICA 1 Experimento aleatorio. Espazo de mostra. Sucesos 1 Experimento aleatorio. Concepto e exemplos Experimentos aleatorios son aqueles que ao repetilos nas mesmas condicións
V. PROBABILIDADE E ESTATÍSTICA 1 Experimento aleatorio. Espazo de mostra. Sucesos 1 Experimento aleatorio. Concepto e exemplos Experimentos aleatorios son aqueles que ao repetilos nas mesmas condicións
CIENCIAS DA NATUREZA:
 TRABALLOS DE RECUPERACIÓN PARA AS MATERIAS NON SUPERADAS 2º ESO ADAPTACIÓNS CURRICULARES CIENCIAS DA NATUREZA: 1. Pasa estas unidades: a) 108 km/h a m/s b) 25 m/s a km/h c) 60 ºC a K d) 698,34 m 2 a mm
TRABALLOS DE RECUPERACIÓN PARA AS MATERIAS NON SUPERADAS 2º ESO ADAPTACIÓNS CURRICULARES CIENCIAS DA NATUREZA: 1. Pasa estas unidades: a) 108 km/h a m/s b) 25 m/s a km/h c) 60 ºC a K d) 698,34 m 2 a mm
EJERCICIOS DE VIBRACIONES Y ONDAS
 EJERCICIOS DE VIBRACIONES Y ONDAS 1.- Cando un movemento ondulatorio se atopa na súa propagación cunha fenda de dimensións pequenas comparables as da súa lonxitude de onda prodúcese: a) polarización; b)
EJERCICIOS DE VIBRACIONES Y ONDAS 1.- Cando un movemento ondulatorio se atopa na súa propagación cunha fenda de dimensións pequenas comparables as da súa lonxitude de onda prodúcese: a) polarización; b)
Inecuacións. Obxectivos
 5 Inecuacións Obxectivos Nesta quincena aprenderás a: Resolver inecuacións de primeiro e segundo grao cunha incógnita. Resolver sistemas de ecuacións cunha incógnita. Resolver de forma gráfica inecuacións
5 Inecuacións Obxectivos Nesta quincena aprenderás a: Resolver inecuacións de primeiro e segundo grao cunha incógnita. Resolver sistemas de ecuacións cunha incógnita. Resolver de forma gráfica inecuacións
RADIACTIVIDADE. PROBLEMAS
 RADIACTIVIDADE. PROBLEMAS 1. Un detector de radiactividade mide unha velocidade de desintegración de 15 núcleos/minuto. Sabemos que o tempo de semidesintegración é de 0 min. Calcula: a) A constante de
RADIACTIVIDADE. PROBLEMAS 1. Un detector de radiactividade mide unha velocidade de desintegración de 15 núcleos/minuto. Sabemos que o tempo de semidesintegración é de 0 min. Calcula: a) A constante de
A ciencia estuda o universo
 1 A ciencia estuda o universo Ten algún valor a ciencia? Creo que o poder de crear cousas é valioso. Que o resultado sexa unha cousa boa ou unha cousa mala depende do uso que se faga del, pero o poder
1 A ciencia estuda o universo Ten algún valor a ciencia? Creo que o poder de crear cousas é valioso. Que o resultado sexa unha cousa boa ou unha cousa mala depende do uso que se faga del, pero o poder
Exercicios de Física 02a. Campo Eléctrico
 Exercicios de Física 02a. Campo Eléctrico Problemas 1. Dúas cargas eléctricas de 3 mc están situadas en A(4,0) e B( 4,0) (en metros). Caalcula: a) o campo eléctrico en C(0,5) e en D(0,0) b) o potencial
Exercicios de Física 02a. Campo Eléctrico Problemas 1. Dúas cargas eléctricas de 3 mc están situadas en A(4,0) e B( 4,0) (en metros). Caalcula: a) o campo eléctrico en C(0,5) e en D(0,0) b) o potencial
Probabilidade. Obxectivos. Antes de empezar
 12 Probabilidade Obxectivos Nesta quincena aprenderás a: Distinguir os experimentos aleatorios dos que non o son. Achar o espazo da mostra e distintos sucesos dun experimento aleatorio. Realizar operacións
12 Probabilidade Obxectivos Nesta quincena aprenderás a: Distinguir os experimentos aleatorios dos que non o son. Achar o espazo da mostra e distintos sucesos dun experimento aleatorio. Realizar operacións
VALORACIÓN DOS RESULTADOS DAS PAU DE QUÍMICA (ENQUISAS RESPONDIDAS POLOS CORRECTORES/AS DA MATERIA) XUÑO 2011
 VALORACIÓN DOS RESULTADOS DAS PAU DE QUÍMICA (ENQUISAS RESPONDIDAS POLOS CORRECTORES/AS DA MATERIA) XUÑO 2011 A) AVALIACIÓN DOS RESULTADOS DA PROBA nº alumnado presentado Porcentaxe aptos/as Nota media
VALORACIÓN DOS RESULTADOS DAS PAU DE QUÍMICA (ENQUISAS RESPONDIDAS POLOS CORRECTORES/AS DA MATERIA) XUÑO 2011 A) AVALIACIÓN DOS RESULTADOS DA PROBA nº alumnado presentado Porcentaxe aptos/as Nota media
PROBA DE AVALIACIÓN DO BACHARELATO PARA O ACCESO Á UNIVERSIDADE (ABAU) CONVOCATORIA DE XUÑO Curso
 PROBA DE AVALIACIÓN DO BACHARELATO PARA O ACCESO Á UNIVERSIDADE (ABAU) CONVOCATORIA DE XUÑO Curso 2017-2018 Elixir e desenvolver unha das dúas opcións. As solución numéricas non acompañadas de unidades
PROBA DE AVALIACIÓN DO BACHARELATO PARA O ACCESO Á UNIVERSIDADE (ABAU) CONVOCATORIA DE XUÑO Curso 2017-2018 Elixir e desenvolver unha das dúas opcións. As solución numéricas non acompañadas de unidades
PLANETA PLAST 1. INTRODUCIÓN OBXECTIVOS RECURSOS E MATERIAIS Para facer o modelo de planeta...2
 PLANETA PLAST GUTIÉRREZ PELAYO, LAURA LEMA IGLESIAS, DIEGO 1. INTRODUCIÓN...1 2. OBXECTIVOS...2 3. RECURSOS E MATERIAIS...2 3.1.Para facer o modelo de planeta...2 3.2.Para realizar a actividade...3 4.
PLANETA PLAST GUTIÉRREZ PELAYO, LAURA LEMA IGLESIAS, DIEGO 1. INTRODUCIÓN...1 2. OBXECTIVOS...2 3. RECURSOS E MATERIAIS...2 3.1.Para facer o modelo de planeta...2 3.2.Para realizar a actividade...3 4.
SOLUCIONES DE LAS ACTIVIDADES Págs. 101 a 119
 Página 0. a) b) π 4 π x 0 4 π π / 0 π / x 0º 0 x π π. 0 rad 0 π π rad 0 4 π 0 π rad 0 π 0 π / 4. rad 4º 4 π π 0 π / rad 0º π π 0 π / rad 0º π 4. De izquierda a derecha: 4 80 π rad π / rad 0 Página 0. tg
Página 0. a) b) π 4 π x 0 4 π π / 0 π / x 0º 0 x π π. 0 rad 0 π π rad 0 4 π 0 π rad 0 π 0 π / 4. rad 4º 4 π π 0 π / rad 0º π π 0 π / rad 0º π 4. De izquierda a derecha: 4 80 π rad π / rad 0 Página 0. tg
Exercicios de Física 03a. Vibracións
 Exercicios de Física 03a. Vibracións Problemas 1. No sistema da figura, un corpo de 2 kg móvese a 3 m/s sobre un plano horizontal. a) Determina a velocidade do corpo ó comprimirse 10 cm o resorte. b) Cal
Exercicios de Física 03a. Vibracións Problemas 1. No sistema da figura, un corpo de 2 kg móvese a 3 m/s sobre un plano horizontal. a) Determina a velocidade do corpo ó comprimirse 10 cm o resorte. b) Cal
PAAU (LOXSE) Xuño 2006
 PAAU (LOXSE) Xuño 006 Código: FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica).
PAAU (LOXSE) Xuño 006 Código: FÍSICA Elixir e desenvolver unha das dúas opcións propostas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado). Cuestións 4 puntos (1 cada cuestión, teórica ou práctica).
Funcións e gráficas. Obxectivos. Antes de empezar. 1.Funcións páx. 4 Concepto Táboas e gráficas Dominio e percorrido
 9 Funcións e gráficas Obxectivos Nesta quinceer na aprenderás a: Coñecer e interpretar as funcións e as distintas formas de presentalas. Recoñecer ou dominio e ou percorrido dunha función. Determinar se
9 Funcións e gráficas Obxectivos Nesta quinceer na aprenderás a: Coñecer e interpretar as funcións e as distintas formas de presentalas. Recoñecer ou dominio e ou percorrido dunha función. Determinar se
Το παρόν σχέδιο μαθήματος δημιουργήθηκε από την κα. Radost Mazganova, καθηγήτρια Ισπανικών και την κα. Yordanka Yordanova, καθηγήτρια χημείας
 Μάθημα (τίτλος) Καθαρές ουσίες και μείγματα Επίπεδο γλωσσικής επάρκειας Α1 Α2 Β1 Β2 C1 Τάξη/βαθμίδα: πέμπτη Αριθμός μαθητών στην τάξη: 15 Θέμα: Άνθρωπος και φύση / Ουσίες και οι ιδιότητές τους Προϋποθέσεις
Μάθημα (τίτλος) Καθαρές ουσίες και μείγματα Επίπεδο γλωσσικής επάρκειας Α1 Α2 Β1 Β2 C1 Τάξη/βαθμίδα: πέμπτη Αριθμός μαθητών στην τάξη: 15 Θέμα: Άνθρωπος και φύση / Ουσίες και οι ιδιότητές τους Προϋποθέσεις
