1. Κωνσταντίνος Γυφτόπουλος, Αναπληρωτής Καθηγητής, Επιβλέπων Καθηγητής. 2. Ελένη Παπαδάκη, Καθηγήτρια, Μέλος Τριμελούς Συμβουλευτικής Επιτροπής
|
|
|
- Χρύσης Δημαράς
- 8 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ-ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΜΕΤΑΠΤΥΧΙΑΚΟ ΠΡΟΓΡΑΜΜΑ ΣΤΙΣ ΒΑΣΙΚΕΣ ΙΑΤΡΙΚΕΣ ΕΠΙΣΤΗΜΕΣ ΚΑΤΕΥΘΥΝΣΗ ΜΟΡΙΑΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΕΡΓΑΣΤΗΡΙΟ ΑΝΑΤΟΜΙΑΣ-ΙΣΤΟΛΟΓΙΑΣ-ΕΜΒΡΥΟΛΟΓΙΑΣ Διευθύντρια: Ελένη Παπαδάκη, Καθηγήτρια Επιβλέπων Καθηγητής: Κωνσταντίνος Γυφτόπουλος, Αναπλ. Καθηγητής ΜΕΛΕΤΗ ΤΟΥ ΡΟΛΟΥ ΤΗΣ ΕΝΔΟΘΗΛΙΝΗΣ ΚΑΙ ΤΩΝ ΥΠΟΔΟΧΕΩΝ ΤΗΣ ΣΤΗΝ ΠΑΘΟΓΕΝΕΙΑ ΤΗΣ ΚΙΡΣΟΚΗΛΗΣ Χονδρογιάννη Κ. Χριστίνα Τεχνολόγος Ιατρικών Εργαστηρίων Διδακτορική Διατριβή ΠΑΤΡΑ 2012
2 ΜΕΛΗ ΤΡΙΜΕΛΟΥΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗΣ ΕΠΙΤΡΟΠΗΣ 1. Κωνσταντίνος Γυφτόπουλος, Αναπληρωτής Καθηγητής, Επιβλέπων Καθηγητής 2. Ελένη Παπαδάκη, Καθηγήτρια, Μέλος Τριμελούς Συμβουλευτικής Επιτροπής 3. Πέτρος Περιμένης, Καθηγητής, Μέλος Τριμελούς Συμβουλευτικής Επιτροπής ΜΕΛΗ ΕΠΤΑΜΕΛΟΥΣ ΕΞΕΤΑΣΤΙΚΗΣ ΕΠΙΤΡΟΠΗΣ 1. Κωνσταντίνος Γυφτόπουλος, Επιβλέπων Καθηγητής 2. Ελένη Παπαδάκη, Καθηγήτρια Ανατομίας, Ιστολογίας, Εμβρυολογίας 3. Πέτρος Περιμένης, Καθηγητής Ουρολογίας 4. Αναστάσιος Αθανασόπουλος, Αναπλ. Καθηγητής Ουρολογίας 5. Χριστόδουλος Φλωρδέλλης, Καθηγητής Φαρμακολογίας 6. Αδαμαντία Μητσάκου, Καθηγήτρια Φυσιολογίας 7. Μάρθα Ασημακοπούλου, Αναπλ. Καθηγήτρια Ανατομίας, Ιστολογίας, Εμβρυολογίας 2
3 Η παρούσα διατριβή εκπονήθηκε στο Εργαστήριο Ανατομίας, Ιστολογίας και Εμβρυολογίας του Τμήματος Ιατρικής του Πανεπιστημίου Πατρών κατά τα έτη Η εκπόνηση κάθε διδακτορικής διατριβής είναι έργο συλλογικό. Για αυτό το λόγο αισθάνομαι την ανάγκη να ευχαριστήσω όλους όσοι συνέβαλλαν στην υλοποίησή της. Η επιστημονική κατάρτιση και η κλινική εμπειρία του επιβλέποντα Καθηγητή μου κυρίου Γυφτόπουλου Κωνσταντίνου, ο ευφυής λόγος του, η λογική του και το ήθος του με ενέπνευσαν. Θα ήθελα να τον ευχαριστήσω θερμά για την εξασφάλιση των δειγμάτων και των κλινικών πληροφοριών αυτών που χρησιμοποιήθηκαν για στη μελέτη αυτή. Η άρτια επιστημονική καθοδήγηση του, σε επίπεδο θεωρητικό και πειραματικό και η στατιστική επεξεργασία των αποτελεσμάτων, αποτέλεσαν πολύτιμη βοήθειά στην εκπόνηση αυτής της εργασίας. Επιπλέον τον ευχαριστώ πολύ για τη μεγάλη υπομονή του στη συγγραφή του παρόντος κειμένου! Επίσης θα ήθελα να ευχαριστήσω για την υποστήριξη, το ενδιαφέρον της, καθώς και την επιστημονική συμβολή της στο παθολογοανατομικό μέρος στην παρούσα εργασία, την Καθηγήτρια κυρία Πέτρου-Παπαδάκη Ελένη. Τέλος,ευχαριστώ τον κύριο Καθηγητή Περιμένη Πέτρο για την τιμή που μου έκανε να συμμετάσχει στην τριμελή επιτροπή. Θα ήταν παράλειψη από μέρους μου να μην ευχαριστήσω τον Καθηγητή κύριο Ιωάννη Βαράκη για την εμπιστοσύνη που μου έδειξε από την πρώτη στιγμή που βρέθηκα στο Τμήμα Ιατρικής για να πάρω μέρος στη συνέντευξη επιλογής των μεταπτυχιακών φοιτητών και για τη συμπαράσταση του τόσο σε επιστημονικό και επαγγελματικό, όσο και προσωπικό επίπεδο. Ένα ευχαριστώ, όσο μεγάλο και ειλικρινές και να είναι, δεν αρκεί για να εκφράσει την ευγνωμοσύνη μου για όλα όσα μου προσέφεραν. 3
4 Στην οικογένεια μου, που με αγαπά και με στηρίζει 4
5 ΠΕΡΙΕΧΟΜΕΝΑ Σελίδα Περιεχόμενα 5 Πρόλογος και Σκοπός της μελέτης 8 Introduction and Aim of the study 11 Γενικό Μέρος 13 Εισαγωγή 14 Ανατομία γεννητικού συστήματος ανδρός 14 Εμβρυολογικά στοιχεία 19 Εμβρυολογική ανάπτυξη όρχεων 21 Κάθοδος των όρχεων 22 Εμβρυολογική ανάπτυξη αγγείων 23 Διάκριση των αγγείων σε φλέβες και αρτηρίες κατά την εμβρυική ανάπτυξη 24 Το αγγειακό τοίχωμα 26 Ιστολογική δομή αιμοφόρων αγγείων 27 Έσω χιτώνας 28 Μέσος χιτώνας 30 Έξω χιτώνας 31 Μικρά αιμοφόρα αγγεία των αγγείων (vasa vasorum) 31 Νεύρωση των αγγείων 32 Διάκριση αιμοφόρων αγγείων 32 Αρτηρίες 33 Μεγάλες ελαστικές αρτηρίες 33 Μυϊκές αρτηρίες 34 Αρτηρίδια 35 Οι λειτουργίες των αρτηριών 35 Φλέβες 36 Μετατριχοειδή φλεβίδια 37 Μυϊκές φλέβες 38 Μεγάλες φλέβες 38 Δομή των κυτταρικών συστατικών του αγγειακού τοιχώματος 39 Ενδοθηλιακά κύτταρα 39 Αγγειακά λεία μυϊκά κύτταρα 40 Δομή των εξωκυτταρικών συστατικών του αγγειακού τοιχώματος 41 Ελαστικές ίνες 42 Κολλαγόνο 44 Βαλβίδες φλεβών 44 Κιρσοκήλη 45 Εισαγωγή 45 Επιδημιολογία 46 Αιτιολογία δημιουργίας κιρσοειδών φλεβών 47 Αιτιολογία κιρσοκήλης 49 5
6 Παθοφυσιολογία των επιπτώσεων της κιρσοκήλης στην σπερματογένεση 56 Υπερθερμία 56 Επινεφριδική παλινδρόμηση αίματος 57 Υποξία Οξειδωτικό Stress 57 Αύξηση της ενδοορχικής πίεσης 61 Ενδοκρινική ανισορροπία 63 Ιστολογικές αλλαγές και μοριακοί μηχανισμοί που εμπλέκονται στη δημιουργία των κιρσοειδών φλεβών 64 Ενδοθήλιο 65 Μέσος χιτώνας Λεία μυϊκά κύτταρα 68 Έξω χιτώνας Εξωκυττάριο στρώμα 72 Συγκέντρωση ινών στο εξωκυττάριο στρώμα 72 Εκφύλιση του εξωκυττάριου στρώματος 74 Διάγνωση 76 Εξέταση του όσχεου και του σπερματικού τόνου 77 Εξέταση των όρχεων 78 Έλεγχος του σπέρματος 81 Σπερμοδιάγραμμα 83 Βιοχημικός έλεγχος του σπέρματος 85 Ανοσοβιολογικός και ορμονικός έλεγχος 86 Απεικονιστικές μέθοδοι 87 Υπερηχογράφημα όσχεου 87 Φλεβογραφία 88 Αγγειακό υπερηχογράφημα των όρχεων-έγχρωμο Doppler 89 Ραδιενεργό σπινθηρογράφημα και θερμογραφία όσχεου 89 Θεραπεία Αντιμετώπιση 90 Χειρουργικές τεχνικές 91 Διαδερμικές τεχνικές 98 Μετεγχειρητική παρακολούθηση 99 Αποτελέσματα της χειρουργικής αντιμετώπισης της κιρσοκήλης στην ανδρική υπογονιμότητα 99 Επίδραση στα ποσοστά κύησης 99 Επίδραση στις παραμέτρους του σπέρματος 102 Προγνωστικές παράμετροι αποτελεσματικότητας της χειρουργικής επέμβασης για την κιρσοκήλη 103 Ενδοθηλίνη 108 Ιστορική αναδρομή 108 Μεταβολισμός ενδοθηλίνη 108 Σύνθεση 112 Μετα-μεταφραστικές τροποποιήσεις prepro-endothelin 112 Μετατρεπτικό ένζυμο της ενδοθηλίνης 114 Αποδόμηση 116 Υποδοχείς ενδοθηλίνης 116 Κατανομή ΕΤΑ και ΕΤΒ 121 Σηματοδοτικό μονοπάτι της ενδοθηλίνης Ενδοκυττάρια μεταγωγή σήματος μετά τη σύνδεση της ενδοθηλίνης με τους υποδοχείς της 123 Βιολογική δράση της ενδοθηλίνης Δράση της ενδοθηλίνης στα αγγεία 127 6
7 Κινάσες Ενεργοποιημένες από μιτογόνα Mitogen Activated Protein Kinases MAPKs 130 Το σύστημα των ΜΑΡ Κινασών 130 Η μεταβίβαση της πληροφορίας σε μία τυπική οδό MAPKs 131 Ενεργοποίηση των MAPKs 132 Οργάνωση και ρύθμιση των οδών των MAPKs 132 Οι οδοί μεταγωγής σημάτων MAPKs στα θηλαστικά 135 Η οδός MAPK ERK 135 Ειδικό Μέρος 143 Υλικά και Μέθοδος 144 Ανοσοϊστοχημεία 144 Τεχνική 144 Ταξινόμηση αντισωμάτων 145 Μέθοδος υπεροξειδάσης αντιυπεροξειδάσης (PAP method) 147 Μέθοδος βιοτίνης αβιδίνης (biotin-avidin procedure) 150 Προβλήματα μεθόδου ανοσοϊστοχημείας 152 Προβλήματα αξιολόγησης και ποσοτικοποίηση ανοσοϊστοχημείας 154 Αυτοματοποιημένη ανάλυση 157 Ασθενείς και Δείγματα 158 Περιγραφή της ανοσοϊστοχημικής μεθόδου βιοτίνης στρεπταβιδίνης /υπεροξειδάσης με τη χρήση φούρνου 160 Ανοσοϊστοχημική εκτίμηση 162 Στατιστική ανάλυση 163 Αποτελέσματα 164 Ακτίνη 166 Ενδοθηλίνη ΕΤ-1 και Υποδοχείς ΕΤΑ και ΕΤΒ 169 ERK1/2 178 Συζήτηση 183 Περιορισμοί της μελέτης 191 Συμπεράσματα και προοπτικές 193 Βιβλιογραφία 197 7
8 ΠΡΟΛΟΓΟΣ ΚΑΙ ΣΚΟΠΟΣ ΤΗΣ ΜΕΛΕΤΗΣ Η κιρσοκήλη είναι η κιρσοειδής ανεύρεση του οσχεϊκού τμήματος των φλεβών του σπερματικού τόνου (ελικοειδούς πλέγματος). Η κιρσοκήλη έχει αναγνωρισθεί ως μια από τις πιο κοινές αιτίες της ανδρικής υπογονιμότητας. Η συχνότητα στο γενικό πληθυσμό είναι περίπου 15%. Περίπου το 30% - 50% των ανδρών που πάσχει από πρωτοπαθή υπογονιμότητα εμφανίζει κιρσοκήλη. Η κιρσοκήλη είναι περισσότερο συνηθισμένη στην αριστερή πλευρά. Επίσης είναι δυνατόν να εμφανιστεί νωρίς στην ήβη, καθώς και περιστασιακά στα αγόρια που βρίσκονται σε προεφηβική ηλικία. Στα παιδιά η συχνότητα εμφάνισής της θεωρούνταν μικρή, αλλά σε πρόσφατες μελέτες διαπιστώθηκε η ύπαρξή της στο 6% των παιδιών ηλικίας 10 ετών, ενώ σε εφήβους το ποσοστό αυτό ανήλθε στο 16%. Πολύ σπάνια εμφανίζεται πριν από την ηλικία των 7-8 ετών. Παρόλο όμως που η κιρσοκήλη αποτελεί μία τόσο συχνή «πάθηση» στους υπογόνιμους άνδρες και μία συχνή «ανατομική ιδιομορφία» στον γενικό πληθυσμό, η αιτιολογία της παραμένει ασαφής. Παλαιότερες θεωρίες σε σχέση με το μήκος των φλεβών, φαινόμενα «συμπίεσης» κ.α. δεν επαρκούν να εξηγήσουν την τόσο συχνή δημιουργία των κιρσοειδών φλεβών, ούτε την ετερογενή επίδραση που έχουν στη λειτουργία του σπερματικού επιθηλίου. Ένα εξάλλου σημαντικό ερώτημα παραμένει πως είναι δυνατόν η ετερόπλευρη κιρσοκήλη να επηρεάζει τη λειτουργία και των δύο όρχεων! Έτσι τα τελευταία χρόνια διαφαίνεται η ανάγκη ανάπτυξης και επιβεβαίωσης κάποιου βιολογικού μηχανισμού που πιθανώς βρίσκεται πίσω από την ανάπτυξη κιρσοκήλης σε ένα μεγάλο κομμάτι του ανδρικού πληθυσμού. Πρόσφατες μελέτες υποστηρίζουν πως η ανάπτυξη κιρσοειδών φλεβών έχει έναν κληρονομικό χαρακτήρα, ειδικά στους πρώτους βαθμούς συγγένειας. Έρευνες σε περιπτώσεις χρόνιας φλεβικής ανεπάρκειας σε κιρσούς κάτω άκρων, υποδηλώνουν ως πιθανή αιτία την κληρονομική αδυναμία-λέπτυνση του αγγειακού τοιχώματος και δυσλειτουργία του ενδοθηλίου, καθώς καταδεικνύονται από μία παρεκκλίνουσα έκφραση της Ενδοθηλίνης-1 (ΕΤ-1, Endothelin-1) και των υποδοχέων της ΕΤΑ και ΕΤΒ (Endothelin Receptors A, 8
9 B). Η ενδοθηλιακή δυσλειτουργία και η απρόσφορη παραγωγή της ΕΤ-1 ή των υποδοχέων μπορεί να εμπλέκονται στη δημιουργία νέο-ενδοθηλίου και στη διαστολή των φλεβών οδηγώντας στην ανάπτυξη κιρσοειδών φλεβών. Σε μελέτες κιρσών κάτω άκρων έχει αναδειχθεί ως σημαντικό αίτιο η ελαττωμένη έκφραση των υποδοχέων ΕΤΒ στο τοίχωμα των κιρσοειδών φλεβών, το οποίο οδηγεί σε μειωμένη συσταλτική επίδραση της Ενδοθηλίνης-1. Μία αντίστοιχη δυσλειτουργία θα ήταν αναμενόμενη και στην κιρσοκήλη, στα πλαίσια της γενικότερης βιολογικής συμπεριφοράς των φλεβών που υπόκεινται σε κιρσοειδή διάταση. Ωστόσο τα υπάρχοντα δεδομένα στην σύγχρονη βιβλιογραφία όσον αφορά στους κιρσούς σπερματικών φλεβών είναι υπερβολικά πτωχά. Μέχρι και την έναρξη αυτής της μελέτης μία μόνο μελέτη αναφερόταν σε πιθανή δυσλειτουργία του ενδοθηλίου των σπερματικών φλεβών. Ως εκ τούτο, αναπτύξαμε ως βάση αυτής της μελέτης την υπόθεση εργασίας ότι: η ανάπτυξη κιρσοειδών σπερματικών φλεβών οφείλεται όχι σε «εξωτερικά» αίτια όπως συμπίεση κλπ. αλλά σε ενδογενή βλάβη στην λειτουργία του ενδοθηλίου και συγκεκριμένα σε ενδογενή ελάττωση της έκφρασης της ενδοθηλίνης ή/και των υποδοχέων των σπερματικών φλεβών. Για να ελεγχθεί λοιπόν πειραματικά η υπόθεση εργασίας, οργανώθηκε η παρούσα προοπτική μελέτη ανοσοϊστοχημικού προσδιορισμού της ενδοθηλίνης και των υποδοχέων της σε δείγμα κιρσοειδών σπερματικών φλεβών από ασθενείς που υπεβλήθησαν σε χειρουργική αποκατάσταση κιρσοκήλης λόγω υπογονιμότητας. Η σύγκριση με φυσιολογικές φλέβες έγινε με χρήση φυσιολογικού υλικού από τον αντίστοιχο ασθενή ώστε κάθε ασθενής να είναι ταυτόχρονα και μάρτυρας. Επιπλέον μελετήθηκαν οι μορφολογικές αλλοιώσεις των κιρσοειδών καθώς και ένα σημαντικό μέλος του σηματοδοτικού μονοπατιού της ενδοθηλίνης, η ERK1/2 MAP Κινάση, η οποία σχετίζεται με την συστολή των λείων μυϊκών κυττάρων των αγγείων αλλά και με τη ρυθμιστική δράση στον πολλαπλασιασμό, διαφοροποίηση, μετανάστευση των λείων μυϊκών κυττάρων, κοινά ευρήματα στην ανάπτυξη 9
10 κιρσοειδών φλεβών. Τέλος, σε μία προσπάθεια διερεύνησης της επίδρασης της παραμέτρου του χρόνου στην επίδραση της ενδοθηλιακής δυσλειτουργίας, χρησιμοποιήθηκε υλικό από παιδία που είχαν υποβληθεί σε επέμβαση κιρσοκήλης. 10
11 INTRODUCTION AND AIM OF THE STUDY Varicocele is the pathological finding of varicose veins at the scrotal portion of the spermatic cord (pampiniform plexus) and occurs more selectively on the left side. Varicocele has been recognized as one of the most common causes of male infertility. The frequency in the general population is approximately 15%. Almost 30% to 50% of men who suffer from primary infertility display varicocele. It is also possible to be discovered in early puberty and occasionally in prepubertal boys. In children the frequency of varicocele is considered to be rare but recent studies have shown its presence in 6% of children aged 10 years, while in adolescents this figure rises up to 16%. Before the age of 7-8 years it occurs very rarely. Although varicocele is such a common disease in subfertile men and a common anatomic entity in the general population, its etiology remains unclear. Previous theories concerning the length of the veins, compression phenomena etc. are insufficient to explain the frequency of varicose veins and the heterogeneous effect they may have on the seminiferous epithelium dysfunction. An even more difficult question is how the unilateral varicocele can affect the function of both testicles! Therefore, confirmation of a biological mechanism that probably lies behind the development of varicocele in a large part of the male population seems necessary nowadays. Recent studies suggest that the development of varicoce veins has a hereditary character, especially in first degree relatives. Research in cases of chronic venous insufficiency in lower limbs varicose veins implies the hereditary failure - thinning of the vessel wall and endothelial dysfunction as a cause for varicosity. This is often attributed to aberrant expression of endothelin-1 (ΕΤ-1) and its receptors ETA and ETB (endothelin receptors A, B). The endothelial dysfunction and the inappropriate production of ET-1 or its receptors may be involved in vein wall remodeling and the dilation of veins, leading to the development of varicose veins. In studies concerning 11
12 varicose veins of the lower limbs decreased expression of ETB receptors in the varicose vein wall and a reduced contractile effect of endothelin-1, have emerged as an important mechanism of varicose veins. A similar dysfunction would be expected in the varicocele setting, as part of the broader biological behavior of veins which are subjected to varicose dilatation. However, the data available in contemporary bibliography regarding the varicose spermatic veins are extremely poor. Until the beginning of this study only one study referring to a possible dysfunction of the endothelium of the spermatic veins was available. Therefore, we developed a working hypothesis that the development of the varicose spermatic veins is not due to external causes such as compression, etc. but due to endogenous damage to the endothelial function and specifically in reduction of endogenous endothelin and/or its receptors at the spermatic vein wall level. In order to test this hypothesis in an experimental setting we organized this prospective study of the immunohistochemical detection of endothelin-1 and its receptors in varicose veins specimens from infertile patients undergoing surgical correction of varicocele. Normal subcutaneous veins were harvested from each patient at the time of surgery and used as control specimens, so that each patient should serve as its own control. Furthermore, we studied the morphological alterations of varicose veins as well as a substantial part of the endothelin - ERK1/2 MAP kinase signaling pathway, which is related to the contraction as well as with the regulation of proliferation, differentiation and migration of smooth muscle cells at the vein wall. Finally, we also included surgical specimens from children who had undergone surgery for varicocele correction at an early age in an effort to investigate the effect of time parameters on endothelial dysfunction. 12
13 ΓΕΝΙΚΟ ΜΕΡΟΣ 13
14 ΕΙΣΑΓΩΓΗ ΑΝΑΤΟΜΙΑ ΓΕΝΝΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΑΝΔΡΟΣ Το ανδρικό γεννητικό σύστημα αποτελείται από τα έξω και τα έσω γεννητικά όργανα. Στα έξω γεννητικά όργανα, που βρίσκονται εκτός του σώματος, ανήκουν το πέος και το όσχεο [Εικόνα 1]. Το όσχεο περιέχει τα κυριότερα έσω γεννητικά όργανα που είναι οι όρχεις, δηλαδή οι γεννητικοί αδένες του άνδρα. Το πέος χωρίζεται σε δύο μοίρες, την περινεϊκή (ρίζα του πέους) και την ελεύθερη μοίρα. Η ρίζα του πέους βρίσκεται κάτω ακριβώς από την ηβική σύμφυση και είναι καλυμμένη από τα ανατομικά μόρια του περινέου. Η ελεύθερη μοίρα αποτελεί το τμήμα του πέους που προβάλλει μπροστά από την ηβική χώρα και αποτελείται από το σώμα και την βάλανο, τα οποία διαχωρίζονται με σαφές όριο που καλείται αυχένας του πέους. Κύριο χαρακτηριστικό στοιχείο του πέους αποτελούν τα δύο σηραγγώδη σώματά του (corpora cavernosa), που περιέχουν το στυτικό ιστό. Στη μεγαλύτερη έκταση του σώματος, μέχρι τη βάση του πέους, τα δύο σηραγγώδη σώματα του πέους είναι στενά συνδεδεμένα μεταξύ τους ώστε να αποτελούν ένα σώμα με ένα ινώδες διάφραγμα, που τα διαχωρίζει σε δεξιό και αριστερό. Στη βάση του πέους τα σηραγγώδη σώματα διαχωρίζονται και απομακρύνονται μεταξύ τους, σχηματίζοντας τα σκέλη των σηραγγωδών σωμάτων, που φέρονται στην κάτω επιφάνεια των ηβοϊσχιακών κλάδων όπου προσφύονται στερεά και αποτελούν την ονομαζόμενη ρίζα του πέους. Τα περιβλήματα του πέους είναι εξωτερικά η πόσθη και εσωτερικά η περιτονία. Η πόσθη αποτελεί το δέρμα που καλύπτει την ελεύθερη μοίρα και εμφανίζει στην κάτω επιφάνεια τη ραφή του πέους. Το τμήμα της πόσθης που καλύπτει την βάλανο ονομάζεται ακροποσθία. Η περιτονία του πέους αποτελεί ένα πέταλο ινώδους ιστού που περιβάλλει τα σηραγγώδη σώματα. Από ιστολογική άποψη τα σηραγγώδη σώματα συνίστανται από δοκίδες 14
15 ινώδους συνδετικού ιστού μεταξύ των οποίων εντοπίζονται χώροι για την υποδοχή αίματος κατά τη διάρκεια της στύσης του πέους. Οι μύες του περινέου που σχετίζονται με τη λειτουργία του πέους είναι ο βολβοσηραγγώδης και οι ισχιοσηραγγώδεις μύες. Ο βολβοσηραγγώδης μυς περιβάλλει τον βολβό του σηραγγώδους σώματος της ουρήθρας, ενώ οι ισχυοσηραγγώδεις μύες πορεύονται κάτω από κάθε σκέλος του πέους. Το όσχεο είναι ένας σάκος από δέρμα που εμφανίζει πτυχώσεις, εντοπίζεται κάτω από το πέος και περιέχει τους όρχεις [Εικόνα 1]. Εικόνα 1: Το όσχεο, όπου απεικονίζεται στην αριστερή πλευρά ανοικτός ο ελυτρώδης χιτώνας και στη δεξιά πλευρά έχουν απομακρυνθεί μόνο οι επιφανειακοί χιτώνες του που καλύπτουν τον κρεμαστήρα μυ. Το όσχεο χωρίζεται στη μέση σε δυο ημιόσχεα από μια ινώδη μεμβράνη, η οποία στην επιφάνεια διακρίνεται σαν μια ραφή, την οσχεΐκη ραφή. Το δέρμα του όσχεου είναι σκουρόχρωμο και λεπτό και περιλαμβάνει πολλούς σμηγματογόνους αδένες. Κάτω από την επιδερμίδα υπάρχει ο δαρτός χιτώνας. Σε ημιόσχεο, ο όρχις «κρέμεται» από τα στοιχεία του σπερματικού πόρου, περιβαλλόμενος από τον ιδίως ελυτροειδή χιτώνα ο οποίος έχει ένα δεύτερο 15
16 πέταλο, που υπαλείφει εκ των έσω τον κύριο χιτώνα του όρχι, τον κοινό ελυτροειδή χιτώνα. Μεταξύ των δύο πετάλων του ιδίως ελυτροειδούς χιτώνα, υπάρχει ένας χώρος σχισμοειδής, που περιέχει λίγο υγρό και μέσα σε αυτόν τον χώρο κινείται και διολισθαίνει ο όρχις. Οι όρχεις εξυπηρετούν δύο λειτουργίες, την παραγωγή σπέρματος και των ανδρικών ορμονών, των ανδρογόνων, με πρώτη την τεστοστερόνη. Το ύψος των όρχεων καθορίζεται από μικρούς μυς, τους κρεμαστήρες μυς. Οι όρχεις βρίσκονται εκτός του σώματος διότι τα σπερματοζωάρια για να αναπτυχθούν φυσιολογικά πρέπει να παράγονται σε μια θερμοκρασία δύο με τρεις βαθμούς χαμηλότερη από εκείνη του σώματος. Κάθε όρχις περιβάλλεται [Εικόνα 3] από τον ινώδη χιτώνα (tunica albuginea), ο οποίος στην άνω πρόσθια επιφάνεια σχηματίζει μια πάχυνση, το μεσόρχιο (mediastinum), από το οποίο ξεκινούν ινώδη διαφράγματα και διαχωρίζουν το παρέγχυμα σε 250 περίπου λόβια. Κάθε λόβιο περιέχει 1-4 σπερματικά σωληνάρια (semineferous tubules) τα οποία συγκλίνουν προς το μεσόρχιο, σχηματίζοντας το δίκτυο του Haller. Από εκεί ξεκινούν ευθεία σωληνάρια, που εκβάλλουν στην επιδιδυμίδα και απάγουν τα σπερματοζωάρια προς τον πόρο της. Κάθε σπερματικό σωληνάριο έχει μια βασική μεμβράνη πάνω στην οποία επικάθονται τα σπερματικά κύτταρα (semineferous cells) κύτταρα Leydig και τα κύτταρα του Sertoli [Εικόνα 2]. Εικόνα 2: Τομή σπερματικού σωληναρίου (χρώση Ηωσίνης- Αιματοξυλίνης [H&E]) 1=αυλός σπερματικού σωληναρίου, 2=σπερματίδες, 3=σπερματοκύτταρα, 4=σπερματοζωάριο, 5=κύτταρα Sertoli, 6=μυοινοβλάστες, 7=κύτταρα Leydig, 8=τριχοειδή 16
17 Εικόνα 3: Εγκάρσια τομή στην οποία απεικονίζεται η αριστερή πλευρά του όσχεου και ο αριστερός όρχις με τους χιτώνες που τον περιβάλλουν. Η επιδιδυμίδα (epididymis) είναι ένας σωλήνας που στο σχήμα μοιάζει με το κόμμα της στίξης, δίνει την εντύπωση συμπαγούς οργάνου με κεφαλή και βρίσκεται προσκολλημένη στην πίσω πλευρά του όρχεως. Η άκρη κάθε μιας αποτελεί συνέχεια του αντίστοιχου σπερματικού πόρου (spermatic cord). Μέσα από τον λεπτό αυτόν πόρο, τα σπερματοζωάρια που παράγονται στους όρχεις, μεταφέρονται στην επιδιδυμίδα όπου και αποθηκεύονται. Η επιδιδυμίδα είναι ένα περιελιγμένο σωληνάριο, το οποίο τεντωμένο φτάνει τα πέντε με επτά μέτρα. Κατά αυτόν τον τρόπο ο σπερματικός πόρος μεταφέρει σπέρμα μέσα από το σπερματικό τόνο του όρχεως στην πύελο. Κάθε πόρος επεκτείνεται πίσω από την ουροδόχο κύστη, σχηματίζοντας έναν αγωγό εκσπερμάτωσης (ejaculator duct). Οι δύο αυτοί αγωγοί περνούν μέσα από τον προστάτη (prostate) και την ουρήθρα (urethra). Καθεμία από τις δύο σπερματοδόχους κύστεις περιέχουν δύο με τρία χιλιοστά του λίτρου παχύρευστο υγρό - μέρος του σπέρματος- όπου τρέφονται και κινούνται τα σπερματοζωάρια. Ο σπερματικός πόρος αποτελείται από αρτηρίες, φλέβες, λεμφαγγεία, νεύρα και τον εκφορητικό αγωγό του όρχι [Εικόνα 4]. Οι δομές αυτές συνδέονται μεταξύ τους με χαλαρό συνδετικό ιστό και επενδύονται από 17
18 τους χιτώνες του όρχι. Ο σπερματικός πόρος είναι η συνέχεια της ουράς της επιδιδυμίδας. Έχει συνολικό μήκος 40 cm περίπου. Η αρχή του βρίσκεται στον κάτω πόλο του σύστοιχου όρχι και το τέλος του στη βάση του προστάτη. Περιγραφικά διακρίνουμε την τονική, τη βουβωνική και την πυελική μοίρα. Η πυελική μοίρα διασταυρώνεται με τον ουρητήρα πίσω από την ουροδόχο κύστη (=κυστική μοίρα). Η τελευταία μοίρα του σπερματικού πόρου είναι οζώδης και ανώμαλη και έχει λοξή θέση πίσω από την ουροδόχο κύστη και ονομάζεται σπερματοδόχος λήκυθος. Η σπερματοδόχος λήκυθος αναστομώνεται με τη σπερματοδόχο κύστη, αντίστοιχα προς τη βάση του προστάτη. Από την αναστόμωση αυτή προκύπτει ο εκσπερματιστικός πόρος. Ο σπερματικός πόρος αποτελείται από το μυϊκό χιτώνα με τις τρείς στοιβάδες, τις λείες μυϊκές ίνες, την υποβλεννογόνιο και τη βλεννογόνο. Οι όρχεις κρέμονται μέσα στο όσχεο από το σπερματικό τόνο. Ο σπερματικός τόνος αποτελείται από το σπερματικό πόρο, τα αγγεία και τα νεύρα του όρχι. Ο σπερματικός τόνος έχει μήκος 15 cm. Αρχίζει από τον όρχι και φτάνει μέχρι το κοιλιακό στόμιο του βουβωνικού πόρου. Εκεί τα ανατομικά του μορφώματα ξεχωρίζουν και το καθένα ακολουθεί το δρόμο του. Τοπογραφικά είναι η οσχεϊκή και η βουβωνική μοίρα. Τα έλυτρα του σπερματικού τόνου είναι: 1) η κρεμαστήριος περιτονία, 2) ο έξω κρεμαστήρας μυς και 3) ο κοινός ελυτροειδής χιτώνας. Οι αρτηρίες του σπερματικού πόρου είναι οι έσω, οι έξω σπερματικές αρτηρίες και η αρτηρία του εκφορητικού πόρου. Οι έσω σπερματικές αρτηρίες είναι κλάδοι της κοιλιακής αορτής. Οι έξω σπερματικές αρτηρίες είναι κλάδοι της έσω επιγαστρικής αρτηρίας Η αρτηρία του εκφορητικού πόρου είναι μια αρτηρία που ακολουθεί την πορεία του εκφορητικού πόρου. 18
19 Εικόνα 4: Απεικόνιση του σπερματικού πόρου στη βουβωνική περιοχή. Οι σπερματικές φλέβες προβάλουν πίσω από τον όρχι και λαμβάνουν κλάδους και από την επιδιδυμίδα. Ενώνονται και σχηματίζουν ένα περιτυλιγμένο πλέγμα, το ελικώδες πλέγμα (plexus pampiniformis), το οποίο και σχηματίζει τον κύριο όγκο του σπερματικού πόρου [Εικόνα 5]. Τα αγγεία που σχηματίζουν το ελικώδες πλέγμα είναι πολυάριθμα και πορεύονται σε όλο το μήκος του σπερματικού πόρου, ενώ κάτω από το υποδόριο βουβωνικό δακτύλιο ενώνονται για να σχηματίσουν τρεις με τέσσερις φλέβες οι οποίες διαπερνούν το βουβωνικό πόρο και εισέρχονται στην κοιλιακή χώρα μέσω του κοιλιακού βουβωνικού δακτυλίου, όπου και διαχωρίζονται συνήθως σε δύο φλέβες. Οι δύο αυτές φλέβες συνενώνονται και πάλι σε μια φλέβα, η οποία στη δεξιά πλευρά εκβάλλει στην κάτω κοίλη φλέβα υπό οξεία γωνία και στην αριστερή πλευρά στην αριστερή νεφρική φλέβα. 19
20 Εικόνα 5: Απεικόνιση των σπερματικών φλεβών και ο σχηματισμός του ελικώδους πλέγματος. Τα νεύρα που σχηματίζουν το σπερματικό πλέγμα ανήκουν στο συμπαθητικό νευρικό σύστημα και συνενώνονται με κλάδους του πυελικού πλέγματος. Συγκεκριμένα τα νεύρα προέρχονται από τον έξω σπερματικό, το λαγονοβουβωνικό και το νεύρο του περινέου (Henry Gray, 2000). 20
21 ΕΜΒΡΥΟΛΟΓΙΚΑ ΣΤΟΙΧΕΙΑ ΕΜΒΡΥΟΛΟΓΙΚΗ ΑΝΑΠΤΥΞΗ ΟΡΧΕΩΝ Η εμφάνιση των όρχεων λαμβάνει χώρα συνήθως κατά την 26 η εβδομάδα. Η σπερματική οδός και τα μέλη αυτής προέρχονται από την πλευρική πλάκα και το ενδιάμεσο μεσόδερμα (Philip R. Brauer). Κατά τη διάρκεια της 7 ης εβδομάδας, γίνονται οι ακόλουθες μεταβολές, στον αμετάπλαστο γεννητικό αδένα: Οι κυτταρικές δοκίδες οι οποίες βρίσκονται στο βάθος του αμετάπλαστου γεννητικού αδένα σε ακτινοειδές σχήμα, σχηματίζουν στις πύλες του αδένα ύστερα από αναστόμωση των μέσων άκρων, λεπτό δίκτυο από κύτταρα, το όποιο ονομάζεται «βλάστημα του δικτύου». Κατά το ίδιο διάστημα κάτω από το βλαστικό επιθήλιο αναπτύσσεται στιβάδα από πυκνό συνδετικό ιστό, η οποία αποτελεί τον ινώδη χιτώνα του όρχι και χωρίζει τελείως το βλαστικό επιθήλιο από τις κυτταρικές δοκίδες που βρίσκονται στο βάθος. Όταν το έμβρυο βρίσκεται στον 4 ο μήνα της διαμόρφωσης οι κυτταρικές δοκίδες παίρνουν σχήμα ιππείου πετάλου και συνδέονται στις πύλες του όρχι με δίκτυο που υπάρχει εκεί. Το υπόκυρτο μέρος των κυτταρικών δοκίδων καθώς μεγαλώνει και ελίσσεται φθάνει ως τον ινώδη χιτώνα. Αργότερα στις άκρες των δοκίδων θα σχηματισθούν τα ευθέα σωληνάρια. Από το δίκτυο των πυλών θα σχηματιστεί το δίκτυο του Haller και όταν από την υπόκυρτη ελισσόμενη μοίρα θα σχηματιστούν τα εσπειραμένα σπερματικά σωληνάρια. Κατά τη διάρκεια της εμβρυικής ζωής οι κυτταρικές δοκίδες σχηματίζονται από αρχέγονα γεννητικά κύτταρα, μεταξύ των οποίων στηρικτικά τα κύτταρα του Sertoli. Αυτές οι δοκίδες μένουν συμπαγείς ως την ηλικία πριν την ήβη. Την σωληνοποίηση των εσπειραμένων σπερματικών σωληναρίων, ακολουθεί και η σωληνοποίηση των ευθέων σωληναρίων και στη 21
22 συνέχεια η σωληνοποίηση των δοκίδων του δικτύου των Haller, όπου ακριβώς τελικά (αναστομώνονται) συναντώνται με τα σωληνάρια των λοβίων της επιδιδυμίδας. Τα διάμεσα κύτταρα του Leudig προέρχονται από μεσεγχυματικά κύτταρα, που βρίσκονται μεταξύ των σπερματικών σωληναρίων. Κατά την 7 η εβδομάδα της διαμόρφωσης σε κάθε έμβρυο, ανεξάρτητα του φύλου, υπάρχουν κάτω από τους αμετάπλαστους γεννητικούς αδένες δύο ζεύγη πόρων, ο μεσοφρονικός πόρος του Wolff και ο παραμεσοφρονικός πόρος του Muller. Η μελλοντική τύχη αυτών των πόρων εξαρτάται από το φύλο του εμβρύου. Σε περίπτωση που το έμβρυο είναι άρρεν, ο πόρος του Wolff παραμένει και εξελίσσεται και σχηματίζει την επιδιδυμίδα, το σπερματικό πόρο με τη σπερματοδόχο κύστη και τον σπερματικό πόρο. Παράλληλα από τον πόρο του Muller σχηματίζεται το σπερματικό λοφίδιο. Κάθοδος των όρχεων Οι όρχεις στην αρχή της διαμόρφωσης βρίσκονται στο οπίσθιο κοιλιακό τοίχωμα, κάτω από την οσφυϊκή μοίρα της σπονδυλικής στήλης. Παράλληλα συνδέονται με το πρόσθιο κοιλιακό τοίχωμα με πτυχή του περιτοναίου, μέσα στην οποία βρίσκεται κλεισμένη λεπτή ταινία από συνδετικό ιστό με λείες μυϊκές ίνες. Η λεπτή αυτή ταινία αποτελεί τον ονομαζόμενο σύνδεσμο του όρχι και μετά την ανάπτυξη του βουβωνικού θυλάκου φθάνει ως το όσχεο και σχηματίζει έτσι το γεννητικό βουβωνικό σύνδεσμο. Μέχρι το 2 ο μήνα της διαμόρφωσης οι όρχεις βρίσκονται στο ίδιο ύψος με τον 2 ον - 3 ον οσφυϊκό σπόνδυλο. Ύστερα κατεβαίνουν στην πύελο. Μεταξύ του 4 ου 6 ου μήνα μετακινούνται έως την έσω επιφάνεια του πρόσθιου κοιλιακού τοιχώματος, αντίστοιχα προς τη θέση του έσω στομίου του βουβωνικού πόρου. 22
23 Στο διάστημα μεταξύ 6 ο 7 ο μήνα της ενδομητρίας ζωής ο όρχις καθώς εισέρχεται μέσα στο βουβωνικό θύλακα, «γλιστράει» προοδευτικά μεταξύ της ελυτροειδούς απόφυσης και του οπίσθιου τοιχώματος. Στο τέλος της κύησης έχει εγκατασταθεί πλήρως μέσα στο όσχεο. Η κάθοδος του όρχι διευκολύνεται από το γεννητικοβουβωνικό σύνδεσμο, επειδή αυτός βραχύνεται. Με την κάθοδο ο όρχις παρασύρει μαζί του το σπερματικό πόρο, τα αγγεία και τα νεύρα του, τα οποία σχηματίζουν έτσι το σπερματικό τόνο. Με την κάθοδο του όρχι και την εγκατάσταση του μέσα στο όσχεο, η ελυτροειδής απόφυση από το έσω στόμιο του βουβωνικού πόρου ως τον άνω πόλο του όρχι φυσιολογικά συγκλείεται, και αποκλείει έτσι κάθε επικοινωνία μεταξύ της περιτοναϊκής κοιλότητας και του βουβωνικού θυλάκου. Το τυφλό άκρο της που παραμένει, καθώς περιβάλλει τον όρχι, σχηματίζει τον ίδιον και τον κοινό ελυτροειδή χιτώνα. Ο γεννητικοβουβωνικός σύνδεσμος μετατρέπεται σε οσχεϊκό σύνδεσμο. Είναι όμως δυνατό σε μερικές περιπτώσεις η ελυτροειδής απόφυση να μην εξαφανισθεί, οπότε κατ αυτόν τον τρόπο σχηματίζεται η λεγόμενη συγγενής οσχεοκήλη. Μερικές φορές η εξαφάνιση τμήματος της ελυτροειδούς απόφυσης δεν είναι πλήρης. Εγκαταλείπεται μικρή περιοχή κατά μήκος του βουβωνικού πόρου ή και χαμηλότερα. Στις θέσεις αυτές μπορεί να αναπτυχθεί υγρό και να σχηματισθεί υδροκήλη (Philip R. Brauer). ΕΜΒΡΥΟΛΟΓΙΚΗ ΑΝΑΠΤΥΞΗ ΑΓΓΕΙΩΝ Οι πρώτες ενδείξεις ανάπτυξης αιμοφόρων αγγείων στο έμβρυο εντοπίζονται στο λεκιθικό ασκό ως εστιακές συναθροίσεις μεσεγχυματικών κυττάρων, οι οποίες είναι γνωστές ως αιματικές νησίδες. Στις αρχές του 1900 παρατηρήθηκε ότι κύτταρα από έμβρυα ήταν ικανά να δημιουργήσουν νέα αγγεία. Τότε εμφανίστηκε και ο όρος «αγγειοβλάστη» για να περιγράψει το κύτταρο από όπου προέρχονται όλα τα ενδοθηλιακά κύτταρα και ο όρος 23
24 «αιμαγγειοβλάστη» που αναφέρεται σε έναν κοινό αρχέγονο κύτταρο από όπου προκύπτουν τα ενδοθηλιακά και τα αιμοποιητικά κύτταρα. Η παρουσία της αιμαγγειοβλάστης επιβεβαιώθηκε 100 χρόνια αργότερα (Choi K et al., 1998). Στη διαφοροποίηση του πολυδύναμου αρχέγονου εμβρυϊκού κυττάρου σε αιμαγγειοβλάστη, ο FGF-2 (Fibroblast Growth Factor-2) παίζει σημαντικό ρόλο (Krah K et al., 1994). Τα πρώτα στάδια διαφοροποίησης της αιμαγγειοβλάστης λαμβάνουν χώρα στις αιματικές νησίδες, αλλά ο μοριακός μηχανισμός με τον οποίο πραγματοποιείται δεν είναι γνωστός. Αρκετά γονίδια έχουν αναγνωριστεί ότι ενέχονται σε αυτή τη διαδικασία (Carmeliet P, 1999) όπως τα Ets-1 (Vandenbunder B et al., 1989), Hex (Thomas PQ et al., 1998),Vegf (Xiong M et al., 1998), Hox (Belotti D et al., 1998, Boudreau N et al., 1997), οι Id-πρωτεΐνες (Lyden D et al., 1999) κτλ. Κοινοί δείκτες για τα αρχέγονα ενδοθηλιακά και τα αιμοποιητικά κύτταρα αποτελούν το CD31, το CD34 και ο υποδοχέας του VEGF, VEGFR-2 (Yamaguchi T et al., 2007). Κατ αυτό τον τρόπο απαλοιφή του γονιδίου του VEGFR-2 στα ποντίκια έχει ως αποτέλεσμα εμβρυϊκό θάνατο και απώλεια ανάπτυξης του αγγειακού και του αιμοποιητικού συστήματος (Shalaby F et al., 1995). Επίσης σε ποντίκια στα οποία έγινε απαλοιφή του VEGFR-1, τα αρχέγονα κύτταρα την αιμαγγειοβλάστη αποτυγχάνουν να οργανωθούν σε φυσιολογικές αγγειακές δομές οδηγούμενα σε υπερανάπτυξη ανώμαλων ενδοθηλιακών κυττάρων (Fong GH et al., 1995). Διάκριση των αγγείων σε φλέβες και αρτηρίες κατά την εμβρυική ανάπτυξη Η διάκριση των αγγείων σε αρτηρίες και φλέβες λαμβάνει χώρα πρώιμα κατά την εμβρυϊκή ανάπτυξη. Πρόσφατες μελέτες έδειξαν ότι συγκεκριμένα Notch προσδέματα όπως το Delta-like-4 (DLL4) (Wilkinson DG et al., 2000) εκφράζονται στο ενδοθήλιο των αρτηριών και ότι ελαττωματική μεταγωγή του σήματος από το Notch προκαλεί προβληματική αγγειακή αναδιαμόρφωση. Κατά την αγγειογενετική διαδικασία, κάποια ενδοθηλιακά κύτταρα από το 24
25 τοίχωμα του τριχοειδούς αγγείου επιλέγονται για μετανάστευση, οδηγώντας στη δημιουργία νέας εκβλάστησης. Αυτά τα κύτταρα ονομάζονται tip cells (ακραία κύτταρα) και καθοδηγούν την εκβλάστηση. Τα κύτταρα αυτά είναι συγκεκριμένα, διαφορετικά το αγγειακό δίκτυο δε θα ήταν λειτουργικό. Οι υποδοχείς Notch και ο προσδέτης τους DLL4 (Delta-like-4) διαδραματίζουν σημαντικό ρόλο για την εκβλάστηση του νέου αγγείου. Μειωμένα επίπεδα του DLL4 ή αναστολή της μεταγωγής σήματος από τους Notch υποδοχείς επάγουν τη δημιουργία πολλών tip cells, οδηγώντας σε δραματική αύξηση της εκβλάστησης και αναστόμωσης των αγγείων (Krebs LT et al., 2000). Επίσης μέλη της οικογένειας των εφρινών (ephrins) και των υποδοχέων τους φαίνεται να παίζουν ρόλο σε αυτή τη διαδικασία (Wilkinson DG et al., 2000). Οι εφρίνες είναι ειδικοί αγγειακοί αυξητικοί παράγοντες, όπως ο VEGF και οι αγγειοποιητίνες Ang-1 και Ang-2. Έτσι κατά τη διάρκεια της εμβρυϊκής ανάπτυξης η εφρίνη Β2 (ephrin B2) εκφράζεται ειδικά στα ενδοθηλιακά κύτταρα των αρτηριών και στη συνέχεια επεκτείνεται και στα αρτηριακά λεία μυϊκά κύτταρα (Gale NW et al., 2001). Αυτή η ειδικότητα της έκφρασης της εφρίνης Β2 συνεχίζεται και στην ενήλικη ζωή (Gale NW et al., 2001; Shin et al., 2001). Σε αντίθεση ο υποδοχέας της EphB4 εκφράζεται στις φλέβες. Παρόλο που αρχικά είχε θεωρηθεί ότι η αγγειακή διαφοροποίηση περιορίζεται αυστηρά στην εμβρυϊκή ζωή, έχει δειχθεί πλέον ότι Ενδοθηλιακά Προγονικά Κύτταρα (EΠK) (Endothelial Progenitor Cells, EPCs) κυκλοφορούν και μετά τη γέννηση και προσελκύονται σε περιοχές in situ ανάπτυξης αγγείων (Asahara T et al., 1999; Kalka C et al., 2000; Rafii S et al., 2000), όπου και συμμετέχουν στην δημιουργία των νέων αγγείων. Tα θετικά στους δείκτες CD34/VEGFR-2 /AC133 EΠK, που προέρχονται από το μυελό των οστών των ενηλίκων έχουν υψηλό πολλαπλασιαστικό δυναμικό (Lin S et al., 2000). Ως προς τον μηχανισμό με τον οποίο τα EΠK κινητοποιούνται και προσελκύονται στις περιοχές της αγγειακής διαφοροποίησης, η συμμετοχή της ΜΜP-9 και της skitl (stem-cell cytokine-soluble kit ligand) έχει περιγραφεί. Αρκετοί επίσης αυξητικοί παράγοντες συμπεριλαμβανομένων των VEGF και GM-CSF 25
26 (Granulocyte Macrophage Colony Stimulating Factor) έχουν δειχθεί, ότι μπορούν να προσελκύσουν EΠK από το μυελό των οστών σε περιοχές νεοαγγείωσης μετά τη γέννηση (Asahara T et al, 1999; McBride JL et al., 1998, Takahaski T et al., 1999). Η διαφοροποίηση των EΠK πιθανώς επάγεται από τον VEGF (μέσω του VEGFR-2) και τον FGF-2 (Carmeliet P et al., 1996; Salaby F et al., 1997), ενώ ο VEGFR-1 έχει δειχθεί ότι καταστέλλει την κατεύθυνση διαφοροποίησης των EΠK (Fong TA et al., 1999). ΤΟ ΑΓΓΕΙΑΚΟ ΤΟΙΧΩΜΑ Σε γενικές γραμμές, τα αγγεία στην πλειοψηφία τους έχουν κοινά χαρακτηριστικά. Ωστόσο, παρατηρούνται ορισμένες διαφοροποιήσεις, οι οποίες αποτελούν και τη βάση για την κατάταξη των αγγείων σε συγκεκριμένες κατηγορίες. Τα τοιχώματα των αγγείων που δέχονται υψηλές πιέσεις (όπως οι υποκλείδιες αρτηρίες) είναι παχύτερα από αυτά που μεταφέρουν αίμα με χαμηλή πίεση (όπως οι υποκλείδιες φλέβες). Η διάμετρος των αρτηριών ελαττώνεται σε κάθε διακλάδωση, η διάμετρος των φλεβών αυξάνει μετά από κάθε σύγκλιση, μεταβάλλοντας επομένως και τα αντίστοιχα στρώματα του τοιχώματος των αγγείων. Συνεπώς, δεν μπορεί να χρησιμοποιηθεί μόνο το πάχος του τοιχώματος για τη διάκριση συγκεκριμένων αρτηριών από φλέβες, καθώς η σύγκριση δεν είναι απόλυτη. Αντίθετα, τα τοιχώματα των τριχοειδών και των φλεβιδίων παρουσιάζουν ιδιαιτερότητες και είναι λιγότερο πολύπλοκα από αυτά των μεγαλύτερων αγγείων, γεγονός που τα καθιστά εύκολα διακριτά. Γενικά, πάντως, οι αρτηρίες διαθέτουν παχύτερο τοίχωμα και μικρότερη διάμετρο από τις αντίστοιχες φλέβες [Εικόνα 6] (Landmesser U et al., 2004; Wali MA et al., 2002 [i], Arnoldi CC et al., 1957). 26
27 Εικόνα 6: Σχηματικό διάγραμμα μυϊκού τύπου αρτηρίας (αριστερά) και ελαστικής αρτηρίας (δεξιά). Ο μέσος χιτώνας της ελαστικής αρτηρίας σχηματίζεται από στρώματα λείων μυϊκών κυττάρων που διαχωρίζονται από ελαστικά πέταλα. Ο έξω χιτώνας και το εξωτερικό τμήμα του μέσου χιτώνα περιέχει μικρά αιμοφόρα αγγεία, ελαστικές ίνες και ίνες κολλαγόνου. Το τοίχωμα των αγγείων απαρτίζεται από τρία βασικά δομικά συστατικά: ενδοθήλιο, μυϊκό ιστό και συνδετικό ιστό με ελαστικά στοιχεία. Η αναλογία και η οργάνωση των τριών αυτών στοιχείων κατά μήκος του κυκλοφορικού συστήματος επηρεάζεται από μηχανικούς και μεταβολικούς παράγοντες, όπως είναι η αρτηριακή πίεση και οι μεταβολικές ανάγκες των ιστών. Σε διαφορετικές αναλογίες, οι ιστοί αυτοί σχηματίζουν το τοίχωμα όλων των αγγείων, εκτός από αυτό των τριχοειδών και μετατριχοειδικών φλεβιδίων, των οποίων τα μόνα δομικά συστατικά είναι το ενδοθήλιο, ο βασικός υμένας αυτού και τα περικύτταρα (Landmesser U et al., 2004; Wali MA et al., 2002, Arnoldi CC et al., 1957). ΙΣΤΟΛΟΓΙΚΗ ΔΟΜΗ ΑΙΜΟΦΟΡΩΝ ΑΓΓΕΙΩΝ Το τοίχωμα ενός τυπικού αιμοφόρου αγγείου απαρτίζεται από τρία ξεχωριστά, στρώματα ιστού (χιτώνες) [Εικόνα 7]. Πρώτος βρίσκεται ο έσω χιτώνας, που αποτελείται από μονή στοιβάδα πεπλατυσμένων, πλακωδών 27
28 ενδοθηλιακών κυττάρων, τα οποία σχηματίζουν ένα σωλήνα που επενδύει τον αυλό του αγγείου, μαζί με τον υποκείμενο υπενδοθηλιακό συνδετικό ιστό. Το μεσαίο στρώμα ιστού, ο μέσος χιτώνας συντίθεται κυρίως από λεία μυϊκά κύτταρα με ομόκεντρη διάταξη γύρω από τον αυλό του αγγείου. Το πλέον εξωτερικό στρώμα, ο έξω χιτώνας αποτελείται κυρίως από ινοελαστικό συνδετικό ιστό με επιμήκη προσανατολισμό (Arnoldi CC et al., 1957). Εικόνα 7: Σχηματική απεικόνιση της ιστολογικής δομής ενός αιμοφόρου αγγείου (Pugsley MK 2000). Ο έσω χιτώνας περιλαμβάνει στο εξωτερικό του τμήμα την έσω ελαστική μεμβράνη, μία λεπτή ζώνη ελαστικών ινών που είναι ιδιαίτερα αναπτυγμένη στις μεσαίου μεγέθους αρτηρίες. Αντίστοιχα, το εξώτατο τμήμα του μέσου χιτώνα περιλαμβάνει μία επίσης λεπτή ζώνη ελαστικών ινών, την έξω ελαστική μεμβράνη, που όμως δεν παρατηρείται σε όλες τις αρτηρίες. Τα κύτταρα που βρίσκονται βαθιά στο μέσο χιτώνα καθώς και τα κύτταρα του έξω χιτώνα αιματώνονται από τα αγγεία των αγγείων (Landmesser U et al., 2004; Wali MA et al., 2002, Arnoldi CC et al., 1957). ΕΣΩ ΧΙΤΩΝΑΣ Τα ενδοθηλιακά κύτταρα (μονόστοιβο πλακώδες επιθήλιο), που επενδύουν τον αυλό του αιμοφόρου αγγείου, στηρίζονται στο βασικό υμένα. 28
29 Τα πεπλατυσμένα αυτά κύτταρα είναι διατεταγμένα σε ένα λεπτό στρώμα με τέτοιο τρόπο ώστε ο επιμήκης άξονάς τους να είναι σχεδόν παράλληλος με τον επιμήκη άξονα του αγγείου, γεγονός που επιτρέπει σε μεμονωμένα ενδοθηλιακά κύτταρα να επενδύουν μόνα τους τον αυλό τουλάχιστον μικρού διαμετρήματος αγγείου [Εικόνα 8]. Τα ενδοθηλιακά κύτταρα δεν παρέχουν μόνο μία απόλυτα λεία επιφάνεια για τη ροή του αίματος, αλλά επιπλέον έχουν και εκκριτική λειτουργία, αφού παράγουν και εκκρίνουν μεταξύ άλλων και κολλαγόνο. Εικόνα 8: Σχηματική αναπαράσταση των ενδοθηλιακών κυττάρων (αριστερά) και ηλεκτρονική μικροφωτογραφία του ενδοθηλίου μικρής φλέβας (δεξιά). Αξίζει να σημειωθεί η παράλληλη με τη ροή του αίματος διάταξη των ενδοθηλιακών κυττάρων (Ross MH 2006). Κάτω ακριβώς από τα ενδοθηλιακά κύτταρα βρίσκεται η υπενδοθηλιακή στοιβάδα. Αυτή αποτελείται από χαλαρό συνδετικό ιστό και λίγα διάσπαρτα λεία μυϊκά κύτταρα, αμφότερα διαταγμένα κατά τον επιμήκη άξονα του αγγείου. Κάτω και από την υπενδοθηλιακή στοιβάδα βρίσκεται η έσω ελαστική μεμβράνη, που είναι ιδιαίτερα αναπτυγμένη στις μυϊκές αρτηρίες. Η μεμβράνη αυτή είναι ένα λεπτό ινώδες στρώμα αποτελούμενο από ελαστίνη, που χωρίζει τον έσω από το μέσο χιτώνα του αγγείου, και εμφανίζει θυρίδες που επιτρέπουν τη διάχυση ουσιών από τον αυλό του αγγείου προς βαθύτερα στρώματα του αρτηριακού τοιχώματος για τη θρέψη των κυττάρων που 29
30 βρίσκονται σε αυτά (Landmesser U et al., 2004; Wali MA et al., 2002 [i], Arnoldi CC et al., 1957). Σε υγιή νεαρά άτομα, ο έσω χιτώνας είναι λεπτός και διαδραματίζει σημαντικό ρόλο στον καθορισμό των μηχανικών ιδιοτήτων των αγγείων. Με την ηλικία όμως επέρχεται πάχυνση του έσω χιτώνα καθώς και αύξηση της αγγειακής διαμέτρου, αλλαγές που επιδρούν καταλυτικά στις μηχανικές ιδιότητες του αγγείου (Brand FN et al., 1998). ΜΕΣΟΣ ΧΙΤΩΝΑΣ Ο μέσος χιτώνας αποτελεί τη μεσαία στοιβάδα και το παχύτερο στρώμα του αιμοφόρου αγγείου. Οι ομόκεντρες στοιβάδες κυττάρων, που σχηματίζουν το μέσο χιτώνα, αποτελούνται κυρίως από ελικοειδώς διατεταγμένα λεία μυϊκά κύτταρα. Διάσπαρτες μεταξύ των στοιβάδων των λείων μυϊκών κυττάρων βρίσκονται ελαστικές ίνες, ίνες κολλαγόνου και πρωτεογλυκάνες. Τα ινώδη στοιχεία σχηματίζουν πέταλα εντός της θεμέλιας ουσίας που εκκρίνουν τα λεία μυϊκά κύτταρα. Ο μέσος χιτώνας είναι περισσότερο αναπτυγμένος στις αρτηρίες, ενώ δεν είναι ευκρινής στις φλέβες και τέλος στα πολύ μικρά αγγεία ουσιαστικά είναι ανύπαρκτος. Στα αγγεία που είναι πολύ κοντά στην καρδιά και δέχονται όλο τον όγκο του κύματος της συστολικής πίεσης, ο ελαστικός ιστός είναι πολύ καλά αναπτυγμένος και για αυτό ονομάζονται ελαστικές αρτηρίες. Στις μυϊκές αρτηρίες και αρτηρίδια το κύριο ελαστικό πέταλο αμέσως κάτω από τον έσω χιτώνα ονομάζεται έσω ελαστική μεμβράνη. Οι μεγαλύτερες μυϊκές αρτηρίες διαθέτουν και έξω ελαστική μεμβράνη, που είναι λεπτότερη από την έσω ελαστική μεμβράνη και χωρίζει το μέσο χιτώνα από το υπερκείμενο έξω χιτώνα (Landmesser U et al., 2004; Wali MA et al., 2002 [i], Arnoldi CC et al., 1957). 30
31 ΕΞΩ ΧΙΤΩΝΑΣ Ο έξω χιτώνας καλύπτει την εξωτερική επιφάνεια των αγγείων, αποτελούμενος κατά κύριο λόγο από ινοβλάστες, ίνες κολλαγόνου και ελαστικές ίνες με επιμήκη προσανατολισμό. Ο χιτώνας αυτός συνήθως συνέχεται με τα υπόλοιπα στοιχεία του συνδετικού ιστού που περιβάλλουν το αγγείο και είναι συχνά ο πιο εμφανής χιτώνας του τοιχώματος των φλεβών. Μέσα στον έξω χιτώνα με παχιά τοιχώματα διεισδύουν μικρά αγγεία, τα αγγεία των αγγείων, τα οποία διακλαδιζόμενα τροφοδοτούν με αίμα το μέσο χιτώνα (Mirloy CM et al., 1989; Landmesser U et al., 2004). ΜΙΚΡΑ ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΤΩΝ ΑΓΓΕΙΩΝ (VASA VASORUM) Το πάχος και η μυϊκή σύσταση των μεγάλων αγγείων κυρίως του μέσου και έξω χιτώνα δεν επιτρέπουν στα κύτταρα που απαρτίζουν αυτούς τους χιτώνες να προσλαμβάνουν θρεπτικά συστατικά με διάχυση από τον αυλό του αγγείου. Αυτά τα κύτταρα, επομένως, τρέφονται από τα αγγεία των αγγείων, μικρές αρτηρίες που εισέρχονται στο αγγειακό τοίχωμα και αποσχίζονται σε πολλούς κλάδους για να εξυπηρετήσουν τις ανάγκες των κυττάρων του μέσου και έξω χιτώνα των αγγείων. Σε σύγκριση με τις αρτηρίες, οι φλέβες έχουν περισσότερα κύτταρα που δεν είναι δυνατόν να προσλάβουν οξυγόνο και θρεπτικά συστατικά με διάχυση, εξαιτίας και της μικρότερης περιεκτικότητας του φλεβικού αίματος σε οξυγόνο και θρεπτικές ουσίες. Ως εκ τούτου, τα αγγεία των αγγείων απαντούν σε μεγαλύτερο βαθμό στα φλεβικά από ότι στα αρτηριακά τοιχώματα, ενώ απουσιάζουν από τα λεπτότερα αγγεία, τα οποία προσλαμβάνουν οξυγόνο με διάχυση από τον αυλό (Landmesser U et al., 2004; Wali MA et al., 2002 [i]). 31
32 ΝΕΥΡΩΣΗ ΤΩΝ ΑΓΓΕΙΩΝ Ένα δίκτυο αγγειοκινητικών νεύρων του συμπαθητικού αυτόνομου νευρικού συστήματος παρέχει νεύρωση στα λεία μυϊκά κύτταρα των αιμοφόρων αγγείων. Τα νεύρα σπάνια εισέρχονται στο μέσο χιτώνα των αγγείων, επομένως δε σχηματίζουν συνάψεις άμεσα με τα κύτταρα. Αντίθετα, απελευθερώνουν κάποια νευροδιαβιβαστική ουσία, που με διάχυση φτάνει στο μέσο χιτώνα και δρα στα παρακείμενα κύτταρα. Οι ώσεις διαδίδονται σε όλα τα λεία μυϊκά κύτταρα μέσω των χασματικών συνδέσεών τους, παράγοντας μία συντονισμένη συστολή όλων των λείων μυϊκών κυττάρων του τοιχώματος του αγγείου, με αποτέλεσμα την ελάττωση της διαμέτρου του αυλού του. Οι αρτηρίες δέχονται πλουσιότερη αγγειοκινητική νεύρωση από ότι οι φλέβες, αλλά οι φλέβες δέχονται επιπλέον αγγειοκινητικές νευρικές απολήξεις στον έξω χιτώνα τους (Landmesser U et al., 2004; Wali MA et al., 2002[i], Arnoldi CC et al., 1957). ΔΙΑΚΡΙΣΗ ΑΙΜΟΦΟΡΩΝ ΑΓΓΕΙΩΝ Ο βασικός σκοπός του κυκλοφορικού συστήματος είναι να μεταφέρει θρεπτικά συστατικά και οξυγόνο σε όλο το ανθρώπινο σώμα και να απομακρύνει τις βλαβερές ουσίες. Η πίεση που δημιουργείται από την καρδιά ωθεί το αίμα στα διάφορα όργανα και ιστούς μέσω αιμοφόρων αγγείων. Τα αιμοφόρα αγγεία διακρίνονται σε αρτηρίες, φλέβες και τριχοειδή. Με βάση το σχετικό μέγεθος των αγγείων και τα μορφολογικά τους χαρακτηριστικά, καθεμία από αυτές τις κατηγορίες μπορεί να υποδιαιρεθεί σε περισσότερες [Εικόνα 9]. Έτσι, οι αρτηρίες διακρίνονται σε μεγάλες ελαστικές αρτηρίες, μυϊκού τύπου αρτηρίες και αρτηρίδια. Οι φλέβες αντίστοιχα διακρίνονται σε φλεβίδια και μικρές, μέσου μεγέθους και μεγάλες φλέβες, ενώ τα τριχοειδή διακρίνονται περαιτέρω σε συνεχή (σωματικού τύπου), θυριδωτά (σπλαχνικού τύπου) και κολπώδη (κολποειδή) τριχοειδή. Καθώς η διάμετρος των αρτηριών και φλεβών ελαττώνεται και αυξάνεται, αντίστοιχα, με συνεχή τρόπο, υπάρχει βαθμιαία αλλαγή στα μορφολογικά χαρακτηριστικά των 32
33 αγγείων κατά τη μετάπτωση από τη μία κατηγορία στην άλλη. Συνεπώς, ορισμένα αγγεία είναι δυνατό να εμφανίζουν χαρακτηριστικά δύο κατηγοριών και να μην κατατάσσονται με βεβαιότητα σε μία κατηγορία (Liu SQ et al., 2002; Liu SQ et al., 2003; Zhang SX et al., 2003). Εικόνα 9: Σχηματική απεικόνιση των διαφορών στη δομή του τοιχώματος των αιμοφόρων αγγείων, ήτοι των αρτηριών, φλεβών και τριχοειδών. ΑΡΤΗΡΙΕΣ ΜΕΓΑΛΕΣ ΕΛΑΣΤΙΚΕΣ ΑΡΤΗΡΙΕΣ Η αορτή και οι κλάδοι που εκφύονται από το αορτικό τόξο (κοινή καρωτίδα και υποκλείδιος αρτηρία), οι κοινές λαγόνιες αρτηρίες και το στέλεχος της πνευμονικής αρτηρίας ανήκουν στις ελαστικές αρτηρίες, που επίσης ονομάζονται και μεταφορικές. Το τοίχωμα αυτών των αγγείων σε νωπά παρασκευάσματα έχει κίτρινο χρώμα, λόγω της άφθονης ελαστίνης που περιέχει (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005). Ο έσω χιτώνας των ελαστικών αρτηριών αποτελείται από ενδοθήλιο, που υποστηρίζεται από λεπτή στοιβάδα υποκείμενου συνδετικού ιστού, αποτελούμενη από λίγους ινοβλάστες, περιστασιακά λεία μυϊκά κύτταρα και ίνες κολλαγόνου. Επίσης, παρατηρούνται ελαστικές ίνες που σχηματίζουν λεπτή έσω ελαστική μεμβράνη. Τα ενδοθηλιακά κύτταρα των ελαστικών 33
34 αρτηριών έχουν πλάτος μm και μήκος μm, με τους επιμήκεις άξονές τους παράλληλους στον επιμήκη άξονα του αγγείου. Ο μέσος χιτώνας των ελαστικών αρτηριών αποτελείται από διάτρητα πέταλα ελαστίνης, γνωστά και ως διάτρητες ή θυριδωτές μεμβράνες, που εναλλάσσονται με κυκλοτερώς διαταγμένες στοιβάδες λείων μυϊκών κυττάρων. O αριθμός των μεμβρανών ελαστίνης αυξάνει με την ηλικία και από περίπου 40 στο νεογνό φτάνει τις 70 στους ενήλικες. Οι μεμβράνες αυξάνουν επίσης σε πάχος, λόγω της συνεχούς εναπόθεσης ελαστίνης, που συνθέτει το μεγαλύτερο μέρος του μέσου χιτώνα. Τα λεία μυϊκά κύτταρα είναι πολύ λιγότερα σε αριθμό στις ελαστικές από ότι στις περισσότερες μυϊκές αρτηρίες. Η εξωκυττάρια θεμέλια ουσία, που εκκρίνεται από τα λεία μυϊκά κύτταρα, αποτελείται κυρίως από κολλαγόνο, καθώς και δικτυωτές και ελαστικές ίνες. Στο μέσο χιτώνα παρατηρείται επίσης έξω ελαστική μεμβράνη (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005). Ο έξω χιτώνας των ελαστικών αρτηριών είναι σχετικά λεπτός και συντίθεται από χαλαρό ινοελαστικό συνδετικό ιστό που περιέχει λίγους ινοβλάστες. Τροφοδοτικά αγγεία των αγγείων απαντούν σε αφθονία στον έξω χιτώνα. Μάλιστα, δίκτυα τριχοειδών που ξεκινούν από αυτά τα αγγεία επεκτείνονται στους ιστούς του μέσου χιτώνα για την παροχή οξυγόνου και θρεπτικών συστατικών στο συνδετικό ιστό και στα λεία μυϊκά κύτταρα. Οι θυρίδες των ελαστικών πετάλων επιτρέπουν ως ένα βαθμό τη διάχυση οξυγόνου και ουσιών από τον αυλό του αγγείου στα κύτταρα του μέσου χιτώνα, αλλά η κύρια πηγή θρεπτικών συστατικών για τα κύτταρα αυτού του χιτώνα είναι οι κλάδοι των τροφοφόρων αγγείων του αγγείου (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005; Kockx MM et al., 1998). ΜΥΪΚΕΣ ΑΡΤΗΡΙΕΣ Οι μυϊκές αρτηρίες, γνωστές και ως αρτηρίες κατανομής, περιλαμβάνουν τους περισσότερους κλάδους της αορτής εκτός από τους μεγάλους κλάδους του αορτικού τόξου και του τελικού διχασμού της κοιλιακής αορτής, που αναγνωρίζονται ως ελαστικές ίνες. Το χαρακτηριστικό των μυϊκών 34
35 αρτηριών είναι ο σχετικά παχύς μέσος χιτώνας που αποτελείται κυρίως από λεία μυϊκά κύτταρα (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005; Kockx MM et al., 1998). Ο έσω χιτώνας στις μυϊκές αρτηρίες είναι λεπτότερος από τον αντίστοιχο των ελαστικών αρτηριών. Στο μέσο χιτώνα των μυϊκών αρτηριών κυριαρχούν τα λεία μυϊκά κύτταρα, παρόλο που αυτά είναι σημαντικά μικρότερα σε μέγεθος από τις σπλαχνικές λείες μυϊκές ίνες. Αυτά είναι προσανατολισμένα κυκλοτερώς γύρω από τον αυλό στα σημεία επαφής με τον έσω χιτώνα, ενώ λίγα δεμάτια λείων μυϊκών ινών είναι διαταγμένα κατά τον επιμήκη άξονα των αγγείων στον έξω χιτώνα. Διάσπαρτες μεταξύ των στοιβάδων των λείων μυϊκών κυττάρων βρίσκονται ελαστικές ίνες και ίνες κολλαγόνου, παραγόμενες από τα λεία μυϊκά κύτταρα. Ο έξω χιτώνας τους αποτελείται από ελαστικές ίνες, ίνες κολλαγόνου (διαμέτρου nm) και θεμέλια ουσία. Αυτή η ουσία παράγεται από ινοβλάστες του έξω χιτώνα. Οι ίνες κολλαγόνου, καθώς και οι ελαστικές ίνες είναι προσανατολισμένες κατά τον επιμήκη άξονα του αγγείου και αναμιγνύονται με τον περιβάλλοντα συνδετικό ιστό. ΑΡΤΗΡΙΔΙΑ Οι αρτηρίες με διάμετρο μικρότερη του 0,1 μm ονομάζονται αρτηρίδια. Τα αρτηρίδια αποτελούν τα τελευταία αρτηριακά αγγεία που ρυθμίζουν την αιματική ροή στα δίκτυα των τριχοειδών. Το πάχος του τοιχώματος των αρτηριδίων είναι περίπου ίσο με τη διάμετρο του αυλού τους (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005; Kockx MM et al., 1998). ΟΙ ΛΕΙΤΟΥΡΓΙΑ ΤΩΝ ΑΡΤΗΡΙΩΝ Οι μεγάλες αρτηρίες κοντά στην καρδιά, όπως είναι η αορτή και οι καρωτίδες, είναι ιδιαίτερα ελαστικές. Κατά τη συστολική φάση, η καρδιά εκτοπίζει το αίμα με υψηλή πίεση. Το αίμα αυτό εισέρχεται στην αορτή, η 35
36 οποία εξαιτίας της ελαστικότητάς της, διαστέλλεται. Μετά τη συστολή, όταν η πίεση του αίματος ελαττώνεται πάλι, τα αορτικά τοιχώματα είναι υπό διαστολή και σπρώχνουν το αίμα προς τα υπόλοιπα αγγεία. Κατ αυτό τον τρόπο, τα μεγαλύτερα αιμοφόρα αγγεία, που βρίσκονται κοντά στην καρδιά ρυθμίζουν και εξομαλύνουν την παλμική ροή του αίματος (Kockx MM et al., 1998). Η αύξηση της επιφάνειας του αυλού των αιμοφόρων αγγείων, εξαιτίας της αύξησης της πίεσης, καλείται ενδοτικότητα. Οι μεγάλες αρτηρίες υπό φυσιολογικές συνθήκες έχουν μεγάλη ενδοτικότητα. Οι μικρότερες και πιο μυώδεις αρτηρίες, οι οποίες βρίσκονται κοντά στα όργανα, μπορούν να συσπώνται έτσι ώστε να μειώνουν τη διάμετρό τους και συνεπαγωγικά να αυξάνουν την αντίσταση στη ροή του αίματος ή να διαστέλλονται ώστε να μειώνουν την αντίσταση. Αυτή η διαδικασία ρυθμίζει την εισροή του φρέσκου αίματος ανάλογα με τις ανάγκες των οργάνων του σώματος που περιβάλλουν αυτές τις μικρότερες αρτηρίες (Psaila JV et al., 1989). ΦΛΕΒΕΣ Η σύσταση των τριών χιτώνων ποικίλει στις διάφορες κατηγορίες φλεβών και αποτελεί βασικό κριτήριο για τη διάκρισή τους. Οι φλέβες ποικίλουν σε μέγεθος, με διάμετρο που κυμαίνεται από 1 mm έως 4 cm (έναντι της διαμέτρου των αρτηριών από 1 cm έως 0,5 cm). Σε σχέση με τις αρτηρίες με συγκρίσιμη εξωτερική διάμετρο, οι φλέβες έχουν μεγαλύτερο αυλό και σχετικά λεπτότερο τοίχωμα [Εικόνα 10]. Στα ιστολογικά παρασκευάσματα παρατηρείται σύμπτωση των τοιχωμάτων τους, εκτός και αν έχει προηγηθεί ειδική ενδοαγγειακή έγχυση μονιμοποιητικού υγρού, η οποία διατηρεί σε διάταση τον αυλό του αγγείου. Αν και οι φλέβες φέρουν έσω, μέσο και έξω χιτώνα, αυτοί δε διαχωρίζονται καλά, σε αντίθεση με τις αρτηρίες, ώστε συχνά είναι δύσκολο να αναγνωριστεί πότε τελειώνει ο ένας χιτώνας και πότε αρχίζει ο επόμενος. Οι φλέβες ανάλογα με τη θέση τους εμφανίζουν διαφορετική δομή στο τοίχωμά τους (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005; Kockx MM et al., 1998). 36
37 Εικόνα 10: Σχηματική απεικόνιση αρτηρίας και φλέβας, όπου παρατηρείται ότι η φλέβα έχει μεγαλύτερη διάμετρο και λεπτότερο τοίχωμα από την αρτηρία. ΜΕΤΑΤΡΙΧΟΕΙΔΗ ΦΛΕΒΙΔΙΑ Τα άμεσα μετατριχοειδή φλεβίδια (περικυτταρικές φλέβες) ποικίλουν σε διάμετρο από 0,1-0,5 mm και σε μήκος από 0,5-70 mm, και χαρακτηρίζονται από παρουσία περικυττάρων. Ο έσω χιτώνας αυτών των αγγείων αποτελείται από ενδοθήλιο και μία πολύ λεπτή υπενδοθηλιακή στοιβάδα. Στα αγγεία αυτά παρατηρούνται οι χαλαρότερες συνδέσεις μεταξύ των ενδοθηλιακών κυττάρων σε όλο το καρδιαγγειακό σύστημα. Ο μέσος χιτώνας τους μπορεί να περιέχει μόνο συσταλτικά περικύτταρα. Τα μετατριχοειδή φλεβίδια έχουν πολλά κοινά ιστολογικά χαρακτηριστικά με τα τριχοειδή, όπως η συμμετοχή στις φλεγμονώδεις διαδικασίες και η ανταλλαγή μορίων, ακόμα και κυττάρων μεταξύ αίματος και ιστών (Zhang SX et al., 2003; Vane JR et al., 1994; Kockx MM et al., 1998; Psaila JV et al., 1989). 37
38 ΜΥΪΚΕΣ ΦΛΕΒΕΣ Τα περισσότερα φλεβίδια έχουν μυϊκά κύτταρα στο τοίχωμά τους. Τα αγγεία αυτά συχνά συνοδεύουν αρτηρίδια, από τα οποία διακρίνονται εύκολα σε ιστολογικές τομές, εξαιτίας του λεπτότερου τοιχώματος και του ανώμαλου αυλού, λόγω της σύμπτωσης των τοιχωμάτων τους. Τα φλεβίδια αυτά είναι δυνατόν να επηρεάζουν την αιματική ροή στα αρτηρίδια με την παραγωγή και έκκριση αγγειοδραστικών ουσιών (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005; Kockx MM et al., 1998). Από τα φλεβίδια, το αίμα συλλέγεται σε φλέβες μεγαλύτερου μεγέθους, με διάμετρο μεταξύ 1 και 9 mm. O έσω χιτώνας συνήθως διαθέτει λεπτή υπενδοθηλιακή στοιβάδα, που όμως μπορεί και να απουσιάζει. Ο μέσος χιτώνας αποτελείται από μικρές δεσμίδες λείων μυϊκών ινών, που αναμιγνύονται με δικτυωτές ίνες και ένα λεπτό δίκτυο ελαστικών ινών. Ο έξω χιτώνας, αποτελούμενος κυρίως από κολλαγόνο, είναι καλά αναπτυγμένος (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005; Kockx MM et al., 1998). ΜΕΓΑΛΕΣ ΦΛΕΒΕΣ Οι μεγάλες φλέβες περιλαμβάνουν κυρίως τα πλησίον της καρδιάς μεγάλα φλεβικά στελέχη. Τα αγγεία αυτά έχουν καλά αναπτυγμένο έσω χιτώνα, αλλά ο μέσος χιτώνας είναι αρκετά λεπτότερος, με λίγες στοιβάδες λείων μυϊκών κυττάρων και άφθονο συνδετικό ιστό [Εικόνα 11]. Ο έξω χιτώνας είναι ο παχύτερος και ο καλύτερα ανεπτυγμένος χιτώνας στις φλέβες και συχνά περιέχει επιμήκη δεμάτια λείων μυϊκών κυττάρων. Αυτές οι φλέβες, ειδικά οι μεγαλύτερες, έχουν βαλβίδες στο εσωτερικό τους, που αποτελούνται από δύο ημισεληνοειδείς πτυχές του έσω χιτώνα που προβάλλουν στον αυλό. Συντίθενται από συνδετικό ιστό πλούσιο σε ελαστικές ίνες και επενδύονται και στις δύο πλευρές από ενδοθήλιο. Οι βαλβίδες, που είναι πολυάριθμες στις φλέβες των άκρων, συμβάλλουν στην επαναφορά του φλεβικού αίματος στην καρδιά, σε συνδυασμό με τη σύσπαση των σκελετικών μυών που περιβάλλουν 38
39 τις φλέβες (Liu SQ et al., 2003; Zhang SX et al., 2003; Knaapen M et al., 2005; Kockx MM et al., 1998). Εικόνα 11: Συγκριτική σχηματική παράσταση των συστατικών του τοιχώματος μίας φλέβας μεσαίου μεγέθους (αριστερά) και μεγάλου μεγέθους (δεξιά) (Wali MA et al., 2002[i]). ΔΟΜΗ ΤΩΝ ΚΥΤΤΑΡΙΚΩΝ ΣΥΣΤΑΤΙΚΩΝ ΤΟΥ ΑΓΓΕΙΑΚΟΥ ΤΟΙΧΩΜΑΤΟΣ Τα ενδοθηλιακά και τα αγγειακά λεία μυϊκά κύτταρα (vascular smooth muscle cells, VSMCs) αποτελούν τα κύρια κυτταρικά συστατικά του αγγειακού τοιχώματος. ΕΝΔΟΘΗΛΙΑΚΑ ΚΥΤΤΑΡΑ Τα ενδοθηλιακά κύτταρα σχηματίζουν ένα στρώμα που επενδύει εσωτερικά ολόκληρο το αγγειακό σύστημα, δημιουργώντας έτσι το πιο σημαντικό φράγμα διαπερατότητας των αιμοφόρων αγγείων. Τα ενδοθηλιακά κύτταρα έχουν επίπεδο σχήμα, αποτελούνται από λεπτή στοιβάδα κυτταροπλάσματος και ένα μοναδικό ελλειψοειδή πυρήνα, ο οποίος προεξέχει στον ενδοαυλικό χώρο (Travers JP et al., 1996). 39
40 ΑΓΓΕΙΑΚΑ ΛΕΙΑ ΜΥΙΚΑ ΚΥΤΤΑΡΑ Τα αγγειακά λεία μυϊκά κύτταρα (VSMCs) αποτελούν δομική μονάδα με κύρια λειτουργία τη συστολή. Η δομή τους, επομένως, είναι τέτοια που εξυπηρετεί τη βασική τους λειτουργία. Κυρίαρχη θέση στα VSMCs κατέχει η συσταλτική συσκευή, ενώ ο κυτταροσκελετός και οι συνδέσεις των κυττάρων με τα γειτονικά τους και με την εξωκυττάρια θεμέλια ουσία είναι εξίσου σημαντικές, καθώς χρησιμεύουν στη σηματοδότηση και μεταφορά μηνυμάτων από τον εξωκυττάριο χώρο (Badier-Commander C et al., 2000). Τα VSMCs, επειδή έχουν τη δυνατότητα να συστέλλονται και να αλλάζουν τις ελαστικές τους ιδιότητες, παίζουν σημαντικό ρόλο στο συντονισμό της μηχανικής συμπεριφοράς του αγγείου. Έχουν τη μορφή ενός τυλιγμένου νήματος και απλούς επιμηκυμένους πυρήνες. Το σχήμα των πυρήνων εξαρτάται από την κατάσταση συστολής ή διαστολής των κυττάρων. Οι πυρηνικές μεμβράνες περιελίσσονται όταν τα κύτταρα συστέλλονται και ομαλοποιούνται στη φάση που τα κύτταρα χαλαρώνουν. Οι δομικές ιδιότητες και η μηχανική συμπεριφορά των αιμοφόρων αγγείων εξαρτάται σε μεγάλο βαθμό από την ποσότητα και την οργάνωση του συνδετικού τους ιστού. Έχει αποδειχτεί ότι η αύξηση και ο πολλαπλασιασμός των VSMCs επηρεάζεται από τις μηχανικές δυνάμεις, που σχετίζονται με τη ροή του αίματος εντός του αγγείου, καθώς και από διάφορους χημικούς παράγοντες του αίματος. Πιο συγκεκριμένα, στην περίπτωση των αρτηριών τα VSMCs είναι συνδεδεμένα στα φύλλα της ελαστίνης και συσπώνται ή χαλαρώνουν ανάλογα με το άμεσο μηχανικό ή βιοχημικό ερέθισμα που δέχονται (Travers JP et al., 1996). Για παράδειγμα, τα VSMCs χαλαρώνουν όταν έρχονται σε επαφή με μονοξείδιο του αζώτου (ΝΟ) (Badier-Commander C et al., 2000). Το ΝΟ συντίθεται από τα ενδοθηλιακά κύτταρα (ΕΚ), που βρίσκονται στον έσω χιτώνα της αρτηρίας σε μια στοιβάδα. Τα ΕΚ παράγουν ΝΟ, όταν εκτίθενται σε αυξημένες διατμητικές τάσεις εξαιτίας της αύξησης της ροής του αίματος. Όταν το ΝΟ φθάσει στα VSMCs και αυτά χαλαρώσουν, η διάμετρος του αυλού της αρτηρίας θα μεγαλώσει επιτρέποντας τη διέλευση μεγαλύτερης ποσότητας 40
41 αίματος μειώνοντας τη διατμητική τάση που ασκείται στα ΕΚ. Το πιο σημαντικό μηχανικό ερέθισμα, που είναι γνωστό ότι προκαλεί τις αλλαγές στον τόνο των VSMC, είναι μια ξαφνική αύξηση της πίεσης του αίματος, η οποία μπορεί να προκαλέσει την έκταση του τοιχώματος του αιμοφόρου αγγείου και έτσι να αυξήσει την παραμόρφωση των VSMCs, που περιέχονται στο τοίχωμα. Τα VSMCs αντιδρούν σε αυτή την ξαφνική παραμόρφωση με άμεση σύσπαση. Αυτή καλείται μυογενής αντίδραση και έχει ως σκοπό να προστατεύσει την αρτηρία από καταστροφή, καθιστώντας το τοίχωμα μέσω της συστολής των VSMCs περισσότερο δύσκαμπτο και μην επιτρέποντας την υπερέκτασή του (Badier-Commander C et Al., 2001). Επιπλέον, η συστολή των VSMCs διατηρεί σταθερή τη ροή του αίματος σε φυσιολογικά επίπεδα επαναφέροντας το αγγείο στην ομοιοστατική του διάμετρο, παρά την αυξημένη πίεση. Όταν τα VSMCs δεν είναι υπό διέγερση, βρίσκονται σε κατάσταση ελαφράς συστολής, η οποία καλείται βασικός VSMCs τόνος ή κατάσταση φυσιολογικού VSMCs τόνου. Παραμένοντας τα VSMCs σε κατάσταση ελαφριάς συστολής δίνουν στην αρτηρία τη δυνατότητα τόσο να χαλαρώσει όσο και να συσπασθεί χωρίς να καταναλώνει ένα υπερβολικό ποσό ενέργειας, το οποίο θα χρειαζόταν προκειμένου να διατηρηθεί σε ένα υψηλότερο επίπεδο συστολής. ΔΟΜΗ ΤΩΝ ΕΞΩΚΥΤΤΑΡΙΚΩΝ ΣΥΣΤΑΤΙΚΩΝ ΤΟΥ ΑΓΓΕΙΑΚΟΥ ΤΟΙΧΩΜΑΤΟΣ Τα εξωκυτταρικά στοιχεία των αιμοφόρων αγγείων αναφέρονται εν γένει ως συστατικά του συνδετικού ιστού και περιλαμβάνουν μεταξύ άλλων τις ίνες κολλαγόνου και τις ελαστικές ίνες και συνεισφέρουν σε σημαντικό βαθμό στη διατήρηση της αγγειακής ομοιοστασίας (Badier-Commander C et al., 2001; Waksman Y et al., 1997). Τα μακρομόρια του κολλαγόνου και της ελαστίνης ασκούν πολλαπλές δράσεις, όπως για παράδειγμα διαμορφώνουν το σκελετό πάνω στον οποίο εναποτίθενται τα ενδοθηλιακά κύτταρα και τα λεία μυϊκά κύτταρα, χρησιμεύουν στη μεταφορά σημάτων, δεσμεύουν και κατακρατούν λιποπρωτεΐνες και αποτελούν δεξαμενή αυξητικών παραγόντων (Sansilvestri-Morel P et al., 1998; Sansilvestri-Morel P et al., 2001). Επιπλέον 41
42 το κολλαγόνο και η ελαστίνη συμβάλλουν στη δύναμη και τη δομική ακεραιότητα του αγγειακού τοιχώματος (Sansilvestri-Morel P et al., 2001). Σε φυσιολογικούς ιστούς, η έκφραση και αναδιοργάνωση του εξωκυττάριου υλικού αποτελεί μία καλά ρυθμισμένη δυναμική ισορροπία. Αντίθετα σε παθολογικές καταστάσεις, όπως η ρευματοειδής αρθρίτιδα, η αθηρωμάτωση και η ινομυϊκή υπερπλασία η παραπάνω ισορροπία διαταράσσεται ευνοώντας την εξέλιξη και κλινική εκδήλωση των παραπάνω διαταραχών (Kirsch D et al., 1999). ΕΛΑΣΤΙΚΕΣ ΙΝΕΣ Οι ελαστικές ίνες αποτελούν το κύριο συστατικό του εξωκυττάριου υλικού των μεγάλων αγγείων και είναι απαραίτητες για την αντιμετώπιση των μηχανικών φορτίων της αρτηριακής πίεση. Το σύστημα ελαστικών ινών αποτελείται από δύο βιοχημικά και υπερδομικά συστατικά, την ελαστίνη, το συστατικό που είναι υπεύθυνο για την ελαστικότητα των ελαστικών ινών, και τα συστατικά των μικροïνιδίων. Η ελαστίνη αποτελεί τον πυρήνα της ελαστικής ίνας και είναι δομικά άμορφη (Notbohm H et al., 1993). Οι ελαστικές της ιδιότητες οφείλονται στη διασταυρούμενη αναδίπλωση των μονομερών της σε ελαστικά ινίδια, όπου τα μικροïνίδια αυτά επιτρέπουν τη διάταση και αναδίπλωση της ελαστίνης και είναι αυτά που περιβάλλουν τους πυρήνες, με διάμετρο nm και συνήθως σωληνοειδή εμφάνιση. Τα μικροϊνίδια έχουν την τάση να μειώνονται σε αριθμό με την αύξηση της ηλικίας και την ωρίμανση των ελαστικών ινών. Με τη δομή αυτή, οι ελαστικές ίνες, που διαπλέκονται στη συνέχεια με ίνες κολλαγόνου, επιτρέπουν στο αγγειακό τοίχωμα να ανθίσταται, χωρίς να παραμορφώνεται από τα μηχανικά φορτία που του ασκούνται (Sansilvestri-Morel P et al., 2001). Η αποδόμηση των πρωτεϊνών του εξωκυττάριου υλικού, μεταξύ αυτών και της ελαστίνης, αποτελεί κεντρικό σημείο της εξέλιξης της ινομυϊκής υπερπλασίας. Προάγει τη μετανάστευση των VSMCs από το μέσο στον έσω χιτώνα, διαμέσου των ελαστικών στοιβάδων και προωθεί την προς τα έξω 42
43 (θετική) ανακατασκευή του αγγειακού τοιχώματος, την εμφάνιση της ινομυϊκής υπερπλασίας και την επακόλουθη εξέλιξή της. Όσο αφορά την ελαστίνη, η ποσότητά της στο αγγειακό τοίχωμα βρίσκεται σε μία δυναμική ισορροπία, καθώς υπάρχει συνεχής αναδιοργάνωση των ελαστικών ινιδίων. Για να διατηρηθεί η ομοιοστασία του αγγειακού τοιχώματος νέες ελαστικές ίνες παράγονται και εναποτίθενται συνεχώς (Waksman Y et al., 1997). Οι μηχανικές ιδιότητες των μικροϊνιδίων δεν είναι μέχρι σήμερα γνωστές (Sansilvestri-Morel P et al., 1998), ενώ οι μηχανικές ιδιότητες των ελαστικών ινών έχουν προσομοιωθεί με κατάλληλα μοντέλα, χωρίς η εν λόγω προσομοίωση να είναι ιδανική (Waksman Y et al., 1997; Sansilvestri-Morel P et al., 1998; Sansilvestri-Morel P et al., 2001). Το φορτίο θραύσης του ελαστικού ιστού είναι 0,1 MPa, ενώ το μέτρο ελαστικότητας και η παραμόρφωση αστοχίας είναι περίπου ίση με 0,1 MPa και 300% αντίστοιχα (Sansilvestri-Morel P et al., 1998). Σε σύγκριση με τις ίνες κολλαγόνου, οι ελαστικές ίνες είναι ασθενέστερες, μαλακότερες και περισσότερο διατάσιμες. Στα αγγεία, η ελαστίνη παρουσιάζεται σε περιοχές οι οποίες εκτίθενται σε χρονικά μεταβαλλόμενη τάση (Kirsch D et al., 2000). Η ποσότητα ελαστίνης στους διάφορους ιστούς εξαρτάται από το τοπικό πλάτος του παλμικού κύματος. Η αορτική ρίζα εκτείνεται ιδιαίτερα κατά τη διάρκεια της συστολής, ενώ «ξεφουσκώνει» κατά τη διάρκεια της διαστολής και έχει τη μεγαλύτερη ποσότητα ελαστίνης. Τα αγγεία που διαστέλλονται σε μικρότερο βαθμό από το παλμικό κύμα, όπως η θωρακική και η κοιλιακή αορτή και τα μικρότερα περιφερειακά, έχουν προοδευτικά μικρότερη περιεκτικότητα ελαστίνης. Τα τριχοειδή και τα φλεβίδια, τα οποία δεν εκτίθενται σε υψηλούς ρυθμούς μεταβολής της τάσης, δεν περιέχουν ελαστίνη. Μετά τη γέννηση, η ελαστίνη αυξάνεται ιδιαίτερα στο τοίχωμα της αορτής με την αύξηση της συστολικής πίεσης, ενώ παράλληλα μειώνεται στην πνευμονική αρτηρία. Εν κατακλείδι, η ποσότητα και η τοπογραφική συγκέντρωση της ελαστίνης στους διάφορους ιστούς μεταβάλλεται ανάλογα με το ρυθμό μεταβολής της τάσης, η οποία ασκείται τοπικά στα μεσεγχυματικά κύτταρα. 43
44 ΚΟΛΛΑΓΟΝΟ Το μακρομόριο αυτό συνήθως συντίθεται από αγγειακά λεία μυϊκά κύτταρα της έσω στοιβάδας του αγγείου και εξασφαλίζει την ακεραιότητα του αγγείου έναντι των μηχανικών δυνάμεων που ασκούνται με την κυκλοφορία του αίματος. Η ποσοτική παρουσία του κολλαγόνου στον αγγειακό ιστό είναι το τελικό αποτέλεσμα μίας δυναμικής ισορροπίας μεταξύ της σύνθεσης και της αποδόμησής του και καθορίζει τη δομή του αγγειακού τοιχώματος. Τα ινίδια κολλαγόνου αποτελούν βασικό δομικό συστατικό των αιμοφόρων αγγείων. Κατά τη διάρκεια σχηματισμού ινιδίων, οι τρεις έλικες του κολλαγόνου ελίσσονται σε μία δεξιόστροφη υπερέλικα. Η ελικοειδής αυτή διαμόρφωση δίνει στο μόριο μία πολύ σταθερή και στέρεα μορφή. Οι Silver και συνεργάτες το 1989 παρατήρησαν ότι κατά την απομάκρυνση του ελαστικού ιστού από τα αιμοφόρα αγγεία διατηρείται άθικτο το δίκτυο κολλαγόνου, το δίκτυο που αποτελεί το πιο βασικό μηχανικό στοιχείο όλων των ιστών. Ακόμα, οι ίνες κολλαγόνου είναι ιξωδοελαστικές και εμφανίζονται στους συνδετικούς ιστούς σε ποικιλία διαμέτρων και γεωμετριών (Waksman Y et al., 1997). Σημειώνεται ότι η αυξημένη παρουσία κολλαγόνου σε ένα αγγείο που εμφανίζει ινομυϊκή υπερπλασία μπορεί να προέλθει από αυξημένη παραγωγή του από τα VSMCs λόγω αύξησή τους. Συνοψίζοντας, το κολλαγόνο είναι αρκετά δύσκαμπτο και σχηματίζει κυματοειδείς ίνες στο αρτηριακό τοίχωμα. Αυτές οι ίνες κολλαγόνου μπορούν είτε να είναι διατεταγμένες σε ομάδες σχηματίζοντας ένα ολόκληρο αρτηριακό χιτώνα, των έξω χιτώνα, είτε να διανέμονται σε δέσμες ανάμεσα στην ελαστίνη και τα VSMCs είτε να διατάσσονται σαν μεμονωμένες λεπτές ίνες γύρω από τα VSMCs. ΒΑΛΒΙΔΕΣ ΦΛΕΒΩΝ Οι βαλβίδες είναι λεπτές πτυχές του έσω χιτώνα που προβάλλουν προς τον αυλό, με τα ελεύθερα άκρα τους να κατευθύνονται προς την καρδιά. Έτσι, επιτρέπουν τη ροή του αίματος από την περιφέρεια προς την καρδιά εμποδίζοντας τη 44
45 παλινδρόμησή του. Βαλβίδες βρίσκονται στις μεσαίου μεγέθους και στις μεγάλες φλέβες και ο αριθμός τους εξαρτάται από το αν η φλέβα μεταφέρει αίμα αντίθετα στη βαρύτητα ή όχι. Οι κιρσοί, είναι η πάθηση των φλεβών του επιπολής φλεβικού δικτύου των κάτω άκρων. Η πάθηση των κιρσών πολύ συχνά αναφέρεται και ως επιπολής φλεβική ανεπάρκεια. Οι βαλβίδες των φλεβών καταστρέφονται, με αποτέλεσμα οι φλέβες να διατείνονται, επιμηκύνονται ενώ η πορεία τους κάτω από το δέρμα γίνεται ανώμαλη και οφιοειδής. Το αίμα που μέσω των αρτηριών φτάνει στα κάτω άκρα δυσκολεύεται να επιστρέψει στην καρδιά μέσω των φλεβών του επιπολής φλεβικού δικτύου με αποτέλεσμα να λιμνάζει στις φλέβες των κάτω άκρων. Η φλεβική ανεπάρκεια θεωρείται η πιο συχνή πάθηση των κάτω άκρων. Αφορά το 35-40% του γενικού πληθυσμού άνω των 40 ετών ενώ το 15% των ενηλίκων εμφανίζουν την πάθηση πριν την ηλικία των σαράντα. Οι γυναίκες είναι πιο ευάλωτες στην πάθηση και εμφανίζουν τη νόσο 5 φορές συχνότερα από ότι οι άντρες. Οι σπερματικές φλέβες διαθέτουν βαλβίδες. Η συχνότερη απουσία φλεβικών βαλβίδων στην σπερματική φλέβα και κυρίως στην αριστερή, αποτελεί μία από την αιτία της εμφάνισης της κιρσοκήλης. Ο παραπάνω παράγοντας έχει ως αποτέλεσμα τη μεγαλύτερη αντίσταση στη φλεβική αποχέτευση με αποτέλεσμα την ανάπτυξη υψηλότερων υδροστατικών πιέσεων στην αριστερή σπερματική φλέβα (ειδικά σε όρθια θέση) σε σύγκριση με τη δεξιά (Kirsch D et al., 2000). ΚΙΡΣΟΚΗΛΗ ΕΙΣΑΓΩΓΗ Ως κιρσοκήλη ορίζεται η κιρσοειδής διεύρυνση των σπερματικών φλεβών του ελικοειδούς πλέγματος του όρχεως. Η ιδιοπαθής κιρσοκήλη είναι συνήθως ασυμπτωματική και γίνεται αντιληπτή από την ασυμμετρία στο μέγεθος του όσχεου, ενώ σπάνια υπάρχει αίσθημα πόνου ή βάρους στην περιοχή. Στις περισσότερες περιπτώσεις οι ενήλικες πάσχοντες από κιρσοκήλη 45
46 αγνοούν την ύπαρξή της και το ανακαλύπτουν κατά την καθιερωμένη εξέταση με την κατάταξή τους στο στρατό ή έπειτα από μια επίσκεψη στον ουρολόγο στα πλαίσια διερεύνησης υπογονιμότητας (Skoog SJ et al., 1997; Buch JP et al., 1985; Vasavada S et al., 1993). Είναι γνωστό από την αρχαιότητα ότι η κιρσοκήλη επιδρά αρνητικά στη σπερματογένεση (Amelius Cornelius Celsus 42π.Χ.-37μ.Χ.). Από το 1950 ο Hamley ανακοίνωσε ότι το σπερμοδιάγραμμα βελτιώνεται μετά από μικρό χρονικό διάστημα κατόπιν της απολίνωσης της έσω σπερματικής φλέβας σε υπογόνιμους άνδρες (Sharfik A et al., 1983; Kass E et al., 1987). Η πάθηση πιθανώς οφείλεται σε ανεπάρκεια των βαλβίδων, που υπάρχουν μέσα στις φλέβες και κανονικά επιτρέπουν τη ροή του αίματος μόνο από την περιφέρεια προς το κέντρο. Όταν οι βαλβίδες εμφανίσουν ανεπάρκεια το αίμα μπορεί να παλινδρομεί από τις μεγαλύτερες προς τις μικρότερες φλέβες, πράγμα που έχει ως συνέπεια την κιρσοειδή διεύρυνση των σπερματικών φλεβών. Η κιρσοκήλη αποτελεί τη συχνότερη διορθώσιμη αιτία ανδρικής υπογονιμότητας. Η επίπτωσή της στο γενικό πληθυσμό κυμαίνεται στο 10-15%, ενώ στους υπογόνιμους άνδρες στο 30%. Η κιρσοκήλη εμφανίζεται πιο συχνά στην αριστερή πλευρά και αποτελεί μια καλά τεκμηριωμένη αιτία ανδρικής υπογονιμότητας. Υπάρχει μια σαφής σχέση μεταξύ κιρσοκήλης, υπογονιμότητας και φυσιολογικής ανάπτυξης την όρχεων (Goldstein M et al., 1997; WHO, 1992; Belloli G et al., 1993) και έχει δειχθεί ότι επεμβαίνοντας χειρουργικά μπορεί να διορθωθεί η επίδραση της κιρσοκήλης σε όρχεις εφήβων (Paduch DA et al., 1997; Kass EJ et al., 1995; Atassi O et al., 1995; Lenzi A et al., 1998). ΕΠΙΔΗΜΙΟΛΟΓΙΑ Περίπου το 30% - 50% των ανδρών που πάσχει από πρωτοπαθή υπογονιμότητα εμφανίζει κιρσοκήλη (Pryor JL et al., 1987; Nashan D et al., 1990; Jarow JP et al., 1996). Η κιρσοκήλη είναι περισσότερο συνηθισμένη στην αριστερή πλευρά. Επίσης είναι δυνατόν να εμφανιστεί νωρίς στην ήβη, καθώς και περιστασιακά στα αγόρια που βρίσκονται σε προεφηβική ηλικία 46
47 (Buch JP et al., 1985). Σύμφωνα με την ουρολογική μελέτη του Skoog et al. σε μη γόνιμους άνδρες, αναφέρεται ότι η ετερόπλευρη κιρσοκήλη εμφανίζεται στην αριστερή πλευρά σε ποσοστά της τάξης του 85-90%, ενώ στη δεξιά πλευρά ανευρίσκεται κυρίως σε αμφοτερόπλευρη κιρσοκήλη στο 10% των περιστατικών και σπανιότερα μόνη της (Skoog SJ et al., 1997). Σε πρόσφατη μελέτη του Gat et al. αναφέρεται ότι η ετερόπλευρη κιρσοκήλη στην αριστερή πλευρά εμφανίζεται σε ποσοστά της τάξης του 17,6%, η ετερόπλευρη δεξιά πλευρά ανευρίσκεται σε 1,5% των περιστατικών και η αμφοτερόπλευρη κιρσοκήλη στο 80,8% των περιστατικών (Gat Y et al., 2004). Στα παιδιά η συχνότητα εμφάνισής της θεωρούνταν μικρή, αλλά σε πρόσφατες μελέτες διαπιστώθηκε η ύπαρξή της στο 6% των παιδιών ηλικίας 10 ετών, ενώ σε εφήβους το ποσοστό αυτό ανήλθε στο 16%. Πολύ σπάνια εμφανίζεται πριν από την ηλικία των 7-8 ετών. Συνήθως ανακαλύπτεται τυχαία, είτε από το παιδί ή από τους γονείς του (ως μια μάζα που αλλάζει το σχήμα και το μέγεθος του οσχέου), είτε από τον παιδίατρο κατά την διάρκεια μιας εξέτασης ρουτίνας. Στην ψηλάφηση δίνει την εντύπωση μιας μαλακής μάζας, χωρίς σαφή όρια, αποτελούμενης από μικρότερα στοιχεία, που το μέγεθός της υποχωρεί όταν το άτομο ξαπλώνει και αυξάνει ξαφνικά όταν σηκωθεί όρθιο. Επειδή συνήθως δεν προκαλεί πόνο ή κάποια έντονη ενόχληση, πολλές φορές οι ασθενείς ή οι γονείς τους δεν δίνουν την απαιτούμενη σημασία, αδιαφορούν και δεν απευθύνονται στον γιατρό, με δυσμενείς, ενίοτε, συνέπειες στην ανάπτυξη του όρχεως και στην γονιμότητα του ατόμου (Sawczuk IS et al., 1993). ΑΙΤΙΟΛΟΓΙΑ ΔΗΜΙΟΥΡΓΙΑΣ ΚΙΡΣΟΕΙΔΩΝ ΦΛΕΒΩΝ Ο όρος κιρσοειδής (varicose) προέρχεται από το Λατινικό όρο varix που σημαίνει «στριμμένος». Ο ορισμός των κιρσοειδών φλεβών είναι ευρύς, αλλά ακολουθώντας τα κριτήρια του Arnoldi (Arnoldi CC et al., 1957), αραχνοειδείς φλέβες, τηλαγγειεκτασίες και φλέβες με μη λειτουργικές βαλβίδες, ορθώς θεωρούνται ως κιρσοειδείς φλέβες. Τα αίτια της εμφάνισης των κιρσοειδών φλεβών είναι αμφισβητήσιμα και περιλαμβάνουν τόσο την ανικανότητα των 47
48 βαλβίδων να επιτελέσουν το ρόλο τους, όσο και τις μορφολογικές και λειτουργικές αλλαγές του ενδοθηλίου, των λείων μυϊκών κυττάρων ή ακόμα και του εξωκυττάριου στρώματος του τοιχώματος των φλεβών. Η παραμόρφωση των παραπάνω τμημάτων του τοιχώματος των φλεβών μπορεί να είναι αποτέλεσμα της παρατεταμένης στάσης του αίματος και της αύξησης της έντασης της πίεσης στο αγγειακό σύστημα. Αξίζει να σημειωθεί πως παρόμοιες αλλαγές και παραμορφώσεις παρατηρούνται και σε αρτηρίες, όπως στις υπερτασικές αρτηρίες στις οποίες εμφανίζεται επαναδόμηση του αγγειακού τοιχώματος ως αντισταθμιστικό αποτέλεσμα της αυξημένης πίεσης (Liu SQ et al., 1998; Zhang WD et al., 1999). Παλαιότερες μελέτες εμφάνιζαν αντικρουόμενα αποτελέσματα στην προσπάθεια τους να χαρακτηρίσουν τις κιρσοειδείς φλέβες και ανέφεραν ποικιλία ευρημάτων όπως, μείωση, (Svejcar J et al., 1963; Jurukova Z et al., 1982; Psaila JV et al., 1989) αύξηση, (Rose SS et al., 1986; Maurel E et al., 1990; Gandhi RH et al., 1993; Porto LC et al., 1995; Travers JP et al., 1996) ή αμετάβλητη αναλογία του κολλαγόνου (Venturi M et al., 1996), μείωση ή σταθερό ποσοστό ελαστίνης και αύξηση του ποσοστού των λείων μυϊκών κυττάρων (Svejcar J et al., 1963). Η ακριβής αιτία της δημιουργίας των κιρσοειδών φλεβών δεν έχει αποσαφηνιστεί πλήρως. Οι ποικίλοι επιβαρυντικοί παράγοντες και ο Δυτικός τρόπος ζωής που περιλαμβάνουν χαρακτηριστικά όπως οι ορμονικές διαταραχές, η παχυσαρκία, οι φλεγμονές, η ορθοστασία, η φτωχή σε θρεπτική αξία διατροφή και τα στενά είδη ρουχισμού, είναι κάποια από τα στοιχεία που έχουν περιγραφεί και πιθανώς εμπλέκονται στη δημιουργία κιρσοειδών φλεβών (Burkitt DP et al., 1976; Lee AJ et al., 2003). Επιπλέον έχει αναφερθεί ότι η ηλικία είναι ένας παράγοντας που ευνοεί την εμφάνιση κιρσών αφού παρατηρούνται διαφορές στην ιστολογική δομή του κυτταρικού τοιχώματος, κυρίως σε ηλικίες άνω των πενήντα ετών (Bujan J et al., 2003). Παλαιότερα ως κύρια αιτία στη δημιουργία κιρσών, θεωρείτο η ανικανότητα των βαλβίδων των φλεβών να αποτρέψουν την παλινδρόμηση του αίματος. Μετέπειτα μελέτες εντούτοις επιβεβαίωσαν την αδυναμία του 48
49 τοιχώματος των φλεβών ως τον πρωταρχικό παράγοντα στις ασθένειες που σχετίζονται με τους κιρσούς. ΑΙΤΙΟΛΟΓΙΑ ΚΙΡΣΟΚΗΛΗΣ Στην προσπάθεια να ερμηνευθεί η αιτιολογία της κιρσοκήλης έχουν αναπτυχθεί διάφορες θεωρίες. Καμία θεωρία όμως από μόνη της δεν επαρκεί για να ερμηνευθεί η αιτιολογία της κιρσοκήλης, λόγω της ετερογένειας των περιστατικών. Η υπερίσχυση της εμφάνισης της κιρσοκήλης στην αριστερή πλευρά και η ανατομία των σπερματικών φλεβών αποτελούν τη βάση των θεωριών που αναπτύχθηκαν σε σχέση με την αιτιολογία της κιρσοκήλης. Η αριστερή σπερματική φλέβα είναι μεγαλύτερη κατά 8-10cm από την δεξιά λόγω της συνήθως χαμηλότερης θέσης του αριστερού όρχεως στο όσχεο και της υψηλότερης κατάληξης της στην αριστερή νεφρική φλέβα. Η αριστερή σπερματική φλέβα, στη μεγάλη διαδρομή της, εκβάλλει κάθετα στην αριστερή νεφρική φλέβα. Η διαδρομή της δεξιάς σπερματικής φλέβας είναι πλάγια. Η τελευταία εκβάλλει υπό οξεία γωνία στην κάτω κοίλη φλέβα (Wishahi MM et al., 1992). Η κατά κύριο λόγο αριστερή εμφάνιση της κιρσοκήλης πιθανώς να οφείλεται στην ανατομική διαμόρφωση με την πιο κάθετη είσοδο της αριστερής έσω σπερματικής φλέβας στην νεφρική φλέβα, σε αντίθεση με την πιο πλάγια είσοδο στη δεξιά πλευρά, καθώς η ροή του αίματος υπό ορθή γωνία στην νεφρική φλέβα φαίνεται πως γίνεται δυσχερέστερα, λόγω και της σημαντικής αιματικής ροής στην νεφρική φλέβα. Η ύπαρξη μόνο δεξιάς κιρσοκήλης, παρότι σπάνια, εξηγείται από παραλλαγές στην ανατομική πορεία της αντίστοιχης σπερματικής φλέβας. Έτσι σε περιπτώσεις με αμιγή δεξιά κιρσοκήλη, βρέθηκε ότι η δεξιά σπερματική φλέβα εκβάλλει κατευθείαν στη νεφρική φλέβα στο 7,5% των περιπτώσεων, στο 22,5% εκβάλλει με δύο στελέχη στη δεξιά νεφρική και στην κάτω κοίλη 49
50 φλέβα παρουσιάζοντας διάταση και παλινδρόμηση αίματος (Wishahi MM et al., 1992). Η δεύτερη θεωρία βασίζεται στο γεγονός της διαφορετικής υδροστατικής πίεσης μεταξύ των δύο πλευρών στο επίπεδο των όρχεων που πιθανόν έχει ως αποτέλεσμα την εμφάνιση κιρσοκήλης στην αριστερή πλευρά. Η αριστερή σπερματική φλέβα είναι μεγαλύτερη στο μήκος κατά 8 10 cm της δεξιάς και πιστεύεται πως αυτό έχει ως αποτέλεσμα την αύξηση της υδροστατικής πίεσης, η οποία μεταφέρεται μέσω της φλέβας στο ελικώδες πλέγμα, προκαλώντας διεύρυνση και συστροφή των αγγείων (Safik A et al., 1980). Σε παρελθούσα μελέτη μετρήθηκε η αγγειακή τάση σε υπογόνιμους άνδρες σε κατάσταση ηρεμίας, οι οποίοι εμφάνισαν κατά μέσο όρο τάση 81,88mmHg (με εύρος 70-92mmHg). Κατά τη δοκιμασία Valsalva η μέση τιμή της αγγειακής τάσης ανήλθε στα 85,8mmHg, ενώ η μέση τιμή στην ομάδα ελέγχου ήταν 60,5mmHg (με εύρος 52-74mmHg) (Coolsaet BL, 1980). Η συγκεκριμένη μελέτη παρέθεσε την αύξηση της πίεσης στην αριστερή σπερματική φλέβα στους ασθενείς με κιρσοκήλη, σε σχέση με τα φυσιολογικά controls σε κατάσταση ηρεμίας και κατά τη δοκιμασία Valsalva. Σε μία άλλη μελέτη πραγματοποιήθηκε αντίστοιχη σύγκριση πιέσεων μεταξύ υπογόνιμων ανδρών με κιρσοκήλη, γόνιμων με κιρσοκήλη και γόνιμων ανδρών. Σε αυτήν μετρήθηκε η πίεση στις σπερματικές φλέβες μεταξύ των μελετηθέντων ομάδων και δεν παρατηρήθηκε σημαντική διαφορά στην πίεση των σπερματικών φλεβών των ανδρών σε ύπτια θέση και σε θέση Trendelenburg (Sayfan J et al., 1978). Η κιρσοκήλη αναπτύσσεται από την παλίνδρομη ροή του αίματος στις έσω σπερματικές και στις κρεμαστήριες φλέβες. Η αντιστροφή της αιματικής ροής λαμβάνει χώρα λόγω των απόντων ή των ατελών βαλβίδων. Οι σπερματικές φλέβες εξάλλου διαθέτουν βαλβίδες, όπως και όλες οι φυσιολογικές φλέβες, οι οποίες αποτρέπουν την παλινδρόμηση του αίματος. Ανατομικές μελέτες σε ασθενείς με κιρσοκήλη κατέδειξαν την απουσία βαλβίδων στο σημείο ένωσης της αριστερής νεφρικής φλέβας με την έσω σπερματική φλέβα (Kohler FP et al., 1967). Επιπλέον, σε μελέτες όπου 50
51 διενεργήθηκε φλεβογραφία σε άνδρες με κιρσοκήλη, τεκμηριώθηκε η απουσία ή η ανεπάρκεια των βαλβίδων κατά μήκος των έσω σπερματικών φλεβών (Ahlberg NE et al., 1966; Ahlberg NE, 1980; Comhaire F et al., 1981). Η παλίνδρομη αιματική ροή οδηγεί σε αύξηση της υδροστατικής πίεσης, σε παρατεταμένη στάση του αίματος και σε αύξηση της θερμοκρασίας εντός του όρχι. Η αύξηση της πίεσης στην αριστερή σπερματική φλέβα πιθανότατα να είναι και αποτέλεσμα της συμπίεσης της αριστερής νεφρικής φλέβας μεταξύ της αορτής και της άνω μεσεντερίου αρτηρίας. Αυτό έχει σαν αποτέλεσμα την ανάπτυξη υπέρτασης στην αριστερή νεφρική φλέβα και συνακόλουθα τη δημιουργία αριστερής κιρσοκήλης (Unlu M et al., 2007; Ahmed K et al., 2006; Coolsaet BL, 1980; Ting AC et al., 2002). Το παραπάνω φαινόμενο είναι γνωστό ως «nutcracker effect φαινόμενο του καρυοθραύστη» και αποτελεί την τέταρτη θεωρία δημιουργίας της πάθησης. Το φαινόμενο αυτό, το πρωτοπεριέγραψε ο Schepper το 1972 (De Schepper A, 1972). Πιστεύεται ότι αυτό το φαινόμενο είναι το μόνο που εξηγεί την εμφάνιση κιρσοκήλης συχνότερα από την αριστερή πλευρά (Bushi AJ et al., 1980). Ο Graif M και οι συνεργάτες του πραγματοποίησαν μία μελέτη (Graif M et al., 2000) όπου σκοπό είχαν να ποσοτικοποιήσουν τις ανατομικές και αιμοδυναμικές συνιστώσες της ορχικής φλεβικής παροχέτευσης ώστε να κατανοηθούν οι μηχανισμοί που διέπουν την παθοφυσιολογία της κιρσοκήλης, όπως το «φαινόμενο καρυοθραύστη», η παλινδρόμηση και η κιρσοκήλη. Μελετήθηκαν εβδομήντα πέντε άνδρες σε κατάσταση ηρεμίας και κατά τη διάρκεια της δοκιμασίας Valsalva. Η αορτομεσεντέρια απόσταση και η γωνία, η ταχύτητα ροής σε διαφορετικά τμήματα των νεφρικών φλεβών, η διάμετρος των ορχικών φλεβών και η παλίνδρομη αιματική ροή αξιολογήθηκαν χρησιμοποιώντας έγχρωμο υπέρηχο Doppler. Η ταχύτητα της ροής στην εγγύς αριστερή νεφρική φλέβα (17,5 cm / s) βρέθηκε να είναι σημαντικά χαμηλότερη από εκείνη τόσο στην άπω αριστερή νεφρική φλέβα (121 cm / s) και όσο και στη δεξιά νεφρική φλέβα (37 cm / s). Η ταχύτητα ροής στην εγγύς αριστερή νεφρική φλέβα ελαττώνεται όσο περισσότερο μειώνεται η 51
52 αορτομεσεντέρια απόσταση και η γωνία. Όταν η διάμετρος των ορχικών φλεβών βρέθηκε μεγαλύτερη από 3 mm, συσχετίστηκε στατιστικά με μειωμένη γωνία της άνω μεσεντερίου αρτηρίας. Μια επίσης σημαντική συσχέτιση βρέθηκε μεταξύ της διαμέτρου της αριστερής ορχικής φλέβας (έλεγχος με δοκιμασία Valsalva) και της παλινδρόμησης της ροής του αίματος. Η μείωση της ταχύτητα ροής στην εγγύς αριστερή νεφρική φλέβα προς τη διακλάδωση της άνω μεσεντερίου αρτηρίας από την αορτή υποστηρίζει το «φαινόμενο καρυοθραύστη» (Graif M et al., 2000). Η κιρσοκήλη φαίνεται επίσης να σχετίζεται με το ύψος και το βάρος του ατόμου (Delaney DP et al., 2004; May M et al., 2006). Η βιβλιογραφία είναι ασαφής, όσον αφορά τον σωματότυπο των παιδιών και των εφήβων που πάσχουν από κιρσοκήλη. Έχουν πραγματοποιηθεί μελέτες στο παρελθόν όπου σκοπός τους ήταν να ερευνήσουν την πιθανή επίδραση του βάρους, του ύψους και του δείκτη μάζας σώματος (BMI, Body Mass Index) στη δημιουργία της κιρσοκήλης κατά τη διάρκεια της παιδικής ηλικίας και της εφηβείας. Προκειμένου να συγκριθούν τα ευρήματα των μελετών χρησιμοποιήθηκαν ομάδες φυσιολογικών ατόμων ταυτόσημων ηλικιών με τους ασθενείς. Τα αποτελέσματα των μελετών υποδεικνύουν συσχέτιση μεταξύ της σωματικής διάπλασης και της δημιουργίας της κιρσοκήλης στα παιδία και στους εφήβους. Οι συγγραφείς υποστήριξαν ότι οι ασθενείς με κιρσοκήλη ήταν ψηλότεροι και βαρύτεροι από τα φυσιολογικά άτομα που χρησιμοποιήθηκαν σαν μάρτυρες. Μεταξύ των δύο μελετών, η μόνη τους διαφορά στα ευρήματα, ήταν ως προς τον δείκτη μάζας σώματος. Ο Delaney DP και οι συνεργάτες του δεν παρατήρησαν διαφορά στον ΒΜΙ μεταξύ των ασθενών και των φυσιολογικών μαρτύρων (Delaney DP et al., 2004), ενώ ο May και οι συνεργάτες του εντόπισαν σημαντική μείωση του ΒΜΙ στους ασθενείς με κιρσοκήλη (May M et al., 2006). Το αποτέλεσμα αυτό ίσως υποδηλώνει ότι τα ψηλότερα άτομα είναι δυνατόν να θεωρηθούν περισσότερο «ύποπτα» για να εμφανίσουν κιρσοκήλη λόγω της αυξημένης υδροστατικής πίεσης εξαιτίας του μεγαλύτερου μήκους που απαιτείται για να παροχετευτεί αίμα στην αριστερή 52
53 σπερματική φλέβα. Πιθανώς το ύψος να σχετίζεται και με τη μικρότερη αγκύλη που δημιουργείται μεταξύ της άνω μεσεντερίου αρτηρίας και της αορτής και κατ αυτόν τον τρόπο να αυξάνεται η πιθανότητα εμφάνισης «nutcracker effect» στην αριστερή νεφρική φλέβα. Η αυξημένη συχνότητα κιρσοκήλης στα ψηλότερα άτομα, οι οποίοι έχουν συνήθως και μικρότερο ΒΜΙ, αποδόθηκε στο μεγαλύτερο μήκος της έσω σπερματικής φλέβας με αποτέλεσμα την υψηλότερη υδροστατική πίεση σύμφωνα με το νόμο του Pascal (Gat Y et al., 2004). Στα βαρύτερα άτομα με περισσότερο λιπώδη ιστό, η εξήγηση που προτάθηκε από τους ερευνητές ήταν η αυξημένη συμπίεση της αριστερής νεφρικής λόγω της τοπικής εναπόθεσης λίπους και την δυσκολία στην κλινική διάγνωση της κιρσοκήλης λόγω της ύπαρξης λίπους στο σπερματικό τόνο (Nielsen ME et al., 2006). Η κληρονομικότητα της κιρσοκήλης και η πιθανή μετάδοση της σε συγγενείς πρώτου βαθμού σπανίως έχει διερευνηθεί. Στη μελέτη του Gokce A και των συνεργατών του, εξετάστηκαν οι συγγενείς πρώτου βαθμού ασθενών με κιρσοκήλη ώστε να αποκαλυφθεί τυχόν οικογενειακή προδιάθεση για κιρσοκήλη. Η εξεταζόμενη ομάδα συγκρίθηκε με μία ομάδα-ελέγχου φυσιολογικών ατόμων που δεν εμφάνιζαν κανένα πρόβλημα υπογονιμότητας ούτε και κιρσοκήλη. Η ύπαρξη ψηλαφητής κιρσοκήλης σε συγγενείς πρώτου βαθμού έναντι των ασθενών με γνωστή κιρσοκήλη ήταν περίπου 3-φορές μεγαλύτερη (Ρ< 0,005) σε σχέση με την ομάδα ελέγχου. Μεταξύ του πρώτου βαθμού συγγενείς, το 36,2% ήταν αδέλφια και το 21,1% ήταν πατέρες που είχαν ψηλαφητή κιρσοκήλη. Εξήχθη το συμπέρασμα ότι μια σημαντική αύξηση στην συχνότητα εμφάνισης της κιρσοκήλης υφίσταται στους συγγενείς πρώτου βαθμού ανδρών με κιρσοκήλη (Gökçe A et al., 2010). Επίσης ο Mokhtari G και οι συνεργάτες του ασχολήθηκαν με την αξιολόγηση της κληρονομικής συμπεριφοράς της κιρσοκήλης σε σύγκριση την επικράτηση της νόσου σε συγγενείς πρώτου βαθμού ασθενών με γνωστή κιρσοκήλη και σε φυσιολογικά υγιή άτομα που υπήρξαν εθελοντές νεφρού. Από τους 88 συγγενείς πρώτου βαθμού των ασθενών με γνωστή κιρσοκήλη, το 45,4% είχαν ψηλαφητή κιρσοκήλη κατά την κλινική εξέταση. Αυτό ήταν σημαντικά 53
54 μεγαλύτερο από το 11% των ανδρών της ομάδας ελέγχου (Ρ <0,001). Από τους συγγενείς πρώτου βαθμού, το 55,1% ήταν αδέρφια και το 26,6% πατέρες που είχαν ψηλαφητή κιρσοκήλη. Η κλινική κιρσοκήλη είναι πιο διαδεδομένη μεταξύ των συγγενών πρώτου βαθμού, ιδιαιτέρως των αδερφών των ασθενών με γνωστή κιρσοκήλη και μπορεί να είναι ένας δείκτης της κληρονομικής συμπεριφοράς της νόσου και της αναγκαιότητας του ελέγχου για τους άνδρες της οικογένειας (Mokhtari G et al., 2008). Τέλος, ο Raman JD και οι συνεργάτες του διεξήγανε μία παρόμοια μελέτη για τον κληρονομικό χαρακτήρα που μπορεί να υπάρχει μεταξύ συγγενών πρώτου βαθμού με ασθενείς με κιρσοκήλη και στην οποία χρησιμοποιήθηκε ομάδα-ελέγχου ένα δείγμα ανδρών χωρίς προβλήματα υπογονιμότητας και κιρσοκήλη. Από τους 62 συγγενείς πρώτου βαθμού των ασθενών με γνωστή κιρσοκήλη, το 56,5% είχαν ψηλαφητή κιρσοκήλη κατά την κλινική εξέταση. Αυτό ήταν σημαντικά μεγαλύτερο από το 6,8% των ανδρών της ομάδας ελέγχου (Ρ <0,0001). Από τους συγγενείς πρώτου βαθμού το 41% ήταν πατέρες, το 74% ήταν αδέρφια και το 67% ήταν υιοί. Παρόμοια με τις δύο προηγούμενες μελέτες, και σε αυτήν την μελέτη, η μεγαλύτερη συχνότητα εμφάνισης κιρσοκήλης εντοπίζεται μεταξύ των αδερφών. Με δεδομένη την επιζήμια επίπτωση της κιρσοκήλης στη σπερματογένεση και στεροειδογένεση, οι ασθενείς θα πρέπει να ενημερώνονται σχετικά με αυτό το αυξημένο κίνδυνο σε άρρενα μέλη της οικογένειας (Raman JD et al., 2005). Αν και υπάρχουν στοιχεία που υποστηρίζουν μια πιθανή σχέση μεταξύ της πρωτοπαθούς κιρσοκήλης και της φλεβικής ανεπάρκειας της σαφηνομηριαίας συμβολής σε ενήλικες, δεν υπάρχουν ενδείξεις για μια τέτοια σχέση κατά τη διάρκεια της εφηβείας. Σε μελέτη των Karadeniz-Bilgili MY και συνεργατών αξιολογήθηκε η επάρκεια της σαφηνομηριαίας συμβολής σε μια επιλεγμένη ομάδα εφήβων που έπασχαν από πρωτοπαθή κιρσοκήλη και σύγκριναν τα αποτελέσματα τους με μία ομάδα υγιών εφήβων ίδιας ηλικίας (Karadeniz-Bilgili MY et al., 2003). Σε όλες τις περιπτώσεις πραγματοποιήθηκε φυσική εξέταση και χρήση έγχρωμου Doppler για τη διάγνωση ή τον αποκλεισμό της παρουσίας πρωτοπαθούς κιρσοκήλης και για να αξιολογηθεί η 54
55 ακράτεια της σαφηνομηριαίας σύναψης. Οι συγγραφείς αναδεικνύουν σημαντική συσχέτιση της κιρσοκήλης και της αυξημένης πίεσης στους όρχεις, με τη βαλβιδική ανεπάρκεια της σαφηνομηριαίας συμβολής. Παρόλο που ο αριθμός των περιστατικών ήταν σχετικά μικρός (25 ασθενείς και 23 μάρτυρες), οι ερευνητές εντόπισαν ανεπάρκεια της σαφηνομηριαίας συμβολής σε 11/25 νεαρούς με κιρσοκήλη (44%) σε σχέση με ποσοστό 8-17% στους μάρτυρες. Ως εκ τούτου προτείνουν τον υπερηχογραφικό έλεγχο της ΣΜ συμβολής σε ασθενείς που εμφανίζονται με κιρσοκήλη, καθώς μπορεί να συμβάλλει στην πρώιμη διάγνωση της φλεβικής ανεπάρκειας των κάτω άκρων μεταξύ αυτών των ασθενών. Η κιρσοκήλη μπορεί να είναι πρωτοπαθής ή δευτεροπαθής. Η δευτεροπαθής κιρσοκήλη συνήθως εμφανίζεται στη δεξιά πλευρά. Οι πιο κοινές αιτίες δημιουργίας των δευτεροπαθών κιρσοκηλών είναι οι ακόλουθες: 1. καρκίνος νεφρού: προκαλείται από απόφραξη της αριστερής νεφρικής φλέβας ή της κάτω κοίλης φλέβας από όγκο. 2. οπισθοπεριτοναϊκοί όγκοι. 3. οπισθοπεριτοναϊκή ίνωση. 4. κίρρωση ήπατος: προκαλείται από πυλαία υπέρταση (Schulte-Baukloh H et al., 2005). Μια άλλη πιθανή αιτία ανάπτυξης δευτεροπαθούς κιρσοκήλης αφορά καλοήθη (και όχι κακοήθη) μηχανισμό συμπίεσης της αριστερής σπερματικής φλέβας λόγω χρόνιας δυσκοιλιότητας. Παρόλο που η βιβλιογραφία είναι περιορισμένη, σε μελέτη των Turgut et al βρέθηκε πως η χρόνια δυσκοιλιότητα σχετίζεται με αυξημένη συχνότητα εμφάνισης αριστερής κιρσοκήλης, σε ποσοστό 52% έναντι 19% σε ομάδα μαρτύρων. Πιθανολογείται πως η διάταση του κατιόντος κόλου και του σιγμοειδούς οδηγεί σε πίεση της αριστερής σπερματικής φλέβας στο οπισθοπεριτοναικό χώρο. Μια άλλη πιθανή ερμηνεία περιλαμβάνει την επαναλαμβανόμενη αύξηση της ενδοκοιλιακής πίεσης λόγω δυσκολίας αφόδευσης σε άτομα με χρόνια δυσκοιλιότητα (Turgut A et al., 2007). 55
56 ΠΑΘΟΦΥΣΙΟΛΟΓΙΑ ΤΩΝ ΕΠΙΠΤΩΣΕΩΝ ΤΗΣ ΚΙΡΣΟΚΗΛΗΣ ΣΤΗΝ ΣΠΕΡΜΑΤΟΓΕΝΕΣΗ Παρά το μεγάλο αριθμό μελετών που έχει πραγματοποιηθεί σε ζώα και ανθρώπους, ο ακριβής μηχανισμός της υπογονιμότητας δεν έχει κατανοηθεί πλήρως. Εμπλέκονται διάφορες θεωρίες, όπως αυτές που είναι σχετικές με την αυξημένη θερμοκρασία στο όσχεο, την υποξία, τη μη ομαλή ροή αίματος, τις ενώσεις και τα μόρια που εντοπίζονται στους όρχεις (πχ. τεστοστερόνη) και με την απορύθμιση της ισορροπίας του άξονα υποθάλαμου-υπόφυσης-όρχεων. Επιπροσθέτως το νιτρικό οξείδιο (Atassi O et al., 1995) και οι ρυθμιστές της απόπτωσης (Sayfan J et al., 1980) φαίνεται να διαδραματίζουν σημαντικό ρόλο στην παθοφυσιολογία της κιρσοκήλης. ΥΠΕΡΘΕΡΜΙΑ Η ύπαρξη κιρσοκήλης σχετίζεται με αύξηση της θερμοκρασίας στο όσχεο και στους όρχεις και επιφέρει αλλαγές στη σπερματογένεση. Πειραματικές μελέτες αποδεικνύουν πως η σπερματογένεση είναι θερμοευαίσθητη διαδικασία και ευοδώνεται ιδανικά στους 35 ο C. Πολλά από τα ένζυμα που ρυθμίζουν τη σύνθεση του DNA είναι θερμοερξαρτώμενα και αυτά είναι η τοποϊσομεράση Ι και οι πολυμεράσες άλφα, βήτα και γάμα. Η τοποϊσομεράση Ι ρυθμίζει το μεταβολισμό του DNA. Η DNA πολυμεράση-α δρα κατά την πυρηνική αντιγραφή του DNA και η πολυμεράση-γ ενεργοποιείται κατά τη μιτοχονδριακή αντιγραφή του DNA. Η πολυμεράση-β ρυθμίζει μαζί με τα άλλα δύο ένζυμα την αποκατάσταση της σύνθεσης του DNA (Fujisawa M et al, 1988 [i, ii]). Η θέση του όρχι εκτός του σώματος, μέσα στο όσχεο και το σύστημα «ψύξης» που παρέχεται από το ελικώδες πλέγμα, επιτρέπουν την εναλλαγή της θέρμανσης και ευθύνονται για την ύπαρξη ευνοϊκών συνθηκών για τη σπερματογένεση. Η έσω σπερματική αρτηρία (περιβαλλόμενη από το ελικοειδές πλέγμα) διατηρεί τους όρχεις σε αυτή τη θερμοκρασία, 2.2 ο C μικρότερη από το υπόλοιπο σώμα. Η απόσταση των όρχεων από τον κορμό καθορίζεται από τους κρεμαστήρες μύες, οι οποίοι 56
57 είναι τμήμα των σπερματικών πόρων. Όταν οι μύες αυτοί συσπώνται, το μήκος του πόρου μικραίνει και οι όρχεις πλησιάζουν στο σώμα. Αυτό μπορεί να συμβεί για να αυξηθεί η θερμοκρασία τους. Αντίθετη διαδικασία ακολουθείται για να μειωθεί η θερμοκρασία τους (Zorgniotti AW, 1980). Η ύπαρξη κιρσοκήλης προκαλεί, κατά μέσο όρο, αύξηση της θερμοκρασίας στους όρχεις κατά 2.6 ο C. Η στασιμότητα του αίματος είναι πιθανό να ευθύνεται για την επιβλαβή δράση της πάθησης στη σπερματογένεση (Hienz HA et al., 1980). Η αυξημένη θερμοκρασία στην περιοχή σχετίζεται με μειωμένο αριθμό σπερματοζωαρίων και με αυξημένη απόπτωση των εμβρυικών επιθηλιακών κυττάρων (Shikone T et al., 1994). ΕΠΙΝΕΦΡΙΔΙΚΗ ΠΑΛΙΝΔΡΟΜΗΣΗ ΑΙΜΑΤΟΣ Η παλινδρόμηση του αίματος από τις νεφρικές στις σπερματικές φλέβες παρατηρείται κατά την κιρσοκήλη και λαμβάνει χώρα από την αριστερή νεφρική φλέβα προς τη σύστοιχη έσω σπερματική, με αποτέλεσμα τοξικοί μεταβολίτες της νεφρικής και επινεφριδιακής λειτουργίας (κυρίως κατεχολαμίνες και προσταγλανδίνες) να μεταφέρονται στον αριστερό αλλά και στο δεξιό όρχι (λόγω της φλεβικής επικοινωνίας ανάμεσα στα δύο ημιόσχεα) (Mali WP et al., 1984; Mali WP et al., 1986). Ωστόσο τα επίπεδα των επινεφριδικών και νεφρικών μεταβολιτών στους όρχεις δεν έχουν τεκμηριωθεί πλήρως (Kay R et al., 1979; Turner TT et al., 1989). Σε μελέτες με πειραματικά μοντέλα και συγκεκριμένα επίμυες, που τους αφαιρέθηκαν οι νεφροί και έπασχαν από κιρσοκήλη, δεν ελαττώθηκαν οι επιδράσεις αυτής (Sofikitis N et al., 1993; York JP et al., 1990). ΥΠΟΞΙΑ-ΟΞΕΙΔΩΤΙΚΟ STRESS Το οξειδωτικό στρες, σε οποιονδήποτε ιστό, αναφέρεται στην ανισσοροπία μεταξύ παραγωγής ROS (Reactive Oxygen Species) και επαρκούς εξουδετέρωσής τους από τους διαθέσιμους αντιοξειδωτικούς μηχανισμούς. Τα ROS είναι μικρά μόρια που έχουν βάση το οξυγόνο και είναι ιδιαιτέρως ενεργά λόγω των μη συζευγμένων ηλεκτρονίων που διαθέτουν. Τα κυριότερα είναι το 57
58 υπεροξειδικό ανιόν ( O 2 -), το υπεροξείδιο του υδρογόνου (H 2 O 2 ) και το υδροξυλικό ιόν ( OH). Στον άνθρωπο το οξειδωτικό στρες φαίνεται να διαδραματίζει σημαντικό ρόλο σε μια πλειάδα καταστάσεων παθολογικών και όχι μόνο. Πρώτα από όλα συμβάλλει στην ιστική βλάβη που επέρχεται μετά από ακτινοβολία και υπεροξία. Πιθανολογείται, χωρίς να έχει αποδειχθεί, ότι είναι σημαντικό σε νευροεκφυλιστικές ασθένειες όπως η νόσος Parkinson και Alzheimer,η χορεία Huntington και η νόσος Lou Gehrig.Το οξειδωτικό στρες φαίνεται ακόμα να συνδέεται με συγκεκριμένες καρδιαγγειακές νόσους, όπως αθηροσκλήρυνση και καρδιακή ανεπάρκεια μια που η οξείδωση της LDL στο αγγειακό ενδοθήλιο είναι πρόδρομος της δημιουργίας αθηρωματικής πλάκας. Επίσης παίζει ρόλο στο καταρράκτη αντιδράσεων μετά από υποξία που λαμβάνει χώρα τόσο στα αγγειακά εγκεφαλικά όσο και στα στεφανιαία επεισόδια. Έχει ακόμα ενοχοποιηθεί σε νεοπλασίες, παθήσεις του συνδετικού ιστού, στο χρόνιο καταθλιπτικό σύνδρομο καθώς επίσης και στο σύνδρομο Επίκτητης Ανοσολογικής Ανεπάρκειας (AIDS) (Boulanger C et al., 1990; Yokokawa K et al., 1993) [Εικόνα 12]. Εικόνα 12: Ο ρόλος της υποξίας. Η υποξία πυροδοτεί αλληλεπιδράσεις του ενδοθηλίου με φλεγμονώδη κύτταρα προκαλώντας βλάβες του τοιχώματος των αγγείων, μείωση της διαπερατότητας και αύξηση της ευαισθησίας του σε αγγειοσυσπαστικούς παράγοντες. Επί 58
59 πλέον, η ενεργοποίηση παραγόντων πήξης προκαλεί μικροαποφράξεις με συνέπεια τη μείωση της πυκνότητας της ΜΚ. Φλεγμονώδεις και ανοσολογικοί μεσολαβητές συνεχίζουν να ενεργοποιούνται, συμβάλλοντας σε βλάβες στους αγγειοδιασταλτικούς μηχανισμούς του ενδοθηλίου (NO), στην παραγωγή δραστικών μορφών οξυγόνου (ROS) και στην περαιτέρω επιδείνωση της ενδοθηλιακής δυσλειτουργίας. Το αποτέλεσμα όλων αυτών των αλληλεπιδράσεων είναι η επιδείνωση της υποξίας, της ενδοθηλιακής και της ιστικής βλάβης. Το οξειδωτικό στρες μπορεί όμως να αποβεί και ευεργετικό μιας που συμβάλλει, για παράδειγμα, στην άμυνα του οργανισμού. Το ανοσοποιητικό σύστημα χρησιμοποιεί την παραγωγή οξειδωτικών παραγόντων ως το κεντρικό σημείο του μηχανισμού καταστροφής παθογόνων, με τα ενεργοποιημένα φαγοκύτταρα να παράγουν τόσο ROS όσο και ενεργούς αζωτούχους παράγοντες. Αυτά περιλαμβάνουν υπεροξείδιο ( O 2 -), νιτρικό οξείδιο ( NO) και το ιδιαιτέρως ενεργό τους παράγωγο, το περοξυνιτρικό (ONOO-) (Goligoski MS et al., 1994). Στην περίπτωση βλάβης του σπερματικού επιθηλίου, τα ROS επιτίθενται στα πολυακόρεστα λιπαρά οξέα στη μεμβράνη του σπερματοζωαρίου επάγοντας ένα καταρράκτη χημικών αντιδράσεων, που καλείται λιπιδική υπεροξείδωση. Τα ROS έχουν έφεση προς τις αλυσιδωτές αντιδράσεις. Σε αυτές ένα συστατικό που περιέχει ένα μη-συζευγμένο ηλεκτρόνιο θα αντιδράσει με ένα άλλο συστατικό, ώστε να παραχθεί ένα μησυζευγμένο ηλεκτρόνιο, με τέτοιο τρόπο δηλαδή που «η ρίζα γεννά ρίζα». Οι αντιδράσεις προχωρούν μέσω τριών βημάτων: Έναρξη, αναπαραγωγή και τερματισμός. Ένα από τα παραπροϊόντα της λιπιδικής υπεροξείδωσης είναι η Μαλονδυαλδεϋδη (MDA). Αυτή χρησιμοποιείται για να υπολογίζουμε το βαθμό του οξειδωτικού στρες, στο οποίο υποβάλλεται το σπερματοζωάριο (Kohan DE et al., 1994; Verhaar MC et al., 1998). Το βασικό ερώτημα που προκύπτει είναι κατά πόσο η κιρσοκήλη ευθύνεται για την πρόκληση οξειδωτικού στρες στον υπογόνιμο άνδρα. Χωρίς να είναι απόλυτα διευκρινισμένο, οι λόγοι που ακολούθως θα παραθέσουμε 59
60 συνηγορούν ότι πραγματικά μεταξύ κιρσοκήλης και οξειδωτικού στρες υφίσταται μια σχέση αιτίου-αιτιατού. α) Η κιρσοκήλη (κλινική ή υποκλινική) έχει φανεί ότι προκαλεί υπογονιμότητα περίπου στο 15% των υπογόνιμων ζευγαριών, με σημαντικό αριθμό ασθενών να έχουν αυξημένα επίπεδα ROS. Υπάρχει, δε, ισχυρή συσχέτιση μεταξύ των επιπέδων των ROS και του βαθμού της κιρσοκήλης. Πιο συγκεκριμένα, τα επίπεδα των ROS είναι σημαντικά μεγαλύτερα σε grade III και II (κατά Dubin- Amelar) από ότι σε grade I κιρσοκήλης, ενώ δεν υπάρχει συσχέτιση με τον όγκο του όρχι (Napoli C et al., 2006). β) Σε ασθενείς με κιρσοκήλη έχουν, ακόμα, ανευρεθεί αυξημένα επίπεδα Μονοξειδίου του Αζώτου (ΝΟ) στις διατεταμένες σπερματικές τους φλέβες. Το ΝΟ σχετίζεται ισχυρά με αυξημένο οξειδωτικό στρες. Όταν σε καταστάσεις όπως η κιρσοκήλη, παράγεται σε συγκεντρώσεις μεγαλύτερες του φυσιολογικού διαχέεται ελεύθερα ανάμεσα στις κυτταρικές μεμβράνες και αντιδρά με O 2. Σχηματίζονται έτσι ιδιαιτέρως οξειδωτικές ουσίες (π.χ. ΟΝΟΟ - και περοξυνιτρικό οξύ) που είναι επιβλαβείς για λειτουργίες του ορχικού κυττάρου και του σπερματοζωαρίου, όπως η κυτταρική αναπνοή και η μεταγωγή σήματος (Araujo M et al., 2006). γ) Ένα άλλο γεγονός που καθιστά εύλογο το χαρακτηρισμό της σχέσης μεταξύ κιρσοκήλης και οξειδωτικού στρες ως σχέση αιτίου-αιτιατού είναι τα δεδομένα που προκύπτουν μετά τη χειρουργική αποκατάστασή της. Η απολίνωση των σπερματικών φλεβών ομαλοποιεί τους διάφορους δείκτες οξειδωτικού στρες. Ελαττώνει την εμφάνιση 4977-bp απαλοιφών στο μιτοχονδριακό DNA, την ποσότητα της 8-υδροξυ-2 -δεοξυγουανοσίνης (8-0ΗdG) στο σπερματικό DNA καθώς και την αναλογία νιτρικού προς νιτρώδες. Επιπρόσθετα, η χειρουργική αποκατάσταση της κιρσοκήλης ομαλοποιεί τα επίπεδα των ενζυματικών αντιοξειδωτικών (υπεροξειδική δισμουτάση, καταλάση, περοξειδάση της γλουταθειόνης κ.α.) αλλά και των μη ενζυματικών (Ασκορβικό, Σελήνιο, Ψευδάργυρος κ.α.) αυξάνοντας παράλληλα τις πιθανότητες για βελτίωση της ποιότητας του σπέρματος από τη διενέργεια της επέμβασης. 60
61 Η μεγάλη πλειοψηφία των μελετών των δράσεων του οξειδωτικού στρες στον ορό, όρχι και σπέρμα των ανδρών με κιρσοκήλη καθιερώνει το οξειδωτικό στρες ως ένα από τους σημαντικότερους παθοφυσιολογικούς παράγοντες για τις αλλοιώσεις που παρατηρούνται στις παραμέτρους του σπέρματος αυτών των ασθενών, χωρίς να θεωρείται ότι είναι τυχαία η συνύπαρξή του με την κιρσοκήλη (Guan Z et al., 2006). ΑΥΞΗΣΗ ΤΗΣ ΕΝΔΟΟΡΧΙΚΗΣ ΠΙΕΣΗΣ Κατά τη Μηχανική των ρευστών η διατμητική τάση (shear stress) είναι η δύναμη που συνηθέστερα παραμορφώνει τα ρευστά, στη ροή τους, ανεξάρτητα το πόσο μικρή μπορεί να είναι. Ως διατμητική τάση χαρακτηρίζεται το πηλίκο της παράλληλης ή εφαπτομενικής δύναμης που εφαρμόζεται σε μια επιφάνεια ρευστού, προς το εμβαδόν της επιφάνειας αυτής. Συμβολίζεται δε με το ελληνικό μικρό γράμμα τ (ταυ) και έχει τύπο τ = F / A, όπου F η παράλληλη συνιστώσα της δύναμης εφαρμογής και Α η επιφάνεια εφαρμογής του ρευστού. Μονάδα μέτρησης της διατμητικής τάσης στο Διεθνές Σύστημα Μονάδων είναι το Pa (πασκάλ) που είναι ίσο με 1N (Νιούτον=μονάδα ασκούμενης δύναμης) ανά τετραγωνικό μέτρο (μέτρο επιφάνειας εφαρμογής στο IS). Η διατμητική τάση εφαρμόζεται εφαπτομενικά σε αντίθεση με την πίεση που εφαρμόζεται κάθετα στην επιφάνεια του ρευστού. Συνέπεια του παραπάνω ορισμού είναι ότι κάθε ρευστό (υγρό ή αέριο) που βρίσκεται σε ισορροπία δε δέχεται διατμητική τάση. Η επίδραση της τοιχωματικής διατμητικής τάσης (wall shear stress - WSS) στο ενδοθήλιο ενεργοποιεί ποικίλους μηχανισμούς. Οι περιοχές στις οποίες αρχικά εμφανίζονται βλάβες του εσωτερικού χιτώνα των αγγείων είναι αυτές στις οποίες διαφοροποιούνται τα χαρακτηριστικά της ροής (π.χ. έσω διχασμοί των αγγείων), δηλαδή περιοχές όπου μεταβάλλεται έντονα η WSS. Ως εκ τούτου, οι μηχανικές δυνάμεις που ασκούνται στα τοιχώματα των αιμοφόρων αγγείων σε συνδυασμό με τους βιοχημικούς μηχανισμούς 61
62 αποτελούν αντικείμενο ιδιαίτερου ερευνητικού ενδιαφέροντος (Haidekker MA et al., 2002; Malek AM et al., 1999). Επιπλέον, η έκκριση μονοξειδίου του αζώτου (ΝΟ) επηρεάζεται από την ασκούμενη WSS. Συγκεκριμένα, αν σε μία περιοχή η αντίσταση στη ροή είναι αυξημένη, λόγω υψηλής WSS, τότε εκκρίνεται ΝΟ από το ενδοθήλιο, προκειμένου να αυξηθεί η διάμετρος του αγγείου και ως εκ τούτου να μειωθεί η αντίσταση στη ροή και να διατηρηθεί η κυκλοφορία του αίματος. Αν αυτή η έκκριση μειωθεί (λ.χ. λόγω δυσλειτουργίας του ενδοθηλίου), δημιουργείται μεγαλύτερη αντίσταση στη ροή οπότε η αποκατάσταση της ροής επιτυγχάνεται με αύξηση της πίεσης. Το αποτέλεσμα της αύξησης των δυνάμεων που ασκούνται στους λείους μύες του μέσου και του έσω χιτώνα των αγγείων, διατείνοντάς τους και προκαλώντας μηχανικές βλάβες, είναι η υπερτροφία των χιτώνων. Αναφέρεται ότι υπάρχει ένα φυσιολογικό πλαίσιο μέσα στο οποίο η WSS εξασφαλίζει την ομοιόσταση του τοιχώματος και την προστασία του [Εικόνα 13]. Αν η WSS είναι χαμηλή (-0.4 έως 0.4 Pa) προκαλείται αθηροσκλήρωση, ενώ αν είναι ιδιαίτερα υψηλή (>7 Pa) προκαλείται μηχανική βλάβη στο ενδοθήλιο (Napoli C et al., 2006). Αύξηση τοιχωματικής διατμητικής τάσης -0,4 έως 0,4 Pa 1 έως 7 Pa 7 έως >10 Pa Σχηματισμός αθηρωματικής πλάκας Φυσιολογικό αγγείο Βλάβες του ενδοθηλιού Εικόνα 13: Επίδραση της τοιχωματικής διατμητικής τάσης Το αγγειακό τοίχωμα ακολουθεί ορισμένους παραμέτρους για την ορθή λειτουργία του. Αυτοί είναι το εύρος της πίεσης που του ασκείται, η αγγειακή τάση, η πίεση της ροής του αίματος και το πάχος του αγγειακού τοιχώματος. Οι παραπάνω παράμετροι ακολουθούν το νόμο του Laplace : T=P(R/W), 62
63 όπου (Τ) η αγγειακή τάση. Σε περίπτωση αύξησης της πίεσης της ροής του αίματος (Ρ), θα αυξηθεί το πάχος του αγγείου (W) και θα μειωθεί η ακτίνα του αγγείου (R). Βάσει του παραπάνω νόμου, η υψηλή πίεση προκαλεί την πάχυνση του αγγειακού τοιχώματος (Tao L et al., 2005). Η ισχύουσα υπόθεση υποδεικνύει ότι η αυξημένη πίεση του αίματος στους όρχεις δύναται να επηρεάσει τη σπερματογένεση (Harrison RM et al., 1983; Saypol DC et al., 1981). Η αύξηση της ενδοορχικής πίεσης από τη χρόνια φλεβική στάση έχει ως αποτέλεσμα τη διαταραχή της ορχικής μικροκυκλοφορίας. Η αύξηση στην υδροστατική πίεση μπορεί θεωρητικά να μεταβάλλει τη σύνθεση του υγρού που βρίσκεται υπό πίεση (Sweeney TE et al., 1995). Η μεταβολή αυτή μπορεί να διαφοροποιήσει την παρακρινική επικοινωνία μεταξύ των Leydig κυττάρων, των περισωληναριακών μυϊκών κυττάρων και των Sertoli κυττάρων που επηρεάζουν τη σπερματογένεση (Skoog SJ et al., 1997). Οι παθολογικές μεταβολές των μυϊκών κυττάρων και των τριχοειδών του ενδοθηλίου που σχετίζονται με την κιρσοκήλη μπορούν να επηρεάσουν τη διαμεμβρανική μεταφορά μορίων στο ενδοθήλιο (Santamaria L et al., 1992). ΕΝΔΟΚΡΙΝΙΚΗ ΑΝΙΣΟΡΡΟΠΙΑ Η σπερματογένεση και η ανάπτυξη των όρχεων ρυθμίζονται μέσου του άξονα υποθάλαμου-υπόφυσης-όρχεων. Υπάρχει ένα μεγάλο εύρος ενδοκρινικών ανωμαλιών που σχετίζονται με την κιρσοκήλη. Τα Leydig κύτταρα βρίσκονται υπό τον έλεγχο της ωχρινοτρόπου ορμόνης (LH) και ευθύνονται για την παραγωγή της τεστοστερόνης. Ορισμένες μελέτες υποστηρίζουν πως τα επίπεδα της τεστοστερόνης στον ορό του αίματος μεταβάλλονται στην κιρσοκήλη (Su LM et al., 1995; Hampl R et al., 1992; Rajfer J et al., 1987). Οι Ando et al. πραγματοποίησαν πέντε μελέτες όπου παρατήρησαν μειωμένα επίπεδα τεστοστερόνης στο πλάσμα 63
64 ασθενών με κιρσοκήλη και αυξημένα έπειτα από επέμβαση για την αποκατάστασή τους (Ando S et al., 1982; Szabo R et al., 1984; Palomo A et al., 1948; Tulloch WS, 1955; Sun N et al., 2001). Οι Swerdloff και Walsh ωστόσο σε αντίστοιχη μελέτη ισχυρίστηκαν πως δεν υπάρχει διαφορά των επιπέδων της τεστοστερόνης μεταξύ ατόμων με και χωρίς κιρσοκήλη (Swerdloff RS et al., 1975). Αρκετά συχνά ανευρίσκεται παθολογικό GnRH (gonadotropin releasing hormone) test τόσο σε υπογόνιμους άνδρες, όσο και σε εφήβους με κιρσοκήλη. Η παθολογική αυτή δοκιμασία συνίσταται στην υπέρμετρη έκκριση γοναδοτροπινών, τόσο της LH, που αποτελεί ένδειξη δυσλειτουργίας των κυττάρων Leydig, όσο και της FSH ως ένδειξη βλάβης των σπερματικών σωληναρίων και των κυττάρων Sertoli (Kass EJ et al., 1989; Bickel A et al., 1989; McFadden MR et al., 1986; Sirvent JJ et al., 1990). Η απόκριση των κυττάρων Sertoli στην ωοθυλακιοτρόπο ορμόνη FSH μπορεί να απουσιάζει. Η διέγερση των κυττάρων Sertoli με FSH αναιρεί τη σπερματογένεση σε πειραματικά μοντέλα (Sofikitis N et al., 1992). Παλαιότερες μελέτες υποστηρίζουν πως κάθε επίδραση στα κύτταρα Sertoli πρωταρχικώς θα μεταβάλλει τη δομή των σπερματικών σωληναρίων και έπειτα θα οδηγήσει σε διαταραχή της σπερματογένεσης (Cameron DF et al., 1980; Cameron DF et al., 1982). ΙΣΤΟΛΟΓΙΚΕΣ ΑΛΛΑΓΕΣ ΚΑΙ ΜΟΡΙΑΚΟΙ ΜΗΧΑΝΙΣΜΟΙ ΠΟΥ ΕΜΠΛΕΚΟΝΤΑΙ ΣΤΗ ΔΗΜΙΟΥΡΓΙΑ ΤΩΝ ΚΙΡΣΟΕΙΔΩΝ ΦΛΕΒΩΝ Σε βιοψίες όρχεων με κιρσοκήλη εντοπίζεται ένα εύρος ανωμαλιών. Οι πιο κοινές όλων είναι η υπερπλασία των κυττάρων Leydig, η μείωση του αριθμού των σπερματοζωαρίων, η παρεμπόδιση της σπερματογένεσης με την αναστολή της ωρίμανσης των σπερματοζωαρίων και η αποδιάταξη του ενδοθηλίου των σπερματικών σωληναρίων (Aragona F et al., 1994; Ponchietti R et al., 1986; Kass EJ et al., 1987; Hadziselimovic F et al, 1995; Castro- 64
65 Magana M et al., 1990). Η πάχυνση της βασικής μεμβράνης των σπερματικών σωληναρίων και οι πολλαπλές αλλοιώσεις του ενδοθηλίου είναι συχνά εμφανείς και πιθανότατα να επιδρούν στη μεταφορά οξυγόνου και γλυκόζης μέσω αυτών των δομών (Hadziselimovic F et al., 1989). ΕΝΔΟΘΗΛΙΟ Τα ενδοθηλιακά κύτταρα ελέγχουν πολυάριθμες λειτουργίες των λείων μυϊκών κυττάρων του μέσου χιτώνα, όπως είναι η συστολή, η μετανάστευση και ο πολλαπλασιασμός. Διαταραχές του μεταβολισμού του ενδοθηλίου μπορεί να οδηγήσει σε βλάβη και αλλαγή στην αναδόμηση του αγγειακού τοιχώματος, όπως έχει παρατηρηθεί στην αθηροσκλήρωση (Landmesser U et al., 2004). Το ερώτημα που γεννάται είναι εάν η αλλαγή του ενδοθηλίου διαδραματίζει ένα σημαντικό ρόλο στις κιρσοειδείς φλέβες πέρα από την αγγειοδιαστολή και την επαναδιάταξη των λείων μυϊκών κυττάρων που έχει παρατηρηθεί στο μέσο χιτώνα. Τα ενδοθηλιακά κύτταρα στις κιρσοειδείς φλέβες εμφανίζονται με πολυγωνικό σχήμα και παρουσιάζουν υψηλά επίπεδα των παραγόντων intercellular adhesion molecule-1 (ICAM-1) και von Willebrand factor (vwf), που εντοπίζονται κατά την ενεργοποίηση του ενδοθηλίου (Saharay M et al., 1998). Μέσω των ενδοθηλιακών κυττάρων με πολυγωνικό σχήμα επιτυγχάνεται μια μετανάστευση λεύκων αιμοσφαιρίων στο εσωτερικό του μέσου χιτώνα (Wali MA et al., 2002 [ii]). Στην έρευνα του Michielis και των συνεργατών του (Michiels C et al., 2002) παρατηρήθηκε ότι ουδετερόφιλα κύτταρα προσκολλούνται στο ενδοθήλιο των φλεβών όταν βρεθούν σε κατάσταση υποξίας. Συγκεκριμένα το ενδοθήλιο ενεργοποιείται όταν η μερική πίεση του οξυγόνου (PO 2 ) μειωθεί κάτω από ένα συγκεκριμένο επίπεδο όπως συμβαίνει στη στάση του αίματος. Επιπροσθέτως, η προσκόλληση των ουδετερόφιλων στο υποξικό ενδοθήλιο προάγει την απελευθέρωση ελεύθερων ριζών οξυγόνου ως απάντηση στην αύξηση των αντιφλεγμονωδών παραγόντων όπως είναι οι κυττοκίνες και λευκοτριένιο (Steiner DRS et al., 2001). Όταν απελευθερώνονται στο αγγειακό τοίχωμα οι παραπάνω 65
66 παράγοντες, οδηγούν σε ενίσχυση της αντιφλεγμονώδους απάντησης και ιδιαίτερα στην μικροκυκλοφορία. Πράγματι, είναι δυνατόν να εμφανιστεί χρόνια αγγειακή εξέλκωση όταν κατά τη διάρκεια της διακοπής της ροής του αίματος και της υποξίας διαταραχθούν και παγιδευτούν τα λευκά αιμοσφαίρια στην μικροκυκλοφορία (Steiner DRS et al., 2001; Thomas PR et al., 1991; Ciuffetti G et al., 1994). Από την άλλη μεριά, η υποξία στο ενδοθήλιο μπορεί να απελευθερώσει παράγοντες που εμπλέκονται στη μετανάστευση και στον πολλαπλασιασμό των λείων μυϊκών κυττάρων, προάγοντας την πλάτυνση και πάχυνση του μέσου χιτώνα. Το ενδοθήλιο των κιρσοειδών φλεβών απελευθερώνει τους παράγοντες fibroblast growth factor (bfgf) και platelet growth factor (PDGF) ως αποτέλεσμα των μεταβολικών αλλαγών και των διαταραχών στις αντλίες ιόντων που λαμβάνουν χώρα κατά την υποξία (Michiels C et al., 2002; Michiels C et al., 2000). Όταν αυτοί οι παράγοντες βρεθούν στο μέσω χιτώνα, πραγματοποιείται μετανάστευση των λείων μυϊκών κυττάρων προς τον έσω χιτώνα και προκαλείται παραγωγή κολλαγόνου. Η διαταραχή, λοιπόν, του ενδοθηλίου δεν εμπλέκεται μόνο στις αντιφλεγμονώδεις απαντήσεις κατά τις χρόνιες αγγειακές εξελκώσεις αλλά και στην επαναδιάταξη των λείων μυϊκών κυττάρων στο εσωτερικό του αγγειακού τοιχώματος. Κάθε δυσλειτουργία των ενδοθηλιακών κυττάρων εμπλέκεται και στον έλεγχο της κινητικότητας του αγγειακού τοιχώματος. Τα ενδοθηλιακά κύτταρα στις κιρσοειδείς φλέβες εκκρίνουν λιγότερο ορισμένους παράγοντες που ευθύνονται για την αγγειοσυστολή του τοιχώματος, σε σχέση με τις φυσιολογικές φλέβες. Η νοραδρεναλίνη, που δρα ως αγγειοσυσπαστικός παράγοντας, εμφανίζεται σε αρκετά μειωμένη συγκέντρωση στο τοίχωμα των κιρσοειδών φλεβών εξαιτίας των αλλαγών που εμφανίζει το ενδοθήλιο. Αντίθετα τα αυξημένα επίπεδα της ενδογενούς νοραδρεναλίνης διαστέλλουν τις φλέβες ως αποτέλεσμα της αυξημένης δραστηριότητας του αδρενεργικού συμπαθητικού νευρικού συστήματος. Η ακριβής αναλογία της μειωμένης έκκρισης νοραδρεναλίνης και των αυξημένων επιπέδων της ενδογενούς αυτής, δεν έχει κατανοηθεί πλήρως (Crotty TP, 1991). 66
67 Η νοραδρεναλίνη δεν είναι ο μόνος παράγοντας που εμπλέκεται στη διαστολή των φλεβών. Έχει αποδειχθεί ότι το σύστημα Νιτρικού Οξειδίου (ΝΟ)/κυκλικής Μονοφωσφορικής Γουανοσίνης (cgmp) υπερεκφράζεται στις κιρσοειδείς φλέβες με αποτέλεσμα να ανατρέπεται η ισορροπία των παραγόντων που μεσολαβούν στην αγγειοδιαστολή. Το νιτρικό οξείδιο υπερέχει στο οξειδωτικό στρες και ανταγωνίζεται τη δράση της αγγειοτενσίνης-ιι. Αυτό έχει ως αποτέλεσμα την χαλάρωση του μέσου χιτώνα του αγγειακού τοιχώματος των κιρσών (Schuller-Petrovic S et al., 1997). Το ΝΟ είναι μια ελεύθερη ρίζα με μικρή διάρκεια ζωής και δράση σε διάφορα συστήματα του ανθρώπινου οργανισμού μεταξύ αυτών και το αναπαραγωγικό. Παράγεται από L-Αργινίνη υπό την καταλυτική επίδραση της συνθάσης του ΝΟ (ΝΟS). Στους άνδρες διαφορετικές ισομορφές της ΝΟS έχουν απομονωθεί στα κύτταρα Sertoli και Leydig, στην επιδιδυμίδα, στη σπερματοδόχο κύστη, στη βασική μεμβράνη των σπερματικών σωληναρίων, στα ενδοθηλιακά κύτταρα των ορχικών αγγείων κ.α. Το ΝΟ φαίνεται να διαδραματίζει συγκεκριμένο ρόλο στην ορμονική, συσταλτική και αιμοδυναμική έκφανση της ορχικής και επιδιδυμικής λειτουργίας όπως επίσης και στη σπερματογένεση και την εκφύλιση των γεννητικών κυττάρων. Οι δράσεις του ΝΟ είναι δοσοεξαρτώμενες. Σε φυσιολογικές συγκεντρώσεις δρα σαν διαμεσολαβητής στις προαναφερθείσες λειτουργίες. Σε καταστάσεις, όπως η κιρσοκήλη παράγεται σε συγκεντρώσεις μεγαλύτερες του φυσιολογικού και διαχυόμενο ελεύθερα ανάμεσα στις κυτταρικές μεμβράνες δρα μέσω βιολογικά ενεργοποιημένων μορίων σε διάφορα επίπεδα. Φυσιολογικά διάφοροι μηχανισμοί, ενζυματικοί και πρωτεολυτικοί, προστατεύουν τα κύτταρα από τη μη επιθυμητή προσθήκη επιπλέον ατόμων αζώτου στις πρωτεΐνες τους. Σε καταστάσεις, όπως η κιρσοκήλη, όπου παράγονται αυξημένες ποσότητες RNS (Reactive Nitrosylated Species) μπορεί να υπερνικηθούν οι επιδιορθωτικοί μηχανισμοί και να καταλήξουμε σε παθολογικό αποτέλεσμα. Μάλιστα σε μια πρόσφατη μελέτη ανευρέθηκαν 67
68 αυξημένα επίπεδα καρβονυλικών ομάδων στη σπερματική φλέβα νεαρών ενηλίκων με κλινική ή υποκλινική κιρσοκήλη, υποδεικνύοντας την ύπαρξη οξειδωτικής βλάβης και στις πρωτεΐνες του πλάσματος (Schuller-Petrovic S et al., 1997; Sharma RK et al., 1996). ΜΕΣΟΣ ΧΙΤΩΝΑΣ-ΛΕΙΑ ΜΥΪΚΑ ΚΥΤΤΑΡΑ Αναδιάταξη λείων μυϊκών κυττάρων Αναμφίβολα δημιουργείται η απορία πως δρουν διάφοροι παράγοντες στην αναδιάταξη των λείων μυϊκών κυττάρων στην ανάπτυξη των κιρσοειδών φλεβών. Σε μελέτη σε γερασμένες αρτηρίες κουνελιών, έχει παρατηρηθεί αύξηση στα επιμήκη λεία μυϊκά κύτταρα ώστε να αντιμετωπίσουν επιτυχώς την τάση αύξησης μήκους των αρτηριών (Kockx MM et al., 1993). Επιπλέον η χρόνια επαυξημένη πίεση, είναι δυνατόν να προσανατολίσει τα λεία μυϊκά κύτταρα σε επιμήκη κατεύθυνση ώστε να ενισχυθεί η ελαστική δύναμη του αγγειακού τοιχώματος (Liu SQ et al., 1998). Αναμενόμενο αποτέλεσμα των παραπάνω αποτελεί η αναδιοργάνωση του τοιχώματος στους κιρσούς όπου προάγεται η αναδιάταξη του έσω χιτώνα καθώς και η αύξηση του πάχους του μέσου χιτώνα προκειμένου να εξουδετερώσει την αυξημένη πίεση που ασκείται στις κιρσοειδείς φλέβες. Συγκεκριμένα η πάχυνση του μέσου χιτώνα συμβαίνει λόγω της απελευθέρωσης ενδοθηλιακών παραγόντων οι οποίοι επαναδομούν τα λεία μυϊκά κύτταρα εξαιτίας του μηχανικού stress, της υποξίας και της καταστροφής των ενδοθηλιακών κυττάρων (Michiels C et al., 2002; Michiels C et al., 2000). Μετανάστευση λείων μυϊκών κυττάρων Οι σημαντικότεροι παράγοντες που απελευθερώνονται και εμπλέκονται στη μετανάστευση και στον πολλαπλασιασμό των λείων μυϊκών κυττάρων είναι ο PDGF και ο bfgf (Kenagy RD et al., 1997; Liu SQ et al., 2003). Εκτός αυτού, τα αυξημένα επίπεδα υποξίας, που έχουν παρατηρηθεί στις κιρσοειδείς φλέβες, μπορούν να οδηγήσουν στην ενεργοποίηση αυτοκρινών και παρακρινών μηχανισμών που εμπλέκονται στην υπερέκφραση των PDGF και 68
69 PDGF-β υποδοχέα που απαντώνται στο σηματοδοτικό μονοπάτι της PI3K/Akt (Zhang SX et al., 2003). Ένα από τα άλλα μόρια που εμπλέκονται στο ίδιο μονοπάτι είναι η ενδοθηλίνη-1 η οποία απελευθερώνεται από το ενδοθήλιο και δύναται να προκαλέσει μορφολογικές αλλαγές στο αγγειακό τοίχωμα διεγείροντας τα λεία μυϊκά κύτταρα και ενισχύοντας την δράση των PDGF και bfgf παραγόντων (Vane JR et al., 1994). Η δράση αυτή θεωρείται ως «φλεγμονή του ενδοθηλίου» και οδηγεί στην ενεργοποίηση της πάχυνσης του μέσου χιτώνα στις κιρσοειδείς φλέβες. Υπερτροφία λείων μυικών κυττάρων Επίσης σε πρόσφατη έρευνα μελετήθηκε ο ρόλος του οιστρογονικού υποδοχέα-β (estrogen receptor-β, ERβ) και συσχετίσθηκε με τη πρόκληση υπερτροφίας των λείων μυϊκών κυττάρων. Όπως για παράδειγμα, οι ορμονικές διαταραχές που λαμβάνουν χώρα κατά τη διάρκεια της εγκυμοσύνης και της εμμηνόπαυσης και πιθανώς να σχετίζονται με την επιδείνωση των κιρσών των κάτω άκρων, δύνανται να προάγουν την εμφάνιση υπερτροφίας στα λεία μυϊκά κύτταρα (Knaapen M et al., 2005). Τέλος, η τροποποίηση στοιχείων [Εικόνα 14], που φυσιολογικά απαντώνται στο μέσω χιτώνα, όπως η ακτίνη [Εικόνα 15], η ελαστίνη και τα κολλαγόνο, αλλά με διαφοροποιημένη και ακανόνιστη πλέον δομή, είναι δυνατόν να αποδιοργανώσουν τη συνοχή των λείων μυϊκών κυττάρων και να οδηγήσουν σε υπερτροφία αυτών, γεγονός που συναντάται στις κιρσοειδείς φλέβες [Εικόνα 16] (Wali MA et al., 2002; Kockx MM et al., 1998). 69
70 Εικόνα 14: Ιστολογική δομή του αγγειακού τοιχώματος με Τρίχρωμη χρώση Masson. (A) Φυσιολογική φλέβα-μάρτυρας σαφηνούς φλέβας. (Β) Ατροφικό τμήμα κιρσοειδούς φλέβας, όπου τα λεία μυικά κύτταρα και το εξωκυττάριο στρώμα εμφανίζονται κατά πολύ ελαττωμένα. (C) Υπετροφικό τμήμα κιρσοειδούς φλέβας όπου η οργάνωση των χιτώνων εμφανίζεται έντονα διαταραγμένη από τη συγκέντρωση λείων μυικών κυττάρων και ινώδους ιστού (μεγέθυνση x20) (I=Έσω χιτώνας, M=Μέσος χιτώνας, Ad=Εξωκυττάριο στρώμα, +=Εσωτερικές επιμύκεις δεσμίδες, #= κυκλικές δεσμίδες λείων μυικών κυττάρων που οριοθετούνται από ομόκεντρες μεμβράνες, *= κυκλικές δεσμίδες λείων μυικών κυττάρων στο εξωκυττάριο στρώμα (Commander Cecile B et al., 2001). 70
71 Εικόνα 15: Ανοσοϊστοχημική χρώση Ακτίνης σε σαφηνή φλέβα. (Α) Η χρώση των λείων μυικών κυττάρων είναι έντονη στη φυσιολογική φλέβα-μάρτυρα. Στο ατροφικό (Β) και στο υπερτροφικό τμήμα (C) η χρώση των λείων μυικών κυττάρων είναι διάχυτη, μέτρια στην ένταση και ετερογενής σε σχέση με τη φυσιολογική φλέβα (μεγέθυνση x20) TI=Υπερτροφικός Έσω χιτώνας, M=Μέσος χιτώνας (Krah K et al., 1994). Εικόνα 16: Α. Διακρίνεται η φυσιολογική δομή της ελαστίνης που εντοπίζεται μεταξύ των λείων μυϊκών κυττάρων (χρώση Verhoeff) στις φυσιολογικές φλέβες. Στις κιρσοειδείς φλέβες (Β) έχει τροποποιηθεί η δομή της ελαστίνης και έχει χαθεί η συσταλτική της ικανότητα (βέλη) ως συνέπεια της υπερτροφίας των λείων μυϊκών κυττάρων του μέσου χιτώνα. Κλίμακα 100μm (Somers P et al., 2006) 71
72 ΕΞΩ ΧΙΤΩΝΑΣ ΕΞΩΚΥΤΤΑΡΙΟ ΣΤΡΩΜΑ Ο έξω χιτώνας καλύπτει την εξωτερική επιφάνεια των αγγείων, αποτελούμενος κατά κύριο λόγο από ινοβλάστες, ίνες κολλαγόνου και ελαστικές ίνες με επιμήκη προσανατολισμό. Ο χιτώνας αυτός συνήθως συνέχεται με τα υπόλοιπα στοιχεία του συνδετικού ιστού που περιβάλλουν το αγγείο και είναι συχνά ο πιο εμφανής χιτώνας του τοιχώματος των φλεβών. Μέσα στον έξω χιτώνα φλεβών με παχιά τοιχώματα διεισδύουν μικρά αγγεία, τα αγγεία των αγγείων, τα οποία διακλαδιζόμενα τροφοδοτούν με αίμα το μέσο χιτώνα. Το εξωκυττάριο στρώμα του αγγειακού τοιχώματος παρέχει ένα σκελετικό δίκτυο που αποτελείται από κολλαγόνο, ελαστίνη, πρωτεογλυκάνες και γλυκοπρωτεΐνες, το οποίο περιβάλλει τα λεία μυϊκά κύτταρα και διαδραματίζει σημαντικό ρόλο στη διατήρηση της αγγειακής σταθερότητας και της κυτταρικής ομοιόστασης. Η διαταραχή της ισορροπίας μεταξύ λείων μυϊκών κυττάρων και εξωκυττάριου στρώματος είναι δυνατόν να οδηγήσει στην απώλεια των μηχανικών ιδιοτήτων του τοιχώματος, φαινόμενο που αποτελεί χαρακτηριστικό των κιρσοειδών φλεβών (Psaila JV et al., 1989; Rose SS et al., 1986). Στο τοίχωμα των κιρσοειδών φλεβών συναντώνται διαφορές στη συγκέντρωση και εμφανίζεται εκφυλισμός των ινών του κολλαγόνου και της ελαστίνης (Travers JP et al., 1996; Venturi M et al., 1996). ΣΥΓΚΕΝΤΡΩΣΗ ΙΝΩΝ ΣΤΟ ΕΞΩΚΥΤΤΑΡΙΟ ΣΤΡΩΜΑ Το κολλαγόνο και η ελαστίνη είναι εξωκυττάριες πρωτεΐνες και συμβάλουν στις μηχανικές ικανότητες που διαθέτει το αγγειακό τοίχωμα. Γενικά το κολλαγόνο καταλαμβάνει το 47% και η ελαστίνη το 7% του βάρους του τοιχώματος των φλεβών (Svejcar J et al., 1963). Ο αριθμός των ινών κολλαγόνου αυξάνεται με την ηλικία, ένα φαινόμενο γνωστό ως «φλεβοσκλήρυνση», το οποίο δεν εμπλέκεται άμεσα στη δημιουργία κιρσοειδών φλεβών (Milroy CM et al., 1989). Από την άλλη μεριά, η ύπαρξη νέων κυτταρικών και εξωκυτταρικών στοιχείων που παρατηρούνται στις περιοχές που εμφανίζουν υπερτροφία, σε αντίθεση με τις ατροφικές, πιθανώς 72
73 να εξηγούν την συστροφή που εμφανίζουν οι κιρσοειδείς φλέβες (Badier- Commander C et al., 2000; Badier-Commander C et al., 2001). Η υφή και η αντοχή της ελαστικότητας του αγγειακού τοιχώματος χαρακτηρίζονται από τη διάμετρο των ινιδίων και την ικανότητά τους να σχηματίζουν δεσμίδες (Parry DA, 1988). Το κολλαγόνο Ι βρίσκεται σε περίσσια στο εξωκυττάριο στρώμα και σχηματίζει παχιά ινίδια προσδίδοντας σταθερότητα και στερεότητα στο τοίχωμα του αγγείου, ενώ το κολλαγόνο ΙΙΙ εμπλέκεται με την ελαστικότητα αυτού. Φαίνεται ότι η σύνθεση και η ρύθμιση των ινών του κολλαγόνου Ι και ΙΙΙ είναι αναμφίβολα συνδεδεμένα με τις μηχανικές ικανότητες του τοιχώματος των φλεβών. Σε περίπτωση που διαταραχθεί ο λόγος της συγκέντρωσης κολλαγόνου Ι/κολλαγόνο ΙΙΙ, είναι δυνατόν να παρατηρηθεί κινητική αδυναμία στο τοίχωμα των φλεβών που σχετίζεται με μείωση της διαμέτρου των ινών κολλαγόνου Ι και ΙΙΙ και να αυξηθεί η έκταση των φλεβών (Fleischmajer R et al., 1990; Notbohm H et al., 1993). Επιπλέον έχει δειχθεί ότι το σύνολο των ινών κολλαγόνου Ι είναι σημαντικά αυξημένο, ενώ εκείνο του κολλαγόνου ΙΙΙ ελαττώνεται στις κιρσοειδείς φλέβες σε σχέση με φυσιολογικές φλέβες (Sansilvestri-Morel P et al., 2001; Waksman Y et al., 1997). Η μείωση του λόγου κολλαγόνου Ι/κολλαγόνου ΙΙΙ προάγει την ελάττωση της ελαστικότητας, κάτι που μπορεί να αποτελέσει ερέθισμα για την ανάπτυξη κιρσοειδών φλεβών. Παρόλα αυτά η αιτία της αλλαγής του λόγου κολλαγόνου Ι/κολλαγόνου ΙΙΙ δεν είναι αποσαφηνισμένη και η μείωση του κολλαγόνου ΙΙΙ δε συσχετίζεται με τη μείωση της έκφρασης του mrna του (Sansilvestri-Morel P et al., 1998). Ωστόσο η έλλειψη ινιδίων κολλαγόνου ΙΙΙ πιθανώς να ευθύνεται για την υπερέκφραση του κολλαγόνου Ι σε επίπεδο μεταγραφής (Sansilvestri-Morel P et al., 2001). Η έλλειψη ενός συμμετρικού δικτύου κολλαγόνου/ελαστίνης και η μη φυσιολογική αναλογία τους, πιθανολογείται ότι επίσης εμπλέκεται στην ανάπτυξη κιρσοειδών φλεβών (Wali MA et al., 2002). Η ελαστίνη συντίθεται και εκκρίνεται από τα λεία μυϊκά κύτταρα, σχηματίζοντας με το κολλαγόνο ένα δίκτυο που παρέχει αντοχή στην έκταση των φλεβών. Επιπλέον δημιουργείται μια στιβάδα γύρω από τα λεία μυϊκά κύτταρα, από συσταλτές ελαστικές 73
74 υπομονάδες, που προσδίδουν αντίσταση και ελαστικότητα στα στοιχεία του μέσου χιτώνα ώστε να εξισορροπείται το φορτίο της έντασης των φλεβών. Στις κιρσοειδείς φλέβες, τα ποσοστά της ελαστίνης είναι μειωμένα και εμφανίζεται αποδιοργανωμένη (Gandhi RH et al., 1993; Venturi M et al., 1996). Ποικίλες άλλες πρωτεΐνες του εξωκυττάριου στρώματος, όπως λαμινίνη, τενσασίνη και φιμπρονεκτίνη, έχουν μελετηθεί τόσο σε φυσιολογικές όσο και σε κιρσοειδείς φλέβες όπου έχει παρατηρηθεί μία μέτρια αύξηση του ποσοστού τους (Kirsch D et al., 1999; Kirsch D et al., 2000). ΕΚΦΥΛΙΣΗ ΤΟΥ ΕΞΩΚΥΤΤΑΡΙΟΥ ΣΤΡΩΜΑΤΟΣ Η εκφύλιση του εξωκυττάριου στρώματος ρυθμίζεται από σύνολο πρωτεϊνασών, συμπεριλαμβανομένου του δικτύου των μεταλλοπρωτεϊνασών (matrix metalloproteinases MMPs), των διεγερτών τους και των αναστολέων τους (Mignatti P, 1995). Επί του παρόντος έχουν αναφερθεί 25 μέλη της MMP οικογένειας και έχουν ταξινομηθεί σε 5 ομάδες σύμφωνα με τις διαφορές στη δομή και στην ειδικότητα του υποστρώματός τους (Katsuda S et al., 2003). Τα υποστρώματα των MMPs είναι το κολλαγόνο τύπου Ι και ΙΙΙ, η ελαστίνη και οι πρωτεογλυκάνες που όπως αναφέραμε αποτελούν σημαντικά συστατικά του εξωκυττάριου στρώματος [Εικόνα 17]. Συγκεκριμένα η MMP-1 εντοπίζεται στους ινοβλάστες, στα λεία μυϊκά και στα ενδοθηλιακά κύτταρα των κιρσοειδών φλεβών των κάτω άκρων. Αντίθετα, στις φυσιολογικές φλέβες, η MMP-1 εντοπίζεται μόνο στα ενδοθηλιακά κύτταρα (Woodside KJ et al., 2003). Επίσης η MMP-13, που έχει μελετηθεί σε κιρσούς των κάτω άκρων, μειώνεται σημαντικά και εμφανίζει διαφορές στα σημεία εντοπισμού της στις φλέβες (Bujan J et al., 2000). Η MMP-9 ανευρέθηκε υπερεκφρασμένη στο αγγειακό τοίχωμα και φαίνεται να εμπλέκεται με τον εκφυλισμό της ελαστικής μεμβράνης (Kosugi I et al., 2003). Είναι σημαντικό να αναφερθεί ότι η MMP-9 εμφανίζει τόσο αλλαγές στην τρισδιάστατη δομή της, όσο και στη δράση της στο αγγειακό τοίχωμα, προκαλώντας την μετανάστευση των λείων μυϊκών κυττάρων αφού 74
75 εντοπίζεται στο μέσω χιτώνα. Σε μία μελέτη φάνηκε ότι η αυξημένη δραστηριότητα της MMP-9 είναι δυνατόν να προκαλέσει αύξηση και των επιπέδων της προγενέστερης μορφής της, pro-mmp-9, στο πλάσμα ασθενών που εμφάνισαν κιρσοειδείς φλέβες (Jacob MP et al., 2002). Η αυξημένη συγκέντρωση της pro-mmp-9 μπορεί να αποτελέσει στοιχείο πρώιμης πρόγνωσης της αυξημένης λίμνασης του αίματος στις κιρσοειδείς φλέβες. Η έκφραση της MMP-2 και pro-mmp-2 σε επίπεδο πρωτεΐνης και mrna στον έσω και μέσω χιτώνα των φλεβών, έχει αποδειχτεί ότι ελαττώνεται σε κιρσοειδείς φλέβες σε σχέση με τις φυσιολογικές. Η διαφορά αυτή δεν μπορεί να αποδοθεί στο μεγάλο αριθμό αναστολέων των μεταλλοπρωτεϊνασών αλλά στη μειωμένη παραγωγή MMP-2 από τα κύτταρα του αγγειακού τοιχώματος που τη συνθέτουν (Badier-Commander C et al., 2000). Η MMP-12 εμπλέκεται στενά κυρίως με την εκφύλιση της ελαστίνης αλλά και άλλων συστατικών του εξωκυττάριου στρώματος. Ωστόσο δεν εμφανίζεται διαφορά στην έκφραση της MMP-12 μεταξύ των κιρσοειδών και των φυσιολογικών φλεβών (Wali MA et al., 2002). Έρευνες που διενεργήθηκαν με αντικείμενο τους αναστολείς των MMPs, απέδειξαν ότι η έκφραση του TIMP-1 (tissue inhibitor of metalloprotease-1) είναι σημαντικά αυξημένη σε σχέση με του TIMP-2 που δεν διαφοροποιείται στις κιρσοειδείς φλέβες (Badier-Commander C et al., 2000). Επιπροσθέτως παράγοντες που εμπλέκονται στη δόμηση του αγγειακού τοιχώματος είναι οι MMP-2 και TIMP-2, ενώ οι MMP-9 και TIMP-1 ενεργοποιούνται από εξωτερικά ερεθίσματα (Borden P et al., 1997). Υπάρχουν κυτοκίνες όπως ο παράγοντας platelet-derived growth factor (PDGF), ο transforming growth factor-β (TGFβ) και η αγγειοτενσίνη-ιι που δρώντας στον TIMP-1, πιθανώς να προάγουν την αύξηση των επιπέδων υποξίας στο αγγειακό τοίχωμα των κιρσοειδών φλεβών. Αξίζει να αναφερθεί ότι σε καλλιέργειες κυτταρικών σειρών, η ύπαρξη TIMP-1 και TIMP-2 πιθανώς να ενοχοποιούνται για την αλλαγή του μορφολογικού φαινοτύπου στα λεία μυϊκά κύτταρα των κιρσοειδών φλεβών (Edwards DR et al., 1996). 75
76 Εικόνα 17: Σχηματική αναπαράσταση των παραγόντων που εμπλέκονται στην ανάπτυξη των κιρσοειδών φλεβών. Η υποξία στο ενδοθήλιο δύναται να προάγει την προσκόλληση ουδετερόφιλων κυττάρων και να οδηγήσει σε αγγειακή εξέλκωση. Επίσης το υποξικό ενδοθήλιο, προκαλεί μεταβολές στο μέσω χιτώνα απελευθερώνοντας παράγοντες που εμπλέκονται στον πολλαπλασιασμό και στη μετανάστευση των λείων μυϊκών κυττάρων από το μέσω στον έσω χιτώνα. Οι MMPs και οι TIMPS διαδραματίζουν έναν ζωτικής σημασίας ρόλο στην εκφύλιση του εξωκυττάριου στρώματος. Είναι φανερό ότι οι αλλαγές (ιστολογικές, μορφολογικές, μηχανικές) που παρατηρούνται στις κιρσοειδείς φλέβες δεν αποδίδονται σε έναν παράγοντα [Εικόνα 17] αλλά σε μια πλειάδα αυτών, οι οποίοι ενεργοποιούν και αναστέλλουν μοριακά σηματοδοτικά μονοπάτια, με αποτέλεσμα να διαταράσσονται η δομή και η λειτουργία των φλεβών. ΔΙΑΓΝΩΣΗ Παρά τις πολυάριθμες τεχνολογικές εξελίξεις, το κλειδί για τη διάγνωση της κιρσοκήλης παραμένει η ενδελεχής φυσική και κλινική εξέταση [Εικόνα 18] του ασθενή και η λήψη ενός λεπτομερούς ιατρικού ιστορικού του. 76
77 Εικόνα 18: Κλινική εμφάνιση κιρσοκήλης. Η κλινική εξέταση του ασθενούς αποτελεί το πιο σημαντικό μέρος της διάγνωσης (Lipshultz L et al., 2007). Λαμβάνει χώρα σε όρθια αλλά και σε κεκλιμένη θέση του ασθενούς, αρκεί αυτός να βρίσκεται σε ηρεμία και σε χώρο με ικανοποιητική θερμοκρασία ώστε το όσχεο να παραμένει χαλαρό. ΕΞΕΤΑΣΗ ΤΟΥ ΟΣΧΕΟΥ ΚΑΙ ΤΟΥ ΣΠΕΡΜΑΤΙΚΟΥ ΤΟΝΟΥ Με τον ασθενή αρχικά σε κατακεκλιμένη και ακολούθως σε όρθια στάση και σε θερμό περιβάλλον, εκτελούνται: (α) Επισκόπηση για ορατή διόγκωση του όσχεου διαμέσου του δέρματος (βαθμού ΙΙΙ ή μεγάλη κιρσοκήλη) [Εικόνα 19] (β) Ψηλάφηση του όσχεου και του σπερματικού τόνου για διαπίστωση κιρσοειδών ανευρέσεων (βαθμού ΙΙ ή μετρίου μεγέθους κιρσοκήλη) (γ) Εκτέλεση χειρισμού Valsalva (αύξηση της ενδοκοιλιακής πίεσης) επί μη ψηλαφητής διάτασης των φλεβών που προκαλεί πλήρωση των φλεβών με αίμα όταν υπάρχει κιρσοκήλη (βαθμού Ι ή μικρή κιρσοκήλη) 77
78 Οι παραπάνω τρεις βαθμοί κιρσοκήλης προκύπτουν σύμφωνα με τη βαθμονόμηση κατά Dubin Amelar (Dubin L et al., 1977). Εικόνα 19: Κιρσοκήλη βαθμού ΙΙΙ που εμφανίζεται ως ένα εξόγκωμα κάτω από το δέρμα του ασθενούς, στον αριστερό όρχι. ΕΞΕΤΑΣΗ ΤΩΝ ΟΡΧΕΩΝ Η εξέταση των όρχεων συνιστάται κυρίως στην εκτίμηση του μεγέθους και της σύστασης τους, προκειμένου να διαπιστωθούν δυστροφικές αλλοιώσεις ως συνέπεια της κιρσοκήλης. Στα ανήλικα άτομα η εκτίμηση του μεγέθους των όρχεων γίνεται με το ορχιδόμετρο. Ο όγκος του φυσιολογικού προεφηβικού όρχεος κυμαίνεται μεταξύ 1-2 ml. Μέγεθος όρχεων μεγαλύτερο των 3 ml συνήθως υποδεικνύει την έναρξη της εφηβείας. Μεταξύ 11 και 16 ετών ο όγκος μεταβάλλεται από τα 3 στα 16 ml (Comhaire F, 1996). Αξίζει να σημειωθεί ότι κατά την εφηβική περίοδο και ιδιαίτερα την πρώιμη, παρατηρείται ευρεία διακύμανση του ρυθμού της ανάπτυξης μεταξύ των ατόμων. Επίσης η εκτίμηση του μεγέθους των όρχεων ορθότερο είναι να 78
79 συσχετίζεται με την κλίμακα ανάπτυξης κατά Tanner, δηλαδή της ανάπτυξης των έξω γεννητικών οργάνων και των χαρακτηριστικών του φύλου. Η συσχέτιση των σταδίων Tanner [Εικόνα 20] με τη χρονολογική ηλικία, τη σωματική αύξηση και τους βασικούς σταθμούς της εφηβείας (όπως η αυξητική αιχμή) μπορεί να παρέχει σημαντικές πληροφορίες για την ανίχνευση γενετικών συνδρόμων, ενδοκρινολογικών και ανατομικών διαταραχών (Marshall WA et al., 1970). Εικόνα 20: Η κλίμακα ανάπτυξης κατά Tanner (γεννητικό σύστημα άρρενος). Απεικονίζεται το μέσο μέγεθος των όρχεων και ο όγκος τους σε ml. Συνοπτικά τα 5 στάδια ανάπτυξης κατά Tanner ως αναφορά το μέγεθος του πέους και τον όγκο των όρχεων είναι τα εξής: Tanner I προεφηβεία (όγκος όρχεων μικρότερος του 1.5 ml, μήκος πέους 3 cm ή μικρότερο) [ηλικία 9 ετών ή και νεότερη]. 79
80 Tanner II όγκος όρχεων 1.6 με 6 ml, λεπτό δέρμα όσχεου ερυθρού χρώματος, μέγεθος πέους αμετάβλητο [ηλικία 9-11]. Tanner III όγκος όρχεων 6 με 12 ml, διευρυμένο μέγεθος όσχεου, αύξηση πέους περίπου κατά 6 cm [ηλικία ]. Tanner IV όγκος όρχεων 12 με 20 ml, μεγαλύτερο μέγεθος όσχεου και σκουρότερου χρώματος, αύξηση μεγέθους πέους κατά 10 cm και περιφερικά [ηλικία ]. Tanner V όγκος όρχεων μεγαλύτερος των 20 ml, ενήλικο όσχεο και πέος μήκους 15 cm [ηλικία 14+]. Η κιρσοκήλη σχετίζεται με τη παρεμπόδιση της ορχικής ανάπτυξης στους εφήβους (Sayfan J et al., 1997). Σε μία μελέτη έχει παρατηρηθεί σημαντική ελάττωση του όγκου των όρχεων, της τάξης του 77% σε ανήλικα άτομα και το 10% αυτών διέθεταν τον αριστερό τους όρχι στο ένα τέταρτο του μεγέθους του δεξιού (Lyon RP et al., 1982). Η ατροφία των όρχεων είναι χρονο-εξαρτώμενη. Η συστροφή του όρχεως είναι μια επείγουσα ιατρική που απαιτεί άμεση ιατρική αντιμετώπιση. Συμβαίνει όταν ο όρχις περιστρέφεται γύρω από το σπερματικό πόρο. Η περιστροφή του όρχεως σε σχέση με το σπερματικό πόρο διακόπτει την κυκλοφορία του αίματος από και προς τον όρχι. Εάν η θεραπεία γίνει εντός των πρώτων ωρών από την έναρξη του προβλήματος, ο όρχις είναι δυνατόν να ιαχθεί (Lipshultz LI et al, 1977). Ο όγκος των όρχεων στην προεφηβική ηλικία είναι σταθερός και κατά την έναρξη της ήβης αυξάνεται ακόμα και πριν αρχίσουν να εμφανίζεται οι άλλες αλλαγές που συμβαίνουν εκείνη την περίοδο. Στους έφηβους με κιρσοκήλη, η γρήγορη ανάπτυξη των όρχεων μεταξύ της ηλικίας των 11 και 16 ετών, επηρεάζεται από την κιρσοκήλη, η οποία προκαλεί και ασυμμετρία μεταξύ δεξιού και αριστερού όρχι (Witt MA et al., 1993). 80
81 Η κλινική εκτίμηση του μεγέθους των όρχεων γίνεται συνήθως με: Οπτική καταγραφή Παχύμετρα Ορχιδόμετρα (Prader ή Takihara) Υπερηχογράφημα Το υπερηχογράφημα αποτελεί απαραίτητο συμπλήρωμα της κλινικής εξέτασης σε άντρες που προσέρχονται για διερεύνηση υπογονιμότητας. Το υπερηχογράφημα είναι ιδιαίτερα χρήσιμο στην επιβεβαίωση των ευρυμάτων της κλινικής εξέτασης, στη διάγνωση της υποκλινικής κιρσοκήλης και της υποτροπιάζουσας ή εμμένουσας κιρσοκήλης μετά από χειρουργική επέμβαση (Comhaire F, 1996). Θα αναφερθούμε σε μετεγενέστερο κεφάλαιο όπου να αναλυθούν οι απεικονιστικές μέθοδοι για τον έλεγχο της κιρσοκήλης. ΕΛΕΓΧΟΣ ΤΟΥ ΣΠΕΡΜΑΤΟΣ Το σπέρμα αποτελείται από σπερματοζωάρια και σπερματικό υγρό. Τα σπερματοζωάρια παράγονται με τη διαδικασία της σπερματογένεσης [Εικόνα 21] στα σπερματικά σωληνάρια των όρχεων [Εικόνα 22]. Το σπερματικό υγρό είναι εξωκυττάριο υγρό και προέρχεται από την ανάμειξη των εκκρίσεων των επικουρικών, γεννητικών αδένων. Ο έλεγχος του σπέρματος περιλαμβάνει: α) το σπερμοδιάγραμμα, β) το βιοχημικό έλεγχο και γ) ανοσοβιολογικό και ορμονικό έλεγχο. 81
82 Εικόνα 21: Απεικόνιση της διαδικασίας της σπερματογένεσης. Εικόνα 22: Η παραγωγή του σπέρματος πραγματοποιείται στα σπερματικά σωληνάρια των όρχεων. 82
83 Σπερμοδιάγραμμα Η ανάλυση σπέρματος παίρνει υπ' όψιν πολλές παραμέτρους και πραγματοποιεί διάφορες δοκιμές στο σπέρμα. Μια ανάλυση σπέρματος για να είναι αξιόπιστη θα πρέπει να πραγματοποιείται σε τουλάχιστον δύο δειγματοληψίες, με διαφορά το λιγότερο επτά ημερών στη διάρκεια μιας περιόδου δύο έως τριών μηνών, επειδή ορισμένες συνθήκες μπορεί να επηρεάσουν τα επίπεδα σπέρματος. Τα περισσότερα εργαστήρια δέχονται διεθνώς τον προκαθορισμένο χρόνο αποχής. Η Π.Ο.Υ. (Παγκόσμια Οργάνωση Υγείας) το 1980 καθόρισε το χρόνο αποχής από 2 έως 7 ημέρες, καθώς και τα χαρακτηριστικά του δείγματος [Πίνακας 1]. Το δείγμα θα πρέπει σε 20 λεπτά από τη συλλογή του να εξετάζεται. Η αξία της ανάλυσης σπέρματος εξαρτάται πολύ από την σωστή συνεργασία και λειτουργία της τριάδας, ασθενής-ουρολόγος-μικροβιολόγος. Η εξέταση του σπέρματος γίνεται με μικροσκοπική ανάλυση. Κριτήρια Αξιολόγησης Φυσιολογικού Σπέρματος κατά ΠΟΥ Κριτήρια Όγκος Παράμετροι 2,0-5,0 ml ph 7,2-7,8 Συγκέντρωση περισσότερα από 20 εκατομμύρια / ml Συνολικός Αριθμός Σπερματοζωαρίων περισσότερα από 40 εκατομμύρια σπερματο ωάρια Κινητικότητα περισσότερα από 50% των σπερματοζωαρίων με προωθητική κίνηση ή 25% των σπερματοζωαρίων με γρήγορη προωθητική κίνηση εντός 60min από τη συλλογή Μορφολογία περισσότερα από 50% με φυσιολογική μορφολογία Βιωσιμότητα περισσότερα από 75% ζωντανά σπερματοζωάρι Λευκοκύτταρα λιγότερα από 1 εκατο μύριο /ml Ψευδάργυρος (ολικός) περισσότερα από 2,4 mol ανά εκσπερμ τ ση Κιτρικό Οξύ (ολικό) περ σσότερα από 5 mol (10 mg) ανά εκσπερμάτιση Φρουκτόζη (ολική) περισσότε α από 13 mol ανά εκσπερμάτιση Πίνακας 1: Δίδονται τα κριτήρια αξιολόγησης ενός σπέρματος ως φυσιολογικού από τον Παγκόσμιο Οργανισμό Υγείας (ΠΟΥ). 83
84 Αρχικά αξιολογούνται τα φυσικά χαρακτηριστικά του δείγματος όπως η πυκνότητα, η κινητικότητα και η μορφολογία των σπερματοζωαρίων. Επιπρόσθετα γίνεται αξιολόγηση του pη, που φυσιολογικά θα πρέπει να είναι αλκαλικό, καθώς και της ρευστοποίησης, του ιξώδους του και της ύπαρξης αντισπερμικών αντισωμάτων. Τα επίπεδα σακχάρων επίσης θα πρέπει να μετρηθούν αφού έλλειψη φρουκτόζης στην εκσπερμάτιση συνδυάζεται με απόφραξη. Αυτή είναι μια από τις περιπτώσεις στις οποίες ενδείκνυται βιοψία όρχεων. Τέλος συγκέντρωση λευκοκυττάρων στο δείγμα έχει αρνητική επίδραση στη γονιμοποιητική ικανότητα του σπέρματος. Ο τυπικός όγκος σπέρματος που συλλέγεται είναι περίπου 2-6 millilitres. Η πυκνότητα των σπερματοζωαρίων μέσα στο σπέρμα, μετριέται σε εκατομμύρια σπερματοζωάρια ανά millilitre σπέρματος. Κανονική είναι η πυκνότητα μεγαλύτερη ή ίση με 20 εκατ. ανά millilitre (και πάνω από 80 εκατομμύρια σπερματοζωάρια σε μία εκσπερμάτιση). Ένα δείγμα σπέρματος μπορεί να χαρακτηριστεί από: ολιγοσπερμία, όταν ο αριθμός των σπερματοζωαρίων είναι χαμηλότερος από το φυσιολογικό (<20 εκατ. / ml) ασθενοσπερμία, όταν το ποσοστό κινητικότητας των σπερματοζωαρίων είναι χαμηλό ολιγοασθενοσπερμία, όταν ο αριθμός και η κινητικότητα είναι χαμηλότερα από το κανονικό τερατοσπερμία, όταν παρατηρείται ένα υψηλό ποσοστό δύσμορφων σπερματοζωαρίων αζωοσπερμία, όταν δεν ανιχνεύονται καθόλου σπερματοζωάρια (Micic S et al., 1983; Paduch DA et al., 1996; Nagao RR et al., 1986). Η κινητικότητα των σπερματοζωαρίων, περιγράφει το ποσοστό αυτών που κινούνται σε ένα δείγμα. Η πρόοδος του σπέρματος βαθμολογείται με βάση το μηδέν (δεν υπάρχει κίνηση) έως 4 ή υψηλότερη για το σπέρμα που 84
85 κινείται σε ευθεία γραμμή με καλή ταχύτητα. Η κίνηση των σπερματοζωαρίων διακρίνεται σε 3 τύπους την προωθητική κίνηση, την επιτόπια καθώς και στα ακίνητα σπερματοζωάρια. Σε ένα δείγμα σπέρματος το σύνολο των σπερματοζωαρίων με προωθητική κίνηση πρέπει να ξεπερνά το 50% στην πρώτη ώρα παρατήρησης. Μορφολογία της ανάλυσης, είναι η μελέτη για το μέγεθος, το σχήμα, και την εμφάνιση των κυττάρων του σπέρματος. Αν χρησιμοποιηθούν τα αυστηρά κριτήρια των Kruger and Menkveld τότε η τιμή αναφοράς για την παράμετρο της μορφολογίας, σύμφωνα με την WHO, είναι 15% φυσιολογικές μορφές σπερματοζωαρίων. Σύμφωνα με τα αυστηρά κριτήρια των Kruger and Menkveld όταν οι φυσιολογικές μορφές των σπερματοζωαρίων είναι > 14% το σπέρμα χαρακτηρίζεται ως φυσιολογικό/ γόνιμο. Όταν οι φυσιολογικές μορφές των σπερματοζωαρίων κυμαίνονται μεταξύ 5-14% το σπέρμα χαρακτηρίζεται ως υπογόνιμο. Η ανάλυση αξιολογεί τη δομή 200 σπερματοζωαρίων και οποιαδήποτε ελαττώματα καταγράφονται. Επιμήκης κεφαλή παρατηρείται συνήθως στην κιρσοκήλη και στις λοιμώξεις των επικουρικών γεννητικών αδένων, όμως η επίδραση της στη γονιμότητα δεν έχει απόλυτα διευκρινισθεί. Επιπλέον ανωμαλίες του αυχένα παρατηρούνται στην κιρσοκήλη (Homonnai ZT et al., 1980). Βιοχημικός έλεγχος του σπέρματος Έχει αποδειχτεί ότι το κιτρικό οξύ, η όξινη φωσφατάση, ο ψευδάργυρος και το μαγνήσιο προέρχονται από τον προστάτη και ο προσδιορισμός τους στο σπερματικό υγρό δίνει χρήσιμες πληροφορίες για την φυσιολογική λειτουργία του προστάτη. Η φρουκτόζη και οι προσταγλανδίνες προέρχονται από τις σπερματοδόχους κύστες. Η καρνιτίνη και η γλυκερόλη, η φωσφορόλη, η χολίνη αποτελούν δείκτες καλής λειτουργίας των επιδιδυμίδων. Ενδείξεις για βιοχημικές αναλύσεις 1. Χαμηλός όγκος σπέρματος (λιγότερος από 2 κ. εκ.) 2. Ταχεία μείωση της κινητικότητας των σπερματοζωαρίων (μικρότερη του 40%) 2 ώρες μετά την εκσπερμάτωση 85
86 3. Ανάγκη εκτίμησης της εκκριτικής ικανότητας των επικουρικών γεννητικών αδένων. Χαμηλός όγκος σπέρματος, χαμηλά επίπεδα φρουκτόζης, μείωσης εκκριτικής ικανότητας σπερματοδόχων κύστεων, αζωοσπερμία με απουσία ανώριμων μορφών της σπερματικής σειράς και χαμηλός όγκος σπέρματος, είναι συμβατά με απόφραξη στο επίπεδο της εκσπερματικών πόρων ή με συγγενή απουσία σπερματοδόχων κύστεων (Derek H et al., 2005). Ανοσοβιολογικός και Ορμονικός έλεγχος Έχει βρεθεί ότι στο 4% περίπου των ανδρών με πρόβλημα γονιμότητας υπάρχουν στον ορό ή στο σπερματικό υγρό αντισώματα κατά των σπερματοζωαρίων. Διατυπώνεται η άποψη ότι η παραγωγή των αντισωμάτων αυτών προκαλείται όταν τα σπερματοζωάρια αυτούσια ή ορισμένα αντιγονικά τους στοιχεία, περάσουν από τον αυλό στο διάμεσο ιστό των επιδιδυμίδων και έρθουν εκεί σε επαφή με ανοσοπαράγωγα κύτταρα. Τα αντισώματα κατά των σπερματοζωαρίων βρίσκονται σε περιπτώσεις με λοίμωξη των γεννητικών επικουρικών αδένων, σε ασθενείς με τραύματα των όρχεων, κρυψορχία, ανασπώμενους όρχεις ή με ιστορικό ορχίτιδας (Kendirci M et al., 2006). Ο ορμονικός έλεγχος θα πρέπει να γίνεται σε άτομα με βαριά ολιγοσπερμία ή αζωοσπερμία και σε εκείνους που το ιστορικό και η κλινική εξέταση θέτουν την υποψία ενδοκρινοπάθειας. Θυλακιοτρόπος ορμόνη FSH - Φυσιολογικές τιμές 4-10 mg/ml Ο προσδιορισμός της FSH δεν θα πρέπει να παραλείπεται όταν στο σπερμοδιάγραμμα υπάρχει αζωοσπερμία ή βαριά ολιγοσπερμία. Χαμηλή FSH είναι συμβατή με διάγνωση ανεπάρκειας του συστήματος «υποθάλαμοςυπόφυσης». Η FSH σε υψηλά επίπεδα είναι συμβατή με ανορχία, κρυψορχία, χρωμοσωμικές ανωμαλίες (σύνδρομο Klinefelter), βαριάς μορφής υποσπερματογένεσης, διακοπή στην ωρίμανση του σπερματικού επιθηλίου ή ολική απλασία αυτού (Zohdy W et al., 2010). 86
87 Ωχρινοτρόπος ορμόνη LH - Φυσιολογικές τιμές 4-12 mg/ml Πρέπει να γίνει όταν υπάρχει αζωοσπερμία ή βαριά ολιγοσπερμία, κάτω των 20x10 6 ανά εκσπερμάτωση. Όταν η LH είναι χαμηλή είναι συμβατή με διάγνωση υπογοναδισμού, ενώ υψηλά επίπεδα LH απαντώνται στην ανορχία και σε χρωμοσωμική ανωμαλία των όρχεων (Zohdy W et al., 2010; Sakamoto H et al., 2009). Τεστοστερόνη Τ Φυσιολογικές τιμές 3-14 mg/ml Χαμηλή Τ παρατηρείται όταν υπάρχει απουσία όρχεων (FSH και LH υψηλές), υπογοναδοτροφικός υπογοναδισμός (FSH και LH συνήθως χαμηλές ή μη ανιχνεύσιμες). Οριακά χαμηλές τιμές Τ υπάρχουν σε περιπτώσεις κρυψορχίας ή χρωμοσωμικής βλάβης των όρχεων. Φυσιολογική τιμή Τ είναι συμβατή με μεμονωμένες βλάβες του σπερματικού επιθηλίου, κιρσοκήλη, λοιμώξεις επικουρικών αδένων, αποφρακτική αζωοσπερμία και μεταπαρωτιδική ορχίτιδα (Tanrikut C et al., 2010). ΑΠΕΙΚΟΝΙΣΤΙΚΕΣ ΜΕΘΟΔΟΙ [1] Υπερηχογράφημα όσχεου Θεωρείται σήμερα ως η ακριβέστερη και πλέον αναπαραγώγιμη μέθοδος μετρήσεως του όγκου των όρχεων καθώς, έχει παρατηρηθεί στενή συσχέτιση υπερηχογραφικά υπολογιζόμενου και πραγματικού (αυτοψία) μεγέθους, ενώ φαίνεται να υπερέχει σημαντικά σε διαγνωστική ακρίβεια σε σχέση με το ορχιδόμετρο. Πρέπει να σημειωθεί ότι κοινό χαρακτηριστικό των μεθόδων μέτρησης του όγκου των όρχεων, είναι η τάση τους να υπερεκτιμούν το πραγματικό μέγεθος των μικρότερων αδένων και αντίθετα, να υποεκτιμούν τις διαστάσεις των υπερμεγεθέστερων. Γενικά όμως, διαφορές μεγέθους μεταξύ των δύο όρχεων μικρότερες των 2 ml δεν αξιολογούνται κλινικά ενώ, υπερηχογραφικά καταδεικνυόμενη διαφορά μεγαλύτερη των 2ml, αποτελεί σήμερα τον πλέον αξιόπιστο δείκτη ορχικής δυστροφίας. Το 87
88 υπερηχογράφημα οσχέου [Εικόνα 23] εξετάζει τους όρχεις, τις επιδιδυμίδες, το περιεχόμενο του οσχέου (π.χ. αν υπάρχει καθόλου υγρό) ενώ παράλληλα μπορεί να ελεγχθεί η αιμάτωση των όρχεων. Εικόνα 23: Υπερηχογράφημα αριστερού όρχι (Τ) με κιρσοκήλη (V). Απεικονίζονται φλέβες διαμέτρου mm μεταξύ του άνω και του μέσου πόλου του όρχι. Η διάμετρος των φλεβών αυξάνεται κατά mm διενεργώντας με μέθοδο Valsalva (δεν απεικονίζεται). [2] Φλεβογραφία Η φλεβογραφία της έσω σπερματικής φλέβας αποτελεί την πλέον ακριβή μέθοδο απεικόνισης της κιρσοκήλης. Ωστόσο λόγω της ύπαρξης πιθανών κινδύνων από την εφαρμογή της, λόγω έκθεσης των γονάδων του ασθενούς στην ακτινοβολία, η χρήση της είναι περιορισμένη και συνδυάζεται μόνο με θεραπευτικούς χειρισμούς (πχ. έγχυση σκληρυντικών ουσιών, εμβολική απόφραξη).[εικόνα 24] Εικόνα 24: Φλεβογραφία αριστερού όρχι. 88
89 [3] Αγγειακό υπερηχογράφημα των όρχεων-έγχρωμο Doppler Η μέθοδος παρέχει πληροφορίες για το εύρος των φλεβών του ελικοειδούς σπερματικού πλέγματος καθώς και την παρουσία ή όχι της παλινδρόμησης αίματος κατά την εκτέλεση της δοκιμασίας Valsalva, στοιχεία σημαντικά για τη διάγνωση της υποκλινής κιρσοκήλης [Εικονα 25]. Γενικά όμως στους εφήβους, το έγχρωμο Doppler υπερηχογράφημα δεν αποτελεί διαγνωστική μέθοδο ρουτίνας καθώς η υποκλινική κιρσοκήλη δεν θεωρείται ως σημαντικό κλινικό πρόβλημα στην εφηβεία (Kass E et al., 1987). Εικόνα 25: Άνω εικόνα-υπερηχογράφημα στο ελικοειδές πλέγμα αριστερού όρχι με κιρσοκήλη. Κάτω εικόνα-απεικόνιση έγχρωμου Doppler στον ίδιο όρχι. [4] Ραδιενεργό σπινθηρογράφημα και Θερμογραφία όσχεου Και οι δύο αυτές μέθοδοι, δεν έχουν υψηλή διαγνωστική ειδικότητα που απαιτείται για την εφαρμογή στην κλινική πράξη και χρησιμοποιούνται σπάνια σε εξαιρετικές περιπτώσεις (Skoog JS et al., 1997). Η θερμογραφία του οσχέου με ειδικές θερμικές κάμερες δεν πλεονεκτεί έναντι των άλλων διαγνωστικών τεχνικών και έχει εγκαταλειφθεί. Τέλος θα πρέπει να αναφερθεί πως στη διαφορική διάγνωση της κιρσοκήλης θα πρέπει να λάβουμε υπόψη τυχόν ύπαρξη βουβωνοκήλης, υδροκήλης, κήλης του σπερματικού πόρου καθώς και κύστεων της επιδιδυμίδας. 89
90 ΘΕΡΑΠΕΙΑ-ΑΝΤΙΜΕΤΩΠΙΣΗ Η χειρουργική επέμβαση αποτελεί την θεραπεία εκλογής για την διόρθωση της κιρσοκήλης. Η χειρουργική αποκατάσταση της κιρσοκήλης αποτελεί την συχνότερη επέμβαση για την αντιμετώπιση της ανδρικής υπογονιμότητας (Schlesinger MH et al., 1994). Υπό φυσιολογικές συνθήκες η αγγείωση του όρχεως παρέχεται από τρεις διαφορετικές αρτηριακές παροχές, την σπερματική (ορχική) αρτηρία, την αρτηρία του κρεμαστήρα και την εκφορητική αρτηρία. Η φλεβική παροχέτευση παρέχεται βασικά από το φλεβικό πλέγμα του όρχι μέσω της έσω σπερματικής φλέβας, ωστόσο έχει διαπιστωθεί η ύπαρξη πολλών παράπλευρων φλεβικών δικτύων όπως της έξω σπερματικής, της εκφορητικής, της κρεμαστηριακής φλέβας και των φλεβών του οίακα. Η ύπαρξη αυτών των φλεβικών δικτύων ενδεχομένως εξηγεί την υποτροπή της κιρσοκήλης παρά την χειρουργική απολίνωση της έσω σπερματικής φλέβας (Sayfan J et al., 1980). Ο στόχος στην χειρουργική αντιμετώπιση της κιρσοκήλης είναι η πλήρης διακοπή της παλινδρομούσας φλεβικής αποχέτευσης του όρχι με διατήρηση της αρτηριακής παροχής του σπερματικού πόρου και διατήρηση των λεμφαγγείων (Schlegel PN et al., 1992). Η θεραπεία της κιρσοκήλης γίνεται χειρουργικά, με την απολίνωση των φλεβών που δεν επαρκούν, δηλαδή της σπερματικής φλέβας (αλλά και άλλων φλεβών που μπορεί να συμμετέχουν στη κιρσοκήλη, όπως οι κρεμαστήριες και οι έξω σπερματικές). Ενδείξεις δε, για αντιμετώπιση της αποτελούν: Ο χρόνιος πόνος και η ενόχληση. Η ατροφία του όρχι στην εφηβεία. Υπογονιμότητα στην ενηλικίωση. Ένας υπογόνιμος άνδρας θεωρείται υποψήφιος για τη χειρουργική αποκατάσταση της κιρσοκήλης, αν ισχύουν και οι τέσσερεις από τις παρακάτω 90
91 συνθήκες: α) το ζευγάρι έχει γνωστή υπογονιμότητα, β) η σύντροφος είναι γόνιμη ή φέρει κάποιο διορθώσιμο αίτιο υπογονιμότητας, γ) η κιρσοκήλη είναι ψηλαφητή κατά τη κλινική εξέταση ή επί υποψίας επιβεβαιώνεται στον υπερηχογραφικό έλεγχο και δ) ο ασθενής έχει παθολογικό σπερμοδιάγραμμα. Υποψήφιοι μπορούν επίσης να θεωρηθούν και ενήλικοι άνδρες με κιρσοκήλη και παθολογικό σπερμοδιάγραμμα που επιθυμούν να τεκνοποιήσουν στο μέλλον. Η επέμβαση μπορεί να εκτελεστεί με διάφορες τεχνικές: (α) υψηλή απολίνωση (μέθοδος Palomo) (β) βουβωνική απολίνωση (μέθοδος Ivannisevich) (γ) μικροχειρουργική υποβουβωνική απολίνωση (μέθοδος Marmar ή Goldstein) (δ) λαπαροσκοπική απολίνωση. Οι επεμβάσεις κιρσοκήλης είναι μικρής βαρύτητας και ο ασθενής παραμένει στην κλινική συνήθως μια ημέρα. Οι επιπλοκές είναι σπάνιες και περιλαμβάνουν πόνο και οίδημα στον όρχι ή τη βουβωνική χώρα, αιμάτωμα, υδροκήλη και σπανίως ορχική ατροφία. Ο πίνακας 2 συνοψίζει τις διάφορες μεθόδους απολίνωσης που χρησιμοποιούνται καθώς και τα ποσοστά επιτυχίας και επιπλοκών τους (Szabo R et al., 1984). ΤΕΧΝΙΚΗ ΔΙΑΤΡΗΣΗ ΥΔΡΟΚΗΛΗ ΑΡΤΗΡΙΑΣ % ΥΠΟΤΡΟΠΗ Οπισθοπεριτοναϊκή Όχι Κλασσική βουβωνική Όχι Λαπαροσκοπική Ναι 5-8 <2 Με χρήση Μικροσκοπίου (βουβωνική ή υποβουβωνική) Ναι 0 <2 [Εικόνα 22α-δ] Πίνακας 2: Οι διάφορες τεχνικές αποκατάστασης της κιρσοκήλης (Szabo R et al., 1984). Χειρουργικές τεχνικές Διάφορες τεχνικές και προσπελάσεις έχουν κατά καιρούς χρησιμοποιηθεί για την επίτευξη αυτού του στόχου. Κάνοντας μια μικρή ιστορική αναδρομή θα δούμε ότι η οσχεική προσπέλαση ήταν η πρώτη που 91
92 περιγράφηκε για την αντιμετώπιση της κιρσοκήλης, όταν το 1904 ο Hartman περιέγραψε οσχεική τομή με εξωτερική απολίνωση των κιρσοειδών φλεβών. Η προσπέλαση αυτή γρήγορα εγκαταλείφθηκε λόγω του αυξημένου κινδύνου τρώσης της ορχικής αρτηρίας και του υψηλού ποσοστού υποτροπών. Οι ανοικτές χειρουργικές τεχνικές που χρησιμοποιούνται σήμερα περιλαμβάνουν την οπισθοπεριτοναϊκή προσπέλαση (επέμβαση κατά Palomo), καθώς και την υποβουβωνική και βουβωνική προσπέλαση. Η λαπαροσκοπική μέθοδος αποτελεί μια ενδεχομένως λιγότερο επεμβατική επιλογή για την αντιμετώπιση της κιρσοκήλης καθώς επίσης και οι ελάχιστα επεμβατικές τεχνικές της διαδερμικής σκληροθεραπείας και του εμβολισμού. Η οπισθοπεριτοναϊκή προσπέλαση- επέμβαση κατά Palomo περιγράφηκε το 1948 από τον Palomo με σκοπό την ανακούφιση από τον πόνο και το βάρος της κιρσοκήλης και στη συνέχεια εφαρμόστηκε από τον Tulloch στην αντιμετώπιση της σχετιζόμενης με την κιρσοκήλη υπογονιμότητας. Η επέμβαση κατά Palomo συνίσταται σε οπισθοπεριτοναϊκή προσπέλαση και υψηλή απολίνωση, ύπερθεν του έσω βουβωνικού δακτυλίου, των έσω σπερματικών φλεβών και της σπερματικής αρτηρίας. Την φλεβική επαναφορά του αίματος του όρχι μετά την επέμβαση αναλαμβάνει το δίκτυο της έξω σπερματικής φλέβας, της εκφορητικής και κρεμαστηριακής φλέβας καθώς και των φλεβών του οίακα (Palomo A, 1948; Tulloch WS, 1955). Η σύγχρονη εκδοχή της επέμβασης κατά Palomo γίνεται με τομή μήκους 3cm περίπου, 1cm κεντρικά και 1cm κάτωθεν της πρόσθιας άνω λαγόνιας άκανθας. Μετά από διατομή των μυών, το περιτόναιο απωθείται προς τη μέση γραμμή και με τον τρόπο αυτό οι έσω σπερματικές φλέβες αναγνωρίζονται στον οπισθοπεριτοναϊκό χώρο παράλληλα με τον ουρητήρα. Η ορχική αρτηρία αναγνωρίζεται επίσης και διατηρείται. Οι φλέβες παρασκευάζονται, απολινώνονται με ράμματα και διατέμνονται. Η προσπέλαση αυτή συνοδεύεται από σημαντική συχνότητα μετεγχειρητικής υδροκήλης λόγω της en block απολίνωσης των λεμφαγγείων και υποτροπής της κιρσοκήλης, ενώ ο κίνδυνος ορχικής ατροφίας είναι μικρός λόγω της ύπαρξης παράπλευρης 92
93 ορχικής αιμάτωσης από την εκφορητική αρτηρία του κρεμαστήρα (Sun N et al., 2001). Η βουβωνική προσπέλαση ή τεχνική κατά Ivanissevich η οποία επίσης κατά την εισαγωγή της είχε σαν ένδειξη την αντιμετώπιση του πόνου από την παρουσία κιρσοκήλης στη συνέχεια κατέστη δημοφιλής από τους Dubin και Amelar στην θεραπεία της σχετιζόμενης με την κιρσοκήλη υπογονιμότητας (Dubin L et al., 1977). Στην κατά Ivanissevich προσπέλαση γίνεται τομή 3-4cm άνωθεν του έξω στομίου του βουβωνικού πόρου, διατέμνεται η περιτονία του έξω λοξού κοιλιακού μυ και παρασκευάζεται ο σπερματικός τόνος (Beck EM et al., 1992). Αφού εντοπιστεί η ορχική αρτηρία παρασκευάζεται και διατηρείται, στη συνέχεια απολινώνονται οι έσω σπερματικές φλέβες και διατηρούνται και τα λεμφαγγεία. Ο σπερματικός τόνος έρχεται στην επιφάνεια της τομής και οι έξω σπερματικές φλέβες που πορεύονται παράλληλα με τόνο ή διαπερνούν το έδαφος του πόρου ανευρίσκονται και απολινώνονται. Η βουβωνική καθώς και η υποβουβωνική προσπέλαση έχουν το πλεονέκτημα ότι επιτρέπουν την πρόσβαση στις έξω σπερματικές φλέβες και στις φλέβες του πόρου σε επίπεδο στο οποίο δεν είναι προσπελάσιμες με την τεχνική Palomo και την λαπαροσκόπηση (Hoops CV et al., 2003). Η τεχνική Ivanissevich συνοδεύεται από παραπλήσια με την Palomo ποσοστά υδροκήλης ενώ ενέχει τον κίνδυνο διαταραχής της αιμάτωσης του όρχι και ορχικής ατροφίας δεδομένου ότι στο επίπεδο του βουβωνικού πόρου στο 67% των περιπτώσεων ανευρίσκεται μόνο μία αρτηρία η οποία και πρέπει να παρασκευασθεί με προσοχή για την αποφυγή κάκωσής της (Szabo R et al., 1984; Hoops CV et al., 2003; Silber SJ et al., 1979). Μία πρόσφατη καινοτομία είναι η χρήση οπτικής μεγέθυνσης είτε με loupes είτε με τη βοήθεια χειρουργικού μικροσκοπίου στην βουβωνική και υποβουβωνική προσπέλαση για την χειρουργική αντιμετώπιση της κιρσοκήλης. Η οπτική μεγέθυνση που επιτυγχάνεται με τον τρόπο αυτό ενισχύει τη διακριτική ικανότητα του χειρουργού και βοηθάει σημαντικά στην αναγνώριση ανατομικών δομών από τις οποίες άλλες θα διατηρηθούν (λεμφαγγεία, 93
94 αρτηρίες) και άλλες θα απολινωθούν (φλεβικά στελέχη). Με τον τρόπο αυτό έχει σημειωθεί σημαντική μείωση των ποσοστών μετεγχειρητικής υδροκήλης και υποτροπιάζουσας-εμμένουσας κιρσοκήλης συγκριτικά με τις άλλες τεχνικές. Η μικροχειρουργική υποβουβωνική τεχνική θεωρείται σήμερα ως πρώτη επιλογή στη χειρουργική θεραπεία της κιρσοκήλης και για το λόγο αυτό θα συζητηθεί εκτενέστερα στη συνέχεια. Οι Marmar et al περιέγραψαν πρώτοι την μικροχειρουργική υποβουβωνική επέμβαση για την κιρσοκήλη με τη βοήθεια οπτικής μεγέθυνσης (Marmar JL et al., 1985). Στην προσπέλαση αυτή ο αντικειμενικός στόχος είναι η απολίνωση όλων των φλεβικών στελεχών που αποχετεύουν τον όρχι με εξαίρεση την εκφορητική φλέβα και η διατήρηση της ορχικής, εκφορητικής και κρεμαστηριακής φλέβας καθώς και των λεμφαγγείων (Schlegel PN et al., 1992). Η υποβουβωνική προσπέλαση δεν περιλαμβάνει διατομή μυϊκών περιτονιών με όφελος ως προς τον μετεχγειρητικό πόνο και τον χρόνο ανάρρωσης. Από την άλλη η προσπέλαση αυτή είναι τεχνικά δυσκολότερη, καθώς απαιτεί ικανότητες και εξοικείωση με την μικροχειρουργική, συγκεκριμένο τεχνολογικό εξοπλισμό ενώ παρά τις τεχνικές τροποποιήσεις συνοδεύεται από αυξημένο χειρουργικό χρόνο, τουλάχιστο στο αρχικό στάδιο εκμάθησης (Zini A et al., 2006). Η μικροχειρουργική υποβουβωνική προσπέλαση αρχίζει με πλάγια τομή 2-3cm κάτω από το έξω στόμιου του βουβωνικού πόρου. Η τομή επεκτείνεται στις περιτονίες των Scarpa και Camper και ο σπερματικός τόνος ανευρίσκεται και φέρεται από την τομή με μία λαβίδα [Εικόνα 26α]. Ο σπερματικός τόνος περιβάλλεται από ένα Penrose [Εικόνα26β], το χειρουργικό μικροσκόπιο εισάγεται στο χειρουργικό πεδίο και τα στοιχεία του τόνου εξετάζονται υπό μεγέθυνση x8-x15. Η έσω σπερματική αρτηρία αναγνωρίζεται καθώς σφύζει ελαφρά και στη συνέχεια παρασκευάζεται από τους γύρω ιστούς και περιβρογχίζεται με ράμμα. Ο σπερματικός πόρος και τα συνοδά του φλεβικά στελέχη αναγνωρίζονται και διατηρούνται όπως επίσης και η αρτηρία του κρεμαστήρα. Οι έσω σπερματικές φλέβες και οι φλέβες του κρεμαστήρα 94
95 απολινώνονται με ράμμα και διατέμνονται [Εικόνα 26γ]. Στο τέλος της επέμβασης παραμένει μέσα στον τόνο η ορχική αρτηρία, η αρτηρία του κρεμαστήρα, ο κρεμαστήρας μυς, τα λεμφαγγεία και ο πόρος με τα αγγεία του [Εικόνα 26δ]. Εικόνα 26α: Εντοπίζεται ο σπερματικός τόνος. Εικόνα 26β: Ο σπερματικός τόνος περιβάλλεται από ένα Penrose. Εικόνα 26γ: Απωλινώνοται και διατέμνονται οι έσω σπερματικές φλέβες και οι φλέβες του κρεμαστήρα. 95
96 Εικόνα 26δ: Στο τέλος της χειρουργικής επέμβασης παραμένουν, η ορχική αρτηρία, η αρτηρία του κρεμαστήρα, ο κρεμαστήρας μυς, τα λεμφαγγεία και ο πόρος με τα αγγεία του. Η τεχνική της μικροχειρουργικής υποβουβωνικής επέμβασης τροποποιήθηκε από τον Goldstein το 1992 σε μια προσπάθεια περαιτέρω μείωσης της συχνότητας της εμμένουσας-υποτροπιάζουσας κιρσοκήλης. Ο Goldstein θεώρησε ότι η παρασκευή και η έξοδος του όρχι στο χειρουργικό πεδίο για την αναζήτηση παράπλευρων φλεβικών δικτύων και η ανεύρεση και απολίνωση των φλεβών του οίακα θα συνέβαλλε στην μείωση των υποτροπών (Goldstein M et al., 1997). Γεγονός είναι ότι η έξοδος του όρχι από το όσχεο στο χειρουργικό πεδίο πέραν του ότι επιτρέπει την πρόσβαση στις φλέβες του οίακα, διευκολύνει την αναγνώριση των έξω σπερματικών φλεβών καθώς αυτές διαπερνούν το έδαφος του βουβωνικού πόρου (Beck EM et al., 1992). Κατά την τεχνική του Goldstein ο όρχις και τα περιβλήματα του παρασκευάζονται και ο όρχις εξέρχεται πριν την εισαγωγή του χειρουργικού μικροσκοπίου. Η περιοχή του οίακα επισκοπείται για διατεταμένες φλέβες που εξέρχονται από τους χιτώνες του όρχι. Οι φλέβες αυτές καυτηριάζονται ή απολινώνονται και ο όρχις επανατοποθετείται στο όσχεο. Ωστόσο η συμβολή του παράπλευρου δικτύου των φλεβών του οίακα στη συχνότητα μετεγχειρητικής υποτροπής και στη βελτίωση των παραμέτρων του σπέρματος δεν έχει σαφώς τεκμηριωθεί. Παρά το γεγονός ότι ο Goldstein et al αναφέρουν σημαντική ελάττωση της συχνότητας μετεγχειρητικής υδροκήλης και υποτροπής της κιρσοκήλης με την τεχνική 96
97 αυτή, δεν υπάρχουν μελέτες που να συγκρίνουν ευθέως την υποβουβωνική κιρσοκηλεκτομή με και χωρίς παρασκευή του όρχι (Goldstein M et al., 1997). Οι φλέβες αυτές που ανευρίσκονται στο 7% περίπου των περιπτώσεων, συνήθως απολινώνονται προφυλακτικά χωρίς να έχει αποδειχθεί υπερηχογραφικά ότι ευθύνονται για τις περιπτώσεις μετεγχειρητικής υποτροπής της κιρσοκήλης (Murray RR Jr et al., 1986). Η υποβουβωνική μικροχειρουργική τεχνική συνοδεύεται από σχεδόν μηδενικά ποσοστά μετεγχειρητικής υδροκήλης και τα χαμηλότερα συγκριτικά με τις άλλες τεχνικές ποσοστά ψηλαφητών υποτροπών (<1%) (Hoops CV et al., 2003; Marmar JL et al., 1994). Η λαπαροσκόπηση έχει θέση στη σύγχρονη αντιμετώπιση της κιρσοκήλης. Πλεονεκτήματα της λαπαροσκοπικής επέμβασης είναι η οπτική μεγέθυνση του χειρουργικού πεδίου που διευκολύνει την αναγνώριση των ανατομικών δομών, καθώς και η μικρότερη διάρκεια νοσηλείας και μετεγχειρητικού πόνου σε σχέση με την ανοικτή επέμβαση Palomo (Ulker V et al., 1997; Podkamenev VV et al., 2002). Η λαπαροσκοπική επέμβαση για κιρσοκήλη γίνεται με τον ασθενή υπό γενική νάρκωση και με διαπεριτοναϊκή προσπέλαση. Τα σπερματικά αγγεία αναγνωρίζονται και οι μεν φλέβες απολινώνονται και διατέμνονται, η δε αρτηρία διατηρείται. Ποσοστά επιτυχίας από 89% ως 100% έχουν αναφερθεί στην βιβλιογραφία με τη λαπαροσκοπική μέθοδο (Ulker V et al., 1997; Iselin CE et al., 1997; Diamond DA et al., 2009). Τα ποσοστά μετεγχειρητικής υδροκήλης που αναφέρονται μετά από λαπαροσκόπηση κυμαίνονται μεταξύ 3-8% και δεν διαφέρουν από το αντίστοιχα ποσοστά της επέμβασης κατά Palomo. Τα ποσοστά είναι υψηλά παρά το ότι η λαπαροσκόπηση προσφέρει το θεωρητικό πλεονέκτημα της καλύτερης ορατότητας για την αναγνώριση των λεμφαγγείων (Iselin CE et al., 1997; Itoh K et al., 2003; Riccabona M et al., 2003; Cayan S et Al., 2009). Με σκοπό τη μείωση της μετεγχειρητικής υδροκήλης έχουν προταθεί τεχνικές τροποποιήσεις της λαπαροσκοπικής μεθόδου καθώς επίσης και έγχυσης μπλε χρωστικής για την αποφυγή απολίνωσης των λεμφαγγείων, οι 97
98 οποίες συνοδεύτηκαν από ενθαρρυντικά αποτελέσματα (Podkamenev VV et al., 2002; Kocvara R et al., 2005; Barot P et al., 2004; Tan HL et al., 2004). Διαδερμικές τεχνικές Ορισμένοι ουρολόγοι, προτιμούν αντί μίας από τις επεμβατικές τεχνικές που περιγράφηκαν παραπάνω, τις διαδερμικές ακτινολογικές τεχνικές (διαδερμικός εμβολισμός, σκληροθεραπεία) οι οποίες σήμερα κατέχουν σημαντική θέση στην αντιμετώπιση της κιρσοκήλης (Lima SS et al., 1978). Στις τεχνικές αυτές προηγείται πάντοτε τοπική αναισθησία και φλεβογραφία με σκοπό την επιβεβαίωση της σωστής τοποθέτησης του καθετήρα. Ο διαδερμικός εμβολισμός συνήθως ενδείκνυται σε περιπτώσεις υποτροπιάζουσας ή εμμένουσας κιρσοκήλης ή σε περιπτώσεις κιρσοκήλης όπου απαιτείται ιδιαίτερη διερεύνηση της ανατομίας του φλεβικού δικτύου. Αφού τοποθετηθεί ο καθετήρας στην έσω σπερματική φλέβα γίνεται υπό ακτινοσκοπικό έλεγχο, παλίνδρομη έγχυση σκληρυντικών παραγόντων (Feneley MR et al., 1997). Η ανιούσα σκληροθεραπεία έχει περιγραφεί από τον Tauber. Εγχύεται σκιαγραφικό από την καθετηριασμένη διατεταμένη φλέβα και σκιαγραφείται η έσω σπερματική φλέβα και η εκβολή της στη νεφρική φλέβα. Στη συνέχεια ζητείται από τους ασθενείς να κάνουν τη δοκιμασία Valsalva και εγχύεται σκληρυντική ουσία στην έσω σπερματική φλέβα (Tauber R et al., 1994). Οι διαδερμικές τεχνικές συνοδεύονται από άμεση τεχνική επιτυχία με τεκμηριωμένη απόφραξη της φλέβας σε περισσότερες από το 80% των περιπτώσεων και από βελτίωση των παραμέτρων του σπέρματος παραπλήσια με αυτήν των ανοικτών χειρουργικών τεχνικών (Ficcara V et al., 2002; Nabi G et al., 2004). Υποτροπή της κιρσοκήλης ή αποτυχία του εμβολισμού ή της σκληροθεραπείας παρατηρείται στο 5-15% των περιπτώσεων και οι επιπλοκές κυμαίνονται μεταξύ 3-9% σύμφωνα με σχετικές μελέτες (Beutner S et al., 2007). 98
99 Μετεγχειρητική παρακολούθηση Η παρακολούθηση μετά από μετά από επέμβαση για κιρσοκήλη συνίσταται σε έλεγχο για την εμφάνιση υποτροπιάζουσας ή εμμένουσας κιρσοκήλης. Το αποτέλεσμα της επέμβασης πρέπει να ελέγχεται σε διάστημα όχι μικρότερο από 3 μήνες, ώστε να υποχωρήσει το μετεγχειρητικό στρες και να υπάρξει ολοκληρωμένη σπερματογένεση με τις νέες συνθήκες, δεδομένου ότι ο χρόνος που χρειάζεται ένα σπερματοζωάριο να μεταφερθεί από το αρχικό δίκτυο έως τη σπερματοδόχο λήκυθο διαρκεί 72 ημέρες (transit time). Βελτίωση παρατηρείται σε ποσοστό περίπου 80% (κυρίως βελτιώνεται η κινητικότητα και η μορφολογία των σπερματοζωαρίων), στασιμότητα στο 15% και υποτροπή στο 5% ενώ το μέσο ποσοστό κυήσεων σε 20 40%. Τα ποσοστά αυτά είναι ενδεικτικά και μπορεί να διαφοροποιηθούν ανάλογα με την ηλικία του άνδρα και τυχόν συνυπάρχουσες νοσηρές καταστάσεις (Hargreave TB, 1997). Αποτελέσματα της χειρουργικής αντιμετώπισης της κιρσοκήλης στην ανδρική υπογονιμότητα Επίδραση στα ποσοστά κύησης Η αναφορά του Tulloch το 1995 ήταν η πρώτη στην οποία η χειρουργική διόρθωση της κιρσοκήλης οδήγησε σε επιτυχημένη κύηση (Tulloch WS, 1955). Η αναφορά αυτή πυροδότησε το ενδιαφέρον στη μελέτη της επίδρασης της χειρουργικής επέμβασης της κιρσοκήλης στην ανδρική υπογονιμότητα σε μεγαλύτερες σειρές ασθενών (Charny CW, 1962). Οι πρώτες αναφορές εστίαζαν περισσότερο στη βελτίωση της ποιότητας του σπέρματος, μιας παραμέτρου που αποτελεί μόνο έμμεση ένδειξη γονιμότητας, και λιγότερο στο ποσοστό επίτευξης επιτυχημένων κυήσεων που αποτελεί αμεσότερο δείκτη βελτίωσης της γονιμοποιητικής ικανότητας. Επίσης, ένα δεύτερο μειονέκτημα στις αρχικές εκείνες σειρές ήταν ότι δεν περιελάμβαναν ομάδες ελέγχου. Η πλειονότητα των μελετών που δημοσιεύθηκαν τις δεκαετίες του 70 και 80, διαπίστωσαν θετική επίδραση της χειρουργικής θεραπείας της 99
100 κιρσοκήλης στη γονιμότητα, τόσο αναφορικά με τη βελτίωση των παραμέτρων του σπέρματος, όσο και με τα ποσοστά κυήσεων, με κάποιες από αυτές να περιλαμβάνουν και ομάδα ελέγχου (Newton R et al., 1980; Okuyama A et al., 1988; Bsat FA et al., 1988). Από την άλλη πλευρά υπήρχαν και μελέτες που συμπέραναν ότι η χειρουργική θεραπεία της κιρσοκήλης έχει μικρή ή και καμία επίδραση στην υπογονιμότητα (Rodriguez-Rigau LJ et al., 1978; Nilsson S et al., 1979; Baker HW et al., 1985; Vermeulen A et al., 1986; Breznik R et al., 1997). Κάποιες από τις μελέτες αυτές ωστόσο δέχτηκαν κριτική για τη μεθοδολογία τους και συγκεκριμένα για την έλλειψη τυχαιοποίησης και ομάδων ελέγχου και τον ανεπαρκή αριθμό ασθενών (Cozzolino DJ et al., 2001). Οι Pryor και Howards το 1987 σε μία ανασκόπηση της υπάρχουσας ως τότε βιβλιογραφίας κατέγραψαν βελτίωση του σπερμοδιαγράμματος στο 66% και ποσοστά εγκυμοσύνης 43% επί συνόλου 2466 υπογόνιμων ανδρών με κιρσοκήλη που υποβλήθησαν σε επέμβαση. Ωστόσο οι περισσότεροι από τις μελέτες που περιλήφθησαν στην ανασκόπηση δεν περιελάμβαναν ομάδα ελέγχου (Pryor JL et al., 1987). Σε μεταγενέστερη ανασκόπηση της βιβλιογραφίας, το 1994 ο Schlesinger δεν κατάφερε να καταλήξει σε συμπέρασμα για το αν η χειρουργική θεραπεία της κιρσοκήλης είναι αποτελεσματική στην αντιμετώπιση της ανδρικής υπογονιμότητας. Ο λόγος ήταν η σημαντική απόκλιση στα αποτελέσματα μεταξύ των δημοσιεύσεων που περιλήφθησαν στην ανασκόπηση. Οι συγγραφείς απέδωσαν την απόκλιση αυτή σε διαφορές μεταξύ των μελετών, στον τρόπο διάγνωσης και το μέγεθος της κιρσοκήλης, τις προεγχειρητικές παραμέτρους του σπέρματος και τη διάρκεια της υπογονιμότητας (Schlesinger MH et al., 1994). Η ανασκόπηση αυτή ωστόσο ανέδειξε για άλλη μία φορά το πρόβλημα της ετερογένειας μεταξύ των υφισταμένων κλινικών μελετών σχετικά με την αποτελεσματικότητα της χειρουργικής αντιμετώπισης της κιρσοκήλης. Πράγματι από μία πλειάδα μελετών πάνω στην κιρσοκήλη, υπάρχουν ελάχιστες καλά σχεδιασμένες προοπτικές τυχαιοποιημένες μελέτες υπογόνιμων 100
101 ανδρών με ψηλαφητές κιρσοκήλες, γόνιμες συντρόφους και την επιτυχημένη σύλληψη ως παράμετρο της μελέτης. Από τις μελέτες που συγκέντρωναν τέτοια χαρακτηριστικά, οι συχνότερα αναφερόμενες είναι αυτές των Nieschlag et al και Madgar et al. Οι Nieschlag et al σε σύνολο 125 υπογόνιμων ζευγαριών δεν διαπίστωσαν στατιστικά σημαντική διαφορά στις κυήσεις στην ομάδα των ανδρών που υποβλήθησαν σε χειρουργική επέμβαση ή αγγειογραφικό εμβολισμό της κιρσοκήλης έναντι της ομάδας ελέγχου (29% έναντι 25,4% αντίστοιχα) μετά από 1 χρόνο παρακολούθησης. Ωστόσο παρατηρήθηκε σημαντική βελτίωση στη ποιότητα του σπέρματος και στον όγκο του όρχι στην ομάδα ανδρών που υποβλήθησαν σε κάποια μορφή επέμβασης (Nieschlag E et al., 1998). Αντίθετα στη μελέτη των Madgar et al, τα ποσοστά επιτυχημένων κυήσεων σε 1 χρόνο παρακολούθησης ήταν 10% για την ομάδα ελέγχου έναντι του εντυπωσιακού 60% για την ομάδα των ανδρών που υποβλήθησαν σε επέμβαση κατά Palomo. Ακόμη στους άνδρες της ομάδας αυτής παρατηρήθηκε σημαντική βελτίωση στις παραμέτρους του σπέρματος, ενώ καμία βελτίωση δεν φάνηκε στους άνδρες της ομάδας ελέγχου μετά από 1 χρόνο παρακολούθησης (Madgar I et al., 1995). Παρά το γεγονός ότι η μελέτη αυτή δέχτηκε κριτική λόγω του ασυνήθιστα υψηλού ποσοστού κυήσεων, αποτέλεσε σημείο αναφοράς για τους υπερασπιστές της χειρουργικής θεραπείας της κιρσοκήλης στην αντιμετώπιση της ανδρικής υπογονιμότητας (Krause W et al., 2002). Λιγότερα θεαματικά, αν και σχεδόν διπλάσια ποσοστά κύησης (33% έναντι 16% στην ομαδά ελέγχου) σε υπογόνιμα ζευγάρια μετά από επέμβαση για κιρσοκήλη και μετά από παρακολούθηση αντίστοιχα αναφέρει η ανασκόπηση του Schlegel (Schlegel PN et al., 1997). Μία τυχαιοποιημένη προοπτική μελέτη από την Ολλανδία ήρθε να προσθέσει επιχειρήματα υπέρ της ευεργετικής επίδρασης της χειρουργικής επέμβασης της κιρσοκήλης στην πιθανότητα αυτόματης κύησης. Η μελέτη περιέλαβε 31 υπογόνιμους άνδρες με ψηλαφητή κιρσοκήλη που υποβλήθησαν σε χειρουργική απολίνωση των σπερματικών φλεβών και 30 υπογόνιμους 101
102 άνδρες με κιρσοκήλη ως ομάδα ελέγχου. Μέσα σε χρονικό διάστημα ενός έτους, κύηση επιτεύχθηκε στο 36% των ασθενών που χειρουργήθηκαν έναντι μόλις 9% των ανδρών της ομάδας ελέγχου (Dohle GR et al., 2003). Παραπλήσια ποσοστά αυτόματης (μη υποβοηθούμενης) κύησης της τάξης του 48% αναφέρονται σε μελέτη 159 ανδρών οι οποίοι υποβλήθησαν σε μικροχειρουργική υποβουβωνική επέμβαση για κιρσοκήλη. Οι ερευνητές εντόπισαν συσχέτιση μεταξύ του προεγχειρητικού αριθμού των σπερματοζωαρίων με τα ποσοστά αυτόματης κύησης θέτοντας ως προγνωστικό όριο για επιτυχημένη κύηση την συγκέντρωση περισσότερων από 5 εκατομμύρια σπερματοζωάρια ανά ml στο προεγχειρητικό σπερμοδιάγραμμα (Kamal KM et al., 2001). Σε ότι αφορά τη σύγκριση της αποτελεσματικότητας των χειρουργικών τεχνικών η μετά-ανάλυση 36 μελετών που δημοσιεύθηκαν μεταξύ 1980 και 2008 έδειξε σημαντικές διαφορές στα ποσοστά αυτόματης κύησης ως τελικό αποτέλεσμα. Η μικροχειρουργική τεχνική εμφανίζει τα υψηλότερα ποσοστά αυτόματης κύησης με 42%, ακολουθεί η προσπέλαση κατά Palomo με ποσοστά κύησης 37%, η μακροσκοπική βουβωνική τεχνική (Ivanissevich) με 36% και έπονται ο εμβολισμός με 33,2% και η λαπαροσκοπική με 30% (Cayan S et al., 2009). Επίδραση στις παραμέτρους του σπέρματος Οι διαταραχές της ποιότητας και της ποσότητας του σπέρματος συνοδεύουν τις περιπτώσεις ανδρικής υπογονιμότητας που σχετίζονται με την παρουσία της κιρσοκήλης. Οι παράμετροι του σπέρματος αποτελούν κατά συνέπεια και έναν μετρήσιμο δείκτη βελτίωσης της γονιμότητας σε ασθενείς που υποβάλλονται σε επέμβαση για κιρσοκήλη. Η απολίνωση των σπερματικών φλεβών συνοδεύεται από στατιστικά σημαντική βελτίωση όλων ή των περισσοτέρων από τις παραμέτρους του σπέρματος σε περισσότερα από τα 2/3 των ασθενών (Schlesinger MH et al., 1994; Su LM et al., 2001; Kamal KM et al., 2001; Nagler HM et al., 1997; Matkov TG et al., 2001). 102
103 Σε πρόσφατες μελέτες μετά από μικροχειρουργική απολίνωση των σπερματικών φλεβών διαπιστώθηκε στατιστικά σημαντική μετεγχειρητική αύξηση της πυκνότητας και της κινητικότητας του σπέρματος, βελτιωμένης μέχρι και κατά 120% των προεγχειρητικών τιμών σε ορισμένες μελέτες (Kamal KM et al., 2001; Cayan S et al., 1999; Kumar R et al., 2003; Baazeem A et al., 2009; Kondo Y et al., 2009; Hussein AF et al., 2006). Όπως έχει αναφερθεί η μειωμένη κινητικότητα αποτελεί μία από τις απαντούμενες διαταραχές του σπέρματος σε άνδρες με κιρσοκήλη. Η πλειονότητα των μελετών, με ελάχιστες εξαιρέσεις αναφέρουν στατιστικά σημαντική βελτίωση της κινητικότητας μετά την χειρουργική επέμβαση της κιρσοκήλης (Schlesinger MH et al., 1994; Seftel AD et al., 1997; Pierik FH et al., 1998). Θα περίμενε κανείς ότι η χειρουργική επέμβαση της κιρσοκήλης πέρα από τον αριθμό και την κινητικότητα, βελτιώνει και τη μορφολογία των σπερματοζωαρίων όπως αυτή καθορίζεται τόσο με τα κριτήρια του ΠΟΥ όσο και με τα κριτήρια του Kruger (Franken DR et al., 2000; Van Waart J et al., 2001). Ωστόσο παρά το γεγονός ότι τα κριτήρια που εισήγαγε ο Kruger είναι χρήσιμα μετά από εξωσωματική γονιμοποίηση (in vitro fertilization-ivf), δεν διαπιστώθηκε ομοιόμορφα σταθερή βελτίωση της κατά Kruger μορφολογίας των σπερματοζωαρίων στις μελέτες ανδρών με κιρσοκήλη μετά από χειρουργική επέμβαση (Seftel AD et al., 1997; Kruger TF et al., 1988; Vazquez-Levin MH et al., 1997; Schatte EC et al., 1998; Kibar Y et al., 2002). Επιπρόσθετα ενώ η βελτίωση της κινητικότητας έχει βρεθεί ότι αποτελεί προγνωστική επιτυχημένης κύησης, η μορφολογία των σπερματοζωαρίων κατά Kruger δεν φαίνεται να σχετίζεται με την πιθανότητα αυτόματης κύησης (Check JH et al., 1992). Προγνωστικές παράμετροι αποτελεσματικότητας της χειρουργικής επέμβασης για την κιρσοκήλη Η μη σταθερή αποτελεσματικότητα της χειρουργικής αντιμετώπισης της κιρσοκήλης, οδήγησε στη σκέψη να αναζητηθούν παράμετροι οι οποίες θα 103
104 μπορούσαν με σχετική ασφάλεια να προγνώσουν ποίοι από τους ασθενείς με κιρσοκήλη θα ωφεληθούν περισσότερο από τη χειρουργική επέμβαση αναφορικά με τις παραμέτρους του σπέρματος και τα ποσοστά κύησης. Τέτοιες προγνωστικές παράμετροι περιλαμβάνουν το είδος της χειρουργικής επέμβασης, την ηλικία, το μέγεθος της κιρσοκήλης, το βαθμό της παλινδρόμησης και το μέγεθος των όρχεων (Kondo Y et al., 2009; Ishikawa T et al., 2005). Η χειρουργική τεχνική αποτελεί έναν σημαντικό παράγοντα που επηρεάζει την επιτυχία της επέμβασης όπως έχει αποδειχθεί σε πρόσφατες συγκριτικές μελέτες. Οι Cayan et al το 2000 συνέκριναν την υψηλή απολίνωση των σπερματικών φλεβών με την μικροχειρουργική βουβωνική προσπέλαση σε ότι αφορά μεταξύ των άλλων την μεταβολή στις παραμέτρους του σπέρματος και τα ποσοστά κύησης. Η μικροχειρουργική τεχνική φάνηκε να υπερτερεί σημαντικά στη βελτίωση της κινητικότητας του σπέρματος, ενώ στις άλλες παραμέτρους δε διαπιστώθηκε στατιστικά σημαντική διαφορά (Cayan S et al., 2000). Υπάρχουν οι υποστηρικτές της άποψης ότι η ανταπόκριση στη χειρουργική θεραπεία της κιρσοκήλης σχετίζεται με το βαθμό της κιρσοκήλης με την έννοια ότι υπογόνιμοι άνδρες με μεγάλου βαθμού κιρσοκήλες και ποιοτικά επηρεασμένο σπέρμα φαίνεται να εμφανίζουν μεγαλύτερη μετεγχειρητική βελτίωση στον αριθμό και την κινητικότητα των σπερματοζωαρίων έναντι υπογόνιμων ανδρών με μέτριο και μικρό βαθμό κιρσοκήλη (Jarow JP et al., 1996; Steckel J et al., 1993). Εξαίρεση αποτελούν οι μεγάλες κιρσοκήλες οι οποίες έχουν ήδη οδηγήσει σε ορχική ατροφία με μείωση του μεγέθους του όρχι και σε μη αναστρέψιμη βλάβη της σπερματογένεσης (Uygur MC et al., 1999; Marks JL et al., 1986). Η αντίθετη άποψη, ότι η αποτελεσματικότητα της χειρουργικής επέμβασης δεν σχετίζεται με το μέγεθος της κιρσοκήλης, έχει αφετηρία την μελέτη-σταθμό των Dubin και Amelar το 1970 σύμφωνα με την οποία οι μικρές κιρσοκήλες μπορούν να έχουν εξίσου βλαπτική επίδραση στη σπερματογένεση όπως και οι κιρσοκήλες μεγάλου βαθμού (Dubin L et al., 104
105 1977). Η άποψη αυτή βρήκε αρκετούς υποστηρικτές οι οποίοι ανέδειξαν ότι το μέγεθος της κιρσοκήλης δεν έχει καμία επίδραση στα ποσοστά κύησης μετά από χειρουργική επέμβαση για κιρσοκήλη με αποτέλεσμα να ανοίξει η συζήτηση για τη χρησιμότητα της διόρθωσης και κατ επέκταση της διάγνωσης, των υποκλινικών κιρσοκηλών (McClure RD et al., 1986; Dhabuwala CB et al., 1992). Υπάρχουν ενδείξεις ότι η προεγχειρητική συγκέντρωση των σπερματοζωαρίων συνιστά σημαντικό προγνωστικό παράγοντα της επιτυχούς έκβασης της χειρουργικής θεραπείας της κιρσοκήλης. Η προεγχειρητική συγκέντρωση των σπερματοζωαρίων ως προγνωστικό παράγοντα επιτυχίας της επέμβασης για κιρσοκήλη μελετήθηκε για πρώτη φορά πριν 20 και πλέον χρόνια. Οι ερευνητές διαπίστωσαν σημαντική διαφορά στη μετεγχειρητική συγκέντρωση των σπερματοζωαρίων σε άνδρες με προεγχειρητική συγκέντρωση μεγαλύτερη από 10 εκατομμύρια/ml έναντι με λιγότερα από 10 εκατομμύρια/ml (Dubin L, 1977; Rodriguez-Rigau LJ et al., 1978). Πρόσφατες μελέτες από τους Kamal et al έδειξαν ότι οι άνδρες με πυκνότητα σπερματοζωαρίων άνω των 5 εκατομμυρίων/ml είχαν ποσοστά αυτόματης κύησης 61% έναντι μόνο 8-10% για άνδρες με πυκνότητα μικρότερη από την τιμή αυτή (Kamal KM et al., 2001). Οι ερευνητές λόγω της πολύ χαμηλής πιθανότητας κύησης συνέστησαν στους άνδρες της κατηγορίας αυτής την υποβοηθούμενη αναπαραγωγή ως καταλληλότερη της χειρουργικής επέμβασης θεραπευτική επιλογή. Η σύσταση για υπογόνιμα ζευγάρια όπου ο άνδρας έχει μέτρια προς ικανοποιητική πυκνότητα σπέρματος (>5 εκατομμύρια/ml) είναι η χειρουργική διόρθωση της κιρσοκήλης (Schlegel PN et al., 1997; Kamal KM et al., 2001). Αντίθετα, σε πρόσφατη μελέτη 97 υπογόνιμων ανδρών που υποβλήθηκαν σε μικροχειρουργική βουβωνική επέμβαση, ο βαθμός της κιρσοκήλης, το μέγεθος των όρχεων και η προεγχειρητική πυκνότητα του σπέρματος δεν αποδείχθηκαν σημαντικές παράμετροι. Η ανάλυση των παραμέτρων ανέδειξε ως προγνωστικούς παράγοντες μετεγχειρητικής 105
106 βελτίωσης του σπέρματος μόνο την παρουσία χαμηλής FSH και υψηλής τεστοστερόνης προεγχειρητικά (Kondo Y et al., 2009). Υπερηχογραφικά ευρήματα όπως η μέγιστη διάμετρος των φλεβών καθώς και η παρουσία και ο βαθμός της φλεβικής παλινδρόμησης, έχουν επίσης αποτελέσει αντικείμενα μελέτης ως προγνωστικοί παράγοντες επιτυχίας μετά από επέμβαση για κιρσοκήλη. Η παρουσία παλινδρόμησης καθώς και ο βαθμός αυτής, αναγνωρίζονται ως προγνωστικοί παράγοντες σε όλες τις μελέτες και συνδέονται με ανάλογη με το βαθμό της παλινδρόμησης βελτίωση της πυκνότητας και της κινητικότητας των σπερματοζωαρίων μετεγχειρητικά (Hussein AF, 2006; Schiff JD et al., 2006). Η διάμετρος των φλεβών αντίθετα δε συνιστά προγνωστικό δείκτη σε όλες τις μελέτες. Οι Hussein et al θέτοντας ως όριο τα 2,5mm φλεβικής διαμέτρου διαπίστωσαν μια οριακά στατιστικά σημαντική συσχέτιση με μεγαλύτερη βελτίωση στην μετεγχειρητική ποιότητα του σπέρματος, ενώ αντίθετα οι Schiff et al χρησιμοποιώντας ως όριο τα 3mm φλεβικής διαμέτρου δεν κατόρθωσαν να αποδείξουν την ύπαρξη στατιστικά σημαντικής συσχέτισης με την μετεγχειρητική βελτίωση των παραμέτρων του σπέρματος (Hussein AF, 2006; Schiff JD et al., 2006). Τέλος σε σχετική μελέτη των Donkol και Salem, ως προγνωστικοί παράμετροι επιτυχημένης επέμβασης για κιρσοκήλη αναγνωρίστηκαν η παρουσία φυσιολογικού όγκου όρχεων (>15ml), η παρουσία ψηλαφητής κιρσοκήλης και ο βαθμός της φλεβικής παλινδρόμησης ενώ η διάμετρος των φλεβών δεν θεωρήθηκαν σημαντικός παράγοντας (Donkol RH et al., 2007). Η κιρσοκήλη αποτελεί την πιο συχνά απαντούμενη κατάσταση στη διαγνωστική προσέγγιση του υπογόνιμου άνδρα. Η ύπαρξη συσχέτισης μεταξύ κιρσοκήλης και ανδρικής υπογονιμότητας έχει αποδειχθεί σε πλήθος μελετών. Επί δεκαετίες η έρευνα έχει επικεντρωθεί στη διερεύνηση της συσχέτισης αιτίου και αιτιατού μεταξύ της κιρσοκήλης και της ανδρικής υπογονιμότητας χωρίς ωστόσο να καταλήξει σε αδιαμφισβήτητα συμπεράσματα κυρίως λόγω της έντονης επίδρασης αδιευκρίνιστων παραγόντων. Η ποικιλομορφία στα αποτελέσματα της χειρουργικής αντιμετώπισης των υπογόνιμων ανδρών με κιρσοκήλη έχει οδηγήσει πολλούς στο να αμφισβητήσουν το κατά πόσο η 106
107 χειρουργική θεραπεία μιας διαγνωσμένης κιρσοκήλης έχει ένδειξη στη βελτίωση της γονιμότητας ενός ζεύγους, όμως το συμπέρασμα που προκύπτει μέσα από πλήθος σχετικών μελετών είναι η θετική επίδραση της χειρουργικής θεραπείας στην ποιότητα του σπέρματος. 107
108 ΕΝΔΟΘΗΛΙΝΗ ΙΣΤΟΡΙΚΗ ΑΝΑΔΡΟΜΗ Από τα τέλη της δεκαετίας του '80, είχε διαπιστωθεί ότι τα ενδοθηλιακά κύτταρα παράγουν ουσίες, οι οποίες επιδρούν στον αγγειακό τόνο. Μελέτες σε καλλιέργειες ενδοθηλιακών κυττάρων διαφόρων ειδών (μεταξύ των οποίων και ανθρώπινων), επιβεβαίωσαν την παραγωγή ουσιών που προκαλούν διαστολή, αλλά και άλλων που προκαλούν σύσπαση των αγγείων. Ο Yanagisawa και οι συνεργάτες του απέδειξαν ότι η αγγειοσυσπαστική δράση του ενδοθηλίου σχετίζεται κυρίως με το σχηματισμό ενός πεπτιδίου, στο οποίο δόθηκε μετά την απομόνωση του το όνομα ενδοθηλίνη, η οποία πρώτα αναγνωρίστηκε σε καλλιέργειες αορτικών ενδοθηλιακών κυττάρων χοίρου (Yanagisawa M et al., 1998). Ακολούθησαν μελέτες οι οποίες ανέδειξαν την ύπαρξη τεσσάρων ισομορφών ενδοθηλίνης (ΕΤ-1, ΕΤ-2, ΕΤ-3, ΕΤ-4), αποκάλυψαν τους μηχανισμούς βιοσύνθεσης και αποικοδόμησης των μορίων αυτών, καθώς και την εμπλοκή τους σε διάφορες παθολογικές καταστάσεις. Τέλος μελετήθηκε η αλληλεπίδραση των ενδοθηλινών με τους δύο εξειδικευμένους τύπους υποδοχέων της (ETA και ETB), καθώς και τα πειραματικά αποτελέσματα της χορήγησης τόσο in vitro όσο και in vivo εκλεκτικών και μη ανταγωνιστών τους. Στις 20 Νοεμβρίου 2001 o Αμερικανικός Οργανισμός Φαρμάκων (FDA) ενέκρινε για πρώτη φορά τη χορήγηση στον άνθρωπο ανταγωνιστή ΕΤ-1 με τη μορφή πόσιμων δισκίων, με το εμπορικό όνομα Tracleer (Actelion, Allschwill, Switzerland), γνωστό από τις πειραματικές μελέτες ως Bosentan, για τη θεραπεία της πνευμονικής αρτηριακής υπέρτασης. ΜΕΤΑΒΟΛΙΣΜΟΣ ΕΝΔΟΘΗΛΙΝΩΝ Οι ενδοθηλίνες, ΕΤ-1, ΕΤ-2, ΕΤ-3 και ΕΤ-4, είναι πεπτίδια 21 αμινοξέων τα οποία παράγονται από ποικιλία κυττάρων. Και τα τέσσερα μέλη της οικογένειας έχουν κοινό C-τελικό άκρο ενώ διαφέρουν στο N-τελικό τους άκρο. Στο Ν-τελικό άκρο υπάρχουν δύο δισουλφιδικές γέφυρες που 108
109 δημιουργούν στο μόριο μορφή αγκύλης. Σημειώνεται ότι η δομή του μορίου έχει σημαντικές ομοιότητες με την τοξίνη σαραφατοξίνη [Εικόνα 27].Οι διαφορές αυτές καταδεικνύουν και το διαφορετικό τρόπο σύνδεσης των ισομορφών της ενδοθηλίνης με τους υποδοχείς της. Κάθε μια από τις ισομορφές αυτές προκύπτει από τη διάσπαση σε δύο στάδια ενός πρόδρομου μορίου της prepro endothelin, η οποία είναι το προϊόν της έκφρασης του γονιδίου της ενδοθηλίνης. Εικόνα 27: Η δομή των τριών ισομορφών της ενδοθηλίνης και η ομοιότητα με τη δομή της σαραφατοξίνης. Με έντονο χρώμα φαίνονται οι διαφορές στην αμινοξική αλληλουχία μεταξύ των ισομορφών (Yanagisawa M, 1998). ΕΤ-1 Η ενδοθηλίνη-1 (ΕΤ-1) είναι το μόνο μέλος της οικογένειας που παράγεται από τα ενδοθηλιακά κύτταρα των αγγείων καθώς επίσης και από αγγειακά λεία μυϊκά κύτταρα, επιθηλιακά κύτταρα των βρόγχων και λεία μυϊκά 109
110 κύτταρα των βρόγχων. Η ΕΤ-1 δεν αποθηκεύεται σε εκκριτικά κοκκία μέσα στα ενδοθηλιακά κύτταρα και σημαντικοί ερεθιστικοί παράγοντες όπως η υποξία, η ισχαιμία, το stress προάγουν τη μετάφραση του mrna της ΕΤ-1 και τελικά τη σύνθεση και έκκριση της ΕΤ-1 σε διάστημα λεπτών. Ο χρόνος ημίσειας ζωής του mrna είναι περίπου 15-20min ενώ ο χρόνος ημίσειας ζωής της ΕΤ-1 στο πλάσμα είναι 4-7 min. Γι αυτό το λόγο τα αγγειακά κύτταρα μπορούν γρήγορα να προσαρμόζουν την παραγωγή της ΕΤ-1 όπως απαιτείται για την ρύθμιση του αγγειακού τόνου. Η ΕΤ-1 του πλάσματος καθαιρείται σε μεγαλύτερο ποσοστό (80-90%) από τους πνεύμονες. Όπως φαίνεται το 75% της έκκρισης της από καλλιεργηθέντα ενδοθηλιακά κύτταρα πηγαίνει προς τα λεία μυϊκά κύτταρα των αγγείων όπου δεσμεύεται σε ειδικούς υποδοχείς των μυϊκών κυττάρων και προκαλείται αγγειόσπασμος. Είναι απίθανο η δεσμευμένη αυτή ΕΤ- 1 να αντιστοιχεί στην συνολική ΕΤ-1 του πλάσματος. Γι αυτό η ΕΤ-1 θα πρέπει να θεωρείται περισσότερο σαν παρακρινική παρά σαν ενδοκρινική ορμόνη. Επίσης η ΕΤ-1 παράγεται από νευρώνες και αστροκύτταρα στο ΚΝΣ, ενδομητρικά κύτταρα, ηπατοκύτταρα, νεφρικά μεσαγγειακά κύτταρα, κύτταρα Sertoli και από τα επιθηλιακά κύτταρα του μαστού (Epstein HF et al., 1995; Spieker EL et al., 2003). ΕΤ-2, ΕΤ-3, ΕΤ-4 Η ΕΤ-2 παράγεται κυρίως από τους νεφρούς και το έντερο και λιγότερο από το μυοκάρδιο, τον πλακούντα και τη μήτρα. Η ΕΤ-3 κυκλοφορεί στο πλάσμα αλλά η πηγή της δεν είναι γνωστή. Έχει βρεθεί σε υψηλές συγκεντρώσεις στον εγκέφαλο και πιθανότατα ρυθμίζει σημαντικές λειτουργίες στους νευρώνες και τα αστροκύτταρα όπως τον πολλαπλασιασμό και την ανάπτυξη. Επίσης έχει βρεθεί στον γαστρεντερικό σωλήνα, στους πνεύμονες και στους νεφρούς. Η ΕΤ-4 κυκλοφορεί στο πλάσμα αλλά η πηγή της δεν είναι γνωστή (Kanyicksa B et al., 1991; McKay KO et al., 1993; Shinmi O et al., 1989). Όπως αναφέρθηκε υπάρχουν τέσσερα γνωστά πεπτίδια ενδοθηλίνης στα θηλαστικά, ΕΤ-1, ΕΤ-2, ΕΤ-3, ΕΤ-4. Εξ αυτών, οι ΕΤ-1, ΕΤ-2, ΕΤ-3 110
111 κωδικοποιούνται από τρία γονίδια στα χρωμοσώματα 6, 1 και 20 αντίστοιχα, τα οποία εντοπίζονται σε διαφορετικά χρωμοσώματα τόσο στον άνθρωπο όσο και στο χοίρο και τον επίμυ. Κάθε ένα από τα γονίδια αυτά κωδικοποιεί ένα πρόδρομο μόριο για κάθε μια από τις ισομορφές της ενδοθηλίνης. Τα πεπτίδια αυτά σχετίζονται στενά όσο αναφορά στη δομή και στις δράσεις τους με τις σαραφοτοξίνες, πεπτίδια που βρίσκονται στο δηλητήριο του φιδιού Atractaspis Εngaddensis (Masaki T et al., 1992). Συγκεκριμένα, στο ανθρώπινο γονιδίωμα το γονίδιο για την prepro endothelin-1 βρίσκεται στο χρωμόσωμα 6 (Bloch KD et al., 1989[i]), για την prepro endothelin-2 στο χρωμόσωμα 1 (Bloch KD et al., 1991) και για την prepro endothelin-3 στο χρωμόσωμα 20 (Bloch KD et al., 1989[ii]). Έκφραση του γονιδίου της ενδοθηλίνης, εκτός από το αγγειακό ενδοθήλιο, έχει διαπιστωθεί σε μια πλειάδα οργάνων όπως τον εγκέφαλο, το νωτιαίο μυελό, τον πνεύμονα, την καρδιά, τον νεφρό, το έντερο, τον οφθαλμό, την υπόφυση. Στα όργανα αυτά η ενδοθηλίνη φαίνεται να διαδραματίζει σημαντικό ρόλο τόσο στη φυσιολογική λειτουργία όσο και σε παθολογικές καταστάσεις (Simonson MS, 1993; Hunley TE et al., 2001). Το 5 -άμινο άκρο των γονιδίων αυτών έχει περιοχές όπου εξωτερικοί παράγοντες επιδρούν ρυθμίζοντας την έκφρασή τους είτε θετικά είτε αρνητικά (Benatti L et al., 1994). Έτσι υπάρχει θέση για τη σύνδεση μεταγραφικών παραγόντων όπως ο AP-1 και ο NF-1. Πιθανόν μέσω αυτών των παραγόντων επάγεται η σύνθεση ενδοθηλίνης από παράγοντες όπως ο TGF-β (NF-1) και η αγγειοτενσίνη ΙΙ (AP-1). Επαγωγή της σύνθεσης της ενδοθηλίνης προκαλείται και από άλλους παράγοντες όπως η ινσουλίνη, η αδρεναλίνη, η θρομβίνη, η προσταγλανδίνη F2α, κυτταροκίνες όπως η ιντερλευκίνη 1, αλλά και φυσικούς παράγοντες όπως η μηχανική πίεση και το οξειδωτικό stress. Επίσης η ίδια η ενδοθηλίνη προάγει τη σύνθεσή της δημιουργώντας ένα θετικό ανατροφοδοτικό μονοπάτι (Benatti L et al., 1994). Οι παραπάνω παράγοντες διεγείρουν την πρωτεϊνική κινάση C, που με τη σειρά της οδηγεί σε ενεργοποίηση των 111
112 πρωτοογκογονιδίων jun και fos και τη σύνδεσή τους στη θέση σύνδεσης για τον ΑΡ-1 (Lee ME et al., 1991). Αντίθετα, παράγοντες όπως η αγγειοτενσίνη ΙΙ, το νιτρικό οξείδιο (Boulanger C et al., 1990), οι κατεχολαμίνες (Kohno M et al., 1991), η ινσουλίνη (Yokokawa K et al., 1993) και το υψηλό διατμητικό shear stress (Malek AM et al., 1993) επιδρούν στην αύξηση της έκφρασης του γονιδίου. Οι ανωτέρω παράγοντες διεγείρουν τη γουανιλική κυκλάση με αποτέλεσμα την αύξηση της διαθεσιμότητας του ενδοκυτταρίου ασβεστίου, η οποία με τη σειρά της αυξάνει την έκφραση του γονιδίου της ενδοθηλίνης (Kuchan MJ et al., 1993). Επίσης ειδικές ρυθμιστικές περιοχές (AUUUA αλληλουχίες) υπάρχουν και στο 3 άκρο μέσω των οποίων προάγεται η διάσπαση του mrna των προδρόμων της ενδοθηλίνης, το οποίο έχει δειχθεί ότι έχει πολύ μικρό χρόνο ημιζωής (Epstein HF et al., 1995). Σύνθεση Μετα-μεταφραστικές τροποποιήσεις prepro-endothelin Το προϊόν της έκφρασης των γονιδίων αυτών είναι η prepro ET, ένα πεπτίδιο αποτελούμενο από 212 αμινοξέα. Από το πεπτίδιο αυτό προκύπτει, με πρωτεολυτική διάσπαση που συμβαίνει σε δύο στάδια, η ενδοθηλίνη των 21 αμινοξέων [Εικόνα 28]. 112
113 Εικόνα 28: Σχηματική παράσταση των μετα-μεταφραστικών τροποποιήσεων της prepro endothelin, ώστε να προκύψει η ενδοθηλίνη-1. Παρατηρούμε τα δύο στάδια πρωτεολυτικής διάσπασης [από ενδοπεπτιδάσες και από το μετατρεπτικό ένζυμο της ενδοθηλίνης (ECE)] (Yanagisawa M, 1998). Αρχικά το μόριο αυτό διασπάται σε δύο θέσεις από μία ενδοπεπτιδάση (πιθανότατα τη φουρίνη) ειδική για ζεύγος διβασικών αμινοξέων (Lys-Arg). Από τη διάσπαση προκύπτει ένα ενδιάμεσο πεπτίδιο 38 αμινοξέων με ελάχιστη βιολογική δράση (περίπου το 1% της συσπαστικής δράσης του ώριμου πεπτιδίου), η big ενδοθηλίνη [Εικόνα 29] (Jernigan S et al., 1999). 113
114 Εικόνα 29: Στερεοτακτική δομή της ενδοθηλίνης-1. Μετατρεπτικό ένζυμο της ενδοθηλίνης Η ελάχιστη βιολογική δράση του πεπτιδίου της μεγάλης (big) ενδοθηλίνης καθιστά την ενεργοποίησή του, μέσω διάσπασης από το μετατρεπτικό ένζυμο της ενδοθηλίνης (ECE: endothelin converting enzyme), βασική διαδικασία στο βιοσυνθετικό μονοπάτι των ενδοθηλινών [Εικόνα 30]. Τουλάχιστον τρεις διαφορετικές μορφές του ECE (ECE-1, ECE-2, ECE-3), μια για κάθε μορφή ενδοθηλίνης, έχουν απομονωθεί και αποτελούν ένζυμα που ανήκουν στην οικογένεια των μεταλλοπρωτεασών. Περιέχουν ψευδάργυρο και η δράση τους αναστέλλεται από τη φωσφοραμιδόνη, που αποτελεί έναν αναστολέα των ουδέτερων μεταλλοενδοπεπτιδασών (ΝΕΡ). Καταλύουν τη διάσπαση του πεπτιδικού δεσμού μεταξύ Trp21-Val22 στο καρβοξυτελικό άκρο της big ενδοθηλίνης με αποτέλεσμα την απελευθέρωση της ενεργούς ώριμης ενδοθηλίνης των 21 αμινοξέων [Εικόνα 28]. 114
115 Εικόνα 30: Σύνθεση και έκκριση Ενδοθηλίνης-1 Το ECE-1 είναι το πρώτο ένζυμο που απομονώθηκε και το καλύτερα μελετημένο. Το γονίδιο που το κωδικοποιεί εδράζεται στο χρωμόσωμα 1p36. Από το ίδιο γονίδιο προκύπτουν τουλάχιστον τέσσερις διαφορετικές ισομορφές του ενζύμου (ECE1a, 1b, 1c, 1d), με τη χρήση διαφορετικών εκκινητών ή διαφορετικών τρόπων εναλλακτικού ματίσματος (splicing) (Harris RC et al., 1996; Wolf G et al., 1993). Το ECE-1c είναι το επικρατέστερο και μαζί με το ECE-1a και 1d εντοπίζονται στην κυτταρική μεμβράνη, παίζοντας ρόλο στην ενεργοποίηση της κυκλοφορούσας big endothelin (Ruiz Ortega M et al., 1997). Αντίθετα το ECE-1b εντοπίζεται κυρίως ενδοκυττάρια στην περιοχή της συσκευής του Golgi, παίζοντας ρόλο στην ενεργοποίηση της ενδογενώς παραγόμενης big endothelin (Harris RC et al., 1996). Η ενδοθηλίνη δηλαδή εκκρίνεται από το κύτταρο είτε με την ενεργό μορφή των 21 αμινοξέων είτε με την ελάχιστα δραστική μορφή της big endothelin. Αν και δεν υπάρχουν μέχρι σήμερα πειραματικές ενδείξεις, είναι πιθανόν το ECE να αποτελεί στοιχείο ρύθμισης της τοπικής παραγωγής ενδοθηλίνης, καθορίζοντας το ποσοστό ενεργού ενζύμου που θα εκκριθεί από το κύτταρο, αλλά και το ρυθμό μετα-εκκριτικής ενεργοποίησης της κυκλοφορούσας 115
116 ανενεργούς big endothelin. Θα πρέπει να αναφερθεί ωστόσο ότι πιθανόν και άλλες πρωτεάσες συμμετέχουν στην ενεργοποίηση της ενδοθηλίνης, καθώς σε knock-out ποντίκια για το γονίδιο των ECE-1 και ECE-2 τα επίπεδα των ώριμων ΕΤ1 και ΕΤ2 δεν διέφεραν από τα φυσιολογικά. Έτσι δραστικότητα ECE παρουσιάζουν πρωτεάσες σερίνης, πρωτεάσες ασπαρτικού (πεψίνη, καθεψίνη D) και διαλυτές πρωτεάσες θειόλης (Wolf G et al., 1999). Αποδόμηση Οι ενδοθηλίνες αποικοδομούνται ταχύτατα μέσω της κυκλοφορίας από τους πνεύμονες, το ήπαρ και τους νεφρούς. Επιπρόσθετα της αγγειοδιασταλτικής του δραστικότητας, ο υποδοχέας ΕΤΒ δρα και ως παράγοντας κάθαρσης της κυκλοφορούσας ΕΤ 1. Ο χρόνος ημιζωής της ΕΤ 1 είναι περίπου 1 min, ενώ ο κύριος μηχανισμός αποδόμησης της ΕΤ 1 είναι μέσω των ΕΤΒ υποδοχέων οι οποίοι συνδέονται με την ενδοθηλίνη και ακολουθεί η ενδοκύττωση του συμπλόκου στο κυτταρόπλασμα με τελικό αποτέλεσμα την πέψη από ειδικά ένζυμα. Κατά συνέπεια, ελάττωση του αριθμού των ΕΤΒ υποδοχέων ή αναστολή αυτών έχει ως αποτέλεσμα την αύξηση των επιπέδων ΕΤ 1 στο πλάσμα χωρίς να αυξηθεί η παραγωγή αυτής (Wolf G et al., 1999; Aramori I et al., 1992). ΥΠΟΔΟΧΕΙΣ ΕΝΔΟΘΗΛΙΝΗΣ Καθώς η ενδοθηλίνη είναι υδρόφιλο μόριο και δε μπορεί να διαπεράσει την κυτταρική μεμβράνη, πρέπει να συνδεθεί με ειδικούς μεμβρανικούς υποδοχείς για να προκαλέσει τις δράσεις της στο κύτταρο. Έχουν αναγνωριστεί δύο υποδοχείς ενδοθηλίνης οι ΕΤΑ και οι ΕΤΒ (180, 181). Ανήκουν στην οικογένεια των συζευγμένων υποδοχέων με G πρωτεΐνες, που έχουν επτά διαμεμβρανικές έλικες. Οι ΕΤΑ κωδικοποιούνται στο χρωμόσωμα 4, περιέχουν 427 αμινοξέα και συνδέονται ισχυρά με την ΕΤ1 και την ΕΤ2 και ασθενέστερα με την ΕΤ3 [Εικόνα 31Α]. Οι ΕΤΒ κωδικοποιούνται στο 116
117 χρωμόσωμα 13, έχουν 442 αμινοξέα και παρουσιάζουν την ίδια συγγένεια για όλες τις ισομορφές της ενδοθηλίνης [Εικόνα 31Β]. Εικόνα 31Α: Η δομή του υποδοχέα τύπου Α της ενδοθηλίνης (ΕΤΑ receptor) (Arai H, 1990) Εικόνα 31Β: Σχηματική αναπαράσταση του υποδοχέα τύπου Β της ενδοθηλίνης (ΕΤΒ receptor). Επίσης και στις δύο εικόνες διακρίνονται οι επτά διαμεμβρανικές έλικες του μορίου των υποδοχέων (Sakurai T, 1990). Και οι τέσσερις ενδοθηλίνες συνδέονται σε δύο τύπους υποδοχέων (Α και Β) στα κύτταρα των περισσοτέρων ειδών, συμπεριλαμβανομένου και του ανθρώπου. Σύμφωνα με αυτοραδιογραφικές μελέτες που έχουν γίνει στις 117
118 λείες μυϊκές ίνες των αεραγωγών, συχνά συνυπάρχουν οι υποδοχείς τύπου Α και τύπου Β αλλά σε διαφορετικές αναλογίες. Οι υποδοχείς είναι μέλη της υπεροικογένειας των υποδοχέων (Aramori I et al., 1992) οι οποίοι συνδέονται με guanine-nucleotide-binding (G) proteins (Simonson MS et al., 1993) και έχουν μέγεθος από έως daltons στους σημαντικότερους ιστούς. Η δομή των αμινοξέων των δύο ειδών υποδοχέων είναι κατά 50% όμοια. Οι υποδοχείς τύπου Α της ενδοθηλίνης έχουν δέκα φορές μεγαλύτερη συνδετική ικανότητα για την ΕΤ-1 από ότι για την ΕΤ-3 και εκφράζονται σε πολύ μεγάλο βαθμό στα αγγειακά λεία μυϊκά κύτταρα, στο ενδοθήλιο των αγγείων, στα καρδιακά μυοκύτταρα, κατά μήκος του αναπνευστικού συστήματος και στα νεφρικά αγγεία. Αυτοί οι υποδοχείς μεσολαβούν στην αγγειοσυσπαστική δράση της ΕΤ-1. Συνοπτικά, η αγγειοσύσπαση συνδέεται με την ικανότητα των υποδοχέων, που είναι συνδεδεμένοι με την ενδοθηλίνη, να ενεργοποιούν την φωσφολιπάση - C η οποία οδηγεί στον σχηματισμό της 1, 4, 5 τριφωσφορικής ινοσιτόλης και της διακυλογλυκερόλης. Οι σχηματισμοί αυτοί αυξάνουν την συγκέντρωση του ενδοκυτταρίου Ca ++, το οποίο με τη σειρά του προκαλεί την αγγειοσύσπαση. Η αγγειοσύσπαση συμβαίνει αφού η ΕΤ-1 αποδεσμευτεί από τον υποδοχέα, πιθανότατα επειδή η συγκέντρωση του ενδοκυτταρίου Ca ++ αυξάνεται. Το ΝΟ βραχύνει την διάρκεια της αγγειοσύσπασης ενεργοποιώντας την επιστροφή του ενδοκυτταρίου Ca ++ στις βασικές του συγκεντρώσεις. Η διακυλογλυκερόλη και το Ca ++ ενεργοποιούν την πρωτεινική κινάση C, η οποία είναι μεσολαβητής της μιτογόνου δράσεως της ΕΤ-1 [Εικόνα 32]. Οι υποδοχείς ενδοθηλίνης τύπου Β εκφράζονται κυρίως στα ενδοθηλιακά κύτταρα, στα λεία μυϊκά κύτταρα των βρόγχων, στα αθροιστικά σωληνάρια των νεφρών και σε μικρότερο βαθμό στα αγγειακά λεία μυϊκά κύτταρα. Συνδέονται με την ΕΤ-1 και την ΕΤ-3 με απλή σύνδεση και μεσολαβούν στον αγγειακό πολλαπλασιασμό, στην κάθαρση της ΕΤ-1 από τους πνεύμονες, στην επαναρρόφηση H 2 O, Na + και στην αγγειοδιαστολή. Επιπλέον, μπορούν να μεσολαβήσουν στην δραστηριοποίηση άλλων πεπτιδίων. Τα αποτελέσματα αυτής της δραστηριοποίησης των υποδοχέων 118
119 τύπου Β είναι όμοια με αυτά των υποδοχέων τύπου Α στην ενεργοποίηση της δραστηριότητας της φωσφολιπάσης-c, στην δημιουργία της 1, 4, 5 τριφωσφορικής ινοσιτόλης και διακυλογλυκερόλης και κινητοποίησης του Ca ++. Οι υποδοχείς τύπου Β σχετίζονται με ανασταλτικές G-πρωτείνες οι οποίες σε μερικά κύτταρα οδηγούν στην καταστολή της παραγωγής του c- AMP και στη δραστηριοποίηση της αντλίας Να + -Η +. Η σύνδεση της ΕΤ-3 στους υποδοχείς τύπου Β μπορεί να οδηγήσει σε αγγειοδιαστολή η οποία οφείλεται στην αυξημένη παραγωγή ΝΟ και προστακυκλίνης, καθώς και στη δραστηριοποίηση των διαύλων Κ +. Αξίζει να σημειωθεί ότι η δραστηριοποίηση των υποδοχέων Β από την ΕΤ-3 είναι κριτικής σημασίας για την φυσιολογική ανάπτυξη των κυττάρων που προέρχονται από πρόδρομα νευρικά κύτταρα (Aramori I et al., 1992; Simonson MS et al., 1993). Εικόνα 32: Σύνδεση ενδοθηλίνης ΕΤ-1 με υποδοχέα τύπου Α ΕΤΑ. Η δέσμευση των ενδοθηλινών στους υποδοχείς τους είναι πολύ ισχυρή και η απομάκρυνση τους από αυτούς πραγματοποιείται με αργό ρυθμό. Η αλληλεπίδραση της ΕΤ-1 με τους υποδοχείς της είναι αξιοσημείωτη στο ότι 119
120 παρουσιάζει ασυνήθιστα μακράς διάρκειας βιολογική δράση. Αυτό σχετίζεται με την σχεδόν μη αντιστρεπτή δέσμευση του πεπτιδίου σε ένα υποδοχέα. Η ΕΤ-1 μπορεί να μείνει μέχρι και 2 ώρες δεσμευμένη στον ΕΤΑ, μετά την ενδοκύττωση, υποδηλώνοντας ότι το πεπτίδιο συνεχίζει να ενεργοποιεί την μεταγωγή του σήματος για αρκετό χρόνο μετά την εισαγωγή του στο κύτταρο, με αποτέλεσμα να διαρκεί περισσότερο η ενεργοποίηση του δευτερεύοντος μηνύματος (cgmp) (Chun M et al., 1995). Τα χαρακτηριστικά αυτά της αλληλεπίδρασης ΕΤ-1 / ΕΤΑ έδωσαν εναύσματα για τη μελέτη ανταγωνιστών της ΕΤ-1. Έτσι, έχουν μελετηθεί αρκετοί ανταγωνιστές της ΕΤ- 1. Οι πιο σημαντικοί ανταγωνιστές που έχουν μελετηθεί σε μεγάλη ένταση είναι αυτοί οι οποίοι είναι ενεργοί και λαμβάνονται από το στόμα [Πίνακας 3]. Η βιολογική δράση των ενδοθηλινών εξαρτάται από τον αριθμό και το είδος των υποδοχέων μεταξύ των διαφόρων ιστών και κυττάρων. Ο αριθμός των υποδοχέων μπορεί να τροποποιηθεί ανάλογα με το είδος του υποδοχέα και του μορίου ενεργοποίησης. Η επίδραση πολλών ενδογενών ουσιών αλλά και φαρμακευτικών σκευασμάτων στο σύστημα των ενδοθηλινών είναι αποτέλεσμα των μεταβολών στην έκφραση ή/και στην ενεργοποίηση του ενός ή/και των δύο ειδών των υποδοχέων ενδοθηλίνης. Έτσι π.χ. έχει αποδειχτεί ότι η κυκλοσπορίνη δεν επηρεάζει τη συγκέντρωση του ΕΤΑ στα μεσαγγειακά κύτταρα του σπειράματος, αλλά αυξάνει την συγκέντρωση των ΕΤΒ (Iwasaki S et al., 1994). Το γεγονός αυτό αναμένεται να είναι λειτουργικά σημαντικό, αφού οι υποδοχείς ΕΤΒ φαίνεται ότι σχετίζονται με την ενεργοποίηση της σύνθεσης ΕΤ-1. Ανταγωνιστής Υποδοχέας δράσης Bosentan Α και Β SB Α και Β BQ 132 Α BMS Α PD Α Πίνακας 3: Ανταγωνιστές ενδοθηλίνης, ενεργοί με χορήγηση από το στόμα 120
121 Κατανομή υποδοχέων ΕΤΑ και ΕΤΒ Η κατανομή των υποδοχέων των ενδοθηλινών είναι εκτεταμένη και παράλληλη με την παραγωγή ενδοθηλινών στους διάφορους ιστούς. Όλοι οι ιστοί που παράγουν ενδοθηλίνη εκφράζουν και τους υποδοχείς της, καθώς φαίνεται ότι η ενδοθηλίνη έχει αυτοκρινή και παρακρινή και όχι ενδοκρινή δράση. Θέσεις σύνδεσης της ενδοθηλίνης έχουν αναγνωρισθεί εκτός από το τοίχωμα των αγγείων, στον πνεύμονα, την καρδιά, τον εγκέφαλο και το νεφρό. Έτσι, στο αγγειακό τοίχωμα, τα ενδοθηλιακά κύτταρα εκφράζουν κυρίως Β υποδοχείς ενώ τα λεία μυϊκά κύτταρα, τόσο στα διάφορα είδη ζώων όσο και στον άνθρωπο, εκφράζουν τόσο Α όσο και Β υποδοχείς. Στους κόλπους της καρδιάς επικρατούν οι Α υποδοχείς αν και αναγνωρίζονται και Β σε μικρότερο βαθμό. Ο υποδοχέας ΕΤΒ κυριαρχεί στην αορτή στον εγκέφαλο και στους πνεύμονες. Στον εγκέφαλο οι κύρια αναγνωριζόμενοι υποδοχείς είναι οι Β. Η σχέση ΕΤΑ/ΕΤΒ στο νεφρό φαίνεται ότι διαφέρει ανάλογα με το είδος και έτσι στον επίμυ υπάρχει ισορροπία στην έκφραση των δύο υποδοχέων ενώ στον άνθρωπο επικρατούν οι Β υποδοχείς (Benigni A et al., 1999). Μελέτες δέσμευσης με παράλληλη χρήση ανταγωνιστών της ΕΤ-1 με μεθόδους αυτοραδιογραφίας και ανοσοϊστοχημείας απέδειξαν ότι έκφραση της ΕΤ-1 και των υποδοχέων Α και Β εντοπίζεται κυρίως στα Sertoil και Leydig κύτταρα (Ergün S et al., 1999) των σπερματικών σωληναρίων, που είναι ανήκουν στο πεδίο της μελέτης μας. Οι υποδοχείς ΕΤΑ προκαλούν αγγειοσύσπαση, κυτταρικό πολλαπλασιασμό και εναπόθεση εξωκυττάριας ουσίας. Τα αποτελέσματα της δράσης των ΕΤΒ υποδοχέων δεν έχουν πλήρως διευκρινιστεί. Γενικότερα σε μερικούς ιστούς ορισμένων ειδών έχει αποδειχτεί ότι έχουν αγγειοσυσπαστική και υπερπλαστική δράση. Εντούτοις, στα ενδοθηλιακά κύτταρα οι ΕΤΒ συμμετέχουν στην απελευθέρωση προσταγλανδινών (PGI2) και μονοξειδίου του αζώτου (NO), τα οποία αντισταθμίζουν την αγγειοσύσπαση και τη μιτογενετική δράση της ΕΤ-1 μέσω των υποδοχέων ΕΤΑ [Εικόνα 33]. Οι υποδοχείς ΕΤΒ επιδρούν επίσης στην σύνθεση της ΕΤ-1, η οποία στη συνέχεια αλληλεπιδρά τόσο με τους ΕΤΑ όσο 121
122 και με τους ΕΤΒ. Το τελικό αποτέλεσμα εξαρτάται από το είδος και τη συγκέντρωση των δύο υποδοχέων στον κάθε ιστό (Iwasaki S et al., 1995 [i]). Όλες οι παραπάνω παρατηρήσεις είναι πολύ σημαντικές για το σχεδιασμό της χρήσης ανταγωνιστών ΕΤ-1 για θεραπευτικούς σκοπούς. Αρκετοί ερευνητές έχουν αντιρρήσεις όσον αφορά τη χρήση ανταγωνιστών που δεσμεύονται και στα δύο είδη υποδοχέων και προτείνουν τη χρήση ανταγωνιστών με εκλεκτική δράση και ανάλογα με το είδος της νόσου. Το σκεπτικό τους είναι ότι επιλεκτική μείωση της αγγειοσύσπασης, που προκαλείται από τους ΕΤΑ υποδοχείς μπορεί να επιτρέψει διέγερση της παραγωγής ουσιών, που προκαλούν αγγειοδιαστολή μέσω των υποδοχέων ΕΤΒ (Kohan DE et al., 1997). Εικόνα 33: ET-1 στο αγγειακό τοίχωμα. Οι περισσότεροι παράγοντες διεγείρουν ή αναστέλλουν την σύνθεση ΕΤ-1 στα ενδοθηλιακά κύτταρα μέσω ενεργοποίησης της πρωτεϊνικής κινάσης C (PKC) ή του cgmp/νο. Η ενδοθηλίνη-1 αυτοπεριορίζει η ίδια τις δράσεις της μέσω διέγερσης των ΕΤΒ υποδοχέων της, επάγοντας έτσι την παραγωγή ΝΟ και προστακυκλίνης (ΡGI2). [PLC: φωσφολιπάση C, ΕΑ: ενδοπλασματικό δίκτυο, PLA2: φωσφολιπάση Α2, IΡ3: τριφωσφορική ινοσιτόλη] 122
123 Σηματοδοτικό μονοπάτι της Ενδοθηλίνης - Ενδοκυττάρια μεταγωγή σήματος μετά τη σύνδεση της ενδοθηλίνης με τους υποδοχείς της Μετά τη σύνδεση της ενδοθηλίνης με τον υποδοχέα προκαλούνται δευτερογενή μηνύματα που οδηγούν στη βιολογική έκφραση της ενδοθηλίνης (Nord EP et al., 1996). Δεν υπάρχει πλήρης επιστημονική συμφωνία για το ποια μονοπάτια ενεργοποιούνται και για τις διαφορές μεταξύ των μηνυμάτων που προκαλούνται από τη σύνδεση με διαφορετικό υποδοχέα. Φαίνεται ωστόσο ότι το κύριο μονοπάτι που ενεργοποιείται μετά τη σύνδεση της ενδοθηλίνης είναι η ενεργοποίηση της φωσφολιπάσης C [Εικόνα 34], που οδηγεί στην υδρόλυση της φωσφατίδυλο-ινοσιτόλης σε διάκυλο-γλυκερόλη (DAG) και τριφωσφορική ινοσιτόλη (IP3). Εικόνα 34: Ενδοκυττάρια μονοπάτια μεταγωγής σήματος μετά τη διέγερση διαμεμβρανικών υποδοχέων με τη δομή των υποδοχέων της ενδοθηλίνης (7 διαμεμβρανικές έλικες) που συνδέονται με G πρωτεϊνες (αριστερή πλευρά του σχήματος) και διαφορές με τους υποδοχείς με δομή κινασών τυροσίνης. 123
124 Η ΙΡ3 προκαλεί άμεση αύξηση του ασβεστίου μέσω κινητοποίησης των ενδοκυττάριων αποθεμάτων του ενδοπλασματικού δικτύου. Επίσης μέσω GTP binding πρωτεϊνών ανοίγουν κανάλια ασβεστίου οδηγώντας σε παρατεταμένη αύξηση του ενδοκυττάριου ασβεστίου. Ένα δεύτερο ενδοκυττάριο μήνυμα μεσολαβείται από την ενεργοποίηση της πρωτεϊνικής κινάσης C, τόσο από τη DAG όσο και από την ενεργοποιημένη από τη ΕΤ φωσφολιπάση D. Θα πρέπει να αναφέρουμε πως η ενεργοποίηση των ET-A και ET-B υποδοχέων, έχει ως αποτέλεσμα την φωσφορυλίωση των ERK1/2. Οι ERK1/2 που ονομάζονται και p44/42 MAPKs (mitogen-activated protein kinases) είναι κινάσες οι οποίες σχετίζονται άμεσα και επιδρούν στη συστολή των λείων μυϊκών κυττάρων των αγγείων. Δραστηριοποιούνται ως ρυθμιστές στον κυτταρικό πολλαπλασιασμό, στη μετανάστευση, στη διαφοροποίηση και στη συστολή των λείων μυϊκών κυττάρων των αγγείων. Η ενδοθηλίνη ενεργοποιεί επίσης τη φωσφολιπάση Α2, αυξάνοντας τους μεταβολίτες του αραχιδονικού οξέος (προσταγλανδίνες, προστακυκλίνη, θρομβοξάνη). Η ενεργοποίηση αυτή γίνεται είτε άμεσα, από τις συνδεόμενες με τον υποδοχέα G πρωτεΐνες, είτε έμμεσα από το αυξημένο ενδοκυττάριο ασβέστιο. Η σύνδεση της ενδοθηλίνης με τους Α υποδοχείς επάγει τη σύνθεση c- AMP [Εικόνα 34], ενώ η σύνδεσή της με τους Β υποδοχείς επάγει την προκαλούμενη από το νιτρικό οξείδιο αύξηση του c- GMP, μέσω διέγερσης της γουανιλικής κυκλάσης (Goligoski MS et al., 1994). Επίσης, συμμετέχει στη διαδικασία κάθαρσης της κυκλοφορούσας ενδοθηλίνης (Fukuroda T et al., 1994), αλλά και στην αυτοεπαγωγή της σύνθεσής της (Iwasaki S et al., 1995 [ii]). Η σύνδεση της ενδοθηλίνης με διαφορετικό υποδοχέα και σε διαφορετικό κυτταρικό τύπο προκαλεί και διαφορετική βιολογική δράση πιθανότατα μέσω ενεργοποίησης διαφορετικών δευτερογενών μηνυμάτων. Αν και το θέμα αυτό δεν έχει διευκρινιστεί πλήρως όπως αναφέραμε, φαίνεται ότι μέσω της σύνδεσης με τους Α υποδοχείς η ενδοθηλίνη προκαλεί σύσπαση των λείων μυϊκών ινών των αγγείων οδηγώντας σε αγγειοσύσπαση, ενώ μέσω των 124
125 Β υποδοχέων των ενδοθηλιακών κυττάρων απελευθερώνεται νιτρικό οξείδιο οδηγώντας σε αγγειοδιαστολή (Hunley TE et al., 2001) [Εικόνα 35]. Εικόνα 35: Ενδοκυττάρια σήματα και δράσεις της ενδοθηλίνης μετά τη σύνδεση με τους υποδοχείς της σε ενδοθηλιακά και λεία μυϊκά κύτταρα. Οι Α υποδοχείς εκφράζονται κατά κύριο λόγο στα λεία μυϊκά κύτταρα και η διέγερσή τους οδηγεί σε αγγειοσύσπαση. Σε αγγειοσύσπαση οδηγεί και η διέγερση των Β υποδοχέων όταν αυτοί εκφράζονται στα ίδια κύτταρα. Αντίθετα τα ενδοθηλιακά κύτταρα εκφράζουν μόνο Β υποδοχείς και η σύνδεση της ενδοθηλίνης με αυτούς οδηγεί σε αγγειοδιαστολή, μέσω απελευθέρωσης νιτρικού οξειδίου και προστακυκλίνης (PGI2). Στη συνέχεια παραθέτουμε μια συνοπτική σχηματική απεικόνιση [Εικόνα 36] του σηματοδοτικού μονοπατιού της ενδοθηλίνης. Η βασική πληροφορία σε αυτήν την εικόνα είναι ότι η ενδοθηλίνη, συνδεόμενη με τους υποδοχείς ΕΤΑ και ΕΤΒ, οδηγεί στην ενεργοποίηση των ΜΑΡ Κινασών. Αυτοί με τη σειρά τους προκαλούν κυτταρικό πολλαπλασιασμό, μετανάστευση νεοδημιουργημέων κυττάρων, διαφοροποίηση και συστολή των λείων μυϊκών κυττάρων των αγγείων. 125
126 Εικόνα 36: Σχηματική απεικόνιση της σύνδεσης του μορίου της ενδοθηλίνης με τους υποδοχείς ΕΤΑ και ΕΤΒ. Επίσης παρουσιάζονται τα σηματοδοτικά μονοπάτια που ακολουθούνται και τα μηνύματα που παράγονται στα λεία μυϊκά κύτταρα (Clozel M, 2003). 126
127 Βιολογική δράση της Ενδοθηλίνης - Δράση της Ενδοθηλίνης στα αγγεία Η κύρια δράση των ενδοθηλινών στα αγγεία είναι μια προσωρινή αγγειοδιαστολή, που ακολουθείται από μια παρατεταμένη αγγειοσύσπαση (Kiowski W et al., 1991). Η δράση της ενδοθηλίνης στα λεία μυϊκά κύτταρα των αγγείων ξεκινάει με την δέσμευση της σε ένα υποδοχέα ΕΤ, συζευγμένου με μια πρωτεΐνη G, μέσω της οποίας ενεργοποιείται η φωσφολιπάση C, που με τη σειρά της υδρολύει την φωσφατιδυλoϊνοσιτόλη σε τριφωσφορική ινοσιτόλη (IP3) και διακυλογλυκερόλη (DAG). Η IP3 προκαλεί ταχεία, μικρής διάρκειας (sec), κινητοποίηση του ενδοκυττάριου Ca2+, ανεξάρτητα από το εξωκυττάριο Ca2+ και στη συνέχεια διάνοιξη των διαύλων Ca2+ με αποτέλεσμα την εισροή ιόντων μέσα στο κύτταρο. Η ενδοθηλίνη όχι μόνο ενεργοποιεί διάφορα κανάλια ιόντων της κυτταρικής μεμβράνης, αλλά επιμηκύνει το χρόνο, που αυτά μένουν ανοικτά (Nord EP, 1996; Simonson MS et al., 1990). Η καθυστερημένη αυτή δράση της ΕΤ-1 προκαλεί μια χρονικά παρατεταμένη (min) αύξηση της μετακίνησης ιόντων Ca2+ και κατά συνέπεια διατήρηση αυξημένων ενδοκυττάριων συγκεντρώσεων για μεγαλύτερο χρονικό διάστημα, προκαλώντας μια αντίστοιχα παρατεταμένη σε διάρκεια κυτταρική σύσπαση. Ο μηχανισμός αυτός δράσης του πεπτιδίου εξηγεί γιατί οι ανταγωνιστές διαύλων Ca2+ (drugs blocking voltage-dependent calcium channels) αμβλύνουν έστω μερικά την αγγειοσύσπαση που προκαλείται από την ΕΤ-1 τόσο σε πειραματικά μοντέλα (Montanes I et al., 1994; Takenaka T et al., 1993; Takahashi K et al., 1993) όσο και στον άνθρωπο (Rabelinsk TJ et al., 1994; Kaasjager KAH et al., 1995). Με παρόμοιο τρόπο μέσω μιας πρωτεΐνης G, μπορεί να ενεργοποιηθεί στο ενδοθήλιο και η φωσφολιπάση Α2 που αυξάνει τους μεταβολίτες του αραχιδονικού οξέως οι οποίοι επάγουν την παραγωγή λευκοτριενών, προστακυκλίνης και θρομβοξάνης Α2. Οι παραπάνω μηχανισμοί διέγερσης στο επίπεδο της πρωτεΐνης G σχετίζονται με την ενεργοποίηση της γουανυλικής κυκλάσης (ένζυμο που υδρολύει το GTP σε cgmp) (Kohan DE et al., 1994). Η ενεργοποίηση του ΕΤΒ υποδοχέα διεγείρει/ενισχύει στο ενδοθηλιακό κύτταρο 127
128 την σύνθεση ΝΟ, που με τη σειρά του άμεσα ή/και μέσω cgmp αναστέλλει την παραγωγή της ΕΤ-1. Κατ αναλογία η αυξημένη σύνθεση ΝΟ μετά από ενεργοποίηση του ΕΤΒ υποδοχέα οδηγεί στα λεία μυϊκά κύτταρα των αγγείων, συμπεριλαμβανομένων και αυτών των σπειραμάτων, σε αντίστοιχη αύξηση της παραγωγής cgmp μέσω διέγερσης της γουανυλικής κυκλάσης. Η διέγερση παραγωγής ΝΟ/cGMP από την ΕΤ-1, είναι καθοριστική για το τελικό αποτέλεσμα της δράσης της ΕΤ στην αγγειοσύσπαση και στην μιτογένεση, αφού το ΝΟ είναι ένας από τους παράγοντες, που διευκολύνει την αποδέσμευση της ΕΤ από τους υποδοχείς της καθορίζοντας άμεσα τη δράση της [Εικόνα 37] (Goligoski MS et al., 1994). Εικόνα 37: Δράσεις της ενδοθηλίνης στο αγγειακό σύστημα μετά από τη δέσμευσή της στος υποδοχείς τύπου Α (ΕΤΑ) και τύπου (Β ΕΤΒ). Η χορήγηση εκλεκτικών αναστολέων των ETA υποδοχέων σε υγιείς ενήλικες προκαλεί αγγειοδιαστολή και πτώση της αρτηριακής πίεσης, ενώ η χορήγηση εκλεκτικών ETB υποδοχέων αγγειοσύσπαση και αύξηση της αρτηριακής πίεσης (Verhaar MC et al., 1998; Spratt JCS et al., 2001; Strachan FE et al., 1999). Αυτό δείχνει ότι η ΕΤ 1 συμμετέχει μέσω των ETA 128
129 υποδοχέων στη διατήρηση του αγγειακού τόνου και αρτηριακής πίεσης. Η μιτογόνος δραστικότητα της ΕΤ 1 είναι επίσης επιβεβαιωμένη σε πληθώρα πειραμάτων. Ο μηχανισμός αυτής της δράσης περιλαμβάνει την επαγωγή της έκφρασης διαφόρων πρωτοογκογονιδίων, όπως τα c fos, c myc και c jun, του VL 30 και του συμπλέγματος proto oncogene/activator protein I, την ενεργοποίηση διαφόρων αυξητικών παραγόντων όπως οι PDGF, EGF, TGF β, bfgf, IGF 1 και της ινσουλίνης, καθώς και την πρόκληση του κυτταρικού πολλαπλασιασμού σε ενδοθηλιακά, σωληναριακά κύτταρα και ινοβλάστες (Takagi N et al., 1990; Simonson MS et al., 1989; Ong ACM et al., 1994). Τέλος, τόσο ο ETA όσο και ο ETB αυξάνουν τη σύνθεση του κολλαγόνου και εξασθενούν τη δράση κολλαγενασών επιτείνοντας την εναπόθεση εξωκυττάριας ουσίας, ενώ ταυτόχρονα ενεργοποιούν μόρια προσκόλλησης (ICAM 1, VCAM 1, E selectin) και χημειοτακτικούς παράγοντες (TNF α, MCP 1, IL 1b και 8) (Naicker S et al., 2001). Ιδιαίτερο ενδιαφέρον παρουσιάζει η μελέτη του σηματοδοτικού μονοπατιού της ΕΤ-1 και των υποδοχέων της ΕΤΑ και ΕΤΒΑ σε σχέση με τις ΜΑΡ Κινάσες ERK1/2 οι οποίες ονομάζονται και p44/42 MAPKs (mitogenactivated protein kinases). Οι κινάσες ERK1/2 επιδρούν άμεσα στη συστολή των λείων μυϊκών κυττάρων των αγγείων. Επίσης η ενεργοποίηση των ET-A και ET-B υποδοχέων, έχει ως αποτέλεσμα την φωσφορυλίωση των ERK1/2. Αξίζει να σημειωθεί ότι οι ERK1/2 με την φωσφορυλιωμένη μορφή δρούν ως ρυθμιστές στον κυτταρικό πολλαπλασιασμό, στη μετανάστευση νεοδημιουργημένων κυττάρων, στη διαφοροποίηση και στη συστολή των λείων μυϊκών κυττάρων των αγγείων. 129
130 ΚΙΝΑΣΕΣ ΕΝΕΡΓΟΠΟΙΗΜΕΝΕΣ ΑΠΟ ΜΙΤΟΓΟΝΑ Mitogen-Activated Protein Kinases MAPKs Το σύστημα των ΜΑΡ κινασών Το σύστημα των ΜΑΡ κινασών είναι ένα κυτταροπλασματικό σύνολο από κινάσες πρωτεϊνών, οι οποίες συμβάλλουν ώστε να φθάσει το μήνυμα από τους υποδοχείς της μεμβράνης στον πυρήνα του κυττάρου. Όλα τα ευκαρυωτικά κύτταρα κατέχουν πολλαπλά μονοπάτια ΜΑΡΚs, καθένα από τα οποία ενεργοποιείται από διαφορετικά ερεθίσματα [Εικόνα 38]. Στα θηλαστικά τα μονοπάτια των ΜΑΡΚs μπορούν να ενεργοποιούνται από πολλαπλά ερεθίσματα, μέσω διαφορετικών οικογενειών υποδοχέων. Εικόνα 38: Διαφορετικά ερεθίσματα οδηγούν στην ενεργοποίηση διαφορετικών μονοπατιών ΜΑΡΚs. Για παράδειγμα: Οι ορμόνες [ινσουλίνη] και οι αυξητικοί παράγοντες [αυξητικοί παράγοντες (EGF), platelet-derived growth factor (PDFG), fibroblast growth (FGF), ενεργοποιούν τις ΜΑΡΚs μέσω υποδοχέων κινασών τυροσίνης. Οι αυξητικές ορμόνες δρουν μέσω υποδοχέων των κυτταροκινών. 130
131 Πολυπεπτίδια που σχετίζονται με τον TGF-β δρουν μέσω υποδοχέων κινασών σερίνης/θρεονίνης. Κυτταροκίνες της οικογένειας TNF και περιβαλλοντικά ερεθίσματα όπως το ωσμωτικό σοκ, το μηχανικό στερς, οι ιονίζουσες ακτινοβολίες αλλά και οι ισχαιμικές βλάβες ενεργοποιούν τις οδούς ΜΑΡΚs μέσω υποδοχέων της οικογένειας των TNF υποδοχέων. Αγγειοδραστικά πεπτίδια όπως η ANG II και η ενδοθηλίνη, ενεργοποιούν οδούς ΜΑΡΚs, μέσω διαμεμβρανικών υποδοχέων οι οποίοι συνδέονται με G πρωτεΐνες στο κυτταρόπλασματικό τους τμήμα (Herskowitz I et al., 1995; Kyriakis JM et al., 1996). Η μεταβίβαση της πληροφορίας σε μία τυπική οδό ΜΑΡΚs Μια τυπική οδός μεταγωγής σήματος μέσω ΜΑΡΚs ακολουθεί μια αλληλουχία γεγονότων ξεκινά από τη δέσμευση του σηματοδοτικού μορίου στον υποδοχέα του, την ενεργοποίηση του υποδοχέα, τη στρατολόγηση των πρωτεϊνών-συνδετήρων (adaptor receptors) και την ενεργοποίηση των Ras πρωτεϊνών. Στη συνέχεια, ακολουθεί μια σειρά από τρεις ή τέσσερίς κινάσες. Ειδικότερα, οι ΜΑΡΚΚΚΚs ή ΜΕΚΚΚs (Mitogen and ERK kinase kinase kinases) φωσφορυλιώνουν και ενεργοποιούν τις ΜΑΡΚΚΚs ή MEKKs οι οποίες φωσφορυλιώνουν και ενεργοποιούν τις ΜΑΡΚΚs ή MEKs. Έπειτα αυτές οι διπλής εξειδίκευσης κινάσες σερίνης/θρεονίνης/τυροσίνης φωσφορυλιώνουν και ενεργοποιούν τις ΜΑΡΚs. Οι ΜΑΡΚs στη συνέχεια, φωσφορυλιώνουν και ενεργοποιούν τα υποστρώματα τους σε κατάλοιπα σερίνης/θρεονίνης. Τα υποστρώματα των ΜΑΡΚs είναι κυρίως μεταγραφικοί παράγοντες, οι οποίοι δραστηριοποιούνται και ρυθμίζουν τη γονιδιακή έκφραση, καθώς επίσης και κυτταροπλασματικές πρωτεΐνες, όπως κινάσες και φωσφο-λιπάσες που σχετίζονται με τον κυτταροσκελετό (Cobb MH et al., 1995; Hagemann C et al., 2001; Windmann C et al., 1999). 131
132 Ενεργοποίηση των ΜΑΡΚs Οι ΜΑΡΚs κινάσες φωσφορυλιώνουν μόνο υποστρώματα, τα οποία περιέχουν προλίνη στη θέση Ρ-1. Για τις ERK1/2 το γενικό μοτίβο είναι Pro-X- Ser/Thr-Pro (Alvarez E et al., 1991). H ενεργότητα των ΜΑΡΚs ελέγχεται από τη διπλή φωσφορυλίωση μιας αμινοξικής αλληλουχίας που είναι γνωστή ως βρόγχος ενεργοποιήσης. Η αλληλουχία Thr-X-Thr στο βρόγχο ενεργοποίησης (όπου Χ είναι συγκεκριμένο αμινοξύ αναλόγως του τύπου της ΜΑΡΚ) είναι η θέση διπλής φωσφορυλίωσης που καταλύεται από την ειδική ΜΑΡΚΚ. Για τις ERK 1/2 οι θέσεις φωσφορυλίωσης είναι οι Thr 183 και Thr 185. Διπλή φωσφορυλίωση στις θέσεις αυτές έχει ως αποτέλεσμα την αναδίπλωση του βρόγχου και την αλληλεπίδραση με επιφανειακές θέσεις δέσμευσης αργινίνης αυξάνοντας έτσι, την ειδική ενεργότητα των ΜΑΡΚs τουλάχιστον 1000 φορές (Windmann C et al., 1999; Canagarajah BJ et al., 1997). Θα πρέπει να σημειωθεί ότι η αντικατάσταση των δύο παραπάνω θέσεων φωσφορυλίωσης από κάποιο όξινο αμινοξύ, όπως το Glu δεν οδηγεί σε ενεργοποίηση, αφού τα χαρακτηριστικά του βρόγχου ενεργοποίησης και η διπλή φωσφορυλίωση σε Thr και Tyr επάγουν αρκετές αλλαγές στη διαμόρφωση του πρωτεϊνικού μορίου, οι οποίες δεν μπορούν να επαχθούν από το γλουταμινικό οξύ. Γι αυτό το λόγο, οι σημειακές μεταλλάξεις στις ΜΑΡΚs δεν επάγουν την ενεργοποίηση τους. Φαίνεται επομένως, ότι το μοτίβο pthr-x-ptyr είναι απαραίτητο για τη ρύθμιση της ενεργοποίησης των ΜΑΡΚs κινασών, γεγονός που εξηγεί το λόγο που οι ΜΑΡΚs δεν έχουν ταυτοποιηθεί ποτέ ως ογκογονίδια όπως θα ήταν αναμενόμενο για πρωτεΐνες οι οποίες ρυθμίζουν την κυτταρική αύξηση (Canagarajah BJ et al., 1997; Oldenhof AD et al., 2002). Οργάνωση και ρύθμιση των οδών των ΜΑΡΚs Οι ΜΑΡΚs παίρνουν μέρος στη ρύθμιση σύνθετων κυτταρικών διεργασιών όπως είναι η μίτωση, η διαμόρφωση, η διαφοροποίηση, η επιβίωση, η απόπτωση και η μετανάστευση. Η εξειδίκευση στην απόκριση μέσω των ΜΑΡΚs επιτυγχάνεται με την ενεργοποίηση διαφορετικών 132
133 συστημάτων ΜΕΚΚ-ΜΕΚ- ΜΑΡΚ σε απόκριση διαφορετικών ερεθισμάτων. Έτσι διαφορετικά συστήματα ΜΑΡΚs ενεργοποιούνται από κυτταροκίνες, αυξητικού παράγοντες και ορμόνες, καθώς επίσης και από κυτταρικό στρες (ακτινοβολία, θερμικό στρες, οσμωτικές διαταραχές, καταστροφή του DNA και βακτηριακούς παράγοντες). Η ενεργοποίηση των ΜΑΡΚs προς απόκριση στα παραπάνω ερεθίσματα συνιστάται για τη ρύθμιση της γονιδιακής έκφρασης, του μεταβολισμού, της διάταξης του κυτταροσκελετού και άλλων ρυθμιζόμενων κυτταρικών γεγονότων (Garrington TP et al., 1999). Μέχρι σήμερα έχουν ταυτοποιηθεί στα θηλαστικά 14 ΜΑΡΚΚΚs, 7 ΜΑΡΚΚs και 15 ΜΑΡΚs [Εικόνα 39]. Κάθε τύπος κινάσης υποδιαιρείται σε υποοικογένειες με κριτήρια τη λειτουργία και την ομολογία της αλληλουχίας [Πίνακας 4]. Όπως φαίνεται στον παρακάτω πίνακα, οι ΜΑΡΚs διακρίνονται σε 6 υπο-οικογένειες, τη ΜΑΡΚ ERK1/2, τη ΜΑΡΚ ERK3/4, ΜΑΡΚ ERK5/6, ΜΑΡΚ ERK7/8, τη ΜΑΡΚ p38 και τη ΜΑΡΚ JNK, οι οποίες δίνουν και το όνομα στην οδό της ΜΑΡΚ στην οποία μετέχουν (π.χ. η οδός των MAPKs που χρησιμοποιεί τη ΜΑΡΚ p38 ονομάζεται οδός της p38 ΜΑΡΚ). Εικόνα 39: Το σηματοδοτικό μονοπάτι των ΜΑΡ κινασών 133
134 Τύπος κινάσης Υπο-οικογένεια Raf Μέλη MAPKKK A-RAF,MAPKKK B-RAF,MAPKKK RAF1 ΜΑΡΚΚΚs MAPKKs MAPKs MEKK MEK MAPK ERK1/2 MAPK ERK3/4 MAPK ERK5/6 MAPK ERK7/7 MEKK MEKK1, MEKK MEKK2, MEKK MEKK3, MEKK MEKK4 MAPKKK ASK1, MAPKKK TPL2 MAPKKK MST, MAPKKK SPRK, MAPKKK MUK, MAPKKK TAK1, MAPKKK MOS MAPKK MKK1, MAPKK MKK2 MAPKK MKK3, MAPKK MKK6 MAPKK MKK4 MAPKK MKK5 MAPKK MKK7 ERK1, ERK2 ERK3, ERK4 ERK5, ERK6 ERK7, ERK8 MAPK p38 p38α, p38β, p38γ, p38δ MAPK JNK JNK1, JNK2, JNK3 Πίνακας 4: Τα μέλη της οικογένειας των ΜΑΡΚs που έχουν ταυτοποιηθεί μέχρι σήμερα στα θηλαστικά. Οι ΜΑΡΚΚs αντιπροσωπεύονται με τα λιγότερα μέλη στο σύστημα των ΜΑΡΚs και εμφανίζουν υψηλό βαθμό εξειδίκευσης για τα υποστρώματα τους επιτρέποντας έτσι, ελάχιστους συνδυασμούς του τμήματος ΜΕΚ- ΜΑΡΚs των ΜΑΡΚs. Αντιθέτως, οι 14 ΜΑΡΚΚΚs ποικίλουν δομικά και έχουν διαφορετικές δομικές περιοχές που δεν απαντώνται στις ΜΑΡΚΚs ή τις ΜΑΡΚs. Στις περιοχές αυτές ανήκουν αλληλουχίες πλούσιες σε προλίνη για τη δέσμευση SH 3 περιοχών, θέσεις δέσμευσης για πρωτεΐνες που δεσμεύουν GTP, αλληλουχίες διμερισμού του τύπου φερμουάρ λευκίνης καθώς επίσης και θέσεις φωσφορυλίωσης για κινάσες τυροσίνης ή σερίνης/θρεονίνης. Μ αυτόν τον τρόπο, οι ΜΑΡΚΚΚs ρυθμίζονται διαφορικά από ένα ευρύ σύνολο σημάτων που προηγούνται (upstream), ενώ ρυθμίζουν εκλεκτικά τις ΜΑΡΚΚs (Garrington TP et al., 1999). Σε αυτήν την ποικιλομορφία των ρυθμιστικών περιοχών οφείλεται η ευελιξία των συστημάτων των ΜΑΡΚs να αποκρίνονται σε μια ευρεία κλίμακα κυτταρικών ερεθισμάτων όμως, δεν έχει διευκρινιστεί ακόμα τι είναι αυτό που προσδίδει την ικανότητα σε μια ΜΑΡΚΚΚ να δρα εκλεκτικά σε μια οδό ΜΑΡΚ φωσφορυλιώνοντας, και κατ επέκταση ενεργοποιώντας διαφορετικές ΜΑΡΚΚs. Σύμφωνα με πρόσφατες ενδείξεις, η εξειδίκευση αυτή επιτυγχάνεται εν μέρει μέσω πρωτεϊνών «πρόσδεσης», οι οποίες συντονίζουν τη δέσμευση 134
135 των ΜΑΡΚΚΚs είτε σε ειδικές πρωτεΐνες για σήματα που προηγούνται (upstream) είτε σε ειδικά συμπλέγματα ΜΑΡΚΚs- ΜΑΡΚs που έπονται (downstream) (Pawson T et al., 1997). Η νέα θεωρία για τη μεταγωγή σήματος υποστηρίζει ότι οι κυτταρικές οδοί ρυθμίζονται από την οργάνωση τους σε μακρομοριακά συμπλέγματα. Μέχρι πρόσφατα η κυτταρική οργάνωση ήταν άρρηκτα συνδεδεμένη με τα κυτταρικά οργανίδια όμως τώρα γίνεται αποδεκτό ότι η μακρομοριακή οργάνωση είναι εξίσου σημαντική για τις κυτταροπλασματικές πρωτεΐνες. Τα συστήματα μεταγωγής σήματος συμπεριλαμβάνουν πρωτεΐνες χωρίς καταλυτική ενεργότητα και ένζυμα που είναι φυσικά αναπόσπαστα μέλη του συστήματος. Οι οδοί μεταγωγής σημάτων MAPKs στα θηλαστικά Η οδός MAPK ERK Η οδός MAPK ERK είναι η καλύτερη χαρακτηρισμένη αλληλουχία αντιδράσεων των ΜΑΡΚs και ενεργοποιείται από διάφορες κυτταροκίνες και αυξητικούς παράγοντες (Platanias LC et al., 2003). Είναι ένα εξελικτικά διατηρημένο μεταγωγικό μονοπάτι που εμπλέκεται στον έλεγχο πολλών θεμελιωδών κυτταρικών διεργασιών συμπεριλαμβανομένων του κυτταρικού πολλαπλασιασμού, της επιβίωσης, της απόπτωσης, της διαφοροποίησης, της κυτταρικής κίνησης και του μεταβολισμού (Kolch W, 2005). Από το σύνολο των πρωτεϊνών που αναφέρονται ως ERKs, οι ERK1 και ERK2 είναι οι πιο καλά μελετημένες και αποτελούν την υπο-οικογένεια MAPK ERK1/2 [Εικόνα 40A-B]. Πρόκειται για πρωτεινες μοριακού βάρους 44kDa και 42kDa αντιστοίχως και εμφανίζουν ομολογία 85% στο σύνολο του μορίου, ποσοστό το οποίο αυξάνεται για τις περιοχές πρόσδεσης υποστρωμάτων (Boulton TG et al., 1991). Οι δύο θέσεις φωσφορυλίωσης, στην Thr 183 και Thr 185, χωρίζονται από ένα αμινοξύ γλουταμινικού οξέος τόσο στην ERK1 όσο και στην ERK2 δημιουργώντας το μοτίβο Thr-Glu-Tyr στο βρόγχο ενεργοποίησης. Και οι δύο εκφράζονται ευρέως με το ποσοστό έκφρασης να ποικίλει στους διαφορετικούς ιστούς. 135
136 Α Εικόνα 40Α-Β: Σχηματική απεικόνιση της δομής ERK1(A) και ERK2(B). Οι ERK 1 και ERK2 ενεργοποιούνται από ένα ζεύγος MEKs, τις ΜΕΚ1 και 2. Και οι δύο αυτές MEKs μπορούν να ενεργοποιήσουν πλήρως τις ERK1/2 in vitro. Η ρύθμιση της ενεργοποίησης της ERK είναι σύνθετη και εξαρτάται από τις δύο φωσφορυλιώσεις στις θέσεις που προαναφέρθηκαν και οι οποίες γίνονται σε δύο φάσεις. Η πρώτη φωσφορυλίωση γίνεται στην Tyr 185 και 136 Β
137 προκαλέι τη μεταβολή της καρβοξυλικής περιοχής, ενώ μόλις αυτή ολοκληρωθεί πραγματοποιείται μια δεύτερη φωσφορυλίωση στη Thr 183, η οποία οδηγεί σε αναδιαμόρφωση της αμινοτελικής περιοχής. Η ERK καθίσταται ενεργή μόνο μετά την ολοκλήρωση και των δύο φωσφορυλιώσεων (Galetic I et al., 2003). Οι ΜΕΚ1/2 φωσφορυλιώνονται από μέλη των ΜΕΚΚs και συγκεκριμένα από ισομορφές Raf και Mos. Μάλιστα, οι πρωτεΐνες αυτές φωσφορυλιώνουν αποκλειστικά τις ΜΕΚ1/2 γεγονός που τις εντάσσει στην οδό ERK1/2 (Kyriakis JM et al., 1992). Η οικογένεια των Raf αποτελείται από την Α-Raf, τη Β-Raf και τη Raf-1. Οι περισσότερες μελέτες έχουν εστιάσει στη Raf-1. Η ρύθμιση της κινάσης αυτής είναι σύνθετη καθώς αφορά πρωτεϊνικές αλληλεπιδράσεις, φωσφορυλίωση σε τυροσίνη, σερίνη και θερονίνη και κατάλληλη ενδοκυτταρική τοποθέτηση (Morrrison DK et al., 1997). Αυτοί οι πολλαπλοί τρόποι ρύθμισης επιτρέπουν στη Raf-1 να κυμαίνεται μεταξύ διαφόρων επιπέδων ενεργοποίησης. Ίσως η καλύτερα χαρακτηρισμένη οδός ERK1/2 είναι αυτή που διέρχεται μέσω υποδοχέων με ενεργότητα κινάσης τυροσίνης. Η δέσμευση του κατάλληλου προσδέματος στους υποδοχείς αυτούς έχει ως αποτέλεσμα την αύξηση της καταλυτικής τους ενεργότητας και ακολούθως την αυτοφωσφορυλίωση σε τυροσίνες. Η φωσφορυλίωση των υποδοχέων αυτών οδηγεί στο σχηματισμό πολυπρωτεϊνικών συμπλεγμάτων, η οργάνωση των οποίων καθορίζει τα μετέπειτα σήματα. Πολύ συχνά το αποτέλεσμα είναι η ενεργοποίηση μιας μονομερούς G πρωτεΐνης, Ras. Αυτό επιτυγχάνεται με συνάθροιση στον υποδοχέα διαφόρων πρωτεϊνών-συνδετήρων, όπως η Shc και η Grb2, λόγω των αλληλεπιδράσεων των SH2 περιοχών τους με φωφσοτυροσίνες. Τότε ο παράγοντας ανταλλαγής νουκλεοτιδίων γουανίνης (GEF), SOS (Son of Sevenless), εισέρχεται στο σύμπλεγμα, καθώς βρίσκεται διαρκώς δεσμευμένος με την SH3 περιοχή της Grb2, επάγοντας την ανταλλαγή του GDP της Ras με την GTP στην κυτταροπλασματική μεμβράνη. Η Ras δεσμευμένη με την GTP αλληλεπιδρά άμεσα με διάφορους τελεστές όπως ισομορφές της Raf. Η δέσμευση της Ras στην Raf οδηγεί είτε σε αλλαγές της στερεοδιαμόρφωσης της Raf οι οποίες αυξάνουν την ενεργότητα 137
138 της ως κινάση, είτε απλώς δημιουργεί το κατάλληλο περιβάλλον για τη μεταγωγή σημάτων από τη Raf-1 (Moodie SA et al., 1993; Jelinek T et al., 1996). Η τοποθέτηση της Raf στην κυτταροπλασματική μεμβράνη επιτρέπει επίσης σε κινάσες όπως η Src και η PKC, να τροποποιούν περαιτέρω τη Raf ώστε να αυξηθεί η ενεργότητα της (Dent P et al., 1995; Diaz B et al., 1997). Η αύξηση αυτή μεταβιβάζεται στη συνέχεια μέσω των MEK-ERK [Εικόνα 41]. Εικόνα 41: Η οδός μεταγωγής σημάτων MAPK ERK1/2. Οι ενεργοποιημένες ERK1 και ERK2 φωσφορυλιώνουν πολυάριθμα υποστρώματα σε όλα τα κυτταρικά διαμερίσματα συμπεριλαμβανομένων 138
139 μεμβρανικών πρωτεϊνών (CD120a, Syk και Calnexin), πυρηνικών υποστρωμάτων (SRC-1, Rax6, NF-AT, Elk-1, MEF2, c-fos, c-myc και STAT3), πρωτεϊνών κυτταροσκελετού και αρκετές κινάσες ΜΑΡΚs (Roux PP et al., 2004). Επειδή τα υποστρώματα των ERK1/2 βρίσκονται σε διαφορετικά υποκυτταρικά διαμερίσματα [Εικόνα 42], η βιολογική έκβαση της ενεργοποίησης τους θα εξαρτηθεί εν μέρει από τον εντοπισμό των ERK1/2 και την προσβασιμότητα σε ενδεχόμενα υποστρώματα μέσα στο διαμέρισμα. Επίσης είναι πιθανό ότι τα μοριακά ικριώματα, τα οποία κατευθύνουν τη δράση των ΜΑΡΚs σε ειδικά υποστρώματα, έχουν μοναδική σύνθεση μέσα σε διακριτά διαμερίσματα και κυτταρικούς τύπους, οι οποίοι προστίθενται στην ευελιξία της μεταγωγής σήματος που οφείλεται στη δράση των ERK1/2. Έρευνες σε κύτταρα ζύμης και κύτταρα θηλαστικών έχουν δείξει ρυθμιστές της διαμερισματοποίησης των ERK1/2 στους οποίους συμπεριλαμβάνονται και οι πρωτεΐνες αγκυροβολίας που τις περιορίζουν στο κυτταροπλασματικό ή το πυρηνικό διαμέρισμα (Chu CT et al., 2004). Η μεταγωγή σήματος στις ERKs μέσω GPCRs (υποδοχείς συνδεδεμένοι με G πρωτεΐνες) είναι επίσης άρρηκτα συνδεδεμένη με τροποποίηση της ενεργοποίησης της Raf. Παρ όλα αυτά, οι μηχανισμοί που χρησιμοποιούνται από τους συγκεκριμένους υποδοχείς ποικίλουν. Η πολυπλοκότητα των GPCRs, η διαφορετική αλληλεπίδραση τους με ετεροτριμερείς ισομορφές G πρωτεϊνών, η ικανότητα ορισμένων υποδοχέων να ενεργοποιούν περισσότερες από μια τάξεις G πρωτεϊνών και οι κυτταροειδικοί μηχανισμοί συμβάλλουν σε αυτήν την εκπληκτική ποικιλότητα (Belcheva MM et al., 2002). Οι μεγάλου μοριακού βάρους G πρωτεΐνες, όπως είναι γνωστό, αποτελούνται από 3 υπομονάδες α, β και γ. Σύμφωνα με ένα προτεινόμενο μοντέλο, οι β και γ ενεργοποιούν μέλη της οικογένειας Src μέσω της κινάσης ΡΙ3Κ (Loppez-Ilasaca M et al., 1997). Η Src μπορεί τότε να φωσφορυλιώσει την Pyk2 ή την FAK δημιουργώντας SH 2 θέσεις πρόσδεσης (Della Rocca GJ et al., 1999). Στη συνέχεια, ανάλογα με το μηχανισμό που χρησιμοποιείται από τους υποδοχείς με ενεργότητα κινάσης τυροσίνης, σχηματίζεται στη μεμβράνη ένα σύμπλοκο που περιλαμβάνει τις Shc, Grb2 και SOS και το οποίο 139
140 ενεργοποιεί τη Ras και ακολούθως τη Raf-1. Σε κυτταρικούς τύπους, όπου η έκφραση της ΡΙ3Κ είναι μικρή, η ενεργοποίηση της ERK εξαρτάται από εναλλακτικές οδούς ενεργοποίησης του συμπλέγματος FAK/Src (Dikic I et al., 1996). Εικόνα 42: Κυτταροπλασματικά και πυρηνικά υποστρώματα των ERK1/2. Σύμφωνα με τη βιβλιογραφία οι ERK1/2 κατανέμονται παντού σε κύτταρα που βρίσκονται σε ηρεμία, ενώ ύστερα από κάποιο ερέθισμα ένας σημαντικός πληθυσμός ERK1/2 συσσωρεύεται στον πυρήνα. Ενώ οι μηχανισμοί που εμπλέκονται δεν είναι εντελώς γνωστοί, ο διμερισμός, φωσφορυλίωση και η απελευθέρωση από κυτταροπλασματικές «άγκυρες» φαίνεται να παίζουν κάποιο ρόλο (Roux PP et al., 2004). Έτσι μεταλλαγμένα μόρια ERK που δεν μπορούν να διμεριστούν, δε μετατοπίζονται στον πυρήνα. Επίσης, η πυρηνική μετατόπιση των ERKs διευκολύνεται από τη φωσφορυλίωση τους στο βρόγχο ενεργοποίησης, αλλά δεν απαιτεί από αυτές την απόκτηση της ενεργότητας κινάσης (Schaeffer HJ et al., 1999). Ωστόσο, από τη βιβλιογραφία είναι γνωστό ότι σε νευρικά κύτταρα η φωσφορυλιωμένη ERK (perk) ανιχνεύεται στον πυρήνα, το κυτταρόπλασμα και τους δενδρίτες 140
141 (Sgambato V et al., 1998). Τέλος, η μετατόπιση της ERK στον πυρήνα είναι θεμελιώδης για την είσοδο στην S φάση. Έτσι, σε κατάσταση κυτταρικής αναμονής, η ERK παραμένει στο κυτταρόπλασμα σε σύνδεση με τη ΜΕΚ, το δίκτυο των μικροσωληνίσκων καθώς και φωσφατάσες όπως την ΜΚΡ-3. Σε προσκολλημένα κύτταρα η ERK απαντάται κυρίως στον πυρήνα και η ΜΕΚ στο κυτταρόπλασμα, ενώ σε μη προσκολλημένα κύτταρα οι ERK και MEK συνεντοπίζονται στο κυτταρόπλασμα. Η ERK δηλαδή, χρειάζεται μια κατάσταση κυτταρικής προσκόλλησης για την ουσιώδη μετατόπιση της στον πυρήνα και οι συνδέσεις ιντεγκρίνης-κυτταροσκελετού είναι σημαντικές για τη διαδικασία αυτή (Aplin AE et al., 2001). Ένα άλλο μέρος των ERKs, η ERK3, αμφισβητήθηκε και δεν της δόθηκε η απαιτούμενη σημασία αρχικά, παρόλο που η αλληλουχία της έγινε γνωστή ταυτόχρονα με εκείνες των ERK1 και ERK2. Προκειμένου για μια κινάση μοριακού βάρους 63kDa, η οποία απαντάται και στον πυρήνα και στο κυτταρόπλασμα, φαίνεται να παρουσιάζει στην καταλυτική περιοχή 50% ομολογία με την ERK1, ενώ η λειτουργία της καρβοξυτελικής της περιοχής δεν έχει ακόμα διευκρινιστεί. Επιπροσθέτως, στη θηλιά ενεργοποίησης το μοτίβο που απαντάται είναι Ser-Glu-Gly αντί Thr-Glu-Tyr. Επειδή μάλιστα η φωσφορυλίωση της τυροσίνης είναι απαραίτητη για την ενεργοποίηση και την αλληλεπίδραση με τα υποστρώματα, αντικατάσταση της με τη γλυκίνη γεννά ερωτήματα για το πώς μπορεί η ERK3 να ενεργοποιείται και να δεσμεύεται στα υποστρώματα της. Η ERK3 λοιπόν παρουσιάζει κάποιες ομοιότητες με τις ERK1/2 ως προς την αλληλουχία, επειδή όμως, οι λειτουργίες και η ρύθμιση είναι διαφορετική έχει τοποθετηθεί μαζί με την ERK4 σε διαφορετική υποοικογένεια, τη MAPK ERK3/4 (Bogoyevitch MA et al., 2004; Cheng M et al., 1996; Pearson G et al., 2001). Η ERK4 έχει μοριακό βάρος 45kDa και η αμινοξική της αλληλουχία δεν είναι ακόμα γνωστή (Bogoyevitch MA et al., 2004). Η ERK5 λόγω του μεγάλου μεγέθους της, 98kDa, ονομάζεται και μεγάλη ΜΑΡΚ (Big MAPK, BMK). Η πρωτοταγής δομή της καταλυτικής περιοχής της ERK5 εμφανίζει ομολογία με την αντίστοιχη της ERK2. Η 141
142 έκφραση της στα θηλαστικά είναι ευρύτατη και όπως οι άλλες MAPKs, η ρύθμιση της υπόκειται σε μια ποικιλία παραγόντων πολλαπλασιασμού (αυξητικοί παράγοντες, φορβολικοί εστέρες) καθώς και κυτταρικού στρες (σορβιτόλη, Η 2 Ο 2, ακτινοβολία UV κ.ά.). Η ERK5 ενεργοποιείται από τη ΜΕΚ5 και μάλιστα αποτελεί το μόνο γνωστό υπόστρωμα της. Βάσει πρωτοταγούς δομής, η ΜΕΚ5 σχετίζεται περισσότερο με τις ΜΕΚ1/2. Ως συνέπεια αυτής της σύνδεσης, η ERK5 αναστέλλεται από τους PD98059 και U0126, δύο πολύ εξειδικευμένους αναστολείς των ΜΕΚ1/2 (Bogoyevitch MA et al., 2004; Kamakura S et al., 1999). Πάντως η ΜΕΚ5 δε φωσφορυλιώνεται και δεν ενεργοποιείται από τη Raf-1 όπως οι ΜΕΚ1/2. Η ERK6 έχει μοριακό βάρος 40.3kDa και παρουσιάζει 41% ομολογία με την ERK1, 39% με την ERK2 και 33% με την ERK3, όμως με την p38mapk εμφανίζει τη μεγαλύτερη ομολογία (60%), γι αυτό και της δόθηκαν επίσης τα ονόματα SAPK-3 και p38β. Όπως και οι κινάσες p38, η ERK6 στη θηλία ενεργοποίησης φέρει το μοτίβο Thr-Gly-Tyr και ενεργοποιείται κατά το κυτταρικό στρες και υπό την επίδραση κυτταροκινών. Παρ όλα αυτά, η ERK6 παρουσιάζει και διαφορές ως προς τις p38 κινάσες, αφού δεν επηρεάζεται από τον SB203580, έναν αναστολέα των p38α/β (Bogoyevitch MA et al., 2004). Το 1999 κλωνοποιήθηκε με PCR η ΕRΚ7 (61kDa) χρησιμοποιώντας ενακτήριες αλληλουχίες (primers) βασιζόμενες στις υψηλά συντηρημένες αλληλουχίες των ΜΑΡΚs, ενώ πρόσφατα απομονώθηκε άλλο ένα μέλος των ERKs, η ERK8 (60kDa) με τη χρήση της ERK7 ως ανιχνευτής (probe). Η θηλία ενεργοποίησης και των δύο περιέχουν το μοτίβο Thr-Glu-Tyr, όπως και οι ERK1, ERK2 και ERK5, ενώ η ERK7 παρουσιάζει 40% ομολογία με τις δύο πρώτες. Η ERK7 φαίνεται να φωσφορυλιώνει τα υποστρώματα c-fos και c- myc, όχι όμως και τα υποστρώματα Elk-1, c-jun ή ATF2 και PHAS-I, ενώ η ERK8 δε φαίνεται να φωσφορυλιώνει τα c-jun, c-myc, c-max, Elk-1, Ets-1, ιστόνη Η1 και παξιλλίνη. Επίσης, η ERK8 παρουσιάζει 69% ομολογία με την ERK7, ποσοστό που αυξάνεται σε 80% στην καταλυτική περιοχή (Bogoyevitch MA et al., 2004). 142
143 ΕΙΔΙΚΟ ΜΕΡΟΣ 143
144 ΥΛΙΚΑ ΚΑΙ ΜΕΘΟΔΟΣ Η παρούσα εργασία πραγματοποιήθηκε σύμφωνα με τις οδηγίες Βιοηθικής του Πανεπιστημίου Πατρών. ΑΝΟΣΟΪΣΤΟΧΗΜΕΙΑ Η εφαρμογή τεχνικών ανοσοϊστοχημείας στο ιστοπαθολογικό εργαστήριο, είχε χωρίς αμφιβολία, καταλυτική επίδραση, τόσο σε πρακτικό όσο και σε θεωρητικό επίπεδο. Ο ρόλος του παθολογοανατόμου στην παροχή περίθαλψης, απέκτησε και αποκτά συνεχώς μεγαλύτερη σημασία, χάρις στις συνεχώς αυξανόμενες δυνατότητες που του παρέχουν οι ανοσοϊστοχημικές τεχνικώς, δυνατότητες που ξεπερνούν τη διάγνωση και μπαίνουν δυναμικά στο χώρο της πρόγνωσης και της απόφασης για τον θεραπευτικό χειρισμό. Ιδιαιτέρα στον τομέα της διάγνωσης των νεοπλασμάτων, η εφαρμογή των τεχνικών ανοσοϊστοχημείας αποτέλεσε κατά γενική ομολογία μια πραγματική επανάσταση και θεωρείται δίκαια η σημαντικότερη εξέλιξη των τελευταίων 50 ετών (Chan JK, 2000; Mukai K et al., 1980; Rosai J, 1994). ΤΕΧΝΙΚΗ Ανοσοϊστοχημεία ονομάζουμε μια εργαστηριακή τεχνική που συνδυάζει την ιστοπαθολογία με την ανοσολογία και τη χημεία. Ένα αντίσωμα κατευθύνεται προς ένα ειδικό αντιγόνο-στόχο και μια χημική αντίδραση λαμβάνει χώρα για να καταστήσει ορατό το σύμπλεγμα αντιγόνουαντισώματος, εφόσον είναι παρόν. Επομένως, με τον όρο ανοσοϊστοχημεία εννοούμε μια ομάδα τεχνικών σήμανσης, που επιτυγχάνουν να καταστήσουν ορατά διάφορα αντιγόνα σε ιστούς και κύτταρα. Οι τεχνικές αυτές βασίζονται στην ικανότητα των ειδικών αντισωμάτων να εντοπίζουν και να συνδέονται με το αντίστοιχο αντιγόνο. Η σήμανση του αντισώματος με την κατάλληλη ουσία-δείκτη καθιστά το σύμπλεγμα αντιγόνου αντισώματος ορατό. Ανάλογα με τη φύση της ανοσοϊστοχημικής τεχνικής και το είδος της ουσίας-δείκτη που χρησιμοποιούμε, η αντίδραση μεταξύ αντιγόνου-αντισώματος ελέγχεται με 144
145 κοινό, φθορίζον ή ηλεκτρονικό μικροσκόπιο (Rosai and Ackerman s Surgical Pathology, 2004). Η αρχική μέθοδος ξεκίνησε το 1941 από τον Coons που πρώτος είχε τη ιδέα να σημάνει με φθορίζοντα ιχνηθέτη ένα αντίσωμα που ανέπτυξε σε πειραματόζωο και κατόπιν να αναζητήσει σε ιστική τομή το αντιγόνο εναντίον του οποίου είχε αναπτυχθεί το αντίσωμα εξετάζοντας τον ιστό (μετά την επώαση) με φθορίζον μικροσκόπιο. Αλλά μόνο μετά την εισαγωγή των σεσημασμένων με ένζυμα αντισωμάτων η ανοσοϊστοχημεία έγινε γενικά αποδεκτή σαν ένα απλό, έξυπνο και πρακτικό εργαλείο στη διαγνωστική ιστοπαθολογία (Avrameas S et al., 1966; Nakane PK et al., 1966). Το αμέσως επόμενο βήμα, που ήταν η εισαγωγή των μονοκλωνικών αντισωμάτων στην ανοσοϊστοχημεία, πρόσφερε στο παθολογοανατομικό εργαστήριο μια ανεξάντλητη πηγή ειδικών αντιδραστηρίων μεγάλης εξειδίκευσης για την ανίχνευση διαφόρων αντιγόνων σε ιστούς και κύτταρα. Το σύμπλεγμα αντισώματος-ενζύμου διατηρεί τόσο τις ανοσολογικές όσο και τις ενζυμικές του ιδιότητες και έτσι είναι σε θέση να δεσμεύει τόσο το αντιγόνο που αναζητούμε στον ιστό, όσο και να μεταβάλλει το χρώμα του κατάλληλου χρωμογόνου καθιστώντας το ορατό με το μικροσκόπιο (Silverberg SG, 1990). ΤΑΞΙΝΟΜΗΣΗ ΑΝΤΙΣΩΜΑΤΩΝ Ο συνεχώς αυξανόμενος αριθμός των αντισωμάτων δεικτών που διατίθενται προς χρήση, δημιουργεί σε κάθε εργαστήριο την ανάγκη ταξινόμησης τους, που μπορεί να γίνεται: α) ανάλογα με το είδος των ιστών στους οποίους ανιχνεύονται και να έχουμε έτσι δείκτες επιθηλιακούς, μεσεγχυματικούς, λεμφικούς κ.λ.π., β) ανάλογα με τον τρόπο παρασκευής τους και έχουμε έτσι μονοκλωνικούς ή πολυκλωνικούς δείκτες ή γ) ανάλογα με την ειδικότητά τους και να έχουμε δείκτες ειδικούς και μη ειδικούς. Σαν ειδικούς χαρακτηρίζουμε τους δείκτες που η έκφρασή τους περιορίζεται σε μια κυτταρική σειρά και χαρακτηριστικό παράδειγμα τέτοιου δείκτη είναι το ειδικό προστατικό αντιγόνο που εκφράζεται στο αδενικό 145
146 επιθήλιο του προστάτη αδένα. Όμως οι περισσότεροι από τους δείκτες που χρησιμοποιούμε είναι μη ειδικοί εκφραζόμενοι σε περισσότερους από έναν κυτταρικούς τύπους. Αυτό βέβαια δεν μειώνει τη χρησιμότητά τους καθώς μας επιτρέπουν να εντάξουμε έναν κυτταρικό πληθυσμό σε μια γενική κατηγορία π.χ. επιθηλιακός, μεσεγχυματικός, λεμφικός κ.α. Η διαγνωστική αξία των διαφόρων δεικτών εξαρτάται από διάφορους παράγοντες οι σπουδαιότεροι από τους οποίους είναι η ειδικότητα και η ευαισθησία. Με βάση αυτές τις δύο ιδιότητες μπορούμε να διακρίνουμε τους δείκτες μας σε πολύ χρήσιμους και απλά χρήσιμους. Στην κατηγορία των πολύ χρήσιμων δεικτών ανήκουν αυτοί που είναι όχι μόνο ειδικοί για μια κυτταρική σειρά αλλά και εκφράζονται από την συγκεκριμένη σειρά με πολύ μεγάλη συχνότητα. Τέτοιοι δείκτες είναι,επομένως, πολύ χρήσιμοι τόσο όταν το αποτέλεσμα είναι θετικό, αλλά και όταν είναι αρνητικό. Το ειδικό προστατικό αντιγόνο είναι ένας δείκτης αυτής της κατηγορίας γιατί όχι μόνο εκφράζεται αποκλειστικά από τα φυσιολογικά και νεοπλασματικά αδενικά κύτταρα του προστάτη αλλά εκφράζεται και σε ποσοστό μεγαλύτερο του 97% των περιπτώσεων. Δυστυχώς δείκτες με τέτοια ειδικότητα και ευαισθησία υπάρχουν λίγοι, ο αριθμός τους όμως αυξάνεται σταδιακά. Στην κατηγορία των χρήσιμων δεικτών ανήκει η μεγάλη πλειοψηφία των χρησιμοποιούμενων στην διάγνωση δεικτών μας. Μερικοί από αυτούς έχουν πολύ μεγάλη ειδικότητα για έναν κυτταρικό τύπο αλλά δεν εκφράζονται με μεγάλη συχνότητα από νεοπλάσματα του τύπου αυτού, π.χ. η μυοσφαιρίνη είναι ειδική για τις ραβδομυοβλάστες, υπάρχουν όμως ραβρομυοσαρκώματα που δεν την εκφράζουν (Silverberg SG, 1990). Η ανοσοϊστοχημεία συγκεντρώνει τα περισσότερα πλεονεκτήματα από οποιαδήποτε άλλη διαγνωστική μέθοδο ή τεχνική. Πολύ ικανοποιητική ευαισθησία, ειδικότητα, δυνατότητα εφαρμογής σε αρχειακό υλικό ρουτίνας ακόμα και μετά την παρέλευση μεγάλου χρονικού διαστήματος, επαναληψιμότητα και δυνατότητα συσχέτισης με τις μορφολογικές παραμέτρους. Είναι συμβατή με όλα σχεδόν τα μονιμοποιητικά υλικά που 146
147 χρησιμοποιούνται σήμερα (Jacobsen M et al., 1984; Larsson L et al., 1993; Mukai K et al., 1986), δίνει αποτελέσματα και σε υλικά που έχουν υποστεί αυτόλυση ή ακόμα και νέκρωση (Judkins AR et al., 1998) και τέλος σε περίπτωση που αυτό απαιτείται μπορεί να εφαρμοσθεί και σε ιστολογική τομή που είχε προηγουμένως υποστεί χρώση ρουτίνας (Ordonez NG et al., 1987). Εφαρμόζεται με πολύ καλά αποτελέσματα σε κυτταρολογικό υλικό (Chess Q et al., 1985; Domagala W et al., 1986; Li C Y et al., 1987), σε υλικό για ηλεκτρονικό μικροσκόπιο (Herrera GA, 1992; Mount SL et al., 1993) και μπορεί να συνδυαστεί με άλλες, ιστοχημικές χρώσεις στην ίδια τομή (Lundqvist M et al., 1983). Πολλές τεχνικές είναι σήμερα διαθέσιμες για την ανοσοϊστοχημική ανίχνευση αντιγόνων με πλέον χρησιμοποιούμενες, αυτές του ανοσοσυμπλέγματος υπεροξειδάσης-αντιυπεροξειδάσης (PAP method) και της ανοσοενζυμικής τεχνικής βιοτίνης-αβιδίνης (Biotin Avidin procedure). ΜΕΘΟΔΟΣ ΥΠΕΡΟΞΕΙΔΑΣΗΣ-ΑΝΤΙYΠΕΡΟΞΕΙΔΑΣΗΣ (PAP METHOD) Η μέθοδος χρησιμοποιεί ένα δεύτερο αντίσωμα γέφυρα, για την ένωση του πρωτοταγούς αντισώματος με το αντιδραστήριο PAP. To αντιδραστήριο PAP, έχει τη μορφή ενός σταθερού ανοσοσυμπλέγματος, αποτελούμενου από το αντιγόνο υπεροξειδάση του φυτού armoracia rusticana (horseradish) και από το αντίσωμα έναντι του αντιγόνου αυτού. Το αντιδραστήριο PAP και το πρωτοταγές αντίσωμα είναι αναγκαίο να έχουν παραχθεί στο ίδιο είδος ζώου, ενώ το αντίσωμα γέφυρα παράγεται σε διαφορετικό είδος ζώου (Sternberger LA, 1974). Το τελευταίο έχει ειδικότητα έναντι του πρωτοταγούς αντισώματος και έναντι της ανοσοσφαιρίνης του PAP ανοσοσυμπλέγματος, με αποτέλεσμα τη σταθερή διασύνδεσή τους. H τεχνική χρησιμοποιείται ευρέως σε τομές παραφίνης με πολύ καλά αποτελέσματα λόγω της υψηλής ευαισθησίας, ειδικότητας και σταθερότητας των αντιδραστηρίων [Εικόνα 43, 44, 45]. 147
148 Εικόνα 43: Εμποτισμένοι ιστοί σε παραφίνη. Εικόνα 44: Μικροτόμος που χρησιμοποιείται για τη λήψη τομών πάχους πολύ λίγων μm. Εικόνα 45: Τοποθέτηση ιστικών τομών παραφίνης σε αντικειμενοφόρες πλάκες ώστε να χρησιμοποιηθούν σε ιστολογικές χρώσεις και στη μέθοδο της ανοσοϊστοχημείας. 148
149 Περιορισμό της μεθόδου αποτελεί το γεγονός ότι το αντίσωμα του αντιδραστηρίου PAP και το πρωτοταγές αντίσωμα πρέπει να παράγονται στο ίδιο είδος ζώου. Σήμερα υπάρχουν διαθέσιμα αντιδραστήρια PAP που έχουν παραχθεί σε όλα τα είδη ζώων που παράγονται και τα πρωτοταγή αντισώματα (Sternberger LA, 1974). Ανάλογες με τις παραπάνω είναι και οι αρχές της τεχνικής αλκαλικής φωσφατάσης αντι αλκαλικής φωσφατάσης (τεχνική APAAP) στην οποία, στη θέση του συμπλόκου ΡΑΡ χρησιμοποιείται το σύμπλοκο ΑΡΑΑΡ. Η τεχνική αυτή χρησιμοποιείται όταν στους υπό εξέταση ιστούς υπάρχουν υψηλά επίπεδα ενδογενούς υπεροξειδάσης, όταν θέλουμε να ανιχνεύσουμε ειδικά κύτταρα που ευνοούνται από το έντονο κόκκινο χρώμα των υποστρωμάτων της αλκαλικής φωσφατάσης και σε περιπτώσεις διπλής ανοσοχρώσης σε συνδυασμό με μέθοδο υπεροξειδάσης (Dabbs David J, 2002) [Εικ. 46 & 47]. Εικόνα 46: Μέθοδοι ανοσοϋπεροξειδάσης. Α, Σύμπλοκο αντισώματος έναντι υπεροξειδάσης, άμεση μέθοδος. Β, Σύμπλοκο αντισώματος έναντι υπεροξειδάσης, έμμεση μέθοδος. Γ, Μέθοδος σεσημασμένου αντιγόνου. Δ, Μέθοδος ενζυμικής γέφυρας. Ε, Μέθοδος ανοσοσυμπλέγματος υπεροξειδάσης αντιϋπεροξειδάσης (ΡΑΡ). Το χρωματιστό ημικύκλιο αναπαριστά το αντιγόνο. 149
150 Εικόνα 47: Ανοσοενζυμικές τεχνικές βιοτίνης αβιδίνης. Χρωματιστό ημικύκλιο: αντιγόνο, ΡΧ: υπεροξειδάση, : βιοτίνη, σταυρός: αβιδίνη. Α, Μέθοδος πρωτοταγούς αντισώματος συνδεδεμένου με βιοτίνη. Β, Μέθοδος υπεροξειδάσης συνδεδεμένης με βιοτίνη. Γ, Μέθοδος συμπλόκου αβιδίνης βιοτίνης υπεροξειδάσης. ΜΕΘΟΔΟΣ ΒΙΟΤΙΝΗΣ ΑΒΙΔΙΝΗΣ (BIOTIN AVIDIN PROCEDURE) Στη μέθοδο αυτή εκμεταλλευόμαστε τον υψηλό βαθμό συγγένειας μεταξύ βιοτίνης και αβιδίνης. Με χημική διαδικασία συνδέεται η βιοτίνη με το πρωτοταγές αντίσωμα σχηματίζοντας σύμπλοκη ένωση. Με την τοποθέτηση της ένωσης αυτής στον ιστό γίνεται σύνδεσή της με το ανάλογο αντιγόνο, όπου και αν υπάρχει αυτό. Κατόπιν προστίθεται η αβιδίνη η οποία έχει σημανθεί με υπεροξειδάση. Η αβιδίνη εντοπίζει το σύμπλοκο βιοτίνης αντισώματος με το οποίο ενώνεται σταθερά, μεταφέροντας την υπεροξειδάση στη θέση όπου βρίσκεται το αντιγόνο. Μειονέκτημα της μεθόδου αποτελεί το γεγονός ότι μερικοί ιστοί διαθέτουν σημαντικές ποσότητες ενδογενούς βιοτίνης, με αποτέλεσμα να συνδέουν άμεσα το σύμπλοκο αβιδίνης υπεροξειδάσης, δίνοντας ψευδώς θετικό αποτέλεσμα. Επί πλέον φαίνεται ότι οι διαφορετικές παρτίδες βιοτίνης και αβιδίνης εμφανίζουν μεταξύ τους ποικίλης έντασης συγγένεια με αποτέλεσμα να επηρεάζεται η αναπαραγωγιμότητα της μεθόδου σε δια 150
151 φορετικά εργαστήρια. Αρκετά από τα προβλήματα αυτά επιλύονται με τη χρήση στρεπταβιδίνης αντί της βιοτίνης (B SA method). H στρεπταβιδίνη είναι ένα τετραμερές ανάλογο της αβιδίνης που απομονώθηκε από το βακτήριο streptomyces avidinii και έχει την ιδιότητα να συνδέεται με τη βιοτίνη με πολύ υψηλή συγγένεια. Θεωρητικά, η συγγένεια αυτή είναι περίπου 10 φορές μεγαλύτερη από τη συγγένεια των περισσοτέρων αντισωμάτων προς τα αντιγόνα τους και παρέχει ανίχνευση της σύνδεσης αντιγόνου αντισώματος με αυξημένη ειδικότητα. Το μόριο της στρεπταβιδίνης δεν περιέχει υδατάνθρακες, γεγονός που εμποδίζει την μη ειδική σύνδεση με μόρια ανάλογα των λεκτινών που βρίσκονται σε αρκετούς ιστούς όπως νεφροί, ήπαρ και εγκέφαλος (Dabbs David J, 2002). Το σύμπλοκο στρεπταβιδίνης βιοτίνης, σχηματίζει ένα πολύ σταθερό αντιδραστήριο, που μπορεί να αραιωθεί και να αποθηκευθεί για μεγάλο χρονικό διάστημα και δεν δημιουργεί μη ειδικούς ηλεκροστατικούς δεσμούς. Πολύ σημαντική εξέλιξη στην ανοσοϊστοχημεία ήταν η επινόηση μεθόδων τεχνικών που ενίσχυαν την ευαισθησία της. Ο σκοπός αυτών των τεχνικών ήταν να αποκαλύψουν επιτόπους (αντιγονικές θέσεις) που κανονικά είναι καλυμμένοι γιαυτό και ονομάστηκαν μέθοδοι αποκάλυψης ή επανάκτησης του αντιγόνου (McCarty KS Jr et al., 1985; Gown A et al., 1993; Momose J et al., 1993). Τέτοιες μέθοδοι είναι η πέψη του ιστού με πρωτεολυτικά ένζυμα, η επεξεργασία του με μικροκύματα, και η έκθεσή του σε υψηλή θερμοκρασία και υψηλή πίεση συγχρόνως (Silverberg SG, 1990). Παράλληλα η πρόσφατα εξελισσόμενη τεχνική tissue microarrays η οποία επιτρέπει την σύγχρονη εκτίμηση σε πάνω από 100 διαφορετικά δείγματα με μια μόνο σταγόνα αντισώματος πάνω σε ένα πλακίδιο, αναπτύσσεται συνεχώς και νέες εκδοχές της ανακοινώνονται καθημερινά στη σχετική βιβλιογραφία (Callagy G et al., 2003; Hoos A et al., 2001). Στην προσπάθεια να αυξηθεί η ευαισθησία της ανοσοϊστοχημείας έχουν επινοηθεί διάφοροι συνδυασμοί των παραπάνω μεθόδων και κυκλοφορούν στο εμπόριο συσκευασίες (kits) που αυξάνουν τη 151
152 σταθερότητα των αποτελεσμάτων, αφού μειώνουν σημαντικά τις πιθανότητες λάθους στην αραίωση των αντιδραστηρίων ή στη σειρά των σταδίων της τεχνικής. Η παράλληλη ανάπτυξη συσκευών και οργάνων επιτρέπει την αυτοματοποίηση της μεθόδου και την καθιστά οικονομικά συμφερότερη λιγότερο χρονοβόρα και πιο αξιόπιστη. Σήμερα η πλειοψηφία των παραγομένων αντισωμάτων χρησιμοποιείται στην ανίχνευση αντιγόνων που βρίσκονται σε νεοπλασματικά κύτταρα. Τα αντιγόνα αυτά είναι πρωτεΐνες ή γλυκοπρωτείνες εντοπιζόμενες στον πυρήνα, το κυτταρόπλασμα ή την κυτταρική μεμβράνη. Η ακριβής γνώση της εντόπισης του κάθε αντιγόνου καθώς και τυχόν ιδιαίτερη ποιότητα της θετικής έκφρασης του, είναιπροαπαιτούμενα για την σωστή και αποτελεσματική εκτίμηση του αποτελέσματος. Για παράδειγμα, τα περισσότερα αντισώματα έναντι αντιγόνων των λευκοκυττάρων εντοπίζονται στην κυτταρική μεμβράνη, οπότε εκεί αναμένεται η θετική χρώση. Το ίδιο ισχύει και για το αντίσωμα cerb B2. Αντίθετα, αναμένεται πυρηνική χρώση για τ αντισώματα έναντι των ορμονικών υποδοχέων είτε έναντι του δείκτη κυτταρικού πολλαπλασιαμού Ki 67. Τα περισσότερα εκ των λοιπών αντισωμάτων εντοπίζουν αντιγόνα του πρωτοπλάσματος των κυττάρων. ΠΡΟΒΛΗΜΑΤΑ ΜΕΘΟΔΟΥ ΑΝΟΣΟΪΣΤΟΧΗΜΕΙΑΣ ΠΡΟΒΛΗΜΑΤΑ ΑΝΟΣΟΤΕΧΝΙΚΗΣ Όπως και κάθε άλλη εργαστηριακή τεχνική η ανοσοϊστοχημεία για να αποβεί χρήσιμη πρέπει να εκτιμάται με την απαιτούμενη προσοχή και από παθολογοανατόμους που γνωρίζουν τις παγίδες που μπορεί να κρύβει. Πολλές παγίδες κρύβει το τεχνικό μέρος της μεθόδου, που οι περισσότερες μπορούν να αποφευχθούν, όταν η τεχνική είναι σχολαστικά ακριβής, γίνεται περιοδικά έλεγχος της δραστηριότητας των αντισωμάτων και χρήση θετικών και αρνητικών μαρτύρων (Rosai and Ackerman s Surgical Pathology, 2004). Όταν διαπιστώνουμε τεχνικό πρόβλημα, σκόπιμο είναι να θυμόμαστε ότι αυτό μπορεί να δημιουργήθηκε πριν από τη χρώση, να αφορά δηλαδή σε 152
153 καθυστέρηση της μονιμοποίησης του ιστού, ανεπαρκή μονιμοποίηση, άνιση μονιμοποίηση, ανεπαρκή αφυδάτωση προ της εμπέδωσης στην παραφίνη λόγω βλάβης του μηχανήματος επεξεργασίας των ιστών, επιλογή ακατάλληλων αντικειμενοφόρων πλακών και κακή τομή του ιστού με αναδιπλώσεις ή ρωγμές, ή να δημιουργήθηκε στη διάρκεια της χρώσης και να αφορά σε χρησιμοποίηση ληγμένων αντιδραστηρίων, ακατάλληλη αραίωση, παράλειψη βημάτων της χρώσης, ξήρανση του δείγματος, ακατάλληλο χρωμογόνο ή ακατάλληλο μέσο επικάλυψης (Silverberg SG, 1990). Οπωσδήποτε είναι σε κάθε περίπτωση βασικό είναι να θυμόμαστε ότι ψευδώς αρνητικά αποτελέσματα έχουμε όταν : 1. Το αντίσωμα είναι ακατάλληλο, εξασθενημένο ή χρησιμοποιείται σε λάθος πυκνότητα. 2. Υπάρχει απώλεια του αντιγόνου λόγω διάχυσης ή αυτόλυσης. 3. Το αντιγόνο στον ιστό βρίσκεται σε πυκνότητα χαμηλότερη από την πυκνότητα που απαιτείται για να ανιχνευθεί από τα αντιδραστήρια και την χρησιμοποιούμενη μέθοδο (Rosai and Ackerman s Surgical Pathology, 2004). Για τους παραπάνω λόγους ένα αρνητικό ανοσοϊστοχημικό αποτέλεσμα ακόμα και όταν υπάρχει θετικός μάρτυρας, δεν είναι αρκετό για να αποκλείσει μια διάγνωση κυρίως όταν η διάγνωση αυτή υποστηρίζεται από τα μορφολογικά χαρακτηριστικά και τα στοιχεία του κλινικού ιστορικού. Απαιτείται ιδιαίτερη προσοχή στην αξιολόγηση λόγω της πιθανότητας ψευδώς θετικού αποτελέσματος. Σε αυτή την περίπτωση, η αντίδραση δίνει ένα θαμπό καφέ χρώμα, με κοκκώδη είτε «αραχνοΰφαντη» υφή, και εντοπίζεται σχεδόν πάντα στο κυτταρόπλασμα (Chan JK, 2000). Ψευδώς θετικά αποτελέσματα έχουμε όταν : 1. Το αντίσωμα αντιδρά με διαφορετικά αντιγόνα από αυτά που αναζητούμε. 2. Υπάρχει μη ειδική πρόσδεση του αντισώματος στον ιστό (Buffa R et al., 1979). 3. Παρουσία ενδογενούς υπεροξειδάσης ή έλξη για το σύμπλεγμα αβιδίνης βιοτίνης σε ή από κάποια στοιχεία του ιστού. 153
154 4. Φαγοκυττάρωση (εγκλωβισμός) φυσιολογικών ιστών από νεοπλασματικά κύτταρα4. 5. Απελευθέρωση πρωτεϊνών από το κυτταρόπλασμα φυσιολογικών κυττάρων, τα οποία καταστρέφονται από ένα διηθητικό νεόπλασμα και εισχώρηση τους στα νεοπλασματικά κύτταρα όπου ακολούθως ανιχνεύονται ανοσοϊστοχημικά (Dranoff G et al., 1984). 6. Έκτοπη αντιγονική έκφραση οφειλόμενη σε άγνωστη μέχρι τώρα διασταυρούμενη αντίδραση, ή στο γεγονός ότι ένα, θεωρούμενο ειδικό, για κάποιον όγκο αντίσωμα, αποδεικνύεται ότι αντιδρά και με άλλα νεοπλάσματα (Rosai and Ackerman s Surgical Pathology, 2004; Agu O et al., 2002). ΠΡΟΒΛΗΜΑΤΑ ΑΞΙΟΛΟΓΗΣΗΣ ΚΑΙ ΠΟΣΟΤΙΚΟΠΟΙΗΣΗ ΑΝΟΣΟΪΣΤΟΧΗΜΕΙΑΣ Ο όρος «ημιποσοτική μέθοδος» που χαρακτηρίζει την ανοσοϊστοχημεία, στερείται σαφούς ορισμού, όμως δύναται να συνεπάγεται από ορισμένα χαρακτηριστικά της «ποσοτικής» μεθόδου. Η ανοσοϊστοχημική αντίδραση είναι δυνατόν να εντοπιστεί στην κυτταροπλασματική μεμβράνη, στο κυτταρόπλασμα, στον πυρήνα των κυττάρων ή και στο στρώμα. Η αξιολόγηση της αντίδρασης μπορεί να κυμαίνεται από την παρουσία ή την απουσία της έκφρασης του εξεταζόμενου μορίου. Εάν η ένταση είναι αξιολογήσιμη, τότε θα πρέπει να υπάρχει ένας θετικός μάρτυρας (control) που θα έχει περάσει ακριβώς από τα ίδια στάδια με το ελεγχόμενο δείγμα και το τελευταίο θα αξιολογηθεί βάσει του μάρτυρα. Έχοντας αυτήν τη συνθήκη, υπερπηδάται το πρόβλημα των ποικίλων πειραματικών συνθηκών (αραιώσεις αντισωμάτων, χρόνοι επωάσεων αντισωμάτων κλπ) και είναι εφικτή η αξιολόγηση. Κατά αυτόν τον τρόπο, δεν αρμόζει η αυθαιρεσία του αξιολογητή που θα χαρακτηρίσει τη χρώση «ασθενή, μέτρια, ισχυρή» με βάση την προσωπική του εμπειρία και γνώση. Η αξιολόγηση της έντασης της ανοσοαντίδρασης μπορεί να κυμαίνεται μεταξύ μίας πολύ προσεκτικής μέτρηση των ανοσοθετικών στοιχείων και μίας 154
155 γρήγορης μικροσπόπησης ολόκληρης της τομής. Είναι δυνατόν να περιλαμβάνει τη μέτρηση άνω των 1000 κυττάρων που εμφανίζουν ανοσοϊστοχημική χρώση, ώστε να αποδοθεί ένα ποσοστό αυτών, αλλά και τη μέτρηση των θετικών κυττάρων σε 10 οπτικά πεδία που οι τομές εμφανίζουν την καλύτερη δομή, διάταξη και χρώση. Τα πεδία αυτά ονομάζονται υψηλής δύναμης πεδία (high-power fields, HPF). Λιγότερη ακρίβεια στην αξιολόγηση της αναλογίας των ανοσοθετικών κυττάρων σε μία τομή, είναι η απόδοση σε ποσοστά επί τοις εκατό. Το πρόβλημα στην αξιολόγηση με ποσοστά είναι ότι διαφορετικές ερευνητικές ομάδες μπορεί να καταλήξουν σε διαφορετικά ποσοστά για το ίδιο αντίσωμα που θα έχει υποβληθεί στις ίδιες πειραματικές συνθήκες. Η σύγκριση μεταξύ διαφορετικών μελετών είναι δύσκολη. Έχουν εισαχθεί συστήματα αξιολόγησης και βαθμολόγησης ώστε να ξεπεραστούν οι παραλλαγές και ειδικότερα για μόρια-δείκτες που χρησιμοποιούνται για θεραπευτικούς σκοπούς. Το H-score (McCarty KS Jr et al., 1985) πρωτοεισήχθηκε για την αξιολόγηση των οιστρογονικών υποδοχέων (ER, Estrogen Receptors) αλλά έχει χρησιμοποιηθεί σε ένα μεγάλο φάσμα δεικτών (Gee JM et al., 2000; Abd El-Rehim DM et al., 2005). Λαμβάνει υπόψιν του την ανοσοαντίδραση και την κατανομή και αποτελεί το άθροισμα του επί τοις εκατό ποσοστού των κυττάρων με ασθενή, μέτρια και ισχυρή χρώση, ενώ το εύρος του κυμαίνεται μεταξύ του 0 και του 400. Είναι δυνατόν η αξιολόγηση να είναι ακριβής αλλά δεν παύει να είναι χρονοβόρα και για αυτόν το λόγο έχουν εισαχθεί και άλλα συστήματα αξιολόγησης και βαθμολόγησης. Οι McCarty et al., περιέγραψαν πρώτη φορά την αξιολόγηση του ER με τη χρήση ενός μαθηματικού τύπου που περιελάμβανε το ποσοστό των ανοσοθετικών κυττάρων και την ένταση της ανοσοαντίδρασης που εμφάνιζαν. Το H-score υπολογίστηκε βάσει του εξής τύπου: HS = x(+) + 2x(++) + 3x(+++), 155
156 όπου: x(+): ποσοστό κυττάρων με ασθενη ένταση στη χρώση, x(++): ποσοστό κυττάρων με μέτρια ένταση στη χρώση, x(+++): ποσοστό κυττάρων με έντονη ένταση στη χρώση. Η έκφραση του ER βαθμολογήθηκαν σε σχέση με το H-score: h-score = (0) απουσία της έκφρασης-μη ανιχνεύσιμη χρώση, h-score = (1+) ασθενής έκφραση, h = (2+) μέτρια έκφραση, h-score = (3+) έντονη έκφραση (McCarty KS Jr et al., 1985). Η γρήγορη μέτρηση quick score (Reiner A et al., 1990) βασίζεται στο ποσοστό των ανοσοθετικών κυττάρων με εύρος από 1 έως 4 και στη συνολική ένταση από 1 έως 3, η οποία προστίθεται, αλλά για τους ER έχει αντικατασταθεί από το Allred score (Harvey JM et al., 1999), το οποίο επεκτείνεται από το χαμηλότερο άκρο της βαθμολόγησης, δίνοντας ένα εύρος της τάξεως 1 έως 5. Αυτό το score προέρχεται από την αξιολόγηση μίας ομάδας καρκίνων του μαστού, στην οποία προηγουμένως είχαν αναλυθεί οι ER με βιοχημικές δοκιμασίες. Η επίκριση αυτών των συστημάτων είναι ότι απαιτούν χρόνο και οι βαθμοί έντασης προστίθονται, ενώ εάν πολλαπλασιαζόνταν θα ήταν περισσσότερο κατάλληλα (Detre S et al., 1995). Στην πραγματικότητα, όλα τα συστήματα αξιολόγησης φαίνεται πως δίνουν στατιστικά σημαντική συσχέτιση με τη κλινική έκβαση, όταν χρησιμοποιούνται από άτομα με επιστημονική εμπειρία (Barnes DM et al., 1996; Fisher ER et al., 2005). Ωστόσο απαιτείται πολύ περισσότερη προσπάθεια ώστε να βελτιωθεί η ποιότητα των ανοσοϊστοχημικών χρώσεων, χρησιμοποιώντας έναν ασφαλή ποιοτικό φορέα όπως η Εθνική Υπηρεσία Εξωτερικής Ποιοτικής Αξιολόγησης (θα αναφερθούμε σε παρακάτω παράγραφο). Χαρακτηριστικό είναι το παράδειγμα μελέτης του Fisher et al., όπου ερμηνεύτηκαν 24% ψευδώς θετικά περιστατικά για ER χρώση (Rudiger T et al., 2002). 156
157 Ένα τελείως διαφορετικό σύστημα εισήχθει για ένα δείκτη που χρησιμοποιείται για θεραπευτικούς σκοπούς, τον HER-2 (Human Epidermal Growth Factor Receptor 2). Πρόκειται για το σύστημα που εγκρίθηκε από το HercepTest United States Food and Drug και αξιολογεί με 0, 1+, 2+, 3+. Για να λάβει η τομή 3+, θα πρέπει να διαθέτουν τα κύτταρά του έντονη χρώση στην κυτταροπλασματική μεμβράνην και σε ποσοστό >10% των καρκινικών κυττάρων. Ενώ για το 2+ για πρέπει η χρώση να είναι μέτρια και για το 1+ να είναι ασθενής και να μην υπάρχει πλήρης χρώση του κυττάρου. Η κυτταροπλασματική χρώση δεν αξιολογείται. Η αναγνώριση της έντονης χρώσης των καρκινικών κυττάρων ως 3+ δεν είναι δύσκολη. Το πρόβλημα δημιουργείται με την αναλογία των 1+ και 2+ περιστατικών (Barlett JM et al., 2001; Tubbs RR et al., 2001; Zarbo Rj et al., 2001) και απαντάται πολύ συχνά σε εργαστήρια που ερευνούν μικρό πλήθος δειγμάτων (Paik S et al., 2002). Αυτοματοποιημένη Ανάλυση Η αξιολόγηση της ανοσοϊστοχημείας συνήθως γίνεται «χειροκίνητα» και εξαρτάται από την εμπειρία και την εγρήγορση του αξιολογητή. Το να αυτοματοποιηθεί η αξιολόγηση με image analysis, έχει λάβει χώρα από το 1980 (Bacus S et al., 1988) και φαίνεται να διαθέτει μεγαλύτερη ακριβεία σε σχέση με το H-score, το οποίο χαρακτηρίζεται από διακυμάνσεις (McClelland RA et al., 1991). Ένα πρόβλημα από τη χρήση διαμινοβενζιδίνης ως χρωμογόνο, είναι ότι υπάρχει μια μονοδιάστατη σχέση μεταξύ του συνόλου του αντιγόνου και της έντασης της χρώσης στα χαμηλά επίπεδα της τελευταίας (Fritz P et al., 1995). Τα προγράμματα ανάλυσης της εικόνας αξιολογούν το σύνολο της χρώσης μετρώντας την απορρόφηση, και έτσι η μη-μονοδιάστατη σχέση μεταξύ αντιγόνου και έντασης που συμβαίνει στα υψηλά επίπεδα της χρώσης, μπορεί να είναι αποτέλεσμα ανακριβών ερμηνειών. Η ανάλυση της εικόνας έχει προταθεί ως μια πιο αξιόπιστη μεθοδός για την αξιολόγηση του HER-2 (Wang S et al., 2001; Bloom K et al., 2004; Tawfik OW et al., 2006). 157
158 Ασθενείς και δείγματα Το υλικό της μελέτης αυτής περιελάμβανε ιστοτεμάχια φλεβών τα οποία ελήφθησαν από 55 άνδρες με κιρσοκήλη και συνοδό υπογονιμότητα που υπεβλήθησαν σε απολίνωση των έσω σπερματικών φλεβών κατά Marmar. Κάθε ασθενής αποτελούσε και τον δικό του «μάρτυρα», καθώς ως υλικό ελέγχου (control) χρησιμοποιήθηκαν δείγματα από επιπολής φλέβες του υποδόριου λίπους (κλάδοι των επιπολών κάτω επιγαστρικών φλεβών), οι οποίες συνήθως απολινώνονται κατά την διενέργεια της υποβουβωνικής τομής. Στην προσπάθειά μας να εκτιμήσουμε πιθανές διαφορές της ΕΤ1 και των υποδοχέων της ΕΤΑ και ΕΤΒ σε ασθενείς μικρότερης ηλικίας που έπασχαν από κιρσοκήλη, ελήφθησαν κιρσοειδείς φλέβες δεκαέξι (n=16) παιδιών τα οποία χειρουργήθηκαν με την τεχνική Palomo στο Καραμανδάνειο Νοσοκομείο Πατρών. Οι ιστοί μονιμοποιήθηκαν σε ισότονο ρυθμιστικό διάλυμα φορμαλδεΰδης (ουδέτερη φορμόλη) 10% σε θερμοκρασία δωματίου για 24 έως 48 ώρες. Οι ιστικές τομές υπεβλήθησαν στα απαιτούμενα στάδια προετοιμασίας προκειμένου να καταστούν κατάλληλες προς εξέταση στο φωτονικό μικροσκόπιο. Τα στάδια προετοιμασίας πραγματοποιούνται στην ιστοκινέτα και περιλαμβάνουν: α) αφυδάτωση, μέσω διαδοχικών εμβαπτίσεων σε υδατικά διαλύματα αιθανόλης από %, β) διαύγαση. Ο ιστός διαποτίσθηκε με ειδικό διαλύτη, την ξυλόλη, η οποία αναμειγνύεται με το υλικό έγκλεισης και γ) σκήνωση σε παραφίνη. Ο ιστός τοποθετήθηκε σε λιωμένη παραφίνη σε κλίβανο σε θερμοκρασία ο C. Η υψηλή θερμοκρασία προκαλεί εξάτμιση της ξυλόλης και αντικατάστασή της από την παραφίνη. Ο εμποτισμένος με παραφίνη ιστός στερεοποιείται μετά την έξοδό του από τον κλίβανο [Εικ. 43]. Από τους σκηνωμένους σε παραφίνη ιστούς ελήφθησαν, με ειδικό μικροτόμο [Εικ. 44], εν σειρά ιστολογικές τομές πάχους 4μm, οι οποίες 158
159 τοποθετήθηκαν σε αντικειμενοφόρους πλάκες Menzel-Gläser SuperFrost, για την εφαρμογή των ιστοχημικών και ανοσοϊστοχημικών μεθόδων [Εικόνα 45]. Η επικόλληση βελτιώθηκε με θέρμανση των τομών στους 56 o C επί 30 min. Στον πίνακα 5 φαίνεται το είδος των αντισωμάτων (μονοκλωνικό - mab ή πολυκλωνικό pab), η μέθοδος ανάδειξης των αντιγονικών επιτόπων, ο χρονός επώασης, η αραίωση και η κατασκευάστρια εταιρεία. Οι αραιώσεις που τελικά χρησιμοποιήθηκαν (optimal concentrations) για όλα τα αντισώματα καθορίστικα μετά από δοκιμαστικές χρώσεις στις οποίες εκτιμήθηκαν τα ποιοτικά αποτελέσματα πολλών αραιώσεων. Από αυτές επιλέχθηκαν οι αραιώσεις εκείνες στις οποίες συνδυαζόταν η βέλτιστη ένταση της χρώσης με το μικρότερο δυνατό βαθμό μη ειδικής χρώσης του υποστρώματος (background). Αντίσωμα Προεργασία Συνθήκες Επώασης Αραίωση Προέλευση- Είδος Abs anti-et1 ΟΧΙ Blocking 5% TBS/BSA 1h RT / Ολονύκτια- (ΟΝ) (4 0 C) 1:100 Acris Antibodies GmbH (μονοκλωνικό anti-eta anti-etb Μικροκύματα -Κιτρικό Νάτριο Μικροκύματα -Κιτρικό Νάτριο anti-erk1/2 Μικροκύματα -Κιτρικό Νάτριο Anti-ACTIN Μικροκύματα -Κιτρικό Νάτριο No blocking/ Ολονύκτια-(ΟΝ) (4 0 C) No blocking/ Ολονύκτια-(ΟΝ) (4 0 C) No blocking/ Ολονύκτια-(ΟΝ) (4 0 C) No blocking/ 1h (RT) (θερμοκρασια δωματίου) Πίνακας 5: Πρωτογενή αντισώματα και συνθήκες επώασης mab) 1:250 Acris Antibodies GmbH (πολυκλωνικό pab) 1:250 Acris Antibodies GmbH (πολυκλωνικό pab) 1:500 Acris Antibodies GmbH (μονοκλωνικό mab) 1:50 Novocastra (μονοκλωνικό mab) 159
160 Περιγραφή της ανοσοϊστοχημικής μεθόδου βιοτίνηςστρεπταβιδίνης/υπεροξειδάσης με τη χρήση φούρνου 1. Αποπαραφίνωση των τομών με ολονύκτια επώαση στον κλίβανο, στους 56 0 C, και διαδοχική εμβάπτιση των τομών σε τέσσερις ξυλόλες (Surgipath) (3x5min στους 56 0 C και 1x5min σε θερμοκρασία δωματίου). Εμβάπτιση των τομών σε ισομοριακό μίγμα ξυλόλης/αλκοόλης για 2 min. 2. Ενυδάτωση των τομών σε κατιούσα αλκοολών (100 0, 96 0 ) για 1 min σε κάθε διάλυμα. 3. Έκπλυση με νερό βρύσης και απιονισμένο (2-3 φορές). 4. Τοποθέτηση των τομών σε διάλυμα Tris-HCL-buffered saline (TBS) 0.05 Μ, ph=7.6 για 5 min. 5. Ανάκτηση αντιγονικών επιτόπων με θερμική επεξεργασία σε φούρνο μικροκυμάτων. Οι τομές τοποθετούνται σε κυβέτες με ρυθμιστικό διάλυμα κιτρικού νατρίου 10 mm, ph=6, και θερμαίνονται στα 800 Watt για 2 min και στα 300 Watt για 7 min. Οι τομές παραμένουν σε θερμοκρασία δωματίου για min. 6. Έκπλυση των τομών με απιονισμένο νερό. 7. Έκπλυση των τομών με TBS για 2x5 min. 8. Κατανάλωση ενδογενούς υπεροξειδάσης σε υδατικό διάλυμα Η 2 Ο 2 30% για 20 min. Η αντίδραση λαμβάνει χώρα σε σκοτεινό θάλαμο. 9. Έκπλυση των τομών με απιονισμένο νερό. 10. Έκπλυση των τομών με TBS για 2x5 min. 11. Κάλυψη των μη ειδικών θέσεων πρόσδεσης του αντισώματος (αποφυγή της μη ειδικής ανοσοϊστοχημικής χρώσης) με επώαση των τομών με TBS/BSA 3% για 10 min. 12. Έκπλυση των τομών με διάλυμα TBS (2x5 min). 13. Επώαση με το πρωτογενές αντίσωμα στην κατάλληλη αραίωση. Η αραίωση έγινε στο ειδικό διάλυμα Antibody Diluent ChemΜate S2022 (DakoCytomation, USA). 14. Έκπλυση των τομών με διάλυμα TBS, ph=7.6, για 3x5 min. 160
161 15. Επώαση των τομών σε υδατικό διάλυμα Η 2 Ο 2 30% για 3 min. Η αντίδραση λαμβάνει χώρα σε σκοτεινό θάλαμο. 16. Έκπλυση των τομών με διάλυμα TBS, ph=7.6, για 2x5 min. 17. Eπώαση των τομών με το ειδικό σημασμένο πολυμερές DAKO EnVisionTM+, HRP, (Dakocytomation, USA) για 30 min. 18. Έκπλυση των τομών με διάλυμα TBS, ph=7.6, για 2x5 min. 19. Ανίχνευση των θέσεων δέσμευσης της υπεροξειδάσης με την εφαρμογή διαλύματος Η 2 Ο 2 και 3,3 -τετραϋδροχλωρικής διαμινο-βενζιδίνης (DAB) για 5-10 min. Η DAB δίδει ένα καφέ παράγωγο ανθεκτικό στην αλκοόλη και την ξυλόλη. 20. Έκπλυση των τομών με νερό βρύσης για 2x5 min. 21. Χρώση αντίθεσης των πυρήνων (counterstain) με αιματοξυλίνη Harris (Surgipath) για 5 min και στιγμιαία εμβάπτιση των τομών σε οξυνισμένη αλκοόλη για την αφαίρεση της περίσσειας αιματοξυλίνης. 22. Έκπλυση των τομών με νερό βρύσης. 23. Αφυδάτωση του ιστού σε ανιούσα αλκοολών (80 0, 96 0, 100 0, ). 24. Διαύγαση των τομών σε ξυλόλες (3x5 min). 25. Επικόλληση καλυπτρίδων με τη χρήση διαλυτού στην ξυλόλη μέσου (Entellan, Merck, Germany). Διαλύματα TRIS-BUFFER 0,05M: 6,1gr TRIS σε 1000ml H 2 O απεσταγμένο. Ρύθμιση ph 7,6 με 1N HCl. Διάλυμα NaCl: 8,1gr NaCl σε 900ml H 2 O απεσταγμένο. Tris-buffer saline (TBS) ph 7,6: 900ml NaCl (διάλυμα) + 100ml TRIS BUFFER ph 7,6. Διάλυμα Η 2 Ο 2 0,3%: 98ml μεθανόλη + 2ml Η 2 Ο 2 30%. Διάλυμα Κιτρικού Νατρίου 0,01mM: 2,94gr Κιτρικού Νατρίου σε 1lt απεσταγμένο νερό. Ρύθμιση ph 6. Οξυνισμένη αλκοόλη: 105ml απόλυτη αλκοόλη + 45ml H 2 O απεσταγμένο + 1,5ml HCl. 161
162 Ανοσοϊστοχημική εκτίμηση Η εκτίμηση της ανοσοϊστοχημικής χρώσης έγινε με τη χρήση φωτονικού μικροσκοπίου και κάμερας Nikon eclipse TE 200U, ανεξάρτητα από έναν παθολογοανατόμο (Ε.Π.) και έναν ερευνητή (Χ.Χ.). Σε περιπτώσεις ασυμφωνίας στην αξιολόγηση των περιστατικών καταλήγαν σε ένα κοινό αποτέλεσμα κατόπιν συζήτησης. Η ανοσοϊστοχημική αντίδραση εκτιμήθηκε με ημιποσοτική μέθοδο, κατά την οποία δημιουργείται μία βαθμολογία που ονομάζεται Histoscore, η οποία προκύπτει από συνδυασμό της έντασης και της κατανομής της χρώσης. Η κατανομή βαθμολογείται με μια κλίμακα από το 0 έως το 3 βάσει του ποσοστού των θετικών κυττάρων. Συγκεκριμένα: 0: ανοσοαντίδραση σε <10% των κυττάρων 1: 10%-35% των κυττάρων 2: 35%-70% των κυττάρων 3: >70% των κυττάρων. Η διαβάθμιση της έντασης της χρώσης έγινε με τη χρήση κλίμακας 4 βαθμών, σύμφωνα με την παραδοχή: 0: μη ανιχνεύσιμη χρώση 1+: ασθενούς έντασης χρώση 2+: μέτριας έντασης χρώση 3+: ισχυρής έντασης χρώση. Η αρνητική χρώση αντιστοιχεί στη συνολική απουσία της χρώσης, η ισχυρή σε αυτήν που είναι δυνατόν να διακρίνεται εύκολα με φωτονικό μικροσκόπιο σε μεγέθυνση (x20), η ασθενής χρώση απαιτεί μεγέθυνση (x40), και τέλος η μέτρια είναι αυτή που η ένταση κυμαίνεται μεταξύ της ασθενούς και της ισχυρής χρώσης. Οι δύο παράγοντες προστέθηκαν και διαιρέθηκαν με το 2 ώστε να προκύψει το Histoscore που καταλαμβάνει τιμές από 0 έως 3, με προσαυξήσεις της τάξης του 0.5. Οι παράμετροι της έντασης και της κατανομής εκτιμήθηκαν συνδυαστικά, εφόσον κρίνεται πως μετέχουν 162
163 ισάξια στην εκτίμηση της έκφρασης των συγκεκριμένων μορίων που μελετώνται στην παρούσα εργασία. Ελήφθησαν φωτογραφίες των ιστολογικών τομών με τη χρήση ψηφιακής φωτογραφικής μηχανής Nikon DXM 1200C τοποθετημένης σε φωτονικό μικροσκόπιο Nikon Eclipse 80i με τη χρήση λογισμικού ACT-1C software (Nikon Instruments Inc., Melville, NY, USA). ΣΤΑΤΙΣΤΙΚΗ ΑΝΑΛΥΣΗ Για τη στατιστική ανάλυση των αποτελεσμάτων χρησιμοποιήθηκε το λογισμικό πρόγραμμα GraphPad PRISM 5.0 και κάθε τιμή p<0.05 θεωρήθηκε ως στατιστικώς σημαντική. Το Wilkoxon signed rank test και το Mann Whitney test εφαρμόστηκαν για τη σύγκριση μεταξύ των κιρσοειδών και των φυσιολογικών φλεβών σε ενήλικες και παιδιά αντίστοιχα. Στις περιπτώσεις που συγκρίναμε παραμέτρους σε περισσότερες από δύο ομάδες ασθενών, χρησιμοποιήσαμε το Kruskal-Wallis test. Τυχόν συσχετίσεις παραμέτρων μηκανονικής κατανομής ελέχθησαν με Spearmann r 2 test. 163
164 ΑΠΟΤΕΛΕΣΜΑΤΑ Ενήλικοι ασθενείς Στον πίνακα 6 παραθέτουμε τα κλινικά χαρακτηριστικά των ασθενών και τις παραμέτρους των σπερμοδιαγραμμάτων τους. Ηλικία ασθενών Μέσος όρος 5 η -95 η % Ηλικία - ενήλικοι (έτη) Ηλικία ανήλικοι(έτη) Παράμετροι σπέρματος Μέσος όρος 5 η -95 η % Όγκος (ml) Συγκέντρωση (10 6 /ml) Κινητικότητα 1hr, προωθητική κίνηση(%) Κινητικότητα 3hr, προωθητική κίνηση(%) Μορφολογία (% φυσιολογικά) Περιστατικά n % Σύνολο περιστατικών 55 Ετερόπλευρη Αριστερή κιρσοκήλη Ετερόπλευρη Δεξιά κιρσοκήλη Αμφοτερόπλευρη κιρσοκήλη Grade 1 κιρσοκήλη Grade 2 κιρσοκήλη Grade 3 κιρσοκήλη Πίνακας 6: Συνολικά στοιχεία των ασθενών για την ηλικία που επεβλήθησαν σε επέμβαση απολίνωσης των σπερματικών φλεβών, τις παραμέτρους του σπερμαδιαγραμμάτων τους, τον ή τους όρχεις που εντοπιζόταν οι κιρσοειδείς σπερματικές φλέβες και τις βαθμίδες της κιρσοκήλης που εμφάνιζαν. 164
165 Γράφημα 1: Σχηματική απεικόνιση της εμφάνισης της κιρσοκήλης στους αθενείς. Ο μέσο όρος ηλικίας των ενήλικων ασθενών που εξετάστηκαν ήταν τα 32.6 έτη (±0.832 sem). Αξίζει να σημειωθεί ότι το υψηλότερο ποσοστό των ασθενών (n=29, 52.8%) εμφάνιζαν αμφοτερόπλευρη κιρσοκήλη [Γράφημα 1]. Αμέσως μετά ακολούθησαν οι ασθενείς που εμφάνιζαν ετερόπλευρη κιρσοκήλη από την αριστερή πλευρά (n=25, 45,4%). Το μικρότερο ποσοστό κατέχει η ύπαρξη της κιρσοκήλης μόνο από τη δεξιά πλευρά (n=1, 1.8%). Γράφημα 2: Σχηματική απεικόνιση των βαθμίδων κιρσοκήλης των ασθενών που εξετάστηκαν. Οι περισσότεροι ασθενείς που εξετάστηκαν εμφάνιζαν βαθμίδα κιρσοκήλης Grade 2 (n=31, 56.4%). Ακολούθησαν εκείνοι με βαθμίδα κιρσοκήλης Grade 3 (n=13, 23.6%) και με μικρότερο ποσοστό ήταν οι ασθενείς με βαθμίδα κιρσοκήλης Grade 1 (n=11, 20.0%) [Γράφημα 2]. 165
Γεννητικό Σύστημα. Ioannis Lazarettos. MD PhD Orthopaedic Surgeon
 Γεννητικό Σύστημα Ioannis Lazarettos MD PhD Γεννητικό Σύστημα Άνδρα 2 Γεννητικό Σύστημα Άνδρα Όρχεις (Γεννητικοί Αδένες) Εκφορητική Οδός Σπέρματος Επιδιδυμίδα Σπερματικός Πόρος Σπερματοδόχος Κύστη Εκσπερματικός
Γεννητικό Σύστημα Ioannis Lazarettos MD PhD Γεννητικό Σύστημα Άνδρα 2 Γεννητικό Σύστημα Άνδρα Όρχεις (Γεννητικοί Αδένες) Εκφορητική Οδός Σπέρματος Επιδιδυμίδα Σπερματικός Πόρος Σπερματοδόχος Κύστη Εκσπερματικός
Τα αναπαραγωγικά όργανα του άνδρα. Όρχεις
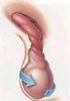 Τα αναπαραγωγικά όργανα του άνδρα Όρχεις Οι όρχεις είναι οι γεννητικοί αδένες του άνδρα. Είναι όργανα µε διπλή λειτουργία: η εξωκρινής λειτουργία είναι η παραγωγή σπερµατοζωαρίων και η ενδοκρινής είναι
Τα αναπαραγωγικά όργανα του άνδρα Όρχεις Οι όρχεις είναι οι γεννητικοί αδένες του άνδρα. Είναι όργανα µε διπλή λειτουργία: η εξωκρινής λειτουργία είναι η παραγωγή σπερµατοζωαρίων και η ενδοκρινής είναι
ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ. Σχηµατική απεικόνιση της µεγάλης και της µικρής κυκλοφορίας
 ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΑΝΑΤΟΜΙΑ Ι ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΑΙΜΟΦΟΡΑ ΑΓΓΕΙΑ ΑΡΤΗΡΙΕΣ - ΦΛΕΒΕΣ - ΤΡΙΧΟΕΙ Η 1 ΓΕΝΙΚΑ ΣΤΟΙΧΕΙΑ ΓΙΑ ΤΗΝ ΚΥΚΛΟΦΟΡΙΑ Μεγάλη και µικρή κυκλοφορία Σχηµατική
Κυκλοφορικό Σύστηµα. Σοφία Χαβάκη. Λέκτορας
 Κυκλοφορικό Σύστηµα Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας Εβρυολογίας, Ιατρική Σχολή, ΕΚΠΑ Κυκλοφορικό Σύστηµα Αιµοφόροκυκλοφορικό σύστηµα Λεµφoφόροκυκλοφορικό σύστηµα Αιµοφόρο Κυκλοφορικό Σύστηµα
Κυκλοφορικό Σύστηµα Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας Εβρυολογίας, Ιατρική Σχολή, ΕΚΠΑ Κυκλοφορικό Σύστηµα Αιµοφόροκυκλοφορικό σύστηµα Λεµφoφόροκυκλοφορικό σύστηµα Αιµοφόρο Κυκλοφορικό Σύστηµα
ΟΥΡΟΠΟΙΟΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΣΥΣΤΗΜΑ
 ΟΥΡΟΠΟΙΟΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΓΕΝΙΚΑ: Αποτελείται από όργανα που παράγουν και αποβάλουν τα ουρά => απομακρύνονται άχρηστες και επιβλαβές ουσίες + ρυθμίζεται η ισορροπία
ΟΥΡΟΠΟΙΟΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΓΕΝΙΚΑ: Αποτελείται από όργανα που παράγουν και αποβάλουν τα ουρά => απομακρύνονται άχρηστες και επιβλαβές ουσίες + ρυθμίζεται η ισορροπία
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ
 ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ
 ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Εκλ. Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Εκλ. Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
Μυικός ιστός Συσταλτά κύτταρα. Κυκλοφορικό Σύστημα. Αθανάσιος Κοτσίνας, Επικ. Καθηγητής. Εργαστήριο Ιστολογίας Εβρυολογίας, Ιατρική Σχολή, ΕΚΠΑ
 Μυικός ιστός Συσταλτά κύτταρα Κυκλοφορικό Σύστημα Αθανάσιος Κοτσίνας, Επικ. Καθηγητής Εργαστήριο Ιστολογίας Εβρυολογίας, Ιατρική Σχολή, ΕΚΠΑ ΚΑΤΗΓΟΡΙΕΣ ΣΥΣΤΑΛΤΩΝ ΚΥΤΤΑΡΩΝ 1. Μυϊκά 2. Μυοεπιθηλιακά 3. Περικύτταρα
Μυικός ιστός Συσταλτά κύτταρα Κυκλοφορικό Σύστημα Αθανάσιος Κοτσίνας, Επικ. Καθηγητής Εργαστήριο Ιστολογίας Εβρυολογίας, Ιατρική Σχολή, ΕΚΠΑ ΚΑΤΗΓΟΡΙΕΣ ΣΥΣΤΑΛΤΩΝ ΚΥΤΤΑΡΩΝ 1. Μυϊκά 2. Μυοεπιθηλιακά 3. Περικύτταρα
ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ Α. ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΑΡΡΕΝΟΣ
 1 ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ Α. ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΑΡΡΕΝΟΣ Το γεννητικό σύστημα στον άνδρα παράγει τα γεννητικά κύτταρα( σπερματοζωάρια) και τις γεννητικές ορμόνες(τεστοστερόνη) Αποτελείται από τους όρχεις Επιδιδυμίδα
1 ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ Α. ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ ΑΡΡΕΝΟΣ Το γεννητικό σύστημα στον άνδρα παράγει τα γεννητικά κύτταρα( σπερματοζωάρια) και τις γεννητικές ορμόνες(τεστοστερόνη) Αποτελείται από τους όρχεις Επιδιδυμίδα
ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ. Κάντε κλικ για να επεξεργαστείτε τον υπότιτλο του υποδείγματος
 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κάντε κλικ για να επεξεργαστείτε τον υπότιτλο του υποδείγματος ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κυκλοφορικό σύστημα Αιμοφόρο 1. 2. Καρδιά Αιμοφόρα αγγεία Λεμφοφόρο Αρτηρίες Λεμφικά τριχοειδή Φλέβες
ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κάντε κλικ για να επεξεργαστείτε τον υπότιτλο του υποδείγματος ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Κυκλοφορικό σύστημα Αιμοφόρο 1. 2. Καρδιά Αιμοφόρα αγγεία Λεμφοφόρο Αρτηρίες Λεμφικά τριχοειδή Φλέβες
Οσφυϊκό Πλέγµα και Νεύρα
 Οσφυϊκό Πλέγµα και Νεύρα Εισαγωγή Σχηµατισµός Κλάδοι του Οσφυϊκού Πλέγµατος Μηριαίο Νεύρο (Ο2-Ο4) Εισαγωγή Η κινητικότητα και η γενική αισθητικότητα του κάτω άκρου εξυπηρετούνται από τους τελικούς κλάδους
Οσφυϊκό Πλέγµα και Νεύρα Εισαγωγή Σχηµατισµός Κλάδοι του Οσφυϊκού Πλέγµατος Μηριαίο Νεύρο (Ο2-Ο4) Εισαγωγή Η κινητικότητα και η γενική αισθητικότητα του κάτω άκρου εξυπηρετούνται από τους τελικούς κλάδους
ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ ΚΑΡΔΙΑ
 1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Αποτελείται από την καρδιά και τα αγγεία( αρτηρίες, φλέβες, τριχοειδή αγγεία). Η καρδιά με τους παλμικούς ρυθμούς στέλνει το αίμα στο σώμα. Οι αρτηρίες παίρνουν το αίμα από την καρδιά
1 ΚΥΚΛΟΦΟΡΙΚΟ ΣΥΣΤΗΜΑ Αποτελείται από την καρδιά και τα αγγεία( αρτηρίες, φλέβες, τριχοειδή αγγεία). Η καρδιά με τους παλμικούς ρυθμούς στέλνει το αίμα στο σώμα. Οι αρτηρίες παίρνουν το αίμα από την καρδιά
Βιολογία Α Λυκείου Κεφ. 3. Κυκλοφορικό Σύστημα. Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα
 Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
Βιολογία Α Λυκείου Κεφ. 3 Κυκλοφορικό Σύστημα Καρδιά Αιμοφόρα αγγεία Η κυκλοφορία του αίματος Αίμα Η μεταφορά των θρεπτικών ουσιών στα κύτταρα και των ιστών και η απομάκρυνση από αυτά των άχρηστων γίνεται
Μαθήματα Ανατομίας 2011-2012
 Μαθήματα Ανατομίας 2011-2012 Πρόσθιο κοιλιακό τοίχωμα Κ. Αλπαντάκη Όρια της κοιλιάς Άνω: Πλευρικό τόξο 7-12 Ξιφοειδής απόφυση: επίπεδο 10ου πλευρικού χόνδρου = Ο3 Κάτω : Ηβικά οστά και λαγόνια ακρολοφία:
Μαθήματα Ανατομίας 2011-2012 Πρόσθιο κοιλιακό τοίχωμα Κ. Αλπαντάκη Όρια της κοιλιάς Άνω: Πλευρικό τόξο 7-12 Ξιφοειδής απόφυση: επίπεδο 10ου πλευρικού χόνδρου = Ο3 Κάτω : Ηβικά οστά και λαγόνια ακρολοφία:
ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ
 ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ ΡΙΝΙΚΗ ΚΟΙΛΟΤΗΤΑ ΣΤΟΜΑΤΙΚΗ ΚΟΙΛΟΤΗΤΑ ΦΑΡΥΓΓΑΣ ΛΑΡΥΓΓΑΣ ΤΡΑΧΕΙΑ ΒΡΟΓΧΟΙ ΠΝΕΥΜΟΝΕΣ ΠΛΕΥΡΑ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ Θυρεοειδής χόνδρος Κρικοθυρεοειδής σύνδεσμος ΤΡΑΧΕΙΑ Κρικοειδής χόνδρος
ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ ΡΙΝΙΚΗ ΚΟΙΛΟΤΗΤΑ ΣΤΟΜΑΤΙΚΗ ΚΟΙΛΟΤΗΤΑ ΦΑΡΥΓΓΑΣ ΛΑΡΥΓΓΑΣ ΤΡΑΧΕΙΑ ΒΡΟΓΧΟΙ ΠΝΕΥΜΟΝΕΣ ΠΛΕΥΡΑ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ Θυρεοειδής χόνδρος Κρικοθυρεοειδής σύνδεσμος ΤΡΑΧΕΙΑ Κρικοειδής χόνδρος
Όρχεις -Χειρισμός παρασκευάσματος -Εισαγωγή στους όγκους. Α.. Κιζιρίδου, Αναπ. Διευθύντρια Παθολογοανατομικού Τμήματος A.Ν.Θ.
 Όρχεις -Χειρισμός παρασκευάσματος -Εισαγωγή στους όγκους Α.. Κιζιρίδου, Αναπ. Διευθύντρια Παθολογοανατομικού Τμήματος A.Ν.Θ.Θεαγένειο Περιγραφική Ανατομική 2 αδένες με σχήμα δαμάσκηνου διαστ.5χ3χ2.5 Κρέμονται
Όρχεις -Χειρισμός παρασκευάσματος -Εισαγωγή στους όγκους Α.. Κιζιρίδου, Αναπ. Διευθύντρια Παθολογοανατομικού Τμήματος A.Ν.Θ.Θεαγένειο Περιγραφική Ανατομική 2 αδένες με σχήμα δαμάσκηνου διαστ.5χ3χ2.5 Κρέμονται
ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΑΤΟΜΙΑ ΟΡΘΟΥ. Γιάννης Τσιαούσης Χειρουργός, Επίκ. Καθηγητής Ανατομίας Ιατρική Σχολή, Παν/μιο Κρήτης
 ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΑΤΟΜΙΑ ΟΡΘΟΥ Γιάννης Τσιαούσης Χειρουργός, Επίκ. Καθηγητής Ανατομίας Ιατρική Σχολή, Παν/μιο Κρήτης Βασικές Ανατομικές Δομές Πυέλου πυελικό έδαφος κυρίως από διάφραγμα πυέλου χωνοειδές σχήμα
ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΑΤΟΜΙΑ ΟΡΘΟΥ Γιάννης Τσιαούσης Χειρουργός, Επίκ. Καθηγητής Ανατομίας Ιατρική Σχολή, Παν/μιο Κρήτης Βασικές Ανατομικές Δομές Πυέλου πυελικό έδαφος κυρίως από διάφραγμα πυέλου χωνοειδές σχήμα
ΟΠΙΣΘΙΟ ΚΟΙΛΙΑΚΟ ΤΟΙΧΩΜΑ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ
 ΟΠΙΣΘΙΟ ΚΟΙΛΙΑΚΟ ΤΟΙΧΩΜΑ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΟΣΤΑ (ΟΣΦΥΙΚΟΙ ΣΠΟΝΔΥΛΟΙ ΙΕΡΟ) ΟΣΦΥΙΚΟΙ ΣΠΟΝΔΥΛΟΙ Μεγαλύτεροι σε μέγεθος και όγκο, με κοντούς και παχείς αυχένες, ευρύτερες
ΟΠΙΣΘΙΟ ΚΟΙΛΙΑΚΟ ΤΟΙΧΩΜΑ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΟΣΤΑ (ΟΣΦΥΙΚΟΙ ΣΠΟΝΔΥΛΟΙ ΙΕΡΟ) ΟΣΦΥΙΚΟΙ ΣΠΟΝΔΥΛΟΙ Μεγαλύτεροι σε μέγεθος και όγκο, με κοντούς και παχείς αυχένες, ευρύτερες
Γεώργιος Τρανταλής. Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική
 Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Η αορτική
Γεώργιος Τρανταλής Επιμελητής Καρδιολογίας Κ. Υ. Καπανδριτίου Α Πανεπιστημιακή Καρδιολογική Κλινική Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Ανατομία Φυσιοπαθολογία Μελλοντικές προεκτάσεις Η αορτική
Επανάληψη πριν τις εξετάσεις Καλό διάβασμα
 Επανάληψη πριν τις εξετάσεις Καλό διάβασμα 2013-2014 Θέματα πολλαπλής επιλογής Κύτταρα όμοια μορφολογικά και λειτουργικά αποτελούν α. ένα όργανο. β. ένα ιστό. γ. ένα οργανισμό. δ. ένα σύστημα οργάνων.
Επανάληψη πριν τις εξετάσεις Καλό διάβασμα 2013-2014 Θέματα πολλαπλής επιλογής Κύτταρα όμοια μορφολογικά και λειτουργικά αποτελούν α. ένα όργανο. β. ένα ιστό. γ. ένα οργανισμό. δ. ένα σύστημα οργάνων.
ΥΔΡΟΚΗΛΗ ΠΑΘΗΣΕΙΣ ΟΣΧΕΟΥ - ΥΔΡΟΚΗΛΗ - ΚΙΡΣΟΚΗΛΗ - ΣΥΣΤΡΟΦΗ ΣΠΕΡΜΑΤΙΚΟΥ ΤΟΝΟΥ - ΚΥΣΤΗ ΕΠΙΔΙΔΥΜΙΔΑΣ - ΣΠΕΡΜΑΤΟΚΥΣΤΗ - ΚΥΣΤΕΣ ΟΣΧΕΟΥ
 ΠΑΘΗΣΕΙΣ ΟΣΧΕΟΥ - ΥΔΡΟΚΗΛΗ - ΚΙΡΣΟΚΗΛΗ - ΣΥΣΤΡΟΦΗ ΣΠΕΡΜΑΤΙΚΟΥ ΤΟΝΟΥ - ΚΥΣΤΗ ΕΠΙΔΙΔΥΜΙΔΑΣ - ΣΠΕΡΜΑΤΟΚΥΣΤΗ - ΚΥΣΤΕΣ ΟΣΧΕΟΥ ΥΔΡΟΚΗΛΗ Είναι η συλλογή υγρού μεταξύ των πετάλων του ιδίως ελυτροειδούς χιτώνα
ΠΑΘΗΣΕΙΣ ΟΣΧΕΟΥ - ΥΔΡΟΚΗΛΗ - ΚΙΡΣΟΚΗΛΗ - ΣΥΣΤΡΟΦΗ ΣΠΕΡΜΑΤΙΚΟΥ ΤΟΝΟΥ - ΚΥΣΤΗ ΕΠΙΔΙΔΥΜΙΔΑΣ - ΣΠΕΡΜΑΤΟΚΥΣΤΗ - ΚΥΣΤΕΣ ΟΣΧΕΟΥ ΥΔΡΟΚΗΛΗ Είναι η συλλογή υγρού μεταξύ των πετάλων του ιδίως ελυτροειδούς χιτώνα
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΘΗΝΑΣ ΓΙΑΓΚΙΝΗ ΧΗΜΙΚΟΥ Μελέτη των ιστολογικών και βιοχημικών αλλοιώσεων
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟΔΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΑΡΜΑΚΟΛΟΓΙΑΣ ΠΕΡΙΛΗΨΗ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΘΗΝΑΣ ΓΙΑΓΚΙΝΗ ΧΗΜΙΚΟΥ Μελέτη των ιστολογικών και βιοχημικών αλλοιώσεων
ΑΥΤΟΝΟΜΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ (ΑΝΣ) ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ
 ΑΥΤΟΝΟΜΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ (ΑΝΣ) ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΑΥΤΟΝΟΜΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ (ΑΝΣ) ΑΝΣ ΚΙΝΗΤΙΚΑ ΝΕΥΡΑ (λείοι μύες, καρδιακός μυς, αδένες) (Σπλαχνικά Νεύρα)
ΑΥΤΟΝΟΜΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ (ΑΝΣ) ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΑΥΤΟΝΟΜΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ (ΑΝΣ) ΑΝΣ ΚΙΝΗΤΙΚΑ ΝΕΥΡΑ (λείοι μύες, καρδιακός μυς, αδένες) (Σπλαχνικά Νεύρα)
ΕΡΓΑΣΤΗΡΙΟ ΙΣΤΟΛΟΓΙΑΣ Μ. ΠΑΥΛΙ ΗΣ
 ΕΡΓΑΣΤΗΡΙΟ ΙΣΤΟΛΟΓΙΑΣ Μ. ΠΑΥΛΙ ΗΣ Hράκλειο, εκέμβριος 2011 ΤΥΠΟΙ ΙΣΤΩΝ 1. Eπιθηλιακός Πολυεδρικά κύτταρα που είναι πάρα πολύ στενά συνδεδεμένα και φέρουν ελάχιστη μεσοκυττάρια ουσία 2. Συνδετικός Κύτταρα
ΕΡΓΑΣΤΗΡΙΟ ΙΣΤΟΛΟΓΙΑΣ Μ. ΠΑΥΛΙ ΗΣ Hράκλειο, εκέμβριος 2011 ΤΥΠΟΙ ΙΣΤΩΝ 1. Eπιθηλιακός Πολυεδρικά κύτταρα που είναι πάρα πολύ στενά συνδεδεμένα και φέρουν ελάχιστη μεσοκυττάρια ουσία 2. Συνδετικός Κύτταρα
Μετωπιαίο, Σφηνοειδές, Ηθμοειδές, Δακρυϊκό, Άνω γνάθος, Ζυγωματικό, Υπερώιο
 Μετωπιαίο, Σφηνοειδές, Ηθμοειδές, Δακρυϊκό, Άνω γνάθος, Ζυγωματικό, Υπερώιο Οφρύς Βλέφαρα Βλεφαρίδες Βλεφαρικοί και Σμηγματογόνοι αδένες των βλεφάρων Ανελκτήρας μυς του άνω βλεφάρου Σφιγκτήρας μυς των
Μετωπιαίο, Σφηνοειδές, Ηθμοειδές, Δακρυϊκό, Άνω γνάθος, Ζυγωματικό, Υπερώιο Οφρύς Βλέφαρα Βλεφαρίδες Βλεφαρικοί και Σμηγματογόνοι αδένες των βλεφάρων Ανελκτήρας μυς του άνω βλεφάρου Σφιγκτήρας μυς των
ΑΝΑΤΟΜΙΑ ΦΥΣΙΟΛΟΓΙΑ ΙΙ - Γ ΕΠΑΛ 13:45
 ΑΝΑΤΟΜΙΑ ΦΥΣΙΟΛΟΓΙΑ ΙΙ - Γ ΕΠΑΛ 13:45 Σελίδα 2 από 5 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΠΑΓΓΕΛΜΑΤΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ ΕΞΕΤΑΣΗΣ: ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: 14 / 06 / 2018 Ανατομία Φυσιολογία ΙΙ Γ ΕΠΑΛ
ΑΝΑΤΟΜΙΑ ΦΥΣΙΟΛΟΓΙΑ ΙΙ - Γ ΕΠΑΛ 13:45 Σελίδα 2 από 5 ΠΑΝΕΛΛΑΔΙΚΕΣ ΕΞΕΤΑΣΕΙΣ Γ ΤΑΞΗΣ ΗΜΕΡΗΣΙΟΥ ΕΠΑΓΓΕΛΜΑΤΙΚΟΥ ΛΥΚΕΙΟΥ ΗΜΕΡΟΜΗΝΙΑ ΕΞΕΤΑΣΗΣ: ΕΞΕΤΑΖΟΜΕΝΟ ΜΑΘΗΜΑ: 14 / 06 / 2018 Ανατομία Φυσιολογία ΙΙ Γ ΕΠΑΛ
12. ΑΝΑΠΑΡΑΓΩΓΗ - ΑΝΑΠΤΥΞΗ
 12. ΑΝΑΠΑΡΑΓΩΓΗ - ΑΝΑΠΤΥΞΗ Η αναπαραγωγή είναι μία χαρακτηριστική λειτουργία, η μόνη που δεν είναι απαραίτητη για την επιβίωση του ίδιου του οργανισμού αλλά για τη διαιώνιση του είδους. Η αναπαραγωγή στον
12. ΑΝΑΠΑΡΑΓΩΓΗ - ΑΝΑΠΤΥΞΗ Η αναπαραγωγή είναι μία χαρακτηριστική λειτουργία, η μόνη που δεν είναι απαραίτητη για την επιβίωση του ίδιου του οργανισμού αλλά για τη διαιώνιση του είδους. Η αναπαραγωγή στον
ΜΥΟΣΚΕΛΕΤΙΚΟ ΣΥΣΤΗΜΑ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ
 ΜΥΟΣΚΕΛΕΤΙΚΟ ΣΥΣΤΗΜΑ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΟΣΤΑ ΚΑΙ ΣΚΕΛΕΤΙΚΟ ΣΥΣΤΗΜΑ Τα οστά είναι μια στερεά μορφή συνδετικού ιστού, σχηματίζουν το μεγαλύτερο μέρος
ΜΥΟΣΚΕΛΕΤΙΚΟ ΣΥΣΤΗΜΑ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΟΣΤΑ ΚΑΙ ΣΚΕΛΕΤΙΚΟ ΣΥΣΤΗΜΑ Τα οστά είναι μια στερεά μορφή συνδετικού ιστού, σχηματίζουν το μεγαλύτερο μέρος
Νικολέττα Χαραλαμπάκη Ιατρός Βιοπαθολόγος
 Νικολέττα Χαραλαμπάκη Ιατρός Βιοπαθολόγος ΚΝΣ ΕΓΚΕΦΑΛΟΣ ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ Περιβάλλονται και στηρίζονται με τις εγκεφαλικές και νωτιαίες μήνιγγες μεταξύ των οποίων περικλείεται ο υπαραχνοειδής χώρος γεμάτος
Νικολέττα Χαραλαμπάκη Ιατρός Βιοπαθολόγος ΚΝΣ ΕΓΚΕΦΑΛΟΣ ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ Περιβάλλονται και στηρίζονται με τις εγκεφαλικές και νωτιαίες μήνιγγες μεταξύ των οποίων περικλείεται ο υπαραχνοειδής χώρος γεμάτος
Βουβωνική Χώρα. Ι. Βουβωνικός Χώρα
 Βουβωνική Χώρα Ι. Βουβωνικός Χώρα Α. Βουβωνικός Σύνδεσµος (του Poupart) Δεν είναι πραγµατικός σύνδεσµος Είναι η αναδίπλωση προς τα έσω του ελευθέρου κάτω χείλους του έξω λοξού µυός από την εκφυσή του από
Βουβωνική Χώρα Ι. Βουβωνικός Χώρα Α. Βουβωνικός Σύνδεσµος (του Poupart) Δεν είναι πραγµατικός σύνδεσµος Είναι η αναδίπλωση προς τα έσω του ελευθέρου κάτω χείλους του έξω λοξού µυός από την εκφυσή του από
Εμβρυολογία, ανατομεία, ιστολογία νεφρού
 Εμβρυολογία, ανατομεία, ιστολογία νεφρού Τα νεφρά αναπτύσσονται από αμφοτερόπλευρες μάζες ενδιαμέσου μεσοδέρματος νεφρογενείς πτυχές 3-4 εβδομάδα πρόνεφρος μεσόνεφρος μετάνεφρος δημιουργία νεφρών μετάνεφρος
Εμβρυολογία, ανατομεία, ιστολογία νεφρού Τα νεφρά αναπτύσσονται από αμφοτερόπλευρες μάζες ενδιαμέσου μεσοδέρματος νεφρογενείς πτυχές 3-4 εβδομάδα πρόνεφρος μεσόνεφρος μετάνεφρος δημιουργία νεφρών μετάνεφρος
ΟΡΓΑΝΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
 ΟΡΓΑΝΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΟΡΓΑΝΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ Διακρίνονται σε: - Πρωτογενή και - Δευτερογενή Πρωτογενή είναι τα όργανα στα οποία γίνεται η ωρίμανση των κυττάρων του ανοσοποιητικού: - Θύμος
ΟΡΓΑΝΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΟΡΓΑΝΑ ΤΟΥ ΑΝΟΣΟΠΟΙΗΤΙΚΟΥ Διακρίνονται σε: - Πρωτογενή και - Δευτερογενή Πρωτογενή είναι τα όργανα στα οποία γίνεται η ωρίμανση των κυττάρων του ανοσοποιητικού: - Θύμος
Εργαστήριο Ανατοµίας Ιατρική Σχολή Πανεπιστήµιο Αθηνών
 Εργαστήριο Ανατοµίας Ιατρική Σχολή Πανεπιστήµιο Αθηνών ΣΥΝΟΠΤΙΚΕΣ ΣΗΜΕΙΏΣΕΙΣ ΑΝΑΤΟΜΙΑΣ Το Μυοσκελετικό Σύστηµα Δρ. Ε. Τζόνσον Αναπληρώτρια Καθηγήτρια Αθήνα 2012 2 ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΑΝΑΤΟΜΙΑ Ι. Α. Τα µέρη και
Εργαστήριο Ανατοµίας Ιατρική Σχολή Πανεπιστήµιο Αθηνών ΣΥΝΟΠΤΙΚΕΣ ΣΗΜΕΙΏΣΕΙΣ ΑΝΑΤΟΜΙΑΣ Το Μυοσκελετικό Σύστηµα Δρ. Ε. Τζόνσον Αναπληρώτρια Καθηγήτρια Αθήνα 2012 2 ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΑΝΑΤΟΜΙΑ Ι. Α. Τα µέρη και
ΣΤΑΣΙΝΟΠΟΥΛΟΥ ΜΥΡΣΙΝΗ ΑΟΝΑ «Ο ΑΓΙΟΣ ΣΑΒΒΑΣ»
 ΣΤΑΣΙΝΟΠΟΥΛΟΥ ΜΥΡΣΙΝΗ ΑΟΝΑ «Ο ΑΓΙΟΣ ΣΑΒΒΑΣ» ΤΟ ΜΥΟΚΑΡΔΙΟ ΕΜΠΡΟΣ ΤΟ ΜΥΟΚΑΡΔΙΟ ΠΙΣΩ ΠΝΕΥΜΟΝΙΚΗ ΑΡΤΗΡΙΑ Η πνευμονική αρτηρία (pulmonary trunk) εκφύεται από τον αρτηριακό κώνο της δεξιάς κοιλίας. Έχει κατεύθυνση
ΣΤΑΣΙΝΟΠΟΥΛΟΥ ΜΥΡΣΙΝΗ ΑΟΝΑ «Ο ΑΓΙΟΣ ΣΑΒΒΑΣ» ΤΟ ΜΥΟΚΑΡΔΙΟ ΕΜΠΡΟΣ ΤΟ ΜΥΟΚΑΡΔΙΟ ΠΙΣΩ ΠΝΕΥΜΟΝΙΚΗ ΑΡΤΗΡΙΑ Η πνευμονική αρτηρία (pulmonary trunk) εκφύεται από τον αρτηριακό κώνο της δεξιάς κοιλίας. Έχει κατεύθυνση
Μύες Θώρακα - Κορμού
 Μύες Θώρακα - Κορμού Μύες μαστικής περιοχής Μύες πρόσθιου θωρακικού τοιχώματος Μύες κοιλιακού τοιχώματος Μύες ράχης Μύες οπίσθιου κοιλιακού τοιχώματος 1 2 3 1 Μείζων θωρακικός 1 Ελάσσων θωρακικός 2 3Υποκλείδιος
Μύες Θώρακα - Κορμού Μύες μαστικής περιοχής Μύες πρόσθιου θωρακικού τοιχώματος Μύες κοιλιακού τοιχώματος Μύες ράχης Μύες οπίσθιου κοιλιακού τοιχώματος 1 2 3 1 Μείζων θωρακικός 1 Ελάσσων θωρακικός 2 3Υποκλείδιος
12. ΑΝΑΠΑΡΑΓΩΓΗ - ΑΝΑΠΤΥΞΗ
 12. ΑΝΑΠΑΡΑΓΩΓΗ - ΑΝΑΠΤΥΞΗ Η αναπαραγωγή είναι μία χαρακτηριστική λειτουργία, η μόνη που δεν είναι απαραίτητη για την επιβίωση του ίδιου του οργανισμού αλλά για τη διαιώνιση του είδους. Η αναπαραγωγή στον
12. ΑΝΑΠΑΡΑΓΩΓΗ - ΑΝΑΠΤΥΞΗ Η αναπαραγωγή είναι μία χαρακτηριστική λειτουργία, η μόνη που δεν είναι απαραίτητη για την επιβίωση του ίδιου του οργανισμού αλλά για τη διαιώνιση του είδους. Η αναπαραγωγή στον
ΒΑΣΙΚΑ ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ Μάθημα 7 Το κυκλοφορικό μας σύστημα
 jk ΒΑΣΙΚΑ ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ Μάθημα 7 Το κυκλοφορικό μας σύστημα Εισαγωγή στο Κυκλοφορικό μας Σύστημα (ΚΣ) Το ΚΣ αποτελείται από - τα αιμοφόρα αγγεία την καρδιά Αέρας που εισπνέουμε Αέρας που εκπνέουμε
jk ΒΑΣΙΚΑ ΘΕΜΑΤΑ ΒΙΟΛΟΓΙΑΣ ΑΝΘΡΩΠΟΥ Μάθημα 7 Το κυκλοφορικό μας σύστημα Εισαγωγή στο Κυκλοφορικό μας Σύστημα (ΚΣ) Το ΚΣ αποτελείται από - τα αιμοφόρα αγγεία την καρδιά Αέρας που εισπνέουμε Αέρας που εκπνέουμε
Κάθοδος των όρχεων. 60% νεογνών: πλήρης κάθοδος μέσα στον πρώτο χρόνο της ζωής
 Κρυψορχία Εισαγωγή Πιο συχνή συγγενής ανωμαλία στα αγόρια Περίπου 30% στα πρόωρα νεγνά Περίπου 3-4% στα τελειόμηνα νεογνά τη στιγμή της γέννησης Περίπου 1% στα τελειόμηνα νεογνά στην ηλικία του ενός έτους
Κρυψορχία Εισαγωγή Πιο συχνή συγγενής ανωμαλία στα αγόρια Περίπου 30% στα πρόωρα νεγνά Περίπου 3-4% στα τελειόμηνα νεογνά τη στιγμή της γέννησης Περίπου 1% στα τελειόμηνα νεογνά στην ηλικία του ενός έτους
 ΚΑΡΔΙΑ ΚΑΡΔΙΑ Ινομυώδες κοίλο όργανο Εντόπιση: στο θώρακα - λοξή θέση Κορυφή: προς τα κάτω, εμπρός και αριστερά Βάση: προς τα πίσω, άνω και δεξιά Δεξιές κοιλότητες: δεξιός κόλπος - δεξιά κοιλία Αριστερές
ΚΑΡΔΙΑ ΚΑΡΔΙΑ Ινομυώδες κοίλο όργανο Εντόπιση: στο θώρακα - λοξή θέση Κορυφή: προς τα κάτω, εμπρός και αριστερά Βάση: προς τα πίσω, άνω και δεξιά Δεξιές κοιλότητες: δεξιός κόλπος - δεξιά κοιλία Αριστερές
ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ
 1 ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ Το ανθρώπινο σώμα προμηθεύεται οξυγόνο και αποβάλει διοξείδιο του άνθρακα με την αναπνοή. Η αναπνοή έχει δύο φάσεις: την εισπνοή κατά την οποία ο αέρας εισέρχεται στους πνεύμονες
1 ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ Το ανθρώπινο σώμα προμηθεύεται οξυγόνο και αποβάλει διοξείδιο του άνθρακα με την αναπνοή. Η αναπνοή έχει δύο φάσεις: την εισπνοή κατά την οποία ο αέρας εισέρχεται στους πνεύμονες
ΘΩΡΑΚΑΣ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ
 ΘΩΡΑΚΑΣ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΜΕΣΟΠΛΕΥΡΙΑ ΔΙΑΣΤΗΜΑΤΑ Σχηματίζονται μεταξύ παρακείμενων πλευρών και καταλαμβάνονται από τους μεσοπλεύριους μύες. Έσω θωρακική
ΘΩΡΑΚΑΣ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΜΕΣΟΠΛΕΥΡΙΑ ΔΙΑΣΤΗΜΑΤΑ Σχηματίζονται μεταξύ παρακείμενων πλευρών και καταλαμβάνονται από τους μεσοπλεύριους μύες. Έσω θωρακική
ΣΤΟΙΧΕΙΑ ΑΝΑΤΟΜΙΑΣ ΤΗΣ ΜΗΤΡΑΣ
 ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΣΤΟΙΧΕΙΑ ΑΝΑΤΟΜΙΑΣ ΤΗΣ ΜΗΤΡΑΣ Η µήτρα (εικόνα 1) είναι κοίλο µυώδες όργανο µήκους περίπου 8 cm που προέρχεται από την συνένωση
ΤΕΙ ΠΑΤΡΑΣ ΤΜΗΜΑ ΝΟΣΗΛΕΥΤΙΚΗΣ ΥΠΕΥΘΥΝΟΣ ΚΑΘΗΓΗΤΗΣ : Γεράσιµος Π. Βανδώρος ΣΤΟΙΧΕΙΑ ΑΝΑΤΟΜΙΑΣ ΤΗΣ ΜΗΤΡΑΣ Η µήτρα (εικόνα 1) είναι κοίλο µυώδες όργανο µήκους περίπου 8 cm που προέρχεται από την συνένωση
Υπερηχοτομογραφικη. αρθρο ανασκοπησησ
 Ανδριανάκη Αικατερίνη Ιατρός Ακτινολόγος Ηράκλειο Κρήτης Υπερηχοτομογραφικη απεικονιση του πεουσ αρθρο ανασκοπησησ MEΡΟΣ Α ΕΙΣΑΓΩΓΗ Η υπερηχοτομογραφία συμπεριλαμβανομένης και της χρήσης του έγχρωμου Doppler,
Ανδριανάκη Αικατερίνη Ιατρός Ακτινολόγος Ηράκλειο Κρήτης Υπερηχοτομογραφικη απεικονιση του πεουσ αρθρο ανασκοπησησ MEΡΟΣ Α ΕΙΣΑΓΩΓΗ Η υπερηχοτομογραφία συμπεριλαμβανομένης και της χρήσης του έγχρωμου Doppler,
ΗΚΑΡΔΙΑ ΗΚΑΡΔΙΑ. Ροβίθης Μιχαήλ
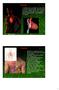 ΗΚΑΡΔΙΑ Η καρδιά που το μέγεθός της είναι λίγο μεγαλύτερο από μία γροθιά, είναι μία διπλή αυτόνομη μυώδης αντλία. Ενώ το βάρος της κυμαίνεται από 280 340 γραμμάρια. Είναι η κεντρική αντλία του κυκλοφορικού
ΗΚΑΡΔΙΑ Η καρδιά που το μέγεθός της είναι λίγο μεγαλύτερο από μία γροθιά, είναι μία διπλή αυτόνομη μυώδης αντλία. Ενώ το βάρος της κυμαίνεται από 280 340 γραμμάρια. Είναι η κεντρική αντλία του κυκλοφορικού
Πρόσθιο Κοιλιακό Τοίχωµα & Πύελος
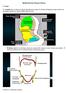 Πρόσθιο Κοιλιακό Τοίχωµα & Πύελος Ι. Γενικά Α. Η κοιλία είναι το τµήµα του κόρµου που βρίσκεται µεταξύ του θώρακα (διάφραγµα) προς τα πάνω και της πυέλου (είσοδο της µικρής πυέλου) προς τα κάτω. Η πύελος
Πρόσθιο Κοιλιακό Τοίχωµα & Πύελος Ι. Γενικά Α. Η κοιλία είναι το τµήµα του κόρµου που βρίσκεται µεταξύ του θώρακα (διάφραγµα) προς τα πάνω και της πυέλου (είσοδο της µικρής πυέλου) προς τα κάτω. Η πύελος
ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ ΑΝΑΤΟΜΙΑ -ΦΥΣΙΟΛΟΓΙΑ
 ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ ΑΝΑΤΟΜΙΑ -ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ ΑΝΩ ΑΕΡΟΦΟΡΟΣ ΟΔΟΣ ρίνα φάρυγγας στοματική κοιλότητα ΚΑΤΩ ΑΕΡΟΦΟΡΟΣ ΟΔΟΣ λάρυγγας τραχεία 2 βρόγχοι πνεύμονες ΛΕΙΤΟΥΡΓΙΕΣ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ ΑΝΑΤΟΜΙΑ -ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΥΣΤΗΜΑ ΑΝΩ ΑΕΡΟΦΟΡΟΣ ΟΔΟΣ ρίνα φάρυγγας στοματική κοιλότητα ΚΑΤΩ ΑΕΡΟΦΟΡΟΣ ΟΔΟΣ λάρυγγας τραχεία 2 βρόγχοι πνεύμονες ΛΕΙΤΟΥΡΓΙΕΣ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
Ονοματεπώνυμο ΑΝΑΠΑΡΑΓΩΓΙΚΌ ΣΥΣΤΗΜΑ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ Ι
 Ονοματεπώνυμο ΑΝΑΠΑΡΑΓΩΓΙΚΌ ΣΥΣΤΗΜΑ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ Ι ΑΝΑΠΑΡΑΓΩΓΙΚΟ ΣΥΣΤΗΜΑ ΤΟΥ ΑΝΤΡΑ 1. Να ταξινομήσετε τις παρακάτω έννοιες σε τέσσερις θεματικές ομάδες: Σπερματικός πόρος, σηραγγγώδη σώματα, λοβοί, σπερματικά
Ονοματεπώνυμο ΑΝΑΠΑΡΑΓΩΓΙΚΌ ΣΥΣΤΗΜΑ ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ Ι ΑΝΑΠΑΡΑΓΩΓΙΚΟ ΣΥΣΤΗΜΑ ΤΟΥ ΑΝΤΡΑ 1. Να ταξινομήσετε τις παρακάτω έννοιες σε τέσσερις θεματικές ομάδες: Σπερματικός πόρος, σηραγγγώδη σώματα, λοβοί, σπερματικά
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ
 ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
ΚΥΚΛΟΦΟΡΙΚΟ ΕΠΑΝΑΛΗΨΗ Α ΛΥΚΕΙΟΥ ΘΕΜΑ 1ο 1. Ποιος είναι ο ρόλος των ερυθρών κυττάρων του αίματος; α. μεταφέρουν οξυγόνο σε όλο το σώμα β. μεταφέρουν θρεπτικά συστατικά, άλατα, ορμόνες και πρωτεΐνες γ. μεταφέρουν
ΜΑΘΗΜΑ 9ο ΜΕΡΟΣ Α Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ
 ΜΑΘΗΜΑ 9ο ΜΕΡΟΣ Α Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Ο εγκέφαλος αρδεύεται από : 1. Τις δύο έσω καρωτίδες και τους κλάδους τους 2. Τις δύο σπονδυλικές αρτηρίες και τους κλάδους τους Οι τέσσερις
ΜΑΘΗΜΑ 9ο ΜΕΡΟΣ Α Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Η ΑΙΜΑΤΩΣΗ ΤΟΥ ΕΓΚΕΦΑΛΟΥ Ο εγκέφαλος αρδεύεται από : 1. Τις δύο έσω καρωτίδες και τους κλάδους τους 2. Τις δύο σπονδυλικές αρτηρίες και τους κλάδους τους Οι τέσσερις
Φυσιολογία της στύσεως Παθοφυσιολογία της στυτικής δυσλειτουργίας
 Φυσιολογία της στύσεως Παθοφυσιολογία της στυτικής δυσλειτουργίας ΦΛΙΑΤΟΥΡΑΣ ΧΡΗΣΤΟΣ MD,FEBU ΧΕΙΡΟΥΡΓΟΣ ΟΥΡΟΛΟΓΟΣ ΑΝΔΡΟΛΟΓΟΣ ΑΝΔΡΟΛΟΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ ΑΘΗΝΩΝ Φυσιολογία της Στύσης Η στύση είναι νευροαγγειακό
Φυσιολογία της στύσεως Παθοφυσιολογία της στυτικής δυσλειτουργίας ΦΛΙΑΤΟΥΡΑΣ ΧΡΗΣΤΟΣ MD,FEBU ΧΕΙΡΟΥΡΓΟΣ ΟΥΡΟΛΟΓΟΣ ΑΝΔΡΟΛΟΓΟΣ ΑΝΔΡΟΛΟΓΙΚΟ ΙΝΣΤΙΤΟΥΤΟ ΑΘΗΝΩΝ Φυσιολογία της Στύσης Η στύση είναι νευροαγγειακό
ΜΑΘΗΜΑ 4ο ΜΕΡΟΣ Α ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ
 ΜΑΘΗΜΑ 4ο ΜΕΡΟΣ Α ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ (ΚΝΣ) ΕΓΚΕΦΑΛΟΣ ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ Είναι το πιο ουραίο τμήμα του Κ.Ν.Σ. Εκτείνεται από τη βάση του κρανίου μέχρι τον 1 ο οσφυϊκό
ΜΑΘΗΜΑ 4ο ΜΕΡΟΣ Α ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ ΚΕΝΤΡΙΚΟ ΝΕΥΡΙΚΟ ΣΥΣΤΗΜΑ (ΚΝΣ) ΕΓΚΕΦΑΛΟΣ ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ ΝΩΤΙΑΙΟΣ ΜΥΕΛΟΣ Είναι το πιο ουραίο τμήμα του Κ.Ν.Σ. Εκτείνεται από τη βάση του κρανίου μέχρι τον 1 ο οσφυϊκό
Κινητικό σύστημα του ανθρώπου Μέρος Ι: Ερειστικό, μυϊκό και συνδεσμικό σύστημα. Μάλλιου Βίβιαν Καθηγήτρια ΤΕΦΑΑ ΔΠΘ Φυσικοθεραπεύτρια
 Κινητικό σύστημα του ανθρώπου Μέρος Ι: Ερειστικό, μυϊκό και συνδεσμικό σύστημα Μάλλιου Βίβιαν Καθηγήτρια ΤΕΦΑΑ ΔΠΘ Φυσικοθεραπεύτρια Τα συστήματα του ανθρώπινου σώματος Αναπνευστικό σύστημα (αποτελείται
Κινητικό σύστημα του ανθρώπου Μέρος Ι: Ερειστικό, μυϊκό και συνδεσμικό σύστημα Μάλλιου Βίβιαν Καθηγήτρια ΤΕΦΑΑ ΔΠΘ Φυσικοθεραπεύτρια Τα συστήματα του ανθρώπινου σώματος Αναπνευστικό σύστημα (αποτελείται
1. Λεμφοφόρα τριχοειδή.
 Κυκλοφορικό σύστημα Αιμοφόρο 1. Καρδιά 2. Αιμοφόρα αγγεία Αρτηρίες Φλέβες τριχοειδή Λεμφοφόρο Λεμφικά τριχοειδή Λεμφαγγεία Λεμφοκυττογόνα όργανα (λεμφαδένες) Το λεμφικό σύστημα η λεμφοφόρο, αθροίζει από
Κυκλοφορικό σύστημα Αιμοφόρο 1. Καρδιά 2. Αιμοφόρα αγγεία Αρτηρίες Φλέβες τριχοειδή Λεμφοφόρο Λεμφικά τριχοειδή Λεμφαγγεία Λεμφοκυττογόνα όργανα (λεμφαδένες) Το λεμφικό σύστημα η λεμφοφόρο, αθροίζει από
Το μυϊκό σύστημα αποτελείται από τους μύες. Ο αριθμός των μυών του μυϊκού συστήματος ανέρχεται στους 637. Οι μύες είναι όργανα για τη σωματική
 Μύες Το μυϊκό σύστημα αποτελείται από τους μύες. Ο αριθμός των μυών του μυϊκού συστήματος ανέρχεται στους 637. Οι μύες είναι όργανα για τη σωματική κινητικότητα, την σπλαχνική κινητικότητα και τη κυκλοφορία
Μύες Το μυϊκό σύστημα αποτελείται από τους μύες. Ο αριθμός των μυών του μυϊκού συστήματος ανέρχεται στους 637. Οι μύες είναι όργανα για τη σωματική κινητικότητα, την σπλαχνική κινητικότητα και τη κυκλοφορία
ρ Έλενα Κουλλαπή 2014
 ρ Έλενα Κουλλαπή 2014 Αγγείωση του έρµατο Αρτηρίε Φλέβε Τριχοειδή Λεµφαγγεία Χρησιµεύουν για : Θερµορρύθµιση και Θρέψη του δέρµατο. Το δέρµα αιµατώνεται πολύ καλά από τα αγγεία του υποδέρµατο, τα οποία
ρ Έλενα Κουλλαπή 2014 Αγγείωση του έρµατο Αρτηρίε Φλέβε Τριχοειδή Λεµφαγγεία Χρησιµεύουν για : Θερµορρύθµιση και Θρέψη του δέρµατο. Το δέρµα αιµατώνεται πολύ καλά από τα αγγεία του υποδέρµατο, τα οποία
15 λεπτη προετοιμασία φοιτητή για τη στυτική δυσλειτουργία
 15 λεπτη προετοιμασία φοιτητή για τη στυτική δυσλειτουργία Ας ξεκαθαρίσουμε κάποια πράγματα για να μπορέσουμε να κατανοήσουμε καλύτερα την ανδρολογία. ΟΡΙΣΜΟΊ Τί είναι η στυτική δυσλειτουργία ; Στυτική
15 λεπτη προετοιμασία φοιτητή για τη στυτική δυσλειτουργία Ας ξεκαθαρίσουμε κάποια πράγματα για να μπορέσουμε να κατανοήσουμε καλύτερα την ανδρολογία. ΟΡΙΣΜΟΊ Τί είναι η στυτική δυσλειτουργία ; Στυτική
Κάτω Άκρο Οι Χώρες του Μηρού
 Κάτω Άκρο Οι Χώρες του Μηρού Ι. Γενικά Α. 3εις σηµαντικές ζώνες των κάτω άκρων 1. Μηριαίο τρίγωνο 2. Ο πόρος των προσαγωγών 3. Ο ιγνυακός βόθρος Β. Μηριαίο οστό 1. Είναι το επιµηκέστερο, το ισχυρότερο
Κάτω Άκρο Οι Χώρες του Μηρού Ι. Γενικά Α. 3εις σηµαντικές ζώνες των κάτω άκρων 1. Μηριαίο τρίγωνο 2. Ο πόρος των προσαγωγών 3. Ο ιγνυακός βόθρος Β. Μηριαίο οστό 1. Είναι το επιµηκέστερο, το ισχυρότερο
ΕΠΑΝΑΛΗΨΗ ΚΕΦΑΛΑΙΩΝ 1-7-8
 ΕΠΑΝΑΛΗΨΗ ΚΕΦΑΛΑΙΩΝ 1-7-8 Α. ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ 1. Στον ανθρώπινο οργανισµό a) όλα τα κύτταρα έχουν το ίδιο σχήµα και την ίδια λειτουργία b) υπάρχουν κύτταρα µε το ίδιο σχήµα και την ίδια λειτουργία
ΕΠΑΝΑΛΗΨΗ ΚΕΦΑΛΑΙΩΝ 1-7-8 Α. ΕΡΩΤΗΣΕΙΣ ΠΟΛΛΑΠΛΗΣ ΕΠΙΛΟΓΗΣ 1. Στον ανθρώπινο οργανισµό a) όλα τα κύτταρα έχουν το ίδιο σχήµα και την ίδια λειτουργία b) υπάρχουν κύτταρα µε το ίδιο σχήµα και την ίδια λειτουργία
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΙΣ ΕΦΑΡΜΟΓΕΣ ΤΩΝ ΒΑΣΙΚΩΝ ΙΑΤΡΙΚΩΝ ΕΠΙΣΤΗΜΩΝ
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΙΣ ΕΦΑΡΜΟΓΕΣ ΤΩΝ ΒΑΣΙΚΩΝ ΙΑΤΡΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΟ ΑΓΓΕΙΑΚΟ ΛΕΙΟ ΜΥΙΚΟ ΚΥΤΤΑΡΟ Μοριακή δομή και ρόλος στην παθογένεια
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ ΣΤΙΣ ΕΦΑΡΜΟΓΕΣ ΤΩΝ ΒΑΣΙΚΩΝ ΙΑΤΡΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΤΟ ΑΓΓΕΙΑΚΟ ΛΕΙΟ ΜΥΙΚΟ ΚΥΤΤΑΡΟ Μοριακή δομή και ρόλος στην παθογένεια
ΤΟ ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ. 1. την εκκριτική, που αποτελείται από τους δύο νεφρούς, και
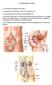 ΤΟ ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Το ουροποιητικό σύστημα έχει δύο μοίρες: 1. την εκκριτική, που αποτελείται από τους δύο νεφρούς, και 2. την αποχετευτική, με την οποία τα ούρα απεκκρίνονται. Τα όργανα που αποτελούν
ΤΟ ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Το ουροποιητικό σύστημα έχει δύο μοίρες: 1. την εκκριτική, που αποτελείται από τους δύο νεφρούς, και 2. την αποχετευτική, με την οποία τα ούρα απεκκρίνονται. Τα όργανα που αποτελούν
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΨΗ
 ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΨΗ ΘΕΜΑ 1ο 1. Κυτταρική διαφοροποίηση ονομάζουμε: α. Την δομική κυρίως εξειδίκευση των συστημάτων β. Την δομική και λειτουργική εξειδίκευση των κυττάρων γ. Την λειτουργική εξειδίκευση
ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ ΕΠΑΝΑΛΗΨΗ ΘΕΜΑ 1ο 1. Κυτταρική διαφοροποίηση ονομάζουμε: α. Την δομική κυρίως εξειδίκευση των συστημάτων β. Την δομική και λειτουργική εξειδίκευση των κυττάρων γ. Την λειτουργική εξειδίκευση
ΑΙΜΑ πρόκειται για έναν ιστό.
 ΑΙΜΑ πρόκειται για έναν ιστό. Αίμα είναι το υγρό που κυκλοφορεί διαμέσου της καρδιάς, των αρτηριών, των φλεβών και των τριχοειδών αγγείων μεταφέροντας θρεπτικές ουσίες, ορμόνες, βιταμίνες, θερμότητα και
ΑΙΜΑ πρόκειται για έναν ιστό. Αίμα είναι το υγρό που κυκλοφορεί διαμέσου της καρδιάς, των αρτηριών, των φλεβών και των τριχοειδών αγγείων μεταφέροντας θρεπτικές ουσίες, ορμόνες, βιταμίνες, θερμότητα και
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ Ι ΣΠΛΗΝΑΣ ΠΑΓΚΡΕΑΣ ΗΠΑΡ
 ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ Ι ΣΠΛΗΝΑΣ ΠΑΓΚΡΕΑΣ ΗΠΑΡ Φωτεινή Μάλλη 2 3 Ωοειδής, ιώδης, μαλακός ΣΠΛΗΝΑΣ Μεγεθος και σχημα γροθιάς Το πιο ευαισθητο κοιλιακό όργανο Ανω και εξω μοίρα αριστερού
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ Ι ΣΠΛΗΝΑΣ ΠΑΓΚΡΕΑΣ ΗΠΑΡ Φωτεινή Μάλλη 2 3 Ωοειδής, ιώδης, μαλακός ΣΠΛΗΝΑΣ Μεγεθος και σχημα γροθιάς Το πιο ευαισθητο κοιλιακό όργανο Ανω και εξω μοίρα αριστερού
Ιερό Πλέγµα και Νεύρα λκλλκλκλλκκκκ
 Ιερό Πλέγµα και Νεύρα λκλλκλκλλκκκκ Εισαγωγή Σχηµατισµός Παράπλευροι Κλάδοι του Ιερού Πλέγµατος Μυϊκοί Παράπλευροι Κλάδοι Δερµατικοί Παράπλευροι Κλάδοι Σπλαγχνικοί Παράπλευροι Κλάδοι Τελικοί Κλάδοι του
Ιερό Πλέγµα και Νεύρα λκλλκλκλλκκκκ Εισαγωγή Σχηµατισµός Παράπλευροι Κλάδοι του Ιερού Πλέγµατος Μυϊκοί Παράπλευροι Κλάδοι Δερµατικοί Παράπλευροι Κλάδοι Σπλαγχνικοί Παράπλευροι Κλάδοι Τελικοί Κλάδοι του
4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ. περιλαμβάνονται ο σπλήνας και ο θύμος αδένας (εικ.4.1). Το λεμφικό σύστημα είναι πολύ σημαντικό γιατί:
 ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
ΚΕΦΑΛΑΙΟ 4 4. ΛΕΜΦΙΚΟ ΣΥΣΤΗΜΑ Το λεμφικό σύστημα αποτελείται από τα λεμφαγγεία, τη λέμφο και τους λεμφαδένες. Οι λεμφαδένες είναι δομές που αποτελούνται από εξειδικευμένη μορφή συνδετικού ιστού, το λεμφικό
Φυσιολογία της Άσκησης
 ΕΛΛΗΝΙΚΟ ΜΕΣΟΓΕΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΩΝ ΔΙΑΤΡΟΦΗΣ & ΔΙΑΙΤΟΛΟΓΙΑΣ Φυσιολογία της Άσκησης Λειτουργία καρδιαγγειακού συστήματος Καρδιαγγειακός έλεγχος κατά τη διάρκεια της
ΕΛΛΗΝΙΚΟ ΜΕΣΟΓΕΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΕΠΙΣΤΗΜΩΝ ΔΙΑΤΡΟΦΗΣ & ΔΙΑΙΤΟΛΟΓΙΑΣ Φυσιολογία της Άσκησης Λειτουργία καρδιαγγειακού συστήματος Καρδιαγγειακός έλεγχος κατά τη διάρκεια της
Δρόσος Βασίλειος Ειδικευόμενος χειρουργικής θώρακος ΓΝΝΘΑ Η ΣΩΤΗΡΙΑ
 Δρόσος Βασίλειος Ειδικευόμενος χειρουργικής θώρακος ΓΝΝΘΑ Η ΣΩΤΗΡΙΑ Γένικά στοιχεία ανατομίας Δύο μεσολόβιες σχισμές στον δεξιό πνεύμονα : μικρή-οριζόντια μεγάλη-λοξή Τον χωρίζουν σε 3 λοβούς Άνω Μέσο
Δρόσος Βασίλειος Ειδικευόμενος χειρουργικής θώρακος ΓΝΝΘΑ Η ΣΩΤΗΡΙΑ Γένικά στοιχεία ανατομίας Δύο μεσολόβιες σχισμές στον δεξιό πνεύμονα : μικρή-οριζόντια μεγάλη-λοξή Τον χωρίζουν σε 3 λοβούς Άνω Μέσο
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ. Οι ρυθμιστές του οργανισμού
 ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
ΕΝΔΟΚΡΙΝΕΙΣ ΑΔΕΝΕΣ Οι ρυθμιστές του οργανισμού Είδη αδένων στον άνθρωπο o Εξωκρινείς αδένες: εκκρίνουν το προϊόν τους μέσω εκφορητικού πόρου είτε στην επιφάνεια του σώματος (π.χ. ιδρωτοποιοί και σμηγματογόνοι
Εργαστήριο Πειραματικής Φυσιολογίας, Ιατρική Σχολή ΑΠΘ, Διευθυντής: Καθηγητής κ. Γεώργιος Ανωγειανάκις
 1 Πόσα λίτρα πρόουρο σχηματίζονται ημερησίως; α) 15-18 L β) 1,5-1,7 L γ) 170-180 L δ) 1700-1800 L ε) 100-120 L 2. Ποιο τμήμα του νεφρού ανήκει στον μυελό του νεφρού; α) Τα νεφρικά σωμάτια β) Η κάψα του
1 Πόσα λίτρα πρόουρο σχηματίζονται ημερησίως; α) 15-18 L β) 1,5-1,7 L γ) 170-180 L δ) 1700-1800 L ε) 100-120 L 2. Ποιο τμήμα του νεφρού ανήκει στον μυελό του νεφρού; α) Τα νεφρικά σωμάτια β) Η κάψα του
ΙΣΤΟΙ Ως προς τη µορφή και τη λειτουργία τους. Κυτταρική διαφοροποίηση.
 ΙΣΤΟΙ 1. Τα κύτταρα που αποτελούν τον οργανισµό µας, διακρίνονται σε διάφορους τύπους, παρά το γεγονός ότι όλα, τελικώς, προέρχονται από το ζυγωτό, δηλαδή το πρώτο κύτταρο µε το οποίο ξεκίνησε η ζωή µας.
ΙΣΤΟΙ 1. Τα κύτταρα που αποτελούν τον οργανισµό µας, διακρίνονται σε διάφορους τύπους, παρά το γεγονός ότι όλα, τελικώς, προέρχονται από το ζυγωτό, δηλαδή το πρώτο κύτταρο µε το οποίο ξεκίνησε η ζωή µας.
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ
 ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
ΕΡΑΣΜΕΙΟΣ ΕΛΛΗΝΟΓΕΡΜΑΝΙΚΗ ΣΧΟΛΗ Ιδιωτικό Γενικό Λύκειο Όνομα: Ημερομηνία:./04/2014 ΤΑΞΗ : A Λυκείου ΕΡΩΤΗΣΕΙΣ ΓΙΑ ΤΟ 1 ο ΘΕΜΑ ΕΠΑΝΑΛΗΠΤΙΚΕΣ ΕΡΩΤΗΣΕΙΣ ΚΕΦΑΛΑΙΟ 11: Ενδοκρινείς αδένες ΒΙΟΛΟΓΙΑ Α ΛΥΚΕΙΟΥ
Εργασία στο μάθημα της βιολογίας υπεύθυνη καθηγήτρια : Ζαρφτσιάν Μαρία Ελένη
 Εργασία στο μάθημα της βιολογίας υπεύθυνη καθηγήτρια : Ζαρφτσιάν Μαρία Ελένη Εισαγωγή: Το κυκλοφορικό είναι από τα πιο σημαντικά αλλά και από τα πιο ευαίσθητα συστήματα του οργανισμού μας. Τα προβλήματα
Εργασία στο μάθημα της βιολογίας υπεύθυνη καθηγήτρια : Ζαρφτσιάν Μαρία Ελένη Εισαγωγή: Το κυκλοφορικό είναι από τα πιο σημαντικά αλλά και από τα πιο ευαίσθητα συστήματα του οργανισμού μας. Τα προβλήματα
Ειδικά Αισθητήρια Όργανα
 Ειδικά Αισθητήρια Όργανα Οφθαλμός Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας-Εμβρυολογίας ΟΦΘΑΛΜΟΣ ΧΙΤΩΝΕΣ ΟΦΘΑΛΜΙΚΟΥ ΒΟΛΒΟΥ 1. Σκληρός: εξωτερικός ινοκολλαγονώδης χιτώνας 2. Ραγοειδήςήμέσοςήαγγειώδης:
Ειδικά Αισθητήρια Όργανα Οφθαλμός Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας-Εμβρυολογίας ΟΦΘΑΛΜΟΣ ΧΙΤΩΝΕΣ ΟΦΘΑΛΜΙΚΟΥ ΒΟΛΒΟΥ 1. Σκληρός: εξωτερικός ινοκολλαγονώδης χιτώνας 2. Ραγοειδήςήμέσοςήαγγειώδης:
ΑΝΑΤΟΜΙΑ I. Συνήθως περιλαµβάνουν 5 ερωτήσεις, κάποιες από τις οποίες. αφορούν το παρασκευασµένο πτώµα. Η επιτυχής αντιµετώπισή τους
 ΑΝΑΤΟΜΙΑ I ΠΤΩΜΑ: Συνήθως περιλαµβάνουν 5 ερωτήσεις, κάποιες από τις οποίες αφορούν το παρασκευασµένο πτώµα. Η επιτυχής αντιµετώπισή τους προσφέρει τη δυνατότητα, µετά από ερωτήσεις του κ. Παπαδόπουλου,
ΑΝΑΤΟΜΙΑ I ΠΤΩΜΑ: Συνήθως περιλαµβάνουν 5 ερωτήσεις, κάποιες από τις οποίες αφορούν το παρασκευασµένο πτώµα. Η επιτυχής αντιµετώπισή τους προσφέρει τη δυνατότητα, µετά από ερωτήσεις του κ. Παπαδόπουλου,
Κώστας, 32 χρονών. Άρτεμις, 30 χρονών
 Να προχωρήσουν η Άρτεμις και ο Κώστας σε υποβοηθούμενη αναπαραγωγή; Ο Κώστας και η Άρτεμις είναι ένα ζευγάρι που δυσκολεύονται να αποκτήσουν παιδί. Επισκέφθηκαν τον γιατρό τους και ανέφεραν τα πιο κάτω
Να προχωρήσουν η Άρτεμις και ο Κώστας σε υποβοηθούμενη αναπαραγωγή; Ο Κώστας και η Άρτεμις είναι ένα ζευγάρι που δυσκολεύονται να αποκτήσουν παιδί. Επισκέφθηκαν τον γιατρό τους και ανέφεραν τα πιο κάτω
Χόνδρος Αρθρώσεις. Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας-Εμβρυολογίας
 Χόνδρος Αρθρώσεις Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας-Εμβρυολογίας Χόνδρος συνδετικός-στηρικτικός ς ιστός συμπαγής αλλά εύκαμπτος Λειτουργίες Χόνδρου υποστήριξη μαλακών ιστών απορρόφηση κραδασμών
Χόνδρος Αρθρώσεις Σοφία Χαβάκη Λέκτορας Εργαστήριο Ιστολογίας-Εμβρυολογίας Χόνδρος συνδετικός-στηρικτικός ς ιστός συμπαγής αλλά εύκαμπτος Λειτουργίες Χόνδρου υποστήριξη μαλακών ιστών απορρόφηση κραδασμών
ΡΑΧΗ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ
 ΡΑΧΗ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΡΑΧΗ Αποτελεί τον μυοσκελετικό άξονα στήριξης του κορμού με κύριο οστικό στοιχείο τους σπονδύλους και την παράλληλη συμβολή
ΡΑΧΗ ΠΑΥΛΟΣ Γ. ΚΑΤΩΝΗΣ ΑΝΑΠΛ. ΚΑΘΗΓΗΤΗΣ ΙΑΤΡΙΚΗΣ ΣΧΟΛΗΣ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΚΡΗΤΗΣ ΡΑΧΗ Αποτελεί τον μυοσκελετικό άξονα στήριξης του κορμού με κύριο οστικό στοιχείο τους σπονδύλους και την παράλληλη συμβολή
Μύες του πυελικού τοιχώματος
 Μύες Πυέλου Μύες του πυελικού τοιχώματος Συμβάλλουν στο σχηματισμό των εσωτερικών πλάγιων τοιχωμάτων της πυελικής κοιλότητας. Εκφύονται μέσα από τη πυελική κοιλότητα αλλά καταφύονται έξω από αυτήν (μηριαίο).
Μύες Πυέλου Μύες του πυελικού τοιχώματος Συμβάλλουν στο σχηματισμό των εσωτερικών πλάγιων τοιχωμάτων της πυελικής κοιλότητας. Εκφύονται μέσα από τη πυελική κοιλότητα αλλά καταφύονται έξω από αυτήν (μηριαίο).
ΡΑΧΗ. 3. Μύες (ανάλογα µε την εµβρυολογική προέλευση και την νεύρωσή τους διαχωρίζονται σε: α. Εξωγενείς (ετερόχθονες) β. Ενδογενείς (αυτόχθονες)
 ΡΑΧΗ Ι. Γενικά Α. Η ράχη αποτελείται από την οπίσθια επιφάνεια του σώµατος 1. Αποτελεί µυοσκελετικό άξονα στήριξης του κορµού 2. Οστικά στοιχεία α. Σπόνδυλοι β. Κεντρικά τµήµατα των πλευρών γ. Άνω επιφάνειες
ΡΑΧΗ Ι. Γενικά Α. Η ράχη αποτελείται από την οπίσθια επιφάνεια του σώµατος 1. Αποτελεί µυοσκελετικό άξονα στήριξης του κορµού 2. Οστικά στοιχεία α. Σπόνδυλοι β. Κεντρικά τµήµατα των πλευρών γ. Άνω επιφάνειες
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ ΕΝΔΟΚΡΙΝΙΚΟ ΣΥΣΤΗΜΑ
 ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΕΝΔΟΚΡΙΝΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΕΝΔΟΚΡΙΝΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
Προεκλαμψία. Έγκαιρη εκτίμηση κινδύνου στις 11 13+6 εβδομάδες
 Προεκλαμψία Έγκαιρη εκτίμηση κινδύνου στις 11 13+6 εβδομάδες Ο έλεγχος για προεκλαμψία μεταξύ των εβδομάδων 11 έως 13+6 μπορεί να εντοπίσει κυήσεις υψηλού κινδύνου, επιτρέποντας τη θεραπεία με α σπιρίνη
Προεκλαμψία Έγκαιρη εκτίμηση κινδύνου στις 11 13+6 εβδομάδες Ο έλεγχος για προεκλαμψία μεταξύ των εβδομάδων 11 έως 13+6 μπορεί να εντοπίσει κυήσεις υψηλού κινδύνου, επιτρέποντας τη θεραπεία με α σπιρίνη
Χρήστος Κωστόπουλος Ιατρός Διδακτορική Διατριβή
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΜΕΛΕΤΗ ΤΗΣ ΕΚΦΡΑΣΗΣ ΛΙΠΟΚΙΝΩΝ ΚΑΙ ΤΩΝ ΥΠΟΔΟΧΕΩΝ ΤΟΥΣ ΣΕ ΠΕΡΙΑΓΓΕΙΑΚΟ ΛΙΠΩΔΗ ΙΣΤΟ ΑΝΘΡΩΠΟΥ ΚΑΙ ΣΥΣΧΕΤΙΣΗ ΜΕ ΤΗΝ ΑΘΗΡΟΣΚΛΗΡΩΣΗ Χρήστος Κωστόπουλος
ΠΑΝΕΠΙΣΤΗΜΙΟ ΠΑΤΡΩΝ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΜΕΛΕΤΗ ΤΗΣ ΕΚΦΡΑΣΗΣ ΛΙΠΟΚΙΝΩΝ ΚΑΙ ΤΩΝ ΥΠΟΔΟΧΕΩΝ ΤΟΥΣ ΣΕ ΠΕΡΙΑΓΓΕΙΑΚΟ ΛΙΠΩΔΗ ΙΣΤΟ ΑΝΘΡΩΠΟΥ ΚΑΙ ΣΥΣΧΕΤΙΣΗ ΜΕ ΤΗΝ ΑΘΗΡΟΣΚΛΗΡΩΣΗ Χρήστος Κωστόπουλος
15λεπτη Προετοιμασία του φοιτητή για την παρακολούθηση του μαθήματος νευροουρολογίας, γυναικολογικής ουρολογίας και ακράτειας ούρων.
 15λεπτη Προετοιμασία του φοιτητή για την παρακολούθηση του μαθήματος νευροουρολογίας, γυναικολογικής ουρολογίας και ακράτειας ούρων. Η ουροδόχος κύστη δεν είναι απλά μία κοιλότητα η οποία γεμίζει απλά
15λεπτη Προετοιμασία του φοιτητή για την παρακολούθηση του μαθήματος νευροουρολογίας, γυναικολογικής ουρολογίας και ακράτειας ούρων. Η ουροδόχος κύστη δεν είναι απλά μία κοιλότητα η οποία γεμίζει απλά
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ
 ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΤΟ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΕ ΚΑΤΑΣΤΑΣΕΙΣ STRESS ΦΥΣΙΟΛΟΓΙΑ ΜΕΓΑΛΟΥ ΥΨΟΜΕΤΡΟΥ Η ατμοσφαιρική
ΦΥΣΙΟΛΟΓΙΑ ΑΝΑΠΝΕΥΣΤΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΙΩΑΝΝΑ ΔΗΜΟΠΟΥΛΟΥ ΚΑΘΗΓΗΤΡΙΑ ΕΡΓΑΣΤΗΡΙΟ ΠΕΙΡΑΜΑΤΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΕΚΠΑ ΤΟ ΑΝΑΠΝΕΥΣΤΙΚΟ ΣΕ ΚΑΤΑΣΤΑΣΕΙΣ STRESS ΦΥΣΙΟΛΟΓΙΑ ΜΕΓΑΛΟΥ ΥΨΟΜΕΤΡΟΥ Η ατμοσφαιρική
ΩΣΜΩΣΗ ΚΑΙ ΟΙ ΝΕΦΡΟΙ
 ΩΣΜΩΣΗ ΚΑΙ ΟΙ ΝΕΦΡΟΙ ΠΩΣ ΜΕΤΑΦΕΡΟΝΤΑΙ ΟΙ ΟΥΣΙΕΣ ΣΤΑ ΥΓΡΑ Μεταφορά τροφών και αποβολή μη χρήσιμων ουσιών: Διάχυση (π.χ. το CO 2 που παράγεται κατά τον μεταβολισμό των κυττάρων, διαχέεται από τα κύτταρα
ΩΣΜΩΣΗ ΚΑΙ ΟΙ ΝΕΦΡΟΙ ΠΩΣ ΜΕΤΑΦΕΡΟΝΤΑΙ ΟΙ ΟΥΣΙΕΣ ΣΤΑ ΥΓΡΑ Μεταφορά τροφών και αποβολή μη χρήσιμων ουσιών: Διάχυση (π.χ. το CO 2 που παράγεται κατά τον μεταβολισμό των κυττάρων, διαχέεται από τα κύτταρα
«ΥΠΕΡΗΧΟΓΡΑΦΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΤΗΣ ΓΥΝΑΙΚΑΣ ΕΝΑ ΥΠΟΓΟΝΙΜΟ ΖΕΥΓΑΡΙ ΜΗΤΕΡΑ «ΜΟΝΑΔΑ ΑΝΑΠΑΡΑΓΩΓΙΚΗΣ ΙΑΤΡΙΚΗΣ» ΤΖΕΦΕΡΑΚΟΣ ΑΛΕΞΑΝΔΡΟΣ
 «ΥΠΕΡΗΧΟΓΡΑΦΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΤΗΣ ΓΥΝΑΙΚΑΣ ΣΕ ΕΝΑ ΥΠΟΓΟΝΙΜΟ ΖΕΥΓΑΡΙ ΠΡΙΝ ΚΑΙ ΚΑΤΑ ΤΗΝ ΔΙΕΓΕΡΣΗ ΤΩΝ ΩΟΘΗΚΩΝ» ΤΖΕΦΕΡΑΚΟΣ ΑΛΕΞΑΝΔΡΟΣ «ΜΟΝΑΔΑ ΑΝΑΠΑΡΑΓΩΓΙΚΗΣ ΙΑΤΡΙΚΗΣ» ΜΗΤΕΡΑ Η εξέλιξη στην υπερηχογραφική τεχνολογία
«ΥΠΕΡΗΧΟΓΡΑΦΙΚΗ ΑΞΙΟΛΟΓΗΣΗ ΤΗΣ ΓΥΝΑΙΚΑΣ ΣΕ ΕΝΑ ΥΠΟΓΟΝΙΜΟ ΖΕΥΓΑΡΙ ΠΡΙΝ ΚΑΙ ΚΑΤΑ ΤΗΝ ΔΙΕΓΕΡΣΗ ΤΩΝ ΩΟΘΗΚΩΝ» ΤΖΕΦΕΡΑΚΟΣ ΑΛΕΞΑΝΔΡΟΣ «ΜΟΝΑΔΑ ΑΝΑΠΑΡΑΓΩΓΙΚΗΣ ΙΑΤΡΙΚΗΣ» ΜΗΤΕΡΑ Η εξέλιξη στην υπερηχογραφική τεχνολογία
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ ΕΝΔΟΚΡΙΝΙΚΟ ΣΥΣΤΗΜΑ
 ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΕΝΔΟΚΡΙΝΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Εκλ. Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
ΔΙΔΑΣΚΑΛΙΑ ΘΕΩΡΗΤΙΚΩΝ ΜΑΘΗΜΑΤΩΝ ΑΝΑΤΟΜΙΑ ΙΙ 1 ΕΝΔΟΚΡΙΝΙΚΟ ΣΥΣΤΗΜΑ Φωτεινή Μάλλη Πνευμονολόγος Εκλ. Αναπλ. Καθηγητρια ΤΕΙ Νοσηλευτικής Επιστημονικός Συνεργάτης Πνευμονολογικής Κλινικής ΠΘ Καθηγητής-Σύμβουλος
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ ΟΝΟΜΑ ΜΑΘΗΤΗ-ΜΑΘΗΤΡΙΑΣ:... 1. Το πιο κάτω σχεδιάγραμμα δείχνει ανθρώπινο σπερματοζωάριο.
 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ ΕΝΟΤΗΤΑ: ΑΝΑΠΑΡΑΓΩΓΗ ΗΜΕΡΟΜΗΝΙΑ:... ΚΑΘΗΓΗΤΗΣ: ΠΑΤΗΡ ΑΝΑΣΤΑΣΙΟΣ ΙΣΑΑΚ ΤΜΗΜΑ:... ΑΡ. ΜΑΘΗΤΗ-ΜΑΘΗΤΡΙΑΣ:... ΟΝΟΜΑ ΜΑΘΗΤΗ-ΜΑΘΗΤΡΙΑΣ:... 1. Το πιο κάτω σχεδιάγραμμα δείχνει
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΗ ΒΙΟΛΟΓΙΑ Γ ΛΥΚΕΙΟΥ ΕΝΟΤΗΤΑ: ΑΝΑΠΑΡΑΓΩΓΗ ΗΜΕΡΟΜΗΝΙΑ:... ΚΑΘΗΓΗΤΗΣ: ΠΑΤΗΡ ΑΝΑΣΤΑΣΙΟΣ ΙΣΑΑΚ ΤΜΗΜΑ:... ΑΡ. ΜΑΘΗΤΗ-ΜΑΘΗΤΡΙΑΣ:... ΟΝΟΜΑ ΜΑΘΗΤΗ-ΜΑΘΗΤΡΙΑΣ:... 1. Το πιο κάτω σχεδιάγραμμα δείχνει
Ο Σκελετός της Πυέλου
 Ο Σκελετός της Πυέλου E Johnson Αν. Καθηγήτρια Εργαστήριο Ανατοµίας Η Πύελος το κατώτερο σηµείο του κορµού προς τα κάτω συνέχεια της κοιλιάς η πυελική κοιλότητα = κατώτερο τµήµα της κοιλιακής χώρας εντοπίζεται
Ο Σκελετός της Πυέλου E Johnson Αν. Καθηγήτρια Εργαστήριο Ανατοµίας Η Πύελος το κατώτερο σηµείο του κορµού προς τα κάτω συνέχεια της κοιλιάς η πυελική κοιλότητα = κατώτερο τµήµα της κοιλιακής χώρας εντοπίζεται
Οπισθοπεριτοναϊκή θέση Θ12 - Ο4 Δεξιός νεφρός χαμηλότερα από τον αριστερό ΔΕ νεφρός πίσω και κάτω από το ήπαρ/χοληδόχο κύστη ΑΡ νεφρός κάτω και επί
 Οπισθοπεριτοναϊκή θέση Θ12 - Ο4 Δεξιός νεφρός χαμηλότερα από τον αριστερό ΔΕ νεφρός πίσω και κάτω από το ήπαρ/χοληδόχο κύστη ΑΡ νεφρός κάτω και επί τα έσω του σπλήνα Τα επινεφρίδια είναι άνω, πρόσθια και
Οπισθοπεριτοναϊκή θέση Θ12 - Ο4 Δεξιός νεφρός χαμηλότερα από τον αριστερό ΔΕ νεφρός πίσω και κάτω από το ήπαρ/χοληδόχο κύστη ΑΡ νεφρός κάτω και επί τα έσω του σπλήνα Τα επινεφρίδια είναι άνω, πρόσθια και
Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις :
 Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις : Οι όρχεις αποτελούν κομμάτι του αναπαραγωγικού συστήματος (παραγωγή σπερματοζωάριων) του άνδρα αλλά
Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις : Οι όρχεις αποτελούν κομμάτι του αναπαραγωγικού συστήματος (παραγωγή σπερματοζωάριων) του άνδρα αλλά
ΜΕΡΟΣ Α: ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΑΝΑΠΑΡΑΓΩΓΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΤΟΥ ΑΝΤΡΑ
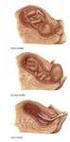 ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 12 ο ΚΕΦΑΛΑΙΟ «ΑNAΠΑΡΑΓΩΓΗ-ΑΝΑΠΤΥΞΗ» ΜΕΡΟΣ Α: ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΑΝΑΠΑΡΑΓΩΓΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΤΟΥ ΑΝΤΡΑ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος της αναπαραγωγής και
ΦΥΛΛΟ ΕΡΓΑΣΙΑΣ ΣΤΟ 12 ο ΚΕΦΑΛΑΙΟ «ΑNAΠΑΡΑΓΩΓΗ-ΑΝΑΠΤΥΞΗ» ΜΕΡΟΣ Α: ΔΟΜΗ ΚΑΙ ΛΕΙΤΟΥΡΓΙΑ ΤΟΥ ΑΝΑΠΑΡΑΓΩΓΙΚΟΥ ΣΥΣΤΗΜΑΤΟΣ ΤΟΥ ΑΝΤΡΑ Α. ΔΡΑΣΤΗΡΙΟΤΗΤΕΣ ΜΕΣΑ ΣΤΗΝ ΤΑΞΗ 1. Ποιος είναι ο ρόλος της αναπαραγωγής και
«Μηχανική του Τοιχώµατος της Αρτηρίας & Ιστολογία του Τοιχώµατος της Φλέβας στην Αρτηριοφλεβική Αναστόµωση» ιπλωµατική Εργασία
 «Μηχανική του Τοιχώµατος της Αρτηρίας & Ιστολογία του Τοιχώµατος της Φλέβας στην Αρτηριοφλεβική Αναστόµωση» ιπλωµατική Εργασία Σασσάνη Σοφία Αθήνα 2010 1 ΠΡΟΛΟΓΟΣ Η παρούσα διπλωµατική εργασία εκπονήθηκε
«Μηχανική του Τοιχώµατος της Αρτηρίας & Ιστολογία του Τοιχώµατος της Φλέβας στην Αρτηριοφλεβική Αναστόµωση» ιπλωµατική Εργασία Σασσάνη Σοφία Αθήνα 2010 1 ΠΡΟΛΟΓΟΣ Η παρούσα διπλωµατική εργασία εκπονήθηκε
ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ
 ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Ουροποιητικό Σύστημα Νεφροί Αποχετευτικό Σύστημα Καλυκοπυελικό Σύστημα Ουρητήρες, Ουροδόχος κύστη, Ουρήθρα Παραγωγή Μεταφορά Αποθήκευση Ποιοτικός έλεγχος ούρων Παροχέτευση Λειτουργίες
ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Ουροποιητικό Σύστημα Νεφροί Αποχετευτικό Σύστημα Καλυκοπυελικό Σύστημα Ουρητήρες, Ουροδόχος κύστη, Ουρήθρα Παραγωγή Μεταφορά Αποθήκευση Ποιοτικός έλεγχος ούρων Παροχέτευση Λειτουργίες
Καλοήθεις Παθήσεις Γεννητικού Συστήματος
 Καλοήθεις Παθήσεις Γεννητικού Συστήματος 1. Επίκτητες παθήσεις πέους και ανδρικής ουρήθρας 2. Παθήσεις του σπερματικού τόνου όρχεως 3. Παθήσεις οσχέου ΕΠΙΚΤΗΤΕΣ ΠΑΘΗΣΕΙΣ ΠΕΟΥΣ ΚΑΙ ΑΝΔΡΙΚΗΣ ΟΥΡΗΘΡΑΣ επίκτητες
Καλοήθεις Παθήσεις Γεννητικού Συστήματος 1. Επίκτητες παθήσεις πέους και ανδρικής ουρήθρας 2. Παθήσεις του σπερματικού τόνου όρχεως 3. Παθήσεις οσχέου ΕΠΙΚΤΗΤΕΣ ΠΑΘΗΣΕΙΣ ΠΕΟΥΣ ΚΑΙ ΑΝΔΡΙΚΗΣ ΟΥΡΗΘΡΑΣ επίκτητες
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ
 ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΙΚΡΟΣΚΟΠΙΚΗ ΠΑΡΑΤΗΡΗΣΗ ΜΟΝΙΜΩΝ ΠΑΡΑΣΚΕΥΑΣΜΑΤΩΝ ΚΥΤΤΑΡΩΝ ΚΑΙ ΙΣΤΩΝ Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ
ΕΡΓΑΣΤΗΡΙΑΚΟ ΚΕΝΤΡΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ Ν. ΜΑΓΝΗΣΙΑΣ ( Ε.Κ.Φ.Ε ) ΕΡΓΑΣΤΗΡΙΟ ΒΙΟΛΟΓΙΑΣ Θέμα: ΜΙΚΡΟΣΚΟΠΙΚΗ ΠΑΡΑΤΗΡΗΣΗ ΜΟΝΙΜΩΝ ΠΑΡΑΣΚΕΥΑΣΜΑΤΩΝ ΚΥΤΤΑΡΩΝ ΚΑΙ ΙΣΤΩΝ Μέσος χρόνος πειράματος: 45 λεπτά Α. ΑΝΑΛΩΣΙΜΑ
Απελευθερώνει ορμόνες, που αυξάνουν την πίεση του αίματος στους νεφρούς και επηρεάζουν την παραγωγή ερυθροκυττάρων
 ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Το ουροποιητικό σύστημα (εικ.6.2), αποτελείται από τους νεφρούς, τους ουρητήρες, την ουροδόχο κύστη και την ουρήθρα. Στους νεφρούς μικρά μόρια απομακρύνονται από το αίμα. Πολλά από
ΟΥΡΟΠΟΙΗΤΙΚΟ ΣΥΣΤΗΜΑ Το ουροποιητικό σύστημα (εικ.6.2), αποτελείται από τους νεφρούς, τους ουρητήρες, την ουροδόχο κύστη και την ουρήθρα. Στους νεφρούς μικρά μόρια απομακρύνονται από το αίμα. Πολλά από
Από το βιβλίο του Δρ. Πέτρου Α. Πουλμέντη
 Από το βιβλίο του Δρ. Πέτρου Α. Πουλμέντη Κεφάλαιο 1 Εισαγωγή στη βιολογική μηχανική Κεφάλαιο 2 Εκβιομηχανική των οστών Οι διαφάνειες που ακολουθούν Η ΑΝΑΤΟΜΙΚΗ ΘΕΣΗ ΤΟΥ ΑΝΘΡΩΠΟΥ Για να περιγράψουμε τα
Από το βιβλίο του Δρ. Πέτρου Α. Πουλμέντη Κεφάλαιο 1 Εισαγωγή στη βιολογική μηχανική Κεφάλαιο 2 Εκβιομηχανική των οστών Οι διαφάνειες που ακολουθούν Η ΑΝΑΤΟΜΙΚΗ ΘΕΣΗ ΤΟΥ ΑΝΘΡΩΠΟΥ Για να περιγράψουμε τα
ΚΥΤΤΑΡΑ. Καρβουντζή Ηλιάνα (Βιολόγος) 1
 ΚΥΤΤΑΡΑ ΖΥΓΩΤΟ: Το πρώτο κύτταρο του οργανισμού από το οποίο με συνεχείς κυτταρικές διαιρέσεις προκύπτουν όλα. ΔΙΑΦΟΡΟΠΟΙΗΣΗ: Διαδικασία με την οποία τα κύτταρα αποκτούν διαφορετικά μορφολογικά και λειτουργικά
ΚΥΤΤΑΡΑ ΖΥΓΩΤΟ: Το πρώτο κύτταρο του οργανισμού από το οποίο με συνεχείς κυτταρικές διαιρέσεις προκύπτουν όλα. ΔΙΑΦΟΡΟΠΟΙΗΣΗ: Διαδικασία με την οποία τα κύτταρα αποκτούν διαφορετικά μορφολογικά και λειτουργικά
TO ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ. α) Από τους δύο όρχεις, από τους οποίους παράγονται τα σπερματοζωάρια και οι ορμόνες.
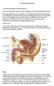 TO ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ Το γεννητικό σύστημα του άνδρα αποτελείται: α) Από τους δύο όρχεις, από τους οποίους παράγονται τα σπερματοζωάρια και οι ορμόνες. β) Από την εκφορητική οδό του σπέρματος, η οποία αποτελείται
TO ΓΕΝΝΗΤΙΚΟ ΣΥΣΤΗΜΑ Το γεννητικό σύστημα του άνδρα αποτελείται: α) Από τους δύο όρχεις, από τους οποίους παράγονται τα σπερματοζωάρια και οι ορμόνες. β) Από την εκφορητική οδό του σπέρματος, η οποία αποτελείται
