P 1 V 1 = σταθ. P 2 V 2 = σταθ.
|
|
|
- Αγρίππας Σκλαβούνος
- 8 χρόνια πριν
- Προβολές:
Transcript
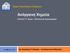
1 ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ 83 Την κατάσταση ενός αερίου μέσα σε ένα δοχείο μπορούμε να την κατανοήσουμε, άρα και να την περιγράψουμε πλήρως, αν γνωρίζουμε τις τιμές των παραμέτρων εκείνων που επηρεάζουν την συμπεριφορά του αερίου. Οι παράμετροι αυτές είναι : 1. η πίεση (P) που ασκεί το αέριο μέσα στο δοχείο, 2. ο όγκος (V) του δοχείου που περιέχει το αέριο, 3. η απόλυτη θερμοκρασία (Τ) του αερίου μέσα στο δοχείο και 4. ο αριθμός των μορίων (Ν) του αερίου μέσα στο δοχείο ( τα mol n του αερίου στο δοχείο ). Ας υποθέσουμε ότι σε δοχείο όγκου V, περιέχονται Ν μόρια ( που αντιστοιχούν σε n mol ) ενός αερίου σε θερμοκρασία Τ Kelvin (K). Τα μόρια του αερίου μέσα στο δοχείο κινούνται με σχετικά μεγάλες ταχύτητες και συγκρούονται με τα τοιχώματα του δοχείου. Το αποτέλεσμα αυτών των συγκρούσεων είναι η πίεση P που ασκεί το αέριο μέσα στο δοχείο. Εφόσον ο όγκος V του δοχείου, η θερμοκρασία Τ και ο αριθμός των μορίων Ν (δηλ ο αριθμός των n mol), διατηρούνται σταθερά, τότε και η πίεση P του αερίου μέσα στο δοχείο διατηρείται σταθερή (δεν μεταβάλλεται). Αν μεταβάλλουμε κάποιον ή κάποιους από τους παράγοντες V, n, T τότε και η πίεση P του αερίου μέσα στο δοχείο θα μεταβληθεί. Πειραματιζόμενοι παρατηρούμε ότι διατηρώντας σταθερή την τιμή δύο από τους παράγοντες V, n, T και ρυθμίζοντας την τιμή του τρίτου από αυτούς, ελέγχουμε την πίεση του αερίου μέσα στο δοχείο. Οι μαθηματικές σχέσεις οι οποίες δείχνουν πώς μεταβάλλεται η τιμή μιας από τις παραμέτρους P, V, n και T, όταν μεταβάλλεται η τιμή κάποιας άλλης ονομάζονται νόμοι των αερίων. 1 ος νόμος (νόμος του Boyle) : PV P = σταθ, P = f (V) ( Ισόθερμη μεταβολή ) αν n και T Διατύπωση του νόμου : «Για μία ορισμένη ποσότητα αερίου ( n= σταθερό ) και σε ορισμένη θερμοκρασία ( Τ=σταθερή ) η πίεση P είναι αντιστρόφως ανάλογη του όγκου V του αερίου». Αν σε όγκο V 1 αέριο ασκεί πίεση P 1 ισχύει : P 1 V 1 ( με n και T ) P 1 V 1 = P 2 V 2 Αν σε όγκο V 2 αέριο ασκεί πίεση P 2 ισχύει : P 2 V 2 Η γραφική παράσταση της πίεσης P έναντι του όγκου V, για ορισμένη ποσότητα αερίου υπό σταθερή θερμοκρασία T, δίνεται από το διάγραμμα που ακολουθεί και ονομάζεται ισόθερμος μεταβολή. Το διάγραμμα αυτό δείχνει ότι η πίεση P ορισμένης ποσότητας αερίου είναι αντιστρόφως ανάλογη του όγκου του V, υπό σταθερή θερμοκρασία T. Επί πλέον με τις τιμές p, V επαληθεύεται η σχέση : P / atm Ισόθερμος μεταβολή Ν = αριθμός μορίων σταθερός T = σταθερό P 1 V 1 = P 2 V 2 2 Παρατηρήστε τις τιμές της γραφικής παράστασης : PV 63 = Το διάγραμμα P = f(v) V / L
2 84 8ο ΓΕΛ Πειραιά - Χημεία Α Λυκείου 2ος νόμος (νόμος του Charles) : ( ισοβαρής μεταβολή ) αν n =σταθ V T, V = f (T) και P =σταθ. Διατύπωση του νόμου : «Για μία ορισμένη ποσότητα αερίου ( n=σταθ ) και σε σταθερή πίεση ( Ρ=σταθ ) ο όγκος V είναι ανάλογος της απόλυτης θερμοκρασίας T του αερίου». Αν σε θερμοκρασία T1 το αέριο έχει όγκο V1 ισχύει : ( με n και Ρ ) Αν σε θερμοκρασία T2 το αέριο έχει όγκο V2 ισχύει : Η γραφική παράσταση του όγκου V έναντι της θερμοκρασίας T, για ορισμένη ποσότητα αερίου, υπό σταθερή πίεση P, δίνεται από το διάγραμμα που ακολουθεί και ονομάζεται ισοβαρής μεταβολή. Το διάγραμμα αυτό δείχνει ότι ο όγκος V, ορισμένης ποσότητας αερίου, είναι ανάλογος της απόλυτης θερμοκρασίας του T, υπό σταθερή πίεση Ρ. Ισοβαρής μεταβολή V/L 8 N = σταθερό Επί πλέον με τις τιμές V, T του διαγράμματος επαληθεύεται η σχέση P = σταθερή Στο διπλανό διάγραμμα = T/K Το διάγραμμα V = f (T) 3ος νόμος ( νόμος Gay Lussac ) : ( ισόχωρος μεταβολή ) 600 αν n = σταθ P T, P = f (T) και V Διατύπωση του νόμου : «Για μία ορισμένη ποσότητα αερίου ( n=σταθ ) και σε σταθερό όγκο ( V=σταθ ) η πίεση P είναι ανάλογος της απόλυτης θερμοκρασίας T του αερίου». Αν n mol αερίου ασκούν πίεση Ρ1, σε θερμοκρασία T1 ισχύει : με n =σταθ. και V =σταθ. Αν n mol αερίου ασκούν πίεση Ρ2, σε θερμοκρασία T2 ισχύει :
3 85 8ο ΓΕΛ Πειραιά - Χημεία Α Λυκείου Η γραφική παράσταση της πίεσης Ρ, ορισμένης ποσότητας αερίου n, υπό σταθερό όγκο V, έναντι της θερμοκρασίας T, P = f (T), δίνεται από το διάγραμμα που ακολουθεί. Το διάγραμμα αυτό δείχνει ότι η πίεση Ρ, υπό σταθερό όγκο V, είναι ανάλογος της απόλυτης θερμοκρασίας του αερίου. Iσόχωρος μεταβολή P / atm 10 N = σταθερό V = σταθερό Επί πλέον με τις τιμές P, T επαληθεύεται η σχέση 5 Στο διπλανό διάγραμμα Συνδυαστικός νόμος : 400 = 800 Το διάγραμμα P = f (T) P = f ( V, T ) για n = σταθερό. Αν n mol αερίου ασκούν πίεση Ρ1, σε δοχείο όγκου V1 και σε θερμοκρασία T1, ισχύει : (1) Αν n mol αερίου ασκούν πίεση Ρ2, σε δοχείο όγκου V2 και σε θερμοκρασία T2, ισχύει : (2) Από τις σχέσεις ( 1 ) και ( 2 ) προκύπτει η σχέση : = T/K
4 86 4 ος νόμος : Συσχετίζει την πίεση P P n P = f (n) με τον αριθμό των μορίων. ( δηλαδή με τα mol του αερίου) αν T και V Διατύπωση του νόμου : «Η πίεση P ενός αερίου, σε δοχείο σταθερού όγκου ( V=σταθ. ) και υπό σταθερή θερμοκρασία ( T=σταθ. ), είναι ανάλογη με τον αριθμό των μορίων (ή των mol n) του αερίου». Με απλά λόγια διπλασιασμός του αριθμού των μορίων του αερίου θα έχει σαν αποτέλεσμα το διπλασιασμό της πίεσης. Αν n 1 mol αερίου ασκούν πίεση P 1 ισχύει : ( με V και T ) Αν n 2 mol αερίου ασκούν πίεση P 2 ισχύει : Η γραφική παράσταση της πίεσης P έναντι του αριθμού των mol του αερίου, υπό σταθερό όγκο V, και υπό σταθερή θερμοκρασία T, είναι ευθεία που διέρχεται από την αρχή των αξόνων. P / atm 2P 1 V = σταθερό T = σταθερό P 1 x 2x n / mol Το διάγραμμα P = f(n)
5 Καταστατική εξίσωση των αερίων 87 Με βάση τους τρεις νόμους που αναφέραμε, προκύπτει ως συμπέρασμα ότι : πίεση P ενός αερίου είναι συνάρτηση, του όγκου V, των mol n και της απόλυτης θερμοκρασίας T του αερίου. «Η πίεση P ενός αερίου είναι : Δηλαδή : P = f (, n, T ) α. αντιστρόφως ανάλογη του όγκου V του αερίου, ( ο όγκος V του αερίου ταυτίζεται με τον όγκο V του δοχείου που περιέχει το αέριο) β. ανάλογη του αριθμού των mol (n) του αερίου, και γ. ανάλογη της απόλυτης θερμοκρασίας T του αερίου». Η εξάρτηση αυτή της πίεσης P ενός αερίου από τον αριθμό των mol (n), την απόλυτη θερμοκρασία T και τον όγκο V του αερίου, αποδίδεται από την παρακάτω μαθηματική εξίσωση, που είναι γνωστή ως καταστατική εξίσωση των αερίων. P = R PV = nrt Η σταθερά αναλογίας R ονομάζεται παγκόσμια σταθερά των αερίων και η τιμή της εξαρτάται από τις μονάδες των μεγεθών P, V και T, έχει δε την ίδια τιμή για όλα τα αέρια. Αν η πίεση P είναι μετρημένη σε atm, ο όγκος V σε L και η θερμοκρασία T σε K : R = 0,082 Για την μετατροπή των βαθμών Κελσίου (θ) σε Kelvin (T) : T = θ Για την μετατροπή της πίεσης από mm στήλης υδραργύρου (Hg) σε atm : 1 atm = 760 mm Hg y atm =
6 Λυμένα προβλήματα Ορισμένη ποσότητα αερίου ασκεί πίεση Ρ 1 = 4 atm, σε δοχείο σταθερού όγκου V και σε θερμοκρασία θ 1 = 27 o C. Σε ποια θερμοκρασία η ίδια ποσότητα αερίου και στο ίδιο δοχείο όγκου V, θα ασκεί πίεση 5 atm; Σταθερή ποσότητα αερίου : n = σταθερό. Επί πλέον δίνεται ότι και V = σταθερό. Έχουμε επομένως εξάρτηση της πίεσης Ρ του αερίου μόνο από την θερμοκρασία Τ. Ρ = f(t). Ρ 1 = 4 atm, T 1 = θ T 1 = T 1 = 300 k Ρ 2 = 5 atm, T 2 = ; Σύμφωνα με τον νόμο Gay Lussac : T 2 = T 2 = T 2 = 575 T 2 = 375 k Όμως T 2 = θ θ 2 = T θ 2 = θ 2 = 102 o C ( Να προτείνετε μία δεύτερη μέθοδο επίλυσης του προβλήματος ) 2. Ορισμένη ποσότητα αερίου ασκεί πίεση Ρ 1 σε δοχείο σταθερού όγκου V 1 και σε θερμοκρασία θ 1 = 127 o C. Πόσες φορές θα μεταβληθεί η πίεση αν η θερμοκρασία αυξηθεί στους 327 o C και ο όγκος του δοχείου υποδιπλασιαστεί; Σταθερή ποσότητα αερίου : n = σταθερό. Ρ 1, T 1 = θ T 1 = T 1 = 400 k Ρ 2 = ; φορές το Ρ 1, T 2 = θ T 2 = T 2 = 600 k, V 1 =2V 2 Στον συνδυαστικό νόμο των αερίων = P 2 = με V 1 =2V 2 P 2 = P 2 = P 2 = P 2 = P 2 = 3P 1 Δηλαδή η πίεση στο δοχείο θα τριπλασιαστεί
7 89 3. Ορισμένη ποσότητα CO 2 έχει όγκο 600 ml, υπό πίεση 4,1 atm και θερμοκρασία 27 o C. Να υπολογίσετε : α. την μάζα του CO 2 β. τον όγκο αυτής της ποσότητας του CO 2 σε stp, γ. την πυκνότητα του CO 2 i. σε p=4,1 atm, θ=27 o C, και ii. σε stp Δίνονται οι σχετικές ατομικές μάζες (Ar) C:12, O:16. V 1 = 600 ml = 0,6 L, T = θ T = T = 300 K, Mr (CO2) =... =44 α. Από την καταστατική εξίσωση των αερίων PV = nrt λύνουμε ως προς n και αντικαθιστούμε: n = n = n = n = 0,1 mol CO 2 όμως m = nmr m = 0,144 m = 4,4 g CO 2 β. Για stp από τη σχέση: V 2 = n22,4 V 2 =0,122,4 V 2 = 2,24 L = 224 ml. γ. i. Από τον τύπο της πυκνότητας ρ 1 = ρ 1 = ρ 1 = 7,33 g/l ii. Από την ίδια σχέση ρ 2 = ρ 2 = ρ 2 = 1,96 g/l 4. Σε κενό δοχείο σταθερού όγκου 16,4 L εισάγονται 16 g οξυγόνου. Να βρείτε : α. την πίεση του οξυγόνου στο δοχείο στους 27 o C, β. σε ποια θερμοκρασία η πίεση του οξυγόνου στο δοχείο θα είναι 0,8 atm; Για το οξυγόνο Ar = 16. Ο 2 : Mr = 2Ar Mr = 216 = 32, T 1 = T 1 = 300 K α. Στην καταστατική εξίσωση των αερίων P 1 V = nrt 1 αντικαθιστούμε όπου n = και παίρνουμε : P 1 V = RT 1 P 1 = P 1 = P 1 = 0,75 atm β. από την : P 2 V = T 2 = T 2 = T 2 = 320 K Όμως Τ 2 = θ 2 θ 2 = Τ θ 2 = θ 2 = 47 o C.
8 90 5. Ισομοριακό αέριο μίγμα Η 2, Ν 2 έχει μάζα 12 g. α. Να βρείτε τον αριθμό των mol και την μάζα του κάθε συστατικού αυτού του μίγματος. β. Το μίγμα αυτό εισάγεται σε δοχείο Δ και ασκεί πίεση 0,82 atm στους 27 o C. Να βρείτε τον όγκο του δοχείου V Δ. Δίνονται οι Ar, H:1, N:14. H 2 : Mr = 2Ar Mr = 21 = 2, N 2 : Mr = 2Ar Mr = 214 = 28 α. Ισομοριακό μίγμα σημαίνει ότι τα mol των συστατικών του είναι ίσα : n H2 = n N2 =x m μίγμ. = 12 g m H2 + m N2 = 12 g όμως m i = n i Mr Mr H2n H2 + Mr N2 n N2 =12 g 2x + 28x = 12 30x = 12 x = 0,4 επομένως : το αέριο μίγμα αποτελείται από : x = 0,4 mol H 2 και x= 0,4 mol N 2. β. T = θ T = T =300 Κ, n μίγμ. = n H2 + n N2 = x + x = 0,8 mol Από την καταστατική εξίσωση PV = n μίγμ. RT λύνουμε ως προς V και έχουμε : V Δ = μίγμ V Δ = V Δ = V Δ = 24 L 6. Ένα μίγμα CO και ΝΟ 2 έχει μάζα 10,2 g και όγκο 6,72 L σε stp. α. Να βρείτε την μάζα του κάθε συστατικού αυτού του μίγματος. β. Το μίγμα αυτό εισάγεται σε δοχείο Δ και ασκεί πίεση 0,82 atm στους 27 o C. Να βρείτε τον όγκο του δοχείου V Δ. Δίνονται οι Ar, H:1, N:14. Έστω x mol CO και y mol ΝΟ 2 στο μίγμα. CO : Mr = Mr = 28, NΟ 2 : Mr = Mr = 46 m μίγμ. = 10,2 g m CO + m NO2 = 10,2 g όμως m i = n i Mr Mr (CO) n (CO) + Mr (N2) n (N2) = 10,2 g 28x + 46y =10,2 (1) Όμως V μίγματος = 6,72 L σε stp n μίγματος = n μίγματος = n μίγματος = 0,3 x + y = 0,3 (2) Οι εξισώσεις (1) και (2) αποτελούν σύστημα : 28x + 46y = 10,2 1 28x + 46y = 10,2 28x + 46y = 10,2 x + y = 0, x + 28y = 0, x + 28y = 8,4 ( 28x + 46y ) ( 28x + 28y ) = 10,2 8,4 28x + 46y 28x 28y = 1,8 18y = 1,8 y = 0,1 και από την (2) x = 0,2 Δηλαδή το μίγμα CO, NO 2 αποτελείται από y = 0,1 mol CO και 0,2 mol NO 2. Μάζες : m (CO) = n (CO) Mr (CO) m (CO) = 0,228 m (CO) = 5,6 g στο μίγμα m (N2) = n (N2) Mr (N2) m (N2) = 0,146 m (N2) = 4,6 g στο μίγμα.
9 91 7. Σε δοχείο σταθερού όγκου V = 8,2 L περιέχεται ένα αέριο χημικό στοιχείο Α σε θερμοκρασία 227 o C και πίεση 950 mmhg. Το αέριο που περιέχεται στο δοχείο ζυγίζει 7 g και αποτελείται από 3, άτομα. Να υπολογίσετε : α. τη σχετική μοριακή μάζα Mr του αερίου Α, β. τον αριθμό των μορίων του αερίου Α που περιέχονται στο δοχείο, γ. τον αριθμό των ατόμων που αποτελούν το μόριο του αερίου Α, δ. την πίεση που θα ασκείται στο δοχείο αν ψυχθεί στους 27 o C. V = 16,4 L, T = θ T 1 = T 1 = 500 K, P 1 = = 1,25 atm. α. Στην καταστατική εξίσωση των αερίων P 1 V = nrt 1 αντικαθιστούμε όπου n = και παίρνουμε : P 1 V = RT 1 Mr = Mr = Mr = 28 β. Από τη σχέση : n = n = n =0,25 mol αερίου A, οπότε από τη σχέση: n = μόρια Ν Α μόρια = n N A μόρια A = 0,25 N A μόρια A = μόρια A = μόρια A = 1, τα μόρια του αερίου Α στο δοχείο. γ. Από τη σχέση: άτομα = μόρια ατομικότητα ατομικότητα = άτομα μόρια δ. Από την : P 2 V= RT 2 P 2 = = 2 άτομα στο μόριο του αερίου Α P 2 = P 2 = 0,75 atm
10 Ασκήσεις και προβλήματα α. Αν διπλασιάσουμε τον όγκο V ορισμένης ποσότητας αερίου υπό σταθερή θερμοκρασία T, η πίεσή του P θα β. Αν διπλασιάσουμε τη θερμοκρασία T ορισμένης ποσότητας αερίου διατηρώντας τον όγκο του V σταθερό, η πίεσή του P θα γ. Αν διπλασιάσουμε τη θερμοκρασία T ορισμένης ποσότητας αερίου διατηρώντας σταθερή την πίεσή του P, ο όγκος του V θα 2. Ένα δοχείο Α όγκου 0,5 L περιέχει αέριο Η 2 σε θερμοκρασία θ o C. Σε ένα δοχείο Β όγκου 2 L περιέχει την ίδια ποσότητα Η 2 με το δοχείο Α, στην ίδια θερμοκρασία. Η πίεση στο δοχείο Β μετρήθηκε και βρέθηκε 1 atm. Να βρείτε τη πίεση που ασκεί το Η 2 στο δοχείο Α. 3. Χρησιμοποιήστε την καταστατική εξίσωση των αερίων και βρείτε : α. τη σχέση που δίνει την πυκνότητα ενός αερίου ως συνάρτηση της πίεσης (P), της θερμοκρασίας (T) και της σχετικής μοριακής του μάζας (Mr). β. τη σχέση με την οποία μπορούμε να βρούμε τη σχετική μοριακή μάζα (Mr) ενός αερίου, αν γνωρίζουμε την μάζα του (m), τον όγκο του (V), την πίεση (P) και την θερμοκρασία (T). 4. Χρησιμοποιήστε την καταστατική εξίσωση των αερίων και αποδείξτε ότι : α. «ίσοι όγκοι αερίων στις ίδιες συνθήκες πίεσης και θερμοκρασίας περιέχουν τον ίδιο αριθμό μορίων» και αντίστροφα β. «ίσοι αριθμοί μορίων κάτω από τις ίδιες συνθήκες πίεσης και θερμοκρασίας καταλαμβάνουν τον ίδιο όγκο». 5. Να συμπληρώσετε τα κενά του παρακάτω πίνακα για τα αέρια που δίνονται στη πρώτη στήλη. μάζα m σε g όγκος σε stp σε L αριθμός mol αριθμός μορίων CO 12, O 2 11,2 H 2 S Σε ένα δοχείο όγκου 8,2 L περιέχονται 8 g αερίου CH 4 σε θερμοκρασία 27 o C. Υπολογίστε : α. τον αριθμό των mol του CH 4 β. την πίεση του CH 4. Σχετικές ατομικές μάζες H:1, C : Σε ένα δοχείο όγκου V, περιέχονται 4 g H 2 και 14 g N 2 σε θερμοκρασία 400 Κ. Αν το μίγμα των δύο αυτών αερίων ασκεί πίεση 16,4 atm, να υπολογίσετε : α. τον όγκο V του δοχείου. Δίνονται οι σχετικές ατομικές μάζες H:1, N :14. β. το τμήμα της πίεσης που οφείλεται στα μόρια του Η 2, γ. το τμήμα της πίεσης που οφείλεται στα μόρια του Ν 2, 8. Σε ένα δοχείο όγκου 82 L περιέχονται 4 g H 2 και 22 g CO 2 σε θερμοκρασία θ=127 o C. Να υπολογίστε : α. τον συνολικό αριθμό mol των αερίων. β. την συνολική πίεση του αερίου μίγματος. Σχετικές ατομικές μάζες H:1, C : Ένα δοχείο χωρητικότητας 5,6 L περιέχει CO 2 σε stp. Υπολογίστε : α. τον αριθμό των mol του CO 2 β. την μάζα του CO 2 γ. τον αριθμό των μορίων του CO 2. Σχετικές ατομικές μάζες C :12, Ο:16. δ. την πίεση Ρ που θα ασκείται στο δοχείο, αν υποδιπλασιάσουμε τον όγκο και διπλασιάσουμε τον αριθμό των μορίων του CO 2 στους 27 o C. Σχετικές ατομικές μάζες C :12, Ο: Αέριο N 2 ασκεί πίεση P A =2 atm σε ένα δοχείο Α όγκου V A, σε θερμοκρασία 127 o C. Αέριο O 2 ασκεί πίεση P B =1,5 atm σε ένα δοχείο B, διπλάσιου όγκου από το Α, σε θερμοκρασία 27 o C. Αν η μάζα του Ο 2 στο δοχείο Β είναι 6,4 g, να βρείτε την μάζα του Ν 2 στο δοχείο Α. Δίνονται οι Ar, Ν :14, Ο:16.
2.2 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΕΡΙΩΝ
 2.2 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΕΡΙΩΝ Έστω ότι μια ποσότητα αερίου έχει όγκο V, πίεση P και απόλυτη θερμοκρασία Τ. Διατηρώντας σταθερή τη θερμοκρασία Τ του αερίου, μεταβάλλουμε τον όγκο μέχρι την τιμή V,
2.2 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΤΩΝ ΑΕΡΙΩΝ Έστω ότι μια ποσότητα αερίου έχει όγκο V, πίεση P και απόλυτη θερμοκρασία Τ. Διατηρώντας σταθερή τη θερμοκρασία Τ του αερίου, μεταβάλλουμε τον όγκο μέχρι την τιμή V,
(1 mol οποιουδήποτε αερίου σε συνθήκες STP καταλαμβάνει όγκο 22,4 L, κατά συνέπεια V mol =22,4 L)
 ΑΠΑΝΤΗΣΕΙΣ σε ol ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ) Πόσα ol είναι τα 4,48 L αέριας NH 3 τα οποία μετρήθηκαν σε συνθήκες ST; n= n= 4,48 n= 0, ol ol,4 ( ol οποιουδήποτε αερίου σε συνθήκες ST καταλαμβάνει όγκο,4 L, κατά
ΑΠΑΝΤΗΣΕΙΣ σε ol ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ) Πόσα ol είναι τα 4,48 L αέριας NH 3 τα οποία μετρήθηκαν σε συνθήκες ST; n= n= 4,48 n= 0, ol ol,4 ( ol οποιουδήποτε αερίου σε συνθήκες ST καταλαμβάνει όγκο,4 L, κατά
ΜΕΤΑΒΟΛΕΣ-ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ
 ΜΕΤΑΒΟΛΕΣ-ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ ΕΙΣΑΓΩΓΗ Η αέριος κατάσταση είναι μία από τις τρείς καταστάσεις της ύλης. Η κατάσταση αυτή χαρακτηρίζεται, όπως γνωρίζετε, από το γεγονός ότι τα σώματα σε αυτήν δεν έχουν σταθερό
ΜΕΤΑΒΟΛΕΣ-ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ ΕΙΣΑΓΩΓΗ Η αέριος κατάσταση είναι μία από τις τρείς καταστάσεις της ύλης. Η κατάσταση αυτή χαρακτηρίζεται, όπως γνωρίζετε, από το γεγονός ότι τα σώματα σε αυτήν δεν έχουν σταθερό
Παρουσίαση Εννοιών στη Φυσική της Β Λυκείου. Κεφάλαιο Πρώτο Ενότητα: Νόμοι των αερίων
 Παρουσίαση Εννοιών στη Φυσική της Β Λυκείου Κεφάλαιο Πρώτο Ενότητα: Νόμοι των αερίων ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ 1.1. Νόμος του Boyle (ισόθερμη μεταβολή) Η πίεση ορισμένης ποσότητας αερίου, του
Παρουσίαση Εννοιών στη Φυσική της Β Λυκείου Κεφάλαιο Πρώτο Ενότητα: Νόμοι των αερίων ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ 1.1. Νόμος του Boyle (ισόθερμη μεταβολή) Η πίεση ορισμένης ποσότητας αερίου, του
Καταστατική εξίσωση ιδανικών αερίων
 Καταστατική εξίσωση ιδανικών αερίων 21-1. Από τι εξαρτάται η συμπεριφορά των αερίων; Η συμπεριφορά των αερίων είναι περισσότερο απλή και ομοιόμορφη από τη συμπεριφορά των υγρών και των στερεών. Σε αντίθεση
Καταστατική εξίσωση ιδανικών αερίων 21-1. Από τι εξαρτάται η συμπεριφορά των αερίων; Η συμπεριφορά των αερίων είναι περισσότερο απλή και ομοιόμορφη από τη συμπεριφορά των υγρών και των στερεών. Σε αντίθεση
ΦΥΣΙΚΗ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Β ΛΥΚΕΙΟΥ. Κινητική Θεωρία Αερίων. Επιμέλεια: ΑΓΚΑΝΑΚΗΣ A.ΠΑΝΑΓΙΩΤΗΣ, Φυσικός
 ΦΥΣΙΚΗ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Β ΛΥΚΕΙΟΥ Κινητική Θεωρία Αερίων Επιμέλεια: ΑΓΚΑΝΑΚΗΣ A.ΠΑΝΑΓΙΩΤΗΣ, Φυσικός / Νόμος του Boyle: με τον όγκο. Η πίεση ορισμένης ποσότητας αερίου του οποίου η θερμοκρασία
ΦΥΣΙΚΗ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Β ΛΥΚΕΙΟΥ Κινητική Θεωρία Αερίων Επιμέλεια: ΑΓΚΑΝΑΚΗΣ A.ΠΑΝΑΓΙΩΤΗΣ, Φυσικός / Νόμος του Boyle: με τον όγκο. Η πίεση ορισμένης ποσότητας αερίου του οποίου η θερμοκρασία
- 31 Ερωτήσεις Αξιολόγησης για ΤΕΣΤ Θεωρίας.
 Κεφάλαιο 1 ο :ΝΟΜΟΙ ΑΕΡΙΩΝ ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Επιμέλεια ύλης: Γ.Φ.ΣΙΩΡΗΣ- Φυσικός - 31 Ερωτήσεις Αξιολόγησης για ΤΕΣΤ Θεωρίας. 1. Να διατυπώσετε το νόμο του Robert Boyle και να κάνετε το αντίστοιχο
Κεφάλαιο 1 ο :ΝΟΜΟΙ ΑΕΡΙΩΝ ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Επιμέλεια ύλης: Γ.Φ.ΣΙΩΡΗΣ- Φυσικός - 31 Ερωτήσεις Αξιολόγησης για ΤΕΣΤ Θεωρίας. 1. Να διατυπώσετε το νόμο του Robert Boyle και να κάνετε το αντίστοιχο
ΔΙΑΓΩΝΙΣΜΑ ΦΥΣΙΚΗΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ
 Θέμα 1 ο ΔΙΑΓΩΝΙΣΜΑ ΦΥΣΙΚΗΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ 1--015 1. Ορισμένη ποσότητα ιδανικού αερίου υπόκειται σε μεταβολή κατά τη διάρκεια της οποίας η θερμοκρασία του παραμένει σταθερή, ενώ η πίεση του
Θέμα 1 ο ΔΙΑΓΩΝΙΣΜΑ ΦΥΣΙΚΗΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ 1--015 1. Ορισμένη ποσότητα ιδανικού αερίου υπόκειται σε μεταβολή κατά τη διάρκεια της οποίας η θερμοκρασία του παραμένει σταθερή, ενώ η πίεση του
Μεθοδολογία Προβλημάτων
 Μεθοδολογία Προβλημάτων 39 Α. Προβλήματα εύρεσης του Μοριακού Τύπου χημικής ένωσης Ο Μοριακός τύπος μιας ένωσης μας δίνει το είδος των ατόμων που περιέχονται στο μόριο της ένωσης, αλλά και τον ακριβή τους
Μεθοδολογία Προβλημάτων 39 Α. Προβλήματα εύρεσης του Μοριακού Τύπου χημικής ένωσης Ο Μοριακός τύπος μιας ένωσης μας δίνει το είδος των ατόμων που περιέχονται στο μόριο της ένωσης, αλλά και τον ακριβή τους
Στοιχειομετρικοί Υπολογισμοί στη Χημεία
 Στοιχειομετρικοί Υπολογισμοί στη Χημεία Δομικές μονάδες της ύλης ΑΤΟΜΑ ΜΟΡΙΑ ΣΤΟΙΧΕΙΑ ΕΝΩΣΕΙΣ Αριθμός Avogadro N A = 6,02 10 23 mol -1 Δηλαδή αυτός ο αριθμός παριστάνει την ποσότητα μιας ουσίας που περιέχει
Στοιχειομετρικοί Υπολογισμοί στη Χημεία Δομικές μονάδες της ύλης ΑΤΟΜΑ ΜΟΡΙΑ ΣΤΟΙΧΕΙΑ ΕΝΩΣΕΙΣ Αριθμός Avogadro N A = 6,02 10 23 mol -1 Δηλαδή αυτός ο αριθμός παριστάνει την ποσότητα μιας ουσίας που περιέχει
ΚΕΦΑΛΑΙΟ 3 Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ
 Σχολικό Έτος 016-017 67 ΚΕΦΑΛΑΙΟ Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Α. ΕΙΣΑΓΩΓΗ ΣΤΑ ΑΕΡΙΑ 1. Σχετικές Ατομικές και Μοριακές Μάζες Σχετική Ατομική Μάζα (Α r) του ατόμου ενός στοιχείου, ονομάζεται ο αριθμός
Σχολικό Έτος 016-017 67 ΚΕΦΑΛΑΙΟ Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Α. ΕΙΣΑΓΩΓΗ ΣΤΑ ΑΕΡΙΑ 1. Σχετικές Ατομικές και Μοριακές Μάζες Σχετική Ατομική Μάζα (Α r) του ατόμου ενός στοιχείου, ονομάζεται ο αριθμός
1 IΔΑΝΙΚΑ ΑΕΡΙΑ 1.1 ΓΕΝΙΚΑ
 1 1 IΔΑΝΙΚΑ ΑΕΡΙΑ 1.1 ΓΕΝΙΚΑ Θα αρχίσουμε τη σειρά των μαθημάτων της Φυσικοχημείας με τη μελέτη της αέριας κατάστασης της ύλης. Η μελέτη της φύσης των αερίων αποτελεί ένα ιδανικό μέσο για την εισαγωγή
1 1 IΔΑΝΙΚΑ ΑΕΡΙΑ 1.1 ΓΕΝΙΚΑ Θα αρχίσουμε τη σειρά των μαθημάτων της Φυσικοχημείας με τη μελέτη της αέριας κατάστασης της ύλης. Η μελέτη της φύσης των αερίων αποτελεί ένα ιδανικό μέσο για την εισαγωγή
Θεωρία και Μεθοδολογία
 Θεωρία και Μεθοδολογία Εισαγωγή/Προαπαιτούμενες γνώσεις (κάθετη δύναμη) Πίεση p: p = F A (εμβαδόν επιφάνειας) Μονάδα μέτρησης πίεσης στο S.I. είναι το 1 Ν m2, που ονομάζεται και Pascal (Pa). Συνήθως χρησιμοποιείται
Θεωρία και Μεθοδολογία Εισαγωγή/Προαπαιτούμενες γνώσεις (κάθετη δύναμη) Πίεση p: p = F A (εμβαδόν επιφάνειας) Μονάδα μέτρησης πίεσης στο S.I. είναι το 1 Ν m2, που ονομάζεται και Pascal (Pa). Συνήθως χρησιμοποιείται
Σ Τ Ο Ι Χ Ε Ι Ο Μ Ε Τ Ρ Ι Α
 71 Σ Τ Ο Ι Χ Ε Ι Ο Μ Ε Τ Ρ Ι Α Οι μάζες των ατόμων και των μορίων είναι πολύ μικρές και δεν ενδείκνυται για τον υπολογισμό τους η χρήση των συνηθισμένων μονάδων μάζας ( Kg ή g ) γιατί προκύπτουν αριθμοί
71 Σ Τ Ο Ι Χ Ε Ι Ο Μ Ε Τ Ρ Ι Α Οι μάζες των ατόμων και των μορίων είναι πολύ μικρές και δεν ενδείκνυται για τον υπολογισμό τους η χρήση των συνηθισμένων μονάδων μάζας ( Kg ή g ) γιατί προκύπτουν αριθμοί
Print to PDF without this message by purchasing novapdf (http://www.novapdf.com/)
 ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ ΓΙΑ ΤΟΥΣ ΧΗΜΙΚΟΥΣ ΥΠΟΛΟΓΙΣΜΟΥΣ ΘΕΩΡΙΑ 1 Μol μιας ουσίας (στοιχείου ή ενώσεως) είναι η ποσότητα ύλης που αποτελείται από N A = 6,0220453 x 10 23 σωματίδια. O αριθμός N A = 6,0220453 x 10
ΒΑΣΙΚΕΣ ΕΝΝΟΙΕΣ ΓΙΑ ΤΟΥΣ ΧΗΜΙΚΟΥΣ ΥΠΟΛΟΓΙΣΜΟΥΣ ΘΕΩΡΙΑ 1 Μol μιας ουσίας (στοιχείου ή ενώσεως) είναι η ποσότητα ύλης που αποτελείται από N A = 6,0220453 x 10 23 σωματίδια. O αριθμός N A = 6,0220453 x 10
Επανάληψη των Κεφαλαίων 1 και 2 Φυσικής Γ Έσπερινού Κατεύθυνσης
 Επανάληψη των Κεφαλαίων 1 και Φυσικής Γ Έσπερινού Κατεύθυνσης Φυσικά µεγέθη, µονάδες µετρήσεως (S.I) και µετατροπές P: Η πίεση ενός αερίου σε N/m (1atm=1,013 10 5 N/m ). : Ο όγκος τουαερίου σε m 3 (1m
Επανάληψη των Κεφαλαίων 1 και Φυσικής Γ Έσπερινού Κατεύθυνσης Φυσικά µεγέθη, µονάδες µετρήσεως (S.I) και µετατροπές P: Η πίεση ενός αερίου σε N/m (1atm=1,013 10 5 N/m ). : Ο όγκος τουαερίου σε m 3 (1m
2. Να αποδείξετε ότι δυο ισόθερμες καμπύλες δεν είναι δυνατό να τέμνονται.
 Λυμένα παραδείγματα 1.Οι ισόθερμες καμπύλες σε δυο ποσοτήτων ιδανικού αερίου, n 1 και n 2 mol, στην ίδια θερμοκρασία Τ φαίνονται στο διπλανό διάγραμμα. Να αποδείξετε ότι είναι n 2 > n 1. ΑΠΑΝΤΗΣΗ: Παίρνουμε
Λυμένα παραδείγματα 1.Οι ισόθερμες καμπύλες σε δυο ποσοτήτων ιδανικού αερίου, n 1 και n 2 mol, στην ίδια θερμοκρασία Τ φαίνονται στο διπλανό διάγραμμα. Να αποδείξετε ότι είναι n 2 > n 1. ΑΠΑΝΤΗΣΗ: Παίρνουμε
ΛΥΣΕΙΣ. ΘΕΜΑ A Να γράψετε στο τετράδιο σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση.
 ΜΑΘΗΜΑ / ΤΑΞΗ: ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ / B ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1η ΗΜΕΡΟΜΗΝΙΑ: 04/11/1 ΛΥΣΕΙΣ ΘΕΜΑ A Να γράψετε στο τετράδιο σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράμμα που αντιστοιχεί
ΜΑΘΗΜΑ / ΤΑΞΗ: ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ / B ΛΥΚΕΙΟΥ ΣΕΙΡΑ: 1η ΗΜΕΡΟΜΗΝΙΑ: 04/11/1 ΛΥΣΕΙΣ ΘΕΜΑ A Να γράψετε στο τετράδιο σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράμμα που αντιστοιχεί
: Μιγαδικοί Συναρτήσεις έως και αντίστροφη συνάρτηση. 1. Ποιο από τα παρακάτω διαγράμματα παριστάνει γραφικά το νόμο του Gay-Lussac;
 Τάξη : Β ΛΥΚΕΙΟΥ Μάθημα : ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Εξεταστέα Ύλη : Μιγαδικοί Συναρτήσεις έως και αντίστροφη συνάρτηση Καθηγητής : Mάρθα Μπαμπαλιούτα Ημερομηνία : 14/10/2012 ΘΕΜΑ 1 ο 1. Ποιο από τα παρακάτω διαγράμματα
Τάξη : Β ΛΥΚΕΙΟΥ Μάθημα : ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Εξεταστέα Ύλη : Μιγαδικοί Συναρτήσεις έως και αντίστροφη συνάρτηση Καθηγητής : Mάρθα Μπαμπαλιούτα Ημερομηνία : 14/10/2012 ΘΕΜΑ 1 ο 1. Ποιο από τα παρακάτω διαγράμματα
ΤΟ MOL ΣΤΑ ΑΕΡΙΑ Η καταστατική εξίσωση των ιδανικών αερίων
 ΤΟ MOL ΣΤΑ ΑΕΡΙΑ Η καταστατική εξίσωση των ιδανικών αερίων Ελένη ανίλη, Χηµικός, Msc., Ph.D Η καταστατική εξίσωση των ιδανικών αερίων 2 Έχεις ποτέ χρησιµοποιήσει τρόµπα για να φουσκώσεις το λάστιχο του
ΤΟ MOL ΣΤΑ ΑΕΡΙΑ Η καταστατική εξίσωση των ιδανικών αερίων Ελένη ανίλη, Χηµικός, Msc., Ph.D Η καταστατική εξίσωση των ιδανικών αερίων 2 Έχεις ποτέ χρησιµοποιήσει τρόµπα για να φουσκώσεις το λάστιχο του
Σχέσεις ποσοτήτων χημικών σωματιδίων
 Σχέσεις ποσοτήτων χημικών σωματιδίων 20-1. Σχέση mol Ar (για άτομα) και mol Mr (για μόρια) To 1 mol ατόμων ζυγίζει Ar g Tα n mol ατόμων ζυγίζουν m g n m m 1 Ar Ar To 1 mol μορίων ζυγίζει Μr g Tα n mol
Σχέσεις ποσοτήτων χημικών σωματιδίων 20-1. Σχέση mol Ar (για άτομα) και mol Mr (για μόρια) To 1 mol ατόμων ζυγίζει Ar g Tα n mol ατόμων ζυγίζουν m g n m m 1 Ar Ar To 1 mol μορίων ζυγίζει Μr g Tα n mol
Συναρτήσει πάλι των x και ψ μπορούμε να υπολογίσουμε τον όγκο του μίγματος σε STP.
 Παράδειγμα 4.7 Αέριο μίγμα περιέχει CO και SO. Το μίγμα αυτό ζυγίζει 7,6 g, ενώ ο όγκος του σε STP συνθήκες είναι 3,36 L. α. Πόσα ol κάθε αερίου περιέχει το μίγμα; β. Ποια είναι η μάζα του CO στο μίγμα;
Παράδειγμα 4.7 Αέριο μίγμα περιέχει CO και SO. Το μίγμα αυτό ζυγίζει 7,6 g, ενώ ο όγκος του σε STP συνθήκες είναι 3,36 L. α. Πόσα ol κάθε αερίου περιέχει το μίγμα; β. Ποια είναι η μάζα του CO στο μίγμα;
Μετά το τέλος της μελέτης του 4ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση:
 Μετά το τέλος της μελέτης του 4ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει το πως ορίζονται η ατομική μονάδα μάζας, η σχετική ατομική μάζα (Αr) και η σχετική μοριακή μάζα (Μr). Να υπολογίζει
Μετά το τέλος της μελέτης του 4ου κεφαλαίου, ο μαθητής θα πρέπει να είναι σε θέση: Να γνωρίζει το πως ορίζονται η ατομική μονάδα μάζας, η σχετική ατομική μάζα (Αr) και η σχετική μοριακή μάζα (Μr). Να υπολογίζει
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις. Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι
 Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
Οι ιδιότητες των αερίων και καταστατικές εξισώσεις Θεόδωρος Λαζαρίδης Σημειώσεις για τις παραδόσεις του μαθήματος Φυσικοχημεία Ι Τι είναι αέριο; Λέμε ότι μία ουσία βρίσκεται στην αέρια κατάσταση όταν αυθόρμητα
Α. ΝΟΜΟΙ ΑΕΡΙΩΝ. 1. Β1.3 Να αντιστοιχίσετε τις µεταβολές της αριστερής στήλης σε σχέσεις τις δεξιάς στήλης. 1) Ισόθερµη µεταβολή α)
 Α. ΝΟΜΟΙ ΑΕΡΙΩΝ 1. Β1.3 Να αντιστοιχίσετε τις µεταβολές της αριστερής στήλης σε σχέσεις τις δεξιάς στήλης. 1) Ισόθερµη µεταβολή α) P = σταθ. V P 2) Ισόχωρη µεταβολή β) = σταθ. 3) Ισοβαρής µεταβολή γ) V
Α. ΝΟΜΟΙ ΑΕΡΙΩΝ 1. Β1.3 Να αντιστοιχίσετε τις µεταβολές της αριστερής στήλης σε σχέσεις τις δεξιάς στήλης. 1) Ισόθερµη µεταβολή α) P = σταθ. V P 2) Ισόχωρη µεταβολή β) = σταθ. 3) Ισοβαρής µεταβολή γ) V
ΣΧΕΔΙΟ ΜΑΘΗΜΑΤΟΣ. Ενότητα : ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ: ΙΣΟΧΩΡΗ ΜΕΤΑΒΟΛΗ ΝΟΜΟΣ CHARLES ΔΙΔΑΚΤΙΚΟΙ ΣΤΟΧΟΙ. Θεωρητική υποστήριξη
 1 ΣΧΕΔΙΟ ΜΑΘΗΜΑΤΟΣ Διδάσκων καθηγητής: Αντώνιος Αλεξ. Κρητικός Τάξη : Β Μάθημα : Φυσική Κατεύθυνσης Ενότητα : ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ: ΙΣΟΧΩΡΗ ΜΕΤΑΒΟΛΗ ΝΟΜΟΣ CHARLES Οι μαθητές/τριες να μπορέσουν: ΔΙΔΑΚΤΙΚΟΙ
1 ΣΧΕΔΙΟ ΜΑΘΗΜΑΤΟΣ Διδάσκων καθηγητής: Αντώνιος Αλεξ. Κρητικός Τάξη : Β Μάθημα : Φυσική Κατεύθυνσης Ενότητα : ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ: ΙΣΟΧΩΡΗ ΜΕΤΑΒΟΛΗ ΝΟΜΟΣ CHARLES Οι μαθητές/τριες να μπορέσουν: ΔΙΔΑΚΤΙΚΟΙ
διαιρούμε με το εμβαδό Α 2 του εμβόλου (1)
 1)Συνήθως οι πτήσεις των αεροσκαφών γίνονται στο ύψος των 15000 m, όπου η θερμοκρασία του αέρα είναι 210 Κ και η ατμοσφαιρική πίεση 10000 N / m 2. Σε αεροδρόμιο που βρίσκεται στο ίδιο ύψος με την επιφάνεια
1)Συνήθως οι πτήσεις των αεροσκαφών γίνονται στο ύψος των 15000 m, όπου η θερμοκρασία του αέρα είναι 210 Κ και η ατμοσφαιρική πίεση 10000 N / m 2. Σε αεροδρόμιο που βρίσκεται στο ίδιο ύψος με την επιφάνεια
Τμήμα Τεχνολογίας Τροφίμων. Ανόργανη Χημεία. Ενότητα 7 η : Αέρια Ιδιότητες & συμπεριφορά. Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής.
 Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 7 η : Αέρια Ιδιότητες & συμπεριφορά Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Αέρια & Πίεση Αερίων 2 Ο αέρας είναι ένα τυπικό αέριο
Τμήμα Τεχνολογίας Τροφίμων Ανόργανη Χημεία Ενότητα 7 η : Αέρια Ιδιότητες & συμπεριφορά Οκτώβριος 2018 Δρ. Δημήτρης Π. Μακρής Αναπληρωτής Καθηγητής Αέρια & Πίεση Αερίων 2 Ο αέρας είναι ένα τυπικό αέριο
Α3. Όταν η πίεση ορισμένης ποσότητας ιδανικού αερίου διπλασιάζεται υπό σταθερή θερμοκρασία, τότε η μέση κινητική ενέργεια των μορίων του αερίου:
 ΜΑΘΗΜΑ / ΤΑΞΗ : ΦΥΣΙΚΗ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / B ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΑΠΑΝΤΗΣΕΙΣ Α ΗΜΕΡΟΜΗΝΙΑ: 04-01-2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΑΡΧΩΝ Μ.-ΑΓΙΑΝΝΙΩΤΑΚΗ ΑΝ.-ΠΟΥΛΗ Κ.-ΚΟΡΚΙΔΑΚΗΣ Κ. ΘΕΜΑ Α Οδηγία: Να γράψετε
ΜΑΘΗΜΑ / ΤΑΞΗ : ΦΥΣΙΚΗ ΟΜΑΔΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ / B ΛΥΚΕΙΟΥ ΣΕΙΡΑ: ΑΠΑΝΤΗΣΕΙΣ Α ΗΜΕΡΟΜΗΝΙΑ: 04-01-2015 ΕΠΙΜΕΛΕΙΑ ΔΙΑΓΩΝΙΣΜΑΤΟΣ: ΑΡΧΩΝ Μ.-ΑΓΙΑΝΝΙΩΤΑΚΗ ΑΝ.-ΠΟΥΛΗ Κ.-ΚΟΡΚΙΔΑΚΗΣ Κ. ΘΕΜΑ Α Οδηγία: Να γράψετε
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 5-ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ. α. Να βρείτε τη σύσταση του δοχείου σε mol τις χρονικές στιγμές t 1 και t 2.
 ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 5-ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ 1. Σε δοχείο όγκου V=2L εισάγονται τη χρονική στιγμή t o =0, 10mol N 2(g) και 24mol H 2(g) τα οποία αντιδρούν σύμφωνα με τη (μονόδρομη) αντίδραση
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 5-ΧΗΜΙΚΗ ΚΙΝΗΤΙΚΗ 1. Σε δοχείο όγκου V=2L εισάγονται τη χρονική στιγμή t o =0, 10mol N 2(g) και 24mol H 2(g) τα οποία αντιδρούν σύμφωνα με τη (μονόδρομη) αντίδραση
3o ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΘΗΒΑΣ ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΩΝ ΕΠΙΣΤΗΜΩΝ ΕΠΙΜΕΛΕΙΑ: ΖΑΧΑΡΙΟΥ ΦΙΛΙΠΠΟΣ (ΧΗΜΙΚΟΣ)
 Σχετική ατομική μάζα Σχετική ήμ μοριακή μάζα Mole Αριθμός Avogadro Γραμμομοριακός όγκος Νόμοι των αερίων Ατομική μονάδα μάζας (amu): Σχετική ατομική μάζα (ar): Σχετική Μοριακή μάζα (Μr): Υπολογισμός
Σχετική ατομική μάζα Σχετική ήμ μοριακή μάζα Mole Αριθμός Avogadro Γραμμομοριακός όγκος Νόμοι των αερίων Ατομική μονάδα μάζας (amu): Σχετική ατομική μάζα (ar): Σχετική Μοριακή μάζα (Μr): Υπολογισμός
ΑΣΚΗΣΕΙΣ. 4. Για την αντίδραση 2Α + Β Γ βρέθηκαν τα παρακάτω πειραματικά δεδομένα:
 ΑΣΚΗΣΕΙΣ 1. Αν είναι γνωστό ότι οι παρακάτω αντιδράσεις είναι απλές (ενός μόνον σταδίου), να βρεθεί η τάξη καθεμίας από αυτές, καθώς επίσης οι διαστάσεις (μονάδες) της σταθεράς της ταχύτητας. α) Α Π β)
ΑΣΚΗΣΕΙΣ 1. Αν είναι γνωστό ότι οι παρακάτω αντιδράσεις είναι απλές (ενός μόνον σταδίου), να βρεθεί η τάξη καθεμίας από αυτές, καθώς επίσης οι διαστάσεις (μονάδες) της σταθεράς της ταχύτητας. α) Α Π β)
Διαγώνισμα Φυσικής κατεύθυνσης Β Λυκείου (3/11/2013)
 Διαγώνισμα Φυσικής κατεύθυνσης Β Λυκείου (//0) Ονοματεπώνυμο εξεταζόμενου: Καμιά άλλη σημείωση δεν επιτρέπεται στα θέματα τα οποία θα παραδώσετε μαζί με το γραπτό σας. Έτσι οι απαντήσεις όλων των θεμάτων
Διαγώνισμα Φυσικής κατεύθυνσης Β Λυκείου (//0) Ονοματεπώνυμο εξεταζόμενου: Καμιά άλλη σημείωση δεν επιτρέπεται στα θέματα τα οποία θα παραδώσετε μαζί με το γραπτό σας. Έτσι οι απαντήσεις όλων των θεμάτων
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ
 ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 1. Σε δοχείο σταθερού όγκου και σε σταθερή θερμοκρασία, εισάγονται κάποιες ποσότητες των αερίων Η 2(g) και Ι 2(g) τα οποία αντιδρούν σύμφωνα με
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 6-ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 1. Σε δοχείο σταθερού όγκου και σε σταθερή θερμοκρασία, εισάγονται κάποιες ποσότητες των αερίων Η 2(g) και Ι 2(g) τα οποία αντιδρούν σύμφωνα με
ΠΕΙΡΑΜΑΤΙΚΗ ΕΡΓΑΣΙΑ ΓΙΑ ΤΟ ΝΟΜΟ ΤΟΥ BOYLE
 2ο ΠΕΙΡΑΜΑΤΙΚΟ ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΑΘΗΝΩΝ ΠΕΙΡΑΜΑΤΙΚΗ ΕΡΓΑΣΙΑ ΓΙΑ ΤΟ ΝΟΜΟ ΤΟΥ BOYLE Β ΛΥΚΕΙΟΥ Β2α ΦΥΣΙΚΗΚΑΤΕΥΘΥΝΣΗΣ 17/1/2012 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΑΕΡΙΩΝ Τα δυο πρώτα κεφάλαια,στην υλη της Β λυκείου στη Φυσική
2ο ΠΕΙΡΑΜΑΤΙΚΟ ΓΕΝΙΚΟ ΛΥΚΕΙΟ ΑΘΗΝΩΝ ΠΕΙΡΑΜΑΤΙΚΗ ΕΡΓΑΣΙΑ ΓΙΑ ΤΟ ΝΟΜΟ ΤΟΥ BOYLE Β ΛΥΚΕΙΟΥ Β2α ΦΥΣΙΚΗΚΑΤΕΥΘΥΝΣΗΣ 17/1/2012 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΑΕΡΙΩΝ Τα δυο πρώτα κεφάλαια,στην υλη της Β λυκείου στη Φυσική
ΔΙΑΓΩΝΙΣΜΑ Α. και d B οι πυκνότητα του αερίου στις καταστάσεις Α και Β αντίστοιχα, τότε
 ΔΙΑΓΩΝΙΣΜΑ Α Θέµα ο Στις ερωτήσεις -4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση Σύµφωνα µε την κινητική θεωρία των ιδανικών αερίων, η πίεση
ΔΙΑΓΩΝΙΣΜΑ Α Θέµα ο Στις ερωτήσεις -4 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα που αντιστοιχεί στη σωστή απάντηση Σύµφωνα µε την κινητική θεωρία των ιδανικών αερίων, η πίεση
ΚΕΦΑΛΑΙΟ 3 Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ
 82 ΚΕΦΑΛΑΙΟ 3 Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Α. ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ 1. Η πίεση του αέρα στα λάστιχα ενός ακίνητου αυτοκινήτου με θερμοκρασία θ 1 =7 ο C είναι P 1 =3 atm. Κατά την
82 ΚΕΦΑΛΑΙΟ 3 Ο ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ Α. ΝΟΜΟΙ ΤΩΝ ΑΕΡΙΩΝ ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ 1. Η πίεση του αέρα στα λάστιχα ενός ακίνητου αυτοκινήτου με θερμοκρασία θ 1 =7 ο C είναι P 1 =3 atm. Κατά την
ΧΗΜΕΙΑ. Α Λυκείου 12/4/ Στοιχειομετρία Εισαγωγή. Κεφάλαιο 4 - Στοιχειομετρία. 4. Στοιχειομετρία
 12/4/2014 Σελ: 103 Ε1 4. Στοιχειομετρία Εισαγωγή Θεμέλιος λίθος για τους χημικούς υπολογισμούς αποτέλεσε η ατομική θεωρία του Dalton (1803) η οποία σε γενικές γραμμές περιγράφεται από το παρακάτω σχήμα:
12/4/2014 Σελ: 103 Ε1 4. Στοιχειομετρία Εισαγωγή Θεμέλιος λίθος για τους χημικούς υπολογισμούς αποτέλεσε η ατομική θεωρία του Dalton (1803) η οποία σε γενικές γραμμές περιγράφεται από το παρακάτω σχήμα:
 P = 1 3 Nm V u2 ή P = 1 3 ΦΥΣΙΚΗ (ΚΑΤΕΥΘΥΝΣΗ Β ΛΥΚΕΙΟΥ) ΤΥΠΟΛΟΓΙΟ ΘΕΡΜΟΔΥΝΑΜΙΚΗΣ Καταστατική Εξίσωση Αερίων PV = nrt Nm u V εν PV = m M r RT P = drt M r Κινητική Θεωρία 2 ή P = 1 3 du2 ή P = 1 du 3 εν
P = 1 3 Nm V u2 ή P = 1 3 ΦΥΣΙΚΗ (ΚΑΤΕΥΘΥΝΣΗ Β ΛΥΚΕΙΟΥ) ΤΥΠΟΛΟΓΙΟ ΘΕΡΜΟΔΥΝΑΜΙΚΗΣ Καταστατική Εξίσωση Αερίων PV = nrt Nm u V εν PV = m M r RT P = drt M r Κινητική Θεωρία 2 ή P = 1 3 du2 ή P = 1 du 3 εν
ΣΥΣΚΕΥΗ ΝΟΜΟΥ ΤΩΝ ΑΕΡΙΩΝ
 ΣΥΣΚΕΥΗ ΝΟΜΟΥ ΤΩΝ ΑΕΡΙΩΝ Σύριγγα για εισαγωγή αέρα Μανόμετρο για την μέτρηση του Δp Κλίμακα για την μέτρηση του όγκου Έμβολο Μοχλός για την ελευθέρωση του εμβόλου Δύο στρόφιγγες τριών εισόδων Χειροκίνητος
ΣΥΣΚΕΥΗ ΝΟΜΟΥ ΤΩΝ ΑΕΡΙΩΝ Σύριγγα για εισαγωγή αέρα Μανόμετρο για την μέτρηση του Δp Κλίμακα για την μέτρηση του όγκου Έμβολο Μοχλός για την ελευθέρωση του εμβόλου Δύο στρόφιγγες τριών εισόδων Χειροκίνητος
Ισόχωρη και Ισοβαρής Μεταβολή Μια πρόταση για Συνθετική Δημιουργική Εργασία
 Ισόχωρη και Ισοβαρής Μεταβολή Μια πρόταση για Συνθετική Δημιουργική Εργασία Α. Ο προβληματισμός για την Συνθετική Δημιουργική Εργασία Σύμφωνα με το σχολικό βιβλίο: Στην ισόχωρη μεταβολή των αερίων ο όγκος
Ισόχωρη και Ισοβαρής Μεταβολή Μια πρόταση για Συνθετική Δημιουργική Εργασία Α. Ο προβληματισμός για την Συνθετική Δημιουργική Εργασία Σύμφωνα με το σχολικό βιβλίο: Στην ισόχωρη μεταβολή των αερίων ο όγκος
Περιεχόµενα 1. Εισαγωγή Νόµος του Boyle Πειραµατική ιάταξη ιαδικασία Πειράµατος Μετρήσεις Συµπεράσµατα...8 2
 2 o Πειραµατικό Γενικό Λύκειο Αθηνών Σχολικό Έτος 2012-2013 Πειραµατική επαλήθευση του νόµου του Boyle Με βάση την 1 η ραστηριότητα του φύλλου εργασίας για τους Νόµους των Αερίων. Κωνσταντίνος Κλοκανάς
2 o Πειραµατικό Γενικό Λύκειο Αθηνών Σχολικό Έτος 2012-2013 Πειραµατική επαλήθευση του νόµου του Boyle Με βάση την 1 η ραστηριότητα του φύλλου εργασίας για τους Νόµους των Αερίων. Κωνσταντίνος Κλοκανάς
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ
 23-10-11 ΣΕΙΡΑ Α ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράµµα που αντιστοιχεί στη σωστή
23-10-11 ΣΕΙΡΑ Α ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράµµα που αντιστοιχεί στη σωστή
ΕΚΦΕ Μαγνησίας, Θεοδώρα Γουρλά, Σεπτέμβρης /5 ΣΥΣΚΕΥΗ ΝΟΜΟΥ ΤΩΝ ΑΕΡΙΩΝ
 ΕΚΦΕ Μαγνησίας, Θεοδώρα Γουρλά, Σεπτέμβρης 2012 1/5 ΣΥΣΚΕΥΗ ΝΟΜΟΥ ΤΩΝ ΑΕΡΙΩΝ ΕΚΦΕ Μαγνησίας, Θεοδώρα Γουρλά, Σεπτέμβρης 2012 2/5 Επαλήθευση του Νόμου των Ιδανικών Αερίων Α. Νόμος Boyle Ισόθερμη μεταβολή
ΕΚΦΕ Μαγνησίας, Θεοδώρα Γουρλά, Σεπτέμβρης 2012 1/5 ΣΥΣΚΕΥΗ ΝΟΜΟΥ ΤΩΝ ΑΕΡΙΩΝ ΕΚΦΕ Μαγνησίας, Θεοδώρα Γουρλά, Σεπτέμβρης 2012 2/5 Επαλήθευση του Νόμου των Ιδανικών Αερίων Α. Νόμος Boyle Ισόθερμη μεταβολή
ΣΥΜΠΕΡΙΦΟΡΑ ΤΩΝ ΑΕΡΙΩΝ
 ΣΥΜΠΕΡΙΦΟΡΑ ΤΩΝ ΑΕΡΙΩΝ Στην αέρια φυσική κατάσταση όλες οι καθαρές ουσίες ακολουθούν μια παρόμοια συμπεριφορά. Δηλαδή, εάν παρατηρηθεί ο μοριακός τους όγκος στους 0 ο C και 1 ατμ., 1 mol του κάθε αερίου
ΣΥΜΠΕΡΙΦΟΡΑ ΤΩΝ ΑΕΡΙΩΝ Στην αέρια φυσική κατάσταση όλες οι καθαρές ουσίες ακολουθούν μια παρόμοια συμπεριφορά. Δηλαδή, εάν παρατηρηθεί ο μοριακός τους όγκος στους 0 ο C και 1 ατμ., 1 mol του κάθε αερίου
Πρόχειρο Τεστ Β Τάξης Ενιαίου Λυκείου Ιδανικά Αέρια - Κινητική Θεωρία Σύνολο Σελίδων: έξι (6) - ιάρκεια Εξέτασης: 90 min Κυριακή 13 Μάρτη 2016.
 Πρόχειρο Τεστ Β Τάξης Ενιαίου Λυκείου Ιδανικά Αέρια - Κινητική Θεωρία Σύνολο Σελίδων: έξι (6) - ιάρκεια Εξέτασης: 90 min Κυριακή 13 Μάρτη 2016 Βαθµολογία % Ονοµατεπώνυµο: Θέµα Α Στις ηµιτελείς προτάσεις
Πρόχειρο Τεστ Β Τάξης Ενιαίου Λυκείου Ιδανικά Αέρια - Κινητική Θεωρία Σύνολο Σελίδων: έξι (6) - ιάρκεια Εξέτασης: 90 min Κυριακή 13 Μάρτη 2016 Βαθµολογία % Ονοµατεπώνυµο: Θέµα Α Στις ηµιτελείς προτάσεις
ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων)
 ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων) 1. Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές. i. H σχετική ατομική μάζα μετριέται σε γραμμάρια. ii. H σχετική ατομική μάζα είναι
ΧΗΜΙΚΟΙ ΥΠΟΛΟΓΙΣΜΟΙ I (Ar, Mr, mol, N A, V m, νόμοι αερίων) 1. Να εξηγήσετε ποιες από τις παρακάτω προτάσεις είναι σωστές. i. H σχετική ατομική μάζα μετριέται σε γραμμάρια. ii. H σχετική ατομική μάζα είναι
Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C.
 4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
4.1 Βασικές έννοιες Ατομική μονάδα μάζας (amu) ορίζεται ως το 1/12 της μάζας του ατόμου του άνθρακα 12 6 C. Σχετική ατομική μάζα ή ατομικό βάρος λέγεται ο αριθμός που δείχνει πόσες φορές είναι μεγαλύτερη
ΤΥΠΟΛΟΓΙΟ-ΠΑΡΑΤΗΡΗΣΕΙΣ ΣΤΗ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ
 ΤΥΠΟΛΟΓΙΟ-ΠΑΡΑΤΗΡΗΣΕΙΣ ΣΤΗ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 1 ο ΚΑΙ ο : 1. ΝΟΜΟΣ ΤΟΥ oyle:.=σταθ. για Τ =σταθ. για δύο καταστάσεις Α και Β : Α. Α = Β. Β (α)ισόθερμη εκτόνωση:αύξηση όγκου > και μείωση της πίεσης
ΤΥΠΟΛΟΓΙΟ-ΠΑΡΑΤΗΡΗΣΕΙΣ ΣΤΗ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΚΕΦΑΛΑΙΟ 1 ο ΚΑΙ ο : 1. ΝΟΜΟΣ ΤΟΥ oyle:.=σταθ. για Τ =σταθ. για δύο καταστάσεις Α και Β : Α. Α = Β. Β (α)ισόθερμη εκτόνωση:αύξηση όγκου > και μείωση της πίεσης
ΦΥΣΙΚΗ Ο.Π Β Λ. Α1. Ποιο από τα παρακάτω διαγράμματα παριστάνει γραφικά το νόμο της ισόχωρης μεταβολής; α. β. γ. δ.
 ΦΥΣΙΚΗ Ο.Π Β Λ 04-02 - 2018 Άρχων Μάρκος ΘΕΜΑ Α Οδηγία: Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις Α1-Α5 και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Ποιο
ΦΥΣΙΚΗ Ο.Π Β Λ 04-02 - 2018 Άρχων Μάρκος ΘΕΜΑ Α Οδηγία: Να γράψετε στο τετράδιό σας τον αριθμό καθεμιάς από τις παρακάτω ερωτήσεις Α1-Α5 και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση. Α1. Ποιο
ΤΥΠΟΛΟΓΙΟ ΚΙΝΗΤΙΚΗΣ ΘΕΩΡΙΑΣ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ T 1 <T 2 A
 ΤΥΠΟΛΟΓΙΟ ΚΙΝΗΤΙΚΗΣ ΘΕΩΡΙΑΣ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ 1. ΝΟΜΟΣ OYLE-MRIOTTE = σταθ. (όταν Τ = σταθ.) (1) Ο νόμος των oyle Mariotte εφαρμόζεται σε ισόθερμη μεταβολή (Τ = σταθ.) π.χ. στην μεταβολή Α T 1
ΤΥΠΟΛΟΓΙΟ ΚΙΝΗΤΙΚΗΣ ΘΕΩΡΙΑΣ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ 1. ΝΟΜΟΣ OYLE-MRIOTTE = σταθ. (όταν Τ = σταθ.) (1) Ο νόμος των oyle Mariotte εφαρμόζεται σε ισόθερμη μεταβολή (Τ = σταθ.) π.χ. στην μεταβολή Α T 1
Χηµική κινητική - Ταχύτητα αντίδρασης. 6 ο Μάθηµα: Μηχανισµός αντίδρασης - Νόµος ταχύτητας
 5 ο Μάθηµα: Χηµική κινητική - Ταχύτητα αντίδρασης 6 ο Μάθηµα: Μηχανισµός αντίδρασης - Νόµος ταχύτητας 95 5 o Χηµική κινητική Ταχύτητα αντίδρασης Α ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Χηµική κινητική: Χηµική κινητική
5 ο Μάθηµα: Χηµική κινητική - Ταχύτητα αντίδρασης 6 ο Μάθηµα: Μηχανισµός αντίδρασης - Νόµος ταχύτητας 95 5 o Χηµική κινητική Ταχύτητα αντίδρασης Α ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Χηµική κινητική: Χηµική κινητική
Χ Η Μ Ι Κ Η Ι Σ Ο Ρ Ρ Ο Π Ι Α
 Χ Η Μ Ι Κ Η Ι Σ Ο Ρ Ρ Ο Π Ι Α ( θ ε ω ρ ί α κ α ι μ ε θ ο δ ο λ ο γ ί α π ρ ο β λ η μ ά τ ω ν ) Εισαγωγή Οι χημικές αντιδράσεις, ανάλογα με το ποσοστό μετατροπής των αντιδρώντων, προς τα προϊόντα, χωρίζονται
Χ Η Μ Ι Κ Η Ι Σ Ο Ρ Ρ Ο Π Ι Α ( θ ε ω ρ ί α κ α ι μ ε θ ο δ ο λ ο γ ί α π ρ ο β λ η μ ά τ ω ν ) Εισαγωγή Οι χημικές αντιδράσεις, ανάλογα με το ποσοστό μετατροπής των αντιδρώντων, προς τα προϊόντα, χωρίζονται
ΝΟΜΟΙ ΑΕΡΙΩΝ. αντιστοιχεί στο αέριο με τη μεγαλύτερη ποσότητα ύλης. Δικαιολογήσατε την απάντηση σας.
 ΝΟΜΟΙ ΑΕΡΙΩΝ 1. Στο παρακάτω διάγραμμα να βρείτε την ισόθερμη καμπύλη του αντιστοιχεί στο αέριο με τη μεγαλύτερη ποσότητα ύλης. Δικαιολογήσατε την απάντηση σας. 2. Ο όγκος δεδομένης ποσότητας ιδανικού
ΝΟΜΟΙ ΑΕΡΙΩΝ 1. Στο παρακάτω διάγραμμα να βρείτε την ισόθερμη καμπύλη του αντιστοιχεί στο αέριο με τη μεγαλύτερη ποσότητα ύλης. Δικαιολογήσατε την απάντηση σας. 2. Ο όγκος δεδομένης ποσότητας ιδανικού
ιαγώνισµα : ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ.Β ΛΥΚΕΙΟΥ
 ιαγώνισµα : ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ.Β ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Α. Να σηµειώσετε τη σωστή απάντηση : 1. Όταν αυξάνουµε τη θερµοκρασία, η απόδοση µιας αµφίδροµης αντίδρασης : Α. αυξάνεται πάντοτε Β. αυξάνεται,
ιαγώνισµα : ΧΗΜΕΙΑ ΘΕΤΙΚΗΣ ΚΑΤΕΥΘΥΝΣΗΣ.Β ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Α. Να σηµειώσετε τη σωστή απάντηση : 1. Όταν αυξάνουµε τη θερµοκρασία, η απόδοση µιας αµφίδροµης αντίδρασης : Α. αυξάνεται πάντοτε Β. αυξάνεται,
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Τράπεζα θεμάτων. Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ
 ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Β Θέμα ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΑΕΡΙΩΝ 16111 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση
Επιμέλεια: Φροντιστήρια «ΟΜΟΚΕΝΤΡΟ ΦΛΩΡΟΠΟΥΛΟΥ»
 Τρίτη 27 Μαΐου 2014 Α ΛΥΚΕΙΟΥ ΝΕΟ ΕΞΕΤΑΣΤΙΚΟ ΣΥΣΤΗΜΑ ΧΗΜΕΙΑ Επιμέλεια: Φροντιστήρια «ΟΜΟΚΕΝΤΡΟ ΦΛΩΡΟΠΟΥΛΟΥ» ΧΗΜΕΙΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1-Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και
Τρίτη 27 Μαΐου 2014 Α ΛΥΚΕΙΟΥ ΝΕΟ ΕΞΕΤΑΣΤΙΚΟ ΣΥΣΤΗΜΑ ΧΗΜΕΙΑ Επιμέλεια: Φροντιστήρια «ΟΜΟΚΕΝΤΡΟ ΦΛΩΡΟΠΟΥΛΟΥ» ΧΗΜΕΙΑ ΘΕΜΑ Α Για τις ερωτήσεις Α1-Α3 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και
Χημεία Α Λυκείου - Κεφάλαιο 4. Χημικοί Υπολογισμοί. Άσκηση 4.14 Αέρια Μείγματα
 Σελίδα: 1 Χημεία Α Λυκείου - Κεφάλαιο 4 Όνομα & Επώνυμο : Τάξη: Α Ημερομηνία: Χημικοί Υπολογισμοί Άσκηση 4.14 Αέρια Μείγματα Αέριο μείγμα αποτελείται από 2 ουσίες. H ΟΥΣΙΑ #1 έχει Μοριακό Βάρος Mr#1, περιέχει
Σελίδα: 1 Χημεία Α Λυκείου - Κεφάλαιο 4 Όνομα & Επώνυμο : Τάξη: Α Ημερομηνία: Χημικοί Υπολογισμοί Άσκηση 4.14 Αέρια Μείγματα Αέριο μείγμα αποτελείται από 2 ουσίες. H ΟΥΣΙΑ #1 έχει Μοριακό Βάρος Mr#1, περιέχει
Εργαστηριακή άσκηση 1: ΕΠΑΛΗΘΕΥΣΗ ΤΩΝ ΝΟΜΩΝ ΤΩΝ Ι ΑΝΙΚΩΝ ΑΕΡΙΩΝ
 ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Εργαστηριακή άσκηση 1: ΕΠΑΛΗΘΕΥΣΗ ΤΩΝ ΝΟΜΩΝ ΤΩΝ Ι ΑΝΙΚΩΝ ΑΕΡΙΩΝ Τροποποίηση της διαδικασίας η οποία περιγράφεται στον εργαστηριακό οδηγό (Βαγγέλης ηµητριάδης, 4 ο ΓΕΛ Ζωγράφου)
ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Εργαστηριακή άσκηση 1: ΕΠΑΛΗΘΕΥΣΗ ΤΩΝ ΝΟΜΩΝ ΤΩΝ Ι ΑΝΙΚΩΝ ΑΕΡΙΩΝ Τροποποίηση της διαδικασίας η οποία περιγράφεται στον εργαστηριακό οδηγό (Βαγγέλης ηµητριάδης, 4 ο ΓΕΛ Ζωγράφου)
ΑΕΡΙΑ ΚΑΤ ΚΑ Α Τ ΣΤ ΑΣΗ
 ΑΕΡΙΑ ΚΑΤΑΣΤΑΣΗ H αποστολή Pthfid Pathfinder το 1997 με το μικρό όχημα της ("Sojourner") ") ήταν δραστήρια στην Αρειανή επιφάνεια για αρκετούς μήνες, επιστρέφοντας μια μεγάλη συλλογή στοιχείων για το Αρειανό
ΑΕΡΙΑ ΚΑΤΑΣΤΑΣΗ H αποστολή Pthfid Pathfinder το 1997 με το μικρό όχημα της ("Sojourner") ") ήταν δραστήρια στην Αρειανή επιφάνεια για αρκετούς μήνες, επιστρέφοντας μια μεγάλη συλλογή στοιχείων για το Αρειανό
Physics by Chris Simopoulos
 ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΑΕΡΙΩΝ Η εξίσωση που συνδέει την πίεση τον όγκο και την θερμοκρασία ενός ιδανικού αερίου που βρίσκεται σε κατάσταση ισορροπίας ονομάζεται καταστατική εξίσωση αερίου και δίνεται όπως
ΚΑΤΑΣΤΑΤΙΚΗ ΕΞΙΣΩΣΗ ΑΕΡΙΩΝ Η εξίσωση που συνδέει την πίεση τον όγκο και την θερμοκρασία ενός ιδανικού αερίου που βρίσκεται σε κατάσταση ισορροπίας ονομάζεται καταστατική εξίσωση αερίου και δίνεται όπως
Μεταβολή Q, W, ΔU Παρατηρήσεις (3) ) Q = nrt ln V 1. W = Q = nrt ln U = 0 (5). Q = nc V T (8) W = 0 (9) U = nc V T (10)
 Θερμοδυναμική 1 1 Θερμοδυναμική 11 Τυπολόγιο Θερμοδυναμικής Πίνακας 1: Οι Μεταβολές Συνοπτικά Μεταβολή Q, W, ΔU Παρατηρήσεις Ισόθερμη Μεταβολή Νόμος oyle = σταθερό (1) 1 1 = 2 2 (2) Q = nrt ln ( 2 W =
Θερμοδυναμική 1 1 Θερμοδυναμική 11 Τυπολόγιο Θερμοδυναμικής Πίνακας 1: Οι Μεταβολές Συνοπτικά Μεταβολή Q, W, ΔU Παρατηρήσεις Ισόθερμη Μεταβολή Νόμος oyle = σταθερό (1) 1 1 = 2 2 (2) Q = nrt ln ( 2 W =
Φυσική Προσανατολισμού Β Λυκείου Κεφάλαιο 2 ο. Σύντομη Θεωρία
 Φυσική Προσανατολισμού Β Λυκείου 05-06 Κεφάλαιο ο Σύντομη Θεωρία Θερμοδυναμικό σύστημα είναι το σύστημα το οποίο για να το περιγράψουμε χρησιμοποιούμε και θερμοδυναμικά μεγέθη, όπως τη θερμοκρασία, τη
Φυσική Προσανατολισμού Β Λυκείου 05-06 Κεφάλαιο ο Σύντομη Θεωρία Θερμοδυναμικό σύστημα είναι το σύστημα το οποίο για να το περιγράψουμε χρησιμοποιούμε και θερμοδυναμικά μεγέθη, όπως τη θερμοκρασία, τη
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ
 31-10-10 ΣΕΙΡΑ Α ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράµµα που αντιστοιχεί στη σωστή
31-10-10 ΣΕΙΡΑ Α ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ ΘΕΜΑ 1 ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω ερωτήσεις 1-4 και δίπλα το γράµµα που αντιστοιχεί στη σωστή
Ονοματεπώνυμο: Χημεία Γ Λυκείου Υλη: Χημική Κινητική Χημική Ισορροπία Ιοντισμός (K a K b ) Επιμέλεια διαγωνίσματος: Τσικριτζή Αθανασία Αξιολόγηση :
 Ονοματεπώνυμο: Μάθημα: Χημεία Γ Λυκείου Υλη: Χημική Κινητική Χημική Ισορροπία Ιοντισμός (K a K b ) Επιμέλεια διαγωνίσματος: Τσικριτζή Αθανασία Αξιολόγηση : Θέμα Α Να επιλέξετε τη σωστή απάντηση σε καθεμία
Ονοματεπώνυμο: Μάθημα: Χημεία Γ Λυκείου Υλη: Χημική Κινητική Χημική Ισορροπία Ιοντισμός (K a K b ) Επιμέλεια διαγωνίσματος: Τσικριτζή Αθανασία Αξιολόγηση : Θέμα Α Να επιλέξετε τη σωστή απάντηση σε καθεμία
P,V PV=nRT : (p), ) ) ) :
 Εισαγωγή: ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΑΕΡΙΩΝ ΘΕΡΜΟ ΥΝΑΜΙΚΟ ΣΥΣΤΗΜΑ 1.Τι ονοµάζουµε σύστηµα και τι περιβάλλον ενός φυσικού συστήµατος; Σύστηµα είναι ένα τµήµα του φυσικού κόσµου που διαχωρίζεται από τον υπόλοιπο
Εισαγωγή: ΚΙΝΗΤΙΚΗ ΘΕΩΡΙΑ ΤΩΝ ΑΕΡΙΩΝ ΘΕΡΜΟ ΥΝΑΜΙΚΟ ΣΥΣΤΗΜΑ 1.Τι ονοµάζουµε σύστηµα και τι περιβάλλον ενός φυσικού συστήµατος; Σύστηµα είναι ένα τµήµα του φυσικού κόσµου που διαχωρίζεται από τον υπόλοιπο
ΔΙΑΓΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ
 3-0- ΣΕΙΡΑ Α ΔΙΑΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ ΛΥΣΕΙΣ ΘΕΜΑ ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω ερωτσεις -4 και δίπλα το γράµµα που αντιστοιχεί στη σωστ
3-0- ΣΕΙΡΑ Α ΔΙΑΩΝΙΣΜΑ ΣΤΗ ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β' ΛΥΚΕΙΟΥ ΛΥΣΕΙΣ ΘΕΜΑ ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό καθεµιάς από τις παρακάτω ερωτσεις -4 και δίπλα το γράµµα που αντιστοιχεί στη σωστ
Α. Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα σε κάθε αριθμό το γράμμα που αντιστοιχεί στη σωστή απάντηση.
 1 ΘΕΜΑ Α Α. Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα σε κάθε αριθμό το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1. Για τη μεταβολή που παθαίνει ένα ιδανικό αέριο
1 ΘΕΜΑ Α Α. Στις ερωτήσεις 1-4 να γράψετε στο τετράδιό σας τον αριθμό της ερώτησης και δίπλα σε κάθε αριθμό το γράμμα που αντιστοιχεί στη σωστή απάντηση. 1. Για τη μεταβολή που παθαίνει ένα ιδανικό αέριο
ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΘΕΩΡΙΑ & ΑΣΚΗΣΕΙΣ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 693 946778 ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΘΕΩΡΙΑ & ΑΣΚΗΣΕΙΣ Περιεχόμενα. Φαινόμενα μεταφοράς Ορισμοί. Ενεργός διατομή 3. Ενεργός διατομή στο μοντέλο των σκληρών σφαιρών
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 693 946778 ΦΑΙΝΟΜΕΝΑ ΜΕΤΑΦΟΡΑΣ ΘΕΩΡΙΑ & ΑΣΚΗΣΕΙΣ Περιεχόμενα. Φαινόμενα μεταφοράς Ορισμοί. Ενεργός διατομή 3. Ενεργός διατομή στο μοντέλο των σκληρών σφαιρών
Να επιλέξετε την σωστή απάντηση σε κάθε μία από τις παρακάτω ερωτήσεις: α) την πίεση β) την θερμοκρασία
 ΘΕΜΑ 1 ο Να επιλέξετε την σωστή απάντηση σε κάθε μία από τις παρακάτω ερωτήσεις: 1) Δίνεται η θερμοχημική εξίσωση: Ν 2(g) + 3Η 2 (g) 2ΝΗ 3 (g) ΔΗ ο = - 88 kj α) Η ενθαλπία σχηματισμού της ΝΗ 3 είναι 88
ΘΕΜΑ 1 ο Να επιλέξετε την σωστή απάντηση σε κάθε μία από τις παρακάτω ερωτήσεις: 1) Δίνεται η θερμοχημική εξίσωση: Ν 2(g) + 3Η 2 (g) 2ΝΗ 3 (g) ΔΗ ο = - 88 kj α) Η ενθαλπία σχηματισμού της ΝΗ 3 είναι 88
Γραµµοµοριακός όγκος. Ο Νόµος του Avogadro
 ΤΟ MOL ΣΤΑ ΑΕΡΙΑ Γραµµοµοριακός όγκος Ο Νόµος του Avogadro Ελένη ανίλη, Χηµικός, Msc., Ph.D 2 Η ΧΡΗΣΙΜΟΤΗΤΑ ΤΟΥ MOL ΣΤΑ ΑΕΡΙΑ Όπως ήδη ξέρεις τα αέρια είναι πολύ ελαφρά. Είναι δύσκολο να τα ζυγίσουµε όµως
ΤΟ MOL ΣΤΑ ΑΕΡΙΑ Γραµµοµοριακός όγκος Ο Νόµος του Avogadro Ελένη ανίλη, Χηµικός, Msc., Ph.D 2 Η ΧΡΗΣΙΜΟΤΗΤΑ ΤΟΥ MOL ΣΤΑ ΑΕΡΙΑ Όπως ήδη ξέρεις τα αέρια είναι πολύ ελαφρά. Είναι δύσκολο να τα ζυγίσουµε όµως
Μεταβολή Q, W, ΔU Παρατηρήσεις (3) ) Q = nrt ln V 1. W = Q = nrt ln U = 0 (5). Q = nc V T (8) W = 0 (9) U = nc V T (10)
 Θερμοδυναμική 1 1 Θερμοδυναμική 11 Τυπολόγιο Θερμοδυναμικής Πίνακας 1: Οι Μεταβολές Συνοπτικά Μεταβολή Q, W, ΔU Παρατηρήσεις Ισόθερμη Μεταβολή Νόμος oyle = σταθερό (1) 1 1 = 2 2 (2) Q = nrt ln ( 2 W =
Θερμοδυναμική 1 1 Θερμοδυναμική 11 Τυπολόγιο Θερμοδυναμικής Πίνακας 1: Οι Μεταβολές Συνοπτικά Μεταβολή Q, W, ΔU Παρατηρήσεις Ισόθερμη Μεταβολή Νόμος oyle = σταθερό (1) 1 1 = 2 2 (2) Q = nrt ln ( 2 W =
2 mol ιδανικού αερίου, η οποία
 ΦΥΣΙΚΗ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ ΕΡΓΑΣΙΑ 7 ΘΕΡΜΙΚΕΣ ΜΗΧΑΝΕΣ 1. Μια μηχανή Carnot λειτουργεί μεταξύ των θερμοκρασιών Τ h =400Κ και Τ c =300Κ. Αν στη διάρκεια ενός κύκλου, η μηχανή αυτή απορροφά
ΦΥΣΙΚΗ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Β ΛΥΚΕΙΟΥ ΕΡΓΑΣΙΑ 7 ΘΕΡΜΙΚΕΣ ΜΗΧΑΝΕΣ 1. Μια μηχανή Carnot λειτουργεί μεταξύ των θερμοκρασιών Τ h =400Κ και Τ c =300Κ. Αν στη διάρκεια ενός κύκλου, η μηχανή αυτή απορροφά
Παρουσίαση Εννοιών στη Φυσική της Β Λυκείου. Κεφάλαιο Πρώτο Ενότητα: Θερμοδυναμική
 Παρουσίαση Εννοιών στη Φυσική της Β Λυκείου Κεφάλαιο Πρώτο Ενότητα: Θερμοδυναμική ΣΤΟΙΧΕΙΑ ΘΕΡΜΟ ΥΝΑΜΙΚΗΣ Εισαγωγή Η θερμοδυναμική μελετά τη συμπεριφορά ενός συστήματος με βάση τα πειραματικά δεδομένα
Παρουσίαση Εννοιών στη Φυσική της Β Λυκείου Κεφάλαιο Πρώτο Ενότητα: Θερμοδυναμική ΣΤΟΙΧΕΙΑ ΘΕΡΜΟ ΥΝΑΜΙΚΗΣ Εισαγωγή Η θερμοδυναμική μελετά τη συμπεριφορά ενός συστήματος με βάση τα πειραματικά δεδομένα
Ημερομηνία: Σάββατο 4 Νοεμβρίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ
 ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Ημερομηνία: Σάββατο 4 Νοεμβρίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να κυκλώσετε την σωστή απάντηση στις παρακάτω περιπτώσεις. Α1. Τα
ΤΑΞΗ: ΜΑΘΗΜΑ: Α ΓΕΝΙΚΟΥ ΛΥΚΕΙΟΥ ΧΗΜΕΙΑ ΓΕΝΙΚΗΣ ΠΑΙΔΕΙΑΣ Ημερομηνία: Σάββατο 4 Νοεμβρίου 2017 Διάρκεια Εξέτασης: 3 ώρες ΕΚΦΩΝΗΣΕΙΣ ΘΕΜΑ Α Να κυκλώσετε την σωστή απάντηση στις παρακάτω περιπτώσεις. Α1. Τα
ΣΧΕΔΙΟ ΜΑΘΗΜΑΤΟΣ. Ενότητα : ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ: ΙΣΟΘΕΡΜΗ ΜΕΤΑΒΟΛΗ ΝΟΜΟΣ BOYLE ΔΙΔΑΚΤΙΚΟΙ ΣΤΟΧΟΙ
 1 ΣΧΕΔΙΟ ΜΑΘΗΜΑΤΟΣ Διδάσκων καθηγητής: Αντώνιος Αλεξ. Κρητικός Τάξη : Β Μάθημα : Φυσική Κατεύθυνσης Ενότητα : ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ: ΙΣΟΘΕΡΜΗ ΜΕΤΑΒΟΛΗ ΝΟΜΟΣ BOYLE Οι μαθητές/τριες να μπορέσουν: ΔΙΔΑΚΤΙΚΟΙ
1 ΣΧΕΔΙΟ ΜΑΘΗΜΑΤΟΣ Διδάσκων καθηγητής: Αντώνιος Αλεξ. Κρητικός Τάξη : Β Μάθημα : Φυσική Κατεύθυνσης Ενότητα : ΝΟΜΟΙ ΙΔΑΝΙΚΩΝ ΑΕΡΙΩΝ: ΙΣΟΘΕΡΜΗ ΜΕΤΑΒΟΛΗ ΝΟΜΟΣ BOYLE Οι μαθητές/τριες να μπορέσουν: ΔΙΔΑΚΤΙΚΟΙ
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ ΝΟΜΟΙ ΑΕΡΙΩΝ
 ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ ΝΟΜΟΙ ΑΕΡΙΩΝ ΘΕΜΑ 2 1. Β.2 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση 1 atm και θερμοκρασία 27 C). Το μπαλόνι με κάποιο τρόπο ανεβαίνει σε
ΤΡΑΠΕΖΑ ΘΕΜΑΤΩΝ ΝΟΜΟΙ ΑΕΡΙΩΝ ΘΕΜΑ 2 1. Β.2 Ένα παιδί κρατάει στο χέρι του ένα μπαλόνι γεμάτο ήλιο που καταλαμβάνει όγκο 4 L (σε πίεση 1 atm και θερμοκρασία 27 C). Το μπαλόνι με κάποιο τρόπο ανεβαίνει σε
panagiotisathanasopoulos.gr
 Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Χημική Ισορροπία 61 Παναγιώτης Αθανασόπουλος Χημικός, Διδάκτωρ Πανεπιστημίου Πατρών Χημικός Διδάκτωρ Παν. Πατρών 62 Τι ονομάζεται κλειστό χημικό σύστημα; Παναγιώτης Αθανασόπουλος Κλειστό ονομάζεται το
Ζήτημα 1 0. Επώνυμο... Όνομα... Αγρίνιο 1/3/2015. Επιλέξτε τη σωστή απάντηση
 1 Επώνυμο... Όνομα... Αγρίνιο 1/3/2015 Ζήτημα 1 0 Επιλέξτε τη σωστή απάντηση 1) Η θερμότητα που ανταλλάσει ένα αέριο με το περιβάλλον θεωρείται θετική : α) όταν προσφέρεται από το αέριο στο περιβάλλον,
1 Επώνυμο... Όνομα... Αγρίνιο 1/3/2015 Ζήτημα 1 0 Επιλέξτε τη σωστή απάντηση 1) Η θερμότητα που ανταλλάσει ένα αέριο με το περιβάλλον θεωρείται θετική : α) όταν προσφέρεται από το αέριο στο περιβάλλον,
panagiotisathanasopoulos.gr
 Παναγιώτης Αθανασόπουλος. Κεφάλαιο 3ο Χημική Κινητική Παναγιώτης Αθανασόπουλος Χημικός, 35 Διδάκτωρ Πανεπιστημίου Πατρών Χηµικός ιδάκτωρ Παν. Πατρών 36 Γενικα για τη χημικη κινητικη και τη χημικη Παναγιώτης
Παναγιώτης Αθανασόπουλος. Κεφάλαιο 3ο Χημική Κινητική Παναγιώτης Αθανασόπουλος Χημικός, 35 Διδάκτωρ Πανεπιστημίου Πατρών Χηµικός ιδάκτωρ Παν. Πατρών 36 Γενικα για τη χημικη κινητικη και τη χημικη Παναγιώτης
P A V A = P B V B, Nόμος Boyle
 ΟΙ ΝΟΜΟΙ ΣΩΝ ΑΕΡΙΩΝ Η κατάσταση στην οποία βρίσκεται ένα αέριο περιγράφεται μακροσκοπικά από την πίεση, τον όγκο και τη θερμοκρασία του. Η μέτρηση αυτών των μεγεθών και η πιθανή συσχέτιση μεταξύ οδήγησε
ΟΙ ΝΟΜΟΙ ΣΩΝ ΑΕΡΙΩΝ Η κατάσταση στην οποία βρίσκεται ένα αέριο περιγράφεται μακροσκοπικά από την πίεση, τον όγκο και τη θερμοκρασία του. Η μέτρηση αυτών των μεγεθών και η πιθανή συσχέτιση μεταξύ οδήγησε
Χημεία Α ΓΕΛ 15 / 04 / 2018
 Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
Α ΓΕΛ 15 / 04 / 2018 Χημεία ΘΕΜΑ Α Για τις ερωτήσεις Α1 έως Α4 να γράψετε στο τετράδιο σας τον αριθμό της ερώτησης και δίπλα το γράμμα που αντιστοιχεί στη σωστή απάντηση: A1. Το χημικό στοιχείο Χ ανήκει
ΑΝΤΙΣΤΡΕΠΤΕΣ ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΜΕΤΑΒΟΛΕΣ ΘΕΩΡΙΑ
 ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΑΝΤΙΣΤΡΕΠΤΕΣ ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΜΕΤΑΒΟΛΕΣ ΘΕΩΡΙΑ Περιεχόμενα 1. Μελέτη Ισόχωρης μεταβολής 2. Μελέτη Ισοβαρής μεταβολής 3. Μελέτη Ισόθερμης μεταβολής 4.
ΦΡΟΝΤΙΣΤΗΡΙΑΚΑ ΜΑΘΗΜΑΤΑ ΦΥΣΙΚΗΣ Π.Φ. ΜΟΙΡΑ 6932 946778 ΑΝΤΙΣΤΡΕΠΤΕΣ ΘΕΡΜΟΔΥΝΑΜΙΚΕΣ ΜΕΤΑΒΟΛΕΣ ΘΕΩΡΙΑ Περιεχόμενα 1. Μελέτη Ισόχωρης μεταβολής 2. Μελέτη Ισοβαρής μεταβολής 3. Μελέτη Ισόθερμης μεταβολής 4.
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ. α. Χρησιμοποιώντας τον πρώτο θερμοδυναμικό νόμο έχουμε : J J J
 ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ 1 ος θερμοδυναμικός νόμος 1. α. Αέριο απορροφά θερμότητα 2500 και παράγει έργο 1500. Να υπολογισθεί η μεταβολή της εσωτερικής του ενέργειας. β. Αέριο συμπιέζεται ισόθερμα και αποβάλλει
ΛΥΜΕΝΕΣ ΑΣΚΗΣΕΙΣ 1 ος θερμοδυναμικός νόμος 1. α. Αέριο απορροφά θερμότητα 2500 και παράγει έργο 1500. Να υπολογισθεί η μεταβολή της εσωτερικής του ενέργειας. β. Αέριο συμπιέζεται ισόθερμα και αποβάλλει
Συνοπτική Θεωρία Χημείας Α Λυκείου. Στοιχειομετρία. Σχετική ατομική μάζα σχετική μοριακή μάζα- mole- γραμμομοριακός όγκος
 1 Web page www.a8eno.gr e-ail vrentzou@a8eno.gr Η αποτελεσματική μάθηση δεν θέλει κόπο αλλά τρόπο, δηλαδή a8eno.gr Συνοπτική Θεωρία Χημείας Α Λυκείου Στοιχειομετρία Σχετική ατομική μάζα σχετική μοριακή
1 Web page www.a8eno.gr e-ail vrentzou@a8eno.gr Η αποτελεσματική μάθηση δεν θέλει κόπο αλλά τρόπο, δηλαδή a8eno.gr Συνοπτική Θεωρία Χημείας Α Λυκείου Στοιχειομετρία Σχετική ατομική μάζα σχετική μοριακή
ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ
 29. 2 o Ιδιότητες υγρών Αέρια - Νόµος µερικών πιέσεων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Ιδιότητες υγρών α. Ιξώδες: Ιξώδες ενός υγρού είναι η αντίσταση του υγρού στη ροή. Το ιξώδες εξαρτάται: 1. από τη θερµοκρασία:
29. 2 o Ιδιότητες υγρών Αέρια - Νόµος µερικών πιέσεων Α. ΑΠΑΡΑΙΤΗΤΕΣ ΓΝΩΣΕΙΣ ΘΕΩΡΙΑΣ Ιδιότητες υγρών α. Ιξώδες: Ιξώδες ενός υγρού είναι η αντίσταση του υγρού στη ροή. Το ιξώδες εξαρτάται: 1. από τη θερµοκρασία:
Η πυκνότητα του νερού σε θερμοκρασία 4 C και ατμοσφαιρική πίεση (1 atm) είναι ίση με 1g/mL.
 Πυκνότητα Πυκνότητα ορίζεται το φυσικό μέγεθος που δίνεται από το πηλίκο της μάζας του σώματος προς τον αντίστοιχο όγκο που καταλαμβάνει σε σταθερές συνθήκες πίεσης (όταν πρόκειται για αέριο). Ο Συμβολισμός,
Πυκνότητα Πυκνότητα ορίζεται το φυσικό μέγεθος που δίνεται από το πηλίκο της μάζας του σώματος προς τον αντίστοιχο όγκο που καταλαμβάνει σε σταθερές συνθήκες πίεσης (όταν πρόκειται για αέριο). Ο Συμβολισμός,
ΦΡΟΝΤΙΣΤΗΡΙΑ Μ.Ε ΠΡΟΟΔΟΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ' ΛΥΚΕΙΟΥ ΗΜ/ΝΙΑ: 08-11-2015 ΔΙΑΡΚΕΙΑ: 3 ώρες
 ΦΡΟΝΤΙΣΤΗΡΙΑ Μ.Ε ΠΡΟΟΔΟΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ' ΛΥΚΕΙΟΥ ΗΜ/ΝΙΑ: 08--05 ΔΙΑΡΚΕΙΑ: 3 ώρες ΘΕΜΑ Α Για τις ερωτήσεις Α. Α.5 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα
ΦΡΟΝΤΙΣΤΗΡΙΑ Μ.Ε ΠΡΟΟΔΟΣ ΔΙΑΓΩΝΙΣΜΑ ΧΗΜΕΙΑΣ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ Γ' ΛΥΚΕΙΟΥ ΗΜ/ΝΙΑ: 08--05 ΔΙΑΡΚΕΙΑ: 3 ώρες ΘΕΜΑ Α Για τις ερωτήσεις Α. Α.5 να γράψετε στο τετράδιό σας τον αριθµό της ερώτησης και δίπλα το γράµµα
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 4-ΘΕΡΜΟΧΗΜΕΙΑ
 ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 4-ΘΕΡΜΟΧΗΜΕΙΑ 1. Κατά την τέλεια καύση 1g ακετυλενίου (C 2 H 2 ) εκλύεται θερμότητα 50KJ. Να γράψετε την θερμοχημική εξίσωση για την καύση του ακετυλενίου. 2. Σε
ΧΗΜΕΙΑ ΘΕΤΙΚΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΥ ΕΡΓΑΣΙΑ 4-ΘΕΡΜΟΧΗΜΕΙΑ 1. Κατά την τέλεια καύση 1g ακετυλενίου (C 2 H 2 ) εκλύεται θερμότητα 50KJ. Να γράψετε την θερμοχημική εξίσωση για την καύση του ακετυλενίου. 2. Σε
ΚΕΦΑΛΑΙΟ 4 Ο ΘΕΡΜΟΔΥΝΑΜΙΚΗ
 103 Α. ΠΡΩΤΟΣ ΘΕΡΜΟΔΥΝΑΜΙΚΟΣ ΝΟΜΟΣ ΚΕΦΑΛΑΙΟ 4 Ο ΘΕΡΜΟΔΥΝΑΜΙΚΗ 1. Ιδανικό αέριο εκτελεί διαδοχικά τις αντιστρεπτές μεταβολές ΑΒ, ΒΓ, ΓΑ που παριστάνονται στο ακόλουθο διάγραμμα P-V. α. Αν δίνονται Q ΑΒΓ
103 Α. ΠΡΩΤΟΣ ΘΕΡΜΟΔΥΝΑΜΙΚΟΣ ΝΟΜΟΣ ΚΕΦΑΛΑΙΟ 4 Ο ΘΕΡΜΟΔΥΝΑΜΙΚΗ 1. Ιδανικό αέριο εκτελεί διαδοχικά τις αντιστρεπτές μεταβολές ΑΒ, ΒΓ, ΓΑ που παριστάνονται στο ακόλουθο διάγραμμα P-V. α. Αν δίνονται Q ΑΒΓ
ΚΕΦΑΛΑΙΟ 4ο ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ. 3. Σε κλειστό δοχείο εισάγεται μείγμα των αερίων σωμάτων Α και Β, τα οποία αντιδρούν στους θ 0 C
 ΚΕΦΑΛΑΙΟ 4ο ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 4.1. Ερωτήσεις πολλαπλής επιλογής 1. Μία χημική αντίδραση είναι μονόδρομη όταν: α. πραγματοποιείται μόνο σε ορισμένες συνθήκες β. πραγματοποιείται μόνο στο εργαστήριο γ. μετά
ΚΕΦΑΛΑΙΟ 4ο ΧΗΜΙΚΗ ΙΣΟΡΡΟΠΙΑ 4.1. Ερωτήσεις πολλαπλής επιλογής 1. Μία χημική αντίδραση είναι μονόδρομη όταν: α. πραγματοποιείται μόνο σε ορισμένες συνθήκες β. πραγματοποιείται μόνο στο εργαστήριο γ. μετά
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ. Τράπεζα θεμάτων. Δ Θέμα ΘΕΡΜΟΔΥΝΑΜΙΚΗ
 ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Δ Θέμα ΘΕΡΜΟΔΥΝΑΜΙΚΗ 15949 Ποσότητα ιδανικού αέριου ίση με /R mol, βρίσκεται αρχικά σε κατάσταση ισορροπίας στην οποία έχει
ΜΑΝΩΛΗ ΡΙΤΣΑ ΦΥΣΙΚΗ Β ΛΥΚΕΙΟΥ ΠΡΟΣΑΝΑΤΟΛΙΣΜΟΣ ΘΕΤΙΚΩΝ ΣΠΟΥΔΩΝ Τράπεζα θεμάτων Δ Θέμα ΘΕΡΜΟΔΥΝΑΜΙΚΗ 15949 Ποσότητα ιδανικού αέριου ίση με /R mol, βρίσκεται αρχικά σε κατάσταση ισορροπίας στην οποία έχει
ΑΝΤΙΚΕΙΜΕΝΟ ΘΕΜΑ 1 Ο
 ΑΝΤΙΚΕΙΜΕΝΟ 1 ο κεφάλαιο: «Κινητική Θεωρία των Αερίων» ο κεφάλαιο: «O 1 ος θερµοδυναµικός νόµος» ΘΕΜΑ 1 Ο 1Α Ερωτήσεις πολλαπλής επιλογής. Σηµειώστε τη σωστή από τις προτάσεις που ακολουθούν. 1) Κατά την
ΑΝΤΙΚΕΙΜΕΝΟ 1 ο κεφάλαιο: «Κινητική Θεωρία των Αερίων» ο κεφάλαιο: «O 1 ος θερµοδυναµικός νόµος» ΘΕΜΑ 1 Ο 1Α Ερωτήσεις πολλαπλής επιλογής. Σηµειώστε τη σωστή από τις προτάσεις που ακολουθούν. 1) Κατά την
Θερμοδυναμική. Ερωτήσεις πολλαπλής επιλογής
 Ερωτήσεις πολλαπλής επιλογής Θερμοδυναμική 1. Η εσωτερική ενέργεια ορισμένης ποσότητας ιδανικού αερίου α) Είναι αντιστρόφως ανάλογη της απόλυτης θερμοκρασίας του αερίου. β) Είναι ανάλογη της απόλυτης θερμοκρασίας
Ερωτήσεις πολλαπλής επιλογής Θερμοδυναμική 1. Η εσωτερική ενέργεια ορισμένης ποσότητας ιδανικού αερίου α) Είναι αντιστρόφως ανάλογη της απόλυτης θερμοκρασίας του αερίου. β) Είναι ανάλογη της απόλυτης θερμοκρασίας
AquaTec Φυσική των Καταδύσεων
 Σημειώσεις για τα σχολεία Τεχνικής Κατάδυσης 1.1 AquaTec Φυσική των Καταδύσεων Βασικές έννοιες και Αρχές Νίκος Καρατζάς www.aquatec.gr Προειδοποίηση: Το υλικό που παρουσιάζεται παρακάτω δεν πρέπει να θεωρηθεί
Σημειώσεις για τα σχολεία Τεχνικής Κατάδυσης 1.1 AquaTec Φυσική των Καταδύσεων Βασικές έννοιες και Αρχές Νίκος Καρατζάς www.aquatec.gr Προειδοποίηση: Το υλικό που παρουσιάζεται παρακάτω δεν πρέπει να θεωρηθεί
Φ Ρ Ο Ν Τ Ι Σ Τ Η Ρ Ι Α ΘΕΩΡΗΤΙΚΗ ΘΕΤΙΚΗ ΤΕΧΝΟΛΟΓΙΚΗ ΚΑΤΕΥΘΥΝΣΗ ΕΠΑ.Λ
 Προτεινόµενα Θέµατα Β Λυκείου Οκτώβριος 01 Φυσική ΘΕΜΑ Α Στις ερωτήσεις από 1-4 να επιλέξετε την σωστή απάντηση. κατεύθυνσης 1. Η καταστατική εξίσωση των ιδανικών αερίων εφαρμόζεται και στα πραγματικά
Προτεινόµενα Θέµατα Β Λυκείου Οκτώβριος 01 Φυσική ΘΕΜΑ Α Στις ερωτήσεις από 1-4 να επιλέξετε την σωστή απάντηση. κατεύθυνσης 1. Η καταστατική εξίσωση των ιδανικών αερίων εφαρμόζεται και στα πραγματικά
ΛΥΣΕΙΣ. µεταφορική κινητική ενέργεια του K η θερµοκρασία του αερίου πρέπει να: β) τετραπλασιαστεί δ) υποτετραπλασιαστεί (Μονάδες 5) δ) 0 J
 ΔΙΑΓΩΝΙΣΜΑ ΕΚΠ. ΕΤΟΥΣ 0-0 ΜΑΘΗΜΑ / ΤΑΞΗ : ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ/Β ΛΥΚΕΙΟΥ ΣΕΙΡΑ: Α ΗΜΕΡΟΜΗΝΙΑ: 30// ΛΥΣΕΙΣ ΘΕΜΑ ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό κάθε µίας από τις παρακάτω ερωτήσεις Α.- Α.4
ΔΙΑΓΩΝΙΣΜΑ ΕΚΠ. ΕΤΟΥΣ 0-0 ΜΑΘΗΜΑ / ΤΑΞΗ : ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ/Β ΛΥΚΕΙΟΥ ΣΕΙΡΑ: Α ΗΜΕΡΟΜΗΝΙΑ: 30// ΛΥΣΕΙΣ ΘΕΜΑ ο Οδηγία: Να γράψετε στο τετράδιό σας τον αριθµό κάθε µίας από τις παρακάτω ερωτήσεις Α.- Α.4
Επαναληπτικές ασκήσεις. Επαναληπτικές ασκήσεις Β Λυκείου Θετικής Κατεύθυνσης.
 Επαναληπτικές ασκήσεις Θετικής Κατεύθυνσης. Θεόδωρος Ζήκας 1. Μια ποσότητα χαλκού αντιδρά πλήρως µε πυκνό διάλυµα H SO 4 και το αέριο που εκλύεται, χωρίζεται σε δύο ίσα µέρη. Το πρώτο µέρος αποχρωµατίζει
Επαναληπτικές ασκήσεις Θετικής Κατεύθυνσης. Θεόδωρος Ζήκας 1. Μια ποσότητα χαλκού αντιδρά πλήρως µε πυκνό διάλυµα H SO 4 και το αέριο που εκλύεται, χωρίζεται σε δύο ίσα µέρη. Το πρώτο µέρος αποχρωµατίζει
ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β ΛΥΚΕΙΟΥ
 Φυσική Κατεύθυνσης Β Λυκείου ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β ΛΥΚΕΙΟΥ κ ΙΑΓΩΝΙΣΜΑ Β Θέµα ο Να επιλέξετε τη σωστή απάντηση σε κάθε µία από τις παρακάτω ερωτήσεις: Σε ισόχωρη αντιστρεπτή θέρµανση ιδανικού αερίου, η
Φυσική Κατεύθυνσης Β Λυκείου ΦΥΣΙΚΗ ΚΑΤΕΥΘΥΝΣΗΣ Β ΛΥΚΕΙΟΥ κ ΙΑΓΩΝΙΣΜΑ Β Θέµα ο Να επιλέξετε τη σωστή απάντηση σε κάθε µία από τις παρακάτω ερωτήσεις: Σε ισόχωρη αντιστρεπτή θέρµανση ιδανικού αερίου, η
Χημεία: Μεταθετικές αντιδράσεις - Σχετική ατομική μάζα - Σχετική μοριακή μάζα - mole
 Χημικές αντιδράσεις - Σχετική ατομική μάζα - Σχετική μοριακή μάζα - mole 46 Να γραφούν οι αντιδράσεις διπλής αντικατάστασης με τις οποίες μπορούν να παρασκευαστούν: α ΗΒr β Pb(OH) γ KNO α Το HBr είναι
Χημικές αντιδράσεις - Σχετική ατομική μάζα - Σχετική μοριακή μάζα - mole 46 Να γραφούν οι αντιδράσεις διπλής αντικατάστασης με τις οποίες μπορούν να παρασκευαστούν: α ΗΒr β Pb(OH) γ KNO α Το HBr είναι
