Η ΣΥΜΒΟΛΗ ΤΗΣ ΠΟΛΥΠΑΡΑΜΕΤΡΙΚΗΣ ΜΑΓΝΗΤΙΚΗΣ ΜΑΣΤΟΓΡΑΦΙΑΣ ΣΤΗ ΔΙΑΓΝΩΣΗ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΥΣΧΕΤΙΣΜΟΣ ΜΕ ΙΣΤΟΠΑΘΟΛΟΓΙΚΑ ΕΥΡΗΜΑΤΑ
|
|
|
- Μακάριος Θεοδωρίδης
- 6 χρόνια πριν
- Προβολές:
Transcript
1 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΟΜΕΑΣ ΑΚΤΙΝΟΛΟΓΙΑΣ-ΙΑΤΡΙΚΗΣ ΦΥΣΙΚΗΣ-ΠΛΗΡΟΦΟΡΙΚΗΣ ΔΙΕΥΘΥΝΤΡΙΑ : ΚΑΘΗΓΗΤΡΙΑ ΑΦΡΟΔΙΤΗ ΧΑΡΙΤΑΝΤΗ ΠΑΝΕΠ. ΕΤΟΣ ΑΡΙΘΜΟΣ: 3351 Η ΣΥΜΒΟΛΗ ΤΗΣ ΠΟΛΥΠΑΡΑΜΕΤΡΙΚΗΣ ΜΑΓΝΗΤΙΚΗΣ ΜΑΣΤΟΓΡΑΦΙΑΣ ΣΤΗ ΔΙΑΓΝΩΣΗ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΥΣΧΕΤΙΣΜΟΣ ΜΕ ΙΣΤΟΠΑΘΟΛΟΓΙΚΑ ΕΥΡΗΜΑΤΑ ΓΛΥΚΕΡΙΑ Σ. ΜΠΟΥΛΟΓΙΑΝΝΗ ΙΑΤΡΟΣ ΑΚΤΙΝΟΛΟΓΟΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΥΠΟΒΛΗΘΗΚΕ ΣΤΟ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΗΣ ΣΧΟΛΗΣ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΟΥ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΘΕΣΣΑΛΟΝΙΚΗ 2017
2 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΟΜΕΑΣ ΑΚΤΙΝΟΛΟΓΙΑΣ-ΙΑΤΡΙΚΗΣ ΦΥΣΙΚΗΣ-ΠΛΗΡΟΦΟΡΙΚΗΣ ΔΙΕΥΘΥΝΤΡΙΑ : ΚΑΘΗΓΗΤΡΙΑ ΑΦΡΟΔΙΤΗ ΧΑΡΙΤΑΝΤΗ ΠΑΝΕΠ. ΕΤΟΣ ΑΡΙΘΜΟΣ: 3351 Η ΣΥΜΒΟΛΗ ΤΗΣ ΠΟΛΥΠΑΡΑΜΕΤΡΙΚΗΣ ΜΑΓΝΗΤΙΚΗΣ ΜΑΣΤΟΓΡΑΦΙΑΣ ΣΤΗ ΔΙΑΓΝΩΣΗ ΚΑΙ ΔΙΑΧΕΙΡΙΣΗ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΥΣΧΕΤΙΣΜΟΣ ΜΕ ΙΣΤΟΠΑΘΟΛΟΓΙΚΑ ΕΥΡΗΜΑΤΑ ΓΛΥΚΕΡΙΑ Σ. ΜΠΟΥΛΟΓΙΑΝΝΗ ΙΑΤΡΟΣ ΑΚΤΙΝΟΛΟΓΟΣ ΔΙΔΑΚΤΟΡΙΚΗ ΔΙΑΤΡΙΒΗ ΥΠΟΒΛΗΘΗΚΕ ΣΤΟ ΤΜΗΜΑ ΙΑΤΡΙΚΗΣ ΤΗΣ ΣΧΟΛΗΣ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΤΟΥ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΘΕΣΣΑΛΟΝΙΚΗ 2017 i
3 ΤΡΙΜΕΛΗΣ ΣΥΜΒΟΥΛΕΥΤΙΚΗ ΕΠΙΤΡΟΠΗ ΙΩΑΝΝΗΣ ΧΡΥΣΟΓΟΝΙΔΗΣ, ΕΠΙΚ. ΚΑΘΗΓΗΤΗΣ ΑΚΤΙΝΟΛΟΓΙΑΣ ΑΝΤΩΝΙΟΣ ΔΡΕΒΕΛΕΓΚΑΣ, ΚΑΘΗΓΗΤΗΣ ΑΚΤΙΝΟΛΟΓΙΑΣ ΧΑΡΙΤΑΝΤΗ ΑΦΡΟΔΙΤΗ, ΚΑΘΗΓΗΤΡΙΑ ΑΚΤΙΝΟΛΟΓΙΑΣ ΕΠΤΑΜΕΛΗΣ ΕΞΕΤΑΣΤΙΚΗ ΕΠΙΤΡΟΠΗ ΙΩΑΝΝΗΣ ΧΡΥΣΟΓΟΝΙΔΗΣ, ΕΠΙΚ. ΚΑΘΗΓΗΤΗΣ ΑΚΤΙΝΟΛΟΓΙΑΣ ΑΝΤΩΝΙΟΣ ΔΡΕΒΕΛΕΓΚΑΣ, ΚΑΘΗΓΗΤΗΣ ΑΚΤΙΝΟΛΟΓΙΑΣ ΧΑΡΙΤΑΝΤΗ ΑΦΡΟΔΙΤΗ, ΚΑΘΗΓΗΤΡΙΑ ΑΚΤΙΝΟΛΟΓΙΑΣ ΖΑΡΑΜΠΟΥΚΑΣ ΘΩΜΑΣ, ΚΑΘΗΓΗΤΗΣ ΠΑΘΟΛΟΑΝΑΤΟΜΙΑΣ ΑΣΗΜΑΚΟΠΟΥΛΟΣ ΕΥΣΤΡΑΤΙΟΣ, ΚΑΘΗΓΗΤΗΣ ΓΥΝΑΙΚΟΛΟΓΙΑΣ ΤΙΜΟΘΕΑΔΟΥ ΕΛΕΝΗ, ΕΠΙΚ. ΚΑΘΗΓΗΤΡΙΑ ΟΓΚΟΛΟΓΙΑΣ ΠΑΠΑΔΟΠΟΥΛΟΣ ΒΑΣΙΛΕΙΟΣ, ΚΑΘΗΓΗΤΗΣ ΧΕΙΡΟΥΡΓΙΚΗΣ «H ΕΓΚΡΙΣΗ ΤΗΣ ΔΙΔΑΚΤΟΡΙΚΗΣ ΔΙΑΤΡΙΒΗΣ ΑΠΟ ΤΗΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΤΟΥ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΔΕΝ ΥΠΟΔΗΛΩΝΕΙ ΤΗΝ ΑΠΟΔΟΧΗ ΤΩΝ ΓΝΩΜΩΝ ΤΟΥ ΣΥΓΓΡΑΦΕΑ». (ΝΟΜΟΣ 5343/32, ΑΡΘΡ ΚΑΙ Ν. 1268/82, ΑΡΘΡ. 50 8) ii
4 ΑΡΙΣΤΟΤΕΛΕΙΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ ΣΧΟΛΗ ΕΠΙΣΤΗΜΩΝ ΥΓΕΙΑΣ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΠΡΟΕΔΡΟΣ ΤΟΥ ΤΜΗΜΑΤΟΣ ΚΑΘΗΓΗΤΗΣ ΑΛΕΞΑΝΔΡΟΣ-ΑΝΑΣΤΑΣΙΟΣ ΓΑΡΥΦΑΛΛΟΣ iii
5 Στα παιδιά μου Γρηγόρη και Παρασκευή που με την αγάπη τους με εμπνέουν συνεχώς Στον αδερφό μου Κώστα για την διαρκή στήριξη του Στους γονείς μου για τη συμπαράστασή τους iv
6 Πίνακας Περιεχομένων ΠΙΝΑΚΕΣ... VIII ΓΡΑΦΗΜΑΤΑ... IX ΣΧΗΜΑΤΑ... X ΕΙΚΟΝΕΣ... XI ΣΥΝΤΟΜΟΓΡΑΦΙΕΣ... XIV ΕΥΧΑΡΙΣΤΙΕΣ... XVI ΠΡΟΛΟΓΟΣ... 1 ΓΕΝΙΚΟ ΜΕΡΟΣ ΙΣΤΟΡΙΚΗ ΑΝΑΔΡΟΜΗ ΕΠΙΔΗΜΙΟΛΟΓΙΑ - ΕΠΙΠΤΩΣΗ ΑΙΤΙΟΠΑΘΟΓΕΝΕΙΑ ΠΡΟΓΝΩΣΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ ΙΣΤΟΛΟΓΙΑ ΚΑΙ ΤΑΞΙΝΟΜΗΣΗ ΤΩΝ ΚΑΡΚΙΝΩΝ ΤΟΥ ΜΑΣΤΟΥ ΚΑΡΚΙΝΩΜΑ IN SITU Καρκίνωμα In Situ Πόρων (DCIS, Ενδοπορικό Καρκίνωμα) Καρκίνωμα In Situ Λοβίων (LCIS) ΔΙΗΘΗΤΙΚΟ ΚΑΡΚΙΝΩΜΑ Διηθητικό Καρκίνωμα Πόρων (IDC) Διηθητικό Καρκίνωμα Λοβίων (ILC) Σωληνώδες Καρκίνωμα Μυελοειδές Καρκίνωμα Βλεννώδες (Κολλοειδές) Καρκίνωμα Θηλώδες Καρκίνωμα Μεταπλαστικό Καρκίνωμα Αποκρινές Καρκίνωμα Αδενοκυστικό Καρκίνωμα Νόσος Paget Φλεγμονώδες Καρκίνωμα Τριπλά αρνητικοί καρκίνοι μαστού ΑΠΕΙΚΟΝΙΣΗ ΤΟΥ ΜΑΣΤΟΥ ΜΑΓΝΗΤΙΚΗ ΜΑΣΤΟΓΡΑΦΙΑ (MRΜ) v
7 6.1 ΒΑΣΙΚΕΣ ΑΡΧΕΣ ΜΕΘΟΔΟΥ Καταστολή λίπους Επεξεργασία εικόνων Δυναμική έγχυση παραμαγνητικής ουσίας Εικόνες Διάχυσης (DWI) Μαγνητική φασματοσκοπία MΑΓΝΗΤΗΣ 3Τ ΕΙΔΙΚΟ ΜΕΡΟΣ ΣΚΟΠΟΣ ΤΗΣ ΜΕΛΕΤΗΣ ΥΛΙΚΟ ΜΕΘΟΔΟΣ ΤΥΠΟΣ ΜΕΛΕΤΗΣ ΚΡΙΤΗΡΙΑ ΕΠΙΛΟΓΗΣ ΤΩΝ ΑΣΘΕΝΩΝ Κριτήρια αποκλεισμού ΥΛΙΚΟ ΔΙΑΔΙΚΑΣΙΑ ΕΞΕΤΑΣΗΣ ΠΡΩΤΟΚΟΛΛΟ ΕΞΕΤΑΣΗΣ ΣΤΑΤΙΣΤΙΚΗ ΑΝΑΛΥΣΗ Συσχετίσεις ΑΠΟΤΕΛΕΣΜΑΤΑ ΔΙΗΘΗΤΙΚΟΣ ΛΟΒΙΑΚΟΣ ΚΑΡΚΙΝΟΣ (ILC) ΕΙΚΟΝΕΣ ILC IN SITU ΚΑΡΚΙΝΟΣ ΤΩΝ (DCIS) ΕΙΚΟΝΕΣ DCIS ΔΙΗΘΗΤΙΚΟΣ ΚΑΡΚΙΝΟΣ ΤΩΝ (IDC) ΜΗ ΠΑΡΑΜΕΤΡΙΚΑ ΣΤΑΤΙΣΤΙΚΑ ΤΕΣΤ Kruskal-Wallis ΜΗ ΠΑΡΑΜΕΤΡΙΚΑ ΣΤΑΤΙΣΤΙΚΑ ΤΕΣΤ Spearman s rho ΕΙΚΟΝΕΣ IDC ΕΚΤΙΜΗΣΗ ΤΩΝ ΚΑΡΚΙΝΩΝ ΤΟΥ ΜΑΣΤΟΥ ΠΟΥ ΥΠΟΒΛΗΘΗΚΑΝ ΣΕ ΠΡΟΕΓΧΕΙΡΗΤΙΚΗ ΧΗΜΕΙΟΘΕΡΑΠΕΙΑ (NAC) ΕΙΚΟΝΕΣ NAC ΣΥΖΗΤΗΣΗ ΑΝΑΛΥΣΗ ΑΠΟΤΕΛΕΣΜΑΤΩΝ ΔΙΗΘΗΤΙΚΟΣ ΛΟΒΙΑΚΟΣ ΚΑΡΚΙΝΟΣ (ILC) ΚΑΙ ΔΙΗΘΗΤΙΚΟΣ ΚΑΡΚΙΝΟΣ (IDC) Συχνότητα, Εμφάνιση, Ιστολογικός τύπος στα διηθητικά καρκινώματα Ηλικία και διηθητικά καρκινώματα Μέγεθος και διηθητικά καρκινώματα Πολυεστιακότητα, πολυκεντρικότητα και διηθητικά καρκινώματα vi
8 4.1.5 Μασχαλιαίοι Λεμφαδένες και διηθητικά καρκινώματα Ιστολογικός υποτύπος, Βαθμός κακοήθειας και διηθητικά καρκινώματα Εμπλουτισμός και διηθητικά καρκινώματα Ακολουθίες Διάχυσης (DWI) και διηθητικά καρκινώματα Φασματοσκοπία και διηθητικά καρκινώματα IN SITU ΚΑΡΚΙΝΩΜΑ (DCIS) Συχνότητα, εμφάνιση και ιστολογικός τύπος στο DCIS Ιστολογικός τύπος, Βαθμός κακοήθειας και DCIS Ηλικία και DCIS Μέγεθος, όρια βλάβης, πολυεστιακότητα και DCIS Εμπλουτισμός στο DCIS Ακολουθίες Διάχυσης (DWI) στο DCIS Φασματοσκοπία στο DCIS ΕΚΤΙΜΗΣΗ ΤΗΣ ΑΝΤΑΠΟΚΡΙΣΗΣ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΣΤΗΝ ΠΡΟΕΓΧΕΙΡΗΤΙΚΗ ΧΗΜΕΙΟΘΕΡΑΠΕΙΑ (NAC) Γενικά Ηλικία Μέγεθος όγκου Όρια βλαβών Πολυεστιακότητα, Βαθμός κακοήθειας Μασχαλιαίοι λεμφαδένες Καμπύλες εμπλουτισμού Συντελεστής Προφανούς Διάχυσης (ADC) Φασματοσκοπία ΠΕΡΙΛΗΨΗ SUMMARY ΒΙΒΛΙΟΓΡΑΦΙΑ ΠΑΡΑΡΤΗΜΑ ΠΙΝΑΚΩΝ ΠΙΝΑΚΑΣ IDC ΠΙΝΑΚΑΣ ILC ΠΙΝΑΚΑΣ NAC ΠΙΝΑΚΑΣ DCIS vii
9 Πίνακες Πίνακας 2.1 Πρωτόκολλο εξέτασης Πίνακας 3.1 Ηλικιακή κατανομή ILC Πίνακας 3.2 Τύπος καμπύλης εμπλουτισμού ILC Πίνακας 3.3 ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec στο ILC Πίνακας 3.4 Spectroscopy - Φασματοσκοπία (Χολίνη ppm) στο ILC Πίνακας 3.5 Πολυεστιακότητα ILC Πίνακας 3.6 Παρουσία μασχαλιαίων λεμφαδένων στο ILC Πίνακας 3.7 Συνυπάρχουσες βλάβες εκτός της κύριας κύριας ILC βλάβης Πίνακας 3.8 Αναλυτικός κατάλογος ιστολογικών τύπων συνυπαρχουσών βλαβών πλην της κύριας ILC βλάβης Πίνακας 3.9 Γενικά στατιστικά στο DCIS Πίνακας 3.10 Ηλικιακή κατανομή στο DCIS Πίνακας 3.11 Όρια βλαβών στο DCIS Πίνακας 3.12 Μέγεθος (διάμετρος σε cm) στο DCIS Πίνακας 3.13 Πρώιμος Εμπλουτισμός - wash in στο DCIS Πίνακας 3.14 Συχνότητα τύπου καμπύλης στο DCIS Πίνακας 3.15 ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec στο DCIS Πίνακας 3.16 Spectroscopy - Φασματοσκοπία (Χολίνη ppm) στο DCIS Πίνακας 3.17 Ιστολογικός Τύπος στο DCIS Πίνακας 3.18 Πολυεστιακότητα στο DCIS Πίνακας 3.19 Γενικά Στατιστικά στο IDC Πίνακας 3.20 Ηλικιακή κατανομή στο IDC Πίνακας 3.21 Όρια βλαβών στο IDC Πίνακας 3.22 Μέγεθος (ομάδες) στο IDC Πίνακας 3.23 Πρώιμος Εμπλουτισμός στο IDC Πίνακας 3.24 Τύπος καμπύλης στο IDC Πίνακας 3.25 ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec στο IDC Πίνακας 3.26 Spectroscopy - Φασματοσκοπία (Χολίνη ppm) στο IDC Πίνακας 3.27 Ιστολογικός Τύπος στο IDC Πίνακας 3.28 Βαθμός Κακοήθειας (GRADE) στο IDC Πίνακας 3.29 Πολυεστιακότητα στο IDC Πίνακας 3.30 Πολυκεντρικότητα στο IDC Πίνακας 3.31 Μασχαλιαίοι λεμφαδένες στο IDC Πίνακας 3.32 Kruskal-Wallis Test A στο IDC Πίνακας 3.33 Kruskal-Wallis Test B στο IDC - Ομαδοποίηση της ανίχνευσης ή όχι χολίνης Πίνακας 3.34 Kruskal-Wallis Test A στο IDC Πίνακας 3.35 Kruskal-Wallis Test B στο IDC - Ομαδοποίηση με Όρια viii
10 Πίνακας 3.36 Kruskal-Wallis Test A στο IDC Πίνακας 3.37 Kruskal-Wallis Test B στο IDC - Ομαδοποίηση με Τύπο καμπύλης Πίνακας 3.38 Συσχετίσεις στο IDC Πίνακας 3.39 Ηλικιακή κατανομή Πίνακας 3.40 Εκτίμηση ορίων στις βλάβες προ NAC Πίνακας 3.41 Εκτίμηση ορίων στις βλάβες μετά NAC Πίνακας 3.42 Εκτίμηση μεγέθους (cm) στις βλάβες προ NAC Πίνακας 3.43 Εκτίμηση μεγέθους (cm) στις βλάβες μετά NAC Πίνακας 3.44 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού προ NAC Πίνακας 3.45 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού μετά NAC Πίνακας 3.46: Εκτίμηση του συντελεστή προφανούς διάχυσης ADC Χ 10-3 mm2/sec προ NAC Πίνακας 3.47 Εκτίμηση του συντελεστή προφανούς διάχυσης ADC Χ 10-3 mm2/sec μετά NAC Πίνακας 3.48 Φασματοσκοπία (Χολίνη ppm) προ NAC Πίνακας 3.49 Φασματοσκοπία (Χολίνη ppm) μετά NΑC Πίνακας 3.50 Ιστοπαθολογικός Βαθμός Κακοήθειας (grade) προ NAC Πίνακας 3.51 Ιστοπαθολογικός Βαθμός Κακοήθειας (grade) μετά NAC Πίνακας 3.52 Πολυεστιακότητα βλαβών προ NAC Πίνακας 3.53 Πολυεστιακότητα βλαβών μετά NAC Πίνακας 3.54 Παρουσία θετικών μασχαλιαίων λεμφαδένων προ NAC Πίνακας 3.55 Παρουσία θετικών μασχαλιαίων λεμφαδένων μετά NAC Πίνακας 3.56 Ιστολογικός τύπος μικτών καρκινωμάτων Πίνακας 3.57 Ιστολογικός τύπος καρκινωμάτων Πίνακας 3.58 Wilcoxon Signed Ranks Test Γραφήματα Γράφημα 3.1 Ηλικιακή κατανομή ILC Γράφημα 3.2 Ποσοστιαία κατανομή της κινητικής του σκιαστικού στο ILC Γράφημα 3.3 Ποσοστιαία κατανομή του ADC στο ILC Γράφημα 3.4 Ποσοστιαία κατανομή της ανίχνευσης χολίνης στο ILC Γράφημα 3.5 Ποσοστιαία κατανομή της πολυεστιακότητας του ILC Γράφημα 3.6 Ποσοστιαία κατανομή της πολυκεντρικότητας στο ILC Γράφημα 3.7 Παρουσία μασχαλιαίων λεμφαδένων στο ILC Γράφημα 3.8 Κατανομή μεγέθους στο ILC Γράφημα 3.9 Εμφάνιση της βλάβης ως μάζα ή μη μάζα στο ILC Γράφημα 3.10 Πρώιμος εμπλουτισμός στο ILC Γράφημα 3.11 Ποσοστιαία κατανομή του ιστολογικού τύπου του ILC Γράφημα 3.12 Ηλικιακή κατανομή στο DCIS Γράφημα 3.13 Κατανομή ορίων βλάβης στο DCIS ix
11 Γράφημα 3.14 Μέγεθος βλαβών στο DCIS Γράφημα 3.15 Συχνότητα πρώιμου εμπλουτισμού στο DCIS Γράφημα 3.16 Τύπος Καμπύλης στο DCIS Γράφημα 3.17 Κατανομή συντελεστή προφανούς διάχυσης (ADC) στο DCIS Γράφημα 3.18 Κατανομή ανίχνευσης χολίνης στο DCIS Γράφημα 3.19 Κατανομή ιστολογικών τύπων στο DCIS Γράφημα 3.20 Πολυεστιακότητα στο DCIS Γράφημα 3.21 Ηλικιακή κατανομή στο IDC Γράφημα 3.22 Ηλικιακή κατανομή στο IDC Γράφημα 3.23 Όρια βλαβών στο IDC Γράφημα 3.24 Μέγεθος (ομάδες) στο IDC Γράφημα 3.25 Πρώιμος Εμπλουτισμός στο IDC Γράφημα 3.26 Τύπος Καμπύλης στο IDC Γράφημα 3.27 Συντελεστής Προφανούς Διάχυσης (ΑDC) στο IDC Γράφημα 3.28 Φασματοσκοπία στο IDC Γράφημα 3.29 Ιστολογικός Τύπος στο IDC Γράφημα 3.30 Βαθμός Κακοήθειας (grade) στο IDC Γράφημα 3.31 Πολυεστιακότητα στο IDC Γράφημα 3.32 Πολυκεντρικότητα στο IDC Γράφημα 3.33 Παρουσία ή Απουσία θετικών μασχαλιαίων λεμφαδένων στο IDC Γράφημα 3.34 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού προ NAC Γράφημα 3.35 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού μετά NAC Σχήματα Σχήμα 6.1 Το διάγραμμα της Spin Echo (SE) ακολουθίας δείχνει τους σχετικούς χρόνους κατά τους οποίους λαμβάνουν χώρα τα διάφορα γεγονότα, κατά τη διάρκεια της απόκτησης δεδομένων Σχήμα 6.2 Σχηματική αναπαράσταση των καμπυλών εμπλουτισμού x
12 Εικόνες Εικόνα 3.1 Διηθητικό Λοβιακό Καρκίνωμα σε γυναίκα ασθενή 56 ετών με ψηλαφητό μόρφωμα στο ουραίο τμήμα του αριστερού μαστού Εικόνα 3.2 Διηθητικό Λοβιακό Καρκίνωμα πολυκεντρικό σε γυναίκα ασθενή 52 ετών με ψηλαφητή σκληρία στο δεξιό μαστό και αρνητικό μαστογραφικό και υπερηχογραφικό έλεγχο Εικόνα 3.3 Διηθητικό Πλειόμορφο Λοβιακό Καρκίνωμα σε γυναίκα ασθενή 62 ετών που προσήλθε με ψηλαφητούς λεμφαδένες στην αριστερή μασχάλη Εικόνα 3.4 Διηθητικό Λοβιακό Καρκίνωμα σε γυναίκα ασθενή 47 ετών με ψηλαφητή βλάβη στο δεξιό μαστό Εικόνα 3.5. In Situ Καρκίνωμα Πόρων σε γυναίκα ασθενή 39 ετών με μαστογραφία στην οποία απεικονίζονταν ύποπτες μικροεπασβεστώσεις στον αριστερό μαστό Εικόνα 3.6 In Situ Καρκίνωμα Πόρων σε γυναίκα ασθενή 42 ετών με αιματηρό έκκριμα από τη θηλή του δεξιού μαστού Εικόνα 3.7 Πολυεστιακό In Situ Καρκίνωμα Πόρων σε γυναίκα ασθενή 43 ετών με μαστογραφία στην οποία απεικονίστηκε μία ομάδα ύποπτων μικροεπασβεστώσεων στο δεξιό μαστό Εικόνα 3.8 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 52 ετών, θετική για μετάλλαξη του γονιδίου BRCA 1 με ιστορικό μαστεκτομής δεξιά και αρνητικό μαστογραφικό και υπερηχογραφικό έλεγχο στον αριστερό μαστό Εικόνα 3.9 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 33 ετών με αρνητική μαστογραφία ενώ υπήρχε εύρημα στο δεξιό μαστό υπερηχογραφικά. α Εικόνα 3.10 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 42 ετών με ύποπτο μαστογραφικό εύρημα στον αριστερό μαστό Εικόνα 3.11 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 47 ετών με ψηλαφητό μόρφωμα στον αριστερό μαστό Εικόνα 3.12 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 46 ετών με ψηλαφητό μόρφωμα στον αριστερό μαστό Εικόνα 3.13 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 53 ετών με ψηλαφητό μόρφωμα στο ουραίο τμήμα του αριστερού μαστού Εικόνα 3.14 Αμφοτερόπλευρο Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 44 ετών Εικόνα 3.15 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 55 ετών με οικογενειακό ιστορικό καρκίνου μαστού και ατομικό ιστορικό σμίκρυνσης μαστών Εικόνα 3.16 Ενδοκυστικό θηλωματώδες Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 51 ετών με έκκριμα θηλής αριστερού μαστού Εικόνα 3.17 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 46 ετών με ιστορικό μερικής μαστεκτομής προ 8ετίας και τοποθέτησης ενθέματος σιλικόνης. Η μαστογραφία και το υπερηχογράφημα ανέδειξαν ύποπτο εύρημα Εικόνα 3.18 Διηθητικό Καρκίνωμα Πόρων βαθμού κακοήθειας ΙΙΙ πριν τη χορήγηση NAC σε γυναίκα ασθενή 36 ετών με ψηλαφητή σκληρία στον αριστερό μαστό xi
13 Εικόνα 3.19 Μετά τη χορήγηση NAC η ανταπόκριση ήταν πλήρης Εικόνα 3.20 Διηθητικό Καρκίνωμα Πόρων βλεννώδους τύπου, βαθμού κακοήθειας ΙΙΙ πριν τη χορήγηση NAC σε γυναίκα ασθενή 46 ετών με εισολκή θηλής στον αριστερό μαστό Εικόνα 3.21 Μετά τη χορήγηση NAC η ανταπόκριση ήταν μερική : Εικόνα 3.22 Διηθητικό Καρκίνωμα Πόρων, τριπλά αρνητικό, βαθμού κακοήθειας ΙΙΙ, πριν τη χορήγηση NAC σε γυναίκα ασθενή 33 ετών με ιστορικό δεξιάς μαστεκτομής και ψηλαφητή σκληρία στον αριστερό μαστό Εικόνα 3.23 Μετά τη χορήγηση NAC δεν υπήρξε ανταπόκριση: Εικόνα 3.24 Διηθητικό Καρκίνωμα Πόρων, βαθμού κακοήθειας ΙΙΙ, πριν τη χορήγηση NAC σε γυναίκα ασθενή 35 ετών με ψηλαφητή σκληρία στο δεξιό μαστό Εικόνα 3.25 Μετά τη χορήγηση NAC υπήρξε πλήρης ανταπόκριση xii
14 xiii
15 Συντομογραφίες MRI: Magnetic Resonance Imaging MRM: Magnetic Resonance Mammography ADC: Apparent Diffusion Coefficient ROI: Region Of Interest PRESS: Point Resolved Spectroscopy TE: Echo Time TR: Time Repetition 1H-MRS: Proton Magnetic Resonance Spectroscopy SVS: Single Voxel Spectroscopy Cho: Choline DWI: Diffusion Weighted Imaging ILC: Infiltrating Lobular Carcinoma IDC: Infiltrating Ductal Carcinoma DCIS: In Situ Ductal Carcinoma LCIS: In Situ Lobular Carcinoma HER2: Human epidermal growth factor receptor 2 P53: protein 53 BRCA 1/2: Breast Cancer 1/2 NOS: Not Otherwise Specified VEGF: Vascular Endothelial Growth Factor ADC: Apparent Diffusion Coefficient BIRADS: Breast Imaging Reporting Data System DWI: Diffusion Weighted Imaging PRESS: Fat Suppressed Point Resolved Spectroscopy 1HMRS: Proton Magnetic Resonance Spectroscopy NEX: Number of Excitation FS: Fat Suppressed DCE-MRI: Dynamic Contrast Enhancement Magnetic Resonance Imaging UI: Unit Intensity GRE: Gradient Echo STIR: Short-inversion-time inversion recovery T1 W: T1-weighted T2 W: T2-weighted T: Tesla(field strength) xiv
16 xv
17 ΕΥΧΑΡΙΣΤΙΕΣ «πού είναι η σοφία που χάσαμε μέσα στη γνώση; πού είναι η γνώση που χάσαμε μέσα στις πληροφορίες;» T.S. ELIOT Το έργο αυτό εμπνεύστηκε και δημιουργήθηκε από τις γενναίες ασθενείς μου, που με το καθημερινό θάρρος τους μου έδιναν μαθήματα ζωής. Χτίστηκε όμως και από πλειάδα άλλων ανθρώπων που μου πρόσφεραν αφειδώς την αρωγή και στήριξή τους. Τον δάσκαλο και άοκνο υποστηρικτή μου, Καθηγητή κ. Αντώνιο Δρεβελέγκα. Τον επιβλέποντα Επ. Καθηγητή Ακτινολογίας κ. Ιωάννη Χρυσογονίδη, που αδιάκοπα και υπομονετικά με παρότρυνε. Την Καθηγήτρια κ. Αφροδίτη Χαριτάντη, που επέδειξε πραγματικό ενδιαφέρον. Τους εξειδικευμένους στη Μαγνητική Μαστογραφία, Τεχνολόγους, κ.κ. Τασούλα Συροπούλου και Πέτρο Πετρίδη, για την ακούραστη καθημερινή τους βοήθεια. Το Στατιστικολόγο κ. Λευτέρη Παντέρη και τον Πληροφορικό κ. Ηλία Αραβίδη για την πολύτιμη συμβολή τους στην εκπόνηση αυτής της διατριβής. Τον Καθηγητή Παθολογοανατομίας κ. Ζαραμπούκα, τον Καθηγητή Γυναικολογίας κ. Ασημακόπουλο, τον Καθηγητή Χειρουργικής κ. Παπαδόπουλο, την Επ. Καθηγήτρια κ. Τιμοθεάδου για τη συνολική συμβολή τους. Το Χειρουργό Μαστού κ. Κώστα Καραπαναγιώτη για τις πολύτιμες συμβουλές του, την εμπιστοσύνη και συνεχή στήριξή του. Τη Χειρουργό κ. Κατερίνα Σαββίδου για την άψογη συνεργασία μας και την αδιάκοπη συμπαράσταση. Όλους τους ογκολόγους, χειρουργούς μαστού, που με τίμησαν με την εμπιστοσύνη τους. Σε όλους εσάς αφιερώνω τη διατριβή μου. xvi
18 xvii
19 ΠΡΟΛΟΓΟΣ Ο καρκίνος του μαστού, αντικείμενο εκτεταμένης έρευνας τα τελευταία χρόνια, αποτελεί ένα από τα σημαντικότερα προβλήματα υγείας που μπορεί να εμφανιστεί στις γυναίκες κατά τη διάρκεια της ζωής τους και δυνητικά να την απειλήσει. Ο τρόπος με τον οποίο διερευνούμε τον καρκίνο του μαστού έχει αλλάξει τα τελευταία χρόνια εν όψει τόσο της πληθώρας επιστημονικών δεδομένων που αφορούν το μοριακό και γενετικό του προφίλ όσο και της εφαρμογής νέων απεικονιστικών μεθόδων. Στο παρελθόν υπήρχε η δυνατότητα εξέτασης μόνο της μορφολογίας του καρκίνου με μαστογραφικό και υπερηχογραφικό έλεγχο. Τώρα εξετάζονται οι παράγοντες κινδύνου και η γενετική προδιάθεση των ασθενών για καρκίνο του μαστού με βάση τους υποδοχείς και το γενετικό προφίλ του ίδιου του καρκίνου. Παράλληλα, με τις νέες τεχνικές της μαγνητικής μαστογραφίας μπορούμε να διεισδύσουμε σε λειτουργικές παραμέτρους που αφορούν τις βλάβες. Παρ όλα αυτά, η θεμελιώδης προσέγγιση στη διαχείριση του καρκίνου του μαστού συνεχίζει να περιλαμβάνει αφενός μεν την ανίχνευσή του, τη διαφορική διάγνωση από καλοήθεις βλάβες με τη λήψη βιοψιών και αφετέρου τη σταδιοποίηση, το σχεδιασμό της θεραπείας, τον έλεγχο της ανταπόκρισης και την παρακολούθηση των ασθενών. Η μαγνητική μαστογραφία έχει αναδειχθεί σε σημαντικό και αναπόσπαστο στοιχείο μελέτης των ασθενών με καρκίνο του μαστού. Πρωταρχικός και πρωτότυπος στόχος της παρούσης ερευνητικής εργασίας ήταν ο καθορισμός της συμβολής των νεότερων τεχνικών της μαγνητικής μαστογραφίας στη διάγνωση και διαχείριση του καρκίνου του μαστού. Συγκεκριμένα έγινε προσπάθεια σε κάθε περίπτωση λεπτομερούς χαρτογράφησης του καρκίνου για πιθανή ανάδειξη πολυεστιακότητας ή /και πολυκεντρικότητας. Επιπρόσθετα σε κάθε επιμέρους βλάβη μελετήθηκαν όχι μόνο τα μορφολογικά αλλά και τα λειτουργικά χαρακτηριστικά με τη βοήθεια της δυναμικής έγχυσης σκιαστικού, των εικόνων διάχυσης και της φασματοσκοπίας.
20 2
21 ΓΕΝΙΚΟ ΜΕΡΟΣ 3
22 4
23 1 ΙΣΤΟΡΙΚΗ ΑΝΑΔΡΟΜΗ Η συχνότητα των νόσων του μαστού, η αναγνώρισή τους και οι πρώτες προσπάθειες για τη θεραπεία τους σε διάφορους λαούς και πολιτισμούς χρονολογικά προηγούνται της θεραπείας νόσων άλλων συμπαγών οργάνων. Παρά το συνεχές επιστημονικό ενδιαφέρον και τις σημαντικές προόδους που έχουν επιτευχθεί, ο καρκίνος του μαστού παραμένει μία από τις πιο σοβαρές και συχνές νόσους για τον άνθρωπο (Parkin DM et al 1992). Από την αρχαιότητα όγκοι του μαστού είχαν περιγραφεί από Αιγύπτιους και μετά το 460 π.χ. Έλληνες και αργότερα Ρωμαίοι μελετητές περιέγραψαν θανατηφόρους όγκους του μαστού, των οποίων η συχνότητα ήταν άγνωστη. Αναμφίβολα, η Ευρωπαϊκή Ιατρική έχει τις ρίζες της στην αρχαία Ελληνική, με σημαίνον πρόσωπο τον Ιπποκράτη. Μετά από πολλούς αιώνες στασιμότητας κατά τους οποίους η Ιατρική βασιζόταν στις διδαχές του Ιπποκράτη, του Ηρόφιλου, του Γαληνού, του Ασκληπιού και άλλων, η μετάβαση στη σύγχρονη Ιατρική άρχισε ως συνέπεια της Αναγέννησης, στο δεύτερο μισό του 15 ου αιώνα, κυρίως με έρευνες που επικεντρώθηκαν στην ανατομία, φυσιολογία και αργότερα στην ιστολογία που διευκολύνθηκαν με την ανακάλυψη του μικροσκοπίου και τη διατύπωση της κυτταρικής θεωρίας. Στο τέλος του 19 ου αιώνα περιγράφηκε η ριζική μαστεκτομή, η οποία παρέμεινε η σταθερή μέθοδος χειρουργικής θεραπείας για περίπου 70 χρόνια, μέχρι την επινόηση και εφαρμογή των αποτελεσματικότερων χειρουργικών τεχνικών και των πολυπαραγοντικών θεραπειών του 20 ου αιώνα (Rosen PP et al 1989). Στο δεύτερο μισό του 20 ου αιώνα υπήρξε αξιοσημείωτη διαγνωστική και θεραπευτική προσέγγιση του καρκινοπαθούς και ειδικά αυτού με καρκίνο του μαστού. Η μαστογραφία και η σταδιοποίηση του καρκίνου του μαστού αποτέλεσαν δύο από τις σημαντικότερες εξελίξεις. Σήμερα η κατανόηση του ρόλου των ογκογονιδίων και η εφαρμογή γενετικής θεραπείας, μας εισάγουν στη νέα εποχή των ποικίλων μορφών θεραπευτικών επιλογών (Van t Veer LJ 2002). 5
24 2 ΕΠΙΔΗΜΙΟΛΟΓΙΑ - ΕΠΙΠΤΩΣΗ Στις περισσότερες χώρες ο καρκίνος του μαστού είναι η συχνότερη μορφή καρκίνου στις γυναίκες, ενώ στους άνδρες εμφανίζεται σπανιότατα. Σε κάθε 100 περιπτώσεις καρκίνου του μαστού σε γυναίκες αναλογεί μία περίπτωση καρκίνου του μαστού σε άνδρα (Brinton L et al 2002). Έτσι, αναφερόμενοι στον καρκίνου του μαστού γενικά, εννοούμε τον καρκίνο του μαστού της γυναίκας. Αν και η αργή αλλά σταθερή αύξηση της επίπτωσης του καρκίνου του μαστού σχετίζεται και με την αύξηση του μέσου όρου ζωής, η συχνότητά του διαφέρει από χώρα σε χώρα. Στις ΗΠΑ ο καρκίνος του μαστού ήταν η πρώτη αιτία θανάτου από καρκίνο στις γυναίκες μέχρι το 1985, ενώ σήμερα αποτελεί την δεύτερη κατά σειρά αιτία θανάτου(american Cancer Society,GA ). Με βάση τα στοιχεία του Connecticut Cancer Registry για το 1973, η συχνότητα του καρκίνου του μαστού είναι λίγο μεγαλύτερη στις λευκές γυναίκες. Ωστόσο έχει αυξηθεί στις έγχρωμες κατά 25%, στις οποίες μάλιστα παρουσιάζεται σε πιο προχωρημένο στάδιο με αυξημένους δείκτες θνησιμότητας, σε σχέση με τις γυναίκες της λευκής φυλής (Newman LA et al 2002, Shavers VL et al 2002). Κοινωνικοί παράγοντες όπως η μειωμένη πρόσβαση σε υπηρεσίες υγείας ευθύνονται εν μέρει για τις διαφορές αυτές, αν και σίγουρα συνυπάρχουν γενετικοί παράγοντες. Συγκριτικά με τις λευκές γυναίκες, σε γυναίκες της μαύρης φυλής οι καρκίνοι εμφανίζονται συχνότερα πριν τα 40 έτη, έχουν υψηλότερη πυρηνική ατυπία, είναι σπανιότερα θετικοί για ορμονικούς υποδοχείς και έχουν διαφορετικούς τύπους μετάλλαξης του γονιδίου p53. O κίνδυνος ανάπτυξης διηθητικού καρκίνου μαστού εντός 20ετίας μετά τα 50 έτη είναι 1 προς 15 για Καυκάσιες, 1 προς 20 για Αφροαμερικανές, 1 προς 26 για Ασιάτισσες κατοίκους νησιών Ειρηνικού και 1 προς 27 για γυναίκες Ισπανικής καταγωγής (Morris et al, 2001). Μετανάστες από χώρες με χαμηλή επίπτωση καρκίνου του μαστού σε χώρες με υψηλή επίπτωση, τείνουν μετά τη δεύτερη γενιά να έχουν μεγαλύτερη επίπτωση, πράγμα που σημαίνει ότι οι διακυμάνσεις της επίπτωσης από χώρα σε χώρα οφείλονται και σε διαφορές του περιβάλλοντος, καθώς και σε άλλες συνήθειες και συνθήκες διαβίωσης (Fitzgibbons PL et al 2000, Mirza An et al 2002). 6
25 Το γεγονός ότι η επίπτωση του καρκίνου του μαστού έχει αρχίσει να αυξάνεται σε μεγαλύτερες γυναίκες, έχει θέσει την υπόνοια της επίδρασης κάποιου άγνωστου περιβαλλοντικού παράγοντα. Όμως, ουσιαστικά από τις αρχές του 1980 έχει ξεκινήσει ο προληπτικός έλεγχος με μαστογραφία και ο αριθμός των γυναικών που υποβάλλονται σε αυτόν αυξήθηκε σταθερά από το 60% στο 80% (Page DL et al 2003). Ο προληπτικός έλεγχος σαφέστατα οδηγεί σε αυξημένη ανίχνευση μικρών διηθητικών και in situ καρκινωμάτων. Τα τελευταία διαγιγνώσκονται σχεδόν αποκλειστικά με μαστογραφία, με αποτέλεσμα σαφή αύξηση των in situ καρκινωμάτων στις γυναίκες. Παράλληλα, μετά την έναρξη του προληπτικού ελέγχου ο αριθμός των γυναικών που εμφανίζονται με μεγάλους όγκους έχει μειωθεί. Κατά συνέπεια, η αύξηση της επίπτωσης του καρκίνου του μαστού βάσιμα αποδίδεται στην επίδραση του προληπτικού ελέγχου (Rhodes DJ 2002, Morris CR et al 2001). Περίπου το ένα τρίτο των γυναικών που διαγιγνώσκονταν με καρκίνο του μαστού, μέχρι πρόσφατα κατέληγαν από τη νόσο. Κατά τη διάρκεια του 1980 ο αριθμός των θανάτων από τη νόσο, παρά την αύξηση της επίπτωσης, παρέμεινε σταθερός, πιθανότατα διότι με τον προληπτικό έλεγχο ανιχνεύονταν έγκαιρα υποκλινικές κακοήθειες. Ο δείκτης θνησιμότητας έχει αρχίσει να υποχωρεί από το 1994 και αναμένεται αυτή η πτωτική πορεία να συνεχιστεί, αφ ενός μεν διότι ο προληπτικός έλεγχος ανιχνεύει καρκίνους σε θεραπεύσιμο στάδιο και αφ ετέρου διότι έχουν αναπτυχθεί καλύτερα θεραπευτικά σχήματα. Σύμφωνα με τα νεότερα δεδομένα, μόνο το 20% των γυναικών με καρκίνο του μαστού αναμένεται να πεθάνουν από τη νόσο (Pharoah PDP et al 2002, Hanahan D et al 2000). Η υψηλή συχνότητα της νόσου στις γυναίκες έχει πυροδοτήσει εντατικές μελέτες των παραγόντων κινδύνου, με σκοπό τη διερεύνηση της αιτιοπαθογένειας του καρκίνου του μαστού, την τροποποίηση των παραγόντων κινδύνου, σε συνδυασμό με τον παράλληλο σχεδιασμό αποτελεσματικότερων στρατηγικών πρόληψης. Με βάση επιδημιολογικές μελέτες έχει αναπτυχθεί ένα στατιστικό μοντέλο με σκοπό τον υπολογισμό του κινδύνου που υπάρχει στο να αναπτύξει καρκίνο μαστού μια γυναίκα, μέσα στα επόμενα πέντε έτη ή μέχρι την ηλικία των 90 ετών (Gail MH et al 1989). Το μοντέλο αυτό έχει σχεδιαστεί για γυναίκες άνω των 35 ετών, χωρίς προηγούμενη διάγνωση καρκίνου μαστού και χωρίς οικογενειακό ιστορικό που να υποδηλώνει συγκεκριμένη μετάλλαξη (Rhodes DJ 2002). 7
26 Όσον αφορά την ηλικία, ο καρκίνος του μαστού σπάνια εμφανίζεται πριν τα 25 έτη, εκτός από συγκεκριμένες οικογενείς περιπτώσεις. Η επίπτωσή του αυξάνεται στη διάρκεια της ζωής της γυναίκας και το 77% των περιπτώσεων αφορά γυναίκες άνω των 50 ετών, ενώ η μέση ηλικία διάγνωσης είναι τα 64 έτη. Οι γυναίκες με εμμηναρχή μικρότερη των 11 ετών έχουν αυξημένο κίνδυνο εμφάνισης καρκίνου μαστού κατά 20%, συγκριτικά με εκείνες στις οποίες η εμμηναρχή ήταν σε ηλικία μεγαλύτερη των 14 ετών. Αντίθετα, η καθυστέρηση της εμμηνόπαυσης αυξάνει τον κίνδυνο, χωρίς όμως ακόμη να υπάρχει ποσοτικοποίηση της αύξησης αυτής. Γυναίκες με πρώτη τελειόμηνη κύηση σε ηλικία μικρότερη των 20 ετών έχουν το μισό κίνδυνο σε σχέση με άτοκες γυναίκες ή γυναίκες άνω των 35 ετών στην πρώτη τους γέννα. Θεωρείται ότι η εγκυμοσύνη βοηθά τη διαφοροποίηση των επιθηλιακών κυττάρων, απομακρύνοντας πιθανούς καρκινικούς προδρόμους. Το αποτέλεσμα όμως αυτό επισκιάζεται από το ότι σε κυήσεις γυναικών μεγαλύτερης ηλικίας, νωρίς στην εγκυμοσύνη ευνοείται ο πολλαπλασιασμός κυττάρων που έχουν ήδη υποστεί προνεοπλασματικές αλλοιώσεις. Σε γυναίκες με ιστορικό καρκίνου μαστού σε άτομο πρώτου βαθμού συγγένειας ο κίνδυνος είναι αυξημένος, αν και στην πλειονότητα των κακοηθειών αφ ενός μεν δεν υπάρχει οικογενειακό ιστορικό και αφ ετέρου το 87% των γυναικών με οικογενειακό ιστορικό δεν αναπτύσσει καρκίνο του μαστού. Επίσης μόνο το 13% των προσβεβλημένων γυναικών έχουν οικογενειακό ιστορικό με ένα συγγενή πρώτου βαθμού και, ακόμη περισσότερο, μόνο στο 1% υπάρχουν δύο ή παραπάνω προσβεβλημένοι συγγενείς. Οι παραπάνω στατιστικές δεν ισχύουν όταν η γυναίκα εμφανίζει τη συγκεκριμένη γονιδιακή μετάλλαξη BRCA1 ή BRCA2 (Hedenfalk I et al 2001). Αυξημένος κίνδυνος καρκίνου μαστού σχετίζεται με προηγούμενες βιοψίες οι οποίες δείχνουν άτυπη υπερπλασία, όχι όμως όταν υπάρχουν υπερπλαστικές αλλοιώσεις χωρίς ατυπία. 8
27 Η μετεμμηνοπαυσιακή θεραπεία ορμονικής υποκατάστασης αυξάνει ελαφρά τον κίνδυνο καρκίνου του μαστού, πιθανότατα όμως δεν αυξάνει τον κίνδυνο θανάτου (Mahavani V et al 2001, Nelson HD et al 2002). Ο συνδυασμός οιστρογόνων προγεστερόνης αυξάνει περισσότερο τον κίνδυνο, ιδίως για διηθητικό λοβιακό καρκίνωμα και άλλους καρκίνους με θετικούς οιστρογονικούς υποδοχείς. Τα per os αντισυλληπτικά θεωρείται ότι δεν αυξάνουν τον κίνδυνο καρκίνου του μαστού (Nelson HD et al 2002, Marchbanks PA et al 2002) και από την άλλη πλευρά πιθανότατα μειώνουν τον κίνδυνο άλλων κακοηθειών, όπως ο καρκίνος των ωοθηκών. Η ελάττωση των ενδογενών οιστρογόνων με ωοθηκεκτομή μειώνει τον κίνδυνο ανάπτυξης καρκίνου του μαστού έως και 75%. Η έκθεση σε υψηλές δόσεις ακτινοβολίας, θεραπευτική ή μη αυξάνει τον κίνδυνο για καρκίνο του μαστού, ιδίως σε νεαρές γυναίκες. Η ακτινοθεραπεία για νόσο Hodgkin σε γυναίκες στην εφηβεία αυξάνει κατά 20 έως 30% τον κίνδυνο τα επόμενα 10 έως 30 έτη, ενώ αυτό δεν ισχύει όταν η ακτινοθεραπεία αφορά γυναίκες μεγαλύτερες των 20 ετών (Clemons M et al 2000). Με τις σύγχρονες μαστογραφίες που χρησιμοποιούν χαμηλές δόσεις ακτινοβολίας, είναι απίθανο να αυξάνεται ο κίνδυνος καρκίνου του μαστού Αυξημένος κίνδυνος υπάρχει για καρκίνο στον αντίθετο μαστό ή στο ενδομήτριο, πιθανότατα λόγω κοινών παραγόντων κινδύνου. Συσχετισμός της διατροφής με την ανάπτυξη καρκίνου του μαστού έχει δείξει μειωμένο κίνδυνο με την αυξημένη λήψη β-καροτενίου και αυξημένο από τη μέτρια ή έντονη κατανάλωση αλκοόλ, πιθανότατα μέσω μηχανισμού μείωσης των επιπέδων φυλλικού οξέος και αύξησης του επιπέδου των οιστρογόνων (Hamajima N et al 2002). Συσχετισμός της αυξημένης λήψης λίπους με τη διατροφή και του καρκίνου του μαστού δεν έχει αποδειχθεί ενώ παχύσαρκες γυναίκες κάτω των 40 ετών θεωρούνται μειωμένου κινδύνου λόγω ύπαρξης ανωορρηκτικών κύκλων, σε αντίθεση με παχύσαρκες μετεμμηνοπαυσιακές γυναίκες, οι οποίες θεωρούνται αυξημένου κινδύνου, λόγω σύνθεσης οιστρογόνων στις αποθήκες λίπους, ενώ είναι γεγονός ότι ο θηλασμός μειώνει τον κίνδυνο ανάπτυξης καρκίνου του μαστού (Beral V et al 2002). Η 9
28 χαμηλότερη συχνότητα καρκίνου του μαστού στις αναπτυσσόμενες χώρες σε μεγάλο βαθμό αποδίδεται στο συχνότερο και μεγαλύτερης διάρκειας βρεφικό θηλασμό. Ο ρόλος περιβαλλοντικών τοξινών, όπως τα οργανικο-χλωρινικά φυτοφάρμακα που εμφανίζουν οιστρογονικές επιδράσεις, διερευνάται έντονα χωρίς να υπάρχουν ακόμα τεκμηριωμένα αποτελέσματα, ενώ για το κάπνισμα έχει αποδειχθεί ότι σχετίζεται με περιπορική μαστίτιδα ή υποθηλαίο απόστημα, χωρίς να σχετίζεται άμεσα με καρκίνο μαστού. 10
29 3 ΑΙΤΙΟΠΑΘΟΓΕΝΕΙΑ Ο καρκίνος του μαστού θεωρείται πολυπαραγοντική διαταραχή με παράγοντες κινδύνου ενδογενείς και εξωγενείς. Διαχωρίζεται σε σποραδικό, που πιθανότατα συσχετίζεται με ορμονική έκθεση και κληρονομικό, που σχετίζεται με οικογενειακό ιστορικό ή κληρονομούμενες γονιδιακές μεταλλάξεις. Το 25% των κληρονομικών καρκίνων μαστού (ή το 3% όλων των καρκίνων μαστού) μπορεί να αποδοθεί σε δύο αυτοσωματικά επικρατούντα γονίδια υψηλής διεισδυτικότητας, το BRCA1 και το BRCA2. Φορείς αυτών έχουν υψηλότατο κίνδυνο 60% έως 85% να εμφανίσουν καρκίνο με μέση ηλικία διάγνωσης του καρκίνου του μαστού κατά 20 έτη μικρότερη. Η διεισδυτικότητα ποικίλλει ανάλογα με τον τύπο της μετάλλαξης. Επιπρόσθετα το BRCA1 αυξάνει τον κίνδυνο ανάπτυξης καρκίνου των ωοθηκών στο 20% έως 40%, ενώ το BRCA2 τον αυξάνει στο 10% έως 20%, συνδέεται όμως πιο συχνά με καρκίνο μαστού σε άνδρες. Αυτό πιθανότατα σχετίζεται με το ότι το BRCA1, όχι όμως το BRCA2, αλληλεπιδρά με οιστρογονικούς υποδοχείς και σχετίζεται με απενεργοποίηση του Χ χρωμοσώματος (Gamsan S et al 2002). Τα δύο αυτά γονίδια είναι ογκοκατασταλτικά, βρίσκονται σε διαφορετικά χρωμοσώματα, στο χρωμόσωμα 17 το BRCA1 και στο 13 το BRCA2, εμφανίζουν δε εκατοντάδες μεταλλάξεις, μόνο ορισμένες από τις οποίες μειώνουν την ογκοκαταστολή, αυξάνοντας τον κίνδυνο καρκινογένεσης. Η ογκοκατασταλτική δράση των γονιδίων αυτών συνίσταται σε αποτελεσματική επιδιόρθωση χωρίς σφάλματα των ρήξεων της διπλής έλικας του DNA που συμβαίνουν συνεχώς κατά τη διάρκεια της κυτταρικής ζωής. Οι επιδιορθωτικοί μηχανισμοί επάγονται από αυτά τα γονίδια είτε έμμεσα, (Venkitaramann AR 2002) είτε μέσω άμεσης πρόσδεσης στο DNA (Yang H et al 2002). Η απώλεια αυτών των λειτουργιών λόγω μετάλλαξης στα γονίδια BRCA1 και BRCA2 επηρεάζει κυρίως το μαστό και όχι άλλα όργανα όπως το δέρμα ή το παχύ έντερο, πιθανότατα είτε διότι στο μαστό η υπερπλασία του επιθηλίου των πόρων είναι διαλείπουσα, σε αντίθεση με τη συνεχή υπερπλασία και απόπτωση επιθηλίων άλλων οργάνων, είτε διότι σε άλλα όργανα υπάρχουν επιπρόσθετοι μηχανισμοί επιδιόρθωσης του DNA, τους οποίους στερείται ο μαστός. 11
30 Οι μεταλλάξεις των γονιδίων BRCA1 και BRCA2 είναι σπάνιες (0,1% έως 0,2% στο γενικό πληθυσμό). Αυτές που μειώνουν την ογκοκατασταλτική λειτουργία των γονιδίων είναι καρκινογόνες, ενώ άλλες μεταλλάξεις αποτελούν ασήμαντες τροποποιήσεις. Ο γενετικός έλεγχος συχνά είναι δύσκολος ή μη διαγνωστικός. Επιβάλλεται αν προσβάλλονται πολλά μέλη της ίδιας οικογένειας ή αν το άτομο ανήκει σε εθνότητα με υψηλή επίπτωση τέτοιων μεταλλάξεων (Carter RF 2001). Για παράδειγμα οι Εσκενάζι Εβραίοι έχουν 2% έως 3% κίνδυνο τριών συγκεκριμένων μεταλλάξεων. Η αναγνώριση φορέων κλινικά σημαντικών μεταλλάξεων είναι σημαντική, δεδομένου ότι η προληπτική μαστεκτομή και ωοθηκεκτομή μπορεί να μειώσει τη θνησιμότητα από καρκίνο του μαστού (Hartmann LC et al 1999, Kauff ND et al 2002 ). Αν και σε σποραδικούς καρκίνους του μαστού σπάνια ανευρίσκονται μεταλλάξεις στα γονίδια BRCA1 και BRCA2, το 50% αυτών εμφανίζει μειωμένη ή καθόλου έκφραση του BRCA1, γεγονός που αποδίδεται σε απενεργοποίησή του μέσω μεθυλιωτικού κυτταρικού παράγοντα. Ο παράγοντας αυτός ανιχνεύεται πιο συχνά στους μυελοειδείς και στους βλεννώδεις καρκίνους του μαστού. Οι κακοήθειες του μαστού που σχετίζονται με το BRCA1 συνήθως εμφανίζουν πολύ χαμηλή διαφοροποίηση και δεν εκφράζουν ορμονικούς υποδοχείς είτε υπερεκφράζουν τον υποδοχέα HER2/neu (υποδοχέας ενός επιδερμικού αυξητικού παράγοντα ο οποίος συχνά υπερεκφράζεται στον καρκίνο του μαστού και προσδίδει επιθετικότητα). Σποραδικοί καρκίνοι μαστού με μοριακό προφίλ παρόμοιο με αυτό των καρκινωμάτων του BRCA1 έχουν ονομαστεί basal like λόγω του ότι εκφράζουν γονίδια που είναι χαρακτηριστικά των μυοεπιθηλιακών κυττάρων ή πιθανόν πρόδρομων κυττάρων μαζικού αδένα. Με άλλα λόγια, ορισμένοι σποραδικοί καρκίνοι έχουν γενετικές ομοιότητες με τους κληρονομικούς καρκίνους. Η γενετική ευπάθεια που οφείλεται σε άλλα γνωστά γονίδια ευθύνεται για λιγότερο από το 10% των κληρονομικών καρκίνων του μαστού (De Jong MM et al 2002). Mόνο πέντε γονίδια έχουν μελετηθεί αρκετά. Μεταξύ αυτών είναι το γονίδιο CHEΚ2, το οποίο κωδικοποιεί ένα ένζυμο (μία κινάση) που ρυθμίζει τον κυτταρικό κύκλο. Η ρύθμιση επιτυγχάνεται επιδιορθώνοντας βλάβες του DNA και ενεργοποιώντας το BRCA1 (Meijers-Heijboer H et al 2002). Γυναίκες με το σύνδρομο Li-Fraumeni που 12
31 οφείλεται σε μετάλλαξη του γονιδίου p53 έχουν 18 φορές μεγαλύτερο κίνδυνο ανάπτυξης καρκίνου του μαστού πριν τα 45 έτη. Μεταλλάξεις στο p53 υπάρχουν στο 19% έως 57% των σποραδικών καρκίνων του μαστού. Μετάλλαξη στο PTEN γονίδιο του χρωμοσώματος 10q ευθύνεται για το σύνδρομο πολλαπλών αμαρτωμάτων Cowden, στο οποίο ο κίνδυνος ανάπτυξης καρκίνου του μαστού είναι 25% έως 50%. Μετάλλαξη στο γονίδιο LKB1, η οποία υπάρχει στο σύνδρομο Peutz-Jeghers, προδιαθέτει επίσης για καρκίνο του μαστού όπως και το ATM γονίδιο της αταξίας - τηλαγγειεκτασίας που έχει μελετηθεί πάρα πολύ λόγω του μεγάλου αριθμού των φορέων στο γενικό πληθυσμό (περίπου 7%) και λόγω του ότι οι φορείς εμφανίζουν αυξημένη ευαισθησία στην ακτινοβολία, γεγονός που προκαλεί προβληματισμό σχετικά με τον προληπτικό μαστογραφικό έλεγχο. Ακόμα και αν ληφθούν υπόψιν όλα αυτά τα γονίδια, τα 2/3 τουλάχιστον του κληρονομικού καρκίνου του μαστού παραμένουν ανεξήγητα, ενώ η αναζήτηση ενός θεωρητικού BRCA3 γονιδίου υψηλής διεισδυτικότητας δεν έχει αποδώσει ακόμα καρπούς (Wooster R et al 2003). Πιθανότατα υπάρχουν πολλά γονίδια με μικρή διεισδυτικότητα, ο συνδυασμός των οποίων θα μπορούσε να εξηγήσει τους περισσότερους κληρονομικούς καρκίνους του μαστού, όπως και τον κίνδυνο καρκίνου του μαστού στο γενικό πληθυσμό (Pharoah PDP et al 2002, Antoniou AC et al 2002, Peto J 2002). Με βάση αυτό το μοντέλο, οι περισσότερες περιπτώσεις κληρονομικού καρκίνου μαστού αφορούν μικρό ποσοστό γυναικών οι οποίες έχουν συνδυασμούς αυτών των γονιδίων. Η αναγνώριση αυτών των συνδυασμών θα μπορούσε να επιτρέψει την καλύτερη ταξινόμηση των γυναικών σε ομάδες χαμηλού και υψηλού κινδύνου, γεγονός που θα βοηθούσε την πρόληψη και πρώιμη ανίχνευση καρκίνου σε αυτές τις γυναίκες. Οι περισσότεροι σποραδικοί καρκίνοι του μαστού εμφανίζονται μετά την εμμηνόπαυση και χαρακτηρίζονται από υπερέκφραση οιστρογονικών υποδοχέων. Τα οιστρογόνα προξενούν μεταλλάξεις μέσω ελευθέρων ριζών που αλλοιώνουν το DNA, ευνοώντας έτσι τη δημιουργία προκαρκινικών αλλοιώσεων αλλά και καρκίνων. Δεδομένου όμως ότι πολλοί καρκίνοι του μαστού είναι αρνητικοί για οιστρογονικούς υποδοχείς, πιθανότατα συνυπάρχουν και άλλοι μηχανισμοί που διαδραματίζουν κάποιο ρόλο. 13
32 4 ΠΡΟΓΝΩΣΤΙΚΕΣ ΠΑΡΑΜΕΤΡΟΙ Το μέγεθος του όγκου αποτελεί πολύ σημαντική προγνωστική παράμετρο για την εκτίμηση του σταδίου της νόσου. Ο κίνδυνος λεμφαδενικών μεταστάσεων στη μασχάλη αυξάνεται με το μέγεθος του καρκινώματος. Γυναίκες με καρκίνους μικρότερους του εκατοστού, και αρνητικούς λεμφαδένες έχουν ποσοστό δεκαετούς επιβίωσης περίπου 90% χωρίς θεραπεία. Το σχήμα του όγκου είναι συχνά ανώμαλο και για την εκτίμηση του μεγέθους λαμβάνεται υπ όψιν η μεγαλύτερη διάμετροs (Goldhirsch A et al 2005, Fitzgibbons PL et al 2000, Mirza AN et al 2002). Καλά περιγεγραμμένοι όγκοι φαίνεται ότι έχουν καλύτερη πρόγνωση από τους όγκους με ανώμαλη, ακτινωτή παρυφή. Οι τελευταίοι συνδέονται με μεγαλύτερο αριθμό διηθημένων λεμφαδένων στη μασχάλη. Επιπρόσθετα, οι όγκοι με αστεροειδές σχήμα και κεντρική νέκρωση έχουν δυσμενέστερη πρόγνωση (Tavassoli FA, 1999). Η κατάσταση των λεμφαδένων της μασχάλης αποτελεί τον πιο σημαντικό προγνωστικό παράγοντα για το διηθητικό καρκίνωμα εφόσον δεν υπάρχουν απομακρυσμένες μεταστάσεις. Η δεκαετής επιβίωση χωρίς λεμφαδενική συμμετοχή αγγίζει το 70-80% (Mirza AN et al 2001). Τα περισσότερα καρκινώματα του μαστού παροχετεύονται από ένα ή δύο λεμφαδένες φρουρούς οι οποίοι είναι ιδιαίτερα προγνωστικοί της κατάστασης των υπόλοιπων λεμφαδένων. Οι μακρομεταστάσεις (> 0,2 εκατ.) έχουν αποδεδειγμένη προγνωστική σημασία, ενώ η κλινική σημασία των μικρομεταστάσεων διερευνάται στις τρέχουσες μελέτες (Zanghi G. et al 2014). Ο βαθμός της κακοήθειας (grading) αφορά κατά κανόνα το διηθητικό τμήμα του όγκου. Το πιο συνηθισμένο σύστημα βαθμολόγησης που χρησιμοποιείται για την εκτίμηση του βαθμού καρκινικής διαφοροποίησης (Scarff Bloom Richardson) συνδυάζει το βαθμό πυρηνικής ατυπίας, το σχηματισμό σωληνίσκων και το ποσοστό μιτώσεων. Ο βαθμός κακοήθειας σύμφωνα με το σύστημα ταξινόμησης των Bloom και Richardson, κατηγοριοποιείται: Στην κατηγορία Ι στην οποία ταξινομούνται τα καλά διαφοροποιημένα νεοπλάσματα, στην κατηγορία ΙΙ τα μέτρια διαφοροποιημένα και στην κατηγορία ΙΙΙ αυτά που εμφανίζουν μικρή διαφοροποίηση (Rosen PP 1997). 14
33 Kατά την ιστολογική εξέταση του παρασκευάσματος το μέγεθος του όγκου, ο βαθμός κακοήθειας και ο αριθμός των διηθημένων λεμφαδένων αποτελούν αναμφισβήτητες προγνωστικές παραμέτρους, οι οποίες συνθέτουν τον προγνωστικό δείκτη του Nottingham. Ο δείκτης αυτός υπολογίζεται από τον τύπο: Δ= 0,2 Χ Τ + Ν + G, όπου Τ είναι η μέγιστη διάμετρος του όγκου σε εκατοστά, Ν η παρουσία ή όχι διηθημένων λεμφαδένων στη μασχάλη (με Ν=1 όταν δεν υπάρχουν διηθημένοι λεμφαδένες, Ν=2 όταν ο αριθμός των λεμφαδένων είναι από 1 έως 3 και Ν=3 όταν οι θετικοί λεμφαδένες είναι περισσότεροι από 3) και G ο βαθμός διαφοροπόίησης του πρωτοπαθούς όγκου (με διαβάθμιση του G από 1 έως 3). Η πρόγνωση γίνεται χειρότερη όταν αυξάνεται η τιμή του Δ. Χρησιμοποιώντας σαν διαχωριστικές τιμές το 3,4 και 5,4 οι ασθενείς διακρίνονται σε 3 ομάδες. Στην πρώτη ομάδα με καλή πρόγνωση ο Δ είναι μικρότερος του 3,4. Στη δεύτερη ομάδα με ενδιάμεση πρόγνωση ο Δ είναι μικρότερος του 5,4 και μεγαλύτερος του 3,4. Στην τρίτη ομάδα με δυσμενή πρόγνωση ο Δ είναι μεγαλύτερος του 5,4. Οι θνησιμότητες αντίστοιχα είναι 3%, 7% και 30% (Hunt KK et al 2001). Ο πυρηνικός δείκτης (nuclear grade, ΝG) εκφράζει τους μορφολογικούς χαρακτήρες των πυρήνων των νεοπλασματικών κυττάρων. O πυρηνικός δείκτης διαβαθμίζεται σε τρείς κατηγορίες: Καλή διαφοροποίηση G=3, μέση διαφοροποίηση G=2 και ελάχιστη διαφοροποίηση G=1 (Simpson JF 1992). Ο βαθμός διαφοροποίησης και ο πυρηνικός δείκτης συχνά συμφωνούν, αλλά όχι πάντοτε (Payne SJL et al 2008). Οι ασθενείς με όγκους χαμηλής διαφοροποίησης έχουν μεγαλύτερη πιθανότητα θετικών μασχαλιαίων λεμφαδένων, εμφανίζουν υποτροπή της νόσου συχνότερα, το χρονικό διάστημα ελεύθερο νόσου είναι μικρότερο, με αποτέλεσμα χειρότερη πρόγνωση συγκριτικά με τους όγκους. ασθενείς με καλά διαφοροποιημένους Η λεμφοπλασματοκυτταρική διήθηση του όγκου αποτελεί σημαντικό ιστολογικό εύρημα, η αξιοποίηση του οποίου ως προγνωστικού παράγοντα έχει μελετηθεί πολύ. Εκτεταμένη διήθηση του όγκου από λεμφοκύτταρα και πλασματοκύτταρα χαρακτηρίζει το λεμφο-επιθηλιόμορφο και το μυελοειδές 15
34 καρκίνωμα, τα οποία περιγράφονται ως ιδιαίτερες μορφές καρκίνου του μαστού. Μερική διήθηση του όγκου από τα κύτταρα αυτά χαρακτηρίζει το άτυπο μυελοειδές καρκίνωμα, το οποίο, σύμφωνα με ορισμένους ερευνητές, μπορεί να έχει καλύτερη πρόγνωση από το μυελοειδές καρκίνωμα που δεν εμφανίζει αυτό το γνώρισμα (Simpson JF 1992). Καρκινικά κύτταρα μπορεί να εντοπιστούν μέσα στα αγγεία, είτε λεμφαγγεία είτε μικρά τριχοειδή που περιβάλλουν τον όγκο και συνδέεται με την παρουσία λεμφαδενικών μεταστάσεων. Η διήθηση των λεμφαγγείων από νεοπλασματικά κύτταρα θεωρείται ότι συνδέεται με δυσμενή πρόγνωση και είναι ένας φτωχός προγνωστικός παράγοντας σε γυναίκες χωρίς λεμφαδενικές μεταστάσεις. Έχει ιδιαίτερη σημασία σε ασθενείς με μικρούς όγκους και αρνητικούς μασχαλιαίους λεμφαδένες ενώ σε ασθενείς με θετικούς λεμφαδένες η σημασία του ευρήματος είναι αβέβαιη (Tavassoli FA 1999, Chia SK et al 2004). Η παρουσία καρκινικών κυττάρων στα λεμφαγγεία του χορίου συνδέεται με την κλινική εμφάνιση του φλεγμονώδους καρκίνου και προμηνύει μια φτωχή πρόγνωση. Η διήθηση των αγγείων από τον όγκο θεωρείται μη αμφισβητήσιμη, όταν αφ ενός μεν ανιχνευτούν νεοπλασματικά κύτταρα σε ένα ή και στα δύο συμπορευόμενα μέσα στον όγκο αγγεία (φλέβα και/ή αρτηρία) και αφ ετέρου όταν οι ελαστικές ίνες του τοιχώματος των αγγείων χρωματίζονται ανοσοϊστοχημικά (Rosen PP 1997). Ο ρυθμός πολλαπλασιασμού μπορεί να μετρηθεί από την ανοσοιστοχημική ανίχνευση των κυτταρικών πρωτεινών (κυκλίνη, Ki-67) που παράγονται κατά τη διάρκεια του κυτταρικού κύκλου. Η περιεκτικότητα σε κυκλίνη Ε αποτελεί ισχυρό προγνωστικό παράγοντα της επιβίωσης. Το Ki-67 είναι μια πρωτείνη του πυρήνα που βρίσκεται σε όλες τις φάσεις του κυτταρικού κύκλου και αποτελεί δείκτη κυτταρικού πολλαπλασιασμού. Ετσι όγκοι με υψηλό δείκτη πολλαπλασιασμού, έχουν χειρότερη πρόγνωση (Keyomarsi K et al, 2002). Τρέχουσες μέθοδοι χρησιμοποιούν την ανοσοιστοχημεία για να ανιχνεύσουν υποδοχείς στον πυρήνα του κυττάρου. Γυναίκες με όγκους που είναι θετικοί σε ορμονικούς υποδοχείς έχουν ελαφρώς καλύτερη πρόγνωση από γυναίκες με όγκους αρνητικούς σε ορμονικούς υποδοχείς. Το 80% των όγκων με οιστρογονικούς και 16
35 προγεστερονικούς υποδοχείς ανταποκρίνονται στην ορμονική θεραπεία, ενώ όγκοι που δε διαθέτουν υποδοχείς οιστρογόνων και προγεστερόνης έχουν λιγότερο από 10% πιθανότητα ανταπόκρισης (Simpson JF et al 1992). O ανθρώπινος υποδοχέας του επιδερμικού αυξητικού παράγοντα 2 (HER2 ή c- erb B2) είναι μια γλυκοπρωτείνη με σημαντικό ρόλο στον έλεγχο της κυτταρικής αύξησης. Η υπερέκφραση του HER/2 συνδέεται με φτωχή πρόγνωση με βάση τα αποτελέσματα πολλών μελετών (Hayes DF et al 2002). Η διήθηση νεύρων δεν έχει αναδειχθεί ως ανεξάρτητος προγνωστικός παράγοντας, και συχνά συνυπάρχει με τη διήθηση των λεμφαγγείων. Η ποσότητα του στρώματος, και ο ινώδης συνδετικός ιστός που αναπτύσσεται γύρω από ένα διηθητικό καρκίνωμα μαστού, όπως και η ποσότητα της ελαστίνης μπορεί να ποικίλλουν και παρ όλο που δυνητικά συσχετίζονται με τη συμπεριφορά του όγκου, δεν θεωρούνται ανεξάρτητοι προγνωστικοί παράγοντες (Fletcher MS 2000). H παρουσία αυξημένου ποσοστoύ μη διηθητικού καρκινώματος μέσα στον όγκο φαίνεται ότι σχετίζεται με πολυκεντρικότητα της βλάβης, δηλαδή με τη συνύπαρξη πολλαπλών μικροσκοπικών εστιών μη διηθητικού καρκινώματος στο μαστό με αποτέλεσμα αυξημένη πιθανότητα υποτροπής μετά από μερική μαστεκτομή (Silverstein MJ 2000). Τα τελευταία χρόνια έχουν αναπτυχθεί διάφορες μέθοδοι που αναλύουν την έκφραση πολλών ογκογονιδίων ταυτόχρονα και καταλήγουν σε μια συνολική βαθμολόγηση επικινδυνότητας (Oncotype, Mammaprint). Παρόλο που έχουν γίνει αποδεκτά στην κλινική πράξη, αναμένονται τα αποτελέσματα προοπτικών κλινικών μελετών για την επακριβή διευκρίνιση του ρόλου τους. 17
36 5 ΙΣΤΟΛΟΓΙΑ ΚΑΙ ΤΑΞΙΝΟΜΗΣΗ ΤΩΝ ΚΑΡΚΙΝΩΝ ΤΟΥ ΜΑΣΤΟΥ Ο μαζικός αδένας αποτελείται από 15 έως 20 τμήματα ή λοβούς, που διατάσσονται ακτινωτά σε σχέση με τη θηλή. Οι πόροι των τμημάτων συγκλίνουν προς τη θηλή και σχηματίζουν τους γαλακτοφόρους κόλπους. Στη θηλή τελικά εκβάλλουν 15 έως 20 μείζονες γαλακτοφόροι πόροι που επαλείφονται από πολύστιβο πλακώδες επιθήλιο. Κάθε τμήμα ή λοβός του μαστού αποτελείται από 20 έως 40 λόβια και κάθε λόβιο από 10 έως 100 αδενικές κυψέλες (Osborne MP, 1997). Η λειτουργική μονάδα του μαστού αποτελείται από το λόβιο και τον τελικό πόρο, ο οποίος έχει εξωλοβιακό και ενδολοβιακό τμήμα. Το εξωλοβιακό τμήμα περιβάλλεται από ινώδη συνδετικό ιστό, ενώ τα λόβια από χαλαρό αγγειακό στρώμα. Ο μαζικός αδένας περιβάλλεται από λιπώδη ιστό. Τροφοδοτείται από δίκτυο αιμοφόρων και λεμφοφόρων αγγείων και στηρίζεται στον υποδόριο λιπώδη ιστό με δομές γνωστές ως σύνδεσμοι Cooper. Αυτοί οι σύνδεσμοι ξεκινούν από το στρωματικό ιστό του αδένα και εισέρχονται στην περιτονία του θωρακικού μυός και στο δέρμα. Ο μαζικός αδένας που μπορεί να ποικίλει σε σχήμα, μέγεθος και σύσταση συγκλίνει προς τη θηλή. Είναι γενικά συμμετρικός και υπερέχει κυρίως στο άνω έξω τεταρτημόριο του αδένα. Το επιθήλιο των αδενικών κυψελών και των τελικών πόρων είναι μονόστιβο κυβοειδές, το οποίο γίνεται δίστιβο στο θηλασμό. Πέριξ του τοιχώματος των κυψελών και των πόρων υπάρχουν τα μυοεπιθηλιακά κύτταρα, τα οποία υπό την επίδραση της ωκυτοκίνης συσπώνται και προωθούν το γάλα στους μεγαλύτερους πόρους (Hughes et al 1989). Οι μείζονες γαλακτοφόροι πόροι κάτω από τη θηλή επαλείφονται από πολύστιβο πλακώδες επιθήλιο με κερατινοποίηση. Βαθύτερα, το επιθήλιο γίνεται κυβοειδές με παχιά βασική μεμβράνη και συνεχές στρώμα μυοεπιθηλιακών κυττάρων. Από τους μεγαλύτερους πόρους προέρχονται τα θηλώματα, από τον τελικό πόρο και λόβιο (λειτουργική μονάδα του μαστού) τα ιναδενώματα και οι κύστεις, ενώ από το 18
37 ενδολοβιακό τμήμα των τελικών πόρων η μεγάλη πλειοψηφία των καρκίνων του μαστού (Ellis H et al 1993). Σχεδόν όλες οι κακοήθειες του μαστού είναι αδενοκαρκινώματα, ενώ όλοι οι άλλοι τύποι (πλακώδη καρκινώματα, φυλλοειδείς όγκοι, σαρκώματα και λεμφώματα) αποτελούν λιγότερο από 5% του συνόλου (Rosen PP 1997). Τα καρκινώματα διακρίνονται σε in situ και διηθητικά. Το in situ καρκίνωμα περιορίζεται στους πόρους και τα λόβια χωρίς να διασπά τη βασική μεμβράνη αν και σπανίως, καρκινικά κύτταρα μπορούν να επεκταθούν στο δέρμα της θηλής χωρίς να διαπεράσουν τη βασική μεμβράνη και εμφανίζονται κλινικά ως νόσος Paget. Το καρκίνωμα in situ δεν εισβάλλει σε λεμφαγγεία και αιμοφόρα αγγεία και δεν δίνει μεταστάσεις. Το διηθητικό καρκίνωμα διασπά τη βασική μεμβράνη, εισχωρεί στο στρώμα και μπορεί να εισβάλλει σε αγγεία δίνοντας μεταστάσεις σε επιχώριους λεμφαδένες ή απομακρυσμένες περιοχές. Θεωρείται ότι όλα τα καρκινώματα προέρχονται από την τελική πορολοβιακή μονάδα και οι όροι πορογενές και λοβιακό δεν υποδηλώνουν περιοχή ή κυτταρικό τύπο προέλευσης (West M et al 2001). 5.1 Καρκίνωμα In Situ Τις τρείς τελευταίες δεκαετίες ο αριθμός των περιπτώσεων in situ καρκινώματος πόρων έχει αυξηθεί σε πληθυσμούς που υποβάλλονται σε προληπτικό έλεγχο με μαστογραφία από 5% σε 15-30%. Εμφανίζονται στη μαστογραφία ως επασβεστώσεις και λιγότερο συχνά ως πύκνωση. Κλινικά μπορεί να εμφανιστούν ως ψηλαφητή μάζα ή έκκριμα από θηλή. Μπορεί επίσης να αποτελούν τυχαίο εύρημα σε βιοψία που γίνεται για άλλη βλάβη. Τα καρκινώματα in situ είναι κλωνικοί πολλαπλασιασμοί κυττάρων, συνήθως περιλαμβάνουν ένα σύστημα πόρων και λοβίων μέσα στο οποίο περιορίζονται, χωρίς να διασπούν τη βασική μεμβράνη. Τα μυοεπιθηλιακά κύτταρα διατηρούνται, αν και μπορεί να ελαττωθούν σε αριθμό. Ορισμένες φορές τα κύτταρα του in situ καρκινώματος πόρων εξαπλώνονται σε πολλούς πόρους και λόβια και δημιουργούν 19
38 εκτεταμένες βλάβες. Όταν το in situ καρκίνωμα πόρων καταλαμβάνει λόβια, τα βοτρύα παραμορφώνονται και προσομοιάζουν με μικρούς πόρους (Wellings SR 1980) Καρκίνωμα In Situ Πόρων (DCIS, Ενδοπορικό Καρκίνωμα) To DCIS ορίζεται ως ενδοπορική κακοήθεια, η οποία δεν διηθεί τη βασική μεμβράνη και, τουλάχιστον θεωρητικά, δεν μεθίσταται. Δεν θεωρείται άμεσα απειλητικό για τη ζωή της ασθενούς. Μπορεί όμως να μετεξελιχθεί σε διηθητικό ή να έχει εξ αρχής διηθητικό στοιχείο, το οποίο δεν φαίνεται κλινικά ή με συμβατική απεικόνιση. Κατά συνέπεια, η ακριβής ανίχνευση και ο χαρακτηρισμός του DCIS μπορεί τελικά να επηρεάζει την επιβίωση. Το DCIS εμφανίζει μεγάλη βιολογική πολυπλοκότητα. Παραδοσιακά η ταξινόμησή του βασιζόταν σε αρχιτεκτονικά χαρακτηριστικά και χωριζόταν σε δύο κατηγορίες με βάση το αν υπήρχε ή όχι φαγεσωρική νέκρωση. Τα DCIS χωρίς φαγεσωρική νέκρωση περαιτέρω χωριζόταν ηθμοειδή, συμπαγή, θηλώδη και μικροθηλώδη. Αυτή όμως η κατηγοριοποίηση είναι σχετικά υποκειμενική, οδηγεί σε ιστοπαθολογικές ασάφειες και δεν σχετίζεται με το αν υπάρχει τάση υποτροπής ή εξαλλαγής σε διηθητικό καρκίνωμα πόρων (Tsikitis VL et al 2006). H ταξινόμηση που βασίζεται στο βαθμό κακοήθειας του όγκου και την παρουσία ή απουσία νέκρωσης είναι πιο καθοριστική δυνητικής υποτροπής. Έχουν προταθεί πολλά σχήματα κατηγοριοποίησης βασισμένα στο βαθμό κακοήθειας και στην παρουσία ή απουσία νέκρωσης, χωρίς όμως να υπάρχει ένα καθολικά αποδεκτό σχήμα ταξινόμησης. Τα υψηλής και τα χαμηλής κακοήθειας DCIS συμπεριφέρονται με διαφορετικό τρόπο και έχουν διαφορετικά απεικονιστικά χαρακτηριστικά στη μαστογραφία. Το 90% των DCIS που ανιχνεύονται στη μαστογραφία εμφανίζονται ως μικροεπασβεστώσεις, αλλά η όλη βλάβη μπορεί να μην επασβεστώνεται (Kuhl CK 2009). Τα χαμηλής κακοήθειας DCIS τυπικά εμφανίζονται ως άμορφες επασβεστώσεις ενώ τα υψηλής κακοήθειας ως πλειόμορφες και λεπτές γραμμοειδείς επασβεστώσεις. Όμως, υπάρχει μεγάλη αλληλοεπικάλυψη των μαστογραφικών χαρακτηριστικών και ο βαθμός κακοήθειας δεν καθορίζεται από αυτά (Slanetz PJ et al 2001). Τα υψηλής κακοήθειας DCIS εμφανίζονται συχνότερα με επασβεστώσεις, ενώ τα χαμηλής κακοήθειας συχνότερα δεν 20
39 απεικονίζονται και υποεκτιμώνται (Takayuki Y et al 2010). Ο βαθμός υποεκτίμησης είναι μικρότερος στα υψηλής κακοήθειας φαγεσωρικά DCIS από ό,τι στα χαμηλής κακοήθειας μικροθηλώδη και ηθμοειδή DCIS (Kuhl CK et al, 2007). Η εμφάνιση του DCIS ως μάζα είναι δυνατή και μπορεί να οφείλεται είτε άμεσα στον όγκο είτε σε περιπορική ίνωση ή ελάστωση (Silverstein MJ 2000). Μόνο το 30 40% του διηθητικού καρκίνου εμφανίζει επασβεστώσεις. Επειδή το DCIS πιθανόν αποτελεί πρόδρομο του διηθητικού καρκίνου έχει υποστηριχθεί ότι η πλειονότητα των DCIS δεν επασβεστώνεται και δεν ανιχνεύεται μαστογραφικά (Μenell JH et al 2005). Ο καθορισμός του βαθμού κακοήθειας στο DCIS είναι παρόμοιος με αυτόν του διηθητικού καρκινώματος πόρων και διακρίνεται σε υψηλό, μέτριο και χαμηλό. Τα DCIS χαμηλού βαθμού κακοήθειας εμφανίζουν ομοιόμορφα κύτταρα με μικρούς πυρήνες, ελάχιστο πυρηνικό πολυμορφισμό και σπάνιες μιτώσεις. Η κυτταρική πολικότητα σε σχέση με τη βασική μεμβράνη διατηρείται καλά. Τα υψηλού βαθμού κακοήθειας DCIS αποτελούνται από κύτταρα με μεγάλους πλειομορφικούς πυρήνες, συχνές μιτώσεις και φαγεσωρική νέκρωση. Οι βλάβες ενδιάμεσου βαθμού κακοήθειας δεν έχουν χαρακτήρες χαμηλού ή υψηλού βαθμού κακοήθειας (Takayuki Y et al 2010, Mossa-Basha M et al 2010). Πρέπει να σημειωθεί ότι βλάβες με ετερογενή βαθμό κακοήθειας, τυποποιούνται με βάση τον υψηλότερο βαθμό κακοήθειας. To DCIS έχει άριστη πρόγνωση με τη θνησιμότητα 10 ετών μετά από τοπική εξαίρεση ή μαστεκτομή να ανέρχεται στο 2% (Virnig BA et al 2010). Σύμφωνα με τους Kuerer HM et al (2009) όταν το DCIS υποτροπιάζει, στο 50% υποτροπιάζει ως διηθητικός καρκίνος. Ο ρυθμός εξέλιξής του σε διηθητικό καρκίνωμα πόρων αναφέρεται ότι κυμαίνεται από 14% έως 75%. Παράγοντες που αυξάνουν την πιθανότητα υποτροπής είναι η ηλικία (συχνότερη η υποτροπή όταν η διάγνωση γίνει σε νέα γυναίκα), η ύπαρξη παραγόντων αυξημένου κινδύνου για καρκίνο μαστού, η τυποποίηση του αρχικού όγκου ως υψηλής κακοήθειας, η παρουσία νέκρωσης και το μεγάλο μέγεθος της βλάβης. Σπάνια εκδήλωση DCIS αποτελεί η νόσος Paget της θηλής, η οποία εμφανίζεται ως ερυθηματώδης έκθυση της θηλής με λεπιδώδη εφελκίδα, μπορεί να εκληφθεί ως 21
40 έκζεμα και οφείλεται στην εκροή από τη θηλή κακοήθων κυττάρων DCIS (κυττάρων Paget), τα οποία ανιχνεύονται εύκολα με βιοψία ή από τις κυτταρολογικές αναλύσεις του εξιδρώματος. Στο 50% έως 60% των γυναικών με νόσο Paget, συνυπάρχει ψηλαφητή μάζα, η οποία αφορά υποκείμενο διηθητικό καρκίνωμα πόρων. Στη νόσο Paget τα κύτταρα είναι συνήθως ασθενώς διαφοροποιημένα και υπερεκφράζουν HER2/neu (Schelfout VR et al 2000, Kothari AS et al 2002) Καρκίνωμα In Situ Λοβίων (LCIS) Το LCIS αποτελεί τυχαίο εύρημα σε βιοψία που γίνεται για άλλο λόγο, δεδομένου ότι δεν συνδέεται με επασβεστώσεις ή στρωματική αντίδραση που θα έδινε εικόνα πύκνωσης. Είναι αμφοτερόπλευρο στο 20% - 40%, έναντι 10% - 20% στις περιπτώσεις DCIS και από τη στιγμή της διάγνωσης θεωρείται πολυεστιακό. Είναι συχνότερο στις νέες γυναίκες, εμφανίζεται με ίση συχνότητα και στους δύο μαστούς και από ορισμένους δεν θεωρείται αληθινό νεόπλασμα αλλά δείκτης κινδύνου για καρκίνο μαστού. Τα κύτταρά του είναι όμοια με τα κύτταρα του διηθητικού λοβιακού καρκινώματος (ILC), ενώ λείπει και από τα δύο η διαμεμβρανική πρωτείνη E-cadherin, που είναι υπεύθυνη για την επιθηλιακή προσκόλληση των κυττάρων (Hajra KM 2002). Η ιστολογική εμφάνιση των λοβιακών καρκινωμάτων σχετίζεται με την απώλεια έκφρασης της E-cadherin που εδράζεται στο 16q χρωμόσωμα σε γειτονική περιοχή γονιδίου διηθητικού λοβιακού καρκινώματος (ILC), γεγονός που υποδηλώνει ότι το LCIS πιθανόν να αποτελεί πρόδρομο του ILC (Lakhani SR 2001). To LCIS σπάνια καταστρέφει την αρχιτεκτονική του αδένα, είναι σχεδόν πάντα θετικό για υποδοχείς οιστρογόνων και προγεστερόνης και δεν εμφανίζει υπερέκφραση HER2/neu. Γυναίκες με LCIS αναπτύσσουν ILC με συχνότητα παρόμοια με αυτήν των γυναικών με μη θεραπευμένο DCIS. Αν και παλαιότερες μελέτες ανέφεραν ότι και οι δύο μαστοί είχαν τον ίδιο κίνδυνο, πιο σύγχρονες υποστηρίζουν ότι ο σύστοιχος μαστός έχει μεγαλύτερο κίνδυνο (Page DL et al 2003). 5.2 Διηθητικό Καρκίνωμα Μαστογραφικά τα διηθητικά καρκινώματα συνηθέστερα παρουσιάζονται ως πύκνωση. Τα μεγαλύτερα καρκινώματα μπορεί να καθηλωθούν στο θωρακικό τοίχωμα 22
41 ή να προκαλέσουν ρυτίδωση του δέρματος. Η προσβολή των λεμφαγγείων μπορεί να προξενήσει λεμφοίδημα και πάχυνση του δέρματος δίκην φλοιού πορτοκαλιού. Καθήλωση του δέρματος λόγω επινέμησης συνδέσμων Cooper μπορεί να μιμηθεί εμφάνιση φλοιού πορτοκολιού. Όταν ο όγκος εντοπίζεται κεντρικά, μπορεί να αναπτυχθεί εισολκή θηλής. Μέχρι ένας διηθητικός καρκίνος να γίνει ψηλαφητός πάνω από το 50% των ασθενών έχει μεταστάσεις μασχαλιαίων λεμφαδένων. Σπάνια ο διηθητικός καρκίνος του μαστού παρουσιάζεται ως μασχαλιαία λεμφαδενική ή απομακρυσμένη μετάσταση οπότε πρόκειται για μικρό πρωτοπαθές καρκίνωμα μη εμφανές λόγω του υποκείμενου πυκνού μαζικού αδένα. Οι πιο συχνοί ιστολογικοί τύποι διηθητικών καρκινωμάτων του μαστού είναι το πορογενές (IDC) με συχνότητα 85% και το λοβιακό (ILC) με συχνότητα 5 έως 15% (Lakhani SR et al 2012). Το υπόλοιπο ποσοστό καταλαμβάνεται από άλλους σπάνιους τύπους διηθητικών καρκινωμάτων και από σαρκώματα. Σε αυτούς τους τύπους περιλαμβάνονται τα σωληνώδη, τα μυελοειδή και τα βλεννώδη. Το φλεγμονώδες καρκίνωμα του μαστού δεν αντιπροσωπεύει συγκεκριμένο ιστολογικό υποτύπο αλλά διακρίνεται από την ιδιαίτερη κλινική του εικόνα αλλά και από το ότι η θεραπεία του διαφέρει από αυτήν των υπόλοιπων καρκίνων του μαστού. Η αναγνώριση των παραπάνω σπάνιων τύπων καρκίνου του μαστού μπορεί να επηρεάσει σημαντικά τη διαχείριση της νόσου (Dixon JM 1985) Διηθητικό Καρκίνωμα Πόρων (IDC) Τα IDC αποτελούν τα πιο συχνά κακοήθη νεοπλάσματα του μαστού και προέρχονται από το επιθήλιο των πόρων. Έχουν περιγραφεί διάφοροι ιστολογικοί τύποι και από ορισμένους παθολογοανατόμους προσδιορίζονται ως διηθητικά πορογενή καρκινώματα μη ειδικού τύπου, όσα δεν μπορούν να ταξινομηθούν σε οποιαδήποτε άλλη κατηγορία (Νot Otherwise Specified, NOS). Μακροσκοπικά τα περισσότερα είναι συμπαγή και σκληρά, με ανώμαλα όρια και κεντρικά με μικρές εστίες επασβέστωσης. Σπανιότερα είναι καλά περιγεγραμμένα και μαλακά. Τα IDC εμφανίζονται με διάφορες μορφές, είτε καλά διαφοροποιημένα με θετικούς ορμονικούς υποδοχείς, χωρίς υπερέκφραση HER2/neu, είτε αδιαφοροποίητα, με υπερέκφραση HER2/neu και αρνητικούς υποδοχείς. Η πλειοψηφία των IDC βρίσκεται μεταξύ αυτών των δύο άκρων. Τα περισσότερα IDC 23
42 προκαλούν χαρακτηριστικά αυξημένη δεσμοπλαστική αντίδραση που τους προσδίδει σκληρή υφή στην ψηλάφηση ( σκίρρος καρκίνος). Στα IDC συνυπάρχει σε ποικίλο βαθμό DCIS. Ο βαθμός κακοήθειας του DCIS συνήθως συσχετίζεται με το βαθμό κακοηθείας του IDC. Για παράδειγμα το φαγεσωρικό DCIS συνήθως συνδέεται με χαμηλής διαφοροποίησης IDC και τα χαμηλής κακοήθειας DCIS συνδέονται συνήθως με υψηλής διαφοροποίησης IDC. Τα IDC στα οποία συνυπάρχει μεγάλο ποσοστό DCIS απαιτούν ευρείες χειρουργικές εκτομές για να μειωθούν οι τοπικές υποτροπές Διηθητικό Καρκίνωμα Λοβίων (ILC) Στις περισσότερες μελέτες ο διηθητικός λοβιακός καρκίνος (ILC) αποτελεί το 5-15% του συνόλου των καρκίνων του μαστού, ενώ ο διηθητικός καρκίνος των πόρων αποτελεί το 70-90% ( Arpino G et al 2004, Yeatman TJ et al 1995). O ILC προέρχεται από το ενδοθήλιο των λοβίων και ιστοπαθολογικά χαρακτηρίζεται από ομοιόμορφα κύτταρα με στρογγύλους πυρήνες που διατάσσονται μονόστιχα, κατά μήκος των πόρων, προσομοιάζουν δε με τα φυσιολογικά ενδοθηλιακά κύτταρα. (Rakha EA et al 2010). Εμφανίζουν χαμηλό μιτωτικό δείκτη και το πρότυπο ανάπτυξής τους πιθανότατα οφείλεται στην έλλειψη της συγκολλητικής πρωτείνης E- cadherin. Η απουσία της E-cadherin διαπιστώνεται ιστολογικά και βοηθά στη διαφοροδιάγνωση του ILC από το διηθητικό καρκίνο των πόρων (IDC) (Mann RM 2010). Μερικές φορές η επέκταση του IDC στο εσωτερικό ενός λοβίου, η λεγόμενη λοβιακή καρκινοποίηση μπορεί να μιμηθεί ILC. Σ αυτή την περίπτωση η χρώση για την ανίχνευση της Ε-cadherin είναι καθοριστική για τη σωστή διάγνωση. Αποτέλεσμα της απουσίας της E-cadherin είναι η μειωμένη συνοχή των καρκινικών κυττάρων, έτσι ώστε ο καρκίνος να αναπτύσσεται διηθητικά μέσα στο μαζικό αδένα σαν ιστός αράχνης, χωρίς την ανάπτυξη σημαντικής δεσμοπλαστικής αντίδρασης. Για το λόγο αυτό η ανίχνευση του ILC είναι δύσκολη, τόσο κλινικά όσο και απεικονιστικά. Στα ιστολογικά χαρακτηριστικά περιλαμβάνεται και η απουσία επασβεστώσεων, νέκρωσης ή αιμορραγίας ( Schnitt SJ et al 2004, Qureshi HS et al 2006). 24
43 Υπάρχουν δύο τύποι ILC: O κλασσικός και ο πλειόμορφος τύπος, με τον τελευταίο να εμφανίζει μεγαλύτερη προδιάθεση για μεταστάσεις και χειρότερη πρόγνωση από τον κλασσικό τύπο. Αν και δεν υπάρχει ιδιαίτερο γενετικό προφίλ για τον ILC, ένα από τα κύρια γονιδιακά χαρακτηριστικά είναι η απώλεια γενετικού υλικού στο βραχύ σκέλος του χρωμοσώματος 16, που περιλαμβάνει μια ομάδα τουλάχιστον οκτώ γονιδίων αρμόδιων για την προσκόλληση κυττάρων, συμπεριλαμβανομένων των γονιδίων της Ε- cadherin και β-catenin. Το γονίδιο της Ε-cadherin ανιχνεύεται στον ILC και στα χαμηλού βαθμού κακοήθειας (low grade) DCIS (Rakha EA et al 2010, Berx G 2001). Τα βιολογικά χαρακτηριστικά του ILC είναι συνήθως λιγότερο ανησυχητικά από αυτά του IDC: Οι περισσότεροι όγκοι έχουν οιστρογονικούς και προγεστερονικούς υποδοχείς, ενώ η έκφραση των HER2 και του P53 είναι συχνότερα φυσιολογική. Οι μασχαλιαίοι λεμφαδένες συχνά δεν είναι θετικοί, αν και ο ILC είναι συχνά μεγαλύτερος σε μέγεθος από το IDC (Arpino G et al 2004, Li CI et al 2005). Πιθανόν λόγω του προτύπου της διάχυτης διηθητικής ανάπτυξης, ο ILC συχνά δεν ανιχνεύεται στη μαστογραφία (Yeatman TJ et al 1995). Ο ILC συχνά έχει πυκνότητα μικρότερη ή όμοια με αυτή του φυσιολογικού μαζικού αδένα στη μαστογραφία (Yeatman TJ et al 1995, Le Gal M et al 1992). Για τη σωστή θεραπεία του ILC η ακριβής σταδιοποίηση είναι ιδιαίτερα σημαντική. Η μαγνητική μαστογραφία προτείνεται ως εξέταση εκλογής για την εκτίμηση του ILC, αν και μέχρι σήμερα οι μελέτες που έχουν δημοσιευτεί αφορούν μικρές σειρές. Παρόλο που στον ILC υπάρχουν ορισμένοι καλοί προγνωστικοί παράγοντες όπως ο χαμηλός βαθμός κακοήθειας, ο χαμηλός μιτωτικός δείκτης, οι θετικοί ορμονικοί υποδοχείς και η απουσία της υπερέκφρασης του HER2, η διαφορά στο ποσοστό επιβίωσης των ασθενών δεν είναι μεγάλη (Molland JG et al 2004), γεγονός το οποίο μπορεί να οφείλεται στο ότι ο ILC διαγιγνώσκεται σε πιο προχωρημένο στάδιο, συγκριτικά με τον IDC (Yeatman TJ et al 1995). 25
44 5.2.3 Σωληνώδες Καρκίνωμα Είναι ο πιο καλά διαφοροποιημένος τύπος διηθητικού πορογενούς καρκινώματος και αποτελεί λιγότερο από το 5% όλων των καρκίνων του μαστού. Χαρακτηρίζεται από την παρουσία σωληνωδών σχηματισμών, που επαλείφονται από μονόστιβο στοίχο καλά διαφοροποιημένων κυττάρων, με ομοιόμορφους πυρήνες και χαμηλό μιτωτικό δείκτη. Χαρακτηρίζεται από άφθονο κυτταρόπλασμα και έντονη δεσμοπλαστική αντίδραση, συχνά με κεντρική ουλή, προς την οποία προσανατολίζονται ακτινωτά τα σωληνάρια. Ιστολογικά η διάκριση από την ακτινωτή ουλή την οποία και μιμείται, μπορεί να γίνει από την απουσία των μυοεπιθηλιακών κυττάρων στη βασική μεμβράνη των σωληναρίων του σωληνώδους καρκινώματος. Συχνά συνδυάζεται με μη νεκρωτικό πορώδες καρκίνωμα in situ (Mitnik JS 1999). Ο όγκος είναι συχνά μικρός (συνήθως μικρότερος του ενός εκατοστού) και αργούς εξέλιξης. Με τη χρήση της προληπτικής μαστογραφίας η ανίχνευση του καρκινώματος είναι ευκολότερη. Τόσο στη μαστογραφία, όσο και μακροσκοπικά το σωληνώδες καρκίνωμα μπορεί να μιμείται καλοήθη βλάβη όπως ακτινωτή ουλή ή σκληρυντική αδένωση. Μαστογραφικά συχνά απεικονίζεται ως μικρή μάζα με μακριές ακτινοειδείς προσεκβολές. Στην MR μαστογραφία εμφανίζει μετρίου ή χαμηλού βαθμού εμπλουτισμό μετά τη χορήγηση σκιαστικού. Οι μεταστάσεις στη μασχάλη δεν είναι συνήθεις και η πρόγνωσή του θεωρείται εξαιρετική με 95% πενταετή επιβίωση. Η συνύπαρξη καρκίνου στον άλλο μαστό είναι αρκετά συνήθης (12-40%), ενώ η βλάβη είναι πολυεστιακή στο 28% των περιπτώσεων. Περισσότερο από το 95% των σωληνωδών καρκινωμάτων είναι διπλοειδή και εκφράζουν ορμονικούς υποδοχείς (Wagner TD et al 2008) Μυελοειδές Καρκίνωμα Τά μυελοειδή καρκινώματα, αποτελούν το 2% έως το 10% του συνόλου των διηθητικών καρκινωμάτων, παρατηρούνται κυρίως σε νεότερες γυναίκες (Tominaga J et al 2009). Το 11% των καρκίνων μαστού σε γυναίκες κάτω των 35 ετών είναι μυελοειδούς τύπου. Είναι ταχέως αναπτυσσόμενοι όγκοι που τυπικά παρουσιάζονται ως ψηλαφητή μάζα σε νέες ή μέσης ηλικίας γυναίκες(yoo JL et al 2010). Μακροσκοπικά είναι μαλακοί όγκοι, με ομοιογενή εμφάνιση, σχετικά καλά περιγεγραμμένοι. Μικροσκοπικά τα κύτταρά τους έχουν πλειόμορφους πυρήνες με πολλές μιτώσεις, και συχνά εμφανίζουν διηθήσεις από λεμφοπλασματοκύτταρα μέσα και γύρω από τον 26
45 όγκο. Ετσι μικροσκοπικά με την πρώτη ματιά το μυελοειδές καρκίνωμα προσομοιάζει με ένα επιθετικό διηθητικό καρκίνωμα των πόρων IDC. Τα όρια του όγκου είναι ομαλά και στην περιφέρειά του μπορεί να υπάρχουν λίγες εστίες DCIS. Υπάρχει σημαντική διαφορετικότητα στην ιστολογική διάγνωση του μυελοειδούς καρκινώματος γεγονός που εξηγεί την ποικίλη έκβαση του ασθενούς. Τo άτυπο μυελοειδές καρκίνωμα που εμφανίζει μερικούς από τους χαρακτήρες του μυελοειδούς αποτελεί αμφιλεγόμενη οντότητα(liberman L et al 1996). Όλα τα μυελοειδή καρκινώματα αν και ασθενώς διαφοροποιημένα δεν εμφανίζουν λεμφαγγειακές ή αγγειακές διηθήσεις. Oι προγνωστικοί παράγοντες που τα χαρακτηρίζουν είναι κακοί, όπως ο υψηλός βαθμός πυρηνικής κακοήθειας, η ανευπλοειδία, η απουσία ορμονικών υποδοχέων και ο υψηλός μιτωτικός δείκτης. Αντίθετα δεν εμφανίζουν υπερέκφραση του HER2/neu και δεν παρουσιάζουν συχνές λεμφαδενικές μεταστάσεις. Οι γυναίκες που είναι φορείς μεταλλαγμένου γονιδίου BRCA1 στο 13% αναπτύσσουν μυελοειδές καρκίνωμα. Παρ όλα αυτά, τα περισσότερα μυελοειδή καρκινώματα δεν συνδέονται άμεσα με μεταλλάξεις του γονιδίου BRCA1. Όμως, το 67% των μυελοειδών καρκίνων εμφανίζει υπερμεθυλίωση άλλου γονιδίου που σχετίζεται με το BRCA1(Ian PT et al 2004). Μαστογραφικά, το μυελοειδές καρκίνωμα τυπικά απεικονίζεται ως στρογγύλη ή ωοειδής καλά περιγεγραμμένη μάζα χωρίς επασβεστώσεις, συχνά ψηλαφητή (Yoo JL et al 2010) Βλεννώδες (Κολλοειδές) Καρκίνωμα Το βλεννώδες ή κολλοειδές καρκίνωμα αποτελεί το 1-3% του συνόλου των IDC με μικροσκοπική εικόνα που χαρακτηρίζεται από νησίδες καρκινικών κυττάρων που επιπλέουν σε λίμνη άφθονης βλέννας. Σαν αποτέλεσμα στη μαστογραφία, το αμιγές βλεννώδες καρκίνωμα που περιέχει μεγάλη ποσότητα βλέννας εμφανίζεται σαν χαμηλής πυκνότητας μάζα με αρκετά σαφές περίγραμμα, ενώ στην MR μαστογραφία απεικονίζεται με υψηλό σήμα στις Τ2 εικόνες και με ετερογένεια σήματος στις Τ1 εικόνες (Yoo JL et al 2010). Ο μικτός τύπος βλεννώδους καρκινώματος μπορεί να έχει ασαφή ή δοκιδωτή παρυφή. Τα βλεννώδη καρκινώματα είναι όγκοι καλά αφορισμένοι, με επιφάνεια λεία και κολλοειδή, αναπτύσσονται αργά, μπορεί να προσλάβουν μεγάλες διαστάσεις και εμφανίζονται συχνότερα σε γυναίκες μεγαλύτερης ηλικίας (Monzawa S et al 2009). Είναι μαλακός όγκος στην ψηλάφηση και μπορεί στην κλινική εξέταση να εκληφθεί ως καλοήθης. Ο αμιγής τύπος 27
46 χαρακτηρίζεται από καλοήθη βιολογική συμπεριφορά, εκφράζει ορμονικούς υποδοχείς και δεν εμφανίζει ανευπλοειδίες. Ο μικτός τύπος εμφανίζει πρόγνωση ίδια με των διηθητικών καρκινωμάτων χωρίς άλλα ειδικά χαρακτηριστικά (NOS). Η επίπτωση των βλεννωδών καρκίνων είναι ελαφρώς υψηλότερη στις γυναίκες με μεταλλάξεις στο γονίδιο BRCA1. Αντίστοιχα με τους μυελοειδείς καρκίνους το 55% των βλεννωδών καρκίνων εμφανίζει υπερμεθυλίωση άλλου γονιδίου που σχετίζεται με το BRCA1 (Ian PT et al 2004) Θηλώδες Καρκίνωμα Είναι σπάνια μορφή καρκινώματος και αποτελεί το 1-2% του συνόλου των καρκίνων του μαστού. Εμφανίζεται σε μεγαλύτερες σε ηλικία ασθενείς με μέση ηλικία τα 65 έτη, αργό ρυθμό ανάπτυξης και μπορεί να είναι μονήρες ή πολλαπλό. Χαρακτηρίζεται από δύο τύπους, το συμπαγή και τον κυστικό που μπορεί να αναπτυχθεί μέσα σε διατεταμένο λόβιο ή πόρο. Το θηλώδες καρκίνωμα που εμφανίζεται ενδοκυστικά (μέσα σε κύστη) συνήθως είναι μη διηθητικού τύπου. Το διηθητικό θηλώδες καρκίνωμα συνήθως αναπτύσσεται σε κεντρικό τμήμα του μαστού και σε περισσότερο από το 1/3 των περιπτώσεων υπάρχει αιμορραγικό έκκριμα από την θηλή. Το θηλώδες καρκίνωμα στην ψηλάφηση του μαστού είναι σφαιρικό, συχνά με λοβωτή παρυφή και μεγάλο μέγεθος λόγω του κυστικού στοιχείου. Στη μαστογραφία το θηλώδες καρκίνωμα εμφανίζεται ως στρογγύλο, ακτινοσκιερό μόρφωμα με ομαλή ή λοβωτή παρυφή και σαφή όρια. Στην MR μαστογραφία ο όγκος αν είναι συμπαγής εμφανίζεται σαν ετερογενής καλά περιγεγραμμένη μάζα με πρόσληψη παραμαγνητικής ουσίας, ενώ αν είναι κυστικός εμφανίζει τοιχωματική οζώδη πρόσληψη του σκιαστικού (Soo MS et al 1995). Το θηλώδες καρκίνωμα έχει ευνοϊκότερη πρόγνωση από το διηθητικό καρκίνωμα των πόρων (NOS) Μεταπλαστικό Καρκίνωμα Συνήθως εκδηλώνεται σαν μεγάλη ψηλαζητή μάζα σε γυναίκες μεγαλύτερες των 55 ετών. Στα μικροσκοπικά χαρακτηριστικά περιγράφονται δύο κύριοι τύποι, ο πλακώδης, που διατηρεί τον επιθηλιακό χαρακτήρα του όγκου, και ο ψευδοσαρκωματώδης με ποικίλη κυτταρική σύσταση και μεσεγχυματικά νεοπλασματικά στοιχεία. Συνήθως δεν υπάρχουν ειδικά απεικονιστικά ευρήματα αλλά 28
47 λόγω της ταχείας τους ανάπτυξης, μπορεί να εμφανιστεί ως μεγάλη μάζα στο μαστό συνήθως καλά περιγεγραμμένη που μπορεί να έχει οστεοποίηση. Μερικά από αυτά τα καρκινώματα εκφράζουν κοινά γονίδια με τα μυοεπιθηλιακά κύτταρα και πιθανόν προέρχονται από αυτά. Λόγω της ετερογένειας αυτών των όγκων και της σπανιότητάς τους δεν υπάρχουν επαρκείς πληροφορίες σχετικά με τα κλινικά τους γνωρίσματα και την πρόγνωσή τους (Reis- Filho JS et al 2003). Αναφέρεται πρόγνωση παρόμοια με του διηθητικού καρκινώματος υψηλού βαθμού κακοήθειας(rayson D et al 1999). Το μεταπλαστικό καρκίνωμα αποτελεί ποσοστό μικρότερο του 1% του συνόλου των IDC, και έχει σε μικρότερο ποσοστό θετικούς ορμονικούς υποδοχείς. Το καρκίνωμα εξ ατρακτοειδών κυττάρων (spindle cell carcinoma) αποτελεί υποτύπο του μεταπλαστικού καρκινώματος Αποκρινές Καρκίνωμα Τα αποκρινή καρκινώματα είναι ασυνήθη και εμφανίζουν μορφολογία παρόμοια με αυτών των κυττάρων των αποκρινών αδένων του δέρματος χωρίς όμως ιδιαίτερους κλινικούς ή απεικονιστικούς χαρακτήρες. Η πρόγνωσή τους είναι παρόμοια των διηθητικών καρκινωμάτων (NOS). Tο φαινόμενο της αποκρινούς μεταπλασίας παρατηρείται και σε καλοήθεις καταστάσεις του μαστού, όπως κύστεις, ιναδενώματα και στη σκληρυντική αδένωση(rosen PP 1997) Αδενοκυστικό Καρκίνωμα Ο όγκος αυτός αποτελεί σπάνιο τύπο αδενοκαρκινώματος και εμφανίζεται σε ποσοστό μικρότερο του 0,1% του συνόλου των καρκινωμάτων του μαστού. Είναι συνηθέστεροι σε μεγάλες γυναίκες και παρουσιάζονται τόσο κλινικά όσο και απεικονιστικά, συνήθως ως μάζα με ασαφές περίγραμμα. Στο μικροσκόπιο τα χαρακτηριστικά του όγκου προσομοιάζουν με αυτά του αδενοκυστικού καρκινώματος που παρατηρείται στους σιελογόνους αδένες. Χαρακτηριστικό των όγκων αυτών είναι η τάση να διηθούν τα νεύρα. Πολύ συχνά εντοπίζεται στην υποθηλαία περιοχή. Αναφέρονται μεμονωμένες περιπτώσεις σε άνδρες και παιδιά. Οι περισσότεροι όγκοι είναι αρνητικοί σε οιστρογονικούς και προγεστερονικούς υποδοχείς (ER/PR) (Arpino G et al 2002). 29
48 Οι απομακρυσμένες μεταστάσεις είναι ασυνήθεις με συχνότερη θέση τον πνεύμονα. Οι λεμφαδενικές μεταστάσεις στη μασχάλη είναι σπάνιες. Η πρόγνωσή του είναι πολύ καλή αν εξαιρεθεί πλήρως χειρουργικά(mc Clenathan JH 2002) Νόσος Paget Αποτελεί σπάνια κακοήθεια η οποία περιγράφηκε πρώτα από τον Sir James Pajet το 1874, και συνίσταται στο 1-3% όλων των καρκίνων του μαστού. Αποτελεί λιγότερο από 5% των καρκίνων μαστού στους άνδρες και συνδυάζεται με σύνδρομο Klinefelter. Στις περισσότερες περιπτώσεις υπάρχει υποκείμενη κακοήθεια, είτε DCIS είτε διηθητικό καρκίνωμα. Κλινικά εμφανίζεται με έκζεμα της θηλής ή της θηλαίας άλω. Κατά την εξέλιξη της νόσου μπορεί να υπάρχει έκκριμα από τη θηλή με συνοδό εξέλκωση αυτής. Η εκζεματοειδής απεικόνιση προκαλείται από εμφύτευση καρκινικών κυττάρων προδιηθητικού ή διηθητικού πορογενούς καρκινώματος στο σύμπλεγμα θηλής- θηλαίας άλω (Burke ET 1998). Μαστογραφικά πολλές φορές δεν υπάρχουν απεικονιστικά ευρήματα, ενώ η MR μαστογραφία αναδεικνύει την ακριβή έκταση της νόσου. Η πρόγνωση είναι πολύ καλή όταν υπάρχει μόνο DCIS, ενώ καθορίζεται από το στάδιο του διηθητικού καρκίνου όταν αυτό συνυπάρχει (Ikeda DM 1993) Φλεγμονώδες Καρκίνωμα Tο φλεγμονώδες καρκίνωμα του μαστού αποτελεί επιθετική μορφή καρκινώματος σε ποσοστό μικρότερο του 1% των καρκίνων του μαστού. Κλινικά χαρακτηρίζεται από οίδημα, ερυθρότητα, θερμότητα και διάχυτη πάχυνση δέρματος με όψη δίκην φλοιού πορτοκαλιού. Επίσης εμφανίζει αυξημένη πάχυνση της δοκίδωσης του υποδορίου ιστού και του μαζικού παρεγχύματος που οφείλεται σε καρκινωματώδη διήθηση των λεμφαγγείων (Dawood S et al 2011). Η βιοψία του δέρματος συχνά εμφανίζει νεοπλασματικά έμβολα στα λεμφαγγεία. Συγχέεται κλινικά με μαστίτιδα λόγω των παρόμοιων κλινικών χαρακτηριστικών, σε αντίθεση όμως με αυτήν δεν απαντάει στα αντιβιοτικά. Ως εκ τούτου, αν υπάρχει υποψία φλεγμονώδους καρκίνου, η χειρουργική βιοψία συμπεριλαμβανομένης και της βιοψίας του δέρματος, είναι επιβεβλημένη. Μαστογραφικά το φλεγμονώδες καρκίνωμα εμφανίζει πάχυνση του δέρματος, ως και διάχυτη αύξηση της πυκνότητας και της δοκίδωσης του μαστού. Μπορεί ωστόσο να εμφανίσει απεικονιστικά ευρήματα καρκίνου όπως μάζα, ασύμμετρη σκίαση, μικροεπασβεστώσεις, έλξη της θηλής ή μασχαλιαία 30
49 λεμφαδενοπάθεια ( Kushwaha AC 2000). Στην MR μαστογραφία εμφανίζει έντονο πρώιμο εμπλουτισμό μετά τη χορήγηση παραμαγνητικής ουσίας και αιμοδυναμική συμπεριφορά καμπύλης τύπου ΙΙΙ. Επίσης μπορεί να απεικονιστεί ο εμπλουτισμός του δέρματος. Ο συνήθης θεραπευτικός σχεδιασμός αφού προηγηθεί βιοψία, είναι προεγχειρητική χημειοθεραπεία με πιθανότητα χειρουργικής εξαίρεσης σε δεύτερο χρόνο, ακτινοθεραπεία ή συνδυασμός των παραπάνω. Η πρόγνωση του όγκου αυτού είναι ιδιαίτερα δυσμενής ( Hance KW et al 2005) Τριπλά αρνητικοί καρκίνοι μαστού Οι τριπλά αρνητικοί καρκίνοι μαστού δεν εκφράζουν οιστρογονικούς υποδοχείς (ER) ή προγεστερονικούς υποδοχείς (PR) και δεν εμφανίζουν υπερέκφραση του γονιδίου για τον υποδοχέα του επιδερμικού αυξητικού παράγοντα τύπου-2 (HER2). Επειδή αυτός ο ορισμός είναι αφαιρετικός, οι τριπλά αρνητικοί καρκίνοι πιθανότατα αντιπροσωπεύουν μια ετερογενή ομάδα καρκίνων. Πρόσφατες μελέτες γενετικού προφίλ ανέδειξαν τέσσερεις διαφορετικούς υποτύπους καρκίνου του μαστού: τους luminal A και Β, τον HER2 και τον basal like (Martincich L et al, 2012). Οι luminal A και Β τύποι είναι θετικοί για υποδοχείς ορμονών και έχουν καλύτερη πρόγνωση από τους άλλους τύπους. Οι HER2 και basal like τύποι είναι πιο επιθετικοί. Δεν υπάρχει συμφωνία για τον καθορισμό ενός καρκίνου basal like αλλά ο τριπλά αρνητικός καρκίνος θεωρείται ότι αντιπροσωπεύει τον basal like τύπο. Οι τριπλά αρνητικοί καρκίνοι αποτελούν το 7% έως 15% όλων των καρκίνων του μαστού (Boisserie Lacroix M et al 2012). Είναι συχνότεροι στις προεμμηνοπαυσιακές Αφροαμερικανές γυναίκες (Krizmanich-Conniff KM et al 2012) και σχετίζονται με γυναίκες παχύσαρκες και μικρότερης ηλικίας (Eiermann W et al 2012). Αποτελούν περίπου το 70% των καρκίνων σε γυναίκες που είναι θετικές για το γονίδιο BRCA1 (Boisserie Lacroix M et al 2012). Οι τριπλά αρνητικοί καρκίνοι εμφανίζουν επιθετικά ιστολογικά χαρακτηριστικά, έχουν υψηλό βαθμό κακοήθειας και υψηλό μιτωτικό δείκτη (Chen JH et al 2007). Γενικά έχουν κακή πρόγνωση, δεν αποκρίνονται στη συνήθη ορμονική θεραπεία, αποκρίνονται όμως στη συμβατική χημειοθεραπεία. Μεθίστανται πρώιμα στον εγκέφαλο και στον πνεύμονα και σπανιότερα στα οστά, υποτροπιάζουν δε 31
50 πρώιμα εντός δύο ή τριών ετών. Παρ όλα αυτά μετά την πενταετία ο κίνδυνος απομακρυσμένων μεταστάσεων είναι χαμηλός (Eiermann W et al 2012). 32
51 6 ΑΠΕΙΚΟΝΙΣΗ ΤΟΥ ΜΑΣΤΟΥ ΜΑΓΝΗΤΙΚΗ ΜΑΣΤΟΓΡΑΦΙΑ (MRΜ) Ο καρκίνος του μαστού αποτελεί μεγάλο πρόβλημα για το γυναικείο πληθυσμό. Υπολογίστηκε ότι αποτέλεσε το αίτιο θανάτων το 2003 για τις Αμερικανίδες. Σε αντίθεση με άλλους τύπους καρκίνων, μεταξύ των γυναικών υπάρχει ικανοποιητικός βαθμός επίγνωσης του κίνδυνου που εγκυμονεί ο καρκίνος του μαστού και αυτό οφείλεται τόσο σε υγειονομικά προγράμματα ενημέρωσης που προάγουν τον προληπτικό έλεγχο, όσο και σε εκτεταμένη κάλυψη του θέματος από τα μέσα μαζικής ενημέρωσης, αλλά και στην άμεση πληροφόρηση από φιλικό και συγγενικό περιβάλλον. Η ψηφιακή μαστογραφία που αποτελεί άριστο εργαλείο πρόληψης, αποδίδει ψευδώς αρνητικά στοιχεία που κυμαίνονται από 10% έως 25%, ανάλογα με τη συγκεκριμένη μελέτη. Κάθε χρόνο εκατοντάδες γυναίκες που συμμετέχουν στον προληπτικό έλεγχο εφησυχάζουν ψευδώς με βάση τα αποτελέσματα της ψηφιακής μαστογραφίας. Επιπλέον η ψηφιακή μαστογραφία εμφανίζει περιορισμούς ως προς τη δυνατότητά της να εκτιμήσει με ακρίβεια την έκταση της νόσου στο μαστό στις γυναίκες που πρόκειται να υποβληθούν σε θεραπεία. Για παράδειγμα, υποεκτιμά την έκταση ενός λοβιακού καρκινώματος σε πάνω από το 25% των περιπτώσεων. Κάτω από αυτές τις συνθήκες, το ενδιαφέρον εστιάζεται στη μαγνητική μαστογραφία (MRΜ) που αποτελεί πολύτιμο συμπληρωματικό διαγνωστικό εργαλείο. Η MRM υψηλού μαγνητικού πεδίου (3T) ανοίγει νέους ορίζοντες όσον αφορά στην αποτελεσματικότερη ανίχνευση και χαρακτηρισμό των εξεργασιών του μαστού. Η MRM εφαρμόζεται ολοένα και περισσότερο σαν συμπληρωματική διαγνωστική μέθοδος στην ψηφιακή μαστογραφία και στον υπέρηχο. Την τελευταία δεκαετία χρησιμοποιείται όλο και πιο πολύ για τη διάγνωση των παθήσεων του μαστού. Οι κυριότερες ενδείξεις της MRM περιλαμβάνουν: Διαφορική διάγνωση χειρουργικής ουλής από υποτροπή καρκίνου του μαστού που χειρουργήθηκε. 33
52 Προληπτικό έλεγχο (sreening) σε γυναίκες υψηλού κινδύνου για ανάπτυξη καρκίνου του μαστού (γυναίκες με μετάλλαξη των γονιδίων BRCA 1, BRCA 2. ) Παρουσία μεταστάσεων στη μασχάλη, σε γυναίκες με φυσιολογική ψηφιακή μαστογραφία και υπερηχογράφημα. Eκτίμηση της ανταπόκρισης στη χημειοθεραπεία που εφαρμόζεται προεγχειρητικά, κυρίως σε μεγάλους σε μέγεθος καρκίνους. Ανάδειξη σε διαγνωσμένο καρκίνο μαστού επιπρόσθετων εστιών καρκίνου στον ίδιο μαστό ή σύγχρονου καρκίνου στον άλλο μαστό. Το ποσοστό ανίχνευσης επιπρόσθετης εστίας καρκίνου στον ίδιο μαστό ανέρχεται στο 15% (πολυεστιακός ή πολυκεντρικός καρκίνος), ενώ το ποσοστό ανίχνευσης επιπρόσθετης εστίας καρκίνου στον άλλο μαστό ανέρχεται στο 5%. Ανάδειξη καρκίνων που εντοπίζονται πολύ κοντά στο θωρακικό τοίχωμα και εκτίμηση τυχόν διήθησης του θωρακικού τοιχώματος. Εκτίμηση τυχόν ρήξεως προθεμάτων σιλικόνης. Η MRM παρουσιάζει υψηλή ευαισθησία που είναι πάνω από 90% και σε εξειδικευμένα κέντρα φθάνει το 100%. Οι τελευταίες εξελίξεις στην MRM προσπαθούν να γεφυρώσουν την απόσταση ανάμεσα στην ευαισθησία και την ειδικότητα, με βάση τις διαφορές των κακοήθων και καλοήθων όγκων από το φυσιολογικό αδενικό ιστό, όσον αφορά τα δομικά και βιοχημικά τους χαρακτηριστικά. Στους περιορισμούς της MRM περιλαμβάνεται η αδυναμία εκτέλεσής της σε ασθενείς: Που έχουν βηματοδότη. Που φέρουν μεταλλικές προθέσεις. Που έχουν κλειστοφοβία. Που εμφανίζουν αλλεργία στο σκιαστικό. 34
53 6.1 Βασικές αρχές μεθόδου Η τελειοποίηση του πρωτοκόλλου της MRM που έχει στόχο αφ ενός μεν βέλτιστη ποιότητα εικόνας και αφ ετέρου ικανή ταχύτητα λήψης δεδομένων, έχει επιτευχθεί με αλλεπάλληλες τροποποιήσεις των τεχνικών ανάκτησης της εικόνας, των τύπων των παλμικών ακολουθιών και των παραμέτρων των ακολουθιών αυτών. Με γνώμονα τη μεγιστοποίηση της διαγνωστικής ακρίβειας λαμβάνονται υπ όψιν και οι θεμελιώδεις τεχνικοί περιορισμοί που επηρεάζουν τη χωρική διακριτικότητα (spatial resolution), τον τρόπο λήψης των δεδομένων και το λόγο σήματος προς θόρυβο(snr). Κοινός παρονομαστής όλων των επί μέρους προσπαθειών για την τελειοποίηση του πρωτοκόλλου της MRΜ είναι ο βέλτιστος «χειρισμός» του μαγνητικού σήματος που δίδουν τα πρωτόνια του υδρογόνου των ιστών. Το ισχυρό μαγνητικό πεδίο του ΜR μηχανήματος (κύριο μαγνητικό πεδίο Β0) έχει διεύθυνση τον οριζόντιο άξονα z. Το επίπεδο που είναι κάθετο στο Β0 είναι το εγκάρσιο επίπεδο που ορίζεται από τους άξονες x και y. Υπό την επίδραση του μαγνητικού πεδίου Β0, τα πρωτόνια των ιστών λειτουργούν ως μικροσκοπικοί μαγνήτες και προσανατολίζονται παράλληλα ή αντιπαράλληλα στη διεύθυνση z, ενώ ταυτόχρονα αποκτούν εγκάρσια μαγνήτιση, διότι επιτελούν περιστροφική κίνηση με συχνότητα W0 = B0 X γ (εξίσωση Larmor, όπου γ είναι η γυρομαγνητική σταθερά, χαρακτηριστική των πρωτονίων ενός ιστού). Επειδή ορισμένα πρωτόνια προσανατολίζονται παράλληλα με το Β0 και ορισμένα αντιπαράλληλα, τα μικρά τους μαγνητικά πεδία αλληλοαναιρούνται και παραμένει μικρό ποσοστό πρωτονίων παράλληλα προσανατολισμένων με το Β0, με αποτέλεσμα ένα ποσό καθαρής μαγνήτισης. Αυτή τη μαγνήτιση διαχειρίζονται οι ακολουθίες παλμών και λαμβάνονται τα MR σήματα που είναι διαφορετικά για κάθε είδους ιστό. Ενέργεια με τη μορφή ραδιοσυχνότητας (παλμός RF) μεταβιβάζεται διακοπτόμενα στα πρωτόνια των ιστών που βρίσκονται στο πεδίο B0. Αυτά συντονίζονται και απορροφούν αυτή την ενέργεια, με την προϋπόθεση η συχνότητα του RF παλμού να είναι κοντά στη συχνότητα W0 της περιστροφής τους. Σαν αποτέλεσμα, η καθαρή μαγνήτιση εκτρέπεται από τη διεύθυνση z. 35
54 Η εκτροπή σε μοίρες χαρακτηρίζει τον RF παλμό (π. χ. παλμός 90 μοιρών ή παλμός 180 μοιρών). Μόλις διακοπεί ο RF παλμός, τα πρωτόνια επανέρχονται στην αρχική τους διεύθυνση z (χαλαρώνουν), αποδίδοντας την ενέργεια που είχαν λάβει από την απορρόφηση της ενέργειας του RF παλμού. Υπάρχουν δύο τύποι χαλάρωσης: Τ1 και Τ2. Τ1 χαλάρωση ή επιμήκης χαλάρωση είναι η επάνοδος στη διεύθυνση z και απαιτεί για να επιτευχθεί χρονικό διάστημα (σε msec) που ονομάζεται χρόνος Τ1- χαλάρωσης. Οι εικόνες που βασίζονται σε αυτούς τους χρόνους (διαφορετικούς για τα πρωτόνια διαφορετικών ιστών) λέγονται Τ1 εικόνες. Ιστοί με μικρούς Τ1 χρόνους δίνουν υψηλό σήμα στις Τ1 εικόνες. Ο Τ1 χρόνος των υγρών είναι μεγαλύτερος από τον Τ1 χρόνο του ιναδενικού ιστού και γι αυτό οι κύστεις είναι πιο σκούρες από τον ιναδενικό ιστό. Ο χρόνος Τ1 των πρωτονίων ενός ιστού εξαρτάται τόσο από τη δύναμη του εξωτερικού μαγνητικού πεδίου όσο και από τους ιστούς που γειτνιάζουν με το συγκεκριμένο ιστό. Τ2 χαλάρωση ή εγκάρσια χαλάρωση είναι ο χρόνος που απαιτείται για το μηδενισμό της εγκάρσιας μαγνήτισης, την οποία αποκτούν τα πρωτόνια μετά από ένα RF παλμό 90 μοιρών. Η εγκάρσια μαγνήτιση οφείλεται στο ότι τα πρωτόνια επιτελούν περιστροφική κίνηση (spin) μετά την εκτροπή τους στο εγκάρσιο επίπεδο. Η εγκάρσια μαγνήτιση δίδει σήμα που προσλαμβάνεται από το RF πηνίο. Αμέσως μετά τον παλμό των 90 μοιρών τα πρωτόνια είναι συμφασικά και το MR σήμα είναι υψηλό. Καθώς τα πρωτόνια χάνουν τη συμφασικότητά τους το MR σήμα εξασθενίζει. Οι παράγοντες που είναι υπεύθυνοι για την Τ2 μαγνήτιση είναι οι αλληλεπιδράσεις των περιστρεφόμενων πρωτονίων μεταξύ τους (spin-spin), οι ανομοιογένειες του μαγνητικού πεδίου, η χημική απόκλιση (chemical shift) και η μαγνητική επιδεκτικότητα. Ο ρυθμός μείωσης του σήματος που οφείλεται μόνο στις αλληλεπιδράσεις των περιστρεφόμενων πρωτονίων μεταξύ τους ονομάζεται Τ2 χρόνος (Dixon RL and Ekstrand KE, 1982). Η τεχνική που εκμηδενίζει όλους τους παράγοντες που συντελούν και διαμορφώνουν την Τ2 μαγνήτιση, πλην τις spin-spin αλληλεπιδράσεις είναι η τεχνική Spin Echo (SE) (Patz S, 1986, Kressel HY, 1984, Koutcher JA et al 1984). 36
55 Διαφορετικοί ιστοί έχουν διαφορετικούς χρόνους χαλάρωσης Τ2, πάνω στους οποίους βασίζεται η λήψη Τ2 εικόνων. Σ αυτές τις εικόνες ιστοί με μεγάλο χρόνο Τ2 έχουν υψηλότερο σήμα. Έτσι οι κύστεις είναι πιο άσπρες από τον ιναδενικό ιστό στις Τ2 εικόνες. Oι ακολουθίες παλμών εκμεταλλεύονται τους διαφορετικούς χρόνους χαλάρωσης T1 και Τ2 των διάφορων ιστών και διαχειρίζονται την καθαρή μαγνήτιση με τρόπο που να επιτυγχάνεται η λήψη εικόνας. Υπάρχουν διάφοροι τύποι παλμικών ακολουθιών ανάμεσα στους οποίους περιλαμβάνονται οι παλμικές ακολουθίες Spin Echo (SE), Fast Spin Echo (ή turbo spin echo) και Gradient Echo. Κάθε παλμική ακολουθία έχει παραμέτρους που ρυθμίζονται ώστε η εικόνα να έχει την καλύτερη δυνατή ποιότητα. Για τη χαρτογράφηση των διάφορων τύπων παλμικών ακολουθιών χρησιμοποιούνται διαγράμματα που αναδεικνύουν τα κύρια χαρακτηριστικά κάθε παλμικής ακολουθίας. Στην παλμική ακολουθία SE (Spin Echo) για παράδειγμα, όπως φαίνεται στο Σχήμα 6. 1, ο οριζόντιος άξονας είναι ο άξονας του χρόνου. Η πρώτη γραμμή δείχνει πότε εφαρμόζονται οι RF παλμοί. Φαίνεται ότι χρησιμοποιείται παλμός 90 μοιρών και παλμός 180 μοιρών. Στη δεύτερη γραμμή φαίνεται η εγκάρσια μαγνήτιση, η οποία αποτελεί το MR σήμα και μετράται από το δεκτικό RF πηνίο. Ο παλμός 90 μοιρών παράγει εγκάρσια μαγνήτιση που μειώνεται λόγω αποσυντονισμού των spin συναρτήσει του χρόνου και ο παλμός 180 μοιρών αντιστρέφει σαν ηχώ την εγκάρσια μαγνήτιση, καταργώντας όλες τις επιδράσεις που την επηρεάζουν πλην των αλληλεπιδράσεων μεταξύ πρωτονίων (spin-spin). Έτσι παράγεται η ηχώ του spin (ακολουθία Spin Echo SE). Οι γραμμές 3, 4 και 5 του Σχήματος 6. 1 δείχνουν τη λειτουργία του βαθμιδωτού μαγνητικού πεδίου που χρησιμοποιείται για να διαιρέσει το MR σήμα σε εικόνες τομών και στοιχειώδεις εικόνες (pixels) ή στοιχειώδεις όγκους (voxels). Τρία βαθμιδωτά πεδία είναι υπεύθυνα για την κατάτμηση του σήματος στις 37
56 τρεις ορθογώνιες διευθύνσεις του χώρου. Αυτά τα βαθμιδωτά πεδία ονομάζονται βαθμίδωση επιλογής τομής, βαθμίδωση συχνότητας και βαθμίδωση φάσης. Σχήμα 6.1 Το διάγραμμα της Spin Echo (SE) ακολουθίας δείχνει τους σχετικούς χρόνους κατά τους οποίους λαμβάνουν χώρα τα διάφορα γεγονότα, κατά τη διάρκεια της απόκτησης δεδομένων. Δείχνει επίσης το χρόνο που χορηγούνται οι RF παλμοί, το σήμα που σχηματίζεται από τους παλμούς αυτούς και χρόνους εφαρμογής των βαθμιδωτών μαγνητικών πεδίων. Η εφαρμογή ενός παλμού 90 μοιρών και ενός 180 μοιρών έχουν κάθε φορά σαν αποτέλεσμα την ηχώ του spin. Το TR είναι ο χρόνος που απαιτείται για να πραγματοποιηθεί μία φορά η παλμική ακολουθία. Η βαθμίδωση επιλογής τομής ενεργοποιείται μεταξύ του RF παλμού 90 μοιρών και του RF παλμού 180 μοιρών. Είναι υπεύθυνη γα τη διέγερση των πρωτονίων της τομής που επιλέγεται και μόνον αυτών. Η βαθμίδωση συχνότητας ενεργοποιείται κατά τη λήψη του σήματος της ηχούς του spin (Spin Echo SE) και είναι υπεύθυνη για τη διαίρεση του σήματος κατά μήκος της διεύθυνσης που κωδικοποιεί τη συχνότητα. Τότε λαμβάνεται η ηχώ και τα δεδομένα εισάγονται στο «χώρο k» όπου αποθηκεύονται τα ακατέργαστα δεδομένα (raw data) προκειμένου να χρησιμοποιηθούν για την ανασύνθεση της εικόνας. Η 38
57 παλμική ακολουθία πρέπει να επαναληφθεί πολλές φορές προκειμένου να συλλεγούν όλες οι πληροφορίες που απαιτούνται για την παραγωγή εικόνων. Για 256 Χ 256 εικόνες η παλμική ακολουθία επαναλαμβάνεται 256 φορές. Η βαθμίδωση φάσης προσαρμόζεται κάθε φορά που η παλμική ακολουθία επαναλαμβάνεται και είναι υπεύθυνη για την τοποθέτηση δεδομένων στο «χώρο k». Ο χρόνος που μεσολαβεί από τον RF παλμό των 90 μοιρών μέχρι το κέντρο της ακολουθίας SE είναι ο χρόνος ηχούς ή ΤΕ. Ο χρόνος που απαιτείται για να ολοκληρωθεί η παλμική ακολουθία μία φορά λέγεται χρόνος επανάληψης ή TR. Τα ΤΕ και TR είναι παράμετροι που επιλέγονται σε μια παλμική ακολουθία και χρησιμοποιούνται για την επίτευξη αντίθεσης (contrast) στην εικόνα. Εάν ο χρόνος ΤΕ επιλεγεί ώστε να είναι μεγαλύτερος από το χρόνο Τ2 κάποιων ιστών, αλλά μικρότερος από το χρόνο Τ2 άλλων ιστών, τότε το σήμα που προκύπτει οφείλεται σε πρωτόνια που δεν έχουν ακόμη χάσει τη συμφασικότητά τους (έχοντας μεγαλύτερο χρόνο Τ2) και κατά συνέπεια στο δεκτικό πηνίο επάγουν υψηλότερο σήμα. Αντίθετα, τα πρωτόνια που έχουν χάσει τη συμφασικότητά τους δεν δίδουν σήμα. Εάν ο χρόνος TR επιλεγεί μικρότερος από το χρόνο χαλάρωσης Τ1 κάποιων ιστών, τότε οι ιστοί με μικρότερο χρόνο χαλάρωσης από το TR θα έχουν προλάβει να επαναπροσανατολιστούν στον άξονα z, ενώ οι ιστοί με χρόνο Τ1 μεγαλύτερο από το TR δεν θα έχουν προλάβει. Κατά συνέπεια, μικρότερος αριθμός πρωτονίων με μεγάλο Τ1 θα είναι διαθέσιμος και αν η μέτρηση του σήματος γίνει σε μικρό χρόνο ΤΕ, οι διαφορές που θα αποτυπωθούν στο σήμα της μαγνήτισης θα οφείλονται στη διαφορά της διαθέσιμης μαγνήτισης κάθε ιστού. Με βάση τις μεταβλητές TR και ΤΕ προκύπτουν οι εξής βασικοί συνδυασμοί: 1) Ακολουθία με μικρό χρόνο ΤΕ και μικρό χρόνο TR: Ως αποτέλεσμα η λήψη σήματος βασίζεται στην Τ1 μαγνήτιση. 2) Ακολουθία με μικρό χρόνο ΤΕ και μεγάλο χρόνο TR: Ως αποτέλεσμα η λήψη σήματος βασίζεται στην απόλυτη πυκνότητα πρωτονίων των ιστών. 3) Ακολουθία με μεγάλο χρόνο ΤΕ και μεγάλο χρόνο TR: Ως αποτέλεσμα η λήψη σήματος βασίζεται στην Τ2 μαγνήτιση. 39
58 Η συμβατική MRM ξεκινάει με Τ1 εικόνες για τον προσδιορισμό της θέσης και της ανατομίας του μαστού, καθώς και την ανάδειξη ή όχι παθολογικών λεμφαδένων. Εικόνες Τ2 με/ή χωρίς καταστολή λίπους λαμβάνονται ώστε να βοηθήσουν στο χαρακτηρισμό των βλαβών. Οι διαδοχικές Τ1 ακολουθίες με καταστολή λίπους, οι οποίες λαμβάνονται πριν, κατά τη διάρκεια και μετά τη χορήγηση παραμαγνητικής ουσίας διαρκούν 78 δευτερόλεπτα, χρόνος κατάλληλος για δυναμική εικόνα υψηλής ευκρίνειας. Η εξέταση συμπληρώνεται με εικόνες διάχυσης για την κατασκευή του χάρτη προφανούς διάχυσης και φασματοσκοπία σε ύποπτες περιοχές για την ανίχνευση της χολίνης Καταστολή λίπους Η ικανοποιητική καταστολή λίπους βοηθά στην ανίχνευση μιας μικρής βλάβης, αλλά μεγαλώνει το συνολικό χρόνο εξέτασης. Η καταστολή του λίπους βασίζεται στο φασματικό διαχωρισμό του από το νερό. Χρησιμοποιείται ένας RF παλμός για την επιλεκτική διέγερση του λίπους πριν από τον παλμό έναρξης της ακολουθίας. Επομένως, το σήμα του λίπους θα κορεστεί και δεν συμβάλλει στο σήμα που μετράται για να σχηματιστεί εικόνα. Ο επιπλέον χρόνος που χρειάζεται γι αυτόν τον παλμό αυξάνει το χρόνο επανάληψης της ακολουθίας (ΤR) και επομένως αυξάνει το συνολικό χρόνο εξέτασης. Εναλλακτικός τρόπος για καταστολή του λίπους είναι η αφαίρεση των εικόνων, κατά την οποία μετά την ενδοφλέβια έγχυση σκιαστικού αφαιρείται όλος ο μη εμπλουτιζόμενος ιστός και αναδεικνύονται τα εμπλουτιζόμενα μέρη. Η αφαίρεση των εικόνων θα πρέπει πάντα να χρησιμοποιείται μαζί με τις αρχικές εικόνες, και μόνο όταν η ασθενής έχει παραμείνει εντελώς ακίνητη κατά τη διάρκεια της εξέτασης, καθώς μία κίνηση της ασθενούς θα έδειχνε σκοτεινές και φωτεινές περιοχές στα περιγράμματα που αντιστοιχούν σε λανθασμένη αντιστοιχία θέσης των εικόνων πριν και μετά το σκιαστικό (Scherzinger AL et al 1985) Επεξεργασία εικόνων Η επεξεργασία των εικόνων βοηθά ώστε η πληροφορία να συμπτυχθεί σε μικρότερο αριθμό εικόνων που περιέχουν την ίδια πληροφορία, απλουστεύοντας και διευκολύνοντας την ανάγνωσή της. Εκτός από την αφαίρεση των εικόνων πριν και μετά την έγχυση σκιαστικού, μια άλλη μέθοδος επεξεργασίας είναι η προβολή της μέγιστης έντασης (ΜΙΡ), όπου προβάλλεται το pixel με τη μέγιστη ένταση κατά μήκος μιας 40
59 συγκεκριμένης διεύθυνσης σε μια δισδιάστατη εικόνα. Τέτοιες εικόνες μπορούν να σχηματιστούν από πολλαπλές γωνίες και να παρουσιαστούν με τέτοιο τρόπο ώστε να δίνουν την εντύπωση μιας τρισδιάστατης απεικόνισης της περιοχής. Όταν η τεχνική αυτή χρησιμοποιηθεί βασιζόμενη σε εικόνες μαστού μετά τη χορήγηση σκιαγραφικής ουσίας και με καταστολή λίπους, μπορεί να αναδείξει τα αγγεία και τις εμπλουτιζόμενες περιοχές. Η τεχνική αυτή δεν μπορεί να χρησιμοποιηθεί για την εκτίμηση της εσωτερικής δομής της βλάβης ή την επέκταση της νόσου στο δέρμα ή το θωρακικό τοίχωμα. Μπορούμε να πάρουμε και ποσοτική πληροφορία δημιουργώντας περιοχές ενδιαφέροντος και παραμετρικούς χάρτες, όπου η εικόνα δημιουργείται από τον υπολογισμό της τιμής μιας συγκεκριμένης παραμέτρου σε κάθε pixel. Για παράδειγμα ο χάρτης του συντελεστή προφανούς διάχυσης δημιουργείται από τη χρωματική απεικόνιση των υπολογισμένων τιμών για κάθε pixel σε κάθε τομή Δυναμική έγχυση παραμαγνητικής ουσίας. Η τεχνική ανάδειξης της μικροαγγείωσης δίνει πληροφορίες όσον αφορά τη μικροαγγείωση μιας παθολογικής εξεργασίας (Su MY et al 2003). Ο μέσος χρόνος διέλευσης του σκιαστικού (ΜΤΤ) ή ο σχετικός όγκος αίματος μπορούν να υπολογισθούν και να χρησιμοποιηθούν για τη διαφοροδιάγνωση καλοήθων από κακοήθεις όγκους, νεοπλασμάτων από μετεγχειρητικό ή μετακτινικό ιστό και για τη μελέτη της ανταπόκρισης των όγκων στη χημειοθεραπεία. Χρησιμοποιούνται δυναμικές ακολουθίες ευαίσθητες σε αλλαγές της μαγνητικής επιδεκτικότητας (dynamic susceptibility imaging), κατά τη διάρκεια των οποίων γίνεται έγχυση σκιαστικού (παραμαγνητική ουσία). Η σάρωση του μαστού γίνεται σε Τ1 εικόνες με καταστολή λίπους και διαρκεί 78 sec. Αρχικά επαναλαμβάνεται η ακολουθία 7 φορές. Στο περιβάλλον επεξεργασίας επιλέγεται μια περιοχή ενδιαφέροντος (Region Of Interest - ROI) κοινή και για τις 7 φάσεις και μετρούνται οι μέσες τιμές του MR-σήματος (MR Units) για κάθε μία. Κατασκευάζεται η γραφική παράσταση των MR -Units σε σχέση με το χρόνο και από τα χαρακτηριστικά της καμπύλης (προφίλ πρόσληψης - έκπλυσης, wash in - wash out) λαμβάνονται πληροφορίες για τη φύση και τη συμπεριφορά της βλάβης (Zhang Y et al 2002). 41
60 Πριν και κατά τη διάρκεια της έγχυσης της παραμαγνητικής ουσίας λαμβάνονται εικόνες με τρισδιάστατη ακολουθία (3D spoiled gradient recalled echo), ανά 78 δευτερόλεπτα (μία φάση πριν και 6 κατά τη διάρκεια και μετά τη χορήγηση της παραμαγνητικής ουσίας). Ο χρόνος ηχούς επιλέγεται να είναι ο μικρότερος δυνατός ώστε να ελαχιστοποιηθεί η Τ2 αντίθεση. Χρησιμοποιείται καταστολή του σήματος του λίπους ώστε να μπορούν να διαφοροποιηθούν οι εστίες που προσλαμβάνουν παραμαγνητική ουσία από τις γειτονικές περιοχές του λίπους. Λόγω της ιδιαιτερότητας της περιοχής για την καλύτερη καταστολή χρησιμοποιούνται δύο ανεξάρτητες περιοχές ομοιογένειας (shimming volumes), μία για κάθε μαστό ξεχωριστά. Η έγχυση γίνεται με σταθερό ρυθμό (2 ml/s) και η ποσότητα του σκιαγραφικού μέσου υπολογίζεται με βάση το σωματικό βάρος (0,2 mmol/kg σωματικού βάρους). Από την αφαίρεση των εικόνων που λαμβάνονται πριν την έγχυση παραμαγνητικής ουσίας από τις εικόνες που λαμβάνονται μετά την έγχυση, αναδεικνύονται οι περιοχές εμπλουτισμού. Στις εικόνες που προκύπτουν υπολογίζονται οι καμπύλες που δείχνουν την ποσοστιαία αύξηση του σήματος σε σχέση με το χρόνο. Η καμπύλη χαρακτηρίζεται τύπου Ι εάν η αύξηση του σήματος στη διάρκεια του χρόνου είναι συνεχής, δηλαδή εάν μετά το 3 ο λεπτό μετά την έγχυση μέχρι το 8 ο λεπτό η αύξηση του σήματος είναι μεγαλύτερη του 10% της μέγιστης τιμής. Εάν για το ίδιο χρονικό διάστημα παρατηρείται μείωση του σήματος μεγαλύτερη του 10% η καμπύλη χαρακτηρίζεται τύπου ΙΙΙ (washout). Εάν υπάρχει είτε αύξηση είτε μείωση του σήματος μικρότερη από 10% η καμπύλη χαρακτηρίζεται τύπου ΙΙ (plateau) (Jansen SA et al 2008) (Σχήμα 6.2). 42
61 Σχήμα 6.2 Σχηματική αναπαράσταση των καμπυλών εμπλουτισμού Επεξεργασία δυναμικών εικόνων Η MRM μετά από έγχυση παραμαγνητικής ουσίας είναι ιδιαίτερα ευαίσθητη στην ανίχνευση αγγειογένεσης, ανεξάρτητα από την πυκνότητα του μαστού. Η αγγειογένεση έχει σαν αποτέλεσμα τον επιλεκτικό εμπλουτισμό των καρκινικών βλαβών. Η επεξεργασία των δυναμικών εικόνων γίνεται σε ειδική κονσόλα, όπου υπολογίζεται το ποσοστό του εμπλουτισμού κατά τη διάρκεια των αρχικών φάσεων και εκτιμάται αν υπάρχει γρήγορη έκπλυση (washout) της σκιαγραφικής ουσίας από την περιοχή της βλάβης κατά τις τελευταίες φάσεις. Συνήθως οι καρκινικές βλάβες εμπλουτίζονται έντονα και γρήγορα και στη συνέχεια η ένταση του σήματος παραμένει σταθερή ή μειώνεται. Αντίθετα, οι καλοήθεις βλάβες έχουν συνεχώς αυξανόμενη ένταση σήματος κατά τη διάρκεια των δυναμικών φάσεων (Schelfout K et al 2004) Εικόνες Διάχυσης (DWI) Ως διάχυση ορίζεται η τυχαία και από τη θερμότητα επαγόμενη κίνηση των μορίων του νερού (κίνηση Brown) ή οποιουδήποτε άλλου μορίου. Αυτή η κίνηση επηρεάζεται από το περιβάλλον των γειτονικών ιστών και από την παρουσία εμποδίων φραγμών (π. χ. κυτταρικών μεμβρανών ή άλλων ημιδιαπερατών μεμβρανών). Η κίνηση των μορίων του νερού είναι πιο περιορισμένη σε ιστούς με μεγάλες κυτταρικές πυκνότητες (π. χ. ιστούς καρκινικών όγκων) ή με λιπόφιλες κυτταρικές μεμβράνες που λειτουργούν ως φραγμοί τόσο στον ενδοκυττάριο όσο και στον εξωκυττάριο χώρο. 43
62 Αντίθετα, η κίνηση των μορίων του νερού περιορίζεται σε μικρότερο βαθμό αν η κυτταροβρίθεια είναι μικρή και οι κυτταρικές μεμβράνες κατεστραμένες. Περιβάλλον λιγότερο κυτταροβριθές παρέχει μεγαλύτερο εξωκυττάριο χώρο για τη διάχυση των μορίων του νερού, τα οποία επίσης ελεύθερα περνούν μέσα από αλλοιωμένες κυτταρικές μεμβράνες και κινούνται από τον ενδοκυττάριο στον εξωκυττάριο χώρο. Κατά συνέπεια, ο βαθμός διάχυσης των μορίων του νερού σε ένα ιστό συσχετίζεται αντίστροφα με την κυτταροβρίθεια του ιστού και την ακεραιότητα κυτταρικών μεμβρανών. Η απεικόνιση που βασίζεται στη διάχυση (DWI) χρησιμοποιείται για χαρτογράφηση του βαθμού διάχυσης των μορίων του νερού σε in vivo MR-απεικόνιση. Η ένταση του σήματος στις DWI εικόνες είναι αντιστρόφως ανάλογη με το βαθμό διάχυσης των μορίων του νερού, ο οποίος επηρεάζεται από την ιστολογική δομή. Με άλλα λόγια, η ένταση του σήματος υποδηλώνει την ιστολογική δομή. Επί απουσίας δομών, η διάχυση γίνεται ισοτροπικά προς όλες τις διευθύνσεις. Εάν υπάρχει προτιμητέα κατεύθυνση διάχυσης, τότε η διάχυση γίνεται ανισότροπη. Λόγω του ότι η τεχνική διάχυσης (DWI) είναι ευαίσθητη σε κινήσεις σε μοριακό επίπεδο, είναι ικανή να αναδείξει πρώιμες βλάβες, σε φάση που αυτές δεν μπορούν να απεικονισθούν με άλλη τεχνική. Δεδομένου ότι οι κυτταροβριθείς ιστοί έχουν χαμηλή διάχυση και ότι οι κακοήθεις όγκοι είναι κυτταροβριθέστεροι από τους καλοήθεις, η συγκεκριμένη τεχνική δυνητικά αυξάνει την ειδικότητα της εξέτασης. H πιο διαδεδομένη τεχνική για DWI εικόνες είναι η Spin Echo Echo Planar Imaging DW. Για τη μετατροπή μιας Spin Echo Echo Planar ακολουθίας σε Spin Echo Echo Planar Imaging DW χρησιμοποιούνται δύο ευαίσθητες στη διάχυση βαθμιδώσεις πριν και μετά από ένα RF παλμό 180 μοιρών πριν τη συλλογή των δεδομένων της echoplanar εικόνας. Πιο αναλυτικά, για τις εικόνες διάχυσης χρησιμοποιείται μια Spin Echo Echo Planar Imaging (SE EPI) ακολουθία, στην οποία έχουν προστεθεί δύο πανομοιότυποι βαθμιδωτοί παλμοί, πριν και μετά από τον παλμό των 180 μοιρών. Ο πρώτος βαθμιδωτός παλμός εισάγει μια διαφορά φάσης στα μόρια του νερού, ενώ ο δεύτερος αναιρεί αυτή τη διαφορά φάσης και επανακτάται η συμφασικότητά τους. Τα κινούμενα μόρια όμως θα καταλήξουν με διαφορά φάσης λόγω της κίνησής τους, στο διάστημα μεταξύ της εφαρμογής των δύο παλμών. Με άλλα 44
63 λόγια, οι ακίνητοι πυρήνες θα μείνουν συμφασικοί, ενώ οι κινούμενοι θα έχουν μερική απώλεια της συμφασικότητας που θα προκαλέσει μείωση του σήματός τους. Σε ζωντανούς οργανισμούς, παράγοντες όπως η μικροαγγείωση, η κίνηση των υγρών ή η μακροσκοπική κίνηση συνεισφέρουν στην απώλεια σήματος, οπότε ο όρος συντελεστής διάχυσης αντικαθίσταται από τον όρο συντελεστής προφανούς ή φαινομενικής διάχυσης (Apparent Diffusion Coefficient, ADC) σε mm 2 / sec, o oποίος ορίζει τη μέση επιφάνεια που διατρέχει ένα μόριο νερού στη μονάδα του χρόνου. Η τιμή του ADC υπολογίζεται από τη μέτρηση της μείωσης του σήματος σε DWI εικόνες, με διάφορες τιμές b. Ο ADC υπολογίζεται για κάθε στοιχειώδη εικόνα (pixel) χωριστά και έτσι παράγεται ένας παραμετρικός χάρτης διάχυσης υποβαθμίζοντας τα Τ2 χαρακτηριστικά της εικόνας που θα οδηγούσαν σε παρερμηνεία λόγω του T2 shine through effect (Yabuuchi H et al 2008). Η διάχυση εκφράζεται από την εκθετική εξίσωση ln (SDW/SSE) = ADC (γ. G. δ) 2 Χ (Δ-[δ/3]), όπου G είναι η βαθμίδωση, SDW η εξασθένιση του spin- echo σήματος (G=0), SSE το πλήρες spin-echo σήμα πριν την εξασθένιση λόγω διάχυσης (G=0), γ είναι η γυρομαγνητική σταθερά των πρωτονίων, δ είναι η διάρκεια του G και Δ ο χρόνος μεταξύ ενάρξεων των δύο ευαίσθητων στη διάχυση βαθμιδώσεων. Το γινόμενο των δύο τελευταίων όρων της εξίσωσης, δηλαδή η παράμετρος (γ. G. δ) 2 Χ (Δ - [δ/3]), συνήθως ονομάζεται τιμή b (b value) και εκφράζεται σε sec/mm 2, αντανακλά δε την ισχύ της επιβάρυνσης της ακολουθίας λόγω διάχυσης. Η τιμή του ADC αντανακλά την ποσοτικοποίηση της διάχυσης που υπολογίζεται με βάση την εξασθένιση της έντασης του σήματος μεταξύ τουλάχιστον δύο DWI εικόνων, σύμφωνα με την εξίσωση ADC = ln (SDW/SSE) / b. Χαμηλός συντελεστής ADC υποδηλώνει περιορισμένη διάχυση πρωτονίων, παραπέμπει σε κακοήθεια και απεικονίζει τη σχετική μείωση του σήματος λόγω διάχυσης (Partridge SC et al 2009) In vivo, η τιμή του ADC περιλαμβάνει τους παράγοντες τόσο της διάχυσης του νερού όσο και της επίδρασης της αγγείωσης. Για το λόγο αυτό λέγεται συντελεστής φαινομενικής ή προφανούς διάχυσης, όπως εκφράζεται από τον τύπο ADC = D + (f/b), όπου D o συντελεστής διάχυσης και f ο παράγοντας της αγγείωσης. 45
64 Στους ζωντανούς ιστούς οι DWI εικόνες επηρεάζονται από την κίνηση Brown (διάχυση) και την αιματική ροή τόσο σε μακρο-όσο και σε μικρο-σκοπικό επίπεδο. Η αιματική ροή σε μικροσκοπικό επίπεδο αποτελεί σημαντικό ανταγωνιστή του φαινομένου της διάχυσης. Αυτό σημαίνει ότι το σήμα της DWI εικόνας αναμιγνύεται με σήμα που σχετίζεται με τη μικρο-αιμάτωση, με αποτέλεσμα την αύξηση του ADC, σύμφωνα με την εξίσωση ADC = D + (f/b). Ο παράγοντας f/b μπορεί να αγνοηθεί όταν οι τιμές του b είναι υψηλές, δεδομένου και ότι το f είναι μικρό. Επίδραση της μικροαιμάτωσης δεν έχει παρατηρηθεί σε τιμές b μικρότερες από 600 sec / mm 2 στο φυσιολογικό ιναδενικό ή λιπώδη ιστό, δεδομένου και ότι ο μαζικός αδένας δεν είναι αγγειοβριθές όργανο (Delille JP et al 2005, Baron P et al 2010). Από την άλλη πλευρά είναι γεγονός ότι η αιμάτωση των καλοήθων και κακοήθων όγκων του μαστού είναι υψηλή (Jin G et al 2010). Μέχρι σήμερα η ακολουθία διάχυσης είναι επικουρική συμβάλλοντας στην ελάττωση των ψευδώς θετικών εστιών που ανιχνεύονται στις ακολουθίες με έγχυση σκιαστικού. Πολλές μελέτες έχουν δείξει σημαντικά χαμηλότερο συντελεστή διάχυσης (ADC) στις κακοήθεις βλάβες συγκριτικά με τις καλοήθεις. Σε μια μετα- ανάλυση 13 μελετών βρέθηκε ότι η ευαισθησία και η ειδικότητα του DWI στην διάκριση καλοηθών βλαβών από κακοήθεις είναι 84% και 79% αντίστοιχα(chen X et al 2010).Σε μία άλλη μετα-ανάλυση 14 μελετών επιβεβαιώθηκε ότι η μέτρηση του ADC είναι συμπληρωματική μέθοδος της δυναμικής έγχυσης του σκιαστικού για την ταξινόμηση των ύποπτων βλαβών του μαστού με αποτέλεσμα την αύξηση της ακρίβειας της συμβατικής μαγνητικής μαστογραφίας (Zhang L et al 2016). Πρόσφατα σύμφωνα με τους( Bickelhaupt S et al 2016) η DWI ακολουθία αποτελεί γρήγορη, μη επεμβατική προσέγγιση για την εκτίμηση ύποπτων βλαβών που ανιχνεύονται στην ψηφιακή μαστογραφία. Αυτό έχει ως αποτέλεσμα την ελάττωση μη αναγκαίων βιοψιών. Σύμφωνα με τους (Dorrius MD et al 2014) η ευαισθησία και η ειδικότητα του DWI δεν επηρεάζεται από την τιμή b value, οι οποίοι πρότειναν την μέγιστη τιμή 1000 s/mm2 για τον διαχωρισμό καλοήθων από κακοήθεις βλάβες. Επιπλέον η μελέτη τους επιβεβαίωσε ότι η χορήγηση σκιαστικού δεν επηρεάζει σημαντικά την τιμή του συντελεστή διάχυσης ADC. 46
65 Η ποσοτικοποίηση του ADC μπορεί να βοηθήσει στη διαφοροποίηση των διαφόρων υποτύπων του καρκίνου. Χαμηλή τιμή ADC μπορεί να σχετίζεται με επιθετικό φαινότυπο διηθητικού καρκίνου με υψηλό δείκτη πολλαπλασιασμού και αυξημένη κυτταροβρίθεια. Πράγματι μια μεγάλη μελέτη των (Choi SY et al 2012) έδειξε ότι η χαμηλή τιμή ADC συνοδεύεται με υψηλό δείκτη πολλαπλασιασμού Ki 67 το οποίο επιβεβαιώθηκε και σε μεταγενέστερες μελέτες(kim EJ et al 2015, Kitajima K et al 2016, Mori N et al 2015). Επιπρόσθετα στη μελέτη των Jiang R et al 2016 βρέθηκε αρνητική συσχέτιση μεταξύ κυτταροβρίθειας και τιμών ADC. Αρνητική συσχέτιση βρέθηκε και σε μια μικρή υποομάδα μελετών μεταξύ ADC και βαθμού κακοήθειας (grade)(constantini M et al 2010, Razek AA et al 2010, Cipolla V et al 2014), αν και η πλειονότητα των μελετών δε βρήκε αυτή τη συσχέτιση σημαντική. Ενδιαφέρον αποτελεί το ότι μερικοί συγγραφείς παρατήρησαν ότι οι καρκίνοι με θετικούς οιστρογονικούς υποδοχείς(er) συνοδεύονται με χαμηλότερες τιμές ADC (Choi SY et al 2012, Guvenc I et al 2016, Jeh SK et al 2011, Kamitani T et al 2013, Kim SH et al 2009, Martincich L et al 2012) παρόλο που οι καρκίνοι με θετικούς οιστρογονικούς υποδοχείς συνοδεύονται από καλύτερη πρόγνωση. Ωστόσο πολλές μελέτες δε βρίσκουν σημαντικές συσχετίσεις μεταξύ ADC και προγνωστικών παραγόντων. Μελέτες εξετάζουν το DWI προς χαρακτηρισμό της βιολογικής συμπεριφοράς του DCIS, με υποσχόμενα αποτελέσματα. Η αναγνώριση των σημείων του DWI που αντανακλούν τη βιολογική συμπεριφορά του DCIS είναι κλινικά σημαντική αφού θα μπορούσε να βοηθήσει στην ελάττωση της υπερδιάγνωσης και της υπερθεραπείας αυτού του προδιηθητικού καρκίνου. Στις ακολουθίες διάχυσης το DCIS τυπικά έχει υψηλότερες τιμές ADC συγκριτικά με τον διηθητικό καρκίνο πράγμα το οποίο οφείλεται πιθανότερα στη χαμηλότερη κυτταροβρίθεια του.(choi SY et al 2012, Mori N et al 2015). Σε πολλές μελέτες αναφέρεται ότι τα DCIS που βρίσκονται σε βιοψία με βελόνα και μεταπίπτουν σε διηθητικά στη χειρουργική εκτομή έχουν χαμηλότερη τιμή ADC από αυτά που δεν έχουν διηθητικό στοιχείο (Bickel H et al 2015, Hussein H et al 2015, Mori N et al 2013). Σύμφωνα με τους (Rahbar H et al 2011, Iima M et al 2011, Rahbar H et al 2012) τα αμιγή DCIS σημειώνουν χαρακτηριστικά στο DWI που διαφέρουν μεταξύ υψηλού και χαμηλού πυρηνικού βαθμού κακοήθειας. Οπωσδήποτε 47
66 χρειάζονται πολυκεντρικές μελέτες με μεγαλύτερες ομάδες ασθενών προκειμένου να καθορισθεί ο δυνητικός ρόλος του DWI ως αξιόπιστος δείκτης καρκίνου που συμβάλει καθοριστικά στη θεραπεία. Υπάρχει ένα συνεχές ενδιαφέρον στην ανεύρεση απεικονιστικής, μη επεμβατικής μεθόδου όσον αφορά την παρουσία ή όχι μεταστατικών μασχαλιαίων λεμφαδένων. Ενώ δεν υπάρχουν αξιόπιστα στοιχεία στη συμβατική δυναμική έγχυση σκιαστικού που να διακρίνουν κακοήθεις από καλοήθεις λεμφαδένες με υψηλή ειδικότητα, αρκετές μελέτες είναι υποσχόμενες στη χρησιμοποίηση του DWI στη σταδιοποίηση της μασχάλης και την αύξηση της ειδικότητας της συμβατικής μαγνητικής μαστογραφίας με έγχυση σκιαστικού. Σε πρόσφατη μετα ανάλυση 13 μελετών παρατηρήθηκαν συνολικά χαμηλότερες τιμές ADC στους μεταστατικούς λεμφαδένες συγκριτικά με τους μη μεταστατικούς με ευαισθησία και ειδικότητα του DWI 83% και 82% αντίστοιχα (Xing H et al 2016). Σε άλλες μελέτες δε βρέθηκαν διαφορές στην τιμή του ADC μεταξύ μορφολογικά ύποπτων για κακοήθεια λεμφαδένων και αντιδραστικών καλόηθων λεμφαδένων (Rahbar H et al 2015) ενώ σε άλλες μελέτες αναφέρεται ότι η μέτρηση της διαμέτρου των λεμφαδένων είναι περισσότερο αξιόπιστη συγκριτικά με την τιμή του ADC (Iima M et al 2014). Γεγονός είναι ότι χρειάζονται περισσότερες μελέτες για να καθορισθεί η επιπρόσθετη αξία του DWI στην εκτίμηση των μασχαλιαίων λεμφαδένων. Οι ακολουθίες διάχυσης έχουν επιπλέον ερευνηθεί για την ικανότητα τους στην εκτίμηση της ανταπόκρισης της προεγχειρητικής χημειοπεραπείας. Οι κυτταροτοξικές παρενέργειες της χημειοθεραπείας που περιλαμβάνουν λύση του κυττάρου, απόπτωση και νέκρωση προκαλούν μεταβολές στην διαπερατότητα της μεμβράνης που οδηγούν σε ελεύθερη κίνηση των μορίων του νερού. Επομένως μια αύξηση στην τιμή του ADC μπορεί να αντανακλά ανταπόκριση στη χημειοθεραπεία γρηγορότερα από τις ανατομικές αλλαγές που βασίζονται στη μέτρηση του μεγέθους του όγκου. Κλινικές μελέτες έχουν δείξει πρώιμες αλλαγές στην τιμή του ADC του όγκου μετά τον πρώτο κύκλο της χημειοθεραπείας γεγονός που βοηθά σημαντικά στη διαφοροποίηση των ασθενών που απαντούν στη χημειοθεραπεία από αυτούς που δεν απαντούν (Galban CJ et al 2015, Li XR et al 2012, Sharma U et al 2009). Επιπρόσθετα η τιμή μέτρησης του ADC πριν τη θεραπεία μπορεί να έχει προγνωστική αξία που βοηθά στην 48
67 αναγνώριση ασθενών που θα ανταποκριθούν καλύτερα στην προεγχειρητική χημειοθεραπεία. Τρείς μεγάλης κλίμακας μελέτες γυναικών με τοπικά προχωρημένο καρκίνο που υπεβλήθησαν σε προεγχειρητική χημειοθεραπεία καθεμιά έδειξε ότι χαμηλή τιμή ADC πριν τη θεραπεία ήταν προγνωστική της πλήρους ανταπόκρισης σε τριπλά αρνητικούς καρκίνους, ενώ τα ευρήματα ποικίλουν σε καρκίνους luminal και με θετικούς HER 2 υποτύπους (Richard R et al 2013, Liu S et al 2015, Bufi E et al 2015). Περαιτέρω έρευνα απαιτείται στην καθιέρωση του ADC ως προγνωστικό δείκτη της αποτελεσματικότητας της θεραπείας. Η ακολουθία διάχυσης αποτελεί εναλλακτική λύση της συμβατικής μαγνητικής μαστογραφίας με έγχυση σκιαστικού στον προληπτικό έλεγχο του καρκίνου του μαστού (Kazama T et al 2012, Trimboli RM et al 2014, Yabuuchi H et al 2011, McDonald ES et al 2016). Έρευνες έδειξαν ότι πολλοί καρκίνοι μη αντιληπτοί μαστογραφικά και κλινικά, είναι ορατοί στις DWI εικόνες με χαμηλή τιμή ADC (Patridge SC et al). Σύμφωνα με τους Yabuuchi H et al 2011, η ανίχνευση του καρκίνου του μαστού με την ακολουθία διάχυσης επιτυγχάνει υψηλότερη ακρίβεια συγκριτικά με τη μαστογραφία. Επιπρόσθετα οι Trimboli RM et al 2014 αναφέρουν ευαισθησία 76% και ειδικότητα 90% στην ανίχνευση του καρκίνου του μαστού στις DWI εικόνες. Πρόσφατα οι McDonald ES et al 2016 μελέτησαν την απόδοση του DWI να ανιχνεύσει καρκίνο που δεν έχει φανεί στη μαστογραφία σε γυναίκες με πυκνούς μαστούς. Η μελέτη έδειξε ότι το DWI μπορεί να ανιχνεύσει 8 περισσότερους καρκίνους απ ότι η μαστογραφία σε αριθμό 1000 γυναικών με ειδικότητα και θετική προγνωστική αξία 91% και 62% αντίστοιχα. Η εφαρμογή του DWI στον προληπτικό έλεγχο είναι επίκαιρη λόγω της ελαττωμένης ευαισθησίας της μαστογραφίας και της θέσπισης νομοθεσίας στους πυκνούς μαστούς (Ray KM et al 2015, Slanetz PJ et al 2015). Όσον αφορά την επίδραση του DWI στο μαστό που υπόκειται σε ορμονικές μεταβολές με βάση τον καταμήνιο κύκλο, μελέτες επιβεβαίωσαν ότι δεν υπάρχει σημαντική επίδραση των τιμών ADC στον καταμήνιο κύκλο τόσο σε υγιείς όσο και σε ασθενείς με καρκίνο του μαστού (Ο Flyn EA et al 2012, Kim JY et al 2016, Nissan N et al 2014, Shin S et al 2015).Η σταθερότητα της μέτρησης των τιμών του ADC στις κυκλικές μεταβολές του καταμήνιου κύκλου υποδηλώνει ότι το DWI μπορεί να χρησιμοποιηθεί σε οποιαδήποτε φάση του καταμήνιου κύκλου. 49
68 Κατά τη διάρκεια της γαλουχίας η κλινική εφαρμογή της συμβατικής μαγνητικής μαστογραφίας με έγχυση σκιαστικού είναι περιορισμένη επειδή αυξάνεται η αιματική ροή και το φυσιολογικό παρέγχυμα του μαζικού αδένα κατά τη γαλουχία εμφανίζει αύξηση του εμπλουτισμού μετά τη δυναμική χορήγηση παραμαγνητικής ουσίας(espinosa LA et al 2005). Οι τιμές του ADC σε μαστούς γαλουχίας είναι σημαντικά ελαττωμένες (Nissan N et al 2014) πιθανόν λόγω του υψηλού πρωτεϊνικού περιεχομένου και της αυξημένης γλοιότητας του γάλατος, παραμένοντας όμως υψηλότερες από αυτές της κακοήθειας (Sah RG et al 2015), υποδηλώνοντας ότι ο καρκίνος μπορεί να είναι ευδιάκριτος στις DWI εικόνες στις γυναίκες σε γαλουχία παρόλο των ελαττωμένων επιπέδων διάχυσης του παρεγχύματος. Η πυκνότητα του μαστού είναι γνωστό ότι ελαττώνεται με την ηλικία με βαθμιαία ατροφία του ιναδενικού ιστού μετά την εμμηνόπαυση. Αρκετές μελέτες έχουν δείξει ότι οι τιμές του ADC συσχετίζονται θετικά με την πυκνότητα του μαστού (Mc Donald ES et al 2014, Iacconi C et al 2014) και γενικά είναι χαμηλότερες στις μετεμμηνοπαυσιακές γυναίκες από τις προεμμηνοπαυσιακές (Nissan N et al 2014, Shin S et al 2015). Η παθολοφυσιολογία της μείωσης του ADC στο φυσιολογικό ιναδενικό ιστό στις μεγαλύτερες σε ηλικία γυναίκες δεν είναι ξεκάθαρη αλλά μπορεί να σχετίζεται με αλλαγές της περιεκτικότητας του νερού, της μικροκυκλοφορίας και της περιεκτικότητας σε λίπος στον ιναδενικό ιστό του μαστού με την πάροδο της ηλικίας. Η εμμηνόπαυση και η γαλουχία είναι καταστάσεις που μπορεί να επηρεάσουν σημαντικά τις τιμές του ADC στο φυσιολογικό ιναδενικό ιστό. Ωστόσο το εύρος των τιμών του ADC σε αυτές τις φυσιολογικές καταστάσεις παραμένει σημαντικά υψηλότερο από τις περισσότερες κακοήθειες πράγμα που διευκολύνει τη διάγνωση.ο ρόλος του DWI στην απεικόνιση του μαστού αναμένεται να αυξηθεί στο προσεχές μέλλον. 50
69 6.1.5 Μαγνητική φασματοσκοπία Η μαγνητική φασματοσκοπία πρωτονίων ( 1 H-MRS) είναι μια μη επεμβατική μέθοδος για τη μελέτη διάφορων χημικών στοιχείων. Έχει αποδειχθεί ότι η τεχνική αυτή παρέχει βιοχημικές πληροφορίες που χρησιμεύουν στη διαφοροποίηση του φυσιολογικού από τον παθολογικό ιστό και σε κάποιο βαθμό είναι σημαντικές για τη διαφορική διάγνωση (Aboagye EO et al 1999). Σκοπός της μαγνητικής φασματοσκοπίας είναι να αποκλειστεί ή να επιβεβαιωθεί η ύπαρξη κορυφής στη θέση 3. 22ppm του φάσματος, που αντιστοιχεί σε χημικές ενώσεις που περιέχουν χολίνη (Lenkinski RE 2009). Στη φασματοσκοπία μονήρους στοιχειακού όγκου (SVS) διεγείρεται ένας όγκος ιστού και το ανιχνευόμενο σήμα μετατρέπεται σε φάσμα. Η φασματοσκοπία μονήρους όγκου έχει σαν αποτέλεσμα φάσμα από το συγκεκριμένο στοιχειακό όγκο που συνήθως έχει μέγεθος 8cm 3. Η διαδικασία διαρκεί περίπου 6 λεπτά. Στη φασματοσκοπία, η επιλογή του χρόνου ηχούς γίνεται με τον ίδιο τρόπο που επιλέγεται στις συμβατικές εικόνες Τ2. Οι μεταβολίτες με χαμηλούς χρόνους Τ2 χάνουν γρηγορότερα το σήμα τους και οι αντίστοιχες κορυφές τους δεν είναι εμφανείς σε φάσματα που λαμβάνονται με μεγάλο χρόνο ηχούς. Χαμηλός χρόνος ηχούς θα ανίχνευε υψηλότερο σήμα από τη χολίνη και τα παράγωγά της, όμως ο μεγαλύτερος χρόνος ηχούς (ΤΕ>135 ms) βοηθά στον καλύτερο διαχωρισμό του σήματος της χολίνης από το πολύ υψηλότερο σήμα του λίπους. Ο χρόνος ηχούς που επιλέγεται είναι 155 ms και η ακολουθία είναι double spin echo PRESS, λόγω του υψηλού σήματος που δίνει σε σχέση με άλλες συχνά χρησιμοποιούμενες ακολουθίες PRESS. Οι κλινικές εφαρμογές της μαγνητική φασματοσκοπίας πρωτονίων είναι: Συμπληρωματική τεχνική στην MRM, με αποτέλεσμα αύξηση της ειδικότητάς της στη διαφοροδιάγνωση καλοήθων από κακοήθεις όγκους. Εκτίμηση της ανταπόκρισης στη θεραπεία σε ασθενείς με προεγχειρητική χημειοθεραπεία, καθώς μπορεί να δείξει μέσα σε 24 ώρες απάντηση στην πρώτη δόση της θεραπείας. Ανάδειξη υποτροπής μετά από ακτινοθεραπεία ή Χημειοθεραπεία. Με βάση τα παραπάνω μπορεί να ελαττωθεί ο αριθμός των βιοψιών του μαστού. 51
70 Η φασματοσκοπία μπορεί να βοηθήσει στη διαφορική διάγνωση καλοηθειών από κακοήθειες, στηριζόμενη στα επίπεδα των μεταβολιτών που ανιχνεύονται. Ειδικότερα στο μαστό μελέτες έδειξαν ότι η MRS ανιχνεύει υψηλά επίπεδα μεταβολιτών χολίνης στις κακοήθεις βλάβες συγκριτικά με τις καλοήθεις και το φυσιολογικό ιστό(cecil KM et al 2001, Yeung DK et al 2001).Η υψηλή κορυφή χολίνης (peak) αναπαριστά σύνθεση των διαφορετικών επιπέδων ενώσεων που περιέχουν χολίνη όπως ελεύθερη χολίνη, φωσφοχολίνη και γλυκεροφωσφοχολίνη και τυπικά αναφέρεται ως ολική χολίνη(total choline-tcho).είναι γνωστό ότι η χολίνη εμπλέκεται στον κύκλο εργασιών της κυτταρικής μεμβράνης(σύνθεση και αποδόμηση των φωσφολιπιδίων) και γενικότερα θεωρείται δείκτης κυτταρικού πολλαπλασιασμού. Αν και οι υποκείμενες βιοχημικές διεργασίες δεν έχουν πλήρως διευκρινησθεί, η υψηλή χολίνη που παρατηρείται στις κακοήθειες φαίνεται να είναι το αποτέλεσμα του συνδυασμού της αυξημένης ενδοκυττάριας συγκέντρωσης φωσφοχολίνης και της αυξημένης κυτταροβρίθειας(sitter B et al 2002, Haddadin IS et al 2009). Η MRS μπορεί να αυξήσει τη διαγνωστική ακρίβεια της MR μαστογραφίας στις ύποπτες βλάβες του μαστού με αύξηση της ειδικότητας της μεθόδου στην διαφορική διάγνωση καλοηθών από κακοήθεις βλάβες(bartella L et al 2006, Meisamy S et al 2005, Bartella L et al 2007). Η πλειονότητα των μελετών έχει γίνει σε μαγνητικό τομογράφο 1.5 Tesla χρησιμοποιώντας την τεχνική του μονήρους στοιχειακού όγκου(single voxel). Σε μια πρόσφατη μετα ανάλυση 19 μελετών οι Baltzer και Dietzel 2013 βρήκαν ευαισθησία 73% και ειδικότητα 88% στη διάγνωση των βλαβών.η ανάλυσή τους δεν έδειξε σημαντικά πλεονεκτήματα των μελετών που έγιναν σε υψηλότερο μαγνητικό πεδίο 3Τ συγκριτικά με αυτό του 1.5Τ, όπως και διαφορές μεταξύ μεγαλύτερου και μονήρους στοιχειακού όγκου καθώς και διαφορές στην ποιοτική έναντι της ποσοτικής ανίχνευσης της χολίνης, αν και ο αριθμός των μελετών είναι μικρός. Πρόσφατα οι Pinker et al έχουν αναφέρει υψηλή διαγνωστική ακρίβεια για την εκτίμηση ύποπτων βλαβών του μαστού χρησιμοποιώντας πολυπαραμετρική MR μαστογραφία η οποία περιλαμβάνει τεχνική φασματοσκοπίας με μεγαλύτερο στοιχειακό όγκο(voxel) σε μαγνήτη 3Τ. Ο συνδυασμός MR μαστογραφίας με έγχυση σκιαστικού(dce) και MRS μπορεί να αυξήσει την ειδικότητα της μεθόδου( Jacobs MA et al 2005, Bolan PJ et al 2005). Στη μελέτη των Meissamy S et al 2005 η MRS συμπληρωματικά της DCE είχε σαν 52
71 αποτέλεσμα αυξημένη ευαισθησία, ειδικότητα και ακρίβεια της MR μαστογραφίας.επιπλέον στη μελέτη των Bartella L et al 2007 βρέθηκε ότι η εφαρμογή της MRS μπορεί να αυξήσει σημαντικά τη θετική προγνωστική αξία (PPV) όσον αφορά τις βιοψίες σε βλάβες με απεικόνιση μη μάζας, ελαττώνοντας τον αριθμό των μη αναγκαίων βιοψιών. Ενώ σε προηγούμενες έρευνες η ποιοτική ανίχνευση της χολίνης ήταν αξιόπιστος δείκτης κακοήθειας(katz-brull R et al 2002), νεότερες μελέτες χρησιμοποιούν υψηλότερα μαγνητικά πεδία με υψηλής ευαισθησίας πηνία που απαιτούν ποσοτικές τεχνικές ανίχνευσης χολίνης, λόγω του γεγονότος ότι η χολίνη μπορεί να είναι ανιχνεύσιμη ακόμη και στο φυσιολογικό αδενικό ιστό σε υψηλότερο όμως μαγνητικό πεδίο με αυξημένα επίπεδα SNR (Bolan PJ 2013, Zhao Cet al 2012). Tο κατώτατο όριο της ολικής χολίνης tcho SNR>2 αποτελεί συνήθως το κατώφλι για την κακοήθεια. Η MRS παίζει επίσης σημαντικό ρόλο στην εκτίμηση της ανταπόκρισης στη προεγχειρητική χημειοθεραπεία. Τα επίπεδα χολίνης που ανιχνεύονται στον όγκο μπορεί να αντανακλούν τις μεταβολές που προκαλεί η χημειοθεραπεία στον πολλαπλασιασμό του κυττάρου πριν από τη μεταβολή στο μέγεθος του όγκου, αποτελώντας έτσι ένα πρώιμο προγνωστικό δείκτη της ανταπόκρισης στη θεραπεία. Σύμφωνα με την πιλοτική μελέτη σε 4Τesla των Meisamy and colleagues 2004 βρέθηκε οξεία πτώση της συνολικής συγκέντρωσης της χολίνης του όγκου 24 ώρες μετά την πρώτη δόση του χημειοθεραπευτικού. Σε μελέτη των Shin et al 2012 φάνηκε ότι οι μετρήσεις της χολίνης ήταν υψηλότερες στα διηθητικά από τα in situ καρκινώματα, και έγινε συσχέτιση της χολίνης με προγνωστικούς παράγοντες όπως ο ιστολογικός βαθμός κακοήθειας(histological grade) και η κατάσταση των οιστρογονικών υποδοχέων(er). Σύμφωνα με τους Yeung DK et al 2002 στα DCIS είναι πιθανόν να μην ανιχνεύεται χολίνη στην MRS. Ένας από τους κύριους περιορισμούς της φασματοσκοπίας είναι η χαμηλή ευαισθησία της μεθόδου στην ανίχνευση της χολίνης σε βλάβες <10 χιλιοστά γεγονός το οποίο περιορίζει την εφαρμογή της τεχνικής ως επικουρική στην συμβατική MR μαστογραφία για την ελάττωση των ψευδώς θετικών ευρημάτων (Bolan PJ 2013). Σε υψηλότερα μαγνητικά πεδία με αύξηση του SNR και της διακριτικής ικανότητας, η χολίνη μπορεί 53
72 να ανιχνευτεί και να υπολογιστεί με μεγαλύτερη ακρίβεια και σε μικρότερες βλάβες (Haddadin IS et al 2009). Ένας άλλος περιορισμός της μεθόδου είναι ότι η τοποθέτηση του single voxel γίνεται κατά τη διάρκεια της ακολουθίας(real time) από εξειδικευμένο ακτινολόγο σε MRI μαστού. Επιπλέον η τεχνική single voxel δεν είναι βοηθητική στον προληπτικό έλεγχο με MR μαστογραφία διότι δε μπορεί να καλυφθεί ολόκληρος ο μαστός αφού επιτρέπεται ο έλεγχος μόνο μίας βλάβης κάθε φορά (Bartelle L et al 2007). Εναλλακτικά η τεχνική του multi voxel είναι υπό έρευνα και δυνητικά μπορεί να βελτιώσει την κλινική χρησιμότητα του MRS στην ανίχνευση του καρκίνου και στην τοπική σταδιοποίηση της νόσου. Περισσότερες μελέτες απαιτούνται για να αποδειχθεί η διαγνωστική αξία της MRS στην κλινική πράξη. 6.2 Mαγνήτης 3Τ Στην MR μαστογραφία με μαγνήτη 3Τ ο λόγος σήματος προς θόρυβο είναι αυξημένος κατά δύο φορές περίπου, συγκριτικά με το λόγο αυτό σε μαγνήτη 1,5Τ. Επίσης η ευκρίνεια είναι μεγαλύτερη και ο χρόνος που απαιτείται για τη διενέργεια της εξέτασης μικρότερος (Weinstein S et al 2010, Rausch DR et al 2006, Chatteji M et al 2010, Kuhl CK et al 2006). Επιπλέον η διαφοροποίηση της συχνότητας συντονισμού των πρωτονίων του λίπους και του νερού είναι διπλάσια, πράγμα που διευκολύνει την ομοιογένεια της καταστολής του λίπους (Chatteji M et al 2010, Weinstein S et al 2010). Από την άλλη πλευρά, οι μαγνήτες 3Τ εμφανίζουν αυξημένη ανομοιογένεια RF παλμών (διηλεκτρικό φαινόμενο) που χρησιμοποιούνται για τη διέγερση των πρωτονίων, γεγονός που μπορεί να επηρεάσει αρνητικά την ομοιογένεια του σήματος. Για τη βελτίωση της ομοιογένειας που οφείλεται σ αυτό το φαινόμενο, οι έρευνες συνεχίζονται. Άλλα φαινόμενα που δυνητικά προξενούν artifact και ανομοιογένεια όπως η χημική μετατόπιση και η μαγνητική επιδεκτικότητα είναι μεγαλύτερα στους μαγνήτες 3Τ (Chatteji M et al 2010, Kuhl CK et al 2006). Για το λόγο αυτό έχουν τροποποιηθεί τα πρωτόκολλα λήψης δεδομένων έτσι ώστε να ελαχιστοποιηθούν τα artifact που οφείλονται σ αυτές τις επιδράσεις. Η θέρμανση των ιστών είναι μεγαλύτερη στους μαγνήτες 3Τ, πράγμα που μπορεί να περιορίσει τον αριθμό και την ισχύ των RF παλμών (Chatteji M et al 2010). Επίσης τα ισχυρά μαγνητικά πεδία απαιτούν περισσότερους περιορισμούς ως προς τις ιατρικές συσκευές που πιθανόν συνοδεύουν τον ασθενή. Παρ όλο που οι Τ2 χρόνοι 54
73 χαλάρωσης των ιστών είναι παρόμοιοι στους μαγνήτες 1,5Τ και 3Τ, οι Τ1 χρόνοι χαλάρωσης είναι αυξημένοι, γεγονός που λαμβάνεται υπ όψιν στα πρωτόκολλα (Chatteji M et al 2010, Kuhl CK et al 2006), στα οποία ο χρόνος TR μπορεί να αυξηθεί ή να μειωθεί η γωνία κλίσης (flip angle) για τις GE (Gradient Echo) ακολουθίες. Στους μαγνήτες 3Τ, το Τ1 του λίπους του μαστού αυξάνεται κατά 24% και το Τ1 του ιναδενικού ιστού κατά 14%. Όμως το Τ1 του γαδολινίου δεν μεταβάλλεται τόσο, με αποτέλεσμα η βελτίωση της αντίθεσης (contrast) της εικόνας να είναι μεγαλύτερη (Rakow Penner R et al 2006). Παρ όλο που υπάρχουν έρευνες με μαγνήτες 3Τ για την τελειοποίηση των πρωτοκόλλων απαιτείται μεγαλύτερη εμπειρία. Σε ότι αφορά την ακολουθία διάχυσης, παρ όλο που ο χάρτης του συντελεστή προφανούς διάχυσης δεν είναι συνάρτηση της έντασης του μαγνητικού πεδίου η απεικόνιση με μαγνήτη 3Τ έχει υψηλότερη ευκρίνεια (Matsuoka A et al 2008). Η ακολουθία DWI λαμβάνεται πριν χορηγηθεί η παραμαγνητική ουσία διότι οι τιμές του συντελεστή προφανούς διάχυσης μειώνονται μετά το σκιαστικό. Η φυσική ερμηνεία του φαινομένου αυτού βασίζεται στο γεγονός ότι εξ αιτίας της παρουσίας του σκιαστικού, οι χρόνοι Τ2 μειώνονται λόγω αυξημένης μαγνητικής επιδεκτικότητας, με αποτέλεσμα την αλλαγή των τιμών διάχυσης (Martincich L et al 2012). Το φαινόμενο της χημικής μετατόπισης επίσης ενισχύεται σε υψηλά μαγνητικά πεδία. Η χημική μετατόπιση οφείλεται στο διαφορετικό ηλεκτρονικό περιβάλλον των πρωτονίων. Τα ηλεκτρόνια δημιουργούν μικρές αλλά μετρήσιμες τροποποιήσεις στο εφαρμοζόμενο μαγνητικό πεδίο, με αποτέλεσμα η συχνότητα συντονισμού των πρωτονίων σε διαφορετικά μόρια να είναι διαφορετική. Αυτή η διαφορά είναι γραμμικά εξαρτημένη από την ένταση του σταθερού μαγνητικού πεδίου, οπότε και οι διαφορές στις συχνότητες αυτές είναι άμεσα (γραμμικά) εξαρτώμενες από αυτό. Το τελικό αποτέλεσμα αυτού είναι να παρατηρείται μεγαλύτερη φασματική απόσταση του νερού και του λίπους ή του νερού και μεταβολιτών που είναι κρίσιμοι. Έτσι, η αύξηση στην φασματική απόσταση δίνει πλεονεκτήματα στην ΜRΜ. Εξαιτίας αυτής της αύξησης, οι καμπύλες του νερού και του λίπους είναι περισσότερο διακριτές και άρα οι παλμοί RF που χρησιμοποιούνται για την καταστολή του σήματος του λίπους είναι αποδοτικότεροι συγκριτικά με μικρότερα μαγνητικά πεδία. 55
74 Επίσης, αφ ενός λόγω της αύξησης της φασματικής απόστασης, αφ ετέρου λόγω της αύξησης του σήματος που υπάρχει σε πολύ υψηλά μαγνητικά πεδία, καθίσταται ευκολότερη και πιο αξιόπιστη η φασματοσκοπία σε βλάβες του μαστού (Ei Khouli RH et al 2010). Στην ΜRM η φασματοσκοπία δεν μπορεί να δώσει απόλυτες τιμές των μεταβολιτών διότι ο μετρούμενος αριθμός των πρωτονίων που παρουσιάζεται στο φάσμα είναι συνάρτηση πολλών παραμέτρων (που σχετίζονται με τον ασθενή, το πηνίο, το μαγνητικό τομογράφο κ. α. ) οι οποίες καθιστούν τη μέτρηση σχετική. Έτσι η ποσοτικοποίηση της χολίνης γίνεται με δυαδικό τρόπο (παρουσία ή απουσία κορυφής χολίνης). Εάν η κορυφή της χολίνης (αναμενόμενη να εμφανιστεί στα 3,2 ppm) είναι εμφανώς υψηλότερη από το θόρυβο που καταγράφεται στο φάσμα, τότε θεωρείται ότι η χολίνη είναι παρούσα. 56
75 ΕΙΔΙΚΟ ΜΕΡΟΣ 57
76 58
77 1 ΣΚΟΠΟΣ ΤΗΣ ΜΕΛΕΤΗΣ Ο ρόλος της MRM στην παρακολούθηση του μετεγχειρητικού μαστού θεωρείται καταλυτικός δεδομένου ότι το ερώτημα ύπαρξης υποτροπής ή μετεγχειρητικού ουλώδους ιστού σε ορισμένες περιπτώσεις αποτελεί μείζον διαγνωστικό πρόβλημα. Ομοίως, η ανάδειξη πολυκεντρικού και πολυεστιακού καρκίνου του μαστού, η ακριβής εκτίμηση της έκτασης της νόσου και η σύγχρονη διερεύνηση του αντίθετου μαστού αποτελούν δεδομένα που καθορίζουν το θεραπευτικό σχεδιασμό, δεν επιλύονται όμως εύκολα με τις πιο συμβατικές απεικονιστικές μεθόδους. Επίσης η αποτελεσματικότητα του σχήματος της χημειοθεραπείας που εφαρμόζεται σε πολλές περιπτώσεις θα πρέπει άμεσα να εκτιμηθεί και να αποφασισθεί τυχόν τροποποίησή του. Τα δεδομένα της απεικονιστικής μελέτης του μαστού με MRΜ σε μαγνήτη 3Τ είναι περιορισμένα. Σκοπός της παρούσης μελέτης είναι η εκτίμηση των δεδομένων της μελέτης του καρκίνου του μαστού με τις νεότερες τεχνικές MR, σε συσχετισμό με τα παθολογοανατομικά δεδομένα για την αποτελεσματικότερη παρακολούθηση της πορείας της νόσου, το σχεδιασμό της χειρουργικής θεραπείας και γενικά τη διαχείριση του ασθενούς. Ιδιαίτερη έμφαση δίνεται στη χρησιμοποίηση των νεότερων τεχνικών μαγνητικού συντονισμού (τεχνικές διάχυσης, δυναμικής αιμάτωσης και φασματοσκοπίας). Τα δεδομένα όσον αφορά τη διενέργεια MRM σε μηχανήματα υψηλού μαγνητικού πεδίου (3Τ) είναι επίσης περιορισμένα, θεωρείται όμως ότι ανοίγουν νέους ορίζοντες όσον αφορά στην αποτελεσματικότερη ανίχνευση και χαρακτηρισμό των εξεργασιών του μαστού. Σε συσχετισμό με τα παθολογοανατομικά ευρήματα και τα δεδομένα διαχρονικής παρακολούθησης (follow up) θα γίνει προσπάθεια να εξαχθούν συμπεράσματα σχετικά με την αξιοπιστία των εξελιγμένων τεχνικών και τις πιθανές διαφοροδιαγνωστικές δυσκολίες, με αποτέλεσμα να μεγιστοποιηθεί κυρίως η ειδικότητα αλλά και η ευαισθησία των μεθόδων αυτών. Όσον αφορά τον τομέα της πρόληψης, παρόλο που δεν αποτελεί άμεσο ερευνητικό στόχο της παρούσης μελέτης, τα συμπεράσματα που θα εξαχθούν στο σύνολό τους πιθανότατα να συμβάλλουν και προς αυτή την κατεύθυνση. 59
78 2 ΥΛΙΚΟ ΜΕΘΟΔΟΣ 2.1 Τύπος Μελέτης Η μελέτη μας με την MRM περιέλαβε αφ ενός μεν την τεκμηρίωση της ύπαρξης βλάβης ήδη γνωστής από μαστογραφικό και/ή υπερηχογραφικό έλεγχο και αφ ετέρου την ανίχνευση βλάβης για την οποία υπήρχε κλινική υποψία, αν και τα μαστογραφικά και υπερηχογραφικά ευρήματα ήταν αρνητικά. Στη συνέχεια έγινε εκτίμηση του μεγέθους και των λοιπών μορφολογικών χαρακτηριστικών της βλάβης, όπως το σχήμα της, η παρυφή της και η ομοιογένειά της. Ακολούθησε η εκτίμηση πιθανής πολυεστιακότητας και/ή πολυκεντρικότητας στον προσβεβλημένο μαστό, αλλά και η λεπτομερής εκτίμηση του άλλου μαστού για την πιθανή ανίχνευση σύγχρονων κακόηθων βλαβών. Η μελέτη ολοκληρώθηκε με τη μέτρηση προκαθορισμένων παραμέτρων στις βλάβες που ανιχνεύθηκαν, με στόχο τον ακριβέστερο χαρακτηρισμό τους ώστε να γίνει η πιο ενδεδειγμένη θεραπευτική αντιμετώπιση, χειρουργική ή συντηρητική. Στην περίπτωση της χειρουργικής αντιμετώπισης ο σχεδιασμός τροποποιήθηκε σε ολική ή μερική μαστεκτομή, ανάλογα με τα δεδομένα που προέκυψαν από την MRM. Σε περιπτώσεις που με βάση και τα ευρήματα της MRM ελήφθη απόφαση προεγχειρητικής χημειοθεραπίας (Neo-Adjuvant Chemotherapy NAC), η εκτίμηση της αποτελεσματικότητάς της έγινε με MRM επανέλεγχο και συγκριτική αξιολόγηση, ώστε να ακολουθήσει με ασφάλεια η τελική χειρουργική αντιμετώπιση. Μετά τη χειρουργική εκτομή του όγκου έγινε ανδρομική μελέτη και επανεκτίμηση των ευρημάτων της MRM, συσχετισμός με τα ιστοπαθολογικά ευρήματα και καθορισμός της διαγνωστικής ακρίβειας των μετρήσεων. 2.2 Κριτήρια επιλογής των ασθενών Στη μελέτη εντάχθηκαν ασθενείς στις οποίες υπήρχε κλινική ή απεικονιστική υποψία καρκίνου του μαστού, ασθενείς με θετική βιοψία μαστού, καθώς και ασθενείς με βεβαρημένο ατομικό, οικογενειακό ή κληρονομικό ιστορικό. 60
79 2.2.1 Κριτήρια αποκλεισμού 1. Ασθενείς στις οποίες μετά τη χειρουργική αντιμετώπιση δεν απεδείχθη ύπαρξη κακοήθειας. 2. Ασθενείς στις οποίες υπήρχε απομακρυσμένη μεταστατική νόσος. 3. Ασθενείς οι οποίες δεν ήταν δυνατό να υποβληθούν σε MRM λόγω παχυσαρκίας, κλειστοφοβίας ή ύπαρξης βηματοδότη. 2.3 Υλικό Το υλικό μας αποτέλεσαν 210 γυναίκες, ηλικίας 23 έως 91 ετών. Από αυτές οι 194 οδηγήθηκαν στο χειρουργείο μετά την MR-μαστογραφία και οι 16 υποβλήθηκαν σε NAC, κατά τη διάρκεια και στο τέλος της οποίας επανεκτιμήθηκαν με MRΜ. Οι τιμές των παραμέτρων του υλικού που μελετήθηκε παρουσιάζονται στους πίνακες του παραρτήματος. 2.4 Διαδικασία εξέτασης Πριν την απεικόνιση εισάγεται ενδοφλέβιος καθετήρας, ο οποίος συνδέεται με εγχυτή, συμβατό με το μαγνητικό τομογράφο. Η ασθενής τοποθετείται σε πρηνή θέση, πάνω στο εξειδικευμένο πηνίο του μαστού. Η τοποθέτηση της ασθενούς είναι πολύ σημαντική για να ελαχιστοποιηθούν ψευδοεικόνες (artifacts) από κίνηση, βαθιά αναπνοή και ανομοιογένειες του σήματος στα σημεία επαφής με το πηνίο. Είναι πολύ σημαντικό, η ασθενής να νιώθει άνετα στη θέση εξέτασης και να έχει κατανοήσει το πόσο σημαντική είναι η συνεργασία ώστε να μείνει ακίνητη, κυρίως κατά τη χορήγηση της σκιαγραφικής ουσίας και κατά τη διάρκεια της δυναμικής απεικόνισης. Χορηγούνται επίσης ωτοασπίδες για το δυνατό θόρυβο και ένα κουδούνι το οποίο χρησιμοποιεί η ασθενής σε έκτακτη ανάγκη. Είναι απαραίτητο η ασθενής να μην έχει φάει για 4 ώρες πριν την προγραμματισμένη ώρα της εξέτασης. 2.5 Πρωτόκολλο εξέτασης Όλες οι εξετάσεις έγιναν σε μαγνητικό τομογράφο 3Τ- MR (Signa HDx, General Electric Healthcare, Waukesha, WI, USA) Το πηνίο του μαστού είναι ένα πηνίο πολλαπλής συνέργιας με γεωμετρικό σχήμα, τέτοιο ώστε να εξασφαλίζει καλή αναλογία σήματος προς θόρυβο. Αποτελείται από 8 61
80 κανάλια, τα οποία λειτουργούν ανεξάρτητα στο δεξιό και αριστερό μαστό, επιτυγχάνοντας καλύτερη ομοιογένεια και καταστολή του λίπους, καθώς και καλύτερη αναλογία σήματος προς θόρυβο στις οβελιαίες εικόνες. Το πρωτόκολλο εξέτασης περιλαμβάνει τις παρακάτω ακολουθίες με τη σειρά που αναφέρονται. 1. Τομές σε εγκάρσιο επίπεδο ακολουθία 3D Gradient Echo (GRE) T1 με στοιχεία TR: 5,5 ms, TE: 2,2ms, πάχος τομής: 2mm, διάκενο: 0 mm, μήτρα: 388 x Για τη μελέτη της διάχυσης λαμβάνονται τομές σε εγκάρσιο επίπεδο με την ακολουθία Diffusion Weighted Imaging (DWI) και τιμές b: 0 και 1000 s/mm 2, TR: 11000ms, TE: 68ms, πάχος τομής: 3mm, αριθμό επαναλήψεων: (NEX) 4, μήτρα: 100x100. Η τιμή του φαινομενικού συντελεστή διάχυσης (ADC) υπολογίζεται από τον αντίστοιχο χάρτη όπου καταγράφεται η τιμή του ADC στο συμπαγές τμήμα του όγκου. Η μέτρηση γίνεται με κυκλικό ROI και επιλέγεται η περιοχή με τη χαμηλότερη ένταση σήματος στον ADC χάρτη. Για την αποφυγή επιδράσεων από παρακείμενους ιστούς, νεκρώσεις ή αιμορραγικές περιοχές χρησιμοποιείται κυκλικό ROI, το οποίο τοποθετείται προσεκτικά. 3. Για τη μελέτη της δυναμικής αιμάτωσης λαμβάνονται τομές σε εγκάρσιο επίπεδο τα 10 πρώτα δευτερόλεπτα προκειμένου να καταγραφεί η εικόνα αφετηρίας με την ακολουθία 3D (GRE) T1 με καταστολή λίπους (FS), με στοιχεία TR: 5,5ms, TE: 2,2ms, πάχος τομής: 2mm, διάκενο: 0mm, μήτρα: 388 x 388. Μετά την έγχυση παραμαγνητικής ουσίας 10 έως 15 ml, ανάλογα με το σωματικό βάρος, καταγράφεται η αύξηση της έντασης του σήματος. Η διάρκεια της ακολουθίας είναι 60 δευτερόλεπτα και λαμβάνεται 6 συνεχόμενες φορές για την αιμοδυναμική απεικόνιση του μαστού και μία φορά ως καθυστερημένη φάση (τελευταία ακολουθία). Για την ολοκλήρωση της μελέτης δυναμικής αιμάτωσης τα πρωτογενή δεδομένα μεταφέρονται σε ειδικό παράθυρο εργασίας για επεξεργασία. Η μέτρηση γίνεται με κυκλικό ROI, το οποίο τοποθετείται προσεκτικά στην προς μελέτη βλάβη, λαμβάνονται οι τιμές της έντασης σήματος συναρτήσει του χρόνου και κατασκευάζονται οι καμπύλες δυναμικής αιμάτωσης. 62
81 4. Τομές σε οβελιαίο επίπεδο μετά την έγχυση παραμαγνητικής ουσίας με την ακολουθία T1 (GRE) FS με στοιχεία TR: 4,9ms, TE: 1,9ms, πάχος τομής: 1,5mm, διάκενο: 0mm, μήτρα: 224 x Τομές σε εγκάρσιο επίπεδο με την ακολουθία STIR με στοιχεία TR: 5000ms, TE: 90ms, TI: 17ms, NEX: 1, πάχος τομής: 3mm, διάκενο: 0mm, μήτρα: 320 x Τομές σε εγκάρσιο επίπεδο με την ακολουθία T2, με TR: 5200ms, TE: 100ms, NEX: 1, πάχος τομής: 3mm, διάκενο: 0 mm, μήτρα: 320 x Η φασματοσκοπία πρωτονίων γίνεται σε επιλεγμένη τομή και σε επιλεγμένη περιοχή ενδιαφέροντος (voxel) με ακολουθία τύπου BREASE (TE-averaged Point Resolved Spectroscopy - PRESS), με TR: 2000ms, TE: 155ms, NEX: 4, ελάχιστο μέγεθος στοιχειακού όγκου (voxel): 18mm 3. Η καταστολή του σήματος του ύδατος γίνεται με επιλεκτικό παλμό κορεσμού. Ο χρόνος της ακολουθίας κυμαίνεται από 4 έως 5 λεπτά, ανάλογα με το μέγεθος του voxel, με στόχο τον υψηλότερο λόγο σήματος προς θόρυβο. Η περιοχή ενδιαφέροντος επιλέγεται ώστε να μη γειτνιάζει με περιοχές που εμφανίζουν ανομοιογένειες μαγνητικού πεδίου, όπως περιοχές λίπους ή αιμορραγικών στοιχείων. Σε όλες τις περιπτώσεις η λήψη του φάσματος με την ακολουθία BREASE γίνεται μετά από την χορήγηση παραμαγνητικής ουσίας. Το φάσμα εμφανίζει κορυφές, οι οποίες, ανάλογα με τη θέση τους, αντιστοιχούν σε συγκεκριμένους μεταβολίτες. Ενδεικτικό της ποσότητας του κάθε μεταβολίτη αποτελεί το ύψος και το εύρος κάθε κορυφής, με αποτέλεσμα αδρή ποσοτικοποίηση των πληροφοριών. Από τους μεταβολίτες του φάσματος επιλέγεται η κορυφή της χολίνης στα 3,2 ppm, η οποία και μελετάται. 63
82 Πίνακας 2.1 Πρωτόκολλο εξέτασης Τ1W GRE DWI T1W GRE Τ1W GRE STIR T2W FSE SPECTRO- ΕΓΚΑΡΣΙA (b1000) FAT SAT FAT SAT ΕΓΚΑΡΣΙΑ ΕΓΚΑΡΣΙΑ SCOPY (VIBRANT) ΕΓΚΑΡΣΙΑ VIBRANT ΕΓΚΑΡΣΙA PRESS ΟΒΕΛΙΑΙΑ (VIBRANT) TR (ms) 5.5 > >4000 > TE (ms) 2.2 Various ~ TI (ms) Flip Angle Nr of slices voxel F. O. V. (cm) Acquisition Matrix (Frequency /phase) Slice thickness 388/ / / / / / Slice spacing N. E. X Στατιστική Ανάλυση Η στατιστική ανάλυση των αποτελεσμάτων λόγω του μικρού δείγματος ανά ομάδα περιστατικών, ήταν ως επί το πλείστoν περιγραφική, αναφερόμενη σε συχνότητες και ποσοστά. Για τον υπολογισμό των ποσοστών και τη δημιουργία γραφημάτων, πινάκων και αναλύσεων συσχέτισης με μη παραμετρικές μεθόδους καθώς τα αποτελέσματα θα είναι ποιοτικά (Yates DS et al 2008) χρησιμοποιήθηκε το πρόγραμμα Statistical Package for the Social Sciences (SPSS) Version 20 (SPSS, Inc. Chigago IL, USA). 64
83 Πέραν της περιγραφής των δεδομένων, ως μέθοδος στατιστικής ανάλυσης χρησιμοποιήθηκε το Kruska-Wallis test, διαδικασία αντίστοιχη προς την παραμετρική One-way ANOVA, γιατί τα δεδομένα είναι μη παραμετρικά. Χρησιμοποιήθηκε επίσης ο κατά Mann-Whitney έλεγχος για τις μέσες τιμές και για πιθανή συσχέτιση των εξεταζόμενων μεταβλητών, καθώς και το μη παραμετρικό Wilcoxon Signed Ranks Test στην ομάδα NAC, με όριο στατιστικής σημαντικότητας το p<0. 05 (Yates et al 2008). Η δοκιμασία Wilcoxon signed-rank είναι ένα μη-παραμετρικό τεστ στατιστικής υπόθεσης που χρησιμοποιείται κατά τη σύγκριση των δύο σχετικών μεταξύ τους δειγμάτων, ή επαναλαμβανόμενων μετρήσεων σε ένα μόνο δείγμα. Μπορεί να χρησιμοποιηθεί ως εναλλακτική λύση για το παραμετρικό t-test, όταν ο πληθυσμός δεν μπορεί να υποτεθεί ότι είναι κανονικά κατανεμημένος (Yates DS et al 2008) Συσχετίσεις Η συσχέτιση μετρά το βαθμό συνάφειας - αλληλεπίδρασης ανάμεσα σε δύο ή περισσότερες μεταβλητές. Πρακτικά σημαίνει, ότι από την τιμή ενός δείκτη (συντελεστή συσχέτισης) κατανοούμε πόσο έντονη ή χαλαρή είναι η συσχέτιση δύο μεταβλητών. Η διαδικασία συσχέτισης παρουσιάζεται όχι μόνο σε ποσοτικές μεταβλητές (συντελεστής Pearson) αλλά και σε ποιοτικές ή κατηγοριοποιημένες μεταβλητές, δηλαδή μεταβλητές των οποίων οι τιμές δεν επιδέχονται ιεράρχηση (συντελεστή Spearman) (Corder GW et al 2009). Οι συντελεστές συσχέτισης χωρίζονται σε δύο κατηγορίες. Η πρώτη αφορά το συντελεστή γραμμικής συσχέτισης του Pearson και αναφέρεται σε ποσοτικές μεταβλητές και η δεύτερη κατηγορία αφορά τους συντελεστή Spearman, που χρησιμοποιείται σε ποιοτικές και κατηγοριοποιημένες μεταβλητές. 65
84 3 ΑΠΟΤΕΛΕΣΜΑΤΑ Τα αποτελέσματα της μελέτης μας έχουν κατηγοριοποιηθεί σε 4 ομάδες. Οι τρείς ομάδες έχουν προκύψει με βάση τα τελικά ιστοπαθολογικά δεδομένα, τα οποία ελήφθησαν μετά τη χειρουργική εξαίρεση των όγκων. Στην πρώτη ομάδα περιλαμβάνονται 21 ασθενείς με ιστολογικά επιβεβαιωμένο διηθητικό λοβιακό καρκίνο (ILC). Στη δεύτερη ομάδα περιλαμβάνονται 13 ασθενείς με ιστολογικά επιβεβαιωμένο in situ καρκίνωμα πόρων (DCIS). Στην τρίτη ομάδα περιλαμβάνονται 160 ασθενείς με ιστολογικά επιβεβαιωμένο διηθητικό καρκίνωμα πόρων (IDC). Στην τέταρτη ομάδα περιλαμβάνονται 16 ασθενείς οι οποίες υποβλήθηκαν σε MRM, στη συνέχεια ακολούθησε προεγχειρητική χημειοθεραπεία (NAC), τα αποτελέσματα της οποίας εκτιμήθηκαν με επαναληπτική MRM. 3.1 Διηθητικός λοβιακός καρκίνος (ILC) Και στις 21 περιπτώσεις οι βλάβες είχαν ασαφή όρια στην MRM. Όσον αφορά την ηλικιακή κατανομή η μεγαλύτερη συχνότητα ILC καταγράφεται στην ηλικία των 62 ετών και ο μέσος όρος είναι 56 έτη, ενώ στις 21 περιπτώσεις μόνο μία γυναίκα ήταν ηλικίας μικρότερης των 40 ετών. 66
85 Πίνακας 3.1 Ηλικιακή κατανομή ILC Έτη Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό ,8 4, ,5 14, ,8 19, ,5 28, ,8 33, ,8 38, ,8 42, ,8 47, ,8 52, ,8 57, ,8 61, ,3 76, ,5 85, ,8 90, ,8 95, ,8 100,0 Σύνολο ,0 67
86 Γράφημα 3.1 Ηλικιακή κατανομή ILC Όσον αφορά τους τύπους των καμπυλών που προέκυψαν μετά τη δυναμική ενδοφλέβια έγχυση παραμαγνητικής ουσίας, όπως φαίνεται από τον πίνακα 3.2, στο 14,3% των περιπτώσεων η κινητική του σκιαστικού ήταν τύπου Ι. Στο 33,3% των περιπτώσεων ήταν τύπου ΙΙ και στο 52,4% των περιπτώσεων ήταν τύπου ΙΙΙ. 68
87 Πίνακας 3.2 Τύπος καμπύλης εμπλουτισμού ILC Τύπος καμπύλης Αριθμός Περιστατικών Ποσοστό % ΤΥΠΟΣ Ι PERSISTENT 3 14,3 ΤΥΠΟΣ ΙΙ PLATEAU 7 33,3 ΤΥΠΟΣ ΙΙΙ WASHOUT 11 52,4 Σύνολο ,0 Τα παραπάνω δεδομένα απεικονίζονται παραστατικά και στο γράφημα 3.2 Γράφημα 3.2 Ποσοστιαία κατανομή της κινητικής του σκιαστικού στο ILC 69
88 Όσον αφορά το συντελεστή προφανούς διάχυσης (ADC) οι τιμές του μετρήθηκαν ως εξής: Σε 1 από τις 21 περιπτώσεις (4. 8%) η τιμή ADC ήταν 0,5 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (4,8%) η τιμή ADC ήταν 0,6 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (4. 8%) η τιμή ADC ήταν 0,7 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (4,8%) η τιμή ADC ήταν 0,8 Χ 10-3 mm 2 /sec. Σε 3 περιπτώσεις (14,3%) η τιμή ADC ήταν 0,9 Χ 10-3 mm 2 /sec. Σε 12 περιπτώσεις (57,1%) η τιμή ADC ήταν 1 Χ 10-3 mm 2 /sec. Σε 2 περιπτώσεις (9,5%) η τιμή ADC ήταν 1,1 Χ 10-3 mm 2 /sec. Πίνακας 3.3 ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec στο ILC ADC Αριθμός Περιστατικών Ποσοστό % 0,5 1 4,8 0,6 1 4,8 0,7 1 4,8 0,8 1 4,8 0,9 3 14,3 1, ,1 1,1 2 9,5 Σύνολο ,0 70
89 Τα παραπάνω δεδομένα απεικονίζονται παραστατικά και στο γράφημα 3.3 Γράφημα 3.3 Ποσοστιαία κατανομή του ADC στο ILC Όσον αφορά τη φασματοσκοπική ανίχνευση χολίνης στις βλάβες, όπως φαίνεται στον πίνακα 3.4, σε 11 περιπτώσεις (ποσοστό 52,4%) δεν κατέστη τεχνικά δυνατή στην περιοχή του ενδιαφέροντος η λήψη φάσματος. Από τις υπόλοιπες 10 περιπτώσεις στις οποίες μελετήθηκε το φάσμα, σε 4 περιπτώσεις δεν ανιχνεύθηκε χολίνη, ενώ σε 6 περιπτώσεις το φάσμα ήταν θετικό για χολίνη. 71
90 Πίνακας 3.4 Spectroscopy - Φασματοσκοπία (Χολίνη ppm) στο ILC Χολίνη Αριθμός Περιστατικών Ποσοστό % OXI 4 19,0 NAI 6 28,6 Σύνολο 10 47,6 Έλλειψη Δεδομένων 11 52,4 Σύνολο ,0 Τα παραπάνω δεδομένα απεικονίζονται παραστατικά και στο γράφημα 3.4. Γράφημα 3.4 Ποσοστιαία κατανομή της ανίχνευσης χολίνης στο ILC 72
91 Όσον αφορά την πολυεστιακότητα του ILC, αυτή αφορούσε το 56,5% των περιπτώσεων, ενώ στο 43,5% των περιπτώσεων η βλάβη ήταν μονοεστιακή (Πίνακας 3.5). Είναι σημαντικό να αναφερθεί ότι τα ευρήματα της MRM αντιστοιχούσαν σε αυτά της ιστοπαθολογικής εξέτασης όσον αφορά την πολυεστιακότητα. Σε όλες τις περιπτώσεις που μικροσκοπικά ανιχνεύονταν πολλαπλές εστίες, στη μαγνητική μαστογραφία είχαν αναδειχθεί πολλαπλές εστίες αυξημένου εμπλουτισμού. Πίνακας 3.5 Πολυεστιακότητα ILC ΑΡΙΘΜΟΣ ΕΣΤΙΩΝ Αρ. Περιστατικών Ποσοστό% ΜΟΝΟΕΣΤΙΑΚΟ 9 42,8 ΠΟΛΥΕΣΤΙΑΚΟ 12 57,2 Σύνολο ,0 Τα παραπάνω δεδομένα απεικονίζονται παραστατικά και στο γράφημα 3.5. Γράφημα 3.5 Ποσοστιαία κατανομή της πολυεστιακότητας του ILC 73
92 Όσον αφορά την πολυκεντρικότητα, σε 6 από τις 21 περιπτώσεις, πλην της κύριας βλάβης στην MRΜ συνυπήρχαν εστίες σε άλλα τμήματα του ίδιου μαστού (Γράφημα 3.6). Αυτό αποτέλεσε καθοριστικό εύρημα για την περαιτέρω χειρουργική αντιμετώπιση. Σε όλες τις παραπάνω περιπτώσεις έγινε ολική μαστεκτομή. Η ιστοπαθολογική εξέταση επιβεβαίωσε την πολυκεντρικότητα του νεοπλάσματος. Με την πρώιμη απόφαση της ολικής μαστεκτομής απετράπει ο κίνδυνος της υποτροπής και ενδεχόμενης χειρουργικής επανεκτομής. Γράφημα 3.6 Ποσοστιαία κατανομή της πολυκεντρικότητας στο ILC Όσον αφορά την παρουσία παθολογικών μασχαλιαίων λεμφαδένων στο 66,7% των περιπτώσεων δεν ανιχνεύθηκαν στη μαγνητική μαστογραφία, ενώ στο 33,3% ανιχνεύθηκαν θετικοί μασχαλιαίοι λεμφαδένες (Πίνακας 3.6 και γράφημα 3.7). Τα ευρήματα αυτά συμφωνούσαν απόλυτα με τα ιστοπαθολογικά δεδομένα. 74
93 Πίνακας 3.6 Παρουσία μασχαλιαίων λεμφαδένων στο ILC Παρουσία Λεμφαδένων Αριθμός Περιστατικών Ποσοστό% OXI 14 66,7 NAI 7 33,3 Σύνολο ,0 Γράφημα 3.7 Παρουσία μασχαλιαίων λεμφαδένων στο ILC Όσον αφορά το μέγεθος της βλάβης, όπως φαίνεται στο γράφημα 3.8, τα αποτελέσματα κατηγοριοποιήθηκαν σε τρείς ομάδες. Η πρώτη ομάδα περιέλαβε όγκους που είχαν μέγεθος μέχρι 2cm. Η δεύτερη ομάδα περιέλαβε όγκους με μέγεθος 2 έως 5cm και η τρίτη όγκους με μέγεθος μεγαλύτερο των 5cm. Το ποσοστό της πρώτης ομάδας ήταν το 38,1% του συνόλου, της δεύτερης ήταν επίσης 38,1%, και της τρίτης το 23,8% του συνόλου. 75
94 Γράφημα 3.8 Κατανομή μεγέθους στο ILC Η εμφάνιση της βλάβης στην MRM ως μάζα (mass) ή ως μη μάζα (non mass) παριστάνεται στο γράφημα 3.9. Σύμφωνα με αυτό, η βλάβη στο 23,81% του συνόλου δεν είχε εμφάνιση μάζας, ενώ στο 76,19% εμφανιζόταν ως μάζα. Γράφημα 3.9 Εμφάνιση της βλάβης ως μάζα ή μη μάζα στο ILC 76
95 Σύμφωνα με το γράφημα 3.10, στο 33,33% των περιπτώσεων η βλάβη στο πρώτο λεπτό μετά την ενδοφλέβια έγχυση παραμαγνητικής ουσίας εμφάνισε μέτριο εμπλουτισμό που κυμαινόταν από 50 μέχρι 100 μονάδες. Στο 66,67% ο εμπλουτισμός στο πρώτο λεπτό ήταν υψηλός (άνω των 100 μονάδων). Γράφημα 3.10 Πρώιμος εμπλουτισμός στο ILC Όσον αφορά την ποσοστιαία κατανομή της συνύπαρξης ή όχι επιπρόσθετων ιστολογικών τύπων πλην του κυρίαρχου ILC, τα αποτελέσματα κατηγοριοποιήθηκαν σε τέσσερις επιμέρους ομάδες: Στην πρώτη ομάδα το νεόπλασμα ήταν αμιγώς ILC και αντιπροσώπευε το 52,38% του συνόλου. Στη δεύτερη ομάδα που συνιστούσε το 4,76% του συνόλου, συνυπήρχαν ILC και IDC. Στην τρίτη ομάδα που αντιπροσώπευε το 9,52% συνυπήρχαν ILC και LCIS. Τέλος, στην τέταρτη ομάδα (33,33% του συνόλου) συνυπήρχαν ILC, IDC και in situ καρκίνωμα. Τα αποτελέσματα αυτά φαίνονται στον πίνακα 3.7 και στον αναλυτικό πίνακα 3.8, καθώς και στο γράφημα
96 Πίνακας 3.7 Συνυπάρχουσες βλάβες εκτός της κύριας κύριας ILC βλάβης OΜΑΔΕΣ Αριθμός Περιστατικών Ποσοστό % , , , ,3 Σύνολο ,0 Ομάδα 1: ILC, Ομάδα 2: ILC και IDC, Ομάδα 3: ILC και LCIS, Ομάδα 4: ILC και IDC και LCIS και/ή DCIS Πίνακας 3.8 Αναλυτικός κατάλογος ιστολογικών τύπων συνυπαρχουσών βλαβών πλην της κύριας ILC βλάβης Ιστολογικός Τύπος Ιστολογικός Συνύπαρξη in situ καρκίνου Τύπος ΟΜΑΔΕΣ ΔΙΗΘΗΤΙΚΟ ( Πόρων & Λοβιακό) 2 ΔΙΗΘΗΤΙΚΟ ( Πόρων & Λοβιακό) 4 IN SITU ΛΟΒΙΑΚΟ ΔΙΗΘΗΤΙΚΟ ( Πόρων & Λοβιακό) 4 IN SITU ( Πόρωνκαι Λοβιακό) ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 3 ΙΝ SITU ΛΟΒΙΑΚΟ ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 3 ΙΝ SITU ( Πόρων και λοβιακό) ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 3 ΙΝ SITU ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 3 IN SITU ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 3 IN SITU ΛΟΒΙΑΚΟ ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 3 IN SITU ΛΟΒΙΑΚΟ ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 3 IN SITU ΛΟΒΙΑΚΟ ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 ΔΙΗΘΗΤΙΚΟ ΛΟΒΙΑΚΟ 1 78
97 Γράφημα 3.11 Ποσοστιαία κατανομή του ιστολογικού τύπου του ILC 79
98 3.1.1 ΕΙΚΟΝΕΣ ILC A B Γ Δ Ε ΣΤ Εικόνα 3.1 Διηθητικό Λοβιακό Καρκίνωμα σε γυναίκα ασθενή 56 ετών με ψηλαφητό μόρφωμα στο ουραίο τμήμα του αριστερού μαστού. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρείται έντονα εμπλουτιζόμενη εξεργασία, με κατά τόπους ανώμαλη παρυφή. Η καμπύλη της δυναμικής του σκιαστικού (Β) είναι τύπου ΙΙΙ (washout). Στην ακολουθία STIR (Γ) η βλάβη εμφανίζει ανομοιογενές κύρια υψηλό σήμα. Στις εικόνες διάχυσης DWI (Δ) το σήμα είναι υψηλό,ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (Ε) προκύπτει τιμή ίση με 0. 9 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (ΣΤ) ανιχνεύεται χολίνη στα 3.2ppm. 80
99 Εικόνα 3.2 Διηθητικό Λοβιακό Καρκίνωμα πολυκεντρικό σε γυναίκα ασθενή 52 ετών με ψηλαφητή σκληρία στο δεξιό μαστό και αρνητικό μαστογραφικό και υπερηχογραφικό έλεγχο. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσιες τομές, όπου παρατηρείται έντονα εμπλουτιζόμενη, διάχυτη εξεργασία, με ασαφή όρια. Οι καμπύλες της δυναμικής του σκιαστικού σε διαδοχικά επίπεδα είναι τύπου ΙΙ (plateau) και ΙΙΙ (washout). Στις εικόνες διάχυσης DWI σε διαδοχικά επίπεδα (Β) το σήμα είναι υψηλό,ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτουν τιμές χαμηλές από 0,9 mm 2 /sec έως 1,1 mm 2 /sec. Στις εικόνες τρισδιάστατης ανασύνθεσης ΜΙP (Γ) αναδεικνύεται η μεγάλη έκταση της εξεργασίας η οποία για το λόγο αυτό θεωρήθηκε πολυκεντρική. 81
100 A Β Γ Δ Ε Εικόνα 3.3 Διηθητικό Πλειόμορφο Λοβιακό Καρκίνωμα σε γυναίκα ασθενή 62 ετών που προσήλθε με ψηλαφητούς λεμφαδένες στην αριστερή μασχάλη. Ο μαστογραφικός και υπερηχογραφικός έλεγχος ήταν αρνητικός. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσιες τομές, όπου παρατηρούνται τουλάχιστον τρείς εμπλουτιζόμενες εστίες μικρότερες του ενός εκατοστού, με σαφή όρια. (Β) Η καμπύλη της δυναμικής του σκιαστικού είναι τύπου ΙΙ (plateau). Στις εικόνες Γ, Δ και Ε (Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσιες, οβελιαίες και στεφανιαίες τομές) αναδεικνύεται με σαφήνεια το λεμφαδενικό block της αριστερής μασχάλης. 82
101 Εικόνα 3.4 Διηθητικό Λοβιακό Καρκίνωμα σε γυναίκα ασθενή 47 ετών με ψηλαφητή βλάβη στο δεξιό μαστό. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρείται εμπλουτιζόμενη περιοχή (non mass enhancement). Η καμπύλη της δυναμικής του σκιαστικού (Β) είναι τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Γ) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (Δ) προκύπτει τιμή ίση με 0.8 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Ε) ανιχνεύεται υψηλή κορυφή χολίνης στα 3.2 ppm. 83
102 3.2 In Situ καρκίνος των πόρων (DCIS) Ο συνολικός αριθμός των ασθενών στους οποίους μετά τη χειρουργική εξαίρεση ιστολογικά επιβεβαιώθηκε DCIS ήταν 13. Μελετήθηκε η διακύμανση όσον αφορά την ηλικία, την ύπαρξη σαφών ή ασαφών ορίων στη βλάβη, την παρουσία πρώιμου εμπλουτισμού και την πολυεστιακότητα. Συγκεντρωτικά, τα γενικά στατιστικά παρουσιάζονται στον πίνακα 3.9. Πίνακας 3.9 Γενικά στατιστικά στο DCIS Ηλικία Όρια ΠΡΩΙΜΟΣ ΕΜΠΛΟΥΤΙΣΜΟΣ wash in Τύπος καμπύλης ΠΟΛΥΕΣΤΙ ΑΚΟΤΗΤΑ N Σταθερή Απόκλιση 0,516 0,480 20,878 0,641 0,519 Διακύμανση 0,267 0, ,897 0,410 0,269 Όσον αφορά την ηλικιακή κατανομή, σύμφωνα με τον πίνακα 3.10 και γράφημα 3.12 η συχνότητα της νόσου είναι περίπου ίση πριν και μετά τα 40 έτη, ενώ στις 13 ασθενείς που μελετήθηκαν καμία δεν ήταν κάτω των 30 ετών. Πίνακας 3.10 Ηλικιακή κατανομή στο DCIS Ηλικία (έτη) Αριθμός. Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό (%) ,7 7, ,4 23, ,7 30, ,7 38, ,4 53, ,7 61, ,7 69, ,7 76, ,4 92, ,7 100,0 Σύνολο ,0 84
103 Γράφημα 3.12 Ηλικιακή κατανομή στο DCIS Όσον αφορά τα όρια των βλαβών, όπως φαίνεται στον πίνακα 3.11 και στο γράφημα 3.13, στο 92,3% των περιπτώσεων ήταν ασαφή, ενώ στο 7,7% των περιπτώσεων τα όρια ήταν σαφή. Πίνακας 3.11 Όρια βλαβών στο DCIS Όρια Αριθμός Ποσοστό (%) Αθροιστικό (%) Περιστατικών 12 92,3 92,3 ΣΑΦΗ 1 7,7 100,0 Σύνολο ,0 85
104 Γράφημα 3.13 Κατανομή ορίων βλάβης στο DCIS Όσον αφορά το μέγεθος των βλαβών, όπως φαίνεται στον πίνακα 3.12 και στο γράφημα 3.14, τα αποτελέσματα κατηγοριοποιήθηκαν σε τρείς ομάδες. Στην πρώτη ομάδα που περιελάμβανε όγκους με διαμέτρους μέχρι 2cm, η συχνότητα ήταν 46,2%, ενώ στη δεύτερη ομάδα που περιελάμβανε όγκους με διαμέτρους από 2cm μέχρι 4cm, η συχνότητα ήταν 38,5%. Τέλος στην τρίτη ομάδα που περιελάμβανε όγκους με διαμέτρους μεγαλύτερες των 4cm, η συχνότητα ήταν 15,4%. 86
105 Πίνακας 3.12 Μέγεθος (διάμετρος σε cm) στο DCIS Ομάδες Αριθμός Ποσοστό (%) Αθροιστικό (%) Περιστατικών ,2 46, ,5 84, ,4 100,0 Σύνολο ,0 Ομάδα 1: (0-2cm), Ομάδα 2: (2-4cm), Ομάδα 3: ( >4cm) Γράφημα 3.14 Μέγεθος βλαβών στο DCIS 87
106 Όσον αφορά τον πρώιμο εμπλουτισμό των βλαβών μετά την ενδοφλέβια έγχυση παραμαγνητικής ουσίας, όπως φαίνεται αναλυτικά στον πίνακα 3.13 και στο γράφημα 3.15 μόνο σε 1 περίπτωση (συχνότητα 7,7%) υπήρξε εμπλουτισμός μικρότερος των 100 μονάδων, ενώ στις υπόλοιπες 12 περιπτώσεις (ποσοστό 92,3%) ο πρώιμος εμπλουτισμός ήταν μεγαλύτερος των 100 μονάδων. Πίνακας 3.13 Πρώιμος Εμπλουτισμός - wash in στο DCIS Μονάδες UI συγκέντρωσης σκιαστικού Αριθμός Περιστατικών Ποσοστό % Αθροιστικό (%) ,7 7, ,4 23, ,8 53, ,4 69, ,7 76, ,4 92, ,7 100,0 Σύνολο ,0 88
107 Γράφημα 3.15 Συχνότητα πρώιμου εμπλουτισμού στο DCIS Όσον αφορά τους τύπους των καμπυλών που προέκυψαν μετά τη δυναμική ενδοφλέβια έγχυση παραμαγνητικής ουσίας, όπως φαίνεται από τον πίνακα 3.14 και στο γράφημα 3.16, στο 15,4% των περιπτώσεων η κινητική του σκιαστικού ήταν τύπου Ι. Στο 61,5% των περιπτώσεων ήταν τύπου ΙΙ και στο 23,1% των περιπτώσεων ήταν τύπου ΙΙΙ. Πίνακας 3.14 Συχνότητα τύπου καμπύλης στο DCIS Τύπος καμπύλης Αριθμός Ποσοστό(%) Αθροιστικό (%) Περιστατικών Ι 2 15,4 15,4 ΙΙ 8 61,5 76,9 ΙΙΙ 3 23,1 100,0 Σύνολο ,0 89
108 Γράφημα 3.16 Τύπος Καμπύλης στο DCIS Όσον αφορά το συντελεστή προφανούς διάχυσης (ADC) οι τιμές του μετρήθηκαν ως εξής: Σε 9 από τις 13 περιπτώσεις (69,2%) η τιμή ADC ήταν 1 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (7,7%) η τιμή ADC ήταν 1,1 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (7,7%) η τιμή ADC ήταν 1,2 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (7,7%) η τιμή ADC ήταν 1,3 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (7,7%) η τιμή ADC ήταν 1,5 Χ 10-3 mm 2 /sec. 90
109 Τα παραπάνω φαίνονται παραστατικά στον πίνακα 3.15 και στο γράφημα Πίνακας 3.15 ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec στο DCIS ADC Αριθμός. Ποσοστό % Αθροιστικό (%) Περιστατικών 1,0 9 69,2 69,2 1,1 1 7,7 76,9 1,2 1 7,7 84,6 1,3 1 7,7 92,3 1,5 1 7,7 100,0 Σύνολο ,0 Γράφημα 3.17 Κατανομή συντελεστή προφανούς διάχυσης (ADC) στο DCIS Όσον αφορά τη φασματοσκοπική ανίχνευση χολίνης στις βλάβες, όπως φαίνεται στον πίνακα 3.16 και στο γράφημα σε 3 περιπτώσεις δεν κατέστη τεχνικά δυνατή στην περιοχή του ενδιαφέροντος η λήψη φάσματος. Από τις υπόλοιπες 91
110 10 περιπτώσεις στις οποίες μελετήθηκε το φάσμα, σε 4 περιπτώσεις δεν ανιχνεύθηκε χολίνη, ενώ σε 6 περιπτώσεις το φάσμα ήταν θετικό για χολίνη. Πίνακας 3.16 Spectroscopy - Φασματοσκοπία (Χολίνη ppm) στο DCIS Παρουσία χολίνης Αριθμός Περιστατικών Συχνότητα (%) Αθροιστικό (%) όχι 4 30,8 40,0 ναι 6 46,2 100,0 Σύνολο 10 76,9 3 23,1 Σύνολο ,0 Γράφημα 3.18 Κατανομή ανίχνευσης χολίνης στο DCIS 92
111 Όσον αφορά την ποσοστιαία κατανομή της συνύπαρξης ή όχι επιπρόσθετων ιστολογικών τύπων πλην του κυρίαρχου DCIS, τα αποτελέσματα κατηγοριοποιήθηκαν σε δυο επιμέρους ομάδες: Στην πρώτη ομάδα το νεόπλασμα ήταν αμιγώς DCIS και αντιπροσώπευε το 69,2% του συνόλου. Στη δεύτερη ομάδα που συνιστούσε το 30,8% του συνόλου, συνυπήρχαν DCIS και LCIS. Τα αποτελέσματα αυτά φαίνονται στον πίνακα 3.17 και στο γράφημα 3.19 Πίνακας 3.17 Ιστολογικός Τύπος στο DCIS Ιστολογικός Αριθμός Συχνότητα (%) Αθροιστικό % Τύπος Περιστατικών ,2 69, ,8 100,0 Σύνολο ,0 Ομάδα 1: Αμιγές DCIS, Ομάδα 2: Συνύπαρξη DCIS και LCIS Γράφημα 3.19 Κατανομή ιστολογικών τύπων στο DCIS 93
112 Όσον αφορά την πολυεστιακότητα, σε 7 από τις 13 περιπτώσεις πλην της κύριας βλάβης στην MRΜ συνυπήρχαν εστίες σε άλλες περιοχές του ίδιου τεταρτημορίου του μαστού (Πίνακας 3.18 και γράφημα 3.20). Αυτό αποτέλεσε καθοριστικό εύρημα για το σχεδιασμό της χειρουργικής αντιμετώπισης. Πίνακας 3.18 Πολυεστιακότητα στο DCIS Πολυεστιακότητα Αριθμός Περιστατικών Ποσοστό(%) Αθροιστικό % ναι 7 53,8 53,8 όχι 6 46,2 100,0 Σύνολο ,0 Γράφημα 3.20 Πολυεστιακότητα στο DCIS Όσον αφορά το βαθμό κακοήθειας (grade) 4 στα 13 περιστατικά DCIS ήταν υψηλού βαθμού κακοήθειας (grade III) ενώ τα υπόλοιπα ήταν χαμηλού ή ενδιάμεσου βαθμού κακοήθειας (grade I ή ΙΙ). 94
113 3.2.1 ΕΙΚΟΝΕΣ DCIS Εικόνα 3.5. In Situ Καρκίνωμα Πόρων σε γυναίκα ασθενή 39 ετών με μαστογραφία στην οποία απεικονίζονταν ύποπτες μικροεπασβεστώσεις στον αριστερό μαστό. (Α,Β) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρείται εμπλουτιζόμενη περιοχή (non mass enhancement). Η καμπύλη της δυναμικής του σκιαστικού (Γ) είναι τύπου ΙΙ plateau. Στις εικόνες διάχυσης DWI (Δ) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (Ε) προκύπτει τιμή ίση με 1,1 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (ΣΤ) δεν ανιχνεύεται χολίνη στα 3.2ppm. 95
114 Εικόνα 3.6 In Situ Καρκίνωμα Πόρων σε γυναίκα ασθενή 42 ετών με αιματηρό έκκριμα από τη θηλή του δεξιού μαστού. (Α,Β) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή και τρισδιάστατη ανασύνθεση (Γ), όπου παρατηρείται εκτεταμένη εμπλουτιζόμενη περιοχή (non mass enhancement). Η καμπύλη της δυναμικής του σκιαστικού (Δ) είναι τύπου ΙΙ plateau. Στις εικόνες διάχυσης DWI (Ε) παρατηρούνται εστίες υψηλού σήματος, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (ΣΤ) προκύπτει τιμή ίση με 0,9 mm 2 /sec. 96
115 Εικόνα 3.7 Πολυεστιακό In Situ Καρκίνωμα Πόρων σε γυναίκα ασθενή 43 ετών με μαστογραφία στην οποία απεικονίστηκε μία ομάδα ύποπτων μικροεπασβεστώσεων στο δεξιό μαστό. (Α,Β) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρείται εκτεταμένη εμπλουτιζόμενη περιοχή (non mass enhancement), πολύ μεγαλύτερη συγκριτικά με τη μαστογραφική βλάβη. Η καμπύλη της δυναμικής του σκιαστικού (Γ) είναι τύπου ΙΙΙ washout. Στις εικόνες διάχυσης DWI (Δ) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (Ε) προκύπτει τιμή ίση με 0,8 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (ΣΤ) ανιχνεύεται χολίνη στα 3.2ppm. 97
116 3.3 Διηθητικός καρκίνος των πόρων (IDC) Ο συνολικός αριθμός των ασθενών στους οποίους μετά τη χειρουργική εξαίρεση ιστολογικά επιβεβαιώθηκε IDC ήταν 160. Μελετήθηκε η διακύμανση όσον αφορά την ηλικία, το μέγεθος, την ύπαρξη σαφών ή ασαφών ορίων στη βλάβη, την παρουσία πρώιμου εμπλουτισμού, τον τύπο των καμπυλών εμπλουτισμού, το συντελεστή προφανούς διάχυσης, τη φασματοσκοπία, τους συνυπάρχοντες ιστολογικούς τύπους πλην του IDC, το βαθμό κακοήθειας (grade) των βλαβών, την πολυεστιακότητα, την πολυκεντρικότητα και την παρουσία ή όχι θετικών μασχαλιαίων λεμφαδένων. Συγκεντρωτικά, τα γενικά στατιστικά παρουσιάζονται στον πίνακα Πίνακας 3.19 Γενικά Στατιστικά στο IDC N Μέση τιμή Τυπική απόκλιση Διακύμανση Όρια 160 1,06 0,243 0,059 Μέγεθος 160 1,781 0,7153 0,512 ΠΡΩΙΜΟΣ ΕΜΠΛΟΥΤΙΣΜΟΣ 160 2,99 0,079 0,006 Τύπος καμπύλης 160 2,79 0,421 0,177 ADC (Χ 10-3 mm 2 /sec) Φασματοσκοπία (Χολίνη) 158 0, , ,73 0,447 0,200 Ιστολογικός Τύπος 160 0,48 0,654 0,427 Βαθμός (GRADE) 159 2,32 0,723 0,523 Πολυεστιακότητα 160 0,29 0,457 0,209 Πολυκεντρικότητα 160 0,21 0,406 0,165 Λεμφαδένες 160 0, ,252 98
117 Όσον αφορά την ηλικιακή κατανομή, σύμφωνα με τον πίνακα 3.20 και τα γραφήματα 3.21 και 3.22 η συχνότητα της νόσου είναι μεγαλύτερη στην ηλικιακή ομάδα των 40 έως 60 ετών. Πίνακας 3.20 Ηλικιακή κατανομή στο IDC Ηλικιακή Ομάδα Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό ,0 20, ,3 76,3 > ,8 100,0 Σύνολο ,0 Η ηλικία ομαδοποιημένη σε 3 ομάδες:ομάδα 1: 25-39, Ομάδα 2: 40-59, Ομάδα 3: >60 Γράφημα 3.21 Ηλικιακή κατανομή στο IDC 99
118 Γράφημα 3.22 Ηλικιακή κατανομή στο IDC Όσον αφορά τα όρια των βλαβών, όπως φαίνεται στον πίνακα 3.21 και στο γράφημα 3.23, στο 93,8% των περιπτώσεων ήταν ασαφή, ενώ στο 6,3% των περιπτώσεων τα όρια ήταν σαφή. Πίνακας 3.21 Όρια βλαβών στο IDC Όρια Αριθμός Περιστατικών Ποσοστό(%) Αθροιστικό Ποσοστό Ασαφή ,8 93,8 Σαφή 10 6,3 100,0 Σύνολο ,0 100
119 Γράφημα 3.23 Όρια βλαβών στο IDC Όσον αφορά το μέγεθος των βλαβών, όπως φαίνεται στον πίνακα 3.22 και στο γράφημα 3.24, τα αποτελέσματα κατηγοριοποιήθηκαν σε τρείς ομάδες. Στην πρώτη ομάδα που περιελάμβανε όγκους με διαμέτρους μέχρι 2cm, η συχνότητα ήταν 38,8%, ενώ στη δεύτερη ομάδα που περιελάμβανε όγκους με διαμέτρους από 2cm μέχρι 5cm, η συχνότητα ήταν 44,4%. Τέλος στην τρίτη ομάδα που περιελάμβανε όγκους με διαμέτρους μεγαλύτερες των 5cm, η συχνότητα ήταν 16,9%. Πίνακας 3.22 Μέγεθος (ομάδες) στο IDC Μέγεθος Αριθμός Περιστατικών Ποσοστό(%) Αθροιστικό Ποσοστό(%) Oμάδα 1 (0-2cm) 62 38,8 38,8 Ομάδα 2 (2-5cm) 71 44,4 83,1 Ομάδα 3 (>5cm) 27 16,9 100,0 Σύνολο ,0 101
120 Γράφημα 3.24 Μέγεθος (ομάδες) στο IDC Όσον αφορά τον πρώιμο εμπλουτισμό των βλαβών (wash in) μετά την ενδοφλέβια έγχυση παραμαγνητικής ουσίας, όπως φαίνεται αναλυτικά στους πίνακες 3.24 και 3.25 και στο γράφημα 3.25, μόνο σε 1 περίπτωση (ποσοστό 0,6%) υπήρξε εμπλουτισμός μικρότερος ή ίσος των 100 μονάδων, ενώ στις υπόλοιπες 159 περιπτώσεις (ποσοστό 99,4%) ο πρώιμος εμπλουτισμός ήταν μεγαλύτερος των 100 μονάδων. Πίνακας 3.23 Πρώιμος Εμπλουτισμός στο IDC Μονάδες Αριθμός συγκέντρωσης Περιστατικών σκιαστικού 102 Ποσοστό (%) Αθροιστικό ποσοστό (%) ,6 0, ,4 5, ,. 4 9, ,1 12, ,6 18, ,1 21, ,1 2, ,5 3, ,4 51, ,. 5 6, , ,1 81, ,6 91, ,4 96, ,1 99, ,6 100,0 Σύνολο ,0
121 Γράφημα 3.25 Πρώιμος Εμπλουτισμός στο IDC Όσον αφορά τους τύπους των καμπυλών που προέκυψαν μετά τη δυναμική ενδοφλέβια έγχυση παραμαγνητικής ουσίας, όπως φαίνεται από τον πίνακα 3.25 και στο γράφημα 3.26 μόνο σε 1 περίπτωση (0,6%) η κινητική του σκιαστικού ήταν τύπου Ι. Στο 19,4% των περιπτώσεων ήταν τύπου ΙΙ και στο 80% των περιπτώσεων ήταν τύπου ΙΙΙ. Πίνακας 3.24 Τύπος καμπύλης στο IDC Τύπος καμπύλης Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό (%) Ι 1 0,6 0,6 ΙΙ 31 19,4 20,0 ΙΙΙ ,0 100,0 Σύνολο ,0 103
122 Γράφημα 3.26 Τύπος Καμπύλης στο IDC Όσον αφορά το συντελεστή προφανούς διάχυσης (ADC) οι τιμές του μετρήθηκαν ως εξής: Σε 7 από τις 158 περιπτώσεις που υπήρχαν δεδομένα (4,4%) η τιμή ADC ήταν 0,5 Χ 10-3 mm 2 /sec. Σε 2 περιπτώσεις (1,3%) η τιμή ADC ήταν 0,6 Χ 10-3 mm 2 /sec. Σε 7 περιπτώσεις (4,4%) η τιμή ADC ήταν 0,7 Χ 10-3 mm 2 /sec. Σε 6 περιπτώσεις (3,8%) η τιμή ADC ήταν 0,8 Χ 10-3 mm 2 /sec. Σε 7 περιπτώσεις (4,4%) η τιμή ADC ήταν 0,9 Χ 10-3 mm 2 /sec. Σε 125 περιπτώσεις (78,1%) η τιμή ADC ήταν 1,0 Χ 10-3 mm 2 /sec. Σε 2 περιπτώσεις (1,3%) η τιμή ADC ήταν 1,1 Χ 10-3 mm 2 /sec. Σε 1 περίπτωση (0,6%) η τιμή ADC ήταν 1,2 Χ 10-3 mm 2 /sec. 104
123 Σε 1 περίπτωση (0,6%) η τιμή ADC ήταν 2 Χ 10-3 mm 2 /sec. Τα παραπάνω φαίνονται παραστατικά στον πίνακα 3.26 και στο γράφημα 3.27 Πίνακας 3.25 ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec στο IDC Τιμή ADC (10-3 mm 2 /sec) Αριθμός Περιστατικών Ποσοστό (%), ,4, ,3, ,4, ,8, ,4 1, ,1 1, ,3 1,200 1,6 2,000 1,6 ΣΥΝ ,8 Έλλειψη Δεδομένων 2 Σύνολο ,0 105
124 Γράφημα 3.27 Συντελεστής Προφανούς Διάχυσης (ΑDC) στο IDC Όσον αφορά τη φασματοσκοπική ανίχνευση χολίνης στις βλάβες, όπως φαίνεται στον πίνακα 3.27 και στο γράφημα 3.28 σε 39 περιπτώσεις δεν κατέστη τεχνικά δυνατή στην περιοχή του ενδιαφέροντος η λήψη φάσματος. Από τις υπόλοιπες 121 περιπτώσεις στις οποίες μελετήθηκε το φάσμα στο 27,3% δεν ανιχνεύθηκε χολίνη, ενώ στο 72,7% το φάσμα ήταν θετικό για χολίνη. Πίνακας 3.26 Spectroscopy - Φασματοσκοπία (Χολίνη ppm) στο IDC Παρουσία χολίνης Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό ,6 27, ,0 100,0 Σύνολο ,6 Έλλειψη Δεδομένων 39 24,4 Σύνολο ,0 106
125 Γράφημα 3.28 Φασματοσκοπία στο IDC Όσον αφορά την ποσοστιαία κατανομή της συνύπαρξης ή όχι επιπρόσθετων ιστολογικών τύπων πλην του κυρίαρχου IDC, τα αποτελέσματα κατηγοριοποιήθηκαν σε τέσσερεις επιμέρους ομάδες: Στην πρώτη ομάδα (0) το νεόπλασμα ήταν αμιγώς IDC και αντιπροσώπευε το 58,1% του συνόλου. Στη δεύτερη ομάδα (1) που συνιστούσε το 38,1% του συνόλου, συνυπήρχαν IDC και DCIS. Στην τρίτη ομάδα (2) που συνιστούσε το 1,3% του συνόλου, συνυπήρχαν IDC και LCIS. Στην τέταρτη (3) ομάδα που συνιστούσε το 2,5% του συνόλου, συνυπήρχαν IDC, DCIS και LCIS. Tα αποτελέσματα αυτά φαίνονται στον πίνακα 3.28 και στο γράφημα
126 Πίνακας 3.27 Ιστολογικός Τύπος στο IDC Ομάδα Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό (%) ,1 58, ,1 96, ,3 97, ,5 100,0 Σύνολο ,0 Ομάδες Ιστολογικού τύπου ΔΙΗΘΗΤΙΚΑ ΚΑΡΚΙΝΩΜΑΤΑ IN SITU IDC Ομάδες ΔΙΗΘΗΤΙΚΟ 0 ΔΙΗΘΗΤΙΚΟ ΙΝ SITU 1 ΔΙΗΘΗΤΙΚΟ ΙΝ SITU ΛΟΒΙΑΚΟ 2 ΔΙΗΘΗΤΙΚΟ ΙΝ SITU ( Πόρων & Λοβιακό) 3 108
127 Γράφημα 3.29 Ιστολογικός Τύπος στο IDC Όσον αφορά το βαθμό κακοήθειας (grade) των βλαβών, όπως φαίνεται στον πίνακα 3.29 και στο γράφημα 3.30, βαθμού Ι ήταν το 15% των περιπτώσεων, βαθμού ΙΙ ήταν το 37,5% των περιπτώσεων και βαθμού ΙΙΙ ήταν το 46,9% των περιπτώσεων. Σε ένα περιστατικό δεν υπήρχε μέτρηση. Πίνακας 3.28 Βαθμός Κακοήθειας (GRADE) στο IDC Grade Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό Ι 24 15,0 15,1 ΙΙ 60 37,5 52,8 ΙΙΙ 75 46,9 100,0 Σύνολο ,4 Χωρίς Δεδομένα 1,6 Σύνολο ,0 109
128 Γράφημα 3.30 Βαθμός Κακοήθειας (grade) στο IDC Όσον αφορά την πολυεστιακότητα, σε 47 από τις 160 περιπτώσεις (ποσοστό 29,4%) πλην της κύριας βλάβης στην MRΜ συνυπήρχαν εστίες σε άλλες περιοχές του ίδιου τεταρτημορίου του μαστού (Πίνακας 3.30 και γράφημα 3.31). Αυτό αποτέλεσε καθοριστικό εύρημα για το σχεδιασμό της χειρουργικής αντιμετώπισης. Πίνακας 3.29 Πολυεστιακότητα στο IDC Πολυεστιακότητα Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό (%) Όχι ,6 70,6 Ναι 47 29,4 100,0 Σύνολο ,0 110
129 Γράφημα 3.31 Πολυεστιακότητα στο IDC Όσον αφορά την πολυκεντρικότητα, σε 33 από τις 160 περιπτώσεις πλην της κύριας βλάβης στην MRΜ συνυπήρχαν εστίες σε άλλα τεταρτημόρια του ίδιου μαστού (Πίνακας 3.31 και γράφημα 3.32), γεγονός που οδήγησε σε τροποποίηση του χειρουργικού σχεδιασμού. Πίνακας 3.30 Πολυκεντρικότητα στο IDC Πολυκεντρικότητα Αριθμός Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό (%) Όχι ,4 79,4 Ναί 33 20,6 100,0 Σύνολο ,0 111
130 Γράφημα 3.32 Πολυκεντρικότητα στο IDC Όσον αφορά την παρουσία παθολογικών μασχαλιαίων λεμφαδένων στο 50,6% των περιπτώσεων δεν ανιχνεύθηκαν στη μαγνητική μαστογραφία, ενώ στο 49,4% ανιχνεύθηκαν θετικοί μασχαλιαίοι λεμφαδένες (Πίνακας 3.32 και γράφημα 3.33). Τα ευρήματα αυτά συμφωνούσαν απόλυτα με τα ιστοπαθολογικά δεδομένα. Πίνακας 3.31 Μασχαλιαίοι λεμφαδένες στο IDC Μασχαλιαίοι Αριθμός Λεμφαδένες Περιστατικών Ποσοστό (%) Αθροιστικό Ποσοστό (%) Όχι 81 50,6 50,6 Ναί 79 49,4 100,0 Σύνολο ,0 112
131 Γράφημα 3.33 Παρουσία ή Απουσία θετικών μασχαλιαίων λεμφαδένων στο IDC ΜΗ ΠΑΡΑΜΕΤΡΙΚΑ ΣΤΑΤΙΣΤΙΚΑ ΤΕΣΤ Kruskal-Wallis Συσχετισμοί της ανίχνευσης ή όχι χολίνης στις βλάβες IDC Χρησιμοποιώντας το μη παραμετρικό test Kruskal-Wallis έγινε συσχετισμός της παρουσίας ή όχι χολίνης στις βλάβες IDC, με: τα όρια (σαφή ή ασαφή), το μέγεθος (σε ομάδες), τον πρώιμο εμπλουτισμό (σε ομάδες), τον τύπο καμπύλης, το συντελεστή προφανούς διάχυσης (ADC), το βαθμό κακοήθειας (grade), την πολυεστιακότητα, την πολυκεντρικότητα και την παρουσία ή όχι λεμφαδένων (Πίνακας 3.33). 113
132 Πίνακας 3.32 Kruskal-Wallis Test A στο IDC Ranks Spectroscopy - Φασματοσκοπία (Χολίνη) N Mean Rank ,17 Όρια ,94 Σύνολο 121 Μέγεθος (GROUP) ΠΡΩΙΜΟΣ ΕΜΠΛΟΥΤΙΣΜΟΣ GROUP Τύπος καμπύλης ADC (Χ 10-3 mm 2 /sec) Ιστολογικός Τύπος Βαθμός (GRADE) Πολυεστιακά Πολυκεντρικά Λεμφαδένες , ,73 Σύνολο , ,50 Σύνολο , ,19 Σύνολο , ,39 Σύνολο , ,24 Σύνολο , ,76 Σύνολο , ,06 Σύνολο , ,38 Σύνολο , ,19 Σύνολο
133 Μέγεθος GROUP wash in GROUP Τύπος καμπύλης ADC Χ 10-3 mm 2 /sec Ιστολογικός Τύπος GRADE Πολυεστιακά Πολυκεντρικά Λεμφαδένες Πίνακας 3.33 Kruskal-Wallis Test B στο IDC - Ομαδοποίηση της ανίχνευσης ή όχι χολίνης Chi- Square 2,378 2,667 7,741 6,503 1,812 1,617,480,077 6,287 df Asymp. Sig.,123,102,005,011,178,204,488,781,012 Στατιστικά σημαντικός, όπως προκύπτει από τον πίνακα 3.33 είναι ο τύπος καμπύλης με p< 0,005, ο συντελεστής προφανούς διάχυσης (ADC) με p<0,011 και η παρουσία λεμφαδένων με p<0,012. Όλα τα αποτελέσματα είναι grade ΙΙ ή ΙΙΙ, χωρίς την παρουσία grade Ι. Για το λόγο αυτό δεν παρουσιάζεται στατιστική σημαντικότητα στο βαθμό κακοήθειας Συσχετισμοί των ορίων βλάβης στο IDC Χρησιμοποιώντας το μη παραμετρικό test Kruskal-Wallis έγινε συσχετισμός των ορίων των βλαβών στο IDC (σαφή ή ασαφή), με: την παρουσία ή όχι χολίνης, το μέγεθος (σε ομάδες), τον πρώιμο εμπλουτισμό (σε ομάδες), τον τύπο καμπύλης, το ADC, το βαθμό κακοήθειας (grade), την πολυεστιακότητα, την πολυκεντρικότητα και την παρουσία ή όχι λεμφαδένων. Πίνακας 3.34 Kruskal-Wallis Test A στο IDC 115
134 Μέγεθος GROUP WASH IN (GROUP) Τύπος καμπύλης ΙστολογικόςΤύπος (GROUP) Πολυεστιακότητα Πολυκεντρικότητα Λεμφαδένες Spectroscopy (Χολίνη) ADC ( Χ 10-3 mm2/sec) GRADE Ranks Όρια N Mean Rank , ,40 Σύνολο , ,00 Σύνολο , ,00 Σύνολο , ,40 Σύνολο , ,00 Σύνολο , ,00 Σύνολο , ,00 Σύνολο , ,21 Σύνολο , ,75 Σύνολο , ,15 Σύνολο
135 Μέγεθος GROUP ΠΡΩΙΜΟΣ ΕΜΠΛΟΥΤΙΣΜΟΣ - wash in GROUP Τύπος καμπύλης Ιστολογικός Τύπος (ΠΟΡΟΓΕΝΗ+ΛΟΒΙΑΚΑ) Πολυεστιακά Πολυκεντρικά Λεμφαδένες Spectroscopy - Φασματοσκοπία (Χολίνη ppm) ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec Βαθμός (GRADE) Πίνακας 3.35 Kruskal-Wallis Test B στο IDC - Ομαδοποίηση με Όρια Chi- Square,484,067,023 2,176 4,409,731,002,006,279,503 df Asymp. Sig.,486,796,879,140,036,393,968,937,598,478 Στατιστικά σημαντική όπως προκύπτει από τον πίνακα 3.35 είναι η πολυεστιακότητα με p<0, Συσχετισμοί του τύπου της καμπύλης στο IDC Χρησιμοποιώντας το μη παραμετρικό test Kruskal-Wallis έγινε συσχετισμός του τύπου καμπύλης στο IDC με: τα όρια των βλαβών (σαφή ή ασαφή) την παρουσία ή όχι χολίνης, το βαθμό κακοήθειας (grade), το μέγεθος (σε ομάδες), τον πρώιμο εμπλουτισμό (σε ομάδες), το συντελεστή προφανούς διάχυσης (ADC), την πολυεστιακότητα, την πολυκεντρικότητα και την παρουσία ή όχι λεμφαδένων. 117
136 Πίνακας 3.36 Kruskal-Wallis Test A στο IDC Ranks Τύπος καμπύλης N Mean Rank ,50 Μέγεθος GROUP , ,91 Σύνολο 160 ΠΡΩΙΜΟΣ ΕΜΠΛΟΥΤΙΣΜΟΣ - wash in GROUP Ιστολογικός Τύπος Πολυεστιακά Πολυκεντρικά Λεμφαδένες Spectroscopy - Φασματοσκοπία (Χολίνη) ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec Βαθμός (GRADE) Όρια , , ,00 Σύνολο , , ,19 Σύνολο , , ,50 Σύνολο , , ,25 Σύνολο , , ,38 Σύνολο , ,67 Σύνολο , , ,02 Σύνολο , , ,17 Σύνολο , , ,50 Σύνολο
137 Μέγεθος GROUP ΠΡΩΙΜΟΣ ΕΜΠΛΟΥΤΙΣΜΟΣ - wash in GROUP Ιστολογικός Τύπος Πολυεστιακά Πολυκεντρικά Λεμφαδένες Spectroscopy - Φασματοσκοπία (Χολίνη ppm) ADC Χ 10-3 mm2/sec Βαθμός (GRADE) Όρια Πίνακας 3.37 Kruskal-Wallis Test B στο IDC - Ομαδοποίηση με Τύπο καμπύλης Chi- Square 2,909 4,161 13,172 1,063,338 9,705 7,741 6,451 2,782 15,387 df Asymp. Sig.,234,125,001,588,845,008,005,040,249,000 Στατιστικά σημαντικός όπως προκύπτει από τον πίνακα 3.37 είναι ο συσχετισμός του τύπου καμπύλης με τον ιστολογικό τύπο (o οποίος ομαδοποιήθηκε σε IDC, IDC&LCIS, IDC&DCIS&LCIS και ΙDC&LCIS&DCIS), με p< 0,001, με την παρουσία ή όχι χολίνης με p < 0,005, με το συντελεστή προφανούς διάχυσης (ADC) με p <0,040, με την παρουσία λεμφαδένων με p <0,008 και με τον τύπο των ορίων της βλάβης, με p < 0,
138 ADC Τύπος καμπύλης Πρώιμος Εμπλουτισμός Μέγεθος GROUP Όρια Όρια Μέγεθος GROUP ΠΡΩΙΜΟΣ ΕΜΠΛΟΥΤΙΣΜΟΣ - wash in GROUP Τύπος καμπύλης ADC Φασματοσκοπία (Χολίνη ppm) Ιστολογικός Τύπος (ΠΟΡΟΓΕΝΗ+ΛΟΒΙΑΚΑ) Βαθμός (GRADE) Πολυεστιακά Πολυκεντρικά Λεμφαδένες ΜΗ ΠΑΡΑΜΕΤΡΙΚΑ ΣΤΑΤΙΣΤΙΚΑ ΤΕΣΤ Spearman s rho Πίνακας 3.38 Συσχετίσεις στο IDC Spearman s rho Rho 1,000 -,055,020 -,012,042 -,007 -,117,056 -,167 * -,068,003 P Value.,488,797,879,599,937,141,480,035,394,968 Rho -,055 1,000,091,116,192 *,141 -,026,166 *,495 **,583 **,246 ** P Value,488.,251,145,015,124,742,036,000,000,002 Rho,020,091 1,000,157 *,132,149,066 -,080,051,040,078 P Value,797,251.,047,099,103,403,319,521,612,325 Rho -,012,116,157 * 1,000 -,098,254 ** -,261 **,060 -,052 -,014,245 ** P Value,879,145,047.,222,005,001,452,510,863,002 Rho,042,192 *,132 -,098 1,000 -,235 * -,123 -,066,241 **,006 -,173 * 120
139 Λεμφαδένες Πολυκεντρικά Πολυεστιακά Βαθμός Ιστολογικός Τύπος Φασματοσκοπία Χολίνη P Value,599,015,099,222.,010,125,410,002,945,030 Rho -,007,141,149,254 ** -,235 * 1,000,123,117,063,025,229 * P Value,937,124,103,005,010.,179,205,491,782,012 Rho -,117 -,026,066 -,261 ** -,123,123 1,000,016 b,134 -,070 P Value,141,742,403,001,125,179.,838,000,091,376 Rho,056,166 * -,080,060 -,066,117,016 1,000,127,057,317 ** P Value,480,036,319,452,410,205,838.,109,475,000 Rho -,167 *,495 **,051 -,052,241 **,063,348 **,127 1,000,417 **,186 * P Value,035,000,521,510,002,491,000,109.,000,018 Rho -,068,583 **,040 -,014,006,025,134,057,417 ** 1,000,084 P Value,394,000,612,863,945,782,091,475,000.,293 Rho,003,246 **,078,245 ** -,173 *,229 * -,070,317 ** b,084 1,000 P Value,968,002,325,002,030,012,376,000,018,293. *. στατιστικά σημαντικές σε επίπεδο p<0. 05 **. στατιστικά σημαντικές σε επίπεδο p<0. 01 (2-tailed). 121
140 Στατιστικά σημαντικές συσχετίσεις, θετικές ή αρνητικές είναι αυτές που είναι αρκετά ισχυρές από 0,3 περίπου και άνω. Ο πίνακας 3.38 παραθέτει όλες τις δυνατές συσχετίσεις. Με ένα αστερίσκο σημειώνονται οι στατιστικά σημαντικές σε επίπεδο p<0,05 και με 2 αστερίσκους στατιστικά σημαντικές σε επίπεδο p<0,01. Οι σημαντικότερες συσχετίσεις είναι αυτές του μεγέθους (ομαδοποιημένου) με την πολυεστιακότητα (με ισχυρό Συντελεστή Συσχέτισης Spearmans rho 0,495 και p<0,001), του μεγέθους με την πολυκεντρικότητα (με ισχυρό Συντελεστή Συσχέτισης Spearmans rho 0,583 και p<0,001). Σημαντική είναι και η σχέση του μεγέθους με την παρουσία λεμφαδένων (με Συντελεστή Συσχέτισης Spearmans rho 0,246 και p<0,002), και λιγότερο με τον ADC (με Συντελεστή Συσχέτισης Spearmans rho 0,192και p<0,015). Ο τύπος καμπύλης συσχετίζεται σχετικά ισχυρά με τον Πρώιμο Εμπλουτισμό (με Συντελεστή Συσχέτισης Spearmans rho 0,157 και p<0,047), ενώ ισχυρότερα με την παρουσία χολίνης (με Συντελεστή Συσχέτισης Spearmans rho 0,254 και p<0,005) και τον ιστολογικό τύπο (με Συντελεστή Συσχέτισης Spearmans rho -0,261 και p<0,001). Η παρουσία της Χολίνης συσχετίζεται αρνητικά σχετικά ισχυρά με τον ADC (με Συντελεστή Συσχέτισης Spearmans rho - 0,235και p<0,01), αλλά και με την παρουσία λεμφαδένων (με Συντελεστή Συσχέτισης Spearmans rho 0,229 και p<0,012). Η παρουσία λεμφαδένων συσχετίζεται ισχυρά με τον βαθμό κακοήθειας (με Συντελεστή Συσχέτισης Spearmans rho 0,317 και p<0,0001). Η πολυεστιακότητα συσχετίζεται ισχυρά με την πολυκεντρικότητα (με Συντελεστή Συσχέτισης Spearmans rho 0,417 και p< 0,0001). 122
141 3.3.3 ΕΙΚΟΝΕΣ IDC Εικόνα 3.8 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 52 ετών, θετική για μετάλλαξη του γονιδίου BRCA1 με ιστορικό μαστεκτομής δεξιά και αρνητικό μαστογραφικό και υπερηχογραφικό έλεγχο στον αριστερό μαστό. (Α,Β) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται έντονα εμπλουτιζόμενη εξεργασία, με ανώμαλη παρυφή. Αφαιρετικές εικόνες σε εγκάρσιο και οβελιαίο επίπεδο (Γ,Δ) Η καμπύλη της δυναμικής του σκιαστικού (Ε) είναι τύπου ΙΙΙ (washout). 123
142 ΑΑΑΑ Εικόνα 3.9 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 33 ετών με αρνητική μαστογραφία ενώ υπήρχε εύρημα στο δεξιό μαστό υπερηχογραφικά. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή και (Β) οβελιαία τομή, όπου παρατηρείται έντονα εμπλουτιζόμενη επεξεργασία, με κατά τόπους ανώμαλη παρυφή. Στις τρισδιάστατες εικόνες MIP (Γ) αναδεικνύεται καλύτερα η εξεργασία. Η καμπύλη της δυναμικής του σκιαστικού (Δ) είναι τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Ε) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (ΣΤ) προκύπτει τιμή ίση με 0,7 mm 2 /sec. Ιστολογικά αποδείχθηκε άτυπο μυελοειδές καρκίνωμα. 124
143 Εικόνα 3.10 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 42 ετών με ύποπτο μαστογραφικό εύρημα στον αριστερό μαστό. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρείται έντονα εμπλουτιζόμενη εξεργασία, με ανώμαλη παρυφή. Η καμπύλη της δυναμικής του σκιαστικού (Β) είναι τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Γ) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (Δ) προκύπτει τιμή ίση με 0,9 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Ε) ανιχνεύεται υψηλή κορυφή χολίνης στα 3.2ppm. 125
144 Α Ζ Η Εικόνα 3.11 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 47 ετών με ψηλαφητό μόρφωμα στον αριστερό μαστό. (Α,Β) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρείται έντονα εμπλουτιζόμενη εξεργασία, με ανώμαλη παρυφή. Στις τρισδιάστατες εικόνες MIP (Γ) αναδεικνύεται καλύτερα η εξεργασία. Η καμπύλη της δυναμικής του σκιαστικού (Δ) είναι τύπου ΙΙΙ (washout). (Ε) Ακολουθία Τ2W όπου η βλάβη εμφανίζεται με σχετικά υψηλό σήμα λόγω νέκρωσης. Στις εικόνες διάχυσης DWI (ΣΤ) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (Ζ) προκύπτει τιμή ίση με 0,7 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Η) ανιχνεύεται χαμηλή κορυφή χολίνης στα 3.2ppm. 126
145 Β Εικόνα 3.12 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 46 ετών με ψηλαφητό μόρφωμα στον αριστερό μαστό. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή και οβελιαία τομή (Β), όπου παρατηρείται έντονα εμπλουτιζόμενη, ανομοιογενής εξεργασία, με ανώμαλη παρυφή. Στις τρισδιάστατες εικόνες MIP (Γ) αναδεικνύεται καλύτερα η εξεργασία. Η καμπύλη της δυναμικής του σκιαστικού (Δ) είναι τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Ε) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (ΣΤ) προκύπτει τιμή ίση με 0,9mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Ζ) ανιχνεύεται υψηλή κορυφή χολίνης στα 3.2ppm. 127
146 Εικόνα 3.13 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 53 ετών με ψηλαφητό μόρφωμα στο ουραίο τμήμα του αριστερού μαστού. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή και οβελιαία τομή (Β), όπου παρατηρείται μεγάλη, έντονα εμπλουτιζόμενη εξεργασία, με ανώμαλη παρυφή που διηθεί το θωρακικό τοίχωμα. Στις τρισδιάστατες εικόνες MIP (Γ) αναδεικνύεται καλύτερα η εξεργασία. Η καμπύλη της δυναμικής του σκιαστικού (Δ) είναι τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Ε) το σήμα είναι υψηλό. Στο φασματοσκοπικό έλεγχο (ΣΤ) ανιχνεύεται υψηλή κορυφή χολίνης στα 3.2ppm. 128
147 Εικόνα 3.14 Αμφοτερόπλευρο Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 44 ετών. Στη μαστογραφία και στον υπέρηχο υπήρχε ένα εύρημα στο δεξιό μαστό, ενώ η μαγνητική μαστογραφία ανέδειξε τρείς βλάβες στο δεξιό μαστό και μία στον αριστερό μαστό, στον οποίο δεν υπήρχαν ευρήματα στη συμβατική μαστογραφία και στον υπέρηχο. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρούνται τρείς μικρές εμπλουτιζόμενες εστίες στο δεξιό μαστό με σαφή όρια, στις οποίες οι καμπύλες της δυναμικής του σκιαστικού (Β) ήταν όλες τύπου ΙΙΙ (washout). (Γ) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας εγκάρσια τομή, όπου παρατηρείται μία μικρή εμπλουτιζόμενη εστία στον αριστερό μαστό, η οποία εμφανίζει καμπύλη δυναμικής του σκιαστικού τύπου ΙΙΙ -washout (Δ). Στις εικόνες διάχυσης DWI στο δεξιό μαστό (Ε) και στον αριστερό μαστό (Ζ) το σήμα είναι υψηλό. Από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC τόσο στο δεξιό μαστό (ΣΤ) όσο και στον αριστερό μαστό (Η) προκύπτει τιμή ίση με 0,9 mm 2 /sec. 129
148 Εικόνα 3.15 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 55 ετών με οικογενειακό ιστορικό καρκίνου μαστού και ατομικό ιστορικό σμίκρυνσης μαστών. Η μαστογραφία και το υπερηχογράφημα δεν έδειξαν παθολογικό εύρημα. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή και οβελιαία τομή (Β), όπου παρατηρείται εμπλουτιζόμενο μόρφωμα διαμέτρου 6 χιλιοστών με σχετικά ομαλά όρια. Η καμπύλη της δυναμικής του σκιαστικού (Γ) είναι τύπου ΙΙΙ (washout). Στην Τ2 ακολουθία (Δ) η βλάβη εμφανίζει χαμηλό σήμα, ενδεικτικό κακοήθειας. Στις εικόνες διάχυσης DWI (Ε) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (ΣΤ) προκύπτει τιμή ίση με 0,6 mm 2 /sec. 130
149 Εικόνα 3.16 Ενδοκυστικό θηλωματώδες Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 51 ετών με έκκριμα θηλής αριστερού μαστού. (Α, Γ) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή και οβελιαία τομή (Β), όπου παρατηρείται κυστική εξεργασία με τοιχωματικό εμπλουτιζόμενο όζο. Η καμπύλη της δυναμικής του σκιαστικού στον όζο (Δ) είναι τύπου ΙΙΙ (washout). Στην STIR ακολουθία (Ε) η κύστη εμφανίζεται με υψηλό σήμα και ο όζος με χαμηλό σήμα. Στις εικόνες διάχυσης DWI (ΣΤ) το σήμα του όζου είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (Ζ) προκύπτει τιμή ίση με 0,8 mm 2 /sec. 131
150 Εικόνα 3.17 Διηθητικό Καρκίνωμα Πόρων σε γυναίκα ασθενή 46 ετών με ιστορικό μερικής μαστεκτομής προ 8ετίας και τοποθέτησης ενθέματος σιλικόνης. Η μαστογραφία και το υπερηχογράφημα ανέδειξαν ύποπτο εύρημα. (Α, Β) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, εγκάρσια τομή, όπου παρατηρείται εμπλουτιζόμενο μόρφωμα διαμέτρου 7 χιλιοστών με ανώμαλα όρια. Στις τρισδιάστατες εικόνες MIP (Γ) αναδεικνύεται καλύτερα η εξεργασία. Η καμπύλη της δυναμικής του σκιαστικού (Δ) είναι τύπου ΙΙ (plateau). Στις εικόνες διάχυσης DWI (Ε) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC (ΣΤ) προκύπτει τιμή ίση με 0,8 mm 2 /sec. 132
151 3.4 Εκτίμηση των καρκίνων του μαστού που υποβλήθηκαν σε προεγχειρητική χημειοθεραπεία (NAC) Στη μελέτη μας περιελήφθησαν 16 γυναίκες ασθενείς με καρκίνο μαστού με ηλικίες που κυμαίνονταν από 28 έως 91 έτη. Η διάγνωση είχε προκύψει μετά από κλινική εξέταση, μαστογραφία, υπέρηχο και βιοψία. Ο καρκίνος ήταν είτε τοπικά προχωρημένος είτε σε πρωιμότερο στάδιο, χωρίς όμως απομακρυσμένες μεταστάσεις. Αποφασίσθηκε να υποβληθούν σε προεγχειρητική χημειoθεραπεία (NAC). Προηγήθηκε προεγχειρητική μαγνητική μαστογραφία αναφοράς (baseline MRΜ) και ακολούθησε η NAC, στο τέλος της οποίας όλες οι ασθενείς επανελέγχθηκαν με ΜRM προκειμένου να γίνει εκτίμηση της πορείας της νόσου και σχεδιασμός της χειρουργικής θεραπείας. Για την καταμέτρηση των ποσοστών και τη δημιουργία των γραφημάτων και πινάκων χρησιμοποιήθηκε το πρόγραμμα SPSS STATISTICS v20. 0 της IBM. Η στατιστική ανάλυση των αποτελεσμάτων έγινε με το μη παραμετρικό Wilcoxon Signed Ranks Test με όριο στατιστικής σημαντικότητας p<0.05. Ο μέσος όρος ηλικιών ήταν 49 έτη και η αναλυτική ηλικιακή κατανομή φαίνεται στον πίνακα Πίνακας 3.39 Ηλικιακή κατανομή Έτη Αριθμός Ποσοστό (%) Περιστατικών , , , , , , , , , , , , , ,3 Σύνολο ,0 133
152 Όπως φαίνεται στους πίνακες 3.40 και 3.41, στην MRM αναφοράς σε 15 από τις 16 περιπτώσεις (93,8%) οι βλάβες είχαν ασαφή όρια και μόνο σε μία περίπτωση (6,3%) η βλάβη είχε σαφή όρια. Στην επαναληπτική MRM, ως αποτέλεσμα της χημειοθεραπείας, μία από τις 15 βλάβες με ασαφή όρια εξελίχθηκε σε σαφών ορίων βλάβη. Πίνακας 3.40 Εκτίμηση ορίων στις βλάβες προ NAC Όρια Αριθμός Περιστατικών Ποσοστό (%) Συγκεντρωτικό Ποσοστό (%) 15 93,8 93,8 ΣΑΦΗ 1 6,3 100,0 Σύνολο ,0 Πίνακας 3.41 Εκτίμηση ορίων στις βλάβες μετά NAC Όρια Αριθμός Ποσοστό (%) Συγκεντρωτικό Ποσοστό (%) Περιστατικών 14 87,5 87,5 ΣΑΦΗ 2 12,5 100,0 Σύνολο ,0 Τα μεγέθη των βλαβών κυμαίνονταν από 0,5cm έως 12cm και η αναλυτική τους κατανομή φαίνεται στον πίνακα Μετά NAC (πίνακας 3.41) τρεις από τις βλάβες υποχώρησαν τελείως (100%), αποκτώντας μη μετρήσιμο μέγεθος στην MRM. Να σημειωθεί ότι τα αρχικά μεγέθη των παραπάνω βλαβών ήταν 2,5cm, 3,5cm και 7cm αντίστοιχα. Η μεγαλύτερη από τις προ NAC βλάβες, αυτή των 12cm δεν μεταβλήθηκε καθόλου σε μέγεθος (μεταβολή 0%). Όλες οι υπόλοιπες βλάβες υποχώρησαν από 16,6% έως 80%. Οι παραπάνω μεταβολές είναι στατιστικά σημαντικές και αναφέρονται και στο συγκεντρωτικό πίνακα 3.57 (Wilcoxon Signed Ranks Test). 134
153 Πίνακας 3.42 Εκτίμηση μεγέθους (cm) στις βλάβες προ NAC Μέγεθος Αριθμός Περιστατικών Ποσοστό (%) μέχρι ,5 πάνω από 2 μέχρι ,3 πάνω από ,3 Σύνολο ,0 Πίνακας 3.43 Εκτίμηση μεγέθους (cm) στις βλάβες μετά NAC Μέγεθος Αριθμός Περιστατικών Ποσοστό (%) μέχρι ,0 πάνω από 2 μέχρι ,3 πάνω από ,8 Σύνολο ,0 Με βάση τις καμπύλες που προέκυψαν μετά τη δυναμική ενδοφλέβια έγχυση παραμαγνητικής ουσίας, όπως φαίνεται στον πίνακα 3.42 και στο γράφημα 3.34 μόνο σε ένα περιστατικό (6,3%) η κινητική του σκιαστικού ήταν τύπου IΙ. Στο 93,8% των περιπτώσεων, δηλαδή στα υπόλοιπα 15 περιστατικά ήταν τύπου ΙΙΙ. Μετά NAC, η εκτίμηση των καμπυλών εμπλουτισμού (πίνακας 3.43 και γράφημα 3.35) έδωσε διαφορετικά αποτελέσματα, δεδομένου ότι σε ποσοστό 62,5% οι καμπύλες ήταν τύπου Ι, σε 12,5% ήταν τύπου ΙΙ και σε ποσοστό 25% παρέμειναν τύπου ΙΙΙ. Σε κανένα περιστατικό δεν παρατηρήθηκε μεταβολή καμπύλης τύπου Ι ή ΙΙ σε καμπύλη τύπου ΙΙΙ. Οι παραπάνω μεταβολές είναι στατιστικά σημαντικές και αναφέρονται και στο συγκεντρωτικό πίνακα 3.57 (Wilcoxon Signed Ranks Test). 135
154 Πίνακας 3.44 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού προ NAC Κινητική Σκιαστικού Αριθμός Ποσοστό (%) Περιστατικών ΤΥΠΟΣ ΙΙ PLATEAU 1 6,3 ΤΥΠΟΣ ΙΙΙ WASHOUT 15 93,8 Σύνολο ,0 Πίνακας 3.45 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού μετά NAC Κινητική Σκιαστικού Αριθμός Ποσοστό (%) Περιστατικών ΤΥΠΟΣ Ι PERSISTENT 10 62,5 ΤΥΠΟΣ ΙΙ PLATEAU 2 12,5 ΤΥΠΟΣ ΙΙΙ WASHOUT 4 25,0 Σύνολο ,0 Γράφημα 3.34 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού προ NAC 136
155 Γράφημα 3.35 Εκτίμηση του τύπου της καμπύλης εμπλουτισμού μετά NAC Όπως φαίνεται στον πίνακα 3.46, ο συντελεστής προφανούς διάχυσης (ADC) σε μία από τις 16 περιπτώσεις (6,3%) ήταν 0,5 Χ 10-3 mm 2 /sec. Σε 2 περιπτώσεις (12,5%) η τιμή του ADC ήταν 0,6 Χ 10-3 mm 2 /sec. Σε 3 περιπτώσεις (18,8%) η τιμή του ADC ήταν 0,7 Χ 10-3 mm 2 /sec. Σε 7 περιπτώσεις (43,8%) η τιμή του ADC ήταν 0,8 Χ 10-3 mm 2 /sec και σε 3 περιπτώσεις (18,8 %) η τιμή του ADC ήταν 0,9 Χ 10-3 mm 2 /sec. Σε καμία περίπτωση ο συντελεστής ADC δεν ξεπερνούσε το 0,9 Χ 10-3 mm 2 /sec. Μετά NAC σε 11 περιπτώσεις ο συντελεστής προφανούς διάχυσης ADC ήταν μεγαλύτερος από 0,9 Χ 10-3 mm 2 /sec και σε 5 περιπτώσεις μικρότερος ή ίσος με 0,9 Χ 10-3 mm 2 /sec (Πίνακας 3.46). Οι παραπάνω μεταβολές είναι στατιστικά σημαντικές και αναφέρονται και στο συγκεντρωτικό πίνακα 3.57 Wilcoxon Signed Ranks Test. 137
156 Πίνακας 3.46: Εκτίμηση του συντελεστή προφανούς διάχυσης ADC Χ 10-3 mm2/sec προ NAC ADC (Χ 10-3 mm 2 /sec) Αριθμός Περιστατικών Ποσοστό (%) Συγκεντρωτικό Ποσοστό (%) 0,5 1 6,3 6,3 0,6 2 12,5 18,8 0,7 3 18,8 37,5 0,8 7 43,8 81,3 0,9 3 18,8 100,0 Σύνολο ,0 Πίνακας 3.47 Εκτίμηση του συντελεστή προφανούς διάχυσης ADC Χ 10-3 mm2/sec μετά NAC ADC (Χ 10-3 mm 2 /sec) Συχνότητα Ποσοστό (%) 0,6 1 6,3 0,8 1 6,3 0,9 2 12,5 1,0 5 31,3 2,0 7 43,8 Σύνολο ,0 Όσον αφορά τη φασματοσκοπική ανίχνευση χολίνης στις βλάβες, όπως φαίνεται στον πίνακα 3.48, σε όλες τις περιπτώσεις κατέστη δυνατή η λήψη φάσματος, σε 4 περιπτώσεις (25%) δεν ανιχνεύθηκε χολίνη, ενώ στο 75% (12 περιστατικά) το φάσμα ήταν θετικό για χολίνη. Μετά NAC σε μια περίπτωση δεν κατέστη δυνατή η λήψη φάσματος, ενώ στις υπόλοιπες 15 ελήφθη φάσμα, το οποίο σε 13 περιπτώσεις ήταν αρνητικό για χολίνη, ενώ μόνο σε 2 περιπτώσεις παρέμεινε θετικό (πίνακας 3.49). Οι παραπάνω μεταβολές 138
157 είναι στατιστικά σημαντικές και αναφέρονται και στο συγκεντρωτικό πίνακα 3.57 (Wilcoxon Signed Ranks Test). Πίνακας 3.48 Φασματοσκοπία (Χολίνη ppm) προ NAC Αριθμός Παρουσία χολίνης Περιστατικών Ποσοστό (%) ΟΧΙ 4 25,0 ΝΑΙ 12 75,0 Σύνολο ,0 Πίνακας 3.49 Φασματοσκοπία (Χολίνη ppm) μετά NΑC Παρουσία χολίνης Αριθμός Περιστατικών Ποσοστό (%) OXI 13 81,3 NAI 2 12,5 σύνολο 15 93,8 Έλλειψη Δεδομένων 1 6,3 Σύνολο ,0 Ο ιστοπαθολογικός προσδιορισμός του βαθμού κακοήθειας (grade) των καρκινωμάτων προσδιορίστηκε σε 14 από τα 16 περιστατικά. Τα 2 περιστατικά στα οποία δεν υπάρχουν δεδομένα, αφορούν περιπτώσεις διηθητικού λοβιακού καρκίνου, αμιγούς τύπου ή μικτού τύπου με κυρίαρχο το λοβιακό στοιχείο. Στα υπόλοιπα 14 περιστατικά μόνο σε ένα (6,3%) ο βαθμός κακοήθειας ήταν Ι, σε 5 περιστατικά (31,3%) ο βαθμός κακοήθειας ήταν ΙΙ, σε 7 περιστατικά (43,8%) ο βαθμός κακοήθειας ήταν ΙΙΙ και σε ένα περιστατικό (6,3%) ο βαθμός κακοήθειας ήταν μικτός ΙΙ και ΙΙΙ (πίνακας 3.50). Σύμφωνα με τον πίνακα 3.50 μετά NAC ο ιστοπαθολογικός προσδιορισμός του βαθμού κακοήθειας (grade) έδειξε ότι ακόμα ένα περιστατικό απέκτησε βαθμό κακοήθειας Ι, έτσι ώστε το τελικό ποσοστό νεοπλασμάτων με βαθμό κακοήθειας Ι να είναι 12,5%. Το ποσοστό νεοπλασμάτων με βαθμό κακοήθειας ΙΙ κατέβηκε στο 18,8% (από 31,3% σύμφωνα και με τον πίνακα 3.51), ενώ το ποσοστό νεοπλασμάτων με βαθμό κακοήθειας ΙΙΙ κατέβηκε στο 31,3% (από 43,8% σύμφωνα και με τον πίνακα 3.49). Τέλος, στη μοναδική περίπτωση του νεοπλάσματος που είχε μικτού βαθμού 139
158 κακοήθεια ΙΙ και ΙΙΙ, δεν υπήρξε διαφοροποίηση μετά NAC. Οι παραπάνω μεταβολές είναι στατιστικά σημαντικές και αναφέρονται και στο συγκεντρωτικό πίνακα 3.58 (Wilcoxon Signed Ranks Test). Πίνακας 3.50 Ιστοπαθολογικός Βαθμός Κακοήθειας (grade) προ NAC Βαθμός Κακοήθειας Αριθμός Περιστατικών Ποσοστό (%) I 1 6,3 II 5 31,3 III 7 43,8 II+III 1 6,3 Σύνολο 14 87,5 Έλλειψη Δεδομένων 2 12,5 Σύνολο ,0 Πίνακας 3.51 Ιστοπαθολογικός Βαθμός Κακοήθειας (grade) μετά NAC Βαθμός Κακοήθειας Αριθμός Περιστατικών Ποσοστό (%) I 2 12,5 II 3 18,8 III 5 31,3 II+III 1 6,3 Σύνολο 11 68,8 Έλλειψη Δεδομένων 5 31,3 Σύνολο ,0 Όπως φαίνεται στον πίνακα 3.52, στο 43,8% των περιπτώσεων η βλάβη ήταν μονοεστιακή ενώ στο 56,3% των περιπτώσεων υπήρχε πολυεστιακότητα, τόσο στην MRM όσο και ιστοπαθολογικά. Μετά NAC το ποσοστό των μονοεστιακών περιπτώσεων ανέβηκε κατά 13 ποσοστιαίες μονάδες, ενώ το ποσοστό των πολυεστιακών περιπτώσεων κατέβηκε κατά 13 ποσοστιαίες μονάδες (Πίνακας 3.53). 140
159 Πίνακας 3.52 Πολυεστιακότητα βλαβών προ NAC Αριθμός Εστιών Αριθμός Περιστατικών Ποσοστό (%) Συγκεντρωτικό Ποσοστό (%) ΜΟΝΟΕΣΤΙΑΚΟ 7 43,8 43,8 ΠΟΛΥΕΣΤΙΑΚΟ 9 56,3 100,0 Σύνολο ,0 Πίνακας 3.53 Πολυεστιακότητα βλαβών μετά NAC Αριθμός Εστιών Αριθμός Ποσοστό Ποσοστό (%) Περιστατικών (%) ΜΟΝΟΕΣΤΙΑΚΟ 9 56,3 56,3 ΠΟΛΥΕΣΤΙΑΚΟ 7 43,8 100,0 Σύνολο ,0 Όσον αφορά την παρουσία παθολογικών μασχαλιαίων λεμφαδένων στο 37,5% των περιπτώσεων δεν ανιχνεύθηκαν στη μαγνητική μαστογραφία αναφοράς, ενώ στο 62,5% ανιχνεύθηκαν θετικοί μασχαλιαίοι λεμφαδένες (πίνακας 3.55). Μετά NAC το ποσοστό των αρνητικών λεμφαδένων ανέβηκε κατά 6 ποσοστιαίες μονάδες, ενώ το ποσοστό των θετικών λεμφαδένων παρέμεινε 62,5%, δεδομένου ότι σε ένα περιστατικό δεν υπήρχαν δεδομένα (πίνακας 3.56). Τα ευρήματα αυτά συμφωνούσαν απόλυτα με τα ιστοπαθολογικά δεδομένα. Οι παραπάνω μεταβολές είναι στατιστικά σημαντικές και αναφέρονται και στο συγκεντρωτικό Πίνακα 3.58 (Wilcoxon Signed Ranks Test). 141
160 Πίνακας 3.54 Παρουσία θετικών μασχαλιαίων λεμφαδένων προ NAC Λεμφαδένες Αριθμός Περιστατικών Ποσοστό (%) ΟΧΙ 6 37,5 ΝΑΙ 10 62,5 Σύνολο ,0 Πίνακας 3.55 Παρουσία θετικών μασχαλιαίων λεμφαδένων μετά NAC Λεμφαδένες Αριθμός Περιστατικών Ποσοστό (%) ΟΧΙ 7 43,8 ΝΑΙ 8 50,0 Σύνολο 15 93,8 Έλλειψη δεδομένων 1 6,3 Σύνολο ,0 Σύμφωνα με τους πίνακες 3.56 και 3.57 στις 4 από τις 16 περιπτώσεις ο καρκίνος ήταν μικτού ιστοπαθολογικού τύπου. Συγκεκριμένα σε 3 περιπτώσεις επρόκειτο για συνδυασμό in situ καρκινώματος πόρων (DCIS) και διηθητικού καρκινώματος πόρων (IDC) και σε μία περίπτωση μικτό διηθητικό καρκίνωμα πόρων και λοβίων. Οι υπόλοιπες 12 περιπτώσεις ήταν αμιγή διηθητικά καρκινώματα, εκ των οποίων 11 περιπτώσεις IDC και μία περίπτωση ILC. Πίνακας 3.56 Ιστολογικός τύπος μικτών καρκινωμάτων Ιστολογικός Τύπος Αριθμός Συγκεντρωτικό Ποσοστό (%) Περιστατικών Ποσοστό (%) ILC και IDC IDC και DCIS Σύνολο 4 100,0 142
161 Πίνακας 3.57 Ιστολογικός τύπος καρκινωμάτων Ιστολογικός Τύπος Αριθμός Περιστατικών Ποσοστό (%) , , , ,0 Σύνολο ,0 Ομάδα 1: ILC, Ομάδα 2: ILC & IDC, Ομάδα 3: ILC & LCIS, Ομάδα 4: ILC & IDC & LCIS 143
162 Πίνακας 3.58 Wilcoxon Signed Ranks Test Μέγεθος Τύπος Spectroscopy - καμπύλης Φασματοσκοπία (Χολίνη ppm)1 Βαθμός (GRADE) ΛΕΜΦΑΔΕΝΕΣ ADC (Συντελεστής προφανούς Διάχυσης) Χ 10-3 mm2/sec Z -3,297 b -3,217 b -3,000 b,000 c -1,414 b -3,417 d Asymp. Significance (2-tailed),001,001,003 1,000,157,001 a. Wilcoxon Signed Ranks Test b. Με βάση τις θετικές τάξεις c. Το άθροισμα των αρνητικών τάξεων ισούται με το άθροισμα των θετικών τάξεων d. Με βάση την αρνητική τάξη Στατιστικά σημαντική είναι η διαφορά που παρουσιάζεται μετά τη θεραπεία για το μέγεθος (p<0. 001), τον τύπο της καμπύλης (p<0,001), την παρουσία ή όχι χολίνης (p<0. 003) και το συντελεστή προφανούς διάχυσης (ADC) ( p<0,001). 144
163 3.4.1 ΕΙΚΟΝΕΣ NAC Εικόνα 3.18 Διηθητικό Καρκίνωμα Πόρων βαθμού κακοήθειας ΙΙΙ πριν τη χορήγηση NAC σε γυναίκα ασθενή 36 ετών με ψηλαφητή σκληρία στον αριστερό μαστό. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται εκτεταμένη, εμπλουτιζόμενη εξεργασία στο έσω ημιμόριο του αριστερού μαστού με καμπύλη της δυναμικής του σκιαστικού τύπου ΙΙΙ (washout) και παρουσία διογκωμένων λεμφαδένων στην αριστερή μασχάλη. Στις εικόνες διάχυσης DWI (Β) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτει τιμή ίση με 0,9mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Γ) ανιχνεύεται μικρή κορυφή χολίνης στα 3.2ppm. 145
164 Β Γ Εικόνα 3.19 Μετά τη χορήγηση NAC η ανταπόκριση ήταν πλήρης : (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται εξάλειψη του παθολογικού εμπλουτισμού, μετατροπή της καμπύλης του σκιαστικού σε τύπο Ι (persistent) και υποχώρηση των διογκωμένων λεμφαδένων της αριστερής μασχάλης. Στις εικόνες διάχυσης DWI (Β) δεν υπάρχει παθολογικό σήμα, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτει τιμή ίση με 1,2 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Γ) δεν ανιχνεύεται κορυφή χολίνης στα 3.2ppm. 146
165 Εικόνα 3.20 Διηθητικό Καρκίνωμα Πόρων βλεννώδους τύπου, βαθμού κακοήθειας ΙΙΙ πριν τη χορήγηση NAC σε γυναίκα ασθενή 46 ετών με εισολκή θηλής στον αριστερό μαστό. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται ανομοιογενής εμπλουτιζόμενη εξεργασία οπισθοθηλαία, με καμπύλη της δυναμικής του σκιαστικού τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Β) το σήμα είναι υψηλό,ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτει τιμή ίση με 0,8mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Γ) ανιχνεύεται μικρή κορυφή χολίνης στα 3.2ppm. 147
166 Εικόνα 3.21 Μετά τη χορήγηση NAC η ανταπόκριση ήταν μερική :(Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται μερική εξάλειψη του παθολογικού εμπλουτισμού και μετατροπή της καμπύλης του σκιαστικού σε τύπο Ι (persistent). Στις εικόνες διάχυσης DWI (Β) έχει ελαττωθεί η ένταση του σήματος, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτει τιμή ίση με 1,8 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Γ) παραμένει χαμηλή κορυφή χολίνης στα 3.2ppm. 148
167 Α Β Γ Εικόνα 3.22 Διηθητικό Καρκίνωμα Πόρων, τριπλά αρνητικό, βαθμού κακοήθειας ΙΙΙ, πριν τη χορήγηση NAC σε γυναίκα ασθενή 33 ετών με ιστορικό δεξιάς μαστεκτομής και ψηλαφητή σκληρία στον αριστερό μαστό. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται πολυεστιακή και πολυκεντρική εμπλουτιζόμενη εξεργασία, με καμπύλη της δυναμικής του σκιαστικού τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Β) το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτει τιμή ίση με 0,9 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Γ) ανιχνεύεται υψηλή κορυφή χολίνης στα 3.2ppm. 149
168 Εικόνα 3.23 Μετά τη χορήγηση NAC δεν υπήρξε ανταπόκριση: (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παραμένει ο παθολογικός εμπλουτισμός, χωρίς σημαντική διαφοροποίηση της έκτασης και της έντασής του, ενώ η καμπύλη του σκιαστικού επίσης παραμένει τύπου ΙΙΙ (washout). Στις εικόνες διάχυσης DWI (Β) η ένταση του σήματος και ο συντελεστής προφανούς διάχυσης ADC παραμένουν αμετάβλητα. Στο φασματοσκοπικό έλεγχο (Γ) παραμένει υψηλή κορυφή χολίνης στα 3.2ppm. 150
169 Α Β Γ Δ Εικόνα 3.24 Διηθητικό Καρκίνωμα Πόρων, βαθμού κακοήθειας ΙΙΙ, πριν τη χορήγηση NAC σε γυναίκα ασθενή 35 ετών με ψηλαφητή σκληρία στο δεξιό μαστό. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται πολυεστιακή και πολυκεντρική εμπλουτιζόμενη εξεργασία, με καμπύλη της δυναμικής του σκιαστικού τύπου ΙΙΙ (washout). (Β) Στις MIP εικόνες αναδεικνύεται τρισδιάστατα η πολυκεντρικότητα και η πολυεστιακότητα της νόσου. Επίσης ανδεικνύονται οι διογκωμένοι μασχαλιαίοι λεμφαδένες καθώς και ο διογκωμένος λεμφαδένας της έσω μαστικής δεξιά. (Γ) Στις εικόνες διάχυσης DWI το σήμα είναι υψηλό, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτει τιμή ίση με 0,8 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Δ) ανιχνεύεται υψηλή κορυφή χολίνης στα 3.2ppm. 151
170 Εικόνα 3.25 Μετά τη χορήγηση NAC υπήρξε πλήρης ανταπόκριση. (Α) Ακολουθία Τ1W FAT SAT μετά χορήγηση παραμαγνητικής ουσίας, όπου παρατηρείται εξάλλειψη του εμπλουτισμού, με αλλαγή της καμπύλης σε τύπου Ι (persistent). (Β) Στις εικόνες διάχυσης DWI έχει ελαττωθεί η ένταση του σήματος, ενώ από τη χαρτογράφηση του συντελεστή προφανούς διάχυσης ADC προκύπτει τιμή ίση με 1,6 mm 2 /sec. Στο φασματοσκοπικό έλεγχο (Γ) δεν ανιχνεύεται κορυφή χολίνης στα 3.2ppm. 152
H ΣΥΜΒΟΛΗ ΤΗΣ ΜΑΓΝΗΤΙΚΗΣ ΦΑΣΜΑΤΟΣΚΟΠΙΑΣ (SPECTROSCOPY-MRS) ΣΕ ΜΑΓΝΗΤΙΚΟ ΤΟΜΟΓΡΑΦΟ 3Τ ΣΤΗ ΔΙΑΓΝΩΣΗ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ
 H ΣΥΜΒΟΛΗ ΤΗΣ ΜΑΓΝΗΤΙΚΗΣ ΦΑΣΜΑΤΟΣΚΟΠΙΑΣ (SPECTROSCOPY-MRS) ΣΕ ΜΑΓΝΗΤΙΚΟ ΤΟΜΟΓΡΑΦΟ 3Τ ΣΤΗ ΔΙΑΓΝΩΣΗ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ Γ. Μπουλογιάννη 1, Α. Δρεβελέγκας 1, Ι. Χρυσογονίδης 2 1.Ιατρικό Διαβαλκανικό Κέντρο
H ΣΥΜΒΟΛΗ ΤΗΣ ΜΑΓΝΗΤΙΚΗΣ ΦΑΣΜΑΤΟΣΚΟΠΙΑΣ (SPECTROSCOPY-MRS) ΣΕ ΜΑΓΝΗΤΙΚΟ ΤΟΜΟΓΡΑΦΟ 3Τ ΣΤΗ ΔΙΑΓΝΩΣΗ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ Γ. Μπουλογιάννη 1, Α. Δρεβελέγκας 1, Ι. Χρυσογονίδης 2 1.Ιατρικό Διαβαλκανικό Κέντρο
Προληπτική Μαστογραφία Ανακαλύπτοντας το DCIS. Ιωάννης Θ. Νατσιόπουλος Ειδικός Χειρουργός Μαστού
 Προληπτική Μαστογραφία Ανακαλύπτοντας το DCIS Ιωάννης Θ. Νατσιόπουλος Ειδικός Χειρουργός Μαστού Ductal Carcinoma in Situ Πορογενές καρκίνωμα in Situ In Situ = επί τόπου Τοπικό πορογενές καρκίνωμα; Ductal
Προληπτική Μαστογραφία Ανακαλύπτοντας το DCIS Ιωάννης Θ. Νατσιόπουλος Ειδικός Χειρουργός Μαστού Ductal Carcinoma in Situ Πορογενές καρκίνωμα in Situ In Situ = επί τόπου Τοπικό πορογενές καρκίνωμα; Ductal
21. ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ
 21. ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ ΕΠΙΔΗΜΙΟΛΟΓΙΑ Ο καρκίνος του μαστού είναι ο πιο συχνός καρκίνος της γυναίκας. Η επίπτωση παγκόσμια είναι περίπου 89 περιστατικά/100.000 γυναίκες ενώ αναφέρονται 800.000 νέα περιστατικά
21. ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ ΕΠΙΔΗΜΙΟΛΟΓΙΑ Ο καρκίνος του μαστού είναι ο πιο συχνός καρκίνος της γυναίκας. Η επίπτωση παγκόσμια είναι περίπου 89 περιστατικά/100.000 γυναίκες ενώ αναφέρονται 800.000 νέα περιστατικά
Πρώιμος καρκίνος μαστού. Σπύρος Μηλιαράς MD, MRCS(Glasg), AFRCS(Edin) Αναπλ. Καθηγητής Χειρουργικής ΑΠΘ Α Χειρουργική Κλινική ΑΠΘ, ΠΓΝΘ Παπαγεωργίου
 Πρώιμος καρκίνος μαστού Σπύρος Μηλιαράς MD, MRCS(Glasg), AFRCS(Edin) Αναπλ. Καθηγητής Χειρουργικής ΑΠΘ Α Χειρουργική Κλινική ΑΠΘ, ΠΓΝΘ Παπαγεωργίου Ορισμός.. Πρώιμος καρκίνος του μαστού είναι η νόσος που
Πρώιμος καρκίνος μαστού Σπύρος Μηλιαράς MD, MRCS(Glasg), AFRCS(Edin) Αναπλ. Καθηγητής Χειρουργικής ΑΠΘ Α Χειρουργική Κλινική ΑΠΘ, ΠΓΝΘ Παπαγεωργίου Ορισμός.. Πρώιμος καρκίνος του μαστού είναι η νόσος που
ΠΑΘΗΣΕΙΣ ΜΑΖΙΚΟΥ ΑΔΕΝΑ. Τριανταφυλλιά Κολέτσα Λέκτορας
 ΠΑΘΗΣΕΙΣ ΜΑΖΙΚΟΥ ΑΔΕΝΑ Τριανταφυλλιά Κολέτσα Λέκτορας ΕΓΠΠΑ, Α.Π.Θ. Μαστός Λοβοί: εκβάλουν στη θηλή με γαλακτοφόρο πόρο. Διακλαδιζόμενοι πόροι κατάληξη-λοβιακές λοβιακές μονάδες. Λοβιακή μονάδα: αποτελείται
ΠΑΘΗΣΕΙΣ ΜΑΖΙΚΟΥ ΑΔΕΝΑ Τριανταφυλλιά Κολέτσα Λέκτορας ΕΓΠΠΑ, Α.Π.Θ. Μαστός Λοβοί: εκβάλουν στη θηλή με γαλακτοφόρο πόρο. Διακλαδιζόμενοι πόροι κατάληξη-λοβιακές λοβιακές μονάδες. Λοβιακή μονάδα: αποτελείται
 ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ: ΣΤΡΑΤΗΓΙΚΕΣ ΠΡΟΛΗΨΗΣ Αντωνίου Χαρά Διευθύντρια Β Χειρουργικής Κλινικής Γενικού Νοσοκομείου Χανίων ΣΕ ΤΙ ΘΑ ΑΝΑΦΕΡΘΟΥΜΕ??? Πόσο συχνός είναι ο καρκίνος του μαστού? Ποια αίτια τον προκαλούν?
ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ: ΣΤΡΑΤΗΓΙΚΕΣ ΠΡΟΛΗΨΗΣ Αντωνίου Χαρά Διευθύντρια Β Χειρουργικής Κλινικής Γενικού Νοσοκομείου Χανίων ΣΕ ΤΙ ΘΑ ΑΝΑΦΕΡΘΟΥΜΕ??? Πόσο συχνός είναι ο καρκίνος του μαστού? Ποια αίτια τον προκαλούν?
Σύμφωνα με τον παγκόσμιο οργανισμό υγείας, κάθε χρόνο υπάρχουν 1.38 εκατομμύρια καινούρια περιστατικά και περίπου 458 000 θάνατοι από τον καρκίνο του
 1 Σύμφωνα με τον παγκόσμιο οργανισμό υγείας, κάθε χρόνο υπάρχουν 1.38 εκατομμύρια καινούρια περιστατικά και περίπου 458 000 θάνατοι από τον καρκίνο του μαστού. Ο καρκίνος του μαστού είναι με μεγάλη διαφορά
1 Σύμφωνα με τον παγκόσμιο οργανισμό υγείας, κάθε χρόνο υπάρχουν 1.38 εκατομμύρια καινούρια περιστατικά και περίπου 458 000 θάνατοι από τον καρκίνο του μαστού. Ο καρκίνος του μαστού είναι με μεγάλη διαφορά
Κυριακή, 3 Σεπτεµβρίου 2006
 Χρήστος Μαρκόπουλος Αν. Καθηγητής Χειρουργικής Ιατρικής Σχολής Αθηνών /ντης Κλινικής Μαστού Ιατρικού Κέντρου Αθηνών Πρόεδρος Ελληνικής Χειρουργικής Εταιρείας Μαστού - Στατιστικά στοιχεία Στη χώρα µας,
Χρήστος Μαρκόπουλος Αν. Καθηγητής Χειρουργικής Ιατρικής Σχολής Αθηνών /ντης Κλινικής Μαστού Ιατρικού Κέντρου Αθηνών Πρόεδρος Ελληνικής Χειρουργικής Εταιρείας Μαστού - Στατιστικά στοιχεία Στη χώρα µας,
ΜΑΣΤΟΛΟΓΙΑ ΚΑΙ Ο ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ
 ΜΑΣΤΟΛΟΓΙΑ ΚΑΙ Ο ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ Τι είναι η μαστολογία? Μαστολογία είναι ο κλάδος της ιατρικής πού ασχολείται με τον μαστικό αδένα (μαστός) και τις παθήσεις αυτού. Τι είναι ο μαστός? Ο Μαστός αποτελείται
ΜΑΣΤΟΛΟΓΙΑ ΚΑΙ Ο ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ Τι είναι η μαστολογία? Μαστολογία είναι ο κλάδος της ιατρικής πού ασχολείται με τον μαστικό αδένα (μαστός) και τις παθήσεις αυτού. Τι είναι ο μαστός? Ο Μαστός αποτελείται
Οι σκοποί της Εταιρείας μας είναι επιστημονικοί και κοινωνικοί και αφορούν στην:
 Ο καρκίνος του μαστού αποτελεί τη συχνότερη νεοπλασματική νόσο που προσβάλλει τις γυναίκες, με αρνητικές επιπτώσεις όχι μόνο για την ίδια την ασθενή, αλλά και για το οικογενειακό και φιλικό της περιβάλλον.
Ο καρκίνος του μαστού αποτελεί τη συχνότερη νεοπλασματική νόσο που προσβάλλει τις γυναίκες, με αρνητικές επιπτώσεις όχι μόνο για την ίδια την ασθενή, αλλά και για το οικογενειακό και φιλικό της περιβάλλον.
ΥΠΕΡΠΛΑΣΙΑ ΤΟΥ ΕΝΔΟΜΗΤΡΙΟΥ ΚΑΛΠΑΚΤΣΙΔΟΥ ΒΑΚΙΑΝΗ ΜΑΧΗ
 ΥΠΕΡΠΛΑΣΙΑ ΤΟΥ ΕΝΔΟΜΗΤΡΙΟΥ ΚΑΛΠΑΚΤΣΙΔΟΥ ΒΑΚΙΑΝΗ ΜΑΧΗ Ανωορρηκτικοί κύκλοι Εξωγενή οιστρογόνα Σύνδρομο πολυκυστικών ωοθηκών Παχυσαρκία Όγκοι ωοθηκών Εφηβία Παραγωγική ηλικία Κλιμακτήριο εμμηνόπαυση ΥΠΕΡΠΛΑΣΙΑ
ΥΠΕΡΠΛΑΣΙΑ ΤΟΥ ΕΝΔΟΜΗΤΡΙΟΥ ΚΑΛΠΑΚΤΣΙΔΟΥ ΒΑΚΙΑΝΗ ΜΑΧΗ Ανωορρηκτικοί κύκλοι Εξωγενή οιστρογόνα Σύνδρομο πολυκυστικών ωοθηκών Παχυσαρκία Όγκοι ωοθηκών Εφηβία Παραγωγική ηλικία Κλιμακτήριο εμμηνόπαυση ΥΠΕΡΠΛΑΣΙΑ
Βούρτση Α, Λαζάρου Σπ, Αθανασίου Α, Ρουσάκης Α, Κουφόπουλος Κ, Καντζάβελος Κ, Πανουργιά Ε, Χρυσογονίδης Ι. www,hbis.gr
 Βούρτση Α, Λαζάρου Σπ, Αθανασίου Α, Ρουσάκης Α, Κουφόπουλος Κ, Καντζάβελος Κ, Πανουργιά Ε, Χρυσογονίδης Ι. www,hbis.gr Γυναίκα ηλικίας 74 ετών προσήλθε για μαστογραφία. Ατομικό ιστορικό αρνητικό. Κλινική
Βούρτση Α, Λαζάρου Σπ, Αθανασίου Α, Ρουσάκης Α, Κουφόπουλος Κ, Καντζάβελος Κ, Πανουργιά Ε, Χρυσογονίδης Ι. www,hbis.gr Γυναίκα ηλικίας 74 ετών προσήλθε για μαστογραφία. Ατομικό ιστορικό αρνητικό. Κλινική
ΠΑΘΟΓΕΝΕΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΚΟΙ ΤΥΠΟΙ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ
 ΠΑΘΟΓΕΝΕΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΚΟΙ ΤΥΠΟΙ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ Χρ.Τσοµπανίδου Παθολογοανατόµος Συντονίστρια Διευθύντρια Νοσοκοµείο Θεσ/νίκης «Άγιος Δηµήτριος» προέρχονται από το φυσιολογικό επιθήλιο µε την
ΠΑΘΟΓΕΝΕΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΚΟΙ ΤΥΠΟΙ ΤΟΥ ΚΑΡΚΙΝΟΥ ΤΟΥ ΠΝΕΥΜΟΝΑ Χρ.Τσοµπανίδου Παθολογοανατόµος Συντονίστρια Διευθύντρια Νοσοκοµείο Θεσ/νίκης «Άγιος Δηµήτριος» προέρχονται από το φυσιολογικό επιθήλιο µε την
Κλινικές επιλογές σε μεταλλάξεις των BRCA 1/2 γονιδίων. Ιωάννης Θ. Νατσιόπουλος Χειρουργός Μαστού
 Κλινικές επιλογές σε μεταλλάξεις των BRCA 1/2 γονιδίων Ιωάννης Θ. Νατσιόπουλος Χειρουργός Μαστού Η ανίχνευση BRCA μετάλλαξης δεν αποτελεί διάγνωση νόσου αλλά γενετική πληροφορία και εκτίμηση κινδύνου Ενδείξεις
Κλινικές επιλογές σε μεταλλάξεις των BRCA 1/2 γονιδίων Ιωάννης Θ. Νατσιόπουλος Χειρουργός Μαστού Η ανίχνευση BRCA μετάλλαξης δεν αποτελεί διάγνωση νόσου αλλά γενετική πληροφορία και εκτίμηση κινδύνου Ενδείξεις
Πανεπιστήμιο Δυτικής Αττικής Τμήμα Βιοϊατρικών Επιστημών Κατεύθυνση: Ακτινολογία και Ακτινοθεραπεία ΜΑΓΝΗΤΙΚΗ ΜΑΣΤΟΓΡΑΦΙΑ
 Πανεπιστήμιο Δυτικής Αττικής Τμήμα Βιοϊατρικών Επιστημών Κατεύθυνση: Ακτινολογία και Ακτινοθεραπεία ΜΑΓΝΗΤΙΚΗ ΜΑΣΤΟΓΡΑΦΙΑ Η Μαγνητική Μαστογραφία λόγω της μεγαλύτερης αντιθετικής διακριτικής ικανότητας
Πανεπιστήμιο Δυτικής Αττικής Τμήμα Βιοϊατρικών Επιστημών Κατεύθυνση: Ακτινολογία και Ακτινοθεραπεία ΜΑΓΝΗΤΙΚΗ ΜΑΣΤΟΓΡΑΦΙΑ Η Μαγνητική Μαστογραφία λόγω της μεγαλύτερης αντιθετικής διακριτικής ικανότητας
ΙΩΑΝΝΗΣ Θ. ΝΑΤΣΙΟΠΟΥΛΟΣ Α ΧΕΙΡΟΥΡΓΙΚΗ ΚΛΙΝΙΚΗ ΝΟΣΟΚΟΜΕΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ «ΠΑΠΑΓΕΩΡΓΙΟΥ»
 8ο ΣΥΝΕΔΡΙΟ ΧΕΙΡΟΥΡΓΙΚΗΣ ΕΤΑΙΡΕΙΑΣ ΒΟΡΕΙΟΥ ΕΛΛΑΔΟΣ ΘΕΣΣΑΛΟΝΙΚΗ 18-21 ΟΚΤΩΒΡΙΟΥ 2007 ΙΩΑΝΝΗΣ Θ. ΝΑΤΣΙΟΠΟΥΛΟΣ Α ΧΕΙΡΟΥΡΓΙΚΗ ΚΛΙΝΙΚΗ ΝΟΣΟΚΟΜΕΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ «ΠΑΠΑΓΕΩΡΓΙΟΥ» ΠΙΘΑΝΗ ΚΑΚΟΗΘΕΙΑ ΚΛΙΝΙΚΗ Ψηλαφητή
8ο ΣΥΝΕΔΡΙΟ ΧΕΙΡΟΥΡΓΙΚΗΣ ΕΤΑΙΡΕΙΑΣ ΒΟΡΕΙΟΥ ΕΛΛΑΔΟΣ ΘΕΣΣΑΛΟΝΙΚΗ 18-21 ΟΚΤΩΒΡΙΟΥ 2007 ΙΩΑΝΝΗΣ Θ. ΝΑΤΣΙΟΠΟΥΛΟΣ Α ΧΕΙΡΟΥΡΓΙΚΗ ΚΛΙΝΙΚΗ ΝΟΣΟΚΟΜΕΙΟ ΘΕΣΣΑΛΟΝΙΚΗΣ «ΠΑΠΑΓΕΩΡΓΙΟΥ» ΠΙΘΑΝΗ ΚΑΚΟΗΘΕΙΑ ΚΛΙΝΙΚΗ Ψηλαφητή
H ΠΡΟΣΑΥΞΗΤΙΚΗ ΑΞΙΑ ΤΗΣ ΜΑΓΝΗΤΙΚΗΣ ΤΟΜΟΓΡΑΦΙΑΣ (ΜΤ) ΣΤΗ ΣΤΑΔΙΟΠΟΙΗΣΗ ΤΩΝ ΑΣΘΕΝΩΝ ΜΕ ΠΡΩΙΜΟ ΔΙΗΘΗΤΙΚΟ ΚΑΡΚΙΝΟ ΤΟΥ ΤΡΑΧΗΛΟΥ ΜΗΤΡΑΣ
 H ΠΡΟΣΑΥΞΗΤΙΚΗ ΑΞΙΑ ΤΗΣ ΜΑΓΝΗΤΙΚΗΣ ΤΟΜΟΓΡΑΦΙΑΣ (ΜΤ) ΣΤΗ ΣΤΑΔΙΟΠΟΙΗΣΗ ΤΩΝ ΑΣΘΕΝΩΝ ΜΕ ΠΡΩΙΜΟ ΔΙΗΘΗΤΙΚΟ ΚΑΡΚΙΝΟ ΤΟΥ ΤΡΑΧΗΛΟΥ ΜΗΤΡΑΣ Μπουργιώτη Χάρις 1, Χατούπης Κωνσταντίνος 1, Αντωνίου Αριστείδης 1, Ροδολάκης
H ΠΡΟΣΑΥΞΗΤΙΚΗ ΑΞΙΑ ΤΗΣ ΜΑΓΝΗΤΙΚΗΣ ΤΟΜΟΓΡΑΦΙΑΣ (ΜΤ) ΣΤΗ ΣΤΑΔΙΟΠΟΙΗΣΗ ΤΩΝ ΑΣΘΕΝΩΝ ΜΕ ΠΡΩΙΜΟ ΔΙΗΘΗΤΙΚΟ ΚΑΡΚΙΝΟ ΤΟΥ ΤΡΑΧΗΛΟΥ ΜΗΤΡΑΣ Μπουργιώτη Χάρις 1, Χατούπης Κωνσταντίνος 1, Αντωνίου Αριστείδης 1, Ροδολάκης
ΠΡΟΚΑΡΚΙΝΩΜΑΤΩΔΕΙΣ ΑΛΛΟΙΩΣΕΙΣ ΤΟΥ ΠΑΓΚΡΕΑΤΟΣ
 ΠΡΟΚΑΡΚΙΝΩΜΑΤΩΔΕΙΣ ΑΛΛΟΙΩΣΕΙΣ ΤΟΥ ΠΑΓΚΡΕΑΤΟΣ Ελένη Σπανίδου-Καρβούνη Καρβούνη, FRCPC Παθολογοανατόμος Αρεταίειο Νοσοκομείο Προκαρκινωματώδεις αλλοιώσεις του παγκρέατος Παγκρεατική Ενδοεπιθηλιακή Νεοπλασία
ΠΡΟΚΑΡΚΙΝΩΜΑΤΩΔΕΙΣ ΑΛΛΟΙΩΣΕΙΣ ΤΟΥ ΠΑΓΚΡΕΑΤΟΣ Ελένη Σπανίδου-Καρβούνη Καρβούνη, FRCPC Παθολογοανατόμος Αρεταίειο Νοσοκομείο Προκαρκινωματώδεις αλλοιώσεις του παγκρέατος Παγκρεατική Ενδοεπιθηλιακή Νεοπλασία
Όλα όσα χρειάζεται να γνωρίζεις
 Όλα όσα χρειάζεται να γνωρίζεις Επιστημονική Επιμέλεια: Χρήστος Μαρκόπουλος, Αναπλ. Καθηγητής Χειρουργικής, Ιατρική Σχολή Πανεπιστημίου Αθηνών για τον καρκίνο του μαστού Δεδομένα για τον καρκίνο του μαστού
Όλα όσα χρειάζεται να γνωρίζεις Επιστημονική Επιμέλεια: Χρήστος Μαρκόπουλος, Αναπλ. Καθηγητής Χειρουργικής, Ιατρική Σχολή Πανεπιστημίου Αθηνών για τον καρκίνο του μαστού Δεδομένα για τον καρκίνο του μαστού
Ταχεία Μαγνητική Μαστογραφία
 Ταχεία Μαγνητική Μαστογραφία Ultra-Fast Breast MRI (3 min MRI) Εάν σε 1000 γυναίκες με φυσιολογική Μαστογραφία και φυσιολογικό Υπερηχογράφημα μαστών προσθέσουμε την Ταχεία Μαγνητική Μαστογραφία θα ανακαλύψουμε
Ταχεία Μαγνητική Μαστογραφία Ultra-Fast Breast MRI (3 min MRI) Εάν σε 1000 γυναίκες με φυσιολογική Μαστογραφία και φυσιολογικό Υπερηχογράφημα μαστών προσθέσουμε την Ταχεία Μαγνητική Μαστογραφία θα ανακαλύψουμε
ΟΡΩΔΕΙΣ ΟΡΙΑΚΟΙ ΟΓΚΟΙ ΩΟΘΗΚΩΝ. Ηβη Αρβανίτη
 ΟΡΩΔΕΙΣ ΟΡΙΑΚΟΙ ΟΓΚΟΙ ΩΟΘΗΚΩΝ Ηβη Αρβανίτη 1898 Pfannenstiel θηλώδη κυσταδενώματα ωοθήκης 1929 Taylor ημικακοήθη νεοπλάσματα WHO του 2003 οριακός ορώδης όγκος (SΒΟΤ( ΒΟΤ) χαμηλής δυνητικής κακοηθείας όγκος
ΟΡΩΔΕΙΣ ΟΡΙΑΚΟΙ ΟΓΚΟΙ ΩΟΘΗΚΩΝ Ηβη Αρβανίτη 1898 Pfannenstiel θηλώδη κυσταδενώματα ωοθήκης 1929 Taylor ημικακοήθη νεοπλάσματα WHO του 2003 οριακός ορώδης όγκος (SΒΟΤ( ΒΟΤ) χαμηλής δυνητικής κακοηθείας όγκος
ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΤΙΜΕΤΩΠΙΣΗ ΚΑΡΚΙΝΟΥ ΕΝ ΟΜΗΤΡΙΟΥ
 ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΤΙΜΕΤΩΠΙΣΗ ΚΑΡΚΙΝΟΥ ΕΝ ΟΜΗΤΡΙΟΥ Κ. ΣΥΚΙΩΤΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ Γ ΜΑΙΕΥΤΙΚΗΣ-ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΠΑΝΕΠΙΣΤΗΜΟΥ ΑΘΗΝΩΝ ΓΥΝΑΙΚΟΛΟΓΟΣ - ΟΓΚΟΛΟΓΟΣ Η ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΤΙΜΕΤΩΠΙΣΗ του καρκίνου του
ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΤΙΜΕΤΩΠΙΣΗ ΚΑΡΚΙΝΟΥ ΕΝ ΟΜΗΤΡΙΟΥ Κ. ΣΥΚΙΩΤΗΣ ΕΠΙΚΟΥΡΟΣ ΚΑΘΗΓΗΤΗΣ Γ ΜΑΙΕΥΤΙΚΗΣ-ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΚΛΙΝΙΚΗΣ ΠΑΝΕΠΙΣΤΗΜΟΥ ΑΘΗΝΩΝ ΓΥΝΑΙΚΟΛΟΓΟΣ - ΟΓΚΟΛΟΓΟΣ Η ΧΕΙΡΟΥΡΓΙΚΗ ΑΝΤΙΜΕΤΩΠΙΣΗ του καρκίνου του
ακολουθιών διάχυσης πριν και μετά τη χορήγηση
 ακολουθιών διάχυσης πριν και μετά τη χορήγηση σκιαγραφικής ουσίας σε Μαγνητική τομογραφία μαστών 3Τ Φαναριώτης Μ. 1, Βάσιου Αικ. 1,3, Αθανασίου Ε. 2, Πουλτσίδη Α. 2, Αρβανίτης Δ. 3 Φεζουλίδης Ι. 1 1 Εργαστήριο
ακολουθιών διάχυσης πριν και μετά τη χορήγηση σκιαγραφικής ουσίας σε Μαγνητική τομογραφία μαστών 3Τ Φαναριώτης Μ. 1, Βάσιου Αικ. 1,3, Αθανασίου Ε. 2, Πουλτσίδη Α. 2, Αρβανίτης Δ. 3 Φεζουλίδης Ι. 1 1 Εργαστήριο
ΑΥΤΟΕΞΕΤΑΣΗ ΤΟΥ ΜΑΣΤΟΥ (ΑΕΜ)
 ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ Συχνότητα και θνησιμότητα Ca μαστού Ο κίνδυνος για την ανάπτυξη καρκίνου του μαστού στο γενικό πληθυσμό υπολογίζεται ότι κυμαίνεται σε 800 νέες περιπτώσεις ανά έτος σε 1.000.000 γυναίκες
ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ Συχνότητα και θνησιμότητα Ca μαστού Ο κίνδυνος για την ανάπτυξη καρκίνου του μαστού στο γενικό πληθυσμό υπολογίζεται ότι κυμαίνεται σε 800 νέες περιπτώσεις ανά έτος σε 1.000.000 γυναίκες
Έκθεση Ιστοπαθολογίας για τον Καρκίνο του Μαστού.
 Ο οδηγός σας αναφορικά µε την Έκθεση Ιστοπαθολογίας για τον Καρκίνο του Μαστού. Κάθε φορά που αφαιρείται ιστός από το σώµα µας για να ελεγχθεί ως προς την ύπαρξη καρκίνου, συντάσσεται µια έκθεση η οποία
Ο οδηγός σας αναφορικά µε την Έκθεση Ιστοπαθολογίας για τον Καρκίνο του Μαστού. Κάθε φορά που αφαιρείται ιστός από το σώµα µας για να ελεγχθεί ως προς την ύπαρξη καρκίνου, συντάσσεται µια έκθεση η οποία
Γενικά. Τί είναι ο κληρονομικός καρκίνος; κληρονομικός και σποραδικός καρκίνος. Κληρονομικός καρκίνος - Site Ε.Ο.Π.Ε. - Μ.Σ.
 1 Γενικά Ο καρκίνος προκαλείται από αλλαγές στα υλικά του σώματος μας που ονομάζονται «γονίδια». Πρόκειται για τις μονάδες πληροφοριών σε κάθε κύτταρο του σώματός μας. Τα γονίδια υπαγορεύουν στπν οργανισμό
1 Γενικά Ο καρκίνος προκαλείται από αλλαγές στα υλικά του σώματος μας που ονομάζονται «γονίδια». Πρόκειται για τις μονάδες πληροφοριών σε κάθε κύτταρο του σώματός μας. Τα γονίδια υπαγορεύουν στπν οργανισμό
Albert Salomon, Γερμανός χειρουργός, 1913 Ακτινογράφησε 3000 μαστούς από μαστεκτομή και συσχέτισε ακτινολογικά, κλινικά και παθολογοανατομικά
 Albert Salomon, Γερμανός χειρουργός, 1913 Ακτινογράφησε 3000 μαστούς από μαστεκτομή και συσχέτισε ακτινολογικά, κλινικά και παθολογοανατομικά ευρήματα. Stafford Warren, 1930, επί ασθενών, (στερεοσκοπική
Albert Salomon, Γερμανός χειρουργός, 1913 Ακτινογράφησε 3000 μαστούς από μαστεκτομή και συσχέτισε ακτινολογικά, κλινικά και παθολογοανατομικά ευρήματα. Stafford Warren, 1930, επί ασθενών, (στερεοσκοπική
ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ ΠΡΟΛΗΠΤΙΚΟΣ ΕΛΕΓΧΟΣ ΤΟΥ ΣΤΗΘΟΥΣ
 ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ ΠΡΟΛΗΠΤΙΚΟΣ ΕΛΕΓΧΟΣ ΤΟΥ ΣΤΗΘΟΥΣ Σ.N. ΓΕΩΡΓΙΑΝΝΟΣ, Μ.D., Ph.D. Ογκολόγος Χειρουργός Αγγειοχειρουργός Στη χώρα μας το ποσοστό της ανακάλυψης καρκίνων του μαστού σε πρώιμο στάδιο ανέρχεται
ΚΑΡΚΙΝΟΣ ΤΟΥ ΜΑΣΤΟΥ ΠΡΟΛΗΠΤΙΚΟΣ ΕΛΕΓΧΟΣ ΤΟΥ ΣΤΗΘΟΥΣ Σ.N. ΓΕΩΡΓΙΑΝΝΟΣ, Μ.D., Ph.D. Ογκολόγος Χειρουργός Αγγειοχειρουργός Στη χώρα μας το ποσοστό της ανακάλυψης καρκίνων του μαστού σε πρώιμο στάδιο ανέρχεται
Παράγοντες κινδύνου για τον καρκίνο του Παγκρέατος. Στέργιος Δελακίδης Γαστρεντερολόγος
 Παράγοντες κινδύνου για τον καρκίνο του Παγκρέατος Στέργιος Δελακίδης Γαστρεντερολόγος Καρκίνος Παγκρέατος: πρόγνωση Κακή πρόγνωση Συνολική πενταετής επιβίωση 6%.
Παράγοντες κινδύνου για τον καρκίνο του Παγκρέατος Στέργιος Δελακίδης Γαστρεντερολόγος Καρκίνος Παγκρέατος: πρόγνωση Κακή πρόγνωση Συνολική πενταετής επιβίωση 6%.
Χειρουργική αντιμετώπιση Καρκίνου Μαστού. Ξενοφών Ξενάκης MD PhD Χειρουργός Μαστού Ειδικός Μαστολόγος Επιστημονικός Συνεργάτης ΙΑΣΩ General Hospital
 Χειρουργική αντιμετώπιση Καρκίνου Μαστού Ξενοφών Ξενάκης MD PhD Χειρουργός Μαστού Ειδικός Μαστολόγος Επιστημονικός Συνεργάτης ΙΑΣΩ General Hospital Καρκίνος Μαστού Ο καρκίνος Πολυπαραγοντική Νόσος Δυτικός
Χειρουργική αντιμετώπιση Καρκίνου Μαστού Ξενοφών Ξενάκης MD PhD Χειρουργός Μαστού Ειδικός Μαστολόγος Επιστημονικός Συνεργάτης ΙΑΣΩ General Hospital Καρκίνος Μαστού Ο καρκίνος Πολυπαραγοντική Νόσος Δυτικός
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ. ΝΙΚΟΛΑΟΣ ΚΑΒΑΝΤΖΑΣ Επίκουρος Καθηγητής
 ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ ΝΙΚΟΛΑΟΣ ΚΑΒΑΝΤΖΑΣ Επίκουρος Καθηγητής ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ Επιφυσιοβλάστωµα Επιφυσιοκύττωµα Ογκος
ΕΘΝΙΚΟ ΚΑΙ ΚΑΠΟ ΙΣΤΡΙΑΚΟ ΠΑΝΕΠΙΣΤΗΜΙΟ ΑΘΗΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ Α ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ ΝΙΚΟΛΑΟΣ ΚΑΒΑΝΤΖΑΣ Επίκουρος Καθηγητής ΟΓΚΟΙ ΕΠΙΦΥΣΗΣ Επιφυσιοβλάστωµα Επιφυσιοκύττωµα Ογκος
ΜΑΣΤΟΣ. Ανατομία- Φυσιολογία Επιδημιολογικά στοιχεία. Στατιστικά στοιχεία Παράγοντες κινδύνου ανάπτυξης καρκίνου μαστού
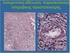 ΜΑΣΤΟΣ Ανατομία- Φυσιολογία Επιδημιολογικά στοιχεία Στατιστικά στοιχεία Παράγοντες κινδύνου ανάπτυξης καρκίνου μαστού ΝΙΚΗΤΑ ΑΛΕΞΑΝΔΡΑ Ακτινοδιαγνωστής Διδάκτωρ Πανεπιστημίου Αθηνών Consultant breast Radiologist
ΜΑΣΤΟΣ Ανατομία- Φυσιολογία Επιδημιολογικά στοιχεία Στατιστικά στοιχεία Παράγοντες κινδύνου ανάπτυξης καρκίνου μαστού ΝΙΚΗΤΑ ΑΛΕΞΑΝΔΡΑ Ακτινοδιαγνωστής Διδάκτωρ Πανεπιστημίου Αθηνών Consultant breast Radiologist
Ακανθοκυτταρικό καρκίνωμα κατωτέρου γεννητικού συστήματος θήλεος. Μαρία Σωτηροπούλου Νοσοκομείο Αλεξάνδρα
 Ακανθοκυτταρικό καρκίνωμα κατωτέρου γεννητικού συστήματος θήλεος Μαρία Σωτηροπούλου Νοσοκομείο Αλεξάνδρα Ακανθοκυτταρικό καρκίνωμα αιδοίου Σπάνιο, 1,5 ανά 100 000 γυναίκες στις ΗΠΑ Τρειςομάδεςγυναικών:
Ακανθοκυτταρικό καρκίνωμα κατωτέρου γεννητικού συστήματος θήλεος Μαρία Σωτηροπούλου Νοσοκομείο Αλεξάνδρα Ακανθοκυτταρικό καρκίνωμα αιδοίου Σπάνιο, 1,5 ανά 100 000 γυναίκες στις ΗΠΑ Τρειςομάδεςγυναικών:
18. ΚΑΡΚΙΝΟΣ ΕΝΔΟΜΗΤΡΙΟΥ
 18. ΚΑΡΚΙΝΟΣ ΕΝΔΟΜΗΤΡΙΟΥ Ο καρκίνος του ενδομητρίου είναι η συχνότερη μορφή γυναικολογικού καρκίνου στις ΗΠΑ ( 6% όλων των νεοδιαγνωσθέντων καρκίνων στις γυναίκες). Η πρόγνωση είναι σχετικά καλή καθώς
18. ΚΑΡΚΙΝΟΣ ΕΝΔΟΜΗΤΡΙΟΥ Ο καρκίνος του ενδομητρίου είναι η συχνότερη μορφή γυναικολογικού καρκίνου στις ΗΠΑ ( 6% όλων των νεοδιαγνωσθέντων καρκίνων στις γυναίκες). Η πρόγνωση είναι σχετικά καλή καθώς
Γεώργιος Α. Ανδρουτσόπουλος Επίκουρος Καθηγητής Μαιευτικής - Γυναικολογίας Πανεπιστημίου Πατρών. Πυελική μάζα
 Γεώργιος Α. Ανδρουτσόπουλος Επίκουρος Καθηγητής Μαιευτικής - Γυναικολογίας Πανεπιστημίου Πατρών Πυελική μάζα Επιδημιολογία Η πυελική μάζα είναι ένα σχετικά συχνό κλινικό εύρημα. Σε αρκετές περιπτώσεις
Γεώργιος Α. Ανδρουτσόπουλος Επίκουρος Καθηγητής Μαιευτικής - Γυναικολογίας Πανεπιστημίου Πατρών Πυελική μάζα Επιδημιολογία Η πυελική μάζα είναι ένα σχετικά συχνό κλινικό εύρημα. Σε αρκετές περιπτώσεις
Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις :
 Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις : Οι όρχεις αποτελούν κομμάτι του αναπαραγωγικού συστήματος (παραγωγή σπερματοζωάριων) του άνδρα αλλά
Δεκαπεντάλεπτη προετοιμασία του φοιτητή ιατρικής για το μάθημα του καρκίνου του όρχη βασικές γνώσεις : Οι όρχεις αποτελούν κομμάτι του αναπαραγωγικού συστήματος (παραγωγή σπερματοζωάριων) του άνδρα αλλά
Σήμερα η παγκόσμια ημέρα κατά του καρκίνου: Στατιστικά-πρόληψη
 Σήμερα η παγκόσμια ημέρα κατά του καρκίνου: Στατιστικά-πρόληψη Η Παγκόσμια Ημέρα κατά του Καρκίνου καθιερώθηκε με πρωτοβουλία της Διεθνούς Ένωσης κατά του Καρκίνου και πραγματοποιείται κάθε χρόνο στις
Σήμερα η παγκόσμια ημέρα κατά του καρκίνου: Στατιστικά-πρόληψη Η Παγκόσμια Ημέρα κατά του Καρκίνου καθιερώθηκε με πρωτοβουλία της Διεθνούς Ένωσης κατά του Καρκίνου και πραγματοποιείται κάθε χρόνο στις
Καλοήθεις παθήσεις των μαστών
 Καλοήθεις παθήσεις των μαστών Dr. Παναγιώτης Παπαλάμπρος MD, DFFP, BMS, BSCCP, CCST Μαιευτήρας - Χειρουργός Γυναικολόγος Εισαγωγή Ως γνωστόν, όπως όλα τα θηλαστικά ζώα, έτσι και ο άνθρωπος έχουν μαστούς.
Καλοήθεις παθήσεις των μαστών Dr. Παναγιώτης Παπαλάμπρος MD, DFFP, BMS, BSCCP, CCST Μαιευτήρας - Χειρουργός Γυναικολόγος Εισαγωγή Ως γνωστόν, όπως όλα τα θηλαστικά ζώα, έτσι και ο άνθρωπος έχουν μαστούς.
ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΠΑΘΟΛΟΓΙΚΗ ΑΝΑΤΟΜΙΚΗ (PATHOLOGY) Πρόδρομος Χυτίρογλου Εργαστήριο Γενικής Παθολογίας και Παθολογικής Ανατομικής Tμήματος Ιατρικής Α.Π.Θ.
 ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΠΑΘΟΛΟΓΙΚΗ ΑΝΑΤΟΜΙΚΗ (PATHOLOGY) Πρόδρομος Χυτίρογλου Εργαστήριο Γενικής Παθολογίας και Παθολογικής Ανατομικής Tμήματος Ιατρικής Α.Π.Θ. Παθολογική Ανατομική εξέταση των δομικών αλλοιώσεων
ΕΙΣΑΓΩΓΗ ΣΤΗΝ ΠΑΘΟΛΟΓΙΚΗ ΑΝΑΤΟΜΙΚΗ (PATHOLOGY) Πρόδρομος Χυτίρογλου Εργαστήριο Γενικής Παθολογίας και Παθολογικής Ανατομικής Tμήματος Ιατρικής Α.Π.Θ. Παθολογική Ανατομική εξέταση των δομικών αλλοιώσεων
TI NEOTEΡΟ ΣΤΟΥΣ ΝΕΥΡΟΕΝΔΟΚΡΙΝΕΙΣ ΟΓΚΟΥΣ ΤΟ 2015. Ορισμοί-Κατάταξη-Ιστολογία. Δ Ροντογιάννη
 TI NEOTEΡΟ ΣΤΟΥΣ ΝΕΥΡΟΕΝΔΟΚΡΙΝΕΙΣ ΟΓΚΟΥΣ ΤΟ 2015 Ορισμοί-Κατάταξη-Ιστολογία Δ Ροντογιάννη Νευροενδοκρινή νεοπλάσματα Ταξινόμηση Βιολογικοί δείκτες Μοριακή Παθολογία Νευροενδοκρινή νεοπλάσματα Ταξινόμηση
TI NEOTEΡΟ ΣΤΟΥΣ ΝΕΥΡΟΕΝΔΟΚΡΙΝΕΙΣ ΟΓΚΟΥΣ ΤΟ 2015 Ορισμοί-Κατάταξη-Ιστολογία Δ Ροντογιάννη Νευροενδοκρινή νεοπλάσματα Ταξινόμηση Βιολογικοί δείκτες Μοριακή Παθολογία Νευροενδοκρινή νεοπλάσματα Ταξινόμηση
Απεικονιστική Διερεύνηση & Παρακολούθηση του Χειρουργημένου Μαστού
 Απεικονιστική Διερεύνηση & Παρακολούθηση του Χειρουργημένου Μαστού Αρκάδιος Χ. Ρουσάκης Διευθυντής τμήματος Αξονικής & Μαγνητικής Τομογραφίας Δ.Θ.Κ.Α. «Υγεία» & «Μητέρα» Τύποι Επεμβάσεων στο Μαστό Διαδερμικές
Απεικονιστική Διερεύνηση & Παρακολούθηση του Χειρουργημένου Μαστού Αρκάδιος Χ. Ρουσάκης Διευθυντής τμήματος Αξονικής & Μαγνητικής Τομογραφίας Δ.Θ.Κ.Α. «Υγεία» & «Μητέρα» Τύποι Επεμβάσεων στο Μαστό Διαδερμικές
Εντοπίζεται συνήθως τυχαία διότι δεν εκδηλώνεται με πόνο. Εξαίρεση αποτελούν κάποιες πολύ σπάνιες προχωρημένες περιπτώσεις.
 8SELIDO ENTIPO AGALIAZO.indd 1 Εισαγωγή Το έντυπο που κρατάτε στα χέρια σας έχει γραφτεί για να ρίξει φως στα σημαντικά σημεία για τον καρκίνου του θυρεοειδούς ο οποίος αποτελεί έναν από τους πιο σπάνιους
8SELIDO ENTIPO AGALIAZO.indd 1 Εισαγωγή Το έντυπο που κρατάτε στα χέρια σας έχει γραφτεί για να ρίξει φως στα σημαντικά σημεία για τον καρκίνου του θυρεοειδούς ο οποίος αποτελεί έναν από τους πιο σπάνιους
Κατευθυντήριες οδηγίες της EAU για τον ουροθηλιακό καρκίνο ανώτερης αποχετευτικής μοίρας ουροποιητικού
 Κατευθυντήριες οδηγίες της EAU για τον ουροθηλιακό καρκίνο ανώτερης αποχετευτικής μοίρας ουροποιητικού M. Rouprêt, M. Babjuk, M. Burger, E. ompérat, N.. owan P. Gontero, A.H. Mostafid, J. Palou, B.W.G.
Κατευθυντήριες οδηγίες της EAU για τον ουροθηλιακό καρκίνο ανώτερης αποχετευτικής μοίρας ουροποιητικού M. Rouprêt, M. Babjuk, M. Burger, E. ompérat, N.. owan P. Gontero, A.H. Mostafid, J. Palou, B.W.G.
PET/CT versus DWI-MRI στην ογκολογία του θώρακος. Ευθυμιάδου Ρωξάνη Τμήμα Αξονικής, Μαγνητικής Τομογραφίας & PET-CT ΔΘΚΑ «Υγεία»
 PET/CT versus DWI-MRI στην ογκολογία του θώρακος. Ευθυμιάδου Ρωξάνη Τμήμα Αξονικής, Μαγνητικής Τομογραφίας & PET-CT ΔΘΚΑ «Υγεία» Ca πνεύμονος Η πρώτη αιτία θανάτου από καρκίνο στο δ υτικό κόσμο. 3.000.000
PET/CT versus DWI-MRI στην ογκολογία του θώρακος. Ευθυμιάδου Ρωξάνη Τμήμα Αξονικής, Μαγνητικής Τομογραφίας & PET-CT ΔΘΚΑ «Υγεία» Ca πνεύμονος Η πρώτη αιτία θανάτου από καρκίνο στο δ υτικό κόσμο. 3.000.000
ΚΑΡΚΙΝΟΣ ΩΟΘΗΚΩΝ. Θ. Πανοσκάλτσης MD, PhD, FRCOG, CCST (UK) Γυναικολόγος Ογκολόγος. Αρεταίειον Νοσοκομείο, Αθήνα
 ΚΑΡΚΙΝΟΣ ΩΟΘΗΚΩΝ Θ. Πανοσκάλτσης MD, PhD, FRCOG, CCST (UK) Γυναικολόγος Ογκολόγος Λέκτορας, 2 η Πανεπιστημιακή Κλινική Μαιευτικής Γυναικολογίας Αρεταίειον Νοσοκομείο, Αθήνα ΕΙΣΑΓΩΓΗ Ο καρκίνος ωοθηκών
ΚΑΡΚΙΝΟΣ ΩΟΘΗΚΩΝ Θ. Πανοσκάλτσης MD, PhD, FRCOG, CCST (UK) Γυναικολόγος Ογκολόγος Λέκτορας, 2 η Πανεπιστημιακή Κλινική Μαιευτικής Γυναικολογίας Αρεταίειον Νοσοκομείο, Αθήνα ΕΙΣΑΓΩΓΗ Ο καρκίνος ωοθηκών
Α. ΜΑΖΕΣ ACR BI - RADS ATLAS - ΜΑΣΤΟΓΡΑΦΙΑ
 ACR BI - RADS ATLAS - Μια μάζα είναι τρισδιάστατη και καταλαμβάνει χώρο. Είναι ορατή σε δύο διαφορετικές μαστογραφικές προβολές. Έχει εξολοκλήρου ή μερικώς κυρτά όρια και (αν είναι ακτινοσκιερή) παρουσιάζει
ACR BI - RADS ATLAS - Μια μάζα είναι τρισδιάστατη και καταλαμβάνει χώρο. Είναι ορατή σε δύο διαφορετικές μαστογραφικές προβολές. Έχει εξολοκλήρου ή μερικώς κυρτά όρια και (αν είναι ακτινοσκιερή) παρουσιάζει
ΜΕ ΑΦΟΡΜΗ ΤΟ ΜΕΛΑΝΩΜΑ ΔΙΑΛΕΥΚΑΝΣΗ ΟΡΩΝ ΚΑΙ ΕΞΕΛΙΞΕΩΝ
 ΜΕ ΑΦΟΡΜΗ ΤΟ ΜΕΛΑΝΩΜΑ ΔΙΑΛΕΥΚΑΝΣΗ ΟΡΩΝ ΚΑΙ ΕΞΕΛΙΞΕΩΝ Η Χειρουργική προσέγγιση του Μελανώματος Χρ. Σ. Κοσμίδης, Επίκουρος Καθηγητής Χειρουργικής ΑΠΘ, Γ Χειρουργική Κλινική, ΠΓΝΘ ΑΧΕΠΑ Μελάνωμα-Αρχική προσέγγιση
ΜΕ ΑΦΟΡΜΗ ΤΟ ΜΕΛΑΝΩΜΑ ΔΙΑΛΕΥΚΑΝΣΗ ΟΡΩΝ ΚΑΙ ΕΞΕΛΙΞΕΩΝ Η Χειρουργική προσέγγιση του Μελανώματος Χρ. Σ. Κοσμίδης, Επίκουρος Καθηγητής Χειρουργικής ΑΠΘ, Γ Χειρουργική Κλινική, ΠΓΝΘ ΑΧΕΠΑ Μελάνωμα-Αρχική προσέγγιση
ΑΣΘΕΝΕΙΣ ΙΑΤΡΕΙΟ ΠΑΘΗΣΕΩΝ ΜΑΣΤΟΥ: ΟΙ 1000 ΠΡΩΤΟΙ ΑΣΘΕΝΕΙΣ ΠΑΡΑΣΚΕΥΑΚΟΥ Γ MD, ΚΑΠΙΡΗΣ Σ MD, ΚΟΛΟΒΕΛΩΝΗΣ Γ MD, ΜΑΛΛΙΔΗΣ Ε MD,
 Γ ΧΕΙΡΟΥΡΓΙΚΟ ΤΜΗΜΑ ΤΟΥ ΓΝΑ ΕΥΑΓΓΕΛΙΣΜΟΣ Εισαγωγή Ο καρκίνος του μαστού είναι ο συχνότερος καρκίνος των γυναικών στον Δυτικό κόσμο. Από την έναρξη λειτουργίας του Ιατρείου Παθήσεων Μαστού (του Γ Χειρουργικού
Γ ΧΕΙΡΟΥΡΓΙΚΟ ΤΜΗΜΑ ΤΟΥ ΓΝΑ ΕΥΑΓΓΕΛΙΣΜΟΣ Εισαγωγή Ο καρκίνος του μαστού είναι ο συχνότερος καρκίνος των γυναικών στον Δυτικό κόσμο. Από την έναρξη λειτουργίας του Ιατρείου Παθήσεων Μαστού (του Γ Χειρουργικού
φυσιολογικό δέρμα - 1
 φυσιολογικό δέρμα -1 Επιδερμίδα (επιθήλιο, εξωδερμική προέλευση) Α Α Α Μ θηλώδες χόριο (επιπολής) ακανθωτή στιβάδα βασική στιβάδα χόριο Μ = Μελανοκύτταρο (νευροεξωδερμική προέλευση, νευρική ακρολοφία)
φυσιολογικό δέρμα -1 Επιδερμίδα (επιθήλιο, εξωδερμική προέλευση) Α Α Α Μ θηλώδες χόριο (επιπολής) ακανθωτή στιβάδα βασική στιβάδα χόριο Μ = Μελανοκύτταρο (νευροεξωδερμική προέλευση, νευρική ακρολοφία)
Ανατομία του προστάτη σε ζώνες κατά McNeal
 15/1/2018 Νέα απεικονιστική προσέγγιση του καρκίνου του προστάτη. Θέσεις και περιορισμοί του σύγχρονου ακτινολόγου. ΠΑΠΑΪΩΑΝΝΟΥ ΣΟΦΙΑ ΕΠΙΜΕΛΗΤΡΙΑ Α Ακτινολογικό Εργαστήριο Νοσ.Παπαγεωργίου ΣΥΝΤΟΝΙΣΤΗΣ
15/1/2018 Νέα απεικονιστική προσέγγιση του καρκίνου του προστάτη. Θέσεις και περιορισμοί του σύγχρονου ακτινολόγου. ΠΑΠΑΪΩΑΝΝΟΥ ΣΟΦΙΑ ΕΠΙΜΕΛΗΤΡΙΑ Α Ακτινολογικό Εργαστήριο Νοσ.Παπαγεωργίου ΣΥΝΤΟΝΙΣΤΗΣ
Α ΜΑΙΕΥΤΙΚΗ & ΓΥΝΑΙΚΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΤΜΗΜΑ ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Γ.Ν.Α. «ΑΛΕΞΑΝΔΡΑ» ΝΟΣΟΣ PAGET ΑΙΔΟΙΟΥ
 Α ΜΑΙΕΥΤΙΚΗ & ΓΥΝΑΙΚΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΤΜΗΜΑ ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Γ.Ν.Α. «ΑΛΕΞΑΝΔΡΑ» ΝΟΣΟΣ PAGET ΑΙΔΟΙΟΥ Κουτρούµπα Ι, Χαϊδόπουλος Δ, Θωµάκος Ν, Σωτηροπούλου Μ, Καθοπούλης Ν, Βλάχος
Α ΜΑΙΕΥΤΙΚΗ & ΓΥΝΑΙΚΟΛΟΓΙΚΗ ΚΛΙΝΙΚΗ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΑΘΗΝΩΝ ΤΜΗΜΑ ΓΥΝΑΙΚΟΛΟΓΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Γ.Ν.Α. «ΑΛΕΞΑΝΔΡΑ» ΝΟΣΟΣ PAGET ΑΙΔΟΙΟΥ Κουτρούµπα Ι, Χαϊδόπουλος Δ, Θωµάκος Ν, Σωτηροπούλου Μ, Καθοπούλης Ν, Βλάχος
Έμυ Μπάμη 7 o Νοσοκομείο Ι.Κ.Α
 Έμυ Μπάμη 7 o Νοσοκομείο Ι.Κ.Α Οι αποτιτανώσεις στη μαστογραφία είναι συχνά μια διαγνωστική πρόκληση. Είναι δύσκολες στην ανίχνευση και στην ανάλυση. Αρκετές γυναίκες ταλαιπωρούνται μετά την ανίχνευση
Έμυ Μπάμη 7 o Νοσοκομείο Ι.Κ.Α Οι αποτιτανώσεις στη μαστογραφία είναι συχνά μια διαγνωστική πρόκληση. Είναι δύσκολες στην ανίχνευση και στην ανάλυση. Αρκετές γυναίκες ταλαιπωρούνται μετά την ανίχνευση
«Η ΜΕΛΕΤΗ ΤΗΣ ΠΡΟΘΥΜΟΣΙΝΗΣ A (PRO ΤΑ) ΣΤΟ ΚΑΡΚΙΝΩΜΑ ΤΟΥ ΜΑΣΤΟΥ»
 V 0 Π Α Ν Ε Π ΙΣ Τ Η Μ ΙΟ ΙΩ Α Ν Ν ΙΝ Ω Ν ΙΑ Τ ΡΙΚ Η Σ Χ Ο Λ Η Μ Ο ΡΦ Ο Λ Ο ΓΙΚ Ο Σ -Κ Λ ΙΝ ΙΚ Ο Ε Ρ Γ Α Σ Τ Η ΡΙΑ Κ Ο Σ Τ Ο Μ Ε Α Σ Ε ΡΓΑ ΣΤΗ ΡΙΟ Π Α Θ Ο Λ Ο Γ ΙΚ Η Σ Α Ν Α Τ Ο Μ ΙΑ Σ «Η ΜΕΛΕΤΗ ΤΗΣ ΠΡΟΘΥΜΟΣΙΝΗΣ
V 0 Π Α Ν Ε Π ΙΣ Τ Η Μ ΙΟ ΙΩ Α Ν Ν ΙΝ Ω Ν ΙΑ Τ ΡΙΚ Η Σ Χ Ο Λ Η Μ Ο ΡΦ Ο Λ Ο ΓΙΚ Ο Σ -Κ Λ ΙΝ ΙΚ Ο Ε Ρ Γ Α Σ Τ Η ΡΙΑ Κ Ο Σ Τ Ο Μ Ε Α Σ Ε ΡΓΑ ΣΤΗ ΡΙΟ Π Α Θ Ο Λ Ο Γ ΙΚ Η Σ Α Ν Α Τ Ο Μ ΙΑ Σ «Η ΜΕΛΕΤΗ ΤΗΣ ΠΡΟΘΥΜΟΣΙΝΗΣ
BIRADS 3 Διαχείριση ασθενούς ΜΟΥΝΔΡΕΑ ΜΑΡΙΑΝΘΗ ΕΠΙΜΕΛΗΤΡΙΑ Α Ε.Α.Ν.Π ΜΕΤΑΞΑ
 BIRADS 3 Διαχείριση ασθενούς ΜΟΥΝΔΡΕΑ ΜΑΡΙΑΝΘΗ ΕΠΙΜΕΛΗΤΡΙΑ Α Ε.Α.Ν.Π ΜΕΤΑΞΑ Κατηγοριοποίηση κατά BI RADS Όταν γίνεται η περιγραφή μίας ανωμαλίας (μάζα, αρχιτεκτονική παραμόρφωση, εστιακή ασυμμετρία ή αποτιτανώσεις),
BIRADS 3 Διαχείριση ασθενούς ΜΟΥΝΔΡΕΑ ΜΑΡΙΑΝΘΗ ΕΠΙΜΕΛΗΤΡΙΑ Α Ε.Α.Ν.Π ΜΕΤΑΞΑ Κατηγοριοποίηση κατά BI RADS Όταν γίνεται η περιγραφή μίας ανωμαλίας (μάζα, αρχιτεκτονική παραμόρφωση, εστιακή ασυμμετρία ή αποτιτανώσεις),
ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΤΟΣ ΚΑΡΚΙΝΟΣ ΚΑΙ ΜΕΤΑΛΛΑΞΕΙΣ
 ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΤΟΣ 2012-2013 ΚΑΡΚΙΝΟΣ ΚΑΙ ΜΕΤΑΛΛΑΞΕΙΣ Τι είναι ο καρκίνος ; Ο Καρκίνος είναι ένα από τα σοβαρότερα προβλήματα υγείας που παρατηρούνται σήμερα στις αναπτυγμένες χώρες. Οι στατιστικές
ΓΥΜΝΑΣΙΟ ΚΕΡΑΤΕΑΣ ΕΤΟΣ 2012-2013 ΚΑΡΚΙΝΟΣ ΚΑΙ ΜΕΤΑΛΛΑΞΕΙΣ Τι είναι ο καρκίνος ; Ο Καρκίνος είναι ένα από τα σοβαρότερα προβλήματα υγείας που παρατηρούνται σήμερα στις αναπτυγμένες χώρες. Οι στατιστικές
ΚΑΡΚΙΝΟΣ ΤΟΥ ΛΑΡΥΓΓΑ
 ΚΩΝΣΤΑΝΤΙΝΟΣ ΒΛΑΧΤΣΗΣ ΙΑΤΡΟΣ ΩΤΟΡΙΝΟΛΑΡΥΓΓΟΛΟΓΟΣ Ι ΑΚΤΟΡΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΚΑΡΚΙΝΟΣ ΤΟΥ ΛΑΡΥΓΓΑ ΟΓΚΟΓΕΝΕΣΗ ΚΑΙ ΣΥΓΧΡΟΝΟΙ ΜΟΡΙΑΚΟΙ ΠΡΟΓΝΩΣΤΙΚΟΙ ΕΙΚΤΕΣ ΘΕΣΣΑΛΟΝΙΚΗ 2006 3 Κωνσταντίνος
ΚΩΝΣΤΑΝΤΙΝΟΣ ΒΛΑΧΤΣΗΣ ΙΑΤΡΟΣ ΩΤΟΡΙΝΟΛΑΡΥΓΓΟΛΟΓΟΣ Ι ΑΚΤΟΡΑΣ ΑΡΙΣΤΟΤΕΛΕΙΟΥ ΠΑΝΕΠΙΣΤΗΜΙΟΥ ΘΕΣΣΑΛΟΝΙΚΗΣ ΚΑΡΚΙΝΟΣ ΤΟΥ ΛΑΡΥΓΓΑ ΟΓΚΟΓΕΝΕΣΗ ΚΑΙ ΣΥΓΧΡΟΝΟΙ ΜΟΡΙΑΚΟΙ ΠΡΟΓΝΩΣΤΙΚΟΙ ΕΙΚΤΕΣ ΘΕΣΣΑΛΟΝΙΚΗ 2006 3 Κωνσταντίνος
Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας
 Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας Απαρτιωμένη διδασκαλία στην Αιματολογία 2015 Αργύρης Σ. Συμεωνίδης Οντότητες μη Hodgkin λεμφωμάτων που θα αναφερθούν Πρωτοπαθές Β-λέμφωμα
Ιδιαίτερες νοσολογικές οντότητες στα λεμφώματα υψηλού βαθμού κακοηθείας Απαρτιωμένη διδασκαλία στην Αιματολογία 2015 Αργύρης Σ. Συμεωνίδης Οντότητες μη Hodgkin λεμφωμάτων που θα αναφερθούν Πρωτοπαθές Β-λέμφωμα
Η παγκόσμια οργάνωση υγείας συνιστά την κατάταξη σε 4 βασικούς ιστολογικούς τύπους: καρκίνωμα μεταβατικού επιθηλίου, καρκίνωμα πλακώδους
 ΚΑΡΚΙΝΟΣ ΟΥΡΟΔΟΧΟΥ ΚΥΣΤΕΩΣ ΣΥΧΝΟΤΗΤΑ ΚΑΡΚΙΝΟΥ ΟΥΡΟΔΟΧΟΥ ΚΥΣΤΕΩΣ. Είναι ο τέταρτος πιο συχνός καρκίνος της στον Δυτικό κόσμο. Η μέση ηλικία κατά την διάγνωση είναι τα 60 με 65 έτη.είναι πιο συχνός στους
ΚΑΡΚΙΝΟΣ ΟΥΡΟΔΟΧΟΥ ΚΥΣΤΕΩΣ ΣΥΧΝΟΤΗΤΑ ΚΑΡΚΙΝΟΥ ΟΥΡΟΔΟΧΟΥ ΚΥΣΤΕΩΣ. Είναι ο τέταρτος πιο συχνός καρκίνος της στον Δυτικό κόσμο. Η μέση ηλικία κατά την διάγνωση είναι τα 60 με 65 έτη.είναι πιο συχνός στους
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων
 Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Συστηματικός ερυθηματώδης λύκος: το πρότυπο των αυτόάνοσων ρευματικών νοσημάτων Φ.Ν. Σκοπούλη Καθηγήτρια τον Χαροκόπειου Πανεπιστημίου Αθηνών συστηματικός ερυθηματώδης λύκος θεωρείται η κορωνίδα των αυτοάνοσων
Η πρώιμη διάγνωση σώζει. Ο ειδικός θεραπεύει
 Κλείσε ένα ραντεβού ζωής Αφιέρωσε 10 λεπτά στον εαυτό σου για μια μαστογραφία Όσα θα θέλατε να μάθετε για τον καρκίνο του μαστού Η πρώιμη διάγνωση σώζει. Ο ειδικός θεραπεύει Τι είναι ο καρκίνος του μαστού;
Κλείσε ένα ραντεβού ζωής Αφιέρωσε 10 λεπτά στον εαυτό σου για μια μαστογραφία Όσα θα θέλατε να μάθετε για τον καρκίνο του μαστού Η πρώιμη διάγνωση σώζει. Ο ειδικός θεραπεύει Τι είναι ο καρκίνος του μαστού;
UROGOLD III: Οι σηµαντικότερες δηµοσιεύσεις της χρονιάς Καρκίνος Όρχεως και Πέους Ευάγγελος Φραγκιάδης Ακαδηµαϊκός Υπότροφος Α Ουρολογική Κλινική ΕΚΠΑ
 UROGOLD III: Οι σηµαντικότερες δηµοσιεύσεις της χρονιάς Καρκίνος Όρχεως και Πέους Ευάγγελος Φραγκιάδης Ακαδηµαϊκός Υπότροφος Α Ουρολογική Κλινική ΕΚΠΑ Καµία σύγκρουση συµφερόντων Some may think this was
UROGOLD III: Οι σηµαντικότερες δηµοσιεύσεις της χρονιάς Καρκίνος Όρχεως και Πέους Ευάγγελος Φραγκιάδης Ακαδηµαϊκός Υπότροφος Α Ουρολογική Κλινική ΕΚΠΑ Καµία σύγκρουση συµφερόντων Some may think this was
Δρ. Μπάμπης Φ. Γιαννουλόπουλος. Μαιευτήρας - Γυναικολόγος Χειρουργός Μαστού. Γαία Μαιευτική-Γυναικολογική
 Δρ. Μπάμπης Φ. Γιαννουλόπουλος Μαιευτήρας - Γυναικολόγος Χειρουργός Μαστού Γαία Μαιευτική-Γυναικολογική Επίπτωση παγκοσμίως 89/100.000 γυναίκες, 800.000 νέα περιστατικά ετησίως. U.S.A. 250.000 νέα περιστατικά,
Δρ. Μπάμπης Φ. Γιαννουλόπουλος Μαιευτήρας - Γυναικολόγος Χειρουργός Μαστού Γαία Μαιευτική-Γυναικολογική Επίπτωση παγκοσμίως 89/100.000 γυναίκες, 800.000 νέα περιστατικά ετησίως. U.S.A. 250.000 νέα περιστατικά,
ΣΥΓΧΡΟΝΟ ΚΕΝΤΡΟ. Με ειδίκευση στο γυναικείο µαστό
 ΣΥΓΧΡΟΝΟ ΚΕΝΤΡΟ Με ειδίκευση στο γυναικείο µαστό Το Κέντρο Μαστού του Ερρίκος Ντυνάν Hospital Center αποτελεί ένα πρότυπο, σύγχρονο ιατρικό κέντρο µε ειδίκευση στο γυναικείο µαστό. Παρέχει ολοκληρωµένες
ΣΥΓΧΡΟΝΟ ΚΕΝΤΡΟ Με ειδίκευση στο γυναικείο µαστό Το Κέντρο Μαστού του Ερρίκος Ντυνάν Hospital Center αποτελεί ένα πρότυπο, σύγχρονο ιατρικό κέντρο µε ειδίκευση στο γυναικείο µαστό. Παρέχει ολοκληρωµένες
Ι) ΗΠΑΤΕΚΤΟΜΗ ΓΙΑ ΕΝ ΟΗΠΑΤΙΚΟ ΧΟΛΑΓΓΕΙΟΚΑΡΚΙΝΩΜΑ: ΜΑΚΡΟΣΚΟΠΙΚΗ ΕΞΕΤΑΣΗ:
 ΧΕΙΡΟΥΡΓΙΚΑ ΠΑΡΑΣΚΕΥΑΣΜΑΤΑ ΕΚΤΟΜΗΣ ΧΟΛΑΓΓΕΙΟΚΑΡΚΙΝΩΜΑΤΟΣ Β. Τζιούφα, Αναπληρώτρια Καθηγήτρια Ιατρικής Σχολής Εργαστηρίου Παθολογικής Ανατοµικής, Αριστοτέλειο Πανεπιστήµιο Θεσσαλονίκης Ι) ΗΠΑΤΕΚΤΟΜΗ ΓΙΑ
ΧΕΙΡΟΥΡΓΙΚΑ ΠΑΡΑΣΚΕΥΑΣΜΑΤΑ ΕΚΤΟΜΗΣ ΧΟΛΑΓΓΕΙΟΚΑΡΚΙΝΩΜΑΤΟΣ Β. Τζιούφα, Αναπληρώτρια Καθηγήτρια Ιατρικής Σχολής Εργαστηρίου Παθολογικής Ανατοµικής, Αριστοτέλειο Πανεπιστήµιο Θεσσαλονίκης Ι) ΗΠΑΤΕΚΤΟΜΗ ΓΙΑ
ΠΡΟΚΑΡΚΙΝΙΚΕΣ ΑΛΛΟΙΩΣΕΙΣ ΣΤΟΜΑΧΟΥ ΠΑΧΕΟΣ ΕΝΤΕΡΟΥ
 ΠΡΟΚΑΡΚΙΝΙΚΕΣ ΑΛΛΟΙΩΣΕΙΣ ΣΤΟΜΑΧΟΥ ΠΑΧΕΟΣ ΕΝΤΕΡΟΥ ΕΛΛΗΝΙΚΗ ΠΑΘΟΛΟΓΟAΝΑΤΟΜΙΚΗ ΕΤΑΙΡΕΙΑ ΟΜΑΔΑ ΠΕΠΤΙΚΟΥ ΑΘΗΝΑ 15 Δεκεμβρίου 2004 Mαρία Δαιμονάκου- Βατοπούλου Αναπληρώτρια Διευθύντρια Σισμανόγλειο ΓΠΝΑ Kαρκινογέννεση
ΠΡΟΚΑΡΚΙΝΙΚΕΣ ΑΛΛΟΙΩΣΕΙΣ ΣΤΟΜΑΧΟΥ ΠΑΧΕΟΣ ΕΝΤΕΡΟΥ ΕΛΛΗΝΙΚΗ ΠΑΘΟΛΟΓΟAΝΑΤΟΜΙΚΗ ΕΤΑΙΡΕΙΑ ΟΜΑΔΑ ΠΕΠΤΙΚΟΥ ΑΘΗΝΑ 15 Δεκεμβρίου 2004 Mαρία Δαιμονάκου- Βατοπούλου Αναπληρώτρια Διευθύντρια Σισμανόγλειο ΓΠΝΑ Kαρκινογέννεση
Όρχεις -Χειρισμός παρασκευάσματος -Εισαγωγή στους όγκους. Α.. Κιζιρίδου, Αναπ. Διευθύντρια Παθολογοανατομικού Τμήματος A.Ν.Θ.
 Όρχεις -Χειρισμός παρασκευάσματος -Εισαγωγή στους όγκους Α.. Κιζιρίδου, Αναπ. Διευθύντρια Παθολογοανατομικού Τμήματος A.Ν.Θ.Θεαγένειο Περιγραφική Ανατομική 2 αδένες με σχήμα δαμάσκηνου διαστ.5χ3χ2.5 Κρέμονται
Όρχεις -Χειρισμός παρασκευάσματος -Εισαγωγή στους όγκους Α.. Κιζιρίδου, Αναπ. Διευθύντρια Παθολογοανατομικού Τμήματος A.Ν.Θ.Θεαγένειο Περιγραφική Ανατομική 2 αδένες με σχήμα δαμάσκηνου διαστ.5χ3χ2.5 Κρέμονται
Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ. Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη
 Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη 2013 ΠΕΡΙΕΧΟΜΕΝΑ : Ορολογία και λίγα λόγια για τον καρκίνο Χαρακτηριστικά του καρκίνου Μεταλλάξεις Μεταλλάξεις και καρκίνος
Γυμνάσιο Κερατέας ΚΑΡΚΙΝΟΣ & ΜΕΤΑΛΛΑΞΕΙΣ Αναστασία Σουλαχάκη Κωνσταντίνα Πρίφτη 2013 ΠΕΡΙΕΧΟΜΕΝΑ : Ορολογία και λίγα λόγια για τον καρκίνο Χαρακτηριστικά του καρκίνου Μεταλλάξεις Μεταλλάξεις και καρκίνος
Συνήθεις νεοπλασματικές βλάβες τραχήλου / σώματοςμήτραςκαι ωοθηκών. Στ Εξάμηνο ΦΡΟΝΤΙΣΤΗΡΙΟ #4
 Συνήθεις νεοπλασματικές βλάβες τραχήλου / σώματοςμήτραςκαι ωοθηκών Στ Εξάμηνο ΦΡΟΝΤΙΣΤΗΡΙΟ #4 Βασιλική Κωτούλα Δημητριάδου, επίκ. καθ. ΕΓΠΠΑ Σωτήρης Μπαρμπάνης, άμ. επιστ. συν. ΕΓΠΠΑ διαφορές? όγκοι από
Συνήθεις νεοπλασματικές βλάβες τραχήλου / σώματοςμήτραςκαι ωοθηκών Στ Εξάμηνο ΦΡΟΝΤΙΣΤΗΡΙΟ #4 Βασιλική Κωτούλα Δημητριάδου, επίκ. καθ. ΕΓΠΠΑ Σωτήρης Μπαρμπάνης, άμ. επιστ. συν. ΕΓΠΠΑ διαφορές? όγκοι από
ΕΝΔΟΒΡΟΓΧΙΚΗ ΒΡΑΧΥΘΕΡΑΠΕΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΠΝΕΥΜΟΝΟΣ. 2,Β.Αναστασάκος2,
 ΕΝΔΟΒΡΟΓΧΙΚΗ ΒΡΑΧΥΘΕΡΑΠΕΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΠΝΕΥΜΟΝΟΣ. Κ. Παπαλλά 1, Δ. Μπισιρτζόγλου2, Αθ. Ζέτος 2,Β.Αναστασάκος2, 2Γ. Ιωαννίδου 1, 2Δ. Ξεσφύγγη 1, Μ.Πλόχωρου1,Μ.Καραβαλλάκης 1 Ι.Τσαλαφουτας 1 Γ. Πολίτης
ΕΝΔΟΒΡΟΓΧΙΚΗ ΒΡΑΧΥΘΕΡΑΠΕΙΑ ΣΤΟΝ ΚΑΡΚΙΝΟ ΠΝΕΥΜΟΝΟΣ. Κ. Παπαλλά 1, Δ. Μπισιρτζόγλου2, Αθ. Ζέτος 2,Β.Αναστασάκος2, 2Γ. Ιωαννίδου 1, 2Δ. Ξεσφύγγη 1, Μ.Πλόχωρου1,Μ.Καραβαλλάκης 1 Ι.Τσαλαφουτας 1 Γ. Πολίτης
Συνέντευξη με τον Παθολόγο - Ογκολόγο, Στυλιανό Γιασσά
 Συνέντευξη με τον Παθολόγο - Ογκολόγο, Στυλιανό Γιασσά Ο καρκίνος του παχέος εντέρου ορθού αποτελεί το δεύτερο πιο συχνό καρκίνο σε γυναίκες και άνδρες και αντιπροσωπεύει το 13% όλων των καρκίνων. Στην
Συνέντευξη με τον Παθολόγο - Ογκολόγο, Στυλιανό Γιασσά Ο καρκίνος του παχέος εντέρου ορθού αποτελεί το δεύτερο πιο συχνό καρκίνο σε γυναίκες και άνδρες και αντιπροσωπεύει το 13% όλων των καρκίνων. Στην
Πυελική μάζα. Ενότητα 3: Πύελος Παθολογία πυέλου
 Πυελική μάζα Ενότητα 3: Πύελος Παθολογία πυέλου Γεώργιος Α. Ανδρουτσόπουλος Επίκουρος Καθηγητής Ιατρική Σχολή Μαιευτικής - Γυναικολογίας Πανεπιστημίου Πατρών Σκοποί ενότητας Παρουσίαση Πυελικής Μάζας Πρόπτωση
Πυελική μάζα Ενότητα 3: Πύελος Παθολογία πυέλου Γεώργιος Α. Ανδρουτσόπουλος Επίκουρος Καθηγητής Ιατρική Σχολή Μαιευτικής - Γυναικολογίας Πανεπιστημίου Πατρών Σκοποί ενότητας Παρουσίαση Πυελικής Μάζας Πρόπτωση
Περιέχει 30-50 αδένες και το (πρόσθιο) ινομυώδες στρώμα
 Ε. ΑΝΔΡΙΩΤΗΣ ΠΡΟΣΤΑΤΗΣ Περιέχει 30-50 αδένες και το (πρόσθιο) ινομυώδες στρώμα οι οποίοι περιβάλλονται από παχιά κάψα συνδετικού ιστού. Οι εκκριτικοί πόροι εκβάλλουν στην προστατική μοίρα της ουρήθρας.
Ε. ΑΝΔΡΙΩΤΗΣ ΠΡΟΣΤΑΤΗΣ Περιέχει 30-50 αδένες και το (πρόσθιο) ινομυώδες στρώμα οι οποίοι περιβάλλονται από παχιά κάψα συνδετικού ιστού. Οι εκκριτικοί πόροι εκβάλλουν στην προστατική μοίρα της ουρήθρας.
Γράφει: Αλίκη Τσερκέζογλου, Γυναικολόγος Ογκολόγος, Τέως Συντονίστρια Διευθύντρια Νοσοκομείου «Ο Άγιος Σάββας», Συνεργάτις Ευρωκλινική Αθηνών
 Γράφει: Αλίκη Τσερκέζογλου, Γυναικολόγος Ογκολόγος, Τέως Συντονίστρια Διευθύντρια Νοσοκομείου «Ο Άγιος Σάββας», Συνεργάτις Ευρωκλινική Αθηνών Ο καρκίνος του ενδομητρίου αναπτύσσεται στο ενδομήτριο, που
Γράφει: Αλίκη Τσερκέζογλου, Γυναικολόγος Ογκολόγος, Τέως Συντονίστρια Διευθύντρια Νοσοκομείου «Ο Άγιος Σάββας», Συνεργάτις Ευρωκλινική Αθηνών Ο καρκίνος του ενδομητρίου αναπτύσσεται στο ενδομήτριο, που
ΣΥΝΥΠΑΡΞΗ ΜΕΤΑΣΤΑΤΙΚΗΣ ΝΟΣΟΥ ΚΑΙ ΦΥΜΑΤΙΩΣΗΣ ΣΕ ΜΑΣΧΑΛΙΑΙΟΥΣ ΛΕΜΦΑΔΕΝΕΣ ΣΕ ΑΣΘΕΝΗ ΜΕ ΑΔΕΝΟΚΑΡΚΙΝΩΜΑ ΜΑΣΤΟΥ.
 ΚΑΙ ΦΥΜΑΤΙΩΣΗΣ ΛΕΜΦΑΔΕΝΕΣ ΣΕ ΑΣΘΕΝΗ Μονάδα Μαστού, 401 ΓΣΝΑ, Αθήνα Εισαγωγή Αναφορές Εισαγωγή Η συνύπαρξη μεταστατικού καρκίνου του μαστού και φυματίωσης σε μασχαλιαίους λεμφαδένες είναι εξαιρετικά σπάνια
ΚΑΙ ΦΥΜΑΤΙΩΣΗΣ ΛΕΜΦΑΔΕΝΕΣ ΣΕ ΑΣΘΕΝΗ Μονάδα Μαστού, 401 ΓΣΝΑ, Αθήνα Εισαγωγή Αναφορές Εισαγωγή Η συνύπαρξη μεταστατικού καρκίνου του μαστού και φυματίωσης σε μασχαλιαίους λεμφαδένες είναι εξαιρετικά σπάνια
Πανεπιστήμιο Θεσσαλίας Τμήμα Ιατρικής Εργαστήριο Ακτινολογίας Ιατρικής Απεικόνισης
 Πανεπιστήμιο Θεσσαλίας Τμήμα Ιατρικής Εργαστήριο Ακτινολογίας Ιατρικής Απεικόνισης Διδάσκοντες Ιωάννης Β. Φεζουλίδης Καθηγητής Μαριάννα Βλυχού Αναπλ. Καθηγήτρια Έφη Καψαλάκη Αναπλ. Καθηγήτρια Αικατερίνη
Πανεπιστήμιο Θεσσαλίας Τμήμα Ιατρικής Εργαστήριο Ακτινολογίας Ιατρικής Απεικόνισης Διδάσκοντες Ιωάννης Β. Φεζουλίδης Καθηγητής Μαριάννα Βλυχού Αναπλ. Καθηγήτρια Έφη Καψαλάκη Αναπλ. Καθηγήτρια Αικατερίνη
ΕΧΕΤΕ ΠΡΟΣΦΑΤΑ ΔΙΑΓΝΩΣΘΕΙ με πρώιμο καρκίνο του μαστού;
 ΕΧΕΤΕ ΠΡΟΣΦΑΤΑ ΔΙΑΓΝΩΣΘΕΙ με πρώιμο καρκίνο του μαστού; Anne-Marie Μητέρα Επιστήμονας Ιατρικής από την Ιρλανδία και ασθενής με καρκίνο μαστού που έκανε το Oncotype DX Ένας εκπαιδευτικός οδηγός που δημιουργήθηκε
ΕΧΕΤΕ ΠΡΟΣΦΑΤΑ ΔΙΑΓΝΩΣΘΕΙ με πρώιμο καρκίνο του μαστού; Anne-Marie Μητέρα Επιστήμονας Ιατρικής από την Ιρλανδία και ασθενής με καρκίνο μαστού που έκανε το Oncotype DX Ένας εκπαιδευτικός οδηγός που δημιουργήθηκε
VIN (Ενδοεπιθηλιακή νεοπλασία αιδοίου)
 VIN (Ενδοεπιθηλιακή νεοπλασία αιδοίου) Διαφορές μεταξύ τραχήλου και αιδοίου Κύτταρο-στόχος: κυρίως πλακώδες δεν υπάρχει εκτεθειμένος πολυδύναμος πληθυσμός, όπως στον τράχηλο Σχετιζόμενοι HPV: κυριαρχούν
VIN (Ενδοεπιθηλιακή νεοπλασία αιδοίου) Διαφορές μεταξύ τραχήλου και αιδοίου Κύτταρο-στόχος: κυρίως πλακώδες δεν υπάρχει εκτεθειμένος πολυδύναμος πληθυσμός, όπως στον τράχηλο Σχετιζόμενοι HPV: κυριαρχούν
ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ
 ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ Βασικές γνώσεις I SBN 960-372-069-0 ΠΕΡΙΕΧΟΜΕΝΑ ΠΑΡΙΣ Α. ΚΟΣΜΙΔΗΣ ΓΕΩΡΓΙΟΣ ΤΣΑΚΙΡΗΣ Μ Ε Ρ Ο Σ Ι ΟΓΚΟΛΟΓΙΑ Κεφάλαιο 1 ΕΙΣΑΓΩΓΗ ΣΤΟΝ ΚΑΡΚΙΝΟ... 3 Το καρκινικό κύτταρο... 3 Κυτταρικός
ΟΓΚΟΛΟΓΙΑ - ΡΑΔΙΟΒΙΟΛΟΓΙΑ Βασικές γνώσεις I SBN 960-372-069-0 ΠΕΡΙΕΧΟΜΕΝΑ ΠΑΡΙΣ Α. ΚΟΣΜΙΔΗΣ ΓΕΩΡΓΙΟΣ ΤΣΑΚΙΡΗΣ Μ Ε Ρ Ο Σ Ι ΟΓΚΟΛΟΓΙΑ Κεφάλαιο 1 ΕΙΣΑΓΩΓΗ ΣΤΟΝ ΚΑΡΚΙΝΟ... 3 Το καρκινικό κύτταρο... 3 Κυτταρικός
ΕΚΤΟΜΗ ΠΝΕΥΜΟΝΙΚΟΥ ΠΑΡΕΓΧΥΜΑΤΟΣ ΜΕΤΑ ΑΠΟ ΕΙΣΑΓΩΓΙΚΗ ΧΗΜΕΙΟ-ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ. Χριστόφορος Ν. Φορούλης Επίκουρος Καθηγητής Θωρακοχειρουργικής Α.Π.Θ.
 ΕΚΤΟΜΗ ΠΝΕΥΜΟΝΙΚΟΥ ΠΑΡΕΓΧΥΜΑΤΟΣ ΜΕΤΑ ΑΠΟ ΕΙΣΑΓΩΓΙΚΗ ΧΗΜΕΙΟ-ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ Χριστόφορος Ν. Φορούλης Επίκουρος Καθηγητής Θωρακοχειρουργικής Α.Π.Θ. Πρόληψη και Θεραπευτικές Προσεγγίσεις του Καρκίνου του Πνεύμονα
ΕΚΤΟΜΗ ΠΝΕΥΜΟΝΙΚΟΥ ΠΑΡΕΓΧΥΜΑΤΟΣ ΜΕΤΑ ΑΠΟ ΕΙΣΑΓΩΓΙΚΗ ΧΗΜΕΙΟ-ΑΚΤΙΝΟΘΕΡΑΠΕΙΑ Χριστόφορος Ν. Φορούλης Επίκουρος Καθηγητής Θωρακοχειρουργικής Α.Π.Θ. Πρόληψη και Θεραπευτικές Προσεγγίσεις του Καρκίνου του Πνεύμονα
Πρόλογος. Δημήτρης Λ. Αβραμόπουλος
 Δημήτρης Λ. Αβραμόπουλος Υπουργός Υγείας και Κοινωνικής Αλληλεγγύης Πρόλογος ΟΔΗΓΟΣ ΓΙΑ ΤΟΝ ΚΑΡΚΙΝΟ ΤΟΥ ΜΑΣΤΟΥ Η πρόληψη αποτελεί έναν από τους βασικούς πυλώνες του στρατηγικού μας σχεδιασμού για την Υγεία.
Δημήτρης Λ. Αβραμόπουλος Υπουργός Υγείας και Κοινωνικής Αλληλεγγύης Πρόλογος ΟΔΗΓΟΣ ΓΙΑ ΤΟΝ ΚΑΡΚΙΝΟ ΤΟΥ ΜΑΣΤΟΥ Η πρόληψη αποτελεί έναν από τους βασικούς πυλώνες του στρατηγικού μας σχεδιασμού για την Υγεία.
Καρκίνος Μαστού Απρίλιος 2015
 ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ Σχολή Επιστημών Υγείας ΜΑΘΗΜΑΤΑ ΑΚΤΙΝΟΘΕΡΑΠΕΥΤΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Καρκίνος Μαστού Απρίλιος 2015 Γιώργος Κύργιας Ογκολόγος Ακτινοθεραπευτής Αναπλ. Καθηγητής Ακτινοθεραπείας ΑΝΑΤΟΜΙΑ ΜΑΣΤΟΥ
ΠΑΝΕΠΙΣΤΗΜΙΟ ΘΕΣΣΑΛΙΑΣ Σχολή Επιστημών Υγείας ΜΑΘΗΜΑΤΑ ΑΚΤΙΝΟΘΕΡΑΠΕΥΤΙΚΗΣ ΟΓΚΟΛΟΓΙΑΣ Καρκίνος Μαστού Απρίλιος 2015 Γιώργος Κύργιας Ογκολόγος Ακτινοθεραπευτής Αναπλ. Καθηγητής Ακτινοθεραπείας ΑΝΑΤΟΜΙΑ ΜΑΣΤΟΥ
Λίγα λόγια για τους καρκίνους, τη γενετική τους βάση και διερεύνηση
 Λίγα λόγια για τους καρκίνους, τη γενετική τους βάση και διερεύνηση Ο καρκίνος είναι μια ιδιαίτερα ετερογενής νόσος, που προκύπτει από συσσώρευση μεταλλάξεων του DNA. Η αιτιολογία του καρκίνου είναι πολυπαραγοντική,
Λίγα λόγια για τους καρκίνους, τη γενετική τους βάση και διερεύνηση Ο καρκίνος είναι μια ιδιαίτερα ετερογενής νόσος, που προκύπτει από συσσώρευση μεταλλάξεων του DNA. Η αιτιολογία του καρκίνου είναι πολυπαραγοντική,
ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ και ΚΑΡΚΙΝΟΣ: συνύπαρξη ή αιτιολογική σχέση;
 ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ και ΚΑΡΚΙΝΟΣ: συνύπαρξη ή αιτιολογική σχέση; Δ. Καραγιάννη, Β. Κουρκούμπας, Δ. Μπαλτζής, Γ. Κοτρώνης, Ε. Κιντιράκη, Χ.Τρακατέλλη, Α. Παυλίδου, Μ. Σιών Γ Παθολογική Κλινική ΑΠΘ, ΓΠΝΘ
ΣΑΚΧΑΡΩΔΗΣ ΔΙΑΒΗΤΗΣ και ΚΑΡΚΙΝΟΣ: συνύπαρξη ή αιτιολογική σχέση; Δ. Καραγιάννη, Β. Κουρκούμπας, Δ. Μπαλτζής, Γ. Κοτρώνης, Ε. Κιντιράκη, Χ.Τρακατέλλη, Α. Παυλίδου, Μ. Σιών Γ Παθολογική Κλινική ΑΠΘ, ΓΠΝΘ
Προχωρημένος Καρκίνος του Μαστού
 Προχωρημένος Καρκίνος του Μαστού 2 Εισαγωγή Περιεχόμενα 3 Εισαγωγή Τα τελευταία 30 χρόνια έχουν διατεθεί σημαντικοί πόροι για την πρόληψη, την έγκαιρη διάγνωση και τη θεραπεία συγκεκριμένων τύπων καρκίνου
Προχωρημένος Καρκίνος του Μαστού 2 Εισαγωγή Περιεχόμενα 3 Εισαγωγή Τα τελευταία 30 χρόνια έχουν διατεθεί σημαντικοί πόροι για την πρόληψη, την έγκαιρη διάγνωση και τη θεραπεία συγκεκριμένων τύπων καρκίνου
Πρόληψη, πρόγνωση και θεραπεία του καρκίνου του μαστού
 Πρόληψη, πρόγνωση και θεραπεία του καρκίνου του μαστού Σταμάτης Βασίλαρος Επίκουρος Καθηγητής Πανεπιστημίου Αθηνών Ευχαριστώ για τα ωραία λόγια, τιμή μου που είμαι εδώ σήμερα και που με καλέσατε να πάρω
Πρόληψη, πρόγνωση και θεραπεία του καρκίνου του μαστού Σταμάτης Βασίλαρος Επίκουρος Καθηγητής Πανεπιστημίου Αθηνών Ευχαριστώ για τα ωραία λόγια, τιμή μου που είμαι εδώ σήμερα και που με καλέσατε να πάρω
Οργανωτική Επιτροπή Πρόεδρος: Μέλη: Επιστημονική Επιτροπή Πρόεδρος: Μέλη:
 Επιτροπές Οργανωτική Επιτροπή Πρόεδρος: Μέλη: Ελένη Φαλιάκου Ηλίας Αθανασιάδης Αλεξάνδρα Αθανασίου Γεώργιος Παπάζογλου Σάββας Παπαδόπουλος Χριστίνα Τσιώνου Επιστημονική Επιτροπή Πρόεδρος: Μέλη: Ηλίας Αθανασιάδης
Επιτροπές Οργανωτική Επιτροπή Πρόεδρος: Μέλη: Ελένη Φαλιάκου Ηλίας Αθανασιάδης Αλεξάνδρα Αθανασίου Γεώργιος Παπάζογλου Σάββας Παπαδόπουλος Χριστίνα Τσιώνου Επιστημονική Επιτροπή Πρόεδρος: Μέλη: Ηλίας Αθανασιάδης
των ακολουθιών διάχυσης
 Επαναληψιμότητα των μετρήσεων ADC των ακολουθιών διάχυσης σε μαγνητική τομογραφία μαστών 3Τ Φαναριώτης Μ. 1, Βάσιου Αικ. 1,3, Αθανασίου Ε. 2, Πουλτσίδη Α. 2, Αρβανίτης Δ. 3 Φεζουλίδης Ι. 1 1 Εργαστήριο
Επαναληψιμότητα των μετρήσεων ADC των ακολουθιών διάχυσης σε μαγνητική τομογραφία μαστών 3Τ Φαναριώτης Μ. 1, Βάσιου Αικ. 1,3, Αθανασίου Ε. 2, Πουλτσίδη Α. 2, Αρβανίτης Δ. 3 Φεζουλίδης Ι. 1 1 Εργαστήριο
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας
 Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
Μια ενημέρωση για ασθενείς και παρόχους φροντίδας Τι είναι το FoundationOne ; Το FoundationOne είναι μια εξέταση που ανιχνεύει γενωμικές μεταβολές (π.χ. μεταλλάξεις) που είναι γνωστό ότι σχετίζονται με
ΑΝΑΤΟΜΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΑ ΜΑΣΤΟΥ
 ΑΝΑΤΟΜΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΑ ΜΑΣΤΟΥ ΔΙΑΦΟΡΙΚΗ ΔΙΑΓΝΩΣΗ ΦΥΣΙΟΛΟΓΙΚΩΝ ΑΠΟ ΝΕΟΠΛΑΣΜΑΤΙΚΕΣ ΚΑΙ ΜΗ ΝΕΟΠΛΑΣΜΑΤΙΚΕΣ ΑΛΛΟΙΩΣΕΙΣ Δρ. Άρτεμις Στυλιανίδου Επιμελήτρια Α Π.Γ.Ν. Μ. Έλενα Βενιζέλου ΑΝΑΤΟΜΙΑ ΦΥΣΙΟΛΟΓΙΑ ΜΑΣΤΟΣ
ΑΝΑΤΟΜΙΑ ΚΑΙ ΙΣΤΟΛΟΓΙΑ ΜΑΣΤΟΥ ΔΙΑΦΟΡΙΚΗ ΔΙΑΓΝΩΣΗ ΦΥΣΙΟΛΟΓΙΚΩΝ ΑΠΟ ΝΕΟΠΛΑΣΜΑΤΙΚΕΣ ΚΑΙ ΜΗ ΝΕΟΠΛΑΣΜΑΤΙΚΕΣ ΑΛΛΟΙΩΣΕΙΣ Δρ. Άρτεμις Στυλιανίδου Επιμελήτρια Α Π.Γ.Ν. Μ. Έλενα Βενιζέλου ΑΝΑΤΟΜΙΑ ΦΥΣΙΟΛΟΓΙΑ ΜΑΣΤΟΣ
Επιδημιολογία καρκίνου του πνεύμονα Ενότητα 1: Ογκολογία Πνεύμονα. Κυριάκος Καρκούλιας, Επίκουρος Καθηγητής Σχολή Επιστημών Υγείας Τμήμα Ιατρικής
 Επιδημιολογία καρκίνου του πνεύμονα Ενότητα 1: Ογκολογία Πνεύμονα Κυριάκος Καρκούλιας, Επίκουρος Καθηγητής Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Επιδημιολογικά στοιχεία καρκίνου του πνεύμονα Ο καρκίνος
Επιδημιολογία καρκίνου του πνεύμονα Ενότητα 1: Ογκολογία Πνεύμονα Κυριάκος Καρκούλιας, Επίκουρος Καθηγητής Σχολή Επιστημών Υγείας Τμήμα Ιατρικής Επιδημιολογικά στοιχεία καρκίνου του πνεύμονα Ο καρκίνος
ΚΑΤΕΥΘΥΝΤΗΡΙΕΣ ΟΔΗΓΙΕΣ ΓΙΑ ΤΑ ΚΑΡΚΙΝΩΜΑΤΑ ΕΚ ΜΕΤΑΒΑΤΙΚΟΥ ΕΠΙΘΗΛΙΟΥ ΑΝΩΤΕΡΟΥ ΟΥΡΟΠΟΙΗΤΙΚΟΥ
 ΚΑΤΕΥΘΥΝΤΗΡΙΕΣ ΟΔΗΓΙΕΣ ΓΙΑ ΤΑ ΚΑΡΚΙΝΩΜΑΤΑ ΕΚ ΜΕΤΑΒΑΤΙΚΟΥ ΕΠΙΘΗΛΙΟΥ ΑΝΩΤΕΡΟΥ ΟΥΡΟΠΟΙΗΤΙΚΟΥ M. Rouprêt, R. Zigeuner, J. Palou, A. öhle, E. Kaasinen, M. abjuk, R. Sylvester, W. Oosterlinck Eur Urol 2011 Apr;59(4):584-94
ΚΑΤΕΥΘΥΝΤΗΡΙΕΣ ΟΔΗΓΙΕΣ ΓΙΑ ΤΑ ΚΑΡΚΙΝΩΜΑΤΑ ΕΚ ΜΕΤΑΒΑΤΙΚΟΥ ΕΠΙΘΗΛΙΟΥ ΑΝΩΤΕΡΟΥ ΟΥΡΟΠΟΙΗΤΙΚΟΥ M. Rouprêt, R. Zigeuner, J. Palou, A. öhle, E. Kaasinen, M. abjuk, R. Sylvester, W. Oosterlinck Eur Urol 2011 Apr;59(4):584-94
ΕΙΣΑΓΩΓΗ. Τι είναι καρκίνος. Ένα σύνολο 100 διαφορετικών νοσολογικών οντοτήτων. Ιδιότητες των καρκινικών κυττάρων και ιστών
 1 Ο KAΡKINOΣ ΤΟΥ ΜΑΣΤΟΥ στις γυναίκες είναι ένα άκρως επίκαιρο θέμα που αφορά τον γυναικείο πληθυσμό και όχι μόνο. Η έγκαιρη διάγνωση και αντιμετώπιση αποβαίνει σωτήρια για τη γυναίκα. Η ανταλλαγή απόψεων
1 Ο KAΡKINOΣ ΤΟΥ ΜΑΣΤΟΥ στις γυναίκες είναι ένα άκρως επίκαιρο θέμα που αφορά τον γυναικείο πληθυσμό και όχι μόνο. Η έγκαιρη διάγνωση και αντιμετώπιση αποβαίνει σωτήρια για τη γυναίκα. Η ανταλλαγή απόψεων
Μαγνητική Μαστογραφία
 ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΙΔΡΥΜΑ ΑΘΗΝΑΣ ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ ΡΑΔΙΟΛΟΓΙΑΣ ΑΚΤΙΝΟΛΟΓΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Μαγνητική Μαστογραφία Τεχνικές απεικόνισης και πρωτόκολλα που χρησιμοποιούνται
ΤΕΧΝΟΛΟΓΙΚΟ ΕΚΠΑΙΔΕΥΤΙΚΟ ΙΔΡΥΜΑ ΑΘΗΝΑΣ ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ ΡΑΔΙΟΛΟΓΙΑΣ ΑΚΤΙΝΟΛΟΓΙΑΣ ΠΤΥΧΙΑΚΗ ΕΡΓΑΣΙΑ Μαγνητική Μαστογραφία Τεχνικές απεικόνισης και πρωτόκολλα που χρησιμοποιούνται
ΜΗ ΨΗΛΑΦΗΤΕΣ ΑΛΛΟΙΩΣΕΙΣ ΜΑΣΤΟΥ ΧΕΙΡΙΣΜΟΣ ΠΑΡΑΣΚΕΥΑΣΜΑΤΟΣ. Πετρούλα Αραπαντώνη-Δαδιώτη Δ/ντρια Παθολογοανατομικού Εργαστ ΕΑΝΠ-ΜΕΤΑΞΑ-ΠΕΙΡΑΙΑΣ
 ΜΗ ΨΗΛΑΦΗΤΕΣ ΑΛΛΟΙΩΣΕΙΣ ΜΑΣΤΟΥ ΧΕΙΡΙΣΜΟΣ ΠΑΡΑΣΚΕΥΑΣΜΑΤΟΣ Πετρούλα Αραπαντώνη-Δαδιώτη Δ/ντρια Παθολογοανατομικού Εργαστ ΕΑΝΠ-ΜΕΤΑΞΑ-ΠΕΙΡΑΙΑΣ οι αλλοιώσεις του μαστού που χειρουργούνται χαρακτηρίζονται ως
ΜΗ ΨΗΛΑΦΗΤΕΣ ΑΛΛΟΙΩΣΕΙΣ ΜΑΣΤΟΥ ΧΕΙΡΙΣΜΟΣ ΠΑΡΑΣΚΕΥΑΣΜΑΤΟΣ Πετρούλα Αραπαντώνη-Δαδιώτη Δ/ντρια Παθολογοανατομικού Εργαστ ΕΑΝΠ-ΜΕΤΑΞΑ-ΠΕΙΡΑΙΑΣ οι αλλοιώσεις του μαστού που χειρουργούνται χαρακτηρίζονται ως
Τμήμα Ιατρικής Πανεπιστημίου Πατρών Πρόγραμμα Μεταπτυχιακών Σπουδών Στη Δημόσια Υγεία
 Τμήμα Ιατρικής Πανεπιστημίου Πατρών Πρόγραμμα Μεταπτυχιακών Σπουδών Στη Δημόσια Υγεία Θέμα: Μαστογραφία στο γενικό πληθυσμό- επιδημιολογικά και οικονομικά δεδομένα του Πανεπιστημιακού Νοσοκομείου Πατρών
Τμήμα Ιατρικής Πανεπιστημίου Πατρών Πρόγραμμα Μεταπτυχιακών Σπουδών Στη Δημόσια Υγεία Θέμα: Μαστογραφία στο γενικό πληθυσμό- επιδημιολογικά και οικονομικά δεδομένα του Πανεπιστημιακού Νοσοκομείου Πατρών
Ρ. Κωτακίδου Αναπλ. Διευθύντρια Γ.Ν.Θ. «Γ.Γεννηματάς»
 Ρ. Κωτακίδου Αναπλ. Διευθύντρια Γ.Ν.Θ. «Γ.Γεννηματάς» Θεσσαλονίκη 8 Ιανουαρίου 2007 Προδιηθητικές επίπεδο ενδοεπιθηλιακό καρκίνωμα δυσπλασία Ο όρος «ουροθηλιακή ενδοεπιθηλιακή νεοπλασία» (urothelial intraepithelial
Ρ. Κωτακίδου Αναπλ. Διευθύντρια Γ.Ν.Θ. «Γ.Γεννηματάς» Θεσσαλονίκη 8 Ιανουαρίου 2007 Προδιηθητικές επίπεδο ενδοεπιθηλιακό καρκίνωμα δυσπλασία Ο όρος «ουροθηλιακή ενδοεπιθηλιακή νεοπλασία» (urothelial intraepithelial
ΤΕΙ ΑΘΗΝΑΣ ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ
 ΤΕΙ ΑΘΗΝΑΣ ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΒΙΟΪΑΤΡΙΚΕΣ ΜΕΘΟΔΟΙ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΣΤΗ ΔΙΑΓΝΩΣΗ» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ Ενδοεπιθηλιακός (in situ)
ΤΕΙ ΑΘΗΝΑΣ ΣΧΟΛΗ ΕΠΑΓΓΕΛΜΑΤΩΝ ΥΓΕΙΑΣ ΚΑΙ ΠΡΟΝΟΙΑΣ ΤΜΗΜΑ ΙΑΤΡΙΚΩΝ ΕΡΓΑΣΤΗΡΙΩΝ ΠΡΟΓΡΑΜΜΑ ΜΕΤΑΠΤΥΧΙΑΚΩΝ ΣΠΟΥΔΩΝ «ΒΙΟΪΑΤΡΙΚΕΣ ΜΕΘΟΔΟΙ ΚΑΙ ΤΕΧΝΟΛΟΓΙΑ ΣΤΗ ΔΙΑΓΝΩΣΗ» ΔΙΠΛΩΜΑΤΙΚΗ ΕΡΓΑΣΙΑ Ενδοεπιθηλιακός (in situ)
Επίδραση θεραπειών στον καλοήθη και κακοήθη προστατικό ιστό. Θ. Γεωργιάδης Επιμελητής A, ΔΘΚΑ ΥΓΕΙΑ
 Επίδραση θεραπειών στον καλοήθη και κακοήθη προστατικό ιστό Θ. Γεωργιάδης Επιμελητής A, ΔΘΚΑ ΥΓΕΙΑ Προεγχειρητικός ανδρογονικός αποκλεισμός LHRH αγωνιστές (μερικός ) ή και μη στεροειδές αντιανδρογόνο (πλήρης
Επίδραση θεραπειών στον καλοήθη και κακοήθη προστατικό ιστό Θ. Γεωργιάδης Επιμελητής A, ΔΘΚΑ ΥΓΕΙΑ Προεγχειρητικός ανδρογονικός αποκλεισμός LHRH αγωνιστές (μερικός ) ή και μη στεροειδές αντιανδρογόνο (πλήρης
1 - jr j - ί ί ) - i l. ί. ϊ
 026000265323 1Λ - jr1 j - ί ί ) - i l. ί. ϊ 4 q. 1353....200.5» ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΜΟΡΦΟΛΟΓΙΚΟΣ-ΚΛΙΝΙΚΟΕΡΓΑΣΤΗΡΙΑΚΟΣ ΤΟΜΕΑΣ ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΔΙΕΥΘΥΝΤΗΣ: ΚΑΘΗΓΗΤΗΣ ΝΙΚΗ
026000265323 1Λ - jr1 j - ί ί ) - i l. ί. ϊ 4 q. 1353....200.5» ΠΑΝΕΠΙΣΤΗΜΙΟ ΙΩΑΝΝΙΝΩΝ ΙΑΤΡΙΚΗ ΣΧΟΛΗ ΜΟΡΦΟΛΟΓΙΚΟΣ-ΚΛΙΝΙΚΟΕΡΓΑΣΤΗΡΙΑΚΟΣ ΤΟΜΕΑΣ ΕΡΓΑΣΤΗΡΙΟ ΠΑΘΟΛΟΓΙΚΗΣ ΑΝΑΤΟΜΙΚΗΣ ΔΙΕΥΘΥΝΤΗΣ: ΚΑΘΗΓΗΤΗΣ ΝΙΚΗ
Urogold III: Οι σημαντικότερες δημοσιεύσεις της χρονιάς (Προστάτης- όρχεις)
 Urogold III: Οι σημαντικότερες δημοσιεύσεις της χρονιάς (Προστάτης- όρχεις) Μουρμούρης Παναγιώτης MD, MSc, PhD, FEBU Πανεπιστημιακός Υπότροφος ΕΚΠΑ Β Ουρολογική Κλινική Σισμανόγλειο ΓΝΑ Καμία σύγκρουση
Urogold III: Οι σημαντικότερες δημοσιεύσεις της χρονιάς (Προστάτης- όρχεις) Μουρμούρης Παναγιώτης MD, MSc, PhD, FEBU Πανεπιστημιακός Υπότροφος ΕΚΠΑ Β Ουρολογική Κλινική Σισμανόγλειο ΓΝΑ Καμία σύγκρουση
